附錄 99.1

Benitec Biopharma發佈2024年第三季度財務業績並提供最新運營情況
-在 4 月份報告的 1b/2a 期臨牀治療研究中,首位眼嚥肌萎縮症 (OPMD) 受試者服用 BB-301 的中期臨牀試驗數據呈陽性-
-第二個 OPMD 受試者 已在 2 月份安全服用 BB-301 劑量-
-預計2024年下半年將有更多中期臨牀安全數據和 臨牀療效數據-
-23 名 OPMD 受試者已報名參加 OPMD 自然史研究,多名受試者有資格參加 BB-301 1b/2a 期臨牀治療研究-
-4月22日完成了4000萬美元的超額認購私募融資 22和,Cash Runway 延長至 2025 年-
加利福尼亞州海沃德,2024年5月13日(GLOBE NEWSWIRE)貝尼特克生物製藥公司(納斯達克股票代碼:BNTC)(貝尼特克或公司)是一家臨牀階段、專注於基因療法的生物技術公司,基於其專有的Silence和 取代DNA導向RNA幹擾(ddrNAI)平臺開發新型基因藥物,今天公佈了截至3月31日的第三財季財務業績,2024。該公司已向美國證券交易委員會提交了10-Q表格的季度報告 。
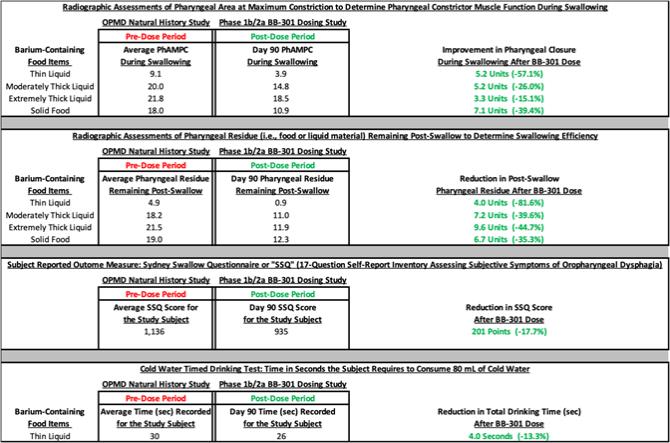
貝尼特克執行主席兼首席執行官傑雷爾·班克斯醫學博士、博士表示, 首位參加 BB-301 1b/2a 期臨牀治療研究的受試者的中期臨牀試驗結果顯示,每個中心研究終點都出現了持續的、具有臨牀意義的改善,吞嚥的射線照相評估以及受試者報告的關鍵結果指標的相應改善。我們 期待在今年晚些時候公佈第一個研究對象的長期隨訪結果,以及其他研究受試者的累積數據。繼最近的 融資之後,貝尼特克完全有能力在2025年底之前推進 BB-301 臨牀開發計劃。