美國
證券交易委員會
華盛頓特區 20549
表單
(標記一號)
在截至的季度期間
要麼
在從到的過渡期內
委員會檔案編號:
(註冊人的確切姓名如其章程所示)
|
(公司或組織的州或其他司法管轄區) |
不適用 (美國國税局僱主識別號) |
(主要行政辦公室地址)(郵政編碼)
(
(註冊人的電話號碼,包括區號)
根據該法第12(b)條註冊的證券:
|
每個班級的標題 |
交易符號 |
註冊的每個交易所的名稱 |
|
|
|
這個 |
用複選標記表明註冊人(1)在過去的12個月中(或註冊人需要提交此類報告的較短期限)是否提交了1934年《證券交易法》第13或15(d)條要求提交的所有報告,以及(2)在過去的90天中是否受此類申報要求的約束。
用複選標記表明註冊人是否在過去 12 個月內(或者在要求註冊人提交此類文件的較短時間內)以電子方式提交了根據第 S-T 法規(本章第 232.405 節)第 405 條要求提交的所有交互式數據文件。
用複選標記指明註冊人是大型加速申報人、加速申報人、非加速申報人、小型申報公司還是新興成長型公司。參見《交易法》第12b-2條中 “大型加速申報人”、“加速申報公司”、“小型申報公司” 和 “新興成長型公司” 的定義。
|
大型加速過濾器 ☐ |
加速過濾器 ☐ |
|
|
規模較小的申報公司 |
| 新興成長型公司 |
如果是新興成長型公司,請用複選標記表明註冊人是否選擇不使用延長的過渡期來遵守根據《交易法》第13(a)條規定的任何新的或修訂後的財務會計準則。☐
用複選標記表明註冊人是否為空殼公司(定義見《交易法》第12b-2條)。是的
截至 2024 年 5 月 3 日,有
Diamedica Therapeutics Inc
表格 10-Q
2024年3月31日
目錄
| 描述 | 頁面 | |
| 關於前瞻性陳述的警示性説明 | 1 | |
| 第一部分 | 財務信息 | |
|
第 1 項。 |
財務報表 |
3 |
|
第 2 項。 |
管理層對財務狀況和經營業績的討論和分析 |
14 |
|
第 3 項。 |
關於市場風險的定量和定性披露 |
20 |
|
第 4 項。 |
控制和程序 |
20 |
| 第二部分。 | 其他信息 | |
|
第 1 項。 |
法律訴訟 |
21 |
|
第 1A 項。 |
風險因素 |
21 |
|
第 2 項。 |
未註冊的股權證券銷售和所得款項的使用 |
21 |
|
第 3 項。 |
優先證券違約 |
21 |
|
第 4 項。 |
礦山安全披露 |
21 |
|
第 5 項。 |
其他信息 |
22 |
|
第 6 項。 |
展品 |
22 |
| 簽名頁面 | 23 | |
本10-Q表季度報告包含經修訂的1933年《美國證券法》第27A條和經修訂的1934年《美國證券交易法》第21E條所指的某些前瞻性陳述,這些陳述受這些條款規定的安全港的約束。有關更多信息,請參見 “關於前瞻性陳述的警示説明。”
如本報告所用,提及 “迪亞梅迪卡,”這 “公司,” “我們,” “我們的”要麼 “我們,”除非上下文另有要求,否則請參閲 Diamedica Therapeutics Inc. 及其子公司,所有這些子公司均合併為 DiameDica’的簡明合併財務報表。本報告中提到 “普通股”是指我們的有表決權的普通股,每股沒有面值。
我們擁有各種未註冊的商標和服務標誌,包括我們的公司徽標。僅為方便起見,本報告中提及的商標和商品名稱不包括 ®和 ™符號,但此類提及不應被解釋為表明此類商標和商品名稱的所有者不會在適用法律規定的最大範圍內維護其權利。我們不打算使用或展示其他公司’商標和商品名稱暗示與任何其他公司有關係,或由任何其他公司對我們的認可或贊助。
關於前瞻性陳述的警示性説明
本報告中未描述歷史事實的陳述是1995年《美國私人證券訴訟改革法》所指的前瞻性陳述,這些陳述基於管理層當前的預期,存在風險和不確定性,可能會對我們的業務、經營業績、財務狀況、前景和股價產生負面影響。我們試圖通過包括 “預期”、“相信”、“可以”、“繼續”、“可能”、“估計”、“預期”、“打算”、“可能”、“計劃”、“潛力”、“預測”、“應該”、“將”、“將”、“這些術語或其他類似術語的否定值以及未來日期的使用” 等術語來識別前瞻性陳述。
本報告中的前瞻性陳述受風險和不確定性的影響,除其他外,包括:
|
● |
我們計劃開發、獲得監管部門批准和商業化用於治療急性缺血性中風 (AIS) 和心腎疾病 (CRD) 的 DM199 候選產品; |
|
● |
我們有能力成功對 AIS 或 CRD 的 DM199 候選產品進行臨牀測試,並在特定預期或目標日期之前完成臨牀研究,包括特別是我們用於治療 AIS 的 DM199 的 2/3 期 Remedy2 臨牀試驗,即 Remedy2 試驗,即 Remedy2 試驗; |
|
● |
我們有能力滿足Remedy2試驗的預期場地激活、入組和中期分析時機,尤其是考慮到部位激活和入組速度低於預期,我們認為部分原因是醫院和醫療機構人員短缺;對先前出現的臨牀重大低血壓事件和2023年6月解除的臨牀暫停情況的擔憂;涉及協議合規性管理,包括管理出院參與者的後勤和協議合規性醫院轉到另一家醫院或中級護理機構;我們在研究方案中修訂的納入/排除標準;以及由於其他未決的中風和神經學試驗而導致的研究人員和試驗受試者的競爭; |
|
● |
與監管申請和相關的申請和批准時間表相關的不確定性,以及將來可能出現與我們的Remedy2試驗相關的其他不良事件或不利結果; |
|
● |
我們的Remedy2試驗的適應性設計,該試驗旨在在全球多達100個地點招募約350名參與者,以及這些數字和該研究的其他方面可能增加的可能性,具體取決於某些因素,包括美國食品藥品監督管理局(FDA)的額外意見以及獨立數據安全監督委員會確定的中期分析結果; |
|
● |
我們對我們的 DM199 候選產品相對於現有的 AIS 和 CRD 治療方案的預期益處的期望; |
|
● |
我們的 AIS 和 CRD 候選產品 DM199 的潛在市場規模,以及我們為這些市場提供服務的能力,以及我們在美國和國際上 AIS 和 CRD 的 DM199 候選產品的市場接受率和程度,以及我們獲得保險和足夠報銷的能力; |
|
● |
我們有能力與生物製藥或製藥合作伙伴合作並從中獲得收入,以開發我們的 AIS 和 CRD 的 DM199 候選產品,獲得監管部門的批准和商業化; |
|
● |
我們的Remedy2試驗的成功、成本和時機,以及我們在Remedy2試驗和我們進行的任何其他臨牀試驗中對第三方的依賴; |
|
● |
我們的商業化、營銷和製造能力和戰略; |
|
● |
對聯邦、州和外國監管要求和發展的期望,例如美國食品藥品管理局可能對我們的 AIS 和 CRD 候選產品 DM199 的監管; |
|
● |
我們對支出、候選產品的市場機會、未來收入、資本需求、我們目前的現金資源將持續多長時間以及額外融資需求的估計; |
|
● |
我們對我們獲得和維持我們的 DM199 候選產品的知識產權保護的能力的期望; |
|
● |
對競爭的期望以及我們獲得 AIS 和 CRD 的 DM199 候選產品的數據排他性的能力;以及 |
|
● |
我們有能力為我們的運營獲得額外資金,包括完成計劃中的臨牀試驗和獲得監管部門批准 AIS 和 CRD 的 DM199 候選產品所需的資金。 |
這些前瞻性陳述受許多風險、不確定性和假設的影響,包括 “” 中描述的風險、不確定性和假設第一部分第1A項。風險因素” 在我們截至2023年12月31日的財政年度的10-K表年度報告以及上述和本報告其他地方描述的年度報告中。此外,我們在競爭激烈且瞬息萬變的環境中運營。新的風險不時出現。我們的管理層無法預測所有風險,也無法評估所有因素對我們業務的影響,也無法評估任何因素或因素組合在多大程度上可能導致實際業績與我們可能做出的任何前瞻性陳述中包含的結果存在重大差異。鑑於這些風險、不確定性和假設,本報告中討論的前瞻性事件和情況可能不會發生,實際結果可能與前瞻性陳述中的預期或暗示結果存在重大和不利的差異。不應將前瞻性陳述作為對未來事件的預測。儘管我們認為前瞻性陳述中反映的預期是合理的,但我們不能保證前瞻性陳述中反映的未來業績、活動水平、業績或事件和情況能夠實現或發生。除非包括美國證券法在內的法律要求,否則我們不打算更新任何前瞻性陳述,以使這些陳述符合實際業績或我們的預期變化。
第一部分-財務信息
|
第 1 項。 |
財務報表 |
Diamedica Therapeutics Inc
簡明合併資產負債表
(以千計,股票金額除外)
|
2024年3月31日 |
2023年12月31日 |
|||||||
|
(未經審計) |
||||||||
|
資產 |
||||||||
|
流動資產: |
||||||||
|
現金和現金等價物 |
$ | $ | ||||||
|
有價證券 |
||||||||
|
預付費用和其他資產 |
||||||||
|
應收金額 |
||||||||
|
流動資產總額 |
||||||||
|
非流動資產: |
||||||||
|
存款 |
||||||||
|
經營租賃使用權資產,淨額 |
||||||||
|
財產和設備,淨額 |
||||||||
|
非流動資產總額 |
||||||||
|
總資產 |
$ | $ | ||||||
|
負債和權益 |
||||||||
|
流動負債: |
||||||||
|
應付賬款 |
$ | $ | ||||||
|
應計負債 |
||||||||
|
經營租賃債務 |
||||||||
|
融資租賃債務 |
||||||||
|
流動負債總額 |
||||||||
|
非流動負債: |
||||||||
|
經營租賃債務 |
||||||||
|
融資租賃債務 |
||||||||
|
非流動負債總額 |
||||||||
|
股東權益: |
||||||||
|
普通股,無面值; 授權; |
||||||||
|
實收資本 |
||||||||
|
累計其他綜合收益(虧損) |
( |
) | ||||||
|
累計赤字 |
( |
) | ( |
) | ||||
|
股東權益總額 |
||||||||
|
負債和股東權益總額 |
$ | $ | ||||||
參見簡明合併財務報表的附註。
Diamedica Therapeutics Inc
簡明合併運營報表和綜合虧損報表
(以千計,股票和每股金額除外)
(未經審計)
|
三個月已結束 3月31日 |
||||||||
|
2024 |
2023 |
|||||||
|
運營費用: |
||||||||
|
研究和開發 |
$ | $ | ||||||
|
一般和行政 |
||||||||
|
運營費用總額 |
( |
) |
( |
) |
||||
|
營業虧損 |
( |
) | ( |
) | ||||
|
其他收入,淨額 |
||||||||
|
所得税支出前的虧損 |
( |
) | ( |
) | ||||
|
所得税支出 |
( |
) |
( |
) |
||||
|
淨虧損 |
( |
) |
( |
) |
||||
|
其他綜合收益(虧損) |
||||||||
|
有價證券的未實現收益(虧損) |
( |
) |
||||||
|
淨虧損和綜合虧損 |
$ | ( |
) |
$ | ( |
) |
||
|
基本和攤薄後的每股淨虧損 |
$ | ( |
) |
$ | ( |
) |
||
|
加權平均已發行股票——基本和攤薄後 |
||||||||
參見簡明合併財務報表的附註。
Diamedica Therapeutics Inc
股東權益簡明合併報表
在截至 2024 年 3 月 31 日和 2023 年 3 月 31 日的三個月
(以千計,股票金額除外)
(未經審計)
|
常見 股份 |
付費 資本 |
累積的 其他 全面 收入(虧損) |
累積的 赤字 |
總計 股東 公平 |
||||||||||||||||
|
截至 2023 年 12 月 31 日的餘額 |
$ | $ | $ | ( |
) | $ | ||||||||||||||
|
在限制性股票單位的歸屬和結算後發行普通股 |
||||||||||||||||||||
|
基於股份的薪酬支出 |
— | — | — | |||||||||||||||||
|
有價證券的未實現虧損 |
— | — | ( |
) | — | ( |
) | |||||||||||||
|
淨虧損 |
— | — | — | ( |
) | ( |
) | |||||||||||||
|
截至 2024 年 3 月 31 日的餘額 |
$ | $ | ( |
) | $ | ( |
) | $ | ||||||||||||
|
常見 股份 |
付費 資本 |
累積的 其他 全面 收入(虧損) |
累積的 赤字 |
總計 股東 公平 |
||||||||||||||||
|
截至2022年12月31日的餘額 |
$ | $ | ( |
) | $ | ( |
) | $ | ||||||||||||
|
發行普通股以結算遞延股票單位 |
— | — | — | — | ||||||||||||||||
|
在限制性股票單位的歸屬和結算後發行普通股 |
||||||||||||||||||||
|
基於股份的薪酬支出 |
— | |||||||||||||||||||
|
有價證券的未實現收益 |
— | |||||||||||||||||||
|
淨虧損 |
— | ( |
) | ( |
) | |||||||||||||||
|
截至2023年3月31日的餘額 |
$ | $ | ( |
) | $ | ( |
) | $ | ||||||||||||
參見簡明合併財務報表的附註。
Diamedica Therapeutics Inc
簡明合併現金流量表
(以千計)
(未經審計)
|
截至3月31日的三個月 |
||||||||
|
2024 |
2023 |
|||||||
|
來自經營活動的現金流: |
||||||||
|
淨虧損 |
$ | ( |
) |
$ | ( |
) |
||
|
為使淨虧損與經營活動中使用的淨現金相一致而進行的調整: |
||||||||
|
基於股份的薪酬 |
||||||||
|
攤銷有價證券的折扣 |
( |
) |
( |
) | ||||
|
非現金租賃費用 |
||||||||
|
折舊 |
||||||||
|
運營資產和負債的變化: |
||||||||
|
應收金額 |
( |
) |
||||||
|
預付費用和其他資產 |
( |
) |
( |
) |
||||
|
存款 |
( |
) | ||||||
|
應付賬款 |
( |
) | ||||||
|
應計負債 |
( |
) | ||||||
|
用於經營活動的淨現金 |
( |
) |
( |
) |
||||
|
來自投資活動的現金流: |
||||||||
|
購買有價證券 |
( |
) |
( |
) |
||||
|
有價證券的到期日 |
||||||||
|
購買財產和設備 |
( |
) |
( |
) |
||||
|
投資活動提供的淨現金 |
||||||||
|
來自融資活動的現金流: |
||||||||
|
融資租賃債務的本金付款 |
( |
) |
( |
) |
||||
|
用於融資活動的淨現金 |
( |
) | ( |
) | ||||
|
現金和現金等價物的淨減少 |
( |
) |
( |
) |
||||
|
期初的現金和現金等價物 |
||||||||
|
期末的現金和現金等價物 |
$ | $ | ||||||
|
非現金交易的補充披露: |
||||||||
|
為所得税支付的現金 |
$ | $ | ||||||
參見簡明合併財務報表的附註。
diamedica Therapeutics Inc. {br簡明合併財務報表附註
(未經審計)
|
1. |
商業 |
DiaMedica Therapeutics Inc.及其全資子公司DiaMedica USA Inc.和Diamedica Australia Pty Ltd.(合稱 “我們”、“我們”、“Diamedica和公司”)存在的主要目的是推進我們專有的名為 DM199 的重組KLK1蛋白的臨牀和商業開發,該蛋白用於治療神經系統和心腎疾病。目前,我們的主要重點是開發 DM199,一種人體組織激素-1(KLK1)蛋白的重組形式,用於治療急性缺血性中風(AIS)和心腎疾病(CRD)。我們的母公司受不列顛哥倫比亞省商業公司法管轄,我們的普通股在納斯達克資本市場上市,股票代碼為 “DMAC”。
|
2. |
風險和不確定性 |
DiaMedica在高度監管和競爭激烈的環境中運營。藥品的開發、製造和銷售需要獲得美國食品藥品監督管理局(FDA)、歐盟的歐洲藥品管理局(EMA)和其他國家的類似機構的批准,並受到它們的持續監督。我們目前正處於開發用於治療急性呼吸綜合徵和慢性心臟病的初始候選產品 DM199 的臨牀階段。我們尚未完成任何候選產品的開發,也沒有從任何候選產品的商業銷售中產生任何收入。在尋求上市批准之前,DM199 需要大量的額外臨牀測試和投資,如果有的話,預計至少在三年內不會上市。
在2022年7月宣佈並於2023年6月解除的Remedy2試驗的臨牀暫停之前,我們的Remedy2試驗的位點激活和註冊速度一直低於預期,現在仍在繼續。我們認為,這些情況可能是由於醫院和醫療機構人員短缺;對先前臨牀上嚴重的低血壓事件和先前臨牀暫停情況的擔憂;管理協議合規性的問題,包括管理出院到另一家醫院或中級護理機構的參與者的後勤和協議合規性;我們在研究方案中修訂的納入/排除標準;以及由於其他未決中風而導致的研究人員和試驗受試者的競爭神經學試驗。為了減輕這些因素的影響,我們決定在全球範圍內擴大試驗,我們正在準備監管文件,並確定和吸引加拿大、澳大利亞、英國和歐洲的研究地點。我們正在與我們的合同研究組織密切合作,制定程序,以根據需要為美國和全球研究地點和潛在參與者提供支持。我們打算繼續監測這些努力的結果,並在必要時採取更多措施來減輕這些因素對我們Remedy2試驗的影響;但是,無法保證這些問題是否以及何時會得到解決。未能解決這些問題將導致我們的Remedy2試用延遲。
我們未來的成功取決於我們開發工作的成功、我們在美國或其他市場證明我們的 DM199 候選產品的臨牀進展的能力、我們或未來任何合作伙伴獲得候選產品所需的政府批准的能力、我們許可或營銷和銷售我們的 DM199 候選產品的能力,以及我們獲得額外資金為這些工作提供資金的能力。
截至2024年3月31日,我們已經蒙受了美元的損失
我們的主要現金來源是股票證券發行的淨收益。儘管我們以前成功地通過股票證券發行獲得了融資,但無法保證將來我們能夠這樣做。如果我們的臨牀數據不正面或者經濟和市場狀況惡化,則尤其如此。
我們預計,我們將需要大量的額外資金來進一步開展我們的研發活動,完成我們的候選產品 DM199 或任何未來候選產品所需的臨牀研究、監管活動和製造開發,直至獲得許可或商業銷售的程度。我們預計,我們目前的現金、現金等價物和有價證券足以繼續我們的Remedy2試驗,並在自這些簡明合併財務報表發佈之日起的至少未來12個月內為我們的計劃運營提供資金。我們未來資金需求的金額和時間將取決於許多因素,包括我們持續開發的時間和結果,包括我們目前的Remedy2試驗以及研究的研究中心激活率和參與者註冊率、我們當前開發計劃的潛在擴展、潛在的新開發計劃、持續的研究中心人員短缺和其他因素對我們的臨牀試驗和運營支出的影響。我們可能比目前的預期更早地需要大量額外資金,並且無法保證在此之前我們不會需要或尋求額外的資金,尤其是在籌集資金的市場條件有利的情況下。
|
3. |
重要會計政策摘要 |
中期財務報表
我們根據美國普遍接受的中期財務信息會計原則(美國公認會計原則)以及美國證券交易委員會(SEC)10-Q表和S-X條例的指示,編制了隨附的簡明合併財務報表。因此,它們不包括美國公認會計原則要求的完整財務報表的所有信息和腳註。這些簡明合併財務報表反映了由正常經常性應計費用組成的所有調整,管理層認為,這些調整是公允列報截至本報告所述期間和日期的簡明合併財務狀況、簡明合併經營業績、簡明合併股東權益表和簡明合併現金流所必需的。我們的財政年度於12月31日結束。截至2023年12月31日的簡明合併資產負債表來自我們經審計的合併財務報表。這些簡明的合併財務報表應與我們的年度合併財務報表及其附註一起閲讀。我們業務的性質使得任何中期的業績都不代表全年預期的業績。
現金和現金等價物
公司將購買的所有銀行存款,包括貨幣市場基金和其他投資,在公司原始到期日為三個月或更短的時間內購買,均為現金及現金等價物。由於投資到期日短,我們的現金等價物的賬面金額接近公允價值。
有價證券
公司的有價證券可能包括美國政府及其機構的債務、銀行存款證和/或投資級公司債務,這些債務被歸類為可供出售。自購買之日起12個月內到期的有價證券包含在流動資產中。證券通常根據使用第三方認證定價來源的類似資產的市場價格進行估值,並按公允價值計值。有價證券的攤銷成本根據保費的攤銷或到期折扣的增加進行調整。此類攤銷或增加包含在利息收入中。已實現的收益和損失(如果有)是根據特定的識別方法計算的。利息收入包含在簡明合併運營報表中的其他收入中。
我們會定期進行審查,以識別和評估每種處於未實現虧損狀況的可出售債務證券,以確定是否存在非臨時減值。當個別證券的當前公允價值低於其攤銷成本基礎時,即存在未實現虧損。公允價值的下降被認為是暫時性的,由發行人的非信貸相關因素引起,計入累計的其他綜合虧損,後者是股東權益的單獨組成部分。非暫時性或由發行人信貸相關因素引起的公允價值下降作為減值損失記入收益。截至2024年3月31日,除了暫時的未實現虧損外,沒有其他虧損。
公允價值測量
根據公允價值計量的權威指導,公允價值被定義為截至衡量之日的退出價格,即出售資產或在有序交易中轉移負債所獲得的金額。該權威指南還規定了用於衡量公允價值的投入的等級制度,通過要求在可用時使用最可觀察的投入,最大限度地使用可觀察的投入,最大限度地減少對不可觀察投入的使用。可觀察的投入是市場參與者在估值根據從公司獨立來源獲得的市場數據開發的資產或負債時使用的投入。不可觀察的輸入是反映公司對市場參與者在估值資產或負債時將使用的因素的假設,這些因素是根據當時可用的最佳信息制定的資產或負債的。估值層次結構中金融資產和金融負債的分類基於對公允價值計量至關重要的最低投入水平。
層次結構分為三個級別,定義如下:
1 級輸入— 相同資產和負債在活躍市場上的報價
2 級輸入— 相同資產和負債的活躍市場報價以外的其他可觀察輸入
3 級輸入— 不可觀察的輸入
截至2024年3月31日,公司認為,由於這些工具的短期到期,其其他金融工具的賬面金額,包括應收賬款、應付賬款和應計負債,接近其公允價值。參見注釋 4,標題為”有價證券” 以獲取更多信息。
|
4. |
有價證券 |
可供出售的有價證券主要由商業票據、公司債券和政府證券的投資組成,包括以下內容,按經常性公允價值計量(以千計):
|
使用截至以下時間所考慮的輸入進行公允價值測量: |
||||||||||||||||||||||||||||||||
| 2024年3月31日 |
2023年12月31日 |
|||||||||||||||||||||||||||||||
|
總計 |
第 1 級 |
第 2 級 |
第 3 級 |
總計 |
第 1 級 |
第 2 級 |
第 3 級 |
|||||||||||||||||||||||||
|
商業票據和公司債券 |
$ | $ | $ | $ | $ | $ | $ | $ | ||||||||||||||||||||||||
|
政府證券 |
||||||||||||||||||||||||||||||||
|
總計 |
$ | $ | $ | $ | $ | $ | $ | $ | ||||||||||||||||||||||||
截至2024年3月31日和2023年12月31日,個別證券的到期日少於一年,所有證券的攤銷成本均接近公允價值。有價證券的應計應收利息包含在應收金額中,為美元
在截至2024年3月31日的三個月中,公允價值衡量層次結構的1級和2級之間沒有資產轉移。
|
5. |
應收金額 |
應收金額主要包括有價證券的應計應收利息
|
6. |
存款 |
我們會定期向參與支持我們臨牀試驗和相關活動的供應商預付資金。預付資金在不同的期限內免息持有,通常由公司根據最終的研究/項目發票申請收回,或在提供的服務完成後退還。如果存款的預期回收不在未來十二個月內,則存款是非流動的。
|
7. |
財產和設備 |
財產和設備包括以下各項(以千計):
|
2024年3月31日 |
2023年12月31日 |
|||||||
|
傢俱和設備 |
$ | $ | ||||||
|
計算機設備 |
||||||||
|
租賃權改進 |
||||||||
|
減去累計折舊 |
( |
) | ( |
) | ||||
|
財產和設備,淨額 |
$ | $ | ||||||
|
8. |
應計負債 |
應計負債包括以下各項(以千計):
|
2024年3月31日 |
2023年12月31日 |
|||||||
|
臨牀試驗成本 |
$ | $ | ||||||
|
研究和開發服務 |
||||||||
|
補償 |
||||||||
|
專業服務費 |
||||||||
|
其他 |
||||||||
|
應計負債總額 |
$ | $ | ||||||
|
9. |
經營租賃 |
辦公室租賃
我們的經營租賃成本是 $
截至2024年3月31日,我們的經營租賃義務的到期日如下(以千計):
|
2024 |
$ | |||
|
2025 |
||||
|
2026 |
||||
|
2027 |
||||
|
2028 |
||||
|
租賃付款總額 |
$ | |||
|
減去利息部分 |
( |
) | ||
|
經營租賃債務的現值 |
$ |
|
10. |
股東權益 |
法定股本
Diamedica已授權無限數量的有表決權普通股的股本,並且這些股票沒有規定的面值。普通股股東有權獲得公司宣佈的股息(如果有),並有權在公司的年度股東大會和任何特別或特別股東大會上獲得每股一票。
截至2024年3月31日的三個月內發行的股票
在截至2024年3月31日的三個月中,
截至2023年3月31日的三個月內發行的股票
在截至2023年3月31日的三個月中,
已保留的股份
留待未來發行的普通股如下:
|
2024年3月31日 |
||||
|
行使員工和非僱員股票期權後可發行的普通股 |
||||
|
遞延股票單位結算後可發行的普通股 |
||||
|
限制性股票單位的歸屬和結算後可發行的普通股 |
||||
|
根據經修訂和重述的2019年綜合激勵計劃可供授予的股份 |
||||
|
2021年就業激勵計劃下可供授予的股份 |
||||
|
總計 |
||||
|
11. |
每股淨虧損 |
我們通過將淨虧損(分子)除以該期間已發行普通股的加權平均數(分母)來計算每股淨虧損。在此期間發行的股票和在此期間重新收購的股份(如果有)按該期間已發行部分進行加權。攤薄後每股收益(EPS)的計算與基本每股收益的計算類似,不同之處在於分母有所增加,以包括髮行攤薄潛在普通股後本應流通的額外普通股數量。我們的攤薄後每股收益與基本每股收益相同,因為普通等價股被排除在計算之外,因為它們的影響是反攤薄的。
下表彙總了我們在所述期間對每股普通股淨虧損的計算(以千計,股票和每股數據除外):
|
三個月已結束 3月31日 |
||||||||
|
2024 |
2023 |
|||||||
|
淨虧損 |
$ | ( |
) |
$ | ( |
) |
||
|
加權平均流通股——基本股和攤薄後股票 |
||||||||
|
基本和攤薄後的每股淨虧損 |
$ | ( |
) |
$ | ( |
) |
||
以下已發行潛在普通股未包含在攤薄後的每股淨虧損計算中,因為其影響不具有攤薄作用:
|
三個月已結束 3月31日 |
||||||||
|
2024 |
2023 |
|||||||
|
員工和非員工股票期權 |
||||||||
|
可根據普通股購買認股權證發行的普通股 |
||||||||
|
可根據遞延股票單位發行的普通股 |
||||||||
|
限制性股票單位的歸屬和結算後可發行的普通股 |
||||||||
|
12. |
基於股份的薪酬 |
經修訂和重述的2019年綜合激勵計劃
Diamedica Therapeutics Inc. 經修訂和重述的2019年綜合激勵計劃(2019年計劃)於2022年3月10日獲得董事會(董事會)通過,並在2022年5月18日舉行的2022年年度股東大會上獲得股東批准。
2019年計劃允許董事會或其委員會或小組委員會向公司的合格員工、非僱員董事和某些顧問授予非法定和激勵性股票期權、股票增值權、限制性股票獎勵、限制性股票獎勵、限制性股票單位(RSU)、遞延股票單位(DSU)、績效獎勵、非僱員董事獎勵和其他基於股份的獎勵。我們授予期權,根據2019年計劃,以不低於授予之日標的普通股的公允市場價值購買普通股。授予員工和非僱員董事的期權的最長期限為十年,通常歸屬期限為十年 到四年。授予非僱員的期權的最長期限為 年份,通常超過一年。根據2019年計劃的規定,公司授權發行的普通股的最大數量為,但須根據2019年計劃的規定進行調整
2021 年就業激勵計劃
2021年12月3日,董事會通過了DiaMedica Therapeutics Inc. 2021年就業激勵激勵計劃(激勵計劃),以促進向加入公司的新員工發放股權獎勵作為激勵材料。激勵計劃是根據納斯達克上市規則5635(c)(4)未經股東批准通過的,由董事會薪酬委員會管理。董事會保留
先前的股票期權計劃
2018年11月6日修訂和重述的Diamedica Therapeutics Inc.股票期權計劃(先前計劃)在股東批准2019年計劃的同時被董事會終止。根據並根據先前計劃的條款,先前計劃下的未付獎勵仍未支付。根據先前計劃授予的期權的條款與2019年計劃中使用的條款類似。截至2024年3月31日,購買期權總額為
先前的遞延股票單位計劃
在股東批准2019年計劃的同時,董事會終止了DiaMedica Therapeutics Inc.修訂和重述的遞延股票單位計劃(之前的DSU計劃)。根據先前DSU計劃的條款,未償還的獎勵仍未兑現。截至 2024 年 3 月 31 日,有
所列每個時期的基於股份的薪酬支出如下(以千計):
|
三個月已結束 3 月 31 日 |
||||||||
|
2024 |
2023 |
|||||||
|
研究和開發 |
$ | $ | ||||||
|
一般和行政 |
||||||||
|
基於股份的薪酬總額 |
$ | $ | ||||||
我們根據使用Black-Scholes期權估值模型估算的每項獎勵的公允價值來確認基於股份的薪酬。歸根結底,在歸屬期內確認的實際支出將僅適用於實際歸屬的股票。
期權活動摘要如下(以千計,股票和每股金額除外):
|
股份 標的 選項 |
加權 平均運動量 每股價格 |
聚合 內在價值 |
||||||||||
|
截至 2023 年 12 月 31 日的餘額 |
$ | $ | ||||||||||
|
已授予 |
||||||||||||
|
過期/已取消 |
||||||||||||
|
被沒收 |
( |
) | ||||||||||
|
截至 2024 年 3 月 31 日的餘額 |
$ | $ | ||||||||||
截至2024年3月31日,有關已流通、已歸屬和預計歸屬的股票期權的信息如下:
|
傑出、既得且有望歸屬 |
既得期權和可行使期權 |
|||||||||||||||||||||
|
每股行使 價格 |
股份 |
加權平均值 剩餘的 合同壽命 (年份) |
加權平均值 行使價格 |
選項 可鍛鍊 |
加權平均值 剩餘的 合同壽命 (年份) |
|||||||||||||||||
| $ |
- |
$ |
$ | |||||||||||||||||||
| $ |
- |
$ |
||||||||||||||||||||
| $ |
- |
$ |
||||||||||||||||||||
| $ |
- |
$ |
||||||||||||||||||||
| $ |
- |
$ |
||||||||||||||||||||
| $ | ||||||||||||||||||||||
第 2 項。管理層對財務狀況和經營業績的討論和分析
以下管理層對財務狀況和經營業績的討論和分析基於美利堅合眾國普遍接受的會計原則,討論了Diamedica Therapeutics Inc.及其子公司截至2024年3月31日和2023年3月31日的三個月的財務狀況和經營業績。
本討論應與本報告其他部分以及截至2023年12月31日止年度的10-K表年度報告中包含的簡明合併財務報表和相關附註一起閲讀。以下討論包含涉及眾多風險和不確定性的前瞻性陳述。由於這些風險和不確定性,我們的實際業績可能與前瞻性陳述存在重大差異。參見”關於前瞻性陳述的警示説明” 以獲取更多警告信息。
業務概述
我們是一家臨牀階段的生物製藥公司,致力於改善患有嚴重疾病的人的生活。我們的主要候選藥物 DM199(rinvecalinase alfa)是第一種在患者中進行臨牀研究的人體組織kallikrein-1(KLK1)蛋白的藥物活性重組(合成)形式。KLK1是亞洲成熟的治療方式,人體尿液KLK1用於治療急性缺血性中風(AIS),豬KLK1用於治療心臟腎臟疾病(CRD),包括高血壓。我們還開發了一種潛在的新型嚴重炎症性疾病療法,即 DM300,該療法目前處於臨牀前開發的早期階段。我們的長期目標是利用我們的專利和授權技術,使我們公司成為開發和商業化新型重組蛋白治療藥物的領導者。我們目前的重點是治療AIS和CRD。我們計劃通過必要的臨牀試驗推進 DM199 的發展,通過確立其作為 AIS 和 CRD 療法的臨牀和商業潛力來創造股東價值。
KLK1 是一種絲氨酸蛋白酶(蛋白質),主要產生於腎臟、胰腺和唾液腺,在調節人體局部血流和血管舒張(血管擴張會降低血管阻力)方面起着至關重要的作用,在減少炎症和氧化應激(可能有害的活性氧或體內自由基和抗氧化劑之間的失衡)方面起着重要作用。我們認為,DM199 有可能治療各種疾病,在這些疾病中,健康的功能需要 KLK1 及其系統 kallikrein-kinin 系統 (KKS) 的足夠活性。
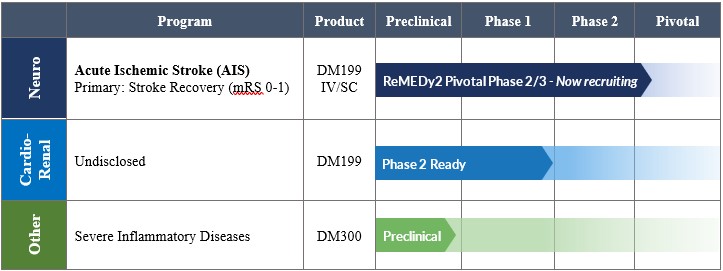
我們的產品開發流程如下:

AIS 2/3 期 Remedy2 試驗
我們目前正在進行用於治療 AIS 的 DM199 的 Remedy2 臨牀試驗。我們的Remedy2臨牀試驗是一項2/3期自適應設計、隨機、雙盲、安慰劑對照試驗,旨在在全球多達100個地點招收約350名患者。參加該試驗的患者將在 AIS 症狀出現後 24 小時內接受 DM199 或安慰劑治療。該試驗不包括接受組織纖溶原激活劑(tPA)(一種旨在溶解血栓的溶栓劑)治療的患者以及大血管閉塞的患者。研究人羣代表了當今約80%的AIS患者沒有治療選擇,這主要是由於tPA和/或機械血栓切除術治療的侷限性。Remedy2試驗的主要終點是中風後的身體恢復,根據公認的修改後的蘭金量表(MRs)在第90天進行測量,特別是恢復到0-1(mRS範圍為0-6)的mRs分數。我們認為,我們的 remedy2 試驗有可能成為該患者羣體中 DM199 的關鍵註冊研究。
在2022年7月宣佈並於2023年6月解除的Remedy2試驗的臨牀暫停之前,我們的Remedy2試驗的位點激活和註冊速度一直低於預期,現在仍在繼續。我們認為,這些情況可能是由於醫院和醫療機構人員短缺;對先前臨牀上嚴重的低血壓事件和先前臨牀暫停情況的擔憂;管理協議合規性的問題,包括管理出院到另一家醫院或中級護理機構的參與者的後勤和協議合規性;我們在研究方案中修訂的納入/排除標準;以及由於其他未決中風而導致的研究人員和試驗受試者的競爭神經學試驗。為了減輕這些因素的影響,我們決定在全球範圍內擴大試驗,我們正在準備監管文件,並確定和吸引加拿大、澳大利亞、英國和歐洲的研究地點。我們正在與我們的合同研究組織密切合作,制定程序,以根據需要為美國和全球研究地點和潛在參與者提供支持。我們打算繼續監測這些努力的結果,並在必要時採取更多措施來減輕這些因素對我們Remedy2試驗的影響;但是,無法保證這些問題是否以及何時會得到解決。未能解決這些問題將導致我們的Remedy2試用延遲。
心臟腎臟項目
我們目前預計將在2024年下半年披露我們的心臟腎臟項目計劃。
財務概覽
我們沒有從產品銷售中獲得任何收入。自成立以來,我們的運營資金來自股票的公開和私募銷售、認股權證和股票期權的行使、可用於投資的資金的利息收入和政府補助。自成立以來,我們每年都蒙受損失。截至2024年3月31日和2023年3月31日的三個月,我們的淨虧損分別為520萬美元和530萬美元。截至2024年3月31日,我們的累計赤字為1.207億美元。我們幾乎所有的營業虧損都源於與我們的候選產品開發計劃、我們的研發(R&D)活動以及與我們的運營和上市公司地位相關的一般和行政(G&A)支持成本所產生的費用。
我們預計,至少在未來幾年內,將繼續產生鉅額支出和增加營業虧損。我們預計,隨着我們在全球範圍內擴展Remedy2試驗以及註冊人數的增加,我們的季度支出將比最近一段時間有所增加。我們努力擴大團隊,為我們的運營提供支持,維護、擴大和保護我們的知識產權組合,也可能促進這種增長。
儘管我們預計,隨着我們恢復Remedy2試驗,包括我們的全球擴張,我們未來的每月負現金流率將普遍上升,但我們預計我們目前的現金資源將足以使我們能夠繼續進行Remedy2試驗,並以其他方式為自本報告中包含的簡明合併財務報表發佈之日起至少未來12個月的計劃運營提供資金。但是,我們未來資金需求的金額和時間將取決於許多因素,包括我們持續開發的時間和結果,以及我們的Remedy2試驗的全球擴張,特別是研究中心激活率和註冊率。研究中心激活率和參與者註冊率在一定程度上取決於研究中心人員短缺以及其他中風和神經學試驗導致的研究人員競爭。其他因素,例如我們當前和新的發展計劃的潛在擴展,以及與此類活動相關的運營費用,也可能導致我們未來資金需求金額和時間的波動。我們可能會比我們目前的預期更早地要求或以其他方式尋求大量額外資金。如果籌集額外資金的市場條件有利,我們可能會選擇在需要之前籌集額外資金。
我們的經營業績的組成部分
研究和開發費用
研發成本包括在進行人體臨牀試驗時產生的費用,例如支付給外部服務提供商(包括合同研究組織)的費用;臨牀支持服務;包括臨牀研究場所成本在內的臨牀開發;外部護理服務;以及實驗室測試。研發成本還包括非臨牀研究;向合同製造和開發組織以及外部實驗室支付的用於開發 DM199 及相關製造工藝的費用;生產足夠數量的 DM199 化合物用於臨牀研究的成本;與執行 DM199 候選產品開發計劃相關的具有專業知識的諮詢資源;以及人事成本,包括工資、福利和基於股份的薪酬。
目前,由於臨牀開發過程和產品開發計劃的臨牀階段固有的風險,我們無法確定地估計通過上市批准或任何臨牀前開發計劃開發 DM199 所產生的成本。開展必要的臨牀研究以獲得監管部門批准和擴大生產規模,以支持擴大開發和未來潛在的商業化,這一過程既昂貴又耗時。我們的任何失敗或延遲完成臨牀研究、擴大生產規模或獲得監管部門批准都可能導致研發費用增加,進而對我們的經營業績產生重大不利影響。
我們預計,如果我們成功地將 DM199 或我們的任何臨牀前項目推向所需的臨牀開發階段,那麼與最近的時期相比,未來的研發費用將增加。開展臨牀試驗是獲得監管部門批准和擴大生產規模以支持擴大開發和未來潛在商業化所必需的過程既昂貴又耗時。
一般和管理費用
G&A 費用主要包括工資、員工福利、基於股份的薪酬以及與我們的高管、財務、業務發展和支持職能相關的其他人事成本。G&A費用還包括保險,包括董事和高級管理人員的責任保險、租金和水電費、差旅費、專利費用和專業費用,包括審計、税務和法律服務。
其他收入,淨額
其他淨收入主要包括有價證券的利息收入。
運營結果
截至2024年3月31日和2023年3月31日的三個月的比較
下表彙總了我們截至2024年3月31日和2023年3月31日的三個月未經審計的經營業績(以千計):
|
截至3月31日的三個月 |
||||||||
|
2024 |
2023 |
|||||||
|
研究和開發費用 |
$ | 3,676 | $ | 3,618 | ||||
|
一般和管理費用 |
2,065 | 1,903 | ||||||
|
其他收入,淨額 |
(597 | ) | (256 | ) | ||||
研究和開發費用
截至2024年3月31日的三個月,研發費用增至370萬美元,而截至2023年3月31日的三個月,研發費用為360萬美元。這一增長受到了許多抵消因素的影響。與2023年完成的臨牀試驗工作、我們的1C期和REDUX試驗,以及為解決我們的Remedy2試驗臨牀暫停問題而於2023年完成的在用研究工作相關的成本削減,部分抵消了與繼續進行Remedy2臨牀試驗相關的成本增加。隨着我們在全球範圍內擴大Remedy2試驗、試點激活和參與者註冊的繼續,我們預計,我們的研發費用將與近期相比略有增加。我們預計,這些預期的增長將受到2023年完成的臨牀試驗工作和在用研究的緩和。
一般和管理費用
截至2024年3月31日的三個月,併購支出從截至2023年3月31日的三個月的190萬美元增加了20萬美元至210萬美元。這一增長主要是由與擴大我們的團隊相關的人員成本增加所推動的,但部分被董事和高級管理人員責任保險費成本的減少所抵消。我們預計,與前一時期相比,併購支出將保持穩定。
其他收入,淨額
截至2024年3月31日的三個月,其他收入淨額為59.7萬美元,而截至2023年3月31日的三個月淨收入為25.6萬美元。這一增長是由截至2024年3月31日的三個月中確認的利息收入增加所致,這與本年度有價證券餘額與去年同期相比增加有關。
流動性和資本資源
下表彙總了我們截至2024年3月31日和2023年12月31日的流動性和資本資源,以及截至2024年3月31日和2023年3月31日的三個月期間每個月的現金流量,旨在補充以下更詳細的討論(以千計):
|
2024年3月31日 |
2023年12月31日 |
|||||||
|
現金、現金等價物和有價證券 |
$ | 46,516 | $ | 52,895 | ||||
|
總資產 |
49,260 | 54,160 | ||||||
|
流動負債總額 |
2,617 | 2,786 | ||||||
|
股東權益總額 |
46,349 | 51,057 | ||||||
|
營運資金 |
44,867 | 50,889 | ||||||
|
截至3月31日的三個月 |
||||||||
|
|
2024 |
2023 |
||||||
| 現金流數據 | ||||||||
|
現金流由(用於): |
||||||||
|
經營活動 |
$ | (6,653 | ) | $ | (5,089 | ) | ||
|
投資活動 |
4,208 | 2,509 | ||||||
|
籌資活動 |
(1 | ) | (1 | ) | ||||
|
現金淨減少 |
$ | (2,446 | ) | $ | (2,581 | ) | ||
營運資金
截至2024年3月31日,我們的現金、現金等價物和有價證券總額為4,650萬美元,流動負債為260萬美元,營運資金為4,490萬美元,而截至2023年12月31日,現金、現金等價物和有價證券總額為5,290萬美元,流動負債為280萬美元,營運資金為5,090萬美元。我們的合併現金、現金等價物和有價證券以及營運資金的減少主要是由於用於為當前業務提供資金的淨現金。
現金流
運營活動
截至2024年3月31日的三個月,用於經營活動的淨現金為670萬美元,而截至2023年3月31日的三個月為510萬美元。經營活動中使用的現金的增加主要是由本年度向支持我們Remedy2臨牀試驗的供應商預付存款所致。
投資活動
投資活動主要包括有價證券的購買和到期。截至2024年3月31日和2023年3月31日的三個月,投資活動提供的淨現金分別為420萬美元和250萬美元。這種變化主要源於到期時間和有價證券的投資。
融資活動
在截至2024年3月31日和2023年3月31日的三個月中,用於融資活動的淨現金分別為1,000美元,其中包括每個期間的融資租賃債務本金支付。
資本要求
自成立以來,我們在推進 DM199 候選產品的研發時蒙受了損失。我們尚未從產品銷售中獲得任何收入,預計至少在三到四年內不會產生任何收入。我們不知道何時或是否會通過產品銷售或超出我們的 DM199 候選產品或任何未來候選產品的許可來獲得任何收入。除非獲得必要的監管部門批准,否則我們預計不會從產品銷售中產生任何收入。我們預計將繼續蒙受鉅額營業虧損,直到未來的任何產品銷售、許可費、里程碑付款和/或特許權使用費足以創造收入為我們的持續經營提供資金。我們預計,隨着我們繼續研究、開發和臨牀研究我們的 DM199 候選產品並尋求監管部門的批准,特別包括我們的 Remedy2 試驗的持續和全球擴張,我們的營業虧損將與前一時期相比增加。從長遠來看,我們的 DM199 候選產品或任何未來候選產品必須獲得監管部門的批准,並且在沒有戰略合作伙伴協助的情況下,我們預計產品銷售、營銷、製造和分銷將產生大量的商業化費用。
因此,我們預計,我們將需要大量的額外資金來推進我們的研發活動、當前和預期的未來臨牀研究、監管活動,以及以其他方式開發我們的候選產品 DM199 或任何未來的候選產品,以至於候選產品可能會被授權或商業銷售。儘管我們正在努力實現這些計劃,但無法保證這些和其他戰略能夠實現,也無法保證以優惠條件獲得額外資金,或者根本無法保證。我們預計,我們未來每月的負現金流率將根據我們的臨牀活動和支出發生的時間而有所不同,隨着我們繼續在全球範圍內擴大我們的Remedy2試驗,並且將與最近的時期相比有所增加。我們預計,自本報告所包含的簡明合併財務報表發佈之日起,我們目前的現金資源將足以繼續我們的Remedy2試驗,並在未來至少十二個月內為我們的計劃運營提供資金。但是,我們未來資金需求的金額和時間將取決於許多因素,包括我們正在進行的開發工作的時機和結果,特別是我們的Remedy2試驗、該試驗的場地激活和註冊率、研究中心人員短缺的影響、Remedy2試驗中其他中風和神經學試驗導致的研究人員和試驗受試者的競爭,以及我們當前和潛在的新開發計劃和運營的潛在擴展與此類活動相關的費用。我們可能比目前的預期更早地需要大量額外資金,並且無法保證在此之前我們不會需要或尋求額外的資金,尤其是在籌集額外資本的市場條件有利的情況下。
從歷史上看,我們的運營資金主要來自股票證券的銷售以及認股權證和股票期權的行使,我們預計在可預見的將來將繼續這種做法。我們沒有任何可以借款的現有信貸額度。我們可能會尋求通過各種來源(例如股權或債務融資)或通過戰略合作和許可協議籌集更多資金。我們無法保證我們能夠獲得額外的資金來源來支持我們的行動,也無法保證如果有此類資金,此類額外資金將足以滿足我們的需求或以我們可接受的條件提供。如果我們的臨牀數據不正面或經濟和市場狀況惡化,則尤其如此。
如果我們通過出售股權或可轉換債務證券籌集額外資金,則股東的所有權權益將被稀釋。債務融資(如果有)可能涉及協議,包括轉換折扣、將我們的知識產權作為抵押品或限制我們採取具體行動(例如承擔額外債務或進行資本支出)的契約。如果我們通過政府或其他第三方資金、營銷和分銷安排或其他合作、戰略聯盟或與第三方的許可安排籌集額外資金,我們可能不得不放棄對我們的技術、未來收入來源、研究計劃或候選產品的寶貴權利,或者以可能對我們不利的條件授予許可。融資的可用性將受到我們的臨牀數據以及其他科學和臨牀研究結果的影響;獲得監管部門批准和其他監管行動的能力;市場對我們候選產品的接受度;資本市場的總體狀況,特別是製藥、生物技術和醫療公司;戰略聯盟協議的現狀;以及其他相關的商業考慮。
如果在需要時沒有足夠的資金,我們可能需要通過採取行動來縮減運營規模,其中可能包括實施降低成本的策略,例如減少對外部專業服務提供商的使用,減少員工人數或員工薪酬,修改或推遲我們的 DM199 候選產品的開發;向第三方許可我們的 DM199 候選產品 AIS、CRD 或其他我們本來會尋求的跡象商業化的權利,或者以其他方式放棄對我們的技術、未來收入來源、研究計劃或候選產品的重要權利,或者以可能對我們不利的條件授予許可;和/或通過合併、出售或清算我們公司來剝離資產或停止運營。
關鍵會計政策與估計
根據中提供的信息,我們的關鍵會計政策和估算沒有重大變化。”第二部分。項目 7,管理’s 對財務狀況和經營業績的討論與分析—關鍵會計政策,” 包含在我們截至2023年12月31日的財政年度的10-K表年度報告中。
|
第 3 項。 |
關於市場風險的定量和定性披露 |
作為一家規模較小的申報公司,我們無需根據本項目提供披露。
|
第 4 項。 |
控制和程序 |
評估披露控制和程序
我們維持披露控制和程序(定義見經修訂的 1934 年《美國證券交易法》(《交易法》)第 13a-15 (e) 條和第 15d-15 (e) 條),旨在提供合理的保證,即我們在根據《交易法》提交或提交的報告中要求披露的信息,是在美國證券交易委員會規則和表格規定的期限內記錄、處理、彙總和報告的,並且此類信息是積累並傳達給我們的管理層,包括我們的首席執行官和首席財務幹事或履行類似職能的人員,以便就要求的披露及時做出決定。截至本報告所涉期末,我們的管理層在首席執行官兼首席財務官的參與下,評估了披露控制和程序的設計和運作有效性。根據該評估,我們的首席執行官兼首席財務官得出結論,我們的披露控制和程序自該期限結束時起生效,可以合理地保證我們在根據《交易法》提交或提交的報告中要求披露的信息是在美國證券交易委員會規則和表格規定的期限內記錄、處理、彙總和報告的,並將此類信息收集並傳達給我們的管理層,包括我們的首席執行官和首席財務官,並酌情就要求的披露作出及時的決定.
財務報告內部控制的變化
在截至2024年3月31日的三個月中,我們對財務報告的內部控制沒有發生任何變化,沒有對我們的財務報告內部控制產生重大影響或合理可能產生重大影響。
|
第二部分- |
其他信息 |
|
第 1 項。 |
法律訴訟 |
與 ICON plc 於 2021 年 7 月 1 日收購的製藥研究協會集團 B.V. 的訴訟(ICON/PRA 荷蘭)
2022 年 11 月 23 日,我們提交了一份請願書,請求允許在判決前附上自 ICON plc(ICON/PRA 荷蘭)持有的所有相關文件,該文件於 2022 年 11 月 28 日獲得荷蘭北部地方法院的批准。地方法院的一名代表在2022年12月7日和8日左右向荷蘭ICON/PRA送達了判決前附件。該案於2022年12月28日正式提交荷蘭商事法院(NCC),NCC定於2023年3月16日舉行聽證會,以確定我們是否有權擁有扣押的記錄。
2023年4月21日,NCC發佈了一項判決,確認了我們對實物文件的所有權,包括51個硬拷貝文件夾和某些數字文件,這些文件與荷蘭ICON/PRA進行並於2022年12月被荷蘭法院沒收的臨牀研究有關。NCC進一步命令荷蘭ICON/PRA允許和容忍交出文件,包括數字和源數據。此外,NCC發現我們沒有違反臨牀研究協議規定的任何義務,ICON/PRA Netherlands沒有理由暫停履行臨牀研究協議規定的義務,即向我們提供所有臨牀數據和對該研究進行審計的權限。2023年6月15日,荷蘭ICON/PRA對該決定提起上訴,並要求全國協調委員會舉行聽證會,聽證會定於2024年9月23日舉行。
針對我們的損害賠償索賠的聽證會於2023年12月7日舉行。2024年2月7日,NCC發佈了一項判決,他們認定,儘管與該研究有關的所有數據均為Diamedica的合法財產,但他們發現荷蘭ICON/PRA扣留的研究數據與我們要求的損害賠償之間沒有足夠的因果關係。我們已通知NCC和荷蘭ICON/PRA,我們打算對該決定提出上訴。
我們可能會不時受到其他各種正在進行或威脅的法律訴訟和訴訟的約束,包括在正常業務過程中發生的訴訟和訴訟,其中可能包括僱傭問題和違約糾紛。此類問題存在許多不確定性,其結果是不可預測的,而且可能在很長一段時間內都不為人所知。除了上面提到的ICON/PRA荷蘭問題外,我們目前沒有參與或意識到任何威脅的法律行動。
|
第 1A 項。 |
風險因素 |
作為一家規模較小的申報公司,我們無需根據本項目提供披露。
|
第 2 項。 |
未註冊的股權證券銷售和所得款項的使用 |
在截至2024年3月31日的季度中,我們沒有出售任何未註冊的公司股權證券。
|
第 3 項。 |
優先證券違約 |
不適用。
|
第 4 項。 |
礦山安全披露 |
不適用。
|
第 5 項。 |
其他信息 |
規則 10b5-1 計劃和非規則 10b5-1 交易安排的採用、終止和修改
在截至2024年3月31日的三個月中,我們的董事或 “高級職員”(定義見《交易法》第16a-1(f)條)均未採用或終止美國證券交易委員會第S-K條例第408(a)和408(c)項分別定義的 “第10b5-1條交易安排” 或 “非規則10b5-1交易安排”。
|
第 6 項。 |
展品 |
本10-Q表季度報告將提交或提供以下證物:
|
展覽 沒有。 |
描述 |
申報方式 |
||
|
3.1 |
Diamedica Therapeutics Inc. 2019 年 5 月 31 日文章通知 |
參照 DiameDica 於 2019 年 6 月 4 日向美國證券交易委員會提交的 8-K 表最新報告附錄 3.1 納入(文件編號 001-36291) |
||
|
3.2 |
經修訂和重述的 Diamedica Therapeutics Inc. 條款 2023 年 5 月 17 日生效 |
參照 DiameDica 於 2023 年 5 月 18 日向美國證券交易委員會提交的 8-K 表最新報告的附錄 3.1 編入(文件編號 001-36291) |
||
|
31.1 |
根據根據2002年《薩班斯-奧克斯利法案》第302條通過的《交易法》第13a-14 (a) /15d-14 (a) 條對首席執行官進行認證 |
隨函提交 |
||
|
31.2 |
根據根據2002年《薩班斯-奧克斯利法案》第302條通過的《交易法》第13a-14 (a) /15d-14 (a) 條對首席財務官進行認證 |
隨函提交 |
||
|
32.1 |
根據根據2002年《薩班斯-奧克斯利法案》第906條通過的《美國法典》第18條第1350條對首席執行官進行認證 |
隨函提供 |
||
|
32.2 |
根據根據2002年《薩班斯-奧克斯利法案》第906條通過的《美國法典》第18條第1350條對首席財務官進行認證 |
隨函提供 |
||
|
101 |
Diamedica Therapeutics Inc.截至2024年3月31日的三個月10-Q表季度報告中的財務報表,格式為Inline XBRL:(i)簡明合併資產負債表,(ii)簡明合併運營和綜合虧損表,(iii)簡明合併股東權益表,(iv)簡明合併現金流量表,以及(v)簡明合併財務報表附註。 |
隨函提交 |
||
|
104 |
封面交互式數據文件 |
嵌入在內聯 XBRL 文檔中 |
簽名
根據1934年《證券交易法》的要求,註冊人已正式促使經正式授權的下列簽署人代表其簽署本報告。
|
DIAMEDICA THERAPEUTICS |
|
|
日期:2024 年 5 月 8 日 |
/s/ Rick Pauls |
|
裏克·保爾斯 |
|
| 總裁兼首席執行官 | |
|
(首席執行官) |
|
|
日期:2024 年 5 月 8 日 |
/s/ 斯科特·凱倫 |
|
斯科特·凱倫 |
|
| 首席財務官 | |
|
(首席財務官兼首席會計官) |