目錄表
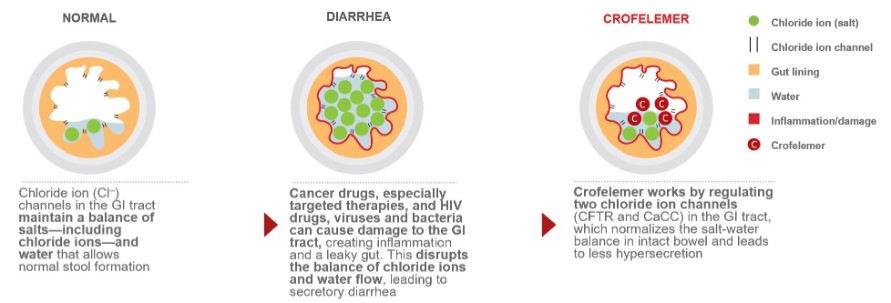
下圖説明瞭克羅非萊姆的作用機制,它可以使腸道的氯離子分泌和液體含量正常化,以改善大便的稠度。
業務戰略
我們的目標是成為一家領先的製藥公司,擁有一流的可持續衍生產品,滿足全球重大的未得到滿足的胃腸道醫療需求。為達致這個目標,我們計劃:
通過利用我們重要的胃腸產品知識、經驗和知識產權組合來擴展Mytesi
Mytesi(克羅非勒姆125 mg緩釋片)是一種新型的、一流的抗分泌性止瀉藥,它對腸道內的電解質和液體平衡具有正常化作用,這種作用機制可能有利於多種胃腸道疾病。我們的Mytesi(CroFelemer)產品獲得FDA批准,用於抗逆轉錄病毒治療的成人艾滋病毒/艾滋病患者的非感染性腹瀉的症狀緩解。捷豹通過Napo和Napo Treateutics擁有Mytesi的全球未受約束的權利。Mytesi正在開發多種可能的後續適應症,包括與使用或不使用標準化療的靶向治療相關的腹瀉預防。CroFelemer緩釋片也在評估IBS-D和特發性/功能性腹瀉。
正在開發用於口服液的克羅非勒粉,以支持患有SBS和/或CDD(如MVID)的嬰兒和/或兒童的孤兒或罕見疾病適應症。
此外,一種NP-300正在開發中,用於緩解症狀和治療中到重度腹瀉,包括細菌、病毒和寄生蟲感染引起的細菌、病毒和寄生蟲感染霍亂弧菌,引起霍亂的細菌。
我們的管理團隊集體在處方藥開發方面擁有豐富的經驗。這種經驗涵蓋了產品開發的方方面面,包括髮現、臨牀前和臨牀開發、GMP製造、監管事務和商業化。這個團隊的主要成員成功地開發了Mytesi。
在Mytesi銷售和營銷工作中保持商業能力
NAPO的直銷組織由Mytesi現場銷售代表組成,這些銷售代表戰略性地部署在不同的地區,以覆蓋最具潛力的美國地理區域。在隨之而來的營銷、促銷活動、患者賦權計劃(包括整合的社交數字活動)和下文所述的醫學教育倡議的支持下,我們預計接受Mytesi治療的患者數量將出現比例反應。
12
