
附錄 99.2

納斯達克:VANI www.vivani.com 2024 年 3 月

免責聲明以下幻燈片和任何隨附的口頭陳述包含經修訂的1933年《證券法》第27A條和經修訂的1934年《證券交易法》第21E條所指的前瞻性陳述,這些陳述旨在由這些條款創建的 “安全港” 所涵蓋。本新聞稿中所有不基於歷史事實的陳述都是 “前瞻性陳述”。這些陳述可以用 “估計”、“預期”、“項目”、“計劃” 或 “計劃”、“戰略”、“目標”、“尋求”、“可能”、“將”、“預期”、“打算”、“相信”、“應該” 等詞語來識別,也可以通過其背景來識別。所有涉及Vivani Medical, Inc.(“Vivani”、“公司”、“我們” 或 “我們”)預期或預期的未來將發生的經營業績或事件或發展的廣告聲明,例如既定目標或目標、我們的產品及其治療潛力和計劃開發、我們打算瞄準的適應症、我們的技術、我們的業務和戰略、里程碑、潛在市場或其他非歷史市場事實,是前瞻性陳述。儘管管理層在本演示文稿中包含的任何前瞻性陳述都是以其當前的預期為基礎的,但此類預期所依據的信息可能會發生變化。前瞻性陳述涉及固有的風險和不確定性,由於各種因素,這些風險和不確定性可能導致實際結果與前瞻性陳述存在重大差異。這些風險和不確定性包括但不限於我們可能無法完成NPM-115所需的任何臨牀前活動。NPM-119 或以其他方式開始計劃對這些正在開發的產品進行臨牀試驗;開展我們其他產品的任何臨牀前活動;我們的產品可能無法在臨牀試驗中表現出安全性或有效性;我們可能無法確保產品的PPR 橢圓形上市;監管機構的批准可能出現延遲或監管框架的變化,這是我們無法控制的;我們對產品潛在市場的估計可能不準確;我們可能無法及時籌集所需的額外資金;更高效的競爭對手或更多可能會出現有效的競爭關係;我們可能會捲入與知識產權的使用有關的爭議,這對我們的成功至關重要;我們可能無法吸引和留住關鍵員工和合格人員;早期的研究結果可能無法預測後期的研究結果;我們的產品製造、研究以及臨牀前和臨牀測試的部分或所有方面都依賴第三同酬。我們在2023年3月31日提交的10-K表年度報告以及我們隨後向美國證券交易委員會提交的文件中描述了其他風險和不確定性。我們敦促您在評估我們的前瞻性陳述時考慮這些風險和不確定性。我們提醒讀者不要過分依賴任何此類前瞻性陳述,這些陳述僅代表截至發表之日。除非聯邦證券法另有要求,否則我們不承擔任何義務或承諾公開發布此處(或其他地方)中包含的任何獎勵聲明的任何更新或修訂,以反映我們對該聲明預期的任何變化,或任何此類聲明所依據的事件、條件或情況的任何變化。本演示文稿中包含的某些信息涉及或基於從第三方來源獲得的研究、出版物、調查和其他數據以及公司自己的內部估計和研究。儘管我們認為截至本演示文稿之日這些第三方來源是可靠的,但我們尚未獨立核實,也沒有對從第三方來源獲得的任何信息的充分性、公平性、準確性或完整性做出任何陳述。最後,儘管我們認為自己的內部研究是可靠的,但此類研究尚未得到任何獨立來源的證實。我們所有的療法仍在研究中,尚未獲得任何監管機構的批准以供使用。2

Vivani 執行領導團隊 • Vivani 技術的聯合創始人/聯合發明者 • 生物工程博士(加州大學舊金山分校/加州大學伯克利分校)• 哈斯商學院技術管理證書 • 研究側重於糖尿病治療 • 曾在波士頓科學和最小化亞當·門德爾鬆博士 — 首席執行官/總監 • 設備和藥物設備公司擔任過多個首席運營官和高管職位,包括:• Dance Biopharm首席技術官、Avipharm首席運營官 d Bio • Prima Biomed執行副總裁、Nektar Therapeutics高級副總裁(負責Exubera的批准)和強生公司全球副總裁Truc Le,工商管理碩士 — 首席運營官 • 艾格生物製藥和丹斯生物製藥前首席醫學官 • AGA Medical 前高級副總裁兼首席財務官 • 葛蘭素史克前董事、文迪雅臨牀戰略全球主管 • ViaCyte, Inc.前董事會成員麗莎·波特,醫學博士 • 前高級副總裁兼首席財務官 Miramar Labs • 前高級副總裁兼首席財務官 AGA Medical • 前首席財務官 Nektar Therapeutics、OraVax 和 Haemonetics • 現任董事會董事:Quantum-Si 和 Elutia, Inc. • 參與/指導了 2 次首次公開募股、2 次反向合併和 1 次 SPAC BrigidA. Makes,工商管理碩士 — 首席財務官 • 阿斯利康前執行董事,在監管事務、藥物開發、商業和業務發展方面擔任領導職務 • 亞利桑那州前維瓦尼董事會觀察員 • 亞利桑那州前PhaseBio董事會觀察員(首次公開募股前)• Cephalon和Rhone Poulenc Rorer 前董事唐納德·德威爾,工商管理碩士 — 首席商務官 3

Vivani Medical, Inc. 4個主要項目NPM-115和NPM-119是正在開發的為期六個月的微型GLP-1(艾塞那肽)植入物,分別用於治療肥胖或超重患者的慢性體重管理以及2型糖尿病。用於慢性體重管理的NPM-139(西瑪魯肽植入物)也在開發中,還有一個額外的潛在好處,那就是每年給藥一次。一家創新的生物製藥公司,正在開發微型、長期的藥物植入物產品組合,用於治療慢性病。我們的NanoPortal™ 平臺技術支持設計植入物,旨在改善藥物不依從性和耐受性。Vivani完全有能力在2024年推動NPM(115)和NPM-119,朝着潛在的轉型里程碑邁進。

Feline Pre-糖尿病和糖尿病>5億美元的人類肥胖>500億美元5家公司管道如果獲得批准,Vivani產品將在臨牀前具有巨大潛在適應症可行性的市場中競爭*人類肥胖 NPM-119 艾塞那肽 >200 億美元 >500 億美元 NPM-139 Vivani * 如果獲得批准,Vivani 產品將競爭的估計市場規模。不代表維瓦尼管道產品的未來銷售額或收入估計,摩根大通分析師理查德·沃瑟估計,到2032年(2023年9月11日),GLP-1市場將達到710億美元。我們假設 2 型糖尿病超過 200 億美元,肥胖或超重患者的慢性體重管理超過 500 億美元 ** 與奧卡瓦製藥公司合作 OKV-119** 艾塞那肽 NPM-115 h 高劑量艾塞那肽索馬魯肽

藥物植入物專有平臺技術
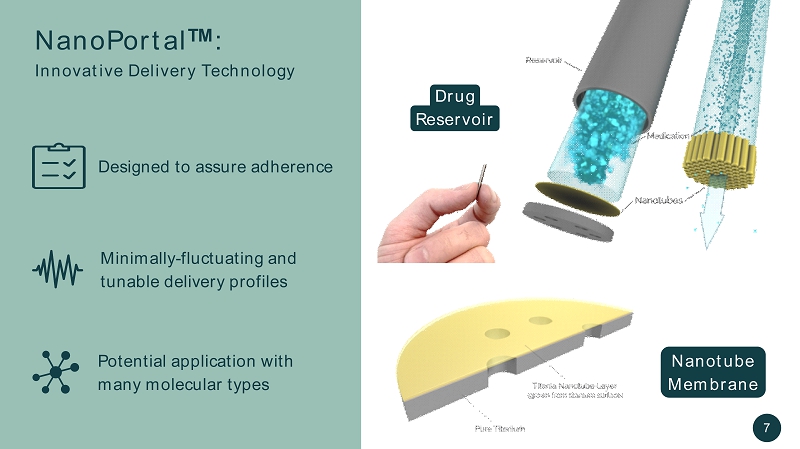
多種分子類型的潛在應用旨在確保附着力最低限度-波動和可調的遞送曲線 NanoPortal TM:創新遞送技術藥物儲存器納米管膜 7

通過根據分子大小精確調整納米管,隨着時間的推移,藥物和納米管壁之間的相互作用可以產生理想的釋放特徵,包括近乎恆定釋放的NanoPortal TM:其工作原理...孔隙太小:無法釋放孔隙目標尺寸:接近恆定釋放 8 孔隙太大:爆裂釋放
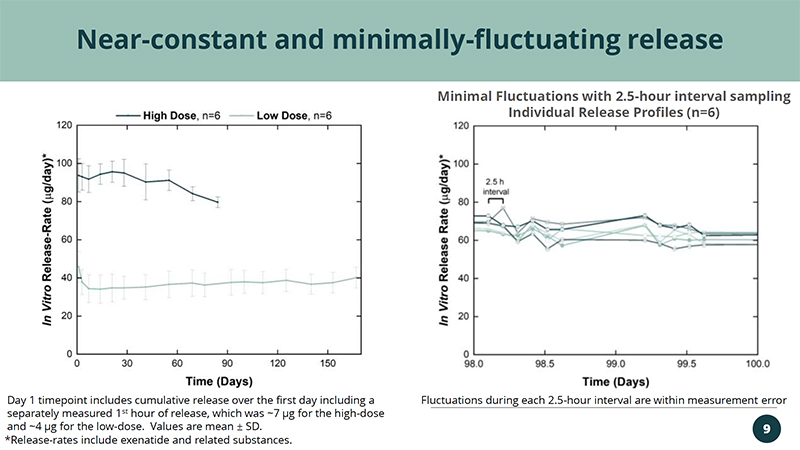
接近-恆定且波動最小-的第一天時間點包括第一天的累積釋放,包括單獨測量的第一個釋放小時,高劑量約為7 µg,低劑量約為4 µg。值是平均值 ± SD。每 2.5 小時間隔內的波動均在測量誤差範圍內 9 最小波動,採樣間隔為 2.5 小時的個體釋放曲線 (n=6) *釋放速率包括艾塞那肽和相關物質。

最小化植體尺寸可延長植入持續時間可調輸送速率可調輸送概況 nanoPortal TM 是一種平臺技術 NanoPortal TM 是一項平臺技術,應用潛力廣泛,可支持新藥植入物組合 10

瞄準快速增長的 GLP-1 RA 市場 Vivani 牽頭項目 NPM-115 用於慢性體重管理的高劑量艾塞那肽植入物

• 肥胖症的巨大未得到滿足的醫療需求 1:• 7.64億肥胖患者 • 1500萬(2%)正在服用抗肥胖藥物 • GLP-1 單一療法可以為大多數患者提供足夠的體重減輕量 2 • NPM-115 的初步臨牀前數據顯示,艾塞那肽和索馬魯肽的減肥幅度相似 • NPM-115 的靶標特徵可能提供一種有吸引力的生命替代方案——長期注射或長期服藥-長期維持 GLP-1 種體重管理療法 6-月艾塞那肽(胰高血糖素)-如肽 1 受體Agonist) 用於肥胖或超重患者慢性體重管理的植入物主要產品 NPM-115:12 1, 2 Novo Nordisk 2023 年年度報告

100% 75% 50% 25% 0% • 持續性再提高 60% 的剩餘機會很大,將轉化為患者預後改善 • NPM-115(艾塞那肽植入)旨在保證 6 個月的依從性/植入最近的回顧性隊列研究(n=1,911)報告稱,與依從性挑戰相關的減肥藥物一年後,使用西瑪魯肽的藥物持續性提高了 40% 大型回顧性隊列研究* (N=1,911) 1,911) 13 * 2023 年 12 月 8 日發表在《肥胖》上 ** NPM-115(艾塞那肽植入物)不包括在內在已發表的研究中,假設一個植入物在六個月後被更換。目前正在開發中,旨在實現 100% 的合規性,未在任何市場上獲得批准。剩餘治療百分比
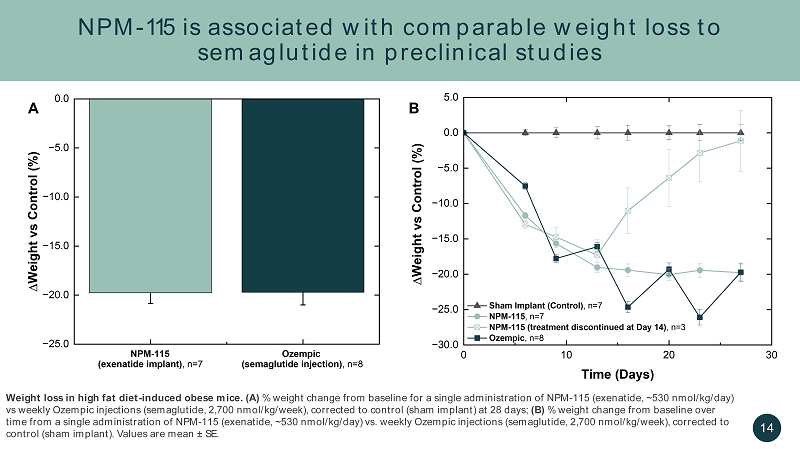
在臨牀前研究 14 高脂飲食誘發的肥胖小鼠中,NPM-115 的體重減輕與索馬魯肽相當。(A) 單次給藥 NPM 的體重變化百分比——115(艾塞那肽,約 530 nmol/kg/天)與每週Ozempic 注射(索瑪魯肽,2,700 nmol/kg/周)的體重變化百分比,修正為28天對照(假植入);(B)單次給藥 NPM-115(艾塞那肽,約 530 nmol/kg/天)與基線相比的體重變化百分比 kg/天)與每週Ozempic注射(索瑪魯肽,2,700 nmo l/kg/周),校正為對照組(假植入)。值是平均值 ± SE。A B
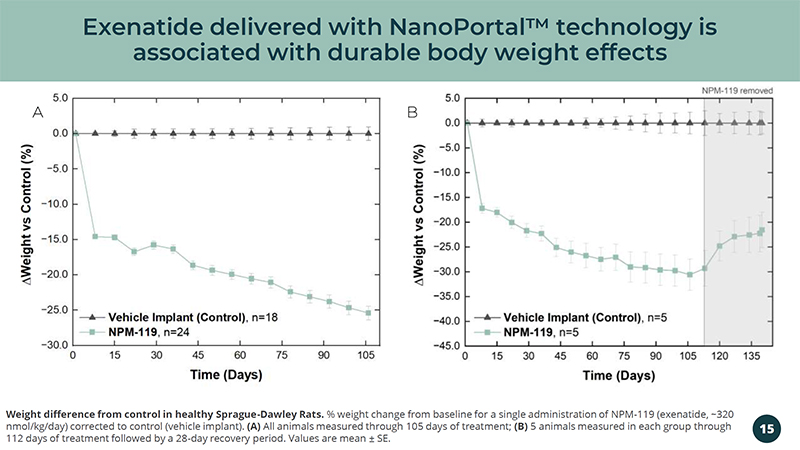
採用NanoPortal™ 技術的艾塞那肽具有持久的體重效果,與健康的Sprague-Dawley大鼠體重相差15%。單次給藥NPM的體重變化百分比——119(艾塞那肽,約320 nmol/kg/天)修正為對照組(車輛植入)。(A)通過105天的治療對所有動物進行了測量;(B)在112天的治療之後,每組對5只動物進行了測量,隨後進行了28天的恢復期。值是平均值 ± SE。A B

NPM-115 臨牀+監管發展近期計劃2023年11月——Vivani宣佈指定NPM-115(高劑量艾塞那肽植入物),並啟動慢性體重管理開發計劃。2024年2月—公司報告了積極的臨牀前研究結果,表明NPM-115植入物和Ozempic/Wegovy(索瑪魯肽注射劑)的體重減輕程度相當。2024年—計劃提交研究性新藥申請,以支持啟動用於治療肥胖或超重患者的慢性體重管理的NPM-115的首次人體試驗。16年裏程碑狀態2023年宣佈指定NPM-115(高劑量)艾塞那肽) 2023 年 11 月報告稱,2024 年 2 月的臨牀前研究顯示體重減輕呈陽性2024 年向美國食品和藥物管理局提交 IND 申請進行首次人體研究(預計於 2024 年)

瞄準快速增長的 GLP-1 RA 市場 Vivani 牽頭項目 NPM-119 艾塞那肽植入治療 2 型糖尿病

1 2023 年諾和諾德年度報告 2 Guo 2016 2,3 Carls 等人,2017 年 4 IMS 2013 報告 • 糖尿病領域大量未得到滿足的需求 1:• 5.37 億糖尿病患者 • 約 15% 的控制良好 • 非依從性是現實世界療效低的主要原因 2,3 • 保證依從性將顯著節省醫療成本 4 • 美國食品藥品管理局表示 505 (b) (2) 簡化的批准途徑可能會在 6 個月內推出用於 2 型糖尿病的胰高血糖素(胰高血糖素類肽 1 受體激動劑)主要產品(NPM-119):18

NPM-119 植入物和塗抹器 19

Ozempic Januvia Invokana NPM-119* 100% 75% 50% 0% GLP-1 種激動劑,每週注射 Mody 等人,2022 DPP-4 種抑制劑,每日藥丸 Polonsky 等人,2016 年 SGLT-每隔 6 個月植入 1 次 GLP-每 6 個月植入 1 次 • 大約 50% 的患者不符合血糖靶點主要歸因於不粘附性 NPM-119* 旨在通過植入持續時間實現 100% 的依從性,採用提高依從性的技術雙重激勵 • 藥品收入增加 • 醫療保健成本降低當前藥物依從性挑戰 “藥物對不服用藥物的人不起作用” 真實依從性* NPM-119 — 正在開發中,旨在實現 100% 的依從性,未在任何市場上獲得批准特定藥物的真實依從性 20

Intarcia的1 ITCA 650(6個月艾塞那肽植入)可能是NPM的相關價值模擬——2014年119日——Intarcia與Servier(不包括美國和日本)簽署了ITCA 650協議——預付1.71億美元、里程碑式增長和兩位數的特許權使用費——融資估值Intarcia高達40億美元(2017年);Intarcia的主要項目是ITCA 650 2016年—Intarcia於2017年首次提交了ITCA 650新藥申請(NDA)——食品和藥物管理局發佈了2019年第一份ITCA 650 CRL 2(引用製造業問題)——Intarcia重新提交了2020年ITCA 650 NDA — FDA發佈了第二份ITCA 650 CRL(引用臨牀安全性)和設備成分問題)2022年——爭議解決後,美國食品和藥物管理局的CDER提議拒絕Intarcia的2023年公開聽證會請求——美國食品藥品管理局顧問委員會一致建議不批准ITCA 650,原因是擔心與不規律和不受控制的艾塞那肽釋放相關的安全風險,長期GLP-1(艾塞那肽)植入物的價值此前經過外部驗證的1 i2o Therapeutics收購了Intarcia Therapeutics的資產,包括ITCA-650 2 CRL:完整的回覆信 — 由 FDA 簽發以查明保密協議的缺陷 21

(Intarcia)• 美國食品和藥物管理局稱,藥物釋放的每日變化可能是臨牀安全信號的原因 • 更大的設備(4 毫米 x 45 毫米)• 使用更大的 6 號針頭插入 • 臨牀前研究中觀察到的藥物釋放曲線波動微乎其微 • 較小的設備(2.2 毫米 x 21.5 毫米)• 使用較小的 11 號針頭插入 NanoPortal TM Osmom-119 正好可以避免 ITCA 650 設備技術挑戰泵 (NPM-119) 22
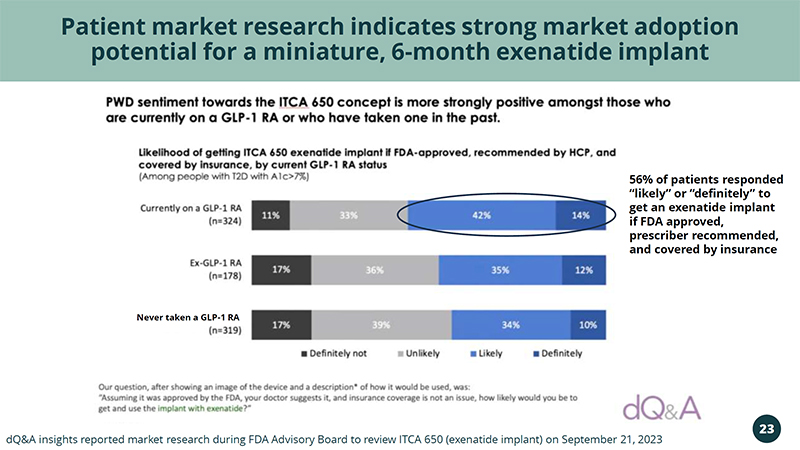
從未服用過 GLP-1 RA 患者市場研究表明,微型 6 個月艾塞那肽植入物的市場採用潛力巨大 dq&a Insights 報告了市場研究,在 FDA 顧問委員會於 2023 年 9 月 21 日審查 ITCA 650(艾塞那肽植入物)期間,23 56% 的患者回應 “可能” 或 “肯定” 接受艾塞那肽植入物,如果美國食品藥品管理局批准、處方者推薦且有保障

0 2 4 6 8 10 可能開處方(1=不太可能,10=極有可能)初級保健醫生(n=10)處方評級,平均每10名處方者和付款人研究為期6個月的微型艾塞那肽植入物提供了強有力的支持評級:總體而言,使用1到10的量表,其中1根本不太可能,10極有可能,你開NPM處方的可能性有多大-119?Vivani 贊助了定性市場研究,2020 年 3 月。約 90% 的患者接受初級保健治療總計:約 5,500 美元(每位患者每年)依從性 = 較低的急診和門診費用 Curtis 等人,2017 年 24
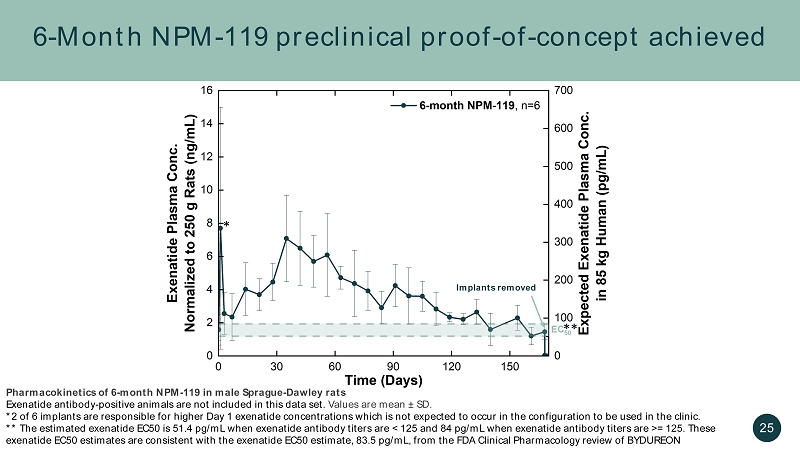
6 個月 NPM-119 臨牀前證實-已獲得概念移除植入物 * 25 雄性 Sprague-Dawley 大鼠艾塞那肽抗體-陽性動物 6 個月 NPM-119 的藥代動力學不包含在本數據集中。值為平均值 ± SD。6種植體中的*2是導致第一天艾塞那肽濃度升高的原因,在臨牀使用的配置中預計不會出現這種情況。**當艾塞那肽抗體滴度為125時,估計的艾塞那肽EC50為51.4 pg /mL。這些艾塞那肽EC50估計值與美國食品藥品管理局對BYDUREON臨牀藥理學審查中艾塞那肽EC50的估計值一致,即83.5 pg /mL **

NPM-119 臨牀和監管途徑

擬議的首次人體試驗:LIBERATE-1 主要目標:安全性/耐受性評估和全面的 PK 表徵血糖控制 (HbA1c) 和體重也將隨機評估 12 周關鍵納入/排除標準 • T2DM 和 HbA1c

NPM-119 臨牀+監管發展近期計劃2023年7月14日——Vivani提交了一種研究性新藥,以支持一項擬議的人體首創研究(也稱為LIBERATE-1),該研究旨在探討NPM-119在2型糖尿病患者中的全部藥代動力學特徵。2023年8月18日——美國食品藥品管理局對擬議的LIBERATE-1研究進行了臨牀擱置,這主要是由於化學、製造和控制(CMC)信息不足。2024年——Vivani繼續生成所需的CMC信息,並將繼續積極參與討論,這是其解除臨牀封鎖和加快啟動LIBERATE-1的努力的一部分。與美國食品和藥物管理局的討論仍在進行中,以解決臨牀擱置問題。Vivani目前預計將在2024年上半年向美國食品藥品管理局提交所需的CMC信息。28年裏程碑狀態2023年IND申請支持第一人類(LIBERATE-1)臨牀研究 2023 年 7 月 14 日 FDA 提供的臨牀擱置信 2023 年 8 月 18 日生成/提交新的 CMC 數據,以解除 2024 年的臨牀擱置
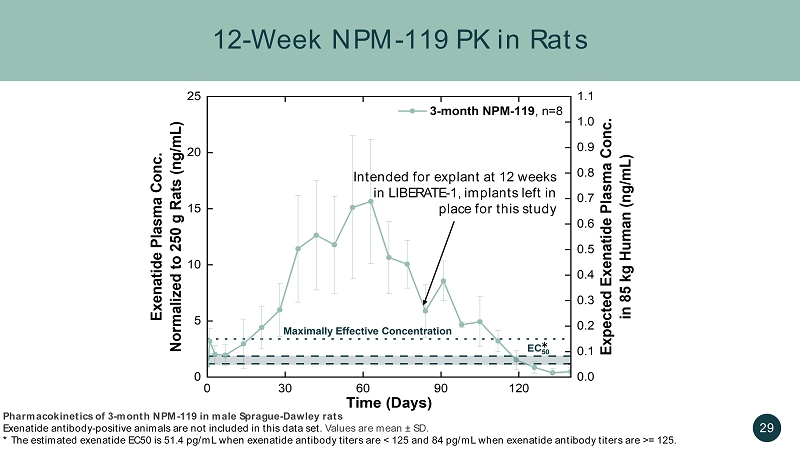
12 周 NPM-大鼠體內 119 PK 計劃在 12 周時在 LIBERATE-1 中進行外植體,本研究的植入物 29 個月 NPM 的藥代動力學-119 個月 NPM-119 在雄性 Sprague-Dawley 大鼠艾塞那肽抗體-陽性動物中,不包括在本數據集中。值為平均值 ± SD。* 當艾塞那肽抗體滴度為 125 時,估計的艾塞那肽 EC50 為 51.4 pg/mL。*

Vivani Medical, Inc. 財務信息
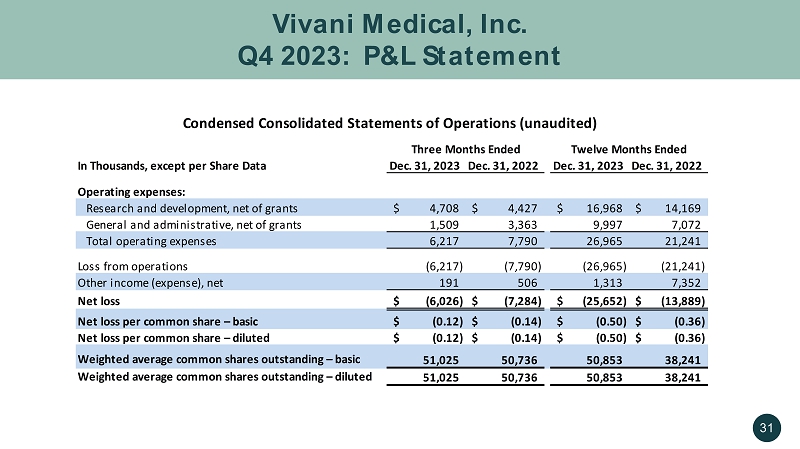
Vivani Medical, Inc. 2023 年第四季度:損益表 31 以千計,每股數據除外 2023 年 12 月 31 日 2023 年 12 月 31 日 2023 年 12 月 31 日運營費用:研發,扣除撥款 4,708 美元 4,427 美元 16,968 美元 14,169 美元,扣除撥款 1,509 3,363 9,997 7,072 總運營費用 6,7217 90 26,965 21,241 運營虧損 (6,217) (7,790) (26,965) (21,241) 其他收益(支出),淨額 191 506 1,313 7,352 淨虧損 (6,026) 美元 (7,284) 美元 (25,652) 美元 (13,889) 美元 — 基本 (0.12) 美元 (0.14) 美元 (0.50) 美元 (0.50) 美元 (0.50) 美元 (0.50) 美元 (0.50) 美元 (0.50) 美元 (0.50) 美元 (0.50) 美元 (0.50) 美元 (0.50) 美元 (0.50) 美元 (0.50) 美元 (0.50) 美元 (0.50) 美元 (0.50) 美元 (0.50) 美元 (0.50) 美元 (0.36) $ 淨虧損每股普通股——攤薄(0.12)美元(0.14)美元(0.50)美元(0.36)美元加權平均已發行普通股——基本51,025 50,736 50,853 38,241 加權平均已發行普通股——攤薄 51,025 50,736 50,853 38,241 截至十二個月的三個月簡明合併運營報表(未經審計)
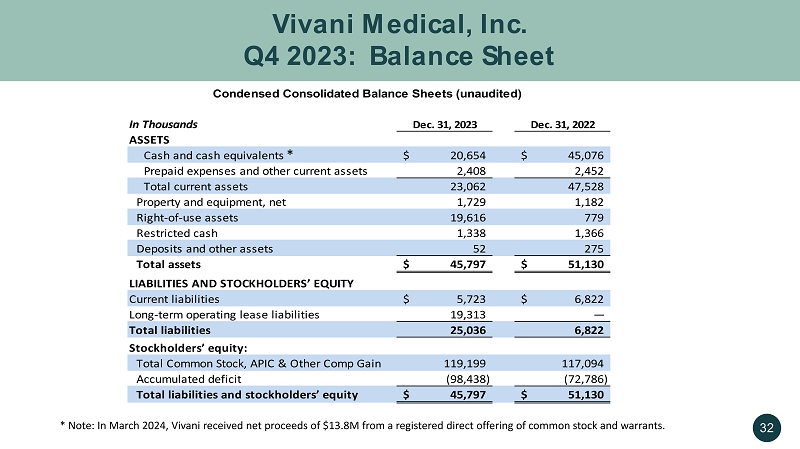
Vivani Medical, Inc. Vivani Medical, Inc. 2023 年第四季度:資產負債表 32 以千計 2023 年 12 月 31 日 2022 年 12 月 31 日資產現金及現金等價物 20,654 美元 45,076 美元預付費用和其他流動資產 2,408 2,452 流動資產總額 23,062 47,528 財產和設備,淨額 1,729 1,182 使用權資產 19,616 779 限制性現金 338 1,366 存款和其他資產 52 275 總資產 45,797 美元 51,130 美元負債和股東權益流動負債 5,723 美元 6,822 美元長期經營租賃負債 19,313 — 總負債 25,036 6,822 名股東股權:普通股、APIC和其他公司收益總額119,199 117,094累計赤字(98,438)(72,786)總負債和股東權益45,797美元簡明合併資產負債表(未經審計)*注:2024年3月,Vivani通過註冊直接發行普通股和認股權證獲得1380萬美元的淨收益。*
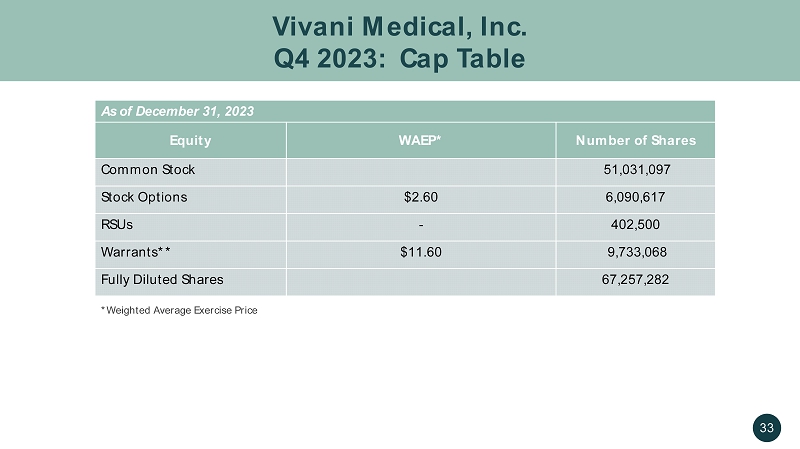
Vivani Medical, Inc. 2023 年第四季度:上限表 33 截至 2023 年 12 月 31 日股權 WAEP* 股票數量普通股 51,031,097 美元股票期權 2.60 美元 6,090,617 美元認股權證——402,500 份認股權證** 11.60 美元 9,733,068 股全面攤薄股票 67,257,282 *加權平均行使價

Vivani Medical, Inc. 34個主要項目NPM-115和NPM-119是正在開發的微型GLP-1(艾塞那肽)植入物,分別用於治療肥胖或超重患者和2型糖尿病的慢性體重管理。用於慢性體重管理的NPM-139(西瑪魯肽植入物)也在開發中,還有一個額外的潛在好處,那就是每年給藥一次。一家創新的生物製藥公司,正在開發用於治療慢性病的微型長期藥物植入物產品組合。我們的NanoPortal™ 平臺技術支持設計植入物,旨在改善藥物不依從性和耐受性。Vivani完全有能力在2024年推動NPM(115)和NPM-119,朝着潛在的轉型里程碑邁進。