

打造一家專注於 ADC 的領先公司納斯達克:PYXS 2024 年 3 月附錄 99.2

前瞻性陳述本演示文稿包含前瞻性陳述,涉及1995年《私人證券訴訟改革法》和其他聯邦證券法中的安全港條款。這些陳述通常使用諸如 “預期”、“相信”、“可以”、“繼續”、“可以”、“估計”、“期望”、“打算”、“可能”、“可能”、“目標”、“持續”、“計劃”、“潛在”、“預測”、“項目”、“應該”、“將來”、“將”、“將”、“將來”、“將來”、“將”、“將”、“將來”、“將來”、“將來”、“將來”、“將來”、“將來”、“將來”、“將來”、“將來”、“將”、“將”、“將”、“將”、“將”、“將”、“將”,” 或這些詞的否定或複數,或類似的表達方式或變體,儘管並非所有前瞻性陳述都包含這些詞語。我們無法向您保證,前瞻性陳述中反映的事件和情況將會實現或發生,實際結果可能與這些前瞻性陳述所表達或暗示的結果存在重大差異。可能導致或促成此類差異的因素包括但不限於此處確定的因素,以及公司於2024年3月21日向美國證券交易委員會提交的10-K表年度報告第二部分第1A項中標題為 “風險因素” 的部分中討論的因素,以及我們的其他文件,每份文件均已向美國證券交易委員會存檔。這些風險並非窮盡無遺。新的風險因素不時出現,我們的管理層無法預測所有風險因素,也無法評估所有因素對我們業務的影響,也無法評估任何因素或因素組合在多大程度上可能導致實際業績與任何前瞻性陳述中包含的結果存在重大差異。此外,“我們相信” 的陳述和類似的陳述反映了我們對相關主題的信念和觀點。這些聲明基於截至本文發佈之日我們獲得的信息,儘管我們認為此類信息構成了此類陳述的合理依據,但此類信息可能有限或不完整,不應將我們的陳述理解為表明我們已對所有可能可用的相關信息進行了詳盡的調查或審查。這些陳述本質上是不確定的,提醒投資者不要過分依賴這些陳述。除非法律要求,否則我們沒有義務更新任何前瞻性陳述以反映此類陳述發佈之日之後的事件或情況。我們在競爭激烈且瞬息萬變的環境中運營。新的風險不時出現,我們的管理層無法預測所有風險,也無法評估所有因素對我們業務的影響,也無法評估任何因素或因素組合在多大程度上可能導致實際業績與我們可能做出的任何前瞻性陳述中包含的結果存在重大差異。鑑於這些風險、不確定性和假設,本演示文稿中描述的前瞻性事件和情況可能不會發生,實際結果可能與本演示文稿中包含的前瞻性陳述中的預期或暗示的結果存在重大和不利的差異。市場和行業數據本演示文稿包含有關我們的行業、業務和候選產品市場的估計、預測和其他信息。這些信息基於估計、預測、預測、市場研究或類似方法,本質上受不確定性、假設和侷限性的影響,實際事件或情況可能與本信息中假設的事件和情況存在重大差異。除非另有明確説明,否則我們從自己的內部估計和研究,以及市場研究公司和其他第三方、行業、醫學和一般出版物、政府數據和類似來源編制的報告、研究調查、研究和類似數據中獲得的行業、業務、市場和其他數據。儘管我們沒有發現本演示文稿中對任何第三方信息有任何錯誤陳述,但他們的估計,特別是與預測相關的估計,涉及許多假設和侷限性,受風險和不確定性的影響,並可能發生變化。我們尚未獨立驗證任何第三方信息。提醒你不要過分重視任何此類信息、預測和估計。商標本演示文稿包含對屬於其他實體的商標和服務標誌的引用。僅為方便起見,本演示文稿中提及的商標和商品名稱可能不帶有® 或符號,但此類提及的目的不在於以任何方式表明適用的許可方不會在適用法律的最大範圍內主張其對這些商標和商品名稱的權利。我們無意使用或展示其他公司的商品名稱、商標或服務標誌,以暗示與任何其他公司的關係,或對我們的認可或贊助。
PYXS:打造下一家專注於ADC的領先公司,在I/O上投注機會主義,經驗豐富的團隊,在製藥和生物技術臨牀階段的投資組合中均有良好的往績,2024年數據催化劑強勁的資產負債表和1.73億美元的現金為進入2026年下半年提供了機會

Lara Sullivan,醫學博士首席執行官楊曉東,醫學博士,傑出研究員 Jan Pinkas,博士首席科學官 Pam Connealy,工商管理碩士首席財務官兼首席運營官 Balu Balasubramanian,博士首席技術官執行領導團隊 PYXS 團隊成員共同為超過 60 項腫瘤藥物批准做出了貢獻 Ken Kobayashi,醫學博士,FACP 首席營銷官
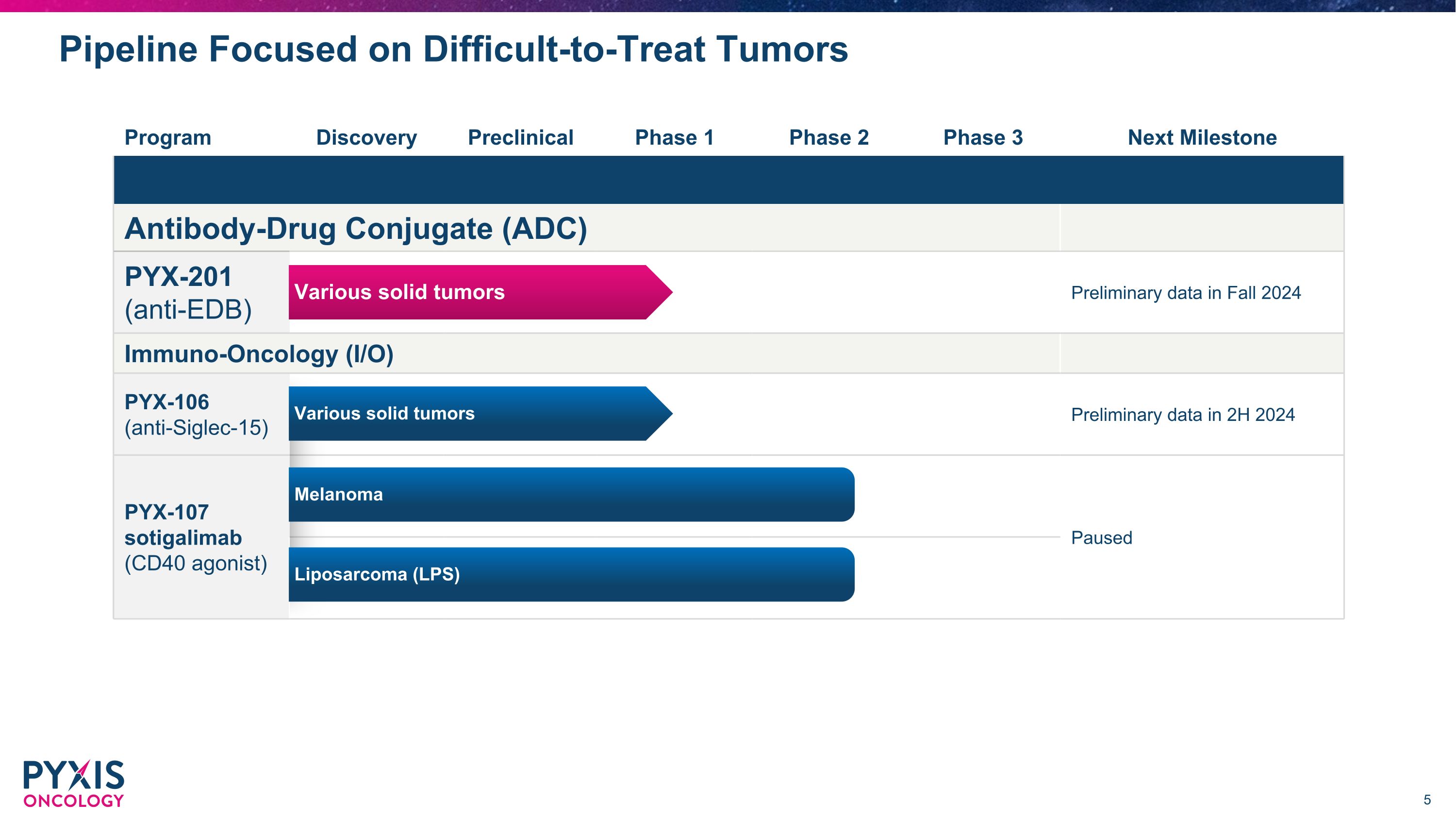
研發管道專注於難以治療的腫瘤項目發現臨牀前 1 期 2 期 3 期下一個里程碑抗體藥物偶聯物 (ADC) PYX-201(抗 EDB)2024 年秋季的初步數據免疫腫瘤學(I/O)PYX-106(抗 SIGLEC-15)2024 年下半年的初步數據 PYX-107 索替利單抗(CD40 激動劑)暫停脂肪肉瘤(LPS)各種實體瘤黑色素瘤各種實體瘤
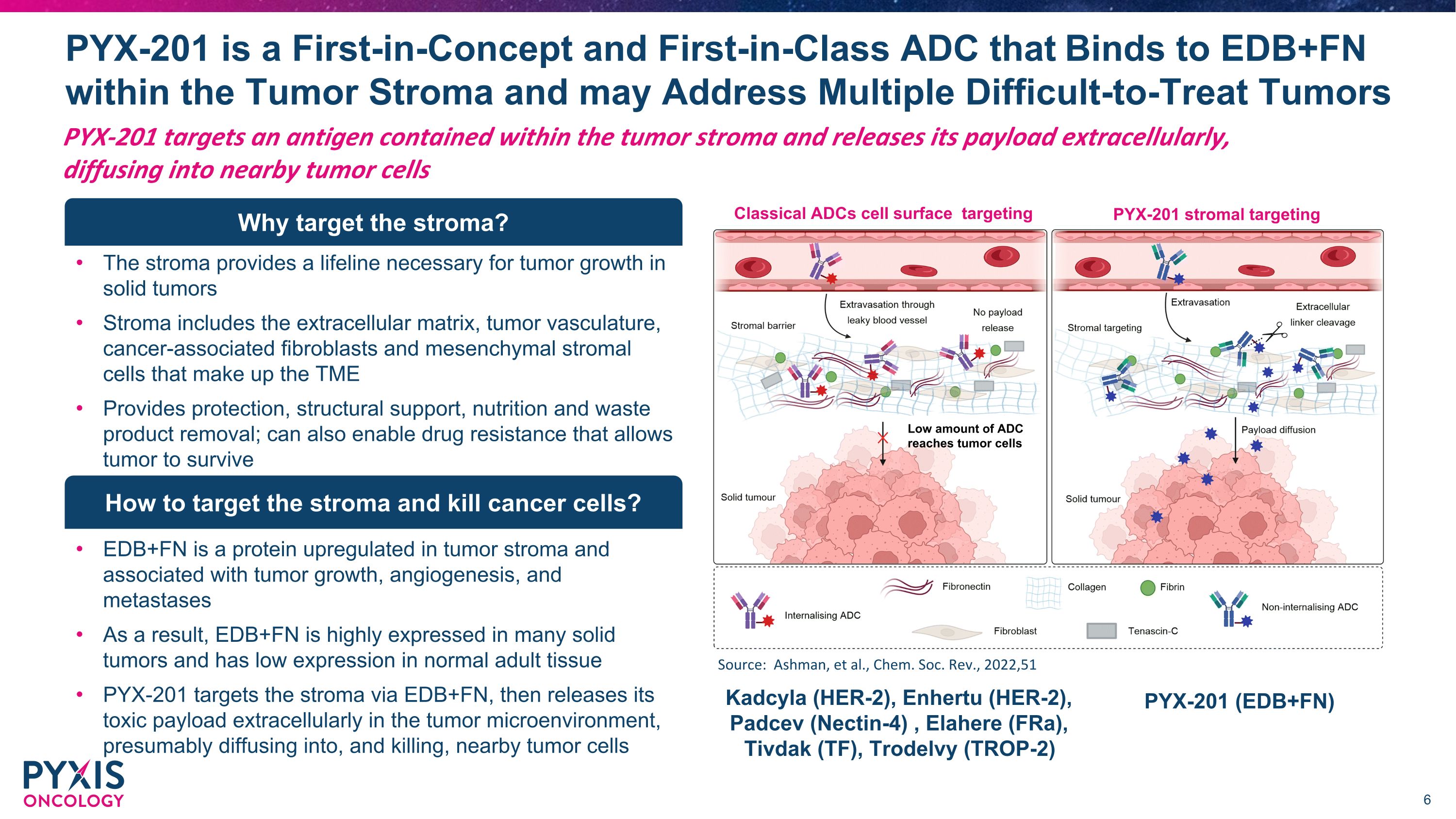
PYX-201 靶向腫瘤基質中含有的抗原並通過細胞外釋放其有效載荷,擴散到附近的腫瘤細胞中 PYX-201 是概念上首創的同類首創的 ADC,可與腫瘤基質內的 EDB+FN 結合,可以解決多種難以治療的腫瘤。該基質為實體瘤的腫瘤生長提供了必要的生命線 Stroma 包括細胞外基質、腫瘤血管、癌症相關成纖維細胞和構成 TME 的間充質基質細胞提供保護、結構支持、營養和廢棄物去除;還可以啟用耐藥性,使腫瘤得以存活為什麼要靶向基質?EDB+FN 是一種在腫瘤基質中上調的蛋白質,與腫瘤生長、血管生成和轉移有關。因此,EDB+FN 在許多實體瘤中高度表達,在正常成體組織中的表達較低 PYX-201 通過 EDB+FN 靶向基質,然後在腫瘤微環境中細胞外釋放其毒性載荷,可能擴散到附近的腫瘤細胞中並殺死該腫瘤細胞。如何靶向基質然後殺死癌細胞?靶向 PYX-201 基質靶向的經典 ADC 細胞表面少量的 ADC 到達腫瘤細胞來源:Ashman 等人,Chem。Soc。Rev.,2022,51 Kadcyla (HER-2)、Enhertu (HER-2)、Padcev (Nectin-4)、Elahere (fRA)、Tivdak (TF)、Trodelvy (TROP-2) PYX-201 (EDB+FN)

腫瘤基質為ADC模式提供了一個令人興奮的機會許多細胞內發現的蛋白酶也存在於細胞外,並參與包括癌症在內的疾病病理學* 腫瘤微環境(TME)呈酸性(即,pH值介於6.4至7.0之間),正常生理pH值為7.4**,在酸性TME中可以減弱免疫反應酸性。TME 已被用來開發具有腫瘤選擇性 pH 依賴性抗原結合的治療性抗體*** *Yadati,Cells (9) 2020:1679-1705;** Boedtkjer,annrevPhys(82) 2020:103-126;*** Chang,PNAS (118) 2021:1-10 腫瘤中的酸性環境和細胞外蛋白酶導致 TME 中的 PYX-201 釋放 AUR-0101(奧瑞他汀微管抑制劑)有效載荷
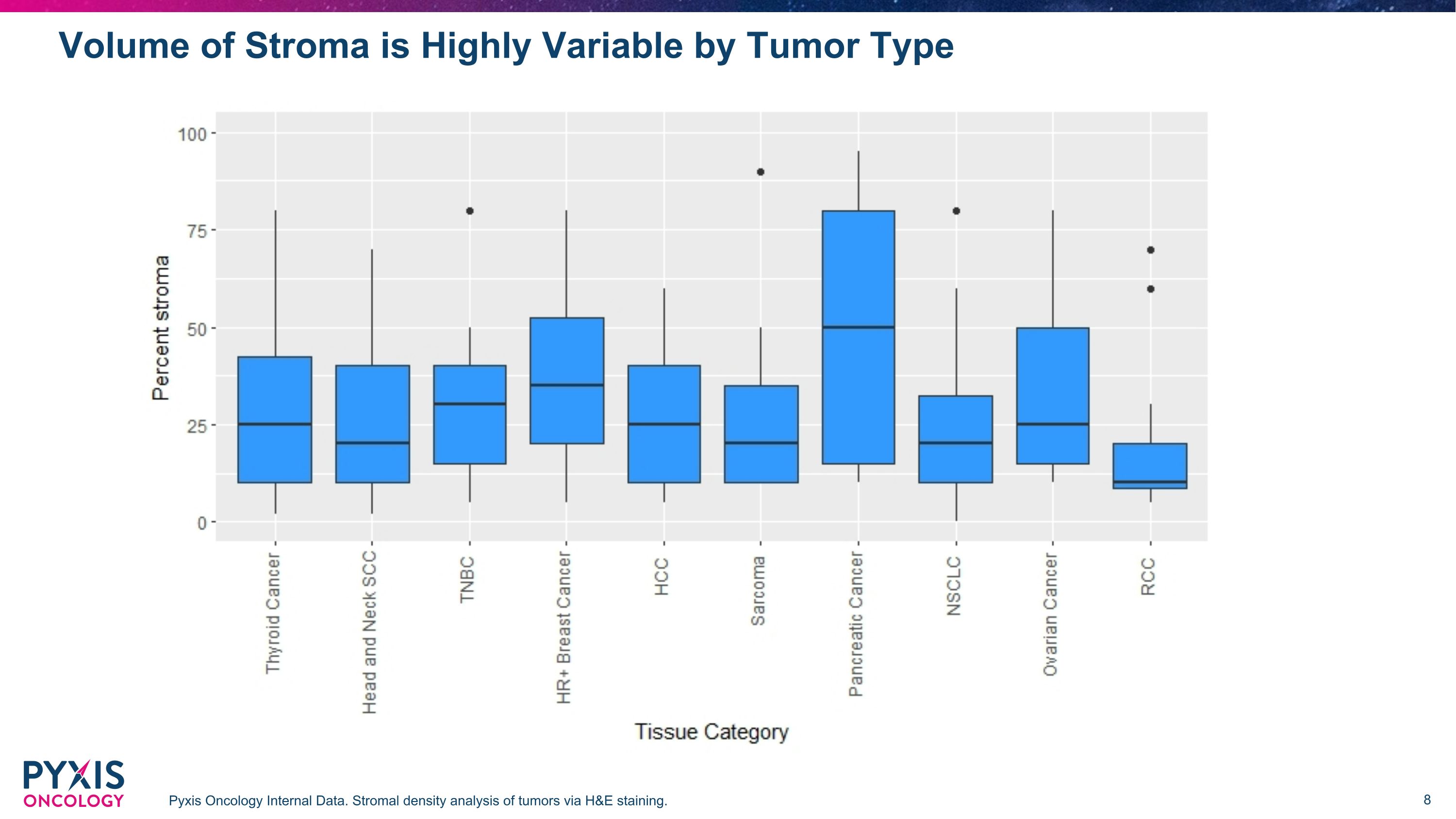
根據腫瘤類型 Pyxis 腫瘤學內部數據,間質體積變化很大。通過 H&E 染色對腫瘤進行基質密度分析。
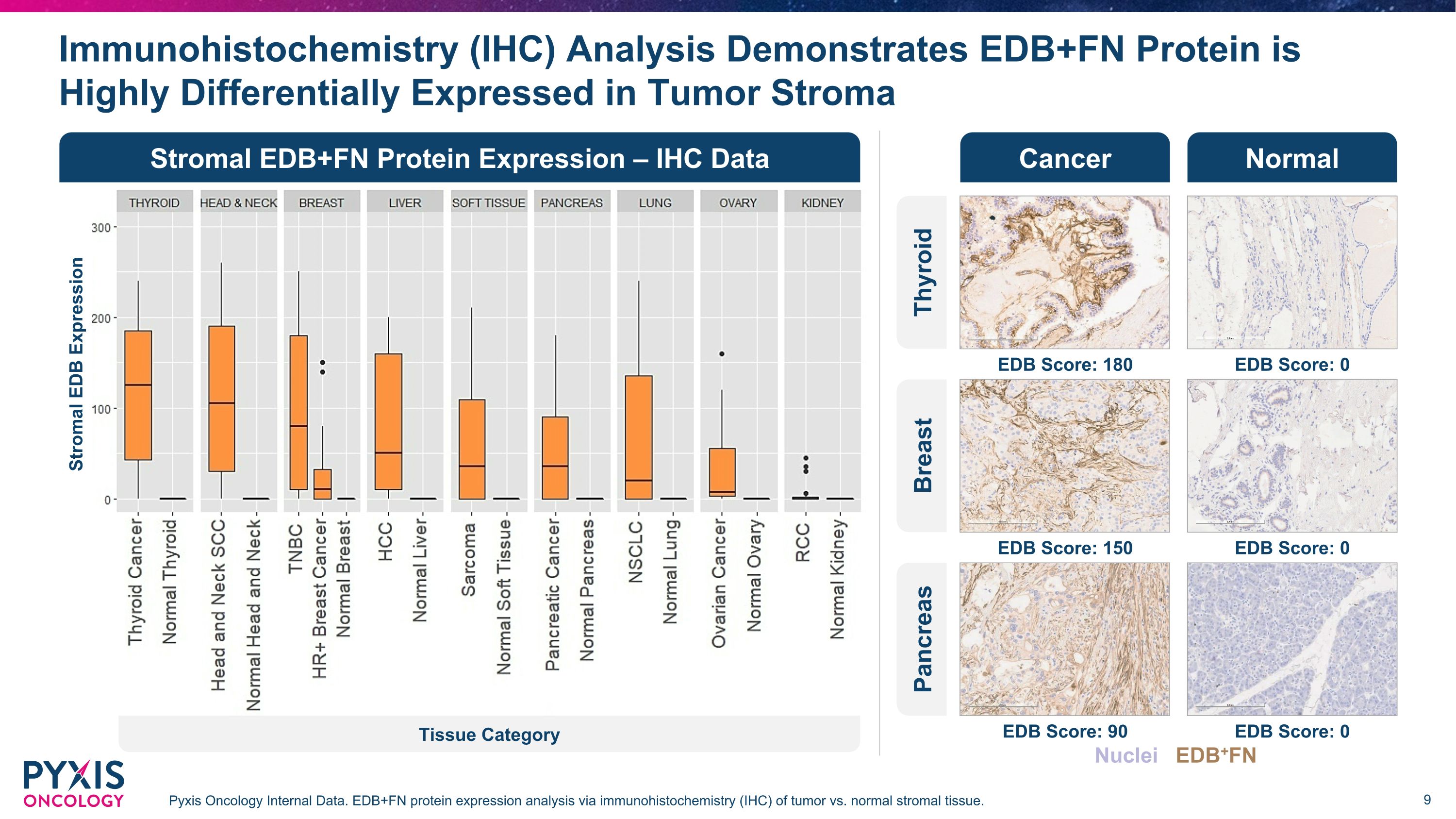
免疫組織化學(IHC)分析表明,EDB+FN蛋白在腫瘤基質Pyxis腫瘤學內部數據中具有高度差異的表達。通過免疫組織化學(IHC)對腫瘤與正常基質組織進行EDB+FN蛋白表達分析。基質 EDB+FN 蛋白表達 — IHC 數據正常癌症甲狀腺 EDB 分數:180 EDB 分數:0 乳房 EDB 分數:150 EDB 分數:0 胰腺 EDB 分數:90 EDB 分數:0 間質 EDB 表達組織類別核 EDB+FN
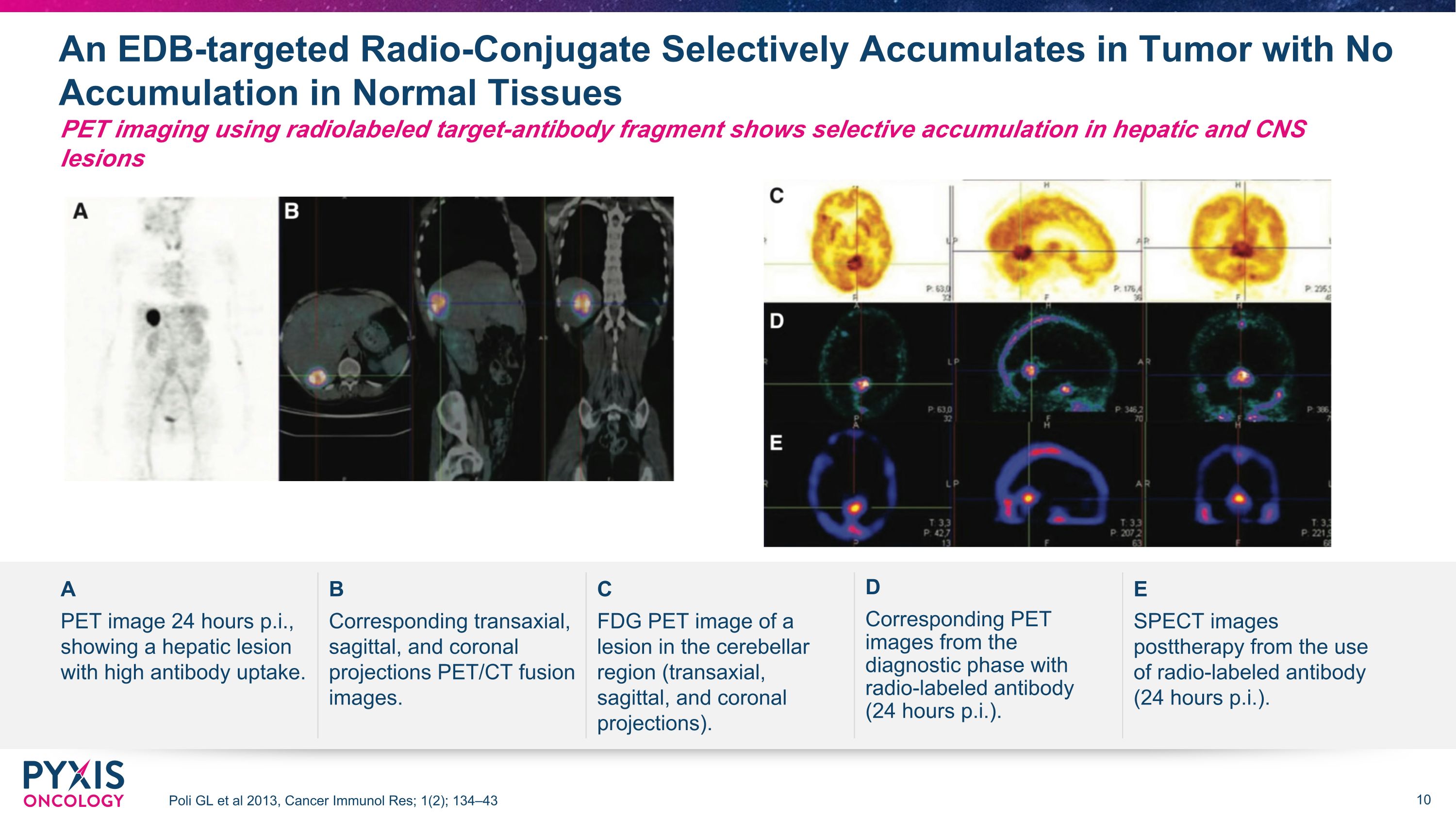
EDB 靶向放射性偶聯物選擇性地在腫瘤中累積,不會在正常組織中積累 Poli GL 等人 2013,《癌症免疫研究》;1(2);使用放射標記靶抗體片段的 134—43 PET 成像顯示肝臟和中樞神經系統病變 A B C D E PET 圖像的選擇性積累,抗體吸收率高。相應的經軸、矢狀和日冕投影 PET/CT 融合圖像。小腦區域病變(經軸、矢狀和冠狀突起)的 FDG PET 圖像。使用放射標記抗體的診斷階段對應的PET圖像(每隔24小時)。SPECT 在治療後使用放射標記的抗體拍攝圖像(每週 24 小時)。
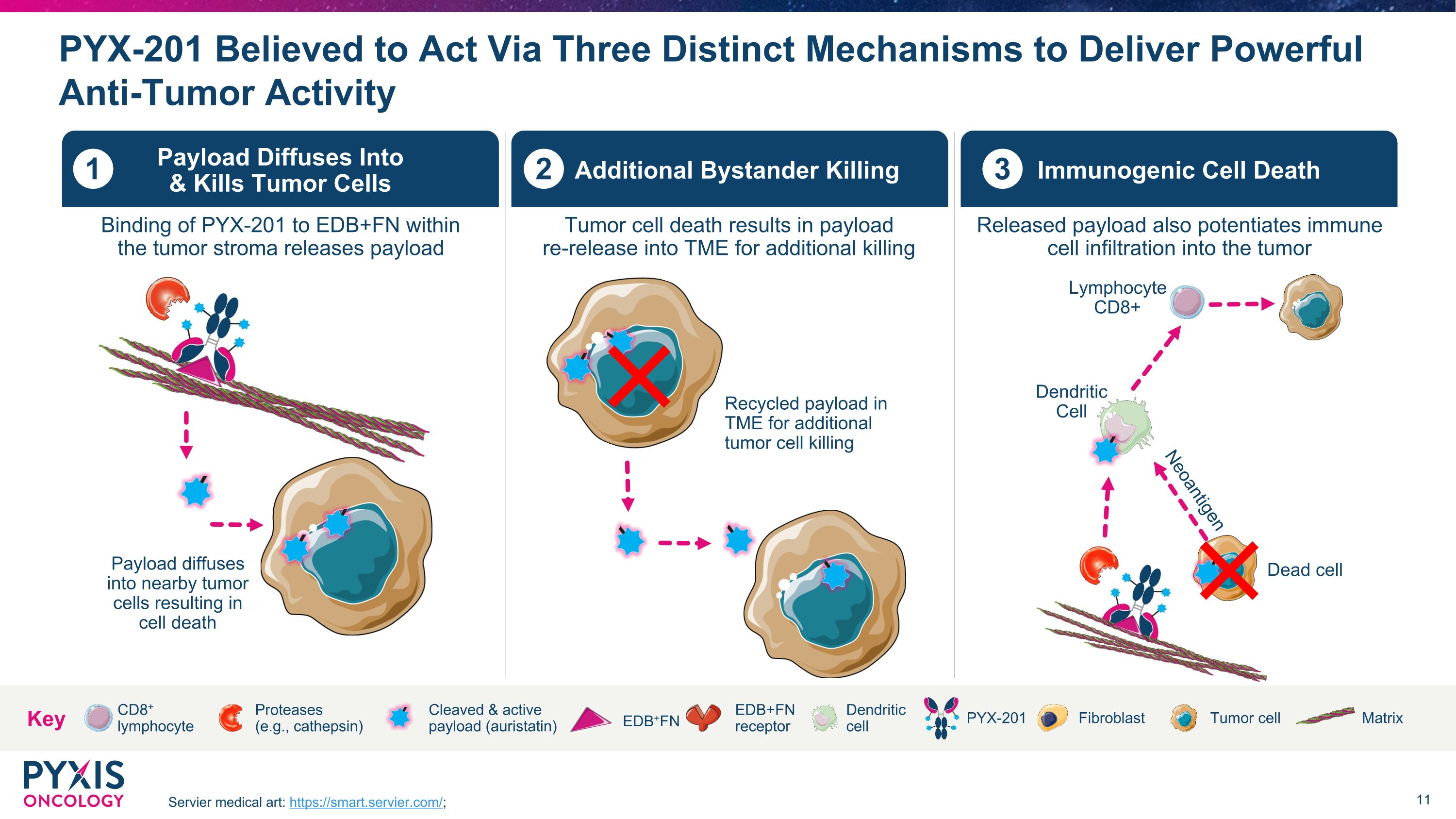
據信 PYX-201 將通過三種不同的機制發揮作用,提供強大的抗腫瘤活性 Servier 醫學藝術:https://smart.servier.com/;CD8+ 淋巴細胞樹突狀細胞 PYX-201 裂解和活性有效載荷(奧里斯他汀)腫瘤細胞成纖維細胞 EDB+FN 矩陣 EDB+FN 受體蛋白酶(例如組織蛋白酶)關鍵附加旁觀者殺死 2 腫瘤細胞死亡會導致有效載荷重新釋放到 TME,從而進一步殺死有效載荷擴散到 & 殺死腫瘤細胞 1 在腫瘤基質內將 PYX-201 與 EDB+FN 結合釋放有效載荷免疫原性細胞死亡 3 已釋放有效載荷還能增強免疫細胞對腫瘤的浸潤有效載荷擴散到附近的腫瘤細胞導致細胞死亡 TME 中的回收載荷可進一步殺滅腫瘤細胞樹突狀細胞淋巴細胞 CD8+ 死細胞新抗原

PYX-201 與其他 ADC 偶聯反應的 ADC 技術改進:經過設計的半胱氨酸殘基可在不破壞將抗體結合在一起的鏈間半胱氨酸鍵的情況下將目標 DAR 設為 4 Linker:與 Adcetris、Padcev 等中使用的 val-cit 連接劑相比,經過優化的 val-cit 連接劑在循環中更穩定(即減少羧酸酯酶裂解)。有效載荷:優化的奧瑞他汀(AUR-0101) 之所以被選中,是因為與 MMAE 相比具有增強的細胞通透性和旁觀者細胞殺傷活性。與 MMAE 相比,AUR-0101 的代謝和排泄特性也有所改善。與傳統 Val-cit-MMAE ADC 相比,PYX-201 的這三個技術改進領域表現出更高的耐受性和穩定性,非臨牀毒理學研究中流通中的遊離奧瑞他汀有效載荷水平較低

PYX-201 專為耐受性和活性而設計 PYXS 優化的 ADC 技術的關鍵改進:專為腫瘤基質中纖維連接蛋白 (EDB+FN) 的外域 B 而設計的單克隆抗體旨在減少脱靶效應和提高耐受性攜帶四個 Auristatin 0101、微管解聚抑制有效載荷最大化腫瘤殺傷和效力 4 個位點的可預測統一藥物抗體比 (DAR) 特異性、可組織蛋白分解的纈氨酸瓜氨酸連接劑經過優化,可提高循環穩定性並減少自由載荷 EDB+FN (HuigG1) 靶向 mAb auristatin 0101 有效載荷 (x4) 纈氨酸瓜氨酸連接劑 PYX-201 藥物設計 MC VC PBAC aur0101 PYX-201 結構人源化 L19 抗 EDB-fn 單抗 (kk183c + K290C) vc0101 MC-VC-PABC 連接劑結構使用馬來酰亞胺己酰基 (MC) 間隔,一種對蛋白酶(組織蛋白酶)敏感的間隔二肽、纈氨酸 (VC)、自焚間隔、對氨基苯甲氧基羰基 (PABC) 和經過優化的奧瑞他汀 — Aur0101
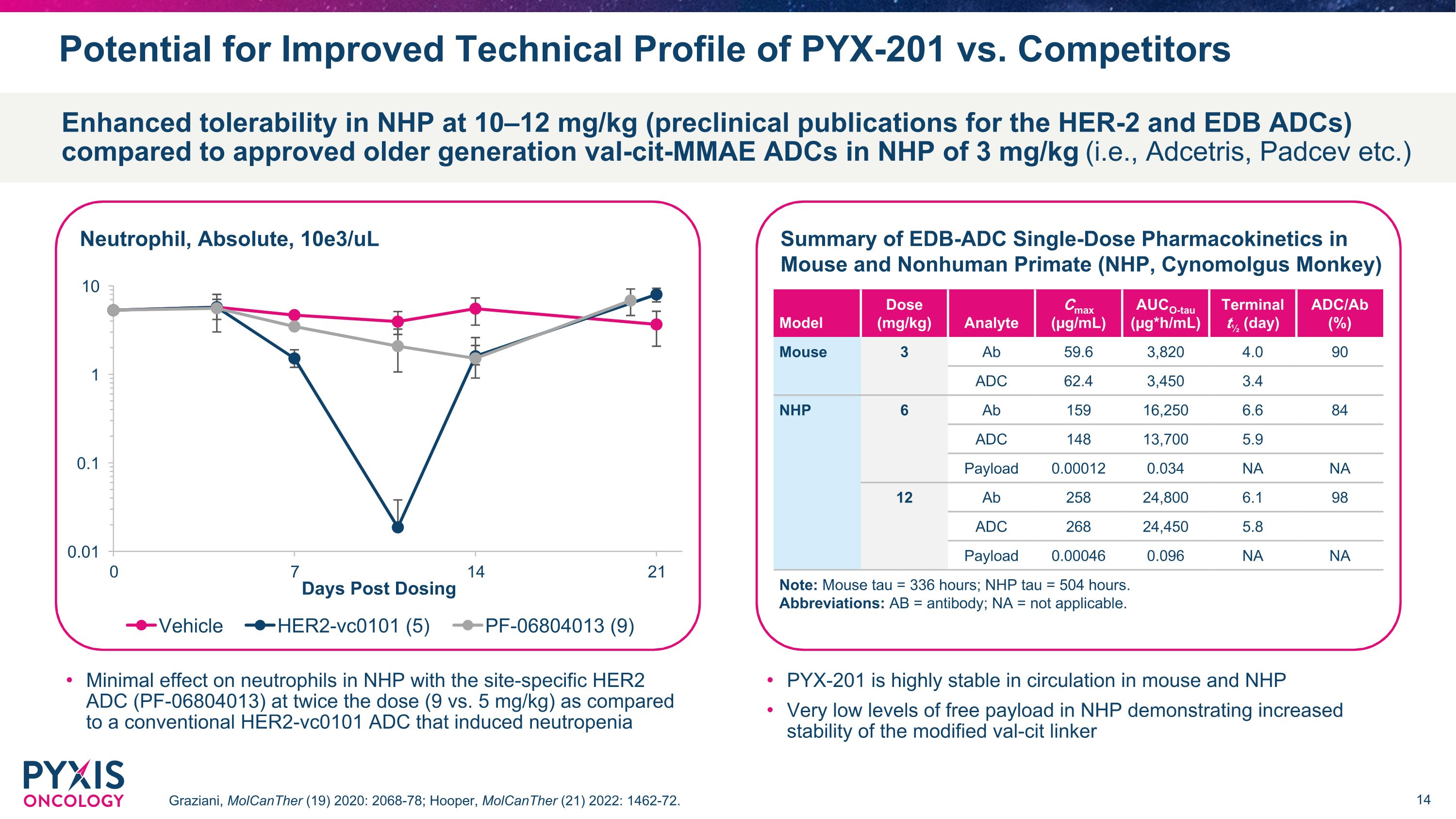
PYX-201 對比競爭對手的技術概況有可能改善 Graziani,MolcAnther(19)2020:2068-78;Hooper,MolcAnther(21)2022年:1462-72。與經批准的 3 mg/kg(即 Adcetris、Padcev 等)的老一代 Val-cit-MMAE ADC 相比,NHP 在 10—12 mg/kg(HER-2 和 EDB ADC 的臨牀前出版物)下的耐受性增強與誘發中性粒細胞減少的傳統 HER2-vc0101 ADC 相比,使用位點特異性 HER2 ADC (PF-06804013) 的劑量(9 與 5 mg/kg)對新生兒中性粒細胞的影響微乎其微 PYX-201 在小鼠和 NHP 的循環中高度穩定 NHP 中的遊離載荷水平非常低,表明改性的 val-cit 連接劑的穩定性更高 EDB-ADC 單劑量藥代動力學摘要非人靈長類動物(NHP、Cynomolgus Monkey)模型劑量(mg/kg)分析物 Cmax(µg/mL)Auco-TAU(µg*H/mL)終端½(天)ADC/Ab(%)小鼠 3 Ab 59.6 3,820 4.0 90 ADC62.4 3,450 3.4 NHP 6 Ab 159 16,250 6.6 84 ADC 148 13,700 5.9 有效載荷 0.00012 0.034 NA NA 12 Ab 258 24,800 6.1 98 ADC 268 24,450 5.8 有效載荷 0.00046 0.096 NA NA 注意:鼠標 tau = 336 小時;NHP tau = 504 小時。縮寫:AB = 抗體;NA = 不適用。中性粒細胞,絕對值,10e3/uL
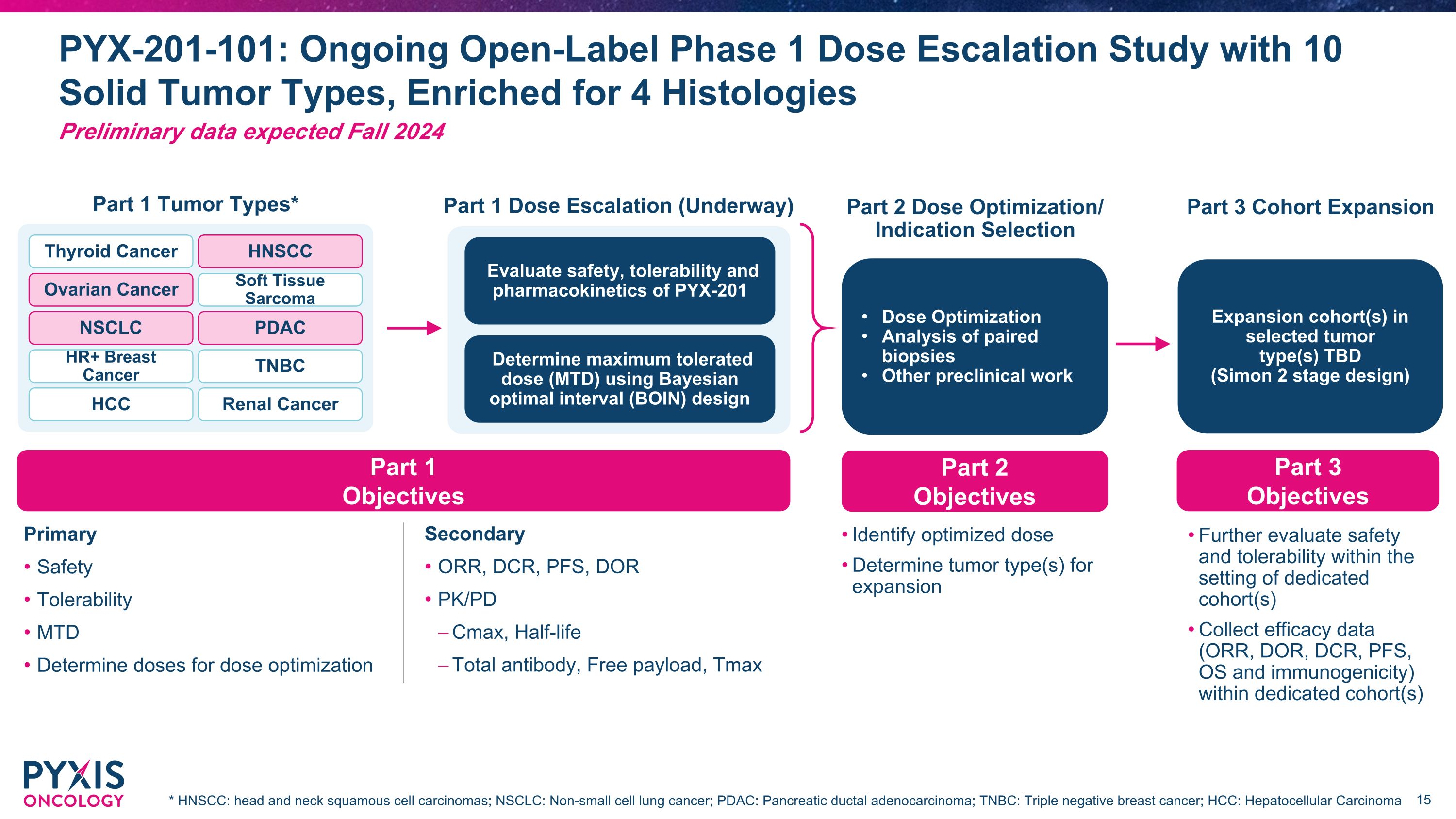
2022 年 2023 年第一季度 PYX-201-101:正在進行的開放標籤 1 期劑量遞增研究,涉及 10 種實體瘤類型,豐富 4 種組織學 2024 年秋季初步數據第 1 部分腫瘤類型* 第 1 部分劑量遞增(進行中)第 2 部分選定腫瘤類型的劑量優化/適應症選擇擴展隊列待定(西蒙 2 階段設計)配對活檢的劑量優化分析其他臨牀前研究使用 Bays 確定最大耐受劑量 (MTD) 最佳間隔 (BOIN) 設計評估 PYX-201 卵巢的安全性、耐受性和藥代動力學癌症 NSCLC HR+ 乳腺癌 HCC 軟組織肉瘤 PDAC TNBC 甲狀腺癌 HNSCC 腎癌第 3 部分隊列擴展 * HNSCC:頭頸部鱗狀細胞癌;NSCC:非小細胞肺癌;PDAC:胰腺導管腺癌;TNBC:三陰性乳腺癌;HCC:肝細胞癌第 2 部分目標第 3 部分確定優化目標劑量確定要擴大的腫瘤類型進一步評估專用隊列中的安全性和耐受性收集其中的療效數據(ORR、DOR、DCR、PFS、OS 和免疫原性)專用隊列第 1 部分目標主要安全耐受性 MTD 確定劑量優化劑量次要 ORR、DCR、PFS、DOR PK/PD Cmax、半衰期總抗體、空閒有效載荷、Tmax
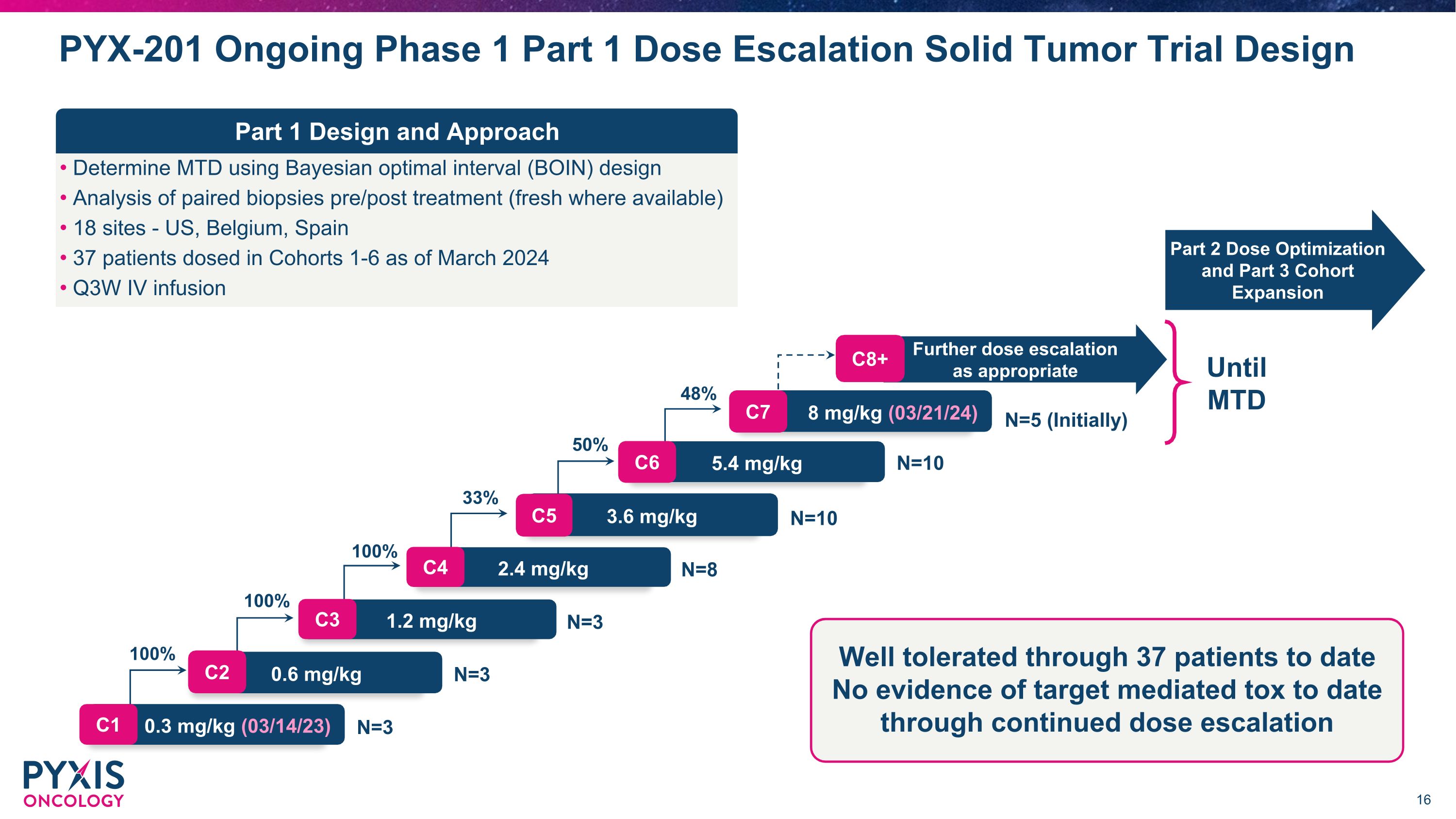
使用貝葉斯最佳間隔 (BOIN) 設計對配對活檢進行分析治療前/後(如果有最新活檢)18 個部位——美國、比利時、西班牙 37 名患者截至 2024 年 3 月 Q3W IV 輸液 PYX-201 正在進行第 1 階段第 1 部分劑量遞增實體瘤試驗設計酌情進一步增加劑量 0.3 mg/kg(03/14/23)N=3 0.6 mg/kg N=3 1.2 mg/kg N=3 1.2 mg/kg N=3 1.2 mg/kg N=3 1.2 mg/kg N=3 1.2 mg/kg N=3 1.2 mg/kg N=3 1.2 mg/kg N=3 3 2.4 mg/kg N=8 3.6 mg/kg N=10 5.4 mg/kg N=10 8 mg/kg (03/21/24) N=5(初始)100% 100% 100% 33% 50% 48% 48% C1 C2 C3 C4 C5 C6 C7 C8+ 第 2 部分劑量優化和第 3 部分隊列擴張直到 MTD 迄今為止 37 名患者耐受性良好,迄今為止,沒有證據表明持續增加劑量會產生靶向介導的毒素(第 1 部分)設計與方法

Anti-Siglec-15(PYX-106):潛在的非小細胞肺癌和實體瘤中同類最佳、高度分化的全人源抗體更高的結合親和力可增強較高劑量水平下的T細胞反應,使免疫系統能夠殺死和抵禦癌細胞。可能與抗PD-(L)1或其他免疫療法聯合使用可能獲得更好的暴露且沒有抗藥抗體證據的臨牀前研究耐受性良好,半衰期為7天減少給藥頻率表現出對人類 Siglec-15 的親和力比基準值高 10 倍發育體外 SIGLEC-15 介導的 T 細胞抑制效果強大、劑量依賴性逆轉
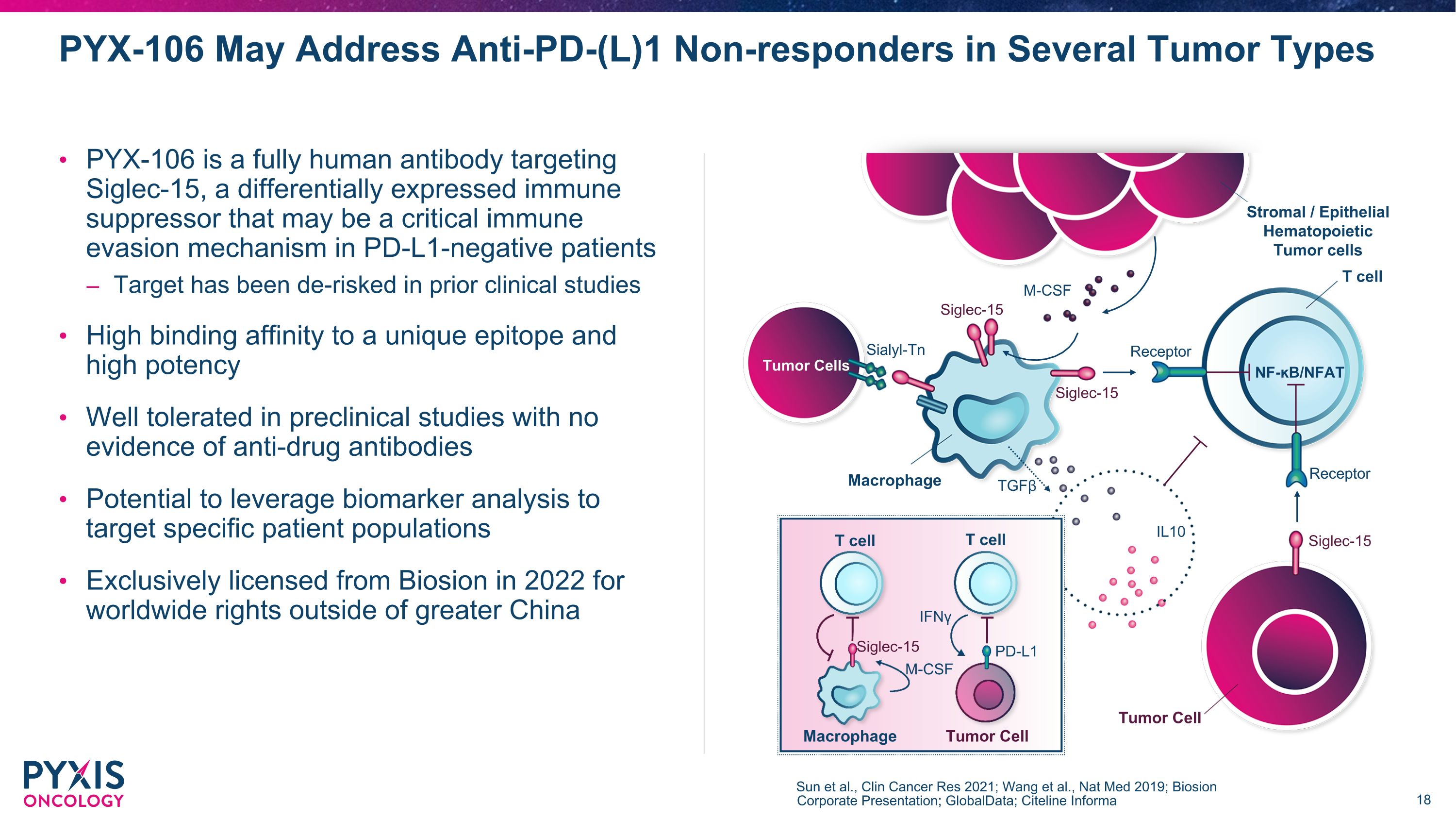
PYX-106 可能會解決幾種腫瘤類型中抗PD-(L) 1 無反應者 Sun 等人,《2021 年臨牀癌症研究報告》;Wang 等人,2019 年 Nat Med;Biosion 企業演講;GlobalData;Citeline Informa 基質/上皮造血腫瘤細胞 T 細胞 NF-B/nFAT 腫瘤細胞巨噬細胞受體 TGFβ Sialyl-Tn M-CSF Siglector -15 Siglec-15 Siglec-15 IL10 Siglec-15 M-CSF PD-L1 IFNγT 細胞 T 細胞巨噬細胞腫瘤細胞 PYX-106 是一種靶向 Siglec-15 的完全人源抗體,這是一種差異表達的免疫抑制劑,可能是一種關鍵的免疫逃避PD-L1 陰性患者的機制在先前的臨牀研究中,靶點已被去除風險,與獨特表位的結合親和力高,在沒有抗藥抗體證據的臨牀前研究中耐受性良好。有可能利用生物標記物分析靶向特定患者羣體 2022 年獲得博奧信獨家許可,可獲得大中華區以外的全球版權
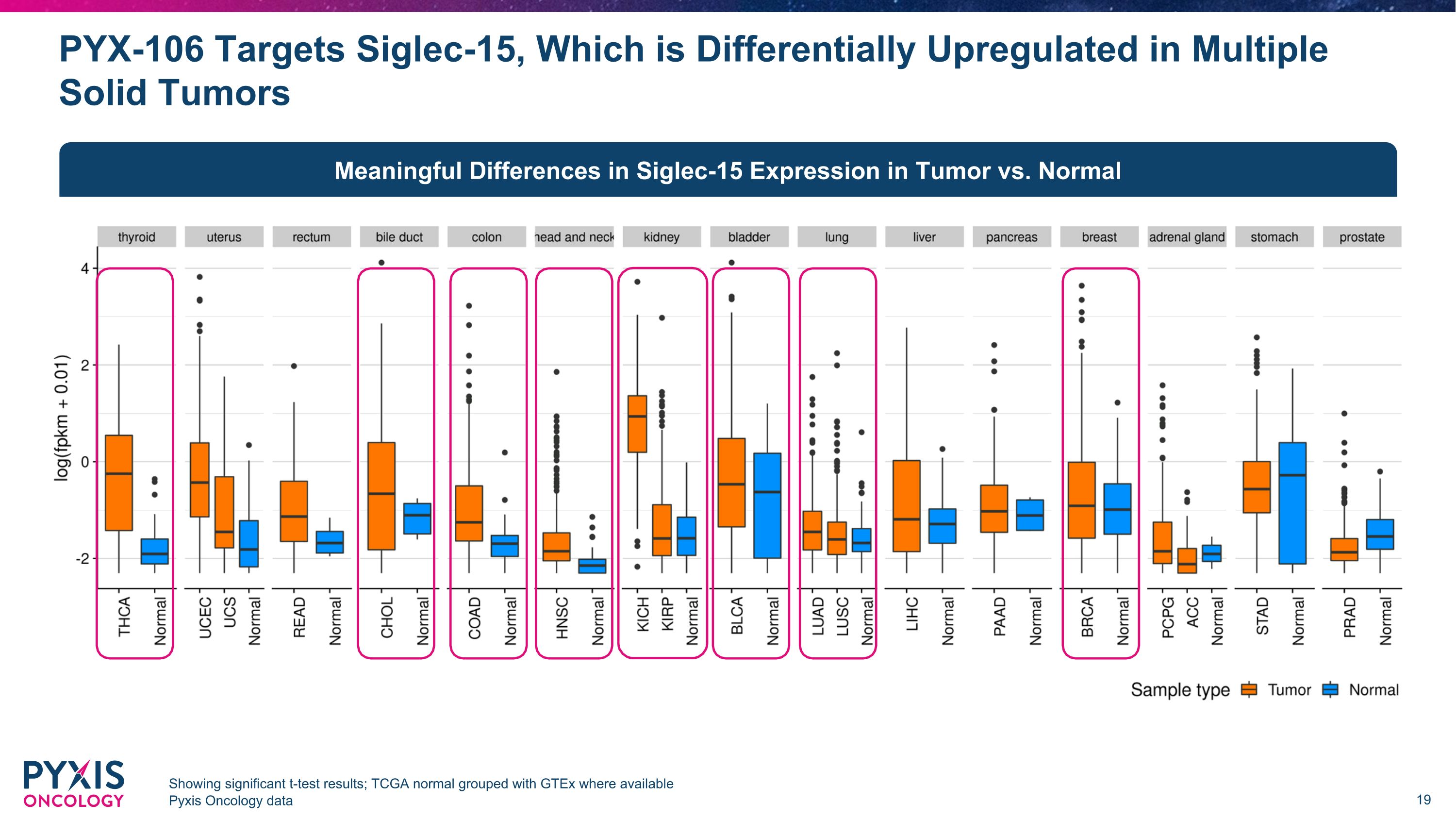
PYX-106 靶向 Siglec-15,在多個實體瘤中差異上調,顯示出顯著的 t 檢驗結果;TCGA 正常與 gTeX 分組,其中 Pyxis Oncology 數據有 Pyxis Oncology 數據,腫瘤與正常腫瘤中 Siglec-15 的表達存在顯著差異
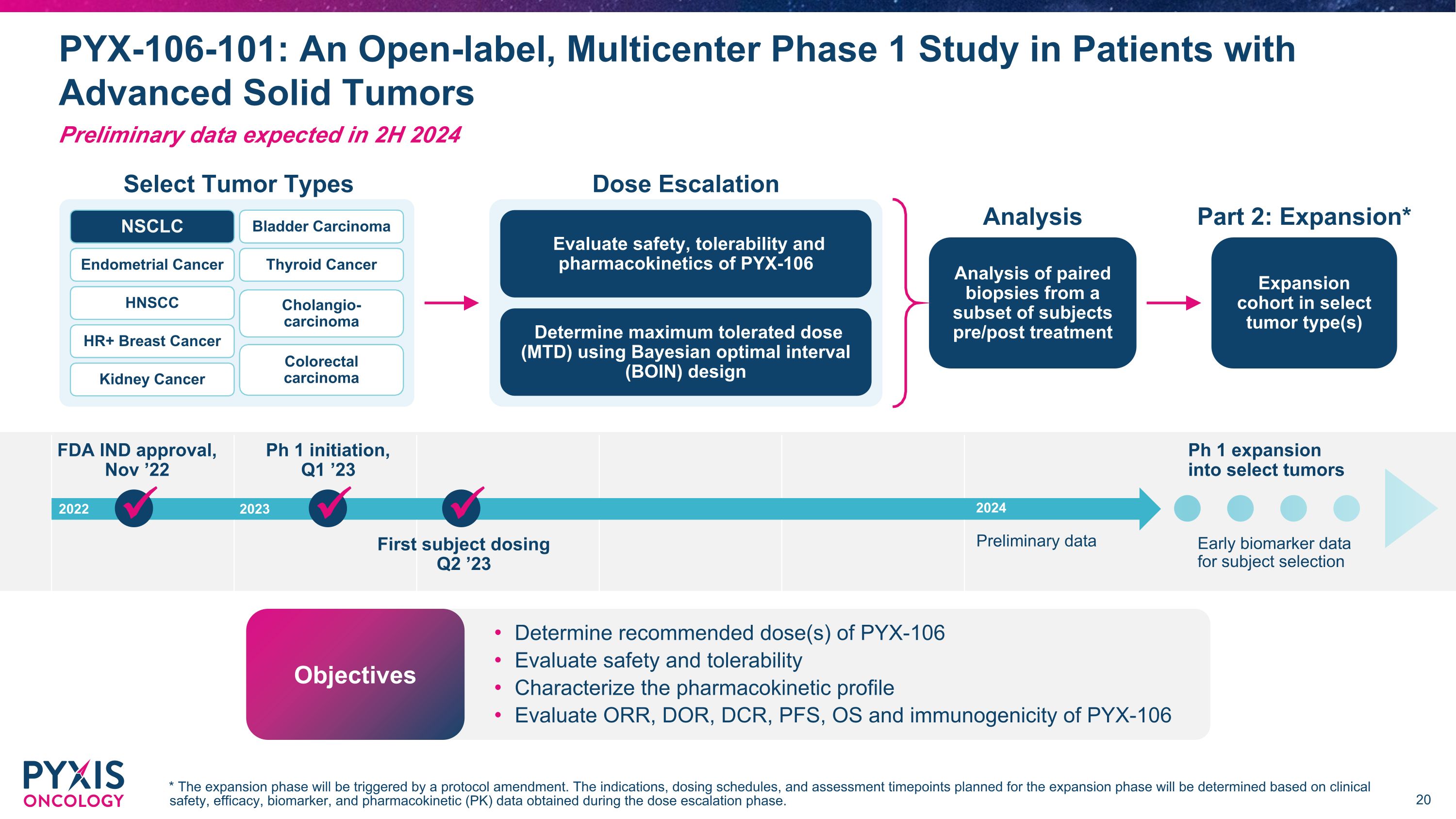
FDA IND 批准,22 年 11 月 Ph 1 啟動,2023 年第一季度 Ph 1 擴展到特定腫瘤受試者選擇的早期生物標誌物數據第一受試者給藥 2023 年 2023 年第二季度初步數據選擇腫瘤類型劑量遞增分析特定腫瘤類型的擴展隊列治療前/後對部分受試者的配對活檢進行分析使用貝葉斯最佳間隔 (BOIN) 設計確定最大耐受劑量 (MTD) 評估安全性,PYX-106 子宮內膜癌的耐受性和藥代動力學 HNSCC HR+ 乳腺癌腎癌甲狀腺癌膽管癌結直腸癌 NSCLC 膀胱癌第 2 部分:擴張* 確定 PYX-106 的推薦劑量評估安全性和耐受性表徵藥代動力學特徵評估 PYX-106 的 ORR、DOR、DCR、PFS、OS 和免疫原性目標 PYX-106-101:一項針對晚期實體瘤患者的開放標籤、多中心 1 期研究 * 擴展階段將由協議修正案觸發。擴張階段計劃的適應症、給藥時間表和評估時間點將根據劑量遞增階段獲得的臨牀安全性、療效、生物標誌物和藥代動力學(PK)數據確定。初步數據預計將在2024年下半年公佈
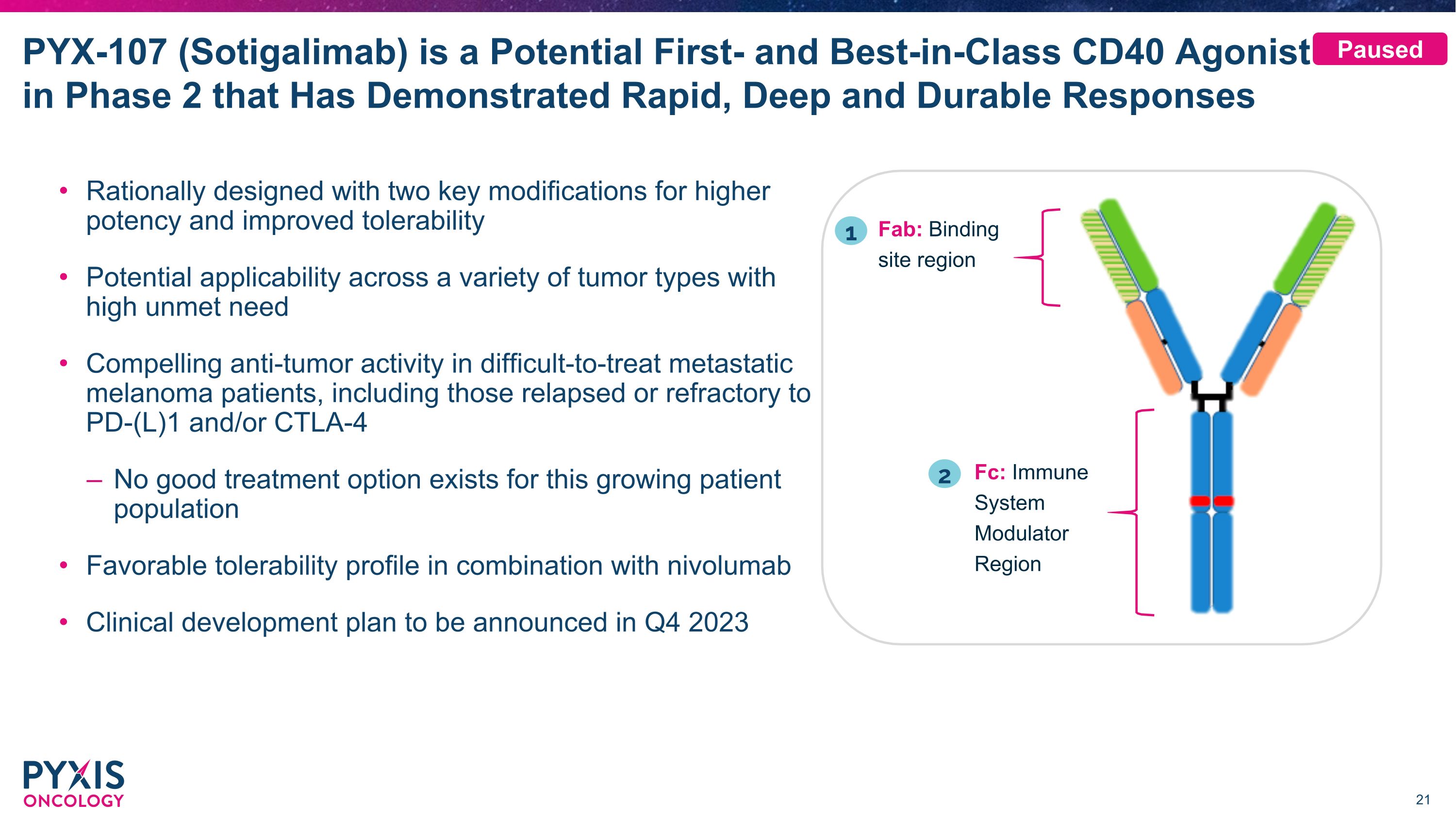
PYX-107(Sotigalimab)是處於第二階段的潛在首創和同類最佳CD40激動劑,已顯示出快速、深層和持久的反應合理設計,具有更高的效力和更高的耐受性。潛在的適用性適用於需求量大的各種腫瘤類型,對難以治療的轉移性黑色素瘤患者,包括PD-(L)1和/或 CTLA-4 復發或難治的患者,具有吸引力的抗腫瘤活性對於這種不斷增長的患者羣體,沒有好的治療選擇良好的耐受性狀況與 nivolumab 聯合臨牀開發計劃將於 2023 年第四季度公佈 Fab:結合位點區域 Fc:免疫系統調節劑區域 1 2 已暫停
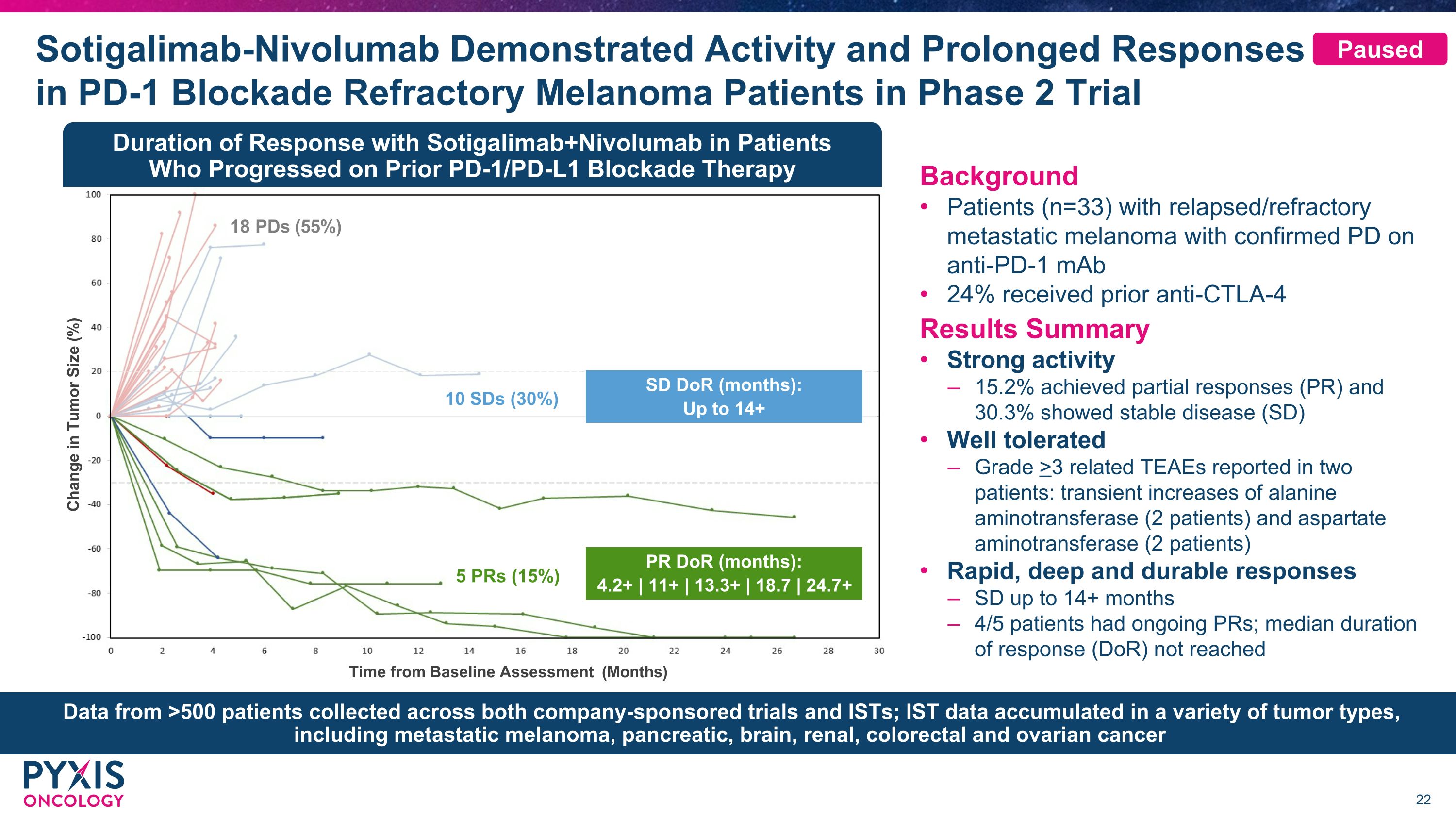
Sotigalimab-Nivolumab 在 PD-1 阻斷難治性黑色素瘤患者的 2 期試驗中表現出活性和長期反應腫瘤大小變化(%)距基線評估時間(月)5 個 PR(15%)PR(月):4.2+ | 11+ | 13.3+ | 18.7 | 24.7+ SD dOR(月):最多 14+ 10 個 SD (30%) 18 個 PD (55%) 背景復發/難治性轉移性黑色素瘤的患者(n=33)在使用抗PD-1單克隆抗體時確診患者 24% 先前接受過抗CTLA-4結果摘要強活性 15.2% 實現部分反應(PR),30.3% 表現出穩定的疾病(SD)耐受性良好在兩名患者中報告的丙氨酸轉氨酶(2名患者)和天冬氨酸氨基轉移酶(2名患者)和天冬氨酸轉氨酶(2名患者)反應快速、深層和持久的SD長達14個月以上 4/5名患者有持續的PR;在先前接受PD-1/PD-L1阻斷療法進展的患者中,Sotigalimab+Nivolumab的中位反應持續時間(DoR)未達到中位緩解持續時間(DoR)在公司贊助的試驗和IST中收集了來自超過500名患者的數據;IST數據積累在各種腫瘤類型中,包括轉移性黑色素瘤、胰腺瘤、腦癌、腎癌、結直腸癌和卵巢癌已暫停

即將舉行的會議 2024 年 5 月 14 日至 15 日在紐約舉行的 RBCCM 全球醫療保健會議 BTIG 虛擬生物技術會議 2024 年 8 月 5 日至 6 日在波士頓舉行的富國銀行醫療保健會議 4 份 AACR 摘要:PYX-201(抗 EDB)、PYX-106(抗 SIGLEC-15)、PYX-102(抗 KLRG1),2024 年 4 月 5 日至 10 日在聖地亞哥舉行 Stifel 虛擬靶向腫瘤日 2024 年 4 月 16 日至 17 日 2024 年 6 月 5 日至 6 日在紐約舉行的系列醫療保健會議

附錄 PYX-201 和 ADC 工具包 PYX-106 apxiMab 平臺和 Sotigalimab
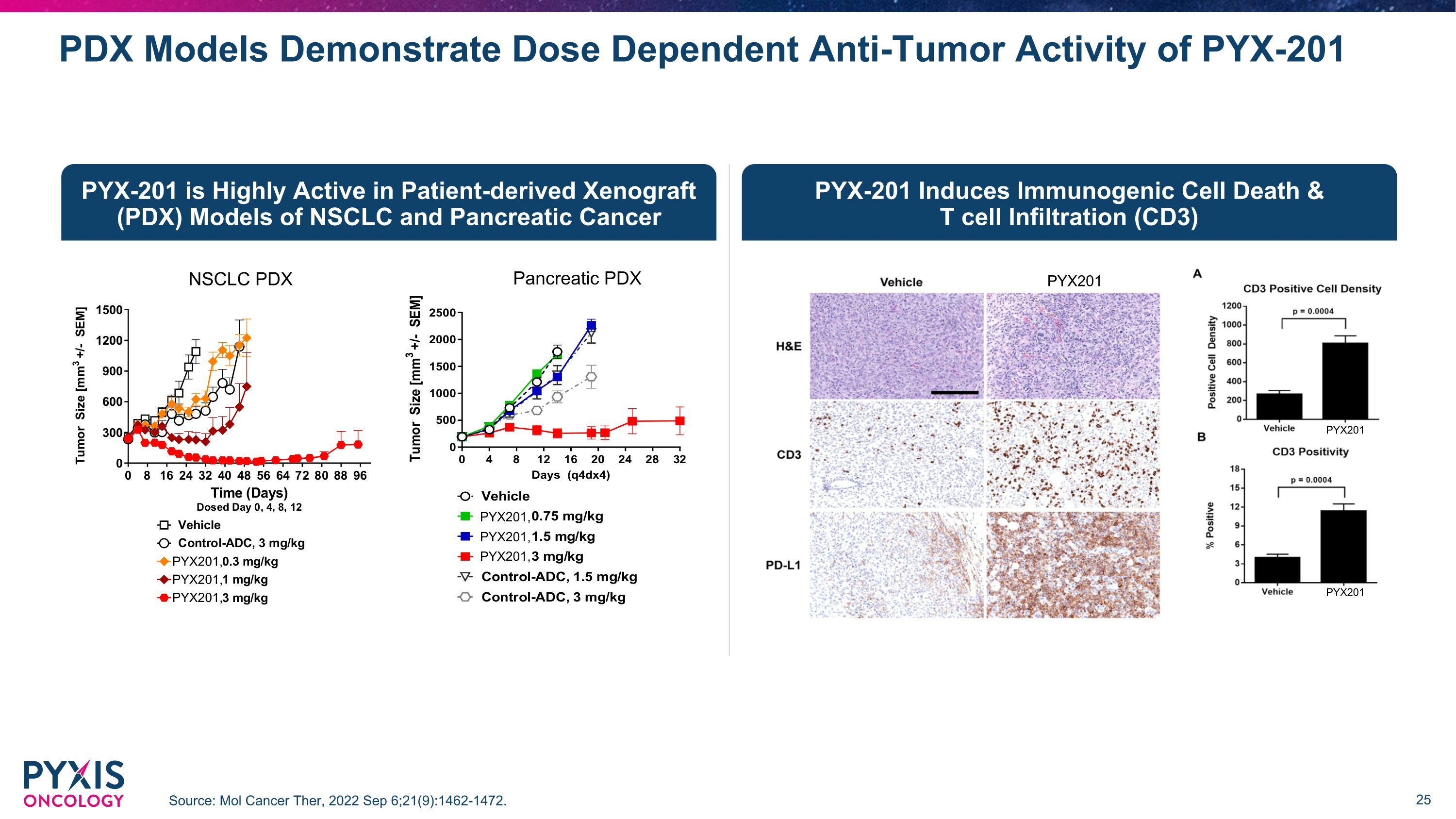
PYX-201 在 NSCLC 和胰腺癌的患者源性異種移植 (PDX) 模型中非常活躍 PYX-201 誘導免疫原性細胞死亡和 T 細胞浸潤 (CD3) PDX 模型顯示 PYX-201 的劑量依賴性抗腫瘤活性來源:Mol Cancer Ther,2022 年 9 月 6 日;21 (9): 1462-1472。PYX201 PYX201 PYX201 PYX201、PYX201、PYX201、胰腺 PDX PYX201、PYX201、PYX201、NSCLC PDX
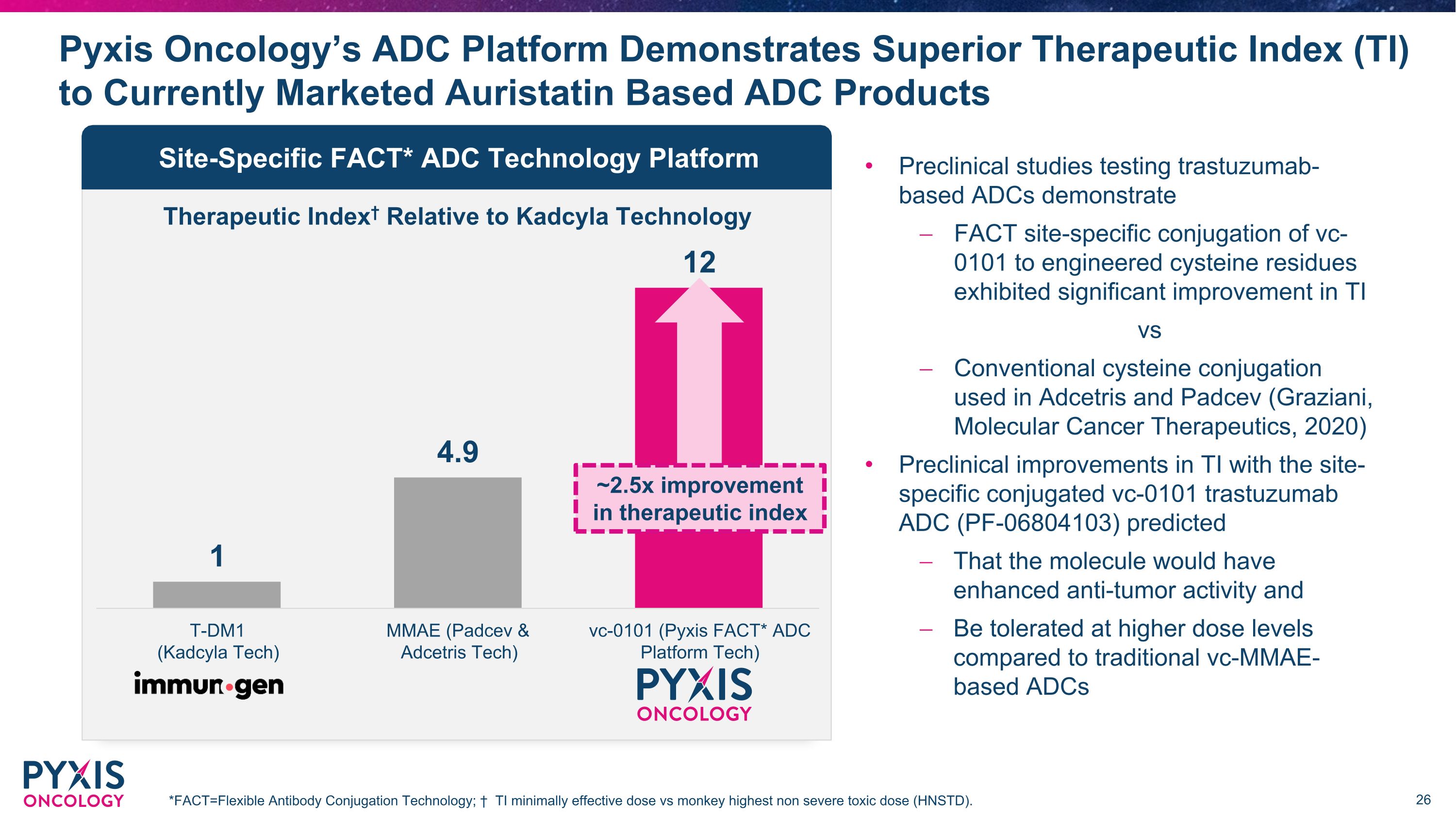
相對於Kadcyla Technology的治療指數,Pyxis Oncology的ADC平臺顯示出優於目前上市的基於奧瑞他汀的ADC產品的治療指數(TI)*fact=靈活的抗體偶聯技術;與猴子最高非重度毒性劑量(HNSTD)相比,TI 的有效劑量最低。位點特異性 FACT* ADC 技術平臺治療指數提高了約 2.5 倍測試曲妥珠單抗藥物的臨牀前研究表明,與Adcetris和Padcev(Graziani,《分子癌療法》,2020年)使用位點特異性偶聯vc-0對TI進行臨牀前改進,與Adcetris和Padcev(Graziani,《分子癌療法》,2020年)與位點特異性偶聯vc-0相比,TI 的臨牀前改進 101 曲妥珠單抗ADC(PF-06804103)預測該分子具有增強的抗腫瘤活性,並且在更高的條件下耐受性與傳統的基於 VC-MMAE 的 ADC 相比的劑量水平
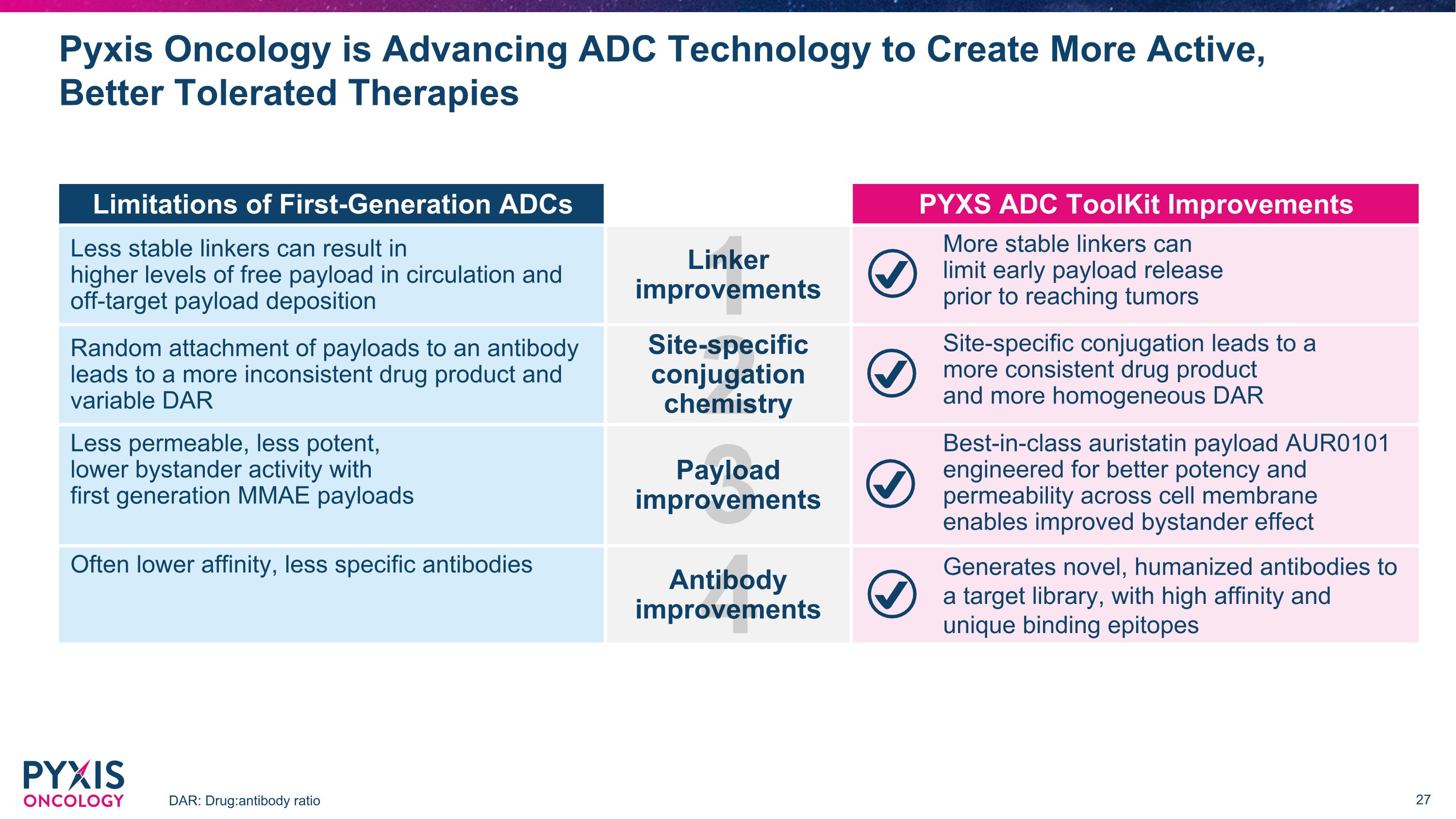
Pyxis Oncology正在推進ADC技術以開發更活躍、更耐受的療法 DAR:藥物:抗體比率第一代 ADC 的侷限性 PYXS ADC 工具包的改進不太穩定的連接劑會導致更高的循環中自由載荷水平和脱靶載荷沉積連接器的改進更穩定的連接劑可以在到達腫瘤之前限制有效載荷的早期釋放。隨機附着在抗體上會導致藥物產物更加不一致和 DAR 位點特異性偶聯化學變化不定特定位點的偶聯導致更穩定的藥物產品和更均勻的 DAR 採用第一代 MMAE 有效載荷的滲透性更低、效力更低、旁觀者活性更低有效載荷改進一流的奧瑞他汀有效載荷 AUR0101 專為提高細胞膜的效力和滲透性而設計可改善旁觀者效應通常較低親和力、特異性抗體改進向靶庫生成具有高親和力和獨特結合表位的新型人源化抗體 1 2 3 4
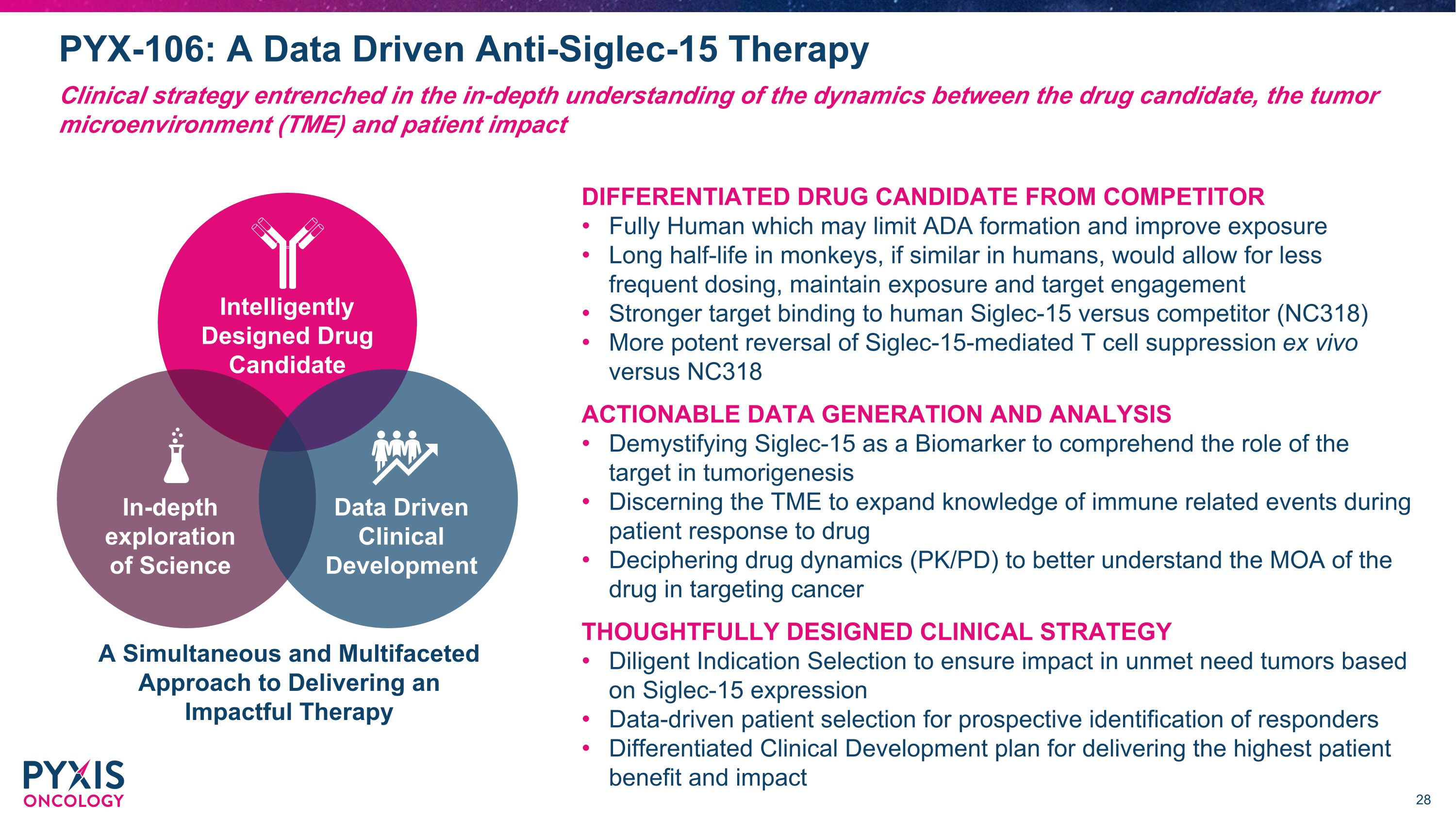
PYX-106:數據驅動的抗Siglec-15療法臨牀策略根深蒂固於對候選藥物、腫瘤微環境(TME)和患者影響之間動態的深入理解,與競爭對手的全人類區分開來,這可能會限制ADA的形成並改善暴露猴子的半衰期,如果人類相似,則可以減少給藥頻率,保持暴露和靶向參與度與人Siglec-15的結合力強於競爭對手(NC318)更有效的逆轉 siglec-15 介導的 T 細胞抑制 ex體內與 NC318 的可操作數據生成和分析揭開 Siglec-15 作為生物標誌物的神祕面紗,以理解靶標在腫瘤發生中的作用辨別 TME 以擴大患者對藥物反應期間的免疫相關事件的瞭解解密藥物動力學 (PK/PD) 以更好地瞭解該藥物在靶向癌症方面的MOA 精心設計的臨牀策略勤奮的適應症選擇,確保根據未滿足的腫瘤產生影響 Siglec-15 表達數據驅動的患者選擇用於前瞻性識別應答者差異化為患者提供最高收益和影響力的臨牀開發計劃提供有影響力的療法的同步和多方面的方法深入探索科學數據驅動的臨牀開發智能設計的候選藥物
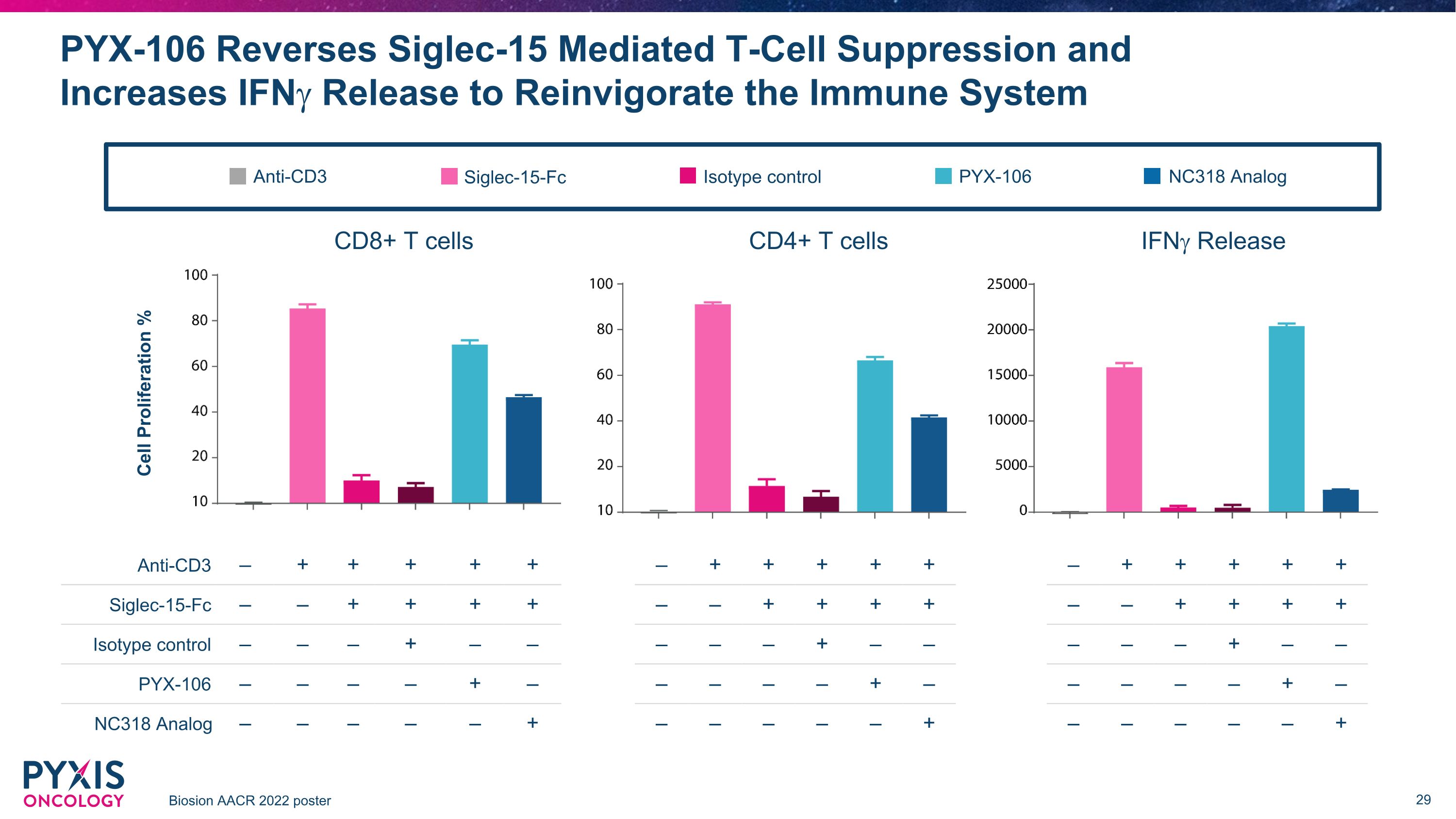
PYX-106 逆轉 Siglec-15 介導的 T 細胞抑制並增加 IfNG 釋放以重振免疫系統 Biosion AACR 2022 海報 CD8+ T 細胞 CD4+ T 細胞 iFnG 釋放抗 CD3 — + + + + Siglec-15-Fc — — — + + 同型控制 — — — — — — + NC318 模擬 — — — — — + 細胞增殖% — — — + + + + — — + + + + — — — — — — — — — — — — — — — — — — — — — — — — — + — + + + + — — + + + — — — — — — — — — — — — — — — — — — — — — + 抗CD3 Siglec-15-Fc同型控制 PYX-106 NC318 模擬 PYX-106
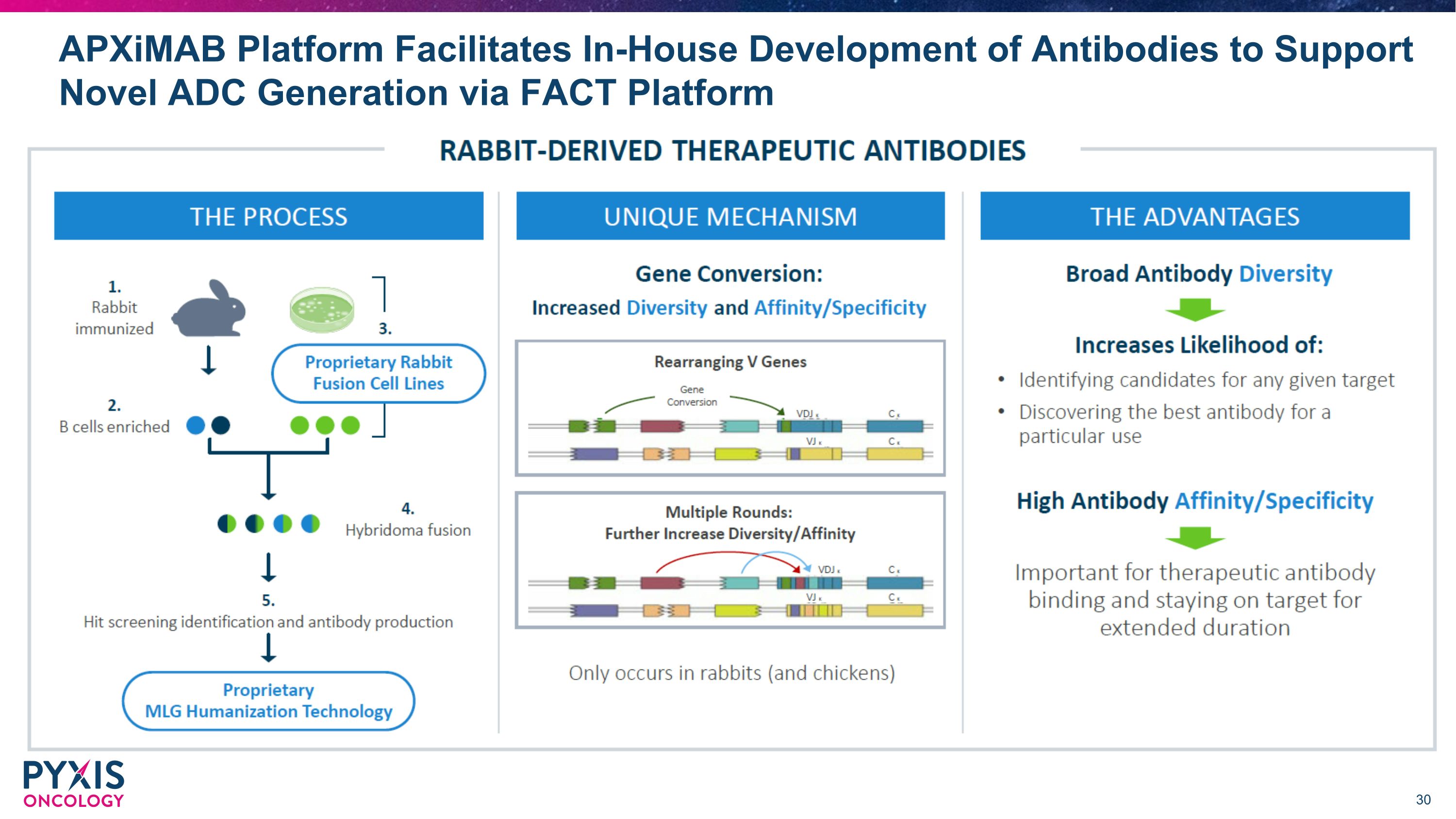
Apximab 平臺促進抗體的內部開發,支持通過 FACT 平臺生成新型 ADC
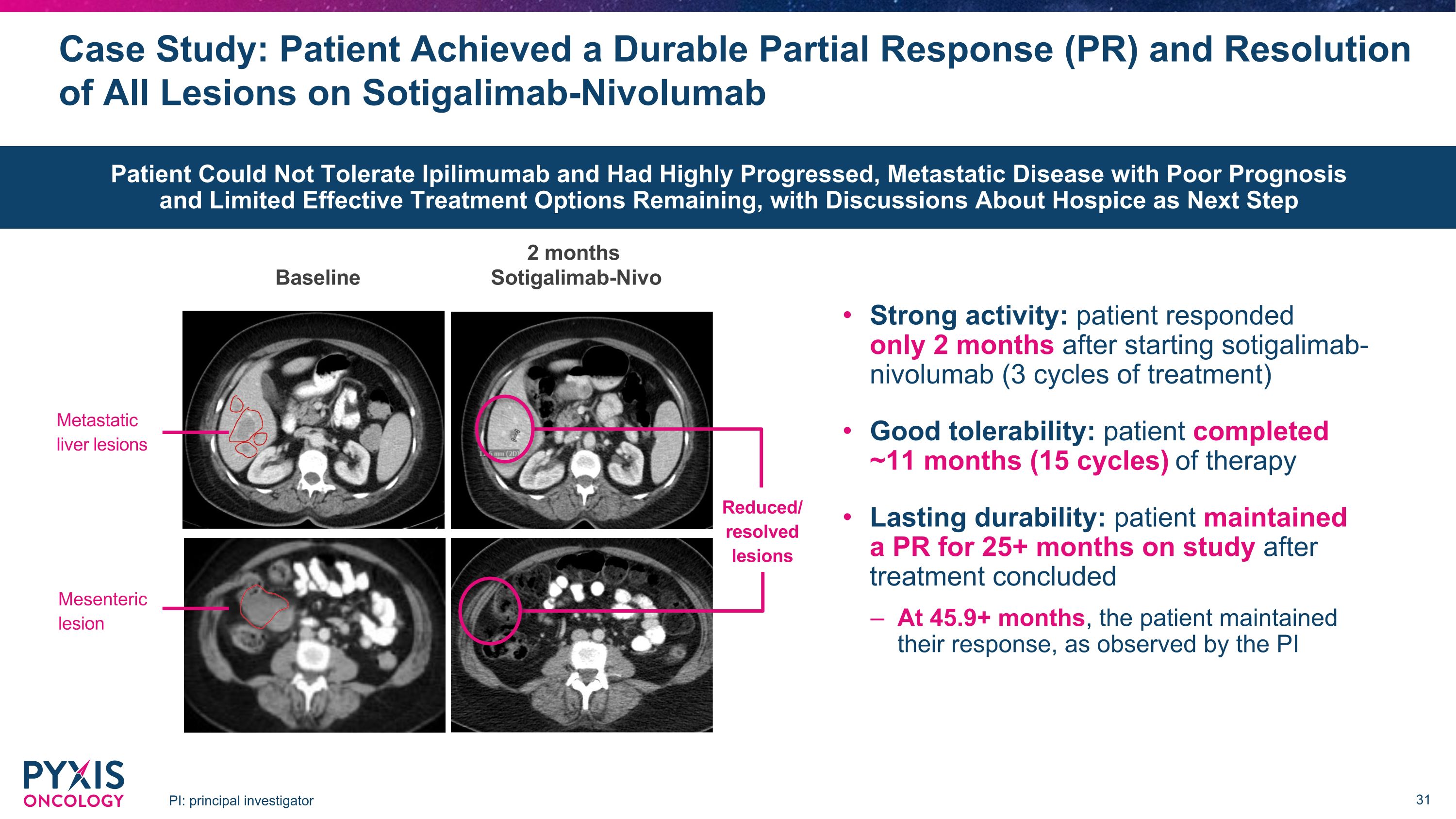
案例研究:患者在使用Sotigalimab-Nivolumab PI時實現了持久的部分反應(PR)和所有病變的緩解:首席研究員 2 個月基線 Sotigalimab-Nivo 活性強:患者在開始索替加利單抗僅兩個月後才出現反應(3 個週期)耐受性良好:患者完成了大約 11 個月(15 個週期)的治療持續時間:患者維持了 PR 25+ 治療結束後數月的研究表明,在45.9個月以上的時候,患者維持了反應,如PI減少/消退的病變轉移所觀察肝臟病變腸繫膜病變患者無法耐受Ipilimumab且進展良好,轉移性疾病預後不佳,有效治療選擇有限,下一步將討論臨終關懷問題
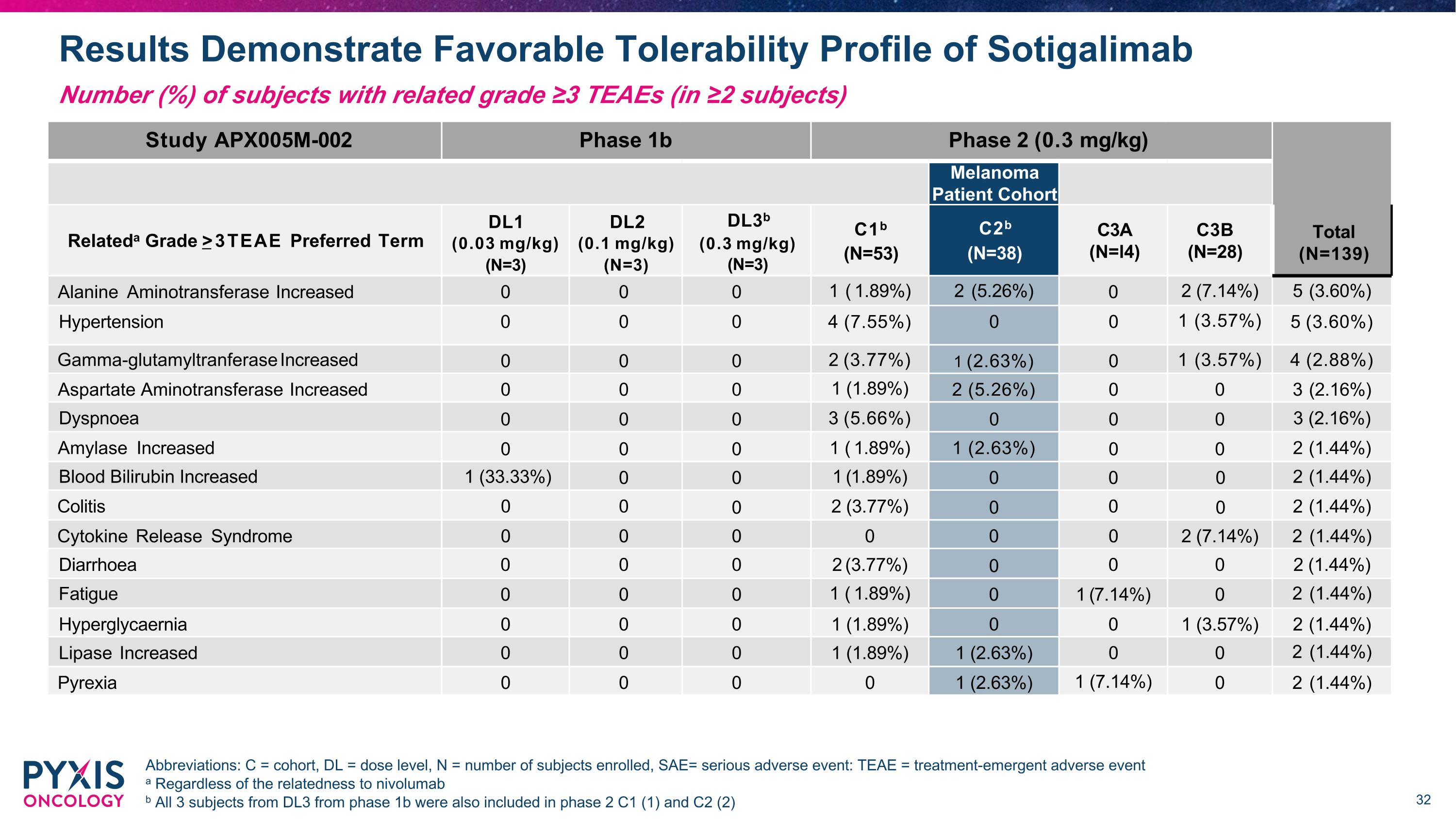
結果顯示Sotigalimab具有良好的耐受性簡稱:C = 隊列,DL = 劑量水平,N = 入組受試者數量,SAE= 嚴重不良事件:TEAE = 治療緊急不良事件 a 無論與 nivolumab 的相關性如何,1b 期 DL3 的所有 3 名受試者也被納入第 2 期 C1 (1) 和 C2 (2) 受試者人數 (%) 相關等級 ≥3 TEAE(在 ≥ 2 名受試者中)研究 APX005M-002 1b 期 2 期(0.3 mg/kg)總計(N = 139)黑色素瘤患者隊列相關等級 > 3 TEAE 首選術語 DL1(0.03 mg/kg)(N = 3)DL2(0.1 mg)/kg) (N=3) DL3b (0.3 mg/kg) (N=3) C1b (N=53) C2b (N=38) C3A (n=L4) C3B (N=28) 丙氨酸氨基轉移酶升高 0 0 0 1 (1.89%) 2 (7.26%) 0 2 (7.14%) 5 (3.60%) 高血壓 0 0 0 4 (7.60%) 55%) 0 0 1 (3.57%) 5 (3.60%) gamma-谷氨酰轉移酶增加 0 0 0 2 (3.77%) 1 (2.63%) 0 1 (3.57%) 4 (2.88%) 天冬氨酸氨基轉移酶增加 0 0 0 1 (1.89%) 2 (5.26%) 0 3 (2.16%) 呼吸困難 0 0 0 0 3 (5.66%) 6%) 0 0 0 3 (2.16%) 澱粉酶增加 0 0 0 1 (1.89%) 1 (2.63%) 0 0 2 (1.44%) 血液膽紅素增加 1 (33.33%) 0 0 1 (1.89%) 0 0 2 (1.44%) 0 0 2 (1.44%) 結腸炎 0 0 0 2 (3.77%) 0 0 00 2 (1.44%) 細胞因子釋放綜合徵 0 0 0 0 0 2 (7.14%) 2 (1.44%) 腹瀉 0 0 0 2 (3.77%) 0 0 2 (1.44%) 疲勞 0 0 0 1 (1.89%) 0 1 (1.89%) 0 1 (7.14%) 0 2 (1.44%) 高甘油 0 0 0 1 (1.89%) 0 0 1 (3.559%) 0 1 (3.559%) 0 1 (3.559%) 0 1 (3.559%) 0 1 (3.554%) 7%) 2 (1.44%) 脂肪酶增加 0 0 0 1 (1.89%) 1 (2.63%) 0 0 2 (1.44%) Pyrexia 0 0 0 0 1 (2.63%) 1 (7.14%) 0 2 (1.44%) 1 (7.14%) 0 2 (1.44%)
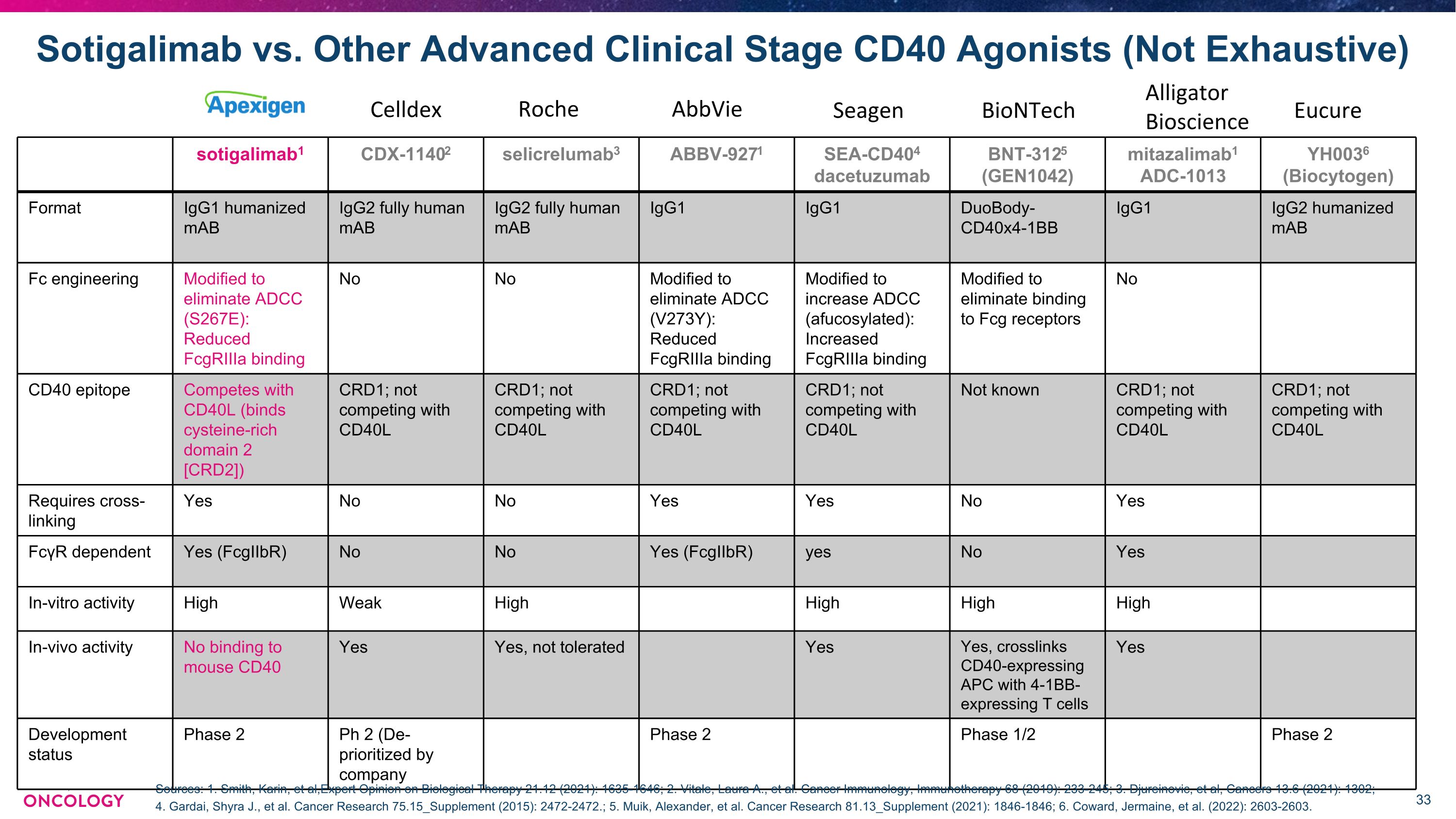
Sotigalimab 對比其他高級臨牀階段 CD40 激動劑(未窮盡)sotigalimab1 CDX-11402 selicrelumab3 ABBV-9271 SEA-CD404 dacetuzumab BNT-3125 (GEN1042) mitazalimab1 ADC-1013 YH0036(Biocytogen)格式 igG1 人源化單抗 IgG2 完全人源化 IgG2 完全人源化 IgG1 iGG1 duoBody-40x4-fully 1bb IgG1 IgG2 人源化單抗 Fc 工程經過改良以消除 ADCC (S267E):降低 fcgriIIA 結合無修飾以消除 ADCC (V273Y):降低 fcgriiia 結合以提高 ADCC(afucosylated):增加 fcgriIIA 結合改性以消除結合到 Fcg 受體沒有 CD40 表位與 CD40L 競爭(結合富含半胱氨酸的結構域 2) [CRD2]) CRD1;不與 CD40L CRD1 競爭;不與 CD40L CRD1 競爭;不與 CD40L CRD1 競爭;不與 CD40L 競爭未知 CRD1;不與 CD40L CRD1 競爭;不與 CD40L 競爭需要交聯是否是否是的依賴於 FcγR 是 (fcGIIBR) 不是 (fcGIIBR) 是的體外活性高弱高高內高 Vivo 活性不與小鼠 CD40 結合是的,不可耐受是的,表達 CD40 的 APC 與表達 4-1bb 的 T 細胞交聯是的發育狀態 2 期 Ph 2(由公司取消優先級 2 階段 1/2 期)第 2 階段 Celldex Roche AbbVie Seagen BioNTech Alligator Bioscience Eucure 來源:1.Smith、Karin等人,《生物療法專家意見》21.12(2021):1635-1646;2.Vitale、Laura A. 等癌症免疫學,免疫療法 68(2019):233-245;3.久雷諾維奇等人,《癌症》13.6(2021):1302;4。Gardai、Shyra J. 等癌症研究 75.15_補編(2015):2472-2472。;5.Muik、Alexander 等。癌症研究 81.13_增刊(2021):1846-1846;6.科沃德、傑梅因等人(2022年):2603-2603。