
投資者演講

前瞻性陳述本演示文稿包括1995年《私人證券訴訟改革法》所指的前瞻性陳述,包括有關Biohaven Ltd.(“公司”)以及我們計劃和正在進行的 BHV-2100、troriluzole、BHV-5500、BHV-1100、Taldefgrobep Alfa、BHV-8000、BHV-7000 和 BHV-7010 開發計劃的試驗、臨牀試驗數據的時間和可用性、進行的時機和決定的陳述我們計劃提交的監管文件、獲得監管的時間和能力我們的候選產品的批准,我們的候選產品的臨牀潛在效用,無論是單獨還是與其他現有潛在治療方案相比,以及我們的早期項目(包括ARM™、MATE™、MODE™、TRPM3、UC1MT、TYK2/JAK1和Kv7)的潛在進展。使用某些詞語,包括 “繼續”、“計劃”、“將”、“相信”、“可能”、“期望”、“預期” 和類似表述,旨在識別前瞻性陳述。投資者請注意,任何前瞻性陳述,包括有關我們的候選開發項目的未來發展、時機和潛在的上市批准和商業化的陳述,都不能保證未來的業績或業績,並涉及重大風險和不確定性。由於各種因素,實際結果、發展和事件可能與前瞻性陳述中的結果存在重大差異,包括:Biohaven計劃和正在進行的臨牀試驗的預期時間、開始和結果;計劃與美國食品藥品監督管理局進行互動和申報的時機;預期監管申報的時間和結果;遵守適用的美國監管要求;Biohaven候選產品的潛在商業化;Biohaven候選產品成為第一的可能性一流或一流的療法;以及Biohaven候選產品的有效性和安全性。因此,您不應依賴這些前瞻性陳述來代表我們在本演講之日之後的任何日期的觀點。公司向美國證券交易委員會提交的文件中描述了與前瞻性陳述相關的其他重要因素,包括標題為 “風險因素” 和 “管理層對財務狀況和經營業績的討論和分析” 的章節。本演示文稿還包含基於行業出版物、市場研究公司的報告或已發佈的獨立來源的市場數據和其他信息。一些市場數據和信息也基於公司的誠信估計,這些估計來自管理層對該行業的瞭解以及上述獨立來源。Biohaven | 投資者演示文稿2023年9月2日

輝瑞以130億美元收購CGRP平臺

高價值平臺創新產品組合久經考驗的商業模式追求新的科學路徑以改變神經系統和神經精神疾病的治療方式內部科學專業知識以實現廣泛的治療產品組合,有意滿足患者需求的持續增長配方建立在經驗豐富的團隊過去的成功以及堅定不移地專注於為患者和股東創造價值的基礎上

臨牀前 1 期 2 期 3 期離子通道:Kv7 激活劑 Kv7 離子通道:TRPM3 抑制劑 TRPM3 炎症:TYK2/JAK1 抑制劑 TYK2/JAK1 穀氨酸平臺 TRORILUZOLE 肌抑素平臺雙特異性靶向細胞療法 CD-38 DISCOVERY RESEARCH IgG 降解劑下一代 ADC 平臺 | BHV-4157 強迫症 BHV-2000 | 脊柱肌萎縮 BHV-1100 | 多發性肌萎縮 eloma BHV-7000 | 癲癇、雙相情感障礙 BHV-1300 | 免疫介導疾病 BHV-7010 | 癲癇、情緒障礙 BHV-2100 | 慢性疼痛症 IgA腎病腫瘤學 BHV-8000 | 神經炎症性疾病 BHV-2000 | 代謝性疾病 2023 年 9 月 Biohaven | 投資者演示文稿5

Kv7 平臺廣泛適用於癲癇以外的過度興奮障礙 Kv7.1:心臟 Kv7.2:中樞神經系統 BHV-7000 激活劑 Kv7.3:中樞神經系統 BHV-7000 激活劑 Kv7.4:平滑肌和內耳 Kv7.5:血管組織、神經元、骨骼 Stria Vascularis 皮質血管組織器官胃腸道 Adnetitia Media Intima 內耳心臟肌肉神經元軸突起始節點 Vier Synapse Serosa 肌肉層 Mucosa Subcosa 5 FAMILY SUBTYPES 主要定位:膀胱來源:改編自 Soldovieri 等人。生理學. 2011; 26 (5): 365-376。2023 年 9 月 Biohaven | 投資者演示文稿6

美國350萬癲癇患者仍有大量未得到滿足的需求在開始ASM後,80%的患者經歷了沉重的不良事件,其中可能包括:• 嗜睡 • 頭暈 • 認知功能障礙 • 儘管有抗癲癇藥物(ASM)、手術和飲食改良,但情緒障礙仍有80%的人難治性治療 Devinsky等人。Nat Rev Dis Primers。2018;4:18024;Kanner,Bicchi。JAMA. 2022; 327 (13): 1269-1281。2023 年 9 月 Biohaven | 投資者演示文稿7

BHV-7000 對光氧化具有化學穩定性 BHV-7000 對 Kv7 的選擇性優於 GABAA 受體 a BHV-7000 在臨牀前具有廣泛的治療指數第一和第二代 Kv7 激活劑顯示出臨牀抗驚厥 POC,但脱靶活性,第三代 Kv7 分化的機會 XEN1101 • XEN1101 和依佐加濱在體外 GABAA 受體變構活化劑明顯優於 BHV-7000 • GABAA 受體激活 somnola:眩暈、疲勞、複視 Ezogabine XEN1101 BHV-7000 G A B A A ct iv at io n a (% B as el in e) 0 20 40 60 GABAA Posi五種變構調製% In cr ea sef om b as el in e e 10 µM BHV-7000 10 µM EZO 10 µM XEN1101 ✱✱ ✱✱ 0 20 40 60 GABAA 陽性變構調製% In cr ea sef om b as el in e e 10 µM EZO 10 µM XEN1101 ✱✱ ✱✱ ** ** ** 與 BHV-7000 顯著不同,均在 10 µM 埃佐加賓下進行測試 • 暴露於時不穩定光 • 皮膚變色標籤警告 • 視網膜異常/視力喪失黑箱警告 FDA 藥物安全通訊:Potiga(依佐加濱)BHV-7000 [04-26-2013]BHV-7000 • Kv7 通道的強效激活劑 • 在臨牀前癲癇發作分析中有效且耐受性良好 Th er ap eu tic In de x ezogabineb xen1101b bhv-7000a 10 20 30 40 50 Kv7 Biohaven | 投資者演示8 a. Biohaven存檔數據(2022年)。b. 按 TD50(旋轉木馬)與 ED50(MES 發作檢測)數據的比率計算作者:Xenon 在舊金山癲癇基金會管道會議(2018 年 2 月)上。臨牀前結果從單獨的報告中合併並繪製成圖表。提供的數據不是任何正面交鋒臨牀試驗的結果,並不意味着或表明 BHV-7000 在臨牀上更安全和有效。2023 年 9 月

大鼠 Rotarod BHV-7000:臨牀開發中首款專為排除 GABAA 受體激活而設計的 Kv7.2/7.3 活化劑 BHV-7000 在有效劑量範圍內觀察到對運動功能沒有影響 Ti m e to ll——R ot ar od Vehicle 0.3 1 3 10 30 0 50 100 150 150 250 BHV-7000 (mg/kg) 於 2023 年 3 月 13 日至 15 日在 2023 年美國實驗神經治療學會 (ASENT) 年會上發表。EC50,最大有效濃度的一半;EZO、ezogabine 100 80 60 50 40 27 20 4 0 XEN1101 Ezogabine Rotarod MES m g/ kg * 改編自 https://www.xenon-pharma.com/wp-content/uploads/2018/05/XEN1101_EILAT_15May2018_FINAL_YPG_web.pdf BHV-7000 Ezogabine *鼠標 ED50 或 TD50(平均置信區間 95%)2023 年 9 月 Biohaven | 投資者演示9

BHV-7000 展現出高度差異化的臨牀前概況 Biohaven | 投資者演示10 Wide 治療指數 Kv7.2/7.3 激活劑 GABAA 活性 “減弱” 依佐加濱 XEN1101 BHV-7000 活性激活劑、臨牀和臨牀前抗癲癇活性激活劑、臨牀和臨牀前抗癲癇活性激活劑 GABAA 活性目前可忽略不計 GABAA 活性可忽略不計 40xb

BHV-7000:在 1 期 SAD/MAD 隊列中耐受性良好 medDRA 系統器官類安慰劑 (N=15) n (%) BHV-7000 (N=46) n (%) 神經系統疾病 1 (6.7) 7 (15.2) 胃腸道疾病 1 (6.7) 6 (13.0) 肌肉骨骼疾病 0 5 (10.9) 感染 0 2 (4.3) 調查 1 (6.7) 2 (4.3) 呼吸系統疾病 0 2 (4.3) 4.3) 皮膚疾病 0 2 (4.3) 眼部疾病 0 1 (2.2) 一般疾病 0 1 (2.2) 程序併發症 1 (6.7) 1 (2.2) 精神疾病 0 1 (2.2) 腎臟疾病 1 (6.7) 1 (2.2) 腎臟疾病 1 (6.7) 1 (2.2) 安全性和耐受性無 SAE 沒有嚴重的 TEAE,1中度 TEAE,其餘 TEAE 的嚴重程度為輕度劑量 SAD:單劑量高達 100 mg MAD:多劑量每日最多 40 mg x15 天 2023 年 9 月 MES 臨牀前發作模型暴露量超過 EC50 Biohaven | 投資者演示11

BHV-7000:按劑量和隊列劃分的第 1 階段 SAD/MAD 中樞神經系統 TEAE Aesa 安慰劑 N=10 4 mg N=6 10 mg N=6 25 mg(快速)N=6 25 mg(Fed)N=6 25 mg(Fed)N=6 50 mg N=6 100 mg N=5 BHV-7000 總體 N=29 頭痛 0 0 1 (16.7) 0 1 (16.7) 0 3 (10.3) 頭暈 0 0 1 (16.7) 0 0 0 0 0 0 1 (3.4) 肌陣攣 0 0 0 1 (16.7) 0 0 0 1 (3.4) CNS AeSA 安慰劑 N=5 10 mg N=5 25 mg N=6 40 mg N=6 BHV-7000 總體 N=17 頭痛 1 (20.0) 0 0 3 (17.6) 單次上升劑量 Ameddra® “神經系統疾病” 系統器官類別中的首選術語 Ameddra® Preferred系統器官類別 “神經系統疾病” 中的術語 2023 年 9 月 Biohaven | 投資者演示文稿12 1.頭痛事件被歸類為輕度頭痛

BHV-7000:與其他 ASM 典型的中樞神經系統不存在關聯 80% 的患者在開始 ASM1 後會出現不良反應。其他 ASM 激活的 GABAA 通路與嗜睡和頭暈等不良反應相關2 幾種 ASM 會導致行為(易怒、憤怒、攻擊性)或精神疾病(抑鬱情緒、焦慮、精神病)AES3,4 Pooled CNS AESA,5 BHV-7000 MAD Pooled N=17 Somnolence 0% 頭痛 18% 平衡障礙 0% 頭暈 0% 記憶障礙 0% 感覺障礙 0% 言語障礙 0% Xen1101 MAD Pooled N=18 39% 39% 17% 17% 28% 11% 33% Ameddra® 首選術語屬於系統器官類別 “神經系統疾病” 提供的數據不是任何正面臨牀試驗的結果,也不意味着或表明 BHV-7000 在臨牀上更安全和有效。5 Devinsky 等人。Nat Rev Dis入門。2018;4:18024. 2.Abou-Khalil。Continuum(明尼蘇達州明尼阿普)。2022;28 (2): 500-535. 3.斯坦霍夫等人。癲癇行為 2021; 123:108270. 4.陳等癲癇行為。2017;76:24-31。5. 2019 年第 73 屆美國癲癇協會年會,摘要 #3 .31。海報於 2019 年 11 月 25 日發佈。AE,不良事件;ASM,抗癲癇藥物;中樞神經系統;GABA,γ-氨基丁酸;MAD,多次遞增劑量;medDRA,監管活動醫學詞典 2023 年 9 月 Biohaven | 投資者演示13

BHV-7000:摘要和臨牀項目現狀 • Kv7.2/Kv7.3 鉀離子通道的強效選擇性激活劑 • 結構/藥理學上與其他 K+ 通道激活劑不同 • 設計用於 “抑制” GABAA 受體激活,提高耐受性 • 在 MES 癲癇模型中有效,無不良神經行為或運動影響 • 在 1 期 SAD/MAD 研究中耐受性良好 • 腦電圖研究;初始 1 期結果證實了低和高的靶點參與度 BHV-7000 劑量,預計在 2023 年有完整結果 • 每日一次緩釋配方劑量有是癲癇治療中缺失的部分,用於耐受性更好、更有效的抗癲癇藥物 1 期腦電圖 2/3 期局灶性癲癇第 1 期 SAD/MAD 中樞神經系統,中樞神經系統;腦電圖;GABA,伽瑪氨基丁酸;MAD,多次遞增劑量;MES,最大電擊發作;SAD,單次遞增劑量 202314 年 9 月 Biohaven | 投資者演示
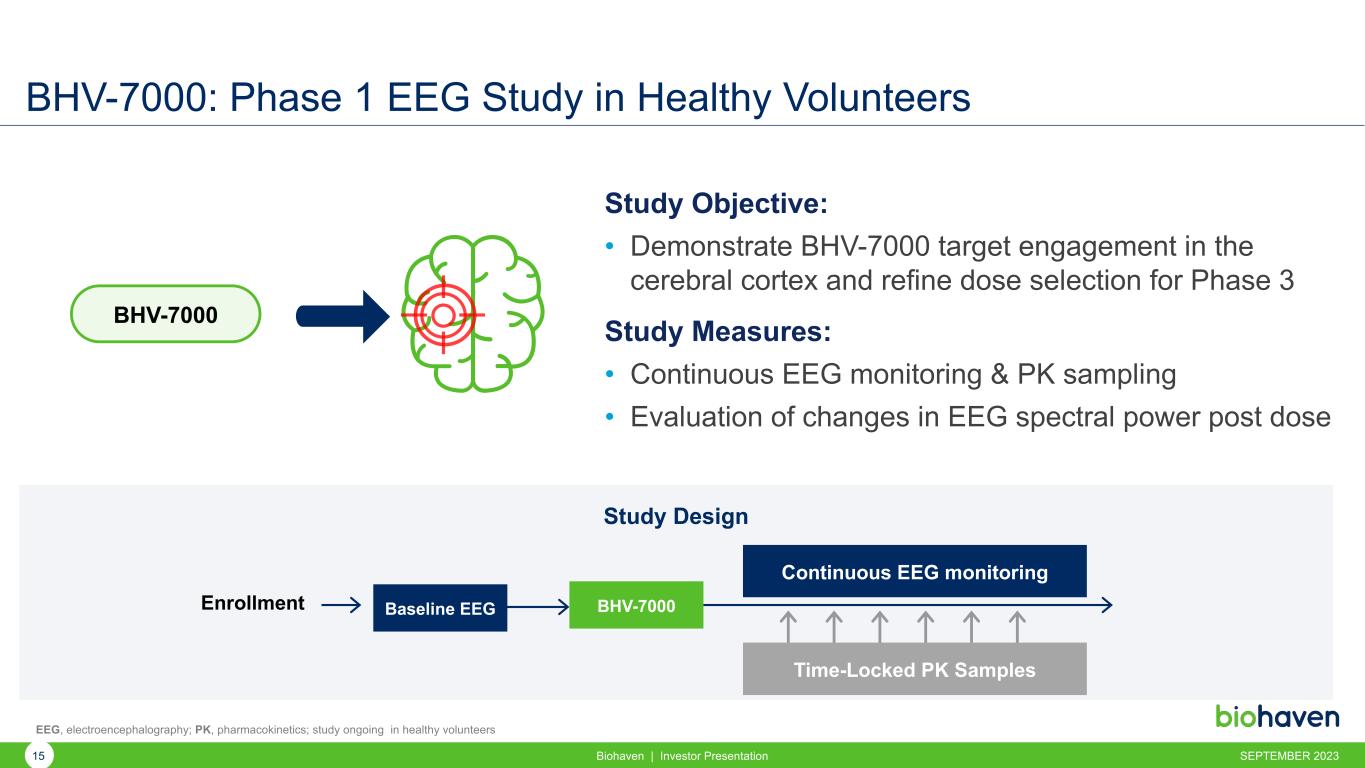
BHV-7000:健康志願者的 1 期腦電圖研究研究目標:• 證明 BHV-7000 靶點參與大腦皮層並完善第 3 期研究的劑量選擇措施:• 持續的腦電圖監測和 PK 採樣 • 評估給藥後腦電圖譜功率的變化設計基準腦電圖持續腦電圖監測入學時間鎖定 PK 樣本 BHV-7000 BHV-7000 腦電圖,腦電圖;PK,藥代動力學;研究正在健康志願者中進行 2023 年 9 月 Bio315 Haven | 投資者演示文稿

藥物濃度 >EC50 的受試者在給藥後服用 10 mg 劑量 BHV-7000 後,觀察到腦電圖譜功率在 β 和 Gamma 波段上會增加 G AM M A BE TA AL PH A ET A D EL TA FR E Q U N N D S E E E G S E E G S P E C TR A L P O W E R BHV-7000:10 mg 劑量後觀察到的光譜功率變化 ≥ EC50 Biohaven | 投資者演示16 *EC50 基於臨牀前最大電擊發作 (MES) 模型,在服用 10 mg 劑量 BHV-7000 後,所有頻段的腦電圖光譜功率均未發生變化有藥物濃度的受試者

BHV-7000:2023 年 9 月劑量 50 mg 後,觀察到所有頻段和所有大腦區域的光譜功率均有所增加 Biohaven | 投資者演示17 熱點新聞報道 50 mg 劑量 BHV-7000 後,觀察到所有頻段的腦電圖譜功率均有所增加,表明中樞神經系統目標參與度 G AM M A BE TA AL PH A TH 等於 D EL TA FR EQ U N EC Y BA N D S EEG SPEC TR AL PO W ER PREDOSE 劑量後

BHV-7000:2023 年 9 月穩定狀態下 25 mg ER、50 mg ER、75 mg ER 的平均預測濃度與 BHV-7000 延期釋放 (ER) 的時間分佈對比 Biohaven | 投資者演示18 *EC20 和 EC50 值來自臨牀前最大電休克發作 (MES) 模型 M ea n Pr ed ic te d BH V-70 00 C on ce no tio n at S te and y St ER QD 50 mg ER QD 75 mg ER QD 預測平均值 BHV-7000 濃度 MES EC50 MES EC50 MES EC20

BHV-7000:局灶性癲癇的三期試驗兩項多中心、國際、安慰劑對照、雙盲研究,旨在評估 BHV-7000 對難治性局灶性癲癇青少年和成人的療效隨機 1:1:1 雙盲 8 期和 12 周延期研究 1 年以上安慰劑 25 mg 持續劑量水平關鍵納入標準:• 12-75 歲 • 難治性局灶性癲癇主要終點:變化中位數(美國),≥ 50% 反應者率(歐盟): QOLIE-31,發作自由 QOLIE-31,《癲癇生活質量清單》;計劃中2023 年 9 月 3 期試驗的研究設計 Biohaven | 投資者演示文稿 19 篩查/觀察階段隨機分配 1:1:1 Placeb 75 mg 50 mg 繼續劑量水平用於評估 BHV-7000 50 mg 的安全性、耐受性和療效

Kv7 平臺摘要新型Kv7活化劑的專有化學庫內部合成具有差異化的藥理和結構特徵並可能出現多種適應症 Kv7.2/7.3 激活經過臨牀驗證的癲癇作用機制 BHV-7000:潛在的差異化臨牀前數據表明,通過撥出GABA風險(嗜睡、鎮靜、頭暈),臨牀治療指數很廣 BHV-7000 系列 COM 專利保護有效期至 2039 年(不包括延期)CE-Daily,緩釋配方已確定狀態更新 BHV-7000 在 1 期 SAD/MAD 研究中耐受性良好 EEG 生物標誌物研究 3 期癲癇和雙相情感障礙研究中證實中樞神經系統靶標參與度預計於 2023 年 9 月啟動 Biohaven | 投資者演示20

躁鬱症影響美國1100萬成年人雖然以躁狂症為特徵,但患者主要患有抑鬱症,但幾乎沒有有效的BPD和維持治療選擇1-4 ~ 50% 的患者不堅持服藥;停藥通常是由於耐受性差4,5~ 50% 除抗精神病藥物外,過去20年沒有批准新的情緒穩定劑6 • 拉莫三嗪——最後一款獲批的新型情緒穩定劑;主要用於維持,療效有限急性抑鬱發作 • 使用當前情緒穩定劑(甲狀腺/腎臟)時觀察到嚴重不良反應功能問題、肝毒素、血小板減少、皮疹、SJS3,9) • 代謝功能障礙、體重增加和認知減緩的風險 • 依從性問題導致治療無效和復發風險5,7,8 20 年 1.Tondo 等人 Curr Neuropharmacol。2017;15 (3): 353-358。2.米勒等J Affect Disord. 2014;169(補編 1): S3-11. 3.卡瓦略等人。N Engl J Med. 2020; 383 (1): 58-66. 4.麥金太爾,卡拉布雷斯。Curr Med Res Opin. 2019; 35 (11): 1993-2005. 5.賈瓦德等人Ther Adv Psychopharmacol。2018;8 (12): 349-363。6.Rhee 等人Am J Psychiatry. 2020; 177 (8): 706-715. 7.馮等J Affect Disord. 2019;257:17-22。8.馬爾扎尼,內夫。我是家庭醫生。2021; 103 (4): 227-239. 9.波波。Mayo Clin Proc. 2017;92 (10): 1532-1551。AE,不良事件;BD,躁鬱症 2023 年 9 月 Biohaven | 投資者演示21

雙相情感障礙治療中激活 Kv7 的令人信服的證據雙相情感障礙的重疊分子、細胞機制 ü ANK-3:雙相情感障礙中高度相關的基因;編碼一種將 Kv7 通道錨定到細胞膜的蛋白質1 ü Kv7.2/7.3 通道雙相情感障礙患者表現出幾種相關的表觀遺傳學變化,與 Kv73 躁狂和抑鬱症的臨牀前證據有關極 ü 上調 Kv7 的小鼠能夠抵禦壓力誘發的抑鬱效應4 ü 反向 Kv7 激活劑和預防抑鬱症和躁狂模型中的病理性多動症5,6 ü Kv7突變可導致跨診斷性情緒障礙,包括多動症、失眠、焦慮和認知功能障礙1 1 1。朱迪等Front Genet. 2013;4:87. 2.克里斯滕森等神經化學雜誌。2012;3:373-382。3.卡明斯基等人。雙相情感障礙。2015;2:150-159。4.弗裏德曼等Nat Commun. 2016; 24 (7): 11671. 5.登克爾等人Behav Brain Res. 2010;1:78-83。6.Redrobe 等人Behav Brain Res. 2009; 198 (2): 481-485。ANK-3,ankyrin 2023 年 9 月 3 日 Biohaven | 投資者演示22

BHV-7000:顯示出雙相情感障礙 Kv7 激活的臨牀轉化潛力 Kv 7. 2 Kv 7. 3 BHV-7000 Retigabine1 增加的 M 電流減少神經元多動症 Lamotrigine2 Lithium3 間接 BHV-7000 與基石雙極療法存在機制重疊之處(間接瑞替加濱對比安慰劑);通過 MADRS 和 fmri4,5 測得的 MDD 在抑鬱症改善中使用瑞替加濱的安慰劑降低 fMRI 研究:邊緣系統介導的作用抗精神病藥和鋰等藥物已在單極和單極中確立了療效雙相抑鬱症 Ezogabine 安慰劑 -0.4 -0.2 0.0 0.2 0.4 0.6 0.8 C 在 V S ac tiv at io n 中有 ng e 在 io n(o ut co m e > ba se lin e)0 1 2 3 4 5 -20 -15 -5 0 C 在 M AD R S sc 或 e 周 1 中有 ng e弗裏德曼等Nat Commun. 2016;24;7:11671. 2.弗裏德曼等科學. 2014; 344 (6181): 313-319. 3.克里斯滕森等神經化學雜誌。2012;3:373-382。4.阿曼等人J Clin Psychopharmacol. 2006;26 (5): 534-536。5.科斯蒂等人Am J Psychiatry。2021;178 (5): 437-446。fMRI,功能性磁共振成像;GSK3B,糖原合酶激酶 3 Beta;MADRS,蒙哥馬利-阿斯伯格抑鬱評級量表;MDD,重度抑鬱症強勁的初步急性療效可能轉化為躁鬱症 2023 年 9 月 Biohaven | 投資者演示文稿23

BHV-7000:通過減少與壓力相關的多動症,同時增強應變能力,有望滿足躁鬱症中未得到滿足的關鍵需求 • 患者在大約 2 個月後更換/停藥 • > 50% 的患者因不耐受在 6 個月時停藥1 ü 與目前的情緒穩定劑和抗精神病藥物相比具有良好的安全性和耐受性 • 一線情緒穩定劑需要滴定或頻繁的實驗室監測,給處方者和患者帶來負擔3 ü 不進行滴定/安全實驗室預期監測 • 療效微乎其微 • 處方廣泛抗抑鬱藥有 “轉換” 風險 ü 新機制——在沒有 “轉換” 風險的情況下可能產生強大的抗抑鬱作用 1.賈瓦德等人Ther Adv Psychopharmacol。2018;8 (12): 349-363。2.Vieta 等Nat Rev Dis入門。2018;4:18008. 3.亞瑟姆等人雙相情感障礙。2018; 20 (2): 97-170。2023 年 9 月 Biohaven | 投資者演示文稿24 BHV-7000目前批准的產品

BHV-7000:現有療法有可能克服挑戰,有可能實現同類最佳的耐受性和安全性 • 為患者和提供者帶來較低的負擔,可實現更安全、更簡便的長期治療 • 沒有預期的長期代謝副作用,沒有 “轉換” 風險,沒有滴定,也沒有藥物監測丙戊酸鋰 SSRI 抗精神病藥物拉莫三嗪代謝AEs肝AES 腎臟AES 皮疹/SJS 性SE鎮靜/認知AE藥物監測切換風險滴定 SJS,史蒂文斯-約翰遜綜合症患者負擔 2023 年 9 月 Biohaven | 投資者演示文稿25

TRPM3:神經病理性疼痛的新外周靶標口服類因體温過高而終止該類別中沒有新分子儘管有望終止多個 TRPA1 程序終止了促傷和抗傷害感受作用的數據相互矛盾;仍在活躍藥物開發中作為新靶標有望:在外周神經元中的表達範圍比 TRPV1 和 TRPA1 更廣泛;不太可能影響體温動態平衡外周感覺神經元疼痛 CGRP X??TRPV1 TRPA1 TRPM8 TRPM3 見 Koivisto 等人。Nat Rev Drug Discov. 2022;21 (1): 41-59,介紹TRP渠道藥物開發的背景。2021年:大衞·朱利葉斯和阿德姆·帕塔普提安因發現温度和壓力的細胞傳感器而獲得諾貝爾生理學或醫學獎 2023年9月Biohaven | 投資者演示26

TRPM3(BHV-2100)在化療和糖尿病神經病的臨牀前模型中減輕疼痛令人鼓舞的證據,如果沒有使用高劑量曲馬多/加巴噴丁 Biohaven 觀察到的鎮靜劑 Biohaven | 投資者演示27 BHV-2100 5 mg/kg BHV-2100 25 mg/kg BHV-2100 1 mg/kg 車輛 BHV-2100 1 mg/kg BHV-2100 25 mg/kg 普瑞巴林 30 mg/kg 加巴噴丁 150 mg/kg 5 mg/kg 車輛探索藥物給藥在大鼠中使用 STZ 誘導糖尿病 7 天后對小鼠進行奧沙利鉑治療 6 天后給藥來源:Biohaven 的相關數據 BHV-21002023 年 9 月檔案

分子特徵分子特徵預測了便捷、安全的分子和最佳的每日口服藥物靶產品特徵 BHV-2100:一種治療多種疼痛症的多功能藥物未滿足的神經病理性疼痛疾病的需求 > 50% 的常見神經病理性疼痛疾病(例如糖尿病周圍神經病變)患者即使使用了 2 種以上的藥物來控制疼痛也無法得到充分控制。臨牀前數據顯示,在多種可翻譯的動物模型中,疼痛有力的逆轉選擇性和強效選擇性而且 TRPM3 的強效抑制為神經病理性疼痛治療提供了一種新的非阿片類藥物治療方法 TRP 家族中的選擇性,避免了潛在的集體責任,例如計劃於 2023 年 9 月 2023 年下半年提交的體温過高研究性新藥申請 Biohaven | 投資者演示28

TYK2 (BHV-8000) 概述同類首創口服大腦穿透劑 TYK2/JAK1 抑制劑獨特強效的 TYK2/JAK1 選擇性腦穿透抑制劑打破神經炎症循環減少小膠質細胞、星形膠質細胞和浸潤性 T 淋巴細胞對多種神經炎症性疾病的潛在炎症影響有力的證據支持帕金森氏病、阿爾茨海默氏病、多發性硬化症和其他神經炎症性疾病的療效 BHV-8000 系列 COM 專利保護期至 2037 年(不包括延期)有利的 PK/PD 和選擇性概況避免與 JAK2/3 抑制相關的類別風險正在進行的 FIH 1 期臨牀試驗取得令人鼓舞的結果令人鼓舞 SAD/MAD 研究的 SAD 部分的多個隊列預計治療濃度達到 BHV-8000 耐受性良好,2023 年 9 月僅報告了輕微的不良事件 Biohaven | 投資者演示29

BHV-8000:神經炎症性疾病中的 TYK2/JAK1 • 雙重抑制 TYK2 和 JAK1 可有效阻斷 Th17 細胞生成、I 型幹擾素信號傳導和炎症 • JAK 抑制劑比抗腫瘤壞死因子更有效 JAK2JAK3JAK1 IFNγIL-6 TYK2 I 型幹擾素 IL-23 → IL-17 IL-12 IL-2、IL-4、IL-7 IL-9、IL-15、IL-21 促紅細胞生成素、GH,瘦素、血栓生成素、催乳素、GM-CSF 改編自 Gonciarz 等人。2021 年免疫療法; 13 (13): 1135-1150。GH,生長激素;GM-CSF,粒細胞巨噬細胞集落刺激因子;幹擾素;IL,白介素;JAK,Janus 激酶;STAT,信號轉換器和轉錄蛋白激活劑;TH,T輔助細胞;腫瘤壞死因子;TYK,酪氨酸激酶 2023 年 9 月 Biohaven | 投資者演示30

神經炎症中的細胞驅動因素:TYK2/JAK1 的主要作用 TYK2/JAK1 細胞因子 • IFN-g • il-b • IFN-G 下游的腫瘤壞死因子 • IL-8 • GM-CSF,MCP-1 小膠質細胞是中樞神經系統的常駐巨噬細胞,在神經炎症、修復和維護中發揮重要作用 • IFN-g • IL-12 • TNF • IL-8 異常星形細胞活性可能加劇炎症反應並導致組織損傷:星形膠質細胞、淋巴細胞、其他白細胞 • IL-23 • IL-17 在 IL-23 的下游 • IL-2、IL-4 有力證據表明 Th17 淋巴細胞參與發病機制多發性硬化症和帕金森氏病 2023 年 9 月 Biohaven | 投資者演示文稿31

BHV-8000:摘要選擇性是差異化因素 • 選擇性抑制 TYK2/JAK1 為神經炎症性疾病提供同類最佳免疫調節潛力 • TYK2/JAK1 的選擇性可減輕非選擇性 JAK 類負債,主要與 JAK2 和 JAK3 抑制有關,並有可能提高高選擇性 BHV-8000 雙激酶抑制劑在多種神經炎症性疾病中的潛在獲益風險 • 補充直接治療神經炎症的其他方法變性,例如澱粉樣蛋白、α-突觸核蛋白、tau和線粒體靶向療法 • 強有力的證據支持帕金森氏病、阿爾茨海默氏病和其他神經炎症性疾病的潛在療效 • 第一階段於2023年5月啟動;SAD/MAD研究的SAD部分使用了多個隊列劑量 • 帕金森氏病的第二階段預計將於2024年開始 • 合作伙伴(Highlightll Pharmicals)預計將於2024年在中國啟動一項針對阿爾茨海默氏病的研究臨牀試驗正在進行中,預計將於2024年9月進行Biohaven | 投資者演示文稿 32
TYK2/JAK1 選擇性抑制劑的特性非常適合治療神經炎症腦穿透力 • 生物製劑不是大腦穿透劑 • 需要專門設計的小分子才能到達作用部位 • 現有藥物排除中樞神經系統中的所有淋巴細胞 • TYK2/JAK1 抑制劑有望選擇性地消耗作用部位的 CD4+ Th17 細胞 JAK2 和 JAK3 抑制劑量限制耐受性問題降至最低 • 嚴重的心血管事件 • 嚴重的免疫抑制 • 貧血、癌症、死亡小分子可以方便地在家中每日口服給藥 2023 年 9 月生物製劑停藥與長期暴露後中樞免疫調節的潛在不良事件迅速得到解決 Biohaven | 投資者演示文稿33

BHV-8000:靶向帕金森氏病神經炎症的兩個軸多巴胺能神經元 1. 多巴胺能神經元 Microglia 5 中的 a-syn 聚集體。小膠質細胞向 T 細胞呈現 α-syn 和 MHCII Th1/Th17 細胞 3.小膠質細胞釋放趨化因子將T細胞招募到中樞神經系統 6。T 細胞釋放 IFN-α,IFN-γ與其在小膠質細胞 SUBSTANTIA NIGRA 4 上的受體結合。T 細胞從外圍遷移到中樞神經系統 2。小膠質細胞 Th1/Th17 細胞吸收的聚合 a-syn 7.小膠質細胞釋放炎性細胞因子,損害多巴胺能神經元 CD4+ T 細胞腸道神經系統和外周 1. 腸神經元中的 a-syn 聚集體 2.聚合的 a-syn 被 M1 巨噬細胞 M1 巨噬細胞 2 吸收。a-syn 與 MHCII 到 CD4+ T 細胞腸道神經元 3 一起呈現。結合載有 a-syn 的 MHCII 的 CD4+ T 細胞被激活並克隆膨脹 1.艾倫·裏什,Standaert。帕金森雜誌出版社 2015; 5 (1): 1-19. 2.Fu 等人J 神經炎症。2022;19 (1): 98。α-syn,α-突觸核蛋白;CD4,分化羣 4;中樞神經系統;IFN-γ幹擾素-伽馬;IL,白介素;JAK,Janus 激酶;M1,經典激活;MHC,主要組織相容性複合物;TH,T輔助細胞;TYK,酪氨酸激酶 K2/JAK2 抑制帕金森氏神經炎症 CASCADE TYK2/JAK1 抑制劑通過抑制 IL-23 信號傳導降低 Th17 細胞的活化和擴張,通過抑制致病性 α-突觸核蛋白聚集物觸發的 IFN-γ信號傳導來減少小膠質細胞的活化1,2 9 月2023Biohaven | 投資者演示文稿34

• 多發性硬化症是一種炎性疾病,體液免疫和細胞介導的免疫反應靶向中樞神經系統抗原 • IL-17A 缺陷小鼠對誘導 EAE 具有很強的抵抗力 • 由於Th17細胞效應,PKM2 激活劑在 EAE 模型中介導強效抑制作用 • 在文獻薈萃分析中,多發性硬化症患者的腫瘤壞死因子A、IL-15、IL-12、IL-23/IL-17和IfNG升高與對照組比較 • Secukinemab (IL-17A) 顯示出緩解多發性硬化症的作用 • 大腦滲透劑 TYK2/JAK1 激酶抑制劑可減少 Th17 細胞(IL-17 和 IL-23) 並靶向 IL-12 信號傳導 • BHV-8000 非常適合減少多發性硬化症中 MS TYK2/JAK1 炎症通路中的神經炎症 X X X McGinley 等人,免疫 52:342-356,Palle 等人,《醫學科學》,5:23,2017 年 5 月 23 日;Bai 等人,《神經科學前沿》,10.3389,2019 年 10 月 4 日,Havrdova,《多發性硬化症雜誌》,18_50_18_50 2012 年 9 月 9 日;數據來自 Nat Rev Neurosci。2002 年 4 月;3 (4): 291-301. doi:10.1038/nrn784。2023 年 9 月 Biohaven | 投資者演示文稿35

TYK2/JAK1 抑制可減少驅動阿爾茨海默氏病 (AD) 的幾種關鍵細胞因子病理學神經炎症是 AD 發病機制的關鍵事件,表明抗澱粉樣蛋白 β (Aβ) /tau 和抗炎療法的組合是必要1,2 神經炎症 Aβ 斑塊沉積 + tau 積累小膠質細胞激活和細胞因子釋放突觸去除 + 認知衰退 • 細胞因子和趨化因子影響 tau 磷酸化和澱粉樣蛋白 β (Aβ) 沉積 • 釋放的細胞因子包括 IL-1b、IL-6、TNF-α 和 IFN-γ• Aβ 沉積也會誘導表達 TYK2 和 JAK1 • TYK2 是 Aβ3 改變的最顯著的基因 • 伴隨出現 Aβ、tau 和小膠質細胞激活異常會顯著增加出現認知症狀的機率2 Aβ 斑塊小膠質細胞 Tau 神經元炎性細胞因子改編自 Neher。免疫. 2022; 55 (5): 821-823. 1.多明格斯等人。Curr Alzheimer Res. 2017; 14 (8): 870-882. 2.Pascoal 等人。國家醫學雜誌 2021; 27 (9): 1592-1599. 3.Nevado-L 等人。細胞。2019;8:825。2023 年 9 月 Biohaven | 投資者演示文稿36

Biohaven | 投資者演示文稿37 強迫症 (OCD) • 強迫症患者皮質紋狀體穀氨酸異常的令人信服的機制理由 • 2 期強化的 PoC • 1,000多名患者表現良好 • 兩項 3 期研究正在進行中;預計2023 年 9 月完成入組 OCD 摘要穀氨酸平臺 TRORILUZOLE

Troriluzole 治療強迫症:描述未滿足的需求強迫症影響了 1.2% 的美國人口,但只有六分之一的強迫症患者接受藥物治療。Limited正在進行強迫症治療的研究,預測近期將缺乏經批准的新藥物,氯胺酮被證明具有短期療效;與恥辱和不良副作用(例如幻覺、分離症狀)有關 Rapastomine 試點研究表明,Inel還作用於穀氨酸系統,可在數小時內減輕強迫症、焦慮和抑鬱症狀(但持續時間不到1小時)周) SSRI 是唯一獲準用於強迫症的藥物需要數週到數月才能生效通常需要比抗抑鬱藥更高的劑量,從而增加與劑量相關的副作用/並不適用於所有人 GLUTAMATE 2023 年 9 月 Biohaven | 投資者演示文稿38

BHV-4157 Troriluzole 治療的強迫症患者:在 2 期 POC 中觀察到的強烈信號支持進入第 3 期研究 BHV-4157-202 中度至重度強迫症(Y-BOCS 評分 ≥ 19)且對標準護理反應不足的患者樣本量 226 名受試者隨機分配 1:1 劑量曲利魯唑 200 mg QD 與安慰劑 QD(標準護理患者)主要結果 Y-BOCS,先前的結果衡量標準已被美國食品和藥物管理局接受:在第 2/3 階段試驗中,曲利魯唑對強迫症的影響 1 Y-BOCS 與基線第 4 周(n=115a,111b)8(n=108a,96b)12(n=102a,99b)相比的總體變化 a。安慰劑 -2.9 -3.6 -4.9 b. Troriluzoleb -3.4 -5.1* -5.9* -5.9 p 值 0.451 0.041 0.220 1。BHV-4157-202 最終非盲分析 YBOCS 與基線相比每週的總變化 MMRM 模型 MITT 數據集表 2:曲利唑對重度 OCD1 患者的影響 Y-BOCS 與基線第 4 周(n=47c,49d)8(n=45c,42d)12(n=43c,44d)a. 安慰劑 -3.5 -3.1 -4.6 b Trorcs iluzoled -4.1 -6.0* -7.0 p 值 0.584 0.035 0.084 1。基線時 Y-BOCS 總分中位數 > 26(嚴重強迫症症狀)的患者。* p

Myostatin 平臺 TALDEFGROBEP ALFA BHV-2000 非臨牀 • 在 20 多項動物安全性和疾病模型研究中表現良好 • 包括幼體動物,允許安全性低至 2 歲臨牀 • 在先前的研究中,359 名參與者接受了 taldefgrobep:179 名健康參與者和 180 名 5-12 歲杜興氏肌肉萎縮症參與者 • 通過手臂、大腿和腹部皮下注射給藥 en • 遊離血清肌抑制素顯示劑量依賴性抑制 • MRI 和 DXA 數據與陽性結果一致對肌肉健康有益 • 總體安全且耐受性良好 2023 年 9 月 Biohaven | 投資者演示文稿40

肌抑素和激活素 A 是有效的肌肉調節劑 2023 年 9 月 Biohaven | 投資者演示41 阻斷肌肉抑素和激活素 A 會導致肌肉肥大 • 肌抑素是一種分泌蛋白,屬於 TGF-β 信號分子超家族 • 肌抑素通過最初與 2 型激活素 Actriia 和 Actriib 結合發出信號,然後結合激活素 1 型受體 ALKB 4 和 ALK5 • 對包括人類在內的多個物種的遺傳和藥理學研究表明,肌抑素通常起到阻斷骨骼肌生長的作用 •肌肉中肌抑素的功能與相關蛋白激活素 A 的功能部分多餘 Myostatin (GDF-8) 由骨骼肌自然表達,可積極抑制骨骼肌生長 Myostatin 負面調節肌肉生長

Taldefgrobep Alfa:差異化作用機制 2023 年 9 月 Biohaven | 投資者演示文稿42 • Taldefgrobep 是一種融合蛋白,旨在對肌抑素而不是轉化生長因子β途徑的其他成員具有最佳親和力 • 非臨牀研究表明,taldefgrobep 在激活素 1 型受體 (ALK4/5) 結合位點與肌抑素結合,可以抑制信號傳導 • 複雜的 taldefgrobep 與肌抑制素形成的 grobep 可抑制肌抑素活性組織中的肌抑素和激活素 A 信號 • 有可能減少激活素 2 型受體的脱靶阻塞非肌肉組織唯一能減少遊離肌抑素和阻斷受體信號的藥物 Taldefgrobep 與肌抑素結合以抑制信號

不含肌抑素和藥物結合水平 Taldefgrobep Alfa:活性經人體研究證實 2023 年 9 月 Biohaven | 投資者演示43 • 健康志願者每週皮下給藥 4 周後,暴露量會增加劑量依賴性,遊離肌抑制劑/肌抑素複合物的積累推動遊離肌抑素和激活素 A 結合的競爭抑制 • 參與者表現出增加的劑量依賴性瘦骨骼組織(MRI)和瘦體重的增加以及肌肉注射脂肪的減少volume (DXA) 對於ee a 和 B 你和 M 你坐在 d M 裏你坐在 C 裏面 om pl ex% C 在 e Study Day Myostation 藥物複合物中,45mg Q1W 肌肉生長抑素,45mg Q1W 安慰劑給藥週期減少肌肉注射脂肪在我使用 cu la r f at V ol um e (M ea n% C ha ng e ng e) fr om B as el in e) 第 29 天 57 天增加瘦體質量 Le an B od y M as s (M ea n% C ha ng e fr om B as el in e) 第 15 天 29 天 57 天

肌抑素:脊髓性肌萎縮的強有力的科學依據 2023 年 9 月 Biohaven | 投資者演示44 個 SMA 疾病小鼠模型中 SMN 上調的組合療法研究表明:ü 延長壽命和力量,改善肌肉功能 ü 增加神經分支、突觸後區域大小、神經肌肉連接受支配、感覺神經元增大 • SMA 是一種神經退行性疾病;保持肌肉完好無損作為改善功能的目標 • 疾病緩解療法獲得批准且可廣泛獲得並且對 SMA 患者有效 • 疾病領域有完善的經過驗證的臨牀終點和經過驗證的監管途徑 SMN,生存運動神經元;DRG,背根神經節

第三階段彈性研究概述 RESILIEN是一項隨機、安慰劑對照試驗,測試了taldefgrobep作為輔助治療的有效性和安全性,將在參與者出現以下情況時給予Taldefgrobep或安慰劑:• 已經服用穩定劑量的nusinersen和/或•已經服用穩定劑量的ridiplam和/或•有onasemnogene abeparvovec-xioi PRIMARVOVEC-XIOI病史在基線和第 48 周之間,32 項運動功能測量 (MFM-32) 總分的變化 48 周、雙盲、安慰劑對照的兒童和成人脊髓性肌萎縮症研究設計參與者 • 預計入學人數:180 名參與者 • 2:1 隨機分配:taldefgrobep alfa 與安慰劑雙盲期 48 周篩查 ≤ 6 周可選開放標籤延期期 48 周安全隨訪 8 周 R 雙盲期 48 周 Taldefgrobep Alfa 每週以體重計 35 mg 或 50 mg,SC 配對安慰劑 + + SMN 上調劑 nusinersen 的穩定方案 risdiplam 和/或 onasemnogene abeparvovec-xioi SMN Upregulator 穩定的 nusinersen 和/或 risdiplam 治療史和/或 risdiplam 的穩定方案和/或onasemnogene abeparvovec-xioi Taldefgrobep Alfa 每週使用體重 35 mg 或 50 mg 的治療史,SC + SMN Upregulator nusinersen 和/或 risdiplam 的穩定療程和/或奧納塞諾基因 abeparvovec-xioi 的治療史 2023 年 9 月隨機化彈性三期研究設計 Biohaven | 投資者演示文稿45

彈性研究人羣 • 鑑於整個SMA人羣中未得到滿足的需求很高,以及治療模式的變化,我們涵蓋了廣泛的人羣 • 隨着疾病改良療法和廣泛的新生兒篩查、早期治療以及潛在的療法組合,轉向更多地關注功能狀態而不是 SMA 類型;接受治療的患者正在實現原本無法達到的里程碑 • 預計將有大約 180 名 SMA 參與者進入治療階段彈性不限於也不侷限於患者2023 年 9 月 SMA 的動態狀態、背景療法或分類 Biohaven | 投資者演示文稿46

肥胖是一場公共衞生危機 • 肥胖是一種脂肪組織過剩和/或異常的疾病 § 心臟代謝風險與內臟肥胖密切相關 • 到 2030 年,全球將有 10 億人患有肥胖症,其中包括約 50% 的美國成年人1 § 肥胖和相關合並症每年給美國醫療系統造成的損失約為 1750 億美元2 § 一小部分符合條件的人目前正在接受抗肥胖藥物的治療 (AoMs) 3 • 肥胖症的治療是尚未滿足的關鍵醫療需求領域 1,世界肥胖聯合會。2022年世界肥胖地圖集。https://www.worldobesity.org/resources/resource-library/world-obesity-atlas-2022;已訪問 17-NOV-2022。2,CDC。成人肥胖概況。https://www.gov/obesity/data/adult.html;已訪問 13-NOV-2022。3.Saxon DR等人,八個大型醫療保健組織的220萬成年人使用抗肥胖藥物:2009-2015年。dPrimeau V、Coderre L、Karelis AD、Brochu M、Lavoie ME、Messier V、Sladek R、Rabasa-Lhoret R. 描述代謝健康的肥胖患者的概況。Int J Obes(倫敦)。2011 年 7 月;35 (7): 971-81. doi:10.1038/ijo.2010.216。Epub 2010 年 10 月 26 日PMID:20975726。內分泌 • 糖尿病 • 庫欣綜合徵 • 甲狀腺功能減退 • 不孕症 GI • 裂孔疝 • 膽囊疾病 • 腹股溝疝癌 • 乳房 • 結直腸 • 子宮內膜肌肉骨骼 • 骨關節炎 • 背痛心血管 • 猝死 • 心肌病 • 高血壓 • 缺血性心臟病 • 外周血管疾病 • 深靜脈血栓形成 • 呼吸道阻塞 • 限制性肺栓塞肺部疾病 • 阻塞性睡眠呼吸暫停 • 肥胖低通氣綜合徵 • 插管困難泌尿生殖系統 • 月經問題 • 女性尿失禁 • 肥胖的腎結石併發症 2023 年 9 月 4 日 Biohaven | 投資者演示文稿47

成年肥胖症患者進入一個充滿希望和機遇的新時代 • 這是一個體重管理領域快速變化和重新興奮的時代 • 高效抗肥胖藥物(AOM)和聯合療法的療效效果接近減肥手術 • 減肥領域的競爭正在加劇,但存在顛覆機會 0% 5% 10% 15% 20% 25% 30% 35% 強化生活方式幹預 ILI + 較早的藥物(例如 orlistat NAL/BUP、PHEN),TPM,利拉魯肽)索瑪魯肽 2.4mg 曲塞帕肽腹腔鏡Band Sleeve Gastrectomy Roux-en-Y 胃旁路術 Biliopancreatic Diveratic Gastrectomy 2023 年 9 月通過最常見的幹預措施減輕總體重 Biohaven | 投資者演示文稿48

超重和肥胖成人的療效比較結果 • 在臨牀中,抗肌抑素療法一再顯示出增加瘦肉質量、減少脂肪量和改善不同患者羣體的葡萄糖代謝的能力 • 那些可以同時靶向肌抑素和激活素 A 信號藥物劑量的藥物優化了身體成分的藥物劑量總體重瘦體重 A1C 芬特敏/託吡酯 =1,469 PO 每天一次 -7.8% 至 -9.8% NA -0.4% 納曲酮/安非他酮 n=1,161 1-2 PO每日兩次 -5.4% -11.7% NA -0.6% Bimagrumab n=37 IV Q4W -6.5% -20.5% +3.6% -0.76% Semaglutide 2.4 n=1,306 SC QW -14.9% -19.3% -19.3% -9.7% -1.6% Tirzepatide n=1,896 SC QW -20.9% -2.3% 袖胃切除術 n=85 NA -26.3% 4% -40.3% -16.5% 至 -19.5% -2.67% Qsymia USPI;佛羅裏達州格林威等COR-I。《柳葉刀》。2010 (9741): 595-605;Contrave USPI(32/650mg);Heymsfield SB 等JAMA. 2021;Wilding JPH 等人第 1 步。NEJM 2021;384 (11): 989-1002;Wilding JPH 等步驟 1 身體成分。J Endocr Soc. 2021;5 (1): A16-17;Wegovy USPI (STEP2);Jastreboff AM 等克服1。NEJM. 2022;387 (3): 205-16;Mounjaro USPI (15mg);Sylivris A. 等人Obes Rev. 2022;23 (7): e13422;Maimoun L. 等人Surg Obes Relat Dis.2019;15 (11): 1965-73;Zhang H-W 等中國人胃旁路手術伴有糖尿病和肥胖。Ann Transl Med. 2020;8 (6): 372-82;2期bimagrumab研究是針對肥胖和2型糖尿病的成年人進行的,而3期芬特明/託吡酯、納曲酮/安非他酮、索瑪魯肽和替拉肽研究是針對超重或肥胖但沒有T2DM病史的成年人進行的(除非另有説明)。分析時間因資產而異,芬特明/託吡酯(1 年)、納曲酮/安非他酮(56 周)、bimagrumab(48 周)、索馬魯肽(68 周)、替塞帕肽(72 周)、袖狀胃切除術(1 年)。值得注意的是,HbA1c數據的變化已經標準化(均代表超重/肥胖加T2DM的成年人的變化)。在針對超重/肥胖的非糖尿病成人進行的替塞帕肽(15mg)和索瑪魯肽(1mg)研究中,HbA1c的平均變化分別為-0.52%和-0.52%;代表所有替塞帕肽劑量水平下脂肪質量的累積平均變化。Abati E、Manini A、Comi GP 等抑制肌肉抑制素和相關信號通路,用於治療運動神經元疾病中的肌肉萎縮。Cell Mol Life Sci.2022; 79 (7): 374; Lee S-J.靶向肌肉生長抑素信號通路以治療肌肉流失和代謝功能障礙。J Clin Invest. 2021;131(9):e148372,上午;BP,血壓;HDL,高密度脂蛋白;LDL,低密度脂蛋白;NA,不可用;PO,口服;QW,每週一次;TC,總膽固醇;TG,總葡萄糖。2023 年 9 月 Biohaven | 投資者演示文稿49

抑制肌抑素信號傳導顯示重要的身體和代謝變化肌抑素作為藥物靶標改善骨礦物質密度提高基礎代謝率提高胰島素敏感性降低肌肉注射脂肪減少肝內脂肪總量減少內臟脂肪量減少瘦肉質量增加 • 臨牀上,taldefgrobep 總體上是安全且耐受性良好,胃腸道和肌肉骨骼不適發生率低 • 在健康成年人中,taldefgrobep 總體上是安全的,耐受性良好,胃腸道和肌肉骨骼不適的發生率低 • 在健康的成年人中,taldefgrobep 總體上是安全的,耐受性良好相對而言,grobep 顯著改善了身體成分2023 年 9 月使用安慰劑 Biohaven | 投資者演示50

推進 Taldefgrobep 在肥胖領域的發展 • 利用現有的臨牀前和早期臨牀數據可以顯著加快開發進度 • 美國食品藥品管理局完成的肥胖症臨牀前會議 • 針對超重和肥胖的成年人的概念驗證試驗 2023 年 9 月與 GLP-1 類聯合應用的新機制Biohaven | 投資者演示文稿51

肌抑素平臺 TALDEFGROBEP ALFA BHV-2000 阻斷肌抑素和激活素 A 信號的新機制 • 人類數據顯示遊離肌抑素和肌抑素-taldefgrobep 複合物的積累顯著減少 • 短期臨牀研究顯示瘦體質量和脂肪組織流失有所改善高級開發計劃 • 由 BMS 許可的大型臨牀前和臨牀安全包 • 現有數據庫包括兒科和成人的臨牀數據 • 總體上安全和良好在多項臨牀研究中均可耐受脊髓性肌萎縮症 (SMA)) • 單一關鍵研究於2022年年中啟動 • 孤兒藥在美國和歐盟獲得;美國獲得快速通道認定 • 全球研究;2023年第四季度註冊完成開發機會 • 肥胖等代謝性疾病的誘人機會 • 其他神經肌肉、骨骼和代謝適應症正在評估2023年9月Biohaven | 投資者演示文稿52

降解器平臺概述一系列療法有可能通過靶向致病蛋白和抗體來支持涵蓋各種適應症的眾多臨牀候選藥物潛在的首創靶向蛋白降解 MOA 具有獨特的優勢,例如,加快了從發現到臨牀的道路 BHV-1300 人類首例 MOA 可有效去除致病性 IgG,具有行之有效的自身免疫性疾病機制半乳糖缺乏 IgA1 降解用於治療 IgA 腎病的新型基於抗體的降解劑特定於 E,自身抗體靶向降解劑選擇性去除與多種免疫驅動的退行性疾病有關的自身抗體 2023 年 9 月 Biohaven | 投資者演示文稿53 極具競爭力的安全性、可製造性和產品開發概況

MoDe™ 降解劑:多種資產機會和高效的時間表關鍵價值轉折點 IgG 和 IgA 抗體是 Biohaven 強大的降解平臺計劃 2023 2024 2025 2026 2027 發現目標價值轉折點的實現將視具體項目而定,並與一致的投資組合策略 AutoAB、自身抗體;Ig,免疫球蛋白;IND,在研新藥;moDe™,細胞外蛋白分子降解劑;RA、類風濕關節炎 IgG RA、自身免疫性 IND 申報 (2H) IgA IgA 腎病 IND 申報 (1H)未披露的 AutoAB #1 IND 申報未披露的 AutoAB #2 IND 申報 2023 年 9 月 Biohaven | 投資者演示文稿54

• 利用人體自身降解蛋白質的機制 • 通過積聚糖蛋白受體 (ASGPR) 消除細胞外蛋白靶標 • 蛋白質靶標通過內溶酶體蛋白水解降解 * 前身為 BH 2640 雙特異平臺:通過 MoDe™ 降解 IgG 2023 年 9 月 Biohaven | 投資者演示55 細胞外蛋白分子降解劑 (MoDe):小分子結合細胞外靶標蛋白質並通過肝臟將其從體內排出結合肝臟(ASGPR)結合蛋白質靶向致病性靶蛋白和MODEs流通中

一流的機制:肝臟ASGPR受體用於高效、安全地去除循環致病靶標2023年9月 Biohaven | 投資者演示56 Mode™ 結合循環靶標並將其有效輸送到肝細胞上的ASGPR • 溶酶體中內化靶標快速降解 • 靶標降解程度得到精確控制 ASGPR 受體快速回收。通過實驗平衡 ASGPR 和靶蛋白的相對親和力,可以實現最佳的安全性和有效性。皮下或靜脈注射 moDes™ 通過 *Stylistic 表示 ASGPR,亞洲糖蛋白受體;moDe™,細胞外蛋白的分子降解劑 2 3 4 1 符號圖例降解靶向肝細胞雙功能模式™ 降解劑亞洲糖蛋白受體 (ASGPR)。) *

肝臟 ASGPR 受體用於高效、安全地去除致病靶標 • 高容量 ASGPR 肝細胞受體內化具有特定基序的血漿蛋白 • 帶靶結合劑的雙特異性 ASGPR 結合劑可有效將致病靶標從循環中去除 • IgG 可能比 fcRN 抑制性抗體或抗體片段更快地從循環中清除,不會導致低白蛋白血癥或血脂異常血癥 • 改善、可調效力(可進一步降低 IgG/IgA)• 改善藥效學(起效更快)•提高安全性(減少副作用,快速消除藥物)2023 年 9 月 Biohaven | 投資者演示文稿57 BHV-1300:高度優化的 Biohaven ASGPR 粘合劑作為候選藥物推出 ü 平衡肝臟切除 ü 優化安全性與有效性 ü 改善靶標去除動力學 ü 適合每週或更少頻率的 SC 給藥的快速起效藥物的目標產品簡介

HepG2 細胞內化 Igg-BHV-1300 複合物體外 BHV-1300 介導 IgG 的去除、攝取和降解 2023 年 9 月 Biohaven | 投資者演示58 1 10 100 1000 0 20000 40000 40000 60000 nM FI 在 HepG2 中攝取 IgG 110 BHV-1300 125nM BHV-1300 HepG2 中未經處理的 IgG 攝取 1 10 100 1000 1000 20000 20000 20000 0000 0000 0000 20000 60000 80000 nM M FI HepG2 EC50 99 BHV-1300 1 10 100 1000 0 20000 20000 20000 60000 80000 60000 80000 nM M FI 在 HepG2 EC50 110 BHV-1300 中吸收 IgG

BHV-1300 小鼠體內人體 IgG 消耗,單劑量 12 mg/kg BHV-1300 被選為在鼠標屏幕中去除外源給藥的人類 IgG 的顯著效率 2 小時內去除大約 40% 的 IgG,藥物與靶標的摩爾比 = 1.0 Biohaven | 投資者演示59 0 2 4 6 8 10 0 1×109 2×109 3×109 4×109 小時 Ig G p g/ m l BHV-1300 小鼠體內 IgG 消耗,單劑量 12 mg/kg BHV1300 SD,12 mg/kg +IgG IgG

IgG 已特別耗盡:IgA 和 IgM 水平保持不變 2023 年 9 月 Biohaven | 投資者演示60 0 100 200 400 0 100 300 Hours Ig M% T 0t IgM% 按組變化 0 mg/kg 10 mg/kg 30 mg/kg 75 mg/kg 150 mg/kg 250 mg/kg 250 mg/kg • 初步的 BHVN 數據和文獻對血清白蛋白、低密度脂蛋白、高密度脂蛋白或甘油三酯沒有影響,以及靶向 IgG 物種的特異性 • 在具有內源性 IgG 的猴子體內注射外源 IgG 後,小鼠的藥物效率顯著。摩爾比約為 1.0 允許在單劑量 BHV-1300 靜脈注射後降低 60% 的免疫球蛋白 0 5 10 15 0 50 100 150 天 150 天% Ig G T0 IgG 0 5 10 15 0 50 150 200 天 Ig A% T 0t Iga 0 5 10 15 0 50 150 150 200 天 Ig M% T 0t IgmIGG 按組 IgM 變化百分比變化百分比小組日

由 SC、IM 或 IV Routes 管理的 BHV-1300 具有相似的生物利用度 2023 年 9 月 Biohaven | 投資者演示文稿61 可能允許在家中通過皮下注射進行自我給藥 0 10 20 30 10 100 10000 10000 10000 小時 ng/m l 在人體 IgG BHV-1300 IV 10 mg/kg 存在下 SQ 10 mg/kg F SQ ~ 99% F IM ~ 93% 在人體 IgG 存在下單劑量為 10 mg/kg 後血漿中的 BHV-1300 水平 BHV-1300 BHV-1300 BHV1300
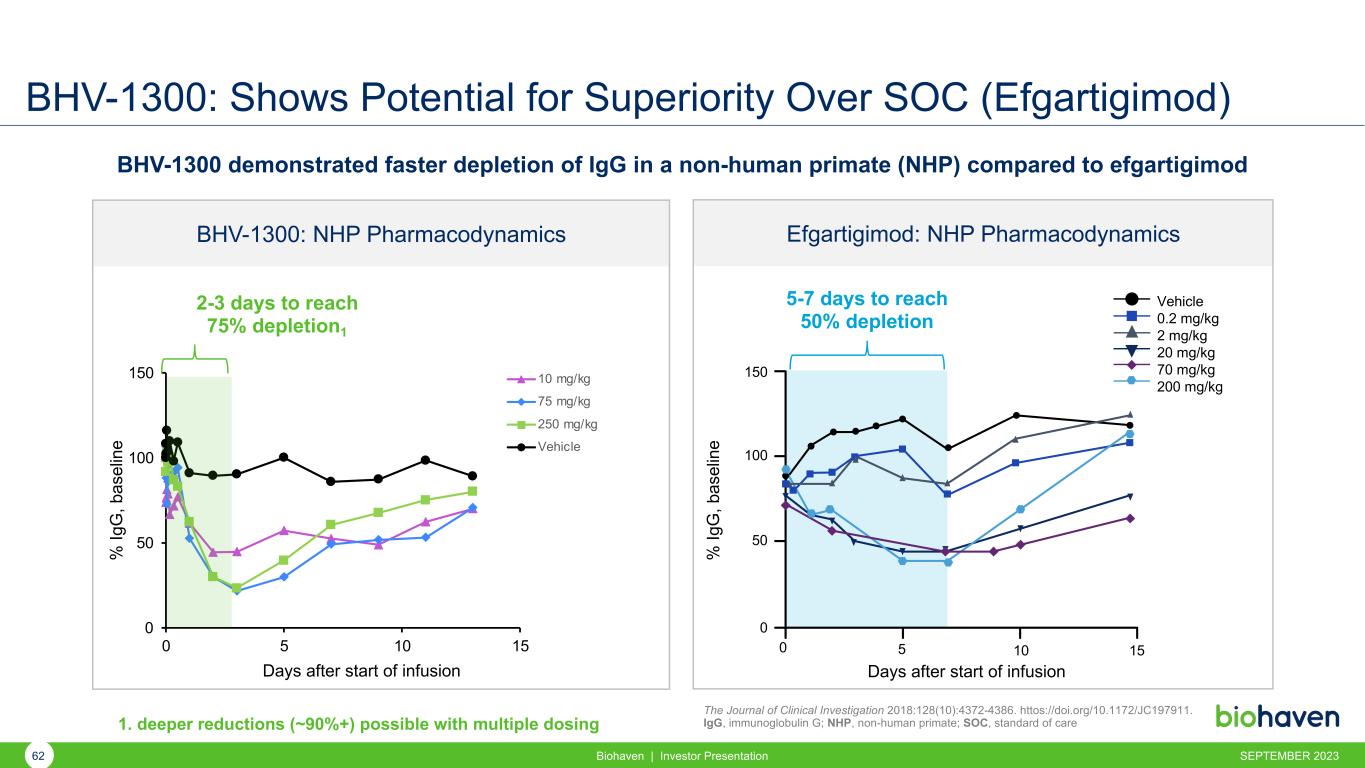
BHV-1300:顯示出比 SOC(Efgartigimod)Biohaven 更具優勢的潛力 | 投資者演講《臨牀研究雜誌》2018:128 (10): 4372-4386. httos: //doi.org/10.1172/JC197911。IgG、免疫球蛋白 G;NHP,非人類靈長類動物;SOC,標準護理 BHV-1300 表現出非人靈長類動物 (NHP) 的 IgG 消耗速度更快 5-7 天,達到 50% 的消耗 0 5 10 15 0 0 50 100 開始輸液後 150 天車輛 0.2 mg/kg 20 mg/kg 70 mg/kg 200 mg/kg Efgartigimod:NHP 藥效動力學% Ig G,b as el in e 0 50 100 150 0 5 10 15 10 10 mg/kg 75 mg/kg 250 mg/kg 車輛 BHV-1300:NHP 藥效學% Ig G,b as el 在 e 開始輸液後 2-3 天達到 75% 的消耗量1 九月 202362 1。更深多次給藥可減少(約 90% 以上)

BHV-1300:重複給藥可大幅減少 90% 以上 -200 200 400 天 0 ↓ 第 8 天 ↓ 第 15 天 ↓ 0 50 150 小時% c ha ng e/T 0 IgG:按組分列的百分比:1:200 K 對照 BHV1300、75mg/kg BHV1300、250mg/kg BHV1300、375mg/kg BHV1300、500mg/kg 日 -7 0 劑量 BHV-1300:NHP 藥效學多項實驗的綜合結果表明 BHV-1300 中重複給藥 cynomolgus 可導致 IgG Biohaven 降低 90% 以上 | 投資者演示劑量 1 劑量 2 劑量 3 劑量 4 時間框架 63 0 時間 2023 年 9 月

BHV-1300:特異性和快速的致病性靶點切除 • 機制預計不會導致低白蛋白血癥或血脂異常 • 改善和優化靶標去除效力 • 需要時更深入地去除靶標 • 改善藥效學,起效比 fcRN 抑制更快 • 安全性有望提高(副作用更少,藥物快速消除)fcRN,新生兒 Fc 受體;Ig,免疫球蛋白;MoDe™,細胞外蛋白的分子降解劑 BHV-1300 可以比 fcRN 抑制抗體更快地特異性地將靶向 IgG 從循環中移除,抗體片段或免疫抑制劑 HepatocyteBHVN 降解劑 2023 年 9 月 Biohaven | 投資者演示文稿64

BHV-1300 與 fcRN 類競爭對手的區別,例如 efgartigimod 和 nipocalimab,具有獨特的 MOA,發病速度更快,預計會提高安全性 2 期研究於 2024 年開始 BHV-1300:與 fcRN 類類風濕關節炎系統性紅斑狼瘡原發性 fcRN 的狼瘡腎炎比較項目相比,有可能在罕見和常見疾病中增加顯著價值類全身性重症肌無力慢性炎性脱髓鞘性多發性神經病天皰瘡温性自身免疫性溶血性貧血免疫性貧血血小板減少症 R ar e D is ea se s c om m on D 疾病 2023 年 9 月 Biohaven | 投資者演示文稿65

類風濕關節炎是一種異源性自身免疫性疾病,其特徵是各種類別的自身抗體 1.改編自 Van Delft 和 Huizinga,《類風濕關節炎自身抗體概述》;J Autoimmun 2020。2.UptoDate 於 2023 年 1 月訪問。有風險類風濕關節炎過渡到有症狀的類風濕關節炎症狀性關節炎症狀性關節炎症狀性關節炎症狀性關節炎 H E A L G I AS T A R T A U M M U N I T Y 感染/改變微生物組擴張、表位擴散等致病性自身抗體兒童感染/生成自反應 B 細胞生活方式和環境因素(吸煙、遺傳體重、飲食、避孕藥)易感活力/激素因素(HLA、(fe)雄性激素、更年期)如果沒有有效的早期幹預,炎症和關節破壞會導致身體機能喪失而且生活質量極差其他健康風險包括心血管疾病、骨質疏鬆症和某些類型的癌症(例如淋巴瘤)的風險升高自身抗體可能在臨牀關節炎出現前 10 年開始積累1 ACR/EULAR 診斷標準 INCLUDE2:• 涉及 3 個以上關節 • 急性期炎症生物標誌物,包括 ESR 和 CRP 升高 • 症狀持續時間 • 大約 70% 中有 RF 和 ACPA IgG+ ACPA ACPA 隨着越來越多的證據顯示關節炎人羣在 RA 中可能具有致病性 2023 年 9 月 Biohaven | 投資者演示文稿66

• 類風濕因子 (RF) 抗體主要是 IgM,但與 IgG 形成免疫複合物 • 包括抗環瓜氨酸肽 2(抗 CCP2)在內的抗檸檬酸化蛋白抗體 (ACPA) 主要是 IgG,但有一些 IgA 和 IgM 物種存在 • 所有免疫複合物都可能對關節、許多器官的結締組織和骨骼造成損傷 • 合併症從心血管到惡性腫瘤都需要密切監測 • 對於未緩解的患者,需要每 4-12 周進行一次狀態以嚴格控制發作和進展的嚴重程度 • IgG 降解劑可以在不降低B細胞數量的情況下去除這些免疫複合物的主要成分。類風濕病的確切病因是多因素的,包括環境、遺傳和T細胞成分,但是自身抗體的存在是改編自馬爾姆斯特羅姆和格朗沃爾,《ACPA陽性和射頻陽性B細胞的平行世界》;Nature Rev Rheum 2018。2023 年 9 月 Biohaven | 投資者演示文稿67

臨牀前研究表明,Gd-Iga1 特異性 moDE™ 可選擇性降解 IgAn Ab 中存在的 Gd-IgA1,抗體;EC50,最大有效濃度 Gd 的一半,半乳糖缺乏;Ig,免疫球蛋白;IgA 腎病;moDE™,細胞外蛋白的分子降解劑 • 僅減少致病性 Gd-Iga1 • 免疫缺乏 IgA,限制免疫力影響 EC50 缺乏 GD-Iga1 的 IgA1 0.84 總計 IgA 33 Ab 粘合劑抗 GD-Iga1 抗體 BH 3845 基於抗體的模式™ 去除 GD-Iga1 在低濃度下,這種 GD-Iga1 特異性模式™ 有選擇地降解 GD-Iga1 和備用總 IgA,限制對免疫系統的影響 GD-Iga1 特異性模式™ GD-Iga1 特異性模式™ 選擇性降解 GD-Iga1 2023 年 9 月 Biohaven | 投資者演示文稿68 40X 半乳糖缺乏 IgA1 總計 IgA

與對照組治療相比,半衰期大大縮短了半衰期 (h) 抗原模式™

摘要:Biohaven MoDe™ 細胞外降解劑提供可選性皮下或靜脈注射 ü 許多細胞外和循環靶標參與病理學,是具有 “產品管道” 潛力的主導項目 BHV-1300 在 2023 年下半年 • BHV-1300 具有優化的化學成分,與標準護理以及其他正在開發的新藥物相比 ü 正在開發的其他項目探索針對特異性自身抗體和 GD-D-Iga1 ü 一旦確定了目標,降解劑候選藥物大約需要 1 年 • 細胞外降解劑在 IND 中最快需要 1.5-3 年,而典型的小分子項目則為 6-10 年。為有效靶標選擇配體、偶聯開發、發現毒素組合、藥理學雙功能分子 2023 年 9 月 Biohaven | 投資者演示70

雙特異性平臺:CD38 多發性骨髓瘤靶向細胞療法 CD38 抗體招募分子 (ARM™) • 具有兩個部分的模塊化雙特異性分子,每個部分都設計用於與特定靶標進行非共價結合 • 重定向內源性抗體靶向癌性或病毒感染細胞進行免疫破壞 Biohaven | 投資者演示71 與生物製劑相比的主要潛在優勢 ü 更低的製造成本 ü 更多用途 — 更小、可調更快 ü 而且開發成本更低 ü 更好的安全性和有效性 • 非免疫原性;更好的劑量 •增強 PK 特性 • 與 daratumumab ARM BHV-1100 CD38 靶向療法相比,NK 細胞自相殘殺減少了 Mult iple mye lom a Cell Multipl e Myelo ma Cell BHV-1100 + CIML NK 細胞 CD38 ARM™ 與多個骨髓瘤細胞表面的 CD38 受體結合 2023 年 9 月
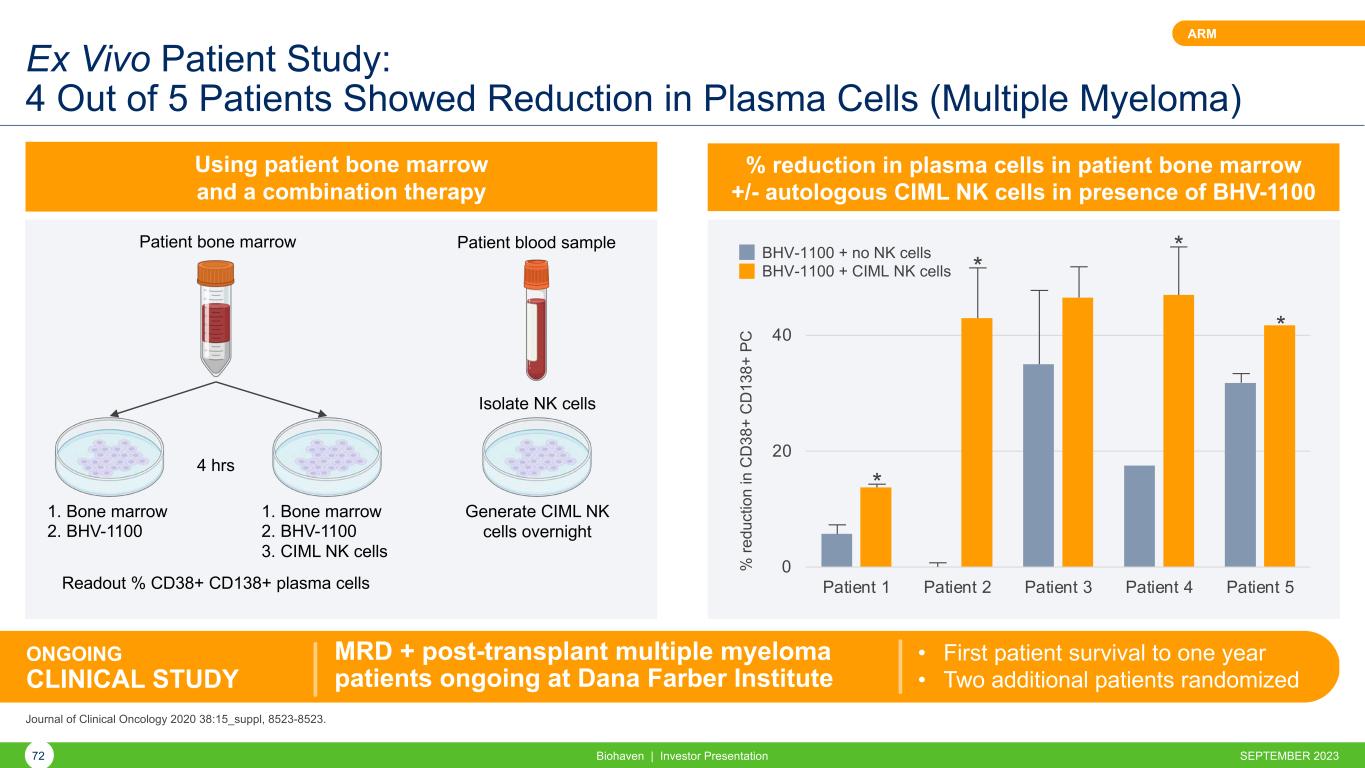
體外患者研究:五分之四的患者表現出漿細胞(多發性骨髓瘤)減少 Biohaven | 投資者演示72 ARM 使用患者骨髓和聯合療法降低患者骨髓中漿細胞的百分比 +/-自體 CIML NK 細胞在 BHV-1100 存在 0 20 40 患者 1 患者 2 患者 3 患者 4 患者 5% re du ct io n in C D 38 + C D 13 8+ P C * * * 患者血液樣本患者骨髓分離 NK 細胞 1.骨髓 2.BHV-1100 4 小時 1.骨髓 2.BHV-1100 3.CIML NK 細胞讀出百分比 CD38+ CD138+ 漿細胞在一夜之間生成 CIML NK 細胞達納法伯研究所正在進行的臨牀研究 MRD + 移植後多發性骨髓瘤患者 • 首例患者存活至一年 • 另外兩名患者隨機抽取 2020 年《臨牀腫瘤學雜誌》38:15 _suppl,8523-8523。BHV-1100 + 無 NK 細胞 BHV-1100 + CIML NK 細胞 2023 年 9 月

第二代 ADC-Linker TechnologiesBioHaven 第三代技術 DISCOVERY RESEARCH 雙特異性平臺:推進下一代位點特異性抗體藥物偶聯物 (ADC) 的潛力每條重鏈都有單一殘留物可供偶聯 • 控制的 DAR* 比率對治療指數至關重要 • 提高了安全性:減少系統性、非靶向載荷 • 提高療效:向有效載荷交付腫瘤使用原生抗體:與當前技術 N N N N N O O O O O Payloand n O O Payload N H 點擊化學設計抗體 Biohaven | 投資者演示文稿73 *DAR = 藥物抗體比率 0 0.1 0.2 0.3 0.4 0.5 1 2 3 4 5 6 Fr ac tio n La be lle d 殘留肽映射(典型卡通)0 0.2 0.4 0.6 1 1 2 3 4 5 6 Fr ac tio n La be lle d 殘留肽映射(典型卡通)0 0.2 0.4 0.6 1 1 2 3 4 5 6 Fr actio n La be le d La be lle d 殘留肽映射(典型卡通)0 0.2 0.4 0.8 1 1 2 3(典型動畫片)2023 年 9 月

Biohaven 的下一代位點特異性 ADC ü ADAPTABLE 補充並改進了多種現有的 ADC 有效載荷連接器技術 ü 穩定性通過受控的 DAR 提高 ADC 血漿穩定性有可能改善治療指數 ü 提高治療指數 ü 多用途偶聯物 IgG1、2 和 4,且可製造:單步偶聯具有可預測的良好產量,低聚集度 ü 新型 IP 在全球主要市場提交的偶聯化學優於行業標準馬耳他 eimide和親脂性點擊化學成分兩種特定賴氨酸的附着可提供穩定一致的藥物抗體比率 (DAR) 2023 年 9 月 Biohaven | 投資者演示文稿74

• 幾乎所有現有方法都涉及廣泛的抗體操作或工程 • 對活性、清除率、免疫原性和COG的潛在影響 • 隨着時間的推移,藥物聯繫可能會逆轉,“泄漏” 替代ADC蛋白質工程和化學面臨的自由載荷挑戰 N Payload S O N Payload O O O DAR、藥物抗體比率 • 高 DAR 物種可能導致 CMC 問題,例如聚集、體內不穩定性導致毒性 • 異質性使 CMC 複雜化,可能會損害 Kadcycy 的療效 La® 0 20 40 60 80 100 0 0 1 2 3 4 5 6 7 8% T ot al a b 藥物/抗體數量通過賴氨酸殘基進行偶聯 0 20 40 60 80 100 0 0 1 2 3 4 5 6 7% T ot al a b 通過減少鏈間二硫鍵進行藥物/抗體數量/抗體偶聯 0 20 40 60 80 100 0 0 0 1 2 3 4 5 6 7% T ot al a b 通過工程半胱氨酸殘基進行藥物/抗體偶聯 DAR 2—4 百萬 >100 One Adcetris® 9月 2023Biohaven | 投資者演示文稿75

N N N N O Payload 點擊化學改造抗體超大親脂性聯動 Biohaven 化學穩定的、物理化學上良性的酰胺鍵 O Payload N H 潛在的 “一流” 位點特異性 ADC N 有效載荷 O O O 行業標準馬來酰亞胺穩定性不佳預計會提高治療指數 ü 提高安全性:減少全身循環中非靶向有效載荷推動毒性 ü 提高療效 ü 提高療效:增加靶向載荷到達腫瘤,可能使用更高的劑量使用原生抗體可能改善 CMC vs.當前基於Adcetris® 製備的特定場地技術 ADC 2023 年 9 月 Biohaven | 投資者演示文稿76

時間,h 鼠標時間,h% C ha ng e Human Time,h mouseHuman% C ha ng e RT 37C 時間,h BH3973:與 Adcetris® 相比血漿穩定性有所提高 • ADC 毒性/耐受性直接與空閒有效載荷有關 • 增強穩定性會減少空閒載荷,並有可能在相同的耐受性條件下提高靶向腫瘤部位的藥物濃度,濃度 37C,高 37C,低 RT,高 RT,Low Adcetris® Biohaven BH3973 2023 年 9 月 Biohaven | 投資者演示文稿77

Adcetris® 和 BH3973 表現出相似的 PK • BH3973 所有劑量的半衰期 7-8 天 • Adcetris® 所有劑量的半衰期 5-6 天 BH3973 Adcetris® 2023 年 9 月 Biohaven | 投資者演示文稿78
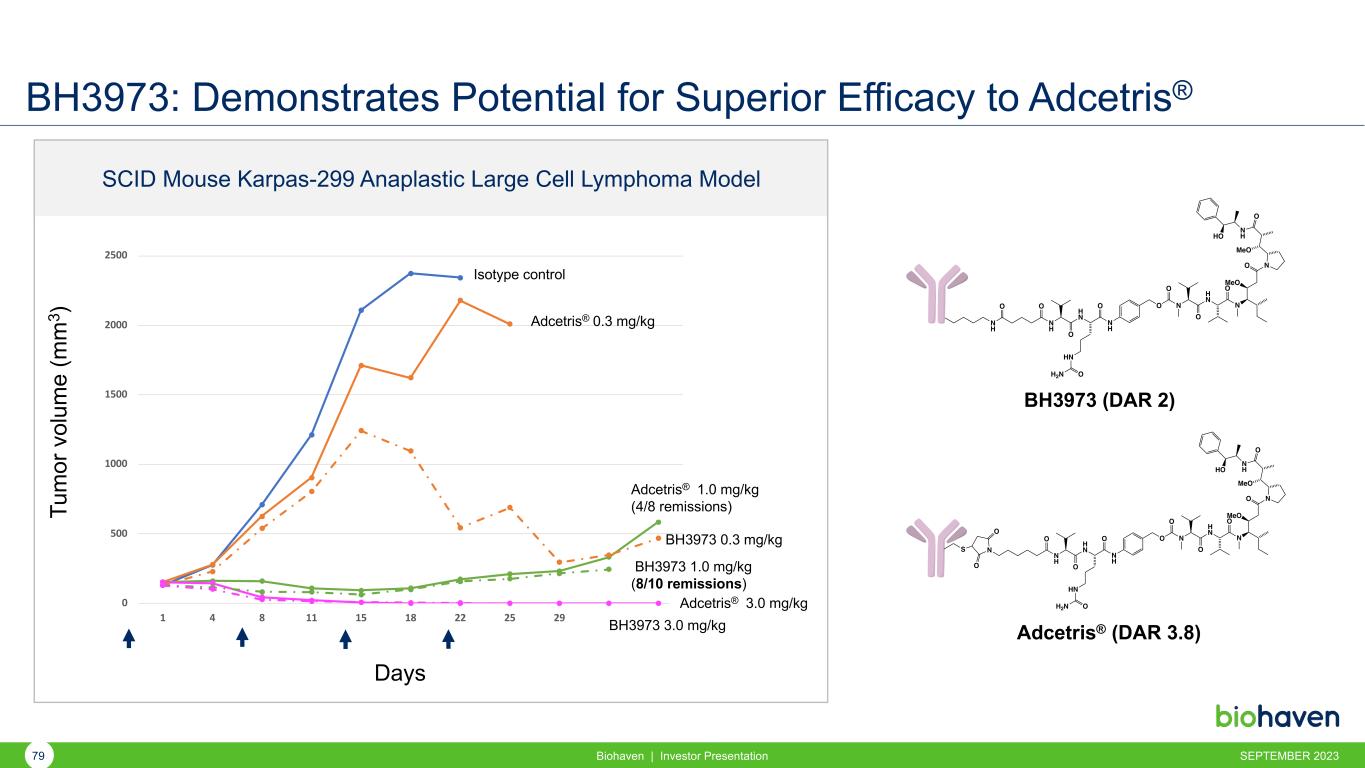
BH3973:顯示出 Adcetris® Biohaven 具有卓越療效的潛力 | 投資者演示文稿 0 500 1000 1500 2500 1 4 8 11 15 18 22 25 29 32 37BH3973 3.0 mg/kg Adcetris® 0.3 mg/kg BH3973 0.3 mg/kg Tu m 或 v ol um e (m m 3) 天同型控制 Adcetris® 3.0 mg/kg BH3973 1.0 mg/kg(8/10 緩解)N H N H O H N O HN O HN HN O HN HN O HN HN O HN HN HN O HN HN HN O HN HN HN O HN HN HN O HN HN HN O HN HN H2 N O N H O O O O O N O O O N O O N O O MeO NO MeO NO MeO N H O MeO NO MeO NO MeO NO MeO N O N O N O N O O N O N O O N O O N O O N O O N O O N O O MeO NO O MeO NO NO MeO NO NO MeO NO NO NO MeO NO NO NO MeO NO NO NO NS O O SCID 小鼠 Karpas-299 間變性大細胞淋巴瘤模型 Adcetris® 1.0 mg/kg (4/kg 8 BH3973緩解) 2023-79 年 9 月

BH3973:與有效載荷為一半的 Adcetris® 相比,提高了臨牀前模型中的存活率 Biohaven | 投資者演示 0 5 10 15 20 25 30 35 40 45 50 55 60 0 10 20 30 50 60 70 90 100 治療對存活率的影響(劑量 @ 0.3 mg/kg + 對照組)研究日 Su rv iv al(%)不治療 BH3973 0.3 mg/kg 車輛 Adcetris 0.3 mg/kg 0 5 10 15 20 25 30 40 45 50 55 60 0 10 20 30 40 50 60 70 80 90 100 研究日 Su rv iv al (%) 治療對存活率的影響(劑量 @ 1.0 mg/kg + 對照組)無治療 BH3973 1.0 mg/kg 車輛 Adcetris 1.0 mg/kg 的影響對存活率的治療(劑量 @ 0.3 mg/kg + 對照組)治療對存活率的影響(劑量 @ 1.0 mg/kg + 對照組)202380 年 9 月

BH3973:摘要:通過提高安全性、有效性、可製造性和專利壽命,Adcetris® 和優化的彈頭等現有的高效 ADC 格式有可能得到增強 ü 與 Adcetris® 相比 BH3973 的體內功效和安全性結果有所不同 üBroad 的專利覆蓋範圍 BIOHAVEN 的 ADC 技術是內部開發的獨特抗體、雙特異性甚至競爭分子的理想補充 2023 年 9 月 Biohaven | 投資者演示81

資本化考量CGRP特許權使用費:輝瑞將對rimegepant和zavegepant的年美國淨銷售額超過52.5億美元的年淨銷售額支付特許權使用費,但受年度上限(每年4億美元)3~3.49億美元2股現金和有價證券潛在特許權使用費1.不包括未完成的選項。2.截至2023年7月27日。3.如果rimegepant和zavegepant的年度總淨銷售額達到81.5億美元,則達到上限。特許權使用費將針對截至40年12月31日或之前的年度支付。Biohaven | 投資者演示文稿82 6830萬2023年9月1日

適應症 2023 年上半年 2023 2024 BHV-7000 Kv7 通道激活劑局灶性癲癇雙相情感障礙 BHV-7010 Kv7 通道激活劑癲癇和情緒障礙 BHV-2100 TRPM3 慢性疼痛症 BHV-8000 TYK2/JAK1 神經炎症 Troriluzole NCE 利魯唑強迫症前藥 Taldefgrobep alfa 抗肌抑素腺激素脊髓肌萎縮代謝障礙 BHV-1300 IgG 降解劑免疫介導疾病 GD-Iga1 降解劑 IgA 腎病提交研究所預期的短期里程碑 2023 年 9 月 Biohaven | 投資者演示文稿83里程碑已完成註冊啟動第 3EEG 生物標記物數據階段 1 Topline 啟動第 3 階段提交 IND 啟動第 1 階段啟動第 2 階段 — PD 完成註冊啟動 3* 計劃進行中 | PD、帕金森氏病提交 IND /開始第 1 階段啟動第 2 階段提交 IND