| 走在 罕見病療法的最前沿 公司概述 2023 年 9 月 |
| 2 前瞻性陳述 本演示文稿包含1995年《私人證券訴訟改革法》所指的 “前瞻性陳述”,涉及我們的候選產品的臨牀前和臨牀開發、臨牀前研究和臨牀試驗結果的時間和報告、我們的候選產品可能獲得監管部門批准的前景和時間、 商業化計劃、製造和供應計劃、融資計劃以及公司的預計收入和現金狀況。包含前瞻性陳述不應被我們視為表示我們的任何計劃都將實現。本演示文稿中的任何或全部前瞻性陳述都可能被證明是錯誤的,並可能受到我們可能做出的不準確假設或已知或未知的風險和不確定性的影響 。例如,關於與監管機構討論的目標、進展、時機和結果(包括受到 COVID-19 相關幹擾的影響)的陳述,均基於當前信息。COVID-19 疫情對運營的潛在影響本質上是未知的,無法充滿信心地預測,並且可能導致實際業績和業績與本新聞稿中的陳述存在重大差異,包括但不限於 ,因為這會對總體政治和經濟狀況產生影響,包括政府當局努力緩解 COVID-19,例如旅行禁令、 就地避難令以及第三方業務關閉和資源分配、製造和供應鏈中斷以及限制患者獲得商業或臨牀 產品。除了 COVID-19 疫情的影響外,由於我們業務固有的風險和不確定性,實際結果可能與本新聞稿中列出的結果存在重大差異, 包括但不限於:臨牀或臨牀前研究的結果可能表明候選產品不安全或無效;可能很難將 患者納入我們的臨牀試驗;監管機構,包括FDA、EMA、MHRA 和 PMDA,可能不會批准或可能推遲對我們產品的批准候選人;需要監管部門檢查的潛在 可能被推遲或不成功並延遲或阻礙產品批准;如果獲得批准,我們可能無法在 歐洲、日本、美國和其他地區或 AT-GAA 成功將 Galafold 商業化;臨牀前和臨牀研究可能會因為我們發現嚴重的副作用或 其他安全問題而被推遲;我們可能無法成功商業化能夠製造或供應足夠的臨牀或商業產品;以及我們的潛力需要額外的資金來完成 我們所有的研究和製造。此外,早期臨牀前研究和/或臨牀試驗的結果可能無法預測未來的結果。關於企業財務 指導和財務目標以及實現這些目標的聲明。關於公司收入和現金狀況預測的報表,根據 市場因素以及公司執行運營和預算計劃的能力,實際業績可能會有所不同。此外,所有前瞻性陳述均受其他風險的影響,詳見我們截至2022年12月31日止年度的 10-K表年度報告和截至2023年6月30日的季度10-Q表格。提醒您不要過分依賴這些前瞻性陳述, 這些陳述僅代表截至本文發佈之日。所有前瞻性陳述均受本警示聲明的全部限制,我們沒有義務修改或更新本新聞 新聞稿以反映本文發佈之日之後的事件或情況。 非公認會計準則財務指標 除了根據美國公認會計原則編制的財務信息外,本演示文稿還包含調整後的財務指標,我們認為這些指標為投資者和管理層提供了 與經營業績和趨勢相關的補充信息,便於各時期之間以及預測信息的比較。這些調整後的財務 指標是非公認會計準則指標,應作為根據美國公認會計原則編制的信息的補充,但不能作為其替代品。我們通常排除某些 GAAP 項目,這些項目管理層認為這些項目不會影響我們的基本運營,也不符合 GAAP 對異常或非經常性項目的定義。其他公司可能以不同的方式定義這些 衡量標準。當我們在前瞻性基礎上提供對非公認會計準則運營支出的預期時,如果不合理的努力,通常無法對非公認會計準則 預期與相應的公認會計準則指標之間的差異進行對賬,這是因為 在相關未來時期被排除在GAAP指標之外的項目(例如異常收益或虧損)可能存在很高的變異性、複雜性和可見性低。排除項目的可變性可能會對我們未來的GAAP業績產生重大影響,而且可能是 不可預測的影響。 |
| 3 一家稀有公司 專注於患者的罕見病生物技術公司,收入持續兩位數增長 ,擁有全球商業基礎設施和後期開發能力 GLOBAL 商業 組織 遍佈20個國家的員工 GALAFOLD & POMBILITI + OPFOLDA Gene Therapy POMBILITI POMBILITI Gene Therapy 平臺 br 利用 } 蛋白質 工程 和糖生物學方面的經驗 14-18% 2023 財年 Galafold 收入增長 CER Non-Gaap 盈利能力 預計在 2023 年下半年累計 150 億美元- 潛在峯值 20 億美元 AT-GAA 截至 23 年 6 月 30 日 Pompe Disease 正在接受美國 監管審查 2.66 億美元 現金 Cash 世界一流的 臨牀 開發 能力 |
| 2023 Strategic 優先事項 CER1 將 Galafold 收入保持兩位數增長 14-18% 獲得 FDA、EMA 和 MHRA 批准 AT-GAA 啟動全球成功推出 AT-GAA Advance 下一代 Fabry and Pompe pipeline 在盈利道路上保持強勁的財務狀況 4 1 2 3 4 5 1 CER:2023 恆定匯率;Galafold 收入指引採用截至2022年12月31日的實際匯率 |
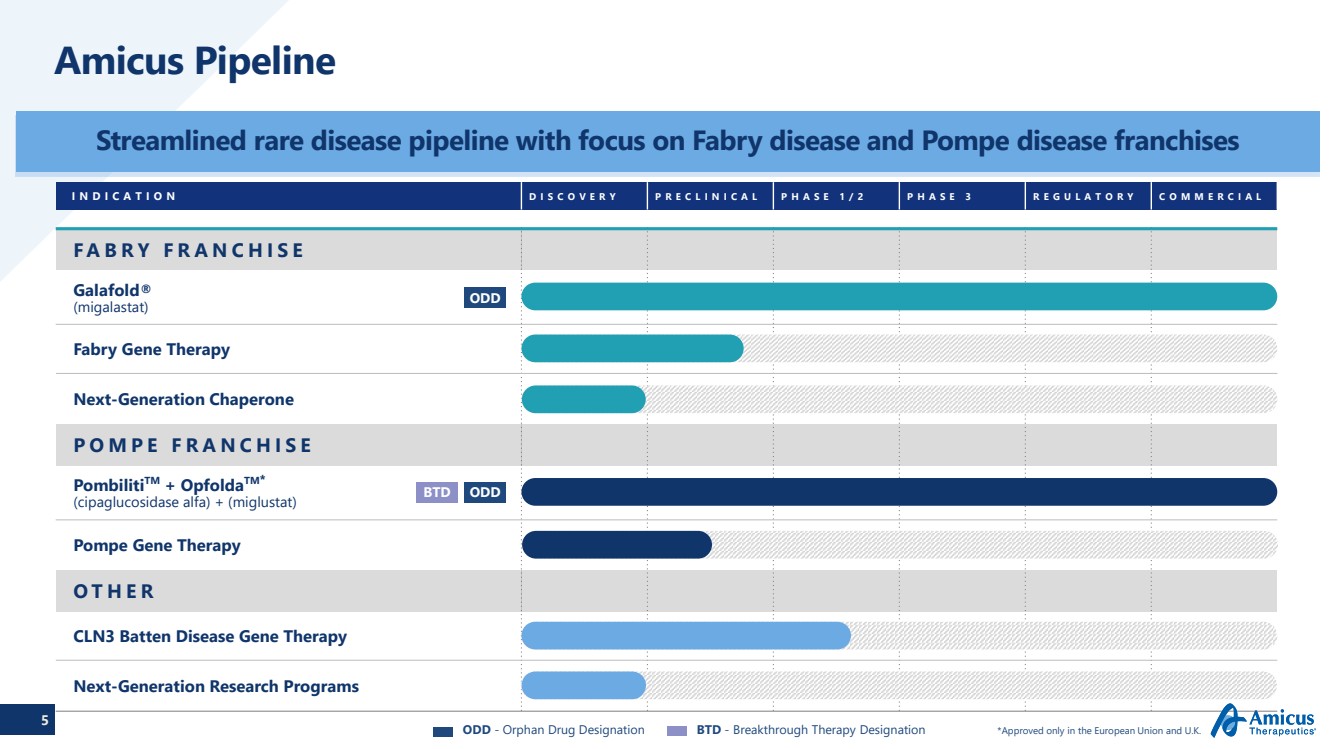
| 5 Amicus Pipeline 精簡了罕見病產品線,重點是法布里病和龐貝氏病特許經營權 適應症臨牀前 1/2 期 3 期監管廣告 Fabry FRANCHISE (migalastat) Fabry 基因療法 Fabry 基因療法 PombilitiTM + opfoldatm* Fabry 基因療法 下一代 Chaperone PombilitiTM + opfoldatm* (cipaglucosidase alfa) + (miglustat) Pompe 基因療法 其他 CLN3 巴頓病基因療法 下一代研究計劃 ODD BTD ODD ODD-孤兒藥名稱 BTD-突破性療法稱號 *僅在歐盟和英國獲得批准 |
| 6 Galafold®(migalastat) 持續增長 在 治療法布里病方面樹立領導地位 |
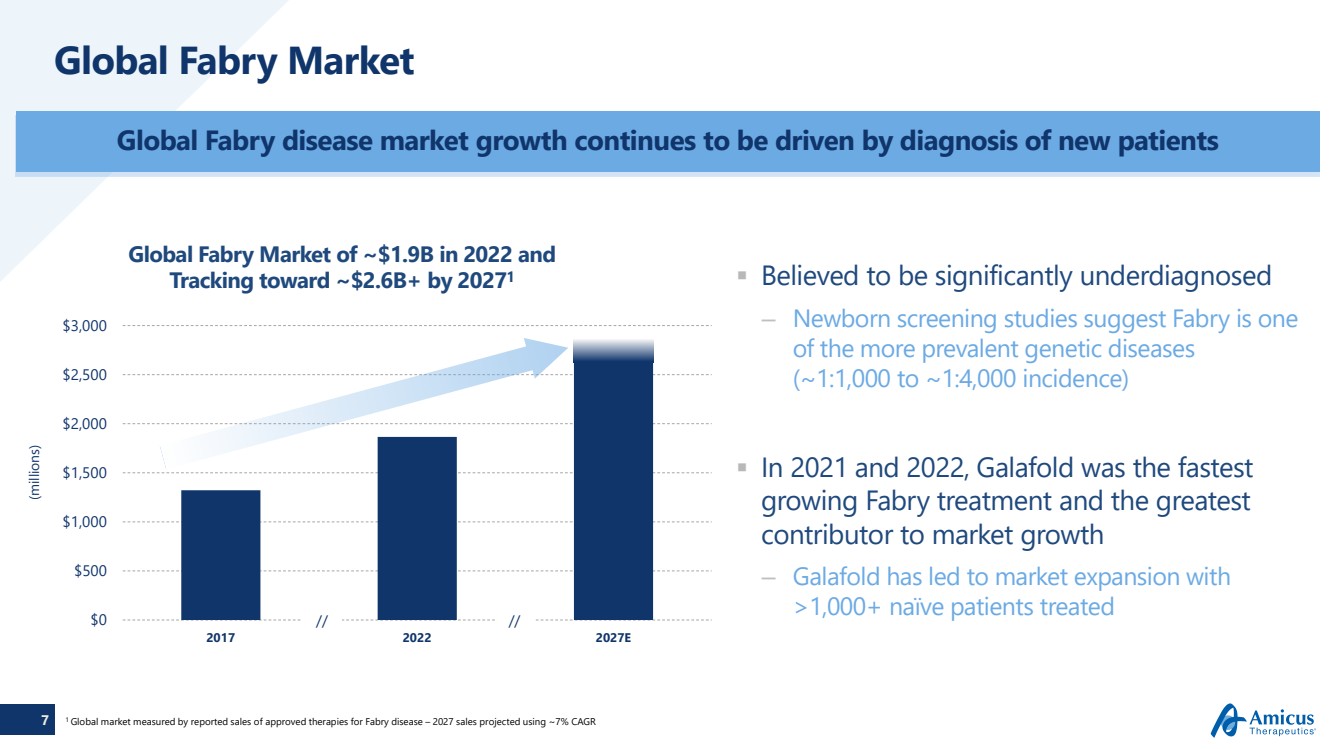
| 7 Global Fabry Market 據信診斷嚴重不足 — 新生兒篩查研究表明,Fabry 是 中較為流行的遺傳病之一 (發病率約為 1:1,000 至約 1:4,000) >1,000多名天真患者接受了治療 Global Fabry 疾病市場的增長繼續由新患者的診斷推動 (百萬) 1 全球市場以報告的已批准銷售額衡量法布里病療法 — 2027 年銷售額預計年複合增長率約為 7% 0 500 美元 1,000 美元 1,500 美元 1,500 美元 2,500 美元 2,500 美元 2017 年 2022 年 2027 年 2027 年 Fabry 全球市場約為 19 億美元 到 2027 年將達到約 26 億美元/// |
| 8 2023 Galafold Success(截至 2023 年 6 月 30 日) 以 Galafold 的成功為基礎,利用領導地位推動持續增長 Galafold 適用於確診為法布里病且變異適宜的成年人。Galafold (≥ 10%) 報告的最常見不良反應是頭痛、鼻咽炎、尿路感染、噁心和發熱。有關 Galafold 的更多信息,包括完整的美國處方信息,請 訪問 https://www.amicusrx.com/pi/Galafold.pdf。有關Galafold的更多重要安全信息,包括毒理學和給藥方法、特殊警告、 藥物相互作用和藥物不良反應,請訪問EMA網站www.ema.europa.europa.eu上提供的歐洲SmPC for Galafold。 Galafold 是第一個也是唯一一個經批准的具有獨特作用機制的口服 治療方案,適用於具有適應變異的 Fabry 患者 35-50% Fabry 患者 Fabry 患者 40+ 獲得 監管機構 批准的國家 53 Orange Book 上市專利 9430萬美元 230萬美元 230萬美元 230萬美元 第 23 季度 Galafold 收入 14-18% 2023 年 Galafold CER 的運營增長 60% 接受治療 Amenable 患者的份額 |
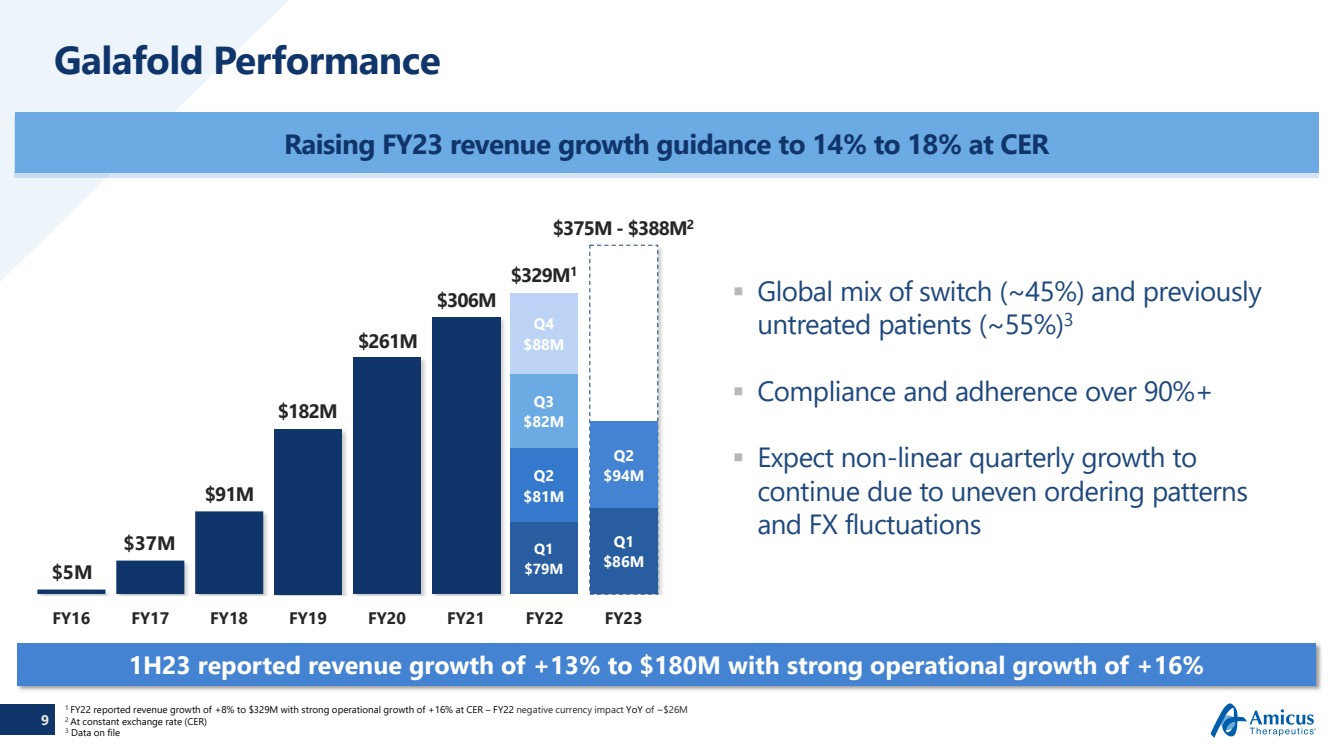
| 9 Galafold Performance 將CER的23財年收入增長預期提高至14%至18% Switch(約45%)和以前未接受治療的患者(約55%)的全球組合 3 合規性和依從性超過90% + 由於訂購模式不均衡和外匯波動 2016財年2018財年2020財年2022財年預計非線性季度增長將繼續 2017財年2017財年2018財年2022財年 500 萬美元 第一季度7.9億美元 第二季度8100萬美元 第三季度8200萬美元 第四季度8,800萬美元 3700萬美元 9100萬美元 1.82億美元 2.61億美元 3.06億美元 2023 年上半年公佈收入增長 +13% 至 1.8 億美元,運營增長強勁 +16% 3.29億美元 3.29億美元強勁的運營增長第一季度8.6億美元 3.75億美元-3.88M2 第二季度9400萬美元 1 2022財年收入增長8%,達到3.29億美元,按固定匯率計算,運營增長強勁增長16% — 22財年匯率負面影響同比約為2600萬美元 2 按固定匯率 (CER) 計算 3 存檔數據 |
| 10 Galafold Global Commercial Momentum(截至2023年6月30日) 強勁的患者需求和關鍵指標表現為2023年持續兩位數增長奠定了基礎 持續滲透現有市場 未經治療的確診人羣進一步增加 持續的地域擴張和標籤延長 保持合規性和依從性 推動報銷和准入 2023 年的持續增長受以下因素推動: |
| 11 Pombiliti®(cipaglucosidase alfa) + Opfolda®(miglustat) 有可能為龐貝病患者建立新的護理標準 |
| 12 缺乏 GAA 會導致溶酶體 糖原積累和細胞 功能障礙 在人生的不同階段,從童年到成年 被診斷出來 症狀包括進行性肌肉 無力,尤其是骨骼和呼吸 肌肉,會隨着時間的推移而惡化 呼吸衰竭是主要的 死亡原因 約5,000-10,000人被診斷出來 } 全球;嚴重的診斷不足 約12億美元+全球 Pompe ERT 銷售額1 大多數採用當前 護理標準的患者在 大約 2 年後下降 晚發性龐貝病 (LOPD) 概述 1 基於截至2022年12月31日的12個月。來源:賽諾菲新聞稿 遲發的龐培病是一種罕見、使人衰弱且危及生命的溶酶體疾病,由 酸 α-葡萄糖苷酶 (GAA) 缺乏引起 |
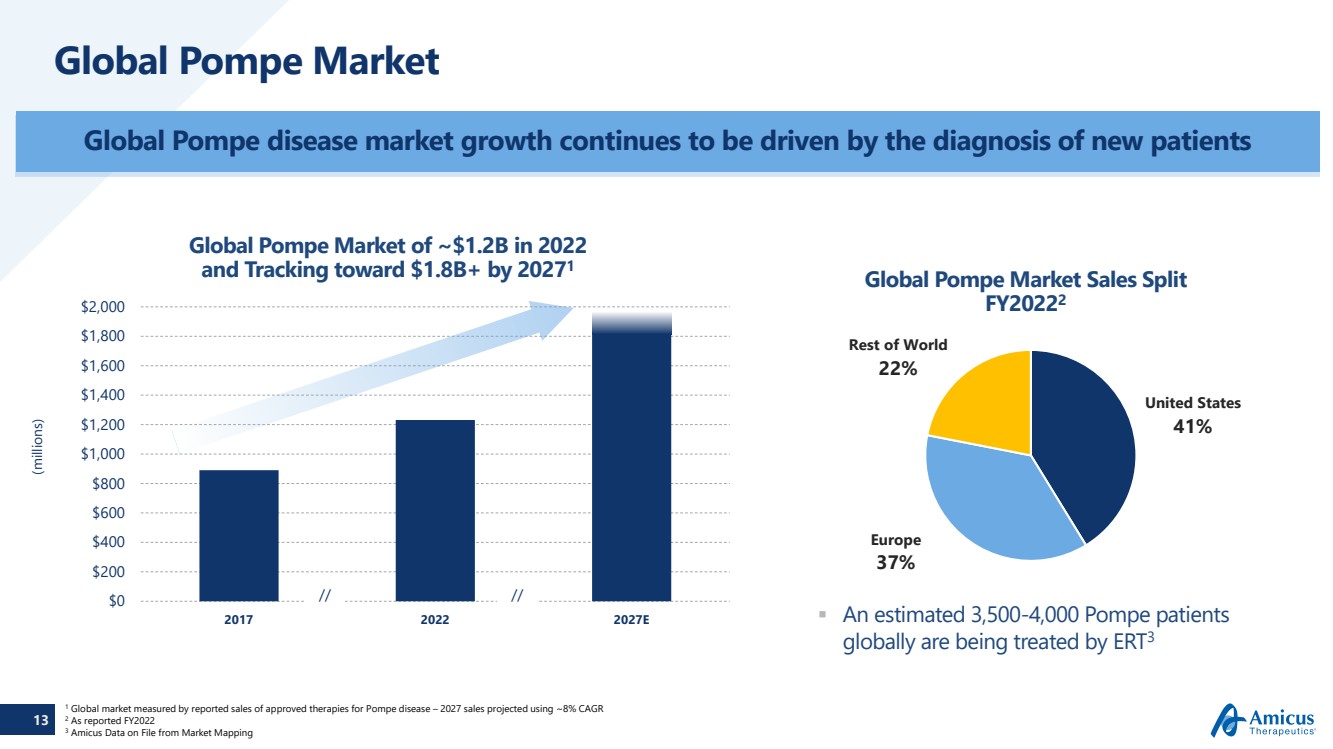
| 13 全球龐貝病市場 全球龐貝病市場的增長繼續由新患者的診斷推動 據估計,全球有3500-4,000名龐貝患者 正在接受ERT3全球龐貝病人的治療,2022年約為12億美元,到2027年將達到18億美元以上(百萬) 0 200 美元 600 美元 800 美元 1,200 美元 1,400 美元 1,600 美元 1,800 美元 1,800 美元 1,200 美元 1,400 美元 1,800 美元 1,800 美元 1,800 美元 1,800 美元 1,800 美元 1,800 美元 1,800 美元 1,800 美元 1,800 美元 1,800 美元 1,800 美元 1,800 美元 1,800 美元 1,800 美元 1,800 美元 1,800 美元 1,800 美元 1,2,000 2017 2022 2027E 1 全球市場以龐貝病獲批療法報告的銷售額來衡量 — 2027 年的銷售額預計複合年增長率約為 8% 2 據報道的 FY2022 3 Amicus 數據來自市場測繪 //// 美國 41% 歐洲 37% 世界其他地區 22% Global Pompe 市場銷售細分 FY20222 |
| 14 AT-GAA:治療龐貝病的創新方法 我們的科學家創造了一種獨特的糖基化和高度磷酸化的 ERT (cipaglucosidase alfa),可顯著增強對關鍵受影響肌肉的靶向 AT-GAA 是一種雙組分療法,結合了 cipaglucosidase alfa(ERT)和口服 酶穩定劑 miglustat 由一種獨特的細胞系組成,該細胞系產生一種天然 糖基化酶,該酶可以在溶酶體內正確處理 成熟形態,這是 以最佳方式分解糖原所必需的cipaglucosidase alfa miglustat 1 Selvan 等人 2021 年,J Biol Chem 2021 年 1 月至 6 月;296:100769 ERT:酶替代療法 |
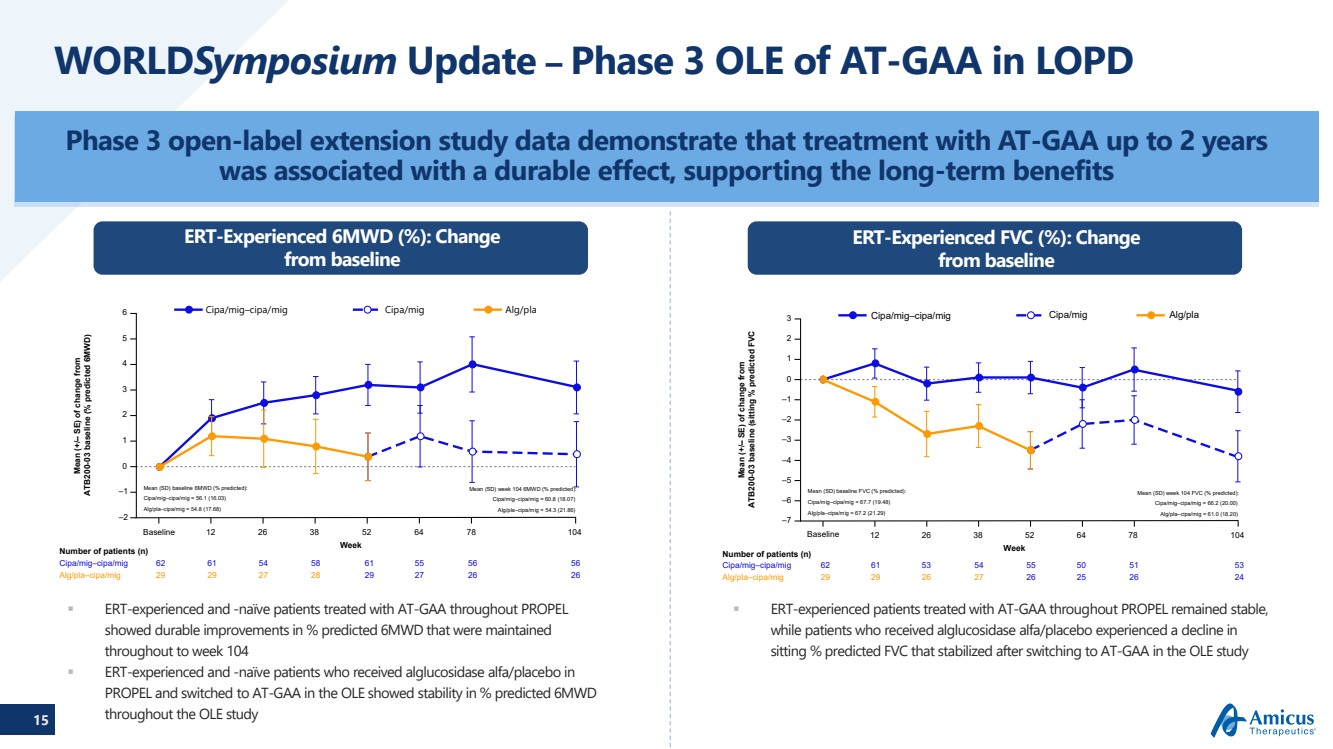
| 15 世界研討會更新 — LOPD 中 AT-GAA 第 3 期 OLE 患者人數 (n) 平均值 (SD) 基線 6MWD(預測百分比): cipa/mig—cipa/mig = 56.1 (16.03) alg/pla—cipa/miG = 54.8 (17.68) Mean (SD) 第 104 周 6MWD(預測百分比)): cipa/mig—cipa/mig = 60.8 (18.07) alg/pla—cipa/mig = 54.3 (21.86) 6 cipa/mig cipa/mig cipa/mig Baseline Week 12 26 38 64 78 104 —1 0 1 2 3 4 5 cipa/2 0 1 2 3 4 5 cipa/mig—cipa/mig 62 61 54 58 61 56 56 alg/pla—cipa/miG 29 29 27 28 29 29 29 29 27 27 27 26 26 與 ATB200-03 基線相比的變化均值(+/— SE)(預測為 6MWD 的百分比) Mean(SD) 基線 FVC(預測百分比): cipa/mig—cipa/mig = 67.7 (19.48) alg/pla—cipa/mig = 67.2 (21.29) Mean (SD) 第 104 周 FVC(預測百分比): cipa/mig—cipa/mig = 66.2 (20.00) alg/mig = 66.2 (20.00) alg/mig —cipa/mig = 61.0 (18.20) —7 —5 —3 —3 —1 0 1 2 3 cipa/mig—mig cipa/mig alg/pla —4 —2 —6 患者人數 (n) 周 12 26 38 52 64 64 78 104 cipa/mig—cipa/mig 62 53 54 50 53 Alg/mig 62 53 54 50 53 Alg/mig —cipa/miG 29 29 26 27 26 26 25 26 24 基線 與 ATB200-03 基線相比的變化均值(+/— SE)(坐姿百分比預測 FVC 第 3 階段開放標籤擴展研究數據顯示AT-GAA 治療長達 2 年 會產生持久的效果,從而支持長期益處 在整個 PROPEL 中使用 AT-GAA 治療的 ERT 經驗豐富且天真的患者 PROPEL 在 PROPEL 中接受了 alglucosidase alfa/安慰劑的百分比顯示出持續改善 PROPEL 中有 104 名在 PROPEL 中接受 alglucosidase alfa/安慰劑的患者 在 OLE 中改用 AT-GAA 在整個 OLE 研究中顯示出穩定性 6MWD 的預測百分比 在整個 PROPEL 中經過 AT-GAA 治療的 ERT 患者保持穩定, 雖然接受algucosidase alfa/安慰劑治療的患者 坐着率下降在 OLE 研究中預測 FVC 在改用 AT-GAA 後會穩定下來 ert 經驗的 6MWD (%):與基線相比變化 ERT 經驗 FVC (%):與基線相比變化 |
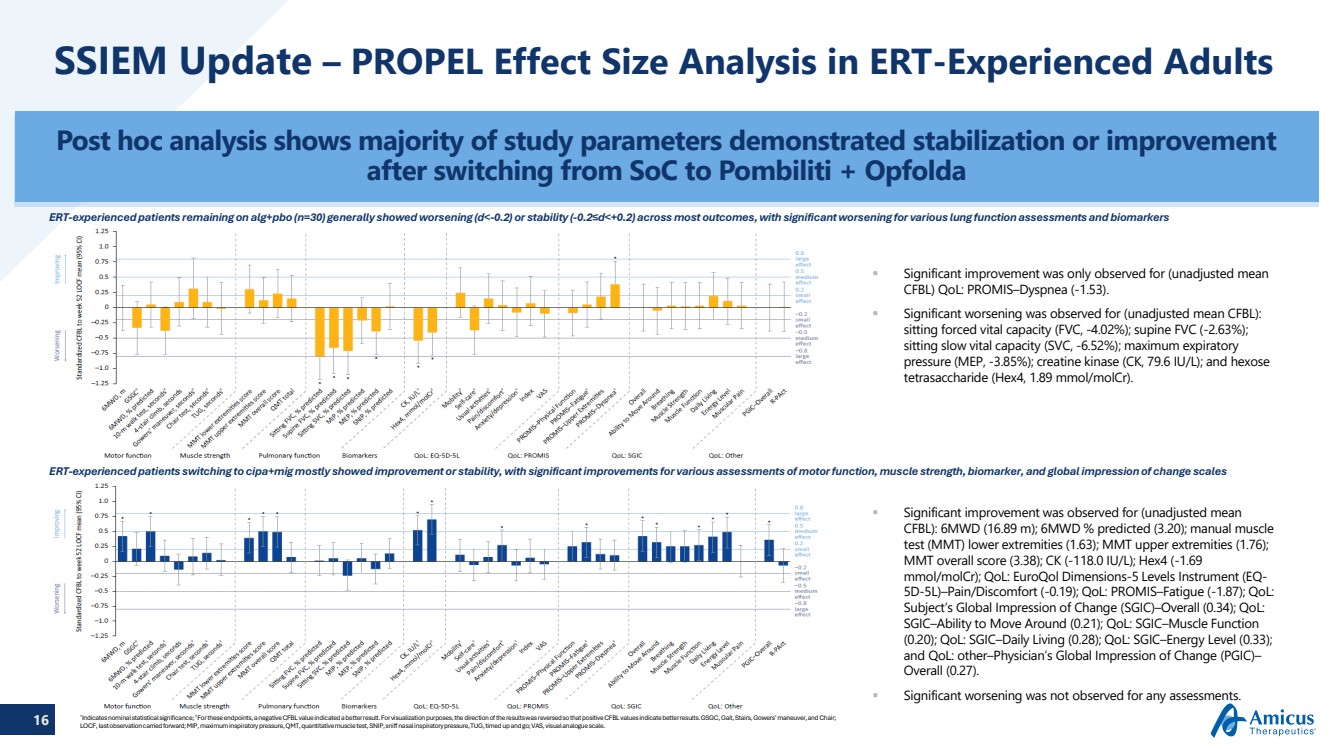
| 16 SSIEM 更新 — 對有 ERT 經驗的成年人進行 PROPEL 效應大小分析 事後分析顯示,從 SoC 切換到 Pombiliti 後,大多數研究參數都顯示出穩定或改善 + Opfolda 僅在(未經調整的平均值 CFBL)QoL:Promis—dyspNEA(-1.53)中才觀察到顯著改善。 觀察到(未經調整的平均CFBL)明顯惡化: 坐姿強制肺活量(FVC,-4.02%);仰卧FVC(-2.63%); 坐姿緩慢肺活量(SVC,-6.52%);最大呼氣 壓力(MEP,-3.85%);肌酸激酶(CK,79.6 IU/L);和己糖 四糖(Hex4,1.89 mmol/molcr)。 觀察到(未經調整的平均值 CFBL):6MWD(16.89 m);6MWD 預測百分比(3.20);手動肌肉 測試(MMT)下肢(1.63);MMT 上肢(1.76); MMT 總分(3.38);CK(-118.0 IU/L);Hex4(-118.0 IU/L);Hex4(-76)1.69 mmol/molcr);QoL:euroQoL Dimensions-5 Levels 儀器 (EQ-5D-5L) — 疼痛/不適 (-0.19);QoL:Promis—疲勞 (-1.87);QoL: sgic—四處走動的能力 (0.21);QoL:sgic—肌肉功能 (0.20);QoL:sgic—Daily Living (0.28);QoL:SGIC—能量水平 (0.33); 和 QoL:其他——醫師對變化的全球印象 (PGIC) — 總體 (0.27)。 在任何評估中均未觀察到明顯惡化。 繼續服用 alg+pbo(n=30)的有急診室復甦經驗的患者通常表現為惡化(d |
| 17 17 1存檔數據 全球監管狀況 預計監管部門將獲得批准並於 2023 年進入龐貝三大市場 Pombiliti® + Opfolda® 現已在英國獲得批准。 Pombiliti® + Opfolda® 現已在歐盟獲得批准 根據最近與美國食品藥品管理局的接觸, 預計將在未來幾天內獲得批准 17 |
| 18 正在進行的臨牀研究和擴大准入機制 正在對患有 LOPD 和嬰兒發作龐貝病 (IOPD) 的兒童和青少年進行臨牀研究 已有多種擴大准入機制,包括 美國、英國、德國、法國、日本和其他國家 在監管部門首次批准時,約有 200 名 Pompe 病患者服用 AT-GAA 跨推廣研究和 擴大准入計劃 全球約有 75 箇中心目前正在參與臨牀試驗 和准入計劃 儘管正在推進科學發展臨牀研究並通過多種機制提供擴大訪問範圍 1 0 至 0 歲兒童和青少年 |
| 19 Pombiliti + Opfolda EU Opportunity 有力的適應症聲明: — Pombiliti®(cipaglucosidase alfa)是一種長期的酶替代療法 ,與酶穩定劑 Opfolda (miglustat)聯合使用,用於治療晚發性龐貝病 (酸 α 葡糖苷酶)的成年人 [GAA]缺陷) >1300名患者估計在歐洲接受治療1 — 歐盟約有60名患者目前正在使用Pombiliti + Opfolda, 包括德國和奧地利的大約20名患者 正在德國上市 — 6個月的 “免費定價” 期和AMNOG報銷流程 — 首批患者已給藥,其他患者計劃開始輸液 1 Amicus 數據存檔在市場地圖中 歐盟龐貝市場目前代表着4.5億美元以上的巨大市場機會 |
| 20 Pombiliti + Opfolda 正在歐盟推出 經驗豐富、充滿激情的罕見病商業和醫療組織 支持啟動初期 Access 和 報銷 與付款人的積極互動 關注廣泛的患者准入 逐個國家 報銷流程 積極討論 以證明價值 患者需求 最初的重點是臨牀試驗 和擴大准入患者 首批患者給藥;多名 計劃輸液 正在軌道上過渡所有試驗 並擴大准入範圍90 天內德國患者 KOL 和患者 Outreach 宣傳和教育 努力 努力 關鍵治療中心與 HCP 的現有關係 在最初的 30 天內聘請頂級處方者 持續的疾病教育 績效 |
| 21 企業展望 履行我們對患者和 股東的使命 |
| 財務展望和盈利之路 建立業務、推進我們的投資組合和實現盈利的明確戰略 22 維持收入 增長 實現 財務目標 獲得批准 AT-GAA 2023 年上半年收入 1.808 億美元, 2023 年同比增長 16% Galafold 收入 2023 年 Galafold 收入 增長指引 br} 按恆定匯率計算 Galafold 和 AT-GAA 預計將推動兩位數的強勁長期增長 專注於謹慎的 支出管理 在2023年下半年實現盈利1 1 基於Amicus非公認會計準則的預測當前運營計劃下的淨收入,包括AT-GAA監管部門的成功批准和Galafold的持續增長。我們將非公認會計準則淨收入定義為GAAP淨收益,不包括基於股份的薪酬支出、或有對價公允價值的變化、折舊和攤銷、收購相關收入(支出)、清償債務虧損、資產減值損失、重組費用和所得税的影響。 2023 年非 GAAP 運營 支出預期為 3.3 億美元至 3.5 億美元 |
| 23 為實現顯著的價值增長做好準備 專注於執行並推動可持續的兩位數收入增長走上盈利之路 繼續 將 Galafold® 帶給儘可能多的 患者,維持 兩位數的運營 收入增長 成功推出 Pompe 病患者的 AT-GAA 推進 Fabry 和 Pompe diseases 的下一代 基因療法 和 Pompe diseases ,充分利用 的全球 能力和 基礎設施 作為罕見 疾病領域的領導者 2023年下半年的盈利能力 1 基於當前運營計劃下對Amicus非公認會計準則淨收入的預測,其中包括AT-GAA監管部門的成功批准和Galafold的持續增長。非公認會計準則淨收入定義為GAAP淨收益,不包括基於股份的 薪酬支出、或有對價公允價值變動、資產減值虧損、折舊和攤銷、收購相關收入(支出)、清償債務虧損、重組費用和所得税的影響。 |
| 24 成功的真正衡量標準: 影響罕見病患者的生活 YE17 2023+ >2,000 名患者* 成千上萬的患者* YE22 >350 名患者* *臨牀和商業,所有數字均為近似值 |
| 附錄 |
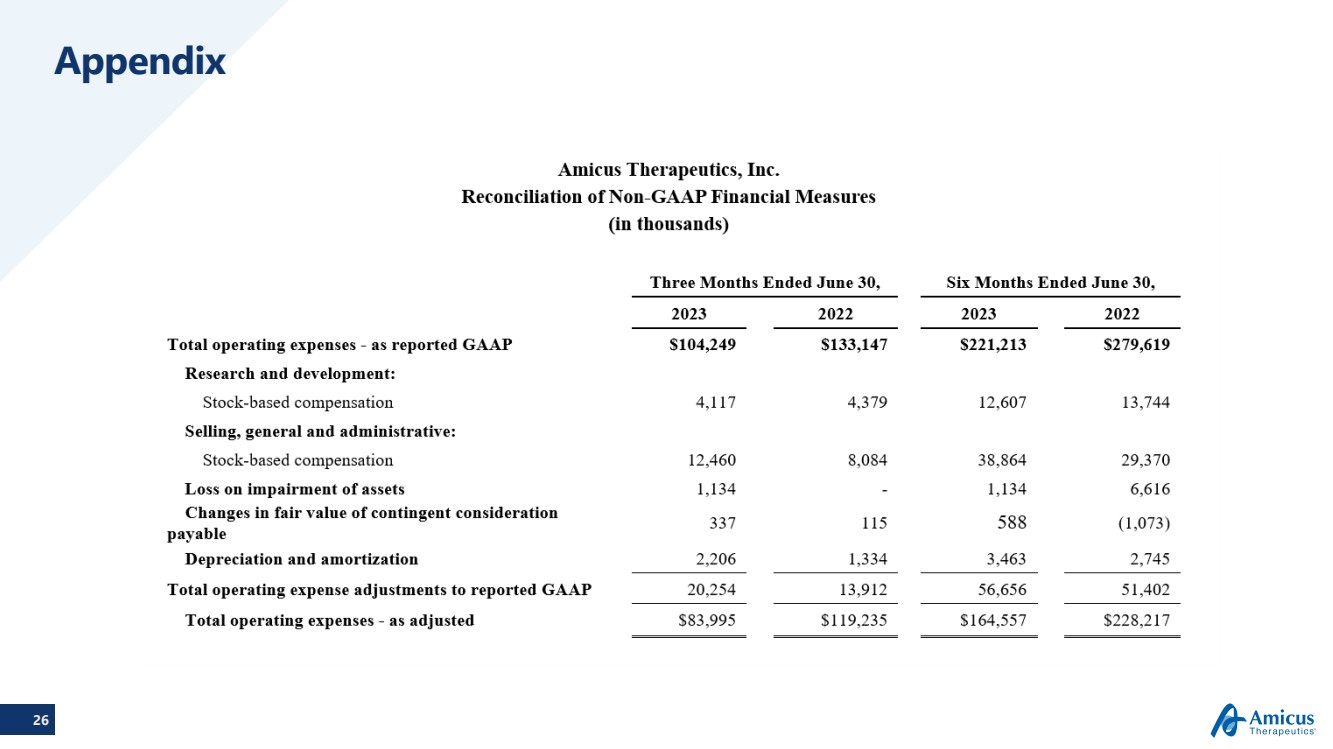
| 26 附錄 |
| 27 2023 環境、社會和治理 (ESG) 快照 董事會 致力於持續更新董事會,實現 背景、性別、技能和經驗的多樣性: 80% 董事會 獨立性 60% 董事會 多元化 解決一種罕見的遺傳病 一流或一流的 為 患者帶來有意義的益處 484 名全球員工 57% % 女性員工 我們為誰服務我們的使命是 通過整合 環境和 可持續發展 原則,與我們的合作伙伴 一起推動可持續發展 在我們所有的商業 關係中 關係中 Pledge for a Cure 將產品收入的一部分返還給 針對該特定疾病的研發,直到找到治癒方法。 我們 投資的項目 有 3 個關鍵 特徵 3 女性 2 退伍軍人身份 1 非裔美國人 董事多元化 % 招聘 Slate Diversity 97% 利用員工的能力和專業知識來提供推動績效並最終吸引、 激勵和留住關鍵人才的 文化。 員工招聘、 敬業度和留存率 Pulse 調查顯示,員工對自己的工作感到很高的個人 滿意度,為自己的工作和對社區的貢獻感到自豪 職業發展 重新構想的績效管理流程,以 衡量內容和方式,獎勵那些模仿我們以使命為中心的行為的人。 致力於為患者生產 變革性藥物 ,同時在我們的 運營中履行環境 責任並堅持 可持續發展最佳實踐。 環境 管理 0% Amicus 自有直接製造和 相關的温室氣體排放 多元化、公平和 包容性 (DEI) 承諾支持更具包容性的文化,以影響 我們的員工、社區和社會。 目標是保持性別多樣性和 提高我們全球員工隊伍的整體多樣性。 580 志願者時長 (美國): 22 Amicus 支持 社區計劃: 79 名患者 /19 個國家 將訪問範圍擴大到 2023 年 2 月: Pricing PROMISE 已分配的捐款: 2,288,998 美元 954,349 美元國際 Charitability Giving 承諾永遠不會將我們 產品的年價格提高得超過消費者通貨膨脹。 |
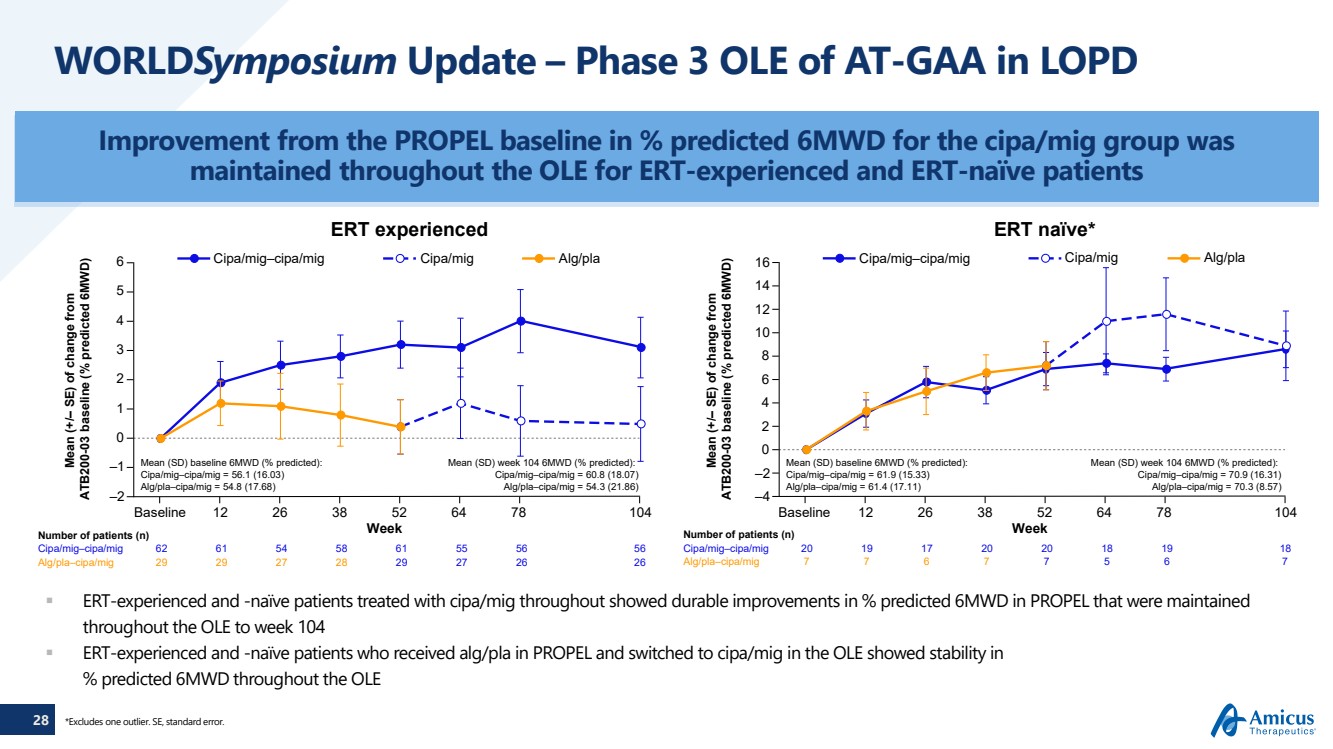
| 28 世界研討會更新 — LOPD 中的 AT-GAA 第 3 期 OLE 與 PROPEL 基線相比的改善百分比為 cipa/mig 組預測 6MWD 的百分比在整個 OLE 中保持不變 有ERT經驗的患者和一直接受cipa/mig治療的天真患者在維持的PROPEL中預測的6MWD百分比顯示出持續改善 在整個 OLE 到第 1 周,104 名在 PROPEL 中接受 alg/pla 然後在 OLE 中改用 cipa/mig 的患者,在整個 OLE 中預測為 6MWD 的 % 中表現出穩定性 %} *不包括一個異常值。SE,標準錯誤。 患者人數 (n) 平均值 (SD) 基線 6MWD(預測百分比): cipa/mig—cipa/mig = 56.1 (16.03) alg/pla—cipa/mig = 54.8 (17.68) Mean (SD) 第 104 周 6MWD(預測百分比): cipa/mig—cipa/mig = 54.8 (17.68) Mean (SD) 第 104 周 6MWD(預測百分比): cipa/mig g = 60.8 (18.07) alg/pla—cipa/mig = 54.3 (21.86) 6 cipa/mig—cipa/mig alg/pla 基線 Week 12 26 38 52 64 78 104 平均值 (SD)) 基線 6MWD(預測百分比): cipa/mig—cipa/mig = 61.9 (15.33) alg/pla—cipa/miG = 61.4 (17.11) Mean (SD) 第 104 周 6MWD(預測百分比): cipa/mig—cipa/mig = 70.9 (16.31) alg/pla—cipa/mig = 70.3 (8.57) —2 —4 0 2 4 6 8 12 14 16 —1 0 1 2 3 4 5 cipa/mig—cipa/mig alg/pla cipa/mig—cipa/mig 61 54 58 61 55 56 56 29 27 26 cipa/mig—cipa/mig 20 19 19 17 20 20 18 19 18 alg/pla—cipa/miG 29 29 27 28 alg/pla—cipa/miG 7 7 7 7 7 7 與 ATB200-03 基線(預測百分比 6MWD)的變化均值(+/ — SE) Mean (+/ — SE) 與 ATB200-03 基線的變化(預測為 6MWD 的百分比) ERT 經歷了 ERT 天真* |
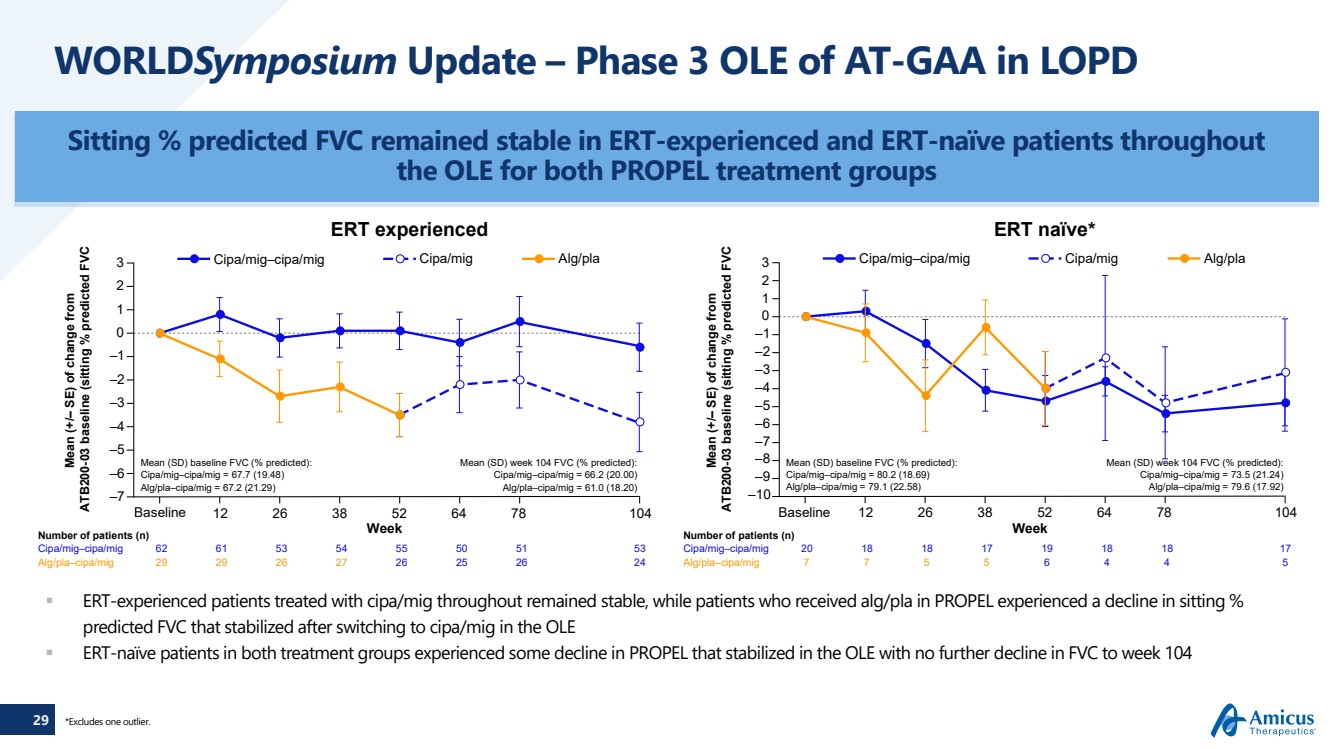
| 29 世界研討會更新 — LOPD 中 AT-GAA 第 3 期 OLE Siting% 預測在整個 中有 ERT 經驗和沒有 ERT 的患者 FVC 保持穩定 兩個 PROPEL 治療組的 ERT 經驗豐富的患者自始至終都保持穩定,而在 PROPEL 中接受 alg/pla 治療的患者坐姿下降% 預測 FVC 在改用 cipa/mig 後會穩定下來 /mig 在兩個治療組中 OLE ERT-naive 患者的 PROPEL 都出現了一些下降,在 OLE 中穩定下來,FVC 沒有進一步下降到第 104 周均值 (SD) 基線 FVC(預測百分比): cipa/mig—cipa/mig = 67.7 (19.48) alg/pla—cipa/mig = 67.2 (21.29) Mean (SD) 第 104 周 FVC(預測百分比): cipa/mig = 66.2 (20.00) {} alg/pla—cipa/mig = 61.0 (18.20) —7 —5 —3 —1 0 1 2 3 cipa/mig—mig cipa/mig alg/PLA —4 —2 —6 平均值(SD)基線 FVC(預測百分比): cipa/mig—cipa/mig = 80.2 (18.69) {} alg/pla—cipa/miG = 79.1 (22.58) Mean (SD) 第 104 周 FVC(預測百分比): cipa/mig—cipa/mig = 73.5 (21.24) alg/pla—cipa/miG = 79.6 (17.92) —7 —10 —4 0 —9 —2 1 —5 —8 —1 2 3 Cipa/mig —cipa/mig cipa/mig alg/PLA 104 —3 患者人數 (n) 周 12 26 38 52 64 78 104 患者人數 (n) 周 12 26 38 52 64 78 cipa/mig—cipa/mig 62 61 54 55 50 51 53 26 26 24 cipa/mig—mig 20 18 18 17 19 18 18 17 alg/pla—cipa/miG 29 29 26 27 alg/pla—cipa/miG 7 7 5 5 5 5 5 5 5 基線基線 ERT 經歷了 ERT 天真* ATB200-03 基線變化的平均值(+/ — SE)與 ATB200-03 基線相比的變化平均值(+/ — SE)(坐着)預測百分比 FVC *不包括一個異常值。 |
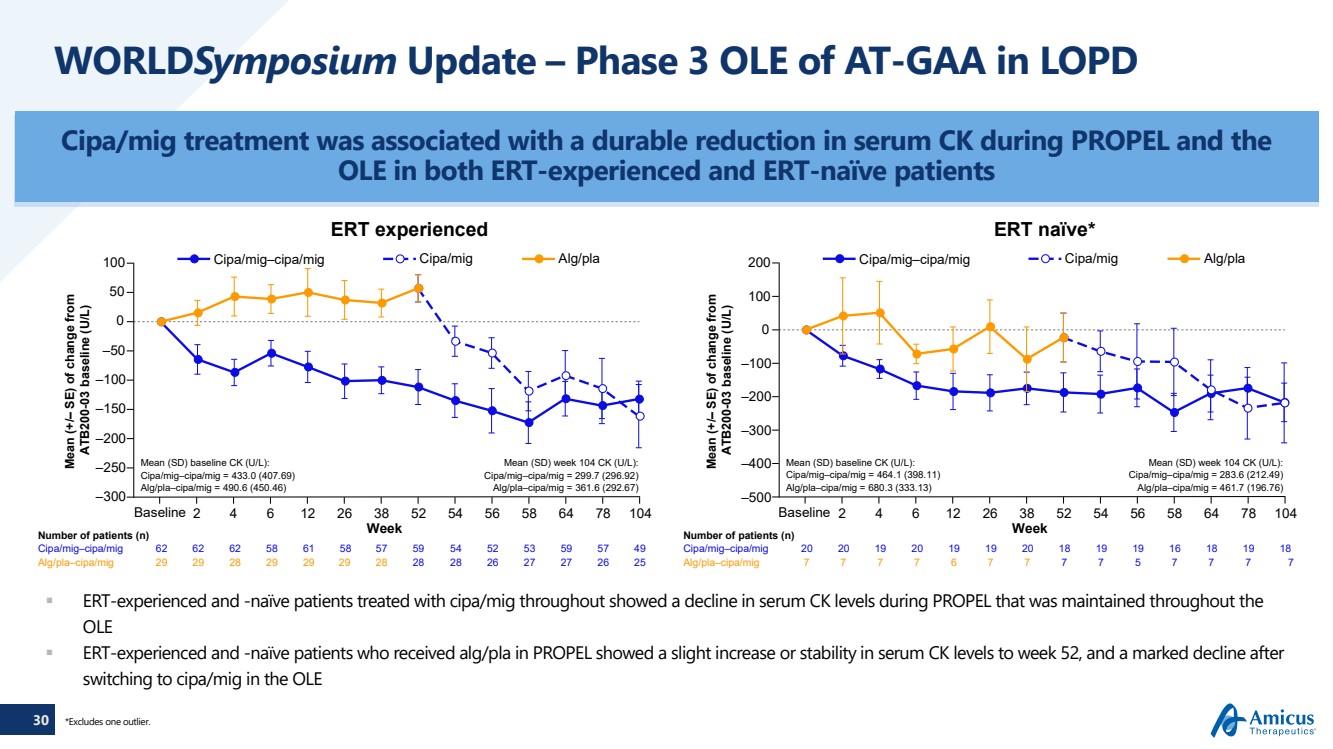
| 30 世界研討會更新 — LOPD cipa/mig 治療中 AT-GAA 的第 3 期 OLE 與 PROPEL 期間血清 CK 的持續降低有關,而在經歷過 ERT 的患者和沒有 ERT 的患者中 OLE 經驗豐富且自始至終都接受 cipa/mig 治療的天真患者在 PROPEL 期間血清 CK 水平有所下降,在 OLE {} 在 PROPEL 中接受 alg/pla 治療的 ERT 經驗豐富且天真的患者在第 52 周之前血清 CK 水平略有上升或穩定,在 改用 cipa/mig 之後,血清 CK 水平明顯下降OLE 患者人數 (n) Mean (SD) 基線 CK (U/L): cipa/mig—cipa/mig = 433.0 (407.69) alg/pla—cipa/mig = 490.6 (450.46) Mean (SD) 周 104 CK (U/L): cipa/mig—cipa/mig = 490.6 (450.46) Mean (SD) 周 104 CK (U/L): cipa/mig = 299.7 (296.92) alg/pla—cipa/miG = 361.6 (292.67) —300 —250 —200 —150 —100 —50 0 50 100 cipa/mig cipa/mig alg/PLA 2 4 6 12 26 38 52 56 64 78 104 104 患者人數 (n) mean (SD) 基線 CK (U/L): cipa/mig—cipa/mig = 464.1 (398.11) alg/pla—cipa/mig = 680.3 (333.13) Mean (SD) 第 104 CK (U/L): cipa/mig—cipa/mig = 283.6 (212.49) Alg/pla—cipa/mig = 461.7 (196.76) —400 —500 —300 —200 —100 200 cipa/mig—cipa/mig cipa/mig alg/pla 2 4 6 6 12 26 38 38 58 58 59 59 59 59 59 59 59 59 59 59 59 59 59 59 59 59 59 59 49 cipa/mig g—cipa/miG 20 19 19 19 19 19 19 19 16 19 19 19 18 alg/pla—cipa/miG 29 29 29 29 29 29 29 28 28 28 28 26 27 27 26 25 alg/pla—cipa/miG 7 7 7 7 7 7 7 7 7 7 7 7 7 7 7 7 7 7 7 7 7 7 與 ATB200-03 基線 (U/L) 的變化平均值 (+/ — SE) Mean (+L) Mean (+L) Mean (+L)/ — SE) 與 ATB200-03 基線 (U/L) 的變化 ERT 經歷了 ERT 天真* 基線基線 Week Week Week *不包括一個異常值。 |
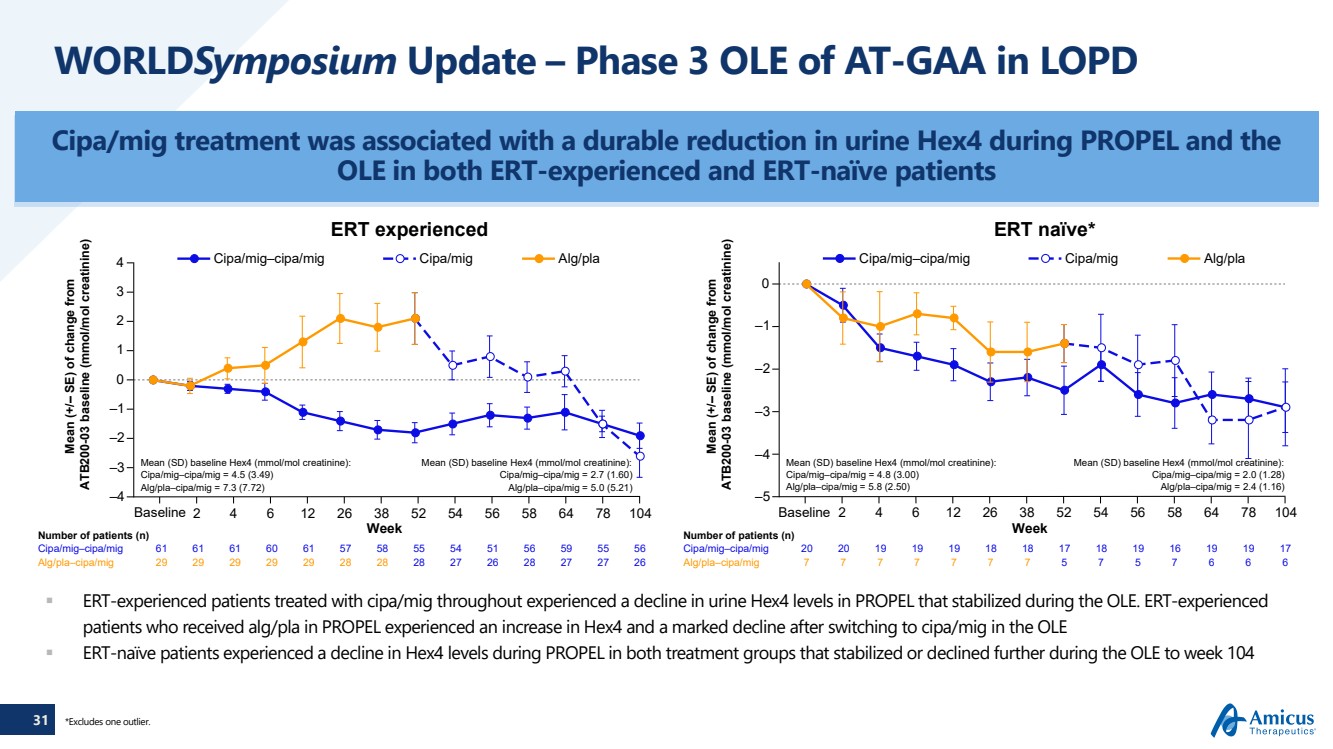
| 31 ERT-experienced patients treated with cipa/mig throughout experienced a decline in urine Hex4 levels in PROPEL that stabilized during the OLE. ERT-experienced patients who received alg/pla in PROPEL experienced an increase in Hex4 and a marked decline after switching to cipa/mig in the OLE ERT-naïve patients experienced a decline in Hex4 levels during PROPEL in both treatment groups that stabilized or declined further during the OLE to week 104 Number of patients (n) Mean (SD) baseline Hex4 (mmol/mol creatinine): Cipa/mig–cipa/mig = 4.5 (3.49) Alg/pla–cipa/mig = 7.3 (7.72) Mean (SD) baseline Hex4 (mmol/mol creatinine): Cipa/mig–cipa/mig = 2.7 (1.60) Alg/pla–cipa/mig = 5.0 (5.21) –4 –3 –2 –1 0 1 2 3 4 Cipa/mig–cipa/mig Cipa/mig Alg/pla Week 2 4 6 12 26 38 52 54 56 58 64 78 104 Number of patients (n) Mean (SD) baseline Hex4 (mmol/mol creatinine): Cipa/mig–cipa/mig = 4.8 (3.00) Alg/pla–cipa/mig = 5.8 (2.50) Mean (SD) baseline Hex4 (mmol/mol creatinine): Cipa/mig–cipa/mig = 2.0 (1.28) Alg/pla–cipa/mig = 2.4 (1.16) –4 –5 –3 –2 –1 0 Cipa/mig–cipa/mig Cipa/mig Alg/pla Week 2 4 6 12 26 38 52 54 56 58 64 78 104 Cipa/mig–cipa/mig 61 61 61 60 61 57 58 55 54 51 56 59 55 56 Cipa/mig–cipa/mig 20 20 19 19 19 18 18 17 18 19 16 19 19 17 Alg/pla–cipa/mig 29 29 29 29 29 28 28 28 27 26 28 27 27 26 Alg/pla–cipa/mig 7 7 7 7 7 7 7 5 7 5 7 6 6 6 Mean (+/ – SE) of change from ATB200-03 baseline (mmol/mol creatinine) Mean (+/ – SE) of change from ATB200-03 baseline (mmol/mol creatinine) WORLDSymposium Update – Phase 3 OLE of AT-GAA in LOPD Cipa/mig treatment was associated with a durable reduction in urine Hex4 during PROPEL and the OLE in both ERT-experienced and ERT-naïve patients Baseline Baseline ERT experienced ERT naïve* *Excludes one outlier. |
| Thank you |