

附錄 99.1 草稿 JPM22 更新 12-14-21 Lyell Immunopharma 2023 年 9 月 11 日 11

前瞻性陳述本 演示文稿中討論的某些事項是1995年《私人證券 訴訟改革法》(“PSLRA”)所指的Lyell Immunopharma, Inc.(以下簡稱 “公司”、“我們” 或 “我們的”)的 “前瞻性陳述”。除歷史事實陳述外,本演示文稿中作出的所有此類書面或口頭陳述均為前瞻性陳述,旨在由PSLRA提供的 前瞻性陳述的安全港所涵蓋。在不限制上述內容的情況下,在某些情況下,我們可能會使用諸如 “預測”、“相信”、“潛在”、“繼續”、“估計”、 、“預期”、“預期”、“計劃”、“預測”、“指導”、“展望”、“可能”、“可能”、“可能”、“可能”、“將”、 “應該” 或其他詞語之類的術語傳達未來事件或結果的不確定性,旨在識別前瞻性陳述。前瞻性陳述基於管理層 的經驗以及對歷史趨勢、當前狀況、預期未來發展和其他被認為適當的因素的看法所做的假設和評估。本演示文稿中的前瞻性陳述自本演示文稿發佈之日起作出,我們 不承擔更新或修改任何此類陳述的責任,無論是由於新信息、未來事件還是其他原因。前瞻性陳述不能保證未來的業績,並且受風險、不確定性和其他 因素的影響,其中許多因素是我們無法控制的,這些因素可能導致實際業績、活動水平、業績、成就、時間表和發展與這些前瞻性 陳述中表達或暗示的結果存在重大差異。我們向 美國證券交易委員會(“SEC”)提交的文件中標題為 “風險因素” 的部分描述了可能導致實際業績、發展和業務決策與前瞻性陳述存在重大差異的重要因素,包括但不限於以下與我們的業務固有的重大已知和未知風險和不確定性有關:地緣政治不穩定的影響; 宏觀經濟狀況和 COVID-19 疫情的揮之不去的影響;我們提交計劃的 IND 的能力或如果有的話,在預期的時間表上啟動或推進臨牀試驗;作為一家公司,我們在報名、 進行或完成臨牀試驗方面的經驗有限;我們為臨牀試驗生產和供應候選產品的能力;未在臨牀試驗中轉化的候選產品的非臨牀特徵; 臨牀試驗的結果可能與非臨牀、早期臨牀、初步或預期結果不同;重大不良事件、毒性或其他非臨牀結果與我們的相關聯的理想副作用候選產品;與 我們的候選產品獲得任何監管部門批准相關的重大不確定性;我們獲得、維護或保護與候選產品相關的知識產權的能力;我們的業務和候選產品的戰略計劃的實施 ;我們的資本資源的充足性以及實現目標所需的額外資金;其他風險,包括總體經濟狀況和監管發展,不在我們控制範圍內;以及 中描述的風險標題美國證券交易委員會文件中的 “風險因素”,包括截至2023年6月30日的季度10-Q表季度報告以及隨後向美國證券交易委員會提交的文件。2 專有
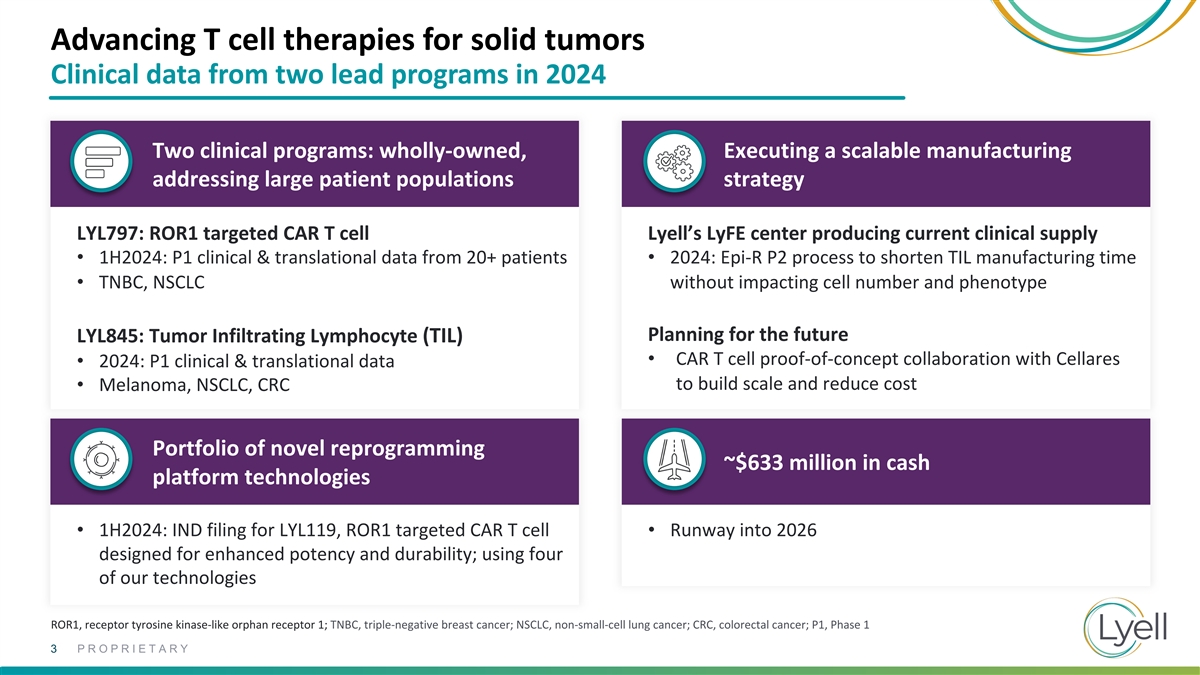
推進實體瘤的 T 細胞療法 2024 年來自兩個主要 項目的臨牀數據兩個臨牀項目:全資,執行鍼對大量患者羣體的可擴展生產戰略 LYL797:ROR1 瞄準了 CAR T 細胞萊爾的 LyfE 中心生產當前的臨牀供應 • 1H2024:來自 20 多名患者的 P1 臨牀和轉化數據 • 2024 年:Epi-R P2 流程可在不影響細胞的情況下縮短 TIL 製造時間 • TNBC、NSCLC 數量和表型規劃未來 LYL845:腫瘤浸潤淋巴細胞 (TIL) • CAR T 細胞證明-與 Cellares 的概念合作 • 2024 年:P1 臨牀和轉化數據以擴大規模並降低成本 • 黑色素瘤、非小細胞肺癌、結直腸癌的新型重編程組合現金平臺約6.33億美元 技術 • 1H2024:LYL119、ROR1 靶向 CAR T 細胞的 IND 申請 • Runnay to 2026 專為增強效力和耐久性而設計;使用我們的四項技術 ROR1,受體酪氨酸激酶樣孤兒受體 1;TNBC, 三陰性乳腺癌;非小細胞肺癌,非小細胞肺癌;結直腸癌;結直腸癌;P1,1 期 3 專有

萊爾正在開發兩種類型的個性化細胞療法:專注於 正確處理 T 細胞我們的目標:重新編程 T 細胞以擊敗實體瘤抵抗疲憊耐久的細胞毒性 CAR T 細胞自我更新持久性轉移性持久的細胞毒性腫瘤-癌症保持多克隆性浸潤右 表型淋巴細胞冷熱腫瘤 CAR,嵌合抗原受體 4 專有

Lyell 的 T 細胞重編程技術旨在解決 成功治療實體瘤的主要障礙要在實體瘤中取得成功,細胞療法必須:抵抗精疲力盡,在免疫抑制的腫瘤微環境中維持癌細胞的殺傷保持功能增強耐用性提高 自我更新和持續推動持久腫瘤細胞毒性的能力 STEMNESS 5 專有

實體瘤驅使 T 細胞走向疲憊之路固體血液學 自體輸液自體輸液腫瘤惡性腫瘤 CAR T 細胞 CAR T 細胞充足的擴張、擴張、持續不足、導致精疲力盡和腫瘤殺傷缺乏耐久性腫瘤細胞缺乏 T 細胞清除功能; 癌細胞持續存在 Riddell 等人,Keystone,2020 6 專有
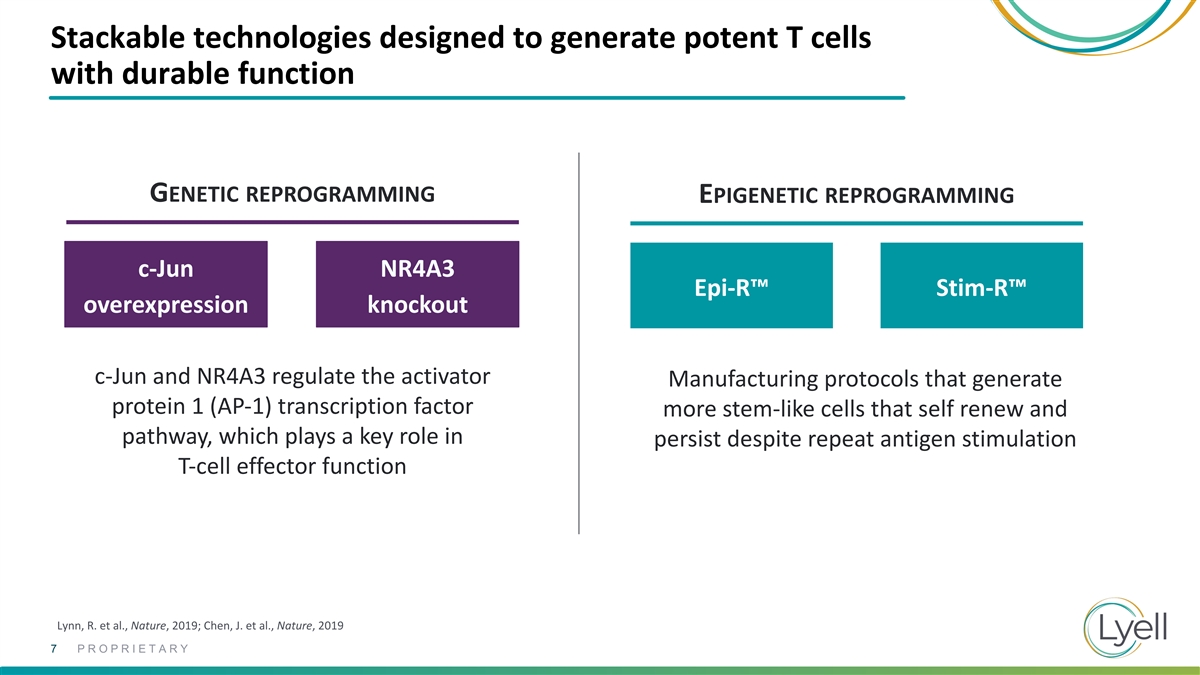
可堆疊技術旨在生成具有持久 功能的強效 T 細胞基因重編程表觀遺傳學重編程 c-jun NR4A3 Epi-R™ Stim-R™ 過度表達敲除 c-jun 和 NR4A3 調節激活劑製造協議,這些協議生成蛋白質 1 (AP-1) 轉錄因子更像莖樣的 細胞,儘管反覆出現抗原刺激,但T細胞效應器功能卻在持續存在中起着關鍵作用,Lynn R. 等人,《自然》,2019;Chen,J. 等人,《自然》,2019 年 7 專有

一家處於臨牀階段的公司 實體瘤的新療法越來越多遺傳表觀遺傳學產品重新編程重編程靶標 2 期/下一個預期候選藥物/靶點臨牀前 1 期適應症關鍵里程碑模式 c-jun NR4A3 Epi-R™ Stim-R™ TNBC LYL797 NSCLC 中的初始數據 ROR1 √ √ CAR T 細胞 1H 2024 其他實體瘤 ROR1+ LYL119 在 ROR1 中提交 CAR T 細胞 √ √ √ 2024 年上半年實體瘤黑色素瘤 LYL845 結直腸癌、非小細胞肺癌抗原中的多個初始數據 √ 其他固體 TIL 2024 腫瘤第二種多遺傳和表觀遺傳學固體腫瘤生成抗原重編程 TIL ROR1,受體酪氨酸激酶樣孤兒受體 1;IND,在研新藥;CAR,嵌合抗原受體;NSCLC,非小細胞肺癌; TNBC,三陰性乳腺癌;TIL,腫瘤浸潤淋巴細胞;CRC,結直腸癌 8 專有

癌症患者需要更好的治療 90%

萊爾候選產品針對的是大量未得到滿足的需求,每年美國約50萬例新增病例和 約18萬例死亡三陰性非小細胞黑色素瘤結直腸乳腺癌肺癌 • 15% 的乳腺癌 • 84% 的新肺部 • 所有皮膚的 80% • 美國第三常見的診斷每年癌症診斷 癌症相關死亡形式為癌症 • 約 40,000 例新發病例 • 約 200,000 例新發病例 • 約 200,000 例新發病例 • 約 200,000 例 • 100,000 例新發病例 • 約 15 萬例新發病例 • 約 10,000 例死亡 • 約 11 萬例死亡 • 約 8,000 例死亡 • 約 53,000 例死亡 LYL797 LYL797 和 LYL845 LYL845 LYL845 美國國家癌症研究所美國國家癌症研究所和美國癌症協會,以美國病例為依據。(2022) 10 PROPERTIVEL

重新編程 T 細胞以靶向侵襲性癌症 LYL797: 在基因和表觀遺傳學上重新編程的 ROR1 CAR T 細胞候選產品,專為差異化效力和耐久性而設計

LYL797 CAR T 細胞 1 期試驗設計 • 患者羣體 臨牀試驗設計 (mtpi-2) — 接受劑量遞增劑量擴展的復發/難治性 TNBC 患者兩條治療線均失敗 RP2D — 復發/難治性非小細胞肺癌患者向前 LYL797 TNBC 擴展 — ROR1 陽性劑量等級 3 隊列(N = ~15)研究目標 LYL797 NSCLC 劑量等級 2 — 患者安全性和耐受性(N = ~15)— 評估細胞毒性和劑量持續時間 1 級 T 細胞功能 — 總體反應率如果需要,還可以降低耐久性 — 推薦的 2 期劑量劑量等級 -1 — CAR T 細胞藥代動力學有可能擴展到其他腫瘤類型 NCT05274451 Spigel 等人,ESMO 2022 mtpi-2,修改後的毒性概率區間 2;非小細胞肺癌;ROR1,受體酪氨酸激酶樣孤兒受體 1;TNBC,三陰性乳腺癌;RP2D,推薦第 2 期劑量 12 專有

ROR1 在許多人類癌症中高度表達,與 預後不佳相關 ROR1 表達約為 60% ~ 40% 三陰性非小細胞乳腺癌肺癌 ~ 50% ~ 95% 慢性卵巢癌淋巴細胞白血病在先前的臨牀試驗和非人靈長類動物 ROR1 CAR T 細胞毒性研究中,沒有報道 ROR1 靶向療法對靶向 的非腫瘤毒性 ROR1,受體酪氨酸激酶樣孤兒受體 1 Jeong,Medicina,2022;Chien,Virchows Arch 2016;Zhang,PNAS,2014;Wang,NEJM 證據,2022 年;Berger,Cancer Immunol Res, 2015;Choi,《細胞幹細胞》,2018 13 專有

萊爾的 ROR1 測定和篩查計劃支持當前和 未來的臨牀試驗使用萊爾測定的篩查數據與文獻中的 ROR1 表達一致三陰性乳腺癌 53% ROR1+ N=77 • 15% 的乳腺癌診斷/年 • 約 40,000 例新發病例/約 10,000 例死亡 33% ROR1+ 非小細胞肺癌 N=18 • 84% 的新肺癌診斷 /年 • 約 200,000 例新發病例/約 11 萬例死亡 ROR1,受體酪氨酸激酶樣孤兒受體 1;美國國家癌症研究所和美國癌症出版社 文獻:Balakrishnan 等人,ClinCancer Res.2017,Society,基於美國病例(2022)TNBC 約60%,非小細胞肺癌約40% 14 專有

LYL797 臨牀項目由可靠的臨牀前數據支持 ROR1 CAR T cell + c-jun + Epi-R 關鍵區分因素 • 在具有 c-jun 的侵襲性非小細胞肺癌同系動物模型中減少腫瘤、增強細胞因子生成和腫瘤浸潤 • 使用 Epi-R 技術實現類幹表型、耐久性和增強細胞毒性 • 在異種移植中結合 c-jun 和 Epi-R 技術 (LYL797),延長存活期非小細胞肺癌動物模型 15 專有

c-jun 在侵襲性非小細胞肺癌模型淋巴枯竭中過度表達 ROR1 CAR T 細胞,以及 • Syngeneic kras/p53 模型概述了人類非小細胞肺癌攜帶腫瘤的小鼠 CAR T 細胞 +/-c-jun • 還概述了使用 ROR1 CAR T 細胞治療人類非小細胞肺癌的障礙第 15 天 30 • 實現腫瘤消退的模型極其困難瘤內功能增強腫瘤內功能增強 50% 的小鼠浸潤腫瘤控制 IFN CAR T 細胞在腫瘤體積中的頻率腫瘤體積 WT ROR1 CAR T 細胞 WT ROR1 CAR T 細胞 WT ROR1 CAR T細胞 WT CAR T 細胞治療的小鼠 c-jun ROR1 CAR T 細胞 c-jun ROR1 CAR T 細胞 c-jun ROR1 CAR T 細胞治療的小鼠 6/12 進展 6/12 穩定/倒退輸注前 4 周 * 是 p<.05 is p riddell lab fred hutch unpublished data proprietary of pe-cd8 mm>

Epi-R™ 技術產生轉錄不同的T細胞羣 ,這些細胞可以抵抗疲憊並保持細胞毒性 Epi-R 擴增細胞的不同基因表達譜 Epi-R 擴增細胞在從 Epi-R 條件中移除後表現出較長的細胞毒性順序細胞 殺傷試驗(ROR1 CAR T 細胞)標準制劑 Epi-R Mock 標準制劑製劑 Epi-R Mock 標準制劑 Epi-R UMAP_1 時間(小時)Park 等人,AACR 2022 腫瘤靶標:H1975 17 專有 UMAP_2 相對靶細胞熒光 (%)
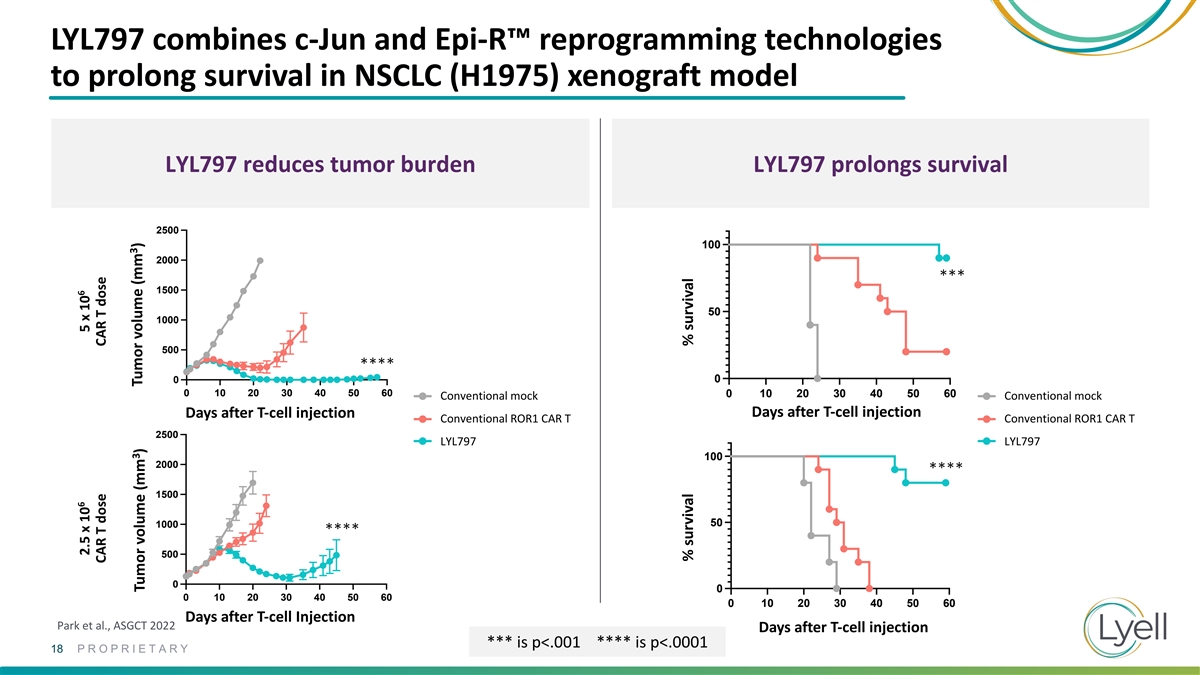
LYL797 結合了 c-jun 和 Epi-R™ 重編程技術來延長非小細胞肺癌 (H1975) 異種移植模型中的存活率 LYL797 減輕腫瘤負擔 LYL797 延長存活率 2500 100 2000 *** 1500 50 1000 500 2500 0 0 20 30 40 50 60 0 0 0 0 20 30 50 60 傳統模擬傳統模擬常規模擬 T 細胞注射後的日子傳統 ROR1 CAR T 傳統 ROR1 CAR T 傳統 ROR1 CAR T 傳統 ROR1 CAR T 2000 2000 2500 LY LYL7 9 9 77 LY LYL7 9 9 9 77 LY L7 9 9 77 77 77 1500 1500 100 2000 **** 1000 1000 1500 50 1000 500 500 **** 500 0 0 10 20 30 40 50 0 0 10 20 30 40 50 0 0 0 0 0 0 0 0 10 20 30 40 50 0 0 10 20 30 40 50 50 0 0 10 20 30 40 50 50 0 0 0 0 0 0 20 30 40 50 50 60 在 T 細胞注射 Park 等人,ASGCT 2022 T 細胞注射後的幾天 *** 是 p<.001 is p proprietary x car t dose tumor volume survival>

旨在提高效力和耐久性的新型可堆疊技術 LYL119:專為增強細胞毒性而設計的創新 ROR1 CAR T 細胞候選產品

LYL119 採用了旨在提高 效力和耐久性的新型可堆疊技術 ROR1 CAR T 細胞 + c-jun + NR4A3 KO + Epi-R + Stim-R 關鍵區別因素 • 結合 NR4A3 基因敲除和 c-jun 過度表達可進一步減少 T 細胞疲憊並增強細胞毒性 — 減少 NR4A 表達 增強與 ap-1 調節基因表達增加相關的 T 細胞功能 — NR4A 家族轉錄因子可能通過抑制 c-jun 活性導致 T 細胞精疲力盡 • Stim-R CAR T 細胞表現出延長 的持久性並得到增強對連續抗原刺激反應的細胞毒性 Lam 等人,SITC,2022 Li 等人,SITC 2022 Chen J 等。自然。2019;Tirosh I 等人科學。2016;Liu X 等人自然。2019;Odagiu I 等人Proc Natl Acad Sci USA 20 專有
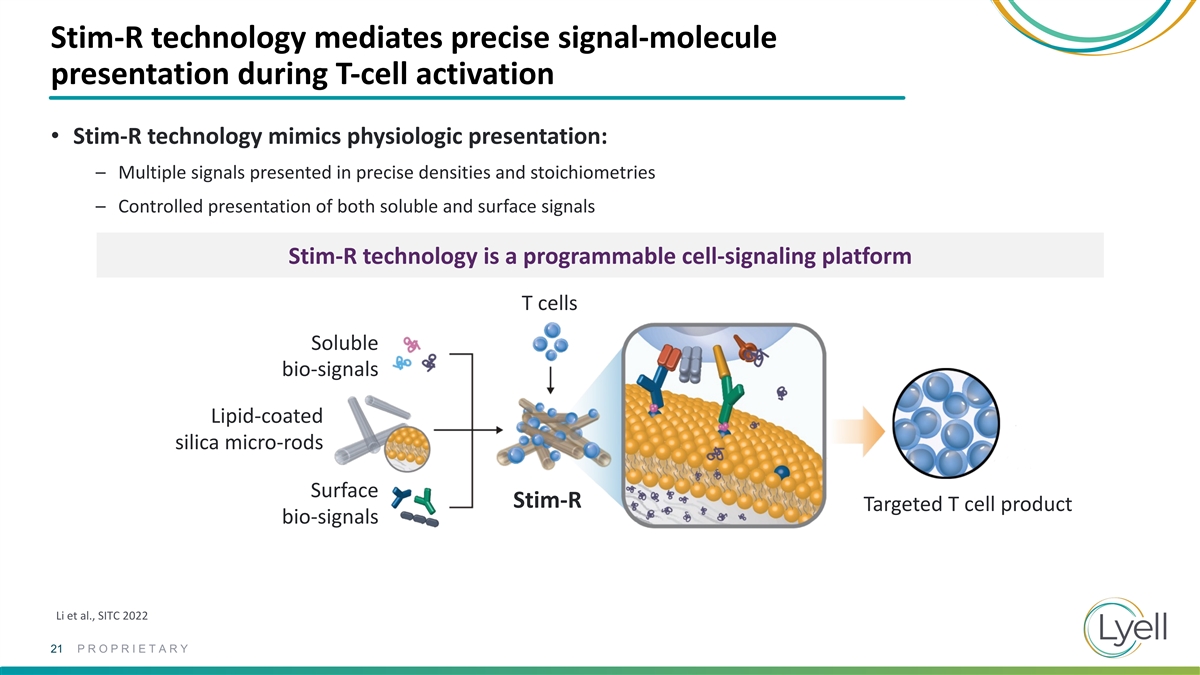
Stim-R 技術在 T 細胞激活期間介導精確的信號分子呈現 • Stim-R 技術模仿生理表現:— 以精確的密度和化學計量呈現的多種信號 — 可溶性和表面信號的可控呈現 Stim-R 技術是一種 可編程細胞信號平臺 T 細胞可溶性生物信號脂質塗層二氧化硅微棒 Surface Stim-R 靶向 T 細胞產品生物信號 Li 等人。,SITC 2022 21 專有
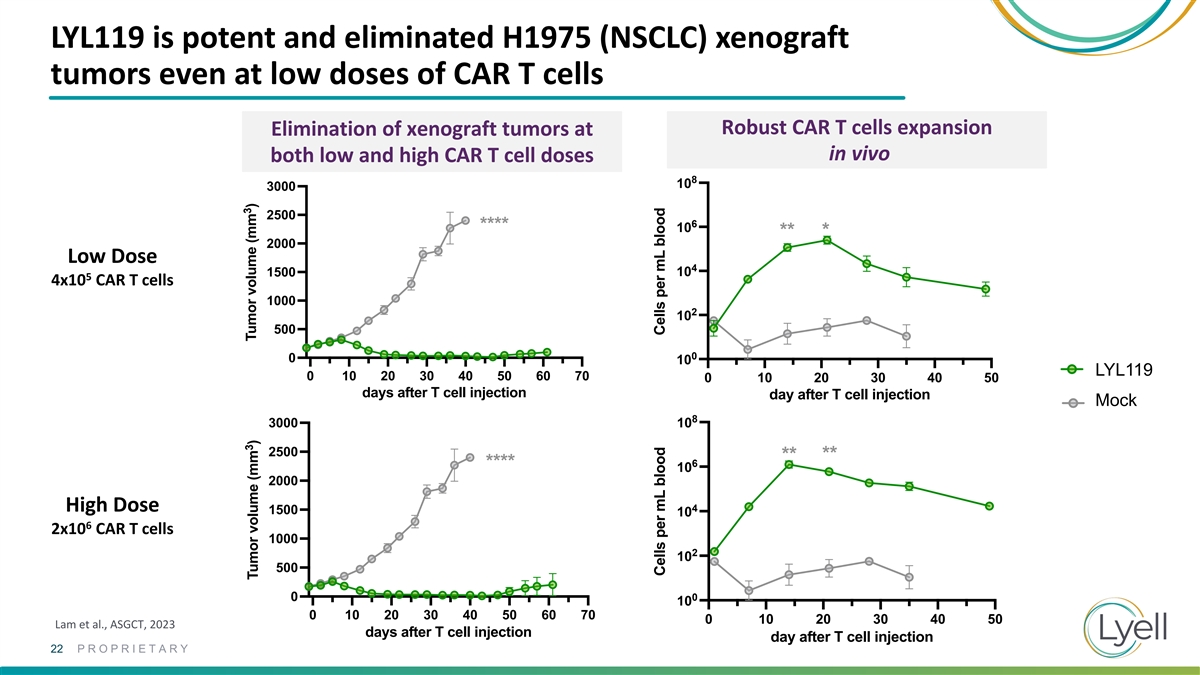
外周血 CD3+CAR+ 數字 LYL119 是有效的,可以消除 H1975 (NSCLC) 異種移植外周血 CD3+CAR+ 數字 0.4e6 CAR T 細胞 8 10 0.4e6 CAR T 細胞 8 個腫瘤即使在低劑量的 CAR T 細胞下 10 6 ** * 10 ** ** * 6 ** * * 6 ** * * * * 在體內消除異種移植腫瘤既低 又高 CAR T 細胞劑量 10 4 8 10 10 3000 2 10 2500 6 2**** 10 10** * 2000 0 10 低劑量 4 1500 10 0 0 10 20 30 40 10 4x10 4x10 4 x10 4x10 CAR T 細胞 T 細胞注射 T 細胞後的第二天 0 10 20 30 40 1000 2 10 10 10 T 細胞注射 10 天后 NR4A3 KO g4 + c-jun R12CAR 500 NR4A3 KO g4 + c-jun R12 CAR NR4A3 KO g47 + c-jun R12 CAR 0 0 10 NR4A3 KO g47 + c-jun R12 CAR LYL119 0 10 20 40 60 70 Control + c-jun R12 CAR 0 10 10 10 20 20 30 40 在 T 細胞注射後的第二天 Control + c-jun R12 CAR Mock Mock 8 3000 10 Mock 2500 ** 6 **** 10 2000 High 劑量 4 1500 10 6 2x10 CAR T 細胞 1000 2 10 500 0 0 10 20 30 40 50 60 0 0 0 10 20 30 40 50 Lam 等人,ASGCT,T 細胞注射 2023 天后 22 專有 3 3 腫瘤體積 (mm) 腫瘤體積 (mm) 每 mL 血細胞中的細胞數 (mm) 每 mL 血細胞中的細胞數每 mL 血細胞每 mL 血細胞每 mL 血液中的細胞數
利用腫瘤浸潤的淋巴細胞對抗癌症 LYL845: 一種經過表觀遺傳學重新編程的新型 TIL 候選產品,專為差異化效力和耐久性而設計

LYL845 TIL 1 期試驗設計 • 患者羣體臨牀 試驗設計 (mtpi-2) — 復發和/或難治性轉移或劑量擴大 * 劑量遞增局部晚期實體瘤:(黑色素瘤)— 黑色素瘤 RP2D 將 LYL845 黑色素瘤——非小細胞肺癌向前推至劑量等級 2(N =)擴大 — 結直腸癌隊列 • 研究目標 LYL845 NSCLC 劑量等級 1 (N = ~ 15) — 患者安全和耐受性如果需要可降級 — 總體反應率和耐久性 LYL845 結直腸劑量 Level -1 — 推薦的 2 期劑量(N = ~ 15)— 評估擴張、表型、克隆多樣性和持久性 NCT05573035 *有可能擴展到其他腫瘤類型 mtpi-2,修改後的毒性概率區間 2;NSCLC, 非小細胞肺癌;RP2D,推薦的 2 期劑量 24 專有

LYL845:一種新穎的差異化 TIL 候選產品 Control TIL 關鍵分化因子標準 TIL 擴展方案 • 與臨牀反應相關的表型(乾性標誌物和細胞毒性細胞)LYL845 腫瘤 Lyell Epi-R 方案包括:組織 • 專有培養基 • 保留的 多克隆腫瘤反應細胞 • 優化的細胞因子成分 • 定義明確的細胞激活和擴張方案 • 在熱腫瘤和冷腫瘤中均具有穩健的 TIL 擴增壽命短效應細胞莖樣細胞 25 專有

LYL845 富含與 改善臨牀結果相關的細胞 增加細胞毒性細胞的百分比增加莖樣 T 細胞的百分比控制 LYL845 Krishna 等人,《科學》2020 年 12 月 Patel 等人,SITC 2022 26 PROPERVICET * 是 p<.05 is p cd8 t cells>

LYL845 TIL 保留了大約 94% 的預測腫瘤反應性克隆以實現 靶向異質性實體瘤 LYL845 T 細胞製劑 LYL845 TIL 臨牀量表惡性腫瘤組織 100 75 50 HIGH Bioinformatics 耗盡頻率 25 分析克隆 0 捐贈者檢查是否保存了預測的腫瘤 活性克隆中預測的腫瘤黑色素瘤 NSCLC 反應性克隆 LYL845 產品 Harris 等人,SITC 2022 Pasetto 等人,CIR 2016,Lowrey 等人,Science 2022,Oliveira 等人,《自然》2021 27個專有預測的腫瘤反應性百分比 克隆

與在新模型中使用標準條件的 TIL 相比,使用我們的 Epi-R 工藝 的 LYL845 TIL 在體內療效更好。在這項研究中:No TIL 2500 • 收集了兩個難治性黑色素瘤捐贈者標準 TIL 樣本。2000 • 使用 1500 Epi-R (LYL845) 或標準工藝對樣本進行拆分處理以生成 TIL 產物。沒有 TIL Control Donor 1 Standard TIL 1000 • 小鼠在第 -8 天植入了捐贈者 1 LYL845 TIL 皮下黑色素瘤細胞系捐贈者 2 標準 TIL。500 Donor 2 LYL845 TIL • 第 0 天 LYL845 或 標準 TIL 在第 0 天靜脈注射。0 LYL845 TIL 0 10 20 30 40 天治療後 28 專有和機密 3 腫瘤體積 (mm)

Epi-R P2 是一種新的製造工藝,旨在縮短向患者交付產品 的時間 • 與 Epi-R 相比,Epi-R P2:— 不影響產量、乾性表型或腫瘤反應性克隆 — 在大大縮短的製造時間內可靠地生產 100 多億個細胞 • 預計 將在 2024 年 TIL 生產中實施 Epi-R™ Epi-R™ P2 超過 100 億個細胞 üü保持莖樣品質和腫瘤殺傷功能 üü保留腫瘤反應性克隆 ümanucture 時間~24 天~16 天 29 專有

Epi-R 和 Epi-R P2 過程在 CD8 細胞中顯示出可比的產品特徵 相當的類幹細胞百分比細胞毒性細胞的百分比 NS Epi-R P1 Epi-R P2 Epi-R P1 Epi-R P1 Epi-R P1 Epi-R P1 Epi-R P2 N=21 包括轉移性黑色素瘤、肺癌和結直腸癌專有 30% CD8+ T 細胞% CD8+CD27+ T 細胞% CD8+CD39-CD69-T 細胞

Epi-R P2 保留並允許擴大腫瘤反應性 TIL 100000 在 本研究中:• T 細胞受體 (TCR) 測序 10000 是在第 0 天腫瘤、1000 和 TIL 樣本中進行的,以評估產品中腫瘤反應性克隆的保留情況 100 • 在第 0 天腫瘤樣本中代表性更高 10 的 T 細胞克隆(例如,1 個頻率排名前 50 或前 100 個)更有可能成為腫瘤反應性 0.1 • 我們還通過實驗證實,第 0 天 0.01 個最高頻的 TCR 克隆腫瘤 Epi-R P1 Epi-R P2 具有腫瘤反應性(以紫色顯示) 已確診腫瘤反應性前 50 名 50-100 前 31 個專有克隆大小(標準化為 30K TCR 序列)

製造業

推進面向未來的製造戰略 • 自動化製造流程以實現快速和成本效益-• 目前生產的 1 期臨牀供應可有效擴大規模,以滿足患者的預期需求 • 能力包括 CAR T 細胞、TIL 和 GMP 載體我們的 CAR T 細胞候選產品 • 每年最多可接受 500 劑量,具體取決於 • LYL797 CAR T 細胞療法 CAR T、嵌合抗原受體的製造產品組合的概念驗證技術轉讓 T 細胞;TIL,腫瘤浸潤 淋巴細胞;GMP,良好 • 單細胞航天飛機容量高達 800 個 LYL797 電池製造實踐劑量/年 33 專有

推進實體瘤的 T 細胞療法 2024 年來自兩個主要 項目的臨牀數據兩個臨牀項目:全資,執行鍼對大量患者羣體的可擴展生產戰略 LYL797:ROR1 瞄準了 CAR T 細胞萊爾的 LyfE 中心生產當前的臨牀供應 • 1H2024:來自 20 多名患者的 P1 臨牀和轉化數據 • 2024 年:Epi-R P2 流程可在不影響細胞的情況下縮短 TIL 製造時間 • TNBC、NSCLC 數量和表型規劃未來 LYL845:腫瘤浸潤淋巴細胞 (TIL) • CAR T 細胞證明-與 Cellares 的概念合作 • 2024 年:P1 臨牀和轉化數據以擴大規模並降低成本 • 黑色素瘤、非小細胞肺癌、結直腸癌的新型重編程組合現金平臺約6.33億美元 技術 • 1H2024:LYL119、ROR1 靶向 CAR T 細胞的 IND 申請 • Runnay to 2026 專為增強效力和耐久性而設計;使用我們的四項技術 ROR1,受體酪氨酸激酶樣孤兒受體 1;TNBC, 三陰性乳腺癌;非小細胞肺癌,非小細胞肺癌;結直腸癌;結直腸癌;P1,第 1 期 34 專有

一切都與細胞有關