

BEACON 研究 Topline 結果 LYR-220-2021-001 一項二期、患者盲法、分為兩部分、隨機、平行分組試驗,旨在評估 LYR-220 在先前接受過篩管切除術的慢性鼻竇炎 (CRS) 患者的安全性、耐受性、藥代動力學和療效 https://clinicaltrials.gov/study/NCT05035654 2023 年 9 月 12 日附錄 99.1

免責聲明本演示文稿包含1995年《私人證券訴訟改革法》所指的 前瞻性陳述。本演示文稿中包含的所有與歷史事實無關的陳述均應被視為前瞻性陳述, 包括有關公司候選產品線和開發以及 LYR-220 和 LYR-210 的進展、有效性和適用性的陳述。這些陳述既不是承諾也不是保證,而是涉及已知和 未知的風險、不確定性和其他重要因素,這些因素可能導致公司的實際業績、業績或成就與 前瞻性陳述所表達或暗示的任何未來業績、業績或成就存在重大差異,包括但不限於以下內容:公司自成立以來蒙受了重大損失,預計在可預見的將來將蒙受額外損失;公司需要額外的 資金,可能無法獲得;公司的運營歷史有限;公司沒有獲批產品的事實;公司的候選產品處於不同的開發階段; 公司從未擴大過用於臨牀或商業用途的內部製造設施;或者公司在確定候選產品併成功將其商業化方面可能無法成功; 臨牀試驗這一事實公司的候選產品要求既昂貴又耗時-消費,其結果尚不確定;FDA可能無法得出公司某些候選產品符合第505 (b) (2) 條監管部門批准途徑的 要求的結論;公司無法獲得所需的監管部門批准;最近頒佈和未來立法的影響;系統故障或安全漏洞的可能性; 激烈競爭的影響;公司候選產品的成功商業化將取決於部分取決於政府在多大程度上當局和健康保險公司確定承保範圍、充足的 報銷水平和定價政策;未能獲得市場認可;產品責任訴訟;公司必須擴大其內部製造能力或依賴第三方為其研究計劃、臨牀前研究和臨牀試驗以及商業供應制造材料;公司依賴第三方進行臨牀前研究和臨牀試驗;公司無法成功建立和維持 合作關係;公司依賴某些對其生產至關重要的供應商;未能獲得、維護或充分保護公司的知識產權;未能留住關鍵人員或招聘 合格人員;難以管理公司的增長;自然災害、恐怖主義和戰爭(包括烏克蘭和俄羅斯之間的戰爭)的影響;COVID-19 引起的全球疫情可能會對包括公司在內的 公司的業務和運營產生不利影響的臨牀試驗;公司普通股的價格可能波動不定且波動幅度很大; 作為上市公司運營以及任何證券集體訴訟所產生的鉅額成本和管理時間。公司於2023年8月8日向美國證券交易委員會提交的10-Q表季度報告及其向美國證券交易委員會提交的其他文件中,在 “風險因素” 標題下討論的這些因素和其他重要因素可能會導致實際業績與本演示文稿中前瞻性陳述所顯示的結果存在重大差異。任何此類前瞻性陳述均代表管理層截至本演示之日的估計。儘管 公司可能會選擇在未來的某個時候更新此類前瞻性陳述,但它不承擔任何這樣做的義務,即使隨後的事件導致其觀點發生變化。本演示文稿還包括 我們從第三方或我們進行的行業、出版物和研究、調查和研究中獲得的統計和市場數據。行業出版物和第三方研究、調查和研究通常表明,他們的信息是從被認為可靠的來源 獲得的,儘管它們不能保證此類信息的準確性或完整性。本演示文稿中使用的所有市場數據都涉及許多假設和侷限性,提醒您不要過分重視此類估計 。儘管我們認為這些行業出版物和第三方研究、調查和研究是可靠的,但我們尚未對此類數據進行獨立驗證。由於各種因素,我們經營的行業面臨高度的不確定性、變化和風險,這可能導致業績與獨立合作伙伴和我們的估計中表達的結果存在重大差異。

LYR-210 和 LYR-220 旨在 全方位解決 CRS 患者候選人 CRS 患者類型 2 期 3 期 LYR-210 長效糠酸莫米鬆 LYR-220 長效 mometasone Furoate Enlighten 3 期項目慢性鼻竇炎患者手術天真 解剖學慢性鼻竇炎術後解剖學患者 BEACON 2 期試驗標題現已公佈 LYR-220 2 BEACON 研究
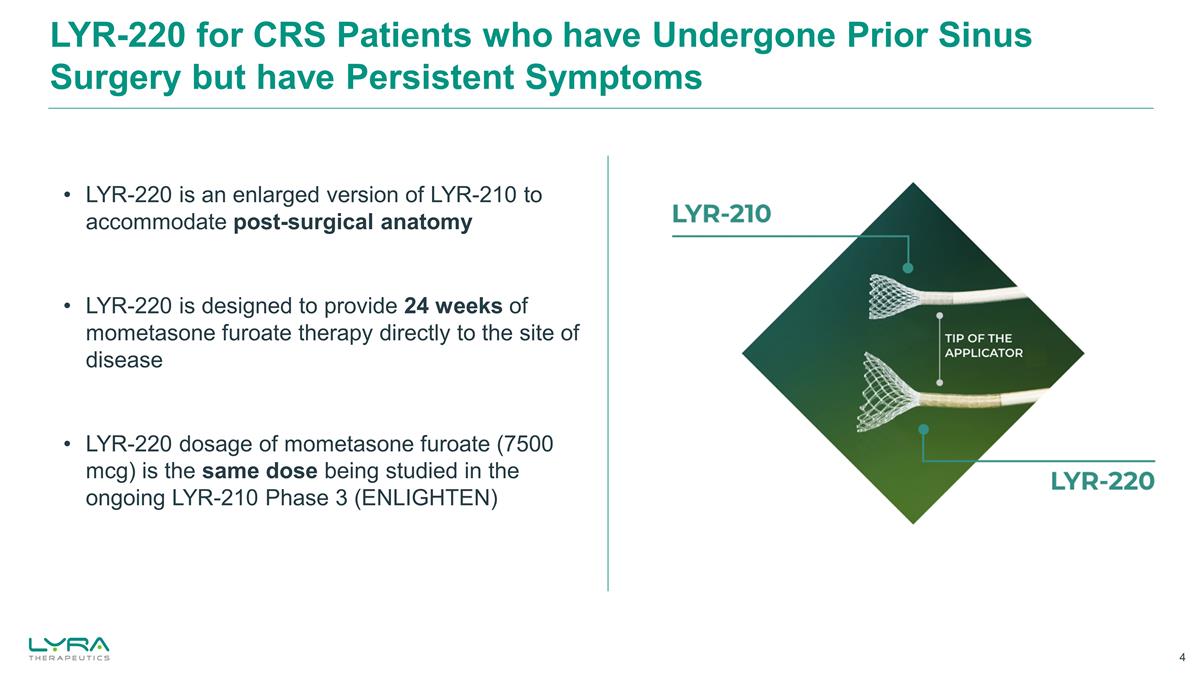
LYR-220 適用於 之前接受過鼻竇手術但症狀持續存在的 CRS 患者 LYR-220 是 LYR-210 的放大版,以適應術後解剖結構 LYR-220 旨在直接向病部提供 24 周的糠酸莫米鬆治療 LYR-220 糠酸莫米鬆劑量 (7500 mcg) 與正在進行的 LYR-210 第 3 階段 (ENLIGHTEN) 中正在研究的劑量相同 3 期 (ENLIGHTEN)
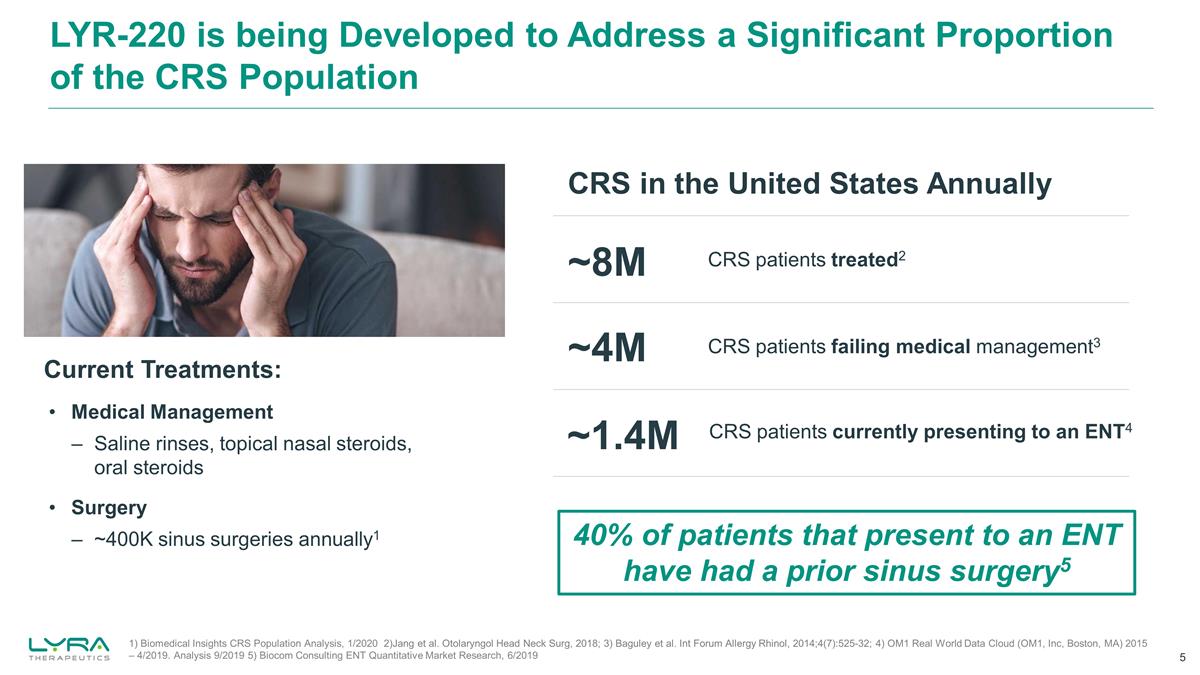
正在開發 LYR-220,以解決美國 CRS 人羣中很大一部分 CRS 患者每年治療 2 名 CRS 患者未通過醫療管理3 ~800萬~400萬目前的治療方法:醫療管理鹽水沖洗、外用鼻用類固醇、口服類固醇 1) Biomedical Insights CRS 人羣分析,2020 年 1 月 2) Jang 等人。Otolaryngol Head Neck Surg,2018;3) Baguley 等人Int Forum Allery Rhinol,2014;4 (7): 525-32;4) OM1 Real World Data Cloud(OM1, Inc,馬薩諸塞州波士頓)2015 — 2019 年 4 月 2019 年 9 月分析 5) Biocom Consulting 耳鼻喉科量化市場研究,2019 年 6 月 6 日 CRS 患者目前在 ENT4 就診約 140 萬例耳鼻喉科患者中有 40% 以前接受過鼻竇手術5 手術每年約 40 萬例鼻竇手術1
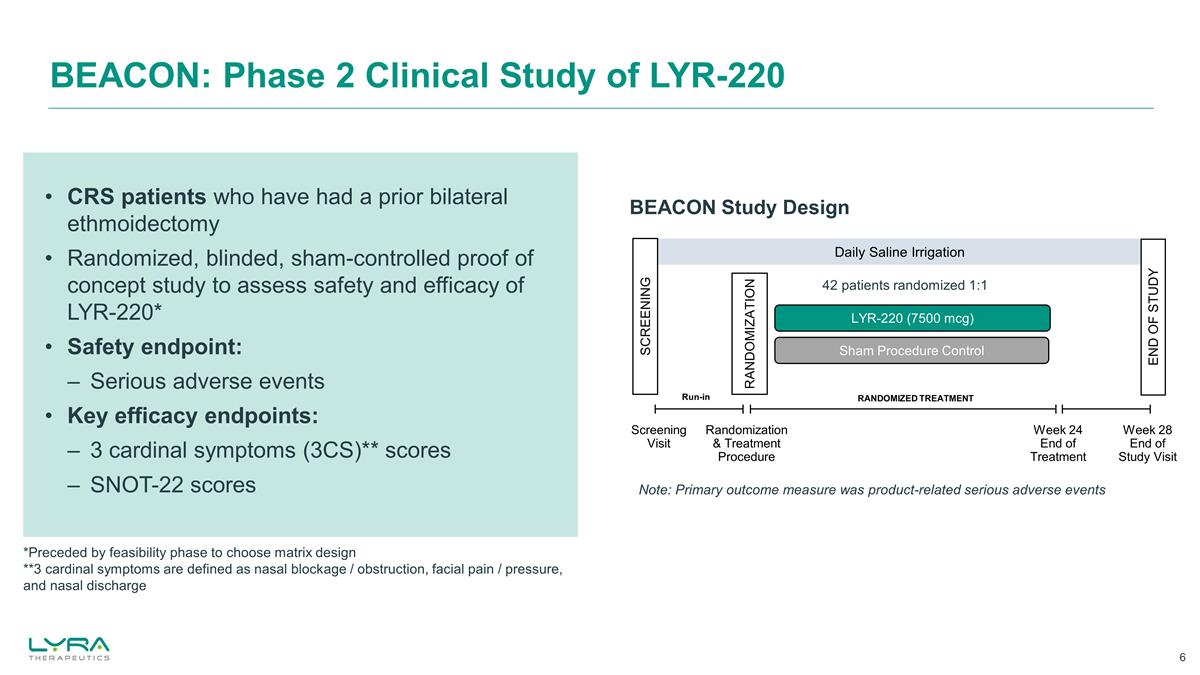
BEACON:先前接受過雙側篩查術的 LYR-220 CRS 患者的 2 期臨牀研究 BEACON 為評估 LYR-220 的安全性和有效性而進行隨機、盲法、羞恥對照的概念驗證研究 * 安全終點:嚴重不良事件關鍵療效終點:3 個主要 症狀 (3CS) ** 分數 SNOT-22 分數 BEACON 研究設計每日鹽水灌溉虛假手術控制 LYR-220 (7500 mcg) 篩查隨機化結束研究隨機治療第 24 周治療結束篩查訪問隨機化和 治療程序磨合第 28 周結束研究訪問 *在選擇基質設計的可行性階段之前 **3 個主要症狀被定義為鼻塞/阻塞、面部疼痛/壓力和鼻腔分泌物 42 名患者隨機 1:1 注意:主要結局衡量標準是與產品相關的嚴重不良事件
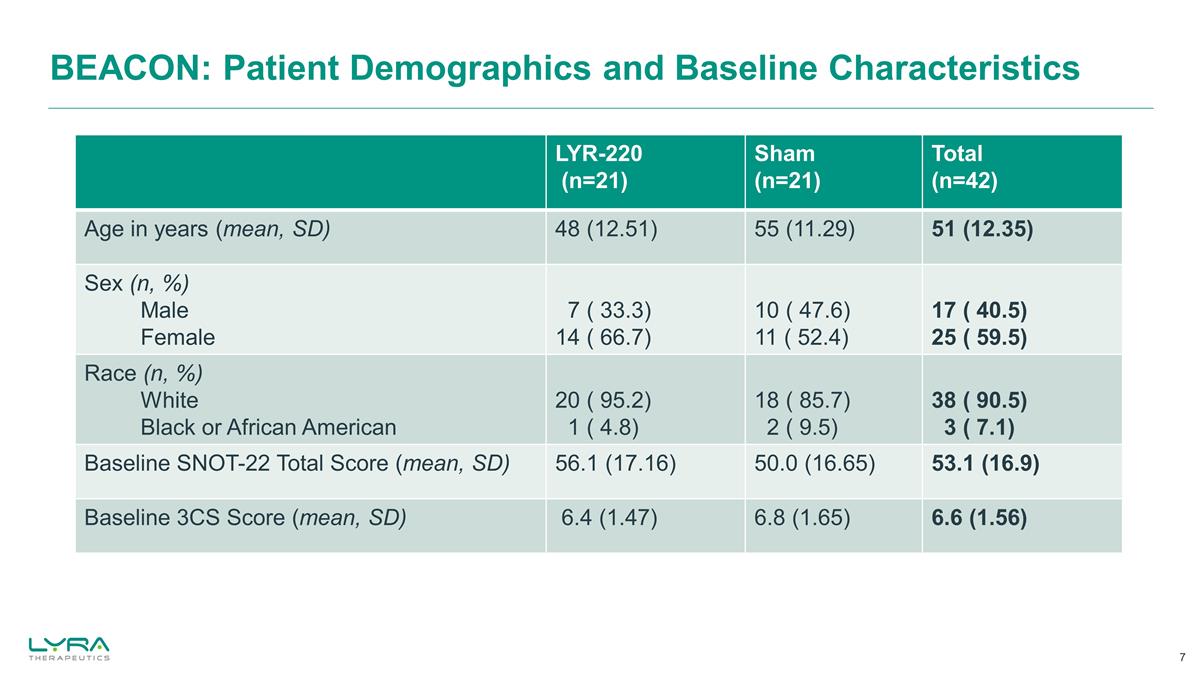
BEACON:患者人口統計和 基線特徵 LYR-220 (n=21) 虛假 (n=21) 總年齡 (n=42) 年齡(平均值,SD)48(12.51)55(11.29)51(12.35)性別(n,%)男女 7(33.3)14(66.7)10(47.6)11(52.4)17(40.5)25(59.5)種族(n,%)%) 白人黑人或非洲人 美國人 20 (95.2) 1 (4.8) 18 (85.7) 2 (9.5) 38 (90.5) 3 (7.1) 基線 SNOT-22 總分(平均值,SD)56.1 (17.16) 50.0 (16.65) 53.1 (16.9) 基線 3CS 分數(平均值,標清)6.4(1.47)6.8(1.65)6.6(1.56)
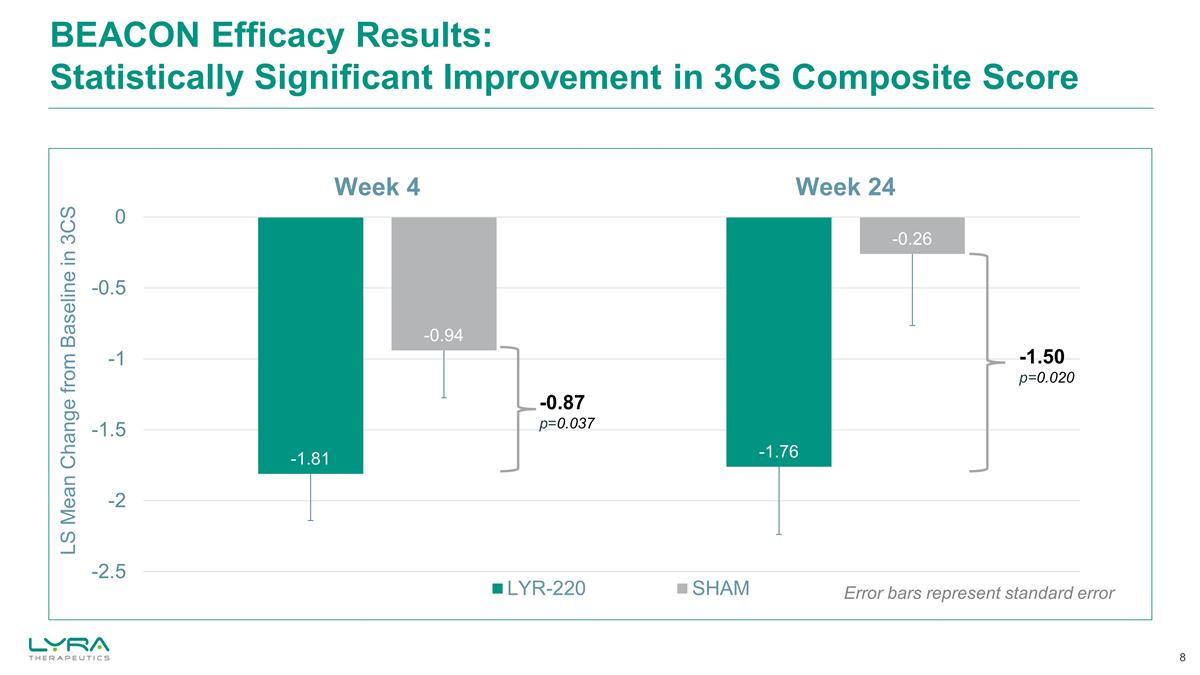
BEACON 功效結果:從統計學上講 3CS 綜合分數的顯著改善誤差條表示標準誤差
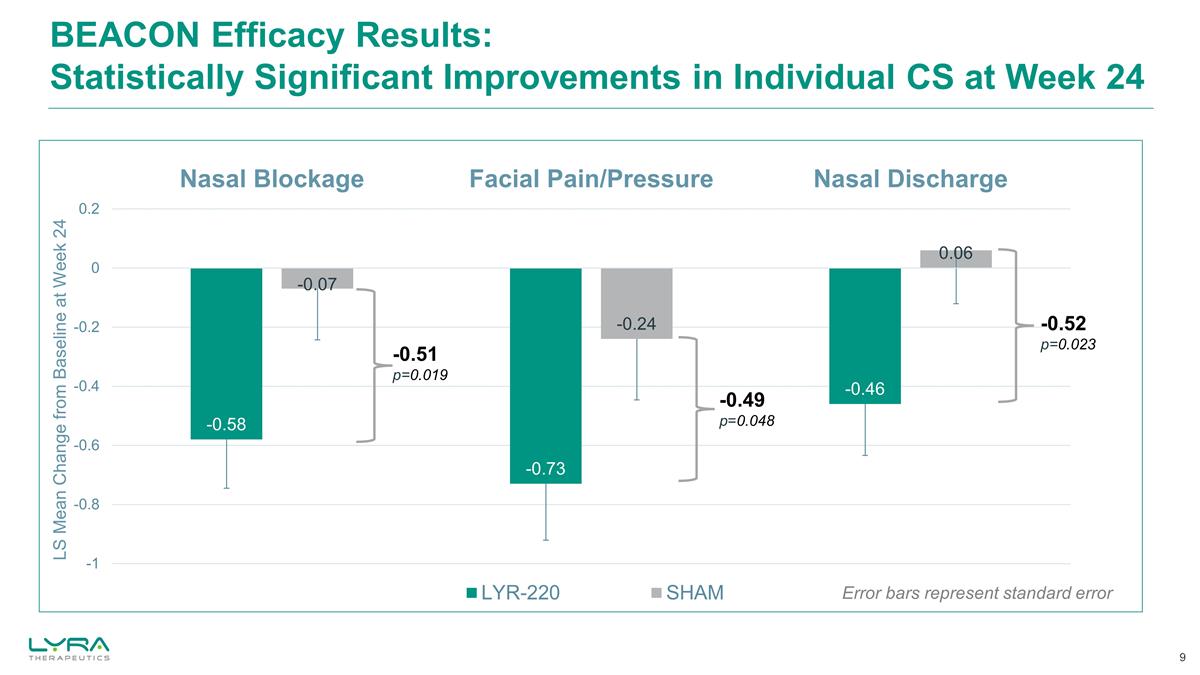
BEACON 功效結果:從統計學上講 第 24 周個人 CS 的顯著改善誤差線代表標準誤差
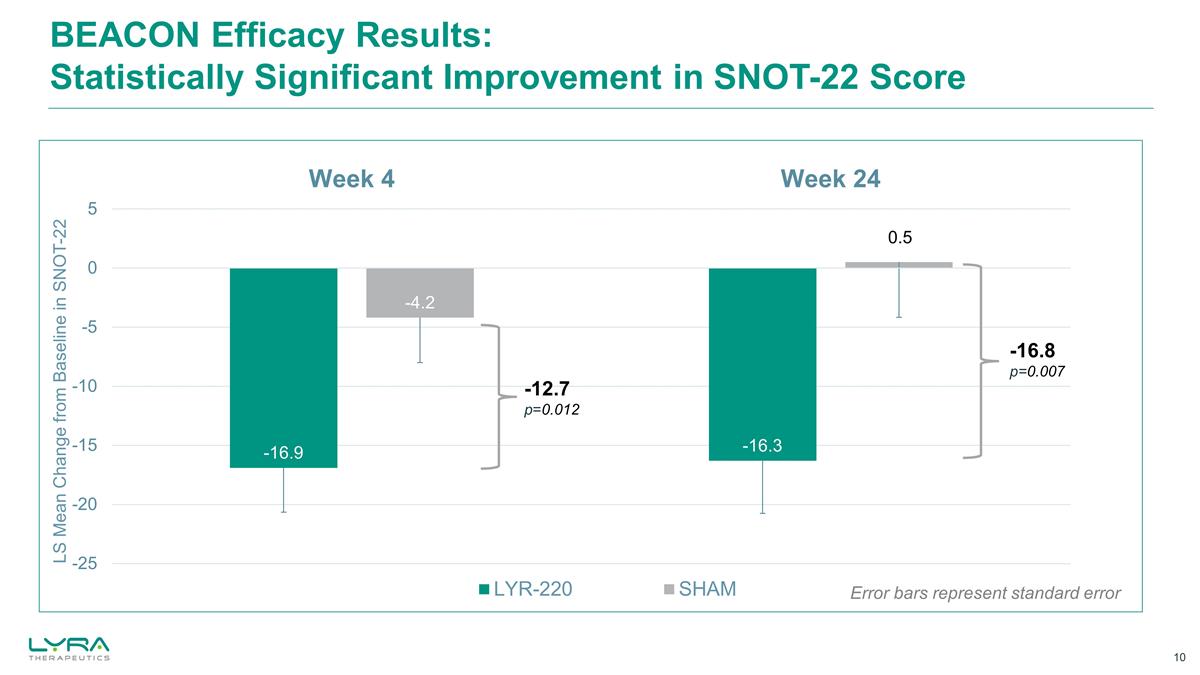
BEACON 功效結果: SNOT-22 分數誤差條的統計學顯著改善表示標準誤差
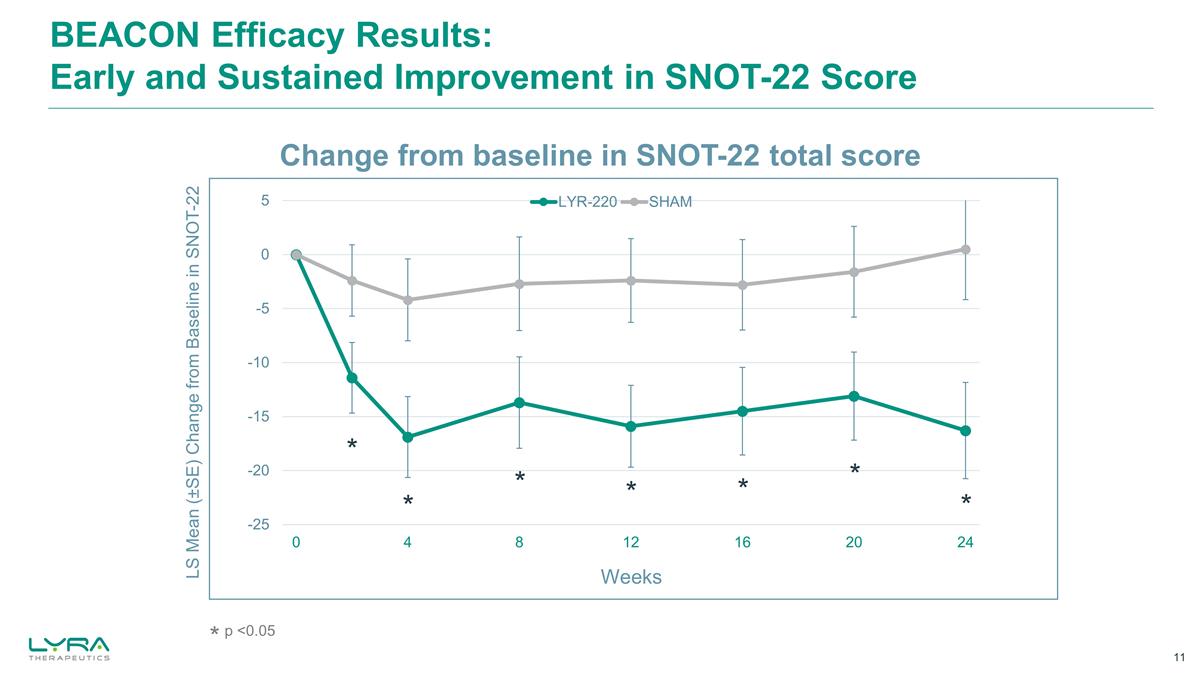
BEACON 功效結果:SNOT-22 分數的早期和 持續改善 LS 平均值 (±SE) 與 SNOT-22 基線相比的變化 * p

BEACON 研究摘要未觀察到嚴重的 不良事件。最常觀察到的不良事件包括鼻竇炎、鼻咽炎、支氣管炎和 COVID-19 第 24 周 CRS 的 3 種主要症狀(鼻塞、鼻腔分泌物、 面部疼痛/壓力)的綜合症狀在統計學上有顯著改善(-1.50;p=0.02)與中鼻結局測試(SNOT-22)分數相比,第 24 周每種主要症狀都有統計學上的顯著改善在第 24 周 24(-16.8;p=0.007)在 3 位紅衣主教的合成中取得了統計學上的顯著改善早在第 4 周(-0.87;p=0.037)就出現了 CRS 症狀(-0.87;p=0.037)早在第 2 周就觀察到了 SNOT-22 的統計學顯著改善(-9.0;p=0.031)在整個研究中持續改善,具有臨牀意義,第 24 周觀察到的最小臨牀重要差異幾乎是假的(-16.8 分)的兩倍沒有 SAE 和關鍵療效終點在統計學上顯著且具有臨牀意義的改善 SNOT-22
