

2023 年 5 月公司發佈會附錄 99.1

前瞻性陳述本演講包含1995年《私人證券訴訟改革法》“安全港” 條款所指的 “前瞻性” 陳述,包括但不限於:我們開發和商業化小分子療法的計劃,我們對開始、註冊或完成臨牀研究、提交數據和臨牀結果或更新,以及獲得監管部門批准 PRT1419、PRT2527、PRT3645、PRT3789、我們的口服 SMARCA2 候選藥物和其他正在開發的候選藥物的時機和能力的預期,那個我們的候選產品治療各種癌症的能力,發現其他合適候選產品供監管部門批准的能力,以及我們的現金和現金等價物足以為我們的運營提供資金。此處包含或口頭提供的任何非歷史事實陳述的陳述均可被視為前瞻性陳述。在某些情況下,你可以用 “相信”、“可能”、“將”、“可能”、“估計”、“繼續”、“預期”、“打算”、“可能”、“將”、“項目”、“計劃”、“期望” 等術語來識別前瞻性陳述,儘管並非所有前瞻性陳述都包含這些詞語。包括前瞻性陳述在內的陳述僅代表其提供日期(除非註明更早的日期)。本演示中的某些數據基於跨研究比較,並非基於任何正面交叉臨牀試驗。交叉研究比較本質上是有限的,可能表明存在誤導性的相似之處或不同之處。本演示不構成出售要約或徵求買入要約,也不得在根據任何此類州或其他司法管轄區的證券法進行註冊或資格認證的任何州或其他司法管轄區出售這些證券。這些前瞻性陳述基於我們管理層的信念以及我們做出的假設和目前可用的信息。儘管我們認為此類前瞻性陳述中反映的預期是合理的,但我們無法保證這種預期會被證明是正確的。如果此類假設未完全實現或被證明不正確,則前瞻性陳述中提及的事件或情況可能不會發生。除非法律要求,否則我們沒有義務在本演示之日之後以任何理由公開更新任何前瞻性陳述,以使這些陳述符合實際業績或我們的預期變化。因此,提醒讀者不要過分依賴這些前瞻性陳述。可能影響我們業務的其他風險和不確定性包含在我們向美國證券交易委員會提交的文件中 “風險因素” 標題下,包括我們截至2022年12月31日的10-K表年度報告。
Prelude Therapeutics:旨在為癌症患者提供精準藥物大型商業機會多元化管道卓越團隊資本充足的強大研發引擎
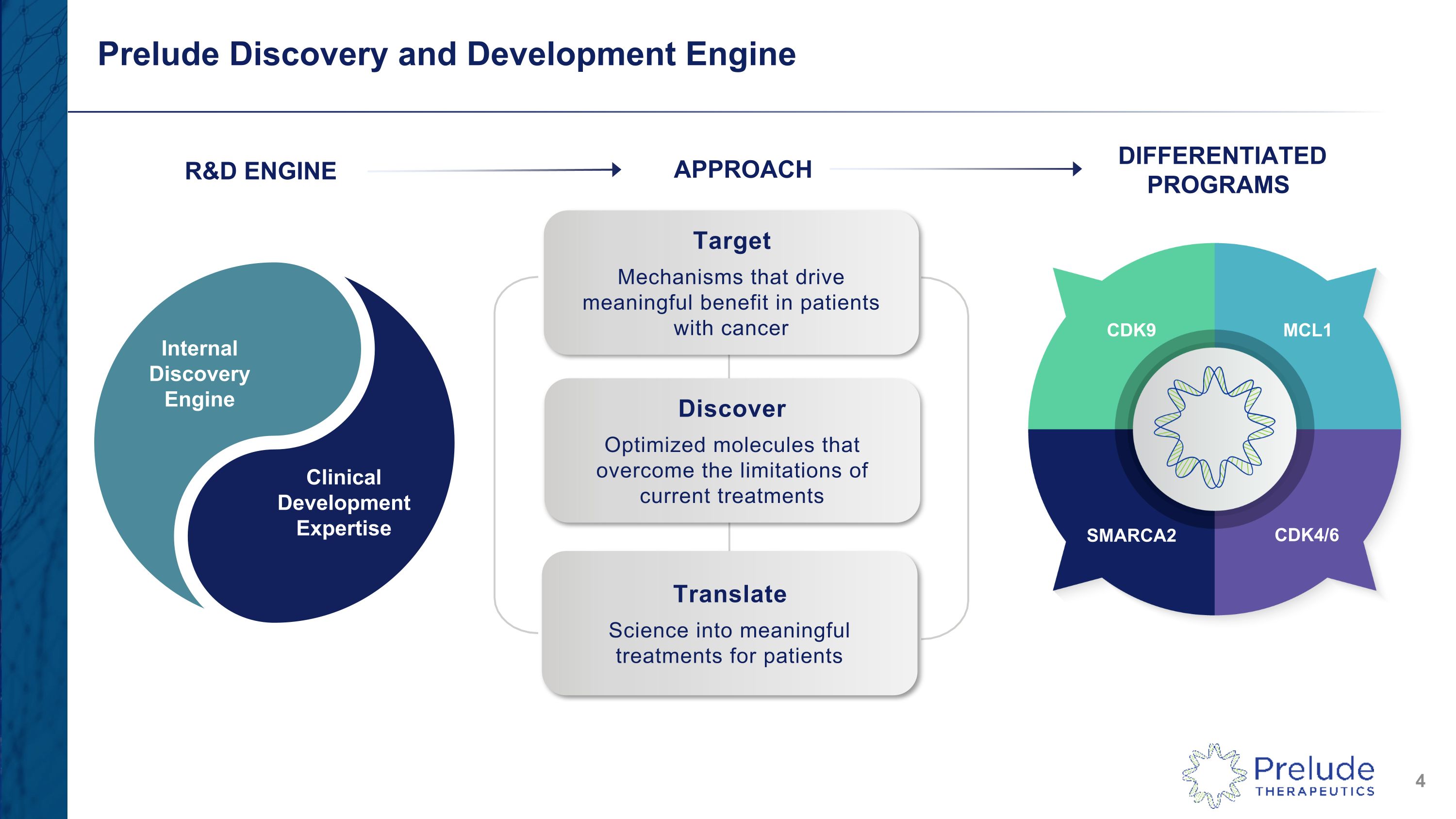
Prelude Discovery and Development Engine 研發引擎差異化計劃方法 CDK9 MCL1 SMARCA2 CDK4/6 為癌症患者帶來有意義的益處發現克服當前治療侷限性的優化分子將科學轉化為對患者有意義的治療內部發現引擎臨牀開發專業知識
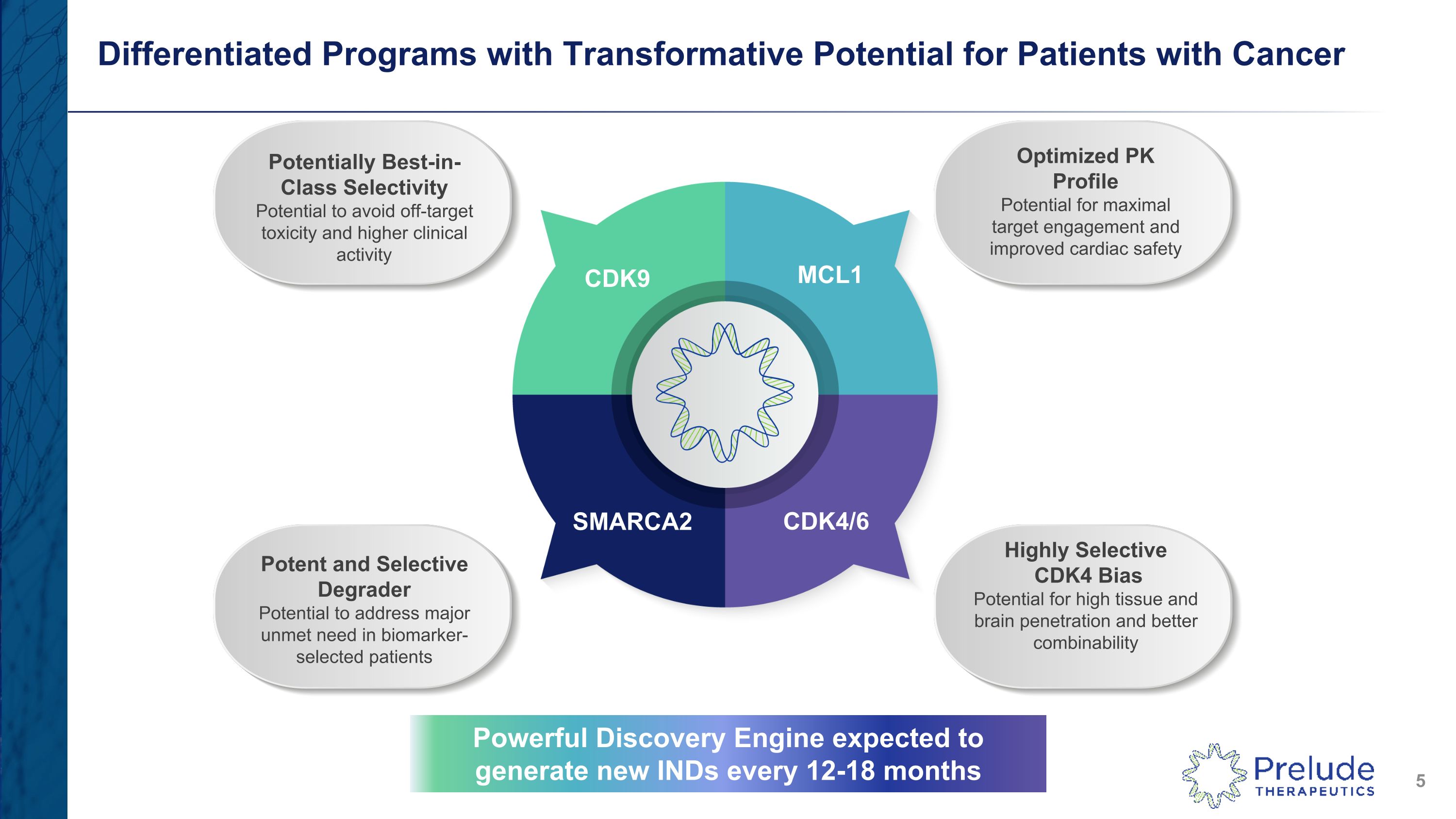
對癌症患者具有變革潛力的差異化項目潛在的同類最佳選擇性潛力避免偏離靶標的毒性和更高的臨牀活性強效和選擇性降解潛力可滿足生物標誌物選定患者未得到滿足的主要需求優化 PK 曲線潛力實現最大靶點參與和提高心臟安全性高選擇性 CDK9 MCL1 SMARCA2 CDK4/6 Powergal Discovery Engine 預計每 12-18 年生成新的 IND月份
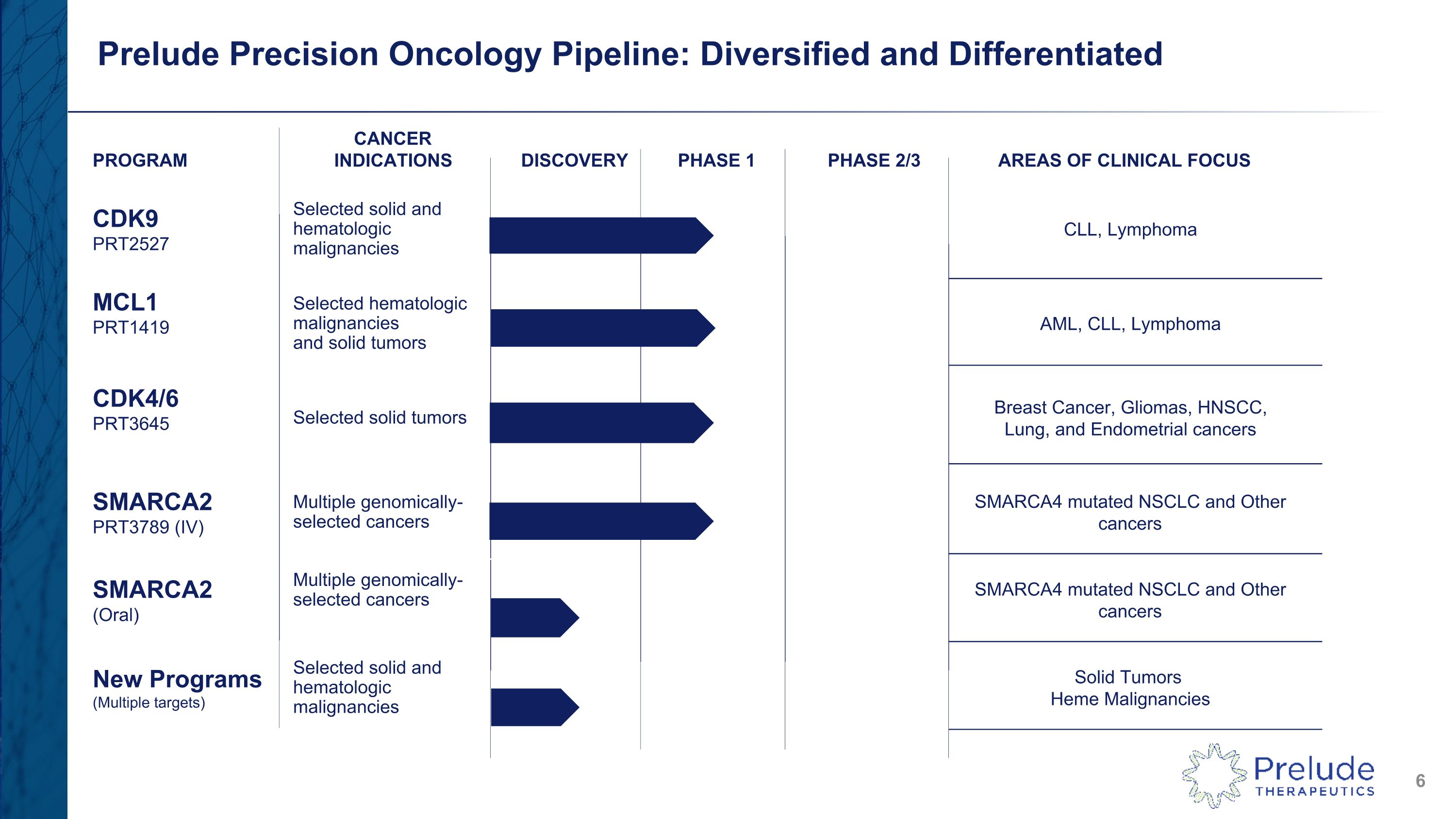
項目癌症適應症發現第 1 階段 2/3 階段臨牀重點領域 CDK9 PRT2527 精選實體和血液系統惡性腫瘤 CLL、淋巴瘤 MCL1 PRT1419 精選血液系統惡性腫瘤和實體瘤 AML、CLL、淋巴瘤 CDK4/6 PRT3645 精選實體瘤乳腺癌、神經膠質瘤、HNSCC、肺癌和子宮內膜癌 SMARCA2 PRT3789 (IV) 多種基因組選擇的癌症 SMARCA4 突變 NSCLC 非小細胞肺癌和其他癌症 SMARCA2(口服)多種基因選擇的癌症突變 NSCLC 和其他癌症新項目(多靶點)已選 SMARCA4實體惡性腫瘤和血液系統惡性腫瘤實體瘤血紅素惡性腫瘤前奏精準腫瘤管道:多元化和差異化
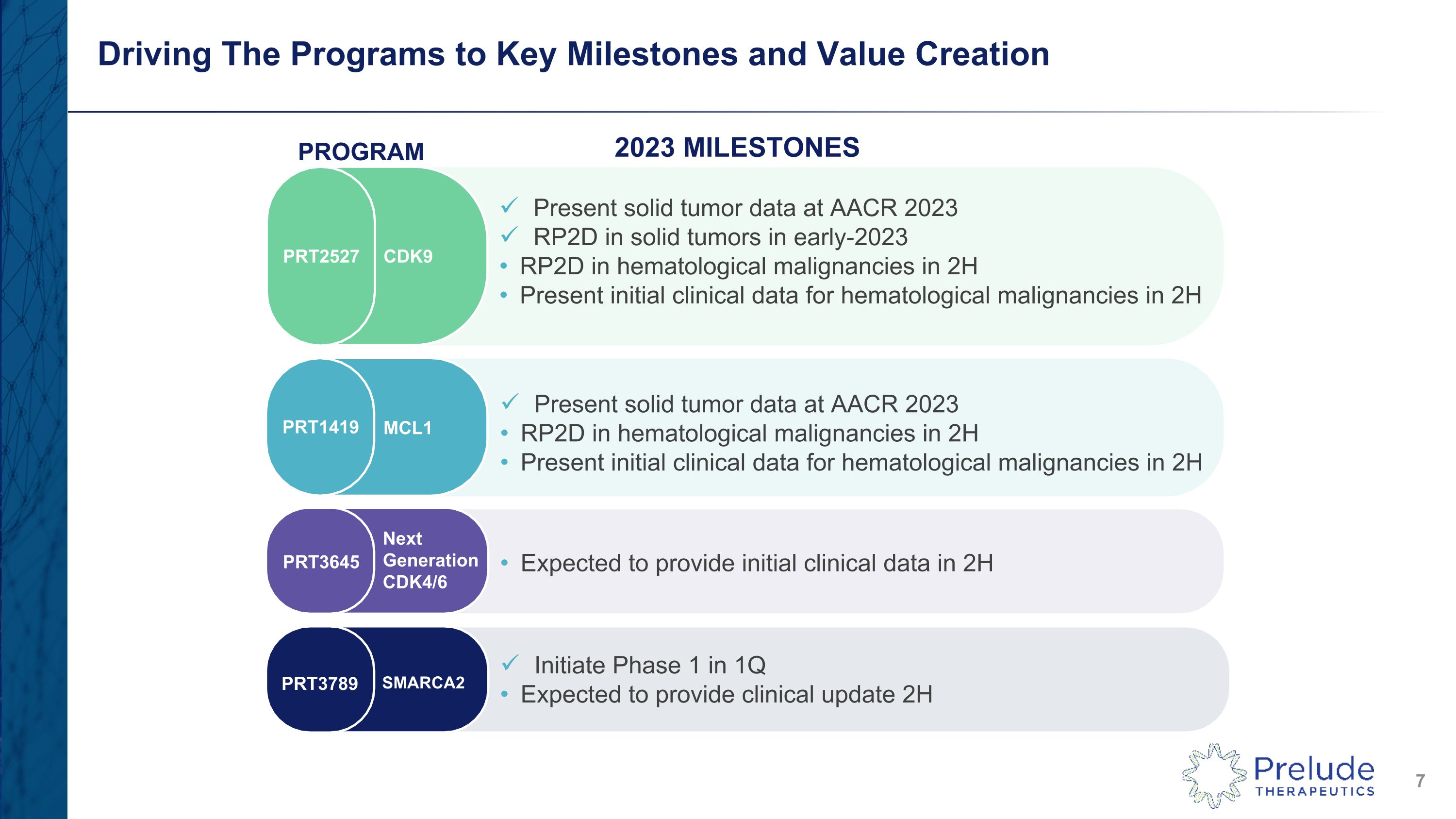
推動項目走向關鍵里程碑和價值創造 PRT2527 PRT1419 PRT3645 SMARCA2 CDK9 MCL1 下一代 CDK4/6 在 AACR 2023 上公佈實體瘤數據 RP2D 在 2H 提交血液學惡性腫瘤的初步臨牀數據在 AACR 2023 RP2D 上公佈下半年血液學惡性腫瘤的初步臨牀數據 2H 預計將在 2023 年下半年計劃里程碑中提供初始臨牀數據第一季度啟動第一階段預計將提供臨牀更新 2H PRT3789

PRT2527 CDK9 抑制劑
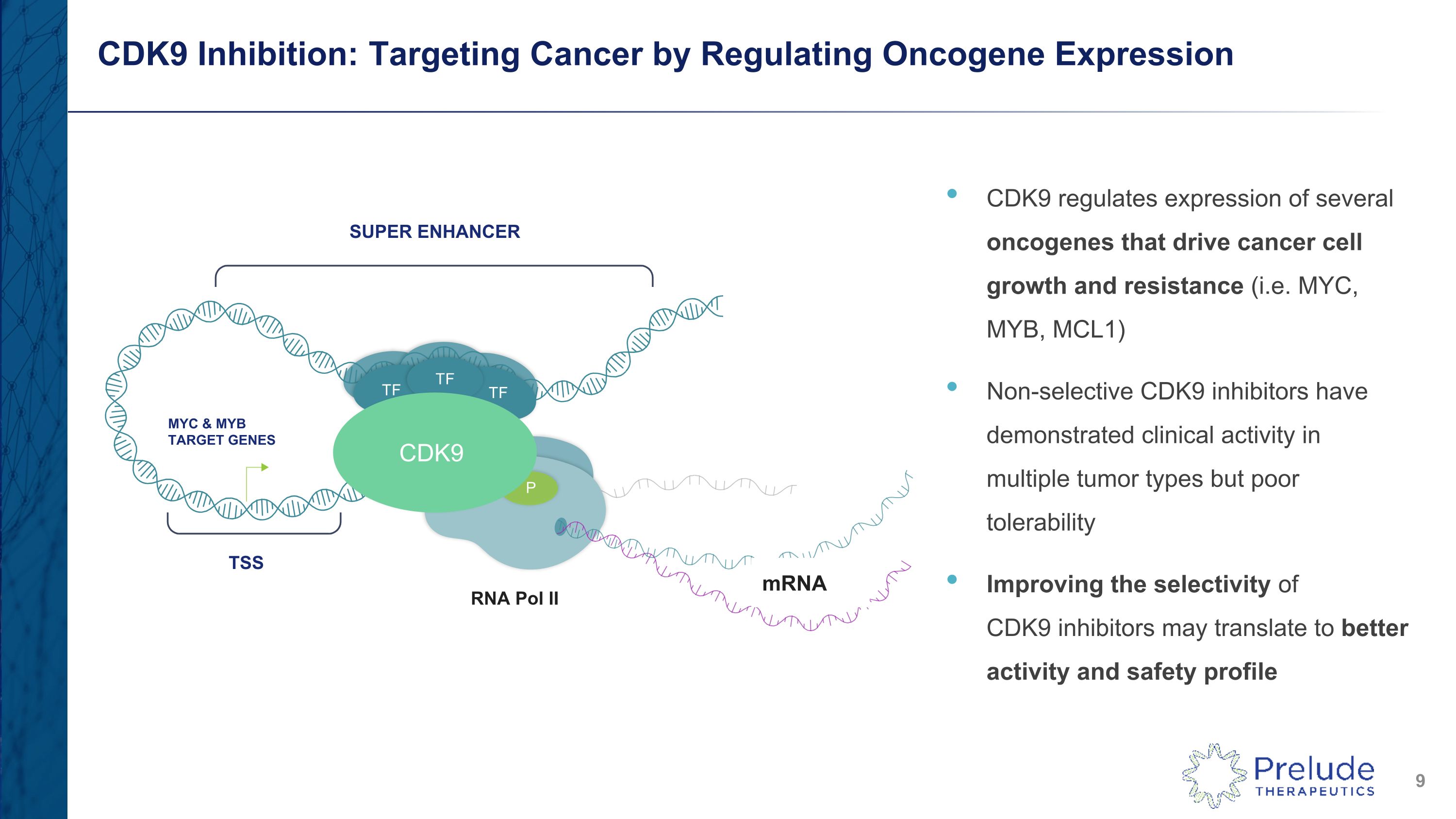
CDK9 抑制:通過調節癌基因表達來靶向癌症 CDK9 調節幾種推動癌細胞生長和耐藥性的癌基因(即 MYC、MYB、MCL1)的表達非選擇性 CDK9 抑制劑已在多種腫瘤類型中顯示出臨牀活性,但耐受性差改善 CDK9 抑制劑的選擇性可以轉化為更好的活性和安全性 SUPER ENCHARER RNA Pol II TSS 和 MYB TARGET 基因 mRNA K9
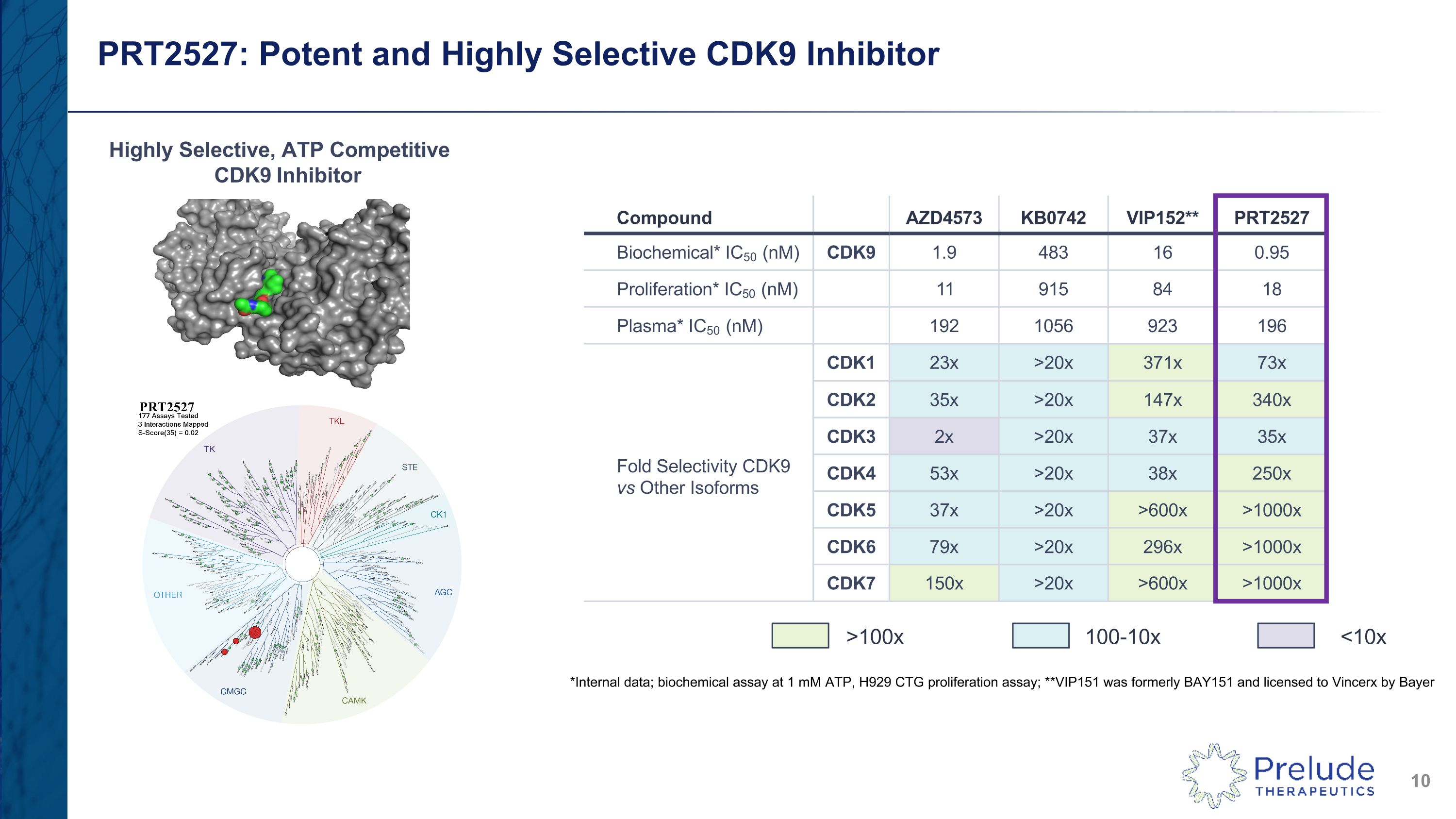
PRT2527:強效高選擇性 CDK9 抑制劑化合物 AZD4573 KB0742 VIP152** PRT2527 生化* IC50 (nM) CDK9 1.9 483 16 0.95 增殖* IC50 (nM) 11 915 84 18 Plasma* IC50 (nM) 192 1056 923 196 摺疊選擇性 CDK9 對比 CDK1 23x 23x >20x 371x 73x CDK2 35x >20x 147x 340x CDK3 2x >20x 37x 35x CDK4 53x >20x 38x 250x CDK5 37x >20x >60x >1000x CDK6 79x >20x 296x >1000x CDK7 150x >20x >600x >1000x 高選擇性,ATP 競爭性 CDK9 抑制劑 >100x 100x 100-10x
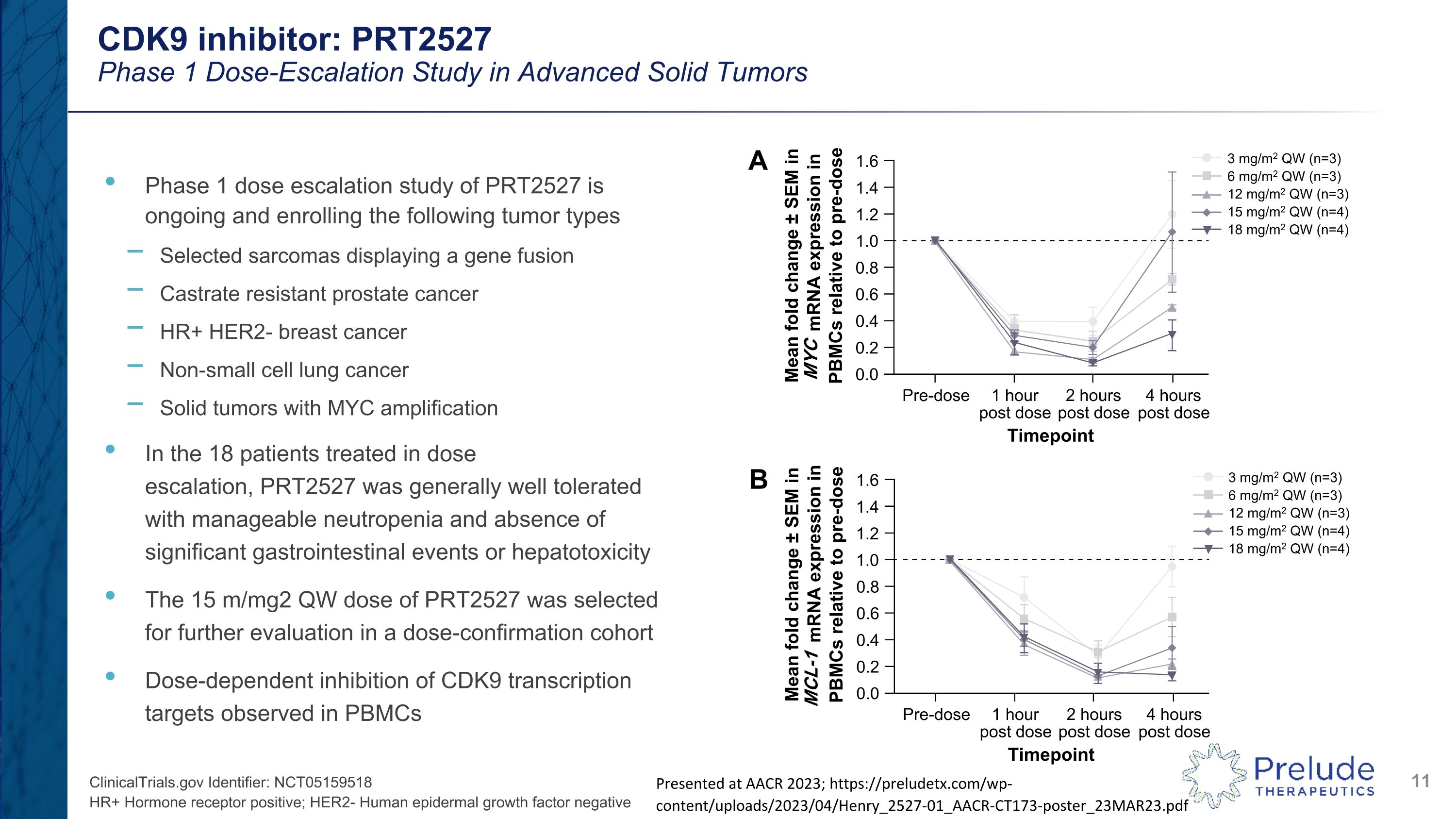
CDK9 抑制劑:PRT2527 晚期實體瘤的 1 期劑量遞增研究 PRT2527 的第 1 期劑量遞增研究正在進行中,招收了以下腫瘤類型顯示基因融合去勢耐藥性前列腺癌 HR+ HER2-乳腺癌非小細胞肺癌具有 MYC 擴增的實體瘤在劑量遞增治療的 18 名患者中,PRT2527 的耐受性總體良好,中性粒細胞減少症可控制,沒有顯著的胃腸道事件或肝臟事件毒性 PRT2527 的 15 m/mg2 QW 劑量被選為在劑量確認隊列中進一步評估在 PBMC 中觀察到的 CDK9 轉錄靶受體呈劑量依賴性抑制 HR+ 激素受體陽性;HER2-人類表皮生長因子陰性 clinicalTrials.gov 標識符:NCT05159518 在 AACR 2023 上發表;https://preludetx.com/wp-content/uploads/2023/04/Henry_2527-01_AACR-CT173-poster_23MAR23.pdf Timepoint mYC mRNA 表達在 PBMC 服藥前 2 小時給藥後 4 小時給藥 1 小時後給藥 1 小時的平均摺疊變化 ± SEM 0.6 0.0 1.0 1.4 1.2 0.4 0.2 A 3 mg/m2 QW (n=3) 6 mg/m2QW (n=3) 12 mg/m2 QW (n=3) 15 mg/m2 QW (n=4) 18 mg/m2 QW (n=4) 給藥前 2 小時後給藥 4 小時後給藥 1 小時 0.6 0.0 1.4 1.6 1.2 0.2 pbmC 中 MCL-1 mrNA 表達的平均摺疊變化 ± SEM 與給藥前 B 3 mg/m2 QW (n=3) 6 mg/m2 QW (n=3) 6 mg/m2 QW (n=3) 12 mg/m2 QW (n=3) 15 mg/m2 QW (n=4) 18 mg/m2 QW (n=4)
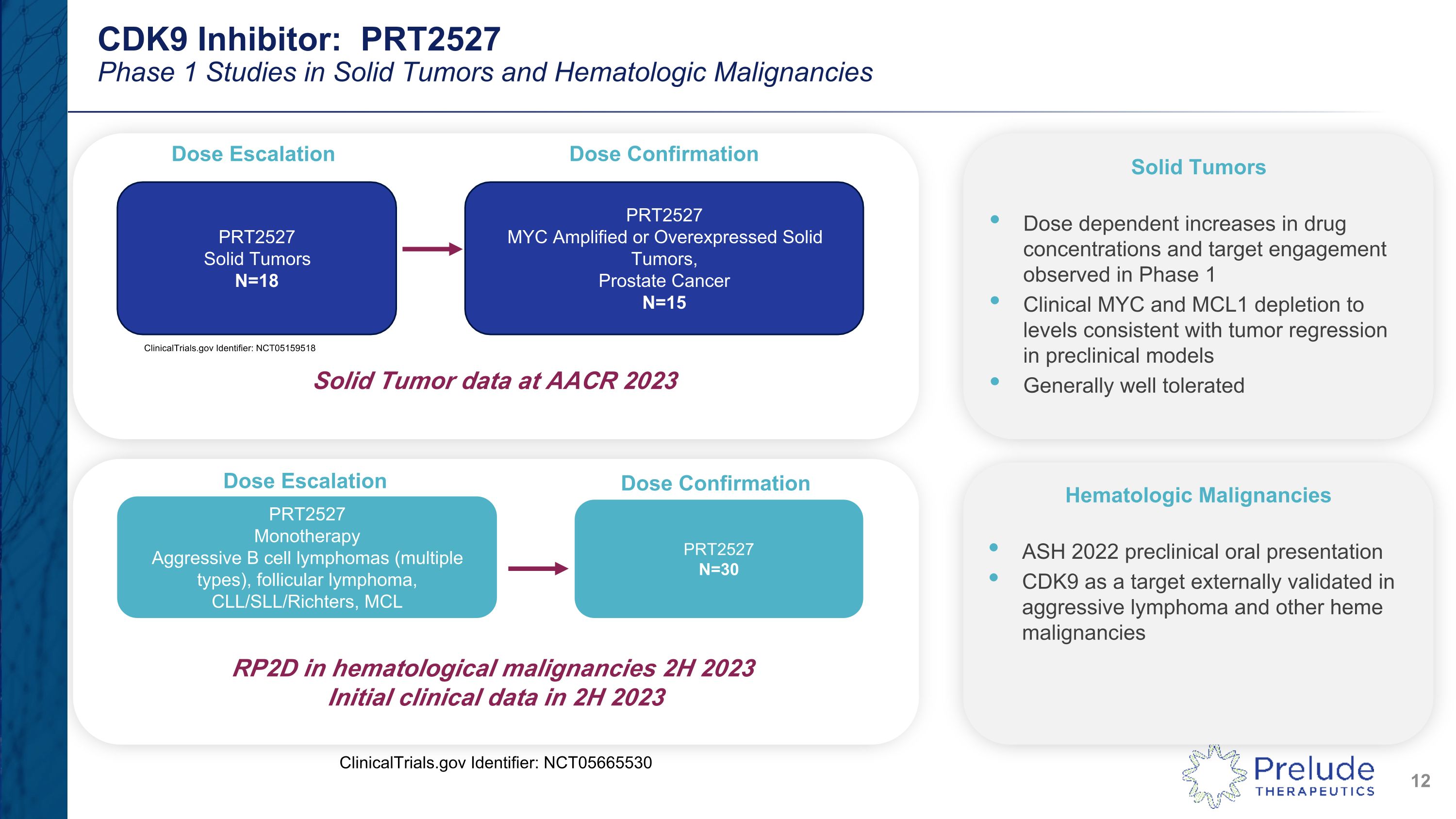
CDK9 抑制劑:prt2527實體瘤和血液系統惡性腫瘤的 1 期研究 PRT2527 實體瘤 N=18 PRT2527 MYC 擴增或過度表達的實體瘤、前列腺癌 N=15 實體瘤劑量依賴性在臨牀前 MYC 和 MCL1 中觀察到的藥物濃度和靶點參與度增加至與腫瘤消退一致的水平總體耐受性劑量確認劑量升級 PRT2527 單一療法侵襲性 B 細胞淋巴瘤(多種類型)、濾泡性淋巴瘤、cll/sll/Richters、MCL PRT2527 N=30血液學惡性腫瘤 ASH 2022 臨牀前口頭表現 CDK9 作為侵襲性淋巴瘤和其他血紅素惡性腫瘤的靶標劑量確認劑量升級 clinicalTrials.gov 標識符:2023 年下半年 AACR RP2D 上的 NCT05159518 實體瘤數據 ClinicalTrials.gov 標識符:NCT05665530
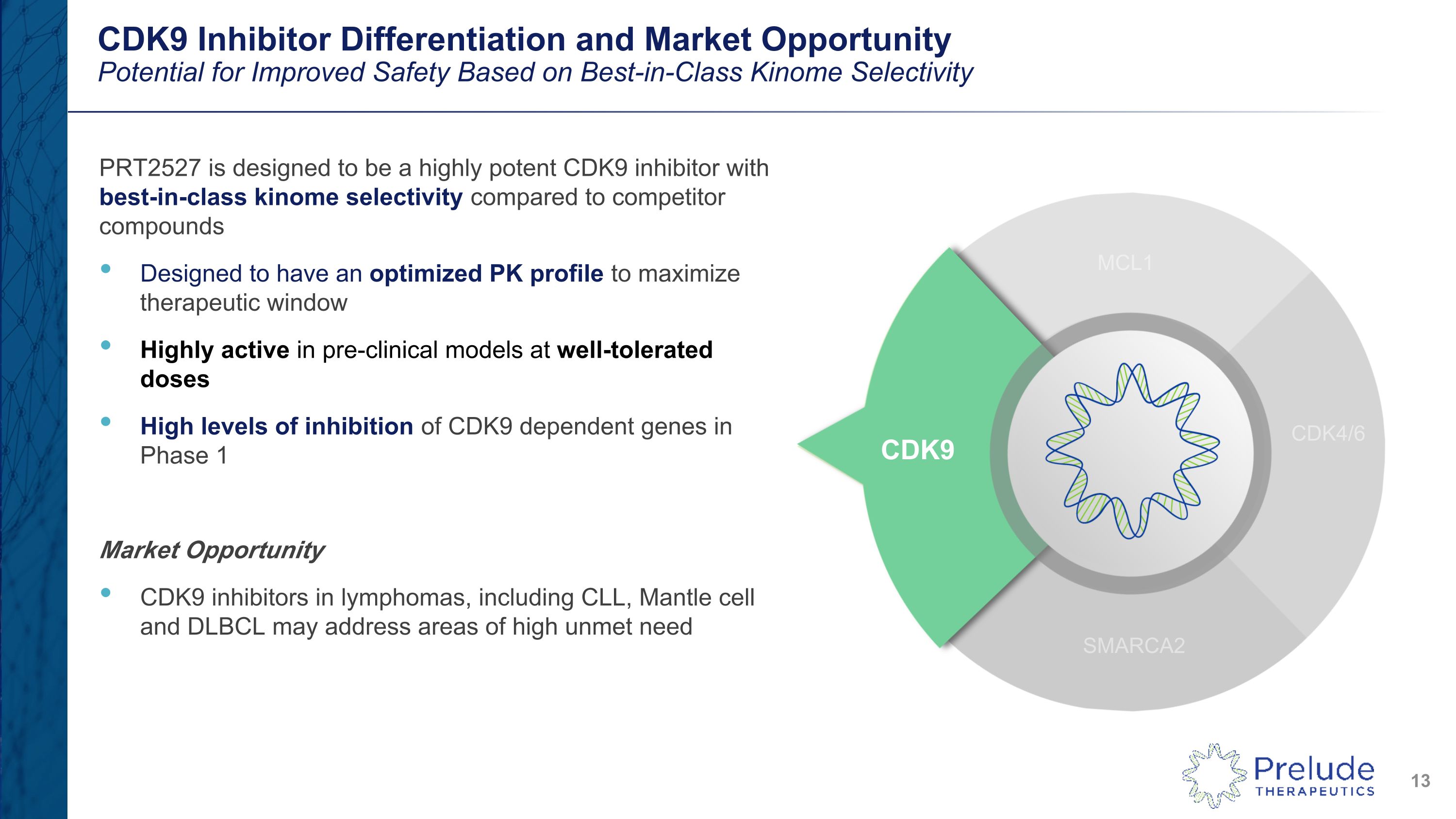
CDK9 抑制劑分化與市場機會基於同類最佳的激組選擇性提高安全性的潛力 PRT2527 旨在成為一種強效的 CDK9 抑制劑,與競爭對手化合物相比,具有同類最佳的激酶組選擇性旨在優化的 PK 譜以最大限度地擴大治療窗口在臨牀前模型中活性在耐受性良好的劑量下在 1 期市場機會 CDK9 抑制劑(包括 CLL)中對淋巴瘤中 CDK9 依賴基因的抑制水平高,Mantle cell 和 DLBCL 可以解決需求高度未得到滿足的領域CDK9 MCL1 SMARCA2 CDK4/6
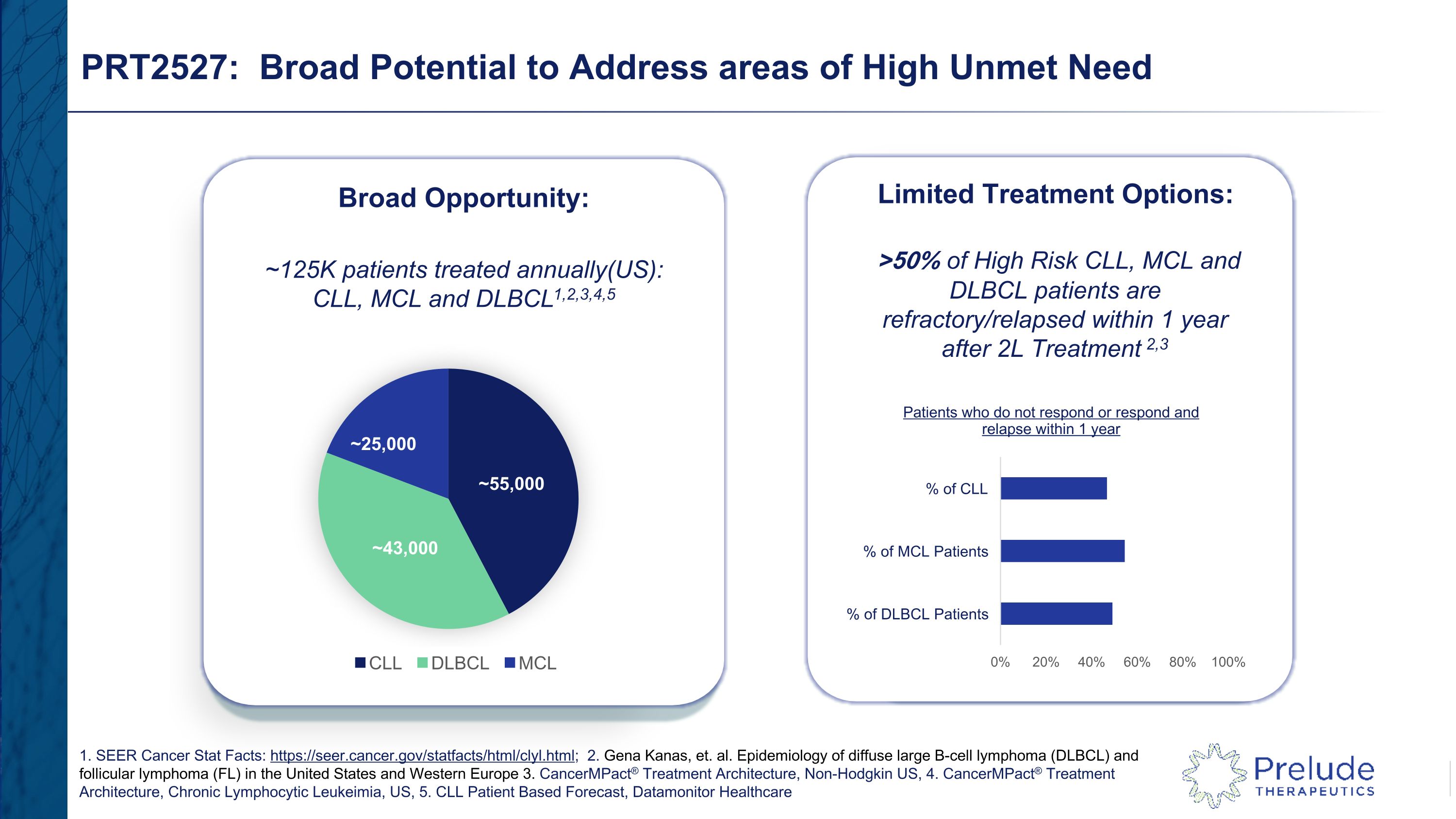
PRT2527:解決高未滿足需求領域的巨大潛力 1.SEER 癌症統計數據:https://seer.cancer.gov/statfacts/html/clyl.html;2.Gena Kanas 等人。美國和西歐瀰漫性大 B 細胞淋巴瘤 (DLBCL) 和濾泡性淋巴瘤 (FL) 的流行病學 3.CancerMpact® 治療架構,美國非霍奇金,4.CancermPact® 治療架構,慢性淋巴細胞白血病,美國,5。CLL 基於患者的預測,Datamonitor Healthcare 廣闊的機會:每年接受治療約 12.5 萬名患者(美國):CLL、MCL 和 DLBCL 1,2,3,4,5 有限的治療選項:超過 50% 的高風險 CLL、MCL 和 DLBCL 患者在 2L 治療後 1 年內出現難治性/復發2,3

PRT1419 MCL1 抑制劑
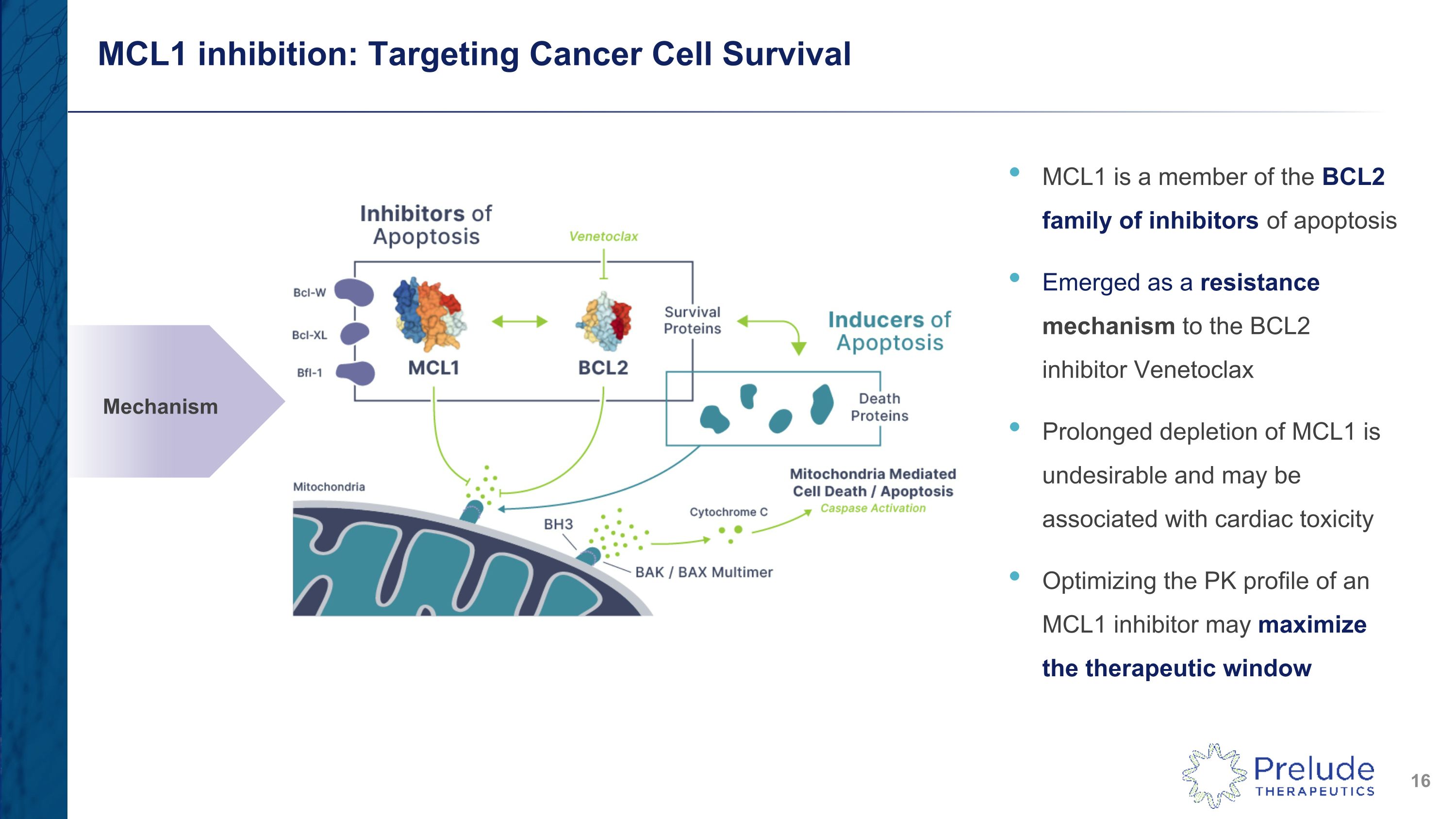
MCL1 抑制:靶向癌細胞存活 MCL1 是 BCL2 細胞凋亡抑制劑家族的一員,作為 BCL2 抑制劑 Venetoclax 的耐藥機制出現 MCL1 的長期耗盡是不可取的,可能與心臟毒性有關。優化 MCL1 抑制劑的 PK 譜可以最大限度地擴大治療窗口機制
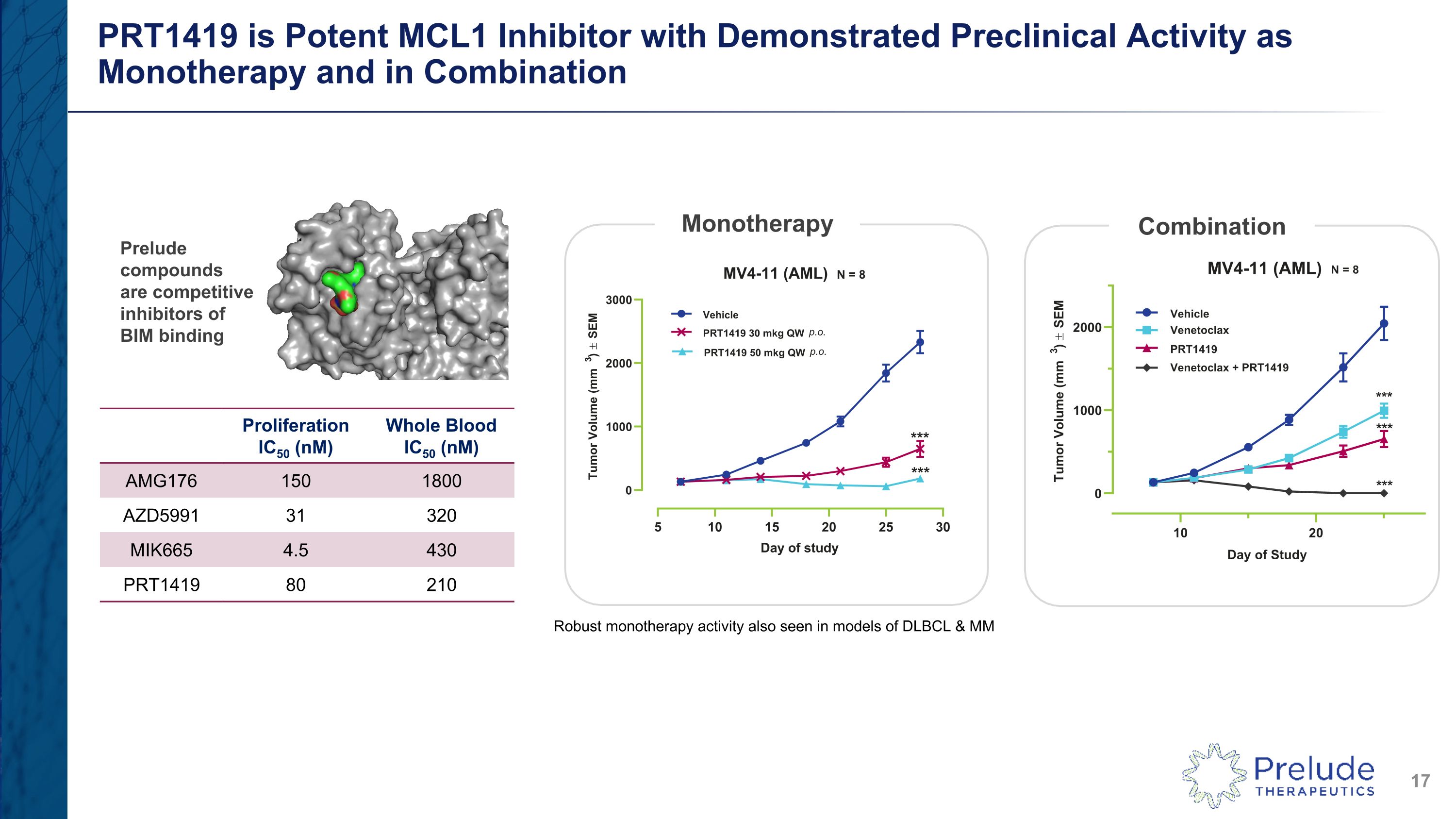
PRT1419 是一種強效的 MCL1 抑制劑,作為單一療法和聯合單一療法組合具有顯著的臨牀前活性。在 DLBCL 和 MM 增殖 IC50 (nM) 的模型中也可以看到強效的 MCL1 抑制劑 IC50 (nM) AMG176 150 1800 AZD5991 31 320 MIK665 4.5 430 PRT1419 80 210 Prelude 化合物是 BIM 結合的競爭性抑制劑
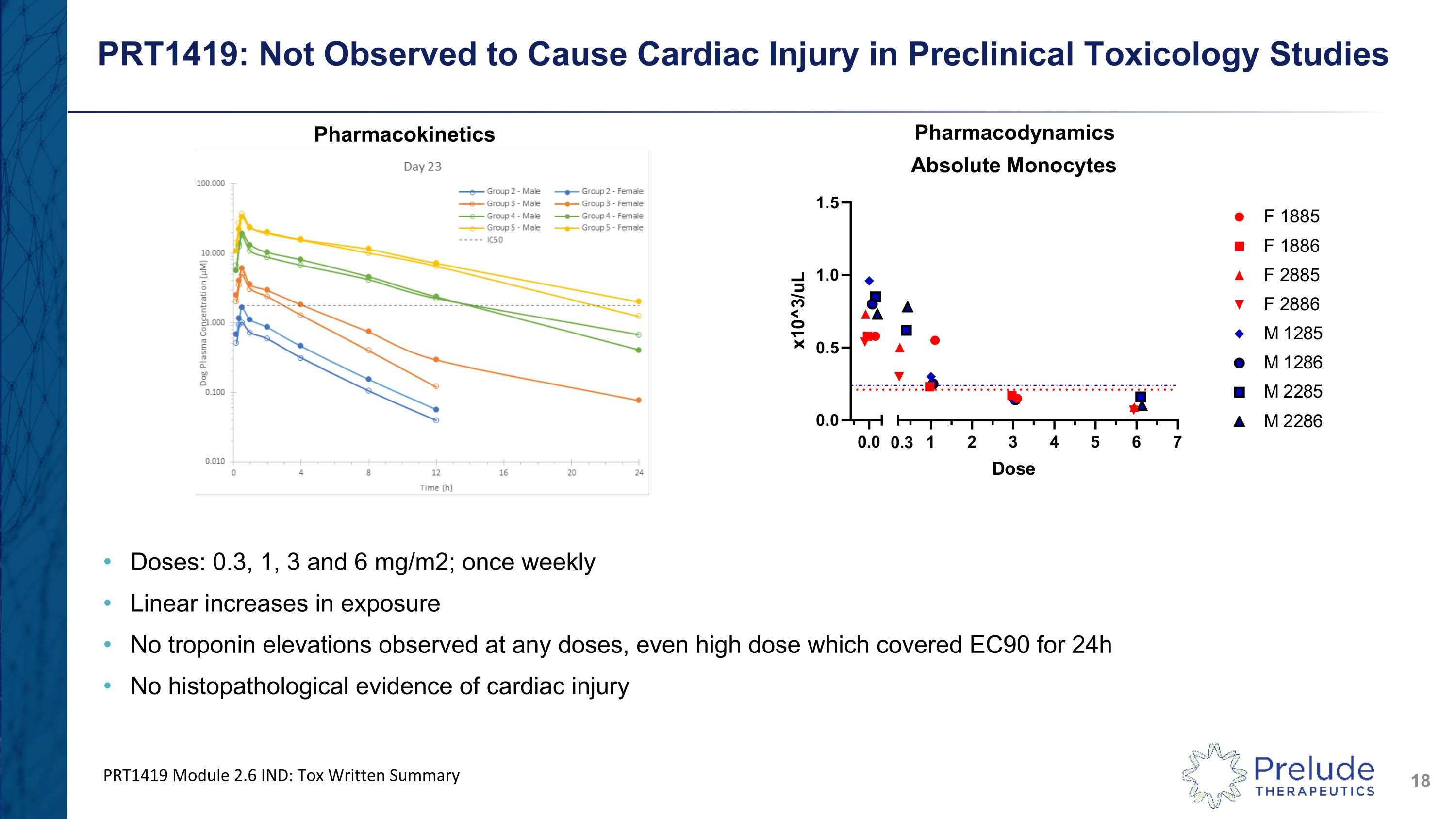
PRT1419:在臨牀前毒理學研究中未觀察到會導致心臟損傷劑量:0.3、1、3 和 6 mg/m2;每週一次暴露量線性增加任何劑量下均未觀察到肌鈣蛋白升高,即使是覆蓋 EC90 的高劑量 24 小時沒有組織病理學證據藥代動力學藥效學 PRT1419 模塊 2.6 IND:Tox 書面摘要

MCL-1 抑制劑:PRT1419 晚期實體瘤的 1 期劑量遞增研究 PRT1419 顯示,晚期轉移性實體瘤患者具有可接受的安全性和耐受性,噁心、嘔吐和腹瀉中最常見的 TRAE 中性粒細胞減少被認為與劑量相關未觀察到心臟毒性誘導活化 bax 和裂解半胱氨酸蛋白酶-3 的濃度為 80 和 120 mg/m2:QW PRT1419,表明 MCL-1 抑制效果最佳 MCL1 是一種對 BCL2 抑制產生耐藥性的機制,尤其是在慢性淋巴細胞白血病和急性髓細胞白血病中;臨牀前很強在 AACR 2023 上發表的血紅素第一階段目標參與度假設;https://preludetx.com/wp-content/uploads/2023/04/Falchook_1419-02_AACR-CT172-poster-23MAR23.pdf
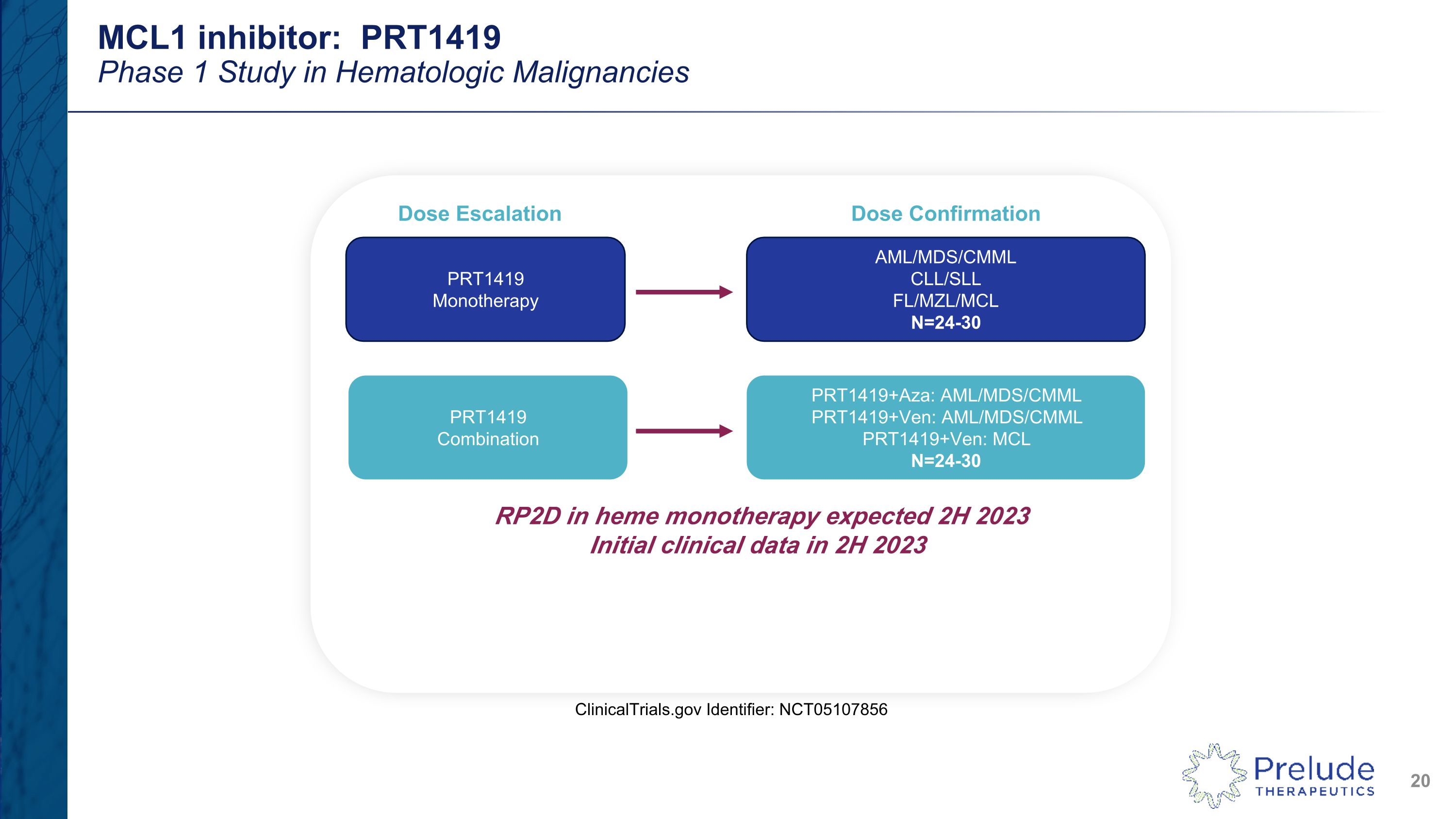
MCL1 抑制劑:PRT1419血液系統惡性腫瘤的 1 期研究 PRT1419 單一療法 AML/MDS/CMML CLL/LL/MZL/MCL N=24-30 PRT1419 組合 prt1419+ven:AML/MDS/CMML prt1419+ven:MCL N=24-30 劑量確認劑量升級 clinicalTrials.gov 標識符:NCT05107856 血紅素單一療法中的 RP2D 預計在 2023 年下半年獲得初步臨牀數據
MCL1 抑制劑差異化與市場機會旨在獲得 PK 特徵以實現預期的靶向參與度 MCL1 CDK9 SMARCA2 CDK4/6 PRT1419 旨在成為一種強效和選擇性的 MCL1 抑制劑,設計為具有高清除率的 PK 譜以提供所需的靶向結合以提高安全性的 GLP 臨牀前研究沒有心臟毒性或肌鈣蛋白變化,在劑量超過療效要求的情況下,沒有證據表明實體瘤 1 期有心臟毒性或肌鈣蛋白變化推薦的第二階段劑量市場機會 AML、CLL 和 MCL 患者需要其他治療選項 PRT1419 模塊 2.6 IND:Tox 書面摘要
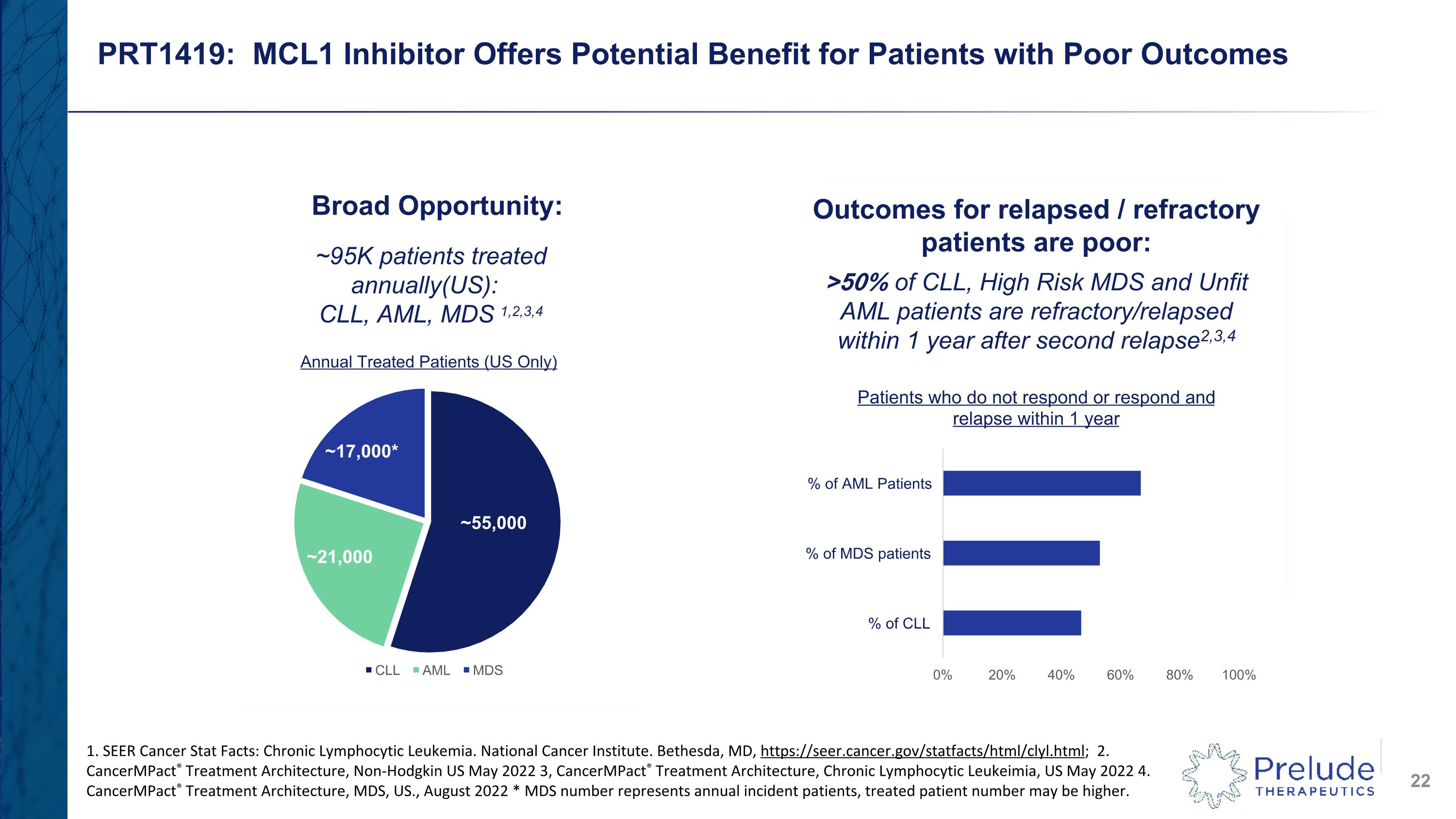
PRT1419:MCL1 抑制劑為預後不佳的患者提供潛在益處廣闊機會:每年接受約 95 萬名患者治療(美國):CLL、AML、MDS 1,2,3,4 復發/難治性患者的預後不佳:超過 50% 的 CLL、高風險 MDS 和 Unfit AML 患者在第二次復發後的 1 年內出現難治性/復發2,3,4 1。SEER 癌症統計數據:慢性淋巴細胞白血病。國家癌症研究所。醫學博士貝塞斯達,https://seer.cancer.gov/statfacts/html/clyl.html;2.CancermPact® 治療架構,非霍奇金美國 2022 年 5 月 3,CancermPact® 治療架構,慢性淋巴細胞白血病,美國 2022 年 5 月 4.CancermPact® 治療架構,MDS,美國,2022 年 8 月 * MDS 數字代表年度發病患者,接受治療的患者人數可能更高。
PRT3645 下一代 CDK4/6 抑制劑

下一代 CDK4/6 抑制:通過細胞週期調節機制靶向癌症 HR+ 乳腺癌中的下一代 CDK4/6 抑制劑獲得批准的機制對 RAS 和 HER2 途徑的其他 RAS 和 HER2 途徑抑制劑的耐藥機制,包括 KRAS G12C 當前抑制劑無法穿透血腦屏障 (BBB) 的下一代 CDK4/6 抑制劑可能在需求未得到滿足的領域轉化為活性 HR+ 乳腺癌連續使用下一代 CDK4/6 抑制劑在乳腺癌也可能改善預後 ASCO 2022 參考文獻:一項針對不可切除或激素受體陽性 (HR+)、HER2 陰性轉移性乳腺癌 (MBC) 的抗雌激素治療和細胞週期蛋白依賴性激酶 4/6 抑制 (CDK 4/6i) 進展後的氟維司羣或依西美坦聯合或不使用利博西利的隨機 II 期試驗:維持試驗. 並參見 AACR 2023;https://preludetx.com/wp-content/uploads/2023/04/Zou_CDK46_AACR-2023_Poster-5973_04APR23.pdf
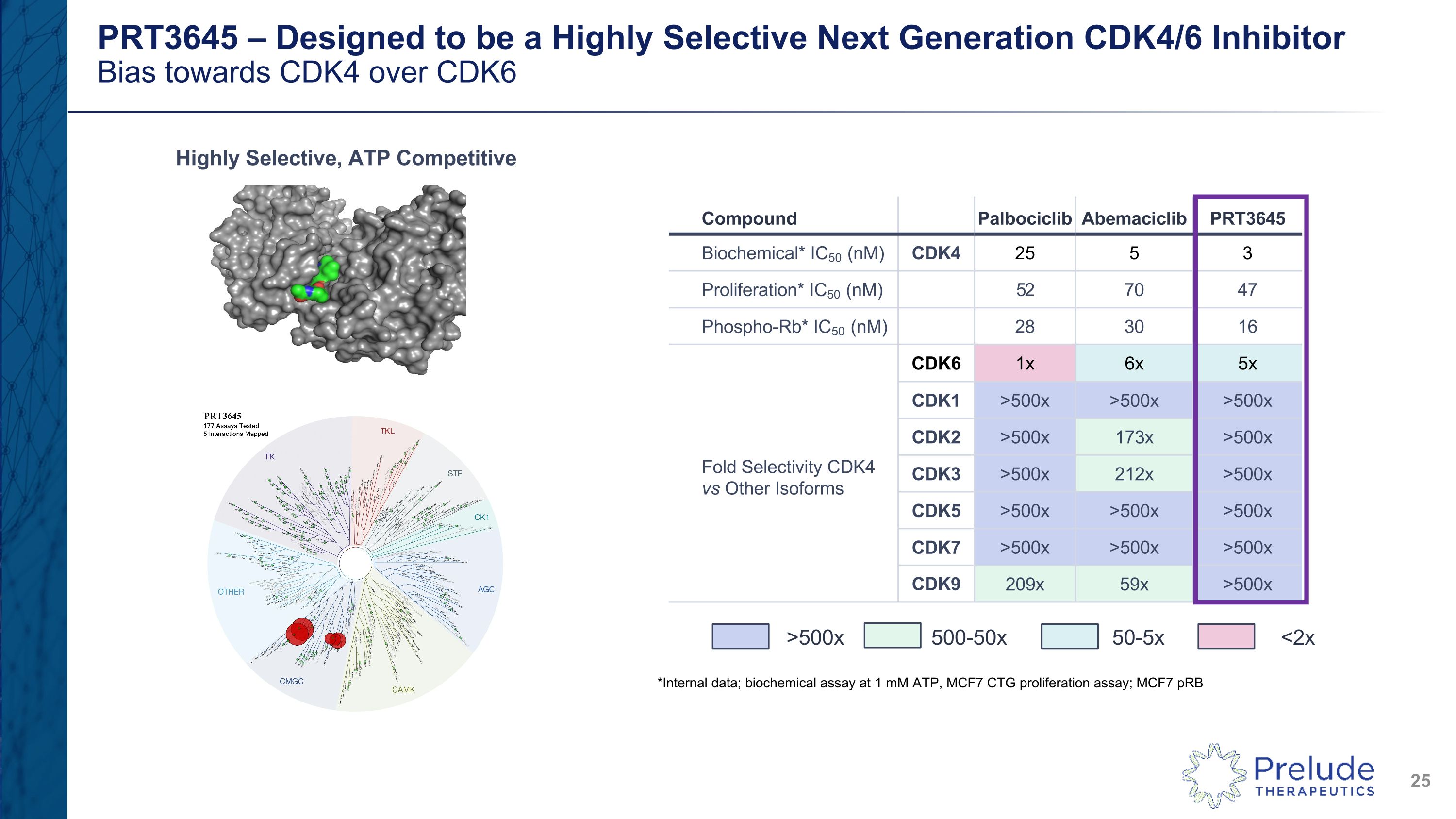
PRT3645 — 旨在成為對 CDK4 具有高度選擇性的下一代 CDK4/6 抑制劑偏向 CDK4 而不是 CDK6 化合物 palbociclib abemaciclib PRT3645 生化* IC50 (nM) CDK4 25 5 3 增殖* IC50 (nM) 52 70 47 phopho-Rb* IC50 (nM) 28 30 16 倍選擇性 CDK6 1x 6x 5x CDK1 >500x >500x >500x CDK2 >500x 173x >500x CDK3 >500x 212x >500x CDK5 >500x >500x >500x >500x >500x >500x >500x >500x CDK9 209x 59x >500x >500x 500-50x 50-5x
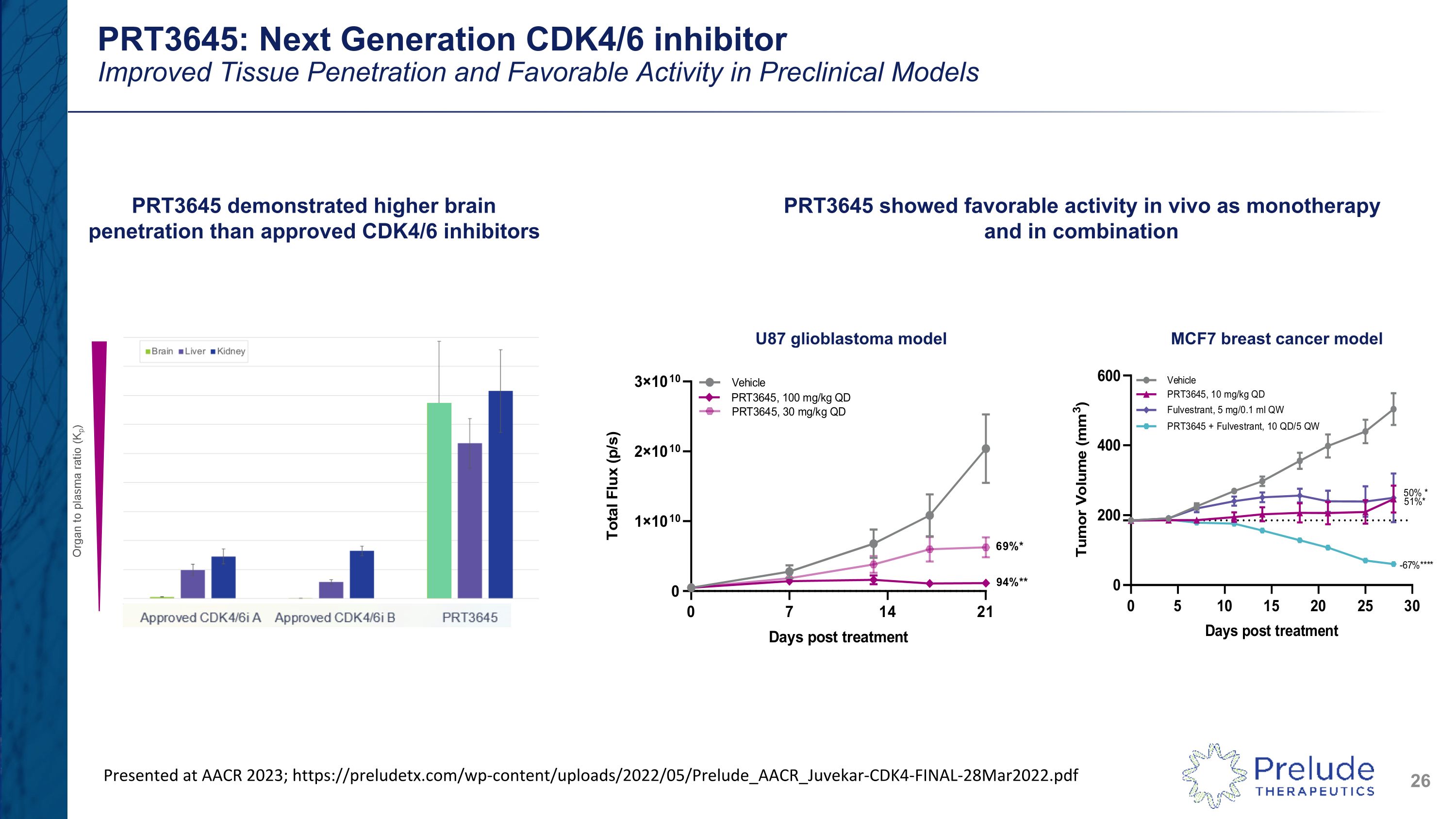
PRT3645:下一代 CDK4/6 抑制劑臨牀前模型中組織穿透率的提高和有利活性 PRT3645 顯示出比批准的 CDK4/6 抑制劑更高的腦穿透率 PRT3645 作為單一療法在體內顯示出良好的活性 U87 膠質母細胞瘤模型 MCF7 乳腺癌模型在 AACR 2023 上發表;https://preludetx.com/wp-content/uploads/2022/05/Prelude_AACR_Juvekar-CDK4-FINAL-28Mar2022.pdf
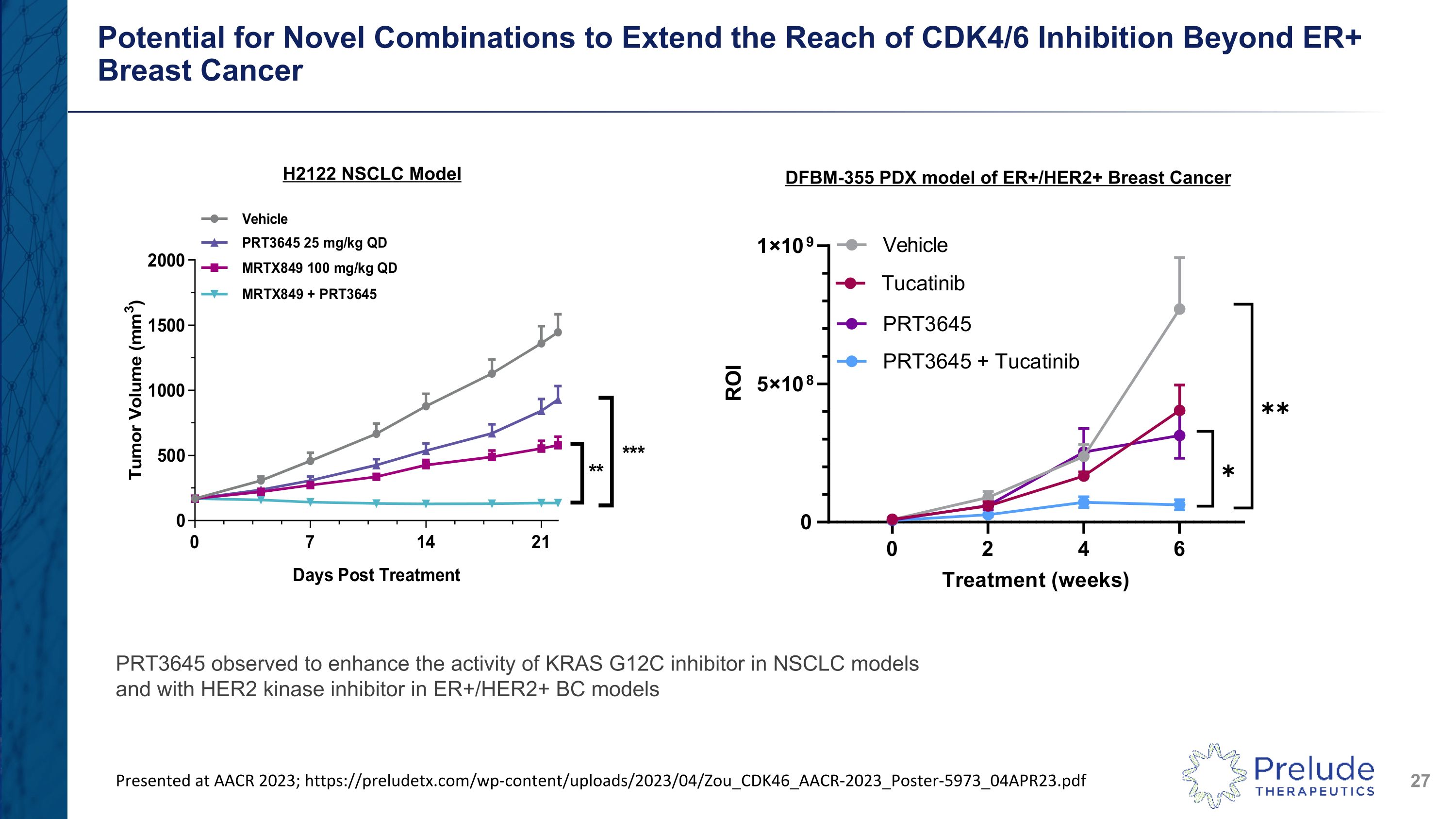
新型組合有可能將 CDK4/6 抑制範圍擴大到 ER+ 乳腺癌以外 H2122 NSCLC 模型 DFBM-355 ER+/HER2+ 乳腺癌的 PDX 模型 PRT3645 觀察到增強非小細胞肺癌模型中 KRAS G12C 抑制劑的活性,在 ER+/HER2+ BC 模型中使用 HER2 激酶抑制劑在 AACR 2023 上發表;https://preludetx.com/wp-content/uploads/2023/04/Zou_CDK46_AACR-2023_Poster-5973_04APR23.pdf

下一代 CDK4/6 抑制劑:PRT3645實體瘤的 1 期研究一種潛在的分化高腦穿透性下一代 CDK4/6 抑制劑有可能將 CDK4/6 抑制範圍擴大到 HR+ 乳腺癌以外,第一代 CDK4/6 抑制劑已獲批 PRT3645 生物標誌物富含特定腫瘤類型的患者,包括肉瘤、間皮瘤、神經膠質瘤、頭頸癌和非腫瘤小細胞肺癌,以及伴有或不伴腦轉移的乳腺癌。劑量遞增和確認臨牀試驗。gov 標識符:NCT05538572 2023 年下半年 RP2D 實體瘤的初始臨牀數據
下一代 CDK4/6 抑制劑分化與市場機會具有潛力的深層組織穿透 PRT3645 有可能成為一種強效和選擇性的下一代 CDK4/6 抑制劑專為包括大腦穿透在內的深層組織穿透而設計用於改善代謝特徵以外的疾病進行聯合治療臨牀前 GLP 研究的有利毒性有可能提高臨牀耐受性市場機會:乳腺癌患者可能從中受益順序 CDK4/6 抑制劑治療 2023 年美國估計有 65,000 名接受了 CDK4/6 抑制劑治療的乳腺癌患者。其他實體瘤(肺癌、神經膠質瘤、HER2+ 乳腺癌)可能表現出聯合使用活性 MCL1 CDK9 SMARCA2 CDK4/6 PRT3645 模塊 2.6 IND PK 書面摘要;ASCO 2022 參考文獻:富維司羣或依西美坦聯合使用 II 期試驗不可切除或激素患者(pts)在抗雌激素治療加細胞週期蛋白依賴性激酶 4/6 抑制(CDK 4/6i)取得進展後,bociclib受體陽性 (HR+)、HER2 陰性轉移性乳腺癌 (MBC):繼續試驗。參見 AACR 2023;https://preludetx.com/wp-content/uploads/2023/04/Zou_CDK46_AACR-2023_Poster-5973_04APR23.pdf
PR3789 SMARCA2 Degrader
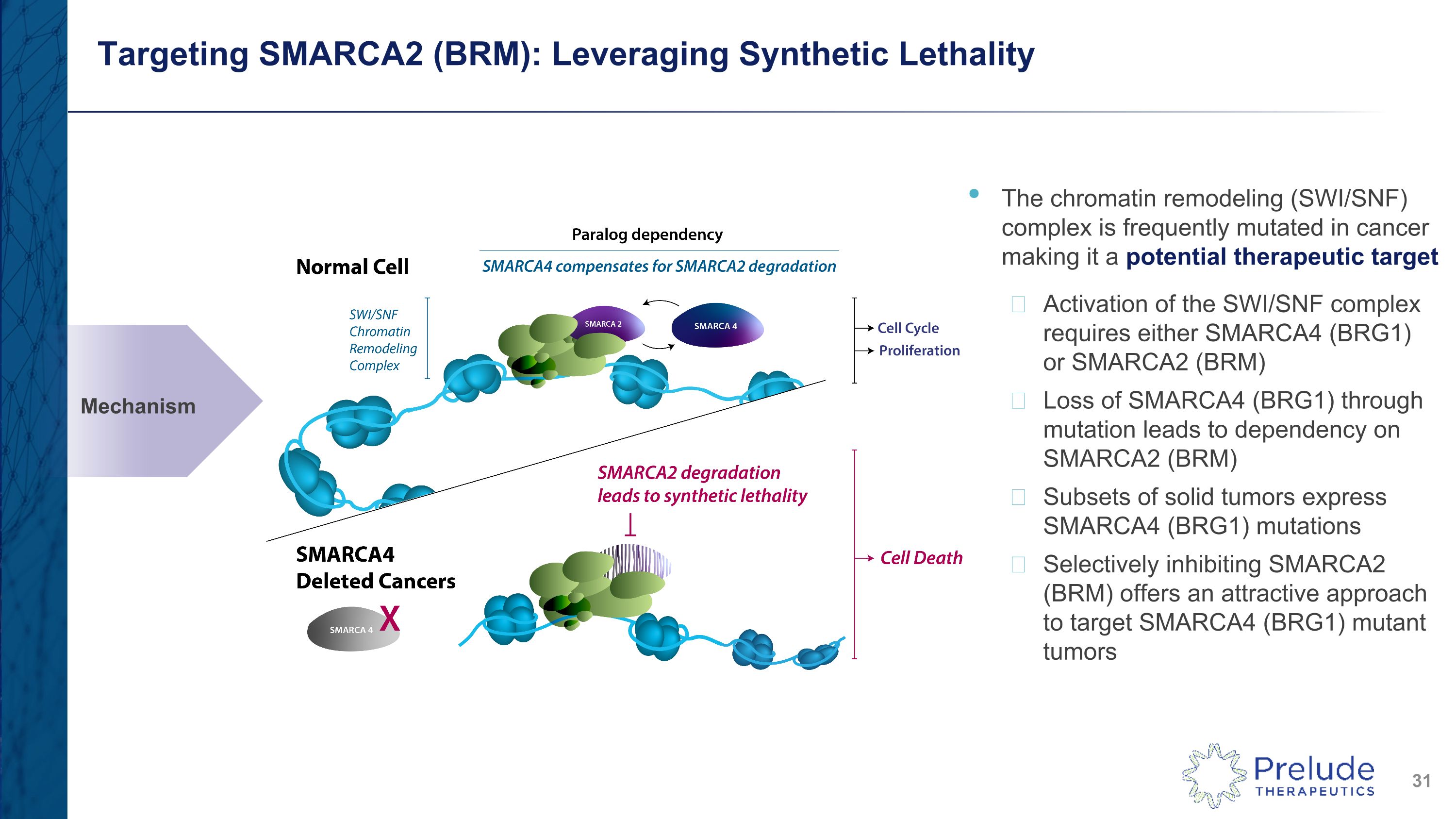
靶向 SMARCA2 (BRM):利用合成殺傷力染色質重塑(SWI/SNF)複合物在癌症中經常發生突變,使其成為潛在的治療靶點激活 SWI/SNF 複合物需要 SMARCA4 (BRG1) 或 SMARCA2 (BRM) 通過突變丟失 SMARCA4 (BRG1) 會導致依賴實體瘤表達的子集選擇性抑制 SMARCA4 (BRG1) 突變 SMARCA2 (BRM) 為靶向 β (BRG1) 突變體腫瘤提供了一種有吸引力的方法機制 SMARCA2 SMARCA4
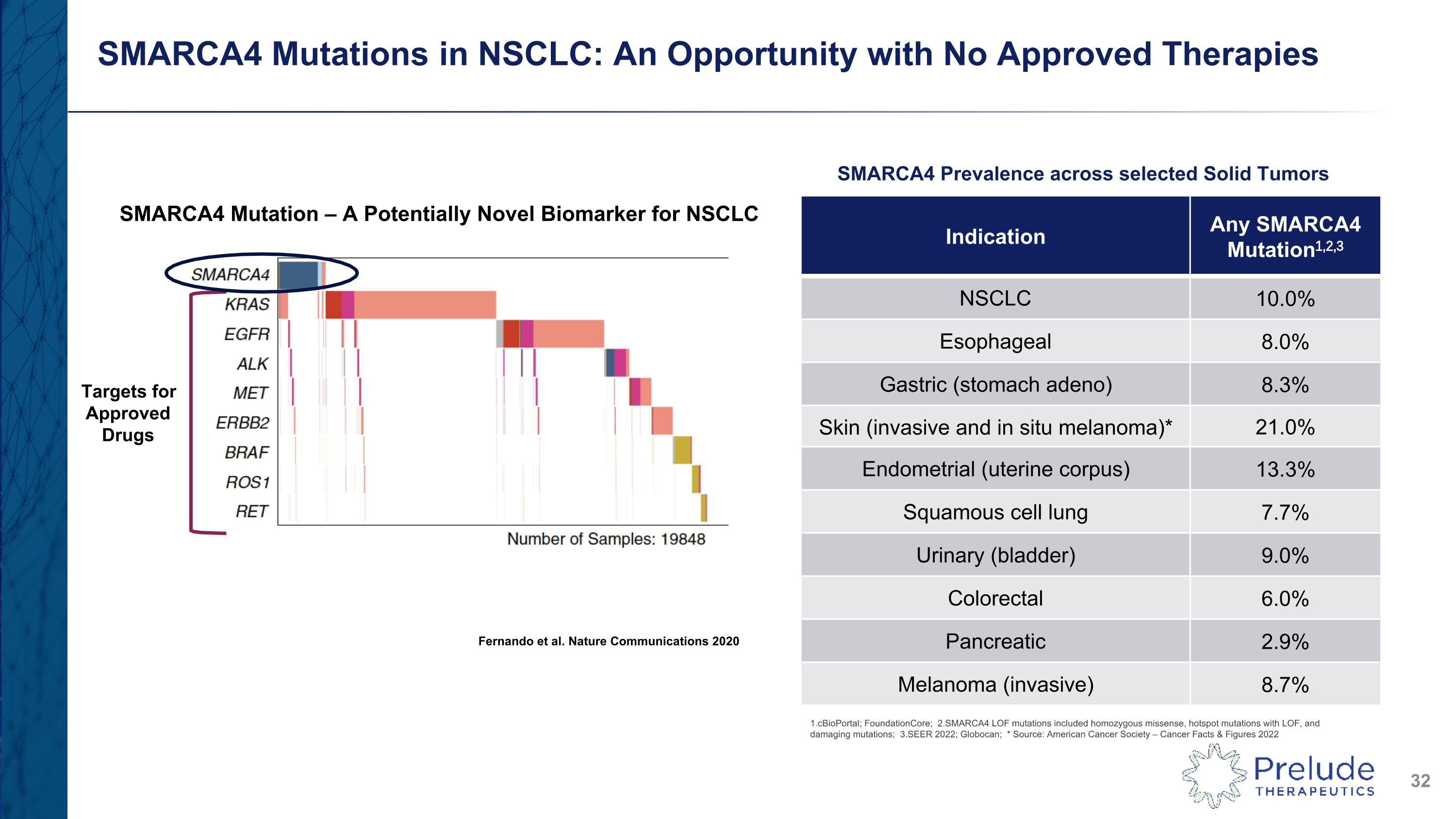
適應症任何 SMARCA4 突變1,2,3 NSCLC 10.0% 食管 8.0% 胃(胃腺腺)8.3% 皮膚(侵襲性和原位黑色素瘤)* 21.0% 子宮內膜(子宮體)13.3% 鱗狀細胞肺 7.7% 尿液(膀胱)9.0% 胰腺 2.9% 黑色素瘤(侵襲性)8.7% 非小細胞肺癌中存在未獲批准療法的機會 SMARCA4 患病率 1.0% cbioPortal;FoundationCore;2.SMARCA4 LOF 突變包括純合錯義、帶有 LOF 的熱點突變和破壞性突變;3.SEER 2022;Globocan;* 來源:SMARCA4美國癌症協會 — 2022 年癌症事實與數據 Fernando 等人Nature Communications 2020 SMARCA4 突變——批准藥物非小細胞肺癌靶點的潛在新生物標誌物
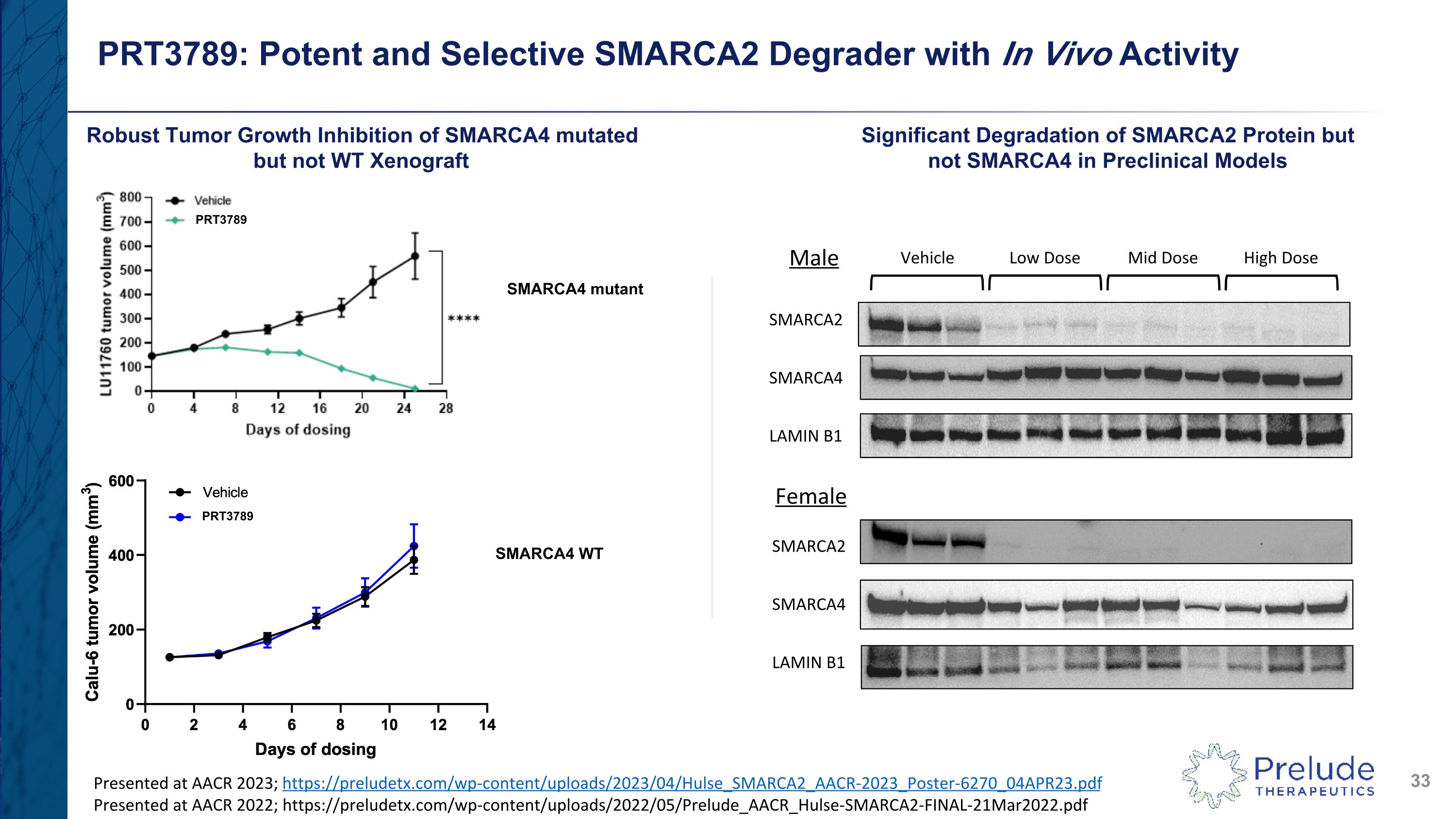
PRT3789:具有體內活性的強效和選擇性的 SMARCA2 降解劑在臨牀前模型中抑制 SMARCA4 突變但不是 WT Xenograft 強效腫瘤生長抑制 SMARCA2 蛋白但不降解 SMARCA4 在臨牀前模型中 SMARCA4 突變體 SMARCA4 WT 車輛低劑量中劑量高劑量抗體 LAMIN B1 脱落 LAMIN B1 男性女性在 AACR 2023 上發表;https://preludetx.com/wp-content/uploads/2023/04/Hulse_SMARCA2_AACR-2023_Poster-6270_04APR23.pdf 在 AACR 2022 上發表;PRT3789 PRT3789 SMARCA2 SMARCA4 SMARCA2 SMARCA4https://preludetx.com/wp-content/uploads/2022/05/Prelude_AACR_Hulse-SMARCA2-FINAL-21Mar2022.pdf

SMARCA2 降解器:PRT3789 實體瘤的 1 期研究 SMARCA2 抑制對缺乏 SMARCA4 的癌症患者具有最大的潛力,包括大約 10% 的非小細胞肺癌 SMARCA2 降解有待評估 1 期研究人羣:晚期、複發性或轉移性疾病,由局部 NGS 或 IHC 在腫瘤組織或血液 HR+ 中選擇的截斷突變和/或缺失導致的 SMARCA4 流失 HR+ 和 HR2 陰性或 HR+ 還有 HER2+乳腺癌復發 GBM(IDH 野生型)或 CDKN2A/B 純合子缺失的 IDH 突變體星形細胞瘤 KRAS-mutant NSCLC CDK 途徑改變:惡性間皮瘤、HPV 陰性 HNSCC(包括口腔、口咽、下嚥和喉)、肉瘤或 NSCLC ClinicalTrials.gov 標識符:NCT05538572 PRT3789 實體瘤缺失 SMARCA4 回填:最多 10 名參與者,至少 6 名參與者流失 SMARCA4 劑量遞增和確認 IND 的 NSCLC 參與者已獲批准 2022 年第四季度臨牀更新預計於 2023 年下半年 clinicalTrials.gov 標識符:NCT05639751
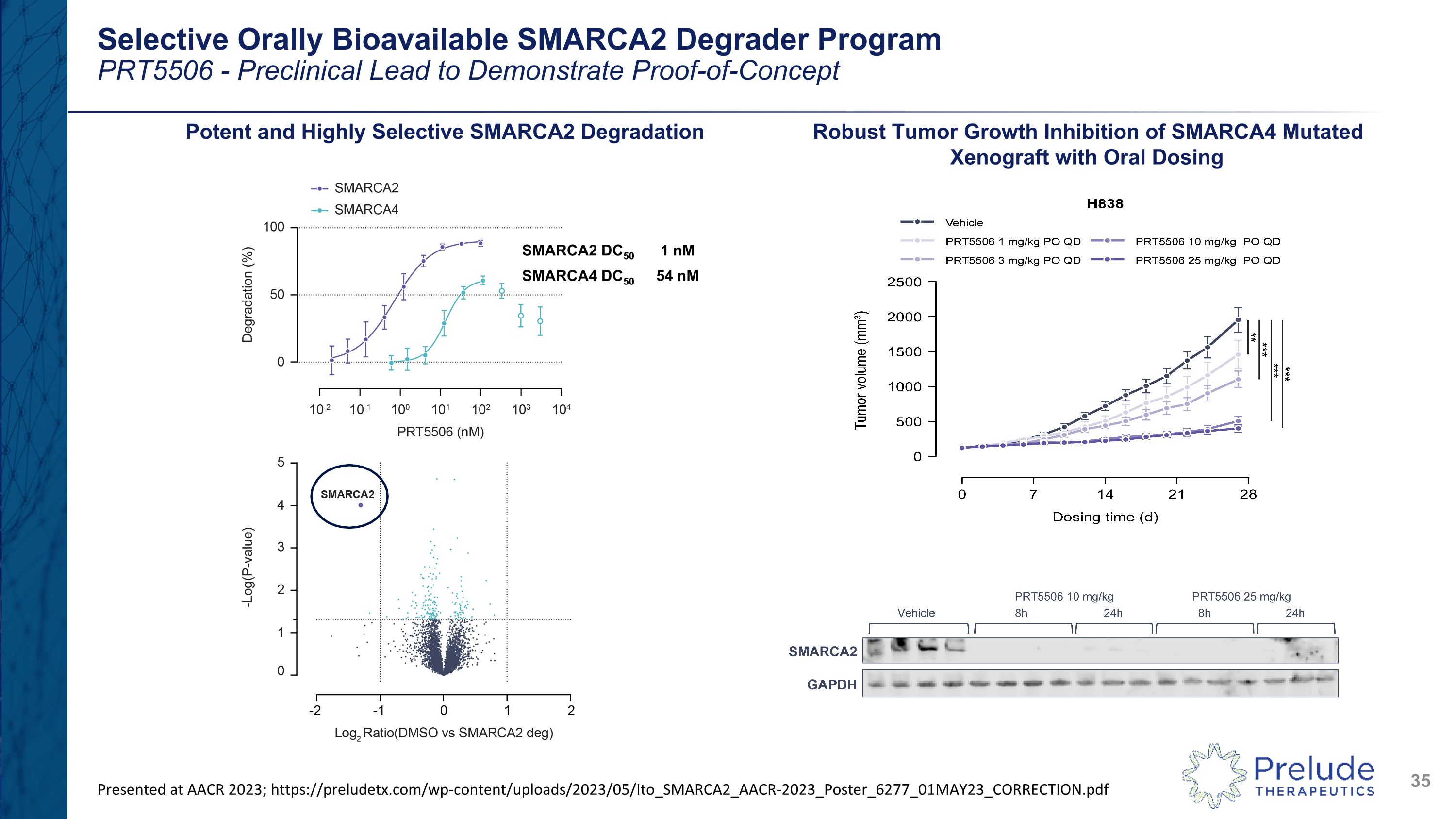
選擇性口服生物可利用性 SMARCA2 降解劑 progrt5506——臨牀前研究人員證明瞭口服給藥強效和高選擇性 SMARCA2 體外降解的 SMARCA4 突變異種移植具有強大的腫瘤生長抑制 SMARCA2 DC50 1 nM SMARCA4 DC50 54 nM 在 AACR 2023 上發表;https://preludetx.com/wp-content/uploads/2023/05/Ito_SMARCA2_AACR-2023_Poster_6277_01MAY23_CORRECTION.pdf
SMARCA2 差異化與市場機會潛在同類首創 SMARCA2 (BRM) 靶向蛋白降解劑 PRT3789 是潛在的同類首創 SMARCA2 降解劑潛在的有效選擇性 SMARCA2 靶向蛋白降解方法我們認為 SMARCA2 選擇性可能提供良好的毒性特徵觀察到 SMARCA4 突變臨牀前模型中有良好的療效,我們認為為臨牀中的患者選擇策略提供了途徑市場機會:美國/歐盟5 有 70,000 名突變患者 CDK4/6 MCL1 CDK9 SMARCA4 SMARCA2
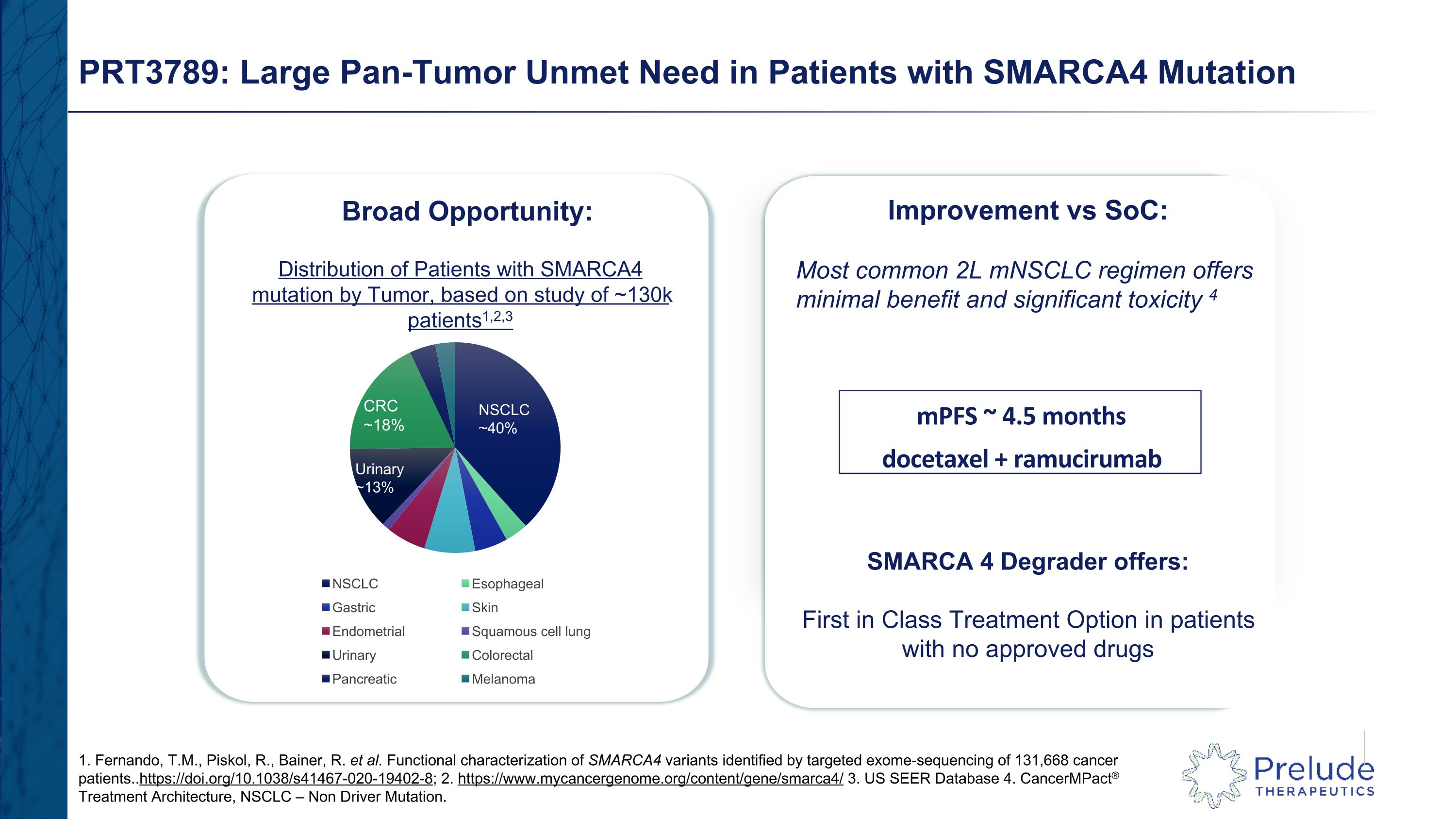
PRT3789:SMARCA4 突變患者的大型泛腫瘤需求未得到滿足的機會廣泛:與 SoC 相比有所改善:最常見的 2L mnsCLC 療法的益處微乎其微,毒性顯著 4 SMARCA 4 Degrader 提供:沒有批准藥物 mpF 的患者中首屈一指的治療選擇 mpF ~ 4.5 個月 + ramucirumab NSCLC ~ 40% 1。費爾南多、T.M.、Piskol、R.、Bainer、R. 等對131,668名癌症患者進行靶向外顯子組測序識別出的 SMARCA4 變異的功能表徵... https://doi.org/10.1038/s41467-020-19402-8; 2. https://www.mycancergenome.org/content/gene/smarca4/ 3.美國 SEER 數據庫 4.CancermPact® 治療架構,非小細胞肺癌——非驅動因素突變。根據對大約 130 萬名患者的研究,CRC ~ 18% 尿 ~ 13% 非小細胞肺癌 ~ 40% CRC ~ 18% 尿液 ~ 13% 腫瘤突變患者的分佈情況1,2,3 SMARCA4

Prelude Therapeutics:關鍵要點我們預計,截至 2023 年 6 月 1 日,我們的現金、現金等價物和有價證券將使我們能夠為 2026 年的運營支出和資本支出需求提供資金。潛在的同類首創 SMARCA2 降解器計劃可能在競爭對手中佔據顯著領先地位,為公司提供變革潛力,在未來 12 — 24 個月內將項目推向關鍵轉折點 CDK9 和 MCL-1 項目的新興臨牀數據表明了類別的潛力領先的機會深度臨牀包含獨特且可能為同類最佳或同類首創分子的產品線

經驗豐富的管理團隊:Proven Track Combs,博士執行副總裁兼化學主管 Peggy Scherle,博士首席科學官 Jane Huang 醫學博士總裁兼首席醫學官 Kris Vaddi,博士創始人兼首席執行官 Laurent Chardonnet,MBA 首席財務官 Bryant Lim,法學博士首席法務官兼公司祕書