

2024年8月の企業プレゼンテーション

将来の見通しに関する記述このプレゼンテーションには、1995年の民間証券訴訟改革法の意味における将来の見通しに関する記述が含まれています。「信じる」、「するかもしれない」、「するだろう」、「期待する」、「続ける」、「予想する」、「意図する」、「期待する」、および同様の表現は、将来の見通しに関する記述を識別するためのものです。このプレゼンテーションに含まれている、歴史的事実に関係のないすべての記述は、将来の見通しに関する記述と見なす必要があります。これには、LYR-210を評価するために進行中の2つのENLIGHTEN第3相試験に焦点を当てていること、現在進行中のENLIGHTEN 1エクステンション研究と2024年第4四半期のデータへの期待、進行中のENLIGHTEN 2試験、および進行中のLYR-210が位置付けられるかどうか、2025年上半期のデータへの期待に関する記述が含まれます。現在のネットの慣行、2026年までのキャッシュランウェイ、そして私たちのキャッシュランウェイについて投資家に最新情報を提供することを計画しています。株主価値を最大化するための潜在的な戦略的オプションを評価する計画です。これらの記述は約束でも保証でもありませんが、会社の実際の業績、業績、または成果が、将来の見通しに関する記述で表明または暗示される将来の結果、業績、または成果と大きく異なる原因となる既知および未知のリスク、不確実性、その他の重要な要因が含まれています。以下が含まれますが、これらに限定されません。株主価値を最大化するために当社が追求する潜在的な財務的または戦略的オプションでは、適切な取引が特定されない場合があります。または1つが確認されたらそして追求しても、魅力的な条件で完了しないか、まったくありません。多額の運用コストとなる3つの借地権を転貸または譲渡できること、創業以来多額の損失が発生し、当面は多額の追加損失が発生すると予想されること、事業から繰り返し発生する損失は、継続企業として継続する能力について大きな疑問を投げかけています。開発を完了するためには多額の追加資金が必要であるためですそして私たちの製品候補の規制当局の承認を得て承認されれば、当社の製品を商品化してください。ENLIGHTEN 1第3相試験が主要評価項目を満たさなかったため、資金調達がより困難になりました。慢性鼻副鼻腔炎(CRS)の治療薬としてLYR-210を評価するENLIGHTEN 1第3相試験が主要評価項目を満たさなかったため、製品開発プログラムまたは商品化の取り組みを延期、削減、または中止せざるを得ない可能性があります。、2024年5月に発表されましたが、当社がLYRの開発を完了する能力については大きな不確実性があります。210 そして、LYR-210の規制当局の承認を得る能力は少なくとも大幅に遅れており、不可能かもしれません。ナスダックの継続的な上場要件へのコンプライアンスを取り戻せない場合、当社の普通株式はナスダック・グローバル・マーケットから上場廃止になる可能性があります。主要人員の喪失は、製品候補の製造能力に著しい悪影響を及ぼします。他の活動の中でも、私たちは製品候補の製造を社内で行うことはもうありません。私たちの事業は依存度が高いです私たちの最も先進的な製品候補の成功について、LYR-210; 現在の製品候補と将来の製品候補に必要な臨床試験は費用と時間がかかり、結果は不確実です。また、当社の臨床試験がこれらの評価の安全性または有効性のエンドポイントを満たさない場合、またはこれらの試験で大幅な遅延が発生した場合、製品候補を商品化する当社の能力と財政状態は損なわれます。第三者が当社の前臨床試験または臨床試験に従って当社の前臨床試験または臨床試験を実施しなかった場合適切な臨床診療を適時に行うと、私たちの臨床が遅れたり、妨げられたりする可能性があります製品候補の規制当局の承認を求めたり取得したり、商品化したりする能力。LYR-210が市販承認を受けたとしても、医師、患者、第三者支払者、または商業的成功に必要な医学界の他の人々による市場での受け入れを得られない可能性があります。LianBioとのコラボレーションが成功しない場合、当社の製品候補は市場の可能性を最大限に発揮できない可能性があります。ライセンスやその他の戦略的契約に基づく義務を管理する当社の能力は、経営陣の注意をそらす可能性があります時間と私たちの限られたリソース、原因事業の遅延または中断、当社の事業活動は、ライセンス契約や戦略的契約における特定の契約によって制限される場合があり、その結果、当社の開発や商業的機会が制限される可能性があります。国際法域でマーケティングの承認を得られないと、そのような法域で当社の製品が販売されなくなります。競合他社による開発により、当社の製品または技術が時代遅れになったり、競争力がなくなったり、市場規模が縮小したりする可能性があります。製品候補の商品化が成功するかどうかは、の一部政府当局や健康保険会社が補償範囲、適切な償還レベル、価格方針をどの程度確立しているか、製品候補に対する補償の取得または維持、および適切な償還が承認された場合、それらの製品のマーケティング能力が制限され、収益を生み出す能力が低下する可能性があります。知的財産権を取得、維持、または適切に保護できない場合、市場で効果的に競争できなくなる可能性があります。国際テロ、政情不安、そして私たちのビジネスにおける戦争。また、COVID-19パンデミックなどの他の出来事の影響は、臨床試験を含む当社の事業と運営に悪影響を及ぼす可能性があります。2024年8月14日にSECに提出されたフォーム10-Qの当社の四半期報告書の「リスク要因」という見出しの下で説明されているこれらおよびその他の重要な要因により、実際の結果がこのプレスリリースに記載されている将来の見通しに関する記述に示されているものと大きく異なる可能性があります。このような将来の見通しに関する記述は、このプレスリリースの日付現在の経営陣の見積もりを反映しています。当社は、将来のある時点でこのような将来の見通しに関する記述を更新することを選択する場合がありますが、その後の出来事により見解が変わったとしても、更新する義務は負いません。このプレゼンテーションには、業界、出版物、研究、第三者または当社が実施した調査や研究から得た統計データや市場データも含まれています。業界の出版物や第三者の調査、調査、調査では、通常、それらの情報は信頼できると思われる情報源から入手されたことが示されていますが、そのような情報の正確性や完全性を保証するものではありません。このプレゼンテーションで使われているすべての市場データには、いくつかの仮定と制限があります。そのような見積もりを過度に重視しないように注意してください。これらの業界出版物や第三者による調査、調査、研究は信頼できると思いますが、そのようなデータを独自に検証したわけではありません。私たちが事業を展開している業界は、さまざまな要因による高度な不確実性、変化、リスクにさらされており、その結果、結果が独立パートナーや当社が行った見積もりで表明されたものと大きく異なる可能性があります。ライラの製品候補であるLYR-210とLYR-220は、FDAの承認を受けていません。このプレゼンテーションは投資家コミュニティのみを対象としています。ここに記載されている内容は、当社の製品候補を宣伝することを意図したものではありません。以前に発表された人員削減に関連して、Lyraは運営費を削減するために、LYR-210の製造と商品化の取り組み、およびLYR-220の開発努力を中止しました。それでも、進行中のLYR-210の2つのENLIGHTEN第3相臨床試験を継続するにつれて、引き続き費用が発生すると予想しています。

1)米国成人の健康統計表の要約:国民健康インタビュー調査、2018年、表A-20億、A-2c; 2)バグリーらInt Forum Allergy Rhinol、2014; 4 (7): 525-3; 6か月間継続的な抗炎症療法を提供するように設計された生体吸収性副鼻腔インプラント適応症:慢性鼻副鼻腔炎 (CRS) ~ 米国人口の 12% ~ 50% の患者が治療に失敗します2 重要な第3相試験 100件以上のグローバル特許が発行済みで、長時間作用型抗炎症薬を開発中の臨床段階のバイオテクノロジー企業慢性鼻副鼻腔炎の治療のための副鼻腔インプラント会社概要

慢性鼻副鼻腔炎(CRS):「認識されない伝染病」1 CRSの主な症状1 鼻づまりと鼻づまり顔の痛みと圧迫鼻汁鼻分泌物鼻汁嗅覚の低下(CRS)毎年CRS患者を治療しました2 CRS患者(医療管理に失敗したCRS)患者3~800,000〜400人(現在ENT4 〜1401)Tan Bk et すべて。Am J Respir CritCare Med、2013; 188 (11): 1275—7; 2) チャンら。耳鼻咽頭頭頸部外科、2018; 3)バグリーら。Int Forum Allergy Rhinol、2014; 4 (7): 525-32; 4) OM1リアルワールドデータクラウド (OM1, Inc、マサチューセッツ州ボストン、米国)、2015 — 2019年4月。分析 2019年9月
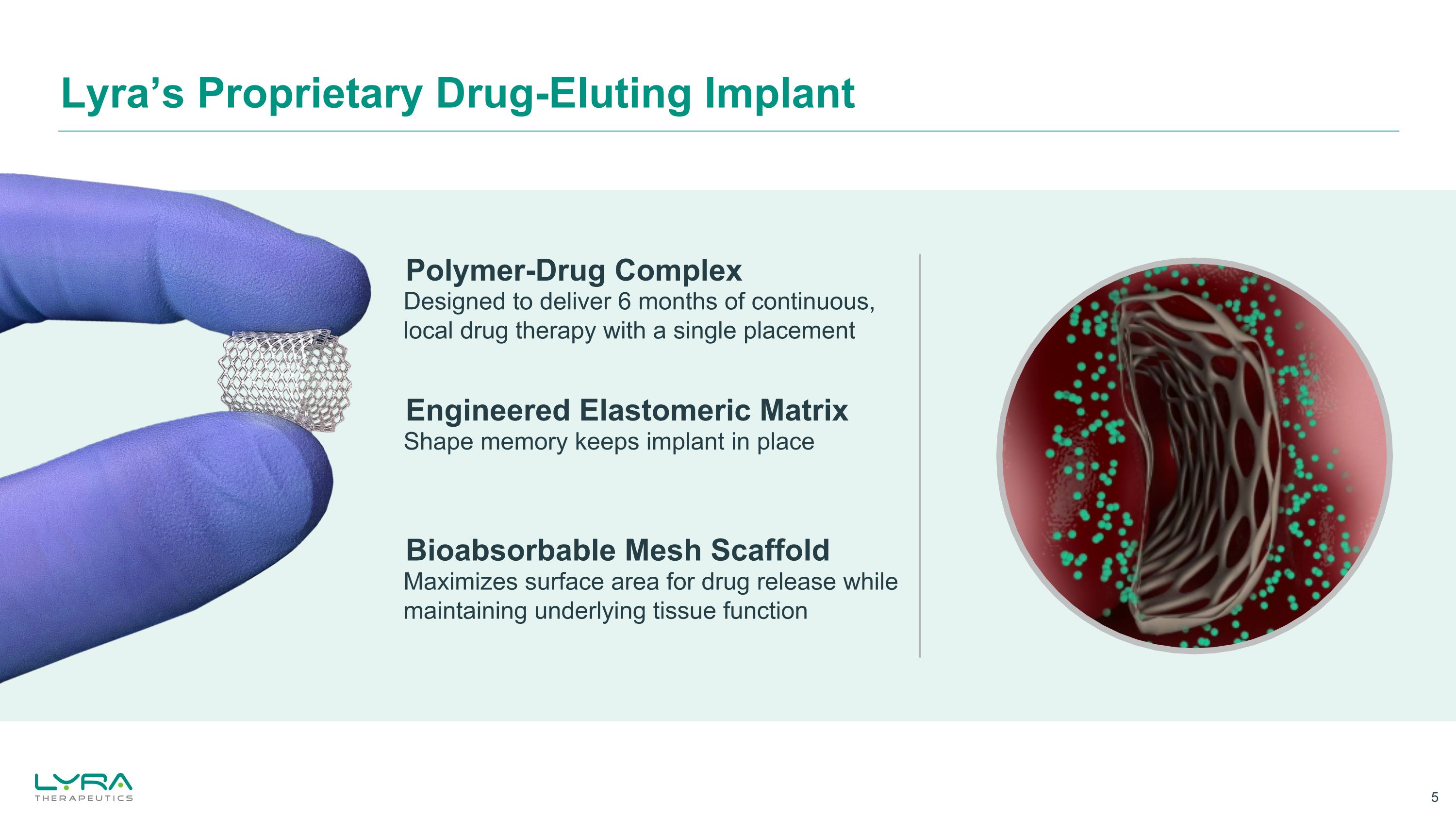
Lyra独自の薬物溶出インプラントで設計されたエラストマーマトリックス形状記憶がインプラントを所定の位置に保ちます。高分子-薬物複合体。生体吸収性メッシュ足場を1回配置するだけで、6ヶ月間連続して局所薬物治療を行うように設計されており、基礎となる組織の機能を維持しながら、薬物放出の表面積を最大化します。
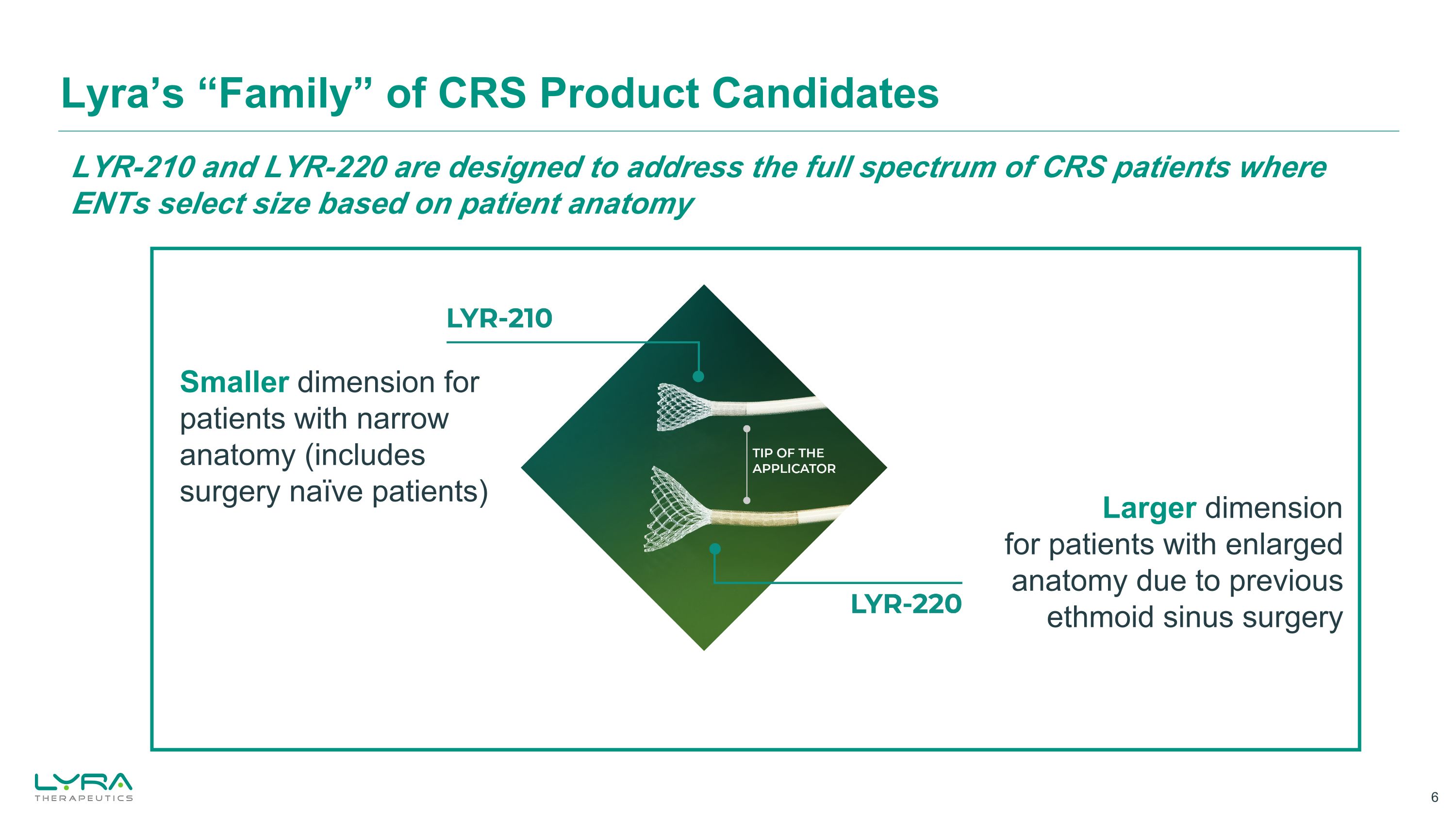
LyraのCRS製品候補の「ファミリー」以前の類縁副鼻腔手術により解剖学的構造が拡大した患者のための大きい寸法より小さい解剖学的構造の患者(手術を受けたことがない患者を含む)用の小さな寸法 LYR-210とLYR-220は、ENTが患者の解剖学的構造に基づいてサイズを選択するCRS患者の全範囲に対応するように設計されています

LYR-210とLYR-220は、耳鼻咽喉科が患者の解剖学的構造に基づいてサイズを選択するCRS患者の全範囲に対応するように設計されています。ライラパイプライン候補CRS患者タイプフェーズ2フェーズ3 LYR-210 長時間作用型モメタゾンフロエート LYR-220 長時間作用型モメタゾンフロエート ENLIGHTEN 1試験、解剖学的構造が狭い慢性鼻副鼻腔炎患者(手術を受けていない患者を含む)1)以前に副鼻腔手術を受けたために解剖学的構造が拡大した慢性鼻副鼻腔炎患者 1)BEACON第2相試験ENLIGHTEN 2 Trial 1)「外科的にナイーブ」および「副鼻腔手術」とは、咽頭洞手術を指します。
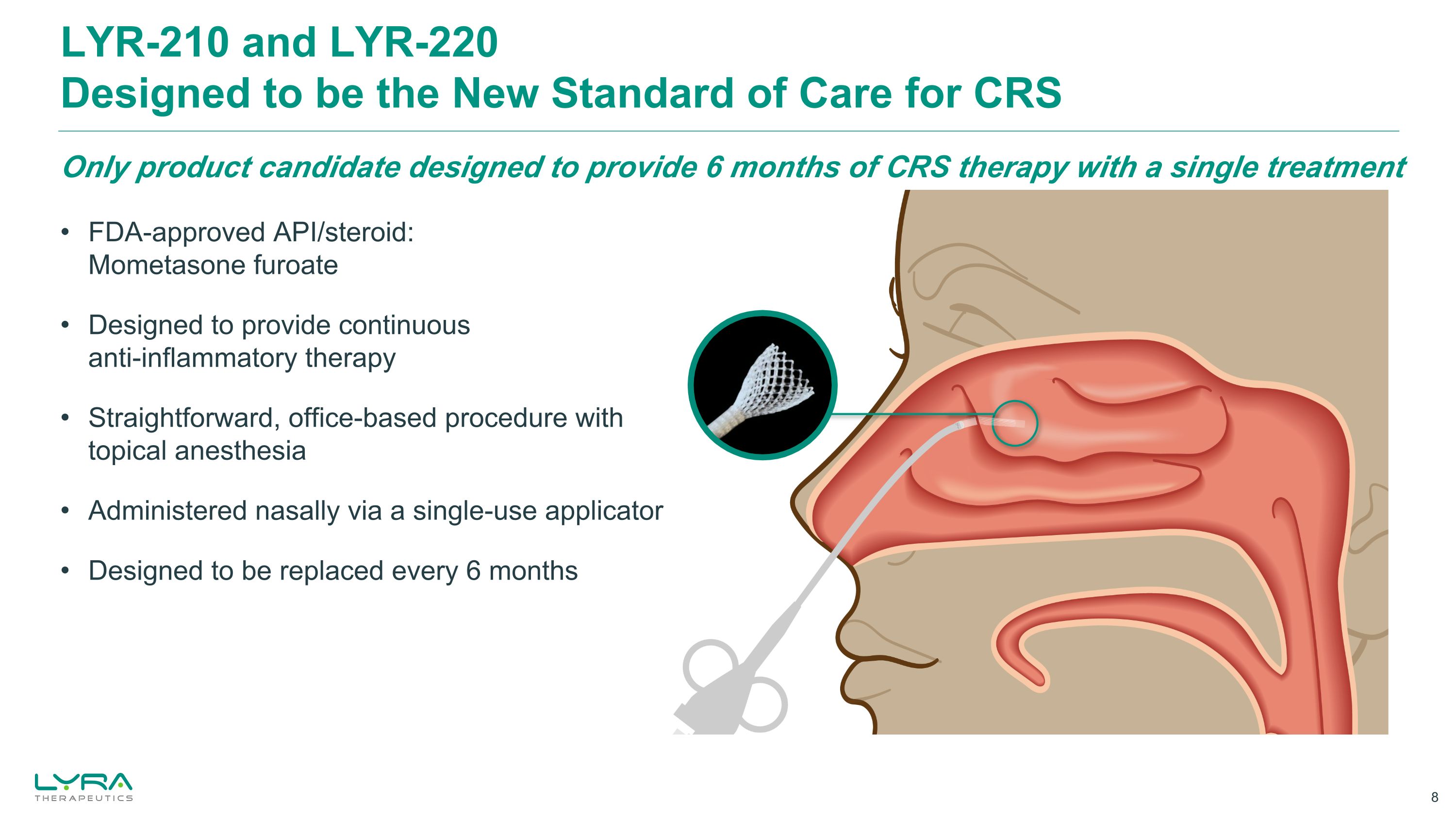
FDA承認のAPI/ステロイド:モメタゾンフロエート継続的な抗炎症療法を提供するように設計された、局所麻酔による簡単なオフィスベースの処置 1回限りのアプリケーターで鼻から投与します。6か月ごとに交換するように設計されています。6ヶ月ごとに交換するように設計された、CRSの新しい標準治療となるように設計された唯一の製品候補です。LYR-210とLYR-220という1回の治療で6か月のCRS治療を提供するように設計された唯一の製品候補です
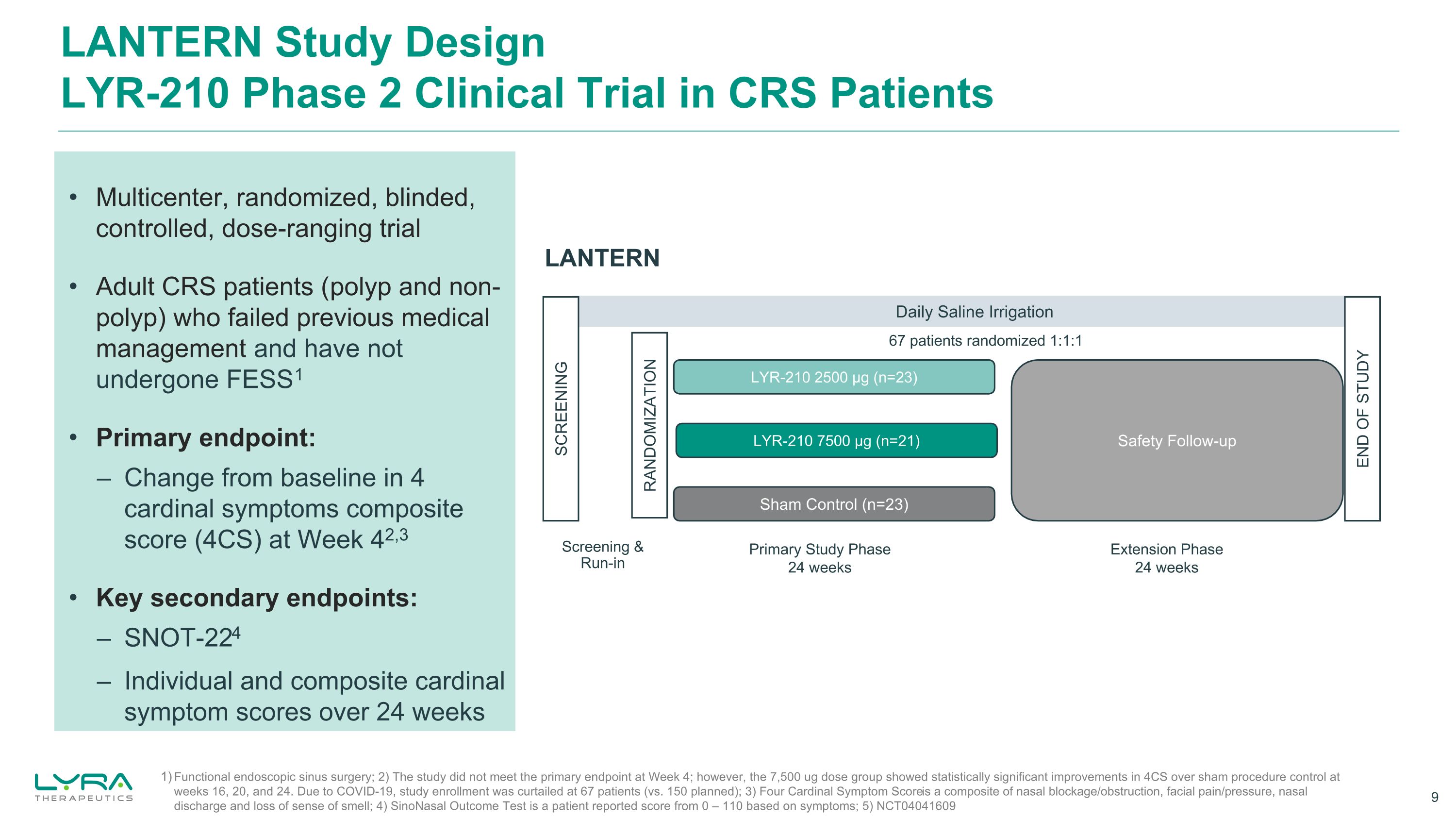
ランタン研究デザインLYR-210 CRS患者を対象とした第2相臨床試験ランタン毎日生理食塩水洗浄シャムコントロール(n=23)LYR-210 2500μg(n=23)スクリーニングランダム化研究終了 LYR-210 7500μg(n=21)一次研究フェーズ 24週間延長フェーズ 24週間スクリーニングとランインセーフティフォローアップ機能性内視鏡副鼻腔手術; 2)研究は 4週目には主要評価項目を満たしていませんでした。しかし、7,500 ugの用量群では、16、20、24週目に偽処置対照と比較して4CSが統計的に有意な改善を示しました。COVID-19により、研究登録者数は67人に減少しました(計画は150人)。3)4つの基本症状スコアは、鼻づまり/閉塞、顔の痛み/圧迫、鼻汁、嗅覚喪失を組み合わせたものです。4)副鼻腔アウトカムテストは、症状に基づいて患者から報告された0〜110のスコアです。5)NCT04041609 67人の患者を1:1:1マルチでランダム化しました参加者、ランダム化、盲検、対照、用量範囲試験以前の医学的管理に失敗し、FESS1を受けていない成人CRS患者(ポリープと非ポリープ)の主要評価項目:— ベースラインからの変更42週目の4つの主要な症状の複合スコア(4CS)、3つの主要な副次的エンドポイント:— SNOT-224 — 24週間にわたる個々の主要症状スコアと複合カーディナル症状スコア
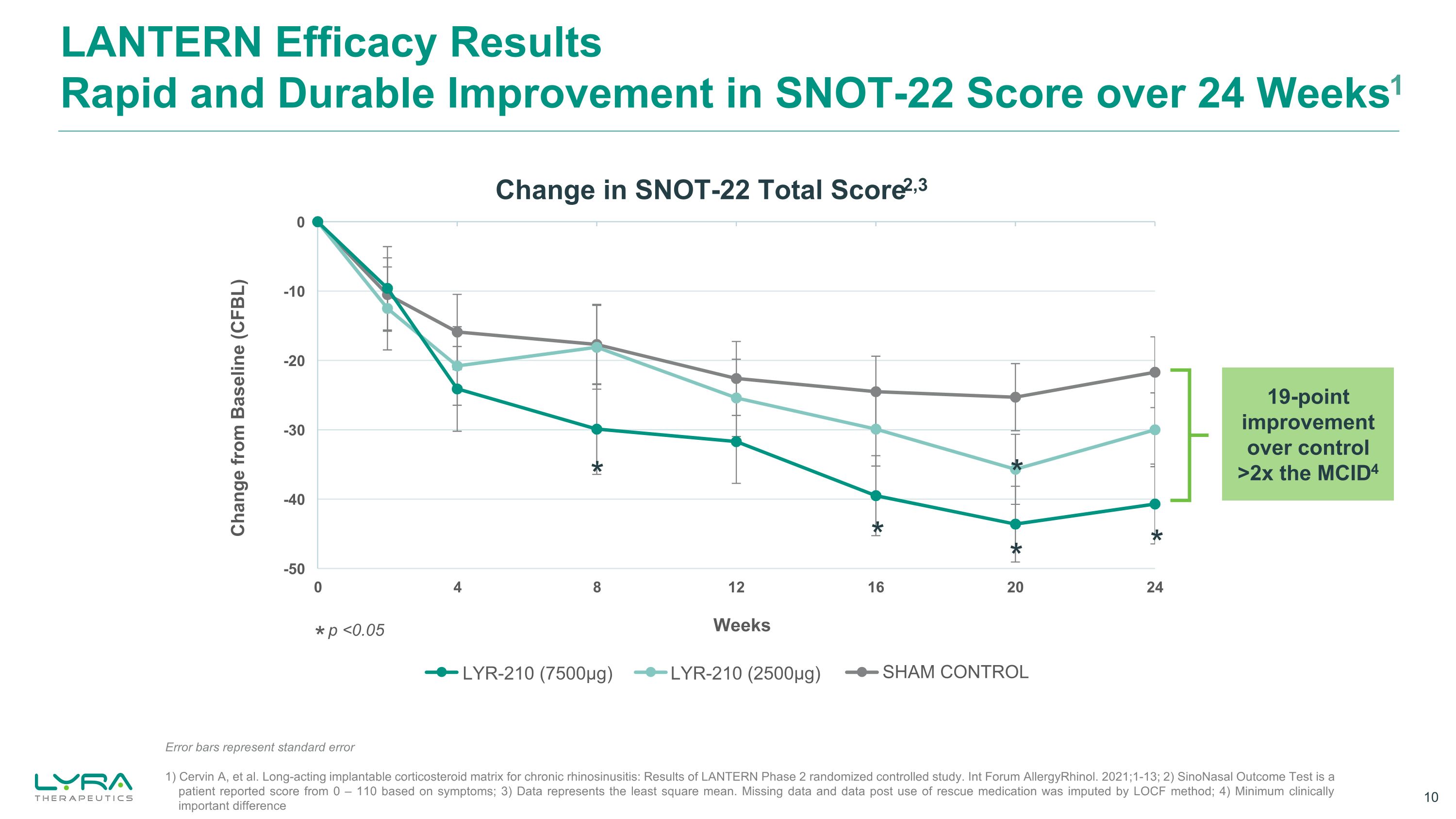
ランタンの有効性の結果24週間にわたるSNOT-22スコアの迅速かつ持続的な改善1 1)Cervin A、他慢性鼻副鼻腔炎のための長時間作用型植込み型コルチコステロイドマトリックス:LANTERN第2相無作為化比較試験の結果。Int Forum AllergyRhinol。2021; 1-13; 2)副鼻腔アウトカムテストは、症状に基づいて患者から報告された0〜110のスコアです。3)データは最小二乗平均を表します。欠損データやレスキュー薬の使用後のデータは、LOCF法によって帰属されました。4)臨床的に重要な最小差* MCID4の2倍LYR-210(2500μg)LYR-210(2500μg)ShAMコントロールエラーバーは標準誤差を表しています
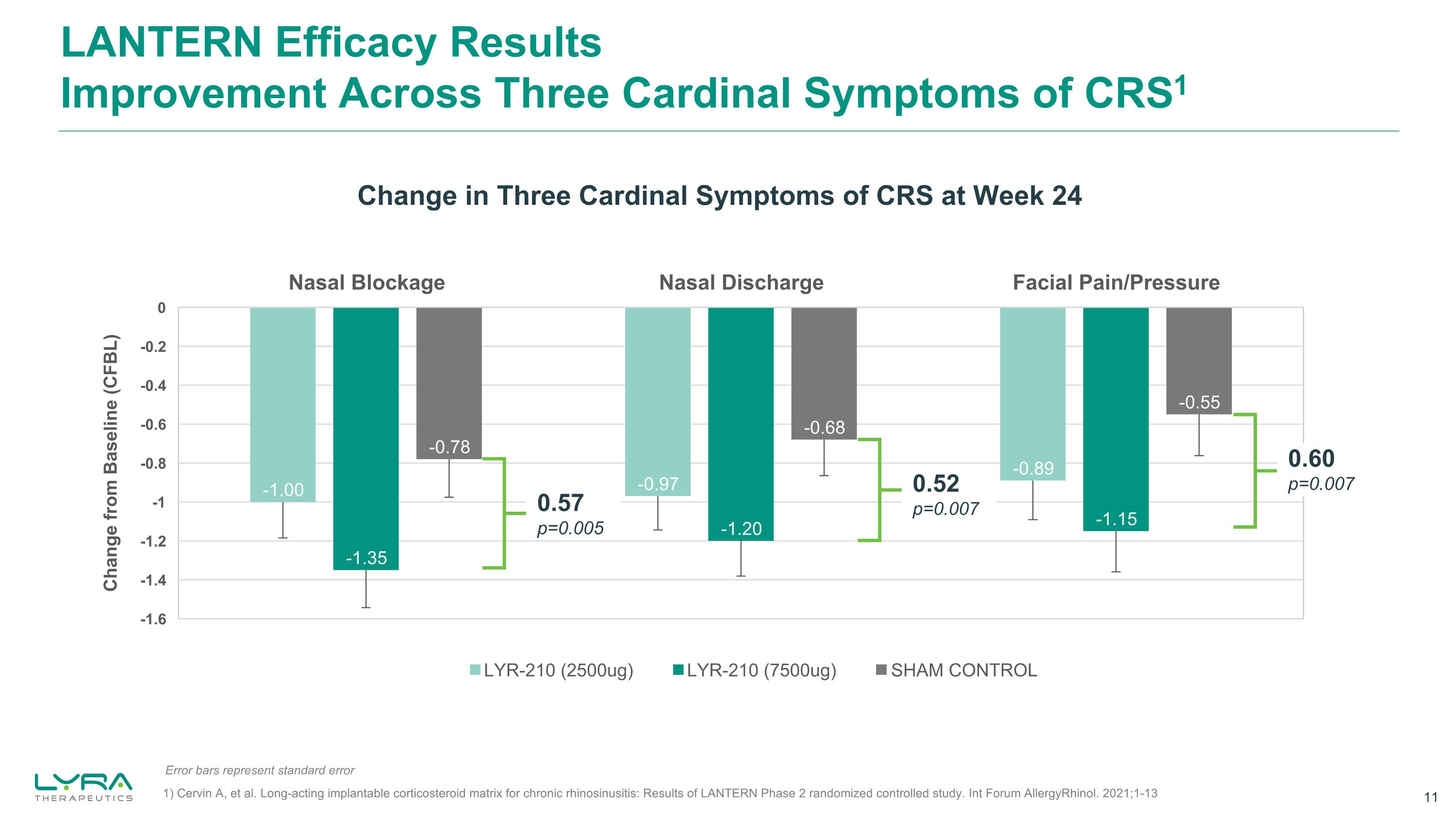
ランタンの有効性結果CRS1の3つの主要な症状にわたる改善24週目のCRSの3つの主要な症状の変化0.57 p=0.005 0.52 p=0.007 0.60 p=0.007 Shamコントロールエラーバーは標準誤差を表します 1) Cervin A, et al.慢性鼻副鼻腔炎のための長時間作用型植込み型コルチコステロイドマトリックス:LANTERN第2相無作為化比較試験の結果。Int フォーラム-アレルギノール。2021; 1-13
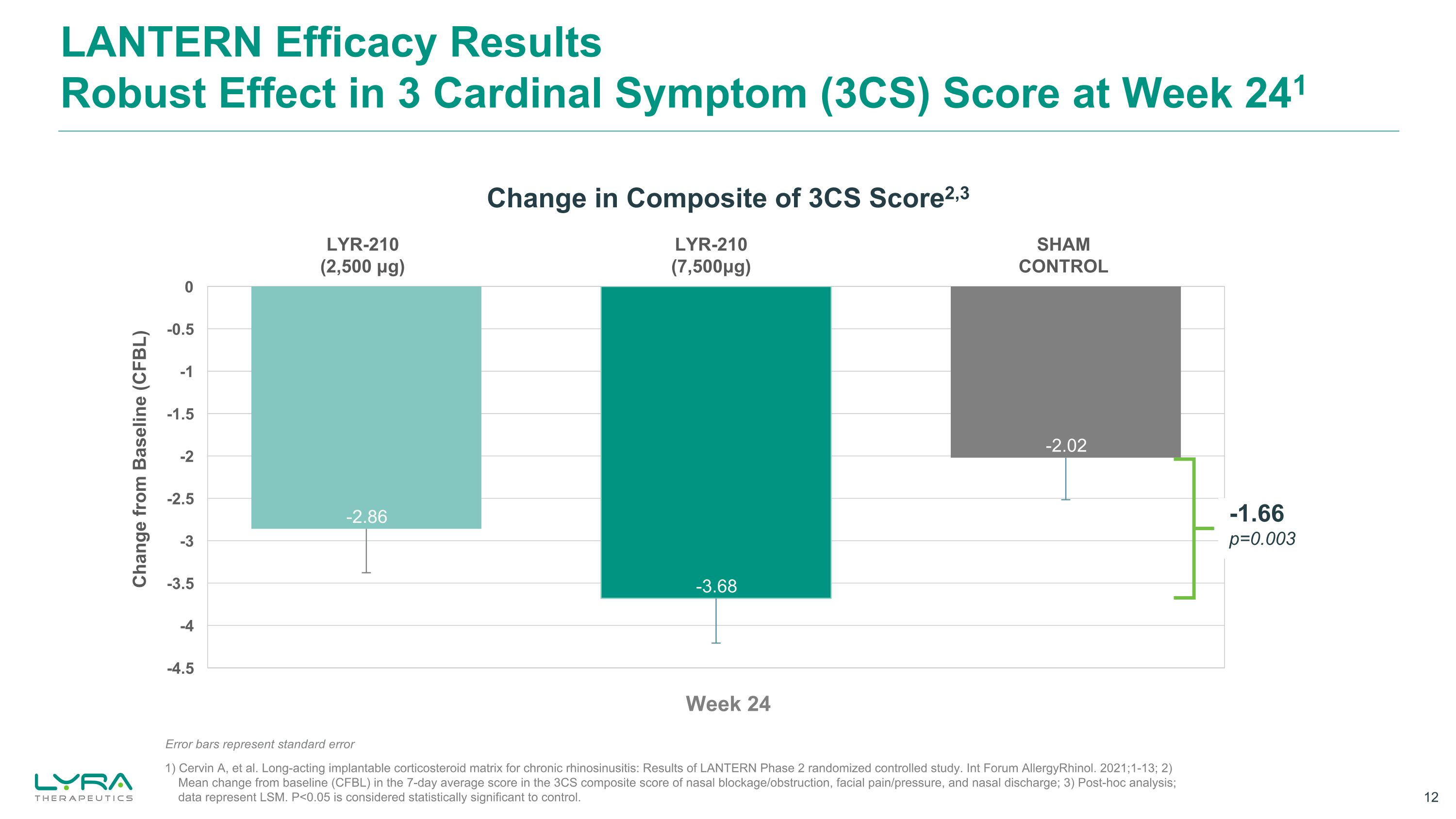
ランタンの効能結果241週目の3つの主要症状(3CS)スコアに強い効果があります。1)Cervin A、他慢性鼻副鼻腔炎のための長時間作用型植込み型コルチコステロイドマトリックス:LANTERN第2相無作為化比較試験の結果。Int Forum AllergyRhinol。2021; 1-13; 2)鼻づまり/閉塞、顔の痛み/圧迫感、鼻汁の3CS複合スコアの7日間の平均スコアにおけるベースライン(CFBL)からの平均変化、3)事後分析、データはLSMを表します。P
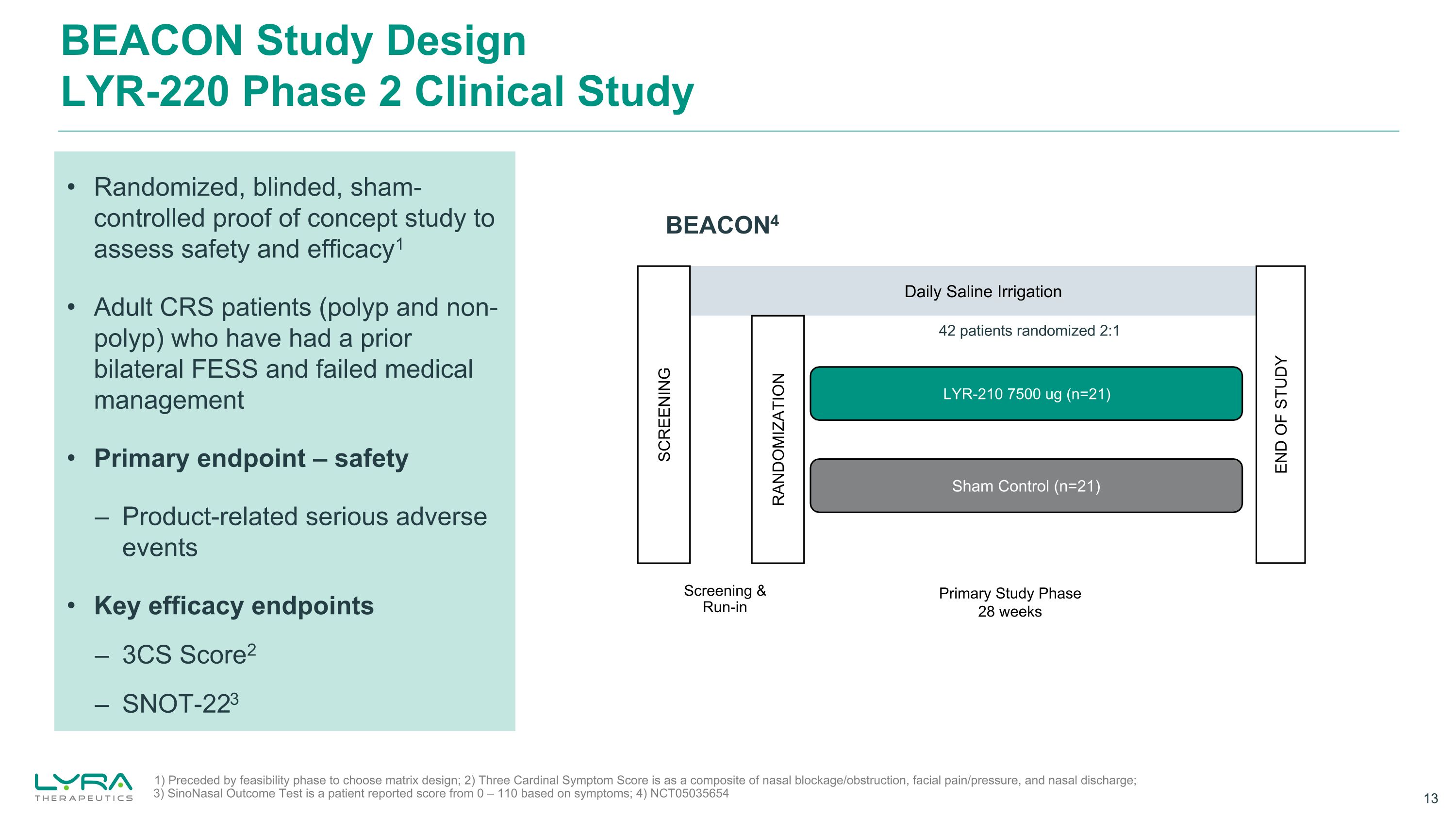
BEACON Study DesignLYR-220 第2相臨床試験安全性と有効性を評価するための無作為化、盲検、擬似対照の概念実証研究1 以前に両側FESSを受けたことがあり、医療管理に失敗した成人CRS患者(ポリープと非ポリープ)主要評価項目-安全性-製品関連の重篤な有害事象主要評価項目 — 3CSスコア2 — SNOT-223 1)実現可能性が先行していますマトリックス設計を選択するためのフェーズ。2)3つの基本症状スコアは、鼻づまり/閉塞、顔の痛み/圧迫感、および鼻汁を合わせたものです。3)副鼻腔結果検査は、症状に基づいて0〜110の範囲で患者が報告したスコアです。4)NCT05035654 BEACON4毎日生理食塩水洗浄シャムコントロール(n=21)LYR-210 7500 ug(n=21)スクリーニングランダム化研究終了プライマリスタディフェーズ 28週間スクリーニング&ランイン 42人の患者をランダム化 2:1
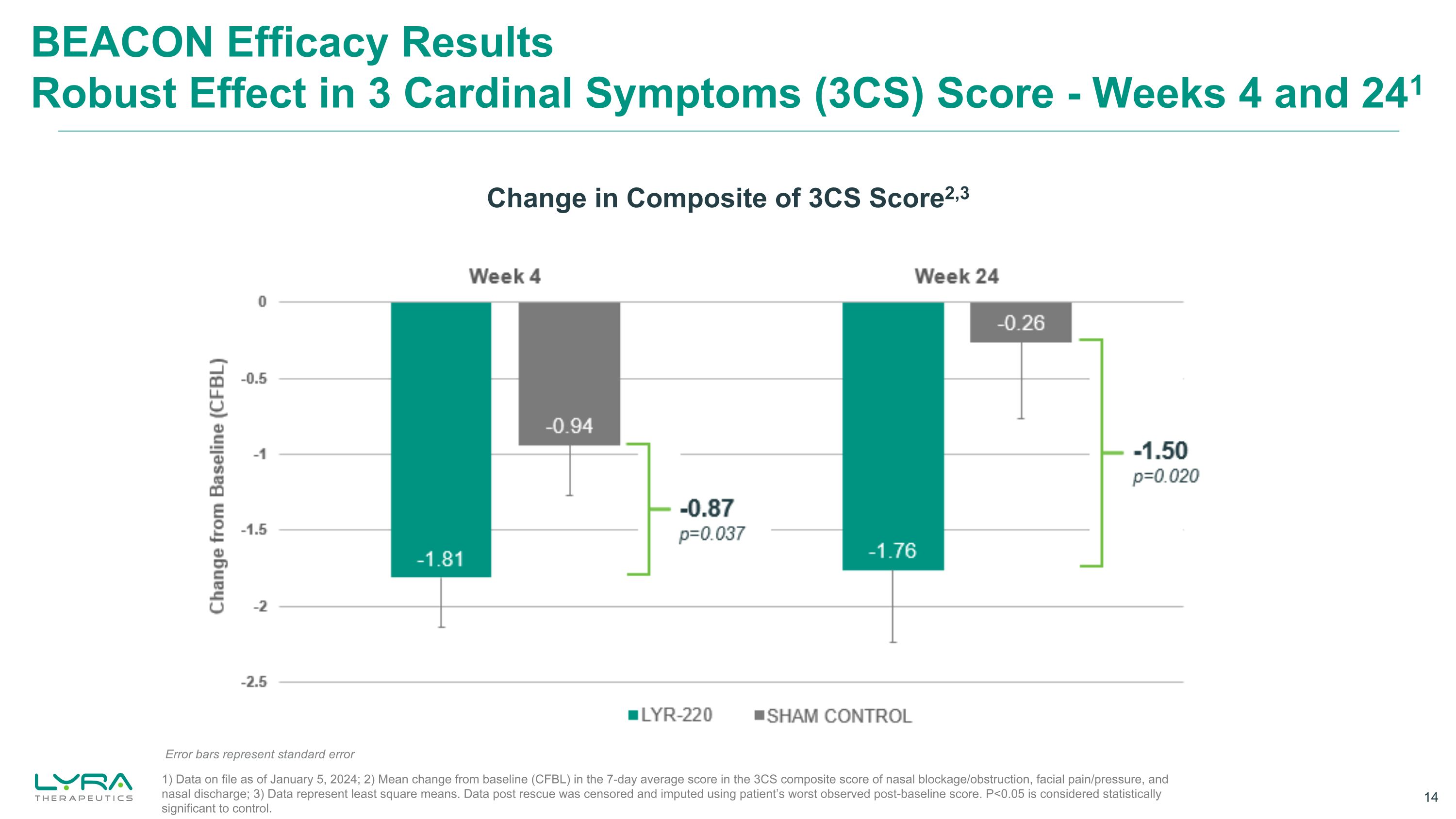
ビーコンの有効性結果:3つの主要な症状(3CS)スコアにおける強力な効果-4週目と241週目の3CSスコアの複合値の変化2、3つのエラーバーは標準誤差を表します。1)2024年1月5日現在の登録データ、2)3CS複合スコアにおける7日間の平均スコアにおけるベースライン(CFBL)からの平均変化です。鼻づまり/閉塞、顔の痛み/圧迫、および鼻づまり放電; 3)データは最小二乗平均を表します。レスキュー後のデータは検閲され、患者のベースライン後の最低スコアを使用して帰属されました。P
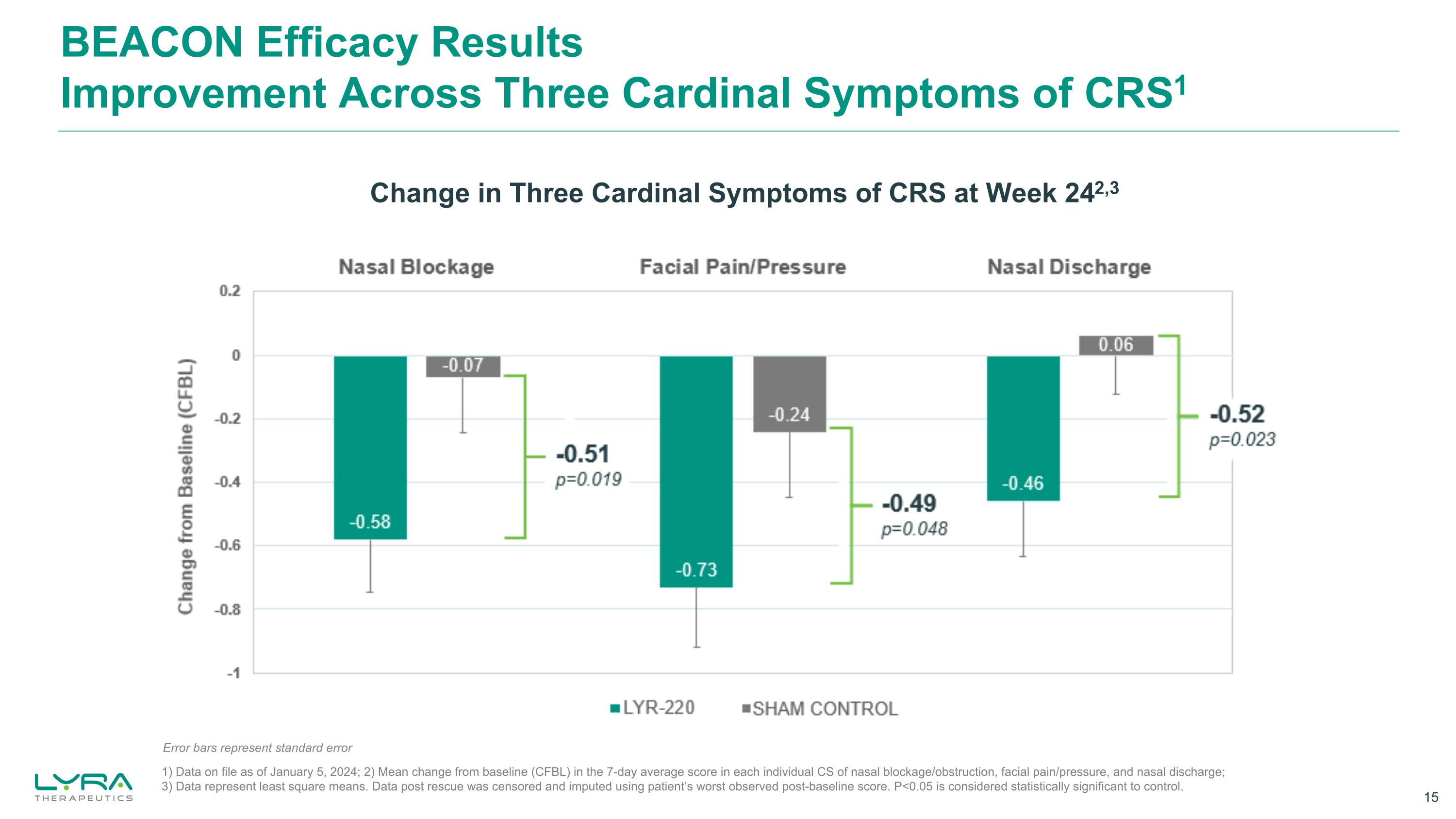
CRS1の3つの主要症状におけるビーコン有効性結果の改善 242週目のCRSの3つの主要症状の変化3 1)2024年1月5日現在の登録データ、2)鼻づまり/閉塞、顔の痛み/圧力、および鼻汁の個々のCSにおける7日間の平均スコアにおけるベースライン(CFBL)からの平均変化、3)データは最小二乗平均を表します。レスキュー後のデータは検閲され、患者のベースライン後の最低スコアを使用して帰属されました。P
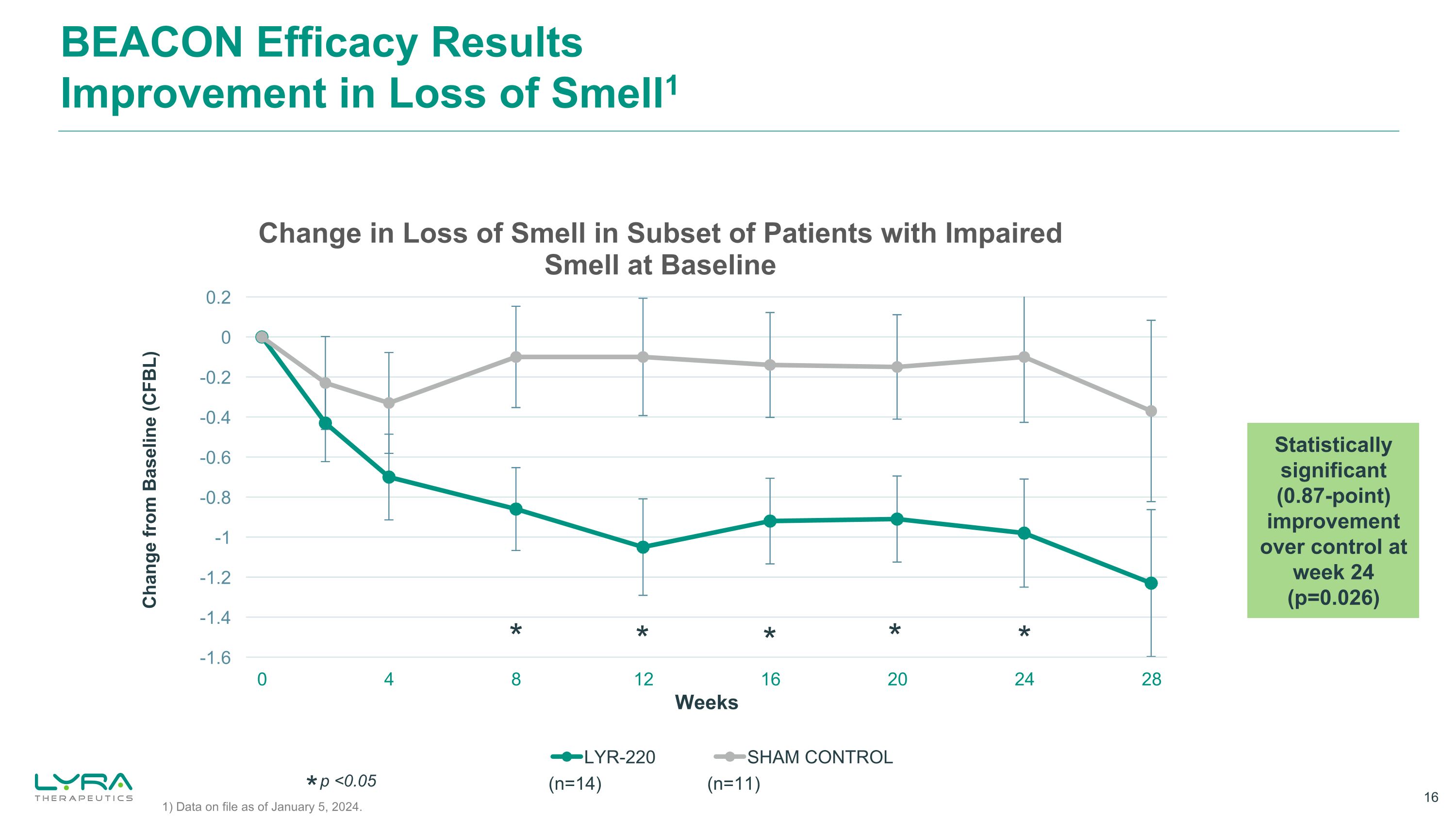
ビーコンの有効性結果臭気消失の改善1 ベースラインからの変化(CFBL)*** * 24週目の対照群よりも統計的に有意な(0.87ポイント)改善* p
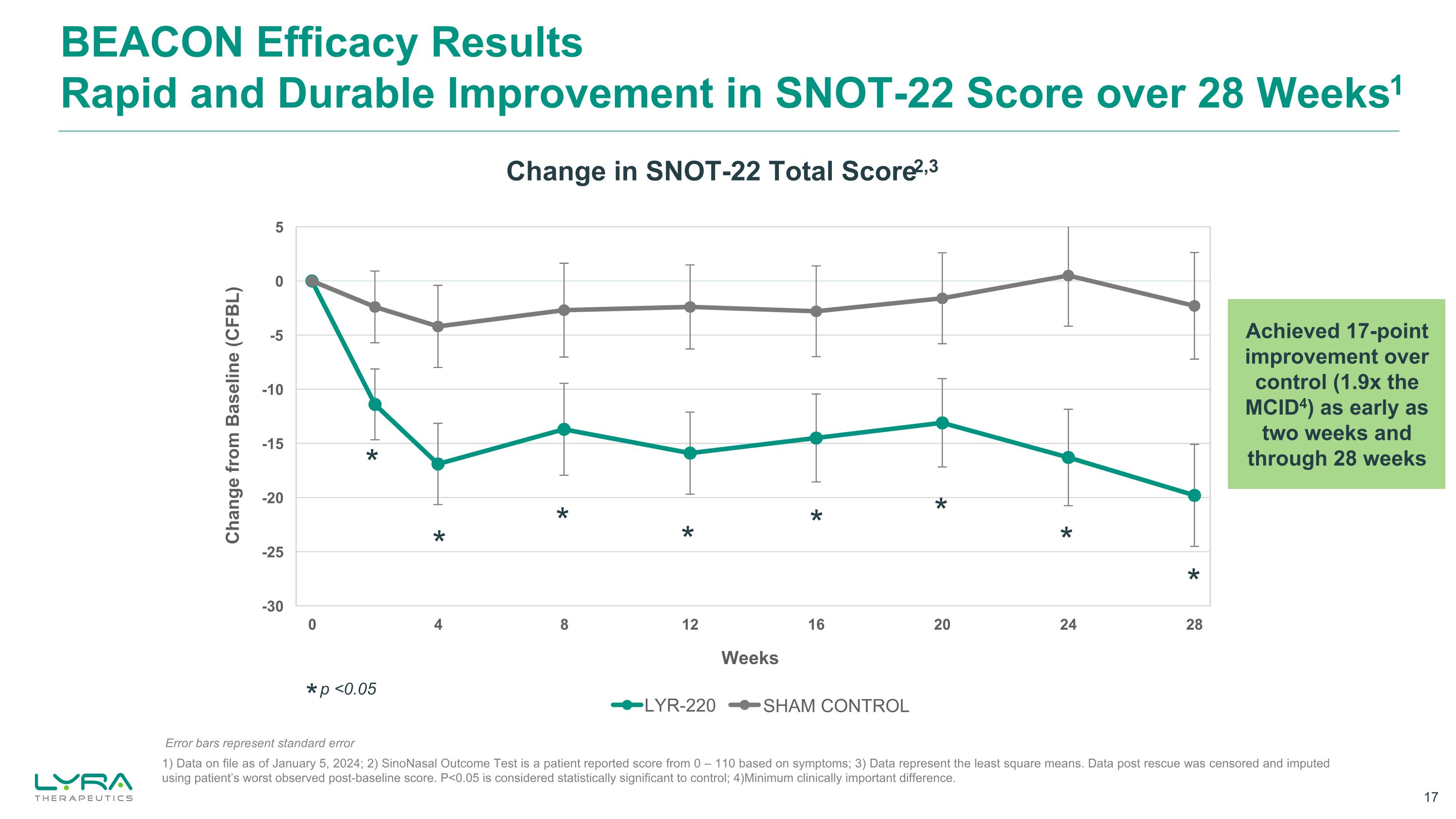
ビーコンの有効性の結果 28週間にわたって、SNOT-22スコアが迅速かつ持続的に向上します1 * p
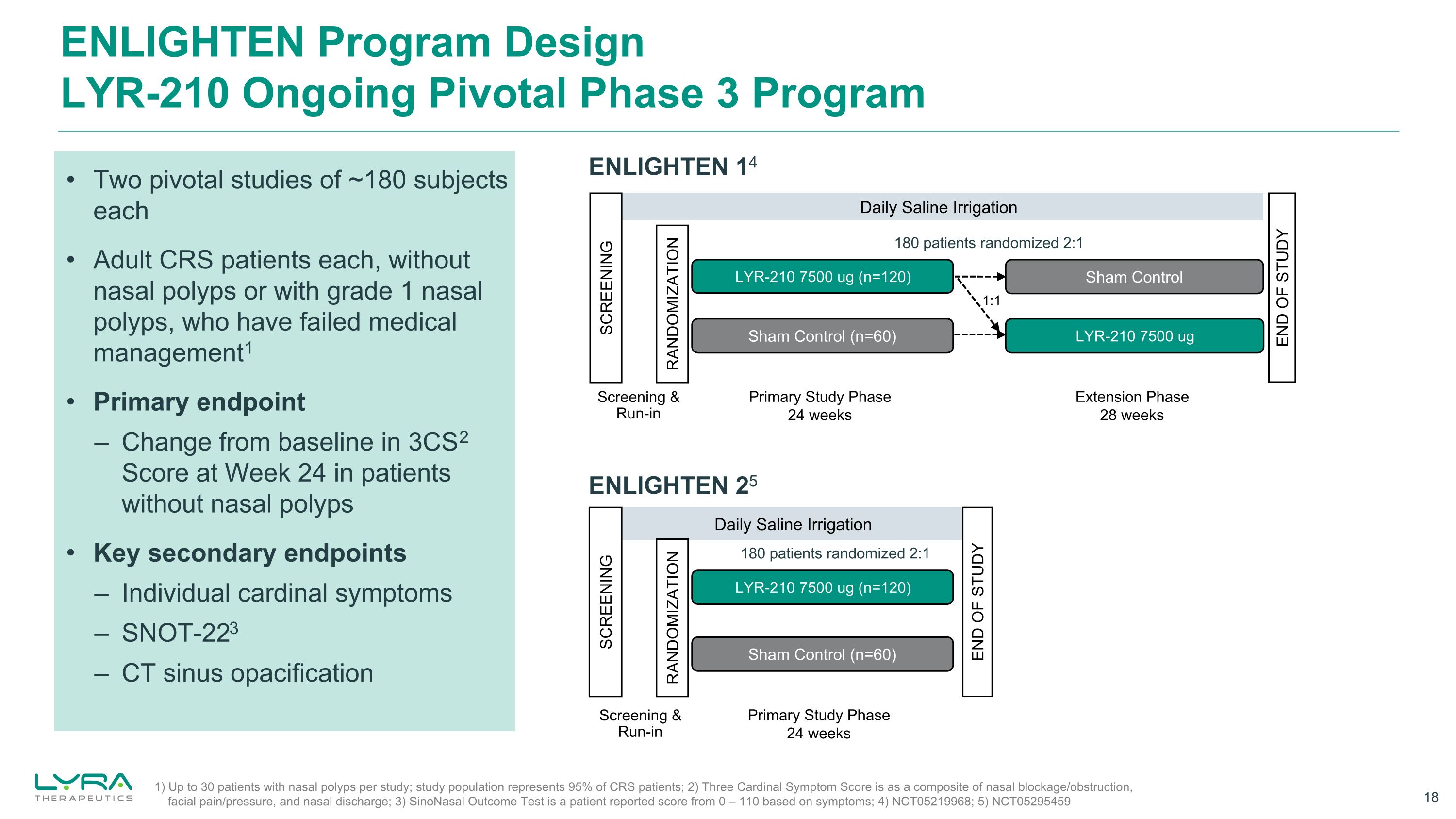
ENLIGHTEN プログラムデザイン LYR-210 継続的なピボタルフェーズ 3 プログラム ENLIGHTEN 14 日次生理食塩水洗浄シャムコントロール (n=60) LYR-210 7500 ug (n=120) LYR-210 7500 ugスクリーニングランダム化一次研究フェーズ 24週間延長フェーズ 28週間スクリーニング&Run-in 1:1 研究あたり最大30人の鼻ポリープ患者、研究対象集団 CRS患者の95%を表します。2)3つの基本症状スコアは、鼻づまり/閉塞、顔の痛み/圧迫、および鼻汁を合わせたものです。3)副鼻腔アウトカムテストは、患者が報告した0からのスコアです。— 110(症状による); 4)NCT05219968; 5)NCT05295459 ENLIGHTEN 25 日次生理食塩水灌注シャムコントロール(n=60)LYR-210 7500 ug(n=120)スクリーニングランダム化研究終了一次研究フェーズ 24週間スクリーニング&ランイン 2つの重要な研究、成人CRS患者1人あたり約180人の被験者、鼻ポリープなし、または鼻の悪性度1の患者1人あたり約180人の被験者を対象とした2つの重要な研究医療管理に失敗したポリープ1 主要評価項目 — 鼻ポリープのない患者の24週目の3CS2スコアのベースラインからの変化主要な副次評価項目 — 個々の心臓症状 — SnoT-223 — Ct副鼻腔混濁1802:1のランダム化された患者 180人の患者を2:1でランダム化しました

2024年5月6日現在の一次測定値と2024年8月14日現在のサブグループ分析 — 鼻ポリープのない患者の24週目の3CSスコアのベースラインからの変化(CFBL)の主要評価項目は満たされませんでした。一次有効性分析では、LYR-210による治療により、3CSスコアは平均(標準偏差、SD)で2.13(2.17)ポイント向上しました。sHAM対照群1の2.06(2.14)ポイント — iTT集団のSNOT-22スコアの副次評価項目は、LYR-210で治療を受けた20.2(21)の患者で、ベースラインと比較して平均(SD)の改善を示しました。.38)点とShAM対照群の15.70(18.55)点との比較1 — EUの非ポリープ患者は、Ctによるエスモイド混濁率でShAM対照1群と比較して客観的な改善を示しました(グラフ右)— ポリープ患者コホート2では、ShAM対照群1と比較して、LYR-210治療を受けた患者の症状が大幅に改善しました(スライド20のデータを参照)— LYR-210は一般的に耐容性が高く、製品関連の重篤な有害事象はありませんでした。ENLIGHTEN 1のトップライン24週での結果 ENLIGHTEN 1と2はENLIGHTEN 2のトップラインで継続しています2025年上半期に期待される結果 1) ShAM患者は、うっ血解消とそれに続く毎日の生理食塩水洗浄を含む模擬処置の形で治療を受け、症状の改善につながる可能性があります。2)ポリープはCRS疾患の客観的な指標です。非ポリープは不均一なCRS集団であり、特に米国では、広告キャンペーンによる患者の募集により、より一過性の病気が増えている可能性があります。69 p=0.024 N=56
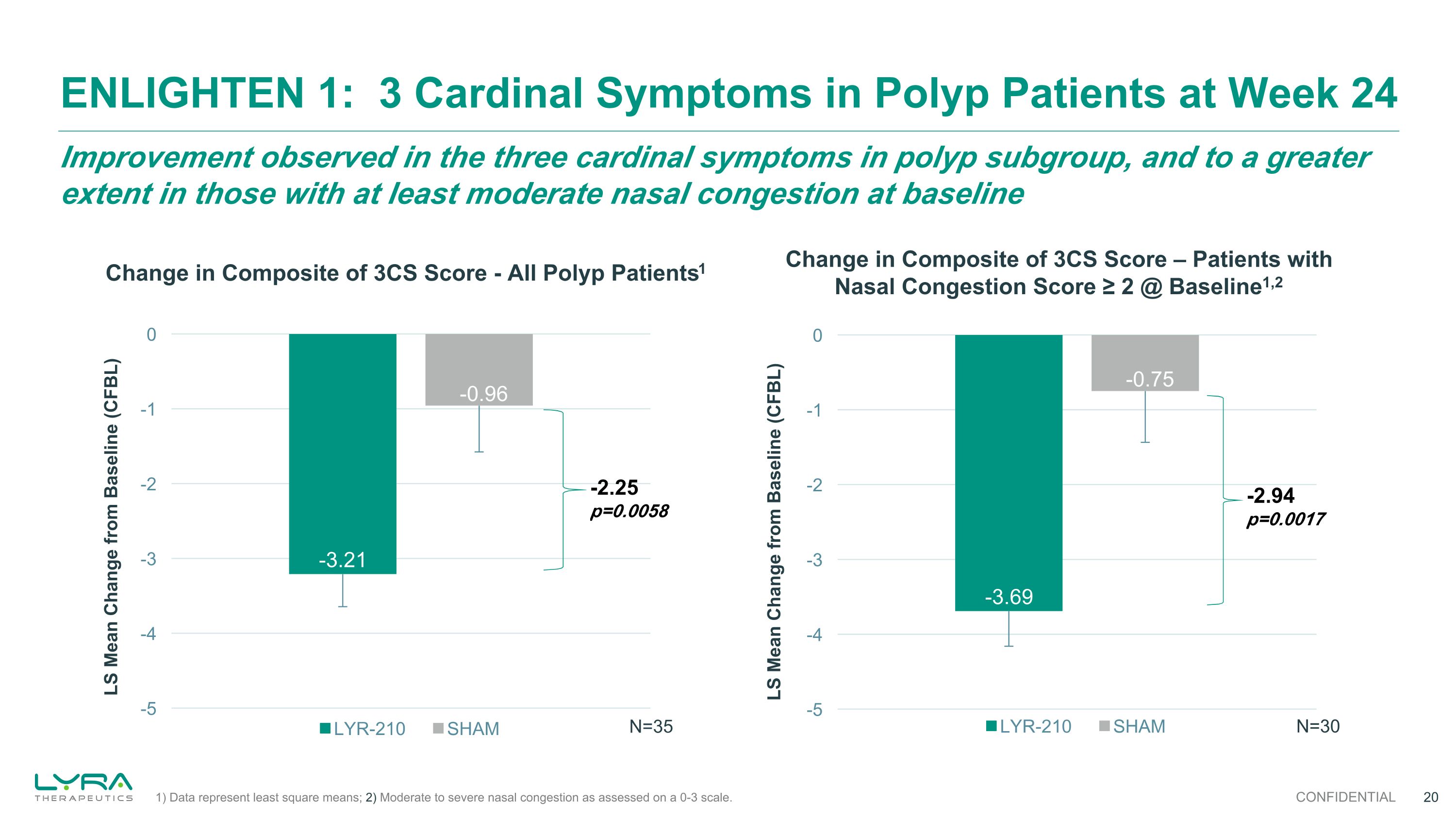
-2.25 p=0.0058 ベースライン時に鼻づまりが中等度以上の患者で改善が見られました ENLIGHTEN 24週目のポリープ患者の主な症状1:3Cスコアの複合体の内密変化-すべてのポリープ患者1 N=35 -2.94 p=0.0017 3CSスコアの複合体の変化 — 3CSスコアの複合体の変化 — 鼻づまりスコア ≥ 2 @ベースライン1,2 N=30 1)データは最小二乗平均を表します。2)0〜3の尺度で評価された中等度から重度の鼻づまりです。
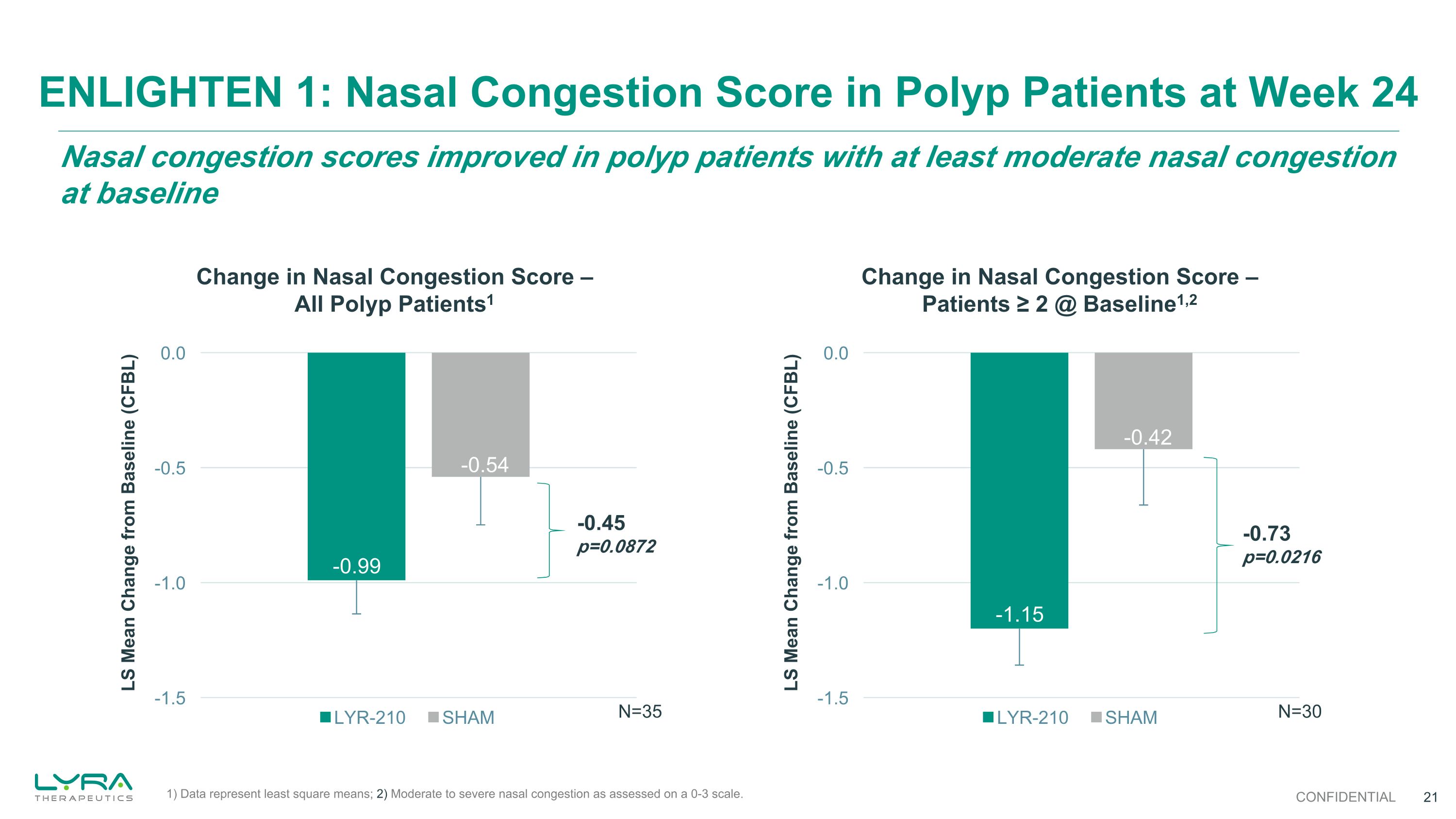
-0.73 p=0.0216 ベースラインで少なくとも中等度の鼻づまりがあったポリープ患者の鼻づまりスコアが改善しました ENLIGHTEN 1:24週目のポリープ患者の鼻づまりスコア — 鼻づまりスコアの機密変化 — すべてのポリープ患者1鼻づまりスコアの変化 — 患者 ≥ 2 @ ベースライン1,2 -0.45 p=0.0872 N=35 N=30 (1) データは最小二乗平均を表しています。2)0〜3のスケールで評価された中等度から重度の鼻づまりです。

LYR-210は、もし高度なものであれば、現在の耳鼻咽喉科診療と一致する位置にあります。耳鼻咽喉科は、手術を受けることを望まない患者に対して治療オプションを行うことに慣れているオフィスベースの処置です。これにより、耳鼻咽喉科はより多くの患者の治療を受けることができます。耳鼻咽喉科診療の償還モデルへの適合が期待されます

予想されるマイルストーン LYR-210:エンライトンフェーズ3プログラム 2024年5月:エンライトン1 2024年第4四半期からのトップラインデータ:エンライトン1 2024年上半期のエクステンション調査データ:エンライトン2への登録完了 2025年上半期エンライトン1からのトップラインデータ

財務プロフィール 2024年6月30日現在の現金、現金同等物および短期投資 6,750万ドル 2024年8月1日現在の発行済普通株式6550万株
