米国
証券取引委員会
ワシントンD.C. 20549
フォーム
(マークワン)
四半期終了時
または
___________から___________への移行期間について
コミッションファイル番号:
(憲章に明記されている登録者の正確な名前)
| (州またはその他の管轄区域 法人または組織) | (IRS) 雇用主 識別番号) |
| | ||
| (主要執行機関の住所) | (郵便番号) |
登録者の電話番号(以下を含む)
エリアコード:
セクション12 (b) に従って登録された証券 取引法の:
| 各クラスのタイトル | トレーディングシンボル | 登録した取引所の名前 | ||
| の |
登録者が本人かどうかをチェックマークで示してください
(1)は、過去12か月間に1934年の証券取引法のセクション13または15(d)によって提出が義務付けられたすべての報告を提出しました
(または、登録者がそのような報告を提出する必要があったほど短い期間)、そして(2)そのような提出要件の対象となった
過去90日間。
登録者が本人かどうかをチェックマークで示してください
規則S-T(§232.405)の規則405に従って提出する必要のあるすべてのインタラクティブデータファイルを電子的に提出しました
この章の)過去12か月間(または、そのようなファイルを送信するために登録が必要だったほど短い期間)。
登録者が本人かどうかをチェックマークで示してください は、大規模なアクセラレーテッド・ファイラー、アクセラレーテッド・ファイラー、非アクセラレーテッド・ファイラー、小規模な報告会社、または新興成長企業です。 「大規模アクセラレーテッドファイラー」、「アクセラレーテッドファイラー」、「小規模報告会社」の定義を参照してください と、証券取引法第12b-2条の「新興成長企業」。
| 大型加速フィルター | ☐ | アクセラレーテッド・ファイラー | ☐ |
| ☒ | 小規模な報告会社 | ||
| 新興成長企業 | |||
新興成長企業の場合は、小切手で示してください 登録者が、新規または改訂された財務会計の遵守に延長された移行期間を使用しないことを選択した場合は、マークを付けてください 取引法のセクション13(a)に従って提供される基準。☐
登録者が本人かどうかをチェックマークで示してください
はシェル会社です(取引法の規則12b-2で定義されています)。はい ☐ いいえ
普通株式の数、額面金額0.0001ドルです
2024年5月13日現在の発行済1株当たり:
サイロファーマ株式会社と子会社
フォーム10-Q
2024年3月31日です
目次
| ページ | ||
| パート I — 財務情報 | ||
| アイテム 1. | 財務諸表 | 1 |
| 2024年3月31日(未監査)および2023年12月31日現在の連結貸借対照表 | 1 | |
| 2024年および2023年3月31日に終了した3か月間の連結営業報告書と包括損失(未監査) | 2 | |
| 2024年および2023年3月31日に終了した3か月間の株主資本の変動に関する連結計算書(未監査) | 3 | |
| 2024年および2023年3月31日に終了した3か月間の連結キャッシュフロー計算書(未監査) | 4 | |
| 連結財務諸表の注記 (未監査) | 5 | |
| アイテム 2. | 経営陣による財政状態と経営成績に関する議論と分析 | 20 |
| アイテム 3. | 市場リスクに関する定量的・質的開示 | 30 |
| アイテム 4. | 統制と手続き | 30 |
| パート II — その他の情報 | ||
| アイテム 1. | 法的手続き | 31 |
| アイテム 1A. | リスク要因 | 31 |
| アイテム 2. | 持分証券の未登録売却および収益の使用 | 31 |
| アイテム 3. | シニア証券のデフォルト | 32 |
| アイテム 4. | 鉱山の安全に関する開示 | 32 |
| アイテム 5. | その他の情報 | 32 |
| アイテム 6. | 展示品 | 32 |
| 署名 | 33 | |
-i-
将来の見通しに関する記述に関する注意事項
Form 10-Qのこの四半期報告書には、将来の見通しが含まれています かなりのリスクと不確実性を伴う声明。これに含まれる歴史的事実の記述を除くすべての記述 当社の戦略、将来の事業、将来の財政状態、将来の収益、予測費用、見通しに関する記述を含む報告書 経営の計画と目標、および予想される市場成長は、将来の見通しに関する記述です。場合によっては、将来を見据えた企業を特定できます 「かもしれない」、「できた」、「するだろう」、「するだろう」、「すべき」などの用語による声明 「期待する」、「計画する」、「予測する」、「信じる」、「見積もる」、「意図する」、 「予測する」、「探る」、「熟考する」、「計画する」、「続ける」、「潜在的な」 これらの用語や他の同等の用語の「継続的」または否定的。
将来の見通しに関する記述はすべて対象となります フォーム10-Qのこの四半期報告書で説明されているリスク要因を参照して、それらのすべてを示しています。いくつかのリスク、不確実性 そして、実際の結果が将来の見通しに関する記述に含まれる見積もりや予測と大きく異なる原因となる可能性のある仮定 以下が含まれますが、これらに限定されません:
| ● | 事業のための追加資金を獲得する当社の能力 |
| ● | 当社の財務実績 |
| ● | 臨床試験の時期と費用、およびその他の費用の時期と費用に関するリスク |
| ● | 製品の市場での受け入れに関するリスク。 |
| ● | 知的財産リスク; |
| ● | 競合他社や業界に関連する政府の規制や動向の影響 |
| ● | 私たちの競争力。 |
| ● | 私たちの業界環境。 |
| ● | 当社の予想される財務および経営成績(予想される収益源を含む) |
| ● | 利用可能な市場の規模、当社製品のメリット、製品の価格設定、および製品発売のタイミングに関する前提条件 |
| ● | 当社の費用、損失、将来の収益、資本要件の見積もり(追加の資金調達の必要性を含む) |
| ● | 資格のある主要管理職および技術者を引き付けて維持する当社の能力。 |
| ● | 新製品や新市場の導入を含む、私たちの目標、意図、計画、期待に関する声明。 |
| ● | 私たちの現金ニーズと資金調達計画。 |
これらの記述は、将来の出来事や私たちに関するものです 将来の事業または財務実績、および既知および未知のリスク、不確実性、および当社の実際の状況を引き起こす可能性のあるその他の要因が含まれます 結果、業績、または成果が、明示または暗示されている将来の業績、業績、または成果と大きく異なること これらの将来の見通しに関する記述によって。実際の結果が現在の予想と大きく異なる原因となる要因には、 その他、このレポートの「リスク要因」というタイトルのセクションに記載されているもの。
このレポートの将来の見通しに関する記述にはすべて反映されています 将来の出来事に関する当社の現在の見解は、当社に関連するこれらおよびその他のリスク、不確実性、および仮定の影響を受けます ビジネス、経営成績、業界、そして将来の成長。これらの不確実性を考えると、これらの将来を見据えたものに過度に依存するべきではありません ステートメント。将来の業績を保証する将来の見通しに関する記述はありません。あなたはこのレポートを完全に、そして理解した上で読むべきです 私たちの実際の将来の業績は、これらの将来の見通しに関する記述によって表明または暗示される将来の結果とは大きく異なる可能性があるということです。
このレポートには、見積もり、予測も含まれています および当社の業界、事業、市場に関するその他の情報(それらの市場の推定規模に関するデータを含む) と彼らの予測成長率。見積もり、予測、予測、または同様の方法論に基づく情報は、本質的に 不確実性がある場合があり、実際の出来事や状況は、この情報に反映されている出来事や状況とは大きく異なる場合があります。 特に明記されていない限り、これらの業界、ビジネス、市場、その他のデータは、レポート、調査、調査から入手しました および第三者、業界、一般出版物、政府データ、および同様の情報源によって作成された同様のデータ。私たちは信じていますが 第三者が作成した報告書、調査調査、調査、および同様のデータが信頼できるものであること、私たちは独自に検証していません それらに含まれるデータ。
過度に依存しないように注意してください このレポートの日付の時点でのみ述べられている、すべての将来の見通しに関する記述について。法律で義務付けられている場合を除き、私たちは何も引き受けません あらゆる出来事や状況を反映するために、これらの将来の見通しに関する記述を更新または改訂する義務があります。 本書の日付以降の、新しい情報、将来の出来事、前提条件の変更などの結果。新しい要因は時とともに現れます 時が経てば、どの要因が生じるかを予測することはできません。さらに、各要因が及ぼす影響を評価することはできません 当社の事業、または何らかの要因または要因の組み合わせにより、実際の結果が記載されているものと大きく異なる可能性がある程度 将来の見通しに関するあらゆる記述で。私たちは、フォーム10-Qのこの四半期報告書に記載されているすべての情報を対象としています。特に これらの注意書きによる、私たちの将来の見通しに関する記述。
-ii-
パートI — 財務情報
アイテム 1.財務諸表
サイロファーマ株式会社と子会社
連結貸借対照表
| 3 月 31 日 | 12月31日 | |||||||
| 2024 | 2023 | |||||||
| (未監査) | ||||||||
| 資産 | ||||||||
| 流動資産: | ||||||||
| 現金および現金同等物 | $ | $ | ||||||
| 短期投資 | ||||||||
| 前払費用およびその他の流動資産 | ||||||||
| 流動資産合計 | ||||||||
| 前払い費用およびその他の資産-非流動 | ||||||||
| 総資産 | $ | $ | ||||||
| 負債と株主資本 | ||||||||
| 流動負債: | ||||||||
| 買掛金と未払費用 | $ | $ | ||||||
| 繰延収益-現在の部分 | ||||||||
| 流動負債の合計 | ||||||||
| 長期負債: | ||||||||
| 繰延収益-長期部分 | ||||||||
| 長期負債総額 | ||||||||
| 負債合計 | ||||||||
| コミットメントと不測の事態(注7を参照) | ||||||||
| 株主資本: | ||||||||
| 優先株式、$ | ||||||||
| 普通株式、$ | ||||||||
| 追加払込資本 | ||||||||
| 自己株式、原価( | ( | ) | ( | ) | ||||
| その他の包括利益 (損失) の累計 | ( | ) | ||||||
| 累積赤字 | ( | ) | ( | ) | ||||
| 株主資本の総額 | ||||||||
| 負債総額と株主資本 | $ | $ | ||||||
未監査の連結財務諸表の添付の注記を参照してください。
-1-
サイロファーマ株式会社と子会社
連結営業報告書および包括損失
(未監査)
| 終了した3か月間 | ||||||||
| 3 月 31 日 | ||||||||
| 2024 | 2023 | |||||||
| ライセンス料収入 | $ | $ | ||||||
| 収益コスト | ||||||||
| 売上総利益 | ||||||||
| 営業費用: | ||||||||
| 報酬費用 | ||||||||
| 専門家手数料 | ||||||||
| 研究開発 | ||||||||
| 保険費用 | ||||||||
| 販売費、一般管理費 | ||||||||
| 営業費用の合計 | ||||||||
| 事業による損失 | ( | ) | ( | ) | ||||
| その他の収入(費用): | ||||||||
| 利息と配当収入、純額 | ||||||||
| 支払利息 | ( | ) | ( | ) | ||||
| 短期投資の純実現利益 | ||||||||
| 預金証書の早期解約によるペナルティ | ( | ) | ||||||
| 株式投資の未実現純利益 | ||||||||
| 外貨取引損失 | ( | ) | ||||||
| その他の収入 (費用) の合計 | ( | ) | ||||||
| 所得税引当金控除前の損失 | ( | ) | ( | ) | ||||
| 所得税引当金 | ||||||||
| 純損失 | $ | ( | ) | $ | ( | ) | ||
| 包括的な損失: | ||||||||
| 純損失 | $ | ( | ) | $ | ( | ) | ||
| その他の包括利益 (損失): | ||||||||
| 短期投資の含み益 | ||||||||
| 包括損失合計 | $ | ( | ) | $ | ( | ) | ||
| 普通株式1株あたりの純損失: | ||||||||
| $ | ( | ) | $ | ( | ) | |||
| 加重平均発行済普通株式: | ||||||||
未監査の連結財務諸表の添付の注記を参照してください。
-2-
サイロファーマ株式会社と子会社
株主資本の連結変動計算書
2024年および2023年3月31日に終了した3か月間
(未監査)
| [追加] | 累積その他 | 合計 | ||||||||||||||||||||||||||||||
| 普通株式 | 支払い済み | 自己株式 | 包括的 | 累積 | 株主の | |||||||||||||||||||||||||||
| 株式 | 金額 | 資本 | 株式 | 金額 | 収益 (損失) | 赤字 | エクイティ | |||||||||||||||||||||||||
| 残高、2023年12月31日 | $ | $ | $ | ( | ) | $ | ( | ) | $ | ( | ) | $ | ||||||||||||||||||||
| 自己株式の購入 | - | ( | ) | ( | ) | |||||||||||||||||||||||||||
| その他の包括損失の累積-短期投資 | - | - | ||||||||||||||||||||||||||||||
| 純損失 | - | - | ( | ) | ( | ) | ||||||||||||||||||||||||||
| 残高、2024年3月31日 | $ | $ | $ | ( | ) | $ | $ | ( | ) | $ | ||||||||||||||||||||||
| [追加] | 累積その他 | 合計 | ||||||||||||||||||||||||||||||
| 普通株式 | 支払い済み | 自己株式 | 包括的 | 累積 | 株主の | |||||||||||||||||||||||||||
| 株式 | 金額 | 資本 | 株式 | 金額 | 収入 | 赤字 | エクイティ | |||||||||||||||||||||||||
| 残高、2022年12月31日 | $ | $ | $ | $ | $ | ( | ) | $ | ||||||||||||||||||||||||
| ストックオプション費用の株式ベースの報酬への増加 | - | - | ||||||||||||||||||||||||||||||
| その他の包括損失の累積-短期投資 | - | - | ||||||||||||||||||||||||||||||
| 純損失 | - | - | ( | ) | ( | ) | ||||||||||||||||||||||||||
| バランス、2023年3月31日 | $ | $ | $ | $ | $ | ( | ) | $ | ||||||||||||||||||||||||
未監査の連結財務諸表の添付の注記を参照してください。
-3-
サイロファーマ株式会社と子会社
連結キャッシュフロー計算書
(未監査)
| 終了した3か月間 | ||||||||
| 3 月 31 日 | ||||||||
| 2024 | 2023 | |||||||
| 営業活動によるキャッシュフロー: | ||||||||
| 純損失 | $ | ( | ) | $ | ( | ) | ||
| 純損失を営業活動に使用された純現金と調整するための調整 | ||||||||
| 株式ベースの報酬と専門家報酬 | ||||||||
| 前払いの株式ベースの専門職費の償却 | ||||||||
| 短期投資の純実現利益 | ( | ) | ||||||
| 株式投資の未実現純利益 | ( | ) | ||||||
| 営業資産および負債の変動: | ||||||||
| 前払費用およびその他の流動資産 | ( | ) | ( | ) | ||||
| 売掛金 | ( | ) | ||||||
| 買掛金と未払費用 | ||||||||
| 繰延収益 | ( | ) | ( | ) | ||||
| 営業活動に使用された純現金 | ( | ) | ( | ) | ||||
| 投資活動によるキャッシュフロー: | ||||||||
| 短期投資の売却による収入 | ||||||||
| 短期投資の購入 | ( | ) | ( | ) | ||||
| 投資活動によって提供された(使用された)純現金 | ( | ) | ||||||
| 財務活動によるキャッシュフロー: | ||||||||
| 自己株式の購入 | ( | ) | ||||||
| 財務活動に使用された純現金 | ( | ) | ||||||
| 現金および現金同等物の純減額 | ( | ) | ( | ) | ||||
| 現金および現金同等物-期初 | ||||||||
| 現金および現金同等物-期末 | $ | $ | ||||||
| キャッシュフロー情報の補足開示: | ||||||||
| 期間中に支払われた現金: | ||||||||
| 利息 | $ | $ | ||||||
| 所得税 | $ | $ | ||||||
| 非現金投資および資金調達活動: | ||||||||
| その他の包括利益の累積増減額 | $ | $ | ||||||
未監査の連結財務諸表の添付の注記を参照してください。
-4-
サイロファーマ株式会社と 子会社
統合に関する注意事項 財務諸表
2024年3月31日
(未監査)
注1 — 組織とビジネス
サイロファーマ株式会社(以下「会社」) は、2010年7月13日にゴールドスワップ社の名前でニューヨーク州で設立されました。2013年1月24日、当社は変更しました ニューヨークからデラウェアまでの設立状況。2023年12月19日、当社は州からの法人設立状況を変更しました デラウェア州からネバダ州まで。
同社は開発段階のバイオ医薬品です 伝統的な治療法とサイケデリックス研究の融合に焦点を当てた会社。同社は知識人の獲得および/または育成を目指しています 幻覚剤の使用を含む、希少疾患を治療するための一流の大学や研究者からの財産権または技術権、 サイロシビンなど。また、うつ病、メンタルヘルスの問題、神経疾患を伴う特定のケースで得られる可能性のある利点 障害。同社は、適応症に苦しむ人々のために、伝統的な治療法とサイケデリックス研究を融合させることに重点を置いています。 うつ病、心的外傷後ストレス障害(「PTSD」)、アルツハイマー病、パーキンソン病、その他のまれな神経疾患など 障害。会社の使命は、変革をもたらすと当社が考える研究にライセンス供与する資産を特定し、資金を提供することです。 患者と医療業界の幸福のために。同社は以前、ストリートウェアの開発に従事していました アパレルブランド、NFID(下記参照)。
2019年5月21日、当社は修正案を提出しました 社名をポイント・キャピタル社からアッパーカット・ブランズ社に変更。その後、デラウェア州法人設立証明書を取得しました。 2020年9月24日、当社は法人設立証明書の修正をデラウェア州に提出し、社名を変更しました アッパーカット・ブランズ社からサイロ・ファーマ社まで
2020年4月8日、当社は新しい会社を設立しました フロリダ州の完全子会社、Silo Pharma Inc.また、会社はwww.silopharma.comというドメイン名も保護しています。 当社は、知識人の獲得および/または育成を目指して、会社の事業を拡大する機会を模索してきました 幻覚剤の使用を含む、希少疾患を治療するための一流の大学や研究者からの財産権または技術権、 サイロシビンなど。また、うつ病、メンタルヘルスの問題、神経疾患を伴う特定のケースで得られる可能性のある利点もあります 障害。2020年7月、当社の新しく設立された子会社を通じて、当社は商業評価ライセンスを締結しました メリーランド大学ボルチモア校(「UMB」)とのオプション契約(注7を参照)とのオプション契約(注7を参照)。これによると、とりわけUMB 特定の技術について、交渉して独占的でサブライセンス可能な、ロイヤリティを伴うライセンスを取得する独占的なオプションを会社に与えました。 オプションは2021年1月13日に延長され、行使されました。2021年2月12日、当社はとマスターライセンス契約を締結しました UMB(注7を参照してください)。同社は、知的財産権または技術権の取得および/または開発を積極的に進める予定です 希少疾患を治療し、最終的にはこの新しい事業に注力するように会社の事業を拡大すること。
2021年9月30日、当社は参入しました
フロリダ州の有限責任会社であるNFID、LLCとの資産購入契約(「資産購入契約」)に入り、締結しました
会社(「購入者」)。これにより、購入者は会社から特定の資産、資産、および関連する権利を購入しました
会社のNFID商標名、ロゴ、ドメイン、アパレルの衣類とアクセサリーで、購入価格は$です
注2 — 重要な会計の概要 ポリシー
プレゼンテーションの基礎と統合の原則
付随する未監査の連結財務 会社の明細書は、アメリカ合衆国で一般に認められている会計原則に従って作成されています 暫定財務情報(「米国会計基準」)については、規則S-Xの第8-03条の指示を参照してください。経営成績 の中間期間は、必ずしも会計年度全体で期待できる結果を示すものではありません。特定の情報 米国会計基準に従って作成された財務諸表に通常含まれる開示が、要約または省略されていることに注意してください これらの記述はそのような会計原則に従っており、したがって必要な情報やメモがすべて含まれているわけではありません 包括的な財務諸表については。これらの未監査の連結財務諸表は、要約と併せて読む必要があります 2023年12月31日に終了した年度の重要な会計方針と連結財務諸表の注記が含まれています 2024年3月25日に証券取引委員会に提出されたフォーム10-Kの会社の年次報告書。
会社の連結財務諸表 Silo Pharma, Inc. およびその親会社であるSiloと同じ名前の非アクティブな完全子会社の財務諸表を含めてください Pharma, Inc. 連結により、会社間取引と残高はすべて削除されました。経営陣はその責任を認めています すべての調整を反映した、通常の調整からなる添付の未監査連結財務諸表の作成用 連結財政状態の公正な記述のために必要と考えられる定期調整と非定期調整 および表示されている期間の連結経営成績。
-5-
サイロファーマ株式会社と 子会社
統合に関する注意事項 財務諸表
2024年3月31日
(未監査)
流動性
添付の未監査連結報告書に反映されているとおり
財務諸表によると、会社は$の純損失を計上しました
プラスの運転資金は軽減に役立ちます 歴史的に、当社が継続企業として存続できるかどうかについて大きな疑問を投げかけてきた状況。会社 会社には、最低12か月間の債務を履行するのに十分な現金と流動性のある短期投資があると考えています この申告日から。
見積もりの使用
連結財務諸表の作成 米国会計基準に準拠して、経営陣は報告された資産と負債の金額に影響する見積もりと仮定を行う必要があります と財務諸表作成日における偶発資産と負債、および報告された収益と費用の金額の開示 報告期間中。見積もりを行うには、経営陣が慎重な判断を下す必要があります。少なくとも合理的には可能です それは、財務諸表の日付に存在していた条件、状況、または一連の状況の影響の推定値、 経営陣が見積もりを作成する際に考慮した内容は、将来1つ以上の出来事によって短期的に変わる可能性があります。したがって、 実際の結果は予想とは大きく異なる可能性があります。2024年および2023年3月31日に終了した3か月間の重要な見積もり 売掛金の回収可能性、研究開発プロジェクトの完了率、資本の評価額などが含まれます 投資、繰延税金資産の評価引当金、およびサービスのために発行された株式とストックオプションの公正価値。
現金および現金同等物
当社は、流動性の高い投資をすべて考慮しています
現金同等物として取得した場合、満期は3か月以内。同社は信用の質が高い財務部門に資金を投入しています
機関。これらの機関の会社の口座は、連邦預金保険公社(「FDIC」)によって保証されています
最大$です
短期投資
会社の短期投資ポートフォリオ 満期以上の高格付けの米国国債のみで構成される、市場性のある債券で構成されています 3か月、ただし1年未満。会社はこれらを購入日に販売可能なものとして分類し、そのような指定を再検討します 各期終了日に。当社は、変更に応じて、これらの有価債務証券を記載された満期より前に売却することがあります 流動性要件。これらの負債証券は、未監査の連結貸借対照表では流動資産として分類され、記録されています 公正価値で、未実現利益または未実現損益はその他の包括利益の累積に含まれ、未監査分の一部として 連結包括損失計算書。利益と損失は実現時に認識されます。利益と損失は以下を使用して決定されます 特定の識別方法で、未監査の連結損益計算書に差し引かれたその他の収益(費用)で報告されます と包括的な損失。
減損損失は次の場合に認識される場合があります 債務証券の公正価値の下落は、一時的なものではないと判断されています。会社は自社の投資を一時的なもの以外で評価しています 四半期ごと、または事象や状況の変化により原価ベースが示されるたびに、公正価値が原価ベースを下回ります の短期投資は回収できない可能性があります。評価は、期間の長さや、さまざまな要素に基づいています 公正価値が原価基準をどの程度下回っているか、および特に証券に関連する不利な状況、 証券の信用格付けの変更や売却意向、または会社が義務付けられる可能性が高いかどうかなど 償却原価ベースが回収される前に証券を売却すること。
会社は$を記録しました
-6-
サイロファーマ株式会社と 子会社
統合に関する注意事項 財務諸表
2024年3月31日
(未監査)
株式投資、公正価値で
実現利益または損失は投資時に計上されます が処分され、会社の帳簿価額とそのような処分から受け取った純収入との差として計算されます。 投資取引による実現損益は、特定の識別によって決まります。純未実現利益または未実現損失が計算されます 投資の公正価値とそのような投資の原価基準との差です。株式の純未実現利益または損失 投資は、期初の帳簿価額と公正価値の差額として事業に反映されます 期末に。
受取手形
会社は損失引当金を認識しています
回収額を差し引いた推定推定損失に等しい金額の受取手形について。手当は過去の分析に基づいています
不良債権の経験、現在の売掛金の経年劣化、将来予想される償却、および特定の識別可能なものの評価
リスクがある、または回収できないと見なされるアカウント。貸倒引当金に関連する費用は、一般会計の一部として計上されます
と管理費。2023年12月31日現在、当社は受取手形と未払手形の損失引当金を計上しました
推定推定損失額に等しい金額の受取利息、したがって会社は不良債権費用を計上しました
前払い経費
前払い費用およびその他の流動資産
収益認識
会社はASCトピック606、収益を適用しています 顧客との契約(「ASC 606」)。ASC 606は、企業が会計に使用する単一の包括的なモデルを確立します 顧客との契約から生じる収益で、既存の収益認識ガイダンスのほとんどに取って代わります。この規格には 対価を反映した金額で、約束された商品やサービスを顧客に譲渡することを表すために、収益を認識する法人 企業がそれらの商品やサービスと引き換えに受けられることを期待していて、特定の追加開示も要求しています。
会社は利息と配当収入を記録します 当社がそのような金額を回収すると予想される範囲で、発生主義で。
ライセンスとロイヤリティ収入の場合、収益は 会社が関連するライセンス契約に基づく履行義務を果たしたときに認められます。ライセンシーから受け取った支払い 将来の期間に関連するものは繰延収益として計上され、関連するライセンスの期間中の収益として認識されます 契約(注7を参照)。
収益コスト
収益コストの主要構成要素は ライセンス料には、ライセンス料の費用が含まれます。将来の期間に関連してライセンサーに支払われた支払いは、前払いとして記録されます 関連するライセンス契約の期間中に償却される費用(注記7を参照)。
株式ベースの報酬
株式ベースの報酬は、株式ベースで会計処理されます ASC 718の「報酬 — 株式報酬」の要件については、財務上の認識が必要です 株式証書の授与と引き換えに受け取った従業員、取締役、および非従業員サービスの費用の明細書 従業員、取締役、または非従業員は、報酬(おそらく権利確定)と引き換えに役務を遂行する必要があります ピリオド)。ASCでは、アワードと引き換えに受け取った従業員、取締役、および非従業員サービスの費用の測定も義務付けています アワードの付与日の公正価値に基づいています。当社は、没収が会計で認められている範囲で発生した場合、それを認めることを選択しました 標準更新(「ASU」)2016-09年従業員の株式ベースの支払いの改善。
所得税
繰延所得税の資産と負債が発生します 制定された税率で測定される、財務諸表と資産と負債の課税基準の一時的な違いから、 これらの違いが逆転したときに有効になると予想されます。繰延税金資産と負債は、流動税資産と非流動税に分類されます。 関連する資産または負債の分類によります。関連しない繰延税金資産と負債 資産または負債は、一時的な差異が予想される期間に応じて、流動資産または非流動資産に分類されます 逆に。評価引当金は、繰延税金資産を実現予定の金額まで減らすために必要なときに設定されます。
-7-
サイロファーマ株式会社と 子会社
統合に関する注意事項 財務諸表
2024年3月31日
(未監査)
会社は財務の規定に従います 会計基準審議会(「FASB」)ASC 740-10、「所得税の不確実性」。特定の認識閾値 税務上の地位が財務諸表に反映される前に満たされなければなりません。企業は税金のみを認識することも、引き続き認識することもできます 「そうでない可能性よりも高い」という基準を満たすポジション。当社は、自社の税務上の立場が不確かなものがあるとは考えていません 2024年3月31日と2023年12月31日の場合は、添付の未監査連結資産での認識または開示が必要です 財務諸表。
研究開発
ASC 730-10に従って、 「研究
と開発全体、」 研究開発費は発生時に支出されます。3月31日に終了した3か月間は、
2024年と2023年、研究開発費は$でした
リース
リースはASU 2016-02を使用して会計処理されています。」リース (トピック 842)」。ASU 2016-02には、以下のリースの認識、測定、表示、開示に関する原則が定められています 契約の両当事者(つまり、借手と貸手)。この基準では、借手は二重のアプローチを採用し、リースを次のように分類しています リースが実質的に借手による購入であるかどうかの原則に基づく、ファイナンスリースまたはオペレーティングリースのいずれか。 この分類によって、リース費用が有効利息法に基づいて計上されるのか、定額法で計上されるのかが決まります。 リース期間を超えています。また、借手は期間のあるすべてのリースについて、使用権資産とリース負債を認識する必要があります 分類に関係なく、12か月以上の。期間が12か月以下のリースは、次のように計上されます 今日のオペレーティングリースに関する既存のガイダンス。2024年3月31日および2023年12月31日現在、当社にはリースはありません。会社は リースを分析して、未監査の連結資産にリース負債と使用権資産を記録する必要があるかどうかを判断してください ASU 2016-02の採用時の貸借対照表は公正価格です。当社は、使用権資産とリース負債を認識しないことを選択しました 期間が12か月以下の短期リースの場合。
普通株式1株当たりの純損失
1株当たりの基本損失は、純額を割って計算されます 各期間に発行された普通株式の加重平均数によって普通株主に配分される損失。希釈しました 1株当たりの損失は、普通株主が利用できる純損失を普通株式の加重平均数で割って計算されます。 当期中に発行された普通株式同等物および潜在的に希薄化の可能性のある有価証券。潜在的に ストックオプションや新株予約権を含む希薄化有価証券は、以下の場合に希薄化後の発行済株式の計算から除外されます それらは会社の純損失に希薄化防止効果をもたらします。
| 3 月 31 日 | 3 月 31 日 | ||||||
| 2024 | 2023 | ||||||
| ストック・オプション | |||||||
| ワラント | |||||||
| 433,4230 | |||||||
最近の会計上の宣言
経営陣は最近それを信じていません 発行されたものの、まだ有効ではない会計上の声明が採択された場合、会社の未監査連結に重大な影響を及ぼします 財務諸表。
-8-
サイロファーマ株式会社と 子会社
統合に関する注意事項 財務諸表
2024年3月31日
(未監査)
注3 — 金融商品の公正価値 と公正価値の測定
公正価値の測定と金融の公正価値 インストゥルメント
ファブアスク 820- 公正価値の測定と 情報開示は、公正価値を、資産を売却するために受け取る価格、または負債を秩序正しく譲渡するために支払われる価格と定義しています 測定日における市場参加者間の取引。FASB ASC 820では、すべての金融商品の公正価値についての開示が義務付けられています 認識されているかどうかにかかわらず、財務諸表用の商品。金融商品の公正価値に関する開示は 2024年3月31日と2023年12月31日に当社が入手した関連情報に基づいています。したがって、提示された見積もりは これらの財務諸表は、必ずしも金融商品の処分によって実現できる金額を示すものではありません。 FASB ASC 820は、それらの評価手法への入力が観察可能かどうか、または、それに基づいて、評価手法の階層を指定します 観察できません。観察可能なインプットは独立した情報源から得られた市場データを反映し、観察できないインプットは市場の仮定を反映しています。 このヒエラルキーでは、活発な市場における同一の資産または負債の未調整相場価格が最優先されます(レベル1の測定) そして、観察できない入力(レベル3の測定)の優先順位が最も低くなります。
| レベル 1- | インプットは、測定日に入手可能な同一の資産または負債の、活発な市場における調整前の相場価格です。 | |
| レベル 2- | インプットは、活発な市場における類似資産と負債の未調整の見積もり価格、活発でない市場における同一または類似の資産と負債の相場価格、観察可能な相場価格以外のインプット、観察可能な市場データから導き出された、または裏付けられたインプットです。 | |
| レベル 3- | インプットは観察できないインプットであり、市場参加者が入手可能な最良の情報に基づいて資産または負債の価格を設定する際にどのような仮定を使用するかについての報告主体自身の仮定を反映しています。 |
特定の金融商品の帳簿価額、 現金および現金同等物、前払費用およびその他の流動資産、売掛金、買掛金および未払費用を含みます は、これらの商品の短期的な性質のため、実際の原価ベースで取引され、これはその公正価値に近いものです。
会社はすべての金融商品を分析します 財務会計基準審議会(「FASB」)の会計に基づく負債と資本の両方の特徴を備えています そのような機器の規格。この基準では、金融資産と負債は全体として最も低いものに基づいて分類されます 公正価値の測定にとって重要なインプットのレベル。
| 2024年3月31日 | 2023年12月31日 | |||||||||||||||||||||||
| 説明 | レベル 1 | レベル 2 | レベル 3 | レベル 1 | レベル 2 | レベル 3 | ||||||||||||||||||
| 短期投資 | $ | $ | $ | $ | $ | $ | ||||||||||||||||||
会社の短期投資と 株式投資はレベル1の測定値であり、各日の償還額に基づいています。
短期投資 — 債務証券、 でフェアバリュー
| 3 か月が終了 3月31日、 | 3 か月 3 月 31 日 | |||||||
| 2024 | 2023 | |||||||
| 残高、期初 | $ | $ | ||||||
| 追加 | ||||||||
| 元の原価での販売 | ( | ) | ||||||
| 短期投資の純実現利益 | ||||||||
| 実現利益と未実現利益 | ||||||||
| 残高、期末 | $ | $ | ||||||
ASC 825-10「金融商品」 企業が特定の金融資産と負債を公正価値(公正価値オプション)で測定することを自発的に選択できるようにします。フェア バリューオプションは銘柄ごとに選択でき、新しい選挙日が発生しない限り取り消すことはできません。公正価値なら ある商品のオプションが選ばれたら、その商品の含み損益はその後の毎回の収益に報告する必要があります 報告日。当社は、未払いの株式商品に公正価値オプションを適用することを選択しませんでした。
-9-
サイロファーマ株式会社と 子会社
統合に関する注意事項 財務諸表
2024年3月31日
(未監査)
メモ4 — 受取手形
| 3 月 31 日 | 12月31日 | |||||||
| 2024 | 2023 | |||||||
| 受取手形の元本 | $ | $ | ||||||
| 未払利息売掛金 | ||||||||
| 小計 | ||||||||
| 控除:疑わしい口座の手当 | ( | ) | ( | ) | ||||
| 受取手形 — 現在の | ||||||||
2023年12月31日現在、当社は認識しています
受取手形および未収利息の損失引当金の、推定推定損失額に等しい金額の引当金
注5 — 株主資本
承認済み株式
2023年12月4日、当社の株主
当社の普通株式の授権株式数の減少を承認しました
サービス用に発行された普通株式
2022年8月29日、当社は
ある企業との投資家向け広報サービスの1年間のコンサルティング契約。このコンサルティング契約に関連して、当社は
発行しました
株式買戻し計画
2023年1月26日、会社の取締役会は
の取締役が、最大$までの自社株買い計画を承認しました
ストックオプション
2021年1月18日、会社の取締役会は
の取締役(「取締役会」)は、サイロファーマ社の2020年オムニバス株式インセンティブプラン(「2020年プラン」)を承認しました。
会社とその関連会社の従業員、役員、取締役、コンサルタントにインセンティブを与えます。
-10-
サイロファーマ株式会社と 子会社
統合に関する注意事項 財務諸表
2024年3月31日
(未監査)
2024年3月31日に終了した3か月間と
2023年、会社はドルを償却しました
| の数 オプション |
加重 平均 エクササイズ 価格 |
加重 平均 残り 契約期間 (年) |
集計 本質的 価値 |
|||||||||||||
| 未払い残高、2023年12月31日 | $ | $ | ||||||||||||||
| 付与されました | - | - | - | - | ||||||||||||
| 未払い残高、2024年3月31日 | $ | $ | ||||||||||||||
| エクササイズ可能、2024年3月31日 | $ | $ | ||||||||||||||
新株予約権
| ワラントの数 | 加重 平均 エクササイズ 価格 | 加重 平均 残り 契約期間 (年) | 集計 本質的 価値 | |||||||||||||
| 未払い残高、2023年12月31日 | $ | $ | ||||||||||||||
| 付与されました | ||||||||||||||||
| 未払い残高、2024年3月31日 | $ | $ | ||||||||||||||
| エクササイズ可能、2024年3月31日 | $ | $ | ||||||||||||||
注6 — 濃度
顧客集中
2024年3月31日に終了した3か月間と
2023年、1人のライセンシーがアカウントを取得しました
ベンダーの集中
2024年3月31日に終了した3か月間と
2023年、1人のライセンサーが
注7 — コミットメントと不測の事態
雇用契約
エリック・ワイスブラム
2020年4月17日、当社は
エリック・ワイスブラムが最高経営責任者兼最高財務責任者を務める雇用契約(「雇用契約」)
会社の。雇用契約の期間は、契約締結日から1年間継続され、自動的に
各期間の終了時に、どちらかの当事者が更新しない旨を書面で通知するまで、連続して1年間更新されます
その時点で発効した期間の満了の少なくとも6か月前。雇用契約では、基本給は$でした
-11-
サイロファーマ株式会社と 子会社
統合に関する注意事項 財務諸表
2024年3月31日
(未監査)
2022年10月12日に、当社は
エリック・ワイスブラムとの新しい雇用契約(「2022年のワイスブラム雇用契約」)に基づき、ワイスブラム氏は
(i) 基本給は $
ダニエル・ライウェック
2022年9月27日、理事会はダニエルを任命しました
ライウェックは会社の最高財務責任者でした。2022年9月28日、当社は雇用契約(「ライウェック」)を締結しました
Ryweck氏との雇用契約」)。10月12日に改正されたRyweck雇用契約の条件に従い、
2022年、ライウェック氏は(私は)年率で基本給を受け取ります
ジェームズ・クオ博士
2022年1月27日、当社とジェームズ博士は
クオは、クオ博士が研究担当副社長を務める雇用契約(「クオ雇用契約」)を締結しました
と開発。Kuo雇用契約は契約日に発効し、自動的に更新されます
どちらかの当事者が書面を提供しない限り、発効日の記念日ごとに1年間有効で、同じ契約条件が適用されます
該当する更新日の少なくとも30日前には、Kuo雇用契約の期間を延長しない意向の通知。
クオ博士には年間基本給$が支払われます
-12-
サイロファーマ株式会社と 子会社
統合に関する注意事項 財務諸表
2024年3月31日
(未監査)
会社とのライセンス契約 ベンダー
メリーランド大学、ボルチモア-ライセンス 中枢神経系ホーミングペプチドの開発と使用に関する合意
商用評価ライセンスとオプション契約 メリーランド大学ボルチモア校と
2020年7月15日より、当社は、 その完全子会社であるSilo Pharma, Inc.(注1を参照)とメリーランド大学ボルチモア校(「UMB」)(まとめて 「当事者」)、商用評価ライセンスおよびオプション契約(「ライセンス契約」)を締結し、付与 当社は、セントラルの潜在的な用途の調査に関して、独占的、サブライセンス不可、譲渡不可のライセンスを取得しています 生体内での神経系ホーミングペプチドと、多発性硬化症やその他の神経炎症の調査と治療へのそれらの使用 病理。また、ライセンス契約により、会社には独占的でサブライセンス可能なロイヤリティを交渉して取得する独占オプションも与えられました 対象技術に関するライセンス(「独占オプション」)。ライセンス契約の期間は、それから 6 ヶ月でした 発効日。ただし、会社が独占オプションを行使した場合、ライセンス契約は交渉の終了時に失効します 期間(使用許諾契約で定義されているとおり)またはマスターライセンス契約の締結時、どちらか早い方。会社は行使しました 2021年1月13日に独占オプションとなり、2021年2月12日にマスターライセンス契約を締結しました。両当事者は解約することができます この契約は、書面で通知して30日以内に提出してください。
メリーランド大学、ボルチモア-ライセンス ジョイントホーミングペプチドの開発と使用に関する契約
商用評価ライセンスとオプション契約 メリーランド大学ボルチモア校と
2021年2月26日より、当社は、
その完全子会社であるSilo Pharma, Inc.、およびメリーランド大学ボルチモア校(「UMB」)(総称して「当事者」)を通じて、
商用評価ライセンスおよびオプション契約(「ライセンス契約」)を締結し、会社に独占的な権利を与えました。
ジョイントホーミングペプチドの使用可能性の調査に関する、サブライセンス不可、譲渡不可のライセンス
関節形成プロセスの調査と治療。使用許諾契約により、会社には独占的な交渉オプションも与えられました
対象技術に関して、サブライセンス可能でロイヤリティを伴う独占ライセンス(「独占オプション」)を取得してください。
2021年7月6日、当社はUMBと契約期間を延長するための憲法修正第1条契約(「憲法修正第1条」)を締結しました
憲法修正第1条が2022年2月25日まで有効になるように、元のライセンス契約をさらに6か月延長します。1月に
2022年28日、両当事者は、2021年2月26日付けの商業評価およびライセンス契約の第2改正を締結しました(「第二次
元のライセンス契約の期間を2022年12月31日まで延長するための改正」)。2022年6月22日に、両当事者は参加しました
2021年2月26日付けの商用評価およびライセンス契約の第3修正(「第3修正」)に。ザ・リクシ・
修正第3条により、ライセンス契約で付与されるライセンスの範囲が拡大され、以下に関する特許権が追加されました
一般的に知られている発明 病気や障害の治療、診断、画像診断のためのペプチド標的リポソームデリバリー。
この修正第3条に基づいて付与されたライセンスの対価として、当社は、返金不可の1回限りの手数料を支払うことに同意しました
大学とのマスターライセンス契約 メリーランド州、ボルチモアの
上記のとおり、2月12日から有効になります。 2021年、当社とメリーランド大学ボルチモア校(「UMB」)は、マスターライセンス契約を締結しました(「マスター」 ライセンス契約」)は、特定の知識人に、世界規模で、サブライセンス可能な、ロイヤリティを伴う独占的なライセンスを会社に付与します 財産:(i)特定のライセンス製品の製造、製造、使用、販売、販売の申し出、輸入、および:(ii)というタイトルの発明を使用するには、 「生体内の中枢神経系ホーミングペプチドと、多発性硬化症などの研究と治療へのそれらの使用 神経炎症病理」と、認可された特定のプロセスを開発および実行するためのUMBの機密情報 神経炎症性疾患の治療法。
マスターライセンス契約は引き続き有効です
ライセンス製品ごと、および国ごとに、(a)の対象となった最後の特許のどちらか遅い方までです
マスターライセンス契約の期限切れ、(b)データ保護の期限切れ、新しい化学主体、希少疾病用医薬品の独占権、規制上の独占権、
または法的強制力のあるその他の市場独占権(該当する場合)、または(c)
-13-
サイロファーマ株式会社と 子会社
統合に関する注意事項 財務諸表
2024年3月31日
(未監査)
会社は譲渡、サブライセンス、付与、または
それ以外の場合は、事前の書面を得ることなく、マスターライセンス契約に基づく権利または義務を会社の関連会社に伝えます
マスターライセンス契約で定義された条件を満たしていれば、UMBからの同意。会社は一部のサブライセンスを付与したり
マスターライセンス契約によって付与されるすべての権利。ただし、未解決の不履行または重大な条項の違反がないことを条件とします。
付与時の会社によるマスターライセンス契約に基づく条件、および付与が契約条件に準拠していること
マスターライセンス契約の。会社は、会社それぞれの業績に対して責任を負うものとし、今後も責任を負うものとします
サブライセンシー。すべてのサブライセンスは、マスターライセンス契約の条件と一致し、その条件に従うものとし、
会社がマスターライセンス契約を遵守できるように十分な条件を組み込んでください。会社または会社の関連会社
サブライセンシーから受け取った全収入の一定割合をUMBに次のように支払うものとします。(i)
マスターライセンス契約に従い、
会社はUMB、(i)ライセンス料、(ii)特定のイベントベースのマイルストーン支払い(支払い条件については以下を参照)、(iii)ロイヤリティの支払いを支払うものとします
純収入(支払い条件については以下を参照)、および(iv)サブライセンス収入の段階的な割合によって異なります。会社はUMB aに支払いました
$のライセンス料
| マイルストーン | 支払 | |||
| $ | ||||
| $ | ||||
| $ | ||||
| $ | ||||
| $ | ||||
ロイヤリティ支払い条件:
| (i) |
| (ii) |
| (iii) |
| 何年も | 最低年間 ロイヤリティ | |||
| $ | N/A | |||
| $ | N/A | |||
| $ | ||||
| $ | ||||
| $ | ||||
2023年11月10日、当社は UMBとのマスターライセンス契約の第3修正(「第3改正」)。これに従って両当事者は マスターライセンス契約のディリジェンスマイルストーンのスケジュールを修正し、改訂しました。
2021年4月、当社に関連して
合気道製薬株式会社とのサブライセンス契約(下記参照)- 合気道製薬株式会社との特許ライセンス契約)、会社が支払いました
-14-
サイロファーマ株式会社と 子会社
統合に関する注意事項 財務諸表
2024年3月31日
(未監査)
会社とのライセンス契約 顧客
合気道との顧客特許ライセンス契約 ファーマ株式会社
2021年1月5日、当社とその子会社 Silo Pharma, Inc. は、特許ライセンス契約(「ライセンス契約」)を締結しました(総称して「ライセンサー」) 2021年4月12日に修正された合気道製薬株式会社(「合気道」または「顧客」)と、これに従ってライセンサーは 合気道に、特定の知的財産に対する独占的、世界的(「地域」)、サブライセンス可能な、ロイヤリティを伴うライセンスを付与しました。 (i)特定のライセンスを製造、製造、使用、提供、輸入、輸出、リース、流通、販売、販売の申し出、開発、宣伝すること 製品、および(ii)がんおよびがんに起因する症状の治療のための特定の認可プロセスを開発および実施すること(「分野 使用の」)。
ライセンス契約には、次のことも規定されていました
ライセンサーは、UMBとの商用評価ライセンスおよびオプション契約に従って、付与されたオプションを行使しました。有効期間は以下のとおりです。
2020年7月15日に、合気道に、次の分野における特定のUMB特許権に対する非独占的なサブライセンス(「権利」)を付与することになります
がん(「フィールド」)と診断された患者に発生する神経炎症性疾患。ライセンス契約によると、合気道
ライセンサーに、とりわけ、(i)返金不可の1回限りの現金支払いを支払うことに同意しました
使用許諾契約に従い、当社は
ライセンス特許の準備、出願、出願、および維持に必要です。早期に終了しない限り、のライセンス期間
ライセンス特許は、ライセンス対象内で発行されたすべての特許と提出された特許出願の有効期限が切れるか放棄されるまで有効です。
特許。合気道が未払い金額と支払い金額を支払わなかった場合、会社は30日の書面による通知をもってライセンス契約を終了することができます。
会社に、または合気道またはその関連会社が会社に対して特許異議申し立てをした場合、他の人が訴訟を起こすのを手伝う場合
または、ライセンスされた特許の有効性、範囲、または執行可能性に関する行政上の異議申し立て、またはライセンスされた特許のいずれかに異議を申し立てる(「パテントチャレンジ」)
会社に対して(裁判所命令または召喚状で義務付けられている場合を除く)。合気道は理由なくいつでも契約を終了することができます。
そして、追加のペナルティを受けることなく、(i)少なくとも30日前に書面で通知し、会社に全額を支払うことで
当該解約発効日までに支払われるべき金額。いずれの当事者も、重大な違反が失敗した場合は契約を終了することができます
書面による通知を受け取ってから60日以内に治療する必要があります。会社は$の返金不可の現金支払いを回収しました
2021年4月12日の普通株式の発行に先立って
前述のように、シリーズM転換優先株式の代わりに、当社が評価したのは
2024年3月31日に終了した3か月間と
2023年、会社はライセンス料収入を$と認識しました
権利は、許される最大限の範囲で
UMBが通常提供する特許および技術ライセンスの期間と一致する期間については、UMBが要求する契約条件に従って
付与します。会社がオプションを行使し、その後40日以内にUMBにUMBの特許権のライセンスを締結した場合
そのようなUMBライセンスの実行。対価は合気道が合意し、支払う必要があります。対価はいかなる場合でもそれを超えないものとします。
-15-
サイロファーマ株式会社と 子会社
統合に関する注意事項 財務諸表
2024年3月31日
(未監査)
との顧客サブライセンス契約 合気道製薬株式会社
2021年4月6日(「サブライセンス契約」) 発効日」)、当社は合気道とサブライセンス契約を締結しました。これに基づいて会社は合気道に (i)ライセンス製品(以下に定義)の製造、製造、使用、販売、販売および輸入の申し出を行うための世界規模の独占サブライセンスと (ii)それに関連して、(A)「生体内での中枢神経系ホーミングペプチド」として知られる発明の使用とその用途 会社にサブライセンスされた「多発性硬化症およびその他の神経炎症性病変」の調査と治療 マスターライセンス契約に従い、(B)治療薬に関する特定の特許権(「特許権」)を実践してください がん患者の神経炎症性疾患の治療。「ライセンス製品」とは、あらゆる製品、サービス、またはプロセスを指します。 開発、製造、使用、販売の申し出、販売、輸入、提供:(i)が特許の1つまたは複数の請求の対象となる 権利、または(ii)発明または特許で開示されている技術を含む、含む、利用する、組み込む、または派生している 権利。
サブライセンス契約に従い、合気道は同意しました
会社に(i)に$の前払いライセンス料を支払うこと
スポンサー付きの研究・研究契約 会社とベンダーの間
との治験責任医師支援研究契約 メリーランド大学、ボルチモア
2021年1月5日、当社は
メリーランド大学ボルチモア校との、研究者が後援する研究契約(「スポンサー研究契約」)。リサーチ
プロジェクトは、多発性硬化症(「MS」)の治療のための新しいペプチド誘導ドラッグデリバリーアプローチを検討する臨床研究です。
具体的には、この研究は、MS-1を表示するリポソームがデキサメタゾンを効果的に送達できるかどうかを評価することを目的としています(1)
CNSと(2)MS-1表示リポソームが再発抑制の点でプレーンリポソーム(遊離薬とも呼ばれる)よりも優れているかどうか、そして
実験的自己免疫性脳脊髄炎の進行。スポンサースタディ契約に従い、研究は3月に開始されます
2021年1月1日、そして実質的な完成まで継続されます。両当事者の書面による相互の同意により更新される場合があります。総費用
スポンサースタディ契約では、$を超えてはなりません
リージェンツとのスポンサーリサーチ契約 カリフォルニア大学の
2021年6月1日(「発効日」)に、
当社は、リージェンツ・オブ・ザ・ユニバーシティとスポンサー・リサーチ契約(「スポンサー・リサーチ契約」)を締結しました
カリフォルニア州のサンフランシスコキャンパス(「UCSF」)を代表して、UCSFはサイロシビンの検査に関する研究を実施します
慢性パーキンソン病の潜在的な治療法としての実施を加速させるヒトの炎症活性への影響
痛み、そして双極性障害。契約に従い、会社はUCSFに合計$の手数料を支払うものとします
-16-
サイロファーマ株式会社と 子会社
統合に関する注意事項 財務諸表
2024年3月31日
(未監査)
大学とのスポンサー研究契約 メリーランド州、ボルチモアの
2021年7月6日に、会社と大学 メリーランド州、ボルチモア(「UMB」)は、スポンサーリサーチ契約(「2021年7月のスポンサーリサーチ契約」)を締結しました これに従って、UMBはリポソームを介して関節炎のラットに送達されたデキサメタゾンの薬物動態を評価します。リサーチ 2021年7月のスポンサードリサーチ契約に従い、2021年9月1日に開始され、実質的に完了するまで続きます そのうち、当事者の書面による同意を得て更新される場合があります。2021年7月のスポンサーリサーチ契約は、次のいずれかで終了することができます 相手方への30日前の書面による通知が必要です。さらに、どちらかの当事者が重大な違反または債務不履行を犯した場合 2021年7月のスポンサーリサーチ契約の条項または条件に関して、そのような不履行または違反を是正できない 相手方からの書面による通知から10営業日後に、通知をした当事者は2021年7月のスポンサードリサーチ契約を終了することができます 相手方がそのような通知を受け取った日現在。当社が2021年7月のスポンサーリサーチ契約を終了した場合 理由の如何を問わず、UMBによる未解決の重大な違反以外の場合、当社はリザルトにおいて保有する可能性のあるすべての権利を放棄するものとします( UMBへの2021年7月のスポンサーリサーチ契約)で定義されています。さらに、2021年7月のスポンサードリサーチ契約が終了した場合 早期に、当社は、とりわけ、解約日の時点でUMBが負担および発生したすべての費用を支払います。2022年6月7日に、 当社とUMBは、2021年7月のスポンサードリサーチ契約を修正しました。これにより、両当事者は元のプロジェクトに変更を加えることに合意しました 仕事と予算。修正は未監査の連結財務諸表には影響しませんでした。
2021年7月のスポンサーの条件に従って
研究契約、UMBは会社に交渉して任意のUMBの独占ライセンスを取得するオプション(「オプション」)を与えました
発生IP(2021年7月のスポンサードリサーチ契約で定義されているとおり)および任意の共同発生IP(で定義されているとおり)におけるUMBの権利
2021年7月スポンサーリサーチ契約)(総称して「UMB IP」)。
| 支払 | |||||||
| 1 | $ | ||||||
| 2 | $ | ||||||
| 3 | $ | ||||||
会社は$の最初の支払いをしました
コロンビアとのスポンサーリサーチ契約 大学
2021年10月1日、当社は
コロンビア大学とのスポンサー付き研究契約に基づき、会社は特定の資産をライセンスするオプションを与えられています
アルツハイマー病に苦しむ患者の潜在的な治療に関連する資産を含め、現在開発中です。
オプションの期間は、本契約の発効日に始まり、(i) 90日後のいずれか早い方に失効します
契約書に定義されている特定の研究提案ごとの最終研究レポートを会社が受領した日付、または(ii)
研究の終了。当社がオプションを行使することを選択した場合、両当事者はライセンス契約の交渉を開始します
オプションの行使日から3ヶ月以内にライセンス契約を締結します。コロンビア大学と
同社は、アルツハイマー病から心的外傷後ストレスに苦しむ患者の治療法の開発に取り組みます
障害。本契約の日付から1年間、
2024年3月31日に終了した3か月間と
2023年、会社は$の研究開発費を記録しました
-17-
サイロファーマ株式会社と 子会社
統合に関する注意事項 財務諸表
2024年3月31日
(未監査)
リプロセルとの研究契約
2022年10月25日(「発効日」)に、
当社は、リプロセル・ヨーロッパ株式会社(「リプロセル」)と研究契約(「リプロセル・リサーチ契約」)を締結しました。
これに従って、Reprocellは、健康な関節リウマチの滑膜組織に対するペプチドの結合を評価するための研究を実施します。
リプロセルの研究契約に従い、会社はリプロセルに合計$の手数料を支払うものとします
アッパートン・ファーマ・ソリューションズとの研究契約
2023年2月28日と2023年10月16日に、(
「発効日」)で、当社はアッパートンと研究契約(「アッパートン研究契約」)を締結しました
ファーマ・ソリューションズ(「アッパートン」)に基づき、アッパートンは開発と実現可能性を支援するための調査を実施します
プルカロプリド点鼻薬の。2023年10月16日のアッパートン研究契約に従い、会社はアッパートンに総額を支払うものとします
合計手数料は約
AmplifyBioとの研究契約
2023年10月16日(「発効日」)に、
当社は、AmplifyBio, LLCと研究契約(「AmplifyBio研究契約」)を締結しました。(「アンプリファイバイオ」)
これに従って、AmplifyBioは、新薬の鼻腔内投与を調査するための料金に関する研究を実施します。に従って
AmplifyBio研究契約に従って、会社はAmplifyBioに合計$の手数料を支払うものとします
シーバー・ファーマ・ソリューションズとの研究契約
2023年4月26日(「発効日」)、
当社は、フォスター・デリバリー・サイエンス社と研究契約(「Sever製薬研究契約」)を締結しました。dbaは
として、Sever Pharma Solutions(「Sever Pharma」)として、これに従ってSever Pharmaは前臨床押出成形の研究を実施します
PLGA/ケタミンインプラントの概念実証です。Sever製薬研究契約に従い、会社はSever Pharmaに総額を支払うものとします
$の手数料
2024年3月31日に終了した3か月間と
2023年、当社は他の研究開発契約を締結しました。そのような契約に関連して、会社は調査を記録しました
と$の開発費
-18-
サイロファーマ株式会社と 子会社
統合に関する注意事項 財務諸表
2024年3月31日
(未監査)
| 3月31日に終了した年度 | 金額 | |||
| 2025 | $ | |||
| 合計 | $ | |||
ザイロ・セラピューティクスとの合弁契約、 株式会社。
2021年4月22日(「発効日」)に、 当社は、ZylöTherapeutics, Inc.(「ZTI」)と合弁契約(「合弁契約」)を締結しました。 これに基づき、両当事者は、Ketamine Joint Venture, LLC(「ジョイントベンチャー」)と名付けられる合弁事業体を設立することに合意しました。 とりわけ、ZTIのZ-pod™ 技術(「ベンチャー」)を使用したケタミンの臨床開発に焦点を当てます。 合弁契約に従い、当社は合弁事業のマネージャー(「マネージャー」)としての役割を果たすものとします。合弁会社は 開発プログラムが合弁契約に定められた特定の仕様やマイルストーンを満たさない場合は、30日以内に終了してください 合弁契約に定められた日付の。上記にかかわらず、マネージャーは独自の裁量でジョイントを解約することができます いつでもベンチャーできます。
JV契約の条件に従って、(A)
会社は (1) $を寄付します
さらに、JV契約の条件に従い、
ZTIは、アルバート・アインシュタインとのライセンス契約(「ライセンス契約」)に従って、合弁事業にサブライセンスを付与するものとします。
2017年11月27日付けの医学部(当社または第三者から、特許を取得したことを示す請求があった場合)
開発を進めるには、ライセンス契約に従ってZTIにライセンスされた技術(「特許技術」)が必要です
合弁事業の、または特許技術の売却が検討または決定されています。さらに、合弁契約に従い、
ZTIは、ZTIを使用してサイロシビンの臨床開発のための別の合弁事業を締結する独占オプションを会社に付与しました
Z-pod™ テクノロジーは、JV契約に定められているのと同じ条件で、どのオプションが期限切れですか
修正されたサービス契約
2021年9月10日(「発効日」)に、
当社は、9月付けの特定のサービス契約の修正契約(「修正サービス契約」)を締結しました
2020年8月8日、テキサス大学オースティン校(「大学」)で、大学がアドバイザリーサービスと支援を行います
会社のライセンスおよびスポンサー付き研究の機会の特定について。会社は大学に$を支払うものとします
注8 — その後のイベント
株式買戻し計画
4月に
2024年4月4日、当社の取締役会は、以前に発表された株式買戻しプログラムの承認の延長を承認しました
最大$の購入
-19-
アイテム 2.経営陣の議論と分析 財政状態と経営成績について
以下は私たちについての議論と分析です 財務状況と経営成績は、記載されている未監査の財務諸表と関連注記と一緒に読む必要があります フォーム10-Qのこの四半期報告書と、12月31日に終了した年度の監査済み財務諸表と関連メモの他の部分には、 2023年は、証券取引委員会(SEC)に提出されたフォーム10-Kの年次報告書に含まれています。歴史に加えて 情報、この議論と分析には、リスク、不確実性、仮定を含む将来の見通しに関する記述が含まれています。私たちの実際の 特定の要因により、結果はこれらの将来の見通しに関する記述で予想されるものと大きく異なる場合があります。要因について話し合います 以下およびForm 10-Qのこの四半期報告書の他の部分で、これらの違いの原因または原因となる可能性があると私たちが信じているもの(それらを含む) 「将来の見通しに関する記述と業界データに関する注意事項」というタイトルのセクションに記載されている要素と パートII、項目1Aの「リスク要因」というタイトルのセクション。
[概要]
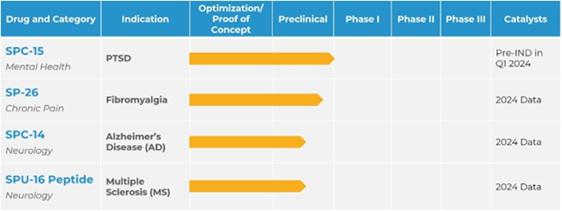
私たちは開発段階のバイオ医薬品です PTSD、ストレス誘発性不安障害、線維筋痛症など、治療が不十分な状態に対処する新しい治療法を開発している会社です。 と中枢神経系(CNS)疾患。私たちは、従来の薬やサイケデリックを含む新しい治療法の開発に注力しています 製剤。同社の主力プログラムであるSPC-15は、PTSDとストレス誘発性不安障害を対象とした鼻腔内投与薬です。SP-26 は、線維筋痛症と慢性疼痛緩和のための徐放性ケタミンベースのローディングインプラントです。Siloの2つの前臨床プログラムはSPC-14です。 アルツハイマー病の治療のための鼻腔内化合物、および中枢神経を標的とする中枢神経系ホーミングペプチドであるSPU-16 多発性硬化症(MS)の初期研究適応症を含むシステム。
希少疾患治療薬
私たちは知識人の獲得および/または育成を目指しています 幻覚剤の使用を含む、希少疾患を治療するための一流の大学や研究者からの財産権または技術権、 サイロシビン、ケタミンなど、うつ病、メンタルヘルスの問題が伴う特定のケースで得られる可能性のある利点や 神経障害。私たちは伝統的な治療法とサイケデリック医学の開発に注力しています。同社は、次のことに重点を置いています うつ病、心的外傷後ストレス障害(「PTSD」)などの適応症による満たされていないニーズに対する治療法の開発と商品化、 、およびその他のまれな神経障害。私たちの使命は、ライセンスを供与する資産を特定し、変革をもたらすと私たちが信じている研究に資金を提供することです。 患者と医療業界の幸福のために。
サイロシビンはセロトニン作動性幻覚剤と考えられています とは、ある種のキノコに含まれる有効成分です。サイロシビンなどのサイケデリックスを使用した最近の業界研究は有望ですが、 そして、うつ病、メンタルヘルスの問題、神経障害に苦しむ多くの人々にとって、満たされていない大きなニーズがあると考えています。 規制物質法(「CSA」)ではスケジュールIの物質として分類されていますが、証拠は蓄積されています そのサイロシビンは、うつ病やその他の精神的健康状態に有益な効果をもたらす可能性があります。そのため、米国食品医薬品局は (「FDA」)と米国麻薬取締局(「DEA」)は、臨床研究でのサイロシビンの使用を許可しています さまざまな精神疾患の治療。
精神におけるサイロシビン療法の可能性 健康状態は、過去10年間に学術機関が後援した多くの研究で実証されています。これらの初期の研究では、 サイロシビン療法は、1回の高用量投与後にうつ病の症状を急速に軽減し、抗うつ効果をもたらすことが観察されました 多くの患者さんが最長で6ヶ月間持続します。これらの研究では、うつ病や不安神経症に関連する症状を次のように評価しました 広く使用され、検証されている多くの尺度。これらの研究によって得られたデータは、サイロシビンは一般的に耐容性が高いことを示唆しています そして、心理的サポートを受けて投与するとうつ病を治療する可能性があります。
私たちは多くの人と話し合ってきました 世界的に有名な教育機関やアドバイザーが潜在的な機会について相談し、科学諮問委員会を結成しました。 は、製品の買収や開発の可能性について経営陣に助言することを目的としています。
さらに、以下で詳しく説明するように、私たちは メリーランド大学ボルチモア校とライセンス契約を締結し、ケタミンポリマーのインプラントを開発しています。さらに、 私たちは最近、コロンビア大学とスポンサー付き研究契約を締結しました。それに基づいてオプションが与えられました アルツハイマー病とストレス誘発性情動障害の治療に関連する特定の特許と発明をライセンスします ケタミンと他の特定の化合物と組み合わせて使用します。
買収を積極的に進める予定ですし、 希少疾患を治療するための知的財産権または技術権の開発、そして最終的にはこれに重点を置いて事業を拡大すること 新しい事業分野。
製品候補者
現在、4つの製品候補に焦点を当てています。 (i) うつ病の治療のためのSPC-15、(ii) 慢性疼痛の治療のためのSP-26、(iii) アルツハイマー病の治療のためのSPC-14 多発性硬化症の初期適応症を伴う中枢神経系障害の治療には、疾患と(iv)SPU-16。
-20-
SPC-15
2021年10月1日、当社は コロンビア大学とのスポンサー付き研究契約に基づき、会社は特定の資産をライセンスするオプションを与えられています うつ病の治療のためのSPC-15に関連する資産を含め、現在開発中です。2022年9月22日に、私たちはエントリーしました コロンビア協定の期間を延長してさらなる研究を行うためのコロンビアとのスポンサーリサーチ契約の修正第1条に 調査。延長は2024年3月31日までです。2023年4月11日に、ライセンスを取得できる開発中の資産 上記のように、米国特許商標庁(USPTO)から「予防効果のバイオマーカー」の特許が発行されました ストレス誘発性情動障害に対する治療」(米国 11,622,948、B2)。会社は独占ライセンスのオプションを行使しました 不安神経症やPTSDを含むストレス誘発性情動障害の予防治療薬であるSPC-15に関する合意。それによると、 会社には、SPC-15を世界中でさらに開発、製造、商品化するための独占ライセンスが付与されます。会社は期待しています 2024年の前半にコロンビアとの完全なライセンス契約を完了させること。
SPC-15は標的を絞った予防治療薬です PTSDを含むストレス誘発性情動障害の治療と予防のための組成物。治療は重症度を予測します またはそのような疾患の進行と薬理学的治療に対するそれらのメタボロームバイオマーカーの反応。私たちは開発するつもりです FDA規則のセクション505 (b) (2) 規制経路に基づくSPC-15です。連邦食品医薬品化粧品法のセクション505(b)(2) (「FDCA」)は、スポンサーが新しい再利用薬の新薬申請(「NDA」)の承認を求めることができるようにするために制定されました そのようなスポンサーが、時間と費用のかかる前臨床安全性研究や第1相安全性研究を実施する必要はありません。続行します この規制経路の下では、NDA提出時に有効成分に関して公開されているデータに頼ることができます FDAに販売承認を求めてください。
2023年11月15日、当社は独占契約を結びました Medspray Pharma BVと、独自の特許取得済みのソフトミスト点鼻薬技術のデリバリーメカニズムに関するライセンス契約を結びました SPC-15、どの契約の発効日は2023年10月31日です。前臨床研究と製剤研究は、に完了する予定です 2024年の第1四半期に、当社は2024年の前半にIND前の会議出席依頼書をFDAに提出する予定です。
SP-26
2023年3月、当社は暫定書類を提出しました 線維筋痛症を含む慢性疼痛の治療にSP-26を使用するという米国特許商標庁への特許出願線維筋痛症は慢性疾患です 筋肉、靭帯、腱など、体全体の結合組織に痛みを引き起こします。筋骨格系の痛みはしばしば伴います 睡眠障害、疲労、気分障害、記憶力や集中力の問題によって。線維筋痛症は約400万人のアメリカ人が罹患しています 成人、または成人人口の約2%。
私たちは、セクションに従ってSP-26を開発するつもりです 505 (b) (2) FDA規則の規制経路。FDCAのセクション505(b)(2)は、スポンサーが小説のNDA承認を求めることができるように制定されました 時間と費用のかかる前臨床安全性試験と第1相試験をそのようなスポンサーが行う必要なく、再利用された医薬品 安全性研究。この規制経路に従って手続きを進めることで、私たちの活動に関して公開されているデータに頼ることができるようになります 市販承認を得るためにFDAに提出するNDAの成分。
SPC-14
2021年10月1日、当社は コロンビア大学(「コロンビア」)とのスポンサー付き研究契約。これに基づき、コロンビアは2つの異なる研究を行うものとします アルツハイマー病の治療のためのSPC-14の使用に関する研究。「医師が後援する研究契約 会社とベンダー---ケタミンと他の薬剤の併用の研究に関するコロンビア大学とのスポンサー研究契約 アルツハイマー病とうつ病の治療に。」詳細については。さらに、会社にはオプションが付与されています アルツハイマー病治療用のSPC-14を含む、現在開発中の特定の資産のライセンスを取得します。会社は行使しました 不安神経症を含むストレス誘発性情動障害の予防治療薬であるSPC-15の独占ライセンス契約の選択肢です そしてPTSDに基づいて、会社はSPC-15をさらに開発、製造、商品化するための独占ライセンスを付与されます 世界的に。同社は、2024年の前半にコロンビアとの完全なライセンス契約が完了する予定です。
-21-
SPC-14は、承認された2つを組み合わせた新薬です 治療薬なので、FDA規則のセクション505(b)(2)の規制経路に従ってSPC-14を開発する予定です。のセクション505 (b) (2) FDCAは、スポンサーがスポンサーに依頼しなくても、新しい再生医薬品のNDA承認を求めることができるようにするために制定されました 時間と費用がかかる前臨床安全性試験と第1相安全性試験。この規制経路のもとで進めると、私たちは 市販承認を得るためにFDAに提出するNDAでは、有効成分に関する公開データを利用することができます。
2022年10月13日、当社は期間を延長しました コロンビアにおけるSPC-14の作用機序に関するさらなる調査研究を行うためのコロンビアとのスポンサー研究契約の期間 アルツハイマー病の治療。2024年には、さらなる前臨床研究の結果が出ることを期待しています。
スパウ-16
2021年2月12日、私たちは修士課程に入りました メリーランド大学ボルチモア校(「UMB」)とのライセンス契約(「UMBライセンス契約」)は、 UMBは、特定の知的財産(i)を製造するための独占的、世界的、サブライセンス可能な、ロイヤリティを伴うライセンスを私たちに与えました 特定のライセンス製品の製造、使用、販売、販売の申し出、輸入、および(ii)「中枢神経系ホーミング」というタイトルの発明の使用について 生体内でのペプチドと、多発性硬化症やその他の神経炎症性病変の調査と治療へのそれらの使用、」 またはSPU-16。「会社とベンダー間のライセンス契約--メリーランド大学ボルチモア校とのベンダーライセンス契約」を参照してください CNSホーミングペプチド用」で詳細をご覧ください。2023年4月11日、UMBライセンス契約に基づく特定の知的財産 上記は、米国特許商標庁(USPTO)から「ペプチド標的リポソームデリバリー」の特許を取得したものです 病気や障害の治療、診断、画像診断に」(米国11,766,403、B2)。
SPU-16は、特に新しいペプチドホーミングです 炎症を起こしている中枢神経系領域に。患者の神経炎症の診断や、脊髄への薬の的を絞った送達に使用できます。 最初の適応症は多発性硬化症(MS)です。ペプチドは、ヒト多発性硬化症のEAEマウスモデルでテストされています。 特に炎症を起こしている中枢神経系領域に帰着します。
-2-
製品開発パイプライン
次の表は、当社の製品開発をまとめたものです パイプライン。
会社とのライセンス契約 ベンダー
大学とのベンダーライセンス契約 メリーランド州、ボルチモア州のCNSホーミングペプチドは
2021年2月12日、私たちは修士課程に入りました メリーランド大学ボルチモア校(「UMB」)とのライセンス契約(「UMBライセンス契約」)は、 UMBは、特定の知的財産(i)を製造するための独占的、世界的、サブライセンス可能な、ロイヤリティを伴うライセンスを私たちに与えました 特定のライセンス製品の製造、使用、販売、販売の申し出、輸入、および(ii)「中枢神経系ホーミング」というタイトルの発明の使用 生体内でのペプチドと、多発性硬化症やその他の神経炎症性病変の調査と治療へのそれらの使用」 (「発明」)とUMBの機密情報は、治療薬のために認可された特定のプロセスを開発および実行するためのものです 神経炎症性疾患の治療。使用許諾契約の期間は、UMBの発効日に始まり、継続されるものとします ライセンス製品の最初の商用販売日(サブライセンス契約で定義されているとおり)から遅くとも(i)10年まで その国で、および(ii)特許権(UMBライセンス契約で定義されている)の最後の有効期限が切れる請求の有効期限が切れる日 その国でのそのようなライセンス製品の対象、または(iii)データ保護の期限切れ、新しい化学物質、希少疾病用医薬品の独占権、 規制上の独占権またはその他の法的強制力のある市場独占権(該当する場合)。ただし、規約に従って早期に終了されない限り 契約の。UMBライセンス契約に従い、UMB(i)に75,000ドルのライセンス料、(ii)特定のイベントベースのマイルストーンを支払うことに同意しました 支払い、(iii)純収益に応じたロイヤリティの支払い、(iv)最低ロイヤリティの支払い、(v)サブライセンスの段階的な割合 収入。UMBライセンス契約は、(a) UMBライセンス契約の対象となる最後の特許のいずれか遅い方まで有効です。 有効期限、(b)データ保護の有効期限、新しい化学主体、希少疾病用医薬品の独占権、規制上の独占権、またはその他の法的法的効力 強制力のある市場独占権(該当する場合)、または(c)その国でライセンス製品が最初に商業的に販売されてから10年後 UMBライセンス契約の規定に従って早期に終了した場合を除きます。UMBライセンス契約の期間は (a) 特許権がなく、(b) データ保護が一切なかった発効日から15年後に失効します、新規 化学物質、希少疾病用医薬品の独占権、規制上の独占権、またはその他の法的強制力のある市場独占権、または(c)一度もありませんでした ライセンス製品の最初の商用販売。
以下に説明するように、当社は 新しいペプチド誘導ドラッグデリバリーアプローチを検討するための臨床研究に関連する、研究者が後援するUMBとの研究契約 多発性硬化症の治療に。
商用評価ライセンスとオプション契約 ジョイントホーミングペプチドにはUMBと一緒に
2021年2月26日より、当社は、 その完全子会社であるSilo Pharma, Inc. とメリーランド大学ボルチモア校(「UMB」)を通じて、コマーシャルを始めました 評価ライセンスおよびオプション契約(「ライセンス契約」)。これにより、当社に独占的でサブライセンス不可の契約が付与されました。 調査に使用するためのジョイントホーミングペプチドの潜在的な用途の調査に関する譲渡不可のライセンス と関節形成プロセスの治療。ライセンス契約により、会社には交渉して取得するための独占オプションも与えられました 対象技術に関する独占的、サブライセンス可能な、ロイヤリティを伴うライセンス(「独占オプション」)。ライセンス 契約の期間は発効日から6か月でした。両当事者は30日以内にライセンス契約を終了できたはずです 書面で通知することによって。
2021年7月6日、当社は最初の取引を開始しました 元のライセンス契約の期間をさらに延長するためのUMBとの修正契約(「修正ライセンス契約」) ただし、会社が独占契約を行使する場合は、修正ライセンス契約が2022年2月25日まで有効になるような6か月 オプション、ライセンス契約は、交渉期間(ライセンス契約で定義されているとおり)の終了時、または締結時に失効します マスターライセンス契約、どちらか早いほうのもの。当社は、以下に従い、2021年3月にUMBに1万ドルのライセンス料を支払いました ライセンス契約は、そのような費用がこの初期段階で回収可能であると当社が結論付けることができなかったため、消滅しました ベンチャー。
-23-
2022年1月28日、会社と大学 メリーランド州のボルチモアは、2021年2月26日付けのライセンス契約の第2改正(「修正第2条」)を締結しました。 憲法修正第2条により、ライセンス契約の期間が2022年12月31日まで延長されました。ただし、会社がエクスクルーシブを行使する場合は オプション、ライセンス契約は、交渉期間(ライセンス契約で定義されているとおり)の終了時、または締結時に失効します マスターライセンス契約、どちらか早いほうのもの。
2022年6月22日に、当社とUMBは参入しました 2021年2月26日付けのライセンス契約の第3改正で、UMBは付与されるライセンスの範囲を拡大することに合意しました CELAに、一般に「ペプチド標的リポソームデリバリー」として知られている発明に関する特許権を追加します 病気や障害の治療、診断、画像診断のため。」2022年12月16日、当社とUMBは4回目の買収契約を結びました ライセンス契約の期間を延長するための2021年2月26日付けのライセンス契約の改正(「第4改正」) 2023年3月31日までです。さらに、両当事者は修正第4条で、当社がライセンス契約の期間を延長することを許可することに合意しました 2023年2月28日までにUMBに1,000ドルの手数料を支払うことで、2023年6月30日までです。この料金は支払われ、したがってライセンス契約の期間が決まりました 2023年6月30日まで延長されました。このライセンスは、2023年12月31日の条件で失効します。
ザイロ・セラピューティクスとの合弁契約、 Z-pod™ テクノロジー用株式会社
2021年4月22日、当社は ZylöTherapeutics, Inc.(「ZTI」)との合弁契約に基づき、両当事者は合弁会社を設立することに合意しました 事業体は、とりわけZTIを使ったケタミンの臨床開発に注力するため、Ketamine Joint Venture, LLCと名付けられる予定です Zポッド™ テクノロジー。合弁契約に従い、当社は合弁事業のマネージャーを務めるものとします。ベンチャー 開発プログラムが合弁契約に定められた特定の仕様やマイルストーンを満たさない場合は終了します 合弁契約に定められた日から30日以内に。上記にかかわらず、マネージャーは独自の裁量で、 いつでもベンチャーを終了させてください。
合弁契約書(A)の条件によると、 会社は(1)225,000ドル、(2)自社の専門知識と科学諮問委員会の専門知識、(B)ZTIが寄付します (1) 合弁契約に定められている特定の特許技術に対する特定の権利、(2) ノウハウと企業秘密へのライセンス ケタミンのローディングと放出のためのZ-pod™ テクノロジーに関しては、(3)臨床目的で使用されるケタミン、(4) その施設と許可証の合理的な使用、および (5) その専門知識とノウハウの合理的な使用。合弁契約によると、利息の 51% では、合弁事業は当初会社が所有し、合弁事業の持分の49%は当初会社が所有することになります ZTI、どちらかの当事者から追加の拠出があった場合は調整される場合があります。上記にかかわらず、いかなる場合も どちらかの当事者が合弁事業の持分の60%以上を所有しています。2024年3月31日現在、およびこの年次報告書の現在の日付の時点で、 合弁会社はまだ設立されていません。
さらに、JV契約の条件に従い、 ZTIは、アルバート・アインシュタインとのライセンス契約(「ライセンス契約」)に従って、合弁事業にサブライセンスを付与するものとします。 2017年11月27日付けの医学部(当社または第三者から、特許を取得したことを示す請求があった場合) 開発を進めるには、ライセンス契約に従ってZTIにライセンスされた技術(「特許技術」)が必要です 合弁事業の、または特許技術の売却が検討または決定されています。さらに、合弁契約に従い、 ZTIは、ZTIを使用してサイロシビンの臨床開発のための別の合弁事業を締結する独占オプションを会社に付与しました Z-pod™ テクノロジーは、合弁契約に定められているのと同じ条件で使用されます。どちらのオプションも、合弁契約から24か月後に失効します 合弁会社の発効日。私たちはZyloを続けるつもりはなく、投薬用のポリマーインプラントを開発する契約を締結しました 慢性疼痛と線維筋痛症のためのケタミンのタイムリリース。
メドスプレー間の独占ライセンス契約 ファーマBVと会社
2023年11月15日、私たちはエクスクルーシブを開始しました メドスプレー・ファーマBV(「メドスプレー」)とのライセンス契約(「メドスプレー・ライセンス契約」)は、メドスプレーの規定に基づいています Medsppray独自の特許取得済みのソフトミスト点鼻薬の、取消不能で世界規模のロイヤリティを伴う独占ライセンスを付与しました Medspprayライセンス契約に基づいてMedsprayが当社にライセンスした製品のマーケティング、プロモーション、販売、流通のための技術。 メドスプレーライセンス契約の発効日は2023年10月31日で、メドスプレーの終了の(i)いずれか早い方に失効します 米国、ドイツ、英国、スペイン、イタリア、フランスにおけるライセンス契約またはすべてのメドスプレーライセンス権の満了。に メドスプレーが私たちに与えた独占権を考慮して、四半期ごとに5%に相当するロイヤリティをメドスプレーに支払うことに同意しました 純売上高の。契約期間は発効日に始まり、最後の(i)満了日のいずれか早い方まで続きます メドスプレーの特許権の有効期限、または (ii) 2023年12月31日(「初期期間」)の満了日、メドスプレーライセンス 契約は、1年前の書面によりいずれかの当事者が終了しない限り、自動的に3年連続で更新されます 任意の期間が終了する前の通知。ただし、Medspprayは、失敗した場合、Medspprayライセンス契約を直ちに終了することができます メドスプレーライセンス契約に基づくライセンス製品を、2028年7月1日までにFDAまたはEMAに登録するか、届出を申請していること 2028年7月1日までに、メドスプレーライセンス契約に基づくライセンス製品の最初の販売場所。
-24-
治験責任医師主催の研究契約 会社とベンダー
コロンビアとのスポンサーリサーチ契約 アルツハイマー病やうつ病の治療のためのケタミンと他の薬剤の併用に関する研究大学
2021年10月1日、当社は コロンビア大学(「コロンビア」)とのスポンサー付き研究契約。これに基づき、コロンビアは2つの異なる研究を行うものとします ケタミンまたはその代謝産物をプルカロプリドと組み合わせたすべての使用に関する研究。そのうちの1つはアルツハイマー病に関連しています もう1つは、うつ病、PTSD、ストレスプロジェクトに関するものです。さらに、会社にはライセンスのオプションが付与されています アルツハイマー病を含む、現在開発中の特定の資産。オプションの期間は、発効日から始まります 本契約の日付で、(i) 会社が最終調査を受け取った日から90日のいずれか早い方に失効します 契約書または (ii) 研究の終了で定義されている特定の研究提案ごとの報告。会社が行使することを選択した場合 オプションでは、両当事者がライセンス契約の交渉を開始し、遅くとも3か月以内にライセンス契約を締結します オプションの行使日以降。当社は、予防策であるSPC-15の独占ライセンス契約のオプションを行使しました 不安神経症やPTSDを含むストレス誘発性情動障害の治療。これに基づいて会社は独占的に治療を受けることになります SPC-15を世界中でさらに開発、製造、商品化するためのライセンス。会社は完全なライセンス契約を結ぶことを期待しています コロンビアは2024年前半に完成しました。コロンビア大学と当社は、治療法の開発に向けて取り組んでいきます アルツハイマー病から心的外傷後ストレス障害に苦しむ患者のために。この日から1年間 契約上、会社は研究支援のためにコロンビア大学に合計1,436,082ドルを支払います スケジュールは次のとおりです。(i) 署名時に 30%、(ii) プロジェクト開始後4か月半後に 30%、(iii) 9か月後に 30% プロジェクトの開始、(iv) プロジェクトの完了時の 10%2022年10月13日、当社は スポンサーリサーチ契約に基づき、両当事者は支払いスケジュールを2024年3月31日まで延長することに合意しました。会社が支払いました 最初の支払いは2021年11月に430,825ドルで、2回目の支払いは2022年7月に430,825ドルです。
大学とのスポンサー研究契約 メリーランド州、ボルチモア州の、関節リウマチのための標的リポソームドラッグデリバリーの研究で
2021年7月6日、私たちはスポンサーリサーチを開始しました UMBが薬物動態を評価するためのUMBとの契約(「2021年7月のスポンサーリサーチ契約」) のリポソームを介して関節炎のラットに送達されるデキサメタゾンのうち。2021年7月のスポンサーリサーチ契約に基づく研究が開始されました 2021年9月1日で、実質的に完成するまで継続されます。当事者の書面による同意を得て更新されることがあります プロジェクトのタイムラインは12か月です。2021年7月のスポンサーリサーチ契約は、30日後にどちらかの当事者によって終了される場合があります。 相手方への事前の書面通知。さらに、いずれかの当事者が何らかの条件に重大な違反または不履行を犯した場合 または2021年7月のスポンサーリサーチ契約の条件で、書面を書いてから10営業日以内にそのような不履行または違反を是正しなかった場合 相手方からの通知。通知をした当事者は、受領日をもって、2021年7月のスポンサードリサーチ契約を終了することができます 相手方からのそのような通知について。未治癒以外の理由で当社が2021年7月のスポンサーリサーチ契約を終了した場合 UMBによる重大な違反です。結果(2021年7月のスポンサーリサーチで定義されているとおり)でUMBが持つ可能性のあるすべての権利を放棄します 同意) をUMBに。さらに、2021年7月のスポンサードリサーチ契約が早期に終了した場合は、とりわけ私たちが全額を支払います 解約日の時点でUMBが負担し、発生した費用。2021年7月のスポンサーリサーチ契約の条項に従い、 UMBは、任意のUMB Arising IP(で定義されているとおり)の独占ライセンスを交渉して取得するオプション(「オプション」)を私たちに与えました 2021年7月のスポンサーリサーチ契約)および共同発生IP(2021年7月のスポンサーリサーチで定義されているとおり)におけるUMBの権利 契約)(総称して「UMB IP」)。オプションを受け取ってから60日以内にUMBに書面で通知することでオプションを行使することができます UMB IPに関するUMBからのお知らせです。2021年7月のスポンサーリサーチ契約に定められているように、合計276,285ドルの手数料を支払うものとします。会社 2021年9月1日に最初の支払いである92,095ドルを支払い、2022年8月31日に会社は2回目の支払いである92,095ドルを支払いました。
リージェンツとのスポンサーリサーチ契約 血液中の炎症に対するサイロシビンの影響については、カリフォルニア大学の
2021年6月1日、当社はスポンサー契約を結びました カリフォルニア大学のサンに代わって、リージェンツと締結した研究契約(「スポンサーリサーチ契約」) フランシスコキャンパス(「UCSF」)に従って、UCSFはサイロシビンの炎症への影響を調べる研究を実施します パーキンソン病、慢性疼痛、双極性障害の潜在的な治療法としての実施を加速するためのヒトでの活動 障害。これの目的は、サイロシビンが血液の炎症にどのような影響を与えるかを示すことです。同社はこの調査を信じています UMBホーミングペプチド研究の支援に役立ちます。契約に従い、調査を実施するためにUCSFに合計342,850ドルの手数料を支払うものとします 2年間にわたって。本契約は、更新またはそれ以前の場合を条件として、発効日から2年間有効です スポンサーリサーチ契約に定められている解約。スポンサー契約によると、2022年12月31日および2021年12月31日に終了した年度中 研究契約に基づき、会社はカリフォルニア大学サンフランシスコ校にそれぞれ181,710ドルと100,570ドルを支払いました。UCSFに通知しました。これを継続する予定はありません 研究。
との治験責任医師支援研究契約 CNSホーミングペプチドのUMB
2021年1月5日、私たちは治験責任医師主催の会社を設立しました UMBとの研究契約。研究プロジェクトは、治療のための新しいペプチド誘導ドラッグデリバリーアプローチを検討する臨床研究です 多発性硬化症(「MS」)の。より具体的には、この研究は(1)MS-1を表示するリポソームが可能かどうかを評価することを目的としています デキサメタゾンを中枢神経系に効果的に送達し、(2) MS-1表示リポソームが普通のリポソームより優れているかどうか、 実験的自己免疫性脳脊髄炎の再発と進行を抑制する点で、フリードラッグとしても知られています。契約に従い、 調査は2021年3月1日に開始され、実質的に完了するまで継続されます。ただし、相互の書面による同意を得て更新されることがあります パーティーの。治験責任医師が後援する研究契約に基づく総費用は81,474ドルを超えてはなりません。これは2回に分けて支払われます スポンサースタディ契約の締結時に40,737ドル、プロジェクトの完了時に40,737ドルを均等に分割して支払います。見積もりでは 9か月のプロジェクトタイムライン。当社は2021年1月13日に40,737ドルを支払いました。このプロジェクトは、追って通知があるまで延期され、 2回目の支払い期限はありません。
-25-
株式買戻し計画
2023年1月26日、会社の取締役会は の取締役が、当社の発行済みおよび発行済み普通株式を最大100万ドルまで買い戻すための株式買戻し計画を承認しました。 時間、このようなプログラムは2023年12月31日まで実施される予定です。2024年1月9日、当社の取締役会は 以前に発表された株式買戻しプログラムの延長。これにより、最大100万ドルの当社普通株の購入が可能になります 株式は2024年3月31日まで、2024年4月4日に、株式買戻し計画は2024年4月30日まで延長されました。12月に終了した年度中に 2023年31日、当社は252,855株の普通株式を471,121ドルで購入しました。これは付随する自己株式に反映されます 未監査の連結貸借対照表 2024年3月31日に終了した3か月間に、当社は72,790株の普通株式を購入しました 115,452ドルの費用がかかりました。2024年3月31日現在、当社は合計325,645株の普通株式を買い戻しました 自社株買戻しプログラムに基づくと586,573ドルの費用。
短期投資
私たちの短期投資ポートフォリオは そのみで構成される市場性のある債券の、すべて満期以上の高格付けの米国国債です 3か月未満、1年未満。これらを購入日に販売可能なものとして分類し、その指定を再検討します 各期終了日に。流動性の変化によっては、これらの市場性のある債務証券を、定められた満期前に売却することがあります 要件。これらの負債証券は、未監査の連結貸借対照表では流動資産として分類され、公正時に計上されます 価値、未実現利益または未実現損益を他の包括利益の累積に含め、未監査連結資産の一部とする 包括損失の明細書。利益と損失は実現時に認識されます。利益と損失は特定のIDを使用して決定されます 方法であり、未監査の連結損益計算書に差し引かれたその他の収益(費用)で報告されます。
減損損失は次の場合に認識される場合があります 債務証券の公正価値の下落は、一時的なものではないと判断されています。会社は自社の投資を一時的なもの以外で評価しています 四半期ごと、または事象や状況の変化により原価ベースが示されるたびに、公正価値が原価ベースを下回ります の短期投資は回収できない可能性があります。評価は、期間の長さや、さまざまな要素に基づいています 公正価値が原価基準をどの程度下回っているか、および特に証券に関連する不利な状況、 証券の信用格付けの変更や売却意向、または会社が義務付けられる可能性が高いかどうかなど 償却原価ベースが回収される前に証券を売却すること。
2024年3月31日と2023年12月31日、短期 公正価値での投資は、それぞれ4,075,849ドルと4,140,880ドルでした。
業務結果
終了した3か月間の経営成績の比較 2024年と2023年3月31日です
次の表は、の結果をまとめたものです 2024年3月31日と2023年3月31日に終了する3か月間の事業は、主に未監査の連結財務の比較に基づいていました 特定された期間の明細書、脚注、および関連情報は、連結財務と併せて読む必要があります このレポートの他の部分に含まれている声明とそれらの記述への注記。
| 3月31日に終了した3か月間 | ||||||||
| 2024 | 2023 | |||||||
| 収入 | $ | 18,026 | $ | 18,026 | ||||
| 収益コスト | 1,460 | 1,460 | ||||||
| 売上総利益 | 16,566% | 16,566% | ||||||
| 営業経費 | 896,079 | 820,051 | ||||||
| 事業による損失 | (879,513です | ) | (803,485) | ) | ||||
| その他の収益(費用)、純額 | 77,846 | (102,911) | ) | |||||
| 純損失 | $ | (801,667) | ) | $ | (906,396) | ) | ||
収入
2024年3月31日に終了した3か月間と 2023年、事業からの収益は最小限に抑えられました。2024年および2023年3月31日に終了した3か月間の収益は18,026ドルに達しました とそれぞれ18,026ドルです。このような収益は、合気道ライセンスおよびサブライセンス契約に関連しており、期間中に計上されます 関連するライセンス契約。
収益コスト
2024年3月31日に終了した3か月間と 2023年、収益費用はそれぞれ1,460ドルと1,460ドルで、UMBライセンスとサブライセンスに関連するライセンス料で構成されていました 契約。それぞれの契約条件で収益原価に償却されます。
-26-
営業経費
2024年3月31日に終了した3か月間と 2023年、営業費用の合計は以下のとおりです。
| 3月31日に終了した3か月間、 | ||||||||
| 2024 | 2023 | |||||||
| 報酬費用 | $ | 173,346 | $ | 162,257 | ||||
| 専門家手数料 | 318,427 | 365,270% | ||||||
| 研究開発 | 318,240 | 202,913 | ||||||
| 保険費用 | 21,704 | 24,645 | ||||||
| 販売費、一般管理費 | 64,362 | 64,966% | ||||||
| 合計 | $ | 896,079 | $ | 820,051 | ||||
| ● | 報酬 経費: |
| 2024年3月31日および2023年3月31日に終了した3か月間の報酬費用はそれぞれ173,346ドルと162,257ドルで、11,089ドル、つまり6.8%増加しました。この増加は、給与支払いおよび関連する福利厚生が15,326ドル増加したことによるもので、株式ベースの報酬が4,237ドル減少したことで相殺されました。 |
| ● | 専門家手数料: |
| 2024年3月31日と2023年3月31日に終了した3か月間、専門家報酬は318,427ドルと365,270ドルで、それぞれ46,843ドル、つまり12.8%減少しました。この減少は主に、その他のコンサルティング料が38,819ドル減少したこと、ビジネスアドバイザリーおよび戦略計画サービスのコンサルタントへの以前に発行された株式の前払い費用の償却に関連する株式ベースのコンサルティング料金が33,775ドル減少し、投資家向け広報手数料が2,888ドル減少したことによるもので、弁護士費用の25,908ドルの増加、会計および監査費用の増加によって相殺されました 2,731ドルの。2024年3月31日に終了した3か月間に、コロンビア大学が当社に代わって負担した特許関連の弁護士費用に関連して11,467ドルを払い戻しました。 |
| ● | 研究開発: |
| 2024年3月31日と2023年3月31日に終了した3か月間、研究開発費はそれぞれ318,240ドルと202,913ドルで、115,327ドル、つまり 56.8% 増加しました。この増加は、UCSF、UMB、コロンビア大学、およびその他の関係者との治験責任医師主催の研究契約に関連して、研究開発費が増加した結果です。 |
| ● | 保険費用: |
| 2024年3月31日と2023年3月31日に終了した3か月間、保険費用はそれぞれ21,704ドルと24,645ドルで、2,941ドル、つまり11.9%減少しました。この減少は、D&O保険契約の更新費用が減少した結果です。 |
| ● | 販売費、一般管理費: |
| 販売費、一般管理費には、広告宣伝費、特許関連費用、公開会社経費、保管手数料、銀行サービス料、旅費、その他の事務費が含まれます。 |
| 2024年3月31日と2023年3月31日に終了した3か月間、販売費、一般管理費はそれぞれ64,362ドルと64,966ドルで、604ドル、つまり0.9%減少しました。この減少は主に、ネバダ州での会社の再設立により、デラウェア州のフランチャイズ税が14,967ドル減少したことによるもので、その他の一般管理費の純増14,363ドルによって相殺されました。 |
事業による損失
2024年3月31日に終了した3か月間と 2023年、継続事業からの損失はそれぞれ879,513ドルと803,485ドルで、76,028ドル、つまり9.5%増加しました。増加 主に上記の営業費用の変化の結果でした。
その他の収入(費用)、純額
2024年3月31日に終了した3か月間と 2023年、その他の収益(費用)の純額はそれぞれ77,846ドルと102,911ドルで、180,757ドル、つまり175.6%のプラスの変化でした。ポジティブな その他の収益(費用)、純額の変化は主に、早期に発生した166,034ドルのペナルティ費用の減少によるものです 預金証書の解約、利息および配当収入の23,789ドルの増加、短期純実現利益の増加 234ドルの投資は、外貨取引損失8,695ドルの増加、株式の未実現純利益の減少によって相殺されました 390ドルの投資、および支払利息215ドルの増加。
-27-
純損失
2024年3月31日に終了した3か月間、純額 損失は801,667ドル、普通株式1株あたり0.28ドル(基本および希薄化後)でしたが、純損失は906,396ドル、普通株式1株あたり0.29ドルでした 2023年3月31日に終了した3か月間の(基本および希薄化後)は、104,729ドル、つまり 11.6% 減少しました。この変化は主に 上で説明した変更。
流動性と資本資源
流動性とは、企業が生み出す能力です 必要な現金のニーズを満たすのに十分な金額の現金。私たちの運転資本は6,004,214ドル、短期投資は4,075,849ドルでした。 2024年3月31日現在の現金および現金同等物は2,668,273ドル、短期投資の運転資本は6,905,568ドル、4,140,880ドルです 2023年12月31日現在、現金および現金同等物はそれぞれ3,524,308ドルです。
| 2024年3月31日です | 12月31日 2023 | 働いています 資本 変更します | パーセンテージ 変更します | |||||||||||||
| 運転資本: | ||||||||||||||||
| 流動資産合計 | $ | 6,877,886 | $ | 7,681,158 | $ | (803,272 | ) | (10) | )% | |||||||
| 流動負債合計 | (873,672 | ) | (775,590 | ) | (98,082 | ) | (13) | )% | ||||||||
| 運転資本: | $ | 6,004,214 | $ | 6,905,568 | $ | (901,354) | ) | (13) | )% | |||||||
運転資本の901,354ドルの減少は 主に現金が856,035ドル減少し、短期資産が減少したことによる流動資産が803,272ドル減少したことが主な原因です 65,031ドルの投資、前払い費用およびその他の流動資産の117,794ドルの減少、および流動負債の増加 98,082ドルです。
キャッシュフロー
キャッシュフロー活動の概要は以下の通りです。
3 か月が終了 3 月 31 日 | ||||||||
| 2024 | 2023 | |||||||
| 営業活動に使用された純現金 | $ | (838,179 | ) | $ | (692,688) | ) | ||
| 投資活動によって提供された(使用された)純現金 | 97,596 | ) | (6,008,339) | ) | ||||
| 財務活動に使用された純現金 | (115,452 | ) | - | |||||
| 現金および現金同等物の純減少 | $ | (856,035) | ) | $ | (6,701,027 | ) | ||
営業活動に使用された純現金
の営業活動に使用された純現金 2024年3月31日と2023年3月31日に終了した3か月は、それぞれ838,179ドルと692,688ドルで、145,491ドル、つまり 21% 増加しました。
| ● | 2024年3月31日に終了した3か月間の営業活動に使用された純現金は、主に801,667ドルの純損失を反映しています。これは、234ドルの短期投資による純実現利益などの非現金項目と、主に前払費用およびその他の流動資産の116,334ドルの増加、買掛金および未払費用の98,0ドルの増加からなる営業資産および負債の変動を加算したものです。そして繰延収益は18,026ドルの減少です。 |
| ● | 2023年3月31日に終了した3か月間の営業活動に使用された純現金は、主に906,396ドルの純損失を反映しています。これは、株式投資の未実現純利益390ドル、株式ベースの報酬4,237ドル、前払いの株式ベースの専門家報酬の償却、33,775ドルの前払いの株式ベースの専門職報酬の償却、および主に営業資産と負債の増加からなる変動などの非現金項目の加算を調整したものです前払費用およびその他の流動資産が100,769ドル、受取利息が1,183ドルの増加、買掛金と未収金の増加経費は296,064ドルで、繰延収益は18,026ドル減少しました。 |
-28-
投資活動によって提供された(使用された)純現金
投資活動によって提供された(使用された)純現金 2024年3月31日と2023年3月31日に終了した3か月間は、それぞれ97,596ドルと(6,008,339ドル)で、6,105,935ドル、つまり102%の変化でした。
| ● | 2024年3月31日に終了した3か月間の投資活動によって提供された純現金は97,596ドルで、これは150,389ドルの短期投資の売却による収益でしたが、52,793ドルの短期投資の購入による支払いの総額によって相殺されました。 |
| ● | 2023年3月31日に終了した3か月間の投資活動に使用された純現金は6,008,339ドルで、これは短期投資の購入に対する支払いの合計です。 |
財務活動に使用された純現金
の財務活動に使用された純現金 2024年3月31日に終了した3か月間は115,452ドルでしたが、これは当社の株式に基づく当社の普通株式の買戻しのみでした 買戻し計画。2023年3月31日に終了した3か月間、財務活動によって提供または使用された現金はありませんでした。
現金要件
私たちは、現在の現金と現金同等物を信じています 金額と短期投資額により、最低12か月間、当社の債務を履行するために必要な十分な現金が得られます この申告の日付。
調査に基づく現金要件以外 と開発契約。現在、資本支出に関するその他の重要な約束はありません。
流動性
添付の連結会計に反映されているとおり 財務諸表によると、3月に終了した3か月間の純損失は801,667ドル、使用済み現金は838,179ドルでした 31、2024年。さらに、2024年3月31日の累積赤字は11,673,478ドルです。2024年3月31日現在、運転資金はあります 6,004,214ドルの。
プラスの運転資金は軽減に役立ちます 歴史的に、私たちが継続企業として存続できるかどうかについて大きな疑問を投げかけていた状況。私たちは、同社を信じます この申告日から最低12か月間、債務を履行するのに十分な現金があります。
リスクと不確実性
2022年8月16日、インフレ削減法が成立しました 2022年(「IR法」)が連邦法に署名されました。IR法は、とりわけ、米国連邦政府による新しい1%の物品税を規定しています 上場している米国国内企業および上場企業の特定の米国国内子会社による特定の株式の買い戻しに対する税金 2023年1月1日以降に設立された外国企業。物品税は、買戻し法人に課せられるのであって、その法人自体に課されるのではありません 株式の買い戻し元となる株主。物品税の額は通常、買い戻した株式の公正市場価値の1%です 買い戻しの時。ただし、物品税を計算する目的で、買い戻し法人は税金を差し引くことができます 特定の新規株式発行の公正市場価格と、同じ課税年度中の自社株買いの公正市場価値との比較。さらに、 物品税には特定の例外が適用されます。米国財務省(「財務省」)に権限が与えられました 消費税の乱用や回避を実施および防止するための規制やその他のガイダンスを提供します。
オフバランスシートアレンジメント
[なし]。
重要な会計上の見積もり
株式ベースの報酬
株式ベースの報酬は、株式ベースで会計処理されます ASC 718の「報酬 — 株式報酬」の要件については、財務上の認識が必要です 株式証書の授与と引き換えに受け取った従業員、取締役、および非従業員サービスの費用の明細書 従業員、取締役、または非従業員は、報酬(おそらく権利確定)と引き換えに役務を遂行する必要があります ピリオド)。ASCでは、アワードと引き換えに受け取った従業員、取締役、および非従業員サービスの費用の測定も義務付けています アワードの付与日の公正価値に基づいています。当社は、没収が会計で認められている範囲で発生した場合、それを認めることを選択しました 標準更新(「ASU」)2016-09年従業員の株式ベースの支払いの改善。
研究開発
ASC 730-10に従って、 「研究 と開発全体、」 研究開発費は発生時に支出されます。
-29-
アイテム 3.量的および質的開示 市場リスクについて
私たちは情報を提供する必要はありません 当社は、取引法の規則12b-2で定義されている「小規模な報告会社」であるため、この項目で義務付けられています。
アイテム 4.統制と手続き
開示管理と手続きの評価
私たちは開示管理と手続きを維持しています 証券取引所に提出される定期報告書で重要な情報を確実に開示するように設計されています 改正された1934年の法律、または1934年法は、SECで指定された期間内に記録、処理、要約、報告されます 規則やフォーム、そしてそのような情報が蓄積され、最高経営責任者を含む経営陣に確実に伝達されるようにする そして、必要に応じて最高財務責任者を務め、必要な開示に関してタイムリーな決定を下せるようにします。で評価を行いました 最高執行責任者や最高財務責任者を含む経営陣の監督と参加を得て (最高財務責任者)は、定義されている当社の開示管理と手続きの設計と運用の有効性について 1934年法の規則13 (a) -15 (e) で、このレポートの対象期間の終了時点のものです。この評価に基づいています、会社のせいで 限られたリソースと限られた従業員数で、経営陣は、私たちの開示管理と手続きは効果がないと結論付けました 2024年3月31日現在です。
に対する当社の内部統制の非効率性 財務報告は、財務報告に関する内部統制で特定した以下の重大な弱点によるものでした。
| ● | 人材の雇用を支える財源が限られているため、経理職務における職務の分離が欠けています。そして。 | |
| ● | 適切なシステム制御と手動制御を実装していません。 |
私たちがスタッフを増やして以下を含めるまでは 経理担当者が増えたら、財務報告に関する内部統制の重大な弱点を引き続き報告する可能性があります。
重大な弱点とは、欠陥またはその組み合わせです 財務報告に関する内部統制における統制上の欠陥について、重大な虚偽表示の可能性が十分にある の年次財務諸表または中間財務諸表が適時に防止または検出されることはありません。
財務に関する内部統制の変更 報告します
内部統制に変更はありません この四半期報告書の対象期間中に行われた、重大な影響を及ぼした、または合理的に影響を受けた財務報告について 財務報告に対する当社の内部統制に重大な影響を与える可能性があります。
-30-
パート II — その他の情報
アイテム 1.法的手続き
時々、私たちは訴訟の対象となるかもしれません そして、通常の業務過程で生じるクレーム。私たちは現在、重要な法的手続きの当事者ではありません。また、 当社の事業、運営に重大な悪影響を及ぼす可能性があると考えられる、当社に対して係争中または脅迫されている法的手続きを認識している 結果、キャッシュフロー、または財政状態。
アイテム 1A.リスク要因
私たちのビジネスと財務に影響するリスク要因 結果は、12月31日に終了した年度のForm 10-Kの年次報告書のパートI、項目1A「リスク要因」で説明されています。 2023年は、2024年3月25日にSECに提出されたものです(「年次報告書」)。当社のリスク要因に重大な変化はありませんでした 当社の年次報告書で以前に開示されたもの。当社の年次報告書に記載されているリスクを慎重に検討してください。重大なリスクが及ぶ可能性があります 当社の事業、財政状態、または将来の業績に影響を与えます。私たちが直面しているリスクは、年次報告書に記載されているリスクだけではありません。追加です 現在私たちが知らないリスクや不確実性、または現在重要ではないと判断しているリスクや不確実性も、私たちに重大な悪影響を及ぼす可能性があります 事業、財政状態、および/または経営成績。リスクのいずれかが実際に発生した場合は、当社の事業、財務状況、および/または 経営成績は悪影響を受ける可能性があります。
アイテム 2.株式の未登録売却 と収益の使用
[なし]。
発行者による株式の購入
2023年1月26日、当社の取締役会は承認しました 当社の発行済普通株式および発行済普通株式を最大1,000,000ドルまで随時買い戻すための株式買戻し計画です。 2023年12月31日まで実施される予定です。2024年1月9日、当社の取締役会は、以前に発表された株式の延長を承認しました 2024年3月31日と4月まで、最大100万ドルの当社の普通株式の購入を許可する買戻しプログラム 2024年4月4日、株式買戻しプランは2024年4月30日まで延長されました。2023年12月31日に終了した年度中に、252,855株を購入しました 471,121ドルで普通株式を購入しました。これは、添付の未監査連結貸借対照表の自己株式に反映されます。 2024年3月31日に終了した3か月間に、72,790株の普通株式を115,452ドルで購入しました。2024年3月31日現在、 株式買戻しプログラムに従い、合計325,645株の普通株式を総額586,573ドルで買い戻しました。
-31-
以下は当社の普通株式の概要です 2024年3月31日に終了した四半期期間中の買戻し:
| ピリオド | の合計数 株式 購入しました | 平均 支払った価格 一株当たり | 合計 の数 株式 購入しました の一部として 公に 発表されました プログラム | [最大] 番号 (または おおよその値 ドルの価値) 株式の それはかもしれない まだね 購入しました 下に プログラム | ||||||||||||
| 2024年1月1日から2024年1月31日まで | 28,944 | $ | 1.45 | 28,944 | ||||||||||||
| 2024年2月1日から2024年2月29日まで | 21,318 | $ | 1.59 | 21,318 | ||||||||||||
| 2024年3月1日から2024年3月31日まで | 22,528 | $ | 1.79 | 22,528 | ||||||||||||
| 合計 | 72,790 | $ | 1.59 | 72,790 | $ | 413,427 | ||||||||||
4月に 2024年4月4日、サイロファーマ株式会社(以下「当社」)の取締役会は、以前に発表された株式の延長を承認しました 2024年4月30日までに最大100万ドルの当社の普通株式の購入を許可する買戻しプログラム。4月から 2024年1月1日から2024年4月30日まで、当社は30,065株の普通株式を57,661ドル、つまり平均費用1.92ドルで購入しました。
アイテム 3.シニア証券のデフォルト
[なし]。
アイテム 4.鉱山の安全に関する開示
該当しません。
アイテム 5.その他の情報
10b5-1トレーディングプラン
3月31日に終了した会計四半期中に、
2024、第16条の取締役または役員はいません
「ルールなし」の10b5-1取引はありませんでした 取り決め」(取引法の規則S-Kの項目408で定義されているとおり)は、会計年度中に採択、変更、または終了されました 2024年3月31日に終了した四半期に、当社の取締役および第16課役員が出席しました。
アイテム 6.展示品
| 展示品番号 | 展示品の説明 | |
| 31.1* | 2002年のサーベンス・オクスリー法第302条に従って採択された1934年の証券取引法に基づく規則13a-14 (a) および15d-14 (a) に基づく最高経営責任者の認定 | |
| 31.2* | 2002年のサーベンス・オクスリー法第302条に従って採択された1934年の証券取引法に基づく規則13a-14 (a) および15d-14 (a) に基づく最高財務責任者の認定 | |
| 32.1** | 2002年のサーベンス・オクスリー法第906条に基づいて採択された米国法第18条第1350条に基づく最高経営責任者の認定 | |
| 32.2** | 2002年のサーベンス・オクスリー法第906条に基づいて採択された米国法第18条第1350条に基づく最高財務責任者の認定 | |
| 101.インチ* | インライン XBRL インスタンスドキュメント。 | |
| 101.SCH* | インライン XBRL タクソノミー拡張スキーマドキュメント | |
| 101.CAL* | インライン XBRL タクソノミー拡張計算リンクベースドキュメント。 | |
| 101.DEF* | インライン XBRL タクソノミー拡張定義リンクベースドキュメント。 | |
| 101.LAB* | インライン XBRL タクソノミー拡張ラベルリンクベースドキュメント。 | |
| 101.PRE* | インライン XBRL タクソノミー拡張プレゼンテーションリンクベースドキュメント。 | |
| 104* | 表紙インタラクティブデータファイル(インラインXBRLとしてフォーマットされ、別紙101に含まれています)。 |
| * | ここに提出しました。 |
| ** | ここに付属しています。 |
-32-
署名
証券の要件に従って 1934年の取引法により、登録者は、正式に権限を与えられた署名者に、登録者に代わってこの報告書に署名させました。
| サイロファーマ株式会社 | ||
| 日付:2024年5月13日 | 作成者: | /s/ エリック・ワイスブラム |
| 名前: | エリック・ワイスブラム | |
| タイトル: | 会長兼最高経営責任者 (最高執行役員) | |
| 日付:2024年5月13日 | 作成者: | /s/ ダニエル・ライウェック |
| 名前: | ダニエル・ライウェック | |
| タイトル: | 最高財務責任者 (最高財務会計責任者) |
-3-