

ADI-270: 多くの固形および血液学的がんを対象としたアーマードアロジェニック抗CD70 CAR γδ T細胞治療候補 27th ASGCT Annual Meeting 2024Baltimore, MD Shon Green, PhD VP, Nonclinical Development
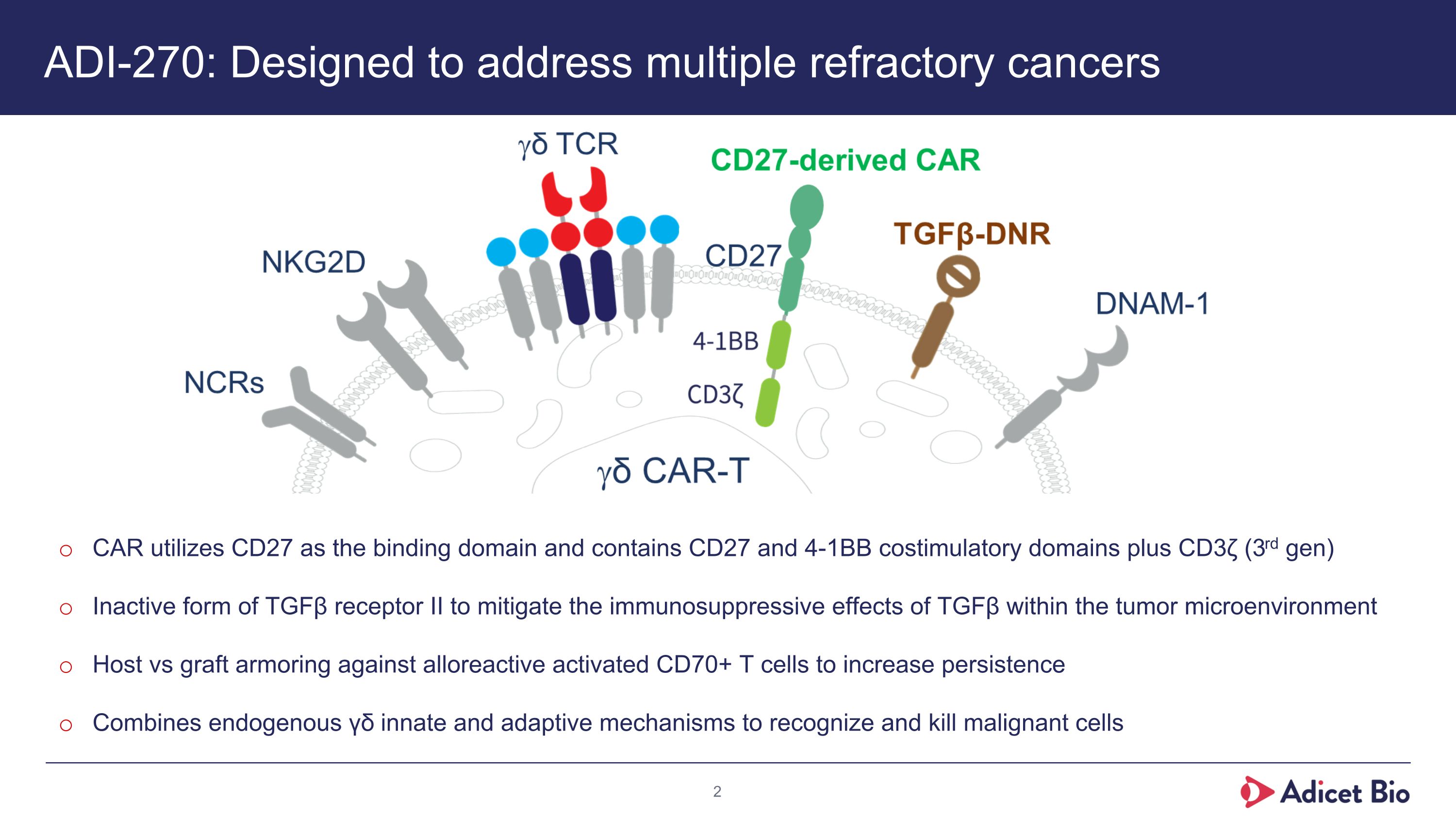
ADI-270:多くの治療抵抗性がんに対応するよう設計されたCARは、CD27を結合ドメインとし、CD27および4-1BBコストバイモチームのドメインに加えて、CD3ζ(3世代)を含め、TGFβの免疫抑制効果を緩和するための非活性TGFβ受容体II 使用する。 その他の免疫抑制効果の軽減のため、移植対宿主兵器は、CD70 + T細胞のアロ反応性活性化に対するものである。内因性γδ特異的な宿主対種の攻撃的な機構と共に、悪性細胞を認識し、殺す。
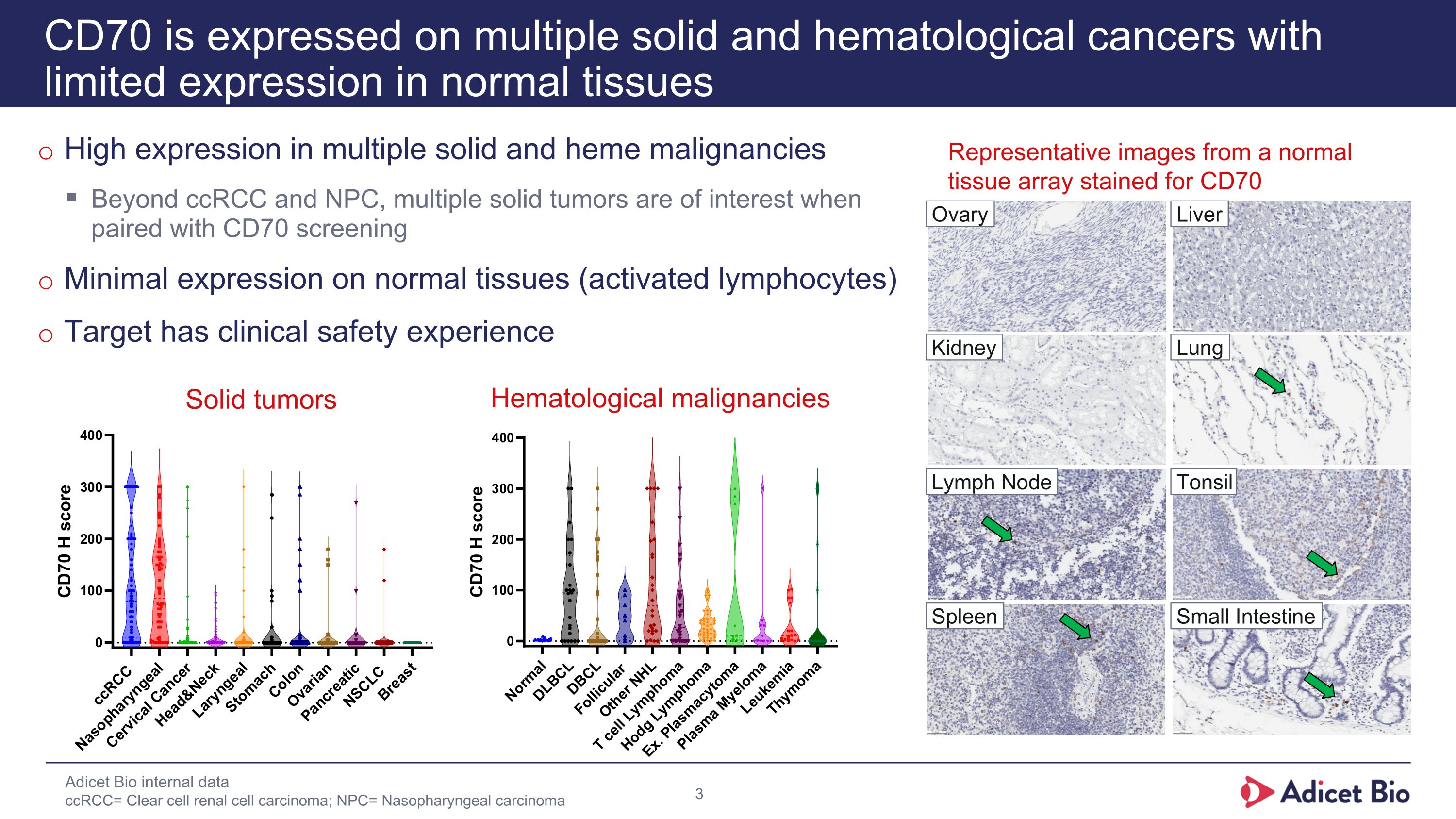
多くの固形および血液系悪性腫瘍で高い発現:CC-RCCとNPC以外にも、CD70スクリーニングとペアリングされると興味がある他の腫瘍がある最小限の正常組織(活性化したリンパ球)での発現を示す。ターゲットは臨床的な安全性の経験がある多くの固形および血液学的がんで発現し、正常組織での発現は限定的である。CD70が染色された正常組織アレイからの代表的な画像 アディセットバイオ内部データ ccRCC =透明細胞型腎細胞癌; NPC =鼻咽頭癌 肺 肝臓 腎 卵巣 リンパ節 扁桃腺 脾臓 小腸 固形腫瘍 血液学的悪性腫瘍
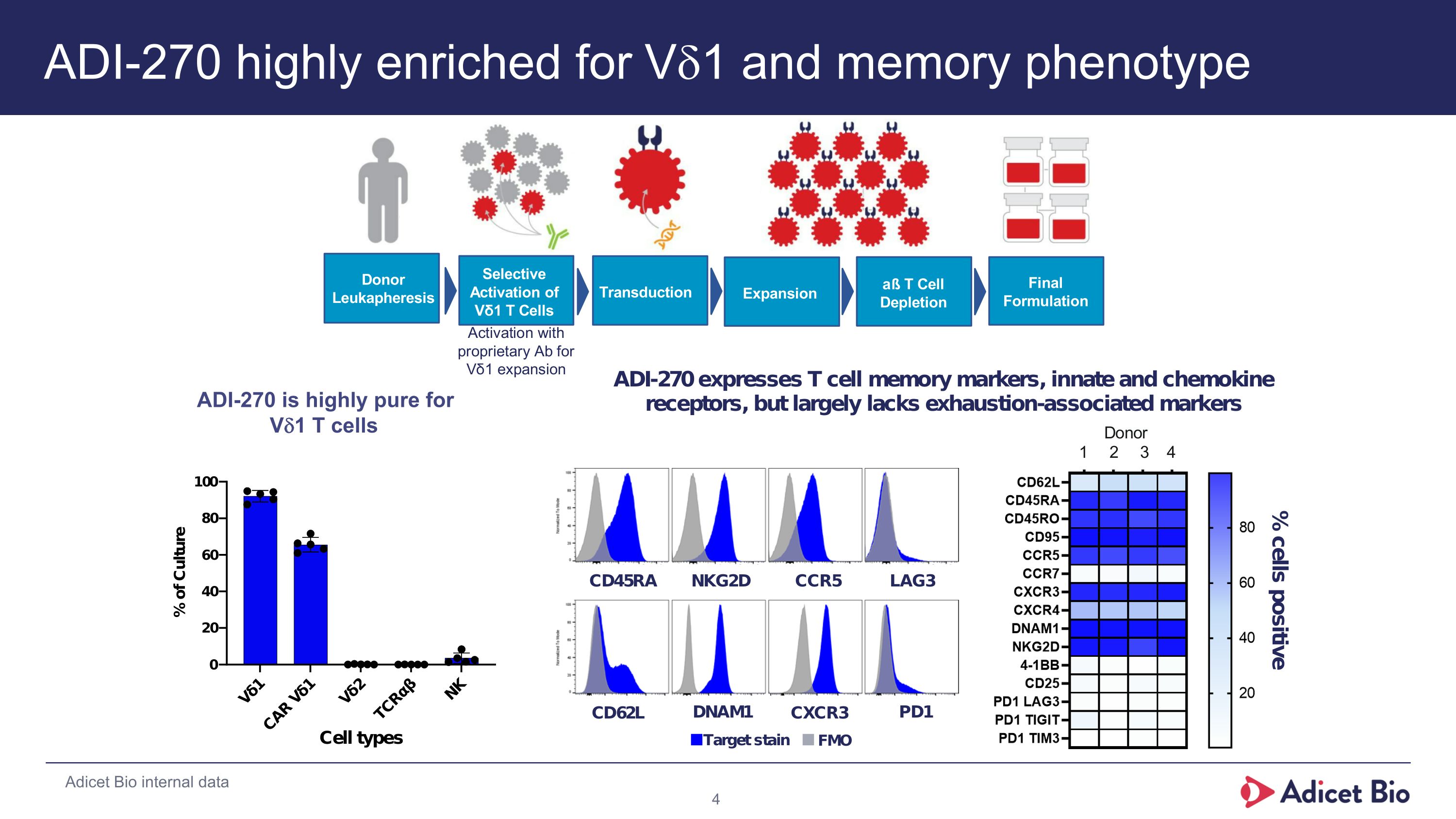
ADI-270はVd1および記憶表現型に高く富む細胞%細胞陽性供与者Leukapheresis Transduction Expansion aßT細胞除去 final formulation 選択的活性化Vδ1 T細胞アディセットバイオ内部データADI-270はVd1 T細胞に非常に純度が高いADI-270はVd1 T細胞に高度に純度が高い
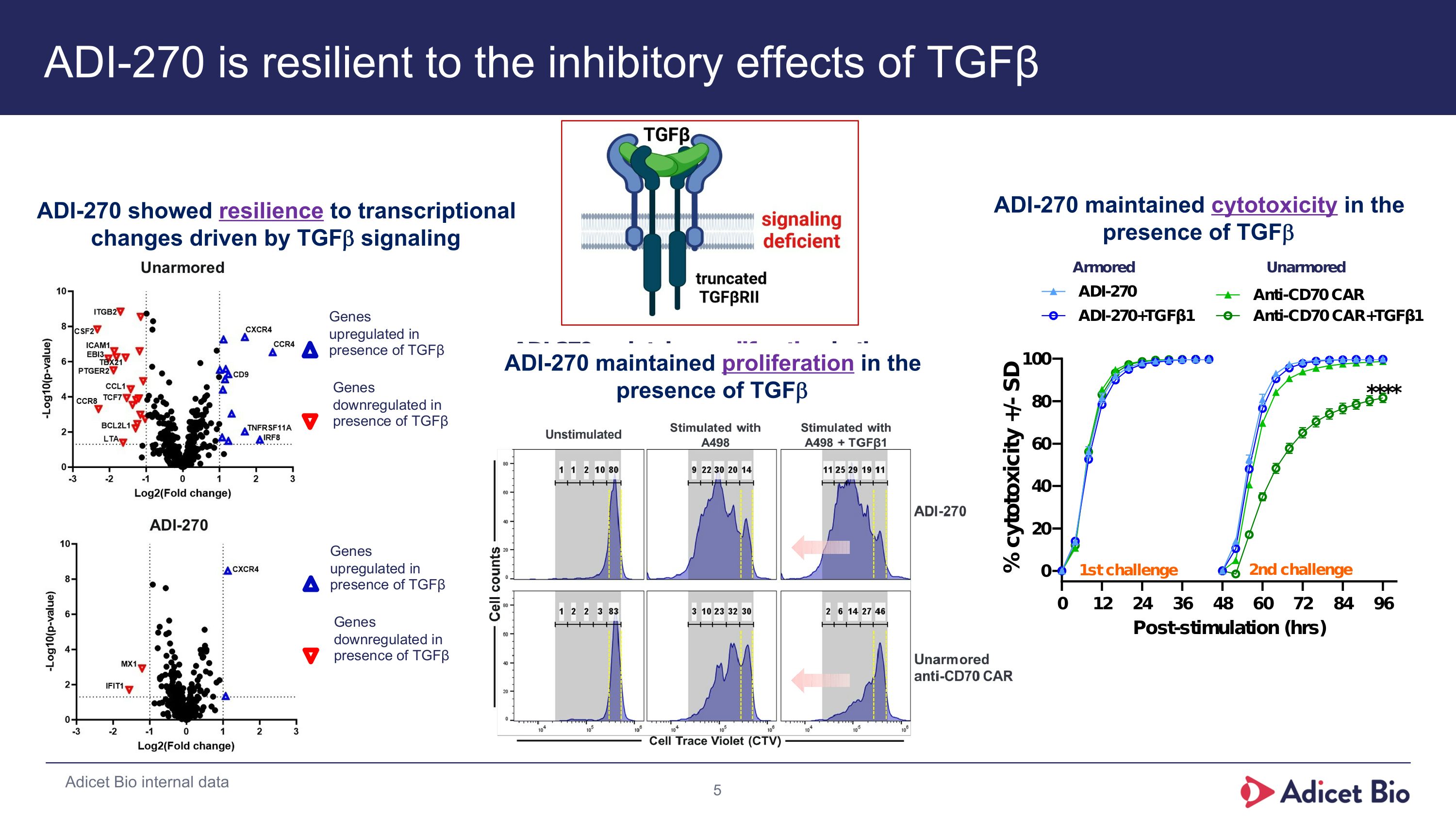
ADI-270は、TGFβの抑制効果に対する強靱な耐性を示した アディセットバイオ内部データADI-270は、TGFbシグナル伝達による転写制御の変化に対して強靭な耐性を示した。ADI-270はTGFbが存在する環境でも増殖を維持した。ADI-270は、TGFbが存在する環境でも細胞毒性を維持した。
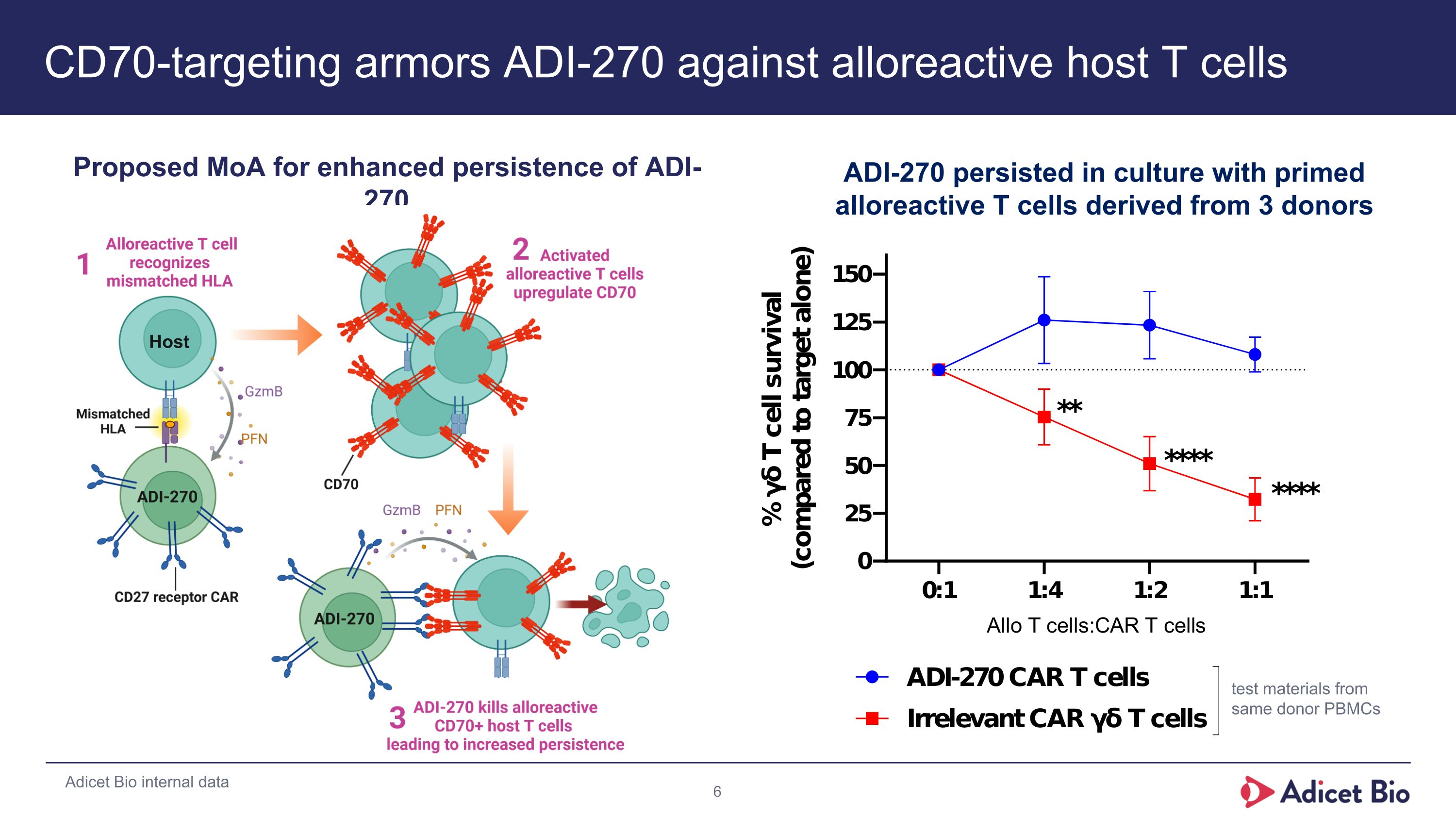
CD70ターゲットアーマーADI-270は、アロ反応性ホストT細胞に対してアーマーをかけたADl-270 ADl-270の増殖を高めたMoA提案内部的なアディセットバイオのテスト材料 、同じ供与者から派生したプライムアロ反応性T細胞と共に培養されたADI-270は、3つのドナーから派生したプライムアロ反応性T細胞と共に培養されたとき、生存し続けた。

ADI-270は、多彩な一連の固形および血液性の悪性腫瘍のCD70レベルに対して、強力なin vitro細胞毒性を示した。アディセットバイオ内部データ CD70 Ag density E:T ratio = 1:1

ADI-270は、臨床的に有用なCD70ターゲットαβ CAR T細胞ベンチマークに比べて、CD70低腫瘍の文脈で強力な活性を維持した アディセットバイオ内部データ

ADI-270は、腫瘍のCD70レベルの幅広い範囲に対して強力なin vitro細胞毒性を示す アディセットバイオ内部データ CAR T細胞Ag活性化A498腫瘍とCD70 KO A498 E:T比= 1:1、N = 2ドナー、****p

ADI-270は、広範なCD70レベルの一連の固形および血液性の悪性腫瘍に対して、臨床的に有用なCD70をターゲットとしたαβ CAR T細胞ベンチマークと比較して、CD70陰性腫瘍細胞に対するより高い内因性細胞溶解活性を示した。***p
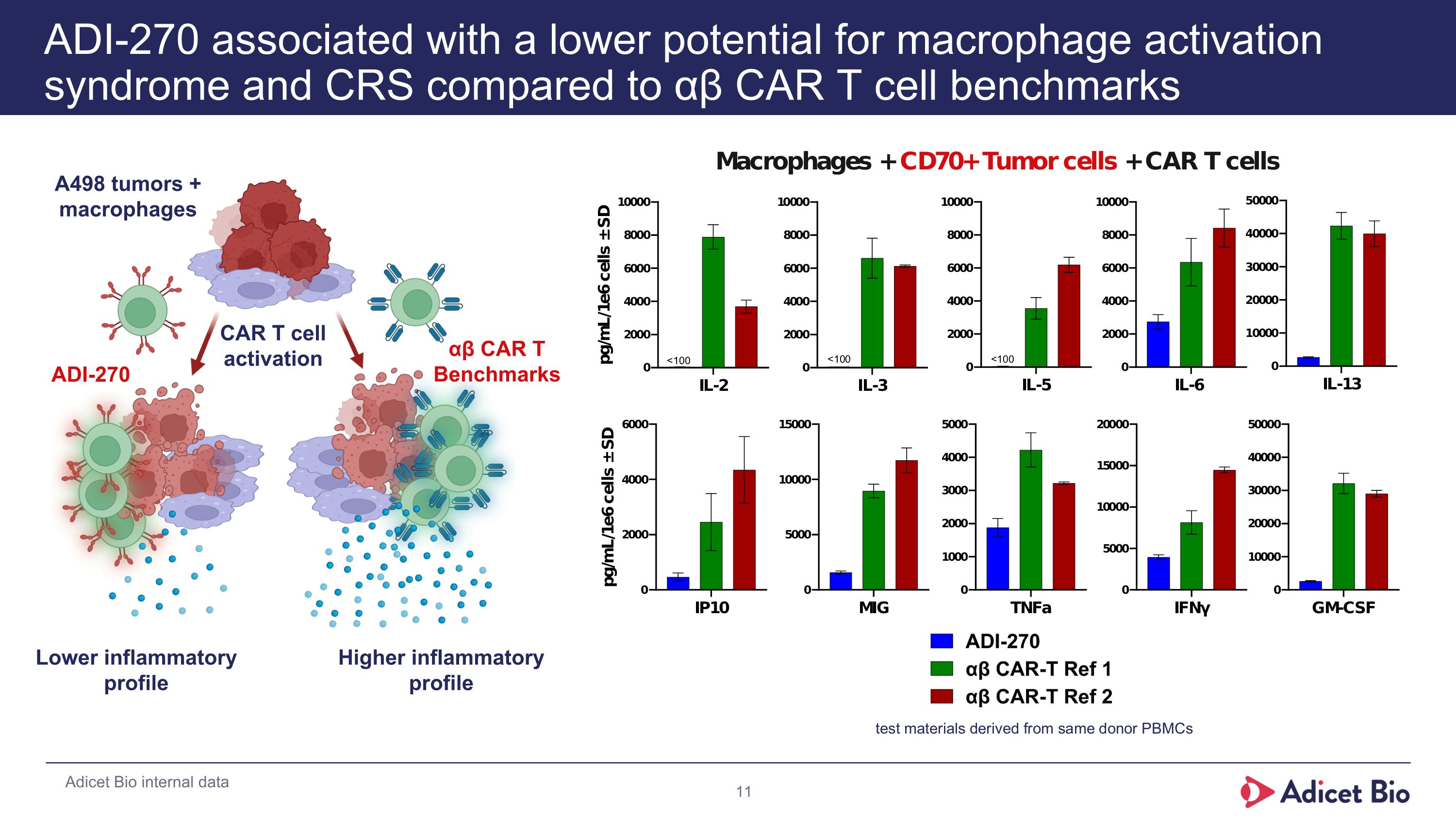
ADI-270は、αβCAR T細胞の基準に比べて、マクロファージ活性化症候群とCRSの発症リスクが低く、炎症プロファイルも低いです。また、ADI-270は、A498の腫瘍とマクロファージにおいても、αβCAR T細胞に比べて低い炎症プロファイルを示すことが内部データで確認されています。ADICETバイオの内部データです。
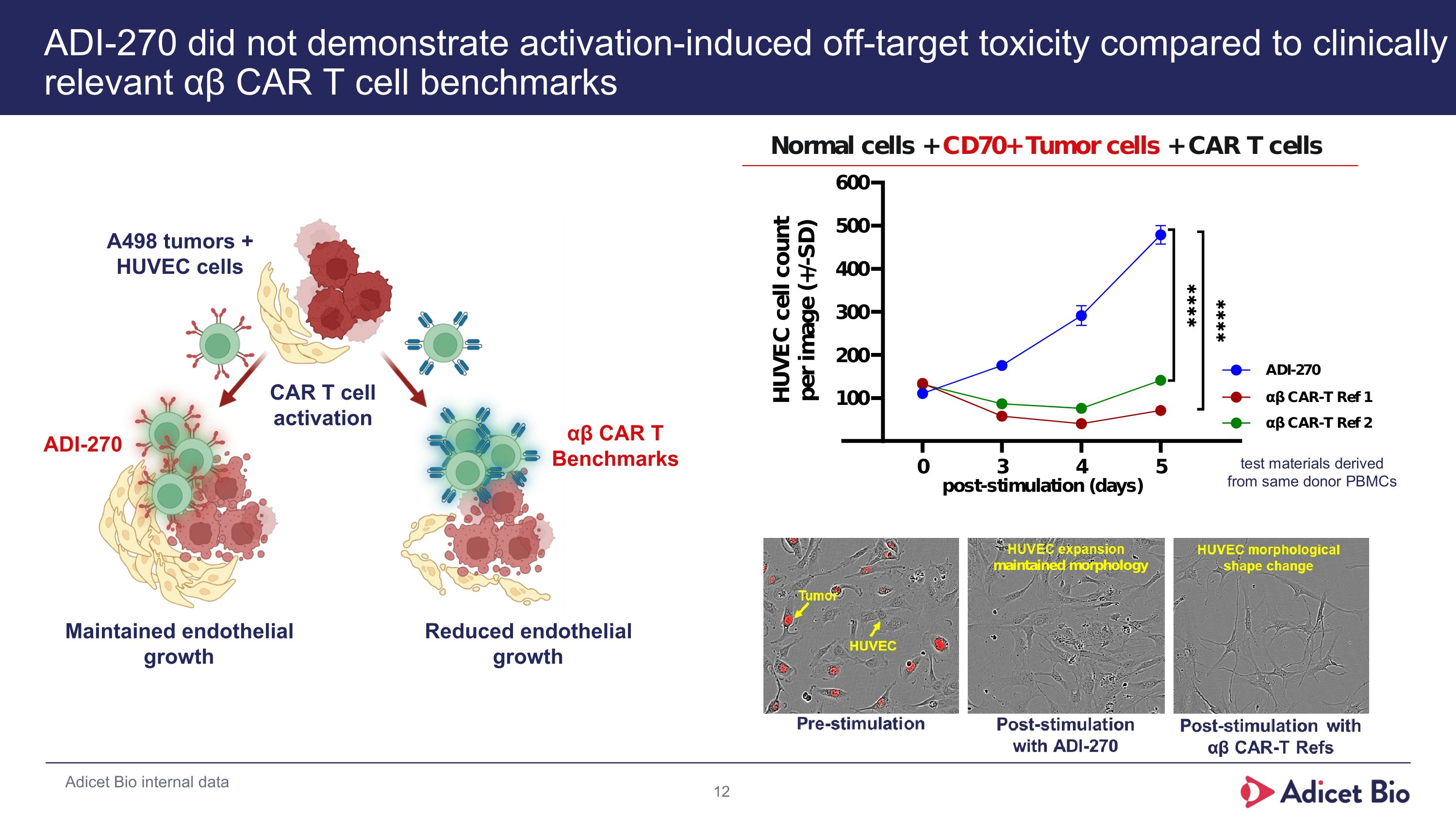
ADI-270は、臨床的に有用なαβCAR T細胞の基準に比べて、活性化誘因のオフターゲット毒性を示さなかったばかりか、血管内皮細胞の成長を維持し、αβCAR T細胞に比べて低い炎症プロファイルを示すことも内部データで確認されています。ADI-270は、A498腫瘍とHUVEC細胞においても、CAR T細胞の活性化に伴う細胞内標的外毒性を示さず、ADICETバイオの内部データに基づきます。

ADI-270を単回投与することで、ccRCC移植モデルにおいて強力な腫瘍の後退と持続的な全身抗腫瘍作用が観察されました。ADI-270(5、10、または15 x 106 I.V.)またはADI-270(5または10 x 106 I.V.)が使用され、小さな腫瘍(約100mm3)および中程度の腫瘍(約500mm3)の両方において、腫瘍体積をモニターしました。腫瘍の体積をモニターしました。ADICETバイオの内部データです。****p
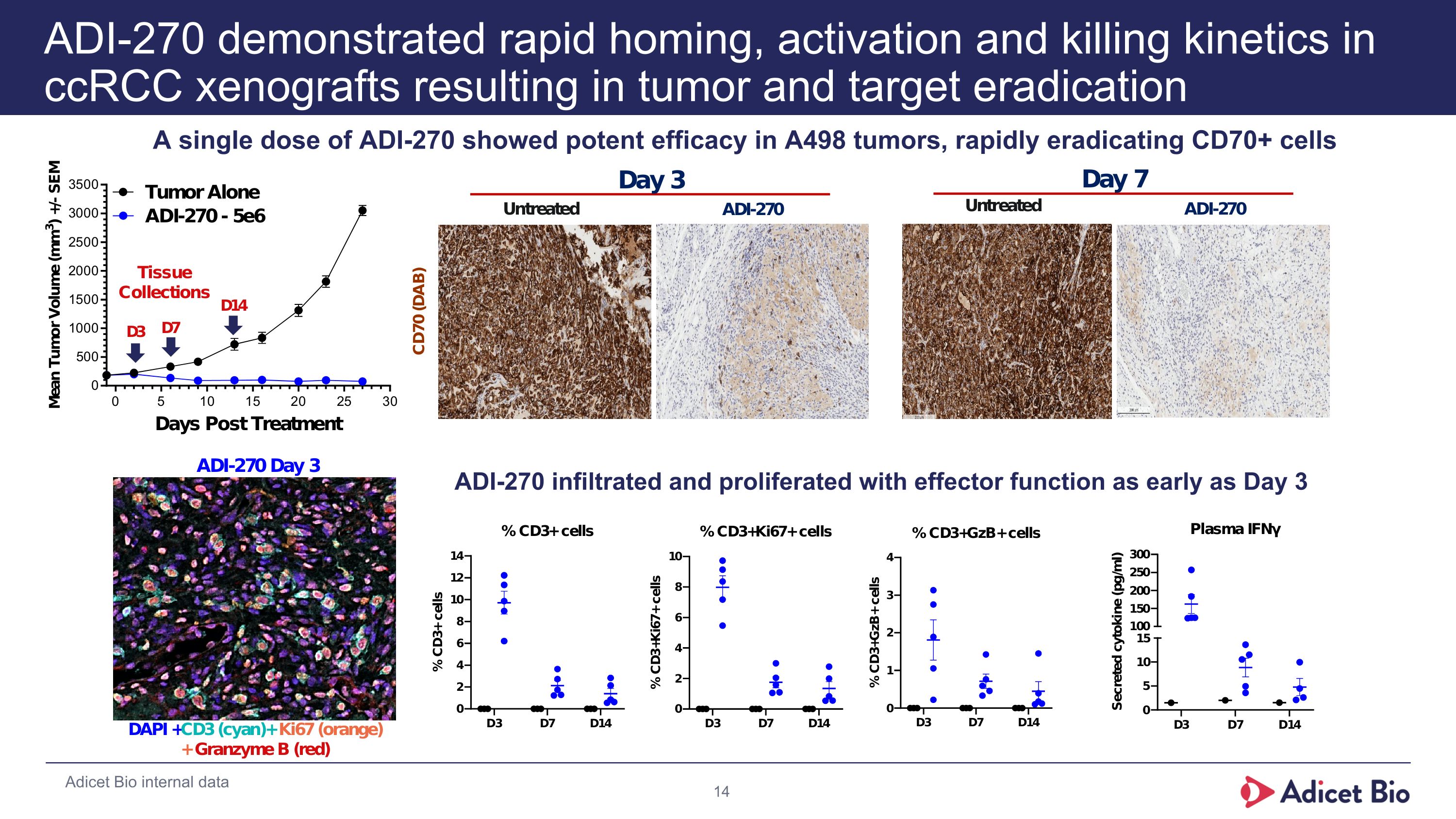
ADI-270は、ccRCC移植モデルにおいて、迅速なホーミング、活性化、殺セル運動学を示し、腫瘍およびターゲットの排除につながりました。Adicet Bioの内部データにより、ADI-270は、CD70 +細胞を迅速に排除し、A498腫瘍で強力な有効性を示し、デイ3以降の初期段階において効率的に浸潤増殖し、殺セル機能を示すことが確認されています。

ADI-270の抗腫瘍作用は、CD70発現の低い複数の造血性腫瘍移植モデルにまで拡大されました。Adicet Bioの内部データにより、NSGマウスにSC腫瘍移植を有するADI-270を単回IV投与することで、維持された強力な有効性が示されました。

次のステップ:ADI-270は、γδCAR T細胞をベースとした治療の進化を可能にするものであり、CD27をターゲットとする第3世代カーの重要性を示す先行研究に基づき、TGFβ、および免疫学的機序に対するアーマリングが事前に確認され、さまざまな厳しさの腫瘍モデルで強力な療法効果を維持し、CRSおよびマクロファージ活性化症候群のリスクが低い安全性プロファイルが望ましいものであることが確認されています。ccRCCへのIND申請は2024年第2四半期に期待されます。Shaffer et al.、Blood 2011年、Acharya et al.、Blood 2023年、Leick et al.、Cancer Cell 2022年、Kasap et al.、BioRxiv 2024年の1,2,3,4を参照してください。