米国
証券取引委員会
ワシントンD.C. 20549
フォーム
(マークワン)
四半期終了時
または
からへの移行期間について
コミッションファイル番号:
(憲章に明記されている登録者の正確な名前)
|
(法人または組織の州またはその他の管轄区域) |
該当なし (IRS雇用者識別番号) |
(主要行政機関の住所) (郵便番号)
(
(登録者の電話番号、市外局番を含む)
同法第12条 (b) に従って登録された証券:
|
各クラスのタイトル |
トレーディングシンボル |
登録された各取引所の名前 |
|
|
|
の |
登録者が(1)1934年の証券取引法のセクション13または15(d)によって提出が義務付けられているすべての報告を過去12か月間(または登録者がそのような報告を提出する必要があったほど短い期間)提出したかどうか、および(2)過去90日間にそのような提出要件の対象であったかどうかをチェックマークで示してください。
登録者が過去 12 か月間(または、登録者がそのようなファイルの提出を求められたほど短い期間)に、規則 S-T の規則 405(本章の §232.405)に従って提出する必要のあるすべてのインタラクティブデータファイルを電子的に提出したかどうかをチェックマークで示してください。
登録者が大規模な加速申告者、加速申告者、非加速申告者、小規模な報告会社、または新興成長企業のいずれであるかをチェックマークで示してください。取引法規則12b-2の「大規模加速申告者」、「加速申告者」、「小規模報告会社」、および「新興成長企業」の定義を参照してください。
|
大型アクセラレーテッドファイラー ☐ |
アクセラレーテッドファイラー ☐ |
|
|
小規模な報告会社 |
| 新興成長企業 |
新興成長企業の場合は、登録者が取引法第13条 (a) に従って規定された新規または改訂された財務会計基準を遵守するために延長された移行期間を使用しないことを選択したかどうかをチェックマークで示してください。☐
登録者がシェル会社(証券取引法の規則12b-2で定義されている)かどうかをチェックマークで示してください。はい
2024年5月3日の時点で、
ダイアメディカ・セラピューティクス株式会社
フォーム 10-Q
2024年3月31日
目次
| 説明 | ページ | |
| 将来の見通しに関する記述に関する注意事項 | 1 | |
| 第一部。 | 財務情報 | |
|
アイテム 1. |
財務諸表 |
3 |
|
アイテム 2. |
経営陣による財政状態と経営成績の議論と分析 |
14 |
|
アイテム 3. |
市場リスクに関する定量的・質的開示 |
20 |
|
アイテム 4. |
統制と手続き |
20 |
| 第二部 | その他の情報 | |
|
アイテム 1. |
法的手続き |
21 |
|
アイテム 1A. |
リスク要因 |
21 |
|
アイテム 2. |
持分証券の未登録売却および収益の使用 |
21 |
|
アイテム 3. |
シニア証券のデフォルト |
21 |
|
アイテム 4. |
鉱山の安全に関する開示 |
21 |
|
アイテム 5. |
その他の情報 |
22 |
|
アイテム 6. |
展示品 |
22 |
| 署名ページ | 23 | |
このフォーム10-Qの四半期報告書には、改正された1933年の米国証券法のセクション27Aおよび改正された1934年の米国証券取引法のセクション21Eの意味の範囲内で、それらのセクションによって作成されたセーフハーバーの対象となる特定の将来の見通しに関する記述が含まれています。詳細については、を参照してください 」将来の見通しに関する記述に関する注意事項。」
このレポートで使われているように、への言及 」ディアメディカ、」 その 」会社、」 」私たち、」 」私たちの」 または 」私たち、」 文脈上別段の定めがない限り、DiaMedica Therapeutics Inc. とその子会社を参照してください。これらはすべてDiamedicaに統合されています'の要約連結財務諸表。このレポートでの参考文献 」普通株式」 私たちの議決権のある普通株式を意味し、1株あたりの額面金額はありません。
私たちは、企業ロゴを含む、さまざまな未登録の商標やサービスマークを所有しています。便宜上、このレポートに記載されている商標と商号は、 ® そして ™ 記号。ただし、そのような言及は、そのような商標や商名の所有者が、適用法に基づく最大限の範囲で、それに対する権利を主張しないことを示すものとして解釈されるべきではありません。私たちは他の会社の使用や表示を意図していません' 他の企業との関係、または他の企業による当社の支持または後援を示唆する商標や商号。
将来の見通しに関する記述に関する注意事項
このレポートに記載されている歴史的事実の記述ではないものは、1995年の米国民間証券訴訟改革法の意味における将来の見通しに関する記述であり、経営陣の現在の期待に基づいており、当社の事業、経営成績、財政状態、見通し、株価に悪影響を及ぼす可能性のあるリスクと不確実性の影響を受けます。私たちは、将来の見通しに関する記述を、「予想する」、「信じる」、「できる」、「できる」、「できる」、「できる」、「見積もり」、「期待」、「意図」、「かもしれない」、「計画」、「可能性」、「予測」、「すべき」、「意志」、「するだろう」、これらの用語または他の同等の用語の否定的表現とその使用法によって特定しようとしました将来の日程。
このレポートの将来の見通しに関する記述は、リスクと不確実性の影響を受けやすく、とりわけ次のものが含まれます。
|
● |
急性虚血性脳卒中(AIS)と心腎疾患(CRD)の治療のためのDM199製品候補を開発、規制当局の承認を得て、商品化する計画です。 |
|
● |
AISまたはCRDのDM199製品候補の臨床試験を成功裏に実施し、当社の臨床研究に関する特定の予定日または目標期日を満たす当社の能力。特に、AISの治療を目的としたDM199の第2/3相Remedy2臨床試験、またはRemedy2試験が含まれます。 |
|
● |
Remedy2試験に関して予想されるサイト活性化、登録、中間分析のタイミングを満たす能力。特に、サイトの活性化と登録が予想よりも遅く、これは病院や医療施設の人員不足によるもの、以前の臨床的に重大な低血圧イベントや2023年6月に解除された臨床保留を取り巻く状況に関する懸念、プロトコルの管理に関する懸念コンプライアンス(退院した参加者のロジスティクスとプロトコルコンプライアンスの管理を含む)病院から別の病院または中間医療施設への移行、研究プロトコルにおける改訂された包含/除外基準、および保留中の他の脳卒中および神経学的試験による研究スタッフと被験者の競争。 |
|
● |
規制当局への申請および関連する申請と承認のスケジュールに関する不確実性、およびRemeDy2試験に関連する、または当社のRemeDy2試験から不利な結果に関連して、将来さらに有害事象が発生する可能性について。 |
|
● |
世界中の最大100施設で約350人の参加者を対象としたRemeDy2試験のアダプティブデザイン。また、米国食品医薬品局(FDA)からの追加インプットや、独立したデータ安全監視委員会によって決定された中間分析の結果など、特定の要因によってこれらの数や研究の他の側面が増加する可能性。 |
|
● |
当社のDM199製品候補が、AISとCRDの既存の治療選択肢よりも優れていると認識されていることについての私たちの期待 |
|
● |
AISとCRD用のDM199製品候補の潜在的な市場規模、それらの市場へのサービス提供能力、および米国および海外でのAISとCRD用のDM199製品候補の市場受け入れ率と程度、および補償と適切な償還を受ける能力。 |
|
● |
AISおよびCRD用のDM199製品候補を開発、規制当局の承認を得て、商品化するために、バイオ医薬品または製薬パートナーと提携し、収益を生み出す当社の能力。 |
|
● |
RemeDy2試験の成功、費用、タイミング、およびRemedy2試験や当社が実施するその他の臨床試験に関連する第三者への依存。 |
|
● |
当社の商業化、マーケティング、製造能力と戦略 |
|
● |
AISおよびCRD用のDM199製品候補に対する潜在的なFDA規制など、連邦、州、および外国の規制要件と開発に関する期待。 |
|
● |
経費、製品候補の市場機会、将来の収益、資本要件、現在の現金資源の存続期間、追加の資金調達の必要性に関する見積もりです。 |
|
● |
DM199製品候補の知的財産保護を取得および維持する能力に関する私たちの期待。 |
|
● |
競争に関する期待と、AISおよびCRD用のDM199製品候補のデータ独占権を獲得する当社の能力。そして |
|
● |
計画された臨床試験を完了し、AISおよびCRD用のDM199製品候補の規制当局の承認を得るために必要な資金を含む、事業のための追加資金を獲得することができます。 |
これらの将来の見通しに関する記述には、以下で説明されているものを含め、多くのリスク、不確実性、仮定の影響を受けます。パートI。アイテム1Aです。リスク要因」2023年12月31日に終了した会計年度のForm 10-Kの年次報告書および上記および本報告書の他の箇所に記載されています。さらに、私たちは非常に競争が激しく、急速に変化する環境で事業を行っています。新しいリスクは時々現れます。当社の経営陣がすべてのリスクを予測することは不可能です。また、すべての要因が当社の事業に与える影響や、何らかの要因や要因の組み合わせにより、実際の結果が当社の将来の見通しに関する記述に含まれるものと大きく異なる可能性がある程度を評価することもできません。これらのリスク、不確実性、仮定に照らして、このレポートで説明されている将来の見通しに関する出来事や状況は発生しない可能性があり、実際の結果は、将来の見通しに関する記述で予想または暗示されているものと大きく異なる可能性があります。将来の見通しに関する記述は、将来の出来事の予測として信頼すべきではありません。将来の見通しに関する記述に反映されている期待は妥当だと考えていますが、将来の見通しに関する記述に反映されている将来の結果、活動レベル、業績、出来事、状況が達成または実現することを保証することはできません。米国の証券法を含む法律で義務付けられている場合を除き、将来の見通しに関する記述を実際の結果や期待の変化に適合させるために将来の見通しに関する記述を更新するつもりはありません。
パート I-財務情報
|
アイテム 1. |
財務諸表 |
ダイアメディカ・セラピューティクス株式会社
要約連結貸借対照表
(千単位、株式金額を除く)
|
2024年3月31日 |
2023年12月31日 |
|||||||
|
(未監査) |
||||||||
|
資産 |
||||||||
|
流動資産: |
||||||||
|
現金および現金同等物 |
$ | $ | ||||||
|
市場性のある証券 |
||||||||
|
前払費用およびその他の資産 |
||||||||
|
売掛金額 |
||||||||
|
流動資産合計 |
||||||||
|
非流動資産: |
||||||||
|
預金 |
||||||||
|
オペレーティングリースの使用権資産、純額 |
||||||||
|
資産および設備、純額 |
||||||||
|
非流動資産合計 |
||||||||
|
総資産 |
$ | $ | ||||||
|
負債と資本 |
||||||||
|
現在の負債: |
||||||||
|
買掛金 |
$ | $ | ||||||
|
未払負債 |
||||||||
|
オペレーティングリース義務 |
||||||||
|
ファイナンスリース義務 |
||||||||
|
流動負債合計 |
||||||||
|
非流動負債: |
||||||||
|
オペレーティングリース義務 |
||||||||
|
ファイナンスリース義務 |
||||||||
|
非流動負債合計 |
||||||||
|
株主資本: |
||||||||
|
普通株式、額面なし、無制限、認可数無制限、 |
— | — | ||||||
|
払込資本金 |
||||||||
|
その他の包括利益 (損失) の累計 |
( |
) | ||||||
|
累積赤字 |
( |
) | ( |
) | ||||
|
株主資本の総額 |
||||||||
|
負債総額と株主資本 |
$ | $ | ||||||
要約連結財務諸表の添付注記を参照してください。
ダイアメディカ・セラピューティクス株式会社
要約連結営業報告書および包括損失計算書
(千単位、1株あたりの金額を除く)
(未監査)
|
3 か月が終了 3 月 31 日 |
||||||||
|
2024 |
2023 |
|||||||
|
営業経費: |
||||||||
|
研究開発 |
$ | $ | ||||||
|
一般と管理 |
||||||||
|
営業費用の合計 |
( |
) |
( |
) |
||||
|
営業損失 |
( |
) | ( |
) | ||||
|
その他の収益、純額 |
||||||||
|
所得税費用控除前損失 |
( |
) | ( |
) | ||||
|
所得税費用 |
( |
) |
( |
) |
||||
|
純損失 |
( |
) |
( |
) |
||||
|
その他の包括利益 (損失) |
||||||||
|
有価証券の含み損益 (損失) |
( |
) |
||||||
|
純損失と包括損失 |
$ | ( |
) |
$ | ( |
) |
||
|
基本および希薄化後の1株当たり純損失 |
$ | ( |
) |
$ | ( |
) |
||
|
加重平均発行済株式数 — 基本株式と希薄化後株式 |
||||||||
要約連結財務諸表の添付注記を参照してください。
ダイアメディカ・セラピューティクス株式会社
要約連結株主資本計算書
2024年および2023年3月31日に終了した3か月間
(千単位、株式金額を除く)
(未監査)
|
共通 株式 |
支払い済み 資本 |
累積 その他 包括的 収益 (損失) |
累積 赤字 |
合計 株主の エクイティ |
||||||||||||||||
|
2023年12月31日現在の残高 |
$ | $ | $ | ( |
) | $ | ||||||||||||||
|
制限付株式ユニットの権利確定および決済時の普通株式の発行 |
||||||||||||||||||||
|
株式ベースの報酬費用 |
— | — | — | |||||||||||||||||
|
有価証券の含み損失 |
— | — | ( |
) | — | ( |
) | |||||||||||||
|
純損失 |
— | — | — | ( |
) | ( |
) | |||||||||||||
|
2024年3月31日現在の残高 |
$ | $ | ( |
) | $ | ( |
) | $ | ||||||||||||
|
共通 株式 |
支払い済み 資本 |
累積 その他 包括的 収益 (損失) |
累積 赤字 |
合計 株主の エクイティ |
||||||||||||||||
|
2022年12月31日現在の残高 |
$ | $ | ( |
) | $ | ( |
) | $ | ||||||||||||
|
繰延株式ユニットの決済における普通株式の発行 |
— | — | — | — | ||||||||||||||||
|
制限付株式ユニットの権利確定および決済時の普通株式の発行 |
||||||||||||||||||||
|
株式ベースの報酬費用 |
— | |||||||||||||||||||
|
有価証券の含み益について |
— | |||||||||||||||||||
|
純損失 |
— | ( |
) | ( |
) | |||||||||||||||
|
2023年3月31日時点の残高 |
$ | $ | ( |
) | $ | ( |
) | $ | ||||||||||||
要約連結財務諸表の添付注記を参照してください。
ダイアメディカ・セラピューティクス株式会社
要約連結キャッシュフロー計算書
(千単位)
(未監査)
|
3月31日に終了した3か月間 |
||||||||
|
2024 |
2023 |
|||||||
|
営業活動によるキャッシュフロー: |
||||||||
|
純損失 |
$ | ( |
) |
$ | ( |
) |
||
|
純損失を営業活動に使用された純現金と調整するための調整: |
||||||||
|
株式ベースの報酬 |
||||||||
|
有価証券の割引償却 |
( |
) |
( |
) | ||||
|
非現金リース費用 |
||||||||
|
減価償却 |
||||||||
|
営業資産および負債の変動: |
||||||||
|
売掛金額 |
( |
) |
||||||
|
前払費用およびその他の資産 |
( |
) |
( |
) |
||||
|
預金 |
( |
) | ||||||
|
買掛金 |
( |
) | ||||||
|
未払負債 |
( |
) | ||||||
|
営業活動に使用された純現金 |
( |
) |
( |
) |
||||
|
投資活動によるキャッシュフロー: |
||||||||
|
有価証券の購入 |
( |
) |
( |
) |
||||
|
有価証券の満期 |
||||||||
|
資産および設備の購入 |
( |
) |
( |
) |
||||
|
投資活動によって提供される純現金 |
||||||||
|
財務活動によるキャッシュフロー: |
||||||||
|
ファイナンスリース債務の元本支払い |
( |
) |
( |
) |
||||
|
財務活動に使用された純現金 |
( |
) | ( |
) | ||||
|
現金および現金同等物の純減少 |
( |
) |
( |
) |
||||
|
現金および現金同等物の期首残高 |
||||||||
|
現金および現金同等物の期末残高 |
$ | $ | ||||||
|
非現金取引の補足開示: |
||||||||
|
所得税として支払われた現金 |
$ | $ | ||||||
要約連結財務諸表の添付注記を参照してください。
ダイアメディカ・セラピューティクス株式会社 要約連結財務諸表の注記
(未監査)
|
1. |
ビジネス |
DiaMedica Therapeutics Inc. とその完全子会社であるDiamedica USA Inc.およびDiamedica Australia Pty Ltd.(総称して、私たち、当社、DiaMedicaおよび当社)は、神経疾患および心腎疾患の治療のためのDM199と呼ばれる当社独自の組換えKLK1タンパク質の臨床的および商業的開発を進めることを主な目的としています。現在、私たちの主な焦点は、急性虚血性脳卒中(AIS)と心臓腎疾患(CRD)の治療のためのヒト組織カリクレイン-1(KLK1)タンパク質の組換え型であるDM199の開発です。当社の親会社はブリティッシュコロンビア州の事業会社法に基づいて管理されており、当社の普通株式はナスダック・キャピタル・マーケットで「DMAC」のシンボルで上場されています。
|
2. |
リスクと不確実性 |
DiaMedicaは厳しく規制された競争の激しい環境で運営されています。医薬品の開発、製造、マーケティングには、米国の米国食品医薬品局(FDA)、欧州連合の欧州医薬品庁(EMA)、およびその他の国の同等の機関の承認が必要であり、継続的な監督の対象となります。私たちは、AISとCRDの治療のための最初の製品候補であるDM199の開発の臨床段階にあります。私たちは製品候補の開発を完了しておらず、どの製品候補の商業販売からも収益を上げていません。DM199は、市販承認を求める前に多額の追加臨床試験と投資を必要とし、もしあったとしても、少なくとも3年間は市販されない見込みです。
2022年7月に発表され、2023年6月に解除されたRemeDy2試験の臨床保留前は、サイトの活性化とRemedy2試験への登録が予想よりも遅かったことがありましたが、現在も続いています。これらの状況は、病院や医療施設の人員不足、以前の臨床的に重大な低血圧イベントや前回の臨床保留を取り巻く状況に関する懸念、病院から別の病院または中間医療施設に退院する参加者のロジスティクスとプロトコルコンプライアンスの管理を含むプロトコルコンプライアンスの管理に関する懸念、研究プロトコルへの改訂された包含/除外基準、および保留中の他の脳卒中による研究スタッフと被験者をめぐる競争が原因であると考えています。神経学試験。これらの要因の影響を軽減するために、私たちは試験をグローバルに拡大することを決定しました。現在、規制当局への提出を準備し、カナダ、オーストラリア、英国、ヨーロッパの治験実施地を特定して関与させています。私たちは受託研究機関と緊密に協力して、必要に応じて米国および世界の研究施設と潜在的な参加者を支援するための手順を開発しています。私たちはこれらの取り組みの結果を引き続き監視し、必要に応じて、これらの要因がRemeDy2試験に与える影響を軽減するために追加の措置を講じるつもりです。ただし、これらの問題が解決するかどうか、いつ解決するかについては保証できません。これらの問題を解決しないと、RemeDy2のトライアルが遅れます。
私たちの将来の成功は、開発努力の成功、米国または他の市場でDM199製品候補の臨床的進歩を示す能力、製品候補の必要な政府承認を取得する当社または将来のパートナーの能力、DM199製品候補のライセンスまたはマーケティングおよび販売能力、およびこれらの取り組みの資金を調達するための追加資金を獲得できるかどうかにかかっています。
2024年3月31日現在、私たちはドルの損失を被っています
私たちの主な資金源は、株式の発行による純収入です。私たちは以前、株式の募集を通じて資金調達に成功してきましたが、将来それが可能になるという保証はありません。これは、当社の臨床データが肯定的でない場合や、経済や市場の状況が悪化した場合に特に当てはまります。
研究開発活動をさらに進め、当社の製品候補であるDM199または将来の製品候補について、必要な臨床研究、規制活動、製造開発を完了し、ライセンスまたは商業的に販売できるようになるには、多額の追加資本が必要になると予想しています。現在の現金、現金同等物、および有価証券は、これらの要約連結財務諸表の発行日から少なくとも今後12か月間は、RemeDy2の試験を継続し、それ以外の場合は計画事業に資金を提供するのに十分であると予想しています。将来の資金調達要件の金額とタイミングは、現在のRemedy2試験を含む継続的な開発努力のタイミングと結果、サイトの活性化率と研究への参加者の登録率、現在の開発プログラムの拡大の可能性、潜在的な新しい開発プログラム、継続的な施設人員不足の影響、臨床試験と運営費に対するその他の要因など、多くの要因に左右されます。現在の予想よりも早く多額の追加資金が必要になる可能性があり、特に資金調達の市場状況が好調であれば、その前に追加の資金を必要としない、または求めることがないという保証はありません。
|
3。 |
重要な会計方針の要約 |
中間財務諸表
中間財務情報として米国で一般に認められている会計原則(米国会計基準)と、証券取引委員会(SEC)のフォーム10-Qおよび規則S-Xの指示に従って、添付の要約連結財務諸表を作成しました。したがって、これらには、米国会計基準で完全な財務諸表に必要なすべての情報や脚注が含まれているわけではありません。これらの要約連結財務諸表には、表示されている期間および日付における当社の要約連結財政状態、要約連結経営成績、要約連結株主資本計算書、および要約連結キャッシュフローを公正に表示するために必要な、通常の定期発生額からなるすべての調整が反映されています。当社の会計年度は12月31日に終了します。2023年12月31日現在の要約連結貸借対照表は、当社の監査済み連結財務諸表から導き出されました。これらの要約連結財務諸表は、当社の年次連結財務諸表とその注記と併せて読む必要があります。当社の事業の性質上、どの中間期間の業績も、年間を通じて期待される業績を示すものではない場合があります。
現金および現金同等物
当社は、当初の満期が3か月以内に購入された、マネーマーケットファンドやその他の投資を含め、すべての銀行預金を、現金および現金同等物と見なします。当社の現金同等物の帳簿価額は、投資の満期が短いため、公正価値に近似しています。
市場性のある証券
会社の有価証券には、米国政府およびその機関の債務、銀行預金証書および/または投資適格社債が含まれる場合があり、これらは売却可能として分類されます。購入日から12か月以内に満期を迎える有価証券は流動資産に含まれます。有価証券は通常、第三者の認定価格ソースを使用して類似資産の市場価格に基づいて評価され、公正価値で保有されます。有価証券の償却費用は、保険料の償却または満期までの割引額の増加に合わせて調整されます。このような償却または増額は利息収入に含まれます。実現損益がある場合は、特定の識別方法で計算されます。利息収入は、要約連結損益計算書のその他の収益に含まれています。
私たちは定期的に見直しを行い、一時的減損以外の減損が存在するかどうかを判断するために、未実現損失のポジションにある売却可能な各債務証券を特定して評価します。未実現損失は、個々の証券の現在の公正価値がその償却原価基準を下回っている場合に発生します。発行体の非信用関連要因による一時的なものと考えられる公正価値の下落は、株主資本とは別の構成要素であるその他の包括損失の累計に記録されます。一時的なもの以外、または発行体の信用関連の要因によって引き起こされた公正価値の下落は、減損損失として収益に記録されます。2024年3月31日現在、一時的な含み損失以外はありませんでした。
公正価値の測定
公正価値測定のための権威あるガイダンスでは、公正価値とは終了価格、つまり測定日時点で市場参加者間の秩序ある取引において資産を売却するために受け取る金額、または負債を譲渡するために支払われる金額と定義されています。権威あるガイダンスでは、公正価値の測定に使用されるインプットの階層も確立しています。これにより、観察可能なインプットを最大限に活用し、可能な場合は最も観察可能なインプットを使用することを義務付けることで、観察不可能なインプットの使用を最小限に抑えます。観察可能なインプットとは、市場参加者が会社とは独立した情報源から入手した市場データに基づいて作成された資産または負債を評価する際に使用するインプットです。観察不可能なインプットとは、市場参加者がその状況で入手可能な最良の情報に基づいて作成された資産または負債を評価する際に使用する要素に関する当社の仮定を反映したインプットです。評価階層における金融資産と金融負債の分類は、公正価値の測定にとって重要な最低レベルのインプットに基づいています。
階層は次の3つのレベルに分かれています。
レベル1の入力 — 同一の資産と負債の活発な市場における相場価格
レベル2の入力 — 同一の資産と負債の活発な市場における相場価格以外の観察可能なインプット
レベル3の入力 — 観察できない入力
2024年3月31日現在、当社は、売掛金、買掛金、未払負債を含むその他の金融商品の帳簿価額は、これらの商品の短期満期による公正価値に近いと考えています。「」というタイトルの注記4を参照してください市場性のある証券追加情報については、」を参照してください。
|
4。 |
市場性のある証券 |
売却可能な有価証券は、主にコマーシャル・ペーパー、社債、政府証券への投資で構成されており、定期的に公正価値で測定されるものは次のとおりです(千単位)。
|
以下のように考慮されたインプットを使用した公正価値の測定: |
||||||||||||||||||||||||||||||||
| 2024年3月31日 |
2023年12月31日 |
|||||||||||||||||||||||||||||||
|
合計 |
レベル 1 |
レベル 2 |
レベル 3 |
合計 |
レベル 1 |
レベル 2 |
レベル 3 |
|||||||||||||||||||||||||
|
コマーシャルペーパーと社債 |
$ | $ | $ | $ | $ | $ | $ | $ | ||||||||||||||||||||||||
|
政府証券 |
||||||||||||||||||||||||||||||||
|
合計 |
$ | $ | $ | $ | $ | $ | $ | $ | ||||||||||||||||||||||||
個々の有価証券の満期は1年未満で、すべての有価証券の償却費は2024年3月31日および2023年12月31日現在の公正価値に近いものです。有価証券の未収利息は売掛金に含まれ、金額は$でした
2024年3月31日に終了した3か月間、公正価値測定階層のレベル1とレベル2の間で資産の移転はありませんでした。
|
5。 |
売掛金額 |
売掛金の金額は、主に$の有価証券の未収利息でした
|
6。 |
預金 |
私たちは定期的に、臨床試験および関連活動の実施を支援するために従事しているベンダーに資金を前払いしています。前払いされた資金は、さまざまな期間無利子で保有され、通常、最終的な研究/プロジェクトの請求書に対する申請を通じて会社によって回収されるか、提供されるサービスの完了時に返金されます。今後12か月以内に回収が見込まれない場合、預金は流動しません。
|
7。 |
資産と設備 |
資産と設備は次のもので構成されていました(単位:千):
|
2024年3月31日 |
2023年12月31日 |
|||||||
|
家具と備品 |
$ | $ | ||||||
|
コンピューター機器 |
||||||||
|
借地権の改善 |
||||||||
|
減価償却累計額が少ない |
( |
) | ( |
) | ||||
|
資産および設備、純額 |
$ | $ | ||||||
|
8。 |
未払負債 |
未払負債は以下のとおりです(千単位)。
|
2024年3月31日 |
2023年12月31日 |
|||||||
|
臨床試験費用 |
$ | $ | ||||||
|
研究開発サービス |
||||||||
|
補償 |
||||||||
|
専門サービス料 |
||||||||
|
その他 |
||||||||
|
未払負債合計 |
$ | $ | ||||||
|
9。 |
オペレーティングリース |
オフィスリース
私たちのオペレーティングリースの費用は $でした
2024年3月31日現在のオペレーティングリース債務の満期は次のとおりです(千単位)。
|
2024 |
$ | |||
|
2025 |
||||
|
2026 |
||||
|
2027 |
||||
|
2028 |
||||
|
リース料総額 |
$ | |||
|
利息の少ない部分 |
( |
) | ||
|
オペレーティングリース債務の現在価値 |
$ |
|
10。 |
株主資本 |
授権資本株式
DiaMedicaは、無制限の議決権付き普通株式の授権株式資本を付与していますが、株式の額面金額は記載されていません。普通株主は、会社が申告した配当金があれば、それを受け取る権利があり、会社の年次総会、臨時株主総会、臨時株主総会または特別総会で1株あたり1票の議決権があります。
2024年3月31日に終了した3か月間に発行された株式
2024年3月31日に終了した3か月間は、
2023年3月31日に終了した3か月間に発行された株式
2023年3月31日に終了した3か月間は、
予約済み株式
将来の発行のために留保されている普通株式は次のとおりです。
|
2024年3月31日 |
||||
|
従業員および非従業員ストックオプションの行使時に発行可能な普通株式 |
||||
|
繰延株式ユニットの決済時に発行可能な普通株式 |
||||
|
制限付株式ユニットの権利確定および決済時に発行可能な普通株式 |
||||
|
修正および改訂された2019年オムニバスインセンティブプランに基づいて付与可能な株式 |
||||
|
2021年雇用誘致インセンティブプランに基づいて付与可能な株式 |
||||
|
合計 |
||||
|
11。 |
一株当たり純損失 |
1株当たりの純損失は、純損失(分子)をその期間の発行済み普通株式の加重平均数(分母)で割って計算します。その期間中に発行された株式、およびその期間中に再取得した株式(ある場合)は、発行された期間の分だけ加重されます。希薄化後の1株当たり利益(EPS)の計算は、基本的なEPSの計算と似ていますが、希薄化後の潜在的な普通株式が発行された場合に発行されていたであろう追加の普通株式の数を含むように分母が増える点が異なります。当社の希薄化後のEPSは、希薄化防止効果があるため、普通同等株式が計算から除外されている点が基本EPSと同じです。
次の表は、提示された期間の普通株式1株あたりの純損失(千単位、1株あたりのデータを除く)の計算をまとめたものです。
|
3 か月が終了 3 月 31 日 |
||||||||
|
2024 |
2023 |
|||||||
|
純損失 |
$ | ( |
) |
$ | ( |
) |
||
|
加重平均発行済株式数—基本株と希薄化後株式 |
||||||||
|
基本および希薄化後の1株当たり純損失 |
$ | ( |
) |
$ | ( |
) |
||
以下の発行済み潜在普通株式は、その影響が希薄化作用ではなかったため、希薄化後の1株当たり純損失の計算には含まれていませんでした。
|
3 か月が終了 3 月 31 日 |
||||||||
|
2024 |
2023 |
|||||||
|
従業員と非従業員のストックオプション |
||||||||
|
普通株式購入新株予約権に基づいて発行可能な普通株式 |
||||||||
|
繰延株式単位で発行可能な普通株式 |
||||||||
|
制限付株式ユニットの権利確定および決済時に発行可能な普通株式 |
||||||||
|
12。 |
株式ベースの報酬 |
2019年オムニバスインセンティブプランが修正され、改訂されました
DiaMedica Therapeutics Inc.の修正および改訂された2019年オムニバスインセンティブプラン(2019年プラン)は、2022年3月10日に取締役会(取締役会)で採択され、2022年5月18日に開催された2022年定時株主総会で株主によって承認されました。
2019年プランでは、取締役会、またはその委員会または小委員会が、会社の適格従業員、非従業員取締役、および特定のコンサルタントに、非法定およびインセンティブのストックオプション、株式評価権、制限付株式報酬、制限付株式ユニット(RSU)、繰延株式ユニット(DSU)、業績賞、非従業員取締役賞、その他の株式ベースの賞を付与することができます。2019年プランに基づき、付与日現在の原株の公正市場価値以上で普通株式を購入するオプションを付与します。従業員および非従業員取締役に付与されるオプションの有効期間は最長10年で、通常1〜4年に渡って権利が確定します。非従業員に付与されるオプションの有効期間は最長5年で、通常は1年間にわたって権利が確定します。2019年計画に規定されているように調整される場合がありますが、2019年計画に基づいて発行が承認された当社の普通株式の最大数は
2021年雇用誘致インセンティブプラン
2021年12月3日、取締役会はDiamedica Therapeutics Inc. 2021雇用誘致インセンティブプラン(インセンティブプラン)を採択しました。これは、入社する新入社員への誘因となる株式報奨の付与を促進するためです。インセンティブ・プランは、ナスダック上場規則5635 (c) (4) に従って株主の承認なしに採択され、取締役会の報酬委員会によって管理されています。ボードは予約済みです
以前のストックオプションプラン
2018年11月6日に修正および改訂されたDiaMedica Therapeutics Inc.のストックオプションプラン(以前のプラン)は、2019年プランの株主承認に伴い、取締役会により終了されました。以前のプランで未払いのアワードは、その条件に従って未払いのままになります。以前のプランで付与されたオプションには、2019年プランで使用されていたものと同様の条件があります。2024年3月31日現在、購入できるオプションの合計は
以前の繰延株式ユニットプラン
Diamedica Therapeutics Inc.の修正および改訂された繰延株式ユニットプラン(以前のDSUプラン)は、2019年プランの株主承認に伴い、取締役会によって終了されました。以前のDSUプランで未払いのアワードは、その条件に従って未払いのままです。2024年3月31日現在、
表示されている各期間の株式ベースの報酬費用は次のとおりです(千単位)。
|
3 か月が終了 3 月 31 日 |
||||||||
|
2024 |
2023 |
|||||||
|
研究開発 |
$ | $ | ||||||
|
一般と管理 |
||||||||
|
株式ベースの報酬総額 |
$ | $ | ||||||
株式ベースの報酬は、Black-Scholesオプション評価モデルを使用して推定された各アワードの公正価値に基づいて評価されます。最終的に、権利確定期間中に計上される実際の費用は、実際に権利が権利が確定した株式のみになります。
オプションアクティビティの概要は次のとおりです(1株と1株あたりの金額を除く千単位)。
|
株式 基になる [オプション] |
加重 平均的なエクササイズ 一株当たりの価格 |
集計 本質的価値 |
||||||||||
|
2023年12月31日現在の残高 |
$ | $ | ||||||||||
|
付与されました |
||||||||||||
|
期限切れ/キャンセルされました |
||||||||||||
|
没収 |
( |
) | ||||||||||
|
2024年3月31日現在の残高 |
$ | $ | ||||||||||
2024年3月31日現在の発行済ストックオプション、権利確定済みストックオプション、権利確定予定のストックオプションに関する情報は次のとおりです。
|
優良品、既得品、権利確定見込み |
権利が確定していて行使可能なオプション |
|||||||||||||||||||||
|
一株当たりの行動 価格 |
株式 |
加重平均 残り 契約生活 (年) |
加重平均 行使価格 |
[オプション] 運動可能 |
加重平均 残り 契約生活 (年) |
|||||||||||||||||
| $ |
- |
$ |
$ | |||||||||||||||||||
| $ |
- |
$ |
||||||||||||||||||||
| $ |
- |
$ |
||||||||||||||||||||
| $ |
- |
$ |
||||||||||||||||||||
| $ |
- |
$ |
||||||||||||||||||||
| $ | ||||||||||||||||||||||
アイテム 2.経営陣による財政状態と経営成績の議論と分析
以下の経営陣による財政状態と経営成績に関する議論と分析は、米国で一般に認められている会計原則に基づいており、2024年および2023年3月31日に終了した3か月間のDiamedica Therapeutics Inc. とその子会社の財政状態と経営成績について説明しています。
この議論は、このレポートの他の部分に含まれる要約連結財務諸表と関連注記、および2023年12月31日に終了した年度のForm 10-Kの年次報告書と併せて読む必要があります。次の議論には、多くのリスクと不確実性を伴う将来の見通しに関する記述が含まれています。これらのリスクと不確実性の結果として、実際の結果は将来の見通しに関する記述とは大きく異なる可能性があります。見る」将来の見通しに関する記述に関する注意事項」その他の注意事項については。
事業概要
私たちは臨床段階のバイオ医薬品会社で、重篤な病気に苦しむ人々の生活を改善することに尽力しています。私たちの有力候補であるDM199(リンベカリナーゼアルファ)は、患者を対象に臨床研究された最初のヒト組織カリクレイン-1(KLK1)タンパク質の薬学的に活性な組換え(合成)型です。KLK1はアジアで確立された治療法で、急性虚血性脳卒中(AIS)の治療にはヒトの尿中KLK1、高血圧を含む心腎疾患(CRD)の治療にはブタのKLK1があります。また、現在、前臨床開発の初期段階にある重度の炎症性疾患に対する潜在的な新しい治療法、DM300も製造しました。私たちの長期的な目標は、特許取得済みでライセンス取得済みの技術を使用して、新しい組換えタンパク質からの治療法の開発と商業化におけるリーダーとしての会社を確立することです。私たちの現在の焦点は、AISとCRDの治療です。私たちは、DM199をAISとCRDの治療薬としての臨床的および商業的可能性を確立することで株主価値を創造するために、必要な臨床試験を通じてDM199を前進させる予定です。
KLK1は、主に腎臓、膵臓、唾液腺で産生されるセリンプロテアーゼ(タンパク質)で、体内の局所的な血流と血管拡張(血管の拡張により血管抵抗が減少する)の調節に重要な役割を果たすだけでなく、炎症や酸化ストレス(潜在的に有害な活性酸素、またはフリーラジカンの間の不均衡)の軽減にも重要な役割を果たします体内の抗酸化物質と抗酸化物質)。DM199は、健康な機能がKLK1とそのシステムであるカリクレイン-キニン系(KKS)の十分な活動を必要とするさまざまな病気の治療に役立つと考えています。
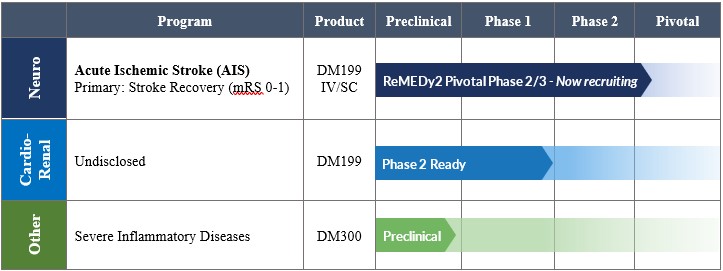
私たちの製品開発パイプラインは以下の通りです:

AISフェーズ 2/3 レメディ2 トライアル
私たちは現在、AISの治療を目的としたDM199のRemeDy2臨床試験を実施しています。私たちのReMedy2臨床試験は、世界中の最大100か所の約350人の患者を登録することを目的とした、フェーズ2/3、アダプティブデザイン、ランダム化、二重盲検、プラセボ対照試験です。試験に登録された患者は、AISの症状が現れてから24時間以内にDM199またはプラセボのいずれかで治療されます。この試験には、血栓を溶かすことを目的とした血栓溶解剤である組織プラスミノーゲン活性化因子(tPA)で治療された患者、および大きな血管閉塞のある患者は除外されます。研究対象集団は、主にtPAや機械的血栓摘出術による治療の制限により、現在治療法の選択肢がないAIS患者の約80%を代表しています。RemeDy2試験の主要評価項目は、定評のある修正ランキンスケール(MRS)で90日目に測定された脳卒中からの身体的回復です。具体的には、MRSスコアは0〜1(MRsの範囲は0〜6)まで回復します。私たちのReMedy2試験は、このような患者集団におけるDM199の登録研究の中心的な役割を果たす可能性があると考えています。
2022年7月に発表され、2023年6月に解除されたRemeDy2試験の臨床保留前は、サイトの活性化とRemedy2試験への登録が予想よりも遅かったことがありましたが、現在も続いています。これらの状況は、病院や医療施設の人員不足、以前の臨床的に重大な低血圧イベントや前回の臨床保留を取り巻く状況に関する懸念、病院から別の病院または中間医療施設に退院する参加者のロジスティクスとプロトコルコンプライアンスの管理を含むプロトコルコンプライアンスの管理に関する懸念、研究プロトコルへの改訂された包含/除外基準、および保留中の他の脳卒中による研究スタッフと被験者をめぐる競争が原因であると考えています。神経学試験。これらの要因の影響を軽減するために、私たちは試験をグローバルに拡大することを決定しました。現在、規制当局への提出を準備し、カナダ、オーストラリア、英国、ヨーロッパの治験実施地を特定して関与させています。私たちは受託研究機関と緊密に協力して、必要に応じて米国および世界の研究施設と潜在的な参加者を支援するための手順を開発しています。私たちはこれらの取り組みの結果を引き続き監視し、必要に応じて、これらの要因がRemeDy2試験に与える影響を軽減するために追加の措置を講じるつもりです。ただし、これらの問題が解決するかどうか、いつ解決するかについては保証できません。これらの問題を解決しないと、RemeDy2のトライアルが遅れます。
カーディオ・レンアル・プログラム
現在、2024年後半に心臓腎プログラムの計画を開示する予定です。
財務概要
私たちは製品販売から何の収益も生み出していません。創業以来、株式の公的および私的売却、新株予約権とストックオプションの行使、投資に利用できる資金の利息収入、および政府の助成金から事業の資金を調達してきました。私たちは創業以来、毎年損失を被っています。2024年3月31日および2023年3月31日に終了した3か月間の当社の純損失は、それぞれ520万ドルと530万ドルでした。2024年3月31日現在、当社の累積赤字は1億2,070万ドルでした。当社の営業損失のほとんどすべてが、製品候補開発プログラム、研究開発(R&D)活動、および当社の事業と上場企業としての地位に関連する一般管理(G&A)サポート費用に関連して発生した費用によるものです。
少なくとも今後数年間は、多額の出費と営業損失の増加が続くと予想しています。RemeDy2トライアルをグローバルに拡大し、登録者数が増えるにつれて、四半期ごとの費用は、最近の前期と比較して増加すると予想しています。私たちの運営をサポートするためにチームを拡大し、知的財産ポートフォリオを維持、拡大、保護しようとする私たちの努力も、このような増加の一因となる可能性があります。
グローバル展開を含め、Remedy2の試験を再開するにつれて、1か月あたりの将来のマイナスキャッシュフロー率は一般的に最近の前期と比較して増加すると予想していますが、現在の現金資源は、このレポートに含まれる要約連結財務諸表の発行日から少なくとも今後12か月間は、Remedy2の試験を継続し、計画された事業に資金を提供するのに十分であると予想しています。ただし、将来の資金調達要件の金額とタイミングは、継続的な開発努力のタイミングと結果、RemeDy2トライアルの世界的拡大、特にサイトのアクティベーションと登録率など、多くの要因に左右されます。サイトの活性化率と参加者の登録率は、一部には、サイトの人員不足と、他の脳卒中や神経学試験による研究スタッフの競争に左右されます。現在および新規の開発プログラムの拡大の可能性、そのような活動に関連して発生する運営費などの他の要因も、将来の資金調達要件の金額と時期の変動の一因となる可能性があります。現在の予想よりも早く、多額の追加資金が必要になったり、求められたりする可能性があります。追加資金を調達する市場の状況が好調であれば、必要になる前に追加の資金を調達することを選択することがあります。
当社の経営成績の構成要素
研究開発費用
研究開発費には、受託研究機関を含む外部のサービスプロバイダーに支払われる料金、臨床サポートサービス、臨床現場費用を含む臨床開発、外部の看護サービス、臨床検査など、人体臨床試験の実施にかかる費用が含まれます。研究開発費には、非臨床研究、DM199および関連する製造プロセスの開発のために受託製造開発組織および外部研究所に支払われる手数料、臨床研究に使用するのに十分な量のDM199化合物を製造するための費用、DM199製品候補の開発計画の実行に関連する専門知識を持つコンサルティングリソース、および給与、福利厚生、株式ベースの報酬を含む人件費も含まれます。
現時点では、臨床開発プロセスと製品開発プログラムの臨床段階に内在するリスクのため、市販承認または前臨床開発プログラムを通じてDM199を開発する際に発生する費用を確実に見積もることはできません。規制当局の承認を得るために必要な臨床研究を実施し、開発の拡大と将来の商業化の可能性をサポートするために製造のスケールアップを行うプロセスは、費用と時間がかかります。私たちが失敗したり、臨床研究の完了、製造のスケールアップ、規制当局の承認の取得が遅れたりすると、研究開発費が増加し、ひいては当社の業績に重大な悪影響を及ぼす可能性があります。
DM199または当社の前臨床プログラムのいずれかを臨床開発に必要な段階に進めることに成功した場合、当社の研究開発費は将来、最近の前期と比較して増加すると予想しています。規制当局の承認を得るために必要な臨床試験を実施し、開発の拡大と将来の商業化の可能性をサポートするための製造のスケールアップには、費用と時間がかかります。
一般管理費
G&A費用は、主に給与、従業員福利厚生、株式ベースの報酬、および役員、財務、事業開発、サポート機能に関連するその他の人件費で構成されています。G&A費用には、取締役および役員の賠償責任保険を含む保険、家賃と光熱費、旅費、特許費用、監査、税務、法務サービスを含む専門家費用も含まれます。
その他の利益、純額
その他の収益、純利益は、主に有価証券から得られる利息収入です。
業務結果
2024年3月31日と2023年3月31日に終了した3か月間の比較
次の表は、2024年3月31日および2023年3月31日に終了した3か月間の未監査の経営成績(千単位)をまとめたものです。
|
3月31日に終了した3か月間 |
||||||||
|
2024 |
2023 |
|||||||
|
研究開発費用 |
$ | 3,676 | $ | 3,618 | ||||
|
一般管理費 |
2,065 | 1,903 | ||||||
|
その他の収益、純額 |
(597) | ) | (256) | ) | ||||
研究開発費用
研究開発費は、2023年3月31日に終了した3か月間の360万ドルに対し、2024年3月31日に終了した3か月間で370万ドルに増加しました。この増加は、多くの相殺要因の影響を受けました。ReMedy2臨床試験の継続に関連する費用の増加は、2023年に完了した臨床試験作業、フェーズ1CおよびREDUX試験、およびRemedy2試験の臨床保留に対処するために実施された使用中の研究作業が2023年に完了したことに関連するコスト削減によって部分的に相殺されました。Remedy2トライアルをグローバルに拡大し、サイトのアクティベーションと参加者の登録が続くにつれて、研究開発費は最近の前期と比較して緩やかに増加すると予想しています。これらの予想される増加は、2023年に完了した臨床試験作業と現在実施中の研究によって緩和されると予想しています。
一般管理費
一般管理費は、2023年3月31日に終了した3か月間の190万ドルから、2024年3月31日に終了した3か月間で20万ドル増加して210万ドルになりました。この増加は主に、チームの拡大に伴う人件費の増加によるもので、取締役および役員賠償責任保険料の費用の削減によって一部相殺されました。一般管理費は、前期と比較して安定していると予想しています。
その他の利益、純額
2024年3月31日に終了した3か月間のその他の収益は、5億97,000ドルでした。これに対し、2023年3月31日に終了した3か月間の純利益は256,000ドルでした。この増加は、当年度中の有価証券残高が前年同期と比較して増加したことに関連して、2024年3月31日に終了した3か月間に認識された利息収入の増加によるものです。
流動性と資本資源
次の表は、2024年3月31日および2023年12月31日現在の当社の流動性と資本資源、および2024年3月31日および2023年3月31日に終了した3か月間のキャッシュフローをまとめたもので、以下のより詳細な説明(千単位)を補足することを目的としています。
|
2024年3月31日 |
2023年12月31日 |
|||||||
|
現金、現金同等物および有価証券 |
$ | 46,516 | $ | 52,895 | ||||
|
総資産 |
49,260% | 54,160 | ||||||
|
流動負債合計 |
2,617 | 2,786 | ||||||
|
株主資本の総額 |
46,349% | 51,057 | ||||||
|
運転資本 |
44,867 | 50,889 | ||||||
|
3月31日に終了した3か月間 |
||||||||
|
|
2024 |
2023 |
||||||
| キャッシュフローデータ | ||||||||
|
によって提供される(使われる)キャッシュフロー: |
||||||||
|
営業活動 |
$ | (6,653) | ) | $ | (5,089 | ) | ||
|
投資活動 |
4,208 | 2,509 | ||||||
|
資金調達活動 |
(1) | ) | (1) | ) | ||||
|
現金の純減少 |
$ | (2,446) | ) | $ | (2,581) | ) | ||
ワーキングキャピタル
2024年3月31日現在の現金、現金同等物および有価証券の総額は4,650万ドル、流動負債は260万ドル、運転資本は4,490万ドルでしたが、2023年12月31日現在の現金、現金同等物および有価証券の総額は5,290万ドル、流動負債は280万ドル、運転資本は5,090万ドルでした。当社の現金、現金同等物、有価証券の合計、および運転資本の減少は、主に現在の事業の資金調達に使用された純現金によるものです。
キャッシュフロー
営業活動
2024年3月31日に終了した3か月間の営業活動に使用された純現金は、2023年3月31日に終了した3か月間の510万ドルに対し、670万ドルでした。営業活動に使用される現金の増加は、主に当年度中にRemeDy2臨床試験を支援するベンダーに資金を前払いしたことによるものです。
投資活動
投資活動は、主に有価証券の購入と満期で構成されます。2024年3月31日と2023年3月31日に終了した3か月間の投資活動によって提供された純現金は、それぞれ420万ドルと250万ドルでした。この変化は主に、満期と有価証券への投資のタイミングによるものです。
資金調達活動
2024年3月31日および2023年3月31日に終了した3か月間の財務活動に使用された純現金は、各期間のファイナンスリース債務の元本支払いで構成されていました。
資本要件
創業以来、DM199製品候補の研究開発を進めている間に損失を被りました。私たちは製品販売から何の収益も生み出しておらず、少なくとも3、4年はそうなるとは考えていません。DM199製品候補または将来の製品候補の製品販売またはアウトライセンスからいつ、または収益を生み出すかどうかはわかりません。必要な規制当局の承認を得ない限り、製品の販売から収益が得られるとは考えていません。将来の製品販売、ライセンス料、マイルストーンの支払い、および/またはロイヤルティの支払いが、当社の継続事業に必要な収益を生み出すのに十分になるまで、引き続き多額の営業損失が発生すると予想しています。特にRemedy2試験の継続と世界展開を含め、DM199製品候補の研究、開発、臨床研究を継続し、規制当局の承認を求めるにつれて、営業損失は前期と比較して増加すると予想しています。長期的には、DM199製品候補または将来の製品候補の規制当局の承認を得て、戦略的パートナーの支援がなければ、製品の販売、マーケティング、製造、流通に多額の商品化費用が発生すると予想されます。
したがって、研究開発活動、現在および予想される将来の臨床研究、規制活動を促進し、その他の方法で製品候補であるDM199または将来の製品候補を開発して、製品候補がライセンス切れになったり、商業的に販売されたりするまでに、多額の追加資本が必要になると予想しています。私たちはこれらの計画の達成に努めていますが、これらの戦略やその他の戦略が達成されるという保証や、有利な条件で追加の資金が得られるという保証はまったくありません。将来の1か月あたりのマイナスキャッシュフロー率は、当社の臨床活動と発生した費用のタイミングによって異なり、Remedy2試験を継続してグローバルに拡大するにつれて、最近の過去の期間と比較して増加すると予想しています。現在の現金資源は、このレポートに含まれる要約連結財務諸表の発行日から少なくとも今後12か月間は、RemeDy2の試験を継続し、その他の方法で計画された事業に資金を提供するのに十分であると予想しています。しかし、私たちが将来必要とする資金の金額と時期は、私たちの継続的な開発努力のタイミングと結果、そのような試験へのサイトの活性化と登録の速度、サイトの人員不足の影響、Remedy2試験における他の脳卒中および神経学的試験による研究スタッフと被験者の競争、現在および可能性の潜在的な拡大など、多くの要因に左右されます。新しい開発プログラム、およびそのような活動に関連して発生する運営費。現在の予想よりも早く多額の追加資金が必要になる可能性があり、特に追加資本調達の市場状況が好調であれば、その前に追加資金を必要としない、または求めることがないという保証はありません。
これまで、私たちは主に株式の売却、新株予約権とストックオプションの行使で事業資金を調達してきましたが、当面の間この慣行が続くと予想しています。資金を借りることができる既存の信用枠はありません。エクイティファイナンスやデットファイナンスなど、さまざまな資金源、または戦略的コラボレーションやライセンス契約を通じて、追加の資金調達を検討する場合があります。私たちは、事業を支援するための追加の資金源を確保できること、またはそのような資金が利用できる場合でも、そのような追加の資金が私たちのニーズを満たすために、または私たちが受け入れられる条件で十分であるという保証はできません。これは、私たちの臨床データが肯定的でない場合や、経済や市場の状況が悪化している場合に特に当てはまります。
株式または転換社債の売却を通じて追加資本を調達する限り、株主の所有権は希薄化されます。デットファイナンスは、可能であれば、転換割引、知的財産を担保として質入れする契約、または追加の債務の発生や資本支出などの特定の行動を取る能力を制限または制限する契約を含む契約が含まれる場合があります。政府やその他の第三者の資金調達、マーケティングと流通の取り決め、その他の協力、または第三者との戦略的提携やライセンス契約を通じて追加の資金を調達した場合、当社の技術、将来の収益源、研究プログラム、製品候補に対する貴重な権利を放棄するか、当社にとって不利な条件でライセンスを付与しなければならない場合があります。資金調達の可否は、当社の臨床データやその他の科学・臨床研究結果、規制当局の承認やその他の規制措置の取得能力、製品候補の市場での受け入れ、特に製薬、バイオテクノロジー、医療企業を中心とした資本市場全体の状況、戦略的提携契約の状況、およびその他の関連する商業上の考慮事項によって影響を受けます。
必要なときに十分な資金が得られない場合は、とりわけ、外部の専門サービスプロバイダーの利用の削減、従業員数または従業員報酬の削減、DM199製品候補の開発の変更または延期、AIS、CRD、またはその他の適応症に対するDM199製品候補の商品化権を第三者にライセンスするなど、コスト削減戦略の実施を含む措置を講じることにより、事業を縮小する必要がある場合がありますそうでなければ追求する、あるいはそうでなければ当社の技術、将来の収益源、研究プログラム、製品候補に対する重要な権利を放棄すること、または当社にとって不利な条件でのライセンスの付与、および/または当社の合併、売却、清算による資産の売却または事業の停止を行うこと。
重要な会計方針と見積もり
で提供された情報に基づく当社の重要な会計方針と見積もりには、重大な変更はありません。パートII。項目7、管理's 財政状態と経営成績に関する議論と分析—重要な会計方針、」2023年12月31日に終了した会計年度のForm 10-Kの年次報告書に含まれています。
|
アイテム 3. |
市場リスクに関する定量的および質的開示 |
小規模な報告会社なので、この項目に従って開示する必要はありません。
|
アイテム 4. |
統制と手続き |
開示管理と手続きの評価
私たちは、取引法に基づいて提出または提出する報告書で当社が開示する必要のある情報が、SECの規則とフォームで指定された期間内に記録、処理、要約、報告されることを合理的に保証することを目的とした開示管理と手続き(改正(取引法)に基づく1934年の米国証券取引法の規則13a-15(e)および15d-15(e)で定義されているとおり)を維持しています。そのような情報は蓄積され、当社の最高経営責任者を含む当社の経営陣に伝えられます。必要に応じて、最高財務責任者、または同様の職務を遂行する人を、必要な開示に関して適時に決定できるようにしています。当社の経営陣は、最高経営責任者および最高財務責任者の参加を得て、このレポートの対象期間の終了時点における開示管理と手続きの設計と運用の有効性を評価しました。その評価に基づいて、当社の最高経営責任者および最高財務責任者は、取引法に基づいて提出または提出する報告書で開示する必要のある情報が、SECの規則とフォームで指定された期間内に記録、処理、要約、報告され、そのような情報が蓄積され、当社の最高経営責任者および最高財務責任者を含む当社の経営陣に伝達されることを合理的に保証するために、当社の開示管理と手続きはその期間の終了時に有効であると結論付けました。財務責任者、必要な開示について適時に決定できるように。
財務報告に関する内部統制の変更
2024年3月31日に終了した3か月間に発生した、財務報告に対する当社の内部統制に重大な影響を及ぼした、または重大な影響を与える可能性が合理的に高い変更はありませんでした。
|
パートII- |
その他の情報 |
|
アイテム 1. |
法的手続き |
2021年7月1日付けでICON plcに買収されたファーマシューティカル・リサーチ・アソシエイツ・グループB.V. との訴訟(ICON/PRAオランダ)
2022年11月23日、ICON plcが2021年7月1日に買収した製薬リサーチ・アソシエイツ・グループB.V.(ICON/PRAオランダ)が所有するすべての関連書類の判決前の添付許可を求める請願書を提出し、2022年11月28日にオランダ北部の地方裁判所により承認されました。地方裁判所の代表が、2022年12月7日と8日頃にICON/PRAオランダに判決前の添付書類を提出しました。この訴訟は2022年12月28日にオランダ商事裁判所(NCC)に正式に提出され、押収された記録を当社が所有する権利があるかどうかを決定する公聴会が2023年3月16日に予定され、開催されました。
2023年4月21日、NCCは、ICON/PRAオランダが実施し、2022年12月にオランダの裁判所に押収された臨床研究に関連する、51のハードコピーフォルダーと特定のデジタルファイルを含む物理文書の所有権を確認する判決を下しました。NCCはさらに、ICON/PRAオランダに、デジタルデータやソースデータを含む文書の引き渡しを許可し、容認するよう命じました。さらに、NCCは、私たちが臨床研究契約に基づくいかなる義務にも違反していないと判断し、ICON/PRAオランダには、すべての臨床データと研究の監査を実施するためのアクセスを提供するという臨床研究契約に基づく義務の履行を一時停止する根拠はありませんでした。2023年6月15日、ICON/PRAオランダはこの決定に対して上訴し、2024年9月23日に予定されているNCCへの聴聞会を要請しました。
当社の損害賠償請求に関する公聴会は、2023年12月7日に行われました。2024年2月7日、NCCは、調査に関連するすべてのデータはDiaMedicaが正当な財産であるにもかかわらず、ICO/PRAオランダが研究データを差し控えることと当社が請求した損害との因果関係が不十分であると判断した判決を下しました。この決定に対して上訴する意向をNCCとICON/PRAオランダに通知しました。
時々、雇用問題や契約違反紛争など、通常の業務で発生するものを含め、進行中または脅威にさらされているさまざまな法的措置や手続きの対象となることがあります。このような問題には、多くの不確実性や、保証では予測できない結果や、長期間にわたってわからない結果が生じる可能性があります。上記のICON/PRAオランダの問題を除いて、私たちは現在、脅威にさらされている法的措置には関与しておらず、認識もしていません。
|
アイテム 1A. |
リスク要因 |
小規模な報告会社なので、この項目に従って開示する必要はありません。
|
アイテム 2. |
持分証券の未登録売却および収益の使用 |
2024年3月31日に終了した四半期には、当社の未登録株式を売却しませんでした。
|
アイテム 3. |
シニア証券のデフォルト |
該当しません。
|
アイテム 4. |
鉱山の安全に関する開示 |
該当しません。
|
アイテム 5. |
その他の情報 |
ルール10b5-1プランとノンルール10b5-1トレーディングアレンジメントの採用・解約・変更
2024年3月31日に終了した3か月間、当社の取締役または「役員」(証券取引法の規則16a-1(f)で定義されている)の誰も、SEC規則S-Kの項目408(a)および408(c)でそれぞれ定義されているように、「規則10b5-1取引契約」または「非規則10b5-1取引契約」を採用または終了しませんでした。
|
アイテム 6. |
展示品 |
フォーム10-Qのこの四半期報告書には、次の展示品が提出または提出されています。
|
示す いいえ。 |
説明 |
申告の仕方 |
||
|
3.1 |
2019年5月31日付けのダイアメディカ・セラピューティクス社の記事のお知らせ |
2019年6月4日に証券取引委員会に提出されたDiamedicaの最新報告書(ファイル番号001-36291)のフォーム8-Kの最新報告書の別紙3.1を参照して組み込まれています。 |
||
|
3.2 |
2023年5月17日発効のダイアメディカ・セラピューティクス社の修正および改訂された条項 |
2023年5月18日に証券取引委員会に提出されたDiamedicaの最新報告書(ファイル番号001-36291)のフォーム8-Kの最新報告書の別紙3.1を参照して組み込まれています |
||
|
31.1 |
2002年のサーベンス・オクスリー法第302条に従って採択された、取引法規則13a-14(a)/15d-14(a)に基づく最高経営責任者の認定 |
ここに提出 |
||
|
31.2 |
2002年のサーベンス・オクスリー法第302条に従って採択された、取引法規則13a-14(a)/15d-14(a)に基づく最高財務責任者の認定 |
ここに提出 |
||
|
32.1 |
2002年のサーベンス・オクスリー法第906条に基づいて採択された米国法第18条第1350条に基づく最高経営責任者の認定 |
ここに備え付けられています |
||
|
32.2 |
2002年のサーベンス・オクスリー法第906条に従って採択された、米国合衆国法第18条第1350条に基づく最高財務責任者の認定 |
ここに備え付けられています |
||
|
101 |
2024年3月31日に終了した3か月間のDiamedica Therapeutics Inc.のフォーム10-Qの四半期報告書のインラインXBRL形式の財務諸表:(i)要約連結貸借対照表、(ii)要約連結営業報告書および包括損失計算書、(iii)株主資本の要約連結計算書、(v)要約キャッシュフロー計算書、(v)要約連結キャッシュフロー計算書連結財務諸表。 |
ここに提出 |
||
|
104 |
表紙インタラクティブデータファイル |
インライン XBRL ドキュメントに埋め込まれています |
署名
1934年の証券取引法の要件に従い、登録者は署名者に代わってこの報告書に正式に署名させ、正式に権限を与えられました。
|
ダイアメディカ・セラピューティクス株式会社 |
|
|
日付:2024年5月8日 |
/s/ リック・ポールズ |
|
リック・ポールズ |
|
| 社長兼最高経営責任者 | |
|
(最高執行役員) |
|
|
日付:2024年5月8日 |
/s/ スコット・ケレン |
|
スコット・ケレン |
|
| 最高財務責任者 | |
|
(最高財務責任者および最高会計責任者) |