VRTX-20240331バーテックス・ファーマシューティカルズ株式会社/MA000087532012/312024Q1偽午後 1 時372442339468427340382エクセルリ:シェアISO 4217: 米ドルISO 4217: 米ドルエクセルリ:シェアVRTX: セグメントVRTX: ターゲットエクセルリ:ピュア00008753202024-01-012024-03-3100008753202024-04-3000008753202023-01-012023-03-3100008753202024-03-3100008753202023-12-310000875320米国会計基準:普通株式会員2022-12-310000875320米国会計基準:追加払込資本構成員2022-12-310000875320米国会計基準:その他の包括利益の累計メンバー2022-12-310000875320米国会計基準:利益剰余金メンバー2022-12-3100008753202022-12-310000875320米国会計基準:その他の包括利益の累計メンバー2023-01-012023-03-310000875320米国会計基準:利益剰余金メンバー2023-01-012023-03-310000875320米国会計基準:普通株式会員2023-01-012023-03-310000875320米国会計基準:追加払込資本構成員2023-01-012023-03-310000875320米国会計基準:普通株式会員2023-03-310000875320米国会計基準:追加払込資本構成員2023-03-310000875320米国会計基準:その他の包括利益の累計メンバー2023-03-310000875320米国会計基準:利益剰余金メンバー2023-03-3100008753202023-03-310000875320米国会計基準:普通株式会員2023-12-310000875320米国会計基準:追加払込資本構成員2023-12-310000875320米国会計基準:その他の包括利益の累計メンバー2023-12-310000875320米国会計基準:利益剰余金メンバー2023-12-310000875320米国会計基準:その他の包括利益の累計メンバー2024-01-012024-03-310000875320米国会計基準:利益剰余金メンバー2024-01-012024-03-310000875320米国会計基準:普通株式会員2024-01-012024-03-310000875320米国会計基準:追加払込資本構成員2024-01-012024-03-310000875320米国会計基準:普通株式会員2024-03-310000875320米国会計基準:追加払込資本構成員2024-03-310000875320米国会計基準:その他の包括利益の累計メンバー2024-03-310000875320米国会計基準:利益剰余金メンバー2024-03-310000875320VRTX:トリカフタカフトリオのメンバー2024-01-012024-03-310000875320VRTX:トリカフタカフトリオのメンバー2023-01-012023-03-310000875320VRTX:その他の嚢胞性線維症製品のメンバー2024-01-012024-03-310000875320VRTX:その他の嚢胞性線維症製品のメンバー2023-01-012023-03-310000875320国:米国2024-01-012024-03-310000875320国:米国2023-01-012023-03-310000875320SRT: ヨーロッパメンバー2024-01-012024-03-310000875320SRT: ヨーロッパメンバー2023-01-012023-03-310000875320VRTX:その他の非米国メンバー2024-01-012024-03-310000875320VRTX:その他の非米国メンバー2023-01-012023-03-310000875320米国会計基準:米国非会員2024-01-012024-03-310000875320米国会計基準:米国非会員2023-01-012023-03-310000875320VRTX:CRISPRセラピューティクスAGメンバー2019-01-012019-12-310000875320VRTX:クリスプルJDCAメンバー2024-01-012024-01-310000875320VRTX: CRISPRメンバー2024-03-310000875320VRTX:クリスプルJDCAメンバー2024-01-012024-03-310000875320VRTX:クリスプルJDCAメンバー2021-12-310000875320VRTX:クリスプルJDCAメンバーVRTX: CRISPRメンバー2021-12-310000875320VRTX:クリスプルJDCAメンバー2023-01-012023-03-310000875320VRTX: クリスプルT1Dメンバー2023-03-012023-03-310000875320VRTX:エントラーダ・セラピューティクス会員2023-02-012023-02-280000875320VRTX:エントラーダ・セラピューティクス会員2024-01-012024-03-310000875320米国会計基準:RSU 加盟国の制限付株式単位2024-01-012024-03-310000875320米国会計基準:RSU 加盟国の制限付株式単位2023-01-012023-03-310000875320米国会計基準:従業員ストックオプションメンバー2024-01-012024-03-310000875320米国会計基準:従業員ストックオプションメンバー2023-01-012023-03-310000875320米国会計基準:RSU 加盟国の制限付株式単位2024-01-012024-03-310000875320米国会計基準:RSU 加盟国の制限付株式単位2023-01-012023-03-310000875320米国会計基準:公正価値測定経常委員2024-03-310000875320米国会計基準:フェアバリューインプットレベル1メンバー米国会計基準:公正価値測定経常委員2024-03-310000875320米国会計基準:公正価値インプットレベル2メンバー米国会計基準:公正価値測定経常委員2024-03-310000875320米国会計基準:フェアバリューインプットレベル3メンバー米国会計基準:公正価値測定経常委員2024-03-310000875320米国会計基準:公正価値測定経常委員2023-12-310000875320米国会計基準:フェアバリューインプットレベル1メンバー米国会計基準:公正価値測定経常委員2023-12-310000875320米国会計基準:公正価値インプットレベル2メンバー米国会計基準:公正価値測定経常委員2023-12-310000875320米国会計基準:フェアバリューインプットレベル3メンバー米国会計基準:公正価値測定経常委員2023-12-310000875320米国会計基準:株式証券メンバー米国会計基準:公正価値測定経常委員2024-03-310000875320米国会計基準:フェアバリューインプットレベル1メンバー米国会計基準:株式証券メンバー米国会計基準:公正価値測定経常委員2024-03-310000875320米国会計基準:公正価値インプットレベル2メンバー米国会計基準:株式証券メンバー米国会計基準:公正価値測定経常委員2024-03-310000875320米国会計基準:フェアバリューインプットレベル3メンバー米国会計基準:株式証券メンバー米国会計基準:公正価値測定経常委員2024-03-310000875320米国会計基準:株式証券メンバー米国会計基準:公正価値測定経常委員2023-12-310000875320米国会計基準:フェアバリューインプットレベル1メンバー米国会計基準:株式証券メンバー米国会計基準:公正価値測定経常委員2023-12-310000875320米国会計基準:公正価値インプットレベル2メンバー米国会計基準:株式証券メンバー米国会計基準:公正価値測定経常委員2023-12-310000875320米国会計基準:フェアバリューインプットレベル3メンバー米国会計基準:株式証券メンバー米国会計基準:公正価値測定経常委員2023-12-310000875320米国会計基準:公正価値測定経常委員米国会計基準:米国財務省証券会員2024-03-310000875320米国会計基準:フェアバリューインプットレベル1メンバー米国会計基準:公正価値測定経常委員米国会計基準:米国財務省証券会員2024-03-310000875320米国会計基準:公正価値インプットレベル2メンバー米国会計基準:公正価値測定経常委員米国会計基準:米国財務省証券会員2024-03-310000875320米国会計基準:フェアバリューインプットレベル3メンバー米国会計基準:公正価値測定経常委員米国会計基準:米国財務省証券会員2024-03-310000875320米国会計基準:公正価値測定経常委員米国会計基準:米国財務省証券会員2023-12-310000875320米国会計基準:フェアバリューインプットレベル1メンバー米国会計基準:公正価値測定経常委員米国会計基準:米国財務省証券会員2023-12-310000875320米国会計基準:公正価値インプットレベル2メンバー米国会計基準:公正価値測定経常委員米国会計基準:米国財務省証券会員2023-12-310000875320米国会計基準:フェアバリューインプットレベル3メンバー米国会計基準:公正価値測定経常委員米国会計基準:米国財務省証券会員2023-12-310000875320米国会計基準:米国政府機関債務証券メンバー米国会計基準:公正価値測定経常委員2024-03-310000875320米国会計基準:米国政府機関債務証券メンバー米国会計基準:フェアバリューインプットレベル1メンバー米国会計基準:公正価値測定経常委員2024-03-310000875320米国会計基準:米国政府機関債務証券メンバー米国会計基準:公正価値インプットレベル2メンバー米国会計基準:公正価値測定経常委員2024-03-310000875320米国会計基準:フェアバリューインプットレベル3メンバー米国会計基準:米国政府機関債務証券メンバー米国会計基準:公正価値測定経常委員2024-03-310000875320米国会計基準:米国政府機関債務証券メンバー米国会計基準:公正価値測定経常委員2023-12-310000875320米国会計基準:米国政府機関債務証券メンバー米国会計基準:フェアバリューインプットレベル1メンバー米国会計基準:公正価値測定経常委員2023-12-310000875320米国会計基準:米国政府機関債務証券メンバー米国会計基準:公正価値インプットレベル2メンバー米国会計基準:公正価値測定経常委員2023-12-310000875320米国会計基準:フェアバリューインプットレベル3メンバー米国会計基準:米国政府機関債務証券メンバー米国会計基準:公正価値測定経常委員2023-12-310000875320米国会計基準:資産担保証券メンバー米国会計基準:公正価値測定経常委員2024-03-310000875320米国会計基準:資産担保証券メンバー米国会計基準:フェアバリューインプットレベル1メンバー米国会計基準:公正価値測定経常委員2024-03-310000875320米国会計基準:資産担保証券メンバー米国会計基準:公正価値インプットレベル2メンバー米国会計基準:公正価値測定経常委員2024-03-310000875320米国会計基準:資産担保証券メンバー米国会計基準:フェアバリューインプットレベル3メンバー米国会計基準:公正価値測定経常委員2024-03-310000875320米国会計基準:資産担保証券メンバー米国会計基準:公正価値測定経常委員2023-12-310000875320米国会計基準:資産担保証券メンバー米国会計基準:フェアバリューインプットレベル1メンバー米国会計基準:公正価値測定経常委員2023-12-310000875320米国会計基準:資産担保証券メンバー米国会計基準:公正価値インプットレベル2メンバー米国会計基準:公正価値測定経常委員2023-12-310000875320米国会計基準:資産担保証券メンバー米国会計基準:フェアバリューインプットレベル3メンバー米国会計基準:公正価値測定経常委員2023-12-310000875320米国会計基準:預金証書メンバー米国会計基準:公正価値測定経常委員2024-03-310000875320米国会計基準:フェアバリューインプットレベル1メンバー米国会計基準:預金証書メンバー米国会計基準:公正価値測定経常委員2024-03-310000875320米国会計基準:預金証書メンバー米国会計基準:公正価値インプットレベル2メンバー米国会計基準:公正価値測定経常委員2024-03-310000875320米国会計基準:フェアバリューインプットレベル3メンバー米国会計基準:預金証書メンバー米国会計基準:公正価値測定経常委員2024-03-310000875320米国会計基準:預金証書メンバー米国会計基準:公正価値測定経常委員2023-12-310000875320米国会計基準:フェアバリューインプットレベル1メンバー米国会計基準:預金証書メンバー米国会計基準:公正価値測定経常委員2023-12-310000875320米国会計基準:預金証書メンバー米国会計基準:公正価値インプットレベル2メンバー米国会計基準:公正価値測定経常委員2023-12-310000875320米国会計基準:フェアバリューインプットレベル3メンバー米国会計基準:預金証書メンバー米国会計基準:公正価値測定経常委員2023-12-310000875320米国会計基準:企業債務証券メンバー米国会計基準:公正価値測定経常委員2024-03-310000875320米国会計基準:企業債務証券メンバー米国会計基準:フェアバリューインプットレベル1メンバー米国会計基準:公正価値測定経常委員2024-03-310000875320米国会計基準:企業債務証券メンバー米国会計基準:公正価値インプットレベル2メンバー米国会計基準:公正価値測定経常委員2024-03-310000875320米国会計基準:企業債務証券メンバー米国会計基準:フェアバリューインプットレベル3メンバー米国会計基準:公正価値測定経常委員2024-03-310000875320米国会計基準:企業債務証券メンバー米国会計基準:公正価値測定経常委員2023-12-310000875320米国会計基準:企業債務証券メンバー米国会計基準:フェアバリューインプットレベル1メンバー米国会計基準:公正価値測定経常委員2023-12-310000875320米国会計基準:企業債務証券メンバー米国会計基準:公正価値インプットレベル2メンバー米国会計基準:公正価値測定経常委員2023-12-310000875320米国会計基準:企業債務証券メンバー米国会計基準:フェアバリューインプットレベル3メンバー米国会計基準:公正価値測定経常委員2023-12-310000875320米国会計基準:コマーシャル・ペーパー・メンバー米国会計基準:公正価値測定経常委員2024-03-310000875320米国会計基準:フェアバリューインプットレベル1メンバー米国会計基準:コマーシャル・ペーパー・メンバー米国会計基準:公正価値測定経常委員2024-03-310000875320米国会計基準:公正価値インプットレベル2メンバー米国会計基準:コマーシャル・ペーパー・メンバー米国会計基準:公正価値測定経常委員2024-03-310000875320米国会計基準:フェアバリューインプットレベル3メンバー米国会計基準:コマーシャル・ペーパー・メンバー米国会計基準:公正価値測定経常委員2024-03-310000875320米国会計基準:コマーシャル・ペーパー・メンバー米国会計基準:公正価値測定経常委員2023-12-310000875320米国会計基準:フェアバリューインプットレベル1メンバー米国会計基準:コマーシャル・ペーパー・メンバー米国会計基準:公正価値測定経常委員2023-12-310000875320米国会計基準:公正価値インプットレベル2メンバー米国会計基準:コマーシャル・ペーパー・メンバー米国会計基準:公正価値測定経常委員2023-12-310000875320米国会計基準:フェアバリューインプットレベル3メンバー米国会計基準:コマーシャル・ペーパー・メンバー米国会計基準:公正価値測定経常委員2023-12-310000875320米国会計基準:株式証券メンバー2024-03-310000875320米国会計基準:フェアバリューインプットレベル3メンバー2019-12-310000875320米国会計基準:フェアバリューインプットレベル3メンバーSRT: 最低メンバー数米国会計基準:測定入力割引率メンバー2024-03-310000875320米国会計基準:フェアバリューインプットレベル3メンバーSRT: 最大メンバー数米国会計基準:測定入力割引率メンバー2024-03-310000875320米国会計基準:米国財務省証券会員2024-03-310000875320米国会計基準:米国財務省証券会員2023-12-310000875320米国会計基準:米国政府機関債務証券メンバー2024-03-310000875320米国会計基準:米国政府機関債務証券メンバー2023-12-310000875320米国会計基準:資産担保証券メンバー2024-03-310000875320米国会計基準:資産担保証券メンバー2023-12-310000875320米国会計基準:預金証書メンバー2024-03-310000875320米国会計基準:預金証書メンバー2023-12-310000875320米国会計基準:企業債務証券メンバー2024-03-310000875320米国会計基準:企業債務証券メンバー2023-12-310000875320米国会計基準:現金および現金同等物会員にはコマーシャルペーパーは含まれていません2024-03-310000875320米国会計基準:現金および現金同等物会員にはコマーシャルペーパーは含まれていません2023-12-310000875320VRTX:有価証券およびその他の非流動資産メンバー2024-03-310000875320VRTX:有価証券およびその他の非流動資産メンバー2023-12-3100008753202023-01-012023-12-310000875320米国会計基準:現金および現金同等物メンバー2024-03-310000875320米国会計基準:現金および現金同等物メンバー2023-12-310000875320VRTX: 有価証券会員2024-03-310000875320VRTX: 有価証券会員2023-12-310000875320VRTX:有価証券の非現会員です2024-03-310000875320VRTX:有価証券の非現会員です2023-12-310000875320米国会計基準:その他の資産メンバー2024-03-310000875320米国会計基準:累積翻訳調整メンバー2023-12-310000875320米国会計基準:累積純未実現投資利益損失メンバー2023-12-310000875320US-GAAP: 累積損益純キャッシュフローエッジ親メンバー2023-12-310000875320米国会計基準:累積翻訳調整メンバー2024-01-012024-03-310000875320米国会計基準:累積純未実現投資利益損失メンバー2024-01-012024-03-310000875320US-GAAP: 累積損益純キャッシュフローエッジ親メンバー2024-01-012024-03-310000875320米国会計基準:累積翻訳調整メンバー2024-03-310000875320米国会計基準:累積純未実現投資利益損失メンバー2024-03-310000875320US-GAAP: 累積損益純キャッシュフローエッジ親メンバー2024-03-310000875320米国会計基準:累積翻訳調整メンバー2022-12-310000875320米国会計基準:累積純未実現投資利益損失メンバー2022-12-310000875320US-GAAP: 累積損益純キャッシュフローエッジ親メンバー2022-12-310000875320米国会計基準:累積翻訳調整メンバー2023-01-012023-03-310000875320米国会計基準:累積純未実現投資利益損失メンバー2023-01-012023-03-310000875320US-GAAP: 累積損益純キャッシュフローエッジ親メンバー2023-01-012023-03-310000875320米国会計基準:累積翻訳調整メンバー2023-03-310000875320米国会計基準:累積純未実現投資利益損失メンバー2023-03-310000875320US-GAAP: 累積損益純キャッシュフローエッジ親メンバー2023-03-310000875320米国会計基準:キャッシュフロー・ヘッジングメンバーSRT: 最低メンバー数米国会計基準:外国為替先渡会員2024-01-012024-03-310000875320米国会計基準:キャッシュフロー・ヘッジングメンバーSRT: 最大メンバー数米国会計基準:外国為替先渡会員2024-01-012024-03-310000875320米国会計基準:キャッシュフロー・ヘッジングメンバー米国会計基準:ヘッジング・インストゥルメント・メンバーに指定通貨:ユーロ米国会計基準:外国為替先渡会員2024-03-310000875320米国会計基準:キャッシュフロー・ヘッジングメンバー米国会計基準:ヘッジング・インストゥルメント・メンバーに指定通貨:ユーロ米国会計基準:外国為替先渡会員2023-12-310000875320米国会計基準:キャッシュフロー・ヘッジングメンバー米国会計基準:ヘッジング・インストゥルメント・メンバーに指定通貨:カナダドル米国会計基準:外国為替先渡会員2024-03-310000875320米国会計基準:キャッシュフロー・ヘッジングメンバー米国会計基準:ヘッジング・インストゥルメント・メンバーに指定通貨:カナダドル米国会計基準:外国為替先渡会員2023-12-310000875320米国会計基準:キャッシュフロー・ヘッジングメンバー米国会計基準:ヘッジング・インストゥルメント・メンバーに指定通貨:英ポンド米国会計基準:外国為替先渡会員2024-03-310000875320米国会計基準:キャッシュフロー・ヘッジングメンバー米国会計基準:ヘッジング・インストゥルメント・メンバーに指定通貨:英ポンド米国会計基準:外国為替先渡会員2023-12-310000875320通貨:オーストラリアドル米国会計基準:キャッシュフロー・ヘッジングメンバー米国会計基準:ヘッジング・インストゥルメント・メンバーに指定米国会計基準:外国為替先渡会員2024-03-310000875320通貨:オーストラリアドル米国会計基準:キャッシュフロー・ヘッジングメンバー米国会計基準:ヘッジング・インストゥルメント・メンバーに指定米国会計基準:外国為替先渡会員2023-12-310000875320米国会計基準:キャッシュフロー・ヘッジングメンバー米国会計基準:ヘッジング・インストゥルメント・メンバーに指定通貨:スイスフランです米国会計基準:外国為替先渡会員2024-03-310000875320米国会計基準:キャッシュフロー・ヘッジングメンバー米国会計基準:ヘッジング・インストゥルメント・メンバーに指定通貨:スイスフランです米国会計基準:外国為替先渡会員2023-12-310000875320米国会計基準:キャッシュフロー・ヘッジングメンバー米国会計基準:ヘッジング・インストゥルメント・メンバーに指定米国会計基準:外国為替先渡会員2024-03-310000875320米国会計基準:キャッシュフロー・ヘッジングメンバー米国会計基準:ヘッジング・インストゥルメント・メンバーに指定米国会計基準:外国為替先渡会員2023-12-310000875320米国会計基準:非指定メンバー米国会計基準:外国為替先渡会員2024-01-012024-03-310000875320米国会計基準:キャッシュフロー・ヘッジングメンバー米国会計基準:非指定メンバー米国会計基準:外国為替先渡会員2024-03-310000875320米国会計基準:ヘッジング・インストゥルメント・メンバーに指定US-GAAP: その他の包括所得累計額からの再分類米国会計基準:累積翻訳調整メンバー米国会計基準:外国為替先渡会員2024-01-012024-03-310000875320米国会計基準:ヘッジング・インストゥルメント・メンバーに指定US-GAAP: その他の包括所得累計額からの再分類米国会計基準:累積翻訳調整メンバー米国会計基準:外国為替先渡会員2023-01-012023-03-310000875320US-GAAP: その他の包括所得累計額からの再分類米国会計基準:累積翻訳調整メンバー米国会計基準:非指定メンバー米国会計基準:外国為替先渡会員2024-01-012024-03-310000875320US-GAAP: その他の包括所得累計額からの再分類米国会計基準:累積翻訳調整メンバー米国会計基準:非指定メンバー米国会計基準:外国為替先渡会員2023-01-012023-03-310000875320米国会計基準:キャッシュフロー・ヘッジングメンバー米国会計基準:ヘッジング・インストゥルメント・メンバーに指定US-GAAP: 前払費用およびその他の流動資産メンバー米国会計基準:外国為替先渡会員2024-03-310000875320米国会計基準:キャッシュフロー・ヘッジングメンバー米国会計基準:ヘッジング・インストゥルメント・メンバーに指定米国会計基準:その他の流動負債メンバー米国会計基準:外国為替先渡会員2024-03-310000875320米国会計基準:キャッシュフロー・ヘッジングメンバー米国会計基準:ヘッジング・インストゥルメント・メンバーに指定US-GAAP: 前払費用およびその他の流動資産メンバー米国会計基準:外国為替先渡会員2023-12-310000875320米国会計基準:キャッシュフロー・ヘッジングメンバー米国会計基準:ヘッジング・インストゥルメント・メンバーに指定米国会計基準:その他の流動負債メンバー米国会計基準:外国為替先渡会員2023-12-310000875320米国会計基準:制限付株式会員2024-01-012024-03-310000875320米国会計基準:制限付株式会員2023-01-012023-03-310000875320米国会計基準:従業員株式会員2024-01-012024-03-310000875320米国会計基準:従業員株式会員2023-01-012023-03-310000875320米国会計基準:売上原価メンバー2024-01-012024-03-310000875320米国会計基準:売上原価メンバー2023-01-012023-03-310000875320米国会計基準:研究開発費メンバー2024-01-012024-03-310000875320米国会計基準:研究開発費メンバー2023-01-012023-03-310000875320米国会計基準:一般管理費の売上メンバー2024-01-012024-03-310000875320米国会計基準:一般管理費の売上メンバー2023-01-012023-03-3100008753202023-02-280000875320US-GAAP: リボルビング・クレジット・ファシリティ・メンバー2022-07-310000875320米国会計基準:信用状メンバー2022-07-310000875320米国会計基準:基本利率メンバーSRT: 最低メンバー数US-GAAP: リボルビング・クレジット・ファシリティ・メンバー2022-07-012022-07-310000875320米国会計基準:基本利率メンバーUS-GAAP: リボルビング・クレジット・ファシリティ・メンバーSRT: 最大メンバー数2022-07-012022-07-310000875320SRT: 最低メンバー数US-GAAP: リボルビング・クレジット・ファシリティ・メンバーVRTX:R会員の安全なオーバーナイトファイナンスレート2022-07-012022-07-310000875320US-GAAP: リボルビング・クレジット・ファシリティ・メンバーVRTX:R会員の安全なオーバーナイトファイナンスレートSRT: 最大メンバー数2022-07-012022-07-310000875320US-GAAP: リボルビング・クレジット・ファシリティ・メンバー2022-07-012022-07-310000875320VRTX: アルパイン会員米国会計基準:後任イベントメンバー2024-04-012024-04-300000875320VRTX:明日、モレイ・アトキンソンIIIメンバー2024-01-012024-03-310000875320VRTX:明日、モレイ・アトキンソンIIIメンバー2024-03-310000875320VRTX: ジョナサン・ビラーメンバー2024-01-012024-03-310000875320VRTX: ジョナサン・ビラーメンバー2024-03-310000875320VRTX:カルメン・ボジックメンバー2024-01-012024-03-310000875320VRTX:カルメン・ボジックメンバー2024-03-310000875320VRTX:レシュメイクウォルラマニメンバー2024-01-012024-03-310000875320VRTX:レシュメイクウォルラマニメンバー2024-03-310000875320VRTX:オウラニアタッツのメンバー2024-01-012024-03-310000875320VRTX:オウラニアタッツのメンバー2024-03-310000875320VRTX:チャールズ・ファグナー・ジュニアメンバー2024-01-012024-03-310000875320VRTX:チャールズ・ファグナー・ジュニアメンバー2024-03-310000875320VRTX: ブルース・サックスのメンバー2024-01-012024-03-310000875320VRTX: ブルース・サックスのメンバー2024-03-31 米国
証券取引委員会
ワシントンD.C. 20549
____________________________________________________
フォーム 10-Q
☒ 1934年の証券取引法のセクション13または15 (d) に基づく四半期報告書
四半期終了時の 2024年3月31日です
または
☐ 1934年の証券取引法のセクション13または15(d)に基づく移行レポート
からへの移行期間について
コミッションファイル番号000-19319
________________________________________
バーテックス・ファーマシューティカルズ・インコーポレイテッド
(憲章に明記されている登録者の正確な名前)
マサチューセッツ
(法人または組織の州またはその他の管轄区域)
50 ノーザンアベニュー、 ボストン、 マサチューセッツ
(主要執行機関の住所)
04-3039129
(IRS雇用者識別番号)
02210
(郵便番号)
登録者の電話番号 (市外局番を含む)617)341-6100
________________________________________
| | | | | | | | | | | | | | |
同法第12条 (b) に従って登録された証券: |
各クラスのタイトル | | トレーディングシンボル | | 登録された各取引所の名前 |
普通株式、1株あたり額面0.01ドル | | VRTX | | ナスダック・グローバル・セレクト・マーケット |
登録者が、(1)1934年の証券取引法のセクション13または15(d)によって提出が義務付けられたすべての報告を過去12か月間(または登録者がそのような報告を提出する必要があったほど短い期間)に提出したかどうか、および(2)過去90日間にそのような提出要件の対象であったかどうかをチェックマークで示してください。はい☒ いいえ ☐
登録者が、過去12か月間(または登録者がそのようなファイルを提出する必要があったほど短い期間)に、規則S-Tの規則405(この章の§232.405)に従って提出する必要のあるすべてのインタラクティブデータファイルを電子的に提出したかどうかをチェックマークで示してください。 はい☒ いいえ ☐
登録者が大規模な加速申告者、加速申告者、非加速申告者、小規模な報告会社、または新興成長企業のいずれであるかをチェックマークで示してください。取引法規則12b-2の「大規模加速申告者」、「加速申告者」、「小規模報告会社」、および「新興成長企業」の定義を参照してください。
大型加速フィルター☒ アクセラレーテッドファイラー ☐ 非アクセラレーテッドファイラー ☐ 小規模な報告会社 ☐ 新興成長企業 ☐
新興成長企業の場合は、登録者が取引法のセクション13(a)に従って規定された新規または改訂された財務会計基準を遵守するために延長された移行期間を使用しないことを選択したかどうかをチェックマークで示してください。☐
登録者がシェル会社(証券取引法の規則12b-2で定義されている)かどうかをチェックマークで示してください。はい☐ いいえ ☒
発行可能な最新の日付現在の、発行者の各クラスの普通株式の発行済み株式数を記載してください。
| | | | | | | | |
普通株式、額面価格1株あたり0.01ドル | 258,053,387 | 2024年4月30日に未払い |
バーテックス・ファーマシューティカルズ・インコーポレイテッド
フォーム 10-Q
2024年3月31日に終了した四半期については
目次
| | | | | | | | |
| | ページ |
第I部財務情報 |
アイテム 1. | 財務諸表 | 2 |
| 要約連結財務諸表(未監査) | 2 |
| 要約連結損益計算書-2024年および2023年3月31日に終了した3か月間 | 2 |
| 包括利益の要約連結計算書-2024年および2023年3月31日に終了した3か月間 | 3 |
| 要約された連結貸借対照表-2024年3月31日と2023年12月31日 | 4 |
| 要約連結株主資本計算書-2024年および2023年3月31日に終了した3か月間 | 5 |
| 要約連結キャッシュフロー計算書-2024年および2023年3月31日に終了した3か月間 | 6 |
| 要約連結財務諸表の注記 | 7 |
アイテム 2. | 経営陣による財政状態と経営成績に関する議論と分析 | 20 |
アイテム 3. | 市場リスクに関する定量的・質的開示 | 32 |
アイテム 4. | 統制と手続き | 32 |
第二部。その他の情報 |
アイテム 1. | 法的手続き | 32 |
アイテム 1A. | リスク要因 | 32 |
アイテム 2. | 持分証券の未登録売却および収益の使用 | 34 |
アイテム 5. | その他の情報 | 34 |
アイテム 6. | 展示品 | 35 |
署名 | | 36 |
フォーム10-Qのこの四半期報告書で使用されている「Vertex」、「私たち」、「私たち」、および「私たち」とは、マサチューセッツ州の企業であるVertex Pharmaceuticals Incorporatedとその子会社を指します。
「Vertex®」、「KALYDECO®」、「ORKAMBI®」、「SYMDEKO®」、「SYMKEVI®」、「TRIKAFTA®」、「KAFTRIO®」、「CASGEVY™」はVertexの登録商標です。このForm 10-Qの四半期報告書に含まれるその他のブランド、名称、商標は、それぞれの所有者に帰属します。
承認された製品を指すとき、および承認されたラベルの表示に関しては、製品のブランド名を使用します。それ以外の場合は、開発プログラムの議論を含め、私たちの化合物や治療法を科学的(またはジェネリック)名またはVX開発上の名称で呼んでいます。
パートI。財務情報
アイテム 1.財務諸表
バーテックス・ファーマシューティカルズ・インコーポレイテッド
要約連結損益計算書
(単位:百万、1株あたりの金額を除く) (未監査)
| | | | | | | | | | | | | | | |
| | | 3月31日に終了した3か月間 |
| | | | | 2024 | | 2023 |
| 製品収益、純額 | | | | | $ | 2,690.6 | | | $ | 2,374.8 | |
| 費用と経費: | | | | | | | |
| 売上原価 | | | | | 342.6 | | | 266.9 | |
| 研究開発費用 | | | | | 789.1 | | | 742.6 | |
| 進行中の研究開発費の取得 | | | | | 76.8 | | | 347.1 | |
| 販売費、一般管理費 | | | | | 342.7 | | | 241.1 | |
| 条件付対価の公正価値の変更 | | | | | (0.1) | | | (1.9) | |
| 費用と経費の合計 | | | | | 1,551.1です | | | 1,595.8 | |
| 事業からの収入 | | | | | 1,139.5 | | | 779.0 | |
| 利息収入 | | | | | 181.2 | | | 122.6 | |
| 支払利息 | | | | | (10.4) | | | (11.4) | |
| その他(費用)収入、純額 | | | | | (31.2) | | | 1.3 | |
| 所得税引当前利益 | | | | | 1,279.1 | | | 891.5です | |
| 所得税引当金 | | | | | 179.5 | | | 191.7 | |
| 純利益 | | | | | $ | 1,099.6 | | | $ | 699.8 | |
| | | | | | | |
| 普通株式1株あたりの純利益: | | | | | | | |
| ベーシック | | | | | $ | 4.26 | | | $ | 2.72 | |
| 希釈 | | | | | $ | 4.21 | | | $ | 2.69 | |
| 一株当たりの計算に使用される株式: | | | | | | | |
| ベーシック | | | | | 258.2 | | | 257.4 | |
| 希釈 | | | | | 261.1 | | | 260.3 | |
添付の注記は、これらの要約連結財務諸表の不可欠な部分です。
バーテックス・ファーマシューティカルズ・インコーポレイテッド
要約連結包括利益計算書
(百万単位) (未監査)
| | | | | | | | | | | | | | | |
| | | 3月31日に終了した3か月間 |
| | | | | 2024 | | 2023 |
| 純利益 | | | | | $ | 1,099.6 | | | $ | 699.8 | |
その他の包括利益 (損失): | | | | | | | |
売却可能な負債証券の未実現保有(損失)利益(税引後)5.4 と $ (0.8)、それぞれ | | | | | (19.7) | | | 2.9 | |
外貨先渡契約の未実現利益(損失)、税引後($)12.3) と $7.4、それぞれ | | | | | 44.5 | | | (26.8) | |
| 外貨換算調整 | | | | | 6.8 | | | 10.0 | |
その他の包括利益 (損失) の合計 | | | | | 31.6 | | | (13.9) | |
| 包括利益 | | | | | $ | 1,131.2 | | | $ | 685.9 | |
添付の注記は、これらの要約連結財務諸表の不可欠な部分です。
バーテックス・ファーマシューティカルズ・インコーポレイテッド
要約連結貸借対照表
(百万単位、株式データを除く) (未監査)
| | | | | | | | | | | |
| 2024年3月31日 | | 2023年12月31日 |
資産 | | | |
| 流動資産: | | | |
| 現金および現金同等物 | $ | 9,158.0 | | | $ | 10,369.1 | |
| 市場性のある証券 | 1,013.3 | | | 849.2 | |
| 売掛金、純額 | 1,793.2 | | | 1,563.4 | |
| インベントリ | 813.1 | | | 738.8 | |
前払費用およびその他の流動資産 | 511.1 | | | 623.7 | |
流動資産合計 | 13,288.7 | | | 14,144.2 | |
| 資産および設備、純額 | 1,172.8 | | | 1,159.3 | |
| グッドウィル | 1,088.0 | | | 1,088.0 | |
その他の無形資産、純額 | 834.9 | | | 839.9 | |
繰延税金資産 | 1,963.0です | | | 1,812.1 | |
オペレーティングリース資産 | 312.9 | | | 293.6 | |
| 長期市場性のある証券 | 4,381.4です | | | 2,497.8 | |
その他の資産 | 875.7 | | | 895.3 | |
総資産 | $ | 23,917.4 | | | $ | 22,730.2 | |
負債と株主資本 | | | |
| 現在の負債: | | | |
| 買掛金 | $ | 351.4 | | | $ | 364.9 | |
| 未払費用 | 2,795.9 | | | 2,655.3 | |
その他の流動負債 | 648.6 | | | 527.2 | |
流動負債合計 | 3,795.9 | | | 3,547.4 | |
| 長期ファイナンスリース負債 | 361.5です | | | 376.1 | |
| 長期オペレーティングリース負債 | 359.8 | | | 348.6 | |
その他の長期負債 | 853.6 | | | 877.7 | |
負債総額 | 5,370.8 | | | 5,149.8 | |
| コミットメントと不測の事態 | — | | | — | |
| 株主資本: | | | |
優先株式、$0.01 額面価格; 1,000,000 承認された株式; 無し 発行済みで未処理です | — | | | — | |
普通株式、$0.01 額面価格; 5億,000 承認済み株式、 258,296,249 そして 257,695,221 発行済株式と発行済株式をそれぞれ | 2.6 | | | 2.6 | |
| 追加払込資本 | 7,284.7 | | | 7,449.7 | |
| その他の包括利益 (損失) の累計 | 17.3 | | | (14.3) | |
利益剰余金 | 11,242.0 | | | 10,142.4 | |
株主資本の総額 | 18,546.6 | | | 17,580.4 | |
負債総額と株主資本 | $ | 23,917.4 | | | $ | 22,730.2 | |
添付の注記は、これらの要約連結財務諸表の不可欠な部分です。
バーテックス・ファーマシューティカルズ・インコーポレイテッド
要約連結株主資本計算書
(百万単位) (未監査)
| | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | |
| |
| | | | | | | | | |
| | | | | | | |
| | | | | | | | | | | |
| | | | | | | | | | | |
| | | | | | | | | | | |
| | | | | | | | | | | |
| | | | | | | | | | | |
| | | | | | | | | | | |
| | | | | | | | | | | |
| | | | | | | | | | | |
| | | | | | | | | | | |
| | | | | | | | | | | |
| | | | | | | | | | | |
| | | | | | | | | | | |
| | | | | | | | | | | |
| | | | | | | | | | | |
| | | | | | | | | | | |
| | | | | | | | | | | |
| | | | | | | | | | | |
| | | | | | | | | | | |
| 3 か月が終了 |
| 普通株式 | | 追加払込資本 | | その他の包括利益 (損失) の累計 | | 利益剰余金 | | 株主資本の合計 |
| 株式 | | 金額 | | | | |
| 2022年12月31日現在の残高 | 257.0 | | | $ | 2.6 | | | $ | 7,386.5 | | | $ | 0.8 | | | $ | 6,522.8 | | | $ | 13,912.7 | |
| その他の包括損失(税引後) | — | | | — | | | — | | | (13.9) | | | — | | | (13.9) | |
純利益 | — | | | — | | | — | | | — | | | 699.8 | | | 699.8 | |
| 普通株式の買戻し | (0.5) | | | (0.0) | | | (135.6) | | | — | | | — | | | (135.6) | |
| 従業員の納税義務のために源泉徴収される普通株式 | (0.6) | | | (0.0) | | | (166.6) | | | — | | | — | | | (166.6) | |
| 福利厚生制度に基づく普通株式の発行 | 1.6 | | | 0.0 | | | 13.1 | | | — | | | — | | | 13.1 | |
株式ベースの報酬費用 | — | | | — | | | 122.8 | | | — | | | — | | | 122.8 | |
| 2023年3月31日現在の残高 | 257.5 | | | $ | 2.6 | | | $ | 7,220.2 | | | $ | (13.1) | | | $ | 7,222.6 | | | $ | 14,432.3 | |
| | | | | | | | | | | |
| 2023年12月31日現在の残高 | 257.7 | | | $ | 2.6 | | | $ | 7,449.7 | | | $ | (14.3) | | | $ | 10,142.4 | | | $ | 17,580.4 | |
| その他の包括利益(税引後) | — | | | — | | | — | | | 31.6 | | | — | | | 31.6 | |
純利益 | — | | | — | | | — | | | — | | | 1,099.6 | | | 1,099.6 | |
| 普通株式の買戻し | (0.3) | | | (0.0) | | | (140.4) | | | — | | | — | | | (140.4) | |
| 従業員の納税義務のために源泉徴収される普通株式 | (0.6) | | | (0.0) | | | (233.5) | | | — | | | — | | | (233.5) | |
| 福利厚生制度に基づく普通株式の発行 | 1.5 | | | 0.0 | | | 15.9 | | | — | | | — | | | 15.9 | |
株式ベースの報酬費用 | — | | | — | | | 193.0 | | | — | | | — | | | 193.0 | |
| 2024年3月31日現在の残高 | 258.3 | | | $ | 2.6 | | | $ | 7,284.7 | | | $ | 17.3 | | | $ | 11,242.0 | | | $ | 18,546.6 | |
添付の注記は、これらの要約連結財務諸表の不可欠な部分です。
バーテックス・ファーマシューティカルズ・インコーポレイテッド
要約連結キャッシュフロー計算書
(百万単位) (未監査)
| | | | | | | | | | | |
| 3月31日に終了した3か月間 |
| 2024 | | 2023 |
| 営業活動によるキャッシュフロー: | | | |
| 純利益 | $ | 1,099.6 | | | $ | 699.8 | |
| 純利益を営業活動によって提供される純現金と調整するための調整: | | | |
| 株式ベースの報酬費用 | 191.9 | | | 122.4 | |
| 減価償却費および償却費 | 53.5 | | | 38.8 | |
| 繰延所得税 | (158.3) | | | (113.4) | |
| 株式の損失(利益) | 27.0 | | | (6.4) | |
| 偶発的対価の公正価値の低下 | (0.1) | | | (1.9) | |
| その他の現金以外の商品、純額 | (36.3) | | | 21.7 | |
| 営業資産および負債の変動: | | | |
| 売掛金、純額 | (251.6) | | | (90.5) | |
| インベントリ | (80.1) | | | (82.6) | |
| 前払費用およびその他の資産 | 99.2 | | | 46.2 | |
| 買掛金 | 0.1 | | | 35.7 | |
| 未払費用 | 194.1 | | | 140.7 | |
| その他の負債 | 167.6 | | | 89.4 | |
| 営業活動による純現金 | 1,306.6 | | | 899.9 | |
| 投資活動によるキャッシュフロー: | | | |
| 売却可能な債務証券の購入 | (2,598.5) | | | (1,816.6) | |
| 売却可能な負債証券の売却と満期 | 710.5 | | | 50.0 | |
| 資産および設備の購入 | (68.4) | | | (42.1) | |
| 有期無形資産に関連する純支払い額 | (180.0) | | | — | |
| 株式への投資 | — | | | (24.9) | |
| 投資活動に使用された純現金 | (2,136.4) | | | (1,833.6) | |
| 財務活動によるキャッシュフロー: | | | |
| 福利厚生制度に基づく普通株式の発行 | 16.9 | | | 14.2 | |
| 普通株式の買戻し | (131.2) | | | (132.8) | |
| 従業員の納税義務のために源泉徴収された普通株式に関連する支払い | (233.5) | | | (166.6) | |
| ファイナンスリースの支払い | (13.2) | | | (10.6) | |
| その他の財務活動 | 3.5 | | | 1.1 | |
| 財務活動に使用された純現金 | (357.5) | | | (294.7) | |
| 為替レートの変動が現金に与える影響 | (15.6) | | | 12.0 | |
| 現金、現金同等物および制限付現金の純減少 | (1,202.9) | | | (1,216.4) | |
| 現金、現金同等物および制限付現金—期初 | 10,372.3 | | | 10,512.0です | |
| 現金、現金同等物および制限付現金—期末 | $ | 9,169.4 | | | $ | 9,295.6 | |
| | | |
| キャッシュフロー情報の補足開示: | | | |
| 所得税として支払われた現金 | $ | 34.8 | | | $ | 120.3 | |
| 利息として支払われた現金 | $ | 10.0 | | | $ | 11.1 | |
添付の注記は、これらの要約連結財務諸表の不可欠な部分です。
目次
バーテックス・ファーマシューティカルズ・インコーポレイテッド
要約連結財務諸表の注記(未監査)
A。プレゼンテーションの基礎と会計方針
プレゼンテーションの基礎
添付の要約連結財務諸表は未監査であり、Vertex Pharmaceuticals Incorporated(「Vertex」、「私たち」、「私たち」または「当社」)が米国で一般に認められている会計原則(「米国会計基準」)に従って作成しています。
要約された連結財務諸表には、Vertexと当社の完全子会社の事業が反映されています。重要な会社間残高と取引はすべて削除されました。私たちは事業を行っています 一 セグメント、医薬品。
2023年12月31日に終了した会計年度のフォーム10-Kの年次報告書(「フォーム10-Kの2023年次報告書」)に通常含まれている特定の情報と脚注の開示は、要約または省略されています。これらの中間財務諸表は、経営陣の見解では、2024年および2023年3月31日に終了した中間期間の財政状態と収益結果を公正に表示するために必要な、通常の定期的な調整をすべて反映しています。
中間期の経営成績は、必ずしも会計年度全体で予想される経営成績を示すものではありません。これらの中間財務諸表は、フォーム10-Kの2023年次報告書に含まれる2023年12月31日に終了した年度の監査済み財務諸表と併せて読む必要があります。
見積もりの使用
米国会計基準に従って要約連結財務諸表を作成するには、要約連結財務諸表の日付における報告された資産と負債の金額と偶発資産と負債の開示、および報告期間中の収益と費用の金額に影響する特定の見積もりと仮定を行う必要があります。私たちは、歴史的経験やその他のさまざまな仮定に基づいて見積もりをしています。その中には、特定の状況下では合理的であると当社が考える将来の予測も含まれます。実際の結果はそれらの見積もりとは異なる可能性があります。見積もりの変更は、判明した時期に報告される結果に反映されます。
最近採択された会計基準
フォーム10-Kの2023年次報告書の注記A「事業の性質と会計方針」に記載されているように、2023年12月31日に終了した3年間、連結財務諸表に大きな影響を与える会計基準は採用しませんでした。
最近発行された会計基準
セグメントレポート
2023年、財務会計基準審議会(「FASB」)は、2023-07年会計基準更新(「ASU」)2023-07「セグメント報告(トピック280):報告対象セグメント開示の改善(「ASU 2023-07」)を発表しました。これにより、公的機関は重要なセグメント費用やその他のセグメント項目の開示を求めています。ASU 2023-07はまた、公的機関に対し、報告対象セグメントの損益と、現在毎年必要とされている資産に関するすべての開示を中間期間に行うことを義務付けています。ASU 2023-07は、2024年1月1日から始まる年間期間と、2025年1月1日から始まる中間期間に有効になります。ASU 2023-07の採用がセグメントの開示に与える影響を分析中です。
所得税の開示
2023年、FASBはASU 2023-09「所得税(トピック740):所得税開示の改善」(「ASU 2023-09」)を発行しました。これにより、公的機関は、連邦、州、および外国の所得税に関する追加のカテゴリの情報を税率調整表に開示し、項目が量的基準を満たしている場合は、一部のカテゴリの調整項目に関する詳細情報を提供する必要があります。ASU 2023-09は、2025年1月1日から始まる年間期間に有効になります。ASU 2023-09の採用が所得税の開示に与える影響を分析中です。
重要な会計方針の要約
当社の重要な会計方針は、フォーム10-Kの2023年次報告書の注記A「事業の性質と会計方針」に記載されています。
目次
バーテックス・ファーマシューティカルズ・インコーポレイテッド
要約連結財務諸表の注記(未監査)
B。収益認識
収益の細分化
製品別の収益
「製品収益、純額」は次のもので構成されていました:
| | | | | | | | | | | | | | | |
| | | 3月31日に終了した3か月間 |
| | | | | 2024 | | 2023 |
| | | | | | | |
| | | | | (百万単位) |
| トリカータ/カトリオ | | | | | $ | 2,483.6 | | | $ | 2,096.7 | |
| その他のCF製品 | | | | | 207.0 | | | 278.1 | |
| 製品の総収入、純額 | | | | | $ | 2,690.6 | | | $ | 2,374.8 | |
地理的位置別の製品収益
お客様の所在地に基づく、地域別の「製品収益、純額」は、次のもので構成されます。
| | | | | | | | | | | | | | | |
| | | 3月31日に終了した3か月間 |
| | | | | 2024 | | 2023 |
| | | | | | | |
| | | | | (百万単位) |
| 米国 | | | | | $ | 1,519.9 | | | $ | 1,403.8 | |
| 米国以外では | | | | | | | |
| ヨーロッパ | | | | | 967.4 | | | 807.2 | |
その他 | | | | | 203.3 | | | 163.8 | |
| 米国以外の製品の総収入 | | | | | 1,170.7 | | | 971.0です | |
製品の総収入、純額 | | | | | $ | 2,690.6 | | | $ | 2,374.8 | |
契約負債
私たちの契約負債は$でした275.8 百万と $170.3 2024年3月31日および2023年12月31日時点でそれぞれ100万件です。これは、当社の嚢胞性線維症(「CF」)製品について受け取ることができる年間償還額が制限されている、国際市場の政府所有および支援を受けている顧客との年間契約に関するものです。 お客様と当社との契約で定められた年間払い戻し額を超えると、当社のCF製品は無料で提供されます。これは重要な権利です。これらの契約には、前払いと手数料が含まれます。契約に基づく年間払い戻し額を超えると予想される場合は、年間払い戻し限度額に達した出荷に対して受け取った対価の一部を、「その他の流動負債」の一部として繰り延べます。払い戻し限度額に達すると、無料の商品を発送するときに、繰延金額が収益として認識されます。当社のCF商品収益契約には、1年以内の履行義務が含まれています。
各会計年度末の当社の契約負債は、契約に関連する年間期間が当社の会計年度とは異なる国際市場におけるCFの年間償還限度額のある契約に関するものです。これらの市場では、過去数年間に履行された履行義務に関連する収益を認識しています。ただし、これらの収益は、今年度の初めの12か月以上前に履行された履行義務には含まれていません。
C。コラボレーション、ライセンス、その他の取り決め
私たちは、研究、開発、商品化プログラムの協力、技術のライセンス供与、または資産の取得について、第三者と多数の契約を締結しています。私たちの「取得した製造中の研究開発費」には$が含まれていました76.8 百万と $347.1 2024年3月31日および2023年3月31日に終了した3か月間で、それぞれ100万ドルです。これは、前払い、偶発的なマイルストーン、または当社の事業開発取引に基づくその他の支払いに関連します。
目次
バーテックス・ファーマシューティカルズ・インコーポレイテッド
要約連結財務諸表の注記(未監査)
コラボレーション、第三者技術のライセンス、進行中の研究開発とみなされる資産の取得。
2024年3月31日および2023年3月31日に終了した3か月間の財務諸表に大きな影響を与えた、または2024年3月31日に終了した3か月間に新規または大幅に改訂された、当社のコラボレーション、ライセンス、および資産取得契約は以下のとおりです。その他の契約は、フォーム10-Kの2023年次報告書の注記B「コラボレーション、ライセンス、その他の取り決め」に記載されています。
インライセンス契約
CRISPR Therapeutics AG
CRISPR-Cas9遺伝子編集療法に関する契約
2015年、私たちはCRISPR Therapeutics AGおよびその関連会社(「CRISPR」)と戦略的協力、オプション、ライセンス契約(「CRISPR契約」)を締結しました。これは、CRISPR-Cas9遺伝子編集技術を使用して、ヒトの疾患の根底にある遺伝的原因を対象とした潜在的な新しい治療法の発見と開発に協力するためです。私たちは特定のターゲットをライセンスする独占権を持っていました。2019年に、私たちは独占ライセンスを選択しました 三 CRISPR協定に基づくCFを含むターゲット。それぞれについて 三 ライセンスを取得することを選択したターゲット、CRISPRは最大$の追加収入を得る可能性があります410.0 開発、規制、商業上のマイルストーンとして100万件に上り、その結果生じる純製品売上高に対するロイヤルティもあります。
2017年、私たちはCRISPR(「CRISPR JDCA」)と共同開発および商品化契約を締結しました。CRISPR JDCA」)は、CRISPR契約の条件に従って2021年に修正および再表示しました。CRISPR JDCAの下で、私たちとCRISPRは、重度の鎌状赤血球症(「SCD」)や輸血依存性ベータサラセミアの治療を含む、ヘモグロビノパシーの治療薬としてCASGEVYを共同開発し、共同商品化する準備を進めていました。
CRISPR JDCAに従い、私たちはCRISPRの支援を受けて、CASGEVYの世界的な開発、製造、商品化を主導しています。また、CRISPRの特定の活動を行う権利を条件として、CRISPR JDCAのもとで、他の製品候補や製品に関連するすべての研究、開発、製造、商品化活動を世界中で実施しています。
CASGEVYは、2023年12月に米国食品医薬品局によってSCDの治療薬として承認されました。この承認に関連して、私たちは$を稼ぎました200.02024年1月にCRISPRに100万マイルストーン支払いました。これは「その他の流動負債」として計上され、2023年12月31日現在の連結貸借対照表の「その他の無形資産、純額」に記録されています。CASGEVYの販売承認を受けた後も、CRISPRの特定の活動を行う権利を条件として、CRISPR JDCAの下で研究開発活動を主導し続けています。私たちはCRISPRからその代金を払い戻されています 40これらの研究開発活動の割合は、一定の調整を条件とします。CRISPRからのこの払い戻しは、「研究開発費」のクレジットとして計上されます。また、CRISPRと共有しています 40CASGEVYに関して発生した純商業利益または損失の割合。一定の調整を条件として、「売上原価」に記録されます。純商業利益または純損失は、CRISPR JDCAに関連して当社が認識した製品収益、売上原価、販売原価、一般管理費の合計に等しくなります。
2024年3月31日に終了した3か月間で、CRISPR JDCAに基づくCRISPRからの純償還額を、「売上原価」のクレジットとして計上しました15.8 百万、CRISPR JDCAの純商業損失に占めるCRISPRのシェア、および「研究開発費」のドルに関連します11.7 百万。CRISPR JDCAの研究開発活動におけるCRISPRのシェアに関するものです。
2023年12月からさまざまな市場でCASGEVYの販売承認を受ける前に、私たちは費用分担の取り決めとしてCRISPR JDCAを会計処理し、CASGEVYに関連して発生した費用を割り当てました。 60%を私たちに 40CRISPRへの%、一定の調整が必要です。2023年3月31日に終了した3か月間で、CRISPRからの純償還額は「研究開発費」のクレジットとして計上されました17.9 百万ドル、そして「販売費、一般管理費」に5.8 百万。CRISPR JDCAの営業経費に占めるCRISPRのシェアに関するものです。
CRISPR-Cas9遺伝子編集低免疫細胞療法契約
2023年3月、1型糖尿病(「T1D」)の低免疫細胞療法の開発を加速するために、CRISPRのCRISPR-Cas9遺伝子編集技術を使用するための非独占的ライセンス契約(「CRISPR T1D契約」)を締結しました。CRISPR T1D契約に従い、私たちは1ドルを稼ぎました100.0 CRISPRへの100万件の前払い金で、当社の前払いの公正価値のほぼすべては、進行中の研究開発に起因するものであり、そのために代替の将来的な用途はなく、そのような実質的なプロセスは取得されていないと判断しました
目次
バーテックス・ファーマシューティカルズ・インコーポレイテッド
要約連結財務諸表の注記(未監査)
ビジネスを構成します。CRISPRは最大$の追加を受け取る資格があります160.0 契約によって生じる可能性のあるあらゆる製品の研究、開発、規制、および商業上のマイルストーンが100万件に達しました。また、その結果生じる製品の純売上高に対するロイヤルティも含まれます。
エントラーダ・セラピューティクス株式会社
2023年2月、私たちは、筋緊張性ジストロフィー1型(「DM1」)の細胞内治療薬の発見と開発に焦点を当てた戦略的コラボレーションおよびライセンス契約(「Entrada契約」)をEntrada Therapeutics, Inc.(「Entrada」)と締結しました。決算時に、$を前払いしました225.1 エントラーダに100万ドル、そして$を購入しました24.9 エントラーダ契約に関連するエントラーダの普通株式100万株。私たちは、前払いの公正価値のほぼすべてが進行中の研究開発に起因するものであり、将来の代替用途はなく、事業を構成する実質的なプロセスは取得されていないと判断しました。2023年3月31日に終了した3か月間の「取得した進行中の研究開発費」の前払い金を記録しました。Entradaの普通株式への投資を公正価値で要約した連結貸借対照表の「有価証券」に記録しました。2024年の第1四半期に、エントラーダは1ドルを稼ぎました75.0百万マイルストーン。これは、2024年3月31日に終了した3か月間の「処理中の研究開発費用」に記録され、2024年3月31日現在の「その他の流動負債」に計上されました。Entradaは最大$の追加を受け取る資格があります335.0 Entrada契約によって生じる可能性のあるあらゆる製品の開発、規制、および商業上のマイルストーンが100万件に達しました。また、その結果生じる製品の純売上高に対するロイヤルティも同様です。
嚢胞性線維症財団
2004年、私たちは嚢胞性線維症財団セラピューティクス社の後継者として、研究開発活動を支援するために、嚢胞性線維症財団と協力契約を締結しました。修正されたコラボレーション契約に従い、2014年2月28日以前に研究期間中に最初に合成および/または試験された対象化合物には、イバカフトール、ルマカフトール、テザカフトール、テザカフトールを含め、1桁台から10ドル以下の段階的なロイヤルティを支払うことに合意しました。また、3月1日の間に最初に合成および/または試験された特定の化合物の潜在的な純売上高については、1桁台前半から一桁台半ばまでのロイヤルティを支払うことに合意しました、2014 年と 2016 年 8 月 31 日、エレキサカプターを含みます。2016年9月1日以降に最初に合成および試験された化合物については、ロイヤリティ義務はありません。ORKAMBI、SYMDEKO/SYMKEVI、TRIKAFTA/KAFTRIOなどのコンビネーション製品では、売上高はコンビネーション製品の各医薬品有効成分に均等に割り当てられます。これらのロイヤリティ義務に関連する費用を「売上原価」に記録します。
D。一株当たり利益
次の表は、終了した期間の普通株式1株あたりの基本および希薄化後の純利益の計算を示しています。
| | | | | | | | | | | | | | | |
| | | 3月31日に終了した3か月間 |
| | | | | 2024 | | 2023 |
| | | | | | | |
| | | | | (百万単位、1株あたりの金額を除く) |
| 純利益 | | | | | $ | 1,099.6 | | | $ | 699.8 | |
| | | | | | | |
| 基本加重平均発行済普通株式 | | | | | 258.2 | | | 257.4 | |
| 希薄化が懸念される有価証券の影響: | | | | | | | |
制限付株式ユニット(業績ベースの制限付株式ユニット(「PSU」)を含む) | | | | | 1.7 | | | 1.6 | |
| ストック・オプション | | | | | 1.2 | | | 1.3 | |
従業員の株式購入プログラム | | | | | 0.0 | | | 0.0 | |
| 希薄化後の加重平均発行済普通株式 | | | | | 261.1 | | | 260.3 | |
| | | | | | | |
| 普通株式1株当たりの基本純利益 | | | | | $ | 4.26 | | | $ | 2.72 | |
| 普通株式1株当たりの希薄化後純利益 | | | | | $ | 4.21 | | | $ | 2.69 | |
目次
バーテックス・ファーマシューティカルズ・インコーポレイテッド
要約連結財務諸表の注記(未監査)
普通株式1株あたりの希薄化後純利益の計算には、次の表の有価証券を含めませんでした。これは、各期間において希薄化防止効果が生じるためです。
| | | | | | | | | | | | | | | |
| | | 3月31日に終了した3か月間 |
| | | | | 2024 | | 2023 |
| | | | | | | |
| | | | | (百万単位) |
| 権利が確定していない制限付株式ユニット(PSUを含む) | | | | | — | | | 0.6 | |
| | | | | | | |
E。公正価値測定
以下の公正価値階層は、当社の金融資産と負債の公正価値を決定するために使用される観察可能なインプットと観察不可能なインプットに基づいて資産と負債を分類するために使用されます。
| | | | | |
レベル 1: | 同一の資産または負債の活発な市場における相場価格。資産または負債の活発な市場とは、継続的に価格情報を提供するのに十分な頻度と量で資産または負債の取引が行われる市場です。 |
レベル 2: | レベル1の入力以外の観測可能な入力。レベル2のインプットの例としては、類似の資産または負債の活発な市場における相場価格や、活発でない市場における同一の資産または負債の相場価格などがあります。 |
レベル 3: | 市場参加者が資産または負債の価格設定に使用するであろう仮定の評価に基づいた、観察できないインプット。 |
次の表は、公正価値測定の対象となる当社の金融資産と負債を公正価値階層内のレベル別に示しています。
| | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | |
| 2024年3月31日現在 | | 2023年12月31日現在 |
| 合計 | | レベル 1 | | レベル 2 | | レベル 3 | | 合計 | | レベル 1 | | レベル 2 | | レベル 3 |
| | | | | | | | | | | | | | | |
| (百万単位) |
公正価値で保有される金融商品(資産ポジション): |
| 現金同等物 | $ | 5,865.3 | | | $ | 4,921.3 | | | $ | 944.0 | | | $ | — | | | $ | 7,033.9 | | | $ | 5,397.3 | | | $ | 1,636.6 | | | $ | — | |
市場性のある証券: | | | | | | | | | | | | | | | |
| コーポレートエクイティ証券 | 43.4 | | | 43.4 | | | — | | | — | | | 46.0 | | | 46.0 | | | — | | | — | |
| 米国財務省証券 | 1,389.4 | | | 1,389.4 | | | — | | | — | | | 546.5 | | | 546.5 | | | — | | | — | |
米国政府機関の証券 | 356.7 | | | — | | | 356.7 | | | — | | | 425.2 | | | — | | | 425.2 | | | — | |
| 資産担保証券 | 792.6 | | | — | | | 792.6 | | | — | | | 306.0 | | | — | | | 306.0 | | | — | |
| 預金証書 | 42.6 | | | — | | | 42.6 | | | — | | | 33.7 | | | — | | | 33.7 | | | — | |
| 企業債務証券 | 2,632.2 | | | — | | | 2,632.2 | | | — | | | 1,802.8 | | | — | | | 1,802.8 | | | — | |
| コマーシャル・ペーパー | 137.8 | | | — | | | 137.8 | | | — | | | 186.8 | | | — | | | 186.8 | | | — | |
| 前払費用およびその他の流動資産: | | | | | | | | | | | | | | | |
| 外貨先渡契約 | 26.3 | | | — | | | 26.3 | | | — | | | 1.8 | | | — | | | 1.8 | | | — | |
| | | | | | | | | | | | | | | |
| | | | | | | | | | | | | | | |
金融資産総額 | $ | 11,286.3 | | | $ | 6,354.1 | | | $ | 4,932.2 | | | $ | — | | | $ | 10,382.7 | | | $ | 5,989.8 | | | $ | 4,392.9 | | | $ | — | |
| | | | | | | | | | | | | | | |
公正価値で保有される金融商品(負債ポジション): |
| その他の流動負債: | | | | | | | | | | | | | | | |
外貨先渡契約 | $ | (1.4) | | | $ | — | | | $ | (1.4) | | | $ | — | | | $ | (33.7) | | | $ | — | | | $ | (33.7) | | | $ | — | |
| | | | | | | | | | | | | | | |
| その他の長期負債: | | | | | | | | | | | | | | | |
| | | | | | | | | | | | | | | |
| 不測の事態への対価 | (77.3) | | | — | | | — | | | (77.3) | | | (77.4) | | | — | | | — | | | (77.4) | |
金融負債合計 | $ | (78.7) | | | $ | — | | | $ | (1.4) | | | $ | (77.3) | | | $ | (111.1) | | | $ | — | | | $ | (33.7) | | | $ | (77.4) | |
投資の種類別の帳簿価額および関連する未実現利益(損失)については、注記F「有価証券および株式投資」を参照してください。当社の現金同等物には、主にマネーマーケットファンドと定期預金が含まれます。
コーポレート・エクイティ証券の公正価値
私たちは、上場企業株式への投資を、要約連結貸借対照表では「有価証券」として分類しています。一般的に、上場企業の普通株式への投資は評価に基づいています
目次
バーテックス・ファーマシューティカルズ・インコーポレイテッド
要約連結財務諸表の注記(未監査)
レベル1のインプットは、公正価値が簡単に決定できるからです。ただし、上場企業への当社の投資の中には、投資に伴う譲渡制限により、レベル2のインプットに基づいて評価されてきた、または今後も評価され続けているものがあります。
2024年3月31日現在、上場企業株式への当社の投資の1つに、2024年に一部が満了し、一部が2025年に失効する契約上の販売制限の対象となっており、公正価値の合計はドルです。23.0 百万。この投資は、2023年の第1四半期に上場企業から直接購入しましたが、上記の期間の前にこの制限が失効するような状況はないと予想しています。
これらの投資の詳細については、注記F「有価証券および株式投資」を参照してください。
偶発的対価の公正価値
2019年に、デュシェンヌ型筋ジストロフィー(「DMD」)やDM1を含むその他の重度の神経筋疾患を引き起こす突然変異を修復するための革新的な遺伝子編集療法の開発に焦点を当てた非公開企業であるExonics Therapeutics、Inc.(「Exonics」)を買収しました。私たちのレベル3の偶発対価負債は、$に関連しています678.3 Exonicsの元株主には、開発と規制に関する何百万ものマイルストーンが支払われる可能性があります。私たちは、遺伝子治療に起因する業界データと、プログラムの進捗状況と実行可能性に関する知識に基づいて、偶発的支払いの公正価値に関連するマイルストーンを達成する確率を推定しています。条件付支払いの評価モデルで使用された割引率。 5.1% と 5.32024年3月31日現在の%は、負債の決済に関連する信用リスクと市場リスクの指標です。各報告期間におけるこれらの仮定の妥当性の判断には、慎重な判断が下されます。
次の表は、当社の偶発的対価負債の公正価値の繰り越しを示しています。
| | | | | | | | | | | |
| 2024年3月31日に終了した3か月間 | | | | | | |
| (百万単位) | | | | | | |
| 2023年12月31日現在の残高 | $ | 77.4 | | | | | | | |
条件付支払いの公正価値の低下 | (0.1) | | | | | | | |
| 2024年3月31日現在の残高 | $ | 77.3 | | | | | | | |
F。市場性のある証券と株式投資
公正価値で記録されている当社の現金同等物および有価負債および株式の概要を以下に示します。
| | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | |
| 2024年3月31日現在 | | 2023年12月31日現在 |
| 償却コスト | | キモい
未実現
利益 | | キモい
未実現
損失 | | フェア 価値 | | 償却コスト | | キモい
未実現
利益 | | キモい
未実現
損失 | | フェア 価値 |
| | | | | | | | | | | | | | | |
| (百万単位) |
現金同等物 | $ | 5,865.3 | | | $ | — | | | $ | — | | | $ | 5,865.3 | | | $ | 7,033.9 | | | $ | — | | | $ | — | | | $ | 7,033.9 | |
| 市場性のある証券: | | | | | | | | | | | | | | | |
| 米国財務省証券 | 1,395.1 | | | 1.1 | | | (6.8) | | | 1,389.4 | | | 544.5 | | | 3.0 | | | (1.0) | | | 546.5 | |
米国政府機関の証券 | 357.7 | | | 0.1 | | | (1.1) | | | 356.7 | | | 424.8 | | | 0.9 | | | (0.5) | | | 425.2 | |
| 資産担保証券 | 793.5 | | | 0.7 | | | (1.6) | | | 792.6 | | | 304.9 | | | 1.4 | | | (0.3) | | | 306.0 | |
| 預金証書 | 42.6 | | | 0.0 | | | (0.0) | | | 42.6 | | | 33.7 | | | 0.0 | | | (0.0) | | | 33.7 | |
企業債務証券 | 2,637.4 | | | 4.3 | | | (9.5) | | | 2,632.2 | | | 1,794.0 | | | 10.5 | | | (1.7) | | | 1,802.8 | |
コマーシャル・ペーパー | 137.9 | | | 0.0 | | | (0.1) | | | 137.8 | | | 186.8 | | | 0.1 | | | (0.1) | | | 186.8 | |
市場性のある売却可能な負債証券の総数 | 5,364.2 | | | 6.2 | | | (19.1) | | | 5,351.3 | | | 3,288.7 | | | 15.9 | | | (3.6) | | | 3,301.0 | |
コーポレートエクイティ証券 | 72.1 | | | — | | | (28.7) | | | 43.4 | | | 72.1 | | | — | | | (26.1) | | | 46.0 | |
市場性のある有価証券の合計 | 5,436.3 | | | 6.2 | | | (47.8) | | | 5,394.7 | | | 3,360.8 | | | 15.9 | | | (29.7) | | | 3,347.0 | |
| 現金同等物と有価証券の合計 | $ | 11,301.6 | | | $ | 6.2 | | | $ | (47.8) | | | $ | 11,260.0です | | | $ | 10,394.7 | | | $ | 15.9 | | | $ | (29.7) | | | $ | 10,380.9 | |
目次
バーテックス・ファーマシューティカルズ・インコーポレイテッド
要約連結財務諸表の注記(未監査)
上記の表の公正価値での金額は、当社の要約連結貸借対照表では次のように分類されています。
| | | | | | | | | | | |
| 2024年3月31日現在 | | 2023年12月31日現在 |
| | | |
| (百万単位) |
| 現金および現金同等物 | $ | 5,865.3 | | | $ | 7,033.9 | |
市場性のある証券 | 1,013.3 | | | 849.2 | |
| 長期市場性のある証券 | 4,381.4です | | | 2,497.8 | |
合計 | $ | 11,260.0です | | | $ | 10,380.9 | |
契約満期別の市場性のある売却可能な債務証券は次のとおりです。
| | | | | | | | | | | |
| 2024年3月31日現在 | | 2023年12月31日現在 |
| | | |
| (百万単位) |
| 1年以内に成熟します | $ | 969.9 | | | $ | 803.2 | |
1年から5年後に成熟します | 4,273.3 | | | 2,495.6 | |
| 5年後に成熟します | 108.1 | | | 2.2 | |
合計 | $ | 5,351.3 | | | $ | 3,301.0 | |
やった いいえ2024年および2023年3月31日に終了した3か月間の当社の市場性のある売却可能な負債証券の公正価値または総実現損益を調整するために、信用損失引当金をすべて記録します。さらに、私たちは いいえ2024年および2023年3月31日に終了した3か月間の当社の要約連結損益計算書に重要な実現利益または損失を記録します。2024年3月31日現在、私たちは公正価値総額$の市場性のある売却可能な負債証券を保有していました4.0 未実現損失のポジションにあった10億ドル19.1 百万。この金額には、公正価値の合計が$の市場性のある売却可能な負債証券が含まれていました53.8百万ドル、未実現損失の合計は0.412か月以上にわたって未実現損失のポジションにあった100万件。私たちはこれらの投資を満期まで保有する予定であり、満期時にこれらの投資から実現損失が発生することはないと予想しています。
私たちは、企業株式への投資の公正価値の変動を、要約連結損益計算書に「その他(費用)収益、純額」に記録します。 2024年3月31日および2023年3月31日に終了した3か月間の、各期間の終了時に保有されていた公正価値が容易に決定できる企業株式の未実現(損失)純利益は次のとおりです。
| | | | | | | | | | | | | | | |
| | | 3月31日に終了した3か月間 |
| | | | | 2024 | | 2023 |
| | | | | | | |
| | | | | (百万単位) |
未実現(損失)純利益 | | | | | $ | (2.7) | | | $ | 6.4 | |
2024年3月31日現在、当社の要約連結貸借対照表の「その他の資産」に記録されている、公正価値が容易に決定できない当社の株式投資の帳簿価額は$でした74.3 百万。2024年3月31日に終了した3か月間に、公正価値が容易に決定できない株式投資の帳簿価額をドル引き下げました24.3価格の目に見える変化に基づくと100万です。
目次
バーテックス・ファーマシューティカルズ・インコーポレイテッド
要約連結財務諸表の注記(未監査)
G。その他の包括利益 (損失) の累計
次の表は、その他の包括利益(損失)の累計の推移を構成要素別にまとめたものです。
| | | | | | | | | | | | | | | | | | | | | | | |
| | | 未実現持株利益(損失)、税引後 | | |
| 外貨換算調整 | | 売却可能な負債証券について | | 外貨先渡契約について | | 合計 |
| | | | | | | |
| (百万単位) |
| 2023年12月31日現在の残高 | $ | 1.1 | | | $ | 9.6 | | | $ | (25.0) | | | $ | (14.3) | |
| 再分類前のその他の包括利益 (損失) | 6.8 | | | (20.5) | | | 47.2 | | | 33.5 | |
| その他の包括利益(損失)の累計から再分類された金額 | — | | | 0.8 | | | (2.7) | | | (1.9) | |
| 当期の純その他の包括利益 (損失) | 6.8 | | | (19.7) | | | 44.5 | | | 31.6 | |
| 2024年3月31日現在の残高 | $ | 7.9 | | | $ | (10.1) | | | $ | 19.5 | | | $ | 17.3 | |
| | | | | | | |
| 2022年12月31日現在の残高 | $ | (25.0) | | | $ | (0.1) | | | $ | 25.9 | | | $ | 0.8 | |
| 再分類前のその他の包括利益 (損失) | 10.0 | | | 2.9 | | | (9.6) | | | 3.3 | |
| その他の包括利益(損失)の累計から再分類された金額 | — | | | — | | | (17.2) | | | (17.2) | |
| 当期の純その他の包括利益 (損失) | 10.0 | | | 2.9 | | | (26.8) | | | (13.9) | |
| 2023年3月31日現在の残高 | $ | (15.0) | | | $ | 2.8 | | | $ | (0.9) | | | $ | (13.1) | |
H。ヘッジング
外貨先渡契約-ヘッジ商品として指定されています
私たちは、特定の外貨建ての予測商品収益の一部について、為替レートの変動の影響を緩和することを目的としたヘッジプログラムを維持しています。このプログラムには、米国会計基準に基づくキャッシュフローヘッジとして指定されている外貨先渡契約が含まれており、契約期間は1から 十八ヶ月。私たちは、ヘッジされた為替レートの変動の影響を受けた製品収益を認識したのと同じ時期に、要約連結損益計算書の「製品収益、純額」で、そのような契約の有効部分の実現損益を認識しています。
私たちは、外貨先渡契約(ヘッジ手段)と予測される商品収益(ヘッジ項目)との関係、およびさまざまなヘッジ活動を行うためのリスク管理の目的と戦略を正式に文書化します。これには、キャッシュフローヘッジとして指定されたすべての外貨先渡契約を予測取引と一致させることが含まれます。また、ヘッジの開始時と継続的な両方で、外貨先渡契約がヘッジ項目のキャッシュフローの変化を将来的にも遡及的に相殺するのに非常に効果的であるかどうかを正式に評価します。(i)外貨先渡契約がキャッシュフローヘッジとしてあまり効果的ではない、(ii)外貨先渡契約が非常に効果的なヘッジではなくなった、または(iii)予測取引が発生する可能性がなくなったと判断した場合、ヘッジ会計処理は将来的に中止します。私たちは、先渡契約の公正価値の変動と、ヘッジされるリスクの重要な条件と一致する条件での架空の外貨先渡契約の公正価値の変動に基づいて有効性を測定します。2024年3月31日現在、すべてのヘッジは非常に効果的であると判断されました。
私たちは、取引相手の信用リスクが外貨先渡契約の公正価値に与える影響を考慮しています。2024年3月31日および2023年12月31日現在、信用リスクは当社の外貨先渡契約の公正価値を変更しませんでした。
目次
バーテックス・ファーマシューティカルズ・インコーポレイテッド
要約連結財務諸表の注記(未監査)
次の表は、米国会計基準に基づくキャッシュフローヘッジとして指定されている未払いの外貨先渡契約の想定額を米ドルでまとめたものです。
| | | | | | | | | | | |
| 2024年3月31日現在 | | 2023年12月31日現在 |
| | | |
| 外国通貨 | (百万単位) |
| ユーロ | $ | 1,305.5 | | | $ | 1,720.6 | |
カナダドル | 190.0 | | | 229.5 | |
英国ポンド | 186.4 | | | 225.0 | |
オーストラリアドル | 122.1 | | | 153.3 | |
| スイスフラン | 50.5 | | | 63.9 | |
外貨先渡契約の総額 | $ | 1,854.5 | | | $ | 2,392.3 | |
外貨先渡契約-ヘッジ商品として指定されていません
また、契約満期未満の外貨先渡契約も締結しています 一か月は、為替レートの変動が会社間残高を含む金融資産と負債に与える影響を軽減することを目的としています。これらの契約は、米国会計基準に基づくヘッジ商品として指定されていません。このような契約の実現損益は、各期間の要約連結損益計算書の「その他(費用)収益、純額」で認識しています。2024年3月31日現在、私たちは じゃない 米国会計基準に基づくヘッジ会計が適用されていない未払いの外貨先渡契約があります。
2024年3月31日および2023年3月31日に終了した3か月間、要約連結損益計算書に外貨先渡契約に関連して次のことが確認されました。
| | | | | | | | | | | | | | | |
| | | 3月31日に終了した3か月間 |
| | | | | 2024 | | 2023 |
| | | | | | | |
| | | | | (百万単位) |
| ヘッジ商品として指定-AOCIから再分類されました | | | | | | |
| 製品収益、純額 | | | | | $ | 3.4 | | | $ | 22.0 | |
| ヘッジ商品として指定されていません | | | | | | | |
| その他(費用)収入、純額 | | | | | $ | (2.4) | | | $ | 3.6 | |
| | | | | | | |
| 要約連結損益計算書に報告された合計値 | | | | | | |
| 製品収益、純額 | | | | | $ | 2,690.6 | | | $ | 2,374.8 | |
| その他(費用)収入、純額 | | | | | $ | (31.2) | | | $ | 1.3 | |
次の表は、当社の要約連結貸借対照表に含まれる米国会計基準に基づくキャッシュフローヘッジとして指定されている未払いの外貨先渡契約の公正価値をまとめたものです。
| | | | | | | | | | | | | | | | | | | | |
| 2024年3月31日現在 |
| 資産 | | 負債 |
| クラス分け | | 公正価値 | | クラス分け | | 公正価値 |
| | | | | | |
| (百万単位) |
| 前払費用およびその他の流動資産 | | $ | 26.3 | | | その他の流動負債 | | $ | (1.4) | |
| | | | | | |
| | | | | | |
| | | | | | | | | | | | | | | | | | | | |
| 2023年12月31日現在 |
| 資産 | | 負債 |
| クラス分け | | 公正価値 | | クラス分け | | 公正価値 |
| | | | | | |
| (百万単位) |
| 前払費用およびその他の流動資産 | | $ | 1.8 | | | その他の流動負債 | | $ | (33.7) | |
| | | | | | |
| | | | | | |
目次
バーテックス・ファーマシューティカルズ・インコーポレイテッド
要約連結財務諸表の注記(未監査)
2024年3月31日現在、「前払費用およびその他の流動資産」および「その他の流動負債」に記録されている米国会計基準に基づくキャッシュフローヘッジとして指定されている外国為替先渡契約に関連する金額は、12か月以内に収益に再分類される予定です。
私たちは、外貨先渡契約の公正価値を総額ベースで要約連結貸借対照表に示しています。 次の表は、米国会計基準に基づくキャッシュフローヘッジとして指定されている金融商品の種類別にデリバティブを相殺することが、当社の要約連結貸借対照表に及ぼす潜在的な影響をまとめたものです。
| | | | | | | | | | | | | | | | | | | | | | | | | | | | | |
| 2024年3月31日現在 |
| 認識された総額 | | 総額オフセット | | 提示された総額 | | 総額は相殺されません | | リーガルオフセット |
| | | | | | | | | |
| 外貨先渡契約 | (百万単位) |
| 総資産 | $ | 26.3 | | | $ | — | | | $ | 26.3 | | | $ | (1.4) | | | $ | 24.9 | |
| 負債総額 | (1.4) | | | — | | | (1.4) | | | 1.4 | | | — | |
| | | | | | | | | | | | | | | | | | | | | | | | | | | | | |
| 2023年12月31日現在 |
| 認識された総額 | | 総額オフセット | | 提示された総額 | | 総額は相殺されません | | リーガルオフセット |
| | | | | | | | | |
| 外貨先渡契約 | (百万単位) |
| 総資産 | $ | 1.8 | | | $ | — | | | $ | 1.8 | | | $ | (1.8) | | | $ | — | |
| 負債総額 | (33.7) | | | — | | | (33.7) | | | 1.8 | | | (31.9) | |
私は。インベントリ
インベントリは次のもので構成されていました。
| | | | | | | | | | | |
| 2024年3月31日現在 | | 2023年12月31日現在 |
| | | |
| (百万単位) |
| 原材料 | $ | 95.7 | | | $ | 78.7 | |
| 作業中の作業 | 601.8 | | | 525.1 | |
完成品 | 115.6 | | | 135.0 | |
合計 | $ | 813.1 | | | $ | 738.8 | |
2024年の第1四半期に、急性疼痛に対するスゼトリジン(旧VX-548)とCFに対するバンザカフトール/テザカフトール/デューティバカフトールの2つの第3相試験に関する肯定的な結果を発表した後、計画されている製品発売に備えて生産された在庫の資産計上を開始しました。これらの決定は、とりわけ、安全性と有効性の結果、規制当局の承認と商業的成功の予想可能性などの評価に基づいて行いました。2024年の第1四半期以前は、これらの製品候補に関連する在庫費用と関連費用を「研究開発費」として支出していました。2024年3月31日現在、これらの在庫は当社の要約連結財務諸表にとって重要ではありませんでした。
目次
バーテックス・ファーマシューティカルズ・インコーポレイテッド
要約連結財務諸表の注記(未監査)
J。株式ベースの報酬費用と自社株買いプログラム
株式ベースの報酬費用
2024年3月31日および2023年3月31日に終了した3か月間に、以下の株式ベースの報酬費用が発生しました。
| | | | | | | | | | | | | | | |
| | | 3月31日に終了した3か月間 |
| | | | | 2024 | | 2023 |
| | | | | | | |
| | | | | (百万単位) |
| 賞の種類別の株式報酬費用: | | | | | | | |
| 制限付株式ユニット(PSUを含む) | | | | | $ | 187.2 | | | $ | 115.9 | |
| ESPPの株式発行 | | | | | 5.8 | | | 5.5 | |
| ストック・オプション | | | | | — | | | 1.4 | |
在庫に関連する株式ベースの報酬費用 | | | | | (1.1) | | | (0.4) | |
「総費用と経費」に含まれる株式ベースの報酬費用の総額 | | | | | $ | 191.9 | | | $ | 122.4 | |
| | | | | | | |
| 品目別の株式ベースの報酬費用: | | | | | | | |
| 売上原価 | | | | | $ | 1.8 | | | $ | 1.9 | |
| 研究開発費用 | | | | | 119.4 | | | 76.3 | |
| 販売費、一般管理費 | | | | | 70.7 | | | 44.2 | |
費用と費用に含まれる株式ベースの報酬費用の総額 | | | | | 191.9 | | | 122.4 | |
| 所得税効果 | | | | | (79.0) | | | (40.6) | |
株式ベースの報酬費用の合計、税引後 | | | | | $ | 112.9 | | | $ | 81.8 | |
株式買戻しプログラム
2023年2月、当社の取締役会は自社株買いプログラムを承認しました。これに基づき、当社は最大$までの自社株買いを行う権限を与えられています。3.010億の普通株式。このプログラムには有効期限がなく、いつでも中止できます。2024年と2023年3月31日に終了した3か月間に、私たちは買い戻しました335,773 そして 459,017 プログラムに基づく当社の普通株式をそれぞれ、合計で$の買い戻し140.4 百万と $135.6 それぞれ 100 万です。2024年3月31日現在、私たちは$を持っていました2.4 このプログラムによる残りの承認は10億です。
K。所得税
私たちは、米国の連邦税、州税、および外国所得税の対象となります。 2024年3月31日および2023年3月31日に終了した3か月間に、所得税引当金引当前利益と比較して、以下の所得税引当金と実効税率引当金を計上しました。
| | | | | | | | | | | | | | | |
| | | 3月31日に終了した3か月間 |
| | | | | 2024 | | 2023 |
| | | | | | | |
| | | | | (百万単位、パーセンテージを除く) |
| 所得税引当前利益 | | | | | $ | 1,279.1 | | | $ | 891.5です | |
| 所得税引当金 | | | | | $ | 179.5 | | | $ | 191.7 | |
2024年3月31日に終了した3か月間の当社の実効税率は、主に認識されていない税務上の地位の変化と、株式ベースの報酬に関連する超過税制上の優遇措置により、米国の法定税率よりも低くなりました。
2023年3月31日に終了した3か月間の当社の実効税率は、米国の法定税率を上回りました。これは主に、認識されていない税務上の地位の増加が、株式ベースの報酬に関連する超過税制上の優遇措置によって一部相殺されたためです。
目次
バーテックス・ファーマシューティカルズ・インコーポレイテッド
要約連結財務諸表の注記(未監査)
現在、税務当局による審査の対象となっているすべての課税年度について、納税申告書で取られた、または取るべき税務上の立場を確認しました。2024年3月31日と2023年12月31日の時点で、私たちはドルを持っていました301.6 百万と $288.7 未認識の税制上の優遇措置の純額はそれぞれ100万件で、認識されれば税率に影響します。
私たちは、さまざまな州、地方、外国の管轄区域で米国連邦所得税申告書と所得税申告書を提出します。私たちは世界中でいつでもさまざまな所得税監査を行っています。純営業損失または税額控除の繰越がある管轄区域を除き、連結財務諸表に重大な影響を与える法域では、2015年より前の数年間は税務当局からの税務評価の対象ではなくなりました。2023年に、2015年から2020年までの税務上の問題について英国の歳入関税庁(「HMRC」)と和解し、その後、2024年3月31日に終了した3か月間にその期間の閉鎖通知を受け取りました。調整の性質上、これらの事項に関する二重課税の軽減に関する相互合意手続きに従って、米国/英国の所得税条約に基づく権利を主張します。
2022年12月、欧州連合加盟国は、経済協力開発機構(「OECD」)のグローバルな国際税制改革イニシアチブである最低税要素(「第2の柱」)を実施することで合意しました。発効日は2024年1月1日と2025年1月1日です。2023年7月、OECDは、特定の発効日を2027年1月1日まで事実上延長する特定のセーフハーバーを提案する行政ガイダンスを発表しました。2024年の予測結果に基づいて、国ごとの世界最低税率15%が2024年に発生する可能性のあるリスクの評価は、当社の要約連結財務諸表にとって重要ではありません。当社が事業を展開するほとんどの法域の実効税率は 15% を超えているからです。
L。コミットメントと不測の事態
2022 クレジットファシリティ
2022年7月、Vertexとその一部の子会社はドルを締結しました500.0 管理代理人を務めるバンク・オブ・アメリカおよびそこに記載されている貸し手(以下「貸し手」)との100万件の無担保リボルビング・ファシリティ(「信用契約」)。2027年7月1日に満期を迎えます。クレジット契約は締結時に成立しておらず、現在も引き出していません。クレジット契約に従って引き出された金額は、もしあれば、一般的な企業目的に使用されます。特定の条件を満たすことを条件として、クレジット契約の借入能力をさらに1ドル増やすよう要求する場合があります500.0 百万。さらに、クレジット契約では$のサブリミットが定められています100.0 信用状の場合は100万です。
クレジット契約に基づいて借入された金額には、当社の選択により、基本金利または担保付オーバーナイト融資金利(「SOFR」)のいずれかで、いずれの場合にも該当する証拠金を加えた利息がかかります。クレジット契約に基づき、基本金利ローンに適用されるマージンは 0.000% から 0.500SOFRローンの%と適用されるマージンの範囲は 1.000% から 1.500%、いずれの場合も、当社の連結レバレッジ比率(直近の4会計四半期における連結積立負債総額と連結EBITDAの比率)に基づいています。
クレジット契約に従って借入された金額は、特定の例外を除いて、既存および将来の国内子会社によって保証されます。
信用契約には、慣習的な表明と保証、肯定契約と否定契約(特定の限られた例外の場合を除いて維持すべき財務契約を含む)の連結レバレッジ比率が含まれています 3.50 1.00まで、増える可能性があります 4.00 資料の購入後、1.00まで。2024年3月31日現在、私たちは上記の規約を遵守していました。クレジット契約には、慣習的なデフォルトイベントも含まれています。債務不履行が続く場合、管理代理人は、未払いのローンの未払い額の繰り上げなど、さまざまな救済策を行使する権利があります。
クレジット契約に関連する直接費用は、契約期間中に計上され、当社の財務諸表には重要ではありませんでした。
保証と補償
マサチューセッツ州の法律で認められているように、当社の組織規約および付則では、役員または取締役としての職務に関連して特定の役員および取締役に対して申し立てられた特定の請求について、その役員および取締役に補償することが規定されています。これらの補償条項に基づいて当社が支払う必要がある将来の最大支払い額は無制限です。しかし、私たちは、金銭的リスクを軽減し、将来支払われた金額の一部を回収できるようにする、取締役および役員の賠償責任保険を購入しました。 いいえ 補償請求は現在未解決であり、これらの補償契約の推定公正価値は最小限であると考えています。
目次
バーテックス・ファーマシューティカルズ・インコーポレイテッド
要約連結財務諸表の注記(未監査)
私たちは通常、製品開発プログラムにおける臨床試験研究者および施設との契約、学術機関や非営利機関とのスポンサーリサーチ契約、当社のサービスを行う当事者が関与するさまざまな同等の契約、および不動産リースにおける補償条項に、通常の事業過程で同意します。また、創薬、開発、商品化の協力契約における特定の補償条項にも慣習的に同意しています。当社の臨床試験および受託研究契約に関して、これらの補償規定は通常、当社の化合物または製品候補の研究または臨床試験に起因する人身傷害または物的損害、法律違反、または契約上の義務の特定の違反に関連して、治験責任医師または治験責任医師機関に対して申し立てられたすべての請求に適用されます。賃貸契約に関しては、補償規定は通常、当社が引き起こした人身傷害または物的損害、当社の法律違反、または契約上の義務の特定の違反に関連して家主に対して申し立てられた請求に適用されます。当社のコラボレーション契約に記載されている補償条項は、上記の他の契約のものと似ていますが、さらに、知的財産権の侵害を主張する第三者からの請求があった場合に、協力者に限定的な補償を提供します。上記のいずれの場合も、補償義務は通常、契約の終了後も一定期間存続しますが、通常、契約期間中とその後の短期間は、補償義務が最も重要であると考えています。これらの規定に基づいて当社が将来行うことが義務付けられる可能性のある最大支払い額は、通常無制限です。私たちは、人身傷害、物的損害、一般賠償責任を対象とする保険を購入しました。これにより、補償の対象が減り、多くの場合、将来支払われた金額の全部または一部を回収できるようになります。私たちは、これらの補償条項に関連する訴訟の弁護や請求の解決のために多額の支払いをしたことはありません。したがって、これらの補償契約の推定公正価値は最小限であると考えています。
その他の不測の事態
私たちには、通常の事業活動の過程で発生する特定の偶発債務があります。このような偶発負債は、将来の支出が発生する可能性が高く、そのような支出を合理的に見積もることができる場合に発生します。注記E「公正価値測定」で説明されている当社の偶発対価負債以外に、 いいえ 2024年3月31日または2023年12月31日の時点で発生した重要な偶発負債。
M。その他のキャッシュフロー情報
要約連結キャッシュフロー計算書に記載されている各期の初めと最後の現金、現金同等物、制限付現金は次のとおりでした。
| | | | | | | | | | | | | | | | | | | | | | | |
| 3月31日に終了した3か月間 |
| 2024 | | 2023 |
| 期間の開始 | | 期間終了 | | 期間の開始 | | 期間終了 |
| | | | | | | |
| (百万単位) |
| 現金および現金同等物 | $ | 10,369.1 | | | $ | 9,158.0 | | | $ | 10,504.0 | | | $ | 9,289.9 | |
前払費用およびその他の流動資産 | 3.2 | | | 11.4 | | | 8.0 | | | 5.7 | |
| | | | | | | |
| 要約連結キャッシュフロー計算書あたりの現金、現金同等物、制限付現金 | $ | 10,372.3 | | | $ | 9,169.4 | | | $ | 10,512.0です | | | $ | 9,295.6 | |
N。後続イベント
2024年4月、革新的なタンパク質ベースの免疫療法の発見と開発に注力する上場バイオテクノロジー企業であるアルパイン免疫科学株式会社(「アルパイン」)の発行済みおよび発行済み株式のすべてを約ドルで取得する契約と合併計画(「アルパイン合併契約」)を締結しました。4.910億の現金。アルパインの主要分子であるポベタシセプトは、BAFF(「B細胞活性化因子」)とAPRIL(「増殖誘導リガンド」)の非常に強力で効果的な二重拮抗薬です。第2相開発を通じて、ポベタシセプトはIgA腎症(「IgAN」)においてクラス最高の効力を示しました。IgA腎症は、末期腎疾患につながる可能性のある重篤で進行性の腎臓の自己免疫疾患です。この取引は、公開買付けの完了、ハート・スコット・ロディーノ独占禁止法に基づく待機期間の満了、その他の条件など、特定の慣習的な完了条件に従い、2024年の第2四半期に完了する予定です。買収が完了する期間に買収の会計処理を行います。買収資金は現金および現金同等物で賄うつもりです。
アイテム 2.経営陣による財政状態と経営成績の議論と分析
概要
私たちは、専門市場を中心に、重篤な疾患を持つ人々のための革新的な医薬品を開発するために科学革新に投資するグローバルなバイオテクノロジー企業です。生命を脅かす遺伝病である嚢胞性線維症(「CF」)の根本的な原因を治療する4つの医薬品と、重度の鎌状赤血球症(「SCD」)と寿命を縮める遺伝性血液疾患である輸血依存性ベータサラセミア(「TDT」)を治療する承認された治療法が1つあります。私たちのパイプラインには、CF、鎌状赤血球症、ベータサラセミア、急性および神経障害性疼痛、APOL1介在性腎疾患、1型糖尿病、筋緊張性ジストロフィー1型、アルファ1アンチトリプシン欠乏症、常染色体優性多発性嚢胞腎症の臨床段階のプログラムが含まれています。
TRIKAFTA/KAFTRIO(エレキサカフトール/テザカフトール/イバカフトールとイバカフトール)を中心に、当社が承認した4つのCF治療薬は、北米、ヨーロッパ、オーストラリアの約92,000人のCF患者のほぼ4分の3の治療に使用されています。私たちは、私たちのCFTRモジュレーターに反応する嚢胞性線維症の膜貫通コンダクタンスレギュレーター(「CFTR」)遺伝子に少なくとも1つの変異があるすべての人に低分子治療を提供することを目標に、年少の子供を含む他の患者集団でCF薬を評価しています。また、フルレングスのCFTRタンパク質を作らず、その結果、現在のCF薬の恩恵を受けられないCF患者のために、メッセンジャーリボ核酸(「mRNA」)と遺伝子療法を追求しています。
2023年後半から2024年初頭にかけて、非ウイルス性のCRISPR/Cas9遺伝子編集細胞療法であるCASGEVY(exagamglogene autotemcelまたは「exa-cel」)が、米国、EU、英国(「英国」)、サウジアラビア王国(「サウジアラビア」)、バーレーン王国(「バーレーン」)で承認されました。)SCDまたはTDTを患っている12歳以上の人の治療用です。米国とヨーロッパでは、重度のSCDまたはTDTを持つ約35,000人がCASGEVYの対象となり、サウジアラビアとバーレーンではさらに多くの人々がCASGEVYの対象となると推定しています。さらに、CFと急性疼痛の潜在的な新製品の短期的な発売に備えています。
財務ハイライト
| | | | | |
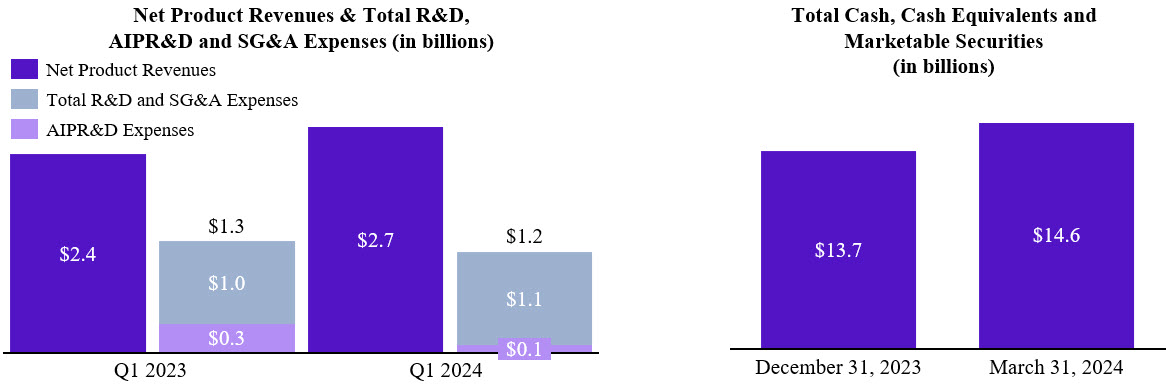
| 収入 | 2024年の第1四半期には、当社のCF製品の純収益は、2023年の第1四半期の24億ドルから27億ドルに増加しました。この増加は主に、米国以外の市場でのTRIKAFTA/KAFTRIOの継続的な好調な普及によるものでした。最近、若い年齢層での償還とラベルの拡張、および2歳から5歳のCFの小児を対象としたTRIKAFTAの発売後、米国でのTRIKAFTAのパフォーマンスも達成されました。 |
| 経費 | 当社の研究開発(「研究開発」)、買収中の研究開発費(「AIPR&D」)、販売費および一般管理費(「販管費」)の総額は、2023年第1四半期の13億ドルに対し、2024年第1四半期には12億ドルに減少しました。この減少は主にAIPR&Dの減少によるものです。売上原価は、2023年第1四半期の 11% に対し、2024年第1四半期は13%でした。これは主にCASGEVYに関連する売上原価によるものです。 |
| 現金 | 当社の現金、現金同等物および有価証券の総額は、2023年12月31日現在の137億ドルに対し、2024年3月31日時点で146億ドルに増加しました。これは主に、純製品収益による事業からの現金によるもので、事業開発費および普通株式の買戻しにより一部相殺されました。 |
注:上のグラフは四捨五入の関係で足し合わない場合があります。
ビジネスアップデート
市販製品
嚢胞性線維症
私たちは、(i)立ち上げの初期段階にある国の患者による継続的な導入、(ii)若い患者グループを含むラベルの拡大、(iii)CF患者の数の増加により、CF事業を拡大することを期待しています。継続的な普及とラベル拡大を支援する最近の活動の進捗状況は以下のとおりです。
•欧州委員会は、CFTR遺伝子に特異的な変異がある生後1か月から4か月未満のCF乳児の治療薬としてKALYDECOを承認しました。
鎌状赤血球症とベータサラセミア
•CASGEVYは、米国、EU、英国、サウジアラビア、バーレーンで、12歳以上のSCDまたはTDT患者を対象に承認されています。
•スイスとカナダのSCDとTDTの両方でCASGEVYの規制当局への提出を完了し、カナダでの規制当局への提出は優先審査されました。
•私たちは世界中で25以上の認定治療センターを活性化し、複数の患者が細胞採取を開始しました。
•CASGEVYへのアクセスを提供するために、米国の民間および政府の健康保険会社と複数の契約を締結しました。また、サウジアラビアとバーレーンのSCDまたはTDT患者、およびフランスでTDTを患っている人の早期アクセスプログラムを通じて、払い戻しを受けることができるようにしました。
潜在的な短期的なローンチの機会
私たちは、潜在的な新製品の以下の短期的な発売に備えています。
CFのヴァンザカフトール/テザカフトール/デューティバカクター
•2024年2月、私たちは、6歳以上のCF患者を対象としたバンザカフトール/テザカフトール/デューティバカフトールの次世代トリプルコンビネーション(「バンザカフトールトリプル」)のピボタルプログラムの肯定的な結果を発表しました。
•私たちは、優先審査券を使用して、6歳以上のCF患者を対象としたバンザカフトートリプルの規制マーケティング申請書を米国食品医薬品局(「FDA」)と欧州医薬品庁(「EMA」)に提出しました。2024年には、6歳以上のCF患者を対象とした世界的な規制当局への追加の提出を完了する予定です。
急性疼痛におけるスゼトリギン
•2024年1月、中等度から重度の急性疼痛の治療のための選択的NaV1.8阻害剤である当社の主要化合物であるスゼトリジン(旧VX-548)を評価した第3相臨床試験の肯定的な結果を発表しました。
•米国では、FDAが中等度から重度の急性疼痛の治療薬であるスゼトリギンの新薬申請(「NDA」)への順次提出を許可し、NDAの提出手続きを開始しました。2024年の第2四半期に提出を完了する予定です。Suzetrigineは、中等度から重度の急性疼痛の治療薬として、FDAからファストトラックおよびブレークスルーセラピーの指定を受けています。
パイプライン
私たちは、さまざまなモダリティを活用して、重篤な疾患に対して潜在的に変革をもたらす医薬品の多様なパイプラインを推進し続けています。これらの取り組みを支援する活動の最近の、または予想される進捗は以下のとおりです。
嚢胞性線維症
•2024年の後半には、第3相臨床試験の新しいコホートであるリッジラインを開始する予定です。このコホートでは、F508del変異またはトリプルコンビネーションCFTRモジュレーターに反応する変異が少なくとも1つあるCF2〜5歳の小児を対象に、バンザカフトールトリプルを評価する予定です。
•モデルナ社(「モデルナ」)と共同で、完全長CFTRタンパク質を産生しないCF患者を治療するためのネブライズドmRNA療法VX-522を開発しています。私たちは引き続き、CF患者を対象としたVX-522の第1/2相臨床試験の複数回漸増投与部分に患者を登録し、投与しています。この臨床試験のデータを2024年後半または2025年初頭に共有する予定です。
鎌状赤血球症と輸血依存性ベータサラセミア
•5歳から11歳のSCDまたはTDTの小児を対象にCASGEVYを評価する2つのグローバル第3相臨床試験への登録を完了しました。
•私たちは、副作用が軽度で、CASGEVYと組み合わせて使用できる骨髄除去コンディショニング剤の前臨床資産の開発に引き続き取り組んでいます。これにより、対象となる患者数が増える可能性があります。
急性の痛み
•2024年に、中等度から重度の急性疼痛の治療を目的とした次世代の選択的NaV1.8阻害剤であるVX-993の経口製剤を評価する第2相臨床試験を開始する予定です。
•FDAは、中等度から重度の急性疼痛の治療のためのVX-993の静脈内製剤の治験中の新薬申請(「IND」)を承認しました。第1相臨床試験を開始しました。
•私たちは、研究と開発の初期段階を通じて、複数のNaV1.7阻害剤を開発中です。これらは、急性および末梢神経障害性疼痛の治療に単独で、またはNaV1.8阻害剤と併用して使用できます。
末梢神経障害性疼痛
•FDAとのフェーズ2の終了会議が成功裏に終了した後、慢性末梢神経障害性疼痛の一般的な形態である糖尿病性末梢神経障害患者のスゼトリギンを評価するフェーズ3のピボットプログラムを2024年後半に開始する予定です。FDAは、この適応症でスゼトリギンにブレークスルーセラピーの指定を与えました。
•私たちは、末梢神経障害性疼痛の第2のタイプである腰仙神経根症患者を対象としたスゼトリギンを評価する第2相臨床試験に引き続き患者を登録し、投与しています。2024年末までに第2相臨床試験への登録を完了する予定です。
•末梢神経障害性疼痛の治療のためのVX-993の経口製剤を評価する第2相臨床試験を2024年に開始する予定です。
アポロ1が媒介する腎臓病
•イナキサプリンは、APOL1を介した限局性分節性糸球体硬化症(「FSGS」)を含む、APOL1を介した腎疾患(「AMKD」)の治療のための私たちの小分子です。独立データ安全監視委員会(「IDMC」)が審査した非盲検データの全体に基づいて、AMKD患者を対象としたグローバルな第2/3相臨床試験の第3相試験に進みました。この試験は、AMKDの10歳から17歳の青年を対象に拡大されました。
•この臨床試験は、48週目に、イナキサプリン群とプラセボ群で、タンパク尿のベースラインからのベースラインからの変化率を裏付けて、eGFRの傾きを評価する暫定分析を48週目に予定しています。肯定的であれば、中間分析が米国での承認を早めるための基礎となると期待しています。
1型糖尿病
•VX-880は、移植された細胞を保護するために標準的な免疫抑制法を使用する、同種幹細胞由来の完全分化型インスリン産生膵島細胞補充療法です。私たちは、VX-880を1型糖尿病(「T1D」)の潜在的な治療法として、3部構成の連続第1/2相臨床試験で評価しています。IDMCがレビューしたデータの全体に基づいて、T1Dを患い、低血糖症や再発する低血糖イベントに対する意識障害のある人を対象とした第1/2相臨床試験で投与を再開しました。17人の患者を対象としたグローバルな臨床試験のパートA、B、Cへの登録が完了し、今後数か月以内に投与が完了する予定です。
•T1Dの2番目のフェーズ1/2プログラムでは、同じVX-880の膵島細胞を免疫抑制が不要になるように設計された新しいデバイスにカプセル化するVX-264を評価します。この試験は、VX-264の安全性、耐容性、有効性を評価するための複数部にわたる連続研究です。臨床試験のパートAを完了し、パートBを開始しました。
•私たちの低免疫膵島細胞プログラムは、CRISPR/Cas9技術を使用して、VX-880とVX-264プログラムで使用されているのと同じ同種幹細胞由来の完全分化した膵島細胞を遺伝子編集します。目標は、免疫系から細胞を隠して、免疫抑制療法の必要性をなくすための別の可能な方法を模索することです。このプログラムは研究段階を経て発展し続けています。
筋緊張性ジストロフィー1型
•1型筋緊張性ジストロフィー(「DM1」)に対する当社の主たるアプローチであるVX-670は、エントラーダ・セラピューティクス株式会社(「Entrada」)から認可されました。VX-670は、細胞への効果的な送達を促進するために環状ペプチドに接続されたオリゴヌクレオチドで、DM1の根本的な原因に対処する可能性があります。
•米国でのVX-670のINDが承認され、カナダ、英国、EUでの臨床試験申請とオーストラリアでの臨床試験通知も承認されました。登録と投与が進行中です。
常染色体優性多発性嚢胞腎臓
•健康なボランティアを対象に、PKD1変異のサブセットを持つ人々の常染色体優性多発性嚢胞腎症(「ADPKD」)の根本的な原因を標的とするクラス初の小分子補正剤、VX-407を評価する第1相臨床試験を開始しました。
外部イノベーションへの投資
•2024年4月、私たちはアルパイン免疫科学株式会社(「アルパイン」)の発行済みおよび発行済み株式のすべてを約49億ドルで取得する契約および合併計画(「アルパイン合併契約」)を締結しました。アルパインの合併契約に従い、アルパインの普通株式の発行済み株式すべてを1株あたり65ドルで現金で購入する公開買付けを開始しました。公開買付けの完了、ハート・スコット・ロディーノ独占禁止法に基づく待機期間の満了、その他の条件など、特定の慣習的な条件に従い、取引は2024年の第2四半期に完了する予定です。
•アルパインの主要分子であるポベタシセプトは、BAFF(「B細胞活性化因子」)とAPRIL(「増殖誘導リガンド」)の非常に強力で効果的な二重拮抗薬です。第2相開発を通じて、ポベタシセプトはIgA腎症(「IgAN」)においてクラス最高の効力を示しました。IgA腎症は、末期腎疾患につながる可能性のある重篤で進行性の腎臓の自己免疫疾患です。米国では世界中で約13万人が罹患している原発性(特発性)糸球体腎炎の最も一般的な原因であるiGaNの根本的な原因を標的とする承認された治療法はありません。ポベタシセプトは、2024年の後半にiGaNの第3相臨床開発に入ると予想しています。自己免疫性腎疾患と血球減少症の第1/2相臨床試験が進行中で、データは2024年に発表される予定です。
•2024年の第1四半期にDM1でVX-670の臨床マイルストーンを達成し、その結果、Entradaに7,500万ドルのマイルストーンが支払われました。
私たちのビジネス環境
2024年の第1四半期に、当社の純製品収益は、CF治療用医薬品の販売によるものでした。私たちのCF戦略には、すべてのCF患者に利益をもたらす治療法の開発と承認と償還を継続的に行い、CFの適格者で当社の医薬品を受け取ることができる人の数を増やすことが含まれます。これには、ラベルの拡大、償還の拡大、新薬の開発などが含まれます。私たちは、米国、EU、英国、サウジアラビア、バーレーンでSCDとTDTの治療薬として販売承認を受けているCASGEVYを含む、CF以外の重篤な疾患の治療のための製品候補のパイプラインを進めています。
私たちの戦略は、因果関係のある人間生物学と治療科学の理解における変革的進歩を組み合わせて、革新的な医薬品を発見し開発することです。このアプローチには、複数のモダリティにまたがる各プログラムの複数の化合物または治療法を早期の臨床試験に進めて、後期開発のための最も有望な治療法の選択に役立つ患者データを取得することが含まれます。また、発見や開発努力の参考にもなります。私たちは、臨床的にも商業的にも永続的な成功を収めるために、潜在的にクラス最高の候補となる概念実証を達成したファーストインクラスの治療法を迅速にフォローすることを目指しています。
専門市場における新製品候補と治療法を追求するために、私たちは研究開発に投資しています。私たちは、さまざまな分野で研究を進めることで、製品開発に内在するリスクのバランスを取ることができ、今後数年間でパイプラインとなる製品候補を提供する可能性があると考えています。社内の研究プログラムを補完するために、私たちは技術やプログラムを取得し、一流の学術機関であるバイオ医薬品やテクノロジー企業と協力しています
必要に応じて、研究機関、政府研究所、財団、その他の組織が、治療上の関心のある分野の研究を進め、当社の戦略を実行するために必要な技術にアクセスします。
新しい医薬品や生物学的製剤の発見と開発は困難で時間のかかるプロセスであり、多大な財源と幅広い技術的および規制上の専門知識が必要です。業界全体で、ほとんどの潜在的な医薬品や生物製剤は開発段階に進むことはなく、開発段階に進んだほとんどの製品は販売承認を受けることはありません。製品候補への投資にはかなりのリスクが伴います。私たちは、発見、研究、臨床試験、非臨床研究の結果を注意深く監視し、リスクと可能性のバランスをとる目的で、新しいデータや科学的、ビジネス的、商業的な洞察に照らして製品開発プログラムを頻繁に評価しています。このプロセスにより、新しい情報が入手可能になり、進行中のプログラムや潜在的な新しいプログラム、および競合他社のプログラムについての理解が深まるにつれて、焦点や優先順位が急速に変化する可能性があります。
私たちのビジネスでは、製品の適切な製造と償還の確保も必要です。製品候補を臨床開発から商品化に向けて進め、承認された製品を市場投入して販売する中で、サプライチェーンと品質保証のリソースを構築して維持しています。私たちは、商業販売や承認後の臨床試験のための製品の製造と流通、および臨床試験用の製品候補の製造と流通を、中国を含む第三者のグローバルネットワークと社内の能力に頼っています。新たに承認された各製品のサプライチェーンを確立することに加えて、既存の製品のサプライチェーンを調整して、追加の配合を含めたり、必要に応じて既存製品の生産規模を拡大したりしています。当社の外国の第三者メーカーおよびサプライヤーは、バイオセキュア法、制裁、貿易制限、その他の外国の規制要件を含む米国の法律の対象となる場合があります。これにより、コストが増加したり、入手可能な材料の供給が減少したり、そのような材料の調達や供給が遅れたりする可能性があります。細胞療法や遺伝子治療のプロセスは、低分子医薬品に必要なプロセスよりも複雑で、さまざまなシステム、機器、施設、専門知識への追加投資が必要になる場合があります。私たちは、現在の製品とパイプラインプログラムのサプライチェーンの安定性を確保することに重点を置いています。
当社製品の売上は、政府の健康プログラム、商業保険、管理医療機関などの第三者支払者による当社製品の払い戻し額に大きく依存します。潜在的なパイプライン療法を含め、当社製品の払い戻しは保証できず、受け取るまでにかなりの時間がかかる場合があります。私たちは、米国および米国以外の市場の政府機関を含む第三者支払者から当社製品に対する適切なレベルの償還を得て維持するために、多大な管理およびその他のリソースを費やしています。
米国では、CF医薬品について適切な水準の償還を迅速に受けるために、第三者支払者と協力して成功を収めています。さらに、CASGEVYに関しては、米国政府や企業の支払者と協力しています。米国では、政府や企業の支払者がCASGEVYに幅広くアクセスできるようになると予想しています。最近、政府や企業の健康保険会社と、CASGEVYへのアクセスを提供するための複数の契約を締結しました。私たちは、支払者が私たちのすべての治療法がもたらす大きな利点を認識し、現在および将来、患者に適切なレベルで私たちの医薬品や治療法へのアクセスを提供できるように、通常は個々の州の当局によって管理される政府の健康プログラムとともに、多数の民間保険会社や管理医療機関と引き続き話し合いを続ける予定です。しかし、2022年のインフレ削減法や州法(透明性に関する法律や処方薬適正化委員会など)の成立など、最近の法律の変更が、第三者支払者との交渉を成功させ、製品を販売する能力にどのように影響するかは予測できません。同様に、米国以外の市場では、必要に応じて、国ごと、または地域ごとに、医薬品に対する政府からの償還を求めています。これは、新薬のたびに、また現在の医薬品のラベルを拡張するためにも必要です。CASGEVYに関しては、米国の元支払者と協力しており、長期の償還契約を結んでいます。私たちは、拡大されたアクセスプログラムを通じて、サウジアラビアとバーレーンではSCDまたはTDTを持っている人、フランスではTDTを持っている人のための払い戻しアクセスを確保しました。私たちは、CF医薬品、CASGEVY、そして最終的にはパイプライン療法の米国および米国以外の市場での償還を拡大および維持するために、引き続き多大なリソースを集中させていく予定です。
戦略的取引
買収
事業戦略の一環として、当社の企業戦略や研究開発戦略に合致し、継続的な研究開発活動を補完し、推進する技術、製品、製品候補およびその他の事業の獲得を目指しています。私たちは過去数年にわたり、非公開のバイオテクノロジー企業の買収を何度も行ってきました。2019年に、T1Dプログラムを確立したSemma Therapeutics, Inc. と、DM1やデュシェンヌ型筋ジストロフィーなどの重度の神経筋疾患を引き起こす突然変異を修復する遺伝子編集能力を強化したExonics Therapeutics, Inc. を買収しました。2022年に、T1Dプログラムの開発を加速させる可能性のある知的財産、ツール、技術、資産を保有するViaCyte、Inc.(「ViaCyte」)を買収しました。私たちの
ViaCyteの3億1,500万ドルでの買収は、企業結合として計上されました。買収日現在、現金による支払いは、主に製造中の研究開発資産ののれんと公正価値に割り当てられていました。
2023年と2022年には、資産買収として計上されたプログラムも買収しました。その結果、それぞれ4,750万ドルと6,000万ドルのAIPR&Dが得られました。
2024年4月、上記のようにアルパインを買収するためのアルパイン合併契約を締結しました。アルパインは、革新的なタンパク質ベースの免疫療法の発見と開発に焦点を当てた上場バイオテクノロジー企業です。アルパインの主要分子であるポベタシセプトは、フェーズ2の開発を通じて、iGaNでクラス最高の効力を示す可能性があります。取引完了時に約49億ドルの現金を支払い、買収資金は当社の現金および現金同等物で賄う予定です。買収が完了する期間に買収の会計処理を行います。
コラボレーションとインライセンスの取り決め
私たちは、継続的な研究開発活動を補完する可能性のある製品、製品候補およびその他の技術の開発、製造、商品化について、コラボレーションやライセンス契約を含む第三者と契約を結んでいます。過去数年にわたって、私たちはCRISPR Therapeutics AG(「CRISPR」)、エントラーダ、モデルナなど、多くの企業と協力契約を締結しました。通常、技術や製品の候補をライセンスする場合、協力者に前払いをしたり、プログラムの費用を負担したり、マイルストーン、ロイヤリティ、オプションの支払いなどの条件付支払いを行うことに同意します。これらのコラボレーションの支払いのほとんどはAIPR&Dとして支出されます。これには、2024年の第1四半期にEntradaに支払われる7,500万ドルのマイルストーンや、2023年の第1四半期にEntradaに2億2,510万ドル、T1Dに関連してCRISPRに1億ドルの前払い金が含まれます。これらの支払いは、主に買収した進行中の研究開発によるもので、将来的に代替手段がなかったため、AIPR&Dに支出されました。ただし、コラボレーションの構造、取得した技術の開発段階、コラボレーターの業務におけるライセンス製品候補の重要性、およびコラボレーターが従事するその他の活動など、多くの要因によって、これらの取引の会計処理は大幅に異なる場合があります。私たちは、これまで取り組んできたコラボレーションやライセンスと似ている、または異なる可能性のあるコラボレーションとライセンスの機会を引き続き特定し、評価していくことを期待しています。
獲得した製造中の研究開発費
2024年と2023年の第1四半期に、当社のAIPR&Dには、前払い、偶発的なマイルストーン、または上記のコラボレーション、第三者技術のライセンス、資産の取得など、事業開発取引に基づくその他の支払いに関連して、それぞれ7,680万ドルと3億4,710万ドルが含まれていました。コラボレーション、ライセンス契約、および資産取得に関する詳細については、注記C「コラボレーション、ライセンス、その他の取り決め」を参照してください。
操作の結果
| | | | | | | | | | | | | | | | | | | | | | | |
| | | | | 3月31日に終了した3か月間 | | |
| | | | | | | 2024 | | 2023 | | 変更 |
| | | | | | | | | | | |
| | | | | | | (百万単位。パーセンテージと1株当たりの金額を除く) |
製品収益、純額 | | | | | | | $ | 2,690.6 | | | $ | 2,374.8 | | | 13% |
| 運用コストと経費 | | | | | | | 1,551.1です | | | 1,595.8 | | | (3)% |
事業からの収入 | | | | | | | 1,139.5 | | | 779.0 | | | 46% |
| その他の営業外収益、純額 | | | | | | | 139.6 | | | 112.5 | | | 24% |
所得税引当金 | | | | | | | 179.5 | | | 191.7 | | | (6)% |
純利益 | | | | | | | $ | 1,099.6 | | | $ | 699.8 | | | 57% |
| | | | | | | | | | | |
| 希薄化後の普通株式1株あたりの純利益 | | | | | | | $ | 4.21 | | | $ | 2.69 | | | |
1株当たりの計算に使用される希薄化後の株式 | | | | | | | 261.1 | | | 260.3 | | | |
| | | | | | | |
製品収益、純額
| | | | | | | | | | | | | | | | | | | | | | | |
| | | | | 3月31日に終了した3か月間 | | |
| | | | | | | 2024 | | 2023 | | 変更 |
| | | | | | | | | | | |
| | | | | | | (百万単位、パーセンテージを除く) |
| トリカータ/カトリオ | | | | | | | $ | 2,483.6 | | | $ | 2,096.7 | | | 18% |
| その他のCF製品 | | | | | | | 207.0 | | | 278.1 | | | (26)% |
| 製品収益、純額 | | | | | | | $ | 2,690.6 | | | $ | 2,374.8 | | | 13% |
| | | | | | | | | | | |
| | | | | | | | | | | |
| | | | | | | |
2024年の第1四半期に、当社の純製品収益は、2023年の第1四半期と比較して3億1,580万ドル、つまり 13% 増加しました。この増加は主に、米国以外の市場でのTRIKAFTA/KAFTRIOの堅調な普及と、若い年齢層でのラベルの拡張、および2歳から5歳のCFの小児を対象としたTRIKAFTAの発売後の米国でのTRIKAFTAの業績によるものです。トリカフタ/カフトリオ以外のCF製品の収益の減少は、主に患者がこれらの医薬品からトリカフタ/カフトリオに切り替えたことが原因です。
米国および米国以外の市場からの当社の純製品収益は次のとおりです。
| | | | | | | | | | | | | | | | | | | | | | | |
| | | | | 3月31日に終了した3か月間 | | |
| | | | | | | 2024 | | 2023 | | 変更 |
| | | | | | | | | | | |
| | | | | | | (百万単位、パーセンテージを除く) |
| 米国 | | | | | | | $ | 1,519.9 | | | $ | 1,403.8 | | | 8% |
| 元米国人。 | | | | | | | 1,170.7 | | | 971.0です | | | 21% |
| 製品収益、純額 | | | | | | | $ | 2,690.6 | | | $ | 2,374.8 | | | 13% |
運用コストと経費
| | | | | | | | | | | | | | | | | | | | | | | |
| | | | | 3月31日に終了した3か月間 | | |
| | | | | | | 2024 | | 2023 | | 変更 |
| | | | | | | | | | | |
| | | | | | | (百万単位、パーセンテージを除く) |
| 売上原価 | | | | | | | $ | 342.6 | | | $ | 266.9 | | | 28% |
| 研究開発費用 | | | | | | | 789.1 | | | 742.6 | | | 6% |
| 進行中の研究開発費の取得 | | | | | | | 76.8 | | | 347.1 | | | (78)% |
| 販売費、一般管理費 | | | | | | | 342.7 | | | 241.1 | | | 42% |
| 条件付対価の公正価値の変更 | | | | | | | (0.1) | | | (1.9) | | | ** |
| 費用と経費の合計 | | | | | | | $ | 1,551.1です | | | $ | 1,595.8 | | | (3)% |
| | | | | | | | | | | |
| | | | | | | ** 意味がありません |
売上原価
当社の売上原価は主に、CF製品の純売上高に対して支払われる第三者のロイヤルティと在庫製造費で構成されています。嚢胞性線維症財団との契約に従い、TRIKAFTA/KAFTRIO、SYMDEKO/SYMKEVI、KALYDECO、ORKAMBIの売上に対する段階的な第三者ロイヤルティは、純売上高に対する割合として計算され、1桁から10桁未満の範囲で、TRIKAFTA/KAFTRIOの売上に対するロイヤルティは他の製品よりも低くなっています。過去数年間、当社の売上原価は、製品の純収益の増加により増加しています。当社の純製品収益に占める売上原価の割合は、2023年第1四半期の 11% から、2024年第1四半期には 13% に増加しました。これは主に、2023年第4四半期に規制当局が承認された後のCASGEVYに関連する売上原価によるものです。
研究開発費用
| | | | | | | | | | | | | | | | | | | | | | | |
| | | | | 3月31日に終了した3か月間 | | |
| | | | | | | 2024 | | 2023 | | 変更 |
| | | | | | | | | | | |
| | | | | | | (百万単位、パーセンテージを除く) |
| 研究費 | | | | | | | $ | 196.1 | | | $ | 166.8 | | | 18% |
開発費 | | | | | | | 593.0 | | | 575.8 | | | 3% |
研究開発費の合計 | | | | | | | $ | 789.1 | | | $ | 742.6 | | | 6% |
当社の研究開発費には、当社の製品および製品候補の研究開発にかかる内部および外部費用が含まれます。当社の研究開発グループの従業員は通常、複数の研究開発プログラムに分散しているため、給与や福利厚生、株式ベースの報酬費用、実験用品、その他の直接経費やインフラ費などの内部費用を、個々の製品や製品候補に割り当てません。私たちは、臨床研究機関やその他の外部委託研究から提供されたサービスの外部費用を個々のプログラムごとに割り当てます。私たちの内部コストは外部コストよりも大きいです。当社の製品および製品候補の研究開発費はすべて、発生時に支出されます。
2022年1月以降、製品の発見と開発に関連する研究開発費とAIPR&D費の合計で約72億ドルが発生しています。製品候補の開発が成功するかどうかは非常に不確実で、多くのリスクにさらされています。さらに、臨床試験の期間は、製品候補の種類、複雑さ、新規性、および対象となる疾患適応症によって大きく異なる場合があります。FDAや海外の同等の機関は、治療用医薬品の導入にかなりの要件を課しており、通常、長くて詳細な臨床検査手順、サンプリング作業、その他の費用と時間のかかる手順が必要です。試験プロセスのどの段階でも非臨床および臨床活動から得られたデータは有害であり、開発活動の中止または方向転換につながる可能性があります。これらの活動から得られたデータもさまざまな解釈の影響を受けやすく、規制当局の承認が遅れたり、制限されたり、妨げられたりする可能性があります。発見、非臨床研究、臨床試験の期間と費用は、プロジェクトの存続期間を通じて大きく異なる場合があり、予測が困難です。そのため、製品候補を市場に出すための最終的なコストを正確かつ有意義に見積もることはできません。
製品候補の開発と規制のスケジュールに関する見積もりは、非常に主観的なものであり、変更される可能性があります。第3相臨床試験のデータが得られるまで、臨床開発プログラムが収益とキャッシュフローを生み出す時期、または創出するかどうかについて、意味のある見積もりをすることはできません。
研究費
| | | | | | | | | | | | | | | | | | | | | | | |
| | | | | 3月31日に終了した3か月間 | | |
| | | | | | | 2024 | | 2023 | | 変更 |
| | | | | | | | | | | |
| | | | | | | (百万単位、パーセンテージを除く) |
| 研究費: | | | | | | | | | | | |
| 給与と福利厚生 | | | | | | | $ | 53.0 | | | $ | 45.5 | | | 16% |
| 株式ベースの報酬費用 | | | | | | | 29.9 | | | 20.2 | | | 48% |
| アウトソーシングサービスやその他の直接経費 | | | | | | | 64.4 | | | 53.6 | | | 20% |
インフラコスト | | | | | | | 48.8 | | | 47.5 | | | 3% |
研究費総額 | | | | | | | $ | 196.1 | | | $ | 166.8 | | | 18% |
| | | | | | | | | | | |
| | | | | | | |
パイプラインに投資し、細胞および遺伝子治療能力を拡大したため、研究費は過去数年間で増加しています。その結果、人員が増加し、外部サービスやその他の直接的な費用が発生しました。私たちは、重篤な疾患に対する革新的な医薬品の開発に焦点を当てた研究プログラムに引き続き投資していく予定です。
開発費
| | | | | | | | | | | | | | | | | | | | | | | |
| | | | | 3月31日に終了した3か月間 | | |
| | | | | | | 2024 | | 2023 | | 変更 |
| | | | | | | | | | | |
| | | | | | | (百万単位、パーセンテージを除く) |
| 開発費: | | | | | | | | | | | |
| 給与と福利厚生 | | | | | | | $ | 170.1 | | | $ | 144.2 | | | 18% |
| 株式ベースの報酬費用 | | | | | | | 89.5 | | | 56.1 | | | 60% |
| アウトソーシングサービスやその他の直接経費 | | | | | | | 236.1 | | | 295.3 | | | (20)% |
インフラコスト | | | | | | | 97.3 | | | 80.2 | | | 21% |
開発費総額 | | | | | | | $ | 593.0 | | | $ | 575.8 | | | 3% |
| | | | | | | | | | | |
| | | | | | | |
当社の開発費は、2023年3月31日に終了した3か月間と比較して、2024年3月31日に終了した3か月間で1,720万ドル(3%)増加しました。これは主に、株式ベースの報酬費用を含む人件費と、臨床試験をサポートするためのインフラストラクチャコストの増加によるもので、アウトソーシングサービスやその他の直接費用の減少によって一部相殺されました。
私たちは、進行中のパイプラインをサポートするために、社内の人員とインフラに多額の投資を行っています。過去数年間に人員が増えたことで、株式ベースの報酬費用が増加しました。当社の株式ベースの報酬費用は歴史的に変動しており、業績ベースの報酬に関連するマイルストーンを達成する確率に基づいて、期間ごとに変動し続けると予想されます。当社のアウトソーシングサービスおよびその他の直接費用は、2023年3月31日に終了した3か月と比較して減少しました。これは主に、CASGEVYの商品化による臨床試験費用の削減と、急性疼痛におけるスゼトリギンプログラムとCF用バンザカフトルトリプルの両方の進歩によるものです。これらの臨床試験費用の減少は、T1Dプログラムを支援するための費用の増加によって一部相殺されました。
獲得した製造中の研究開発費
| | | | | | | | | | | | | | | | | | | | | | | |
| | | | | 3月31日に終了した3か月間 | | |
| | | | | | | 2024 | | 2023 | | 変更 |
| | | | | | | | | | | |
| | | | | | | (百万単位、パーセンテージを除く) |
| 進行中の研究開発費の取得 | | | | | | | $ | 76.8 | | | $ | 347.1 | | | (78)% |
| | | | | | | |
2024年第1四半期のAIPR&Dは、主にEntradaによる7,500万ドルのマイルストーンに関連していました。2023年第1四半期のAIPR&Dは、主にエントラーダへの2億2,510万ドル、CRISPRへの1億ドルの前払い金に関連していました。当社のAIPR&Dは歴史的に変動しており、コラボレーション、第三者技術のライセンス、資産の取得など、既存および将来の事業開発取引に基づく前払い、偶発的なマイルストーン、その他の支払いにより、期間ごとに変動し続けると予想されます。
販売費、一般管理費
| | | | | | | | | | | | | | | | | | | | | | | |
| | | | | 3月31日に終了した3か月間 | | |
| | | | | | | 2024 | | 2023 | | 変更 |
| | | | | | | | | | | |
| | | | | | | (百万単位、パーセンテージを除く) |
| 販売費、一般管理費 | | | | | | | $ | 342.7 | | | $ | 241.1 | | | 42% |
2024年の第1四半期の販売、一般、および管理費は、2023年の第1四半期と比較して42%増加しました。これは主に、当社の治療薬のグローバルな発売を支援し、複数の潜在的な新製品の短期的な発売に備えるための投資が増加したためです。
不測の事態に備えて
当社の偶発対価の公正価値は、2024年と2023年の第1四半期にそれぞれ10万ドルと190万ドル減少しました。
その他の営業外収益(費用)、純額
利息収入
利息収入は、2023年第1四半期の1億2,260万ドルに対し、2024年第1四半期には1億8,120万ドルに増加しました。これは主に、市場金利の上昇、現金同等物および売却可能な負債証券の増加、およびより高い利回りを獲得した売却可能な債務証券の組み合わせによるものです。当社の将来の利息収入は、未払いの現金同等物および売却可能な債務証券の金額と実勢市場金利によって決まります。
支払利息
2024年と2023年の第1四半期の支払利息は、それぞれ1,040万ドルと1,140万ドルでした。この期間の支払利息の大部分は、ボストンの本社をリースしたことに関連する帰属利息費用に関連していました。
その他の収益(費用)、純額
2024年と2023年の第1四半期のその他の収益(費用)の純額は、それぞれ3,120万ドルの費用と130万ドルの収益でした。これらの金額は主に、当社の戦略的株式投資の公正価値の変動に起因する純未実現利益または損失に関するものです。これらの投資には、公開企業または非公開企業である当社の協力者への投資が含まれます。上場企業への戦略的株式投資を継続する限り、バイオテクノロジー企業の株価の変動により、当社のその他の収益(費用)は、戦略的株式投資の公正価値の増減に基づいて、将来の期間に変動すると予想しています。2024年3月31日現在、上場企業への投資の公正価値は4,340万ドルでした。
所得税
当社の実効税率は、事業のグローバルな性質により、期間ごとに変動します。当社の実効税率に最も大きな影響を与える要因には、税法の変更、複数の法域における課税所得の配分のばらつき、研究開発費の金額と特徴、特定の控除額と控除の水準、不確実な税務上の地位の価値調整、買収、第三者との協力およびライセンス取引などがあります。
2024年と2023年の第1四半期に、それぞれ1億7,950万ドルと1億9,170万ドルの所得税引当金を計上しました。2024年第1四半期の当社の実効税率は 14.0% で、米国の法定税率よりも低くなりました。これは主に、認識されていない税務上の地位の変化と、株式ベースの報酬に関連する超過税制上の優遇措置によるものです。2023年第1四半期の21.5%という当社の実効税率は、米国の法定税率を上回りました。これは主に、認識されていない税務上の地位の増加が、株式ベースの報酬に関連する超過税制上の優遇措置によって一部相殺されたためです。
流動性と資本資源
次の表は、2024年3月31日および2023年12月31日現在の当社の財政状態の構成要素をまとめたものです。
| | | | | | | | | | | | | | | | | |
| 2024年3月31日現在 | | 2023年12月31日現在 | | 変更 |
| | | | | |
| (百万単位、パーセンテージを除く) |
| 現金、現金同等物、有価証券: | | | | | |
| 現金および現金同等物 | $ | 9,158.0 | | | $ | 10,369.1 | | | |
| 市場性のある証券 | 1,013.3 | | | 849.2 | | | |
| 長期市場性のある証券 | 4,381.4です | | | 2,497.8 | | | |
| 現金、現金同等物および有価証券の総額 | $ | 14,552.7 | | | $ | 13,716.1 | | | 6% |
| | | | | |
| 運転資本: | | | | | |
| 流動資産合計 | $ | 13,288.7 | | | $ | 14,144.2 | | | (6)% |
| 流動負債合計 | (3,795.9) | | | (3,547.4) | | | 7% |
| 運転資本の総額 | $ | 9,492.8 | | | $ | 10,596.8 | | | (10)% |
ワーキングキャピタル
2024年3月31日現在、運転資本総額は95億ドルで、2023年12月31日現在の106億ドルから11億ドル減少しました。2024年第1四半期の総運転資本の減少は、主に21億ドルの長期有価証券の純購入によるものです。
キャッシュフロー
| | | | | | | | | | | |
| 3月31日に終了した3か月間 |
| 2024 | | 2023 |
| | | |
| (百万単位) |
| 提供した純現金(使用量): | | | |
| 営業活動 | $ | 1,306.6 | | | $ | 899.9 | |
| 投資活動 | $ | (2,136.4) | | | $ | (1,833.6) | |
| 資金調達活動 | $ | (357.5) | | | $ | (294.7) | |
営業活動
営業活動によって提供された現金は、2023年第1四半期の8億9,990万ドルに対し、2024年第1四半期は13億ドルでした。これは主に、純製品収益の増加による純利益の増加によるものです。
投資活動
2024年と2023年の第1四半期の投資活動に使用された現金は、それぞれ21億ドルと18億ドルでした。これは主に、売却可能な債務証券の純購入によるものです。
資金調達活動
財務活動に使用された現金は、2024年と2023年の第1四半期にそれぞれ3億5,750万ドルと2億9,470万ドルでした。これらの各期間における当社の資金調達活動の大部分は、従業員の株式給付制度に関連する支払いと、自社株買戻しプログラムに基づく当社の普通株式の買戻しでした。
流動性の源と用途
私たちは、流動性の主な源泉として、既存の現金、現金同等物、および現在の市場性のある有価証券を、製品販売によるキャッシュフローとともに信頼するつもりです。製品販売によるキャッシュフローは、現金、現金同等物、現在の有価証券と合わせて、少なくとも今後12か月間は事業資金を調達するのに十分であると予想しています。将来の営業および資本要件を満たすために利用可能な資金が十分かどうかは、将来の製品販売、1つまたは複数の他の製品候補の市場への導入の可能性、事業開発活動、研究開発プログラムの数、幅、コスト、見通しなど、多くの要因に左右されます。
クレジットファシリティと資金調達戦略
2022年7月に締結したリボルビング・クレジット・ファシリティに従って、合計5億ドルまで借りることができ、このリボルビング・クレジット契約に基づく金額を違約金なしで返済および借り換えることができました。特定の条件に応じて、借入能力をさらに5億ドル、合計10億ドル増やすよう要求できます。私たちの信用契約に否定的な契約があると、この流動性源にアクセスすることが禁止または制限される可能性があります。2024年3月31日現在、施設は未定で、私たちはこれらの契約を遵守していました。
また、信用契約に基づく借入、公募または私募による借り入れ、新たな協力契約の確保、またはその他の資金調達方法により、追加の資本を調達することもあります。私たちは引き続き資本構造を管理し、長期的な流動性プロファイルを強化する可能性のあるすべての資金調達機会をいつでも検討します。そのような資金調達の機会が、たとえあったとしても、許容できる条件で利用できるという保証はありません。
将来の資本要件
私たちには、次のような重要な将来の資本要件があります。
•2024年4月、私たちはアルパインを上記のように約49億ドルの現金で買収するというアルパイン合併契約を締結しました。この取引は、特定の慣習的な完了条件を条件として、2024年の第2四半期に完了する予定です。買収資金は現金および現金同等物で賄うつもりです。
•研究開発活動の実施、既存および将来の製品の製造と商品化、および組織の運営に予想される営業費用。
•所得税に支払う現金。
•CF製品の販売に関連して当社が支払うロイヤルティ。
•ファシリティ、オペレーティング、ファイナンスリース義務。
•当社の供給および製造プロセスに関連する確固たる購入義務。
さらに、将来発生する可能性のあるその他の重要な資本要件には、次のものが含まれる可能性があります。
•私たちは、特定の研究、開発、製造、商品化の取り組みへの資金提供を含む、特定の事業開発関連および戦略的契約を第三者と締結しています。コラボレーション、ライセンス契約、資産取得を含む特定の取引には、事前に設定された開発および規制上の目標および/または商業的目標を達成した場合に、将来のマイルストーンやロイヤルティの支払いが発生する可能性があります。その他の取引には、将来のリース関連費用やその他の費用の可能性が含まれます。これらの研究開発と商品化の取り組みに資金を提供し、これらの潜在的なマイルストーン、費用、ロイヤルティを支払う当社の義務は、プログラムへの継続的な関与および/またはプログラムの中止を引き起こす可能性のある有害事象がないことを条件としています。買収、コラボレーション、ライセンス契約、株式投資など、追加の事業開発取引や戦略的契約を締結する場合がありますが、これには追加の資本が必要です。
•既存のクレジット契約に基づいて金額を借りる限り、2027年に未払いの元本を返済する必要があります。
•2024年3月31日現在、株式買戻しプログラムに基づく残りの承認は24億ドルあり、2023年2月に取締役会で承認されました。私たちは、手持ち現金と事業によって生み出された現金を組み合わせて、普通株式の買い戻し資金を調達することを期待しています。このプログラムには有効期限がなく、いつでも中止できます。
アルパインを買収するための上記の支払い以外に、2024年2月15日に証券取引委員会(SEC)に提出された2023年12月31日に終了した年度のフォーム10-Kの年次報告書に開示されている将来の資本要件に重要な変更はありません。
重要な会計方針と見積もり
当社の財政状態と経営成績に関する議論と分析は、米国で一般に認められている会計原則に従って作成された要約連結財務諸表に基づいています。これらの財務諸表を作成するには、報告された資産と負債の金額、要約連結財務諸表の日付における偶発資産と負債の開示、および報告中の報告された収益と費用の金額に影響する特定の見積もりと仮定を行う必要があります。ピリオド。これらの項目は、事実や状況の変化について経営陣によって監視および分析されており、これらの見積もりには将来大きな変化が生じる可能性があります。見積もりの変更は、変更が発生した期間の報告結果に反映されます。私たちは、歴史的経験や、その状況下では合理的であると私たちが考えるその他のさまざまな仮定に基づいて見積もりをしています。過去の経験やその他の仮定が実質的に正確でない場合、実際の結果は私たちの見積もりと異なる場合があります。2024年2月15日にSECに提出された2023年12月31日に終了した年度のForm 10-Kの年次報告書で報告されているように、2024年3月31日に終了した3か月間、当社の重要な会計方針に重大な変更はありませんでした。
最近の会計上の宣言
最近の会計上の声明の議論については、注記A「表示の基礎と会計方針」を参照してください。
アイテム 3.市場リスクに関する定量的および定性的な開示
この項目に必要な情報は、2024年2月15日にSECに提出された2023年12月31日に終了した年度のフォーム10-Kの年次報告書のパートII、項目7A「市場リスクに関する量的および質的開示」で説明した内容を参照して組み込まれています。
アイテム 4.統制と手続き
開示管理と手続きの評価
当社の経営陣(最高経営責任者および最高財務責任者の監督および参加を得て)は、フォーム10-Qのこの四半期報告書の対象期間の終了時点における当社の開示管理および手続き(改正された1934年の証券取引法に基づく規則13a-15(e)および15d-15(e)で定義されている)の有効性を評価した結果、そのような評価に基づいて、3月の時点で、次のように結論付けました 2024年3月31日、当社の開示管理と手続きは効果的で、情報が合理的に保証されるように設計されました開示が義務付けられているのは、SECの規則とフォームで指定された期間内に記録、処理、要約、報告されます。当社の開示管理と手続きを設計および評価するにあたり、当社の経営陣は、どの統制や手続きも、どんなにうまく設計・運用されても、望ましい統制目標の達成を合理的に保証することしかできないことを認識していました。そして、当社の経営陣は、可能な統制と手続きの費用対効果の関係を評価する際に必ず判断を下す必要がありました。
財務報告に関する内部統制の変更
2024年3月31日に終了した3か月間、財務報告に対する当社の内部統制(改正された1934年の証券取引法に基づく規則13a-15(f)および15d-15(f)で定義されているとおり)に、財務報告に対する当社の内部統制に重大な影響を及ぼした、または重大な影響を与える可能性が合理的に高い変更はありませんでした。
パートII。その他の情報
アイテム 1.法的手続き
現在、私たちは重要な法的手続きの対象にはなっていません。
アイテム1A。リスク要因
以下の情報は、パートI、項目1Aに記載されているリスク要因を補足するものです。2024年2月15日にSECに提出された2023年12月31日に終了した年度のフォーム10-Kの年次報告書の「リスク要因」。
保留中のアルパインの戦略的買収を完了できなかったり、アルパインの事業をうまく統合できなかったりして、当社の事業と財政状態に悪影響を及ぼす可能性があります。
保留中のアルパインの買収を完了できなかったり、この新しい買収をうまく統合できなかったりすると、当社の事業に重大な悪影響を及ぼす可能性があります。長期戦略を実行できるかどうかは、パイプラインを増やしたり、新しい商業的機会を提供したりする他の事業体との取引やコラボレーションを行う能力に一部依存します。私たちは、事業を買収したり、コラボレーションをしたり、既存の強みを補完するその他の投資を行うための魅力的な機会を引き続き模索する可能性があります。しかし、戦略的な買収機会が生まれるという保証や、もし生じたとしても、それが完結するという保証はありません。保留中のアルパインの買収は、慣習的な完了条件を満たす必要性、独占禁止法やその他の規制当局の承認の必要性、発生する可能性のある紛争や訴訟など、さまざまな理由で完了するのが難しい場合があります。保留中のアルパインの買収から得られる価値の実現は、統合の成功と事業の継続にかかっています。できないかもしれません
アルパインの事業を既存の事業にうまく統合したり、アルパインの事業を収益性の高いものにしたり、主要な従業員を維持したり、この保留中の買収により予想されるコスト削減や相乗効果(ある場合)を実現したりすると、当社の事業と財政状態に悪影響を及ぼす可能性があります。さらに、進行中の事業が中断される可能性があり、保留中のアルパインの買収、移行、および/または統合活動によって経営陣の注意がそらされる可能性があります。
将来の見通しに関する記述に関する特記事項
フォーム10-Qのこの四半期報告書、特にパートIの項目2に記載されている財務状況と経営成績に関する経営陣の議論と分析には、多くの将来の見通しに関する記述が含まれています。将来の見通しに関する記述は純粋に歴史的なものではなく、「予想する」、「かもしれない」、「予測する」、「期待する」、「意図する」、「計画する」、「潜在的に」、「信じる」、「求める」、「見積もる」などの言葉や、同様の意味を持つ言葉や用語が添えられていることがあります。そのような記述は以下に関連するかもしれません:
•収益、費用、費用、その他の損益を含む、当社の財務実績に関する金額、時期、傾向に関する当社の期待。
•患者登録への期待、開発スケジュール、進行中および計画中の臨床試験からのデータの予想時期、規制当局への提出およびその他の治療法に関する提出、規制当局とのコミュニケーション、予想される規制当局への承認など、当社の臨床試験とパイプラインプログラムに関する当社の期待
•当社の製品を維持し、適切な償還を受ける能力、当社の製品または規制当局の承認を得たその他の治療法を発売、商品化、販売する能力、および既存の治療法のラベル拡張を取得する能力。
•CFの資格があり、当社の医薬品を受け取ることができる人の数を増やし、すでに当社の医薬品のいずれかの対象となっている人に改善された治療オプションを提供し、現在当社の薬の恩恵を受けられないCF患者への遺伝子治療を追求することで、CF事業を成長させ続けることができることへの期待です。
•進行中および計画中の臨床試験によって生成されるデータと、そのデータを使用して化合物の開発を進めたり、開発を継続したり、規制当局への提出を支援したりする能力。
•さらなる調査、臨床試験、または治療としての潜在的な用途のために、当社の治療法の臨床試験および前臨床および非臨床研究によって提供されるサポートに関する私たちの信念。
•当社の研究開発プログラムへの投資を継続する計画。これには、プログラムの予定スケジュールや、単独で、または第三者の協力者と共同でパイプラインプログラムを開発するための戦略が含まれます。
•私たちが重点を置いている疾患領域のおおよその患者数に関する私たちの信念。
•アルパインの事業と運営、ポベタシセプトの治療範囲と潜在的な利益、ポベタシセプトの対象患者集団に関する私たちの信念、および現在のアルパインパイプラインからの臨床の進歩と臨床データの入手可能性に関する私たちの信念を含む、保留中のアルパイン買収に関する私たちの期待、計画、および予想されるスケジュール。
•当社の事業開発活動の計画と見通し。これには、コラボレーションの潜在的な利益と治療範囲、買収した事業を統合して継続する当社の能力、およびこれらの機会を成功裏に活用する能力が含まれます。
•潜在的なマイルストーン支払いやその他の義務を含む、協力関係の確立、発展、維持。
•潜在的な事業開発活動(潜在的な協力パートナーや買収対象の特定を含む)
•知的財産ポートフォリオを拡大および保護し、その他の方法で製品に対する独占権を維持する当社の能力。
•外貨為替レートの潜在的な変動と当社の外貨管理プログラムの有効性
•事業によって生み出される現金、当社の現金残高、予想収益および利息収入に関する当社の期待
•当社の所得税引当金または繰延税金資産の活用に関する当社の期待
•当社の研究プログラムを利用して、重篤な疾患や満たされていない重大な医療ニーズに対応する新製品候補を特定および開発する能力。
•細胞治療や遺伝子治療を含む、グローバルなサプライチェーンと製造インフラと能力を拡大、強化、投資する計画。そして
•当社の流動性と、追加資本調達の可能性に関する期待。
将来の見通しに関する記述は、特定のリスク、不確実性、または予測が困難なその他の要因の影響を受けやすく、実際の出来事や結果がそのような記述に示されているものと大きく異なる可能性があります。これらのリスク、不確実性、およびその他の要因には、2024年2月15日にSECに提出された2023年12月31日に終了した年度のフォーム10-Kの年次報告書の項目1Aの「リスク要因」に記載されているものと、証券取引委員会に提出される将来の報告書に随時記載されているものが含まれますが、これらに限定されません。
このような将来の見通しに関する記述は、提出日現在の当社の見解と仮定に基づいて作成されており、将来の業績を予測するものではありません。法律で義務付けられている場合を除き、当社は将来の見通しに関する記述を公に更新する義務を負いません。読者は、そのような記述に過度に依存しないように注意してください。
アイテム 2.株式の未登録売却と収益の使用
発行者による株式の買戻し
2023年2月、当社の取締役会は自社株買戻しプログラム(「自社株買戻しプログラム」)を承認しました。これに基づき、当社は最大30億ドルの普通株式を買い戻す権限を与えられました。当社の自社株買戻しプログラムには有効期限がなく、いつでも中止できます。以下の表は、2024年3月31日に終了した3か月間に当社が株式買戻しプログラムに基づいて行った有価証券の買戻しを示しています。
| | | | | | | | | | | | | | | | | | | | | | | |
| ピリオド | 合計数
購入した株式の割合 | | 平均価格
一株あたりの支払額 | | 株式の総数
の一部として購入しました
公に発表された
プランやプログラム (1) | | おおよそのドル価値
まだ存在している可能性のある株式の
で購入
プランやプログラム (1) |
2024年1月1日から2024年1月31日まで | — | | | $ | — | | | — | | | $ | 2,572,394,027 | |
2024年2月1日から2024年2月29日まで | 94,000 | | | $ | 425.87 | | | 94,000 | | | $ | 2,532,362,623 | |
2024年3月1日から2024年3月31日まで | 241,773 | | | $ | 415.22 | | | 241,773 | | | $ | 2,431,973,750 | |
| 合計 | 335,773 | | | $ | 418.20 | | | 335,773 | | | $ | 2,431,973,750 | |
(1) 当社の自社株買戻しプログラムでは、公開市場または私的に交渉した取引を通じて随時株式を購入する権限を与えられています。このような購入は、規則10b5-1の計画、または当社の経営陣が決定したその他の手段、および証券取引委員会の要件に従って行われる場合があります。
アイテム 5.その他の情報
ルール 10b5-1 取引計画
当社の取締役、役員、従業員による証券取引に関する当社の方針により、当社の役員、取締役、従業員は、改正された1934年の証券取引法に基づく規則10b5-1に従って取引プランを締結することができます。 次の表は、2024年の第1四半期に当社の執行役員および取締役によって採択された当社の有価証券売却に関する書面による計画を示しています。各計画は、規則10b5-1の肯定的防衛条件(それぞれ「取引計画」)を満たすことを目的としています。
| | | | | | | | | | | | | | | | | | | | |
| 名前とタイトル | | トレーディングプランの採択日 | | 取引プランの有効期限予定日 (1) | | 取引プランの対象となる最大株式数 |
E. モロー「モリー」アトキンソン、III 執行副社長、最高技術執行責任者、バイオ医薬品科学および製造事業責任者 | | 2/22/2024 | | 2/28/2025 | | 25,290%(2) |
ジョナサン・ビラー EVP、最高法務責任者 | | 2/13/2024 | | 4/30/2025 | | 9,825(2) |
カルメン・ボジックさん グローバル医薬品開発・医療問題担当執行副社長、最高医療責任者 | | 2/27/2024 | | 1/31/2025 | | 13,680 |
レシュマ・ケワルラマニ 最高経営責任者兼社長 | | 2/7/2024 | | 5/20/2025 | | 96,388です(2) |
オウラニア「ニア」タチス 執行副社長、最高規制・品質責任者 | | 2/29/2024 | | 5/1/2025 | | 9,484(2) |
チャールズ・F・ワグナー・ジュニア EVP、最高財務責任者 | | 2/26/2024 | | 1/31/2025 | | 6,500 |
ブルース・サックス ディレクター | | 2/12/2024 | | 2/28/2025 | | 12,368 |
(1) 取引プランの有効期限より前に、ブローカーまたは取引プランの保有者による解約時、または取引プランに別段の定めがある場合に、予定されているすべての取引が完了した場合、取引プランはより早い日に期限切れになることがあります。
(2) 将来の権利確定日に源泉徴収義務を満たすために源泉徴収される普通株式の数は、上場株式の最大数によって減額されていません。そのような株式数はまだ決定できないからです。 |
アイテム 6.展示品
| | | | | |
展示品番号 | 展示品の説明 |
| 2.1* | 2024年4月10日付けのアルパイン・イミュン・サイエンス社、バーテックス・ファーマシューティカルズ・インコーポレイテッドおよびアダムズ・マージャー・サブ社による合意と合併計画(2024年4月10日にアルパイン免疫科学社が証券取引委員会に提出したフォーム8-Kの最新報告書の別紙2.1を参照して組み込まれています)。 |
| 31.1 | 2002年のサーベンス・オクスリー法第302条に基づく最高経営責任者の認定。 |
| 31.2 | 2002年のサーベンス・オクスリー法第302条に基づく最高財務責任者の認定。 |
| 32.1 | 2002年のサーベンス・オクスリー法第906条に基づく最高経営責任者および最高財務責任者の認定。 |
| 101.インチ | XBRLインスタンス-XBRLタグがインラインXBRLドキュメントに埋め込まれているため、インスタンスドキュメントはインタラクティブデータファイルに表示されません。 |
| 101.SCH | XBRL タクソノミー拡張スキーマ |
| 101.CAL | XBRL タクソノミー拡張計算 |
| 101.LAB | XBRL タクソノミー拡張ラベル |
| 101.PRE | XBRL タクソノミー拡張プレゼンテーション |
| 101.DEF | XBRL タクソノミー拡張定義 |
| 104 | カバーページインタラクティブデータファイル—カバーページのインタラクティブデータファイルは、そのXBRLタグがインラインXBRLドキュメントに埋め込まれているため、インタラクティブデータファイルには表示されません。 |
| |
| * | スケジュールや同様の添付ファイルは、規則S-Kの項目601(a)(5)に従って省略されています。省略されたスケジュールのコピーは、要求に応じてSECに補足的に提供されます。 |
署名
1934年の証券取引法の要件に従い、登録者は署名者に代わってこの報告書に正式に署名させ、正式に権限を与えられました。
| | | | | | | | |
| バーテックス・ファーマシューティカルズ・インコーポレイテッド |
| | |
| 2024年5月7日 | 作成者: | /s/ チャールズ・F・ワグナー・ジュニア |
| | チャールズ・F・ワグナー・ジュニア |
| | 執行副社長、最高財務責任者
(最高財務責任者と
正式に権限を与えられた役員) |