biib-20240331000087504512/312024Q1偽145,596,895146.7148.5296.6192.8197.000008750452024-01-012024-03-3100008750452024-04-23エクセルリ:シェア0000875045米国会計基準:プロダクトメンバー2024-01-012024-03-31ISO 4217: 米ドル0000875045米国会計基準:プロダクトメンバー2023-01-012023-03-310000875045BiiB:ANTICD20治療プログラムのメンバーからの収入2024-01-012024-03-310000875045BiiB:ANTICD20治療プログラムのメンバーからの収入2023-01-012023-03-310000875045US-GAAP: 製品およびサービスその他のメンバー2024-01-012024-03-310000875045US-GAAP: 製品およびサービスその他のメンバー2023-01-012023-03-3100008750452023-01-012023-03-31ISO 4217: 米ドルエクセルリ:シェア00008750452024-03-3100008750452023-12-310000875045US-GAAP: 無関係な当事者メンバー2024-03-310000875045US-GAAP: 無関係な当事者メンバー2023-12-310000875045米国会計基準:関連当事者メンバー2024-03-310000875045米国会計基準:関連当事者メンバー2023-12-310000875045US-GAAP: 無関係な当事者メンバー2024-01-012024-03-310000875045US-GAAP: 無関係な当事者メンバー2023-01-012023-03-310000875045米国会計基準:関連当事者メンバー2024-01-012024-03-310000875045米国会計基準:関連当事者メンバー2023-01-012023-03-3100008750452022-12-3100008750452023-03-310000875045米国会計基準:優先株会員2023-12-310000875045米国会計基準:普通株式会員2023-12-310000875045米国会計基準:追加払込資本構成員2023-12-310000875045米国会計基準:その他の包括利益の累計メンバー2023-12-310000875045米国会計基準:利益剰余金メンバー2023-12-310000875045米国会計基準:米国財務省株式普通会員2023-12-310000875045米国会計基準:利益剰余金メンバー2024-01-012024-03-310000875045米国会計基準:その他の包括利益の累計メンバー2024-01-012024-03-310000875045米国会計基準:普通株式会員2024-01-012024-03-310000875045米国会計基準:追加払込資本構成員2024-01-012024-03-310000875045米国会計基準:優先株会員2024-03-310000875045米国会計基準:普通株式会員2024-03-310000875045米国会計基準:追加払込資本構成員2024-03-310000875045米国会計基準:その他の包括利益の累計メンバー2024-03-310000875045米国会計基準:利益剰余金メンバー2024-03-310000875045米国会計基準:米国財務省株式普通会員2024-03-310000875045米国会計基準:優先株会員2022-12-310000875045米国会計基準:普通株式会員2022-12-310000875045米国会計基準:追加払込資本構成員2022-12-310000875045米国会計基準:その他の包括利益の累計メンバー2022-12-310000875045米国会計基準:利益剰余金メンバー2022-12-310000875045米国会計基準:米国財務省株式普通会員2022-12-310000875045米国会計基準:親会員2022-12-310000875045米国会計基準:非支配持分メンバー2022-12-310000875045米国会計基準:利益剰余金メンバー2023-01-012023-03-310000875045米国会計基準:親会員2023-01-012023-03-310000875045米国会計基準:非支配持分メンバー2023-01-012023-03-310000875045米国会計基準:その他の包括利益の累計メンバー2023-01-012023-03-310000875045米国会計基準:普通株式会員2023-01-012023-03-310000875045米国会計基準:追加払込資本構成員2023-01-012023-03-310000875045米国会計基準:優先株会員2023-03-310000875045米国会計基準:普通株式会員2023-03-310000875045米国会計基準:追加払込資本構成員2023-03-310000875045米国会計基準:その他の包括利益の累計メンバー2023-03-310000875045米国会計基準:利益剰余金メンバー2023-03-310000875045米国会計基準:米国財務省株式普通会員2023-03-310000875045米国会計基準:親会員2023-03-310000875045米国会計基準:非支配持分メンバー2023-03-31biib: セグメントエクセルリ:ピュア0000875045Biib:リアタ製薬社のメンバー2023-09-260000875045Biib:リアタ製薬社のメンバー2023-09-262023-09-260000875045SRT: シナリオ予測メンバー2024-04-012024-06-300000875045BiiB:クレジットファシリティのメンバー米国会計基準:ライン・オブ・クレジット・メンバーUS-GAAP:担保付債務メンバーBiib:リアタ製薬社のメンバー2023-09-260000875045Biib:リアタ製薬社のメンバー2024-03-310000875045Biib: スカイクラリーズのメンバーBiib:リアタ製薬社のメンバー2024-03-310000875045Biib:リアタ製薬社のメンバー米国会計基準:インプロセス研究開発メンバー2024-03-310000875045BiiB: 優先審査バウチャーメンバーBiib:リアタ製薬社のメンバー2024-03-310000875045BiiB:その他の臨床プログラムのメンバーBiib:リアタ製薬社のメンバー2024-03-310000875045Biib:リアタ製薬社のメンバー2024-01-012024-03-310000875045Biib: スカイクラリーズのメンバーBiib:リアタ製薬社のメンバー2023-09-260000875045Biib:リアタ製薬社のメンバー米国会計基準:インプロセス研究開発メンバー2023-09-260000875045BiiB: 優先審査バウチャーメンバーBiib:リアタ製薬社のメンバー2023-09-260000875045BiiB:その他の臨床プログラムのメンバーBiib:リアタ製薬社のメンバー2023-09-26UTR: 平方フィート0000875045米国会計基準:一般管理費の売上メンバーBiib:リアタ製薬社のメンバー2023-01-012023-12-310000875045BiiB:サムスンバイオシミラー契約メンバー2022-03-310000875045BiiB:サムスンバイオシミラー契約メンバー2022-04-012022-04-300000875045BiiB:サムスンバイオシミラー契約メンバー2022-04-012022-04-300000875045BiiB:サムスンバイオシミラー契約メンバー2022-04-300000875045BiiB: 1周年記念メンバーの支払い期限BiiB:サムスンバイオシミラー契約メンバー2022-04-300000875045BiiB: 2周年記念メンバーでの支払い期限BiiB:サムスンバイオシミラー契約メンバー2022-04-300000875045BiiB:サムスンバイオシミラー契約メンバー米国会計基準:測定入力割引率メンバーBiiB: 1周年記念メンバーの支払い期限米国会計基準:公正価値測定経常委員2024-03-310000875045BiiB:サムスンバイオシミラー契約メンバー米国会計基準:公正価値測定経常委員2024-03-310000875045BiiB: 2周年記念メンバーでの支払い期限BiiB:サムスンバイオシミラー契約メンバー2024-01-012024-03-310000875045BiiB: 1周年記念メンバーの支払い期限BiiB:サムスンバイオシミラー契約メンバー2023-01-012023-03-310000875045BiiB: 2周年記念メンバーでの支払い期限BiiB:サムスンバイオシミラー契約メンバー2023-01-012023-03-310000875045Biib: 2023年コスト削減イニシアチブのメンバー2023-09-262023-09-260000875045Biib: 2023年コスト削減イニシアチブのメンバー2024-01-012024-03-31BiiB: 従業員0000875045SRT: 最低メンバー数2023-07-310000875045SRT: 最大メンバー数2023-07-310000875045米国会計基準:一般管理費の売上メンバーBiib: 2023年コスト削減イニシアチブのメンバー2024-01-012024-03-310000875045米国会計基準:研究開発費メンバーBiib: 2023年コスト削減イニシアチブのメンバー2024-01-012024-03-310000875045米国会計基準:リストラ費用メンバーBiib: 2023年コスト削減イニシアチブのメンバー2024-01-012024-03-310000875045BiiB:REATAインテグレーションメンバーSRT: 最低メンバー数2024-03-310000875045SRT: 最大メンバー数BiiB:REATAインテグレーションメンバー2024-03-310000875045米国会計基準:一般管理費の売上メンバーBiiB:REATAインテグレーションメンバー2024-01-012024-03-310000875045BiiB:REATAインテグレーションメンバー米国会計基準:研究開発費メンバー2024-01-012024-03-310000875045米国会計基準:リストラ費用メンバーBiiB:REATAインテグレーションメンバー2024-01-012024-03-310000875045BiiB:REATAインテグレーションメンバー2024-01-012024-03-310000875045米国会計基準:従業員退職金メンバーBiib: 2023年と2022年のコスト削減イニシアチブのメンバー2023-12-310000875045米国会計基準:従業員退職金メンバーBiib: 2023年と2022年のコスト削減イニシアチブのメンバー2022-12-310000875045米国会計基準:従業員退職金メンバーBiib: 2023年と2022年のコスト削減イニシアチブのメンバー2023-07-012023-09-300000875045米国会計基準:従業員退職金メンバーBiib: 2023年と2022年のコスト削減イニシアチブのメンバー2022-07-012022-09-300000875045米国会計基準:従業員退職金メンバーBiib: 2023年と2022年のコスト削減イニシアチブのメンバー2023-09-300000875045米国会計基準:従業員退職金メンバーBiib: 2023年と2022年のコスト削減イニシアチブのメンバー2022-09-300000875045国:米国Biib: テックフィデラのメンバー2024-01-012024-03-310000875045米国会計基準:米国非会員Biib: テックフィデラのメンバー2024-01-012024-03-310000875045Biib: テックフィデラのメンバー2024-01-012024-03-310000875045国:米国Biib: テックフィデラのメンバー2023-01-012023-03-310000875045米国会計基準:米国非会員Biib: テックフィデラのメンバー2023-01-012023-03-310000875045Biib: テックフィデラのメンバー2023-01-012023-03-310000875045国:米国Biib: 優待会員2024-01-012024-03-310000875045米国会計基準:米国非会員Biib: 優待会員2024-01-012024-03-310000875045Biib: 優待会員2024-01-012024-03-310000875045国:米国Biib: 優待会員2023-01-012023-03-310000875045米国会計基準:米国非会員Biib: 優待会員2023-01-012023-03-310000875045Biib: 優待会員2023-01-012023-03-310000875045Biib: フマルレート会員国:米国2024-01-012024-03-310000875045米国会計基準:米国非会員Biib: フマルレート会員2024-01-012024-03-310000875045Biib: フマルレート会員2024-01-012024-03-310000875045Biib: フマルレート会員国:米国2023-01-012023-03-310000875045米国会計基準:米国非会員Biib: フマルレート会員2023-01-012023-03-310000875045Biib: フマルレート会員2023-01-012023-03-310000875045国:米国Biib: アボネックス会員2024-01-012024-03-310000875045米国会計基準:米国非会員Biib: アボネックス会員2024-01-012024-03-310000875045Biib: アボネックス会員2024-01-012024-03-310000875045国:米国Biib: アボネックス会員2023-01-012023-03-310000875045米国会計基準:米国非会員Biib: アボネックス会員2023-01-012023-03-310000875045Biib: アボネックス会員2023-01-012023-03-310000875045国:米国Biib: プレグリディ会員2024-01-012024-03-310000875045米国会計基準:米国非会員Biib: プレグリディ会員2024-01-012024-03-310000875045Biib: プレグリディ会員2024-01-012024-03-310000875045国:米国Biib: プレグリディ会員2023-01-012023-03-310000875045米国会計基準:米国非会員Biib: プレグリディ会員2023-01-012023-03-310000875045Biib: プレグリディ会員2023-01-012023-03-310000875045国:米国BiiB: インターフェロンメンバー2024-01-012024-03-310000875045米国会計基準:米国非会員BiiB: インターフェロンメンバー2024-01-012024-03-310000875045BiiB: インターフェロンメンバー2024-01-012024-03-310000875045国:米国BiiB: インターフェロンメンバー2023-01-012023-03-310000875045米国会計基準:米国非会員BiiB: インターフェロンメンバー2023-01-012023-03-310000875045BiiB: インターフェロンメンバー2023-01-012023-03-310000875045国:米国Biib:ティサブリプロダクトメンバー2024-01-012024-03-310000875045米国会計基準:米国非会員Biib:ティサブリプロダクトメンバー2024-01-012024-03-310000875045Biib:ティサブリプロダクトメンバー2024-01-012024-03-310000875045国:米国Biib:ティサブリプロダクトメンバー2023-01-012023-03-310000875045米国会計基準:米国非会員Biib:ティサブリプロダクトメンバー2023-01-012023-03-310000875045Biib:ティサブリプロダクトメンバー2023-01-012023-03-310000875045Biib: ファンピラメンバー国:米国2024-01-012024-03-310000875045Biib: ファンピラメンバー米国会計基準:米国非会員2024-01-012024-03-310000875045Biib: ファンピラメンバー2024-01-012024-03-310000875045Biib: ファンピラメンバー国:米国2023-01-012023-03-310000875045Biib: ファンピラメンバー米国会計基準:米国非会員2023-01-012023-03-310000875045Biib: ファンピラメンバー2023-01-012023-03-310000875045BiiB: MS製品収益メンバー国:米国2024-01-012024-03-310000875045BiiB: MS製品収益メンバー米国会計基準:米国非会員2024-01-012024-03-310000875045BiiB: MS製品収益メンバー2024-01-012024-03-310000875045BiiB: MS製品収益メンバー国:米国2023-01-012023-03-310000875045BiiB: MS製品収益メンバー米国会計基準:米国非会員2023-01-012023-03-310000875045BiiB: MS製品収益メンバー2023-01-012023-03-310000875045国:米国Biib:スピンラザのメンバー2024-01-012024-03-310000875045米国会計基準:米国非会員Biib:スピンラザのメンバー2024-01-012024-03-310000875045Biib:スピンラザのメンバー2024-01-012024-03-310000875045国:米国Biib:スピンラザのメンバー2023-01-012023-03-310000875045米国会計基準:米国非会員Biib:スピンラザのメンバー2023-01-012023-03-310000875045Biib:スピンラザのメンバー2023-01-012023-03-310000875045国:米国Biib: QAlsodyメンバー2024-01-012024-03-310000875045米国会計基準:米国非会員Biib: QAlsodyメンバー2024-01-012024-03-310000875045Biib: QAlsodyメンバー2024-01-012024-03-310000875045国:米国Biib: QAlsodyメンバー2023-01-012023-03-310000875045米国会計基準:米国非会員Biib: QAlsodyメンバー2023-01-012023-03-310000875045Biib: QAlsodyメンバー2023-01-012023-03-310000875045国:米国Biib: スカイクラリーズのメンバー2024-01-012024-03-310000875045米国会計基準:米国非会員Biib: スカイクラリーズのメンバー2024-01-012024-03-310000875045Biib: スカイクラリーズのメンバー2024-01-012024-03-310000875045国:米国Biib: スカイクラリーズのメンバー2023-01-012023-03-310000875045米国会計基準:米国非会員Biib: スカイクラリーズのメンバー2023-01-012023-03-310000875045Biib: スカイクラリーズのメンバー2023-01-012023-03-310000875045Biib:希少疾患製品収益メンバー国:米国2024-01-012024-03-310000875045米国会計基準:米国非会員Biib:希少疾患製品収益メンバー2024-01-012024-03-310000875045Biib:希少疾患製品収益メンバー2024-01-012024-03-310000875045Biib:希少疾患製品収益メンバー国:米国2023-01-012023-03-310000875045米国会計基準:米国非会員Biib:希少疾患製品収益メンバー2023-01-012023-03-310000875045Biib:希少疾患製品収益メンバー2023-01-012023-03-310000875045Biib: ベネパリ会員国:米国2024-01-012024-03-310000875045米国会計基準:米国非会員Biib: ベネパリ会員2024-01-012024-03-310000875045Biib: ベネパリ会員2024-01-012024-03-310000875045Biib: ベネパリ会員国:米国2023-01-012023-03-310000875045米国会計基準:米国非会員Biib: ベネパリ会員2023-01-012023-03-310000875045Biib: ベネパリ会員2023-01-012023-03-310000875045国:米国Biib: イムラルディ会員2024-01-012024-03-310000875045米国会計基準:米国非会員Biib: イムラルディ会員2024-01-012024-03-310000875045Biib: イムラルディ会員2024-01-012024-03-310000875045国:米国Biib: イムラルディ会員2023-01-012023-03-310000875045米国会計基準:米国非会員Biib: イムラルディ会員2023-01-012023-03-310000875045Biib: イムラルディ会員2023-01-012023-03-310000875045Biib: フリクサビメンバー国:米国2024-01-012024-03-310000875045Biib: フリクサビメンバー米国会計基準:米国非会員2024-01-012024-03-310000875045Biib: フリクサビメンバー2024-01-012024-03-310000875045Biib: フリクサビメンバー国:米国2023-01-012023-03-310000875045Biib: フリクサビメンバー米国会計基準:米国非会員2023-01-012023-03-310000875045Biib: フリクサビメンバー2023-01-012023-03-310000875045国:米国Biib: Oovizメンバーによると2024-01-012024-03-310000875045米国会計基準:米国非会員Biib: Oovizメンバーによると2024-01-012024-03-310000875045Biib: Oovizメンバーによると2024-01-012024-03-310000875045国:米国Biib: Oovizメンバーによると2023-01-012023-03-310000875045米国会計基準:米国非会員Biib: Oovizメンバーによると2023-01-012023-03-310000875045Biib: Oovizメンバーによると2023-01-012023-03-310000875045国:米国BiiB: バイオシミラー会員2024-01-012024-03-310000875045米国会計基準:米国非会員BiiB: バイオシミラー会員2024-01-012024-03-310000875045BiiB: バイオシミラー会員2024-01-012024-03-310000875045国:米国BiiB: バイオシミラー会員2023-01-012023-03-310000875045米国会計基準:米国非会員BiiB: バイオシミラー会員2023-01-012023-03-310000875045BiiB: バイオシミラー会員2023-01-012023-03-310000875045国:米国Biib:フマデルマンダドゥヘルムメンバー2024-01-012024-03-310000875045米国会計基準:米国非会員Biib:フマデルマンダドゥヘルムメンバー2024-01-012024-03-310000875045Biib:フマデルマンダドゥヘルムメンバー2024-01-012024-03-310000875045国:米国Biib:フマデルマンダドゥヘルムメンバー2023-01-012023-03-310000875045米国会計基準:米国非会員Biib:フマデルマンダドゥヘルムメンバー2023-01-012023-03-310000875045Biib:フマデルマンダドゥヘルムメンバー2023-01-012023-03-310000875045米国会計基準:プロダクトメンバー国:米国2024-01-012024-03-310000875045米国会計基準:プロダクトメンバー米国会計基準:米国非会員2024-01-012024-03-310000875045米国会計基準:プロダクトメンバー国:米国2023-01-012023-03-310000875045米国会計基準:プロダクトメンバー米国会計基準:米国非会員2023-01-012023-03-31biib: 卸売業者0000875045BiiB:ディストリビューター1人のメンバー2024-01-012024-03-310000875045Biib:ディストリビューター/2人のメンバー2024-01-012024-03-310000875045BiiB:ディストリビューター1人のメンバー2023-01-012023-03-310000875045Biib:ディストリビューター/2人のメンバー2023-01-012023-03-310000875045BiiB:リザーブ・フォー・キャッシュディスカウント会員2023-12-310000875045BiiB: 契約調整メンバー2023-12-310000875045米国会計基準:売上収益率および引当金メンバー2023-12-310000875045BiiB:リザーブ・フォー・キャッシュディスカウント会員2024-01-012024-03-310000875045BiiB: 契約調整メンバー2024-01-012024-03-310000875045米国会計基準:売上収益率および引当金メンバー2024-01-012024-03-310000875045BiiB:リザーブ・フォー・キャッシュディスカウント会員2024-03-310000875045BiiB: 契約調整メンバー2024-03-310000875045米国会計基準:売上収益率および引当金メンバー2024-03-310000875045米国会計基準:売掛金勘定メンバー2024-03-310000875045米国会計基準:売掛金勘定メンバー2023-12-310000875045米国会計基準:その他の流動負債メンバー2024-03-310000875045米国会計基準:その他の流動負債メンバー2023-12-310000875045BiiB:OCRevusメンバーに帰属するロイヤリティ2024-01-012024-03-310000875045BiiB:OCRevusメンバーに帰属するロイヤリティ2023-01-012023-03-310000875045biib: ロシュグループジェネンテック会員2024-01-012024-03-310000875045biib: ロシュグループジェネンテック会員2023-01-012023-03-310000875045BiiB:受託製造およびその他の収益メンバー2024-01-012024-03-310000875045BiiB:受託製造およびその他の収益メンバー2023-01-012023-03-310000875045米国会計基準:ロイヤリティ会員2024-01-012024-03-310000875045米国会計基準:ロイヤリティ会員2023-01-012023-03-310000875045Biib: ル・ケンビコラボレーションメンバー2024-03-310000875045BiiB:権利と特許を取得し、ライセンス取得済みのメンバーSRT: 最低メンバー数2024-03-310000875045BiiB:権利と特許を取得し、ライセンス取得済みのメンバーSRT: 最大メンバー数2024-03-310000875045BiiB:権利と特許を取得し、ライセンス取得済みのメンバー2024-03-310000875045BiiB:権利と特許を取得し、ライセンス取得済みのメンバー2023-12-310000875045米国会計基準:先進技術権利会員SRT: 最低メンバー数2024-03-310000875045米国会計基準:先進技術権利会員SRT: 最大メンバー数2024-03-310000875045米国会計基準:先進技術権利会員2024-03-310000875045米国会計基準:先進技術権利会員2023-12-310000875045米国会計基準:インプロセス研究開発メンバー2024-03-310000875045米国会計基準:インプロセス研究開発メンバー2023-12-310000875045BiiB: 優先審査バウチャーメンバー2024-03-310000875045BiiB: 優先審査バウチャーメンバー2023-12-310000875045米国会計基準:商標および商号メンバー2024-03-310000875045米国会計基準:商標および商号メンバー2023-12-310000875045BiiB:コンプリートテクノロジーメンバーSRT: 最低メンバー数2024-03-310000875045BiiB:コンプリートテクノロジーメンバーSRT: 最大メンバー数2024-03-310000875045米国会計基準:公正価値測定経常委員2024-03-310000875045米国会計基準:公正価値測定経常委員米国会計基準:フェアバリューインプットレベル1メンバー2024-03-310000875045米国会計基準:公正価値インプットレベル2メンバー米国会計基準:公正価値測定経常委員2024-03-310000875045米国会計基準:公正価値測定経常委員米国会計基準:フェアバリューインプットレベル3メンバー2024-03-310000875045BiiB:サムスンバイオシミラー契約メンバー米国会計基準:フェアバリューインプットレベル1メンバー米国会計基準:公正価値測定経常委員2024-03-310000875045米国会計基準:公正価値インプットレベル2メンバーBiiB:サムスンバイオシミラー契約メンバー米国会計基準:公正価値測定経常委員2024-03-310000875045BiiB:サムスンバイオシミラー契約メンバー米国会計基準:フェアバリューインプットレベル3メンバー米国会計基準:公正価値測定経常委員2024-03-310000875045BiiB:サムスンバイオシミラー契約メンバー2024-03-310000875045米国会計基準:公正価値測定経常委員2023-12-310000875045米国会計基準:公正価値測定経常委員米国会計基準:フェアバリューインプットレベル1メンバー2023-12-310000875045米国会計基準:公正価値インプットレベル2メンバー米国会計基準:公正価値測定経常委員2023-12-310000875045米国会計基準:公正価値測定経常委員米国会計基準:フェアバリューインプットレベル3メンバー2023-12-310000875045BiiB:サムスンバイオシミラー契約メンバー米国会計基準:公正価値測定経常委員2023-12-310000875045BiiB:サムスンバイオシミラー契約メンバー米国会計基準:フェアバリューインプットレベル1メンバー米国会計基準:公正価値測定経常委員2023-12-310000875045米国会計基準:公正価値インプットレベル2メンバーBiiB:サムスンバイオシミラー契約メンバー米国会計基準:公正価値測定経常委員2023-12-310000875045BiiB:サムスンバイオシミラー契約メンバー米国会計基準:フェアバリューインプットレベル3メンバー米国会計基準:公正価値測定経常委員2023-12-310000875045米国会計基準:シニアノートメンバーBiib:シニアノートスリーポイントシックスツー 5パーセントデュエットトゥエンティトゥエンティトゥエンティツーメンバー2024-03-310000875045米国会計基準:シニアノートメンバーBiib:シニアノートスリーポイントシックスツー 5パーセントデュエットトゥエンティトゥエンティトゥエンティツーメンバー2023-12-310000875045米国会計基準:シニアノートメンバーBiib:シニアノート 3年間有期2023メンバー2024-03-310000875045米国会計基準:シニアノートメンバーBiib:シニアノート 3年間有期2023メンバー2023-12-310000875045米国会計基準:シニアノートメンバーBiib: 現在の支払手形と期間限定の貸付会員2024-03-310000875045米国会計基準:シニアノートメンバーBiib: 現在の支払手形と期間限定の貸付会員2023-12-310000875045米国会計基準:シニアノートメンバーBiiB:タームローン2023 3年契約トランシェメンバー2024-03-310000875045米国会計基準:シニアノートメンバーBiiB:タームローン2023 3年契約トランシェメンバー2023-12-310000875045米国会計基準:シニアノートメンバーBiib:シニアノート4ポイント0/5パーセントのデュエット25メンバー2024-03-310000875045Biib:シニアノート4ポイント0/5パーセントのデュエット25メンバー2023-12-310000875045米国会計基準:シニアノートメンバーBiib:シニアノート4ポイント0/5パーセントのデュエット25メンバー2023-12-310000875045BiiB:シニアノート5ポイント2パーセントデュエンティフォーティファイブメンバー米国会計基準:シニアノートメンバー2024-03-310000875045BiiB:シニアノート5ポイント2パーセントデュエンティフォーティファイブメンバー2023-12-310000875045BiiB:シニアノート5ポイント2パーセントデュエンティフォーティファイブメンバー米国会計基準:シニアノートメンバー2023-12-310000875045米国会計基準:シニアノートメンバーBiib: A2.25 5月期満期シニアノート、メンバー12時30分2024-03-310000875045Biib: A2.25 5月期満期シニアノート、メンバー12時30分2023-12-310000875045米国会計基準:シニアノートメンバーBiib: A2.25 5月期満期シニアノート、メンバー12時30分2023-12-310000875045Biib: 3.15 5月期満期シニアノート 1250メンバー米国会計基準:シニアノートメンバー2024-03-310000875045Biib: 3.15 5月期満期シニアノート 1250メンバー2023-12-310000875045Biib: 3.15 5月期満期シニアノート 1250メンバー米国会計基準:シニアノートメンバー2023-12-310000875045米国会計基準:シニアノートメンバーBiib:シニアノート3.250 2051年2月15日締め切りのメンバー2024-03-310000875045Biib:シニアノート3.250 2051年2月15日締め切りのメンバー2023-12-310000875045米国会計基準:シニアノートメンバーBiib:シニアノート3.250 2051年2月15日締め切りのメンバー2023-12-310000875045米国会計基準:シニアノートメンバーBiiB:支払手形の非流動部分とタームローンメンバー2024-03-310000875045米国会計基準:シニアノートメンバーBiiB:支払手形の非流動部分とタームローンメンバー2023-12-310000875045米国会計基準:ライン・オブ・クレジット・メンバーBiib:クレジットファシリティフローティングレート 364デイトランシェメンバー2023-09-260000875045米国会計基準:ライン・オブ・クレジット・メンバーBiib:クレジット・ファシリティ・フローティング・レート 3年間トランシェメンバー2023-09-260000875045US-GAAP: マネー・マーケット・ファンド・メンバー2024-03-310000875045US-GAAP: マネー・マーケット・ファンド・メンバー2023-12-310000875045BiiB:株式証券現在のメンバー2024-03-310000875045BiiB:株式証券の非現会員です2024-03-310000875045BiiB:株式証券現在のメンバー2023-12-310000875045BiiB:株式証券の非現会員です2023-12-310000875045BiiB: ストラテジック・インベストメンツのメンバー米国会計基準:その他の非流動資産メンバー2024-03-310000875045BiiB: ストラテジック・インベストメンツのメンバー米国会計基準:その他の非流動資産メンバー2023-12-310000875045SRT: 最低メンバー数2024-03-310000875045SRT: 最大メンバー数2024-03-310000875045SRT: 最低メンバー数2023-12-310000875045SRT: 最大メンバー数2023-12-310000875045米国会計基準:ヘッジング・インストゥルメント・メンバーに指定通貨:ユーロ米国会計基準:外国為替契約メンバー2024-03-310000875045米国会計基準:ヘッジング・インストゥルメント・メンバーに指定通貨:ユーロ米国会計基準:外国為替契約メンバー2023-12-310000875045米国会計基準:ヘッジング・インストゥルメント・メンバーに指定通貨:スイスフランです米国会計基準:外国為替契約メンバー2024-03-310000875045米国会計基準:ヘッジング・インストゥルメント・メンバーに指定通貨:スイスフランです米国会計基準:外国為替契約メンバー2023-12-310000875045通貨:カナダドル米国会計基準:ヘッジング・インストゥルメント・メンバーに指定米国会計基準:外国為替契約メンバー2024-03-310000875045通貨:カナダドル米国会計基準:ヘッジング・インストゥルメント・メンバーに指定米国会計基準:外国為替契約メンバー2023-12-310000875045通貨:日本円米国会計基準:ヘッジング・インストゥルメント・メンバーに指定米国会計基準:外国為替契約メンバー2024-03-310000875045通貨:日本円米国会計基準:ヘッジング・インストゥルメント・メンバーに指定米国会計基準:外国為替契約メンバー2023-12-310000875045米国会計基準:ヘッジング・インストゥルメント・メンバーに指定米国会計基準:外国為替契約メンバー2024-03-310000875045米国会計基準:ヘッジング・インストゥルメント・メンバーに指定米国会計基準:外国為替契約メンバー2023-12-310000875045米国会計基準:外国為替先渡会員2024-01-012024-03-310000875045米国会計基準:外国為替先渡会員2023-01-012023-03-310000875045米国会計基準:セールスメンバー米国会計基準:外国為替契約メンバー2024-01-012024-03-310000875045米国会計基準:セールスメンバー米国会計基準:外国為替契約メンバー2023-01-012023-03-310000875045Biib: キャッシュフロー収益メンバー米国会計基準:セールスメンバー米国会計基準:外国為替契約メンバー2024-01-012024-03-310000875045Biib: キャッシュフロー収益メンバー米国会計基準:セールスメンバー米国会計基準:外国為替契約メンバー2023-01-012023-03-310000875045米国会計基準:外国為替契約メンバー米国会計基準:営業費用メンバー2024-01-012024-03-310000875045米国会計基準:外国為替契約メンバー米国会計基準:営業費用メンバー2023-01-012023-03-310000875045Biib:キャッシュフロー営業経費メンバー米国会計基準:外国為替契約メンバー米国会計基準:営業費用メンバー2024-01-012024-03-310000875045Biib:キャッシュフロー営業経費メンバー米国会計基準:外国為替契約メンバー米国会計基準:営業費用メンバー2023-01-012023-03-310000875045米国会計基準:非指定メンバー2024-03-310000875045米国会計基準:非指定メンバー2023-12-310000875045米国会計基準:その他の流動資産メンバー米国会計基準:ヘッジング・インストゥルメント・メンバーに指定2024-03-310000875045米国会計基準:その他の流動資産メンバー米国会計基準:ヘッジング・インストゥルメント・メンバーに指定2023-12-310000875045米国会計基準:ヘッジング・インストゥルメント・メンバーに指定米国会計基準:未払負債メンバー2024-03-310000875045米国会計基準:ヘッジング・インストゥルメント・メンバーに指定米国会計基準:未払負債メンバー2023-12-310000875045米国会計基準:非指定メンバー米国会計基準:その他の流動資産メンバー2024-03-310000875045米国会計基準:非指定メンバー米国会計基準:その他の流動資産メンバー2023-12-310000875045米国会計基準:非指定メンバー米国会計基準:未払負債メンバー2024-03-310000875045米国会計基準:非指定メンバー米国会計基準:未払負債メンバー2023-12-310000875045BiiB:生物製剤製造メンバー2024-01-012024-03-310000875045Biib:倉庫のユーティリティとサポートスペースメンバー2024-01-012024-03-310000875045BiiB: 行政スペースメンバー2024-01-012024-03-310000875045Biib: ゾロトゥルンスイス会員2023-12-310000875045Biib: ゾロトゥルンスイス会員2024-01-012024-03-310000875045BiiB:クレジットファシリティのメンバー米国会計基準:ライン・オブ・クレジット・メンバー2023-09-260000875045BiiB:クレジットファシリティはメンバーを終了しました米国会計基準:ライン・オブ・クレジット・メンバー2023-09-260000875045Biib:2023タームローンメンバー米国会計基準:ライン・オブ・クレジット・メンバーBiiB:フローティングレート 364日トランシェメンバー2023-09-262023-09-260000875045Biib:2023タームローンメンバー米国会計基準:ライン・オブ・クレジット・メンバーBiiB:フローティングレート 364日トランシェメンバー2024-03-310000875045米国会計基準:ライン・オブ・クレジット・メンバーBiib:クレジット・ファシリティ・フローティング・レート 3年間トランシェメンバーBiiB:フローティングレート 364日トランシェメンバー2024-03-310000875045Biib:2023タームローンメンバー米国会計基準:ライン・オブ・クレジット・メンバーBiiB:タームローン2023 3年契約トランシェメンバー2024-03-310000875045BiiB:2020年の自社株買いプログラムのメンバー2020-10-310000875045BiiB:2020年の自社株買いプログラムのメンバー2024-03-310000875045米国会計基準:累積純未実現投資利益損失メンバー2023-12-310000875045US-GAAP: 累積損益純キャッシュフローエッジ親メンバー2023-12-310000875045米国会計基準:累積確定給付制度調整メンバー2023-12-310000875045米国会計基準:累積翻訳調整メンバー2023-12-310000875045米国会計基準:累積純未実現投資利益損失メンバー2024-01-012024-03-310000875045US-GAAP: 累積損益純キャッシュフローエッジ親メンバー2024-01-012024-03-310000875045米国会計基準:累積確定給付制度調整メンバー2024-01-012024-03-310000875045米国会計基準:累積翻訳調整メンバー2024-01-012024-03-310000875045米国会計基準:累積純未実現投資利益損失メンバー2024-03-310000875045US-GAAP: 累積損益純キャッシュフローエッジ親メンバー2024-03-310000875045米国会計基準:累積確定給付制度調整メンバー2024-03-310000875045米国会計基準:累積翻訳調整メンバー2024-03-310000875045米国会計基準:累積純未実現投資利益損失メンバー2022-12-310000875045US-GAAP: 累積損益純キャッシュフローエッジ親メンバー2022-12-310000875045米国会計基準:累積確定給付制度調整メンバー2022-12-310000875045米国会計基準:累積翻訳調整メンバー2022-12-310000875045米国会計基準:累積純未実現投資利益損失メンバー2023-01-012023-03-310000875045US-GAAP: 累積損益純キャッシュフローエッジ親メンバー2023-01-012023-03-310000875045米国会計基準:累積確定給付制度調整メンバー2023-01-012023-03-310000875045米国会計基準:累積翻訳調整メンバー2023-01-012023-03-310000875045米国会計基準:累積純未実現投資利益損失メンバー2023-03-310000875045US-GAAP: 累積損益純キャッシュフローエッジ親メンバー2023-03-310000875045米国会計基準:累積確定給付制度調整メンバー2023-03-310000875045米国会計基準:累積翻訳調整メンバー2023-03-310000875045米国会計基準:累積純未実現投資利益損失メンバーUS-GAAP: その他の包括所得累計額からの再分類2024-01-012024-03-310000875045米国会計基準:累積純未実現投資利益損失メンバーUS-GAAP: その他の包括所得累計額からの再分類2023-01-012023-03-310000875045US-GAAP: 累積損益純キャッシュフローエッジ親メンバーUS-GAAP: その他の包括所得累計額からの再分類2024-01-012024-03-310000875045US-GAAP: 累積損益純キャッシュフローエッジ親メンバーUS-GAAP: その他の包括所得累計額からの再分類2023-01-012023-03-310000875045US-GAAP: その他の包括所得累計額からの再分類2024-01-012024-03-310000875045US-GAAP: その他の包括所得累計額からの再分類2023-01-012023-03-310000875045Biib:タイムベスター限定在庫ユニットメンバー2024-01-012024-03-310000875045Biib:タイムベスター限定在庫ユニットメンバー2023-01-012023-03-310000875045BiiB:マーケットストックユニットメンバー2024-01-012024-03-310000875045BiiB:マーケットストックユニットメンバー2023-01-012023-03-310000875045BiiB:パフォーマンスストックユニットはストックメンバーに決済されました2024-01-012024-03-310000875045BiiB:パフォーマンスストックユニットはストックメンバーに決済されました2023-01-012023-03-310000875045米国会計基準:研究開発費メンバー2024-01-012024-03-310000875045米国会計基準:研究開発費メンバー2023-01-012023-03-310000875045米国会計基準:一般管理費の売上メンバー2024-01-012024-03-310000875045米国会計基準:一般管理費の売上メンバー2023-01-012023-03-310000875045米国会計基準:親会員2024-01-012024-03-310000875045米国会計基準:親会員2023-01-012023-03-310000875045Biib:タイムベスター限定在庫ユニットメンバー2024-01-012024-03-310000875045Biib:タイムベスター限定在庫ユニットメンバー2023-01-012023-03-310000875045BiiB:パフォーマンスストックユニットはストックメンバーに決済されました2024-01-012024-03-310000875045BiiB:パフォーマンスストックユニットはストックメンバーに決済されました2023-01-012023-03-310000875045BiiB:従業員株式購入プランメンバー2024-01-012024-03-310000875045BiiB:従業員株式購入プランメンバー2023-01-012023-03-310000875045BiiB:現金会員で決済されたパフォーマンスストックユニット2024-01-012024-03-310000875045BiiB:現金会員で決済されたパフォーマンスストックユニット2023-01-012023-03-310000875045米国会計基準:従業員ストックオプションメンバー2024-01-012024-03-310000875045米国会計基準:従業員ストックオプションメンバー2023-01-012023-03-310000875045BiiB:マーケットストックユニットメンバー2024-01-012024-03-310000875045BiiB:マーケットストックユニットメンバー2023-01-012023-03-310000875045Biib:イオニッサンガモデナリとセージメンバー2024-01-012024-03-310000875045Biib: サンガモ会員2024-01-012024-03-310000875045Biib:イオニッサンガモデナリとセージメンバー2023-01-012023-03-310000875045BiiB:セイジ・セラピューティクス社のメンバー2023-01-012023-03-310000875045Biib: オクレバス会員SRT: 最低メンバー数2017-03-012017-03-310000875045SRT: 最大メンバー数Biib: オクレバス会員2017-03-012017-03-310000875045Biib: オクレバス会員2017-03-012017-03-310000875045米国会計基準:外国メンバーBiib: オクレバス会員2017-03-012017-03-310000875045Biib:モスネツズマブ会員2024-01-012024-03-310000875045Biib:リツクサン会員2024-03-310000875045Biib: ガジーバ会員2024-03-310000875045Biib: ガジーバ会員2024-01-012024-03-310000875045Biib: ル・ケンビコラボレーションメンバー2023-12-310000875045Biib:エーザイ会員2023-12-310000875045Biib:エーザイ会員Biibe:2609とバン2401のメンバー2024-01-012024-03-310000875045Biib:エーザイ会員Biibe:2609とバン2401のメンバー2023-01-012023-03-310000875045Biib:エーザイ会員米国会計基準:一般管理費の売上メンバーBiibe:2609とバン2401のメンバー2024-01-012024-03-310000875045Biib:エーザイ会員米国会計基準:一般管理費の売上メンバーBiibe:2609とバン2401のメンバー2023-01-012023-03-310000875045Biib:エーザイ会員2024-03-310000875045Biib: UCBファーマ.A. メンバー米国会計基準:研究開発費メンバー2024-01-012024-03-310000875045Biib: UCBファーマ.A. メンバー米国会計基準:研究開発費メンバー2023-01-012023-03-310000875045SRT: シナリオ予測メンバーBiiB:セイジ・セラピューティクス社のメンバー2024-12-310000875045BiiB:セイジ・セラピューティクス社のメンバー2024-01-012024-03-310000875045BiiB:セイジ・セラピューティクス社のメンバー米国会計基準:研究開発費メンバー2024-01-012024-03-310000875045BiiB:セイジ・セラピューティクス社のメンバー米国会計基準:研究開発費メンバー2023-01-012023-03-310000875045BiiB:セイジ・セラピューティクス社のメンバー米国会計基準:一般管理費の売上メンバー2024-01-012024-03-310000875045BiiB:セイジ・セラピューティクス社のメンバー米国会計基準:一般管理費の売上メンバー2023-01-012023-03-310000875045米国会計基準:研究開発費メンバーBiiB:デナリ・セラピューティクス社のメンバー2024-01-012024-03-310000875045米国会計基準:研究開発費メンバーBiiB:デナリ・セラピューティクス社のメンバー2023-01-012023-03-310000875045BiiB:その他のリサーチ・アンド・ディスカバリーのメンバー2024-01-012024-03-310000875045BiiB:その他のリサーチ・アンド・ディスカバリーのメンバー2023-01-012023-03-310000875045BiiB:サムスンバイオシミラー契約メンバー2019-12-012019-12-31biib: 製品0000875045BiiB:サムスンバイオシミラー契約メンバー2024-01-012024-03-310000875045BiiB:サムスンバイオシミラー契約メンバー2024-01-012024-03-310000875045BiiB:サムスンバイオシミラー契約メンバー2023-01-012023-03-310000875045米国会計基準:関連当事者メンバーBiiB:サムスンバイオシミラー契約メンバー2024-03-310000875045米国会計基準:関連当事者メンバーBiiB:サムスンバイオシミラー契約メンバー2023-12-310000875045BiiB:ニューイミュンメンバー2024-01-012024-03-3100008750452019-12-3100008750452023-06-300000875045biiB: ジェネンテック会員2023-02-012023-02-280000875045Biib: 貸主紛争メンバー2023-09-262023-09-260000875045米国会計基準:ライセンスメンバーBiib:スピンラザのメンバー米国会計基準:後任イベントメンバー2024-04-24 米国
証券取引委員会
ワシントンD.C. 20549
フォーム10-Q
| | | | | |
| ☒ | 1934年の証券取引法のセクション13または15 (d) に基づく四半期報告書 |
四半期終了時 2024年3月31日
または
| | | | | |
| ☐ | 1934年の証券取引法第13条または第15条 (d) に基づく移行報告書 |
コミッションファイル番号 0-19311
バイオジェン株式会社
(憲章に明記されている登録者の正確な名前)
| | | | | | | | |
| デラウェア州 | | 33-0112644 |
(州またはその他の管轄区域)
法人または組織) | | (IRS) 雇用主
識別番号) |
225 ビニーストリート、 ケンブリッジ、 MA02142
(617)679-2000
(郵便番号を含む住所、および電話番号(以下を含む)
登録者の主要行政機関のエリアコード)
同法第12条 (b) に従って登録された証券:
| | | | | | | | | | | | | | | | | |
| 各クラスのタイトル | | トレーディングシンボル | | 登録された各取引所の名前 |
| 普通株式、額面0.0005ドル | | ビブ | | ナスダック・グローバル・セレクト・マーケット |
登録者が(1)1934年の証券取引法のセクション13または15(d)によって提出が義務付けられているすべての報告を過去12か月間(または登録者がそのような報告を提出する必要があったほど短い期間)提出したかどうか、および(2)過去90日間にそのような提出要件の対象となっていたかどうかをチェックマークで示してください。はいx いいえ
登録者が、過去12か月間(または登録者がそのようなファイルを提出する必要があったほど短い期間)に、規則S-Tの規則405(この章の§232.405)に従って提出する必要のあるすべてのインタラクティブデータファイルを電子的に提出したかどうかをチェックマークで示してください。はいx いいえ
登録者が大規模な加速申告者、加速申告者、非加速申告者、小規模な報告会社、または新興成長企業のいずれであるかをチェックマークで示してください。取引法の規則12b-2の「大規模加速申告者」、「加速申告者」、「小規模報告会社」、「新興成長企業」の定義を参照してください。
| | | | | | | | | | | | | | |
| 大型加速フィルター | x | | アクセラレーテッド・ファイラー | ☐ |
| 非加速ファイラー | ☐ | | 小規模な報告会社 | ☐ |
| | | 新興成長企業 | ☐ |
新興成長企業の場合は、登録者が取引法第13条 (a) に従って定められた新規または改訂された財務会計基準を遵守するために延長された移行期間を使用しないことを選択したかどうかをチェックマークで示してください。o
登録者がシェル会社(取引法の規則12b-2で定義されている)であるかどうかをチェックマークで示してください。はい☐いいえ x
2024年4月23日時点で発行されている発行者の普通株式数、額面0.0005ドルは 145,596,895 株式。
バイオジェン株式会社
フォーム10-Q — 四半期報告書
2024年3月31日に終了した四半期期間について
目次
| | | | | | | | |
| | | ページ |
パートI — 財務情報 |
| | |
| アイテム 1. | 財務諸表 (未監査) | |
| | |
| 要約された連結損益計算書 — 2024年および2023年3月31日に終了した3か月間 | 7 |
| | |
| 包括利益の要約連結計算書 — 2024年および2023年3月31日に終了した3か月間 | 8 |
| | |
| 要約された連結貸借対照表 — 2024年3月31日および2023年12月31日現在 | 9 |
| | |
| 要約連結キャッシュフロー計算書 — 2024年および2023年3月31日に終了した3か月間 | 10 |
| | |
| 要約連結株主資本計算書 — 2024年および2023年3月31日に終了した3か月間 | 11 |
| | |
| 要約連結財務諸表の注記 | 12 |
| | |
| アイテム 2. | 経営陣による財政状態と経営成績に関する議論と分析 | 43 |
| | |
| アイテム 3. | 市場リスクに関する定量的・質的開示 | 65 |
| | |
| アイテム 4. | 統制と手続き | 67 |
|
パートII — その他の情報 |
| | |
| アイテム 1. | 法的手続き | 68 |
| | |
| アイテム 1A. | リスク要因 | 68 |
| | |
| アイテム 2. | 持分証券の未登録売却および収益の使用 | 83 |
| | |
| アイテム 5. | その他の情報 | 83 |
| | |
| アイテム 6. | 展示品 | 84 |
| |
署名 | 85 |
将来の見通しに関する記述に関するメモ
このレポートには、1995年の民間証券訴訟改革法(以下「法」)の「セーフハーバー」規定の恩恵を受けることを目的として作成された将来の見通しに関する記述が含まれています。これらの将来の見通しに関する記述には、「目的」、「期待する」、「信じる」、「できる」、「熟考する」、「続ける」、「見積もる」、「期待」、「予測」、「目標」、「意図」、「かもしれない」、「計画」、「可能性」、「予測」、「プロジェクト」、「すべき」、「目標」、「予定」、「目的」、「予測」、「プロジェクト」、「すべき」、「目標」、「予定」、「目標」、「予測」、「プロジェクト」、「すべき」、「目標」、「意図」、「すべき」、「目標」、「意図」、「すべき」、「目標」、「意図」、「すべき」、「目標」、「予定」、」「するだろう」またはこれらの単語や他の似た意味の言葉や用語の否定語。特に、以下に関する将来の見通しに関する記述が参照されます。
•収益の予想額、時期、会計処理、ライセンス、コラボレーション、買収、売却契約に基づく偶発的、マイルストーン、ロイヤルティ、その他の支払い、税務上のポジションと不測の事態、売掛金の回収可能性、承認前の在庫、売上原価、研究開発費、報酬およびその他の販売、一般管理費、無形資産の償却、外貨為替リスク、資産の推定公正価値と負債、および減損評価;
•製品の承認、販売、価格設定、成長、償還、および市販およびパイプライン製品の発売に関する期待、計画、および展望
•競合市場における製品競争の激化による潜在的な影響。これには、既存の製品および短縮された規制経路の下で承認された製品(当社製品または競合製品のジェネリックまたはバイオシミラー版を含む)の新しいオリジネーター療法、ジェネリック医薬品、プロドラッグ、バイオシミラーとの競争の激化が含まれます。
•特許条件、特許期間の延長、特許庁の訴訟、予想される入手可能性と規制上の独占期間。
•私たちの計画とポートフォリオへの投資、そして企業戦略の実施。
•当社の戦略的および成長的イニシアチブの実行。これには、Reataの買収の最終的な成功、SKYCLARYS製品の将来の業績や予想される相乗効果など、買収から期待される利益を実現する能力、バイオシミラー事業の戦略的オプションの探求が含まれます。
•当社の事業成長の原動力。これには、発見、研究開発プログラム、事業開発の機会に関連するリソースを投入する計画と意図、および特定の事業開発取引による潜在的な利益と結果、および当社のFit for Growthプログラムを含むコスト削減措置の潜在的な利益と結果、および完了予定のものが含まれます。
•当社製品、薬剤候補、パイプラインプログラム(第三者との協力を含む)の期待、開発計画、予想されるスケジュール(潜在的な臨床試験の費用と時期、規制当局への提出と承認を含む)、ならびに当社および当社の協力者のパイプライン製品の開発と商品化における潜在的な治療範囲
•当社の特許およびその他の所有権および知的財産権、税務監査、査定と和解、価格問題、販売および販売促進慣行、製造物責任、調査およびその他の事項に関連する行政、規制、法律、およびその他の手続きの時期、結果、および影響
•当社の事業および事業イニシアチブの資金を調達し、そのような活動のための資金を調達する当社の能力。
•市販またはパイプライン製品、市販製品のジェネリック版またはバイオシミラー版、または当社製品と同じクラスのその他の製品に関係する安全上の有害事象。
•地政学的な緊張、戦争行為、その他の大規模な危機の現在および潜在的な影響。これには、当社の事業、販売への影響、およびロシアのウクライナ侵攻や中東での軍事紛争の影響を受けた地域など、地政学的に緊張している地域で臨床試験活動を実施する計画の中断または遅延の可能性が含まれます。
•売上高、費用、準備金と手当、サプライチェーン、製造、研究開発費、臨床試験費用、従業員など、世界的な健康被害が当社の事業と運営に与える直接的および間接的な影響。
•当社による情報システムおよびデータの使用、およびそのようなシステムまたは当社のビジネスパートナーのシステムの故障、侵入、破損、破壊、侵害による潜在的な影響
•IRAを含む米国における医療改革の潜在的な影響、および医療費を削減し、政府支出の全体的な水準を制限するために世界中で講じられている措置(価格設定措置や当社製品の償還額削減の影響を含む)。
•当社の製造能力、第三者の委託製造組織の利用、製造能力の変更に関連する計画と時期、新規または既存の製造施設での活動、およびノースカロライナ州RTPの遺伝子治療製造施設の稼働予定スケジュール
•特定の国における信用および経済状況の不確実性が続いていること、およびそのような国での売掛金の回収の影響。
•リース契約、購入義務、その他の契約上の義務の時期と履行。そして
•新しい法律(税を含む)、規制要件、司法上の決定、会計基準の影響。
これらの将来の見通しに関する記述には、項目1Aに記載されているものを含め、リスクと不確実性が伴います。このレポートやこのレポートの他の部分に含まれるリスク要因により、実際の結果がそのような記述に反映されているものと大きく異なる可能性があります。これらのリスクや不確実性の中には、予測または定量化できないものもあれば、当社の制御が及ばないものもあるため、将来の出来事の予測として当社の将来の見通しに関する記述に頼るべきではありません。また、これらの記述に過度に依存しないでください。さらに、私たちは非常に競争が激しく、急速に変化する環境で事業を行っており、新しいリスクや不確実性が時折出現する可能性があり、すべてのリスクを予測したり、すべての不確実性を特定したりすることは不可能です。将来の見通しに関する記述は、この報告の日付の時点でのみ述べられており、現時点で入手可能な情報と見積もりに基づいています。法律で義務付けられている場合を除き、当社は、新しい情報、将来の動向、またはその他の結果として、将来の見通しに関する記述を公に更新する義務を負いません。私たちの実際の将来の業績、業績、出来事、状況は、私たちが期待するものと大きく異なる可能性があることを理解した上でこのレポートを読んでください。
会社と製品の参考資料に関するメモ
このレポートでの参考文献:
•「バイオジェン」、「会社」、「私たち」、「私たち」とは、バイオジェン社とその連結子会社を指します。そして
•「リツキサン」とは、リツキサン(米国、カナダ、日本におけるリツキシマブの商品名)とMabThera(米国、カナダ、日本以外ではリツキシマブの商品名)の両方を指します。
商標に関するメモ
ADUHELM®、AVONEX®、BYOOVIZ®、PLEGRIDY®、QALSODY®、RITUXAN®、RITUXAN®、RITUXAN®、RITUXAN® HYCELA®、SKYCLARYS®、SPINRAZA®、TYSABRI®、VUMERITY® はバイオジェンの登録商標です。
ベネパリ™、フリクサビ™、フマダーム™、イムラルディ™、トフィデンス™ はバイオジェンの商標です。
ACTEMRA®、COLUMVI®、ENBREL®、EYLEA®、FAMPYRA™、GAZYVA®、LEQEMBI®、HUMIRA®、LUCENTIS®、LUNSUMIO®、OCREVUS®、REMICADE®、ZURZUVAE™、およびこのレポートで言及されているその他の商標は、それぞれの所有者の財産です。
定義済みの用語
| | | | | |
| 2023 フォーム 10-K | 2023年12月31日に終了した年度のフォーム10-Kの年次報告書 |
| 2020年の自社株買いプログラム | 取締役会は、最大50億ドルの当社の普通株式を買い戻すプログラムを承認しました |
アッヴィー | アッヴィ |
| アコルダ | アコーダ・セラピューティクス株式会社 |
| アイ | 人工知能 |
| アルケルメス | アルケルメス株式会社 |
| また | 筋萎縮性側索硬化症 |
| AOCI | その他の包括利益 (損失) の累計 |
| ASU | 会計基準の更新 |
| ATV | 抗体輸送車両 |
| BLA | 生物製剤ライセンス申請 |
| ブラックストーン | ブラックストーン・ライフサイエンス |
| CCPA | カリフォルニア州消費者プライバシー法 |
| チャンプ | ヒト用医薬品委員会 |
CISA | サイバーセキュリティ・アンド・インフラストラクチャー・セキュリティ・エージェンシー |
| チェウ | 欧州連合司法裁判所 |
| クル | 皮膚エリテマトーデス |
| 電話してください | 慢性リンパ性白血病 |
| CLO | 最高法務責任者 |
コドム | 最高業務意思決定者 |
| コンバージェンス | コンバージェンス・ファーマシューティカルズ株式会社 |
| カール | 回答書一式 |
| CRO | 受託研究機関 |
デア | 麻薬取締局 |
| デナリ | デナリ・セラピューティクス株式会社 |
地方裁判所 | マサチューセッツ州連邦地方裁判所 |
| 道場 | 米国司法省 |
| EC | 欧州委員会 |
| エーザイ | エーザイ株式会社 |
| エマ | 欧州医薬品庁 |
| EPO | 欧州特許庁 |
| えーと | 企業リスク管理 |
| E.U。 | 欧州連合 |
| ファン | フリードライヒ運動失調症 |
| ファブ | 財務会計基準審議会 |
| FCPA | 海外腐敗行為防止法 |
| FDA | 米国食品医薬品局 |
| FDIC | 連邦預金保険公社 |
| 成長に適している | 2023年に開始されたコスト削減プログラム |
FSS | 連邦供給スケジュール |
| ジェネンテック | ジェネンテック株式会社 |
| ギルティ | 世界の無形資産低税収入 |
| グローブ | グローバルアンチベースエロージョン |
| GMP | 適正製造基準 |
定義済みの用語(続き)
| | | | | |
| ヒューマナ | 株式会社ヒューマナ |
| IPR&D | 製造中の研究開発 |
| イオニス | アイオーニス・ファーマシューティカルズ |
| IRA | 2022年のインフレ削減法 |
| それ | インフォメーションテクノロジー |
| 点滴 | 静脈内投与 |
| ラーク2 | ロイシンリッチリピートキナーゼ2 |
| マア | マーケティング承認申請書 |
| MDD | 大うつ病性障害 |
| ミリ秒 | 多発性硬化症 |
| マイラン・アイルランド | マイラン・アイルランド株式会社 |
| NCD | 全国補償の決定 |
| NDA | 新薬申請 |
| 神経免疫 | ニューロイムン・サブワン AG |
| NMPA | 国家医薬品管理局 |
| OECD | 経済協力開発機構 |
| おい | その他(収入)費用、純額 |
| ポルファーマ | ポルファーマ・バイオロジクスS.A. |
| オパカ | 患者保護および手ごろな価格の医療に関する法律 |
| PPD | 産後うつ病 |
| PPMS | プライマリー・プログレッシブMS |
| PRV | 優先審査券 |
| 研究開発 | 研究開発 |
| レアータ | レアタファーマシューティカルズ株式会社 |
| 両腕は | 再発しているMS |
| RRMS | 再発・送金型MS |
| RTP | リサーチ・トライアングル・パーク |
| セージです | セイジ・セラピューティクス株式会社 |
| サムスン・バイオエピス | サムスン・バイオエピス株式会社 |
| サムスン・バイオロジクス | サムスン・バイオロジクス株式会社 |
| サンガモ | サンガモ・セラピューティクス株式会社 |
秒 | 米国証券取引委員会 |
| SG&A | 販売、総務、管理 |
| 売る | 全身性エリテマトーデス |
| SMA | 脊髄性筋萎縮症 |
| SMN | サバイバルモーターニューロン |
| SOD1 | スーパーオキシドジスムターゼ1 |
| スイスメディック | スイス治療薬庁 |
| 未定 | 技術控訴委員会 |
| 移行通行料税 | 累積された外国子会社の以前は課税されていなかった海外収益に対する1回限りの強制みなし本国送還税 |
| 英国。 | イギリス |
| アメリカ | 米国 |
| 米国会計基準 | 米国で一般的に受け入れられている会計原則 |
VA | 退役軍人管理局 |
パートI 財務情報
バイオジェン株式会社と子会社
要約連結損益計算書
(未監査、百万単位、一株当たりの金額を除く)
| | | | | | | | | | | | | | | |
| 3月31日に終了した3か月間、 | | |
| 2024 | | 2023 | | | | |
| 収益: | | | | | | | |
| 製品、ネット | $ | 1,711.9 | | | $ | 1,763.3 | | | | | |
| 抗CD20治療プログラムからの収入 | 394.0 | | | 399.5 | | | | | |
| 受託製造、ロイヤリティ、その他の収入 | 184.6 | | | 300.2 | | | | | |
| 総収入 | 2,290.5です | | | 2,463.0 | | | | | |
| 費用と費用: | | | | | | | |
| 取得した無形資産の償却と減損を除いた売上原価 | 542.2 | | | 662.8 | | | | | |
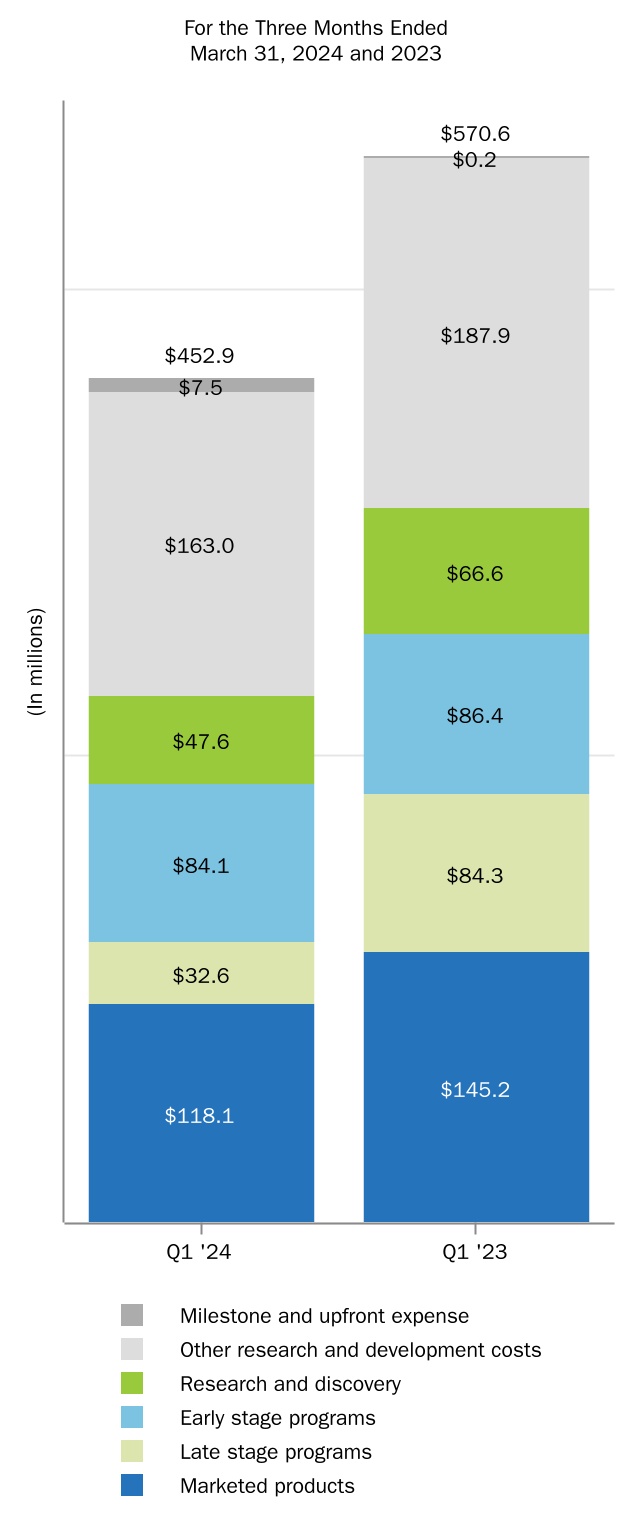
| 研究開発 | 452.9 | | | 570.6 | | | | | |
| 販売、一般および管理 | 581.5です | | | 605.0 | | | | | |
| 取得した無形資産の償却と減損 | 78.3 | | | 50.2 | | | | | |
| コラボレーションの利益分配/(損失の払い戻し) | 65.6 | | | 57.1 | | | | | |
| | | | | | | |
| | | | | | | |
| リストラ費用 | 11.5 | | | 9.6 | | | | | |
| | | | | | | |
| その他(収入)費用、純額 | 93.7 | | | 69.4 | | | | | |
| 総費用と経費 | 1,825.7 | | | 2,024.7 | | | | | |
| 所得税(給付)費用を差し引く前の収入 | 464.8 | | | 438.3 | | | | | |
| 所得税(給付)費用 | 71.4 | | | 50.7 | | | | | |
| | | | | | | |
| 当期純利益 | 393.4 | | | 387.6 | | | | | |
| 非支配持分に帰属する純利益(損失)、税引後 | — | | | (0.3) | | | | | |
| バイオジェンに帰属する純利益。 | $ | 393.4 | | | $ | 387.9 | | | | | |
| | | | | | | |
| 1株当たり当期純利益: | | | | | | | |
| バイオジェンに帰属する1株当たりの基本利益 | $ | 2.71 | | | $ | 2.69 | | | | | |
| バイオジェンに帰属する希薄化後の1株当たり利益 | $ | 2.70 | | | $ | 2.67 | | | | | |
| | | | | | | |
| 計算に使用した加重平均株数: | | | | | | | |
| バイオジェンに帰属する1株当たりの基本利益 | 145.2 | | | 144.4 | | | | | |
| バイオジェンに帰属する希薄化後の1株当たり利益 | 145.9 | | | 145.2 | | | | | |
これらの未監査の要約連結財務諸表の添付注記を参照してください。
バイオジェン株式会社と子会社
要約連結包括利益計算書
(未監査、百万単位)
| | | | | | | | | | | | | | | |
| | 3月31日に終了した3か月間、 | | |
| | 2024 | | 2023 | | | | |
| バイオジェンに帰属する純利益(損失) | $ | 393.4 | | | $ | 387.9 | | | | | |
| その他の包括利益: | | | | | | | |
売却可能な有価証券の未実現利益(損失)、税引後 | — | | | 5.7 | | | | | |
キャッシュフローヘッジの未実現利益(損失)、税引後 | 14.7 | | | (35.4) | | | | | |
| | | | | | | |
年金給付債務の未実現利益(損失)、税引後 | (0.1) | | | 0.5 | | | | | |
通貨換算調整 | (21.4) | | | 22.1 | | | | | |
| その他の包括利益(損失)の合計(税引後) | (6.8) | | | (7.1) | | | | | |
| バイオジェンに帰属する包括利益(損失) | 386.6 | | | 380.8 | | | | | |
| 非支配持分に帰属する包括利益(損失)、税引後 | — | | | (0.3) | | | | | |
| 包括利益 (損失) | $ | 386.6 | | | $ | 380.5 | | | | | |
これらの未監査の要約連結財務諸表の添付注記を参照してください。
バイオジェン株式会社と子会社
要約連結貸借対照表
(未監査、百万単位、一株当たりの金額を除く)
| | | | | | | | | | | |
| 2024年3月31日現在 | | 2023年12月31日現在 |
| 資産 |
| 流動資産: | | | |
| 現金および現金同等物 | $ | 1,074.4 | | | $ | 1,049.9 | |
| | | |
売掛金(ドルの貸倒引当金を差し引いたもの)2.2 と $2.4、それぞれ | 1,604.5 | | | 1,664.1 | |
| 抗CD20治療プログラムのため | 395.2 | | | 435.9 | |
| インベントリ | 2,516.8 | | | 2,527.4 | |
| その他の流動資産 | 1,165.3 | | | 1,182.0 | |
| 流動資産合計 | 6,756.2 | | | 6,859.3 | |
| | | |
| 不動産、プラント、設備、純額 | 3,275.3 | | | 3,309.7 | |
| オペレーティングリース資産 | 428.1 | | | 420.0 | |
| 無形資産、純額 | 8,284.7 | | | 8,363.0です | |
| グッドウィル | 6,227.4 | | | 6,219.2 | |
| 繰延税金資産 | 898.3 | | | 928.6 | |
| 投資およびその他の資産 | 697.6 | | | 745.0 | |
| 総資産 | $ | 26,567.6 | | | $ | 26,844.8 | |
| 負債と資本 |
| 現在の負債: | | | |
| 現在のタームローンの部分 | $ | 250.0 | | | $ | 150.0 | |
| 支払うべき税金 | 231.2 | | | 257.4 | |
| 買掛金 | 387.0 | | | 403.3 | |
| 未払費用とその他 | 2,354.6 | | | 2,623.6 | |
| 流動負債合計 | 3,222.8 | | | 3,434.3 | |
| 支払手形とタームローン | 6,290.1です | | | 6,788.2 | |
| 繰延税金負債 | 658.1 | | | 641.8 | |
| 長期オペレーティングリース負債 | 406.5 | | | 400.0 | |
| その他の長期負債 | 777.1 | | | 781.1 | |
| 負債総額 | 11,354.6 | | | 12,045.4 | |
| コミットメント、不測の事態、保証 | | | |
| 株式: | | | |
| バイオジェン株主資本: | | | |
優先株式、額面価格 $0.001 一株当たり | — | | | — | |
普通株式、額面価格 $0.0005 一株当たり | 0.1 | | | 0.1 | |
| 追加払込資本 | 329.5 | | | 302.5 | |
| その他の包括利益 (損失) の累計 | (160.5です) | | | (153.7) | |
| 利益剰余金 | 18,021.0 | | | 17,627.6 | |
| 自己株式(原価) | (2,977.1) | | | (2,977.1) | |
| | | |
| | | |
| 総資本 | 15,213.0です | | | 14,799.4 | |
| 負債と資本の合計 | $ | 26,567.6 | | | $ | 26,844.8 | |
これらの未監査の要約連結財務諸表の添付注記を参照してください。
バイオジェン株式会社と子会社
要約連結キャッシュフロー計算書
(未監査、百万単位)
| | | | | | | | | | | |
| | 3月31日に終了した3か月間、 |
| | 2024 | | 2023 |
| 営業活動によるキャッシュフロー: | | | |
| 当期純利益 | $ | 393.4 | | | $ | 387.6 | |
| 純利益を営業活動による純キャッシュフローと調整するための調整: | | | |
| 減価償却と償却 | 147.5 | | | 112.3 | |
| | | |
| 在庫に関連する超過費用と陳腐化費用 | 27.5 | | | 17.4 | |
| 在庫ステップアップの償却 | 44.1 | | | — | |
| | | |
| 株式ベースの報酬 | 72.8 | | | 75.6 | |
| | | |
| 繰延所得税 | 39.9 | | | (64.5) | |
| 戦略的投資の(利益)損失 | 31.3 | | | 79.6 | |
| | | |
| | | |
| | | |
| その他 | 25.4 | | | 31.4 | |
| 買収した事業の影響を差し引いた営業資産と負債の変動: | | | |
| 売掛金 | 43.7 | | | 77.2 | |
| 抗CD20治療プログラムのため | 40.7 | | | 37.6 | |
| インベントリ | (77.7) | | | 27.9 | |
| 未払費用およびその他の流動負債 | (177.1) | | | (295.0) | |
| 所得税の資産と負債 | (2.2) | | | 65.0 | |
| 営業資産と負債のその他の変動、純額 | (56.1) | | | (96.8) | |
| 営業活動によって提供される(使用された)純キャッシュフロー | 553.2 | | | 455.3 | |
| 投資活動によるキャッシュフロー: | | | |
| 不動産、プラント、設備の購入 | (45.9) | | | (66.6) | |
| 有価証券の売却および満期による収入 | — | | | 406.7 | |
| 有価証券の購入 | — | | | (1,321.2) | |
| | | |
| | | |
| | | |
| | | |
| | | |
| 無形資産の取得 | (75.0) | | | (5.0) | |
| 戦略的投資の売却による収入 | 55.6 | | | 33.8 | |
| その他 | (0.7) | | | (0.7) | |
| 投資活動によって提供される(使用された)純キャッシュフロー | (66.0) | | | (953.0です) | |
| 財務活動によるキャッシュフロー: | | | |
| | | |
| 株式ベースの報酬契約のための株式発行に関連する支払い、純額 | (46.9) | | | (60.1) | |
| 支払った借入金と保険料の返済 | (400.0) | | | — | |
| | | |
| | | |
| 非支配持分への純額(分配)拠出額 | — | | | 0.2 | |
| その他 | 7.3 | | | 16.5 | |
| 財務活動によって提供される(使用された)純キャッシュフロー | (439.6) | | | (43.4) | |
| 現金および現金同等物の純増額(減少) | 47.6 | | | (541.1) | |
| 現金および現金同等物に対する為替レートの変動の影響 | (23.1) | | | 20.0 | |
| 現金および現金同等物、期初 | 1,049.9 | | | 3,419.3 | |
| 現金および現金同等物、期末 | $ | 1,074.4 | | | $ | 2,898.2 | |
これらの未監査の要約連結財務諸表の添付注記を参照してください。
バイオジェン株式会社と子会社
要約連結株主資本計算書
(未監査、百万単位)
| | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | |
| 2024年3月31日 |
| | 優先株式 | | 普通株式 | | [追加]
支払い済み
資本 | | 累積
その他
包括的
損失 | | 保持
収益 | | 自己株式 | | | | | | 合計
公平 |
| | 株式 | | 金額 | | 株式 | | 金額 | | | | | 株式 | | 金額 | | | |
| 残高、2023年12月31日 | — | | | $ | — | | | 168.7 | | | $ | 0.1 | | | $ | 302.5 | | | $ | (153.7) | | | $ | 17,627.6 | | | (23.8) | | | $ | (2,977.1) | | | | | | | $ | 14,799.4 | |
| 当期純利益 | — | | | — | | | — | | | — | | | — | | | — | | | 393.4 | | | — | | | — | | | | | | | 393.4 | |
| その他の包括利益(損失)(税引後) | — | | | — | | | — | | | — | | | — | | | (6.8) | | | — | | | — | | | — | | | | | | | (6.8) | |
| | | | | | | | | | | | | | | | | | | | | | | |
| | | | | | | | | | | | | | | | | | | | | | | |
| | | | | | | | | | | | | | | | | | | | | | | |
| | | | | | | | | | | | | | | | | | | | | | | |
| ストックオプションと株式購入プランに基づく普通株式の発行 | — | | | — | | | 0.1 | | | — | | | 15.7 | | | — | | | — | | | — | | | — | | | | | | | 15.7 | |
| 株式報奨制度に基づく普通株式の発行 | — | | | — | | | 0.6 | | | — | | | (62.6) | | | — | | | — | | | — | | | — | | | | | | | (62.6) | |
| 株式ベースの支払いに関連する報酬 | — | | | — | | | — | | | — | | | 76.1 | | | — | | | — | | | — | | | — | | | | | | | 76.1 | |
| その他 | — | | | — | | | — | | | — | | | (2.2) | | | — | | | — | | | — | | | — | | | | | | | (2.2) | |
| 残高、2024年3月31日 | — | | | $ | — | | | 169.4 | | | $ | 0.1 | | | $ | 329.5 | | | $ | (160.5です) | | | $ | 18,021.0 | | | (23.8) | | | $ | (2,977.1) | | | | | | | $ | 15,213.0です | |
| | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | |
| 2023年12月31日 |
| | 優先株式 | | 普通株式 | | [追加]
支払い済み
資本 | | 累積
その他
包括的
損失 | | 保持
収益 | | 自己株式 | | 合計
バイオジェン
株主の
公平 | | 非制御
興味 | | 合計
公平 |
| 株式 | | 金額 | | 株式 | | 金額 | | | | | 株式 | | 金額 | | | |
| 残高、2022年12月31日 | — | | | $ | — | | | 167.9 | | | $ | 0.1 | | | $ | 73.3 | | | $ | (164.9) | | | $ | 16,466.5 | | | (23.8) | | | $ | (2,977.1) | | | $ | 13,397.9 | | | $ | (9.5) | | | $ | 13,388.4 | |
| 当期純利益 | — | | | — | | | — | | | — | | | — | | | — | | | 387.9 | | | — | | | — | | | 387.9 | | | (0.3) | | | 387.6 | |
| その他の包括利益(損失)(税引後) | — | | | — | | | — | | | — | | | — | | | (7.1) | | | — | | | — | | | — | | | (7.1) | | | — | | | (7.1) | |
| | | | | | | | | | | | | | | | | | | | | | | |
| 非支配持分からの資本拠出 | — | | | — | | | — | | | — | | | — | | | — | | | — | | | — | | | — | | | — | | | 0.2 | | | 0.2 | |
| | | | | | | | | | | | | | | | | | | | | | | |
| | | | | | | | | | | | | | | | | | | | | | | |
| ストックオプションと株式購入プランに基づく普通株式の発行 | — | | | — | | | 0.1 | | | — | | | 20.1 | | | — | | | — | | | — | | | — | | | 20.1 | | | — | | | 20.1 | |
| 株式報奨制度に基づく普通株式の発行 | — | | | — | | | 0.6 | | | — | | | (80.2) | | | — | | | — | | | — | | | — | | | (80.2) | | | — | | | (80.2) | |
| 株式ベースの支払いに関連する報酬 | — | | | — | | | — | | | — | | | 78.9 | | | — | | | — | | | — | | | — | | | 78.9 | | | — | | | 78.9 | |
| その他 | — | | | — | | | — | | | — | | | (0.9) | | | — | | | — | | | — | | | — | | | (0.9) | | | — | | | (0.9) | |
| バランス、2023年3月31日 | — | | | $ | — | | | 168.6 | | | $ | 0.1 | | | $ | 91.2 | | | $ | (172.0) | | | $ | 16,854.4 | | | (23.8) | | | $ | (2,977.1) | | | $ | 13,796.6 | | | $ | (9.6) | | | $ | 13,787.0 | |
これらの未監査の要約連結財務諸表の添付注記を参照してください。
目次
バイオジェン株式会社と子会社
要約連結財務諸表の注記
(未監査)
これらの注記での「バイオジェン」、「会社」、「私たち」、「私たち」、「私たち」とは、バイオジェン社とその連結子会社を指します。
事業概要
バイオジェンは、世界中の重篤で複雑な疾患を抱える人々のための革新的な治療法の発見、開発、提供に焦点を当てたグローバルなバイオ医薬品企業です。私たちは多発性硬化症の治療薬の幅広いポートフォリオを持っており、SMAの最初に承認された治療法を導入し、アルツハイマー病の決定的な病状に対処するための治療法を共同開発し、ALSの遺伝的原因を標的とする最初の承認された治療法を開始しました。2023年にReataを買収したことで、16歳以上の成人と青年のフリードライヒ運動失調症の治療薬として、米国とEUで承認された最初で唯一の薬を販売しました。私たちは、神経学、専門免疫学、希少疾患のパイプラインを発展させることに注力しています。私たちは、社内の研究開発プログラムと外部のコラボレーションを通じて、私たちの創薬と開発の取り組みを支援しています。
私たちが市販している製品には、多発性硬化症の治療用のテクフィデラ、ヴメリティ、アボネックス、プレグリディ、タイサブリ、ファンピラ、SMA治療用のスピンラザ、フリードライヒ運動失調症の治療用のSKYCLARYS、ALSの治療用のQALSODY、重度の尋常性乾癬の治療用のFUMADERMなどがあります。
また、アルツハイマー病の治療のためのLEQEMBIの商品化ではエーザイと、PPD治療用のZURZUVAEの商品化ではSageと協力しており、非ホジキンリンパ腫、CLLなどの治療用のリツキサン、非ホジキンリンパ腫、CLLなどの治療用のリツキサン、非ホジマー病の治療用のリツキサンハイセラに関して特定の事業上および財務上の権利がありますグキンリンパ腫とCLL、CLLと濾胞性リンパ腫の治療にはGAZYVA、PPMSとRMSの治療にはOCREVUS、再発または難治性濾胞の治療にはルンスミオリンパ腫、非ホジキンリンパ腫の治療のための二重特異性抗体であるCOLUMVI、およびロシュグループの完全子会社であるジェネンテックとのコラボレーション契約により、他の潜在的な抗CD20療法を追加することができます。
ヨーロッパの特定の国では、エンブレルを指すエタネルセプトバイオシミラーのベネパリ、ヒュミラを指すアダリムマブのバイオシミラーであるイムラルディ、レミケードを参照するインフリキシマブのバイオシミラーであるフリクサビ、ラニビズマブのバイオシミラーであるBYOOVIZなど、先端生物製剤のバイオシミラーのポートフォリオを商品化しています米国および特定の国際市場におけるLUCENTISを指します。また、アクテムラを参考にしたトシリズマブのバイオシミラーであるトフィデンスを商品化する独占権もあります。私たちは、EYLEAを参考にしたアフリベルセプトのバイオシミラーとして提案されているバイオシミラーである潜在的なバイオシミラー製品SB15の開発を続けています。
当社のコラボレーション契約に関する追加情報については、これらの未監査の要約連結財務諸表(要約連結財務諸表)の注記19「協力およびその他の関係」を参照してください。
プレゼンテーションの基礎
経営陣の見解では、当社の要約連結財務諸表には、米国会計基準に準拠した中間期間の財務諸表の公正な計算書に必要な、通常の定期発生額からなるすべての調整が含まれています。フォーム10-Qのこの四半期報告書に含まれる情報は、監査済み連結財務諸表および2023フォーム10-Kに含まれる添付の注記と併せて読む必要があります。当社の会計方針は、2023年フォーム10-Kの連結財務諸表の注記に記載されており、必要に応じてこのレポートで更新されています。比較目的で提示されている年末の要約連結貸借対照表データは、当社の監査済み財務諸表から導き出されたものですが、米国会計基準で要求されるすべての開示が含まれているわけではありません。2024年3月31日に終了した3か月間の経営成績は、必ずしも通期またはそれ以降の中間期間の業績を示すものではありません。
私たちは次のように運営しています 一 事業セグメントでは、重篤な神経疾患や神経変性疾患を患っている人々、および関連する治療法の隣接疾患を患っている人々のための革新的な治療法を世界中で発見、開発、提供することに重点を置いています。
目次
バイオジェン株式会社と子会社
要約連結財務諸表の注記
(未監査、続き)
統合
当社の要約連結財務諸表には、当社の財務諸表、完全子会社、および当社が主な受益者である特定の変動持分法人の財務諸表が反映されています。当社が所有している、または投資対象が以下の事業体である連結対象事業体の場合 100.0経済に占める割合は、非支配持分に帰属する非支配持分に帰属する純利益(損失)を税引後要約連結損益計算書に記録します。これは、それぞれの非支配当事者が当該事業体に留保している経済的または所有権のパーセンテージに等しくなります。連結では、会社間の残高と取引はなくなります。
私たちが変動持分法人の主な受益者であるかどうかを判断する際には、(1)事業体の経済的に重要な活動を指示する権限と、(2)その事業体にとって潜在的に重要となる可能性のある事業体の損失を吸収する義務、または利益を受ける権利の両方があるかどうかを判断する定性的アプローチを適用します。既存の関係や将来の取引の変化により、1人または複数の協力者やパートナーを統合または連結解除する可能性があるため、私たちは変動持分法人の主な受益者であるかどうかを継続的に評価しています。2023年11月、私たちは神経免疫契約を終了し、その結果、当社の変動持分事業体であるニュー免疫は連結解除されました。Neurimmune の連結解除に関する追加情報については、これらの要約連結財務諸表の注記20「変動持分事業体への投資」をご覧ください。
見積もりの使用
要約連結財務諸表を作成するには、報告された資産、負債、資本、収益、費用の金額、および偶発資産と負債の関連する開示に影響を与える可能性のある見積もり、判断、仮定を行う必要があります。私たちは継続的に見積もり、判断、仮定を評価します。私たちは、過去の経験や合理的と思われるその他のさまざまな仮定に基づいて見積もりをしています。その結果は、資産、負債、資本の帳簿価額と収益と費用の金額を判断するための基礎となります。実際の結果は、これらの見積もりとは異なる場合があります。
重要な会計方針
注記1「重要な会計方針の要約」に開示されている当社の重要な会計方針や、2023年フォーム10-Kに含まれる監査済み連結財務諸表に重大な変更はありません。
新しい会計上の宣言
時々、指定された発効日に、FASBまたは当社が採用するその他の基準設定機関によって、新しい会計上の宣言が発行されます。以下で特に説明しない限り、最近発行された基準の採用が、当社の要約連結財務諸表または開示に重大な影響を与えたとは考えていません。
気候関連の開示
2024年3月、SECはSECリリース第33-11275号「投資家向けの気候関連開示の強化と標準化」に基づく最終規則を発表しました。この新しい規則により、大規模な加速申告者は、事業、経営成績、または財政状態に重大な影響を与える可能性が合理的に高い重要な気候関連リスクを開示することが義務付けられます。気候関連リスクについて必要な情報には、所有または管理されている事業所からの実質的な直接温室効果ガス排出量(スコープ1)や、所有または管理対象事業で消費される購入エネルギーからの重要な間接温室効果ガス排出量(スコープ2)の開示も含まれます。さらに、新しい規則では、特定の重要基準を条件として、厳しい気象現象やその他の自然条件の影響と、気候関連の目標や目標に関する情報を財務諸表の注記に開示することが義務付けられます。最終規則が採択された場合、2025年12月31日に終了する年度の年次報告書から段階的に導入される段階的なコンプライアンス期間が含まれます。
2024年4月、SECは司法審査を待つ間、新しい気候関連の開示要件の実施を自主的に延期しました。現在、この新しい規則が当社の開示に与える潜在的な影響を評価しています。
目次
バイオジェン株式会社と子会社
要約連結財務諸表の注記
(未監査、続き)
セグメントレポート
2023年11月、FASBはASU第2023-07号「セグメント報告(トピック280):報告対象セグメント開示の改善」を発行しました。この基準では、CODMに定期的に提供され、報告された各セグメントの損益指標に含まれる重要なセグメント費用、セグメントの利益または損失と照合するための他のセグメント項目の金額とその構成の説明、および企業のCODMのタイトルと位置の開示が義務付けられています。このアップデートの改正により、暫定的なセグメント開示要件も拡大されています。この基準に基づくすべての開示要件は、報告対象セグメントが1つしかない公的機関にも必要です。この基準は、2023年12月15日以降に開始する会計年度と、2024年12月15日以降に開始する会計年度内の中間期間に有効です。早期採用は許可されており、このアップデートの修正は遡及的に適用する必要があります。現在、この新しい基準が当社の要約連結財務諸表および関連する開示に与える潜在的な影響を評価しています。
レアタファーマシューティカルズ株式会社
2023年9月26日、重篤な神経疾患の細胞代謝と炎症を調節する治療薬の開発に注力するバイオ医薬品企業であるReataの発行済み株式および発行済み株式の取得を完了しました。この取引の結果、私たちはSKYCLARYS(オマベロキソロン)を買収しました。SKYCLARYS(オマベロキソロン)は、16歳以上の成人および青年のフリードライヒ運動失調症の治療薬として、米国とEUで最初で唯一の承認薬であり、その他の臨床および前臨床パイプラインプログラムでもあります。Reataの買収は、当社の神経筋および希少疾患治療薬のグローバルポートフォリオを補完することが期待されています。SKYCLARYSの加入は、SPINRAZAとQALSODYとの潜在的な営業上の相乗効果をもたらすと予想されます。
この買収の条件に基づき、私たちはReataの株主に$を支払いました172.50 発行済みおよび発行済みのReata株式1株につき現金で、合計で約$です6.610億。さらに、私たちはおよそ$を支払うことに同意しました983.9Reataの発行済み株式報奨のための100万ドルの現金(雇用者税を含む)、そのうち約$590.5です百万は購入前のサービスによるもので、したがって支払った購入金額の合計に反映されます。$の983.9Reataの株式報奨保有者に支払われた100万ドル、私たちは約$を認識しました393.4買収後のサービス期間に起因する報酬として100万ドル、そのうち$196.4百万ドルは、販売費、一般管理費と残りの$の費用として計上されました197.02023年12月31日に終了した年度の要約連結損益計算書内の研究開発費への費用として百万ドルです。これらの金額は、以前にReata従業員に付与されていたストックオプションとRSUの迅速な権利確定に関連しており、権利確定に将来のサービスを必要としませんでした。
この買収は、利用可能な現金、現金同等物、および有価証券を通じて資金を調達し、さらに$の発行によって補われました1.0 タームローンクレジット契約に基づく10億タームローン。当社のタームローンクレジット契約の詳細については、これらの要約連結財務諸表の注記13「負債」をご覧ください。
この買収は、ASCトピック805「企業結合」に従った買収会計方法、および取得日現在のそれぞれの公正価値で引き受けた記録資産と引き受けた負債を使用して、企業結合として会計処理しました。
購入価格の考慮事項
Reataの買収のために譲渡された対価の総額は次のように要約されます。
| | | | | | | | |
| (百万単位) | | 2023年9月26日現在 |
Reata株主に支払われる現金対価 (1) | | $ | 6,602.9 | |
Reata株式報酬取得前サービスの公正価値と関連税金 (2) | | 590.5です | |
| 総対価額 | | $ | 7,193.4 | |
(1) $の送金された現金対価を表します172.50 REATA発行済普通株式1株あたりに基づく 38.3クロージング時に発行された100万株のReata株。
(2) Reata株式報奨保有者に発行されたReataストックオプションと株式ユニットの公正価値、および買収前の権利確定サービスに帰属する関連税金を表します。
目次
バイオジェン株式会社と子会社
要約連結財務諸表の注記
(未監査、続き)
暫定購入価格配分
次の表は、取得日時点で取得された資産と引き受けた負債について計上された暫定金額と、取得日の時点で最初に記録された金額に対して年初から今日まで行われた測定期間の調整をまとめたものです 2023年9月26日。以下に要約する測定期間の調整は、特定の無形資産に関連する将来のキャッシュフローの推定額とタイミングに関する評価仮定の更新、数量、販売場所、取得した在庫の残りの製造および販売コスト、およびその他の資産と負債に関する仮定の更新によるものです。買収日の時点で調整が認識されていれば、前の期間に認識されていたであろう要約連結損益計算書への関連する影響は重要ではありません。
| | | | | | | | | | | | | | |
| (百万単位) | | | | | | | | 買収日時点で認識されている金額
(調整後)
2024年3月31日 |
| 現金および現金同等物 | | | | | | | | $ | 267.3 | |
| 売掛金 | | | | | | | | 15.9 | |
| インベントリ | | | | | | | | 1,259.0 | |
| その他の流動資産 | | | | | | | | 53.6 | |
| 無形資産: | | | | | | | | |
| スカイクラリス(米国)の完成したテクノロジー | | | | | | | | 4,200.0 | |
| 製造中の研究開発(オマベロキソロン) | | | | | | | | 2,300.0 | |
| 優先審査券 | | | | | | | | 100.0 | |
| その他の臨床プログラム | | | | | | | | 40.0 | |
| オペレーティングリース資産 | | | | | | | | 121.2 | |
未払費用とその他 (1) | | | | | | | | (106.4) | |
| 未払債務です | | | | | | | | (159.9) | |
| ブラックストーンに支払われる派遣団 | | | | | | | | (300.0) | |
繰延税金負債 (1) | | | | | | | | (916.5) | |
| オペレーティングリース負債 | | | | | | | | (151.8) | |
| その他の資産および負債、純額 | | | | | | | | (2.5) | |
| 識別可能な純資産総額 | | | | | | | | 6,719.9 | |
グッドウィル (1) | | | | | | | | 473.5 | |
| 取得した総資産と引き受けた負債 | | | | | | | | $ | 7,193.4 | |
(1) 2024年の第1四半期に記録された測定期間の調整により、未払費用などがドル増加したものを含みます4.9百万、繰延税金負債(ドル)4.1百万、のれんは$で9.0百万。
在庫:取得した在庫の合計は約$でした1.310億。これは、SKYCLARYSの完成品と仕掛品在庫の公正価値の上昇を反映しています。公正価値は、在庫の推定販売価格から、残りの製造および販売コストと、それらの製造および販売努力による通常の利益率を差し引いたものに基づいて決定されました。この公正価値のステップアップ調整は、在庫が売却されると、要約連結損益計算書内の売上原価に償却されます。これは、おおよその範囲内になると予想されます 3 買収日から何年も。2024年3月31日に終了した3か月間、売却された在庫による公正価値のステップアップ調整による償却額は約$でした44.1 百万。
無形資産:無形資産はドルで構成されています4.210億ドルは、米国でのSKYCLARYSの商品化権に関するものです。2.3買収日の時点でまだEUで規制当局の承認を受けていない、米国外のオマベロキソロンプログラムに関連する10億件の知的財産権、$100.0将来の規制当局への提出に備えてFDAによる優先審査を受けるために使用したり、第三者に売却したりできる、希少な小児疾患に関する優先バウチャーに関する100万ドル40.0百万は他の臨床プログラムに関連しています。プログラム関連の無形資産の推定公正価値は、インカムアプローチの一形態である複数期間の超過収益法を使用して決定されました。割引率は次のとおりです。 14.3% と優先審査バウチャーの推定公正価値は、同様のバウチャーの最近の外部売買取引に基づいています。
目次
バイオジェン株式会社と子会社
要約連結財務諸表の注記
(未監査、続き)
SKYCLARYSの商業化権に対する当社の評価は、経済消費モデルを用いると、関連する費用という仮定を反映しています4.210億の無形資産は、予想される経済期間にわたって償却されます。
SKYCLARYSが2024年2月にEU規制当局の承認を受けると、ヨーロッパの特定の国で製品の販売を開始し、ドルの償却を開始しました2.3経済消費モデルを使用した、予想される経済寿命にわたる米国外のプログラムに関連する10億件の知的財産権保護資産。
これらの公正価値の測定は、市場では観察できない重要なインプットに基づいており、したがってレベル3の公正価値の測定値を表しています。
リース:私たちは、おおよそ1テナントのビルド・トゥ・スーツの建物の責任を引き受けました 327,400です テキサス州プラノにあるオフィスと研究室のスペースの面積。最初のリース期間は 16 何年も。約$のリース負債を記録しました151.8百万は、残りのリース期間における賃貸費用の正味現在価値を表します 15 何年も、それに対応する使用権資産は約$です121.2百万。これは、テキサス州ダラス地域の現在の賃貸市場における市場参加者の公正価値の推定値です。市場賃貸料の見積もりには、建物に関連する借地権の改善やテナント手当の価値が含まれます。私たちはこの建物を占有するつもりはなく、物件を転貸する機会を検討しています。
のれん:のれんは、譲渡された対価の額が認識された純資産を上回った額として計算され、個別に特定したり認識したりすることができなかった他の資産から生じる将来の経済的利益を表しています。約$のれんを認識しました473.5百万ですが、これは税務上控除できません。Reataの買収により認識されるのれんは、主に財務諸表の目的で記録された取引による繰延税金上の影響によるものです。
買収関連費用:買収関連の費用は、主に規制費用、顧問費用、弁護士費用、およびその他の取引費用で構成され、合計で約$28.4百万ドルで、2023年12月31日に終了した年度の要約連結損益計算書の販売費、一般管理費に計上されました。
購入価格の配分における前提条件
2023年9月26日のReataの買収完了以降、Reataの経営成績は、取得した資産と引き受けた負債の推定公正価値とともに、要約連結財務諸表に含まれています。
買収日時点で取得された具体的に特定可能な資産および引き受けた負債の公正価値の暫定的な見積もりは、所得税の査定の最終決定など、特定の事項に関する経営陣の分析の最終決定を条件としています。これらの公正価値の最終決定は、追加情報が入手でき次第、取得日から1年以内に完了します。最終決定により、資産と負債の公正価値が暫定的な見積もりとは異なる場合があります。
サムスン・バイオエピスの合弁持分の売却
2022年4月、私たちは私たちの販売を完了しました 49.9対価総額約$と引き換えに、サムスンバイオロジクスにサムスンバイオエピスの持分%2.310億。この取引の条件では、約$を受け取りました1.0決算時に10億円の現金、約$1.32回の支払いで10億の現金が繰り延べられます。$の最初の繰延支払い812.52023年4月に100万ドルが受領され、2回目の繰延支払いが行われました437.52024年4月に100万が受領されました。
私たちは公正価値オプションを選択し、Samsung Biologicsからの当社への支払い額を公正価値で測定しました。2024年3月31日現在、リスク調整後の割引率を使用した場合の2回目の繰延支払いの推定公正価値は 6.0% は約$でした436.1 百万。この支払いはレベル3の指標として分類され、2024年3月31日現在の当社の要約連結貸借対照表内の他の流動資産に反映されています。
2024年3月31日に終了した3か月間で、約$の利益を計上しました6.1100万は、当社に支払うべき2回目の繰延支払いに関連する公正価値の変化を反映しています。2023年3月31日に終了した3か月間で、私たちは約$の利益を計上しました11.1百万と $6.2に関連する公正価値の変動を反映して100万です
目次
バイオジェン株式会社と子会社
要約連結財務諸表の注記
(未監査、続き)
それぞれ当社に支払うべき1回目と2回目の繰延支払い。これらの変化は、当社の要約連結損益計算書に差し引かれたその他(収益)費用に計上されました。
Samsung Bioepisの持分の売却に関する追加情報については、2023年フォーム10-Kに含まれる当社の連結財務諸表の注記3「処分」をご覧ください。
2023 フィット・フォー・グロースリストラクチャリング・プログラム
2023年7月、私たちはFit for Growthプログラムの一環として、業務の効率と効果を向上させながら運営コストを削減するための追加のコスト削減策を開始しました。Fit for Growth プログラムは約$の収益を見込んでいます1.02025年末までに総営業経費を節約でき、その一部はさまざまな取り組みに再投資される予定です。Fit for Growth プログラムには、現在、約 1,000 従業員と私たちは、約$の範囲のリストラ費用が発生すると予想しています260.0百万からドル280.0百万。
2023年のコスト削減イニシアチブから発生した費用の合計は、次のようにまとめられます。
| | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | |
| | 3月31日に終了した3か月間、 |
| | 2024 | | |
| (百万単位) | | セブランス
費用 | | 加速減価償却およびその他の費用 | | | | 合計 | | | | | | | | |
| 販売、一般および管理 | | $ | — | | | $ | 1.4 | | | | | $ | 1.4 | | | | | | | | | |
| 研究開発 | | — | | | 4.9 | | | | | 4.9 | | | | | | | | | |
| リストラ費用 | | 9.3 | | | — | | | | | 9.3 | | | | | | | | | |
| 合計請求額 | | $ | 9.3 | | | $ | 6.3 | | | | | $ | 15.6 | | | | | | | | | |
| | | | | | | | | | | | | | | | |
| | |
| | | | |
| | | | | | | | | | | | | | | | |
| | | | | | | | | | | | | | | | |
| | | | | | | | | | | | | | | | |
| | | | | | | | | | | | | | | | |
| | | | | | | | | | | | | | | | |
その他の費用:資産の放棄や償却、施設閉鎖費用、特定のリースの終了による税引前損益、従業員の退職防止費用、コンサルティング料、その他の費用などの項目に関連する費用が含まれます。
リアータ・インテグレーション
2023年9月にReataの買収が完了した後、私たちはコスト削減と回避を通じて業務上の相乗効果を実現するための統合計画を実施しました。このイニシアチブでは、統合費用の総額は約$程度になると見積もっています35.0百万からドル40.0百万ドル。退職金と雇用費用に関連しており、2024年末までに支払われる予定です。これらの金額は2023年に大幅に発生しました。
Reata統合によって発生した合計請求額は次のように要約されます。
| | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | |
| | 3月31日に終了した3か月間、 |
| | 2024 | | |
| (百万単位) | | セブランス
費用 | | 加速減価償却およびその他の費用 | | | | 合計 | | | | | | | | |
| 販売、一般および管理 | | $ | — | | | $ | 1.8 | | | | | $ | 1.8 | | | | | | | | | |
| 研究開発 | | — | | | 2.7 | | | | | 2.7 | | | | | | | | | |
| リストラ費用 | | 2.2 | | | — | | | | | 2.2 | | | | | | | | | |
| 合計請求額 | | $ | 2.2 | | | $ | 4.5 | | | | | $ | 6.7 | | | | | | | | | |
| | | | | | | | | | | | | | | | |
| | |
| | | | |
| | | | | | | | | | | | | | | | |
| | | | | | | | | | | | | | | | |
| | | | | | | | | | | | | | | | |
| | | | | | | | | | | | | | | | |
| | | | | | | | | | | | | | | | |
Reataの買収に関連して、私たちは、およそ1テナントのビルド・トゥ・スーツの建物の責任を引き受けました 327,400です テキサス州プラノにあるオフィスと研究室のスペースの面積。最初のリース期間は 16 何年も。私たちはこの建物を占有するつもりはなく、物件を転貸する機会を検討しています。
2023年のFit for GrowthプログラムとReata Integrationによる人員削減に関連する費用と支出は、次のように要約されています。
目次
バイオジェン株式会社と子会社
要約連結財務諸表の注記
(未監査、続き)
| | | | | | | | | | | | | | | | | | | | | | |
| | 3月31日に終了した3か月間、 | | | | |
| (百万単位) | | 2024 | | 2023 |
| | | | | | | | | | | | |
| 12月31日現在の事業再編準備金 | | $ | 75.4 | | | | | | | $ | 35.9 | | | | | |
| 経費 | | 11.5 | | | | | | | 7.1 | | | | | |
| 支払 | | (42.2) | | | | | | | (15.6) | | | | | |
| 外貨やその他の調整 | | 0.8 | | | | | | | 0.6 | | | | | |
| 3月31日現在のリストラ準備金 | | $ | 45.5 | | | | | | | $ | 28.0 | | | | | |
| | | | | | | | | | | | |
| | | | | | | | | | | | |
| | | | | | | | | | | | |
| | | | | | | | | | | | |
| | | | | | | | | | | | |
| | | | | | | | | | | | |
| | | | | | | | | | | | |
| | | | | | | | | | | | |
目次
バイオジェン株式会社と子会社
要約連結財務諸表の注記
(未監査、続き)
製品収益
製品別の収益は次のように要約されます。
| | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | |
| | | 3月31日に終了した3か月間、 |
| | 2024 | | 2023 |
| (百万単位) | | ユナイテッド
州 | | 残りの
世界 | | 合計 | | ユナイテッド
州 | | 残りの
世界 | | 合計 |
| 多発性硬化症: | | | | | | | | | | | | |
| テフィデラです | | $ | 43.7 | | | $ | 210.6 | | | $ | 254.3 | | | $ | 74.7 | | | $ | 199.8 | | | $ | 274.5 | |
| 多数 | | 105.9 | | | 21.6 | | | 127.5 | | | 93.5 | | | 14.7 | | | 108.2 | |
| 総フマル酸塩 | | 149.6 | | | 232.2 | | | 381.8 | | | 168.2 | | | 214.5 | | | 382.7 | |
| アボネックス | | 111.2 | | | 67.3 | | | 178.5 | | | 102.6 | | | 69.8 | | | 172.4 | |
| プレグリディー | | 28.6 | | | 36.5 | | | 65.1 | | | 29.9 | | | 43.3 | | | 73.2 | |
| トータルインターフェロン | | 139.8 | | | 103.8 | | | 243.6 | | | 132.5 | | | 113.1 | | | 245.6 | |
| タイサブリ | | 213.8 | | | 217.5 | | | 431.3 | | | 245.4 | | | 227.4 | | | 472.8 | |
| ファンパイラ | | — | | | 19.2 | | | 19.2 | | | — | | | 24.1 | | | 24.1 | |
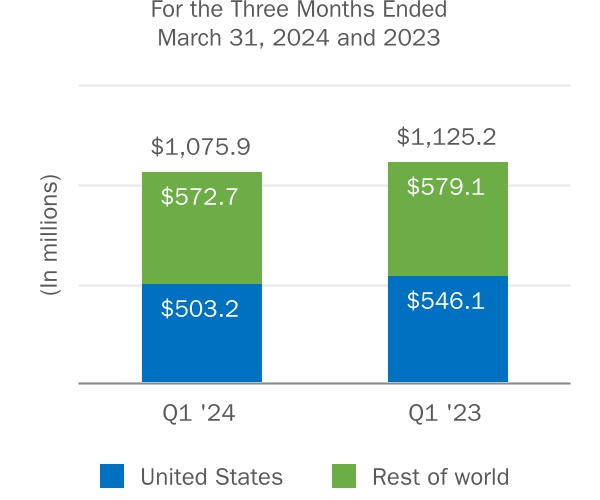
| 小計:多発性硬化症 | | 503.2 | | | 572.7 | | | 1,075.9 | | | 546.1 | | | 579.1 | | | 1,125.2 | |
| | | | | | | | | | | | |
| 希少疾患: | | | | | | | | | | | | |
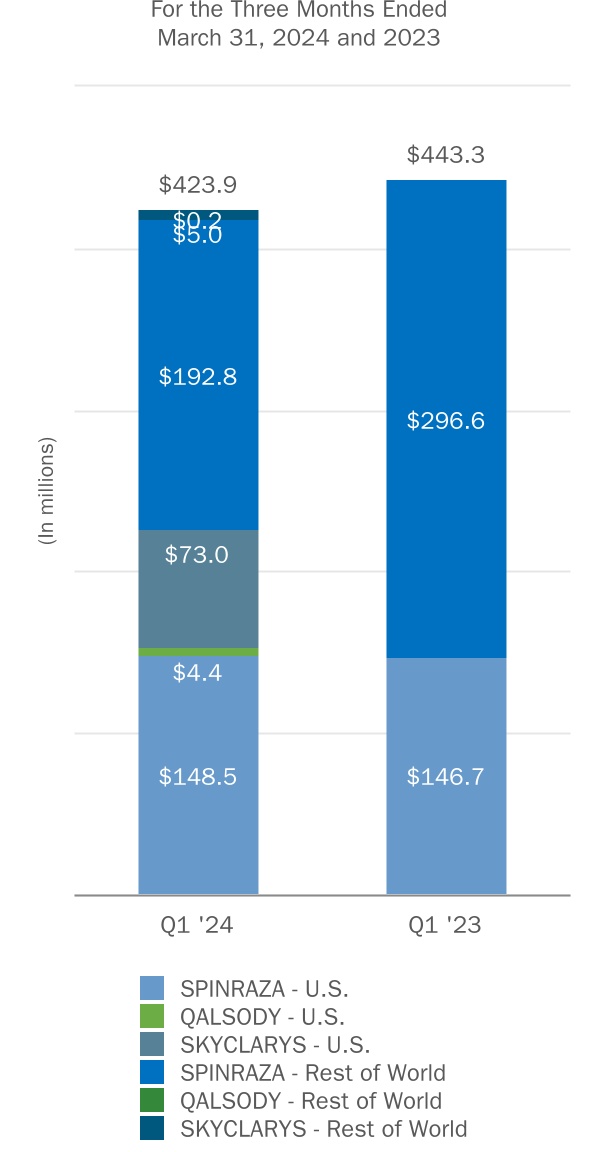
| スピンラザ | | 148.5 | | | 192.8 | | | 341.3 | | | 146.7 | | | 296.6 | | | 443.3 | |
アルコディ (1) | | 4.4 | | | 0.2 | | | 4.6 | | | — | | | — | | | — | |
スカイクラリーズ (2) | | 73.0 | | | 5.0 | | | 78.0 | | | — | | | — | | | — | |
| 小計:希少疾患 | | 225.9 | | | 198.0 | | | 423.9 | | | 146.7 | | | 296.6 | | | 443.3 | |
| | | | | | | | | | | | |
| バイオシミラー: | | | | | | | | | | | | |
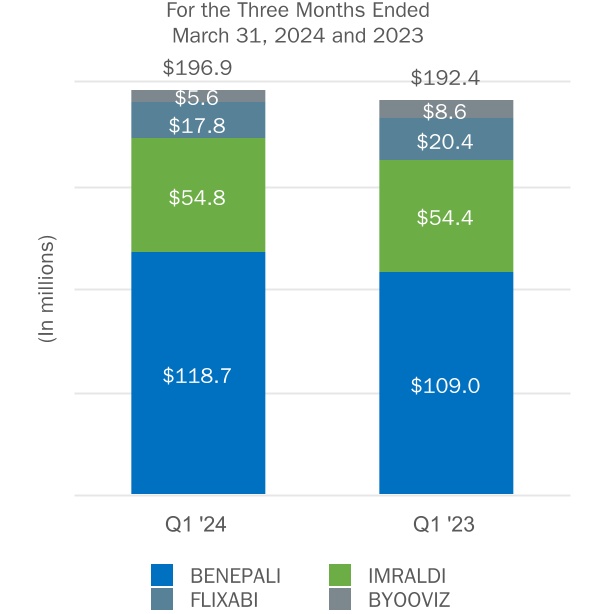
| ベネパリです | | — | | | 118.7 | | | 118.7 | | | — | | | 109.0 | | | 109.0 | |
| イムラルディ | | — | | | 54.8 | | | 54.8 | | | — | | | 54.4 | | | 54.4 | |
| フリクサビ | | — | | | 17.8 | | | 17.8 | | | — | | | 20.4 | | | 20.4 | |
ブービズ (3) | | 3.7 | | | 1.9 | | | 5.6 | | | 8.2 | | | 0.4 | | | 8.6 | |
| 小計:バイオシミラー | | 3.7 | | | 193.2 | | | 196.9 | | | 8.2 | | | 184.2 | | | 192.4 | |
| | | | | | | | | | | | |
| | | | | | | | | | | | |
| | | | | | | | | | | | |
| | | | | | | | | | | | |
| | | | | | | | | | | | |
その他 (4) | | 13.3 | | | 1.9 | | | 15.2 | | | 0.4 | | | 2.0 | | | 2.4 | |
| 製品総収入 | | $ | 746.1 | | | $ | 965.8 | | | $ | 1,711.9 | | | $ | 701.4 | | | $ | 1,061.9 | | | $ | 1,763.3 | |
(1) QALSODYは、2023年の第2四半期に米国で市販されました。
(2) SKYCLARYSは、2023年9月にReataを買収した際に買収されました。SKYCLARYSは2023年の第2四半期に米国で市販され、買収後の2023年の第4四半期に米国でSKYCLARYSからの収益が計上され始めました。SKYCLARYSは承認され、2024年の第1四半期にEUで市販されるようになりました。
(3) BYOOVIZは、2023年に特定の国際市場で市販されました。
(4) その他には、2023年の第4四半期に米国で市販されたFUMADERM、ADUHELM、ZURZUVAEが含まれます。
からの収益を認識しました 二 の会計処理を行う卸売業者 25.6% と 11.72024年3月31日に終了した3か月間の総製品収益の割合、および 27.3% と 7.42023年3月31日に終了した3か月間の総製品収益の割合。
目次
バイオジェン株式会社と子会社
要約連結財務諸表の注記
(未監査、続き)
割引引当金と手当引当金の変動の分析は次のように要約されます。
| | | | | | | | | | | | | | | | | | | | | | | | | | |
| (百万単位) | | 割引 | | 契約上
調整 | | 返品について | | 合計 |
| 残高、2023年12月31日 | | $ | 173.3 | | | $ | 857.1 | | | $ | 31.6 | | | $ | 1,062.0 | |
| 当年度の売上に関する現在の規定 | | 181.5です | | | 682.6 | | | 5.0 | | | 869.1 | |
| 過年度に関連する調整 | | 6.1 | | | (16.9) | | | 5.6 | | | (5.2) | |
| 今年度の売上に関連する支払い/クレジット | | (109.1) | | | (262.1) | | | (0.2) | | | (371.4) | |
| 過去数年間の売上に関連する支払い/クレジット | | (94.2) | | | (358.0) | | | (5.6) | | | (457.8) | |
| 残高、2024年3月31日 | | $ | 157.6 | | | $ | 902.7 | | | $ | 36.4 | | | $ | 1,096.7 | |
当社の要約連結貸借対照表に含まれる上記の準備金の総額は、次のように要約されます。
| | | | | | | | | | | | | | |
| (百万単位) | | 2024年3月31日現在 | | 2023年12月31日現在 |
| 売掛金の削減 | | $ | 139.7 | | | $ | 135.5 | |
| 未払費用の構成要素とその他 | | 957.0 | | | 926.5 | |
| 収益関連の準備金の総額 | | $ | 1,096.7 | | | $ | 1,062.0 | |
抗CD20治療プログラムからの収入
抗CD20治療プログラムからの収益は、以下の表にまとめられています。この脚注では、リツキサンとリツキサンハイセラを総称してリツクサンと呼びます。
| | | | | | | | | | | | | | | | | | |
| | | 3月31日に終了した3か月間、 | | |
| (百万単位) | | 2024 | | 2023 | | | | |
| OCREVUSの売り上げに対するロイヤリティ収入 | | $ | 302.7 | | | $ | 283.6 | | | | | |
| リツキサン、ガジバ、ルンスミオの米国における税引前利益に占めるバイオジェンのシェア | | 87.1 | | | 112.5 | | | | | |
| 抗CD20治療プログラムからのその他の収入 | | 4.2 | | | 3.4 | | | | | |
| 抗CD20治療プログラムの総収入 | | $ | 394.0 | | | $ | 399.5 | | | | | |
ジェネンテックとのコラボレーション契約の詳細については、このレポートに含まれる当社の連結財務諸表の注記19「協力およびその他の関係」を参照してください。
受託製造、ロイヤリティ、その他の収入
受託製造、ロイヤリティ、その他の収益は、以下の表にまとめられています。
| | | | | | | | | | | | | | | | | | |
| | | 3月31日に終了した3か月間、 | | |
| (百万単位) | | 2024 | | 2023 | | | | |
| 受託製造収入 | | $ | 152.2 | | | $ | 306.9 | | | | | |
ロイヤリティとその他の収入 | | 32.4 | | | (6.7) | | | | | |
| 受託製造、ロイヤリティ、その他の収益の合計 | | $ | 184.6 | | | $ | 300.2 | | | | | |
受託製造収入
受託製造収益は、主に戦略的顧客との委託製造契約に基づいて得られる金額を反映しています。2023年の第1四半期に、米国でのLEQEMBIの承認が加速され、LEQEMBIの受託製造収益の計上を開始しました。承認が加速される前は、LEQEMBIに関連する受託製造金額の当社のシェアは、要約連結損益計算書の研究開発費に計上されていました。
ロイヤリティとその他の収入
ロイヤルティやその他の収益は主に、私たちがアウトライセンスした特許に関連する製品の純売上高から受け取るロイヤルティと、ライセンス契約によるバイオシミラー製品のロイヤルティ収入を反映しています
目次
バイオジェン株式会社と子会社
要約連結財務諸表の注記
(未監査、続き)
サムスンのバイオエピスと私たちの 50.0LEQEMBI製品の収益、純額および売上原価に占める割合(ロイヤリティを含む)。私たちは主要企業ではないからです。
エーザイとのコラボレーション契約およびSamsung Bioepisとのライセンス契約の詳細については、これらの要約連結財務諸表の注記19「協力およびその他の関係」を参照してください。
インベントリの構成要素は次のように要約されます。
| | | | | | | | | | | | | | |
| (百万単位) | | 2024年3月31日現在 | | 2023年12月31日現在 |
| 原材料 | | $ | 412.5 | | | $ | 426.9 | |
| 作業中 | | 1,851.3 | | | 1,926.8 | |
| 完成品 | | 347.9 | | | 255.4 | |
| 在庫合計 | | $ | 2,611.7 | | | $ | 2,609.1 | |
| | | | |
| 貸借対照表の分類: | | | | |
| インベントリ | | $ | 2,516.8 | | | $ | 2,527.4 | |
| 投資およびその他の資産 | | 94.9 | | | 81.7 | |
| 在庫合計 | | $ | 2,611.7 | | | $ | 2,609.1 | |
W彼は約$を記録しました1.32023年9月にReataを買収した結果、SKYCLARYSに関連して、測定期間の調整を含む10億件のインベントリを取得しました。公正価値は、在庫の推定販売価格から、残りの製造および販売コストと、それらの製造および販売努力による通常の利益率を差し引いたものに基づいて決定されました。この公正価値のステップアップ調整は、在庫が売却されたときに、要約連結損益計算書内の売上原価に償却されます。在庫は約範囲内になると予想されます 3 買収日から何年も。2024年3月31日に終了した3か月間、売却された在庫による公正価値のステップアップ調整による償却額は約$でした44.1 百万。Reataの買収に関する追加情報については、これらの要約連結財務諸表の注記2「買収」を参照してください。
無形資産
無形資産(累積償却額、減損費用および調整額を差し引いたもの)は次のように要約されます。
| | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | |
| | | | | 2024年3月31日現在 | | 2023年12月31日現在 |
| (百万単位) | | 推定寿命 | | 費用 | | 累積
償却 | | ネット | | 費用 | | 累積
償却 | | ネット |
| 完成したテクノロジー: | | | | | | | | | | | | | | |
| 取得およびライセンス供与された権利と特許 | | 2-22 何年も | | $ | 10,480.2 | | | $ | (2,514.0) | | | $ | 7,966.2 | | | $ | 8,180.2 | | | $ | (2,440.7) | | | $ | 5,739.5 | |
| 開発した技術やその他 | | 13-31 何年も | | 3,548.6 | | | (3,434.1) | | | 114.5 | | | 3,548.6 | | | (3,429.1) | | | 119.5 | |
| 完成したテクノロジー全体 | | | | 14,028.8 | | | (5,948.1) | | | 8,080.7 | | | 11,728.8 | | | (5,869.8) | | | 5,859.0 | |
| 進行中の研究開発 | | 商品化までは無期限 | | 40.0 | | | — | | | 40.0 | | | 2,340.0 | | | — | | | 2,340.0 | |
| 優先審査券 | | 無期限 | | 100.0 | | | — | | | 100.0 | | | 100.0 | | | — | | | 100.0 | |
| 商標と商号 | | 無期限 | | 64.0 | | | — | | | 64.0 | | | 64.0 | | | — | | | 64.0 | |
| 無形資産合計 | | | | $ | 14,232.8 | | | $ | (5,948.1) | | | $ | 8,284.7 | | | $ | 14,232.8 | | | $ | (5,869.8) | | | $ | 8,363.0です | |
償却と減損
2024年3月31日に終了した3か月間、取得した無形資産の償却と減損の合計額は78.3 百万、ドルと比較50.2 前年の比較期間で百万。この増加は主に
目次
バイオジェン株式会社と子会社
要約連結財務諸表の注記
(未監査、続き)
Reata買収による償却は、SKYCLARYSに関連する無形資産を取得しました。2024年と2023年3月31日に終了した3か月間、減損費用はありませんでした。
完成したテクノロジー
完成したテクノロジーは主に、資産取得、ライセンス、企業結合を通じて取得した他の市場に出回っている製品やプログラムに関するものです。完成したテクノロジーの無形資産は、推定耐用年数にわたって償却されます。耐用年数の範囲は 2 に 31 年、残りの加重平均耐用年数は 12 取得およびライセンス供与された権利と特許、および 10 開発技術やその他に何年も。2023年9月のReataの買収に関連して、米国で商業的に承認された製品であるSKYCLARYSを買収しました。推定公正価値は約$です4.210億。これには測定期間の調整も含まれます。2024年の第1四半期に、SKYCLARYSはEUで承認され、商業的に利用可能になりました。その結果、関連する無形資産の再分類が行われ、推定公正価値は約$になりました2.3知的財産権の研究開発から完成した技術まで、10億ドル。
企業結合に関連するIPR&D
IPR&Dは、当社が企業結合の一環として取得し、買収日にはまだ技術的実現可能性に達していなかった研究開発資産に割り当てられた公正価値を表します。IPR&D残高には、外貨為替レートの変動に関連する調整が含まれます。2023年9月のReataの買収に関連して取得したIPR&Dプログラムに関連する、2023年12月31日現在の当社のIPR&D資産の帳簿価額。推定公正価値は約$です2.310億。これには測定期間の調整も含まれます。2024年の第1四半期に、SKYCLARYSはEUで承認され、商業的に利用可能になりました。その結果、関連する無形資産がIPR&Dから完成技術に再分類されました。
優先審査券
2023年9月のReata買収に関連して、希少小児疾患優先審査券を取得しました。このバウチャーは、将来の規制当局への提出に備えてFDAによる優先審査を受けるために使用したり、第三者に売却したりすることができます。優先審査バウチャーは、推定公正価値$に基づいて記録しました100.0無形資産として百万。推定公正価値は、同様のバウチャーの最近の外部売買取引に基づいています。
Reataの買収に関する追加情報については、これらの要約連結財務諸表の注記2「買収」を参照してください。
無形資産の将来の推定償却額
今後5年間の有限無形資産の将来の推定償却額は、次のようになると予想されます。
| | | | | | | | |
| (百万単位) | | 2024年3月31日現在 |
| 2024年 (残りの9か月間) | | $ | 265.0 | |
| 2025 | | 565.0 | |
| 2026 | | 660.0 | |
| 2027 | | 685.0 | |
| 2028 | | 710.0 | |
| 2029 | | 715.0 | |
グッドウィル
次の表は、当社ののれん残高の変動の繰り越しを示しています。
| | | | | | | | |
| (百万単位) | | 2024年3月31日現在 |
| グッドウィル、2023年12月31日 | | $ | 6,219.2 | |
| Reataの買収によるのれんが | | 9.0 | |
| その他 | | (0.8) | |
| グッドウィル、2024年3月31日 | | $ | 6,227.4 | |
Reataの買収に関する追加情報については、これらの要約連結財務諸表の注記2「買収」を参照してください。
目次
バイオジェン株式会社と子会社
要約連結財務諸表の注記
(未監査、続き)
2024年3月31日現在、私たちは いいえ のれんに関連する減損損失の累積。その他には、外貨為替レートの変動に関連する調整が含まれます。
以下の表は、定期的に公正価値で測定・運用されている当社の資産と負債に関する情報を示しており、当社がそのような公正価値を決定するために利用した評価手法の公正価値階層内のレベルを示しています。
| | | | | | | | | | | | | | | | | | | | | | | | | | |
| | 定期的な公正価値の測定 |
| | 2024年3月31日現在 |
| (百万単位) | | 合計 | | 見積価格
アクティブ中
マーケット
(レベル 1) | | 重要なその他
観察可能な入力
(レベル 2) | | 重要な
観察不能
インプット
(レベル 3) |
| 資産: | | | | | | | | |
| 現金同等物 | | $ | 484.8 | | | $ | — | | | $ | 484.8 | | | $ | — | |
| | | | | | | | |
| | | | | | | | |
| | | | | | | | |
| | | | | | | | |
| 市場性のある株式証券 | | 329.5 | | | 329.5 | | | — | | | — | |
| その他の流動資産: | | | | | | | | |
サムスン・バイオロジクスからの売掛金 (1) | | 436.1 | | | — | | | — | | | 436.1 | |
| デリバティブ契約 | | 9.9 | | | — | | | 9.9 | | | — | |
| その他の非流動資産 | | | | | | | | |
| 繰延報酬用の計画資産 | | 39.0 | | | — | | | 39.0 | | | — | |
| | | | | | | | |
| 合計 | | $ | 1,299.3 | | | $ | 329.5 | | | $ | 533.7 | | | $ | 436.1 | |
| 負債: | | | | | | | | |
| デリバティブ契約 | | $ | 27.3 | | | $ | — | | | $ | 27.3 | | | $ | — | |
| | | | | | | | |
| 合計 | | $ | 27.3 | | | $ | — | | | $ | 27.3 | | | $ | — | |
(1)は、当社の売却の結果としてSamsung Biologicsから支払われるべき現在の支払いの公正価値を表します 49.92022年の第2四半期におけるサムスン・バイオロジクスへのサムスン・バイオエピスの持分の割合。そのために公正価値オプションを選択しました。Samsung Bioepisの持分の売却に関する追加情報については、これらの要約連結財務諸表の注記3「処分」をご覧ください。
2023年の第3四半期に、私たちは市場性のある債務証券をすべて売却し、その収益の一部をReataの買収資金に充てました。Reataの買収に関する追加情報については、これらの要約連結財務諸表の注記2「買収」を参照してください。
目次
バイオジェン株式会社と子会社
要約連結財務諸表の注記
(未監査、続き)
| | | | | | | | | | | | | | | | | | | | | | | | | | |
| | 定期的な公正価値の測定 |
| | 2023年12月31日現在 |
| (百万単位) | | 合計 | | 見積価格
アクティブ中
マーケット
(レベル 1) | | 重要なその他
観察可能な入力
(レベル 2) | | 重要な
観察不能
インプット
(レベル 3) |
| 資産: | | | | | | | | |
| 現金同等物 | | $ | 610.7 | | | $ | — | | | $ | 610.7 | | | $ | — | |
| | | | | | | | |
| | | | | | | | |
| | | | | | | | |
| | | | | | | | |
| 市場性のある株式証券 | | 416.8 | | | 416.8 | | | — | | | — | |
| その他の流動資産: | | | | | | | | |
サムスン・バイオロジクスからの売掛金 (1) | | 430.0 | | | — | | | — | | | 430.0 | |
| デリバティブ契約 | | 11.9 | | | — | | | 11.9 | | | — | |
その他の非流動資産 | | | | | | | | |
| | | | | | | | |
| 繰延報酬用の計画資産 | | 37.5 | | | — | | | 37.5 | | | — | |
| 合計 | | $ | 1,506.9 | | | $ | 416.8 | | | $ | 660.1 | | | $ | 430.0 | |
| 負債: | | | | | | | | |
| デリバティブ契約 | | $ | 31.6 | | | $ | — | | | $ | 31.6 | | | $ | — | |
| | | | | | | | |
| 合計 | | $ | 31.6 | | | $ | — | | | $ | 31.6 | | | $ | — | |
(1)は、当社の売却の結果としてSamsung Biologicsから支払われるべき現在の支払いの公正価値を表します 49.92022年の第2四半期におけるサムスン・バイオロジクスへのサムスン・バイオエピスの持分の割合。そのために公正価値オプションを選択しました。Samsung Bioepisの持分の売却に関する追加情報については、これらの要約連結財務諸表の注記3「処分」をご覧ください。
当社の有価証券は、上場株式への投資です。デナリ、セージ、サンガモへの投資を清算する能力は、当社の持分の規模、市場関連活動の量、所有権の集中、および協力者としての地位に起因する可能性のある制限によって制限される場合があります。したがって、そのような投資の現在の価値を大幅に下回る可能性があります。
デナリ、サンガモ、セージの普通株式への投資に関する追加情報については、2023年フォーム10-Kに含まれる連結財務諸表の注記19「協力およびその他の関係」をご覧ください。
ありました いいえ 2024年3月31日および2023年12月31日現在の公正価値で測定および計上された当社資産の重大な減損です。さらに、2024年3月31日および2023年12月31日現在、当社の評価手法に変更はありません。
第三者価格設定サービスによって提供される価格および当社のオプション価格評価モデルに関する当社の検証手続きの説明については、2023年フォーム10-Kに含まれる当社の連結財務諸表の注記1「重要な会計方針の要約-公正価値測定」をご覧ください。
公正価値で保有されているレベル3の資産と負債
2024年3月31日および2023年12月31日現在、レベル3への資産または負債の移転またはレベル3からの移転はありませんでした。
公正価値で保有されていない金融商品
その他の金融商品
特定の金融商品は短期的な性質を持っているため、反CD20治療プログラム、その他の流動資産、買掛金および未払費用、その他から支払われるべき当座売掛金、その他の要約連結貸借対照表に反映されている帳簿価額は、公正価値に近似します。
目次
バイオジェン株式会社と子会社
要約連結財務諸表の注記
(未監査、続き)
債務証券
レベル2の負債である当社の債務証書の公正価値と帳簿価額は次のように要約されます。
| | | | | | | | | | | | | | | | | | | | | | | | | | |
| | | 2024年3月31日現在 | | 2023年12月31日現在 |
| (百万単位) | | フェア
価値 | | 持ち運び
価値 | | フェア
価値 | | 持ち運び
価値 |
| 現在の部分: | | | | | | | | |
2023 タームローン 364日トランシェ (1) | | $ | — | | | $ | — | | | $ | 150.0 | | | $ | 150.0 | |
2023 タームローン3年分トランシェ (1) | | 250.0 | | | 250.0 | | | — | | | — | |
| 支払手形とタームローンの現在の部分 | | 250.0 | | | 250.0 | | | 150.0 | | | 150.0 | |
| | | | | | | | |
| 非電流部分: | | | | | | | | |
2023 タームローン3年分トランシェ (1) | | — | | | — | | | 500.0 | | | 500.0 | |
| 2025年9月15日に満期の 4.050% シニアノート | | 1,717.5 | | | 1,747.1 | | | 1,721.5 | | | 1,746.6 | |
| 2030年5月1日が満期の 2.250% シニアノート | | 1,267.8 | | | 1,494.0 | | | 1,279.3 | | | 1,493.8 | |
| 5.200% 2045年9月15日に期限が切れるシニアノート | | 1,055.6 | | | 1,100.8 | | | 1,089.7 | | | 1,100.7 | |
| 2050年5月1日が満期の 3.150% シニアノート | | 1,004.5 | | | 1,474.5 | | | 1,049.0 | | | 1,474.3 | |
| 2015年2月15日満期の 3.250% シニアノート | | 486.6 | | | 473.7 | | | 498.2 | | | 472.8 | |
| 支払手形とタームローンの非流動部分 | | 5,532.0 | | | 6,290.1です | | | 6,137.7 | | | 6,788.2 | |
| 支払手形とタームローンの総額 | | $ | 5,782.0 | | | $ | 6,540.1です | | | $ | 6,287.7 | | | $ | 6,938.2 | |
(1) Reataの買収に関連して、私たちは$を引き出しました1.0 2023年のタームローンからの10億、合計は500.0 100万回の変動金利364日トランシェと1ドル500.0 百万変動金利制の3年間のトランシェ。2023年のタームローンの追加情報については、これらの要約連結財務諸表の注記13「負債」をご覧ください。
当社の一連のシニアノートそれぞれの公正価値は、市場で、観察可能で、裏付けのある情報源を通じて決定されました。2023年12月31日と比較した2024年3月31日現在の当社のシニアノートの公正価値の変動は、主に米国財務省利回りの上昇が、2023年12月31日以降の当社のシニアノートの評価に使用されたクレジットスプレッドの減少によって一部相殺されたことによるものです。シニアノートに関連する追加情報については、2023年フォーム10-Kに含まれる連結財務諸表の注記13「債務」をご覧ください。
次の表は、要約連結貸借対照表の現金および現金同等物に含まれる購入日から満期が90日未満の当社の金融資産をまとめたものです。
| | | | | | | | | | | | | | |
| (百万単位) | | 2024年3月31日現在 | | 2023年12月31日現在 |
| | | | |
| | | | |
| マネー・マーケット・ファンド | | $ | 484.8 | | | $ | 610.7 | |
| | | | |
| | | | |
合計 | | $ | 484.8 | | | $ | 610.7 | |
当社のマネー・マーケット・ファンドの帳簿価額は、満期が短いので、おおよその公正価値です。
Reataの買収資金の一部は、利用可能な現金、現金同等物、および有価証券を通じて賄われました。2023年12月31日現在、私たちは市場性のある債券をすべて売却しました。Reataの買収に関する追加情報については、これらの要約連結財務諸表の注記2「買収」を参照してください。
目次
バイオジェン株式会社と子会社
要約連結財務諸表の注記
(未監査、続き)
当社の有価証券利益(損失)はその他(収益)費用に計上され、差し引いた金額は要約連結損益計算書に計上されます。 次の表は、売却可能に分類される当社の有価証券をまとめたものです。
| | | | | | | | | | | | | | | | | | | | | | | | | | |
| | 2024年3月31日現在 |
| (百万単位) | | 償却済み
費用 | | グロス
未実現
利益 | | グロス
未実現
損失 | | フェア
価値 |
| | | | | | | | |
| | | | | | | | |
| | | | | | | | |
| | | | | | | | |
| | | | | | | | |
| | | | | | | | |
| | | | | | | | |
| | | | | | | | |
| | | | | | | | |
| | | | | | | | |
| | | | | | | | |
| | | | | | | | |
| 市場性のある株式証券 | | | | | | | | |
| 市場性のある株式証券、現在の | | $ | 11.7 | | | $ | — | | | $ | (11.0) | | | $ | 0.7 | |
| 市場性のある株式証券、非流動株式 | | 916.7 | | | — | | | (587.9) | | | 328.8 | |
| 市場性のある株式の総数 | | $ | 928.4 | | | $ | — | | | $ | (598.9) | | | $ | 329.5 | |
| | | | | | | | | | | | | | | | | | | | | | | | | | |
| | 2023年12月31日現在 |
| (百万単位) | | 償却済み
費用 | | グロス
未実現
利益 | | グロス
未実現
損失 | | フェア
価値 |
| | | | | | | | |
| | | | | | | | |
| | | | | | | | |
| | | | | | | | |
| | | | | | | | |
| | | | | | | | |
| | | | | | | | |
| | | | | | | | |
| | | | | | | | |
| | | | | | | | |
| | | | | | | | |
| | | | | | | | |
| 市場性のある株式証券 | | | | | | | | |
| 市場性のある株式証券、現在の | | $ | 31.6 | | | $ | — | | | $ | (21.0) | | | $ | 10.6 | |
| 市場性のある株式証券、非流動株式 | | 948.3 | | | — | | | (542.1) | | | 406.2 | |
| 市場性のある株式の総数 | | $ | 979.9 | | | $ | — | | | $ | (563.1) | | | $ | 416.8 | |
市場性のある負債証券からの収入
有価負債証券の満期および売却による収入、および結果として生じる実現損益は次のように要約されます。
| | | | | | | | | | | | | | |
| | | | | | |
| (百万単位) | | | | 2023年3月31日に終了した3か月間 | | | | |
| 満期と売却による収入 | | | | $ | 406.7 | | | | | |
| 実現した利益 | | | | 0.1 | | | | | |
| 実現損失 | | | | 0.7 | | | | | |
2023年3月31日に終了した3か月間の実現損失は、主に米国債と社債の売却に関連しています。
2023年の第3四半期に、私たちは市場性のある債務証券をすべて売却し、その収益の一部をReataの買収資金に充てました。Reataの買収に関する追加情報については、これらの要約連結財務諸表の注記2「買収」を参照してください。
戦略的投資
当社の戦略的投資ポートフォリオには、これらの要約連結財務諸表の注記8「公正価値測定」に含まれる開示に反映されている、特定のバイオテクノロジー企業の株式証券への投資と、特定のバイオテクノロジー企業の株式および市場性のない株式を基礎とするベンチャーキャピタルファンドへの投資が含まれます。
2024年3月31日および2023年12月31日の時点で、当社の戦略的投資ポートフォリオは合計$の投資で構成されていました382.0 百万と $460.7 それぞれ百万円で、その他の流動資産と投資、および当社の要約連結貸借対照表内のその他の資産に含まれています。
2024年3月31日現在の戦略的投資ポートフォリオの減少は、主にセージとデナリの普通株式への投資の公正価値の減少によるものです。さらに、2024年の第1四半期に、デナリとサンガモの普通株式の一部を売却しました。
デナリ、サンガモ、セージの普通株式への戦略的投資の詳細については、2023年フォーム10-Kに含まれる連結財務諸表の注記19「協力およびその他の関係」をご覧ください。
目次
バイオジェン株式会社と子会社
要約連結財務諸表の注記
(未監査、続き)
外貨先渡契約-ヘッジ商品
当社の事業はグローバルに展開しているため、収益と営業費用の一部は米ドル以外の通貨で記録されています。したがって、米ドルで測定される収益と営業費用の価値は、外貨為替レートの変動の影響を受けます。私たちは、外貨為替レートの変動が当社の国際収益と運営費用に与える影響を軽減することを主な目的として、金融機関と外貨先渡契約および外貨オプションを締結しています。
2024年3月31日および2023年12月31日の時点で有効な外貨先渡契約と外貨オプションの期間は 1 に 9 数ヶ月と 1 に 12 それぞれ月です。これらの契約はキャッシュフローヘッジとして指定されており、これらの外貨先渡契約と有効性テストに含まれる外貨オプションの一部の未実現損益はAOCIで報告されています。このような契約やオプションの実現損益は、ヘッジされている通貨での商品の販売が認識された場合は収益に、ヘッジされている通貨での費用が記録された場合は営業費用に計上されます。AOCIによるすべてのキャッシュフロー・ヘッジ再分類と、要約連結損益計算書の同じ明細項目の除外部分の公正価値変動は、ヘッジ項目の影響を受けていることを認識しています。
予測収益と営業費用をヘッジするために締結された外貨先渡契約と外貨オプションの想定額は、次のように要約されます。
| | | | | | | | | | | | | | |
| | 想定金額 |
| (百万単位) | | 2024年3月31日現在 | | 2023年12月31日現在 |
| ユーロ | | $ | 1,274.6 | | | $ | 1,169.0 | |
| 英国ポンド | | 45.9 | | | — | |
| スイスフラン | | 215.6 | | | — | |
| | | | |
| カナダドル | | 39.7 | | | — | |
| 外貨先渡契約とオプションの合計 | | $ | 1,575.8 | | | $ | 1,169.0 | |
AOCIの総資本に含まれていたこれらの外貨先渡契約および外貨オプションの公正価値の税引前部分は、次のように要約されます。
| | | | | | | | | | | | | | |
| | | | |
| (百万単位) | | 2024年3月31日現在 | | 2023年12月31日現在 |
| 未実現利益 | | $ | 4.6 | | | $ | — | |
| 未実現(損失) | | (23.3) | | | (34.8) | |
| 純含み益 (損失) | | $ | (18.7) | | | $ | (34.8) | |
未実現純損失は約$になると予想しています18.7次回に決済される予定の100万ドル 9 月数。収益または営業費用の調整として、AOCIの任意の金額を報告します。私たちは、当社および取引相手の信用リスクが契約の公正価値に与える影響と、各当事者が契約上の義務を履行する能力に与える影響を考慮しています。2024年3月31日および2023年12月31日現在、信用リスクは当社の外貨先渡契約と先物通貨オプションの公正価値を大きく変えていません。
次の表は、当社の要約連結損益計算書でヘッジ手段として指定された外貨先渡契約と先物通貨オプションの影響をまとめたものです。
| | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | |
| 3月31日に終了した3か月間、 |
純利益/(損失)
AOCIから営業利益に再分類されました | | 純利益/(損失)
営業利益に計上されました |
| 場所 | | 2024 | | 2023 | | 場所 | | 2024 | | 2023 |
| 収入 | | $ | 2.9 | | | $ | 17.6 | | | 収入 | | $ | 0.2 | | | $ | 1.6 | |
| 営業経費 | | (2.1) | | | (0.5) | | | 営業経費 | | (1.2) | | | (2.1) | |
| | | | | | | | | | |
|
| | |
| | | | | | | | | | |
| | | | | | | | | | |
| | | | | | | | | | |
目次
バイオジェン株式会社と子会社
要約連結財務諸表の注記
(未監査、続き)
外貨先渡契約-その他のデリバティブ商品
また、特定の貸借対照表のポジションに関連する外貨リスクを軽減するために、通常1か月以内の他の外貨先渡契約も締結しています。これらの取引にはヘッジ会計を選択していません。
これらの未払いの外貨先渡契約の想定総額は $1,308.3 百万と $1,301.5です 2024年3月31日および2023年12月31日時点でそれぞれ百万です。$の純損失24.3 百万ドル、純利益は1.8 これらの契約に関連する100万件が、それぞれ2024年3月31日および2023年3月31日に終了した3か月間のその他(収益)費用の一部として計上されました。
デリバティブ商品の概要
当社のデリバティブ商品の中には、取引相手とのネッティング契約の対象となるものもありますが、要約連結貸借対照表ではデリバティブ資産と負債を相殺していません。デリバティブ資産と負債を相殺しても、以下の表の金額に大きな違いはありません。
次の表は、ヘッジ商品として指定されているものを含む、当社の未払いのデリバティブ商品の公正価値と要約連結貸借対照表における表示をまとめたものです。
| | | | | | | | | | | | | | | | | | | | |
| (百万単位) | | 貸借対照表の場所 | | 2024年3月31日現在 | | 2023年12月31日現在 |
| キャッシュフローヘッジ商品: | | | | | | |
| 資産デリバティブ商品 | | その他の流動資産 | | $ | 8.6 | | | $ | 0.3 | |
| | | | | | |
| 賠償責任デリバティブ商品 | | 未払費用とその他 | | 19.8 | | | 26.5 | |
| | | | | | |
| | | | | | |
| | | | | | |
| | | | | | |
| | | | | | |
| | | | | | |
| | | | | | |
| その他のデリバティブ商品: | | | | | | |
| 資産デリバティブ商品 | | その他の流動資産 | | 1.3 | | | 11.6 | |
| 賠償責任デリバティブ商品 | | 未払費用とその他 | | 7.5 | | | 5.1 | |
不動産、プラント、設備は、減価償却累計額を差し引いた実績原価で計上されます。不動産、プラント、設備の減価償却累計額は $2,468.2 百万と $2,402.5 2024年3月31日および2023年12月31日時点でそれぞれ百万です。2024年3月31日に終了した3か月間の減価償却費は合計$でした69.3 $の比較で百万62.1 前年の比較期間で百万。
ゾロトゥルン、スイスの製造施設
将来の成長と医薬品開発パイプラインをサポートするために、スイスのゾロトゥルンに大規模な生物製剤製造施設を建設しました。この施設には以下が含まれます 393,000 大規模な生物製剤製造施設に関連する平方フィート、 290,000 倉庫、ユーティリティ、サポートスペースの平方フィートと 51,000 管理スペースの平方フィートです。2023年12月31日現在、私たちの持っていた金額は約$です728.8 この施設に関連して建設が進行中であるため、100万が資本化されました。2021年の第2四半期に、この施設の一部(最初の製造スイート)がSWISSMEDICからGMPマルチプロダクトライセンスを取得し、稼働を開始しました。2番目の製造スイートは2024年の第1四半期に稼働し、その結果は約$になりました717.3何百万もの固定資産が運用されています。ゾロトゥルンは、FDAによってLEQEMBIの製造が承認されました。
目次
バイオジェン株式会社と子会社
要約連結財務諸表の注記
(未監査、続き)
6100 レガシードライブリース
Reataの買収に関連して、私たちは、およそ1テナントのビルド・トゥ・スーツの建物の責任を引き受けました 327,400です テキサス州プラノにあるオフィスと研究室のスペースの面積。最初のリース期間は 16 何年も。約$のリース負債を記録しました151.8百万は、残りのリース期間における賃貸費用の正味現在価値を表します 15 何年も、それに対応する使用権資産は約$です121.2百万。これは、テキサス州ダラス地域の現在の賃貸市場における市場参加者の公正価値の推定値です。市場賃貸料の見積もりには、建物に関連する借地権の改善やテナント手当の価値が含まれます。私たちはこの建物を占有するつもりはなく、物件を転貸する機会を検討しています。
Reataの買収に関する追加情報については、これらの要約連結財務諸表の注記2「買収」を参照してください。
2023 タームローン クレジット契約
2023年9月のReataの買収に関連して、私たちは$を締結しました1.510億タームローンクレジット契約(2023年タームローン)。Reata買収の締切日に、私たちは$を引き出しました1.0 2023年のタームローンからの10億、合計金額は500.0100万回の変動金利364日トランシェと1ドル500.0百万変動金利制の3年間のトランシェ。$の残りの未使用のコミットメント500.0ミリオンは終了しました。2023年12月31日時点で、私たちはドルを返済しました350.0364日のトランシェのうち100万個。残りの $150.0その後、364日間のトランシェのうち100万部が2024年の第1四半期に支払われました。さらに、2024年の第1四半期に、ドルを返済しました250.03年間のトランシェのうち100万個。2024年3月31日現在、私たちは$を持っていました250.02023年のタームローンの3年間のトランシェで未払いの金額が100万件です。
株式買戻し
2020年10月、当社の取締役会は、2020年の自社株買戻しプログラムを承認しました。これは、最大ドルを買い戻すプログラムです5.0 10億の普通株式。2020年の自社株買戻しプログラムには有効期限はありません。2020年の自社株買戻しプログラムに基づくすべての自社株買いは廃止されます。2024年3月31日および2023年3月31日に終了した3か月間、当社の普通株式の自社株買いはありませんでした。およそ $2.1 2024年3月31日現在、2020年の自社株買戻しプログラムでは10億株が引き続き利用可能です。
その他の包括利益 (損失) の累計
次の表は、AOCIの税引後における変化をコンポーネント別にまとめたものです。
| | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | |
| | 2024年3月31日 |
| (百万単位) | | 売却可能な有価証券の未実現利益(損失)、税引後 | | キャッシュフローヘッジの未実現利益(損失)、税引後 | | | | 年金給付債務の未実現利益(損失)、税引後 | | 通貨換算の調整 | | 合計 |
| 残高、2023年12月31日 | | $ | — | | | $ | (25.0) | | | | | $ | (2.6) | | | $ | (126.1) | | | $ | (153.7) | |
| 再分類前のその他の包括利益 (損失) | | — | | | 15.4 | | | | | (0.1) | | | (21.4) | | | (6.1) | |
| AOCIから再分類された金額 | | — | | | (0.7) | | | | | — | | | — | | | (0.7) | |
| 当期の純その他の包括利益 (損失) | | — | | | 14.7 | | | | | (0.1) | | | (21.4) | | | (6.8) | |
| 残高、2024年3月31日 | | $ | — | | | $ | (10.3) | | | | | $ | (2.7) | | | $ | (147.5) | | | $ | (160.5です) | |
目次
バイオジェン株式会社と子会社
要約連結財務諸表の注記
(未監査、続き)
| | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | |
| | 2023年3月31日 |
| (百万単位) | | 売却可能な有価証券の未実現利益(損失)、税引後 | | キャッシュフローヘッジの未実現利益(損失)、税引後 | | | | 年金給付債務の未実現利益(損失)、税引後 | | 通貨換算の調整 | | 合計 |
| 残高、2022年12月31日 | | $ | (15.7) | | | $ | 15.1 | | | | | $ | (1.1) | | | $ | (163.2) | | | $ | (164.9) | |
| 再分類前のその他の包括利益 (損失) | | 5.3 | | | (20.3) | | | | | 0.5 | | | 22.1 | | | 7.6 | |
| AOCIから再分類された金額 | | 0.4 | | | (15.1) | | | | | — | | | — | | | (14.7) | |
| 当期の純その他の包括利益 (損失) | | 5.7 | | | (35.4) | | | | | 0.5 | | | 22.1 | | | (7.1) | |
| バランス、2023年3月31日 | | $ | (10.0) | | | $ | (20.3) | | | | | $ | (0.6) | | | $ | (141.1) | | | $ | (172.0) | |
次の表は、AOCIから再分類された金額をまとめたものです。
| | | | | | | | | | | | | | | | | | | | | | | | |
| (百万単位) | | AOCIから再分類された金額 | | 損益計算書の場所 |
| 3月31日に終了した3か月間、 | | | |
| 2024 | | 2023 | | | | | |
| 売却可能な有価証券の利益(損失) | | $ | — | | | $ | (0.5) | | | | | | | その他(収入)費用 |
| | — | | | 0.1 | | | | | | | 所得税(給付)費用 |
| | | | | | | | | | |
| キャッシュフローヘッジの利益(損失) | | 2.9 | | | 17.6 | | | | | | | 収入 |
| | (2.1) | | | (0.5) | | | | | | | 営業経費 |
| | 0.1 | | | (0.1) | | | | | | | その他(収入)費用 |
| | (0.2) | | | (1.9) | | | | | | | 所得税(給付)費用 |
| | | | | | | | | | |
| | | | | | | | | | |
| | | | | | | | | | |
| | | | | | | | | | |
| | | | | | | | | | |
| 再分類総額(税引後) | | $ | 0.7 | | | $ | 14.7 | | | | | | | |
当社の1株当たり利益の計算に使用される基本および希薄化後の発行済株式は次のように計算されます。
| | | | | | | | | | | | | | | | | | |
| | 3月31日に終了した3か月間、 | | |
| (百万単位) | | 2024 | | 2023 | | | | |
| 分子: | | | | | | | | |
| バイオジェンに帰属する純利益。 | | $ | 393.4 | | | $ | 387.9 | | | | | |
| 分母: | | | | | | | | |
| 加重平均発行済普通株式数 | | 145.2 | | | 144.4 | | | | | |
| 希薄化証券の影響: | | | | | | | | |
| | | | | | | | |
| 期限付き譲渡制限付株式ユニット | | 0.5 | | | 0.6 | | | | | |
| 市場株式単位 | | — | | | 0.1 | | | | | |
| 株式で決済されたパフォーマンス株式ユニット | | 0.2 | | | 0.1 | | | | | |
| 希薄化可能な普通株式 | | 0.7 | | | 0.8 | | | | | |
| 希薄化後の1株当たり利益の計算に使用される株式 | | 145.9 | | | 145.2 | | | | | |
希薄化防止効果があったため、希薄化後1株当たりの純利益の計算から除外された金額はわずかでした。
目次
バイオジェン株式会社と子会社
要約連結財務諸表の注記
(未監査、続き)
株式ベースの報酬費用
次の表は、当社の要約連結損益計算書に含まれる株式ベースの報酬費用をまとめたものです。
| | | | | | | | | | | | | | | | | | |
| | 3月31日に終了した3か月間、 | | |
| (百万単位) | | 2024 | | 2023 | | | | |
研究開発 | | $ | 27.4 | | | $ | 31.3 | | | | | |
| 販売、一般および管理 | | 44.0 | | | 50.1 | | | | | |
| | | | | | | | |
| 小計 | | 71.4 | | | 81.4 | | | | | |
| 資本化された株式ベースの報酬費用 | | (3.3) | | | (3.3) | | | | | |
| 株式ベースの報酬費用は、総費用と費用に含まれます | | 68.1 | | | 78.1 | | | | | |
| 所得税効果 | | (12.9) | | | (14.7) | | | | | |
| バイオジェンに帰属する純利益に含まれる株式ベースの報酬費用 | | $ | 55.2 | | | $ | 63.4 | | | | | |
次の表は、当社の各株式ベースの報酬プログラムに関連する株式ベースの報酬費用をまとめたものです。
| | | | | | | | | | | | | | | | | | |
| | 3月31日に終了した3か月間、 | | |
| (百万単位) | | 2024 | | 2023 | | | | |
| 期限付き譲渡制限付株式ユニット | | $ | 57.3 | | | $ | 61.7 | | | | | |
| | | | | | | | |
| | | | | | | | |
| 株式で決済されたパフォーマンス株式ユニット | | 10.5 | | | 9.5 | | | | | |
| 従業員株式購入制度 | | 4.5 | | | 4.7 | | | | | |
| 現金で決済されたパフォーマンス株ユニット | | (2.1) | | | 2.5 | | | | | |
| ストック・オプション | | 0.9 | | | 0.8 | | | | | |
| 市場株式単位 | | 0.3 | | | 2.2 | | | | | |
| 小計 | | 71.4 | | | 81.4 | | | | | |
| 資本化された株式ベースの報酬費用 | | (3.3) | | | (3.3) | | | | | |
| 株式ベースの報酬費用は、総費用と費用に含まれます | | $ | 68.1 | | | $ | 78.1 | | | | | |
私たちは、各報告期間の終わりに予定決済を通じて現金で決済されたパフォーマンス株式ユニットに関連する債務の公正価値を見積もります。これらの債務の累積調整は、株価の変動と業績関連条件の推定結果を反映して、四半期ごとに計上されます。
目次
バイオジェン株式会社と子会社
要約連結財務諸表の注記
(未監査、続き)
インフレ削減法
2022年8月、IRAは米国で法制化されました。IRAは、15.0%の法人代替最低税と1.0%の株式買戻しに対する物品税を含む新しい税制を導入しました。IRAの規定は、2022年12月31日以降の期間に有効です。IRAにより、2024年3月31日および2023年12月31日現在、当社の所得税引当金やその他の所得税残高に実質的な調整は行われていません。IRSは暫定的なガイダンスを発行しており、今後追加のガイダンスや規制が発行される予定です。さらなる情報が入り次第、当社の事業と経営成績への潜在的な影響を引き続き評価していきます。
税率
米国連邦法定税率と当社の実効税率との調整は、次のように要約されます。
| | | | | | | | | | | | | | | |
| 3月31日に終了した3か月間、 | | |
| | 2024 | | 2023 | | | | |
| 法定税率 | 21.0 | % | | 21.0 | % | | | | |
| 州税 | 1.5 | | | 1.3 | | | | | |
| 海外収益に対する税金 | (3.6) | | | (5.6) | | | | | |
| 税額控除 | (2.5) | | | (6.6) | | | | | |
| 購入した無形資産 | 1.3 | | | 0.4 | | | | | |
| | | | | | | |
| | | | | | | |
| | | | | | | |
| ギルティ | (2.6) | | | 0.5 | | | | | |
| | | | | | | |
| | | | | | | |
| | | | | | | |
| | | | | | | |
| | | | | | | |
| | | | | | | |
| | | | | | | |
| その他、パーマネントアイテムを含む | 0.3 | | | 0.6 | | | | | |
| 実効税率 | 15.4 | % | | 11.6 | % | | | | |
税率の変更
2024年3月31日に終了した3か月間の2023年の同時期と比較して、当社の実効税率の引き上げには、税額控除に関連する前年の不確実な税務問題の解決の影響と、前年に記録された未実現損失が大きかった株式投資の価値の変動による非現金税効果が含まれます。
所得税の不確実性の会計処理
当社とその子会社は、さまざまな税務当局によって定期的に審査されています。私たちは、米国のさまざまな州、米国連邦およびその他の外国の管轄区域で所得税申告書を提出します。いくつかの例外を除いて、2019年より前の年は米国連邦税務審査の対象ではなく、2013年より前の年は州、地方、または米国以外の所得税審査の対象ではなくなりました。
IRSやその他の国の税務当局は、知的財産関連の取引に関する当社の会社間移転価格を定期的に調べていますが、そのような評価に関して当社がとった1つ以上の立場に同意しない可能性があります。
特定の移転価格、協力事項、源泉徴収税、その他の問題に関連する不確実な税務上の立場について、さまざまな税務当局から追加の情報を受け取り、そのような当局との和解を含め、価値を調整することは合理的に可能です。
私たちは、利息を除いた未認識の税制上の優遇措置の総額が、可能である可能性は十分にあると推定しています
最大で約$まで減額します25.0さまざまな監査の終了、和解、時効の満了により、今後12か月で100万件になります。
目次
バイオジェン株式会社と子会社
要約連結財務諸表の注記
(未監査、続き)
その他(収入)費用、純額
その他(収益)経費(純額)の構成要素は、次のように要約されます。
| | | | | | | | | | | | | | | | | | |
| | 3月31日に終了した3か月間、 | | |
| (百万単位) | | 2024 | | 2023 | | | | |
| | | | | | | | |
| | | | | | | | |
| 利息収入 | | $ | (17.4) | | | $ | (80.9) | | | | | |
| 支払利息 | | 69.2 | | | 62.5 | | | | | |
| 投資の(利益)損失、純額 | | 30.6 | | | 77.7 | | | | | |
| 外国為替(利益)損失、純額 | | 9.4 | | | 10.7 | | | | | |
| その他、ネット | | 1.9 | | | (0.6) | | | | | |
| その他(収入)費用の合計、純額 | | $ | 93.7 | | | $ | 69.4 | | | | | |
上の表に示されているように、投資の(利益)損失の純額は、負債証券、特定のバイオテクノロジー企業の株式証券、ベンチャーキャピタルファンドに関するものです。基礎となる投資が特定のバイオテクノロジー企業の株式および非市場株式です。
次の表は、以下の期間に保有していた当社の株式に関連する投資による(利益)損失を差し引いたものです。
| | | | | | | | | | | | | | | | | | |
| | 3月31日に終了した3か月間、 | | |
| (百万単位) | | 2024 | | 2023 | | | | |
| 持分証券で認識された純損失(利益) | | $ | 30.6 | | | $ | 78.1 | | | | | |
| 控除:株式で実現した純損失(利益) | | 4.9 | | | 1.6 | | | | | |
| 株式に計上された純未実化(利益)損失 | | $ | 25.7 | | | $ | 76.5 | | | | | |
2024年3月31日に終了した3か月間に計上された純未実現損失は、主にセージとデナリの普通株式への投資の公正価値の総額が約$減少したことを反映しています27.7百万、サンガモ普通株式の公正価値が約$増加したことで一部相殺されました1.4百万。
2023年3月31日に終了した3か月間に計上された純未実現損失は、主にデナリ、サンガモ、イオニスの普通株式への投資の公正価値総額が約$減少したことを反映しています100.0百万、Sageの普通株式の公正価値が約$増加したことで一部相殺されました23.8百万。
未払費用とその他
未払費用などは次のもので構成されます。
| | | | | | | | | | | | | | |
| (百万単位) | | 2024年3月31日現在 | | 2023年12月31日現在 |
| 割引や手当のための収益関連の準備金 | | $ | 957.0 | | | $ | 926.5 | |
| 従業員の報酬と福利厚生 | | 164.1 | | | 335.1 | |
| コラボレーション費用 | | 278.0 | | | 214.6 | |
| ロイヤリティとライセンス料 | | 161.5 | | | 191.5 | |
| | | | |
| | | | |
| Reata買収関連の未払費用 | | 79.2 | | | 117.5 | |
| その他 | | 714.8 | | | 838.4 | |
| 未払費用の合計と、その他 | | $ | 2,354.6 | | | $ | 2,623.6 | |
その他の長期負債
その他の長期負債は $777.1 百万と $781.1 2024年3月31日および2023年12月31日時点でそれぞれ百万ドル。合計金額の未払所得税が含まれています411.0 百万と $403.2 それぞれ 100 万。
目次
バイオジェン株式会社と子会社
要約連結財務諸表の注記
(未監査、続き)
ジェネンテック株式会社 (ロシュグループ)
私たちは、非ホジキンリンパ腫、CLL、その他の症状の治療のためのリツキサン、非ホジキンリンパ腫とCLLの治療のためのリツキサンハイセラ、CLLと濾胞性リンパ腫の治療のためのGAZYVA、PPMSとRMSの治療のためのOCREVUS、LUNSUMIOに関して、特定の事業上および財務上の権利を持っています再発または難治性の濾胞性リンパ腫の治療、非ホジキンリンパ腫の治療のための二重特異性抗体であるCOLUMVI、その他の潜在的な抗CD20療法を追加するオプションもあります。との協力契約により、他の潜在的な抗CD20療法を追加することもできますジェネンテックは、ロシュ・グループの完全子会社です。この脚注では、リツキサンとリツキサンハイセラを総称してリツクサンと呼びます。
リツキサン
ジェネンテックとその関連会社は、次のようにリツキサンの世界的な製造だけでなく、すべての開発と商品化活動を担当しています。
•米国:私たちは、リツクサンを米国で開発、商品化、販売する権利を共同独占的にライセンスしています。
•カナダ:私たちは、カナダでリツクサンを開発、商品化、販売する権利を共同独占的にライセンスしています。
ガジーバ
ロシュグループとそのサブライセンシーは、米国でのGAZYVAの開発、製造、商品化について単独で責任を負います。以下の表に要約されているように、米国でのGAZYVAの総売上高は、RITUXANとLUNSUMIOの共同プロモーション利益の割合に影響を与えました。
オクレバス
ジェネンテックとのコラボレーション契約の条件に従い、米国の純売上高に対して段階的なロイヤリティを受け取ります 13.5% そして増加しています 24.0年間純売上高が$を超える場合は%900.0百万。あるでしょう 50.0OCREVUSのバイオシミラーが米国で承認された場合、これらのロイヤリティの%減額になります。
さらに、総額を受け取ります 3.0米国外でのOCREVUSの純売上高に対するロイヤルティ(ロイヤリティ期間が続く場合) 11 OCREVUSの最初の商用販売からの年数を国ごとに示します。
OCREVUSの商品化は、リツキサン、ルンスミオ、ガジバで受け取る共同プロモーション利益の割合には影響しません。ジェネンテックは、OCREVUSの開発と商品化、および将来の費用の資金調達について単独で責任を負います。ジェネンテックは、CLL、非ホジキンリンパ腫、または関節リウマチではOCREVUSを発症できません。
OCREVUSのロイヤリティ収入は、第三者からの推定値と、同時期に発生したOCREVUSの売上に関する市場調査データに基づいています。実際のロイヤリティ収益と見積もりロイヤリティ収益の差異は、判明した時期、つまり通常は次の四半期になると予想される時期に調整されます。
ルンスミオ(モスネツズマブ)
2022年1月、私たちはジェネンテックとオプションを行使して、LUNSUMIOの共同開発と商品化に参加しました。ジェネンテックとのコラボレーションのもと、私たちは次のことを担当しました 30.0FDA承認前のLUNSUMIOの開発費の割合。以下の表に要約されているように、米国における共同プロモーションの営業利益と損失の段階的配分を受けることができます。さらに、米国外でのLUNSUMIOの販売に対して、1桁台という低いロイヤリティが支払われます。2022年12月、LUNSUMIOは再発または難治性の濾胞性リンパ腫の治療薬としてFDAから迅速承認を受けました。
規制当局の承認前に、抗CD20製品の開発のために協力して発生した費用の研究開発費と、販売費、一般管理費に含まれる商品化前の費用のうち、当社の負担分を要約した連結損益計算書に記録しています。抗CD20製品が承認された後、その製品に関連する開発、販売、マーケティング費のうち、抗CD20治療プログラムからの収益に占める税引前利益の割合を差し引いた金額として計上します。
目次
バイオジェン株式会社と子会社
要約連結財務諸表の注記
(未監査、続き)
コロンビア(グロフィタマブ)
2022年12月、B細胞非ホジキンリンパ腫の治療のための二重特異性抗体であるCOLUMVIの商業化と経済学の共有に関する契約をジェネンテックと締結しました。その後、2023年6月にFDAから迅速承認されました。本契約の条項に基づき、当社には支払い義務はありません。ジェネンテックは、米国内でのCOLUMVIの商品化に関する唯一の意思決定権を持ち、米国でのCOLUMVIの純売上高に対して一桁台半ばの範囲の段階的なロイヤルティを受け取ります。COLUMVIの商品化は、RITUXAN、LUNSUMIO、またはGAZYVAで受け取る共同プロモーション利益の割合には影響しません。
2024年4月、ロシュは、COLUMVIと化学療法GemOx(glofitamab-gxbm)を併用すると、再発または難治性のびまん性大細胞型B細胞リンパ腫の患者の全生存率が統計的に有意に改善されたことを発表しました。
利益配分の公式
リツクサンとルンスミオの利益配分
米国におけるリツクサンとルンスミオの現在の税引前共同プロモーションによる利益配分方式では、 30.0最初の $のシェア%50.0各暦年に獲得した共同プロモーションの営業利益は合計で100万件です。 FDAがLUNSUMIOを承認した結果、RITUXANとLUNSUMIOの年間共同プロモーション利益の合計に占める当社のシェアは、ドルを超えました50.0以下の表に要約されているように、100万は次のイベントによって異なります。
| | | | | |
| |
| |
| LUNSUMIOの承認後、最初の基準日まで | 37.5 | % |
| 最初の閾値日から2番目の閾値日まで | 35.0 | % |
| 2回目の敷居日以降 | 30.0 | % |
最初の基準日とは、連続して12か月以内に米国でのGAZYVAの総売上高が$に達した日の次の暦四半期の初日のうち、早い方の日を意味します500.0百万または(ii)任意の暦年でLUNSUMIOの米国総売上高が初めて$に達した日付150.0百万。
2番目の基準日とは、(i)任意の暦年の総売上高が、LUNSUMIOの米国総売上高が$に達する最初の日付の遅い方を指します350.0100 万または (ii) 第 1 しきい日が発生する暦年の翌暦年の1月1日。
2023年3月、最初の基準日が達成されました。その結果、2023年4月以降、リツクサンとルンスミオの税引前利益シェアは 35.0%。
ガジバ利益シェア
GAZYVAの現在の税引前利益配分方式では、 35.0最初の $のシェア%50.0各暦年で得た営業利益は100万件です。 共同プロモーションの年間利益に占める当社のシェアは、1ドルを超えています50.0以下の表に要約されているように、100万は次のイベントによって異なります。
| | | | | |
| |
| GAZYVAの2回目の基準日まで | 37.5 | % |
| GAZYVAの2回目の敷居日以降 | 35.0 | % |
| |
GAZYVAの第2期限日とは、連続して12か月以内に米国でのGAZYVAの総売上高が$に達した日の翌暦四半期の初日を意味します500.0百万。GAZYVAの2回目の基準日は、GAZYVAがCLL以外の適応症で承認されているかどうかに関係なく達成できます。
2023年3月、第2回GAZYVA基準日が達成されました。その結果、2023年4月以降、GAZYVAの税引前利益シェアは 35.0%。
ジェネンテックとのコラボレーション契約の詳細については、2023年フォーム10-Kに含まれる監査済み連結財務諸表の注記19「協力およびその他の関係」を参照してください。
目次
バイオジェン株式会社と子会社
要約連結財務諸表の注記
(未監査、続き)
エーザイ株式会社
2023年の第1四半期に、私たちは1ドルを計上しました31.0エーザイが特定のアジア太平洋地域の市場および環境で当社のMS製品を共同販売または販売する契約の終了に関連して、エーザイに100万ドルを支払います。2023年12月31日現在、私たちはおよそ$を支払いました16.0 100万ドルのうち31.0百万円が支払われます。残りの部分はその後2024年1月に支払われました。この解約手数料は、2023年3月31日に終了した3か月間の当社の要約連結損益計算書の販売費、一般管理費に含まれています。
LEQEMBI(レカネマブ)コラボレーション
私たちはエーザイと、アルツハイマー病の治療のための抗アミロイド抗体であるLEQEMBI(レカネマブ)を共同開発および商品化するためのコラボレーション契約を結んでいます(LEQEMBIコラボレーション)。
エーザイは、LEQEMBIの開発と規制当局への提出をグローバルにリードしています。両社は製品の共同商品化と共同宣伝を行い、最終的な意思決定権はエーザイにあります。研究、開発、販売、マーケティングの費用を含むすべての費用は、私たちとエーザイの間で均等に分担されます。私たちとエーザイはLEQEMBIを共同で宣伝し、利益と損失を平等に分配します。私たちは現在、LEQEMBI原薬と医薬品を製造していますが、2022年3月に、LEQEMBI原薬の製造に関するLEQEMBIに関連するエーザイとの供給契約を5年から10年に延長しました。
2023年7月、FDAはLEQEMBIの従来の承認を与えました。従来の承認を受ける前に、LEQEMBIは2023年1月にFDAから迅速承認を受け、その時点で米国で市販されました。2023年9月、日本の厚生労働省は日本でLEQEMBIを承認し、その後2023年12月に発売され、2024年1月に中国で承認されました。
LEQEMBIが商品化されると、私たちの製品が認識され始めました 50.0LEQEMBI製品の収益(ロイヤリティを含む)の純額および売上原価(ロイヤリティを含む)の、要約連結損益計算書におけるその他の収益の割合(当社が主要企業ではないため)。
LEQEMBIの販売およびマーケティング費用と開発費の当社のシェアは、それぞれ販売費、一般管理費と研究開発費に、要約連結損益計算書に記録されています。
LEQEMBIコラボレーションに関連する開発、販売、マーケティング費の概要は次のとおりです。
| | | | | | | | | | | | | | | | | | |
| | 3月31日に終了した3か月間、 | | |
| (百万単位) | | 2024 | | 2023 | | | | |
| LEQEMBIの進歩に関連するコラボレーションによって発生した開発費の合計 | | $ | 87.3 | | | $ | 107.9 | | | | | |
| LEQEMBIコラボレーション開発費におけるバイオジェンのシェアは、要約連結損益計算書の研究開発費に反映されています | | 43.6 | | | 54.0 | | | | | |
LEQEMBIコラボレーションによって発生した販売およびマーケティング費用の総額 | | 173.9 | | | 10.5 | | | | | |
| LEQEMBI Collaborationの販売およびマーケティング費のうち、バイオジェンが負担しているのは、当社の要約連結損益計算書に販売費、一般管理費に反映されています | | 86.9 | | | 5.3 | | | | | |
上記の契約に関連してエーザイから受取可能な金額は約$でした15.9百万と $1.42024年3月31日および2023年12月31日時点でそれぞれ百万です。上記の契約に関連してエーザイに支払われる金額は、$180.7百万と $118.42024年3月31日および2023年12月31日時点でそれぞれ百万です。
エーザイとのコラボレーション契約の詳細については、2023年フォーム10-Kに含まれる連結財務諸表の注記19「協力およびその他の関係」を参照してください。
UCB
私たちはUCBと2003年11月付けで協力契約を結んでおり、SLEやその他の将来合意された適応症の潜在的な治療薬として、抗CD40Lペグ化ファブであるダピロリズマブペゴルを共同開発して商品化しています。私たちかUCBのどちらかが、追加の適応症としてダピロリズマブペゴールの開発を提案するかもしれません。両当事者が合意された適応症として共同開発薬に追加することに同意しない場合、当社またはUCBは、該当する当事者の単独費用で、臨床活動の証明後に非追跡当事者のオプトイン権を得ることを条件として、当該除外適応症の開発を進めることができます。
目次
バイオジェン株式会社と子会社
要約連結財務諸表の注記
(未監査、続き)
研究、開発、販売、マーケティングの費用を含む、合意された適応症のために発生するすべての費用は、私たちとUCBで均等に分担されます。マーケティングの承認が得られれば、両社はダピロリズマブペゴルを共同販売し、利益と損失を均等に分配します。
UCBコラボレーション契約に関連する開発費の概要は次のとおりです。
| | | | | | | | | | | | | | | | | | |
| | 3月31日に終了した3か月間、 | | |
| (百万単位) | | 2024 | | 2023 | | | | |
| UCBのコラボレーション開発費総額 | | $ | 16.6 | | | $ | 18.3 | | | | | |
| UCBのコラボレーション開発費のうち、バイオジェンが負担している研究開発費は、要約連結損益計算書に反映されています | | 8.3 | | | 9.2 | | | | | |
セイジ・セラピューティクス株式会社
2020年11月、私たちはSageとグローバルなコラボレーションおよびライセンス契約を締結しました。これは、てんかんなどの他の神経疾患で発生する可能性のある本態性振戦の治療薬として、PPDの治療薬としてZURZUVAE(ズラノロン)とMDDおよび潜在的治療薬であるBIIB124(SAGE-324)を共同で開発および商品化することです。
2023年8月、FDAは成人のPPD患者に対するZURZUVAEを承認しましたが、DEAのスケジュールは保留中で、2023年10月に完了しました。承認されると、ZURZUVAEは、PPDの女性の15日目までに抑うつ症状を急速に改善できる、最初で唯一の1日1回、14日間の経口治療薬となりました。PPD用のZURZUVAEは、2023年の第4四半期に米国で市販されました。さらに、FDAは、成人のMDD治療におけるズラノロンのNDAのCRLを発行しました。CRLは、申請書にはMDDの治療薬としてのズラノロンの承認を裏付ける有効性の実質的な証拠は得られておらず、追加の研究が必要であると述べました。私たちとSageは引き続きFDAからのフィードバックを求め、次のステップを検討しています。
この提携により、両社は米国での開発に対する責任と費用、および商品化の利益と損失を同等に分担することになります。米国以外では、ズラノロンに関しては、日本、台湾、韓国を除く開発と商品化を担当し、10代前半から20代前半にSageに潜在的な段階的ロイヤルティを支払う場合があります。2023年の第4四半期に、Sageによるマイルストーン支払いが発生しました75.0米国でZURZUVAE for PPDを初めて商業的に売却した際に、100万ドル。これは無形資産に計上され、当社の要約連結貸借対照表に差し引かれ、その後2024年1月に支払われました。
2024年3月31日に終了した3か月間で、純利益分配費用は約$でした5.0 Sageのものを反映して100万です 50.0ZURZUVAE for PPDの米国における純コラボレーション実績の割合。これは、当社の要約連結損益計算書にコラボレーション利益分配/(損失補償)で計上されています。
Sageとのコラボレーションに関連する開発、販売、マーケティング費の概要は次のとおりです。
| | | | | | | | | | | | | | | | | | |
| | 3月31日に終了した3か月間、 | | |
| (百万単位) | | 2024 | | 2023 | | | | |
| Sageコラボレーション開発費の合計 | | $ | 11.6 | | | $ | 34.8 | | | | | |
| Sageのコラボレーション開発費のうち、バイオジェンが負担している研究開発費は、要約連結損益計算書に反映されています | | 5.8 | | | 17.4 | | | | | |
| Sageとのコラボレーションによって発生した販売およびマーケティング費用の総額 | | 27.6 | | | 38.2 | | | | | |
| 販売、一般管理費、コラボレーション利益分配/(損失の払い戻し)に反映されているSageのコラボレーション販売およびマーケティング費のうち、バイオジェンのシェアは、要約連結損益計算書に反映されています | | 13.8 | | | 19.1 | | | | | |
デナリ・セラピューティクス株式会社
2020年8月、私たちはデナリのパーキンソン病に対するLRRK2の小分子阻害剤を共同開発および共同商品化するためのコラボレーションおよびライセンス契約を締結しました(LRRK2コラボレーション)。また、ATV対応の抗アミロイドベータプログラムとその輸送を利用した2つ目のプログラムを含む、デナリの輸送車両プラットフォームから2つの前臨床プログラムをライセンスする独占オプションを取得する別の契約を締結しました。車両技術。
目次
バイオジェン株式会社と子会社
要約連結財務諸表の注記
(未監査、続き)
2023年4月、私たちはデナリとオプションを行使して、ATV対応の抗アミロイドベータプログラムのライセンスを取得しました。この取り組みに関連して、私たちはこのプログラムに関連するすべての開発および商業活動、および関連費用の責任を負いました。さらに、私たちはデナリに1回限りのオプション行使支払いを行いました。特定のマイルストーンが達成された場合、将来の純売上高に基づいて、追加の開発および商業マイルストーンの支払いとロイヤルティをデナリに支払うことがあります。デナリとの契約は2023年8月に修正され、特定のマイルストーン基準が変更されましたが、開発、規制、商業のマイルストーンの合計額は変わりません。さらに、セカンドオプションプログラムのオプション権を放棄することに同意しました。
LRRK2コラボレーションでは、米国と中国での商業化による利益と損失だけでなく、特定の割合に基づいて、両社がグローバル開発に対する責任と費用を分担します。米国と中国以外では、当社が商品化を担当し、Denaliに段階的なロイヤルティを支払う可能性があります。
デナリとのコラボレーションに関連する開発費の概要は次のとおりです。
| | | | | | | | | | | | | | | | | | |
| | 3月31日に終了した3か月間、 | | |
| (百万単位) | | 2024 | | 2023 | | | | |
| デナリのコラボレーション開発費総額 | | $ | 14.2 | | | $ | 16.6 | | | | | |
| 当社の要約連結損益計算書の研究開発費に反映されているデナリの共同開発費のうち、バイオジェンの分担分は研究開発費に反映されています | | 8.5 | | | 10.0 | | | | | |
その他の研究と発見の取り決め
これらの取り決めには、数年間にわたって支払われる特定の臨床および商業開発の成果に基づいて、将来のマイルストーン支払いの可能性が含まれる場合があります。
その他
2024年3月31日に終了した3か月間、私たちは約$を記録しました7.5その他の研究開発関連の取り決めに関連する当社の要約連結損益計算書では、研究開発費として100万ドル(米ドル)0.2前年の比較期間で百万。
サムスン・バイオエピス株式会社
2019年の開発および商品化契約
2019年12月、私たちはサムスンバイオエピスとの取引を完了し、商品化の独占権を確保しました 二 潜在的な眼科用バイオシミラー製品、BYOOVIZ(ranibizumab-nuna)、LUCENTISを参照するラニビズマブのバイオシミラーであるBYOOVIZ(ranibizumab-nuna)、およびEYLEAを参照するアフリベルセプトバイオシミラーとして提案されているSB15は、米国、カナダ、ヨーロッパ、日本、オーストラリアを含む世界中の主要市場で販売されています。Samsung Bioepisが開発を担当し、事前に指定されたおよそ粗利益率で両方の製品を供給します 45.0%。
この取引に関連して、Samsung Bioepisに最大約$を支払うこともあります180.0 開発、規制、販売に基づく追加のマイルストーンが100万件に達しました。
また、ベネパリ、イムラルディ、フリクサビとの2013年の商業契約の期間をさらに延長するオプションも取得しました 五年、$のオプション行使手数料の支払いを条件とします60.0 2024年8月までに100万で、これらの製品を中国で商品化する独占権を取得するオプションを取得しました。
2013年の商業契約
BENEPALI、IMRALDI、FLIXABIの第三者への販売収益を製品収益に反映し、純額を要約連結損益計算書に反映し、これらの費用が発生した場合、関連する収益費用と販売およびマーケティング費用を要約連結損益計算書に記録します。IMRALDIの販売に対するアッヴィへのロイヤリティの支払いは、要約された連結損益計算書の売上原価に計上されます。
私たちは共有します 50.0Samsung Bioepisとの商業契約に関連する利益または損失の割合。これは、当社の要約連結損益計算書で共同利益分配/(損失の払い戻し)で計上されます。2024年3月31日に終了した3か月間、純利益分配費用は$でした60.6サムスンのバイオエピスを反映した100万ドル 50.0純利益分配費用の場合と比較して、コラボレーション純利益に占める割合は57.1 前年の比較期間で百万。
目次
バイオジェン株式会社と子会社
要約連結財務諸表の注記
(未監査、続き)
その他のサービス
サムスンバイオエピスの設立と同時に、サムスンバイオエピスとライセンス契約も締結しました。このライセンス契約に基づき、私たちはSamsung Bioepisに、バイオジェン製品固有の技術を使用してSamsung Bioepisが作成したバイオシミラー製品を使用、開発、製造、および商品化するための独占ライセンスを付与しました。引き換えに、Samsung Bioepisが開発し商品化したバイオシミラー製品に対して、一桁のロイヤリティを受け取ります。ライセンス契約に基づくロイヤリティ収入は、当社の要約連結損益計算書では、受託製造、ロイヤリティ、その他の収益の一部として認識されています。
上記の契約に関連してSamsung Bioepisから受取可能な金額は$でした18.5百万と $9.92024年3月31日および2023年12月31日時点でそれぞれ百万です。上記の契約に関連してSamsung Bioepisに支払われる金額は$でした35.6百万と $73.72024年3月31日および2023年12月31日時点でそれぞれ百万です。
Samsung Bioepisとのコラボレーション契約およびその他の重要なコラボレーション契約の詳細については、注記19「協力およびその他の関係」を参照してください。 2023年のフォーム10-Kに含まれる連結財務諸表をご覧ください。
連結変動持分法人
当社の要約連結財務諸表には、当社が主な受益者である変動持分法人の財務結果が含まれています。以下は当社の重要な変動持分事業体です。
ニューロイムン・サブワン AG
2007年から、私たちはNeurmuneの結果を統合しました。私たちが主な受益者であると判断したからです。なぜなら、このコラボレーションを通じて、企業の経済パフォーマンスに最も大きな影響を与える活動を指揮する権限があり、資金が必要だったからです。 100.0コラボレーションを支援するために発生した研究開発費の割合。Neurimmuneとのコラボレーションおよびライセンス契約は、ADUHELM(修正後のNeurimmune契約)を含む、アルツハイマー病の潜在的な治療のための抗体の開発と商品化に関するものでした。
2023年11月、私たちはニューロイミューン契約を終了する決定をニューロイミューンに通知しました。解約後、私たちはNeurmuneとの関係を再考し、私たちはもはや変動持分法人の主な受益者ではないと判断しました。その結果、Neurmunimuneの分離により、約$の純利益を記録しました3.02023年フォーム10-Kに含まれる、2023年12月31日に終了した年度の連結損益計算書に差し引かれた、その他(収益)費用に計上された百万ドル。
非連結変動持分法人
私たちはさまざまな変動持分事業体と関係を築いていますが、これらの事業体の経済的成功に大きな影響を与える活動を指示する権限がないため、統合していません。これらの関係には、特定のバイオテクノロジー企業への投資や研究協力契約が含まれます。
2024年3月31日および2023年12月31日の時点で、潜在的な非連結変動持分事業体を代表する特定のバイオテクノロジー企業への投資の帳簿価額は合計ドルでした23.8 百万と $16.4 それぞれ 100 万です。これらの変動持分事業体に関連する損失に対する当社の最大リスクは、投資の帳簿価額に限定されます。
また、特定の開発活動への資金提供が義務付けられている特定の変動持分法人と研究協力契約を締結しています。これらの開発活動は、発生時に当社の要約連結損益計算書の研究開発費に含まれます。これらの変動持分事業体には、以前に契約上必要な金額以外の融資は提供していません。
Neurimmune およびその他の変動持分事業体への投資に関する追加情報については、2023年フォーム10-Kに含まれる当社の連結財務諸表の注記20「変動持分事業体への投資」をご覧ください。
目次
バイオジェン株式会社と子会社
要約連結財務諸表の注記
(未監査、続き)
私たちは現在、以下に説明する事項を含む、さまざまな請求、調査、法的手続きに携わっています。見積もりや不測の事態の使用を含む、請求や法的手続きに関連する当社の会計方針に関する情報については、2023年フォーム10-Kに含まれる連結財務諸表の注記1「重要な会計方針の要約」をご覧ください。
一部の不測の事態に関しては、経営陣がさらなる情報を得るまで、起こり得る損失または損失の範囲を見積もることができません。たとえば、(i) もしあれば、どの請求が処分申立ての実務に耐えられるか、(ii) 証拠開示を通じて入手すべき情報、(iii) 当事者の損害賠償請求と裏付けとなる証拠に関する情報、(iv) 当事者の法的理論、(v) 当事者の和解の立場などです。現時点で発生する可能性のある損失または損失の範囲を見積もることができれば、それは以下の潜在的な損失に関する不測の事態の説明に含まれます。
私たちが関与している請求や法的手続きには、当社の製品、パイプライン、またはプロセスに関連する特許の範囲、有効性、または執行可能性に対する異議申し立て、および他者が保有する特許の範囲、有効性、または執行可能性に対する異議申し立ても含まれます。これらには、当社が自社の特許を侵害しているという第三者からの申し立てが含まれます。これらの手続きのいずれかで不利な結果が生じた場合、(i)特許保護の喪失、(ii)特定の活動への継続不能、(iii)多額の損害賠償、ロイヤリティ、罰金、および/またはライセンス料の第三者への支払いなど、当社の事業または連結業績および財政状態に重大な影響を与える可能性があります。
不測の事態による損失
アドヘルム証券訴訟
私たちと特定の現役および元役員は、地方裁判所に提起されたADUHELMに関連する2つの訴訟の被告です。1つは2020年11月に提起され、もう1つは2022年2月に提起されました。2024年3月、地方裁判所は2022年2月に提起された訴訟の却下を取り消しました。どちらの訴訟も、15 U.S.C. §78j (b) と§78t (a) および17 C.F.R. §240.10b-5に基づく連邦証券法の違反を主張し、集団訴訟および金銭的救済としての訴訟の宣言を求めています。
デリバティブアクション
私たちと取締役会のメンバーは、2022年2月と7月に株主が地方裁判所に提起したデリバティブ訴訟の被告として指名されました。訴訟は、15 U.S.C. §78n (a) および17 C.F.R. §240 14.a-9に基づく連邦証券法の違反、および受託者責任の違反と企業資産の浪費を主張し、宣言的および差止命令による救済、バイオジェンに支払われる金銭的救済、原告に支払われる弁護士費用および費用を求めています。地方裁判所は2022年2月に提起された訴訟を保留し、両当事者は2022年7月に提起された訴訟の執行停止の継続を要求しました。
イムラルディの特許訴訟
2035年5月に失効するフレゼニウス・カビの欧州特許3 145 488(EP '488特許)は、EPO技術控訴委員会の異議申し立て手続きの対象となっています。2022年6月、フレゼニウス・カビ・ドイツ社(フレゼニウス・カビ)は、バイオジェンがヨーロッパで商業化しているサムスン・バイオエピスのアダリムマブバイオシミラー製品であるIMRALDIが、EP '488のフランスの同等品を侵害しているとして、パリ大審裁判所でバイオジェン・フランスSASに対して損害賠償および差止命令による救済を請求しました。特許。2022年8月、フレゼニウス・カビは、ドイツ版EP '488特許の侵害を理由に、デュッセルドルフ地方裁判所にバイオジェン社に対して損害賠償および差止命令による救済を請求し、2024年3月、裁判所は侵害を認めず、訴訟を却下しました。フレゼニウス・カビはデュッセルドルフ高等地方裁判所に控訴しました。
目次
バイオジェン株式会社と子会社
要約連結財務諸表の注記
(未監査、続き)
コンバージェンスの元株主との訴訟
2015年、バイオジェンは英国の企業であるコンバージェンスを買収しました。2019年、株主代表サービスLLCは、コンバージェンスの元株主に代わって、ドルの請求を主張しました200.0 Convergenceを買収した際の契約違反の疑いで100万件です。2023年6月、Shareholder Relationment Services LLCと24人の元株主が、以前に主張された請求の1つについて、イングランドとウェールズの高等裁判所に米国ドルでの支払いを求める訴訟を提起しました49.9百万、利息と費用。
ヒューマナ・ペイシェント・アシスタンス訴訟
2023年3月、地方裁判所は、2020年9月にヒューマナが当社に対して提起した以前に開示された訴訟を却下しました。ヒューマナは、多発性硬化症患者に無料の薬を提供し、多発性硬化症患者を支援する非営利団体に慈善寄付を行ったことに関連して損害賠償を請求し、連邦RICO法および州法の違反を申し立てていました。2023年12月、ヒューマナは米国第一巡回区控訴裁判所に控訴し、控訴は保留中です。
ジェネンテック訴訟
2023年2月、ジェネンテック社は、ジェネンテックがバイオジェンにライセンスした特許の失効後に発生したTYSABRIの販売に対して、利息と費用とともにロイヤルティを支払う義務があるとして、米国カリフォルニア州北部地区地方裁判所に当社に対して訴訟を起こしました。同社は、請求されたロイヤリティの総額は約$と見積もっています88.3百万。
バルドキソロン証券訴訟
2024年3月、テキサス州東部地区連邦地方裁判所は、Reata(後にバイオジェンに買収)の推定株主が、15U.S.C. §78j (b) および§78t (a)、C.F.R. §17に基づき、Reataとその元役員および取締役、および特定の引受人が連邦証券法違反を理由に提起した以前に開示された訴訟の和解を最終承認しました。240.10b-5、15 U.S.C. §§77k、77l (a) (2)、77o、そして偏見を持って訴訟を却下しました。
貸し手紛争
2024年4月、BioPharma Credit PLC、BPCRリミテッド・パートナーシップ、およびバイオファーマ・クレジット・インベストメンツV(マスター)LPは、Reataとのローン契約違反を理由に、ニューヨーク州最高裁判所に当社とReata Pharmaceuticals, Inc. に対して訴訟を起こし、約$の支払いを求めました。23.2100万ドル、さらに利息、費用、弁護士費用。
その他の事項
政府調査
当社は、ADUHELMとその発売に関する情報を求める召喚状をSECから受け取りました。当社は、いくつかの海外での事業運営に関する情報を求める召喚状を司法省から受け取りました。同社はまた、いくつかの海外での事業運営に関する情報をSECに提供しています。
TYSABRIバイオシミラーの特許問題
2022年9月、私たちは生物製剤価格競争革新法42 U.S.C. §262に基づき、Sandoz Inc.、その他のSandoz事業体およびPolpharma Biologics S.A. に対して、特許侵害の宣言的判決を求める訴訟を米国デラウェア州地方裁判所に提起しました。
TECFIDERAに関連する欧州連合の一般裁判所での無効化手続き
2020年11月、Mylan Irelandは、TECFIDERAが規制上のデータ保護の恩恵を受けているという理由で、TECFIDERAのジェネリック版市場への申請を検証しないというEMAの決定を取り消すよう欧州連合の一般裁判所に訴訟を提起しました。
VUMERITYオレンジブック上場特許に関連するハッチ・ワックスマン法訴訟
2023年7月、バイオジェンとAlkermes Pharma Ireland Limitedは、1984年の医薬品価格競争および特許期間回復法(ハッチ・ワックスマン法)に基づき、VUMERITYオレンジブックに掲載された特許(米国特許番号8,669,281、9,090,558および10,080,733号)に関する特許侵害訴訟を米国地方裁判所に提起しましたデラウェア地区がザイダス・ワールドワイドDMCCに反対しています。
目次
バイオジェン株式会社と子会社
要約連結財務諸表の注記
(未監査、続き)
製造物責任およびその他の法的手続き
また、通常の事業活動に付随する製造物責任請求やその他の法的手続きにも関与しています。これらの手続きの結果を正確に予測することはできませんが、これらの既存の問題の最終的な解決が当社の事業または財政状態に重大な悪影響を及ぼすとは考えていません。
優先レビューバウチャーの販売
2024年4月24日、まれな小児疾患優先審査券を販売する最終契約を第三者と締結しました。PRVの対価として、$を受け取りました103.0ですPRVの購入が完了すると100万になります。
アイテム 2.経営陣による財政状態と経営成績の議論と分析
以下の説明は、フォーム10-Qの未監査の要約連結財務諸表(要約連結財務諸表)およびこの四半期報告書の7ページ目から始まる付随する注記、および監査済み連結財務諸表、および2023年のフォーム10-Kに含まれる添付の注記と併せて読む必要があります。2023年9月26日のReataの買収完了以降、Reataの経営成績は、取得した資産と引き受けた負債の推定公正価値とともに、要約連結財務諸表に含まれています。
エグゼクティブサマリー
前書き
バイオジェンは、世界中の重篤で複雑な疾患を抱える人々のための革新的な治療法の発見、開発、提供に焦点を当てたグローバルなバイオ医薬品企業です。私たちは多発性硬化症の治療薬の幅広いポートフォリオを持っており、SMAの最初に承認された治療法を導入し、アルツハイマー病の決定的な病状に対処するための治療法を共同開発し、ALSの遺伝的原因を標的とする最初の承認された治療法を開始しました。2023年にReataを買収したことで、16歳以上の成人と青年のフリードライヒ運動失調症の治療薬として、米国とEUで承認された最初で唯一の薬を販売しました。私たちは、神経学、専門免疫学、希少疾患のパイプラインを発展させることに注力しています。私たちは、社内の研究開発プログラムと外部のコラボレーションを通じて、私たちの創薬と開発の取り組みを支援しています。
私たちが市販している製品には、多発性硬化症の治療用のテクフィデラ、ヴメリティ、アボネックス、プレグリディ、タイサブリ、ファンピラ、SMA治療用のスピンラザ、フリードライヒ運動失調症の治療用のSKYCLARYS、ALSの治療用のQALSODY、重度の尋常性乾癬の治療用のFUMADERMなどがあります。
また、アルツハイマー病の治療のためのLEQEMBIの商品化ではエーザイと、PPD治療用のZURZUVAEの商品化ではSageと協力しており、非ホジキンリンパ腫、CLLなどの治療用のリツキサン、非ホジキンリンパ腫、CLLなどの治療用のリツキサン、非ホジマー病の治療用のリツキサンハイセラに関して特定の事業上および財務上の権利がありますグキンリンパ腫とCLL、CLLと濾胞性リンパ腫の治療にはGAZYVA、PPMSとRMSの治療にはOCREVUS、再発または難治性濾胞の治療にはルンスミオリンパ腫、非ホジキンリンパ腫の治療のための二重特異性抗体であるCOLUMVI、およびロシュグループの完全子会社であるジェネンテックとのコラボレーション契約により、他の潜在的な抗CD20療法を追加することができます。
ヨーロッパの特定の国では、エンブレルを指すエタネルセプトバイオシミラーのベネパリ、ヒュミラを指すアダリムマブのバイオシミラーであるイムラルディ、レミケードを参照するインフリキシマブのバイオシミラーであるフリクサビ、ラニビズマブのバイオシミラーであるBYOOVIZなど、先端生物製剤のバイオシミラーのポートフォリオを商品化しています米国および特定の国際市場におけるLUCENTISを指します。また、アクテムラを参考にしたトシリズマブのバイオシミラーであるトフィデンスを商品化する独占権もあります。私たちは、EYLEAを参考にしたアフリベルセプトのバイオシミラーとして提案されているバイオシミラーである潜在的なバイオシミラー製品SB15の開発を続けています。私たちはバイオシミラー事業の戦略的オプションを引き続き評価しています。
当社のコラボレーション契約に関する追加情報については、本レポートに含まれる要約連結財務諸表の注記19「協力関係およびその他の関係」をご覧ください。
私たちは、世界中の患者さんに医薬品を途切れることなく供給できるように努めています。そのために、私たちは製造能力、能力、プロセス、設備を継続的に見直しています。将来の成長と医薬品開発パイプラインをサポートするために、私たちは高分子の生産能力を拡大し、スイスのゾロトゥルンに大規模な生物製剤製造施設を建設しました。2021年の第2四半期に、この施設の一部(最初の製造スイート)がSWISSMEDICからGMPマルチプロダクトライセンスを取得し、稼働を開始しました。2番目の製造スイートは、2024年の第1四半期に稼働しました。ゾロトゥルンは、FDAによってLEQEMBIの製造が承認されました。ゾロトゥルンの施設は、生物資産の製造に関して予想される短期から中期のニーズに応えてくれると信じています。このプラントにより、当社の全体的な製造能力が大幅に向上しましたが、まだ完全には稼働していないため、超過生産能力料金が計上されています。製造施設を十分に活用できない場合、追加の超過生産能力料金が発生し、当社の財政状態と経営成績に悪影響を及ぼします。
長期的には、当社の収益の伸びは、臨床開発、規制当局の承認、新しい商用製品の発売の成功、既存製品の追加適応症、入手能力にかかっています
また、当社が販売している製品、当社の研究開発努力から生じた資産、および/または外部事業開発機会の成功事例に関連する特許やその他の権利を維持します。
ビジネス環境
バイオ医薬品業界と私たちが事業を展開する市場は非常に競争が激しいです。競合他社の多くは、私たちが販売している、または開発中の製品と同様の製品の開発に取り組んでいるか、商品化しており、臨床試験を実施し、医薬品を販売するための規制当局の承認を得た経験が豊富です。さらに、当社が承認した特定の製品、協力者の製品、およびパイプライン製品候補の商品化は、既存製品の将来の売上に悪影響を及ぼす可能性があります。
当社の製品と収益源は、既存製品のジェネリック版、プロドラッグ、バイオシミラーのほか、短縮された規制経路の下で承認された製品など、多くの市場で引き続き競争の激化に直面しています。このような製品は、ブランド製品よりも大幅に安い価格で販売される可能性があります。したがって、そのような製品やその他の低価格の競合製品を導入すると、製品に請求できる価格と販売する製品の量の両方が大幅に下がり、収益に悪影響を及ぼす可能性があります。さらに、一部の市場では、当社製品のジェネリック版またはバイオシミラー版が商品化されると、自動的に当社製品の代わりに使用され、短期間で収益が大幅に減少することがあります。
当社製品の販売は、政府の保健管理当局、民間の健康保険会社、その他の組織からの適切な補償の有無と範囲、価格設定、および償還に大きく依存します。新しい医薬品が承認された場合、その製品に対する政府および民間の償還が可能かどうか、またその製品の価格や償還額が不確実になることがあります。
私たちの製品が処方されている市場では、薬価が厳しく監視されています。たとえば、IRAには医薬品の価格に関する特定の規定があります。医薬品の価格設定やその他の医療費は、今後も世界的に強い政治的および社会的圧力にさらされると予想しています。
当社製品に関する適切な補償、価格設定、または償還を取得または維持できない場合、当社の事業、評判、収益、経営成績に悪影響を及ぼしたり、新製品の発見と商品化のための研究開発プログラムに十分な資金を提供する当社の能力が低下または排除されたり、株価が下落または変動したりする可能性があります。
医療費を削減し、政府支出の全体的なレベルを制限するために世界中で講じられている競争、価格設定措置、その他の措置の影響に加えて、当社の販売と事業は、公衆衛生上の流行が従業員に与える影響、世界経済、医療治療の提供、地政学的な出来事、サプライチェーンの混乱、外貨の変動、知的財産の法的保護の変更など、国際的に事業を行う際の他のリスクの影響も受ける可能性がありますとでの変更取引規制と手続き。
私たちのビジネス環境に関する詳細な議論については、項目1を読んでください。ビジネス、2023年のフォーム10-Kで。製品の売上に悪影響を及ぼす可能性のある競争リスクと価格リスクに関する追加情報については、項目1Aをお読みください。このレポートにはリスク要因が含まれています。
テフィデラです
現在、複数のTECFIDERAジェネリック医薬品企業は、北米、ブラジル、および特定のEU諸国にあり、TECFIDERAと比較して価格が大幅に割引されています。TECFIDERAをめぐるジェネリック医薬品の競争により、TECFIDERAの収益は大幅に減少し、TECFIDERAの収益は今後も減少し続けると予想しています。
2023年3月、CJEUがTECFIDERAに規制データとマーケティング保護を受ける権利があることを確認したこと、および2023年5月にECがTECFIDERAは小児用適応症についてさらに1年間の市場保護を受ける権利があるとの決定を受けて、TECFIDERAは少なくとも2025年2月2日まではEUで規制上のマーケティング保護を受ける権利があると考えており、この保護の強化に努めています。2024年3月31日現在、一部のTECFIDERAジェネリック医薬品はまだ一部のEU市場から完全に撤退していません。私たちはこのような状況を注意深く監視し、市場保護を受ける法的権利の行使に取り組んでいます。さらに、2028年に失効するTECFIDERAに関連するEP 2 653 873特許を引き続き行使します。
追加情報については、このレポートに含まれる要約連結財務諸表の注記21「訴訟」を参照してください。
マクロ経済状況やその他の混乱に関するビジネス最新情報
私たちの事業の大部分は、ヨーロッパ、アジア、その他の国際地域で行われています。世界的な健康問題、悪天候、地政学的な出来事、インフレ、労働力や原材料の不足、その他のサプライチェーンの混乱などの要因により、製品不足やその他の困難や遅延、製品の製造コストの増加が発生する可能性があります。
現在の経済状況
市場はインフレ率の上昇、金利の上昇、グローバルなサプライチェーンの不確実性、地政学的紛争に関連するリスクの影響を一部受け続けているため、経済状況は依然として脆弱です。
地政学的な緊張
関税、貿易保護措置、輸出入許可要件、米国や他の政府による貿易制裁や同様の制限など、グローバルな紛争や国際関係の中断は、私たちの事業遂行能力に影響を及ぼします。たとえば、米国と中国の間の緊張により、米国は中国本土からの輸入品に一連の関税や制裁を課したり、その他の事業上の制限を課したりして、追加の制限措置が提案されています。
私たち、そして製薬業界は、医薬品とその配送装置の特定の原材料、成分、部品を中国に拠点を置くパートナーを利用しています。代替サプライヤーを雇うには、追加の規制当局の承認を求める必要があり、必要な時間とリソースの面でコストがかかります。たとえば、新たに買収したSKYCLARYS製品に関連する初期のプロセスの一部は、中国に拠点を置く単一のサプライヤーに依存しています。私たちは引き続きSKYCLARYSのサプライチェーンを評価し、その製造と患者への供給能力に関連するリスクを軽減するための行動に優先順位を付けています。
ロシアのウクライナ侵攻と最近の中東での軍事紛争に関連して続いている地政学的な緊張は、世界的なビジネスの混乱と経済の不安定をもたらしています。
例えば。ロシアの政府や企業には制裁やその他の制限が課されています。ロシアにもウクライナにも関連会社や従業員はいませんが、販売代理店を通じてロシアの患者にさまざまな治療法を提供しています。さらに、特定の製造材料のロシアへの輸出に対する政府の新たな制裁措置により、新製品の承認が遅れたり、制限されたりする可能性があります。紛争が当社の事業と財務実績に与える影響は依然として不明であり、ロシアとウクライナの間の紛争の深刻さと期間、地域および世界の経済状況への影響、紛争がウクライナとロシア以外の国に広がったり影響を及ぼしたりするかどうかなど、将来の動向によって異なります。
私たちは、ロシアとウクライナの間で進行中の紛争、および中東での軍事紛争を引き続き監視し、当社の事業、サプライチェーン、パートナー、または顧客への潜在的な影響、および当社の業績に悪影響を及ぼす可能性のある要因を評価します。ロシアとウクライナでの販売から生み出される収益は、2024年3月31日および2023年3月31日に終了した3か月間の総収益の2.0%未満です。さらに、2024年3月31日および2023年3月31日に終了した3か月間の総収益のうち、より広い中東地域での売上から生み出される収益は総収益の2.0%未満です。
気候関連の開示
2024年3月、SECは気候関連問題の影響に関する開示を強化するための最終規則を採択しました。最終規則では、重大な気候関連リスク、そのようなリスクを軽減または適応するための活動、取締役会による気候関連リスクの監督と重大な気候関連リスクの管理における経営陣の役割に関する情報、および当社の事業、経営成績、または財務状況にとって重要な気候関連の目標または目標に関する情報を開示することが義務付けられています。さらに、EUとカリフォルニア州も同様の法律と規制を制定しています。現在、これらの新しい規則や法律が当社の事業に与える潜在的な影響を評価しています。
下記の経営成績で説明しているように、2024年3月31日に終了した3か月間のバイオジェン社に帰属する当社の純利益および希薄化後の1株当たり利益は、2023年3月31日に終了した3か月間と比較して、次のことを反映しています。
減りました
5,140万ドル、つまり 2.9%
•MSの収益は4,930万ドル、つまり 4.4% 減少しました
•希少疾患の収益は1,940万ドル、つまり 4.4% 減少しました
•多発性硬化症製品の収益の減少は主に、北米、ブラジル、および特定のEU諸国で複数のTECFIDERAジェネリック医薬品が参入したことによるTECFIDERA需要の減少、患者がより効能の高い治療法に移行するにつれて競争によるインターフェロン需要の減少、および主に競争の激化と割引や手当の増加による米国のTYSABRI収益の減少によるものです。
•希少疾患収益の減少は、主に出荷時期に起因するSPINRAZAのその他の地域の収益の減少によるもので、2024年の残りの期間を通じてほぼ正常化すると予想しています。その他の国の患者数は、2024年の第1四半期まで概ね安定しています。また、競争の激化と外貨両替の悪影響による中程度のマイナスの影響も見られました。この減少は、2024年第1四半期のSKYCLARYSの世界売上高7,800万ドルによって一部相殺されました。
減りました
1億9,900万ドル、つまり 9.8%
•売上原価は1億2,060万ドル、つまり 18.2% 減少しました
•研究開発費は1億1,770万ドル、つまり 20.6% 減少しました
•販管費は2350万ドル、つまり 3.9% 減少しました
•売上原価の減少は、主に受託製造収益の減少とアイドルキャパシティチャージの減少による好調な製品構成によるもので、買収したSKYCLARYS在庫の公正価値の引き上げ調整に関連する4,410万ドルの償却費用によって一部相殺されました。
•研究開発費の減少は主に、当社のFit for Growthプログラムに関連して2024年に実現したコスト削減措置と、ADUHELMに関連して2023年に発生した臨床試験の終了費用によるものです。
•販売費、一般管理費の減少は、主に「Fit for Growth」プログラムに関連して2024年に実現したコスト削減措置によるものでしたが、米国および海外での製品発売を拡大し続ける中で、LEQEMBIとSKYCLARYSを支援する販売およびマーケティング活動への運営費の増加によって相殺されました。
•現金、現金同等物、および有価証券は、2023年12月31日現在の約10億ドルに対し、2024年3月31日現在の総額は約11億ドルです。
•2024年3月31日に終了した3か月間の営業活動による純キャッシュフローは5億5,320万ドルでした。
最近の進展
主要な協力関係の発展
LEQEMBI(レカネマブ)
米国
•2024年3月、エーザイは早期アルツハイマー病の治療のための毎月の点滴維持投与のためのLEQEMBIサプリメントBLAのFDAへの提出を完了しました。
その他の地域
•2024年3月、エーザイは、EUでのルカネマブのMAAに関するCHMPでの審議が、EMAでの手続き上の理由により再スケジュールされたと発表しました。
•2024年1月、NMPAは中国でのLEQEMBIを承認しました。2024年に発売される予定です。
その他の重要な開発
アルソディ (トーファーセン)
2024年2月、私たちはEMAのCHMPが、SOD1遺伝子の変異に関連するALSの成人の治療のために、例外的な状況下でトーファーセンにMAAを推奨する肯定的な意見を採択したことを発表しました。ECによって承認されれば、トファーセンはALSの遺伝的原因を標的とするEUで最初に承認された治療法になります。
スカイクラリーズ (オマベロキソロン)
2024年2月、欧州委員会は16歳以上の成人と青少年のFA治療薬としてSKYCLARYSをEUで承認しました。SKYCLARYSは、このまれな遺伝性の進行性神経変性疾患に対してEU内で承認された最初の治療法です。
優先審査券の販売
2024年4月24日、まれな小児疾患優先審査券を販売する最終契約を第三者と締結しました。PRVの対価として、$を受け取りました103.0ですPRVの購入が完了すると100万になります。
中止されたプログラムと研究
アコーダコラボレーション
2024年1月、私たちは2025年1月1日をもってコラボレーションとライセンス契約を終了する決定をAcordaに通知しました。この終了により、AcordaはFAMPYRAのグローバルな商品化権を取り戻します。2024年4月1日、Acordaは破産保護を申請し、実質的にすべての資産を第三者に売却する意向を発表しました。私たちは、これらの進展がFAMPYRAの権利の移行プロセスに与える影響を評価しています。
操作の結果
収入
以下の収益に関する説明は、このレポートに含まれる要約連結財務諸表の注記5「収益」と併せて読む必要があります。
収益の概要は次のとおりです。
| | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | |
| | | 3月31日に終了した3か月間、 |
| (百万単位、パーセンテージを除く) | | 2024 | | 2023 | | $ 変更 | | % 変更 |
| 製品の収入: | | | | | | | | | | | | |
| 米国 | | $ | 746.1 | | | 32.6 | % | | $ | 701.4 | | | 28.5 | % | | $ | 44.7 | | | 6.4 | % |
| その他の地域 | | 965.8 | | | 42.1 | | | 1,061.9 | | | 43.1 | | | (96.1) | | | (9.0) | |
| 製品総収入、純額 | | 1,711.9 | | | 74.7 | | | 1,763.3 | | | 71.6 | | | (51.4) | | | (2.9) | |
| | | | | | | | | | | | |
| 抗CD20治療プログラムからの収入 | | 394.0 | | | 17.2 | | | 399.5 | | | 16.2 | | | (5.5) | | | (1.4) | |
受託製造、ロイヤリティ、その他の収入 | | 184.6 | | | 8.1 | | | 300.2 | | | 12.2 | | | (115.6) | | | (38.5) | |
| 総収入 | | $ | 2,290.5です | | | 100.0 | % | | $ | 2,463.0 | | | 100.0 | % | | $ | (172.5) | | | (7.0) | % |
| | | | | | | | | | | | |
| | |
| | | | | | | | |
| | | | | | | | | | | | |
| | | | | | | | | | | | |
| | | | | | | | | | | | |
| | | | | | | | | | | | |
| | | | | | | | | | | | |
| | | | | | | | | | | | |
| | | | | | | | | | | | |
| | | | | | | | | | | | |
nm 意味がありません
製品収益の概要は次のとおりです。
| | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | |
| | | 3月31日に終了した3か月間、 |
| | 2024 | | 2023 | | | | |
| (百万単位) | | ユナイテッド
州 | | 残りの
世界 | | 合計 | | %
合計 | | ユナイテッド
州 | | 残りの
世界 | | 合計 | | %
合計 | | $
変更 | | % 変更 |
| | | | | | | | | | | | | | | | | | | | |
| | | | | | | | | | | | | | | | | | | | |
| | | | | | | | | | | | | | | | | | | | |
| | | | | | | | | | | | | | | | | | | | |
| | | | | | | | | | | | | | | | | | | | |
| | | | | | | | | | | | | | | | | | | | |
| | | | | | | | | | | | | | | | | | | | |
| | | | | | | | | | | | | | | | | | | | |
| | | | | | | | | | | | | | | | | | | | |
| 多発性硬化症 | | $ | 503.2 | | | $ | 572.7 | | | $ | 1,075.9 | | | 62.8 | % | | $ | 546.1 | | | $ | 579.1 | | | $ | 1,125.2 | | | 63.8 | % | | $ | (49.3) | | | (4.4) | % |
| | | | | | | | | | | | | | | | | | | | |
| | | | | | | | | | | | | | | | | | | | |
| | | | | | | | | | | | | | | | | | | | |
| | | | | | | | | | | | | | | | | | | | |
| | | | | | | | | | | | | | | | | | | | |
| 希少疾患 | | 225.9 | | | 198.0 | | | 423.9 | | | 24.8 | | | 146.7 | | | 296.6 | | | 443.3 | | | 25.2 | | | (19.4) | | | (4.4) | |
| | | | | | | | | | | | | | | | | | | | |
| | | | | | | | | | | | | | | | | | | | |
| | | | | | | | | | | | | | | | | | | | |
| | | | | | | | | | | | | | | | | | | | |
| | | | | | | | | | | | | | | | | | | | |
| | | | | | | | | | | | | | | | | | | | |
| バイオシミラー | | 3.7 | | | 193.2 | | | 196.9 | | | 11.5 | | | 8.2 | | | 184.2 | | | 192.4 | | | 10.9 | | | 4.5 | | | 2.3 | |
| | | | | | | | | | | | | | | | | | | | |
| | | | | | | | | | | | | | | | | | | | |
| | | | | | | | | | | | | | | | | | | | |
| | | | | | | | | | | | | | | | | | | | |
その他 (1) | | 13.3 | | | 1.9 | | | 15.2 | | | 0.9 | | | 0.4 | | | 2.0 | | | 2.4 | | | 0.1 | | | 12.8 | | | nm |
| 製品総収入、純額 | | $ | 746.1 | | | $ | 965.8 | | | $ | 1,711.9 | | | 100.0 | % | | $ | 701.4 | | | $ | 1,061.9 | | | $ | 1,763.3 | | | 100.0 | % | | $ | (51.4) | | | (2.9) | % |
| | | | | | | | | | | | | | | | | | | | |
| | |
| | | | | | | | |
| | | | | | | | | | | | | | | | | | | | |
| | | | | | | | | | | | | | | | | | | | |
| | | | | | | | | | | | | | | | | | | | |
| | | | | | | | | | | | | | | | | | | | |
| | | | | | | | | | | | | | | | | | | | |
| | | | | | | | | | | | | | | | | | | | |
nm 意味がありません
(1) その他には、2023年の第4四半期に米国で市販されたFUMADERM、ADUHELM、ZURZUVAEが含まれます。
•TECFIDERAの世界売上高は、北米、ブラジル、および特定のEU諸国で複数のTECFIDERAジェネリック医薬品参入による需要の減少により、2023年の2億7,450万ドルから2024年には2億5,430万ドル、つまり 7.4% に2,020万ドル減少しました。
•インターフェロンの全世界の収益は、2023年の2億4560万ドルから2024年には2億4,360万ドル、つまり 0.8% に200万ドル減少しました。これは、患者がより効能の高い治療法に移行するにつれて需要が減少したことによるもので、米国のインターフェロンの好調なチャネル動態によって一部相殺されました。
•グローバルVUMERITYの収益は、主に世界的な需要の増加と好調なチャネルダイナミクス、および米国のVUMERITYの価格上昇により、2023年の1億820万ドルから2024年には1億2,750万ドル、つまり 17.8% に1,930万ドル増加しました。
•世界のTYSABRI収益は、2023年の4億7,280万ドルから2024年の4億3,130万ドル、つまり8.8%へと4,150万ドル減少しました。これは主に、競争の激化と割引や手当の増加により、米国のTYSABRI収益が減少したためです。
MSの収益には、TECFIDERA、VUMERITY、AVONEX、PLEGRIDY、TYSABRI、FAMPYRAの売上が含まれます。
2024年には、米国およびその他の世界市場の両方で多くのMS製品をめぐる競争が激化した結果、MSの総収益は減少し続けると予想しています。また、2023年8月に米国で、2023年9月にEUで承認されたTYSABRIのバイオシミラーの参入企業も知っています。このバイオシミラーの登場により、TYSABRIの将来の売上が悪影響を受ける可能性があると考えています。
•米国のSPINRAZAの収益は、主に有利な純価格設定により、2023年の1億4,670万ドルから2024年には1億4850万ドル、つまり 1.2% に180万ドル増加しました。
•その他の国々のSPINRAZAの収益は、2023年の2億9,660万ドルから2024年には1億2,280万ドル、つまり 35.0% に減少しました。この前年比の減少の大部分は出荷のタイミングによるもので、2024年の残りの期間を通じてほぼ正常化すると予想しています。その他の国の患者数は、2024年の第1四半期まで概ね安定しています。また、競争の激化と外貨両替の悪影響による中程度のマイナスの影響も見られました。
•2024年のSKYCLARYSの世界収益は7,800万ドルでした。これには、Reataを買収した後の2023年の第4四半期に認識し始めたSKYCLARYSの米国での収益7,300万ドルと、EUで承認され、2024年の第1四半期に商業的に利用可能になったその他の世界のSKYCLARYS収益500万ドルが含まれます。
希少疾患の収益には、2023年の第2四半期に米国で市販化されたSPINRAZA、QALSODY、および2023年9月にReataを買収した際に買収したSKYCLARYSの売上が含まれます。
SKYCLARYSは2023年の第2四半期に米国で市販され、Reataを買収した後の2023年の第4四半期に米国でSKYCLARYSからの収益が計上され始めました。2024年2月、欧州委員会は16歳以上の成人と青少年のFA治療薬としてSKYCLARYSをEUで承認しました。これは2024年の第1四半期にEUで市販されました。
2024年には、米国でSKYCLARYSを発売し続けることで、希少疾患の収益は増加すると予想しています。SPINRAZAの世界的な収益は一桁台前半に減少すると予想しています。
•2024年3月31日に終了した3か月間、2023年の同時期と比較して、バイオシミラー収益の増加は主にチャネルのダイナミクスによるもので、競争圧力による価格の下落によって一部相殺されました。
バイオシミラーの収益には、ベネパリ、イムラルディ、フリクサビ、ビオビズの売上が含まれます。2023年に、BYOOVIZは特定の国際市場で市販されるようになりました。2023年の第3四半期に、FDAはアクテムラを参考にしたトシリズマブのバイオシミラーであるトフィデンスを承認しました。これは2024年に市販される予定です。
2024年には、バイオシミラー事業からの収益は緩やかに増加すると予想しています。私たちは、供給の制約に対処するために、イムラルディとベネパリの第三者委託製造業者と引き続き協力しています。解決されなければ、これらの供給制約は2024年の売上に悪影響を及ぼす可能性があります。さらに、イムラルディとベネパリの委託製造業者の1つが、第三者による買収案を締結しました。買収は2024年末に完了する予定です。現在、これがバイオシミラー事業に与える影響を評価し、緩和活動の実施に取り組んでいます。
私たちはバイオシミラー事業の戦略的オプションを引き続き評価しています。
抗CD20治療プログラムからの収入
米国でのRITUXAN HYCELA、GAZYVA、LUNSUMIOのコラボレーション営業利益、OCREVUSの売上に対するロイヤルティ収入、および抗CD20治療プログラムからのその他の収益を含むリツキサンのシェアは、以下の表にまとめられています。このディスカッションでは、リツキサンとリツキサンハイセラを総称してリツクサンと呼びます。
| | | | | | | | | | | | | | | | | | |
| | | 3月31日に終了した3か月間、 | | |
| (百万単位) | | 2024 | | 2023 | | | | |
| OCREVUSの売り上げに対するロイヤリティ収入 | | $ | 302.7 | | | $ | 283.6 | | | | | |
| リツキサン、ガジバ、ルンスミオの米国における税引前利益に占めるバイオジェンのシェア | | 87.1 | | | 112.5 | | | | | |
| 抗CD20治療プログラムからのその他の収入 | | 4.2 | | | 3.4 | | | | | |
| 抗CD20治療プログラムの総収入 | | $ | 394.0 | | | $ | 399.5 | | | | | |
OCREVUSの売り上げに対するロイヤリティ収入
2024年3月31日に終了した3か月間、2023年の同時期と比較して、OCREVUSの売上に対するロイヤリティ収入の増加は、主に米国におけるOCREVUSの売上の増加によるものでした。
OCREVUSのロイヤリティ収入は、第三者からの推定値と、同時期に発生したOCREVUSの売上に関する市場調査データに基づいています。実際のロイヤリティ収益と見積もりロイヤリティ収益の差異は、判明した時期、つまり通常は次の四半期になると予想される時期に調整されます。
リツキサン、ガジバ、ルンスミオの米国における税引前利益に占めるバイオジェンの割合
2024年3月31日に終了した3か月間、2023年の同時期と比較して、米国におけるリツキサン、ガジバ、ルンスミオの税引前利益に占める当社のシェアが減少したのは、主に複数のバイオシミラー製品との競争による米国でのリツキサンの売上が減少したためです。
規制当局の承認前に、抗CD20製品の開発のために協力して発生した費用の研究開発費と、販売費、一般管理費に含まれる商品化前の費用のうち、当社の負担分を要約した連結損益計算書に記録しています。抗CD20製品が承認された後、その製品に関連する開発、販売、マーケティング費のうち、抗CD20治療プログラムからの収益に占める税引前利益の割合を差し引いた金額として計上します。
抗CD20治療プログラムからのその他の収入
抗CD20治療プログラムからのその他の収益には、カナダでのRITUXANからの税引前共同プロモーション利益の当社のシェア、米国外でのLUNSUMIOの売上に対するロイヤルティ収入、および2023年の第2四半期に市販されたCOLUMVIの米国での純売上高に対するロイヤルティ収入が含まれます。
税引前利益配分方式や、抗CD20治療プログラムによる将来の収益への影響など、ジェネンテックとのコラボレーション契約に関する追加情報については、本レポートに含まれる要約連結財務諸表の注記19「協力関係およびその他の関係」をご覧ください。
受託製造、ロイヤリティ、その他の収入
受託製造、ロイヤリティ、その他の収益をまとめると、次のようになります。
| | | | | | | | | | | | | | | | | | |
| | | 3月31日に終了した3か月間、 | | |
| (百万単位) | | 2024 | | 2023 | | | | |
| 受託製造収入 | | $ | 152.2 | | | $ | 306.9 | | | | | |
ロイヤリティとその他の収入 | | 32.4 | | | (6.7) | | | | | |
| 受託製造、ロイヤリティ、その他の収益の合計 | | $ | 184.6 | | | $ | 300.2 | | | | | |
受託製造収入
2024年3月31日に終了した3か月間、2023年の同時期と比較して、受託製造収益の減少は主に、バッチ生産のタイミングによる2023年の生産量の増加によるものです。これには、米国でLEQEMBIの承認が加速され、2023年の第1四半期に認識され始めたLEQEMBIに関連するバッチが含まれます。
さらに、2020年にデンマークのヒレレズの製造事業を富士フイルムに売却する一環として、委託製造契約に関連するバッチを含め、富士フイルムに一定の最低バッチ生産コミットメント保証を提供しました。2023年12月31日現在、これらのバッチコミットメントは満たされており、2024年の受託製造収益は2023年と比較して低くなると予想しています。これは、ヒレリーズをこのような方法で利用している委託製造のお客様への供給がなくなったためです。
ロイヤリティとその他の収入
ロイヤルティやその他の収益は主に、私たちがアウトライセンスした特許に関連する製品の純売上から受け取るロイヤリティ、Samsung Bioepisとのライセンス契約によるバイオシミラー製品のロイヤルティ収入、LEQEMBI製品の収益の50.0%(ロイヤルティを含む)の純および売上原価の50.0%のシェア(私たちはプリンシパルではないため)を反映しています。
Samsung Bioepisおよびエーザイとのコラボレーション契約の詳細については、このレポートに含まれる要約連結財務諸表の注記19「協力およびその他の関係」を参照してください。
割引や手当のための準備金
製品販売による収益は、当社が事業を展開する特定の国際市場での価格設定措置の実施に関連するものを含め、適用される割引や手当のために設定された準備金を差し引いて計上されます。
総製品収益を減少させた割引、契約上の調整、返品のための準備金は次のように要約されます。
| | | | | | | | | | | | | | | | | | |
| | 3月31日に終了した3か月間、 | | |
| (百万単位) | | 2024 | | 2023 | | | | |
| 契約上の調整 | | $ | 665.7 | | | $ | 629.9 | | | | | |
| 割引 | | 187.6 | | | 181.2 | | | | | |
| 返品について | | 10.6 | | | 4.5 | | | | | |
| 割引と手当の合計 | | $ | 863.9 | | | $ | 815.6 | | | | | |
2024年3月31日に終了した3か月間、製品総収益に占める割引引当金の割合は、前年の比較期間の 31.4% に対し、33.2% でした。
契約上の調整
契約上の調整は主に、米国のメディケイドとマネージドケアリベート、薬局リベート、自己負担金(自己負担)支援、VA、3,400億ドルの割引、専門薬局プログラムの手数料、その他の政府リベートまたは該当する手当に関するものです。
2024年3月31日に終了した3か月間、2023年の同時期と比較して、契約調整の増加は、主に米国でのメディケイドと政府リベートの増加によるもので、他の地域での政府リベートの減少によって一部相殺されました。
割引
割引には、取引期間割引や卸売業者のインセンティブが含まれます。
2024年3月31日に終了した3か月間は、2023年の同時期と比較して、主にバイオシミラーの購入割引と数量割引の増加によるものです。
戻り値
製品の返品準備金は、卸売業者による返品に対して設定されます。契約条件に従い、卸売業者は製品の破損や期限切れなどの理由で製品を返品することが許可されています。卸売業者の返品の大部分は製品の有効期限によるものです。商品の返品見込み引当金は、関連収益が計上された期間に計上されるため、商品の売上が減少します。
2024年3月31日に終了した3か月間は、2023年の同時期と比較して、主に米国での返品率の上昇によるものでした。
当社の歳入準備金に関する追加情報については、このレポートに含まれる要約連結財務諸表の注記5「収益」をご覧ください。
費用と経費
総費用と費用の概要は次のとおりです。
| | | | | | | | | | | | | | | | | | | | | | | | | | |
| | | 3月31日に終了した3か月間、 |
| (百万単位、パーセンテージを除く) | | 2024 | | 2023 | | $ 変更 | | % 変更 |
| 取得した無形資産の償却と減損を除いた売上原価 | | $ | 542.2 | | | $ | 662.8 | | | $ | (120.6) | | | (18.2) | % |
| 研究開発 | | 452.9 | | | 570.6 | | | (117.7) | | | (20.6) | |
| 販売、一般および管理 | | 581.5です | | | 605.0 | | | (23.5) | | | (3.9) | |
| 取得した無形資産の償却と減損 | | 78.3 | | | 50.2 | | | 28.1 | | | 56.0 | |
| コラボレーションの利益分配/(損失の払い戻し) | | 65.6 | | | 57.1 | | | 8.5 | | | 14.9 | |
| | | | | | | | |
| | | | | | | | |
| リストラ費用 | | 11.5 | | | 9.6 | | | 1.9 | | | 19.8 | |
| | | | | | | | |
| その他(収入)費用、純額 | | 93.7 | | | 69.4 | | | 24.3 | | | 35.0 | |
| 総費用と経費 | | $ | 1,825.7 | | | $ | 2,024.7 | | | $ | (199.0) | | | (9.8) | % |
| | | | | | | | |
| | |
| | | | | | | | |
| | | | | | | | |
| | | | | | | | |
| | | | | | | | |
| | | | | | | | |
| | | | | | | | |
| | | | | | | | |
| | | | | | | | |
| | | | | | | | |
| | | | | | | | |
| | | | | | | | |
| | | | | | | | |
取得した無形資産の償却と減損を除いた売上原価
| | | | | | | | | | | | | | | | | | |
| | 3月31日に終了した3か月間、 | | |
| (百万単位) | | 2024 | | 2023 | | | | |
| プロダクト | | $ | 377.7 | | | $ | 481.4 | | | | | |
| 王族 | | 164.5 | | | 181.4 | | | | | |
| 総売上原価 | | $ | 542.2 | | | $ | 662.8 | | | | | |
2024年3月31日に終了した3か月間、2023年の同時期と比較して、製品の売上原価が下がったのは、主に受託製造収益に関連する売上原価の低下とアイドルキャパシティチャージの減少によるもので、SKYCLARYSの償却費4,410万ドルによって一部相殺されました。受託製造収益には、米国でのLEQEMBIの承認が加速された2023年の第1四半期から、エーザイ向けに生産されたLEQEMBI在庫が含まれます。収益に占める売上原価の割合は、マージンが最小限であったため、LEQEMBIバッチによる悪影響を受けました。
2023年9月にReataを買収した結果、SKYCLARYSの取得した在庫に関連して約13億ドルの公正価値引き上げ調整が行われました。この公正価値のステップアップ調整は、在庫が売却されたときに、要約された連結損益計算書内の売上原価に償却されます。これは、取得日から約3年以内に予定されています。2024年3月31日に終了した3か月間、SKYCLARYSに関連する公正価値のステップアップ調整による在庫売却による償却額は約4,410万ドルでした。Reataの買収に関する追加情報については、このレポートに含まれる要約連結財務諸表の注記2「買収」をご覧ください。
書き留めやその他の費用
2023年3月31日に終了した3か月間で、合計で約4,480万ドルのアイドル容量料金を記録しました。
エーザイとのコラボレーション契約の詳細については、このレポートに含まれる要約連結財務諸表の注記19「協力およびその他の関係」を参照してください。
2024年3月31日および2023年3月31日に終了した3か月間の研究開発費は、総収益に占める割合はそれぞれ19.8%と23.2%でした。2024年3月31日に終了した3か月間、2023年の同時期と比較して、研究開発の減少は主に、当社のFit for Growthプログラムに関連して2024年に実現したコスト削減措置と、ADUHELMに関連して2023年に発生した臨床試験の終了費用によるものです。
アーリーステージプログラム
2024年第1四半期と2023年第1四半期
初期段階のプログラムの減少は、以下に関連する費用の減少によるものです。
•急性虚血性脳卒中の治療のためのBIIB131の中止。そして
•多発性硬化症の治療のためのBIIB135の中止
この減少は、以下に関連するコストの増加によって一部相殺されました。
•糖尿病性神経障害性疼痛の治療のためのセムドメスピブの開発。そして
•アルツハイマー病の治療のためのBIIB080の開発。
レイトステージプログラム
2024年第1四半期と2023年第1四半期
後期プログラムの減少は、以下に関連する費用の減少によるものです。
•米国でのPPD用ZURZUVAEの承認を受けて、ZURZUVAEを後期段階から市販段階に進めました。
•米国でのQALSODYの承認が加速したことで、QALSODYが後期段階から市販段階へと進んでいます。
•大半球梗塞のための BIIB093の中止。そして
•ACTEMRAを参考にしたトシリズマブのバイオシミラーであるTOFIDENCEは、米国でのトフィデンスの承認を得て、後期段階から市販段階へと進めました。
市販プログラム
2024年第1四半期と2023年第1四半期
市販プログラムの減少は、以下に関連する費用の減少によるものです。
•アルツハイマー病の治療のためのADUHELMの中止。そして
•臨床支出のタイミングにより、LEQEMBIへの支出が減少しました。
この減少は、以下に関連するコストの増加によって一部相殺されました。
•米国でのQALSODYの承認が加速したことで、QALSODYが後期段階から市販段階へと進みました。そして
•2023年9月にReataを買収した結果、SKYCLARYSへの支出が増加しました。
研究開発費は、以下の分類に基づいて上記で報告されています。報告されている開発段階は、発生したときのプログラムの状況に基づいています。したがって、同じプログラムが、同じ年のさまざまな開発段階に反映される可能性があります。私たちのプログラムのいくつかでは、研究開発活動は私たちの協力関係やその他の関係の一部です。私たちの費用は、発生した総費用に占める私たちの負担を反映しています。
•研究と発見:私たちの発見研究とトランスレーショナルサイエンスの取り組みを支援するためにかかる費用を表します。
•初期段階のプログラム:第1段階または第2段階の開発段階にあるプログラムです。
•後期プログラム:開発フェーズ3または登録段階のプログラムです。
•市販製品:製品ライフサイクル管理活動に関連する費用を含みます。該当する場合は、既存製品の新しい適応症の開発に関連する費用も含まれます。
•その他の研究開発費用:当社の研究開発費の大部分は、研究開発活動全体および非特定のプログラムを支援するために発生する間接費です。これには、管理費などの複数のプログラムに役立つ活動や、減価償却、情報技術、施設ベースの費用が含まれます。これらの費用は、上の表ではその他の研究開発費と見なされ、特定のプログラムや段階には配分されません。
マイルストーンと前払いを除くと、パイプラインへの投資を継続しながら、中核となる研究開発費は2024年に減少すると予想しています。これは主に、コスト削減の取り組みが継続的に実現されているためです。私たちは、まだ満たされていない大きなニーズがあり、医薬品候補が高度に差別化される可能性がある場合に、対象を絞った研究開発の機会に引き続き多大なリソースを投入していくつもりです。
販売、一般、管理
2024年3月31日に終了した3か月間、販売費、一般管理費は2023年の同時期と比較して約3.9%減少しました。これは主に、Fit for Growthプログラムに関連して2024年に実現したコスト削減措置によるものです。これは、米国および海外での製品発売を拡大し続ける中で、LEQEMBIとSKYCLARYSを支援する販売およびマーケティング活動への運営費の増加によって相殺されました。2023年3月31日に終了した3か月間、販売、一般管理費には、2023年の第1四半期に日本でのMS製品の共同プロモーション契約が終了したことに関連する、エーザイへの3,100万ドルの債務が含まれていました。コスト削減策により、一般管理費は2024年第1四半期に2023年の同時期と比較して約880万ドル、5.1%減少しました。2024年の第1四半期に発生した出口関連費用と買収関連費用を除くと、一般管理費は約1,930万ドル、つまり11.3%減少しました。
Reataの買収に関する追加情報については、このレポートに含まれる要約連結財務諸表の注記2「買収」をご覧ください。エーザイとのコラボレーション契約の詳細については、このレポートに含まれる要約連結財務諸表の注記19「協力およびその他の関係」を参照してください。
取得した無形資産の償却と減損
当社の償却費用は、無形資産の経済的消費と減損に基づいています。私たちの最も重要な償却可能な無形資産は、2023年9月にReataを買収した際に取得したTYSABRI、AVONEX、SPINRAZA、VUMERITY、SKYCLARYSに関連しています。Reataの買収に関する追加情報については、このレポートに含まれる要約連結財務諸表の注記2「買収」をご覧ください。
2024年3月31日に終了した3か月間、2023年の同時期と比較して、取得した無形資産の償却および減損が増加したのは、主にReataが買収したSKYCLARYSに関連する無形資産の償却によるものです。2024年と2023年3月31日に終了した3か月間、減損費用はありませんでした。
当社が取得した無形資産の償却および減損に関する追加情報については、本レポートに含まれる要約連結財務諸表の注記7「無形資産およびのれんについて」をご覧ください。
コラボレーションの利益分配/(損失の払い戻し)
コラボレーションの利益分配/(損失の払い戻し)には、主にサムスンバイオエピスと2013年のバイオシミラーの商業契約に関連する利益または損失の50.0%の部分が含まれます。2023年の第3四半期に、PPDのZurzuvaeに関連する米国での収益と費用の50.0%のシェアに関連するコラボレーション利益分配/(損失の払い戻し)を認識し始めました。
2024年3月31日に終了した3か月間、サムスンバイオエピスの純コラボレーション利益の50.0%のシェアを反映した純利益分配費用は6,060万ドルでしたが、前年の比較期間の純利益分配費用は5,710万ドルでした。
2024年3月31日に終了した3か月間、純利益分配費用は約500万ドルでした。これは、PPD向けZurzuvaeの米国での純コラボレーション実績に占めるSageの50.0%のシェアを反映しています。
Samsung BioepisおよびSageとのコラボレーションおよびライセンス契約の詳細については、このレポートに含まれる要約連結財務諸表の注記19「協力およびその他の関係」を参照してください。
リストラ費用
2023年フィット・フォー・グロース・リストラクチャリング・プログラム
2023年7月、私たちはFit for Growthプログラムの一環として、業務の効率と効果を向上させながら運営コストを削減するための追加のコスト削減策を開始しました。Fit for Growthプログラムは、2025年末までに総営業経費を約10億ドル削減すると予想されており、その一部はさまざまな取り組みに再投資される予定です。Fit for Growthプログラムには現在、約1,000人の従業員の純人員削減が含まれると推定されており、約2億6,000万ドルから2億8,000万ドルのリストラ費用が発生すると予想しています。
2023年のコスト削減イニシアチブから発生した費用の合計は、次のようにまとめられます。
| | | | | | | | | | | | | | | | | | | | | | | | | | | | | | |
| | 2024年3月31日に終了した3か月間 | | |
| | | | | | | | | | |
| (百万単位) | | セブランス
費用 | | 加速減価償却およびその他の費用 | | | | 合計 | | | | | | | | |
| 販売、一般および管理 | | $ | — | | | $ | 1.4 | | | | | $ | 1.4 | | | | | | | | | |
| 研究開発 | | — | | | 4.9 | | | | | 4.9 | | | | | | | | | |
| リストラ費用 | | 9.3 | | | — | | | | | 9.3 | | | | | | | | | |
| 合計請求額 | | $ | 9.3 | | | $ | 6.3 | | | | | $ | 15.6 | | | | | | | | | |
| | | | | | | | | | | | | | | | |
| | |
| | | | |
| | | | | | | | | | | | | | | | |
| | | | | | | | | | | | | | | | |
| | | | | | | | | | | | | | | | |
| | | | | | | | | | | | | | | | |
| | | | | | | | | | | | | | | | |
その他の費用:資産の放棄や償却、施設閉鎖費用、特定のリースの終了による税引前損益、従業員の退職防止費用、コンサルティング料、その他の費用などの項目に関連する費用が含まれます。
リアタ統合
2023年9月にReataの買収が完了した後、私たちはコスト削減と回避を通じて業務上の相乗効果を実現するための統合計画を実施しました。このイニシアチブでは、退職金と雇用費用に関連して、合計で約3,500万ドルから4,000万ドルの統合費用が発生し、2024年末までに支払われる予定です。これらの金額は2023年に大幅に発生しました。
Reata統合によって発生した合計請求額は次のように要約されます。
| | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | |
| | 2024年3月31日に終了した3か月間 |
| | | | |
| (百万単位) | | セブランス
費用 | | 加速減価償却およびその他の費用 | | | | 合計 | | | | | | | | |
| 販売、一般および管理 | | $ | — | | | $ | 1.8 | | | | | $ | 1.8 | | | | | | | | | |
| 研究開発 | | — | | | 2.7 | | | | | 2.7 | | | | | | | | | |
| リストラ費用 | | 2.2 | | | — | | | | | 2.2 | | | | | | | | | |
| 合計請求額 | | $ | 2.2 | | | $ | 4.5 | | | | | $ | 6.7 | | | | | | | | | |
| | | | | | | | | | | | | | | | |
| | |
| | | | |
| | | | | | | | | | | | | | | | |
| | | | | | | | | | | | | | | | |
| | | | | | | | | | | | | | | | |
| | | | | | | | | | | | | | | | |
| | | | | | | | | | | | | | | | |
Reataの買収に関連して、テキサス州プラノにある約327,400平方フィートのオフィスと研究所スペースのシングルテナントのビルド・トゥ・スーツの責任を引き受けました。最初のリース期間は16年です。私たちはこの建物を占有するつもりはなく、物件を転貸する機会を検討しています。
当社のコスト削減の取り組みに関する追加情報については、このレポートに含まれる要約連結財務諸表の注記4「リストラクチャリング」をご覧ください。
その他の (収入) 費用、純額
2024年3月31日に終了した3か月間、2023年の同時期と比較して、その他(収益)費用の純変動は、主に2023年の同時期と比較して2024年の現金残高が減少したことによる利息収入の減少を反映しており、株式の保有による純未実現損失の減少によって一部相殺されました。
株式の純損失(利益)
2024年3月31日に終了した3か月間、当社が保有する株式の未実現損失と実現損失はそれぞれ約2,570万ドルと490万ドルでしたが、前年の比較期間の未実現損失と実現損失はそれぞれ約7,650万ドルと160万ドルでした。
•2024年3月31日に終了した3か月間に計上された純未実現損失は、主にセージおよびデナリ普通株式への投資の公正価値総額が約2,770万ドル減少したことを反映していますが、サンガモ普通株式の公正価値が約140万ドル増加したことにより一部相殺されました。
•2023年3月31日に終了した3か月間に計上された純未実現損失は、主にデナリ、サンガモ、イオニスの普通株式への投資の公正価値総額が約1億ドル減少したことを反映していますが、セージの普通株式の公正価値が約2,380万ドル増加したことにより一部相殺されました。
所得税規定
| | | | | | | | | | | | | | | | | | |
| | 3月31日に終了した3か月間、 | | |
| (百万単位、パーセンテージを除く) | | 2024 | | 2023 | | | | |
| 所得税(給付)費用を差し引く前の収入 | | $ | 464.8 | | | $ | 438.3 | | | | | |
| 所得税(給付)費用 | | 71.4 | | | 50.7 | | | | | |
| 実効税率 | | 15.4 | % | | 11.6 | % | | | | |
当社の実効税率は、事業のグローバルな性質により年ごとに変動します。当社の実効税率に最も大きな影響を与える要因には、税法の変更、複数の法域における課税所得の配分のばらつき、研究開発費の金額と特徴、特定の控除とクレジットの水準、買収とライセンス取引などがあります。
2024年3月31日に終了した3か月間の2023年の同時期と比較して、当社の実効税率の引き上げには、税額控除に関連する前年の不確実な税務問題の解決の影響と、前年に記録された未実現損失が大きかった株式投資の価値の変動による非現金税効果が含まれます。
二つ目の柱
OECDはモデルルールを発行しました。これは通常、管轄区域の最低実効税率を15.0%と規定しています。さまざまな国が、原則を効果的に実施するための法律を制定しているか、制定中です
2024年1月1日。2024年3月31日に終了した3か月間の当社の所得税規定は、OECDモデルルールに関連する現在制定されている法律とガイダンスを反映しています。
当社の所得税に関する追加情報については、このレポートに含まれる要約連結財務諸表の注記17「所得税」をご覧ください。
財政状態、流動性、資本資源
私たちの財政状態は以下のように要約されます。
| | | | | | | | | | | | | | | | | | | | | | | | | | |
| (百万単位、パーセンテージを除く) | | 2024年3月31日現在 | | 2023年12月31日現在 | | $ 変更 | | % 変更 |
| 金融資産: | | | | | | | | |
| 現金および現金同等物 | | $ | 1,074.4 | | | $ | 1,049.9 | | | $ | 24.5 | | | 2.3 | % |
| 有価証券 — 現在の | | — | | | — | | | — | | | — | |
| 有価証券 — 非流動証券 | | — | | | — | | | — | | | — | |
| 現金、現金同等物および有価証券の総額 | | $ | 1,074.4 | | | $ | 1,049.9 | | | $ | 24.5 | | | 2.3 | % |
| 借入: | | | | | | | | |
現在のタームローンの部分 | | $ | 250.0 | | | $ | 150.0 | | | $ | 100.0 | | | 66.7 | % |
支払手形とタームローン | | 6,290.1です | | | 6,788.2 | | | (498.1) | | | (7.3) | |
| 借入総額 | | $ | 6,540.1です | | | $ | 6,938.2 | | | $ | (398.1) | | | (5.7) | % |
| 運転資本: | | | | | | | | |
| 流動資産 | | $ | 6,756.2 | | | $ | 6,859.3 | | | $ | (103.1) | | | (1.5) | % |
| 現在の負債 | | (3,222.8) | | | (3,434.3) | | | 211.5 | | | (6.2) | |
| 運転資本の総額 | | $ | 3,533.4 | | | $ | 3,425.0 | | | $ | 108.4 | | | 3.2 | % |
概要
私たちはこれまで、主に事業を通じて得たキャッシュフローと既存の現金資源を通じて、営業支出と資本支出の資金を調達してきましたが、今後も資金を調達していく予定です。私たちは、主要製品の多くをめぐるジェネリック医薬品とバイオシミラーの競争、MS事業全体の継続的な衰退、主要な新製品の発売とパイプラインの開発への投資が、将来の事業からのキャッシュフローに大きな悪影響を及ぼすと考えています。
既存の資金を、事業から生み出される現金、および必要に応じて追加の資金調達リソースを利用できることと合わせると、当面の間、営業資本、運転資本、戦略的提携、マイルストーン支払い、資本支出、および債務返済の要件を満たすのに十分であると考えています。さらに、日和見的に株主に現金を還元したり、買収やライセンス活動など、他の事業イニシアチブを追求したりすることもあります。また、新しい協力契約、戦略的提携、追加の株式や負債の資金調達を組み合わせて、あるいは重要な新しい機会が見つかった場合は、他の資金源から追加の資金を求めることもあります。
2024年4月、サムスン・バイオエピスの売却に関連して、サムスン・バイオロジクスから残りの4億3,750万ドルの支払いを受けました。さらに、2024年には、2023年のタームローンの3年間のトランシェの残りの2億5,000万ドルの残高を返済する予定です。
当社の財政状態または将来の経営成績に悪影響を及ぼす可能性のある特定のリスクに関する追加情報については、項目1Aをお読みください。リスク要因と項目3。このレポートには、市場リスクに関する量的および質的開示が含まれています。
流動性
運転資本
運転資本は、流動資産から流動負債を差し引いたものとして定義されます。2024年3月31日および2023年12月31日現在、当社の運転資本はそれぞれ35億ドルと34億ドルでした。運転資本の変化は、流動資産総額が約1億310万ドル減少し、流動負債総額が約2億1,150万ドル減少したことを反映しています。流動資産合計と流動負債合計の変化は、主に次の要因によるものです。
流動資産
•現金、現金同等物、および現在の市場性のある有価証券が2,450万ドル増加しました。
•当社の継続事業に関連する売掛金(純額)が5,960万ドル減少しました。そして
•短期戦略投資の一部の売却もあって、その他の流動資産が1,670万ドル減少しました。
流動負債
•主に年間インセンティブ報酬の支払時期により、未払費用などが2億6,900万ドル減少しました。そして
•2023年のタームローンの3年間のトランシェに関連して、長期から短期の2億5,000万ドルに再分類されたため、現在の負債部分が1億ドル増加しました。これは、2023年のタームローンの365日間のトランシェに関連する1億5000万ドルの返済によって一部相殺されました。
Samsung Bioepisの持分の売却に関する追加情報については、このレポートに含まれる要約連結財務諸表の注記3「処分」をご覧ください。
現金、現金同等物、有価証券
2024年3月31日現在、当社の現金、現金同等物、有価証券の合計は約11億ドルでしたが、2023年12月31日時点では約10億ドルでした。残高の増加は、主に営業活動によるキャッシュフローによるもので、2023年のタームローンの返済に使用された4億ドルの現金によって一部相殺されました。
事業で別の用途に必要になるまで、私たちは通常、当社の投資方針に従い、現金準備金を銀行預金、預金証書、コマーシャルペーパー、コーポレートノート、米国および外国の政府証券、オーバーナイト・リバース・リパーチェス契約、その他の有利子市場性のある債務証書に投資します。機関、満期、投資の種類によってエクスポージャーの量を制限する、十分に分散されたポートフォリオを維持することにより、現金準備金と有価証券の信用リスクを軽減することが私たちの方針です。銀行セクターの不確実性による流動性への大きな制限は発生していません。
次の表は、当社の戦略的投資ポートフォリオにおける当社の重要な普通株式投資の公正価値をまとめたものです。
| | | | | | | | | | | | | | |
| (百万単位) | | 2024年3月31日 | | 2023年12月31日 |
| デナリ | | $ | 205.4 | | | $ | 273.6 | |
| セージです | | 117.0 | | | 135.3 | |
| サンガモ | | 7.1 | | | 7.9 | |
| 合計 | | $ | 329.5 | | | $ | 416.8 | |
デナリ、セージ、サンガモへの投資を清算する能力は、当社の持分の規模、市場関連活動の量、所有権の集中、および協力者としての地位に起因する可能性のある制限によって制限される場合があります。したがって、そのような投資の現在の価値を大幅に下回る可能性があります。
当社のコラボレーション契約に関する追加情報については、本レポートに含まれる要約連結財務諸表の注記19「協力関係およびその他の関係」をご覧ください。
キャッシュフロー
次の表は、当社のキャッシュフロー活動をまとめたものです。
| | | | | | | | | | | | | | | | | | | | |
| | | 3月31日に終了した3か月間、 |
| (百万単位、パーセンテージを除く) | | 2024 | | 2023 | | % 変更 |
| 営業活動によって提供される(使用された)純キャッシュフロー | | $ | 553.2 | | | $ | 455.3 | | | 21.5 | % |
| 投資活動によって提供される(使用された)純キャッシュフロー | | (66.0) | | | (953.0) | | | (93.1) | |
| 財務活動によって提供される(使用された)純キャッシュフロー | | (439.6) | | | (43.4) | | | 912.9 | |
営業活動
営業キャッシュフローは、当社の純利益を次のように調整することによって得られます。
•減価償却費、減損費用、戦略的投資による未実現損失(利益)損失、株式ベースの報酬などの非現金営業項目
•営業資産と負債の変化。これは、取引に関連する現金の受領と支払いのタイミングの違いと、それらが経営成績に計上された時期を反映しています。そして
• 資産の処分による(利益)損失、繰延所得税、当社による事業の買収および買収による知的財産権の取得に伴う偶発的支払いの公正価値の変動。
2024年3月31日に終了した3か月間、2023年の同時期と比較して、営業活動によってもたらされた純キャッシュフローの増加は主に、2023年の同時期と比較して2024年の第1四半期に行われた従業員給付金の支払い、支払時期、および純利益に対する非現金調整の変更によるものです。この増加は、在庫の不利な変化によって部分的に相殺されました。
投資活動
2024年3月31日に終了した3か月間、2023年の同時期と比較して、投資活動に使用された純キャッシュフローの減少は、主に2023年の有価証券の純購入額の増加によるものです。
資金調達活動
2024年3月31日に終了した3か月間、2023年の同時期と比較して、財務活動に使用された純キャッシュフローの増加は、主に2024年の第1四半期に2023年のタームローンを4億ドルで返済したことによるものです。
Reataの買収に関する追加情報については、このレポートに含まれる要約連結財務諸表の注記2「買収」をご覧ください。
資本資源
負債と信用枠組み
長期債務とタームローンクレジット契約
当社の長期債務は、主にシニアノートに関連する長期債務で構成されており、最終満期日は2025年から2051年です。2024年3月31日現在、長期債務に関連する当社の未払い残高は62億9010万ドルでした。
2023年9月のReataの買収に関連して、15億ドルのタームローンクレジット契約(2023年のタームローン)を締結しました。Reata買収の締切日に、2023年のタームローンから10億ドルを引き出しました。これは、5億ドルの変動金利364日トランシェと5億ドルの変動金利の3年間のトランシェで構成されています。残りの未使用の5億ドルのコミットメントは終了しました。2023年12月31日時点で、364日間のトランシェのうち3億5,000万ドルを返済しました。その後、364日間のトランシェの残りの1億5000万ドルの部分は、2024年の第1四半期に支払われました。さらに、2024年の第1四半期に、3年間のトランシェのうち2億5,000万ドルを返済しました。2024年3月31日現在、2023年のタームローンの3年間のうち未払い額は2億5,000万ドルでした。
2020年のリボルビング・クレジット・ファシリティ
2020年1月、私たちは運転資金や一般的な企業目的で資金を引き出すことが許可されている、10億ドルの5年間のシニア無担保リボルビング・クレジット・ファシリティを締結しました。リボルビング・クレジット・ファシリティの条件には、連結レバレッジの最大比率を超えないことを義務付ける財務規約が含まれています。2024年3月31日と2023年12月31日の時点で、未払いの借入金はなく、このファシリティに基づくすべての契約を遵守していました。
2024年3月31日および2023年12月31日現在の未払いの借入金の公正および帳簿価額の概要については、本レポートに含まれる要約連結財務諸表の注記8「公正価値の測定」をご覧ください。
当社のシニアノートとクレジットファシリティの詳細については、2023年フォーム10-Kに含まれる連結財務諸表の注記13「債務」をご覧ください。
自社株買戻しプログラム
2020年10月、当社の取締役会は、最大50億ドルの普通株式を買い戻すプログラムである2020年の自社株買戻しプログラムを承認しました。2020年の自社株買戻しプログラムには有効期限はありません。2020年の自社株買戻しプログラムに基づくすべての自社株買いは廃止されます。2024年3月31日および2023年3月31日に終了した3か月間、当社の普通株式の自社株買いはありませんでした。2024年3月31日現在、2020年の自社株買戻しプログラムでは約21億ドルが残っています。
契約上の義務と貸借対照表外の取り決め
契約上の義務
当社の契約上の義務は、主にキャンセル不可のオペレーティングリース、長期債務、確定給付およびその他の購入債務で構成されます。ただし、以下に説明するように、不確実な税務ポジション、資金調達コミットメント、偶発的開発、規制上および商業上のマイルストーンの支払い、および条件付支払いに関連する金額は除きます。
さらに、当社のコラボレーションやライセンス契約の一部には、ロイヤリティの支払い義務が含まれています。ロイヤリティの支払いに関する追加情報については、2023年フォーム10-Kに含まれる連結財務諸表の注記22「コミットメントと不測の事態」をご覧ください。
2023年12月31日以降、契約上の義務に重大な変更はありません。
偶発開発、規制、商業マイルストーンの支払い
2024年3月31日現在の開発計画に基づくと、ライセンスや開発プログラムを含むさまざまなコラボレーションの一環として、約10億ドルの開発マイルストーン、約4億ドルの規制上のマイルストーン、約37億ドルの商業的マイルストーンを含め、将来的に最大約51億ドルのマイルストーンを第三者に支払う可能性があります。これらの契約に基づく支払いは、通常、開発、規制、または商業上の特定のマイルストーンの達成時に支払期日となります。2024年3月31日現在、これらのマイルストーンの達成はありそうもないと考えられていたため、このような不測の事態は当社の財務諸表には記録されていません。偶発的なマイルストーンの支払いに関連する金額は、特定の開発、規制、または商業上のマイルストーンの成功を条件としているため、契約上の義務とは見なされません。
特定の臨床上および商業上のマイルストーンが達成された場合、現在の契約では、2024年に最大約8,250万ドルのマイルストーンを支払う可能性があります。これには、潜在的なオプトイン決済は含まれません。
その他の資金拠出契約
2024年3月31日現在、さまざまな臨床試験段階でいくつかの臨床研究が進行中です。私たちの最も重要な臨床試験支出はCROへのものです。CROとの契約は通常、通知があれば、私たちの選択でキャンセルできます。2024年3月31日現在、CROが負担した支出について、要約連結貸借対照表に約4,060万ドルの未収費用を記録しました。2024年3月31日現在の既存のCRO契約に基づくと、約6億730万ドルのキャンセル可能な将来のコミットメントがあります。
税務関連の義務
各税務当局との現金決済期間の信頼できる見積もりができないため、不確実な税務状況に関連する負債は契約上の義務の概要から除外しています。2024年3月31日現在、不確実な税務上の地位に関連する負債は約1億6,040万ドルです。
2024年3月31日および2023年12月31日の時点で、移行通行料税に基づき、それぞれ約4億2,130万ドルと4億1,950万ドルの所得税負債が発生しています。2024年3月31日時点で発生した金額のうち、約1億8,730万ドルが1年以内に支払われる予定です。移行通行料税は、2018年に開始された8年間にわたって分割払いで支払われ、利息は発生しません。
新しい会計基準
新しい会計基準についての議論については、このレポートに含まれる要約連結財務諸表の注記1「重要な会計方針の要約」をお読みください。
重要な会計上の見積もり
米国で一般に認められている会計原則に従って作成された要約連結財務諸表を作成するには、報告された資産、負債、資本、収益、費用の金額、および偶発資産と負債の関連する開示に影響を与える可能性のある見積もり、判断、仮定を行う必要があります。私たちは継続的に見積もり、判断、仮定を評価します。私たちは、過去の経験や合理的と思われるその他のさまざまな仮定に基づいて見積もりをしています。その結果は、資産、負債、資本の帳簿価額と収益と費用の金額を判断するための基礎となります。実際の結果は、これらの見積もりとは異なる場合があります。
2023年のフォーム10-K以降、重要な会計上の見積もりに重要な変更はありません。その他の重要な会計上の見積もりについては、パートII、項目7をお読みください。2023年のフォーム10-Kで財務状況と経営成績に関する経営陣の議論と分析を行っています。
アイテム 3.市場リスクに関する定量的および質的開示
私たちは、外貨為替レートの変動、金利変動、株価エクスポージャーのほか、ロシアとウクライナの紛争や中東での軍事紛争の結果として事業を展開する市場の経済状況の変化など、経営成績、キャッシュフロー、資産と負債の公正価値に影響を与える可能性のある特定のリスクにさらされています。私たちは、外貨先渡契約、外貨オプション、金利ロック契約、金利スワップ契約などのデリバティブ商品を含むさまざまな金融商品を通じて、外貨為替レートと金利の影響を管理しています。取引や投機目的で金融商品を取引することはありません。これらの契約の取引相手は大手金融機関であり、どの取引相手にもエクスポージャーが大きく集中しているわけではありません。
外貨両替リスク
当社の経営成績は、事業のグローバルな性質により、外貨為替レートの変動の影響を受けます。その結果、当社の連結財政状態、経営成績、およびキャッシュフローは、主にユーロ、英ポンド、カナダドル、スイスフランに関する外貨為替レートの市場変動の影響を受ける可能性があります。
当社のグローバル活動の財務結果は米ドルで報告されていますが、ほとんどの海外子会社の機能通貨はそれぞれの現地通貨です。私たちが事業を行っている国の外貨為替レートの変動は、多くの場合、予測が難しい方法で当社の業績に影響を与えます。特に、米ドルが他の通貨と比較して上昇するにつれて、米ドルで報告された場合、米国以外の収益の価値は減少します。米ドル高による純利益への影響は、米国以外の経費の価値によって部分的に緩和されます。米ドルで報告した場合も減少します。米ドルが他の通貨と比較して下落するにつれて、米ドルで報告された場合、米国以外の収益と費用の価値は増加します。
将来の外貨キャッシュフローの変動や外貨為替レートの変動による公正価値の変動を防ぐために、収益と営業費用のヘッジと貸借対照表のリスク管理プログラムを確立しています。
2018年の第2四半期に、監査品質センターの国際慣行タスクフォースは、アルゼンチンを3年間の累積インフレ率が100.0%を超えると予測される国として分類しました。これは、アルゼンチンの経済がインフレ率が高いことを示しています。この分類は、2024年3月31日現在の当社の経営成績や財政状態に重大な影響を与えておらず、将来の当社の経営成績や財政状態に重大な影響を与えるとは予想されていません。2023年12月、アルゼンチンペソは大統領選挙後に大幅に切り下げられました。切り下げの結果、2023年第4四半期に、2023年フォーム10-Kに含まれる2023年12月31日に終了した年度の連結損益計算書に差し引かれたその他の(収益)費用として1,600万ドルが計上されました。
収益と営業費用のヘッジプログラム
当社の外貨ヘッジプログラムは、為替レートの変動による収益と運営費への影響の一部を長期的に軽減するように設計されています。私たちは外貨リスクを管理するために外貨建て先渡契約と外貨オプションを使用しており、先渡契約とオプションの大部分は、今後9か月以内に外貨建てになると予測される特定の収益および営業費用の取引をヘッジするために使用されます。私たちは通貨投機は行いません。当社の収益と営業費用のヘッジプログラムの詳細な開示については、このレポートに含まれる要約連結財務諸表の注記10「デリバティブ商品」をご覧ください。
外貨為替レートの大幅な変動が長期間続くと、外貨為替レートの変動が収益と純利益に与える影響を軽減する当社の能力は低下します。特に、外貨為替レートの切り下げや大幅な悪化は緩和が難しく、収益に悪影響を及ぼす可能性があります。これらの契約によるキャッシュフローは、当社の要約連結キャッシュフロー計算書に営業活動として報告されます。
貸借対照表リスク管理ヘッジプログラム
また、特定の貸借対照表項目に関連する外貨リスクを軽減するために、先渡契約を使用しています。当社の貸借対照表リスク管理プログラムの主な目的は、外貨建ての純金銭的資産と外国関連会社の負債のリスクを軽減することです。このような場合、私たちは主に通貨先渡契約を利用します。貸借対照表関連の項目にヘッジ会計を選択していません。これらの契約によるキャッシュフローは、当社の要約連結キャッシュフロー計算書に営業活動として報告されます。
以下の定量的情報には、当社の収益、営業費用、貸借対照表ヘッジプログラムで使用される先渡契約に対する通貨変動の影響が含まれています。2024年3月31日および2023年12月31日の時点で、すべての満期にわたって米ドルと比較して外貨為替レートが10.0%不利に変動したと仮定すると、先渡契約の公正価値がそれぞれ約2億4,650万ドルと2億4,940万ドル減少すると仮定されます。推定公正価値の変動は、架空の為替レートの変動が未払いの先渡契約に与える影響を測定することによって決定されました。このような商品の市場リスクを定量化するためにこの方法論を使用することは、仮定の対象であり、実際の影響は大きく異なる可能性があります。市場リスクに関する定量的な情報は、すべての外貨による営業取引を考慮していないため、限られています。
信用リスク
信用リスクの集中の対象となる可能性のある金融商品には、現金および現金同等物、投資、デリバティブ、売掛金などがあります。私たちは、幅広く多様な金融商品に投資することで、現金および現金同等物や投資に関連するリスクを最小限に抑えるよう努めています。元本残高を保護し、流動性を維持するために、信用格付けと満期に関するガイドラインを制定しました。当社の投資ポートフォリオは、許容される投資を定義し、信用の質基準を指定し、単一発行体の信用リスクを制限する投資方針に従って維持されています。取引相手として格付けの高い金融機関のみを選ぶことで、デリバティブ商品から生じる信用リスクを最小限に抑えます。
私たちは、ロシアとウクライナの紛争や中東の軍事紛争の影響など、経済状況の低迷により回収期間が延長される可能性がある特定の国で事業を展開しています。私たちは、国際経済や関連する金融市場に関連するボラティリティを含め、これらの状況を引き続き監視し、それらが当社の事業に与える可能性のある影響を評価しています。現在まで、売掛金の回収に関して大きな損失は発生していません。
2024年3月31日と2023年12月31日の時点で、貸倒引当金は十分だったと考えています。
株価リスク
当社の戦略的投資ポートフォリオには、特定のバイオテクノロジー企業の株式への投資が含まれます。このような証券を保有している間は、株価リスクにさらされており、これにより、株式投資の公正価値の変動により、将来の収益のボラティリティが高まる可能性があります。私たちは、価格リスクの制限を含むビジネス上の考慮事項に基づいて、そのような株式を売却することがあります。
これらの株式の公正価値の変動は、株式市場のボラティリティや一般的な経済状況の変化などの影響を受けます。株価に敏感な商品の公正価値の潜在的な変動は、10.0% の不利な動きを想定して評価されています。2024年3月31日と2023年12月31日の時点で、仮説上の不利な10.0%の動きにより、公正価値はそれぞれ約3,300万ドルと4,170万ドル減少することになります。
アイテム 4.統制と手続き
財務報告に関する開示管理と手続き、および内部統制
統制と手続き
2024年3月31日現在、当社の開示管理および手続き(改正された1934年の証券取引法の規則13a-15(e)または15d-15(e)で定義されている)の設計と運用の有効性について、最高執行役員や最高財務責任者を含む経営陣の監督と参加を得て評価を実施しました。その評価に基づいて、当社の最高経営責任者および最高財務責任者は、このレポートの対象期間の終了時点で、当社の開示管理と手続きは次のことを保証する上で有効であると結論付けました。
(a) 証券取引法に基づいて提出または提出する報告書で当社が開示することを義務付けられている情報は、米国証券取引委員会の規則とフォームで指定された期間内に記録、処理、要約、報告されます。そして
(b) このような情報は、必要な開示に関する迅速な決定ができるよう、必要に応じて蓄積され、当社の最高執行責任者や最高財務責任者を含む当社の経営陣に伝達されます。
当社の開示管理と手続きを設計および評価するにあたり、当社の経営陣は、どの統制や手続きも、どんなにうまく設計・運用されても、望ましい統制目標の達成を合理的に保証することしかできないことを認識していました。そして、当社の経営陣は、可能な統制と手続きの費用対効果の関係を評価する際に必ず判断を下す必要がありました。
財務報告に関する内部統制の変更
2024年3月31日に終了した四半期に、財務報告に対する当社の内部統制に重大な影響を及ぼした、または財務報告に対する内部統制に重大な影響を与える可能性がかなり高い変更はありませんでした。
パートII その他の情報
アイテム 1.法的手続き
2024年3月31日現在の法的手続きの詳細については、このレポートに含まれる要約連結財務諸表の注記21「訴訟」を参照してください。この情報は、参考までにこの項目に組み込まれています。
アイテム 1A。リスク要因
事業に関するリスク
私たちは製品からの収益に大きく依存しています。
当社の収益は、当社製品の継続的な販売と、抗CD20治療プログラムの経済的権利によって決まります。収益のかなりの部分は、競争が激化する市場での製品の販売に集中しています。当社の製品または抗CD20治療プログラムに関連する以下のマイナスの進展のいずれかは、当社の収益と経営成績に悪影響を及ぼしたり、株価の下落を引き起こす可能性があります。
•既存の製品および短縮された規制経路の下で承認された製品の新規創薬療法、ジェネリック医薬品、プロドラッグ、バイオシミラーを含む競合製品の紹介、受け入れの拡大、またはより有利な償還を行います。
•安全性または有効性の問題。
•製品の価格設定または値上げに対する制限や追加の圧力。これには、インフレに関連するもの、政府または規制上の要件(IRAの下での将来の潜在的な医薬品価格交渉に関連するものを含む)、競争の激化(当社製品のジェネリック版またはバイオシミラー版を含むものを含む)、または支払者およびその他の第三者の償還方針および慣行の変更または実施が含まれます。
•法的、行政的、地政学的な不利な出来事、規制または立法上の不利な発展。または
•患者、医療提供者などの間で良い評判を維持する当社の能力。これは、当社の価格設定や償還に関する決定の影響を受ける可能性があります。
LEQEMBIは米国および特定の国際市場での商業的発売の初期段階にあり、SKYCLARYSは米国および特定のヨーロッパ市場での商業的発売の初期段階にあります。新製品の発売に関連するリスクや、これらのリスク要因に記載されているその他の要因に加えて、バイオジェンとエーザイがLEQEMBIの商品化を成功させる能力、およびSKYCLARYSの商品化を成功させる能力は、以下の理由により悪影響を受ける可能性があります。
•LEQEMBIに対する適切な払い戻しを受け、維持するエーザイの能力。
•LEQEMBIのマーケティングにおけるエーザイとバイオジェンの商業戦略の有効性
•レジストリへの参加、LEQEMBIの画像検査やその他の診断法の使用などの要件。
•他の市場でも承認を得る当社の能力。
•同じまたは類似の適応症に対する他の新製品の承認。
•エーザイとバイオジェンがアルツハイマー病コミュニティの患者、医療提供者、その他の人々の間で良い評判を維持している能力。これは、エーザイおよび/または第三者がLEQEMBIに関連する価格設定や償還の決定によって影響を受ける可能性があります。
•バイオジェンのSKYCLARYSへの適切な償還を受け、維持する能力。そして
•スカイクラリスのマーケティングにおけるバイオジェンの商業戦略の有効性。
私たちの長期的な成功は、新製品の開発と既存製品の追加適応症の成功にかかっています。
私たちの長期的な成功は、研究開発活動による新製品の開発の成功、第三者からのライセンスまたは買収、および既存の製品に対する追加の適応にかかっています。
製品開発は非常に費用がかかり、高い不確実性とリスクを伴い、成功しない可能性があります。製品の商品化につながる研究開発プログラムはごくわずかです。治療のための新しいアプローチの製品開発の成功と時間とコストを予測することは困難です
病気の。アンチセンスオリゴヌクレオチドプラットフォームや遺伝子治療に基づくものなどの新しいモダリティの開発を含む、病気の治療のための新しいアプローチの開発は、そのような治療法の開発経験が少ない規制当局からの承認を得るなど、さらなる課題とリスクをもたらす可能性があります。たとえば、現在、ヨーロッパではLEQEMBIの承認を、米国ではLEQEMBIの皮下製剤の承認を求めています。遅延や課題があれば、LEQEMBIから期待される効果を実現する能力に影響を与える可能性があります。
臨床試験データはさまざまな解釈の対象となり、治験中の治療法の安全性、有効性、および/または承認を裏付けるのに十分であると当社が判断した場合でも、規制当局はこれに同意せず、追加のデータを要求したり、承認の範囲を制限したり、承認を完全に拒否したりすることがあります。さらに、ある規制機関が製品候補を承認したからといって、他の規制機関もその製品候補を承認するわけではありません。
前臨床研究や初期段階の臨床試験が成功しても、後期または大規模な臨床試験が成功するとは限りません。臨床試験では、当社の製品候補に効能がない、有害な副作用がある、予期しない有害事象が発生する、または規制当局の承認の可能性を大幅に低下または遅延させる可能性のあるその他の懸念が生じる場合があります。その結果、プログラムが中止されたり、使用が大幅に制限されたり、承認されたラベルに安全上の警告が表示されたり、治療パラダイム内での位置付けが悪くなったり、製品候補の商業的可能性が大幅に低下したりする可能性があります。
新製品や適応症の開発に成功できたとしても、商品化が標準治療に比べて難しいと思われる場合や、パイプラインの他の機会を優先する場合など、製品候補または適応症の開発を中止するという戦略的決定を下すことがあります。
新製品やその他の表示のある製品の販売は、投資家の期待に応えない可能性があります。
効果的に競争できなければ、ビジネスと市場での地位が損なわれます。
バイオ医薬品業界と私たちが事業を展開する市場は非常に競争が激しいです。私たちは、製品のマーケティングと販売、新製品とプロセスの開発、商業的可能性を秘めた新製品の権利の取得、人材の雇用と維持において競争しています。私たちは、市場や製品パイプラインの製品数が多く、財務、マーケティング、研究開発、その他のリソース、その他の技術的または競争上の優位性が大幅に高いバイオテクノロジー企業や製薬会社と競争しています。
既存の製品や短縮された規制経路の下で承認された製品の新しいオリジネーター療法、ジェネリック、プロドラッグ、バイオシミラーの導入により、当社の製品は引き続き競争の激化に直面しています。これらの製品の中には、当社のブランド製品よりも大幅に安い価格で販売されるものがあります。このような製品やその他の低価格の競合製品の導入により、当社の製品に請求できる価格と販売する製品の量の両方が減少し、将来的には大幅に下がる可能性があります。これは当社の収益に悪影響を及ぼします。たとえば、2020年に複数のTECFIDERAジェネリック医薬品が米国市場に参入した結果、TECFIDERAの需要と価格は大幅に下落しました。さらに、一部の市場では、当社製品のジェネリック版またはバイオシミラー版が商品化されると、自動的に当社製品の代わりに使用され、短期間で収益が大幅に減少することがあります。
私たちの競争力、事業維持、成長能力も、次のような多くの要因によって悪影響を受ける可能性があります。
•自社製品や協力者の製品を含む、当社の製品に代わるより効果的、より安全、より安価な、またはより便利な代替品を含む他の製品の紹介。
•医師が患者を治療するために他の疾患で適応となる治療法を適応外で使用すること。
•患者様の動態。患者集団の規模や、新規患者と現在の患者を特定し、当社の治療法に引き付け、維持する能力など。
•そのような製品の有効性と安全性に関する追加データがないのに、医師が当社の製品を処方したり、患者が当社の製品を使用したりするのを嫌がること。
•当社製品、当社製品のジェネリックまたはバイオシミラー、または当社製品と同じクラスの他の製品に対する医師や患者の信頼、またはラベルの変更、価格設定と償還の決定、または当社製品、または当社製品のジェネリックまたはバイオシミラーで治療された患者に発生する可能性のある不利な経験や出来事の結果として、当社の販売と評判が損なわれる。
•主要市場の競合他社と比較して、自社製品の適切な価格設定と適切な償還を得ることができず、維持できない、または
•当社製品の特許、データ、または市場独占権を取得および維持する当社の能力。
戦略的および成長的取り組みを成功裏に実行できなかったり、期待される利益を実現できなかったりすると、当社の事業に悪影響が及ぶ可能性があります。
当社の戦略的および成長的イニシアチブが成功するかどうかは、製品、技術、企業の買収とライセンス供与、戦略的提携やコラボレーションへの参入、またはFit for Growthプログラムなど、社内の開発プロジェクト、商業的イニシアチブ、および外部機会、およびバイオシミラー事業の戦略的オプションの探求など、以前に発表されたイニシアチブを実行する能力にかかっている可能性があります。
パイプラインには有望なプログラムが数多くあると考えていますが、内部開発プロジェクトの進行の失敗や遅延、または商業的イニシアチブの実施の困難は、現在および将来の成長に影響を与え、その結果、成長のために外部の開発機会への依存度が高まる可能性があります。
既存の製品やパイプラインにある潜在的な新製品のさらなる開発を支援するには、研究開発、販売とマーケティング、製造能力、その他の事業分野への投資を含む、多額の設備投資と経営資源が必要です。規制当局の承認前に、潜在的な新製品に対して多額の営業および資本支出を行ってきましたが、そのような投資が回収されるという保証はありません。これは、当社の財政状態、事業、運営に悪影響を及ぼす可能性があります。
高品質でかなり価値のある外部製品開発は限られており、買収の機会は非常に競争が激しいです。そのため、買収に適した候補者を特定できるかどうか、または適切な候補者が特定された場合にそのような買収を行うことで合意に達できるかどうかは定かではありません。
規制当局やその他の承認を得られなかったり、紛争や訴訟の結果など、さまざまな理由で取引を開始または完了できない場合があります。さらに、取引から期待される戦略的および財務的利益を十分に得られない場合や、利益が遅れたり、まったく得られない場合があります。また、完了前には想定されていなかった追加の費用や負債が発生する可能性もあります。
取引の実行、買収した資産または事業の統合、または期待される相乗効果の達成に失敗した場合、成長が遅くなり、予想を上回るコストが発生し、資産減損費用の計上など、当社の事業、財政状態、経営成績に悪影響を及ぼす可能性があります。たとえば、私たちは最近Reataを買収し、Reataを当社に統合する過程にあります。Reataの買収が最終的に成功し、SKYCLARYS製品や予想される相乗効果など、買収から期待される利益を実現できるかどうかは、とりわけ、バイオジェンとレアータの事業を統合する上でどれだけ効果的かにかかっています。
私たちは、Fit for Growthプログラムに関連するリスクに直面しています。これにより、予想される節約や業務効率を達成する能力が損なわれたり、事業に悪影響が及ぶ可能性があります。これらのリスクには、コスト最適化措置の実施の遅れ、労働力の喪失、予想を上回る離職費用、訴訟、財務目標と事業目標の達成の失敗などがあります。さらに、Fit for Growthプログラムから得られる予想されるコスト削減やその他のメリットの計算には、多くの見積もりや仮定が適用されます。これらの見積もりや仮定は、ビジネス、経済、競争、その他の重大な不確実性や不測の事態の影響を受けやすく、その多くは当社の制御が及ばないものです。これらの見積もりや仮定が正しくない場合、または遅延や予期しない出来事が発生した場合、当社の事業と財務結果に悪影響を及ぼす可能性があります。
当社製品の販売は、政治、社会、競争、その他の情報源からのますます強い圧力にさらされている、適切な補償範囲、価格設定、および第三者支払者からの払い戻しに大きく依存しています。十分な補償範囲を取得して維持できない場合や、価格や償還額が引き下げられると、当社の事業、評判、収益、経営成績に悪影響を及ぼす可能性があります。
当社製品の販売は、適切な補償範囲、価格設定、および第三者支払者からの払い戻しに大きく依存します。新しい医薬品が承認された場合、その製品に対する政府および民間からの償還の有無、治療対象となる状態の診断、投与費用が不確実になる場合があります。また、その製品の価格や払い戻しの金額も不確実です。
当社製品の価格設定と払い戻しは、次のようなさまざまな要因によって悪影響を受ける可能性があります。
•連邦、州、または外国の政府規制または民間の第三者支払者の償還方針の変更と実施。
•民間健康保険プランに対する雇用主からのコスト削減の圧力。
•フォーミュラリーへの当社製品の掲載に関連して、価格割引やリベートを求める支払者の統合と主張の高まり、場合によっては、特定の医薬品へのアクセスや適用範囲、または認識された価値に基づいて決定される価格に制限を課すこと。
•当社製品に対する償還を受ける当社の能力、または競合製品と同等の償還を受ける能力。そして
•当社の価値に基づく契約プログラムは、患者の治療成績に合わせて価格を調整するか、有効性や忍容性の懸念を含む何らかの理由で治療を中止した患者のために価格を調整することにより、製品の価格を臨床的価値に結び付けることを目的としています。
製品の価格を設定できるかどうかは国によって大きく異なり、その結果、製品の価格も異なります。政府は、値下げ、強制リベート、価値に基づく価格設定、参考価格(つまり、他の国の価格を参照し、それらの参照価格を使用して価格を設定する)など、さまざまなコスト抑制策を講じることがあります。当社の製品が処方されている市場では、医薬品の価格が厳しく監視されています。たとえば、IRAには医薬品の価格に関する特定の規定があります。医薬品の価格設定やその他の医療費は、今後も世界的に強い政治的および社会的圧力にさらされると予想しています。特定の国では、当社の製品が販売されている他の国の価格を基準に価格を設定しています。特定の国で適切な価格を取得および維持できないと、その国内での製品からの収益が制限されるだけでなく、既存および潜在的な新規市場で許容可能な価格を確保する能力に悪影響を及ぼす可能性があり、その結果、市場の成長が制限され、収益が減少する可能性があります。これにより、第三者による国境を越えた取引の機会が生まれたり、製品を販売するかどうかの決定に影響を与えたりして、当社の地理的拡大計画と収益に悪影響を及ぼす可能性があります。さらに、特定の法域では、政府の保健機関が当社製品の償還率を遡及的および/または将来的に調整する場合があります。政府による当社製品の償還は、償還の時期を含め、特に厳しい経済環境では、予算上または政治上の制約の影響を受ける可能性があります。多くの場合、政府機関は独自の予算を設定しないため、支出できる金額の管理が限られています。さらに、これらの機関は政治的圧力にさらされており、それがお金の使い方を決定づける可能性があります。経済的、予算的、政治的な問題が悪化し、当社製品の販売や償還に悪影響を及ぼさないという保証はありません。
現在および将来の競合他社との競争は、当社の価格維持能力と市場シェアに悪影響を及ぼす可能性があります。競合他社が販売する新製品は、潜在的な値下げや販売量の減少により、当社の収益を減少させる可能性があります。さらに、当社製品、後続製品、プロドラッグ、または短縮された規制経路の下で承認された製品のジェネリック版またはバイオシミラー版を導入すると、当社製品に請求できる価格と販売する製品の量が大幅に下がる可能性があります。
多くの支払者は、処方費用の大部分を患者に転嫁する給付制度の変更を引き続き採用しています。これには、より限定的な給付制度の設計、患者の自己負担または共同保険の義務の増加、民間製造業者の自己負担支払い支援プログラムの患者による使用の制限(自己負担額アキュムレータ調整または最大化プログラムを含む)が含まれます。健康保険業界の大幅な統合により、いくつかの大手保険会社や薬局の福利厚生管理者が製薬会社との価格設定や使用交渉にさらに圧力をかけ、製造業者に求められる割引やリベートが大幅に増加し、患者へのアクセスと利用が制限されています。保険会社、薬局の給付管理者、その他の支払者がさらに統合されれば、そのような企業が当社や他の製薬会社に対して持つ交渉力が高まるでしょう。上記のような追加の割引、リベート、補償範囲またはプランの変更、制限または除外は、影響を受ける製品の売上に重大な悪影響を及ぼす可能性があります。
当社製品に関する適切な補償、価格設定、または償還の取得または維持を怠ると、当社の事業、評判、収益、および経営成績に悪影響を及ぼす可能性があります。
私たちは、収益、特定の製品や製品候補の開発、規制当局の承認、商品化、マーケティングのために、協力者や他の第三者との関係に依存していますが、これらは完全に制御できません。
私たちは、特定の製品や製品候補の収益、開発、規制当局の承認、商品化、マーケティングにおいて、多くの協力関係やその他の第三者関係に依存しています。また、当社の製品や製品候補に関連する規制業務や臨床開発の特定の側面を第三者に外注しています。第三者に頼ることは、次のような多くのリスクにさらされます。
•協力者や第三者が当社のプログラム、製品、製品候補に費やすリソースを管理できない場合があり、それが開発目標やマイルストーンの達成に影響する可能性があります。
•マイルストーンの達成と支払い、開発または商業費の支払い、開発された技術の権利の所有権などに関する紛争が契約に基づいて発生する可能性があり、協力者や第三者が履行しなかった場合、基礎となる契約が当社に重要な保護を提供できなかったり、効果的に執行されなかったりする可能性があります。
•協力者または第三者の利益は、常に当社の利益と一致しているとは限りません。そのような当事者は、当社と同じ方法または程度で規制当局の承認を求めたり、製品を販売したりしない場合があります。これにより、収益に悪影響が及ぶ可能性があります。また、当社の事業、経営成績、または財政状態に悪影響を及ぼす可能性のある税務戦略を採用する可能性があります。
•第三者関係には当事者の協力が必要であり、効果的に協力しないと、共同管理下にある製品候補の製品販売や臨床開発または規制当局の承認に悪影響を及ぼしたり、製品候補の研究、開発、商品化が終了したり、訴訟や仲裁につながる可能性があります。
•当社の協力者または第三者が、税法、規制要件、および/または該当する契約上の義務を含む適用法を遵守しなかったり、当社の製品の基礎となる知的財産権を保護および執行するために負う可能性のある責任を果たさなかったりすると、当社の収益や評判に悪影響を及ぼしたり、法的手続きに当社が関与したりする可能性があります。そして
•協力者や第三者の不適切な行為や行動は、民事または刑事捜査や金銭的および差止命令による罰則の対象となり、経営陣の注意が必要になったり、財務報告の正確性とタイミングに影響を与えたり、当社の事業遂行能力、経営成績、評判に悪影響を及ぼしたりする可能性があります。
これらのリスクを考えると、現在および将来の共同作業の成功にはかなりの不確実性があります。これらの努力が失敗した場合、当社の製品開発や新製品の商品化が遅れたり、製品からの収益が減少したり、これらの取り決めから期待されるメリットが実現できなくなったりする可能性があります。
当社の経営成績は、現在および将来の医療改革によって悪影響を受ける可能性があります。
米国では、連邦議会、州議会、保健機関、第三者支払者が引き続き医療費の抑制に注力しています。立法上および規制上の提案、医療保険プログラム(IRAに含まれるものを含む)を改革するための制定、および社会的ソースからの圧力の高まりは、当社製品の処方、購入、および償還の方法に大きな影響を与える可能性があります。たとえば、PPACAの規定により、メディケイド医薬品リベートプログラムに基づいてメーカーが支払うべきリベートの増加、特定のブランドの処方薬のメーカーに対する年会費と税金、メーカーがメディケアパートDに基づく特定の外来医薬品の割引プログラムに参加することが義務付けられたこと、セクションに基づく割引の対象となる病院数の拡大など、政府と民間の保険会社の両方による医療費の支払い方法が変化しました公衆衛生サービス法の340億ドル。これらの変化は、当社の事業に大きな影響を与えており、今後もそうなると予想されます。
PPACAの条項の一部または全部を廃止、大幅に修正、または無効にしようとした結果、不確実性に直面する可能性があります。現在制定されている、または将来改正されるPPACAが当社の事業および財務結果に悪影響を及ぼさないという保証はありません。また、医療改革に関連する将来の連邦または州の立法または行政上の変更が当社の事業にどのように影響するかを予測することはできません。
処方薬の費用には世間の注目が非常に高く、医薬品の価格設定やその他の医療費は、今後も世界的に強い政治的および社会的圧力にさらされると予想されます。さらに、処方薬の価格設定に関する立法案(IRAの要素を含む)があり、今後もそうなると予想されます。これらの提案の中には、2020年9月に発行された、償還率を国際的な医薬品価格指標に結び付けるパートBおよびパートDの医薬品の「最恵国待遇」モデルをテストする大統領命令など、当社の事業に大きな影響を与えるものもあります。これらの措置と、PPACAと医療法の将来に関する不確実性は、医薬品価格の下落圧力をかけ、規制上の負担と運営コストを増大させる可能性があります。
また、州の予算には大きな経済的圧力がかかっています。その結果、州は医薬品の補償範囲や支払いを制限するメカニズムを通じて予算を節約しようとすることが増えている可能性があります。近年、一部の州では、米国外の低コストの管轄区域からの医薬品の輸入を許可する法律や、州の医薬品購入に価格統制を課すことを目的とした法律など、医薬品の価格を管理する法律や投票イニシアチブを検討しています。州のメディケイドプログラムでは、メーカーに追加のリベートを支払うよう求めており、追加リベートが支払われていない医薬品の使用については、州のプログラムによる事前の承認が必要です。メディケイド経費を削減するための政府の取り組みは、メディケイドプログラムによるマネージドケア組織の利用の増加につながる可能性があります。その結果、マネージドケア組織が処方に影響を与える可能性があります
より多くの人々のための決定と、それに対応する製品の価格と償還の制限があります。
EUやその他の国際市場では、政府は消費者に低コストで医療を提供し、政府が後援する医療制度の費用を管理するために、医薬品の価格、患者の資格、または償還レベルを規制しています。多くの国が、政府支出の全体的な水準を制限するために医療費を削減するための措置を発表または実施しており、将来的には新しい措置または追加の措置を実施する可能性があります。これらの措置は国によって異なり、とりわけ、患者のアクセス制限、値上げの一時停止、将来的かつ可能な事後的な値下げやその他の回収、強制割引またはリベートの増加、過去の価格上昇の回収、低コスト国からの医薬品の輸入の増加などが含まれる場合があります。これらの措置は当社の収益に悪影響を及ぼし、今後も当社の収益と経営成績に悪影響を及ぼし続ける可能性があります。
バイオシミラーの商品化における当社の成功は、バイオシミラーの開発、製造、商品化に内在するリスクと不確実性の影響を受けます。そのような活動に失敗した場合、私たちのビジネスに悪影響が及ぶ可能性があります。
バイオシミラー製品の開発、製造、商品化には専門知識が必要で、非常に費用がかかり、複雑な規制の対象となります。バイオシミラーの商品化における私たちの成功には、次のような多くのリスクが伴います。
•第三者への依存。私たちは、バイオシミラー製品の開発と製造において、私たちがほとんどまたはまったく管理できないコラボレーションパートナーやその他の第三者の努力に一部依存しています。たとえば、最近発表された開発・製造受託組織の第三者による買収の可能性は、その事業上、戦略上、または財務上のリスクに影響を与える可能性があります。これらの第三者が成功しなかったり、第三者製造生産を削減したりすると、当社のバイオシミラー製品の開発やバイオシミラー製品の商品化が遅れたり、バイオシミラー製品からの収益が減少したり、これらの取り決めから期待される利益が実現できなくなる可能性があります。
•規制コンプライアンス。バイオシミラー製品は、特定の法域におけるバイオシミラー製品の規制や商業経路が進化し不確実なため、規制上のハードルや遅延に直面する可能性があります。
•十分な供給を提供する能力。バイオシミラーの製造は複雑です。製造やサプライチェーンの問題が発生した場合、需要に応えられない可能性があります。私たちはバイオシミラー製品の製造を第三者に依存しています。そのような第三者は、適時かつ費用対効果の高い方法で、または適用される規制に従って義務を履行せず、既存または将来のバイオシミラー製品の需要に見合った生産能力を増やすことができない、または増やしたくない場合があります。
•知的財産と規制上の課題。バイオシミラー製品は、広範囲にわたる知的財産権のクリアランスや侵害訴訟、差し止め命令、規制上の問題に直面する可能性があります。これにより、製品の商業的発売が妨げられたり、何年も遅れたり、金銭的損害、罰則、その他の民事制裁が科せられ、当社の評判が損なわれる可能性があります。
•市場を獲得できず、患者に受け入れられませんでした。患者、医師、支払者が、バイオシミラー製品を、既存の治療法よりも競争力のある価格やその他の利点を提供する安全で効果的な製品として受け入れなければ、バイオシミラー製品の市場での成功は悪影響を受けます。そして
•競争上の課題。バイオシミラー製品は大きな競争に直面しています。イノベーター製品や他社が提供するバイオシミラー製品などは、より受け入れられたり、より有利な償還を受けたりする可能性があります。現地の入札手続きにより、一部の法域ではバイオシミラー製品の販売と販売が制限される場合があります。ある管轄区域内の競合他社の数、承認のタイミング、バイオシミラー製品をタイムリーかつ費用対効果の高い方法で成功させる能力なども、この事業分野での当社の成功に影響を与える可能性があるその他の要因です。バイオシミラー事業に関連する戦略的オプションを検討するという決定は、バイオシミラー事業に関連する事業に悪影響を及ぼす可能性があります。
知的財産に関連するリスク
データ、知的財産、その他の所有権に対する適切な保護を得ることができず、維持できない場合、当社の事業が損なわれる可能性があります。
長期的な存続と成長を含め、私たちの成功は、製品や製品候補の商品化に重要な、特定の規制上の独占権を含む、特許権やその他の知的財産権を取得し、守る能力に一部かかっています。米国およびその他の重要な市場における特許保護および/または規制上の独占権は依然として不確実であり、一部はこれらの国の特許庁、裁判所、行政機関、および議員の決定に依存しています。特許やその他の取得、擁護、保存に失敗する可能性があります
特定の規制形態の独占権を含む知的財産権、または当社が取得する保護は、当社が事業を行うすべての国における当社の商業的利益を保護するには十分な範囲と程度ではない場合があります。その結果、当社に財務、ビジネス、または評判が損なわれたり、株価の下落や変動が発生したりする可能性があります。さらに、このような手続きの和解により、独占権やその他の保護期間が短縮され、影響を受ける製品からの収益が減少することがよくあります。
米国を含む多くの市場では、メーカーはイノベーターの製品の安全性と有効性のデータに頼ることが許可されている場合があり、特許や規制上の独占権がなくなった後は、競合バージョンの製品を販売する前に臨床試験を実施する必要がなくなります。このような場合、メーカーは大幅に低い価格を請求することが多く、会社の収益の大部分が短期間で減少する可能性があります。さらに、ジェネリック医薬品やバイオシミラーのメーカーは、当社の特許やその他の知的財産保護の期限が切れる前に、製品を発売したり、発売を試みたりすることがあります。
さらに、当社の製品は、第三者が保有する特許またはその他の知的財産権を侵害していると判断される場合があります。当社製品の製造、使用、販売に関連して第三者が主張する特定の特許権の有効性、範囲、または非侵害を判断するには、法的手続き、行政上の異議申し立て、またはその他の種類の手続きが必要であり、また将来必要になる可能性があります。また、当社が第三者と締結した知的財産ライセンス契約の満了中および満了後に請求される権利、義務、および支払いを決定するために、法的手続きが必要になる場合があります。このような手続きは予測がつかず、多くの場合、長引いて費用がかかります。このような手続きの結果、製品の製造やマーケティングが妨げられたり、妨げられたり、侵害された製品や技術のライセンスを求める必要が生じたり、財務諸表で発生した金額を超える可能性のある多額の金銭的損害賠償が当社に対して請求されたりする可能性があります。侵害された製品や技術に必要なライセンスを取得しないと、製品の製造や販売ができなくなる可能性があります。さらに、取得可能なライセンスに基づく支払いは、対象となる製品やサービスからの利益を減少させる可能性があります。これらの状況はいずれも、当社の財務、ビジネス、評判に損害を与えたり、株価の下落や変動を引き起こしたりする可能性があります。
当社製品および製品候補品の開発、臨床試験、規制に関連するリスク
前臨床研究や初期段階の臨床試験が成功しても、後期試験の成功、規制当局の承認、または製品の商業的実行可能性が保証されるわけではありません。
臨床試験で肯定的な結果が出ても、その後の試験や確認試験では再現されない場合があります。さらに、前臨床研究や初期段階の臨床試験が成功しても、後期または大規模な臨床試験が成功したり、規制当局の承認が得られたりするとは限りません。後期段階の臨床試験が成功したとしても、規制当局は当社の製品候補の承認を延期または拒否することがあります。規制当局は、私たちのデータに対する見方に異議を唱えたり、追加の研究を要求したり、私たちの試験デザインやエンドポイントに同意しなかったり、適切な償還を承認しなかったりすることがあります。規制当局は、候補製品の製造に使用される設備やプロセス、当社の投与方法や配送方法、またはコンパニオンデバイスの承認を怠ることもあります。規制当局は、限られた患者集団への適応の制限、安全性モニタリング、教育要件、確認試験やリスク評価および軽減戦略の要求など、予想以上に制限された販売承認を与える場合があります。これらの出来事のいずれかが発生すると、多額の費用や費用が発生したり、当社の事業、財務状況、経営成績に悪影響を及ぼしたり、株価が下落したり、ボラティリティが高まったりする可能性があります。
臨床試験とバイオ医薬品の開発は長く複雑なプロセスです。臨床活動を適切に管理できなければ、臨床試験や潜在的な規制当局の承認が遅れたり、却下されたりする可能性があります。
臨床試験の実施は複雑で時間と費用のかかるプロセスです。臨床試験をタイムリーに完了できるかどうかは、プロトコルの設計、規制当局および機関の審査委員会の承認、患者登録率、現在の優良臨床基準の遵守など、多くの重要な要素に左右されます。当社、または第三者の臨床試験提供者、または第三者のCROがこれらの臨床活動を成功裏に実施できない場合、当社の臨床試験または製品候補の潜在的な規制当局の承認が遅れたり、拒否されたりする可能性があります。
私たちは臨床試験施設を開設し、私たちの経験が限られている多くの国で患者を登録しています。ほとんどの場合、私たちは臨床試験関連の活動を行うために第三者のサービスを利用し、結果を正確に報告するためにそのような機関に頼っています。これらの活動を第三者に依存していると、臨床試験のタイミング、実施、費用、品質を管理する当社の能力に影響を与える可能性があります。1人のCROが、当社の臨床試験に関連する当社の活動と報告のかなりの部分を担当しています。そのようなCROが適切に機能しない場合、そのような試験に関連する費用への悪影響を含め、多くの試験が影響を受ける可能性があります。CROを交換する必要があるかもしれません。その結果、影響を受ける試験が遅れたり、規制当局の承認を得て製品候補を商品化する取り組みに悪影響が及ぶ可能性があります。
安全上の不利な事象や使用制限、当社製品の安全上の警告は、当社の事業、製品販売、株価に悪影響を及ぼす可能性があります。
当社の市販製品、市販製品のジェネリック版またはバイオシミラー版、または当社製品と同じクラスの製品に関連する安全上の有害事象は、当社の事業に悪影響を及ぼす可能性があります。当社製品の安全上の問題が発見された場合、製造物責任が発生し、規制当局によるさらなる精査や追加の表示や安全監視の要求、製品の市場からの撤回、罰金や刑事罰が科せられる可能性があります。安全上の有害事象は、当社の製品に対する医師、患者、および/または投資家の信頼や評判を損なう可能性もあります。これらのいずれも、当社の経営成績に悪影響を及ぼす可能性があります。
規制当局は、定期的な安全性更新報告書、患者登録、その他の報告要件を通じて、より多くの独立した安全情報を直接一般に公開しています。当社の製品または当社に類似した製品に関する安全上の不利な事象の報告、およびそのような出来事に関する公の噂は、当社に対する請求を増やし、製品の売上が減少したり、株価が変動したりする原因となる可能性があります。
当社製品のラベルに使用制限や安全上の警告を記載する必要がある場合、それらの製品の期待収益が大幅に減少し、多額の費用と管理時間が必要になる場合があります。
事業に関連するリスク
情報システムの故障や違反により、当社が責任を負ったり、事業運営が中断されたりする可能性があります。
私たちは、事業を運営するために情報システムとデータにますます依存するようになっています。私たちの運営方法の変化により、米国やその他の主要市場のオフィスを拠点とする従業員のほとんどがオフィスで働くという要件を変更するなど、この依存度を高めるようにビジネス慣行を変更しました。現在、当社の従業員の多くはハイブリッドまたはフルリモートワークで働いています。その結果、私たちは事業運営において情報システムにますます依存するようになり、事業を効果的に管理する能力は、サービスとしてのソフトウェア(SaaS)、サービスとしてのプラットフォーム(PaaS)、サービスとしてのプラットフォーム(PaaS)、サービスとしてのインフラストラクチャ(IaaS)などのクラウドテクノロジーの使用を含む、情報システムとデータのセキュリティ、信頼性、および妥当性にかかっています。故障、侵入、破損、破壊、および/または侵害は、当社またはビジネスパートナーの情報システム(クラウドテクノロジーを含む)の容量、信頼性またはセキュリティ、および/またはデータや情報への不正アクセスが含まれますが、これらに限定されません。また、当社のデータや情報への不正アクセスにより、当社が重大な責任を負ったり、事業運営に悪影響を及ぼしたり、技術の交換や多額の身代金の支払いが必要になったりする可能性がありますが、これらに限定されません。クラウド技術を含む私たちの情報システムは、多様性と複雑さを増し続けており、故障、悪意のある侵入、ランダムな攻撃が発生した場合の脆弱性が高まっています。データプライバシーやセキュリティ侵害は、当社、患者、顧客、その他のビジネスパートナーが所有する知的財産、企業秘密、個人情報などの機密データが、権限のない人や一般に公開されるリスクもあります。
サイバーセキュリティの脅威とインシデントは、その頻度、巧妙さ、強度が増しており、特にベンダー、顧客、サプライヤー、およびサプライチェーンの他の企業に影響を与える場合、検出がますます困難になっています。サイバーセキュリティの脅威とインシデントは、多くの場合、国家、組織犯罪グループ、「ハクティビスト」など、やる気があり、十分なリソースを持ち、熟練した粘り強いアクターによって実行され、不注意または悪意を持って行動する従業員や請負業者が含まれたり標的にしたりすることがあります。脅威環境における最近の進展には、AIと機械学習の使用、金銭的身代金の要求量の増加、ランサムウェアの手法と方法論の高度化と多様化に伴うサイバー恐喝攻撃の増加などがあります。ロシアのウクライナ侵攻や中東紛争に関連するものを含め、地政学的な不安定性は、サイバーセキュリティの脅威のリスクを高める可能性があります。サイバーセキュリティの脅威やインシデントには、有害なマルウェアやキーロガー、ランサムウェア、サービス拒否攻撃、悪意のあるWebサイト、ソーシャルエンジニアリングの使用、および情報システムやデータの機密性、完全性、可用性に影響を与えるその他の手段が含まれます。サイバーセキュリティの脅威やインシデントには、製造業、ハードウェアまたはソフトウェアのサプライチェーン攻撃も含まれます。これにより、製品や委託製造向けに製造された製品の製造が遅れたり、データのプライバシーやセキュリティが侵害されたりする可能性があります。私たちの主要なビジネスパートナーも同様のリスクに直面しており、システムのセキュリティ侵害は当社のセキュリティ体制に悪影響を及ぼす可能性があります。さらに、クラウドテクノロジーの使用が増えると、これらおよびその他の運用上のリスクが高まります。クラウドやその他のテクノロジーサービスプロバイダーがシステムを適切に保護し、サイバー攻撃を防止できない場合、当社の業務が中断され、機密情報や専有情報の不正流用、破損、損失が発生する可能性があります。
事業継続計画を含め、システムとインフラストラクチャの構築と改善を続けていますが、私たちの取り組みがサイバーセキュリティの脅威やシステム内のインシデントなどを防ぐという保証はありません。
インシデントは、当社の事業や運営に重大な悪影響を及ぼしたり、重要または機密情報を失ったりする可能性があります。その結果、当社に重大な財務、法律、運用、評判上の損害が発生したり、競争上の優位性が失われたり、消費者の信頼が失われたりする可能性があります。当社の賠償責任保険は、セキュリティ違反、サイバー攻撃、その他の関連する違反に関連する請求に対する補償には、種類や金額が不十分な場合があります。
世界中の規制当局が新しい規則を検討するにつれて、規制は変化し続けています。たとえば、SECは、公開企業によるサイバーセキュリティリスク管理、戦略、ガバナンス、インシデント報告に関する追加の開示規則を採用しています。ヨーロッパや世界中で検討されているこれらの新しい規制やその他の規制は、私たちの運営方法に影響を与える可能性があります。
規制当局は、プライバシー侵害に対する新たな罰金や罰金など、データプライバシーとセキュリティの新しい要件を課しています。たとえば、EUの一般データ保護規則は、個人データの取り扱いに関する規制を定め、執行権限を定め、違反した場合は多額の罰則を課しています。CCPAなどの新しい米国のデータプライバシーおよびセキュリティ法、および成立する可能性のあるその他の法律でも、同様に個人情報に関する要件が導入されており、CCPAに違反すると、私的訴訟(特定のデータ侵害が発生した場合は法的に定められた損害賠償の対象となります)および執行を通じて責任が生じる可能性があります。これらの現在および将来の法律、方針、業界基準、法的義務に従わなかったり、個人情報への不正アクセス、取得、公開、転送につながるセキュリティ上の問題が生じたりすると、政府の執行措置、訴訟、罰金、罰則、または不利な評判を招き、お客様の信頼を失い、当社の事業と経営成績に重大な悪影響を及ぼす可能性があります。
製造上の問題により、コストが大幅に増加したり、製品の供給が制限されたり、収益が減少したりする可能性があります。
当社の製品の製造プロセスは複雑で規制が厳しく、次のような多くのリスクにさらされています。
•サードパーティやシングルソースプロバイダーへの依存のリスク。私たちは、製品や製品候補の製造プロセスの多くの面で、第三者のサプライヤーやメーカーに頼っています。場合によっては、当社の製品の製造方法が独特なため、原材料と製造資材のシングルソースプロバイダーに頼っています。これらの第三者は、当社の管理外にある独自の事業的、戦略的、財務的リスクの対象となる独立企業です。たとえば、最近発表された開発・製造受託組織の第三者による買収の可能性は、その事業上、戦略上、または財務上のリスクに影響を与える可能性があります。これらの第三者は、適時かつ費用対効果の高い方法で、または適用される規制に従って義務を履行しない場合があり、当社の既存または将来の製品の需要に見合った生産能力を増やすことができない、またはしたくない場合があります。サービスの専門性や、サプライヤーや製造方法に重大な変更があった場合は規制当局の承認を得る必要があるため、代替プロバイダーを見つけるにはかなりの時間がかかり、多額の費用がかかる可能性があります。代替プロバイダーと合意に達できるかどうか、あるいはFDAや他の規制当局がそのような代替品の使用を承認するかどうかは定かではありません。
•グローバルな大量供給リスク。私たちは、高分子製品や製品候補の原薬の製造は、製造施設に頼っています。これらの製品や候補製品の世界的な大量供給は、これらの施設の中断のない効率的な運営にかかっています。設備の故障、労働力や原材料の不足、地政学的な不安定性、公衆衛生上の伝染病、自然災害、停電、サイバー攻撃、その他多くの要因によって悪影響を受ける可能性があります。
•現在のGMP(cGMP)の遵守に関連するリスク。当社と第三者プロバイダーは通常、cGMPやその他の厳しい要件の遵守を維持する必要があり、遵守を確認するためにFDAやその他の規制当局による検査の対象となります。当社の施設や事業または第三者の施設や事業が規制当局の承認を受けられなかったり、規制機関の検査に合格しなかったりした結果として、当社製品の製造、充填仕上げ、包装、保管に遅延、中断、その他の問題が発生すると、製品の開発と商品化の能力が著しく損なわれる可能性があります。重大な違反は、金銭的罰則やその他の民事または刑事上の制裁を科され、当社の評判を損なう可能性もあります。
•製品損失のリスク。当社製品の製造プロセスは、汚染、酸化、機器の故障、機器の不適切な設置や操作、またはベンダーやオペレーターのミスによる製品損失の影響を非常に受けやすいです。通常の製造プロセスからのわずかな逸脱でも、生産量の低下、製品の欠陥、その他の供給の中断につながる可能性があります。当社の製品や製造施設で微生物、ウイルス、その他の汚染が発見された場合、汚染物質の調査と修復のため、製造施設を長期間閉鎖する必要がある場合があります。
当社の製造事業または第三者のサプライヤーや製造業者の事業に影響を及ぼす不利な展開により、出荷の遅延、在庫不足、ロットの不足、製品の撤回またはリコール、またはその他の当社製品の商業的供給の中断が発生する可能性があります。
さらに、地政学的な出来事、世界的な健康問題、気象現象、労働力や原材料の不足、その他のサプライチェーンの混乱などの要因により、製品の製造が困難になったり遅れたりして、当社の業績に悪影響を及ぼしたり、製品が不足したりする可能性があります。また、仕様を満たさない製品や、費用のかかる修復作業を行ったり、より費用のかかる製造代替品を探したりすると、在庫の償却やその他の費用が発生する場合があります。このような開発により、製造コストが増加したり、患者や医師が競合する治療法に頼るにつれて収益や市場シェアが失われたり、収益性が低下したり、評判が損なわれたりする可能性があります。
さらに、製造の中断や遅延の可能性を減らし、混乱を招くような出来事の深刻さを軽減するための事業継続計画がありますが、これらの計画が適切であるという保証はなく、事業や運営に悪影響を及ぼす可能性があります。
経営陣、人事、その他の組織の変更により、当社の事業が混乱する可能性があります。また、経営陣やその他の退職者のために、人員の確保や、資格のある交代要員を適時に確保することが困難な場合があります。
経営陣、その他の人員、および当社の全体的な定着率の変化は、当社の事業に混乱をもたらす可能性があり、そのような混乱は、当社の事業、プログラム、成長、財政状態、または経営成績に悪影響を及ぼす可能性があります。経営陣の新しいメンバーは、私たちのビジネスのプログラムや機会について異なる見方をしているかもしれません。そのため、私たちは新しい機会に集中したり、既存のプログラムを減らしたり、重点を変えたりする可能性があります。
私たちの成功は、競争の激しい環境で、資格のある経営陣やその他の人材を引き付けて維持できるかどうかにかかっています。有能な人材は需要が高く、その人材を引き付けたり維持したりするために多額の費用がかかる可能性があります。経営陣の変更、Reataの買収に関連する統合、1つまたは複数の市販プログラム、前臨床または臨床プログラムの業績不振または中止、競合他社による採用、または労働市場全体の変化など、さまざまな理由で人材の誘致と維持が困難になる可能性があります。さらに、組織構造や柔軟な勤務形態の変化は、従業員の生産性や士気だけでなく、従業員を引き付け、維持し、やる気を引き付ける能力にも影響を与える可能性があります。私たちは、事業に必要な人材を雇用または維持できること、または人員の喪失が当社の財政状態や経営成績に重大な影響を及ぼさないことを保証することはできません。
医療業界に影響する広範な法的および規制上の要件に従わないと、コストや罰金の増加、ビジネスの損失に直面する可能性があります。
当社の活動、および当社の協力者、販売業者、その他の第三者プロバイダーの活動は、米国および外国の法域における広範な政府の規制と監督の対象であり、解釈が変更および進化する可能性があり、コンプライアンスに関連して多額の費用が発生したり、1つまたは複数のビジネス慣行を変更したりする必要があります。FDAと同等の外国機関は、前臨床試験や臨床試験の実施、製品の製造、広告とプロモーション、製品の流通、有害事象の報告、製品リスク管理、グッドプラクティス品質ガイドラインや規制の遵守など、当社の最も重要な事業活動の多くを直接規制しています。当社の製品を処方または購入する医師やその他の医療提供者とのやり取りも、製品の販売や使用における詐欺や悪用を防止し、医療企業のマーケティング慣行に重大な制限を課すための法律や政府規制の対象となります。ヘルスケア企業は、医療提供者との関係について厳しい監視にさらされており、法律や政府規制の違反を申し立てる訴訟や調査の対象となっています。これには、誤った価格情報の提出、医薬品の適応外宣伝、ヘルスケアビジネスの紹介に影響を与えることを目的とした支払い、政府への償還に関する虚偽の請求の提出、独占禁止法違反、環境問題に関連する違反などが含まれます。また、検査、保険料、自己負担支援プログラムや、そのような支援を提供する第三者の慈善団体への寄付など、会社が後援する患者支援プログラムの精査も強化されています。米国政府は、患者支援を提供する第三者の慈善団体への寄付の一部に異議を申し立てています。私たち、私たちのベンダー、寄付先が、これらまたは他の患者支援プログラムの運営において関連する法律、規制、または政府のガイダンスを遵守していないことが判明した場合、多額の罰金または罰則の対象となる可能性があります。当社がグローバル事業を拡大し続け、患者集団の異なる新しい治療分野に参入するにつれて、法律や規制の遵守に関するリスクが高まる可能性があります。これらの分野では、現在利用またはサポートしているものとは異なる製品流通方法、マーケティングプログラム、または患者支援プログラムが存在する可能性があります。
医療業界を統制する条件や規制は変更される可能性があり、遡及的に影響する可能性があります。これには以下が含まれます。
•医療の提供、価格設定やマーケティング慣行、雇用の遵守に関連する新しい法律、規制、司法上の決定、または既存の法律、規制、司法上の決定に対する新しい解釈
慣行、提供方法、ヘルスケア製品およびサービスの支払い、健康情報とデータのプライバシーとセキュリティに関する法律と規制の遵守、医師や教育病院への支払いやその他の価値の移転の追跡と報告、贈収賄防止と腐敗防止の広範な禁止、製品のシリアル化と表示の要件、使用済み製品の回収要件
•新製品の承認を遅らせたり妨げたりして、市場機会の喪失につながる可能性のあるFDAおよび外国の規制当局の承認プロセスまたは見方の変更。
•政府の閉鎖や移転により、審査と承認のプロセスが遅れ、新薬候補の審査や承認に必要な時間が遅くなり、当社の事業に悪影響を及ぼす可能性があります。
•臨床試験結果と品質データの透明性を高めるための要件(EMAの臨床透明性ポリシーなど)は、承認申請に含まれる企業秘密や競争上機密性の高い情報を保護する当社の能力に影響を与えたり、誤解されて評判の低下、誤解や法的措置につながり、当社の事業に悪影響を及ぼす可能性があります。そして
•FDAおよび外国の規制の変更により、当社製品の市場投入後に、追加の安全監視、表示の変更、製品の流通や使用の制限、またはその他の措置が必要となる場合があります。これにより、事業コストが増加したり、承認された製品の将来の許可された使用法に悪影響を及ぼしたり、当社製品の市場に悪影響を及ぼす可能性があります。
政府の規制に違反すると、罰金や民事罰金、メディケアやメディケイドなどの政府プログラムへの参加の除外、および当社の事業を監督する経営幹部に対する刑事上および民事上の制裁の対象となる場合があります。また、政府に提出した価格情報を誤って計算したことが判明した場合、政府の支払者から受け取った金額を返済したり、追加のリベートや利息の支払いを求められることもあります。さらに、法的手続きや調査は本質的に予測がつかず、大規模な判決や和解が起こることもあります。私たちは、当社が事業を展開する管轄区域の法律または規制を遵守するための適切なコンプライアンス管理、方針、手続きが整っていると考えていますが、当社の従業員、代理店、販売業者、協力者、または第三者プロバイダーによる行為が、そのような法律または規制に違反するリスクがあります。法律を遵守しているかどうかにかかわらず、違法行為の疑いに関連する調査または訴訟は、費用を増やし、評判を傷つけ、経営陣の時間と注意をそらし、事業に悪影響を及ぼす可能性があります。
私たちの販売と運営は、国際的に事業を行う際のリスクにさらされています。
私たちは国際市場での存在感を高めており、事業と収益に悪影響を及ぼす可能性のある多くのリスクにさらされています。国際市場での売り上げを拡大するための私たちの努力と戦略が成功する保証はありません。新興市場国は、世界的、地域的な政治、法律、規制、金融が不安定な時期に特に脆弱で、汚職や不正な商慣行の発生率が高くなる可能性があります。特定の国では、グローバルな臨床試験に加えて、医薬品登録プロセスの一環として現地の臨床試験データが必要な場合があります。これにより、医薬品開発と登録の全体的なスケジュールが長くなる可能性があります。また、新興市場で協力したり買収したりした企業が、以前はサードパーティの代理店や販売業者や、なじみのない業務や取り決めへの依存度を高める必要がある場合もあります。
私たちの販売と運営は、国際的にビジネスを行う際のリスクにさらされます。次のようなリスクがあります。
•公衆衛生上の流行が世界経済と医療の提供に与える影響。
•不利な知的財産またはその他の適用法。
•製品の必要な外国規制当局の承認を適時に取得できないこと。
•政府または規制上の要件に起因するものを含め、製品の価格設定、払い戻し、または値上げを受ける当社の能力に対する制限やその他の圧力。
•インフレやサプライチェーンの混乱などの要因による商品コストの上昇。
•中国で製造された材料や中国のCROとの協力など、海外での製造または臨床研究の実施がさらに複雑になります。
•ロシアのウクライナ侵攻と中東での軍事紛争に関連する地政学的な不安定性に関する臨床試験の遅れ。
•私たちの経験が限られている国で、その後の臨床試験や確認のための臨床試験を無事に完了できないこと。
•支払いと償還のサイクルが長く、売掛金の回収可能性に関する不確実性。
•当社の収益、純利益、および特定の投資の価値に悪影響を与える可能性のある外貨為替レートの変動。
•政府による統制の強制。
•多様なデータプライバシーと保護要件。
•国によって大きく異なり、対応する米国の法律や規制と矛盾する可能性のある外国の法律や規制を遵守するための基準がますます複雑になっています。
•2010年の英国贈収賄法などを含む、英国における広範囲にわたる贈収賄防止および腐敗防止法、およびそのような法律に基づく調査と訴追の激化。
•複雑な輸出入管理法の遵守。
•税法の変更、そして
•関税、禁輸措置、その他の貿易制限の賦課。
さらに、当社の国際事業は米国法に基づく規制の対象となります。たとえば、米国のFCPAは、ビジネスを獲得または維持するため、または公的な立場で働く人に有利な待遇を得たり、影響を与えたりする目的で、米国企業とその代表者が外国の政府高官、政府職員、政党、または政治家候補に価値のあるものを支払い、支払いを申し出たり、支払いを約束したり、支払いを約束したり、承認したりすることを禁じています。多くの国で、私たちが定期的に接している医療従事者は、FCPAの外国政府職員の定義を満たす場合があります。国内外の法律に従わないと、製品の承認の遅延または拒否、承認された製品のリコール、差し押さえ、または市場からの撤回、製品の供給または入手の中断、輸出または輸入特権の停止、民事または刑事制裁の賦課、国際事業を監督する役員の起訴、当社の評判の低下など、さまざまな悪影響が生じる可能性があります。米国外での製品販売能力の著しい障害は、当社の事業と財務結果に悪影響を及ぼす可能性があります。さらに、FCPAに準拠するための適切なコンプライアンス管理、ポリシー、手順が整っていると私たちは考えていますが、従業員、代理人、販売業者、協力者、または第三者プロバイダーによる行為がFCPAに違反し、責任を問われるリスクがあります。当社の従業員、代理店、販売業者、協力者、または第三者プロバイダーがそのような行為を行ったことが判明した場合、厳しい罰則が科せられ、その他の責任の対象となる可能性があり、当社の事業、経営成績、および財政状態に悪影響を及ぼす可能性があります。
私たちは大規模な生物製剤製造施設を建設し、遺伝子治療製造施設を建設中です。その結果、多額の投資が発生し、そのような投資が回収される保証はありません。
将来の成長と医薬品開発パイプラインをサポートするために、スイスのゾロトゥルンに大規模な生物製剤製造施設を建設することで高分子の生産能力を拡大しました。追加の生産能力が必要になったり、この投資が回収されたりする保証はありません。
ゾロトゥルン施設はFDAによってLEQEMBIの承認を受けましたが、規制当局がゾロトゥルン施設を他の製品の製造に承認するという保証はありません。
さらに、ノースカロライナ州RTPに新しい遺伝子治療製造施設を建設中ですが、この投資が十分に活用される保証はありません。この遺伝子治療製造施設を十分に活用できない場合、過剰生産能力による費用が発生し、当社の財政状態と経営成績に悪影響を及ぼす可能性があります。
製造施設を十分に活用できなければ、事業に支障をきたす可能性があります。過剰生産能力による請求は引き続き発生する可能性があり、当社の財政状態と経営成績に悪影響を及ぼす可能性があります。
当社の製品の偽造品や不適切なバージョン、または盗品を第三者によって違法に配布および販売すると、当社の評判とビジネスに悪影響を及ぼす可能性があります。
第三者は、当社の厳しい製造、流通、および試験基準を満たしていない当社製品の偽造品または不適切なバージョンを違法に配布および販売する可能性があります。偽造医薬品や不適切な医薬品を受け取った患者は、健康にさまざまな危険な影響を与えるリスクがあります。私たちのブランド名で販売された偽造医薬品や不適切な医薬品が原因で、当社の評判とビジネスが損なわれる可能性があります。倉庫、工場、または輸送中に在庫が盗まれ、その後不適切に保管され、許可されていないチャネルを通じて販売された在庫は、患者の安全、当社の評判、およびビジネスに悪影響を及ぼす可能性があります。
ソーシャルメディアプラットフォームと人工知能ベースのソフトウェアの使用の増加は、新たなリスクと課題を提示しています。
ソーシャルメディアは、当社の製品や、当社の治療法が治療するために設計されている疾患について伝えるために使用されることが増えています。バイオ医薬品業界におけるソーシャルメディアの慣行は進化し続けており、そのような使用に関する規制は必ずしも明確ではなく、不確実性や、当社の事業に適用される規制に違反するリスクを生み出しています。たとえば、患者はソーシャルメディアチャネルを使用して、製品の有効性についてコメントしたり、有害事象の疑いを報告したりすることがあります。このような開示が行われると、適用される有害事象の報告義務を監視および遵守できなくなるリスクがあります。また、ソーシャルメディアから生じる政治的および市場的圧力に直面して、当社の製品について私たちが発言できる内容の制限により、会社や国民の正当な利益を守ることができなくなるリスクがあります。また、機密情報の不適切な開示や、ソーシャルメディアへの当社に関する否定的または不正確な投稿やコメントのリスクもあります。また、ソーシャルメディアで、当社、経営陣、製品候補や製品に関する批判に遭遇することもあります。ソーシャルメディアの即時性により、事実か意見かを問わず、ソーシャルメディアを介して私たちに関してなされた投稿をリアルタイムで管理することができません。否定的な宣伝や、ソーシャルメディアプラットフォームや同様の媒体に当社に関する不利な情報が投稿された場合、当社の評判が損なわれる可能性があります。それを元に戻すことができない場合があります。これらの出来事のいずれかが発生した場合、または適用される規制を遵守しなかった場合、責任を負ったり、制限的な規制措置に直面したり、その他の事業に損害を与えたりする可能性があります。さらに、バイオ医薬品業界では、AIベースのソフトウェアの使用が増えています。AIベースのソフトウェアを使用すると、機密の専有情報が公開され、知的財産の利益を実現する能力に影響を与える可能性があります。
当社の普通株式の保有に関連するリスク
当社の経営成績は大きく変動する可能性があります。
当社の四半期ごとの収益、費用、純利益(損失)は過去に変動してきましたが、これらのリスク要因に記載されているリスクと、当社が負担する可能性のある費用と費用のタイミングにより、将来は大幅に変動する可能性があります。次のような請求を記録した、または記録する必要がある場合があります。
•事業を合理化し、リソースを再配分するためのリストラやその他のイニシアチブの費用。
•研究開発プログラムの終了決定に関連する費用
•投資、固定資産、および知的財産権やその他の無形資産を含む長期資産に関する減損。
•品質仕様を満たさない場合の在庫減額、生産能力超過の料金、超過または古くなった在庫の料金、および製品の一時停止、有効期限、またはリコールに関連する在庫減価償却の手数料。
•条件付対価または当社の株式投資の公正価値の変動。
•不良債権費用と不良債権準備金の増加。
•訴訟およびその他の法的または行政手続の結果、規制事項および税務問題。
•買収、売却、その他の事業開発活動に関連して、またライセンス契約やコラボレーション契約に基づく支払い。
•特定の契約上の約束を果たさないこと。そして
•公衆衛生上の流行が従業員、世界経済、医療の提供に与える影響。
当社の収益と特定の資産と負債も、当社の事業のグローバルな性質により、外貨為替レートの変動の影響を受けます。為替レートの変動による影響を緩和するための私たちの努力は成功しないかもしれません。その結果、報告通貨、米ドル、および当社が事業を行うその他の通貨間の通貨変動は、多くの場合、予測できない方法で当社の業績に影響を与えます。外貨ヘッジ取引に関して請求される可能性のある費用の影響により、当社の純利益も変動する可能性があります。特に、ヘッジ関係の早期終了により、予想よりも高い費用が発生する可能性があります。
ある期間の当社の業績は、必ずしも将来の期間の予想される業績を示唆しているわけではありません。
私たちの不動産への投資は完全には実現しないかもしれません。
私たちは、主に研究所、オフィススペース、製造事業を含む建物で構成される不動産を所有またはリースしています。私たちは、事業運営の特定の側面を統合または共同配置したり、1つ以上の物件を処分したりする場合があります。その中には、空室率が高く不動産価値が下がっている市場にあるものもあります。私たちが所有する物件の公正価値が
帳簿価額よりも低い場合、施設の閉鎖予定により特定の資産の期待耐用年数が短縮された場合、これらの物件への全投資を実現できず、多額の減損費用や追加の減価償却が発生する可能性があります。物件の全部または一部を空けることにした場合、施設の閉鎖費用、従業員の離職および維持費用、リース解約料、サブリース収入を超える家賃費用、借地権の改善による減損、資産の加速減価償却など、多額の費用が発生する可能性があります。これらの出来事はいずれも、当社の経営成績に悪影響を及ぼす可能性があります。
私たちは、私たちにとって有利な条件で資本市場や信用市場にアクセスできないかもしれません。
運転資本、資本支出、債務返済の要件、その他の事業イニシアチブのために、事業から生み出された既存の資金や現金を補うために、資本市場や信用市場へのアクセスを求める場合があります。資本市場と信用市場は、借り手と投資家の両方にとって不確実性と流動性の問題につながる、極端なボラティリティと混乱を経験しており、これまでも経験してきました。市況が不利な場合、有利な条件で資本または信用市場での融資を得ることができず、資金調達コストが大幅に増加する可能性があります。全国的に認められた信用格付け機関が発行した信用格付けの変化も、当社の資金調達コストと有価証券の市場価格に悪影響を及ぼす可能性があります。
私たちの負債は、当社の事業に悪影響を及ぼし、事業の変化に対する計画や対応の能力を制限する可能性があります。
当社の負債は、マイルストーンやロイヤリティの支払い義務を含む当社の重大な偶発債務とともに、当社の事業に重大な影響を及ぼす可能性があります。例えば、そのような義務には次のようなものがあります。
•一般的な不利な経済状況や産業状況に対する私たちの脆弱性を高めます。
•資本市場へのアクセスが制限され、将来的に追加の負債が発生する。
•事業からのキャッシュフローのかなりの部分を負債の支払いに充てることを要求します。これにより、事業開発、研究開発、合併や買収など、他の目的でのキャッシュフローの利用可能性が低くなります。そして
•当社の事業や事業を展開する業界の変化に対する計画や対応における柔軟性が制限されているため、負債の少ない競合他社と比較して不利な立場にあります。
当社の投資ポートフォリオは、市場リスク、金利リスク、信用リスクの影響を受けやすく、その価値が低下する可能性があります。
私たちは、現金の投資や特定のバイオテクノロジー企業の株式への投資のために、有価証券のポートフォリオを維持しています。投資ポートフォリオの価値の変動は、当社の収益に悪影響を及ぼす可能性があります。金利の上昇、ポートフォリオ内の債券やその他の有価証券の格下げ、企業固有のネガティブなニュース、バイオテクノロジー市場のセンチメント、ポートフォリオ内の有価証券の流動性を低下させる世界の金融市場の不安定性、ポートフォリオの有価証券の基礎となる担保の価値の下落、その他の要因により、投資額が下落する可能性があります。これらの各事象により、投資ポートフォリオの帳簿価額を下げたり、買収費用よりも安く投資を売却したりするための費用を記録することがあります。私たちは、投資の分散とポートフォリオ全体のリスクプロファイルの継続的な監視を通じてこれらのリスクを軽減しようとしていますが、それでも投資の価値は低下する可能性があります。
私たちが引き続き株式を買い戻すという保証や、有利な価格で株式を買い戻すという保証はありません。
時々、当社の取締役会は自社株買いのプログラムを承認します。自社株買いの金額と時期は、資本の入手可能性と、自社株買いが株主の最善の利益になり、それぞれの法律と適用される契約をすべて遵守していると当社が判断したことに左右されます。当社が株式を買い戻す能力は、とりわけ、当社の現金残高や戦略的取引のための潜在的な将来の資本要件、経営成績、財務状況、および関連すると考えられる当社の制御が及ばないその他の要因に左右されます。さらに、最近制定されたIRAには、自社株買いにかかる物品税が含まれているため、自社株買いの費用が増加します。当社の自社株買戻しプログラムに基づく買戻しの減少または完了は、当社の株価に悪影響を及ぼす可能性があります。たとえあったとしても、有利な価格で株式を買い戻すという保証はありません。
当社の協力契約の中には、第三者が当社を買収しようとするのを思いとどまらせる可能性のある統制条項の変更が含まれているものがあります。
私たちのコラボレーション契約の中には、買収者が喜んで支払う可能性のある買収価格を下げたり、株主にとって有益と見なされる可能性のある買収の試みを阻止したりする可能性のある統制条項の変更が含まれています。支配権が変更されると、これらの条項の一部がマイルストーン、利益、またはロイヤリティの減額につながる可能性があります
当社への支払い、またはコラボレーションパートナーに、コラボレーション契約の解除、運営管理の取得、またはコラボレーションの対象となるプログラムの購入または販売の強制を行う権利を与えてください。
一般的なリスク要因
当社の実効税率は変動し、未払額を超える債務を税務管轄区域で負担する可能性があります。
グローバルなバイオ医薬品企業として、私たちは多くの国、州、その他の法域で課税の対象となっています。その結果、当社の実効税率は、事業を展開するさまざまな場所で適用される源泉徴収税を含む税率の組み合わせから導き出されます。財務諸表を作成する際、それぞれの場所で支払うべき税額を見積もります。当社の実効税率は、国ごとの収益性構成の変化、税務申告の審査と監査の結果、不確実な税務ポジションの価値の調整、税務当局またはその他の管轄機関による解釈、税務事件の結果、所得税の会計処理上の変更、税法および規制の変更など、多くの要因により、過去または現在の予想とは異なる場合があります。または遡及的に、そしてReata統合の影響。
特に、税務当局との受け入れ可能な取り決めを確保または維持できないことや、税法の将来の変更などにより、財務諸表に計上された金額を超える納税義務が発生する可能性があります。
私たちが事業を展開している国の税務当局や経済圏が、OECDの「税源浸食と利益移転」に関するプロジェクトで定められた、または今後発表される可能性のある勧告の一部または全部を制定すると、当社の実効税率に悪影響を及ぼす可能性があります。これらのイニシアチブは、世界の企業利益に対する課税資格と世界の最低税率に関する共通の国際原則に焦点を当てています。多くの国が、2024年1月1日に発効するOECD Globeモデル規則の実施を目的とした法律を制定しているか、制定中です。会社への影響は、実施の時期、各国のGloBe法、ガイダンス、規制の正確な性質、および税務当局による将来的または遡及的な適用によって異なります。
私たちのビジネスには、コンプライアンスのコストや汚染や怪我のリスクなど、環境リスクが伴います。
当社の事業およびいくつかの戦略的パートナーの事業には、危険物、化学物質、生物製剤、放射性化合物の管理された使用が含まれており、規則や解釈の変化や進化の影響を受けやすく、コンプライアンスに関連して多額の費用が発生したり、1つ以上の事業慣行を変更したりする必要があります。このような材料の取り扱いと廃棄に関する当社の安全手順は、州、連邦、および外国の基準に準拠していると考えていますが、偶発的な汚染や怪我のリスクは常にあります。事故の責任を問われたり、施設の閉鎖が長期化したりした場合、事業に害を及ぼす可能性のある多額の費用、損害、罰則が発生する可能性があります。当社の製品や製品候補品の製造には、給水および廃水排出に関する政府機関からの許可も必要です。十分な量の上下水道に関する許可を含め、適切な許可を得なければ、多額のコストや製造量の制限が発生し、事業に悪影響を及ぼす可能性があります。さらに、規制当局は新しい環境開示規則を可決しました。たとえば、SEC、EU、カリフォルニア州は、一般的に追加の開示を必要とする新しい気候情報開示規則を実施しました。さらに、他の規制当局も環境開示規則を検討しています。これらの新しい規則をまとめると、気候関連のリスクと排出量の開示に関する追加の開示要件が課されます。温室効果ガス排出と気候関連の金融リスクに関する広範な報告義務を課すこれらの新しい法律の対象になると予想しています。最近制定され提案されているこれらの規制では、コンプライアンスや開示の費用が発生する可能性があり、経営陣のかなりの注意が必要になる可能性があります。
アイテム 2.株式の未登録売却と収益の使用
発行者による株式の購入
次の表は、2024年の第1四半期における2020年の自社株買戻しプログラムに基づく当社の普通株式の買戻し活動をまとめたものです。
| | | | | | | | | | | | | | | | | | | | | | | | | | |
| ピリオド | | の合計数
株式の購入
(#) | | 平均価格
一株当たりの支払額
($) | | の合計数
株式の購入
パブリックの一環として
発表されたプログラム
(#) | | おおよそのドル価値
まだ購入できる可能性のある株式の
私たちのプログラム
(百万ドル) |
| 2024年1月 | | — | | | $ | — | | | — | | | $ | 2,050.0です | |
| 2024年2月 | | — | | | $ | — | | | — | | | $ | 2,050.0です | |
| 2024年3月 | | — | | | $ | — | | | — | | | $ | 2,050.0です | |
合計 (1) | | — | | | $ | — | | | | | |
(1) 2024年の第1四半期には、自社株買いはありませんでした。
2020年10月、当社の取締役会は、最大50億ドルの普通株式を買い戻すプログラムである2020年の自社株買戻しプログラムを承認しました。2020年の自社株買戻しプログラムには有効期限はありません。2020年の自社株買戻しプログラムに基づくすべての自社株買いは廃止されます。2024年3月31日および2023年3月31日に終了した3か月間、当社の普通株式の自社株買いはありませんでした。2024年3月31日現在、2020年の自社株買戻しプログラムでは約21億ドルが残っています。
アイテム 5.その他の情報
取引アレンジメント
あった いいえ または締結された当社の有価証券の購入または売却のための取引契約 終了しました 2024年の第1四半期に当社の取締役または役員によって。
アイテム 6.展示品
以下の展示品は、フォーム10-Qのこの四半期報告書の一部として提出または提供されています。
展示品索引
| | | | | | | | |
示す 番号 | | 展示品の説明 |
| 31.1+ | | 2002年のサーベンス・オクスリー法第302条に基づく最高経営責任者の認定。 |
| | |
| 31.2+ | | 2002年のサーベンス・オクスリー法第302条に基づく最高財務責任者の認定。 |
| | |
| 32.1++ | | 2002年のサーベンス・オクスリー法の第906条に基づく認証。 |
| | |
| 101++ | | iXBRL(インライン拡張ビジネス報告言語)でフォーマットされた、バイオジェン社の2024年3月31日に終了した四半期のフォーム10-Q四半期報告書からの次の資料:(i)要約連結損益計算書、(ii)包括利益の要約計算書、(iii)要約連結貸借対照表、(iv)要約連結キャッシュフロー計算書、(v)要約連結計算書株式と(vi)要約連結財務諸表の注記です。 |
| | |
| 104++ | | 2024年3月31日に終了した四半期のフォーム10-Qのこの四半期報告書の表紙は、インラインXBRLでフォーマットされています。 |
+ ここに提出してください
++ ここに付属しています
署名
1934年の証券取引法の要件に従い、登録者は署名者に代わってこの報告書に正式に署名させ、正式に権限を与えられました。
| | |
|
| バイオジェン株式会社 |
|
| /s/ マイケル・R・マクドネル |
| マイケル・R・マクドネル |
|
| 最高財務責任者 |
| (最高財務責任者) |
2024年4月24日