アメリカです
証券取引委員会
ワシントン20549
表
あるいは…。
本財政年度末まで
あるいは…。
あるいは…。
依頼文書番号:
(登録者の正確な氏名はその定款に定められている)
登録者名英語訳:適用されない
状態:
(会社または組織の管轄権)
電話:
(主に実行オフィスアドレス )
電話番号:+972.4.6230333
(会社の連絡先の名前、電話、電子メールおよび/またはファックス番号および住所)
この法第12(B)節に基づいて登録または登録される証券:
| クラスごとのタイトル | 取引コード | に登録されている各取引所の名称 | ||
|
|
この法第12(G)節に基づく登録又は登録された証券:なし
同法第15(D)条により報告義務を有する証券:なし
年次報告に記載されている期間終了までの発行者の1種類当たりの資本または普通株の流通株数:
登録者が証券法規則405で定義されている経験豊富な発行者である場合は、再選択マークで示してください。
はい、そうです☐
この報告が年次報告または移行報告である場合、 は、登録者が1934年の取引法第13条または15(D)条に従って報告を提出する必要がないかどうかを再選択マークで示してください。
はい、そうです☐
再選択マークは、登録者 (1)が過去12ヶ月以内(または登録者がそのような報告を提出する必要があるより短い期間)に1934年の取引法第13または15(D)節に提出されたすべての報告書を提出したかどうか、および(2)過去90日以内にそのような提出要件に適合しているかどうかを示す。
はい、そうです☐
登録者 が過去12ヶ月以内(または登録者がそのような文書の提出を要求されたより短い時間)にS−T法規(本章232.405節)規則405に従って提出されることを要求したすべての対話データファイルが、再選択マークで示されている。
登録者 が大型加速ファイルサーバ,加速ファイルサーバ,非加速ファイルサーバであるか新興成長型会社であるかをチェックマークで示す.取引法第12 b-2条の規則における“大型加速申請者”、“加速申請者”、“新興成長型会社”の定義を参照されたい。
| 大型加速ファイルサーバ | ☐ | ファイルマネージャを加速する | ☐ | |
| ☒ | 新興成長型会社 |
もしある新興成長型会社が米国公認会計原則に従ってその財務諸表を作成する場合、登録者が延長された過渡期間
を使用しないことを選択したかどうかを示すマークをつけて、“取引所法案”第13(A)節に提供された任意の新しいまたは改正された財務会計基準を遵守する
イ用語“新たまたは改正された財務会計基準”とは、財務会計基準委員会が2012年4月5日以降にその会計基準まとめを発表した任意の更新を意味する。
登録者 が報告書を提出したか否かを再選択マークで示し、その経営陣が“サバンズ−オキシリー法案”(“米国法典”第15編7262(B)節)第404(B)条に基づいてその財務報告の内部統制の有効性の評価を行うことを証明し、この報告は、その監査報告を作成又は発表する公認会計士事務所によって行われる。
はい、そうです☐
No
証券がこの法(Br)12(B)節に基づいて登録されている場合は、届出文書に含まれる登録者の財務諸表が以前に発表された財務諸表の誤りを反映して訂正されたか否かをチェックマークで示してください
これらのエラー のより真ん中に再記載が必要であるかどうかをチェックマークで示すことは、登録者の任意の幹部が関連回復中に受信したインセンティブベースの報酬を§240.10 D−1(B)に従って回復分析する必要がある☐
登録者がどのような会計基盤を用いて本文書に含まれる財務諸表を作成したかをチェックマークで示す。
国際会計基準理事会が発表した国際財務報告基準☐
他にも☐
前の質問に回答する際に“その他”をチェックした場合は、登録者が従う財務諸表項目をチェック番号で表示してください。
☐ 第17項☐プロジェクト18
もしこれが年次報告であれば、登録者が空殻会社であるかどうかをチェックしてください。
はい、そうです☐
No
カタログ表:
| ページ | ||
| 序言:序言 | 三、三、 | |
| 前向き陳述に関する警告的説明 | v | |
| リスクファクターの概要 | 第七章 | |
| 第 部分I | ||
| 第1項。 | 役員·上級管理職·コンサルタントの身分 | 1 |
| 第二項です。 | 見積もり 統計データと予想スケジュール | 1 |
| 第三項です。 | 鍵 情報 | 1 |
| A. | [保留されている] | 1 |
| B. | 資本化と負債。 | 1 |
| C. | 報酬の提供と使用の原因 | 1 |
| D. | リスク要因 | 1 |
| 第四項です。 | 会社に関する情報 | 41 |
| A. | 会社の歴史と発展 | 41 |
| B. | 業務 の概要 | 42 |
| C. | 組織構造 | 74 |
| D. | 財産と工場と設備 | 74 |
| プロジェクト4 Aです。 | 未解決 従業員意見 | 74 |
| 五番目です。 | 運営と財務回顧と展望 | 74 |
| A. | 経営実績 | 74 |
| B. | 流動性 と資本資源 | 80 |
| C. | 研究開発、特許、ライセンスなど。 | 81 |
| D. | トレンド 情報 | 81 |
| E. | キー会計試算 | 81 |
| 第六項です。 | 役員、役員、上級管理職、従業員。 | 82 |
| A. | 役員と上級管理職です。 | 82 |
| B. | 補償します。 | 86 |
| C. | 取締役会 実践 | 87 |
| D. | 従業員 | 99 |
| E. | 所有権を共有する | 100 |
| F | 開示登録者が誤って判断した賠償を取り戻す行動 | 101 |
| 第七項。 | 主要株主と関係者の取引 | 101 |
| A. | 大株主 | 101 |
| B. | 関連する 側取引 | 102 |
| C. | 専門家と弁護士の興味 | 103 |
| 第八項です。 | 財務情報 | 103 |
| A. | レポートおよびその他の財務情報 | 103 |
| B. | 重大な変化 | 105 |
| 第九項です。 | 割引と発売 | 105 |
| A. | 割引 とリスト詳細 | 105 |
| B. | 流通計画 | 105 |
| C. | 市場 | 105 |
| D. | 売却株主 | 105 |
| E. | 薄めにする | 105 |
| F. | 発行費用 | 105 |
| 第10項。 | その他 情報 | 105 |
| A. | 株式資本 | 105 |
| B. | 覚書と会社規約 | 105 |
| C. | 材料 契約 | 106 |
| D. | Exchange 制御 | 106 |
| E. | 税収 | 106 |
| F. | 配当 と支払いエージェント | 113 |
| G. | 専門家発言 | 113 |
| H. | 展示されている文書 | 114 |
| I. | 子会社 情報 | 114 |
| J. | 証券保有者への年次報告 | 114 |
i
| 第十一項。 | 市場リスクの定量的·定性的開示について | 114 |
| 第十二項。 | 株式証券を除く他の証券説明 | 115 |
| A. | 債務証券 | 115 |
| B. | 株式証書及び権利を承認する | 115 |
| C. | その他の証券 | 115 |
| 第 第2部分 | ||
| 十三項。 | 違約、延滞配当金、延滞配当金 | 116 |
| 14項です。 | 所有者を担保する権利と収益の使用を実質的に改正する | 116 |
| 第十五項。 | 制御とプログラム | 116 |
| 第十六項。 | [保留されている] | 117 |
| プロジェクト16 A。 | 監査委員会財務専門家 | 117 |
| プロジェクト16 B。 | 道徳的準則 | 117 |
| プロジェクト16 Cです。 | チーフ会計士 費用とサービス | 117 |
| プロジェクト16 Dです。 | 免除監査委員会の上場基準 | 118 |
| プロジェクト16 E。 | 発行者と関連購入者持分証券 | 118 |
| プロジェクト16 Fです。 | 登録者の認証会計士 を変更する | 118 |
| プロジェクト16 Gです。 | 会社の管理 | 118 |
| 16 H項です。 | 炭鉱安全情報開示 | 121 |
第 項16 i |
検査阻止に関する外国司法管区の情報開示 | 121 |
第 項16 J |
インサイダー取引政策 | 121 |
第 項16 K |
ネットワーク·セキュリティ | 121 |
| 第 第3部分 | ||
| 17項です。 | 財務諸表 | 122 |
| 第十八項。 | 財務諸表 | 122 |
| プロジェクト19. | 展示品 | 122 |
| サイン | 123 | |
II

Inspira Technologies Oxy B.H.N.Ltd
序言:序言
著者らは専門医療設備会社であり、独自の生命支持技術の研究、開発、製造とマーケティング に従事し、伝統的な機械呼吸器或いは機械換気の代わりに、後者は現在急性呼吸不全を治療する標準看護 である。機械換気は時々生命を救うことができるが、それはリスク、看護コストを増加し、入院時間を延長し、感染が頻繁に発生し、呼吸器依存と死亡率を増加させる。我々の最先端の生命支持技術を用いて、著者らの目標は新しい看護標準を確立し、急性呼吸不全患者に自発呼吸を維持する機会を提供し、挿管、昏睡と機械換気の使用に関連する各種のリスクを避けることである。我々がこの目標を達成するための戦略の一部として,規制承認を求めるとともに,戦略パートナー,世界ランキングの病院,医療機器会社,流通業者と積極的に連携して を構築し,承認と早期臨床採用 を得ている。われわれは集中治療室(ICU),一般医療ユニット,手術室,小型都市·農村病院に目標を合わせる予定であり,世界の数百万人の患者がわれわれの解決策を獲得しやすいようにすることを目標としている。私たちはこれらの活動が市場浸透を実現し、私たちの生命支援技術を採用するために、私たちの戦略計画を支持すると予想している。
私たちは以下の製品を開発しています:
“Inspira”TM 芸術(2代目)
INSPIRA ART装置(増強呼吸技術)(INSPIRA ART 500,ARTシステムあるいはARTとも呼ばれる)であり,ここではINSPIRA ART,INSPIRA ART(Gen 2),INSPIRA ART装置あるいはINSPIRA ARTシステムと記述し,我々のフラッグシップ製品であり,直接血液酸素化を利用して患者の覚醒と自発呼吸の数分以内に患者の飽和度レベルを向上させることを目的としている。その設計目的は,患者の血液パラメータを連続的にリアルタイムで測定し,必要な酸素量を直接血液中に輸送し,適応的な血液酸素化を行うことである。我々の製品の目標は,機械的換気を必要とせずに患者を治療することであり,関連するレガシーリスク,合併症,高コストを減少させる可能性があり,ICU内外でより多くの患者を治療する可能性がある。INSPIRA ARTは,急性呼吸不全を有する成人患者にbr補助体外循環と生理的ガス交換(酸素と二酸化炭素除去) を提供し,覚醒時の治療を可能にするための長期(6時間を超える)生命支援の新しい用途として設計されている。INSPIRA ARTは侵襲的人工呼吸の需要を潜在的に防止することを目的としており,ICUと一般医療機関の急性呼吸不全患者を目指している。画期的なINSPIRA ARTはまだ開発中であり,人体ではまだテストや使用が行われておらず,発売前の承認申請やデノボ監督管理(Br)経路を介して米国食品·薬物管理局(FDA)に提出されて規制承認を行う予定である。
“Inspira”TM ART 100(初代)
INSPIRA ART 100デバイス(以前はAlice、LibyまたはECLSシステムと呼ばれていた)は、ここではINSPIRA ART 100(Gen 1)、INSPIRA ART 100またはINSPIRA ART 100デバイスとして記述されており、医療業界ではより多くの体外循環システムまたはCPBと呼ばれ、体外循環6時間以上を必要とする外科手術において設計されている。INSPIRA ART 100設備は2023年9月にFDAに提出され510 K承認されており,2024年上半期に対応する予定である。INSPIRA ART 100は 設計の新世代CPBシステムであり、医療設備設計の潜在的な優勢を持ち、人体工学に符合する配置と直感的なユーザを中心としたソフトウェアとディスプレイを持って機能を増加させ、そして新しいカラー図形表示を持つ大きなタッチパネル は医療従事者に表示するデータの可視性と機能を高めることができる。INSPIRA ART 100機器の設計コンセプトは,軽量で耐久性が高く,長い電池寿命を搭載し,携帯性を最大限に向上させることである。INSPIRA ART 100デバイスはCPBとして設計されており,体外循環6時間以上を要する外科手術に応用されている。この装置 は多機能として設計されており、この分野で市場参加者をリードして生産されたいくつかの使い捨てデバイスと協働して使用することができる。
三、三、
“Hyla”TM血液センサー
Hyla血液センサは本稿ではHylaまたはHyla血液センサとして記述されており,最初はInspira ART(Gen 2)の鍵とコア技術として設計されており,その第1の変種(Hyla 1)はInspira ART 100と互換性があり,計画も独立した装置であり,体外プログラムに統合または される。Hylaは非侵襲的光学血液センサであり、リアルタイムと連続的な血液測定を実行し、潜在的に医師患者の臨床状況の変化を注意することを目的としている。Hyla血液センサはクリップセンサーとして設計されており,血管の外壁に付着しており,リスク,合併症,コストを潜在的に低下させる可能性がある。Hyla血液センサーは広範な応用潜在力を持っている可能性があり、体外循環手術、体外膜酸素化或いはECMOと体外循環などの手術を受けている患者に利益を得させ、現在まだ監督部門の許可を待たなければならない。
我々の目標は,患者看護の各分野に新たな看護基準を設定することである。私たちがこれらの目標を達成するための戦略の一部として、規制承認を求めるとともに、戦略パートナーや世界ランキングの健康センターと協力し、私たちの製品や技術の地域展開を認め、臨床採用を提供するために積極的に努力しています。ICU,一般医療機関,運営中の劇場,小型都市·農村病院にターゲットを合わせる予定であり,数百万人の患者が我々の解決策を得やすいようにすることを目標としている。
私たちはイスラエルの会社で、イスラエルのラアナナに本社を置き、2018年にイスラエルに登録設立され、名前はClearx Medical Ltd.です。2018年4月10日、私たちの名前はInSense Medical Ltd.,2020年7月30日、私たちの名前は現在の名前に変更され、Inspira Technologies Oxy B.H.N.Ltd. 私たちの主な実行オフィスはイスラエルのラアナナ市2 Ha-Tidhar St.,Ra‘anana,4366504に位置しています。私たちのイスラエルでの電話番号は九七二九九六六四八八です。私たちのサイトの住所はWwws.spirira-Technologies.comそれは.本年度報告に含まれる情報や我々のサイトを介してアクセス可能な情報は本年度報告にはない。本年度報告では,我々のサイトアドレスのみを不活発なテキストとして参照している.
四
前向き陳述に関する警告的説明
本年度報告でForm 20-Fの形態で含まれるまたは引用されたいくつかの情報は、“1995年個人証券訴訟改革法”および他の連邦証券法の“br”の意味に適合する“前向き陳述”とみなされる可能性がある。前向き表現の特徴は、一般に、“可能”、“将”、“予想”、“予想”、“推定”、“継続”、“信じ”、“予測”、“すべき”、“意図”、“br}”“項目”または他の同様の言葉のような前向き用語を使用することであるが、これはこれらの表現を識別する唯一の方法ではない。
これらの前向きな陳述は、経営結果または財務状況、予想される資本需要および費用の予測に関する陳述、我々の製品の研究、開発、完了および使用に関連する陳述、ならびに私たちの意図、予想、計画、信じまたは予想、または将来に発生する可能性のある活動、イベントまたは発展に関するすべての陳述(歴史的事実陳述を除く)を含むが、我々の目標、計画、および戦略に関する陳述を含むことができるが、これらに限定されない。
前向き陳述 は将来の業績の保証ではなく,リスクや不確実性の影響を受ける可能性がある。私たちは、経営陣が彼らの経験と、彼らの歴史的傾向、現在の状況、予想される未来の発展、および彼らが適切だと思う他の要素に対する見方に基づいて行ったbrの仮説と評価に基づいている。
これらの前向きな陳述において予想されるものとは大きく異なる重要な要素は、実際の結果、発展および業務決定をもたらす可能性があるが、これらに限定されない
| ● | 私たちが計画している収入レベルと資本支出は |
| ● | 私たちは現金で追加資金を得ることができます |
| ● | 私たちが製品をマーケティングし販売する能力は |
| ● | 私たちは既存の現金と現金等価物が私たちの現在の業務に資金を提供するのに十分であるかどうかを期待している |
| ● | 私たちの製品と未来の潜在的な製品候補製品の開発を推進する能力は |
| ● | 私たちの製品と未来の潜在的候補製品と、私たちの製品または任意の他の未来の潜在候補製品の将来の販売状況を商業化する能力 |
| ● | 私たちの製品と将来の治療のいくつかの適応の潜在的候補製品の潜在的な評価 |
| ● | 私たちが計画している資本支出水準と流動性 |
| ● | 私たちは研究開発に投資して新製品のための技術を開発する予定です |
| ● | 私たちはサプライヤー、製造業者、流通業者、および他のパートナーと関係を維持する能力 |
| ● | FDA、州規制機関(ある場合)または他の外国規制機関のような予想される行動は、臨床試験の承認、これらの試験の時間および範囲、および私たちの製品またはサービスに対する規制許可または許可または他の規制行動の将来性を含む |
| ● | 医療機器業界の法規や立法変化に影響を与える可能性のある影響を含む、業務を展開する国·地域の規制環境と衛生政策や制度の変化を含む |
v
| ● | 私たちは製品の商業供給と未来の候補製品に対する私たちの期待を満たすことができます |
| ● | 私たちは重要なポストを維持する能力 |
| ● | 私たちの内部では新しい発明と知的財産権の能力を開発しています |
| ● | 世界経済の大きな環境は |
| ● | 競争と新技術の影響 |
| ● | サイバーセキュリティ事件が私たちの業務と運営に及ぼす可能性のある影響 |
| ● | 我々が事業を展開している国の一般市場、政治、経済状況には、イスラエルや中東の他の地域で最も近い動乱や実際または潜在的な武力衝突に関する状況が含まれている。 |
| ● | 競争と新技術の影響 |
| ● | 私たちの内部では新しい発明と知的財産権の能力を開発しています |
| ● | 私たちの戦略を変え |
| ● | 訴訟を起こす |
読者は、本年度報告でForm 20-F形式で開示された様々な情報を慎重に検討し、考慮してください。これらの情報は、関心のある当事者に、私たちの業務、財務状況、運営結果、および将来性に影響を与える可能性のあるリスクおよび要因に関する情報を提供することを目的としています。
あなたはどんな展望的な陳述にも過度に依存してはいけない。本年度報告におけるForm 20−Fに関するいかなる前向き陳述も本報告の日から行われており,我々は法律が別途要求されない限り,新たな情報,未来のbr}イベント,その他の理由でも,いかなる前向き陳述も公開更新または修正する義務はない。
また,本年度報告表格20−Fでは“第4項.会社に関する情報”とタイトルされた部分には,独立した 業界ソースと我々が独立して確認していない他のソースから得られた情報が含まれている.
別の説明がない限り、“会社”、“私たち”、“私たち”および“Inspira”に言及するすべてはInspira Technologies Oxy B.H.N.Ltd.を指す。“ドル”、“ドル”、“$”とはアメリカ合衆国の通貨 を意味し、豪ドルとはオーストラリアドルを指し、“NIS”とは新イスラエルシェケルを意味する。
2023年12月31日までの年度から、国際会計基準委員会(IASB)によって発表された国際財務報告基準(IFRS)に基づいて、私たちの財務諸表を作成して報告することから、米国公認の会計原則または米国GAAPに基づいて私たちの財務諸表を作成して報告することに移行し、これは、私たちの財務結果が結果と異なること、あるいはIFRSによって作成された財務諸表の比較可能性に影響を与える可能性がある。
上述したにもかかわらず、我々は、米国公認会計基準に従ってこのような財務諸表を列記するために、IFRSに従って作成され、本報告書に含まれる歴史的財務諸表 を遡及的に変換した。
本テーブル20-Fで言及されているすべての 商標または商品名は,それぞれの所有者の財産である.便宜上、本20-F表年次報告書で言及されている商標および商品名は、記号および記号を付与されていないが、このような言及は、それらのそれぞれの所有者が、適用法に従ってその権利を最大限に主張するいかなる指示も解釈すべきではない。 私たちは、任意の他社との関係または裏書き または私たちのスポンサーを示唆するために、他の会社の商標および商品名を使用または展示することを意図していない。
この テーブル20-Fには,我々が開発している様々な製品の様々な記述やイラストが含まれている.これらのイラストは私たちの製品の現在の予想設計を表していて、変更されるかもしれません。
VI
リスク要因をまとめる
以下に紹介するリスク要因は,在米投資に関する主要なリスク要因の概要である。これらは私たちが直面している唯一の危険ではない。あなたはこのようなリスク要因と3 D項目に列挙されたリスク要素をよく考慮しなければならない。本年度報告書(Form 20−F)及び我々が米国証券取引委員会に提出した他の報告書及び文書。
| ● | 私たちが2023年12月31日までの年次財務諸表には説明段落が含まれており、私たちが経営を続ける能力があるかどうかを示しています。このような持続的な経営の意見は、合理的な条項や新たな融資を得ることができず、継続的な経営を続ける企業としての私たちの運営能力を危うくする可能性がある |
| ● | 私たちの証券の市場価格は大きく変動する可能性があります。あなたが支払った価格以上であなたの証券を転売することができないかもしれません |
| ● | 私たちの主要株主、上級管理者、取締役は現在実益が私たちの約23.6%の証券を持っているので、私たちの株主に提出された承認事項を制御できるかもしれません |
| ● | 我々の運営歴史は限られており,設立以来重大な運営損失が発生しており,予見可能な未来には損失が続くと予想される。 |
| ● | 私たちは製品販売から何の収入も得ていないし、永遠に利益を上げないかもしれない。 |
| ● | 私たちは受け入れ可能な条項で獲得できないかもしれない、あるいは全く得られないかもしれない大量の追加資金を集める必要があるだろう。受け入れ可能な条項とbrに基づいて資金を得ることができない場合、私たちは私たちの製品開発作業や他の操作を削減、延期、または停止する必要があるかもしれない |
| ● | 追加資本を募集することは、既存の株主の希釈を招き、既存の株主の権利に悪影響を及ぼす可能性がある |
| ● | 私たちは私たちの製品の成功的な開発、マーケティング、販売、そして必要な規制の承認を得ることに強く依存しています |
| ● | 私たちの成功は私たちの製品に対する市場の受け入れの程度、私たちが新製品を開発して商業化し、収入を創出する能力と、私たちの技術のために新しい市場を探す能力にかかっている |
| ● | 医療機器開発はコストが高く、持続的な技術変革に関連しており、これは私たちの現在または未来の製品を時代遅れにするかもしれない |
| ● | 私たちの顧客獲得戦略は成功できないかもしれません |
| ● | 我々は第三者サービスプロバイダ に依存する.もしこのような第三者サービスプロバイダが質の高いサービスを維持できなければ、私たちの製品の実用性は損なわれる可能性があり、これは私たちの製品の浸透率、私たちの業務、経営業績、名声に悪影響を及ぼす可能性があります |
| ● | 私たちは通貨レートの変動の影響を受けることが予想され、これは私たちの経営業績に悪影響を及ぼす可能性がある |
| ● | 私たちは少量の従業員と重要なコンサルタントを通じて私たちの業務を管理しています |
| ● | 私たちは私たちの組織を拡張する必要があるかもしれません。私たちは必要な追加従業員やコンサルタントを募集することで困難に直面するかもしれません |
| ● | 私たちの業務の国際拡張は、アメリカやイスラエル以外での業務展開に関連するビジネス、規制、政治、運営、金融、経済リスクに直面しています |
| ● | もし第三者支払者が私たちの製品やサービスまたは任意の未来の候補製品を使用するために十分な保険と精算を提供しなければ、私たちの収入は負の影響を受けるだろう |
第七章
| ● | 私たちの候補製品と運営はアメリカと海外で広範な政府の監督と監督を受けています。もし私たちが適用されたbrの要求を守らなければ、私たちの業務を損なうかもしれません |
| ● | 私たちは、私たちの製品の必要な許可や承認を受けることを受け入れていないか、または遅延している可能性があります。もし私たちの製品が適時に必要な許可や承認を得ることができなければ、私たちの業務成長能力に悪影響を与えます |
| ● | 上場後の監督管理要求を守らなかった場合、私たちは巨額の処罰を含む法執行行動を受ける可能性があり、市場から製品をリコールするか、あるいは市場から製品をリコールすることを要求する可能性があります |
| ● | 私たちの製品は、brの不良医療事件を引き起こすか、またはFDAに報告する必要がある故障または故障を引き起こす可能性があり、そうしなければ、私たちは私たちの名声、業務、財務状況、および運営結果を損なう可能性のある制裁を受けるだろう。もし私たちの製品に深刻な安全問題があることが発見された場合、あるいはFDAや他の政府機関の指示の下で私たちの製品をリコールすることは、私たちにマイナスの影響を与える可能性があります |
| ● | 医療立法と規制改革措置は私たちの業務と運営結果に実質的な悪影響を及ぼす可能性がある |
| ● | 米国やEUの立法や規制改革は、私たちの製品を規制許可または承認を得ることや、承認または承認を得た後に私たちの製品を製造、マーケティング、または流通させることができ、より困難でコストが高くなる可能性がある |
| ● | もし私たちが私たちの製品とサービスの有効な特許権を獲得して保持できなければ、私たちは私たちの市場で効果的に競争できないかもしれません。もし私たちが私たちの商業秘密やノウハウの機密性を保護できない場合、これらの固有情報は他の人によって私たちと競争するために使用されるかもしれない |
| ● | 私たちは連邦と州の医療詐欺と乱用法律、虚偽申告法、および医療情報プライバシーと安全法律の制約を直接または間接的に受ける可能性があります。もし私たちがこれらの法律を完全に遵守できないか、完全に遵守できなければ、私たちは重大な処罰に直面する可能性があります |
| ● | 私たちの業務と運営は、任意のネットワークセキュリティ事件を含むセキュリティホールの悪影響を受ける可能性があります |
| ● | 我々の本部、管理チームのメンバー、研究開発施設があるイスラエル国民には潜在的な政治、経済、軍事的不安定が存在し、これは私たちの行動結果に悪影響を及ぼす可能性がある。 |
VIII
第1部
項目1.役員、上級管理者、コンサルタントの身分
適用されません。
第二項です見積もり 統計データと予想スケジュール
適用されません。
プロジェクト3.重要な情報
A.
[保留されている]
| B. | 資本化と負債化。 |
適用されません。
| C. | 要約原因と収益用途 |
適用されません。
| D. | リスク要因 |
以下に説明するリスクと不確実性、および本20-F表の年次報告書の他のすべての情報を慎重に考慮しなければなりません。これらのリスクのいずれかが実際に発生すれば、私たちの業務や財務状況が影響を受ける可能性があり、私たちの証券の価格は低下する可能性がある。
私たちのビジネスや産業に関するリスクは
私たちは私たちの製品の成功的な開発、マーケティング、販売に高度に依存し、必要な規制承認を得る。
私たちの製品は呼吸不全の治療に集中していて、私たちの業務の基礎です。したがって、私たちの業務計画の成功は、私たちのbrが製品を開発、製造、商業化する能力に大きく依存しており、それができなければ、私たちの業務に失敗する可能性があります。医療機器の成功商業化は複雑かつ不確定な過程であり、管理層、メーカー、現地事業者、集積業者、医療専門家、第三者支払人及びその他の要素の努力に依存する。私たちの製品開発と商業化に悪影響を及ぼすいかなる要素も、私たちの業務、財務状況、運営結果、将来性にマイナス影響を与えるだろう。製品の商業化における私たちの経験は限られており、商業化努力の面で、私たちはいくつかの挑戦に直面しているかもしれません
| ● | 私たちは私たちの製品の開発を達成するのに十分な資金や他の資源がないかもしれない |
| ● | 私たちは商業数量、十分な品質、あるいは許容可能なコストで私たちの製品を生産することができないかもしれない |
| ● | 十分な販売、マーケティング、流通ルートを作ることができないかもしれません |
1
| ● | 医療専門家や患者は私たちの製品を受け入れないかもしれません |
| ● | 私たちは私たちの製品を実際に使用する上での臨床経験が限られているので、私たちの製品を使用し続けることができる合併症を知らないかもしれない |
| ● | 私たちは既存の呼吸不全解決策と競争できないかもしれません |
| ● | 呼吸支持ソリューションの技術的突破は、私たちの製品に対する需要を減少させる可能性がある |
| ● | 第三者支払者は我々の製品の任意または全部の購入価格を患者に精算することに同意しない可能性があり,患者がわれわれの製品を使用する意思に悪影響を及ぼす可能性がある |
| ● | 私たちは知的財産権侵害の第三者クレームに直面する可能性があります;そして |
| ● | 私たちは私たちの目標市場でbr規制許可や承認を得たり維持したりすることができないかもしれないし、規制承認を得ても不利な規制や法的行動に直面する可能性がある。 |
もし私たちがそのいずれか1つ以上の挑戦に対応できなければ、私たちが製品やサービスを効果的に商業化する能力は制限される可能性があり、これはまた私たちの業務、財務状況、および運営結果に大きな悪影響を及ぼす可能性がある。
私たちの成功は私たちの製品に対する市場の受容度、私たちが新製品を開発して商業化し、収入を創出する能力、そして私たちの技術のために新しい市場を探す能力にかかっている
私たちは呼吸支援技術の開発に参加してきた。私たちの成功は私たちの製品 と医療市場の未来の任意の製品が承認されて受け入れられるかどうかにかかっているだろう。私たちが直面しているリスクは、市場が競争相手の製品ではなく、私たちの製品や未来の製品を受け入れないということであり、私たちは効果的に競争できないだろう。私たちが現在と未来の潜在的な製品を商業化する能力に影響を与える可能性がある要素:
| ● | 次世代 設計課題の要求を満たす上で十分な競争力を有する技術的解決策を開発(または外部開発を得る)技術的解決策の課題; |
| ● | 私たちの製品を販売し、私たちのサービスを提供する時の医者の推薦への依存。 |
私たちの製品や未来の製品が広く市場に受け入れられることは保証できません。もし私たちの製品の市場がbrを発展させたり、発展速度が期待より遅くなったら、私たちの業務と経営業績は実質的な不利な影響を受けるだろう。
もし私たちがInnovimed、Glo-Med、および私たちの他の販売業者と既存の戦略関係を維持できなかった場合、あるいは私たちの製品または任意の未来の製品と技術の他の販売業者を決定できなければ、私たちの収入は低下するかもしれない。
現在、私たちはInnovimed Spとの戦略関係と流通プロトコルを通じて相当な収入を得ることを望んでいる。Zo.oまたはInnovimed, Bepex Ltd.,Anita Técnica S.LまたはWAAS Group,Glo-MedおよびCIO MED Group,Corp,および我々の製品を展開する他の販売業者。もし私たちと総エージェントとの関係が何らかの理由で終了したり損傷したりすれば、これらの関係を他の流通方式で置き換えることができなければ、私たちの収入は大幅に低下する可能性がある。
2
私たちは、将来の製品および技術をマーケティングおよび流通し、既存または新しい市場または地理的地域に当社のINSPIRA ART(Gen 2)デバイス、INSPIRA ART 100デバイス、Hyla血液センサ、Vortxデバイス、およびInspira使い捨て製品をマーケティングおよび流通するために、より多くの流通業者の助けを得る必要があるかもしれません。私たちは他のディーラーを見つけることができないかもしれません。彼らはbrに同意し、商業合理的な条項で私たちのシステムと技術のマーケティングと流通に成功することができます。もし私たちが優遇条項でもっと多くの流通関係を作ることができなければ、私たちの収入は下がるかもしれません。また、私たちのディーラー は私たちの競争相手を優先する製品を選択するかもしれません。
上記のディーラーとの合意によると、私たちは私たちの製品の任意およびすべての規制承認を取得して維持する責任があります。もし私たちがこのような承認を得たり維持したりすることができない場合、あるいは流通協議当事者が合意された価格で合意された製品を購入できない場合、これらのディーラーとの関係に悪影響を及ぼすかもしれませんので、これらの合意出荷からいかなる収入も得られないかもしれません。
医療機器の開発コストが高く、持続的な技術変化に関連しており、これは私たちの現在または未来の製品を時代遅れにするかもしれない。
医療機器技術と製品市場の特徴は迅速な技術変革、医療進歩、絶えず変化する消費者需要、比較的に短い器械ライフサイクル、絶えず変化する法規要求と絶えず発展する業界標準である。これらの要素のいずれも、技術または市場の時代遅れを回避するために、特に研究、設計、および開発のために、私たちの設備の需要を減少させるか、または大量の資源および支出を必要とする可能性がある。
私たちの成功は私たちが既存技術を強化し、新しい技術を開発或いは獲得し、技術発展と絶えず発展する業界標準について、同時に顧客需要の変化に応答する能力があるかどうかにかかっている。変化する技術および顧客のニーズを十分に満たすことができるデバイス増強機能 または新しいデバイスを十分に開発または取得できなかったり、そのようなデバイスをタイムリーに発売できなかったりすることは、私たちの業務、財務状況、および運営結果に重大な悪影響を及ぼす可能性がある。
私たちは私たちの製品を改善し、技術を推進し、競争力のある価格で新しい設備を開発するのに十分な財力がないかもしれない。1つまたは複数の競争相手または将来この分野に進出する競争者の技術的進歩は、現在のサービスまたはデバイスが競争力を持たなくなったり、時代遅れになったりする可能性があり、これは、収入および利益を減少させ、私たちの業務および運営結果に悪影響を及ぼす可能性がある。
私たちは私たちの製品ラインと、私たちがそれぞれ異なる会社からの製品やサービスを販売する市場で激しい競争に遭遇するかもしれません。その中には、いくつかの会社の財務とマーケティング資源が私たちよりも多いかもしれません。私たちの競争相手は、呼吸支援ソリューションおよび技術の研究、開発、製造、およびマーケティングに従事する任意の会社、ならびに単一または限られた数の競争力のある製品およびサービスを販売するか、または特定の細分化された市場にのみ参加する複数の医療機器会社を含むことができる。
私たちの顧客獲得戦略は成功しないかもしれません。私たちはすでに異なる地理地域の各方面と流通協定に署名しましたが、私たちはこのような協定からいかなる収入も得られないかもしれません.
私たちの業務は私たちの顧客獲得戦略の成功に依存するだろう。これまで、私たちは様々な地理的地域で様々な流通協定 に署名しており、これらの協定は監督部門の承認を待たなければならない。もし私たちが規制部門の承認を得ていない場合、あるいは流通協定の当事者が合意された価格で合意された製品を購入できなかった場合、私たちはこのような合意から何の収入も得られないかもしれない。
また、私たちが高品質の設備技術を維持できなければ、新しい顧客を維持したり増やすことができない可能性があります。もし私たちが失敗したら、私たちの収入、財務業績、そしてbr業務は深刻な損害を受けるかもしれない。私たちの将来の成功は、アメリカ、イスラエル、ヨーロッパでのビジネスを拡大し、より多くの市場に進出し、私たちの製品と任意の未来の製品を商業化することにかかっています。私たちは私たちの拡大された成長が私たちの製品のさらなる開発、規制承認、そして商業化にかかっていると信じている。もし私たちの製品の使用を適時に拡大できなければ、私たちは私たちの市場を拡大したり、私たちの収入を増加させることができないかもしれません。私たちの業務は不利な影響を受けるかもしれません。もし人々が私たちの製品が有用で信頼できると思わなければ、私たちは新しい顧客を引き付けることができないかもしれません。顧客増加の減少は開発者への吸引力を低下させる可能性があり、これは私たちの収入、業務、財務状況、運営結果に実質的な悪影響を及ぼす可能性がある。
3
コンピュータシステムの障害、ネットワーク攻撃、あるいは私たちのネットワークセキュリティ欠陥が発生すれば、私たちの業務と運営は影響を受けるだろう。
我々のデータをアクセスを許可せずにデータの完全性および機密性を保護するためのセキュリティ対策が実施されているにもかかわらず、我々の内部コンピュータシステムおよび私たちが依存する第三者のコンピュータシステムは、コンピュータウイルス、マルウェア、自然災害、テロ、戦争、電気通信および電気故障、ネットワーク攻撃またはインターネット上のネットワーク侵入、電子メール添付ファイル、組織内部者、または組織内部システムにアクセスする権利を有する者によって破壊されやすい。世界各地からの未遂攻撃および侵入の数、強度および複雑性の増加に伴い、セキュリティホールまたは破壊のリスク、特にネットワーク攻撃またはネットワーク侵入(コンピュータハッカー、外国政府、およびネットワークテロリストを含む)を介したリスクが一般的に増加する。このような事件が発生して我々の運営が中断されると,我々の薬物開発計画が実質的に破壊される可能性がある。例えば、完成、進行中、または計画中の臨床試験における臨床試験データの損失は、私たちの規制承認作業を遅延させ、データを回復または複製するコストを著しく増加させる可能性がある。Br}の任意の中断またはセキュリティホールが、私たちのデータまたはアプリケーションの損失または破損をもたらし、または の機密または独自の情報を適切に開示しない場合、私たちは、データプライバシー法、例えば、データ保護法規またはGDPRに従って、私たちの名声を損なうことを含む重大な法的クレームおよび責任を招く可能性があり、私たちの候補薬剤のさらなる開発は、br}のさらなる開発が延期される可能性がある。
私たちは第三者製造業者とサプライヤーに依存しており、これにより、潜在的な供給不足や問題、コスト増加、品質やコンプライアンス問題の影響を受けやすくなり、これらの問題はいずれも私たちの業務を損なう可能性があります。
私たちの製品は複数のコンポーネントで構成されている。私たちは組み立てられた製品とその使い捨て呼吸支持装置の販売を計画している。製品および使い捨てコンポーネントを組み立てるコンポーネント は、独自コンポーネントおよび既製コンポーネントからなる。独自コンポーネントは、規制要件に適合した良好な製造仕様またはGMP承認された生産工場で私たちに代わって製造され、既製コンポーネントはGMPベンダーによって調達および製造される。GMP下請けは、独自のコンポーネントと既製コンポーネントを組み合わせて、私たちの製品を作成します。
したがって,我々は第三者 に依存して製造し,独自のカスタマイズコンポーネントを提供する.私たちは複数のサプライヤーに材料とコンポーネントを提供し、私たちの製品のいくつかのコンポーネントを製造して組み立ててくれるにもかかわらず、単一ソースのサプライヤーに依存しません。我々のbrサプライヤーは、製造過程において、例えば、特定の合意および手順に従わなかったこと、適用された法律および法規要件を遵守できなかったこと、設備故障および環境要因、br}が自分の業務を正しく処理できなかったこと、および第三者知的財産権を侵害することができず、これらのいずれも、私たちの要求を満たす能力を遅延または阻害する可能性がある。私たちのこれらの第三者サプライヤーへの依存はまた私たちを他のリスクに直面させて、 は私たちの業務を損なう可能性があります
| ● | 私たちは現在私たちの多くのサプライヤーの主要な顧客ではありませんので、これらのサプライヤーは他のお客様の需要を優先するかもしれません |
| ● | 私たちはタイムリーにあるいは商業的に合理的な条件で十分な供給を得ることができないかもしれない |
| ● | 私たちのサプライヤー、特に新しいbrサプライヤーは、製造過程でエラーが発生し、それによって私たちの製品の有効性や安全性にマイナスの影響を与えたり、出荷遅延を招いたりする可能性があります |
| ● | 私たちはbrを見つけて代替サプライヤーの資格を決定することが難しいかもしれない |
| ● | コンポーネントまたはサプライヤーの交換は、製品を再設計し、FDAまたは他の同様の外国の規制機関に提出する必要がある可能性があり、これは、私たちのビジネス活動を阻害または延期する可能性があります |
4
| ● | 私たちの1つまたは複数のサプライヤー は、私たちの製品のコンポーネントを提供したくないか、または供給できないかもしれません |
| ● | 私たち一人以上のサプライヤーに影響を与える火災、自然災害、または他の災害の発生は、彼らが直ちに私たちに製品を渡す能力に影響を与える可能性があります |
| ● | 私たちのサプライヤーは私たちの需要とは関係のない財務や他の業務困難に直面する可能性があり、これは彼らが私たちの注文を履行し、私たちの要求を満たす能力を抑制することができるかもしれない。 |
必要であれば、私たちは他のサプライヤーや代替サプライヤーを迅速に確立することができない可能性があります。一部の理由は、規制承認プロセスの要求に応じて他の活動を展開して のようなサプライヤーを確立する必要があるからです。第三者サプライヤーから製品を取得する任意の中断または遅延、または適切な代替源から製品を許容可能な価格でタイムリーに取得することができない場合、顧客のニーズを満たす能力を弱める可能性があり、競争製品に移行する可能性があります。私たちのあるサプライヤーへの依存を考慮して、私たちは代替サプライヤーを探す時に供給不足の影響を受ける可能性があります。
私たちはヨーロッパにおけるロシアとウクライナの地政学的および軍事的緊張に関連する地政学的リスクに直面する可能性がある。
我々は現在、ロシアとウクライナで事業を展開していないが、ロシアとウクライナの地政学的不安定なアップグレードやロシアルーブルの通貨変動は世界市場にマイナスの影響を与えている。この影響は私たちのサプライチェーン、私たちの運営、そして地域の未来の成長見通しに否定的な影響を及ぼすかもしれない。ウクライナ危機のため、アメリカと他の国はいくつかのロシア個人と実体に制裁を加えた。私たちのグローバル業務は、ロシアとウクライナの現在の情勢、実施されている関税、経済制裁、輸出入制限、および報復行動がロシアと他の国との緊張を激化させる可能性がある、私たちの業務、財務状況、運営結果、キャッシュフロー、または私たちの証券の市場価格に悪影響を及ぼす可能性のあるリスクに直面させます。ロシアとウクライナの現在の地政学的不安定および特定の会社および個人に対する米国および他の国政府の関連制裁は、これらの国の潜在的顧客およびサプライヤーとの業務能力を阻害する可能性がある。
私たちは限られた製造歴史だけで私たちの業務の将来性を評価して、私たちは内部製造を始めると、私たちの製品を世界で商業化することに成功するまで、大きな損失を受けることが予想されます。
もし私たちの未来の製造 操作や現在または未来に契約した製造操作が信頼できなくなったり、利用できなくなったら、私たちの予想される業務操作 を進めることができなくなり、私たちの業務計画全体が失敗する可能性があります。我々の製造業務 または任意の第三者メーカーが、適切または適用基準に従って商業化規模の生産要求を満たすことができる保証はない。
私たちは私たちの製造能力をタイムリーに交換できないかもしれない。
もし私たちの将来の製造施設または任意の現在または未来の契約製造事業が任意のタイプの長期中断を受けた場合、規制機関の行動、設備故障、重要施設サービス(例えば、浄水、清浄蒸気発電または建築管理および監視システム)、火災、自然災害、または他の任意の生産活動停止の事件によっても、長期的な販売および利益損失に直面する可能性がある。私たちのいくつかの製品や候補製品を代行生産できる施設は限られています。私たちの既存の製造能力の交換は私たちの業務や財務状況に実質的な悪影響を及ぼす可能性があります。
我々は第三者サービスプロバイダ に依存する.もしこれらの第三者サービスプロバイダが質の高いサービスを維持できなければ、私たちの製品の実用性が損なわれる可能性があり、これは私たちの製品の浸透率、私たちの業務、経営業績、名声に悪影響を及ぼす可能性があります
私たちが提供するいくつかのサービスと製品の成功は第三者サービス提供者にかかっている。このようなサービスプロバイダは、当社の製品に独自のカスタマイズコンポーネントを提供する製造業者を含む。私たちが私たちのビジネス活動を拡大するにつれて、このような第三者プロバイダの質はより大きな負担に直面するだろう。第三者プロバイダが質の高いサービスを維持できない場合、私たちの製品、業務、名声、運営結果は不利な影響を受ける可能性があります。さらに、第三者サービスプロバイダの悪いサービス品質は、私たちに責任クレームを提起し、損害や傷害について私たちに訴訟を提起する可能性があります。
5
非米国政府は常に厳しいbr価格制御を実施しており、これは私たちの将来の収益力に悪影響を及ぼす可能性がある。
私たちのbrは、アメリカと非アメリカの司法管轄区域の私たちの製品または任意の未来の製品に関する規則と法規によって制限されるかもしれません。いくつかの国/地域では、EU諸国やEUを含めて、各国は自分の規則と法規を制定しており、場合によっては価格設定は政府によって制御される可能性があります。これらの国/地域では,候補医療機器のマーケティング承認を受けた後,政府機関との定価交渉にかなりの時間を要する可能性がある。ある国/地域で精算や価格設定の承認を得るためには、臨床試験を行い、私たちの製品の費用対効果を他の利用可能な製品と比較する必要があるかもしれません。もし私たちの製品が精算を得られない場合、範囲や金額が制限されている場合、あるいは価格がbr}が満足できないレベルに設定されている場合、利益を達成したり維持したりすることができないかもしれません。
私たちは少数の職員たちと重要な顧問を通じて私たちの業務を管理する。
2024年3月22日現在、37人のフルタイム従業員 (私たちの高級管理チームを含む)、5人のアルバイト従業員、および他の3人の独立請負業者とコンサルタントがいます。私たちの将来の成長と成功は、私たちの現経営陣メンバーの持続的なサービス、特に最高経営責任者のダギカノンと社長に大きく依存しています。一定の通知期間内に、私たちのどの従業員とコンサルタントもbrのいつでも会社を出ることができます。私たちの役員や任意の重要な従業員やコンサルタントのサービスを失うことは、私たちの業務計画を実行する能力に悪影響を与え、私たちの経営業績を損なうことになります。私たちの運営成功は高度管理者、技術者、その他の重要な人員の継続的な採用に大きく依存するだろう。重要な人員の流出は私たちの運営と財政的業績に悪影響を及ぼすかもしれない。
私たちは私たちの組織を拡張する必要があるかもしれませんが、採用に必要な追加従業員やコンサルタントの面で困難に直面する可能性があり、これは私たちの運営を乱す可能性があります。
私たちの開発と商業化計画と戦略の制定、そして私たちの人手不足のため、私たちは追加の管理、運営、販売、マーケティング、財務、br法律、その他の資源が必要かもしれません。医療機器業界は人材の争奪が激しい。激しい競争のため、私たちは業務発展に必要な合格者を誘致し、維持することができず、適切な代替人員を募集することもできない可能性がある。
私たちの経営陣は、私たちの日常活動から注意を移し、これらの成長活動を管理するために多くの時間を投入する必要があるかもしれません。私たちは私たちの業務の拡張を効果的に管理できないかもしれません。これは、私たちのインフラが弱く、操作ミス、ビジネス機会の喪失、従業員の流失、残りの従業員の生産性の低下を招く可能性があります。私たちの予想成長は大量の資本支出を必要とし、より多くの医療機器製品の開発など、他のプロジェクトから財務資源を分流する可能性がある。私たちの経営陣が私たちの成長を効果的に管理できなければ、私たちの支出増加は予想を超える可能性があり、私たちの収入を創出および/または増加させる能力は低下する可能性があり、私たちは私たちの業務戦略を実施できないかもしれない。私たちの将来の財務業績と私たちが医療機器製品とサービスを商業化し、効果的に競争する能力は、将来の任意の成長を効果的に管理する能力にある程度依存するだろう。
私たちの業務の国際拡張は、アメリカやイスラエル以外での業務展開に関するビジネス、規制、政治、運営、金融、経済リスクに直面させています。
私たちの本社とイスラエルにある他の業務(以下に述べる)に加えて、私たちの業務戦略には、重大な国際拡張、特に私たちの製品に対する規制承認の拡大が期待されています。国際的な業務展開は多くのリスクに関連しているが、これらに限定されない
| ● | プライバシー法規、税法、輸出入制限、就業法、規制要件、その他の政府の承認、許可、許可証など、複数の、互いに衝突し、変化する法律法規、例えば、プライバシー法規、税法、輸出入制限、就業法、監督管理要件 |
| ● | 私たちは様々な国·地域で私たちの製品やサービスを使用した時、規制部門の承認を得られなかった |
| ● | 他の関連する可能性のある第三者特許権; |
6
| ● | 私たちの知的財産権の保護と実行の複雑さと困難 ; |
| ● | 人員配置が困難で海外業務の管理が困難である |
| ● | 複数の規制、政府、補償制度の管理に関連する複雑さ |
| ● | 私たちが国際市場に進出する能力は限られている |
| ● | 長い支払い周期のような財務リスクは、売掛金の回収が困難であり、ローカル金融危機が私たちの製品の需要と支払いに与える影響、外貨為替レートの変動の影響を受ける |
| ● | 戦争、テロ、政治的動揺、疾病の発生、ボイコット、貿易削減、その他の商業的制限を含む自然災害、政治的、経済的不安定 |
| ● | 出張、翻訳、および保険費用が含まれているいくつかの費用; |
| ● | 規制とコンプライアンスリスク は、正確な情報の保持と販売および活動の制御に関連しており、これらの販売および活動は、米国の“反海外腐敗法”または“海外腐敗防止法”、その帳簿と記録条項またはその反賄賂条項の権限に属する可能性がある。 |
これらの要素のいずれも、私たちの将来の国際拡張と運営を深刻に損害し、私たちの運営結果に影響を及ぼす可能性がある。
私たちは激しい競争に直面しており、私たちは私たちの産業で効果的に競争できないかもしれない。
集中治療室および急性呼吸ケア分野の市場参加者は、ボストン科学社(ニューヨーク証券取引所コード:BSX)、ResMed Inc.(ニューヨーク証券取引所コード:RMD)、Masimo Corporation (ニューヨーク証券取引所コード:MASI)、Becton、Dickinson and Company(ニューヨーク証券取引所コード:BDX)、チャット工業社(Chart Industries,Inc.)(ニューヨーク証券取引所コード:GTLS)、フィリップスヘルスケア社、美敦力(ニューヨーク証券取引所コード:MDT)、Fisher&Paykel Healthare Corporation Limited、Dr werk&CogerAG、Gakr&Medcare Corporation Limitedシーメンスヘルスケア社ADR(場外取引市場コード:SMMNY),バクスター国際社(ニューヨーク証券取引所コード:BAX),ゲッティンガー社(OTCMKTS:GNGBY),汎用電気ヘルスケア社,Terumo社(TYO:4543,日経225成分),Liva Nova PLC(ナスダックコード:LIVN),フェゼンユスKGaao(場外取引市場コード:FSNUY),ジョンソン(ニューヨーク証券取引所コード:JNJ),Resusciec,Spectrum Medical。これらの会社は呼吸器、ECMO装置、血液センサなどの呼吸器看護設備と解決策を開発または買収した。
私たちと比較して、上記の会社はより多くのブランド認知度、研究開発と監督管理能力、および財務、技術、製造、マーケティングと人的資源を持っており、医療機器の研究開発において著しい多くの経験とインフラを持っており、FDAと他の監督機関の許可を得て、世界各地でこれらの設備を商業化している。しかも、その中のいくつかの会社はかなりの市場シェアを占めている。彼らの市場主導的地位と市場に対する重大な制御は、私たちが私たちの製品販売を発売または効果的にマーケティングし、創造する能力を大幅に制限するかもしれない。
私たちの多くの競争相手は長い歴史と業界での良い名声を持っている。彼らのブランド認知度、財力、人的資源は私たちよりずっと大きい。彼らはテスト設備の研究と開発、規制許可の獲得と維持、その他の要求、製造とマーケティングなどの製品の面でも私たちよりも多くの経験と能力を持っている。私たちは競争相手の持つ優位性を克服できないかもしれません。これは大きなリスクであり、私たちがそれができなければ、私たちの業務に失敗する可能性があります。また、私たちは未来にもっと多くの製品を開発したり、市場発展と革新のペースについて、市場シェア を私たちの競争相手に譲ることができないかもしれません。
7
医療機器、より具体的には、呼吸支援技術および解決策市場の競争は非常に激しく、これは、brの値下げ、より長い販売サイクル、より低い製品利益率、市場シェアの喪失、および追加の運営資金要求をもたらす可能性がある。成功するためには、 は他の重要な事項に加えて、現在市場で呼吸不全を治療するための他の解決策ではなく、消費者に私たちの製品を受け入れてもらわなければならないし、私たちの主要な技術を採用したり、他の高度な呼吸支援解決策を提供する潜在的な未来の医療設備ではない。もし私たちの競争相手がいくつかの製品と解決策で大幅な割引を提供すれば、私たちは競争に勝つために価格を下げたり、他の割引条項を提供する必要があるかもしれません。しかも、私たちの価格と価格政策のどんな広範囲な変化も、私たちが収入を生み出すことを難しくしたり、収入を低下させたりする可能性がある。また、私たちの競争相手が私たちが開発する可能性のある製品や解決策よりも効果的またはより望ましい製品と解決策を開発して商業化すれば、私たちの顧客に私たちの製品や解決策を使用するように説得できないかもしれません。このような変化はいずれも私たちのビジネス機会と収入潜在力を減少させ、私たちの経営業績に重大な悪影響を及ぼす可能性があります。
第三者決済者が私たちの製品や未来の製品を使用するために十分な保証範囲と精算を提供しなければ、私たちの収入はマイナス影響を受けるだろう。
私たちの製品はまだ第三者支払者保険や精算の承認を得ていません。このような精算は,サービスを提供する際に使用する特定のデバイスによって異なる可能性があり,第三者のアイデンティティに基づく.私たちが医療機器市場でリードを獲得し、維持できるかどうかは、特に呼吸看護市場では、私たちと個人第三者との関係にかかっている。
私たちは個人第三者と協力して、私たちの顧客が私たちの製品の精算を受けることを許可したいです。br}大量の個人第三者契約を失うことは私たちの収入に悪影響を及ぼす可能性があり、これは私たちの業務、財務状況、運営結果に悪影響を及ぼす可能性があります。過去数年間、いくつかの第三者の販売率は低下し、場合によっては大幅に低下した。この傾向がより多くの第三者 に継続または適用されない保証はない.
さらに、個人第三者は、私たちが提供したいかなる新製品も精算したり、商業的に実行可能なレートでこれらの新製品を精算しない可能性があります。もし私たちの既存または未来の製品が十分なレベルの精算を得ることができなければ、これらの製品の需要、私たちの収入、予想成長に悪影響を及ぼすかもしれない。これは私たちの業務、財政状況、そして運営結果に悪影響を及ぼすかもしれない。
私たちは様々なクレームによって訴訟を受けるかもしれません。これは私たちの運営結果に悪影響を与え、私たちの名声を傷つけたり、他の方法で私たちの業務にマイナスの影響を与えるかもしれません。
私たちは正常業務活動における様々なクレームによって訴訟を受ける可能性があります。これらは労働者、賃金、労働時間、商業、そして他の事項に関するクレーム、訴訟、そして訴訟を含むことができる。いかなる訴訟の結果も、その是非にかかわらず、本質的には不確定である。いかなるクレームや訴訟、およびそのようなクレームおよび訴訟の処置は、時間的かつ高価な解決策である可能性があり、管理職の注意と資源を分散させ、他の当事者が類似したクレームを提起しようとすることにつながる可能性がある。訴訟に関連するいかなる不利な裁決も、私たちの運営結果に悪影響を与え、私たちの名声を損なう、あるいは他の方法で私たちの業務に否定的な影響を与える可能性がある。また、どのような紛争の性質や時間によっても、法的問題の解決は、私たちの将来の経営業績および/または私たちのキャッシュフローに大きな影響を与える可能性があります。
私たちは製品責任、保証、または同様のクレームや製品リコールの影響を受ける可能性があり、これは巨大な費用を消費し、管理層の注意を分散させ、私たちの商業的名声と財務業績を損なう可能性があります。
私たちの業務は潜在的な製品責任、保証あるいは類似のクレームと製品リコールの固有のリスクに直面させます。医療機器業界は従来から訴訟が好きで、もし私たちのいかなる製品を使用して傷害或いは死亡を招く或いは促進すれば、私たちは製品責任、保証或いは類似のクレームの財務リスクに直面します。私たちのどの製品の設計や製造欠陥も製品をリコールする必要がある可能性があります。私たちは製品責任保険を維持する予定ですが、これらの保険証書の保証範囲は将来のクレームをカバーするのに十分ではないかもしれません。将来、私たちは受け入れ可能な条項や合理的な費用で製品責任保険を維持できないかもしれませんし、このような保険は私たちに十分な潜在的責任保険を提供できないかもしれません。製品責任クレーム、brは是非曲直あるいは最終結果にかかわらず、あるいは任意の製品リコールは私たちの巨額のコストを払って、私たちの名声、顧客の不満と落胆、そして管理層の注意を大量に移転させる可能性があります。もしクレーム金額が私たちの保険範囲を超えたり、超えたりすれば、私たちの業務、財務状況、経営結果に重大な悪影響を及ぼす可能性があります。
8
我々の業務は全体的な経済状況の変化の影響を受ける可能性がある
私たちの業務は、私たちの市場の不利な経済状況を含めて、国内と世界の経済状況の変化によるリスクを受けており、これは私たちの業務を損なう可能性があります。例えば、新冠肺炎疫病はアメリカと国際市場で巨大な変動と不確定性 をもたらした。私たちの将来の顧客が私たちの技術や製品を使用する分野の支出を大幅に減らしたり、他の支出を私たちの技術や製品より優先したりすれば、私たちの業務、財務状況、運営結果、見通しは実質的な悪影響を受けるだろう。
グローバル経済の中断はまた、顧客支出の減少による減速を含む、私たちの業務に一連の後続の影響を与える可能性があり、 顧客は製品、解決策、またはサービスの費用を時間通りに支払うことができない(もしあれば);より厳しい輸出規制は私たちの潜在的な顧客基盤を制限する可能性がある;私たちの流動性、財務状況、株価に負の影響を与え、これは私たちに有利な条項で市場で資金を調達し、融資を獲得し、他の資金源を確保する能力に影響を与える可能性がある。
また、ハリケーン、嵐、地震、津波、洪水、医療流行病、その他の災害などの悲劇的な事件の発生は、私たちのどの市場のビジネス環境にも悪影響を及ぼす可能性があり、私たちの業務、財務状況、運営業績に大きな悪影響を及ぼす可能性があります。私たちのいくつかの業務は過去と未来にこのような事件が発生するかもしれない地域に位置している。
不安定な市場や経済状況 は私たちの業務、財務状況、株価に深刻な悪影響を及ぼす可能性があります。
信用と金融市場を含む全世界経済は極端な変動と破壊を経験し、流動性と信用供給の深刻な減少、消費者自信の低下、経済成長の減速、失業率の上昇、インフレ率の上昇及び経済安定性の不確定性を含む。例えば、新冠肺炎の疫病は広範な失業、経済減速と資本市場の極端な変動 を招いた。同様に、ウクライナとロシアの間の衝突は世界資本市場の極端な変動をもたらし、グローバルサプライチェーンとエネルギー市場の中断を含むさらなるグローバル経済結果が生じると予想される。また、現在ガザ地区のテロ組織とイスラエルとの衝突は中東地域の動乱をエスカレートさせ、世界経済に影響を与える可能性もある。このような変動と中断は、私たちまたは私たちが依存している第三者に悪影響を及ぼす可能性がある。政治的動揺や戦争の結果を含む株や信用市場が悪化した場合、任意の必要な債務や株式融資をタイムリーまたは有利な条件で得ることが難しくなり、コストがより高くまたは希釈度が高くなる可能性がある。しかも、インフレ は私たちの費用を増加させ、私たちに悪影響を及ぼすだろう。世界各地の生活コストの増加は、賃金上昇、直接サービスコストの増加、送料コスト、部品コストの増加、製造コストの上昇などのコスト増加を招く可能性がある。インフレと関連金利のいずれの大幅な上昇も、私たちの業務、運営業績、財務状況に重大な悪影響を及ぼす可能性があります。
私たちの管理チームが上場企業を管理する経験は限られています。
私たちの管理チームの大多数のメンバーは上場会社の管理、上場会社の投資家との相互作用、及びアメリカの上場会社に関連するますます複雑な法律を遵守する上での経験は限られている。私たちの管理チームは、アメリカ連邦証券法で規定されている重大な監督管理と報告義務の制約を受け、証券アナリストと投資家の持続的な審査を受けることができないかもしれません。これらの新しい義務と構成要素は、私たちの上級管理層に大きな関心を与える必要があり、私たちの業務の日常管理に対する彼らの注意をそらす可能性があり、これは私たちの業務、財務状況、運営結果、および将来性に不利な影響を与える可能性がある。
9
私たちの証券がナスダックに上場して取引されたため、私たちのコストは大幅に増加した。私たちの経営陣は新しいコンプライアンス計画を立て、アメリカの持続的な要求を守るために多くの時間を投じる必要があります。
アメリカで上場している会社として、追加の巨額の会計、法律、その他の費用が発生しています。これは私たちがアメリカで発売されるまで起きていないbrです。米国証券取引委員会のコーポレート·ガバナンス要件や第404節やサバンズ·オキシリー法案の他の条項の要件に関するコストも発生しています。これらの規則と法規は私たちの法律と財務コンプライアンスコストを増加させ、投資家関係、証券取引所の市費と株主報告などの新しいコストを導入し、いくつかの活動をより時間と高価にする。このようなプロセスやシステムを実施してテストするには、外部コンサルタントを招聘し、他の重大なコストを発生させる必要があるかもしれません。今後、サバンズ-オクスリ法案の404節やその他の条項、米国証券取引委員会が採択した規則や法規を含む、米国上場企業の法律や法規のいかなる変化にも影響を与え、それらが私たちに適用される限り、このような変化に対応する際にコストを増加させることになる。これらの法律、規則、および法規は、取締役および上級者責任保険を含むいくつかのタイプの保険をより難しくするか、またはより高価にするかもしれません。私たちは、低減された保険限度額および保証範囲を受け入れさせられるか、または同じまたは同様の保険範囲を得るためにより高いコストを発生させるかもしれません。これらの要求の影響brはまた、合格した人を私たちの取締役会、私たちの取締役会委員会、または役員に参加することを引き付け、維持することを困難にする可能性がある。
もし私たちが高い技能の管理、科学、技術とマーケティングスタッフを誘致し、維持することができなければ、私たちは私たちのビジネスモデルを成功的に実施することができないかもしれない。
著者らの成功はある程度私たちが引き続き高い素質の管理、臨床と科学者の能力を吸引、維持と激励することにかかっている。私たちは、私たちの上級管理職や他の従業員、コンサルタント、科学、医療協力者に強く依存しています。私たちの管理チームは、競争の急速な変化に参加する市場で私たちの業務モデルを適用し、調整することができるように果敢に行動しなければなりません。さらに、私たちは、技術および科学的従業員または第三者請負業者に依存して、私たちの業務を効率的に構築、管理、発展させます。したがって、私たちの未来の生存能力は私たちが高い技能管理、販売と科学技術者を引き付ける能力に大きく依存すると信じている。そのためには、私たちの従業員やコンサルタントに、現在予想されているより高い報酬や費用を支払う必要があるかもしれません。このように、より高い報酬支払いは、私たちの経営業績にマイナス影響を与える可能性があります。医療機器分野では、経験豊富な高素質の人員に対する競争が非常に激しいです。私たちは私たちの業務戦略を実施するために必要な人員を募集したり保留したりすることができないかもしれない。もし私たちが受け入れ可能な条件で質の高い従業員を採用し、維持することができなければ、私たちの新製品とサービスの開発、業務を効果的に管理する能力を弱めるかもしれません。
もし私たちが将来の買収や戦略協力に従事すれば、これは私たちの資本要求を増加させ、私たちの株主を希釈し、私たちに債務を発生させたり、負債を抱えたり、私たちを他のリスクに直面させるかもしれない。
相互補完製品、知的財産権、技術、または業務の許可または買収を含む様々な買収機会および戦略的パートナーシップを評価することができます。潜在的な買収や戦略的パートナーシップは、多くのリスクをもたらす可能性がある
| ● | 業務費用と現金需要増加 ; |
| ● | 追加の債務や負債を負担しています |
| ● | 株式証券を発行し |
| ● | 新人員の統合に関する困難を含む業務同化、買収された会社の知的財産権と製品 |
| ● | 私たちの経営陣の関心を既存の製品計画と計画からこのような戦略的合併や買収を求めることに移しました |
| ● | 重要な従業員の保留、肝心な人員の流失、そして私たちが肝心な業務関係能力を維持する不確実性 |
| ● | そのような取引の他方に関連するリスクおよび不確実性は、その当事者およびその既存製品または候補製品の将来性およびbr}販売許可を含む; |
| ● | 私たちは買収の目標を満たすために、買収された技術および/または製品から十分な収入を得ることができず、関連するbrの買収と維持コストを相殺することさえできない。 |
10
私たちはアメリカと外国のいくつかの反腐敗、反マネーロンダリング、輸出規制、制裁、その他の貿易法律法規の制約を受けている。もし違反したら、私たちは深刻な結果に直面するだろう。
他の事項を除いて、米国および外国の反腐敗、反マネーロンダリング、輸出規制、制裁および他の貿易法律法規は、総称して貿易法と呼ばれ、会社およびその従業員、代理、臨床研究組織、法律顧問、会計士、コンサルタント、請負業者および他のパートナーの直接または間接的な許可、承諾、提供、提供、誘致、または受け入れを禁止し、公共または民間部門の受取人の腐敗または不当な支払いまたは任意の他の価値のあるものである。貿易法違反は巨額の刑事罰金と民事処罰、監禁、貿易特権の喪失、資格取り消し、税収の再評価、違約と詐欺訴訟、名声損害とその他の結果を招く可能性がある。私たちは役人、政府機関、あるいは政府付属病院、大学、その他の組織の従業員と直接または間接的な相互作用を持っている。私たちはまたアメリカ以外での私たちの活動が時間とともに増加すると予想している。我々は、第三者を招いて臨床試験および/または必要な許可、許可、特許登録、および他の規制承認を得ることを計画しており、私たちは、このような活動を明確に許可していなくても、事前にそのような活動を知っていなくても、私たちの人員、代理店、またはパートナーの腐敗または他の不正活動のために責任を負わなければならないかもしれない。
私たちの業務と運営はどんなサイバーセキュリティ事件も含めてセキュリティホールの悪影響を受ける可能性がある。
私たちは、私たちのコンピュータおよび通信システム、ならびに私たちのコンサルタント、請負業者、およびサプライヤーのシステムの効率的かつ断続的な動作に依存しており、これらのシステムを、私たちの知的財産権、財務データ、および他の独自の業務情報を含む敏感な会社データに使用します。
我々のいくつかの業務 には、IT関連の中断の影響を防止し、最大限に低減することを目的とした業務連続性および災害復旧計画および他のセキュリティ対策があるが、我々のITインフラおよび私たちのコンサルタント、請負業者、およびサプライヤーのITインフラは、ネットワーク攻撃、コンピュータウイルス、不正アクセス、電気故障および自然災害、または他の悲劇的な事件の破壊を受けやすい。我々は情報システムやコンピュータサーバの故障に遭遇する可能性があり,これにより我々の正常な業務運営が中断され,大量の財務や行政資源をかけて救済する必要がある可能性がある.システム障害,事故やセキュリティホール は,我々の運営中断を招く可能性があり,我々の製品開発活動や他の業務運営の実質的な中断を招く可能性がある.完成した或いは未来の研究或いは臨床試験中のデータ損失は私たちの研究、開発或いは監督管理の承認作業の遅延を招く可能性があり、私たちのデータの回復或いは複製のコストを著しく増加させる。もし任意の中断またはセキュリティホールが私たちのデータやアプリケーションを紛失したり、破損したり、機密または独自の情報を適切に開示しない場合、私たちは規制機関の調査と救済、処罰、責任を招く可能性があり、私たちの候補製品の開発は遅延したり、他の悪影響を受ける可能性があります。
私たちは商業上の合理的な業務中断と責任保険を保証したと信じていますが、私たちは私たちの保険契約範囲を超えたり、私たちが保証範囲を超えていない業務中断によって損失を受ける可能性があります。例えば、私たちはテロやサイバー攻撃に保険をかけていない。どんな自然災害や悲劇的な事件も、私たちの運営と財務業績に大きな否定的な影響を及ぼすかもしれない。しかも、このような活動は私たちの候補製品の開発を延期するかもしれない。
11
データ保護に関連する法律や法規の変化、または私たちが実際にまたはそのような法律法規や私たちのプライバシー政策を遵守できていないと考えていることは、私たちの業務に大きな影響を与えたり、政府の法執行行動や私たちへの重大な処罰を招き、私たちの経営業績に悪影響を及ぼす可能性があります。
我々は,健康情報や他の高度に敏感あるいは機密な患者や他の第三者(例えば,患者のスキャンを推奨する医療提供者)の情報やデータを受け取ることが予想され,それをまとめて分析したい。これらのデータを収集して使用することは,プライバシーやデータ保護上の懸念 を引き起こす可能性があり,我々の業務に悪影響を与える可能性がある.プライバシー、データ保護、情報セキュリティ、および個人情報および他のデータの収集、記憶、共有、使用、処理、送信、開示、および保護については、多くの連邦、州、および国際法律法規があり、このような法律法規の範囲は変化する可能性があり、異なる解釈の影響を受けて、私たちが業務を展開しようとしている国と地域(例えば、アメリカ、EU、イスラエル)、 または他の法律法規と衝突している。グローバルプライバシーおよびデータ保護の規制枠組みは、予測可能な未来においても不確実で複雑であり、これまたは他の実際または主張された義務は、私たちが予想していなかった方法で解釈および適用される可能性があり、または1つの管轄区域から別の管轄区へと一致せず、私たちを含む他の規則または慣行と衝突する可能性がある。さらに、データの収集、使用、保持、セキュリティ、またはその解釈の適用に関する法律、法規または業界慣行の任意の重大な変更、またはそのようなデータの収集、使用、保持、または開示に関するユーザの同意を得なければならない方法に関する任意の変更は、私たちのコストを増加させる可能性があり、私たちのサービスおよび候補製品を達成できない可能性のある実質的な方法で修正し、患者データを格納して処理すること、または新しいサービスおよび機能を開発する能力を制限することができることを要求する。
特に,連邦と州の2レベルでは米国のデータ保護法律(すなわちプライバシーとデータセキュリティに関連する法律法規)の制約を受ける.データ保護の立法と規制構造は引き続き発展しており、近年、プライバシーとデータセキュリティ問題がますます注目されている。多くの連邦と州法律は、州データ漏洩通知法、州健康情報プライバシー法及び連邦と州消費者保護法を含み、健康に関連するbrとその他の個人情報の収集、使用と開示を管理する。このような法律法規を遵守しないことは、政府の法執行行動を招き、私たちに責任(重大な民事または刑事罰の適用を含む)、個人訴訟および/または負の宣伝をもたらす可能性があり、私たちの業務に負の影響を与える可能性がある。例えば、カリフォルニア州は2018年6月28日に“カリフォルニア消費者プライバシー法”(CCPA)を公布し、2020年1月1日に施行された。CCPAはカリフォルニアの消費者のためのプライバシー権を創出し、ある個人データを処理するエンティティのプライバシーとセキュリティ義務を増加させた。CCPAは,違反行為に対する民事処罰と,データ漏洩訴訟が増加すると予想されるデータ漏洩行為に対する個人訴訟権利を規定している。CCPAは私たちのコンプライアンスコストと潜在的な責任を増加させる可能性があり、連邦レベルと他の州も多くの類似した法律を提出した。
また,“経済·臨床健康情報技術”(HITECH)とその実施条例におけるプライバシーやセキュリティ要求に応じた健康情報の取得が望まれる。HIPAA下のプライバシー基準と安全基準は、健康計画、医療保健情報交換所とある医療保健提供者(保険実体と呼ぶ)とそれとサービス関係を締結した商業パートナーが個人が識別可能な健康情報を交換することによって、個人が識別可能な健康情報を保護するための標準を確立した。注目すべきは、HIPAA以前に直接規制されていたのは保証エンティティのみであり、HITECHがHIPAAのプライバシーやセキュリティ基準を確保することは、保証エンティティの業務パートナーにも直接適用されることである。そのため、保証実体と業務パートナーはプライバシー基準と安全基準を遵守できなかったため、重大な民事と刑事罰を受けた。 私たちの正常な運営の一部として、保証エンティティとしての業務パートナーを含む患者に関する個人識別情報を収集、処理、および保持する予定であるため、HITECHによる変更を含むHIPAAの制約を受けることが予想され、もしHIPAAによって許可されていない方法で個人の健康情報を故意に取得または許可されていない方法で開示すれば、刑事罰を受ける可能性がある。敏感な個人情報(健康情報を含む)に影響を与えるデータ漏洩は、重大な法律および財務リスクおよび名声 損失をもたらす可能性もあり、これは私たちの業務に悪影響を及ぼす可能性がある。
12
HIPAAは、行政、物理、および技術保障措置 を採用してこのような情報を保護することを含む、保護された健康情報の使用または開示に関する政策およびプログラムを作成および維持することを含む、保証エンティティ (私たちの多くの潜在的顧客と同じ)およびビジネスパートナー(例えば、私たち)に要求される。HITECHは患者の身分健康情報に違反する通知要求を拡大し、ある患者の身分健康情報の開示と販売を制限し、HIPAA違反に対する民事と刑事罰を規定している。 HITECHはまた、カバーする可能性のある実体と商業パートナーに適用される民事と刑事罰を増加させ、州総検察長に新たな権力を与え、連邦裁判所に民事訴訟を提起し、損害賠償または禁止を求めて、HIPAAとその執行の法規を執行し、連邦民事訴訟に関連する弁護士費と費用を求めることができる。さらに、いくつかの州では、HIPAAよりも厳しい可能性がある類似のプライバシーおよびセキュリティ法律法規が採択されている。
国際的に、多くの司法管轄区域 は、個人データの収集、使用、記憶、送信、開示、および/または他の処理に関連するプライバシーまたはデータ保護法律または法規、ならびにホストされた健康データに特化した認証要件を作成することを検討しているか、または検討されている。このような法律および法規は、データホスト、データ常駐、またはデータ局所化要件(一般に、ある国で収集されたいくつかのタイプのデータがその国内で記憶および処理されなければならないことを要求する)、データ輸出制限、国際転送法(そのようなデータを1つの国から別の国に転送することを禁止するか、またはそれに条件を適用することを禁止する)、またはユーザがそのような会社によって記憶または維持されている個人データにアクセス、訂正、および削除することができるように、企業にbrプライバシーまたはデータ保護およびセキュリティポリシーを実施することを要求することができる。個人がその個人データに影響を与えるセキュリティホールを通知したり,個人の同意を得てその個人データ を使用したりする.例えば、欧州立法者は、EUの一般データ保護条例(2016/679)、またはGDPRを通過し、2018年5月25日に施行され、欧州電子プライバシー指令(指令2009/136/EC改正指令 2002/58/EC)の代わりに電子プライバシー条例が決定されている。GDPRは国家法により補完され,欧州データ保護委員会からの拘束力のある指導 によりさらに実施され,より厳しいEUデータ保護要求が実施され,違反行為に対する厳しい処罰 が規定されている。また、イギリスがEU離脱手続きを開始することは、イギリスのデータ保護規制に不確実性をもたらした。特に,連合王国は“2018年データ保護法”によりGDPRを国内法に組み入れ,連合王国がEUから離脱しても有効であると考えられる。
私たちが運営するほとんどの管轄区域では、自分のデータセキュリティとプライバシーの法的枠組みが構築されていると予想されていますが、私たちは遵守しなければなりません。私たちの目標顧客 も上記の規則や法規を含む遵守が必要です。私たちはまた他の管轄区域が違って衝突する可能性のあるプライバシーの法律と法規を遵守する必要があるかもしれない。したがって、私たちは巨額の罰金または処罰、マイナスの宣伝、および可能な業務損失を含む規制行動に直面する可能性がある。
我々は,適用されるプライバシーやデータ保護法律,法規,契約義務を遵守できるようにするための様々な措置を実施しようとしているが,これらの措置はつねに有効ではなく,遵守が保証されていない可能性がある.私たちがプライバシー、データ保護または情報セキュリティに関連する契約または法的義務または法規要件を遵守できないか、または遵守できない場合、政府の調査または法執行行動、訴訟、クレームまたは消費者権益提唱団体または他の人の私たちに対する公開声明を招き、重大な責任を招く可能性があり、私たちの顧客、パートナー、または患者が私たちへの信頼を失う可能性があり、そうでなければ、 は私たちの名声と業務に実質的かつ不利な影響を与えるだろう。また、私たちの顧客やパートナー業務に適用される法律、法規、政策を遵守するコスト、それによる他の負担は、私たちの製品やサービスの採用と使用を制限し、私たちの製品やサービスに対する全体的な需要を減らす可能性があります。さらに、私たちと協力する第三者が適用される法律、法規または合意に違反した場合、このような違反は、私たちが受け取ったデータをリスクに直面させる可能性があり、政府調査または消費者権益提唱団体または他の人の私たちに対する法執行行動、罰金、訴訟、クレームまたは公開声明を招き、私たちの顧客、パートナーまたは患者が私たちに対する信頼を失い、他の側面が私たちの名声や業務に実質的かつ不利な影響を与える可能性がある。さらに、科学技術会社またはそのデータ処理またはデータ保護慣行に対する公衆の審査または苦情は、私たちの業務、業界または運営とは無関係であっても、科学技術会社(私たちを含む)のより厳しい審査を招く可能性があり、政府機関が追加の規制要件を制定したり、その法執行または調査活動を修正したりする可能性があり、これは私たちのコストとリスクを増加させる可能性がある。
13
私たちの財務状況と資本金要求に関連するリスク
我々の2023年12月31日までの年次財務諸表には説明段落が含まれており,継続経営企業としての継続経営能力に対する深刻な疑いを説明している。このような持続的な経営意見は、合理的な条項や新たな融資が得られないことを阻止し、持続的な経営企業としての運営を継続する能力を危うくする可能性がある。
当社はbr日現在、その活動から重大な収入が発生しておらず、重大な運営損失が発生しているBr部分では,我々は設立以来毎年赤字が発生しているため,2023年12月31日までの監査財務諸表には解釈的段落が含まれており,継続的に経営する企業としての能力があるかどうかを示している。これらの事件やbr}条件およびその他の事項は,2023年12月31日までに重大な不確実性があることを示しており,継続経営企業としての能力を大きく疑っている。2023年12月31日までの年次財務諸表の作成仮説は、引き続き経営を継続する企業とします経営陣は、当社は引き続き重大な運営損失を発生させると予想し、主に既存の財務資源を利用し、その製品を販売し、追加資本を調達することで、その運営に資金を提供していきます2023年12月31日現在、私たちは累計約5,550万ドルの赤字を計上しています。持続的な経営意見は、将来的に株式や債務証券の発行やその他の方法で追加資金を調達する能力を大きく制限する可能性がある。さらなる財務諸表には、継続的な経営企業としての私たちの経営能力に関する説明的な段落も含まれている可能性があります。私たちが相当な日常的な収入を生み出すことができる前に、私たちは既存の現金、債務、または株式融資を通じて私たちの未来の現金需要を満たす予定だ。私たちは近い将来に追加の資金が私たちの運営に資金を提供する必要があると予想しています。私たちは受け入れ可能な条件で追加の資金を提供するかどうか(あれば)確定できません。利用可能な資金がなければ、私たちの製品に関連する研究や開発計画や商業化を延期、縮小、または廃止する必要があるかもしれません。これは、持続的な経営企業としての私たちの運営を継続する能力を危うくします。
私たちの主要株主、高級管理者、br取締役は現在実益が私たちの23.6%の普通株を持っています。したがって、彼らは私たちの株主承認に提出された事項を統制することができるかもしれない。
2024年3月22日現在、私たちの主要株主、役員、取締役実益は約23.6%の普通株を持っています。したがって、これらの株主 が一緒に行動すれば、取締役選挙や合併または他の業務合併取引の承認を含む、我々の株主の承認を必要とする事項に影響を与える可能性がある。このような株主の利益はいつも私たちの利益や他の株主の利益と一致しないかもしれない。
私たちの経営の歴史は限られており、設立以来大きな運営赤字を受けており、予見可能な未来には赤字が続くと予想されています。
私たちは発展段階にある医療機器会社で、運営の歴史は限られています。これまで,我々は我々のINSPIRA ART(第2世代)デバイス,INSPIRA ART 100(第1世代)デバイス,次いで我々のHyla血液センサ,Vortxデバイス,Inspira使い捨てデバイスの開発にほぼ完全に集中してきた。これまで、私たちは主に株式の初公開、転換可能な融資、イスラエルの革新機関(IIA、前身は経済産業省首席科学者室)から提供された特許権使用料の贈与によって、私たちの運営に資金を提供してきた。
私たちは限られた運営履歴だけで、あなたはこれらの歴史に基づいて私たちの業務と将来性を評価することができます。また,我々の経験は限られており,会社が急速に発展する新分野でしばしば遭遇する多くのリスクや不確実性,特に医療機器業界での克服に成功していることは証明されていない。これまで私たちは販売候補製品から収入を得ていません( “第5項を参照してください経営と財務回顧と展望“もっと情報を知っている)。設立以来、我々は毎年赤字を出しており、その中で2023年12月31日と2022年12月31日までの年度の純損失はそれぞれ約1,130万ドルと1,500万ドルだった。2023年12月現在、私たちの累計赤字は約5550万ドルです。私たちのほとんどの運営損失は私たちの製品開発に関するコストと、私たちの運営に関する一般的かつ行政コストに起因しています。
我々の研究と 開発費用は我々が計画した拡張研究によって増加することが予想される.また、私たちの製品が市場の承認を得たら、大量の販売、マーケティング、アウトソーシング製造費用、持続的な研究開発費用、上場企業の運営に関連するコストが発生する可能性があります。したがって、予測可能な未来には、重大で増加していく運営損失を受け続けることが予想される。医療機器の開発に関わる多くのリスクや不確実性により,将来の損失の程度やいつ利益が達成されるかは予測できない(あれば)。
14
私たちは私たちの製品を商業化することができ、私たちは成功できないかもしれないまで、大きな損失を被ることが予想される。私たちは次のような状況が発生すれば、私たちの支出は大幅に増加すると予想している
| ● | 私たちの製品の開発を続けています |
| ● | 私たちの製品のために規制とマーケティングの承認を求めます |
| ● | 販売、マーケティング、流通インフラを構築し、私たちの製品を商業化します |
| ● | 他の候補製品および現在の候補製品の後続バージョンの識別、評価、取得、br}許可、および/または開発を求める; |
| ● | 私たちの知的財産権の組み合わせを維持し保護し拡大することを求めています |
| ● | 技術人材の誘致と維持に努めている |
| ● | 私たちの上場企業としての運営と、私たちの製品候補開発と計画の将来の商業化努力を支援するために、追加のインフラを作成します |
| ● | 上述のいずれかに関連する任意の遅延或いは 問題に遭遇し、研究失敗、結果複雑、安全問題或いは他の監督管理 挑戦を含むが、既存の研究或いは他の支持性研究に対してより長い時間の追跡を行って初めて上場承認を得る必要がある。 |
私たちの未来の運営損失の金額は私たちの未来の支出の比率にある程度依存するだろう。私たちが規制部門の許可を得て私たちの製品または任意の未来の候補製品を販売しても,私たちの将来の収入は、私たちの製品または任意の未来の候補製品が承認された任意の市場の規模に依存し、第三者支払者が私たちの製品または任意の未来の候補製品に対して十分な市場受容度、定価、および精算能力を得ることに依存するだろう。また,我々が発生する運営損失は四半期ごとに毎年大きく変動する可能性があるため,我々の運営結果を経時的に比較することは我々の将来の業績の良い指示ではない可能性がある.他の予期せぬコストもまた現れるかもしれない。
私たちは製品brの販売から何の収入も得ていないので、永遠に利益を上げないかもしれません。
私たちはどの管轄区で販売することを許可された製品もなく、私たちは製品販売から何の収入も得たことがありません。私たちが収入を創出し、利益を達成する能力は、私たちが単独でまたは戦略的協力パートナーと製品開発を成功させ、私たちの製品または任意の未来の候補製品を商業化するために必要な規制とマーケティング承認を得る能力にかかっています。私たちはいつ、またはそのような収入が生じるかどうかを知りません。私たちが未来に製品販売から収入を得る能力は、私たちの多くの分野での成功に大きく依存するだろうが、これらに限定されない
| ● | 私たちの製品と未来の任意の候補製品の研究開発を適時、成功的に完成させる |
| ● | 規制とマーケティング部門の任意の候補製品の承認を得る |
| ● | 現在の良好な製造実践またはcGMPに適合する、私たちの製品および任意の未来の候補製品のために維持され、商業的に実行可能で、持続可能で、拡張可能で、反復可能で譲渡可能な製造プロセス を強化する |
| ● | (適用される場合)第三者との供給および製造関係を確立し、維持することができ、これらの第三者は、私たちの製品および任意の将来の候補製品に対する開発および市場の需要を支援するために、数量および品質に十分な製品を提供することができる(承認されれば) |
| ● | 新しい候補製品の決定、評価、買収、および/または開発; |
| ● | 直接販売チーム、マーケティング、流通インフラを構築することによって、および/または協力者または流通業者と協力することによって、規制およびマーケティングの許可を得た任意のbr候補製品を発売し、商業化する |
| ● | 私たちの製品または未来の任意の候補製品の需要を正確に識別する |
| ● | 医師や他の医療専門家が私たちの製品を使って宣伝し教育しています |
15
| ● | もし私たちの製品と医療界と第三者支払者からの任意の未来の製品候補製品が承認されれば、市場の承認を得る |
| ● | 私たちの候補製品が発売が許可された司法管轄区域内で政府機関、医療保険提供者、保険会社の精算許可を得ることを確保する |
| ● | 我々の製品の任意の相互競争に影響を与える技術および市場発展、ならびに任意の将来の候補製品または医療専門家におけるその予期される使用を解決する; |
| ● | どんな協力、許可、または他の手配で有利な条項を交渉することで、私たちはこれらの協力に加入して私たちの義務を履行することができます |
| ● | 特許、特許出願、商業秘密、およびノウハウを含む、私たちの知的財産権の組み合わせを維持、保護、および拡大する |
| ● | 第三者の介入または侵害クレームを回避して防御する; |
| ● | 合格した人を引き付け、採用し、引き留める |
| ● | 私たちの臨床開発、製造施設、商業拡張を支援するために、適切な施設を探してレンタルしたり買収したりします。 |
私たちの製品や将来の候補製品がマーケティングや販売を許可されていても、このような候補製品の商業化に関連した巨額の増量コストが生じることが予想される。FDAまたは他の国内または海外の監督管理機関が生産プロセスの変更や分析を要求したり、現在予想されている基礎の上で研究を行ったりすると、私たちの費用は予想を超える可能性がある。私たちが規制部門の承認を得て私たちの製品や任意の未来の候補製品を販売することに成功したとしても、私たちがこれらの候補製品から得た収入は、私たちが規制部門の承認を受けた地域の市場規模、そのような製品の受け入れ可能な価格、私たちがどのような価格でそのような製品の精算能力を得るか、そのような製品が承認された地域の商業権を持っているかどうか、そしてそのような市場のためのそのような製品の製造とマーケティングに関する費用にある程度依存するだろう。したがって,承認されても,このような製品の販売から相当な収入を得ることはない.また、私たちが承認した製品の販売から相当な収入を得ることができなければ、私たちは運営を縮小または停止させることを余儀なくされるかもしれない。製品開発には多くのリスクや不確実性が含まれているため、費用を増加させる時間や金額を予測したり、いつ、または利益を達成または維持できるかどうかを予測することは困難だ。
私たちは受け入れ可能な条項で獲得できないかもしれない、あるいは全く得られないかもしれない大量の追加資金を調達する必要があるだろう。受け入れ可能なbr条項でタイムリーに資金を得ることができない場合、私たちは私たちの製品開発作業や他の操作を減少、延期、または停止する必要があるかもしれません。
2023年12月31日現在、私たちの現金と現金等価物、短期預金、長期預金は約740万ドルで、 8.9万ドルの制限的な現金は含まれておらず、私たちの運営資本は約480万ドル、累計赤字は約5550万ドルです。現在予想されている運営支出レベルによると、私たちの既存の現金と現金等価物は、今後6ヶ月の運営に資金を提供するのに十分だと予想されています。私たちは私たちの製品を運営し、それを商業化するために多くの追加資金が必要になると予想しています。私たちはテキスト12ヶ月の運営に資金を提供できるように追加資金を求める必要があります。私たちの未来の資金需要は多くの要素に依存するだろうが、これらに限定されない
| ● | 私たちが行っている研究と計画中の研究の進捗、結果とコスト、ならびに製品および任意の未来の候補製品の臨床試験(適用すれば) |
| ● | 製品と未来の候補製品に対する規制審査のコスト、時間、結果 |
| ● | 規制適合性の獲得および維持に関連するコスト、および/またはそれのために第三者メーカーを招聘するコストを含む、私たち自身の商業規模cGMP製造施設を維持するコスト |
16
| ● | 製品開発、テスト、製造、臨床前開発の範囲、進捗、結果およびコスト、ならびに私たちが将来開発または他の方法で得られる可能性のある任意の他の候補製品の臨床試験(適用すれば) |
| ● | 私たちの将来の活動のコストは、任意の特定の地域の任意の候補製品のための販売、マーケティング、および流通能力を確立することを含み、この地域では、私たちはこのような候補製品のマーケティング承認を得た |
| ● | 私たちが構築する可能性のある任意の協力、許可、および他の計画の条項と時間 |
| ● | 特許出願を準備し、提出し、起訴し、私たちの知的財産権を維持し、実行し、知的財産権に関連するクレームを弁護するコスト; |
| ● | 私たちが市場承認を得た任意の候補製品の商業販売から得られる収入水準(あれば)。 |
いかなる追加的な拠出活動も、私たちの経営陣を日常活動から気を配る可能性があり、これは私たちの製品や任意の未来の候補製品の開発や商業化能力に悪影響を及ぼす可能性がある。また、将来的には十分な金額や私たちが受け入れられる条項 (あれば)を得ることができないかもしれない。さらに、任意の融資条項は、私たちの証券保有者の所有権や権利に悪影響を及ぼす可能性があり、私たちが追加証券(株式や債務を問わず)を発行したり、そのような証券を発行したりする可能性は、私たちの証券の市場価格の下落を招く可能性があります。債務の発生は固定支払い義務の増加を招く可能性があり、私たちは追加債務を発生させる能力の制限、私たちが知的財産権を得ることができるかもしれない能力の制限、私たちの業務を展開する能力に悪影響を及ぼす可能性のある他の運営制限など、いくつかの限定的な契約に同意する必要があるかもしれない。私たちはまた、他の場合ではなく、パートナーとの手配や他の方法でより早い段階で資金を求めることが要求される可能性があり、私たちは、私たちのいくつかの技術または候補製品の権利を放棄すること、または他の方法で私たちに不利な条項に同意することを要求されるかもしれません。いずれも、私たちの業務、運営結果、および見通しに大きな悪影響を及ぼす可能性があります。たとえ私たちが現在または未来の運営計画のために十分な資金を持っていると思っていても、市場状況が有利であれば、または特定の戦略的考慮があれば、追加の資金を求めることができるかもしれない。
もし私たちがすぐにbr資金を得ることができない場合、私たちは私たちの1つまたは複数の研究または開発計画を大幅に削減、延期、または停止する必要があるかもしれないし、私たちの製品や任意の他の候補製品の開発または商業化(ある場合)、または必要に応じて私たちの業務を拡大したり、他の方法で私たちのビジネスチャンスを利用することができなくなり、これは私たちの業務、財務状況、およびbr}運営結果に大きな影響を与える可能性がある。
追加資本の調達は、私たちの既存株主の持分を希釈し、既存株主の権利に悪影響を及ぼす可能性がある。
私たちは、私募と公開株式発行、債務融資と協力、および戦略と許可手配を組み合わせた方法で追加資本を求めることができます。 もし私たちが株式または他の方法(転換可能な債務証券を含む)を発行することで追加資本を調達すれば、あなたの所有権権益は希釈され、条項は清算または株主としての権利に悪影響を及ぼす他の特典を含む可能性があります。将来的に私たちの普通株を売却したり、私たちの普通株に変換できる証券を売却したり、このようなbr売却が発生する可能性があると考えて、直ちに希釈を招き、私たちの普通株の市場価格に悪影響を及ぼす可能性があります。
17
製品開発と規制承認に関するリスク
私たちの候補製品と運営はアメリカと海外で広く政府の監督と監督を受けており、私たちが適用されるbrの要求を守らなければ、私たちの業務を損なう可能性があります。
私たちの製品と未来に開発されたどんな製品も医療機器としてFDAの規制を受けることを願っています。私たちの候補製品はアメリカおよび他の場所で広く規制されており、FDAとその外国の同業者、アメリカ司法省あるいはアメリカ司法省、ならびにアメリカ衛生·公衆サービス部-監察長事務室またはHHSを含む。他の事項に加えて、FDAと外国の監督機関は、医療機器を監督する:設計、開発と製造、使用と貯蔵のためのテスト、ラベル、内容と説明書言語、臨床試験、製品安全、施設登録と設備上場、マーケティング、販売と流通、上場前承認、合格評価手順、記録保存プログラム、広告と販売促進、リコールと現場安全是正行動、上場後監視、死亡または深刻な傷害と故障を報告することを含み、発生すれば、死亡または深刻な損傷を招く可能性がある。発売後の審査研究;および製品の輸出入。
我々の候補製品 が遵守すべき法規は複雑であり,時間の経過とともにより厳しくなることが多い.規制の変化は、私たちが業務を継続または拡大する能力が制限される可能性があり、任意の承認された製品のコストが予想以上であるか、または予想された売上よりも低い場合、許可または承認された場合、適用された法規を遵守しなければ、将来の製品を販売する能力を危険にさらす可能性があり、例えば、警告または無見出しの手紙、罰金、禁止、法令の同意、民事処罰、顧客通知、流通終了、リコールまたは製品の差し押さえ、偽またはブランドの間違っていると信じられる医療機器の行政拘留、製品の市場への延期、操作制限、すべてまたは一部の生産停止; は、将来の新製品の承認または承認、新しい予期された用途、または私たちの製品の修正を拒否します。現在の承認を撤回または一時停止することは、私たちの製品の販売を禁止することになります。最悪の場合、刑事起訴または処罰されます。 これらの事件の発生は、私たちの業務、財務状況、および運営結果に実質的な悪影響を与え、株主のすべての投資損失を招く可能性があります。
私たちは私たちの製品の必要な許可や承認を受けることや遅延することができないかもしれません。私たちの製品の必要な承認や承認をタイムリーに得ることができなければ、私たちの業務成長能力に悪影響を与えます。
米国では、新しい医療機器、新しい用途、既存製品の新しい声明、または重大な修正を販売することができる前に、私たちは、免除が適用されない限り、連邦食品、薬物および化粧品法案510(K)(私たちのINSPIRA ART 100デバイスは許可を得なければならない)またはFDCAの許可を最初に取得しなければならない。510(K)許可プログラムでは、装置が が発売される前に、FDAは、510(K)のプロセスによって以前に承認された装置、1976年5月28日以前に合法的に販売された装置(改訂前の装置)、承認されたPMAに従って最初に米国市場で発売され、後に降格した装置、 または510(K)免除装置を含む、提案された装置が合法的に発売された“アサート”装置“と実質的に等しい”と決定しなければならない。“実質的同等”を達成するためには,提案デバイスは述語デバイスと同じ期待用途を持ち,述語デバイスと同じ技術的特徴を持つか,異なる技術的特徴 を持ち,述語デバイスとは異なる安全性や有効性の問題を起こさない必要がある. がほぼ同等であることを支援するために臨床データが必要となる場合がある。PMA承認を得る過程で、FDAは、技術、臨床前、臨床試験、製造、およびラベルデータを含むが、これらに限定されない大量のデータにある程度基づいて、提案された装置がその予期される用途に対して安全かつ有効であることを決定しなければならない。生命を維持する、生命を支援する、または移植可能な装置のような最大のリスクを構成すると考えられる装置の場合、PMAプロセスが一般的に必要である。
PMA申請によって承認された製品 修正には、通常、FDA承認が必要である。同様に、510(K)認証された製品のいくつかの修正は、新しい510(K)認証を必要とする可能性がある。PMA承認と510(K)承認プロセスはいずれも高価で、時間がかかる可能性があり、確定していない。FDAの510(K)承認プロセスは、通常、3~12ヶ月を要するが、より長く継続する可能性もある。PMAを取得するプロセスは、510(K)の承認プロセスよりもはるかにコストが高く、不確実であり、通常、出願からFDAに提出されるまでに1年から3年以下の時間を要する。さらに、PMAは通常、1つまたは複数の臨床 試験を実行する必要がある。FDAは私たちが承認または承認を求める可能性のあるいかなる設備も承認しないかもしれない。どんな遅延や必要な規制許可や承認を得られなかった場合も、私たちの業務を損なう可能性がある。さらに、私たちが規制許可または承認を得ても、それらの は、デバイスの指定された用途の重大な制限または他の制限または要件を含むことができ、これは、デバイスの市場 を制限する可能性がある。
18
米国では, が多段方式で規制承認の流れを行うことが予想される.第一歩として,我々の先進的なInspira ART(Gen 2)デバイスのためにQ-提出またはQ-Sub申請をFDAに提出する予定であり,Vortxデバイスとして選択することも可能である.統合開発前計画は1995年に設立され、申請を提出する前に将来の調査デバイス免除またはIDE申請に対するFDAのフィードバックを得るためのメカニズムを提供することを目的としている。IDEは、食品および医薬品局に提出された上場前承認申請または発売前通知をサポートするために、調査装置を使用して安全性および有効性データを収集することを可能にします。時間の経過とともに、統合開発前計画 は、PMAS、人道主義設備免除またはHDE、De Novo要求および510(K)提出に関するフィードバックを含むようになり、臨床研究が統合開発環境を提出する必要があるかどうかの問題を解決する。この変化を把握するために、衛生·公衆サービス部部長(HHS)は、2012年の医療機器使用料改正案(MDUFA III)が国会に提出した2012年の承諾状について、FDA約束brを含む構造化されたプロセスを構築してこれらの相互作用を管理し、これを事前提出または事前提出と呼ぶ。2023年6月2日に発表されたQ提出ガイドラインは、“医療機器提出のフィードバックおよび会議要求:Q提出計画” という名称で、Pre-SubおよびFDAと接触するより多くの機会を含むより広範なQ計画を実施した。
FDAと計画中の非臨床と臨床研究、リスク確定と真剣にFDAのフィードバックを考慮して早期相互作用を行うことは、後続提出の品質を高め、総審査時間を短縮し、そして新しい設備の開発過程を促進する可能性がある。FDAは、Pre-Sub内で提供される相互作用は、FDAと提出者のより透明な審査過程に役立つ可能性があると考えている。 私たちは、Q-Subプロセスの一部として、FDAのフィードバックに基づいて、私たちの監督と臨床計画を調整し、更新する予定である。
私たちは2023年9月にINSPIRA ART 100デバイスに510(K)申請 を提出しました。審査プロセスは、まだ行われている反復プロセスであり、私たちが予想しているコストよりも高く、時間がかかる可能性があり、私たちは最終的に審査プロセスを成功させることができない可能性があり、私たちの510(K)申請は、タイムリーでないか、またはFDAによって完全に承認されないかもしれない。承認された場合、私たちINSPIRA ART 100デバイスの任意の修正が以前に承認されなかった場合、変更を実施する前に新しい510(K)販売前通知を提出して承認を得るか、またはPMAを提出してFDA承認 を得る必要があるかもしれません。特に、510(K)によって許可された装置の任意の修正は、その安全性または有効性に著しく影響を与える可能性がある場合、またはその予期される用途、設計、または製造に大きな変化をもたらす可能性がある場合、新しい510(K)許可 が必要とされるか、またはPMAの承認を得る必要がある場合がある。FDAは各メーカーに最初にこの決定を下すことを要求するが、FDAは任意の製造業者の決定を審査することができる。FDAは、新しい許可または承認が必要かどうかに関する私たちの決定に同意しないかもしれません。 私たちは将来、新しい510(K)の承認または承認を必要としないと考えられる追加機能を修正または追加するかもしれません。FDAが我々の決定に同意せず、新たな510(K)通知またはPMA申請を提出することを要求した場合、以前に承認された製品を修正することを要求し、新たな承認または承認を必要としないと結論した場合、承認または承認を得るまで、マーケティングの停止または修正された製品のリコールを要求される可能性があり、巨額の監督管理や罰金または処罰を受ける可能性がある。FDAが将来の製品または既存製品の修正を期待しているよりも長く、より厳しい検査を要求する場合、製品の発売または修正は延期またはキャンセルされる可能性があり、これは私たちの業務を発展させる能力に悪影響を及ぼす可能性がある。
19
FDAは、様々な理由で、医療機器の承認を延期、制限、または拒否することができる
| ● | FDAまたは適用可能な規制エンティティまたは通知機関に、私たちの候補製品がその予期される用途に対して安全または有効であることを証明することはできません | |
| ● | FDA或いは適用される外国の監督管理機関は臨床前研究或いは臨床試験データの設計或いは解釈に対して異なる意見を持っている | |
| ● | 私たちの臨床試験では、参加者は深刻で予期せぬ副作用を経験した | |
| ● | 私たちの臨床前研究および臨床試験のデータは、必要に応じて承認または承認を支持するのに十分ではないかもしれない | |
| ● | この装置の臨床的利益や他の利益がリスクよりも大きいことは証明できません | |
| ● | 私たちが使用している製造プロセスや施設は、適用されるbrの要件を満たしていない可能性があります | |
| ● | FDAまたは適用される外国の規制機関の承認政策や法規の可能性は大きく変化する可能性があり、私たちの臨床データや規制文書は承認または承認を得るのに十分ではない。 |
欧州経済圏またはEEA加盟国で我々の製品を販売するためには,我々の製品はEU医療機器規制(EU)2017/745)の一般的な安全と性能要件に適合しなければならない。これらの要求を守ることは、私たちの製品に基準を満たすヨーロッパあるいはCEマークを貼り付けることができる前提条件であり、これらのマークがなければ、私たちの製品はヨーロッパ経済区で販売したりマーケティングすることができません。一般的な安全と性能要求に適合していることを証明するためには,医療機器のタイプとその分類によって異なる合格評価プログラムが必要である。低リスク医療機器(I類非無菌,非測定機器)に加えて, メーカーはその製品がEU“医療機器条例”の一般的な安全と性能要求に適合する自己評価に基づいてヨーロッパ共同体やEC適合性声明を発表することができる場合,適合性評価プログラム は欧州経済圏加盟国が認めた組織や通知の機関が介入してこそ適合性評価を行うことができる。関連する適合性評価プログラムによると、通知機関は通常、我々の設備の製造、設計、最終検査の技術文書と品質体系を審査·検査する。医療機器とそのメーカーに対する合格評価プログラムの完成に成功し、一般的な安全と性能要求に適合した後、機関に合格証明書を発行することを通知する。この証明書ライセンスメーカーは,関連するEU適合性宣言に準備して署名した後,その医療機器にCEマークを貼り付ける。
私たちのいくつかの製品はヨーロッパ経済区で販売するために、以下のヨーロッパ指令を遵守する必要があるかもしれません
| ● | (EU)2017/2102改正欧州議会·欧州理事会2011年6月8日電気·電子機器への何らかの有害物質の使用制限に関するRoHS指令2011/65/EU。 |
| ● | 2012年7月4日に電気·電子機器の廃棄に関する欧州議会と欧州理事会のWEEE指令2012/19/EU。 |
| ● | 2014年4月16日、欧州議会および理事会は、無線装置市場で無線装置を提供し、欧州経済地域に関連する命令1999/5/ECテキストを廃止することに関する統一加盟国法律の赤色命令2014/53/EUに関する。2016年6月13日から適用されます。 |
| ● | 2006年5月17日機械に関する欧州議会·理事会第2006/42/EC号機械指令、及び第95/16/EC号指令の改正 |
| ● | 欧州議会·理事会2016年4月27日自然人の個人データの処理とこのようなデータの自由な移動の保護に関する(EU)2016/679号条例、第95/46/EC号指令(一般データ保護条例)を廃止 |
私たちの製品は他のEU指示を遵守するように要求されるかもしれない。
20
一般的なルールとして,医療機器とそのメーカーが一般安全と性能要求および基本要求に適合していることの証明は,製品の正常使用条件下での安全性と性能を支援する臨床データの評価に基づいていなければならない。具体的には、製造業者は、デバイスが正常な使用条件下で予想される性能 を達成したことを証明しなければならない。デバイスの予想される性能の利益を考慮する際に、既知および予測可能なリスクおよび任意の不良イベントが最小化および許容可能であり、デバイスの性能および安全性に関する宣言が適切な証拠支持を有することを証明しなければならない。br}もし私たちが適用されるヨーロッパの法律、法規、および指示を遵守し続けることができなければ、私たちは私たちの製品にbr CEマークを貼り続けることができず、ヨーロッパ経済圏でこれらの製品を販売することを阻止する。
上場後の監督管理の要求を守らなければ、私たちは重罰を含めて法執行行動を受ける可能性があり、市場から製品をリコールまたは撤回することを要求する可能性があります。
もし私たちが規制許可または製品または他の未来の製品の承認を得たら、私たちは設備の製造、マーケティング、広告、医療機器報告、販売、販売促進、輸入、輸出、登録、br、および発売を含む持続的かつ一般的な規制要件を守り続けるだろう。例えば、510(K)承認の条件として、FDAへの定期報告の提出が要求されるであろう。これらの 報告は、デバイス除去後の障害およびいくつかの有害事象に関する情報を含む。そのような報告書が提出されていない、または報告書がタイムリーに提出されていないことは、FDAが法執行行動を取ることをもたらす可能性がある。定期的な報告を検討した後、FDAは、より多くの情報を提供することを要求するか、またはさらなる調査を開始することを要求する可能性がある。
我々 が遵守すべき法規は複雑であり,時間の経過とともにより厳しくなる.規制の変化により、私たちがbrを継続したり、業務を拡大する能力が制限されたり、予想されるコストよりも高く、あるいは予想される売上高を下回ったりする可能性があります。私たちが販売設備の適切な規制許可を得た後も、FDA法規と適用される外国法律法規に基づいて、私たちは継続的な責任を負っています。FDA、州、そして外国の規制機関は広範囲な法執行権力を持っている。我々が適用される規制要件を遵守できないことは、FDA、州、または外国の規制機関が法執行行動をとる可能性があり、その中には以下のいずれかの制裁が含まれている可能性がある
| ● | 無見出しの手紙や警告状 | |
| ● | 罰金、禁止、同意法令、民事処罰 |
| ● | 私たちの製品をリコール、流通中止、行政拘留、または差し押さえます | |
| ● | お客様に通知または修理、交換、または返金; | |
| ● | 生産制限、一部生産停止、全面生産停止 | |
| ● | 新製品、新しい予想用途、または既存製品の修正の将来の許可または承認または海外マーケティング許可の承認を遅延または拒否する要求; |
| ● | 製品の許可や承認を取り消したり一時停止したりすることで、私たちの製品の販売が禁止されます | |
| ● | FDAは、他国で販売するために必要な外国政府への証明書の発行を拒否した | |
| ● | 刑事起訴する。 |
これらの制裁のいずれも、予想以上のコストまたは予想よりも低い売上をもたらし、私たちの名声、業務、財務状況、および運営結果に重大な悪影響を及ぼす可能性がある。
さらに、FDAや国や外国当局は、追加的な法規を採用したり、既存の法規を改正したり、他の行動を取ったりする可能性があり、これは、将来開発中の製品の承認を阻止または延期する可能性がある。このようなbr政策や規制変更は、私たちに追加的な要求を加えるかもしれません。新しい許可または承認を得る能力を延期するかもしれません。 は、コンプライアンスコストを増加させたり、私たちが得ることができる任意の承認を維持する能力を制限したりするかもしれません。
21
私たちの製品は連邦、州、外国の法規に従って生産しなければなりません。もし私たちがこれらの法規を守らなければ、私たちは私たちの設備を呼び戻したり、生産を停止させられたりするかもしれません。
私たちの製品生産に使用する方法と施設は品質体系法規或いは国際標準化組織13485標準の要求に符合しなければならず、会社のための品質管理システムを構築するための基本的な参考としなければならない。これは複雑な監督管理方案であり、医療機器の設計、テスト、生産、過程制御、品質保証、ラベル、包装、運搬、貯蔵、流通、設置、サービスと輸送のプログラムと文書をカバーする。電子放射製品のメーカーとして、私たちも放射線衛生法規といくつかの放射安全性能基準を遵守する責任がある。
また、私たちは、私たちのサプライヤーが維持している施設、プログラム、操作が私たちの品質基準と適用される規制要件に適合しているかどうかを検証する必要があります。FDAは、医療機器製造施設(下請け業者を含む場合がある施設)の検査を定期的に発表または発表しないことによって、品質システム(QS)法規またはQSRを実行する。私たちの製品も似たような国家法規と外国の製造に関する様々な法律法規によって制限されています。
私たちの第三者メーカー は適用された法規を遵守するために必要な手順を取らない可能性があり、これは私たちの製品の納品を遅延させる可能性があります。さらに、適用されるFDAまたは国または外国の要求を遵守できなかった、または後に、私たちの製品または製造プロセスに以前に未知の問題があることが発見され、引き起こされる可能性があるが、これらに限定されないが、これらに限定されない:警告手紙または無タイトル手紙;罰金、禁止または民事処罰; 承認の一時停止または撤回;私たちの製品の差し押さえまたはリコール;生産または流通の完全または部分的一時停止; 行政または司法制裁;FDAは私たちの製品に未定または未来の許可または承認を与えることを拒否する; 臨床的一時停止;私たちの製品の輸出入を許可することを拒否する;私たち、私たちの供給者、または私たちの従業員に対する刑事起訴もあります。
このような行動のいずれも私たちの製品の供給に大きな否定的な影響を及ぼすかもしれない。これらの事件のいずれかが発生すれば、私たちの名声は損なわれるかもしれません。私たちは製品責任クレームに直面するかもしれません。私たちは顧客を失い、売上が減少し、コストが増加する可能性があります。
誤用やラベルの外で私たちの製品を使用することは、私たちの市場での名声を損なう可能性があり、製品責任訴訟またはコストの高い調査を招く可能性があり、もし私たちがこれらの用途の普及に参加していると考えられた場合、 規制機関は罰金または制裁に処せられ、いずれも私たちの業務に代価をもたらす可能性がある。
アメリカで承認された私たちの将来の製品の広告や販売促進はFDA、司法省、HHS、州総検察長、国会議員、公衆の厳しい審査を受ける可能性があります。また、米国国外で承認された将来の製品の広告や販売促進活動は、同様の外国規制機関の厳しい審査を受けることになる。
承認または承認が得られれば,我々の製品は特定の適応を得るために必要な規制機関の承認を得ることが予想される。我々は、FDAが承認した使用適応以外の用途のための、または関連地域での使用の適応を承認する他の規制機関が、いわゆる“ラベルなし使用”を許可しないように、我々の市場者および直売者の訓練を行いたい。しかし,医師が医師の独立した専門医療判断の下で,ラベル外で我々の設備を使用することを阻止することはできない。医師がラベル外で我々の設備を使用しようと試みると,患者の受傷のリスクが増加する可能性がある。さらに、FDA承認または任意の外国規制機関によって承認された他の適応のために、我々の装置を使用することは、このような疾患を有効に治療できない可能性があり、これは、医療提供者および患者における私たちの市場的名声を損なう可能性がある。
22
FDAまたは任意の州または外国の規制機関が、私たちの宣伝材料または訓練が非ラベル使用の宣伝を構成していると判断した場合、私たちの訓練または宣伝材料を修正することを要求することができ、または警告手紙、禁止、差し押さえ、民事罰金または刑事罰を必要としない違反者 の発行または実施を含む規制または法執行行動を要求することができる。他の連邦、州、または外国の法執行機関が私たちの業務活動がラベル外使用の普及を構成していると考えていれば、他の規制機関(例えば虚偽申告法)に基づいて行動する可能性もあり、これは刑事、民事と行政処罰、損害賠償、罰金、返還、brの参加を含むが、政府医療計画への参加を排除し、私たちの業務を削減することを含む大きな処罰を招く可能性がある。私たちはこのような行動の影響を受ける可能性があります もし私たちがこのような行動を防御できなかったら、これらの行為は私たちの業務、財務状況、運営結果に大きな悪影響を及ぼす可能性があります。外国の管轄区域には同等の法律と潜在的な結果が存在する。
さらに、私たちの製品brが承認または承認された場合、医療提供者は、私たちの製品を乱用したり、不適切な技術を使用したりする可能性があり、彼らが十分な訓練を受けていなければ、怪我を招き、製品責任のリスクを増加させる可能性がある。もし私たちの装置が誤用されたり、不適切な技術が使用されたりすれば、私たちは私たちの顧客または彼らの患者の高価な訴訟対象になるかもしれない。上述したように、製品責任クレームは、経営陣のコア業務に対する注意力を分散させ、弁護コストが高く、私たちに対する巨額の損害賠償を招く可能性があり、これらの賠償は保険カバー範囲内にない可能性があります。
私たちの製品は、brの不良医療事件を引き起こすか、または故障や故障を引き起こす可能性があり、FDAまたは関連地域の任意の他の規制機関に報告しなければなりません。そうしなければ、私たちは私たちの名声、業務、財務状況、および運営結果を損なう可能性のある制裁を受けることになります。私たちの製品に深刻な安全問題があることが発見された場合、あるいは自発的に私たちの製品をリコールしたり、FDAや他の政府機関の指示の下で私たちの製品をリコールしたりすることは、私たちにマイナスの影響を与える可能性があります。
もし私たちの製品または私たちの他のbrの未来の製品が承認または承認された場合、私たちは、私たちの1つまたは複数の製品が死亡または重傷を引き起こす可能性があることを合理的に示す情報を受けたか、またはそれを理解したときに、FDAに報告するか、または故障が再び発生した場合、死亡または重傷の故障を引き起こす可能性があることを、FDAに報告することを要求する。私たちが報告する義務がある時間は、私たちが不良事件とイベントの性質を知っている日から触発される。私たちは規定された時間内に私たちが知っている有害事象 を報告できないかもしれない。私たちはまた、私たちが報告可能な有害事象を認識していない場合、特にそれが有害事象報告として報告されていない場合、またはそれが意外な有害事象である場合、または製品を使用する際に直ちに除去されることを認識していないかもしれない。もし私たちが報告義務を履行できなかった場合、FDAまたは他の規制機関は、警告状、見出しなし手紙、行政行動、刑事起訴、民事罰金の適用、私たちの設備許可または承認の撤回、私たちの製品の差し押さえ、または未来の製品の承認または承認を延期する行動をとることができる。
製品の設計又は製造に重大な欠陥又は欠陥がある場合、又は製品が健康に対して許容できないリスクを構成する場合、FDA及び外国監督機関は商業化製品のリコールを要求する権利がある。通常、規制機関がリコールを要求する権力は、設備が深刻な損傷や死亡を招く可能性がある合理的な可能性に基づいていなければならない。もし重大な欠陥が発見された場合、私たちは自発的に製品をリコールすることも選択することができる。健康リスクは受け入れられない、部品故障、故障、製造欠陥、ラベル或いは設計欠陥、包装欠陥或いはその他の欠陥或いは適用法規を遵守できないため、政府の強制或いは自発的なリコールが発生する可能性がある。将来的に製品欠陥や他のミス が発生する可能性があります。
製品の欠陥や欠陥を是正するための我々の修正措置 ,FDAおよび任意の他の規制機関が要求する可能性があること、または私たちは が決定する可能性があり、私たちはその装置の新しい許可または承認を得て、その後、修正された設備を販売または流通する必要があります。このような許可や承認を求めることは、リコール設備を適時に交換する能力を遅らせる可能性があります。さらに、私たちが私たちの設備に関連する問題を十分に解決していない場合、私たちはFDA警告状、br製品の差し押さえ、禁止、行政処罰、または民事または刑事罰金を含む追加の規制法執行行動に直面する可能性がある。
会社はFDAに報告する必要がなくても、いくつかのリコールと訂正の記録を保存することを要求されている。FDAや関連地域の他の規制機関に通知する必要がないと考える場合、将来的に私たちの製品を自発的に撤回または修正することができます。FDAや関連地域の他の規制機関が私たちの決定に同意しない場合、それは私たちにこれらの行動をリコールとして報告することを要求することができ、私たちは法執行行動の影響を受ける可能性がある。将来のリコール声明はお客様の名声を損なう可能性があり、私たちの製品責任に対するクレームを招き、私たちの販売にマイナス影響を与える可能性があります。任意の是正措置は、自発的でも非自発的でも、訴訟で自分を弁護するにも、私たちに時間と資金を投入する必要があり、br経営陣は私たちの業務を運営し、私たちの名声と財務業績を損なう可能性があります。
23
我々は,連邦や州医療詐欺や乱用法律,虚偽申告法および医療情報プライバシーと安全法の制約を直接あるいは間接的に受ける可能性がある。もし私たちがこのような法律を遵守できないか、または完全に遵守できなければ、私たちは巨額の処罰に直面するかもしれない。
多くの連邦、州、そして国外の医療法律法規は医療機器に適用される。私たちは、インフォームドコンセントおよび意図的な場合に、連邦医療保険および医療補助などの連邦医療計画に従って支払い可能な任意の物品またはサービスを誘導または奨励するために、直接または間接的に現金または実物で誘致、提供、提供、受け入れまたは支払いを禁止する連邦医療保健計画の反リベート法規を含むいくつかの連邦および州法規の制約を受ける可能性がある。1996年の連邦健康保険携帯および責任法案、またはHIPAAは、任意の医療福祉計画を故意かつ故意に実行または実行しようとした計画、または重大な事実を故意に偽造、隠蔽または隠蔽し、または医療福祉、プロジェクトまたはサービスの交付または支払いに関連する任意の重大な虚偽陳述を行い、刑事および民事責任を適用する。連邦民事通貨罰法は、以下の活動に従事するエンティティに実質的な民事罰金を科すことを許可する:(1)意図的に、要求通りに提供されていないサービスクレームの提出、または任意の方法で虚偽または詐欺を引き起こすこと、(2)連邦医療計画から除外された個人または実体と契約を締結し、連邦医療計画によって精算可能な項目またはサービスを提供すること、(3)連邦反減税法規に違反すること、または(4)既知の追加金を報告し、返還することができないこと。連邦虚偽陳述法令は、重大な事実を知りながら故意に偽造、隠蔽または隠蔽し、または任意の重大な虚偽、架空または詐欺的陳述または陳述を行うこと、または任意の重大な虚偽、架空または詐欺的陳述または記録項を含む任意の虚偽表記または文書を作成または使用することを禁止し、医療福祉、プロジェクトまたはサービスの交付または支払いに関連するbr;連邦民事虚偽請求法案、またはFCAは、他の事項に加えて、このような虚偽または詐欺的クレームの作成、使用、またはそのような虚偽または詐欺的クレームの作成または使用に重要な意味を有する虚偽記録または声明の作成または使用、または虚偽または詐欺的な政府資金支払い請求の提出または提出を禁止するか、または故意に連邦政府への支払い義務を隠蔽または意図的に不正に回避、減少または隠蔽することを禁止する。FCAは、連邦計画(MedicareおよびMedicaidを含む)に支払われた虚偽または詐欺的項目またはサービスのクレーム、クレームによって提供されていないプロジェクトまたはサービスのクレーム、または医療上不必要なbrプロジェクトまたはサービスのクレームを提出または提出するために、誰もが意図的に提出し、共謀して提出し、虚偽のbr声明を作成することを禁止する。この法律はまた誰もが連邦計画の債務を故意に減らすことを禁止している。米国連邦機関は、FCA和解協定で会社の誠実な合意を達成するなど、非通貨救済措置を要求するようになってきている。米司法省は2016年に“イェッツ覚書”に従う意向を発表し、会社のほか、個人をFCA被告 とした。
ほとんどの州にも連邦反リベート法規や虚偽申告法のような法規があり、Medicaid や他の州によって計画されて精算される物品やサービス、またはいくつかの州で適用され、支払者が政府実体であっても個人商業エンティティであっても適用される。連邦公開支払いまたは医師支払い陽光法案計画は、Medicare、Medicaidまたは州児童健康保険計画に従って支払いを提供する製品製造業者が、医師および教育病院に支払ういくつかの支払いおよび他の価値移転、ならびに医師および教育病院に提供される支払いおよび他の価値移転の開示、ならびに医師および他の医療保健提供者およびその直系親族および適用される共同購入組織が所有する所有権および投資権益を毎年追跡し、連邦政府に報告することを要求する。私たちが政府に支払ったお金を適切に追跡し、報告できなかったことは、民事罰金や処罰を招く可能性があり、これは私たちの運営結果に不利な影響を与える可能性がある。また、アメリカのいくつかの州と地方はすでに法律を制定し、医療機器会社にマーケティングコンプライアンス計画を確立し、州政府に定期報告を提出し、及び/或いは定期的に 販売、マーケティング、定価、臨床試験とその他の活動を公開することを要求した。他の州の法律は、いくつかの医療提供者にプレゼント、食事、または他の物品を提供することを含む、いくつかのマーケティング関連活動を禁止している。その中の多くの法律法規は政府職員たちがまだ明確にしていない曖昧な要求を含む。法律とその実施の不明確性を考慮して、私たちの通報行為 は関連連邦と州法律法規の処罰条項の制約を受ける可能性がある。
24
医療機器業界はより厳しい審査を受けており、政府の調査と法執行行動の対象となっており、メーカーが潜在的または既存の顧客に不正な誘引を提供する疑いがあり、医師br顧問との手配を含めて業務を獲得しようとしている。もし私たちの運営や手配がこのような政府法規に違反していることが発見された場合、私たちは民事と刑事罰、損害賠償、罰金、連邦医療保険と医療補助計画から除外され、私たちの業務を削減する可能性があります。これらのすべての処罰は、私たちの業務運営能力および財務業績に悪影響を及ぼす可能性があります。
もし私たちの製品が国際規制登録、許可、承認を得て維持しなければ、私たちはアメリカ以外のところで私たちの製品をマーケティングして販売することができません。
私たちの製品のアメリカ以外の地域での販売は外国の規制要求に制約されており、これらの要求は国/地域によって異なる。承認手続きは国/地域によって異なり、追加的なテストが含まれる可能性がある。米国国外で承認を得るのに要する時間は、FDA承認を得るのに要する時間とは大きく異なる可能性がある。一部の国/地域の法規は、私たちの製品のマーケティングや販売に障害を設定したり、通知だけを要求したりしない可能性がありますが、他の国/地域の法規は、指定された規制機関の承認または承認を得ることを要求しています。登録、許可、または承認を得ることを含む外国法規の要求を遵守することは、高価で時間がかかるかもしれないし、私たちが製品を販売することを計画しているすべての国/地域で規制許可や承認を得ないかもしれないし、私たちは直ちにそうすることができないかもしれない。他の国が要求する場合、登録、許可または承認を得るのに要する時間は、FDAの承認または承認に要する時間よりも長い可能性があり、そのような登録、許可または承認の要求は、FDAの要求とは大きく異なる可能性がある。もし私たちが私たちの製品を修正すれば、追加の規制許可や承認を申請して、修正された製品を販売することができるかもしれません。さらに、私たちは 私たちが獲得した許可を維持するために必要な品質と安全基準を満たし続けることができないかもしれない。もし私たちが特定の国/地域で私たちの許可を維持できなければ、私たちはその国/地域で適用される製品を販売することができなくなるだろう。
FDAの規制許可または承認brは、他の国/地域規制機関の登録、承認または承認を保証せず、登録、承認、または1つまたは複数の外国規制機関の承認は、他の国/地域規制機関またはFDAの登録、承認または承認を保証しない。しかし、1つの国/地域で登録または規制許可または承認を得ることができなかったり、遅延したりすることは、他の国/地域の規制プロセスに悪影響を及ぼす可能性がある。
アメリカやEUの立法や規制改革は、私たちが規制許可や承認を得ることを難しくしたり、承認または承認を得た後に私たちの製品を製造、マーケティング、または流通させるかもしれません。
国会は時々立法を起草し、提出することは、医療機器規制の法定条項を著しく変える可能性がある。また、FDAは、その承認政策を変更し、他の法規を採用したり、既存の法規を改正したり、他の行動を取ったりする可能性があり、これは、将来開発中の製品の承認または承認を阻止または延期し、または現在承認されている製品をタイムリーに修正する能力に影響を与える可能性がある。過去数年間、FDAはその510(K)承認プロセスを改革することを提案し、これらの提案は、臨床データに対する要求およびより長い審査期間を増加させること、または製造業者がその製品に対して510(K)承認プロセスを使用することをより困難にすることを含む可能性がある。例えば、2018年11月、FDA関係者は、FDAはこれから採用するステップをとり、FDCA第510(K)節に基づいて上場前通知経路を現代化しようとしていると発表した。他の事項に加えて、FDAは、510(K)パスを使用する製造業者がより新しい述語を使用することを推進するための提案を計画することを宣言する。 これらの提案は、510(K)経路下で述語として使用されるいくつかの古いデバイスを潜在的に日没させる計画を含み、 は、証明された10年を超える述語 デバイスとの基本的な等価性に基づくクリアされたデバイスリストを公表することができる。2019年5月、FDAはこのような提案について大衆のフィードバックを求めた。FDAは、経路下の述語を除去するためにいくつかが使用されるかどうかのような、新たな許可を必要とする可能性のあるいくつかの行動を考慮すべきであるかどうかを考慮すべきであるかどうかを公衆フィードバックに要求する。これらの提案は最終的に確定または採択されておらず,FDAは国会と協力し,立法によってこれらの提案を実施する可能性がある。したがって、任意の提案が採択されれば、新たな510(K)許可を得る能力を遅らせるために、追加の規制要求がどの程度適用されるか、コンプライアンスコストを増加させること、または既存の許可を維持する能力を制限すること、または他の方法で競争をもたらすことが、私たちの業務に負の影響を与える可能性があるかどうかは不明である。
25
2019年9月、FDA は最終的に指導意見を決定し、このガイドラインはオプションの“安全と性能に基づく”販売前審査経路を記述し、“あるよく知られている設備タイプ”の製造業者に適用し、このような設備 がFDAが確立した客観的な安全と性能基準に適合していることを証明することによって、510(K)の許可経路の下でほぼ同等であることを証明し、それによって製造業者が許可中にその医療設備の安全性と性能を特定の予測設備と比較する必要がないことを除去した。FDAは、“セキュリティおよび性能に基づく”経路に適したデバイスタイプリストを作成し、維持し、各デバイスタイプの性能基準、および実行可能なように、ガイドファイル内で推奨されるテスト方法を決定するために、製品固有のガイドファイルを作成し続ける。FDAは、私たちまたは私たちの競争相手 のために、または現在許可されているデバイスカテゴリのための性能基準を確立する可能性があり、このような性能基準が確立されれば、新しい510(K)の許可を得るか、または他の方法で競合することにどの程度影響を与えるか、それによって、私たちの業務に負の影響を与える可能性があるかどうかは不明である。FDAは、510(K)計画の予測可能性、一貫性、および透明性を向上させるために、510(K)提出ファイルにおいてデバイスのベストプラクティスを選択するためのガイドライン草案を2023年9月に発売する。提案は、完全な方法を用いて除去すること、予期される安全性および性能を達成または超えること、使用または設計に関する明らかなセキュリティ問題がないこと、設計に関連するリコールされた述語デバイスがないことを選択することを含む述語の特徴に重点を置いている。FDAによれば、これらのアプローチは、時間の経過とともに、510(K)計画におけるより安全で効率的な医療デバイスの発展を奨励するであろう。
同様に、特定の汎用仕様または技術および/または臨床要求セット(基準を除く)は、機器、プロセスまたはシステムに適した法的義務を遵守する手段を提供し、EU主管当局によって発表され、CE認証プロセスの一部として強制的である。EUの主管当局は、私たちまたは私たちの競争相手のために、または現在認証を受けているデバイスカテゴリのための性能基準を制定する可能性があり、このような性能基準が確立されていれば、私たちが新しいCE認証を取得する能力にどの程度影響を与えるか、または他の方法で私たちの業務に悪影響を与える可能性のある競争にどの程度影響を与えるかは不明である。
さらに、FDAまたは任意の他の規制機関は、FDAまたは任意の他の関連規制機関、法規、およびガイドラインを修正または再解釈することが多く、その方法は、私たちの業務および製品に重大な影響を与える可能性がある。任意の新しい法規、法規、または既存の法規の改正または再解釈は、任意の将来の製品のコストを増加させたり、審査時間を延長したり、私たちの製品が承認、または承認、製造、マーケティング、または流通を得ることをより難しくする可能性がある。私たちは法規、法規、法律解釈、あるいは政策の変化を確定することができず、公布、公布、採用すれば、私たちの未来の業務にどのような影響を与えるかもしれません。他の事項に加えて、このような変更は、承認または承認を得る前に追加テストを行うこと、製造方法を変更すること、私たちの製品をリコール、交換または停止すること、または追加的な記録を保存することを必要とする場合がある。
FDAや他の規制機関の政策は変わる可能性があり、今後の製品に対する規制部門の承認や承認を阻止、制限、または延期するための追加の政府法規が公布される可能性がある。米国や海外の将来の立法や行政行動によって生じる可能性のある政府規制の可能性、性質、程度を予測することはできない。例えば、バイデン政府のいくつかの政策とアメリカの立法や司法部門の決定は私たちの企業や業界に影響を与える可能性がある。
2020年4月27日、米国の最高裁判所は連邦巡回裁判所の裁決を覆し、これまで国会が“リスク回廊”への120億ドルの資金提供を拒否した決定を維持してきた。国会は、“医療·教育和解法案”(PPACAと略す)で改正された“患者保護·平価医療法案”(Patient Protection And Affordable Care Act)の他の内容を廃止または廃止するための追加立法を考慮する可能性がある。2021年6月17日、米国最高裁は、PPACAが違憲だと考える手続き理由に基づく疑問を却下した。国会が個人強制令brを廃止したためである。したがって、PACAは現在の形で継続的に有効になるだろう。米国最高裁判所が裁決を下す前に、総裁は2021年1月28日に特別な保険加入期間を開始し、PACA市場を通じて医療保険を獲得することを目的とした行政命令を発表した。行政命令はまた、医療補助モデルプロジェクトおよび免除計画の再検討を含む医療補助モデルプロジェクトおよび免除計画の再検討、および医療補助またはPPACAによる医療保険カバー範囲の獲得に不必要な障害をもたらす政策を含む、特定の政府機関に、医療補助またはPPACAの取得を制限する既存の政策およびルールを検討するように指示する。また、2022年8月16日、総裁·バイデンは2022年インフレ削減法案に署名し、個人がPPACA市場で医療保険を購入する増強補助金を2025年計画に延長する。2025年からは,IRAは新たに構築したメーカー割引計画により受益者の最大自己負担コストを著しく低減し,Medicare Part D計画下の“ドーナツホール”を解消した。PPACAは未来に司法や議会の挑戦を受けるかもしれない。これらの挑戦やバイデン政府の医療改革措置がPPACAと我々の業務にどのように影響するかは不明である。このような変化が私たちの業務または財務状況に影響を与える可能性がある程度がまだ不確定であるため、PACAおよびその可能性のある廃止および置換を評価し続ける。もし私たちが既存の要求の変化に適応できない場合、または新しい要求や政策を採用することができない場合、または規制のコンプライアンスを維持できない場合、私たちは私たちが得る可能性のあるマーケティング承認や許可を失う可能性があり、私たちは利益を達成したり維持することができないかもしれない。
26
EUでは、承認されれば、同様の政治的、経済的、法規的発展が、任意の候補製品を利益的に商業化する能力に影響を与える可能性がある。価格およびコスト制御措置の持続的な圧力に加えて、EUまたは加盟国の立法発展は、著しい追加的な要求や障害をもたらす可能性があり、私たちの運営コストを増加させる可能性がある。EUで医療サービスを提供することは、医療サービスの確立と運営、薬品の定価と精算を含み、brはほぼ完全に国家の法律と政策の問題であり、EUの法律や政策ではない。各国政府と衛生サービスプロバイダは衛生保健及び製品の定価と精算を提供する上で異なる優先事項と方法がある。しかし全体的に言えば、大多数のEU加盟国の衛生保健予算の制限は関連する衛生サービスプロバイダの薬品の定価と精算に制限がある。加えて、製品の開発とマーケティングを希望するEUと国家の監督管理負担が増加しており、これは、私たちの候補製品の上場承認を阻止または延期し、承認後の活動を制限または規制し、上場承認を獲得した製品を商業化する能力に影響を与える可能性がある。政治、経済、規制面の発展は定価交渉をさらに複雑化させる可能性があり、精算を受けた後、定価交渉は継続する可能性がある。EUの各加盟国が使用する参考価格と平行貿易、すなわち低価格と高価な加盟国の間の裁定は、価格をさらに下げることができる。薬品の価格制御や精算制限が保証されない任意の国/地域 これらの国/地域で承認されれば、どの製品に対しても優遇された精算や定価手配が許可される。国際市場では、精算や医療支払い制度は国/地域によって異なり、多くの国/地域で特定の製品や療法に価格上限が設けられている。
2017年4月5日,欧州議会は“医療機器条例”(条例2017/745)を採択し,2021年5月26日に施行され,“EU医療機器指令”を廃止し代替した。欧州経済圏加盟国の国家法律で実施されなければならない指令とは異なり、法規 はすべての欧州経済区加盟国に直接適用され、すなわちこれらの法規を実施する欧州経済区加盟国の法律 によって、欧州経済区加盟国間の現在の医療機器規制の違いを除去することを目的としている。医療機器法規はヨーロッパ経済区全体のために統一、透明、予測可能と持続可能な医療機器監督枠組みを構築し、高いレベルの安全と健康を確保し、同時に革新を支持することを目的としている。医療機器条例が含まれています
| ● | 設備を市場に投入するルールを強化し、設備発売後にbrの監視を強化する | |
| ● | 市場に投入された設備の品質、性能、安全をフォローするためのメーカーの責任を明確に規定する | |
| ● | 唯一の識別番号を通じて、サプライチェーン全体の医療機器のエンドユーザー或いは患者に対する追跡可能性を高める |
| ● | 患者、医療専門家、公衆にEUの既存製品に関する全面的な情報を提供する中央データベースを構築する | |
| ● | いくつかの高リスク設備の評価規則が強化されており、これらの設備は市場に投入される前に専門家の追加検査を受ける必要があるかもしれない。 |
27
このような修正は私たちがヨーロッパ経済地域で事業を展開する方法に影響を及ぼすかもしれない。将来的に採用される可能性のあるこれらおよび他の医療改革措置は、より厳しいカバー基準とより低い精算をもたらし、私たちが受け取った任意の承認された製品の価格に追加の下振れ圧力をもたらす可能性があると予想される。連邦医療保険や他の政府援助計画のいかなる精算減少も、個人支払者の支払いの同様の減少を招く可能性がある。また,既存の精算コードや を用いて精算を受けることができる保証はない.上場承認を得ると、コスト制御措置或いは他の医療改革を実施することは私たちの収入を創出し、利益を実現することを阻止し、或いは私たちの薬品を商業化することを阻止するかもしれない。私たちは未来にどのような医療改革措置が取られるのか予測できない。しかし、さらなる立法または法規がある可能性があり、brは業務、財務状況、および運営結果を損なう可能性がある。
医療立法や規制改革措置は,我々の業務や運営結果に実質的な悪影響を及ぼす可能性がある。
私たちの業界は厳しい規制を受けており、法律の変化は私たちの業務、運営、あるいは財務業績に悪影響を及ぼす可能性があります。“医療保健と教育協調法案”(PPACAと略称する)によって改正された“患者保護と平価医療法案”(Patient Protection and Affordable Care Act,PPAAと略称する)は全面的な措置であり、アメリカ国内の医療保険のカバー範囲を拡大することを目的とし、主に雇用主と個人の医療保険への参加を強制すること及び医療補助計画を拡大することである。法律のいくつかの条項は私たちに影響を与え、私たちのいくつかの費用を増加させるかもしれない。
また、PACAが公布されて以来、他の立法改正も採択された。これらの変化は、2013年4月1日に施行された各年度に提供者に支払われる連邦医療保険費用の合計2%減少を含む。これらの削減は2013年4月に施行され,その後法規制が立法 改正されたため,これらの削減は2031年まで有効となる。
2013年1月、オバマ総裁は、いくつかのタイプの提供者への医療保険支払いをさらに減少させ、政府が提供者に多額の支払いを取り戻す訴訟時効を3年から5年に延長する2012年の米国納税者救済法に署名した。これらの法律や新しい法律は、連邦医療保険や他の医療資金のさらなる減少を招く可能性があり、これは私たちの顧客および私たちの財務運営に実質的な悪影響を及ぼす可能性がある。
PPACA,br,および将来とりうる他の医療改革措置は,より厳しいカバー基準を招く可能性があり,我々の顧客が入手可能な製品の精算に追加的なストレスが生じることが予想される。さらに、PACAのいくつかの側面は司法と議会の挑戦を受け続ける可能性がある。例えば、米国の2017年減税および雇用法案、またはTCJA、 は、2019年1月1日から、ある が1年の全部または一部の期間に合格医療保険を維持できなかった個人に対する税金ベースの分担責任支払いを廃止する条項を含み、これは一般に“個人 強制”と呼ばれる。2021年6月17日、米国最高裁は、“個人権限”が国会で廃止されたため、PACA全体が違憲と主張する手続き理由に基づく挑戦を却下した。また,米国最高裁が裁決を下す前に,総裁·バイデンは2021年1月28日に行政命令を発表し,PACA市場による医療保険の取得を目的とした2021年2月26日から2021年8月15日までの特別保険期間を開始した。行政命令はまた,br}の他の機関を含め,作業要求を含む医療補助モデル項目や免除計画の見直し,医療補助やPPACAによる医療保険カバー範囲の獲得に不必要な障害を与える政策を見直し,その制限を見直し,医療保健の獲得を制限する既存の政策やルールを再検討するよう指示している。また、2022年8月16日、バイデン·バイデン総裁は“2022年インフレ削減法案”に署名し、個人がPPACA市場で医療保険を購入する増強補助金を2025年に延長した。2025年からIRAは新たに設立したメーカー割引計画により,受益者の最大自己負担コストを著しく低減し,連邦医療保険D部分計画下の“ドーナツ穴” を解消した。PACA、その実施条例とガイドライン及びその政策に対してより多くの立法と規制改革及び司法挑戦を行う可能性がある。しかしながら、いかなる新しい立法、法規、または法廷での挑戦が、私たちが規制承認を得た任意の製品の価格にどのように影響する可能性があるかは不明である。連邦医療保険や他の政府計画の精算を減らすいかなる場合も,個人支払者の支払いの類似した減少を招く可能性がある。コスト抑制措置や他の医療改革を実施することは、私たちが相当な収入を創出し、利益を実現することを阻止し、あるいは私たちの製品を大規模化して商業化することができるかもしれない。
28
また、EUで医療サービスの確立·運営を含む医療を提供することは、EUの法律や政策の問題ではなく、ほぼ完全に国家の法律や政策の問題である。各国政府と衛生サービス提供者は衛生保健及び製品定価と精算を提供する上で異なる優先事項と方法がある。加えて、EUや国の製品開発·マーケティングを希望する人への規制負担が増加しており、これは、私たちの製品や将来の任意の候補製品の上場承認を阻止または延期し、承認後の活動を制限または規範化し、上場承認を得る任意の製品の商業化能力に影響を与える可能性がある。
私たちは、将来、医療産業に関連する追加の立法または法規(もしあれば)、または最近公布された連邦立法または任意のそのような追加の立法または法規が私たちの業務にどのような影響を与えるかを予測することができない。このような提案や改革の棚上げや承認は、私たちの証券価格を低下させたり、私たちの製品や潜在的な商業化をさらに開発するために資金を調達したり、協力協定を締結したりすることを制限する可能性があります。
FDAや他の政府機関の資金不足や世界的な健康問題による中断は、重要な指導部および他の人員の採用、保留または配置の能力を阻害する可能性があり、あるいは新しい製品や修正された製品がタイムリーに開発、承認または承認または商業化されることを他の方法で阻止する可能性があり、これは私たちの業務にマイナス影響を与える可能性がある。
FDAが新製品を審査·承認または承認する能力は、政府予算および資金レベル、法定、規制および政策の変化、FDAのキーパーソンの雇用および保留、ユーザ費用の支払いを受ける能力、およびFDAが通常の機能を履行する能力に影響を与える可能性があるなど、様々な要素の影響を受ける可能性がある。したがって,FDAの平均審査時間は近年変動している である.また,研究開発活動を援助する他の政府機関への政府の援助は政治過程の影響を受けており,この過程は本質的に不安定で予測不可能である。
FDAおよび他の機関の中断も、新しい医療機器を遅らせることができ、または承認または承認された医療機器の審査および/または必要な政府機関の承認に要する時間を遅らせる可能性があり、これは私たちの業務に悪影響を及ぼす。
環境、社会、および企業ガバナンス(ESG)問題は、気候変動および持続可能な発展に関する問題を含み、私たちの業務、財務状況、および運営結果に悪影響を与え、私たちの名声を損なう可能性がある。
いくつかの投資家、顧客、消費者、従業員、および他の利害関係者は、ESG問題への関心が高まっている。また、公衆利益と上場企業のESG実践に関連する立法圧力は増加し続けている。もし私たちのESG実践が規制要求を満たしていない場合、あるいは投資家、顧客、消費者、従業員または他の利害関係者の環境管理、地域コミュニティへの支援、取締役会と従業員の多様性、人的資本管理、従業員の健康と安全実践、製品品質、サプライチェーン管理、会社の管理と透明性などの分野の責任ある企業市民の絶えず変化に対する期待と基準は、私たちの名声、brブランドと従業員の保留率は負の影響を受ける可能性があり、私たちの顧客とサプライヤーは引き続き私たちとビジネスをしたくないかもしれない。
顧客、消費者、投資家、その他の利害関係者は気候変化、エネルギーと水の使用、プラスチックゴミ とその他の持続可能な発展問題を含む環境問題にますます注目している。気候変動に対する懸念は、環境への影響を低減または軽減するために、新たなまたは増加した法律·法規要件をもたらす可能性がある。顧客および消費者の選好の変化または規制要件の増加は、使い捨ておよび回収不可能なプラスチック製品および包装、私たちの製品の他の構成要素および持続可能な環境への影響、または顧客および消費者のいくつかの製品に存在する物質への影響の懸念brまたは認知(正確であっても不正確であっても)を含むプラスチックおよび包装材料の需要または要求の増加をもたらす可能性がある。これらの要求や要求を遵守することは、追加的な製造、運営、または製品開発コストを発生させる可能性がある。
私たちが新しい法規に適応していないか、または投資家、業界、または利益関係者のESG問題に対する絶えず変化する期待および懸念を満たしていない場合、投資家 は、彼らのわが社への資本投資を再考慮する可能性があり、顧客および消費者は、私たちの製品の購入を停止することを選択する可能性があり、これは、私たちの名声、サービス、または財務状況に重大な悪影響を及ぼす可能性がある。
29
私たちの知的財産権に関するリスク
もし私たちが私たちの製品とサービスの有効な特許権を獲得して維持できなければ、私たちは私たちの市場で効果的に競争できないかもしれません。もし私たちが私たちの商業秘密やノウハウの機密性を保護できなければ、このような固有の情報は他の人たちによって私たちと競争するために使用されるかもしれない。
私たちの成功と将来の収入の増加は私たちが特許権を保護する能力にある程度依存するだろう。付与される可能性のある任意の特許によって提供される保護に加えて、歴史的には、私たちは、当社の従業員、コンサルタント、およびbr契約者と締結された商業秘密保護および秘密協定に依存して、非特許を保護するか、または特許を出願しない独自技術、知りにくいまたは容易に決定され、特許侵害の監視および実行が困難なプロセスを選択し、私たちの候補製品発見および開発中に特許がカバーされていないノウハウ、情報または技術に関する任意の他の要素を選択する。しかし、協定は違反される可能性があり、商業機密は保護されにくい可能性があり、私たちはどんな違反に対しても十分な救済措置を得ることができないかもしれない。さらに、私たちのビジネス秘密および知的財産権は、競争相手 または他の許可されていない第三者によって知られているか、または独立して発見される可能性がある。
私たちの技術について提出された特許出願が特許登録につながる保証はありません。もし が特許登録を完了できなかった場合、私たちの開発は独自ではなく、他のエンティティが私たちの製品を生産したり、私たちのサービスを設計し、彼らと競争することを可能にするかもしれません。
さらに、我々の特許出願に関連するすべての潜在的な既存技術が発見されたことは保証されず、これは、特許を無効にするか、または係属中の特許出願から特許が発行されることを阻止する可能性がある。特許が発行に成功したとしても、そのような特許が私たちの製品またはサービスをカバーしていても、第三者は、その有効性、実行可能性、または範囲に疑問を提起する可能性があり、これは、そのような特許が縮小され、 実行不可能または無効であることが発見される可能性がある。さらに、挑戦されていなくても、私たちの特許出願および将来の任意の特許は、私たちの知的財産権、製品またはサービスを十分に保護することができず、私たちの新製品またはサービスに排他性を提供したり、他の人の私たちの権利要件をめぐる設計を阻止したりすることができないかもしれない。しかも、第三者が私たちの特許や同様の独占権を侵害したり盗用しないという保証はない。しかも、私たちが自分の権利を守るために他の当事者たちに訴訟を提起しないという保証はない。
これらの結果のいずれも、第三者の競争を阻止する能力を弱める可能性があり、第三者競争は私たちの業務に悪影響を及ぼす可能性がある。
私たちの製品やサービスの有効な特許権を獲得して維持できなければ、効果的な競争ができない可能性があり、私たちの業務と運営結果は損害を受けることになります。
我々は,我々のビジネス秘密や他の機密固有情報が我々の秘密協定に違反して漏洩しないことを保証することはできず,競合他社が我々のビジネス秘密や独立開発と実質的に同じ情報や技術 を他の方法で取得しないことを保証することはできない.さらに、私たちのビジネス秘密および知的財産権の不正流用または不正開示は、私たちの競争的地位を損なう可能性があり、私たちの業務に重大な悪影響を及ぼす可能性があります。また,我々のビジネス秘密や知的財産権を保護するための措置が不十分であると考えられる場合,第三者がbrのいかなる商業秘密を盗用しているかを起訴するのに十分な追跡権がない可能性がある.
30
第三者の知的財産権は、製品およびサービスを商業化する能力に悪影響を及ぼす可能性があり、私たちは、私たちの候補製品を開発またはマーケティングするために、訴訟を提起するか、または第三者から許可を得る必要があるかもしれません。このような訴訟や許可証はコストが高いかもしれないし、商業的に合理的な条項では得られないかもしれない。
第三者の権利を侵害することなく私たちの運営自由を最終的に評価すること自体が困難である。所有する既存の特許または第三者に発行された特許出願または他の第三者知的財産権によって生成された特許が、私たちの製品またはサービスまたはその要素をカバーしている場合、または私たちの製造または使用が私たちの開発計画に関連している場合、私たちの競争地位は悪影響を受ける可能性がある。このような ケースでは、関連する第三者知的財産権を無効または無効にするか、または知的財産権所有者とライセンス契約を締結する場合、関連する第三者知的財産権を無効または無効にするか、または知的財産権所有者とライセンス契約を締結することができない場合、このような ケースでは、製品またはサービスまたは私たちの候補製品(および任意の関連サービス) を開発または商業化することができないかもしれない(商業的に合理的な条項で利用可能である)。また処理されなければならない特許出願は、発行された特許をもたらした場合、私たちの新製品またはサービスによって侵害として告発される可能性がある。もしこのような侵害クレームが提起されて成功すれば、私たちは巨額の損害賠償金の支払いを要求され、私たちの新製品やサービスを放棄したり、任意の特許所有者に許可を求めさせられたりする可能性がある。ライセンスが商業的に合理的なbr条項で提供されることは保証されない(あれば).
関連する第三者特許や応用を識別できなかった可能性もある.例えば、2000年11月29日までに出願された米国特許出願およびその日後に提出されたいくつかの米国特許出願は、特許発行前に米国国外に提出されないため、秘密にされるであろう。米国および他の地方の特許出願は、優先権を要求する最初の出願の約18ヶ月後に発行され、この最初の出願日は、一般に優先権日と呼ばれる。したがって,我々の新製品やサービスに関する特許出願は,我々が知らずに他人によって提出されている可能性がある.さらに、公表された係属中の特許出願 は、私たちのサービス、私たちの新製品、または私たちの新製品を使用するために、後で修正することができる。第三者知的財産権権者もまた、私たちに権利侵害クレームを積極的に提起することができるかもしれない。私たちは、私たちがこのような侵害クレームを成功的に解決できるか、または他の方法で解決できる保証はない。もし私たちが受け入れられる条項で未来のクレームを成功的に解決できない場合、私たちは費用が高く、予測不可能で時間のかかる訴訟を行ったり続けたりすることが要求される可能性があり、私たちの新製品やサービスの開発および/またはマーケティングにおいて重大な遅延が阻止されたり、販売されたりする可能性があります。もし私たちがこのような紛争で失敗した場合、損害賠償金の支払いを余儀なくされるほか、権利侵害と考えられる新製品やサービスの商業化が一時的または永久的に禁止される可能性があります。可能であれば、私たちはもう第三者の知的財産権を侵害しないように、私たちの新製品を再設計することを余儀なくされるかもしれない。これらの事件のいずれかは、私たちが最終的に勝っても、私たちが大量の財務と管理資源を移転することを要求するかもしれません。そうでなければ、私たちは私たちの業務に投入することができます。
知的財産権侵害の第三者クレームは、我々の開発と商業化努力を阻害または延期する可能性がある。
私たちの商業的成功は私たちが第三者の特許と固有の権利の侵害を避けることにある程度かかっている。我々が新製品やサービスを開発する分野には、第三者が所有する米国や外国から発行された特許や未解決の特許出願が多く存在する。我々の業務が拡大し、より多くの特許が発行されれば、我々の製品やサービスが第三者特許権侵害の告発を受けるリスクが高まる可能性がある。
第三者は私たちが許可されていない状況で彼らのノウハウを使用していると断言するかもしれない。当社の製品またはサービスの使用または製造に関連する材料、設計または製造方法の第三者特許または特許出願が存在する可能性がある。現在、処理されるべき特許出願または後続の特許出願がある可能性があり、これらの出願は、私たちの製品またはサービスが発行された特許を侵害する可能性がある。さらに、第三者は将来的に特許またはサービスを取得する可能性があり、私たちの技術を使用してこれらの特許を侵害したと主張する。
管轄権のある裁判所が、私たちの設計過程または使用方法のあらゆる面をカバーするために、任意の第三者特許 を持っている場合、任意のこのような 特許の所有者は、許可されているか、またはそのような特許が満了するまで、または最終的に無効または実行不可能であると判定されない限り、私たちが許可されているか、またはそのような特許が最終的に無効または実行不可能であると判断されない限り、私たちが開発および商業化に適用される候補製品を阻止することができるかもしれない。いずれの場合も、そのようなライセンスは、商業的に合理的な条項 で取得できないか、または全く取得できない可能性がある。
私たちにクレームを出した当事者は、禁止または他の公平な救済を受けることができ、これは、私たちの1つ以上の製品やサービスのさらなる開発と商業化を効果的に阻止することができるかもしれない。これらのクレームの弁護は、その是非曲直にかかわらず、巨額の訴訟費用 に関連し、私たちの業務中の従業員資源を大量に分流する。もし私たちに対する侵害クレームが成功した場合、私たちは故意に侵害された3倍の損害賠償と弁護士費、印税の支払い、brの再設計、または第三者から1つまたは複数のライセンスを取得することを含む巨額の損害賠償を支払わなければならないかもしれないし、または大量の時間とお金の支出が必要である可能性がある。
31
特許政策および規則の変化は、私たちの特許出願をめぐる起訴および発行された任意の特許の実施または保護の不確実性およびコストを増加させる可能性がある。
米国および他の国/地域特許法または特許法解釈の変更 は、我々の特許出願において発行される可能性のある任意の特許の価値を低下させるか、または我々の特許保護範囲を縮小する可能性がある。外国の法律はアメリカの法律のように私たちの権利を保護しないかもしれない。科学文献で発見された発表は往々にして実際の発見に遅れており、米国と他の司法管轄区の特許出願は通常提出後18ヶ月以内に発表され、時には全く発表されないこともある。したがって、私たちは、私たちが所有および許可された特許または係属中の出願に保護を要求する最初の発明のbrであるか、または私たちまたは私たちの許可者が、そのような発明のために最初に特許保護された であることを確認することはできない。特許可能性の他のすべての要件が満たされていると仮定すると,2013年3月15日までの米国では,最初に保護を要求した発明を提出し,無断遅延なしに提出した者が特許を取得する権利があるが,通常米国以外では,最初に特許出願を提出した者が特許を取得する権利がある。2013年3月15日以降、2011年9月16日に公布された“Leahy-Smith America発明法”(以下、“Leahy-Smith米国発明法”)に基づき、米国では先行出願後申請制度が開始された。Leahy-Smith法案はまた一連の重大な変化を含み、これらの変化は特許出願の起訴方法に影響を与え、特許訴訟に影響を与える可能性もある。全体的に、“ライシー·スミス法案”およびその実施は、私たちの特許出願をめぐる起訴および発行された特許の実行または保護をめぐる任意の不確実性およびコストを増加させる可能性があり、これらのすべては、私たちの業務および財務状況に重大な悪影響を及ぼす可能性がある。
私たちは費用が高く、時間がかかって成功しない可能性があるbrを保護したり、私たちの知的財産権を強制的に執行する訴訟に巻き込まれるかもしれない
競争相手は私たちの知的財産権を侵害するかもしれない。もし私たちが第三者に対して私たちの新製品またはサービスをカバーする特許を強制的に執行するために法的訴訟を提起した場合、被告は私たちの候補製品をカバーする特許を無効および/または強制執行できないと反訴することができる。米国の特許訴訟では,被告が無効および/または実行不可能と主張する反訴が一般的である。有効性疑問の理由は、新規性の欠如、明らかまたは実行不可能性を含むいくつかの法的要件のいずれかを満たすことができなかったと言われている可能性がある。 実行不可能な主張の理由は、特許訴訟に関連する者が起訴中に米国特許商標局やUSPTOに関する情報を隠蔽したり、誤った声明をしたりした可能性がある。ライシー·スミス法案によると、米国特許の有効性は、米国特許商標局の授権後の訴訟でも問われる可能性がある。法的に無効と実行不可能と断言された後の結果は予測できない。
第三者によって開始されるか、または我々によって提起された派生プログラムは、我々の特許または特許出願または我々の許可者の特許に関連する発明の優先権および/またはその範囲を決定するために必要である可能性がある。不利な結果は、私たちが関連技術の使用を停止したり、勝利者から許可を得ようと試みることを要求するかもしれない。もし勝利者が商業的に合理的な条項に従って許可証を提供しなければ、私たちの業務は損害を受ける可能性があります。私たちの訴訟弁護や介入訴訟は失敗する可能性があり、成功しても巨額のコストを招き、私たちの経営陣や他の従業員の注意を分散させる可能性があります。また,訴訟に関連する不確実性は,我々の臨床試験を継続し,我々の研究計画を継続するために必要な資金を調達し,第三者から必要な技術的許可を得たり,新製品やサービスを市場に出す能力に実質的な悪影響を与えるのを助けるために協力パートナーシップを構築したりする可能性がある。
さらに、知的財産権訴訟は大量の発見を必要とするため、私たちのいくつかの機密情報は、このような訴訟中に開示によって漏洩される可能性がある。公聴会、動議、または他の一時的な手続き、または事態発展の結果 も公表される可能性がある。もし証券アナリストや投資家がこれらの結果がマイナスだと思っていれば、 は私たちの証券価格に実質的な悪影響を及ぼす可能性がある。
32
私たちは私たちの知的財産権リストのクレームに疑問を受けるかもしれない。
私たちは、元従業員、協力者、または他の第三者が、発明者または共同発明者として、現在の特許および特許出願、将来の特許または他の知的財産権において権益を有するか、または賠償を受ける権利を有するというクレームの制約を受ける可能性がある。例えば、私たちは、私たちの製品やサービスの開発に参加するコンサルタントや他の人の義務衝突による在庫紛争があるかもしれません。在庫に挑戦したり、賠償権利を要求するこれらや他のクレームに対抗するために訴訟を起こす必要があるかもしれません。もし私たちがこのようなクレームを弁護できなかった場合、金銭損害賠償を支払うことに加えて、私たちは価値のある知的財産権の独占所有権や使用権のような貴重な知的財産権を失う可能性がある。このような結果は私たちの業務に実質的な悪影響を及ぼすかもしれない。私たちがこのようなクレームを弁護することに成功しても、訴訟は巨額のコストを招き、経営陣や他の従業員の注意を分散させる可能性がある。
私たちは世界的に私たちの知的財産権を保護できないかもしれない。
世界のすべての国/地域で製品やサービスの特許を申請、起訴、保護し、その侵害行為を監視する費用は目を引くほど高く、私たちの特定の国での知的財産権は米国ほど広くないかもしれない。また、一部の国·地域の法律は知的財産権の保護程度は米国の連邦や州法律に及ばない。
競争相手は、私たちの技術を使用して、私たちが特許保護を受けていない司法管轄区で自分の製品やサービスを開発し、私たちに特許保護を持っているが、特許執行はアメリカのような厳格な地域に侵害製品やサービスを輸出することはできません。これらの製品やサービスは、私たちの製品やサービスと競争する可能性があります。将来の特許または他の知的財産権は、それらの競争を効果的にまたは阻止するのに十分ではないかもしれない。
多くの会社は外国の管轄区域の知的財産権の保護と保護に重大な問題に直面している。特定の国の法律制度、特にある発展途上国の法律制度は、特許、商業秘密、および他の知的財産権保護の実施を支持していないことは、私たちの専有権を侵害する競争製品やサービスのマーケティングを全体的に阻止することを困難にするかもしれない。外国の管轄地域で私たちの特許権の訴訟を実行することは、成功するか否かにかかわらず、大きなコストを招く可能性があり、私たちの努力と注意を私たちの業務の他の側面から移行させることは、私たちの将来の特許が無効または偏狭に解釈されるリスクに直面する可能性があり、私たちの特許出願の発行がリスクに直面する可能性がある。第三者が私たちにクレームをつける可能性があります私たちは私たちが始めたいかなる訴訟でも勝てないかもしれません。私たちが得る可能性のある損害賠償や他の救済措置はビジネス的な意味がないかもしれません。したがって、私たちの知的財産権を世界各地で監視し、実行する努力は、私たちが開発または許可した知的財産権から顕著なbr商業的優位性を得るのに十分ではないかもしれません。
33
私たちの証券所有権に関わるリスクは
私たちの証券の市場価格は引き続き高度に変動する可能性があります。お支払いいただいた価格以上で普通株を転売することができないかもしれません。
我々が2021年7月に初公募株を完成させて以来、私たちの普通株と引受権証の取引価格は安定しておらず、変動し続ける可能性がある。株式市場全体、特に医療機器会社の市場は、極端な変動を経験しており、 は往々にして特定の会社の経営業績と関係なく、彼らの基本業務モデルや見通しが根本的に変わっていないにもかかわらず、多くの会社の株価下落を招いている。潜在的な経済状況の悪化、インフレ及びその他の悪影響を含む幅広い市場及び業界要因は、我々の実際の経営実績にかかわらず、我々証券の市場価格に負の影響を与える可能性がある。このような変動のため、あなたはあなたが支払った価格であなたの証券を売ることができないかもしれません。本節で紹介した他のリスク要因を除いて、以下の要素は私たちの証券の市場価格に重大な影響を与える可能性がある
| ● | さらなる臨床試験を実施するための承認を得ることができない | |
| ● | 臨床試験結果は理想的ではなかった | |
| ● | 規制の承認を発表するか、承認を得られなかったか、またはbrを使用した特定のラベル適応または患者集団、または規制審査中の変更または遅延; | |
| ● | 私たちまたは私たちの競争相手は革新や新製品を発表します。 | |
| ● | 規制当局が私たちの臨床試験、製造サプライチェーン、または販売、マーケティング活動に取った不利な行動 | |
| ● | 私たちは製造業者やサプライヤーとの関係のいかなる不利な変化も; | |
| ● | 私たちが関わっている可能性のある知的財産権侵害 | |
| ● | 予想された製品販売および収益性を達成するか、または予期されたbr}を達成できなかった | |
| ● | 私たちは訴訟に参加したり |
| ● | 取締役会や経営陣が大きく変動しています | |
| ● | 私たちには合格した監督、研究開発者を採用し、維持する能力がある |
| ● | アメリカの医療機器販売や定価に関する立法 | |
| ● | 私たちの普通株式と権利証の取引市場の深さ; | |
| ● | インフレや特定の外国経済や市場の政治的不安定を含む経済的疲弊 |
| ● | 局所的または全世界的な疫病、例えば新冠肺炎や他の衛生疫病、戦争やテロ、または自然災害による業務中断を含む地政学的行動 | |
| ● | 従業員の株式オプションまたは他の持分報酬を付与または行使すること; | |
| ● | 投資家や証券アナリストは、我々の業務の業務リスクや状況に対する見方が変化している |
また、株式市場 ,特にナスダックは、極端な価格と出来高変動を経験しており、これらの変動は小さな会社の経営業績に関係なく、あるいは比例しないことが多い。私たちの実際の経営業績にかかわらず、広範な市場と業界要素は私たちの普通株の市場価格にマイナス影響を与える可能性がある。また、金融市場の系統的な下落や私たちのコントロール範囲を超えた関連要素は、私たちの株価を迅速に、意外に下落させる可能性がある。
将来私たちの普通株を売ることは私たちの証券の市場価格を下げるかもしれません。
ナスダックで私たちの普通株を大量に投げ売りすることは私たちの証券の市場価格を下落させるかもしれません。私たちまたは私たちの証券保有者が私たちの普通株を大量に売却したり、これらの売却が将来的に発生する可能性があると考えたり、私たちの証券の市場価格を低下させる可能性があります。
任意の追加の普通株または普通株で行使可能または普通株に変換可能な任意の証券を発行することは、私たちの普通株の市場価格に悪影響を与え、私たちの既存株主および普通株保有者に希釈効果をもたらす可能性がある。
34
私たちの主要株主、高級管理者、br取締役は現在実益が私たちの23.6%の普通株を持っています。したがって、彼らは私たちの株主承認に提出された事項を統制することができるかもしれない。
2024年3月22日現在、私たちの主要株主、役員、取締役実益は約23.6%の普通株を持っています。したがって、これらの株主 が一緒に行動すれば、取締役選挙や合併または他の業務合併取引の承認を含む、我々の株主の承認を必要とする事項に影響を与える可能性がある。このような株主の利益はいつも私たちの利益や他の株主の利益と一致しないかもしれない。
私たちは私たちの株に現金配当金を支払ったことがなく、私たちは予測可能な未来にも現金配当金を支払わないと予想している。
私たちは現金配当金を支払うことを発表したり、発表したことがなく、私たちは予測可能な未来にも現金配当金を支払わないと予想している。したがって、あなたは将来の配当収入の源として、私たちの証券への投資 に依存してはいけません。私たちの取締役会は配当金を割り当てるかどうかを決定する権利が完全にある。私たちの取締役会が配当金を発表して支払うことを決定しても、将来の配当の時間、金額、形式は、私たちの将来の運営結果とキャッシュフロー、私たちの資本要求と黒字、私たちが子会社から受け取った割り当て金額{br)、私たちの財務状況、契約制限、そして私たちの取締役会が関連すると思う他の要素 に依存します。
雇用法案は、投資家を保護するためのいくつかの法律や法規を遵守する締め切りを延期することを可能にし、米国証券取引委員会に提出された報告書で提供される情報量を減少させることができ、これは、当社に対する投資家の信頼を低下させ、私たちの証券の市場価格に悪影響を及ぼす可能性がある。
私たちがまだ“雇用法案”で定義されている“新興成長型企業”である限り、“新興成長型企業”ではない上場企業に適用される様々な要求の免除を利用します
| ● | サバンズ-オキシリー法案の条項は、私たちの独立公認会計士事務所に、私たちの財務報告の内部統制の有効性に関する証明報告書を提供することを要求します | |
| ● | 上場企業会計監督委員会が採用する可能性のある任意の規則は、強制監査会社のローテーションあるいは監査人の財務諸表報告書の補充を要求する。 |
私たちはこれらの免除を利用して、私たちがもはや“新興成長型会社”ではなくなるまで利用しようとしている。私たちは、(1)財政年度の最終日まで、(A)私たちの初公募株(Br)が完成した日の5周年後、(B)私たちの年間総収入が少なくとも12.35億ドルに達するまで、または(C)大型加速br}申請者とみなされています(“取引法”の規則で定義されているように)、(2)前の3年間に10億ドルを超える転換不可能債務の日付を発行する前に。
私たちはこれらの免除に依存する可能性があるので、投資家 が私たちの証券吸引力の低下を発見するかどうかを予測できない。したがって、一部の投資家が私たちの証券吸引力が低下していることを発見すれば、私たちの証券取引市場はそれほど活発ではなくなり、私たちの市場価格はもっと変動し、低下する可能性がある。
“外国の個人発行者”として、他の適用される米国証券取引委員会やナスダック要求 ではなく、いくつかの自国の企業統治実践に従うことが許可され、これは、米国国内発行者に適用されるルールよりも投資家の保護を少なくする可能性がある。
私たちは外国の個人発行者としての身分もまた、私たちはアメリカ証券取引委員会のいくつかの法律法規とナスダックのいくつかの規定を遵守することを免れて、委託書規則、短期利益返還規則及び取締役の役員指名と役員報酬に対する独立監督(Br)などのいくつかの管理要求を含む。また、取引法によれば、証券が取引法に基づいて登録されている米国国内会社のように、最新の報告書および財務諸表を米国証券取引委員会に頻繁にまたはタイムリーに提出する必要はなく、通常、米国証券取引委員会に四半期報告書を提出する必要はない。さらに、イスラエル“会社法”(5759-1999)または“会社法”は、最高報酬の上位5人の上級管理職の年収(全体的な開示ではなく)を単独で開示することを要求しているにもかかわらず、このような開示は、米国内の発行者が要求するほど広くはない。また、外国の個人発行者としても、“取引法”に基づくFD(公平開示)法規の要求を受けていない。
35
これらの免除と寛大な処理は、あなたが投資家として獲得する権利のある情報と保護の頻度と範囲を減少させます。
外国人個人発行者の身分の決定は、発行者が最近完成した第2四半期の最終営業日に毎年行われるため、2024年6月30日に次の決定を行う。将来、私たちの大多数の株主、役員、経営陣がアメリカ市民や住民であり、外国のプライベート発行者のアイデンティティを失うことを避けるために必要な追加の要求を満たすことができなければ、私たちは外国のプライベート発行者のアイデンティティを失うだろう。アメリカ証券法 によると、アメリカ国内登録業者として、私たちの規制とコンプライアンスコストははるかに高いかもしれません。
米国連邦所得税については,我々は本納税年度に“受動型外国投資会社”やPFICである可能性があり,任意の後続納税年度に受動外国投資会社となる可能性もある。もし私たちがPFICになるかどうかなら、一般的にこれらの証券を持つアメリカの納税者に否定的な税金結果をもたらすだろう。
我々の収入の予測構成と我々の資産の推定値に基づいて,2024年にPFICであることは信じられず,2025年にはPFICにはならないと予想され,将来PFICにはならないことが予想されるが,この点では保証されていない。私たちがPFICであるかどうかは年ごとに決定されます は私たちの収入と資産の構成に依存します。いずれの課税年度においても、米国連邦所得税用途のPFIC とみなされ、(1)私たちの総収入の少なくとも75%が“受動収入” である場合、または(2)価値で計算すると、平均少なくとも50%の資産が受動収入を生成するか、または受動収入を生成するために保有される。この目的のための受動的収入は、一般に、受動的収入を生成するいくつかの配当金、利息、特許権使用料、レンタル料、および商品および証券取引から得られる収益、ならびに財産の売却または交換から得られる収益を含む。受動的収入には、公募株で調達した資金も含め、一時資金投資で得られた金額も含まれる。 非米国会社がPFICであるかどうかを決定する際には、直接または間接的に所有する各社の収入と資産の割合シェア の少なくとも25%の利息(価値で計算)を考慮すべきである。PFICの地位を確定するテストは年に1回行われるため、この確定に関連する未来の収入と資産を正確に予測することは困難である。しかも、私たちのPFICの地位は証券の市場価値にある程度依存するかもしれない。したがって,我々が現在PFIC にならないことは保証されない.もし私たちが米国納税者が証券を保有する任意の課税年度のPFICであれば、この米国納税者はいくつかの不利な米国連邦所得税規定の制約を受けるだろう。特に、米国納税者が私たちを“適格な選挙基金”またはQEFとみなすか、または“時価ベース”の選挙を行うことを選択していない場合、米国納税者は、私たちの証券が達成された任意の収益を米国納税者、 および米国納税者に“超過分配”し、(1)米国納税者が私たちの証券を保有している間に比例的に分配する。(2)本課税年度と本課税年度の最初の課税年度の初日までのいずれかの期間に割り当てられた金額を一般収入として課税すること、および(3)他の課税年度に割り当てられたbr年度毎の金額を適用種別の納税者の当該br年度の最高税率で課税し、そのbr}他の課税年度に起因することにより生じる税項目に利子費用を徴収することができる。また、もしアメリカ国税局やアメリカ国税局が私たちが1年以内にPFICであると判断し、私たちがPFICではないと判断した場合、アメリカの納税者にとっては、QEFや時価建ての選挙をタイムリーに行うのは遅すぎるかもしれません。私たちがPFICを担当している間に私たちの証券を持っているアメリカの納税者は、その後数年間PFICでなくても、上記のルールに拘束されます。しかし、QEFや時価計算選挙をタイムリーに行う米国の納税者は除外される。米国納税者 は、8621フォームの関連部分を記入し、フォーム説明に従ってIRSフォームを提出することによって、QEF選挙を行うことができる。私たちは私たちの証券を持っているアメリカの納税者に通知するつもりはありません。もし私たちがどの納税年度にPFICとみなされると信じていれば、アメリカの納税者がQEF選挙を行うかどうかを考慮できるようにします。さらに、IRS Form 8621を記入するために必要な情報を毎年このような米国納税者に提供し、私たちまたは私たちの任意の子会社がPFICのための任意の年に有効なQEF選挙を行い、維持するつもりはない。私たちの証券を持っているアメリカの納税者はPFICルールについて彼らの税務顧問に相談することを強く提案して、納税要求と私たちがPFICである場合、私たちの証券についてQEFあるいは時価建ての選択は彼らに対する資格、方式、結果を含む。
私たちは証券訴訟を受けるかもしれませんが、これは高価で、経営陣の注意をそらすかもしれません。
過去、株式市場価格が変動した会社は証券集団訴訟の影響を受ける。私たちは未来のこのような訴訟の目標かもしれない。このような訴訟は、巨額のコストと経営陣の注意力と資源を移転させる可能性があり、これは私たちの業務を深刻に損なう可能性がある。訴訟のどんな不利な判決もまた私たちに重大な責任を負わせるかもしれない。
36
証券や業界アナリストが、私たち、私たちの業務、または私たちの市場に関する研究や報告を発表または停止しない場合、または彼らが彼らの提案を不利に変えたり、私たちの業務または証券に関する否定的な報告書を発表したりすれば、私たちの株価や取引量は低下する可能性がある。
私たちの証券の取引市場は、業界または証券アナリストが発表する可能性のある、私たちの業務、私たちのbr市場、または私たちの競争相手に関する研究と報告の影響を受けるだろう。私たちはこのようなアナリストに対して何の統制権もなく、アナリストが私たちをカバーしたり、有利なカバー範囲を提供することを保証することもできない。もし私たちのアナリストが私たちの証券に不利に彼らの提案を変えたことを報道することができれば、私たちの競争相手にもっと有利な相対的な提案を提供したり、私たちの証券の価格が下がるかもしれません。私たちのアナリストを追跡する可能性のある任意のアナリストがわが社への報告を停止したり、私たちに関する報告書を定期的に発表できなかったりすれば、金融市場での可視度を失う可能性があり、これは私たちの証券価格や取引量の低下を招く可能性がある。
あなたは未来の株式発行のために未来の希釈を経験するかもしれない。
追加の資本を調達するために、私たちは将来、追加の普通株または他の普通株または普通株に交換可能な証券 を発行する可能性があり、価格は今回発行された1株当たりの価格とは異なる可能性がある。私たちは、投資家が今回の発行で支払った1株当たりの価格よりも低い価格で任意の他の発行された株または他の証券 を売却する可能性があり、将来的に株式または他の証券を購入する投資家は既存の株主よりも高い権利を持つ可能性がある。将来の取引では、追加の普通株または変換可能または普通株に交換可能な証券の1株当たり価格は、今回の発行で投資家が支払った1株当たり価格よりも高いか、または下回る可能性がある。
私たちは未来に追加的な資金調達が必要かもしれない。私たちは追加的な融資を受けることができないかもしれないし、もし私たちが融資を受けたら、私たちに有利な条項を得られないかもしれない。あなたはあなたのすべての投資を失うかもしれません。
私たちの現在の計画によると、私たちは私たちの既存の現金と現金等価物が今後6ヶ月の運営費用と資本需要を支払うのに十分になると信じている。私たちは私たちの製品を運営して商業化するために多くの追加資金が必要になると予想され、今後12ヶ月の運営に資金を提供できるように追加資金を求める予定です。私たちは融資活動を通じて追加資金を得ることができないかもしれません。もし私たちが融資を受けたら、私たちに有利な条項がないかもしれません。もし私たちが私たちに有利な条項で追加資金を得ることができなければ、私たちは私たちの経営活動を停止または減少させることを要求されるかもしれない。もし私たちが私たちの運営活動を停止または減少させなければならないなら、あなたはすべての投資を損失するかもしれない。
私たちは私たちの株に現金配当金を支払ったことがなく、私たちは予測可能な未来にも現金配当金を支払わないと予想している。
私たちは現金配当金を支払うことを発表したり、発表したことがなく、私たちは予測可能な未来にも現金配当金を支払わないと予想している。したがって、あなたは普通株への投資 を将来の任意の配当収入の源として依存すべきではありません。私たちの取締役会は配当金を割り当てるかどうかを決定する権利が完全にあります。私たちの取締役会が配当金を発表して支払うことを決定しても、将来の配当の時間、金額、形式は、私たちの将来の運営結果とキャッシュフロー、私たちの資本要求と黒字、私たちが子会社から受け取った割り当て金額{br)、私たちの財務状況、契約制限、そして私たちの取締役会が関連すると思う他の要素 に依存します。
37
イスラエルの法律とイスラエルでの私たちの行動に関するリスク
私たちの主な実行事務室、私たちの研究開発活動、および他の重要な業務の大部分はイスラエルに位置しているので、私たちの業績は、最近ハマスと他のテロ組織がガザ地区から発動した攻撃と、イスラエルの彼らへの戦争を含むイスラエルの政治的、経済的、軍事的不安定の悪影響を受けるかもしれない。
私たちの行政事務室、会社本部、主要な研究開発機関はイスラエルに設置されている。しかも、私たちのすべての官僚たちと役員たちはイスラエルの住民だ。したがって、イスラエルと周辺地域の政治、経済、軍事、安全状況は私たちの業務に直接影響を及ぼすかもしれない。イスラエルに関するいかなる衝突、政治的不安定、テロ、サイバー攻撃、または任意の他の敵対行動、またはイスラエルとその現在の貿易パートナーとの間の貿易中断または中断は、私たちの行動に悪影響を及ぼす可能性がある。中東で持続的で再台頭する敵対行動やイスラエルの他の政治的または経済的要因は、私たちの行動を損なう可能性がある。
2023年10月、ハマステロリストはイスラエルとガザ地区の境界に浸透し、民間人と軍事目標に対して一連の攻撃を発動した。ハマスはまた、イスラエルとガザ地区の境界沿線やイスラエル列国内の他地域のイスラエル人口と工業センターに対して大規模なロケット弾攻撃を発動した。このような攻撃は多くの死傷者と誘拐をもたらした。襲撃後、イスラエルの安全内閣はハマスに宣戦布告し、ロケット弾やテロを継続するとともに、これらのテロ組織に対する軍事行動を開始した。
イスラエルが現在ハマスと戦っている戦争の強度と持続時間は予測が困難であり、この戦争が会社の業務と運営、イスラエル全体の経済への影響も予測することは困難である。これらの事件の直接的·間接的な結果として、イスラエル経済の潜在的な悪化は、会社とその効率的な業務展開能力に重大な悪影響を及ぼす可能性がある。
イスラエルの安全内閣がハマスに宣戦布告し、他の組織と敵対行動を起こした可能性があることから、イスラエルは数十万人の予備役軍人を動員して直ちに就役した。私たちの5人の職員たちは軍隊に召集された。これらの従業員のうち3人(4)はすでに予備役から帰ってきたが、再び呼び戻されない保証はない。召集された従業員の中でわが社で要職を務めている人は一人もいません。現在または未来のハマスとの戦争や他の武力衝突では、より多くの従業員 が召集される可能性があり、これらの人たちは長期的に欠席するかもしれない。そのため、私たちの運営はこのような欠勤によって中断される可能性があり、さらに私たちの業務、将来性、財務状況、運営結果に重大な悪影響を及ぼす可能性があります。
ハマスがイスラエルを襲った後、レバノンのヒズボラもイスラエル北部のイスラエルの軍事基地、部隊、町にミサイル、ロケット弾、射撃攻撃を発動した。これらの攻撃への対応として、イスラエル国防軍はレバノン南部ヒズボラの場所に的確な打撃を与えた。ヨルダン西岸のパレスチナ軍事組織や、イランのような他の敵対国を含む他のテロ組織も、敵対行動に参加する可能性がある。このような敵対行動には、テロおよびミサイル攻撃が含まれる可能性がある。イスラエルに関するいかなる敵対行動も、イスラエルとその貿易パートナーとの間の貿易中断または中断は、私たちの行動およびプロジェクトスケジュールの遅延に悪影響を及ぼす可能性がある。この地域のいかなる武力衝突や政治的不安定は資金調達と上場時間のビジネス条件にマイナスの影響を与える可能性がある。本年度報告の日まで、私たちは何の状況も経験していません。そして、私たちの研究開発分野での運営能力は実質的に変化しないと予想されます。私たちのスケジュールは私たちが行っているすべてのプロジェクトを再評価しています。
イスラエル諸国とイスラエル社は過去に国家と非国家行為者のボイコット、撤退、制裁の対象となってきた。これらの行動は数量と範囲で拡大する可能性があり、私たちの経営業績、財務状況、または私たちの業務の拡張に悪影響を及ぼす可能性があります。
イスラエル政府はイスラエルの司法制度を広範囲に改革した。上述の事態の発展に対して、イスラエル国内外の個人、組織と機関はすべて提案中の変化がイスラエルの商業環境にマイナス影響を与える可能性があり、一部の原因は外国投資家がイスラエルで投資或いは業務を展開したくなく、イスラエルの新シェケルの為替レートの変動が激化し、イスラエルの信用格付けの引き下げ、証券市場の変動の激化、及びマクロ経済状況のその他の変化に関連している。このすべての危険はハマスに対する現在の戦争によって悪化している。もしこれらの負の発展が確実に発生すれば、それらは私たちの業務、私たちの運営結果、そして私たちが追加資金を調達する能力に悪影響を及ぼすかもしれません。もし私たちの経営陣や取締役会が必要だと思うならば。
38
イスラエル政府がイスラエルの会社に提供した終了または減税と他のインセンティブは私たちのコストと税金を増加させるかもしれない。
イスラエル政府は現在、イスラエルの会社に税金と資本投資の優遇、研究開発とマーケティングと輸出活動に関する贈与と融資計画を提供している。近年、イスラエル政府はこれらの計画の福祉を減少させ、イスラエル政府当局は将来、これらの計画のメリットをさらに減少または廃止する可能性がある。私たちは未来にこのような福祉と計画を利用するかもしれない;しかし、このような福祉と計画が私たちに提供される保証はない。もし私たちがこのような福祉や計画を享受する資格があるが、その中の条件を満たしていなければ、これらの福祉はキャンセルされる可能性があり、私たちは私たちが享受している可能性のある任意の福祉の返還を要求され、処罰される可能性がある。さらに、私たちがこのような 福祉および計画を享受する資格があり、これらの福祉および計画がその後終了または減少された場合、私たちの財務状況およびbr}運営結果に悪影響を及ぼす可能性がある。
私たちはこのような発明の権利が正式に譲渡されても、イスラエルの従業員の発明に金銭報酬 を支払う必要があるかもしれない
私たちは私たちのイスラエルの従業員と協定を締結し、協定によると、これらの個人はその雇用範囲内で作られた任意の発明は私たちが独占的に所有するか、私たちに譲渡するか、具体的には司法管轄区に依存し、従業員はいかなる権利も保持しない。私たちの知的財産権の一部は私たちのイスラエル職員たちが私たちのために働いている間に開発されたものだ。イスラエル第5727−1967号“特許法”[br}又は“特許法”によれば、従業員がその雇用中であり、その被雇用範囲内で発想された発明は、“職務発明”とみなされる。職務発明は、従業員と雇用主との間に明確な合意がない限り、デフォルトで雇用主に属する。特許法はまた,サービス発明の報酬について合意していない場合は,所有権が雇用者に譲渡されても,イスラエル賠償·使用料委員会または特許法により構成された委員会は,従業員がこれらの発明の報酬を得る権利があるかどうかを決定しなければならないと規定している。委員会 はまだ委員会が強制的に執行した報酬の計算方法を決定していない。従来、従業員は書面、口頭、または行動によって報酬を得る権利を放棄できると考えられてきたが、イスラエル労働裁判所が審理している訴訟は、雇用協定に基づいてこのような放棄を強制できるかどうかを疑問視している。私たちイスラエルの従業員は、私たちが彼らの発明に関連する任意の権利を独占的に所有することに同意しているにもかかわらず、私たちは従業員のサービス発明のための報酬の支払いを要求するクレームに直面する可能性があります。したがって、私たちは、私たちの業務に否定的な影響を与える可能性がある追加の報酬または印税を支払うことを要求されるかもしれません。
私たちのいくつかの研究開発活動はイスラエル政府の支出を獲得し、その条項は私たちに印税を支払い、イスラエルの海外で製品を製造し、技術を譲渡するために特定の条件を満たすことを要求するかもしれない。もし私たちがこれらの条件を満たしていなければ、私たちは支払う前に受け取った罰金と払い戻しを要求されるかもしれない。
私たちの研究·開発事業の資金の一部は、IIAが2023年12月31日までに提供した合計800,000ドルの印税と非印税贈与からです。また、IIAは2024年12月31日までの年間追加支出400,000ドルを承認したが、まだ受け取っていない。特許使用料を受け取った贈与については,製品販売収入の特許権使用料を3%の税率 で支払うことを約束し,最高で受け取ることができる贈与総額は,ドルにリンクして利息を計上する。この金利は、2023年10月25日までに、ドル預金に適用された12ヶ月間のロンドン銀行間同業借り換え金利(LIBOR)に基づいて計算される。しかし、2023年10月25日、IIAはLIBOR満期に対応するための印税の変更に関する指令を発表した。この指令によると、IIAが2024年1月1日までに承認されたがその後も返済されていないIIAの贈与については、2024年1月1日現在、年利は12ヶ月保証隔夜融資金利SOFRで計算されるか、イスラエル銀行が公表した代替金利に0.71513%を加えて計算され、2024年1月1日または後に承認された贈与については、年利は(I)12カ月SOFR金利に1%を加えるか、または(Ii)固定年利4%のうち高い者となる。
いかなる特許使用料を支払っても、私たちはイスラエルの改正された“イスラエルの工業研究と発展を奨励する法” 第5744-1984号の要求、および過去の援助に関する関連法規または研究法を遵守しなければならない。ある会社がIIA贈与を使用してノウハウ、技術または製品を開発する場合、これらの贈与の条項および“研究法”は、IIAの事前承認なしに、そのような製品、技術またはノウハウのイスラエル国外での製造または製造権の譲渡を制限する。したがって、イスラエル国内または海外の第三者にこれらの技術のこれらの側面に関連するノウハウまたは製造または製造権利を譲渡するには、国際投資協定委員会の適宜の承認を得る必要がある。私たちはこのような 承認を受けないかもしれない。さらに、IIAは、私たちが技術や開発をイスラエル以外の任意の配置に移すことを可能にするいくつかの条件を適用するかもしれない。
39
イスラエルの現行法によると、私たちは競争しない条項を実行できないかもしれません。これは私たちの製品に対する追加競争を招くかもしれません。
私たちはすべての従業員と競業禁止協定を締結し、これらのすべての協定はイスラエルの法律によって管轄されている。これらの協定は、通常、彼らの在任中と雇用終了後の12ヶ月以内に、私たちの従業員が私たちの競争相手と競争したり、競争相手のために働くことを禁止している。しかし、イスラエルの裁判所は、元従業員の競業禁止約束を実行することを望まず、比較的短い時間(あれば)に限られた地理的地域でこれらの規定を実行する傾向があり、従業員が従業員の職業発展に関する独自の価値だけではなく、雇用主に対してその雇用主に固有の業務を獲得した場合にのみ実行される。もし私たちが競争禁止条項を実行できなければ、私たちは追加的な競争に直面するかもしれない。
イスラエルの法律と私たちが修正して再記載した会社規約の条項は、このような取引の条項が私たちと私たちの株主に有利であっても、私たちと私たちの合併または買収を遅延、阻止、または他の方法で阻害する可能性があり、これは制御権の変更を阻止するかもしれない。
イスラエルの会社法規範は合併し、指定された敷居を超えた株の買収を要求する際に買収要約を提出し、取締役、幹部あるいは大株主に関連する取引は特別な承認が必要であり、このような取引に関連する可能性のある他の事項 を規範化する。例えば、合併は、各合併会社がイスラエルの会社登録所に合併提案を提出した日から少なくとも50日、および2つの合併会社の株主が合併を承認した日から少なくとも30日以内に完了してはならない。また,ターゲット会社の各証券の多くは合併 を承認しなければならない.また、買収側が発行済み株を少なくとも95%保有する株主から積極的な回答を受けた場合にのみ、会社のすべての発行済みおよび流通株に対する要約買収を完了することができる。要約買収の完了には,要約買収に個人的な利益がない多くの要人の承認 を得る必要があり,要約買収完了後でなければ,買収者は少なくとも98%の流通株を保有する.また、株主は、要約買収を受けることを示す株主を含み、要約買収完了後6ヶ月以内に、買収株式の対価格がその公平な市場価値を反映していないことを要求し、買収契約の対価格を相応に変更することをイスラエルの裁判所に要求し、買収者が要約買収に規定されていない限り、要約を受けた株主はこのようなbr}評価権を求めることができず、購入者または会社は回答日までに要約に関するすべての必要な情報を公表した。
さらに、イスラエルの税務考慮は、私たちの居住国がイスラエルと税金条約を締結しておらず、これらの株主のイスラエル税を免除するため、潜在的な取引を私たちまたは私たちの株主にとって魅力的ではないかもしれない。例えば、イスラエル税法は米国税法のように免税株取引所を認めない。合併については、イスラエル税法は、場合によっては納税 の延期を許可しているが、延期はいくつかの条件の満足に依存しており、場合によっては、取引日から2年間の保有期間 を含み、その間、参加会社の株式売却や処分が制限されている。また、ある株式交換取引については、納税を延期する時間は限られており、この期限が満了した場合には、株式を売却しなくても税金を納めなければならない。これらの条項は、このような買収や合併が私たちまたは私たちの株主に有利であっても、私たちの買収、阻止、または私たちの他の会社との合併を遅延、阻止または阻害する可能性がある。
40
米国裁判所による我々と我々のイスラエルまたは米国における幹部や取締役の判決を実行し,イスラエルでは米国証券法のクレームを主張したり,我々の役員や取締役やこれらの専門家に訴訟手続きを送達することは困難かもしれない。
私たち はイスラエルで登録が成立した。私たちのほとんどの幹部と役員はアメリカ以外に住んでいます。私たちのすべての資産とこれらの人員の大部分の資産はアメリカ以外にあります。したがって、得られた私たち、br、またはその中の誰かに対する判決は、アメリカ連邦証券法民事責任条項に基づく判決を含み、アメリカで受け取ることができないかもしれないし、イスラエル裁判所によって強制的に執行されることもできないかもしれない。あなたもアメリカでこれらの人たちに訴訟手続き を送ったり、イスラエルで提起された原始訴訟でアメリカ証券法のクレームを主張するのは難しいかもしれません。さらに、投資家または他の個人または実体は、イスラエルで米国証券法について訴訟を提起することが困難かもしれない。イスラエルの裁判所は、イスラエルがこのようなクレームを提起する最適な裁判所ではないとして、米国証券法違反の疑いに基づくクレームの審理を拒否する可能性がある。また、イスラエルの裁判所が請求の審理に同意したとしても、それは米国の法律ではなく、イスラエルの法律であると判断する可能性がある。米国の法律が適用されていると認定されれば,米国の法律の適用内容が事実であることを専門家の証人が証明しなければならず,時間も高価な過程である可能性がある。特定の手続き事項はまたイスラエルの法律によって管轄されるだろう。イスラエルはこのような事項に対する拘束力のある判例法をほとんど言及していない。イスラエルで私たちに不利な判決を下すことに困難があるため、あなたはアメリカや外国の裁判所が裁定したいかなる損害賠償も得られないかもしれない。
あなたの株主としての権利と責任は重要な点でイスラエルの法律によって管轄され、イスラエルの法律はいくつかの実質的な点で米国会社の株主の権利と責任とは異なる。
私たちの証券保有者の権利と責任は私たちが改正して再説明した会社の定款とイスラエルの法律によって制限されている。これらの権利および責任は、ある実質的な点で米国の会社の株主の権利と責任とは異なる。特に、イスラエルの会社の株主は、その権利を行使し、会社および他の株主への義務を履行する際に、善意と慣用的な方法で行動し、株主総会で会社の定款の修正と再記載、会社の法定株式を増加させるなどの事項を含む同社の権力の乱用を避ける義務がある。株主の承認が必要なM&Aや関連側取引、および他の株主を差別しない一般的な義務。また,株主 は,自分が株主総会での投票結果を決定する権利があることを知っているか,あるいは取締役や会社役員の任命を任命または阻止する権利がある場合には,会社に対して公平な義務がある.このような義務の性質やこれらの条項の影響を理解するのを助けるために使用できる判例法は限られている。これらの規定は、私たち証券の保有者に追加的な義務と責任を課すと解釈されるかもしれませんが、これらの義務や責任は通常、米国会社の株主に押しつけられません。
第四項です 会社に関する情報
| A. | 会社の歴史と発展。 |
私たち はイスラエルの会社で、イスラエルのラアナナに本社を置き、2018年にイスラエルで登録設立され、名称はClearx Medical Ltd. 2018年4月10日、私たちの名称はInSense Medical Ltd.,2020年7月30日、私たちの名称はさらに現在の名称に変更され、Inspira Technologies Oxy B.H.N.Ltd.は2021年7月16日、私たちの普通株と初公開公募株(IPO)で発行された株式証明はそれぞれナスダックでの取引を開始し、コードは“IINN”と“IINNW”である。
私たちの主な実行事務室はイスラエルのラアナナ市ハティハル通り2番地にあります。郵便番号:四三六六五四です。私たちのイスラエルでの電話番号は九七二九九六六四八八です。私たちのサイトの住所はWwws.spirira-Technologies.comそれは.我々のサイトに含まれている,あるいは我々のbrサイトから得られた情報は,本20-Fフォーム年次報告に参照的に組み込まれることはなく,本20-Fフォーム年次報告の一部と見なすべきではなく,本20-Fフォーム年次報告における我々のサイトへの引用は非公式テキスト参照のみである.Puglisi&Associatesはアメリカの代理店で、住所はデラウェア州ニューアーク図書館大通り850号204号室で、郵便番号:19711です。
私たちは、1933年の改正“証券法”第2節または“雇用法案”改正された“証券法”のような“新興成長型企業”である。したがって、私たちは、2002年のサバンズ-オクスリ法案404節またはサバンズ-オクスリ法案の監査役認証要件を遵守することが要求されないなど、“新興成長型企業”ではない他の上場企業の様々な報告要件に適用されるいくつかの免除を資格を有し、利用しようとしている。(A)年間総収入が1.235ドルを超える最初の会計年度の最終日まで、(B)1934年の米国証券取引法または取引法の下で第12 b-2規則で定義された“大型加速申告会社”になるまで、5年間にわたって“新興成長型企業”であることができる。私たちが最近完成した第2四半期の最終営業日までに、非関連会社が持っている私たちの普通株の時価が7億ドルを超えたり、(C)前3年のbr期間に10億ドルを超える転換不可能債券を発行したりすると、このようなことが起こります。
41
私たちは外国の個人発行者です 証券法と取引法のルールによって定義されています。海外の個人発行者として、私たちもアメリカ証券取引委員会のある法律法規とナスダック株式市場のいくつかの規定を遵守する必要はありません。委託書規則、短期利益回収規則、及び取締役の指名と役員の報酬に対する独立監督などのいくつかの管理要求を含む。また、取引法に基づいて登録された米国国内会社のように、年度、四半期、および現在の報告書および財務諸表を米国証券取引委員会に頻繁にまたはタイムリーに提出する必要はない。
2023年、2022年、2021年、私たちの資本支出はそれぞれ206,000ドル、263,000ドル、182,000ドルです。私たちの現在の資本支出は主にコンピュータ、研究開発設備、オフィス施設の購入に使われており、これらは基本的にイスラエルにあり、これらの支出は主に手元の現金から来ると予想される。
| B. | 業務概要。 |
概要
私たちは専門医療機器会社で、独自の生命支援技術の研究、開発、製造、マーケティングに従事しています。我々の技術目標は機械人工呼吸器の代わりに,全世界の機械呼吸器市場を徹底的に変えることであり,2030年までに全世界の機械呼吸器市場は190億ドルに増加すると予想される。
我々のビジョンは,毎年外部機械換気設備による換気と酸素化が必要な2000万人の患者のために外部呼吸補助装置 を変更することである。伝統的な呼吸補助システムは多種の合併症を招く可能性があり、入院時間とコストを延長する可能性がある。brは患者が自発呼吸ができず、機械を使って呼吸を補助する必要がある場合、通常機械呼吸器を使用する。br患者は重度の鎮静(或いは昏睡)状態で、管を喉に押し込んで、呼吸器は酸素富空気を肺に押し込んで、酸素を肺と他の器官に送る。患者は通常残された合併症を経験し、精神錯乱、肺感染、肺損傷を含み、甚だしきに至っては死亡する可能性がある。機械換気は時々生命を救うことができるが、それはリスク、看護コスト、入院時間の延長、感染の頻繁な発生率、呼吸器依存性と50%に達する死亡率を増加させる。
我々の直感的技術 は,覚醒または比較的軽い鎮静状態にある患者の治療を目的としている。人工換気に使用した挿管や昏睡とは異なり,患者の血液に酸素を直接搬送し,酸素が身体器官に到達できるようにすることを目標としている。このような過程で私たちの技術は病気の肺を迂回しました
適応血液酸素化
42

INSPIRA ART(第二世代)設備は適応技術であり、患者の血液パラメータ を持続的にリアルタイムで測定することによって、必要な酸素量を直接血液中に輸送し、それによって覚醒患者の呼吸能力を増強することを目的としている。INSPIRA ARTはHyla血液センサを搭載するため、患者の血液を連続的にスキャンするように設計されており、潜在的に患者の病状の変化をリアルタイムで検出し、医師に意思決定支援データを提供することを可能にする。
これを実現するために、以下のコア技術を開発しています
| ● | ヘラ血液センサー |
我々の技術は,特定の患者の血液パラメータを連続的にリアルタイムで測定することを目的としており,我々のセンサ技術の大きな進歩である。標準血液ガス分析器と比べ、この突破は95%の正確率を実現し、病院で通常間欠性採血を必要とする伝統的な血液ガス分析器システムと比べ、連続とリアルタイムの血液モニタリング能力を許可した。この進歩は私たちが使い捨て製品市場に入る可能性があることを示している。
初のHyla変種の開発はこの進展の鍵であり,510(K)経路で食品·薬物管理局へのこの変種の提出に向けて重要な一歩を踏み出し,2024年下半期に提出される予定であることを示している。このセンサ技術(Hyla 1の形で)は,我々のINSPIRA ART 100心肺転流との統合を目指しており,2023年9月にFDAに提出され,2024年上半期に承認される予定である。
HYLA血液センサシリーズ、HYLA或いは血液センサは、集中治療室或いは集中治療室の操作を変更し、連続、リアルタイムの血液データ収集と分析を提供することを目的としている。これは,医療手順や設備効率の改善を目的とした重要な洞察力と警報により患者ケアを強化することである。
Hyla血液センサーの主な機能は
| ● | 高精度:標準血液ガス分析器と比べ、精度は95%に達した |
| ● | 非侵襲的です採血する必要はありません |
| ● | 耐久性:ICUおよび手術室環境; |
| ● | 多機能性:体外循環、体外膜酸素化、持続性腎臓代替療法、透析を含む様々な医療プログラムと互換性がある |
| ● | モジュール化設計:現有の医療設備を補充するために設計され、全世界の毎年200万人の心内直視手術患者に向けている。 |
血液センサーシリーズを開発する際には,内部実験室テストおよび病院連携を用いて臨床研究と開発を行った。この方法 は,血液センサの使い捨て材料と方法,Hyla計画のブレードビジネスモデルを定義できるようにしている。主にInspira ART装置のために設計されているが,独立した装置として血液センサの変異体の提供も計画されている。
43
| ● | Vortx軌道血液酸素充填送達システム |
我々のコア技術はすでに米国初の軌道血液酸素化送達システム特許を取得し、このシステムは革命的なINSPIRA ART(第2世代)設備のコア技術である。この革新は16個の声明が斬新であることが発見された。軌道血液酸素化輸送システム,あるいはVortx, は線維膜のない血液に酸素を充填することを目指しており,医学的構造を徹底的に変えると信じている。現在血液酸素化に用いられている繊維技術は患者の血球に重大な損害を与える。ヒト内血管中の自然層流血液とは異なり,既存の繊維酸素交換器では,血液は繊維壁内摩擦や剪断力を受けるとともに,有害な乱流に多層繊維を流すことを余儀なくされている。繊維織物は血液流動の重要な抵抗であるため、高圧差を形成し、各種の血液成分に重大な損害を与え、高溶血 (赤血球分解)、白血球の破壊、体内炎症系の活性化、免疫系の活性化、brと血液凝固を含む。
軌道血液酸素輸送システムはINSPIRA ART(Gen 2)設備のもう1つのゲームルールを変更可能なコア技術であり,190億ドルの機械換気市場を狙っていると考えられる。
私たちの目標は機械の換気を防ぐことです

覚醒治療を受け人工呼吸を使用していない患者
昏睡状態がない
酸素は直接血液中に送られ二酸化炭素は除去されます
肺感染なし
血液パラメータを連続的かつリアルタイムに測定する
変化を早期に発見する決定支援データを提供する
44
もっと高いのを狙って…それは.

私たちの設備は医療構造を徹底的に変えると信じています。
| ● | Inspira ART 100(第1世代)装置 |
我々は2023年に510(K)経路でFDAにINSPIRA ART 100を提出し,心肺転流装置であり,2024年上半期に承認される可能性が予想される。

|
第1世代
血液酸素化 (体外循環)
HYLA−1血液センサ2025型 (INSPIRA ART 100と統合) |
2代目
適応血液酸素化
Vortx軌道血液酸素化
HYLA−2型血液センサ
0継続的な血液モニタリングが必要であることを示す
0変更のリアルタイム検出をサポートします。
0意思決定支援データ を提供
|
45

| ● | 使い捨て用品 |
我々の計画では,我々のInspira ART医療機器のために使い捨て用品を発売し,現在開発中の血液酸素化プログラムに使用している。これらの使い捨てデバイスは、様々な他の生命支援デバイスと互換性があり、使い捨て灌流システム市場に進出することを意図している。これらの使い捨て製品は2025年にFDAに承認される予定で、効率的な血液酸素化と二酸化炭素除去を目的とした使い捨て製品である。この使い捨て製品は日常的な収入モデルになる可能性がある。私たちは、いくつかのタイプの心肺転流機のような使い捨てデバイスを他の医療デバイスと互換性を得ることに集中している。
溝.溝
著者らの戦略目標は早期血液酸素化市場を創立とリードし、それを新しい治療選択とし、現在の非侵襲性措置(例えば酸素マスク、双レベル陽圧或いはBiPAP、持続陽圧或いはCPAP、及び高流量鼻腔導管)と機械換気の間の差を埋めることである。多種の成長動力、例えばInspira ART(Gen 2)の潜在力は、機械換気とICUへの依存を解除することによって、都市と農村の小型病院、一般医療機関と救急室ユニットで数百万人の患者を治療する可及性を増加させる。私たちが予想しているように、患者は昏睡状態ではなく、覚醒時に治療を受けている。毎年数百万人の患者が機械換気を受けているため、INSPIRA(第二世代)ARTの潜在的な総潜在市場価値は数十億ドルであり、その基礎は販売された各使い捨て生命支持ユニットの目標患者の治療コストは数千ドルであり、毎年人工呼吸を受ける患者の数(約br)が呼吸不全と慢性肺疾患の急性増悪を有する患者数を乗じていると考えられる。市場規模とコスト仮定 は日常的な収入や使い捨て生命支援設備の大量生産,大規模生産,販売の影響を受ける可能性があるが,Inspira ART(第2世代)設備自体からの基本収入は含まれていない。
インスピレーション芸術へのニーズ(2代目)
呼吸不全(肺では十分なガス交換ができず身体の新陳代謝を支持する)や呼吸不全の発生が速く,最初に観察することは困難であった。これらの場合は通常,肺炎のような呼吸に影響を与える疾患や傷害によるものである。急性呼吸不全は緊急治療が必要であり、全世界の死亡の主要な原因の一つである。
46
2017年に発表された報告書では、世界保健機関(WHO)は、全世界で4億人以上が呼吸不全の影響を受けていると推定している。毎年、全世界で2000万人が人工呼吸を受けると推定され、これは主に急性呼吸不全(69%)と慢性肺疾患(10%)に起因する。国際呼吸学会フォーラムの2017年の報告では,2025年までに世界の呼吸ケア設備市場規模は約298.6億ドルに達すると予想されている。この増加に影響する主要な要素は呼吸器疾患の高発病率、高齢化人口の急速な増加、喫煙の高流行率、上昇する都市化 及び汚染レベルと西洋の生活様式の変化を含む。
新冠肺炎疫病は更に機械通風の弱点と劣勢を暴露し、機械換気はかなり大きな医療リスクと高度に関連し、医源性合併症とも高度に関連し、後者は更に医療システムの負担を増加し、入院時間が長く、治療コストが高い。新冠肺炎は世界のいくつかの最先端の医療システムが柔軟、迅速かつ大規模に急速に増加する生命維持需要に対応する上での失敗を目撃した。新冠肺炎は全世界の集中治療室(ICU)で治療した呼吸不全患者の数の上昇を招き、生命支持解決方案を必要とする患者、例えば機械換気を必要とする。
Inspira ART−人工呼吸の再定義−
われわれのビジョンは,機械的呼吸器の代わりに覚醒患者を治療するための技術を用いて,酸素を直接血液中に輸送し,人体器官に到達できるようにすることである。そこで我々は,患者の血液パラメータを連続的にリアルタイムで測定することで適応的な血液酸素化を行い,必要な酸素量を直接血液中に送達することを目的としたINSPIRA増強呼吸技術装置,あるいはINSPIRA ART(第2世代)を開発した。適応血液酸素化システムは,我々のHyla血液センサ技術とVortxを利用した軌道血液酸素化送達システムを目指している。われわれの装置は,低侵襲の米国特許二腔カニューレbrを用いて,われわれの装置により必要な体積の患者の血液br}を抽出し循環させるために,患者の頸静脈(患者頸部)に挿入する。INSPIRA ART(Gen 2)装置は直感的な技術であるため、患者の血液パラメータを持続的にリアルタイムで測定し、必要な酸素量を直接血液中に輸送することによって、覚醒患者の呼吸能力を増強することを目的としている。酸素富化血液は同じ双腔導管を介して患者の体内に循環し、数分以内に血中酸素飽和度レベルを高め、安定させる。INSPIRA ART(第2世代)は患者の血液を持続的にスキャンし,患者の病状の変化をリアルタイムで検出し,医師に意思決定支援データを提供することを目的とした血液センサを搭載する。INSPIRA ARTの仕組みは,呼吸治療をICU環境外に拡張する可能性を提供し,地域や医療機関がICUを必要とせずに急性呼吸治療を得ることができる。
INSPIRA ART(第2世代)を用いて,治療後数分で軽快した。Inspira ARTは覚醒,活動,自発呼吸で治療を受けることができるため,オフラインの必要や時間を減らす可能性もある。したがって,われわれのINSPIRA ART設備 は,機械換気と比較してICUでの入院時間と費用,病院のリハビリテーション時間,再入院 を減少させる可能性がある。Inspira ARTデバイスはまだ人体でテストされていないため,これらの人間に潜在的な優位性があるという説は実証されておらず推測されている。
我々は2020年にInspira ARTの最初の実験室ユニットを完成してテストした。2020年を通じて、イスラエルのラハフCRO獣医チームの指導の下で、著者らは著者らのチームと一緒に一連の研究中の約40項目の臨床前体内実行可能性テストを行い、直接血液酸素化を検査し、機械換気の実行可能性を先に行った。これらの研究の主な目標は,われわれのINSPIRA技術を用いて,臨床的に著明な酸素を静脈血液に移行させるとともに,大量の二酸化炭素を抽出することにより,呼吸不全期間中の酸素交換の一時的な増加を示すことである。これまでINSPIRA ARTは人体でのテストは行われておらず,将来人体で行われるどのテストもFDAを含む適切な規制機関の要求に依存する。
47
我々はまた,Inspira ART(Gen 2) とInspira ART 100(Gen 1)デバイスのキーテクノロジー部品の製造に複数の協力機会を提供している.2022年12月、世界有数の医療機器会社Terumo Corporationの子会社Terumo心血管社とオリジナル機器製造またはOEM協定を締結したことを発表しました。Terumo Corporationは世界160以上の国と地域で業務を展開し、様々な医療環境中の患者に50,000種類以上の製品とサービスを提供している。Terumo心臓血管会社は酸素システム、心肺機、監視システム分野の専門家である。このプロトコルは、酸素化中の血液の体外循環のために、私たちの製品に統合することを目的とした流動機構の製造を提供する。合意により、市場に対する承認 を獲得し、維持し、流動メカニズムコンポーネントを配信する責任がある。本協定の有効期間は3年であり、発効日から計算され、120日前に終了または120日前に書面で通知されない限り、協定は双方が共同で合意した追加期限を更新します。
臨床研究と予想される制御策略
我々の規制戦略によると,重要成分源に対してはII類510(K)経路を採用する予定であり,その基礎は我々 が現在FDAの承認を得るために人体試験を行う必要がないことを予想している。私たちは多段階の規制承認の流れをとっています。 2022年1月、INSPIRA ARTデバイス(第2世代)とINSPIRA ART 100(第1世代)デバイスの1つのコンポーネントをFDAクラス510(K)免除 リストに入れました。このコンポーネントは、患者がベッド上で、および/または輸送中に体位を変化させる過程で発生する頸静脈挿管移動に関連する潜在的合併症を減少させることを目的としている。
光学技術と機械学習(ML)に基づくアルゴリズムを用いたINSPRIA ART特有の非侵襲性血液センサの開発は2023年に進展した。我々はこの技術を独立製品(Hyla血液センサ)を開発する機会と見なし,2023年第1四半期にSheba医療センターで臨床試験を開始した。Sheba Medical brセンターが心内直視手術を受けた患者100名に対するデータ収集臨床研究は,臨床研究を製品開発サイクルに統合することを目的としている。510(K)経路でFDA提出前に検証·確認(V&V)テストを行っており,2024年上半期に行われる予定である。FDA承認後,2025年までに初期販売注文を受けるとともに,初歩的な市場浸透と採用を行う予定である。
2023年3月、著者らはHyla Research臨床研究において、心内直視手術を受けた最初の患者を発表したイスラエルのシェバ医療センターにあります。 Hyla研究臨床研究は人類研究の第一項であり、非侵襲性Hylaセンサ 測定のパラメータを患者の採血を必要とする標準血液ガス分析器と比較することを目的とした。データ収集は最終的な 製品設計をさらにサポートすることが予想される.
2023年7月、我々は、医療機器業界の品質管理システムの国際標準である国際標準化組織13485:2016年標準認証を取得し、EU規制部門に許可を要求したことを発表した。ISO認証は重要な側面を含み、体外循環、血液モニタリング設備と呼吸看護設備の設計、開発、製造、流通と販売を含む。ISO認証過程はまた、文書、リスク管理と持続的な改善実践を含む会社の品質管理システムを全面的に評価することに関連する。この評価はイギリス標準協会グループによって行われ、このグループは独立した第三者監査会社であり、医療機器品質管理システム に特化している。
2023年9月,510(K)経路でINSPIRA ART 100をFDAに提出し,2024年上半期に承認される可能性が予想される。
そのセキュリティまたは有効性に著しく影響を与える可能性のある修正、またはその予期される用途に重大な変更または修正を構成する任意の修正は、新しい510(K)、先頭から、またはPMAを必要とするであろう。INSPIRA ART(第2世代)の画期的な設備名 をFDAに申請することを計画している
*INSPIRA ART 100は、商業心肺転流サポート装置になることを目的としています。私たちが必要な規制承認を得た時、私たちはICUに最初のINSPIRA ART 100を配備する予定です。私たちはFDAの承認を受けた後にアメリカでINSPIRA ART 100を発売し、AMARの承認を受けた後にイスラエルで発売したい。
48
2023年に達成されたマイルストーンには
| ● | シェバ医学センターの承認を得てHylaの臨床研究を行いますTM血液センサーです。 | |
| ● | ヒラが人間の第一人者だと宣言したTM臨床研究における血液センサー。 | |
| ● | Vortxの開発を発表しましたTM血液酸素交換器は、血液を酸素で満たし、二酸化炭素を除去する独特の技術である。 | |
| ● | 世界最大の体外生命支援会議で新しいINSPIRA ART 100装置が展示された。 | |
| ● | Perfusion Solution Inc.と協力合意に達し、Persion Solution Inc.はアメリカに本部を置く会社であり、アメリカのリードする病院に先進医療設備、訓練と人員を配備するプラットフォームを提供する。 | |
| ● | 医療機器品質管理システム認証を取得した。 | |
| ● | マサチューセッツ州ボストンでINSPIRA ART 100の独立可用性研究が完了した。 | |
| ● | Innovimedと合意し,INSPIRAART呼吸医療機器の臨床試験をヨーロッパのどの国にも拡張した。 | |
| ● | FDAに提出され、510(K)経路で承認され、2024年上半期に受信される予定です。 | |
| ● | 世界最大の体外生命支援大会でINSPIRAART医療機器シリーズが発表された。 | |
| ● | 中米の技術と医療機器流通業者CIO MEDグループと流通協定を締結した。 | |
| ● | INSPIRAART 500医療機器の米国特許を取得した。 | |
| ● | イスラエルの革新機関からVortx使い捨て血液酸素化技術の寄付を受けた。 | |
| ● | Ennocate MedTech Ltd.あるいはEnnocureと協力合意を達成し、ICU患者に関連する血液感染を防止するために、独自の生体電子治療方法を開発した。 | |
| ● | ダン·ゴフィル博士を私たちの医療コンサルタント委員会のメンバーに任命しました | |
| ● | 取得した我々の専門家チームは会社のセンサ技術に重要なマイルストーンであるHYLA血液センサの精度を95%に達した。最初のHylaの開発はTM:変異体、この進歩の鍵は、510(K)経路を介してFDAに提出することに向かって重要な一歩を踏み出したことを示している |
会社は戦略流通プロトコルを実行しようとしているが,これらの既存プロトコルと将来実行可能なプロトコルに基づいていかなる販売も保証されていない.事前条件流通協定の期限は最長7年であり、開発完了と必要な規制承認または許可に依存する。
目標マイルストーン(2024-2025):
私たちは今後2年間に私たちの製品ラインを推進し、明確な戦略を制定し、FDAの監督管理許可と初歩的な市場浸透 と採用を獲得する予定である。
49
2024年第1四半期に達成されたマイルストーンは、
| ● | Glo−Medと戦略的合意に達し,サウジアラビア,アラブ首長国連邦,バーレーンにInspira ART装置531台を配備する。 |
| ● | 使い捨ての使い捨て血液酸素交換器キットを発売し,新たな使い捨て灌流市場の機会を開拓する予定であることを発表した。 |
| ● | 締結したイスラエル中部の有名な医療機関シャミール医療センター(Assaf Harofeh)と締結した非拘束性意向書は、シャミール医療センターの臨床環境におけるINSPIRAART 100設備の集積と性能を評価する双方の共同約束を強固にした。 |
| ● | 米国特許を取得した軌道血液酸素化送達システムは、革命的なINSPIRAART 500装置のコア技術である。 |
| ● | Inspira ART 500のコア技術であるHyla血液センサおよびVortx軌道血液酸素輸送システムの開発および試験を含む、生体シミュレーション血液パラメータのための新しいプラットフォーム が発表された。 |
| ● | 2024年上半期に、INSPIRAとART 100は食品·薬物管理局の510(K)の承認を得て、米国特許商標局の承認を得ており、そのうちの3つの特許はすでにbrを承認しており、他の3つの特許出願は米国特許商標局でいくつかのコア技術の出願を待っている。 |
| ● | 適応酸素化技術を用いて,独自のHyla血液センサとVortx 軌道血液酸素化を用いて酸素を直接血液中に輸送することを目的としたINSPIRA ART(第2世代)のコア血液酸素化技術が発表された。 |
| ● | 米国特許によって支持されている技術、軌道血液酸素充填技術(Vortx)は、異なる血流速度において、血液酸素充填および二酸化炭素除去に関する規制ガイドラインの要求が100%に達しており、装置全体の血液圧力勾配がゼロレベルに維持されていると発表されている。 |
2024年3月17日、私たちはINSPIRA ART 100(Gen 1)設備をイスラエル保健省医療機器司(AMAR)に提出し、brがイスラエルのいくつかの有力病院で設備を発売するために承認した。AMAR承認は通常120営業日程度の時間を要し,臨床データが必要となる可能性がある。
2024年上半期には、我々のINSPIRA ART 100心肺転流装置がFDA 510(K)認証を受けることが予想される。承認されれば、市場浸透を実現し、最終的に収入をもたらす可能性がある医療センターにこの装置を配備することに取り組む。
我々は2024年末にHyla血液センサ(Hyla 1)の初期バージョンを提出する予定であり,510(K)許可の提出である可能性が考えられる。スケジュールと規制方法は変化するかもしれない。
我々は、FDA(510 K)の承認を得るために、INSPIRA ART 100と共に使用される使い捨てコンポーネントを2025年に提出する予定です。スケジュールと調節経路は変化するかもしれない。将来的に整理可能な使い捨て製品は、会社が使い捨て製品を販売することで収入を生み出す潜在的な製品を拡大すると信じており、これは会社がシェービング刃ビジネスモデルを実現する計画の一部である。
50
業界の概要
呼吸不全概要
呼吸不全とは,血液中の酸素不足や二酸化炭素過多,あるいは両者を兼ねた場合である。吸入中、肺は酸素を吸収します。br酸素は肺を通って血液に入り、肺を介して酸素を必要として機能する身体器官に酸素を送ります。二酸化炭素は呼気時に血液から排出される。血液中の二酸化炭素含有量が高すぎると人体の器官を損なう。呼吸中のガス交換不足は呼吸機能不全を招き,低酸素血症や高炭酸血症をきたす可能性があり,生命に危険を及ぼす可能性がある。呼吸に影響を与える疾患、例えば慢性閉塞性肺疾患或いはCOPD、及び呼吸を制御する神経と筋肉を影響する各種の情況は、呼吸不全を招く可能性がある。呼吸不全とは呼吸不全の急性状況 であり,I型(血中酸素レベルが低く,二酸化炭素レベルが正常または低い)またはII型(血中酸素レベルが低く,二酸化炭素レベルが高い)に分類される。疾病予防·健康促進弁公室が2020年に発表した“呼吸器疾患”と題する記事によると、現在約1500万人の米国成人が慢性閉塞性肺疾患と診断されており、数百万人が慢性閉塞性肺疾患を患っているとされているが、慢性閉塞性肺疾患と診断されておらず、治療も受けられていない。慢性閉塞性肺疾患はアメリカで4番目の死因である。
INSPIRA ART(第2世代)設備計画が解決する機械換気に関するリスクと合併症の重要な問題
| 侵襲的機械的通気 | Inspira芸術(2代目) | |||
| プログラム.プログラム | 侵襲的機械換気の定義は,気管内あるいは気管切開管を介して正圧を肺に送達することである。人工呼吸の間には,鎮静と鎮痛が必要である。 | 患者は覚醒と自発呼吸を維持することができ、同時に低侵襲挿管を患者の頸静脈に挿入し、体外酸素化と二酸化炭素除去の目的を達成する。 | ||
| 誘発性昏睡 | 医学的に患者の昏睡を誘導するには鎮静と鎮痛が必要であり、挿管を通じて酸素を陽圧で肺に送ることができる。 |
患者は覚醒し、自発呼吸(Br)(無昏睡):
Delirium を予防できる 筋肉 の紛失を防ぐことができる 患者は食べて飲むことができる 患者は医療従事者に症状と需要を伝えることができる 患者 は家族や友人と交流できる | ||
| 合併症と死亡率 |
死亡率が増えた 呼吸器持続時間を延長しました 呼吸器による肺損傷(VILI) 呼吸器関連肺炎(VAP) 呼吸器による隔壁機能障害 気胸と気管が軟化する Delirium 筋萎縮 患者を呼吸器から離脱させることができない |
肺バイパス術は患者の予後を改善する可能性があり& 潜在的に医源性合併症を減少させることが期待できる:
呼吸器による肺損傷を減らすことができます 呼吸器による隔壁機能障害を減少させることができる 呼吸器関連肺炎の減少(人工呼吸を2日以上受けた患者の5−40%に影響)
| ||
| 在院日数 | 侵襲的機械換気合併症で長時間入院する必要があるかもしれない | 機械換気を回避したため,入院期間は減少する予定である | ||
| 離乳する | 患者は人工呼吸から離脱し、ICU滞在時間を延長しなければならない | 呼吸器を撤去する必要はありません。これはICUと入院期間を減らすのに役立つかもしれない | ||
| 再募集する | 40%の再入院率、患者は最終的に機械換気を延長する結果で死亡した | 比較的に短い治療時間は合併症を減少させ、患者の予後を改善し、再入院を減少させる可能性がある | ||
| 位置 | ICU環境でしか管理できません | ICUにも適用可能であり,非ICU環境(非臥床を含む)にも利用可能である | ||
| 従業員 | 高度に特化した医療従事者が必要で、ICUでしか利用できません | 経歴の低い医療従事者に使用されるかもしれない。灌注者への需要を最大限に減らす |
表1:機械換気と私たちのインスピレーション芸術の比較
51
我々のINSPIRA ART(Gen 2)はまだ開発段階であるにもかかわらず、人体でテストされておらず、FDAや同様の外国規制機関の承認や承認も得られていない。 我々のINSPIRA ART(Gen 2)設備はFDAが承認した治療法よりも競争優位であると考えられているが、INSPIRA ART(Gen 2) は既存の解決策の変更を提供しているので、これらの解決策は重大な健康リスクを有しているので、以下で詳細に検討する。著者らのINSPIRA ART(Gen 2)設備は機械換気と比較したいかなる潜在的な利点も人体試験では観察されていないが、著者らのINSPIRA(Gen 2)ARTは機械換気に侵襲性と侵襲性がより小さい代替方案を提供することを目的としており、後者は患者が侵襲性挿管と薬物誘導昏睡を受ける必要があり、しかもよく罹患した肺部の合併症を増加させる。機械的換気とは異なり,われわれのInspira ART(第二世代)は侵襲的挿管や患者の医学的昏睡への誘導を必要とせず,覚醒,活動,自発呼吸を維持したまま患者を治療できることを意味している。また,我々のINSPIRA ART(Gen 2)は,ICUと一般医療ユニットに独立して使用され,ICUにおける機械的換気 と組み合わせて使用される可能性があるため,多様な潜在的パターンを有するデバイスであると信じている。
現在呼吸支援を提供するための解決策brは、軽度から中等度の呼吸不全の症例のための酸素マスクおよびBiPAPマスクを含み、brは、他の侵襲性の小さい方法が満足できる解決策を提供できない場合、より深刻な呼吸不全の場合の機械的換気を含む。機械的換気は、制御された圧力、流量、および体積に応じて患者に空気を提供することによって呼吸作業を実行する。RT Magazineが2016年に発表した“機械換気上で患者を管理する”と題する文章によると、機械換気はICUで最もよく見られる介入措置の一つであり、半分以上の患者はICUに入る24時間前に侵襲的機械呼吸器 に置かれた。
侵襲的人工呼吸の開始やタイミングの決定は困難である可能性があり,早期に集中治療医と検討することが重要である。呼吸器支援の適切性も患者や家族と深く議論する必要がある問題である可能性がある。いったん挿管の決定を下すと,重篤な患者は覚醒した自発呼吸患者から制御のある侵襲的呼吸器に移行することは非常に困難である可能性がある。大多数の患者は発展或いは既存の臓器機能障害の証拠、特に心血管機能障害(虚血性心臓病、敗血症)があり、通常このような患者は低血容量である。麻酔誘導剤と陽圧換気はすべてよく見られ、それは静脈還流を減少し、心血管抑制と挿管周囲の低血圧を招く。また,これらの患者の辺縁呼吸予備や循環の問題により,自発呼吸停止によりこれらの患者は非常に急速に飽和してしまう可能性がある。
機械換気にはいくつかの方法がある:ラリンジアルマスク、標準気管挿管、気管切開術と体外膜肺酸素化。ECMOでは,透視画像技術を必要とする大挿管を用いて挿管の初期定位を行う必要があり,危険な過程であるため,非常に正確な完成が必要である。そのほか、人工呼吸器は生命を脅かす合併症を引き起こす可能性があり、呼吸器関連性肺損傷(VILI)、呼吸器関連性肺炎(VAP)、気胸と気管軟化を含む。患者はまた褥瘡と筋肉萎縮などの肺外合併症が発生しやすい。人工呼吸を受けた場合,鎮静剤と鎮静剤を投与され,非生理的陽圧換気に関連する不快感を低下させる。鎮静剤や鎮静剤は患者の咳を防止し,分泌物を除去したり家族とコミュニケーションする能力を有する。患者が機械的換気支援を必要としなくなると,彼らは徐々に呼吸器から離脱する。彼らは十分な酸素、二酸化炭素の除去、呼吸筋の力を持ち、彼らの気道を保護する能力を保持しなければならない。不幸にも,呼吸筋は換気中に萎縮するため,正常に回復することは困難である。
VILIは肺水腫、気圧損傷と悪化した低酸素血症を引き起こすことができ、それ自体は機械換気時間を延長し、多系統器官機能障害を招き、死亡の機会を増加させることができる。肺胞過拡張、無気肺と生物損傷はVILIの主要な機序である。肺胞損傷は肺胞透過性の上昇、肺胞間質と肺胞水腫、肺胞出血、透明膜、機能表面活性物質の喪失と肺胞陥没を招く。そのため、VILIを減少する呼吸器策略を採用することは呼吸器管理の重要な目標である。VAPは院内獲得性肺炎であり、ICUによく見られる深刻な問題でもあり、気管挿管後48時間以上に発生する。VAPは死亡リスクの増加と関連している。異なる研究では,VAPに関連する全要因死亡率は20%から50%まで様々であった。
各種の肺症候群の複雑かつ異なる種類の肺病理生理学に対する認識の増強に伴い、伝統的な機械換気の欠点はすでに現れた。アメリカだけで、毎年ICUに入院している570万人の患者の中で、約40%が機械換気 を受けている;これらの患者の中の70%は最終的に潜在疾患或いは機械換気 による合併症で死亡した。高齢者人口の増加やより多くの人の喫煙や汚染への曝露に伴い,機械的換気支援を必要とする人口が急速に増加している。このような状況から,急性肺不全治療の新たな支持的措置に注目が集まっており,この方法には以下に述べる従来技術の欠点はない。
52
ECMOは呼吸器支持が困難な患者にガス交換を行う技術であり、肺機能が更なる構造的肺損傷或いは深刻な血流動力学損害しか代償としない時である。ECMOを考慮したガイドラインは、死亡リスクが50%を超える任意の原因(原発または続発)による低酸素性呼吸不全を含む。ECMOの使用は技術複雑性の制限を受け、次の図4に示すように、溶血、血液伝播感染、空気塞栓、失血などを含む資源と関連合併症に関連する。さらに、いくつかの研究は機械換気の結果が曖昧であることを示しているので、どの患者がECMOから最大の結果を得るかを決定することを目的としている。
呼吸不全および現在利用可能な解決策を使用して患者に呼吸支援を提供することも看護コストの増加と入院時間の延長と関連している。米国では,慢性閉塞性肺疾患のみで毎年150万救急科を受診し,72.6万人が入院している。疾病コントロールと予防センターの報告によると、アメリカではCOPDの年間財務コストは295億ドルであり、その中の直接医療支出は295億ドルであり、間接発病率/死亡率コストは約200億ドルである。

図4:ある患者がECMOデバイスに接続されている. ソース:CvelandClinic.org。
MarketWatchが2020年6月に発表した記事 によると,1人の患者がICUに入院する総費用は数十万ドルに達する可能性があり,特に感染が疑われれば。ICUで機械換気治療を受けた1日の直接費用は1,500ドルであった。各人工呼吸器患者のためには、より多くの病院資源およびコストを生成するために、装置から離脱するための追加の時間が必要である。そのほか、人工呼吸器患者は通常感染(例えば呼吸器関連性肺炎)への曝露による合併症が出現し、8%から28%のICU患者は抗生物質によって治癒されるまで、死亡率は33%~50%に達する可能性がある。現在の人工呼吸治療には医学専門家と看護師チームが必要である。一人がICUに滞在する時間が長いほど,長時間の呼吸を要する可能性が高く,逆に人工呼吸に関連するさらなる合併症に直面することになる。
53
私たちのInspira ART(第2世代)生命支援ソリューション
著者らのリード製品INSPIRA(Br)ART(Gen 2)設備は1種の革命的な生命支持形式であり、適応性血液酸素化に持続的なリアルタイム測定患者の血液パラメータを提供し、必要な酸素量を直接患者の血液に輸送し、低下した酸素飽和度brレベルを向上と安定化し、同時に患者は覚醒、活動と自然呼吸を維持し、その肺部を損傷することを目的とした。INSPIRA ARTは,患者の身体や重要臓器が必要な酸素を得ることを確保することを目的としている。INSPIRA ART(第二世代)設備 を低コスト,大容量の解決策として設計し,高度な呼吸支援を必要とする集中治療患者に適用した。それは機械換気の代替方案を提供し、呼吸不全患者を肺状況から回復させることを目的とし、brは挿管と機械換気による各種のよく見られる合併症のリスクに直面することはない。呼吸不全の治療を容易にし,機械的換気を必要とせず,ICU内外にInspira ART(Gen 2)装置を配備できる実用的かつ携帯的な解決策を提供することでヘルスケアシステムを支援することを目標としている。
INSPIRA ART(第二世代)は適応血液酸素充填技術を利用して患者の血液パラメータを連続的にリアルタイムで測定し、必要な酸素量を直接血液中に輸送し、そして表現の悪い肺と協力して仕事をし、患者が潜在的な医療条件の治療を受けると同時に彼らに支持を提供することを目的としている。この独特な方法は機械呼吸器に関連する合併症を最大限に減少或いは防止し、患者が覚醒を維持し、相対的に鎮静剤を使用せずに肺機能を回復させることができると信じている。また,この技術は様々な環境に適用可能であり,非常に容易に得られ,現在ICUに限られている急性呼吸看護をすべての病院病棟や救急車で行える外来治療に拡張している。

図5:Inspira芸術です
我々のINSPIRA ART(Gen 2)は,現在生命支援を提供するための解決策に比べてユニークな利点を持っているが,我々のINSPIRA ART(Gen 2)デバイスを使用することには多くの潜在的リスク が存在する可能性がある。このようなリスクとしては,血栓形成に関連する低血流,上大静脈の機械的損傷,生体適合性の問題による全身性炎症反応,カテーテルやその構成要素へのアレルギー反応,静脈還流の減少,Inspira ART(Gen 2)取り出し後の局所静脈出血,あるいはわれわれの製品挿入中に動脈を誤って穿刺することが考えられる。また,人体内のどの異物も感染のリスクを増加させ,患者の細胞膜が短時間で閉塞する可能性がある。最後に,個々の患者のガス交換に対する要求は平均レベルと大きく異なる可能性があり,これは我々のINSPIRA ART (第二世代)の使用が最低の血液飽和要求に適合していない可能性があることを意味する。
54
生命支援技術として、私たちのリード製品は以下のような独特の利点を持っています
| ● |
管理の簡単性規制許可が得られれば,我々の製品は小型医療チームが簡単なベッドサイドプログラムを実行でき,われわれの二腔挿管を頸静脈に挿入することができる。
| |
| ● | 血液モニタリングの連続リアルタイム測定:コア技術として、医療チームが血液サンプルを採取する必要はなく、管状血液センサは、チューブを流れる血液を走査する非侵襲的光学センサを含む。私たちのソフトウェアは血液パラメータを測定します。血液センサは患者の血液パラメータをリアルタイムで測定し,必要な酸素量が直接血液に入ることをトリガする予定である。血液センサの他の利点は、持続的な血液モニタリング、モニタリング傾向と異常、患者パラメータの変化と可能な状況をリアルタイムで検出すること、および医師に意思決定支援データを提供することを含む。 |
| ● | 軌道血液酸素輸送:コア技術は、線維膜なしで血液に酸素を充填するように設計されており、医学的構造を完全に変えることが期待できると信じている。現在血液酸素化に用いられている繊維技術は患者の血球に実質的な損害を与える。人体内血管中の自然な層流血液の流れとは異なり,既存の繊維酸素交換器では,血液は有害な乱流で多層繊維を流れることを余儀なくされるとともに,繊維壁内で摩擦やせん断力を経験する。繊維織物は血液流動の重要な抵抗であるため、高圧差を形成し、各種の血液成分に重大な損害を与え、高度溶血(赤血球分解)、白血球に対する損害、体内炎症系の活性化、免疫系の活性化と血液凝固を含む。 |
| ● | 2腔挿管を切り替えることができる:我々の変換可能な二腔カニューレ装置は、血管内で単腔カニューレを初期挿入後に二腔カニューレに変換し、それにより、すべての口点と潜在的に多様な使用を可能にする。変換可能な二腔カニューレの設計は、単腔から二腔カニューレへの切り替えを可能にし、その逆も同様であり、追加のカニューレを交換または追加する際に新たな切開を必要としない。我々の転換可能な双管腔は潜在的に迅速な行動を許容し、リスク、合併症、および追加の感染点を減少させることを目的としている。また我々のINSPIRA ART挿管は それは多くの特許特性を持ち、既存の商業挿管、例えば小径16-21 Fr(必要な流量に依存する)より優れ、患者の覚醒と自発呼吸時に管腔を患者の頸静脈に直接注入することを許可し、長さは比較的に短く、定位を必要とせず、透視或いは他の画像を必要とし、挿管と応用は簡単である。 | |
| ● | コンパクトでポータブルで、様々な環境に展開することができます:我々のINSPIRA ART(Gen 2)は比較的体積が小さいため,大きな経済的負担を招くことなく,病院病棟や外来環境を含めてICUおよび非ICU環境で使用することができる。 |
我々の開発チームは現在,プロトタイプ設計(設計,仕様,動作パラメータ,コンポーネントを含む)を行っている.
研究結果−Inspira ART(第2世代)
私たちは臨床前の体内実行可能性研究を完成した。また,新たに購入したbrや製造されたコンポーネント,プロセス統合,自動化など,テストや制御目的のための研究を継続する予定である.
55
2020年を通じて、著者らは著者らのチームとイスラエルのラハフCRO獣医チームの指導の下で、一連の研究の中で約40項目の臨床前の体内実行可能性試験を行い、直接血液酸素化による機械換気需要の実行可能性を研究する。これらの研究の主な目標は,われわれのINSPIRA ART実験室装置を用いて,臨床的に有意な数の酸素を静脈血液に移しながら大量の二酸化炭素を抽出することにより,呼吸不全中の酸素交換の一時的な増加を示すことである。
研究者は7頭の大きさの白X長白豚(解剖構造、体型の大きさと他の特徴が人類と類似しているため選ばれた)、1頭の体重は約90から130キロであり、人工低酸素状態(即ち個体の血液中の酸素含有量が異常に低い状態)に置き、血酸素飽和度は80%まで低下した。純酸素を医療用空気およびN 2 Oと混合することにより酸素濃度を低下させ,酸素濃度レベルを約15%に低下させた。酸素減少の目的は,損傷した罹患肺の呼吸不全状態をシミュレートすることである。血液酸素飽和度が90%以下に低下した場合,多くの医師は機械換気brを用いて血中酸素レベルを向上させることを考慮している。
2020年8月,イスラエルのLahav C.R.O.で臨床前 実行可能な体内テストを行い,Inspira ARTが数分以内に血中酸素飽和度 レベルを再平衡させる能力を試験した。25個の低酸素誘導事象のうち20個にINSPIRA ART治療を投与し,血流速度は1−1.5リットル/分であった。われわれのINSPIRA ART実験室装置を用い,あらかじめ留置し,ブタの右頸静脈を介してわれわれ独自の二重管腔チューブを介してブタに接続した。われわれの独自の両腔挿管は,静脈ドレナージと頸静脈による血液の輸血を同時に行うことを可能にした。われわれのINSPIRA ARTは遠心ポンプを含み,両腔挿管の出口ドレナージチューブを介してブタの右頸静脈から血液をポンプする。血液がシステムの酸素交換器を介して循環し、血液に豊富な酸素含有量と低減された二酸化炭素レベルを提供する。閉鎖されたシステムでは、酸素含有血液がチューブの入口を通ってチューブに循環する。
試験点から血液サンプルを採取し、一定時間ごとに豚の血中酸素飽和度をモニタリングした。われわれのINSPIRA ARTはただちにブタの血中酸素飽和度レベルを向上させ安定させ,被験者の治療反応が異なる可能性を考慮した。プログラム は,我々のINSPIRA ART活性化後に上昇したbrと安定した血中酸素レベルの一致性と再現性を測定·証明するために,複数の被験者と異なる時期に複数回繰り返した。この効果はわれわれのすべての臨床前生体試験(研究)で実現されている。また,われわれ独自のダブルチューブは挿入·摘出され,合併症はなかった。研究に使用したカニューレの検査により、構造は完全であり、構造損傷の兆候や独特の特徴はないことが分かった。
Inspira ART(第2世代)−臨床前研究の概要

56


57

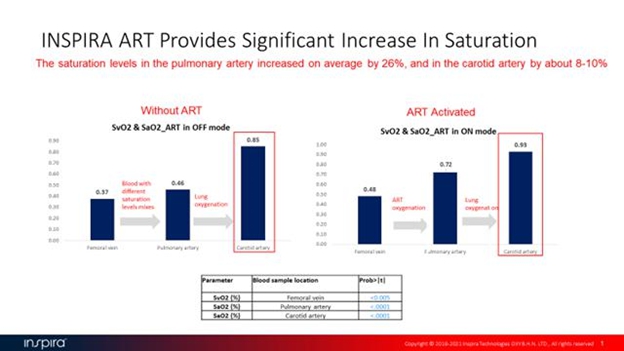
58
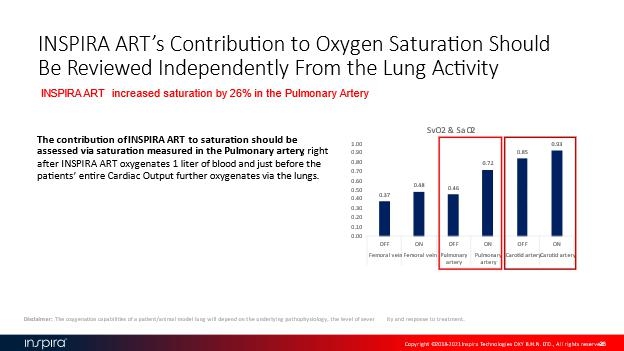
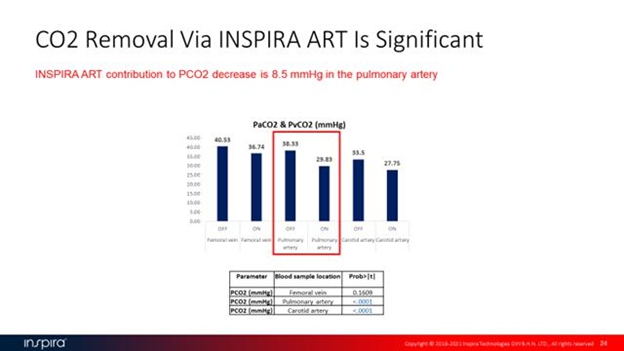
2022年9月、私たちは私たちの科学諮問委員会のメンバー、ICU、呼吸器専門家が指導し、ラハフC.R.Oで行われた動物研究を完成した。動物研究の完成は、Hyla血液センサを用いた人体研究を開始するもう一つの重要なステップである。動物研究期間中、Hyla血液センサは血液パラメータの測定を行い、結果を通常の血液ガス分析器を用いて採取·分析した大量の血液サンプルと比較することが現在の病院で使用されている看護基準と考えられている。動物研究は我々の実験室でHyla血液センサを用いて成功した体外データを得て行った。実験室結果は鼓舞的な動物研究データを伴い、人類研究への重要な一歩である。
59
2023年8月、私たちは米国マサチューセッツ州ボストンでINSPIRA ART 100可用性研究を完了しました。この可用性研究には、ターゲットユーザ、使用および使用環境の人為的要因を考慮することを目的としたINSPIRA ART 100のテストおよび検査に参加する米国の医療専門家が含まれています。
Inspira芸術品-市場機会
WHOによると、2017年、全世界で4億人以上が呼吸不全の影響を受けていると推定されている。毎年約2000万人の患者がICUに収容され,急性気道看護が必要である。2025年までに呼吸ケア設備の市場規模は2019年の160.9億ドルから298.6億ドルに増加すると予想される。この増加に影響する主要な要素は呼吸器疾患の高発病率、高齢化人口の急速な増加、喫煙の高流行率、都市化と汚染レベルの上昇、早産と生活様式変化の増加を含む。
全世界の呼吸看護設備市場の増加は(I)呼吸器疾患に罹患しやすい老年人口の増加、(Ii)慢性呼吸器疾患の高罹患率、及び(Iii)看護標準の向上と治療範囲の拡大により、医療保健業界への政府の支出が増加したためである。これらの要因は,毎年より多くの人が呼吸器疾患や呼吸機能不全と診断されているため,獲得可能かつ入手可能な呼吸治療の需要を拡大し,増加している医療需要を支援している。しかし、機械換気の使用にもいくつかの局限性が存在し、機械呼吸器の高コストと機械換気の使用に関連するリスク、例えば呼吸器関連性肺炎(VAP)の発病率の上昇を含み、これは市場の増加を阻害する。医療の提供と救命の緊急性は,呼吸不全や呼吸不足呼吸治療需要を増加させる駆動要因である。現在の解決策に関連する制限、リスクとコストは多くのレベルで医療システムの過度な圧力と負担を増加させ、患者の結果に直接と間接的な影響を与えた。これは既存の市場参加者に新たな機会を提供し、新会社の市場進出に新たな技術的解決策を提供する可能性があり、これらの企業の需要は高い。
呼吸ケア設備市場は地理的に北米、ヨーロッパ、アジア太平洋地域、ラテンアメリカ、中東、アフリカに分かれている。2019年、北米は呼吸ケア設備市場で最大のシェアを占めた。米国だけで年間570万人以上がICUに入院する必要があり,そのうち40%に達する人が機械換気を必要としているのは1950年代以来使用されてきた現行の看護基準である臨床感染症オックスフォード大学出版社が2020年8月に出版した医学定期刊行物は、“アメリカ国内の11,721名のコロナウイルス病(新冠肺炎)入院患者の特徴と予後”と題されている。高齢者人口の増加やより多くの人の喫煙や汚染への曝露に伴い,治療を必要とする人口が圧倒的な速度で増加している。JAMAが2018年2月に発表した“急性呼吸窮迫症候群:診断と治療の進展”と題する文章の最新推定によると、ARDSは集中治療室入院者数の10%を占め、br}は毎年300万人以上のARDS患者を代表する。ジョン·ホプキンス医学が2017年4月に発表した“呼吸窮迫症候群の高コスト生存”という記事によると,ARDSは毎年約20万人に影響し,ARDS生存者br}は通常認知障害,心理健康問題,身体障害などの長期損傷があり,これらはbr就業に影響する可能性がある。“新冠肺炎時代の急性呼吸窮迫症候群の診断と処置”によると, 診断(バーゼル)ARDSは深刻な臨床疾患であり、深刻な低酸素性呼吸不全と定義され、それは依然として顕著な発病率、死亡率と医療資源の利用と関係がある。同じ情報源によると、ARDSは集中治療室(ICU)の7%-10%の入院患者と15%-25%の人工呼吸患者を占め、30%-50%の患者の中で致命的なbr}であり、1患者のICU滞在の平均コストは90,000ドルを超える。BKS Partnersの“新冠肺炎が雇用主が支援する健康計画にどのように影響するか”という記事によると、呼吸器疾患で96時間以上換気を要する入院総費用の中央値は88,114ドルであった。その増加する老年人口と呼吸器疾患の伝播に有利な環境条件 のため、新冠肺炎はこの地域に深刻な影響を与え、呼吸看護設備の需要を大幅に増加させた。そのため、この市場と隣接市場の参加者は重症看護機器と呼吸看護設備の生産拡大に集中したり協力したりしている。
60
全世界範囲内で、新冠肺炎疫病の発生により、機械呼吸器に対する需要が大幅に増加し、全世界の集中治療室の入院人数が急増した。全世界の新冠肺炎病例は指数級の増加を呈し、長期と短期の呼吸支持が必要であり、新しい解決策に対する需要も増加した。甚だしきに至っては新冠肺炎の前に、毎年約2,000万人の患者がICUで人工呼吸治療を受けている。
市場戦略に向かう
私たちの入市戦略は負担できる製品を提供することに基づいて、使い捨て製品とソフトウェア許可に基づくブレードビジネスモデルに基づいて、私たちの市場カバー範囲を最大限に拡大するとともに、全世界の医療保健の負担性と可獲得性を高める。我々はこの努力に集中して多学科マーケティングや業務方法を全面的に理解することが我々の目標を実現するために必要である.
私たちの入市戦略には
| ● | 世界的な規制承認を求める: 私たちはアメリカ、ヨーロッパ、アジア、中米、南米、アフリカ、中東で規制承認を求める予定です | |
| ● | 最先端の医療センターやWHOと協力して:: 私たちは先進的な医療センターや健康組織と協力しています。これは私たちの製品地域展開戦略の一部です。これには,トップ病院と連携し,医師や医療業界に我々のINSPIRA ART機器 を示すことも含まれている | |
| ● | 潜在的な顧客プロファイルの決定:更新または革命的な生命支援ソリューションが必要なリーディング医療センター、共同購入組織、医療機器会社を目指します。私たちは、注入主義市場における複数回のリコールと、この業界の革新が不足しているため、Inspiraは異なる体験と結果を求める潜在的な顧客を探していると信じている。 | |
| ● | :br医療機器会社,メーカー,流通業者と合意しました。私たちは米国、ヨーロッパ、アジアを含む世界の他の地域のディーラーと同様の協定を締結するつもりだ |
| ● | マーケティングと広報に投資して、私たちの解決策に対する認識を高める :INSPIRA ART(Gen 2)に対する市場の需要を推進するために、CPB装置であり、その後、使い捨て装置および血液センサ(INSPIRA ART 100と統合される)を発売するINSPIRA ART 100(Gen 1)を発売している。シアトルで開催された2023年度体外生命支援組織会議で行われたように,我々が提供する技術や設備 に触れ,これまでINSPIRA ART 100(Gen 1)がFDAに提出され,510(K)の許可を得てINSPIRA ART(Gen 2)が開発されていることを業界に伝えたい。これらの設備は人体で使用されたりテストされたりしておらず、FDAや同様の外国規制機関の承認や承認も得られていない。 | |
| ● | 適切な補償と保険を受ける: 私たちが最も重要なのは精算と保険を得て、病院と医療センターが私たちの製品を利用して治療を提供できるようにすることです。 集中治療がますます高価になるにつれて、Inspira ARTは患者の看護の質に影響を与えることなく、著しく低減されたコストで治療を提供する可能性がある。精算戦略の一部として,医療経済学モデルを研究している。医学文献の発表,医療保険や医療補助サービスセンター(CMS)への実データの提供を目指しており,これらのデータは一流病院とともに提供されている。 |
61
2022年12月、Terumo心血管会社と独占オリジナル機器メーカーまたはOEM協定を締結し、Terumo心血管会社は世界有数の医療機器会社Terumo Corporationの支社である。このプロトコルは,我々のINSPIRA ARTデバイスとともに配布可能な使い捨てフロー装置 を製造することを規定している。
2023年7月、私たちはPerfusion Solution,Inc.と協力協定を締結しました。これはアメリカに本部を置くリーディングカンパニーで、アメリカの大手病院に先進医療設備、訓練、人員を配備するプラットフォームを提供します。この協力には、INSPIRA ART 100製品とPerfusion Solutionの米国における広範なビジネスの足跡とインフラを組み合わせることが含まれている。協力には、要約流通協定が含まれ、その後、より包括的な合意に署名される。このプロトコルの初期期限は5年であり, は製品開発の完了と何らかの購入目標を満たすことに依存する.
また,2023年11月に,ICU患者の関連血流感染を予防するために,生体電子創傷包帯開発先駆者EnnoCUREと協力協定を締結し,br独自の生体電子療法を開発した。私たちの使命の核心は生命支持機械換気の代わりに血液に酸素を直接充填する先駆的な方法である。Inspiraは,生体電子技術 をInspira ART and Company知的財産権の一部とし,血液感染(膿毒症)をきたすことが多い細菌の増殖を防止することを求め,Ennocureと連携してこのような治療法を開発している。開発が完了すると、著者らは生物電子 の新しい物理刺激技術を結合し、潜在的ハイリスク患者の先制措置として、コスト競争力のある解決策 を提供して合併症を減少させる予定である。世界では毎年250,000例の静脈輸液に関する血液感染が発生し,入院期間の延長や医療コストの増加を招くと推定されている。
私たちがこのような合意を締結した流通会社は、Innovimed(すべてのヨーロッパ諸国をカバー)、Bepex、Anita Técnica S.LまたはWAAS Group(スペインとポルトガルをカバー)、Glo-Med(テキサス州、ニュージャージー州、ニューヨーク、フロリダ州、ノースカロライナ州、サウスカロライナ州、湾岸諸国をカバー)、CIO MEDグループ(中央アメリカをカバー)を含む。
我々は戦略流通プロトコルに従って を実行する予定であるが,これらの既存プロトコルや将来実行可能なプロトコルに基づいていかなる販売も保証されていない.事前条件流通協定の期限は最長7年であり、開発完了と必要な規制承認または許可を待たなければならない。
2021年10月、スペインの有力医療機器·用品流通業者および技術サービス提供者Anita Técnica S.L.(Waas Group)と独占販売契約を締結した。協定によれば、Anita Técnica S.L.(WAASグループ)は、監督機関がスペインおよびポルトガルでのINSPIRA ARTデバイスの販売およびマーケティングを許可することを前提として、病院および医療センターに を配備するために、少なくとも1,040台のINSPIRA ARTデバイスおよび35,360台の使い捨てデバイスを7年以内に購入することを約束する。
2021年12月に、私たちはInnovimed Spと独占要約流通協定を締結した。Zo.o,またはInnovimedは,東欧,中東,アフリカで最先端の医療解決策を提供する主流通業者 である。この合意の初期期限は7年であり, は製品開発の完了と規制部門の承認に依存する。双方はInspira ART機器のマーケティングと配備について協力する。2023年8月、私たちはInnovimedとInspira ART呼吸装置の臨床試験を協力して行う拡張協定 を締結し、この試験はヨーロッパの任意の国をカバーした。
62
2022年1月、私たちは米国の6つの州(テキサス州、ニュージャージー州、ニューヨーク州、フロリダ州、ノースカロライナ州、サウスカロライナ州)で販売される増加する革新的な医療機器および関連製品の需要を満たすために、米国会社Glo-Medと独占的な概要流通協定を締結した。要約流通協定の後にもっと包括的な合意があるだろう。Glo-Medと締結した協定の初期期限は7年であり、製品開発の完成と関連監督部門の承認が待たれる。双方の はInspira芸術のマーケティングと配置について協力する。プロトコルに基づいて、および地域で独占的な地位を維持するために、Glo−Medは、上述した米国6州での販売およびマーケティングInspira ARTデバイスの規制承認に依存して、7年以内に病院および医療センターにbrを配置するために、少なくとも2,121台のInspira ARTデバイスおよび131,413台の使い捨てデバイスを購入することを約束している。
2022年4月、私たちはBepex Ltd.またはBepexと将来的に配備される可能性のあるINSPIRA ART装置を含む要約流通協定を締結し、侵襲的な機械換気を防止することを目的とした。Bepexは先進的なイスラエル医療技術会社であり、ハミルトン(機械呼吸器)とLivaNova(ECMO-Extraorporeal膜酸素化システム)などの全世界の医療設備会社が医療設備を輸入、販売とサービスしている。Bepexとの協力の一部として,第1陣のシステムはイスラエル最大の医療センターに配備される予定である。Bepexと要約流通合意を達成した後,より包括的な合意に達する予定である.合意 の初期期限は7年であり、製品開発と関連する監督管理審査を完成する必要がある。
2022年7月、私たちはGlo-Medと独占的な概要流通協定を締結し、米国6州(テキサス州、ニュージャージー州、ニューヨーク州、フロリダ州、ノースカロライナ州、サウスカロライナ州)でHyla血液センサ装置および使い捨て装置を流通させた。要約流通プロトコル の後はより包括的なプロトコルとなる.この合意の初期期限は3年であり、製品開発と監督管理の承認を完了する必要がある。双方はHyla血液センサーのマーケティングと配置で協力するつもりだ。プロトコルによれば、Glo-Medは、この地域における独占経営権を維持するために、病院および医療センターへの配備のための少なくとも3,889台のHyla血液センサおよび264,873台の使い捨て装置の購入を約束しているが、米国6州でHyla血液センサ装置を販売および販売するためには、規制部門の許可を得る必要がある。
2022年11月、私たちはInnovimedとヘラ血液センサーの独占的な概要流通協定を締結した。要約流通プロトコルの後に はより包括的な最終プロトコルを持つであろう.この協定の初期期限は5年であり,製品開発の完了と規制承認を受けることに依存する。双方はHyla 血液センサのマーケティングと配置について協力する。この地域での独占的な地位を維持するために、Innovimedは、ポーランド、チェコ共和国、およびスロバキアの病院および手術室に配置された少なくとも1,364個のHyla血液センサおよび128,511個の使い捨て装置を購入することを約束した。
2023年10月、私たちはCIO MEDグループと中米でInspiraARTデバイスと使い捨てキットの独占的概要流通協定 を締結しました。この協定は、主に5年間の使い捨てキットの経常収入から2,800万ドルの潜在的収入をもたらす可能性があり、監督部門の承認が必要である。体外循環手術を受けた患者のために設計されたINSPIRA ART 100装置に加えて、フラッグシップ製品INSPIRAART(第2世代)装置およびヒラInspira血液センサ技術、br}およびこれらの技術装置と共にプログラムで使用される使い捨てキットも含まれる。
2024年1月、私たちはGlo-Medと簡単な流通協定を締結し、湾岸諸国に531台のART設備を配備した。この協定は5年以内にInspira Technologiesに3260万ドルを提供する可能性があり、これは規制部門の承認が必要だ。この合意によると、Glo-Medはサウジアラビア、アラブ首長国連邦、バーレーンにおける会社の流通業者に指定されるだろう。サウジアラビアが650億ドルを投資し,さらに医療部門を民営化する二重戦略,すなわち2030年のビジョンは,この領土が新興の医療革新市場であることを示していると考えられる。要約流通協定の後にもっと包括的な合意があるだろう。プロトコルによると、Glo-Medは、地域内で承認された顧客へのINSPIRAART(第2世代)デバイスの普及、マーケティング、販売、INSPIRA ART(第2世代)使い捨てキット、INSPIRAART 100デバイス、およびINSPIRA ART 100使い捨てキットを含む地域卸売業者の役割を担う。Glo−Medは地域独占流通業者になるべきであり,同社は最低購入量531個のInspiraART設備と8,794個の使い捨て設備の目標を満たさなければならず,この地域の関連法規が承認された日からbr}を満たさなければならないことを前提としている。
63
我々は戦略流通プロトコルに従って を実行する予定であるが,これらの既存プロトコルや将来実行可能なプロトコルに基づいていかなる販売も保証されていない.事前条件流通協定の期限は最長7年であり、開発完了と必要な規制承認または許可を待たなければならない。
第三者精算
2024年3月まで、私たちは第三者決済協定を持っていない。我々の目標は既存のCPTコードを使用することである.
知的財産権
私たちはアメリカと国際的に私たちの製品と技術のために特許保護や他の効果的な知的財産権を求めています。私たちの政策は内部開発の知的財産権を追求、維持、保護し、私たちの業務発展に重要なビジネス意義を持つ技術、発明と改善を保護することである。
私たちの知的財産権の組み合わせは、3(3)件の許可された特許、2つの(2)件の米国およびイスラエルにおける1つの特許、1つの米国で許可された出願、3つの国際特許出願(PCT)を含む5(5)個の特許シリーズを含み、そのうちの2つは使い切っており、18(18)件の保留特許出願を含み、 は4(4)件の米国実用プログラム特許出願および3つの欧州特許出願を含む。また12件(12)件の国家段階申請 (韓国両(2)部、中国両(2)部、イスラエル両(2)部、日本両(2)部)我々のポートフォリオには、それぞれ“INSPIRA”テキストとロゴ、“INSPIRA ART”と私たちのスローガン“INSPIRA”である4つのイスラエル登録商標が含まれている。呼吸に力が与えられている
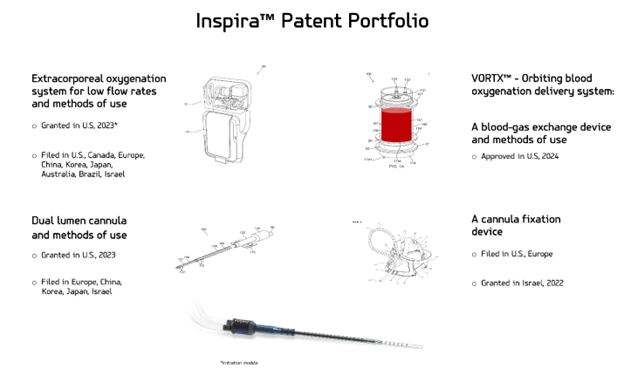
64
体外酸素化システム(*起動brモジュール)
これはInspira ART(Gen 2)のために設計された新しい自動自己起動モジュールであり,この独自の革新的な操作モジュールはInspira ART(Gen 2)の進歩をさらに拡張し,独自の内蔵自動起動モジュールにより患者の安全を確保し,患者の血管系との無血栓接続を確保し,血栓形成のリスクを潜在的に低下させ,血流を減少させることを目的としている。この特許は、9つの異なる特許請求書からなり、すべての特許請求項は、発明価値および実用的適用性を有する新奇なものとみなされる。
この革新は16項目の声明が発見されたが、繊維膜のない血液に酸素を充填することを目的としており、医学構造を徹底的に変えることが期待できると信じている。人体内血管中の自然層流とは異なり,既存の繊維酸素交換器では,血液は有害な乱流で多層繊維を通過させるとともに,繊維壁内で摩擦やせん断力を経験する。繊維織物は血液流動の重要な抵抗であるため、高圧差を形成し、そして各種の血液成分に重大な損害を与え、高溶血(赤血球分解)、白血球の破壊、体内炎症系の活性化、免疫系の活性化と血液凝固を含む。
2腔挿管及びその使用方法
特許承認は、創造的ステップおよび工業的適用性を有する新規であることが発見された20の請求項を含む。Inspira Technologiesの変換可能な二腔カニューレbr装置は,初期挿入後に血管内を介して単腔カニューレを二腔カニューレに変換することで,brがすべての口点と潜在的に多様な用途を可能にする。変換可能な二腔カニューレの設計は、単腔から二腔カニューレへの切り替えを可能にし、その逆も同様であり、追加のカニューレを交換または追加する際に新たな切開を行う必要がない。Inspira Technologies変換可能な双管腔は、潜在的に迅速な行動を実現し、リスク、合併症、その他の感染点を減少させることを目的としている
挿管固定装置
このコンポーネントは、患者がベッド上で発生し、および/または輸送中に姿勢を変化させる際に発生する頸静脈挿管移動に関連する潜在的合併症を減少させることを目的としている。成分br}は毎年体外膜酸素化(ECMO)治療を受けている数千人の患者の治療にも潜在的に用いることができる。この部分は,医療従事者が病院と医療センター内と病院の間で覚醒した挿管患者をより安全に動員することを可能にする予定である。
65
次の表には技術特許が含まれています
| 刊行物番号 | タイトル | 発効申請日 | 状態.状態 | |||
| IL 286271 | 挿管固定装置 | 2021年9月10日 | 承認された | |||
| PCT/IL 2022/050902 | 挿管固定装置 | 2022年8月18日 | 保存済み | |||
| EP 22856981.0;4185347 | 挿管固定装置 | 2022年8月18日 | 決を待つ | |||
| アメリカ17/931,134 | 挿管固定装置 | 2022年9月11日 | 決を待つ | |||
| CN 202180076037.0;16472077 | 2腔挿管及びその使用方法 | 2021年11月10日 | 決を待つ | |||
| EP 21891360.6;4199990 | 2腔挿管及びその使用方法 | 2021年11月10日 | 決を待つ | |||
| IL 302851 | 2腔挿管及びその使用方法 | 2021年11月10日 | 決を待つ | |||
| JP 2023550749;2023548436 | 2腔挿管及びその使用方法 | 2021年11月10日 | 決を待つ | |||
| KR 10-2023年-7019401;20230107622 | 2腔挿管及びその使用方法 | 2021年11月10日 | 決を待つ | |||
| 一ドル。二 | 2腔挿管及びその使用方法 | 2021年11月10日 | 承認された | |||
| 米国18/062,610;2023/0095678 | 単腔挿管に変換可能な2腔挿管及びその使用方法 | 2021年11月10日 | 決を待つ | |||
| AU 2021390218 | 低流量体外酸素化システム及びその使用方法 | 2021年12月1日 | 決を待つ | |||
| BR 12023010627-3 | 低流量体外酸素化システム及びその使用方法 | 2021年12月1日 | 決を待つ | |||
| CA 3200492 | 低流量体外酸素化システム及びその使用方法 | 2021年12月1日 | 決を待つ | |||
| CN 202180091081.9;116782964 | 低流量体外酸素化システム及びその使用方法 | 2021年12月1日 | 決を待つ | |||
| EP 21900219.3;4228717 | 低流量体外酸素化システム及びその使用方法 | 2021年12月1日 | 決を待つ | |||
| IL 303362 | 低流量体外酸素化システム及びその使用方法 | 2021年12月1日 | 決を待つ | |||
| JP 2023533325;2023552754 | 低流量体外酸素化システム及びその使用方法 | 2021年12月1日 | 決を待つ | |||
| KR 10-2023年-7022195;2023018594 | 低流量体外酸素化システム及びその使用方法 | 2021年12月1日 | 決を待つ | |||
| 793,919ドル | 低流量体外酸素化システム及びその使用方法 | 2021年12月1日 | 承認された | |||
| アメリカ18/216,565;2023/0338634 | 低流量体外酸素化システム及びその使用方法 | 2021年12月1日 | 決を待つ | |||
| アメリカ18/235,515 | 血液ガス交換装置及びその使用方法 | 2023年8月18日 | 許可の | |||
| アメリカ18/434,809 | 体外サポート患者看護の自動監視とその相互ユーザインタフェース | 2024年1月7日 | 決を待つ |
66
私たちはまたビジネス秘密、技術ノウハウ、持続的な革新に依存して、私たちの競争地位を発展させ、維持しています。私たちは、私たちの任意の未解決特許出願または未来に提出された任意の特許出願に特許が付与されるかどうかを決定することができず、私たちの任意の既存特許または将来私たちに付与された任意の特許が、私たちの技術を保護する上で商業的用途を有することを保証することはできません。
私たちの成功は知的財産権の組み合わせにある程度依存し、この組み合わせは未来の収入源を支持し、私たちの競争相手に障害を設定する。
このような措置にもかかわらず、私たちの任意の知的財産権と独自の権利は挑戦、無効、回避、侵害、または流用される可能性がある。知的財産権および独自の権利は、現在の市場傾向を利用したり、他の方法で競争力のある傾向を提供するのに十分ではないかもしれない。詳細は“プロジェクト3.D.--リスク要因--我々の知的財産権に関するリスク”である
研究開発と政府支出
著者らは積極的な内部研究開発プロセスを維持しており、その中には臨床活動と監督管理事務も含まれている。2023年12月31日まで、私たちの研究開発チームは36人で構成されている。2023年12月31日と2022年12月31日までの年間で,それぞれ約740万ドルと820万ドルの研究開発費と関連費用が発生した。研究開発費の減少は主に株式ベースの給与支出は約170万ドル減少し,研究開発従業員数の増加により賃金と関係者支出が100万ドル増加し,この部分は減少した費用を相殺している。さらに20万ドル増加しましたはい内部開発に関する材料と関連 費用。
2023年12月31日現在,IIAから得られた総額約800,000ドルの贈与は,我々の研究·開発事業に一部の資金を提供している。これらの贈与を受け,血液酸素化システムの開発に用いられ,直接血液酸素化と血中酸素飽和度レベルの向上による生命支援を提供しながら二酸化炭素を除去することを目的とした。2023年11月、国際投資局がVortxに提供した別の寄付金を受け取りました。国際投資局が承認した初年度予算100万ドルの40%に相当します。私たちは2024-2025年の間に資金を受け取る予定だ。これらの贈与には返済義務はありませんが、商業化段階に達すると、1つの贈与ごとに印税を支払うことが要求され、料率は私たちの収入の3%、最高で受け取ることができる贈与総額に達します。このような 特許使用料を全額支払った後,通常は特許権使用料を支払う必要がない.それにもかかわらず、創新法での制限は引き続き適用され、たとえわが社が贈与に応じて支払うべき印税を全額返済していても。
生産と製造活動
我々のINSPIRA ART(第2世代)デバイスおよび/またはINSPIRA ART 100(第1世代)デバイスは複数のコンポーネントからなる.私たちは、各患者の治療のための、血液酸素化および血液モニタリングのための、brおよび使い捨てユニットとして、組み立てられた製品(デバイス)を販売する予定です。製品および使い捨てコンポーネントを組み立てるコンポーネントは、独自のコンポーネントと既製のコンポーネントからなる。独自のコンポーネントは、規制要件に適合するようにGMPの承認された生産工場で私たちを代表して生産され、既製のコンポーネントはInspiraチームによって調達される。GMP下請けは、独自コンポーネントと既製コンポーネントとを一緒に組み立てて、我々のINSPIRA ARTおよび/またはINSPIRA ART 100デバイスを作成する。
67
2022年12月、私たちはTerumo心血管会社と戦略OEM協定を締結した。このプロトコルはFLOW 機械装置の製造を規定しており,これを我々の製品に集積し,酸素化過程における血液の体外循環 に用いることを目的としている。これはまた、INSPIRA ART(第2世代)および/またはINSPIRA ART 100(第1世代)デバイスに統合されることを含むことができる。
また,エンドツーエンド解決策を提供するリーディングOEMベンダと他の契約製造や流通プロトコルについても検討を開始した.供給チェーン管理アウトソーシング(例えば、製造、物流、輸送とアフターサポート)は資本支出、納期とコストを減少させ、同時に柔軟性と敏捷性を提供してくれた。
2022年12月、我々のINSPIRA ART 100デバイスは、リードする医療電子機器会社にbr新製品紹介、NPI、および量産サービスを提供するエンドツーエンドソリューション提供者によって代理生産されることを発表した。これは、完全交鍵製造、完全システム統合(プリント回路基板またはプリント回路基板を含む)、製造、組立サービス、テスト および良好な製造仕様またはGMPコンプライアンスに適合する施設での包装を含む。製造したInspira ART 100装置は,2023年9月にFDA(FDA)に提出して510(K)の承認を行う前に,br}検証と確認段階を経験する。FDAの承認が得られれば、INSPIRA ART 100設備生産ラインは低速度初期生産或いはLWRIPに拡張され、これは系列化製造、品質管理と輸送を支援するためにインフラを開発する重要な運営段階である。将来的に米国とイスラエルにINSPIRA ART 100装置を初めて配備するために、より多くの設備を組み立てる予定だ。
競争
Br医療機器業界の特徴は、技術進歩が迅速で、競争が激しく、独自製品を高度に重視していることである。多くの医療機器会社、バイオテクノロジー会社、公立と私立大学および研究機関は、私たちの製品に似ている可能性のある製品の研究と開発に積極的に従事している。
集中治療室および急性呼吸ケア分野の市場参加者は、ボストン科学社(ニューヨーク証券取引所コード:BSX)、ResMed Inc.(ニューヨーク証券取引所コード:RMD)、Masimo Corporation(ナスダック:MASI)、Becton、Dickinson and Company(ニューヨーク証券取引所コード:BDX)、チャット工業(ナスダック:GTLS)、フィリップス医療保健会社、美敦力(ニューヨーク証券取引所コード:MDT)、フィッシャー&ペッカーヘルスケア株式会社、Dr.gerwerk AG&Co.KGaA、Dr®gerwerk AG、 Hamilton Medical AG、Dr gerwerk社、MNMNCYバクスター国際(ニューヨーク証券取引所株式コード:BAX),Getinger,GE Healthcare,Terumo Corporation(TYO:4543,日経225成分株),Liva Nova PLC,Fresenius SE&Co.KGaA,ジョンソン,Resusciec,Spectrum医療など,これらの会社は呼吸器,体外膜酸素化装置,血液センサなどの呼吸器系看護設備や解決策を開発あるいは買収している。
これらの会社は、我々と比較して、より多くのブランド認知度、研究開発と監督管理能力、および財務、技術、製造、マーケティング、人的資源を持っており、医療設備の研究開発、FDAおよび他の監督管理許可を得て、世界各地でこれらの設備を商業化する上で著しく多くの経験とインフラを持っている。
その他Inspira技術製品
著者らの旗艦製品はINSPIRA ART(第二世代)設備であり、1つの突破的な技術になり、急性呼吸器看護の方法を組換えし、全世界の患者にその可及性、安全性と医療効果を高めることを目的としている。これを実現するためには,HASEはこの努力を支援するためにより多くの製品を開発する必要があることを認識している.そこで,心肺支持を提供するための体外血液循環装置と,Hyla血液センサであるINSPIRA ART 100(Gen 1)装置を開発しており,体外循環中に血液パラメータを測定するための非侵襲的光学血液センサである。
著者らの入市戦略は価格の安い製品を提供することを重点とし、ブレード商業モデルを基礎として、最大限に著者らの市場カバー範囲を拡大し、同時に全世界の医療保健の負担性と可獲得性を高める。私たちはこの努力に全面的に注目し、その目標を実現する多学科方法を理解した。基本的なビジネスモデルから重要な臨床研究による業界承認まで,これらの研究は我々の製品の有効性と安全性を証明しており,我々は成功した市場浸透と我々の製品を採用する方向に向かっている。
68
生体電子 技術をINSPIRA ARTと我々の知的財産権の一部とし,血液感染(敗血症)をしばしば引き起こす細菌の増殖を防止することが求められている。私たちはEnnocateと協力してこの治療法を開発した。
2020年6月,B.G.Negev Technologies and Applications Ltd.やBGNと協力·許可協定を締結し,BGNはBeer Shevaに位置するNegev大学の完全子会社である.これまで、私たちおよびBGNは、必要に応じて酸素を放出することができる安定なポリマーマイクロバブルまたはMBSプラットフォーム を開発し、特徴付けてきた。開発プロセスは、MBSにおける酸素貪食プロセスを評価し、必要な速度での酸素放出を観察するために、深く研究する必要がある。この新たに提案された技術はさらに開発され,INSPIRA ART(第2世代)デバイスへの統合を目指している.定義されたX 2システムは、酸素交換器の使用寿命を延長し、INSPIRA ART装置における血液凝固を潜在的に防止することを目的としている。このプロジェクトは現在一時停止状態にあり、さらなる通知を待っている。
政府法規と製品承認
私たちの製品と運営はFDAと似たような国際規制機関を含む多くの世界的な監督管理機関によって規制されている。
我々の製品はFDAによって実施·施行されている連邦食品,薬物,化粧品法案(FDCA)によって医療機器として規制されている。FDA は医療機器の開発、設計、非臨床と臨床研究、製造、安全性、有効性、ラベル、包装、貯蔵、設置、サービス、記録保存、発売前承認、輸入、輸出、不良事件報告、広告、販売促進、マーケティングと流通及び輸出入を監督し、国内で流通する医療機器が安全かつ有効であることを確保し、その期待用途に適用し、その他の方法でFDCAの要求を満たす。
アメリカの法規以外に、私たちはヨーロッパ経済区(EEA)の各種法規の制約を受けて、これらの法規は私たちの製品の臨床試験と商業販売と流通を管理しています。FDAの承認または承認された製品が必要かどうかにかかわらず、臨床試験を開始する前に許可を得、米国以外の国の比較可能な規制機関に基づいて私たちの製品のマーケティング許可または承認を得て、これらの国で臨床試験を開始したり、私たちの製品を商業化することができます。承認プロセスは国/地域によって異なり,所要時間はFDA承認に要する時間よりも長いか短い可能性がある.設備のリスクレベルによって、医療設備は通常異なるレベルの監督管理によって制御される。
FDAの上場前の承認と承認要求
適用免除が適用されない限り、米国で商業流通されている各医療機器は、FDA承認510(K)販売前通知、承認最初からの申請、または販売前承認申請またはPMAの承認を必要とする。FDCAによると,医療機器は,I,IIまたはIIIの3つに分類され,各医療機器に関連するリスクの程度と,その安全性と有効性を確保するために必要な規制制御の程度に依存する。クラスIは、患者に対するリスクが最も低いデバイスを含み、 は、FDAによる医療デバイスの一般的な制御を遵守することによって、その安全性および有効性を保証することができるデバイスであり、 は、QSRの適用部分、施設登録および製品リスト、不良医療イベントの報告、 および真および非誤解性のラベルを含む。第2のタイプのデバイスは、デバイスの安全性および有効性を確保するために、FDAの一般的な制御およびFDAによって必要とされる特別な制御を受ける。これらの特殊な制御は性能標準、発売後の監視、患者登録とFDA指導文書を含むことができる。多くのタイプIデバイスは510(K)発売前通知の要求を受けないが、クラスIIデバイスの製造者の多くは、FDCA第510(K)節に従ってFDAに発売前通知を提出する必要があり、このデバイスの商業的な流通を許可することを要求する。FDAは、一般に510(K)許可と呼ばれる510(K)の発売前の通知の影響を受ける商業流通を可能にする装置である。
69
510(K)プロセス
510(K)プロセスによれば、 メーカーは、1976年5月28日(1976年“医療機器修正案”公布の日)前に合法的に発売された設備、 が発売前に承認またはPMAを必要としない設備、III類からII類またはI類に再分類された設備、または510(K)の流れで許可された他の商業利用可能な設備“基本的に同じ”をFDAに提出しなければならない。“実質的同等”を達成するためには, 提案デバイスは述語デバイスと同じ期待用途を持ち,述語セットと同じ技術的特徴を持つか,あるいは異なる技術的特徴を持ち,述語デバイスとは異なる安全性や有効性の問題を起こさない必要がある.実質的な等価性を支援するために臨床データが必要となる場合がある。
510(K)の上場前通知を提出した後、FDAは当該通知を受け入れるか否かを実質的に審査することを決定する。実質的な審査に必要な情報が不足している場合、FDAは510(K)通知を受け入れることを拒否する。もしそれが記録されたら、FDAは実質的な検討を始めた。法規によれば、FDAは、510(K)通知を受信してから90日以内に510(K)通知の審査を完了しなければならない。実際の問題として、通関には通常より長い時間がかかり、通関は決して保証されないだろう。多くの510(K)の発売前通知は、臨床データなしに承認されているが、FDAは、実質的な同等性を決定するために臨床データを含むさらなる情報を必要とする可能性があり、これは、審査プロセスを著しく延長する可能性がある。
*FDAが装置が現在の市場の予測装置に実質的に相当することに同意した場合、510(K)の許可を承認して商業市場 に装置を投入する。FDAが、デバイスが以前に承認されたデバイスと“実質的に等しくない”と判断した場合、デバイス は、FDCAに従ってクラスIIIデバイスに自動的に指定される。次いで、デバイススポンサーは、より厳しいPMA要件 を満たさなければならないか、またはプロセス要求から最初のプロセス要求に基づいてデバイスをリスクベースの分類決定することができ、これは、低中リスクであり、デバイスを予測する新しい医療デバイスの市場進出を予測することと実質的に等しくない経路である。
デバイスが510(K) マーケティング許可を取得した後、そのセキュリティまたは有効性に著しく影響を与える可能性のある任意の修正、またはその予期される用途に対して重大な変更または修正を構成する可能性のある任意の修正は、新しい510(K)マーケティング許可を必要とするか、または修正によっては、承認またはPMA承認を再取得する必要がある。FDAは、提案された変更が510(K)(またはPMA) を提出する必要があるかどうかを最初に決定することを各メーカーに要求するが、FDAは、そのような決定のいずれかを審査することができ、製造業者の決定に同意しない。現在、多くの細かい修正は製造業者によって行われており、メーカーは変更を内部レターファイルに記録している。FDAは、検査中にこれらの手紙を検討して保存することができる。FDAが製造業者の決定に同意しない場合、FDAは、510(K)の許可、最初の承認、またはPMA承認を得るまで、製造業者に の販売を停止し、および/または修正された装置のリコールを要求することができる。このような状況で、私たちは規制部門の巨額の罰金または処罰を受けるかもしれない。
デノボ分類
FDAが従来I類,II類あるいはIII類に分類されていなかった医療機器タイプはFDCAによって自動的にIII類に分類され,それらが構成するリスクレベルは考慮されていない。1997年の食品·医薬品局近代化法案は,低中リスクの医療機器のための市場進出経路を構築し,これらの医療機器は述語装置の欠如により自動的にIII類に分類され,“自動III類指定評価要求 ”,あるいは一から分類プログラムと呼ばれている。このプログラムは、その新しいデバイスが自動的にIII類に分類されることを可能にする製造業者 は、デバイスが低または中リスクがあることに基づいて、その医療デバイスをタイプIまたはIIクラスに格下げすることを要求し、PMA申請の提出および承認を必要としない。 は、“2012年食品·医薬品局安全·革新法”(FDASIA)が公布される前に、製造業者のみが最初に510(K)の発売前通知を提出し、FDAの決定を受け、すなわち合法的に発売された予測デバイスと実質的に等価ではなく、最初から分類する資格がある。FDASIAは、最初から分類する流れを簡略化し、製造業者が最初の分類を直接要求することを可能にし、510(K)の販売前通知 をFDAに最初に提出し、実質的に異なる決定を受信することを必要としない。FDASIAによると,FDAは最初の申請を受けてから120日以内にデバイスを分類しなければならない.製造業者がそれをクラスIIに再分類することを求める場合、製造業者は、医療機器の安全性と有効性を合理的に保証するための特別な制御提案草案を含まなければならない。さらに、FDAが510(K)通知に適した合法的な販売のプリセット装置を発見し、装置のリスクが中程度ではないと判断した場合、または一般的な制御がリスクを制御するのに不十分であり、特別な制御を開発することができない場合、FDAは要求を拒否する可能性がある。デバイスが最初から分類された後、そのセキュリティまたは有効性に著しく影響を与える可能性のある修正、またはその予期される用途に対して重大な変更または修正を構成する可能性のある任意の修正は、新しい510(K) 許可を必要とするか、または修正状況に応じて、別の最初の申請、さらにはPMA承認を必要とする。
70
臨床試験
臨床試験はほとんど常にPMAを支持する必要があり,510(K)の提出をサポートする必要がある場合もある。安全性および有効性を決定するためのすべての研究装置の臨床研究は、研究装置ラベルを管理し、研究装置の普及を禁止し、研究スポンサーおよび研究調査者の一連の記録、報告、および監視責任を指定するFDAの研究装置免除またはIDEに従って行われなければならない。FDAの定義によれば、このデバイスは人間の健康に対して“重大なリスク”を構成し、FDAはデバイススポンサーにIDE申請を提出することを要求し、この申請は人体臨床試験を開始する前に発効しなければならない。重大なリスクデバイスとは、患者の健康、安全または福祉に深刻なリスクを構成する可能性のあるデバイス、またはヒトの生命を支援または維持するためのインプラント、疾患の診断、治癒、緩和または治療、または他の方法でヒトの健康を損なうことを防止するために非常に重要なデバイス、または他の方法で被験者に潜在的な深刻なリスクを構成することを意味する。IDEアプリケーションは、動物および実験室テスト結果のような適切なデータサポートを必要とし、人体上でデバイスをテストすることが安全であり、テストスキームが科学的に合理的であることを示している。FDAが同社に通知して調査を開始しない可能性がない限り、IDEはFDAが通知を受けてから30日以内に自動的に有効になります。FDA がIDEに欠陥や他の問題があると判断した場合,それを修正する必要があり,FDAは臨床 試験を条件付き承認下で行うことを許可する可能性がある。
しかも、この研究は機関審査委員会(IRB)の承認を得て、その監督の下で行われなければならない。IRBはこの研究の初期および継続的な審査を担当し、本研究の実施に追加的な要求を提出する可能性がある。米国食品医薬品局が統合開発環境アプリケーションの発効を許可し,研究が審査機関(S)の承認を得た場合,ヒト臨床試験は研究案に規定されている特定数の研究対象の特定数の研究地点で開始される可能性がある。この装置が患者に重大なリスクがない場合、br}スポンサーは、FDAの単独審査を必要とすることなく、1つまたは複数のIRBsの試験の承認を得た後に臨床試験を開始することができるが、監視調査、研究者のインフォームドコンセントの確保、およびラベルおよび記録保存要件などの簡略化されたIDE要件に従わなければならない。IDEの申請を受けて審査することは、FDAがIDEの有効性を許可することを保証していません。もしこの申請が発効した場合、FDAは、試験から得られたデータがデバイスの安全性および有効性をサポートしているかどうか、または臨床試験を継続することを保証しないかもしれません。スポンサーまたは研究者が研究計画をその科学的合理性、研究計画または人間の被験者に影響を与える可能性のある権利、安全または福祉の変更を行う前に、IDE補充材料をFDAに提出し、その発効を可能にしなければならない。
研究期間中、スポンサー は、例えば、試験モニタリング、臨床研究者の選択、研究計画の提供、IRB審査、有害事象報告、記録保存、および研究装置の普及を禁止すること、またはそれのための安全性または有効性宣言を提示することを含む、適用されるFDA要件を遵守しなければならない。臨床研究の臨床研究者もFDAの規定を守らなければならず、患者のインフォームドコンセントを得て、研究計画と研究方案を遵守し、研究設備の処置を制御し、そしてすべての報告と記録保存要求を守らなければならない。また、試験開始後、著者ら、FDAまたはIRBは、研究対象が直面しているリスクが期待収益よりも大きいと信じることを含む、様々な理由でいつでも臨床試験を一時停止または終了することができる。
発売後監督管理
設備が承認されたり上場が承認されたりした後、多くの幅広い規制要求が適用される可能性がある。これらの措置には限定されるものではない
| ● | FDAの年間および更新された施設登録および設備リスト |
71
| ● | QSR要件は、製造業者に、設計および製造プロセスのすべての点で、厳格な設計、テスト、制御、文書、クレーム処理、および他の品質保証手順に従うことを要求する |
| ● | 広告や販売促進の要求 |
| ● | 販売、流通、または使用設備の制限; |
| ● | 販売促進が真実であり、誤解がなく、十分な使用説明を提供することを要求するラベルおよびマーケティング条例は、すべての主張に根拠があり、許可されていないまたは“ラベル外”用途の製品を宣伝し、ラベルに他の制限を加えることも禁止されている |
| ● | 連邦医師サンシャイン法案と医療顧客との報酬関係を報告する様々な州や外国の法律 |
| ● | 連邦反リベート法規(および同様の州法律)は、連邦医療計画(例えば、MedicareまたはMedicaid)に従って精算可能な項目またはサービスの購入または推薦を誘導するための報酬の請求、受け入れ、提供、または提供を禁止する。個人またはエンティティは、必ずしもこの法規またはその具体的な意図に違反することを実際に理解する必要がなく、違反を実施することができる | |
| ● | 連邦虚偽申告法(および同様の州法)は、虚偽または詐欺的な支払いまたは承認クレームの提出または提出を意図的に禁止し、連邦政府への資金または財産の支払いまたは移転の義務に重大な意味を有する虚偽の陳述を意図的に行うか、または故意に隠したり、連邦政府への資金の支払いまたは移転の義務を故意に回避または減少させる義務を故意に行うことを禁止する。政府は、虚偽請求法規については、連邦反リベート法規違反による物品またはサービスを含むクレームが虚偽または詐欺的クレームを構成していると断言することができる |
| ● | 合法的に販売されている装置の製品修正を承認または承認することは、安全性または有効性に深刻な影響を与える可能性があり、または予期される用途に大きな変化をもたらす可能性がある |
| ● | 医療機器報告条例は、製造業者に、その販売された装置が死亡または深刻な損傷をもたらしたか、または障害を発生させた可能性があり、故障が再び発生した場合、その販売された装置または同様の装置が死亡または深刻な損傷をもたらす可能性があるか、または促進する可能性があることをFDAに報告することを要求する |
| ● | 製造業者に現場修正および製品リコールまたは除去をFDAに報告し、健康構成に対する設備のリスクを低減するため、または健康にリスクを構成する可能性のあるFDCA違反を救済するために、製造業者に現場修正および製品リコールまたは除去を要求する |
| ● | 連邦法および法規に準拠して、デバイスに固有のデバイス識別情報が要求され、各デバイスに関するいくつかの情報がFDAのグローバル固有デバイス識別データベースに提出されることが要求される |
| ● | FDAのリコール権限は、その権限に基づいて、装置の使用が合理的な可能性がある場合、深刻な健康的な結果または死亡をもたらすことができるように、装置製造業者に市場から管理法律および法規に違反した製品をリコールするように命令することができる |
| ● | 上場後のモニタリング活動と法規は、FDAが公衆の健康を保護したり、設備に追加の安全と有効性データを提供することが必要だと考えた場合、これらの活動と法規を適用する。 |
FDAは広範囲な規制コンプライアンスと法執行権力を持っている。FDAが適用される規制要件を遵守できないと判断した場合、それは様々なコンプライアンスまたは法執行行動をとることができ、これは以下のいずれかの処罰をもたらす可能性がある
| ● | 警告状、無見出し状、罰金、禁止、同意法令、民事処罰 |
72
| ● | 私たちの製品をリコール、撤回、行政拘留、または差し押さえます |
| ● | 生産制限、一部生産停止、全面生産停止 |
| ● | 510(K)の上場許可またはPMAが新製品または改良製品を承認することを拒否または遅延させる要求; |
| ● | 承認された510(K)許可またはPMA承認を撤回すること; |
| ● | 私たちの製品の輸出や輸入を承認することを拒否する |
| ● | 刑事起訴する。 |
EUや欧州連合では、私たちは新しい医療機器規制やMDRを遵守することを要求されるだろう。MDRは2017年5月に発表され、過渡期は3年で、現在延長されている。EUで医療機器を販売するために必要なCEマークは,適合性評価を経て指定された独立通知機関の承認を得た後,メーカーにより特定のbr}I系機器を自己認証して貼り付けたものである。CE識別子の選択経路は製品リスク分類に基づいている.CEフラグは,適用するMDRに適合する一般的なセキュリティと性能要求を表す.MDRはCE標識の既存の規制枠組みの多くの態様を変更し、例えば、唯一の設備標識及び多くの他のbr}上場後の義務を含む臨床証拠要求と他の新しい要求を増加させた。MDRはまた業界のコンプライアンス要求を著しく修正し、向上させ、今後数年以内に大量の資金を投入して実施する必要がある。
私たちはまた、製品を商業化する他のすべての国/地域の法規を遵守して、そして市場で新製品を発売したり維持したりすることができなければなりません。以前医療機器法規や最低法規しかなかった国の多くは、現在これらの法規を導入しています。例えば,インドは既存の規制の範囲を拡大しており,すべての医療機器種別を含めており,中東や東南アジアの多くの国で新法規が導入されている。
FDAと全世界の他の監督管理機関と主管機関は審査と検査設計と製造実践、記録保存、不良事件報告、ラベルと宣伝実践を通じて、現地の法律法規の遵守状況を積極的にモニタリングした。FDAはいくつかの医療機器を禁止し,偽やブランドの誤りを混入した医療機器を差し押さえたり差し押さえたりし,これらの機器の修理,交換または払い戻しを命じ,公衆の健康に対して不合理なリスクとなる医療機器について衛生専門家や他の人に通知することを要求することができる。FDAはまた,FDCAや医療機器に関する安全医療機器法案に違反した会社に命じたり制限したり,このような違反に対して刑事訴訟を起こすことも可能である。我々が業務を行っている国の規制機関や当局は,そのそれぞれの国での生産を停止したり,その国内での流通を停止したり,現地の法律法規に基づいて他の行動をとることができる。
米国で製造された医療機器の国際販売は、FDAの承認なしに米国で使用されるか、または合法的な性能 基準から禁止または逸脱され、FDA輸出要求によって制約される。また、輸出設備は、設備が輸出される国/地域ごとの法規要件によって制約されています。 医療機器法規がない国もありますが、多くの外国では医療機器 は法規制があります。一般に、規制要件の違いにより、米国が申請する前にまず外国で規制承認を得ることが可能であるが、中国のような他の国では、まず原産国での承認が要求される。
米国以外の多くの国/地域では定期的な再認証製品が要求されており,通常は5年ごとに行われている。再認証プロセス は、任意のデバイス変更およびデバイスに関連する任意の新しい法規または基準を評価し、必要に応じて継続的なコンプライアンスを記録するために適切な テストを行うことを要求する。再認証申請が必要な場合は、これらの国/地域で私たちの製品を販売し続けるために承認を得なければなりません。
73
予想規制申告数
これまで,我々のシステムは人体でテストを行っておらず,将来人体で行われるどのテストもFDAを含む適切な監督管理機関の要求に依存する.
私たちは規制承認の流れを処理するために多段階 方法を採用している。2022年1月、INSPIRA ART(Gen 2)デバイスおよびINSPIRA ART 100(Gen 1)デバイスの1つのコンポーネントをFDAクラス510(K)免除リストに入れました。このコンポーネントは、患者がベッド上で発生し、および/または輸送中に姿勢を変化させる際に発生する頸静脈挿管移動に関連する潜在的合併症を減少させることを目的としている。2023年9月、心肺転流装置としてINSPIRA ART 100(Gen 1)をFDA第2クラス510(K)に提出したが、これは断言に基づいており、FDAの承認を得るために人体試験を行う必要はないと予想されている。そのセキュリティまたは有効性に深刻な影響を与える可能性のある修正、またはその予期される用途に重大な変更または修正を構成する任意の修正は、修正、510(K)、最初の承認、または他のタイプの承認に依存する新しいマーケティング許可を必要とするであろう。Inspira ART(第2世代)の画期的な設備名 をFDAに申請する予定である。
2024年3月17日、我々はINSPIRA ART 100(Gen 1)設備をAMAR医療機器事業部承認に提出し、イスラエルおよび他の東南アジアと南米市場のいくつかのリード病院brに進出した。AMAR承認は通常120営業日程度の時間を要し,臨床データが必要となる可能性がある。
また,我々の設備を市場に出し,精算コードの簡略化と臨床でINSPIRA ART(Gen 2)を採用する戦略の一部として,新たな使用意図を提供し,トップ病院と協力して人体観察的研究を行い,(承認待ち) :(I)INSPIRA ART(Gen 2)が患者の病態悪化を防ぐことによる侵襲的MVの必要性を証明し,(I)br}患者のMV離脱を支援することに重点を置いた。
| C. | 組織構造です。彼は言いました |
私たち はイスラエルの会社で、本社はイスラエルのラアナナに設置され、2018年にイスラエルに登録設立され、名称はClearx Medical Ltd. 2018年4月10日、私たちの名称はInSense Medical Ltd.,2020年7月30日、私たちの名前はさらに現在の名称に変更され、Inspira Technologies Oxy B.H.N.Ltd.である。私たちの主な実行オフィスは2 Ha-Tidhar St.,Ra‘anana,Ra’anana,4366504にある。私たちのイスラエルでの電話番号は+972 996 644 88です。私たちのサイトの住所はwww.spirira-tech ologies.comです。我々のサイトに含まれる情報や我々のサイトを通じて得られた情報は,本年度報告に引用的に組み込まれることはなく,本年度報告の一部と見なすべきではなく,本年度報告における我々のサイトへの引用は非能動的なテキスト参照のみである.米国証券取引委員会はまた、米国証券取引委員会に電子的に提出された報告書、依頼書および情報声明、および他の発行者に関する情報を含む相互接続サイトを維持する。我々が米国証券取引委員会に提出した書類も、米国証券取引委員会のサイトwww.sec.govを通じて一般公開される。
現在、私たちにはどんな子会社もありません。
| D. | 不動産、工場、設備 |
私たちの主な業務活動はイスラエルで行われている。私たちのオフィス、研究開発と製造施設はイスラエルのラアナナ4366504号ハティハル通り2番地のメリスロン(千年ビル)にあり、敷地は約670平方メートルです。私たちの賃貸契約は2027年8月に満期になります。私たちが毎月支払うレンタル料は約64,000ニューシェケル(約19,600ドル)です。
プロジェクト4 Aです。未解決従業員意見
適用されません。
五番目です運営と財務 回顧と展望
| A. | 経営実績。 |
以下、私たちの財務状況と経営結果の検討と分析は、私たちの財務諸表と本年度報告書の他の場所の20-F表に含まれる関連付記とともに読まなければなりません。以下の議論は,我々が現在期待している前向き に基づく陳述を含み,不確実性や環境変化の影響を受ける可能性がある.不正確な仮定および既知または未知のリスクおよび不確定要因のため、実際の結果は、“前向き陳述に関する警告説明”および本20−F表年次報告の他の部分の“リスク要因”において決定されたものを含むこれらの予想とは大きく異なる可能性がある
74
概要
著者らは専門医療設備会社であり、独自の生命支持技術の研究、開発、製造とマーケティング に従事し、伝統的な機械呼吸器或いは機械換気の代わりに、後者は現在急性呼吸不全を治療する標準看護 である。機械換気は時々生命を救うことができるが、それはリスク、看護コストを増加し、入院時間を延長し、感染が頻繁に発生し、呼吸器依存と死亡率を増加させる。我々の最先端の生命支持技術を用いて、著者らの目標は新しい看護標準を確立し、急性呼吸不全患者に自発呼吸を維持する機会を提供し、挿管、昏睡と機械換気の使用に関連する各種のリスクを避けることである。我々がこの目標を達成するための戦略の一部として,規制承認を求めるとともに,戦略パートナー,世界ランキングの病院,医療機器会社,流通業者と積極的に連携して を構築し,承認と早期臨床採用 を得ている。集中治療室(ICU),一般医療機関,手術室,都市部と農村部の小型病院を目指し,世界の数百万人の患者がわれわれの解決策を獲得しやすいようにすることを目標としている。私たちはこれらの活動が市場浸透を実現し、私たちの生命支援技術を採用するために、私たちの戦略計画を支持すると予想している。
2018年の設立以来、 私たちは運営赤字になりました。2023年12月31日と2022年12月31日の年度まで、私たちの運営損失はそれぞれ約1,210万ドルと1,490万ドルで、同期の私たちの純損失はそれぞれ1,130万ドルと1,500万ドルです。2023年12月31日現在、私たちの累計赤字は5550万ドルです。私たちは予測可能な未来に巨額の費用と運営損失が引き続き発生することを予想して、私たちの損失は毎年大きく変動するかもしれません。私たちは持続的な活動に関連する費用が大幅に増加すると予想しています
| ● | 私たちの製品の臨床開発を続けて | |
| ● | FDAの第510(K)条または米国の他の規制経路に基づいて、製品の規制承認を求めるための新しい申請を提出する | |
| ● | 未来の候補製品の臨床前研究と開発に投資し続けます |
| ● | 製品が監督管理によって承認されれば、製品のマーケティング、販売、流通を支援するための商業インフラを構築する | |
| ● | より多くの研究開発者や一般的な行政者を招いて私たちの運営を支援しています | |
| ● | 私たちの知的財産権の組み合わせを維持し、拡大し、保護する | |
| ● | 上場企業の運営に関するコストを招き続けている。 |
私たちは販売を許可した候補製品 もなく、製品販売から何の収入も得ていません。
2021年7月16日、私たちは初公開(IPO)を完了し、2,909,091株の普通株と3,345,455件の流通可能権証(引受業者に付与された超過配給選択権に従って行使された436,364件の流通可能権証を含む)を売却した。引受割引や他の発行コストを差し引く前に、IPOから受け取った総収益は1,600万ドルです。初めて公募する前に、私たちは主に転換可能な債券とイスラエル革新局(IIA)の寄付によって私たちの運営に資金を提供しました。
75
当面の展望
これまで、私たちは主に私たちの普通株、転換可能な手形とローン、国際保険業協会の贈与によって私たちの運営に資金を提供してきました。2018年の設立以来、私たちの運営は赤字とマイナスキャッシュフローになりました。成立以来,我々は何の収入も生じておらず,近い将来も顕著な収入は生じないと予想される。
2023年12月31日まで、私たちの現金と現金等価物および現金預金は740万ドルです。2021年7月16日、私たちは初公募株を完成させた。IPOから受け取った総収益は1600万ドルで、引受割引や他の発行コスト は含まれていません。2021年10月、一部の投資家は彼らの流通権証を行使したため、私たちは合計930万ドルの毛収入を得た。
我々 は1933年に証券法により米国証券取引委員会に有効な表F-3登録声明(文書番号333-266748)を提出し、 “保留”登録プロセスを使用した。この保留登録手続きによれば、私たちは時々私たちの普通株と普通株を購入する引受権証と、1回または複数回の発売中の2つ以上のこのような証券の単位を販売することができ、総金額 は50,000,000ドルである。
2023年4月4日にRoth Capital Partners,LLCまたは販売エージェントと販売契約を締結し,この合意に基づき,合計17,566株の普通株を売却し,総金額は26,000ドルであった。私たちは販売協定を終了しました。発効日は2023年10月23日です。
2023年12月26日、私たちはある機関投資家と私募契約を締結し、1,375,000株の普通株を直接発売する方式で1,375,000株の普通株を発行することを規定し、購入価格は1,28ドルであり、予備金権証を発行し、1株1,28ドルから1部の資本金権証0.001ドルを引いた価格で、最大1,656,250株の普通株を購入することを規定した。株式承認証は発行時に行使でき、発行後3年半で満了する。また、購入契約に基づき、当社は機関投資家に株式承認証 を発行し、1株1.28ドルの使用価格で最大3,031,250株の普通株を購入する。
H.C.Wainwright& Co.,LLCが今回発行された独占配給エージェントを担当する.購入契約については、吾らは、購入取引で販売されている普通株総数が最大7.0%であるか、または引受権証を発行して、最大212,188株の普通株を購入するか、または代理権証を販売するために、配給代理店に引受権証を発行する。配給代理権証の条項は投資家に発行された引受権証とほぼ同じであり,配給代理権証の行使価格は1株1.60ドルである。彼は言いました
私たちは、2023年12月31日までの既存の現金と現金等価物が、今後6ヶ月の運営費用と資本支出 の需要を満たすことができると予想しています。私たちは私たちの製品を運営して商業化するために多くの追加資金が必要になると予想され、今後12ヶ月の運営に資金を提供できるように追加資金を求める予定です。
我々の現在未知の要素の多くにより,我々のbr}運営計画は変化する可能性があり,計画よりも早く に追加資金を求める必要があるかもしれない。私たちの将来の資本需要は多くの要素に依存します
| ● | 私たちの研究開発活動の進捗とコスト | |
| ● | 私たちの製品を作るコストは | |
| ● | 特許請求の範囲および他の知的財産権の出願、起訴、実行および弁護の費用; | |
| ● | 第三者との契約は、マーケティングおよび流通サービスを提供してくれるか、またはそのような能力を内部に建設する潜在的なコストを提供してくれる | |
| ● | 私たちの一般的で行政費用の額。 |
76
私たちが相当なbrの日常的な収入を生み出すことができる前に、私たちは債務および/または株式融資によって私たちの将来の現金需要を満たす予定だ。私たちは受け入れ可能な条項で私たちに追加的なbr資金を提供するかどうかを確信できない。これは、持続的な経営企業としての私たちの能力を大きく疑う可能性があります。財務諸表には、このような不確実性の結果による可能性のある調整は含まれていません。資金がなければ、私たちは私たちの候補製品に関する研究開発計画または商業化作業を延期、縮小、または廃止する必要があるかもしれない。
運営費
我々の現在の運営費は3つの部分からなる−研究開発費,一般と行政費用およびマーケティング費用 である。
収入.収入
今まで、私たちはどの製品の販売からも収入を生み出していません。私たちは少なくとも来年には著しい収入が発生しないと予想しています。
研究と開発費、純額
私たちの研究開発費には、主に給料と関係者費用、株式ベースの給与費用、材料費用、コンサルタント、その他の製品開発を支援する第三者費用、その他の研究開発費が含まれています。
研究開発費の内訳は以下の通り
年
終わり | ||||||||||||
| 千単位のドル | 2023 | 2022 | 2021 | |||||||||
| シェアに基づく報酬 | 663 | 2,392 | 1,792 | |||||||||
| 賃金および関連費用 | 4,429 | 3,458 | 1,543 | |||||||||
| 下請け業者 | 304 | 850 | 496 | |||||||||
| 材料及び関連費用 | 1,365 | 1,081 | 204 | |||||||||
| IIA参加 | - | - | (106 | ) | ||||||||
| 減価償却 | 291 | 188 | 94 | |||||||||
| 他にも | 268 | 214 | 47 | |||||||||
| 合計する | 7,320 | 8,183 | 4,070 | |||||||||
私たちは、私たちが引き続き私たちの製品を開発し、より多くの研究開発者を募集することに伴い、私たちの研究開発費は大幅に増加すると予想しています。
一般と行政費用
一般及び行政支出は主に賃金及び関連支出、株式補償、会計及び予約の専門サービス料、弁護士費、施設、出張支出及びその他の一般及び行政支出を含む。
77
以下の表に一般費用と行政費用の内訳を示す
| 監査を受けていない | 十二月三十一日までの年度 | |||||||||||
| 千単位のドル | 2023 | 2022 | 2021 | |||||||||
| 株式ベースの報酬 | 675 | 1,984 | 3,696 | |||||||||
| 専門費 | 1,432 | 1,500 | 1,390 | |||||||||
| 関連資金集め費用 | 260 | - | 546 | |||||||||
| 役員謝礼金 | 241 | 239 | 111 | |||||||||
| 賃金および関連費用 | 766 | 716 | 545 | |||||||||
| 保険料 | 300 | 557 | 363 | |||||||||
| 事務室メンテナンス | 129 | 102 | 91 | |||||||||
| 減価償却 | 115 | 104 | 84 | |||||||||
| 海外旅行に行く | 100 | 105 | 65 | |||||||||
| 他の人は | 45 | 68 | 46 | |||||||||
| 合計する | 4,063 | 5,375 | 6,937 | |||||||||
2023年12月31日まで、2022年と2021年12月31日までの年次比較
経営成果
次の表は、2023年、2022年、2021年12月31日までの年間運営結果をまとめています
| 十二月三十一日までの年度 | ||||||||||||
| 千単位のドル | 2023 | 2022 | 2021 | |||||||||
| 研究開発費 | 7,320 | 8,183 | 4,070 | |||||||||
| 一般と行政費用 | 4,063 | 5,375 | 6,937 | |||||||||
| 販売とマーケティング費用 | 746 | 1,328 | 1,980 | |||||||||
| その他の費用(収入) | 4 | 7 | (23 | ) | ||||||||
| 営業損失 | 12,133 | 14,893 | 12,964 | |||||||||
| 預金利子収入 | (318 | ) | (192 | ) | (1 | ) | ||||||
| 財務支出,純額 | (529 | ) | 275 | 4,230 | ||||||||
| 純損失 | 11,286 | 14,976 | 17,193 | |||||||||
| 普通株保有者は損失を占めなければならない | 11,286 | 14,976 | 17,193 | |||||||||
研究と開発費
2023年12月31日までの年間研究開発費は7,320,000 代表 が$を減少させた863,000あるいは、あるいは11一方、2022年12月31日現在の年間は8,183,000ドルです。#ドル減少した1,729,000 株式ベースの 支払い費用増加$971,000 賃金と関係者の支出は研究開発従業員数の増加を反映し、研究開発を支援するために努力している。また、#ドルも減少した546,000 下請け業者は2022年期間にアウトソーシングしますが、2023年に私たちの従業員が内部で実行する開発プロジェクトに関する費用 ,追加追加$284,000インチ材料と関連費用。
2022年12月31日までの年度の我々の研究開発費は8,183,000ドルであり,2021年12月31日までの年度の4,070,000ドルより4,113,000ドル増加し,101%増加した。賃金と関係者支出は1,915,000ドル増加し,株式ベースの支払い支出は600,000ドル増加し,研究開発従業員数の増加を反映して,下請け業者がアウトソーシングで処理した開発プロジェクトに関する支出は354,000ドル増加し,内部人員を用いた材料や関連費用は 877,000ドル増加した。また,我々は2021年12月31日までの年度にIIA贈与106,000ドルを含む研究開発支出 を行った。
78
一般と行政費用
2023年12月31日までの年度の一般·行政費総額は4,063,000ドルであり,2022年12月31日までの5,375,000ドルに比べて1,312,000ドル減少し,減少幅は24%であった。減少の主な原因は、従業員と役員の株式ベースの報酬支出が1,309,000ドル減少したことである。
2022年12月31日までの年度の一般·行政費総額は5,375,000ドルであり,2021年12月31日までの年度の6,937,000ドルに比べて1,562,000ドル減少し,減少幅は23%であった。減少は主に、2021年の従業員および取締役の株式ベースの報酬支出が1,712,000ドル減少したことと、関連IPO支出が546,000ドル減少したためである
販売とマーケティング費用
2023年12月31日までの年度のマーケティング費は746,000ドルであり,2022年12月31日までの年度の1,328,000ドルに比べて582,000ドル減少し,減少幅は44%であった。減少の原因は、従業員の株式ベースの給与支出が414,000ドル減少し、専門費が179,000ドル減少したからだ。
2022年12月31日までの年間マーケティング費は1,328,000ドルであり、2021年12月31日現在の1,980,000ドルに比べて652,000ドル減少し、減少幅は33%であった。減少の原因は、従業員の株式給与支出が712,000ドル減少したことだ。
営業損失
以上のような理由から、当社の2023年12月31日までの年度の経営損失は12,133,000ドルであり、2022年12月31日までの14,893,000ドルより2,760,000ドル減少し、下落幅は19%であった。
2022年12月31日までの年度の私たちの運営損失は14,893,000ドルで、2021年12月31日までの年度の12,964,000ドルに比べて1,929,000ドル、または15.0%増加しました。
財務費用(収入)
財務収入には預金利息、公正価値に応じて申告された金融負債の再評価及び外貨変動反映が含まれる。
318,000ドルの預金の利息収入と財務収入を確認しました合計529,000ドルで、主に為替レート反映と収入です財務負債公正価値の前年度までの変動により2023年12月31日 .
2022年12月31日までに、利息収入預金は192,000ドルと財務支出であることを確認しました総額は275,000ドルで、主に為替レート反映と収入です金融負債が価値の変化を公正にするためだ。
79
純損失合計
以上のような理由から、当社の2023年12月31日期までの純損失総額は11,286,000ドルであり、2022年12月31日までの年度損失14,976,000ドルより3,690,000ドルまたは25%減少している。
以上のような理由から、当社の2022年12月31日期までの純損失総額は14,976,000ドルであり、2021年12月31日までの年度損失17,193,000ドルより2,217,000ドル減少し、下落幅は13%であった。
| B. | 流動性と資本資源 |
概要
2023年12月31日までに$7.4 現金、現金等価物、現金預金。
次の表は,2023年12月31日と2022年12月31日までの年間キャッシュフローを示している
| 十二月三十一日までの年度 | ||||||||||||
| 千単位のドル | 2023 | 2022 | 2021 | |||||||||
| 経営活動のための現金純額 | (9,756 | ) | (9,647 | ) | (6,685 | ) | ||||||
| 投資活動提供の現金純額 | 4,594 | (7,383 | ) | (182 | ) | |||||||
| 融資活動が提供する現金純額 | 3,453 | - | 30,195 | |||||||||
| 現金および現金等価物の純増加(減額) | (1,709 | ) | (17,030 | ) | 23,328 | |||||||
経営活動
私たちが設立して以来、私たちは赤字が続き、経営活動に負のキャッシュフローが生じています。例えば、2023年12月31日までの年間で、私たちの運営損失は12,133,000ドルです。2023年12月31日までの年間で、私たちは主に普通株式と引受証を発行して得られた資金を通じて、私たちの活動に資金を提供して、私たちの製品やサービスを商業化し続け、追加の株式や債務融資で十分なbr融資を得ることができます。しかし,運営に必要な融資レベル を成功させることは保証されず,このような融資が受け入れ可能な条項で提供される保証はない.
2023年12月31日までの年度における経営活動用現金純額は9,756,000ドルであり、2022年12月31日までの年度における経営活動用現金純額は9,647,000ドルであり、2021年12月31日までの年度における経営活動用現金純額は6,685,000ドルであり、主に賃金や関係者費用、材料費用、下請け業者、出張、オフィスメンテナンスに用いられている。また、経営活動のキャッシュフローは、貿易口座br応払いや財務負債を含む経営資産や負債の変化の影響を受けている。
投資活動
2023年12月31日現在、投資活動が提供する現金純額は4,594,000ドルで、主に不動産や設備の購入に206,000ドル、短期預金を売却するための4,800,000ドルの収益が含まれている。2022年12月31日までの年間の投資活動のための現金純額は7,383,000ドル は主に物件や設備を購入するための263,000ドルおよび短期預金に投資する7,120,000ドルを含む。2021年12月31日までの年間で,投資活動用の現金純額は182,000ドルであり,すべて財産や設備の購入に用いられている。
80
融資活動
援助活動を通じて提供された現金の純額は3,453,000ドルです2023年12月31日までの年度内主に普通株式を発行して得られた2,128,000ドルと株式承認証を発行して普通株を購入して得られた1,750,000ドルを含む。
2022年12月31日までの年間、財務活動はいかなる現金も提供または使用していませんそれは.融資活動が提供する現金純額 30,195,000ドル2021年12月31日までの年度内初公募時に普通株を発行し、普通株を購入する流通権証と、2021年10月に株式承認証を行使することが含まれる。
我々 は1933年に証券法により米国証券取引委員会に有効な表F-3登録声明(文書番号333-266748)を提出し、 “保留”登録プロセスを使用した。この保留登録手続きによれば、私たちは時々私たちの普通株と普通株を購入する引受権証と、1回または複数回の発売中の2つ以上のこのような証券の単位を販売することができ、総金額 は50,000,000ドルである。
2023年4月4日、私たちはRoth Capital Partners、LLCまたは販売エージェントと販売契約または販売契約を締結し、この合意によると、私たちは時々販売代理を通じて当社の普通株を発売することができます。br}普通株は2023年4月4日にアメリカ証券取引委員会に提出されたF-3表登録声明(文書番号333-266748)および登録声明補足説明書に基づいて発売されます。2023年10月23日, RothにATMプロトコルの終了通知を出し,ただちに発効する.2023年10月23日までに、ATM計画に従って合計約26,000ドルの普通株を売却しました。
| 5.C | 研究開発、特許、ライセンスなど。 |
我々の研究·開発計画および我々が過去2年間にこれらの計画に基づいて生じた金額の説明については,“第 項5.運営と財務回顧および展望−A.運営結果−運営費用−研究開発費純額” と“第5項.運営と財務回顧と展望−A.運営結果−2023年12月31日までの年度と2022年12月31日までの年度との比較−研究·開発費用”を参照されたい
| 5.D | トレンド情報 |
新冠肺炎疫病はすでにイスラエルと世界各地の会社に影響を与え、その発展軌跡はまだ不明である。本年度報告発表日まで,われわれのbr経営陣は新冠肺炎の影響を検討し続けており,その影響の全程度を見積もることはできない。この段階では、私たちの運営と運営結果に明らかな悪影響はありません。しかし、私たちはそれが未来に私たちの業務に及ぼす影響を予測できない。さらに、私たちは疫病の経済活動、私たちの労働力規模、私たちの第三者パートナー、有価証券への私たちの投資、そして私たちの収入、収入、収益力、流動性または資本資源が実質的な悪影響を受ける可能性の程度 の影響、傾向、不確実性を予測することができない。
| E. | 肝心な会計見積もり |
私たちは、2023年12月31日までの年次財務諸表付記2に、私たちの重要な会計政策をより全面的に説明しました。私たちの財務状況や運営結果を全面的に理解して評価するためには、以下の会計政策が重要であると考えられる。
2023年12月31日までの年度から以下の規定により財務諸表を作成するアメリカは会計原則を公認しているそれは.財務諸表を作成する際には、我々の経営陣は、会計政策の適用および資産、債務、費用報告金額に影響を与える推定、評価、仮説を使用しなければならない。任意の推定および仮定は継続的に検討されます。 会計推定値の変化は、推定が変化している間に貸方に記入されます。Br財務諸表の作成は、株式に基づく補償費用、公正価値財務負債、または負債の確認、計量および開示、リース負債計量のための金利に関する資産および負債の報告金額に影響を与えるために、管理層に推定および仮定を要求する。
81
第六項です役員、上級管理職、従業員
| A. | 役員と上級管理職です。 |
以下の表は、本年度報告日までの当社の役員、主要従業員、取締役に関する情報を表格20-Fで示しています
| 名前.名前 | 年ごろ | ポスト | ||
| 大木本午 | 47 | 取締役最高経営責任者 | ||
| ジョー海雲 | 50 | 総裁と役員 | ||
| アフィトヒラ | 43 | 首席財務官 | ||
| アヴィ·シャブタイ | 50 | 最高経営責任者兼研究開発副総裁 | ||
| Daniella Yechezkeli Hayon | 50 | 首席技術官 | ||
| ベナード·ゴドワサー教授 (3) | 74 | 取締役会議長 | ||
| リオール·アミット(1) (2) (3) | 58 | 役員.取締役 | ||
| タル·パインズ(1) (2) (3) | 55 | 役員.取締役 | ||
| リモ·ロツェン(1) (2) (3) | 50 | 役員.取締役 |
| (1) | 報酬委員会委員 |
| (2) | 監査委員会及び財務諸表審査委員会委員 |
| (3) | 独立取締役(ナスダック証券市場規則の定義参照) |
取締役最高経営責任者ダジベンヌ
Dagiベン·ノーンさん2020年7月から私たちのCEOを務め、2020年3月から取締役CEOを務めます。これまで、Ben-Noonさんは2018年3月から2020年6月までの間に当社の最高経営責任者を務めています。本農業さんは、2018年2月にUdi Nussinovitch博士とJoe Hayonさんと一緒に当社の会社を設立しました。Ben-Noonさんは、アイデアからイラスト、デザイン、製造、製品発表までの15年以上の製品開発経験を持っています。当社の農業さんは、ナノサイズ株式会社(ナスダック·コード:NNDN)を共同創業し、2012年7月から2017年10月までの間に同社の役員と最高経営責任者を務めました。Nano Dimension Ltd.首席運営官Sとして、本-農は会社の研究開発、運営、生産、品質と情報技術を担当している。Ben-Noonさんは、イスラエルのBeer ShevaネゲフBen-Gurion大学で機械工学の学士号を持っている。
ジョー·海雲社長取締役
Joe海雲さん2022年8月から私たちの総裁を務め、2020年11月から取締役を務める。Hayonさんは、2020年6月から2022年8月まで、総裁兼最高財務責任者を務めます。これに先立ち、Hayonさんは2018年3月から2020年6月までの間に当社のCEOを務めています。Hayonさん は、2017年7月にUdi Nussinovitch博士とDagi Ben-Noonさんと共に当社の会社を設立しました。Hayonさんは20年以上の管理経験を持っている。2001年から2005年まで、Hayonさんは財務担当および費用会計を担当するSanmina Ltd.(前身はElscint)で、2006年から2007年まで、HayonさんはArazim Groupで最高財務責任者を務めた。2007年から2018年まで、Platan Sasa Ltd.で働き、同社の首席情報官とグループディレクターを務めた。Hayonさんは、マンチェスター大学のビジネスと経済学の学士号、マーケティング、金融専門のMBAの学位、ダメリン大学のビジネス管理証書を所有しています。
82
アフェット·テヘラ最高財務責任者
アフェット·テヘラさん2022年8月以来、私たちの首席財務官を務めてきました。私たちの最高財務官になる前に、テヘラさんは2021年2月から私たちの財務·法律部副総裁を務めています。テヘラさんは2020年11月から2021年2月まで取締役ナノ有限会社(ナスダック:NNDM)の財務総監を務め、2016年2月から2020年11月まで財務総監を務めた。テヘラは2010年8月から2016年11月までMigdal Capital Marketsの財務ディレクターを務めた。テヘラさんはテルアビブ大学の会計、経済学、工商管理の学士号を持っている。
最高経営責任者アビー·シャブタイと研究開発部副社長
アヴィ·シャブタイさん2020年7月以来最高経営責任者を務め、2019年6月から研究開発副総裁を務めています。Shabtaiさんの専門知識は、概念から生産までの全製品ライフサイクルの工程、試験、品質管理、規制、リスク管理および生産 に関するものです。彼は25年以上のハイテク会社の管理経験があり、特にハイテク会社の研究開発と運営部門で、研究開発部門の総裁副主任と品質工学部門の総裁副主任を含む。2015年7月から2018年3月までの間に、シャバータイさんはナノサイズ株式会社(ナスダック: NNDN)で研究開発の副社長を務めています。これに先立ち、シャバータイさんは、2018年4月から2019年5月まで、ZutaCoreの研究開発副社長を務めています。Shabtaiさん は、ALDアカデミーとイスラエル標準研究所のソフトウェア品質エンジニアの資格を取得しました。
Daniella Yehekely-Hayon博士、MBA、首席技術者。
Daniella Yehekely-Hayon博士2022年1月から私たちの首席技術者を務めてきました。エスケリー·ヘイイン博士は生物医学工学および医療機器会社の重要なポストで包括的なプロジェクト管理経験を持っている。2016年6月以来、葉海斯凱利博士はずっとO 2 Cure Ltd.で研究開発総監と運営総監を務め、O 2 Cure Ltd.は医療機器会社であり、専門に病院のために長期酸素交換器と呼吸補助設備を開発した。2009年10月から2016年5月まで、エスケリー·ヘーン博士は生物医学工学技術学部で高度な研究アシスタントを務めた。Yehekely-Hayon博士はイスラエル工科大学の生物学博士号と小野学院のMBA号を持っています。
ベナード·ゴドワサー教授医学修士取締役会長
ベナード·ゴドワサー教授 2021年2月以来、私たちの取締役会長を務めてきたGoldwasser教授は泌尿外科医師、発明家、企業家とリスク資本投資家であり、高成長、上場を指導する医療会社の方面で豊富な経験を持っている。1993年,ゴールドワーサー教授は他者と共同でVidame Inc.を設立し,同社は美敦力社(ニューヨーク証券取引所コード:MDT)に買収された。1994年、Goldwasser教授は他人と共同でMedinol Ltd.(ニューヨーク証券取引所コード:BSX)を創立した。Goldwasser教授は2018年5月からSave Foods,Inc.(場外取引コード:Safo) 取締役会議長を務め、2019年3月以来ScoutCam Inc.(場外取引コード:SCTC)取締役会議長を務め、2017年9月からInnoventric Ltd.取締役会メンバーを務めた。これまで、Goldwasser教授は2018年9月から2019年12月までナスダックとTASE:MDGの取締役会長を務め、2016年5月から2019年5月まで上海イスラエル投資基金の顧問を務めていた。2016年、ゴッドワサー教授は上海政府投資会社上海協和投資有限公司(SAIL)と協力してリスク投資基金を発売した。Goldwasser教授は2013年から2016年までBioCancell Ltd.(TASE:BICL)取締役会メンバーも務めた。ゴールドヴァザー教授はテルアビブ大学の医学博士と工商管理修士号を持っています
リオール·アミット役員
廖爾·アミノさん2021年8月1日から私たちの取締役会に勤めてきた。アメーバさんは、2014年以降、純資産価値の高い個人および会社のプライベート財務コンサルタントを務め、Scoutcam Inc.,イスラエル信用保険会社ICIC、NirplexおよびRonimar Ltd.の取締役コンサルタントを務めてきた。アミノさんは、1996年から2013年にかけてイスラエルのBBR Saatchi&Saatchi広告グループの最高財務責任者を務め、広告代理店、メディア運営、デジタルコンテンツなど、地域有数の広告会社になるのを支援し、従業員数を40人から250人に増やしました。アーミテージさんは、テルアビブ大学の商工管理修士((金融·保険))と経済学、会計学の学士号を持っている。アミさんはイスラエルの公認会計士であり、イスラエル証券管理局の顧問免許を持っています。
83
リモア·ロツェン、取締役
リモ·ロッツェン夫人2021年7月16日から私たちの取締役会に勤めてきた。2019年以来、ロツェンはVecon Ltd.で上級顧問を務めてきた。これまで、羅岑さんはZzooの共同創業者で、2017-2020年の間にZzooの最高経営責任者と社長を務めていた。 2012-2017年、羅岑さんは365 Technologies Ltdの最高運営官を務めた。2006-2011年、羅岑さんはカリフォルニア州パロアルトCollarityの製品や顧客プロジェクトの副総裁も務め、Right Orderの高級チーム責任者を務めた会社 2000年から2006年までカリフォルニア州サンホセ,1999年から2004年までComverse Technology,Inc.のチーム責任者を務めた。Rozenさんはアリゾナ州フェニックス大学技術管理専攻MBA(br}学位)とバイーラン大学コンピュータ科学学士号(br})を持っている
タル·パインズ役員
タル·パインズさん 2021年7月16日から私たちの取締役会に勤めてきた。バーンズさんは2016年から2020年にかけて共同創業し、ズタコア株式会社のCEOと社長を務めています。以前、Parnesさんは2010-2015年に共同で設立され、HQL製薬会社のCEOを務めています。Parnesさんはまた、2007年から2009年までSilynx Communications Inc.のチーフ運営責任者を務め、2005年から2006年までWavion社の運営副総裁を務め、2002年から2004年までAtrica株式会社の運営副総裁を務めた。1999年から2001年まで、ParnesさんはPrintlife株式会社のチーフ財務官およびビジネス開発役員も務めています。Parnesさんはテルアビブ大学で経済学、歴史学の学士号を持っています。
科学顧問委員会
呼吸器疾患、肺疾患、心臓病、実験室動物科学分野の何人かの活発な医師と専門家からなる科学諮問委員会があります。科学顧問委員会は臨床研究の展開と臨床前研究への参与を通じて、上述の領域で私たちに相談と協力を提供してくれた。私たちの科学顧問委員会の会員たちは現金支払いまたはオプション付与の形で補償を受けた。科学諮問委員会のすべてのメンバーは、本年度報告書に表 20-Fとこれに関連する任意の材料で指名されることに同意することを提供してくれた。
アブトブル博士医学博士は2008年以来、イスラエルエルサレムのハダシャ医療センターで複数のポストを務めてきた。現在、アブブール博士は2017年からハ大沙医療センター医療集中治療室及びその肺疾患研究所で高級医師を務めており、また哈大沙医療センターの全国慢性閉塞性肺疾患研究を指導している。現在の職に就く前に、アブトブル博士は2016年に肺疾患研究所の研究員資格を取得し、2014年に一般集中治療室の研究員資格を取得した。アブターブル博士は2012年に内科の入院医師資格も取得した。アブトブル博士はイスラエルエルサレムヘブライ大学とイスラエルエルサレムハダサ医学院の講師です。アブトブル博士は医学学士号を取得した。イスラエルのハイファのルースとブルース·ラパポートの医学院です
ダニエル教授ブロディコロンビア大学/ニューヨーク長老会病院肺,アレルギーと集中治療医学部,成人体外ペーシング計画の役員と急性呼吸不全センターの集中治療科課長である。ブロディ教授は体外生命支持組織(ELSO)の総裁当選者と国際体外脈拍組織ネットワーク(ECMONet)実行委員会主席であり、この2つのリードする国際組織は体外生命支持領域で科学知識をリードしている。彼は現在,この分野で行われている多くの臨床試験の指導委員会のメンバーである。また、ブロディ教授はアメリカ国家心肺血液研究所(NHLBI)の急性肺損傷(PEATAL)ネットワーク議定書審査委員会のメンバーの予防と早期治療である。ブロディ教授はかつて影響力のある科学定期刊行物の査読者を務め、“新イングランド医学雑誌”、“柳葉刀”と“アメリカ医学会雑誌”を含む。ブロディ教授は300冊以上の同業者評議の出版物と書籍の章を書き、世界各地で400回近くの特別招待講座を発表した。
範志偉教授トロント大学集中治療医学部門と衛生政策、管理と評価研究所の助教授であり、オンタリオ州トロント大学衛生ネットワーク/西奈山病院のスタッフ強化師でもある。範教授は現在トロント総病院体外生命支持プロジェクトの医学取締役である。範博士はトロント大学の学部学位,西安大略大学の医学学位,ジョンホプキンス大学の臨床調査博士号を有している。彼の最も重要な論文は:(1)“アメリカ呼吸と重症看護医学雑誌”に発表された“アメリカ胸科学会/ヨーロッパ集中治療医学会/集中治療医学会の公式臨床実践ガイドライン:急性呼吸窮迫症候群を有する成人患者の機械換気”;(2)“静脈-静脈体外膜酸素化による急性呼吸不全治療:1つの国際専門家グループの臨床概要”を含む。;および(3)
84
オリット·コーエン·ジェイコブ博士Brは獣医であり,実験動物医学において独自の認証専門を持っている。ヤコブ博士はイスラエルのネズツィオナのイスラエル生物研究所で16年以上のポストを務め、同時にイスラエル最大の臨床前動物施設と実験室の設立を指導した。イスラエル生物研究所では、ヤコブ博士はGMP安定施設を設立し、イスラエル諸国のために抗血清を生産した。1999年から2015年にかけて,ジェイコブ博士は外科医やコンサルタントとして,彼女の専門分野で国土安全に関する様々な研究に参加してきた。ジェイコブ博士は衛生部国家動物実験委員会のメンバーで、2013年から2018年まで国家動物実験倫理委員会の議長を務めた。現在、ヤコブ博士はSeruMed GMP Ltd.の共同所有者兼最高経営責任者であり、同社は2016年以来ずっとイスラエル衛生部の抗毒蛇とEchis蛇抗蛇毒血清の唯一のメーカーとサプライヤーである。また、ジェイコブ博士はBiosera Consulting Ltd.の所有者であり、2016年以来、同社を通じてバイオテクノロジー会社に臨床前研究、施設建設、GMP法規、倫理と科学などのあらゆる知識を提供してきた。
ステファン·レド博士各種臨床領域の専門家であり、集中治療医学、麻酔、体外支持と心エコーを含む。彼のキャリアの中で、彼は高度な心血管生命支援(ACLS)指導、理学療法士が指導する重症看護モジュール、重症看護モジュール看護学校指導など、大量の教育職責を担っている。レド医師は集中治療分野で推奨されている講演者である。レド博士はヨーロッパ心血管画像協会の経食道心エコー(TOE)認証を完了し,ヨーロッパ集中治療証書を持っている。ルード博士はかつてイギリス王立ブランプトンとハリフィールド病院で集中治療と麻酔薬の高級臨床医を務め、体外膜酸素化サービスと集中治療の取締役となった。ロイヤル·ブランプトンECMOサービスはヨーロッパ最大のサービスの一つであり、すでに卓越した中心として公認されている。
イェール·リヒター博士テルアビブSourasky医療センター集中治療室の役員で、そこで内科と集中治療の入院医研修を終えた。彼女はまたイスラエルECMO協会の財務責任者を務めている。リヒター博士はイスラエル国防軍医療隊で大尉を務め、戦闘先で野戦医を務めていた。彼女はテルアビブ大学のサグラー医学院で医学訓練を終えた。
シャロン·マルクス博士1996年にエルサレムヘブライ大学で物理有機化学博士号を取得した。1996年以来、マルクス博士はずっとイスラエル生物研究所物理化学系で働いてきた。マルクス博士はイスラエル生物研究所の研究員で、現在物理化学学部の主任を務めている。マルクス博士は2008年から2010年までペンシルバニア大学でアシスタント教授(休暇) を務め,そこでバイオ対応燃料電池を開発した。彼女の研究の興味は,センサとバイオセンサの開発,化学センサネットワーク,分子インプリントポリマー,化学抵抗,気相(空気汚染,有毒物質)センサ,水質センサである。
デッカー·スタヴィ博士医療br取締役は体外生命支持計画の指導及びICUで心血管と血液腫瘍患者の治療に豊富な経験を持っている。トロント大学集中治療に加入する前に,イスラエルテルアビブSourasky医療センターで高度集中治療内科医を務め,そこで施設体外膜酸素化(ECMO)計画を開始した。Stavi博士の有名な出版物には,“中等看護病棟で経皮的拡張床辺気管切開術を受けた患者の長期機械換気の結果−単中心研究”と“85歳患者の気管切開術の結果と生存率”がある
ダン·ゴフィル博士心臓外科と集中治療医学分野の優れた専門家です。ゴフィル博士はイスラエルラビン医学センター心臓外科集中治療室と体外膜酸素化プロジェクトの責任者である。br}ゴフィル博士の専門知識はINSPIRAART 100の配備に大きな貢献を果たすことが期待される。米国食品医薬品局(FDA)は2024年上半期に承認される見通しだ。
85
家族関係
私たちの執行経営陣メンバーと取締役の間には何の家族関係もありません 。
役員と経営陣の選挙手配
私たちは大株主、顧客、サプライヤー、または他の人と何の手配も了解もありません。私たちのどの執行管理層または取締役もこれらの手配または了解に基づいて選択されています。より多くの情報については、“プロジェクト7.B.--関連者取引”を参照されたい。
| B. | 補償する |
次の表は、2023年12月31日までに、最も報酬の高い5人に支払われたすべての報酬を示しています。この表には、その間に私たちがサービスを提供してくれた費用を補償するために、私たちが支払ったいかなる金額も含まれていません。
次の表で報告したすべての金額は,2023年12月31日までの年度の会社コストをドル単位で反映している。
新シェケルが支払った金額を3.56新シェケル=1.00ドルの為替レートでドルに換算したのは、イスラエル銀行がこの期間中に報告した新シェケルとドルの平均代表的な為替レートに基づいている。
給料は、 関わる 優位性 | 年金は 定年退職する 他にも 類似 優位性 | 共有に基づく 補償する | ||||||||||
| 大木本農最高経営責任者 | $ | 269,187 | $ | 21,125 | $ | 230,878 | ||||||
| Joe海雲は総裁と役員 | $ | 271,727 | $ | 21,125 | $ | 230,878 | ||||||
| アフィトヒラは首席財務官 | $ | 178,386 | $ | 38,739 | $ | 109,684 | ||||||
| アヴィ·シャブタイは最高経営責任者兼研究開発副総裁 | $ | 287,006 | $ | 52,357 | $ | 55,811 | ||||||
| ダニエル·ヘイロン博士首席技術者です | $ | 178,396 | $ | 38,739 | $ | 62,313 | ||||||
| アーディ·ニール博士首席医療官(2023年10月退職) | $ | 134,740 | $ | 29,812 | - | |||||||
私たちが外国の個人発行者として資格がある限り、アメリカ国内の会社に適用される代理ルール、すなわちbr}個別の役員の報酬を開示することは要求されません。“会社法”によると、上場企業として、最高報酬の役員5人の個人年収の開示を要求されています。この開示はアメリカ国内の発行者が要求するほど広くないだろう。
86
役員と雇用契約を結ぶ
私たちは私たちのすべての幹部と書面雇用協定を締結した。これらすべてのプロトコルには,eスポーツ禁止,情報セキュリティ,および発明譲渡に関する慣例条項が含まれている.しかし,競業禁止条項の実行可能性は適用法律によって制限される可能性がある.また、吾らは各行政者や取締役と合意を結び、合意に基づき、吾らは彼ら一人一人に一定額の賠償を支払ったが、その責任は取締役や行政者保険の保険の範囲内ではなかった。
私たちのオプションとオプション計画の条項の説明については、“第6.E.株式所有権-持分インセンティブ計画を参照してください。”
役員サービス契約
私たちの取締役だけでなくCEOでもありますが、私たちは取締役と書面で合意していません。彼がわが社で働いているときの福祉を中止することにしています。我々が2021年12月に開催した株主総会では,非執行役員に1人当たり40,000ドルの固定年会費を設定し,取締役会議長に120,000ドルの固定費用を設定した。
| C. | 取締役会が実践する |
序言:序言
私たちの取締役会は6人のメンバーで構成されている。ベナード·ゴッドヴァザー教授、リモア·ロツェン、リオール·アミート、タル·パインズは“ナスダック株式市場規則”の規定に基づいて“独立している”と考えている。当社の定款の改正及び再記載は、取締役会メンバーの人数は株主総会によって決定されなければならず、取締役会メンバーは3(3)人以下であってはならず、かつ12(12)人を超えてはならないことが条件である。会社法によると、私たちの業務管理権は私たちの取締役会に属している。私たちの取締役会はすべての権力を行使することができ、私たちの株主または経営陣に明確に付与されていないすべての行動を取ることができます。私たちの執行者は私たちの日常管理を担当し、私たちの取締役会が個人的な役割を決定します。“会社法”によると、私たちのCEOは私たちの取締役会が任命し、取締役会が適宜決定しますが、私たちが彼と締結した雇用協定を守らなければなりません。他のすべての役員は、私たちの最高経営責任者によって任命されます。“会社法”によると、彼らの採用条項は、取締役会報酬委員会と取締役会の承認(場合によっては株主の承認が必要)であり、私たちが彼らと締結する可能性のある任意の適用可能な雇用契約条項によって制限されます。
会社法および/または当社の改正および再記載された会社定款によると、会社法によると、任命される必要がある場合がある各取締役(外部取締役を除く)の任期は、その任命後の次の株主総会まで継続されるか、または彼または彼女が辞任するまで、または彼または彼女が私たちの株主総会で多数票で、またはいくつかの事件が発生したときに免職されなければならない。
また、場合によっては、当社の定款を改正して再記載することにより、次年度の株主総会又は特別株主総会まで、取締役会の空きを埋めるために取締役を任命したり、代理取締役を除いて(当社定款細則による取締役数の制限を受けて)、次の年度株主総会又は特別株主総会まで、取締役任期を終了する可能性がある。以下に述べる場合、外部取締役(適用される場合)は、その最初の3年間の任期の後に、最大2つの追加の3年間の任期 を再選することができるが、以下に“外部取締役”に記載されるいくつかの例外は除外される。“会社法”に規定されている限られた場合にのみ、外部取締役を免職することができる。
87
“会社法”によると、私たちの少なくとも1%の議決権を持つ株主は、年間株主総会で取締役を指名することを提案することができます。しかし、どのような株主も、その株主が意図的に指名したことに関する書面通知を我々の取締役会に発行した場合にのみ、このような提案を行うことができます。このような通知は、指名された取締役が当選後に私たちの取締役を務めることに同意されたことと、指名された取締役が必要なスキルを持っていることを宣言し、その義務を履行する能力があることとを含むいくつかの情報を含まなければならない。また、著名人は、これらのスキルの詳細な情報を提供し、“会社法”がその当選を阻止する可能性のある制限がないことを証明し、“会社法”によって必要なすべての選挙情報 が提供されていることを確認しなければならない。しかしながら、2024年3月12日から適用される新たな免除によれば、その株式がイスラエル国外に上場するイスラエル企業の1つ以上の株主は、過去に要求された1%(1%)の投票権ではなく、会社取締役会が取締役会の候補者を任命するか、または将来の株主総会(適切と考える場合)の議題項目として取締役会を任命するか、または取締役会メンバーを将来の株主総会(適切と考える場合)の議題項目として少なくとも5%(5%)保有することを要求することができる。
“会社法”によると、我々の取締役会は、会計と財務の専門知識を備えなければならない最低取締役数を決定しなければならない。このような専門知識を持つために必要な取締役数を決定する際には,我々の取締役会は会社のタイプや規模,運営の範囲や複雑さなどを考慮しなければならない.我々の取締役会は、わが社は会計と財務専門知識を備えた取締役数 を最低1人としなければならないと決定しました。
取締役会は1人の取締役を取締役会長に選出し、取締役会会議を主宰しなければならず、brはその取締役の会長職を免除することができる。“会社法”によると、最高経営責任者及びその親族は取締役会の議長を務めてはならず、会社は会長又はその親族の権力を最高経営責任者に付与してはならない。また、直接または間接的にCEOに報告する人は取締役会の議長を務めてはならない;会長は直接または間接的にCEOに報告する権力を持ってはならない;会長は会社または制御された会社で他の職務を担当してはならないが、取締役または制御された会社の会長になることができる。しかしながら、“会社法”は、会社株主が3年以下の期間内に会長またはその親族が最高経営責任者になることができるか、または最高経営責任者に付与する権限を付与することができ、CEOまたはその親族が会長または会長に付与される権限を担当することができることを許可する。会社 株主の決定には,(1)少なくとも出席して採決に参加する株主(持株株主と決定中に個人の利害関係がある株主を除く)の多数の株式承認(棄権株主が保有する株式は考慮されない),または(2)決定に反対する株式総数は会社総投票権の2% を超えない,が必要である.現在、私たちは単独の会長と最高経営責任者を持っている。
取締役会は“会社法”の規定に符合する場合、その一部の権力を取締役会の委員会に転任することができ、時々このような許可を撤回したり、どのような委員会の構成を変更したりすることができるが、いくつかの制限を受けなければならない。委員会がまた明確な規定を持っていない限り、委員会はこのような権力をさらに転任する権利がない。私たちの監査委員会、財務諸表審査委員会、報酬委員会の構成と役割は以下の通りです。
取締役会は、私たちのリスク管理政策とプログラムの適合性をどのように監視し、私たちが直面しているリスク審査リスク管理の枠組みの十分性を監視しています。取締役会は内部監査員によって監督作用を発揮するように協力した。内部監査人はリスク管理制御とプログラムを定期的かつ一時的に審査し,審査結果を我々の監査委員会 に報告する。
外部取締役
“会社法”によると、以下の規定を除いて、イスラエルの法律で登録されている上場企業によると、ナスダックに上場しているイスラエルの会社を含めて、“会社法”の規定の資格要件を満たす外部取締役を少なくとも2人任命しなければならない。会社法の外部取締役の定義は、ナスダック証券市場規則の独立ナスダックの定義と類似しているため、我々の2人の外部取締役も通常、ナスダック証券市場規則の独立性に対する要求を遵守する。
88
会社法の規定によると、我々のような会社の取締役会は、 (I)会社に持株株主がいない(会社法で定義されている)、(Ii)取締役会の多くの取締役 は、ナスダック規則5605(A)(2)で定義されているように“独立”である必要はない。および(Iii)会社は、取締役の指名が完全に独立取締役からなる指名取締役会委員会または独立取締役の多数のメンバーが取締役会に提出または推薦しなければならないことを要求するbr}ナスダック規則5605(E)(1)を遵守する。会社 はこれらのすべての要求を満たしている.私たちの取締役会は、上記のようなコーポレート·ガバナンス免除を採用することを決定しましたので、私たちの取締役会のメンバーとして外部取締役はもういません。
役員候補
我々が改正·重述した会社定款では、“会社法”が許可された場合には、どの取締役もその職務の代わりに一人を補欠に指定することができ、その補欠を罷免して他の人を任命することと、任意の理由で退職した補欠の代わりに補欠を指定することができる。“会社法”によると、取締役に任命される資格がない人、すでに取締役を務めている人、またはすでに別の取締役の補欠取締役を務めている人は、補欠取締役に任命されてはならない。しかし、すでに取締役を務めている人は、取締役会委員会のメンバーの補欠取締役に任命されることができ、彼または彼女がまだその委員会のメンバーを務めていない限り、補欠取締役が外部取締役の代わりになる場合、彼や彼女は外部取締役でなければならず、“財務と会計専門知識” や“専門知識”を備えていなければならない。具体的には、彼または彼女が代わる外部取締役員の経歴にかかっている。必要な“財務·会計経験”や“専門知識”を持たない人は、彼や彼女が代わる外部取締役の資格に依存して、外部取締役の補欠取締役に任命されてはならない。会社法により、独立取締役に任命される資格がない者は、独立取締役の補欠取締役に任命されてはならない。指定された取締役が指定された時間又は範囲 を制限しない限り、指定された取締役が取締役でなくなったり、指定を終了したりするまで、指定された取締役はいずれの場合も有効である。
取締役会各委員会
私たちの取締役会は二つの常設委員会、監査委員会、報酬委員会を設立しました。
監査委員会
“会社法”によると、どの上場企業の取締役会も監査委員会を設置しなければならない。監査委員会は少なくとも3人の取締役で構成されなければならず、適用されれば、すべての外部取締役(そのうちの1人が委員会の議長を務めなければならない)を含む。監査委員会は、取締役会議長;会社または会社の持株株主または持株株主制御の実体に雇用された取締役;持株株主または持株株主の親族;会社、持株株主または持株株主の制御に雇われた実体または定期的に会社、持株株主または持株株主制御の実体にサービスを提供する取締役;および主な収入は持株株主からの取締役を含むことができない。
私たちの監査委員会はLior Amit、Limor Rozen、Tal Parnesで構成されている。
89
会社法によると、私たちの監査委員会は他の事項以外を担当しています
| (i) | 会社の経営管理行為に不足があるかどうかを確定し、取締役会に改善提案を提出する | |
| (Ii) | 特定の関連側取引(公職者が個人的利益を有する取引を含む、およびこのような取引が“会社法”に基づいて非常に取引されているか重大な取引であるかを含む)を決定し、持株株主または持株株主と個人的利益を有するいくつかの取引のための承認手続きを決定する(“項目6.C.取締役、高級管理者および従業員-取締役会のやり方-イスラエルの法律に従って関連側取引を承認する”参照) | |
| (Iii) | “無視できない”取引(すなわち、支配株主との取引は、監査委員会によって無視できない取引に分類され、非常に取引とみなされていなくても)を決定する承認手順と、どのような種類の取引が監査委員会の承認を必要とするかを決定することとは、任意に監査委員会が毎年予め定められている可能性のある基準に基づいている | |
| (Iv) | 内部監査人がその義務を履行するのに十分な資源とツールを持っているかどうかを含む、内部統制と内部監査者の表現をチェックする | |
| (v) | 私たちの監査人の仕事範囲と報酬を審査し、これについて私たちの取締役会または株主に提案します。これは、彼らのどれが私たちの監査人を任命することを考えているかにかかっています | |
| (Vi) | 当社の業務管理不足に対する従業員の苦情を処理し、当該等の従業員に保障を提供するプログラムを作成する | |
| (Vii) | 取締役会は、内部監査役の作業計画を承認し、取締役会に提出する前に当該作業計画を審査し、修正意見を提出する。 |
私たちの監査委員会は、その承認を必要とするいかなる行動も議論したり、承認したりしてはならない(“6.C.取締役、上級管理者、および従業員--取締役会のやり方--イスラエルの法律に基づいて関連者取引を承認する”);“を参照)、承認時に委員会の多数のメンバーが出席しない限り。
我々の取締役会は、米国証券取引委員会とナスダック上場規則に適合する監査委員会の職責(およびこの委員会に対する会社法の要求)を規定した監査委員会規約を採択し、その中にbr}以下を含む
| ● | 独立公認会計士事務所を監督し、イスラエルの法律に基づいて取締役会に採用、補償、または採用を中止することを提案します |
| ● | 私たちの内部監査役の職を採用または終了し、私たちの内部監査人が提供するサービスを検討し、財務報告内部統制制度の有効性を検討することを提案します | |
| ● | 独立公認会計士事務所が提供する監査及び非監査サービスの条項を提案し、当社取締役会が事前に承認すること | |
| ● | 重大な影響を及ぼす法律事項(適用される場合)を審査·監視し、規制当局の調査結果を発見し、違反·コンプライアンスに関する報告を受け、“通報者政策”に基づいて行動し、必要に応じて取締役会に提案する。 |
90
ナスダック証券市場監査委員会は を要求した
ナスダック証券市場規則によると、私たちは、会計または関連財務管理専門知識を有する独立した財務知識を有する少なくとも3人のメンバーからなる監査委員会を維持しなければならない。
上述したように、私たちの監査委員会のメンバーはLior Amit、Tal Parnes、そしてLimor Rozenを含む。アミノさんは私たちの監査委員会の議長です。私たちの監査委員会のすべてのメンバー は“ナスダック株式市場ルール”の金融知識に対する要求に適合している。我々の取締役会は、我々の監査委員会の各メンバーが米国証券取引委員会規則によって定義された監査委員会の財務専門家であり、“ナスダック証券市場ルール”によって定義された必要な財務経験を有することを決定した。
“会社法”によると、我々の監査委員会は財務諸表審査委員会の役割も果たしている。したがって、監査委員会は、(I)財務諸表の作成に関する推定および評価、(Ii)財務諸表に関連する内部統制、(Iii)財務諸表に開示された完全性および適切性、(Iv)採用された会計政策および会社の重大な事項で実施される会計処理、および(V)評価に基づく仮定および評価および財務諸表における支援データを含む価値評価を担当する。
報酬委員会
“会社法”によると、どの上場企業の取締役会も給与委員会を設置しなければならない。報酬委員会は、すべての外部取締役(適用される場合)を含む少なくとも3人の取締役で構成されなければならない。報酬委員会は、監査委員会と同様の会社法によって制限されている:(A)誰が委員会のメンバーではないか、および(B)誰が上記委員会の審議に出席できないか。
私たちの給与委員会は書面規定に基づいて、Lior Amit、Limor Rozen、Tal Parnesで構成されている。タル·パインズは私たちの報酬委員会の議長だ。私たちの給与委員会は、その独立性、権威性、実践に関連するあらゆる面で“会社法”とその公布された規定、および私たちが改正して再説明した会社規約を遵守している。我々の給与委員会(Br)は、ナスダック株式市場規則に規定されている報酬委員会のメンバーや定款要件を遵守するのではなく、自国のやり方に従っている。
私たちの報酬委員会 は、(1)役員および取締役の:(1)年間基本報酬、(2)具体的な目標および金額を含む年間奨励ボーナス、(3)株式報酬、(4)雇用協定、解散費手配および制御プロトコルおよび規定の変更、(5)退職補助金および/または退職ボーナス、および(6)任意の 他の福祉、報酬、報酬政策または手配を提案する。
給与委員会の職責には、役員会に在職者採用条項に関する政策を提案することが含まれており、これを報酬政策と呼ぶ。3年ごと(または初公募から5年後)には、このような政策は、報酬委員会の提案を考慮して会社の取締役会が採択しなければならない。br報酬政策は、特に多数を必要とする株主承認に提出される(“6.C.取締役、上級管理者、従業員--取締役会慣行--イスラエルの法律に基づいて関連者取引を承認する”参照)。“会社法” によると、株主の承認がなければ、取締役会は報酬政策を採用することができ、株主 がこの政策の承認に反対した後、報酬委員会と取締役会はこのことを再審議し、br}報酬政策を採用することが私たちの最適な利益に合致することを決定する。
2021年12月17日、私たちの株主総会は、5年間の役員報酬政策または報酬政策を採択しました。
91
給与政策は、免責、保険、賠償、または雇用または採用に関連する任意の金銭支払いまたは支払い義務を含む、役員および役員の雇用または採用財務条項を決定する基礎である。報酬政策 は、私たちの目標、私たちの業務、および長期戦略を推進すること、および役員のための適切なインセンティブを作ることを含むいくつかの要素に関連する。それはまた私たちのリスク管理、規模、そして私たちの業務の性質などを考慮する。給与政策はまた、以下の追加要因を考慮している
| ● | 関係役員または幹部の教育、技能、専門知識と成果 | |
| ● | 取締役の役割と職責と、それと締結された以前の報酬協定 | |
| ● | 従業員のサービスコストと会社の他の従業員(人力資源会社を通じて採用された従業員を含む)の平均給与中央値との関係は、給与格差が当社の仕事関係に与える影響を含む | |
| ● | 取締役会は、可変報酬の可能性を適宜減少させ、非現金可変報酬の価値行使の可能性を制限する | |
| ● | 解散料補償、役員または担当者のサービス期間、彼または彼女のサービス期間中の給与条項については、このサービス期間中の私たちの表現、この人は私たちの目標と私たちの利益最大化への貢献、そしてその人がどのような状況で会社を出たのか。 |
報酬政策には、以下の原則も含まれる
| ● | 最高経営責任者に直接報告する公職者を除いて、可変報酬と長期業績と測定可能な基準との関係 | |
| ● | 浮動報酬と固定給与との関係、および支給時の変動報酬の最高限度額 | |
| ● | 役員または役員に彼または彼女に支払われた補償の条件の返済を要求し、その後、このような補償に基づいたデータが正確でないことが証明された場合、会社の財務諸表で再説明する必要がある | |
| ● | 株式ベースの可変報酬の最低保有または帰属期間; | |
| ● | 解散費の最高限度額。 |
給与政策はまた長期的な観点から適切なインセンティブを考慮する。
報酬委員会は、(1)承認(その後、株主承認を得るための報酬政策)を会社取締役会に提案し、(2)報酬政策および会社役員報酬に関する職責を担当する
| ● | そのときの補償政策の期限が3年を超えた場合、補償政策を継続すべきかどうかを提案する(いずれの場合も、新たな補償政策を承認するか、既存の補償政策を継続するかは3年ごとに行われなければならない) | |
| ● | 報酬政策の更新を取締役会に定期的に提案します | |
| ● | 補償政策の実行状況を評価する | |
| ● | 特定の公職者の報酬条件が株主の承認を必要とするかどうかを決定する | |
| ● | 委員会の承認を必要とする公職者の報酬条項を承認するかどうかを決定する。 |
92
私たちの報酬政策brは、私たちの長期目標、仕事計画と政策を促進し、私たちの役員と幹部を維持、激励、激励することを目的としています。同時に、私たちの活動に関連するリスク、私たちの活動の性質と範囲、および幹部が私たちの目標と利益を最大化することに対する貢献を考慮し、私たちの役員と役員の利益を私たちの長期業績と一致させます。そのため、役員報酬案の一部は、私たちの短期的かつ長期的な目標、および役員の個人業績を反映することを目的としている。一方、私たちの報酬政策には、キャッシュボーナスや株式ベースの報酬の価値を制限すること、役員報酬と総報酬との間の割合を制限すること、株式ベースの報酬の最短帰属期間を制限することなど、役員が長期的に私たちを損なう可能性のある過剰リスクを低減するためのインセンティブが含まれています。
私たちの給与政策はまた、役員の個人的な特徴(例えば、彼または彼女のそれぞれの職位、教育程度、職責範囲、および我々の目標達成への貢献)を役員報酬変動の基礎とし、役員と取締役と他の従業員の報酬との内部比率を考慮する。例えば、役員に付与される可能性のある報酬は、基本給、年間ボーナス、株式ベースの報酬、福祉、および退職および終了サービススケジュールを含むことができる。すべての現金ボーナスの最高限度額は、執行幹事の基本給にリンクした額である。また、我々の報酬政策は、総可変(現金ボーナスと株式ベースの報酬) と非可変(基本給)給与部分との間の最大許容比率を規定しており、具体的には、上級管理者の会社におけるそれぞれの職に依存する。
あらかじめ設定された定期目標と個人目標を達成した後、実行官に年間現金ボーナスを発行することができる。部下公務員に付与可能な年間現金ボーナスは、完全に適宜評価に基づくことができる。私たちの最高経営責任者は、これらの役員に業績目標を推薦する権利があり、これらの業績目標は、私たちの報酬委員会の承認を得ることができます(法律が要求されていれば、私たちの取締役会が承認することもできます)。
私たちの会長とCEOの業績評価可能な目標は、私たちの報酬委員会と取締役会によって毎年決定されています。会長および/またはCEOの年間現金ボーナスのうち重要でない部分は、報酬委員会および取締役会が定量的および定性的な基準に基づいて、会長またはCEOそれぞれの全体的な表現を適宜評価する可能性がある。
役員(取締役会メンバーを含む)に対する私たちの給与政策によると、私たちの株式報酬 は、基本給と年間現金ボーナスを決定する基本目標と一致しており、その主な目標は、役員利益と私たちと株主の長期利益との間のbr整合性を強化し、br役員の長期留任と激励を強化することである。私たちの報酬政策は、私たちが当時実施していた持分インセンティブ計画に基づいて、株式オプションまたは他の持分ベースの奨励(例えば、制限株式や影オプション)の形で役員報酬 を提供する。役員に付与された株式購入権は帰属期限によって制限され,役員に付与された長期留任を促進する.株式報酬は時々支給され、幹部の表現、教育背景、以前の業務経験、経歴、役割と個人責任によって単独で決定と奨励される。
また、私たちの給与政策 は、ある条件で支払いを超えたボーナスを取り戻すことを可能にし、CEOが役員の雇用条項の非実質的な変更(雇用条項の変化が私たちの給与政策に適合することを前提としていることを前提としています)を含み、その中で規定されているいくつかの制限を遵守して、私たちの役員と役員のために解放、賠償、保険をかけることができます。
私たちの給与政策はまた、(I)2000年の“会社条例”(外部役員の報酬および費用に関する規定)に規定されている金額と、2000年の“会社条例(イスラエル国外上場企業の救済)”によって改正された規定に基づいて、時々改正される可能性がある取締役会メンバーに報酬を提供すること、または(Ii) が私たちの給与政策に基づいて決定された金額を規定している。
93
内部監査師
“会社法”によると、イスラエルの上場企業取締役会は、監査委員会によって指名された内部監査人を任命しなければならない。私たちの内部監査師Chaim Yechezkelyは、2021年10月から公認会計士(ISR)を務めており、公認会計士である。
内部監査人の役割の1つは,会社の行為が法律や適切な業務手順に適合しているかどうかを審査することである。監査委員会 は各活動を監督し、内部監査師の業績を評価し、内部監査師の作業計画を審査する必要がある。内部監査士は、利害関係者または在任者、または任意の利害関係者または在職者の親族であってはならず、会社の独立会計士事務所のメンバーまたはその代表であってもならない。“会社法”は、利害関係者を、1つの会社の5%以上の流通株または投票権を有する任意の個人またはエンティティと定義し、brの少なくとも1人の取締役または会社の社長の誰またはエンティティ、または取締役または会社の社長を務める誰かを任命する権利がある。私たちの内部監査師は、会社の利害関係者でもなく、私たちの従業員でもなく、内部監査に特化した会社のパートナーである。
役員の謝礼金
“会社法”によると、役員の報酬は報酬委員会の承認を受けなければならず、その後は取締役会の承認を経なければならず、その後“会社法”の公布の規定によって免除されない限り、株主総会の承認を受けなければならない。取締役の報酬が外部取締役の報酬に適用される規定に適合している場合、その報酬は株主総会の承認を受けなければならない。取締役も持株株主であれば,持ち株株主との取引承認要求 を適用する.私たちの2021年の株主総会では、全取締役に年間40,000ドルの固定費用を設定しましたが、会長と非公職者取締役は除外しました。
公職者の受託責任
“会社法”は会社のすべての公職者の注意義務と忠誠義務を規定している。
注意義務は,公職者の行動慎重度は,同じ職にある合理的公職者が同じ場合の行動慎重度と同程度であることが求められる。公職者の注意義務には、合理的な手段を使って得ることが含まれている
| ● | 特定の訴訟が利益になるかどうかに関する情報は、その承認またはその地位によって行われることを要求する | |
| ● | このような行動に関する他のすべての重要な情報。 |
公職者の忠誠義務は、公職者が誠実さと会社の利益のために行動することを要求し、以下の義務を含む
| ● | 会社の職責の履行と他の職責または個人事務の履行との間にいかなる利益の衝突もあってはならない | |
| ● | 会社の業務と競争する行為を避ける | |
| ● | 会社のいかなる商機を利用して自分や他人のために私利を図ることを避けること | |
| ● | その役職によって受領された会社の事務に関する任意の資料又は書類を会社に開示する。 |
94
保険
“会社法”によると、会社定款に規定されている範囲内で、会社はその任意の公職者のために、公職者としての行為により生じた次の責任の保険を購入することができる
| ● | 会社や他人への注意義務に違反するが、この違反は公職者の不注意によるものである |
| ● | 会社への忠誠義務に違反し、その人員が誠実に行動すれば、その行為が会社の利益を損なわないと考える合理的な理由がある | |
| ● | 他の人を助けるために彼や彼女に課せられた経済的責任。 |
私たちは現在取締役責任保険と上級管理者責任保険があり、会社と私たちのすべての役員と高級管理者の利益に合計500万ドルの保険を提供し、そのために約21万ドルの12ヶ月の保険料を支払い、保険料は2024年7月に満期になります。
賠償する
“会社法”、“イスラエル証券法”、“第5728-1968号”証券法又は“証券法”によると、会社は事前又は事後に行われた承諾に基づいて、在職者としての行為により生じた以下の責任及び費用を賠償することができるが、会社の定款には、このような賠償を付与する条項が含まれなければならない
| ● | 裁判所によって承認された和解または仲裁裁決、彼または彼女に加えられた別の人に有利な経済的責任を含む、公職者としての行為に関する任意の判決 |
| ● | 公職者の合理的な訴訟費用は、弁護士費を含み、(A)調査または訴訟を行う権利がある当局が調査または訴訟を提起する権利があるため、(1)このような調査や訴訟により当該公職者に公訴書を提起していないことが条件である(“会社法”の定義)。(2)このような調査または訴訟のため、刑事訴訟の代替として、彼または彼女に経済的責任が加えられていない、または、このような経済的責任が適用された場合、犯罪意図証明を必要としない犯罪に対して適用されるか、または(B)金銭制裁に関連する | |
| ● | 弁護士費を含む合理的な訴訟費用は、在任者によって費用がかかるか、または裁判所によって彼または彼女に適用される:(1)会社が彼または彼女に提起した訴訟で、(2)彼または彼女が無罪放免された刑事訴訟において、または(3)有罪判決によって犯罪の意図を証明する必要がない | |
| ● | 職員が証券法に基づいて行政訴訟を行う際に発生する費用には、合理的な訴訟費用と合理的な弁護士費が含まれる。“行政手続き”の定義は,“証券法”第H 3章(イスラエル証券管理局の貨幣制裁),H 4章(行政強制実行委員会の行政実行プログラム)またはI 1章(条件付きでプログラムやプログラムの中断を防ぐ手配)によるプログラムである. |
会社法はまた、会社が公職者への賠償を事前に約束することを可能にするが、このような賠償が上述したように適用される財務的責任に関連する場合、承諾は制限されるべきであり、以下の予測可能な事件および金額 または基準を詳細に説明しなければならない
| ● | 賠償承諾を行う際に、取締役会は、会社の活動によって予見可能な事項と考えている | |
| ● | 取締役会が賠償承諾を行う際に決定した額又は基準は、当時の場合には合理的である。 |
95
私たちはすべての役員と上級管理職の会員たちと賠償協定を締結した。このような賠償協定はいずれも職位保持者に法的に許容される賠償を提供し、最高で一定額に達することができ、これらの責任は取締役や高級職員の保険範囲内ではない。
罪を逃れる
“会社法”によると、イスラエルの会社は在任者がその忠実な義務に違反した責任を免除することはできないが、在任者が注意義務(分配に関するものを除く)に違反することによる会社への損害の全部または一部の責任を事前に免除することができるが、会社定款に責任免除の条項が含まれていることが前提である。私たちが改正し、再記述した会社定款は、任意の在任者がその注意義務に違反して会社に損害を与える責任を全部または部分的に免除することができますが、私たちの持株株主やbrの上級管理者の個人利益による会社取引責任の免除を禁止します。上記の制限を満たした場合、賠償協定により、私たちの公職者は、法律で許容される最大範囲で私たちに対する注意義務に違反するため、私たちに負う任意およびすべての責任を免除し、免除します。
局限性
会社法では、会社は公職者の責任を解放または賠償してはならず、保険契約を締結してはならず、次のいずれかの理由で発生したいかなる責任にも保険を提供しないと規定されている:(1)公職者はその忠誠義務に違反し、(賠償または保険の場合のみ、免責の場合ではない)当該公職者が善意に基づいて行動し、合理的なbr基礎がある限り、この行為は私たちを損なわないと信じている。(2)故意または無謀(不注意だけではなく)の場合、公職者はその注意義務に違反する、(3)不正な個人の利益を得ようとするいかなる行為もしない、または(4)公職者に徴収された任意の罰金、罰金、罰金または没収。
“会社法”によると、上場会社の公職者に対する免責、賠償、保険は給与委員会と取締役会の承認を受けなければならず、ある公職者または場合によっては、株主の承認を得なければならない
私たちが改正して再説明した会社規約は、私たちが会社法で許可されるか、または許容されることを最大限に私たちの公職者のために責任(上記の制限された制約)、賠償、そして保険を解放することを可能にする。
上記の説明 は我々の取締役会の主な側面とやり方を要約した。より詳細については、本年度報告書20-F表の添付ファイルであるbr“会社法”および当社の改正·再記述された会社規約の全文を参照してください。
我々は取締役である取締役との間にサービス契約 がない一方,サービス終了時に福祉 を提供する.
イスラエルの法律に基づいて関係者の取引を承認する
一般情報
“会社法”によると、上述したように、以下の場合、公職者の訴訟を承認することができ、そうでなければ、公職者は上記のような行動を避けなければならない
| ● | 従業員は誠実に行動し、その行為またはその承認は会社に損害を与えない | |
| ● | 在任者は、会社がこの事項を承認する前の合理的な時間に、取引における利益(任意の重大な事実または文書を含む)の性質を会社に開示する。 |
96
公職者の個人的利益を開示する
“会社法”は、在任者が任意の場合に初めて取引を議論する取締役会会議に遅れてはならず、彼または彼女が所有する可能性のある任意の直接的または間接的な個人的利益、および彼または彼女が知っている会社の任意の既存または提案取引に関連するすべての関連する重要な情報を直ちに会社に開示することを要求する。取引が非常に取引されている場合、関係者はまた、以下の者が保有する任意の個人的利益を開示しなければならない
| ● | 公職者の親族 | |
| ● | 在職者又はその親族が5%以上の株式又は投票権を有し、取締役又は社長を担当し、又は少なくとも1人の取締役又は社長を任命する権利がある任意の会社。 |
しかしながら、個人的利益が完全に彼または彼女の親族brの特殊な取引とはみなされない取引における個人利益に起因する場合、その公職者は個人利益を開示する義務がない。会社法によると、非常に取引とは取引のことです
| ● | 通常のビジネスプロセスではありません | |
| ● | 市場条項ではありません | |
| ● | これは同社の収益性、資産、または負債に実質的な影響を及ぼす可能性がある。 |
“会社法”は,我々内部の誰に情報を開示するかを明確に規定しておらず,どのような方法で必要な開示を行うかを具体的に規定していない.私たちは私たちの公職者が私たちの取締役会にこのような情報を開示することを要求する。
“会社法”によると、在任者が上述の開示要求に符合すると、取締役会は会社と在任者或いは在職者と個人利益を有する第三者との間の取引を許可することができ、会社の定款 が別の規定がない限り、取引は会社の利益に符合する。この取引が個人の利益に関連する非常な取引 である場合、監査委員会と取締役会が順次取引 を承認しなければならない。特定の場合、株主の承認が必要になる可能性もある。一般的に、取締役会または監査委員会会議で審議された事項の中で個人的な利害関係がある人は、許可が必要な取引を提出するために出席すべきであることを議長が決定しない限り、このような会議に出席してはならない。取締役会または監査委員会会議で審議された取引中に個人利益がある取締役は、取締役会または監査委員会の多数のメンバーが個人利益がない限り、今回の会議に出席したり、この件について採決してはならない。取締役会の多数のメンバー に個人的な利益がある場合、通常は株主の承認も必要となる。
開示持株株主の個人利益
“会社法”によれば、公職者に適用される開示要求は、上場企業の持株株主にも適用される。持株株主との非常取引または持株株主が個人利益を有する取引は、持株株主が個人利益を有する私募、および持株株主またはその親族またはそのような持株株主によって支配される会社がサービスを提供する取引、および持株株主または持株株主の親族の招聘条項および報酬に関する取引を含む。公職者としても従業員としても,監査委員会や報酬委員会(場合によっては)の承認を得る必要があり,br}取締役会と参加して株主総会で投票した会社株主の多数の株式が必要となる。さらに、株主承認は次の条件のうちの1つを満たさなければならない
| ● | この取引において個人的利益がなく会議で投票した株主が保有する株式のうち、少なくとも過半数の投票がその取引の承認、棄権を除くことに賛成しなければならない | |
| ● | 取引中に個人利益のない株主が取引に反対票を投じた株式は、会社の投票権の2%を超えない。 |
97
また、持株株主の任意の非常取引または持株株主と3年の年限を超える個人権益を持つ取引は、3年ごとに上述の承認を得る必要がある;しかし、このような取引は承認期間が長いが、監査委員会はこの長い期間が当時の状況で合理的であると考えなければならない。また、会社法の規定によると、ある条項に該当する場合には、このような取引は3年後にのみ監査委員会や取締役会の承認または延期を受けることができる。
“会社法”は,自ら,代表または投票ツールを介して持株株主との取引に参加する投票に参加する株主は,その株主が関連する 投票で個人の利益を持っているかどうかをあらかじめまたは投票中に表明しなければならない.そうしなければ、その株主投票が無効になるだろう。
会社法では、公職者ではなく、会社の活動を指揮する能力のある株主として“持株株主”という言葉が定義されている。株主 が会社の50%以上の投票権を持っているか、または会社の50%以上の取締役または社長 を任命する権利がある場合、その株主は持株株主と推定される。会社の株主に関連する取引では、持株株主には、会社の25%以上の投票権を持つ株主 も含まれており、他の株主が会社の50%を超える投票権を持っていなければ。 そのため、同じ取引で個人の利益を持つすべての株主の持株がまとめられる。
役員と役員の報酬を承認する
取締役でない在任者の報酬や約束に対して賠償、保険または無罪を証明するには、我々の報酬委員会の承認を得る必要があり、その後、会社の取締役会の承認を得る必要があり、そのような報酬スケジュールまたは賠償約束、保険または免責が私たちの報酬政策と一致しない場合、または職位保持者が会社の最高経営責任者(Br)である場合(いくつかの特定の例外によって制限される)場合、このような手配は私たちの株主の承認を経て、特別なbrの多くの要求によって制限されなければならない。
役員.取締役それは.会社法によると、私たちの役員の報酬は、会社法の規定に基づいて免除されない限り、私たちの報酬委員会の承認、取締役会のその後の承認、および私たちの株主総会の承認を受ける必要があります。もし私たちの役員の報酬が私たちが宣言した報酬政策と一致しない場合、会社法によって報酬政策に含まれなければならない条項 が報酬委員会と取締役会で審議されている限り、株主の特に多数の承認を得る必要がある。
最高経営責任者以外の他の行政官。“会社法”は、(I)報酬委員会、(Ii)会社取締役会、および(Iii)このような報酬スケジュールが会社が宣言した報酬政策と一致しない場合にのみ、特別多数で承認されることができる上場企業幹部(最高経営責任者を除く)の報酬を以下の順序で承認することを要求する。しかしながら、会社株主が役員との報酬スケジュールを承認しない場合、会社が宣言した報酬政策と一致しない場合、報酬委員会および取締役会は、報酬委員会および取締役会が詳細な理由を提供することを前提として、株主の決定を覆すことができる。
最高経営責任者。“会社法”によると、上場企業の最高経営責任者の報酬は:(I)会社報酬委員会の承認を必要とする。(Ii)会社取締役会、および(Iii)会社株主は、特別多数で通過する。ただし、会社株主がCEOとの報酬スケジュールを承認しない場合、報酬委員会および取締役会は、株主の決定を覆すことができ、報酬委員会および取締役会がそれぞれ報酬条項を審査および再承認した場合、株主が報酬条項を承認しないと判断し、決定する詳細な理由を提供することができる。また、報酬委員会が、報酬スケジュールが会社が宣言した報酬政策と一致すると認定した場合、CEOは会社または会社の持株株主と業務 関係や従属関係がなく、株主 投票承認は、企業が候補者が会社のCEOになる能力を阻害し(後者のためにbrの詳細な理由を提供する)、報酬委員会は、候補者が会社のCEOになる候補者の採用条項を免除することができる。
98
報酬委員会と取締役会の上記の役職者と取締役の承認は、会社が規定する給与政策に適合しなければならないが、特別な場合、報酬委員会と取締役会は、会社の報酬政策と一致しない最高経営責任者の報酬条項を承認することができるが、条件は、“会社法”によって給与政策に組み入れなければならない条項を考慮しており、株主 は特殊な多数の要求によって承認されることである。
株主の責任
会社法によると、株主は、会社における権力の乱用を避け、会社や他の株主に対する権利を行使し、その義務を履行する際に、誠実かつ許容可能な方法で行動する義務があり、その中には、株主総会(および株主総会)で次の事項について採決することが含まれている
| ● | 会社の定款を改正する | |
| ● | 会社の法定配当金を増やす | |
| ● | 合併すること | |
| ● | 株主の承認を必要とする関係者の取引や公職者の行為を承認する。 |
株主には他の株主を圧迫することを避ける一般的な義務もある。契約違反時に通常得られる救済措置 は上記の義務違反行為にも適用され,他の株主が抑圧されていれば,被害株主は追加的な救済措置 を得ることができる。
また、任意の持株株主、その投票が株主投票結果を決定することができる株主、および会社定款に基づいて公職者の任命または任命を阻止する権利がある任意の株主、または会社が他の権力を有するいかなる株主に対しても、会社を公平に扱う責任がある。“会社法”はこの義務の実質を説明しておらず,公平な行動義務に違反した場合には,株主の会社における地位を考慮して,一般に違約時に得られる救済措置も適用されると声明している。
| D. | 従業員。 |
2021年12月31日現在、私たちは23人のフルタイム従業員と3人のアルバイト従業員がいます。2022年12月31日現在、私たちは32人のフルタイム従業員と5人のアルバイト従業員がいます。2023年12月31日現在、私たちは37人のフルタイム従業員(私たちの高級管理チームを含む)、5人のアルバイト従業員 および他の3人の独立請負業者とコンサルタントがいます。
2023年12月31日現在、私たちbrには5人の上級管理職メンバー(私たちの最高経営責任者を含む)があり、彼らは会社の全従業員です。また、私たちはフランスに31人のフルタイム従業員、5人のアルバイト従業員、1人の追加フルタイム従業員がいます。
私たちはイスラエルにいる従業員たちに労働組合代表もなく、集団交渉協定に含まれている職員たちもいない。しかし、イスラエルでは、イスラエル経済産業省が関連労働法に基づいて発表した延期令およびbrが集団交渉協定に署名した労働組合の一部でなくても、このような合意条項を私たちの従業員に適用しなければならないので、イスラエル労働法、法規、国家労働裁判所の前例裁決、および私たちの集団交渉協定に適用されるいくつかの条項を遵守しなければならない。
私たちのすべての雇用と諮問協定には、雇用と秘密保護の過程で形成された知的財産権の競業禁止と譲渡に対する従業員とコンサルタントの約束が含まれている。このような条項の実行可能性はイスラエルの法律によって制限されている。
99
| E. | 所有権を共有する |
以下の“7.A.主要株主”を参照。
持分激励計画
私たちの2019年株式インセンティブ計画または2019年12月に私たちの取締役会によって採択される予定です(2020年4月20日までオプションが付与されていますが)、2021年9月14日に改訂されました。2019年には、当社の従業員、上級管理者、役員またはコンサルタント、および付属会社の取締役、従業員、管理者、コンサルタント、サービスプロバイダに選択権を付与する予定です。2021年9月、我々の取締役会は、制限株式 単位、または“RSU”を付与することを規定するために、2019年計画に対する修正案を承認した。2024年3月22日現在、私たちのbr 2019年計画によると、オプションを行使するために予約された普通株の総数は7,178,569株です。2019年に計画制約されている株は、許可されていますが発行されていない普通株であってもよいし、再買収された普通株であってもよく、具体的には適用される法律に依存しています。
我々の 2019年は、行権価格、支払い方法、授与スケジュール、加速付与、および本計画管理 を管理するために必要な他の事項を含む、私たちの取締役会で構成される委員会が管理する予定です。条件に適合する従業員、高級管理者及び取締役、並びに我々の関連会社の従業員、高級管理者及び取締役は、1961年の“イスラエル所得税条例”(新版)第102節又は“税務条例”の規定を享受する資格がある。税務条例第102条 は、非持株株主であり、イスラエル住民とみなされている従業員、役員及び上級管理者が株式又はオプションの形態で優遇された税収待遇を受けることを可能にする。第102条は、譲受人の利益のために受託者にオプションまたは株式を発行することに関し、オプションまたは株式を譲受人に直接発行する別の代替案を含む2つの税務処理代替案を含む。同条例第102(B)(2)条は,被贈与者に対して最も優遇された税収待遇であり,“資本収益軌道”の下で受託者に債券を発行することを許可する。しかし、この規定によると、発行オプションや株式に関する費用 を差し引くことは許されません。
私たちのコンサルタントと私たちの共同経営会社の顧問、ならびに私たちの従業員、取締役および/または上級管理者、ならびに私たちの関連会社の顧問は、普通株発行前および/または後に持株株主であり、税務条例第3(I)条に基づいてオプション を付与することしかできません。この条には類似の税金優遇は規定されていません。また、2019年に計画されている条項と条件、サービスプロバイダと私たちとの間で適用される制限された株式協定に基づいて、委員会は、当社のサービスプロバイダに制限株式を付与することを自ら決定することができます。
違約として、我々の2019年計画は、サービスプロバイダが任意の理由で契約を終了した場合(死亡、障害または原因を除く)、すべての付与されていないオプションは終了し、関連する普通株は私たちの2019年計画に回復し、2019年計画と管理オプション協定の条項に基づいて、すべての付与されたオプションは通常終了後90日以内に行使できると規定している。上述したにもかかわらず、契約が以下の理由で終了した場合(br}が、私たちまたは私たちの関連会社に不誠実であり、重大な背任または職責を履行しないことによって、私たちまたは関連会社の業務を深刻に損害する場合、または権利者がそのサービス契約に深刻に違反する場合を含む)、サービスプロバイダに付与されたすべてのオプションは、付与されたか否かにかかわらず、行使することができず、そのサービス契約が終了した日に終了するであろう。サービスプロバイダがオプションまたは制限された株式の任意の行使、支払いまたは交付後6ヶ月後に私たちとの契約を終了した場合、サービスプロバイダは、行使、支払いまたは交付が撤回されたことによって達成された任意の収益または受信された支払いの金額を私たちに支払わなければならない。死亡または障害によりサービス契約を終了する場合、終了時および終了日から60日以内に付与されたすべてのオプション は、通常、12ヶ月、 または計画管理者が決定した他の期間内に行使することができるが、2019年計画および管轄オプション協定条項の制限を受ける。
もし私たちが合併、買収、再編または合併に参加し、その合併、買収、再編または合併において、私たちはまだ実体を持っていない場合、または売却、譲渡、交換、または私たちのすべてまたはほぼすべての株式または資産、未償還オプション、および2019年計画に従って買収された株式を処理する場合、合併または合併協定の制約を受ける。この合意は、(I)これらのオプションに対する会社またはその親会社の仮定が残っている;(Ii)既存会社またはその親会社によって新しいオプションを置換する; または(Iii)相続人エンティティがすべての未償還オプションを負担も代替もしない場合、そのオプションは、私などがまだ存在していないエンティティではない合併、買収、再編または合併の日から終了し、または売却、譲渡、交換、または吾などのすべてまたは実質的なすべての株式または資産を処理する。
100
| F. | 登録者が誤って賠償を取り戻す行為 を開示する. |
適用されません。
第七項主要株主と関係者の取引
| A. | 大株主です |
次の表は、2024年3月22日までの私たちの普通株式の利益所有権情報を示しています
| ● | 私たちが知っているすべての人またはグループは、私たちの発行された普通株式の5%以上の実益所有者である | |
| ● | 私たちのすべての役員や行政は | |
| ● | 私たちのすべての役員と幹部はチームです。 |
実益所有権は、普通株の投票権または投資権を含む米国証券取引委員会の規則に基づいて決定される。株式購入または株式承認証によって発行できる普通株は、2024年3月22日後60日以内に行使することができる。
本表に付記されている を除いて,吾らは,当該等株主が吾等に提供した資料に基づいて,本表に示す株主は彼などの実益が持つすべての株式に対して独占投票権および投資権を持つと信じている.別の説明がない限り、各受益者の住所は、C/o Inspira Technologies Oxy B.H.N.Ltd.,2 Ha-Tidhar St.,Ra‘anana,4366504イスラエルである。
| 違います。共
個共有 利益を得る 所有 | パーセント 所有 | |||||||
| 投票権のある証券保有者の5%以上を持っています | ||||||||
| 停戦資本有限責任会社(1) | 1,528,000 | 9.89 | % | |||||
| 役員と上級社員: | ||||||||
| 大木本午(2) * | 1,304,398 | 8.15 | % | |||||
| ジョー海雲(3) * | 1,604,398 | 10.02 | % | |||||
| アヴィ·シャブタイ(4) | 434,722 | 2.71 | % | |||||
| アフィトヒラ(5) | 129,922 | 0.81 | % | |||||
| デニラ·エヘズリー·ヘオン(6) | 52,500 | 0.33 | % | |||||
| タル·パインズ(7) * | 37,736 | 0.24 | % | |||||
| リモ·ロツェン(8) * | 33,035 | 0.2 | % | |||||
| ベナード·ゴドワサー(9) * | 234,469 | 1.46 | % | |||||
| リオール·アミット(10)* | 28,334 | 0.2 | % | |||||
| すべての役員と役員、そして私たちの5%以上の投票権を持つ証券を持つ全体(10人) | 5,387,514 | 34.01 | % | |||||
| * | 会社の役員を表します。 |
| (1) | これらの情報は、停戦資本有限責任会社が2024年2月14日に米証券取引委員会に提出した13 G/Aスケジュールに基づいている。スティーヴン·ボイドさんは停戦資本有限責任会社の保有する株式について投票権と処分権を保有しています。ボイダーさんの郵送先はニューヨークのマディソン通り510番地7階、郵便番号:10022。 |
| (2) | 違います。実益所有株式には,326,739株の普通株, (Ii)920,500株が発行および発行された制限株式単位に帰属する普通株,(Iii)57,159株が60日以内に購入権を行使する際に発行可能な普通株 を含む. |
101
| (3) | 違います。実益所有株式には、(I)626,739株の普通株、(Ii)920,500株の発行および発行された制限株式単位に帰属する普通株、(Iii)57,159株が60日以内に購入持分を行使して発行可能な普通株を含む |
| (4) | 60日以内に1株当たり0.97新シェケル(約0.29ドル)の行権価格で57,144株の普通株を購入できるオプションと、60日以内に1株当たり0.37ニューシェケル(約0.12ドル)の行権価格で57,143株の普通株のオプションを購入することができ、60日以内に得られる2,778株のRSUを含む。シャブタイのオプション期限は2030年4月20日から2030年12月20日まで様々である。 |
| (5) | 13,605株の普通株を購入するオプションを含み、これらの普通株は、60日以内に行使可能であり、1株当たり0.37ネオシェケル(約0.12ドル)の行使価格と、60日以内に得られる7,578株のRSUとを含む。テヘラのオプションは2031年3月16日に満期になる。 |
| (6) | 60日以内に付与される3889個のRSUを含む。 |
| (7) | 9402株の普通株を購入するオプションを含み、これらの普通株は60日以内に行使可能であり、行使価格は1株当たり0.37ネオシェケル(約0.12ドル)、および60日以内に得られる1,668株のRSUである。パナスのオプションは2030年4月20日に満期になる。 |
| (8) | 60日以内に行使可能な4,701株の普通株のオプションの購入、行権価格が1株当たり0.37ネオシェケル(約0.12ドル)であること、および60日以内に得られる1,668株のRSUを含む。ローツェン夫人のオプションは2030年4月20日に満了する。 |
| (9) | 60日以内に行使可能な81,633株の普通株を購入するオプション、行権価格が1株当たり0.37ネオシェケル(約0.12ドル)と、60日以内に得られる23,514株のRSUが含まれる。ゴールドヴァーサーさんのオプションは、2031年3月16日に満了します。 |
| (10) | 60日以内に付与された1,668個のRSUを含む。 |
主要株主の所有権パーセンテージ変化
二零二三年十二月三十一日現在、(I)停戦資本有限責任会社の実益所有権は9.89%に増加し、(Ii)Joe Hayon実益所有権は11.86%から10.02%に減少し、(Iii)大木本濃実益所有率は11.86%から8.15%に減少した。
2022年12月31日及び2021年12月31日までの年度内に、当社が2021年7月に初めて公募し、2021年12月にRSUに付与されたbrの帰属により相対持株率が低下する以外、いかなる主要株主が保有する持分率に大きな変動はない。
記録保持者
2024年3月22日現在、われわれの普通株は18名の登録株主であり、これらの株主はイスラエルに位置している。私たちは、このリストに記載されていない限り、他の会社、いかなる外国政府、または任意の自然人または法人によっても支配されていません。そして、私たちが知っているいかなる手配も、その後の日付で私たちの会社の支配権を変化させません。
| B. | 関係者取引記録。 |
我々役員と上級管理職の報酬については、“6.B.報酬” を参照されたい。
雇用·サービス協定
私たちは私たちのすべての幹部と書面雇用協定を締結しました。これらすべてのプロトコルには,eスポーツ禁止,情報セキュリティ,および発明譲渡に関する慣例条項が含まれている.しかし,競業禁止条項の実行可能性は適用法律によって制限される可能性がある.また,我々は各行政総裁や取締役と合意しており,これにより,吾らは一人一人にある額以下の賠償を支払い,取締役や上級管理者がこれらの責任を保険することに同意した.私たちの何人かの上級管理職の会員たちは毎年ボーナスを得る資格がある。ボーナスは、私たちのCEOが設定し、取締役会の毎年承認された目標と指標を達成した後に支払われ、私たちのCEOにボーナス目標も設定されています。
102
オプション/RSU
私たちの設立以来、私たちは私たちの高級管理者と一部の役員に普通株とRSUを購入する選択権を授与しました。このようなオプション プロトコルは、いくつかの合併、買収、または制御権のための取引を変更する加速条項を含むことができる。我々は“プロジェクト6.E.取締役、上級管理者、従業員-株式-持分インセンティブ計画”の下で私たちのオプション計画を紹介した。もし私たちと役員または役員との関係 が終了した場合、(様々なオプション計画プロトコルで定義されているように)理由を除いて、付与されたオプションは、通常、終了後3ヶ月以内に行使可能である。
株主ローン
オーストラリア交易所での初公募を考えた場合,静脈酸素化装置に重点を置いた。このbr製品の開発は計画通りに行われていないため,Inspira ART製品をあらかじめ開発し,発売期間を約2年短縮し,オーストラリア交易所ではなくナスダックで初公募を行うことにした。2020年11月27日、吾らはIML、創設者およびNewburyportと合意または終了プロトコルを締結し、IPO契約、変更契約 および2019年CLAまたはそれまでの合意を終了する。終了合意に基づき,吾らは1株5.15オーストラリアドル(約3.45オーストラリアドル)または5.88オーストラリアドル(約3.91ドル)の価格で,2020年11月27日に2019年の顧客権益協定に基づく融資金額および利息 を676,061株に変換し,Newburyportまたはその連属会社に80,273株を発起人株式とし,IMLとの契約を推進してくれたDaniel·ゴルツダムに28,572株を購入することに同意し,行価格は0.37新シェケル(1株当たり約0.12ドル)であった。私たちはまたIMFに169,016件の引受権証を発行し、私たちはナスダック資本市場で初めて公募した時に行使することができる。IMLの株式引受証の有効期限は三年です。私たちがナスダック資本市場で初公募を行った後、私たちは私たちの株を購入し、私たちの株を配当として株主に割り当てた。終了プロトコル当事者は,終了プロトコルの他方 とIPO契約,変更契約およびCLAに関するすべての請求を解除することに同意する.また、私たちは、NewburyportとIMLのもう一つの付属会社Peter Marksを私たちの業務開発者として招聘し、潜在投資家に私たちを識別、紹介、普及させ、NewburyportまたはPeter Marksから投資家に紹介してから12ヶ月以内に完成した投資純収益の中で7%の現金手数料を支払うことに同意した。2021年11月28日現在、投資家が紹介した現金手数料として、NewburyportとPeter Marksにそれぞれ403,000豪ドル(約321,000ドル)を支払っている。
| C. | 専門家と弁護士の利益。 |
適用されません。
第八項です財務 情報。
| A. | 報告書やその他の財務情報。 |
“プロジェクト18.財務諸表”を参照
法律訴訟
私たちは時々様々なクレームや私たちの運営で発生したクレームに関する法的手続きに巻き込まれるかもしれません。結果にかかわらず,弁護と和解コスト,管理資源移転,その他の要因により,訴訟 は我々に悪影響を与える可能性がある.我々 は現在,いかなる重大な法律手続きの当事者でもなく,我々の財産もいかなる重大な法律手続きの標的でもない.
103
2021年8月6日、取引所上場有限責任会社または取引所は、双方の間の契約に関連していることを告発するためにニューヨーク州裁判所に訴訟を提起した。このbr契約は、Exchangeが私たちの初公募株に提供しようとしているいくつかのコンサルティングサービスに関するものです。2021年9月9日、私たちはこの事件をニューヨーク南区アメリカ地域裁判所に移した。2021年10月15日、取引所は修正された起訴状、または修正された起訴状を提出し、詐欺の誘導、不当な利益、賠償金額、誠実と公正な取引契約違反、一般法詐欺、書面と口頭契約違反の8つの訴訟理由を提出した。取引所は1,000,000ドルの賠償を要求して、利息、弁護士費、弁護士費、そして少なくとも73,321株の私たちの普通株を発行します。2021年12月16日、双方の書面契約の言葉に基づいて救済可能なクレームを提出できなかったための修正された訴えを却下する動議を提出した。2022年1月28日、取引所上場は自発的にこの件を却下した。
2022年3月4日、取引所はニューヨーク南区連邦裁判所に訴訟を提起し、私たちと私たちの最高財務官Joe Hayon(Br)との間の契約に関連していることを告発し、この契約に基づいて、取引所は私たちの初公募株の準備にいくつかのコンサルティングサービスを提供した。クレームの正確な金額は不明であるが,取引所が要求する賠償金額は約250,000ドルと75,000株の普通株または現金等価物である。2022年7月1日、救済請求を提出できなかったため、双方間の書面契約言語によりbrを付与することができる動議を提出した。
2023年3月8日、裁判所は私たちの動議を部分的に承認し、私たちの動議を部分的に却下する命令を発表した。具体的には、裁判所はジョー·海雲に対するすべての告発を却下し、彼はもはや訴訟の側ではなかった。裁判所はまた、不正終了または挫折に基づいているため、違約訴訟(第1の告発)を却下した。裁判所はまた、4つ目の疑惑(書面協定における量子功績)、6つ目の疑惑(善意黙示契約違反)、7つ目の疑惑(誘引詐欺)を却下した。裁判所は、告発1(疑惑の予期否定に基づいて書面協定に違反する)、疑惑2(告発の口頭合意違反)、告発3(告発に基づく口頭合意の許容禁止) および疑惑V(告発の口頭合意に基づく量子賠償)を訴状または早期却下段階で許可する。私たちはこの問題について積極的に自分自身を弁護し続けるつもりだ。2023年7月,双方が秘密と和解合意を達成した後,この件は自発的に却下された.
2021年12月12日、私たちはUdi Nussinovitch博士との雇用協定を終了し、Udi Nussinovitch博士は私たちの創始者の一人であり、2018年3月以来私たちの首席科学官を務めてきた。2022年2月24日、我々は、さん誠実さと株主および当社の元幹部としての彼の受託責任に違反しているNussinovitchを起訴します。2022年11月9日、我々はさんの苦情のNussinovitchの通知と、2022年11月8日のテルアビブ地域労働裁判所への苦情を受け取りました。Nussinovitchさんが登録者の彼の小株主身分のため、2021年12月17日金曜日に特別株主総会を開催した。また,労使紛争に対する尊重から,Nussinovitchは普通株式を補償して発行することを求めている。2023年7月19日、労使紛争に関する一部の公聴会が開催され、裁判所は、Nussinovitchさんが提起した案件に対する地方裁判所の判断を待つ前に、訴訟の一時停止を要求しました。2024年1月21日、この民事事件は一部の公聴会を開催した。裁判期間中,裁判所は双方に裁判外手配や調停による事件解決の可能性を考慮することを提案した。双方は調停を行うことに同意した私たちはBrはこのような疑いに強く同意せず、私たちが望ましい弁護理由があると信じて、このような疑いについて積極的に自分自身を弁護するだろう。
配当をする
私たちは私たちの普通株についていかなる現金配当金を支払うことを発表したり、予測可能な未来にいかなる現金配当金を支払うことも期待していない。将来現金配当金を支払うかどうか(あれば)は私たちの取締役会が適宜決定し、私たちの財務状況、経営業績、契約制限、資本要求、業務見通し、取締役会が関連すると考えられる他の要素を含む当時の条件に依存するだろう。
会社法は私たちが配当金を発表して支払う能力にさらに制限を加えた。“会社法”によると、取締役会が決定した後、割り当てが満期の既存および予見可能な債務の条項の履行を妨げることを懸念する合理的な理由がない場合にのみ、配当金を発表して支払うことができる。“会社法”によると、割り当て金額は、財務諸表に関連する期間終了 が分配日の6ヶ月前を超えないことを前提として、私たちの当時の最後の審査または監査に基づく財務諸表 が最近2年間合法的に分配可能な留保収益または生成された収益の中で大きいことにさらに制限される。もし私たちがそのような収益基準を満たしていなければ、私たちは配当金を分配するために裁判所の承認を求めることができる。もし裁判所が合理的な理由がないと確信すれば、配当金の支払いが満期の既存かつ予見可能な義務を履行することを阻止することを懸念し、裁判所は私たちの請求を承認するかもしれない。
104
配当金を支払うにはイスラエルの源泉徴収税を払わなければならないかもしれない。より多くの情報については、“プロジェクト10.E.課税”を参照。
| B. | 重大な変化。 |
本20−F年度報告書に財務諸表が含まれている日から、本20−F年度報告書には別途記載されている以外、我々の業務には大きな変化は生じていない。
第九項です 割引と発売
| A. | 特典と発売詳細。 |
2021年7月16日から、私たちの普通株式と引受権証はそれぞれナスダック資本市場で取引され、取引コードはIINNとIINNWである。
| B. | 配送計画。 |
適用されません。
| C. | 市場です。 |
私たちの普通株式と権利証はナスダック資本市場で取引されています。
| D. | 株主を売却する。 |
適用されません。
| E. | 薄めにする。 |
適用されません。
| F. | 発行された費用。 |
適用されません。
第10項その他 情報
| A. | 株です。 |
適用されません。
| B. | 定款の大綱と定款の細則を組織する. |
本年度報告書の20-F表には、添付ファイル1.1として改訂·再記載された会社定款の写しが添付されています。本プロジェクト が提供を要求した資料は,本年度報告テーブル20−Fの添付ファイル2(D)に掲載され,参考として本テーブル20−Fの年次報告に組み込まれる。
105
| C. | 材料契約 |
本年度報告日までの2年間、正常な業務過程で締結された契約を除いて、私たち は上記の“4.A.当社の歴史と発展”、“4.B.業務概要”、“6.C取締役会慣例--賠償”、“6.E株式 株式激励計画”、“7.A.大株主”または“7.B.関連側取引”、“ 以上、または以下に述べる:”
| ● | 当社とH.C.Wainwright&Co.,LLCとの間の証券購入プロトコルは第5.a項を参照“経営と財務回顧と展望“ この文書に関する詳細な情報. |
| D. | 外国為替規制。 |
現在、イスラエルの住民がある取引についてイスラエル銀行に報告書を提出する義務があるほか、イスラエルは私たちの証券や株式を売却して得られた配当金や他の分配に対する支払いにbr通貨規制制限はない。しかし、法律は依然として有効であり、この法律によると、いつでも行政行動によって通貨規制を実施することができる。
非イスラエル住民の私たちの証券に対する所有権または投票権は、イスラエルと戦争状態にある国の市民を除いて、私たちの組織覚書や改正と再記載された組織規約やイスラエル列国の法律のいかなる制限も受けない。
| E. | 税金です。 |
以下はイスラエル所得税に対する私たちの証券所有権の大きな影響について説明する。イスラエル国内会社に適用される現行のイスラエル所得税構造の実質的な関連規定を紹介し,我々への影響を参考にした。議論の基礎が司法や行政解釈のない新税法であれば、税務機関が議論で表明された意見を受け入れる保証はない。 議論の目的は、法律や専門税務提案とみなされるべきでもなく、すべての可能な税務考慮要素の詳細な説明でもない。
以下の説明は、我々の証券の所有権または処置に関連するすべての税金結果を完全に分析するものではない。株主は彼ら自身の税務顧問に問い合わせ、その特定の場合の税務結果、および任意の州、地方、外国または他の税務管轄区の法律によって生じる可能性のある任意の税務結果を理解しなければならない。
イスラエルの一般社税構造
イスラエルの会社は通常会社税を払わなければなりません。2016年1月現在、会社税率は25%だ。2017年1月1日現在、会社税率は24%に低下し、2018年1月1日現在、会社税率は23%となっている。しかし,優先企業(以下に述べる)から収入を得ている会社 が納めるべき実際の税率ははるかに低い可能性がある.イスラエルの会社が獲得した資本利益は通常現行の会社税率が適用される。
イスラエル住民会社が取得した資本収益は現行会社税率で課税される。イスラエル税法によると、次の条件のいずれかに該当する会社は“イスラエル住民会社”とみなされる:(1)会社はイスラエルに登録されているか、または(2)その業務の制御および管理はイスラエルで行われている。
産業奨励法,第5729−1969号
第5729-1969年の“工業(税収)奨励法”、通称“工業奨励法”と呼ばれ、“工業会社”にいくつかの税収割引を提供した
工業奨励法は“工業会社”をイスラエル住民会社と定義し、その任意の納税年度の収入のうち、国防ローン収入を除いて、90%以上の収入はその所有する“工業企業”から来ている。工業企業とは,一定納税年度内に工業生産を主な経営活動とする企業である。
106
工業企業は以下の企業の税収割引およびその他の割引を受けることができます
| ● | 企業の発展または進歩のための特許、特許使用権、およびノウハウを購入するためのコストは、これらの権利を初めて行使した年から8年以内に償却される |
| ● | 限られた条件の下で、選挙は関連するイスラエル工業会社に合併納税申告書を提出し、 |
| ● | 公開発売に関する費用は3年以内に等額控除されます。 |
業界奨励法により福祉の資格を得ることは,どの政府当局の承認にも依存しない。
研究と開発のための税収割引と補助金
改正されたイスラエル第5744-1984号“イスラエルの研究奨励、開発と工業イニシアティブ技術法”および関連法規または“研究法”によると、研究委員会は、特定の基準に適合し、IIAによって承認された研究·開発計画が、IIAによって援助された研究·開発計画またはその結果として開発された製品および関連サービスの販売収入と引き換えに、プロジェクト支出の最高50%の贈与を得る資格があると決定した。特許権使用料は一般に収入の3.0%から5.0%の範囲であり,国際投資協定の全贈与が年間利息とともに返済されるまでである。利息は2023年10月25日までにドル預金に適用される12ヶ月のLIBORをもとに計算されています。しかし、IIAは2023年10月25日、LIBORの満期問題を解決するための印税変化に関する指令 を発表した。この指令によると、IIAが2024年1月1日までに承認されたがその後も返済されていない贈与については、2024年1月1日現在、年利率は12カ月SOFRに基づいて計算されるか、イスラエル銀行が公表した代替金利に0.71513%を加えて計算され、2024年1月1日または後に承認された贈与については、年利は(I)12カ月SOFR金利に1%、または(Ii)固定年利4%のうち高い者となる。
研究法の条項はまた、政府支出で開発された製品の製造をイスラエルで行わなければならないことを要求している。製造活動をイスラエル以外の地域に移すには、事前に国際投資総署の承認を得る必要があるかもしれない。研究法の規定によると、私たちは首席科学者の許可を得て、イスラエル国外でIIAが援助した製品を生産すると仮定して、私たちは増加したbr版税を支払う必要があるかもしれない。特許使用料の増加は、イスラエル国外で行われる生産量に依存し、具体的には以下の通りである
| イスラエル以外の製造業規模は | 最高経営責任者に支払う印税 科学者 一名として パーセント グラントの | |||
| 50%に達します | 120 | % | ||
| 50%から90%の間で | 150 | % | ||
| 90%以上 | 300 | % | ||
もしbr製造が私たちがイスラエル国外で行った場合、イスラエル国外で製造された製品の販売収入に対して支払うべき印税税率は通常の税率より1%増加します。もし製造がイスラエル国外で第三者によって行われた場合、私たちがこれらの収入に対して支払うべき印税比率は、首席科学者室から受け取った寄付金額を、これらの寄付によって資金援助されたプロジェクトに対する私たちの総投資で割った比率に等しいだろう。“研究法”によると、イスラエルの総生産能力の10%以下の製造能力をイスラエル以外の地域に移すことは、事前に国際投資機関の承認を得る必要がない。国際投資機関に資金を申請する会社はまた、国際投資機関の贈与申請でイスラエル以外での部分生産を意図的に宣言することを選択することができ、追加承認の必要性を回避することができる。2011年1月6日、研究法は、上表に規定されている潜在的に増加する特許権使用料を明らかにするために改正され、IIAの承認を必要とせずに製造をイスラエル以外に移転する場合でも適用される。すなわち、移転された生産能力数が総生産能力の10%未満である場合、またはIIA支出申請の枠組み内で海外生産の事前承認を受けた場合。2023年10月25日以降にIIAに提出された海外製造申請については、最高増加した負債はIIA支出の150%に達し、利息を加算しなければならない。300%ではありません
107
首席科学者計画の枠組みで開発された技術ノウハウは,研究法に基づいて制定された政府委員会の事前承認を経ず,イスラエル以外の第三者に譲渡してはならない。しかし、首席科学者が提供した贈与を使用して開発されたどの製品の輸出も承認される必要はない。IIAは、IIAが援助したプロジェクトに関連するノウハウの全部または一部をイスラエル国外の第三者に譲渡することを許可し(譲渡会社は依然としてイスラエル運営エンティティである)、IIAに償還費を支払う必要があり、この償還費は、研究法に規定されている式に基づいて計算され、この式は、一般に、IIAによって援助されたプロジェクトにおける会社の総投資とIIAによって助成されたプロジェクトにおける総投資との比率に基づいて取引対価格に基づく。このような技術をイスラエル国外に譲渡する側は、譲渡した会社がイスラエルの実体として存在しなくなれば、償還費公式を遵守しなければならず、その一般的な根拠は国際投資協定贈与総額と同社の全金融投資の比率に取引対価格を乗じたものである。2011年1月の改正案によると、ノウハウをイスラエル国外の一方に譲渡した場合、償還費は、会社が受け取ったIIAの贈与総額と会社の総研究開発費に取引対価格を乗じた比率に基づく。2011年の改正案によると、ノウハウをイスラエル国外の一方に譲渡する場合、IIAに支払う最高額は、受け取った贈与価値と利息の6倍を超えてはならない。贈与の受給者がイスラエル社でなくなった場合、支払われた金額は、受け取った贈与価値と利息の6倍を超えてはならず、研究開発活動がIIAへの支払い後3年以内にイスラエルに残り、技術移転前の6ヶ月以内に少なくとも75%の研究開発従業員を保留していれば、このような支払いを贈与価値と利息の3倍に減少させ、企業がノウハウ譲渡前の6ヶ月以内に少なくとも75%の研究開発従業員を保留する可能性がある。
イスラエル内でのノウハウの譲渡は、“研究法”および関連条例に記載されているように、独占技術移転の制限および特許権使用料の支払い義務を含む、支援国イスラエルの実体が“研究法”および関連条例を遵守することを約束しなければならない。
これらのbr制限は、私たちがアウトソーシングを製造し、支配権の変更取引に従事するか、または他の方法で私たちの技術をイスラエル以外に譲渡する能力を弱める可能性があり、いくつかの行動および取引についてIIAの承認を得て、IIAに追加の印税を支払うことを要求するかもしれない。特に,我々証券の任意の支配権変更や所有権変更は,非イスラエル市民やbr住民を研究法で定義された“利害関係者”とし,イスラエル以外の製造や技術移転に支払う任意の金のほかに,あらかじめIIAに書面で通知する必要がある可能性がある。もし私たちが研究br法を守らなければ、私たちは私たちが受け取った補助金(利息と罰金と一緒に)を刑事告発されたり強制的に返済されるかもしれない。
研究·開発における税収割引
イスラエル税法は、場合によっては、資本支出を含む支出を許可し、発生当時に減税することができる。以下の場合、支出は科学研究と開発プロジェクトに関連しているとみなされる
| ● | 支出はイスラエルの政府部門が承認し、研究分野で決定された |
| ● | 研究と開発は会社の発展のためでなければならない |
| ● | 研究と開発は,このような税収減免を求める会社またはその代表によって行われる。 |
このような控除可能な費用の金額は、政府支出によって得られた、このような科学研究および開発プロジェクトを援助するための任意の資金の合計を差し引く。これらの研究·開発控除規則が1961年の“所得税条例”一般償却規則に基づいて減価償却可能な資産に投資する費用に関連している場合、これらの研究·開発控除規則による控除は認められない。承認されていない支出は3年以内に等額控除される。
108
私たちは時々首席科学者事務室に承認を申請することができ、発生した年度内にすべての研究と開発費用の減税を許可することができる。そのような申請が受け入れられる保証はない。
資本投資奨励法,第5719-1959号
第5719-1959号“資本投資奨励法”(総称して“投資法”)は、生産施設(又は他の条件に適合する資産)の資本投資に一定のインセンティブを提供する。
税収割引
投資法“は、”優先会社“がその”優先企業“によって生成した収入に税金優遇を与える(このような用語は”投資法“に定義されている)。優先会社の定義には、イスラエルに登録設立された会社が含まれており、その会社は完全に政府の実体によって所有されているわけではなく、他の事項を除いて優先企業の地位を有し、イスラエルによって支配·管理されている。優先会社は、優先企業が獲得した収入に対して16%の減税を受け、優先企業が指定された開発区に位置しない限り、税率は7.5%となる。
優先企業に帰属する収入から支払われる配当金 は、一般に、20%の税率または適用税収条約によって規定される可能性のある低い税率で源源泉徴収税を納付しなければならない。しかし、イスラエル会社にこのような配当金を支払う場合、いかなる税金も源泉徴収される必要はない。
私たちの株主に課税する
非イスラエル住民株主の資本利益税に適用される。非イスラエル住民はイスラエル住民会社の株式brを売却することで資本収益を得ており,これらの株式がこの非住民がイスラエルに設立した常設機関で保有していない限り,イスラエル税を免除することができる。しかし、イスラエル住民が:(I)このような非イスラエル会社において25%以上の持株権を有する場合、または(Ii)このような非イスラエル企業の25%以上の収入または利益の受益者であるか、または25%以上の収入または利益を得る権利がある場合、非イスラエル企業は上述した免除を受ける権利がないであろう。
また、適用される税収条約の規定により、非イスラエル住民が証券を売却することはイスラエル資本利得税を免除することができる。例えば、改正された“アメリカ合衆国政府とイスラエル列国政府の所得税に関する条約”や“米租税条約”によると、株式を資本資産として保有する米国住民株主は、株式を売却、交換、または他の方法で処分し、その住民に付与された利益を享受することを要求する権利がある。一般的にイスラエルの資本利益税を免除するのは、(1)このような売却、交換、または処置によって生じる資本収益がイスラエルに位置する不動産に起因しない限り、(2)売却、交換または処置によって生成された資本収益は、特許使用料に起因する、(3)いくつかの条項によれば、売却、交換または処置によって生成された資本収益は、イスラエルの常設機関に帰属する、(4)処分前12ヶ月の間の任意の部分において、米国住民は、議決権ある資本の10%以上に相当する株式を直接または間接的に保有するが、いくつかの条件によって制限される。又は(V)当該条約は,米国住民が個人であり,関連課税年度内にイスラエル滞在183日以上である。
場合によっては、私たちの株主は彼らの証券を売るためにイスラエル税を支払うかもしれません。対価格を支払うには、源からイスラエル税を源泉徴収する必要があるかもしれません。株主は、販売時に源からの抑留を避けるために、彼らの資本利益が免税であることを証明することを要求されるかもしれない。
109
非イスラエルの株主に配当課税を受ける。非イスラエル住民は一般的に私たちの証券の配当を受けた時にイスラエル所得税を納め、税率は25%であり、イスラエルと株主居住国の間の条約が減免を規定しない限り、源にこの税金を源泉徴収する。配当金を受け取ったとき、または前の12ヶ月以内の任意の時間が“大株主”である人には、適用税率は30%である。“大株主”とは、一般に、その人の親族または他の永久協力者と共に、会社の少なくとも10%の任意の“制御手段”を直接または間接的に保有する人を意味する。“制御手段”は、一般に、投票、利益獲得、取締役または役員の指名、清算時に資産または命令を受けて上記のいずれかの権利を保有する者がどのように行動するかの権利を含む。しかし、配当金が優先企業に帰属する収入から分配されている場合、非イスラエル住民に分配された配当金は、適用される税収条約が税率を低下させない限り、20%の税率で源源泉徴収税を納付しなければならない。例えば、アメリカ-イスラエル税金条約によると、私たちの証券保有者に支払われる配当金は、イスラエル源で源泉徴収された最高税率は25%である。しかし、通常、10%以上の議決権資本を保有する米国会社に支払う配当金の源泉徴収最高税率は12.5%であり、前年の総収入が25%以下であることが条件となる。それにもかかわらず、税条約によれば、優先企業に帰属する所得分配の配当からこのような減免を受ける権利はないが、前年の総収入に関する条件(前に述べたように)が満たされていれば、米国会社である株主に15%の源泉徴収税 税率が課される。もし配当部分が優先企業の収入から来て、 部分が他の収入源から来た場合、予測率はこの2種類の収入の相対的な部分を反映する混合比率となる。株主の納税責任を下げることで分配される可能性のある利益を指定することは保証できません。
アメリカ連邦所得税の考慮要素
以下の要約は参考に供するだけであり、法律または税務提案とみなされてはならない。すべてのアメリカ持株者は普通株を購入、所有、販売する特定のアメリカ連邦所得税の結果について、適用される州、地方、外国或いはその他の税法の影響及び税法の可能な変化を含み、それ自身の税務顧問に相談しなければならない。
以下の2段落で述べた制限を満たすことを前提として,普通株の購入,所有·売却,引受権証および引受権証の行使時に発行または発行可能な普通株を総称して“証券”と呼ぶことによる米国連邦所得税の“米国保有者”への重大な影響についてまとめた。そのため、“米国保有者”とは、以下の証券の所有者を意味する:(1)米国の個人公民又は住民、合法的な米国永住者又は米国連邦所得法に規定されている居留資格基準に適合する外国人を含む。(2)米国またはコロンビア特区またはその任意の行政区の法律に従って作成または組織された会社(または米国連邦所得税の面では会社の実体とみなされる)または組合企業(任意の適用される米国財務省法規によれば、米国人の共同企業とはみなされない)、(3)その収入は、その出所にかかわらず、米国連邦所得税の総収入に含まれる遺産に計上することができる。(4)米国内の裁判所が信託の管理を主に監督することができ、1人以上の米国人が信託のすべての重大な決定を制御する権利がある場合は、信託とするか、または(5)米国財務省法規が規定する範囲内で、有効な選択権を有する信託を米国人とみなす。
本要約は、参考までに、我々の証券購入の決定に関連する可能性のあるすべての米国連邦所得税考慮事項の全面的な説明ではない。この要約は、通常、我々の証券を所有する米国の保有者 のみを資本資産とみなす。以下の議論の限られた範囲を除いて、本要約は、米国所有者ではない米国連邦税の結果を考慮せず、納税者の米国所有者のアイデンティティを特定するのに適したルールも記述しない。本要約は、1986年に改正された“国税法”またはそれに基づいて公布された“国税法”の最終的、一時的かつ提案された“米国財務省条例”、その行政および司法解釈、および“米国/イスラエル所得税条約”の規定に基づいており、これらの規定は本要約の日から発効し、これらの規定は遡及基礎上の変化がある可能性があり、これらの規定はすべて異なる解釈を持つ可能性がある。私たちはアメリカ国税局がアメリカの保有者の私たちの証券への投資brのアメリカ連邦所得税待遇について裁決を求めることはありませんので、国税局が以下の結論に同意する保証はありません。
110
本議論は、特定の米国連邦所得税の特殊な状況に関連する可能性があり、特に遺産、贈与、ジャンプ移転、州、地方、消費税、または外国税考慮事項については言及しない。また、本議論は、以下の米国連邦所得税待遇に関連していない:(1)銀行、生命保険会社、監督されている投資会社、または他の金融機関または“金融サービス実体;“(2)証券または外貨の仲介人またはトレーダー、(3)雇用または他のサービス履行により私たちの証券を取得した人、(4)米国代替性最低税を適用した米国保有者、(5)ヘッジ、ヘッジ、国境を越えた、取引の転換または推定売却または米国連邦所得税目的の他のリスク低減取引の一部として我々証券を保有する米国保有者、(6)免税実体。(7)不動産投資信託又は設保人信託、(8)米国に移住した米国保有者又は前米国長期住民、又は(9)ドル以外の機能通貨を保有する者。本議論は、いつでも、私たちの投票権の10%以上を占める証券を直接または建設的に所有する米国連邦所得税待遇に関するものではない。さらに、提携企業(または他の直通エンティティ)または提携企業または他の直通エンティティを介して証券を保有する個人の米国連邦所得税待遇に関するものではない。
各潜在的投資家 はその自分の税務顧問に相談し、私たちの証券の購入、保有或いは処分のこの投資家に対する具体的な税務結果を理解し、適用される州、現地、外国或いは他の税法の影響及び税法の可能な変化を含むことを提案する。
または権利証の有効期限を行使する
引受権証の行使は何の収益や損失も生じない 株式承認証を行使する場合、米国所有者がこれによって獲得した普通株のコストは、米国所有者の権利証調整コストに普通株支払いの行使価格を加えることに等しい。未行使の権利証の満期は通常、米国の権証保有者に調整後のコストベースに相当する資本損失を発生させる。株式承認証を行使することで得られる普通株の保有期間は、引受権証の保有期間を含む。
普通配当金の課税
私たちは予測可能な未来に配当金を支払うつもりはない。もし私たちが確かに配当金を支払い、以下のタイトル“受動的外国投資会社”の下での議論と“適格配当金収入”に関する以下の議論の制限を受けた場合、米国保有者(米国会社に属するいくつかの米国保有者を除く)は、その割り当てが私たちの現在および累計の収益および利益を超えない限り、“受動的外国投資会社”の下での以下の議論と“適格配当金”に関する以下の議論の制限を受けるであろう。アメリカ連邦所得税の目的のために確定された。私たちの収益と利益を超える分配金額はまず免税資本リターンとみなされ、アメリカの保有者の証券課税基礎をある程度下げ、それから資本収益となる。私たちはアメリカ連邦所得税の原則に基づいて私たちの収益と利益を計算しないと予想されますので、アメリカの保有者はどのように分配されることを期待すべきすべての金額 は通常配当収入として報告されます。
一般的に、“適格配当金収入”と長期資本利益の優遇税率は、個人、遺産または信託基金の米国保有者に適用される。そのため、“合格配当収入”は他を除いて、“合格外国会社”から得られた配当金を指す。“適格外国会社”とは、米国との包括的税収条約の利益を享受する権利を有する会社であり、情報交換計画を含む。アメリカ国税局は、イスラエル/アメリカ税収条約はこの要求を満たしており、私たちはこの条約のメリットを享受する資格があると信じている。
111
さらに、もし私たちの証券がいつでもナスダック資本市場またはアメリカの他の成熟した証券市場で取引できるなら、私たちの配当金は合格した配当収入になるだろう。もし私たちが配当金を支払う年にPFICとして支払うか、または前年にPFICとして支払うとみなされる場合、配当金は以下の“受動外国投資会社”で説明するように割引料率を享受する資格がないだろう。米国の保有者は優遇金利を享受する権利がない:(1)米国の所有者が除利日の60日前から121日間の間に少なくとも61日間私たちの証券を保有していない場合、または(2)米国の所有者は実質的に類似した財産に関連したbr}支払いを義務化する。米国の保有者がその証券損失リスクを低下させたどの日数も61日の保有期間に計上されていない。最後に、規則163(D)(4)節により配当収入を“投資収入”とする米国の保有者を選択すると、優遇税率を受ける資格がない。
私たちの証券の分配金額 については、割り当てられた任意の財産の公平な市場価値によって測定され、米国連邦 所得税については、イスラエルがそこから源泉徴収した任意の税金の金額である。我々がNISで支払った現金分配は,配当金が米国所有者の収入に計上できる日から有効なドル現金を米国所有者のbr収入に計上し,米国所有者はこのNISにおいてこのドル ドル価値に等しい米国連邦所得税ベースを享受する。米国の所有者がその後、新しいシェケルをドルに両替するか、または他の方法で処理する場合、為替変動によって生じる新しいシェケルに関連する任意の後続収益または損失は、米国由来の一般的な為替損益となる。
証券処分の課税問題
以下の“受動型外国投資会社”の項で述べるbr}PFIC規則に規定されている場合を除き,我々の証券を売却,交換またはその他の方法で処分する場合,米国保有者は資本収益や損失を確認し,その金額は当該米国所有者のドル税の税ベースとドル建ての処分現金化金額との差額(あるいはその等値ドル,変動額が外貨建てであれば処分日のスポットレートを参考に決定)に等しい。米国の保有者が証券を売却、交換、または他の方法で処分する際の保有期間が1年を超える場合、証券を売却、交換、または他の方法で処理する際に達成される収益または損失は、長期資本損益となる。長期資本収益を確認した個人は、このような収益を低い税率で課税することができる。資本損失の控除は様々な制限を受けている.
受動型外国投資会社
米国連邦所得税特別税法はPFIC社の株式を持つ米国納税者に適用される。以下のいずれかの納税年度に該当する米国連邦所得税については、PFICとみなされる
| ● | 課税年度内に、私たちの総収入の75%以上(どの会社の総収入のうちの割合を含み、私たちは25%以上の株式を所有していると考えられている)が受動的であるか | |
| ● | 私たちが保有する資産のうち、少なくとも50%は受動的収入を生成または生成するために使用され、これらの資産は年間平均で計算され、一般に公正な市場価値に基づいて決定される(25%以上の株式を所有すると考えられる任意の会社の資産に比例して保有されている価値を含む)。 |
そのため、受動的収入は、通常、配当金、利息、レンタル料、特許使用料、年金、および特定の大口商品取引および名義主要契約からの収入を含む。現金は受動的な収入を生むとみなされている。
本課税年度にはPFICにはならないと信じていますが、予見可能な未来にPFICになるかどうかは決まっていませんが。PFICの地位を確定するテスト は年に1回行われ、この確定に関連する未来の収入と資産を正確に予測することは困難である。しかも、私たちのPFICの地位は私たちの証券の市場価値に部分的に依存するかもしれない。したがって, は現時点でPFICにならないかどうかは保証されない。
現在私たちがbr PFICになっている場合、各株式を市価建て(以下に述べる)を選択していないアメリカ人所有者は、私たちのいくつかの配布brを受信し、収益で私たちの証券を処理する場合:(1)このような配信または収益を米国所有者の証券保有期間に比例して分配する(場合によって決まる)、(2)本納税年度に割り当てられ、PFICの最初の納税年度初日までの任意の期間の金額を一般課税収入とする。(3)他の課税年度ごとに割り当てられた金額は,その年度の適用納税者種別に適用される最高税率で課税され, は,それによって生じる当該等の他の課税年度に起因する税項について利息費用を徴収する.また,死亡により米国の所有者である被相続人からPFICの株を買収した場合,このような株の納税基準 は被相続人が亡くなった日に公正な市場価値の増加を得るのではなく,被相続人の基礎を下回れば,すべての収益が被相続人の確認を得ない限り被相続人の基礎に等しくなる。PFICへの間接投資もこれらの特殊な米国連邦所得税規則に制約される可能性がある。
112
上記PFICルールは,我々がPFICである米国所有者が証券を保有するすべての課税年度にQEF選挙を行う米国所持者には適用されず,特定の報告要求を遵守することを前提としている。代わりに、私たちがPFICである各納税年度について、QEF選挙に参加したアメリカ人の所有者は、私たちの一般収入における米国所有者の割合を一般収入とすることと、私たちの純資本収益における米国所有者の割合を長期資本利益として、このような収益や収益をどのように分配するかにかかわらず、米国所有者の割合を長期資本として利益とすることを要求されている。一般的に、良質な教育基金選挙は、私たちが何か必要なbr情報を提供する時にのみ有効である。QEF選挙は株主単位で行われ、通常は米国国税局の同意を得た場合にのみ撤回される。もし私たちがいかなる納税年度にPFICとみなされると思うなら、私たちはアメリカの保有者に通知するつもりはありません。また,我々はIRS Form 8621を記入するために必要な情報を毎年米国の所持者に提供し,我々または我々のどの子会社もPFICの任意の年に有効なQEF選挙 を行って維持するつもりはない。したがって、QEF選挙は私たちのbr証券に適用されないだろう。
また,我々がPFICであり,米国保有者が時価であれば,上記PFICルール は適用されない。我々の証券の米国保有者が定期的に適格取引所(ナスダック資本市場を含む)で取引していれば,毎年証券を時価で計算し,一般収入や損失と確認することができ,金額は納税年度終了までの証券の公平時価と米国所有者の証券調整後の課税基礎との差額に等しい。赤字は時価ベースの純収益(br}の前に米国保有者が選挙に応じた上位納税年度の収入を含む)に限られている。
私たちがPFICの間に私たちのbr証券を持っているアメリカの保有者は、私たちがPFICでなくても、上記のルールを守ります。米国の保有者がPFIC規則について彼らの税務顧問に相談することを強く促す。
純投資所得税
個人、遺産または信託基金である米国の所有者は、一般に、その純投資収入(私たちの証券の配当および収益を売却または処分することを含む)のために3.8%の連邦医療保険税を納付するか、または遺産および信託基金の場合、遺産または信託基金の受益者に割り当てられていない純投資収入について3.8%の医療保険税を支払うことが要求される。いずれの場合も,連邦医療保険税の3.8%は米国ホルダーの調整後の総収入が適用限界を超える範囲にのみ適用される。
情報報告 と控除
現金配当金と証券処分収益については,米国保有者は24%の比率で予備源泉徴収を行うことができる。通常,米国の保持者が指定されたアイデンティティ識別プログラムを遵守できなかった場合にのみ,バックアップ バックルが適用される.バックアップ源泉徴収は、指定された免税受取人(会社や免税組織のような)に支払われるお金には適用されない。バックアップ源泉徴収は付加税ではなく、直ちに米国国税局に必要な情報を提供すれば、米国保有者の米国連邦所得税責任を相殺することを申請することができる。
最近公布されたbr立法によれば、このようなすべての資産の総価値が納税年度の最終日に50,000ドルを超える場合、または納税年度内のいつでも75,000ドル(または適用される米国国税局ガイドラインによって規定される可能性のあるより高いドル金額)を超える場合、“特定の外国金融資産”(私たちの証券などの資産を含む。このような証券が金融機関を介して米国保有者を代表して保有しない限り)を有する米国の保有者が、米国国税局に情報報告を提出することを要求される可能性がある。外国金融口座の総価値がカレンダー年度内の任意のbr時間が10,000ドルを超える場合、外国銀行および金融口座報告書、またはFBARを提出する必要がある場合がある。あなたはあなた自身の税務コンサルタントに問い合わせて、このような情報報告書を提出する可能性のある義務を理解しなければなりません。
| F. | 配当と有料代理店です。 |
適用されません。
| G. | 専門家の発言。 |
適用されません。
113
| H. | 展示されている書類。 |
我々は、外国のプライベート発行者に適用される取引法に適用される情報報告要件を遵守し、これらの要求に基づいて米国証券取引委員会に報告書を提出する。米国証券取引委員会は、米国証券取引委員会に報告を電子的に提出する発行者に関する報告書やその他の情報を含む相互接続サイトを維持する。我々が米国証券取引委員会に提出した書類は、米国証券取引委員会サイトwww.sec.govを介して公衆に公開することもできる。
外国の個人発行者として、取引所法第16条に記載されている報告書及び短期運転利益回収条項の制約を受けない“取引所法”の委託書の提供及び内容に関する規定を免除する。また、取引法によれば、その証券が取引法に基づいて登録されている米国国内会社のように、年度、四半期、および現在の報告書および財務諸表を米国証券取引委員会に頻繁にまたはタイムリーに提出する必要はない。しかし、各会計年度終了後120日以内、または米国証券取引委員会が要求した適用期間内に、独立公認会計士事務所が監査した財務諸表を掲載した20−F表年次報告書を米国証券取引委員会に提出し、監査されていない四半期財務情報を表 6−Kに提出することができる。
私たちはある会社のサイト www.spirira-Technologies.comを維持しています。我々のサイトと上で引用した他のサイトに含まれる,あるいはそれを介してアクセス可能な情報は,本20-F表年次報告の一部を構成しない.これらのサイトアドレスを本年度報告の表 20-Fに含め,非アクティブなテキストとしてのみ参照する.
| I. | 子会社情報。 |
は適用されない.
| J. | 証券所持者への年次報告 |
適用されません。
第十一項市場リスクの定量的·定性的開示について
正常な経営過程において、私たちは一定の市場リスクに直面しており、主に外貨為替レートと金利の変化である。
市場リスクの定量的·定性的開示について
私たちは正常な業務過程で市場リスク に直面している。市場リスクとは、金融市場の価格や金利の不利な変化により、我々の財務状況に影響を及ぼす可能性のある損失リスクである。私たちの現在の投資政策は、信用格付けが少なくともA-の銀行預金に現金で投資できることだ。したがって、私たちの等価物の大部分は利息のある預金です。 私たちが現在受け取っている低金利を考慮すると、金利を下げると、私たちは悪影響を受けません。我々の市場リスク開放 は主にNIS/ドルレートの結果であり,次段でこの点を詳細に検討する.
114
外貨両替リスク
私たちは主にイスラエルで運営していて、私たちの費用の約70%は新しいシェケルで価格を計算する。したがって、私たちは、金融市場価格と金利の不利な変化によって、私たちの財務状況に影響を及ぼす可能性のある損失リスク という市場リスクに直面しています。私たちはこれらの手配に関連した外貨為替レートの変動の影響を受けるだろう。
私たちは現在、私たちの外貨為替レートリスクを部分的にヘッジして、私たちの主要な経営通貨為替レートの変動による財務リスクを下げる。しかし、このような措置はこのような変動の実質的な悪影響から私たちを保護するのに十分ではないかもしれない。
金利リスク
私たちはどんな重大な長期借入金も負担しないと予想している。現在、私たちの投資は主に現金と現金等価物と短期預金で構成されています。 私たちの投資活動の主な目標は、リスクや損失を著しく増加させることなく元本を残しながら、投資から得られる収入を最大化することです。金利変動により、私たちの投資は市場リスクに直面する可能性があり、これは私たちの金利収入と私たちの投資の公平な市場価値に影響を与える可能性があります(あれば)。
インフレと貨幣変動の影響
インフレは通常、私たちのNIS建ての費用を増加させることによって、賃金と福祉、施設レンタルコストと現地サプライヤーへの支払いを含む私たちに影響を与えます。インフレは,2023年12月31日までの年度内に,我々の業務,財務状況や経営結果に実質的な影響を与えないと考えられる。
第十二項株式証券を除く証券説明
| A. | 債務証券。 |
適用されません。
| B. | 授権書と権利。 |
適用されません。
| C. | 他の証券です。 |
適用されません。
| D. | アメリカ預託株です |
適用されません。
115
第II部
13項目の違約、延滞配当金、延滞
ない。
項目14.保持者の権利を保証するための実質的な修正および収益の使用
2021年7月に、吾らは改訂されたF-1表登録説明書(登録番号:333-253920)に基づいて普通株および引受権証の初公開を完了し、これにより2,909,091株の普通株式および3,345,455件の流通権証(引受業者に付与された超過配給選択権によって行使された436,364部の流通権証を含む)を販売した。これらの普通株と引受権証はいずれも単位あたり5.5ドルの合計価格で販売されており,引受割引 と他の発行コストを差し引いたところ,IPOから受け取った総純収益は1,400万ドルであった.我々は,2021年7月15日に米国証券取引委員会に提出された最終目論見書に記載されているように,今回の発行に関する権利証を行使して得られた金を引き続き使用し,それぞれ333−253920号および333−257880号文書である。
プロジェクト15.制御とプログラム
(A)開示制御及びプログラム
我々の経営陣は、最高経営責任者およびCEOの参加の下で、2023年12月31日までの評価日、開示制御およびプログラムの有効性 を評価した(取引法下のルール13 a-15(E)および15 d-15(E)で定義されている)。このような評価によれば、これらの上級管理者は、評価日までに、我々の開示制御および手順は、取引法の要求に基づいて定期文書に含まれる情報を記録、処理、まとめ、タイムリーに報告する上で有効であり、そのような情報は、必要な開示に関する決定をタイムリーに行うために、我々の主要な幹部および財務管理者を含む管理層に蓄積されて伝達されると結論している。
(B)財務報告の内部統制に関する経営陣の年次報告
我々の経営陣は、“取引法”の下のルール13 a-15(F)に定義されている財務報告の十分な内部統制の確立と維持を担当している。我々の経営陣(最高経営責任者や最高財務責任者を含む)の監督と参加の下、トレデビル委員会後援組織委員会が発表した“内部統制-総合枠組み(2013)”で構築された枠組みと標準 に基づいて、本報告末までの財務報告の内部統制の有効性を評価した。この評価に基づき、我々の経営陣は、2023年12月31日まで、財務報告の内部統制に有効であり、財務報告の信頼性に合理的な保証を提供し、公認された会計原則に基づいて外部目的の財務諸表を作成すると結論した。
(C)公認会計士事務所の認証報告
本年度報告には,我々の独立公認会計士事務所の財務報告の内部統制に関する証明報告 は含まれておらず,“雇用法案”はEGCの免除を規定しているためである。
116
(D)財務報告内部統制の変化
2023年12月31日までの年間で、財務報告の内部統制に大きな影響を与えていないか、または合理的に財務報告の内部統制に大きな影響を与える可能性が高い。
第十六項[保留されている]
プロジェクト16 A。監査委員会財務専門家
我々の取締役会は、我々の監査委員会の各メンバーが監査委員会の財務専門家であり、取引所法案の下の規則に基づいて定義され、適用される取引所法案規則とナスダック株式市場規則とによって独立していることを決定した。
プロジェクト16 B。道徳的準則
私たちは、私たちの最高経営責任者、最高財務官、主要な統制者、類似の機能を実行する人、および私たちの役員を含む、私たちの上級管理者と従業員に適した書面道徳基準を採用しました。私たちのビジネス行動と道徳基準は私たちのbrサイトwww.icecure-Medical.comに掲載されています。我々のサイトに含まれている,あるいは我々のサイトを介してアクセス可能な情報は,本20-Fフォーム年次報告の一部ではなく,ここにも含まれていないことを参考にする.もし吾らが“商業行為規則”および“道徳規範”を任意の改正または“規則”条項に対して任意の黙示免除を含む任意の免除を行う場合、吾らは“米国証券取引委員会”規則および規定によって要求される範囲内で、表 20-F 16 B項の説明を含む、これらの改正または免除の性質を私たちのウェブサイト上に開示する。私たちは私たちの商業行動と道徳的基準に基づいてどんな免除も承認しなかった。
プロジェクト16 Cです。チーフ会計士費用とサービス
独立公認会計士事務所BDOメンバー事務所ZIV Haft.は、2022年12月31日と2023年12月31日までの2年間、毎年主要な独立公認公的会計士事務所を務めています。
次の表は、2022年と2023年12月31日までの年間にZIV Haftおよび/または他のBDOメンバー事務所に支払うすべてのサービス(監査サービスを含む)費用に関する 情報を提供します。
| 十二月三十一日までの年度 | ||||||||
| 2023 | 2022 | |||||||
| 料金を審査する(1) | $ | 170 | $ | 140.5 | ||||
| 登録説明書を審査する | $ | 17.1 | $ | 28 | ||||
| 合計する | $ | 187.1 | $ | 168.5 | ||||
| (1) | 私たちの年次財務諸表の監査と私たちの中期財務諸表の審査に関連する専門サービスが含まれています。 |
117
査定師の報酬をあらかじめ承認する
私たちの監査委員会は、私たちの独立公認会計士事務所を招聘していくつかの監査と非監査サービスを実行することに対して、予め承認された政策があります。この政策によると、監査委員会は、毎年、私たちの独立公認会計士事務所が提供する可能性のある監査サービス、監査関連サービス、および税務サービスカテゴリにおける特定の監査および非監査サービス目録を事前に承認しています。我々の監査人によって提供されるサービスタイプが、このような一般的な事前承認を得ていない場合には、我々の監査委員会が具体的な事前承認を行う必要がある。政策 は、適用される米国証券取引委員会規則で定義されている禁止されている非監査機能を履行するために、独立公認会計士事務所の保留を禁止する。
プロジェクト16 Dです。監査委員会の上場基準に対する免除
適用されません。
プロジェクト16 E。発行者と関連購入者が株式証券を購入する
適用されません。
プロジェクト16 Fです。登録者を変更する認証会計士
適用されません。
プロジェクト16 Gです。会社の管理
ナスダック証券市場規則 によると、私たちは対応するナスダック証券市場規則を遵守してアメリカ国内発行者に適用される会社管理要求の代わりに、会社法によって許可されたいくつかの会社管理やり方を選択することができる。
イスラエルの法律と実践に基づいて、“ナスダック証券市場規則”第5615条に規定されている免除の制限を受け、私たちは“ナスダック証券市場規則”の以下の要求に関する規定ではなく、会社法に従うことを選択した
| ● | 定足数それは.“ナスダック”株式市場規則では、上場企業が普通議決権株式保有者がどの会議を開催するかの定足数は、会社が普通議決権株を発行した33.5%を下回らないと規定されているが、イスラエル 法律によると、会社はその定款の中で株主総会の定足数と必要な持株比率を決定する権利がある。我々が改正および再記述した組織定款細則は,株主総会で営業所を開始するために必要な定足数は2名以上の株主であり,自らまたは委任代表が少なくとも25%の投票権を持っていることを規定している。しかし、我々が改正して再記載した延期会議に関する定款に規定されている定足数には、少なくとも1人の株主が自ら出席または代表出席を依頼することが含まれている。 |
| ● | 上級者の報酬。 イスラエルの法律と私たちが改正して再説明した会社規約は、ナスダック株式市場規則の最高経営責任者および他のすべてのbr幹部に対する一般的な要求である我々の取締役会の独立メンバー(または完全に私たちの取締役会の独立メンバーからなる報酬委員会)に幹部のbr報酬を決定することを要求しない。代わりに、役員の報酬は私たちの報酬委員会と私たちの取締役会が決定して承認し、場合によっては私たちの株主が決定して承認するか、私たちの公職者の給与政策と一致するか、特殊な場合にはそれに反するか、会社法で規定されているいくつかの考慮事項を考慮しながら。より多くの情報は“第6.C.項:役員、高級管理者、従業員--取締役会のやり方--イスラエルの法律に基づいて関連者の取引を承認する”ことを参照されたい。 |
118
| ● | 株主が承認する。我々は、会社法の要求に基づいて、ナスダック上場規則第5635条に基づいて株主の承認を求めるのではなく、株主の承認を必要とするすべての会社行為について株主承認を求める。特に、ナスダック株式市場規則によれば、以下の場合、通常、(I)他の会社の株式/資産の買収は、買収側の20%以上の株式または投票権の発行に関連する場合、または取締役、役員または5%の株主が対象会社において5%を超える権益を有する場合、または受け取る対価格、(Ii)支配権変更を招く株式を発行する場合、株主の承認を得る必要がある。(Iii)採用/改訂持分補償計画(会社法条文によれば、採用/改訂持分補償計画は、株主の承認を必要とすることは規定されていないが)、および(Iv)上場企業は、私募(および/または役員/上級管理者/5%株主販売)を介して20%以上の株式または投票権(株式に変換または株式行使可能な証券を含む)を発行(または売却)し、ただし、これらの株式は、株式の帳簿または時価より大きい者より低い価格で発行(または販売)する。対照的に、“会社法”によると、以下の事項を除いて、以下の事項は、株主承認が必要である:(I)取締役とそのサービス条項またはそのサービス(または彼らが会社で担当する可能性のある他の職)との賠償、免除、および保険による取引は、報酬委員会、取締役会および株主の承認が必要であり、(Ii)上場企業持株株主との特別取引には、特別な承認が必要であり、(Iii)我々の持株株主またはその持株株主の親族の雇用条項または他の採用条項、これは特別な承認が必要だ。 |
| ● | 関連側取引の承認それは.すべての関連側取引は会社法による利害関係側の行為及び取引に対する承認要求及び手続きによって承認され、特定の取引については、ナスダック証券市場規則の要求に従って監査委員会或いは報酬委員会(状況によって決まる)又は取締役会及び株主(状況に応じて決定される)によって承認されなければならず、ナスダック証券市場規則の要求に従って監査委員会又は他の独立取締役会によって承認されなければならない。補足資料については、“プロジェクト6.C.取締役、高級管理者と従業員--取締役会のやり方--イスラエルの法律に基づいて関連側の取引を承認する”を参照した。 | |
| ● | 年度株主総会ナスダック証券市場規則第5620条(A)条は,上場企業は会社の財政年度終了後1年以内に年次株主総会を開催しなければならないことを要求しているが,“会社法”によると,例年および前回の年次株主総会開催後15カ月以内に年次株主総会を開催しなければならない。 | |
| ● | 株主に定期報告書を配布する。上場発行者に様々な具体的な方法の1つで株主にこのような報告を提供することを要求するナスダック株式市場規則とは異なり、イスラエルの法律は、定期的な報告書を株主に直接配布することを要求していない。イスラエルが一般的に受け入れているビジネス慣行は、株主にそのような報告を配布するのではなく、公共サイトを介してこのような報告を提供することである。公的サイトでこのような報告を提供するほか、当社のオフィスで監査された財務諸表を株主に提供しており、株主が要求した場合にのみ株主に郵送しています。海外私募発行者としては,米国証券取引委員会の依頼書募集規則の制約を受けないのが一般的である. |
以下の場合、役員報酬は、通常、株主承認を得る必要がある:(I)取締役会の承認であり、報酬委員会は、我々の報酬政策と一致しない、または(Ii)承認が必要な報酬は、我々のCEOまたは同時にわが社の持株株主(その関連会社を含む)の役員の報酬である。当該等の株主承認は、株主総会に出席して株主総会で議決された株式の多数決を得る必要があり、条件は、(I)当該等の多数の株式は非持株株主の保有株式の多数 を含み、当該等の非持株株主が総会で議決した報酬スケジュールには個人利益がないため、いかなる棄権及び利益に関与しない多数も含まれていないこと、又は(Ii)当該手配に反対投票した非持株及び利害関係のない株主が保有する株式総数は当社の投票権の2%を超えないことである。
119
また,我々の役員報酬政策に適合すれば,役員であり役員でもある役員の報酬は,株主総会で出席して投票した株の簡単な多数票を獲得して承認される必要がある.我々の報酬委員会及び取締役会は、特別な場合には、特定の論拠に基づいて、株主の反対意見を考慮して、役員(取締役、CEO又は持株株主を除く)の報酬を承認するか、又は株主の反対を無視して報酬政策を承認することができる。CEO職が有名人に採用されたbrと外部取締役の非従属要求に適合する場合、私たちの給与委員会は、このような採用を株主の承認を必要とすることをさらに免除することができ、このような採用が私たちの職位保持者の報酬政策に適合することを前提とし、私たちの給与委員会は特定の論拠に基づいて決定し、このような採用を株主承認に提出することは、このような採用を阻止する可能性がある。持ち株株主とのいずれかのこのような取引の期限が3年を超える場合には、3年ごとに承認する必要がある。
取締役または役員は、会社の取締役会がその個人利益に関連する取引を検討または採決する際に出席してはならないが、通常の取引は除外し、取締役会議長が彼または彼女が承認すべき取引を提出すべきであることを決定しない限り。
| ● | 独立役員ですイスラエルの法律は、我々の取締役会の多くの取締役が、ナスダック上場規則第5605条(A)(2)条で定義された“独立取締役”でなければならないことを要求しているのではなく、上述したように“6.C.取締役会慣行である外部取締役”の少なくとも2人が会社法の要求に適合する外部取締役であることを要求している。イスラエルには法的規定があるにもかかわらず、私たちはナスダック株式市場規則によると、私たちのほとんどの役員は現在“独立”だと信じている。しかし、私たちの監査委員会のすべてのメンバーが適用されるナスダックとアメリカ証券取引委員会の独立性基準の下で“独立”であることを確認しなければなりません(私たちは外国の個人発行者であるにもかかわらず、私たちはアメリカ証券取引委員会の独立性要求を遵守する要求を免除することはできません)、また、私たちの監査委員会の多くのメンバーが会社法で定義されている“非関連取締役”であることを確実にしなければなりません。また、イスラエルは法律を要求せず、私たちの独立役員が彼らだけが出席する会議を定期的に開催することも要求しないが、“ナスダック証券市場規則”には別の要求がある。 |
| ● | 株主が承認する我々は、会社法の要求に応じて、ナスダック上場規則第5635条に基づいて株主承認を求めるのではなく、株主承認を必要とするすべての会社行為について株主承認を求める。 |
| ● | 関連側取引の承認それは.すべての関連側取引は会社法による利害関係側の行為及び取引に対する承認要求及び手続きによって承認され、特定の取引については、ナスダック証券市場規則の要求に従って監査委員会或いは報酬委員会(状況によって決まる)又は取締役会及び株主(状況に応じて決定される)によって承認されなければならず、ナスダック証券市場規則の要求に従って監査委員会又は他の独立取締役会によって承認されなければならない。 |
| ● | 年度株主総会。ナスダック証券市場規則第5620条(A)条は,上場企業は会社の財政年度終了後1年以内に年次株主総会を開催しなければならないことを要求しているが,“会社法”によると,例年および前回の年次株主総会開催後15カ月以内に年次株主総会を開催しなければならない。 |
120
16 H項です。炭鉱安全情報開示
適用されません。
プロジェクト16 I。検査阻止に関する外国司法管轄区の開示
適用されません。
プロジェクト16 Jです。インサイダー取引政策。
プロジェクト16 Kです。ネットワークセキュリティです。
会社はリスクを低減し、安全、可用性と秘密信頼原則の遵守を確保するために、ネットワークセキュリティ政策、プログラム、コンプライアンスと意識計画を含むネットワークセキュリティリスク管理戦略を制定し、維持した。ネットワークセキュリティプロセスは、会社全体のリスク管理システムとプロセスに統合されており、完全に内部管理されている。
リスク自体の影響とリスク実現の可能性を考慮することで,個々の識別されたリスクのレベルを決定し,高得点リスクに行動する。リスク を分析して、リスクが受け入れられた会社のリスク受け入れ基準を満たしているかどうか、または緩和計画 を適用するかどうかを決定する。緩和計画には、その計画を担当する個人または部門も含まれているし、予算考慮要素も含まれている可能性がある。
本報告日まで、私たちは、私たちの業務戦略、運営結果、または財務状況を含む、ネットワークセキュリティ脅威からのいかなる重大なリスクも、私たちに大きな影響を与える可能性があることを知らない。
統治する
私たちの最高経営責任者と最高財務官は私たちのネットワークセキュリティリスク管理と緩和を監督します。取締役会はどんなサイバーセキュリティ事件についてもタイムリーな情報を受け取った。私たちの監査委員会は定期的にネットワークセキュリティについて議論している。
リスク管理と戦略
我々の全体的なリスク管理手法の重要な要素の一部として,我々のネットワークセキュリティ計画は以下の重要な分野に重点を置いている
| ● | 協力方法:同社は機能を越えた全面的な方法を実施し、ネットワークセキュリティ脅威とイベントを識別、予防と緩和し、同時に制御プログラムとプログラムを実施し、特定のネットワークセキュリティイベントを迅速にアップグレードし、管理層がこのようなイベントの公開開示と報告に関する決定を適時に行うことができるようにした。 | |
| ● | 技術保障:会社は、ファイアウォール、侵入防御と検出システム、反マルウェア機能とアクセス制御を含む、会社の情報システムをネットワークセキュリティ脅威から保護するための技術保障措置を配備し、脆弱性評価とネットワークセキュリティ脅威情報による評価と改善を行った。 | |
| ● | イベント応答と回復計画:会社はネットワークセキュリティイベントに対する会社の応答を全面的に解決し、このような計画を定期的にテストし、評価するために、全面的なイベント応答と回復計画を確立し、維持している。 |
121
第三部
17項です財務諸表
私たちは、項目18に従って財務諸表および関連情報を提供することを選択しました。
第十八項財務諸表
財務諸表と本プロジェクトに必要な関連付記は本年度報告の表格20−Fに掲載され,F−1ページから始まる。
プロジェクト19展示品
| 番号をつける | 展示品説明 | |
| 1.1 | 改訂·再改訂されたInspira Technologies Oxy B.H.N.Ltd.会社規約(2021年12月20日に提出され、添付ファイル99.1~Form 6−K(文書番号001−40303)として提出され、引用により本明細書に組み込まれる)。 | |
| 2.1* | 証券説明書 | |
| 4.1 | 賠償プロトコル表 (2021年3月12日に提出され、表F−1の添付ファイル10.1(文書番号333−253920)として提出され、参照によって本明細書に組み込まれる)。 | |
| 4.2 | Inspira Technologies Oxy B.H.N.Ltd.(前身:InSense Medical Ltd.)2019年株式インセンティブ計画(2021年9月14日改訂)は、2021年10月27日に提出されたF−1表発効後の修正案第1号(文書番号333−253920)の添付ファイル10.2として提出され、参照により本明細書に組み込まれる。 | |
| 4.3 | Inspira Technologies Oxy B.H.N.Ltd社の役員報酬政策は、2021年12月20日に添付ファイル99.2としてForm 6−K(文書番号001−4030)に提出され、参照により本明細書に組み込まれる。 | |
| 4.4 | 依頼書代理プロトコル表(2021年7月1日提出,F-1表添付ファイル4.2(アーカイブ番号333-253920)として提出し,引用により本稿に組み込む) | |
| 4.5 | 授権書表(2021年7月1日に提出され、表F−1の添付ファイル4.4(文書番号333−253920)として提出され、参照により本明細書に組み込まれる)。 | |
| 4.6* | 当社と米国株式譲渡と信託会社との間の引受権証合意改訂表は、2022年8月8日となっている。 | |
| 4.7 | 将来株式簡易協議表(2021年7月1日に提出され、F-1表添付ファイル10.7(文書番号333-253920)として提出され、引用により本明細書に組み込まれる) | |
| 4.8 | 株主融資協定は、日付が2018年3月1日であり、当社が大木本農と締結している(添付ファイル10.8として2021年7月1日に提出されたF-1表(第333-253920号文書、引用により本明細書に組み込む))。 | |
| 4.9 | 変換可能な融資契約表(添付ファイル10.9として2021年7月1日に提出されたF-1表(第333-253920号文書)を提出し、参照により本明細書に組み込む) | |
| 4.10 | 証券購入契約表(2023年12月27日に提出された海外発行者報告書6−K表の添付ファイル10.1として提出され、参照により本明細書に組み込まれる) | |
| 12.1* | 1934年証券取引法第13 a-14条に基づく最高経営責任者の証明。 | |
| 12.2* | 1934年証券取引法第13 a-14条(A)に基づいて首席財務官を認証する。 | |
| 13.1% | 米国法第18編第1350条に基づく最高経営責任者の認証。 | |
| 13.2% | “米国法典”第18編第1350条に基づく首席財務官の証明。 | |
| 15.1* | 独立公認会計士事務所BDOのメンバー事務所Ziv Haftの同意。 | |
| 97.1* | Inspira Technologies Oxy B.H.N.Ltd.が政策を取り戻したのは2023年11月28日であった。 | |
| 101* | 以下の財務情報は、登録者から2023年12月31日までの年度20-F報告書、フォーマットはXBRL(拡張可能商業報告言語):(I)2023年12月31日、2022年12月31日、2021年12月31日までの貸借対照表、(Ii)2023年12月31日、2022年12月31日および2021年12月31日までの全面赤字報告書、(Iii)2023年12月31日、2022年12月31日および2021年12月31日までの株主権益変動表。(4)2023年12月31日現在、2022年12月31日現在、2021年12月31日現在のキャッシュフロー表;および(V)財務諸表を付記する。 | |
| 104* | 表紙インタラクションデータファイル(イントラネットXBRL文書に埋め込まれている). |
| * | 本局に提出します。 |
| % | 同封して提供する |
122
サイン
登録者は、それが20-F表の提出のすべての要件に適合していることを証明し、以下の署名者が、それを代表して提出された本20-F表の年次報告書に署名することを正式に手配し、許可した。
| Inspira Technologies Oxy B.H.N.Ltd. | ||
| 日付:2024年3月25日 | 差出人: | /S/大木本午 |
| 大木本午 | ||
| 最高経営責任者 | ||
123
Inspira Technologies Oxy B.H.N.Ltd.
カタログ
| ページ | ||
| 独立公認会計士事務所報告(BDO | F-2 | |
| 貸借対照表 | F-3 | |
| 全面損失表 | F-4 | |
| 株主権益変動表 | F-5 | |
| 現金フロー表 | F-8 | |
| 財務諸表付記 | F-10-F-35 |
これらの金額は数千ドル単位です
F-1
独立公認会計士事務所報告
Inspira Oxy B.H.N.Ltd.取締役会と株主に。
ハハハール通り2ラアナナイスラエル
財務諸表に対する意見
Inspira Technologies Oxy B.H.N.Ltd.(前身:InSense Medical Ltd.)の貸借対照表を監査した。(“当社”)2023年12月31日及び2022年12月31日まで、2023年12月31日までの3年間の各年度の関連全面赤字、株主権益変動及びキャッシュフロー表及び関連付記(総称して“財務諸表”と呼ぶ)。財務諸表 は,すべての重要な面で,会社の2023年12月31日と2022年12月31日までの財務状況,および2023年12月31日までの3年度の経営業績とキャッシュフローを公平に反映しており,米国公認の会計原則(“米国公認会計原則”)に適合していると考えられる。
経営を続ける企業
添付されている財務諸表は、当社が経営を継続すると仮定して作成されています。財務諸表付記1で述べたように、当社は発展段階にあるため、設立以来経常赤字および運営キャッシュフローは負となってきている。2023年12月31日現在、会社は累計5550万ドルの赤字を計上している。会社の運営資金は主に株式の発行と引受権証から来ている。このような状況を考慮すると、同社の運営は外部資金に依存しており、同社の持続経営企業としての持続的な経営能力が大きく疑われている。経営陣のイベントおよび条件の評価およびこれらの事項に関する経営陣の計画は付記1に記載されています。財務諸表には、これらの不確実性の結果によって生じる可能性のあるいかなる調整も含まれていません。
意見の基礎
これらの財務諸表は会社の経営陣が責任を負う。私たちの責任は私たちの監査に基づいてこのような財務諸表に意見を述べることだ。我々は米国上場企業会計監督委員会(PCAOB)(PCAOB)に登録されている公共会計士事務所であり、米国連邦証券法および米国証券取引委員会とPCAOBの適用規則と法規に基づいて、会社から独立しなければならない。
我々はPCAOBの 基準に従って監査を行った。これらの基準は、財務諸表に重大な誤報がないかどうかに関する合理的な保証を得るために、エラーによるものであっても詐欺によるものであっても、監査を計画し、実行することを要求する。当社は必要とせず、brを招聘してその財務報告の内部統制を監査していません。私たちの監査の一部として、財務報告の内部統制を知る必要がありますが、社内財務報告の内部統制の有効性について意見を述べるためではありません。したがって、私たちはそのような意見を発表しなかった
我々の監査には、財務諸表の重大な誤報のリスク(エラーによるものであっても詐欺によるものであっても)を評価するためのプログラムの実行と、これらのリスクに対応するプログラムを実行することとが含まれる。これらの手続きには、テストに基づいて財務諸表中の金額および開示に関する証拠を検討することが含まれています。私たちの監査には、使用された会計原則および経営陣による重大な推定を評価し、財務諸表の全体的なレポートを評価することも含まれています。私たちは私たちの監査が私たちの観点に合理的な基礎を提供すると信じている。
| /S/ジフ·ハフト | |
| 2024年3月19日 | 公認会計士(Isr.) |
| 2018年以来、当社の監査役を務めてきました。 | BDO会員事務所/S/ |
F-2
Inspira Technologies Oxy B.H.N.Ltd.
貸借対照表
(千単位のドル)
| 十二月三十一日 | 十二月三十一日 | ||||||||||
| 注意事項 | 2023 | 2022 | |||||||||
| 資産 | |||||||||||
| 流動資産 | |||||||||||
| 現金と現金等価物 | |||||||||||
| 預金.預金 | 3 | ||||||||||
| その他流動資産 | 4 | ||||||||||
| 流動資産総額 | |||||||||||
| 非流動資産: | |||||||||||
| 使用権資産、純額 | 7(B) | ||||||||||
| 財産·工場·設備·純価値 | 5 | ||||||||||
| 非流動資産総額 | |||||||||||
| 総資産 | |||||||||||
| 負債と株主権益 | |||||||||||
| 流動負債: | |||||||||||
| 応払い貿易勘定 | |||||||||||
| その他の売掛金 | 6 | ||||||||||
| 賃貸負債 | 7(B) | ||||||||||
| 公正な価値で計算された財務負債 | 8 | ||||||||||
| 流動負債総額 | |||||||||||
| 非流動負債: | |||||||||||
| 賃貸負債 | 7(B) | ||||||||||
| 非流動負債総額 | |||||||||||
| 引受金とその他の事項 | 7 | ||||||||||
| 株主権益: | |||||||||||
| 配当金および追加実収資本 | 9 | ||||||||||
| 損失を累計する | ( | ) | ( | ) | |||||||
| 株主権益総額 | |||||||||||
| 総負債と株主権益 | |||||||||||
| /S/アフィトヒラ | /S/大木本午 | 2024年3月19日 | ||
|
アフィトヒラ 首席財務官 |
大木本午 最高経営責任者 |
財務諸表承認日 |
付記は財務諸表の構成要素である。
F-3
Inspira Technologies Oxy B.H.N.Ltd.
全面損失表
(1株当たりの損失を除いて千ドルで)
| 十二月三十一日までの年度 | ||||||||||||||||
| 注意事項 | 2023 | 2022 | 2021 | |||||||||||||
| 研究開発費 | 10 | |||||||||||||||
| 販売とマーケティング費用 | 11 | |||||||||||||||
| 一般と行政費用 | 12 | |||||||||||||||
| その他の費用(収入) | ( | ) | ||||||||||||||
| 営業損失 | ||||||||||||||||
| 預金利子収入 | ( | ) | ( | ) | ( | ) | ||||||||||
| 財務支出,純額 | 13 | ( | ) | |||||||||||||
| 税引き前損失 | ||||||||||||||||
| 所得税 | ||||||||||||||||
| 総総合損失と純損失 | ||||||||||||||||
| ( | ) | ( | ) | ( | ) | |||||||||||
付記は財務諸表の構成要素である。
F-4
Inspira Technologies Oxy B.H.N.Ltd.
株主権益変動表
(千単位のドル)
2023年12月31日までの年度:
| 普通株資本 | ||||||||||||||||
| 共有数: | 株と株 追加実収資本 | 積算 赤字 | 合計する | |||||||||||||
| 2023年1月1日現在の残高: | ( | ) | ||||||||||||||
| この期間の変化: | ||||||||||||||||
| 普通株式と私募株式権証の発行,純額 | ||||||||||||||||
| 配給代理権証の発行(付記9) | - | |||||||||||||||
| 普通株発行(市場(“ATM”)に応じて手配) | ||||||||||||||||
| 株式ベースの支払いを行使する | ||||||||||||||||
| 限定株式単位(“RSU”)帰属 | ||||||||||||||||
| 株式ベースの報酬 | - | |||||||||||||||
| 総合純損失 | - | ( | ) | ( | ) | |||||||||||
| 2023年12月31日現在の残高 | ( | ) | ||||||||||||||
| (*) |
F-5
Inspira Technologies Oxy B.H.N.Ltd.
株主権益変動表
(千単位のドル)
2022年12月31日までの年度:
| 普通株資本 | ||||||||||||||||
| 株式数 | 配当金および追加実収資本 | 赤字を累計する | 合計する | |||||||||||||
| 2022年1月1日現在の残高: | ( | ) | ||||||||||||||
| この期間の変化: | ||||||||||||||||
| 株式ベースの支払いを行使する | ||||||||||||||||
| RSU帰属 | ||||||||||||||||
| 株式ベースの報酬 | - | |||||||||||||||
| 総合純損失 | - | ( | ) | ( | ) | |||||||||||
| 2022年12月31日現在の残高 | ( | ) | ||||||||||||||
| (*) | 千ドル以下です |
付記は財務諸表の構成要素である。
F-6
Inspira Technologies Oxy B.H.N.Ltd.
株主権益変動表
(千単位のドル)
2021年12月31日までの年度:
| 普通株資本 | その他の内容 | |||||||||||||||||||
| 共有数: | 共有 資本 | すでに納めた 資本 | 積算 赤字 | 合計する | ||||||||||||||||
| 2021年1月1日現在の残高: | ( | ) | ( | ) | ||||||||||||||||
| この期間の変化: | ||||||||||||||||||||
| 額面価値相殺 | - | ( | ) | |||||||||||||||||
| 初公募(“IPO”) | ||||||||||||||||||||
| 財務負債の転換 | ||||||||||||||||||||
| 流通権証を行使する | ||||||||||||||||||||
| RSU帰属 | ||||||||||||||||||||
| 株式ベースの支払いを行使する | ||||||||||||||||||||
| 株式ベースの報酬 | - | |||||||||||||||||||
| 総合純損失 | ( | ) | ( | ) | ||||||||||||||||
| 2021年12月31日現在の残高 | ( | ) | ||||||||||||||||||
| (*) | 千ドル以下です |
付記は財務諸表の構成要素である。
F-7
Inspira Technologies Oxy B.H.N.Ltd.
現金フロー表
(千単位のドル)
| 12月31日までの年度 | ||||||||||||
| 2023 | 2022 | 2021 | ||||||||||
| 経営活動のキャッシュフロー: | ||||||||||||
| 純損失 | ( | ) | ( | ) | ( | ) | ||||||
| 純損失を経営活動に提供する現金純額に調整する | ||||||||||||
| 減価償却 | ||||||||||||
| 取り分で計算した報酬費用 | ||||||||||||
| 株式による補償−配給代理権証(注9) | ||||||||||||
| 公正な価値によって未来の株式と転換可能な融資の簡単な合意を再評価する | ||||||||||||
| 公正な価値で財務負債を評価する | ( | ) | ( | ) | ||||||||
| 発行コスト | ||||||||||||
| リース債務を前払いする | ( | ) | ( | ) | ( | ) | ||||||
| 使用権資産が減少する | ( | ) | ( | ) | ||||||||
| その他流動資産の減少(増加) | ( | ) | ||||||||||
| 貿易売掛金の増加 | ||||||||||||
| その他の売掛金が増加する | ( | ) | ||||||||||
| 経営活動のための現金純額 | ( | ) | ( | ) | ( | ) | ||||||
| 投資活動によるキャッシュフロー: | ||||||||||||
| 家屋·工場·設備を購入する | ( | ) | ( | ) | ( | ) | ||||||
| 短期預金投資 | ( | ) | ||||||||||
| 短期預金を売却して得た金 | ||||||||||||
| 投資活動提供の現金純額 | ( | ) | ( | ) | ||||||||
| 資金調達活動のキャッシュフロー: | ||||||||||||
| 将来の株式(SAFE)と転換可能なローンに関する簡単な合意を受け取る | ||||||||||||
| 普通株の発行 | ||||||||||||
| 非公開株式証明書を発行する | ||||||||||||
| 現金発行コスト | ( | ) | ||||||||||
| 選択権を行使する | ||||||||||||
| 普通株発行(ATMによる発行) | ||||||||||||
| 融資活動が提供する現金純額 | ||||||||||||
| 現金および現金等価物の純増加(減額) | ( | ) | ( | ) | ||||||||
| 期初の現金、現金等価物と制限現金 | ||||||||||||
| 期末現金、現金等価物、および制限現金 | ||||||||||||
付記は財務諸表の構成要素である。
F-8
Inspira Technologies Oxy B.H.N.Ltd.
現金フロー表
(千単位のドル)
付録A--非現金取引:
| 十二月三十一日までの年度 | ||||||||||||
| 2023 | 2022 | 2021 | ||||||||||
| 転換可能なローンを株式に変換する | ||||||||||||
| 取引可能株式証の初回公募時の財務責任 | ( | ) | ||||||||||
| 株式ベースの報酬-IPOの引受業者費用 | ( | ) | ||||||||||
| 株式ベース補償·配給代理追加実収資本に対する引受権証(注9) | ( | ) | ||||||||||
付録B- の間に支払われた金額:
| 十二月三十一日までの年度 | ||||||||||||
| 2023 | 2022 | 2021 | ||||||||||
| 支払の利子 | ||||||||||||
付記は財務諸表の構成要素である
F-9
Inspira Technologies Oxy B.H.N.Ltd.
財務諸表付記
千ドル(共有 および1株当たりのデータは含まれていない)
注1--一般的に:
| 1. | Inspira Technologies Oxy B.H.N.Ltd.(前身:InSense Medical Ltd.)(“当社”)2018年2月27日にイスラエルに登録設立され、運営を開始しました。同社は医療技術業界で呼吸支援技術分野の業務を経営しており,独自製品や技術の研究,開発,製造に関する活動や上場活動に従事している。同社は以下の製品を開発している |
| ● | INSPIRA ART(呼吸増強技術) は1種の呼吸支持技術であり、直接の血液酸素化を利用して患者の覚醒と自発呼吸の数分以内に患者の飽和度を高めることを目的としている。その目的は侵襲的機械換気に対する需要を減少させることであり、リスク、合併症と高いコストを下げる潜在力がある。 | |
| ● | Hyla血液センサは非侵襲的光学血液センサであり、リアルタイムかつ連続的な血液測定を行い、患者から実際の血液サンプルを採取する必要を潜在的に最大限に減少させることを目的としている。 | |
| ● | INSPIRA ART 100設備は先進的な生命支援システムであり、医療業界ではより多くの体外循環システムと呼ばれ、現在体外循環6時間以上を必要とする外科手術のために設計されている。 |
| 2. | 同社の製品は開発段階にあります。Inspira ART 100デバイスやInspira ART は人体でテストや使用されていない。同社の製品は米国食品医薬品局(FDA)の承認を得ていない。INSPIRA ART 100設備は2023年9月にFDAに提出され510 k承認されており,同社は2024年上半期にFDAの承認を得る予定である。 |
| 3. | 当社は2023年12月26日に機関投資家と登録直接発売(“登録直接発売”)について購入契約(“購入契約”)を締結し、これにより、当社は(I)を発行する |
| 4. | 添付されている財務諸表(“財務諸表”)は、当社が経営を継続すると仮定して作成されています。現在まで、同社はまだ発展段階にある。そのため、会社は設立以来運営の経常赤字と運営キャッシュフローが負の状況にさらされてきた。2023年12月31日まで、会社は累計損失
ドル |
F-10
Inspira Technologies Oxy B.H.N.Ltd.
財務諸表付記
千ドル(共有 および1株当たりのデータは含まれていない)
注1- 一般:(続)
| 5. | 私たちの事務所はイスラエルに設置されている。2023年10月7日、ハマステロリストはガザ地区からイスラエル南部国境に浸透し、民間人と軍事目標に対して一連の攻撃を発動した。襲撃発生後、イスラエルはハマスに対して宣戦布告し、イスラエル軍は予備役を募集して現役に参加し始めた。同時に、ハマスへの宣戦布告により、レバノンでのイスラエルとヒズボラの衝突がエスカレートし、将来的にはより大きな地域紛争に発展する可能性がある。本財務諸表が発表された日まで、これらの事件は会社の運営に実質的な影響を与えなかった。 |
| 6. | 我々は現在、ロシアとウクライナで事業を展開していないが、ロシアとウクライナの地政学的不安定なアップグレードやロシアルーブルの通貨変動は世界市場にマイナスの影響を与えている。この影響は、この地域における私たちのサプライチェーン、業務、および将来の成長見通しに悪影響を及ぼす可能性があります。ウクライナ危機のため、アメリカと他の国は、あるロシア個人と実体に対して制裁を実施しています。私たちのグローバル業務は、ロシアとウクライナの現在の情勢が、ロシアと他の国との間の緊張の激化、実施された関税、経済制裁および輸出入制限、回復行動、およびその地域における私たちの潜在的な業務および販売に潜在的なマイナス影響をもたらす可能性がある、私たちの業務、財務状況、運営結果、キャッシュフロー、または私たちの証券の市場価格に悪影響を及ぼす可能性のあるリスクに直面させる。ロシアとウクライナの現在の地政学的不安定性や、米国や他の国政府のある会社や個人に対する制裁は、これらの国の潜在的な顧客やサプライヤーとの業務を行う能力を阻害する可能性がある。 |
| 7. | これらの財務諸表は2024年3月19日に取締役会によって許可された。 |
注2--重要な会計政策:
添付の財務諸表は米国公認会計基準 に基づいて作成されている。財務諸表を作成する際に従う主要会計政策 は以下のとおりである
A. IFRSから米国GAAPへの変換-
当社は国際財務報告基準(“IFRS”)に基づいて作成された歴史財務諸表 を米国公認会計基準に基づいて当該等の財務諸表に列記することに遡及的に変換している。これは米国公認会計基準に基づいて提出された最初の財務諸表だ。
同社はイスラエルの会社であり,呼吸支援技術分野の医療技術業界を経営しており,そのビジネス努力を主に米国に集中させようとしている。同社の長期的かつ短期的な意図はいずれも米国での臨床試験であり,FDAの承認を目指すことであり,最初としても重要なマイルストーンである。
これらの財務諸表における国際財務報告基準とアメリカ公認会計原則の重大な違いは以下の通りである
F-11
Inspira Technologies Oxy B.H.N.Ltd.
財務諸表付記
千ドル(共有 および1株当たりのデータは含まれていない)
注2-重要会計政策:(続)
(A)賃借証書
“国際財務報告基準”によると、米国公認会計原則を採用する前に、当社はテナントとして、米国公認会計基準下の融資リース会計と類似した単一賃貸モデルを採用している。費用 は,リース期間が早い場合に総費用の高い割合を占めることを確認しており,これは資産を使用する直線減価償却とリース負債適用の有効金利法を組み合わせた結果であり,リース期間全体の利息 費用確認が減少している。また,リース費用は総合損失表における列報方式も異なる。米国公認会計原則ではリース費用として列記されているが、国際財務報告基準の下では減価償却·利息費用として列記されている。
アメリカ公認会計原則によると、テナントには2種類のレンタル会計モードがある:融資リースと経営性賃貸。当社はテナントとして、そのすべてのレンタルを経営的賃貸に分類し、借地期間全体で単一賃貸費用を直線原則で確認し、使用権資産減価償却部分と利息支出部分を含む。
(B)財務負債
当社は初公開(“IPO”)で売買可能株式証を投資家に発行し、初公開前に投資家に株式承認証を発行する。国際財務報告基準によると、当社が発行した引受権証は財務負債に分類され、公正価値に応じて計量され、損益の中で変動を確認する。しかし、米国公認会計原則によると、 はその機能通貨の変化により、これらの権利証は株式ツールに分類される。
アメリカ公認会計原則に移行した後、会社はすでに株式証の分類を再評価し、それらが株式ツールとしての分類基準に符合することを確定した。そのため、財務諸表では、株式証は財務負債から権益に再分類されている。
この再分類は、米国公認会計基準に基づいて列報を要求するすべての期間 に適用されている。そこで、従来期間の財務諸表を調整して、株式証明書の財務負債から権益への再分類を反映する。
株式証明書の分類を確定した後、当社は株式と発行費用の間の初公開募集費用の分配を変更した。
(C)機能通貨報告の変化
“国際財務報告基準”によると、機能通貨は実体経営が置かれている主要な経済環境の通貨に基づいて決定される。しかし、米国公認会計原則によると、本位貨幣 は、実体が現金を生成し、支出する主要な経済環境の通貨によって決定される。
この変化により、当社はその本位貨幣を再評価し、米国公認会計基準の要求に基づいて、現在現金収入と支払いが発生した主要な経済環境の通貨と一致していることを確定した。
ビットコインレポートにおけるこの変更は に遡って適用されている.
経営陣は、機能通貨報告のこの変化は、会社運営の経済実質をよりよく反映していると考えている。
F-12
Inspira Technologies Oxy B.H.N.Ltd.
財務諸表付記
千ドル(共有 および1株当たりのデータは含まれていない)
注2-重要会計政策:(続)
(D)政府補助金
国際会計基準(“IAS 20”)(国際財務報告基準による)によると、当社は収入予測に基づいて政府からの贈与を資本化し、一定期間財務支出を確認する。
しかし、米国公認会計原則によると、同社は収入発生開始時にのみ 印税を確認しています。これは国際財務報告基準とは異なり、国際財務報告基準では、会社は資本化負債、財務費用、より低い研究開発費支出を確認している。
国際財務報告基準から米国公認会計原則に基づくドルに転換し、我々の運営通貨とし、他の米国公認会計原則の違いに従うことで、私たちの財務業績が変化した
| 注意事項 | 国際財務報告基準 (前報告) | アメリカは会計原則を公認している | ||||||||
| その他流動資産 | 2 a(C) | |||||||||
| 使用権資産、純額 | 2 a(A) | |||||||||
| 応払い貿易勘定 | 2 a(C) | |||||||||
| その他の売掛金 | 2 a(C) | |||||||||
| 流動賃貸負債 | 2 a(A) | |||||||||
| 公正な価値で計算された財務負債 | 2 a(B) | |||||||||
| 長期賃貸負債 | 2 a(A) | |||||||||
| イスラエル革新局(IIA)からの融資 | 2 a(G) | |||||||||
| 外貨準備 | 2 a(C) | ( | ) | |||||||
| 配当金および追加実収資本 | 2 a(B) | |||||||||
| 損失を累計する | 2A | ( | ) | ( | ) | |||||
| 株主権益総額 | 2A | |||||||||
F-13
Inspira Technologies Oxy B.H.N.Ltd.
財務諸表付記
千ドル(共有 および1株当たりのデータは含まれていない)
注2-重要会計政策:(続)
| 国際財務報告基準 (前報告) | アメリカは会計原則を公認している | |||||||
| 研究開発費 | ||||||||
| 販売とマーケティング費用 | ||||||||
| 一般と行政費用 | ||||||||
| その他の費用(収入) | ( | ) | ||||||
| 営業損失 | ||||||||
| 預金利子収入 | ( | ) | ||||||
| 財務支出,純額 | ||||||||
| 税引き前損失 | ||||||||
| 所得税 | ||||||||
| 純損失合計 | ||||||||
| 列報貨幣への両替による為替利益 | ( | ) | ||||||
| 全面損失総額 | ||||||||
| 国際財務報告基準 (前報告) | アメリカ(Br)公認会計原則 | |||||||
| 研究開発費 | ||||||||
| 販売とマーケティング費用 | ||||||||
| 一般と行政費用 | ||||||||
| その他の費用(収入) | ||||||||
| 営業損失 | ||||||||
| 預金利子収入 | - | ( | ) | |||||
| 財務支出,純額 | ( | ) | ||||||
| 税引き前損失 | ||||||||
| 所得税 | ||||||||
| 純損失合計 | ||||||||
| 列報貨幣への両替による為替利益 | ||||||||
| 全面損失総額 | ||||||||
F-14
Inspira Technologies Oxy B.H.N.Ltd.
財務諸表付記
千ドル(共有 および1株当たりのデータは含まれていない)
注2-重要会計政策:(続)
B. 使用推定数:
米国公認会計原則に基づいて財務諸表を作成することは、報告期間内に報告された資産および負債金額、財務諸表日の開示または資産および負債および報告の費用金額に影響を与えるために、管理層に推定および仮定を要求する。
このような推定および仮定に制約されている項目には,
| ● | 株の報酬に基づいて |
| ● | 公正価値財務負債 |
| ● | 負債の確認、計量、開示 |
| ● | 賃貸負債の金利を測定するために使用される。 |
財務諸表の発行日まで、当社は、その資産または負債の帳簿価値を修正するために、その更新推定、判断、または が必要な重大な特定のイベントまたは状況があることを知りません。新しいイベントの発生やより多くの情報の取得に伴い、これらの見積もりは変化する可能性があり、一度知ったら財務諸表で確認します。実際の結果はこれらの見積もりとは異なる可能性があり,どのような違いも会社の財務諸表に大きな影響を与える可能性がある。
C. 外貨?外貨
会社運営を行う主な経済環境の通貨はドル(“ドル”)である。同社の資金と期待のbr収入は主にドルで計算されている。したがって、会社の本位貨幣はドルです。
最初にドル建ての取引と残高はその元の金額に記載されています。非ドル通貨の残高はそれぞれ非通貨残高と通貨残高の過去の為替レートと現在の為替レートを用いてドルに換算される。非ドル取引および損益表の他の項目(以下に示す )については、(I)取引である取引日の為替レートまたは平均レート、 および(Ii)他の項目(減価償却や償却などの非貨幣貸借対照表項目から)--履歴レートが使用される。貨幣取引損益は適宜財務費用(収入)純額に列報する。当社の本位貨幣はドルです
D.財産、工場、設備
財産と設備はコストに応じて列記する.減価償却 は資産の推定耐用年数から直線法で計算される。
| % | ||||
| コンピューター | ||||
| 現像装置 | ||||
| 家具と事務設備 | ||||
| 賃借権改善 | ||||
F-15
Inspira Technologies Oxy B.H.N.Ltd.
財務諸表付記
千ドル(共有 および1株当たりのデータは含まれていない)
注2-重要会計政策:(続)
E. 借約
当社は,この日までのすべてのレンタルスケジュールに対して会計基準更新 (“ASU”)2016−02,レンタル(テーマ842)(“ASU 2016−02”)を実施し,修正された遡及方法 を採用した。同社はオフィススペースや車両をレンタルする形でレンタルしている。
賃貸定義に適合する手配は、経営的または融資的賃貸に分類され、貸借対照表に使用権資産と賃貸負債 として記録され、計算方法は、レンタル中の暗黙的な金利またはbr社の増額借入金利に従ってレンタル期間内の固定賃貸支払いを割引する。賃貸負債は期ごとに利息を増加させ、支払いを減少させ、使用権資産はレンタル期間内に償却する。
賃貸負債は、残りの賃貸支払いの現在値
で計量し、当社の逓増借款金利を用いて割引します。適用した加重平均金利
は
経営性賃貸では、賃貸負債の利息と使用権資産の償却により、賃貸期間内の賃貸料が直線的に増加している。可変レンタル料金 は発生時に記録します。
F. 研究開発コスト。
研究開発費 は主に給与明細、給与明細関連費用、下請け業者と材料を含む。コストは発生時に費用を計上する。
G.政府支出
同社はIIAから承認された研究·開発プロジェクトの特許権使用料贈与を取得した。イスラエルの法律によると、このような贈与を用いて開発された製品やサービスの収入の特許権使用料はイスラエル政府に支払われなければならない。
1999年1月1日以降に承認された計画で受け取った贈与が支払うべき特許権使用料に基づき、ドル預金に適用されるロンドン銀行間同業借り換え金利(LIBOR)の年利 でドルにリンクした贈与総価値の利息を受け取る。2021年9月、年利決定を担当するイスラエル銀行は、2024年1月にドルローンの年間金利がLIBOR金利にリンクする保証のある隔夜融資金利(SOFR)に置き換えられることを規定する指令を発表した。各列報期間中に受け取って収入に記入した贈与金額を開示しなければならない。研究と開発贈呈は,関連研究と開発費用の相殺としてbr経営報告書に記載されている。会社は指定された料率でこのような贈与に関する印税を支払うことを要求されており、最高でこのような贈与のドルにリンクした総金額を超えない。
H.財務収入と支出。
財務収入は預金利息から構成され、財務支出は信用を優先的に保証する利息、銀行手数料と純貨幣為替レート差からなる。
F-16
Inspira Technologies Oxy B.H.N.Ltd.
財務諸表付記
千ドル(共有 および1株当たりのデータは含まれていない)
注2-重要会計政策:(続)
I.当期税額
現在の税金負債brは、報告日までに公布または実質的に公布された税率と税法、および例年の税項に関連する必要な調整 に基づいて計量される。当社は繰越赤字でいかなる税務責任も負いません。
J. 株式に基づく報酬。
株式の補償 が従業員、取締役および下請け業者の購入権または制限された株式単位に関連する費用(“RSU”)に基づいて、その公正価値によって確認され、この公正価値は、関連普通株の公正価値に基づいており、この公正価値は、br級帰属方法を採用した非最低行使価格に基づく関連普通株の公正価値である。
当社は、付与日の推定公正価値に基づいて、従業員に株式に基づく奨励金を付与する補償費用を確認します。報酬の補償コストは必要なサービス期間内に を確認し,授権期間とほぼ同じである.株式ベースの報酬には、研究開発、販売、マーケティング、および一般的および管理費用が含まれる。株式贈与の喪失は発生したことが確認された。
すべての非従業員に株式オプション或いは他の権益ツールを発行して当社が受信した商品或いはサービスの代価として、発行済み権益ツールの公正価値 に従って入金する。
K. 株式証明書
会社はその融資活動または補償手配の一部として株式承認証を発行する。権利証は、所有者が所定の使用価格で指定数の自社普通株を購入する権利を有するデリバティブ金融商品である。当社が発行する引受権証には、満期日、行権価格、条件を含む様々な条項がある可能性があります。
当社は特定の条項と条件に基づいて、会計基準に基づいて(“ASC”) 815派生ツール及びヘッジを編纂し、株式証明書を発行時の権益或いは負債によって分類する。権証がASC 815−40に要約された持分分類基準に適合する場合、株式として分類される。 でなければ、権証は負債に分類される。
L. 重症度
イスラエル労働法は一般的に従業員が解雇されたり、いくつかの他の場合に雇用を終了した場合に解散費を支払うことを要求する。当社の退職金と解散費は主に保険証書で保証します。1963年イスラエル“解散費補償法”第14節(“第14節”)によると、同社の従業員は月ごとに預金を受け取る権利があり、料率は
M. 1株当たり基本損失と希釈損失
1株当たり基本及び希薄損失は、当社株主が占めるべき損失を財政年度内に発行された普通株の加重平均で計算し、本財政年度に発行された普通株を調整した後(適用すれば)。
F-17
Inspira Technologies Oxy B.H.N.Ltd.
財務諸表付記
千ドル(共有 および1株当たりのデータは含まれていない)
注2-重要会計政策: (続)
N.公正価値計測
当社は財務会計基準委員会(“FASB”)、ASC 820、公正価値計量と開示(“ASC 820”)に基づいて公正価値を計量と開示する。ASC 820は公正価値を定義し、公正価値計量枠組みを構築し、公正価値計量方法について指導を提供し、公正価値計量に関する開示を拡大した。公正価値は、計量日に市場参加者間の秩序ある取引において資産を売却するか、または移転負債を支払うことによって受信された金額を表す脱退価格である。したがって、公正価値は市場に基づく計量であり、資産または負債の定価のために市場参加者が使用する仮定に基づいて決定されるべきである。このような仮定を考慮する基礎として,公正価値を計測する際に用いる投入の優先順位を以下のようにする三級公正価値クラスが存在する
レベル1-測定日までに会社がアクセスする能力がある同じ資産または負債について、未調整オファー をアクティブ市場で提供します。
第2レベル-定価入力とは、資産または負債が直接観察されるか、または観察可能な市場データとの証左によって間接的に観察されることができる活発な市場上のオファーを意味する。
第3級-非金融資産又は負債の定価投入は観察できず、計量日に非金融資産又は負債の市場活動が少ない(あれば)場合にのみ使用する。公正な価値を決定するための投入は管理職が重大な判断や推定をする必要がある。第3レベル投入は、公正価値階層構造における最低優先度とみなされる。
このような階層構造は,公正な価値を決定する際に観察可能な市場データを使用し,観察できない投入を最大限に削減することが求められている.
現金の公正価値はその需要価値を基礎とし、この価値はその帳簿価値に等しい。さらに、これらのツールの短期的な性質のため、他のすべての短期通貨資産および負債の帳簿価値は、その公正価値に等しいと推定される。
O. 信用リスク集中
同社は有名なイスラエル銀行とアメリカに本部を置く銀行に一定の現金残高を持っている。
当社の運営費は主に新イスラエルシェケル(“新シェケル”)で計算されているため、外貨リスクの影響を受けている。
P. 現金と現金等価物
現金等価物は流動性の高い投資 であり、いつでも現金に変換することができ、通常原始期限は3ヶ月以下である購入日は、引き出しや使用制限を受けず、いつでも既知の金額の現金に両替することができます。
制限されたbr現金には、リース契約によって契約上銀行保証に制限された資金が含まれる。会社は貸借対照表に限定的な現金を現金と現金等価物と分けて列挙している期限が
ヶ月以上、1年未満で制限されていない銀行預金は、短期預金に入れます。この等預金は市価に近いコストで入金される.2022年12月31日、2023年12月31日現在、会社の短期預金金額は
ドルです
F-18
Inspira Technologies Oxy B.H.N.Ltd.
財務諸表付記
千ドル(共有 および1株当たりのデータは含まれていない)
注2-重要会計政策: (続)
Q: 細分化市場情報
会社 は単一の運営と報告可能な部門を持っている。会社の最高経営決定者(“CODM”)は最高経営責任者であり、添付されている財務諸表の陳述と一致する財務データに基づいてその業務パフォーマンスを評価し、運営決定を行い、財務業績を評価し、資源を分配する。
R. 新しい会計宣言
会計 2023年に採用した基準
ASU 2023-03
2023年7月、米国財務会計基準委員会はASU 2023-03を発表し、米国証券取引委員会(“米国証券取引委員会”)会計基準の複数の段落を修正し、米国証券取引委員会従業員会計公告第120号の発表を主に反映する。米国会計基準第2023−03号,“財務諸表列報 (主題205),損益表−報告包括収益(主題220),負債と持分の区別(主題480),持分 (主題505)と報酬−株式報酬(主題718):米国証券取引委員会従業員会計公告 第120号による米国証券取引委員会段落の改正により、米国証券取引委員会従業員の2022年3月24日の企業投資信託基金会議における公告、及び従業員会計公告テーマ6.B、会計シリーズ発行 280-規則S-X:普通株の損益に適用される”ASU 2023-03米国証券取引委員会従業員公告第120号米国証券取引委員会従業員会計公告に基づいて米国証券取引委員会従業員会計基準を改訂する2022年3月24日の会議では、新興問題ワーキンググループ(“EITF”) 会議;およびスタッフ会計公報テーマ6.B、会計シリーズ第280版である法規S-Xの全面改正:普通株の収益または損失 に適用される。このような更新は直ちに施行され、私たちの財務諸表に実質的な影響を与えない。
2022年6月、FASBはASU 2022-03、公正価値計量(テーマ820)、“契約販売制限された持分証券の公正価値計量”を発表し、株式証券販売に対する契約制限が証券 会計単位の一部とみなされないことを明らかにしたため、公正価値を計量する際には考慮しない。さらに、これらの制限は、別個の課金単位として確認および測定されてはならない。このような制限に関する開示もまた必要だ。この改正案は,2023年12月15日以降に開始される財政年度と,当該等の財政年度内の移行期間(予想ベース)に適用される。同社はASU 2022-03がその財務諸表や関連開示に実質的な影響を与えないと予想している
会計 は発表されましたが採用されていない公告
2023年11月、FASBはASU 2023-07、支部報告(テーマ280):報告可能支部開示の改善を発表した。本ASUは,公開されているbr}エンティティの支部開示を拡大し,定期的にCODMに提供される重大な分部費用の開示と,報告ごとの支部損益計測に含まれる 他の支部項目の金額と構成説明, および対応報告分部の損益と資産の中期開示を要求している。単一の報告可能部分を有するパブリックエンティティについても、ASU 2023−07でのすべての開示要件が必要である。ASUの改正案は,2023年12月15日以降の財政年度と2024年12月15日以降の財政年度内の移行期間内にすべての公共実体に対して有効であり,早期採用を許可している。私たちは現在この声明が私たちの財務諸表に及ぼす影響を評価している。
F-19
Inspira Technologies Oxy B.H.N.Ltd.
財務諸表付記
千ドル(共有 および1株当たりのデータは含まれていない)
注2-重要会計政策: (続)
FASBは、2023-08、無形資産-営業権および他の暗号化資産(サブトピック350-60):暗号化資産の会計および開示 を発表し、いくつかの暗号化資産の会計および開示要件を含む。本ASUは、エンティティがその後、特定の暗号化資産を公正な価値で計量し、公正な価値の変化が各報告期間の純収入に記録されることを要求する。さらに、エンティティは、いくつかの暗号化資産の保有量に関する追加的な開示を提供することを要求される。ASUの修正案 は、資産を保有するすべてのエンティティに適用され、これらのエンティティが保有する資産は、2024年12月15日以降の会計年度(当該年度内の移行期間を含む)がある範囲基準を満たしている。中期と年度はいずれも早期採用を許可する.1つのエンティティが移行期間内に修正案を通過する場合には、その移行期間を含む財政年度の開始時に修正案を採択しなければならない。私たちはこの声明が私たちの財務諸表に実質的な影響を与えないと予想する。
FASBは、2023-09、所得税(主題740):改良所得税開示を発表した。本ASUによれば、公共エンティティは、毎年(1)税率調整における特定のカテゴリを開示し、(2)量子化閾値に適合する調整項目に追加情報を提供しなければならない(これらの調整項目の影響が、税前収入または損失に適用される法定所得税率を乗じて計算された金額の5%以上である場合)。本ASU修正案は、主題740(所得税)に制約されたすべてのエンティティ に適用され、2024年12月15日以降の年間期間において、早期採用が許可される。私たちは現在この声明が私たちに開示した影響を評価している。
注3-預金:
当社の預金には三種類の期限が三ヶ月以上ありますが一年未満の短期銀行預金が含まれています。預金はドル建てで、年単位で利息を計算します。 当社が短期預金を持っている年度内に、稼いだ利息は財務収入と記入され、純額は営業報告書に計上される。
2023年12月31日現在、会社はLeumi銀行(イスラエル)にドル預金を持っており、金額は$
2022年12月31日までの会社預金総額は$
注4--その他の流動資産:
| 2023年12月31日 | 十二月三十一日 2022 | |||||||
| 前払い費用 | ||||||||
| 大学.学校 | ||||||||
| 制限現金 | ||||||||
| 他の人は | ||||||||
| 合計する | ||||||||
F-20
Inspira Technologies Oxy B.H.N.Ltd.
財務諸表付記
千ドル(共有 および1株当たりのデータは含まれていない)
注5--財産と設備、純額:
| コンピューター | 賃借権改善 | 発展する 装備 | 家具.家具 そしてオフィスは 装備 | 合計する | ||||||||||||||||
| コスト | ||||||||||||||||||||
| 2023年1月1日 | ||||||||||||||||||||
| 足し算 | ||||||||||||||||||||
| 2023年12月31日 | ||||||||||||||||||||
| 減価償却累計 | ||||||||||||||||||||
| 2023年1月1日 | ||||||||||||||||||||
| 減価償却 | ||||||||||||||||||||
| 2023年12月31日 | ||||||||||||||||||||
| 帳簿純価値: | ||||||||||||||||||||
| 2023年12月31日まで | ||||||||||||||||||||
| * | 千ドル以下です |
| コンピューター | 賃借権 改善 | 発展する 装備 | 家具.家具 そしてオフィスは 装備 | 合計する | ||||||||||||||||
| コスト | ||||||||||||||||||||
| 2022年1月1日 | ||||||||||||||||||||
| 足し算 | ||||||||||||||||||||
| 2022年12月31日 | ||||||||||||||||||||
| 減価償却累計 | ||||||||||||||||||||
| 2022年1月1日 | ||||||||||||||||||||
| 減価償却 | ||||||||||||||||||||
| 2022年12月31日 | ||||||||||||||||||||
| 帳簿純価値: | ||||||||||||||||||||
| 2022年12月31日まで | ||||||||||||||||||||
| * | 千ドル以下です |
F-21
Inspira Technologies Oxy B.H.N.Ltd.
財務諸表付記
千ドル(共有 および1株当たりのデータは含まれていない)
備考6--その他の売掛金:
| 2023年12月31日 | 十二月三十一日 2022 | |||||||
| 従業員の賃金及び負債に関する | ||||||||
| 関連先 | ||||||||
| 費用を計算する | ||||||||
| 他にも | ||||||||
| 合計する | ||||||||
付記7--支払引受及び又は事項
| A. | IIAに支払われる特許使用料: |
2019年9月、IIAは会社の製造能力のアップグレードを支援する申請を承認し、総予算は新シェケルです
IIAとの合意により、同社は…を支払う
IIAは2023年10月に同社の別の開発プロジェクトへの支援を承認し、総予算は新シェケルとなった
研究·開発費から差し引かれた研究·開発助成金はゼロ,#ドルである
F-22
Inspira Technologies Oxy B.H.N.Ltd.
財務諸表付記
千ドル(共有 および1株当たりのデータは含まれていない)
付記7--支払引受及び又は事項 (続)
| B. | レンタル約束- 経営レンタル: |
2022年8月、当社はイスラエルのラアナナ施設の賃貸契約を締結した。レンタル契約は2021年9月1日から69ヶ月間、レンタルが満3ヶ月後にレンタルと関連費用の支払いを開始します。同社はレンタル期間を短縮し、45ヶ月のレンタル料を完了した後、一定額の新しいシェケルを支払って賃貸契約を終了する権利がある
レンタルに関連する総費用は$
使用権資産と賃貸負債は、最初にリース支払いの現在値で計量され、レンタルに隠れている金利を用いて割引 を行い、その金利が容易に決定できなければ、リース支払いの現在値を決定する日の情報に基づいて、会社の逓増借入金金利を割引する。当社の増額借入金金利は、賃貸資産のある経済環境下で類似条項や支払いの金利に近いと推定されています。
十二月三十一日 2023 | 2022年12月31日 | |||||||
| 賃貸負債を経営し、流動 | ||||||||
| 長期経営賃貸負債 | ||||||||
| リース負債総額を経営する | ||||||||
| 残りのレンタル期間の加重平均値 | ||||||||
| 加重平均割引率-レンタル経営 | % | % | ||||||
F-23
Inspira Technologies Oxy B.H.N.Ltd.
財務諸表付記
千ドル(共有 および1株当たりのデータは含まれていない)
付記7--支払引受及び又は事項 (続)
| 2023年12月31日 | ||||
| 2024 | ||||
| 2025 | ||||
| 2026 | ||||
| 2027 | ||||
| 未割引賃貸支払総額 | ||||
| 差し引く:利息* | ( | ) | ||
| 賃貸負債現在価値 | ||||
| * |
| C. | 法律クレーム |
正常業務過程では、様々な法的クレームやその他の事項 が発生する可能性がある。経営陣は、このようなことが生じる可能性のあるいかなる責任も、当社の2023年12月31日までおよび2022年12月31日までの年度の経営業績や財務状況に重大な悪影響を与えないと信じている。
2021年12月12日、会社はUdi Nussinovitch博士との雇用協定 を終了し、Udi Nussinovitch博士は会社の創業者の一人であり、2018年3月から会社の首席科学官を務めた。2022年2月24日、当社は、さん誠実さと株主および元会社の役員としての彼の受託責任に違反するNussinovitchを起訴します。当社は、2022年11月9日に、Nussinovitchさんからの苦情の通知と、2022年11月8日にイスラエルのテルアビブ地域労働裁判所にクレームを受け取りました。Nussinovitchさんは、彼が小株主であるため、2021年12月17日(金)に開催される第3回特別株主総会にいくつかの欠陥があるとして会社を告発しました。また、ヌーシノビッチさんは労使紛争への尊重から、普通株式の賠償と発行を求めている。2023年7月19日、地域労働裁判所は一部の公聴会を開催し、裁判所は原告が地域裁判所に事件を裁く前に、訴訟手続きを一時停止し、自分の立場を提出することを求めた。
2024年1月21日に地域裁判所で予審が行われた。裁判期間中,裁判所は双方に裁判外手配や調停による事件解決の可能性を考慮することを提案した。双方は調停を行うことに同意した.
本財務諸表の日まで、当社はクレームが当社の支払いにつながらないと信じています。
F-24
Inspira Technologies Oxy B.H.N.Ltd.
財務諸表付記
千ドル(共有 および1株当たりのデータは含まれていない)
付記8--公正価値で計算された財務負債:
十二月三十一日 2023 | 2022年12月31日 | |||||||
| 財務負債(1) | ||||||||
| 非流通権証(2) | ||||||||
| 合計する | ||||||||
| 1. | 財務負債 |
その会社は以下の費用を支払うことに同意した
2023年12月31日と2022年12月31日までの財務負債公正価値は$
| 2. | 個人株式証明書 |
2023年12月26日に、当社は購入契約(付記1及び付記9)を締結し、これにより未登録株式権証を発行し、合算を購入する
協定に規定されている条項によると、株式証明書にはキャッシュレス行使メカニズムが含まれている。
権証には義務が生じる可能性があり,可変投入を含むブラック·スコアモデルの公正価値により,ファンダメンタル取引で投資家に現金を移行させる。
そこで、当社は株式証明書を公正価値に応じて計量し、損益で財務支出や収入を確認する金融負債ツールとして入金する。
発行日
及び2023年12月31日までの権証公正価値は
発行日 まで、私募株式証公正価値に使用する主な投入は、:
| ● | 無リスク金利 |
| ● | 予想変動率 |
| ● | 期待配当収益率は |
| ● | 株式証明書の予想期限- |
2023年12月31日までの私募株式公開価値で使用される重要な投入には、以下のようなものが含まれる
| ● | 無リスク金利 |
| ● | 予想変動率 |
| ● | 期待配当収益率は |
| ● | 株式証明書の予想期限- |
F-25
Inspira Technologies Oxy B.H.N.Ltd.
財務諸表付記
千ドル(共有 および1株当たりのデータは含まれていない)
注9-株主権益(赤字):
| 12月31日までの株式数は | 現在の株式数 十二月三十一日 | |||||||||||||||
| 2023 | 2022 | |||||||||||||||
| 授権 | 発行済みと未償還 | 授権 | 発行済みと未償還 | |||||||||||||
| 普通株 | ||||||||||||||||
当社が2018年2月に登録設立から初公募まで、当社は以下の普通株を発行しました:(I)合算
2020年には同社が共同発行しました
2021年3月18日、会社株主
が承認した
2021年6月1日、会社株主brは、会社の株式構造(許可および発行されたものを含む)に対する修正案を承認し、普通株式の額面を廃止し、同時に追加の実施を実施した
2021年6月1日、会社の株主
は会社の株式構造(授権と発行)の修正を許可し、会社株の額面
を廃止し、1株当たりの額面を新シェケルの普通株とした
2021年6月1日、会社の株主は会社の法定株式を20%に増やすことを許可した
2021年7月16日、会社はナスダック資本市場での初公募株を完成させ、それに基づいて会社を売却した
初公募後,会社は発行した
当社が初公募から受け取った総収益は約$であった
F-26
Inspira Technologies Oxy B.H.N.Ltd.
財務諸表付記
千ドル(共有 および1株当たりのデータは含まれていない)
注9-株主権益(赤字)(続):
IPOにおける非現金直接費用総額は以下のとおりである:(I)公正価値
非現金支出総額は$
また,会社には非直接費用
があり以下のようになる:(I)現金料金は#ドルである
直接および非直接、現金、および非現金のIPO総支出は、ドルです
利益と損失に割り当てられたIPO費用総額は$
2021年に当社は
を共同発行した
2021年12月17日、会社の株主は会社の法定配当金の増加を許可した
当社は2022年12月31日までに発行します
当社は2023年4月4日、販売代理であるRoth Capital Partners,LLCとbr販売プロトコル(“販売プロトコル”)を締結し、この合意により、当社は時々販売エージェントを介して市場のATM(“ATM”)に基づいて普通株を発売·販売することができる。
は2023年の間、当社は
2023年12月26日、当社は登録直接発売を完了し、これにより、当社は(I)を販売します
前払い助成権は取引当日および翌日に全数行使され,行使価格は$となる
当社が登録直接発売から得た総収益は約#ドルである
会社はbrプロトコルで配給エージェントに発行された数に相当する
F-27
Inspira Technologies Oxy B.H.N.Ltd.
財務諸表付記
千ドル(共有 および1株当たりのデータは含まれていない)
注9-株主権益(赤字) (続):
当該等現金及び非現金発行コストは、登録直接発売された負債と権益比率に基づいて、発行費用及び追加実収資本減少額に比例して入金される。
当社は2023年12月31日までに発行します
| B. | 権利証備蓄--構成と変動: |
| 1. |
| 手令の数 | 加重平均行権値 | 加重平均残契約期間 (単位:年) | 骨材 内在的価値 | |||||||||||||
| 2022年12月31日現在の残高 | ||||||||||||||||
| 発表されました | ||||||||||||||||
| 鍛えられた | ||||||||||||||||
| 没収される | ||||||||||||||||
| 期限が切れる | ||||||||||||||||
| 2023年12月31日現在の残高 | ||||||||||||||||
| 2. |
行権価格 | 未弁済持分証 時点で 十二月三十一日 | 期日まで | 骨材 固有の 価値がある | |||||||||
F-28
Inspira Technologies Oxy B.H.N.Ltd.
財務諸表付記
千ドル(共有 および1株当たりのデータは含まれていない)
注9-株主権益(赤字)(続):
C.1株当たり損失:
| 2013年12月31日までの年度 2023 | 現在までの年度 十二月三十一日 2022 | 現在までの年度 十二月三十一日 2021 | ||||||||||
| 当期損失 | ||||||||||||
| 普通株式総数 | ||||||||||||
| 普通株式加重平均 | ||||||||||||
| ( | ) | ( | ) | ( | ) | |||||||
付記10--研究と開発費:
| 2013年12月31日までの年度 2023 | 現在までの年度 十二月三十一日 2022 | 現在までの年度 十二月三十一日 2021 | ||||||||||
| 賃金および関連費用 | ||||||||||||
| 材料及び関連費用 | ||||||||||||
| 株式ベースの支払い | ||||||||||||
| 下請け業者 | ||||||||||||
| 減価償却 | ||||||||||||
| IIA参加 | ( | ) | ||||||||||
| 他にも | ||||||||||||
| 合計する | ||||||||||||
注11--販売とマーケティング費用:
| 2013年12月31日までの年度 2023 | 現在までの年度 十二月三十一日 2022 | 現在までの年度 十二月三十一日 2021 | ||||||||||
| 賃金および関連費用 | ||||||||||||
| 株式支払 | ||||||||||||
| 他にも | ||||||||||||
F-29
Inspira Technologies Oxy B.H.N.Ltd.
財務諸表付記
千ドル(共有 および1株当たりのデータは含まれていない)
付記12--一般と行政費用:
| 2013年12月31日までの年度 2023 | 現在までの年度 十二月三十一日 2022 | 現在までの年度 十二月三十一日 2021 | ||||||||||
| 専門費 | ||||||||||||
| 賃金および関連費用 | ||||||||||||
| 役員の料金基準 | ||||||||||||
| ナスダックの発売関連費用 | ||||||||||||
| 拠出費用 | ||||||||||||
| 株式支払 | ||||||||||||
| 保険料 | ||||||||||||
| 事務室メンテナンス | ||||||||||||
| 減価償却 | ||||||||||||
| 海外旅行に行く | ||||||||||||
| 他の人は | ||||||||||||
| 合計する | ||||||||||||
付記13--財務(収入)と支出:
| 2013年12月31日までの年度 2023 | 現在までの年度 十二月三十一日 2022 | 現在までの年度 十二月三十一日 2021 | ||||||||||
| 公正価値による損益による金融負債の見直し | ( | ) | ( | ) | ||||||||
| 金融負債利息 | ||||||||||||
| 外貨取引収入 | ( | ) | ||||||||||
| 賃貸負債に関する財務費用 | ( | ) | ||||||||||
| 他の人は | ( | ) | ||||||||||
| 費用(収入)合計 | ( | ) | ||||||||||
付記14--所得税:
| A. | 所得税: |
イスラエルの会社の税率は
| B. | 純営業損失繰越: |
当社の2023年12月31日までの繰り越し税額損失は約$
F-30
Inspira Technologies Oxy B.H.N.Ltd.
財務諸表付記
千ドル(共有 および1株当たりのデータは含まれていない)
注14--所得税:(続)
| 2023年12月31日 | 十二月三十一日 2022 | |||||||
| 繰延税金資産: | ||||||||
| 純営業損失が繰り越す | ||||||||
| 費用を計算する | ||||||||
| 研究開発資本化 | ||||||||
| 2021年の拠出コスト | ||||||||
| 2023年の拠出コスト | ||||||||
| リース負債を経営する | ||||||||
| 繰延税金資産総額 | ||||||||
| 推定免税額 | ( | ) | ( | |||||
| 繰延税金負債: | ||||||||
| 繰延税金負債総額 | ||||||||
| 繰延税金純額 | ||||||||
| C. | 理論税: |
| 2013年12月31日までの年度 2023 | 現在までの年度 十二月三十一日 2022 | 現在までの年度 十二月三十一日 2021 | ||||||||||
| 税引き前損失 | ( | ) | ( | ) | ( | ) | ||||||
| 法定税率を適用した理論税収控除: | ( | ) | ( | ) | ( | ) | ||||||
| 不許可費用 | ( | ) | ( | ) | ( | ) | ||||||
| 繰延納税資産の一時的な差異と税収損失は確認されていない | ( | ) | ( | ) | ( | ) | ||||||
| 所得税割引 | ||||||||||||
F-31
Inspira Technologies Oxy B.H.N.Ltd.
財務諸表付記
千ドル(共有 および1株当たりのデータは含まれていない)
注15-株式支払:
2019年12月、当社は株式 オプション計画(“2019年計画”)を策定しました。
これらの選択権はイスラエル税務条例第102節に基づいて従業員に付与され、この条例は従業員の支払いを許可します
この2019年計画によると、各購入株式またはRSUは自社普通株として行使することができる。“2019年計画”によると発行可能なオプションの最長期限は
以下は、2021年12月31日までの年度と2022年12月31日までの年度内に従業員、取締役会メンバー、非従業員と行う重要株式オプションとRSU取引である
2021年2月21日、会社取締役会は非流通株引受権の付与を許可した
2021年3月16日、会社取締役会が許可
2021年8月12日、会社取締役会は、この計画下のオプションプールを追加することを決定した
2021年11月2日会社取締役会は
2021年11月2日、会社取締役会が許可
2022年3月24日会社取締役会は
2022年3月24日、会社取締役会は授与を許可した
2022年4月6日、会社取締役会は授与を許可した
2022年5月19日、会社取締役会は授与を許可した
F-32
Inspira Technologies Oxy B.H.N.Ltd.
財務諸表付記
千ドル(共有 および1株当たりのデータは含まれていない)
注15-株式支払(続):
2022年11月22日会社取締役会は
2023年12月31日までの年度内に、株式購入または販売制限株式は授与されていない。
オプションが付与されたすべての公正価値は、会社資産の長期価値をモデル化することを目的としたブラック-スコアモデルを用いて推定された。シミュレーション方法 は,いくつかの仮定が与えられた日に基づいて株式購入の条項や条件,および当社の資本構造とその資産の変動性を考慮することを目的としている.これらの条件には
| (i) | 期待変動率は
|
| (Ii) | 配当率 |
| (Iii) | 予想期限- |
経営陣の仮定によると、評価は独立した評価士の協力の下で行われた。
2023年12月31日までの年間で,会社は従業員,役員,下請け業者に支払われた株式ベースのbr支出を記録しており,金額は$である
2022年12月31日までの年度内に,会社は従業員,役員,下請け業者に支払われた株式ベースのbr支出を記録しており,金額は$である
2021年12月31日までの年間で,会社は従業員,役員,下請け業者に支払われた株式ベースのbr支出を記録しており,金額は$である
| 2023年12月31日までの年度 | 現在までの年度 2022年12月31日 | 現在までの年度 2021年12月31日 | ||||||||||||||||||||||
| オプション数 | 加重平均行権値NIS | オプション数 | 加重平均行権値NIS | 選択肢の数 | *加重平均行権価格NIS | |||||||||||||||||||
| 年初未済債務 | ||||||||||||||||||||||||
| 従業員と役員に改称する | ( | ) | ||||||||||||||||||||||
| 授与する | ||||||||||||||||||||||||
| 鍛えられた | ( | ) | ( | ) | ||||||||||||||||||||
| 没収される | ( | ) | ||||||||||||||||||||||
| 未償還オプション | ||||||||||||||||||||||||
| 行使可能なオプション | ||||||||||||||||||||||||
| 株式ベースの支払費用 | $ | $ | $ | |||||||||||||||||||||
F-33
Inspira Technologies Oxy B.H.N.Ltd.
財務諸表付記
千ドル(共有 および1株当たりのデータは含まれていない)
注15-株式支払(続):
| 2013年12月31日までの年度 2023 | 現在までの年度 十二月三十一日 2022 | 現在までの年度 十二月三十一日 2021 | ||||||||||
| RSU数 | RSU数 | RSU数 | ||||||||||
| 年初未済債務 | ||||||||||||
| 授与する | ||||||||||||
| 既得 | ||||||||||||
| 未完成RSU | ||||||||||||
| RSUは許可されています | ||||||||||||
| 株式ベースの支払費用 | $ | $ | $ | |||||||||
| 現在までの年度 2023年12月31日 | 現在までの年度 2022年12月31日 | 現在までの年度 2021年12月31日 | ||||||||||||||||||||||
| オプション数 | 加重平均行権値NIS | オプション数 | 加重平均行権値NIS | 選択肢の数 | *加重平均行権価格NIS | |||||||||||||||||||
| 年初未済債務 | ||||||||||||||||||||||||
| 従業員と役員に改称する | ||||||||||||||||||||||||
| 授与する | ||||||||||||||||||||||||
| 鍛えられた | ( | ) | ||||||||||||||||||||||
| 没収される | ( | ) | ||||||||||||||||||||||
| 未償還オプション | ||||||||||||||||||||||||
| 行使可能なオプション | ||||||||||||||||||||||||
| 株式ベースの支払費用 | $ | - | $ | - | $ | - | ||||||||||||||||||
| 2013年12月31日までの年度 2023 | 現在までの年度 十二月三十一日 2022 | 現在までの年度 十二月三十一日 2021 | ||||||||||
| RSU数 | RSU数 | RSU数 | ||||||||||
| 年初未済債務 | ||||||||||||
| 授与する | ||||||||||||
| 没収される | ||||||||||||
| 既得 | ||||||||||||
| 未完成RSU | ||||||||||||
| RSUは許可されています | ||||||||||||
| 株式ベースの支払費用 | $ | $ | $ | |||||||||
F-34
Inspira Technologies Oxy B.H.N.Ltd.
財務諸表付記
千ドル(共有 および1株当たりのデータは含まれていない)
注16-関連先:
以下は,関連側との取引である
関係者との取引と残高:
| 1. |
| 2023年12月31日 | 十二月三十一日 2022 | 十二月三十一日 2021 | ||||||||||
| 給与と関連費用−上級職員と役員 | ||||||||||||
| 株式ベースの支払い-上級管理者と役員 | ||||||||||||
| 2. |
| 名前.名前 | 取引性質 | 十二月三十一日 2023 | 十二月三十一日 2022 | |||||||
| 高級乗組員 | ( | ) | ( | ) | ||||||
| 役員.取締役 | ( | ) | ( | ) | ||||||
注17--後続の事件:
2024年1月22日、会社取締役会は授与を許可しました
これらの財務諸表の日から購入可能なオプション
2024年2月5日、会社取締役会は授与を許可した
2024年2月27日、会社取締役会は株式承認証の発行を許可し、最大購入
F-35