AQST-202312310001398733虚像2023会計年度364P 8 YP 8 YP 1 YHttp://Fasb.org/us-GAAP/2023#CostOfGoodsAndServicesSoldHttp://Fasb.org/us-GAAP/2023#LongTermDebtAndCapitalLeaseObligationsP 3 YP 3 Y00013987332023-01-012023-12-3100013987332023-06-30ISO 4217:ドル00013987332024-03-01Xbrli:共有00013987332023-10-012023-12-310001398733Aqst:MarkSchobelMember2023-10-012023-12-310001398733Aqst:MarkSchobelMember2023-12-3100013987332023-12-3100013987332022-12-31ISO 4217:ドルXbrli:共有00013987332022-01-012022-12-310001398733アメリカ-アメリカ公認会計基準:普通株式メンバー2021-12-310001398733US-GAAP:AdditionalPaidInCapitalMembers2021-12-310001398733アメリカ-公認会計基準:前払いメンバーを保留2021-12-3100013987332021-12-310001398733US-GAAP:AdditionalPaidInCapitalMembers2022-01-012022-12-310001398733Aqst:PrivateEquityMemberアメリカ-アメリカ公認会計基準:普通株式メンバー2022-01-012022-12-310001398733US-GAAP:AdditionalPaidInCapitalMembersAqst:PrivateEquityMember2022-01-012022-12-310001398733Aqst:PrivateEquityMember2022-01-012022-12-310001398733アメリカ-アメリカ公認会計基準:普通株式メンバー2022-01-012022-12-310001398733アメリカ-公認会計基準:前払いメンバーを保留2022-01-012022-12-310001398733アメリカ-アメリカ公認会計基準:普通株式メンバー2022-12-310001398733US-GAAP:AdditionalPaidInCapitalMembers2022-12-310001398733アメリカ-公認会計基準:前払いメンバーを保留2022-12-310001398733アメリカ-アメリカ公認会計基準:普通株式メンバー2023-01-012023-12-310001398733US-GAAP:AdditionalPaidInCapitalMembers2023-01-012023-12-310001398733アメリカ-公認会計基準:前払いメンバーを保留2023-01-012023-12-310001398733アメリカ-アメリカ公認会計基準:普通株式メンバー2023-12-310001398733US-GAAP:AdditionalPaidInCapitalMembers2023-12-310001398733アメリカ-公認会計基準:前払いメンバーを保留2023-12-310001398733Aqst:EquityDistributionAgreementメンバ2019-09-112019-09-110001398733Aqst:AtTheMarketOfferingamendmentOneMemberSRT:最大メンバ数2019-09-112019-09-110001398733SRT:最大メンバ数Aqst:EquityDistributionAgreementメンバ2019-09-112019-09-110001398733Aqst:EquityDistributionAgreementメンバ2023-01-012023-12-310001398733Aqst:AtTheMarketOfferingMember2023-01-012023-12-310001398733Aqst:EquityDistributionAgreementメンバ2022-01-012022-12-310001398733Aqst:AtTheMarketOfferingMember2022-01-012022-12-310001398733Aqst:リンカーン公園の合意メンバー2022-04-120001398733Aqst:リンカーン公園の合意メンバーSRT:最大メンバ数2022-04-122022-04-12Xbrli:純0001398733Aqst:リンカーン公園の合意メンバーSRT:最大メンバ数2023-12-310001398733Aqst:リンカーン公園の合意メンバー2022-01-012022-12-310001398733Aqst:リンカーン公園協定はメンバーの共有を約束しました2022-01-012022-12-310001398733Aqst:SecuritiesPurcheAgreementメンバー2022-06-060001398733Aqst:SecuritiesPurcheAgreementメンバー2022-06-062022-06-060001398733AQST:CommonStockWarrantsMember2023-06-142023-06-140001398733Aqst:既存保証メンバー2023-08-010001398733Aqst:新保証メンバー2023-08-010001398733Aqst:既存保証メンバー2023-08-022023-08-020001398733AQST:CommonStockWarrantsMember2023-08-022023-08-020001398733Aqst:既存保証メンバー2023-01-012023-12-310001398733AQST:CommonStockWarrantsMember2023-01-012023-12-310001398733SRT:最小メンバ数2023-01-012023-12-310001398733SRT:最大メンバ数2023-01-012023-12-310001398733アメリカ-GAAP:高齢者の注意事項メンバーAQST:13時5高齢者安全注意事項12028 11月2023-11-010001398733SRT:最小メンバ数2023-11-012023-11-010001398733SRT:最大メンバ数2023-11-012023-11-0100013987332023-11-010001398733米国-GAAP:制限株式単位RSUメンバー2023-01-012023-12-310001398733アメリカ-公認会計基準:公正価値入力レベル2メンバー2023-12-310001398733アメリカ-GAAP:高齢者の注意事項メンバーAqst:十二時五高級セキュリティノード302025年6月2023-12-310001398733Aqst:AtTheMarketOfferingMember2020-11-012023-12-310001398733Aqst:メーカーとサプライヤー収入メンバー2023-01-012023-12-310001398733Aqst:メーカーとサプライヤー収入メンバー2022-01-012022-12-310001398733Aqst:ライセンスと印税収入メンバー2023-01-012023-12-310001398733Aqst:ライセンスと印税収入メンバー2022-01-012022-12-310001398733Aqst:FeesMemberの共同開発と研究2023-01-012023-12-310001398733Aqst:FeesMemberの共同開発と研究2022-01-012022-12-310001398733Aqst:PropretaryProductSalesMember2023-01-012023-12-310001398733Aqst:PropretaryProductSalesMember2022-01-012022-12-310001398733国:アメリカ2023-01-012023-12-310001398733国:アメリカ2022-01-012022-12-310001398733アメリカ-GAAP:非アメリカのメンバー2023-01-012023-12-310001398733アメリカ-GAAP:非アメリカのメンバー2022-01-012022-12-310001398733US-GAAP:顧客集中度リスクメンバー米国-GAAP:SalesRevenueNetMembersAQST:ビジネス開発プロトコルと個人メンバー2023-01-012023-12-310001398733US-GAAP:顧客集中度リスクメンバーAQST:ビジネス開発プロトコルと個人メンバーアメリカ公認会計基準:売掛金メンバー2023-01-012023-12-310001398733US-GAAP:顧客集中度リスクメンバーAQST:ビジネス開発プロトコルとZevraMembersアメリカ公認会計基準:売掛金メンバー2023-01-012023-12-310001398733US-GAAP:顧客集中度リスクメンバー米国-GAAP:SalesRevenueNetMembersAQST:ビジネス開発プロトコルと個人メンバー2022-01-012022-12-310001398733US-GAAP:顧客集中度リスクメンバーAQST:ビジネス開発プロトコルと個人メンバーアメリカ公認会計基準:売掛金メンバー2022-01-012022-12-310001398733AQST:ビジネス開発プロトコルと個人メンバー2023-01-012023-12-310001398733AQST:ビジネス開発プロトコルと個人メンバー2023-03-022023-03-020001398733AQST:ビジネス開発プロトコルと個人メンバー2023-03-020001398733Aqst:個人改訂メンバー2023-03-032023-03-030001398733Aqst:個人と補足合意に達したメンバ2017-09-242019-02-200001398733Aqst:ライセンスと印税収入メンバーAQST:SunovionPharmPharmticalsIncMilestonesとライセンス契約を結んだメンバー2016-04-012016-04-010001398733AQST:ライセンスプロトコルとSunovionPharmPharmticalsIncMember2023-10-232023-10-230001398733AQST:ライセンスプロトコルとSunovionPharmPharmticalsIncUpFrontMember2023-10-232023-10-230001398733AQST:SunovionPharmPharmticalsIncMilestonesとライセンス契約を結んだメンバー2023-10-232023-10-230001398733Aqst:貨幣化プロトコルメンバAQST:マラソンで山甲を着て皇室メンバー2020-11-032020-11-030001398733Aqst:貨幣化プロトコルメンバAQST:マラソンで山甲を着て皇室メンバー2020-11-032020-12-310001398733Aqst:貨幣化プロトコルメンバAQST:マラソンで山甲を着て皇室メンバー2020-11-032022-12-310001398733SRT:最大メンバ数AQST:マラソンで山甲を着て皇室メンバー2020-11-032020-11-030001398733Aqst:ライセンスと印税収入メンバーAqst:Agreement ToTerminateCLAWithKemPharmMember2023-01-012023-12-310001398733Aqst:Haisco PharmPharmticalGroupCoLtd.前置報酬メンバー2022-09-3000013987332022-05-17Utr:D00013987332022-05-172022-05-17Aqst:分割払い0001398733第1四半期:最初の7ヶ月のメンバー2022-05-172022-05-170001398733Aqst:8ヶ月メンバー2022-05-172022-05-170001398733AQST:9~18ヶ月2022-05-172022-05-170001398733AQST:AtnahsPharmaUKLimitedMemberAqst:ライセンス供給プロトコルのメンバー2022-09-262022-09-260001398733Aqst:ライセンス供給プロトコルのメンバーAqst:AtnahsPharmaUKLimitedAmendedAgreementメンバー2023-03-272023-03-270001398733Aqst:AssertioHoldingsIncMember2022-10-262022-10-260001398733Aqst:十二時五高級セキュリティノード302025年6月2019-07-150001398733Aqst:SecuritiesPurcheAgreementメンバー2022-06-012022-06-300001398733SRT:最小メンバ数アメリカ-GAAP:機械とデバイスのメンバー2023-12-310001398733SRT:最大メンバ数アメリカ-GAAP:機械とデバイスのメンバー2023-12-310001398733アメリカ-GAAP:機械とデバイスのメンバー2023-12-310001398733アメリカ-GAAP:機械とデバイスのメンバー2022-12-310001398733SRT:最小メンバ数アメリカ-GAAP:家具と固定機器のメンバー2023-12-310001398733SRT:最大メンバ数アメリカ-GAAP:家具と固定機器のメンバー2023-12-310001398733アメリカ-GAAP:家具と固定機器のメンバー2023-12-310001398733アメリカ-GAAP:家具と固定機器のメンバー2022-12-310001398733アメリカ-公認会計基準:リース改善メンバー2023-12-310001398733アメリカ-公認会計基準:リース改善メンバー2022-12-310001398733SRT:最小メンバ数AQST:ComputerNetworkEquipmentAndSoftwareMember2023-12-310001398733SRT:最大メンバ数AQST:ComputerNetworkEquipmentAndSoftwareMember2023-12-310001398733AQST:ComputerNetworkEquipmentAndSoftwareMember2023-12-310001398733AQST:ComputerNetworkEquipmentAndSoftwareMember2022-12-310001398733アメリカ-アメリカ公認会計基準:建設中のメンバー2023-12-310001398733アメリカ-アメリカ公認会計基準:建設中のメンバー2022-12-31Aqst:レンタル0001398733アメリカ-公認会計基準:会計基準更新201602メンバーSRT:最小メンバ数2023-12-310001398733SRT:最大メンバ数2023-12-310001398733US-GAAP:技術ベース無形資産メンバ2023-12-310001398733US-GAAP:技術ベース無形資産メンバ2022-12-310001398733米国-GAAP:特許メンバー2023-12-310001398733米国-GAAP:特許メンバー2022-12-310001398733AQST:ライセンスプロトコルとSunovionPharmPharmticalsIncMemberUS-GAAP:RoyaltyMember2020-04-012020-06-30Aqst:印税_支払い0001398733AQST:ライセンスプロトコルとSunovionPharmPharmticalsIncMember2023-12-310001398733AQST:ライセンスプロトコルとSunovionPharmPharmticalsIncMember2023-01-012023-12-31Aqst:支払い0001398733アメリカ-GAAP:高齢者の注意事項メンバーAqst:十二時五高級セキュリティノード302025年6月2019-07-150001398733SRT:最大メンバ数Aqst:十二時五高級セキュリティノード302025年6月2019-07-1500013987332019-07-1500013987332019-07-152019-07-150001398733アメリカ-GAAP:高齢者の注意事項メンバーAqst:十二時五高級セキュリティノード302025年6月2020-11-032020-11-030001398733アメリカ-GAAP:高齢者の注意事項メンバーAqst:十二時五高級セキュリティノード302025年6月2020-11-030001398733アメリカ-GAAP:高齢者の注意事項メンバー2020-11-032020-11-030001398733アメリカ-GAAP:高齢者の注意事項メンバーAqst:十二時五高級セキュリティノード302025年6月2020-12-310001398733アメリカ-GAAP:高齢者の注意事項メンバーAqst:十二時五高級セキュリティノード302025年6月2023-01-012023-12-310001398733SRT:最大メンバ数AQST:マラソンで山甲を着て皇室メンバー2023-01-012023-12-310001398733Aqst:十二時五高級セキュリティノード302025年6月米国-GAAP:PutOptionMembers2022-12-310001398733Aqst:十二時五高級セキュリティノード302025年6月2023-01-012023-12-310001398733Aqst:十二時五高級セキュリティノード302025年6月2021-08-060001398733アメリカ-GAAP:高齢者の注意事項メンバーAqst:十二時五高級セキュリティノード302025年6月2022-05-130001398733アメリカ-GAAP:高齢者の注意事項メンバーAqst:十二時五高級セキュリティノード302025年6月2022-05-152023-02-280001398733アメリカ-GAAP:高齢者の注意事項メンバーAqst:十二時五高級セキュリティノード302025年6月2023-02-012023-02-280001398733SRT:最小メンバ数アメリカ-GAAP:高齢者の注意事項メンバーAqst:十二時五高級セキュリティノード302025年6月2019-07-152019-07-150001398733アメリカ-GAAP:高齢者の注意事項メンバーSRT:最大メンバ数Aqst:十二時五高級セキュリティノード302025年6月2019-07-152019-07-150001398733アメリカ-GAAP:高齢者の注意事項メンバーAqst:十二時五高級セキュリティノード302025年6月2019-07-152019-07-1500013987332022-12-16Aqst:通知0001398733Aqst:十二時五高級セキュリティノード302025年6月2022-11-040001398733Aqst:十二時五高級セキュリティノード302025年6月2022-12-160001398733アメリカ-GAAP:高齢者の注意事項メンバーAqst:十二時五高級セキュリティノード302025年6月2022-01-012022-12-310001398733アメリカ-GAAP:高齢者の注意事項メンバーAqst:十二時五高級セキュリティノード302025年6月2022-12-310001398733アメリカ-GAAP:高齢者の注意事項メンバーAqst:十二時五高級セキュリティノード302025年6月2023-11-012023-11-010001398733アメリカ-GAAP:高齢者の注意事項メンバーAqst:FirstAdditionalOfferingMember2023-11-012023-11-010001398733アメリカ-GAAP:高齢者の注意事項メンバーAQST:13時5高齢者安全注意事項12028 11月2023-11-012023-11-010001398733アメリカ-GAAP:高齢者の注意事項メンバーAQST:13時5高齢者安全注意事項12028 11月2023-01-012023-12-310001398733Aqst:救いのシーン1月1日AQST:13時5高齢者安全注意事項12028 11月アメリカ-GAAP:高齢者の注意事項メンバー2023-11-012023-11-010001398733Aqst:救いのシーン1月1日アメリカ-GAAP:高齢者の注意事項メンバー米国-公認会計基準:米国財務省利子率メンバー2023-11-012023-11-010001398733AQST:13時5高齢者安全注意事項12028 11月アメリカ-GAAP:高齢者の注意事項メンバーAqst:RedemptionScenario 2メンバー2023-11-012023-11-010001398733Aqst:ABLFacilityMember2023-11-012023-11-010001398733Aqst:ABLFacilityMember2023-11-010001398733米国-公認会計基準:投入割引率を測るメンバー2023-12-310001398733Aqst:入力確率を測定するOfSuccessMember2023-12-310001398733AQST:13時5高齢者安全注意事項12028 11月2023-12-310001398733AQST:13時5高齢者安全注意事項12028 11月2023-01-012023-12-310001398733アメリカ-GAAP:高齢者の注意事項メンバーAQST:13時5高齢者安全注意事項12028 11月2023-12-310001398733アメリカ-GAAP:高齢者の注意事項メンバーAQST:13時5高齢者安全注意事項12028 11月2022-12-310001398733SRT:最大メンバ数Aqst:FirstAdditionalOfferingMember2023-12-310001398733AQST:A 2020追加説明メンバー2023-01-012023-12-310001398733Aqst:FirstAdditionalOfferingMember2023-12-310001398733Aqst:FirstAdditionalOfferingMember2022-12-310001398733Aqst:PreFundedWarrantsMember2022-06-300001398733AQST:CommonStockWarrantsMember2022-06-300001398733SRT:最小メンバ数AQST:CommonStockWarrantsMember2022-06-300001398733SRT:最大メンバ数AQST:CommonStockWarrantsMember2022-06-300001398733Aqst:PublicEquityMember2022-04-012022-06-300001398733Aqst:新保証メンバー2023-08-022023-08-020001398733Aqst:新保証メンバー2023-08-020001398733Aqst:貨幣化プロトコルメンバAQST:マラソンで山甲を着て皇室メンバー2020-11-032023-12-310001398733Aqst:貨幣化プロトコルメンバ2023-01-012023-12-310001398733AQST:ライセンスプロトコルとSunovionPharmPharmticalsIncMemberUS-GAAP:RoyaltyMember2022-04-012022-06-300001398733AQST:ライセンスプロトコルとSunovionPharmPharmticalsIncMember2020-06-300001398733Aqst:貨幣化プロトコルメンバ2020-11-030001398733US-GAAP:RoyaltyMember2023-01-012023-12-310001398733米国-GAAP:PutOptionMembers2023-12-310001398733Aqst:十二時五高級セキュリティノード302025年6月米国-GAAP:PutOptionMembers2023-12-310001398733米国-公認会計基準:従業員株式オプションメンバー2023-01-012023-12-310001398733米国-公認会計基準:従業員株式オプションメンバー2022-01-012022-12-310001398733米国-GAAP:制限株式単位RSUメンバー2023-01-012023-12-310001398733米国-GAAP:制限株式単位RSUメンバー2022-01-012022-12-310001398733アメリカ公認会計基準:保証メンバー2023-01-012023-12-310001398733アメリカ公認会計基準:保証メンバー2022-01-012022-12-310001398733米国-公認会計基準:従業員株式オプションメンバー2023-01-012023-12-310001398733Aqst:メーカーとサプライヤーのメンバー2023-01-012023-12-310001398733Aqst:メーカーとサプライヤーのメンバー2022-01-012022-12-310001398733米国-公認会計基準:研究·開発費メンバー2023-01-012023-12-310001398733米国-公認会計基準:研究·開発費メンバー2022-01-012022-12-310001398733アメリカ-公認会計基準:一般と行政費用メンバー2023-01-012023-12-310001398733アメリカ-公認会計基準:一般と行政費用メンバー2022-01-012022-12-310001398733米国-GAAP:制限株式単位RSUメンバー2022-01-012022-12-310001398733米国-公認会計基準:従業員株式オプションメンバー2022-01-012022-12-310001398733アメリカ公認会計基準:従業員ストックメンバー2023-01-012023-12-310001398733アメリカ公認会計基準:従業員ストックメンバー2022-01-012022-12-310001398733米国-GAAP:制限株式単位RSUメンバーAqst:ServiceBasedMember2021-12-310001398733米国-GAAP:制限株式単位RSUメンバーAqst:ServiceBasedMember2022-01-012022-12-310001398733米国-GAAP:制限株式単位RSUメンバーAqst:ServiceBasedMember2022-12-310001398733米国-GAAP:制限株式単位RSUメンバーAqst:ServiceBasedMember2023-01-012023-12-310001398733米国-GAAP:制限株式単位RSUメンバーAqst:ServiceBasedMember2023-12-310001398733米国-GAAP:制限株式単位RSUメンバー2023-12-310001398733Aqst:MarketBasedMember米国-GAAP:制限株式単位RSUメンバー2022-12-310001398733Aqst:MarketBasedMember米国-GAAP:制限株式単位RSUメンバー2023-01-012023-12-310001398733Aqst:MarketBasedMember米国-GAAP:制限株式単位RSUメンバー2023-12-310001398733米国-GAAP:制限株式単位RSUメンバー答え:MarketConditionRangeOneMember2023-12-310001398733米国-GAAP:制限株式単位RSUメンバー答え:MarketConditionRangewoMember2023-12-310001398733答え:MarketConditionRangeThreeMemberSRT:最小メンバ数米国-GAAP:制限株式単位RSUメンバー2023-12-310001398733答え:MarketConditionRangeThreeMemberSRT:最大メンバ数米国-GAAP:制限株式単位RSUメンバー2023-12-310001398733米国-GAAP:制限株式単位RSUメンバー答え:MarketConditionRangeFourMember2023-12-310001398733SRT:最小メンバ数米国-GAAP:制限株式単位RSUメンバー答え:MarketConditionRangeFiveMember2023-12-310001398733SRT:最大メンバ数米国-GAAP:制限株式単位RSUメンバー答え:MarketConditionRangeFiveMember2023-12-310001398733米国-GAAP:制限株式単位RSUメンバー答え:MarketConditionRangeSixMember2023-12-310001398733SRT:最小メンバ数米国-公認会計基準:従業員株式オプションメンバー2023-01-012023-12-310001398733SRT:最大メンバ数米国-公認会計基準:従業員株式オプションメンバー2023-01-012023-12-310001398733SRT:最小メンバ数2023-12-310001398733米国-公認会計基準:従業員株式オプションメンバー2021-12-310001398733米国-公認会計基準:従業員株式オプションメンバー2021-01-012021-12-310001398733米国-公認会計基準:従業員株式オプションメンバー2022-12-310001398733米国-公認会計基準:従業員株式オプションメンバー2023-12-310001398733Aqst:BlackScholesMemberSRT:最小メンバ数米国-公認会計基準:従業員株式オプションメンバー2023-01-012023-12-310001398733Aqst:BlackScholesMember米国-公認会計基準:従業員株式オプションメンバー2023-01-012023-12-310001398733Aqst:BlackScholesMember米国-公認会計基準:従業員株式オプションメンバー2022-01-012022-12-310001398733Aqst:BlackScholesMemberSRT:最小メンバ数米国-公認会計基準:従業員株式オプションメンバー2022-01-012022-12-310001398733Aqst:BlackScholesMemberSRT:最大メンバ数米国-公認会計基準:従業員株式オプションメンバー2022-01-012022-12-310001398733SRT:ExecutiveOfficerMember米国-公認会計基準:従業員株式オプションメンバー2023-01-012023-12-310001398733米国-GAAP:国内/地域メンバー2023-12-310001398733米国-GAAP:国内/地域メンバー2022-12-310001398733アメリカ-公認会計基準:州と地方法律法規のメンバー2023-12-310001398733アメリカ-公認会計基準:州と地方法律法規のメンバー2022-12-310001398733アメリカ-公認会計基準:外国人メンバー2023-12-31Aqst:weitingPeriod0001398733AQST:PatentLitigationSettlementWithBDSMembers2023-03-032023-03-030001398733AQST:Neurelis IncVA問題治療IncMember2019-12-05Aqst:原因0001398733AQST:Neurelis IncVA問題治療IncMember2022-05-032022-05-030001398733Aqst:個人改訂メンバー2023-03-022023-03-020001398733Aqst:メーカーとサプライヤー収入メンバーAqst:個人改訂メンバー2023-01-012023-12-310001398733アメリカ公認会計基準:副次的事件メンバーAqst:EquityDistributionAgreementメンバ2024-01-012024-03-040001398733アメリカ公認会計基準:副次的事件メンバーAqst:ProductLiablityLitigationMember2024-02-21Aqst:未解決の声明 アメリカです
アメリカ証券取引委員会
ワシントンD.C.,20549
表10-K
(マーク1)
| | | | | |
| ☒ | 1934年証券取引法第13条又は15条に基づいて提出された年次報告 |
本財政年度末まで十二月三十一日, 2023
あるいは…。
| | | | | |
| ☐ | 1934年証券取引法第13条又は15条に基づいて提出された移行報告 |
_からの過渡期 _まで
依頼書類番号:001-38599
Aqutive Treeutics,Inc.
(登録者の正確な氏名はその定款に記載)
| | | | | | | | |
| デラウェア州 | | 82-3827296 |
| (法団または組織の州またはその他の管轄区域) | | (国際税務局雇用主身分証明書番号) |
| | |
30テクノロジーの駆動力, ウォーレン, ニュージャージー州 | | 07059 |
| (主な行政事務室住所) | | (郵便番号) |
(908) 941-1900
(登録者の電話番号、市外局番を含む)
同法第12条(B)に基づいて登録された証券:
| | | | | | | | | | | | | | |
| クラスごとのタイトル | | 取引コード | | 登録された各取引所の名称 |
| 普通株は一株当たり0.001ドルの価値があります | | AQST | | ナスダック世界市場 |
この法第12(G)条に基づいて登録された証券:規制機関ありません
登録者が証券法第405条で定義された経験豊富な発行者であるか否かをチェックマークで示す£はい、そうですS 違います。
登録者が当該法第13条又は第15条(D)に従って報告書を提出する必要がないか否かを,再選択マークで示す£はい、そうですS 違います。
登録者が(1)過去12ヶ月以内(または登録者がそのような報告の提出を要求されたより短い期間)に、1934年の証券取引法第13または15(D)節に提出されたすべての報告を提出したかどうか、および(2)このような提出要求を過去90日以内に遵守してきたかどうかを、再選択マークで示すS はい、そうです £違います。
再選択マークは、登録者が過去12ヶ月以内(または登録者がそのような文書の提出を要求されたより短い時間以内)に、S−T法規第405条(本章232.405節)に従って提出を要求した各相互作用データファイルを電子的に提出したか否かを示すS はい、そうです £違います。
登録者が大型加速申告会社,加速申告会社,非加速申告会社,小さな報告会社,あるいは新興成長型会社であることを再選択マークで示す。1934年の証券取引法第12 b-2条規則における“大型加速申告会社”、“加速申告会社”、“小さい申告会社”、“新興成長型会社”の定義を参照されたい。
| | | | | | | | | | | |
| 大型加速ファイルサーバ | ☐ | ファイルマネージャを加速する | ☐ |
| 非加速ファイルサーバ | ☒ | 規模の小さい報告会社 | ☒ |
| | | 新興成長型会社 | ☐ |
新興成長型会社であれば、登録者が延長された移行期間を使用しないことを選択して証券法第7(A)(2)(B)節に規定する任意の新たな又は改正された財務会計基準を遵守するか否かを再選択マークで示す。☐
登録者が空殻会社であるか否かをチェックマークで示す(取引法第12 b-2条で定義されている)。☐そうなのS 違います。
登録者が報告書を提出したか否かを再選択マークで示し、その経営陣が“サバンズ·オクスリ法案”(“米国法典”第15編、第7263(B)節)第404(B)条に基づいて財務報告書の内部統制の有効性を評価したことを証明する。この評価は、その監査報告書を作成または発行する公認会計士事務所によって行われる☐
証券が同法第12条(B)に基づいて登録されている場合は,登録者の財務諸表が以前に発表された財務諸表の誤り訂正を反映しているか否かを示すチェックマークを適用する☐
再選択フラグは、これらのエラーのより真ん中に、登録者の任意の実行幹事に対して、関連する回復期間中に受信された報酬ベースの補償に従って回復分析を行う必要があるかどうかを示す
2023年6月30日現在,すなわち登録者が最近完成した第2財期の最終日,登録者の非関連会社が保有する普通株の総時価は約$である82.7登録者の普通株のその日の終値に基づく。
登録者の額面0.001ドルの普通株の流通株数2024年3月1日かつては…73,301,201.
登録者は,2023年12月31日までの財政年度終了後120日以内に,その2024年株主総会に関する最終依頼書を第14 A条に基づいて提出する予定である。この最終依頼書の部分内容は,本年度報告の表格10−Kの第III部分に引用的に組み込まれている。
カタログ表
| | | | | | | | |
| | ページ番号. |
| 用語、略語、頭文字の略語 | |
| | |
第1部 | | 7 |
第1項。 | 業務.業務 | 9 |
| 第1 A項。 | リスク要因 | 29 |
項目1 B。 | 未解決従業員意見 | 67 |
プロジェクト1 C。 | ネットワーク·セキュリティ | 67 |
第二項です。 | 属性 | 67 |
第三項です。 | 法律訴訟 | 67 |
第四項です。 | 炭鉱安全情報開示 | 67 |
| | | |
第II部 | | 67 |
五番目です。 | 登録者普通株市場、関連株主事項及び発行者による株式証券の購入 | 67 |
第六項です。 | 保留されている | 68 |
第七項。 | 経営陣の財務状況と経営成果の検討と分析 | 69 |
第七A項。 | 市場リスクの定量的·定性的開示について | 80 |
第八項です。 | 財務諸表と補足データ | 80 |
第九項です。 | 会計と財務情報開示の変更と相違 | 80 |
第9条。 | 制御とプログラム | 80 |
プロジェクト9 B。 | その他の情報 | 81 |
プロジェクト9 Cです。 | 検査妨害に関する外国司法管区の開示 | 81 |
| | | |
第三部 | | 82 |
第10項。 | 役員·幹部と会社の管理 | 82 |
第十一項。 | 役員報酬 | 82 |
第十二項。 | 特定の実益所有者の担保所有権及び経営陣及び関連株主の事項 | 82 |
十三項。 | 特定の関係や関連取引、取締役の独立性 | 82 |
14項です。 | 最高料金とサービス | 82 |
| | | |
第4部 | | 83 |
第十五項。 | 展示·財務諸表明細書 | 83 |
用語、略語、略語
以下の用語、略語、および略語は、本報告において使用され得る一般的な用語およびフレーズを決定するために使用される:
| | | | | |
用語.用語 | 定義する |
| 12.5%債券 | 2025年に満期となる12.5%の高度担保手形 |
13.5%債券 | 13.5%高度な保証手形 |
多動症 | 欠陥多動障害に注意する |
筋萎縮性側索硬化症 | 筋萎縮性側索硬化症 |
安達 | 簡明新薬申請 |
| ANVISA | ブラジル衛生監督局 |
アプリケーションプログラミングインタフェース | 活性薬物成分 |
AQST | Aqutive Treateutics社の普通株式コード |
| アロ | 資産廃棄債務 |
ASC | 会計準則編集 |
| 断言する | Assertioホールディングス |
| 資産管理協定 | AqutiveとAssertio Holdingsの子会社Otter PharmPharmticals,LLCとの間のライセンスプロトコル |
ASU | 会計基準が更新される |
現金自動支払機 | 市場でAQST普通株を購入する便利さ |
| 基托義歯 | 債券利子率12.5%の債券 |
BBA | 2018年両党予算法案 |
BDSI | 生物送達科学国際会社です |
| CGMP | 現在の良好な製造規範 |
塩化ナフタレン | 中枢神経系 |
| 普通株 | 会社の普通株は一株当たり0.001ドルの価値があります |
普通株式引受証 | 私募方式で発行された引受権証は、元金総額が10万元、元本が12.5%に達し、2025年に満期になる予定だった |
COSO | トレデビル委員会は組織委員会を後援しています |
CRL | 完全返信(FDA) |
CRO | 契約研究機関 |
| DEA | 麻薬取締署 |
| DSCSA | 医薬品サプライチェーン安全法 |
EMA | ヨーロッパ医薬品局は |
| ERTC | 従業員は税収控除を保留する |
EU.EU | EU.EU |
“取引所法案” | 1934年証券取引法 |
| 現有引受権証 | 残りの5,000,000件の株式承認証所持者の普通株式引受権証と |
FASB | 財務会計基準委員会 |
林業局 | アメリカ食品医薬品局は |
FDAAA | 2007年食品医薬品局改正法案 |
FDIC | アメリカ連邦預金保険会社 |
FDII | 海外で得られた無形収入 |
| 第一修正案 | Sunovionライセンス契約の最初の改訂 |
| フォルトビア | Fortovia治療会社(前身はMidatech Pharma PLC |
FQHC | 連邦資格を持つ医療センター |
会計原則を公認する | 会計原則を公認する |
プロス | 良好な実験室操作規範 |
| ハイスコ | ハイスコ薬業集団有限公司です。 |
| | | | | |
| ハイスコ協定 | 深セン証券取引所に上場している中国海スコ有限公司と許可証、開発と供給協定を締結する |
HHS | アメリカ衛生·公衆サービス部 |
| HIPAA | 1996年“健康保険移行性と責任法案” |
| HITECH | 衛生情報技術促進経済·臨床衛生法案 |
工業 | 研究中の新薬の応用 |
契約協定 | 13.5%高度な保証手形の管理に関する合意 |
個体 | Indior Inc.(前身は利潔時当キサー製薬会社) |
個人修正案11 | 改正案第11号“個人許可協定” |
| 個人許可協定 | 利潔時当キザー製薬会社と締結した商業開発協定(後続改訂を含む) |
IRB | 大学検討委員会 |
リンカーン公園 | リンカーン公園資本基金有限公司 |
| リンカーン公園購入契約 | リンカーンパーク資本基金有限責任会社との購入協定 |
| マラソン.マラソン | マラソン資産管理 |
| 貨幣化協定 | AqutiveとSunovionの間の売買協定 |
MSSP | ホスト·セキュリティ·サービス·プロバイダ |
MTHA | 三菱Tanabe医薬ホールディングスアメリカ社 |
適用されない | 意味がありません百分率変化のために |
ナスダック | ナスダック株式市場 |
NDA | 新薬申請 |
新規引受権証 | 株式承認証は2,750,000株の普通株を購入します |
国立衛生研究院 | 国立衛生研究院 |
PD | 薬効学 |
PDUFA | “処方薬使用料法案” |
| Pharmanovia | Atnahs Pharma UK Limited、イングランドとウェールズに登録されている会社 |
| Pharmanovia協定 | Atnahs Pharma UK Limitedとのライセンスと供給契約は |
Pharmanovia修正案 | Atnahs Pharma UK Limitedとの許可と供給協定を修正し、2023年3月27日現在 |
Pk | 薬物動態学 |
PPACA | 患者保護·平価医療法案、2010年“医療·教育和解法案”改正 |
PTO.PTO | アメリカ特許商標局は |
| REMS | リスク評価と緩和策 |
印税義務 | 特許使用料協定に関する責任 |
| 特許権使用料協定 | 特許使用料協定、13.5%高度担保手形の構成要素 |
RSU | 限定株単位 |
アメリカ証券取引委員会 | アメリカ証券取引委員会 |
| 証券購入協定 | ある購入者と2022年6月6日に締結した証券購入契約 |
| 別居協定 | キース·J·ケンデルとの相談協定を含む別居協定 |
| 太陽のかすかな光 | Sunovion製薬会社 |
| Sunovionライセンスプロトコル | KYNMOBI商業化協定 |
領土.領土 | 欧州連合のある国、連合王国、スイス、ノルウェー、中東、北アフリカは“パルマノビア協定”に基づいている |
TGA | オーストラリア政府衛生部治療薬品管理局 |
| | | | | |
賛本 | ザン邦会社 |
| ゼヴラ | Zevra Treateutics,Inc.(前身はケンパム製薬会社) |
第1部
前向きに陳述する
このForm 10-K年次報告書と私たちがした他のいくつかの通信には、1995年の個人証券訴訟改革法の意味に適合する前向きな声明が含まれている。前向き陳述を識別することが意図された、“信じる”、“予想”、“計画”、“予想”、“推定”、“意図”、“可能”、“できる”、またはこれらの用語の否定または同様の表現
これらの展望的陳述は、重要なPK臨床試験および他のアレルギーを支持する臨床研究の提出を含む、臨床開発およびFDA承認過程における我々の候補製品(アドレナリン)舌下膜の臨床開発およびFDA承認過程における進展および関連タイミングに関する陳述を含むが、アレルギー薬に提出されたセキュリティプロトコルにおいて十分なデータを提供する能力を提供し、FDAが提案したキーPK研究案に対するフィードバックおよびFDAとの第2段階終了会議を解決するために、Libervantに提出されたPDUFA目標日は2024年4月28日である™ 間欠性、陳旧性頻回発作の急性治療に用いられる口腔薬膜(ジセパン)即2歳から5歳までのてんかん患者において、患者の通常のてんかん発作パターンと異なるのは、Libervantが米国市場への進出を許可され、これらの2歳以上のてんかん患者のために使用され、FDAが許可した競合鼻スプレー製品の孤児薬物市場独占性を克服したことであり、これらの患者集団に対して2027年1月まで延長された。候補製品AQST-108 SF(アドレナリン)の臨床開発と規制過程の進展と関連タイミングを通過した;アレルギー薬とLibervantの許可を含む米国と海外での製品導管の潜在的な許可;Suboxoneの生産継続に重点を置いている®Exservan®Sympazan®Ondif®これらの展望的表現は、会社および他の許可製品の財務状況、会社製品が患者にもたらす可能性のある潜在的な利益、臨床および商業マイルストーンの実現、製品注文および履行状況、会社の現金需要、現金資金および現金消費、短期的および長期的流動性、および業務運営に資金を提供する能力、会社の成長と将来の財務および運営結果および財務状況、2024年の財務展望に関連する状況、および業務戦略、市場機会、および他の非歴史的事実を含む表現を含む。
これらの展望性陳述は著者らの現在の期待と信念に基づいて、多くのリスクと不確定要素の影響を受けることができ、これらのリスクと不確定要素は実際の結果と展望性陳述に記述されたものと大きく異なることを招く可能性がある。このようなリスクおよび不確実性は、アレルギー関連のリスクを含むが、我々の製品開発活動および臨床試験および計画の時間、コスト、および成功の任意の遅延または変化を含む私たちの開発に関連するリスクを含むが、アレルギー薬、Libervantおよび他の候補薬に対するFDAによる規制の進行遅延またはFDAの承認が得られないリスクを含むが、私たちは、Libervantが米国市場への参入を許可するために、FDAが米国の別の会社に承認した鼻スプレー製品の承認された7年間の孤児薬物独占経営権を克服できないかもしれない。新製品の商業化に固有のリスクと不確実性(技術リスク、財務リスク、市場リスク、実施リスクおよび規制制限を含む)、当社製品KYNMOBI特許権の貨幣化の収入フローに関連するリスクおよび不確実性、ならびにKYNMOBI貨幣化取引下または支払いに必要なグローバルまたは任意の司法管轄区域の特許権使用料目標およびいくつかの他の商業目標の達成状況;私たちの候補製品の将来の商業化販売およびマーケティング能力発展のリスク;利用可能な債務および株式融資の機会を得ることを含む十分な資本および現金資源のリスク、当社のATM施設およびリンカーン公園による購入契約、および私たちのすべての短期的および長期的な流動性および現金需要および他の現金需要を満たすための運営収入、短期債務償却スケジュールを含む所要時間および金額、すべての財務および他の債務契約およびいかなる違約のリスクを満たすことができないこと、私たちがSuboxoneを許可、製造、販売する政府クレームに関連するリスクは、私たちの現在の運営収入の大きな部分を占めている。いくつかの販売、マーケティングおよび他の運営および従業員機能を第三者にアウトソーシングすることに関連するリスク;私たちの製品および候補製品に対する市場の受容度と受容度のリスク;任意の競合製品(模倣薬を含む)の成功のリスク;私たちの製品市場の規模と成長リスク;FDAおよび他の政府および顧客の私たちの製造施設に対する要求に適合するリスク;私たちの製品に関連する知的財産権および侵害クレームに関連するリスク;意外な特許開発のリスク;私たちの製品および製品候補および製品の価格設定、清算または訪問に関連するリスクを含む、私たちの業務の立法および規制行動および法律または法規の変化に影響を与える。重要な顧客を失うリスク;特許侵害、証券、商業侵害、調査、製品安全または効果および反独占訴訟事項を含むクレームおよび法的訴訟に関連するリスク;製品リコールおよび撤回のリスク;ネットワーク攻撃の影響を含む当社の情報技術ネットワークおよびシステム中断に関連するリスク;ネットワークセキュリティ攻撃増加および遠隔作業手配によるデータアクセス中断のリスク;金融サービス業の不利な発展に影響を与えるリスク;インフレおよび金利上昇に関連するリスク;新冠肺炎の世界的大流行が私たちの業務に与える影響に関するリスク、私たちの臨床試験とサイト開始、患者登録とこれらの臨床試験の時間と十分性、私たちの候補製品の規制提出と監督審査と承認、私たちの製品と候補製品で使用される薬物成分と他の原材料の可用性、サプライチェーン、私たちの製品と候補製品の製造と流通に関連するリスク;
前向き表現は、一般経済、政治(戦争およびテロ行為を含む)、商業、業界、規制および市場状況、および他の異常なプロジェクトに関連する不確実性要因を含むが、AQUCITY社に影響を与える他のリスクおよび不確実性要因を含むが、本10-K年報、10-Q表季報、および米国証券取引委員会が提出した現在の8-K表季報の“リスク要因”の一部および他の章に記載されているリスクおよび不確実性を含む。このような不確実性を考慮して、あなたは日付しか説明できないので、このような前向きな陳述に過度に依存してはいけない。私たちまたは私たちを代表する誰のためにも、すべての後続の展望的陳述は、この警告声明によって明確に完全に制限されている。法律の適用に別途要求がない限り、本年度報告書の発行日後に前向き陳述、展望、または指導をForm 10−K形式で更新する義務は負いません。新しい情報、未来のイベント、または他の理由によるものです。読者は、本10-K年次報告書の提出日以降の任意の日付の観点を代表するので、本10-K年度報告に含まれる前向き陳述に依存してはならない
これらの前向き陳述は既知および未知のリスク、不確定性および他の要素に関連し、私たちの実際の結果、活動レベル、業績または成果はこれらの陳述と明示的または暗示的なものとは大きく異なる可能性がある。これらの要素は、項目1 Aで議論され言及された事項の第1の部分を含む。本表の格子10−Kのリスク要因。
文意が別に指摘されているほか、本年度報告で言及された“愛可”、“会社”、“私たち”、“私たち”と“私たち”はいずれも治療可能な会社とその子会社を指す
プロジェクト1.レポートとビジネスの概要
Aqutiveは製薬会社であり、革新的な科学と技術を通じて薬物を改善し、患者の生活に意義のある改善をもたらす。我々は,侵襲性や不便な標準看護療法の代替品である薬物製品を開発し,投与により複雑な分子を伝達している。私たちは5種類の許可された商業化製品を持っていて、私たちの許可メーカーがアメリカと世界各地で販売しています。私たちはこれらの特許製品の独占メーカーです。Aqutiveは製薬会社と協力し,PharmFilmのような独自の同種最高の技術を用いて新分子を市場に投入している®成熟した薬物開発と商業化能力を有している。我々はアレルギー反応を含む重篤なアレルギー反応を治療する製品ラインを進めている。中枢神経系疾患の治療に専念する製品ラインも開発した。私たちの生産施設はインディアナ州のポティチにあり、私たちの会社の本部と主要な研究実験室施設はニュージャージー州のウォーレンにあります。
私たちの工場でライセンス製品を生産し、私たちの現在の製造能力は、私たちのライセンス製品と現在開発されている候補製品の商業数量を満たすのに十分であると予想されます。我々の施設はFDA,TGA,DEAの検査を受けており,ANVISA,EMAを含むすべての適用可能な衛生機関の検査を受けている。将来商業的に発売される可能性のあるAqutiveなすべての協力または許可製品が必ずしもKYNMOBIのケースのような私たちによって生産されるとは限らない。
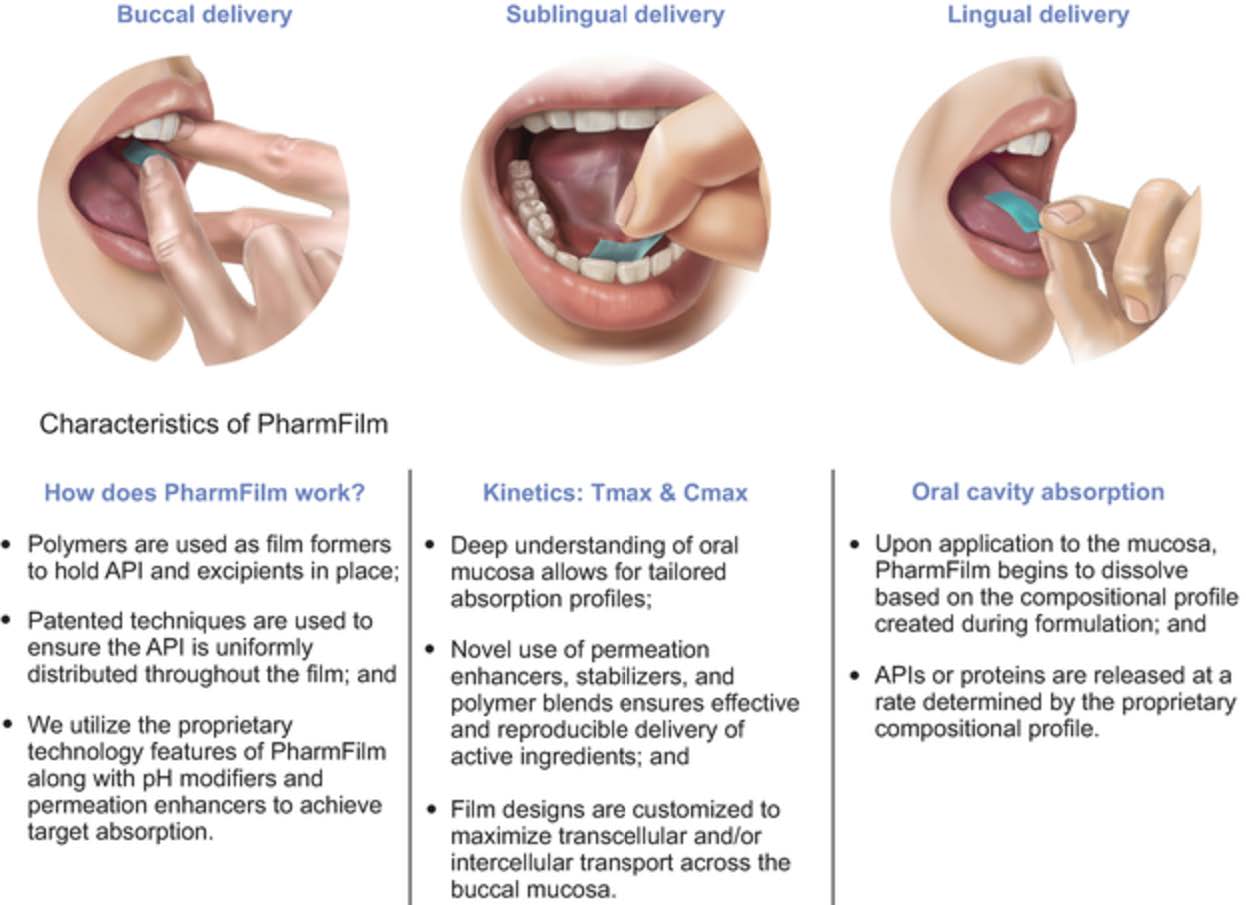
薬膜-我々の口腔膜技術は
私たちは今世界の先頭者口腔フィルムの薬物輸送と製造において、私たちは歴史的に世界の大部分の処方薬のための口腔フィルムを提供し、私たちは毎年10億剤を超える商業投与量を生産することができる。我々は,他の既存剤形と比較して有意な臨床的および治療的優位性を提供し,逆に患者や介護者の生活を改善するためのPharmFilm技術を開発した。PharmFilmは、現在、世界で少なくとも150件の発行された特許を含み、少なくとも30件が米国特許であり、世界130件以上の係属中の特許出願を含む、我々の特許組合せによって保護されている。この知的財産権の組み合わせのいくつかの特許は、私たちのすべての独自のパイプ製品に使用される。我々は,PharmFilmの応用や工程に関する他の知的財産権や技術ノウハウ,あるいは他の技術と組み合わせて,納得できる価値主張を持つ製品能力を創出し続けている。
PharmFilmは、活性医薬成分または原料薬および賦形剤の所定の位置を維持するためのフィルム形成剤として機能する特許ポリマー組成物からなる。原料薬がフィルム全体に均一に分布し、目標吸収レベルを達成することを確実にするために、特許および特許保護された組成物、配合および製造技術および技術を採用する。我々の特許技術および製造プロセスは、PharmFilmが特定の疾患状態で満たされていない患者の需要を最適に満たすために、様々な目標製品に適合するように設計することを可能にする。薬膜の厚さと大きさは切手と類似しており,口腔,舌下あるいは舌で経口投与することができる。
現在の標準的な看護療法と比較して、私たちの薬物送達プラットフォームの革新的な性質は、患者、介護者、医師に多くの有意義な利点を提供する可能性があると信じている
•行動の開始速度はより速いか、または少なくとも同等である
•管理および利用可能性が容易である(いかなるデバイスも必要としない);
•血液中に直接吸収し、肝臓の“初過”効果を減少または回避する
•胃腸や胃腸の副作用を減少させ
•積極的な投与結果、特に身体には(例えば:嚥下困難)や他の投与方法の心理的障害;
•安定、耐久性、携帯性、急速溶解(水を加えるか、または水を加えない);
•カスタマイズ可能なPK、プロファイル(口腔、舌下または言語)の送達経路;
•カスタマイズ可能なセンスプロファイル。
私たちの製品の組み合わせとルートは
次の表は私たちの独自の成長動力と許可製品について概説する。
Sympazan®Zuplenz®、PharmFilter®和AQUECTIVEロゴは、AQUCTIVE治療会社の登録商標です。文中で言及されている他のすべての登録商標は、それぞれの所有者の財産です。
専有成長動力
複雑な分子結合
われわれのPharmFilm技術は,非侵襲的送達,嚥下障害や嚥下障害患者に対するカスタマイズ適応を提供する薬剤を開発し,水を加えずに投与し,一致した治療量を確保することができる。これらの特徴は,期待される患者結果を実現するとともに,患者看護の総コストを潜在的に低減することができると信じている。
我々は,侵襲的管理の標準看護療法の代替として,巨大な市場機会に対応するために,複雑分子に基づく候補製品の独自パイプラインを開発している。私たちの複雑な分子パイプライン製品の組み合わせの活発なプロジェクトは
•過敏症(アドレナリン舌下膜、“ana膜”と発音する)-最初も非装置ベースの唯一の経口アドレナリン候補製品であり、緊急治療にアレルギー反応を含むアレルギー反応において、自動注射器(例えば、EpiPenおよびAUVI-Q)に相当する臨床効果を示す。アドレナリンはアレルギー反応を治療する標準的なケアであり、現在、EpiPenおよびAuvi-Qなどの自動注射器を含む筋肉注射(IM)によって投与されており、緊急アレルギー反応中に患者またはその介護者にアドレナリンの大腿への注射を要求する。このような投与経路のため、多くの患者および彼らの介護者は、現在利用可能な製品を使用することを望まない;しかし、FDAが承認した場合、アレルギー薬は、患者が舌の下に溶解可能なストリップ、約切手の大きさおよび重量を配置することを可能にし、必要な場所で、必要なときに、患者が好きな形態で適切な薬剤を提供することを可能にするであろう。
私たちはカナダで初めてアレルギー反応に対するヒト第一段階の臨床試験を終えた。この1期ランダム,単回漸増用量研究は,アレルギーの安全性,耐性と薬理学的特徴を評価するためである。
FDAは2022年2月に我々のINDを承認し、米国でのアレルギー性臨床研究を許可した。FDAは505(B)(2)承認経路がアレルギー性疾患の開発に利用できることを明らかにした。FDAは2022年3月にアレルギー薬迅速チャネルの称号を付与し,アレルギー反応を含むアレルギー反応の緊急治療に用いられている。
2022年2月,われわれのアレルギー交差研究EPIPHASTの第1部の陽性背線データを報告し,ランダム,開放ラベル,3部の適応設計であり,健常成人被験者で交差研究を行い,アレルギー経口膜とエピネフリン筋注により投与されたエピネフリンのPKとPDを比較した。EPIPHAST研究もカナダで行われている。EPIPHAST研究の第1部では,複数の口腔膜剤とアレルギー剤の用量強度を評価した。アレルギーの鉛製剤は2種類の異なる物理配置で投与したところ臨床的意義のある血中濃度を示し,最大濃度までの中位時間(Tmax)はそれぞれ13.5分と22.5分であった。第1の部分はまた、2つの構成の算術平均最大濃度(Cmax)がそれぞれ771 pg/m Lおよび580 pg/m Lであるか、または幾何平均Cmaxがそれぞれ258 pg/m Lおよび268 pg/m Lであることを示している。これらの幾何平均値Cmaxと中央値Tmaxは,先に報告したEpiPenらが注射エピネフリン装置を承認したCmaxと中央値Tmaxと一致している。EPIPHAST研究の第1の部分によれば、健常ボランティアは、承認用量範囲の高いエンドエピネフリンのPK、安全性、および耐性と比較するために、0.5 mgの筋肉注射アドレナリンにも曝露され、これは、FDAが我々のIND治療アレルギー反応に対する書面応答で受けた指導と一致する。その結果、選択されたアレルギー製剤の2つの構成は、注射よりも高用量のエピネフリンよりも早く臨床的に意味のあるアドレナリン血中濃度を提供することができ、既存のアドレナリン自動注射器と一致することが示された。また,アレルギー剤の服用は血圧や心拍数の変化を招き,アドレナリン自動注射器に相当する。第一部分EPIPHAST研究により、治療耐性は良好であり、深刻な不良事件、重大な医療事件或いは治療に関連する深刻な不良事件は報告されていない。
2022年4月,EPIPHASTアレルギー検討第二部のTOPLINE陽性結果を報告した。第二部はランダム交差設計であり,アレルギー薬12 mgとエピネフリン0.3 mgを筋注した。重複交差設計を用いて、第2部分は24名の健康被験者のより大きな集団でEPIPHAST研究第1部分と第1ヒトPK研究で観察されたキーPKとPD指標を確認した。アレルギー薬のTmax中央値は15分であったのに対し,エピネフリン筋注0.3 mgの中央値は50分であった
2022年7月,EPIPHASTアレルギー研究第3部最後の両腕の背線陽性結果を報告した。第三部の目的は,薄膜の様々な条件下での投与状況を引き続き検討し,そのPK,PD,安全性をさらに特徴付けることである。最後の両腕は,(1)ピーナッツバターサンドイッチを食べた2分後にフィルムを舌下で服用することと,(2)フィルム全体を直ちに水で飲み込む影響を評価するように設計されている。第三部の研究の結果,ピーナッツバターサンドイッチを食べた後,アレルギー性エピネフリン経口膜を舌下投与したTmaxは12分と一致した。第三部の研究でも積極的な結果が示されており,ただちにアレルギー薬を水で丸ごと飲み込んだ後,胃腸吸収レベルが意外に高く,舌下吸収の場合とは異なる。
2022年9月にEPIPHAST IIアレルギー試験のTopline陽性結果を報告した。EPIPHAST II試験の目的は、単回用量のアレルゲンとEpiPen 0.3 mgおよびアドレナリン0.3 mg、および反復用量のアレルゲンと反復用量のアドレナリン0.3 mgを比較することである。単回投与の結果,EpiPen(22.5分)やエピネフリン0.3 mg(45分)に比べてアレルギー薬のTmax(12分)の方がはるかに速いことが分かった。アレルギー重複投与は薬物の血中濃度を有意に向上させ,投与後Tmaxは8 minであり,広範な吸収が観察された。1回投与後のCmax平均値は465 pg/mL,2回投与後のCmax平均値は2958 pg/mLであった。エピネフリンIM 0.3 mgCmaxは1回投与で489 pg/m L,2回投与で911 pg/m Lであった。単剤EpiPenのCmaxは869 pg/m Lであった。単剤アレルギー後の収縮圧と心拍数の変化は単剤EpiPenと比較して類似していた。これらのデータ,および完成したEPIPHAST研究からのデータは,FDAと開催された第2回第2段階末(EoP 2)会議の基礎である。第1回EoP 2会議でアレルギーの化学,製造,制御(CMC)の検討を求めた後,FDAから積極的な書面フィードバックを受け,アレルギー属性を記述する方法が将来提出可能な出願において合理的であるように見えることを示していると考えられる
2022年12月下旬、FDAと開催されたEoP 2会議の最終議事録を受け取り、重要プロジェクト分野に対するFDAの期待を明らかにした。2023年3月、FDAからさらなる解明を得て、FDAがその参考発売薬(RLD)を選択したら、私たちの重要な研究案を提出して検討すべきであることを指摘した。我々はすでに他の研究を完成し、適切な自動注射器RLDを決定し、最適な投与パラメータを研究し続けた。
FDAは2023年4月,アレルギーの提案商標名として独自名称過敏症を条件付きで受け入れた。アレルギー剤特許名称の最終承認は、FDAによるアレルギー剤の承認(あれば)に依存する。
2023年5月,PKとPD所見を評価した最新の臨床研究の積極的な結果を報告した。アレルギー反応が最大血中濃度に達するまでの時間(中央値Tmax)は10分,範囲は5−20分であった。アレルギーの早期薬物曝露10分間はアドレナリン手動注射と類似しており、4を超える
アドレナリン手動注射器より数倍高いですアレルギーと自動シリンジでは,2分前にPD効果が観察された。
2023年7月、アレルギー反応のための最新の臨床交差試験AQ 109103(“103研究”)の背線データを発表した。103番目の研究から,予想される最終用量投与説明を用いて,アレルギー薬システムがエピネフリンを提供する効果は,市販の自動注射器や手動筋注射(IM)と同様に有効であることが示唆された。12 mg投与後,エピネフリンの幾何平均最大濃度(Cmax)は457 pg/mL,最大濃度までの中央時間(Tmax)は15分であった。投与後10~60分のすべての時点で、曲線下で測定された部分領域(PAUC)は、以前に生成された手動0.3 mg筋肉注射とアドレナリン0.3 mg自動注射器データとの間に囲まれている。重要なことは,重要なPK研究で測定されることが予想されるすべてのキーパラメータについて,12 mgはTmaxの自動シリンジと同様に維持しながら,キー早期期間のCmaxおよびpAUCを含む103研究における分類基準を満たしていることである。103の研究は、代替用量で示される12 mgとアレルギー交差腕と、14 mgおよび最終用量で示されるアレルギー性薬剤とをさらに含む。103研究中の全例で安全と耐性が良好と考えられ,重篤な副作用はなかった。
われわれは最近,われわれが提出したアレルギー反応に対する重要な段階3 PK臨床研究案に対するFDAのコメントを受けた。FDAはそのコメントの中で,我々が提案した終点,サンプル量,統計分析が合理的であることを示している.予想されるように,FDAは投与後のPK持続可能性(30−60分)が重要な要素であることを注意し,PKの持続可能性を支援するために繰り返し用量データを使用することを提案している。
2023年12月、第1の患者は、アレルギー(アドレナリン)初期段階3重要薬物動態(PK)臨床研究において服用した。この2つの部分、第3段階、単中心、開放ラベルのランダム研究は、健康な成人対象における単回および反復用量のアレルゲンと単回および反復用量のアドレナリン筋注およびアドレナリン自動注射器(EpiPenおよびAUVI-Q)のPKおよび薬効学(PD)を比較することを目的としている。主な目的は,健常成人被験者のアレルギー単回注射とエピネフリン後エピネフリン単回投与のPKを比較することである。第2の目標は、反復投与後のPKの持続可能性を評価することと、アドレナリン筋注およびアドレナリン自己注射器と比較した単回および反復投与の安全性および耐性を評価することとを含む
完全な成人および小児科人為的因子計画は、アレルギー臨床開発計画の予想および進行中の一部であり、将来のラベルおよび予期される患者の製品の使用をサポートするためにアレルギーNDAにも含まれるであろう。
•AQST-108(舌下膜)-AQST-108は、プロドラッグであるピボリンからなり、投与後、その酵素をアドレナリンに切断する。Dipivefrinは現在米国以外の地域で眼科適応に応用可能である。Aqutiveは,アレルギー反応以外の他の疾患の治療に用いられる全身エピネフリンを提供する舌下膜製剤を開発している。Aqutive社が健康成人ボランティア28名で行った先の1期PK試験のTOPLINE結果によると,AQST−108は全体的に耐性が良好であり,観察された全身有害事象はエピネフリンの既知の有害事象と一致した。
•アドレナリン反復症-(アドレナリンプロドラッグプラットフォーム)-私たちのアドレナリンプロドラッグプラットフォームは現在、Adrenavseと命名されたより多くの適応および投与方法を模索している。著者らはすでにAdrenavseプラットフォームを用いてAQST-108局部製品の初歩的な調合を完成し、今後数ケ月以内に人体でこの調合をテストする予定である。体外データに基づいて、豚皮膚組織におけるAQST-108の急速な吸収が見られた。エピネフリンは血管収縮薬であり,皮膚をうまく透過できないが,エピネフリン嫌悪プラットフォームは局所吸収を許容し,様々な皮膚疾患に潜在的な治療法を創出している可能性が考えられる。この計画に関連する臨床前と実行可能性が完了した後,FDAとAdrenavseのIND前会議を要求し,FDAからのフィードバックを受けて開発の適応と進路を開示する予定である。
候補独自CNS製品
私たちの独自の薬膜の応用は®ある中枢神経系疾患を有する患者にとって、技術は特に価値と相関性があり、患者が満足されていない医療需要を満たし、そして患者の治療問題を解決する。CNS市場ではまだより多くの製品を開発する重要な機会があると信じています。また、著者らの独自技術と特許地位は中枢神経系以外に広く応用されており、著者らは他の疾患領域における薬物フィルムの応用を探索する予定である。私たちの独自のCNS製品の組み合わせの中で最も先進的な資産は、以下のようにてんかんに集中している
•解放者−口腔または頬内で使用されるジセパン可溶性フィルム製剤は、我々の最先端の特許研究製品候補である。AqutiveはLibervantを開発し,現在難治性てんかん患者に利用可能なデバイス依存救援療法の代替案として直腸ゲルと鼻腔スプレーである。2022年8月、FDAは間欠性疾患の急性治療のためのLibervantの予備承認を許可した
頻繁に発作するステレオタイプ発作(即…,てんかん叢集,急性反復発作)は,12歳以上のてんかん患者の通常発作パターンとは異なる。FDAは、Libervantが承認に必要なすべての品質、安全性、および有効性基準を達成したと結論した。FDAの既存の法規がValtocoを承認して孤児薬物市場の独占経営権を獲得したため、これは別の会社によって販売された12歳以上の患者のための安定鼻スプレー製品であり、FDAはLibervantがまだアメリカでマーケティングする資格がないことを決定した。この決定により,FDAは孤児薬物市場の独占経営権が2027年1月に満期になるまでLibervantに最終承認を与えることができなかった
2023年6月、間欠性、ステレオタイプの頻繁なてんかん発作の急性治療のための秘密保持プロトコルをLibervantに提出した(即2歳から5歳のてんかん患者において,患者の通常のてんかん発作パターンと異なるのは,てんかんの発作パターンが他のタイプのてんかん(例えば,てんかん,てんかん群集,急性反復発作)とは異なることである。FDAは申請を受けて審査を行い,PDUFAの目標日を2024年4月28日に指定した。悲劇的な®(安定)直腸ゲルは現在の年齢層の患者に適用される唯一の治療法である。Libervantの小児科NDAがFDAの承認を得られれば,FDAがValtocoに付与した孤児薬物の独占経営権を克服し,この患者年齢層の米国市場参入を付与される保証はない。また,別の会社がFDAの他の市場独占経営権を獲得しない保証はなく,Libervantがこの患者集団のどの年齢層でも米国市場に進出することを阻止している。この候補製品の許可スケジュールの検討については、“許可された商業製品および候補製品および他の製品−Libervant”を参照されたい。
許可を得た商業製品及び候補製品その他の製品
私たちの製品組み合わせには、私たちが許可しているか、または許可を求めている他の製品および候補製品、または私たちの知的財産権を商業化のために許可している他の製品および候補製品も含まれています。2023年12月31日と2022年12月31日までの年間で、我々のライセンス製品の組み合わせはそれぞれAqutiveのために5060万ドルと4770万ドルの収入を創出した。これらの製品には
•アブクセン®ブプレノルフィンおよびナロキソンの舌下薬膜製剤は、それぞれオピオイド依存性の治療のために米国および国際的に販売されているオピオイド作動薬およびアンタゴニストである。Suboxoneは2010年に我々のライセンシーIndior Inc.またはIndiorによって発売された。Suboxoneは同種製品の中で最も多く処方されているブランド製品であり,オピオイド依存治療のための初めての舌下膜製品でもある。私たちはSuboxoneの唯一のサプライヤーと独占サプライヤーであり、2010年の発売以来、27億剤を超えるSuboxoneを生産している。2023年12月31日現在,非特許フィルムベースの製品がこの市場に浸透するにつれ,Suboxoneブランド製品は約31%のフィルム市場シェアを維持している。私たちはブプレノルフィン-ナロキソンの非特許薄膜製品に関するいくつかの会社に特許侵害訴訟を提起した。これらの訴訟の詳細については第2部第8項を参照。財務諸表と補足データ、付記22、事件があったりここに載せてください。
•Exservan®Aqutive社は、筋萎縮性側索硬化症を治療するリルゾール口腔膜剤を開発した。ExservanはALSと診断され,従来の嚥下薬の困難に直面している患者に有意義な助けをもたらすと信じている。艾司朗は2019年11月22日にFDAの承認を得た。2019年第4四半期には、ALSを治療するためのExservanの開発と商業化のためのZambonにライセンスを付与することを発表した。Zambonは中枢神経系治療領域に集中している多国籍製薬会社である。Zambonとのライセンス契約条項によると、ExservanのEUでの開発と商業化権利の前払いがAqutiveに支払われ、Aqutiveは開発と販売マイルストーン支払いとEUでの純売上のより低い2桁の印税を獲得し、Emylifによってマーケティングされる 元本を讃える。ZambonはExservanを担当し,Zambonはこの製品を販売する国の規制承認とマーケティングを求め,Aqutiveはこの製品の開発と製造を担当している。Aqutiveは2022年第4四半期に、Zambonと合意した許可協定条項に基づいて規制部門のExservanに対する承認を得ることに関連する50万ドルの記念碑的支払いを受けた。2023年第2四半期、Aqutiveはザン邦との許可協定条項に基づいて、Exservanの許可地域の最初の国での初の商業販売と関連した50万ドルの記念碑的支払いを受けた。2021年1月、私たちはMTHAにExservanの米国での商業化の独占許可を授与したと発表した。MTHAはALS患者に専念する多国籍製薬会社である。この製品はMTHAによって2021年6月に発売された。MTHA許可プロトコルの条項によると,Aqutiveは米国MTHAのExservanの独占メーカーとサプライヤである.艾司朗はALS患者の重要な需要を満たす可能性があり,安全かつ容易に投与できるため,1日2回,水を必要としない。
2022年3月、私たちはハイスコに独占許可を授与し、中国で筋萎縮性側索硬化症を開発·商業的に治療するエストラランを開発·商業化させることを発表した。ハイスコは中国に本社を置く上場製薬会社です。ハイスコはエクソンモービルの中国での規制と商業化活動を指導する。エクソンはエクソンモービルの中国における独占メーカーとサプライヤーになる。修正されたHaiscoとの許可協定条項によると、Aqutiveは2022年9月に700万ドルの前払いを受け、規制のマイルストーンを得る
支払いは、2桁の特許権使用料の純売上高が中国であり、製造収入を稼いだ販売が中国である
•キエンモビ® パーキンソン病の間欠期の治療のためのドパミン作動薬であるアポモルフィン舌下膜製剤の開発。私たちの知的財産権をCynapsus Treateutics,Inc.にライセンスし,同社は2016年4月1日の合意(Sunovionライセンス協定により改訂)によりKYNMOBIの商業化のためにSunovionによって買収された。KYNMOBIは2020年5月21日にFDAの承認を得て、2020年9月にSunovionによって商業化された。2020年11月3日、マラソンの付属会社MAM穿山甲皇室有限責任会社と貨幣化協定を締結した。貨幣化協定の条項に基づいて、Sunovion許可協定に従ってSunovionのアポモルフィン製品KYNMOBIに関連する特許権使用料およびマイルストーン支払いを請求すべきすべての契約権利を販売した。2023年6月、SunovionはKYNMOBIを米国およびカナダ市場から自発的に撤退させることを発表したため、私たちは貨幣化協定下での追加または支払いを受けない可能性が高い。
•ズプレンツ®化学療法に関連する吐き気および嘔吐および術後回復の治療のためのセロトニン拮抗薬エンダンシドンの経口可溶性フィルム製剤の開発。エンダンシドンはブランドと模倣薬として提供され、例えば静脈注射、筋肉注射、口腔溶解錠、経口溶液錠とフィルムである。我々はZupenzの商業権をブラジルのHyperaに権限を与える(HyperaはOndifの名前で販売する).Hyperaは2022年2月21日にANVISAの承認を得てブラジルでZupenzを販売した。私たちはこの取引に関連した90万ドルの記念碑的支払いを受けた。私たちはZuplenzの商業権利をFortovia(以前はMidatech Pharma PLC)に許可して、アメリカ、カナダ、そして中国に許可した。Fortoviaは2015年に米国でZupenzを発売した。私たちはフォルトビア社Zuplenzの唯一で独占的な製造業者だった。Fortoviaは2020年8月31日,ノースカロライナ州東区破産裁判所に破産保護を申請した。2021年1月29日、破産裁判所は、AqutiveとFortoviaとの間の許可および供給協定が終了し、Zuplenz商業化されたすべての権利が私たちに返還され、2021年1月30日から発効する協定を承認した。
•アズスタリスTM6歳以上の患者のADHDの治療のためのFDA承認された1日1回の製品。AZSTARYSはD−メチルピペラレート(d−MPH)のプロドラッグである思デセチルからなり,即時放出されたD−MPHとともに調製された。2012年3月、私たちはZevraと協定を締結し、AqutiveとZevraが2011年4月に締結した協力と許可協定を終了した。この終了スケジュールによれば、私たちは、ZevraがKP-415およびKP-484化合物またはその誘導体の商業化または任意の他の金銭化から得られる任意およびすべての価値に関与する権利がある。これらの金銭化取引には、Zevraおよび協力、特許権使用料スケジュールに関する任意のビジネス合併に関連する取引、または製品Azstarysを含むZevraがこれらの化合物から価値を達成することができる他の取引が含まれる。2021年3月2日、ZevraはFDAがAzstarysによるADHDの治療を承認したと発表した。2023年12月31日までの1年間に、Zevraのマイルストーン収入として150万ドルの収入を記録した。
•解放者TM - FDAが初歩的に許可した安定口腔膜剤は、間欠性、板状印象の頻繁てんかん発作の急性治療に用いられる即…,てんかん叢集,急性反復発作)は,12歳以上のてんかん患者の通常発作パターンとは異なる。私たちはPharmanoviaと2022年9月26日から発効するPharmanovia協定を締結し、この協定に基づいて、私たちはPharmanovia協定の有効期間内にLibervantを開発し、それを商業化し、領土のある国のすべての年齢の長期或いは急性、痙攣発作の治療に使用するために、Pharmanoviaに私たちのある知的財産権の独占的な許可を与えた。Pharmanoviaプロトコルによると、Pharmanoviaはこの領土でのLibervantの規制と商業化活動をリードし、私たちはLibervantのこの領土での独占的な製造業者とサプライヤーとなる。協定に署名した後、私たちは350万ドルを受け取った。2023年3月27日からPharmanovia協定を改訂し,Libervantの許可領土範囲を米国,カナダ,中国を含まない世界の他の地域に拡大した。Pharmanoviaは拡大された地域で適切な規制承認を求める責任があるだろう。Pharmanovia修正案の条項によると、私たちはPharmanovia修正案を実行する時にPharmanoviaが支払った200万ドルの払い戻しできないお金を受け取った。
•Sympazan® 2018年11月1日、FDAは、2歳以上の患者のまれで難治性てんかんLennox-Gastaut症候群(LGS)に関連する発作を治療するためのクロロバザム経口可溶性フィルム剤を承認した。私たちは2018年12月にSympazanを商業化した。2022年10月26日、我々はAssertioの子会社Otter PharmPharmticals,LLCとライセンス契約を締結し、Assertioは患者に差別化製品を提供する専門製薬会社であり、この協定によると、私たちは協定期間内にそのSympazanの全世界独占知的財産権許可をUsertioに付与し、前金は900万ドルである。また,2022年11月には,米国特許商標局の特許出願に関する許可通知を受けた後,600万ドルのマイルストーン支払いを受けた
アメリカのシリアル番号16/561,573は、関連手当費用を支払います。Sympazan for Assertioの独占メーカーとサプライヤーであり、このようなプロビジョニング協定が満了した後、Usertioからその製品の製造費を取得します。私たちはAssertio社Sympazanの独占製造業者とサプライヤーです。
市場の概要
アレルギー反応
アレルギー反応は深刻な全身性アレルギー反応であり、ある食物、薬物、昆虫刺されとラテックスなどのアレルゲンによって引き起こすことができる。アレルギー反応のバイタルサインと症状は通常接触後数秒または数分以内に出現し、低血圧、皮疹或いは掻痒、収縮を含む可能性がある気道閉塞、呼吸困難、吐き気嘔吐。すぐに治療しないと,アレルギー反応は気道制限や心停止により死亡する可能性がある。アレルギー反応は生命を脅かす潜在的な全身性アレルギー反応であり、毎年10万人当たり50~112例が発作すると推定されている。ある国際研究では,15年の研究期間中にアレルギー反応により入院した人数が増加していることが分かった。アレルギー反応を引き起こす最もよく見られる原因は薬物、食物(例えば落花生)と昆虫に刺されて産生した毒である。アレルギー反応の進展が迅速であるため、反応発生後にできるだけ早く信頼性と正確な用量のアドレナリンを投与する能力は患者の回復と生存に重要である
アレルギー反応の治療には,通常,エピネフリンを早期に筋肉注射し,必要に応じて追加の筋肉または静注を行うことが含まれる。アドレナリン自動注射器の一種の模倣形式(ブランド形式EpiPen)はアドレナリンの主要な自己投与形式である。アレルギーやアレルギーのリスクがあることが知られている人は,いつでも2つのアドレナリン自動注射器を携帯し,アレルギー反応の第1の兆候が出現した場合に自己投与することを推奨されている。自動注射器は輸送が不便である可能性があり、多くの患者と看護人員は注射を分娩方式として好まない。アレルギー反応を経験した患者にとっては,適切な用量とタイムリーで確実にエピネフリンを有効に使用する能力が重要である。しかし,経口投与では複雑な分子を投与することはできず,患者に有意なメリットをもたらす可能性のある治療法の開発が制限されていると考えられる。著者らはAqutiveの専用PharmFilter技術を用いて、“第一種”口腔舌下膜配合を設計し、全身アドレナリンを提供し、アレルギー反応を治療する救急薬物として、患者のコンプライアンスを高め、総看護コストを低減した。私たちは非注射、より管理しやすく、効果の速い製品に大きな市場機会があると信じている。このような特徴を有する製品は,アレルギー反応中に信頼性と正確な副腎投与量を容易かつ迅速に自己投与することができ,患者のコンプライアンスを向上させると信じている。この候補製品の規制承認(保証できない)によると、アレルギー薬は現在の筋肉注射に関連する治療負担を軽減する可能性があり、用量が不正確またはタイムリーでないため、アレルギー反応に関連する医療システムのコストを低下させる可能性があると信じている。
てんかん?てんかん
てんかんは反復発作を特徴とする慢性中枢神経系疾患である。アメリカでは340万人がてんかんを患っている。SymMusic Healthのデータによると,2022年,抗てんかん薬は米国で数十億ドルの売上を創出した。米国では,てんかん患者に関連する直接的(医療)や間接(賃金や生産性損失)の年間コストは莫大である。
てんかんの治療案には通常,慢性と急性管理療法が含まれる。てんかん発作を抑制するために慢性薬が毎日使用されている。約110万のてんかん患者は引き続き突破的なてんかん発作を受け、急性(救援)管理策略が必要かもしれない。患者は通常,抗てんかん薬,あるいはAEDsと呼ばれ,慢性てんかん発作を制御する“維持”療法として処方される。多くの抗てんかん薬は神経細胞の興奮或いは神経細胞抑制経路に特化している。通常患者にベンゾジアゼピン類薬物を処方し、“救急”として急性てんかん発作を治療する方法である。
急性てんかん発作が発生した場合には,必要に応じて救急治療を行い,てんかん発作活動を迅速に中止する。現在、急性てんかん発作の治療に応用できる最も有効なベンゾジアゼピン類薬物の一つは安定である。安定は従来から直腸投与製品として市場に出されてきたが、最近では鼻腔スプレー製品が市場に導入されている。この薬の直腸投与は患者にとって特別な挑戦である。我々は,現在難治性てんかん患者の依存機器に利用可能な救急療法の代替案として,我々の候補製品Libervantを開発した。Libervant FDA承認プログラムおよび市場参入問題に関するより多くの情報は、上記の“我々の製品組合せとパイプ”と以下の本項目1における“競合”の節を参照されたい。
LGSを含む多くのてんかん症候群があり,まれな難治性てんかんである。LGS患者は通常薬剤耐性を有し,繰り返し発作しやすく,通常は抗てんかん薬の組み合わせが処方され,その中には通常クロバザムが含まれている。クロバザム(ブランド名Onfi)には錠剤と懸濁剤の2種類の剤形がある。患者もクロバザム錠剤や懸濁剤の模造バージョンを得ることができる。シンパザンはクロロバクタムといった他の投与経路の代替薬として開発された。
製造業と製品供給
私たちはインディアナ州のポティチで二つの製造と主要な包装施設を経営しています。現在私たちはそこで私たちの特許製品Suboxone、Exservan、OndifとSympazanを独占的に生産しています。これらの施設は、当社の独自製品パイプライン候補製品やライセンス製品の生産に適応するための総合的な能力を備えており、現在は追加のインフラを必要としていません。2022年には、シリーズ化と二次パッケージを含む製造能力を拡大する作業を完了しました。この拡張は私たちが私たちの既存と未来の可能なビジネス協力をより広く支援することができるようにする。インディアナ州におけるcGMPの施設に伴い、2023年に可能な追加製造能力を探索し続ける。製品開発の発展に伴い、私たちはまた、私たちが予想している施設とインフラ需要を考慮していきます。過去5年間で10億以上のワクチンを生産しましたインディアナ州のcGMP製造業務はDEAに登録されており,別表II−Vに適合している。
FDA、DEA、EU、ANVISA、その他の外国衛生当局の法規など、様々な法規の要求を受けていますTGAです。WEは私たちの施設を登録し、cGMP規格を守らなければならない。これらの標準は、製造プロセス全体にわたって、製造業者が詳細な設計、テスト、制御、文書、および他の品質保証手順に従うことを必要とする。我々の工場ではFDA,DEA,TGAの検査,および製薬会社によるcGMPコンプライアンスのいくつかの品質保証検査に合格している。いずれのケースにおいても,これらの施設は検査に合格し,定期的な再検査を受けている。これらおよび他の法律および規制要件を遵守しない場合、製造業者は、警告状、製品の差し押さえまたはリコール、禁止、製造業務に重大な制限または一時停止を加える同意法令、および民事および刑事罰を含む可能性のある法律または規制行動に直面する。製品または製品苦情の有害事象を報告しなければならず、ラベルを変更したり、製品を除去したりすることによって市場制限を実施することになる可能性がある。規制要件の遵守が維持されていない場合、または承認後に製品の安全性または有効性に関する問題が生じた場合、製品承認は撤回される可能性がある。
私たちは国内と国際的に合格した承認されたサプライヤーから活性薬物成分を含む原材料を購入します。可能な場合には、利用可能な場所でも適切な場所でも、キー原材料に対してマルチベンダー戦略を実行し続ける。私たちの製品包装アルミ箔はメーカーが提供しています。このようなメーカーは複数の生産施設を利用して私たちの包装アルミ箔を生産している。生産量の増加とより予測性に伴い、私たちは未来により正式な供給協定を締結し続けるかもしれない。
我々の内部臨床運営の監督の下で,我々は第三者CROを用いて我々の計画した臨床試験を管理·実行する多くの面で,監視と管理データを含み,これらのCROおよび医療機関,臨床研究者,コンサルタントに依存してわれわれの臨床計画に従ってわれわれの試験を行う。これらのCROは,このような実験のデータをその後に収集·分析する上で重要な役割を果たす予定である。
競争
我々は製薬やバイオテクノロジー会社と競争し,これらの会社は様々な疾患分野や適応を治療する治療法を開発·商業化している。また、著者らは先進的な投与プラットフォーム(例えば、経口、注射、鼻腔、経皮パッチと肺投与)を利用する会社と競争し、現在の看護標準よりも良い治療方法を創造する。この業界は競争が激しく、新製品と新技術の発展と発売速度が速い。この市場で運営されている会社には、多国籍企業、老舗バイオテクノロジー会社、単一製品製薬とバイオテクノロジー会社、専門製薬会社、後発薬会社が含まれている。多くの大きな成熟した組織は現在、内部で商業化能力を有しており、商業化権利を得るために、より小さい会社とパートナーシップまたはライセンス契約を締結する可能性がある。これらの会社は,我々の目標の適応を治療するための新薬を開発したり,既存の薬物を承認して我々の目標の適応を治療したりする可能性がある。
私たちは私たちが承認して承認を求めているすべての市場で商業化製品と競争するつもりだ。
バイオテクノロジーと製薬業界の特徴は、技術の急速な変化と進歩、競争が激しく、知的財産権の保護が強力であることである。私たちが開発と商業化に成功したいかなる製品や候補製品も、既存の治療法や将来出現する可能性のある新しい療法と競争する。他の治療法との効果的な競争に影響を与える重要な製品機能は、我々の製品の有効性、安全性と利便性、および任意のセットの診断方法の使いやすさと有効性を含む。後発薬競争の程度や政府と他の第三者支払者が提供する補償もまた私たちの製品の定価と競争力に著しく影響するだろう。
2020年1月10日,Aqutiveのライバルの一人がFDAによる安定鼻噴霧剤Valtoco候補の承認を得,この薬剤の孤児薬物排他性を獲得し,2020年1月10日から開始した。FDAの承認を得た孤児薬物指定会社は、承認日から7年以内に、米国でこの薬物指定適応の孤児市場独占経営権を獲得した。この孤児薬物独占的承認は、FDAの承認を求める後続製品が、候補薬物スポンサーが証明できない限り、同一孤児薬物適応の同じ活性部分の排他期間内に米国で販売されることを阻止し、FDAは、後者が承認された製品よりも臨床的に優れていると結論している(例えば:より安全で効率的で
患者看護に対する主要な貢献)はFDA法規とガイドラインの意味に符合する。候補薬物スポンサーがその候補薬が現在承認されている薬物以外に患者ケアに“大きな貢献をしている”ことを証明しているかどうかを評価する際には,FDAは具体的な状況に応じて評価を行い,単一の客観的基準がなく,適切な場合,FDAは治療場所の利便性,治療持続時間,患者の快適性,軽減された治療負担,投与の容易性と快適性の進歩,両剤間の時間間隔が長いこと,自己投与の可能性を考慮する可能性がある。
2022年8月、FDAは間欠性、ステレオタイプの頻繁なてんかん発作の急性治療にLibervantの使用を初歩的に許可した(即…,てんかん叢集,急性反復発作)は,12歳以上のてんかん患者の通常発作パターンとは異なる。FDAの結論は,Libervantは承認に必要なすべての品質,安全,治療効果基準を達成したことである。FDAの既存の法規が我々の競争相手に上記地西潘鼻噴霧剤製品の孤児薬物市場での独占経営権を付与しているため,Libervantはまだ米国で上場する資格がない。FDAの決定により,FDAは孤児薬物市場排他性が満了するまでLibervantに最終的な承認を与えることができない。特にわれわれが提出した食物の安定製剤吸収への影響に関する研究では,Libervantは独自の利点を持ち,食物を考慮することなく,必要に応じて随時投与することができ,患者に重要な利点を提供していると信じている
FDAは2023年9月にAqutiveな利楽(安定)口腔薬膜のNDAを受け,間欠的,板的印象を急性治療するための頻回てんかん発作活動(即2歳から5歳の患者にてんかん,てんかん叢,急性反復発作)が出現した。Diastat(安定)直腸ゲルはFDAが承認した現在唯一この患者集団に適した治療法である。LibervantのNDAがPDUFAに割り当てられる目標行動日は2024年4月28日である。Libervantの小児科NDAがFDAの承認を得られれば,FDAがValtocoに付与した孤児薬物の独占経営権を克服し,この患者年齢層の米国市場参入を付与される保証はない。また,別の会社がFDAの他の市場独占経営権を獲得しない保証はなく,Libervantがこの患者集団のどの年齢層でも米国市場に進出することを阻止している。
材料協定
重大な合意の詳細については、連結財務諸表第4部付記6、材料協定.
知的財産権
私たちは現在、商業的に合理的であれば、私たちの候補製品および関連技術の任意の特許可能な側面、または私たちが将来獲得する任意の新製品または候補製品について、特許保護を求め続けるつもりである。もし私たちの知的財産権が特許によって保護されていなければ、私たちは商業秘密を維持し、私たちの固有情報を慎重に保護することを含む他の方法でそれを保護することができる。
また,孤児薬が得られる司法管轄区で孤児薬の独占経営権を求める予定である。米国とEUで孤児薬の排他性を得るための前提条件は孤児薬を指定することだ。1つの薬物が稀またはあまり見られない疾患の治療に特化して開発された場合、孤児薬物の称号を与えることができる。孤児薬物の称号を有する製品がその後、その称号を有する適応の最初の規制承認を得た場合、その製品は、孤児薬物排他性を得る権利があり、これは、適用された規制当局が、いくつかの非常に限られた場合に、米国の7年以内およびEUの10年以内に、同じ適応について同一の薬物を販売する他のいかなる出願も許可しないことを意味する。孤立薬物排他性は,競争相手が排他的に保護された適応のために異なる薬物の開発や販売を阻止したり,異なる適応のために同じ薬物を開発あるいは販売したりすることを阻止しない。
特許
我々の特許組合せは現在、世界で少なくとも150件の発行された特許を含み、そのうちの少なくとも30件は米国特許であり、世界130件以上の係属中の特許出願である。これらの承認された特許および出願中の特許出願は、Suboxoneおよび私たちの薬膜配合タダラフィル、安定、クロバゾール、リルゾールおよびアドレナリンを含む、我々の薬膜技術および製品および候補製品に製造プロセスおよび物質組成保護を提供する。これらの特許は,特許として発行された場合,係属中の特許出願は2024年から2041年の間に満了する可能性がある。2017年に提出された未解決の特許出願は、特許として発行されれば、2041年に満了する可能性がある薬物フィルム用量製剤安定およびアドレナリンに物質組成および製造保護のプロセスを提供する。予想される満期日には、いかなる特許期限調整または特許期限延長も含まれていない。
薬膜-我々の口腔膜技術は
私たちの薬物フィルム技術は少なくとも12個の特許家族を持っている。これらの特許シリーズは、世界で少なくとも49件の発行された特許を含む技術、物質組成保護を我々のPharmFilter技術に提供し、そのうちの少なくとも12件は米国特許、および世界的に関連する係属中の特許出願である。特許及び係属特許出願は,特許として発行された場合,特許期限調整又は特許期間延長を含まずに2024年から2041年までの間に満了する可能性がある。
PharmFilm技術特許および/または特許出願はまた、一般的に、我々のCNS計画、我々の複雑な分子計画、および私たちの許可者計画の製品および候補製品で使用される技術を保護するために一般的かつ専門的である。例えば、我々のプラットフォームに含まれる技術特許および/または特許出願は、安定などのCNS分子のためのPharmFilm用量配合物の特定のカバー範囲である。私たちのプラットフォーム技術にはアドレナリンなどの分子を含む複雑な分子計画のカバー範囲も含まれています私たちのプラットフォーム技術特許および/または特許出願は、製品SuboxoneおよびZuplenz、ならびに私たちのアポモルフィンおよびタダラ非分子製剤をさらに含み、これらは私たちが許可した計画の一部である。これらの製品および候補製品をカバーする特許および特許として発表された保留出願の期限は2024年から2041年に延長され、いかなる特許期限調整または特許期限延長も含まれない。
私たちが発行したいくつかの特許は、米国特許商標局(USPTO)の再審と当事者間の審査、欧州特許機関(EPO)の反対など、行政訴訟に関連しているか、または関連していることに注目している。
私たちのいくつかの特許および特許出願は、承認されれば、FDAによって承認された治療同等性評価付き医薬製品に発表され、一般にオレンジブックと呼ばれる。逆に、オレンジブックに記載されている薬剤は、ANDAまたは505(B)(2)NDAの承認をサポートするために、潜在的な模倣薬競争相手によって参照されることができる。これらの潜在的な模倣薬競争相手が、彼らの製品が私たちが列挙した特許を侵害しない、またはこれらの特許が無効であると主張した場合、彼らはANDAまたは505(B)(2)NDAがFDAによって届出を受けた後に私たちに通知を送らなければならない。次に、特許満了、訴訟和解または侵害事件においてANDAまたは505(B)(2)NDA出願人に有利な裁決の30ヶ月前まで、FDAがANDAまたは505(B)(2)NDAを承認することを自動的に阻止する第4項の認証の通知に対して特許侵害訴訟を開始することができる。
私たちの残りの特許の組み合わせは、主に私たちが持っている特許および出願に関連し、私たちの製品開発組み合わせおよび他の候補製品、ならびに関連成分および/または製造プロセスに関する。
ビジネス秘密やその他の独自の情報
私たちは、私たちのビジネス秘密とノウハウを含めて、私たちの同僚、コンサルタント、および他のコンサルタントが雇用や採用を開始する際に秘密協定を実行することを要求する、私たちの固有の情報を保護することを求めています。これらの協定は、一般に、我々との関係構築中に開発または開示されたすべての機密情報を秘密にしなければならず、特定の場合を除き、第三者に開示してはならず、その雇用範囲外で使用してはならないと規定されている。私たちの同僚の場合、協定は一般的に、法的に許可された範囲内で、私たちのために働き、私たちの財産を利用し、または私たちの業務に関連し、雇用中に構想または完成されたすべての発明が私たちの固有の財産でなければならないと規定している。適切な場合、私たちが私たちのコンサルタントと合意した合意は、一般に同様の発明条項譲渡も含まれている。しかも、私たちは一般的に私たちの機密情報を受け取った第三者の秘密協定を取得しなければならない。しかし、許可されていない場合、または商業秘密を開示する場合、これらの合意は、私たちの商業秘密に意味のある保護または十分な救済措置を提供することは保証されない。
商標
私たちはまた商標に依存して私たちの競争地位を発展させて維持する。私たちの商標または登録商標は、米国および他の選択された地理的地域に提出される。
監督管理
FDA承認プロセス
アメリカでは、医薬品はFDAによって広く規制されている。連邦食品、薬物と化粧品法案、あるいはFDCAと他の連邦と州法規、その他のほか、薬品の研究、開発、テスト、製造、保存、記録保存、承認、ラベル、販売促進とマーケティング、流通、承認後のモニタリングと報告、サンプリング、および薬品の輸出入を管理する。適用されるFDAまたは他の要件を遵守しないことは、FDAが係属中の申請の承認、臨床封印、警告または無タイトル手紙、製品リコール、製品差し押さえ、生産または流通の完全または部分的な一時停止、製品の市場からの撤回、禁止、罰金、民事処罰、および刑事起訴のような様々な行政または司法制裁を受ける可能性がある。
以前に承認された薬物の新しい使用を含む任意の新薬または剤形は、米国で発売されるためにFDAの承認を得なければならない。FDAが新薬が米国で発売される前に要求されるプログラムは、一般に、以下のようなものを含む
•FDAのGLP規定に従って臨床前実験室と動物試験及び調合研究を完成した
•米国がヒト臨床試験を開始する前に発効しなければならないヒト臨床試験申請をFDAに提出する
•各臨床試験が開始される前に、各臨床試験場所の独立したIRB承認;
•現在の良好な臨床実践またはGCPに基づいて十分かつ制御されたヒト臨床試験を行い、各予期される用途に対する提案された医薬製品の安全性と有効性を決定する
•食品医薬品局に秘密保持協定を提出し
•FDAの現在のcGMP規制に適合するかどうかを評価して、施設、方法、および薬物の特性、強度、品質、および純度を維持するのに十分な制御を保証するために、製品を製造するためのFDAの1つまたは複数の施設の承認前検査を満足するように完了する
•FDA諮問委員会が適用可能な審査を満足的に完了させること;および
•NDAに対するFDAの審査と承認。
臨床前と臨床テストと承認過程は長年の時間を要し、もしあれば、承認を得るのに要する実際の時間は製品或いは疾病のタイプ、複雑性と意外性によって大きく異なる可能性がある。
臨床前試験は製品の化学、調合と毒性に対する実験室評価、及び製品特性と潜在安全性と有効性を評価する動物研究を含む。臨床前試験の進行は現在のGLPを含む連邦法規と要求に適合しなければならない。臨床前試験の結果はIND申請の一部として他の情報とともにFDAに提出され,製品化学,製造と制御に関する情報および提案された臨床試験案が含まれている。IND申請を提出した後,生殖毒性や発ガン性の動物試験など,長期的な臨床前試験を継続する可能性がある。
IND申請はFDAが受け取った30日後に自動的に発効し、FDAが30日以内に1つ以上の提案された臨床試験に対して懸念或いは問題を提起しなければ、人類の研究対象が不合理な健康リスクに直面することを心配することを含む臨床試験を保留する。この場合,INDスポンサーやFDAは臨床試験開始前に未解決の問題を解決しなければならない。製品開発期間中に行われる後続の臨床試験ごとに既存のIND申請を単独で提出しなければならない。さらに、各臨床試験が予定されている場所をカバーする独立したIRBは、その場所が試験を開始する前に、任意の臨床試験の計画および被験者のインフォームドコンセント情報を審査および承認しなければならず、完成まで研究を監視しなければならない。FDA、IRB、またはスポンサーは、対象または患者が受け入れられない健康リスクに直面していること、またはIRBの要件を遵守できないことを発見すること、または他の条件を適用する可能性があることを含む、様々な理由で臨床試験を随時一時停止することができる。臨床試験はGCP要求に基づいて、合格した研究者の監督の下で、健康ボランティア或いは患者に研究用新薬を提供することに関連し、その中にはすべての研究対象に任意の臨床試験に参加することを要求するインフォームドコンセントを書面で提供することが含まれている。臨床試験のスポンサーは通常、NIHが維持しているウェブサイトClinicalTrials.govに登録し、いくつかの臨床試験の重要なパラメータを報告しなければならない。
秘密協定の提出と承認のために、ヒト臨床試験は通常、以下の順序で行われ、これらの段階は重複または合併する可能性がある
| | | | | |
位相.位相 1 | 第1段階では、新陳代謝、薬物動態、薬理作用、用量増加に関連する副作用、および可能であれば有効性を評価するために、薬物を最初に健康なヒト対象または患者に導入することによって、有効性を評価するための早期証拠を評価する。 |
位相.位相 2
| 第2段階は、一般に、特定の適応、用量耐性、および最適用量での薬剤の有効性を決定し、よく見られる副作用および安全リスクを決定するために、限られた患者集団で試験を行うことに関連する。 |
位相.位相 3
| 第三段階試験を行うことは、より多くの患者の臨床治療効果と安全性の追加情報を得るためであり、通常は地理的に分散した臨床試験地点であり、FDAが薬物の全体的な効果-リスク関係を評価することができ、薬物のラベルに十分な情報を提供することができる。多くの場合、FDAはこの薬物の治療効果を証明するために、十分かつ良好にコントロールされた2つの3期臨床試験を必要とする。少数の情況下で、もし研究が大型多中心試験であり、内部一致性を証明し、しかも統計学的に説得力のある発見は死亡率、不可逆的な発病率或いは疾病の予防に臨床意義があり、そして潜在的な深刻な結果があり、第二回の試験で結果を確認すれば、他の確実な証拠を持つ単一第三段階試験で十分であるかもしれない。
|
必要な臨床試験が完了した後,NDAを用意してFDAに提出する。この製品が米国で発売される前に、FDAがNDAを承認する必要がある。秘密保護協定にはすべてが含まれていなければならない
臨床前、臨床とその他のテスト、及び製品の薬理、化学、製造と制御に関するデータアセンブリ。連邦法によると、多くのNDAの提出には巨額の申請使用料が必要であり、承認されたNDA申請に基づく出願人は、処方薬製品毎の年間計画費を納付する必要があり、2018年度から、この費用は製品や開設費に代わる。
FDAはNDAを受信した日から60日の時間があり,当該機関の敷居に基づいて申請が届出を受けているかどうかを決定し,申請が十分完全であると考え,実質的な審査を行うことができる。FDAは秘密協定の申請を受け入れるのではなく、より多くの情報を提供することを要求するかもしれない。この場合、セキュリティプロトコルは、追加の情報と共に再提出されなければならず、追加の使用料を支払う必要がある。再提出された申請はFDAが届出を受ける前にも審査を行わなければならない。提出された申請が受け入れられると、FDAは深い実質的な審査を開始する。PDUFAによると、FDAは二級分類システム--標準審査と優先審査--新しい開発薬物のいくつかの業績目標を審査することに同意した。優先審査は、治療において大きな進展を得るか、または適切な治療法がない場合に治療を提供する薬剤として指定される。FDAは10~12ヶ月以内に標準審査を受けた出願を審査するように努力しているが、FDAは6~8ヶ月以内に優先審査申請を審査することを目標としている。
NDAを承認する前に、FDAは、通常、GCP要件に適合することを確実にするために、1つまたは複数の臨床場所を検査する。FDAは、製造プロセスおよび施設がcGMP要件に適合していることを決定し、要求された仕様内で製品が一貫して生産されることを保証するのに十分でない限り、製品を承認しないであろう。NDAに含まれるデータは、研究された適応において安全かつ有効であることを証明する多くの証拠を提供する。
FDAがNDAと製造施設を評価し、スポンサー検査を行う可能性がある後、それは承認状または完全な返信状を発行する。完全な応答文は、一般に、NDAにおける不足点を概説し、FDAが出願を再検討するために、大量の追加のテストまたは情報を必要とする可能性がある。この補足情報を提出しても、FDAは最終的に承認された規制基準を満たしていないことを決定する可能性がある。NDAが再提出されたとき、またはいつ、これらの欠陥がFDAによって満足的に解決された場合、FDAは承認書を発行するであろう。FDAの審査は2カ月のI類再提出と6カ月の2類再提出である。この薬物の商業マーケティングを許可し、特定の適応の具体的な処方情報を提供する。
NDA承認の条件として、FDAは、この薬剤の利点が潜在的なリスクよりも大きいことを保証するのを助けることをREMSに要求するかもしれない。FDAが審査申請中にREMSを行う必要があると判断した場合,医薬品スポンサーは承認時にREMS計画に同意しなければならない。REMSは、薬物ガイドラインまたは患者パッケージ挿入、医療保健提供者に薬品リスクを理解するためのコミュニケーション計画、誰が薬物を発行または分配することができるかの制限、または処方または割り当てのための専門的なトレーニングまたは認証のような安全な使用を確保する他の要素、場合によってはのみ割り当て、特殊な監視、および患者登録簿の使用などの様々な要素を含む必要があるかもしれない。また,再生可能エネルギー管理システムは,再生可能エネルギー管理システム計画が有効であるかどうかを定期的に評価するスケジュールを含まなければならない。REMSに対する要求は1種の薬物の潜在的な市場と利益能力に重大な影響を与える可能性がある。
また、製品承認には、薬物の安全性または有効性を監視するために大量の承認後試験·監督が必要となる可能性があり、FDAはこれらの上場後計画の結果に基づいて製品のさらなる販売を阻止または制限する権利がある。承認されると、規制基準が守られていない場合、あるいは最初のマーケティング後に問題が発見された場合、製品承認は撤回される可能性がある。医薬品は、承認された適応でのみ販売され、承認されたラベルの規定に基づいて販売され、FDAが製品を承認しても、ラベルまたは流通制限または他のリスク管理メカニズムを含む他の条件を適用するために、承認された適応を制限することができる。
承認申請において確立されたいくつかの条件のさらなる変更は、適応、ラベルまたは生産プロセスまたは施設の変更を含み、新しいNDAまたはNDA補充剤を提出し、FDAの承認を得てから変更を実施する必要があり、これは、より多くのデータを開発するか、またはより多くの臨床前研究および臨床試験を行う必要があるかもしれない。新適応のNDAサプリメントは通常,オリジナル出願のような臨床データを必要とし,FDAがNDAサプリメントを審査する際に使用するプログラムはNDAを審査する際に使用するプログラムと類似している。
承認後に要求する
FDAがNDAを承認した後,継続的な有害事象報告と定期報告の提出が必要である。FDAはまた、承認製品の効果を監視するために、いわゆる第4段階試験、REMSおよび監督を要求することができ、またはFDAは、承認時に条件を付加して、その製品の流通または使用を制限する可能性がある。また、品質管理、薬品製造、包装、ラベルプログラムは承認された後、引き続きcGMPとNDA仕様に適合しなければならない。薬品メーカーとそのいくつかの下請け業者はFDAに彼らの工場を登録し、ある州機関から許可証を取得しなければならない。Fdaの登録要求エンティティはfdaの定期抜き打ち検査を受け,その間,fdaは製造施設を検査してcgmpsのコンプライアンスを評価する
または有害事象記録や報告などの他の法律が適用される。したがって、製造業者は、不良事象記録および報告要件のようなcGMPまたは他の適用法律の遵守を維持するために、生産および品質管理の分野で時間、資金、訓練、およびコンプライアンス努力を継続しなければならない。もしある会社が規制基準を遵守できなかった場合、もし同社が初期マーケティング後に問題に遭遇した場合、あるいはその後以前に意識されていなかった問題や新しい懸念が発見された場合、監督管理機関は救済、製品承認の撤回、または製品のリコールを要求する可能性がある。また、他の規制行動をとることができ、他にも、警告状の発行、製品の差し押さえ、禁止令、生産作業の重大な制限または一時停止の同意法令、民事処罰、刑事起訴を含むことができる。
また,いずれの処方薬製品の流通も米国処方薬販売法やPDMAに適合しなければならず,これはFDCAの一部である。また、2013年に連邦薬品品質と安全法案第2章、すなわちDSCSAは、薬品サプライチェーンにおけるメーカー、流通業者、その他の実体の処方薬製品流通に対して新たな“追跡”要求を提出した。このような要求は10年以内に段階的に施行されるだろう。DSCSAは最終的に製品表示が必要になります(即米国で流通されているいくつかの処方薬を識別および追跡するために、相互操作可能な電子処方薬製品システムを確立するためである。DSCSAはPDMA中の以前の薬物“系統”の要求を代替し、そして現有の国家薬物系統の法律と法規を先制した。DSCSAはまた,卸と第三者物流サプライヤーの許可に対して新たな要求を規定している.これらの許可要求は先制され、各州がDSCSAに基づいてFDAによって確立された基準と一致しない、それほど厳しくない、それに直接関連する、または他の方法で含まれる許可要求を実施することを防止する。FDAがDSCSAの新しい国家許可基準を解決するための法規を公布する前に、現在の州許可要求は一般的に有効である。
“ハッジ·ワックスマン修正案”
ANDA承認プロセス
Hatch−Waxman修正案は、FDA以前にそのNDAプログラムによって承認されたものと同等であることが証明された薬剤のための簡略化されたFDA承認プログラムを確立する。これらの薬物の販売·流通の承認は,ANDAをFDAに提出することで得られた。ANDAは,他を除いて,活性薬物成分,医薬製品調製,規格,模倣薬の安定性に関するデータと情報,分析方法,製造過程検証データ,品質制御プログラムを含む総合報告である。後発薬の発売前応用は略称と呼ばれ、それらは通常安全性と有効性を証明する臨床前と臨床データを含まないからである。逆に、後発薬申請者はその製品と革新薬物が生物学的同等性があることを証明しなければならない。場合によっては、ANDA適合性出願の提出および承認に基づいて、出願人は、参照革新薬とは異なる強度または剤形に対するANDAの模倣薬の承認を得ることができる。FDAがこの模造製薬が革新者製品と比較して新たな安全性と有効性の問題を提起していないことが発見された場合、この模倣薬のANDA申請への適合を承認する。FDAが、製品が参照イノベーター薬と同等ではないと判断した場合、製品が異なる用途に使用されることが意図されている場合、または承認された適切な申請を受けていない場合、製品はANDA承認を得る資格がない。しかし,このような製品はNDAで承認され,臨床試験の支持的なデータがある可能性がある。
505(B)新規開発エリア×2
以前のFDAによって承認された製品の処方または用途を修正することをFDAが承認する代替経路として、出願人は、FDCA第505(B)(2)条に従ってNDAを提出することができる。第505条(B)(2)条は、ハッジ·ワックスマン改正案の一部として制定され、承認に必要な情報の少なくとも一部が、出願人又は出願人のための研究からでない場合に機密協定を提出することを可能にする。505(B)(2)出願人がFDAに依存する以前の安全および有効性発見が科学的に適切であることを証明することができる場合、新製品のいくつかの臨床前または臨床研究の必要性を除去することができる。FDAはまた、承認されたブランドからの参照薬物の変化を支援するための臨床試験を含む追加の研究または測定を企業に要求する可能性がある。次いで、FDAは、ブランド参照薬のすべてまたは一部が承認されたラベル適応の新製品候補、および505(B)(2)出願人が求める任意の新しい適応を承認することができる。
オレンジ図書リスト
NDA(505(B)(2)NDAを含む)を介して薬物承認を求める場合、出願人は、特定の特許をFDAに列挙することを要求され、その権利が出願人の製品をカバーすることを要求される。秘密協定の承認が得られると、薬物出願に記載されている各特許はオレンジ書に発表される。任意の出願人がOrange Bookに記載されている薬物の模倣薬等価バージョンまたはOrange Bookに記載されている薬物に関連する505(B)(2)NDAを承認するためにANDAを提出する場合には、(I)出願の対象となる医薬製品の特許情報がFDAに提出されていないこと、(Ii)特許が満了していること、(Iii)その特許が満了した日、または(Iv)当該特許が無効であるか、またはその出願が対象とする医薬製品の製造、使用または販売によって侵害されないことをFDAに証明しなければならない。最後の認証を第4項認証と呼ぶ。各船主に第4段落の認証の通知を提供しなければならない
認証対象の特許,およびANDAまたは505(B)(2)出願が指す承認されたセキュリティプロトコルの所持者である.出願人はまた、記載された使用方法特許を証明するのではなく、その提案されたラベルが特許使用方法に関連するいかなる言語も含まない(または刻まれた)ことを証明する“第8節”宣言を提出することを選択することができる。
第4項の認証通知を受けてから45日以内にOrange Bookに記載されている特許に特許挑戦を行った場合、FDAは、第4項の認証、特許満了、訴訟和解又は侵害事件において出願人に有利な裁決を受けてから30ヶ月まで、当該出願を承認してはならない。ANDAまたは505(B)(2)の出願も、オレンジブックに記載されているブランド参照薬の任意の適用非特許排他性満了まで承認されないであろう。
非特許排他性
特許排他性に加えて、上場薬品の守秘協定保持者は、特許とは無関係な排他期間を有する権利がある可能性があり、その間、FDAは、上場薬品に依存するANDAまたは505(B)(2)の出願を審査または承認することができない。例えば、ある会社は、NDAが新しい化学物質またはNCEを承認した後、5年間の非特許排他性を得ることができ、新しい化学物質またはNCEは、FDAが任意の他のNDAで承認されていない活性部分を含む医薬である。活性部分“は、医薬物質の生理的または薬理作用を担う分子またはイオンとして定義される。5年間の排他期間内に、FDAは、薬剤の模倣薬バージョンの承認を求めるいかなるANDAまたは505(B)(2)NDAの申請を受け入れることができず、これは、FDAによる薬物の調査結果に依存するが、後続の申請者が第4段落の認証を行った場合、FDAは4年後の申請を受け入れることができる。
第505条(B)(2)条に従って承認された薬剤を含む医薬であって、1つ以上の新しい臨床研究(バイオアベイラビリティまたは生物学的同等性研究を除く)が承認申請に重要であり、出願人によって/賛助された場合、特定の承認条件下で3年間の排出期間を得ることができるか、または以前に承認された製品の新しい処方のような市販製品を変更することができる医薬。これが発生した場合、FDAは、3年の排他期間が終了するまで、任意のANDAまたは505(B)(2)保護修正の申請を許可することを禁止される。しかし,NCE排他性とは異なり,FDAは申請を受け入れ,排他的な間にプログラムの審査を開始することができる.
孤児薬の指定と排他性
孤児医薬品法は、まれな疾患または疾患の治療のための製品の開発にインセンティブを提供する。孤児医薬品法によれば、FDAは、米国では20万人未満または米国で20万人を超える影響を及ぼす疾患または疾患であることが一般的であり、このような疾患または疾患を治療する医薬または生物製品を米国で開発および生産するコストは、製品の販売から回収されるという、まれな疾患または疾患の治療のための医薬または生物製品に孤児の称号を付与することができる。スポンサーが稀な疾患または疾患の治療を目的としていることをスポンサーが証明した場合、FDAは、この製品の孤児を孤児疾患適応として指定することを許可する。秘密保護協定を提出する前に、孤児としての指定を要請しなければならない。FDAが孤児製品の指定を承認した後、FDAは、治療剤の識別情報およびその潜在的な孤児の使用を開示する。しかしながら、指定孤児薬は、規制審査および承認過程においていかなる利点も伝達されず、規制審査および承認過程の持続時間を短縮することもない。
孤児薬物の指定はメーカーに研究支出、税収控除、孤児薬物の独占資格を提供する。孤児薬物指定を有する製品がその後、そのような指定された疾患または疾患の活性部分を有するFDAの最初の承認を得た場合、この製品は、限定された場合を除き、FDAが同じ適応を有する同じ活性成分を有する別の製品を承認することを7年以内に禁止する権利がある。孤児製品に指定された薬物が市販承認された場合,その適応範囲は指定された孤児適応を超えており,孤児薬物排他性を得る権利はない。場合によっては、孤児特許は、同じ適応を有する同じ有効成分の後続製品が、より良い治療効果または安全性に基づいて承認された製品よりも臨床的に優れていることが証明された場合、または患者ケアに重大な貢献をする場合、または孤児の薬物特許を有する会社が市場ニーズを満たすことができない場合を含む別の製品の承認を阻止しない。また、FDAは、これらの製品が異なる有効成分を含む限り、1つ以上の製品を同一の孤児適応または疾患に使用することを許可することができる。さらに、競争相手は、異なる製品が孤児製品に対して排他的な指示を有する承認を得るか、または同一製品に対して排他的であるが孤児製品に対して排他的な異なる指示の承認を得ることができる。したがって、私たちの候補製品が孤児排他性を獲得しても、私たちは競争の影響を受ける可能性がある。もし競争相手が同じ薬物の承認を得た場合、または私たちの候補製品が競争相手の製品に含まれていると決定された場合、同じ適応や疾患のために、孤立独占も7年以内に私たちの製品が承認されることを阻止する可能性がある。
逆控除及び虚偽申告法その他の規制事項
米国では、医療保健の“詐欺や乱用”に関する複雑な法律法規の制約を受けており、“連邦反リベート法規”、“連邦虚偽申告法”、その他の州と連邦法律法規を含むが、これらに限定されない。連邦反リベート規制は、処方薬製造業者(またはそれを代表する側)を含む誰でも、インフォームドコンセントおよび故意の場合、特定の薬剤の購入、注文または処方を含む業務推奨を誘導するための任意の報酬を請求、受け入れ、提供、または支払うことは不法であり、これらの報酬は、連邦医療保険または医療補助などの連邦医療計画に従って支払われる可能性がある。この法律に違反した人は最高5年の禁錮刑、刑事罰金、行政民事罰金を科され、連邦医療計画から除外されることができる。しかも、多くの州は連邦反リベート規制のような法律を採択した。その中のいくつかの州禁止は、連邦医療保険や医療補助などの連邦医療計画だけではなく、転介患者が任意の保険会社の精算を受ける医療サービスに適用される。
連邦虚偽請求法案は、虚偽または詐欺的な物品またはサービス(薬品を含む)を連邦計画(連邦医療保険および医療補助を含む)に提出する誰もが、要求に応じて提供されていない物品またはサービスのクレーム、または医療上不必要な物品またはサービスのクレームを提出することを禁止する。支払者に直接クレームを提出することはありませんが、これらの法律によると、メーカーが顧客に不正確な請求書やコード情報を提供したり、ラベル外で製品を宣伝したりすることによって“原因”とみなされて虚偽または詐欺的なクレームを提出しているとみなされた場合、責任が問われる可能性があります。また,報告卸売業者や我々製品の推定小売価格,報告医療補助フィードバック情報を計算するための価格やその他,我々の製品に影響を与える連邦,州,第三者精算の情報,製品の販売やマーケティングに関する活動は,この法律の審査を受けている。例えば、連邦虚偽請求法案によると、製薬会社はその薬品のラベル外普及に責任があることが発見された。虚偽請求法案違反の処罰には、政府が実際に受けた被害の3倍に加え、個々の虚偽請求に対して10,000~25,000ドルの強制民事罰金が科され、連邦医療保健計画への参加から除外される可能性があり、連邦虚偽請求法案は民事法規であるにもかかわらず、虚偽請求法案違反を招く行為には様々な連邦刑事法規が関与している可能性がある。また,個人は連邦虚偽申告法に基づいて訴訟を起こすことができ,ある州では連邦虚偽申告法に倣って法律が制定されている。
HIPAAはまた、医療詐欺や医療問題に関する虚偽陳述を含むいくつかの追加的な連邦犯罪を拡大し、創出した。医療詐欺法規は、個人第三者支払者を含む任意の医療福祉計画を意図的かつ故意に詐欺する計画を禁止する。虚偽陳述法令は、重大な事実を故意に偽造、隠蔽または隠蔽すること、または任意の重大な虚偽、架空または詐欺的な陳述または陳述を行うこと、または任意の重大な虚偽、架空または詐欺的陳述または記録項を含む任意の虚偽文字または文書を作成または使用して、医療福祉、プロジェクトまたはサービスを提供または支払いすることを禁止する。
医薬品製造業者および/または営業者に要求する州法も増えている。一部の州は、医薬品マーケティングおよび販売促進に関連する費用の報告と、これらの州の個人保健事業者に支払われたプレゼントと支払いを報告することを要求している。他の州では、いくつかのタイプのプレゼントや食事を提供するなど、マーケティング関連の様々な活動が禁止されている。値上げに関する情報や値上げの理由、あるいは処方薬の価格詐欺を禁止することを含むいくつかの価格設定情報の報告を要求する州もある。また,カリフォルニア州,コネチカット州,ネバダ州,マサチューセッツ州,コロンビア特区などの州は製薬会社にコンプライアンス計画および/またはマーケティングコードの実施を求めている。その中の多くの法律はこのような法律を遵守するために要求される内容に対して曖昧だ。さらに、以下に説明するように、同様の連邦は、製造業者に、過去数年間に医師、医師アシスタント、看護師従事者、臨床看護師専門家、登録看護師麻酔科医、登録看護師助産師、および教育病院に支払われたいくつかのお金を追跡して連邦政府に報告することを要求する。また、これらの法律とその実施は明確性が不足していることから、私たちの通報行動は関連州や連邦当局の処罰条項によって制限される可能性がある。
“医師支払い陽光法案”は開放支払い計画の形で実施され、その実施条例は連邦医療保険、医療補助或いは児童健康保険計画に基づいて精算可能なある薬品、器械、生物製品と医療用品のメーカーが毎年CMSに前年のいくつかの支払いに関する情報を報告し、そして医師、医師アシスタント、勤務看護師、臨床看護師専門家、登録看護師麻酔師、登録助産師と教育病院への他の価値移転、及び医師及びその直系親族が持つ所有権と投資権益を要求する。
さらに、HIPAAおよびその実施条例は、健康計画および大多数のヘルスケア提供者、およびそのような業務パートナーのような法的拘束されたエンティティに対して、そのような保護された健康情報のプライバシーおよびセキュリティの面で、HIPAAが保護された健康情報の使用または開示に関連するいくつかのサービスを提供することに、いくつかの義務が規定されている。また、ほとんどの州では法律が公布されており、場合によっては健康情報のプライバシーとセキュリティを管理しています
場合によっては、その多くは大きく異なり、特定の疾患状態のような場合の契約遵守作業を複雑化させるために、同じ効果を生じない可能性がある。
このような法律法規を遵守するためには多くの資源が必要だ。私たちはもう独自の薬品の商業販売に従事していませんが、私たちは将来的に独自製品の商業販売に従事するかもしれません。さらに、このような様々な詐欺や法律の乱用の範囲が広いため、私たちの過去のいくつかの商業活動は、1つ以上のそのような法律の挑戦を受けるかもしれない。このような挑戦は、私たちの業務、財務状況、運営結果に実質的な悪影響を及ぼす可能性がある。政府当局が、我々の業務行為が現在または将来、詐欺および乱用または他の医療関連法律および法規を適用する現行または将来の法規、法規または判例法に適合していないと結論付けた場合、これらの法律に基づいて制裁を実施することができ、これらの制裁は重大である可能性があり、民事罰金、損害賠償、実体または個人を政府医療計画から除外すること、刑事罰金および個人監禁、これらの法律違反の告発を解決するために会社の誠実な合意または他の和解協定の制約を受けた場合、私たちの業務を削減または再構築する可能性がある場合、追加の報告要求がある可能性がある。しかも、このような規定が遵守されていないので、私たちは契約の損害と名声の損害を受けるかもしれない。私たちがこれらの法律に違反していると判断されなくても、政府のこれらの問題の調査には通常、大量の資源がかかり、否定的な宣伝が必要だ。
国際規則
アメリカの法規以外に、私たちは今と将来、私たちの製品の開発、承認、商業販売、流通に関する様々な外国法規の制約を受けるだろう。私たちの製品がFDAの承認を得ているかどうかにかかわらず、私たちはこれらの国で臨床試験を開始したり、販売したりするために、外国の比較可能な規制機関の必要な承認を得なければならない。承認プロセスは国によって異なり、追加の製品テストおよび追加の審査期間に関連する可能性があり、FDAの承認を得るのに要する時間よりも長いか短い場合があります。その他の事項以外にも,臨床試験,製品許可,定価,精算などを管理する要求は国によって異なる。一方の国の規制承認は他の国の規制承認を確保することはできないが、1つの国で規制承認を得られなかったり、遅延したりすることは、他の国の規制過程に悪影響を及ぼす可能性がある。もし私たちが適用された外国の規制要求を遵守できなかった場合、私たちは罰金、一時停止、規制承認の撤回、製品のリコール、製品の差し押さえ、運営制限、刑事起訴を受ける可能性がある。連合やEUでは、私たちは集中権限手続きや国家許可手続きを通じてマーケティング許可を求めることができる。
集中手順それは.ヨーロッパ薬品管理局(European Medicines Agency、EMAと略称する)は人類薬物の集中審査プログラムを実施し、EU全体で有効なマーケティング許可を促進した。この手続きにより、欧州委員会はEMAの有利な意見に基づいて単一のマーケティング許可を発行し、この許可はEU全体およびアイスランド、リヒテンシュタイン、ノルウェーで有効である。以下のヒト薬剤は強制的である:遺伝子工学のようなバイオテクノロジープロセスに由来し、HIV/エイズ、癌、糖尿病、神経変性疾患または自己免疫疾患および他の免疫機能障害などの特定の疾患の治療のための、ならびに公式に指定された孤児薬の治療のための新しい活性物質を含む。これらのカテゴリに属さない医薬品の場合、関連する薬剤が重大な治療、科学的または技術的革新である限り、またはその許可が公衆の健康に有利である限り、出願人は、集中販売許可出願をEMAに提出することを選択することができる。
国家認可手続きそれは.いくつかの欧州連合国でも、他の2つの可能な経路が医薬製品を許可しており、これらの経路は集中プログラムの範囲に属さない研究用医薬製品:分散プログラムと相互承認プログラムに適している。分権手続きの下で、出願人は、1つ以上のEU諸国において、どのEU諸国でも許可されていない薬品出願のために同時に許可することができ、集中手続の強制範囲に属さない。相互認識手続きによると、薬物はまずEU加盟国でその国の国家手続きに従って許可される。国家認可を取得した後、出願人は、関連国が元の国家マーケティング許可を認めることに同意した手続きに基づいて、他のEU諸国にさらなるマーケティング許可を求めることができる。
EUでは、孤児製品として指定された医薬製品は、マーケティング認可申請費または減免費用の削減、および医薬製品の承認後10年の市場排他性のような財政的インセンティブから利益を得る。孤児の条件に適合するための医薬製品であって、(I)生命または慢性衰弱を脅かす疾患の治療、予防または診断に使用されなければならない、(Ii)このような疾患のEUでの流行率が万分の5を超えてはならない、またはその開発に必要な投資が合理的であることを証明するのに十分な見返りをもたらすことが不可能でなければならないこと、および(Iii)疾患の診断、予防または治療に関する任意の満足できる方法が許可されていないか、または、そのような方法が存在する場合、その疾患の影響を受けている人に顕著な利益を与えなければならない、医薬製品。
アメリカの医療改革
米国や他の地方の政策立案者や支払者の中で,医療システムの改革を推進することに大きな興味があり,医療コストの抑制,質の向上および/または参入拡大を既定の目標としている。米国では,PACAは政府と民間保険会社が医療保健に資金を提供する方式を大きく変え,製薬業に重大な影響を与えている。私たちの業務に影響を与える可能性のある変化は、連邦医療計画の登録、精算変化の管理、Medicare Part D処方薬計画の保証不足内の患者の福祉、または一般的に言われるドーナツホール(製造業者は、保証不足中に条件を満たす受益者に適用ブランド薬品交渉価格の70%の販売時点割引を提供することに同意しなければならない)、医療保険取引所の処方薬福祉に関するルール、Medicaid薬品返却計画の変化、公衆衛生サービス340 B薬品定価割引計画の拡大、または340 B計画、詐欺および乱用、および法執行を含む。これらの変化は現有の政府医療保健計画に影響を与え、業績計画のための連邦医療保険の支払い、及び医師の品質報告システムとフィードバック計画の改善を含む新しい計画の発展を招いた。
一部の州はその医療補助計画を連邦貧困レベル133%まで収入の高い個人に拡大しないことを選択し、これはPACAが許可した。医療補助計画の拡大を選択しない州では,全体的に保険に加入する患者が少なくなる可能性があり,規制承認を得た製品の販売,業務,財務状況に影響を与える可能性がある。新しい患者がPACAが提供する任意の新しい医療補助オプションに基づいて保険を受けると,メーカーはこのような場合に使用する薬物として医療補助リベートを支払うことを要求される可能性があり,この決定はメーカーの収入に影響を与える可能性がある。
公布以来、PACAのいくつかの側面は多くの司法、行政、行政、立法方面の挑戦を受けており、私たちは将来的にPACAに対してより多くの挑戦と修正案を提出することが予想される。PPACAの各部分は現在アメリカ最高裁判所で法律と憲法の挑戦に直面しており、前のいくつかの政府は各種の行政命令を発表し、コスト分担補助金と各種条項を廃止し、これらの条項は各州に財政負担をもたらすか、あるいは個人、医療保健提供者、健康保険会社或いは薬品或いは医療機器メーカーにコスト、費用、税収、罰金或いは監督管理負担をもたらす;国会はPPACAを大幅に改正或いは廃止するためのいくつかの立法を提出した。PPAAが覆されるか、廃止されるか、代替されるか、またはさらに修正されるかどうかは不明だ
処方薬や生物製品価格の上昇を受けて、米国政府は薬品定価のやり方の審査を強化した。このような審査は最近のいくつかの国会調査を招き、製品価格の透明性の向上、価格設定とメーカー患者計画との関係の審査、政府計画の製品精算方法の改革を目的とした連邦と州立法を提案し、採択した。2020年7月24日、衛生·公衆サービス部長に指示する4つの行政命令が署名され、公布された:(1)医薬品メーカーが連邦医療保険D部分計画の発起人または薬局福祉マネージャーに提供した特定の遡及値下げの安全港保護を廃止し、これらの値下げは販売所では適用されず、これは最近の総合支出法案によって2032年に延期される可能性がある;(2)個人免除によって他の国から特定の薬物を輸入することを許可し、インスリン製品の再輸入を許可し、FDAが2019年12月に提出したカナダからの薬物の輸入を許可する規則を優先的に決定する。(3)Medicare計画のいくつかのMedicare B部分の薬剤の支払いが他の比較可能な国/地域の支払いよりも高くないことを確実にすること(製薬業者が他の措置に同意するかどうかに依存する);および(4)FQHCによって購入されたインスリンおよびアドレナリンのいくつかの低収入個人を許可し、340 B医薬計画の一部として、FQHC支払いの割引価格でこれらの薬剤を購入する。FDAは2020年10月1日、カナダからある処方薬の輸入を許可する最終規定を発表した。2020年9月13日、トランプ総裁は、連邦医療保険B部分がカバーするいくつかの高コスト処方薬と生物製品の支払い調整後の最恵国価格(すなわち最低価格)のために、連邦医療保険B部分がカバーするいくつかの高コスト処方薬と生物製品の支払い調整後の最恵国価格(すなわち最低価格)をテストするための規則制定計画を実施するよう行政命令に署名し、この薬品メーカーは1人当たりの国内総生産に比較可能な経済協力と発展組織加盟国で販売された薬品を有する。いくつかの提案された措置は、発効するために追加の立法許可を必要とするが、国会は、価格または患者の精算制限、割引、特定のアクセスおよびマーケティングコスト開示の制限および透明性措置を含む新たな立法および/または行政措置を継続して、他の国からの輸入および大量調達を奨励することを目的としていることを示している
最近、2022年の“インフレ率低減法”(IRA)には、HHS内に薬品価格交渉計画(2026年から)を確立し、ある選定された薬物の徴収協議をメーカーに要求する“最高公平価格”や規定を守らないための消費税の支払いを含む一連の重大な薬品定価改革が含まれており、連邦医療保険B部分とD部分に基づいてメーカーに対して税金還付要求を制定し、インフレを超える価格上昇(初2023年満期)を懲罰し、D部分福祉を再設計し、メーカーにD部分薬物への割引の一部を提供することを要求する(2025年から)。
薬品の価格設定に関する追加行政や立法措置が提案されるかどうかを予測することは困難である。州レベルでは、立法機関は、価格または患者の精算制限、割引、特定の製品参入およびマーケティングコスト開示の制限、および透明性措置を含む、価格または患者の精算制限、割引、特定の製品参入およびマーケティングコスト開示の制限および透明性措置を含む医薬品および生物製品の定価を制御するための法規を立法および実施することが増えており、場合によっては、他の国からの輸入および大量購入を奨励することが目的である。将来的にとりうる医療改革措置は,我々の業界全体および規制承認を得た製品の販売を維持または増加させることや,我々の候補製品の商業化に成功する能力に実質的な悪影響を及ぼす可能性が予想される。
保証と精算を請け負う
私たちの製品と候補製品の商業が成功し、承認されれば、保険の利用可能性と公共にある程度依存する(即連邦と州政府と個人(即、商業)支払人。これらの第三者支払者が、製品または療法が医学的に不適切または不必要であると判断した場合、彼らは、製品または療法の全部または一部の保証または精算を拒否することができる。また、第三者決済者は、処方や他のコスト制御機構を用いてカバー範囲を制限し、特定のプログラムや薬物治療の精算金額を制限し、コストを制御し続ける。
以上のように,薬品コストは政府や第三者支払者の大きな興味を引き起こし続けている。管理型ヘルスケアの傾向を考慮すると,管理型ヘルスケア組織の影響力が大きくなっていることや,追加的な規制や立法提案を考慮すると,製薬業は定価圧力に直面することが予想される。私たちの運営や業務結果は、現在と将来の第三者支払者政策や医療立法改革の悪影響を受ける可能性があります。
また、薬品を購入するには、各種の連邦と州医療保健計画に基づいて割引定価或いはリベートを提供しなければならず、連邦医療保険と医療補助サービスセンターの医療補助薬品返却計画、連邦医療保険B部分計画と連邦医療保険D部分カバーギャップ割引計画、アメリカ退役軍人事務部の連邦供給スケジュール計画及び衛生資源とサービス管理局の340 B薬品定価計画を含む。具体的な価格は医療補助薬品リベート計画のような医療計画下の政府機関に報告しなければならない。報告された価格を決定するために必要な計算は複雑であり、価格を正確に報告できなければ、私たちは罰を受けるかもしれない。
一部の第三者支払者は、任意のMedicare精算計画の任意の変更、これらの要件または発表、またはそのような提案を含む、将来的にコスト制御措置をとるか、または実施する可能性があり、候補製品のために十分な価格および利益運営を得る能力に実質的な悪影響を及ぼす可能性がある。
国際市場では,精算や医療保険支払い制度は国によって異なり,多くの国で特定製品や治療法に価格上限が設定されている。私たちの製品や候補製品が医学的に合理的であることは保証されず、特定の適応が必要であり、私たちの製品や候補製品が第三者支払者によって費用対効果があると考えられている保証はなく、十分な精算レベルが保証されていないし、第三者支払者の精算政策が私たちの製品や候補製品を販売する能力に悪影響を与えない保証もなく(承認されれば)、利益を得ることはできない。
これらの計画に関するより多くの情報は、本年度報告10−K表の“リスク要因”部分のタイトル“我々の製品または候補製品の十分な保険および補償レベルを実現して維持することができなければ、承認されれば、彼らの商業成功は深刻な阻害を受ける可能性がある”というタイトルで、これらの計画の他の情報を議論している。
その他の法規
我々はまた,我々の研究に関連する実験室実践,動物実験使用,および危険あるいは潜在的危険物質の使用と処置に関する様々な法律や法規に支配されている。我々は、適用される環境法規および他の法規を遵守していると信じているが、上述したように、FDAおよび他の政府機関は、罰金および民事処罰の徴収、承認の一時停止または延期、製品の差し押さえまたはリコール、および承認の撤回を含む幅広い規制および法執行権力を有しており、そのいずれかまたは複数は、私たちに重大な悪影響を及ぼす可能性がある。
人力資本
2023年12月31日まで、私たちは約135人の同僚を雇用した。我々のすべての同僚は米国で雇用されており,そのうち20人が直接研究開発に参加し,92人が製造運営に参加し,23人が業務開発および一般·行政活動に参加している。私たちの同僚たちは労働組合代表を持っていない
文化と同僚の敬業度
私たちは私たちの同僚たちが私たちの戦略の重要な構成要素であり、私たちの持続的な成功に必須的だと信じている。私たちの企業価値観-安全、コンプライアンス、協力、誠実さと高業績-私たちが雇った同僚、私たちが彼らを引き付けるためのステップ、そして私たちがお互いに扱う方法に基づいて、これらはAQUINTの成功の創造力、革新と生産性を促進します。
私たちの管理チームはこの理念を支持し、リスク管理、道徳、コンプライアンスに関連する政策や手順を含む、私たちの政策や手続きが私たちの希望する企業文化を反映して強化することを保証します。
私たちは、組織の成功を推進する適切な技能と人材を持つ多様な従業員チームを誘致し、維持するために、競争力のある報酬戦略と福祉計画を設計、計画、実行するためにコンサルタントを招聘した。また、私たちの同僚に組織パフォーマンスに関する重要な対話に参加させ、それに応じて私たちの同僚に報酬を与えて、成功と魅力的な職場を作ってもらいました。私たちはすべての同僚たちが耳を傾けられ、影響を与え、すくすくと成長する機会がある包容的な文化を作るために努力している。
同僚の健康、健康、安全
私たちの同僚たちの福祉は重要であり、私たちは安全で健康な職場を作るために努力している。私たちはこの約束を支持するために持続的な訓練を提供する。
私たちは引き続き積極的に私たちの同僚、彼らの家族、私たちの患者、私たちの製品の安全を確保するとともに、アメリカと世界の新冠肺炎の構造にも引き続き注目していきます。早期に同僚を動員し、常に安全に対する私たちの約束を強化するための組織情報を通じて、私たちは全世界の新冠肺炎疫病による多くの挑戦を克服することができる。私たちは私たちの同僚と接触し、彼らに新冠肺炎の伝播を防止するように教育して、私たちの業務に与える影響を最小限に抑える。私たちは疾病管理センターのガイドラインに従い、必要に応じて同僚を検査と隔離した。
環境安全
私たちは環境リスクがほとんどないが、私たちは世界的な解決策の一部になるために努力している。私たちは環境に責任のある実験室廃棄物収集、回収、処分計画を展開している。私たちは私たちの同僚たちが環境に責任を負うことを教育して奨励する。私たちは2023年12月31日まで政府と環境規制を遵守した。
利用可能な情報
私たちは、私たちの年度、四半期、定期および現在の報告、依頼書、および取引法の情報要件に適合する他の情報を米国証券取引委員会に提出または提出します。これらの材料を電子的にアーカイブまたは米国証券取引委員会に提供した後、私たちは、適切な可能な範囲内で、私たちの委託書、Form 10-K年間報告、Form 10-Q四半期報告、Form 8-K現在の報告、およびこれらの報告の修正および他の公開された提出された情報をできるだけ早く無料で提供します。インターネット上でこれらのファイルや他の情報を見つけることができるアドレスはhttps://aQuesve.comである.当サイトに含まれている情報は、引用で本年度報告書に組み込まれることはありません。この情報を本年度報告の一部と見なすべきではありません。私たちの年度、四半期、定期と現在の報告、依頼書、その他の公開申告書類もアメリカ証券取引委員会のエドガーデータベースで無料で入手できます。サイトはwww.sec.govです。
新冠肺炎関連商業動態
新冠肺炎は私たちの業務、運営、臨床試験、監督許可過程、資本、財務と貨幣化市場、財務結果と財務状況、及び私たちの業務に必要なサプライヤー、流通業者、顧客と他の第三者(規制承認過程に参加する第三者を含む)への影響の程度は、未来の発展に依存し、これらの発展は非常に高い不確定性を持っており、疫病の持続時間と持続深刻度、疫病の巻き返し、政府が新冠肺炎の持続或いは追加行動を抑制し、ワクチンの治療効果、及び新冠肺炎の短期と長期影響に関する新しい情報を正確或いは明確に予測することができない。
これまで私たちは製品の生産と供給を継続することができ、現在は供給に大きな中断は発生しないと予想されているが、この状況を注視し続けているにもかかわらず、新冠肺炎による中断や遅延が発生しない保証はない。私たちはまた私たちの製品に対する需要を監視しています。これは新冠肺炎の流行中にマイナスの影響を受ける可能性があり、私たちの顧客とライセンシーの財務状況を監視しています。
プロジェクト1 A.様々なリスク要因の評価
我々の普通株への投資は重大なリスクに関連しており、投資家は、以下に説明するリスクと、本年度報告書にForm 10−Kフォーマットで含まれるまたは参照される他のすべての情報とを慎重に考慮しなければならない。多くの様々なリスクがあり、既知のものもあれば、未知のものもあり、それらは私たちの目標達成を阻害するかもしれない。以下に説明する危険は私たちが直面する唯一の危険ではない。本年度報告の10-K表の他の情報を除いて、以下に列挙する任意の要因は、当社の業務、財務状況、運営または見通しの結果、および当社の株式の取引価格に大きなマイナス影響を与える可能性があります。この部分には前向きな陳述が含まれている。本年度報告書の冒頭のForm 10-Kにおける前向き記述の制限および制限の説明を参照すべきである。本節で示したドルの金額は千単位である
リスク要因の概要
私たちの業務、経営業績、財務状況に影響を及ぼす可能性のある重大なリスクは、必ずしも以下に関連するリスクに限定されるとは限らない
•私たちは未来に多くの資金を集めて、私たちの運営に資金を提供する必要があるかもしれない。これらの資金は受け入れ可能な条件で獲得できないか,あるいはまったく獲得できない可能性があり,業務目標を実行するために資金を提供する能力も保証されていない.必要に応じて必要な資本を得ることができない場合、私たちに行動の一部または全部を延期、制限、削減、または停止させることができるかもしれない。
•私たちは設立以来重大な運営損失を出しており、私たちが利益を達成したり維持したりすることを保証することはできません
•私たちはアメリカや他の国で私たちの製品を販売する規制の承認を得ることができないかもしれない
•競争相手の孤児薬品市場の独占的な地位のため、現在のLibervantの米国市場進出の障害を克服できなかった
•医薬製品の開発は長くて高価な過程と関連があり、結果は不確定である。私たちはどんな製品の開発と商業化を完了する過程で追加コストが発生したり、遅延が発生したり、最終的には完成できないかもしれません
•もし私たちの競争相手が私たちのPharmFilter技術よりも安全で、より効果的で、安く、より使いやすい、またはより魅力的な中枢神経系疾患の診断と治療、およびアレルギー反応治療製品を開発できれば、私たちの業務は不利な影響を受けるだろう
•私たちの候補製品が商業販売に承認されても、販売やマーケティングインフラを発展させることができなければ、アメリカで私たちの製品を商業化することに成功できないかもしれません
•候補製品を商業化する能力は、政府と衛生行政当局、個人健康維持組織、健康保険会社、その他の医療支払者が精算を提供する程度にある程度依存する
•アレルギー薬および私たちの他の候補製品の臨床試験の時間、コスト、および成否の任意の遅延または変更;
•私たちのPKとPDの比較可能性がFDAに承認されたアレルギー反応で十分なデータを生成できなかった
•FDAに提出されたLibervantの2~5年のPKとPD比較可能なデータ不足:
•私たちはすでに第三者と協力、許可手配、合弁企業、戦略連合またはパートナーシップに到達する可能性があり、これらの協力、許可手配、合弁企業、戦略連合、またはパートナーシップは、商業的に実行可能な製品の開発、または重大な将来の収入をもたらすことができないかもしれない
•私たちは現在も将来も第三者CROに依存して私たちのすべての臨床試験を行うつもりだ。これらの第三者がその契約義務または監督義務の履行に成功しなかった場合、または予想される期限内に完了した場合、第三者を交換する必要がある場合、または私たちの臨床計画または規制要件または他の理由を遵守できなかったために、彼らが得たデータの品質または正確性が損なわれた場合、私たちの臨床前開発活動または臨床試験は、延長、遅延、一時停止または終了される可能性があり、規制部門の任意の候補製品の承認を得ることができない可能性がある
•私たちの未来の成功は私たちが肝心な管理者を維持し、合格者を引き付け、維持し、激励する能力にかかっている
•私たちが知的財産権とノウハウを保護する能力は不確実だ
•私たちまたは私たちの同僚は、競争相手のいわゆる商業秘密を誤って使用したり、開示したり、競争相手との競争禁止または入札協定に違反したりして、損害賠償を招く可能性がある
•私たちの製品と運営は広く政府によって規制されており、適用された要求を守らないことは、私たちの業務に影響を与える可能性があります
•もし私たちがより多くの普通株を発行して資本を調達すれば、私たちの既存の株主は深刻な希釈を受けるだろう
•私たちはAqutiveに対する現在の訴訟事項の損害賠償を受けるかもしれない
•ネットワークセキュリティは企業に影響を与え続け、企業の中断を招く可能性がある
•私たちの業務と運営は新冠肺炎の悪影響を受けるかもしれない
•金融サービス業の不利な発展に影響を与え、現在及び予想されている業務運営及び当社の財務状況及び運営結果に悪影響を及ぼす可能性がある
私たちの財務状況と追加資本需要に関連するリスク
設立以来、私たちは重大な損失を受けており、予測可能な未来には、永遠に実現できないか、利益を維持することができないかもしれない重大な損失を受け続けると予想される。
私たちの候補製品のいくつかは、多くの追加の開発時間と資源を必要とし、その後、私たちは規制の承認を得て、商業化インフラと戦略を実施するか、または製品の販売または版税流からの収入を開始するために製品を許可することができるだろう。私たちの現在の候補製品はまだ初期段階にあり、短期的には候補製品の販売や版税から大量の収入を得ることはできないかもしれない。
私たちは製品開発に大部分の財力を投入した。これまで、私たちは主に株式と債務証券、債務融資収益、特定の製品許可と協力の収入を売却することで、私たちの運営に資金を提供してきた。将来の純損失の程度は将来の支出の速度と私たちの創収能力にある程度依存するだろう。
候補薬物の開発、監督管理審査過程と商業化は重大なリスクと重大な不確定性に関連し、私たちがコントロールできない事項を含む。薬品開発に関連する多くのリスクと不確実性のため、私たちが支出した時間や金額を完全に予測することはできない。私たちは将来的に大量の費用が発生することを予想し、私たちが開発活動と製品の組み合わせを拡大するにつれて、この費用は増加すると予想される。私たちが将来生じると予想している費用は
•候補製品の臨床試験を行いました
•私たちが臨床開発に成功した任意の候補製品のために規制の承認を求める
•私たちの知的財産権の組み合わせを維持し、拡大し、保護する
•新しい技術または開発段階または承認された製品を得ることができる
•製品の事前商業化に関する活動
•我々の製品開発を支援し、上場企業としての私たちの運営を支援する人員を含む、臨床、科学、運営、財務、管理情報システムの人員を増加させる
•失敗または不完全成功の試験、複雑な結果、セキュリティ問題、または他の規制課題を含むが、これらに限定されないが、上述した任意の問題に遅延または遭遇することによって増加するコスト。
少なくとも今後数年以内に、候補製品の開発努力と商業化に伴い、純損失が続くと予想される。私たちの純損失は異なる時期に大きく変動する可能性があります。これは私たちの候補製品に関する監督管理の承認発展、私たちが計画した臨床試験の時間、そして私たちの他の研究と開発の支出に依存します。私たちの支出は2024年と今後も大幅に増加すると予想されています
•引き続き臨床でアレルギー反応を開発し、FDAが発売を許可するために必要な支持データを提供する
•私たちの候補製品のために許可と他の取引を求め続けています
•現在の競争相手の孤児薬物市場の独占的な地位によるLibervantの米国市場進出の遅延を克服するためにFDAと接触し続ける。
Suboxone収入の低下を踏まえ,支出のタイミングやレベルの管理を継続するとともに,アレルギー薬の開発と商業化に重点を置く予定である。
私たちが利益を達成する前に、将来的には株式や債券または両方を発行することで大量の追加資本を調達し、私たちの費用を管理し続けて、私たちの資本滑走路を拡大し、私たちの製品や製品候補製品をさらに開発し、規制部門の承認を得て、私たちの業務を展開する必要があると予想されます。私たちは約束された追加的な資本源もなく、これらの必要な資本や債務融資が有利な条件で提供されるか、または根本的に保証されないという保証もない。私たちは、将来的に私たちの普通株を発行することによって、他の公共またはプライベートエクイティまたは債務融資、潜在的な非希釈融資イベントによって追加資本を得ることを求めることができ、これらのイベントは、私たちの許可製品からの可能性があり、知的財産権は、他の会社との協力または許可によって現金化された使用料フローを手配することができるかもしれないS、製品、製品候補、工場又はその他の有形資産を含む資産を売却することにより、他の方法でも可能であれば私たちが受け入れられる条項で追加資本や他の資金を調達することができない場合や、資金を調達することができないかもしれませんが、必要な場合に資金を調達できない場合は、業務計画を実行する能力を危うくし、そのような資金を受け取るまで業務を延期または削減する可能性があります。私たちが株式証券を発行することで追加資金を調達する場合、私たちの株主は希釈に直面し、債務融資(利用可能であれば、私たちの債務ツールの下のすべての既存の制限および条件の制約を受ける)は、制限的な契約の増加と固定支払いの増加、または他の方法で私たちの財務的柔軟性をさらに制限することに関連する可能性がある。私たちが協力や許可手配を通じて追加資金を調達する場合には、私たちの知的財産権のいくつかの権利を放棄したり、私たちに不利な条項で許可を付与する必要があるかもしれません。さらに、潜在的な協力者または許可された側が支払うお金は、通常、交渉開発と規制マイルストーンを達成したかどうかにかかっている。このようなマイルストーンを達成できなかったことは私たちの未来の資本状況を損なうかもしれない。
私たちは私たちの業務を支援するために多くの追加資金が必要になるだろうし、これらの資金は全くなければ受け入れられる条件で提供できないかもしれない。
私たちの2024年以降の現金需要には、当社製品の持続的な開発と臨床評価に関連する費用、製造·供給コスト、規制出願コスト、特許訴訟費用および訴訟費用、当社製品の商業化に関連する費用、および規制されている業界で運営されている上場企業の要求に応じたコストが含まれています。2023年12月31日現在、私たちは2390万ドルの現金と現金等価物を持っている。
私たちが2019年に最初に設立したATM施設は資金を提供する可能性があり、この施設によると、私たちは時々私たちの普通株の株を提供して売ることができます。ATM施設は2023年12月31日に約2400万ドルの普通株が利用可能である。2022年4月、リンカーン公園と購入契約を締結しました。この協定によると、リンカーン公園に時々私たちの普通株の株式を購入させるかもしれません。2023年12月31日現在,リンカーン公園との購入契約は約6,486,623株に相当する。
2023年11月1日、元金総額45,000ドルの13.5%債券を発行し、債務返済義務を削減しました。次発行で得られた純額の一部はすべての未償還12.5%債券の償還および次発行に関する支出の支払いに用いられ、残りは一般会社用途として使用される。債権率は13.5厘、年利は13.5厘で、四半期ごとに配当され、それぞれ毎年3月30日、6月30日、9月30日、12月30日(日付ごとに“支払日”)に配当されている。13.5%債券の利息は2026年6月30日にのみ適用され、13.5%債券の元金分割払いと、前金、支払い、加速、買い戻し、償還(場合に応じて)の適用日に決定された部分脱退費用を固定的な償却スケジュールに基づいて支払います。
私たちの流動性需要や現金需要を満たすための十分な資金がなければ、必要な場合には、上記のソースや他のソースから、あるいは十分な資金がない場合には、リストラ、延期、大幅削減、さらには現在または計画されている研究開発計画や臨床および他の製品開発活動の一部または全部を停止したり、将来の商業化努力を減少させたりすることが要求され、そうでなければ、他の支出を大幅に削減し、私たちの運営計画を調整し、私たちの流動性を改善するための他の措置を求める必要がある。私たちはまた、私たちの独自製品候補計画の追加的な許可機会(ある場合)を評価することを要求される可能性があり、現在、私たちは、これらの行動のいずれも合理的な条項で利用可能または利用可能であることを保証できないにもかかわらず、これらの機会を自己商業化するか、または他の潜在的な流動性機会または他の代替案またはオプションまたは戦略代替案を探索することを計画している。もし私たちが運営を続けるのに十分な資金がなければ、私たちは破産保護や他の代替案を求めることが要求されるかもしれないが、これは私たちの株主がAqutiveでの投資の大部分を損失させる可能性がある(すべてでなければ)。
私たちは追加の株式を売却したり、債務を発生させたり、許可手配によって資金を調達して私たちの運営に資金を提供するかもしれません。これは、私たちの株主が希釈され、私たちの業務に制限を加えたり、所有権を放棄することを要求したりする可能性があります。
Aqutiveは純損失の歴史を経て,2023年12月31日までの累計赤字総額は3.191億ドルであった。純損失と累積赤字が販売された毛利部分が相殺される
商業実施許可側と共同開発側が支払う商業化許可と独自製品,許可料,マイルストーン,特許権使用料。
2020年11月、私たちはATM施設の使用を開始した。2023年12月31日までの年間で4,958,341株を売却し,手数料やその他の取引コスト50万ドルを差し引いた純収益は約900万ドルであった。このATM施設は2023年12月31日までに約2400万ドルが利用可能である。
私たちが私たちの運営を十分に支援するのに十分な収入を生成することができる前に、私たちは、公共またはプライベート·エクイティまたは債務融資、第三者融資、マーケティングおよび流通スケジュール、ならびに他の協力、戦略連合および許可スケジュール、またはこれらの方法の任意の組み合わせによって追加の資本および現金資源を求める必要があるだろう。私たちが株式または転換可能な債務証券を売却することによって追加資本を調達する場合、株主の既存の所有権権益は希釈され、条項は清算または既存の株主権利に悪影響を及ぼす他の特典を含む可能性がある。債務融資は、私たちの普通株の株式を購入する引受権証のような株式成分と組み合わせることができ、既存の株主の所有権が希釈される可能性もある。追加債務の発生は、固定支払義務の増加を招き、特定の限定的な契約の増加をもたらす可能性もあり(その多くは、すべてでなければ、現在私たちの既存の債務配置の下に存在しています)、例えば、追加債務を生成する能力が制限されており、私たちが知的財産権や資産を売却できる可能性がある能力が制限されていることや、私たちが業務を展開する能力に悪影響を及ぼす可能性があり、私たちのすべての資産および知的財産が留置される可能性のある経営制限を継続しています。もし私たちがこのような債務で約束を破ったら、私たちはこのようなすべての資産と知的財産権、そして私たちが業務を運営する能力を失うかもしれない。
もし私たちが第三者との協力または戦略連合、マーケティング、流通、または許可手配によってより多くの資金を調達する場合、私たちは、私たちの技術、候補製品、または未来の収入流の貴重な権利を放棄するか、または私たちに不利な条項にライセンスを付与する必要があるかもしれない。
私たちが将来私たちの運営から収入を生むことができても、私たちの収入と運営収入は毎年または四半期の間に大幅に変動し、私たちの株価変動をもたらす可能性がある。
私たちが将来の収入を作ることができても、私たちの運営結果は毎年と四半期の間に大きな差があり続けるかもしれない。他の要因を除いて、差は以下の要素によって引き起こされる可能性がある
•FDAまたは任意の他の規制機関が承認した時間、任意のFDAまたは他の規制機関の承認の遅延、またはそのようなFDAまたは他の規制機関の承認を得ることができなかった
•競合他社の候補製品がFDAまたは他の規制承認を得ることは、私たちの製品が任意のこのような規制承認および/または孤立薬物独占許可を得る前に、米国で7年間の孤立薬物市場独占経営権を得ること、または私たちの製品候補製品の米国市場への進出を阻止する他のFDAマーケティング独占許可を得ることを含むことができる
•特定の候補製品のプロセス検証のためのスケジュール;
•FDAによって承認されたアレルギー薬を処理するのに必要な任意の追加のデータの時間およびそれによる遅延;
•私たちは新製品候補製品の研究、開発、買収、許可、または普及の時間と金額の変化を研究、開発、買収、許可した
•私たちが研究、開発、臨床前研究、臨床試験計画にかかる時間、金額、結果
•私たちの製品または候補製品に関連する深刻または予期しない健康または安全問題
•他の人は新しいブランドと非特許製品を発売して、私たちの候補製品を時代遅れにして、より激しい競争に直面したり、競争力に欠けたりします
•私たちは製品の価格と毛金利を維持する能力を維持しています
•Medicare、Medicaidの変更を含む健康計画と他の健康保険会社の保険範囲と補償政策を変更する
政府の医療計画のようなものです
•私たちは複雑な政府法規を守ることができますこれらの法規は私たちの業務の多くの側面に適用されています
•私たちの製品と候補製品を製造するための原材料コストが増加した
•製造仕様または現在の良好な製造仕様に準拠していないことによる製品のリコールまたはリコールを含む製造および供給中断;
•私たちの協力協定に関する収入確認時間
•私たちは、私たちの知的財産権を保護し、任意の関連する法的手続きまたは任意の性質の他の法的手続きにおいて他人の知的財産権およびいかなる不利な発展を侵害することを回避することができる
•既存または未来に第三者と行われる可能性のある訴訟の結果および費用。
私たちの債務レベルと巨大な債務超過義務は、私たちが私たちの業務に投資する能力を制限し、私たちの運営に資金を提供することを難しくするかもしれない。
私たちは大量の債務と大量の債務返済義務を持っている。2023年12月31日現在、我々の未返済債務元金総額は4,500万ドルで、13.5%の債券に相当する。未来に、私たちはもっと多くの資金を集める必要があるだろう。
なぜなら私たちの借金は
•私たちはこのような債務を返済することを含めて、私たちの既存の債務に関する義務を履行することが難しいかもしれない
•私たちは将来的に運営資本、資本支出、買収、または他の目的のための融資を得ることが困難になるかもしれない(既存の債務ツールの下で任意の追加債務の発生に大きな制限がある)
•私たちは私たちが利用できるキャッシュフローの大部分で債務の利息と元本を支払う必要があり、これは私たちの運営や他の商業活動に資金を提供するために使用できる金額を減らすだろう
•私たちは全体的な経済低迷と不利な産業状況の影響を受けやすいかもしれない
•特許製品または協力手配からの収入のキャッシュフローが既存の債務に対する私たちの義務を履行するのに十分でない場合、私たちは資産の売却(契約項目の同意を得ることに依存する)や追加資本を求めることを余儀なくされる可能性があり、もし実現されていなければ、有利な条件下でこれを達成できないかもしれない
•事業や業界全体の変化を計画したり対応したりする上での私たちの柔軟性は制限されるかもしれない
•債務が少なく、債務制限が少ない、または債務契約制限が少ない競争相手と比較して、競争が不利になる可能性がある
•私たちは、私たちが追加債務を生成し、資産を売却または処分する能力を制限することを含む債務ツール内の財務および他の制限条約を遵守することができず、これは違約を招く可能性があり、是正または免除を加えなければ、私たちの業務または将来性に重大な悪影響を及ぼす
•私たちの知的財産権を含め、優先的な留置権の制約を受け、私たちの未済債務を返済するために使用することができる私たちの有形無形資産。
私たちは私たちの既存の現金と現金等価物と他の資金を潜在的に得る方法で私たちの現在と未来の債務超過義務を履行するつもりだ。しかし、私たちは十分な資金を持っていないかもしれないし、追加の融資を手配することができないかもしれないし、契約および13.5%の債券または私たちが締結する可能性のある他の債務ツールによって満期になった金額を支払うために追加的な融資を手配できないかもしれない。我々の既存の債務融資手配や当該などの他の債務ツールによる支払いに必要な債務超過金や他の契約を遵守できなかったことは、違約及び対応金額の加速を招き、当社の業務、財務状況及び経営業績に重大な悪影響を与える。
私たちは近い将来の収入を創出するために、私たちの許可製品と他の許可活動のビジネス成功に依存している。
候補特許製品をテスト·開発し、他の承認薬を得る権利を求める可能性があるにもかかわらず、近い将来収入を創出し、利益を達成できるかどうかは、米国でのSympazan、Suboxone、Exservan、Azstarysの持続的な商業成功、Ondifのブラジルでの持続的な商業成功、および私たちの候補製品Libervantを商業化する能力に依存するが、米国市場に進出するためにはFDAの承認が必要であり、この排他性を確立することは困難であり、前例が限られている。FDAがこのような市場排他性を克服してLibervantの米国市場進出を承認することを求める立場に同意する保証はない。しかも、私たちが商業的に成功し、利益に必要な程度になるという保証はない。もし私たちの現在の製品が商業的に成功しなければ、私たちが製造と販売利益率と許可または特許使用料収入を創出する能力は損なわれるだろう。このような収入がなければ、私たちは発展計画と商業化努力の能力を計画し続けます
限られたものになります私たちは私たちの製品の商業成功に依存しているので、これらの製品の商業成功の遅延や挫折は、私たちの業務、将来性、結果と運営、および財務的考慮に重大な悪影響を及ぼす可能性があります。
私たちの収入の大部分は単一の顧客とライセンスから来ており、このような重要な顧客からの収入のいかなる損失や実質的な減少も私たちの業務に悪影響を及ぼすだろう。
歴史的には、各四半期と年度の収入の大部分は単一顧客からのものであり、規制機関の承認を求め、独自製品や候補製品の商業化を求めていく傾向が続くと予想される。これらの主要顧客からの収入が大幅に低下すれば、私たちの業務、財務状況、運営結果に大きな悪影響を及ぼす。2023年と2022年、個人収入はそれぞれ私たちの収入の約80%と76%を占め、私たちは未来が私たちの収入の大きな部分を占め続けると信じている
さらに、何らかの原因や事件が発生した場合、SuboxoneがIndiorに提供するIndior許可プロトコルは終了する可能性がある。例えば、単独ライセンス契約のいずれか一方は、他方がその契約義務に実質的に違反することにより関係を終了することができる。FDAまたは他の適用可能な規制機関が、私たちの生産拠点がSuboxoneの生産にもはや適していないと発表した場合、またはSuboxoneが健康または安全上の理由で生産に適していない場合、IndiorはIndior許可プロトコルを終了することもできる。また、“個人許可協定”の現在の期限は1年であり、いずれか一方が12ヶ月前に他方に継続しないことを通知しない限り、自動的に1年間継続することができる。したがって、いずれの当事者も、将来のいかなる違反義務、他の終了原因またはイベント、または更新通知なしで“個人許可プロトコル”を終了しない保証はない。このような終了は、私たちの業務、運営結果、資本状況、および将来性に重大な悪影響を及ぼすだろう。
Suboxoneは相当な市場シェアを維持し続けているにもかかわらず、この日没ブランド製品は時間の経過とともに侵食され、私たちの総収入と私たちの運営業績にさらに影響を与えると予想される。
InDiorは複数の訴訟の当事者であり,これらの訴訟はIndiorがそのSuboxoneの流通や販売において詐欺性や誤ったマーケティングや流通に従事していることを告発し,金銭救済を求めている.私たちはこの和解と処置が私たちの業務、将来性、流動性、財務状況、経営業績に実質的な財務的影響を及ぼすかどうかを評価することができない。
私たちはSuboxoneの導入に関連した反独占訴訟に巻き込まれてきましたが、このような訴訟ではどんな不利な決定も、追加資本を調達する能力を弱化させ、私たちの業務を深刻に損なう可能性があります。
私たちとIndiorに対する反独占訴訟で、私たちは被告にされた。この訴訟は私たちが後発薬製品の発売を妨害するための行動をしていることを告発し、これらの製品は市場でSuboxoneと競争するだろう。2022年10月19日、この訴訟中の裁判所は、訴訟におけるAqutiveに対するすべてのクレームを却下する命令を発表した。Aqutiveに対するすべてのクレームを却下する命令は、その事件の原告によって控訴することができる。私たちは、原告がその命令または本訴訟の最終結果に対して控訴するかどうかを確定または予測することができず、その可能性のある結果または損失(ある場合)の合理的な推定または推定範囲を提供することもできない。詳細は第2部第8項:財務諸表と補足データ、付記22、事件があったり.
我々の製品や候補製品の開発と商業化に関するリスク
FDAはLibervantが承認可能であると認定しているが,米国市場への進出を許可しておらず,我々の業務に深刻な悪影響を与えている。
2020年9月25日,FDAが発行したLibervantに対するCRLを受信した.FDAがCRLを発行することは,申請の審査期間が完了したことを示しているが,その申請は現在の形で承認されることはできない.CRLでは,FDAはAqutiveとNDAが提出した研究を引用しており,いくつかの体組換えは予想よりも低い薬物曝露レベルを示している。2021年11月にFDAと開催されたA型会議で、FDAは、これらの問題が、更新された用量スキームのモデリングおよびシミュレーションを利用することによって解決できることを確認した。2020年12月に改訂された体重ベース用量案を再提出し,モデリングとシミュレーションを行った。2021年2月、FDAは、研究に含まれる患者集団に特に関連するので、FDAが我々の集団薬物動態学(PK)モデルおよびセキュリティデータに見られることを望む情報を明らかにする2020年12月に提出された報告書にフィードバックを提供する。2021年6月、私たちはFDAに秘密保持協定を再提出した。FDAは2021年7月、我々が再提出したNDA申請を受け入れ、PDUFAの目標日を2021年12月23日に指定した。いくつかの情報要求に応答する以外に、FDAは私たちの発売後の不良事件報告能力の監査を完了し、製品特許カバー範囲に関するより多くの情報を要求し、Libervantの商標名の使用を許可し、私たちのパッケージに関連する言語変化に対して提案を提出した。また,FDA孤児製品開発オフィスと話し,我々が最初にそのグループに与えた通信を補完するより多くの情報を提供した。2021年12月20日FDAから通知を受けました
PDUFA目標日2021年12月23日までに行動する準備はできておらず,我々のLibervant口腔映画セキュリティプロトコルも予想される行動の推定時間を提供することはできない
FDAは2022年2月15日、別の承認された製品に付与された孤児薬物独占経営権がLibervantの承認に影響を与えるかどうかを考慮し続けており、Libervantの承認の即時性または予想される行動日に関する具体的な最新情報を提供できないことを通知した。FDAは2022年8月30日、Libervantに承認状を提供し、Libervantは競合製品Valtocoの孤児薬物市場排他性が2027年1月に終了するまで、米国市場参入の許可を得ていないことを指摘した。
FDAの承認を得た孤児薬物指定会社は,米国でこの薬物指定適応の市場排他性を獲得し,承認日から7年以内である。この孤児薬物排他的承認は、FDA承認を求める後続製品が、候補薬物スポンサーが証明できない限り、同じ孤児薬物適応の同じ活性部分の排出期間内に米国で発売されることを阻止する可能性があり、FDAは、後者が承認された製品よりも臨床的に優れていると結論している(例えば:より安全、より有効、或いは患者看護に重大な貢献をする)はFDA法規とガイドラインの意味に符合する。候補薬物スポンサーが現在承認されている薬物以外に患者看護に“重大な貢献”を果たしていることを候補薬物スポンサーが証明しているかどうかを評価することは,FDAによってケースによって評価されており,客観的な基準はなく,FDAはLibervantがValtocoよりも“臨床的に良い”ではないことを決定している。FDAが2027年1月までにLibervantがValtocoより臨床的に優れていることは保証されないため,それまで米国では何の収入も得られなかった(もしあれば)。
私たちは私たちの候補製品の開発に成功したか、規制部門の私たちの候補製品の承認を得ることができるかどうかを確認することができない。
私たちの任意の医薬製品を商業化することが承認される前に、私たちは厳格に制御された臨床試験を通じて大量の証拠を提供し、FDAおよび/または米国および他の国の他の規制機関に、私たちの特定の候補製品が安全で効果的であることを満足させなければならない。それぞれの医薬製品について,その有効性を証明し,その安全性を全過程で監視しなければならない。これらのパラメータの範囲内で発展が成功しなければ、私たちの業務は損害を受ける可能性があり、私たちの株価は不利な影響を受ける可能性があります。
私たちは現在臨床前と臨床開発の候補製品を持っている。私たちの業務は主に私たちの候補製品の成功した臨床開発、監督管理の承認と商業化に依存している。私たちの候補製品が発売される前に、FDAや他の同様の外国規制機関は、私たちが適用する機密協定または同様の規制提出を承認しなければならない。臨床試験は費用が高く,設計や実施が困難であり,完成には数年かかる可能性があり,結果は非常に不確定である。1つまたは複数の臨床試験の失敗は、試験の任意の段階で発生する可能性がある。そのほか、早期臨床試験の陽性結果は今後の臨床試験或いはその他の監督管理発展を予測できない可能性がある。また、多くの製薬や生物科学技術業界の会社は早期開発で積極的な成果を得た後、後期臨床試験で重大な挫折を経験し、私たちが類似した挫折に直面しないことを確定することはできない。そのほか、臨床前と臨床データはよく異なる解釈と分析の影響を受けやすく、多くの会社は彼らの候補製品が臨床前研究と臨床試験で満足できると考えているが、依然としてFDAの承認を得られなかった。臨床試験に成功した後であっても,FDAは我々の発見に同意しないか,あるいは他の方法で提出された材料の長い審査を要求することが可能である。我々はまた、競争相手の候補薬が、類似の候補薬のFDAまたは他の規制承認を得る前に、孤立薬物市場の独占経営権を含むFDAまたは他の規制部門の承認を得たため、障害や挫折に直面している。FDAが私たちの秘密協定を承認しても、私たちは私たちの製品と候補製品を商業化することに成功できないかもしれない。
場合によっては、多くの要素のため、同一候補製品の異なる臨床試験間の安全性或いは有効性結果は有意差が存在する可能性があり、これらの要素は方案中に規定された臨床試験プログラムの変化、患者群の大きさとタイプの差異、投与方案と他の臨床試験方案に対する堅持、及び臨床参加者の退学率を含む。もし私たちが計画した任意の候補製品の臨床前研究または臨床試験で積極的な結果を得ることができなければ、私たちの候補製品の開発スケジュール、規制承認と商業化の見通し、そしてそれに応じた私たちの業務と財務の見通しは、重大な悪影響を受けるだろう。
FDAは私たちが提出する可能性のある申請を承認しないかもしれないし、私たちの候補製品は私たちが候補製品の臨床試験を開始するために必要な適切な規制承認を得られないかもしれない。必要な承認を得るためのどんな遅延や失敗も、私たちの業務に実質的な悪影響を及ぼす可能性がある。開発から商業化までの過程には長年の時間がかかる可能性があり、現在の手元の収益を超えて大量の資源がかかる可能性があるが、規制部門の承認、あるいはこのような候補製品の商業成功を得ることに成功する保証や保証はない。
現在および将来の候補製品がFDAや同様の外国規制機関の承認を得ても、どの承認にも特定の年齢層の使用制限に関する重大な制限が含まれている可能性がある
警告、予防または禁忌症、または重い承認後の研究またはリスク管理要求の影響を受ける可能性がある。もし私たちが規制部門の承認を得ることができない場合、あるいはいかなる承認にも重大な制限が含まれていれば、私たちはその候補製品を開発し続けるために十分な資金を得ることができないか、または私たちが将来許可、開発、または買収する可能性のある他の任意の候補製品を継続することができないかもしれない。
もし私たちのある製品が市場独占経営権を獲得していなければ、孤児薬品の独占経営権を含めて、私たちの業務は損害を受ける可能性があります.
著者らはすでに著者らの候補薬物Libervantのために孤児薬物市場の独占経営権を求め、そして未来に他の候補製品のために市場独占経営権を求める可能性があり、孤児薬物市場の独占経営権を含む。米国を含むいくつかの管轄区域の規制機関は、患者数が相対的に少ない薬物を孤児薬に指定する可能性がある。孤児医薬品法によれば、1つの製品がまれな疾患または疾患を治療するための薬剤である場合、FDAは、その製品を孤児薬として指定することができる。米国では、まれな疾患または疾患は、通常、患者数が20万人未満と定義されている。
一般に、孤児薬物名を有する製品がその後、そのような名称を有する適応の最初の発売許可を得た場合、製品は市場排他期を有する権利があり、これにより、FDAは7年以内に同じ疾患に対する同じ薬物の別のマーケティング申請を承認することができない。FDAが指定要求に重大な欠陥があると判断した場合、または製造業者が稀な疾患または疾患を有する患者の需要を満たすのに十分な数の薬剤を保証できない場合、孤児薬の排他性を失う可能性がある。上場承認申請を提出する前に、孤児薬の指定を申請しなければならない。
指定された疾患または疾患を治療するための指定孤児薬の治療のためにFDAによって初めて承認された会社は、米国で7年間の孤児薬物市場における独占経営権を獲得する。このような孤児薬物排他性は、FDAが別の申請を承認することを阻止し、同じ活性部分を含む薬物を同じ孤児適応に使用し、非常に限られた場合に、FDAを含めて、後者の薬剤がより安全で、より効果的であると結論した場合、またはFDA法規およびガイドラインによって示される患者ケアに大きな貢献をした場合である。また,指定された孤児薬物が孤児指定の適応を得るよりも広い用途で許可されていれば,孤児薬物排他性を得ることはできない。
私たちの1つ以上の候補薬が孤児薬物指定を受けても、候補品の開発に関連する不確実性のため、孤児指定薬の発売承認を得た最初の会社ではないかもしれない。これらの他の製薬会社のいずれかが、同じ適応に対する同じ活性部分を有する1つ以上の候補薬剤の承認を得る前にNDA承認を得ることができる場合、候補薬剤が臨床的に承認された製品よりも優れているか、またはそのような孤児薬の独占性を満たす他の限られた例外のうちの1つよりも臨床的に優れていることが証明できない限り、7年間の孤児薬専営期間内に米国で製品を販売することを禁止される。
また、異なる活性部分を有する異なる薬剤が同じ病態のために承認されるか、または同じ活性部分を有する薬剤が異なる適応のために承認されることができるので、製品の孤立薬物排他性が得られても、この排他性は競合から効果的に保護できない可能性がある。孤児薬物を指定することは薬物の開発時間や監督審査時間を短縮することもなく、監督審査或いは承認過程において薬物にいかなる利点をもたらすこともない。さらに、私たちが私たちの任意の候補製品や適応のために孤児薬の称号を求めようとしても、私たちは決してそのような称号を得たり、孤児薬の排他性を得ることはできないかもしれない。
また,孤児薬物の排他性を克服することは困難であり,前例が限られており,FDAがこのような市場排他性の克服を求める立場に同意する保証はなく,Libervantが孤児薬物排他性で米国市場に進出することを許可している。もし私たちがそのような独占的な権利を得ることができなければ、競争相手の競争製品の製造、マーケティング、販売を阻止する能力は重大な損害を受け、私たちの経営業績と財務状況は重大な悪影響を受ける可能性がある。
C臨床試験は多くの理由で延期、一時停止または終了される可能性があり、これは私たちの費用を増加させ、私たちの候補製品の開発に要する時間を遅らせるだろう。
私たちは進行中あるいは未来の臨床前試験で遅延に遭遇する可能性があり、未来の臨床前研究或いは臨床試験が時間通りに開始されるかどうか、再設計が必要かどうか、時間通りに十分な数の患者を募集するかどうか、あるいは予定通りに完成するかどうかを知らない。著者らの候補臨床製品の臨床試験の開始と完成は多くの要素によって延期、一時停止或いは終了する可能性がある
•FDAは私たちの臨床研究の設計、計画、または実施に同意しない
•規制機関やIRBsが予想される試験場所で臨床試験を開始することを遅延または拒否した
•規制要件、政策、指針の変化
•遅延または予期されるCROおよび臨床試験場所で許容可能な条項と合意できなかった
•試験に参加するのに十分な数の患者を募集または遅延させることができず、特に孤児の適応下で、試験中の統計的に顕著な治療効果を観察する
•臨床サイトが試験案から外れているのは
•現在行われている前臨床研究または臨床試験の陰性または不確定な結果は、より多くの臨床前研究または臨床試験を行う必要があるかもしれないし、私たちが本来期待していた有望な項目を放棄する必要があるかもしれない
•安全性や治療効果の問題を引き起こす他の類似療法からの臨床前試験の報告;
•監督機関やIRBsは様々な理由で、規制要求や安全問題などを含む、私たちまたは私たちの研究者に臨床研究の一時停止または中止を要求している
•患者とボランティアの臨床試験における保持率は予想より低かった
•私たちのCROまたは臨床試験サイトは、法規の要求を直ちに遵守することができなかったか、または私たちに対する契約義務を履行することができなかったか、または計画から外れたり、試験を脱退したりすることができなかった
•適切な用量レベルの決定を遅延させる;および
•臨床試験に関するコストを正確に予測することは困難であるため,予算コストを超えている。
もし私たちの候補製品の任意の臨床試験の開始または完了が遅延した場合、または任意の臨床試験が一時停止または終了した場合、私たちのコストは大幅に増加する可能性があり、私たちの候補製品の商業的見通しが損なわれる可能性があり、任意の候補製品の販売から収入を得る能力は延期されるか、または全く実現できないだろう。重大な臨床前研究や臨床試験遅延は、候補製品を商業化する独占的な権利を持つ時間を短縮するか、または私たちの競争相手が私たちの前に製品を市場に出し、候補製品を商業化することに成功する能力を弱めることを可能にするかもしれない。
私たちはただ一つの製品、Sympazanを直接販売しました。経験が限られているため、私たちは私たちの他の候補製品を商業化することに成功するために必要な専門知識、人員、資源が不足している可能性があり、これらの製品はまず規制部門の承認を得なければならない。
私たちは私たちの第三者許可側によって私たちの多様なライセンス製品を商業化し、これまで、私たち自身の努力と契約販売者を含む第三者アウトソーシングサプライヤーのサービスを通じて、私たちが最初に自主開発した製品Sympazanが2018年12月に発売されました。2022年10月、SympazanがUsertioに許可されるにつれて、私たちは販売チームの削減やマーケティングチームの削減など、多くのビジネスビジネスを削減しました。候補製品を商業化する上での直接的な経験が限られている歴史と、現在の限られた商業運営を考慮して、将来の候補製品を商業化する能力や成功、または将来の候補製品の財務結果や将来の見通しを予測する能力(承認されれば)を評価する長期的な経験はない
私たちが候補製品のために行っているビジネス戦略は、複数の管轄区域にまたがるビジネスインフラを開発することを含み、これは、私たちのビジネス製品発表戦略を実施できるインフラを構築する能力に依存します。私たちの商業インフラを設立して発展させることは高価で時間がかかるだろうし、私たちは私たちの商業インフラを成功またはタイムリーに発展させることができないかもしれない。これを行うためには、広告慣行の制限、知的財産権の実行、定価または割引の制限、透明性の法律および法規、および規制要件および関税の意外な変化を含む、米国、各州、および私たちが業務を展開している他の国/地域の法律および法規を含む多くの地域の法律および法規を高度に調整し、遵守する必要がある。もし私たちがこのような活動を効果的に調整したり、このような法律法規を遵守することができなければ、アメリカや他の既存または可能性のある製品の司法管轄区域で私たちの候補製品を商業化する能力は重大な悪影響を受けるだろう。
また,第三者と戦略許可を締結し,我々の候補製品を米国以外の地域で商業化する予定である。私たちが受け入れられる条項の下で第三者と関係を作ることは難しいかもしれません。あるいは私たちの製品を商業化したいすべての地域で、あるいは全くありません。もし私たちが自分の流通やマーケティング能力を確立できない場合、あるいは適切な許可者を見つけることができなければ、私たちの製品と候補製品を商業化し、承認されれば、これらの製品や候補製品から収入を得ることが困難になる可能性があり、私たちの業務、運営結果、財務状況、見通し、そして私たちの株の取引価格は大きな悪影響を受ける可能性がある。
私たちの成功は患者、医師、薬剤師と医学界が私たちのライセンス製品と候補製品が市場に広く受け入れられているかどうかにかかっている。
私たちは候補製品の開発を完了できないかもしれないし、規制部門のこれらの候補製品の承認を得られないかもしれない。私たちの候補製品を完全に開発し、監督部門の許可を得ても、私たちの候補製品は患者、医者、看護師、薬剤師、医学界あるいは
第三者支払者、これが商業成功の鍵だ。私たちの製品と私たちが承認された任意の候補製品に対する市場の受け入れ度は、多くの要素に依存します
•候補製品と競合製品の発売タイミング
•製品候補が承認された臨床適応
•代替療法に対するこの候補製品の潜在的かつ知覚可能な利点
•優遇された定価と第三者支払者と政府当局が提供する保険と適切な補償
•相手が便利で管理しやすい
•私たちまたは私たちの競争相手の製品に関連する同じ活性成分を含む任意の否定的な宣伝
•FDAによって承認された製品ラベルに含まれる制限または警告を含む副作用の発生率および重症度
•販売とマーケティング努力の有効性。
1種の潜在的な製品が臨床試験において良好な治療効果と安全性を示しても、市場のこの製品に対する受け入れ程度はこの製品が発売されてから一定時間後に知ることができる。もし我々の製品や候補製品が承認されれば,患者,医師,看護師,薬剤師,医療界あるいは第三者支払者の十分な受け入れが得られなければ,相当な収入が生じず,利益を達成したり維持したりすることができない可能性がある。
しかも、私たちの候補製品の潜在的な市場機会を推定することは難しい。我々の潜在市場機会の推定は、業界知識と出版物、第三者研究報告或いは分析とその他の分析情報など、いくつかの重要な仮定に基づいている。私たちは私たちの内部仮定が合理的だと信じているが、このような仮定は不正確かもしれない。もしどんな仮定が不正確であることが証明されたら、私たちの候補製品の実際の市場は私たちの潜在的な市場機会の推定よりも小さいかもしれない。もし私たちの候補製品の実際の市場が私たちが予想していたより小さい場合、あるいは製品が医師、医療支払者、患者の十分な受容度に達しなければ、私たちの製品の販売収入は制限される可能性があり、私たちは利益を達成したり維持することができないかもしれません。
また、医療市場で十分な規模や十分な専門知識を持つ販売チームを雇用したり契約したりすることはできないかもしれませんが、将来的には私たちの製品候補者に目標を合わせるつもりです。承認されれば、販売、マーケティング、流通能力の発展における私たちのどんな失敗や遅延も、私たちの候補製品の商業化に悪影響を及ぼすだろう。
FDAの任意の承認された製品に対する規制承認は、臨床的安全性および有効性が証明された特定の適応および条件に限定され、私たちがこのような承認適応を遵守できなかったという疑惑は、私たちの販売努力を制限し、私たちの業務に実質的な悪影響を及ぼす可能性がある。
FDAは処方薬のマーケティング、ラベル、広告、販売促進を厳格に規制する。これらの規定には、消費者向け広告、業界スポンサーの科学的および教育活動、インターネットに関連する販売促進活動、ラベル外販売促進の基準および制限が含まれる。FDAが付与したいかなる規制承認も,FDAが製品の安全かつ有効であると考えている特定の疾患や適応に限られている。新処方にはFDA承認が必要であるほか,任意の承認製品の新適応にもFDA承認が必要である。FDAが私たちの製品や候補製品の任意の期待された未来の適応を承認できなければ、私たちの製品を効果的にマーケティングし、販売する能力は低下する可能性があり、私たちの業務は実質的な悪影響を受ける可能性がある。
米国の医師は、製品ラベルに記載されていない用途や、臨床試験で試験され、監督機関によって承認された用途とは異なる薬剤を選択し、一般的に許可することができるが、我々の製品を普及させる能力は、FDAが特に承認した適応に限られる。これらの“ラベル外”の使用は医学専門科でよく見られ、異なる場合にはいくつかの患者に対する適切な治療を構成する可能性がある。アメリカの規制機関は通常、治療を選択する際の医師の行動を規制しない。しかし、規制機関は非ラベル使用問題に対する製薬会社のコミュニケーションを制限している。FDA法規またはガイドラインに準拠していない販促活動は、これらの当局の警告または法執行行動を受ける可能性があり、FDAが警告状または無タイトル状を発行すること、法執行行動を提起すること、許可された製品を市場から一時停止または撤回すること、リコールまたは罰金を要求すること、または資金の返還、経営制限、禁止または刑事起訴を招く可能性があり、これらのいずれもが私たちの名声および業務に大きな損害を与える可能性がある。
もし私たちの競争相手および/またはパートナーが私たちに法的訴訟を提起すれば、私たちの業務と運営業績を損なう可能性があり、私たちは巨大なコストと業務中断、そして私たちの候補製品の発表遅延を招く可能性があります。
私たちの競争相手または潜在的な競争相手(その中のいくつかは私たちと協力する)が、私たちの研究、開発および商業化活動、ならびに任意の製品候補またはこれらの活動によって生成された製品に基づいて、(他を除いて)その知的財産権の侵害、契約違反、他の会社の製品または候補製品の虚偽または中傷声明または他の法律理論を主張するかどうかを予測することはできません。今まで、私たちはこのような種類の多くのクレームを受けた。このような訴訟を弁護する際に、これらの訴訟に根拠があるかどうか、あるいは最終決定が私たちに有利であるかどうかにかかわらず、私たちはコストの高い訴訟と技術と管理者の分流に直面し続ける。これらの訴訟は、私たちの候補製品市場に早期に参入する能力を阻害し、市場に進出する潜在的な競争相手が少ない(あれば)使用モデルの能力に影響を与えることを阻害する可能性があり、このような候補製品からの潜在的収入に悪影響を及ぼす可能性がある。私たちのいくつかの競争相手は私たちよりもはるかに多くの資源を持っていて、より大きな時間とより長い時間で訴訟費用を受けることができる。さらに、紛争の不利な結果は、私たちが一方の特許または他の知的財産権を故意に侵害していることが発見された場合、損害賠償金を支払う必要があり、損害賠償金と弁護士費の3倍を含む可能性がある;他人の知的財産権に組み込まれたり、使用されていると言われている製品の製造、許可または使用を停止すること;追加の開発資源をかけて私たちの製品を再制定したり、私たちの製品を販売することを阻止すること;および必要な技術を使用する権利を得るために不利な使用料を締結することができるかもしれないことを要求するかもしれない。
政府機関が発表したガイドラインと提案は、私たちの製品や候補製品の使用を減らすことができる。
政府機関はいくつかの薬物カテゴリーに適した法規とガイドラインを公布し、その中には私たちの製品と候補製品が含まれている可能性がある。政府機関の法規やガイドラインは,随伴療法の使用,投与量,投与経路,使用などに関与している可能性がある。特定の薬物カテゴリ(私たちの製品および候補製品を含む可能性がある)の使用を減少させること、または患者および医療提供者が準拠する看護基準として競合製品または代替製品を使用することを提案する法規またはガイドラインは、私たちの製品または候補製品の使用を減少させること、または市場受容度および市場シェアを得る能力に悪影響を及ぼす可能性がある。例えば,オピオイド嗜癖に対するSuboxoneの活性成分の1つはオピオイドブプレノルフィンである。ブプレノルフィンなどのオピオイドの使用削減を推奨する法規やガイドラインの改正はアブドンの使用減少につながる可能性がある。
私たちは他の製薬会社からの激しい競争に直面しています。もし効果的に競争できなければ、私たちの経営業績は影響を受けます。
製薬業界は競争が激しく、迅速で重大な技術変革の影響を受けている。我々は,大手多国籍製薬会社,バイオテクノロジー会社,大学,その他の研究機関を含む米国と国際的に競争相手がいると予想している。私たちの多くの競争相手は、より多くの研究開発者と経験豊富なマーケティングと製造組織のような、より多くの財務、技術、および他の資源を持っている。バイオテクノロジーと製薬産業の合併と買収は、私たちの競争相手により多くの資源を集中させる可能性がある。したがって、これらの会社は私たちよりも早く規制部門の承認を得ることができ、彼らの製品をより効率的に販売し、マーケティングすることができるかもしれない。規模が小さいか早い段階にある会社も重要な競争相手になる可能性があり、特に大手老舗会社との協力で手配されている。技術の商業適用性の進歩やこれらの会社に投資する資本の増加により、競争はさらに激化する可能性がある。私たちの競争相手は独占的な基礎の上で開発、買収に成功するかもしれません。私たちの製品や候補製品よりも有効な薬物製品や薬物管理技術を開発することができるかもしれません。さらに、私たちの競争相手はFDAに市民請願書を提出し、FDAを説得しようとし、私たちの候補製品またはその承認を支持する臨床研究に欠陥が含まれているかもしれない。我々の競争相手のこのような行動は、FDAが505(B)(2)条または他の提出経路に従って提出した任意の秘密協定を承認することを遅延または阻止する可能性がある。
私たちが競争に成功するかどうかは他の要素を除いて
•私たちの製品と候補製品の有効性と安全性
•私たちの候補製品が臨床前と臨床開発を完了し、発売承認を得るのに要する時間
•私たちは規制部門と良好な関係を維持する能力がある
•私たちは規制部門の承認を得た後、私たちの任意の候補製品を商業化し、市場に出すことができる
•私たちの製品はブランドや模造薬の競争相手に対して価格を決めます
•個人と政府の健康保険計画の下でカバー範囲と十分な補償レベルがあるかどうか
医療保険や医療補助が含まれています
•私たちは私たちの製品と候補製品に関連する知的財産権を保護することができる
•私たちは費用効果に基づいて私たちの製品と規制の承認を受けた候補製品のために製品を製造する能力;
•医師や他の医療提供者は私たちの任意の製品と規制部門の承認を受けた候補製品を受け入れます。
もし私たちの競争相手の市場製品が私たちの候補製品よりも効果的で、安全で、あるいは私たちの候補製品よりも早く市場に入ったら、私たちの製品は周期的に市場に入るのが遅すぎて、商業成功が得られないかもしれません。しかも、生物製薬産業の特徴は技術の変化が迅速だということだ。私たちの研究開発能力が限られているため、私たちはすべての技術の急速な変化に追いつくことが難しいかもしれない。もし私たちが技術変革の最前線にいられなければ、私たちは効果的に競争できないかもしれない。私たちの競争相手が開発した技術の進歩や製品は、私たちの技術や候補製品を時代遅れにし、競争力に欠けたり、経済的ではないかもしれません。
もし私たちが第三者支払者の私たちの許可製品または候補製品に対する保証範囲と十分な補償を達成し、維持できなければ、承認されれば、彼らの商業成功は深刻に阻害されるかもしれない。
我々の許可製品や候補製品の商業化成功(承認されれば)は,第三者支払者(連邦医療保険や医療補助などの政府医療保健計画,商業健康保険会社,管理医療機関を含む)が提供する保険範囲と十分な精算,およびそのような保険·精算を得る速度にある程度依存するであろう(あれば)。第三者支払者たちは彼らがどの薬をカバーし、精算レベルを確立するかを決定する。第三者支払者の精算決定は、各第三者支払者の製品使用状況の判断を含む一連の要因に依存する
•健康計画の下で保障された福祉
•特定の状況や病気に適切で医学的に必要である
•費用対効果に合致しています
•実験的でも調査的でもない。
第三者支払人から保険と精算承認を得ることは時間がかかり、高価な過程である可能性があり、これは市場承認を得るために必要なデータではなく、高価な薬物経済学研究結果を含む各第三者支払人に支持的な科学的、臨床と費用効果データを提供する必要があるかもしれない。私たちが保証と補償の承認を得るのに十分なデータを提供できる保証はない。
コスト統制はアメリカの医療業界と他の地方および政府当局の主な懸念だ。第三者決済者は,医療製品やサービスのカバー範囲や精算レベルを制限することで医療コストを抑制しようとしている。第三者支払者が、医療製品が第三者支払者の引受政策に従って使用されていないと判断した場合、例えば、第三者支払者が製品を使用するために保証を提供する前に満たさなければならない費用便益診断方法に必要なプログラムや他の条件を決定した場合、第三者支払者は、引受製品の精算を拒否することができる。例えば、保険会社は、まず価格の低い代替製品を使用して、価格の高い製品の精算を受ける資格がある“階段編集”システムを構築することができる。第三者支払者は,実験的と考えられる薬物,プログラム,設備の精算を拒否したり,未承認の適応のために処方したりすることも可能である。第三者支払者も,我々の製品や候補製品を安価な療法で代替できると考え,患者に安い製品を精算することのみを提案している可能性がある。私たちが私たちの製品または候補製品に対してより良い治療効果またはより良い管理利便性を示しても、既存の薬物の価格は私たちの許可製品または候補製品の料金金額を制限するかもしれない。これらの支払者は、特定の製品の精算状態を拒否または撤回したり、新製品や既存市場製品の価格を低すぎるレベルに設定したりして、製品開発投資の適切なリターンを実現できない可能性がある。さらに、第三者支払者は、FDAによって承認された特定の適応のすべての製品を含まない可能性がある承認されたリストまたは処方表上の特定の製品にカバー範囲を制限することもできる。また,第三者支払者の中には医療製品の価格を疑問視し,価格規制を実施したり,製薬会社に価格に基づいてあらかじめ定められた割引を提供したりすることが求められている可能性がある。
清算状態を獲得して維持するのは時間もかかるし、費用もかかる。米国の第三者支払者には、製品保険精算に関する統一政策はない。そのため、製品の保証範囲と精算範囲は支払人によって異なります。そのため、保証範囲の確定過程は通常時間がかかり、高価な過程であり、各支払人に私たちの製品を使用する科学的かつ臨床的な支援を提供する必要があります
また、保証範囲および適切な補償が一貫して適用されるか、または最初に得られる保証はない。また、精算に関する規則や条例は常に変化しており、場合によっては短時間で通知されており、これらの規則や条例が変わる可能性があると考えられる。
支払者が商品に保険を提供するか否かを判定するプロセスは、保険が承認された後に支払者が製品に支払う価格または販売率を設定するプロセスと分離することができる。将来の精算レベルも低下する可能性があり、将来の第三者支払者の立法、法規、あるいは精算政策は私たちの候補製品の精算や定価に悪影響を及ぼす可能性があり、承認されると、逆に候補製品の需要にマイナスの影響を与える可能性がある。もし支払人が私たちの許可製品や候補製品のために十分な精算を受けていない場合、彼らはこれらの製品の購入を減少または停止する可能性があり、これは収入予想を達成するための重大な不足を招き、私たちの業務、将来性、財務状況にマイナスの影響を与える。
私たちと顧客、医師、第三者支払者との関係は、連邦と州医療詐欺と乱用法律、虚偽クレーム法律、医療情報プライバシーと安全法律、その他の医療法律法規の制約を直接または間接的に受けるだろう。もし私たちがこのような法律を遵守できないか、または完全に遵守できなければ、私たちは巨額の処罰に直面するかもしれない。
米国や他の地域の医療提供者、医師、第三者支払者は、現在販売されている任意の許可製品と、将来マーケティングの承認を得た任意の候補製品を推薦し、処方する上で主な役割を果たすだろう。私たちの現在と未来の医療専門家、主要な調査者、コンサルタント、顧客、および第三者支払者の手配は、連邦反バックル法規、連邦民事と刑事虚偽クレーム法律、および一般的に医師支払い陽光法案と呼ばれる法律およびその公布された法規を含む、様々な連邦および州詐欺および乱用法律および他の医療保健法律の制約を受ける可能性がある。承認されれば、これらの法律は私たちの臨床研究計画及び私たちの候補製品のために提出した販売、マーケティングと教育計画などに影響を与えるだろう。さらに、私たちは連邦政府と私たちが業務を展開したり、業務を展開する可能性のある州の患者プライバシー法の制約を受けるかもしれない。私たちの運営に影響を与える法律は含まれているが、これらに限定されない
•連邦反リベート法規は、個人または実体が直接または間接的に、現金または実物で直接または間接的に、公開的または隠蔽的に請求、受信、提供、または任意の報酬(任意のリベート、賄賂またはリベートを含む)を請求、推薦、レンタル、または提供することを禁止し、連邦医療保険および医療補助計画のような連邦医療計画下で精算可能な物品またはサービスを提供する。この法規は,一方が薬品メーカーである一方で,処方者,購入者,処方管理人の間の手配に適用されると解釈されている。改正された“患者保護と平価医療法案”(PPACA)は連邦“反リベート法規”の意図要求を改正した。個人または実体は、この規制またはそれに違反する具体的な意図を実際に理解する必要はない
•連邦民事および刑事虚偽精算法は、“虚偽精算法”および民事金銭罰法を含むが、これらに限定されず、他の事項に加えて、個人または実体が虚偽または詐欺的な連邦医療保険、医療補助または他の政府支払者の支払いまたは承認クレームの提出を意図的に、または隠蔽することを禁止し、または虚偽陳述によって連邦政府に金銭を支払う義務を回避、減少または隠蔽することを禁止する。PACAの規定によると、最近の薬品と医療機器メーカーの政府案件に対する支持の観点は、連邦反リベート法規の違反といくつかのマーケティングやり方は、ラベル外販売促進を含み、虚偽クレーム法案に関連している可能性がある
•HIPAAは、支払者が誰であろうと、任意の医療福祉計画を詐欺するために、誰もが知らず、故意に計画を実行したり、虚偽または詐欺的な陳述をしたりすることを禁止する連邦刑法を制定した例えば公共または個人);
•HIPAAは、“健康情報技術促進経済·臨床健康法”(HITECH)の改正を経て、この規則によって拘束された実体、例えば健康計画、医療情報交換所、およびいくつかの医療提供者、およびそれらのそれぞれの商業パートナーに対して、HIPAAによって保護された健康情報の作成、使用または開示に関するサービスを提供し、適切な許可なしに、個人が識別可能な健康情報のプライバシー、安全および送信に何らかの要求を加えた
•PACAの一部である連邦医師支払い日光法案を含む連邦透明性法は、(I)医師、医師アシスタント、勤務看護師、臨床看護師専門家、登録看護師麻酔科医、登録助産師および教育病院への支払いまたは他の“価値移転”および(Ii)所有権および投資に関する情報を毎年連邦医療保険および医療補助サービスセンター(CMS)に報告することを要求するいくつかの薬品、機器、生物製品、および医療用品の製造業者に毎年報告することを含む
医師およびその直系親族が持っている利益は、検索可能なウェブサイトを介して公衆に提供される
•州および外国の法律は、上記の各連邦法律に相当する;州法律は、製造業者に、医師および他の医療保健提供者への支払いおよび他の方法での価値移転に関する情報、マーケティング支出または定価情報を報告することを要求する;州法律は、製薬会社が製薬業界の自発的コンプライアンスガイドラインおよび連邦政府によって公布された関連コンプライアンスガイドラインを遵守することを要求するか、または州法律および法規の規定に従ってコンプライアンス計画をとるか、または他の方法で医療保健提供者への支払いを制限することを要求する;および州および地方の法律は、医薬品販売代表の登録を要求する
•健康情報のプライバシーや安全を管理する国や外国の法律がある場合もあり、その多くの法律は互いに大きく異なり、HIPAAに先を越されず、コンプライアンス作業を複雑化させることが多い。
これらの法律の範囲が広く、法定例外状況と選択可能な避難港が限られていることから、私たちのいくつかの商業活動は1つ以上のこのような法律の挑戦を受けるかもしれない。
政府当局は、私たちの業務実践が現在または未来に適用される詐欺および乱用または他の医療保健法律および法規に関連する現行または未来の法規、法規または判例法に適合していない可能性があると結論するかもしれない。もし私たちの運営がこれらの法律または任意の他の私たちに適用される可能性のある政府法規に違反していることが発見された場合、私たちは重大な民事、刑事と行政処罰、損害賠償、罰金、返還、個人監禁、政府援助の医療計画(例えばMedicareおよびMedicaidなど)から除外され、追加の報告要件および監督に直面する可能性があります(もし私たちが会社の誠実な合意または同様の合意の制約を受けていれば、これらの法律違反に関する告発、契約損害、名声損害、および私たちの業務の削減または再編を解決します)。
その多くの法律が規制部門や裁判所によって十分に解釈されていないため、これらの法律に違反するリスクが増加していることが発見され、これらの条項は様々な解釈が可能である。私たちが第三者の業務配置と適用される医療法律や法規に適合するように努力することは、多くのコストに関連することを確実にします。これらの法律に違反して私たちにとった行動は、たとえ私たちが弁護に成功しても、巨額の法的費用を招き、私たちの経営陣の業務運営への注意をそらす可能性があります。持続的に変化するコンプライアンス環境、および異なるコンプライアンスおよび/または報告要件を有する複数の司法管轄区域の必要性に適合するために、強力かつ拡張可能なシステムを確立し、維持することは、医療会社が1つまたは複数の要件と衝突する可能性を増加させる。
最近公布され、将来の医療改革法律または法規は、私たちと任意の未来のパートナーが私たちの候補製品のマーケティング承認を獲得し、それを商業化する難しさとコストを増加させる可能性があり、私たちまたは彼らが獲得する可能性のある価格に悪影響を与え、私たちの業務や運営結果に悪影響を及ぼす可能性がある。
米国および一部の外国司法管轄地域では、医療システムに関する立法および規制変更および提案された変更は、候補製品の上場承認を阻止または延期し、承認後の活動を制限または規制し、私たちまたは任意の未来のパートナーがマーケティング承認を得た任意の製品を販売する能力に影響を与える可能性がある。米国や他の地方の政策立案者や支払者の中で,医療システムの改革を推進することに大きな興味があり,医療コストの抑制,質の向上および/または参入拡大を既定の目標としている。米国では、製薬業はこれらの努力の重点であり、重大な立法計画の大きな影響を受けてきた。私たちは、現在の法律、および将来取られる可能性のある他の医療改革措置は、より厳しいカバー基準をもたらす可能性があり、私たちまたは未来のパートナーが受け取る可能性のある任意の承認された製品の価格に追加の下振れ圧力をもたらす可能性があると予想している。2010年3月、総裁·オバマ氏はPACAに署名し、法律にした。PACAで当社の業務に重要な条項には、私たちの商業化能力と、私たちが入手可能な任意の製品と販売が許可されている製品の価格が含まれています
•指定されたブランドの処方薬および生物製剤を生産または輸入する任意のエンティティに徴収される控除不可能な年間費用は、特定の政府医療計画におけるこれらのエンティティの市場シェアに基づいてこれらのエンティティ間で分担され、この費用は、孤児適応のために許可された特定の製品の販売には適用されないが、
•医療補助計画の資格基準を拡大し、他を除いて、各州が連邦貧困レベル133%以下の収入のある個人に医療補助を提供することを許可し、それによってメーカーの医療補助リベート責任を潜在的に増加させる
•医療補助薬品還付計画におけるメーカーの還付責任を拡大し、ブランドと後発薬の最低還付率を引き上げ、“メーカー平均価格”やAMPの定義を修正し、
外来処方薬の価格を計算して報告するための医療補助薬品のリベートを行い、リベート責任を連邦医療保険優勢計画に参加する個人処方に拡大する
•公衆衛生サービス340 B医薬品定価計画または340 B計画に参加する資格があるエンティティタイプを増加させる
•連邦医療保険D部分引受切欠き割引計画を確立し、メーカーに保証間隔期間内に条件を満たす受益者に適用ブランド薬品交渉価格50%の販売時点割引を提供することを要求し、メーカーの外来薬物として連邦医療保険D部分で保険を受ける条件とした
•2019年から、この計画の下でメーカーの補助金を交渉価格の50%から70%に引き上げることを含むBBA
•患者を中心とした新しい結果研究所は、監督、優先事項を決定し、臨床治療効果の比較研究を行い、このような研究に資金を提供する
•CMS内に医療保険と医療補助革新センターを設立し、革新的な支払いとサービス交付モデルをテストし、医療保険と医療補助支出を低減し、処方薬支出を含む可能性がある。
また、PACAが公布されて以来、他の立法改正も提案され、採択された。例えば、2013年4月1日から、薬品や生物製品を含むすべての項目やサービスの医療保険支出は自動減額計画に基づいている(つまり、支出の自動削減)は、2012年に米国納税者救済法が改正された2011年の予算制御法案に求められている。その後の立法は、イギリス銀行家協会を含め、2%の減税幅を平均2027年に延長するが、国会で追加行動を取らなければならない。自動減額は、連邦医療保険や他の医療資金のさらなる減少を招く可能性があり、規制部門の承認を得た場合、他の方法で入手可能な候補製品の価格に影響を与える可能性があり、または承認されれば、候補製品の処方や使用頻度に影響を与える可能性がある。我々の業務に影響を与える可能性のある他の変化は、2015年の“連邦医療保険アクセスとチップ再許可法案”(MACRA)に基づいて医師の業績計画に連邦医療保険(Medicare Payment)を支払うなど、新しい計画の拡大を含み、この法案は2022年に全面的に実施される。現在,連邦医療保険品質支払い計画の導入が医師全体の精算や使用する薬剤の選択にどのように影響するかは不明である。
また、米国議会とバイデン政府の指導の下で、PACAの立法改正や規制改正は依然として可能である。PPAAの廃止と代替イニシアティブを含む、PACAに対するいかなる立法または規制変化の性質と程度はまだ確定されていない。PPACAの廃止や代替イニシアティブが法律となれば,最終的に医療保険を持つ個人の減少,あるいは保険を持つ個人の福祉は薬品の限られたカバーを含めてそれほど寛大ではない可能性がある。国会では廃止立法は成立していないが、トランプ総裁が法律となった2017年減税·雇用法案に署名した条項は、2019年1月1日からPPACAを廃止し、1年の全部または一部で合格医療保険を維持できなかった個人の税収ベースの分担責任支払いを廃止することを一般的に“個人強制医療保険”と呼ぶ。また、イギリス銀行家協会は、多くの医療保険薬物計画におけるカバーギャップを埋めるためにPACAを修正し、通常は“ドーナツ穴”と呼ばれている。PACA条項の将来の改正または廃止と代替の潜在的立法の範囲は多くの点で非常に不確実である。私たちはPACAの潜在的な影響とそれが廃止または代替される可能性がある私たちの業務への影響を評価し続けます。
米国でも処方薬のコストは多くの議論のテーマとなっており、国会議員や政府は、新たな立法や行政措置でこのようなコスト問題を解決すると表明している。この関心はいくつかの国会調査を招き、製品価格の透明性の向上、定価の審査とメーカー患者計画との関係及び政府計画薬品精算方法を改革するための連邦と州立法を提出し、公布したバイデン政府はすでに行政行動を取り始め、薬品定価と他の医療政策の変化問題を解決している。2021年7月9日、バイデン総裁は、処方薬問題を解決するいくつかの取り組みを含む米国経済競争を促進する行政命令に署名した。他の条項では、行政命令は、連邦政府がそのような薬剤のために支払う価格を含む処方薬価格を低減する計画を含む45日以内にホワイトハウスに報告書を提出するように衛生·公衆サービス部長官に指示する。行政命令への対応として、2021年9月9日、HHSは高薬価に対応する総合計画を発表し、その中で国会と同機関が取ることができる潜在的な立法政策と行政ツールを決定し、薬品価格をより負担と公平にし、処方薬業界全体の競争を改善し、促進し、科学革新を促進する州レベルでは、立法機関は、価格または患者の精算制限、割引、特定の製品参入およびマーケティングコスト開示の制限、および透明性措置を含む、価格または患者の精算制限、割引、特定の製品参入およびマーケティングコスト開示の制限および透明性措置を含む医薬品および生物製品の定価を制御するための法規を立法および実施することが増えており、場合によっては、他の国からの輸入および大量購入を奨励することが目的である。
将来的にこれらや他の医療改革措置がとられる可能性があるため,より厳しいカバー基準と追加的な価格設定引き下げ圧力を経験する可能性が予想される。連邦医療保険や他の政府が計画している精算のいかなる減少も、個人支払者の支払いの同様の減少を招く可能性がある。コスト抑制措置や他の医療改革を実施することは、私たちの収入の創出、利益の実現、あるいは私たちの薬物の商業化を阻止するかもしれない。私たちは将来、より多くの州と連邦医療改革措置を取ることが予想され、そのいずれも連邦と州政府が医療製品やサービスのために支払う金額を制限する可能性があり、これは私たちの候補製品に対する需要の減少または追加の価格設定圧力を招く可能性がある。
最近、“2022年インフレ低減法案”(IRA)は、米国衛生·公衆サービス部(HHS)内に薬品価格交渉計画(2026年から)を確立することを含むいくつかの重大な薬品定価改革を含み(2026年から)、ある選択された薬物に対する交渉後の“最高公平価格”をメーカーに要求し、あるいは規定を守らないために消費税を支払い、連邦医療保険B部分とD部分に基づいてメーカーに対して税金還付支払い要求を確立し、インフレを超える価格上昇(第1回は2023年に満期になる)を処罰し、D部分福祉を再設計する。その一部として,メーカーはD部分薬の割引(2025年から)の提供を求められている
処方薬の定価もアメリカ以外の政府によって統制されている。これらの国では、製品の発売許可を受けた後、政府当局との定価交渉にかなりの時間がかかる可能性がある。一部の国で精算或いは定価の承認を得るためには、私たちの候補製品のコスト効果を他の利用可能な候補製品と比較する臨床試験を行う必要があるかもしれない。もし私たちの製品が精算を得られない場合、あるいは範囲や金額が制限されている場合、あるいは定価が満足できないレベルに設定されている場合、収入と収益性が損なわれる可能性があります。
私たちの第三者への依存に関するリスクは
私たちは第三者に依存して臨床前研究と臨床試験を行う。もしこれらの第三者がその契約の責務を成功的に履行できない場合、あるいは予想される期限までに完了することができなければ、規制機関から候補製品の承認を得られないか、商業化される可能性があり、私たちの業務は深刻な損害を受ける可能性がある。
著者らは引き続き第三者CROに依存して、著者らの臨床前と臨床プロジェクトのデータを監視と管理することを計画してきた。私たちはこれらの方に依存して、私たちの臨床前研究と臨床試験を実行し、そして彼らの活動のいくつかの方面だけを制御する。しかし、私たちは私たちのすべての実験が適用された合意、法律、法規、そして科学的基準に従って行われ、私たちのCROへの依存が私たちの規制責任を免除しないことを確実にする責任がある。私たちと私たちのCROは、現在の良好な臨床実践またはGCPに関するFDAの法律および法規を遵守しなければならない。これは、欧州経済圏加盟国の主管当局および同様の外国規制機関が国際調整会議(ICH)の形で私たちのすべての製品の臨床開発を要求するガイドラインでもある。監督管理機関は定期的に試験スポンサー、主要調査者、試験地点を検査することでGCPを実行する。もし私たちまたは私たちのいかなるCROも適用されたGCPに従わなかった場合、私たちの臨床試験で生成された臨床データは信頼できないと考えられるかもしれませんが、FDAまたは同様の外国の規制機関は、私たちのマーケティング申請を承認する前に追加の臨床試験を行うことを要求するかもしれません。特定の規制機関が検査を行った後、この監督機関は私たちのいかなる臨床試験がGCP規定に適合しているかどうかを確認することを保証することはできません。また,われわれの臨床試験は現在のcGMP法規により生産された製品を用いて行わなければならない。我々はCROの活動に合意しているが,彼らの実際の表現に対する影響力は限られている.また,我々の候補製品の一部の臨床試験は米国以外で行われる予定であり,CROの監視と臨床試験場所への訪問を困難にし,われわれの臨床試験が正確かつタイムリーに行われることを確保し,GCPを含む適用法規を遵守することを余儀なくされる。私たちの候補製品のための臨床試験を行う際に、適用する法規を守らなければ、臨床試験を繰り返す必要があるかもしれません。これは監督部門の審査過程を遅延させます。
私たちのいくつかのCROは、(他の理由を除いて)私たちの臨床試験に参加した被験者の安全が合意を終了する必要があることを合理的に証明することができれば、債権者の利益のために一般的に譲渡される場合、または清算された場合、それぞれ私たちとの合意を終了することができる。もし私たちがこれらの第三者CROとの任意の関係が終了すれば、私たちは代替CROと合意したり、商業的に合理的な条項でそうすることができないかもしれない。また、私たちのCROは私たちの従業員ではなく、私たちがこのようなCROとの合意に基づいて私たちに提供した救済措置を除いて、彼らが私たちの臨床前と臨床プロジェクトに十分な時間と資源を投入しているかどうかを制御することができない。CROがその契約責任または義務を成功裏に履行できなかった場合、または予期された期限内に達成できなかった場合、CROがCROを交換する必要がある場合、またはCROによって得られた臨床データの品質または正確性が私たちの臨床方案、法規の要求または他の原因を遵守できなかった場合、私たちの臨床試験は延長、延期または終了される可能性があり、私たちは監督部門の私たちの候補製品の承認を得ることができないか、または商業化に成功する可能性がある。したがって、私たちの運営結果と私たちの候補製品のビジネス見通しは損なわれ、私たちのコストは大幅に増加する可能性があり、私たちの収入を創出する能力は著しく遅れる可能性がある。
CROを交換または追加することは、追加のコストをもたらし、管理時間と労力を必要とします。しかも、新しいCROが仕事を始める時、自然な過渡期がある。したがって,遅延が生じ,期待される臨床開発スケジュールを満たす能力に実質的な影響を与える可能性がある。私たちはCROとの関係を管理するために努力しているが、私たちが未来に挑戦や遅延に遭遇しないことを保証することはできず、これらの遅延や挑戦が私たちの業務、財務状況、および見通しに実質的な悪影響を与えないことを保証することはできない。
我々の薄膜箔は限られた供給源に依存し、サプライチェーン内のいかなる中断も生産と販売に影響を与える可能性があり、当社独自のPharmFilm Technology候補製品の開発と商業化遅延を招く可能性がある。
私たちは現在二つの第三者と協力して私たちのフィルムアルミ箔を生産しています。我々が薄膜アルミニウム箔を製造する独自の設備とプロセスにより,我々のアルミ箔の製造活動を代替サプライヤーに移すことは時間がかかりコストの高い作業となり,この機能を履行できるメーカーの数は限られていると考えられる。フィルム箔の交換サプライヤーは大量のコストを関連する可能性があり、著者らが必要な臨床と商業スケジュールの遅延を招く可能性がある。もし私たちのいかなる薄膜アルミニウム箔メーカーが私たちとの合意を違反または終了した場合、私たちは適用される製品を開発し、商業化するために、薄膜アルミニウム箔の製造と供給のための代替源を探す必要があるだろう。これらの候補製品のいずれか1つ以上のために適切な合格した代替フィルム箔供給源を探すのに非常に時間がかかる可能性があり、候補製品の開発および商業化の過程で大きな遅延を生じることなく、または許可製品の製造および供給約束と義務を履行することができない可能性があり、これは、私たちの財務状況、許可製品および候補製品の商業的潜在力および私たちの運営結果を損なう可能性があり、私たちの供給約束と義務を違約させる可能性がある。いかなる代替薄膜箔供給者もNDA補充により資格を取得する必要があり,これはさらなる遅延を招く可能性がある。もし私たちが新しいメーカーを指定して私たちの許可製品を供給する場合、そのメーカーはそのような製品を臨床開発するためのメーカーとは異なり、FDAや米国以外の他の規制機関も追加的な研究を行う必要があるかもしれない。私たちの候補製品については、最初は1つのサプライヤーだけがFDAのサプライヤーになる資格があると予想されています。承認されたサプライヤーの供給が中断されれば、私たちの開発と供給活動は深刻な妨害を受ける可能性がある。
これらの要素は、私たちの承認された製品と候補製品の臨床試験、規制提出、必要な承認または商業化の遅延を招き、私たちにより高いコストを発生させ、私たちの許可製品と候補製品の成功した商業化を阻止するかもしれない。また、私たちのサプライヤーが必要な商業数量の成分および活性医薬成分を商業的に合理的な価格でタイムリーに渡すことができず、実質的に同じコストで生産できる1つ以上の代替サプライヤーを得ることができない場合、私たちは約束を違約する可能性があり、これは供給協定を終了させる可能性があり、潜在的な違約損害を招き、私たちの重大な収入損失を招く可能性がある。
私たちは第三者が私たちの許可製品と候補製品のための活性医薬成分または原料薬を生産することに依存し、第三者が他の承認された製品のための原料薬を生産することに依存するつもりだ。第三者が十分な量の原料薬を提供できなかった場合、または許容可能な品質レベルまたは価格でそうすることができなかった場合、または満足できる法規準拠を維持または達成できなかった場合、私たちの任意の許可製品および候補製品の商業化は阻止され、延期され、または利益が低下する可能性がある。
私たちは現在、第三者が私たちの許可された製品と候補製品のための原料薬を製造し、彼らの活動のいくつかの側面だけを制御することに依存し、引き続き依存すると予想されている。
このような第三者のいずれかはいつでも私たちとの契約を終わらせることができる。もし私たちが代替計画を達成する必要があれば、私たちの特許製品、独自製品候補計画、商業化活動の供給を延期するかもしれない。私たちのこれらの第三者への依存は、これらの活動に対する私たちの統制を減少させたが、必要なすべての法律、法規、科学的基準、および任意の適用された試験案または製品供給約束と義務の下での私たちの義務を保証する責任は免除されない。これらの第三者がその契約責任の履行に成功しなかった場合、または予想される期限内に完了することができない場合、将来の規制機関が候補製品の提出と承認を支援するために必要な臨床試験の完了を完了または遅延させることができず、許可製品への供給約束や義務を違約する可能性があり、これにより、供給協定の終了を招く可能性があり、潜在的な違約被害を招き、重大な収入損失を招く可能性があります。
私たちと私たちの第三者原料薬製造業者が私たちの許可製品や候補製品を生産するための施設は、FDAまたは他の適用規制機関が受け入れられるコンプライアンス状態を維持しなければなりません。これらの検査は、NDAをFDAに提出した後に行われます。もし私たちまたは私たちの任意の第三者原料薬メーカーが私たちの規格と適用規制機関の厳格な規制要求に適合した材料を生産することに成功しなかった場合、あるいは監督検査によって、私たちまたは彼らは製造施設の規制承認を得たり維持することができないだろう。また、第三者原料薬メーカーが十分な品質管理、品質保証、合格者の能力を維持することを制御することはできない。また製品の生産規模を拡大するにつれて
私たちは、計画中の臨床試験を継続し、規制部門の許可を得て、候補製品を商業化するために、候補製品および必要な安定性試験、製品、包装、設備、およびプロセスに関連する問題を改善または解決する必要があるかもしれない。例えば、将来的には、私たちが製造したり、提供してくれた商業的に供給された製品に不純物を発見することができ、これは、規制機関が審査を強化し、私たちの臨床計画や規制承認を延期し、私たちの運営費用を増加させたり、私たちの許可製品や候補製品の承認を得たり維持できない可能性があります。もしFDAや他の適用可能な規制機関がこれらの施設が私たちの製品を生産するために承認していない場合、あるいは彼らが将来このような承認を撤回した場合、または私たちのサプライヤーや第三者メーカーが私たちの製品を再生産しないと決定した場合、私たちは代替製造施設を探す必要があり、これは私たちが規制機関の承認を得たり、私たちの候補製品を販売したりする能力に深刻な影響を与え、これはまた私たちの許可製品への供給約束と義務を違約し、潜在的な違約損害と私たちの重大な収入損失を招く可能性がある。
より広く言えば、私たちと私たちの薬品原料薬メーカーは生産過程において常に困難に直面している可能性があり、特に初歩的な生産の拡大と検証に直面している。これらの問題は生産コストと生産量の困難、品質管理、製品の安定性、品質保証テスト、合格者不足、及び厳格に実行されている連邦、州と外国法規を遵守することを含む。さらに、私たちと私たちの原料薬製造業者は、資源制限や労使紛争や不安定な政治環境(例えば、最近ウクライナとロシアで発生した事件)や他の地政学的不確実性のために製造困難に遭遇する可能性がある。もし私たちまたは私たちのメーカーがこれらの困難に遭遇したり、彼らの契約義務を履行できなかったりすれば、私たちは私たちの製品を生産したり、臨床試験および開発目的のために私たちの候補製品を提供したり、さらに私たちの任意の許可製品および候補製品を米国で商業化する能力が脅かされるだろう。私たちが商業需要能力を満たすいかなる遅延や中断も、大量の潜在的収入の損失を招く可能性があり、市場で認められた承認製品を得る能力や、私たちの供給約束または義務の潜在的な違約に悪影響を及ぼす可能性がある。そのほか、臨床試験供給のいかなる遅延或いは中断も臨床試験の完成を遅らせる可能性があり、臨床試験計画の維持に関連するコストを増加させ、そして遅延した時間帯に基づいて、追加費用で新しい臨床試験を開始するか、或いは臨床試験を完全に中止することを要求する。また、承認された原料薬メーカーの供給が中断されれば、商業供給が深刻に中断される可能性がある。新しいメーカーに依存して商業生産を行う場合、規制機関も追加的な研究を行う必要があるかもしれない。交換メーカーは大量のコストを伴う可能性があり、私たちに必要な臨床的およびビジネススケジュールの遅延を招き、私たちの供給約束と義務を乱す可能性がある。
これらの要素の発生は、私たちの業務、経営結果、財務状況、将来性に重大な悪影響を及ぼす可能性がある。
私たちは製品と候補製品の設計、開発、製造、供給と流通が厳格に規制され、技術が複雑であることを許可した。
臨床試験あるいは商業販売のための治療薬の準備に参加するすべての実体は広範な監督管理を受けている。商業販売または末期臨床試験のための完成品治療製品の使用が許可された成分は、cGMPと同等の海外標準で生産されなければならない。これらの条例は、調査製品および承認販売された製品の品質を制御し、確保するために、生産プロセスおよびプログラム(記録保存を含む)および品質システムの実施および動作を管理する。生産過程の不良な制御は、外来要因または他の汚染物質の導入、または候補製品の性能または安定性の意外な変化をもたらす可能性があり、これらの変化は最終製品テストでは検出できない可能性がある。私たちの製品と候補製品の開発、製造、供給と流通はすべて厳格な監督管理を受けており、技術は複雑です。私たちは私たちの第三者サプライヤーと共に、FDAと外国当局のすべての適用規制要件を守らなければならない。
私たちまたは私たちの原料薬およびコンポーネント製造業者は、私たちの候補製品の規制記録を支援するために、すべての必要な文書をタイムリーに提供しなければならず、FDAがその施設検査計画によって実行されたGLPおよびcGMP規定、および他の国/地域規制機関の同等の基準を遵守しなければならない。私たちまたは私たちの第三者原料薬またはコンポーネント製造業者は、cGMPに準拠できなかったか、または十分な数の候補製品をタイムリーに配送できなかったことを含む、生産プロセスを拡大することができず、私たちの任意の候補製品の遅延または規制部門の承認を得ることができない可能性がある。我々の施設および品質システムおよび第三者原料薬およびコンポーネント製造業者の一部または全部の施設および品質システムも、適用法規に適合する承認前検査によって、規制部門として私たちの候補製品または任意の他の潜在的製品の条件を承認しなければならない。さらに、どの国/地域の規制機関も、私たちの候補製品または他の潜在的製品または関連品質システムの準備に関連する製造施設が、進行中の活動に適用される法規に適合しているかどうかを随時審査または検査することができる。これらの施設と品質システムが承認前の工場検査を通過しなかった場合、FDAは私たちの候補製品、または他の管轄区域の同等の承認を承認しないだろう。
規制当局はまた、製品の販売を承認した後、いつでも、私たちの製造施設または当社の第三者サプライヤーまたは請負業者の製造施設を検査することができます。そのような検査が適用法規に準拠していないことが発見された場合、または私たちの製品仕様または適用法規に違反する行為が、そのような検査または審査から独立して発生した場合、私たちまたは関連規制機関は、私たちまたは関連規制機関に、私たちの承認された製品の臨床試験または商業販売を一時的または永久的に一時的に一時的または永久的に一時的に一時的または永久的に停止することを含む可能性がある修復措置を要求するかもしれない。私たちまたは私たちと契約を締結した第三者に課せられたどのような救済措置も、私たちの業務に実質的な損害を与える可能性があります。もし私たちまたは私たちの任意の第三者原料薬または成分製造業者が規制適合性を維持できなかった場合、FDAは、新薬製品の承認を拒否するか、または以前に存在した承認を撤回することを含む規制制裁を実施することができる。そのため、私たちの業務、財務状況と運営結果は重大な損害を受ける可能性があり、収入と結果の重大な損失を招き、そして私たちの供給承諾或いは義務の違約を招く可能性があり、これは私たちが供給協定を終了し、違約損害賠償を発生させ、そして私たちの重大な収入損失を招く可能性がある。
私たちは開発と商業化協力を成功させることができないかもしれませんが、これは私たちが候補製品を開発する能力に悪影響を与え、製品の開発を禁止するかもしれません。
薬品を開発し、臨床試験を行い、監督管理の許可を得、製造能力とマーケティング許可を確立する製品のコストが高いため、私たちは引き続きアメリカとアメリカ以外の地域で利用可能な資源と経験を持つ第三者との協力或いは許可手配を探索し続けている。米国国内外で我々の製品や候補製品を開発し、商業化するために、第三者との選択的な協力を模索し続けている。しかし、米国以外の地域では、我々の製品や候補製品の開発および/または商業化を進めることができない可能性があり、米国以外での特定の製品や候補製品の市場潜在力を制限する可能性がある。
我々が製品又は候補製品の開発及び商業協力計画を達成する場合には、その製品又は候補製品の第1の連携手配に係る地域以外の地域における開発及び商業化の追加協力を確立することも求められる可能性がある。潜在的な所有者の数は限られており、適切な所有者を探す上で競争に直面することが予想される。もし私たちが受け入れ可能な条項で任意の開発および商業協力および/または販売およびマーケティング計画を行うことができない場合、私たちは私たちの製品または候補製品の開発と規制承認を求めることに成功できないかもしれないし、および/または承認された製品を米国以外のすべての地域で効果的にマーケティングおよび販売することができない場合、そうでなければ価値があるかもしれない。
我々が協力について合意するかどうかは,他に加えて,協力者の資源や専門知識の評価,協調の条項や条件,提案された協力者のいくつかの要因の評価に依存する.これらの要因は、FDAまたは外国規制機関によって承認された可能性、製品または候補製品の潜在的市場、患者にそのような製品または候補製品を提供するコストおよび複雑さ、競合製品、および全体的な業界および市場状態を含むことができる。協力の交渉と記録は複雑で時間がかかる。
私たちはタイムリーに基づいて受け入れ可能な条項で協力することができないかもしれないし、交渉することさえできないかもしれない。もし私たちが私たちの支出を増やし、私たち自身の開発や商業化活動に資金を提供することを選択すれば、私たちは大量の追加資本を得る必要があるかもしれません。これらの資本は受け入れ可能な条件で私たちに提供できないかもしれません。もし私たちが十分な資金がなければ、私たちは私たちの候補製品をさらに開発したり、それらを市場に出して製品収入を作ることができないかもしれない。
私たちは開発と商業化協力の維持に成功できない可能性があり、どの協力者も私たちの製品や候補製品を開発または商業化するのに十分な資源を投入していないかもしれないし、開発または商業化努力に失敗する可能性があり、これは私たちがいくつかの製品や候補製品を開発し、それを商業化することに成功する能力や、私たちの財務状況や経営業績に悪影響を及ぼす可能性がある。
私たちが協力計画を立てる時、このような協力は最終的に成功しない可能性があり、これは私たちの業務、運営結果、財務状況、将来性にマイナスの影響を与える可能性がある。もし私たちが第三者と協力して製品や候補製品の開発と商業化を行えば、その製品または候補製品の将来成功した制御権の一部または全部を第三者に譲ることが予想される。第三者パートナーは、我々の製品または候補製品を開発または商業化するのに十分な資源を投入していない可能性があり、または開発または商業化努力に失敗する可能性があり、この場合、製品または候補製品の開発および商業化は延期または終了される可能性があり、私たちの業務は深刻な損害を受ける可能性がある。さらに、私たちが設立した任意の協力または他の手配の条項は、私たちに不利であることが証明されるか、または不利とみなされる可能性があり、これは私たちの普通株の取引価格に否定的な影響を与えるかもしれない。場合によっては、私たちは協力下の製品または候補製品または研究計画の持続的な開発を担当することができ、私たちが許可者から得た支払いは、この開発のコストを支払うのに十分ではないかもしれない。また、協力、販売、マーケティング
交渉、記録、そしてこれらの計画を実施するには複雑で時間がかかり、維持するために大量の資源が必要かもしれない。
私たちは第三者との協力に依存しているので、私たちはまた多くの追加的なリスクに直面しています。これらのリスクの発生は、私たちの協力計画を失敗させる可能性があります
•私たちは多くの業務、財政、そして管理資源の支出を負担する必要があるかもしれない
•私たちは株主の所有権パーセントを希釈する株式証券の発行を要求されるかもしれない
•私たちは相当な実際的または負債を負担することを要求されるかもしれない
•戦略的パートナーは、契約を終了したり、期限を許可したりすることができ、これは開発と商業化を延期し、私たちの製品および候補製品の開発と商業化のコストを大幅に増加させる可能性がある
•戦略協力者の業務組合または戦略協力者の業務戦略の重大な変化は、任意の手配の下で戦略協力者がその義務を履行する意欲または能力に影響を与える可能性がある
•戦略的パートナーは、独立または私たちの競争相手を含む他の人と協力して開発された競合製品または候補製品を推進することを決定することができる
•協力者は期待通りに義務を履行していないかもしれない
•これらの協力の一部としての臨床試験は成功しないかもしれない
•協力者は、規制の承認を求めたり、承認を得たりする候補製品を積極的または積極的に開発し、商業化してはならない
•私たちは、協力の下で開発または商業化されている候補製品に関するいくつかの情報の開示にアクセスできないか、または制限される可能性がある
•私たちの1つまたは複数の候補製品にマーケティングおよび分配権を持ち、規制承認を得た協力者は、そのような候補製品をマーケティングおよび流通するのに十分なリソースを投入しない可能性がある
•協力者は第三者の知的財産権を侵害する可能性があり、これは私たちを訴訟と潜在的な責任に直面させるかもしれない。
このような協力が候補製品の開発と商業化に成功していない場合、または私たちの協力者が私たちとの合意を終了した場合、私たちの製品または候補製品の開発または商業化は延期され、私たちの業務や将来性を損なう可能性がある。製品開発、規制承認、商業化に関連するすべてのリスクは、私たちの既存と将来の協力者の活動に適用されます。
さらに、私たちと私たちの第三者協力者との間には、例えば、臨床データの解釈、マイルストーンの実現、財務条項の解釈、または協力中に開発された知的財産権に関する衝突が生じる可能性がある。例えば、私たちの既存の収入源はIndiorに大きく依存しており、それは私たちが承認した製品Suboxoneの世界的な商業化権利を持っている。InDiorは,2023年12月31日,2023年12月31日,2022年12月31日までの年間で,それぞれ我々の総収入の80%と76%を占めている。InDiorまたは任意の他の第三者パートナーとこのような衝突が発生した場合、各イベントは、私たちの製品または候補製品の開発または商業化を遅延または阻止し、私たちの業務を損なう可能性がある以下の1つまたは複数のイベントを引き起こす可能性があります
•特許使用料の支払いを減らすこと、または適用される協力計画に基づいて支払うべきと考えられる他のお金
•第三者協力者が私たちの協力の内部または外部で取った、協力下の私たちの権利または利益に悪影響を及ぼす可能性のある行動;
•第三者協力者は、その開発および商業化活動の進捗状況をいつでも通報したり、これらの活動の結果を公開することを許可したりすることを望まない
•私たちの第三者協力者たちは関係を終わらせるか減少させることを決定した。
私たちの業務運営や業界に関連するリスク
もし私たちの業務が将来の需要を満たすために拡張すれば、私たちは成長を管理する上で困難に直面する可能性があり、これは私たちの運営を混乱させるかもしれない。
すぐには実現しないと予想されるが、私たちの製造業務の成長、Libervant商業化の需要(米国市場への参入が許可された場合)、あるいは将来的に私たちの製品ラインを増加させるために規模を拡大する必要があれば、私たちの管理、科学と工学、運営、販売、マーケティング、財務、その他の資源を増加させ、より多くのコンサルタントや請負業者を招聘することが予想される。将来の成長は、決定、採用、維持、インセンティブ、より多くの従業員、コンサルタント、請負業者、および契約従業員を含む、私たちの経営陣により多くの責任を負わせるだろう。また、私たちの経営陣は、私たちの日常活動から不比例な注意を移し、これらの成長活動を大量に管理する必要があるかもしれない。私たちは私たちの業務の拡張を効果的に管理できない可能性があり、これは私たちのインフラが弱く、操作ミスを招き、ビジネス機会を失い、従業員を失い、残りの従業員の生産性を低下させる可能性がある。将来の成長は大量の資本支出を必要とする可能性があり、我々の既存または将来の候補製品を開発するなど、他のプロジェクトから財務資源を移転する可能性がある。私たちの経営陣が私たちの成長を効果的に管理できなければ、私たちの費用は予想以上に増加する可能性があり、私たちの収入を創出および/または増加させる能力は低下する可能性があり、私たちは私たちの業務戦略を実施できないかもしれない。私たちの将来の財務業績と、私たちが製品や候補製品を商業化し、効果的に競争する能力は、私たちが未来の成長を効果的に管理する能力にある程度依存するだろう。
しかも、私たちの管理チームのどんな成長も私たちが吸収しなければならない支出を増加させる可能性があり、私たちの収入は必ずしもそれに応じて増加するとは限らない。しかも、今まで、私たちはただ一つの製品を市場で直接販売してきた。Libervantを商業化して直接マーケティングすれば、アメリカ市場への進出が許可されれば、多額の前払いが必要となり、私たちの労働力の急速な成長を作ることができるかもしれない。費用の増加は私たちの運営結果に悪影響を及ぼす可能性があり、追加資金の需要を増加させる可能性がある。
私たちの許可製品と候補製品(承認されれば)は潜在的な製品責任クレームや虚偽マーケティングクレームを招く可能性があり、私たちに成功クレームを提出すれば、重大な責任を招く可能性があります。
製薬会社として、私たちが経営する市場は重大な責任リスクに直面している。私たちは、市販承認を得ることができる任意の許可製品および候補製品の販売、および臨床試験において私たちの候補製品を使用して、製品責任クレームのリスクを直面させ、これらのクレームは、そのような製品または候補製品の悪影響、およびそのような製品または候補製品の商業化に関連する虚偽マーケティングクレームを主張する。製品責任クレームは、消費者、ヘルスケア提供者、製薬会社、販売または他の方法で私たちの製品または候補製品に接触する他の人または政府機関によって提出される可能性がある。オピオイド依存症に対するSuboxoneの活性成分の1つはオピオイドブプレノルフィンである。オピオイドを販売する会社のようにオピオイド依存症に関するクレームの目標とならない保証はない。どんな製品責任クレームや虚偽マーケティングクレームも、私たちの業務、財務状況、運営結果、および将来の成長見通しに実質的な悪影響を及ぼす可能性があります。製品責任クレームや虚偽マーケティングクレームを成功的に防御できなければ、巨額の責任とコストを招く可能性があります。さらに、製品責任クレームまたは虚偽マーケティングクレームは、是非曲直または最終結果にかかわらず、以下のような結果をもたらす可能性がある
•私たちのビジネス的名声を損なうことは
•臨床研究者は脱退しました
•訴訟による巨額の費用
•私たちの主な業務に対する管理職の関心を分散させる
•患者や他のクレーム者に巨額のお金の報酬を提供し
•私たちの許可品や候補品を商業化することはできません
•商業販売のために承認された場合、私たちのライセンス製品または候補製品に対する需要が減少します。
私たちは保険範囲を維持できないかもしれません。私たちの既存または任意の未来の保険証書や私たち自身の資源は、私たちが将来受け取る可能性のある損害クレームをカバーするのに十分ではないかもしれません。
私たちの業務は私たちを潜在的な製品責任と他の責任リスクに直面させます。これらのリスクは人類治療製品の臨床開発、製造、マーケティング、販売と使用に固有のものです。私たちは通常一定の保険レベルを確保する必要があります。臨床試験と任意の販売あるいは私たちの製品を使用する条件として。私たちは製品責任保険を購入しました。許可された製品の販売と、今まで私たちが担当してきたすべての臨床試験に関連していますつまり、私たちの内部製品ラインについて)。さらに、私たちは私たちの保険範囲の拡大を求めるかもしれない
許可された製品と私たちの将来の任意の承認された候補製品のマーケティングと商業化、そして私たちの業務に関連する他のリスク。
私たちの現在の製品責任保険のカバー範囲は、私たちが受ける可能性のあるいかなる費用や損失を補償するのに十分ではないかもしれません。保険範囲はますます高くなっており、将来、私たちは私たちが受け入れられるコストで保険範囲を維持したり、責任による損失から私たちを保護するのに十分な金額を提供できないかもしれない。思わぬ悪影響を持つ薬物に基づく集団訴訟では,多額の判決が下されることがある。成功した製品責任クレームあるいは一連の私たちに対するクレームは私たちの株価を下落させる可能性があり、もし私たちの保険範囲を超えたと判断すれば、私たちの運営と業務結果に実質的な悪影響を与える可能性があります。
私たちは情報技術に深刻に依存しています。この技術のどんな故障、不足、中断、またはセキュリティホールは、任意のネットワークセキュリティイベントを含めて、私たちが業務を効率的に運営する能力を損なう可能性があります。
セキュリティ対策が取られているにもかかわらず、私たちの内部コンピュータシステムおよび私たちと契約した第三者のコンピュータシステムは、ネットワーク攻撃、コンピュータウイルス、不正アクセス、自然災害、テロ、戦争、および電気通信および電気故障の破壊を受けやすい。私たちは以前インターネット釣り攻撃の目標になり、不正に私たちの電子メールシステムにアクセスしたことがある。我々のシステムはすでに保護と強化されているが、未来にネットワーク攻撃に遭遇しないことを保証することはできず、第三者がネットワーク攻撃を受けることによって間接的な結果を受けることもなく、潜在的なネットワーク攻撃やセキュリティホールの脅威を適時に予測、識別、相殺することもできない。特にネットワーク攻撃技術の性質を考慮すると,このような技術はつねに変化し,長い間発見されることは困難であり,成功するまで認識されることが多い.システム故障、事故或いはセキュリティホールは私たちの運営中断を招く可能性があり、そして私たちの製品開発、臨床活動と業務運営の実質的な中断を招く可能性があり、そのほかに大量の資源をかけて救済する必要があるかもしれない。製品開発や臨床試験データの紛失は、私たちの規制承認作業を遅延させる可能性があり、データを回復または複製するコストを著しく増加させます。任意の中断またはセキュリティホールが、私たちのデータやアプリケーションを紛失したり、破損したり、機密または独自の情報を適切に開示しない場合、私たちは責任を招く可能性があり、私たちの開発計画および候補製品の開発が延期される可能性があります。
私たちの製造施設の業務中断は候補製品を開発する過程が遅れる可能性があります。
ニュージャージー州のウォーレンに本社を置き、インディアナ州のポティッチに製造工場を設置しています。もし私たちがこれらの場所で運営が中断されたり、火災、自然災害(例えば、ハリケーン、竜巻または深刻な嵐)、停電、システム故障、労使紛争、または他の予測不可能な中断に遭遇した場合、私たちは私たちの業務を効果的に運営することを阻止されるかもしれません。自然災害の保険範囲は洪水や地震に制限されている可能性があり、発生する可能性のある損失を補償するために十分な業務中断保険をかけていない可能性があります。私たちが受けたどんな損失や損害も、私たちの業務運営に実質的な悪影響を及ぼすかもしれない。
動物試験が制限される可能性があるため,我々の研究や開発活動は影響を受けたり延期されたりする可能性がある。
ある法律法規は私たちが人類に関する臨床試験を開始する前に、まず動物に私たちの候補製品をテストすることを要求しています。動物実験活動は論争と否定的な宣伝のテーマだった。動物権利組織や他の組織や個人は,これらの分野の立法や規制を推進し,抗議や他の手段でこれらの活動を撹乱することで,動物実験活動を阻止しようとしている。もしこれらの組織の活動が成功すれば、私たちの研究と開発活動は中断、延期、あるいはもっと高価になるかもしれない。
私たちの業務は危険材料に関連しており、私たちと契約した第三者は環境法律と法規を遵守しなければなりません。これらの法律と法規はコストが高く、私たちの業務方式を制限しなければなりません。
製薬会社として、私たちは危険材料の使用を管理する法律法規を含む環境と安全法令の制約を受けている。健康と安全規制を遵守する費用は巨大だ。私たちの業務活動は危険材料の制御された使用と関連がある。我々の研究開発活動は,我々の候補製品の成分や他の危険化合物を含む危険材料の制御貯蔵,使用,処分に関するものである。私たちと私たちがそれと契約を締結するかもしれない製造業者とサプライヤーは、これらの危険材料の使用、製造、貯蔵、運搬、処分に関する法律と法規を遵守しなければならない。場合によっては、これらの危険材料とそれらを使用して発生した様々な廃棄物は、私たちと私たちの製造業者の施設に貯蔵され、使用と処分を待っている。これらの材料の意外な汚染や傷害のリスクを除去することはできません。これらのリスクは、私たちの商業化努力、研究開発努力、業務運営の中断、環境破壊による高価な整理、およびこれらの材料と指定廃棄物製品の使用、貯蔵、処理、処分を管理する適用法律と法規に規定された責任を招く可能性があります。私たちがそれと契約を締結する可能性のある第三者製造業者とサプライヤーが使用するセキュリティ手続きが法律法規に適合することは保証できません
このような材料の意外な汚染や傷害の危険を除去するだろう。この場合、私たちはそれによって生じるいかなる損害に対しても責任を負うことができ、このような責任は私たちの資源範囲を超える可能性があり、アメリカ連邦、州、または他の適用機関は、いくつかの材料の使用を制限し、および/または私たちの業務運営を中断するかもしれない。また,環境法律法規は複雑で変化が頻繁であり,より厳しくなる傾向にある。私たちはこのような変化の影響を予測することもできないし、私たちの未来のコンプライアンス状況を決定することもできない。私たちは事故や環境排出時の私たちのリスクを減らすために環境責任保険を維持している。もし私たちが私たちの保険限度額と財務資源を超える可能性のある任意の結果的な損害とそれによって生じる損害に責任を負うことを要求される可能性があれば、私たちの業務、運営、将来性、そして私たちの株式価値に大きな悪影響を及ぼす可能性のあるコストが生じるかもしれません。
政府の規制に関連するリスク
FDAが505(B)(2)規制承認経路の要求を満たしていると結論していない場合、または505(B)(2)条による任意の候補製品の承認要求が私たちが予想していたようにでなければ、候補製品の承認経路は予想よりも時間がかかり、コストが高く、より大きな複雑性とリスクに遭遇し、どうしても成功しない可能性がある。
我々は、505(B)(2)規制経路を介して、本報告に記載された各候補製品についてFDAの承認を求めることを意図している。1984年の医薬品価格競争と特許期限回復法案は、ハッジ·ワックスマン法案とも呼ばれ、連邦食品、薬物、化粧品法案(FDCA)に505(B)(2)節が追加された。第505条(B)(2)条は、出願人又は出願人による研究ではない場合に、少なくとも部分的な承認に必要な情報が機密協定を提出することを可能にする。
FDAが予想したように候補製品のために505(B)(2)規制経路に従うことを許可しない場合、より多くの臨床試験を行い、より多くのデータと情報を提供し、規制承認のより多くの基準を満たす必要があるかもしれない。このような状況が発生すれば、我々の候補製品のFDA承認に要する時間と財政資源が大幅に増加する可能性がある。さらに、505(B)(2)の規制経路に従うことができないことは、新しい競争製品が私たちの候補製品よりも早く市場に参入する可能性があり、これは私たちの競争地位および将来性に実質的な悪影響を及ぼす可能性がある。505(B)(2)規制経路に従って候補製品のために許可されていても、候補製品を商業化するために必要なまたはタイムリーな承認を得ることを保証することはできません。
さらに、FDAは過去数年間に505(B)(2)条に従っていくつかの製品を承認したにもかかわらず、いくつかの競合他社および他の人は、505(B)(2)条のFDAの解釈に反対する。私たちは、私たちの競争相手がFDAに市民請願書を提出し、FDAを説得しようとし、私たちの候補製品または彼らの承認を支持する臨床研究に欠陥が含まれていると予想する。第505条(B)(2)条に対するFDAの解釈が成功的に挑戦された場合、FDAは505(B)(2)条の政策およびやり方の変更を要求される可能性があり、これは、FDAが505(B)(2)条に従って提出した任意の秘密協定を承認することを延期または阻止する可能性がある。
私たちの製品または候補製品は、悪影響をもたらす可能性があり、または他の性質を持ち、その規制承認を延期または阻止するか、または承認されたラベルまたは市場受容度の範囲を制限する可能性があり、それは、私たちが臨床試験を一時停止または停止し、候補製品を放棄すること、または上場承認後の重大な負の結果をもたらす可能性がある。
多くの薬品や生物製品と同様に、私たちの製品や候補製品を使用した治療は、副作用や副作用やイベントが生じる可能性がある。私たちの製品または候補製品が承認された有効成分を含む性質は、私たちの製品または候補製品において活性成分または医薬カテゴリを使用することによって生じる副作用が知られているが、私たちの製品または候補製品は依然として不良副作用を引き起こす可能性があることを意味する。これらは、活性成分または医薬カテゴリ、またはそのような製品または候補製品に対する我々の独自の処方、または他の潜在的な有害特徴に起因する可能性がある。これらの特徴は、私たち、私たちのIRBs、臨床試験場所、FDA、または他の規制機関が臨床試験を中断、延期、または停止させる可能性があり、より厳しいラベルまたは規制承認の遅延、拒否、または撤回をもたらす可能性があり、これは私たちの業務、財務状況、および将来性を深刻に損なう可能性がある。
さらに、もし私たちのすべての製品が市場の承認を得た後に深刻または予期しない副作用を招く場合、いくつかの潜在的な重大な負の結果を招く可能性がある
•規制部門は製品の承認を撤回したり、その販売に制限を加えたりすることができる
•FDAは、リスク評価および緩和戦略、またはREMSの実施を要求する可能性がある
•規制当局は警告や禁忌症のようなラベル宣言の追加を要求するかもしれない
•私たちは製品の投与方法の変更や追加の臨床研究を要求されるかもしれません
•私たちは起訴され、患者への傷害によって重大な損害賠償責任を負うかもしれない
•私たちの名声は損なわれるかもしれない。
上記のいずれの事件も、影響を受けた製品または候補製品に対する市場の受容度を獲得または維持することを阻止することができ、このような製品からの収入および収益性に著しく影響を与え、私たちの製品および候補製品の商業化コストを大幅に増加させる可能性がある。
我々の業務は広範な規制要求を受けており,我々が承認した製品と規制承認された候補製品は継続的な規制審査を受けることになり,巨額の費用を招き,そのような製品を商業化する能力を制限する可能性がある。
製品が承認された後であっても、私たちは、ラベル、包装、貯蔵、流通、安全監視、広告、販売促進、輸出入、記録保存、および安全および他の発売後の情報の報告に関するFDAおよび他の法規の継続的な要求を遵守する。承認されたセキュリティプロトコルの所有者は、不良イベントまたは有害イベントを監視および報告する義務があり、製品がセキュリティプロトコルの仕様に適合しない任意の障害を有する。承認された機密協定の保持者はまた、承認された製品、製品ラベル、または製造プロセスを特定の変更するために、新しいまたは追加の出願を提出し、FDAの承認を得なければならない。他の適用可能な連邦および州法律に加えて、広告および販売促進材料はFDAの規定に適合し、FDAの審査を受けなければならない。さらに、FDAは、製品が発売される可能性のある承認の指示用途または承認条件に重大な制限を加える可能性がある。例えば、製品の承認は、製品の安全性および有効性を監視するために、またはREMS計画を実施するために、コストの高い可能性の高い承認後の研究および監視の要件を含むことができる。
秘密協定保持者は使用料を支払い、秘密協定で行われた約束を守らなければならない。メーカーはまた、cGMPに適合することを確実にするために、FDAおよび他の規制機関の持続的な審査および定期検査を受けている。私たちまたは規制機関が、予期しない深刻度または頻度の副作用、または製品の製造施設に問題があるような以前に未知の問題があることを発見した場合、規制機関は、製品のリコールを要求し、医師に通知し、製品を市場からリコールまたは生産を一時停止することを含む、製品または製造施設に制限を加える可能性がある。
もし私たちまたは私たちの製品または候補製品または私たちの製造施設が適用される規制要求を遵守できない場合、監督管理機関は:
•私たちが違法だと主張する警告状や無題の手紙を出します
•製品の販売や製造に制限を加える
•民事、刑事および/または行政処罰、損害賠償、金銭罰金の評価、返還要求、連邦医療保険、医療補助、および他の連邦医療保健計画から除外されることを考慮し、私たちの業務の削減または再編成を要求する禁止令または適用を求める
•規制承認の一時停止または撤回;
•進行中の臨床試験を一時停止します
•私たちが提出した保留秘密協定または秘密保持協定を承認することを拒否する追加合意;
•製品を差し押さえる
•私たちが政府契約を結ぶことを許可することを拒否する。
似たような発売後の要求は、私たちが私たちの製品を承認することを求める外国司法管轄区に適用されるかもしれません。政府は違法の疑いのあるいかなる調査にも対応するために多くの時間と資源を必要とする可能性があり、否定的な宣伝が生じる可能性がある。上記の任意の事件や処罰の発生は、私たちの製品をマーケティングしたり、私たちの候補製品を商業化して収入を創出する能力を抑制する可能性があります。
さらに、FDAの法規、政策、または指導は変化する可能性があり、米国および他の管轄区域は、私たちの候補製品に対する規制承認を阻止または延期するために、または承認後の活動をさらに制限または規範化するために、新しいまたは追加の法規または政府法規を公布する可能性がある。米国や国外の未解決または未来の立法または行政行動によって生じる可能性のある不利な政府規制の可能性、性質、程度を予測することはできない。もし私たちが規制コンプライアンスを達成して維持することができなければ、私たちはマーケティングを許可されないかもしれないが、私たちの製品および/または候補製品は、私たちの収入を創出し、利益を達成または維持する能力に大きな悪影響を及ぼすだろう。
このような製品を販売することができるかもしれない各司法管轄区では、私たちのすべての製品は監督部門の承認を得る必要があり、このような承認を得ることができないことは、市場の潜在力を十分に発揮する能力を制限するだろう。
米国国外で製品を販売するためには、私たちまたは私たちのライセンシーは、安全性と有効性に関する他の国の多くの法規的要件を遵守しなければならない。一国で行われる臨床試験は、他の国の規制部門に受け入れられない可能性があり、一国の規制承認は、他のどの国でも規制承認を受けることを意味するものではない。しかし、一方の管轄区域で規制承認を得られなかったことは、別の管轄区域で規制承認を得る能力に悪影響を及ぼす可能性がある。承認の流れは国によって異なり、追加の製品テストと検証、追加の行政審査期間に関連する可能性があります。外国の監督管理機関の承認を求めることは困難とコストを招く可能性があり、追加の非臨床研究或いは臨床試験が必要であり、これは高価で時間がかかる可能性がある。各国の規制要求には大きな違いがある可能性があり、私たちの製品がこれらの国で発売されることを延期または阻止する可能性がある。もし私たちまたは私たちの許可者が国際市場の規制要求を遵守できなかったり、必要な承認を得て維持できなかったり、あるいは国際市場の規制承認が延期された場合、私たちの目標市場は減少し、私たちの製品のすべての市場潜在力を達成する能力は損なわれるだろう。
もし私たちが他の候補製品や製品を開発、買収、許可できなければ、私たちの業務と見通しは制限されるだろう。
私たちの長期成長戦略は、既存製品と候補製品に基づいて候補製品の組み合わせを開発し、商業化することです。早期から中期までの新しい化学物質やNCEを買収する可能性もある。我々には内部開発能力があるにもかかわらず,既存の化合物を改善することができると信じているが,新たな化学物質や化合物を識別·開発する内部薬物発見能力はない。したがって、候補製品チャネルを拡大する主な手段は、既存のFDAによって承認された製品開発のための改善された処方および投与方法、および/または候補製品を選択および買収することができるかもしれない候補製品を治療または現在の目標の治療適応を増強するために使用するか、または私たちが許容できる条項で私たちの開発または戦略計画に適合することである。既存製品の新しい処方を開発したり、将来性のある候補製品を決定、選択、獲得、許可したりするには、大量の技術、財政、人的資源の専門知識が必要である。このような努力は、特定の候補製品の実際の開発、買収または許可を招くことがなく、何のメリットも生じることなく、我々の管理職の時間および大量の資源の支出を分散させる可能性がある。もし私たちの製品ラインにもっと多くの候補製品を増やすことができなければ、私たちの長期業務と見通しは制限されるだろう。
私たちのいかなる薬品の安全性に対する大衆の懸念は、私たちのラベルに不利な情報を含むことを招くかもしれないし、追加コストをもたらす可能性のある他の活動を要求するかもしれない。
ある薬品の安全リスクに関する広く報道された事件を考慮して、FDA、国会議員、政府責任局、医療専門家と一般公衆は潜在的な薬品安全問題に対して懸念を提出した。これらの事件は薬品の撤回を招き、薬品ラベルを改訂し、薬品の使用をさらに制限し、例えば、承認された後の薬品の流通を制限する可能性があるリスク管理計画を構築した。FDAAAはFDAに著しく拡大された権力を与え、その大部分は薬品承認前と承認後の安全性を向上させることを目的としている。特に、FDAAAは、FDAが他に加えて、承認後の研究および臨床試験を行うことを要求し、新しい安全情報を反映するために薬物タグを強制的に変更し、いくつかの現在承認されている薬物を含むいくつかの薬物のリスク評価および緩和策を要求する。FDAAAは連邦政府の臨床試験登録や結果データベースも著しく拡大しており,臨床試験に対する政府の監督が著しく増加することが予想される。FDAAAによれば、本法及びその他の規定に違反した会社は、大量の民事罰金、その他の規制、民事及び刑事罰を受ける。薬物安全問題に対するより多くの関心はFDAが著者らの臨床試験のデータを審査する際により慎重な方法をとることを招く可能性がある。臨床試験からのデータは、より厳しい審査を受ける可能性があり、特に安全性の面では、FDAまたは他の規制機関が追加の臨床前研究または臨床試験を要求する可能性が高いかもしれない。FDAが任意の承認された医薬製品に追加の臨床または臨床前データを提供することを要求する場合、候補製品の承認された適応は限られている可能性があり、または特定の警告または用量制限がある可能性があり、任意の承認された製品を商業化する努力は悪影響を受ける可能性がある。
私たちの知的財産権に関するリスクは
もし私たちが私たちの任意の製品と候補製品の知的財産権を獲得または保護できなければ、私たちは私たちの市場で効果的に競争することができないかもしれない。
私たちは特許、商業秘密保護、秘密協定の組み合わせによって、私たちの製品と私たちの候補製品に関連する知的財産権を保護します。生物技術と製薬分野の特許の発行、範囲、有効性、実行可能性、強度と商業価値は複雑な法律と科学問題に関連し、不確定である可能性がある。私たちが所有しているまたは許可中の特許出願は、発行された特許を生成できない可能性があり、承認された場合、これらの特許は、米国または他の国または地域の製品または候補製品をカバーできない可能性がある。もしこのようなことが起こったら
もし承認されれば、私たちの製品と候補製品は初期の模造薬競争に直面するかもしれない。我々の特許および特許出願に関連する従来技術が存在する可能性があり、これらの技術は、特許を無効にするか、または係属中の特許出願に基づいて特許が発行されることを阻止する可能性がある。特に,我々の多くの候補製品中の活性医薬成分は長年単独の製品として発売されてきたため,これらの製品が以前ラベル外で使用されていた方法は,我々の特許の有効性や特許出願による特許取得能力に影響を与える可能性がある。
特許訴訟過程は高価で時間がかかる。私たちまたは私たちの許可者は、すべての必要または望ましい特許出願を商業的に合理的なコストで、またはすべての管轄区域でタイムリーな方法で準備、提出、起訴することができないかもしれない。私たちまたは私たちのライセンシーも、特許保護を受ける前に、開発および商業化活動中に行われた発明の出願可能な特許の態様を決定できなかった可能性がある。さらに、私たちが将来加入する可能性のある任意の内部許可の条項によれば、私たちは、第三者から内部許可を得る技術を含む特許出願の準備、提出および起訴を制御する権利がないかもしれない。したがって、このような特許と特許出願は、私たちの業務の最適な利益に合った方法で起訴され、強制的に実行されないかもしれない。
特許提供の保護に加えて、私たちは、特許を出願できない独自技術を保護するために、商業秘密保護および秘密保護協定に依存して、特許を実施することが困難であるか、または特許を求めない方法を選択することと、私たちの薬物開発および再処方中に特許に含まれないノウハウ、情報または技術に関する任意の他の要素とを保護する。私たちは通常、私たちのすべての同僚に彼らの発明を譲渡することを要求しているが、私たちは通常、私たちのすべての同僚、コンサルタント、コンサルタント、および私たちの独自技術、情報、または技術にアクセスできる第三者が秘密協定を締結することを求めているが、私たちはこのようなすべての合意が正式に実行されているか、または私たちの商業秘密および他の機密固有情報が漏洩されないか、または競争相手が他の方法で私たちの商業秘密または独立開発と実質的に同じ情報および技術を獲得しないことを保証することはできない。また、私たちは私たちのビルの実体安全と、私たちの情報科学技術システムの実体と電子安全を維持して、私たちの資料と商業秘密の完全性とセキュリティを維持することに力を入れています。私たちはこのような個人、組織、そしてシステムに自信がありますが、合意や安全措置は違反される可能性があり、私たちはどんな違反にも対応する十分な救済措置がないかもしれません。さらに、私たちのビジネス秘密は競争相手や他の第三者によって知られたり独立したりするかもしれない。また,我々のビジネス秘密を守るための手順が不十分であると考えられれば,第三者による商業秘密の流用に対抗する十分な追跡権がない可能性がある.しかも、他の人たちは私たちの商業秘密と固有の情報を独立して発見するかもしれない。例えば、FDAは、商業秘密または他の固有情報と考えられる情報を含む、より多くの情報を定期的に公開するかどうかを考慮しており、FDAの開示政策が将来どのように変化する可能性があるかは不明である。もし私たちが私たちの技術に関連する非特許知的財産権の第三者への実質的な開示を阻止できず、私たちがこのような強制的に実行可能な商業秘密保護を持っている保証がなければ、私たちは私たちの市場で競争優位性を確立または維持することができないかもしれません。これは、私たちの業務、運営結果、および財務状況に大きな悪影響を及ぼす可能性があります。
いくつかの特許については、私たちは限られた地理的保護しか持っていないかもしれないし、私たちは世界各地で私たちの知的財産権を保護できないかもしれない。
もし私たちの製品や候補製品が承認されれば、世界のすべての国で特許出願を提出して起訴し、特許を守ることは目を引くほど高価になるだろう。競争相手は私たちが特許保護を受けていない司法管轄区域で私たちと私たちの許可側の技術を使用して彼ら自身の製品を開発することができ、また、他の侵害製品を私たちと私たちの許可側が特許保護を持っている地域に輸出することもできるが、執行権はアメリカやヨーロッパの地域に及ばない。これらの製品は私たちの製品や候補製品と競争するかもしれませんが、私たちと私たちのライセンシーの特許または他の知的財産権は彼らの競争を効果的にまたは阻止するのに十分ではないかもしれません。
しかも、私たちは付与される前に国と地域の特許出願を放棄することに決定するかもしれない。すべての国や地域の特許出願の審査は独立した手続きだ。したがって、同じファミリーの特許出願は、米国のようないくつかのドメインで特許として発行されることができるが、異なる範囲の特許要件として特許として発行される可能性があり、さらには他のドメインで拒否される可能性もある。同様に一般的な場合は、国によって同じ候補製品または技術の特許保護範囲が異なる可能性があることである。
いくつかの司法管轄区の法律は知的財産権の保護程度はアメリカとヨーロッパの法律或いは規則に及ばず、多くの会社はこれらの司法管轄区の保護とこのような権利を保護する時に重大な困難に直面している。特定の国の法律制度、特に特定の発展途上国の法律制度は、特許、商業秘密、および他の知的財産権保護の実行を支持しておらず、これは、私たちの特許の侵害を阻止したり、私たちの専有権を侵害する方法で競争製品を販売することを困難にするかもしれない。他の管轄区域で私たちの特許権の訴訟を強制的に執行することは、成功するかどうかにかかわらず、巨額のコストを招く可能性があり、私たちの努力と注意を私たちの業務の他の側面から移し、私たちの特許が無効と発表される可能性があります
狭義の解釈と我々の特許出願は,特許として発行されないリスクに直面しており,第三者からのクレームを引き起こす可能性がある.私たちは私たちが起こしたどんな訴訟でも勝てないかもしれないし、判決された損害賠償や他の救済措置(もしあれば)は商業的な意味がないかもしれない。したがって、私たちが世界各地で私たちの知的財産権を実行する努力は、私たちが開発または許可した知的財産権から顕著なビジネスメリットを得るのに十分ではないかもしれません。また、私たちが予想している重要な市場で私たちの知的財産権を保護するつもりですが、候補製品をマーケティングしたいかもしれないすべての司法管轄区域で同様の努力を開始したり維持したりできることを保証することはできません。したがって、これらの国で私たちの知的財産権を保護するための努力が不十分である可能性があり、これは、すべての予想される重要な海外市場で私たちの候補製品を商業化することに成功した能力に悪影響を及ぼす可能性がある。私たちまたは私たちの許可者が知的財産権の保護に困難に直面したり、他の理由でこれらの管轄地域の業務に重要な知的財産権を効果的に保護できない場合、これらの権利の価値は低下する可能性があり、私たちはこれらの管轄区域の他の人からの追加的な競争に直面する可能性がある。
一部の国にも強制許可法があり,これらの法律により特許権者は第三者に強制的に許可を付与される可能性がある。さらに、いくつかの国は、政府機関または政府請負業者に対する特許の実行可能性を制限している。これらの国では,特許権者の救済措置が限られている可能性があり,このような特許の価値を大きく低下させる可能性がある。もし私たちまたは私たちのいかなる許可者も私たちの業務に関連する任意の特許の許可を第三者に付与することを余儀なくされた場合、私たちの競争地位は損なわれる可能性があります。
特許改革立法は、私たちの特許出願をめぐる起訴と、私たちが発表した特許の実行または保護の不確実性とコストを増加させるかもしれない。
私たちが特許を取得する能力は、これまでいくつかの法律原則が解決されていないため、米国特許で許可されている権利要件の広さや解釈に一貫した政策がなく、関連する法律、科学的、および事実的問題の複雑さのために、特許請求項を支援し説明するために必要な特許および特許出願の具体的な内容は非常に不確実である。米国や他の国の特許法や特許法解釈の変化は,我々の知的財産権の価値を低下させたり,我々の特許保護の範囲を縮小したりする可能性がある。例えば、2011年9月16日、“ライシー·スミス米国発明法”または“ライシー·スミス法案”が法律に署名された。“ライシー·スミス法案”は米国特許法を多くの重大な改正を行った。このような条項は特許出願起訴方式に影響を与える条項を含み、特許訴訟に影響を及ぼす可能性もある。米国特許商標局(USPTO)は、“ライシー·スミス法案”の全面的な実施を規範化するために、新たな未検査法規や手続きを制定し、“ライシー·スミス法案”に関連する特許法の多くの実質的な改正、特に最初の提出条項の改正は、2013年3月に発効した。Leahy-Smith法案はまた、第三者が発行された特許に挑戦しやすく、特許出願の起訴に介入するためのいくつかの手続きを導入した。最後に、“ライシー·スミス法案”は新しい法定条項を含み、依然として米国特許商標局にこれらの法規を施行するための新しい法規を発行することを要求しており、裁判所は新しい法規の条項を説明するのに数年かかるかもしれない。
近年、米国最高裁判所はいくつかの特許事件に対して裁決を下し、場合によっては利用可能な特許保護範囲を縮小するか、場合によっては特許所有者の権利を弱めるかを決定している。我々の将来の特許取得能力に関する不確実性の増加に加えて,このようなイベントの結合は,いったん特許を取得する価値に関する不確実性をもたらしている.米国議会、連邦裁判所、および米国特許商標局の行動によれば、特許を管理する法律および法規は、予測不可能な方法で変化する可能性があり、それにより、新しい特許を取得するか、または既存の特許または将来獲得可能な特許を実施する能力を弱める可能性がある。同様に、他の国又は管轄区域の特許法及び法規の変化、又はそれらを実行する政府機関の変化、又は関連する政府当局が特許法律又は法規を実行する方法の変化は、新たな特許を取得したり、既存の特許又は将来入手可能な特許を実施する能力を弱める可能性がある。したがって、Leahy-Smith法案が私たちの業務運営および私たちの知的財産権の保護と実行にどのような影響を与えるかを判断するのは時期尚早だ。しかしながら、“ライシー·スミス法案”およびその実施は、我々の特許出願をめぐる起訴および我々が発行した特許の実行または保護の不確実性およびコストを増加させる可能性がある。私たちのノウハウをカバーしている特許を取得、実行、保護できないことは、私たちのビジネスの将来性と財務状況に大きな悪影響を及ぼすだろう。
また、一部の外国の法律の専有権に対する保護程度や方式は米国の法律とは異なる。したがって、私たちはアメリカでも海外でも、私たちの知的財産権を保護して守ることで大きな問題に直面するかもしれない。例えば、他の国で同じ発明をカバーする特許が発行されているのではなく、特定の国で発明をカバーする特許が発行されている場合、または、ある国で発行された特許の有効性、実行可能性または範囲、または1つの国で発行された特許における書面記述または許可のいずれかの司法解釈が、他の国に発行された対応する特許の解釈と異なる場合、私たちがこれらの国で私たちの知的財産権を保護する能力は制限される可能性がある。米国や他の国の特許法や特許法解釈の変化は,我々の知的財産権の価値を大きく低下させたり,我々の特許保護の範囲を縮小したりする可能性がある。
私たちは現在、未来に私たちの特許を保護したり強制したりする訴訟に巻き込まれ続けるかもしれない。これらの訴訟は費用が高く、私たちは大量の財政資源を必要とし、非常に時間がかかり、1つ以上のクレームは長年続くかもしれないし、成功しないかもしれない。
競争相手は私たちの特許または任意の潜在的な許可者の特許を侵害するかもしれない。権利侵害や不正使用と戦うために、私たちはずっと要求されてきたが、将来的にも侵害請求を要求されるかもしれない。これは高価で時間がかかる。例えば、2013年8月から、米国デラウェア州地方裁判所に疑似製薬会社6社に対する特許侵害訴訟を提起し、Suboxoneの米国での後発薬バージョンの承認をFDAに要求した。これらの事件のうち、模造製薬会社6社に対する事件は1社を除いてすでに解決されている。第2部第8項の財務諸表や補足データのような特許権の執行も求めています22事件があったり.
侵害訴訟では、裁判所は、私たちまたは私たちのライセンシーの特許が無効または強制執行できないと判断することができ、または私たちの特許が関連技術をカバーしていないことを理由に、他方の関連技術の使用を阻止することを拒否することができる。任意の訴訟または弁護手続における不利な結果は、私たちの1つまたは複数の特許を無効または狭義に解釈されるリスクに直面させ、私たちの特許出願を発行できないリスクに直面させる可能性がある。
第三者によって引用されるか、または私たちによって提起された干渉手続きは、私たちの特許または特許出願、または私たちの協力者が人間であってもよい発明に関する優先度を決定するために必要である可能性がある。不利な結果は、私たちが関連技術の使用を停止することを要求するか、または勝利者から許可を得ようとすることを要求するかもしれない。もし勝利者が商業的に合理的な条項で私たちに許可証を提供しなければ、私たちの業務は深刻な損害を受けるかもしれない。私たちが訴訟を提起したり抗弁したり、訴訟に介入したりすることは失敗する可能性があり、成功しても巨額のコストを招き、私たちの経営陣や他の従業員のコア業務に対する関心を分散させる可能性があります。私たちは、特に米国のようにこれらの権利を十分に保護していないかもしれない国では、私たちの知的財産権の盗用を単独でまたは許可者と一緒に防ぐことができないかもしれない。
第2部第8項.財務諸表及び補足データに記載されているように、付記22、事件があったり私たちの連結財務諸表によると、私たちが発表した多くの特許は訴訟に関するものだ。私たちがこれらの訴訟事項で直面している挑戦に加えて、私たちのいくつかの発行された特許は、再審や再審などの行政訴訟に関連しています各方面間USPTOで検討され、EPOで反対された。疑問視されている特許のすべての権利要求が支持される保証はなく、私たちが疑問視している特許が侵害されることが発見される保証もない。私たちは疑問視されている特許を完全に失うかもしれないし、私たちの製品や候補製品をカバーするのに十分ではないと思われる可能性がある程度にクレーム範囲を修正しなければならないかもしれない。もしそのいずれかが発生すれば、私たちは市場での競争優位性を失う可能性があり、私たちの業務は実質的な影響を受けるかもしれない。
さらに、知的財産権訴訟は大量の開示を必要とするため、このような訴訟の間、私たちのいくつかの機密情報は開示によって漏洩される可能性がある。聴聞、動議、または他の一時的手続き、または事態発展の結果を公開することもできる。もし証券アナリストや投資家がこれらの結果がマイナスだと思っていれば、私たちの普通株の価格に実質的な悪影響を及ぼす可能性があるもっと情報を知りたい場合は、SにアクセスしてくださいB第2の部分項目8.財務諸表と補足データ付記22、事件があったり私たちの連結財務諸表までs.
第三者は私たちが彼らの知的財産権を侵害したことを告発する法的訴訟を提起する可能性があり、その結果は不確定であり、私たちの業務成功にマイナスの影響を与える可能性がある。
私たちのビジネスの成功は、私たちの能力、および私たちの既存および未来の協力者が、私たちの製品および候補製品を開発、製造、マーケティング、販売する能力にある程度依存し、私たちの独自技術を使用して、第三者の特許および独自の権利を侵害し、実際に侵害、流用、または他の方法で侵害することなく、私たちの独自技術を使用する。バイオテクノロジーおよび製薬産業では、特許および他の知的財産権に関する訴訟や他の訴訟が多く行われている。我々が候補製品を開発する分野には,第三者が所有する米国や外国から発行される特許や係属中の特許出願が多く存在する.また,特許権の強制執行による特許料の抽出と和解にのみ重点を置いた特許持株会社が我々を対象とする可能性がある。
私たちは、今後、私たちの製品、候補製品、および技術の知的財産権に関連する対抗手続きまたは訴訟の脅威になり、または脅威になる可能性があり、妨害または派生プログラム、許可後審査および各方面間米国特許商標局または任意の司法管轄区域の同様の対抗手続または訴訟で審査される。同様に、私たちまたは私たちのライセンシーまたは協力者は、第三者によって制御された知的財産権の有効性または範囲を疑問視することを含む可能性がある第三者に対するこのような訴訟または訴訟を将来的に開始する可能性がある。第三者はすでに主張しており、将来的には既存の特許または将来付与される可能性のある特許に基づいて、その是非曲直にかかわらず、侵害クレームを主張している。他の第三者が強制執行または他の方法でその特許権を主張するために私たちと訴訟を行うことを選択する可能性があるリスクがあります。これらの主張のいずれかに法的根拠がないと考えても、管轄権のある裁判所は、これらの第三者特許が有効で、強制的に実行可能であり、侵害されていると判断することができ、どのような特許の所有者も、適用される特許によって許可され、またはこれらの特許が満期になるまで、または最終的に満了するまで、これらの製品または候補製品を商業化する能力を阻止することができるかもしれない
無効または強制的に実行できないと判断された。同様に、管轄権のある裁判所が私たちの技術の様々な態様をカバーするために任意の第三者特許を持っている場合、そのような特許の所有者は、許可証を取得しない限り、またはその特許が満了または最終的に無効と判定されるまで、強制的に実行できない、または私たちの製品または技術によって侵害されていない限り、我々が適用可能な製品または候補製品を開発および商業化する能力を阻止することができるかもしれない。いずれの場合も、そのようなライセンスは、商業的に合理的な条項で取得できないか、または全く得られない可能性がある。我々が許可を得ることができても,非排他的である可能性があり,我々の競争相手が我々に許可された同じ技術にアクセスできるようにする.また、訴訟がない場合であっても、第三者からライセンスを取得して、私たちの研究を進めたり、候補製品の商業化を可能にするために、第三者からライセンスを取得する必要があるか、または選択することが可能である。私たちはもしあれば、合理的な費用または合理的な条項でこのような許可証のいずれかを得ることができないかもしれない。この場合、私たちは私たちの技術をさらに実践したり、私たちの任意の候補製品を開発して商業化することができないかもしれません。これは私たちの業務を深刻に損なう可能性があります。
私たちにクレームを出した当事者は禁止または他の公平な救済を受ける可能性があり、承認されれば、私たちの1つ以上の候補製品のさらなる開発と商業化を効果的に阻止することができるかもしれない。これらのクレームの弁護は、その是非にかかわらず、巨額の訴訟費用がかかり、私たちの業務から従業員資源を大量に移転する可能性がある。このようなクレームを提起した第三者は、私たちまたは私たちのライセンシーまたは協力者と比較して、これらの法的行動により多くの資源を投入する能力がある可能性がある。もし私たちに対する侵害クレームが成功した場合、私たちは故意に侵害された3倍の損害賠償と弁護士費、特許権使用料の支払い、私たちの侵害製品の再設計、または第三者から1つまたは複数の許可を得ることを含む大量の損害賠償を支払わなければならないかもしれないし、多くの時間とお金の支出が必要かもしれない。
我々の製品および候補製品が所有する特許および特許出願は、特定の配合および製造プロセスに限定され、我々の製品および候補製品の市場機会は、有効成分の特許保護の欠如、他の配合および製造プロセスからの競争、および競合他社が開発する可能性のある管理方法によって制限される可能性がある.
私たちは、特定の配合および製造プロセスを含む、私たちの製造技術、投与技術、および私たちの製品および候補製品の特許保護を求め続けており、これは、物質被覆の組成のように競争相手の融通を効果的に防止することができないかもしれない。したがって、私たちが私たちの製品をマーケティングする時、私たちが発行した調合およびプロセス特許主張を侵害しない模造薬製品は利用可能であるか、または利用可能である可能性がある。必要な規制承認を得た競争相手は、競合他社が私たちの製品または候補製品のために開発した任意のプロセス、用途、または配合特許を侵害しない限り、私たちの製品または候補製品と同じ有効成分を含む製品を商業化することができ、私たちの製品のために得られる可能性のある任意の規制排他性に適合する。
我々の製品または候補製品と同じ活性成分を含む製品をカバーする特許および特許出願数は、ライバルが開発を求めており、我々の特許および特許出願がカバーされていない可能性のある競合処方を商業化することを求めている可能性があることを示している。競争相手が私たちとは異なる製品や候補製品の代替配合を開発し、商業化することができ、私たちの製品や製品が使用する特許を侵害しない場合、私たちの製品または候補製品のビジネス機会は深刻な損害を受ける可能性がある。
Suboxone、Zuplenz、Sympazan、およびExservanはFDAの承認を得ており、他の候補製品は将来FDAの承認を受けるかもしれない。私たちの他の製品が発売されるにつれて、1つ以上の第三者もまた、私たちがコントロールしている私たちの製品をカバーする特許に挑戦する可能性があり、これは、私たちが発表した私たちの製品をカバーする特許の一部またはすべての関連特許主張が無効または強制的に実行できない可能性がある。
もし私たちまたは私たちの被許可者のうちの1つが第三者に対して法的訴訟を提起して、私たちの製品または候補製品をカバーする特許を強制的に執行する場合、被告は反訴することができ、いくつかの既存の訴訟では、私たちの製品または候補製品をカバーする特許は無効であり、および/または強制的に実行できない。米国の特許訴訟では、被告が特許の無効および/または強制執行不可能と主張する反訴が一般的であり、第三者は様々な理由に基づいて特許が無効または強制的に実行できないと断言することができる。第三者も米国や海外の行政機関に類似したクレームを出すことができ、訴訟範囲外でも同様である。これらのメカニズムには、再審査、支出後審査、および外国司法管轄区における同等の訴訟手続が含まれる(例えば手続きに反対)。このような訴訟は、私たちの製品や候補製品をカバーしないように、私たちの特許が撤回または修正される可能性がある。法的に無効と実行不可能と断言された後の結果は予測できない。例えば、有効性の問題について、私たちは無効な以前の技術がないことを確認することはできないが、私たち、私たちの特許弁護士、特許審査員は起訴中にこれを知らない。もし被告が無効および/または強制執行できない法的主張に勝った場合、私たちは私たちの製品または候補製品の少なくとも一部またはすべての特許保護を失うだろう。このような特許保護の喪失は私たちの業務に実質的な悪影響を及ぼすかもしれない。詳細は参照のこと第4部は付記22、事件があったり私たちの連結財務諸表まで。
私たちの特許保護の獲得と維持は、政府特許機関によって提出された様々なプログラム、書類提出、費用支払い、および他の要求を遵守することに依存し、これらの要求に適合しなければ、私たちの特許保護は減少またはキャンセルされる可能性がある。
私たちが所有および許可する特許および/またはアプリケーション、ならびに私たちが将来所有または許可する可能性のある任意の特許権の有効期間内に、定期保守費、継続費、年金費用、および特許および/またはアプリケーションに関する様々な他の政府費用は、米国特許商標局および米国以外の様々な政府特許機関に支払われる。私たちは、これらの費用の状況を監視するために、私たちの外部弁護士または私たちの許可者に依存して、これらの費用を非米国特許エージェントに支払うべき時に必要な支払いを行うことができるようにします。米国特許商標局および様々な非米国政府特許機関は、特許出願中にいくつかのプログラム、文書、費用支払い、および他の同様の条項を遵守することを要求する。私たちは私たちの遵守を助けるために信用の良い法律事務所や他の専門家を招いて、私たちが許可を得た知的財産権に関するこれらの要求を守るために必要な行動をとることにも依存しています。多くの場合、不注意は、滞納金を支払うことによって、または規則を適用する他の方法によって救済することができる。しかしながら、場合によっては、規定を遵守しないことは、特許または特許出願が放棄または失効される可能性があり、それにより、関連法ドメインの特許権の一部または全部が失われる可能性がある。この場合、潜在的な競争相手が市場に参入する可能性があり、これは私たちの業務を損なう可能性がある。
我々の薬物開発戦略は505(B)(2)規制経路に大きく依存しており,承認された薬物に関する第三者特許を侵害していないことを証明することが求められている。このような認証は、通常、第三者が知的財産権侵害のクレームを出すことになり、弁護は高価で時間がかかり、任意の訴訟における不利な結果は、私たちの開発および商業化努力を阻害または延期する可能性があり、これは私たちの業務を損なうことになる。
知的財産権を実行または保護する訴訟や他の手続きは、しばしば性質が複雑で、非常に高価で時間がかかる可能性があり、私たちの経営陣の注意を私たちの業務の他の側面から移し、不利な結果を招く可能性があり、私たちの候補製品を発売してマーケティングする能力に悪影響を与えたり、第三者が私たちの製品や候補製品との競争を阻止したりする可能性があります。
アメリカ国内外では、生物技術と製薬業界に関連する特許とその他の知的財産権に関する訴訟の数は非常に大きく、特許侵害訴訟、妨害、反対とアメリカ特許商標局に提起された当事者間の再審手続きを含む。我々と我々の協力者が候補製品を開発している分野には,第三者が所有する米国や外国から発行された特許や未解決の特許出願が多く存在する.バイオテクノロジーや製薬業界の拡張や特許の発行に伴い、我々の候補製品が第三者特許権侵害の告発を受けるリスクが高まる可能性がある。
私たちのビジネス成功は、既存の承認された医薬製品に対する第三者の特許および独自の権利の侵害を回避することに大きく依存する。505(B)(2)規制経路を使用して私たちの製品および候補製品を承認するので、私たちは第三者によるこれらの承認された医薬製品に関する研究の全部または一部に依存します。したがって、FDAに私たちの候補製品の承認を申請する際には、(1)FDAのOrange Bookに我々のNDAに関する特許情報が記載されていないこと、(2)Orange Bookに記載されている特許が満了していること、(3)記載された特許が満了していないが、特定の日に満了し、特許が満了した後に承認を求めること、または(4)に記載された特許が無効であるか、または我々が提案する医薬製品の製造、使用または販売によって侵害されることがないことをFDAに証明することが要求される。第4項の認証をFDAに提出する際には、505(B)(2)セキュリティ協定がFDAによって届出を受けると、第4項の認証の通知も特許所有者に送信されなければならない。そして、第三者は通知で決定された特許を守るために私たちに訴訟を提起することができる。通知を受けてから45日以内に特許侵害訴訟を提起することは、最初の30ヶ月または特許満了日、訴訟が和解に達し、または裁判所が侵害訴訟において私たちに有利な判決を下すまで、FDAが私たちの秘密保護協定を承認することを自動的に阻止するだろう。第三者が所定の45日間の期間内に特許侵害訴訟を提起していない場合、私たちの秘密保護協定は30ヶ月の猶予の制限を受けません。
上述した第4段落の訴訟を除いて、特許の第三者全員は、一般的に、私たちが彼らのノウハウを不正に使用したと主張するかもしれない。我々の候補製品の使用または製造に関連する第三者特許または材料、配合または製造方法の請求項に記載の特許出願が存在する可能性がある。特許出願が発行されるまでに数年かかる可能性があるため、現在処理されているか、またはその後に出願されている特許出願が存在する可能性があり、これらの出願は、発行された特許が我々の製品または候補製品によって侵害される可能性がある。管轄権のある裁判所が、配合、任意の候補製品の製造プロセスに関連する任意の方法またはプロセス、製造中に形成された任意の分子または中間体、または最終製品自体の任意の他の属性を含む候補製品の様々な態様をカバーするために、任意の第三者特許を所有している場合、そのような特許の所有者は、適用特許によって許可されるか、またはその特許が満了するまで、候補製品を商業化することを阻止することができるかもしれない。いずれの場合も、そのような許可は商業的に合理的な条項や全く存在しないかもしれない。
私たちの成功は、第三者の知的財産権および独自の権利を侵害することなく運営する私たちの能力にある程度依存するだろう。私たちの業務、製品、候補製品、および方法が第三者の特許または他の知的財産権を侵害しないか、または侵害しないことを保証することはできません。
私たちにクレームを出した当事者は、禁止または他の平衡法救済を要求および/または得ることができ、これは、私たちの1つまたは複数の候補製品を一時的または永久的にさらに開発および商業化することを効果的に阻止することができる。これらのクレームの弁護は、その是非にかかわらず、巨額の訴訟費用がかかり、私たちの業務から従業員資源を大量に移転することが可能である。もし私たちに対する侵害クレームが成功した場合、私たちは故意に侵害した3倍の損害賠償金と弁護士費、第三者から1つ以上の許可証を取得し、印税を支払うか、または私たちの侵害製品または製造プロセスを再設計することを含む大量の損害賠償を支払わなければならないかもしれないし、大量の時間とお金の支出が必要かもしれない。私たちはそのようなライセンスがあるかどうか、あるいは商業的に合理的な条項で提供されるかどうかを予測できない。また、訴訟がない場合であっても、第三者からライセンスを取得して、我々の研究、臨床試験用品の生産、または候補製品の商業化を可能にする必要があるかもしれない。私たちはもしあれば、合理的な費用または合理的な条項でこのような許可証のいずれかを得ることができないかもしれない。この場合、私たちは私たちの1つ以上の製品や候補製品をさらに開発して商業化することができなくなり、これは私たちの業務を深刻に損なう可能性があります。私たちの製品や候補製品に対して強制的に執行される可能性のある第三者特許が存在しない保証はありません。それによって、私たちの販売を禁止したり、私たちの販売に対して、第三者に印税および/または他の形態の賠償を支払う義務があります。
私たちは私たちの特許と他の知的財産権の発明権または所有権のクレームに疑問を受けるかもしれない。
私たちはまた、元従業員、協力者、または他の第三者が私たちの特許または他の知的財産権に対して所有権権益を持っているというクレームを受ける可能性がある。私たちは将来的に所有権紛争の影響を受けるかもしれません。例えば、私たちの候補製品の開発と診断に参加するコンサルタントや他の人の義務紛争のためです。訴訟は、これらと他の挑戦在庫または所有権のクレームに対抗するために必要かもしれない。もし私たちがこのようなクレームを弁護することができなければ、金銭損害賠償を支払うことに加えて、貴重な知的財産権、例えば貴重な知的財産権の独占所有権や使用権を失う可能性がある。このような結果は私たちの業務に実質的な悪影響を及ぼすかもしれない。私たちがこのようなクレームを弁護することに成功しても、訴訟は通常巨額の費用がかかり、経営陣や他の従業員の注意を分散させる可能性がある。
もし私たちのブランド名のために十分な商標保護や監督管理の承認を得ることができなければ、影響を受けた製品の再命名が要求される可能性があり、これはこのような製品の発売遅延を招き、どのような製品の商業化の成功に実質的な影響を与え、私たちのコストを大幅に増加させる可能性がある。
私たちの製品や候補製品に対して使用または使用しようとしている任意の商標の権利を保護するために、私たちはこのような商標の登録を求めることができるかもしれない。商標登録は地域によって適切であり、私たちはアメリカおよび他の任意の他の私たちの製品または候補製品を商業化しようとしている国で商標登録を申請しなければならない。商標登録を獲得できなかったことは、私たちの商標使用をリスクに直面させたり、法的挑戦を受けさせたりする可能性があり、これは、私たちの製品や候補製品のための代替名を選択させる可能性があります。また,FDAと米国以外の他の規制機関は,提案された薬品製品名を独立して審査し,他の薬品名と混同する可能性を評価することを含む。これらの規制機関はまた、その名称が適切に提示されていないと思う場合、または治療主張を示唆する場合、提案された製品名に反対する可能性がある。FDAや米国以外の他の規制機関が私たちが提案した任意の製品名に反対する場合、私たちは私たちの製品または候補製品のために代替名を採用することを要求されるかもしれません。もし私たちが代替名称を採用すれば、私たちが商標登録を得ることができないからであっても、規制機関の反対のために、既存の商標申請の利点を失うだろう。したがって、適用可能な商標法に従って登録され、第三者の既存の権利を侵害せず、FDAおよび他の規制機関によって受け入れられる新しい製品名を採用するために多くの追加資源が必要となる可能性があり、これは、私たちの製品ブランド識別および任意の製品の商業化の成功に悪影響を与え、私たちのコストを増加させる可能性がある。さらに、新しい商標のための成功したブランド識別をタイムリーにまたは根本的に確立できない可能性があり、これは、製品や候補製品を商業化する能力を制限するだろう。
知的財産権は必ずしも私たちの競争優位に対するすべての潜在的な脅威を解決できるとは限らない。
私たちの知的財産権が提供する未来の保護の程度は不確定であり、知的財産権には限界があるため、私たちの業務を十分に保護できないか、あるいは競争優位性を維持することができるかもしれない。以下の例は例示的である
•他の人は、私たちの製品または候補製品と同様の製品を生産することができるかもしれないが、これらの製品は、私たちが所有または独占的に許可された特許請求の範囲内ではない
•私たちまたは潜在的な未来の許可者は、私たちのいくつかの発明をカバーする特許出願を最初に提出した会社ではないかもしれない
•他の人は私たちの知的財産権を侵害することなく、類似または代替技術を開発したり、私たちの任意の技術を複製したりすることができる
•私たちが処理している特許出願は発行された特許を生成しない可能性がある
•私たちが所有または独占的に許可された発行された特許は、競争相手の法的挑戦によって無効または実行不可能と認定される可能性がある
•私たちが所有または独占的に許可された発行された特許は、私たちの製品またはすべての国/地域の候補製品のすべての側面をカバーしないかもしれない
•私たちの競争相手は特許権のない国で研究や開発活動を行い、これらの活動から学んだ情報を利用して競争力のある製品を開発し、私たちの主要な商業市場で販売するかもしれません
•私たちは他の特許を申請できるノウハウを開発しないかもしれない
•他の人たちの特許は私たちの業務に悪影響を及ぼすかもしれない。
このような事件が発生した場合、私たちの業務、運営結果、そして将来性を深刻に損なう可能性がある。
私たちの普通株式所有権に関連するリスク
私たちの四半期の経営業績は大幅に変動する可能性があり、これらの変動は私たちの株価を下落させる可能性があります。
私たちの経営業績は引き続き四半期と年度の大幅な変動の影響を受けると予想されています。このような変動は私たちの株価を下落させるかもしれない。私たちの純損失と他の経営業績は様々な要素の影響を受けます
•FDAは、現在および将来の候補製品を承認する前に、追加的、予期しない研究、試験、または他の活動を完了することを要求するかどうか、このような承認を遅らせる可能性がある
•私たちは他の協力、許可、または同様の手配を実行し、これらのスケジュールに基づいて私たちが支払いまたは支払いを受ける可能性がある時間;
•私たちには限られた現金資源と巨額の債務があります
•私たちの将来の開発計画に関連した費用レベルの変化
•私たちが巻き込まれる可能性のある製品責任や知的財産権侵害訴訟
•FDAと他の規制機関の私たちの候補製品に対する承認を遅延し、獲得できなかったか、または不利な発展が見られた
•私たちの現在および未来の任意の他の候補製品または私たちの競争相手の候補製品に影響を与える他の規制の発展;
•もし私たちが現在または未来の任意の候補製品が規制部門の承認を得たら、その製品候補製品に対する潜在的な需要レベルと卸売業者購入モード。
もし私たちの四半期や年度の経営業績が投資家や証券アナリストの予想を下回れば、私たちの普通株の価格は大幅に低下する可能性がある。また、私たちの経営業績のどの四半期や年度の変動も、私たちの株価を大幅に変動させる可能性があります。
私たちの最大株主と経営陣は私たちのかなりの割合の株を持っており、株主の承認すべき事項に効果的に影響を与えることができる可能性があります。
2023年12月31日現在、私たちの役員と取締役実益は、私たちが発行した普通株の約9.5%を持っています。また,2023年12月31日現在,Bratton Capital Management L.P.とその付属会社は我々が発行した普通株の約14.8%を直接実益している。したがって、これらの株主は、取締役を選挙すること、私たちの組織文書を修正すること、または任意の合併、資産の売却、または他の重大な会社取引を承認することを含む、それぞれの所有権地位によって、株主の承認を必要とする事項に影響を与えることができるかもしれない。これは私たちの普通株に対する能動的な買収提案や要約を阻止または阻止する可能性があり、これらの提案や要約は私たちの株主としての最良の利益に合致していると考えられるかもしれません。
改正された1986年国税法第280 Gと4999条によると、“超過パラシュート支払い”に関連した巨額の費用が発生する可能性がある。
私たちは、もし彼の雇用協定または任意の他の福祉計画および計画における支払いおよび福祉が“1986年国税法”(改正)第499節またはこの規則の“超過パラシュート支払い”に関する消費税負担をトリガした場合、追加の税金補償金または“総”支払いを得る権利がある場合、私たちの首席革新·技術官A·マーク·スコベルと雇用協定を締結した。“規則”第280 G及び4999条によると、消費税は制御に係る支払の変化によって触発され、一般的にはさんの制御の変化前の5つの例年の平均年の課税補償の3倍以上となっている。これはスコベルさんの過去5年間の平均課税報酬の支払額の20%を上回る消費額に相当する(つまり、超過パラシュート支払い)。スコベルさんに税金総額の支払いを提供する以外に、スコベルさんの超過パラシュートへの連邦税金減免は行わないかもしれません。
スコベルさんに“超過パラシュート支払”を支払うと、この毛払いとスコベルさん超過パラシュート支払いの連邦減税損失が生じるため、Aqutive制御権変更に関連する大量のコストが生じるかもしれません。
私たちの純営業損失の繰越と他の税務属性を使用する能力は限られているかもしれません。
会社設立以来、私たちは大きな損失を被っており、私たちは近い将来利益が出ないと予想しています。もしあれば。現在公布されている連邦所得税法によると、今後数年間課税損失が発生し続ける場合、このような未使用損失は将来の課税収入を相殺するために繰り越されるが、今後1年間のこのような損失の控除は通常課税収入の80%に制限される。また、この基準第382条によれば、ある会社が“所有権変更”を経験し、通常3年間にその持分所有権が50%を超える変化が生じたと定義されていれば(価値で計算する)、同社は、変更前の純営業損失の繰越や他の変更前の税収属性(例えば、税収控除を検討する)を用いて変更後の収入を相殺する能力がさらに制限される可能性がある。私たちは私たちの最初の公募株を通じて、私たちが“所有権変更”制限をトリガしたかもしれないと信じている。また、私たちは、私たちの初公募株と未来の株式発行の総合的な影響による所有権変化を含む、私たちの株式所有権の後続の変化による所有権変化を経験し、将来的に経験する可能性がある。したがって,課税収入の純額を稼ぐと,変動前の純営業損失を用いて米国連邦課税収入を繰返す能力が制限される可能性があり,将来の納税義務が増加する可能性がある。
私たちは私たちの普通株に配当金を支払うつもりはないので、どんな見返りも私たちの株の価値に限定されるだろう。
私たちは普通株式に対するどんな現金配当金も発表したり支払ったりしたことがない。私たちは現在、事業の発展、運営、拡張のために未来の収益を保留し、予測可能な未来に現金配当金を発表または支払うことはないと予想している。したがって、株主のどんな見返りもその株の増価に限定されるだろう。
当社の会社登録証明書の改訂及び再記述の定款の条項、並びにデラウェア州法律における条項は、第三者が私たちを買収することを困難にしたり、買収コストを増加させる可能性があります。そうしても、私たちの株主に利益を与えたり、現在の経営陣を失脚させたりすることができます。
私たちの憲章文書やデラウェア州法律のいくつかの条項は反買収効果がある可能性があり、買収が私たちの株主に有利であっても、買収が私たちの株主に有利であっても、私たちの株主が現在の経営陣を交換または更迭しようとするのを阻止するかもしれない。これらの規定には
•“空白小切手”優先株の発行を許可し、その株式を株主の承認なしに発行できるように設定することができる
•株主の取締役罷免を制限する
•分類取締役会を設立し
•絶対多数の株主投票要求を作成して、私たちが改訂して再説明した会社登録証明書と、私たちが改正して再説明した定款のいくつかの条項を修正します
•株主が書面の同意の下で行動することを禁止し、すべての株主の行動が私たちの株主会議で行われなければならないことを要求する
•株主が株主特別会議を開催する能力を廃止する
•米国証券取引委員会のユニバーサル委託書規則を遵守し、取締役会メンバーを指名するか、株主総会で行動可能な事項を提出することを含む事前通知及びその他の要求を確立する。
これらの規定は、株主が責任を持って私たちの経営陣に命じられた取締役会のメンバーを交代させることを難しくし、株主が現在の経営陣を交代または罷免しようとしていることを挫折または阻止する可能性がある。また、私たちはデラウェア州本社の203条項の制約を受けています
このような取引が我々の取締役会の承認を得ない限り、デラウェア州会社が株主が利益株主になった日から3年以内に利益関連株主と広範な業務合併を行うことは一般的に禁止されている。この規定は、我々の株主が望むものであっても、我々の株主に有利であるかにかかわらず、制御権変更を遅延または防止する効果がある可能性がある。さらに、デラウェア州の法律の他の条項もまた、誰かが私たちを買収したり、私たちと合併したりすることを阻害し、延期したり阻止したりする可能性がある。
私たちが改訂し、再記述した会社登録証明書は、デラウェア州衡平裁判所が私たちの株主のために提起する可能性のある特定のタイプの訴訟および訴訟の唯一および独占フォーラムを指定し、これは、私たちまたは私たちの取締役、上級管理者、または従業員との紛争において有利な司法フォーラムを得ることを制限することができる。
私たちが改正して再説明する会社証明書規定は、限られた例外を除いて、デラウェア州衡平裁判所は、私たちが提起した任意の派生訴訟または法律手続きを代表する唯一かつ独占的なフォーラムであり、私たちの任意の取締役、高級管理者または他の従業員が私たちまたは私たちの株主に対して受託責任を持っていると主張するいかなる訴訟も、デラウェア州会社法、私たちの改正および再記載された会社証明書または私たちの改正および再記載された定款の任意の規定に基づいて生成された私たちのクレームに対する訴訟、任意の解釈、適用、適用される。当社の登録証明書又は当社の定款又は内部事務原則によって管轄されている請求を主張する任意の他の訴訟の有効性を強制的に執行又は決定する。任意の者又は実体が自社株の株式を購入又はその他の方法で取得する任意の権益は、当社の上述した改正及び再記載された会社登録証明書の規定に了承され、同意されたものとみなされる。このような裁判所条項の選択は、株主が司法裁判所において、私たちまたは私たちの役員、上級管理者、または他の従業員と紛争することに有利であると考えるクレームを提出する能力を制限する可能性があり、これは、私たちと私たちの役員、上級管理者、および従業員に対するこのような訴訟を阻止する可能性がある。あるいは、裁判所が、私たちが改訂および再記載した会社登録証明書のこれらの条項が、1つまたは複数の指定されたタイプの訴訟または法的手続きに適用されないことを発見した場合、またはそれを実行できない場合、私たちは、他の管轄区域でそのような問題の解決に関連する追加費用を発生させる可能性があり、これは、私たちの業務および財務状況に悪影響を及ぼす可能性がある。
一般リスク因子
私たちの業務は持続的なコロナウイルスの大流行の悪影響を受けるかもしれない。
2019年末から、新冠肺炎の発生はすでに世界的な大流行に発展している。疫病またはいかなる予測できない死の再発の持続時間と重症度に基づいて、私たちは、私たちの業務に実質的かつ悪影響を及ぼす可能性のある中断に遭遇する可能性がある
•著者らの臨床試験の各方面は、著者らの臨床試験における患者の募集、臨床試験場所の起動及び臨床地点の調査人員と臨床場所のスタッフの募集の遅延或いは困難を含む;患者が臨床試験から退出する比率の増加;医療資源が臨床試験の進行から移行する;連邦或いは州政府が強要或いは提案した旅行制限、臨床試験地点データモニタリングなどの肝心な臨床試験活動の中断;従業員と他の人への影響或いは臨床試験訪問或いは研究プログラムの中断は、テーマデータと臨床研究の終点の完全性に影響を与える可能性がある。FDAや同様の外国規制機関の運営中断や遅延は、規制審査·承認のスケジュールに影響を与える可能性がある。
•もし我々のサプライチェーンのいずれかの第三者がコロナウイルスの大流行による制限の悪影響を受けた場合、我々の臨床試験の候補製品および私たちの製造と流通の承認製品に必要な任意の材料を含み、活性医薬成分および他の原材料供給を含み、人員不足、生産減速または貨物輸送および他の輸送サービスおよび配送システムの中断を含む悪影響を受け、私たちのサプライチェーンは中断する可能性があり、それによって、私たちの臨床試験候補製品の生産、研究、開発と臨床運営、および私たちの承認製品の製造、流通、販売の能力を制限する。
•新型コロナウイルスの大流行期間中に数ヶ月閉鎖された後、私たちは業務オフィスを再開しましたが、再び新型肺炎に接触すれば、再び私たちの業務オフィスを閉鎖することを余儀なくされるかもしれません。しかし,我々の研究開発実験室や製造施設の同僚が現場で作業を継続し,大流行期間中に行われたように,伝播リスクを低減するために適切な安全·衛生対策を再実施することを希望している。このような状況が発生した場合、私たちの在宅勤務または健康問題のある同僚および他の第三者への依存は、生産性に悪影響を及ぼす可能性があり、新しい承認製品の商業発表活動を制限したり、妨害、遅延、または他の方法で私たちの業務に悪影響を及ぼす可能性があります。また,これは我々のネットワークセキュリティリスクを増加させ,データアクセス可能性の問題をもたらし,通信中断の影響を受けやすくなり,いずれも我々の業務運営に悪影響を与える可能性がある.私たちの研究や開発活動に従事している同僚は、私たちの施設がさらに閉鎖される可能性があり、政府がさらに制限するかもしれないので、長い間私たちの実験室や製造施設に入れないかもしれない。したがって、これは時間通りの完成を延期するかもしれない
臨床前活動は、新薬(IND)/臨床試験申請(CTA)を完成させ、研究または将来の開発候補を選択させる能力、および臨床または他の我々の開発計画および私たちの製品の生産および交付を開始することを含む。
•FDAと同様の外国の監督管理機関は中断、応答時間が遅い、あるいは資源不足に遭遇する可能性があり、私たちの臨床試験を監視し続けることができず、あるいは規制審査を求める私たちの候補製品に対して必要な活動と審査を行うことができ、このような中断は私たちの候補製品の開発、スケジュール、承認に大きな影響を与える可能性がある。
•コロナウイルスの大流行は私たちの顧客の需要と私たちが承認した製品の増加に影響を及ぼすかもしれない。例えば,我々Suboxoneの重要な顧客であるInDiorは,コロナウイルスがその製品販売に影響を与えることが予想されることを発表した。現在,供給に大きな中断はないと予想されているが,供給中断や遅延が新冠肺炎の灰再発により発生しない保証はなく,Suboxoneを含む承認された製品の注文に及ぼすコロナウイルスの大流行が悪影響を及ぼすことも正確には予測できない。私たちはまた一例で顧客の支払い周期が延長された状況を経験し、将来的にこのような状況を経験するかもしれない。
•コロナウイルスの持続的な影響による懸念により,我々は我々の普通株や他の証券を売却することで資金を調達したり,我々の任意の特許使用料やマイルストーンの権利を貨幣化することを求めたりする際に,問題や投資家の懸念に直面する可能性がある.さらに、不況、不況、または他の持続的な不利な市場事件は、金融市場、私たちの業務、私たちの普通株の価値、および私たちが株式または債務融資または私たちの特許使用料フローの任意の潜在的な貨幣化を有利な条件で得る能力に重大で不利な影響を及ぼすかもしれない。
コロナウイルスの大流行はまだ発展し続けている。コロナウイルスの大流行が我々に与える最終的な影響は高度に不確実であり,変化する可能性があり,未来の事態の発展に依存するが,将来の事態は正確に予測できない。私たちはまだ私たちの業務、私たちの臨床試験、私たちの研究計画、私たちが承認した製品の製造、マーケティング、流通と販売、医療システム、または世界経済の潜在的な遅延または影響のすべての程度を知らない。不確実性を考慮して,新冠肺炎が大流行するまで計画どおりに運営を維持できる保証はない。
私たちの未来の成功は私たちが肝心な管理者を維持し、合格者を吸引、維持、激励する能力にかかっている
私たちは私たちの管理チームの主要なメンバーと他の重要な幹部に強く依存しており、彼らのサービスの喪失は私たちの目標の実現に悪影響を及ぼす可能性がある。私たちのどんな幹部もいつでも退職することができます。私たちの業務のために、科学と技術者を含む他の合格した従業員を募集し、維持することも、私たちの成功の鍵となるだろう。技術人材に対する競争は非常に激しく、離職率が高い可能性がある。多くの製薬会社が似たようなスキルを持つ人を争っているため、受け入れ可能な条件で人材を引き付けることができないかもしれない。そのほか、臨床研究で成功できなかったことは、合格者の採用と維持をもっと挑戦的にする可能性がある。重要な幹部を募集できない、あるいはいかなる幹部や重要な従業員を失ったサービスも、私たちの発展と商業化目標の進展を阻害する可能性がある。
適用された雇用法によると、私たちは競争しない協約を実行できないかもしれない。
私たちの特定の幹部雇用協定には競争しない契約が含まれている。このような合意は私たちの幹部が私たちのために働くことを止め、限られた時間内に私たちと直接競争したり、私たちの競争相手のために働くことを禁止する。私たちはこのような合意を実行できないかもしれないし、法律を適用することによって、私たちはこのような合意を十分に実行できないかもしれない。もし私たちの利益がこのような競争行為によって損なわれることを証明できなければ、私たちの競争相手が私たちの元幹部の専門知識から利益を得ることを阻止できないかもしれないし、私たちの競争力は弱化されるかもしれない。
適用されるデータ保護やプライバシー法律法規を遵守しない行為は、私たちへの重大な処罰を招き、私たちの経営業績に悪影響を及ぼす可能性があります。
私たちはプライバシーとデータセキュリティに関する法律と法規を含む、アメリカのデータ保護法律と法規の制約を受けています。多くの連邦と州法律は、州データ漏洩通知法と州健康情報プライバシー法を含み、健康に関連する個人情報とその他の個人情報の収集、使用、開示と保護を管理する。データ保護の法律および法規を遵守しないことは、政府が法執行行動を取り、私たちに責任をもたらす可能性があり、これには、民事および/または刑事罰、個人訴訟、および/または私たちの経営業績および業務に悪影響を及ぼす可能性のある負の宣伝が含まれる可能性がある。EUや他の国の加盟国もデータ保護法律と法規を採択し、重大なコンプライアンス義務を規定している。EUでは、個人健康データの収集と使用はEUデータ保護指令の規定によって管轄されてきた。EU一般データ保護条例(GDPR)は、データ保護命令(実行日2018年5月25日)の代わりに、欧州全体のデータプライバシー法を調整し、すべてのEU市民のデータプライバシーを保護することを目的としています
特定のデータをどのように処理して処理するか。EUデータ保護法律と法規は個人データ(健康データ臨床試験を含む)を収集、分析と送信する能力に厳格な義務と制限を加えた。
これらの法律法規やその解釈や実施形態を遵守しないいかなる行為も、政府が法執行行動を取り、私たちに重罰を科し、私たちの経営業績に悪影響を及ぼす可能性がある。
私たちの同僚、首席調査員、コンサルタント、そして代理人は、規制基準と要求を遵守しないこと、およびインサイダー取引を含む、不適切な行為や他の不正活動に従事する可能性がある。
私たちは同僚、首席調査員、コンサルタント、そして代理人の詐欺や他の不適切な行為のリスクに直面している。これらの当事者の不適切な行為には、失敗が含まれている可能性がある
•FDA法規または他の管轄区域に適用される法規を遵守する
•FDAや他の規制機関に正確な情報を提供する
•アメリカと海外の医療詐欺と法律法規の乱用
•財務情報やデータを正確に報告する;または
•許可されていない活動を私たちに開示する。
私たちは私たちの同僚、コンサルタント、または独立請負業者が第三者の機密情報を誤って使用または開示したと告発されるかもしれない。
私たちが雇った人たちは以前他のバイオテクノロジーや製薬会社に雇われていた。私たちは、私たちまたは私たちの同僚、コンサルタント、または独立請負業者が無意識に、または他の方法で私たちの同僚の元雇用主または他の第三者の機密情報を使用または漏洩したと告発されるかもしれない。私たちはまた、前雇用主または他の第三者が私たちの特許に対して所有権を持っているというクレームに直面する可能性がある。このような疑いに対抗するために訴訟を提起する必要があるかもしれない。これらのクレームを正当化することに成功した保証はなく、たとえ私たちが成功しても、訴訟は巨額のコストを招き、私たちの経営陣や他の同僚たちのコア業務に対する関心を分散させる可能性がある。
私たちの普通株の市場価格は大きく変動する可能性があり、これは私たちの普通株の購入者に大きな損失をもたらすかもしれない。
初公募以来、我々普通株の市場価格は変動しており、変動する可能性が高い。一般的な株式市場,特にバイオ製薬や製薬会社の市場は,極端な変動を経験しており,この変動は特定の会社の経営業績とは無関係であることが多い。このような変動のため、あなたはあなたの購入価格以上で普通株を売ることができないかもしれません。私たちの普通株の市場価格は多くの要素の影響を受けるかもしれません
•現在の候補製品や競争相手の臨床試験結果と
•競争的薬物や治療法の成功や規制承認;
•米国と他の国の規制または法律の発展は、私たちの製品と候補製品、そして私たちの競争相手の製品と候補製品を含む
•特許出願、発行された特許または他の固有の権利に関連する発展または紛争;
•キーパーソンの採用や退職
•私たちの現在と未来の候補製品や臨床開発計画に関連する費用レベル
•私たちは他の候補製品の結果を発見、開発、取得、または許可するために努力している
•財務結果、開発、臨床試験または規制承認スケジュールまたは証券アナリストの提案に関する推定の実際または予想変化;
•承認された薬の供給を十分に受けたり遅延したりすることはできませんし許容可能な価格で得ることができません
•特許、訴訟事項、および私たちの技術のための特許保護を得る能力を含む、専有権に関する論争または他の発展;
•特許または株主訴訟を含む重大な訴訟;
•私たちの財務業績や私たちと似ていると思われる会社の財務業績の違い、あるいは私たちは予想された財務業績や資金を達成できなかった
•製薬とバイオテクノロジー部門の市場状況
•インフレと上昇する金利
•一般的な経済、産業、市場状況;
•“リスク要因”の節で述べた他の要因。
もし証券アナリストが私たちの業務に関する研究や報告を発表しなければ、あるいは彼らがわが社に対するマイナス評価を発表すれば、私たちの普通株の価格は下がるかもしれません。
私たちの普通株の取引市場は、業界や金融アナリストが発表した私たちまたは私たちの業務に関する研究と報告にある程度依存している。私たちは現在産業と金融アナリストに対する研究報告書が限られている。もし私たちの業務を追跡するアナリストが私たちの株に対する彼らの評価を引き下げたら、私たちの株価は下落するかもしれない。もし私たちの業務を追跡しているアナリストが私たちの株を報道するのを止めたら、私たちの株の市場での可視性を失うかもしれません。これは逆に私たちの株価を下落させる可能性があります。
2023年12月31日現在、私たちはもはや“新興成長型企業”ではありませんが、まだ“小さな報告会社”であり、より小さい報告会社に適用される報告書が、私たちの普通株の投資家に対する吸引力を低下させるかどうかを決定することはできません。
2023年12月31日から、私たちは“雇用法案”で定義されている“新興成長型企業”ではなくなった。我々は新興成長型企業であるが、サバンズ·オックス法第404(B)条に準拠する監査役認証要求の免除、定期報告や依頼書における役員報酬に関する開示義務の削減、役員報酬に対する非拘束性相談投票の免除など、他の非“新興成長型企業”に適用される上場企業に適用される様々な報告要件の免除を利用することができる。私たちはもう新興成長型会社ではないにもかかわらず、アメリカ証券取引委員会規則によると、私たちはまだサバンズ-オックススリー法案404(B)節の監査人認証要求に制約されていない。
証券法第405条の定義によれば、私たちは依然として“より小さい報告会社”であり、これは、私たちが投資会社、資産支援の発行者または親会社の多数の株式子会社ではなく、親会社が“より小さい報告会社”ではなく、本年度報告におけるForm 10-Kを含む多くの同じ開示要求免除を利用することができることを意味する。また、最近完成した第2四半期の最終営業日の公開流通株(我々の普通株式ベース)が2.5億ドル未満、またはその日までの公開流通株(我々の普通株式ベース)が7億ドル未満であり、最近終了した会計年度の年収が1億ドル未満である限り、より小さい報告会社として継続する資格がある。私たちは投資家が私たちがこのような免除に依存する可能性があるために私たちの普通株の吸引力が低下していることを発見するかどうか予測できない。もし一部の投資家がこれらの開示免除で私たちの普通株の吸引力が低下していることを発見すれば、私たちの普通株取引市場はそんなに活発ではなく、私たちの株価はもっと変動するかもしれない。
もし私たちが効果的な財務報告内部統制制度を維持できなければ、私たちは私たちの財務結果を正確に報告したり、不正を防止することができないかもしれない。したがって、株主は私たちの財務や他の公開報告書に自信を失う可能性があり、これは私たちの業務と私たちの普通株の取引価格を損なうだろう。
財務報告に対する効果的な内部統制は、信頼できる財務報告を提供するために必要であり、適切な開示制御や手順とともに詐欺を防止することを目的としている。新しいまたは改善された制御措置を実施できなかったり、実施中に遭遇した困難は、私たちの報告義務を履行できない可能性があります。さらに、“サバンズ-オキシリー法案”第404条に基づいて行われた任意のテスト、または私たちの独立公認会計士事務所がその後に行ったテストは、財務報告の内部統制における私たちの欠陥を明らかにすることができるかもしれません。これらの欠陥は、重大な弱点と考えられているか、または私たちの合併財務諸表を前向きまたは追跡的に変更する必要がある場合があり、または、さらなる関心または改善が必要な他の分野を発見することができます。悪い内部統制はまた、投資家が私たちが報告した財務情報に自信を失う可能性があり、これは私たちの普通株の取引価格にマイナス影響を与える可能性がある。
私たちの既存株主が公開市場で相当の数の普通株を売却することは私たちの株価を下落させるだろう。
既存の株主は、公開市場で我々の業績単位計画やPUP計画を終了することにより同僚や取締役に発行された株式を含む相当数の普通株を売却したり、これらの売却が起こりうると考えたりすることは、我々の普通株の市場価格を低下させ、追加株式証券を売却することで資金を調達する能力を弱める可能性がある。私たちはこのような売却が私たちの普通株の現在の市場価格に及ぼす影響を予測できない。
証券法によると、私たち証券の一部の保有者は彼らの株を登録する権利がある。証券法によるとこれらの株を登録することで,大量のこれらの株が自由になる
証券法により、制限されずに取引することができる。これらの株主のどの証券売却も私たちの普通株の取引価格に重大な悪影響を及ぼす可能性がある。
金融サービス業の不利な発展に影響を与えることは、私たちの現在および予想されている業務運営および私たちの財務状況や運営結果に悪影響を及ぼす可能性がある。
金融機関の不利な事態の発展に影響を与え、例えば噂や実際に発生した流動性に関連した事件は、過去及び未来に銀行倒産や市場全体の流動性問題を招く可能性がある。例えば、2023年3月10日、シリコンバレー銀行はカリフォルニア州金融保護·革新部によって閉鎖され、後者はFDICを担当者に任命した。同様に,2023年3月12日にSignature BankとSilvergate Capital Corp.がそれぞれ破産管理プログラムに置かれた.この場合、財務省、FRB、FDICは、このようなツールの売却の潜在的損失リスクを低減するために行動しているにもかかわらず、広範な顧客引き出し需要や金融機関の即時流動性に対する他の流動性需要がこのような計画の能力を超える可能性があるが、米国財務省、FDIC、連邦準備委員会が将来他の銀行や金融機関が閉鎖された場合に未保険資金のルートを提供するか、またはタイムリーにそうする保証はない。
我々の銀行関係を必要または適切に評価する必要があると考えられるが,我々が獲得した現金額は,現在予想されている将来の業務運営に資金や資本化を提供するのに十分であるが,これらの要因は,我々と銀行関係にある金融機関に深刻な影響を与え,我々自身に影響を与える可能性がある.他にも、これらの要因には、流動性の緊張または失敗、様々な金融、信用または流動資金協定または手配された義務を履行する能力、金融サービス業または金融市場の中断または不安定、または金融サービス業会社の将来性に対する懸念または否定的な予想が含まれる可能性がある。これらの要素はまた、金融市場や一般金融サービス業に関連する要素を含む可能性がある。1つまたは複数のこれらの要因に関連するイベントまたは懸念の結果には、現在および予想されているビジネス運営、ならびに私たちの財務状況および運営結果に生じる様々な重大かつ悪影響が含まれている可能性がある。これらは、預金または他の金融資産または未加入預金または他の金融資産の取得遅延の損失、または現金管理スケジュールの終了および(または)現金管理スケジュールによって制限された資金の取得または実際の損失を遅延させることを含むことができるが、これらに限定されない
さらに、米国または国際金融システムに対する投資家の一般的な懸念は、より高い金利またはコスト、より厳しい財務および運営契約、または信用および流動性源の獲得に対する体系的な制限を含むあまり有利ではない商業融資条項を招く可能性があり、それによって、私たちはより受け入れ可能な条項が融資を受けにくく、さらには融資を得ることができなくなるかもしれない。他のリスクに加えて、利用可能な資金または現金および流動資金源の減少は、運営費用、財務義務、または他の義務を履行する能力に悪影響を及ぼす可能性があり、私たちの財務および/または契約義務に違反したり、連邦または州賃金および労働時間法違反を招いたりする可能性がある。上記のいずれかの影響、または上記の要因または他の関連または同様の要因に起因する任意の他の影響は、我々の流動資金、私たちの現在および/または予想される業務運営、ならびに財務状態および運営結果に重大な悪影響を及ぼす可能性がある。
さらに、キープロバイダーまたはビジネスパートナーは、上述した任意の流動性または他のリスクの悪影響を受ける可能性があり、さらに、現在および/または予想されるビジネス運営および運営結果および財務状態に重大な悪影響を及ぼす可能性がある。いかなる業務パートナー又はサプライヤーが破産したか、又は債務を相殺しない、又は業務パートナー又はサプライヤーの任意の違約又は違約、又は任意の重要な業務パートナー又はサプライヤー関係を失うことは、私たちの現在及び/又は予想される業務運営及び財務状況に重大な悪影響を及ぼす可能性がある
項目1 B:未解決の作業者の意見を処理する
ない。
項目1 C:ネットワークセキュリティに関する問題
リスク管理と戦略
Aqutiveなネットワークセキュリティ計画は三つの重要な柱の上に構築されている:管理、プロセス、コンプライアンスと監査。私たちはサイバーセキュリティ脅威のリスクに直面していますが、これらの脅威は私たちの業務、財務状況、運営結果に実質的な悪影響を及ぼす可能性がありますが、Aqutiveなサイバーセキュリティ計画は訓練と意識によって支持される政策、手続き、基準に基づいています。ネットワークセキュリティチームはネットワークセキュリティプロジェクトの管理において豊富な経験を持ち、MSSPと協力して最先端のネットワークセキュリティ技術を配備し、脅威情報とネットワークリスク傾向を収集した。ネットワークセキュリティ計画はMSSPと共に実行され、MSSPは積極的な脅威監視、リスク評価とイベント応答能力を提供し、著者らの業務運営に影響を与える可能性のある任意の重大なネットワークリスクを適時に評価し、対応する。情報技術総監高級副総裁(“IT官”)はより広範な情報技術機能と共に、AQUCENTIALのネットワークセキュリティリスクの評価と管理を担当し、そして上級管理層にネットワークセキュリティ事件の予防、検査、緩和と修復を通報する。
統治する
管理·取締役会の役割
IT関係者は最高経営責任者に報告し、私たちのサイバーセキュリティ計画をリードした。我々のITスタッフは情報セキュリティ戦略とネットワークセキュリティリスク管理の面で10年以上の経験を持っている。内部AQUAL ITチームは、ネットワークリスクと情報セキュリティの管理において15年を超える技術経験、プロジェクト管理、アーキテクチャ経験を持っている。また、取締役会の監査委員会はAqutiveなネットワークセキュリティリスクを開放している。IT関係者は四半期ごとに監査委員会にAqutiveなネットワークセキュリティ計画の有効性を簡単に紹介し、毎年より深い審査を行っている。また,ネットワークセキュリティリスクも我々全体の企業リスク管理計画の一部として検討する。
私たちは私たちの業務に実質的な影響を及ぼすサイバーセキュリティの脅威や事件に遭遇しなかった。
プロジェクト2.建築と不動産
私たちはインディアナ州ポティッチにある8,400平方フィートの既存の生産施設(ミルトン)をレンタルしました。その中にはいくつかの研究開発オフィスとcGMP製造業務が含まれています。リースには,レンタル期間内にいつでも施設を購入する選択権と,施設を購入する優先購入権が含まれる.2023年2月28日、2028年3月31日に満期となるMelton施設賃貸契約を延長しました。賃貸条項と条件はこれまでの賃貸契約と同じです
私たちはまたインディアナ州ポティッチで73,000平方フィートの施設(Ameriplex)を借りて、追加の包装、研究開発、その他の業務を収容した。改訂後、本契約の期限は2028年9月30日までであり、更新オプションが含まれており、レンタル期間を2033年9月30日まで延長することができます
ニュージャージー州ウォーレンで19,610平方フィートの本部と主要な実験室を借りました改訂後、本契約の期間は2026年8月まで延長でき、更新オプションを含めて2029年8月まで延長することができます
私たちには不動産は何もありません
項目3.法的訴訟を起こす
法律訴訟に関するより多くの情報は、第2部第8項を参照。財務諸表と補足データ、付記22、事件があったり.
プロジェクト4.炭鉱の安全状況の開示
適用されません。
第II部
項目5.登録者の国際市場’普通株·関連株主事項と発行者による株式証券の購入
市場情報
我々の普通株は2018年7月24日にナスダック全世界精選市場で取引を開始し、現在ナスダック全世界市場で取引されており、コードはAQSTである。その前に、私たちの普通株は市場を公開しなかった。
記録保持者
2023年3月1日現在、私たちは約87人の普通株式保有者がいます。一部の株式は“街道”名義で保有されているため、当該等の株式の実益所有者の数は知られていないか、または上記の数字に含まれている。この数の登録所有者は、その株式が他のエンティティが信託形式で保有する可能性のある株主も含まれていない。
配当政策
私たちは普通株式に対するどんな現金配当金も発表したり支払ったりしたことがない。私たちは現在、未来の収益を維持し、私たちの業務の発展と成長に資金を提供するつもりだ。私たちは予測可能な未来に何の現金配当金も支払わないと予想している。任意の未来配当金の決定は私たちの取締役会の指示に基づいて行われ、私たちの財務状況、経営業績、契約制限、資本要求、業務見通しと取締役会が関連すると考えられる他の要素を含む当時の条件に依存するだろう。
最近未登録証券を売却する
ない。
発行者および関連購入者が株式証券を購入する
ない
プロジェクト6.予算を保留する
プロジェクト7.財務管理部門の財務状況と経営成果の検討分析
我々の財務状況及び経営結果に関する以下の議論は、我々の財務諸表及びこれらの財務諸表の付記とともに読まなければならず、これらの財務諸表の付記はForm 10−K年次報告の他の部分に現れる。この討論には重大な危険と不確実性に関する前向きな陳述が含まれている。本年度報告(Form 10−K)第1部1 A項“リスク要因”に記載されているような多くの要因の影響により、我々の実際の結果は、これらの前向き陳述で予想される結果と大きく異なる可能性がある。すべてのドルの金額は千単位です。
概要
AQUEATIOTICS,Inc.は製薬会社であり、革新的な科学と送達技術を通じて薬物を改善し、患者の生活に意義のある改善をもたらす。我々は,侵襲性や不便な標準看護療法の代替品である薬物製品を開発し,投与により複雑な分子を伝達している。私たちは5種類の許可された商業化製品を持っていて、私たちの許可メーカーがアメリカと世界各地で販売しています。私たちはこれらの特許製品の独占メーカーです。Aqutiveは製薬会社とも協力し,特許の同種最高の技術(例えばPharmFilm)を用いて新分子を市場に投入し,検証された薬物開発と商業化能力を有している。我々はアレルギー反応を含む重篤なアレルギー反応を治療する製品ラインを進めている。中枢神経系疾患の治療に専念する製品ラインも開発した。我々の製品と候補製品の概要については、本テーブルの10-Kの項目Iを参照してください。
財務運営の概要
収入.収入
これまで、私たちの収入は、私たちが許可者のためにカスタマイズした製造製品と、私たちが自主開発した現在許可されている独自製品Sympazanの収入から来ています。収入はまた、顧客との契約に基づいて提供される製品開発サービスと、私たちの知的財産権許可から来ています。これらの活動は、製造および供給収入、共同開発および研究費用、許可および特許使用料収入、および独自製品販売純額の4つの主要カテゴリーの収入を生成する。
製造と供給収入
我々は,被許可側から受け取った調達注文に基づいて生産を行い,品質保証が製造製品の品質が合意された仕様に適合していることを確認すると,我々のライセンサー側はこれらの注文を受けることが義務付けられている.私たちのExservanライセンスを除いて、私たちの許可者は、これらの製品の商業化の他のすべての側面を担当しています。私たちは、マーケティング、定価、販売、支払人のアクセス、および規制運営に関連する活動を含む、顧客の商業化活動に直接的または間接的な役割はありません。私たちがMTHAとHaiscoに発行したExservanライセンスについては、私たちは引き続きこの製品の守秘契約を持っていますので、私たちがその製品の秘密協定の所有者である限り、私たちは製品販売に関するいくつかの規制義務に責任があります。
将来のライセンス製品の製造および供給収入は、既存のライセンス製品のバッチ需要と、成功した製品開発協力に基づく既存または新しいプロトコルのライセンスおよび供給プロトコルの下での製造および供給権に基づくと予想される。
共同開発と研究費
私たちは私たちの許可者たちと協力して医薬製品を開発した。この点では,特定のタスク,活動を実行したり,関連する被許可者との契約スケジュールに規定された開発段階を完了したりすることで費用を稼ぐ.これらの履行義務の性質および程度は、一般にマイルストーンまたは成果交付と呼ばれ、一般に、契約に記載されたプロジェクトの範囲および構造、ならびに製品の複雑さおよび製品に必要な特定の規制承認経路に依存する。
ライセンスと印税収入
私たちは私たちの知的財産権許可から収入を達成する。私たちのさらなる開発または他の持続的な活動を必要としない許可については、私たちの許可者は、許可された知的財産権を、その候補製品の自己開発、製造、商業化、または他の特定の目的のために使用する権利を取得しており、これらの権利が効果的に譲渡された後、関連収入は、通常、ある時点で記録され、または制限されている(ある場合)。我々が提供する他の履行義務と組み合わせてのみ、開発サービスまたは特定の製品の製造のような大量の価値を提供することができる許可については、収入は、通常、ライセンス契約期間内に記録される。私たちはまた、私たちの知的財産権を使用した製品をライセンシーが販売することによって印税を稼ぎ、これらの製品は私たちが特許技術の権利を持つ国で販売し、販売している。今後の販売収入に関する特許権使用料収入は本項の重要な会計政策と試算の使用.
専有製品販売,純額
私たちは2018年12月に当社の最初の独自CNS製品Sympazanを商業化しました。独自製品販売収入は、即時支払い割引、卸売サービス料、返品手当、リベート、および自己支払いサポート償還を差し引いた純額に計上され、各項目は以下でより詳細に説明される。これらの準備金は、関連販売によって稼いだ金額または請求された金額の推定に基づいている。これらの金額は可変対価格とされ,販売時の取引価格の減少が推定され確認された.これらの見積り金額を取引価格に計上し,このような取引確認の累積収入が大きく逆転しない可能性が高いことや,可変対価格に関する不確実性が解決される可能性が高いことを前提としている.その中のいくつかの項目の計算は、管理層が販売データ、履歴返品データ、契約、その他の将来知る可能性のある関連情報に基づいて推定する必要がある。このような規定の十分性は四半期ごとに検討される。2022年10月、我々はAssertio(ナスダックコード:ASRT)の子会社Otter PharmPharmticals,LLCとAssertio協定を締結し、この合意に基づいて、協定期間内にUsertioにSympazanのグローバル独占知的財産権許可を付与した。私たちはSympazan for Assertioの独占メーカーとサプライヤーであり、Assertio契約を締結した後、製造と供給収入およびライセンスと印税収入の確認を開始します。
コストと支出
私たちのコストと支出は主に、製造と供給収入の発生、当社の特許製品候補製品の開発、および発売前と発売後の商業化努力、知的財産権調達、保護、起訴と訴訟費用、会社管理機能、医療と臨床事務管理、上場企業コスト、株式ベースの給与費用、および会社の借金の利息を含む販売、一般および管理費用の結果である。私たちは主にコストと費用を以下のカテゴリに記録している
製造と供給コストと費用
製造と供給コストと支出は主に私たちの商業化許可薬品の製造から来て、原材料、直接労働力と間接コストを含み、主に私たちがインディアナ州ボティチにある工場です。私たちの材料コストには、私たち独自の溶解フィルムと一次包装材料を製造するための原材料コストが含まれている。直接人工コストには、生産活動に従事する従業員の賃金コスト(税収や福祉を含む)が含まれる。間接費用には,主に間接賃金,施設賃貸料,光熱費およびリース改善および生産機器および設備の減価償却が含まれる。これらのコストは,市場定価で購入する材料コスト,製品生産に必要な直接人工数量,生産量に応じた固定間接費用の分配に応じて増加または減少することができる。
私たちの製造と供給コストと費用は顧客の供給需要の影響を受ける。生産コストは,市場価格と生産効率(販売可能単位のコストで測定)で購入した原材料のコストを反映している。これらのコストは、製品を生産するために必要な直接労働力および材料の数量および固定間接費用の分配に応じて増加または減少することができ、固定間接費用の分配は生産レベルに依存する。
私たちは引き続き合理化と管理コストを求め、Suboxone販売量の潜在的な低下に備えて、この市場の模倣薬が市場シェアを占め続けているため、2022年10月にSympazanを含む当社の許可製品(Sympazanを含む)が合意した後の予想製造収入によって少なくとも部分的に相殺される見通しだ。私たちの独自製品がオンラインになることを除いて、私たちは生産するために追加的な資源が必要かもしれない許可された製品を追加するかもしれない。SuboxoneやOndansetronなどの生産量の大きい製品機会がこのように増加すれば、独自やライセンス製品の製造数の増加により増加した製造·供給コストをサポートするために、追加人員の募集に関連するコスト増加が生じる。
研究と開発費
設立以来、私たちは私たちの研究開発活動に大量の資源を集中させてきた。研究と開発費は主に
•従業員に関連する費用には、報酬、福祉、株式給与、出張費用が含まれる
•CRO、調査場所、コンサルタントなど、第三者との手配に基づいて発生する外部研究·開発費用
•臨床研究材料の購入、開発、制作のコスト;
•臨床前と臨床活動および規制操作に関連するコスト。
アレルギー、AQST-108、その他の製品のような既存の候補製品の開発を続けるにつれて、私たちの研究と開発費用は今後数年間大幅に増加し、私たちは確定して開発することを予想しています
より多くの候補製品と技術を得る。著者らはより多くの技術に熟練した同僚或いは第三者を招聘或いは採用してこれらの活動を実行し、臨床試験を行い、最終的にこれらの臨床試験を成功させた任意の候補製品のために監督管理の許可を求めるかもしれない。
販売、一般、行政費用
販売、一般および行政費用には、主に賃金、福祉、株式ベースの給与、および役員、財務、および運営者の他の関連コストが含まれる。他の費用には、研究開発費に含まれていない施設および関連費用、例えば、特許関連および他の法律費用の専門費用、規制費用、相談、税務および会計サービス、保険、市場研究、諮問委員会および主要オピニオンリーダー、減価償却、およびITシステムに関連するコストを含む一般会社費用が含まれる。また、これらの費用には、倉庫、配送、販売、業務発展などのコストも含まれている
私たちの一般的かつ行政コストは、取引所の上場とアメリカ証券取引委員会の法規を遵守するために必要な会計、監査、法律規制と税務関連サービスの関連コスト、役員と幹部の保険コスト、および投資家と広報コストを維持することを含む。私たちは、第三者のリスクの高いジェネリック医薬品発売に関する私たちの権利の実行を求めることに関連する巨額の訴訟コストを含む、私たちの知的財産権の保護を求める過程で巨大なコストを発生させ続けている。
私たちは引き続き業務コストを管理し、将来のSuboxone収入の潜在的な低下と、私たちの業務に影響を与える他の外部要因に備えて、私たちは引き続き私たちの核心業務に集中します
•505(B)(2)経路に沿ってアレルギー反応およびAQST-108を継続的に発展させる;および
•Libervantの承認を求めてその後発売することは,FDAの米国市場参入の承認に依存することは保証されない。
利子支出
利息支出には12.5%債券と13.5%債券未償還残高の利息コストが含まれ、固定金利はそれぞれ12.5%と13.5%であり、四半期別支払い、および融資コストと債務割引の償却が含まれる。12.5%債券の償還および13.5%債券の発行の詳細は付記14参照長期債務私たちの連結財務諸表まで。また,参照されたい流動性と資本資源以下は12.5%と13.5%の債券のさらなる詳細である。
印税義務に関する利子支出
13.5%の手形の発行について,吾らは手形所持者と印税権利協定を締結し,手形所持者にアレルギー性(アドレナリン)語下映画の年間世界純売上高1.0%から2.0%に相当する分級特許権使用料を付与し,8年間,アレルギーが世界初販売から計算した。手形保有者は,Libervant(安定)口腔フィルムの世界年間純売上高の1.0%から2.0%の分級印税を得る権利があり,(1)アレルギー薬の初販売と,(2)Libervantの初販売から8年までである。これらの特許権使用料協定は債務に分類され、45,000ドルの価値の13.5%の債券の価値は、債務と特許権使用料義務の相対的に公平な市場価値に基づいて割り当てられている。将来的に特許権使用料の支払いを推定した56,926ドルは、分配公正価値の13,856ドルを超え、特許権使用料合意に関する割引であることが確認され、実際の利息法で利子支出として償却される。13.5%の債券が付記14で議論され、長期債務私たちの連結財務諸表まで。
将来の収入の売却に関する利子支出
2020年11月3日、私たちはマラソンと貨幣化協定を締結した。貨幣化協定の条項によると、私たちは、印税とマイルストーン支払いを得るために、Sunovion許可協定に従ってSunovionのアポモルフィン製品KYNMOBIに関連するすべての契約権利をマラソンに販売した。KYNMOBIはパーキンソン病患者の非発作の治療のためのアポモルフィン薄膜療法であり、2020年5月21日にFDAの承認を得た。これらの中継権を売却する交換として、マラソン会社から40,000ドルの前金を取得し、最初のマイルストーンを実現することで10,000ドルを追加支払いました。貨幣化協定によると、2023年12月31日までに合計50,000ドルを受け取りました。
貨幣化プロトコルによれば、指定された時間内にグローバル特許使用料および他の商業目標を達成する場合、私などは最大75,000ドルの追加または支払いを払わなければならない可能性があり、これは合計125,000ドルの潜在的な収益をもたらす可能性がある。2023年6月、SunovionはKYNMOBIを米国およびカナダ市場から自発的に撤退させることを発表したため、私たちは貨幣化協定下での追加または支払いを受けない可能性が高い
特許使用料がSunovionからマラソンに送金されるにつれて、受取特許権使用料の徴収と将来の収入販売に関する負債残高は合意有効期間内に有効に返済される。確定のために
将来の収入の販売に関連する負債を償却するためには、貨幣化協定の有効期間内にマラソンに支払われる将来の特許権使用料とマイルストーン支払い、マラソンまたはマイルストーン支払いの総額を見積もる必要がある。将来の特許使用料支払いは、受信した50,000ドルの収益と将来または有支払いの合計を減算し、貨幣化プロトコルの有効期間内の利息支出と記す。Sunovionの公開予測によると、私たちは未来の収入の売却に関する利息支出を記録することを停止する。
2020年第2四半期には,Sunovionライセンス契約により,今後8年間で毎年満期となる1,000ドルの年間最低保証特許使用料と関連した8,000ドルの特許使用料収入とそれに応じた受取特許権使用料が確認された。貨幣化プロトコルについては,ASC 860,譲渡およびサービス項目の下で評価を行い,既存の入金がマラソンに移行しているかどうかを決定し,受取金が移行していないと結論した。付記16を参照将来の収入を売る詳細を理解するために、私たちの連結財務諸表を参照してください。
利息収入その他の収入(費用),純額
利息収入及びその他の収入(支出)、純額は、利息勘定からの収入及び他の雑収入及び支出項目を含む。利息口座には最低預金額もなく、固定的な利息期限もありません。
経営成果
2023年12月31日までと2022年12月31日までの年次比較
以下,我々の運営結果の検討について,これらの運営結果の主な駆動要因を説明した。
収入.収入
次の表に私たちが指している時期の収入データを示します。
| | | | | | | | | | | | | | | | | | | | | | | | | | |
| | | | | | | 変わる |
| | | 2023 | | 2022 | | $ | | % |
| (単位は千ですが、%は含まれていません) | | | | | | | | |
| 製造と供給収入 | | $ | 43,805 | | | $ | 36,378 | | | $ | 7,427 | | | 20 | % |
| ライセンスと特許使用料収入 | | 5,376 | | | 2,351 | | | 3,025 | | | 129 | % |
| 共同開発と研究費 | | 1,402 | | | 1,293 | | | 109 | | | 8 | % |
専有権 製品販売、純額 | | — | | | 7,658 | | | (7,658) | | | 適用されない |
| 収入.収入 | | $ | 50,583 | | | $ | 47,680 | | | $ | 2,903 | | | 6 | % |
2022年同期と比較して、2023年の収入は6%増加した2903ドルだった。この増加は,製造と供給収入,許可と特許使用料収入および共同開発と研究費の増加により,2022年10月にAssertioと合意した対外許可協定による2023年の独自製品販売不足によって相殺された。
2022年同期と比較して、2023年12月31日までの1年間で、製造と供給収入は20%増加した7,427ドルだった。この増加は主にSuboxoneの収入が4382ドル増加したためであり,主に価格上昇に関係しており,Zuplenzの収入は2141ドル増加し,Sympazanの収入は2022年10月にUsertioとライセンス合意して587ドル増加した。
2022年同期と比較して、2023年12月31日までの1年間で、許可と特許使用料収入は129%増の3025ドルとなった。この増加は主にZevraがAzstarysに1500ドルのマイルストーン許可収入をもたらし、Sympazanに576ドルの許可収入と680ドルの特許使用料収入を増加させ、Azstarysの特許使用料収入253ドルを増加させたためである
2022年同期と比較して、2023年12月31日までの1年間で、共同開発と研究費は8%増の109ドルとなった。この増加は研究·開発実績義務を実現する時間によって推進され,これらの義務は異なる報告期間の間で変動することが予想される。
2022年同期と比較して、2023年12月31日までの1年間で、専有品純売上高(Sympazanの売上高のみを含む)は7658ドル減少した。減少の原因は,2022年10月にAssertioと対外許可協定が締結されたためである。2022年第4四半期からSympazanの販売を製造と供給収入およびライセンスと特許権使用料収入で確認します。
費用:
次の表に示した期間の費用データを示します
| | | | | | | | | | | | | | | | | | | | | | | | | | |
| | | | | | | 変わる |
| | | 2023 | | 2022 | | $ | | % |
| (単位は千ですが、%は含まれていません) | | | | | | | | |
| 製造と供給 | | $ | 20,831 | | | $ | 19,386 | | | $ | 1,445 | | | 7 | % |
| 研究開発 | | 13,104 | | | 17,481 | | | (4,377) | | | (25 | %) |
| 販売、一般、行政 | | 31,750 | | | 52,879 | | | (21,129) | | | (40 | %) |
| 利子支出 | | 6,337 | | | 6,552 | | | (215) | | | (3 | %) |
使用料義務に関する利子支出 | | 905 | | | — | | | 905 | | | 適用されない |
| 将来の収入の売却に関する利子支出 | | 220 | | | 5,891 | | | (5,671) | | | (96 | %) |
| 利息収入その他の収入,純額 | | (16,321) | | | (99) | | | (16,222) | | | 適用されない |
| 債務返済損失 | | 1,382 | | | — | | | 1,382 | | | 適用されない |
2023年12月31日までの年度の製造および供給コストおよび支出は、2022年同期より7%または1,445ドル増加します。*製造および供給コストの上昇は、原材料、生産および製品の組み合わせ変化に関するコスト上昇によるものです。
2022年同期と比較して、2023年12月31日までの1年間、研究開発費は25%減の4377ドルとなった。次の表は、私たちが参加する各主要臨床開発プロジェクトの各段階の主要な研究と開発費用に含まれる主要なコストとプロジェクトコストの内訳を提供します
| | | | | | | | | | | | | | | | | | | | | | | | | | |
| | | 十二月三十一日までの年度 | | 変わる |
| (単位:千) | | 2023 | | 2022 | | $ | | % |
| 臨床試験 | | $ | 3,597 | | | $ | 3,521 | | | $ | 76 | | | 2 | % |
| 開発と製造 | | 664 | | | 2,831 | | | (2,167) | | | (77 | %) |
| 製品研究費 | | 678 | | | 1,354 | | | (676) | | | (50 | %) |
| プロジェクト総コスト | | 4,939 | | | 7,706 | | | (2,767) | | | (36 | %) |
| 臨床前 | | 659 | | | 1,045 | | | (386) | | | (37 | %) |
| 研究開発者コスト | | 5,775 | | | 6,268 | | | (493) | | | (8 | %) |
| 問い合わせと外部サービス | | 323 | | | 595 | | | (272) | | | (46 | %) |
| シェアに基づく報酬 | | 456 | | | 672 | | | (216) | | | (32 | %) |
| 減価償却·償却 | | 91 | | | 173 | | | (82) | | | (47 | %) |
| 他のすべての研究開発は | | 861 | | | 1,022 | | | (161) | | | (16 | %) |
| 合計する | | $ | 13,104 | | | $ | 17,481 | | | $ | (4,377) | | | (25 | %) |
| | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | |
| 十二月三十一日までの年度 |
| 2023 | | 2022 | | 2023 | | 2022 | | | 2023 | | 2022 | | 2023 | | 2022 | |
| 合計する | % Inc./ 12月 | 過敏症 | % Inc./ 12月 | | AQST-108 | % Inc./ 12月 | 解放者 | % Inc./ 12月 |
| 臨床試験 | $ | 3,597 | | | $ | 3,521 | | 2 | % | $ | 4,687 | | | $ | 3,494 | | 34 | % | | $ | — | | | $ | — | | — | % | $ | (1,090) | | | $ | 27 | | 適用されない |
| 開発と製造 | 664 | | | 2,831 | | (77 | %) | 676 | | | 2,466 | | (73 | %) | | — | | | 65 | | 適用されない | (12) | | | 300 | | 適用されない |
| 製品研究費 | 678 | | | 1,354 | | (50 | %) | 463 | | | 921 | | (50 | %) | | — | | | 211 | | 適用されない | 215 | | | 222 | | (3 | %) |
| プロジェクト総コスト | $ | 4,939 | | | $ | 7,706 | | (36 | %) | $ | 5,826 | | | $ | 6,881 | | (15 | %) | | $ | — | | | $ | 276 | | 適用されない | $ | (887) | | | $ | 549 | | 適用されない |
研究や開発費用は,臨床試験のスケジュールやAqutiveパイプラインに関する他の製品開発活動によって大きく推進されている。アレルギー会社では,試験的臨床研究活動により臨床試験費用が34%,すなわち1193ドル増加したが,開発·製造費は73%にあたる1790ドル減少した年内の生産規模拡大活動に関連する2022 PKモデリングに関連する製品研究のために50%または458ドル。AQST-108では、会社が重点を移しているので、費用は合計276ドル減少しました過敏症私たちの主な候補製品として
pIPLINE。Libervantにとって、臨床試験、開発と製造における支出はそれぞれ1090ドルと12ドルであり、それぞれ研究完了後の監査を完了した第三者請負業者とモデリング作業の完了により3%または7ドル減少した製品研究から来ている。2022年同期と比較して,2023年12月31日までの1年間で,評価候補製品活動に関する臨床前費用は37%,すなわち386ドル低下した。継続的な費用管理により、2023年12月31日までの1年間、研究開発者コストは2022年同期に比べて8%、すなわち493ドル低下した。2022年同期と比較して、2023年12月31日までの年間、すべての他の研究開発費用は、レンタル料、光熱費、メンテナンス、その他の費用と費用を含めて、16%または161ドル低下した。
2022年同期と比較して、2023年12月31日までの1年間、販売、一般、行政費用は40%低下した21,129ドルとなった。この低下は、主に私たちのビジネス組織が2022年10月にSympazanが許可を得た後に8,028ドル減少したためであり、主に私たちの元最高経営責任者が退職して2,530ドルの解散費がなく、株式報酬支出が1,439ドル減少し、保険コストが888ドル減少し、外部サービスが6,100ドル減少したためである
2022年同期と比較して、2023年12月31日までの年間の利息支出は3%減の215ドルとなった。債務減少は、2023年の最初の10カ月の債務帳簿純価値が2022年に比べて低いためであり、12.5%の債券元金支払いが割引償却および13.5%債券の利息部分相殺されたためである。
2023年12月31日までの年度の特許権使用料義務割引償却に関する利息支出は905ドルであるこの額は,13.5%債券発行における特許権使用料義務に関する会計処理によるものである。特許権使用料義務に関する費用はございません2022年同期。
2023年12月31日までの年度、将来の収入の売却に関する利息支出は220ドルこの額は、2020年11月3日にマラソンに売却されたKYNMOBI特許使用料に関する将来の収入の会計処理によるものであり、取引期間中の任意の通貨義務または現金産出を代表または示唆していないからである2023年6月、SunovionはKYNMOBIを米国およびカナダ市場から自発的に撤退させることを発表したため、私たちは貨幣化協定下での追加または支払いを受けない可能性が高い。そのため、2022年第4四半期に将来の収入販売に関する利息支出を記録することを停止し、2023年の将来の収入販売に関する利息支出を2022年比で5,671ドル減少させた参照してください付記16、未来のRevenの販売UE.UE詳細については、我々の総合財務諸表を参照されたい。
利息収入やその他の収入は、2022年同期と比較して、2023年12月31日までの1年間で純16,222ドル増加した。この増加は、主に個人商業開発協定修正案11に関する6,000ドルの他の収入、BDSIと達成された8,500ドルの特許訴訟和解、および2023年に確認された1,250ドルのERTC返金を反映している。
2023年12月31日までに、2023年第1四半期に12.5%債券元金を支払うことによる早期返済罰金と、2023年第4四半期の12.5%債券関連費用の償還による債務弁済損失1,382ドルを確認しました。2022年には債務返済に損失はない。
流動性と資本資源
流動資金源
2023年12月31日まで、私たちは23,872ドルの現金と現金同等物を持っています。私たちは私たちの業務目標を実行し、長期的な利益を達成することができる保証はありませんが、Aqutiveな持続的な業務、既存の現金と等価物、研究開発活動の停止を含むが、これらに限定されない費用管理活動は、そのATM施設とリンカーン公園による購入協定を含む株式資本市場に参入する機会を含めて、少なくとも今後12ヶ月の運営需要を満たすために短期的な流動性を提供してくれます。なぜなら、その業務戦略を実行し続けるからです。
私たちが行っている業務、既存の現金と等価物、費用管理活動、および当社のATM施設とリンカーン公園による購入協定によって、短期資金源を提供することを含む株式資本市場に参入する機会を含む。2023年11月1日、元金総額45,000ドルの債券を発行し、元金は13.5%で、2028年11月1日に満期になります。次発行で得られた純額の一部はすべての未償還12.5%債券の償還および次発行に関する支出の支払いに用いられ、残りは一般会社用途として使用される。
2021年10月7日には,12.5%の債券に補充契約を締結し,これにより12.5%債券の償却スケジュールを改訂し,第1回元本支払日を2023年3月30日に延長することとした。第四期補充契約は、債券の満期日又は債券項における支払利息責任を変更することはない。この補充契約について、12.5%債券の所持者と同意料書簡を締結し、この書簡によると、12.5%債券の所持者に合計2700ドルの追加現金支払いを支払い、2022年5月15日から4四半期に分けて支払うことに同意した。これらのお金は2023年12月31日までに支払われる。
2019年、私たちはATM施設を設立し、現在、ATM施設に基づいて35,000ドルまでの普通株の提供と販売を登録する募集説明書補足資料があります。2023年12月31日までの年間販売しました
4,958,341株は,手数料や他の取引コスト502ドルを差し引いた純収益は約8,962ドルであった。このATM施設は2023年12月31日までに約23,952ドルで利用可能である。2022年12月31日までの年間で、ATM機メカニズムで2,860,538株の株を売却し、手数料や他の取引コスト289ドルを差し引いた純収益は約3,907ドルだった。
2022年4月12日、私たちは“リンカーン公園購入協定”の条項と条件と制限に基づいて、リンカーン公園購入契約の36ヶ月以内に40,000ドルの普通株を時々リンカーン公園に売る権利がありますが、リンカーン公園購入契約の36ヶ月以内にリンカーン公園に時々売る権利があります“リンカーン公園購入協定”を締結しました。リンカーン公園の購入協定には所有権制限が含まれています。もしこれがリンカーン公園が私たちが発行した普通株に対する実益所有権が9.99%を超え、2023年12月31日の6,486,623株に相当すれば、私たちは普通株を発行しません。リンカーン公園も普通株を購入しません。リンカーン公園はすでにリンカーン公園の購入契約に基づいて、いかなる方法でも直接あるいは間接的に空売りしたり、私たちの普通株をヘッジしたりしません。2023年12月31日までの年間で、リンカーン公園購入契約に関連する株は販売されていません。2022年12月31日までの年間で,236,491株の約束株を発行したほか,1,600,000株を売却し,リンカーンパーク購入協定に関連した約1,987ドルの収益を提供した
2022年6月6日、私たちは一部の購入者と証券購入協定を締結した。証券購入協定は、吾等の売却及び発行の合計:(I)4,850,000株普通株、(Ii)最大4,000,000株普通株を購入する予備融資権証、及び(Iii)最大8,850,000株普通株を購入する一般株式承認証を規定する。配給代行費とAqutiveが支払うべき発売費用を差し引いたところ,約7,796,000ドルの純収益を得た。今回発行された純収益を一般企業用途に適用した。予備資金権証は2022年に全面的に行使される。2023年6月14日,証券購入協議により発行された購入3,689,452株の普通株の引受権証が行使され,そのために約3,542ドルの収益がAqutiveに支払われた。
2023年8月1日、吾らは証券購入契約項の下の1人の買い手(“行権所有者”)と書簡合意を締結し、5,000,000株の残り普通株式承認証を売却した。通信契約に基づいて、行権所有者とAqutiveの同意により、行権所有者は普通株式1株当たり0.96ドル、即ち証券購入プロトコルの下で普通株承認株式証の使用価格で、普通株式承認株式証に関連するすべての普通株式承認証を行使する。通信契約によると、行権所有者が既存の株式承認証5,000,000株を行使する代償として、Aqutiveは行権所有者に新株式承認証を発行し、合計2,750,000株の普通株を購入する。新株式証明書は2024年2月2日以降に行使でき、2029年2月2日に満期となり、現金形式でしか発行できないが、新株式証の普通株式が通信契約の条項に基づいて登録されていなければ、新株式証もすべて或いは部分的に“現金なし行使”の方式で行使することができる。新権証の発行価格は1株当たり2.60ドルです。2023年8月2日,行権者と締結された証券購入契約により,既存の株式承認証に関する5,000,000株の普通株が行使され,AQUALが得た総収益は4,800ドルであった。その会社のこの取引に関連した費用は35ドルだ。
証券購入契約に基づいて計8,689,452件の普通株式承認株式証を発行し、2023年12月31日までの年度内にこのなどの普通株式承認証を行使したため、収益約8,342ドルを受け取った。その会社のこの取引に関連した費用は35ドルだ。
2023年11月1日に元金総額45,000ドルの13.5%債券を発行し、2028年11月1日に満期になります。次発行で得られた純額の一部はすべての未償還12.5%債券の償還および次発行に関する支出の支払いに用いられ、残りは一般会社用途として使用される。債権率は13.5厘、年利13.5厘、四半期ごとの配当は、それぞれ毎年3月30日、6月30日、9月30日および12月30日の配当(配当日あたり“支払日”)は、2023年12月30日から発効する。13.5%の債券は、2026年6月30日までに利息のみを受け取り、13.5%の債券の元金分割払いと、前金、支払い、加速、買い戻し、または償還(場合によっては)適用日に決定された部分脱退費用を固定償却スケジュールに基づいて支払います。
キャッシュフロー
次の表は,2023年12月31日,2023年12月31日,2022年12月31日までの年度のキャッシュフロー情報を提供している
| | | | | | | | | | | | | | |
| (単位:千) | | 2023 | | 2022 |
| 経営活動のための現金純額 | | $ | (6,380) | | | $ | (9,819) | |
| 投資活動のための現金純額 | | (995) | | | (2,524) | |
| 融資活動が提供する現金純額 | | 3,974 | | | 11,592 | |
現金と現金等価物の純減少 | | $ | (3,401) | | | $ | (751) | |
| | | | |
経営活動のための現金純額
2022年同期と比較して、2023年12月31日までの年間経営活動用現金純額は3439ドル減少した。減少の主な原因は、純損失が46,540ドル減少し、2023年に許可証と供給協定から受け取った支払いの減少および経営資産と負債の変化によって相殺され、主に売掛金と他の売掛金であり、主にInDior活動およびSympazanのAssertioへの許可による変化である。その他の変化は,将来の売却収入に関する利息支出の減少,株式による補償と減価償却および償却·減価支出の減少により,2022年に発生しなかった2023年の債務返済の一次損失および債務発行コストと割引の償却増加によって相殺された。
投資活動のための現金純額
2022年同期と比較して、2023年12月31日までの年間投資活動用現金純額は1,529ドル減少した。減少の原因は2023年に無形資産に投資されなかったからだ。
融資活動が提供する現金純額
2023年12月31日までの年度、融資活動が提供した現金純額は2022年同期に比べて7618ドル減少した。通貨ベースの減少は,主に12.5%債券の償還51,500ドルと,13.5%債券に関する4,643ドル発行割引と融資コストにより,2023年に13.5%債券を発行した45,000ドルを相殺した。また、2022年と比較して、2023年のATMメカニズムでの普通株購入収益は増加し、私募株式発行下の普通株と引受権証収益の純減少を部分的に相殺した。注1を参照会社概況と持分取引そして付記14長期債務詳細については、我々の総合財務諸表を参照されたい。
資金需要
私たちが行っている業務、既存の現金と等価物、費用管理活動、および当社のATM施設を介してリンカーン公園による購入協定を含む、株式資本市場に参入する機会は、Aqutiveに短期融資機会を提供する可能性があり、“流動性と資本資源”を参照することができる。2023年11月1日に元金総額45,000ドルの13.5%債券を発行し、2028年11月1日に満期になります。次発行で得られた純額の一部はすべての未償還12.5%債券の償還および次発行に関する支出の支払いに用いられ、残りは一般会社用途として使用される。私たちはその臨床プロジェクトを推進し続けるために追加的な資金を集めなければならない。私たちはこれらの資金源のいずれかが、単独でも組み合わせでも、合理的な条項で提供されるか、または私たちの業務目標に資金を提供するのに十分であることを保証することはできない。しかも、私たちは期待よりも早く利用可能な財政資源を利用することを要求されるかもしれない。我々の予想に基づく仮定は変化する可能性があり、あるいは不正確であることが証明される可能性があり、その原因は、資本市場、資産貨幣化市場、規制承認手続きなどの不関連要素、アレルギー薬の承認、FDAの米国市場参入に対するLibervantの全面的な承認、および監督とその他の要素を含む。我々の計画における持続的な運営と予想成長に固有の重要な要素および仮定は、以下の関連要因および仮定を含むが、これらに限定されない
•私たちの顧客は、模造薬と現在予想されている他の競争圧力の影響を含む、製品の現在の契約と将来の予想される注文にタイムリーに支払うことができます
•私たちの顧客は、提供された共同開発および実行可能性サービスの現在の契約および将来の予想される注文にタイムリーに費用を支払い、Exservanのような最近許可された製品に規制支援サービスを提供する能力があり続ける
•現金自動支払機施設とリンカーン公園の購入契約を通じて資金を得る能力を含め、債務や株式市場に入ることができる将来の必要な資金が必要であれば、
•私たちが予想していた収入と資金と一致するように、私たちのコスト構造を検討し、適切に調整し続ける
•Sympazanの持続的な成長と市場浸透率は、予想される患者および医師の受容度、および私たちの許可者が政府機関および他の個人医療保険会社から十分な価格および支払い支援を受ける能力を含む
•FDAが米国市場への進出を許可した場合、私たちの候補製品Libervantは、予想されるコストレベルと予想される生産開始時間の枠組み内で効率的な商業化を達成するだろう
•インフラと行政費用が予想レベルに達し、食品·薬物管理局として、厳格に規制されている上場企業の運営を支援する
•私たちの知的財産権を保護するための持続的な努力の費用制御可能なレベルは、第三者の“リスクのある”模倣薬の発売に関する私たちの権利の強制執行を求めることに関する訴訟費用と、私たちが参加している他の訴訟事項を含む
•私たちが要求する債務返済義務を履行する能力を含む13.5%の債券の下のすべての条約を遵守し続ける
•重大な意外な現金需要はありません
•新冠肺炎疫病は著者らの運営、著者らの主要なサプライヤーと第三者臨床及びその他のサービス提供者、私たちの同僚と請負業者及び債務持分とその他の資本市場に与える影響。
Suboxone収入予想の一般的な低下、および将来の株式融資、将来の資本市場への将来の参入機会、または他の潜在的に利用可能な流動資金源、およびコロナウイルスの大流行に関連する不確実性を含む、他の外部資源または当社の業務に影響を与える要因を適切に反映するために、業務コストを管理し続ける予定である。そのためには,我々が行っているアレルギーやAQST−108を支援する製品開発活動に投資し続けることを含め,我々の株主に価値を創出するコア駆動要因に集中していく予定である。利益を達成する前に、本当に利益を達成する場合、追加の資本および/または他の融資または資金が必要となり、これは、Libervant、アレルギー、およびAQST-108の開発および商業化をさらに推進するために実質的である可能性があり、FDAが米国市場への進出を許可し、債務返済、特に私たちの13.5%の手形を含む他の現金需要を満たす場合。FDAによるLibervantの予備承認に基づき,我々はLibervantに関連する上場前支出の時間とレベルを保守的に管理する予定である。この点で、Sympazanに対する私たちの許可を考慮すると、2022年に比べて2023年に商業化コストを大幅に削減しました。それにもかかわらず,予測可能な未来には損失と負のキャッシュフローが予想されるため,外部融資と資金に依存して運営計画を実現する予定である。
私たちの短期的かつ長期的な流動資金の充足性は、私たちの運営収入レベルと私たちの収入運営計画を実現する能力、候補製品計画のための私たちの期間の規制承認、および私たちが計画された時間範囲内で他の特許権使用料フローや他の許可権利を貨幣化する能力に直接影響され、いかなる貨幣化取引で成功するか保証できません。私たちの営業収入は過去ずっと変動しており、未来も変動することが予想される。予測可能な未来には重大な運営損失と負の運営キャッシュフローが予想され、大量の持続的な利息を支払う必要があり、元金返済は2026年6月から債務満期日までの13.5%の手形と関係があり、付記14でさらに議論される長期債務私たちの連結財務諸表まで。私たちの現在と過去の収入の大部分はInDior顧客との許可、製造、販売に依存しており、この状況は継続され、予想されるキャッシュフローレベルを実現するには、私たちの運営と現金需要のための資金提供を助けるために、計画よりもはるかに長い時間が必要かもしれない。
もし私たちが株式証券を発行することで追加資金を調達すれば、私たちの株主はさらに希釈に直面し、これらの証券の条項は清算または他の特典(契約が許可された範囲内であれば)を含む可能性があり、これは私たちの株主権利に悪影響を及ぼすだろう。私たちが追加株式融資を獲得する能力は、私たちの経営業績と将来性、私たちの独自製品規制承認過程における積極的または消極的な発展、Libervantアメリカ市場参入に対するFDAの適時な監督管理承認を含む多くの要素の重大な影響を受ける可能性があり、競争相手のFDAが承認した鼻スプレー剤の孤児薬物市場独占経営権が2027年1月に満了する前にこのような承認を得ること、私たちの既存の債務レベル(私たちのほとんどの資産を保証する)、Indentureの制限、および一般金融市場状況を保証することはできない。さらに、私たちは私たちが資金調達に成功することを保証することもできませんし、そのような必要な融資が割引または許容可能な条項または時間または必要な金額(あれば)で利用できるという保証もありません
短期的または長期的な流動資金需要を満たすのに十分な資金がなければ、必要な場合の現金需要がなければ、リストラ、大幅な遅延などの費用管理活動を要求される
私たちの現在または計画の一部または全部の研究開発計画および臨床および他の製品開発活動を削減し、さらに停止し、そうでなければ、私たちの他の支出を大幅に削減し、私たちの運営計画を調整し、私たちの流動性を改善するための他の措置を求める必要がある。私たちはまた、私たちの独自製品候補計画の追加的な許可および金銭化の機会(ある場合)を評価することを要求される可能性があり、現在、私たちは、これらの行動のいずれも合理的な条項で利用可能または利用可能であることを保証できないにもかかわらず、これらの機会を自己商業化するか、または他の潜在的な流動性機会または他の代替案またはオプションまたは戦略代替案を探索することを計画している。
また、第一部分の第二項は、全世界のコロナウイルス大流行の影響に関連する業務、業務、財務結果と資本資源方面の重大なリスクと不確定要素に関連している。
契約義務と約束
私たちは様々な契約協定を締結しており、このような合意に基づいて、私たちは長期的な義務を持っている。私たちの約束に関するより多くの情報は、第2部第8項を参照されたい。財務諸表と補足データ、付記22、意外な状況です。
私たちの将来のレンタル支払いに関するより多くの情報は、第二部分、第八項を参照してください。財務諸表と補足データ、付記10、使用権資産と賃貸義務私たちの最低レンタル支払いスケジュールについて。私たちが予想しているレンタル時間は今後数年で異なるかもしれません。これは私たちがレンタル期間を延長することと/あるいは前の数年にレンタル契約を締結することを決定することに依存します。
13.5%債券に関するより多くの情報については、第2部第8項を参照。財務諸表と補足データ、付記14、長期債務.
重要な会計政策と試算の使用
私たちの経営陣は、アメリカ公認会計原則またはGAAPに基づいて作成された当社の総合財務諸表に基づいて財務状況と経営結果の検討と分析を行っています。総合財務諸表の作成は、財務諸表の日付報告に影響を与える資産と負債、報告期間内の収入と費用の推定と判断を要求しています。持続的な基礎の上で、私たちは私たちの推定と判断を評価する。我々は歴史的経験(あり)や当時の状況では合理的であると考えられる他の様々な仮定から推定しているが,これらの仮定の結果は資産や負債の帳簿価値を判断する基礎となっており,そのような資産や負債の帳簿価値は他のソースから容易に見られるわけではない.異なる仮定または条件では、実際の結果は、これらの推定値とは異なる可能性がある。
重要な会計政策は付記3でより全面的に説明されているが、重要会計政策の概要本文書に含まれる総合財務諸表付記では,以下の会計政策が総合財務諸表作成に用いる重大な判断と見積もりが最も重要であると考えられる。
収入確認
独自製品販売、純-この純収入は製品出荷と所有権が顧客に移転する際に確認され、通常交付時に確認される。販売時には,各種収入免税額の推定数は歴史的傾向と判断に基づいて推定記録されている.以前に販売されたSympazan製品については、返品手当および即時支払い割引は、契約条項および履歴収益率(ある場合)に基づいて推定され、これらの推定値は、売掛金の減少として記録される。卸サービス料、共同支払支援償還、医療保険、医療補助及びその他のリベートに関する類似した決定された推定数が記録され、これらの推定数は計算すべき負債の構成要素として反映される。すべての関連変数の考慮要因を解決し,受取金額に関する不確実性を解消すると,見積り数は実際の手当額に調整される.このような推定金額の準備金は四半期ごとに検討され調整されたもの以上だ。
ライセンスと印税収入−ライセンス収入は、ライセンスが基本ライセンススケジュールに含まれる可能性のある任意の他の履行義務とは異なるかどうかの評価に基づいて決定される。クライアントがライセンスから利益を得ることができ、他の履行義務を提供する必要がない場合、したがって、ライセンスがユニークまたは機能的ライセンスとみなされる場合、Aqutiveは、クライアントがライセンスを使用する権利またはライセンスにアクセスする権利を取得したかどうかを判断する。Aqutiveのさらなる開発や他の継続的な活動を必要としない機能ライセンスについては,クライアントは譲渡時および譲渡時に使用許可証を取得する権利とみなされ,収入は通常ある時点に記録され,制限されている.Aqutiveが提供する他の履行義務と共に実質的な価値を提供する象徴的な許可については、収入は通常、許可プロトコルの期限内に記録される。Aqutiveに提供されるこのような他の義務は、一般に、ライセンス期間内に提供される製品、他の開発サービス、または他の交付可能な契約を契約することを含む。支払い
受取または他の方法で稼いだ金額を超える収入は、ライセンス期間内に延期および確認されるか、またはあるか、または他の履行義務として履行されるであろう。
マイルストーン支払いによる収入確認はマイルストーン支払いをめぐる事実と状況にかかっている。非販売指標に基づくマイルストーン支払い、例えば開発のマイルストーンに基づく(例えば:機密協定の届出または監督管理の承認を得る)は、可変対価を表し、任意の制限の場合に取引価格を計上する。記念碑的な支払いが将来の発展に関係すれば、承認のタイミングは歴史的経験と第三者の結果に対する重要性にかかっている。販売敷居に達したときに受け取ったマイルストーン支払いについては、マイルストーン支払いの収入が実際の販売または販売に関する履行義務が履行されたときに確認される。
特許使用料義務と利息支出
13.5%の手形の発行について,吾らは手形所持者と印税権利協定を締結し,手形所持者にアレルギー性(アドレナリン)語下映画の年間世界純売上高1.0%から2.0%に相当する分級特許権使用料を付与し,8年間,アレルギーが世界初販売から計算した。手形保有者は,Libervant(安定)口腔フィルムの世界年間純売上高の1.0%から2.0%の分級印税を得る権利があり,(1)アレルギー薬の初販売と,(2)Libervantの初販売から8年までである。特許使用料協定は債務に分類され、45,000ドルの13.5%の手形の価値は、債務と特許権使用料義務の相対的に公平な市場価値に基づいて割り当てられている。将来推定される特許使用料の支払いの56,926ドルは、割り当てられた13,856ドルの公正価値を超え、特許権使用料協定に関連する割引として確認され、特許権使用料協定の有効期間内に償却される。このような償却は、総合経営報告書と全面赤字に特許権使用料義務に関する利息支出に反映されている。13.5%の債券が付記14で議論され、長期債務私たちの連結財務諸表まで
将来の収入の売却に関する負債と利息支出
KYNMOBIの売却に関連する将来の収入をASC 470債務による債務融資と見なし、実金利法で関連期待特許権使用費フローの推定寿命内に償却する。将来の収入の売却に関する負債は最初に繰延コストを差し引いた収益に入金される。将来の収入や利息支出に関連する負債の売却は、将来の特許権使用料の現在の推定に基づいており、手配された有効期限内に支払われる予定です。私たちは内部予測と外部資源の予測に合わせて、予想される特許権使用料支払いを定期的に評価する。私のような将来の特許権使用料支払いの推定値は、以前の推定値よりも大きいか、またはそれよりも少ないか、またはその支払い時間は、その以前の推定値とは大きな差があり、吾らは、関連する利息支出を前向きに調整するであろう。債務償却は、総合経営と全面赤字報告書に、将来の売却収入に関する利息支出に反映されている。将来の収入の売却についてのさらなる議論は、付記16を参照されたい将来の収入を売る.
最近の会計公告
第二部第八項。財務諸表と補足データ、付記3、重要会計政策の概要私たちの連結財務諸表付記では、最近の会計声明が議論されている。
第7 A項には、市場リスクに関する定量的かつ定性的な開示が含まれる
7 A項は私たちが小さな報告会社として適用されず、省略されている。
項目8.連結財務諸表と補足データ
私たちの財務諸表は、私たちの独立公認会計士事務所の報告とともに、F-1ページから、表格10-Kの形で本年度報告に登場します。
第九項会計と財務情報開示の変更と相違
ない。
項目9 Aは、制御措置およびプログラムを含む。
経営陣の私たちの開示制御と手続きの評価
我々は、取引所法案に基づいて提出または提出された報告書に開示すべき情報を確保するために開示制御を維持し、(1)米国証券取引委員会規則および表に指定された期間内に記録、処理、まとめ、報告すること、(2)私たちの最高経営者および最高財務官を含む私たちの経営陣に蓄積して伝達し、タイムリーに必要な開示について決定することを目的とする。
2023年12月31日現在、我々の経営陣は、我々の最高経営責任者およびCEOの参加の下で、我々の開示制御および手順(“取引法”規則13 a-15(E)および15 d-15(E)で定義されている)の有効性を評価した。我々の経営陣は,どのような制御やプログラムも,どんなに設計や操作が良好であっても,その目標を実現するために合理的な保証を提供することしかできず,管理層は,可能な制御とプログラムのコスト-収益関係を評価する際にその判断を適用しなければならないことを認識している.我々の最高経営責任者及び最高財務責任者は、上記の評価に基づいて、2023年12月31日現在、我々の開示制御及び手続は合理的な保証レベルで有効であると結論した。
経営陣財務報告内部統制年次報告書
我々の経営陣は、取引法第13 a-15(F)及び15 d-15(F)条に規定する財務報告の適切な制御を確立·維持する責任がある。財務報告の内部統制は、財務報告の信頼性を合理的に保証することを目的としたプログラムであり、公認された会計原則に基づいて外部目的の財務諸表を作成する。私たちの財務報告に対する内部統制には、(I)Aqutive Treeutics,Inc.の資産取引および処置を合理的かつ詳細かつ正確に反映するために記録を保存することについて、(Ii)公認会計原則に基づいて財務諸表を作成するために必要な取引を記録するための合理的な保証を提供し、私たちの収入および支出は、私たちの経営陣および取締役の許可のみに基づいて行われる;(Iii)財務諸表に重大な影響を与える可能性のある不正な買収、使用または処分を防止またはタイムリーに発見することが合理的な保証を提供する。
固有の限界のため、財務報告書に対する内部統制は誤った陳述を防ぐことができない可能性がある。また,将来的に任意の有効性評価を行う予測は,条件の変化により制御不足のリスクが生じたり,政策やプログラムの遵守度が悪化したりする可能性がある.
我々の経営陣は、2023年12月31日までの財務報告内部統制の有効性を評価した。この評価を行う際に経営陣は内部統制--統合フレームワーク(2013))は、テレデビル委員会が主催する組織委員会(“COSO”)によって発表された。その評価とこれらの基準に基づき、我々の経営陣は、財務報告書の内部統制が2023年12月31日から有効であると結論した。
本年度報告には、財務報告の内部統制に関する我々の公認独立会計士事務所の証明報告は含まれていません。米国証券取引委員会によれば、本年度報告では経営陣報告のルールのみを提供することが可能であり、経営陣の報告は我々の公認独立会計士事務所による認証を必要としない。
財務報告の内部統制の変化
我々の財務報告の内部統制(“取引法”第13 a-15(F)および15 d-15(F)条参照)は、前四半期に発生したこのような内部統制評価と関連する財務報告の内部統制に重大な影響を及ぼす可能性のある変化は発生していない。
プロジェクト9 Bその他の情報.
開ける2023年12月7日, マーク·スコベル, 首席革新および科学技術官会社のメンバーは通過する1934年改正証券取引法第10 b 5-1条の取引に対する肯定的防御条件を満たすことを目的とした書面販売計画175,000株式です。この計画は2023年12月6日から始まり、2024年12月4日に満期になる。
プロジェクト9 Cです。検査を妨害する外国司法管轄区域を開示する。
ない
第三部
プロジェクト10.取締役会、役員、および企業管理
本プロジェクトに必要な情報は、米国証券取引委員会に提出された依頼書に含まれ、参照して本明細書に組み込まれる。
項目11.役員報酬の増加
本プロジェクトに必要な情報は、米国証券取引委員会に提出された依頼書に含まれ、参照して本明細書に組み込まれる。
プロジェクト12.特定の実益所有者および管理職の保証所有権および関連株主事項の決定
本プロジェクトに必要な情報は、米国証券取引委員会に提出された依頼書に含まれ、参照して本明細書に組み込まれる。
第13項:一定の関係と関係者の取引を構築し、取締役の独立性を実現
本プロジェクトに必要な情報は、米国証券取引委員会に提出された依頼書に含まれ、参照して本明細書に組み込まれる。
プロジェクト14.総会計士費用とサービス料
本プロジェクトに必要な情報は、米国証券取引委員会に提出された依頼書に含まれ、参照して本明細書に組み込まれる。
第4部
項目15.すべての展示品、財務諸表の添付表。
(A)(1)財務諸表。
15項の部分に対する回答は本文書第8項の下に掲載されている.
(A)(2)財務諸表付表。
それらが適用されない、必要ではない、または必要な資料が総合財務諸表または付記で提供されているので、すべての財務諸表の添付表は省略されている。
(A)(3)展示品。
S-K条例第601項及び本10-K年度報告書第15(B)項に要求される証拠物は、本10-K年度報告書署名ページに続く前の“証拠インデックス”に記載されている。展示品索引に記載されている展示品は、引用されて本明細書に組み込まれる。
項目16.表格10-Kの概要
適用されません。
展示品索引
以下の証拠物は本10-K表の一部としてアーカイブされているが,表32.1と表32.2を除いて提供されていると見なすべきである.
| | | | | | | | |
| 番号をつける | | 説明する |
3.1 | | 改訂および再発行されたAqutive Treateutics,Inc.の登録証明書は、2018年7月27日(当社が2018年7月27日に提出したForm 8-Kの現在の報告書の添付ファイル3.1として提出され、参照により本明細書に組み込まれる)である。 |
3.2 | | 改訂·再制定されたAqutive Treateutics,Inc.の定款(当社が2023年2月7日に提出したForm 8−Kの現在の報告書の添付ファイル3.2として提出し、引用により本明細書に組み込む)。 |
4.1 | | Aqutive Treateutics,Inc.普通株式証明書テーブル(会社S-1フォーム登録説明書添付ファイル4.1として提出され、2018年6月27日に提出され、文書番号333-225924、参照により本明細書に組み込まれる)。 |
4.2 | | 2019年7月15日,発行元であるAqutive Treateutics,Inc.の発行元としての契約と,受託者と担保代理である米国銀行全国協会(2019年7月16日に提出された現在の報告である8-Kフォームの添付ファイル4.1が提出され,参照により本明細書に組み込まれる). |
4.3 | | 最初の補足契約日は2020年11月3日であり,このうちAqutive Treeutics,Inc.は発行元として,任意の保証人がこの契約の当事者となり,米国銀行全国協会は受託者と担保代理人として(会社が2021年3月9日に提出したForm 10-K年度報告の添付ファイル4.3として提出し,参照により本明細書に組み込む). |
4.4 | | 第2の補足契約日は2020年11月20日であり、Aqutive Treeutics,Inc.は発行元として、任意の保証人がこの契約の当事者となり、米国銀行全国協会は受託者と担保代理人として(会社が2021年3月9日に提出したForm 10-K年度報告の添付ファイル4.4として提出し、参照により本明細書に組み込む)。 |
4.5 | | 第三補足契約日は2021年8月6日であり、このうちAqutive Treeutics,Inc.は発行元として、任意の保証人が当該契約の当事者となり、米国銀行全国協会は受託者と担保代理人として(当社が2021年8月9日に提出したForm 8−K表の添付ファイル4.1として提出し、参照により本明細書に組み込む)。 |
4.6 | | 日付は2021年10月7日の第4部補充契約であり、Aqutive Treeutics,Inc.は発行元として、任意の保証人がこの契約の当事者となり、米国銀行全国協会は受託者と担保代理人として(当社が2021年8月8日に提出したForm 8-K表の添付ファイル4.1として提出し、参照により本明細書に組み込む)。 |
4.7 | | 2019年株式証明書フォーム(会社現在報告8-Kフォームの添付ファイル4.2として提出され、2019年7月16日に提出され、引用によって本明細書に組み込まれます)。 |
4.8 | | 2020年表承認株式証(会社が2021年3月9日に提出した表格10-K年度報告書の添付ファイル4.6として提出し、引用により本明細書に組み込む)。 |
4.9 | | 2022年事前融資株式証表(当社が2022年6月8日に提出した8-K表の添付ファイル4.1として提出し、参照により本明細書に組み込む) |
4.10 | | 2022年普通株式承認証表(当社が2022年6月8日に提出した8-K表の現在の報告書の添付ファイル4.2として提出し、参照によって本明細書に組み込む) |
| | | | | | | | |
4.11 | | 登録権協定は、日付が2018年6月24日であり、Aqqutive Partners,LLC及びそのあるメンバー権益保持者の間で締結される(当社が2018年6月27日に提出したS−1表登録声明の添付ファイル4.3(文書番号333−225924として、参照により本明細書に組み込む))。 |
4.12 | | 取引法第12条に基づいて登録された証券説明(会社が2020年3月11日に提出したForm 10−K年次報告書の添付ファイル4.7として提出し、引用により本明細書に組み込む)。 |
4.13 | | 第5の補足契約は、期日は2022年5月13日であり、Aquutive Treateutics,Inc.が発行元として、任意の保証人を発行元とし、米国銀行信託会社(National Association)が受託者および担保代理として提出する(当社20222-Kレポートの添付ファイル4.1として提出され、参照により本明細書に組み込まれる)。 |
4.14 | | 2023年11月1日現在,発行元であるAqutive Treateutics,Inc.と受託者と担保代理である米国銀行信託会社(National Association)との契約(会社が2023年11月2日に提出した8-K表現在報告の添付ファイル4.1として提出し,引用により本明細書に組み込む) |
10.1 | | 賠償プロトコル表は,Aqqutive Treateutics,Inc.とその役員と上級管理者との間で提出される(2018年6月27日に提出された会社S-1表登録声明として添付ファイル10.1(文書番号333-225924,参照により本明細書に組み込む)). |
10.2 | | 2019年に12.5%プレミアム保証手形の発行に関連する購入契約フォーム(2019年7月16日に提出された8-Kフォームの現在の報告書の添付ファイル10.1として提出され、参照によって本明細書に組み込まれます)。 |
10.3 | | 2020年に12.5%優先保証手形の発行に関する2020年購入プロトコル表(当社が2021年3月9日に提出したForm 10-K年度報告添付ファイル10.3として提出し、引用により本明細書に組み込む)。 |
10.4 | | 12.5%高度担保手形の発行に関する担保協定は,2019年7月15日であり,発行元であるAqutive Treateutics,Inc.,その手形を随時付与する他の付与者,受託者である米国銀行全国協会,担保代理である米国銀行全国協会(当社が2019年7月16日に提出した8−K表の添付ファイル10.2として提出され,引用により本明細書に組み込まれる)。 |
10.5+ | | 役員採用協定は、期日は2022年7月15日であり、Aqutive Treateutics,Inc.とDaniel Barberによって締結されている(当社が2022年8月2日に提出した10-Q表の現在の報告書の添付ファイル10.1として提出し、参照により本明細書に組み込む)。 |
10.6+ | | 役員採用協定は、2018年7月9日にAqutive Treeutics,Inc.とA.Mark Schobelによって締結された(2018年7月16日に提出された会社S-1表登録声明(文書番号333-225924)発効前修正案第1号の10.8号添付ファイルとして引用により本明細書に組み込む)。 |
10.7† | | MonoSol Rx,LLC(現在Aqutive Treateutics,Inc.)が署名したビジネス開発プロトコル和利潔時製薬有限公司は、2008年8月15日(2009年8月19日、2009年11月13日、2010年3月30日、2010年10月13日、2010年12月15日、2011年12月9日、2012年12月1日、2013年10月14日(付録A)、2014年7月30日(付録B)、2017年1月12日に改訂)(当社が2018年6月27日に提出したS-1表登録説明書(第333-225924号文書)として添付ファイル10.9を提出し、引用により本明細書に組み込む)。 |
10.8† | | プロトコルは,MonoSol Rx,LLC(現在Aqqutive Treateutics,Inc.)によって構成される.及びイギリス株式会社は、2017年9月24日(2018年6月27日に提出し、当社S-1表登録説明書添付ファイル10.10(文書番号333-225924、参照で本明細書に組み込む))としている。 |
10.9† | | 2008年8月15日に施行された“商業開発協定”第11号改正案(同封アーカイブ)。 |
10.10† | | MonoSol Rx,LLC(現在Aqutive Treateutics,Inc.)はCLAのプロトコルを終了する.ケム医薬株式会社とは、日付は2012年3月20日(会社S-1表登録説明書添付ファイル10.11として提出され、2018年6月27日に提出され、書類は333-225924号であり、引用により本明細書に組み込まれている)。 |
10.11† | | ライセンスプロトコルは,MonoSol Rx,LLC(現在AQUEATIOTICS,Inc.)からなる.Cynapsus Treateutics Inc.とは、2016年4月1日である(会社S-1表登録説明書添付ファイル10.12として提出され、2018年6月27日に提出され、文書番号333-225924は、参照により本明細書に組み込まれる)。 |
10.12† | | Aqutive Treateutics,Inc.とSunovion PharmPharmticals,Inc.との間のライセンス契約第1修正案は,2020年3月16日(会社が2021年3月9日に提出したForm 10−K年次報告書の添付ファイル10.14として提出され,参照により本明細書に組み込まれる)。 |
10.13† | | Aqutive Treateutics,Inc.とSunovion PharmPharmticals,Inc.との間のライセンス合意第2修正案は,2020年10月23日(会社が2021年3月9日に提出したForm 10−K年次報告書の添付ファイル10.15として提出され,参照により本明細書に組み込まれる)。 |
| | | | | | | | |
10.14 | | 産業リース協定は,Ashland Northwest Partners,L.P.とMonoSol Rx,LLC(現Aqutive Treateutics,Inc.)によって締結され,2006年10月24日(2011年10月24日と2018年2月8日に改訂された)(会社が2018年6月27日に提出したS-1表登録声明の添付ファイル10.13(文書番号333-225924,参照により本明細書に組み込まれる)である。 |
10.15+ | | Aqqutive Treeutics,Inc.2018年株式インセンティブ計画(2018年7月16日に提出された発効前修正案第1号添付ファイル10.14として、会社S-1表登録説明書(文書番号333-225924)に提出され、参照により本明細書に組み込まれる)。 |
10.16+ | | 改訂されたAqutive Treateutics,Inc.従業員株式購入計画(会社が2021年3月9日に提出したForm 10-K年次報告書の添付ファイル10.18として提出され、参照によって本明細書に組み込まれる)。 |
10.17+ | | 株式オプション契約表(2018年6月27日に提出され、会社S-1表登録説明書添付ファイル10.16(第333-225924号文書、引用により本明細書に編入)) |
10.18+ | | 株式会社2018年株式インセンティブ計画下の株式オプション協定表(2018年7月16日提出の発効前修正案第1号添付ファイル10.17として、会社S-1表登録説明書(書類第333-225924号)に提出され、引用により本明細書に組み込まれる)。 |
10.19+ | | Aqutive Treeutics,Inc.2018年株式インセンティブ計画下の限定株式単位プロトコル表(2018年7月16日提出の発効前修正案第1号添付ファイル10.18として会社S-1表登録説明書(書類第333-225924号)に提出され、参照により本明細書に組み込まれる)。 |
10.20+ | | 役員採用協定は,2018年9月10日にAqutive Treeutics,Inc.とLori J.Braenderによって締結された(会社が2018年11月6日に提出したForm 10-Q四半期報告の添付ファイル10.4として提出し,引用により本明細書に組み込む). |
10.21 | | 購入および販売協定は、2020年11月3日に、Aqutive Treeutics,Inc.およびMAM Pangolin Royalty,LLCによって締結される(会社が2021年3月9日に提出したForm 10-K年度報告の添付ファイル10.23として提出され、参照によって本明細書に組み込まれる)。 |
10.22 | | 購入協定の第1号修正案は,期日は2021年8月6日であり,Aqutive Treeutics,Inc.と購入者によって署名されている(会社が2021年3月31日に提出したForm 10−K年度報告の添付ファイルとして10.22提出し,引用により本明細書に組み込む)。 |
10.23 | | 購入協定の第2号修正案は、日付が2022年5月13日であり、Aqutive Treeutics,Inc.と購入者によって署名される(2022年5月17日に提出された会社現在報告8-K表の添付ファイル10.1として提出され、参照により本明細書に組み込まれる) |
10.24 | | 2021年10月7日、Aqqutive Treeutics,Inc.およびそのチケット保持者間の同意費書簡(2021年10月8日に提出された現在の8-Kフォーム報告書の添付ファイル10.1として提出され、参照によって本明細書に組み込まれる)。 |
10.25+ | | 幹部雇用協定に対する第1修正案は,2021年6月30日にAqutive Treeutics,Inc.とAlexander Mark Schobel(会社が2022年3月8日に提出したForm 10−K年次報告の10.25号文書として提出され,引用により本明細書に組み込まれる)である |
10.26+ | | “役員雇用協定第1修正案”は、2021年6月30日にAqutive Treeutics,Inc.とKeith J.Kendallによって署名された(会社が2022年3月8日に提出したForm 10-K年度報告書の添付ファイル10.26として提出され、参照によって本明細書に組み込まれる) |
10.27† | | 許可および供給協定は、2022年9月26日に、Aquutive Treateutics,Inc.およびAtnahs Pharma UK Limitedによって締結される(会社が2022年11月1日に提出したForm 10-Q四半期報告の添付ファイル10.1として提出され、参照によって本明細書に組み込まれる) |
10.28† | | ライセンス、開発および供給協定は、2022年3月にAqutive Treeutics,Inc.とHaisco製薬グループ株式会社によって署名された(会社が2022年5月4日に提出したForm 10-Q四半期報告書の添付ファイル10.1として提出され、参照によって本明細書に組み込まれる) |
10.29† | | Aqutive Treateutics,Inc.とOtter PharmPharmticals,LLCの間のライセンス契約は,2022年10月26日(ここで提出)である(会社が2023年3月31日に提出したForm 10−K年次報告書の添付ファイル10.29として提出され,参照によって本明細書に組み込まれる) |
10.30 | | 分離協定は、2022年5月17日にAqutive Treateutics,Inc.およびKeith J.Kendallによって署名された(当社が2022年5月17日に提出したForm 8-Kフォームの添付ファイル10.1として提出され、参照によって本明細書に組み込まれる) |
10.31 | | Aqutive Treateutics,Inc.と買い手の間で2022年6月6日に提出された証券購入プロトコルテーブル(当社が2022年6月8日に提出した8-Kフォームの添付ファイル10.1として提出され、参照によって本明細書に組み込まれる) |
10.32 | | 購入契約は、日付が2022年4月12日であり、会社とリンカーン公園との間で締結される(当社が2022年4月13日に提出した8-K表現在の報告書の添付ファイル10.1として提出され、参照によって本明細書に組み込まれる)。 |
| | | | | | | | |
10.33 | | 登録権利協定は、日付が2022年4月12日であり、当社がリンカーンパーク社と締結する(当社が2022年4月13日に提出した8-K表現在の報告書の添付ファイル10.2として提出し、参照により本明細書に組み込む) |
10.34 | | 株式割当契約は、2019年9月11日にAqqutive Treeutics,Inc.とPiper Sandler&Co.が締結した(会社が2019年9月11日に提出したS-3(333-233716)表登録声明の添付ファイル1.2として提出し、参照により本明細書に組み込む) |
10.35 | | Aqutive Treateutics,Inc.とPiper Sandler&Co.の間で2021年3月26日に署名された持分割当協定の第1号修正案(当社が2021年3月26日に提出したForm 8-Kテーブルの添付ファイル10.1として提出し,参照により本明細書に組み込む) |
10.36 | | 2023年8月1日の募集要約は、普通株式引受権証プロトコルを行使する(当社が2023年8月2日に提出した8-K表現在報告の添付ファイル10.1として提出し、参照により本明細書に組み込む) |
10.37 | | 13.5%債券の購入プロトコルフォーマット(2023年11月2日に当社が提出した8-Kフォームの現在の報告書の添付ファイル10.1として提出され、参照によって本明細書に組み込まれる)。 |
10.38 | | 2023年11月1日現在、発行者、他の付与者、米国銀行信託会社が受託者である米国銀行信託会社と米国銀行信託会社を担保代理人とする米国銀行信託会社との間の担保協定(当社が2023年11月2日に提出した8−K表の添付ファイル10.2として提出し、引用により本明細書に組み込む)。 |
10.39† | | 特許使用料契約表(当社が2023年11月2日に提出した8−K表の現在の報告書の添付ファイル10.3として提出され、参照によって本明細書に組み込まれる)。 |
10.40* | | AqutiveとAtnahs Pharma UK Limitedとの間の許可および供給プロトコル修正案は、2023年3月27日に発効する(付箋提供)。 |
23.1* | | 独立公認会計士事務所ピマウェイ会計士事務所同意(z提出)。 |
31.1* | | 2002年サバンズ-オキシリー法302節に基づいて可決された1934年“証券取引法”第13 a-14(A)及び15 d-14(A)条に基づいて発行された最高経営責任者証明書(同封提出)。 |
31.2* | | 2002年のサバンズ-オキシリー法第302節で可決された1934年“証券取引法”第13 a-14(A)及び15 d-14(A)条に基づいて発行された首席財務官証明書(同封提出)。 |
32.1* | | 2002年の“サバンズ-オックススリー法案”906節で採択された“米国法典”第18編1350節に規定されている首席執行幹事証明書(付箋提供)。 |
32.2* | | 2002年の“サバンズ-オックススリー法案”906節で可決された“米国法典”第18編1350節に規定されている首席財務官証明書(付状提供)による。 |
97* | | 奨励的報酬回収政策 |
| 101.INS* | | XBRLインスタンスドキュメントを連結する. |
| 101.Sch* | | インラインXBRL分類拡張アーキテクチャ文書. |
| 101.カール* | | インラインXBRL分類拡張はリンクベース文書を計算する. |
| 101.定義* | | XBRLソート拡張を連結してLinkbase文書を定義する. |
| 101.実験所* | | XBRL分類拡張ラベルLinkbase文書を連結する. |
| 101.前期* | | XBRL分類拡張プレゼンテーションLinkbaseドキュメントを内部接続する. |
| 104* | | 表紙対話データファイル(添付ファイル101に含まれるイントラネットXBRLのフォーマット)。 |
米国証券取引委員会(Securities And Exchange Commission)が承認した機密処理要求によると、本展示品の内容の一部(星番号で示す)は省略されている。*ここで提供され、取引所法案第18条の目的に応じて“保存”されているとはみなされず、1933年の証券法(改正された)または取引所法案(10-K表の日付の前または後に行われたものを問わず)に従って提出された任意の文書を参照して、文書に含まれる任意の一般的な登録言語にかかわらず登録成立されたとみなされてはならない。
+管理契約または補償計画を示します。
イによると、本展示品のいくつかの部分は漏れており、漏れた情報(I)は実質的ではないため、(Ii)公開開示すれば、会社に競争損害を与える可能性がある
項目16.表格10-Kの概要
適用されません。
サイン
1934年“証券取引法”第13又は15(D)節の要求に基づいて、登録者は、次の署名者が代表して本報告書に署名することを正式に許可した。
| | | | | | | | |
| | AQUESTIVE治療会社 |
| | | |
2024年3月5日 | 差出人: | /S/Daniel美容師 |
| | | ダニエル美容師 |
| | | 社長と最高経営責任者 |
| | | (首席行政主任) |
本報告は、1934年の証券取引法の要求に基づき、以下の者によって登録者として指定日に署名された。
| | | | | | | | | | | | | | |
| サイン | | タイトル | | 日取り |
| | | | | |
| /S/Daniel美容師 | | CEO兼取締役社長 | | 2024年3月5日 |
| ダニエル美容師 | | (首席行政主任) | | |
| | | | | |
| /S/A.アーネスト·トス | | 最高財務官上級副社長 | | 2024年3月5日 |
A.アーネスト·トス | | (首席財務官と首席会計官) | | |
| | | | | |
| /S/グレゴリー·B·ブラウン | | 取締役会のメンバー | | 2024年3月5日 |
| グレゴリー·B·ブラウン医学博士 | | | | |
| | | | | |
/S/ジョン·S·コクラン | | 取締役会のメンバー | | 2024年3月5日 |
ジョン·S·コクラン | | | | |
| | | | | |
| /S/サントー·J·コスタ | | 取締役会議長 | | 2024年3月5日 |
| サント·J·コスタ | | | | |
| | | | | |
/S/ジュリー·クロップ | | 取締役会のメンバー | | 2024年3月5日 |
ジュリー·クロップ医学博士 | | | | |
| | | | |
| /S/マルコ·タレティ | | 取締役会のメンバー | | 2024年3月5日 |
Marco Taglietti医学博士 | | | | |
| | | | |
| /S/ティモシー·モリス | | 取締役会のメンバー | | 2024年3月5日 |
ティモシー·モリス | | | | |
連結財務諸表索引
| | | | | |
| | ページ
番号をつける |
独立公認会計士事務所報告(ピマウェイ会計士事務所ニューヨークNY 監査役事務所ID:185) | 2 |
| | |
2023年12月31日と2022年12月までの連結貸借対照表 | 4 |
| | |
2023年,2023年および2022年12月31日までの総合経営報告書と全面赤字報告書 | 5 |
| | |
2023年、2023年、2022年12月31日までの年度株主赤字変動表 | 6 |
| | |
2023年,2023年,2022年12月31日までの連結キャッシュフロー表 | 7 |
| | |
連結財務諸表付記 | 8 |
株主や取締役会に
Aqutive Treeutics,Inc.:
連結財務諸表に対するいくつかの見方
添付のAqutive Treateutics,Inc.およびその子会社(当社)が2023年12月31日まで,2023年および2022年12月31日までの総合貸借対照表,2023年12月31日までの2年間の各年度の関連総合経営と全面赤字報告書,株主赤字変化とキャッシュフロー,および関連付記(総称して総合財務諸表と呼ぶ)を監査した。総合財務諸表は,すべての重要な点で,会社の2023年12月31日まで,2023年12月31日と2022年12月31日までの財務状況,および2023年12月31日までの2年間の運営結果とキャッシュフローを公平に反映しており,米国公認会計原則に適合していると考えられる。
意見の基礎
これらの連結財務諸表は会社の経営陣が責任を負う。私たちの責任は私たちの監査に基づいてこのような連結財務諸表に意見を発表することだ。私たちは米国上場企業会計監督委員会(PCAOB)に登録されている公共会計士事務所であり、米国連邦証券法および米国証券取引委員会とPCAOBの適用規則と法規に基づいて、会社と独立しなければならない。
私たちはPCAOBの基準に従って監査を行っている。これらの基準は、連結財務諸表に重大な誤報がないかどうかに関する合理的な保証を得るために、エラーによるものであっても不正であっても、監査を計画し、実行することを要求する。当社はその財務報告の内部統制を監査することを求められておらず、私たちも招聘されて監査を行っていません。私たちの監査の一部として、財務報告の内部統制を理解することが求められていますが、社内財務報告の内部統制の有効性について意見を述べるためではありません。したがって、私たちはそのような意見を表現しない。
我々の監査には、連結財務諸表の重大な誤報リスクを評価するプログラム、エラーによるものであっても詐欺であっても、これらのリスクに対応するプログラムを実行することが含まれる。これらの手続きは、連結財務諸表中の金額および開示に関する証拠をテストに基づいて検討することを含む。我々の監査には、経営陣が使用する会計原則の評価と重大な見積もり、合併財務諸表の全体列報の評価も含まれています。私たちは私たちの監査が私たちの観点に合理的な基礎を提供すると信じている。
重要な監査事項
以下に述べる重要な監査事項は、監査委員会が監査委員会に伝達または要求する当期総合財務諸表監査によって生じる事項を指すことである:(1)総合財務諸表に対して大きな意味を有する勘定または開示に関するものであり、(2)私たちが特に挑戦的で主観的または複雑な判断に関するものである。重要監査事項の伝達は、総合財務諸表に対する私たちの全体的な意見をいかなる方法でも変えることはなく、以下の重要な監査事項を伝達することによって、重要な監査事項またはそれに関連する勘定または開示について個別の意見を提供することはない。
持続経営企業としての会社の継続経営能力を評価する
総合財務諸表付記4で述べたように、当社は純損失の歴史を経験している。2023年12月31日現在、会社は累計319,077,000ドルの赤字を計上している。歴史的に見て、会社の流動資金源には、現金と現金等価物、株式、債券発行が含まれている。同社は、それが行っている業務、既存の現金と等価物、費用管理活動、および既存の購入プロトコルへのアクセスは、これらの財務諸表の発表日から12ヶ月の運営需要を満たすための流動資金を提供していると考えている。
私たちはその持続的な経営能力に対する会社の評価を重要な監査事項として決定した。ある仮定の不確実性,特に予測費用および会社費用管理活動の可能性から,会社が持続経営分析に用いているキャッシュフローの予測を評価する際には高度な主観的監査人の判断が必要である。
以下は私たちがこの重要な監査問題を解決するために実行した主な手続きだ。当社の持続経営評価とキャッシュフロー予測の内部制御設計の評価を行った。当社の歴史予測のキャッシュフローを実際の結果と比較し、会社の正確な予測能力を評価します。予測費用と費用管理活動の変化が会社の継続経営評価に及ぼす影響を評価することにより,会社の予測キャッシュフローの感受性分析を行った。取締役会に伝達された経営陣計画との比較、および会社費用管理活動の実行可能性を評価した
会社が発表した公開情報。我々は,開示と得られた監査証拠を比較することにより,会社の持続的な経営評価に関する開示を評価した。
/s/ ピマウェイ会計士事務所
2006年以来、当社の監査役を務めてきました。
ショットヒルズニュージャージー州
2024年3月5日
AQUESTIVE治療会社
合併貸借対照表
(千単位、1株/単位金額を除く)
| | | | | | | | | | | |
| | 十二月三十一日 |
| | 2023 | | 2022 |
| 資産 | | | |
| 流動資産: | | | |
| 現金と現金等価物 | $ | 23,872 | | | $ | 27,273 | |
| 貿易その他売掛金純額 | 8,471 | | | 4,704 | |
| 在庫、純額 | 6,769 | | | 5,780 | |
| 前払い費用と他の流動資産 | 1,854 | | | 2,131 | |
| 流動資産総額 | 40,966 | | | 39,888 | |
| 財産と設備、純額 | 4,179 | | | 4,085 | |
| 使用権資産、純額 | 5,557 | | | 5,211 | |
| 無形資産、純額 | 1,278 | | | 1,435 | |
| 他の非流動資産 | 5,438 | | | 6,451 | |
| 総資産 | $ | 57,418 | | | $ | 57,070 | |
| | | |
| 負債と株主赤字 | | | |
| 流動負債: | | | |
| 売掛金 | $ | 8,926 | | | $ | 9,946 | |
| 費用を計算する | 6,497 | | | 7,967 | |
| 賃貸負債、流動 | 390 | | | 255 | |
| 収入を繰り越す | 1,551 | | | 1,513 | |
| 将来の収入に関連した負債、当期 | 922 | | | 1,147 | |
支払手形,当期 | 22 | | | 18,700 | |
| 流動負債総額 | 18,308 | | | 39,528 | |
支払手形,純額 | 27,508 | | | 33,448 | |
印税義務,純額 | 14,761 | | | — | |
| 将来の収入の販売に関する負債、純額 | 63,568 | | | 64,112 | |
| 賃貸負債 | 5,399 | | | 5,085 | |
| 繰延収入,当期分を差し引く | 32,345 | | | 31,417 | |
| 他の非流動負債 | 2,016 | | | 2,034 | |
| 総負債 | 163,905 | | | 175,624 | |
あるいは事項があります(付記22) | | | |
| | | |
| 株主赤字: | | | |
普通株0.001額面価値。授権250,000,000株式;68,533,085そして54,827,734それぞれ2023年12月31日および2022年12月31日に発行および発行された株式 | 69 | | | 55 | |
| 追加実収資本 | 212,521 | | | 192,598 | |
| 赤字を累計する | (319,077) | | | (311,207) | |
| 株主総損失額 | (106,487) | | | (118,554) | |
| 総負債と株主赤字 | $ | 57,418 | | | $ | 57,070 | |
連結財務諸表の付記を参照。
AQUESTIVE治療会社
合併経営報告書と全面赤字
(単位は千、1株あたりのデータ量は除く)
| | | | | | | | | | | |
| | 十二月三十一日までの年度 |
| | 2023 | | 2022 |
| 収入.収入 | $ | 50,583 | | | $ | 47,680 | |
| コストと支出: | | | |
| 製造と供給 | 20,831 | | | 19,386 | |
| 研究開発 | 13,104 | | | 17,481 | |
| 販売、一般、行政 | 31,750 | | | 52,879 | |
| 総コストと費用 | 65,685 | | | 89,746 | |
| 運営損失 | (15,102) | | | (42,066) | |
| その他の収入(支出): | | | |
| 利子支出 | (6,337) | | | (6,552) | |
特許使用料義務に関する利子支出,純額 | (905) | | | — | |
| 将来の収入の売却に関する利子支出 | (220) | | | (5,891) | |
| 利息収入その他の収入,純額 | 16,321 | | | 99 | |
| 債務返済損失 | (1,382) | | | — | |
| 所得税前純損失 | (7,625) | | | (54,410) | |
| 所得税 | (245) | | | — | |
| 純損失 | $ | (7,870) | | | $ | (54,410) | |
| 総合損失 | $ | (7,870) | | | $ | (54,410) | |
| | | |
| 1株当たり純損失--基本損失と赤字 | $ | (0.13) | | | $ | (1.12) | |
| | | |
| 加重-発行された普通株式の平均-基本および希釈後の普通株式 | 61,255,864 | | 48,734,377 |
連結財務諸表の付記を参照。
AQUESTIVE治療会社
合併株主損変動表
(千単位で、1株当たりを除く)
| | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | |
| | | | | | その他の内容
支払い済み
資本 | | 積算
赤字.赤字 | | 合計する
株主の
権益/(赤字) |
| | | 普通株 | | | |
| | | 株 | | 金額 | | | |
| 2022年1月1日の残高 | | 41,228,736 | | | $ | 41 | | | $ | 174,621 | | | $ | (256,796) | | | $ | (82,134) | |
| 発行された権利証の公正価値 | | — | | | — | | | 5,874 | | | — | | | 5,874 | |
| 私募株式発行による普通株 | | 6,686,491 | | | 7 | | | 4,622 | | | — | | | 4,629 | |
| 私募株式発行普通株のコスト | | — | | | — | | | (824) | | | — | | | (824) | |
| 株式承認証行使後に発行された普通株 | | 4,000,000 | | | 4 | | | (4) | | | — | | | — | |
| 株式公開で発行された普通株 | | 2,860,538 | | | 3 | | | 4,193 | | | — | | | 4,196 | |
| 普通株式公開のコスト | | — | | | — | | | (289) | | | — | | | (289) | |
| 従業員の株購入計画に基づいて発行された株 | | 45,304 | | | — | | | 34 | | | — | | | 34 | |
| 既得制限株式単位 | | 6,665 | | | — | | | (3) | | | — | | | (3) | |
| 株式ベースの給与費用 | | — | | | — | | | 4,371 | | | — | | | 4,371 | |
| 他にも | | — | | | — | | | 3 | | | (1) | | | 2 | |
| 純損失 | | — | | | — | | | — | | | (54,410) | | | (54,410) | |
| 2022年12月31日の残高 | | 54,827,734 | | | 55 | | | 192,598 | | | (311,207) | | | (118,554) | |
| | | | | | | | | | |
| | | | | | | | | | |
| | | | | | | | | | |
| 株式承認証行使後に発行された普通株 | | 8,689,452 | | | 9 | | | 8,333 | | | — | | | 8,342 | |
| 私募株式発行普通株のコスト | | — | | | — | | | (35) | | | — | | | (35) | |
| 株式公開で発行された普通株 | | 4,958,341 | | | 5 | | | 9,459 | | | — | | | 9,464 | |
| 株式公開で発行された普通株 | | — | | | — | | | (552) | | | — | | | (552) | |
| 従業員の株購入計画に基づいて発行された株 | | 36,168 | | | — | | | 66 | | | — | | | 66 | |
| 既得制限株式単位 | | 19,515 | | | — | | | (11) | | | — | | | (11) | |
| 株式ベースの給与費用 | | — | | | — | | | 2,662 | | | — | | | 2,662 | |
行使のオプション | | 1,875 | | | | | 1 | | | | | 1 | |
| 他にも | | — | | | — | | | — | | | — | | | — | |
| 純損失 | | — | | | — | | | — | | | (7,870) | | | (7,870) | |
| 2023年12月31日の残高 | | 68,533,085 | | | $ | 69 | | | $ | 212,521 | | | $ | (319,077) | | | $ | (106,487) | |
連結財務諸表の付記を参照。
AQUESTIVE治療会社
統合現金フロー表
(単位:千)
| | | | | | | | | | | |
| | 十二月三十一日までの年度 |
| | 2023 | | 2022 |
| 経営活動のキャッシュフロー: | | | |
| 純損失 | $ | (7,870) | | | $ | (54,410) | |
| 純損失と経営活動用現金純額の調整: | | | |
| 減価償却·償却·減価 | 1,345 | | | 2,387 | |
| 株式ベースの報酬 | 2,689 | | | 4,381 | |
| 債務発行コストと割引償却 | 1,972 | | | 215 | |
| 将来の収入の売却に関する利子支出 | — | | | 5,683 | |
| 債務返済損失 | 1,029 | | | — | |
| その他、純額 | (204) | | | (52) | |
| 経営性資産と負債変動状況: | | | |
| 売掛金とその他の売掛金の純額 | (3,073) | | | 7,352 | |
| 棚卸しをする | (989) | | | (1,743) | |
| 前払い費用と他の資産 | 1,290 | | | 1,399 | |
| 売掛金 | (1,020) | | | 1,633 | |
| 費用とその他の負債を計算すべきである | (2,515) | | | (2,382) | |
| 収入を繰り越す | 966 | | | 25,043 | |
支払手形 | — | | | 675 | |
| 経営活動のための現金純額 | (6,380) | | | (9,819) | |
| 投資活動によるキャッシュフロー: | | | |
| 資本支出 | (995) | | | (1,024) | |
| 無形資産の付加価値 | — | | | (1,500) | |
| 投資活動のための現金純額 | (995) | | | (2,524) | |
| 資金調達活動のキャッシュフロー: | | | |
普通株で得た金を公開発行し,純額 | 8,912 | | 3,907 | |
私募株式発行により発行された普通株式及び引受権証収益,純額 | — | | | 9,679 | |
株式承認証を行使して得られた金は純額である | 8,307 | | | — | |
| 従業員の株購入計画に基づいて株を発行して得た金 | 39 | | 34 | |
| 株式オプションを行使して得られる収益 | 1 | | — | |
| | | |
| 債券発行で得られた金 | 31,144 | | — | |
特許使用料協定を発行して得られた収益 | 13,856 | | — | |
債務を返済する | (51,529) | | — | |
| 融資コストを支払う | (4,643) | | | — | |
| 債務返済のための割増 | (2,102) | | | (2,025) | |
| 株式に基づく報酬の税金を支払う | (11) | | | (3) | |
| 融資活動が提供する現金純額 | 3,974 | | | 11,592 | |
| 現金と現金等価物の純減少 | (3,401) | | | (751) | |
| 現金と現金等価物: | | | |
| 期日の初め | 27,273 | | | 28,024 | |
| 期末 | $ | 23,872 | | | $ | 27,273 | |
| | | |
| キャッシュフロー情報の補足開示: | | | |
| 現金で利子を払う | $ | 4,602 | | | $ | 6,436 | |
| | | |
| | | |
| | | |
連結財務諸表の付記を参照。
AQUESTIVE治療会社
連結財務諸表付記
(千単位で、株や1株当たりの情報は含まれていない)
注1.取引記録会社概況と持分取引
会社の概要
AQUEATIOTICS,Inc.(その子会社,“AQUECTIVE”または“The Company”)は製薬会社であり,既存の看護基準で患者の問題を解決し,変革的な製品を提供して生活を改善することに取り組んでいる。同社は薬物製品を開発しており,侵襲性や不便な標準看護療法の代替投与により複雑な分子を輸送している。同社には5種類の特許商業化製品があり、その特許所有者が米国と世界各地で販売している。同社はこれらの特許製品の独占メーカーである。同社は製薬会社とも協力し,特許,同種最適な技術(例えばPharmFilm)を用いて新分子を市場に投入し,検証された薬物開発と商業化能力を有している。同社はアレルギー反応を含む重篤なアレルギー反応を治療する製品パイプラインを進めている。同社は中枢神経系疾患の治療に専念する製品ラインも開発した。同社の生産施設はインディアナ州のポティチにあり、その会社本部と主要な研究実験室施設はニュージャージー州のウォーレンに設置されている。
株式取引
2019年9月11日、会社はATM施設を設立し、この施設により、会社は最高$を提供することができます25,000普通株の価値。2020年11月20日、会社はATM施設の使用を開始した。2021年3月26日、同社は最大規模の株式募集説明書補充書類を提出した50,000ATM機での普通株の価値。その条項によると、2019年の登録声明は2022年9月17日に満了した。2022年9月7日、会社は募集説明書の補充書類を提出し、登録要約と販売金額は最高でドルに達する35,000米国証券取引委員会が2021年4月5日に発効を発表したS-3表保留登録声明(第333-254775号登録声明、または2021年登録声明)に基づく改正株式分配協定の普通株式価値。会社は2022年9月7日に目論見書補充書類を提出した後、2021年の目論見書の使用を停止した。
当社は2023年12月31日まで販売しております4,958,341純利益約$の株を提供する8,962手数料と他の取引費用を差し引いて#ドル502それは.このATM施設には約$があります23,9522023年12月31日に発売される。当社は2022年12月31日までに販売します2,860,538純利益約$の株を提供する3,907手数料と他の取引費用を差し引いて#ドル289.
2022年4月12日、当社はリンカーン公園購入契約を締結しました。その中で、リンカーン公園購入契約下の条項及び条件と制限により、当社は権利がありますがリンカーン公園への販売義務はありません$を超えません40,000当社の普通株の株式価値は36-リンカーン公園購入契約の1ヶ月の期限。リンカーン公園の購入協定には所有権制限が含まれています。もしこれがリンカーン公園が発行した普通株に対する実益所有権を超えたら、会社は普通株を発行しません。リンカーン公園も普通株を購入しません9.99%は、6,486,6232023年12月31日の株。リンカーン公園はすでにリンカーン公園の購入契約に基づいて、いかなる方法でも直接あるいは間接的に空売りしたり、私たちの普通株をヘッジしたりしません。当社は2023年12月31日まで、リンカーンパーク購入契約に関連する株式を販売していません。当社は2022年12月31日までに販売します1,600,000発行を除く株236,491承諾株は、約#ドルの収益を提供しました1,987リンカーン公園の購入契約と関係があります
二零二二年六月六日、当社は証券購入協定を締結し、当社の売却及び発行合わせを規定した:(I)4,850,000普通株式は,(Ii)予資権証,最大購入可能である4,000,000普通株式及び(Iii)普通株式承認権証は,最大で購入することができる8,850,000普通株株。会社が受け取った純収益は約#ドルだった7,796配給代理費及び支出及び見積もりは当社が支払うべき発売費用を差し引いた。同社は今回発行された純収益を一般企業用途に使用している。予備資金権証は2022年に全面的に行使される。2023年6月14日、引受権証3,689,452証券購入契約により発行された普通株式が行使され,当社に支払われる金は約$である3,542.
当社は2023年8月1日に所有者(“行権所有者”)と書面協議を締結した5,000,000残りの普通株式承認証。通信契約によると、行権所有者と当社の同意行権所有者は、それが保有するすべての普通株承認株式証を行使し、その普通株式承認株式証の価格は$となる0.961株当たりの普通株,普通株は株式証の発行権価格を承認する.通信契約により,所持者の行使を考慮する5,000,000普通株式承認株式証は,会社が行権所有者に新たな株式引受証を発行して,最も多く購入する2,750,000普通株式を行権者に譲渡する。新株式証明書は2024年2月2日以降に行使でき、2029年2月2日に満期となり、現金形式でしか発行できない
新承認株式証の行使は、通信契約の条項に基づいて登録されていない限り、この場合、新株式証は、その時間に“現金なし行使”の方法で全部または部分的に行使することができる。新株式証の行使価格は$である2.60一株ずつです。2023年8月2日5,000,000当社は、行権者と締結した証券購入契約に基づいて一般権証のうちの1つの株式承認証を行使し、当社が当該等株式証から得た総収益は#ドルである4,800それは.全体的には,行使を許可する8,689,452証券購入契約により発行された普通株は,得られた金は約$である8,342二零二三年十二月三十一日までに、当社に支払われた金額は行使されました。その会社は$を生み出した35この取引と関係があります。
注2.取引記録列報根拠と合併原則
これらの連結財務諸表は、米国公認会計基準と米国証券取引委員会の規則に基づいて作成されている。完全子会社の勘定は連結財務諸表に計上する。会社設立活動以外に、このような付属会社はいかなる商業、発展或いは運営活動を行っておらず、いかなる顧客或いはサプライヤーもない。本年度に該当する列報方式で何らかの再指定クラスを行った.
これらの説明における適用指導へのどのような言及も、FASBのASCおよびASUで見つかった権威的な米国公認会計原則を意味する。
注3.取引記録重要会計政策の概要
予算の使用
米国公認会計原則に基づいて財務諸表を作成するには、財務諸表の日付を開示するか、資産および負債があるか、および報告期間内に報告された収入および費用金額を含む、資産および負債報告金額に影響を与える推定および仮定を使用する必要がある。これらの推定および仮定は、本質的に不確実な事象の評価に関連することが多いため、実際の結果はこれらの推定とは異なる可能性がある。推定および仮定の影響を受ける重大な項目には、収入確認、在庫コスト、Assertioに許可される前の独自製品販売のリベート準備、販売差し戻し準備、固定資産の使用寿命、および発行された承認株式証の推定値、特許使用料義務、将来の収入の販売、株式ベースの補償およびまたは事項に関する項目がある。
現金と現金等価物
同社はすべての購入元満期日が3ヶ月以下の短期·高流動性投資を現金等価物と見なしている。現金と現金等価物は、2023年12月31日、2023年12月31日、2022年12月31日まで、銀行口座の現金からなる。
信用リスクが集中する
現金と現金等価物は連邦保険の金融機関が保有しており、経営陣はこれらの機関の信用品質が高いと考えている。同社はこれらの口座で何の損失も受けていません。これらの金額は連邦保険の250ドルの限度額を超える可能性があります。
会社の重要顧客の集中度は、2023年12月31日、2023年12月31日、2022年12月31日まで、付記5に概説されている収入と売掛金の純額
売掛金
売掛金は領収書の金額に応じて入金され,利息は計算されない.会社は通常の業務過程で顧客に信用を提供しますが、通常は担保あるいは他の保証を必要としません 売掛金。その会社の信用条項は一般的に30至れり尽くせり60日数は,具体的には顧客と伝票タイプに依存する.同社は、年末以降に支払われたお金を含む顧客の信用リスクと支払い記録を定期的に審査している。
当社は様々な要因に基づいて売掛金の回収可能性を評価しています。変化している場合には、ある特定の顧客が自社に対する財務責任を履行できない場合には、不良債権準備を支払金額に計上し、売掛金純額を合理的に予想すべき金額に減らすことを確認しなければならない。すべての他の顧客に対して、不良債権準備は、売掛金の期限が過ぎた時間の長さ、現在のビジネス環境、当社の歴史経験などの要素によって入金されています。不良債権は販売、一般、行政費用に計上する準備ができている。売掛金が回収できない可能性が高い場合、口座残高は引当から解約される。売掛金回収可能性に関する不良債権は#ドルに用意されている14そして$40それぞれ2023年、2023年、2022年12月31日まで。
棚卸しをする
在庫は調達材料、直接人工と製造間接費用から構成され、先進先出法或いは可変現純値によって確定されたコストの中の低い者が報告した。当社は定期的に在庫減値を審査し、必要に応じて準備金を作成します。
貸借対照表の日付ごとに、会社は在庫の過剰数量、古い状況、賞味期限の期限を評価します。この評価には、製品の分析履歴による販売レベル、未来の需要の予測、製品競争淘汰のリスク、一般市場状況及び製品賞味期限の期限の審査が含まれている。経営陣が過剰または古い在庫が存在したり、賞味期限が満期に近づきすぎる数量が存在すると判断した場合、当社はそのような製品が満期前に販売または生産に使用できることを合理的に予想することができず、当社は記録に必要な時に帳簿価値を現金化可能な純資産値を推定するために調整する。会社が会社の研究開発活動に関連する在庫を購入または生産する場合、会社はそれを支出する。規制部門が当社の候補品を承認する前に、当社は薬物製品を製造するための研究·開発費を確認し、規制部門の承認を得られれば、これらの費用は自社の候補薬物の商業発売を支援するために使用できる可能性がある。
財産と設備
財産と設備は減価償却と償却後のコスト純額に記載されており、直線法でそれぞれの資産の推定耐用年数に基づいて計算されると、以下のようになる。リース改善は、レンタル期間が短いか、またはリース資産の推定使用年数の短い時間で償却する。維持·修理費用は発生時に費用を計上し、主に更新と改善の支出を資本化に計上する。財産や設備を処分する際には、関連コストと減価償却および償却は勘定から差し引かれ、どの損益も付随する総合経営報告書と全面赤字報告書に反映される。
無形資産
無形資産には、成分および加工技術を買収するコスト、口腔可溶性フィルムを製造するための特許を購入するコスト、および秘密協定を買収するコストがある。会社の直線方法は、これらの資産の法定年限または推定耐用年数が短い時間内にこれらの資産を償却する。
長期資産減価準備
事件や環境変化が発生してある資産の帳簿価値が回収できない可能性があることを示す限り、資産、工場、設備などの長期資産を減値審査する。この場合、当社は、当該資産又は資産群が予想する未割引キャッシュフローと対応する帳簿金額とを比較する。この比較が減値を示していれば,帳票金額がその公正価値を超えた範囲で減値費用を確認する.公正価値は各種の推定方法を通じて決定され、割引現金流量モデル、見積時価及び最適とされる第三者の独立評価を含む。減価費用は#ドルです2162023年12月31日までの年度を確認した違います。2022年12月31日までの年度に減値を確認した。
賃貸借証書
一つの手配がレンタル契約であるかどうかは開始時に確定される。契約が、価格と交換するために、決定された財産および装置の使用を一定期間制御する権利を譲渡した場合、スケジュールは、レンタルを含むと決定される。当社が単独で、または他の読み取り可能なリソースと共にレンタルされた様々な基礎資産から利益を得ることができる場合、または様々な基礎資産とスケジュール内の基礎資産とが高度に依存しても高度に関連していない場合、それらは別個のレンタル構成要素とみなされる。複数の関連資産が確認された場合、リース対価格は、各構成要素の相対的な公正価値に応じて各構成要素に割り当てられる。
経営リース資産は当社がリース期間内に対象資産を使用する権利を代表し、経営リース負債はリース手配によるリース金の支払い義務を代表する。経営リース資産及び経営リース負債は、開始日にレンタル期間内のリース支払いの現在値に基づいて確認される。当社の大部分の賃貸借契約は暗黙的な金利を提供していないため、経営賃貸負債を確定する際には、当社はその増額借入金利の見積もりを使用しています。レンタル資産の計算には、支払い済みのリース支払いが含まれており、レンタルインセンティブは含まれていません。私たちのレンタル条項には、レンタルの選択権を延長または終了し、会社が選択権を行使することを合理的に確定する際に含まれる可能性があります。
当社はその総合貸借対照表に経営リース資産と賃貸負債を記録しています。レンタル支払いのレンタル料金はレンタル期間内に直線的に確認します。短期借約、またはリース期間が完了日が12ヶ月以下のリース契約は、この処理範囲内ではなく、レンタル期間内に直線原則で確認される。2023年12月31日までの年間で、会社はその製造を支援する賃貸契約を確認した
施設は融資リースとして。融資リース項目の下での負担は重大ではなく、総合貸借対照表上の物件及び設備純額、支払手形、流動手形及び支払手形純額に計上されている。
印税義務,純額
発行について“13.5%手形,当社は各手形所持者と印税権利協定を締結し,手形所持者に付与する1.0%和2.0しばらくの間アレルギー(アドレナリン)舌下錠の全世界の純売上高のパーセント8人初めて世界でアレルギーが販売されてから数年。手形保有者は等級別印税を受ける権利があります1.0%から2.0(1)アレルギーの初回販売と(2)までのLibervant(安定)口腔薬膜の全世界年間純売上高のパーセンテージ8人Libervantが初めて販売されてから数年。特許使用料協定は債務に分類され、$45,00013.5%手形は、債務と特許使用料義務の相対的に公平な市場価値に基づいて、債務と特許使用料義務との間に割り当てられています。特許権使用料責任の公正価値は特許権使用料契約の有効期間内に償却され、この等は総合経営報告書及び全面損失に反映され、特許権使用料責任に関する利息支出に反映される。♪the the the13.5%付記は付記14で議論し、長期債務その連結財務諸表まで
将来の収入の売却に関する責任
当社は将来の収入の売却に関する負債を債務融資と見なし、実利法による期待特許権使用料流量の推定年限で償却する。将来の収入および関連する支払利息の売却に関する負債は、計画有効期間内に支払われる予定の将来の特許権使用料の推定値に基づいて計算される。同社は内部予測と外部資源の予測に合わせて、予想される特許権使用料を定期的に評価して支払う。特許使用料の将来の支払いの推定値が以前の推定よりも大きいか、またはそれよりも低い範囲内で、またはその支払いの時間が以前に推定されたものと大きく異なる場合、当社は、関連する利息支出を前向きに確認する。債務償却は、総合経営と全面赤字報告書に、将来の売却収入に関する利息支出に反映されている。将来の収入の売却についてのさらなる議論は、付記16を参照されたい将来の収入を売る。
収入確認
同社の収入には,(I)商業化許可者との契約による完成品販売,(Ii)2022年10月にUsertioに許可される前に,LGSに関連するてんかん発作を治療するための会社独自のクロバザムベースのSympazan経口投与膜製品の販売,(Iii)ライセンスおよび特許権使用料収入,および(Iv)通常マイルストーン支払い形式で支払われる共同開発および研究費用が含まれる。注5を参照収入と貿易売掛金の純額それは.より詳細な情報を知るために。同社が確認した収入は、顧客に譲渡承諾した商品やサービスの金額を反映しており、会社がこれらの商品やサービスと交換する権利があることが期待されていることを反映している。このコア原則を実現するために、(1)顧客との契約を決定すること、(2)契約における履行義務を決定すること、(3)取引価格を決定すること、(4)取引価格を履行義務に割り当てること、および(5)エンティティがいつまたは義務を履行するかを確認することを含む5段階モデルが適用される。
製造と供給収入-この収入は、特定の顧客によって厳密に定義された仕様に従って専門的に製造された製品からであり、指定された品質管理検査のみを受ける。そこで,品質管理要求を満たした時点で,関連割引を差し引いた収入純額を記録する.
専有製品販売,純額-この収入は、製品の出荷および所有権がお客様に転送されたときに確認され、通常、納品時に確認されます。販売時には,各種収入免税額の推定数は歴史的傾向と判断に基づいて推定記録されている.販売返品手当や即時報酬割引は契約条項や歴史的リターン率(あれば)に基づいて推定されますが、このなどは売掛金として減少していると思われます。卸サービス料,自己支援償還,医療保険,医療補助,その他のリベートに関する見積もり数にも類似した記録があり,これらの見積もり数は課税負債の一部として収入減少に反映されている。すべての関連変数の考慮要因を解決し,受取金額に関する不確実性を解消すると,見積り数は実際の手当額に調整される.このような推定金額の準備金は四半期ごとに検討され調整されたもの以上だ。
ライセンスと印税収入−ライセンス収入は、ライセンスが基本ライセンススケジュールに含まれる可能性のある任意の他の履行義務とは異なるかどうかの評価に基づいて決定される。顧客が任意の他の履行義務を提供することなく許可から利益を得ることができ、したがって、許可が独自または機能的許可とみなされる場合、会社は、顧客が使用許可の権利またはアクセス許可の権利を取得したかどうかを判断する。会社がさらなる開発や他の継続的な活動を必要としない機能ライセンスについては、顧客は譲渡時に使用許可証を取得した権利とみなされ、収入は通常ある時点に記録され、または制限される。当社が提供する他の履行義務とともにのみ実質的な価値を提供する象徴的な許可については、収入は通常ライセンス契約の期限内に記録される。その会社が提供するその他の義務は一般に契約規定を含めて
許可条項。受信された課税額または他の方法で稼いだ金額を超える支払いは、ライセンス期間内に延期され、あるか、またはその他の履行義務が履行されることが確認される。
特許権使用料収入は、商業ライセンス所有者との供給契約下での販売を記録する際に推定および確認され、契約制限または収集可能な不確実性はない。特許製品販売に基づく特許権使用料はこのように記録されています
共同開発と研究費−共同開発および研究費用は、契約開発または顧客との実行可能性研究プロトコルに規定された特定のタスク、活動、または開発段階を実行することによって得られる。これらの履行義務の性質は、一般に、契約に記載されたプロジェクトの範囲および構造、ならびに製品の複雑さおよび製品に必要な特定の規制承認経路に依存するマイルストーンまたは成果の交付と呼ばれる。そのため、同社の研究·開発プロジェクトの継続期間は数ヶ月から約2ヶ月になる可能性がある3年それは.各契約スケジュールは唯一無二であるが、これらの配置には、薬効および他の試験の表現、結果報告、初期プロトタイプの制定、臨床および/またはバッチの安定性生産の拡大、およびこれらのバッチの安定性試験が含まれる共通のマイルストーンが含まれる。追加のマイルストーンを確立し、製品提出および/またはFDAによる製品の承認および製品の商業投入の臨床結果に関連付けることができる。
マイルストーン支払いによる収入確認はマイルストーン支払いをめぐる事実と状況にかかっている。非販売指標に基づくマイルストーン支払い、例えば開発のマイルストーンに基づく(例えば:機密協定の届出または監督管理の承認を得る)は、可変対価を表し、任意の制限の場合に取引価格を計上する。記念碑的な支払いが将来の発展に関係すれば、承認のタイミングは歴史的経験と第三者の結果に対する重要性にかかっている。販売の敷居に達したときに受け取ったマイルストーン支払いについては、マイルストーン支払いの収入は、実際の販売発生や販売に関する業績義務が履行されたときに遅く確認される。
契約資産-場合によっては、顧客契約支払条項は、請求書を滞納することを規定する。したがって,このようなプロトコルによりクライアントに伝票を発行する前に,一部またはすべての履行義務を完全に履行する可能性がある.これらの場合、収入確認後に請求書が発行され、履行債務完了部分の推定価値によってサポートされる契約資産が生成される。これらの契約資産は、貿易及び他の売掛金における他の売掛金の構成要素に反映され、連結貸借対照表において純額である
契約責任-場合によっては、顧客契約支払い条項の構造は、貨物またはサービスの交付前に請求書を発行することを可能にする。この場合、顧客の現金支払いは、所定の部分又は任意の履行義務を履行する前に受領されることができる。このような場合、請求書は収入確認の前に発生し、これは契約債務につながる。これらの契約負債は総合貸借対照表に繰延収入として反映される。残りの履行債務が履行されるにつれて、繰延収入残高のうち適切な部分が収益に計上される。
契約を取得するコスト-場合によっては、会社は顧客との契約を取得することによって増分コストが生じる可能性があります。これらのコストが回収可能であることが予想されれば,資産として確認され,総合貸借対照表に他の資産として反映される.この資産は,当該資産に関連する貨物やサービスを顧客に譲渡するようにシステム償却を行う.
研究と開発
研究開発費や研究開発費はASC 730に記録されています研究と開発発生時に費用を計上します。研究開発費には,研究開発活動,外部CROのサービス,その臨床研究地点のコスト,拡大と検証コスト,その他の活動がある。内部研究開発活動支出には、実験室用品、賃金、福祉、非現金シェア給与支出が含まれる。CROS活動は臨床前実験室実験と臨床研究を含む。他の活動費用には規制相談と他の費用が含まれている。規制コンサルタントが負担する研究開発費に分類される活動には、準備案やFDAが提出した書類を含む様々なFDA提出手続き、臨床試験プログラム、科学的作成についての協力、コミュニケーションと提案が含まれている。これらの相談費用は,その臨床試験や研究薬物の準備,受け入れと理解に関わる直接的なコストである。合意された条項に基づいてCROに支払いが行われ、研究開始日前の支払いが含まれている可能性がある。当社の将来の研究開発活動のための商品やサービスの前金は返金されません。イベントが行われた場合や商品やサービスを受け取った場合には、支払い時ではありません。当社は提供されたサービスに基づいてCRO費用と臨床試験研究費用を審査して積算し,CROが提供する研究完了状態に適したこれらのコストの見積もりに依存している。このような研究の進展が完成に近づくにつれて、推定されたCRO費用は改訂される必要がある。当社は改訂を起こした事実が了承された期間内に料金を改定します。
所得税
所得税はFASB ASC主題740に基づいて記録されている所得税またはASC 740は、貸借対照法を使用して繰延税金を規定する。繰延税金資産および負債は、課税収入の年間の現行税率に影響を与えることが予想され、既存資産および負債の帳簿金額とそれぞれの課税基盤との差額による将来の税務結果について確認する。税務状況が監査期間中により持続する可能性がある場合には、税収割引が確認される。既存の証拠の量に基づいて、繰延税金資産の一部または全部が現金化できない可能性が高い場合、推定値減値準備が提供される。
不確定な税務頭寸は、米国会計基準第740条の規定に基づいて会計処理を行う。不確定な税金状況が存在する場合、税金優遇は、その特典がより実現可能であることがある程度確認される。税務優遇がより実現可能かどうかは、税務状況の技術的利点と既存の事実と状況に基づいて決定される。今まで、その会社には何の重大な不確定な税務頭証もなかった。
株式ベースの報酬
当社は、ASC 718記録に基づいて株式オプションと制限株式単位(“RSU”)に付与された株式ベースの報酬支出を記録し、報酬--株式報酬それは.ASU 2018-07を採用する前の非従業員報酬については報酬-株式報酬:非従業員株式支払会計の改善2019年1月1日、会社はASC 505-50を適用した非従業員に持分ベースの支払いを支払うそれは.ASC 718は,付与日の公正価値に応じて株式による補償奨励を発行することによる費用の確認のためのガイドラインを策定した
同社の株式報酬には、従業員、コンサルタント、非従業員役員への株式オプションおよびRSUの付与が含まれている。同社は2019年から、従業員の株式購入計画に参加する機会も提供している
同社の付与日オプション公正価値の推定は、Black-Scholesオプション推定モデルに基づいており、様々な変数と仮定を考慮している
•授権日の株価は
•行権価格
•オプションの契約期間と推定予想期限、
•業界の同業者の株価変動性の推定に基づいて
•期待配当(あれば)と
•無リスク金利です。
当社の授与日や推定値日RSUの公正価値の推定は,奨励の帰属条件が市場条件に基づくかサービス条件に基づくかによって異なる。市場状況に応じて付与された報酬について、会社は、様々な変数および仮定を考慮したモンテカルロシミュレーションを使用する
•シミュレーション30−必要なサービス期間の終了時の日中平均;
•奨励の授与期限に応じて決定される割引期間
•業界の同業者の株価変動性の推定に基づいて
•期待配当(あれば)と
•無リスク金利です。
これらの仮定は見積もりと判断が必要であるが,これらの投入の変化は収益に計上される費用額に影響する可能性がある。当社はRSUと株式オプション奨励の公正価値が奨励に必要なサービス期間内の補償費用であることを確認した。株式補償からの超過税収割引、税収および税収損失は、会社の総合経営報告書と全面赤字の所得税引当金に含まれている。
1株当たりのデータ
普通株1株当たりの基本純損失の計算方法は、普通株株主が純損失を当期発行普通株の加重平均株式数で割るべきである。
普通株1株当たりの純収入の計算方法は、普通株株主が得ることができる償却証券の影響調整後の純収入を当期普通株と薄普通株の加重平均株式数で割る。潜在的希薄普通株には、発行済み株式オプションおよび引受権証を行使する際に発行可能な普通株株式、発行されているが帰属していないRSUの株式、および会社の従業員株式購入計画から株式を購入する(在庫株方法を使用する)ことが含まれる。列報のすべての期間において、潜在的普通株は、それらの影響が逆希釈されるため、1株当たり収益の計算から除外される。
総合損失
総合損失には、純損失および株主との取引や経済事件以外の取引や経済事件による可能性のある株主権益の他の変化、例えば投資の未実現収益または損失が含まれる。当社の総合損失は、2023年12月31日、2023年12月31日および2022年12月31日までの間、純損失のみを含む。
公正価値計量
特定の資産と負債は公正な価値で経常的な原則に従って報告される。公正価値は、計量日市場参加者間の秩序ある取引において、資産または負債が元金または最も有利な市場で負債を移転するために徴収または支払いされる交換価格として定義される。公正価値を計量するための推定技術は,観察可能な投入を最大限に利用し,観察不可能な投入を最大限に減少させなければならない。公正価値別に列挙された金融資産および負債は、公正価値レベルの以下の3つのレベルのうちの1つで分類および開示されなければならず、そのうちの最初の2つのレベルは可視とみなされ、最後のレベルは見えないとみなされる
•第1レベル-活発な市場における同じ資産または負債の見積もり。現金および現金等価物は、銀行口座の現金を含み、いずれも一級資産である。
•第2レベル-観察可能な投入(第1レベルオファーを除く)、例えば、同様の資産または負債アクティブ市場のオファー、同じまたは同様の資産または負債非アクティブ市場のオファー、または観察可能な市場データによって確認され得る他の投入。その会社は現在所有している違います。資産または負債のレベル2。
•第3級-市場活動が非常に少ない或いは市場活動支持のない観察できない投入は、資産或いは負債の公正価値の決定に重要な意義があり、定価モデル、現金フロー方法及び類似技術を含む
貸借対照表に記載されている貿易及びその他の売掛金、前払い帳簿及びその他の流動資産、売掛金、売掛金及び繰延収入の帳簿金額は、当該等の資産及び負債の短期満期日に計算され、公正価値と一致する。
同社は以前,同社のある持分証所有者に持分証を授与したことがある12.5%の債務返済および債務再融資に関連する手形。当社も2022年及び2023年に予融資権証及び引受権証を発行し、証券購入協定について複数の購入者に普通株株式を購入する。権利証の評価値は独立第三者評価によって実行されたBlack-Scholes推定モデルに基づいており、この評価は授与日に準備され、公認された専門評価実践統一標準、アメリカ評価士協会とアメリカ公認会計士協会会計と評価ガイドラインの評価方法に符合する補償として発行された個人持株会社株式証券の推定値。付記15を参照株式承認証このような株式承認証に関する更なる情報を得るために。
その会社の12.5%手形は買い戻し要約または見込オプションを含み,オプション所有者に権利を与えるが,義務はなく,指定された金額の将来の特許権使用料を獲得し,最高上限金額に達する.この承認オプションは第3級投入に基づいて評価を行い、その公正価値は主に独立した第三者評価に基づいており、この評価は統一専門評価実務標準、アメリカ評価士協会とアメリカ公認会計士会計と評価ガイドラインの普遍的に受け入れられた評価方法に符合する。付記14を参照長期債務さらなる議論に供する。
発行について“13.5%付記当社と手形所有者は、2023年11月1日に特許権使用料権利協定を締結します。特許権使用料プロトコルは、第3レベル投入に基づいて推定され、その公正価値は、将来の販売適用確率にキャッシュフローを重み付けすることによって推定され、その後、現在値に割引される。特許権使用料プロトコルの公正価値の変化は、上記の1つまたは複数の投入の変化によって生じる可能性がある。観察できない投入の大きな変化は、特許権使用料プロトコル負債の実質金利の大幅な増加または減少を招く可能性がある。2023年の残り時間内に、特許使用料合意負債を確認するための重大な観察不可能な投入に実質的な変化はない。付記14を参照長期債務さらなる議論に供する。
市場情報を細分化する
業務部門は、エンティティの構成要素として定義され、そのエンティティに関する個別離散情報は、首席業務意思決定者または意思決定グループが、リソースをどのように割り当てるかを決定し、業績を評価する際に評価することができる。業績評価と経営決定を行うために、会社はその運営を単独の部門として管理している。
最近の会計公告
当社は、新たな又は改訂された会計基準の関連日を遵守する前に、当該等の基準を採用した比較的小さい報告会社を要求する
財務会計基準委員会は時々新しい会計声明を出し、指定された発効日から当社が採択する。別の議論がない限り、当社は最近発表されたまだ発効していない基準の影響が、その財務状況や採用後の経営結果に実質的な影響を与えないと信じている。
最近採用された会計公告:
2016年6月、FASBはASU 2016-13を発表した金融商品−信用損失(主題326)現行の金融商品に対する信用損失計算に関する現行の指導意見を改正する。指導意見は展望性予想損失モデルを用いて信用損失を推定し、過去の事件と現在の情況に基づくすでに発生した損失モデルの代わりに規定した。新しい指針はまた、推定された信用損失(およびその後の回収)を記録するために準備を使用することを要求する債務証券を売却するための減価モデルを変更した。同社は2023年1月1日に新たなガイドラインを採用した。このガイドラインの採用は会社の総合財務諸表に実質的な影響を与えていない。
2021年5月、FASBはASU 2021-04を発表した1株当たり収益(主題260)、債務修正および補償(主題470-50)、補償-株式補償(主題718)、派生ツールおよびヘッジ--エンティティ自身の資本契約(主題815-40): 発行者による独立持分分類書面コールオプションのいくつかの修正または交換の会計処理それは.会計基準の更新を発表するのは、独立株式分類の修正または交換に対する発行者の書面コールオプションの会計多様性を明確にし、減少させるためであり、これらのオプションは修正または交換後も持分分類を維持するためである。同社は2023年1月1日に新たなガイドラインを採用した。このガイドラインの採用は会社の総合財務諸表に実質的な影響を与えていない
2022年9月、FASBはASU 2022-04を発表した負債-仕入先財務計画(主題405-50)仕入先財務計画義務の開示買い手(すなわち開示エンティティ)がこのような計画を使用すること、およびこれらの計画が実体運営資本、流動性およびキャッシュフローに与える影響について、サプライヤーの財務計画の透明性を向上させる。ASU 2022-04は2022年12月15日以降の財政年度およびこれらの財政年度内の移行期間内にすべての実体に対して有効である。ロール情報に対する要求は,2023年12月15日以降の会計年度に有効である.早期養子縁組を許可する。このガイドラインの採用は会社の総合財務諸表に実質的な影響を与えていない
2023年12月31日現在採用されていない最近の会計声明:
2020年8月にFASBはASU 2020-06を発表しました債務--転換可能な債務および他のオプション(主題470-20)と派生ツールおよびヘッジ--エンティティ自身の権益の契約(主題815-40): 転換可能な手形と契約の実体自己資本における会計それは.今回の会計基準の更新は、いくつかの負債と権益の特徴を持つ金融商品の会計上の複雑さを解決するためである。他の条項では、本ASUにおける改訂は、変換可能ツールに対する発行者の会計処理に関する指導意見と、より少ない変換特徴が単独で認められるように、株式権証のような独立したツールのより少ない独立したツールについての責任処理が必要となるように、エンティティ自己株契約の派生ツール範囲の例外に関する指導意見を著しく変更する。より具体的には、ASUは、変換可能ツールを計算するために使用可能なモデルを5種類から3種類に減少させ、変換可能ツールの希釈1株当たり収益計算を修正し、実体自己の株式決済の契約で株式に分類される可能性のある要求を修正し、透明性を向上させるための開示を拡大することを要求する。これらの改正案は2024年1月1日から会社に施行され、修正案の早期採用が許可される。当社は現在ASU 2020-06を用いた総合財務諸表への影響を評価していますが、当社の総合財務諸表に大きな影響を与えないと予想されています。
2022年6月、FASBはASU 2022-03を発表した公正価値計量(主題820): 契約販売制限下における持分証券の公正価値計量それは.今回の会計基準の更新は、第820テーマ“公正価値計量”の中で持分証券の売却が禁止されている契約制限を受けた株式証券の公正価値の計量に関する指導を明らかにし、このような持分証券に新たな開示要求を導入するためである。これらの改正案は2024年1月1日から会社に施行され、修正案の早期採用が許可される。当社は現在ASU 2020−03を採用した総合財務諸表への影響を評価しているが、当社の総合財務諸表に大きな影響を与えないと予想される。
2023年12月、FASBはASU 2023-09を発表所得税(主題740)-所得税開示の改善今回の会計基準の更新は、所得税開示の透明性と意思決定の有用性を向上させるためである。ASUは、公共企業エンティティが毎年(1)税率調整において特定のカテゴリを開示することを要求し、(2)定量化しきい値に達した調整項目に追加情報を提供する(これらの調整項目の影響が税前収入(または損失)に適用される法定所得税税率を乗じて計算された金額の5%以上である場合)。また、毎年、以下の納付済み所得税に関する情報を開示することを要求している:1.連邦(国)、州および外国税に区分された納付済み所得税金額(払い戻しを差し引いた)2.納付された所得税(払い戻しを受けた純額を差し引いた)が、納付済み所得税総額(還付を受けた純額)の5%以上の各管轄区域に分割された納付済み所得税金額(還付を受けた純額)以上である。また、1.国内と海外に分類された所得税前持続経営収入(または損失)2.連邦(国)、州および海外に分類された持続経営所得税支出(または収益)の開示を要求する。ASUはいくつかの現在の開示要求事項をキャンセルした。これらの開示要求は、2025年1月1日から会社に対して施行され、修正案の早期採用が許可される。同社は現在、ASU 2023-09を採用した総合財務諸表開示への影響を評価している。
注4.取引記録リスクと不確実性
同社は、現金を生成してその経営、投資、融資活動に資金を提供する能力に基づいて流動性を評価している。同社の2024年以降の現金需要には、その製品の持続的な開発と臨床評価に関する費用、製造·供給コスト、規制出願費用、特許訴訟費用および訴訟費用、その製品の商業化に関する費用、および規制の高い業界で運営されている上場企業の要求に応じた費用が含まれている。2023年12月31日現在、同社は23,872現金と現金等価物。
その会社は純損失の歴史を経験した。同社の累計損失総額は1ドルである319,0772023年12月31日まで。純損失と累積損失部分は、商業化許可と独自製品販売の毛利(SympazanとAssertioが許可合意に達する前)、許可費、商業許可側と共同開発側からのマイルストーンと特許使用料によって相殺される。会社の資金需要は、現金および現金等価物、ならびに既存の持分および債務発行によって満たされている13.5%備考。
同社は2020年11月にATM施設の使用を開始した。設立から2023年12月31日まで会社が販売する15,300,298普通株から発生する現金純収益は約48,703手数料とその他の取引コストを差し引く2,555それは.当社は2023年12月31日まで販売しております4,958,341純利益約$の株を提供する8,962手数料と他の取引費用を差し引いて#ドル502それは.このATM施設には約$があります23,9522023年12月31日に発売される
企業の業務目標の実行や長期収益性の実現は保証されていないが、企業の持続的な業務、既存の現金および現金等価物、費用管理活動は、研究開発活動の停止や、そのATMを介して株式資本市場に参入する機会を含むが、これらに限定されない(付記23参照), 後続事件)リンカーンパーク買収協定によると、会社はその業務戦略を継続するため、少なくとも今後12ヶ月の運営需要を満たすために、会社に短期流動資金を提供する。
注5 収入と貿易売掛金の純額
同社の収入には以下の内容が含まれている
| | | | | | | | | | | |
| | 十二月三十一日までの年度 |
| | 2023 | | 2022 |
| 製造と供給収入 | $ | 43,805 | | | $ | 36,378 | |
| ライセンスと特許使用料収入 | 5,376 | | | 2,351 | |
| 共同開発と研究費 | 1,402 | | | 1,293 | |
| 専有製品販売,純額 | — | | | 7,658 | |
| 収入.収入 | $ | 50,583 | | | $ | 47,680 | |
収入の分類
次の表は、地理的地域別の純収入を提供します
| | | | | | | | | | | |
| | 十二月三十一日までの年度 |
| | 2023 | | 2022 |
| アメリカです | $ | 37,104 | | | $ | 40,792 | |
| 元アメリカ | 13,479 | | | 6,888 | |
| 収入.収入 | $ | 50,583 | | | $ | 47,680 | |
貿易およびその他の売掛金純額は以下の各項目からなる
| | | | | | | | | | | |
| | 十二月三十一日 |
| | 2023 | | 2022 |
| 売掛金 | $ | 5,570 | | | $ | 3,274 | |
| 契約その他売掛金 | 2,915 | | | 2,139 | |
| マイナス:不良債権準備 | (14) | | | (40) | |
| 差し引く:販売に関する手当 | — | | | (669) | |
| 貿易その他売掛金純額 | $ | 8,471 | | | $ | 4,704 | |
契約書とその他の売掛金総額は#ドルです2,915そして$2,1392023年12月31日現在、2023年12月31日現在、2022年12月31日現在、主に契約資産とその他の売掛金が含まれています。契約資産には、特定の契約に従って利益プロセスを満たした顧客に提供される製品およびサービスが含まれる。2022年12月31日までの販売関連手当は、会社が2022年10月にAssertioとライセンス契約を締結する前にSympazanの販売確認のための収入に関係していると推定される。詳細についてはご参照ください 注6実質的な合意。
次の表に不良債権準備の変動状況を示す
| | | | | | | | | | | |
| 十二月三十一日 |
| | 2023 | | 2022 |
| 期初不良債権準備 | $ | 40 | | | $ | 40 | |
手当料(減額) | (26) | | | — | |
| 免税額の減記を計上する | — | | | — | |
| 期末不良債権準備 | $ | 14 | | | $ | 40 | |
不良債権は#ドルに用意されている14そして$402023年12月31日まで、2023年、2022年までの毎年#ドル減少した26至れり尽くせりE 2023年12月31日終了年度の不良債権準備。2022年12月31日までの年度は増加や減記されていない
以下の表に販売関連免税額の変化を示す
| | | | | | | | | | | |
| | 十二月三十一日 |
| | 2023 | | 2022 |
期初残高 | $ | 669 | | | $ | 605 | |
| 2022年の販売に関する準備 | — | | | 1,365 | |
| 信用と支払い | (87) | | | (1,301) | |
| 再分類する | $ | (582) | | | $ | — | |
期末残高 | $ | — | | | $ | 669 | |
販売に関する手当や課税項目から減少した製品販売総額は#ドルであった0Sympazanの許可のため、2023年12月31日までの1年間。返品手当と即時賃金割引の課税項目は,流動負債である貿易売掛金と卸サービス料,共同支払い償還やリベートを支援する課税項目の直接減少に反映される。これらの準備金に関する未払い残高は、貿易や他の受取金、純額、計上費用に含まれています0そして$645それぞれ2023年12月31日までとドル669そして$1,012それぞれ2022年12月31日まで。付記13を参照費用を計算する。
大顧客集中度
純収入が当期総収入の10%を超えた場合、または売掛金残高が売掛金総額の10%を超えた場合、顧客は主要顧客とみなされる。2023年12月31日までの年度、Indivor代表約80総収入の%を占める。2023年12月31日までIndivorとZevra治療会社の代表は65%和13貿易総額とその他の売掛金の%をそれぞれ占めています。2022年12月31日までの年度、Indivor代表約76総収入の%を占める。2022年12月31日までIndior代表80貿易と他の売掛金総額のパーセントを占めている。
注6.取引記録材料協定
個人との商業開発協定
2000年8月,当社はReckitt Benckier PharmPharmticals,Inc.と個人許可協定(その後改訂)を締結し,後者はその後Indiorが権益を継承した。Indiorライセンス契約によると、当社は米国内と海外でSuboxoneに対するIndiorの独占的な製造と供給の要求に同意し、Suboxoneは舌下膜製剤である。
Indiorライセンス契約の条項によると、当社は現在の良好な製造実践基準および当社がIndiorと締結した関連品質協定に規定されている仕様とプロセスに従ってSuboxoneを生産しなければなりません。また,同社はSuboxoneを製造するための原料薬をIndiorから直接入手しなければならない。Indiorライセンスプロトコルは,会社が記入義務のあるSuboxoneの最低年度敷居数を規定し,Indiorに年間別の指定時間でその需要予測を会社に提供することを求めている。個人許可協定は、2025年1月1日までに、個人支払いで合意された単位当たり購入価格を定め、その後合意された価格指数の変化に応じて年次調整を行うこととしている。Indiorは,提供されたSuboxoneの購入価格に加えて,純売上高(Indiorライセンス契約での規定)に関連するいくつかの桁数パーセント印税を米国以外の地域で支払う必要があり,年間最高額や関連特許有効期限の制限を受ける
個人ライセンス契約には、破産または会社解散の申請、Suboxone周囲の知的財産権の無効、およびいずれか一方が個人ライセンス契約に重大に違反する行為を含む慣用的な契約終了条項が含まれる。さらに、FDAまたは他の適用可能な規制機関が、会社の製造場所がSuboxoneまたはSuboxoneの生産にもはや適していないと発表した場合、IndiorはIndior許可プロトコルを終了することができる。“個人許可協定”の初期条項は7年になる発効日から施行される。その後、“個人ライセンス契約”は自動的に更新されます1つは-年周期。
2023年3月2日から、会社と個人が個人許可協定の個人修正案を締結した。“個別人修正案”を締結する主な目的は,“協定”を改正することであり,(1)“協定”の期限を2026年8月16日に延長し,その後連続を規定することである1年個別ライセンス契約に含まれる製品特許の最終期間が満了した後、(Ii)個別ライセンス契約項の下で提供される製品の定価及び支払条項の譲渡に同意することを除いて、個別ライセンス契約がその時点の既存期間の満了前に少なくとも12ヶ月前に当社に通知を提出しない限り、独立許可の意向が継続されないことを表明しなければ、合意は自動的に継続されない。双方の合意を考慮して、会社は#ドルの支払いを受けた11,482個人からのもので金額は$です5,482表示:(A)2022年の価格上昇のうち以前に支払われなかった部分を支払う;(B)2023年に何らかの価格上昇の費用を支払うと推定される。2023年12月31日までにドル5,482価格上昇は製造と供給収入とドルで十分に確認された6,000利息収入とその他の収入、総合経営報告書、全面赤字純額を計上する
個人と締結した補足協定
2017年9月24日、当社はIndiorとIndior補足協定を締結しました。“個別人補充協定”によれば、会社はSuboxone製品に関連する様々な行われている特許法執行行動および紛争に関するすべての既存および将来の権利をIndiorに渡す。同社はまた、InDior許可の非特許ブプレノルフィン製品がInDiorまたはAqutiveとは無関係な当事者によって生産および販売できるように、製造およびマーケティング能力を再許可する権利をInDiorに伝えた。“個人補充協定”によると、“個人補充協定”の日から2023年1月1日まで、当社は個人から何らかの金を受け取る権利がある。一度支払われると、“個人補充協定”によって支払われたすべての金額は返金されません。2019年2月20日現在、Reddy博士実験室とAlvogenの競争模倣薬のリスク発表日までに、同社は全部で受け取りました40,750“個人補充協定”によって個人から獲得される。個人補充協定の下でのさらなる支払いは#年の判決まで一時停止される
関連特許侵害訴訟は既に解決された.個別者補充協定によると、当社はこれ以上何の支払いも受けません。付記22を参照事件があったりもっと詳細を知っています。
個別者補充協議によれば、個別者が当社に支払うすべての金は、代替ではなく、個別人許可協定に基づいて会社に不足しているいかなる金の補充である
Sunovion製薬会社と締結された許可協定。
2016年4月1日、当社はSunovion PharmPharmticals,Inc.によって買収されたCynapsus Treateutics Inc.(後にSunovion Pharmticals,Inc.によって買収された)とSunovion許可協定と呼ばれる許可協定を締結し、この協定に基づいて、Sunovionは、パーキンソン病患者の非発作の治療のための既存および将来の特許および特許出願を含むいくつかの知的財産権のグローバル独占許可(分許可を有する権利)を取得し、アポモルフィンを含むすべての口腔フィルムをカバーした。Sunovionはこの知的財産権を利用してそのアポモルフィン製品KYNMOBIを開発し,2020年5月21日にFDAの承認を得た。この承認は#ドルを送金するというSunovionの義務をトリガする4,000(A)製品が米国薬局で発売された最初の日、または(B)FDAが製品を承認した6ヶ月以内。この金額は2020年9月30日に受信され、2020年12月31日までの12ヶ月の許可と特許使用料収入に含まれています。
当社は2020年3月16日から“Sunovionライセンス契約第1改正案”を締結した。改正の主な目的は、Sunovionライセンス協定に規定されている第3のマイルストーンの義務の支払いをトリガする条件の満足度を決定するために、連合王国および現在欧州連合(EU)に存在する他の任意の国を含む、Sunovionライセンス協定に規定されている第3のマイルストーンの義務の支払いをトリガする条件の満足度を決定することであり、(Ii)Sunovionが便利にSunovionライセンス契約を終了する権利を有する日を2024年12月31日から2028年3月31日に延長し、(Iii)改正Sunovionが当社に支払うべき最初の最低年間使用料の発効日を1月1日から開始する。(Iv)KYNMOBIが2020年1月1日までに商業化された場合にSunovionライセンス契約を終了する権利を反映するために、終了条項を修正する。本Sunovionライセンスプロトコルは,Sunovionライセンスプロトコル修正案による終了条項が終了するまで有効である.Sunovionライセンスプロトコルは,プロトコルに含まれる終了条項に従って早期に終了しない限り,すべての適用可能なライセンス特許が満了するまで有効(国/地域ベース)継続する.Sunovionライセンス契約を終了した後,Sunovionの開発と商業化を付与したアポモルフィン製品のすべての知的財産権は当社が所有する。
二零二年十月二十三日に、当社は、Sunovionライセンス協定内のいくつかの条項に関する契約者の合意、特にSunovionライセンス契約の終了日、及びSunovionライセンス契約がカバーする当社特許の起訴及び維持に関する双方の権利及び義務を明確にするためにSunovionライセンス契約を改訂した。
Sunovionライセンス契約によりSunovionを付与する権利を考慮すると,当社が受信した支払い総額は$である22,000今までです。前払いの$を除いて5,000同社は合計$も稼いでいます17,000米国と欧州の具体的な規制と発展のマイルストーン(“予備マイルストーン支払い”)については、これまでにすべて受け取っている。二零二年十一月三日にKYNMOBIに関する貨幣化協定(以下定義を参照)を締結した後、当社はSunovionライセンス契約の下のいかなる金も再請求する権利がありません。
マラソン会社と締結した購入契約
2020年11月3日、会社はマラソン会社と貨幣化協定を締結した。金銭化協定の条項によると、同社は、Sunovionライセンス契約の下でSunovionのアポモルフィン製品KYNMOBIに関連する特許使用料およびマイルストーン支払いを徴収するすべての契約権利をマラソンに売却した。これらの権利を売る交換として、同社はマラソン会社から#ドルの前金を受け取った40,000追加の支払い$10,000最初のマイルストーンを実現することで当社が受け取った総金額は#ドルです50,000貨幣化協定によると、2023年12月31日まで。
貨幣化協定によると、最高$の追加または支払いがあります75,000規定された時間内に世界的な特許使用料および他のビジネス目標を達成する可能性がある場合は、その会社に支払わなければなりません。これは、潜在的な総収益を$とする可能性があります125,000それは.2023年6月、SunovionはKYNMOBIを米国およびカナダ市場から自発的に撤退させたと発表したため、金銭化協定によると、会社は追加的な支払いや支払いを受けない可能性が高い。付記16を参照将来の収入を売る貨幣化協定に関する会計処理のさらなる詳細。
Zevra Treateutics,Inc.(前身はKemPharm)とCLAのプロトコルを終了する
二零一二年三月、当社はZevraと契約を結び、当社とZevraが二零一一年四月に締結した協力及び許可協定を終了しました。この終了スケジュールによれば、当社は、ZevraがKP-415およびKP-484化合物またはその誘導体の商業化または任意の他の金銭化から得られる任意およびすべての価値に参加する権利がある。これらの金銭化取引には、Zevraとの協力、特許権使用料手配、またはZevraがこれらの化合物またはその派生商品から価値を達成する可能性のある他の取引に関連する任意のビジネス統合が含まれる。年末までに年度を終える2023年12月31日、当社は確認しました$1,500Zevraの記念碑的な収入として。
ハイスコとの筋萎縮性側索硬化症の治療(リルゾール口腔薬膜)の中国における許可と供給協定
当社はHaisco協定を締結し,これにより,Aquictiveは深セン証券取引所に上場している中国会社Haiscoに独占許可を付与し,中国筋萎縮性側索硬化症の開発および商業化を目的とした愛士康(リルゾール口腔膜剤)を開発·商業化した。ハイスコ協定の条項によると、エクソンはエクソンモービルの中国における独占メーカーとサプライヤーとなる。改訂されたハイスコ協定によると、同社は#ドルを受け取った7,0002022年9月に現金を前払いし、監督管理マイルストーン支払いと中国Exservanの純売上高の2桁の特許権使用料を獲得し、中国Exservanを販売する際に製造収入を稼ぐ
一部の人員の給与手配
2022年5月17日、当社は元総裁で当社のキース·J·ケンデル最高経営責任者が2022年5月17日から当社および当社取締役会(“終了合意”)を離れると発表した。ケンデル·さんは、彼の退職について、2022年5月17日に日付を尋ねる契約を含む退職契約を当社と締結しました。ケンデル·さんは、退職契約に基づき、2022年5月17日に当社への雇用を終了しました。退職協定によると、さんKendallは、(1)現金による支払い、終了日までの未払いの基本給と、2022年までの例年の未払いとの合計からなる、Kendallさんによる当時の恒例の解除請求を条件に、(2)現金による支払いは、比例計算の対象となるボーナスの一部を含め、金額は#ドルとなっている280(3)現金で支払い、金額は#ドル150代表、代表90ケンデル·さんの代わりに雇用契約に定められた通知期間に対する基給日数;(4)現金支払#ドルを含む散財料263これは最初の三つケンデルさんの月賦18-雇用契約に基づいて取得する権利のある月解散料;(B)毎月解散料#ドル53終了日後最初の月から7ヶ月目まで毎月;(C)$70(D)毎月の解散料$#88終了日後9ヶ月目から18ヶ月目まで、(V)帰属していない未帰属持分奨励の付与を加速し、各奨励の規定期間内にも選択権を行使することができ、および(Vi)引き続き自社の団体健康と生命保険計画を保証し、保険レベル及び条項及び条件は、状況が類似している幹部に提供されるのと同じであり、期限は18何ヶ月になりますか。別居契約の条項によると、Kendallさんは、移行サービス、戦略計画、財務計画、M&A相談、別居の日から2022年12月31日まで、必要に応じて当社のコンサルタントを務めます。これらのサービスについて、ケンデルさんは#ドルの相談料を請求しています10毎月です。ケンデル·さんに関する義務は、2023年12月31日までにすべて完了しました。
Atnahs Pharma UK Limitedとのライセンスと供給契約
当社は2022年9月26日に発効したPharmanoviaプロトコルを締結し,この合意に基づき,当社はPharmanoviaプロトコル期間中にLibervant(安定)口腔薬膜を開発および商業化し,領土内の全年齢の長期または急性,けいれん発作の治療に使用するために,当社にいくつかの知的財産権の独占ライセンスを付与した。Pharmanoviaプロトコルによると、Pharmanoviaはこの領土でのLibervantの管理と商業化活動をリードし、同社はLibervantのこの領土での独占的なメーカーとサプライヤーとなる。Pharmanovia協定によると、会社は#ドルを受け取った3,500Pharmanoviaプロトコルに規定されているいくつかの条件が合意され、発生した場合、Pharmanoviaプロトコルは、追加のマイルストーン支払いおよび利益シェア、およびPharmanoviaプロトコルによって満了した製造費および特許使用料を得る。
同社は2023年3月27日からPharmanovia協定を改訂し,Libervantの許可地域範囲を米国,カナダ,中国を含まない世界の他の地域に拡大した。Pharmanovia修正案によると、Pharmanoviaは拡大された地域(ラテンアメリカ、アフリカ、アジア太平洋地域を含む)で適用される規制承認を求める責任がある。“Pharmanovia修正案”の条項によると、同社は払戻できない金#ドルを受け取った2,000PharmanoviaからのPharmanovia修正案の施行に関する事件。
Assertio Holdings,Inc.と締結されたライセンス契約
2022年10月26日から、同社はAssertio協定を締結し、Sympazan(クロロバザン)口腔薬膜を2歳以上の患者のLennox-Gastaut症候群に関連するてんかん発作の補助治療に許可した。Assertio協定の条項によると、会社はUsertioライセンス契約期間内にUsertioにSympazan知的財産権のグローバル独占許可を付与し、前金は#ドルである9,000それは.さらにAqutiveは$を受け取りました6,000Aqutiveに会社特許出願米国通し番号16/561,573の許可通知を受けたマイルストーン支払いは、会社が関連する手当費用を支払う。会社は2022年10月27日にPTOの手当通知を受け、関連手当費用を支払った。また,Assertioプロトコルにより,会社はUsertioからUsertioがUsertioプロトコルにより満期になった製品の特許権使用料を取得する.当社はまた、SympazanについてAssertioと長期供給協定を締結し、この協定によると、当社は同製品の世界的な独占メーカーとサプライヤーであり、その供給契約の満了後にUsertioからその製品の製造費を取得する。
注7.取引記録金融商品--公正価値計測
特定の資産と負債は公正な価値で経常的な原則に従って報告される。公正価値は、計量日市場参加者間の秩序ある取引において、資産または負債が元金または最も有利な市場で負債を移転するために徴収または支払いされる交換価格として定義される。公正価値を計量するための評価技術は、観察可能な投入を最大限に使用し、観察不可能な投入を最大限に減少させなければならない。公正価値で入金された金融資産と負債は、公正価値レベルの以下の3つのレベルのうちの1つで分類され、開示されるべきであり、最初の2つのレベルは観察可能であり、最後の1つは観察不可能であると考えられる
•レベル1-アクティブ市場における同じ資産または負債の観察可能な見積もり。
•第2段階で観察される価格は,活発な市場オファーがないことに基づいているが,市場データに実証された投入が得られている。
•第三レベル-市場活動は、定価モデル、割引キャッシュフロー、方法、および類似技術のような市場活動支援の観察不可能な投入が少ないか、または全くない。
貸借対照表に記載されている貿易及びその他の売掛金、前払い及びその他の流動資産、売掛金及び売掛金及び繰延収入の帳簿金額は、当該等の資産及び負債の短期満期日に計算し、その公正価値と同等である。
当社は2020年および2019年にそれぞれ債務返済および債務再融資についていくつかの手形所持者に株式承認証を授与する。この等株式証は第3級投入に基づいて評価を行い、その公正価値は主に授与日までに作成した独立第三者評価に基づいており、この評価は普遍的に受け入れられている専門評価実務統一標準、アメリカ評価士協会とアメリカ公認会計士協会の会計と評価ガイドラインを補償として発行したプライベート持株会社の株式証券の推定方法に符合する。付記15を参照株式承認証このような株式承認証に関する更なる情報を得るために。
その会社の12.5%高級担保手形は、買い戻し要約またはコールバックオプションを含み、オプション所有者に権利を付与するが、会社に償還を要求する義務はない12.5%は、金銭化プロトコルによって生成されたマイルストーン支払いの上限部分に注目します。この承認オプションは第3級投入に基づいて評価を行い、その公正価値は主に独立した第三者評価に基づいており、この評価は専門評価実務統一標準、アメリカ評価士協会とアメリカ公認会計士協会の会計と評価ガイドラインの普遍的に受け入れられた評価方法に符合する。付記14を参照長期債務さらなる議論に供する。
2022年6月、同社は最も多く購入するための予資権証を発行した4,000,000普通株式と普通株式株式承認証株式は最大で購入できます8,850,000特定の購入者の証券購入協定に関連する普通株。これらの株式承認証は第3級投入に基づいて評価を行い、その公正価値は主に許可日までに作成した独立第三者評価に基づいており、この評価は“統一専門評価実務標準”、アメリカ評価士協会とアメリカ公認会計士協会の会計と評価ガイドラインの普遍的に受け入れられた評価方法に符合する。付記15を参照株式承認証このような株式承認証に関する更なる情報を得るために。
2023年8月1日に、当社は余剰株式証明書の行使保有者と書面協議を締結した5,000,000普通株の株です。通信契約により、行権所有者及び当社同意行権所有者は、既存株式承認証関連普通株式のすべての既存引受権証を行使し、価格は$とする0.961株当たりの普通株、すなわち既存の引受権証の現在の行権価格である。通信契約に基づき,当社は既存の引受権証を行使する権利行使所有者の代償として,引受権証を行使する行使保有者に新規株式承認証を発行し,合弁を購入する2,750,000新株式証株式価格は$2.60一株ずつです。この等株式証は第3級投入に基づいて評価を行い、その公正価値は主に授出日に行った独立第三者評価に基づいており、この評価は普遍的に受け入れられている統一標準推定方法と一致する
専門評価実践、アメリカ評価士協会とアメリカ公認会計士協会の会計と評価ガイドライン。付記15を参照株式承認証このような株式承認証に関する更なる情報を得るために。
2023年11月1日リリースについて13.5%手形、当社と手形所有者が2023年11月1日に締結した特許権使用料契約は、手形所有者に提供します
a.両国間の等級別印税1.0%和2.0しばらくの間アレルギー(アドレナリン)舌下錠の全世界の純売上高のパーセント8年アレルギーの世界初の販売から始めました
b.両国間の等級別印税1.0%から2.0(1)アレルギーの初回販売と(2)までのLibervant(安定)口腔薬膜の全世界年間純売上高のパーセンテージ8年Libervantを初めて販売することから始めます
これらの特許権使用料協定は第三級投入に基づいて評価を行い、その公正価値は主に第三者データに基づいて制定した内部管理層の推定に基づいて、管理層の判断、現在の市場状況と予測を反映する。特許権使用料プロトコルの初期公正価値計測は,割引率,推定成功確率,推定アレルギー剤とLibervantの将来の売上を含む重大な観察不可能な投入に基づいて決定された。付記14を参照長期債務さらなる議論に供する。
注8.調査結果在庫、純額
在庫には以下の内容が含まれている
| | | | | | | | | | | |
| | 十二月三十一日 |
| | 2023 | | 2022 |
| 原材料.原材料 | $ | 2,118 | | | $ | 1,899 | |
| 包装材 | 3,028 | | | 2,914 | |
| 完成品 | 1,623 | | | 967 | |
| 総在庫 | $ | 6,769 | | | $ | 5,780 | |
注9 財産と設備、純額
| | | | | | | | | | | | | | | | | | | | | | | |
| | | | | | 十二月三十一日 |
| 有用な寿命 | | 2023 | | 2022 |
| 機械設備 | 3 | - | 15年.年 | | $ | 20,248 | | | $ | 19,810 | |
| 家具と固定装置 | 3 | - | 15年.年 | | 769 | | | 769 | |
| 賃借権改善 | (a) | | 21,386 | | | 21,375 | |
| コンピュータ、ネットワーク装置、ソフトウェア | 3 | - | 7年.年 | | 2,627 | | | 2,627 | |
| 建設中の工事 | | | | | 2,033 | | | 1,467 | |
| | | | | | 47,063 | | | 46,048 | |
| 減算:減価償却累計と償却 | | | | | (42,884) | | | (41,963) | |
| 財産と設備の合計 | | | | | $ | 4,179 | | | $ | 4,085 | |
(a)レンタル改善は、レンタル期間またはその推定耐用年数の短い時間で償却されます。
財産や設備に関する減価償却と償却総額は#ドルである1,153そして$2,2702023年12月31日まで,2023年12月31日と2022年12月31日までである。2023年12月31日まで、当社は確認しました216管理部門が使用しなくなったと評価された建設工事口座に保有している資産を減値する。このような減価費用は製造と供給費合併経営報告書と全面赤字に関する検討違います。2022年12月31日までの減価赤字が確認された。
注10.調査結果使用権資産と賃貸義務
同社は、生産·倉庫施設、会社本部、商業化運営センター、研究·実験室施設として使用されているすべての不動産をレンタルしている。これらはすべて違います三つリースには、ASC 842に規定されている特性、すなわち融資リースのリースに分類される必要があるため、これらのリースが経営リースに計上される。改訂されたこれらのレンタル契約は、次の条項を提供します4.25年和9.80年数には,リース期間の延長が期待される継続期間選択権が含まれる。詳細については、第2部、属性を参照されたい。
当社は2023年12月31日までに,その製造施設を支援するリースを融資リースと確認した。融資リース項目の下での負担は重大ではなく、総合貸借対照表上の物件及び設備、純額、支払手形、流動及び支払手形の純額に計上されている。
当社は、その総合貸借対照表における期間が12ヶ月以下である短期賃貸の資産及びリース負債使用権を認めない。当社の総合貸借対照表で確認された比較的長期賃貸手配については、使用権資産と賃貸負債は、最初にリース満期の賃貸支払いの現在値に基づいて開始日に計量される。これらの支払いは、この手配によって満期になった固定レンタルと固定非レンタル部分の組み合わせです。当社の短期賃貸に関するコストや、当社の賃貸手配に関する変動コストは、総合財務業績にとって重要ではありません。
当社の賃貸手配の隠れた金利は一般的に決定しにくいため、当社は逓増借款金利を採用しており、この増加借入金金利は賃貸開始日の資料に基づいて決定され、手配によって満期になった賃貸支払いの現在値を決定する。経営リース負債の計量が反映した推定割引率の範囲は14.8%から15.6%は、会社担保債務再融資で経験された漸増借入金金利に基づいて、予想継続期間を含む最低賃貸支払いに適用されます
同社のリースコストは、その総合経営報告書と全面赤字報告書に製造と供給、研究開発と販売、一般と行政費用を計上している。2023年12月31日と2022年12月31日までの年間運営リース費用総額は1億ドル1,745そして$1,753公共エリアのメンテナンスと業務費用のような可変レンタル費用がそれぞれ含まれています#ドル447そして$449それぞれ,である.当社のレンタル手配による現金支払いは、その総合キャッシュフロー表に経営活動の流出に反映されています。
同社がその経営賃貸契約に基づいて支払うべき金額は以下の通り
| | | | | |
| 金額 |
| 2024 | $ | 1,230 | |
| 2025 | 1,266 | |
| 2026 | 1,300 | |
| 2027 | 1,328 | |
| 2028 | 1,162 | |
| 2029-2033 | 3,828 | |
| 賃貸支払総額 | 10,114 | |
| 差し引く:推定利息 | (4,306) | |
| リース負債総額を経営する | $ | 5,808 | |
注11.取引記録無形資産、純額
次の表は識別可能な無形資産の構成要素を提供し、これらのすべての資産は有限寿命である。
| | | | | | | | | | | |
| | 十二月三十一日 |
| | 2023 | | 2022 |
| 購入無形資産 | $ | 3,858 | | | $ | 3,858 | |
| 購入した特許 | 509 | | | 509 | |
| 4,367 | | | 4,367 | |
| 差し引く:累計償却 | (3,089) | | | (2,932) | |
| 無形資産、純額 | 1,278 | | | 1,435 | |
償却費用を$とする157そして$1162023年12月31日まで、2023年12月31日、2022年12月31日までの毎年。購入した無形資産の残存寿命では,年間償却費用は#ドルと見積もられている1572024年以降の年度まで
2023年12月31日現在、すべての償却無形資産の残り加重平均年限は8.1何年もです。
12月31日までの財政年度ごとの推定償却費用総額は以下の通り
| | | | | |
| 金額 |
| 2024 | $ | 157 | |
| 2025 | 157 | |
| 2026 | 157 | |
| 2027 | 157 | |
| 2028 | 157 | |
2029-2032 | 493 | |
償却費用総額を予想する | 1,278 | |
付記12.調査結果他の非流動資産
次の表は他の非流動資産の構成要素を提供します
| | | | | | | | | | | |
| 十二月三十一日 |
| | 2023 | | 2022 |
| 特許権使用料を徴収する | $ | 4,000 | | | $ | 5,000 | |
| 他にも | 1,438 | | | 1,451 | |
| その他非流動資産合計 | $ | 5,438 | | | $ | 6,451 | |
2020年第2四半期に、Sunovionライセンス契約により、会社は$を確認しました8,000特許権使用料収入及びそれに応じた受取特許権使用料、並びに8人 $1,000会社に支払う年間最低保証特許権使用料を払わなければなりません。貨幣化協定については、当社はASC 860に基づいて評価を行った接続と修理既存の入金がマラソン会社に移転したかどうかを確認し、移転していないと判断する。請求権使用料は含まれています5人Sunovionが支払わなければならない年間最低支払いは、最後の金額は2028年3月に満了しなければならない。受取特許使用料の現在の部分は貿易および他の入金純額に含まれています。付記16を参照. 将来の収入を売るこの売掛金が貨幣化プロトコル取引にどのように関連するかについてより多くの詳細がある。
注13. 費用を計算する
計算すべき費用には以下が含まれている
| | | | | | | | | | | |
| | 十二月三十一日 |
| | 2023 | | 2022 |
| 補償すべきである | $ | 4,202 | | | $ | 6,389 | |
| 不動産と個人財産税 | 337 | | | 322 | |
| 費用を計上する | 645 | | | 1,012 | |
支払利息 | 1,013 | | | 183 | |
| 他にも | 300 | | | 61 | |
| 費用総額を計算する | $ | 6,497 | | | $ | 7,967 | |
計上すべき賠償金の減少は,主に2023年12月31日終了年度の未払い費と計上手数料費用の支払いに関係している。支払利息が増加したのは13.52024年1月2日に満期となる優先債券の割合。
付記6を参照材料協定は一部の官僚との終了協定と、2022年12月31日までに補償に記録された関連解散費について検討する。付記14を参照長期債務は討論に供する13.5支払手形と関連利息の割合。
注14.調査結果長期債務
12.5高度保証手形の割合
2019年7月15日、当社はドルまでの指向性増発を完了しました100,000ITS元金合計12.52025年に満期になって株式承認証を発行して購入した債券の割合2,000,000普通株、1株$0.001一株当たりの額面。
基礎契約終了時に、同社は$を発行した70,000のです12.5%(“初期手形”)は、株式承認証および初回要件(“最初の要件”)と共に、二次取引に参加する手形所有者を付与します。初期手形および株式証明書の発行による純額は$66,082.
二零二年十一月三日、当社は米国銀行協会と最初の補充契約(“第一補充契約”を締結し、他のすべての後続補充契約及び基礎契約と共に総称して“契約”と呼ぶ)、基礎契約の受託者(“受託者”)及び付属代理人として、当社及び受託者の間で締結した。2020年11月20日付の2件目の補充契約により、同社は#ドルを返済した22,500その$で70,000卓越した12.5金銭化協定に基づいて受け取った前払い金の手形の割合。また、会社は手形所持者と追加購入契約を締結し、これにより会社は合計#ドルを発行した4,000の付加内容12.5%手形(“追加手形”)は、早期償還時に2人の手形所持者に前払い割増を支払う代わりに12.5以上検討した%備考。この二つの取引の結果,会社の純残高が減少した12.5未償還優先手形総額のパーセントから$51,5002020年12月31日現在、この元金総額は2022年12月31日まで返済されていない。これは1ドルです4,000元本発行は他の債券と同じ期限内に比例して償還されます12.5%備考。同社は手形所持者の1人に1ドルを支払いました2,250債務の早期返済による割増。
その会社は$を占めている22,500債務修正としての債務返済12.5%備考。手形所持者に支払う費用は(I)$を含む2,250保険料と(Ii)元を早納する4,000前払い罰金の代わりに追加手形を発行して、追加債務割引と記録されて、残りの時間内に償却します12.5有効利息法の%手形を使用します。ローン発行コストは#ドルです220追加チケットに関連した支出は生成された。既存の繰延割引とローン発行料12.5%手形は、実質金利法で改正債務の残り期間内の支払利息で償却を調整します。
最初の補充契約には,当社が貨幣化協定の任意の現金収益を受け取った場合,各手形所持者は,当社にその手形所持者の全部または一部の未返済金を償還することを要求する権利があるという条項が掲載されている12.5現金での買い戻し価格は112.5元金の%には、課税利息と未払い利息が加算されます。この買い戻しオファーの上限は302025年6月30日現在、会社が受け取ったマイルストーンとしての現金収益の割合(あれば)が実現している。推定研究は独立第三者評価士が行い、2022年12月31日に更新された。評価研究によると,下落オプションの推定値は#ドルである45他の非流動負債に計上されています埋め込みコールオプションはASC 815下のデリバティブとみなされる派生ツールおよびヘッジこれは,公正な価値記録にしたがって見込オプションを埋め込むことを要求するが,各報告期間ごとに再計量しなければならない.また、今回の取引完了時まで、当社は持株者に発行しました12.5購入可能引受権証の割合143,000会社普通株の株です。
2021年8月6日、第三補充契約により、12.5%は2021年12月31日から2022年6月30日に延長され、会社は会社の選択に応じてアクセスする権利があります$30,000のです12.5義歯の下で再び開いたメモの割合。
2022年5月13日、第五補充契約によると、12.5%手形は2022年6月30日から2023年3月31日にさらに延長され、会社は会社の選択に応じてアクセスすることができます$30,000のです12.5%は、Indentureに従ってチケットを再発行するが、米国でのLibervantの販売に対するFDAの完全な承認を得なければならず、完全に承認されたのは、米国におけるLibervantの市場アクセスを含む。同社は2023年3月31日までFDAの完全承認を得ていないため、再開口器の選択権を取得してその日に満了する。
二零二一年十月七日に、当社は第四期補充契約を締結し、この契約により、当社は12.5改訂後、初回元金支払日は2021年9月30日から2023年3月30日に延期された。第4期補充契約は変更されていない12.5%手形または満期利息支払義務12.5%備考。第四項補充契約については、当社は第四項補充契約所持者と同意費用書簡を締結する12.5%付記(“同意料金箱”)は、この手紙により、当社は12.5追加の現金支払い(“同意料”)に注意してください$2,700合計で、2022年5月15日から4四半期に分けて支払いを開始します。当社は2022年12月31日現在、支払うべき余剰同意費$を記録しています675支払手形としては,その総合貸借対照表上でフロー手形とする.このお金は2023年2月に支払われた。
♪the the the12.5%債券は宣言された固定金利を提供します12.5%、四半期ごとに借金を払って、最後に四半期ごとに元金を返済します12.52025年6月30日に満期になった債券の割合。同社は2022年12月31日現在、その総合貸借対照表に満期元本を支払手形、当期、支払手形純額と表記している。
当社は自己選択で償還することができます12.5いつでも次の範囲の保険料で支払われる手形の割合101.56前払い金が初期債券発行日の5周年当日または後に発生した場合、元金の未償還率を占める112.50%支払いが債券発行後3年目以内に発生した場合。契約には制御権を変更する条項も含まれており,これらの条項により,会社は償還を要求される可能性がある12.5%注釈が位置する101手形所持者の選挙では、余剰元金の%に利子を加算する。
協定に基づいて融資に担保を提供する12.5%手形には、企業のほぼすべての財産および資産(知的財産を含む)の第1優先留置権が含まれています。この担保債務は、会社のすべての既存および将来の二次債務よりも優先的な支払い権利を提供し、手形所有者に会社のほとんどの資産に対する完全な保証権益を提供する。
2022年11月4日と2022年12月16日、会社発表二つ2021年7月15日,当社は受託者及び担保代理人を管理する受託者及び担保代理人と契約による単独部分償還通知を発行した12.5%備考。各部分償還通知に基づいて,当社は持株者に与える12.5%注意:当社は$を償還する予定です3,765そして$1,882それぞれ未完成のものです12.5償還価格で計算される債券の割合は、管理に基づいて12.5%手形には、課税と未払いの利息と費用が加算されます。この部分的な償還はそれぞれ2023年1月と2月に発生する。同社は$も支払いました353事前清算債務による前払割増は、当社の総合経営報告書と全面赤字報告書に清算債務損失と弁済債務損失として反映されている。また、2023年の間に同社は三つ予定元金の支払総額は#ドルです11,463.
繰延債務発行コストと債務割引による償却費用12.52023年12月31日までと2022年12月31日までの%手形は$13そして$16それぞれ,である.未償却繰延債務発行コストと繰延債務割引12.5%コメント$0そして$27それぞれ2023年12月31日と2022年12月31日まで。
2023年11月1日、当社は発表しました13.5%手形を発行して得られた金で返済する12.5$の注釈率36,014未払い利息と償還料が含まれています。同社はこの取引を清算債務として入金し、債務返済費用#ドルを確認した1,0292023年12月31日までの年度。債務弁済費用は当社の総合経営報告書及び全面損失における清算債務損失に計上される。
13.5高度保証手形の割合
当社は2023年11月1日に、いくつかの機関投資家(“手形所持者”)と契約契約を結び、$を発行します45,000ITS元金総額13.52028年満期の債券の割合。会社が受け取った純収益は約#ドルだった4,326返済後のこの取引12.5%手形および債務割引控除、および債務発行コスト。
♪the the the13.5%債券は当社の優先保証債務であり、2028年11月1日に満期となります。♪the the the13.5債券金利は固定されており、金利は13.5年利%は、2023年12月30日から四半期ごとに支払い、2024年1月2日に1回目の利息を支払います。2026年6月30日からの支払日ごとに、当社は分割払いをお支払いいたします13.5%固定の償却スケジュールに従って発行されたチケット、および適用される脱退費用。キャンセル料総額は$2,000.
当社は自己選択で償還することができます13.5%全体または一部の注釈:
a.2025年11月1日までに償還すれば、償還価格は100元金の%に計算すべき利息と未払い利息を加え,適用される退場料を加え,適用される保険料を加え,両者の中で大きいものを基準とする
i.1.0元金の%を償還する
二、2025年11月1日に償還された元金の現在値に、その日に満期になった必要利息の額(あれば)を加え、国庫券金利に等しい割引率を用いて計算します100基点は、償還元金を超える金額である
b.償還が2025年11月1日以降に発生すれば、償還価格は108.50元金の%印加応算と未払い利息は、適用される払出料を印加する
もし会社が支配権変更が発生した場合、手形所持者は会社に現金で全部または一部を買い戻すことを要求することができます13.5変更時のチケットパーセント買い戻し価格を制御することは108.5%に加えて、余剰元金の脱退費用に加え、手形所持者が選挙時の応算利息を加算する
契約は、当社が何らかの条件を満たし続ける場合には、当社を含めて(合併に基づいて)少なくとも$を有することを許可する100,000最近完成した12ヶ月間の純収入は、資産ベースの借金手配は#ドルを超えてはいけない10,000(“ABL施設”)。ABLローンは在庫を構成する会社の資産、売掛金とその収益を担保にするしかありません
発表についての13.5%手形、当社と手形所有者が2023年11月1日に締結した特許権使用料協定は、手形所有者に提供します
a.両国間の等級別印税1.0%和2.0しばらくの間アレルギー(アドレナリン)舌下錠の全世界の純売上高のパーセント8年アレルギーの世界初の販売から始めました
b.両国間の等級別印税1.0%から2.0(1)アレルギーの初回販売と(2)までのLibervant(安定)口腔薬膜の全世界年間純売上高のパーセンテージ8年Libervantを初めて販売することから始めます
どちらも13.5%手形および特許使用料プロトコルは、互いに共同で発行された独立したチケットを表します。ASC 470の債務に分類されています債務その後、余剰コストに基づいて測定した。
特許権使用料プロトコルの初期公正価値計測は,割引率,推定成功確率,推定アレルギー剤とLibervantの将来の売上を含む重大な観察不可能な投入に基づいて決定された。これらの投入は,第三者データに基づいて作成した内部管理見積りを用いたものであり,管理職の判断,現在の市場状況,予測を反映している.
特許権使用料プロトコルの公正価値は、将来の販売に確率重み付けキャッシュフローを適用することによって推定され、その後、現在値に割引される。特許権使用料プロトコルの公正価値の変化は、上記の1つまたは複数の投入の変化によって生じる可能性がある。観察できない投入の大きな変化は、特許権使用料プロトコル負債の実質金利の大幅な増加または減少を招く可能性がある。2023年の残り時間内に、特許使用料合意負債を確認するための重大な観察不可能な投入に実質的な変化はない。
次の表は、2023年12月31日までに特許権使用料協定の初期公正価値計量に使用される重大な観察不可能投入をまとめたものである
| | | | | | | | | | | | | | | | | | | | | | | | | | | |
| 推定方法論 | | | | 観察できない重要な入力 | | 加重平均(範囲,適用すれば) |
| | | | | | | 割引率 | | 15% |
| 特許使用料協定 | 確率重み付け
収益法 | | | | | | 成功の確率 | | 75% |
| | | | | | | 支払年数を予想する | | 2025 | - | 2033 |
特許使用料協定は13.5%付記では、当社は、この2つの手形の相対的な公正価値に基づいて、その2つの手形に分配する。その会社は約$を割り当てた13,856特許権使用権協定。同社は、手配有効期間内にチケット所有者に支払われる推定将来の特許権使用料の現在値を計算することによって、割り当てられた公正価値を決定する。
将来推定される特許使用料の超過分#ドル56,926$を超える13,856分配公正価値の割引額は,特許権使用料プロトコルに関する割引であることを確認し,実際の利息法で償却して利息支出とする.このため、会社は特許使用料合意負債未償却部分の推定金利を算出し、約0.5%とした9.682023年12月31日まで。
割り当てられた額は#ドルです13,856出国費を加えて#ドルです2,000、原発割引$1,125債務発行コストは1ドルです3,517債務割引が$になります20,498それは.債務割引は年内に償却する13.5有効利息法の%手形を使用します。
割引による割増費用13.52023年12月31日までの年間手形および特許使用料協定パーセントは$833そして$905それぞれ,である
未償却割引合計$17,665上には13.5%備考および$42,1652023年12月31日までの印税義務。
長期手形と未償却債務割引残高は以下の通り
| | | | | | | | | | | |
| | 十二月三十一日 |
| | 2023 | | 2022 |
未償還手形総額 | $ | 45,000 | | | $ | 51,500 | |
キャンセル料を含めて割引を償却していません | (17,665) | | | (27) | |
| 長期債務の当期部分 | — | | | (18,025) | |
長期支払手形 | $ | 27,335 | | | $ | 33,448 | |
融資リース | 173 | | | — | |
支払手形,純額 | $ | 27,508 | | | $ | 33,448 | |
| | | | | | | | |
| | 十二月三十一日 |
| | 2023 | |
印税義務 | $ | 56,926 | | |
| 未償却割引 | (42,165) | | |
印税義務,純額 | $ | 14,761 | | |
の予定元金支払い13.52023年12月31日までの%注釈は以下の通り
| | | | | |
| 2024 | $ | — | |
| 2025 | — | |
| 2026 | 9,540 | |
| 2027 | 14,535 | |
| 2028 | 20,925 | |
| 合計する | $ | 45,000 | |
注15.取引記録株式承認証
以下の者に発行する引受権証12.5高度保証手形所持者率
初期手形(“初期株式承認証”)および追加手形(“追加株式承認証”)とともに発行された引受証は2025年6月30日に満期となり、手形所有者が最大購入権を持つようになる2,143,000普通株式は、特定の登録権を含む。経営陣は初期株式証明書の公正価値を#ドルと推定した6,800追加株式引受証は$です735いずれも独立した第三者評価士の評価に基づいている.各株式証明書の公正価値は債務割引とみなされ、各株式証明書の期限内に償却することができ、償却していないもの12.5以下の項目の元金総額を減らすための部分12.5%当社の総合貸借対照表に付記します。また、発行された初期株式承認証と追加株式承認証は株式承認証の償還を提供しないか、あるいは権利を所有者の制御下に置くため、これは当社に現金または他の資産を支払い、株式証明書の下の義務を履行することを要求する可能性があるが、“持分現金変動を制御する”場合は除外するため、株式承認証の公正価値は当社の総合貸借対照表中の追加実収資本に記載されている。2023年12月31日までの年度及び2022年12月31日までの年度内に、この等持分証は初期持分証及び追加持分証に関連するため、いかなる引受権証も行使されていない。株式証明書購入合算1,714,429行使価格$の普通株4.25そして$5.38適用することができます1,571,429株式引受証及び143,000それぞれ2023年12月31日と2022年12月31日まで、引受権証はまだ返済されていない。付記14を参照長期債務。
証券購入契約に基づいて発行された引受権証
2022年6月に、当社は証券購入契約についていくつかのバイヤーに予融資権証及び普通株式承認証を発行した。事前出資の引受証は購入者が最も多く購入する権利を持たせる4,000,000普通株および2022年12月31日までの年度内に普通株をすべて行使した。普通株式株式証は2027年6月8日に満期になり、購入者は最も多く購入する権利がある8,850,000普通株は、1ドルから1ドルまで様々です0.96$まで1.09一株ずつです。経営陣は事前資本権証と普通株式承認証の公正価値を#ドルと推定した5,874独立第三者評価士の評価に基づいている。事前資金承認株式証と普通株式承認株式証の公正価値は権益とされ、当社の総合貸借対照表に追加実収資本として登録されている。2023年6月14日3,689,452証券購入協定により発行された一般株式証はすでに行使されており,得られた金は約$である3,542.
2023年8月1日,当社は行権者と書面協議を締結した5,000,000残りの普通株式承認証。通信契約に基づき,行権者および当社は同意する
行使所有者は,既存の普通株式承認権証をすべて行使し,既存の引受権証の基礎とし,価格は$とする0.961株当たりの普通株、すなわち既存の引受権証の現在の行権価格である。通信契約に基づき,当社は既存の引受権証を行使する権利行使所有者の代償として,持分証を行使する行使保有者に新たな引受権証を発行して合弁を購入する2,750,000普通株株。新株式証明書は2024年2月2日以降に行使でき、2029年2月2日に満期となり、現金でしか発行できないが、新株式証関連普通株式が通信契約の条項に基づいて登録されていなければ例外であり、この場合、新株式証も当時“現金なし行使”の方式で全部或いは部分的に行使することができる。新株式証の行使価格は$である2.60一株ずつです。経営陣は株式証明書の公正価値を$と推定している4,671独立第三者評価士の評価に基づいている。新株式証の公正価値は権益とみなされ、会社の総合貸借対照表に追加として資本列報されている。
2023年8月2日5,000,000既存の引受権証の一部は、行権所有者と締結した証券購入協定に基づいて行使されており、当社が当該等株式証から得られる総収益は$である4,800それは.全体的に言えば8,689,452証券購入契約により発行された普通株式承認株式証では,収益は約$である8,3072023年12月31日まで年度内に行使する。その会社は$を生み出した35この取引と関係があります。
2023年12月31日まで、購入を除いて2,750,000上記普通株の株式は,未発行の普通株式承認証がまだ購入可能である160,548行使価格$の普通株1.09元証券購入契約の.
注16.取引記録将来の収入を売る
2020年11月3日、会社はマラソンと貨幣化協定を締結した。貨幣化協定の条項によると、当社はSunovion許可協定によるSunovionのアポモルフィン製品KYNMOBIに関する特許使用料とマイルストーン支払いを徴収するすべての契約権利を販売している。KYNMOBIはパーキンソン病患者の非発作の治療のためのアポモルフィン薄膜療法であり、2020年5月21日にFDAの承認を得た。このような権利を売る交換として、会社は前金#ドルを受け取った40,000追加の支払い$10,000最初のマイルストーンを実現することで当社が受け取った総金額は#ドルです50,000貨幣化協定によると、2023年12月31日まで。
貨幣化協定によると、最高$の追加または支払いがあります75,000規定された時間内に世界的な特許使用料および他のビジネス目標を達成する可能性がある場合は、その会社に支払わなければなりません。これは、潜在的な総収益を$とする可能性があります125,000.
同社は前払い収益#ドルを記録した40,000そして次の最初のマイルストーン$10,000$を減少させる2,909取引コストは、販売将来の収入に関する負債として、貨幣化プロトコルの有効期間内に実際の利息法を用いて償却する。未来の支払いを受けた場合、それらは将来の収入の売却に関連する負債残高を増加させるだろう。会社は特許権使用料とマイルストーンを得るすべての権利を売却しているにもかかわらず、これらの特許権使用料の発生に関する継続的な義務のため、会社はこれらの特許権使用料を収入として入金する。その義務は、知的財産権の維持と保護を含み、SunovionがSunovionライセンス契約に従って許可地域の1つ以上の司法管轄区域でSunovionライセンス契約を終了する場合には、マラソン会社のKYNMOBIの新しいライセンス契約の実行に協力することを含む。今回の取引で発生した会計負債および当該等の負債に関連するいかなる非現金支払利息支出も構成されておらず、いかなる支払義務や将来可能な現金使用も代表しない。
2020年第2四半期に、Sunovionライセンス契約により、会社は$を確認しました8,000特許権使用料収入及びそれに応じた受取特許権使用料、並びに1,000満期の年間最低保証特許権使用料。貨幣化プロトコルについては,会社はASC 860,譲渡·サービスに基づいて評価を行い,既存の入金がマラソンに移行しているかどうかを確認し,売掛金が移行していないと結論した
特許使用料がSunovionからマラソンに送金されるにつれて、受取特許権使用料の徴収と将来の収入販売に関する負債残高は合意有効期間内に有効に返済される。将来の収入の販売に関連する負債の償却を決定するために、会社は、貨幣化協定の有効期間内にマラソンに支払われる将来の特許権使用料およびマイルストーン支払い、ならびにマラソンが会社に支払うか、またはマイルストーン支払いの総額を推定する必要がある。将来の特許使用料支払いの合計から$を差し引く50,000受信した収益及び将来の又は支払があった場合は、貨幣化協定の有効期間内に利息支出として記入する。実行時には、この総利息支出の見積もりにより実際の年利率は約1%となる24.9%です。この推定には,実行時に記録された金額と貨幣化プロトコルの有効期限内に確認される利息支出に影響を与えるという大きな仮定が含まれている.同社は、マラソンへのSunovionの推定特許使用料とマイルストーン支払い、マラソンが会社に支払うかマイルストーン支払いを定期的に評価する。このような支払いの金額または時間が元の推定と大きく異なるように、利息支出を増加または減少させるための調整が予想されるように記録される。多くの要素がSunovionがマラソンに支払う特許使用料とマイルストーン費用の金額と時間、それに応じた利息支出に大きな影響を与える可能性がある
当社に記録されており、その大部分は当社のコントロール下にありません。これらの要因には、看護基準の変化、競争製品の発売、製造または他の遅延、模倣薬競争、知的財産権問題、政府衛生当局が製品の使用に制限を加える有害事象、マラソンに流入する特許使用料のドルで計算される外国為替レートの重大な変化、KYNMOBIの一部の基礎販売がドル以外の通貨で計算されること、および他の現在予測できない事件や状況が含まれるが、これらに限定されない。これらの要因のいずれかの変化は、将来の収入の売却に関連する特許権使用料収入および利息支出の増加または減少をもたらす可能性がある。2023年6月、SunovionはKYNMOBIを米国およびカナダ市場から自発的に撤退させたと発表したため、金銭化協定によると、会社は追加的な支払いや支払いを受けない可能性が高い。また、当社は2022年第4四半期に販売将来の収入に関する利息支出の記録を停止します。
次の表は、2023年12月31日までの年度の将来収入の売却に関する負債活動を示しています
| | | | | |
| |
将来の収入に関する負債の売却、2022年12月31日現在の純額 | $ | 65,259 | |
| 将来の収入の販売に関する特許使用料 | (989) | |
| 発行原価償却 | 220 | |
| 将来の収入の売却に関する利子支出 | — | |
将来の収入の売却に関する負債、純額(#ドルの当期部分を含む)922) | $ | 64,490 | |
注17.取引記録他の非流動負債
2023年12月31日現在、会社の他の非流動負債は#ドルのAROを含む2,016下落オプションの公正な価値があります12.5$の注釈率0それは.2022年12月31日現在、会社の他の非流動負債には#ドルのAROが含まれている1,989長期公正価値の部分を見ています12.5$の注釈率45それは.付記14を参照長期債務討論に供する12.5%備考。
AROSは、インディアナ州ボティチおよびニュージャージー州ウォーレンにある同社の施設を除去するいくつかのレンタル改善と、すべての施設を元の状態に戻すことに関する将来の推定支出を含む。ARO資産に関する減価償却費用は2023年12月31日現在と2022年12月31日現在の総減価償却費用を#ドルに計上している7そして$25それぞれ,である
以下に2023年12月31日と2022年12月31日までの年間会社のARO負債に対する活動スケジュールを示す
| | | | | |
| 2021年12月31日の残高 | $ | 1,712 | |
| 足し算 | 110 | |
| 吸引積 | 167 | |
| 2022年12月31日の残高 | 1,989 | |
| 足し算 | — | |
| 吸引積 | 27 | |
| 2023年12月31日の残高 | $ | 2,016 | |
備考18:001株当たり純損失
1株あたりの基本純損失の計算方法は,普通株の加重平均株式数を純損失で割ることである。
会社は2023年12月31日まで、2023年12月31日と2022年12月31日までの年度に純損失が発生したため、すべての未返済の潜在的希薄化ツールはこの期間の1株当たり計算に逆償却の影響を与えるしたがって,1株当たりの基本純損失と希釈後の1株当たり純損失は以下のすべての期間で同じである。
| | | | | | | | | | | |
| | 2023年12月31日までの年度 | | 2022年12月31日までの年度 |
| 分子: | | | |
| 純損失 | $ | (7,870) | | | $ | (54,410) | |
| 分母: | | | |
| 加重-普通株式平均-基本普通株式と希釈普通株 | 61,255,864 | | | 48,734,377 | |
| 普通株1株当たりの損失--基本損失と赤字 | $ | (0.13) | | | $ | (1.12) | |
(a)2023年12月31日まで、2022年12月31日まで5,733,064そして6,027,997普通株を別々に購入するのは逆希釈です。
(b)2023年12月31日及び2022年12月31日までに、発行された限定株式単位3,280,313そして161,750普通株を購入すると、それぞれ逆希釈されます。
(c)2023年、2023年、2022年12月31日までの年度、株式証明書の未償還4,624,977そして10,564,429普通株を別々に購入するのは逆希釈です。
注19.取引記録株式ベースの報酬
取締役会が2018年6月15日に採択した“急性治療会社株式激励計画”(以下は“計画”と略称する)に基づいて、会社はある従業員、非従業員取締役と顧問に業績激励を提供する。本計画によれば、会社は、選定された参加者の長期財務利益がその株主の長期財務利益と一致するように、限定的な株式単位、株式オプション、または他の株式ベースの奨励を付与することができ、これらの人々の会社に対する約束を強化し、長期成長、収益性および株式価値の向上に努力する能力および奉仕精神のある人を誘致し、維持することができる
付与されたサービスに基づく制限株式単位および株式オプションは、サービス期間内に階層的に付与される。これは、通常、3年それは.市場状況に応じて帰属を行う制限的株式単位は2023年に授与され、第1回授与記念日には3年に分けて授与される。限定株式単位については、サービスベースの報酬であっても、市場条件帰属に基づく報酬であっても、補償コストは、付与された各報酬の必要なサービス期間内に直線的に確認される。株式オプション報酬の補償コストは、付与された各奨励の必要期間に比例して確認される。
2023年12月31日までに1.8譲渡可能な株は1.2億株。
同社はその総合経営報告書と全面赤字報告書の中で株式ベースの補償を確認し、具体的には以下の通りである
| | | | | | | | | | | |
| 費用分類: | 2023年12月31日までの年度 | | 2022年12月31日までの年度 |
| 製造と供給 | $ | 191 | | | $ | 203 | |
| 研究開発 | 456 | | | 672 | |
| 販売、一般、行政 | 2,042 | | | 3,506 | |
| 株式に基づく報酬支出総額 | $ | 2,689 | | | $ | 4,381 | |
| 株式ベースの報酬は | | | |
| 限定株単位 | 993 | | | 127 | |
| 株式オプション | 1,669 | | | 4,244 | |
| 従業員株購入計画 | 27 | | | 10 | |
| 株式に基づく報酬支出総額 | $ | 2,689 | | | $ | 4,381 | |
次の表は、2023年12月31日、2023年12月31日、2022年12月31日までの年間会社限定株式単位と株式オプション活動の情報を提供しています。
限定株単位
次の表は、2023年と2022年に会社が付与したサービス型と市況型制限株式単位をまとめています
| | | | | | | | | | | |
制限株式単位賞(RSU)-サービスベース: | 番号をつける
単位数 | | 加重平均
贈与日交易会
1株当たりの価値 |
| | (単位:千) | | |
帰属していない、2021年12月31日 | — | | $ | — | |
| 授与する | 192 | | 2.37 | |
| 没収される | (20) | | 2.21 | |
| 既得 | (10) | | 2.55 | |
| 帰属していない、2022年12月31日 | 162 | | $ | 2.38 | |
| 授与する | 1,874 | | 0.91 | |
| 没収される | (31) | | 2.33 | |
| 既得 | (57) | | 2.03 | |
| 帰属していません、2023年12月31日 | 1,948 | | $ | 0.97 | |
その会社は授与した1,874,3002023年サービスベースの限定株式単位。その会社は授与した192,0002022年期間のサービスベースの限定株式単位。2023年に、帰属株式の総授出日公平時価は$72.
2023年12月31日までにドル1,278未帰属サービス型限定株式単位に関する未確認報酬支出総額は2.18授与の日から数年。従業員に付与されたサービスベースの制限株式単位三つ年間卒業帰属スケジュールは、継続雇用を除いて、業績基準に制限されない。
2022年インセンティブ持分インセンティブ計画
当社は、当社取締役会報酬委員会が承認した2022年株式インセンティブ計画を採択し、2022年7月29日から発効し、これにより、取締役会報酬委員会は、ナスダック上場規則第5635(C)(4)条の規定に基づいてインセンティブ付与を行うことができます。いくつありますか150,0002023年12月31日現在、本計画に従って付与され、支払われていない報酬は、上記表に記載されたサービスベースの限定株式単位に含まれる。
| | | | | | | | | | | |
制限株式単位賞(RSU)-市場状況に基づく授与: | 番号をつける
単位数 | | 加重平均
贈与日交易会
1株当たりの価値 |
| | (単位:千) | | |
| | | |
| | | |
| | | |
| | | |
| 帰属していない、2022年12月31日 | — | | $ | — | |
| 授与する | 1,332 | | 2.40 | |
| 没収される | — | | — | |
| 既得 | — | | — | |
| 帰属していません、2023年12月31日 | 1,332 | | $ | 2.40 | |
その会社は授与した1,332,0002023年の市況は帰属の制限株式単位に基づいている。2022年には帰属に基づく制限株式単位の市場条件が付与されていない。
2023年12月31日までにドル2,314未得市場状況に関する未確認補償支出総額のうち、帰属に基づく制限株式単位は、加重平均期間中に確認されると予想される2.34授与の日から数年。
市場条件の帰属に基づく制限株式単位は、業績価格帰属に基づいて、30-ナスダック株式市場報告の直後の会社の普通株終値の日平均値、三つ-年間履行期間(贈与の日から3周年終了)。ある程度性能コストは$を下回っています1.75帰属率はゼロそれは.性能コストの範囲内で
はい$です1.75帰属率は50%です。ある程度性能コストは$です1.76それ以上ですが$以下です2.50帰属割合は50.01%和99.99%は、直線補間法に基づきます。ある程度性能コストは$です2.50帰属率は100%です。ある程度性能コストは$です2.51それ以上ですが$以下です3.25帰属割合は100.01%和149.99%は、直線補間法に基づきます。ある程度性能コストは$です3.25それ以上では帰属率は150%です。いずれの場合も帰属率は超えません150%.
当社の付与または推定日の市場条件に基づく帰属報酬の公正価値の推定は、モンテカルロシミュレーションに基づいており、シミュレーションを含む様々な変数および仮定を考慮している30実行期間の終了時の日中平均は、以下の仮定を含む:
| | | | | | | | | | | | | | |
| | 十二月三十一日までの年度 |
| | | 2023 |
| 期待配当収益率 | | 0% |
| 予想変動率 | | 92% | - | 95% |
| 所期期間(年) | | 2.74 | - | 3.00 |
| 無リスク金利 | | 3.6% | - | 4.4% |
授権日の株価 | | $2.01 | - | $2.04 |
株式オプション奨励
次の表は、会社の2023年から2022年までの株式オプション活動をまとめています
| | | | | | | | | | | | | | | | | | | | | | | |
| (2000年代、株価データを除く) | 番号をつける
選択肢の数 | | 重みをつける
平均値
行権価格 | | 重みをつける
平均値
残り
契約書
年単位の期限 | | 骨材
内在的価値 |
2021年12月31日現在の未返済債務 | 4,146 | | | $ | 7.28 | | | 7.88 | | $ | 1,423 | |
| 授与する | 2,015 | | | $ | 1.83 | | | | | |
| | | | | | | |
| 没収と期限切れ | (133) | | $ | 7.81 | | | | | |
| 2022年12月31日に返済されていません | 6,028 | | | $ | 5.48 | | | 7.50 | | $ | 38 | |
| 授与する | 150 | | | 2.02 | | | | | |
鍛えられた | (1) | | | $ | 0.88 | | | | | |
| 没収と期限切れ | (444) | | | $ | 2.27 | | | | | |
| 2023年12月31日現在の未返済債務 | 5,733 | | | $ | 5.58 | | | 6.41 | | $ | 1,082 | |
| すでに帰属しており、2023年12月31日に帰属する予定です | 5,674 | | | $ | 5.62 | | | 6.32 | | $ | 1,050 | |
| 2023年12月31日に行使できます | 4,324 | | | $ | 6.59 | | | 5.98 | | $ | 596 | |
2023年から2022年までの期間に付与された株式オプションの加重平均付与日の公正価値は#ドルである1.50そして$1.46それぞれ,である.2023年12月31日までの年間で150,000株式オプションの発行価格は#ドルです2.02したがって、同社の株価は#ドルであることを考慮すると2.022023年12月31日に、この期間に付与されたいくつかの株式が提供する内在的価値は極めて低い。
付与された株式オプションの公正価値は、以下の仮定に基づいてブラック·スコアモデルを用いて推定される
| | | | | | | | | | | | | | | | | | | | | | | |
| | 十二月三十一日までの年度 |
| | 2023 | | 2022 |
| 期待配当収益率 | 0% | | 0% |
| 予想変動率 | 100% | | 100% |
| 所期期間(年) | 5.50 | | 5.50 | - | 6.13 |
| 無リスク金利 | 4.0% | | 2.0% | - | 4.3% |
| 行権価格 | $2.02 | | $0.71 | - | $2.55 |
同社は予測可能な将来に収益を製品開発や他の株式価値増加に再投資することを予想しているため,使用した配当収益率はゼロそれは.当社の上場普通株は十分な歴史記録が不足していることから、変動率の推定は付与時に上場会社の歴史取引データより株価変動性の推定に基づいて確定されている。簡略化手法を用いて授標の期待期限を計算し,授権期間と契約期限を考慮した場合に重み付き平均を用いる.無リスク金利は,付与された日に発効した米国債収益率曲線から得られ,これらのツールの残存期限はオプションの期待期限と類似している。
2023年12月31日までにドル1,421非既得株式オプションに関する未確認報酬支出総額のうち、1.06授与の日から数年。これらのオプション付与の最長契約期間は10年、加重平均残余契約期間は6.41何年もです。上級管理職とキーパーソンに付与されたオプション3年制階層帰属スケジュールは、取締役会に付与されたオプションは1年間の崖帰属スケジュールを遵守しなければならない。これらの株式オプションは引き続き雇用される以外、業績基準の制約を受けない。
従業員株購入計画
2019年1月1日から施行される会社員株購入計画(ESPP)には2つの特徴がある6か月毎年のサービス期間はそれぞれ1月1日から6月30日までと7月1日から12月31日までである。従業員の持株計画によると、当社の従業員は以下の低い者で当社の普通株を購入することができます85株式は発行期間の初日または最終日の公正価値の%である。ESPPでは250,000普通株の株は最初は発行のために保留されていた。2023年と2022年までの年間で36,168そして45,304株式はESPPで購入·発行され,総割引は$となる27そして$10それぞれ,である.
付記20.取引記録従業員福祉計画
同社は全常勤従業員を対象とした固定納付401(K)計画を開始し、この計画の条項の規定に従って雇用主に相応の支払いを行った。当社も適宜出資を行うことができます。同社の2023年12月31日までおよび2022年12月31日までの年度の同計画への供出総額は761そして$815それぞれ,である.
注21...所得税
所得税準備金の構成要素は以下の通りである
| | | | | | | | | | | |
| 費用分類: | 十二月三十一日までの年度 |
| 2023 | | 2022 |
現在のところ | | | |
連邦制 | $ | 245 | | | $ | — | |
状態.状態 | — | | | — | |
合計する | 245 | | | — | |
延期する | | | |
| 連邦制 | — | | | — | |
| 状態.状態 | — | | | — | |
| 合計する | — | | | — | |
所得税支給 | $ | 245 | | | $ | — | |
2023年12月31日、2023年12月31日と2022年12月31日まで、繰延税金資産と繰延税金項目負債が発生した資産、負債計税基数及び財務報告金額の一時的な差異が税収に与える影響は以下の通りである
| | | | | | | | | | | |
| | 十二月三十一日 |
| | 2023 | | 2022 |
| 繰延税金資産: | | | |
| 売掛金 | $ | 4 | | | $ | 177 | |
| 在庫品 | 345 | | | 449 | |
| 費用を計算する | 73 | | | 1,063 | |
| 繰り越ししない | 27,120 | | | 32,197 | |
| TJCAが適用する利息制限 | 9,880 | | | 10,667 | |
| 株の報酬 | 6,529 | | | 5,813 | |
収入を繰り越す | 7,662 | | | 2,326 | |
印税貨幣化 | 16,750 | | | 17,139 | |
| 財産と設備 | 2,756 | | | 2,576 | |
| 孤児の薬品と研究開発税収控除 | 4,805 | | | 5,625 | |
| 債務費用を計算すべきである | — | | | 697 | |
無形資産 | 154 | | | 1,731 | |
| 第174節研究開発資本化 | 5,039 | | | 3,770 | |
印税義務 | 3,520 | | | — | |
他にも | 58 | | | 82 | |
| 84,695 | | | 84,312 | |
| 繰延税金負債: | | | |
| | | |
| 481(A)調整 | (193) | | | — | |
| 前払い費用 | (449) | | | (524) | |
| (642) | | | (524) | |
| 評価税免除額 | (84,053) | | | (83,788) | |
| | | |
| 繰延税項目純資産/(負債) | $ | — | | | $ | — | |
会社の連邦純営業損失は2023年12月31日、2023年12月31日、2022年12月31日までにドルに転換した101,029そして$123,922その大部分は無期限繰越されている。会社は2023年12月31日、2023年12月31日、2022年12月31日までに、国家純営業損失1ドルを繰り越した104,478そして$104,2382034年に満期になります2017年12月の米国減税·雇用法案(TCJA)の結果として,第163条下の更新法規は控除可能な利息と支出に新たな制限を設けた。当社の163(J)項での利息支出控除は、2023年12月31日までに税務目的で算出されるEBITDAの30%を税務目的として制限されています。2020年3月27日、コロナウイルス援助、救済、経済安全法案が法律に署名され、同社は“米国思いやり法案”と呼ばれている。その他の事項を除いて、米国CARE法案には、純営業損失繰越期間に関する条項と、利息控除制限の改正が含まれている。米国CARE法案は、2019年と2020年に始まる納税年度の商業利息控除調整後の課税収入制限を30%から50%に引き上げる。この改正は許容利息支出控除を増加させ、当社の2019年度の追加純営業損失(NOL)と低い当期課税収入(NOL使用前)を招く。また、米国CARE法案は、会社が2020年の課税収入を数年前のNOL繰越と完全に相殺することを許可している。既存の証拠によると、当社は繰延税項目の純資産が現金にならない可能性が高いことを確定しているため、その繰延税項目の純額について全額評価を提供している。推定免税額は$84,053、と$83,788それぞれ2023年12月31日、2023年12月31日、2022年12月31日に設立された。所有権変更のため、当社は“国内収入法”第382節の純営業損失使用に関する規定を遵守しなければならないかもしれません。そのため,今期と前期に繰り越したNOLの使用は年次制限されている。
TCJAは,2021年12月31日以降に開始された納税年度の研究開発支出を第174条に基づいて資本化·償却するよう納税者に要求している。2023年,2023年,2022年12月31日までの年度,資本化研究開発コストは#ドルである12.6百万ドルとドル16.6それぞれ100万ドルです会社は税務目的でこれらのコストを償却します5年研究開発がアメリカや他の地域で行われていれば15研究開発がアメリカ以外で行われていれば数年です
実体はまた、その所得税申告書上の任意の不確定所得税の評価、測定、確認、および開示を要求される。同社は税務状況を分析し、結論を出した違います。2023年12月31日まで、2023年、2022年までの不確定頭寸。
2023年、2023年、2022年12月31日終了年度の所得税優遇と、21%の法定連邦所得税税率を税前損失計算に適用した金額をそれぞれ照合すると以下のようになる
| | | | | | | | | | | |
| | 十二月三十一日までの年度 |
| | 2023 | | 2022 |
| 法定税率で所得税を徴収する | 21.00 | % | | 21.00 | % |
| 以下の理由で増加(減少): | | | |
| 州所得税 | 4.00 | | | 4.23 | |
| 恒久的差異 | (0.43) | | | (0.20) | |
税金控除 | — | | | 0.20 | |
| 推定免税額 | (26.53) | | | (20.69) | |
| 規定に戻る | (3.28) | | | 0.11 | |
| 国の金利の変化 | (1.78) | | | (4.67) | |
| | | |
FDII控除額 | 3.80 | | | — | |
| 実際の税率 | (3.22) | % | | (0.02) | % |
同社はERTC返金#ドルを受け取りました1,250それは.それは利息収入やその他の収入に含まれ、2023年12月31日の会社の総合経営報告書と全面赤字で純額を達成する。
注22.調査結果事件があったり
当社は、製品責任、知的財産権、証券、民事侵害および商業訴訟、環境またはその他の規制を含む、その業務過程で発生する法的訴訟に時々巻き込まれる可能性がある。
特許に関する訴訟
Indior Inc.,InDior UK Ltd.,Aqutive Treateutics,Inc.Dr.Reddy‘s実験室S.A.とDr.Reddy’s実験室,Inc.,
2018年2月7日、当社はInDior Inc.とInDior UK Ltd.(総称してIndiorと呼ぶ)とDr.Reddy‘s Labats S.A.とDr.Reddy’s Labals,Inc.(総称して“Dr.Reddy‘s”と呼ぶ)に対して訴訟を提起し、米国特許番号9,855,221(“221特許”)を侵害したと主張した。2018年4月3日,当社とInDiorは単独で訴訟を提起し,Reddy博士が米国特許番号9,931,305(“305特許”)を侵害したことを告発した。2018年5月29日、‘221と’305特許に関する訴訟が合併し、最初にInDiorがReddy博士に対して米国第9,687,454号特許(“454特許”)の侵害を主張した訴訟が提起された。2019年2月19日,裁判所は当事者の同意を得て,‘221号特許を案件から取り消す規定を承認した。2020年1月8日,裁判所は裁判所の請求に基づいて裁決を解釈し,305号特許不侵害の規定命令を入力し,会社および個人は権利解釈裁決に対する控訴権利を保持した。2022年6月28日,当事者間の和解協議により,裁判所は却下の規定と命令に入り,訴訟中のすべての偏見のあるクレームと反訴を却下した。
Indior Inc.,InDior UK Ltd.とAqutive Treateutics,Inc.はTeva製薬アメリカ会社を訴えた
2018年2月7日、当社とInDiorはTeva PharmPharmticals USA,Inc.(以下Tevaと略す)に対して‘221号特許を侵害したと訴訟を起こした。2018年4月3日、会社とInDiorは単独でTevaを提訴し、‘305号特許を侵害した。2018年5月29日、‘221及び’305特許に関連する訴訟は、InDiorがTevaに対して最初に提起した454件の特許侵害の訴訟と統合された。この事件は、レイディ博士(上述したように)に対する最終判決によって管轄されることに同意した。2024年1月31日、裁判所は却下の規定と命令に入り、訴訟中のすべての偏見を持つクレームと反訴を却下した。
InDior Inc.,InDior UK Ltd.,Aqutive Treeutics,Inc.Alvogen Pine Brook LLCを訴える
InDiorは2017年9月14日、Alvogen Pine Brook LLC(Alvogenと略す)に対して“454特許を侵害した”と訴訟を起こした。2018年2月7日、会社とInDiorは修正された起訴状を提起し、会社を原告として追加し、“221特許”の侵害を主張した。2018年4月3日、当社とInDiorはAlvogenを単独で提訴し、‘305号特許を侵害したと主張した。2018年5月29日、事件合併。2019年2月26日,裁判所は当事者の同意の撤回‘221号特許の規定を承認した。2020年1月9日
裁判所は裁判所の権利請求構造裁決に基づいて‘305特許を侵害しない規定命令を入力し,会社およびIndiorは権利主張構造裁決を上訴する権利を保持している.
2019年11月21日、Alvogenは連邦とニュージャージー州反独占法に基づいて、会社とIndiorに独占が存在し、独占および共謀独占を企てると主張する修正された答弁書と反訴を提出した。裁判所は2020年8月24日に同社がAlvogen反訴を却下した動議を却下した。Alvogenは2020年11月2日、2つ目の修正された答弁書と反訴書を提出し、会社の独占と独占を企てる疑惑を撤回し、会社に対してのみ共謀独占を行うと主張した。2023年11月9日,当事者間の和解協議により,裁判所は却下の規定と命令に入り,訴訟中のすべての偏見のあるクレームと反訴を却下した
BDSIとの特許訴訟和解
同社は米国でBDSIを販売するBunavailとBelbua薬物薄膜製品に関する特許侵害訴訟で和解し,2023年3月3日から発効した。和解協定の条項によると、BDSIとAqutiveおよびベルブカ訴訟の共同原告InDior Inc.の間では、#ドルの一度支払いと引き換えに、すべての未解決の特許請求が解決されている8,500会社へ。この和解は、会社が可能かつ適切な状況で、未解決の訴訟問題の解決に専念し続けている。この金は利息収入とその他の収入、会社の総合経営報告書と全面赤字後の純額を控除する。
ケンタッキー州訴訟-フマナ
Humana Inc.InDior Inc.,InDior Solutions Inc.,InDior PLC,利潔時ベンキサー集団,リーゼント時医療保健(イギリス)有限会社とAQUCTIVATION,INQUEATIOTICS,Inc
Humanaは2021年8月20日、州法下の詐欺、州法下の不公平および詐欺、保険詐欺、およびInDiorが2010年にSuboxone Sublanguage映画を発売したことに関する会社に対する不当な利益を告発する訴訟をケンタッキー州裁判所に提起した。Humana訴訟は棚上げされ、関連訴訟を待ち、2023年10月30日に解除された。行動にはスケジュールが設定されておらず,裁判日も設定されていない.当社はケンタッキー州裁判所におけるHumanaの訴訟の最終結果を確定または予測することができず、その可能性のある結果や損失(あれば)の合理的な推定や推定範囲を提供することもできない。
カリフォルニア訴訟
Neurelis,Inc.Aqutive Treeutics,Inc.
2019年12月5日、Neurelis Inc.はサンディエゴ県カリフォルニア州上級裁判所に訴訟を起こし、同社は以下のように告発した三つ訴訟理由:(1)カリフォルニア商業·専門法規(UCL)第17200条下の不正競争,(2)誹謗,(3)悪意起訴。Neurelisは2019年12月9日に最初の改訂された訴えを提出し、三つ訴訟の原因。同社は2020年1月31日にカリフォルニア反SLAPP(公衆参加戦略訴訟に反対)法規に基づいて動議を提出し、Neurelisの苦情に打撃を与えたが、Neurelisは反対した。2020年8月6日、裁判所は会社の反SLAPP動議を部分的に承認し、部分的に拒否する命令を発表した。双方はカリフォルニア控訴裁判所に交差控訴を提出した。控訴裁判所は2021年10月14日に控訴に対して口頭弁論を行い、2021年11月17日に判決を下した。判決によると、裁判所は悪意ある起訴疑惑の全内容を却下し、ロンドン大学アカデミーの告発と誹謗中傷容疑の一部を却下した。Neurelisは2022年4月12日、控訴裁判所の裁決に対して第2次改正後の訴えを提出した。二番目の修正された起訴状はまた商業誹謗の訴訟理由を増加させる。2022年5月3日、同社は第2次改正後の訴えの十分性に“異議”を申し立てた。2022年6月17日,会社が提出した反SLAPP動議に関する弁護士費動議および第2次改正後の訴えと抗弁質疑について口頭弁論を行った。裁判所はその会社の弁護士費動議を承認して$を判決する命令を下した156そしてNeurelisに2022年6月17日以降60日以内に費用を支払うよう命じた。裁判所は同社の抗弁者を拒否し,双方の当事者は2通目の修正された起訴状中のクレームを証拠公開し続けた。原告は3つ目の改正された訴えの提出を要求する動議を提出した。裁判所は2023年11月17日に承認した。修正された第3の訴えは、他の事実があると主張するが、第2の改正された訴えと同じ訴えを含む。この問題の裁判は2024年10月25日に行われる予定だ。当社はこの訴訟の最終結果を確定または予測することができず、その可能な結果や損失(あれば)に対して合理的な推定または推定範囲を提供することもできない。
連邦証券集団訴訟
Deanna LewakowskiはAqutive Treateutics,Inc.を訴えた彼らの研究を待っています
2021年3月1日、米国ニュージャージー州地域裁判所は、FDAのLibervant承認に関する同社の公開声明に関する証券集団訴訟を起こし、同社およびその一部の幹部が連邦証券法に違反したことを告発した。裁判所が首席原告を任命した後,原告は2021年6月25日に修正された起訴状を提出した。被告は2021年8月16日に却下動議を提出し、2021年11月1日までに全面通報した。2023年3月14日裁判所は承認する命令を出した
被告が提出した偏見を構成せずに訴訟を却下する動議は,原告が2023年4月14日までに最終的,第2次改訂の訴えを提出することを許可した。2023年4月7日、双方は原告が修正された訴えを提出しないことを決定し、偏見で彼らの訴訟を却下することに同意する自発的却下の規定を提出した。2023年4月10日、裁判所はこの規定を裁定し、訴訟を中止した
株主派生訴訟
ローレリーン·ニewenhuisはKeith Kendall事件を訴えました彼らの研究を待っています
2021年12月15日、いわゆる独立株主がLoreen NiewenhuisがKeith Kendallらを訴えたという派生商品訴訟を起こした。米国ニュージャージー州地方裁判所では、会社を代表して会社の一部の現職および前職の上級管理職や取締役を起訴したという。この事件は,上記で述べた未解決連邦証券集団訴訟Deanna LewakowskiがAqutive Treateutics,Inc.に関連して指定され,証券集団訴訟を主宰する同じ裁判官に受け入れられた.この事項の起訴状は受託責任違反と貢献に対するクレームを主張する。これらのクレームの基礎を構成する事実告発は、集団訴訟で呼ばれる開示に関する告発と類似している。2022年4月4日,原告は修正された起訴状を提出し,同じ被告に対して同様の主張をした。同社は2022年4月25日に動議を提出し、修正後の訴えの却下を求め、2022年6月27日現在、訴えは全面的に通報された。2023年4月20日、双方の当事者は原告が偏見で彼女の訴訟を却下することに同意したとの自発的な却下の規定を提出した。2023年4月21日、裁判所はこの規定を裁定し、訴訟を中止した。
商業協定
“個人ビジネス開発協定”改正案
当社は、2023年3月2日から、個人と“個人許可協定修正案11”を締結した。“個人許可協定改正案11”の主な目的は、“個人許可協定”を改訂することであり、改訂日は、(I)“個人許可協定”の期限を2026年8月16日に延長し、その後、“個人許可協定”当事者が現在の期限満了前に少なくとも12ヶ月以内に当社に“個人意向”が更新されない通知を提出しない限り、“個人許可協定”双方の早期終了権利の制限を受けることを規定する。また、“個人ライセンス契約”は、製品特許の最後の期限が満了してから開始されるいかなる継続期間内にも自動的に継続しないことを規定する。そして(Ii)提供された製品の定価と支払い条件の譲渡に同意する。また,IndiorはInvidiorライセンスプロトコルに従って会社に支払う償還可能金額を会社に支払うことに同意した.双方の合意を考慮して、会社は#ドルの支払いを受けた11,482個人からのもので金額は$です5,482表示:(A)2022年の価格上昇のうち以前に支払われなかった部分を支払う;(B)2023年に何らかの価格上昇の費用を支払うと推定される。これは1ドルです5,482支払いは製造と供給収入とドルに含まれています6,000利息収入とその他の収入を計上し、純額は会社の総合経営報告書と全面赤字に計上する。
注23.調査結果後続事件
市場の施設を引き続きご利用ください
会社は2024年1月1日から3月4日までそのATM施設を引き続き使用して販売しています4,557,220純収益が約$の株を生む12,014.
製品責任訴訟
当社は2024年2月21日までに登録されています40Indiorと他の何人かの被告と一緒に製品責任訴訟を提起した。これらの個人原告は、Suboxone舌下膜を使用して歯を怪我させたと主張した。2024年2月2日、この訴訟は米オハイオ州北区地裁が合併した多地域訴訟(MDL)となった。Indiorはこの訴訟で会社を弁護することに同意した。当社はこの訴訟の最終結果を確定または予測することができず、その可能な結果や損失(あれば)に対して合理的な見積もりや推定範囲を提供することもできません。