アメリカです
アメリカ証券取引委員会
ワシントンD.C.,郵便番号:20549
表
(マーク1)
1934年証券取引法第13条又は15条に基づいて提出された年次報告 |
本財政年度末まで
あるいは…。
1934年証券取引法第13条又は15条に基づいて提出された移行報告 |
_から_への過渡期
依頼書類番号:
(登録者の正確な氏名はその定款に記載)
(明またはその他の司法管轄権 会社や組織) |
(税務署の雇用主 |
(主にオフィスアドレスを実行) |
(郵便番号) |
登録者の電話番号は市外局番を含んでいます
同法第12条(B)に基づいて登録された証券:
クラスごとのタイトル |
|
取引 記号 |
|
登録された各取引所の名称 |
|
|
同法第12条(G)に基づいて登録された証券:ありません
登録者が証券法第405条に規定する有名な経験豊富な発行者である場合は、再選択マークで表示してください
登録者がこの法第13又は15(D)条に従って報告書を提出する必要がないか否かを、再選択マークで示すはい、そうです ☐
登録者が(1)過去12ヶ月以内(または登録者がそのような報告を提出する必要があるより短い期間)に1934年の証券取引法第13条または15(D)条に提出されたすべての報告書を再選択マークで示すかどうか、および(2)このような提出要求を過去90日以内に遵守してきた
再選択マークは、登録者が過去12ヶ月以内(または登録者がそのような文書の提出を要求されたより短い時間以内)に、S−T規則405条(本章232.405節)に従って提出を要求した各相互作用データファイルを電子的に提出したか否かを示す
登録者が大型加速申告会社,加速申告会社,非加速申告会社,小さな報告会社,あるいは新興成長型会社であることを再選択マークで示す。取引法第12 b-2条の規則における“大型加速申告会社”、“加速申告会社”、“小申告会社”、“新興成長型会社”の定義を参照されたい。
|
☒ |
|
ファイルマネージャを加速する |
|
☐ |
|
|
|
|
|
|||
非加速ファイルサーバ |
|
☐ |
|
規模の小さい報告会社 |
|
|
|
|
|
|
|
|
|
|
|
|
|
新興成長型会社 |
|
|
新興成長型企業であれば、登録者が延長された移行期間を使用しないことを選択したか否かを再選択マークで示し、取引所法第13(A)節に提供された任意の新たまたは改正された財務会計基準を遵守する☐
登録者が報告書を提出したかどうかを再選択マークで示し、その経営陣が“サバンズ-オクスリ法案”(“米国連邦法典”第15編、第7262(B)節)第404(B)条に基づいてその財務報告の内部統制の有効性を評価したことを証明する。この評価は、その監査報告書を作成または発行する公認会計士事務所によって行われる
証券が同法第12条(B)に基づいて登録されている場合は,登録者の財務諸表が以前に発表された財務諸表の誤り訂正を反映しているか否かを示すチェックマークを適用する
これらのエラーのより真ん中に登録者の任意のエンタルピーCER幹部が相関回復期間内に§240.10 D−1(B)に基づいて受信したインセンティブベースの補償に基づいて回復分析を行う必要があるかどうかを再選択マークで示す
登録者が空殻会社であるか否かをチェックマークで示す(取引法第12 b-2条で定義されている)。はい、そうです☐違います
登録者非関連会社が保有する投票権と無投票権を有する普通株の総時価は、2023年6月30日(登録者が最近完成した第2四半期の最終営業日)普通株のナスダック全世界精選市場における終値に基づいて、約$
2024年2月23日現在登録者は
引用で編入された書類
本年度報告の10−K表第III部に要求される情報(ここでは明記されていない範囲)は,2024年に開催される年次株主総会に関する登録者の最終委託書を引用して本明細書に組み込まれる。
カタログ表
|
|
ページ |
第1部 |
|
3 |
第1項。 |
業務.業務 |
3 |
第1 A項。 |
リスク要因 |
29 |
項目1 B。 |
未解決従業員意見 |
73 |
プロジェクト1 C。 |
ネットワーク·セキュリティ |
73 |
第二項です。 |
属性 |
73 |
第三項です。 |
法律訴訟 |
73 |
第四項です。 |
炭鉱安全情報開示 |
73 |
|
|
|
第II部 |
|
74 |
五番目です。 |
登録者普通株市場、関連株主事項及び発行者による株式証券の購入 |
74 |
第六項です。 |
[保留されている] |
74 |
第七項。 |
経営陣の財務状況と経営成果の検討と分析 |
75 |
第七A項。 |
市場リスクの定量的·定性的開示について |
87 |
第八項です。 |
財務諸表と補足データ |
88 |
第九項です。 |
会計と財務情報開示の変更と相違 |
118 |
第9条。 |
制御とプログラム |
118 |
プロジェクト9 B。 |
その他の情報 |
120 |
プロジェクト9 Cです。 |
検査妨害に関する外国司法管区の開示 |
120 |
|
|
|
第三部 |
|
121 |
第10項。 |
役員·幹部と会社の管理 |
121 |
第十一項。 |
役員報酬 |
121 |
第十二項。 |
特定の実益所有者の担保所有権及び経営陣及び関連株主の事項 |
121 |
十三項。 |
特定の関係や関連取引、取締役の独立性 |
121 |
14項です。 |
最高料金とサービス |
121 |
|
|
|
第4部 |
|
122 |
第十五項。 |
展示·財務諸表明細書 |
122 |
第十六項。 |
表格10-Kの概要 |
124 |
サイン |
125 |
|
前向きに陳述する
このForm 10-K年次報告書には、経営陣の信念と仮定、および管理職が入手可能な情報に基づく前向きな陳述が含まれている。本年度報告“Form 10-K”の“業務”、“リスク要因”および“経営層の財務状況と経営結果の議論と分析”の部分およびその他の部分のいくつかの陳述には前向きな陳述が含まれている。場合によっては、“可能”、“将”、“可能”、“将”、“すべき”、“予想”、“計画”、“計画”、“予想”、“信じ”、“推定”、“予測”、“プロジェクト”、“潜在”、“継続”、“進行中”、またはこれらの用語または他の同様の用語の否定によって前向き表現を識別することができる。
これらの表現はリスク、不確定要素と他の要素に関連し、実際の結果、活動レベル、業績或いは業績を招く可能性があり、これらの前向き表現と明示或いは暗示の情報は大きく異なる。本年度報告書10-K表に含まれるすべての前向き陳述には合理的な根拠があると信じていますが、これらの陳述は私たちが現在知っている事実と要素と私たちの未来の予測に基づいていて、私たちはこれらの事実と要素を決定することができません。本年度報告におけるForm 10−Kフォーマットで明示的または暗示的な前向き陳述は、以下の説明を含むが、これらに限定されない
1
また,実際の結果が前向き陳述で明示または示唆された結果と大きく異なる可能性のある他の重要な要因の検討については,本年度報告の10−K表の“リスク要因”の部分を参照されたい。これらの要因のため、本年度報告におけるForm 10−Kに関する前向き陳述が正確であることが証明されることは保証できません。さらに、展望的な陳述が不正確であることが証明された場合、不正確さは実質的である可能性がある。このような展望的陳述の重大な不確実性を考慮して、あなたはこれらの陳述を私たちまたは任意の特定の時間枠内で、または私たちの目標と計画の陳述または保証を完全に達成しないために、私たちまたは他の誰もと見なしてはならない。本稿の展望的陳述は,本年度報告10−K表までの日の観点を代表している。私たちはその後に発生した事件と事態の発展が私たちの観点を変化させると予想している。しかし、私たちは未来のある時点でこのような前向きな陳述を更新することを選択するかもしれないが、私たちは現在、法律の要求が適用されない限りそうするつもりはない。したがって、あなたはこのような前向きな陳述に依存して、本年度報告書10-K表の日付までの私たちの任意の日付の観点を代表してはいけません。
本10-K表年次報告では、文意が別に指摘されている以外、すべて“私たち”、“適応性”及び“会社”に言及し、すべて“適応性生物科学技術会社”を指す。
2
第1部
プロジェクト1.ビジネス
概要
著者らの歴史を見ると、著者らは適応性免疫システムの固有生物学を利用することによって疾病の診断と治療を変化させ、免疫医学領域の発展を推進した。適応免疫系は自然界が多くの疾患に対して行っている最も精密な診断や治療であると考えられるが,それを解読することはできず,医学界のその能力の活用を阻害している。著者らの免疫医学プラットフォームは著者らの独自技術を応用して患者免疫システムの各種遺伝子コードを読み取り、免疫システムがどのようにこの患者の疾病を測定と治療するかを正確に理解する。著者らは計算生物学と機械学習に基づく動態臨床免疫組織学データベースと関連抗原注釈の中でこれらの知見を捉え、それらを利用して患者個人の需要量に応じてカスタマイズできる臨床製品とサービスを開発と商業化した。
2023年、我々はリンパ系悪性腫瘍微小残留病(MRD)の臨床評価と免疫薬物(IM)駆動の薬物発見と開発の2つの主要領域を中心に業務を展開し続けた。MRD事業の総目標市場は51億ドルであり,そのうち44億ドルは臨床試験から来ていると信じている。IM業務は,我々のパートナー遺伝子テーク社(“遺伝子テーク”)の腫瘍学におけるTCRによる細胞療法の開発や,自己免疫において新たな利用可能な標的の発見を含む戦略的優先順位を実現する触媒にその研究·開発投資を集中させている。
MRD業務は著者らの高感度次世代シークエンシング(“NGS”)分析を用いて悪性血液病患者のMRDを測定することに集中している。それは私たちが臨床医に提供するclonoSEQ臨床診断テストと、私たちが生物製薬パートナーに提供するclonoSEQアッセイからなり、薬物開発を推進する(“MRD Pharma”)。
ClonoSEQはアメリカ食品と薬物管理局(FDA)が許可した第一種の多発性骨髄腫(MM)、B細胞急性リンパ球性白血病(ALL)と慢性リンパ球性白血病(CLL)患者のMRDの測定とモニタリングであり、CLIA検証の実験室開発テスト(LDT)として他のリンパ癌患者に応用することもでき、瀰漫性大B細胞リンパ腫(DLBCL)を含む。著者らは、clonoSEQは血液系悪性腫瘍MRD測定の第一選択測定方法であり、業界トップの敏感性を有すると信じている。ClonoSEQを用いることにより,提供者,製薬パートナー,支払者と連携することにより,リンパ癌の治療法を変化させている。
IMトラフィックは、TCRおよびB細胞受容体(“BCR”)の大規模シークエンシング、マッピング、ペアリング、および特性化のために、我々の独自の能力を利用する。私たちは新しい治療法の開発を推進するための強力なデータエンジンを作った。これらのデータセットには,100,000以上の癌および自己免疫疾患の署名と,約500,000個のTCRと疾患関連抗原との一致が含まれている。
我々の膨大なデータと差別化の能力は,我々のIM業務を新たな標的の発見とこれらの標的に対する治療候補薬(例えばTCRに基づく療法や抗体)の開発において独自の地位を持たせている。私たちの目標は、自己免疫疾患や癌のような挑戦的な疾患をよりよく理解して治療することだ。IMの薬物発見における巨大な潜在力は,我々と遺伝子テークとの世界的な協力と許可プロトコル(“遺伝子テークプロトコル”)からうかがえる。遺伝子技術プロトコルにより,TCRによる癌細胞療法の開発を継続する。2023年、Genentechは最初のFDAによって承認された抗原細胞療法候補製品を共有するための研究新薬(“IND”)を取得した。このマイルストーンはまた、著者らが発見した最初の細胞治療製品候補製品のためのTCRに重要な概念証明を確立し、TCRに基づく完全個性化方法を実現することを支持した。IMビジネスはまた、多発性硬化症(MS)、クローン病、1型糖尿病、および関節リウマチのような自己免疫疾患の治療に私たちの免疫薬物プラットフォームの潜在力を適用する。
2023年の精選結果
2023年、私たちの収入は1.703億ドルだったが、2022年には1.853億ドルであり、減少の主な原因は遺伝子泰克の前払い償却が減少し、製薬サービスが減速したことであり、これは主に生物製薬業界のより広範なマクロ経済要因に影響し、MRDマイルストーンがなかったためである。これに伴い、年内に業務の簡素化が継続されたため、我々の運営費は顕著なレバー化を得た。2023年の運営支出は3.973億ドルで、うち2540万ドルは非現金減価費用、2022年は3兆855億ドルだった。2023年12月31日現在、現金、現金等価物、有価証券は3億464億ドル。
MRDのハイライト
3
IMのハイライト
私たちの免疫配列決定プラットフォームは
適応免疫系はT細胞とB細胞と呼ばれる特定の免疫細胞からなり,多くの疾患を診断·治療する指令を持っている。これらの命令は、TCRおよびBCR表面に位置する専用受容体が、病原体または外来疾患シグナルを示すヒト細胞(“抗原”)を認識、結合および破壊することを可能にする。ヒトゲノム中のすべての他の遺伝子とは異なり,TCRやBCRの遺伝子配列は時間とともに再配列され,大きな遺伝的多様性を創出している。健常成人の適応免疫系は,約30,000個の遺伝子からなる静的ヒトゲノムと比較して,1億個を超える異なる遺伝子からなる。このような巨大な遺伝的多様性は,免疫系がヒト疾患に関連する数百万種類の異なる抗原を検出·対応できるようにした。
著者らの免疫シークエンシングプラットフォームは特許化学、計算生物学と機械学習を結合して臨床免疫グループ学データを生成し、適応性免疫システムを復号する。それは必要な規模、精度と速度で適応性免疫システムから見解を抽出と解釈し、それによって各患者の免疫システムの特定の遺伝に基づいて臨床製品を設計することができる。
入門読み物:適応免疫システム
数百万年の間、適応免疫システムは人々の健康を維持するための優雅な解決策を進化させた。それは大多数の抗原を認識し、それに反応し、それらが体外からのものであっても、例えばウイルスであっても、体内からのものであっても、例えば癌の突然変異を引き起こす。
先天性免疫系と後天性免疫系はすべてヒト免疫に作用を発揮する。しかしながら、適応免疫システムは、疾患シグナルまたは抗原に対する特定の反応を単独で提供する。これらの疾患特異的抗原は,主に外来と認識されるタンパク質断片,例えばウイルス由来タンパク質である。しかし,抗原がウイルスや病原体由来でなくても,外来と考えられる。癌細胞では,腫瘍関連抗原(TAA)は腫瘍に異常に発現する正常タンパク質であり,新抗原は正常タンパク質の変異バージョンであり,癌特有であり,健康な正常細胞には認められない。TAAsと新規抗原はいずれも免疫系により外来抗原として認識されている。自己免疫疾患では,免疫系は“自己”と“非私”を区別する能力を失い,正常なタンパク質断片(“自己抗原”)を誤って外来と認識し,本来健康な組織を攻撃することになる。
4
適応免疫反応
我々の身体が原反応に対抗できる適応免疫系の重要な細胞はT細胞とB細胞と呼ばれる。T細胞は標的細胞を直接破壊することができるが、B細胞は抗体を分泌し、免疫系の他の部分を活性化して標的細胞を破壊する。
各T細胞およびB細胞は、我々の身体が接触し続ける数百万種類の抗原のうちの1つまたは一部を認識することができるユニークなY型受容体を有する。特定の疾患に対して適応免疫反応を開始すると、疾患特異的標的受容体をコードするT細胞とB細胞はクローン増幅によって迅速に増殖し、強力な免疫反応を産生する。その中のいくつかの拡張細胞は疾病を直接攻撃し、もういくつかは未来に同じ抗原を迅速に認識し、再感染を防止するために長期記憶を形成する。
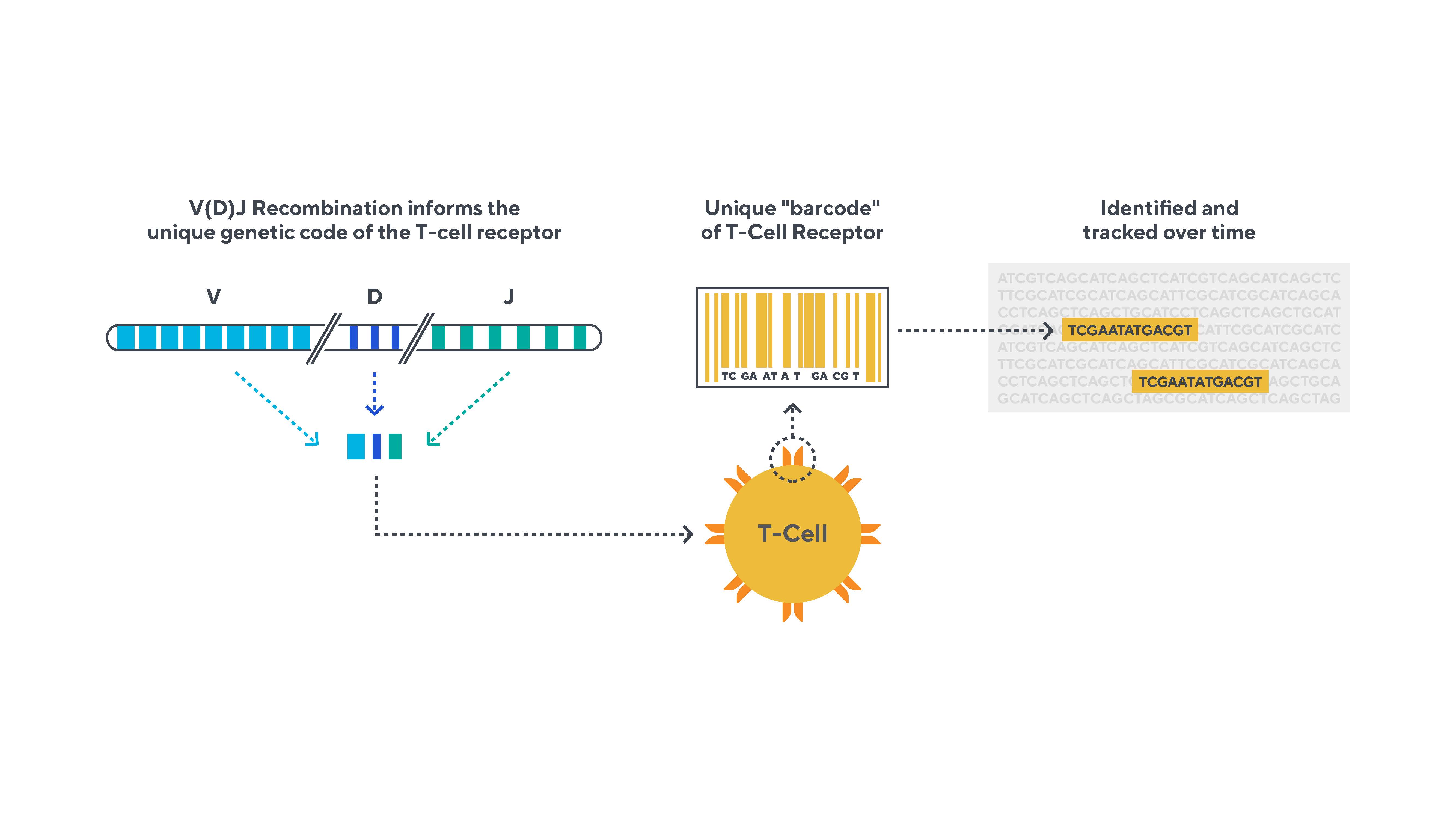
ヒトゲノム中の他のすべての遺伝子とは異なり,TCRやBCRの遺伝子配列は時間とともに複雑な生物過程で再配列され,大きな多様性を招いている。これらの受容体の多様性は,V(D)J組換え(V=可変,D=多様性,J=連結)と呼ばれる遺伝子コードの独自の再シャッフルにより可能となる。この組換え過程はT細胞およびB細胞にのみ発生し、各細胞クローンは唯一の受容体関連デオキシリボ核酸(DNA)配列を有することをもたらす。このユニークなDNA配列は、次の図に示すように、時間の経過とともに単一の受容体を識別および追跡するために使用することができるバーコードのようなものである

5
適応性免疫反応は数百万のこのような独特な受容体が広く分布し、血液中に存在する必要があり、同時に多くの異なる疾病に迅速に反応する能力がある。特定のTCRが抗原に結合してクローニング増幅された後であっても,これらのTCRを含む増幅T細胞クローンの頻度は,推定された数兆の他の循環T細胞と比較して相対的に低い。現在,患者の血液中でクローン増幅された疾患特異的TCRは平均10万細胞あたり1個未満であることが知られている。その豊富度は相対的に低いにもかかわらず、疾患特異性TCRは、免疫反応が高度に専門化された特性を有するので、大多数の摂動に対して系統的、持続的な反応を生じることができるので、以下の表で説明するように:

免疫系の自然特性を活用して臨床製品を開発するためには,血液中の個々の疾患特異的T(あるいはB)細胞の相対頻度を正確かつ確実に測定する能力を含む適応免疫系の巨大な多様性と規模を考慮する必要がある。例えば,癌患者の血液中を循環する癌特異的TCRは10万個の細胞のうち1つのみに存在する。血液中を循環する任意の特定の自己免疫疾患の自己反応性T細胞は100万細胞のうち1つしか出現しない。したがって,疾患特異的T細胞を検出する能力は,各試料から少なくとも数十万から数百万個の血球を定量的に検出する技術が必要である。私たちの技術はこの需要を満たすために構築され検証されている。
著者らの免疫医学プラットフォームは特許化学、計算生物学と機械学習を結合して臨床免疫グループ学データを生成し、著者らはこれらのデータを用いて適応性免疫システムを復号する。それは必要な規模、精度と速度で適応性免疫システムから見解を抽出と解釈し、それによって各患者の免疫システムの特定の遺伝に基づいて臨床製品を設計することができる。そのため、著者らは一連の技術の組み合わせを開発し、以下の重要な機能を実行し、著者らの免疫媒介生物学に対する理解を広げる
6
私たちの製品とパイプ(MRD)
MRD業務領域は著者らの高度に敏感なFDAが許可したNGS測定方法を用いて悪性血液病患者のMRDを測定することに集中している。それは私たちが臨床医師に提供したclonoSEQの臨床診断テストと、私たちが生物製薬パートナーに提供したclonoSEQ測定を含み、薬物開発を推進する。
十分なサンプル入力があれば,clonoSEQは血液系悪性腫瘍MRD検出の第一選択試験であり,業界トップクラスの感度を有し,1,000,000細胞あたり1個と信じられている。治療を開始する前にベースライン測定を行い、その後治療開始後のいくつかの時点で細胞数を追跡することによって、血液学者は彼らの治療反応の評価、患者の長期結果を予測し、一定期間内の疾病負担をモニタリングし、潜在的な再発を検出する能力を高めることができる。
ClonoSEQを用いることにより,生物製薬パートナー,サプライヤー,支払者と連携することにより,リンパ癌の治療法を変化させている。例えば,clonoSEQを用いることにより,リンパ癌薬の開発を加速させ,医師の重要な臨床決定を支援し,不要な高価な薬剤の使用を中止することで,支払いやコストを低減する可能性のある治療決定を行うことが可能である。
技術
ClonoSEQは著者らのFDAが許可したNGS MRD技術であり、腫瘍中のすべての再配置受容体配列を並列配列測定し、正確、高感度と強力なMRDモニタリングを確保することを目的としている。
ClonoSEQで実行した手順の概要は以下のとおりである
7
Clono配列番号
著者らのclono配列番号診断テストは治療期間と治療後の患者体内に残っている癌細胞の数を測定し、モニタリングし、MRDと呼ばれる。ClonoSEQはALL、CLL、MMと非ホジキンリンパ腫(NHL)(DLCBL、マントル細胞リンパ腫(MCL)と皮膚T細胞リンパ腫(CTCL))を含むすべてのリンパ系悪性腫瘍に広く適用されると信じている。
2018年9月、clonoSEQは、最初からの手順に従ってFDAのマーケティング許可を取得し、MMおよびALL患者が骨髄サンプルからそれらのMRDを監視することを可能にした。2020年8月、clono配列番号タグは、骨髄および血液サンプルからなるCLL患者に拡大された。
2022年、この検出はCLIA検証のLDTとして発売され、循環腫瘍DNA(“ctDNA”)を測定することによってDLBCL患者の血液中のMRDを検出し、患者と臨床医に強力な血液ベースの予後ツールを提供した。私たちはFDAが私たちのDLBCLテストを承認して、臨床採用を支持し、私たちの生物製薬パートナーの使用を増加させることを求めている。
ClonoSEQの臨床浸透率は著しく増加しています1以下に示す.


2019年1月、clonoSEQは、MMおよびALLの縦方向監視のためのFDAタグおよび国家総合癌ネットワーク(NCCN)ガイドラインに適合する医療保険カバー範囲を取得した。ClonoSEQは現在NCCNガイドラインに組み込まれ,全33個のNCCN癌センターで使用されている。その後数年間、Medicare、国家個人支払人、大規模地域計画を通じてclonoSEQのために私たちのFDAタグと一致する追加支払人保険を獲得し、保険範囲をすべての人とMMの3億人保険、CLLの2億人保険、DLBCLの7000万人保険に拡大した。
MolDXは2021年11月、MRD検出のためのローカルオーバーレイ決定(LCD)を発表した。このLCDはMRDとclonoSEQのALL、骨髄と血液中でMMとCLLを被覆することの重要性を肯定するだけでなく、NHLの技術評価を通じてClonoSEQのカバー範囲を拡大することを求めるために明確で有効な方法を提供した。
8
2022年7月,DLBCL(最もよく見られるNHL形式)の医療保険カバー範囲が確保されるにつれ,カバー範囲は拡大し続けている。著者らはDLBCL患者のためにMedicareのclonoSEQのカバー範囲を確保し、治療経路、治療方案或いは測定時点を考慮しない。ClonoSEQはDLBCLの中で最初で医療保険を受けた唯一のMRDテストである。2024年初めに別のNHL疾患MCLの医療保険を受ける予定である。
2022年10月、私たちはEpicとパートナーシップを達成し、clonoSEQをEpicの電子カルテシステムに統合し、これはclonoSEQテストをより容易にテストおよび結果を得ることができると信じている。2023年、clonoSEQは5つのクライアントのEMRに統合され、2024年2月にFlatiron Health,Inc.との追加EMR連携を含む2024年の顧客統合が大幅に増加することが予想されます。
私たちはclonoSEQの浸透を深化させ、私たちの商業と運営インフラを改善するための多管理の戦略を持っている
また,電子カルテ統合により顧客体験を強化し,支払者カバー範囲を最適化し,我々の運営インフラを利用して利益率の向上を推進していく。
2023年までに43のバイオ製薬会社は143の活発な臨床試験にclonoSEQを使用しており,これは2023年12月31日までの活発な業界スポンサーのリンパ癌臨床試験の9%から44%の浸透率(MMのピーク)を表している。私たちは、clonoSEQの臨床応用を拡大するために、私たちのビジネス投資を引き続き深化させ、アメリカでの専門販売と顧客支援組織とインフラを支援する実力を強化しました。また、いくつかの排他的に許可されていない配列決定技術を世界の他の地域の複数の実験室に譲渡することに成功しました。
開発されている臨床アプリケーションデータは
ClonoSEQの意思決定ツールとしての価値は、臨床医師がMRD状態に応じて最適な患者治療方案を選択できる可能性があると信じている。最近拡大された臨床例や薬物開発の進展のいくつかの例は
9
他の展望的研究は進行中であり、多くの研究はすでに業界会議で一時的なデータを共有している。より多くの研究の発表に伴い、臨床決定においてMRDがより多く採用される可能性が予想され、これはより多くの患者がClono配列番号から利益を得、各患者により高い試験頻度を提供する可能性がある。
適応支援:患者支援計画
適応支援は我々の患者支援計画であり,NGS MRDテストによって提供された臨床的知見から利益を得ることができる患者がclonoSEQ試験サービスを獲得することを支援することを目的としている。患者は、clonoSEQテストの前に彼らの保証範囲をよりよく理解し、控訴拒否クレームを含む保険プロセスをナビゲーションするために、私たちの専任患者支持代表と彼らの個人状況を議論することができる。著者らはまた条件を満たす未加入と加入不足の患者に経済援助を提供し、これらの患者はclono配列番号に対する経済的責任を負うことができない。
MRD製薬会社
MRD Pharma業務分野は、薬物開発を推進するために、生物製薬パートナーに我々のclono配列測定を提供することに集中している。ClonoSEQの広範な透過性を考慮して、私たちのMRD医薬業務は、他の適応でclonoSEQの成功を複製することを目標としているため、大きな成長機会があると信じている。例えば,MM生物製薬会社が行っている米国の臨床試験の約30%では,clonoSEQは現在終点として決定されている。
私たちの製品とパイプラインは
我々のインスタントメッセンジャー業務の目標は,我々の目標発見と薬物発見努力を拡大し,変革的療法を臨床に導入し,我々自身もパートナーとも導入することである。IMプラットフォームを推進するエンジンは私たちの免疫シークエンシング技術であり、私たちは比類のない規模と特異性で免疫系統の巨大な多様性を利用することができる。著者らの免疫シークエンシング方法は多重、偏差制御のPCRを利用して、数百万個のTCRとBCRに対して大規模な配列決定、マッピング、ペアリングと表現を正確かつ定量的に行った。これまでに我々が生成した独自のデータセットは、100,000を超える疾患(例えば、癌および自己免疫疾患)の署名と、約500,000個の対のTCRと疾患関連抗原との一致を含む。
薬物発見
私たちは私たち自身や協力的な治療法を開発するために私たちの薬物発見計画に集中している。これらの点で、IMは、免疫仲介生物学をよりよく理解し、癌や自己免疫疾患などの挑戦的な疾患を治療するために、TCRに基づくモデル、抗体、潜在的なワクチンなどの治療候補薬剤を唯一無二に発見し、開発することができる独自のデータおよび能力を有する。
10

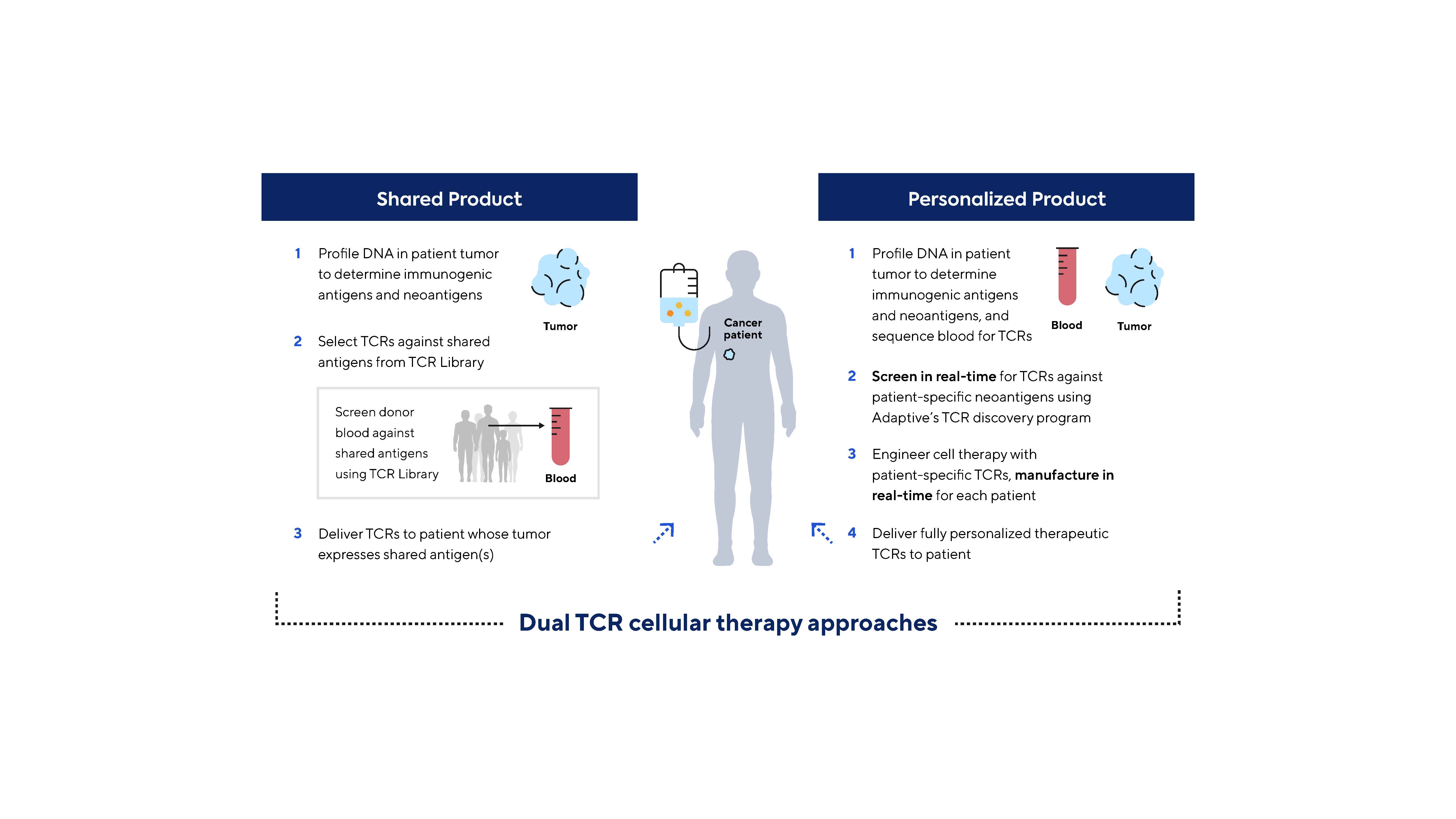
遺伝子技術プロトコルはIMの薬物発見における巨大な潜在力を証明した。Genentechプロトコルによると,癌T細胞免疫療法のための2つの製品開発経路が探索されており,このプロトコルによると,Genentechは我々の免疫薬物プラットフォームを用いてTCRを発見·特徴づけるTCRを用いて細胞薬を設計·製造しようとしている
11
Genentechプロトコルによると,IMはGenentechがTCRに基づく癌細胞療法の2種類の開発をサポートし,固形腫瘍患者の治療に用いられている。最初の新しい抗原指向細胞治療候補製品は最近FDAの承認を得て、臨床に入る予定である。
IM業務はまた、多発性硬化症、クローン病、1型糖尿病、関節リウマチなどの自己免疫疾患の新しい標的を治療するために、一連の潜在的な免疫に基づく療法を進めている。自己免疫では,免疫系が自己抗原を攻撃し,これは通常我々の体内で発見されているヒトタンパク質である。具体的には,T細胞は疾患を引き起こす可能性のある“自己”と“非自己”抗原を区別する能力を失っている。例えば多発性硬化症では新たな自己抗原が発見され,潜在的な治療標的であることが検証されている。多発性硬化症はT細胞を介した疾患であり、主に未知の自己抗原に関連し、現在の治療方法は発病標的に対する特異性が不足し、治療効果が良くなく、そして著しい副作用のリスクがある。MS患者において共有·集積された特定のTCRを認識·検証したことにより,この特定の自己抗原の発現が可能となり,この特定の自己抗原がMSにおいて病原的な役割を果たしている可能性が高いと考えられる。自己抗原の治療標的としての確認が行われており,今後数年以内に薬物発見を行い,その標的に対する薬物治療の最適な治療法を選択し,治療候補薬を指定する予定である。
私たちの以下の分野での能力を拡張します T細胞自然攻撃のヒト白血球抗原提示の疾患特異的エピトープを発見する以外に、著者らは病原性標的抗原を識別し、クローン病、その他の自己免疫疾患、例えば関節リウマチと1型糖尿病を含む炎症性腸管疾患の治療開発に応用しており、これらの疾患の中で、より的確かつ特異的な治療に対して非常に高い満足されていない需要がある。
私たちの競争優位は
著者らは適応性免疫システムの内在生物学を利用して臨床製品とサービスを開発し、私たちの核心競争優位を利用することで人類の健康を改善する。
12
私たちの戦略
著者らの重点は著者らの免疫医学プラットフォームと競争優勢を利用して変革性の臨床解決方案を開発することであり、これらの解決策は一連の疾病を有する患者に使用することができる。
13
戦略的協力と他の合意
遺伝子テークプロトコル
2018年12月,我々はGenentech合意を達成し,多くの癌の治療に新たな抗原ガイドT細胞療法を開発,製造,商業化した。遺伝子テークプロトコルにより、著者らは特定の新しい抗原を最も有効に識別し、直接標的とすることができるTCRをスクリーニングと識別し、遺伝子テークは臨床、監督と商業化を担当する。遺伝子テークプロトコルの間、私たちはいくつかの明確な排他的義務またはいくつかの細胞療法の開発と商業化に関する制限に同意する。
2019年2月、私たちは遺伝子テークから3.00億ドルの前金を受け取り、2023年、私たちはFDA Indが私たちの遺伝子テークプロトコルに従って最初の細胞治療製品候補の1000万ドルの記念碑的支払いを受けた。時間の経過とともに、指定された規制マイルストーンを実現する際に最高6,500万ドル、指定された開発マイルストーンを実現する際に最高3.00億ドル、指定されたビジネスマイルストーンを実現する際に最高14億ドルを支払うなど、約18億ドルを得る資格がある可能性もある。遺伝子テークはまた,戦略協力による共有製品や個人化製品のグローバル純売上高から1桁中央値から10代程度までの分級特許使用料を支払うが,ある程度の削減が必要であり,総下限は最低限度である。遺伝子テークプロトコルは、2023年、2022年、2021年12月31日までの会計年度で、それぞれ私たちの収入の25%、34%、40%を占めている。
Genentech協定はすべての印税支払いが満期になるまで継続されますが、双方の合意、どちらか一方が治癒していない重大な違約、どちらか一方が倒産した場合に終了するか、Genentechが事前に書面で通知して簡単に終了することができます。
マイクロソフト協定
2017年12月、我々はマイクロソフトと戦略的協力協定を達成し、TCR配列とそれに結合した抗原をマッピングし、1回の血液テストから多くの疾患を早期に発見する診断テストの開発を目指した。
マイクロソフトプロトコルによると、マイクロソフトは機械学習と計算統計学を著者らの臨床免疫グループ学データに応用し、予測モデルを生成し、TCR配列をそれらが結合した抗原にマッピングできるようにした。マイクロソフトプロトコルによると、私たちは、私たちのTCR抗原マップを使用して臨床製品を商業化する権利を含む、これらの予測モデルおよび私たちのTCR抗原マップの背後のデータのすべての権利を保持する。私たちとマイクロソフトはお互いに相手の知的財産権のいくつかの許可を与え、マイクロソフト協定とほぼ似た協力とプロジェクトの面でいくつかの明確な排他的義務を負うことに同意した。
マイクロソフト協定の期限内に、マイクロソフトのAzureクラウドサービスを標準バッチ価格で独占的に使用し、最低Azure消費要件を満たすことに同意します。Microsoftプロトコルの全期間内およびその後5年間にMicrosoft Azureプロトコルの直接結果として開発された各診断製品をホストすることにも同意した.また,マイクロソフトの免疫組織学人工知能サービスを独占的に用いてTCR抗原マッピングを行うことにも同意し,これは我々がマイクロソフトと協力して開発したすべての技術,製品,サービスに関連している。
マイクロソフト協定の期限は7年で、双方の合意で終了することもできるし、治癒していない重大な違約の場合はどちらか一方で終了することもできる。マイクロソフトの合意に参加すると同時に、マイクロソフトは2019年7月の初公募終了時に普通株に変換するF-1シリーズ転換可能な優先株株を購入した。
収入権益購入協定
2022年9月,吾らはOrbiMed Advisors LLCの連属会社OrbiMed Royalty&Credit Opportunities IV,LP(“OrbiMed”)と収入利息購入プロトコル(“購入プロトコル”)を締結し,買い手(“買い手”)の担保エージェントおよび行政エージェントとした.購入契約によると、私たちは買い手から1億244億ドル(“第一次支払い”)を受け取り、費用を差し引いた。(I)2025年9月12日までに7500万ドルを得ることを要求すれば、(Ii)2025年9月12日に行われるいくつかの許可された買収(“第3次支払い”)に関連することを要求すれば、5000万ドルを得る権利があり、いずれの場合も資金条件によって制限される場合がある。私たちの購入プロトコルの下での義務を保証するために、私たちと私たちの子会社は、OrbiMedによるコアプラットフォーム技術資産の保証権益を付与していますが、購入プロトコルで定義されているいくつかの慣行から除外されています。
14
この等支払いの対価格として、買い手は、すべての公認会計基準収入(“収入ベース”)のパーセンテージ(“適用支払率”)に基づいて、吾等からいくつかの利息収入(“収入利息”)を受け取る権利があるであろう。1回目の支払いのみを支払った場合、適用される支払率は四半期収入ベースの5%となる。1回目の支払いと2回目の支払いの両方が支払われた場合、適用される支払率は四半期収入ベースの8%となる必要がある。1回目の支払い、2回目の支払い、および3回目の支払いがともに支払われた場合、収入利息に適用される支払率は四半期収入ベースの10%となるべきだ。収入利息の支払いは、各財政四半期終了後45日以内に四半期ごとに支払わなければならない(収入ごとに利息支払い)。OrbiMedが2028年9月12日までにその投資資本の合計(“累積買い手支払い”)以上の収入利息支払いを受けていない場合、収入金利は1つの金利に引き上げられるべきであり、私たちの累積収入基数に遡ると、収入利息支払いはすべての累積買い手支払いの合計に等しいことになる。
OrbiMedは、2032年9月12日までにリターン上限の金額を全額返済していない限り、累積買い手支払いの165%を受信するまで、100%の収入利息支払いを得る権利があり、この場合、リターン上限は、累積買い手支払いの175%に増加しなければならない。
2023年および2022年12月31日までの年度の購入協定では、吾らはそれぞれ1,380万ドルおよび420万ドルの利息支出を発生させている。
加工と製造
私たちはワシントン州シアトルの実験室で臨床と研究サンプルを処理している。著者らのシアトル実験室はCLIA認証、アメリカ病理学者学会認証と国際標準化組織13485認証を通過した。医療提供者や研究や生物製薬顧客から試料を受け取った後,必要であれば試料からDNAを抽出し,増幅し,配列決定やデータ分析に備えている。著者らの全過程において、著者らは厳格な品質管理システムを採用し、品質体系法規(QSR)及びCLIA、CAPとその他の適用する国家許可と認証要求に符合することを目的とした。
我々に提出された試料中の免疫受容体を加工および配列決定するために、多重PCR主混合物、酵素、高スループット多循環配列決定試薬および他の材料を含む独自のプライマー混合物と商業材料との組み合わせを使用し、必要に応じて様々な第三者サプライヤーから必要に応じてこれらの材料を取得し、組み立てた。私たちの多くの処理手順は、一貫性と効率性を確保するために自動化装置を使用している。配列決定はIllumina NextSeqシステムを用いて行われ,我々は製品とサービスの期待用途に応じてこのシステムを適切に同定した.
我々のTCR抗原マップと薬物発見計画については,ワシントン州シアトルとカリフォルニア州サンフランシスコ南部の実験室で業務を行っている。これらの実験室は細胞選別,組織培養などの加工設備を有している。
私たちは限られた数量のサプライヤーを使用したり、場合によっては単一のサプライヤー、私たちの実験室設備と材料を使用します。私たちは過剰在庫レベルを狙ったり蓄積したりすることでこの集中リスクを管理し、必要に応じて代替サプライヤーを見つけることができると信じています。しかし、私たちのサプライヤーが私たちの需要を十分に履行したり、満足したりできない場合、私たちは巨額のコストを負担し、新しいサプライヤーを探すために多くの精力を投入することを要求される可能性があり、サンプルを処理したり、私たちの製品やサービスを開発し、それを商業化する上で遅延に直面する可能性があります。例えば,Illumina NextSeqシステムを購入したが,Illumina,Inc.(“Illumina”)もこのシーケンサーのために設計された試薬を提供してくれた。従来のIlluminaからこれらの試薬を入手しているが,使用する試薬を交換しなければならない場合には,置換シークエンサーを購入·同定し,試薬を検証し,既存の分析の様々な側面を再検証する必要があるかもしれない。
分布
私たちは2011年に最初のサンプルを処理し、2013年に最初のclonoSEQ報告書を発表した。その時から、私たちは私たちの顧客基盤を拡大することに集中してきた。私たちは主に自分の内部販売チームを通じて私たちの製品を販売します。著者らの販売とマーケティング努力はリード学術機関、生物製薬会社、研究機構と契約研究機構の部門責任者、実験室主任、主要な研究者、核心施設主任、臨床医師、支払人及び研究科学者と病理学者を対象としている。私たちは直接電話、貿易展示会、シンポジウム、学術会議、ネット展示、その他の形式のインターネットマーケティングを通じて、ターゲット顧客の私たちの製品とサービスに対する認識を高めることを求めています。我々の薬物発見作業は内部に集中しており,1社以上の生物製薬会社と協力して行うことも可能である。
知的財産権
私たちは私たちの免疫薬物プラットフォーム、このプラットフォームを利用した製品とサービス、業界における私たちの名声を保護するために、広範な全世界の知的財産権の組み合わせを持っている。
15
2023年12月31日現在、私たちは、私たちが何をしているのか、私たちが何をしようとしているのか、他の人が何をしているのか、そして他の人が私たちと競争する可能性がある何をするのかをカバーすることを目的としている450件を超える有効な発行特許と55件を超える特許出願を持っているか、または制御しています。私たちの2009年最初の特許出願から、私たちの製品の組み合わせは、適応免疫システムを利用して研究、診断、治療応用のための私たちの努力を反映するためにオーダーメイドされてきた。我々の特許主張は,適応免疫受容体分子だけでなく,免疫細胞受容体の配列決定,クローンと免疫能の決定,疾患の診断,免疫療法の反応予測,新薬候補の決定のための独自の強力な技術まで延びている。私たちが付与した特許保護は一般的に2029年から2040年の間に満了する。
私たちが開発した重要な技術は、不適切な開示や使用がないことを確実にするために、商業秘密保護計画によって保護されている。我々のノウハウには,免疫受容体のコード配列,抗原反応性,セキュリティプロファイルが含まれており,規模が大きく,拡大している。協力者がいても,契約と入念なコミュニケーションにより,我々の免疫薬物プラットフォーム技術へのアクセスは限られており,厳しく制御されている。私たちは、私たちまたは協力者がそれを改善し、そのプラットフォームを使用することによって生成されたデータを保持する権利を含む自己免疫薬物プラットフォームを持っている。
私たちはまた既存と計画された市場で私たちの製品とサービス名と宣伝スローガンの商標登録を行います。
知的財産権の組み合わせの数の多さ
2023年12月31日現在、私たちの知的財産権の組み合わせは、
特許組合
私たちは重要なビジネス的意味を持つ市場で広範な特許組み合わせを開発し、私たちの技術の重要な側面を持っていると主張し、2009年に私たちの最初の特許出願から始まり、これらの特許出願はフレッド·ハッチンソン癌研究センター(“フレッド·ハッジ”)から独占的に許可された。私たちが行っている特許戦略は、私たちの特許投資からリターンを得ることであり、これは数よりも実質的な品質を重視して、私たちが使用する技術と他の人が開発する可能性のある私たちの地位を中心に設計された防御可能な堀を構築することである。
私たちは合理的な可能性で承認された特許請求を優先する。特定の発明の特許性が疑問視された時、私たちは通常、それを商業秘密として保護することを選択する。しかし、場合によっては、適用される特許法の状態が変化している場合には、米国で自然に産生される分子(TCRを含む)の特許資格のような特許性制限を推進することが求められる可能性がある。
16
適応免疫の測定方法
2009年、私たちの共同創始者であるHarlan Robins博士は免疫配列決定の保護を求めるために米国の臨時特許出願を提出した。本発明は、対象の適応免疫系状態を評価するための方法に関する。1つ以上の時点における免疫系状態を評価するためのバイオマーカーとして、再編成されたTCRまたはBCRのVおよびJセグメント遺伝子が使用される。承認されたクレームは、より多くの評価技術を得るために、特定の増幅プライマーセットを使用するまで延長され、係属中のクレームは行われている。この出願はフレッド·ハッジによって独占的に許可され,それ以来31件以上の特許出願が生成され,その多くは2023年12月31日に米国特許番号9,809,813を含む承認を得ている。
核酸増幅反応を最適化する
核酸の増幅は、増幅された分子が多すぎるか少なすぎるか、由来材料(例えば、血液試料)中に存在する数字を歪曲する。ロビンズ博士は、ポリメラーゼ連鎖反応に基づく試料中のTCRおよびBCRコード配列定量の精度を向上させるために、このような偏差を補正する方法を発明した。請求項1に記載の方法は、合成テンプレートを用いて、試料細胞中の再配置されたVおよびJ受容体断片の核酸配列を反映する。以来、28件を超える関連特許出願が提出されており、その多くは、米国特許番号9,371,558および10,214,770を含む2023年12月31日に承認されている。
病気の診断とモニタリング
2015年にSequenta,Inc.(“Sequenta”)を買収するために、Sequentaの広範な特許組合せを購入した。この製品の組み合わせは、抗原曝露に対応するために、NGSを使用してT細胞ベースの免疫応答を識別および定量化することを要求する124特許出願を含む。血液および骨髄を含む試料中のTCRおよびBCRDNA、リボ核酸または無細胞DNAは、自己免疫疾患、感染および癌を含む疾患の検出、予測および監視に使用される。ポートフォリオは、2023年12月31日現在、米国特許番号8,628,927および8,236,503を含む112以上の特許を付与している。
我々の診断方法は、MRD(私たちのB細胞のclono配列番号診断試験の目標に基づいて、疾患負担が治療または緩和中にどのように変化するかを評価するための)およびT検出(我々のT細胞に基づく診断試験)にも適用可能である。我々が提出したMRD評価、診断方法、および診断意義を有するTCRに関連する他の出願は、米国特許番号9,824,179および11,047,008を含む複数の特許を取得している。新冠肺炎を含む特定適応のTCRによる診断信号の他の特許出願が待っている。
TCR−抗原マップ
マイクロソフトとの協力では,患者の血液中で活性化された免疫受容体のシグナルや反応を知ることで,癌や他の疾患の最初の段階でそれらを検出する診断製品を開発している。協力前に,抗原に曝露された濃縮T細胞集団を産生し,曝露前の細胞集団と比較またはアルゴリズムを用いてその抗原特異性を認識するための10件の関連特許出願を提出した。私たちは、アルゴリズムに基づく方法によって抗原特異性を特徴付けることに関するより多くの特許出願を提出している。
ミラ
我々は,T細胞を1組の複数の抗原に曝露することによりTCRsの抗原特異性を決定するバイオインフォマティクスに基づく方法の特許保護を開発·求めている。抗原曝露は、インキュベーションまたは提示によって行うことができ、例えば、別の細胞における組換え発現によって行うことができる。これらの方法は、2つのTCR鎖を対にし、高い親和性のTCRを同定するためにも使用することができる。2023年12月31日現在、米国特許番号10066,265を含む複数の特許が付与されている。
ペアシーケンス
自然界では,TCRsとBCRsは対をなす鎖のヘテロ二量体の形で存在し,各鎖は異なる染色体にコードされている。免疫シークエンシングは各鎖のヌクレオチド構造を掲示したが、どの鎖が同源対であるかを明らかにすることはできない。我々は、我々のpairSEQ技術に配備された1つの方法の特許保護を含む、TCRおよびBCRの2つのチェーンをペアリングするための様々なバイオインフォマティクスベースの方法を開発し、求めている。我々の方法はまた,特定の抗原標的に対する受容体鎖対の認識を可能にする。2023年12月31日現在、50件以上の関連特許出願が提出されており、そのうちの半分近くが米国特許番号10077478を含むライセンス特許となっている。
17
免疫治療に対する反応性を評価する
我々の免疫シークエンシング技術を用いて,免疫治療,ワクチン,感染に対する反応を予測する方法を開発した。このため、再配列されたTCRまたはBCRシーケンスは量子化され、それらのレベルまたは周波数は、異なる時点で比較される。2023年12月31日現在、20件以上の関連特許出願が提出されており、その大部分は米国特許番号10,221,461を含む承認を受けている。
治療用抗体
我々は,SARS−CoV−2,インフルエンザ,呼吸器合胞体ウイルス,炎症性腸疾患,MSなどで標的抗原に対する中和抗体を製造しているTruABという治療用抗体発現過程を開発し,その中のいくつかの抗体に対する特許出願が提出され待機中である。
ワクチン
我々のパートナーであるニコード治療会社とともに,免疫シークエンシングに基づく薬物発見作業がワクチンの開発に情報を提供している新冠肺炎ワクチンに対する特許出願を提出した。
治療用TCR
WT−1関連癌の細胞治療において潜在的な実用価値を有するWT−1抗原反応に対するTCRの特許出願が承認されている。我々はまた,他の癌に対する抗在来反応のTCRの特許出願を出願しており,これらの抗原は遺伝子テークとの連携に興味を持っている。
許可されていない知的財産権
私たちは私たちの免疫薬物プラットフォーム、製品、サービスの大部分を開発しましたが、私たちはたまに第三者が持っている発明を許可したり、買収したりして、私たちの特許権の実力を強化し、運営の自由を確保します。
Robins博士とFred Hutchの早期作業は、米国および海外の128の特許および特許出願をカバーする免疫配列決定方法およびツールの発見をもたらし、これらの特許および出願は私たちが独占的に許可した。私たちの権利は世界各地のすべての使用分野に適用され、再許可可能だ。ライセンス付与された特許権が私たちが販売している製品またはサービスに延長された場合、ライセンス製品の純売上高の0.75%の使用料をFred Hutchに支払います。
Sequentaを買収することによって、私たちはまた、米国、ヨーロッパ、オーストラリア、および中国で出願されたiRebertoire,Inc.の特許の独占的実付許可、および再許可権を取得した。この許可は、世界的に任意の増殖性疾患の診断、予後、治療およびモニタリングのために使用され、増殖性疾患の細胞をコードすることができる免疫受容体の再配置核酸が、ALL、CLL、急性骨髄性白血病、慢性骨髄性白血病、慢性骨髄性白血病、などの腫瘍浸潤性リンパ球を含まないが、リンパおよび髄系増殖性疾患を含むが、これらに限定されない疾患のマーカーとして使用することができる。ホジキンおよび非ホジキンリンパ腫、MMなどの形質細胞腫瘍、意味不明の単クローン性ガンマ病、単クローン性B細胞リンパ球増加症および骨髄異形成症候群。
Sequentaから取得した特許権に加えて,Imdaptive,Inc.および免疫ID S.A.Sから免疫シークエンシングに関する特許組合せの所有権を取得した。
商標
私たちは、当社の会社名、製品およびサービス名、その他の商標またはサービス商標を含む、米国および他の重要なビジネス的意義を有する市場で、様々な商標、アプリケーション、および未登録商標を持っています。私たちの商標の組み合わせは、現在も準備中の製品とサービスのブランドを保護することを目的としています。
18
貿易守秘計画
私たちは、厳しい秘密条件の下で、私たちの業務に重要なことを開示しない限り、他人に私たちのビジネス秘密を漏洩することを防止するビジネス秘密計画を持っています。私たちの商業秘密はいくつかの試薬の組成、検査方案、免疫シークエンシングに関連するデータ、例えば免疫受容体配列を含む。私たちは、従業員、コンサルタント、科学コンサルタント、請負業者、および協力者と秘密協定および発明譲渡協定を確立することによって、商業秘密およびノウハウを保護します。これらのプロトコルは,個人またはエンティティと我々との関係過程で開発または公表されたすべての機密情報は,関係期間および後に秘密にしなければならないことを規定している.これらのプロトコルはまた、私たちのために履行された仕事または私たちの業務に関連するすべての発明、ならびに雇用または譲渡中に構想または完了したすべての発明を、私たちの固有財産としなければならないことを規定している。さらに、私たちの独自の情報が第三者に盗用されることを防止するために、物理的および技術的セキュリティ対策のような他の適切な予防措置を講じた。
私たちは、当社の従業員やコンサルタントと契約を締結することを含む、当社の独自情報およびビジネス秘密を保護する措置をとっていますが、第三者は、実質的に同じ独自の情報および技術を独立して開発したり、他の方法で私たちのビジネス秘密を取得したり、当社の技術を開示したりすることができます。したがって、私たちは私たちの商業秘密を意味的に保護することができないかもしれない。我々の知的財産権に関連するリスクに関するより多くの情報は、“リスク要因-私たちの知的財産権に関連するリスク”を参照されたい
競争
生物技術と製薬業界は、生命科学研究、臨床診断と薬物研究開発領域を含み、技術進歩が迅速で、競争が激しく、知的財産権を高度に重視する特徴がある。免疫薬物の広さと将来性を考慮して、著者らは生命科学ツール、診断、製薬と生物技術会社、学術研究機構と政府機関及び公共と私営研究機構を含む多くの異なる源からの激しい競争に直面しており、著者らのプラットフォームの各コンポーネント及び製品とサービスに関連している。免疫薬に対するより広範な関心と増加のため、私たちは競争が激化すると予想する。しかし,我々の規模,精度,速度,それによる臨床適応は,競争相手とは異なると信じている。
臨床診断では、clonoSEQが直面している競争は主に内部、特に米国以外のフローサイトメトリー機構から来ている。癌早期検出製品を開発した会社からの競争に直面している可能性もあり、これらの会社が開発した適応は現在のところ固形腫瘍に対するMRD評価法のようなclono配列と競合することはできない。
薬物発見において,免疫医学分野の臨床試験はいくつかの産業界や学術界の参加者に求められている。
いくつかのバイオテクノロジー会社や大手バイオ製薬会社が免疫薬を開発している。私たちの多くの既存または潜在的な競争相手は、単独またはパートナーとの協力にかかわらず、研究開発、製造、規制承認およびコンプライアンス、販売と流通の面で、私たちよりも多くの財務資源と専門知識を持っている。免疫薬物領域に関連する生命科学研究、臨床診断或いは薬物研究開発会社の合併と買収は更に多くの資源が著者らの数の少ない競争相手に集中する可能性がある。規模が小さいかスタートアップ段階にある会社も重要な競争相手になる可能性があり、特に大手や成熟会社との協力で手配する。これらの競争相手はまた、合格した科学·管理職を募集し、維持し、私たちのプロジェクトと相互補完や必要な技術を獲得する面で私たちと競争している。
もし私たちの競争相手が私たちの製品やサービスよりも正確で、使いやすいか、より費用効果のある研究や診断製品やサービスを開発し、商業化すれば、私たちのビジネス機会は減少または消失する可能性がある。競合他社の治療製品は、パートナーと協力して開発した任意の治療製品と比較して、より安全で、より効果的で、管理が容易で、またはよりコスト的であることが証明される可能性がある。私たちの競争相手も私たちよりも早くFDAや他の規制機関のその製品の承認を得ることができ、これは私たちの競争相手が関連市場に入る前に強力な市場地位を確立することをもたらすかもしれない。
政府の監督管理
生命科学研究に限られた技術
我々の核心研究製品適応免疫シークエンシングはアメリカでは研究にのみ使用されている(“RUO”)ツールであり、生物製薬会社などの第三者にデータを提供し、これらの会社自身も潜在的な診断と治療製品とサービスを研究·開発しており、後で規制機関(例えばFDA)の調査と許可、許可或いは承認を求める可能性がある。
19
FDAの長期規定によると、RUO製品は単独の監督管理分類に属する。FDAの角度から見ると、研究用途のみに使用され、RUOと表記された製品は大多数の監督管理によって制御されていないため、以下に議論する臨床診断製品の監督管理要求の制約を受けない。したがって、RUO製品は、FDA承認、許可、または承認を得ることなく、研究用途のために使用または配布することができる。製品は“研究用にのみ使用される”と明記しなければならない。診断手続きには使えない“RUO製品は安全性、有効性或いは診断用途と関係があると主張できず、人類の臨床診断用途にも応用できない。そのため、“連邦食品、薬物と化粧品法”(FDCA)によると、RUOラベルが貼られているが、臨床診断用途に使用しようとしている製品はFDAから偽とミスブランドとみなされ、FDAの法執行行動の影響を受ける可能性がある。FDAは、RUO製品の予期される用途を決定する際に、その製品がどのように販売され、誰に販売されるかを含む、RUO製品の流通および使用に関連するすべての場合を考慮する。FDAがある会社の製品に対するRUO地位に同意しない場合、同社はFDAの法執行活動の影響を受ける可能性があり、これらに限定されないが、同社にその製品の許可、許可、または承認を求めることを要求する。FDAがRUO製品の偽およびミスブランドを混入していると判断した場合、法執行はまた、警告状、差し押さえ、禁止、および/またはFDCA違反に対する刑事罰金を含む可能性がある。
アメリカの臨床診断学
我々の最初の診断製品clonoSEQは、MM患者および最初から処置されているALL患者の骨髄サンプル中のMRDを検出および監視するためのFDAのマーケティング許可を2018年9月に取得し、以下にさらに説明するように、clonoSEQおよび将来の血液悪性腫瘍におけるMRDを測定するためのDNAベースのテストをクラスIIに分類する。2020年8月,510(K)計画を提出した後,ClonoSEQに対するFDAの承認,骨髄および血液試料中のCLLを得た。著者らはまた2021年にFDAによる血液サンプル中のすべてのNHLの許可を得て、CLIAによってLDTとしてNHL(DLBCL)テストを発売し、そしていくつかの他のNHLサブタイプの検証研究を積極的に推進している。
アメリカでは、医療機器はFDAによるFDCA及びその実施条例及び他の連邦と州法規と法規による広範な監督管理を受けている。FDAは医療機器の設計、開発、臨床前、分析と臨床テスト、製造、安全性、有効性、許可、許可或いは承認、記録保存、包装、ラベル、貯蔵、不良事件報告、広告、販売促進、マーケティング、販売、流通と輸出入を監督する。インビトロ診断製品(“IVDS”)は、特定の化学物質、遺伝情報、または他のバイオマーカーの存在を含むが、これらに限定されない疾患、状態または感染を診断または検出するための試薬および装置を含む医療デバイスである。予測性、先見性、およびスクリーニング性テストは、静脈奇形であってもよい。
医療機器が市場に投入された後、多くの監督管理要求を満たす必要がある。これらの措置には
適用される規制要件を遵守しないことは、警告状を含むがこれらに限定されない制裁を含む可能性がある制裁を含む可能性がある法律執行行動をとることができるFDAに、罰金、禁止および民事処罰、設備のリコールまたは差し押さえ、操作制限、部分的な一時停止または完全な生産停止、新規設備の承認を拒否する510(K)の許可または上場前承認(PMA)、許可または承認の撤回、および民事または刑事起訴を引き起こす可能性がある。
EUにおける地位
欧州連合(“EU”)では,静脈内投与薬は“CEマーク”を獲得することで市場に投入され,自己認証により適合していることが示唆された離体する診断医療機器指令(“IVDD”)。ClonoSEQは2019年5月にすべての血液と骨髄B細胞悪性腫瘍のためにCEマーカーを獲得した。この計画の規定には:
20
2017年5月26日、EUは新たな規制枠組みを発表した離体する診断性医療機器条例(“IVDR”)は,IVDDに代わる。私たちのEUの製品は2026年5月までにIVDR要求に適合しなければなりません。これは適用される過渡的な条項に依存して、それから完全に適合する必要があります。そこで,2023年にClono配列番号のIVDR承認申請を提出した。IVDRはIVDDよりも規制がはるかに厳しく,より多くのIVD機器が市場投入前に通知機関の審査を受けることが要求される。その前に、私たちの製品はEUでのIVDDの商業化の要求を満たし続けなければならない。
アメリカ連邦と州の研究室の規制は
私たちのいくつかの施設での業務は臨床実験室としての役割に関連していることを考慮して、私たちはいくつかの連邦と州許可証、証明書と許可証を持っていなければならない。
連邦認証について、CLIAはすべての実験室に厳格な品質標準を確立し、これらの実験室は人類からのサンプルに対してテストを行い、目的は疾病の診断、予防或いは治療に情報を提供し、或いは健康を損害或いは評価することである。臨床実験室としては,高複雑性試験の適合性証明書のような実験室で行われた試験の複雑さに応じてCLIA証明書を取得しなければならない。CLIAはまた各種の運営、人員、施設管理、品質と熟練度の要求を遵守し、その臨床実験室検査サービスの正確、信頼性と適時を確保することを要求した。CLIAコンプライアンスや認証も、政府支払人や多くの個人支払者にサービス料金を提供する資格があるための前提条件である。また、私たちは2年ごとに調査と検査を受けて、計画基準の遵守状況を評価し、追加的な抜き打ち検査を受ける可能性がある。高複雑性試験を実行する実験室は、より簡単な試験を実行する実験室よりも厳しい要求を満たすことが要求される。
CLIAの要求に加え,CAPの認証計画に参加することを選択した。CLIAの監督管理を担当するアメリカ医療保険と医療補助サービスセンター(CMS)は、CAP標準はCLIA法規と同等或いは更に厳格であると考え、そしてすでにCAPを公認の認証組織として許可した。認可された実験室では,CMS検査の代わりにCAPが検査を行った。したがって,CAP実験室認可計画の認可を得たことから,われわれもCLIAに適合していると考えられる。
CLIAは、一つの州は連邦法律下よりもっと厳しい実験室法規を採用することができ、いくつかの州はすでに自分のもっと厳格な実験室法規要求を実施した。ワシントン州を含むいくつかの州は、連邦政府によって少なくともCLIAと同様に厳しいと考えられる実験室法規を有しているため、これらの州制度の下で許可された実験室はCLIAの制限を受けず、州衛生部はCMSによって発行された証明書ではなく、CLIA番号および州医学試験会場許可証の発行を許可されている。私たちの研究室は必要なワシントン許可証を持っています。州法律は実験室人員がある資格に符合し、ある品質制御プログラムを規定し、施設要求或いは記録維持要求を規定することを要求する可能性がある。
いくつかの州はまた、これらの州からの標本を受け入れる州外実験室は許可証を取得しなければならないことを要求している。例えば、ニューヨークは、実験室から提供された各LDTに対して現場検査と許可を行った後に発行され、人員資格、熟練度テスト、実物施設と設備、および品質管理基準の要求を含む様々なCLIAおよびCAPよりも厳しい要求を持つことを実験室に要求する。私たちの研究室はメリーランド州、ロードアイランド州、ペンシルベニア州、ニューヨーク州、カリフォルニア州に必要なライセンスを持っています。
時々、他の州は州外の実験室に許可証を取得して、その州からの標本を受け入れることができるかもしれない。もし私たちが他の州にこのような要求があることを発見した場合、あるいは他の州がこのような要求について私たちに連絡した場合、私たちは私たちがどのようにこのような要求を遵守すべきかに関する州規制機関の指示に従うつもりだ。
もし臨床実験室がCLIA認証、CAP認可或いは国家許可証或いは許可に符合しないことが発見された場合、適用される監督管理機関は臨床実験室の認証、認可、許可証或いは許可証を一時停止、制限或いは保留し、民事罰金を評価し、そして具体的な是正行動計画、及びその他の制裁を実施することができる。
21
LDTSはアメリカにあります
FDAは従来法執行自由裁量権を行使し、大多数のLDTを規制しなかった。そのため,LDTSはFDAによる医療機器の上場許可や承認プログラムや上場後の制御を受けない。LDTは一般に、1つの実験室内で設計、開発、検証、使用されるテストと考えられる。CLIAにより“高複雑性”と認証された実験室は、LDTを開発、製造、検証、実行することができる。我々のワシントン州シアトルの実験室では、ClonoSEQはLDTとしてNHLを含む他のリンパ系悪性腫瘍のMRDを評価し、他のタイプの標本に使用することができる。
この点で,国会は,キットやLDTなどの体外臨床試験(“IVCT”)のマーケティング(“検証正確先端IVCT発展法案”,あるいは“有効法案”)を監督するための枠組みをFDAのための立法を提案している。有効法案によると、FDAはIVCTsを監督し、患者を深刻または不可逆的な傷害に曝露した高リスクIVCTsと新型IVCTsの発売前審査を要求する。現在の草案によれば、有効法案が成立した場合、既存のLDTは承認された方式で廃止される。新たな低リスクIVCTについては、開発者は、特定のIVCT審査および後に開発されたテストの技術証明書を審査して発行するための代表的なIVCTをFDAに提出する。有効法案がどのような形で国会で可決されたかは不明であるが、通過法案は我々LDT製品に必要な規制審査の厳格性を増加させる可能性がある。有効法案が成立しなければ,FDAはLDTに対して法執行自由裁量権を行使することを決定する可能性があり,特にLDTが患者にとってリスクと考えられる場合がある。そのため、FDAの法律や政策の解釈と応用の自由度を考慮して、LDTのマーケティング規制経路は不確実性の影響を受けている。
連邦と州プライバシー、安全、違反通知法
多くの州と連邦法律は個人情報あるいは個人が健康情報を識別できる処理を管理している。連邦レベルでは、1996年の“健康保険携帯性と責任法案”(HIPAA)と2009年の“経済·臨床健康情報技術法案”(HITECH)の行政簡略化条項に基づいて、アメリカ衛生·公衆サービス部(HHS)は法規を発表し、ある医療保健提供者と他の“カバー実体”及びその“ビジネスパートナー”の使用或いは開示された“保護された健康情報”のプライバシーと安全を保護する基準を確立した。HIPAAとHITECHによると、私たちが守らなければならない3つのデータ保護に関連する主要な法規は、プライバシー法規、セキュリティ法規、セキュリティ違反通知法規を最終的に発表しました。
プライバシー法規管理は,医療保健提供者および医療保険計画の“保護された”健康情報の使用と開示を保証する。それらはまた、保護された健康情報を含むいくつかの記録にアクセスまたは修正する権利、または保護された健康情報の使用を制限または開示することを要求する権利を含む、保険医療提供者によって維持されているその保護された健康情報に対して個人が所有するいくつかの権利を規定する。セキュリティ条例は、電子的に送信または電子記憶された保護された健康情報の機密性、完全性、および利用可能性を保障する要求を規定する。他の事項以外に、HITECHはいくつかの健康情報安全違反通知要求を確立した。保証エンティティは、衛生·公衆サービス部及び各影響を受けた個人が保護されていない保護された健康情報に違反することを通知しなければならず、500人以上が漏洩した場合には、メディアにも通知しなければならない。
HIPAA違反行為は民事と刑事処罰を受けるだろう。さらに、私たちが提出した電子医療クレームおよび支払い取引がHIPAAおよびHITECHによって確立された電子データ伝送基準に適合していない場合、私たちへの支払いは遅延または拒否される可能性がある。
連邦貿易委員会法(“FTCA”)第5節(A)節も連邦レベルでデータのプライバシーとセキュリティを規制するために使用されている。米国連邦貿易委員会(FTC)の規定によると、消費者の個人情報の安全を保護する適切な措置を取ることができなかった、あるいは会社のプライバシー通知に違反して個人情報を使用または開示することは、FTCAに違反する不公平または詐欺的な行為またはやり方を構成し、あるいは商業に影響を与える可能性がある。連邦貿易委員会は、ある企業のデータセキュリティ対策が、消費者情報の感度および数、その業務の規模および複雑さ、および安全性の向上および脆弱性を低減するために使用できるツールのコストのために合理的かつ適切になると予想している。プライバシーの法律や法規を遵守するシステムを持って維持しているにもかかわらず、これらの法律や法規を守らなければ、FTCの法執行行動と罰金に直面する可能性がある。
さらに、特定の州の法律は健康情報と個人情報のプライバシーと安全を管理する。健康情報のプライバシーと安全を管理するいくつかの州法律はHIPAAよりも厳格であり(患者のこれらの州法律の執行を規定することを含む)、しかも往々にして重大な面で差があり、同じ効果が生じず、コンプライアンス仕事を複雑化させる可能性がある。最近ではワシントン州の“私の健康私のデータ法案”、カリフォルニア消費者プライバシー法案、カリフォルニアプライバシー権利法案および関連法規、コロラド州プライバシー法案など、同様のコンプライアンス複雑性が導入されている州プライバシー·セキュリティ法も多い。また、州ごとにコロンビア特区、グアム、プエルトリコに州違約通知法があります。適用される場合には,これらの法律を遵守しなければ,重大な民事や刑事罰および私的訴訟を引き起こす可能性があり,詳細は“リスク要因”の節を参照されたい。
22
プライバシーやデータ保護義務を会社に直接課す法律のほかに,データプライバシーに関連するが完全に関連していないデータ分野を管理する法律法規にも興味が高まっている.このような法律の分野は遺伝子とゲノムデータの使用と試験に関するものだ。連邦“遺伝情報非差別法”のほかに、最近成立した州法(例えば“カリフォルニア遺伝情報プライバシー法”)があり、これらの法律は各州の立法スケジュールに引き続き登場している。州一級にも似たような法案草案があり、機械学習、人工知能、モノのインターネット、人類標本の使用を規範化する。
EUの一般データ保護法規とその他の国際プライバシー法
一般データ保護条例(GDPR)は、欧州経済地域(EEA)内の個人の個人情報を収集して処理するための要求を設定する法的枠組みである。GDPRはデータ管理と個人権利の原則を規定するとともに,収入に基づく可能性のある巨額の罰金を処罰した。ヨーロッパ経済圏の人々の個人情報を処理する米国の会社に適用され、これらの個人情報は、これらの人々に製品またはサービスを提供すること、またはこれらの人々の行動を監視することに関する。米国企業が欧州経済圏に設立した実体の活動範囲内で個人情報を処理する場合にも適用可能である。GDPRは2018年5月25日から実施された。この規定は包括的なプライバシー法であり、従業員の人的資源記録、さらにはオンラインサービスを利用する人のインターネットプロトコルアドレスを含むすべてのタイプの個人情報に適用されることを意味する。
他の多くの国や地域にもプライバシーやデータ保護法があり、その中のいくつかはヨーロッパの枠組みを模倣している。これには,イギリスやスイスのようなヨーロッパ内部で欧州経済圏に属さない国が含まれているため,異なるプライバシーやデータ保護の枠組みの下で動作している.
人工知能や機械学習の進歩に対応するために,世界もこれらの技術の使用を規範化しようと努力している.最終決定を待っている有名な法律は連合の人工知能法案だ。
連邦、州、外国の詐欺と法律の乱用
アメリカでは、様々な詐欺や法律の乱用は守らなければなりません。私たちはCMS、HHSの他の部門、例えば監察長事務室(OIG)、米司法省(DoJ)、司法省内の個別連邦検事室、州や地方政府など、様々な連邦、州、地方当局の規制を受けています。私たちはまた外国の詐欺と法の乱用によって拘束されるかもしれない。
米国では、リベート条例(“AKS”)は、患者の回診を誘導または見返りに、または購入、レンタル、注文または購入、レンタルまたは購入の手配、レンタル、または政府支払者計画に従って精算可能な任意の医療項目またはサービスを注文するために、インフォームドコンセントおよび意図的な場合に提供、支払い、請求または報酬を受けることを禁止している。裁判所は、金融手配のいずれかの目的が患者の回診または他の連邦医療計画業務を奨励することであれば、その手配に他の合法的な目的があるかどうかにかかわらず、その手配はAKSに違反する可能性があると表明した。報酬の定義は、プレゼント、割引、食事、旅行、クレジット手配、現金支払い、相談料、共同支払いの免除、所有権権益、およびその公平な市場価値よりも低い何かを含む任意の価値のあるものを含むと広く解釈されている。AKSの範囲が広いことを認識し、技術的には、医療業界内の多くの無害または有益な手配を禁止する可能性があり、OIGは一連の規制“避風港”を発表した。これらの安全港法規はいくつかの条項を列挙しており、これらの条項が該当すれば、医療提供者や他の当事者に保証され、AKSによって起訴されないだろう。1つの取引または手配が特定の安全港に適合できなかったことは、必ずしも取引または手配が不正であることを意味するわけではなく、または“AKS”に従って起訴されるであろう。これらの場合、各スケジュールは、具体的な状況に応じて評価され、強制実行措置がとられているか否かが決定される。AKS違反に対する処罰は厳しく,監禁,刑事罰金,民事罰金,連邦医療計画から除外される可能性がある。安全港保護を確立する規定は変化する可能性があり、未来の行動に影響を及ぼす可能性がある。多くの州にも反リベート法規があり、その中のいくつかは商業保険会社と患者の自費を含む任意の第三者支払人の精算の物品或いはサービスに適用される可能性がある。AKSへの違反は政府または告発者が断言する可能性があり,連邦民事虚偽クレーム法案の目的により,このような違反による物品やサービスへの支払いクレームが虚偽または詐欺的クレームの理由となる。
民事罰金法規は別の可能な法規であり、この法規によると、臨床実験室は強制的に執行される可能性がある。他の事項に加えて、民事罰金法規は、連邦医療計画にクレームを出したか、またはクレームを起こしたと判定された任意の者に罰金を科し、その人は、主張するように提供されていない項目またはサービスまたは虚偽または詐欺的な項目またはサービスであることを知っているか、または知っているべきである。民事罰金法規はまた、個人が特定の提供者または供給者の物品またはサービスを注文または受け入れることに影響を与える可能性があるので、任意の医療保険または医療補助受益者に報酬を提供または提供することを禁止する。
23
排除法規は、連邦計画に関連した犯罪または医療重罪詐欺または制御物質告発された実体および個人を排除することを要求する。この法規はまた、調査または監査の妨害によって任意の形態の詐欺罪が判定されたAKS、特定の制御対象物質犯罪、その医療許可証が取り消されたり、一時停止された人、および過剰料金または不必要なサービスのためにクレームを出す人を排除することを可能にする。もし私たちが排除されれば、私たちの製品とサービスは連邦医療保険と医療補助を含む任意の連邦計画から精算を受ける資格がなく、これらの計画に参加する他のいかなる実体も私たちとの契約を許可されるだろう。有益な医療プロジェクトやサービスを維持するために、政府は、その組織を除外するのではなく、メーカーの官僚およびキー従業員を除外することを選択することができる。このような法執行行動は、私たちがこれらの個人との接触を禁止することで、業務に悪影響を与え、深刻な名声被害を招く可能性がある。
国会はまた、医療詐欺や乱用行為について刑事責任を追及する法規を公布した。医療詐欺法規は、個人支払者を含む任意の医療福祉計画を故意に実行または実行しようとする計画を禁止する。この法規違反は重罪であり、罰金、監禁、あるいは連邦医療保険や医療補助計画などの政府支払者計画から除外される可能性がある。虚偽陳述法は、重大な事実を故意に偽造、隠蔽、または隠蔽すること、または医療福祉計画、プロジェクトまたはサービスの提供または支払い--公共または個人に関して、任意の重大な虚偽、架空、または詐欺的な陳述を行うことを禁止する。この規制に違反することは重罪であり、罰金、監禁、または政府支払者計画から除外される可能性がある。
虚偽請求法は、他の事項を除いて、いかなる個人又は実体が故意に虚偽又は詐欺的な提出を招いた連邦政府支払者が支払請求を計画した者又は実体も責任を負わなければならないと規定している。虚偽請求法のQui tam条項は、個人が連邦政府を代表して訴訟を起こすことを許可し、被告が連邦政府に虚偽のクレームを提出することによって連邦政府をだまし、これらの個人がエンティティが罰金または和解で政府に支払った任意の金額を共有することを許可する。Qui Tam苦情は密封されており,苦情解除やヘルスケア提供者やサプライヤーがその存在を認識するまで,事件は数年続く可能性がある。1つのエンティティが虚偽請求法案に違反していると判定された場合、それは、各虚偽クレームに対する民事罰を加えて、政府の実際の損害賠償金の3倍の支払いを要求される可能性がある。虚偽請求法案は医療詐欺事件における連邦政府の主要な民事ツールである。虚偽請求法案の責任は、健康プロジェクトやサービスの直接提供者に限定されない。虚偽請求法案によると、政府は他方の虚偽請求を招いたメーカーや他の第三者に責任を負うことを主張している。
また、各州では連邦虚偽請求法案のような虚偽請求法が公布されているが、多くの州法は政府支払人計画だけではなく、第三者支払者に請求を提出する場合に適用されている。
2018年10月25日,“2018年患者とコミュニティオピオイドの回復と治療を促進する物質使用−障害予防法案”(“支持法案”)が公布された。支援法案には、2018年の“回復中のリベート法案”(“EKRA”)が含まれており、リハビリの家、臨床実験室、臨床治療施設との手配を含む、すべての支払人のリベートを禁止する禁止令が制定されている。EKRAはいくつかの法定例外を含み、各機関により多くの例外を制定するように指示する。現在の例外はいくつかの場合に参照され、別の場合はAKS安全港とは異なる。これらの禁止は、治療薬の使用障害に関連するか否かにかかわらず、リハビリテーションの家、臨床治療施設、または臨床実験室に転院した誰のために報酬を請求または受け取るのに適していることに注意されたい。さらに、禁止は、そのようなプロバイダ·サービスを使用する個人への転任を促進するために、またはこれを交換するために、報酬を支払うことまたは提供することを含む。この法律は推薦源との関係に問題が生じる可能性があるという追加的なリスクをもたらす。
反腐敗立法において、米国の“反海外腐敗法”(FCPA)は最も広く施行されている法律である。それは会社責任、第三者責任、腐敗犯罪治外法権を初めて導入した国であり、これは会社と個人が海外で犯した腐敗犯罪に対して刑事と民事責任を負うことができることを意味する。この法律の公布の目的は、特定の種類の個人及び実体を外国政府関係者に支払い、業務の取得又は保留を支援する行為を不法とすることである。1998年に公布されたいくつかの改正案に伴い、“海外腐敗防止法”の反賄賂条項は、現在、直接または代理人を介して米国内でこのような腐敗支払い行為を起こした外国企業や個人にも適用されている。“海外腐敗防止法”は、その証券が米国に上場する会社にその会計条項を遵守することを要求しており、これらの条項は、反賄賂条項と同期して動作することを目的としており、条項がカバーする会社(A)が会社の取引を正確かつ公平に反映する帳簿や記録を確立し、保存することを要求し、(B)十分な内部会計制御システムを設計し、維持する。
24
欧州では、収賄罪を犯した個人や会社に刑事罰や巨額の罰金を科す深刻な結果が定められている反収賄法が各国で採択されている。これらの反賄賂法律に違反したり、このような違反を告発したりすることは、私たちの業務、運営結果、名声に悪影響を及ぼす可能性がある。例えば、連合王国では、2011年7月に施行された“2010年収賄法”に基づいて、任意の公共的な機能または活動、すなわち収賄罪を構成する任意の公共的な機能または活動を含む、他の人に経済的または他の利益を与えることを提供、与え、または承諾して、他の人に何らかの機能または活動を不当に履行させるか、または奨励する。外国公職者への賄賂も2010年の反収賄法の範囲に属している。この制度によると、2010年の反収賄法違反が発覚した個人は最高10年の禁錮刑に直面する。また,罪を犯したことが発見されれば,個人は無制限の罰金を科される可能性があり,賄賂を防ぐことができなかった商業組織も同様である.2016年、フランスでは反賄賂和合法(Sapin II)が成立し、フランスの反腐敗機関(AFA)が設立された。Sapin II法律では,法律範囲内の会社は腐敗防止の内部手続きを実施しなければならないと規定されている。準備されなければならないプロジェクトの中の一つは腐敗リスクマップと反腐敗行為規則だ。これらの文書はAFAの調査を受け,これらの要求を守らなければ,会社や幹部に巨額の罰金が科される可能性がある.もし私たちが未来にヨーロッパ市場で成長したら、この法律は私たちに適用されるかもしれない。
アメリカの医師の回診禁止
医師自己転診法(“スタック法”)は、医師が医師または直系親族と財務関係のある実体、例えば所有権、投資または補償のような患者を患者に転任して、MedicareとMedicaidによって支払われる設計健康サービス(“DHS”)を得ることを禁止し、財務手配が適用される例外状況に適合しない限り。国土安全保障省には臨床実験室テストが含まれている。スターク法案違反の処罰には,回診が禁止されているすべての資金の返還,罰金,民事罰金,連邦医療計画から除外される可能性がある。スタックファを除いて、多くの州は自分の自己推薦禁止を持っていて、これは支払人が誰であろうと、すべての自己推薦に及ぶかもしれない。参照してください“リスク要因-政府の規制に関連するリスク-医療詐欺や 法律、虚偽声明法律、健康情報プライバシー、安全法律などを乱用し、これらの法律や法規を守らなければ、私たちの業務に悪影響を及ぼす可能性があります.”
アメリカの企業医学実践。
多くの州で法律が公布されており,我々のような商業会社の医師の行医を禁止し,医師を雇ったり雇ったりすることが禁止されており,一般に企業の医師行禁止と呼ばれている。これらの法律は任意の非勤務医が医療決定過程に介入することを防ぐことを目的としている。例えば、カリフォルニア医学委員会は、どの診断テストが特定の状況に適しているかを決定し、患者の最終的な看護に責任を負うことは、患者に選択可能な治療方案を提供することを含み、もし人が行われなければ、無免許医師を構成する。これらの企業の製薬法違反行為は,民事や刑事罰金,許可手続きによる我々や専門家への制裁を招く可能性がある。一般的に、このような法律はこの州に実体が存在する実体にのみ適用される。
その他の規制要件
私たちの実験室は規制された医療廃棄物、危険廃棄物と生物危険廃棄物を処理し、処理し、化学、生物製剤と化合物、血液と骨髄サンプル、その他の人体組織の面で連邦、州と地方法規を遵守する。通常、私たちはこのような廃棄物を処理するために、契約規定に適用される法律と法規を遵守する義務がある外部供給者を使用する。このような供給者たちは許可証を持っているか、そのような廃棄物を処理して処分する資格がある。
我々の治療剤開発におけるパートナーはこれらの製品の開発と製造を担当している。そうする過程で、彼らは製造、販売促進、価格報告、詐欺、法律の乱用などに関連するFDAや医療保険規制要求の制約を受けている。
私たちの実験室はアメリカの職業安全と健康管理局が制定した職場の安全に関する広範な要求の制約を受けている。これらの要件は、針刺しや同様の貫通傷の接触を防止または最大限に減少させることによって、血液伝播病原体から労働者を保護する計画の策定および実施を含む。
アメリカの医療改革
アメリカでは、最近連邦と州レベルのいくつかの立法と監督管理の変化は医療コストの低減と医療の質の向上を求めている。例えば,2010年3月には“平価医療法案”(“ACA”)が法律となった。この法律は商業と政府が人為的な医療保健に資金を提供する方法を大きく変え、私たちの業界に大きな影響を与えた。
25
連邦と州の両レベルの立法者,規制機関,商業支払者が引き続き提案し,個人医療福祉の拡大とともにコスト低減に努めていくことが予想される。もし通過すれば、いくつかのこのような提案は保険人口を拡大または縮小し、私たちの製品やサービスに対する需要を増加または減少させることができる。一方、いくつかの提案は、私たちがテストに受け取ることができる価格に追加的な制限を加えたり、商業支払者や政府支払人を含む、私たちのテストの保証範囲または支払人から得られる精算金額に追加的な制限を加えることができるかもしれない。
連邦医師支払い透明性要件(“医師支払い陽光法案”)およびその実施条例は、Medicare、Medicaidまたは州児童健康保険計画の下で支払いを受けることができる保険薬品、設備、生物製品および医療用品の適用メーカーが毎年HHSに保険受給者への支払いまたは分配のいくつかの支払いまたは他の価値移転に関する情報を報告することを要求し、医師、歯科医、視光師、足科医師、脊椎マッサージ師、医師アシスタント、看護師勤務者、臨床看護師専門家、登録麻酔科医および麻酔科医アシスタント、登録看護師助産師および病院教育、または以下の要求に基づいて実体または個人に報告する情報として定義される:医師とその直系親族が持つ所有権、投資性権益、あるいは代表医師、教育病院指定。
州透明性とプレゼント禁止法もあり、メーカーに価格設定やマーケティング情報に関する報告書を州政府に提供することを求めている。いくつかの州はすでに立法を公布し、医療機器メーカーにマーケティングコンプライアンス計画を確立し、州政府に定期的な報告を提出し、販売およびマーケティング活動を定期的に公開することを要求しており、これらの法律はまた、いくつかの他の販売およびマーケティング行為を禁止または制限する可能性がある。これらの法律は私たちに行政とコンプライアンスの負担をもたらし、それによって私たちの販売、マーケティング、その他の活動に不利な影響を与えるかもしれない。私たちは陽光法律が要求する情報を追跡して報告するシステムを持っているが、もし私たちが要求通りにそうしなければ、私たちは政府の法執行行動と潜在的な処罰を受けるかもしれない。
保証範囲と一般精算
法律や支払者に適用される診断サービスの精算や請求書の要求は非常に複雑です。実験室は、管理医療機関(MCO)および連邦医療保険および医療補助のような州および連邦医療保健計画を含む個人第三者支払者のような異なる支払者に課金しなければならず、各支払者は異なる請求書要件を有する可能性がある。精算手配と適用法律によると、私たちのサービスを精算する側は、保険会社やMCO、州や連邦医療計画や患者など、患者に保険を提供する第三者である可能性がある。さらに、私たちは適用された法律と法規、そして私たちの内部コンプライアンス政策と手続きに適合することを確実にするために監査要求を満たさなければならず、請求書の流れの複雑さをさらに増加させなければならない。したがって、以下の理由により、私たちの製品は、より少ない価格または支払われない価格の一部を支払われる可能性がある
しかも、私たちは私たちの製品の価格を自由に決定できないかもしれない。例えば、“意外な法案”は2020年12月27日に公布され、2022年1月1日に施行される。NSAの目標の1つは,ネットワーク外提供者(例えば実験室)が提供するネットワーク内施設の患者受診に関するサービスカバー不足による“意外”医療請求書から患者を保護することである。米国国家安全保障局は、ネットワーク外実験室がネットワーク内施設へのアクセス中に注文した実験室サービスが患者に受け取る費用を制限する。さらに、国家安全保障局は、実験室と保険会社が料率について合意できない場合に、実験室サービスの補償金額を決定するための独立した論争解決手順を確立した。
いくつかの国は、いくつかのEU加盟国を含み、診断と医薬製品の価格を制定し、補償決定を下す。また、製品の最高販売価格を承認して市場に投入することを要求する国/地域もあり、製品ライフサイクル内にこの価格を審査したり、強制割引や利益上限を適用したりする可能性がある。多くの国では、定価審査期間は、市場または製品許可の承認またはCEマークの取得後に開始される。したがって、アメリカ以外の市場での私たちの価格設定戦略は制限されるかもしれない。
アメリカでの保証と精算に関するより多くの情報は、ご参照くださいリスク要因−政府規制に関連するリスク−将来の医療保険支払率は不確定である。”
26
私たちのコンプライアンス計画は
私たちのコンプライアンス計画は法律違反や私たちの政策の行動を防止して発見することを目的としている。その策定にはAdvaMed道徳基準を採用する原則も考慮されており,HHS OIGコンプライアンス計画の要素も考えられる。私たちはわが社の規模、資源、市場地位、その他の独特な面に適応するために、私たちのコンプライアンス計画を設計した。私たちの行動指針は私たちが日常的に運営する道徳とコンプライアンスの原則を指導する声明だ。また、私たちは、適用される州や連邦医療計画の要求下での作業機能と法的義務、およびアメリカ以外の従業員に関する基準を効率的に従業員に伝えるための政策や手続き、それに応じた教育や訓練を策定しています。私たちは定期的にリスクに基づく方法でリアルタイムかつプロセス監視活動を行い、私たちの透明性プログラムには監査能力が内蔵されています。私たちは複数のチャンネルを通じて既知または疑わしいコンプライアンス違反を通報するホットラインを維持し、善意で提起されたすべてのクレームに対して厳格な無報復政策を持っている。
私たちの人々と文化は
私たちの従業員は、内部で“アダプタ”と呼ばれ、彼らは免疫薬物に情熱を持ち、科学規律の支持を受け、そして適応性免疫システムに対する先見性と好奇心の推進を受けている。
2023年12月31日現在、私たちは709人の常勤従業員を持っており、そのうち132人が医学や博士号を持っている。私たちは誰も集団交渉協定の制約を受けていないし、私たちは何の中断も経験していない。私たちは従業員との関係が良いと信じている。
私たちの才能あふれる従業員は私たちの使命を推進し、私たちの文化から生まれて定義された核心的な価値観を共有している。これは組織内のすべてのレベルでの私たちの実行能力に計り知れない役割を果たしている。私たちの核心価値は、私たちの組織におけるそれらの重要性を強化するために、候補者の選別、奨励、承認基準、従業員評価に使用されている
私たちは私たちの従業員が高度に尊敬していると信じています。2018年から2022年まで、私たちは連続して“プーケット湾商業日報”によってワシントン州の最適な職場の一つに選ばれました。私たちはまた2021年と2022年に全国で偉大な職場として認証された。
私たちは包括的なチーム建設、製品設計、各レベルの管理層の性別多様性を誇りに思う。私たちは帰属感文化を創造して維持するために努力している。
私たちは市場と競争する報酬と福祉を提供し、従業員を誘致して維持するためのインセンティブを作るために努力している。私たちの給与プランには、市場競争力のある基本給、業績に基づく短期的なインセンティブ、医療、退職福祉、有給休暇、家庭休暇が含まれています。さらに、私たちは制限株式単位を通じて従業員に会社の持分のメリットを提供することを奨励する。私たちはまた様々な健康と健康資源にアクセスする方法を提供する。
企業情報
私たちは2009年9月8日にワシントン州に登録して設立しました。名前は適応TCR会社です。2011年12月21日、私たちは適応バイオテクノロジー会社と改称した。2015年1月、カリフォルニア州サンフランシスコに本社を置くSequenta社を買収し、MRDのためにNGSテストを開発している。私たちの主な実行事務室はワシントン州シアトル東湖大通り1165号にあります。郵便番号:98109、電話番号は(206)659-0067です。
27
利用可能な情報
私たちはwww.AdaptiveBiotech.comでサイトを維持している。我々のサイトの内容は本10-K表年次報告に含まれておらず,本年度報告の一部ともみなされない.これらの報告を電子的に米国証券取引委員会(“米国証券取引委員会”)に提出または提供した後、我々の年間報告書(Form 10-K)、四半期報告(Form 10-Q)、現在のForm 8-K報告、および1934年の“証券取引法”(以下、“取引法”と略す)第13(A)または15(D)節に基づいて提出または提出された報告修正案を合理的で実行可能な範囲内でできるだけ早く無料で提供する。投資家と他の人は、私たちは投資家関係サイト(投資家関係サイト)、アメリカ証券取引委員会の届出文書、プレスリリース、公開電話会議とネット放送を通じて投資家に重要な財務情報を発表することに注意しなければならない。私たちはこれらのチャンネルとソーシャルメディアを使用して、私たちのメンバーと大衆と私たちの会社、私たちのサービス、その他の問題についてコミュニケーションを取ります。私たちがソーシャルメディアで発表した情報は実質的な情報と考えられるかもしれない。したがって、私たちは投資家、メディア、そしてわが社に興味を持っている他の人が私たちがソーシャルメディアチャンネルで発表した情報を検討することを奨励します。
28
第1 A項。リスク要因
わが社に投資するリスクが高い。投資会社の前に、以下のリスクおよび不確定要因、ならびに当社の合併財務諸表および関連付記、ならびに“経営陣の財務状況および経営結果の検討および分析”部分を含む本10-K表年次報告書の他のすべての情報を慎重に考慮しなければなりません。私たちが以下に説明するどんなリスク要因も、私たちの業務、財務状況、運営結果、見通し、または私たちの証券の取引価格に悪影響を及ぼす可能性があります。以下に説明するリスクは私たちが直面している唯一のリスクではなく、私たちは現在知られていないか、または現在どうでもいいと思っている他のリスクは、私たちの業務、財務状況、経営業績、見通し、および私たちの証券の取引価格を損なう可能性がある。
リスク要因の概要
一般に、以下に説明されるリスクは、以下のいくつかの態様に関する
29
私たちの業務に関わるリスク
設立以来、大きな損失が発生しており、将来的に損失が予想され、利益を達成し、維持するために十分な収入を生み出すことができないかもしれない。
設立以来、私たちは大きな損失を受けた。2023年、2022年、2021年12月31日までの年間で、それぞれ2.253億ドル、2.04億ドル、2.073億ドルの純損失を出した。2023年12月31日現在、私たちの累計赤字は11億ドルです。これまで、私たちの運営資金は、主に転換可能な優先株と普通株の売却から来ており、私たちの初公募株での普通株の売却、次いで収入および購入協定の締結を含めています。我々は製品やサービスの開発に投資し続け,我々の免疫薬物プラットフォームを利用して他の臨床診断や治療製品やサービスの検証を支援することに伴い,巨額の費用や運営損失を招き続けると予想される。私たちは利益を達成して維持するために相当な追加収入を作らなければならないだろう。
私たちが私たちの免疫薬物プラットフォームを利用してより多くの製品やサービスを発見、開発、商業化することに成功できなければ、私たちの業務拡大と戦略目標を達成する能力は損なわれるだろう。
私たちの戦略は私たちの免疫医学プラットフォームを利用して、各種の疾病状態に対する追加の診断と治療製品とサービスを商業化することを発見、開発し、そして可能にすることである。特に,clonoSEQでは,ALL,MM,CLL,DLBCL以外の他のリンパ癌へのMRDの応用を支援するのに十分な臨床的エビデンスを産生しようとしているとともに,すべてのリンパ癌試料型としての血液の臨床的有用性を示している。他の適応またはサンプルタイプにおけるclonoSEQの使用を支持する納得できる証拠を提供できなければ、私たちは私たちのclonoSEQ製品プラットフォームを拡張することに成功できないかもしれない。
我々の免疫薬物業務では,抗体や細胞療法を含む標的抗原の発見と治療製品の開発に焦点を当て,新製品の識別,検証,開発,臨床試験,マーケティング承認の面で大きな課題に直面している。我々や我々の協力者が新たな標的を発見し,免疫に基づく変革性療法を開発できなければ,新たな治療製品の商業化に成功できない可能性がある。
新しい製品やサービスを決定するには、どの製品やサービスが最終的に開発または商業化されているかにかかわらず、大量の技術、財政、人的資源が必要である。私たちは私たちのプラットフォームを利用する有望な機会だと思うことを追求するかもしれませんが、結果として、私たちのいくつかのリスクや資源配分決定が正しくないか、不十分であるか、あるいは個別製品、サービス、または私たちの科学は全体的に以前に未知または過小評価された技術または生物学的リスクを持っていることがわかりました。著者らは長期と広範な人類疾病の中で免疫医学プラットフォームの価値を追求する戦略は功を奏しないかもしれない。もしこれらの分野のいずれかの分野の重大な決定が不正確または準優であることが証明された場合、私たちは私たちの業務と私たちの運営に資金を提供する能力に実質的な悪影響を及ぼす可能性があり、私たちは私たちが思う免疫薬物プラットフォームの潜在力を決して認識しないかもしれない。
新製品やサービスの持続的な研究や開発に大きな投資を行う予定ですが、これは成功しないかもしれません。
我々は我々の免疫薬物プラットフォームを利用して,将来の疾患に対する研究,診断,治療製品のパイプラインを開発することを求めている。例えば,我々の免疫組織学的データベースや抗原注釈TCR−抗原マップを拡張し,標的抗原の発見を進め,それを利用して予防や治療性抗体などの治療法の開発を期待している。また,遺伝子テークとの協力プロトコルに基づき,我々のプラットフォームを用いて個人化された細胞治療製品として設計可能なTCRを識別する方法としていくつかの候補治療製品を開発している。
我々はまた,我々の免疫薬物プラットフォームを利用して潜在的な抗体療法を発見·開発しようとしており,これまでの新冠肺炎に関するデータの生産,収集,分析への投資のおかげである。私たちのこのような点での努力はまだ早く、私たちのデータベースと知識プールを拡大するにつれて、絶えず発展して成熟している。私たちがより多くのデータを収集し分析し続けるにつれて、抗体発見目標に関するどの疾患状態の初期仮定も、より大きなデータセットやさらなる分析の支持が得られないことが分かるかもしれない。もし私たちが抗体発見と開発能力の有効性に対する信念が正しくなければ、それは私たちの製品市場に実質的な悪影響を及ぼすかもしれない。
30
新製品を開発することは投機的で冒険的な仕事だ。最初に,所望の製品やサービスが期待される結果を達成できない可能性があること,あるいは許容可能な分析精度や臨床実用レベルを達成できない可能性があることを示した。潜在的な成功製品やサービスを決定する前に、私たちが開発している製品を変えて臨床研究を繰り返す必要があるかもしれません。治療製品の開発費用は高価であり,完成まで数年かかる可能性があり,不確実な結果が生じる可能性がある。失敗は開発のどんな段階でも起こるかもしれない。製品またはサービスが開発後に成功を示す場合、私たちまたは私たちの協力者は、特に製品またはサービスの性質に依存して、FDAおよび他の規制許可、許可または承認を得る必要があるかもしれない。FDAおよび他の規制機関の承認、許可または承認手続きは、多くの時間、および追加の研究、開発、および臨床研究支出に関連する可能性がある。FDAまたは他の規制機関は、私たちが未来に開発したいかなる製品も承認、許可、または承認しないかもしれない。私たちが開発した製品が規制部門の承認、許可、承認を得ても、私たちまたは私たちの協力者は大量の資源を投入してそれを商業化、販売、マーケティングする必要があり、利益を得ることができ、その製品は決して商業的に成功しないかもしれない。また,どの製品の開発も競合製品の開発により中断されたり,そうでなくなったりする可能性がある.
新しい潜在的な製品は開発や商業化のどの段階でも失敗する可能性があるので、もし私たちが現在または未来のどの製品も成功しないと判断すれば、私たちはそれらを放棄するかもしれませんが、私たちの投資は何の見返りもありません。もし私たちがもっと多くの製品を開発することに成功しなければ、私たちの成長潜在力は損なわれるかもしれない。
我々の抗原注釈TCR−抗原図を用いて製品を開発する努力は成功しない可能性があり,予想される知見をまったく生じない可能性があり,新たな診断や治療製品の開発や商業化を許可するスケジュールに沿っていない可能性がある。
私たちはTCR配列をそれらが結合した抗原にマッピングするために、私たちの免疫配列決定能力、独自の計算モデリング、および機械学習を使用している。しかしながら、多くの理由で、検証信号を取得するために必要なサンプルセットを取得することが困難であること、検証すべきTCR署名の複雑さを正確に定義するためにアルゴリズムベースの方法を改善することを含む、十分な完全なTCR-抗原プロファイルの開発に成功しない可能性がある。
また,機械学習の助けを借りても,TCR−抗原地図は計画通りに完全に開発されるまで数年かかると予想される。したがって,我々が開発しているTCR−抗原プロファイルは,我々の製品や我々の協力者の製品の商業的可能性のあるスケジュール上で臨床的に操作可能な知見を生じないか,あるいは全くできない可能性がある。我々の目標は,薬物発見と開発にTCR−抗原プロファイルを利用することである。
SARS−CoV−2,急性ライム病,クローン病,乳糜潟,多発性硬化症患者から発生するTCRから疾患特異的シグナルを識別する概念証拠を確立した。潰瘍性大腸炎や関節リウマチの早期シグナルも認識しており,これらのシグナルの確認を行っている。
新薬の発見と開発を追求する過程で,我々の免疫組織学データベースを利用して,潜在的な新薬標的(抗原)を発見することにより,我々のTCR−抗原マップをさらに開発する。検証された目標があると、私たちは私たちの免疫医学プラットフォームと私たちが増加しているTCR-抗原マップを使用して、TCR、抗原、および抗体に基づく治療法の開発を支援する。
私たちは2024年に期限が切れたマイクロソフトプロトコル期間全体で、マイクロソフトの免疫組織学人工知能サービスを独占的に使用してTCR抗原マッピングを行うことに同意し、私たちのすべての技術、製品とサービスに関連して、これらの技術、製品とサービスは私たちがマイクロソフトと協力した直接の結果である。
もし私たちの計算モデリングと機械学習努力がTCR配列とそれらが結合した抗原との間の関連を検証する速度を加速させることができなければ、私たちのビジネスモデルのスケジュールは商業的に実行できないかもしれない。このスケジュールを加速させることができても、私たちの新技術から派生した製品には製品レベルのミスが生じる可能性があります。私たちのTCR-抗原マップで意義のある進展を得ることができなければ、それを利用して新しい治療製品やサービスの開発と商業化に成功すれば、私たちの業務と手術結果は影響を受ける。
データや文書生成に人工知能を用いることは,我々のデータの信頼性に影響を与える可能性がある.
私たちは、製品やサービスの要素として人工知能を使用しませんが、データセットおよび文書の生成を支援し、トレーニング計算モデルを支援するために使用されています。多くの革新と同様に、人工知能の使用も欠陥、不足、または偏見のあるデータセットを含むリスクと挑戦をもたらす。人工知能固有の挑戦を使用することは、私たちのデータの信頼性に悪影響を与え、遅延と競争損害、規制行動または法的責任、ブランドや名声の損害に直面させる可能性があります。
31
私たちは遺伝子テーク合意に関連するリスクに直面しており、私たちは私たちが予想していた優位性を実現できないかもしれない。
2018年12月,新規癌特異的抗原と新抗原ガイドT細胞療法の開発と商業化を加速し,様々なタイプの腫瘍治療のためのGenentech合意を達成した。遺伝子テイク協定の条項によると、私たちは2019年2月に第1期前払い3,000万ドルを受け取り、指定された開発、規制、ビジネスマイルストーンを実現した後、時間の経過とともに約18億ドルまでの追加支払いを受ける資格がある。また、遺伝子テークは合意に基づいて商業化製品を販売する特許権使用料を支払うだろう。私たちはこれらのマイルストーンを成功させることができないかもしれません。遺伝子テークプロトコルによって開発された製品は、私たちが予想していた時間枠内で商業化、相当な販売または完全な商業化を実現しないかもしれません。
私たちは、私たちの協力研究開発部分の運営のある程度の制御を共有することを含む、遺伝子テークプロトコルに関連する多くのリスクに直面しているが、遺伝子テークと遺伝子テークは、協力によって開発された任意の製品の商業化を独占的に制御している。例えば、2021年に、遺伝子テークは、公表されたデータに基づいて、私たちの最初の共有抗原標的候補に対する薬剤の開発を一時停止し、その後、代替候補を選択する。遺伝子テークプロトコルはまた、腫瘍学分野における任意の第三者との協力範囲外でTCRベースの細胞療法の開発または商業化を禁止している。私たちの協力は遺伝子テーク可能性を含む独立した運営とは異なるリスクに関連しています
遺伝子テークの共同開発と商業化努力に対する制御の程度は,遺伝子テークプロトコルによって得られた金額に影響する可能性がある。例えば、遺伝子テークは、候補製品の開発を一時停止するか、候補製品を全く商業化しないことを決定するか、または第三者に特許使用料を支払うことに同意するか、または価格設定モードを採用して、私たちが本来予想していた特許使用料の金額を低下させる可能性がある。遺伝子テークプロトコルに基づいて有効な細胞療法を開発しない可能性もあり,あるいは,FDAや米国国外の類似規制機関の承認が得られれば,遺伝子テークも便利なときに無断で遺伝子テークプロトコルを中止することができる。
我々は,このプロトコルに基づいて開発·商業化されている製品のTCRスクリーニング活動を含む,遺伝子テークプロトコルの下で我々の製品研究,開発,商業化に関する義務を履行できない可能性がある。例えば、遺伝子テークプロトコルに従って製品を商業化する場合、製品の販売量の増加に伴い、サンプル収集、顧客サービス、および一般的なプロセス改善におけるワークフロー能力を増加させ、予想される回転時間内により大規模なTCRスクリーニングをサポートするために、私たちの内部品質保証計画を拡大する必要があるかもしれない。私たちは、治療に関連する患者固有の新しい抗原を識別および標的化するために、追加の認証実験室科学者および個人化製品の他の科学および技術者を必要とするかもしれない。私たちはまた、調達、設定、検証のために数ヶ月以上かかるかもしれないより多くの実験室空間および設備を購入する必要があるかもしれない。これらのプロセスの改善と規模の拡大、人員、実験室空間、設備の拡大は成功的に実施できない可能性があり、私たちは現在成功する必要があるすべての要求を満たすために十分な実験室施設や資源がないかもしれない。私たちが私たちの義務を履行できない場合、遺伝子テークは、私たちのTCRスクリーニングプロセスの技術移転(個人化製品固有)をトリガするか、または遺伝子テークプロトコルを終了する権利があります。また、遺伝子テークプロトコルの下での我々の重大な義務により、遺伝子テークの実際または潜在的な競争相手である任意のバイオ製薬顧客を含む、既存の顧客、協力者、およびサプライヤーの需要を満たすこと、および新しい顧客を獲得する上で挑戦に直面する可能性がある。
もし私たちが遺伝子テークプロトコルによって1種以上の製品の商業化を支持するならば、私たちは新しい設備を採用し、新しい技術システムと実験室の流れを実施し、そして異なる資質を持つ新しい人員を採用する必要があるかもしれない。このような成長や移行がうまく管理されていないと、回転時間遅延、製品コスト上昇、製品品質低下、顧客サービス悪化、競争挑戦への応答速度が遅くなる可能性がある。上記のいずれの分野の失敗も、私たちの製品に対する市場の期待を達成することを困難にし、遺伝子テークプロトコルによっても他の側面にも、私たちの名声と私たちの業務の将来性を損なう可能性があります。したがって,私たちと遺伝子テークとの関係は期待される利点を実現できないかもしれない。
32
我々の細胞療法の開発と商業化には経験が限られており,我々Genentechの協力の一部として,将来TCRによる細胞療法は決して開発や商業化に成功しない可能性がある。
われわれは細胞療法の発展に経験が限られており,細胞療法の商業化,マーケティング,流通には経験がない。Genentechとの協力の下,我々の候補治療製品は発見·開発の早期段階にあり,この協力の下で使用する我々の流れを開発し,癌治療のためのTCRによる細胞療法の開発を継続している。著者らと遺伝子泰克の協力の下で、遺伝子泰克は大量の財政資源を投入して、将来のTCRに基づく細胞療法を開発し、臨床前研究とその他の早期研究開発活動を展開し、そしてこれらの操作に一般と行政支持を提供する。私たちの将来の成功は、私たちと遺伝子テークが候補治療製品の開発に成功し、これらの製品を臨床に出す能力と、遺伝子テークが適切な状況で規制とマーケティングの承認を得て細胞療法を商業化することに成功する能力にかかっている。私たちと遺伝子テークはまだ何の細胞療法も開発して商業化していませんそれもできないかもしれません
抗体に基づく療法の開発と商業化の経験は限られており、将来的には私たちや私たちの協力者はこのような製品の開発と商業化に成功しないかもしれない。
われわれは臨床適応抗体の開発には経験が限られており,抗体による治療製品の商業化,マーケティング,流通には経験がない。私たちの抗体に基づく候補治療製品は発見と開発の初期段階にある。私たちと協力して治療用抗体製品を開発して商業化するどんなパートナーもこれをすることができないかもしれない。
私たちは現在、協力者を私たちの運営の多くの側面に使用し、将来的に協力者を使用し続け、私たちの薬物発見プラットフォームを商業的に利用しており、必要またはそうすることを望むときに既存の協力者を維持し、それと新たな関係を築くことができなければ、私たちの業務は影響を受けるだろう。
MRDおよびIMビジネスの分野で業務を展開するリソースは限られており、私たちの既存または潜在的な製品に関連する販売、マーケティング、または流通インフラは完全に確立されていません。私たちは協力協定を締結しており、協定によると、私たちの協力者は将来的に資金や他の資源を提供し、私たちの製品やサービスを開発し、商業化することが可能です。例えば,T細胞療法の開発と商業化を加速し,様々なタイプの腫瘍治療のためのGenentech合意を達成し,マイクロソフトプロトコルは,マイクロソフトの研究や機械学習技術にアクセスするアプローチを提供しており,これらの技術を用いて我々のTCR−抗原マップを開発している。
私たちは、私たちの免疫に基づく診断または薬物発見製品またはサービス導管のために、私たちのTCR-抗原プロファイルシグナルの生成および検証を加速させる可能性がある患者キューにアクセスするために、より多くの業界および学術的協力を求めている。これらの協力は、私たちが潜在的な製品やサービスを追求する際に巨額の費用を発生させる可能性があり、私たちはどんな潜在的な製品やサービスを識別、開発、商業化することに成功しないかもしれない。
我々はまた,TCR,抗原,抗体に基づく治療法を開発し,商業化するために,将来的に我々の薬物サービスパートナーとともに薬物を発見·開発する機会を求めている可能性がある。その中の多くの協力は私たちに前金とマイルストーン支払いを提供してくれた。私たちはこれらの協力で治療資産の識別に成功できないかもしれませんが、私たちの協力者はこのような資産の開発に成功して商業化できない可能性があり、協力の期待される金銭的利益を実現できない可能性があります。
多くの要素は、私たちの義務を履行する能力、私たちの協力者の私たちの製品とサービスに対する満足度、私たちの協力者が彼らの私たちに対する義務を履行する状況、私たちの協力者の内部優先事項、資源分配決定と競争機会、規制承認を得る能力、協力者との相違、協力のいずれかに必要なコストと関連する融資需要、および任意の関連司法管轄区域の運営、法律、その他のリスクを含む、このような協力の成功に影響を及ぼす可能性がある。私たちの収入を減少したり、未来の製品とサービスの開発を延期したりする以外に、その中の1つ以上の関係を失うことは、研究、データ、臨床試験或いは計算技術に対する開放を減少させる可能性があり、これらの技術は新しい情報を収集し、それを著者らの臨床免疫組織学データベースとTCR抗原マップに組み込むのに役立つ。本明細書に記載された製品開発、規制許可、許可または承認、および商業化に関連するすべてのリスクは、私たちの協力者の活動によって私たちに派生して適用される。
私たちは持続的な基礎の上で会社と潜在的な協力について対話します。このような対話は商業的合意に到達しないかもしれない。合意に達しても,それによる関係が成功しない可能性があり,協力の一部として開発されたどの製品やサービスも成功しない結果が生じる可能性がある.私たちの既存または潜在的な協力に対する業界の推測は、私たちまたは私たちの製品に対する否定的な推測の触媒になる可能性があり、これは私たちの名声や業務に悪影響を及ぼす可能性がある。
33
私たちまたは私たちの協力者が規制許可、許可または承認を求めるか、または私たちが開発している任意の製品やサービスを商業化する前に、多くの追加の研究と開発が必要であり、場合によっては臨床試験や検証も必要である。
われわれは腫瘍学的細胞療法を含む一連の免疫駆動の診断と薬物療法を開発しているが,われわれとわれわれの協力者がより多くの商業的に可能な製品を実現する機会がある前に,重大な追加研究や開発活動,検証,臨床試験が必要である可能性がある。我々の研究·開発は依然として薬物療法に基づく新製品の開発に関連するすべてのリスクの影響を受けている。基礎技術の開発は,予期しない技術や他の問題や他の研究や開発問題の影響を受ける可能性があり,これらの製品開発を達成するために必要な資金が不足している可能性がある.安全、監督と治療効果の問題、臨床障害あるいは他の挑戦は遅延を招く可能性があり、私たちに追加費用を発生させ、それによって私たちの損失を増加させる。もし私たちと私たちの協力者が完成できなければ、あるいはもし私たちが臨床診断や治療の開発に重大な遅延があったら、T細胞による細胞療法と抗体を含み、特に巨額の支出が発生した後、私たちの業務は失敗する可能性があり、投資家はすべての投資を失う可能性がある。
任意の新しい治療製品またはサービスの商業販売の規制許可、許可、または承認を得る前に、私たちの製品が各目標疾患適応において安全かつ有効であることを証明しなければならない。1つの製品が安全かつ有効であることを証明するために臨床研究を行う必要がある。臨床テストとその他の検証作業はコストが高く、完成するまで数年かかるかもしれないが、その結果自体は不確定である。故障はいつでも発生する可能性がある。治療学では,開発中の製品やサービスの臨床前研究や早期臨床試験の結果は後期臨床試験の結果を予測できない可能性があり,臨床試験の初歩的な成功は臨床試験完了後に得られた結果を示さない可能性がある。開発中の治療製品の臨床試験に伴い,失敗率は通常極めて高い。臨床試験或いは検証後期の段階にある製品も必要な安全性と有効性を示すことができない可能性があり、すでに非臨床研究と初期臨床試験或いは検証を通じて進展が得られたにもかかわらず。私たちの製品とサービス開発のどんな遅延も私たちの業務、財務状況、将来性を深刻に損なう可能性があります。
私たちの製品やサービスのミスや欠陥は私たちの名声を損なう可能性があり、私たちの製品やサービスに対する市場の受容度を下げたり、製品責任クレームに直面させたりする可能性があります。
私たちは新製品を作っています。その中の多くの製品は最初は基本的にテストされていない技術に基づいています。私たちのすべての製品とサービスの進歩に伴い、私たちまたは他の人たちは私たちが製品やサービスレベルの科学的または技術的ミスや漏れを犯したことを確認するかもしれない。テスト過程は多くの複雑と先端の生化学、情報学、光学と機械過程を利用し、その中の多くの過程は外部要素とテスト運行の間の変化に高度に敏感である。プロセスの改善は,最初は予期しない問題を招き,効率を低下させたり,可変性を増加させたりする可能性がある.特に、これらの過程の重要なコンポーネントであるDNAシークエンシングは効率が低下する可能性があり、変異性は予想より高く、それによって総シークエンシングコストを増加させ、そして私たちが所与の時間帯に処理できるサンプル数を減少させ、これは顧客の回転時間に負の影響を与える可能性がある。そのため、非効率或いは可変の流れは私たちの経営結果の変化を招き、そして私たちの名声を損なう可能性がある。
しかも、私たちの開発実験室操作は任意の数のミスや欠陥を招く可能性がある。私たちの品質保証システム或いは製品開発プロセスは私たちがサンプル、サンプル品質、実験室プロセス(シークエンシング、ソフトウェア、データアップロード或いは分析、原材料、試薬製造、検査品質或いは設計を含む)或いは他のコンポーネント或いはプロセスの面で意外な問題が発生することを防止できないかもしれない。さらに、私たちの検出には品質や設計ミスがある可能性があり、サンプルを処理するのに十分なプログラムや機器がないかもしれません。私たちの独自のプライマー混合物と商業材料を組み立てて、データをアップロードし、分析したり、他の方法で私たちの開発実験室操作を行ったりするのに十分ではないかもしれません。お客様に未発見のエラーを有する製品またはサービスを提供する場合、私たちの臨床診断は、患者が疾患に罹患しているか、または治療を必要とする患者の疾患を検出できないことを誤って示す可能性がある。私たちの顧客は、私たちの製品およびサービスが臨床サンプルから残留疾患の存在を高精度に指摘できなかった場合、または私たちのテスト報告書に記載されていない場合、または疾患の存在または不存在を正確に指摘しない場合を含む、製品およびサービスの欠陥、誤り、および遅延に特に敏感である可能性が高いと信じている。薬物発見において,このような誤りは,我々の協力者の臨床研究を妨害したり,彼らの製品の開発に不良な安全性や有効性をもたらしたりする可能性がある。これは私たちの顧客の業務を損なう可能性があり、巨額のコストを発生させ、キーパーソンの注意をそらし、私たちに対する規制執行行動を奨励し、深刻な顧客関係の問題をもたらし、私たちの名声を損なう可能性があります。私たちはまた製品中のミスや欠陥に関する損害賠償責任クレームに直面する可能性があります。このような状況はどんな発展も私たちの業務と経営業績を損なう可能性がある。
34
私たちの現在と未来の製品とサービスは決して重大な商業市場によって認められないかもしれない。
私たちの成功は市場が私たちが免疫駆動型研究、診断と治療製品とサービスを提供できる自信に依存し、これらの製品とサービスは臨床結果を改善し、医療コストを下げ、より良い生物製薬開発を促進することができる。もし私たちの製品とサービスあるいは私たちのパートナーと共同開発した製品とサービスが期待された効果を達成できなければ、私たちの経営業績と名声を深刻に損なう可能性があります。患者、臨床医師、学術機関と生物製薬会社は私たちの製品とサービス中あるいはそれに関連する欠陥、誤り、不正確、遅延と毒性に特に敏感である可能性があると信じている。そのほか、これらの製品或いはサービスの表現が良くないことは人々の著者らの免疫薬物プラットフォームに対する全体的な自信低下を招く可能性がある。
多くの要素のため、私たちと私たちのパートナーは、私たちの現在または未来の製品とサービスを重大な商業市場受容度を得ることに成功できないかもしれません
さらに、私たちの顧客とパートナーは、彼らの研究開発計画の変化、臨床試験の失敗、財務制限、規制環境、私たちの製品とサービスの否定的な宣伝、競争製品や精算状況を減少または停止することを決定するかもしれません。これらのすべての状況は私たちがコントロールできるものではありません。私たちはこれらや他の市場が私たちの製品、サービス、そして技術を受け入れることに影響を与える可能性のある要素を成功的に解決できないかもしれない。もし私たちの免疫薬物プラットフォームと関連製品とサービスが市場の広範な受け入れを得られなかったら、私たちの業務、財務状況と運営結果に重大な損害を与える。
私たちは限られた数のサプライヤーに依存したり、多くの場合、単一のサプライヤーに実験室設備や材料を提供することで、代替品を見つけることができない場合や、すぐに代替サプライヤーに移行する可能性があります。
私たちは限られた数のサプライヤーに依存しているか、または多くの場合、単一のサプライヤーは、私たちが実験室運営および製品開発に使用しているいくつかのシークエンサー、試薬、設備、および他の材料を提供する。もし私たちがこれらのシークエンサー、設備、試薬、または他の材料を得る上で遅延、品質問題、または他の困難に遭遇し、もし私たちが受け入れられる代替品を得ることができなければ、私たちの実験室操作、試薬配布、技術移転、または開発活動が中断される可能性がある。この場合、私たちは大きなコストを負担し、新しいサプライヤーを探し、新しい設備を取得し、同定し、新しい試薬を検証し、私たちの既存の検査のいくつかの側面を再検証する必要があるかもしれません。これは、サンプルや製品の開発と商業化の処理の遅延を招く可能性があります。このような中断は、私たちの業務、財務状況、運営結果、そして名声に深刻な影響を及ぼす可能性がある。私たちの試薬や他の材料のプロセスや成分の内部変更は、私たちの検証作業やサプライヤーの新しい材料供給も必要かもしれませんが、このような変更を実施する際に生産時間や在庫レベルに影響を与える可能性があります。
例えば、私たちはIllumina NextSeqシステムを購入して依存した。Illuminaはこのシークエンサーのために設計された試薬を提供してくれ、IlluminaはIllumina NextSeqシステムの唯一の保守と修理サービスプロバイダである。Illuminaから実験室情報管理ソフトウェアの許可を取得し,Illuminaからそのソフトウェアに関連するサービスを取得した.しかも、Illuminaは私たちの試薬供給に対するすべての要求を満たす義務がない。Illuminaがその生産を停止または減速する場合、または現在の価格または現在の価格に近い価格で私たちの業務に必要な配列測定試薬を供給し続けることができないか、または現在使用されている配列決定試薬を現在の価格で供給し続けることができない場合、私たちは、Illuminaから異なる試薬を購入することを要求されるか、または私たちにあまり有利ではない条項および条件で異なる試薬供給者から購入することが要求されるかもしれない。Illuminaの運営または私たちの試薬、材料、または他の設備サプライヤーの任意の中断は、私たちの業務能力に影響を与える可能性があります。
35
現在,配列測定器や各種関連試薬を含む実験室運営や製品開発に必要な設備を提供できるのは少数の他の設備メーカーのみであると信じている。Illumina以外の会社製シークエンサーを使用して実験室操作を変更することを要求します。新しいシークエンサーに変換して同定するのは時間も高価で、私たちの実験室操作の中断を招く可能性があり、私たちの実験室操作の性能仕様に影響を与えるかもしれないし、私たちが免疫配列決定に使用する試薬を再検証する必要があるかもしれません。私たちのclono配列番号診断試験サービスを含むかもしれませんし、変更のために追加の許可、許可、承認、または許可を得る必要があるかもしれません。我々のワークフローが中断していない場合には,代替シーケンサ,関連試薬,その他の材料を保護·実施できない可能性がある。Illuminaの代替サプライヤーであれば、任意の置換シークエンサーと各種の関連試薬は著者らの実験室操作に対する品質管理と性能要求に符合しない可能性がある。もし私たちが私たちの製品やサービスを取得、再構成、または再検証するために必要な設備や試薬に遅延や困難がある場合、私たちの業務、財務状況、運営結果、名声は不利な影響を受ける可能性があります。
いくつかの製品やサービスをマーケティング·販売する上での経験は限られており、私たちの直販やマーケティングチームを拡大できない場合や、特定の製品分野や市場でパートナーと提携関係を構築して、顧客のニーズを十分に満たすことができなければ、私たちの業務は悪影響を受ける可能性があります。
私たちは治療製品をマーケティングして販売した経験がない。したがって、私たちまたは私たちの薬物発見と開発協力者は、私たちの計画の成長を支援するために、現在または未来の製品やサービスを効果的にマーケティングして販売することができないかもしれない。
私たちの販売とマーケティング努力は巨大で多様な市場を対象としており、その中に高度に専門化された細分化市場を含み、部門担当者、実験室主任、首席調査員、核心施設主任、臨床医師、支払人及びリード学術機関、生物製薬会社、研究機関と契約研究機関の研究科学者と病理学者を含む。したがって,我々の販売代表は関連した専門的な市場経験を持つ必要があると考えられる.経験のある販売とマーケティング担当者の競争は非常に激しく、私たちの販売組織の新しいメンバーは、彼らの経験と専門知識を私たちの製品やサービスに適用するために、高強度の訓練を受ける必要があるかもしれません。私たちは従業員を誘致し、維持することができないかもしれませんし、効率的で有効な販売組織を構築あるいは十分に訓練することもできません。これは私たちの臨床診断の販売と市場受容度にマイナスの影響を与え、私たちの収入増加と潜在的な利益能力を制限するかもしれません。
遺伝子テークプロトコルによれば、遺伝子テークは、このプロトコルに従って開発された製品を商業化する唯一の権利および許可を有する。遺伝子テークは、このプロトコルに従って開発された製品を効率的にマーケティングおよび販売するために、流通パートナー、臨床医師、および業界経験および知識を有する現地病院の探し、同定を担当する。遺伝子テークは優遇条件で流通パートナー、臨床医師或いは病院を吸引できない可能性があり、甚だしきに至っては全くできない。遺伝子テークプロトコルに基づいて開発された製品における遺伝子テークの販売やマーケティング努力が成功しなければ、我々の薬物発見サービスやプラットフォームは市場の広範な承認を得ることができない可能性があり、これは私たちの業務運営に重大かつ不利な影響を与えるであろう。私たちの医薬サービス協力では、私たちは似たようなリスクに直面しており、私たちに支払われる記念碑的支払いは、私たちの協力者が薬の商業化に成功したことにかかっている。
もし私たちまたは私たちの協力者が臨床試験に関連する多くの予測不可能な事件に遭遇した場合、私たちまたは彼らは未来の製品およびサービスまたは既存製品の改善をさらに臨床試験し、規制許可を得る、許可または承認を得るか、またはそれを商業化する能力が延期または阻止されるかもしれない。
私たちまたは私たちの協力者は、臨床試験中に、または臨床試験の結果によって多くの予見不可能なイベントに遭遇する可能性があり、これらのイベントは、私たちまたは彼らのさらなる臨床試験を延期または阻止するか、または将来の製品およびサービスに対する監督部門の承認、許可または承認を得るか、またはそれを商業化するか、または現在の製品およびサービスの改善を含むかもしれない
規制の要求と政策が変化しています
試行設計
36
テストをする
実験結果
このような性質の遅延はまた、競争相手が私たちまたは私たちの協力者の前に製品を市場に出すことを可能にする可能性があり、これは私たちが製品を商業化することに成功する能力を弱化させ、私たちの業務と運営結果を損なう可能性がある。私たちの製品や私たちの協力者と共同開発された製品のどんな遅延も、私たちの業務、財務状況、将来性を深刻に損なう可能性があります。臨床試験の開始または完了遅延をもたらすか、またはもたらす多くの要因は、最終的には、開発中の製品の規制承認、許可または承認を拒否する可能性もある。
37
時間が経つにつれて、私たちは私たちの製品に対する需要を支援するために、私たちの労働力、商業インフラ、実験室運営を拡大する必要があるかもしれない。私たちはこれを管理し、この需要を満たす変動に困難に直面するかもしれない。
私たちは私たちの製品に対する需要を支援するために、私たちの労働力、商業インフラ、実験室運営をさらに拡大する必要があるかもしれない。潜在的な成長需要や他の顧客要求(例えば、回転時間やサービスレベルなど)を満たすのに十分な能力を持っていることを保証することを含む、製品やサービス需要の変動をサポートできなければ、私たちの業務は影響を受ける可能性があります。2023年12月31日現在、709人のフルタイム従業員がおり、潜在的な臨時従業員を含めて従業員数を増やす必要があるかもしれません。私たちと私たちの協力者がもっと多くの製品とサービスを商業化することに伴い、私たちは新しい設備を統合し、新しい技術システムと実験室の流れを実施し、そして異なる資質を持つ新しい人員を採用する必要があるかもしれない。このような成長や移行を管理できないと、回転時間遅延、サービスコストの上昇、サービス品質の低下、顧客サービスの悪化、競争挑戦への応答速度が遅くなる可能性がある。これらの分野のいずれの分野の失敗も、私たちの製品やサービスに対する市場の期待を満たすことを困難にし、私たちの名声と業務の将来性を損なう可能性がある。
私たちの大部分の従業員は熟練した技術を必要としているため、私たちはより多くの合格者を効果的に募集、訓練、維持することができないかもしれない。これは、私たちのインフラが弱く、操作ミス、製品とサービスの開発が遅い、期待や遅延マイルストーンの成果を達成できなかった、深刻なコスト超過、ビジネス機会の喪失、従業員とアルバイトの流失、求人計画を実行できない、残りの従業員とアルバイトの生産性の低下を招く可能性がある。
私たちの経営業績は大幅に変動する可能性があり、これは私たちの将来の経営業績を予測しにくくし、私たちの経営業績が予想を下回ったり、私たちが提供する可能性のあるいかなる指導を招く可能性があります。
過去、私たちの財務状況と経営業績はそれぞれ異なり、未来は様々な要素のため、私たちの財務状況と経営業績は引き続き四半期と年度の間に変動し、その中の多くの要素は私たちがコントロールできない。これらの変動をもたらす可能性のある当社のビジネスに関連する要因は、以下の要因と、本年度報告Form 10−Kの他の部分に記載された他の要因を含む
38
これらの要因の累積影響は,我々の四半期や年度経営業績に大きな変動と予測不可能性をもたらす可能性がある。したがって、異なる時期に私たちの経営業績を比較することは意味がないかもしれない。投資家たちは私たちの過去の業績を私たちの未来表現の指標として依存してはいけない。どの特定の時期においても、私たちの経営業績は証券アナリストや投資家の予想を下回る可能性があり、これは私たちの株価を下落させる可能性がある。
一般的な事項として,期待される次の行動を含む我々の発展挙動の状況を定期的に報告する予定であるが,これらの次の行動のスケジュールについて前向きな指導を提供しない可能性がある。さらに、私たちは、私たちの協力者が管理する任意の製品に関連するこのようなマイルストーンの開示時間を制御しません。私たちまたは私たちの協力者が開示した負のデータは、私たちの株価や全体的な推定値に実質的な悪影響を及ぼすかもしれない。私たちの1つまたは複数の製品の臨床試験結果は予想外であり、報告された任意の製品の不良安全事件を含めて、私たちの株価は下落する可能性がある。
私たちは私たちの現在と未来の製品とサービスの市場規模を推定しました。これらの市場は私たちが推定したものより小さいかもしれません。
我々の現在の製品およびサービスおよび開発中の製品およびサービスの年間潜在的市場の推定は、限定されるものではないが、1つまたは複数の癌に罹患した患者数、1つまたは複数の癌に罹患するリスクがより高い個人数、いくつかの自己免疫疾患を発症または発展させるリスクの高い個人数、および各市場で私たちまたはパートナーの製品によってその需要を満たすことができる患者の割合を含む多くの内部および第三者の推定に基づいている。そして私たちはまだ構築されていない市場に私たちの現在と未来の製品とサービスの仮定価格を販売することができます。我々の仮説と我々の推定を支持するデータは合理的であると信じているが,これらの仮定と推定は正しくない可能性があり,我々の仮説や推定を支持する条件は随時変化し,これらの潜在的要因の予測正確性を低下させる可能性がある.したがって、現在または未来の製品の年間潜在市場の推定は正しくないことが証明されるかもしれない。私たちの製品から利益を得る実際の患者の数、将来の製品やサービスを販売することができる価格、あるいは私たちの製品やサービスの年間目標市場が私たちが予想しているよりも少ない場合、これは私たちの販売増加を弱化させ、私たちの業務に悪影響を及ぼすかもしれません。
もし私たちが競争相手と効果的に競争できなければ、私たちは私たちの製品を商業化することに成功できないかもしれない。
薬物発見分野では、バイオテクノロジーと製薬産業の競争が激しい。これらの分野の特徴は技術の迅速な進歩と知的財産権の高度な重視である。免疫薬物の広さと将来性を考慮して、著者らは診断、製薬と生物技術会社、学術研究機構と政府機構及び公共と私営研究機関を含む多くの異なる源からの激しい競争に直面しており、著者らのプラットフォームの各コンポーネント及び現有と潜在的な製品供給に関連している。免疫薬に対するより広範な関心と増加のため、私たちは競争が激化すると予想する。
例えば、臨床診断において、著者らのclono配列番号MRD測定は目標顧客内部或いは参考実験室からの伝統と新世代フローサイトメトリーからの競争に直面し、実験室と機構からの競争にも直面し、これらの競争は実験室と機構から研究にのみ使用するMRD技術を臨床応用に応用し、商業段階の腫瘍診断会社はその実体腫瘍(CtDNA)MRD製品の応用を血液学MRD領域に拡張した。薬物発見では,一部の業界や学術界の参加者が免疫薬の臨床試験を行っている。
私たちの競争相手は、私たちの任意の製品またはサービスと競合する可能性のある製品またはサービスを識別および開発するために、私たちの既知のデータと同様のデータを生成および記述するために必要な知識を持っているか、または獲得することができる。また,いくつかのバイオテクノロジー会社や大手バイオ製薬会社が免疫薬を開発している。私たちの多くの既存または潜在的な競争相手は、単独またはパートナーとの協力にかかわらず、研究開発、製造、規制承認およびコンプライアンス、販売と流通の面で、私たちよりも多くの財務資源と専門知識を持っている。
39
私たちが私たちの臨床診断や薬物発見製品を開発しなければ、必要な規制や他の許可、許可または承認を得ず、私たちが発見した特許を取得または実行せず、競争相手の前に私たちの製品を発売しなければ、私たちは不利な影響を受けるかもしれない。また,我々の競争相手は,我々の知的財産権を回避する臨床診断や療法の開発に成功する可能性がある。私たちの競争相手は、私たちの製品よりも正確で、使いやすい、またはより費用効果のある治療法や診断製品の開発と商業化に成功するかもしれないし、私たちがパートナーと開発した任意の治療製品よりも安全で、より効果的で、より便利で、コスト的であることが証明されるかもしれません。または私たちの製品は競争力が不足したり、時代遅れになったりするかもしれません。我々の分野の技術進歩の発生に伴い,より広く知られるようになり,これらの分野の競争が激化することが予想される.競争相手の詳細については“を参照されたい”ビジネス-競争“本年度報告の表格10-K部分。
生命科学業界は迅速な変化の影響を受け、これは著者らが開発した免疫薬物プラットフォームと関連製品を時代遅れにする可能性がある。
私たちの業界の特徴は、技術と科学的突破、新製品とサービスの頻繁な発売と改善、そして絶えず発展する業界標準を含む急速な変化であり、これらはすべて私たちの現在と未来の製品を時代遅れにする可能性がある。例えば,生命科学研究や癌や自己免疫疾患の診断や治療に関する技術が多く進展している。非常に大量の生体情報を計算分析するための技術も進んでいる。私たちの未来の成功は私たちが適時かつ費用効果を持って顧客の絶えず変化する需要に追いつくことができるかどうかにかかっており、科学と技術の進歩に従って発展する新しい市場機会を求める。もし私たちがDNAシークエンシング、免疫学、計算生物学、ソフトウェア開発、新しい疾病診断と治療あるいは私たちが治療を求めている疾病に関する新しい科学知識を反映するために、私たちのプラットフォームと製品を更新しなければ、私たちの製品と技術は時代遅れになる可能性があるので、私たちの免疫薬物プラットフォームに基づく製品とサービスは低下するか、あるいは予想通りに増加できないかもしれない。
私たちの高級管理チームのいかなるメンバーの流失、あるいは私たちは高技能の科学者、臨床医師、販売員を引き付けることができなくて、すべて私たちの業務に不利な影響を与える可能性があります。
私たちの成功は私たちの共同創始者と幹部を含む、私たちの高度な管理チームの重要なメンバーのスキル、経験、表現にかかっている。私たちが私たちの免疫薬物プラットフォームに基づいて製品とサービスを開発し続けることに伴い、これらの従業員の個人と集団努力は重要である。私たちが合格後継者の採用に困難があれば、私たちの管理チームの既存メンバーの喪失や能力喪失は、私たちの運営に悪影響を及ぼす可能性があります。私たちの幹部たちは私たちと雇用協定に署名したが、彼らのサービスは任意で、いつでも終わるかもしれない。
私たちの研究開発計画と実験室運営は私たちが高技能科学者、技術者とソフトウェアエンジニアを誘致し、維持する能力にかかっている。生命科学と技術企業間の合格人材に対する競争のため、私たちは未来に合格した科学者、技術者或いはソフトウェアエンジニア、特にワシントン州シアトルにある施設とカリフォルニア州サンフランシスコ南部に位置する実験室施設の近くに引き付けることができないかもしれない。高い素質の科学者を採用し、維持する上で、大学や公共·民間研究機関からの競争にも直面している。私たちは合格した販売員を見つけたり、募集したり、維持するのが難しいかもしれない。採用、訓練、そして困難を維持することは、研究開発と商業化努力を支援する能力を制限するかもしれない。私たちのすべての職員たちは自由であり、これは私たちまたは職員たちがいつでも彼らの雇用関係を終わらせることができるということを意味する。
また、私たちはコンサルタント、請負業者、コンサルタントに依存して、科学と臨床コンサルタントを含めて、私たちの研究開発、監督、商業化戦略の制定を助けてくれます。私たちのコンサルタントとコンサルタントは、他の組織にサービスを提供することができ、他のエンティティとのコンサルティングまたはコンサルティング契約に基づいて約束することができ、これは、彼らに対する私たちの利用可能性を制限するかもしれません。私たちの既存のコンサルタントやコンサルタントの1人以上のサービスを失うことは、研究、開発、規制、商業化の目標を達成することを阻害するかもしれません。
40
もし私たちが重要な思想指導者の支持を失ったら、私たちの免疫薬物プラットフォームによって支持される製品やサービスを業界基準として構築することは困難かもしれません。これは、私たちの収入増加を制限し、利益を達成する能力を制限するかもしれません。
著者らはすでに一流の学術と研究機構のリード腫瘍学、血液学、免疫学、自己免疫或いは炎症性疾患、移植と固形腫瘍思想指導者と関係を樹立した。もしこれらの重要な思想指導者が私たちの免疫薬物プラットフォームあるいは私たちの現在または未来の製品またはサービスが臨床的に効果がないと判断し、代替技術がより有効であることを決定するか、あるいは内部開発されたサービスを使用することを選択すれば、私たちの製品やサービスを検証し、私たちの免疫薬物プラットフォームを業界標準として確立することを推進することに重大な困難があり、これは私たちの収入増加を制限し、利益を達成する能力を制限する。さらに、臨床医、業界組織、または他の重要な利害関係者の否定的な出版物または評論は、私たちの収入増加および利益を達成する能力に負の影響を与える可能性がある。
私たちは私たちの情報技術システムに依存して、これらのシステムのどんな故障も私たちの業務を損なう可能性があります。
私たちは情報技術と電気通信システム(第三者クラウドコンピューティングインフラ、オペレーティングシステムと人工知能プラットフォームを含む)に依存して、著者らの実験室情報管理システム、臨床免疫グループ学データベース、TCR抗原地図、実験室ワークフローツール、顧客と協力者報告及び関連機能を含む著者らの業務の重要な要素を実現する。私たちはまた、新製品の発表とコンプライアンスを支援するために、私たち独自のワークフローソフトウェアに依存している。
複雑なソフトウェアフローとパイプを用いてサンプルを管理し,配列決定結果データを評価する.これらは初期設計や進行中の修正の影響を受ける可能性があり,これらは意外な問題を招く可能性があり,これらの問題は患者の結果の変化を招き,サービス中断や誤りを招き,責任を招く可能性がある。
我々は、人的資源、財務制御および報告、契約管理、コンプライアンス、および他のインフラ業務を処理するシステムを含む、広範なビジネスプロセスおよび機能分野に影響を与えるいくつかの企業ソフトウェアシステムを実装し、拡大することが予想される。これらの業務システムに加えて,我々の技術システムの監視や警報機能,ネットワーク設計,自動対抗操作を強化することで,我々のセキュリティ制御を予防·検出する能力を拡張しようとしている.これらの情報技術と電気通信システムは、実験室業務、検査検証、サンプル追跡、品質管理、顧客サービス支援、請求書と精算、研究と開発活動、科学と医療管理、および一般行政活動を含む様々な機能をサポートしている。さらに、我々の第三者課金および入金プロバイダは、外部プロバイダが提供する技術および電気通信システムに依存する。
我々のサプライヤー、システム、情報技術に直接関連するリスクのほかに、外部サプライヤーや彼らが下請けする第三者に関連するリスクがある。例えば、我々のサードパーティ課金および入金プロバイダは、外部プロバイダによって提供される技術および電気通信システムに依存する。下請けは脆弱性の媒体である可能性があり,その組織の技術や組織制御におけるどの弱点もサプライヤーの運営やデータ管理に影響を与え,さらに我々自身の運営やキーデータを保護する能力に影響を与える可能性があるからである.
情報技術および電気通信システムは、電気通信またはネットワーク障害、悪意のある人為的行動(例えば、恐喝ソフトウェア)および自然災害を含む様々な形態およびソースの攻撃を受けやすい。また,ネットワークセキュリティやバックアップ対策をとっているにもかかわらず,我々のいくつかのサーバは物理的または電子的な侵入,コンピュータウイルス,および同様の破壊的な問題の攻撃を受けやすい可能性がある.我々の情報技術や電気通信システムに影響を与える可能性のある意外な問題を防止するための予防措置を講じているにもかかわらず、これらのシステムまたは私たちの協力者または下請け業者が使用するシステムが故障したり、深刻な停止が発生したりすることが、事業展開を阻止する可能性がある。私たちの運営の重要な側面に依存する情報技術や電気通信システムのいかなる中断や損失も、私たちの業務および私たちの名声に悪影響を及ぼす可能性があり、私たちは将来的に私たちの名声を回復または修復することができないかもしれない。
もし私たちの実験室施設が損傷したり操作できなかったり、既存の施設を空けてほしいと要求された場合、私たちが実験室過程と分析を行い、研究や開発を行う能力が脅かされる可能性があります。
私たちはワシントン州シアトルとカリフォルニア州サンフランシスコ南部で実験室施設を運営しています。私たちの施設および設備は、自然または人為的災害(戦争、火災、地震、停電、通信中断またはテロを含む)によって損傷または操作できない可能性があり、これらは、私たちの免疫医学プラットフォームを一定期間困難または不可能にする可能性がある。もし私たちの施設が短時間で稼働できなかったり、試薬や顧客サンプルなどの在庫を交換したりすることができない場合、私たちは顧客を失ったり、私たちの名声を損なう可能性があり、これらの顧客を再獲得したり、私たちの名声を修復することができないかもしれません。
41
また、研究開発作業を行うための施設や設備は、入手や修理や交換がコストが高く、時間がかかる可能性がある。当社の施設を再構築し、新しい施設を特定し、当社のノウハウを許可したり、第三者に当社のノウハウを譲渡することは困難であり、時間がかかり、高価であり、特にライセンスおよび認証要件を考慮しています。不可能な場合でも、私たちの実験室過程を行うことができるように、このような資格を持つ第三者を見つけることができ、ビジネス的に合理的な条項を交渉できないかもしれません。
私たちの財産損失と業務中断に保険を提供しますが、この保険は私たちの業務破損や中断に関連するすべてのリスクを含まない可能性があり、私たちの潜在的な損失を補うのに十分な保険金額を提供できない可能性があり、受け入れ可能な条項で保険を提供し続けることができないかもしれません(もしあれば)。
私たちはより多くの資金を集め、私たちの既存の業務に資金を提供し、より多くの製品やサービスを開発し、新製品やサービスを商業化したり、私たちの業務を拡大したりする必要があるかもしれない。
私たちの現在の業務計画によると、私たちは現在の現金、現金等価物、および有価証券が、少なくとも今後12ヶ月以内に予想される現金需要を満たすのに十分であると信じている。もし私たちの利用可能な現金および投資残高および予想される運営キャッシュフローが、本明細書で述べたリスクによる私たちの製品およびサービスに対する需要の低下を含む、我々の流動性要件を満たすのに十分でない場合、私たちは、普通株または優先株または転換可能な債務証券の売却、信用手配または他の形態の第三者融資の達成、または他の債務融資を求めることができるかもしれない。
私たちは将来的により多くの資本を調達して、私たちの業務を拡大し、戦略投資を行い、融資機会や他の理由を利用することを考えるかもしれません
私たちの現在と未来の支出需要は、多くの要素に依存するだろう
私たちが追加資本を調達する様々な方法は潜在的な危険を持っている。もし私たちが株式証券を発行することで資金を調達すれば、私たちの株主の権益を希釈するかもしれない。発行された任意の優先株式証券はまた、私たちの普通株式保有者よりも優先的な権利、優先権、または特権を規定することができる。もし私たちが債務証券を発行して資金を調達すれば、これらの債務証券は私たちの普通株保有者よりも優先的な権利、優先権、特権を持つだろう。クレジット協定によって発行または借金された債務証券の条項は、私たちの業務に重大な制限を与える可能性があります。もし私たちが協力と許可手配を通じて資金を調達すれば、私たちは私たちのプラットフォーム技術や製品やサービスに対する重大な権利を放棄するか、または私たちに不利な条項で許可を与えることを要求されるかもしれない。
42
私たちがNOL繰り越しといくつかの他の税金属性を使用する能力は制限されるかもしれない。
設立以来、私たちは純損失を受けて、私たちは決して利益を達成したり維持したりしないかもしれない。一般に、発生した損失は、このような損失満了(2018年1月1日までに発生した損失)または将来の課税収入(あれば)を相殺するために繰り越される。1986年に国税法第382条(“第382条”)や同様の国が規定した所有権変更制限により、我々のNOL繰越及び信用限度額の使用はかなりの年間制限を受ける可能性がある。年間制限はNOL繰越や使用前の信用満期を招く可能性がある。もし所有権が変化すれば、私たちがNOL繰り越しと信用を利用する能力は制限される可能性がある。第382条の2023年6月30日までの所有権変更の分析を完了し、制限をトリガする可能性のある変更を監視していきます。この分析に基づいて、私たちは連邦NOLの使用が永久的に制限されないと予想する。2017年の減税·雇用法案(TCJA)によると、2018年および今後数年に発生する連邦NOLは無期限に繰り越すことができるが、このような連邦NOLの控除額は年間制限されている。2018年前に生まれたNOLは20年に及ぶ資格を持っています。入手可能な客観的証拠によると、経営陣は、2023年12月31日現在、繰延税純資産が現金化できない可能性があると確定した。そこで、経営陣は2023年12月31日までの繰延税項純資産に全額推定手当を適用した。
私たちは未来に株式所有権の変化のために所有権の変化を経験するかもしれないが、これは私たちがコントロールできることではないかもしれない。したがって、純課税所得額を稼ぐ場合、私たちは所有権変更前にこのような課税所得額を繰り越して相殺する能力が制限される。州税法の似たような規定はまた私たちが累積的な州税収属性を使用することを制限するのに適用されるかもしれない。したがって、私たちが利益を達成しても、私たちは私たちのNOL繰り越しや他の税金属性の大部分を使用できない可能性があり、これは私たちの将来のキャッシュフローに悪影響を及ぼすかもしれない。
私たちは海外腐敗防止法や他の世界的な反賄賂法に違反した悪影響を受けるかもしれない。
私たちの地理的拡張に伴い、私たちの製品とサービスを商業化し、製品やサービスを販売するために必要な許可、許可、または承認を得ようとしている。国際顧客が私たちの製品やサービスを注文できるかもしれないので、私たちまたは私たちの協力者は米国以外で事業を展開しているとみなされるかもしれない。したがって、私たちまたは私たちの協力者は、会社およびその中間者が業務を獲得または保留し、または任意の他の不正な利益を得るために、法律に違反して非米国政府関係者にお金を支払うことを禁止する“海外腐敗防止法”の制約を受けるだろう。また、私たちの協力者や任意の第三者流通業者は私たちの代理とみなされる可能性があり、私たちは“海外腐敗防止法”違反を含む彼らの行動に責任を負わなければならないかもしれない。生命科学業界の他の米国会社も、その代理人が非米国政府関係者とビジネスをする際に適切なやり方から外れることを許可したことで、“反海外腐敗法”の刑事罰に直面している。私たちが業務を展開する可能性のある司法管轄区域では、イギリスの2010年の“反賄賂法”を含む同様の反賄賂法律の制約を受ける可能性もあり、商業賄賂も禁止され、会社が賄賂を犯罪とすることを防ぐことができなかった。このような法律は本質的に複雑で深遠であり、私たちは未来にこのような法律に適合するために私たちの1つ以上の接近法を変える必要があるかもしれない。したがって、私たちの国際拡張は、これらの法律に違反した行為、またはそのような違反の疑いが、私たちの運営を混乱させる可能性があり、重大な管理気晴らし、法的費用を含む重大なコストと支出に関連し、私たちの業務、将来性、財務状況、または運営結果に重大な悪影響を及ぼす可能性があることを警戒する必要があるだろう。私たちはまた刑事と民事処罰、返済資金、そして他の救済措置を含む厳しい処罰を受ける可能性がある。
私たちは他の業務を買収したり、合弁企業を作ったり、他の会社や技術に投資したりする可能性があり、これらは私たちの経営業績にマイナスの影響を与え、私たちの株主所有権を希釈し、私たちの債務を増加させたり、巨額の費用を発生させたりする可能性があります。
私たちは事業と資産の買収を求めるかもしれない。私たちはまた、私たちの免疫薬物プラットフォームと業界経験を利用して、私たちの製品や流通を拡大するために、合弁や投資を求めることができる。私たちは合弁企業を作った経験がなく、他の会社に投資したり買収したりする経験が限られている。適切な合弁企業、投資、または買収候補を見つけることができないかもしれませんし、もしあれば、有利な条件でこのような取引を達成できないかもしれません。もし私たちがどんな買収をすれば、買収された会社を既存の業務に成功させることができないかもしれません。“海外腐敗防止法”などの規制違反や同様の法律を含む未知または負債を負担する可能性があります。いずれの将来の買収も、債務、または負債または将来の無形資産または営業権のヒットをもたらす可能性があり、いずれも私たちの財務状況、運営業績、およびキャッシュフローに重大な悪影響を及ぼす可能性がある。買収された会社の統合は、進行中の運営を混乱させ、資源を管理する必要がある可能性もあり、そうでなければ、既存事業の発展に専念します。私たちは他の会社への投資に関連した損失に直面する可能性があり、これは私たちの運営業績や財務状況に実質的なマイナス影響を与える可能性がある。私たちはどんな買収、技術許可、協力、または合弁企業の期待収益を達成できないかもしれない。
43
任意の買収や合弁企業に融資するために、対価格として普通株を発行することを選択する可能性があり、これは私たちの株主の所有権を希釈する。追加的な資金は私たちに有利な条項で提供されないかもしれないし、全くそうではないかもしれない。もし私たちの普通株価格が低いか変動が大きい場合、私たちは他の会社を買収したり、私たちの株を犠牲にして合弁プロジェクトに資金を提供できないかもしれません。
不利な米国や世界的な経済状況は、私たちの業務、財務状況、または経営結果に悪影響を及ぼす可能性がある。
私たちの経営業績は世界経済と金融市場の全体的な状況の悪影響を受ける可能性があります。このような経済状況の変化は最近のインフレ上昇のような急に現れる可能性がある。世界的な大流行やその他の原因による深刻または長期的な経済低迷は、私たちの製品やサービスに対する需要の減弱や、必要に応じて有利な条件で追加資本を調達する能力など、私たちの業務に様々なリスクをもたらす可能性がある。例えば,バイオ製薬業界に影響を与えるマクロ経済要因により,医薬サービスの鈍化が観察された。経済の疲弊や下落はまた私たちの協力者に圧力を与え、供給中断を招くか、あるいは彼らの私たちへの支払いの遅延を招く可能性がある。上記のいずれも私たちの業務を損なう可能性があり、現在の経済気候や金融市場の状況が私たちの業務に悪影響を及ぼす可能性のあるすべての方法を予見することはできません。
私たちが使用している生物と危険材料は処理、貯蔵、処置のためにかなりの専門知識と費用を必要とし、私たちへのクレームを招く可能性がある。
私たちが使用する材料は、化学品、生物学的製剤および化合物、ならびにヒトの健康および安全または環境に有害である可能性のあるサンプルを含む。私たちの業務はまた危険と生物廃棄物製品を発生させる。連邦、州、地方の法律法規はこれらの材料と廃棄物の使用、発生、製造、貯蔵、処理、処理を管理する。適用される環境法律法規を遵守することはコストが高く、現在または未来の環境法律法規は私たちの運営を制限するかもしれない。もし私たちが適用された規制を守らなければ、私たちは罰金と処罰を受けるかもしれない。
また、これらの材料や廃棄物による意外なダメージや汚染のリスクを除去することはできず、これらのリスクは、材料やサンプル移動の数が増加するにつれて増加し、私たちの商業化努力、研究開発計画、業務運営中断、および環境破壊を招き、高価な清掃費用と法律法規に規定された責任を適用する可能性がある。また,環境法律法規は複雑で変化が頻繁であり,より厳しくなる傾向にある。私たちはこのような変化の影響を予測することもできないし、私たちの未来のコンプライアンス状況を決定することもできない。私たちの財産保険リストは、危険と生物製品の汚染とそれによって発生するクリーニング費用の場合、限られた保証範囲を提供していますが、私たちは現在、危険材料の処理、貯蔵、あるいは処分によるクレームの法的責任は何もありません。したがって、汚染や傷害が発生した場合、私たちは損害賠償責任を負い、あるいは私たちの資源を超える罰金を科すことができ、私たちの運営は一時停止したり、他の悪影響を受ける可能性があります。
もし私たちが製品責任や専門責任で起訴されたら、私たちは私たちの資源を超えた巨額の責任に直面するかもしれない。
私たちの製品またはサービスが設計または予想通りに実行されなかったと非難された場合、マーケティング、販売、および私たちの製品およびサービスの使用は、製品または専門責任クレームを引き起こす可能性があります。私たちはまた、私たちが提供したTCR関連配列およびデータに基づいて製造されたGenentechによって販売されている細胞療法のような、私たちの協力で商業化された製品の治療失敗に関するクレームに直面する可能性がある。私たちはまた、正常な業務活動中に提供される情報のミス、誤解、または不適切な依存に責任を負うことができます。製品責任や専門責任クレームは重大な損害賠償を招く可能性があり、私たちの弁護コストが高く、時間がかかります。是非曲直や最終結果にかかわらず、製品責任と専門責任クレームは以下のようになる可能性がある
44
私たちは製品と専門責任保険を維持していますが、この保険は製品責任や専門責任クレームから私たちを完全に保護できないかもしれません。私たちが提起した任意の製品責任または専門責任クレームは、望ましい点があるかどうかにかかわらず、私たちの保険料率を増加させたり、将来的に保険範囲を得ることを阻止したりする可能性があります。さらに、どの製品責任訴訟も、既存の協力者が既存の合意を終了したり、潜在的な協力者が他社を求めたりする可能性があり、これらはいずれも私たちの運営結果に影響を与える可能性があります。
私たちのどんな製品やサービスもEUや他の外国では決して承認されないかもしれません。たとえ私たちが承認されても、私たちまたは私たちの協力者は、任意の他の司法管轄区でそれを商業化することができないかもしれません。これは、私たちがすべての市場潜在力を達成する能力を制限することになります。
最終的に任意の特定の外国司法管轄区で私たちの現在または未来の任意の製品とサービスを販売するために、私たちは各管轄区で品質、安全、性能、効果に関する多くのおよび異なる法規要件を確立し、遵守しなければならない。さらに、一国で行われる臨床試験または臨床調査は、他の国の規制機関によって受け入れられない可能性があり、一国の規制許可、許可または承認は、任意の他の国での規制許可、許可または承認を保証しない。承認の流れは国によって異なり、追加の製品テストと検証、追加の行政審査期間に関連する可能性があります。
外国の監督管理許可、許可或いは承認を求めることは私たちと著者らの協力者に困難とコストをもたらす可能性があり、追加の臨床前研究、臨床試験或いは臨床研究が必要であり、これは高価で時間がかかるかもしれない。規制要求と道徳的な承認義務は国によって異なる可能性があり、私たちの製品やサービスがこれらの国で発売されることを延期または阻止する可能性がある。外国規制機関の承認、許可または承認プロセスは、FDA承認、許可または承認に関連するすべてのリスクおよび不確実性に関連する。我々は,フランス,ドイツ,イタリア,イギリス,スペイン,オーストラリアなどの国際サイトへの研究用途の技術移転プロセスを完了したが,国際市場で規制許可,許可または承認を得た経験はない。もし私たちまたは私たちのパートナーが国際市場の規制要求を遵守できなかったり、国際市場で必要な規制許可、許可または承認を獲得して維持できなかったり、あるいはこれらの承認が延期された場合、私たちの目標市場は減少し、私たちの製品とサービスのすべての市場潜在力を達成する能力は達成できないだろう。
私たちまたは私たちの協力者は、自然または人為的災害または他の業務中断(例えば、ネットワークセキュリティ攻撃)の悪影響を受ける可能性があり、私たちの業務連続性および災害復旧計画または私たちの協力者の計画は、深刻な災害から私たちを十分に保護できない可能性があります。
天災人災や他の私たちがコントロールできない事件は、私たちまたは私たちのパートナーの運営を深刻に混乱させ、私たちの業務、運営結果、財務状況、および見通しに実質的な悪影響を及ぼす可能性がある。自然災害、停電、ネットワークセキュリティ攻撃、または他の事件が発生した場合、私たちは私たちの本部の全部または大きな部分を使用することができず、私たちの実験室施設や私たちの協力者の施設のような重要なインフラを損傷させ、私たちまたは私たちの協力者のアクセスを制限したり、私たちのそれぞれのデジタル情報システムの能力を使用したり、あるいは他の方法で私たちのそれぞれの運営を乱すことができなくなり、私たちまたは私たちの協力者は難しいかもしれないし、場合によっては長い間私たちのそれぞれの業務を継続することはできません。我々のパートナーと現在策定されている災害復旧·事業継続計画は限られており、深刻な災害や同様の事件が発生した場合に十分であることはあまり証明されていない。我々のネットワークセキュリティ責任保険は、(第三者のデータプライバシー権が負の影響を受けることによって生じる潜在的責任を含む)私たちまたは私たちの協力者が、私たちまたは私たちの協力者が受けることができる深刻さおよび程度に依存する、私たちまたは私たちのコンピュータセキュリティプロトコルまたは他のネットワークセキュリティ攻撃に違反することによって、私たちまたは私たちの協力者が受けることができる任意のまたはすべての損害を含まない可能性がある。私たちそれぞれの災害復旧と業務連続計画の性質が限られているため、大量の費用が発生する可能性があり、これは私たちの業務に大きな悪影響を及ぼす可能性があります。
私たちまたは私たちが依存している第三者が重要な実験室運営、製造施設、臨床試験地点が集中あるいは他の業務運営を持っている地域では、私たちの業務は衛生流行病の影響、例えば最近の新冠肺炎の大流行を受ける可能性がある。このような流行病は、私たちの業務および私たちのメーカー、契約研究機関、または私たちと業務の往来があり、または業務を展開する必要がある他の第三者の業務または業務に実質的な影響を及ぼす可能性があります。
私たちの業務は、世界的な疫病または臨床試験場所または他の業務運営地域に集中している私たちの衛生疫病の悪影響を受ける可能性があり、このような疫病または疫病は、私たちが依存する必要がある資本プロジェクトおよびCROに関連する第三者メーカー、サプライヤー、総請負業者、および下請け業者の運営を深刻に中断させる可能性がある。
私たちの製品、サービスまたはサービスが隔離されているため、家にいる注文または同様の政府注文、またはそのような注文、閉鎖または他の業務運営制限が発生する可能性があると考えられ、新冠肺炎または他の感染症に関連しても、米国および他の国の第三者製造またはサプライヤー工場の人員、または材料の可用性またはコストに影響を与え、私たちのサプライチェーンを乱す可能性がある。
45
政府の規制に関するリスク
私たちは、厳しい規制を受けている業界で業務を展開しており、法規の変化や規制違反は、私たちの収入を直接的または間接的に減少させる可能性があり、私たちの運営結果や財務状況に悪影響を与え、私たちの業務を損なう可能性があります。
生命科学産業は高度に規制されており、私たちと私たちの協力者が置かれている規制環境は将来的に大きな変化が起こり、私たちに不利になるかもしれない。私たちの業務を展開する能力に影響を及ぼす可能性のある規制環境分野には、以下のような連邦や州法が含まれているが、これらに限定されない
特に,RUO製品,LDTと臨床診断テストやサービスを管理するマーケティングの法律,法規や政策は極めて複雑であり,裁判所や政府機関の解釈が必要である。私たちの不遵守は民事または刑事罰を招く可能性があり、州や連邦医療計画から除外されたり、私たちの実験室が私たちのサービスを提供したり、支払いを受ける能力を禁止したり制限したりすることができます。私たちは、すべての法律および法規要件を実質的に遵守しているが、1つ以上の政府機関が反対の立場を取る可能性があるリスクが存在するか、または個人当事者が連邦虚偽請求法案または同様の州法律のQui tam条項に従って訴訟を提起する可能性があると信じている。結果にかかわらず、このような事件は、私たちの名声を損なう可能性があり、第三者(信託医療機関および他の個人第三者支払者を含む)との重要な業務関係に悪影響を及ぼす可能性がある。
新たに承認された診断と治療類製品の保険カバー範囲と精算状況はまだ確定していない。現在または将来の製品のために十分な保険や精算を得ることができない場合、私たちと私たちの協力者が私たちの製品を完全に商業化する能力を制限し、私たちの収入を創出する能力を低下させる可能性がある。
政府と個人支払者の獲得性と精算範囲は、大多数の患者が私たちと私たちの協力者計画の開発と販売を負担できる臨床診断テストと治療に重要である。さらに、私たちの臨床診断といくつかの潜在的な治療製品は疾病研究、診断、検査と治療の新しい方法を代表するため、私たちの製品とサービスと私たちの協力者と共同で作成した製品とサービスがどのように価格を設定するか、清算または任意の潜在的な収入を得ることができるかどうかを正確に推定することができない。私たちの製品の販売は、私たちの製品とサービスのコストがどの程度健康維持、管理医療、薬局福祉、および類似の医療管理組織によって支払われるか、あるいは政府衛生行政当局、個人健康保険会社、その他の第三者支払人によってどの程度精算されるかに大きく依存する。精算が得られない場合、あるいは限られた精算しか得られない場合、私たちのいくつかの製品やサービスを商業化することに成功できないかもしれません。保険が提供されても、承認された精算金額は、任意の製品やサービスへの投資に十分なリターンを達成するために、十分な価格設定を確立または維持するのに十分ではない可能性があります。もし私たちがどんな製品やサービスに対しても自己負担戦略を取るなら、私たちは十分に高い価格設定を確立したり維持したりする上で似たような困難に直面するかもしれない。清算構造は変化する可能性があり、これは私たちがコントロールできないことであり、私たちの製品とサービスの商業可能性に影響を与えるかもしれない。
46
新たな清算、認可または承認された製品やサービスの保険カバー範囲や補償に関する不確実性が大きい。アメリカでは、新しい診断と薬物精算に関する多くの重大な決定は通常衛生と公衆サービス部の1つの機関CMS及びその請負業者によって行われる。CMS及びその請負業者はどの程度新しい診断或いは薬物が連邦医療保険下でカバーと精算されるかどうかを決定する。個人支払者はCMS政策に大きく従う傾向がある。CMSおよびその請負業者が、我々のような新製品およびサービスに対する補償をどのように決定するかを予測することは困難である。しかも、ヨーロッパの精算機関はCMSよりもっと保守的かもしれない。これらの固有の制限は、clonoSEQに対する新しい適応を含む、臨床製品から収入を達成する能力に影響する可能性がある。
アメリカ以外では、精算の流れとスケジュールが大きく違う。いくつかの国は、いくつかのEU加盟国を含み、診断および薬品または薬品の価格制定および補償決定を行い、マーケティング許可またはEU(“CE”)マーク保持者に適合する参加は限られているか、または許可またはCEマーク保持者に不利な決定を下す可能性がある。私たちはそのような価格と精算決定が私たちまたは私たちの協力者たちに受け入れられるかどうかを確信できない。もしこれらの外国司法管轄区域の規制機関が制定した価格や補償基準が私たちまたは私たちの協力者に商業的な魅力がなければ、私たちのこれらの国での収入と私たちの製品やサービスの潜在的な収益力はマイナスの影響を受けるだろう。
米国やEUを含むますます多くの国が取り組みを進めており,コスト削減の努力を医療製品に集中させることや,その国営医療システムが提供する医療機器を小さくすることで医療予算を制御しようとしている。また、一部の国は製品の販売価格が発売前に承認されることを要求したり、強制割引や利益上限を実行したりすることができる。また,販売価格を承認した後も,製品ライフサイクル内に審査を行う必要がある。多くの国では、定価審査期間は、市場または製品許可の承認またはCEマークの取得後に開始される。したがって、私たちまたは私たちの協力者は、特定の国/地域で製品またはサービスのマーケティング承認を得る可能性がありますが、その後、精算承認の遅延や価格規制の制約に遭遇する可能性があり、これは、特定の国/地域で製品またはサービスを販売することによる収入に悪影響を及ぼす可能性があります。
さらに、米国および海外では、政府および第三者支払者が医療コストを制限または低減することは、これらの組織が新たに承認、許可または承認された装置および薬物のカバー範囲および精算レベルを制限することをもたらす可能性があり、したがって、彼らは、私たちまたはパートナーが販売する臨床診断または細胞療法のために十分な支払いを提供することができないかもしれない。例えば、米国政府は2019年の“現在の薬品コスト低減法案”を打ち出し、薬品コストを低減している。この青写真には、衛生と公共サービス部が実施しようと努力しているいくつかの措置が含まれている。また、“意外法案”(NSA)は2022年1月に発効した。NSAの目標の1つは,ネットワーク外提供者(例えば実験室)が提供するネットワーク内施設の患者受診に関するサービスカバー不足による“意外”医療請求書から患者を保護することである。NSAは、ネットワーク外の実験室が、ネットワーク内施設アクセス中に注文された実験室サービスの費用を患者に請求することができ、実験室および保険会社がレートについて合意できない場合の実験室サービスの補償金額を決定するための独立した論争解決手順を確立することができる。アメリカ国家安全保障局が私たちの診断製品や細胞療法の価格を制限すれば、これらの製品の商業可能性は不利な影響を受ける可能性があります。
州レベルでは、立法機関は、価格または患者の精算制限、割引、特定の製品参入の制限およびマーケティングコスト開示、および透明性措置を含む、医薬品および生物学的スキームの価格設定を制御するための法規を立法および実施することが増えており、場合によっては、これらの措置は、他の国からの輸入および一括購入を奨励することを目的としている。
価値に基づく価格設定とカバーの傾向、健康維持組織の影響力がますます大きくなり、追加の立法変化により、私たちと私たちの協力者が販売している臨床診断と細胞療法は定価圧力に直面することが予想される。全体的に,医療コストの下振れ圧力は非常に大きくなり,特に処方薬,外科手術,その他の治療が行われている。そのため、新製品の参入にはますます高い壁が設けられている。
47
CLIA、その実施条例、または免許または認証に影響を与える他の州、連邦および外国の法律および法規、またはこれらの法律または法規の将来の変化によれば、私たちの業務は、免許、認証または承認の損失、一時停止または他の制限、または罰金または処罰の適用によって損害を受ける可能性がある。
連邦法律はほとんどの臨床実験室がCLIAを遵守しなければならないことを要求しており、これは通常連邦と州政府が行うテストの認証を取得し、テストサービスの正確で信頼性を確保するための各種運営、人員、施設管理、品質と能力テスト要求を遵守することを含む。CLIA認証も州と連邦医療保健計画及び多くの個人第三者支払人に実験室研究と臨床診断テストサービス請求書を発行する資格がある前提条件である。私たちCLIA認証の条件として、私たちはワシントン州シアトルにある実験室で1年おきに調査と検査を受け、州や連邦規制機関から受けた苦情に基づいて追加的なランダム検査と抜き打ち検査を行う。2年ごとの調査と検査はCMS,CMSエージェントが行い,実験室がCLIA認証証明書を持っていればCMSが承認した認証組織,CAPのように行う。能力試験違反行為を含むCLIA要求を遵守できなかった制裁には、業務を展開するために必要である実験室のCLIA証明書を一時停止、撤回または制限すること、および実験室、その所有者および他の個人に重大な民事、行政または刑事制裁を適用することが含まれる可能性がある。しかも、私たちは特定の実験室許可証を管理する州の法律と法規によって規制されている。ワシントンを含むいくつかの州では、CLIAよりも厳しい実験室ライセンスとコンプライアンス法が制定されている。州許可証法の変化は、私たちの州や国を越えて製品やサービスを研究·診断する能力に影響を与え、私たちの業務に実質的な悪影響を及ぼす可能性がある。さらに、国家および外国の実験室認証に対する要求は費用が高く、または満足しにくい可能性があり、いくつかの州または外国から標本を受け取る能力に影響を与える可能性がある。
CLIA、その実施条例または管理免許の州または外国の法律または法規に基づいて実施される任意の制裁、または私たちがCLIA証明書、州または外国免許または認証を更新することができないことは、私たちの業務に実質的な悪影響を及ぼす可能性がある。
健康保険のカバー範囲や支払いに関する法的変化は、私たちの業務に悪影響を及ぼす可能性があります。
アメリカでは、医療コストを抑えるための多くの立法措置が続いているだろう。例えば,2010年3月,ACAが採択され,政府や民間保険会社が医療保険に融資する方式を大きく変え,米国の臨床診断やバイオ製薬業界に大きな影響を与えた。その他の事項以外に、ACAはメーカーが医療補助薬品返却計画の下で不足している最低医療補助税金還付を高め、税金還付計画を医療補助管理保健組織に参加する個人に拡大し、あるブランドの処方薬と医療機器(実験室キットを含む)のメーカーに対して年会費と税収を創立し、そして新しい連邦医療保険D部分のカバーギャップ割引計画を推進した。
ACAのいくつかの条項は司法と議会によって挑戦された。規制条項と副次的な監督指導がACAの解釈と実施及びわが業務への実際の影響にどのように影響するかは不明であり、両者は絶えず変動している。さらに、我々の製品およびサービスを支払うことを支援するための第三者支払いを求める患者数の変化は、これらの製品およびサービスの需要に影響を与える可能性がある。
私たちは未来にどのような医療改革措置が取られるのか予測できない。連邦、州、外国の立法と規制はさらに発展する可能性があり、私たちが行っている措置は薬品と設備価格の下振れ圧力を増加させると予想される。このような改革は、パートナーと共同開発した製品およびサービスの予想収入を含む、当社の製品およびサービスの予想収入に悪影響を及ぼす可能性があり、私たちの全体的な財務状況および私たちの製品およびサービスの開発または規制承認、許可または承認を得る能力に影響を与える可能性があります。
FDAや他の政府機関の資金不足は、重要な指導部や他の人員を採用して保持する能力を阻害し、新製品やサービスのタイムリーな開発や商業化を阻止したり、これらの機関が私たちの業務運営に依存する可能性のある正常な業務機能を履行することを阻止したりすることができ、これは私たちの業務にマイナスの影響を与える可能性がある。
FDAの新製品の審査と承認、許可或いは承認の能力は、政府予算と資金レベル、肝心な人員を雇用と維持する能力、及び法定、監督管理と政策変化を含む様々な要素の影響を受ける可能性がある。また、研究開発活動に資金を提供する機関を含む、私たちの行動に依存する可能性のある機関への政府の援助は、政治プロセスの影響を受け、このプロセスは本質的に不安定で予測不可能である。
FDAおよび他の機関の中断はまた、新薬および装置が必要な政府機関によって審査、承認、許可または承認されるのに要する時間を遅らせる可能性があり、これは私たちの業務に悪影響を及ぼすだろう。例えば、ここ数年間、米国政府は何度か閉鎖されており、FDAのようないくつかの規制機関は、キー従業員を休暇にし、キー活動を停止しなければならない。政府が長期的に停止すれば、FDAが私たちが提出した規制文書を適時に審査して処理する能力に深刻な影響を与える可能性があり、これは私たちの業務に実質的な悪影響を及ぼす可能性がある。
48
私たちはFDAと対応する外国と州規制機関の私たちの製品とサービスに対するマーケティング許可要求を守らなければならない。これらの製品とサービスの販売はその許可を受けており、FDAの要求を守らなければ、私たちの製品とサービスのマーケティングを阻止または延期するかもしれない。
私たちがマーケティング許可を得ても(私たちがclonoSEQに対してしたように)、私たちはその許可、許可、または承認の範囲を守らなければならない。ニューヨーク州臨床実験室評価計画のようなこれらの制限またはFDAが課した追加、広範かつ持続的な上場後の義務または他の監督機関の他の規制要件を守らない場合、意外なコンプライアンス支出、一連の行政法執行行動、禁止、刑事起訴を招く可能性がある。FDAの上場後の義務は、FDA QSRを遵守し、登録と設備リストを確立し、ラベル要求、ある不良事件と故障を報告し、そしてあるリコールを報告することを含む。また、私たちの製品やサービスに関連する設備をリコールする場合があります。このようなリコールは、私たちがこれらの製品やサービスを提供する能力に悪影響を与え、ひいては私たちの財務状況に悪影響を及ぼす可能性がある。私たちの協力者はまたFDAの許可を維持することを要求され、私たちが共同開発した製品やサービスの他の許可または承認が必要かもしれない。もし私たちまたは私たちの協力者がこのような許可、許可、または承認を維持できなかったら、私たちがこれらの協力から利益を得る能力を弱化または遅延させるかもしれない。
Ruoが提供する製品とサービスは規制機関によって検討される可能性がある。
私たちのいくつかの製品は現在RUOを基礎として提供されており、疾病の診断或いは治療には使用されていない。FDAのRUO製品に関する指導方針に基づいて、会社はRUO製品に対して臨床或いは診断声明を行ってはならず、或いはRUO製品の顧客に臨床指導或いは臨床支持サービスを提供してはならない。FDAが私たちのRUO分類に同意しない場合、またはRUO製品を規制する方法を修正する場合、私たちは収入の減少またはコンプライアンスおよび他のコストの増加に遭遇する可能性があり、これは私たちの業務、将来性、運営結果、および財務状況に悪影響を及ぼす可能性があります。もしFDAが将来私たちのRUO製品の上場許可を要求した場合、FDAは最終的に私たちが要求したいかなる許可、許可、または承認もタイムリーではないか、または全く承認しないかもしれない。
LDT法執行裁量権に対するFDAの将来の変化は、私たちの運営をより重要な規制要求を受ける可能性がある。
いくつかの血液癌のMRDテストとしてクリアランスバージョンのclono配列を提供することに加えて、現在、このテストのLDTバージョンを他の適応のために提供している。FDAはLDTに対して裁量権を実行する政策を有しており,この政策によれば,FDAはこのような試験に対する医療機器規制要求を積極的に実行しない。しかしながら、2014年10月、FDAは、FDAが既存の医療機器分類に適合したリスクに基づく方法でLDTに関する法執行自由裁量政策を修正しようとしていることを示す2つの指導文書草案を発表した。FDAは2016年11月にガイドラインの定稿を停止し、LDTの適切な監督方法をさらに大衆に討論することを可能にし、国会許可委員会に立法解決策を制定する機会を与えたが、国会またはFDAが現在のLDTに対する規制方法を修正するかどうかは不明であり、私たちが現在または未来にLDTとして発売されるサービスがFDA規制要求によって実行されるようにする。FDA専門員と設備と放射線健康センター(CDRH)の取締役はいくつかのLDTと放射線健康の間の差に深刻な関心を示した体外培養FDAによって審査され、承認され、許可され、または承認された診断。FDAがLDTとして提供されるNGS MRDテストが任意の理由(新しいルール、ポリシーまたはガイドラインを含む)または法規の変化によってLDTのポリシー範囲内でないと判断した場合、私たちのテストはFDAの広範な要求を受ける可能性があり、または私たちのトラフィックは悪影響を受ける可能性がある。FDAがLDTの地位を変更したり、LDTを規制する方法を修正したりしない場合、収入の減少やコストの増加に遭遇する可能性があり、これは私たちの業務、将来性、運営結果、および財務状況に悪影響を及ぼす可能性があります。必要に応じて、現在または将来のLDTコンプライアンスに必要なマーケティング許可プロセスを規制することは、他の事項に加えて、追加の臨床検証を成功させ、FDAの上場前許可(510(K))を提出または許可することを含む可能性がある初めからやり直すPMAを承認したりしますまた、最近導入された立法、例えば有効法案が可決されれば、新たなまたは異なる規制やコンプライアンス負担をもたらす可能性があり、新製品を開発する能力に悪影響を及ぼす可能性があり、これは私たちの業務に実質的な影響を与える可能性がある。FDAが将来私たちのLDTに上場許可を要求した場合、FDAは最終的に私たちが要求したいかなる許可、許可、または承認もタイムリーにまたは全く承認しないかもしれません。さらに、FDAがFDAによって承認されたclonoSEQ試験に関する我々の実験室のマーケティング状況を検査する場合、FDAがとる任意の法執行行動は、FDAによって承認されたclonoSEQ試験に限定されるものではなく、我々の低密度リポタンパク質試験サービスも含まれる可能性がある。
49
我々が開発しているFDAの上場前審査または同等の規制承認を必要とするすべての製品について、FDAまたは他の規制機関は、承認、許可、または発売前の承認を与えない可能性があり、将来の製品およびサービスが必要な承認を得られなければ、私たちの業務成長能力に悪影響を及ぼす。
米国で商業診断用途のための他の臨床診断製品の生産、標識、販売を開始する前に、私たちは、免除が適用されない限り、またはFDAがその法執行裁量権を行使しない限り、FDAおよびそのような製品に管轄権を有する州規制機関の承認、マーケティング許可または承認を得る必要があるかもしれない。例えば、FDAの現在の政策は、LDTに関連する医療機器要件を強制的に実行しないことであり、FDAは、LDTは、単一の正式な許可を得た実験室内で設計、製造、および使用されるインビトロ診断テストであると考えている。
510(K)承認プロセスに比べて,FDAからPMAを取得する過程ははるかに厳しく,コストが高く,時間が長く,不確実である.PMA承認過程において、FDAは技術、臨床前、臨床試験、製造、およびラベルデータを含むが、これらに限定されない大量のデータに部分的に基づいて、提案された設備を決定することは、その期待される用途に対して安全かつ有効である。対照的に、510(K)の承認中、FDAは、提案された装置が合法的に発売された“述語”装置“と実質的に等しい”と判断しなければ、製品の発売を承認することができない。“実質的に等しい”ためには,提案するデバイスは述語デバイスと同じ期待用途を持つ必要があり,同じ技術的特徴を持つか,述語デバイスとは異なる技術的特徴を持つ場合,提案デバイスは述語デバイスと同様に安全かつ有効でなければならず,述語デバイスとは異なる安全や有効性の問題を引き起こすことはない.実質的な等価性を支援するために臨床データが必要となる場合がある。本来クラスIIIに自動的に分類される低リスクデバイスの場合、利用可能なアサートされたデバイスがなく、デバイスが既存の510(K)免除分類に属さないので、PMAが必要であり、出願人は、最初から出願を提出し、デバイスをクラスIIまたはクラスIに低減することができ、これはPMAを必要としない。最初からのプロセスでは、FDAは、一般的な制御および特殊な制御が、デバイスの安全性および有効性を合理的に保証するのに十分であることを決定しなければならず、デバイスのリスクは低中程度であり、断言されていない。言い換えれば、出願人は、IまたはIIレベルに“降格”することが合理的であることを新しい製品タイプのために証明しなければならず、そうでなければ、このような新製品タイプは自動的にレベルIIIに分類されるが、リスクは低い。臨床データが必要かもしれません。FDAの承認、許可または承認を必要とする実験室試験については、FDAはまた、データ支援分析および臨床的有効性を要求する可能性がある。
510(K)、最初から、およびPMAプログラムは、高価で長い可能性があり、免除が適用されない限り、多くの費用を支払う必要がある。FDAの510(K)承認経路は、通常、提出まで3~9ヶ月かかるが、新型製品にはより長い時間を要する可能性がある。FDAの最初の分類には通常6ヶ月から12ヶ月が必要ですが、多くの申請者にとっては18ヶ月以上かかるかもしれません。
PMAを取得するプロセスは、通常、PMAがFDAに提出されてから承認を得るまでに1~3年、さらにはより長い時間を要する。必要な規制許可、許可、または承認が遅延されたり、得られなかったりすることは、私たちの業務、財務状況、および見通しに重大な悪影響を及ぼすだろう。
FDAは、多くの理由で、承認、許可、または承認装置を延期、制限、または拒否することができる
50
多くのFDA員がマーケティング提出を審査する異なる側面を割り当てられており、これは審査過程で判断や適宜決定権を行使する能力によって不確実性をもたらす可能性がある。審査中、FDAは追加のデータおよび情報を要求または要求する可能性があり、これらのデータおよび情報を開発および提供することは、時間がかかり、高価である可能性がある。規制許可、許可、または承認を得て医療機器を市場に出す過程は高価で時間がかかる可能性があり、私たちはこれらの許可、許可または承認をタイムリーに得ることができないかもしれないし、私たちが開発している製品のためにこれらの許可、許可、または承認を得ることができないかもしれない。もし私たちが承認、許可、または承認を求めるいかなる製品も承認、許可、または承認を得ることができなければ、私たちの業務は損害を受ける可能性があります。
FDA承認を得る前に、私たちの製品を修正することは、新しいFDA承認、許可または承認を必要とするかもしれません、または修正された臨床診断製品または将来の臨床製品の販売を停止またはリコールすることを要求する可能性があります。
510(K)許可デバイスの任意の修正は、そのセキュリティまたは有効性に著しく影響を与える場合、またはその予期される用途を構成する重大な変化である場合、新しい510(K)許可、新しい最初から許可、またはPMA承認を必要とする可能性がある。FDAは各メーカーに最初にこの決定を下すことを要求するが、FDAはどのメーカーの決定も検討することができる。FDAは新しい許可、許可、または承認が必要かどうかに関する私たちの決定に同意しないかもしれない。
PMAによって承認された任意の製品については、承認された製品の多くのタイプの修正として追加承認を求めることが求められます。FDAは、製造業者に、PMAサプリメントまたは他の規制申請が必要かどうか、またはPMA年次報告によって変化を報告することができるかどうかを最初に決定することを要求するが、会社の評価に同意しない可能性がある。
FDAが私たちの決定に同意しない場合、私たちが年次報告書やFDAを提出して検査や他の調査を行う前に、私たちの決定を審査しない可能性があり、私たちが以前承認、許可、または承認した臨床診断製品を修正するために新しい許可、許可または承認を求めることが要求される可能性があり、新しい許可、許可、または承認が必要ではないと考えられる場合、私たちは承認、許可または承認を得るまで、マーケティングを停止したり、流通を停止したり、修正された製品をリコールすることを要求される可能性があります。私たちはまた巨額の規制罰金や処罰を含む法執行行動の影響を受ける可能性がある。
私たちの従業員、主要な調査人員、顧問と協力者は監督基準と要求を守らないこと、およびインサイダー取引を含む不当な行為或いはその他の不当な活動に従事する可能性がある。
私たちは従業員、コンサルタント、そして協力者の詐欺や他の不適切な行為の危険に直面している。これらの当事者の不正行為は、FDAおよび非米国規制機関の規定を故意に遵守しないこと、米国および海外の医療詐欺および法律法規の乱用を遵守しないこと、財務情報やデータを不正確に報告すること、または不正な活動を私たちに開示することを含む可能性がある。特に、医療保健業界の販売、マーケティングと商業手配は広範な法律法規の制約を受けて、不当なマーケティング、詐欺、不当な行為、リベート、賄賂、自己取引、その他の乱用行為を防止することを目的としている。これらの法律法規は、一連の定価、割引、マーケティングおよび販売促進、販売手数料、顧客インセンティブ計画、および他の商業計画を制限または禁止することができます。このような不正行為はまた臨床研究過程で得られた情報を不当に使用する可能性があり、これは規制制裁を招き、著者らの名声に深刻な損害を与える可能性がある。私たちは現在、すべての従業員とサプライヤーに適用される行動基準を持っているが、いつも不当な行為を識別して阻止できるわけではない。さらに、このような活動を発見し、防止するための行動基準および他の予防措置は、未知または未管理のリスクまたは損失を効果的に制御することができないか、またはこれらの法律または法規を遵守できないことによる政府の調査または他の行動または訴訟から私たちを保護することができない可能性がある。もし私たちにこのような調査や行動を開始し、私たちが自分の権利を弁護したり、維持することに成功しなかったら、これらの行動は巨額の罰金や他の制裁を招く可能性があり、これは私たちの業務に大きな影響を与えるかもしれない。我々は現在、HHS OIG概要の有効な計画の要素に適合したコンプライアンス計画を持っており、これは被害削減に役立つかもしれないが、すべての不正行為を防ぐことはできない。私たちがこのような行為や調査を弁護することに成功するかどうかにかかわらず、私たちは法的費用を含む巨額のコストが発生し、不利な宣伝と名声の損害を受け、経営陣の関心をこのような任意のクレームや調査に対して自分の弁護に移す可能性がある。
51
第三者支払者が、個人支払者や政府医療計画を含めて、私たちの臨床診断製品に保険または十分な補償を提供しなければ、私たちの商業成功は負の影響を受けるだろう。
私たちの診断収入は、私たちの診断テストの広範なカバーを実現し、個人と政府支払者を含む支払人から補償を受けることにある程度依存する。一部の大規模な個人支払者が発表した保険証書拒否は、彼らが試験的または調査的と考えるテスト方法をカバーしている。他の支払人は似たような非保険証書を発行する可能性があります。支払者が診断テストの費用の大部分に保険を提供していない場合、あるいは十分な補償を提供していない場合、法律または契約が禁止されていない場合に患者に支払いを求める必要があるかもしれません。これは私たちのテスト需要に悪影響を及ぼす可能性があります。支払人の保証範囲の決定は多くの要素に依存する可能性があり、支払人がある診断テストに対して適切であるか、医学的に必要であるか、または費用効果のある決定を含むが、これらに限定されない。もし私たちが支払人に私たちの診断テストの臨床的実用性と有効性を証明するのに十分な証拠を提供できなければ、それらは保険を提供できないかもしれない、あるいは限られた保険を提供する可能性があり、これは私たちの収入と成功の能力に悪影響を及ぼすだろう。もしもっと多くの競争相手が私たちの市場に入ったら、私たちのテストと新診断製品のカバー範囲と販売率は競争相手からの定価圧力に直面して低下するかもしれません。
各支払側は自分で私たちのテストのカバー範囲と適用された支払率を決定し、支払い側は私たちの現在または未来の製品に十分なカバー範囲や精算を提供できないかもしれません。ある支払人と契約を結ぶ可能性がありますが、返済が時間と高価であることを保証するために、契約または他の方法で支払人と協力して、結果も確定しません。また,支払者がわれわれの臨床診断製品を保証するかどうかを決定することと,そのために精算する金額は通常適応に基づいて行われる。保証政策がない場合、または参加提供者として約束された精算料率がない場合、患者は通常、より大きなシェアの試験費用を負担しなければならず、これは、私たちの収入をさらに遅延させ、収集コストを増加させたり、収集の可能性を低下させたりする可能性がある。私たちの適応支援患者支援計画によって、私たちは、条件を満たす低収入患者に料金引き下げまたは無料clonoSEQ診断テストを提供し、これは、支払者が、そのような患者が減少した自己支払い金額を支払う資格があるかどうかの証拠を提供することを要求する可能性がある。
私たちが支払者に提出した精算要求は提出後に拒否される可能性があり、拒否に対して控訴するなど、追加の手続きをとる必要があるかもしれません。そのような控訴と他の手続きは時間がかかって費用がかかり、支払いにつながらないかもしれない。支払者が資金支払いが間違っていると思っている場合、または私たちのclonoSEQ診断テストまたは他の臨床診断製品を決定することが医学的に不要である場合、支払者は、歴史的に支払われたクレームを監査し、資金が最初に割り当てられた数年後に資金の回収を試みることができる。また,連邦支払者と同様に,州や連邦法は商業支払者が詐欺を感じた場合にメーカーへの民事·刑事罰を求めることを許可している。支払人が私たちのクレームを監査し、否定的な監査結果を発表し、控訴によって監査結果を覆すことができない場合、賠償は私たちの収入に実質的な悪影響を及ぼす可能性があります。また、場合によっては、提供者に参加していない商業支払者は、いつでも審査前に支払うクレームを選択し、支払い金額が多すぎると判断することができる。このような場合、支払人は通常彼らの決定を私たちに知らせて、彼らが多く払っていることを決定した任意の金額を彼らが現在のクレームで私たちに借りている金額を相殺します。これらのトレーサビリティ調整に異議を唱える仕組みはなく,支払者がいつあるいはどのくらいこれらの審査を行う可能性があるか予測することもできない.
未来の医療保険の支払い率は不確定だ。
2020年1月、CMSは分子診断実験室テストサービスの全国カバー範囲(NCD)を改訂し、NGS方法を採用し、その中に著者らの臨床診断製品を含み、末期癌の連邦医療保険受益者に適用した。CMSはNCDを改訂し,生殖系(遺伝)テストの具体的なカバー範囲を拡大した。CMSは、NCDマニュアルの他の技術、明確化、および適合性変更を継続しており、彼らはまた、身体(獲得性)癌診断試験に関連する既存の政策を解明していると述べている。CMSが政策を実質的に修正した場合、これはclonoSEQのカバレッジ範囲に影響を与える可能性がある。
連邦医療保険B部によると,多くの診断実験室テストの支払いは臨床実験室費用明細書(CLFS)に基づいて行われ,この明細書は請求書コードに基づいて支払い金額をテストに割り当てている。2014年の“保護獲得連邦医療保険法案”(PAMA)によると、ある実験室の大部分の連邦医療保険収入は、CLFSまたは連邦医療保険の医師料金表の下の支払いから来ており、これらの実験室は、3年ごとまたは毎年CMSに“高度診断実験室テスト”、商業支払者支払率、および彼らが実施し、特定の課金コードを割り当てたテストの数を報告しなければならない。PAMAには法規で定義された“高度診断実験室テスト”に関する特別な規定があり,これらの規定は起動時の料率設定および料率報告や改訂の周期に影響を与える。報告書に必要な支払い情報がない実験室は巨額の民事罰金を受けるかもしれない。将来clonoSEQまたは私たちの任意のテストに特定のコードが割り当てられた場合、私たちはこれらのテストの商業支払者支払いデータを報告することを要求されるだろう。雑コードによって料金を徴収するテスト費用は相互委員会が決定し、相互委員会もこれらの料率を変更する権利がある。
52
CMSは実験室から報告されたデータを用いて,プライベート支払率の数に基づいて中央値を重み付けし,各CLFSテストの支払率を計算したが,雑項目コードと何らかの他のコードを用いたテストは除外した.これらの費用率は3年に適用されるが、高度診断実験室試験の費用率は1年に適用される。もし私たちが特定のコードを持つテストを提供するなら、この装置は適用されるだろう。この場合、連邦医療保険のレートは、商業支払者から得られたレートによって決定され、これらの実験室のテストは、私たちが使用する特定のコードを共有する他の実験室および他の実験室によって決定される。この場合、商業支払者から十分な収益率を得ることができなければ、私たちの連邦医療保険料率に悪影響を及ぼす可能性がある。
場合によっては、私たちのテストは入院患者に提供され、連邦医療保険によって異なるルールに従って費用が支払われる可能性がある。例えば,当時Medicareに病院入院患者に分類されていた患者からサンプルを取得した場合,Medicareはテストのために単独で費用を支払うことはなく,病院に費用を支払わなければならない。私たちはこのような状況がどのくらい頻繁に起こるか分からないし、病院が私たちのテスト支払いを拒否するかどうかも分からない。この場合、医療保険カバー範囲は、病院の管轄区域のMACによって決定され、これは私たちのテストを含まない可能性がある。
私どもの製品と私どもの協力者と共同開発した製品は将来製品やサービスリコールの影響を受ける可能性があります。自発的であっても、FDAや他の政府機関の指示の下で製品やサービスをリコールしても、または私たちまたは私たちの協力者の製品またはサービスに深刻なセキュリティ問題があることを発見しても、私たちに大きな悪影響を及ぼす可能性があります。
FDAはFDAによって規制されている商業化製品やサービスのリコールを要求する権利がある。どんな欠陥が発見された場合、製造業者は自発的に製品やサービスをリコールすることができる。FDAは、健康リスクを低減するためのリコールを含むいくつかの訂正および削除を要求し、このような訂正または削除が開始されてから10営業日以内にFDAに報告されなければならない。報告可能な訂正および除去については、企業は、リコール開始後にFDAに追加の定期報告を提出し、リコールを開始する前にFDAとそのリコール戦略について常に接触することが求められている。受け入れられない健康リスク、コンポーネント故障、実験室過程中の故障、故障、製造ミス、設計またはラベル欠陥または他の欠陥と問題のため、私たち、私たちのある販売業者、または私たちの協力者は政府の強制または自発的なリコールが発生する可能性がある。私たちの任意の商業化された製品またはサービス、またはパートナーと共同開発した製品またはサービスをリコールすることは、管理および財務資源を移転し、私たちの名声、運営結果、および財務状態に悪影響を与えます。私たちはまた、責任クレームを受けたり、他のコストを負担したり、他の行動を取ることを要求される可能性があります。これらは、私たちの将来の販売と私たちの利益を創出する能力に悪影響を及ぼすかもしれません。会社はまた、これらがFDAに報告する必要がなくても、いくつかの訂正と除去された記録を保持することを要求されている。私たちまたは私たちの協力者は、将来的に私たちの商業化された製品やサービスに関する自発的なリコールを開始するかもしれませんが、これらの製品やサービスはFDA通知を必要としないと思います。もしFDAが私たちの決定に同意しなければ、彼らは私たちにこのような行動をリコールとして報告することを要求するかもしれない。私たちまたは私たちのパートナーが将来リコールを発表することは、お客様の名声を損なう可能性があり、私たちの運営結果や財務状況に悪影響を及ぼす可能性があります。さらに、FDAまたは他の機関は、リコール進行中にリコールイベントが報告されていないので、法執行行動をとることができる。
もし私たちまたは私たちの協力者が私たちのある商業化された製品またはサービスに対してリコール(訂正または除去を含む)を開始し、セキュリティ警報を発表したり、健康リスクを低減するために現場行動またはリコールを取ったりすれば、FDA、他の政府および規制法執行機関、ならびに私たちまたは私たちの協力者の顧客が私たちの製品およびサービスの品質および安全をより厳格に検討し、FDA警報、プレスリリース、または行政または司法行動を含む負の宣伝をもたらす可能性がある。また、これらの報告書を提出することは、競争相手が私たちに反対するために使用される可能性があり、顧客が購入決定を延期したり、注文をキャンセルしたりすることで、私たちの名声を損なう可能性があります。
任意の追加の商業化製品、または規制許可、許可、認証、または許可を得た任意の未来の製品は、引き続き規制審査を受けるであろうが、私たちが規制許可、許可、承認、承認または許可を維持できなかったことは、私たちの名声、業務、および運営結果に悪影響を及ぼす可能性がある。
私たちまたは私たちの協力者が私たちの製品およびサービスに対する司法管轄区域の規制許可、許可、承認、許可または許可を得ても、適用される規制機関は、私たちの製品およびサービスの指定用途やマーケティングに重大な制限を加えたり、私たちまたは私たちの協力者の製造と流通に費用の高い承認後の研究または上場後の監督の継続的な要求を実施する可能性があります。いくつかのデバイスの広告およびすべてのデバイスのタグは、販促タグを含み、FDAの要件に適合しなければならない。さらに、デバイス広告と販売促進はまた他の連邦と州の法律によって制限される可能性がある。例えば、FDAは、FTCとデバイス広告の規制管轄権を共有する。FDAによって制限されたデバイスとして記述された広告は、FDAによって指定された要件によって制限され、制限されていないデバイスの広告は、FTCによって規制される。
もし私たちまたは私たちの協力者が私たちの任意の製品とサービスが許可、許可、承認、認証、または許可を得た後に適用される法規要件を遵守できない場合、規制機関は:
53
政府は違法の疑いのあるいかなる調査にも対応するために多くの時間と資源を必要とする可能性があり、否定的な宣伝が生じる可能性がある。上述した任意の事件または処罰が発生すると、私たちおよび私たちの協力者が承認、許可または承認された任意の製品およびサービスを商業化し、収入を創出する能力を抑制することができる。
私たちの任意の診断製品またはサービスが特定の方法で死亡、重傷または障害を引き起こすか、または促進する場合、私たちは、適用される医療機器報告法規に基づいて、そのような死亡、重傷、または障害を報告することが要求され、そのようなイベントは、自発的な修正行動または機関の法執行行動をもたらす可能性がある。
FDA医療機器報告条例によれば、医療機器製造業者は、装置が死亡または重傷をもたらしたか、または促進した可能性のある情報をFDAに報告しなければならない、または装置または我々の同様の装置に再び故障が発生した場合、死亡または重傷の故障を引き起こす可能性があるか、または促進する可能性がある。このような死亡、深刻な負傷、または故障が発生し、私たちまたは私たちの協力者が、不良事件が私たちまたは私たちの協力者の製品およびサービス以外の要素によって引き起こされたことを証明できない場合、監督管理機関は、私たちまたは私たちの協力者の任意の製品およびサービスのさらなる開発を停止することを命令することができ、または承認、許可、または任意のまたはすべての目標適応の承認を拒否することができる。たとえ私たちと私たちの協力者がいかなる深刻な不良事件が私たちの製品やサービスと関係がないことを証明することができても、このような事件は患者が試験参加者を募集または入選して試験を完了する能力に影響を与える可能性がある。さらに、私たちまたは私たちの協力者が、開発中の製品の任意の臨床試験の延期、一時停止、または終了を要求された場合、開発中の製品の商業的将来性を損なう可能性があり、製品収入を創出する能力を延期またはキャンセルする可能性がある。このような事件は、私たちと私たちの協力者が未来の製品やサービスを識別し、開発する能力を損なう可能性があり、私たちの業務、財務状況、運営結果、将来性を深刻に損なう可能性があります。
54
医療詐欺や乱用法,虚偽申告法,健康情報プライバシー·セキュリティ法など,様々な法律法規の制約を受けており,これらの法律法規を遵守しなければ,我々の業務に悪影響を及ぼす可能性がある。
医療サービス提供者、医師、病院、および第三者支払者は、通常、許可、許可、または承認を得る可能性のある現在発売されている任意の製品およびサービスを推薦および処方する際に主な役割を果たしています。私たちの現在と未来の医療提供者、医師、病院、第三者支払者との手配、ならびに私たちの製品やサービスに関連する販売、マーケティング、教育活動は、広く適用される詐欺と乱用、連邦および州レベルの他の医療保健法律と法規に直面するかもしれません。これらの法律と法規は、私たちの業務や財務計画を制約し、私たちの製品とサービスのマーケティング、販売、流通の関係を制約するかもしれません。さらに、私たちの業務は、様々な連邦や州詐欺や乱用、医師の支払い透明性、プライバシーおよびセキュリティ法律の制約を受けていますが、これらに限定されません
55
56
これらの法律の範囲は広いため、これらの法律の下の例外的な状況と避難港の範囲は狭いため、私たちのいくつかの商業活動は1つ以上のこのような法律の挑戦を受けるかもしれない。これらの法律の範囲も執行も不確定であり,現在の医療改革環境下では,特に適用の前例や法規が乏しい場合には,急速な変化が生じる可能性がある。連邦と州法執行機関は最近、医療会社と医療提供者の間で行われている相互作用の審査を強化し、医療業界のいくつかの調査、起訴、有罪判決、和解を招いた。第三者の業務手配に適合した医療保健法の確保や,政府当局が可能な調査に対応することは,時間や資源がかかる可能性があり,経営陣の我々の業務への注意を分散させる可能性がある。
もし私たちの操作が上記の任意の衛生規制法律または任意の他の私たちに適用される法律に違反していることが発見された場合、私たちは刑事、民事と行政処罰、損害賠償、罰金、返還、個人監禁、政府医療計画から除外される可能性があり、禁止、プライベートを含む罰を受ける可能性がありますりっぱな担い手個人通報者が政府の名義で提起した訴訟、我々の業務の削減または再構成、および追加の報告義務および監督は、これらの法律を遵守しない疑惑を解決するために、会社の誠実な合意または他の合意の制約を受けていれば、いずれも、私たちの業務運営能力および私たちの運営結果に悪影響を及ぼす可能性がある。
私たちは、健康および従業員情報を含む個人情報を収集、使用、開示し、州、連邦、および外国のプライバシーおよびセキュリティ法規の制約を受けており、これらの法規を遵守していない場合、または私たちが持っている情報を十分に保護できない場合、重大な責任や名声の損害を招く可能性がある。
個人情報の記憶、保守、受信または送信のプライバシーおよびセキュリティは、電子情報を含み、米国と海外の主要な問題である。我々は、連邦貿易委員会および州総検察長が実行する“不公平”および“詐欺”を含む、私たち自身が発表したプライバシー政策、プライバシーの法律基準を含むすべての適用されたプライバシーおよびセキュリティ法律法規を遵守しようと努力しているが、これらの法律および法規はまだ発展しており、遵守できなかったり、遵守できなかったと思われるいかなる行為も、政府の実体や他の人が私たちに訴訟を提起したり、行動したり、あるいは私たちの顧客を失ってしまう可能性があり、これは私たちの業務に実質的な悪影響を及ぼす可能性がある。最近,様々な政府機関のデータ収集活動が暴露され,会社へのプライバシーに関する私的訴訟数の増加(“CCPA”や他の類似した州法による私的訴訟権を含め,以下に述べる)により,プライバシー問題に対する国民の認識が高まっている.個人情報またはその他のプライバシーに関連する事項の収集、使用、保留、開示またはセキュリティに関する我々のやり方への懸念は、根拠がなくても、適用される法律を遵守していても、私たちの名声や業務を損なう可能性がある。また、第三者からPHIを含む個人情報を受け取り、これらの第三者が適用されるプライバシーやセキュリティ法律の遵守に関する声明に違反した場合、政府機関や他の人の訴訟や行動に直面する可能性があります。
多くの外国、連邦、州の法律と法規は、州プライバシー、データ安全と違反通知法、連邦と州消費者保護と雇用法、HIPAA、GINA、GDPR、その他の外国データ保護法を含む、遺伝、生物識別と健康情報を含む個人情報の収集、伝播、使用と秘密を管理する。これらの法律法規は複雑さや数量的に増加しており,頻繁に変化する可能性があり,時には衝突することもある.
57
HIPAAプライバシー、安全と違反通知法規はHITECH下の拡張要求を含み、PHIの機密性、完全性と安全性を保護する標準を設定するほか、医療計画、医療保健提供者(実験室を含む)と医療保健情報交換所の使用とPHIの開示について全面的な連邦標準を確立した。“条例”は様々なテーマについて複雑な規制枠組みを構築した
このような法律違反に対する処罰はそれぞれ違う。例えば、HIPAAとHITECHの要求を守らない処罰の差は大きく、HIPAAの規定に違反するたびに大量の民事罰金を含め、最高法定上限に達し、場合によっては違反行為ごとに罰金と可能な監禁の重大な刑事罰が科される場合がある。一度の違反は、複数の規定に違反することが発見され、例年の任意の適用される違反の上限を超える可能性のある処罰を招く可能性がある。誰でも故意にHIPAA違反の公衆衛生情報を取得または開示することは、重大な刑事罰と最高1年の監禁に直面する可能性がある。不法行為が虚偽の言い訳または意図が商業利益、個人利益または悪意のある傷害売却、譲渡または識別可能な健康情報の使用に関連する場合、刑事罰は増加する。また、これらや他の法律法規違反の疑いのある政府調査や関連第三者個人訴権に応答して、最終的に違反が発見されなかったり、罰が加えられなかったりしても、私たちの資源を消費し、私たちの業務に影響を与え、公開されていれば、私たちの名声を損なうことになる。
コンピュータネットワークは侵入されやすいが,不正な人は将来コンピュータネットワークセキュリティシステムの弱点を利用して公共セキュリティ施設に入る可能性がある.また、私たちは第三者請負者と潜在的危険情報を共有し、ビジネスパートナー協定によると、潜在的危険情報の保護と維持が契約義務を持っているが、彼らの私たちへの賠償は私たちを名声被害から守ることはできない。不正者は、これらの第三者請負業者のコンピュータネットワークに格納されたPHIにアクセスすることができる可能性がある。データが盗まれたか、または当社または第三者請負業者のコンピュータネットワークへの不正アクセスによる開示を含む、私たちまたは私たちの第三者請負者のPHIの任意の不適切な使用または開示は、私たちの業務および運営結果に悪影響を及ぼす可能性がある罰金または処罰に直面する可能性があります。HIPAAおよびその公布された条例に基づいて個人訴訟権利が規定されていないにもかかわらず、州法により、機密健康情報または他の個人個人情報の不適切な使用または開示によって個人当事者に損害を与える可能性がある。
また,カリフォルニア,ニューヨーク州,マサチューセッツ州など多くの州でも同様のプライバシー法律や法規(“カリフォルニア医療情報秘密法”,“カリフォルニア消費者プライバシー法”,“カリフォルニアプライバシー権法案”)が実施されており,個人情報の使用や開示に制限的な要求が加えられており,他の州では同様の条項の採用が検討されている.これらの法律法規は必ずしもHIPAAに先を越されるとは限らないが,HIPAAよりも範囲が広く,個人の保護も大きい。州の法律がもっと保護されているところで、私たちと私たちの協力者たちは彼らが適用されるもっと厳しい条項を守らなければならない。違反者に罰金と罰を加えるほか、いくつかの州法は、自分の個人情報が乱用されたと思う個人に個人訴訟権利を提供している。連邦と州法律の相互作用は裁判所と政府機関の異なる解釈を受ける可能性があり、私たちと私たちの顧客に複雑なコンプライアンス問題をもたらし、私たちを追加的な費用、不利な宣伝、責任に直面させるかもしれない。また、規制機関のプライバシー、安全とデータ使用問題への関心が増加し、個人情報の保護に関する法律法規の拡大とより複雑になるにつれ、私たちの免疫薬物プラットフォームと関連製品とサービスが直面するこれらの潜在的なリスクは激化する可能性がある。PHIのような特定のタイプの敏感なデータの保護の強化に関連する法律や法規の変化に加え、強化されたデータセキュリティインフラに対する顧客の需要の増加に加えて、私たちの製品やサービスを提供するコストを大幅に増加させ、私たちの製品やサービスに対する需要を減少させ、私たちの収入を減少させ、追加の責任を負わせる可能性がある。
私たちは現在、米国以外のいくつかの国で業務を展開しており、最終的には他の国で業務を展開する可能性があり、これらの国の法律は、場合によっては米国の要求よりも厳しい可能性がある。例えば、EUは、米国を含む特定の司法管轄区域への個人データの越境移転に具体的な要求を持っている。また、一部の国では、個人データの収集、使用、または共有のために、より厳しい消費者通知または同意要求を有し、組織のプライバシー計画に対してより厳しい要求があり、より強い個人権利を提供する。
58
また、国際プライバシーとデータセキュリティ法規はより複雑になっており、より厳しい処罰を招く可能性がある。たとえば,GDPRはEUや欧州経済圏データ主体の個人データの収集と使用を管理する.GDPRは、場合によっては域外に適用され、個人データの制御者および処理者に厳しい要求を加え、例えば、個人データを処理するための個人同意または他の法的根拠を得ること、個人に信頼できる開示を提供すること、個人データのセットを格納すること、データセキュリティ規定の違反を意識した後にデータセキュリティ違反通知を提供すること、個人情報の保持を制限すること、および健康データおよび他の特殊なカテゴリの個人データの強化保護を実施することを要求する。GDPRは、“付加的な情報を使用することなく、特定のデータ主体にデータを帰属しないように個人データを処理する”と定義され、第三者プロセッサと任意の個人データの処理に関する契約を締結する際に追加的な義務を課す仮名データにも適用される。GDPRは、EU加盟国は、遺伝子、生体認証、または健康データを含む個人データの処理を制限する独自のさらなる法律法規を制定することができ、これは、個人データの使用および共有能力を制限する可能性があり、コスト増加を招き、財務状況を損なう可能性がある。GDPRの要求やEU加盟国に適用される国家データ保護法を遵守しないことは、巨額の罰金や前会計年度の世界年商の一定の割合(高い者を基準とする)、その他の行政処罰を招く可能性がある。GDPRを遵守するためには、法律とその更新された要求に応じて追加の政策、プログラム、ファイルを作成して維持する必要があり、他の多くの支出を招く可能性があります。これは深刻かもしれないし、私たちの業務に悪影響を及ぼすかもしれない。GDPRや他の国/地域のプライバシーやデータセキュリティに関する法律、規則、または法規を遵守しないことは、規制機関に重大な処罰を加える可能性があり、私たちの協力者や他の第三者支払者との契約を遵守し、私たちの業務や財務状況に悪影響を及ぼす可能性があります。
GDPRはまた、個人データをEUから米国に移すための厳しいルールを実施している。これらの義務の解釈や適用は、異なる司法管轄区域間で一致しない可能性があり、他の要求や私たちのやり方と衝突する可能性がある。
GDPRに加えて、データプライバシー法が制定されているいくつかの国にも私たちの業務を拡張し続けています。このような法律を遵守することは重くて、私たちの業務の拡張に悪影響を及ぼすかもしれない。
これらのデータ保護法の広さ、およびそれらの例外および安全港の狭さのために、私たちの業務またはデータ保護政策は、1つまたは複数のそのような法律の挑戦を受ける可能性がある。これらの法律の範囲も実行も不確定であり,現在データプライバシーやセキュリティ問題に高度に注目されている規制環境では,これらの法律の範囲や執行状況は急速に変化する.もし私たちの操作が上記の任意のデータ保護法または私たちに適用される他の法律に違反していることが発見された場合、私たちは刑事、民事と行政処罰、損害賠償、罰金、返還、個人監禁、政府医療計画から除外される可能性があり、禁止、個人的な禁止を含む罰を受ける可能性がありますりっぱな担い手個人通報者が政府の名義で提起した訴訟、集団訴訟、および私たちの業務を削減または再構成し、これらの法律を遵守しない疑惑を解決するために、修正行動計画または他の合意の制約を受けた場合、追加の報告義務および監督を負う必要があり、これらはいずれも、私たちの業務運営能力および運営結果に悪影響を及ぼす可能性がある。
また、米国内では、ますます多くの州や連邦政府が新たなデータプライバシー法の採用を検討または提案している。これらすべての法案が法律になっているわけではないが、我々が業務を展開する際に直面する可能性のある追加義務や潜在的処罰に関する重大な不確実性を増加させている。これらの不確実性は,機械学習や人工知能やデータ使用に影響を与える法律のようなプライバシーに隣接する法律の平行な変化と混同され,これらの法律を遵守することにより大量の費用や中断を招く可能性があり,業務を展開する能力に悪影響を与えるであろう.
59
セキュリティおよびネットワークセキュリティホール、データ損失、および他の中断は、私たちの業務に関連する機密、個人、および敏感な情報を危険にさらしたり、重要な情報へのアクセスを阻止し、私たちに責任を負わせたりする可能性があり、これは私たちの業務や名声に悪影響を及ぼす可能性があります。
私たちの通常の業務過程で、私たちと私たちの協力者は、私たちまたは私たちの顧客、第三者支払者、私たちの協力者、政府エンティティ、保険会社、および他の当事者が所有または制御するPHI、個人情報、財務情報、知的財産権、および独自の業務情報を含む敏感なデータを収集して保存します。私たちは、オンサイトシステムとクラウドベースのデータセンターを組み合わせることで、私たちのアプリケーションとデータを管理し、維持します。私たちは外部セキュリティとインフラ供給者を利用して私たちのデータセンターのコンポーネントを管理します。著者らはまた、複数の第三者サプライヤーとその下請け業者との手配に基づいて、私たちのウェブサイトを介して患者データを含む敏感なデータを電話で送信した。これらのアプリケーションおよびデータは、研究開発情報、患者データ、ビジネス情報、および財務情報を含む様々な重要なビジネス情報を含む。私たちは、アクセス損失のリスク、許可されていないアクセス、使用、開示、または修正、および私たちが重要な情報の制御を十分に監視、監査、修正できないことを含む、これらの重要な情報の保護に関連する多くのリスクに直面している。このリスクは、第三者サプライヤーおよび下請け業者に委託されたデータまで延長され、これらのサプライヤーおよび下請け業者は、これらの敏感なデータを管理してくれたり、他の方法で私たちに代わってこれらのデータを処理してくれたりする。
これらの重要な情報のセキュリティ処理、保存、維持、転送は、私たちの運営および業務戦略に重要であり、私たちはこれらの情報を保護するために多くの資源を投入しています。私たちは、不正なアクセス、使用、または漏洩から敏感かつ独自のデータを保護する合理的な措置を取っているにもかかわらず、いかなるセキュリティ措置も完璧である可能性はなく、私たちそれぞれの情報技術およびインフラは、ハッカーやウイルスの攻撃を受けやすいか、または従業員のミス、汚職、または他の悪意または意図しない中断によって破壊される可能性がある。このような侵入または中断のいずれも、私たちのネットワークを危険にさらす可能性があり、そこに格納された情報は、不正な当事者によってアクセスされ、開示され、紛失され、または盗まれる可能性がある。任意のこのような情報のアクセス、漏洩、または他の損失は、法的クレームまたは訴訟、HIPAAまたはHITECHのような個人情報のプライバシーを保護する連邦または州法律の責任、および規制処罰をもたらす可能性がある。影響を受けた個人、HHS長官、または他の連邦、州および外国の規制機関、メディア、または州総検察長に違反通知を提供する必要があるかもしれない。そのような通知は私たちの名声と競争能力を損なうかもしれない。様々なタイプのネットワークセキュリティ脅威から私たちを保護する政策およびプログラムを含む、不正な患者および他の個人データへの不正アクセスを防止するためのセキュリティ対策および正式で専用の企業セキュリティ計画が実施されているが、このようなデータは現在、様々なチャネルでアクセス可能であり、1つまたは複数のデータまたはネットワークセキュリティホールに遭遇する可能性がある。不正アクセス、紛失、または伝播は、私たちの運営を混乱させ、私たちの名声を損なう可能性もあり、これは私たちの運営結果や財務状況に悪影響を及ぼす可能性がある。
また,政府付属組織(例えば州立大学)と業務を行う条件として,クラウドベースのサービス提供のネットワークセキュリティ要求を考慮または採用している州が増えており,これらの要求を遵守する必要があるかもしれない.これらの法律を実施するために要求される制御措置は重くなる可能性があり、これらの州の政府付属組織にサービスを提供する能力に影響を与え、私たちの業務結果に悪影響を及ぼす可能性がある。
この新しい潜在的薬物カテゴリーでは,TCRによる細胞療法は承認されておらず,他者やわれわれの努力によって承認されることは決してないかもしれない。TCRに基づく細胞治療薬物の発見は重大な臨床開発と監督管理リスクがあり、このような新しい免疫薬物はかつてない新規性があるためである。
潜在的な新しい薬物カテゴリーとして,これまでTCRによる細胞療法はFDAや他の規制機関の承認を得ていない。われわれとわれわれの協力者はTCRによる細胞療法の発見と開発に成功しており,高度に不確実であり,多くの要因に依存しており,その多くの要因はわれわれと彼らでは制御できない。私たちと私たちの協力者は、TCRベースの細胞療法、伝達技術、および製造プロセスに関連する製品を含む、私たちの開発努力と免疫駆動治療候補製品のパイプラインを推進するために、一連の商業的決定を行い、計算されたリスクを負担し続け、これらは正しくないことが証明される可能性がある。我々の細胞療法候補製品は開発の初期段階で有望に見えるが、様々な原因で進められない可能性があり、臨床遅延、臨床失敗或いは発売できない可能性がある
60
61
私たちの知的財産権に関するリスクは
私たちは私たちの製品、サービス、技術およびその使用のために十分な知的財産権保護を獲得または維持することに成功できないかもしれませんし、得られた知的財産権保護の範囲は十分に広くないかもしれません。
生命科学業界に従事している他の会社と同様に、私たちの成功は、私たちの製品、サービス、および技術を獲得し、私たちが単独でまたは他人と共同で所有する可能性のある知的財産権の保護を維持する能力があるかどうか、または米国および他の国/地域の第三者から許可、特に特許を得る能力があるかどうかに大きく依存する。商標、著作権、商業秘密、および他の知的財産権保護および契約制限に加えて、私たちは特許保護に依存して、私たちの独自技術を保護するために依存しており、これらすべては限られた保護を提供し、私たちの権利を十分に保護することができないかもしれないし、いかなる競争優位性を得ることができるか、または維持することができる。もし私たちが私たちの知的財産権を保護できなければ、第三者は私たちともっと効果的に競争するかもしれない。また、私たちは私たちの知的財産権の使用を取り戻したり制限しようとした場合、巨額の訴訟費用を招く可能性がある。
もし私たちの知的財産権提供の保護が不足していたり、無効であることが発見されたり、実行できない場合、私たちはより大きな直接競争のリスクに直面するだろう。もし私たちの知的財産権が十分な競争障壁を提供できなければ、私たちの競争地位は不利な影響を受ける可能性があり、私たちの業務も影響を受ける可能性がある。
私たちは私たちが適切だと思う場合、私たちの製品と技術とその使用をカバーするライセンス内特許を申請して所有します。しかしながら、特許の取得と実行は高価で、時間がかかり、複雑であり、重要な製品、サービス、および技術の特許をタイムリーにまたは全く申請できない可能性があり、または潜在的な関連司法管轄区で特許を申請することができない可能性がある。私たちは、必要または望ましいすべての特許出願、またはそのような特許出願から発行される可能性のある任意の特許を合理的なコストで、またはタイムリーに提出して起訴することができないかもしれない。我々は,特許保護を得るのが遅くなるまで,我々の研究開発成果で特許を申請できることを確認できない可能性もある.私たちは特許出願の準備、提出、起訴を制御する権利がなく、第三者から許可された特許の権利を維持する権利もないかもしれない。したがって、このような特許と出願は、私たちの業務の最適な利益に合った方法で起訴され、強制的に実行されないかもしれない。
2023年12月31日現在、私たちは、米国、ヨーロッパ、および他の場所で出願された450件以上の有効特許および特許出願の権利を有しているか、または所有している。これらの出願のうち、55件以上が特許を出願している。私たちが処理している特許出願はタイムリーではないかもしれないし、特許を発行することができないかもしれない。特許が付与されても、それらは商業的に実行可能な製品やサービスに知的財産権保護の基礎を提供しない可能性があり、いかなる競争優位性を提供してくれないかもしれないし、第三者の挑戦や無効を受ける可能性がある。他の人たちが私たちの現在または未来の特許技術を中心に設計する可能性もある。
私たちのいくつかの特許、特許特許、または特許出願は将来的に挑戦されるかもしれないが、私たちはこのような挑戦に成功できないかもしれない。例えば、私たちは、第3の方向の米国特許商標局(“USPTO”)によって提出された既存技術の発行前に提出されるか、または反対、派生、再審査、当事者間の審査、付与後の審査、または私たちの特許権の介入手続きに参加する可能性がある。私たちの特許に対する第三者の成功的な挑戦は、特許請求範囲の縮小、または特許の全部または一部の無効または実行不能を招く可能性があり、これは、私たちの業務をより激しい競争に直面させる可能性があります。代わりに、私たちは第三者の特許や特許出願に挑戦しなければならないかもしれない。特許訴訟または他の訴訟の結果は不確定である可能性があり、私たちが他人に特許権を強制したり、他人の特許権に挑戦するいかなる試みも成功しない可能性があり、または成功すれば、多くの時間と大量のコストがかかる可能性があり、業務の他の側面に対する私たちの努力と注意を分散させる可能性がある。さらに、私たちの特許および特許出願によって提供される保護の広さまたは強度が脅かされている場合、結果にかかわらず、会社が現在または将来の製品またはサービスを許可、開発、または商業化することを阻止することができる。生物技術会社の特許地位は非常に不確定である可能性があり、複雑な法律と事実問題に関連し、その重要な法律原則はまだ解決されていない。これまで,米国又は他の場所では,特許保護を取得する資格と,このような会社特許において特許を出願可能な範囲に関する政策とは一致しなかった。裁判所は、診断方法および生体分子の特許性に影響を及ぼす可能性のある意見を含む、いくつかの発明または発見に影響を及ぼす可能性のある特許性の意見をバイオテクノロジーの分野でしばしば提示する。
62
臨床診断試験(例えば、我々のclono配列番号診断試験)およびTCRなどの生体材料の開発および商業化に従事する会社の特許地位は特に不確定である。米国最高裁判所を含む複数の裁判所が下した裁決は、ある診断テスト、自然に産生された分子と関連技術に関連するいくつかの発明或いは発見の資格と特許可能範囲に影響を与える。これらの裁決規定は、他の事項に加えて、抽象概念、自然現象、または自然法則(例えば、特定の免疫受容体と癌との間の関係)を記述する特許請求項が特許に適用されない可能性がある。一体何が自然規則を構成しているのかは不確定であり、著者らの臨床診断のある方面は自然規則と思われるかもしれない。米国で進化し続ける判例法は、私たちが特許を取得したり、私たちが取得または許可された特許を守る能力に悪影響を及ぼす可能性があり、第三者が任意の所有または許可された特許に挑戦することに便利になる可能性がある。一部の国の法律の知的財産権の保護程度やテーマはアメリカの法律とは異なり、私たちは外国の管轄区域でこのような権利を保護し、守ることは困難に直面する可能性がある。多くの他の国の法制度は、特許や他の知的財産権保護、特にバイオテクノロジーに関する保護の強制執行を支持しておらず、これらの国で私たちの特許を侵害することを阻止することを困難にする可能性がある。外国の管轄区域で私たちの特許権を強制執行する訴訟は巨額のコストを招く可能性があり、私たちの努力と注意を私たちの業務の他の側面から移すことができます。
私たちは世界各地で私たちの知的財産権を保護できないかもしれない。
世界のすべての国で私たちの製品とサービス申請、起訴、そして特許保護に対する費用は目を引くほど高いだろう。また、一部の国の法律は知的財産権の保護の程度が米国の法律よりも悪く、私たちは外国の管轄区域でこのような権利を保護し、守ることは困難に直面する可能性がある。したがって、私たちは、米国以外のすべての国/地域で第三者が私たちの発明を実施したり、米国または他の管轄区域で私たちの発明を使用して製造された製品を販売または輸入することを阻止することができないかもしれない。競争相手は私たちが特許保護を受けていない司法管轄区域で私たちの技術を使用して彼ら自身の製品を開発することができ、私たちの特許保護を持っている地域に侵害製品を輸出することもできますが、法執行力はアメリカほど強くありません。これらの製品は私たちの製品と競争する可能性があり、私たちの特許や他の知的財産権は彼らの競争を効果的にまたは阻止することができないかもしれません。
多くの会社は外国の管轄区域の知的財産権の保護と保護に重大な問題に直面している。多くの他の国の法制度は、特許や他の知的財産権保護、特にバイオテクノロジーに関する保護の強制執行を支持しておらず、これらの国で私たちの特許を侵害することを阻止することを困難にする可能性がある。外国の管轄区域で私たちの特許権を強制的に執行する訴訟手続きは、巨額のコストを招き、私たちの努力と注意を私たちの業務の他の側面から移転させる可能性があり、私たちの特許が無効または狭義に解釈されるリスクに直面する可能性があり、私たちの特許出願を発表できないリスクに直面させ、第三者からのクレームを引き起こす可能性がある。私たちは私たちが起こしたどんな訴訟でも勝てないかもしれないし、判決された損害賠償や他の救済措置(もしあれば)は商業的な意味がないかもしれない。したがって、私たちが世界各地で私たちの知的財産権を実行する努力は、私たちが開発または許可した知的財産権から顕著なビジネスメリットを得るのに十分ではないかもしれません。
米国や他の管轄地域の特許法の変化は、特許の全体的な価値を低下させ、製品やサービスを保護する能力を弱める可能性がある。
米国または他の国または地域特許法または特許法解釈の変化は、私たちの知的財産権の価値を低下させる可能性がある。私たちは、私たちの特許または第三者特許で許容または実行される可能性のある特許請求の範囲の広さを予測することができない。さらに、私たちに特許出願を提出した第三者は、その第三者が発明をする前に発明をしたとしても、私たちの発明をカバーする特許を付与することができる。これは私たちが発明から特許出願までの提出時間を認識することを要求するだろう。米国およびほとんどの他の国/地域の特許出願は、提出後または発行前の一定期間秘密であるため、私たちまたは私たちのライセンス者が、私たちの製品またはサービスに関連する特許出願または発明私たちまたは私たちのライセンシーの特許または特許出願で主張されている任意の発明を最初に提出した会社であることを確認することはできません。
第三者はまた、特許訴訟中に特許の有効性を攻撃するために米国特許商標局に既存技術を提出することができ、米国および他の国では、第三者は、米国、ライセンス後審査、当事者間の審査、および派生手続など、特許庁のプログラムを介して付与された特許に疑問を提起することもできる。米国では,USPTO訴訟で実施されている証拠基準は,米国連邦裁判所が特許請求の無効を宣言するために必要な証拠基準に比べて低い。したがって,第三者はUSPTO手続きにおいてUSPTOがクレームを無効にするのに十分な証拠を提供する可能性があり,同じ証拠が最初に地域裁判所訴訟で提出されればクレームを無効にするには不十分である。したがって,第三者は米国特許商標局の手続きを用いて我々の特許主張の無効を宣言しようとする可能性があり,第三者が地域裁判所訴訟で最初に被告として疑問を提起すれば,我々の特許主張は無効ではない.私たちの所有または許可された特許出願を起訴し、私たちが所有または許可した発表された特許を実行または保護することをめぐる不確実性とコストは、私たちの業務に重大な悪影響を及ぼす可能性がある。
63
米国最高裁判所の最近の判決はまた、場合によっては入手可能な特許保護範囲を縮小し、場合によっては自然に産生された生体分子、例えば免疫細胞受容体を含む特許所有者の権利を弱めることが、私たちの免疫薬物プラットフォームの重点である。我々の将来の特許取得能力に関する不確実性の増加に加えて,このようなイベントの結合は,いったん特許を取得する価値に関する不確実性をもたらしている.米国議会、連邦裁判所、および米国特許商標局の決定によると、特許を管理する法律および法規は予測不可能な方法で変化する可能性があり、それにより、私たちが新しい特許を獲得したり、私たちの既存の特許と将来獲得可能な特許を強制的に執行する能力を弱める可能性がある。
もし挑戦された場合、私たちの製品とサービスに関する発行された特許は無効または強制的に実行できないことが発見される可能性がある。
特許の発行は、その発明性、範囲、有効性、または実行可能性に対して決定的ではなく、私たちのいくつかの特許または特許出願は、ライセンス特許を含み、米国および海外の裁判所または特許庁で異議、派生、再審、当事者間の審査、許可後の審査または介入を受ける可能性がある。さらに、私たちと私たちの許可パートナーが、私たちの製品または技術のうちの1つをカバーする特許を強制的に実行するために、第三者のための法的手続きを開始または巻き込まれた場合、被告は、私たちの製品をカバーする特許が無効または強制的に実行できないことを反訴することができる。米国の特許訴訟では、無効または実行不可能と主張する反訴はありふれている。有効性疑問の理由は、特許資格に適合する主題、新規性の欠如、明らかまたは実施できないことを含む、いくつかの法定要件のいずれかを満たすことができなかったと言われている可能性がある。主張を実行できない理由は,特許起訴に関連する者が起訴中に米国特許商標局に関連情報を隠蔽したり,誤った声明をしたりしたためかもしれない.さらに、米国は現在、特許出願を提出する第1の当事者に特許優先権を付与しており、他の人は、私たちの以前の発明をカバーする特許主張を私たちに提出するかもしれない。法的に無効と実行不可能と断言された後の結果は予測できない。例えば、有効性の問題については、私たちは無効な以前の技術がないとは確信できないが、私たちと特許審査員は起訴中にこれを知らない。第三者の私たちの特許への成功的な挑戦は、このような特許が強制的に実行されないか、無効になる可能性があり、これは私たちの業務に実質的な悪影響を及ぼす可能性があります。さらに、私たちの特許および特許出願によって提供される保護の広さまたは強度が脅かされている場合、結果にかかわらず、会社が現在または将来の製品およびサービスを許可、開発、または商業化することを阻止することができる。
私たちは私たちの免疫薬物プラットフォーム、製品、サービスに関連する可能性のあるすべての第三者知的財産権を知らないかもしれない。科学文献で発見された発表は、実際の発見に遅れがちであり、米国および他の司法管轄区の特許出願は、通常、出願後約18ヶ月後に発行され、場合によっては、特許出願が発行されるまで発表されない。私たちは、私たちのすべての未解決特許出願をカバーする最初の発明ではなく、これらの発明のために初めて特許出願を提出した会社でもないかもしれない。これらの発明の優先度を決定するために、私たちは、干渉プログラム、派生プログラム、または米国特許商標局が発表した他の許可された後のプログラムに参加しなければならないかもしれない。このような訴訟の結果は不確定であり、他の特許出願は私たちの特許出願よりも優先される可能性がある。このような訴訟手続きはまた私たちの巨額の費用を招き、私たちの経営陣の関心と資源を移す可能性がある。
私たちは特定のシークエンシング技術に関連する第三者ライセンスに依存しています。もし私たちがこれらのライセンスを失ったら、私たちは未来の訴訟を受けるかもしれません。
私たちは、特許および特許出願を含む特定の知的財産権を使用する権利を付与するライセンス契約の当事者であり、通常、特定の特定の使用分野で使用される。その中のいくつかの許可された権利は私たちの製品とサービスの様々な側面に対する運営自由を提供することができる。私たちは他の会社から追加のライセンスを取得して、私たちの研究、開発、商業化活動を推進する必要があるかもしれない。
私たちの成功は、私たちが許可した知的財産権の特許保護を取得、維持、実行する能力にある程度依存する可能性がある。私たちの許可者たちは私たちが許可した特許出願を起訴することに成功できないかもしれない。これらの特許出願について特許を発行しても,我々の許可者はこれらの特許を維持できない可能性があり,これらの特許を侵害する他の会社に対して訴訟を提起しないか,あるいは我々のように積極的に訴訟を提起しないことに決定する可能性がある.私たちが許可した知的財産権の保護がなければ、他社は販売のために実質的に同じ製品を提供する可能性があり、これは私たちの競争業務の地位に悪影響を与え、私たちの業務の将来性を損なう可能性があります。
上記のいずれも、我々の競争地位、業務、財務状況、経営結果、および見通しに重大な悪影響を及ぼす可能性がある。
また、ライセンス契約によると、私たちとライセンシーとの間に知的財産権紛争が発生する可能性があります
64
もし私たちがこのような紛争に勝利しなければ、私たちはその許可協定の下で私たちの任意またはすべての権利を失うかもしれない。
また,我々が現在第三者から知的財産権や技術許可を得ているプロトコルは複雑であり,このようなプロトコルのいくつかは様々な解釈の影響を受ける可能性がある.
もし私たちが私たちの商業秘密の機密性を保護できなければ、私たちの商業と競争の地位は損なわれるだろう。
特許保護に加えて、私たちは、当社の知的財産権およびノウハウを保護し、当社の従業員、コンサルタント、協力者、学術機関、生命科学研究パートナー、および必要に応じて、守秘協定、秘密協定、および知的財産権譲渡協定を含む当社のコンサルタントおよび他の第三者と協定を締結する措置を取っています。しかし、私たちはすべての関係者とこのような合意を締結したことを確認することはできず、私たちの商業秘密や他の機密固有情報が開示されないか、あるいは競争相手が私たちの商業秘密を取得したり、実質的に同等の情報や技術を独立して開発しないかを決定することもできない。
例えば、いずれの当事者も合意に違反し、私たちのビジネス秘密を含む私たちの固有の情報を漏洩する可能性があり、私たちはこのような違反について十分な救済措置を得ることができないかもしれない。許可されていない使用または開示または他の合意違反の場合、そのようなプロトコルは、私たちの商業秘密または他の固有情報を強制的に実行することができないか、または意味のある保護を提供できない可能性があり、私たちは、そのような許可されていない開示を阻止することができないかもしれない。もし私たちがそのような側に私たちの権利を主張することを要求されたら、巨大な費用と気晴らしを招くかもしれない。許可されていない開示を規制することは困難であり、私たちはまた私たちがこのような開示を防止するための手順が十分であるかどうか、または十分かどうかを知らない。もし私たちが第三者が私たちの商業秘密を不正に取得して使用した疑いを強制するなら、これは高価で時間がかかるだろうし、結果は予測できないだろう。しかも、アメリカ以外の裁判所は商業秘密を保護することをあまり望んでいないかもしれない。
私たちはまた、私たちの場所の実体セキュリティと私たちの情報技術システムのエンティティと電子セキュリティを維持することによって、私たちの機密固有情報の完全性とセキュリティを維持しようとしています。これらのセキュリティ措置が違反される可能性があることに加えて、これらの措置は、従業員またはアクセス許可権限を有する第三者が商業秘密を盗用する場合など、私たちの独自の情報に十分な保護を提供しない可能性がある。私たちの安全対策は、従業員やコンサルタントが私たちのビジネス秘密を盗用して競争相手に提供することを阻止できない可能性もあり、私たちがこのような不正行為に対する追跡権は、私たちの利益を十分に保護するための十分な救済措置を提供できないかもしれません。強制執行側が商業秘密を不正に開示したり流用したりする主張は困難であり、高価で時間がかかる可能性があり、結果は予測できない。また,ビジネス秘密は,我々の法的追跡を阻止するように他の人によって独立して開発されている可能性がある.もし私たちのビジネス秘密のような私たちの任意の機密または独自の情報が漏洩または流用された場合、またはそのような情報が競争相手によって独立して開発された場合、私たちの競争地位は損なわれる可能性がある。
一部の元従業員は会社や学術機関の仕事を獲得しており、これらの会社や学術機関は私たちと競争していると考えられるかもしれない。この競争は契約条項によって制限される可能性があり、これらの条項はいくつかの司法管轄区域で私たちによって強制的に執行される可能性があり、私たちによって強制的に執行されない可能性もあります。さらに、私たちのビジネス秘密が潜在的な競争力のある会社に開示された後、このような競争的な雇用配置を意識するかもしれない。
私たちは、私たちの従業員、コンサルタント、または独立請負業者が第三者の機密情報を誤って使用または開示したか、または私たちの従業員がその前の雇用主によって言われた商業秘密を誤って使用または開示したという疑惑の影響を受けるかもしれない。
私たちは雇用し、将来的には私たちの競争相手や潜在的な競争相手を含む、以前大学や他の会社に雇われていた個人を雇用する予定だ。私たちは、私たちの従業員、コンサルタント、および独立請負業者が、私たちのために働いているときに他人の独自の情報または技術的ノウハウを使用しないことを確実にするために努力しているが、私たちは、私たちの従業員、コンサルタント、または独立請負業者が無意識に、または他の方法で彼らの元の雇用主または他の第三者の商業秘密または他の固有情報を使用または漏洩した、またはそのような商業秘密を不適切に使用または取得したと告発される可能性がある。このような疑いに対抗するために訴訟を提起する必要があるかもしれない。もし私たちがこのようなクレームを弁護できなければ、金銭損害賠償の支払いに加えて、貴重な知的財産権や人員を失う可能性があり、これは私たちの業務に悪影響を及ぼす可能性がある。重要な研究者の作業製品の損失は、潜在的な製品やサービスを商業化する能力を阻害または阻止する可能性があり、これは私たちの業務を損なう可能性がある。これらのクレームを弁護することに成功しても、訴訟は巨額のコストを招き、経営陣や他の従業員の注意を分散させる可能性がある。
65
私たちは私たちの商標を保護して実行できないかもしれない。
私たちはすべての潜在市場に私たちのいくつかの商標を登録していません。私たちはすでにアメリカ、EU、および他のいくつかの国/地域にAdaptive BioTechnologies、私たちの会社識別、clonoSEQ、pairSEQ、および他の商標を登録していますが、私たちの新しい会社識別およびいくつかのスローガンを含めて、より多くの商標の登録を求めています。私たちが米国や他の国で私たちの未登録商標の登録を申請した場合、私たちの出願はタイムリーまたは根本的に登録が許可されない可能性があり、私たちの登録商標は維持されたり強制的に施行されないかもしれません。さらに、私たちの商標出願および登録に反対または撤回訴訟を提起する可能性があり、私たちの商標は継続できないかもしれない。米国以外のある国では,商標権の強制執行には登録商標が必要である。もし私たちが私たちの商標のために登録されていなければ、私たちは第三者に対してこれらの登録を実行する時に他の場合よりも大きな困難に直面するかもしれない。
私たちは私たちの特許と他の知的財産権の発明権または所有権のクレームに疑問を受けるかもしれない。
私たちまたは私たちの許可者は、元従業員、協力者または他の第三者が、発明者または共同発明者として、私たちの所有または許可内の特許、商業秘密、または他の知的財産権において権益を有するというクレームを受ける可能性がある。例えば、所有権紛争は、私たちの将来の製品およびサービスの開発に参加する従業員、コンサルタント、または他の人の義務紛争に起因する可能性がある。
第三者が私たちまたは私たちの許可内の特許、商業秘密、または他の知的財産権の所有権に疑問を提起したこれらおよび他のクレームに対抗するために、私たちまたは私たちの許可内の特許、商業秘密または他の知的財産権の所有権に疑問を提起するために訴訟を提起する必要があるかもしれない。もし私たちまたは私たちのライセンシーがこのようなクレームを弁護できなかった場合、金銭損害賠償を支払うことに加えて、私たちの製品やサービスに重要な知的財産権の独占所有権や使用権のような貴重な知的財産権を失う可能性があります。代替的に、第三者から1つまたは複数の追加のライセンスを取得する必要があるかもしれませんが、これは時間的で高価であり、大量のコストおよびリソース移転をもたらす可能性があり、私たちの業務に実質的な悪影響を及ぼす可能性があります。私たちがこのようなクレームを弁護することに成功しても、訴訟は巨額のコストを招き、経営陣や他の従業員の注意を分散させる可能性がある。上記のいずれも、当社の業務、財務状況、経営結果、見通しに重大な悪影響を及ぼす可能性があります。
もし私たちが特許訴訟や他の権利決定に関連する訴訟に巻き込まれれば、巨額のコストと支出を招き、重大な損害賠償責任を負うことができ、あるいは私たちの製品やサービスの開発と商業化努力を停止することが要求されるかもしれない。
アメリカ国内外には、生命科学、臨床診断と薬物発見業界の特許とその他の知的財産権に関連する訴訟が大量にあり、特許侵害訴訟、宣言性判決訴訟とアメリカ特許商標局に提起された対抗性訴訟を含み、妨害、派生訴訟、一方的再審、許可後再審と当事各方面の再審、及び外国裁判所と外国特許庁の相応の訴訟を含む。
私たちは現在、私たちの4つの特許に関する欧州特許庁の反対訴訟に参加している:EP 2364368、EP 2387627、EP 3059337、EP 3144673。将来、私たちは米国特許商標局や外国特許庁と様々な第三者との訴訟や訴訟に巻き込まれる可能性がある。私たちの業界の拡張、より多くの特許の発行、製品やサービスの数の増加、業界競争の激化に伴い、このようなクレームの数は増加する可能性があると予想しています。任意の侵害クレームは、その有効性にかかわらず、時間と費用をもたらす訴訟を含む当社の業務を損なう可能性があり、経営陣の業務発展に対する時間と注意を分散させ、金銭損害賠償(3倍の損害賠償、弁護士費、コストおよび費用を含む)または特許使用料の支払いを要求する。
私たちは、私たちの特許および固有の権利を実行するために、または他人の固有の権利の範囲、カバー範囲、および有効性を決定するために、特許庁に訴訟または対抗訴訟手続きを提起する必要があるかもしれない。このような訴訟の結果は私たちに不利になる可能性があり、たとえ私たちが勝訴しても、このような訴訟は巨額のコストと資源移転を招き、私たちの業務、運営業績、または財務状況に重大な悪影響を及ぼす可能性がある。
私たちが新しい市場に進出し、私たちの製品やサービス供給を拡大するにつれて、これらの市場の既存の参加者は、彼らの特許と他の独自の権利を主張して、私たちがこのような市場に入る速度を遅くするか、あるいは私たちから大量の許可と特許使用料を得る手段として、彼らの特許と他の独自の権利を主張するかもしれない。さらに、将来の訴訟は、特許保有会社または他の不利な特許権者に関連する可能性があり、彼らは関連する製品またはサービス収入を持っておらず、私たち自身の特許は彼らに対して抑止力や保護作用がほとんどないかもしれない。
第三者は私たちが許可されていない状況で彼らのノウハウを使用していると主張するかもしれない。臨床診断と薬物研究開発領域は競争の激しい領域であることから、他の人は第三者の知的財産権は著者らの免疫薬物プラットフォーム、製品とサービスと関係があるかもしれないと考えているかもしれない。1つまたは複数の第三者特許所有者または許可された人は、1つまたは複数の特許を強制的に執行するために、私たちに訴訟を提起することを脅かす可能性がある。そのような主張を正当化するのは高価で時間がかかるだろう。
66
特許出願は、発行されるまでに数年かかる可能性があるので、現在検討されている特許出願が存在する可能性があり、これらの出願は、現在または将来の製品、技術、およびサービスが発行された特許を侵害する可能性がある。私たちは私たちに権利侵害請求をする前に、重大な意味を持つ可能性のあるすべての第三者特許を確定または解決したことを確認することができない。さらに、私たちの業界の他の会社が経験したのと同様に、私たちの競争相手および他の会社は特許を持っている可能性があること、または将来的に特許を取得する可能性があることを予想し、私たちの製品またはサービスがこれらの特許を侵害したと主張し、製造、製造、使用、販売、販売、提供または輸入している。権利侵害や他のクレームの弁護は、その是非にかかわらず、巨額の訴訟費用がかかり、私たちの業務の経営陣や従業員資源を大量に移転させる。私たちにクレームを出した当事者は、彼らがより多くの資源を持っているので、私たちよりも複雑な特許訴訟の費用を効果的に維持することができるかもしれない。私たちにクレームを出した当事者は、禁止または他の救済を受けることができるかもしれません。これは、私たちの製品またはサービスの開発、商業化、販売能力を阻害し、もし私たちが故意に侵害されたことが発見されたら、私たちの3倍の損害賠償金、弁護士費、費用、費用を含む重大な損害賠償を招く可能性があります。私たちに対する侵害請求が成功した場合、私たちは損害賠償金と持続的な印税の支払いを要求され、第三者から1つ以上の許可証を取得するか、または特定の製品やサービスの販売を禁止される可能性がある。私たちは受け入れ可能または商業的に合理的な条項でこれらの許可を得ることができないかもしれない(もしあれば)、またはこれらの許可は非排他的である可能性があり、これは私たちの競争相手が同じ知的財産権を得ることをもたらす可能性がある。また、第三者の特許や独占権の侵害を回避するために代替製品やサービスを開発しようとすると、製品やサービスの発売遅延に遭遇する可能性がある。いかなる訴訟の抗弁やこのような許可を得られなかった場合、製品またはサービスを商業化することを阻止する可能性があり、私たちのいかなる製品またはサービスの販売を禁止することは、私たちの業務および市場が私たちの製品またはサービスを受け入れる能力を獲得することに実質的な影響を与える可能性がある。
さらに、知的財産権訴訟は大量の開示を必要とするため、このような訴訟の間、私たちのいくつかの機密情報は開示によって漏洩される可能性がある。また,このような訴訟過程では,公聴会,動議や他の一時的な手続きや事態の発展の結果が公表される可能性がある.もし証券アナリストや投資家がこれらの結果がマイナスだと思っていれば、私たちの普通株の価格に大きな悪影響を及ぼす可能性がある。
さらに、私たちは、私たちのいくつかの顧客、サプライヤー、または私たちの業務往来のある他のエンティティと合意し、これらの当事者が侵害クレーム(上記のタイプのクレームを含む)に巻き込まれた範囲内でその弁護または賠償を要求します。私たちはまた、私たちがこれが私たちの業務関係に重要であることを確認すれば、私たちがそうする義務がない場合に第三者の弁護や賠償に自発的に同意することができる。もし私たちが任意の侵害クレームについて第三者を弁護または賠償することを要求または同意された場合、私たちは重大なコストと支出を生じる可能性があり、私たちの業務、経営業績、または財務状況に悪影響を及ぼす可能性がある。
特許条項は製品とサービスでの私たちの競争地位を十分に保護するのに十分ではないかもしれない。
特許の寿命は限られている。米国では、すべての維持費が適時に支払われる場合、特許の自然失効時間は、通常、米国で最初の非臨時出願日から20年である。様々な延期があるかもしれないが、特許の有効期限とその提供される保護は限られている。私たちの製品やサービスをカバーする特許を取得しても、特許の有効期限が満了すると、競争製品からの競争に直面する可能性があります。新製品およびサービスの開発、テスト、および規制審査に要する時間を考慮すると、これらの製品およびサービスを保護する特許は、これらの製品およびサービスの商業化の前または直後に満了する可能性がある。したがって、私たちが持っている特許と許可された特許の組み合わせは、他社が私たちと似ているか同じ製品を商業化することを排除するために十分な権利を提供してくれないかもしれない。
67
私たちの普通株と資本構造に関連するリスク
私たち普通株の市場価格の変動は大きく、引き続き大幅に変動する可能性がある。
私たちの普通株の市場価格はずっと高度に変動し続ける可能性があります。52週の最高終値は10.11ドル、52週の最低終値は3.46ドルで、多くの要素によって大幅に変動する可能性があります。その中の多くの要素はコントロールできません。これらの要素には
近年、株式市場は普遍的に極端な価格と出来高の変動を経験し、これらの変動は往々にして上場会社の経営業績と関係がない或いは比例しない。もし私たちの業界の株式市場や株式市場全体の投資家の信頼にばらつきがあれば、私たちの普通株の市場価格は私たちの業務、経営業績、財務状況とは関係なく低下する可能性があります。私たち普通株の市場価格は、これらの事件が直接私たちに影響を与えなくても、当社内外の他社に影響を与える事件によって下落する可能性があります。私たちの普通株式市場価格のいかなる下落も、株式証券の売却を通じて資金を調達する能力を損なう可能性がある。
過去、証券集団訴訟は会社の株価が変動した後に提起されることが多かった。私たちにこのような訴訟を提起すれば、私たちに巨額のコストをもたらし、私たちの経営陣の注意と資源を分散させる可能性があり、これは私たちの業務、財務状況、運営結果、将来性を深刻に損なう可能性がある。
私たちとOrbiMedとの購入協定は、私たちの業務のキャッシュフローを制限し、私たちの業務、財務状況、運営結果に悪影響を及ぼす可能性があるリスクに直面する可能性があります。
私たちの購入協定の下での義務は、私たちの証券保有者と私たちの業務、経営結果、財務状況に大きなマイナス影響を与える可能性があります
68
また、購入協定には、我々の核心資産に与える優先的な保証権益、および私たちの留置権の発生を制限し、追加債務の発生、融資および投資、特定の制限された支払いまたは核心資産の譲渡を行う能力の契約および制限を含む慣用的なプラスおよび負の非金融契約および違約事件が含まれている。また,購入プロトコル項の下の買手は購入プロトコルを終了する権利があり,破産事件,吾などに不利な重大な判決,重大資産剥離や制御権変更などの事件が発生した場合には,買手の累積支払いの120%から175%の価格で将来の収入権益を買い戻し,吾などがその日までに買手に支払ったすべての収入利息の総和を差し引くことを要求する.これらの契約を遵守できなかったことを含むコールオプションをトリガし、購入者がある金額の即時満期と支払いを宣言することを許可する可能性がある。
もし証券アナリストが私たちの業務に関する研究や報告を発表しなければ、あるいは私たちが否定的な宣伝の対象になれば、私たちの株価は下落する可能性があります。
私たちの普通株の取引市場は、証券や業界アナリストが発表した私たちまたは私たちの業務に関する研究と報告にある程度依存している。私たちはこのようなアナリストを統制することができない。私たちの一人以上のアナリストを追跡して私たちの株式格付けを下げたり、わが社や株の不正確または不利な評価を発表したりすれば、私たちの株価は下落するかもしれません。1人以上のアナリストが私たちの会社の報道を中止したり、当社に関する報告書を定期的に発表できなかったりすれば、私たちの株は市場で知名度を失う可能性があり、株価を下落させる可能性があります。また、もし私たちが否定的な宣伝の対象になれば、アナリスト、学術、業界団体、一般メディア、財経メディアからも、私たちの株価は下落する可能性がある。
もし私たちの重要な会計政策の推定または判断が変更または不正確であることが証明された仮定に基づいている場合、私たちの経営結果は、私たちが公開発表した指導や証券アナリストや投資家の予想を下回って、私たちの普通株の市場価格を低下させる可能性がある。
アメリカ公認会計原則(“GAAP”)に基づいて総合財務諸表を作成する際、管理層は総合財務諸表及び付記所の金額に影響を与える推定と仮定をしなければならない。私たちは過去の経験と私たちが当時の状況で合理的だと思う各種の他の仮定に基づいて推定し、これらの仮説の結果は資産、負債、権益、収入及び支出の帳簿価値を判断する基礎を構成しているが、このような資産、負債、権益、収入及び支出は他の出所から容易に現れない。もし私たちの仮定が変化したり、実態が私たちの仮定と異なっていれば、私たちの経営業績は不利な影響を受ける可能性があり、私たちが公開発表した指針や証券アナリストや投資家の予想を下回る可能性があり、私たちの普通株の市場価格を低下させ、株式証券を売却することで資金を調達する能力を弱める可能性がある。
将来的に私たちの普通株または他の株式証券の公開市場での大量の将来の販売または予想される潜在的な販売は、私たちの普通株の価格を大幅に低下させる可能性がある。
我々の普通株式又は他の株式証券、特に我々の役員、役員及び主要株主を公開市場で売却することは、我々の普通株式又は他の株式証券の発行に関連する任意のロック期間が終了した場合、又はこれらの売却が発生する可能性があると考えられる場合には、我々の普通株式価格に大きな悪影響を与え、株式証券の売却による資金調達能力を弱める可能性がある。
69
私たちは財務報告書と他の要求に制約されており、私たちの会計と他の管理システムと資源はこれらの要求に対して十分な準備ができていないかもしれない。
2002年のサバンズ-オキシリー法(Sarbanes-Oxley Act)第404条(“第404条”)によると、私たちは、私たちの独立公認会計士事務所が発行した財務報告の内部統制に関する認証報告を含む財務報告書の内部統制に関する報告書を提出しなければならない。私たちは第404条の規定に従うと、大量の会計費用を発生させ、多くの管理努力をかけなければならない。内部資源を投入し続け、外部コンサルタントを招聘することが可能であり、詳細な作業計画により、財務報告内部制御の十分性を評価して記録し、適宜手順をとって制御プログラムを改善し、テスト検証制御が文書記録の役割を果たしていることを検証し、財務報告内部制御の継続報告及び改善手順を実施する。我々は努力したにもかかわらず,我々も我々の独立公認会計士事務所も,規定された時間枠内で結論を出すことが可能であり,財務報告の内部統制に有効であり,第404条の要件に適合していることを証明している。これは、総合財務諸表の信頼性に自信を失っているため、金融市場の不利な反応を招く可能性がある。
私たちはまた開示統制と手続きを維持することを要求された。開示制御および手続きとは、取引法に基づいて提出または提出された報告書のうち、開示を要求する情報が、米国証券取引委員会規則および表に指定された期間内に記録、処理、集約および報告されることを保証するための、我々の制御および他の手続きを意味する。私たちは私たちの開示統制と手続き、または財務報告に対する私たちの内部統制がすべてのミスとすべての詐欺を防止または発見することを期待していない。規制システムの設計や運営がどのように整備されていても、絶対的な保証ではなく、合理的な保証しか提供できず、規制システムの目標が達成できるようにするしかないと信じている。すべての制御システムの固有の限界により,どの制御評価も誤りや不正による誤り陳述が発生しないことや,すべての制御問題や不正が検出されたことを絶対に保証することはできない.どの制御システムの設計も、将来のイベント可能性のいくつかの仮定にある程度基づいており、どの設計も、すべての潜在的な未来条件で、そのような目標を成功的に達成することができない可能性がある。時間の経過とともに,条件の変化やポリシーやプログラムの遵守の程度の悪化により,制御が不十分になる可能性がある.したがって,我々の制御システム固有の制限により,誤りや詐欺による誤り陳述が発生し,発見されない可能性がある.
企業責任実践をめぐる絶えず変化する期待、特に環境、社会、およびガバナンス(“ESG”)事項に関する期待は、私たちを名声や他のリスクに直面させる可能性がある。
投資家、株主、顧客、サプライヤー、および他の第三者は、ESGおよび企業の社会的責任の努力および報告にますます注目している。いくつかの機関投資家、投資基金、他の影響力のある投資家、顧客、サプライヤー、および他の第三者もESG実践にますます注目している。特に、多数投票、年次役員選挙、外部取締役超過投票のような株主権利条項に焦点を当てた第三者代理コンサルティングサービスは、過去の選挙で私たちの取締役を選挙しないことを、我々のガバナンス状況によって提案されていた。
投資家や利害関係者が変化していく期待や基準に適応していない会社、または適切な反応をしていないと考えられている会社は、名声被害を受け、会社の業務、財務状況および/または株価が実質的かつ不利な影響を受ける可能性がある。さらに、ESG問題への日々の関心は、私たちのサービスに悪影響を及ぼす可能性があり、またはいくつかの株主が所有している私たちの株を減少またはキャンセルする可能性がある新しい法規および/または第三者要求をもたらす可能性がある。しかも、このような分野で私たちが十分に行動していないという告発や見方は私たちの名声に否定的な影響を及ぼすかもしれない。
すべての業界の会社は、そのESGポリシーに関連したますます厳しい審査に直面している。もし私たちが日々増加するガバナンス問題への関心に適切な対応をしていないと考えられれば、投資家は彼らの私たちのやり方の評価のために彼らの資本投資を再考するかもしれません。私たちの名声、業務、財務状況、経営業績、およびキャッシュフローは悪影響を受ける可能性があります。
当社の定款文書やワシントン法律の条項は、わが社の買収をより困難にし、現在の経営陣を変更または罷免する試みを制限する可能性があります。
当社の定款(“定款”)および当社の改正·再記述された定款(“定款”)およびワシントン法律に含まれる条項は、株主がその最適な利益に適合すると考えられる私たちの支配権変更または経営陣の変更を阻止または遅延する効果がある可能性がある。当社の定款と付例には以下の条項が含まれています
70
これらの条項は、単独または共同で、敵意の買収、統制権の変更、または私たちの管理職または取締役会の変更を延期または阻止する可能性がある。
さらに、私たちはワシントン州で登録されているので、私たちはワシントン州商業会社法(WBCA)第23 B.19章の条項によって管轄されています。この条項は特定の条件が満たされない限り、特定の重要な株主との間のいくつかの業務統合を禁止しています。これらの規定はまたわが社の支配権変更を延期または阻止する効果がある可能性がある。
私たちの会社の定款や定款あるいはワシントン法律のいかなる制御権の変更を延期または阻止する条項は、私たちの株主が彼らが持っている普通株から割増の機会を得ることを制限する可能性があり、また一部の投資家が私たちの普通株に支払いたい価格に影響を与える可能性があります。
私たちの定款は、ワシントン州金県に位置する州裁判所と、強制執行可能な範囲内で、アメリカ合衆国連邦地域裁判所は、私たちと私たちの株主とのほとんどの紛争の独占的なフォーラムとなり、これは、私たちまたは私たちの役員、役員、または従業員との紛争を処理するために、私たちの株主が有利な司法フォーラムを得ることを制限するかもしれません。
私たちの会社規約は、私たちが書面で代替裁判所を選択することに同意しない限り、ワシントン州金県に位置する州裁判所(または、ワシントン州金県に位置する州裁判所に管轄権がなければ、ワシントン州西区の連邦地域裁判所)は、任意の訴訟を開始し、維持する唯一のフォーラムでなければならない、(1)私たちの現職または前任取締役、上級職員、または株主がこの身分でワシントン州法律下の義務に違反してクレームを提出し、(2)わが社の権利に基づいて開始または維持しなければならない。(3)すべての場合において、法律で許容される最大範囲において、WBCA、当社の定款又は当社の附例(時々改正される可能性がある)のいずれかの条項に基づいてクレームを提起するか、又は(4)上記(1)~(3)項に含まれない我々の内部事務に関するクレームを主張し、被告に指定された不可欠な当事者に対して裁判所によって個人管轄権を有することが制限される。これらの規定は、取引法に規定された義務や責任を執行するための訴訟にも適用されず、連邦裁判所が排他的管轄権を有する他のいかなるクレームにも適用されない。
我々の会社規約では,米国連邦地域裁判所は改正された1933年の証券法(“証券法”)に基づいて提出された任意の訴因を解決する独占的なフォーラムとなるが,適用法に適合しなければならない。
任意の個人またはエンティティが、私たちの任意の証券の任意の権益を購入または他の方法で取得することは、これらの規定に了承され、同意されたとみなされるべきである。私たちの独占フォーラム条項は私たちが連邦証券法とその下での規則と法規を遵守する責任を解除しないだろうし、私たちの株主もこのような法律、規則、そして法規の遵守を放棄したとみなされないだろう。これらの排他的フォーラム条項は、私たちまたは私たちの役員、上級管理者、または他の従業員との紛争について司法裁判所で株主がクレームを出す能力を制限する可能性があり、これは、私たちおよび私たちの役員、上級管理者、および他の従業員に対する訴訟を阻止したり、株主が私たちの定款で指定されたフォーラムでクレームを提起する追加費用を引き起こす可能性があります。
71
もし裁判所が私たちの定款におけるこれらの排他的フォーラム条項が訴訟で適用されないか、実行できないことを発見すれば、他の管轄区域での紛争解決に関連する追加費用が発生する可能性があり、これは私たちの運営結果を損なう可能性がある。デラウェア州裁判所は、このような選択された裁判所条項が事実上有効であることを決定したが、株主は、排他的な裁判所条項で指定された司法管轄区域以外の管轄区域でクレームを提出することを求めることができ、当該司法管轄区の裁判所は、この条項を強制的に執行してはならない。ワシントンの法律により、ワシントン裁判所が類似した結論を出すかどうかは不明である。これらのクレームを弁護することに成功しても、訴訟は巨額のコストを招き、経営陣や他の従業員の注意を分散させる可能性がある。
私たちの役員と上級管理者の賠償要求は、成功した第三者からのクレームを満たすために、私たちの利用可能な資金を減らすことができ、私たちの利用可能な資金を減らすことができます。
私たちの会社の定款は、ワシントン法律で許可された最大限に私たちの役員と上級管理者を賠償することを規定しています。
また、WBCA第23 B.08.510~23 B.08.570節の許可の下、当社の定款と、大多数の役員や上級管理職と締結した賠償協定は、以下のように規定されている
私たちは予測可能な未来に私たちの株に現金配当金を支払わないと予想されているので、資本増加(あれば)があなたの唯一の収益源になるだろう。
私たちは現在、運営を支援し、私たちの業務の成長と発展に資金を提供するために、すべての利用可能な資金と未来の任意の収益を維持しようとしており、予測可能な未来には、私たちの普通株に現金配当金は支払われないと予想される。しかも、未来のどんな債務協定の条項も私たちが配当金を支払うことを阻止するかもしれない。したがって、私たちの普通株の資本付加価値は(もしあれば)あなたが予測可能な未来に唯一の収益源になるだろう。
72
項目1 B。国連.国連解決済み従業員意見
適用されない.
プロジェクト1 C。ネットワーク·セキュリティ
医療提供者,患者,生物製薬会社,学術·非営利機関,ビジネスパートナー,従業員信頼できるパートナーとして,包括的かつ信頼できる情報セキュリティ計画を維持することの重要性を認識した。我々の情報セキュリティ計画は我々の運営に完全に溶け込んでおり,我々の計画の特徴の1つは,我々の内部プライバシー目標や利害関係者との機能を越えた方法である.
我々のネットワークセキュリティ計画は、国際標準化組織27001セキュリティ制御セットに基づいており、特にセキュリティ、完全性、および利用可能性の原則を重視している。我々はISO 27001認証を持ち,ISO 27001に準拠する14分野の完全に統合された運用ポリシーとプログラムを持っている.これには、適応において役割および責任を割り当てるための情報セキュリティ組織を含むが、従業員がその役割に関連する情報、情報セキュリティイベント管理、およびコンプライアンスのみを見ることができるように制限するためのアクセス制御が含まれているが、適用される法律法規との一貫性を広く確保するために適合性がある。外部評価者による年間リスク評価を実行し、ネットワークセキュリティイベントが発生したときに当社の業務にどのように影響を与える可能性があるかを評価するために、第三者サプライヤーのためのサプライヤーリスク評価計画を実行する。また、従業員に年間強制サイバーセキュリティ訓練を提供し、ネットワーク釣りの試みのようなネットワークセキュリティ脅威を識別し、対応する知識を身につけるようにしている。
我々のネットワークセキュリティプロジェクトに対して行政監督を行う内部機関は,我々のプライバシーと情報セキュリティ指導委員会(PISC)であり,この委員会は情報セキュリティ,プライバシーと人的資源の専門知識,監督と報告を統合することにより,多学科枠組みをネットワークセキュリティリスクとリスク評価に応用する.PISCは我々の安全主管,プライバシー官,首席運営官,首席財務官,総法律顧問,首席人事官からなり,四半期ごとに会議が行われる。私たちのセキュリティ担当者はベテラン情報セキュリティ専門家で、20年以上セキュリティプロジェクトを実施し、指導した経験を持っている。我々のセキュリティ担当者は計算機科学学部の学位を持ち,全面的な品質管理を持つヘキサシグマ認証は,認証された情報システムセキュリティ専門家(CSSPと略す)である.
我々の取締役会は、定期的に監査委員会に情報セキュリティとプライバシー管理状況および情報セキュリティとプライバシーイベントに関する報告を紹介することで、ネットワークセキュリティリスクと評価を随時理解しています。ネットワークセキュリティ脅威は、過去のいかなるネットワークセキュリティイベントの結果も含めて、我々の業務戦略、運営結果、または財務状況を含む我々に実質的な影響を与えていない。ネットワークセキュリティリスクが私たちのより多くの情報にどのように影響するかについては、“リスク要因”の部分を参照してください。
プロジェクト2.ニュースオペラ?オペラ
私たちの会社の本社はワシントン州のシアトルにあります。そこで約百,000平方フィートを借りました。レンタル契約は2033年8月に満期になります。私たちが2回レンタル期間を5年延長するかどうかによります。ワシントン州シアトルの別の場所で、2032年10月に満期になった賃貸契約によると、私たちは約65,500平方フィートを借りました。二回選択してレンタルを五年間延長することにかかっています。私たちはワシントン州シアトルの二つの場所に事務と実験室があります。
ワシントン州ボゼルで約27,000平方フィートの倉庫を借りました賃貸借契約は2031年10月に満期となり、2028年に早期終了の選択権があることと、2回で借約を5年間延長する権利があることが条件となる。
また、2026年3月に満期になった改訂レンタル契約によると、カリフォルニア州サンフランシスコ南部で約33,300平方フィートの実験室とオフィススペースをレンタルしました。条件はレンタルを5年間延長することができるということです。
2025年11月に満期になった賃貸契約によると、ニューヨーク市で約3100平方フィートのオフィススペースも借りました。
項目3.法律訴訟手続き
時々、私たちは法的手続きの影響を受けるかもしれない。私たちは現在、個別または全体が私たちの業務、財務状況、または経営結果に重大な悪影響を及ぼすと考えている訴訟には参加していません。結果にかかわらず,弁護や和解コスト,管理資源分流などにより,訴訟は我々に悪影響を与える可能性がある。
4つ目:地雷の安全TY開示
適用されない.
73
パー?パーT II
項目5.登録者普通株式市場、関連株持株者事項と発行者による持分証券の購入
普通株式市場情報
我々の普通株式は2019年6月27日にナスダック世界ベスト市場で取引を開始し、コードはADPTである。これまで、私たちの普通株は公開取引市場を持っていなかった。
記録保持者
2024年2月23日現在、私たちの普通株は約85人の登録保有者がいます。我々の多くの普通株は仲介人や他の機関代表株主が保有しているため,これらの記録保有者が代表する株主総数を見積もることはできない.
配当政策
私たちは現在、すべての利用可能な資金と未来のどんな収益も維持し、私たちの業務の成長と発展に資金を提供するつもりだ。予測可能な未来に、私たちは株主に現金配当金を支払うつもりはない。将来配当を発表する任意の決定は、私たちの取締役会が適宜決定し、私たちの財務状況、経営業績、資本要求、一般業務状況と私たちの取締役会が関連する他の要素に依存するかもしれません。私たちが未来に普通株のために現金配当金を支払う能力もまた、未来の債務証券、優先株、または信用手配条項によって制限される可能性がある。
株式表現グラフ
次の図は私たちの普通株の累積総株主リターンとナスダック総合指数とナスダック生物技術指数の累積総リターンを比較した。この図は、2019年6月27日、すなわち私たちの最初の取引日に終値した場合、100ドルが私たちの普通株に投資されていると仮定しています。ナスダック総合指数とナスダックバイオテクノロジー指数のデータ仮説配当は再投資された。私たちの初公募株の普通株発行価格は1株20.00ドル、2019年6月27日終値は40.30ドルだった。次の株価表現は履歴データに基づいており,必ずしも指示されるわけではなく,我々の普通株の未来表現を予測するつもりもない.
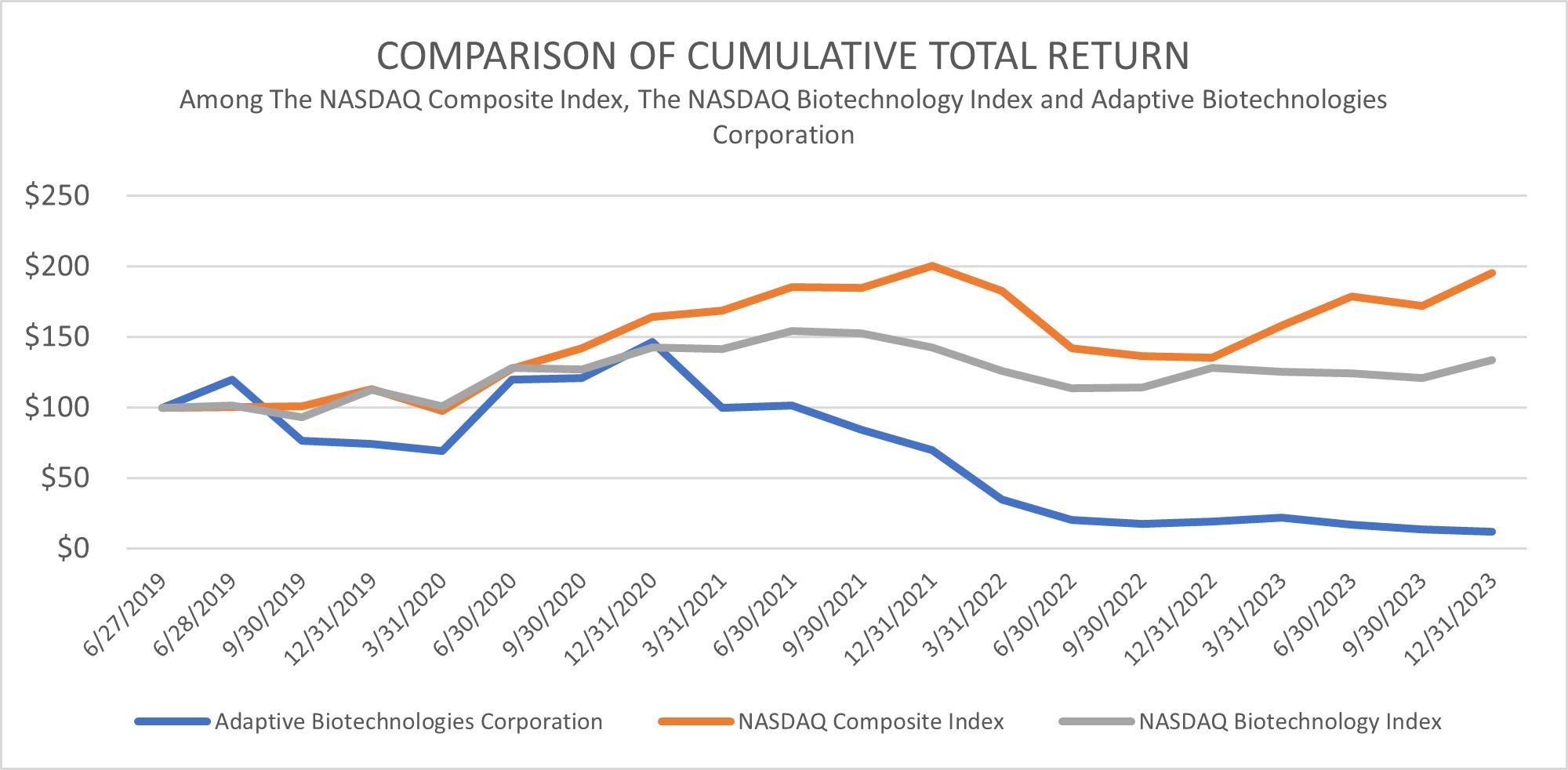
取引法第18節の規定によれば、このグラフは、“募集材料”とみなされてはならないか、または米国証券取引委員会によって“保存”されているか、または参照によって適応バイオテクノロジー会社が証券法または取引法に従って提出された任意の文書に組み込まれてはならない。
第六項です[返事をする料理を出す]
適用されません。
74
プロジェクト7.管理財務状況と経営成果の検討と分析
当社の財務状況及び経営業績に関する以下の議論及び分析、並びに総合財務諸表及び関連付記及び本年報10-K表のその他の部分に掲載されている他の財務資料、並びに我々が米国証券取引委員会に提出したその他の財務資料を読むべきである(“アメリカ証券取引委員会”)時々。本議論および分析に含まれるまたは本報告の他の部分に記載されたいくつかの情報は、私たちの業務および関連融資の計画および戦略に関する情報を含み、前向きな陳述を含み、私たちの将来の計画、目標、予想、意図および財務業績、ならびにこれらの陳述が根拠とする仮定に関連するリスクおよび不確定要素に関するものである。本年度報告10-K表の“リスク要因”の部分に列挙された要素を含む多くの要因の影響により、我々の実際の結果は、以下の議論および分析に含まれる前向き陳述に記載または示唆された結果とは大きく異なる可能性がある。
本節では,一般に2023年と2022年の項目および2023年と2022年の間の同比比較について議論する.2021年プロジェクトに関する検討および2022年と2021年の間の年次比較は,タイトル下の第2部分項目7で見つけることができる“経営陣の財務状況と経営成果の検討と分析”我々が2023年2月14日に米国証券取引委員会に提出した12月31日までのForm 10−K年次報告である。
概要
我々は,適応免疫システムの固有生物学を利用することで疾患の診断や治療を変化させ,免疫医学分野の発展を進めている。適応免疫系は自然界が多くの疾患に対して行っている最も精密な診断や治療であると考えられるが,それを解読することはできず,医学界のその能力の活用を阻害している。著者らの免疫医学プラットフォームは著者らの独自技術を応用して患者免疫システムの各種遺伝子コードを読み取り、免疫システムがどのようにこの患者の疾病を測定と治療するかを正確に理解する。著者らは計算生物学と機械学習に基づく動態臨床免疫組織学データベースと関連抗原注釈の中でこれらの知見を捉え、それらを利用して患者個人の需要量に応じてカスタマイズできる臨床製品とサービスを開発と商業化した。私たちは現在と未来の商業製品とサービスは2つの業務領域と一致し、著者らはMRDと免疫医学と呼ばれる。
著者らが現在MRD市場で提供しているMRD市場に関連する製品とサービスは臨床医師に提供するclonoSEQの臨床診断テスト、及び生物製薬パートナーに提供する薬物開発努力を推進するclono配列番号或いはMRD検査(“MRD Pharma”)を含む。我々の最初の臨床診断製品clonoSEQは、FDAによって承認されたMM、B細胞ALLおよびCLL患者MRDを検出および監視するための最初の試験であり、DLBCLを含む他のリンパ癌患者のためにCLIA検証の実験室で開発された試験として使用することもできる。ClonoSEQを用いることにより,提供者,製薬パートナー,支払者と連携することにより,リンパ癌の治療法を変化させている。
免疫医学は著者らの独自の能力を利用してTCRとBCRに対して大規模シークエンシング、マッピング、ペアリングと表現を行い、癌、自己免疫性疾患、伝染病と神経退行性疾患の中で機会を創造する。著者らの核心研究製品の適応免疫シークエンシングは著者らの基礎研究開発エンジンであり、生物製薬と学術顧客から収入を得る。マイクロソフトとの協力を利用してTCR-抗原マップを作成しています著者らはTCR-抗原マップを用いて疾病の特徴を識別と検証し、多くの疾病の診断と治療を改善している。薬物発見では,我々の特許能力を用いて新たな薬物標的を発見し,我々が検証したTCRとBCR発現方法を用いてTCRや抗体治療資産を発見·開発した。薬物発見には遺伝子技術プロトコルが含まれている。我々の免疫医学分野における一部の戦略は,一次血液テストから複数の疾患に対する診断テストを開発することであり,T−Detectと呼ばれる。2022年には,複数の疾患州で十分な強力なデータを持ち,明確な精算経路で医師の行動に影響を与えるまで,T−Detectのさらなる商業化を延期することにした。
2023年12月31日現在と2022年12月31日現在の会計年度において、それぞれ1.703億ドルと1.853億ドルの収入を確認した。2023年12月31日と2022年12月31日までの年度は、適応バイオテクノロジー会社の純損失がそれぞれ2.253億ドルと20020万ドルだった。これまで、私たちの運営資金は主に転換可能な優先株と普通株の売却、次いで購入合意の収入と収益から来ていた。2023年12月31日と2022年12月31日までに、それぞれ3.464億ドルの現金、現金等価物、4.982億ドルの有価証券を持っている。
75
経営成果の構成部分
収入.収入
著者らは免疫医学とMRD業務領域で診断と研究サービスを提供することによって収入を獲得した。私たちの免疫薬物収入は(1)生物製薬顧客と学術機関に私たちの商業研究製品の適応免疫シークエンシングのサンプル試験サービスを提供すること、(2)私たちは遺伝子テークと他の生物製薬顧客との薬物と標的発見領域の協力協定、および(3)数年前に臨床顧客に私たちのT-Detect CoVIDテストを提供する。私たちのMRD収入は、(1)臨床顧客に当社のclonoSEQ報告を提供すること、(2)生物製薬顧客およびいくつかの学術機関にMRDサンプル検査サービスを提供すること、および(3)技術移転によっていくつかの国際実験室サイトに我々のclonoSEQ報告または結果を提供することを含む。我々が米国および国際技術移転サイトの発注医に提供するclonoSEQ報告および結果の数を含む、我々のclonoSEQ試験量を開示する。これらの数には,我々のバイオ製薬顧客や我々のMRDサービスを使用する学術機関のサンプル結果は含まれていない.
著者らの研究顧客に対して、生物製薬顧客と学術機関を含み、著者らの適応免疫シークエンシングとMRDサービス、それぞれのテスト結果の交付はある程度の専門的な支持と分析を含む可能性がある。バイオ製薬顧客との条項には、通常、サービスの前に支払われた払戻不可能なお金(“前払い”)が含まれており、繰延収入として記録されている。すべての研究顧客に対して、シークエンシング結果を提供する際に収入を確認します。私たちは時々割引を提供して、いくつかのデータセットの権利とアクセス権を得る。収入はこれらの割引を差し引いた純額であることが確認され,これらのサービスに関するコストが収入コストに反映されている.我々のサンプル推定が引き下げられた時期や顧客プロジェクトがキャンセルされた時期には,両方の場合,残りの関連繰延収入があり,累積追跡法を用いて,これまでに納入されたサンプルが予想されるサンプル総数に占める割合に基づいて収入を確認した.著者らが生物製薬顧客と達成したいくつかのMRD収入協定は、それぞれの生物製薬顧客療法の規制マイルストーンを実現する現金対価格を含む。このようなマイルストーンに達する可能性が高い前に、このような収入は制限されており、確認されていない。
私たちのバイオ製薬顧客と達成されたいくつかの合意によると、これらの顧客は、私たちのプラットフォームを使用して彼らの治療開発活動を支援し、私たちが提供する研究開発支援サービスから収入を得ることを求めている。これらのプロトコルには,払戻不可能な前金が多く含まれている可能性があり,それぞれのサービスを実行する際に時間の経過とともにこれを確認する.これらの活動から確認された収入は主に遺伝子技術会社協定と関係がある。
私たちの臨床顧客では,主に発注医にclonoSEQ報告書を提供することで収入を得ている。私たちは注文医に提出した報告書に基づいて商業、政府、医療機関支払人に請求書を発行します。商業,政府,医療機関支払者がclonoSEQに支払う金額は,それぞれの販売率や患者責任によって異なり,我々の目標価格とは異なる可能性がある。私たちは、顧客支払い履歴、契約販売率(適用される場合)および他の調整を評価することによって、臨床収入を確認し、受け取ることができる収入金額を推定する。
連邦医療保険下のclonoSEQ保険では、私たちが最初の合格したテスト報告書を提供する時、一次治療のための請求書を発行します。この請求書は、患者の治療期間に必要なすべての必要なテストを考慮しており、現在、各患者は初期配列同定テストを含む約4つのテストがあると推定されている。収入確認は、初期課金テスト報告書が交付されたときから始まり、これまでに交付された累積テストに基づく。初期課金試験からの任意の未確認収入は、繰延収入として記録され、患者の治療期間における残りの試験の推定値を提供するとき、または患者が追加の試験を受ける可能性がわずかになる場合に確認される。
私たちは短期的に私たちの免疫薬収入が減少することを予想していますが、これは主に遺伝子テークプロトコルによる収入の減少が期待されています。長期的には,われわれあるいはわれわれの協力者が療法を商業化するにつれて,われわれの免疫薬収入が増加することが予想される。私たちの免疫薬物収入は、発生費用の時間、遺伝子テークプロトコルに関連する予想される総コスト推定の変化、および遺伝子テークプロトコルによるマイルストーンの確認、および私たちの生物製薬顧客から顧客サンプルを受け取る時間を含む、私たちの制御範囲内にない他のイベントによって変動する可能性がある。
われわれは,既存の被覆患者群の浸透率の増加,新規患者群への拡大,支払者被覆範囲の最適化に伴い,われわれのMRD臨床試験量を増加させ続けることにより,われわれのMRD収入は長期的に増加すると予想される。私たちのMRD収入は、私たちの生物製薬顧客サンプルを受け取った不確定な時間によって変動する可能性があり、これは、私たちの製品やサービス配送における不確実性、規制機関が私たちのバイオ製薬顧客の治療法を承認することに関するマイルストーンの確認、および私たちの臨床収入収益率推定の変化を招く可能性がある。
76
収入コスト
収入コストには、材料コスト、人員に関連する費用(賃金、福祉、および株式ベースの給与を含む)、輸送および運搬費用、設備コスト、サンプル処理に関連する分配施設コスト、および私たちのサービス収入活動に関連する専門的な支援コストが含まれる。分配される施設費用には、実験室設備の減価償却、分配された施設占有と情報技術費用が含まれる。加工サンプルに関するコストは、収入確認の時間を考慮することなく費用として記録される。したがって,収入コストや関連数の傾向は,必ずしも収入確認や関連数の傾向と同じではない。しかも、遺伝子テーク合意を支持する費用は私たちの研究開発費の構成要素だ。
サンプルテスト量の増加に伴い収入コストは絶対値計算で増加することが予想されるが,長期的には個々のサンプルのコストが低下するのは,実験室能力の利用率,自動化,その他の価値工学的挙動を向上させ,検査量の増加に伴い効率を得ることができるためである。我々のサンプル量のスループットが減少した場合、総収入に占める収入コストの割合は、固定間接コストによって悪影響を受ける可能性がある。
研究と開発費
研究および開発費用には、実験室材料費用、人員に関連する費用(賃金、福祉および株式報酬を含む)、設備費用、分配された施設および情報技術費用、および契約サービス費用が含まれる。研究と開発活動は現有の検査と製品の更なる開発と改善、新技術の発見と著者らの免疫薬物プラットフォームへの投資を支持する。また,ソフトウェア開発に関するコストを研究開発費に含め,将来のビジネス機会を支援し,実験室規模やワークフローの開発活動を支援する.私たちは現在いくつかの製品とサービスの研究開発活動を行っています。私たちは通常、複数の開発プロジェクトで私たちの実験室材料、人員、施設、情報技術、その他の開発資源を使用します。また、これらの研究·開発活動の中のいくつかの活動が私たちに利益をもたらす製品機会は1つ以上ではない。私たちは歴史的に特定の候補製品の研究開発費用を追跡したことがない。
遺伝子テーク合意を支持する費用は私たちの研究開発費の構成要素だ。また、私たちの研究開発費の構成要素は、将来の臨床製品やサービスの規制承認を得るために、臨床と分析検証を支援するコストである。その中のいくつかの活動は収入を生成し、未来に収入を生むかもしれない。
短期的には研究開発費が減少し,長期的には収入に占める割合が低下することが予想されるが,我々の開発や商業化努力のタイミングや程度により,この割合は時間帯によって変化する可能性がある。
販売とマーケティング費用
販売およびマーケティング費用には、当社のプラットフォーム製品の商業化を支援する商業販売、製品および口座管理、マーケティング、精算、医療教育、業務開発者の人事関連費用(賃金、福祉、株式給与を含む)が含まれています。また、これらの費用には、広告費用、顧客教育·販売促進費用、市場分析費用、会議費、出張費用、分配された施設や情報技術費用などの外部コストが含まれる。
私たちは販売とマーケティング費用が短期的に相対的に維持されると予想する。長期的には、製品やサービスの知名度と採用率を高めるためにマーケティング活動を増やすにつれて、販売とマーケティング費用は絶対ドルで増加すると予想されています。しかし、収入に占める販売·マーケティング費用の割合は長期的に低下し、これらの費用の時間や規模の影響を受けて時期によって変動することが予想される。
一般と行政費用
一般及び行政支出は行政、法律、財務及び会計、人力資源及びその他の行政機能における当社人員の人事関連支出(給与、福祉及び株式報酬を含む)を含み、第三者臨床課金サービスを含む。また、これらの費用には、保険料、外部法律費用、会計、税務サービス費用、相談費、分配された施設や情報技術費用が含まれています。
一般と行政費用は短期的には相対的に一致し,長期的には収入の割合が低下すると予想される。
77
減価および関連長期資産支出を使用する
使用権減値および関連長期資産支出には、いくつかの賃貸オフィスおよび実験室空間の減価費用、および関連賃貸改善の減値コストが含まれる。付記10を参照賃貸借証書我々の減価評価と考慮事項の詳細については、本年度報告10−K表に他の部分に添付されている連結財務諸表付記を参照されたい。
利子支出
支払利息には、購入契約に関連する収入利息負債に関するコストと、繰延発行コストに関連する償却に関する非現金支払利息コストとが含まれる。私たちは有効金利法を用いて利息支出を試算した。私たちが計算した実際の金利は私たちの関連債務を予想された返済期間内にゼロに償却するだろう。予想される収入の著しい増加または減少または時間の変化は、私たちの利息支出に予想される影響を与えるだろう。
78
経営報告書データ及びその他の財務及び経営データ
次の表は私たちが列挙した期間の業務報告書データとその他の財務および業務データを示します(千単位で、1株当たりおよび1株当たりの金額は含まれていない):
|
|
十二月三十一日までの年度 |
|
|||||||||
|
|
2023 |
|
|
2022 |
|
|
2021 |
|
|||
運営報告書データ: |
|
|
|
|
|
|
|
|
|
|||
収入.収入 |
|
$ |
170,276 |
|
|
$ |
185,308 |
|
|
$ |
154,344 |
|
運営費 |
|
|
|
|
|
|
|
|
|
|||
収入コスト |
|
|
75,553 |
|
|
|
57,909 |
|
|
|
49,301 |
|
研究開発 |
|
|
122,117 |
|
|
|
141,756 |
|
|
|
142,343 |
|
販売とマーケティング |
|
|
88,579 |
|
|
|
95,603 |
|
|
|
95,465 |
|
一般と行政 |
|
|
83,934 |
|
|
|
88,527 |
|
|
|
74,502 |
|
無形資産の償却 |
|
|
1,699 |
|
|
|
1,699 |
|
|
|
1,699 |
|
使用権および関連長期資産の減価 |
|
|
25,429 |
|
|
|
— |
|
|
|
— |
|
総運営費 |
|
|
397,311 |
|
|
|
385,494 |
|
|
|
363,310 |
|
運営損失 |
|
|
(227,035 |
) |
|
|
(200,186 |
) |
|
|
(208,966 |
) |
利息とその他の収入,純額 |
|
|
15,531 |
|
|
|
4,056 |
|
|
|
1,668 |
|
利子支出 |
|
|
(13,800 |
) |
|
|
(4,238 |
) |
|
|
— |
|
純損失 |
|
|
(225,304 |
) |
|
|
(200,368 |
) |
|
|
(207,298 |
) |
新規:非持株権益の純損失に起因する |
|
|
54 |
|
|
|
177 |
|
|
|
19 |
|
適応バイオテクノロジー会社の純損失によるものです |
|
$ |
(225,250 |
) |
|
$ |
(200,191 |
) |
|
$ |
(207,279 |
) |
適応バイオテクノロジー会社の普通株株主は1株当たり純損失を占めなければならず、基本と希釈後 |
|
$ |
(1.56 |
) |
|
$ |
(1.40 |
) |
|
$ |
(1.48 |
) |
適応バイオテクノロジー会社の普通株主に起因する1株当たり純損失の加重平均株式、基本株主及び希釈株主の計算に用いる |
|
|
144,383,294 |
|
|
|
142,515,917 |
|
|
|
140,354,915 |
|
その他の財務·運営データ: |
|
|
|
|
|
|
|
|
|
|||
調整後EBITDA(1) |
|
$ |
(116,413 |
) |
|
$ |
(121,589 |
) |
|
$ |
(151,743 |
) |
(1)調整後のEBITDAは非GAAP財務指標であり、著者らはそれを利息とその他の収入、純額、利息支出、所得税(費用)収益、減価償却と償却費用、使用権と関連長期資産の減価コスト、再編費用と株式に基づく給与支出調整後の適応性バイオテクノロジー会社の純損失に起因すると定義する。以下の“調整後EBITDA”を参照して,調整後のEBITDAと最も直接比較可能なGAAP財務指標である適応バイオテクノロジー社の純損失との台帳,および調整後EBITDAの限界に関する検討を調べてみた。
2023年12月31日までと2022年12月31日までの年度比較
収入.収入
|
|
十二月三十一日までの年度 |
|
|
変わる |
|
|
収入のパーセントを占める |
|
|||||||||||||||
(百分率を除いて千単位) |
|
2023 |
|
|
2022 |
|
|
$ |
|
|
% |
|
|
2023 |
|
|
2022 |
|
||||||
免疫薬収入 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
サービス収入 |
|
$ |
24,959 |
|
|
$ |
31,777 |
|
|
$ |
(6,818 |
) |
|
(21)% |
|
|
|
|
|
|
|
|||
協力収入 |
|
|
42,578 |
|
|
|
66,387 |
|
|
|
(23,809 |
) |
|
|
(36 |
) |
|
|
|
|
|
|
||
免疫薬総収入 |
|
|
67,537 |
|
|
|
98,164 |
|
|
|
(30,627 |
) |
|
|
(31 |
) |
|
|
40 |
% |
|
|
53 |
% |
MRD収入 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
サービス収入 |
|
|
102,739 |
|
|
|
81,144 |
|
|
|
21,595 |
|
|
|
27 |
|
|
|
|
|
|
|
||
一里塚収入を監督する |
|
|
— |
|
|
|
6,000 |
|
|
|
(6,000 |
) |
|
|
(100 |
) |
|
|
|
|
|
|
||
MRD総収入 |
|
|
102,739 |
|
|
|
87,144 |
|
|
|
15,595 |
|
|
|
18 |
|
|
|
60 |
% |
|
|
47 |
% |
総収入 |
|
$ |
170,276 |
|
|
$ |
185,308 |
|
|
$ |
(15,032 |
) |
|
|
(8 |
) |
|
|
100 |
% |
|
|
100 |
% |
79
免疫薬物収入が3,060万ドル減少したのは,主に遺伝子テークプロトコルによる収入が2,020万ドル減少したためであり,これは協力費用の減少により,2023年5月に実現された規制マイルストーンに関連した820万ドルの収入によって一部が相殺されたためである。私たちのバイオ製薬顧客の収入も910万ドル減少しましたが、そのうち360万ドルは、2022年に2つの協力協定の開発活動を完了し、T-Detectの商業化を延期したことにより、私たちのT-Detect COVID臨床顧客の収入が140万ドル減少したためです。
MRD収入が1,560万ドル増加したのは,主に臨床顧客にclonoSEQを提供することによる収入が1,820万ドル増加したことと,研究者主導の臨床試験にMRD試料検査サービスを提供することによる収入が280万ドル増加したためである。これらの増加は、規制のマイルストーンを達成した後に私たちのいくつかの生物製薬顧客が確認した600万ドルの収入の減少によって相殺された。2023年12月31日までの1年間で,我々のclonoSEQ試験量は53%増加し,2022年12月31日現在の36,871試験から56,496試験に増加した。
収入コスト
|
|
十二月三十一日までの年度 |
|
|
変わる |
|
|
収入のパーセントを占める |
|
|||||||||||||||
(百分率を除いて千単位) |
|
2023 |
|
|
2022 |
|
|
$ |
|
|
% |
|
|
2023 |
|
|
2022 |
|
||||||
収入コスト |
|
$ |
75,553 |
|
|
$ |
57,909 |
|
|
$ |
17,644 |
|
|
|
30 |
% |
|
|
44 |
% |
|
|
31 |
% |
収入コストが1,760万ドル増加した主な原因は、研究開発サンプルと比べ、著者らの生産実験室処理収入サンプルの使用量は860万ドル増加し、主に実験室移転と合併活動による間接コストは510万ドル増加し、収入サンプル量の増加により材料コストは280万ドル増加し、輸送と処理費用は120万ドル増加した。
研究と開発
|
|
十二月三十一日までの年度 |
|
|
変わる |
|
収入のパーセントを占める |
|
||||||||||||||
(百分率を除いて千単位) |
|
2023 |
|
|
2022 |
|
|
$ |
|
|
% |
|
2023 |
|
|
2022 |
|
|||||
研究開発 |
|
$ |
122,117 |
|
|
$ |
141,756 |
|
|
$ |
(19,639 |
) |
|
(14)% |
|
|
72 |
% |
|
|
76 |
% |
以下の表では,期間中の研究と開発費用を費用別に分類した
|
|
十二月三十一日までの年度 |
|
|
|
|
||||||
(単位:千) |
|
2023 |
|
|
2022 |
|
|
変わる |
|
|||
研究開発材料と調達した生産実験室費用 |
|
$ |
20,243 |
|
|
$ |
43,706 |
|
|
$ |
(23,463 |
) |
人員費 |
|
|
74,385 |
|
|
|
68,177 |
|
|
|
6,208 |
|
割り当て可能な施設と情報技術費 |
|
|
11,617 |
|
|
|
8,856 |
|
|
|
2,761 |
|
ソフトウェアとクラウドサービス費用 |
|
|
3,394 |
|
|
|
2,678 |
|
|
|
716 |
|
減価償却その他の費用 |
|
|
12,478 |
|
|
|
18,339 |
|
|
|
(5,861 |
) |
合計する |
|
$ |
122,117 |
|
|
$ |
141,756 |
|
|
$ |
(19,639 |
) |
研究と開発費用が1,960万ドル減少した主な原因は,材料コストと分配された生産実験室費用が2,350万ドル減少したことであり,これは主にT−DetectとTCR抗原マップ開発活動への投資の減少,遺伝子技術会社との協力努力を含む薬物発見作業の投資減少によるものである。相談費用も310万ドル減少し,共同研究や臨床試験に関連する費用が250万ドル減少したことが減価償却やその他の費用が590万ドル減少した要因である。これらの減少額は,人員コスト620万ドルの増加,分配可能施設費用の280万ドルの増加,ソフトウェアとクラウドサービス費用の70万ドル増加によって部分的に相殺された。
販売とマーケティング
|
|
十二月三十一日までの年度 |
|
|
変わる |
|
収入のパーセントを占める |
|
||||||||||||||
(百分率を除いて千単位) |
|
2023 |
|
|
2022 |
|
|
$ |
|
|
% |
|
2023 |
|
|
2022 |
|
|||||
販売とマーケティング |
|
$ |
88,579 |
|
|
$ |
95,603 |
|
|
$ |
(7,024 |
) |
|
(7)% |
|
|
52 |
% |
|
|
52 |
% |
80
販売とマーケティング費用が700万ドル減少したのは主にマーケティング費用が500万ドル減少したためであり、これは主にclonoSEQのマーケティング活動の減少と私たちがT-Detectの商業化を延期し、人員コストが380万ドル減少し、コンサルタントコストが100万ドル減少したためである。これらの減少額は,計算機やソフトウェア費用の240万ドルの増加と建築,施設,減価償却に関する費用の80万ドル増加によって部分的に相殺された。
一般と行政
|
|
十二月三十一日までの年度 |
|
|
変わる |
|
収入のパーセントを占める |
|
||||||||||||||
(百分率を除いて千単位) |
|
2023 |
|
|
2022 |
|
|
$ |
|
|
% |
|
2023 |
|
|
2022 |
|
|||||
一般と行政 |
|
$ |
83,934 |
|
|
$ |
88,527 |
|
|
$ |
(4,593 |
) |
|
(5)% |
|
|
49 |
% |
|
|
48 |
% |
一般と行政費用が460万ドル減少した要因は,建築,施設,減価償却に関する費用が800万ドル減少したことであり,これは主に実験室合併活動を支援するためのオフィス空間転換,コンサルタント費用の200万ドルの削減,保険費用の160万ドルの減少によるものである。これらの減少額は、人件費270万ドルの増加によって部分的に相殺されたが、これは、株式ベースの給与増加、法律および会計費用の160万ドルの増加、コンピュータとソフトウェア費用の130万ドルの増加、第三者請求書のサービス料の120万ドルの増加によるものだ。
使用権および関連長期資産の減価
|
|
十二月三十一日までの年度 |
|
|
変わる |
|
収入のパーセントを占める |
|
||||||||||||||
(百分率を除いて千単位) |
|
2023 |
|
|
2022 |
|
|
$ |
|
|
% |
|
2023 |
|
|
2022 |
|
|||||
使用権および関連長期資産の減価 |
|
$ |
25,429 |
|
|
$ |
— |
|
|
$ |
25,429 |
|
|
*% |
|
|
15 |
% |
|
|
0 |
% |
*適用されない |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
使用権減値および関連長期資産支出が2,540万ドル増加したのは、2023年10月にワシントン州シアトルのいくつかの賃貸空間を空けることと、それによるレンタル改善の減少によるものである。
利息とその他の収入,純額
|
|
十二月三十一日までの年度 |
|
|
変わる |
|
||||||||||
(百分率を除いて千単位) |
|
2023 |
|
|
2022 |
|
|
$ |
|
|
% |
|
||||
利息とその他の収入,純額 |
|
$ |
15,531 |
|
|
$ |
4,056 |
|
|
$ |
11,475 |
|
|
|
283 |
% |
利息やその他の収入の純額が1,150万ドル増加したのは,主に我々が投資した現金と現金等価物および有価証券の金利や関連収益の増加により,純利息収入と投資償却が増加したためである。
利子支出
|
|
十二月三十一日までの年度 |
|
|
変わる |
|
||||||||||
(百分率を除いて千単位) |
|
2023 |
|
|
2022 |
|
|
$ |
|
|
% |
|
||||
利子支出 |
|
$ |
(13,800 |
) |
|
$ |
(4,238 |
) |
|
$ |
(9,562 |
) |
|
|
226 |
% |
利息支出が960万ドル増加したのは、2022年9月に締結された購入契約によるものだ。
調整後EBITDA
調整後のEBITDAは非GAAP財務指標であり、著者らはそれを利息とその他の収入、純額、利息支出、所得税(費用)収益、減価償却と償却費用、使用権と関連長期資産の減価コスト、再編費用と株式に基づく給与支出調整後の適応性バイオテクノロジー会社の純損失に起因すると定義する。
経営陣は、調整されたEBITDAを用いて、我々の業務の財務業績とわが業務戦略の有効性を評価します。調整されたEBITDAを提案したのは,アナリスト,投資家,他の関係者が調整後のEBITDAをよく用いて我々の業界の会社を評価し,報告期間別に一致した比較に役立つと信じているためである。また、コア経営実績を反映できない項目を排除しているため、我々の経営業績の傾向を強調するのに役立つと考えられる。
81
調整後のEBITDAは分析ツールとして限界があり,孤立的に考慮すべきではなく,GAAPによって報告されている我々の結果分析の代替品とすべきではない。私たちは将来的に調整後EBITDA列報と類似した費用が生じるかもしれない。特に、私たちは未来に株に基づいた有意義な報酬支出が生じると予想している。その他の制限には調整後のEBITDAは反映されていない:
また,調整後のEBITDAは,我々の業界や異業種の他社が使用している類似名称の測定基準と比較できない可能性がある。
以下は、本報告で述べた期間が最も直接比較可能なGAAP財務指標である適応バイオテクノロジー社の純損失と調整後のEBITDAの入金(単位:千)である
|
|
十二月三十一日までの年度 |
|
|||||||||
|
|
2023 |
|
|
2022 |
|
|
2021 |
|
|||
適応バイオテクノロジー会社の純損失によるものです |
|
$ |
(225,250 |
) |
|
$ |
(200,191 |
) |
|
$ |
(207,279 |
) |
利息とその他の収入,純額 |
|
|
(15,531 |
) |
|
|
(4,056 |
) |
|
|
(1,668 |
) |
利子支出(1) |
|
|
13,800 |
|
|
|
4,238 |
|
|
|
— |
|
減価償却および償却費用 |
|
|
22,231 |
|
|
|
20,920 |
|
|
|
13,953 |
|
使用権および関連長期資産の減価(2) |
|
|
25,429 |
|
|
|
— |
|
|
|
— |
|
再編成費用(3) |
|
|
— |
|
|
|
2,023 |
|
|
|
— |
|
株式ベースの給与費用(4) |
|
|
62,908 |
|
|
|
55,477 |
|
|
|
43,251 |
|
調整後EBITDA |
|
$ |
(116,413 |
) |
|
$ |
(121,589 |
) |
|
$ |
(151,743 |
) |
(1)私たちの収入利息負債に関するコストと、関連繰延発行コストの償却に関する非現金利息コストを代表します。付記11を参照収入権益購入協定“調達契約”の詳細を理解するために、本年度報告書の他の部分がForm 10-K形式で提供されている連結財務諸表を参照してください。
(2)使用権と関連する長期資産の減価コストを代表する。付記10を参照賃貸借証書本年度報告書の他の場所のForm 10-K連結財務諸表の付記を参照して、減価費用に関する詳細を取得してください。
(3)再構成活動で確認された費用のことです。付記16を参照再編成する我々の再構成費用の詳細については、本年度報告(Form 10-K)に添付されている連結財務諸表付記を参照されたい。
(4)株式オプション、制限株式単位、および市場に基づく制限株式単位報酬に関する株式ベース報酬支出を示す。付記14を参照持分激励計画株式ベースの給与支出の詳細を理解するために、本年度報告書10-K表の他の部分に添付されている総合財務諸表付記を参照してください。
流動性と資本資源
我々は設立以来赤字を続けており,設立以来2018年12月31日までの年度と,2020年,2021年,2022年,2023年12月31日までの年度で,我々の運営には負のキャッシュフローが生じている。2023年12月31日現在、私たちの累計赤字は11億ドルです。
これまで、私たちの運営資金は主に転換可能な優先株と普通株の売却、次いで購入合意の収入と収益から来ていた。2022年9月に締結された購入契約によると、発行コストを差し引いた後、1億244億ドルの現金純収益を受け取りました。その後の分割払いで最大1.25億ドルを得る権利もあります。具体的には、(I)2025年9月12日までに行うことを要求すれば、7500万ドルを獲得します。(Ii)2025年9月12日に行われるいくつかの許可買収に関連することを要求すれば、5000万ドルを獲得し、それぞれの場合はある資金条件によって制限されます。2023年12月31日現在、私たちは3.464億ドルの現金、現金等価物、および有価証券を持っている。
82
私たちは、私たちの既存の現金、現金等価物、および有価証券が、少なくとも今後12ヶ月の運営費用および資本支出需要を支払うのに十分であると信じている。私たちは、より多くの資本を集めて、私たちの業務を拡大し、戦略投資を行い、融資機会やその他の理由を利用することを考えるかもしれない。
もし吾等の利用可能な現金、現金等価物及び有価証券残高及び期待キャッシュフローが吾等の流動資金需要を満たすのに十分でない場合、吾等は購入合意に基づいて追加分割払いを要求し、追加株式又は転換可能な債務証券の売却を求めることができ、クレジット手配又は他の形態の第三者融資又は他の債務融資を求めることができる。株式および転換可能な債務証券の売却は、私たちの株主の権益を希釈する可能性があり、優先持分証券または転換可能債券については、これらの証券は、私たちの普通株よりも優先的な権利、優遇、または特権を提供する可能性がある。クレジット協定によって発行または借金された債務証券の条項は、私たちの業務に重大な制限を与える可能性があります。この追加的な資本は合理的な条項で得られないかもしれないし、根本的にそうではないかもしれない。
私たちは主に手元にある現金、現金等価物、有価証券を利用して、薬物発見に関連する持続的な研究と開発活動、clonoSEQに関連する商業およびマーケティング活動、および実験室運営の簡略化に対する私たちの持続的な投資に資金を提供する予定だ。即時需要を超えた現金は主に保証と流動性のために私たちの投資政策に基づいて投資されるだろう。現在、私たちの資金は、米国政府国債や機関証券、商業手形、社債を含む通貨市場基金と有価証券の形で保有されている。
私たちの収入は短期的に変動する可能性がありますが、長期的には、現在と未来の製品やサービスの収入が増加することが予想されます。したがって、私たちは私たちの売掛金と在庫残高が増加すると予想する。様々な理由で、マイルストーンのトリガの時間とこれらのマイルストーンの関連支払い、および遺伝子テークプロトコルに従って受信されたプリペイドによって生じる収入の減少、および臨床顧客からの収入の増加を含む、私たちの売掛金レベルが私たちの収入に対して変動する可能性があり、これは、前金ではなく、より多くの借金請求書をもたらす可能性がある。売掛金や在庫のいずれの増加も、売掛金や売掛金の増加によって完全に相殺されない可能性があり、より多くの運転資金需要を招く可能性がある。
契約義務
2023年12月31日現在、私たちの契約義務には、ワシントン州シアトルとカリフォルニア州サンフランシスコ南部のオフィスと実験室空間での私たちの最低の約束と、ワシントン州ボセルの倉庫でのレンタル義務が含まれています。付記10を参照賃貸借証書本年度報告書10-K表の他の部分に添付されている連結財務諸表付記を参照して、これらのレンタル債務に関連する現金支払い時間を含むより多くの情報を理解してください。私たちの賃貸契約について、私たちは私たちの既存の金融機関と210万ドルの既存の信用状を締結した。
また、購入プロトコルにより、買い手は収入ベースの適用支払率に応じて吾等から収入利息を受け取る権利がある。1回目の支払いのみを支払った場合、適用される支払率は四半期収入ベースの5%となる。1回目の支払いと2回目の支払いの両方が支払われた場合、適用される支払率は四半期収入ベースの8%となる必要がある。1回目の支払い、2回目の支払い、および3回目の支払いがともに支払われた場合、収入利息に適用される支払率は四半期収入ベースの10%となるべきだ。所得利息支払いは各会計四半期終了後45日以内に四半期ごとに支払わなければなりません。OrbiMedが2028年9月12日までに累積買い手支払いに等しいまたはそれ以上の収入利息支払い総額を受け取っていない場合、収入金利は1つの金利に引き上げられるべきであり、私たちの累積収入基数に遡ると、収入利息支払いはすべての累積買い手支払いの合計に等しいことになる。OrbiMedは、リターン上限を受信するまで、リターン上限の金額が2032年9月12日までに全額返済されていない限り、100%の収入利息支払いを得る権利があり、この場合、リターン上限は、累積買い手支払いの175%に増加しなければならない。予想収入が私たちの最初の見積もりと比較して変化するにつれて、債務金額と支払い時間が変化する可能性がある。付記11を参照収入権益購入協定本年度報告書の他のタブ10-Kに添付されている連結財務諸表の付記を参照して、より多くの情報を理解してください。
私たちはまた実験室材料サプライヤーに対して最低の約束を持っていて、通常1年以内に履行して、ソフトウェアとサービス許可承諾、通常1~3年以内に履行して、印税承諾を履行します。
83
キャッシュフロー
次の表は、2023年12月31日と2022年12月31日までの年間の現金用途と出所(単位:千)をまとめています
|
|
十二月三十一日までの年度 |
|
|||||
|
|
2023 |
|
|
2022 |
|
||
経営活動のための現金純額 |
|
$ |
(156,324 |
) |
|
$ |
(183,945 |
) |
投資活動が提供する現金純額 |
|
|
129,647 |
|
|
|
2,905 |
|
融資活動が提供する現金純額 |
|
|
2,245 |
|
|
|
132,265 |
|
経営活動
2023年12月31日までの年間で、経営活動に用いられる現金は1.563億ドルであり、主な原因は純損失2.253億ドル及び運営資産及び負債純変動4620万ドルであるが、株式ベースの非現金給与6,290万ドル、使用権及び関連長期資産の非現金減価2,540万ドル、非現金減価及び償却1,300万ドル、非現金リース支出690万ドル、購入契約に関する非現金利息支出530万ドル及び在庫備蓄支出140万ドルが部分的に相殺されている。営業資産と負債の純変化は主に繰延収入が2930万ドル減少したためであり、主に遺伝子テイク協定から確認された収入、経営リース使用権資産と負債が870万ドル減少し、売掛金と売掛金が540万ドル減少し、在庫が280万ドル増加し、前払い費用やその他の流動資産が190万ドル増加したためであり、これは主にプリペイドソフトウェア費用の増加によるものである。このような変化は売掛金の純額が200万ドル減少した部分によって相殺される。
2022年12月31日までの年間で、経営活動で使用されている現金は1兆839億ドルで、主な原因は純損失200.4百万ドルおよび営業資産および負債純変動7150万ドルであるが、株式ベースの非現金給与5550万ドル、非現金償却および償却2170万ドル、非現金リース支出720万ドル、研究開発在庫備蓄費用260万ドルおよび購入契約に関する非現金利息支出100万ドルが部分的に相殺されている。私たちの営業資産と負債の純変化は主に繰延収入が5650万ドル減少したためであり、主に遺伝子テークプロトコルから確認された収入、売掛金の増加、純額は2260万ドルであり、その中の710万ドルはclonoSEQに関連する売掛金の増加によるものであり、残りの増加は主にバイオ製薬顧客の売掛金の増加と、運営リース資産と負債の410万ドルの減少によるものである。売掛金と売掛金は710万ドル増加し、前払い費用とその他の流動資産は360万ドル減少し、在庫は80万ドル減少し、これらの変化を部分的に相殺した。
投資活動
2023年12月31日までの年間で、投資活動が提供する現金は1兆296億ドルで、これは主に5.699億ドルの有価証券の満期収益によるものだが、一部は4.296億ドルの有価証券の購入と1070万ドルの不動産や設備の購入によって相殺されている。
2022年12月31日までの1年間に、投資活動が提供した現金は290万ドルであり、これは主に2.98億ドルの有価証券満期収益があったが、2.788億ドルの有価証券購入および1630万ドルの不動産·設備購入部分がこの収入を相殺したためである。
融資活動
融資活動が提供する現金は2023年12月31日までの年間220万ドルであり、これは株式オプション行使の収益によるものである。
2022年12月31日までの1年間に、融資活動が提供した現金は1兆323億ドルであり、これは主に発行コストを差し引いた購入合意収益1.244億ドルと、株式オプションを行使する収益790万ドルによるものである。
84
純営業損失が繰り越す
第382条及び同様の国が定める所有権変更制限により、我々のNOL繰越及び信用の使用はかなりの年間制限を受ける可能性がある。年間制限はNOL繰越や使用前の信用満期を招く可能性がある。もし所有権が変化すれば、私たちがNOL繰り越しと信用を利用する能力は制限される可能性がある。第382条の2023年6月30日までの所有権変更の分析を完了し、制限をトリガする可能性のある変更を監視していきます。この分析に基づいて、私たちは連邦NOLの使用が永久的に制限されないと予想する。TCJAによると,2018年および今後数年に発生する連邦NOLは無期限繰り越しが可能であるが,このような連邦NOLの控除は年次制限を受けている。2018年前に生まれたNOLは20年に及ぶ資格を持っています。入手可能な客観的証拠によると、経営陣は、2023年12月31日現在、繰延税純資産が現金化できない可能性があると確定した。そこで、経営陣は2023年12月31日までの繰延税項純資産に全額推定手当を適用した。
重要な会計政策と試算
当社は公認会計原則に基づいて総合財務諸表を作成しました。これらの連結財務諸表を作成するには、連結財務諸表の日付の資産、負債、および関連開示の報告金額、および報告期間内に記録された収入および費用に影響を及ぼす推定、仮説、判断を行う必要がある。私たちは持続的な基礎の上で私たちの推定と判断を評価する。私たちの見積もりは歴史的経験と当時の状況で合理的だと思う他の関連仮定に基づいています。複数の分野に使用されると推定され、いくつかの履行責任に限定されないが、これまでの進捗推定およびいくつかの顧客と締結された契約の取引価格、購入プロトコルの利息の計算、所得税の計上(関連準備金を含む)、営業権減値分析および長期資産の回収および減値などが含まれる。これらの推定は通常複雑な問題に関連し、判断する必要があり、歴史結果の分析と未来の傾向の予測に関連し、解決するには長い時間を要するかもしれず、時期によって異なる可能性がある。実際の結果は経営陣の見積もりと大きく異なるかもしれない。
私たちの重要な会計政策は付記2にもっと詳しく説明されていますが重大会計政策本年度報告(Form 10−K)の他の部分に添付されている連結財務諸表付記では、以下の会計政策が連結財務諸表の作成に用いる判断と見積もりに重要であると考えられる。
収入確認
私たちの収入計画には、将来のサービス表現の前払いが含まれている可能性があり、これには固定的な考慮もあれば、可変的な考慮もある。払い戻し不可能な前期費用と関連開発サービスの資金は通常固定対価格とみなされ、マイルストーン支払いは可変対価格として決定される。
これらの合意の下での義務を履行する際には、確認すべき収入金額を決定するステップ、(1)1つ以上の契約を決定するステップ、(2)契約背景で異なるか否かを含む約束された貨物またはサービスが履行義務であるかどうかを決定するステップ、(3)可変対価格の制限を含む取引価格を測定するステップ、(4)推定販売価格に基づいて取引価格を履行義務に割り当てるステップ、および(5)(または)各履行義務を満たす場合に収入を確認するステップを実行する。
履行義務は、契約において異なる商品やサービスを顧客に移転する約束であり、会計基準編纂(ASC)テーマ606における課金単位である顧客と契約を結んだ収入。私たちのバイオ製薬顧客に対して、私たちの業績義務にはシークエンシングサービスと規制提出と承認手続きに関連するサービスが含まれている可能性があります。重大な管理判断は,(1)取引価格の計量を決定するためのものであり,可変対価格の制限,(2)取引価格の履行義務への分配,および(3)収入とこれまでの進捗度を確認する適切な投入や産出方法がある。
私たちは制限されない推定可変対価金額を取引価格に計上します。取引価格に含まれる金額は制限されず,確認された累積収入は大きな逆転が生じない可能性が高いからである.その後報告期間ごとに終了すると,吾らは取引価格に含まれる推定変動の価格や何らかの関連制限を再評価し,必要に応じて全体の取引価格の見積りを調整する.
85
進捗の測定基準を選択するために、顧客のサンプルの推定に基づく可能性があり、あるいは顧客と我々の予想開発時間フレームワークによる業績周期の内部推定に基づく可能性がある業績周期の予想を考慮した。著者らと遺伝子テークの協力において、著者らは比例業績モデルを用いて進展程度を推定し、このモデルは1種の入力法を用いて、この方法は共有製品と個性化製品経路を追求するために産生した研究開発仕事の総推定コストに基づいている。これらの推定は我々の内部推定と開発スケジュールに基づいており、2つの製品経路の潜在的な結果、遺伝子テークによる決定、監督フィードバック、あるいは他の現在未知の要素に基づいて修正される可能性がある。私たちは、これ以上可変考慮要素を制限しないかどうかを含めて、進行度の予想を定期的に検討し、何か変化があれば、累積追跡法を用いて収入を確認します。
我々が発注医にclonoSEQ報告を提供するプロトコルについては,clonoSEQ報告を交付する義務を決定した。
我々の商業支払者との手配については,それぞれの支払者の支払いは精算料率や患者責任によって異なる可能性がある。したがって,取引価格は可変であり,取引価格の見積りを納入時の収入として記録するが,可変対価格に制限されると考えられる.取引価格の推定は,異なる支払者の履歴と期待返済率に基づいており,これらの返済率は以降の期間が監視され,必要に応じて実際の入金経験に基づいて調整される。
所得利子負債、純額、関連計上利息
我々が2022年9月にOrbiMedと締結した購入契約に関する収入利息負債残高は、総合貸借対照表に未償却発行コストを差し引いて列報する。私たちは有効金利法を使って私たちの関連利息支出を推定する。私たちが計算した実際の金利は私たちの関連債務を予想された返済期間内にゼロに償却するだろう。合意期間内に、実際の金利は、予測された公認会計原則収入の変化を含むいくつかの要因によって変化する可能性がある。私たちは展望的な方法を利用して、実現された収入と予想される収入に基づいて、四半期ごとに有効金利を評価する。将来の収入とそれによって生じる収入の利息支払いの推定は、人口、浸透率、成功の可能性、販売価格などを含む主要な仮定に基づいている。収入の大幅な増加または減少または時間の変化は、私たちの利息支出と返済期限に影響を与えると予測される。2023年12月31日までに10%を想定しています四半期収入の増加は予想される年度の利息支出に実質的な変化を招くことはないと予想される。
商誉
営業権とは、購入価格が公正価値で計量された企業合併で取得した識別可能な資産と負担する負債純額を超える部分である。私たちは毎年10月1日に減価営業権を評価し、任意のトリガイベントが発生した場合、または潜在的な減値を示す可能性がある状況が実質的に変化した場合に評価を行う。
私たちはまず定性的要素を評価することによって、私たちの報告単位の公正価値がその帳簿価値よりも低い可能性があるかどうかを決定するために、営業権の減価を評価する。私たちは、マクロ経済状況、私たちが経営している市場と業界、コスト要素、全体財務表現、および他の関連エンティティ特定のイベントのようないくつかの定性的要素を評価して、減値を示す可能性のある負の傾向やイベントが存在するかどうかを決定する。この分析中の主な仮定は業界と法規の変化、収入増加とキャッシュフローの傾向を含む、私たちの製品とサービスに対する期待需要を含む。これらの仮定は私たちの歴史的業績と経営陣の予測結果に基づいて決定された。経営陣の予測結果の見積りは合理的と考えられる仮説に基づいているが,これらの仮説自体は不確実で予測不可能であるため,実際の結果は見積り結果とは異なる可能性がある.もし私たちが私たちの報告機関の公正価値がその帳簿価値よりも低い可能性が高いと判断したら、もし私たちが定性的評価を迂回することを選択した場合、私たちは商業権減価定量化テストを行うつもりだ。減値が存在する場合、営業権の帳簿価値は、総合経営報告書に記録された減値費用によって公正価値に低減される。今まで、私たちはどんな営業権の減価も確認していない。
長期資産の回収·減価
我々は毎年,イベントや状況がある資産グループ別の帳票金額が回収できない可能性があることを示す場合には,長期資産の減値状況を検討する.回収可能性をテストするために,資産グループの帳簿価値と予想される将来の未割引キャッシュフローを比較した。帳簿金額が回収できないことが発見された場合、資産グループの公正価値を評価します。我々は利得法を用いて公正価値を計測し,経営陣にキャッシュフロー予測と割引率の推定が求められる.資産グループの帳票金額がその公正価値を超える程度は、確認すべき減価コストを表す。減価損失が発生すると、資産グループの用途に応じて総合経営報告書に分類され、それ自身の財務諸表項目に単独で記載されていなければ。2023年12月31日までの年間で、ある使用権や賃貸関連資産の改善に関する減価支出2540万ドルを確認した。
86
最近の会計公告
注2を参照重大会計政策本年度報告書の他のタブ10-Kに添付されている連結財務諸表の付記を参照して、より多くの情報を理解してください。
第七A項。数量化と高質VE市場リスクの開示について
金利リスク
私たちは主に私たちの現金と現金等価物および有価証券に関連する金利変化の市場リスクに直面している。私たちは2023年12月31日と2022年12月31日まで、それぞれ6510万ドルと9000万ドルの現金と現金等価物を持ち、主に現金預金と通貨市場基金の形で保有している。2023年12月31日現在、米国政府国債と機関証券、商業手形、社債を含む2兆813億ドルの短期有価証券を持っている。2022年12月31日現在、米国政府国債、社債、商業手形を含む4.082億ドルの短期有価証券を持っている。私たちの市場リスクに対する主な開口は利息収入の敏感性であり、これはアメリカの全体的な金利レベルの変化の影響を受ける。2023年12月31日まで、金利が100ベーシスポイント上昇すると仮定すると、証券を売却できる公正価値は120万ドル低下し、2022年12月31日現在、私たちの売却可能な証券の公正価値は150万ドル低下する。この推定は、金利が変化したときの時価変化を測る敏感なモデルに基づいている。このような損失は私たちが満期前に投資を売却する時にのみ達成されるだろう。私たちは取引目的で投資しないし、派生金融商品を使って私たちの金利リスクを管理していません。
87
プロジェクト8.FIN財務諸表と補足データ
適応バイオテクノロジー会社は
連結財務諸表索引
2023年と2022年12月31日まで
2023年12月31日まで,2022年および2021年12月31日まで年度
独立公認会計士事務所報告(PCAOB ID: |
89 |
合併貸借対照表 |
91 |
連結業務報告書 |
92 |
合併全面損失表 |
93 |
合併株主権益報告書 |
94 |
統合現金フロー表 |
95 |
連結財務諸表付記 |
96 |
88
“独立公認会計士報告書”アイレード会計士事務所
適応バイオテクノロジー会社の株主と取締役会へ
財務諸表のいくつかの見方
添付の適応バイオテクノロジー会社(当社)が2023年12月31日まで,2023年12月31日と2022年12月31日までの総合貸借対照表,2023年12月31日までの各年度の関連総合経営表,全面赤字,株主権益とキャッシュフローおよび関連付記(総称して総合財務諸表と呼ぶ)を監査した。総合財務諸表は、すべての重要な点で、2023年12月31日、2023年12月31日、2022年12月31日までの会社の財務状況、および2023年12月31日までの3年度の経営結果とキャッシュフローを公平に反映しており、米国公認会計原則に適合していると考えられる。
また、米国上場企業会計監督委員会(PCAOB)の基準に基づき、テレデビル委員会協賛組織委員会が発表した“内部統制-総合枠組み(2013枠組み)”で確立された基準に基づいて、2023年12月31日までの財務報告内部統制を監査し、2024年2月29日に発表した報告書について保留意見を発表した。
意見の基礎
これらの財務諸表は会社の経営陣が責任を負う。私たちの責任は私たちの監査に基づいて会社の財務諸表に意見を発表することです。私たちはPCAOBに登録されている公共会計士事務所で、アメリカ連邦証券法およびアメリカ証券取引委員会とPCAOBの適用規則と法規に基づいて、私たちは会社と独立しなければなりません。
私たちはPCAOBの基準に従って監査を行っている。これらの基準は、財務諸表に重大な誤報がないかどうかに関する合理的な保証を得るために、エラーによるものであっても不正であっても、監査を計画し、実行することを要求する。我々の監査には、財務諸表の重大な誤報リスクを評価するプログラム、エラーによるものであれ詐欺であっても、これらのリスクに対応するプログラムを実行することが含まれています。これらの手続きは、財務諸表中の金額および開示に関連する証拠をテストに基づいて検討することを含む。我々の監査には、経営陣が使用する会計原則の評価と重大な見積もり、財務諸表の全体列報を評価することも含まれています。私たちは私たちの監査が私たちの観点に合理的な基礎を提供すると信じている。
重要な監査事項
以下に述べる重要な監査事項とは、監査委員会に伝達または要求が監査委員会に伝達された当期財務諸表監査によって生じる事項である:(1)財務諸表に対して重大な意義を有する勘定または開示に関するものであり、(2)特に挑戦的で主観的または複雑な判断に関するものである。重要監査事項の伝達は、総合財務諸表に対する私たちの全体的な意見をいかなる方法でも変えることはなく、以下の重要な監査事項を伝達することによって、重要な監査事項またはそれに関連する勘定または開示について個別の意見を提供することはない。
89
|
遺伝子テークプロトコル |
関係事項の記述 |
総合財務諸表付記3に記載されているように、遺伝子テイクプロトコル収入推定は、発効日から約9年の間に確認される。払い戻しできない3.1億ドルの費用は,発生した費用の研究·開発作業に対する総見積もり費用に基づいて比例業績モデルを採用し,1つの投入方法で確認した。2023年12月31日までの年間収入総額は4,260万ドル,2023年12月31日までの繰延収入総額は5,470万ドルであることが確認された。 監査管理層は完成時に予想される研究開発総コストの推定は複雑であり、製品経路、開発時間と経路及び商業化決定の最終進展に不確定性が存在するため、判断する必要があり、これらはすべて遺伝子テークによって制御される。 |
私たちが監査でどのようにこの問題を解決したのか |
著者らは遺伝子泰克が連合委員会を通じて伝達した重大な決定及びそれによる協力研究開発仕事の総コストに対するいかなる影響に基づいて、会社のフロー制御の操作有効性に対して理解、評価とテストを行い、協力進展と未来の可能な発展経路を評価した。 予想される研究開発総コストの見積もりをテストするために、会計および会社の協力マネージャーと開催された四半期会議を観察し、カスタマイズ製品経路の連携状態と将来の開発を検討し、開発経路の任意の変化を調査する監査プログラムを実行した。また、共同委員会の議事録を含むスケジュール全体の進展と現状を確認するための補助文書を検討した。 |
/s/
われわれは2015年以来当社の監査役を務めてきた
2024年2月29日
90
適応バイオテクノロジー会社は
合併残高シーツ
(単位は千で、1株当たりおよび1株当たりの金額は含まれていない)
|
|
十二月三十一日 |
|
|||||
|
|
2023 |
|
|
2022 |
|
||
資産 |
|
|
|
|
|
|
||
流動資産 |
|
|
|
|
|
|
||
現金と現金等価物 |
|
$ |
|
|
$ |
|
||
短期有価証券(償却コストは#ドル |
|
|
|
|
|
|
||
売掛金純額 |
|
|
|
|
|
|
||
在庫品 |
|
|
|
|
|
|
||
前払い費用と他の流動資産 |
|
|
|
|
|
|
||
流動資産総額 |
|
|
|
|
|
|
||
長期資産 |
|
|
|
|
|
|
||
財産と設備、純額 |
|
|
|
|
|
|
||
経営的リース使用権資産 |
|
|
|
|
|
|
||
制限現金 |
|
|
|
|
|
|
||
無形資産、純額 |
|
|
|
|
|
|
||
商誉 |
|
|
|
|
|
|
||
その他の資産 |
|
|
|
|
|
|
||
総資産 |
|
$ |
|
|
$ |
|
||
負債と株主権益 |
|
|
|
|
|
|
||
流動負債 |
|
|
|
|
|
|
||
売掛金 |
|
$ |
|
|
$ |
|
||
負債を計算すべきである |
|
|
|
|
|
|
||
報酬と福祉に計上すべきである |
|
|
|
|
|
|
||
賃貸負債の当期部分を経営する |
|
|
|
|
|
|
||
繰延収入の当期分 |
|
|
|
|
|
|
||
流動負債総額 |
|
|
|
|
|
|
||
長期負債 |
|
|
|
|
|
|
||
経営賃貸負債から流動分を差し引く |
|
|
|
|
|
|
||
繰延収入,当期分を差し引く |
|
|
|
|
|
|
||
利子負債純額を収入 |
|
|
|
|
|
|
||
総負債 |
|
|
|
|
|
|
||
*(注12) |
|
|
|
|
|
|
||
株主権益 |
|
|
|
|
|
|
||
優先株:$ |
|
|
|
|
|
|
||
普通株:$ |
|
|
|
|
|
|
||
追加実収資本 |
|
|
|
|
|
|
||
他の総合損益を累計する |
|
|
|
|
|
( |
) |
|
赤字を累計する |
|
|
( |
) |
|
|
( |
) |
完全適応バイオテクノロジー会社の株主権益 |
|
|
|
|
|
|
||
非持株権益 |
|
|
( |
) |
|
|
( |
) |
株主権益総額 |
|
|
|
|
|
|
||
総負債と株主権益 |
|
$ |
|
|
$ |
|
||
付記はこれらの連結財務諸表の構成要素である。
91
適応バイオテクノロジー会社は
統合報告書またはF運営
(単位は千で、1株当たりおよび1株当たりの金額は含まれていない)
|
|
十二月三十一日までの年度 |
|
|||||||||
|
|
2023 |
|
|
2022 |
|
|
2021 |
|
|||
収入.収入 |
|
$ |
|
|
$ |
|
|
$ |
|
|||
運営費 |
|
|
|
|
|
|
|
|
|
|||
収入コスト |
|
|
|
|
|
|
|
|
|
|||
研究開発 |
|
|
|
|
|
|
|
|
|
|||
販売とマーケティング |
|
|
|
|
|
|
|
|
|
|||
一般と行政 |
|
|
|
|
|
|
|
|
|
|||
無形資産の償却 |
|
|
|
|
|
|
|
|
|
|||
使用権および関連長期資産の減価 |
|
|
|
|
|
— |
|
|
|
— |
|
|
総運営費 |
|
|
|
|
|
|
|
|
|
|||
運営損失 |
|
|
( |
) |
|
|
( |
) |
|
|
( |
) |
利息とその他の収入,純額 |
|
|
|
|
|
|
|
|
|
|||
利子支出 |
|
|
( |
) |
|
|
( |
) |
|
|
— |
|
純損失 |
|
|
( |
) |
|
|
( |
) |
|
|
( |
) |
新規:非持株権益の純損失に起因する |
|
|
|
|
|
|
|
|
|
|||
適応バイオテクノロジー会社の純損失によるものです |
|
$ |
( |
) |
|
$ |
( |
) |
|
$ |
( |
) |
適応バイオテクノロジー会社の普通株株主は1株当たり純損失を占めなければならず、基本と希釈後 |
|
$ |
( |
) |
|
$ |
( |
) |
|
$ |
( |
) |
適応バイオテクノロジー会社の普通株主に起因する1株当たり純損失の加重平均株式、基本株主及び希釈株主の計算に用いる |
|
|
|
|
|
|
|
|
|
|||
付記はこれらの連結財務諸表の構成要素である。
92
適応バイオテクノロジー会社は
会社合併報告書総合損失
(単位:千)
|
|
十二月三十一日までの年度 |
|
|||||||||
|
|
2023 |
|
|
2022 |
|
|
2021 |
|
|||
純損失 |
|
$ |
( |
) |
|
$ |
( |
) |
|
$ |
( |
) |
その他全面収益(赤字) |
|
|
|
|
|
|
|
|
|
|||
投資は損益変動を実現していない |
|
|
|
|
|
( |
) |
|
|
( |
) |
|
総合損失 |
|
|
( |
) |
|
|
( |
) |
|
|
( |
) |
新規:非持株権益の全面的な損失に帰することができる |
|
|
|
|
|
|
|
|
|
|||
適応バイオテクノロジー会社の全面的な損失に起因しています |
|
$ |
( |
) |
|
$ |
( |
) |
|
$ |
( |
) |
付記はこれらの連結財務諸表の構成要素である。
93
適応バイオテクノロジー会社は
合併報告書株主権益
(単位は千で、シェアは含まれていない)
|
|
普通株 |
|
|
その他の内容 |
|
|
積算 |
|
|
積算 |
|
|
非制御性 |
|
|
合計する |
|
||||||||||
|
|
株 |
|
|
金額 |
|
|
資本 |
|
|
(損を)得る |
|
|
赤字.赤字 |
|
|
利子 |
|
|
権益 |
|
|||||||
2020年12月31日残高 |
|
|
|
|
$ |
|
|
$ |
|
|
$ |
|
|
$ |
( |
) |
|
$ |
— |
|
|
$ |
|
|||||
普通株式承認証の行使時に普通株式を発行する |
|
|
|
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
株式オプションを行使するときは現金と引き換えに普通株を発行する |
|
|
|
|
|
— |
|
|
|
|
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
|
|||
株式単位の帰属を制限する |
|
|
|
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
株式ベースの報酬 |
|
|
— |
|
|
|
— |
|
|
|
|
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
|
||
デジタルバイオテクノロジー会社の出資です |
|
|
— |
|
|
|
— |
|
|
|
|
|
|
— |
|
|
|
— |
|
|
|
|
|
|
|
|||
その他総合損失 |
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
( |
) |
|
|
— |
|
|
|
— |
|
|
|
( |
) |
純損失 |
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
( |
) |
|
|
( |
) |
|
|
( |
) |
2021年12月31日の残高 |
|
|
|
|
|
|
|
|
|
|
|
( |
) |
|
|
( |
) |
|
|
|
|
|
|
|||||
株式オプションを行使するときは現金と引き換えに普通株を発行する |
|
|
|
|
|
— |
|
|
|
|
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
|
|||
株式単位の帰属を制限する |
|
|
|
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
株式ベースの報酬 |
|
|
— |
|
|
|
— |
|
|
|
|
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
|
||
その他総合損失 |
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
( |
) |
|
|
— |
|
|
|
— |
|
|
|
( |
) |
純損失 |
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
( |
) |
|
|
( |
) |
|
|
( |
) |
2022年12月31日の残高 |
|
|
|
|
|
|
|
|
|
|
|
( |
) |
|
|
( |
) |
|
|
( |
) |
|
|
|
||||
株式オプションを行使するときは現金と引き換えに普通株を発行する |
|
|
|
|
|
— |
|
|
|
|
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
|
|||
株式単位の帰属を制限する |
|
|
|
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
株式ベースの報酬 |
|
|
— |
|
|
|
— |
|
|
|
|
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
|
||
その他総合収益 |
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
|
|
|
— |
|
|
|
— |
|
|
|
|
||
純損失 |
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
( |
) |
|
|
( |
) |
|
|
( |
) |
2023年12月31日の残高 |
|
|
|
|
$ |
|
|
$ |
|
|
$ |
|
|
$ |
( |
) |
|
$ |
( |
) |
|
$ |
|
|||||
付記はこれらの連結財務諸表の構成要素である。
94
適応バイオテクノロジー会社は
統合報告書またはFキャッシュフロー
(単位:千)
|
|
十二月三十一日までの年度 |
|
|||||||||
|
|
2023 |
|
|
2022 |
|
|
2021 |
|
|||
経営活動 |
|
|
|
|
|
|
|
|
|
|||
純損失 |
|
$ |
( |
) |
|
$ |
( |
) |
|
$ |
( |
) |
純損失と経営活動で使用した現金純額の調整 |
|
|
|
|
|
|
|
|
|
|||
減価償却費用 |
|
|
|
|
|
|
|
|
|
|||
非現金レンタル費用 |
|
|
|
|
|
|
|
|
|
|||
株式ベースの給与費用 |
|
|
|
|
|
|
|
|
|
|||
無形資産の償却 |
|
|
|
|
|
|
|
|
|
|||
投資償却 |
|
|
( |
) |
|
|
|
|
|
|
||
使用権および関連長期資産の減価 |
|
|
|
|
|
— |
|
|
|
— |
|
|
在庫備蓄 |
|
|
|
|
|
|
|
|
— |
|
||
非現金利子支出 |
|
|
|
|
|
|
|
|
— |
|
||
他にも |
|
|
|
|
|
( |
) |
|
|
( |
) |
|
経営性資産と負債の変動 |
|
|
|
|
|
|
|
|
|
|||
売掛金純額 |
|
|
|
|
|
( |
) |
|
|
( |
) |
|
在庫品 |
|
|
( |
) |
|
|
|
|
|
( |
) |
|
前払い費用と他の流動資産 |
|
|
( |
) |
|
|
|
|
|
|
||
売掛金と売掛金 |
|
|
( |
) |
|
|
|
|
|
|
||
経営的リース使用権資産負債 |
|
|
( |
) |
|
|
( |
) |
|
|
|
|
収入を繰り越す |
|
|
( |
) |
|
|
( |
) |
|
|
( |
) |
他にも |
|
|
( |
) |
|
|
|
|
|
( |
) |
|
経営活動のための現金純額 |
|
|
( |
) |
|
|
( |
) |
|
|
( |
) |
投資活動 |
|
|
|
|
|
|
|
|
|
|||
財産と設備を購入する |
|
|
( |
) |
|
|
( |
) |
|
|
( |
) |
有価証券を購入する |
|
|
( |
) |
|
|
( |
) |
|
|
( |
) |
有価証券満期日収益 |
|
|
|
|
|
|
|
|
|
|||
投資活動が提供する現金純額 |
|
|
|
|
|
|
|
|
|
|||
融資活動 |
|
|
|
|
|
|
|
|
|
|||
株式オプションを行使して得られる収益 |
|
|
|
|
|
|
|
|
|
|||
利子購入契約の収益を収入し、発行コストを差し引く |
|
|
— |
|
|
|
|
|
|
— |
|
|
デジタルバイオテクノロジー会社の初期出資の収益。 |
|
|
— |
|
|
|
— |
|
|
|
|
|
融資活動が提供する現金純額 |
|
|
|
|
|
|
|
|
|
|||
現金、現金等価物、および制限的現金純増加 |
|
|
( |
) |
|
|
( |
) |
|
|
|
|
年初の現金、現金等価物、制限現金 |
|
|
|
|
|
|
|
|
|
|||
年末現金、現金等価物、制限現金 |
|
$ |
|
|
$ |
|
|
$ |
|
|||
非現金投資活動 |
|
|
|
|
|
|
|
|
|
|||
売掛金と売掛金に掲げる設備の購入 |
|
$ |
|
|
$ |
|
|
$ |
|
|||
キャッシュフロー情報を補足開示する |
|
|
|
|
|
|
|
|
|
|||
利子を支払う現金 |
|
$ |
|
|
$ |
|
|
$ |
— |
|
||
付記はこれらの連結財務諸表の構成要素である。
95
適応バイオテクノロジー会社は
総合財務状況の説明文集
適応生物技術会社(“WE”、“私たち”あるいは“OUR”)は商業段階の会社であり、適応性免疫システムの固有生物学を利用することによって疾病の診断と治療を変え、免疫医学領域の発展を推進する。適応免疫系は自然界が多くの疾患に対して行っている最も精密な診断や治療であると考えられるが,それを解読することはできず,医学界のその能力の活用を阻害している。著者らの免疫医学プラットフォームは著者らの独自技術を応用して患者免疫システムの各種遺伝子コードを読み取り、免疫システムがどのようにこの患者の疾病を測定と治療するかを正確に理解する。著者らは計算生物学と機械学習に基づく動態臨床免疫組織学データベースと関連抗原注釈の中でこれらの知見を捉え、それらを利用して患者個人の需要量に応じてカスタマイズできる臨床製品とサービスを開発と商業化した。私たちは商業製品とサービス、そして強力な臨床製品とサービスパイプラインを持っていて、これらの製品とサービスを設計して、癌や自己免疫疾患などの疾患の治療を診断、モニタリング、実現しています。
私たちは2009年9月8日にワシントン州に登録して設立しました。名前は適応TCR会社です。2011年12月21日、私たちは適応バイオテクノロジー会社と改称した。私たちの本部はワシントン州シアトルにあります。
列報根拠と合併原則
連結財務諸表には、適応バイオテクノロジー会社、当社の完全子会社適応バイオテクノロジー会社と当社子会社デジタルバイオテクノロジー会社の勘定が含まれています
予算の使用
アメリカ公認会計原則(“GAAP”)に基づいて総合財務諸表を作成する際、管理層はいくつかの推定、判断及び仮定を行い、総合財務諸表の日付の資産及び負債報告金額及び関連開示、及び列報期間の収入及び支出報告金額に影響を与える必要がある。私たちの見積もりは歴史的経験と当時の状況で合理的だと思う他の関連仮定に基づいています。推定数は、いくつかの履行債務のこれまでの進捗推定および顧客とのいくつかの契約の取引価格、株式ベースの報酬、2022年9月に締結された収入権益購入協定(“購入協定”)の計上利息、所得税引当金(関連準備金を含む)、営業権減価分析、および長期資産の回収および減価を含む複数の分野で使用される他にもありますこれらの推定は通常複雑な問題に関連し、判断する必要があり、歴史結果の分析と未来の傾向の予測に関連し、解決するには長い時間を要するかもしれず、時期によって異なる可能性がある。実際の結果は経営陣の見積もりと大きく異なるかもしれない。
市場情報を細分化する
私たちは私たちの最高経営責任者が運営意思決定者(“CODM”)であることを確認した。CODM定期審査統合に基づいて提出された経営結果及びその他の財務情報。収入の審査は統合エンティティよりも低いレベルで行われるが、リソース割り当て決定は、統合エンティティレベルで提案された結果に基づいてCODMによって行われ、統合エンティティは単一の報告単位として決定される。統合エンティティの動作方式は
現金と現金等価物
現金及び現金等価物は公正価値に従って列報する。現金等価物は、購入時の元の満期日が3ヶ月以下である証券のみを含む。私たちは私たちの投資を信頼性の良い銀行と格付けの高い通貨市場基金に置くことで、現金や現金等価物に関する信用リスクを制限する。現金と現金等価物は主に銀行預金と通貨市場基金への投資を含む。
制限現金
制限された現金残高があります$
96
適応バイオテクノロジー会社は
連結財務諸表付記
有価証券投資
有価証券は、米国(米国)を含む売却可能な証券に分類される)政府国債および機関証券、社債および商業手形は、公正価値に応じて報告される。未実現の持株損益は実現前の累積他の総合損益において株主権益の単独構成要素として反映されている。これらの証券を売却した実現収益と損失は純収益または損失で確認されている。有価証券の販売コストは具体的な識別方法によって決定される。
金融商品の公正価値
財務会計基準委員会(“財務会計基準委員会”)は、公正価値を、計量日市場参加者間の秩序ある取引において、元本または最も有利な市場で負債を移転するために受け取るまたは支払う交換価格、または退出価格として定義している。財務会計基準委員会は公正価値等級を構築し、1つの実体が公正価値を計量する時に観察可能な投入を最大限に利用し、観察できない投入を最大限に減少することを要求した。この階層構造は、公正な価値を測定するために使用することができる3つのレベルの投入を定義する
評価レベル内の金融商品分類は公正価値計量に重要な最低投入レベルに基づいている。場合によっては、評価投入活動が限られている場合や透明性が低い場合には、金融商品は、評価階層構造における第3レベルに分類される。
私たちの金融商品は1級と2級の資産で構成されており、過去に3級の負債を含んでいた。ある金融商品の期限が短いため、その帳簿価値は公正価値に近い。私たちは、2023年12月31日と2022年12月31日まで、公正な価値で恒常的に計量または開示された非金融資産または負債を何も持っていない。
リスクが集中する
私たちのいくつかの実験室機器および材料のリスクは、限られた数の供給者から、または場合によっては単一の供給者から集中している。このリスクは一定数の過剰在庫を狙うことで管理されている。
現金、現金等価物、および有価証券は、私たちを集中的な信用リスクに直面させる可能性のある金融商品だ。私たちは通貨市場基金、アメリカ政府国債と機関証券、社債、高品質認可金融機関の商業手形に投資しています。
大顧客とは、私たちの総収入または売掛金、各期間、および連結貸借対照表日ごとの純残高の10%以上を占める顧客のことです。
重要な顧客ごとに、列報日までの収入が列報期間中の総収入に占める割合と売掛金が売掛金総額に占める純パーセンテージは以下の通りである
|
|
収入.収入 |
|
売掛金純額 |
||||||
|
|
十二月三十一日までの年度 |
|
十二月三十一日 |
||||||
|
|
2023 |
|
2022 |
|
2021 |
|
2023 |
|
2022 |
顧客A |
|
*% |
|
*% |
|
*% |
|
*% |
|
|
顧客B |
|
* |
|
|
* |
|
* |
|
||
遺伝子テーク社と羅氏グループは |
|
|
|
|
* |
|
* |
|||
*10%未満 |
|
|
|
|
|
|
|
|
|
|
売掛金
売掛金には顧客がサービスを提供して当然のお金が含まれています。我々は、売掛金の信用減値を審査し、重大な期限を過ぎた売掛金の状況を定期的に分析して、回収できない可能性のある売掛金があるかどうかを決定し、売掛金をその推定可能な純価値に減少させるために必要な準備金額を推定する。
97
適応バイオテクノロジー会社は
連結財務諸表付記
在庫品
在庫には実験室分析用の実験室材料と用品が含まれている。私たちは購入時に在庫を資本化し、注文完了時に費用を記録し、私たちの研究開発実験室のサービス収入や使用に使います。先進的に先に出した基礎の上で、在庫はコスト或いは市場価格の中で低い者によって価格を計算します。私たちは定期的に古い評価を行い、これ以上利用できない在庫を解約する。長期在庫は#ドルです
財産と設備
財産および装置は、コンピュータ装置、コンピュータソフトウェア、実験室装置、レンタル改善、家具およびオフィス機器、および建設中の資産を含む。財産や設備はコストで入金され、減価償却は推定耐用年数に基づく直線法で確認される。メンテナンスとメンテナンスは発生時に費用を計上し、改善費用は資本化に計上する。
財産や設備に割り当てられる耐用年数は以下のとおりである
実験室装置 |
|
|
賃借権改善 |
|
|
コンピュータ装置及びソフトウェア |
|
|
家具と事務設備 |
|
我々は毎年,イベントや状況がある資産グループ別の帳票金額が回収できない可能性があることを示す場合には,長期資産の減値状況を検討する.資産処分損益及び減価損失は、発生した場合には、資産用途別に総合経営報告書内に分類され、それ自体の財務諸表項目内に分けて示されていない。付記10を参照賃貸借証書2023年12月31日までに年度内に確認されたリース改善減価損に関するより多くの資料。
無形資産
企業合併で買収された無形資産は商誉と分離して確認され、買収日にその公正価値で初歩的に確認され、これはそのコストとみなされる。
無形資産は、企業合併資格を満たしていない取引で資産や知的財産権を購入した結果でもある可能性がある。無形資産はその推定耐用年数内に直線的に償却されており,これはその使用パターンとほぼ同じである。無形資産は少なくとも年に1回減値審査を行うか、または潜在的減値指標が存在する場合。私たちは
商誉
営業権とは、購入価格が公正価値で計量された企業合併で取得した識別可能な資産と負担する負債純額を超える部分である。私たちは毎年10月1日に減価商業権を評価し、もし事件や環境変化が私たちの単一報告単位の公正価値をその帳簿価値より低くする可能性がもっとあれば、商業権をより頻繁に評価する。私たちはまず定性的要素を評価することによって、私たちの報告単位の公正価値がその帳簿価値よりも低い可能性があるかどうかを決定するために、営業権の減価を評価する。もし私たちがこのように決定した場合、または私たちが定性的評価を迂回することを選択した場合、私たちは商業権減価定量化テストを行うつもりだ。減値が存在する場合、営業権の帳簿価値は、総合経営報告書に記録された減値費用によってその公正価値に減少する。これまで私たちは
賃貸借証書
私たちは最初から計画にレンタル契約が含まれているかどうかを確認した。私たちは実験室、オフィス、倉庫施設の運営賃貸協定を持っている。経営リース使用権(“ROU”)資産および経営リース負債は、対象資産が吾等の使用可能な日に確認され、レンタル期間内の将来最低賃貸支払いの現在値に基づいている。純収益資産は、レンタル開始日または前に生成された任意の初期直接コストおよび支払いされた任意のレンタル支払いをさらに含み、受信されたレンタル報酬を減算する。私たちのレンタルは一般的に隠れ金利を提供しないので、私たちの未来の最低賃貸支払いの現在値は私たちの増加借入金利を使用して確定します。この金利は、似たような期間内に将来賃貸支払いが発生する担保借款金利の推定値であり、レンタル開始日に取得した情報に基づいて、または会計基準を用いて2016−02日に開始されたリース情報を更新(ASU)する賃貸借証書(トピック842)(“ASC 842”)。
98
適応バイオテクノロジー会社は
連結財務諸表付記
私たちのいくつかのレンタル契約には、レンタル契約の延長または終了の選択権が含まれています。私たちがこれらの選択権を行使することを合理的に決定した場合にのみ、これらのオプションに応じてレンタル条項を調整します。私たちのレンタル協定には残存価値保証やチェーノが含まれていない。
私たちはすでに私たちの不動産賃貸について政策選択をしました。それらが固定されている限り、非レンタル部分を賃貸部分から分離しません。未固定の非レンタル構成要素は、発生した可変レンタル費用として料金を計上する。私たちの実験室、オフィス、倉庫施設のレンタルには、通常、公共地域維持コストのような可変非レンタル構成要素が含まれています。また、レンタル期間が12ヶ月以下であり、行使する購入選択権を合理的に決定することが含まれていないリースを統合貸借対照表に記録しないことを選択しました。
私たちは毎年、イベントや状況がある資産グループの帳簿金額が回収できない可能性があることを示すたびに、私たちの使用権資産を減値審査します。減価損失は資産の使用状況に応じて総合経営報告書に分類され、それ自体の財務諸表項目に個別に記載されていない場合。付記10を参照賃貸借証書2023年12月31日までの年度内に確認された使用権資産減価損失に関するより多くの情報。
レンタル料金はレンタル条項の直線に基づいて確認します。私たちの施設賃貸契約による奨励は、賃貸休暇を含めて、賃貸契約条項におけるレンタル費用の直線に基づいて調整されることが確認された。
所得利子負債、純額、関連計上利息
私たちが2022年9月に締結した購入契約に関する収入利息負債残高は、総合貸借対照表に未償却発行コストを差し引いて列報します。私たちは有効金利法を使って私たちの関連利息支出を推定する。私たちが計算した実際の金利は私たちの関連債務を予想された返済期間内にゼロに償却するだろう。合意期間内に、実際の金利は、予測された公認会計原則収入の変化を含むいくつかの要因によって変化する可能性がある。私たちは展望的な方法を利用して、実現された収入と予想される収入に基づいて、四半期ごとに有効金利を評価する。収入の大幅な増加または減少または時間の変化は、私たちの利息支出と返済期限に影響を与えると予測される。
収入確認
すべての創出契約について、確認すべき収入金額を決定するステップを実行する:(1)1つまたは複数の契約を決定するステップ、(2)契約背景で異なるかどうかを含む約束された貨物またはサービスが履行義務であるかどうかを決定するステップ、(3)可変対価格の制約を含む取引価格を測定するステップ、(4)推定販売価格に応じて取引価格を履行義務に割り当てるステップ、および(5)(または)各履行義務を満たすときに収入を確認する。
著者らは免疫医学と微小残留病(“MRD”)業務領域で診断と研究サービスを提供することによって収入を得た。私たちの免疫薬物収入は以下の収入を含む:(1)私たちの商業研究製品である適応免疫シークエンシングは生物製薬顧客と学術機関にサンプルテストサービスを提供する;(2)私たちは遺伝子テーク社(“遺伝子テーク”)と他の生物製薬顧客との薬物と標的発見領域の協力プロトコル;および(3)数年前、臨床顧客に私たちのT-Detect CoVIDテストを提供した。私たちのMRD収入は、(1)臨床顧客に当社のclonoSEQ報告を提供すること、(2)生物製薬顧客およびいくつかの学術機関にMRDサンプル検査サービスを提供すること、および(3)技術移転によっていくつかの国際実験室サイトに我々のclonoSEQ報告または結果を提供することを含む。
適応免疫配列決定または我々のMRDサービスを使用する研究顧客の場合、契約は、一般に、サービス前の請求書金額(“前払い”)およびその後の請求書を含み、サンプル結果として顧客に渡される。受け取った前金は繰延収入として記録されており、業績義務を履行した際に収入として確認されています。私たちは確定しました
我々が発注医にclonoSEQ報告を提供するプロトコルについては,clonoSEQ報告を交付する義務を決定した。私たちは商業、政府、医療機関の支払人からこれらの取引の請求書と支払いを受け取ります。個別支払者の支払いは返済率や患者責任によって異なる可能性があるため,取引価格は可変であると考え,取引価格の推定を記録したが,可変対価格の制限を受け,交付時の収入とした。取引価格の推定は,異なる支払者の履歴と期待返済率に基づいており,これらの返済率は以降の期間が監視され,必要に応じて実際の入金経験に基づいて調整される。
99
適応バイオテクノロジー会社は
連結財務諸表付記
連邦医療保険下のclonoSEQのカバー範囲について、私たちが最初の合格したテスト報告書を提供する時、一次治療のための請求書を発行します。この請求書は、患者の治療期間に必要なすべての必要なテストを考慮しており、現在、各患者は初期配列同定テストを含む約4つのテストがあると推定されている。収入確認は、初期課金テスト報告書が交付されたときから始まり、これまでに交付された累積テストに基づく。適応患者の履歴テスト頻度から,患者の治療周期内に提供されると予想されるテスト数を推定した。時間の経過とともに利用率に関する情報がより多く得られ,これらの見積り値が変化する可能性がある.初期課金試験からの任意の未確認収入は、繰延収入として記録され、患者の治療期間における残りの試験の推定値を提供するときに確認されるか、または患者が追加の試験を受ける可能性がわずかになる場合に確認される。
生物製薬顧客と締結されたその治療法の契約をさらに開発および商業化する契約取引価格には、払戻不可能な前払い費用、単独価格のMRD試験料、およびいくつかの規制の承認を得た後に当社の顧客が稼いだマイルストーン費用が含まれる可能性があります。契約によって、このような合意は単一または複数の履行義務を含む。このような業績義務は顧客の治療開発を支援するためのサービスを提供することを含み、私たちは顧客登録試験の一部として使用しようとしている私たちの技術に対して監督管理支援を提供し、私たちのデータの分析計画を制定し、共同研究委員会に参加し、監督提出の完成を協力し、顧客が顧客の監督管理に提出したサンプルに関するMRD検査サービスを提供することを含む。一般に,支援サービスは,MRDテストサービスを含まず,契約範囲内で区別がないため,履行義務として入金される.それぞれの履行義務に割り当てられた取引価格は,規制支援サービスの調整市場評価方法と推定されたMRDテストサービスの独立販売価格を用いて推定される.MRDサンプル検出サービスが個別価格の顧客オプションである場合、材料権利が存在するかどうかを評価し、存在しない場合、クライアントが追加のMRDサンプル検出サービスを購入するオプションは、契約の一部とはみなされない。時間の経過とともに、予想される送達されたサンプル結果の総量に対する送達されたサンプル結果の割合に基づいて、進行が予想される場合に、MRD検出サービスに関連する収入を生成方法を用いて確認する。私たちは規制支援サービスを識別するために同じ方法を使用する。サンプル結果交付割合に基づく産出方法が進捗を忠実に記述できない場合には,完了作業量推定に基づくコストベースのモデルの入力法を用いる.進展の測定基準を選択し、これまでの進展を推定するには重要な判断が必要だ。払い戻し不可能な前払い費用を除いて、他の形態の補償は異なる対価格を表す。契約開始時には、このようなマイルストーンの実現は、第三者規制承認と顧客自身の提出決定に依存するため、規制マイルストーンに関するいかなる考慮も完全に制限する。監督管理のマイルストーンに関連する可変対価格は最も可能な金額法で推定され、その中で可変対価格は制限され、累積収入が大きな逆転が発生しない可能性がある。規制承認のマイルストーン支払いは我々の顧客の制御範囲内ではなく、これらの承認を受ける前に実現可能とは考えられない。規制のマイルストーン支払いが重大な判断を必要とする分野である可能性があるかどうかを確認する。この評価を行う際には,科学,臨床,規制,その他のリスク,それぞれのマイルストーンを実現するために必要な努力と投資レベルを評価した。
2021年には、販売ベースの使用料に関連する可変対価格を含む知的財産権許可協定に署名した。このような特許権使用料に関連する任意の対価格は、以下の遅い時間に収入として確認される:(I)関連販売が発生するか、または(Ii)販売された特許使用料の一部または全部に基づく履行義務が履行された(または部分的に履行されている)。
契約残高
場合によっては、課金はサービスを実行する前に発生する可能性がある。前金は繰延収入または契約負債として記録されている。私たちの履行義務が今後12ヶ月以内に完了すると予想される時、私たちは繰延収入を当期収入に分類する;しかし、私たちは顧客がサンプルを提供する時間をコントロールしない。サービスおよび連携活動については、Genentechとのグローバル連携やライセンス契約に関連する活動は含まれていませんので、お客様が協調した予測交付時間に基づいて業績評価義務を評価し、繰延収入を現在または非現在の収入として確認します。場合によっては、顧客プロジェクトは、顧客プリペイドによってカバーされるすべての関連サービスの配信前にキャンセルまたは終了される可能性がある。この場合、収入が逆転できないという十分な証拠が得られた場合、私たちは収入を確認する。いくつかのプロトコルによって提供される総サンプルの推定値が減少した場合、またはMedicareに関連する契約残高の場合、患者が追加検査を受ける可能性がわずかになる場合にも、収入を確認する。注3を参照収入.収入私たちは遺伝子テークの世界的な協力と許可協定に関連した繰延収入政策だ。
株式ベースの報酬
株式ベースの報酬には、従業員および非従業員への株式オプション、制限株式単位、および市場に基づく制限株式単位の報酬費用が含まれる。これは贈与日贈与の公正価値を表し、贈与の必要なサービス期間内に確認し、通常は授権期間であり、実際に没収されたものを直線的に差し引く。Black-Scholesオプション定価モデルとモンテカルロ推定モデルを用いて株式オプションと市場に基づく制限株式単位付与の公正価値をそれぞれ推定した。
100
適応バイオテクノロジー会社は
連結財務諸表付記
広告.広告
広告費用は発生時に費用を計上する。広告費用は$
収入コスト
収入コストには、材料コスト、人員に関連する費用(賃金、福祉、および株式ベースの給与を含む)、輸送および運搬費用、設備コスト、サンプル処理に関連する分配施設コスト、および私たちのサービス収入活動に関連する専門的な支援コストが含まれる。分配される施設費用には、実験室設備の減価償却、分配された施設占有と情報技術費用が含まれる。加工サンプルに関するコストは、収入確認の時間を考慮することなく費用として記録される。
研究と開発費
研究および開発費用には、実験室材料費用、人員に関連する費用(賃金、福祉および株式報酬を含む)、設備費用、分配された施設および情報技術費用、および契約サービス費用が含まれる。研究と開発活動は現有の検査と製品の更なる開発と改善、新技術の発見と著者らの免疫薬物プラットフォームへの投資を支持する。また,ソフトウェア開発に関するコストを研究開発費に含め,将来のビジネス機会を支援し,実験室規模やワークフローの開発活動を支援する.また、私たちの研究開発費の構成要素は、将来の臨床製品やサービスの規制承認を得るために、臨床と分析検証を支援するコストである研究·開発コストは発生時に費用を計上する。将来の研究開発活動または提供される商品またはサービスのための前払いは、繰延されて資本化され、その後、商品を消費するか、または関連サービスを行う際に費用として確認される。私たちの遺伝子テークとの世界的な協力と許可協定を支持するコストもまた、私たちの研究開発費の構成要素です。
販売とマーケティング費用
販売およびマーケティング費用には、当社のプラットフォーム製品の商業化を支援する商業販売、製品および口座管理、マーケティング、精算、医療教育、業務開発者の人事関連費用(賃金、福祉、株式給与を含む)が含まれています。また、これらの費用には、広告費用、顧客教育·販売促進費用、市場分析費用、会議費、出張費用、分配された施設や情報技術費用などの外部コストが含まれる。
減価および関連長期資産支出を使用する
使用権減値および関連長期資産支出には、いくつかの賃貸オフィスおよび実験室空間の減価費用、および関連賃貸改善の減値コストが含まれる。
利子支出
支払利息には、私たちの収入、利子負債に関するコスト、および繰延発行コストに関する償却に関する非現金利息コストが含まれています。私たちは有効金利法を用いて利息支出を試算した。私たちが計算した実際の金利は私たちの関連債務を予想された返済期間内にゼロに償却するだろう。予想される収入の著しい増加または減少または時間の変化は、私たちの利息支出に予想される影響を与えるだろう。
所得税
所得税は負債法で計算される。繰延税項資産及び負債は、総合財務諸表における既存資産及び負債の帳簿価額及びそれぞれの課税基礎間の差額、及び営業損失及び繰越の税項相殺間の差額に基づいて確認された将来の税項影響である。繰延税金資産を予想現金化金額に減少させるために、必要に応じて評価準備を設ける。
繰延税項資産および負債総合貸借対照表は、その等の一時的な差額の回収や決済が予想される年度の課税収入に適用される予定の制定税率計量を採用している。税率変動が繰延税金資産や負債に及ぼす影響は、当該等税率変動が公布されたときに確認される。私たちの損失の歴史のため、私たちの純繰延税金資産は完全に推定準備金によって相殺された。
101
適応バイオテクノロジー会社は
連結財務諸表付記
所得税の頭寸が審査後にもっと維持される可能性がある時にこそ、私たちはこのような頭寸の影響を認識するだろう。
適応バイオテクノロジー会社の普通株主は1株当たり純損失を占めるべきだ
普通株主が1株当たりの基本純損失を占めるべき方法を計算する方法は、純損失を当期に発行された普通株の加重平均株式数で割ることである。当社の普通株株主が1株当たり純損失を占めるべき計算方法は、在庫株方法で決定されている間、すべての潜在的な未償還希釈普通株等価物を考慮することである。この計算については、すでに発行された普通株承認株式証、購入株式権を行使していない、発行された非既存制限株式単位、および資格に適合して稼ぐ最大非既存市場に基づく制限的株式単位は普通株等価物とみなされているが、計算普通株株主が1株当たりの純損失を占めるべきであることから除外されており、それらの効果は逆薄であるからである。
未採用の新会計公告
2023年11月、FASBはASU 2023-07号を発表した細分化市場報告(話題280):報告可能な部分に開示された改善それは、重要な部門の支出に関する報告可能な部門の開示を強化することを意図している。本ガイドラインは,2023年12月15日以降の財政年度と2024年12月15日以降の財政年度内の移行期間に適用される。早期採用を許可し、そのガイドラインをさかのぼって適用するだろう。私たちは現在、この指針が私たちの連結財務諸表に及ぼす影響を評価している。
FASBは2023年12月にASU 2023-09を発表しました所得税(話題740):所得税開示を改善する主に、税率の帳簿と支払われた所得税の開示を強化するためだ。本ガイドラインは2024年12月15日以降の年次期間に適用される。早期採用が許可され、このガイドラインは前向きに適用される;遡及応用が許可される。私たちは現在、この指針が私たちの連結財務諸表に及ぼす影響を評価している。
私たちは、私たちの収入とキャッシュフローの性質、金額、タイミング、不確実性が経済的要因の影響をどのように受けるかを最もよく表していると考えられるので、業務分野と手配タイプによって顧客との契約収入を分類します。
以下の表に列挙期間中の分類収入(千単位)を示す
|
|
十二月三十一日までの年度 |
|
|||||||||
|
|
2023 |
|
|
2022 |
|
|
2021 |
|
|||
免疫薬収入 |
|
|
|
|
|
|
|
|
|
|||
サービス収入 |
|
$ |
|
|
$ |
|
|
$ |
|
|||
協力収入 |
|
|
|
|
|
|
|
|
|
|||
免疫薬総収入 |
|
|
|
|
|
|
|
|
|
|||
MRD収入 |
|
|
|
|
|
|
|
|
|
|||
サービス収入 |
|
|
|
|
|
|
|
|
|
|||
一里塚収入を監督する |
|
|
— |
|
|
|
|
|
|
|
||
MRD総収入 |
|
|
|
|
|
|
|
|
|
|||
総収入 |
|
$ |
|
|
$ |
|
|
$ |
|
|||
2023年12月31日までの年間で私たちは$を認めた
2022年12月31日までの年間で確認しました
2021年12月31日までの年間で確認しました
102
適応バイオテクノロジー会社は
連結財務諸表付記
2023年12月31日までに、最大の受け取りを受けるかもしれません$
遺伝子タイク協力協定
2018年12月、私たちは腫瘍学の分野で細胞療法を開発する能力を利用するために、遺伝子テークと世界的な協力と許可協定(“遺伝子テークプロトコル”)に署名した。2019年1月に規制部門の承認を得た後、私たちは払い戻しできない前払い$を受け取りました
Genentechプロトコルの条項に基づき,既存の共有抗原パケットの許可を含めて腫瘍学分野でTCRによる細胞療法を開発·商業化するグローバル独占許可をGenentechに付与した。また,遺伝子テークはどの候補製品をさらに商業化目的に開発するかを決定する権利がある。私たちはこの計画が“会計基準アセンブリ”に適合していると思う“ASC”トピック808、協力手配両方が活動の積極的な参加者であり、活動の商業的失敗または成功に応じて重大なリスクおよびリターンに直面するので、(“ASC 808”)。ASC 808は、連携スケジュール下の活動をどのように説明するかに関する指導を提供していないため、ASCテーマ606における指導を適用した取引先と契約した収入(“ASC 606”)は、遺伝子テーク協定に関連する活動を示す。
ASC 606を適用した場合、我々は、プロトコル開始時に以下の履行義務を決定した
契約の範囲内で、ライセンスをさらに開発するための多くの追加的な研究および開発があるので、これらの権利は活動と高度に関連しているので、ライセンス、研究開発サービス、または様々な委員会に参加する義務は異なると確信している。著者らはいくつかの要素、例えばそれぞれの現有抗原パケットの開発段階、2種類の製品経路の下で潜在的な新薬受け入れ目標を識別と提出するために必要な後続の開発、及び遺伝子テークの製品商業化に対する制御に鑑み、研究と開発経路の可変性を考慮した。具体的には,遺伝子テークプロトコルによると,遺伝子テークはこれら2つの製品経路に関する開発や商業化活動に従事する必要がなく,いずれかを選択することができる。そこで,すべての決定された履行義務は,パケットを含む我々のTCR専用プラットフォームをさらに開発し,任意の製品経路を追求するためにGenentechに我々のTCR識別プロセスを提供し続けることを決定した.
103
適応バイオテクノロジー会社は
連結財務諸表付記
また、著者らは遺伝子泰克に対して患者の特定のTCRの供給と製造プロトコルを締結する責任があり、それは任意の個性化製品の治療に関連しているからである。遺伝子テークが個人化された製品療法の商業化を求めるならば、これが彼らの選択権であることを確認した。初期開発段階の不確実性、遺伝子テークとの協力の新しい方法、および将来のビジネスマイルストーンと特許権使用料を支払う私たちの権利のために、この選択権は最初から考慮すべき重要な権利ではないと判断した。したがって、双方が供給と製造協定を締結する場合、私たちはそれを説明するつもりだ。
最初の価格はドルだけで構成されるべきだと決めました
潜在的な実質的な発展が必要であるため,遺伝子テークはこれらの発展を指導できる可能性があり,比例業績モデルを用いて我々の業績義務の収入を確認することにした。著者らは1種の入力法を用いて比例業績を評価し、この方法は共有製品と個性化製品経路を追求するために発生したコストの研究開発仕事に対する総推定コストに基づいている。いかなる潜在的な規制や発展マイルストーンも完全に制限されずに取引価格に計上されている場合には,そのときの割合表現に基づく累積追跡法を用いてこれらの金額を確認する.私たちは現在遺伝子テークプロトコルによる収入の約
全体的に認識しているのは$
遺伝子テークプロトコルからの繰延収入代表$
2023年12月31日までの1年間における繰延収入の変化は以下の通り(千単位)
2022年12月31日までの繰延収入残高 |
|
$ |
|
|
本期間の繰延収入の増加 |
|
|
|
|
期内確認の収入 |
|
|
( |
) |
2023年12月31日までの繰延収入残高 |
|
$ |
|
2023年12月31日までに$
104
適応バイオテクノロジー会社は
連結財務諸表付記
以下の表に、2023年12月31日、2023年、2022年までの公正価値で恒常的に計量された金融資産の公正価値(千計)を示す
|
|
2023年12月31日 |
|
|||||||||||||
|
|
レベル1 |
|
|
レベル2 |
|
|
レベル3 |
|
|
合計する |
|
||||
金融資産 |
|
|
|
|
|
|
|
|
|
|
|
|
||||
貨幣市場基金 |
|
$ |
|
|
$ |
— |
|
|
$ |
— |
|
|
$ |
|
||
商業手形 |
|
|
— |
|
|
|
|
|
|
— |
|
|
|
|
||
アメリカ政府国債と機関証券 |
|
|
— |
|
|
|
|
|
|
— |
|
|
|
|
||
社債 |
|
|
— |
|
|
|
|
|
|
— |
|
|
|
|
||
金融資産総額 |
|
$ |
|
|
$ |
|
|
$ |
— |
|
|
$ |
|
|||
|
|
2022年12月31日 |
|
|||||||||||||
|
|
レベル1 |
|
|
レベル2 |
|
|
レベル3 |
|
|
合計する |
|
||||
金融資産 |
|
|
|
|
|
|
|
|
|
|
|
|
||||
貨幣市場基金 |
|
$ |
|
|
$ |
— |
|
|
$ |
— |
|
|
$ |
|
||
商業手形 |
|
|
— |
|
|
|
|
|
|
— |
|
|
|
|
||
アメリカ政府国債 |
|
|
— |
|
|
|
|
|
|
— |
|
|
|
|
||
社債 |
|
|
— |
|
|
|
|
|
|
— |
|
|
|
|
||
金融資産総額 |
|
$ |
|
|
$ |
|
|
$ |
— |
|
|
$ |
|
|||
一級証券は高流動性の通貨市場基金を含み、私たちは活発な市場で同じ資産または負債の見積もりに基づいてこれらの基金の公正な価値を測定する。二級証券はアメリカ政府国債と機関証券、会社債券と商業手形から構成され、非アクティブ市場における最近の証券取引或いは類似ツールの見積市場価格と観察可能な市場データ或いは観察可能な市場データから実証された他の重要な投入に基づいて推定される。
販売可能な投資には、2023年12月31日と2022年12月31日まで、以下の内容が含まれています(千計)
|
|
2023年12月31日 |
|
|||||||||||||
|
|
原価を償却する |
|
|
未実現収益 |
|
|
未実現損失 |
|
|
公正価値を見積もる |
|
||||
短期有価証券 |
|
|
|
|
|
|
|
|
|
|
|
|
||||
商業手形 |
|
$ |
|
|
$ |
— |
|
|
$ |
— |
|
|
$ |
|
||
アメリカ政府国債と機関証券 |
|
|
|
|
|
|
|
|
( |
) |
|
|
|
|||
社債 |
|
|
|
|
|
|
|
|
— |
|
|
|
|
|||
短期有価証券総額 |
|
$ |
|
|
$ |
|
|
$ |
( |
) |
|
$ |
|
|||
|
|
2022年12月31日 |
|
|||||||||||||
|
|
原価を償却する |
|
|
未実現収益 |
|
|
未実現損失 |
|
|
公正価値を見積もる |
|
||||
短期有価証券 |
|
|
|
|
|
|
|
|
|
|
|
|
||||
商業手形 |
|
$ |
|
|
$ |
— |
|
|
$ |
— |
|
|
$ |
|
||
アメリカ政府国債 |
|
|
|
|
|
|
|
|
( |
) |
|
|
|
|||
社債 |
|
|
|
|
|
— |
|
|
|
( |
) |
|
|
|
||
短期有価証券総額 |
|
$ |
|
|
$ |
|
|
$ |
( |
) |
|
$ |
|
|||
短期有価証券に指定されているすべての米国政府国債および機関証券、社債および商業手形の有効満期日は、それぞれの総合貸借対照表日の1年以下である。長期有価証券に指定された有効期限は、それぞれの総合貸借対照表から1年を超える。
計算すべき利息は私たちの有価証券の分担コストと推定公正価値に含まれていません。受取利息を計算する$
105
適応バイオテクノロジー会社は
連結財務諸表付記
次の表は、2023年12月31日までの未実現保有損失総額と未実現損失頭寸投資の公正価値、および個別証券が赤字頭寸を継続している時間長(千単位)を示している
|
|
12ヶ月以下です |
|
|
12ヶ月以上 |
|
||||||||||
|
|
公正価値 |
|
|
未実現損失 |
|
|
公正価値 |
|
|
未実現損失 |
|
||||
アメリカ政府国債と機関証券 |
|
$ |
|
|
$ |
( |
) |
|
$ |
— |
|
|
$ |
— |
|
|
売却可能証券総額 |
|
$ |
|
|
$ |
( |
) |
|
$ |
— |
|
|
$ |
— |
|
|
私たちは定期的に販売可能な証券を検討して、信用減価を評価します。減値を評価する際に考慮するいくつかの要素は、公正価値が余剰コスト基礎より低い程度、証券に関連する不利な条件、業界或いは地理区域、証券格付け或いは業界信用格付けの変化、及びその他の関連市場データを含む。
2023年12月31日現在、私たちは予定していませんし、販売コストベース(満期日かもしれない)に回収する前に販売可能な投資を売却することを要求される可能性もありません。私たちの評価によると、2023年12月31日までのすべての減値は、金利の変化など、信用損失以外の要因によるものだと結論した。信用準備が確認されておらず、証券売却の減価を他の全面的な損失に計上することができる。
2023年12月31日現在、2022年12月31日現在の財産·設備純額には、以下が含まれています(千計)
|
|
十二月三十一日 |
|
|||||
|
|
2023 |
|
|
2022 |
|
||
実験室装置 |
|
$ |
|
|
$ |
|
||
コンピュータ装置 |
|
|
|
|
|
|
||
家具と事務設備 |
|
|
|
|
|
|
||
コンピュータソフト |
|
|
|
|
|
|
||
建設中の工事 |
|
|
|
|
|
|
||
賃借権改善 |
|
|
|
|
|
|
||
原価で計算した財産と設備総額 |
|
|
|
|
|
|
||
減算:減価償却累計 |
|
|
( |
) |
|
|
( |
) |
財産と設備、純額 |
|
$ |
|
|
$ |
|
||
減価償却費用は$
あったことがある
2023年12月31日現在、2022年12月31日までに償却すべき無形資産には、以下のものが含まれています(千計)
|
|
2023年12月31日 |
|
|||||||||
|
|
総帳簿金額 |
|
|
累計償却する |
|
|
帳簿純額 |
|
|||
得られた発達した技術 |
|
$ |
|
|
$ |
( |
) |
|
$ |
|
||
購入した知的財産権 |
|
|
|
|
|
( |
) |
|
|
|
||
2023年12月31日の残高 |
|
$ |
|
|
$ |
( |
) |
|
$ |
|
||
|
|
2022年12月31日 |
|
|||||||||
|
|
総帳簿金額 |
|
|
累計償却する |
|
|
帳簿純額 |
|
|||
得られた発達した技術 |
|
$ |
|
|
$ |
( |
) |
|
$ |
|
||
購入した知的財産権 |
|
|
|
|
|
( |
) |
|
|
|
||
2022年12月31日の残高 |
|
$ |
|
|
$ |
( |
) |
|
$ |
|
||
106
適応バイオテクノロジー会社は
連結財務諸表付記
開発した技術は,我々が2015年にSequenta,Inc.を買収した際に獲得したものである.買収した開発技術と購入した知的財産権の余剰残高は来年度に償却される予定だ
2023年12月31日現在、無形資産予想将来償却費用は以下の通り(単位:千)
2024 |
|
$ |
|
|
2025 |
|
|
|
|
2026 |
|
|
|
|
2027 |
|
|
|
|
将来の償却費用総額 |
|
$ |
|
2023年12月31日現在と2022年12月31日現在の債務構成は以下の通り(千計)
|
|
十二月三十一日 |
|
|||||
|
|
2023 |
|
|
2022 |
|
||
専門費 |
|
$ |
|
|
$ |
|
||
臨床·契約研究組織コスト |
|
|
|
|
|
|
||
旅行と娯楽 |
|
|
|
|
|
|
||
納税義務 |
|
|
|
|
|
|
||
財産と設備を購入する |
|
|
|
|
|
|
||
コンピュータとソフトウェア |
|
|
|
|
|
|
||
他にも |
|
|
|
|
|
|
||
負債総額を計算すべきである |
|
$ |
|
|
$ |
|
||
私たちは実験室、オフィス、倉庫施設の運営賃貸プロトコルを持っていて、私たちは様々な場所でこれらの施設を占有しています。
2011年7月、私たちはワシントン州シアトルにいた小株主と撤回できない賃貸契約を締結し、オフィスと実験室空間を借りた。レンタル条項はその後何度も修正されました。最近は2019年8月で、当時私たちは既存の物件を約20%に拡大しました
2023年10月、私たちはこのレンタルスペースを空けた。そこで,資産使用権と関連リース改善(総称して“資産グループ”と呼ぶ)の減価を評価し,まず資産グループの帳簿価値と残存リース期間内に予想される将来の未割引キャッシュフロー純額を比較する方法である。これらの予測には,潜在的転貸収入に対する経営陣の現金流入および運営·維持費用流出の推定が含まれている。帳簿金額は回収できないことが発見されたため、資産グループの公正価値を評価した。資産グループの帳票金額がその公正価値を超える程度は、確認すべき減価コストを表す。公正価値は収益法を用いて決定され,我々の見積もり増額借入金金利に見合った比率を用いて推定現金流量純額を割引した。この評価の結果、回収不可能な運営と維持コストを含めて、資産グループが完全に減価されることが確認された。そこで1つは共$
107
適応バイオテクノロジー会社は
連結財務諸表付記
2019年8月に協定を締結しました
2018年4月、レンタル契約を締結し、レンタル契約を結びました
2021年3月、私たちはレンタル契約を締結して、約
私たちは2023年12月31日まで融資リースに参加しなかった。私たちのレンタルの残りの期限は
2023年12月31日と2022年12月31日現在、当社の経営リースに関するその他の情報は以下の通りです
|
|
十二月三十一日 |
|
|||||
|
|
2023 |
|
|
2022 |
|
||
加重平均残存賃貸年限(年) |
|
|
|
|
|
|
||
加重平均割引率 |
|
|
% |
|
|
% |
||
以下の表では、当社の未割引経営リースキャッシュフローと、2023年12月31日現在の総合貸借対照表の現在部分残高(千単位)を差し引いたものを照合します
2024 |
|
$ |
|
|
2025 |
|
|
|
|
2026 |
|
|
|
|
2027 |
|
|
|
|
2028 |
|
|
|
|
その後… |
|
|
|
|
未割引賃貸支払総額 |
|
|
|
|
減算:推定金利 |
|
|
( |
) |
リース負債総額を経営する |
|
|
|
|
マイナス:現在の部分 |
|
|
( |
) |
経営賃貸負債から流動分を差し引く |
|
$ |
|
運営レンタル料金は$
2023年12月31日までの年度、賃貸負債計量額に計上して支払われた現金は$
108
適応バイオテクノロジー会社は
連結財務諸表付記
収入権益購入協定
2022年9月,吾らはOrbiMed Advisors LLCの連属会社OrbiMed Royalty&Credit Opportunities IV,LP(“OrbiMed”)と購入プロトコルを締結し,買い手(“買い手”)の担保エージェントおよび行政エージェントとした.購入契約によると、私たちは$を受け取りました
収入利息支払い
当該等支払いの対価格として、買い手は、すべての公認会計基準収入(“収入ベース”)のパーセンテージ(“適用支払率”)に基づいて、吾等からいくつかの収入利息(“収入利息”)を受け取る権利がある。1回目の支払いのみを支払った場合、適用される支払率は四半期収入ベースの5%となる。1回目の支払いと2回目の支払いの両方が支払われた場合、適用される支払率は四半期収入ベースの8%となる必要がある。1回目の支払い、2回目の支払い、および3回目の支払いがともに支払われた場合、収入利息に適用される支払率は四半期収入ベースの10%となるべきだ。
収入利息に関する支払いは季節ごとにしなければならない
車の蓋に戻る
OrbiMedには
コールオプション/コールオプション
引受オプション事件(定義は購入合意参照)が発生した場合、吾などの重大資産剥離、制御権変更、重大判決あるいは破産事件を含み、購入合意項目の下で少なくとも大部分の購入承諾を代表する買い手は権利があるが義務がない(“承諾オプション”)は、吾などに適用価格(“引受/償還価格”)に従ってすべての未償還収入権益を買い戻すことを要求する。また、最初の支払いを受けた後のいつでも、吾らは引受オプションを行使し、適用された引受/償還価格ですべての収入権益を買い戻すことができる。
支配権変更または重大資産剥離以外のすべてのコールオプションイベントについては、ロールオフオプション/コールオプション価格は、適用されるリターン上限に等しくなければならない。支配権変更や重大資産剥離については、2024年3月12日までに、下落/強気オプション価格は同等であるべきである
会計処理
購入契約の条項を評価し,累積買手の支払いの特徴は債務ツールの特徴に類似していると結論した.そこで、実際の金利法を用いて償却コストで入金された債務に取引を計上する。私たちはさらに債務条項を評価し、購入者がいくつかの事件があった場合に行使可能なコールオプションがデリバティブとして分岐する必要があると判断した。しかし、行使の可能性が低いため、オプションの価値は無関係に決定される。私たちは定期的にコールオプションの価値を評価する。
購入契約債務の償却を決定するためには、将来の収入の時間と金額の推定に基づいて、将来の収入の利息支払いの金額と時間を推定し、債務を償却することを計算する必要がある
109
適応バイオテクノロジー会社は
連結財務諸表付記
購入契約について、私たちは#ドルの債務発行コストを発生させた
債務の予期される償還期間および発行コストの償却期間を決定する際に使用される仮定は、これらのコストに影響を与える可能性のある短期的および長期的な分類、およびこれらのコストがどのくらいの期間にわたって償却されるかの推定を行うことを要求する。私たちは内部予測に基づいて期待収入の利息支払いの金額と時間を定期的に評価する。
このような支払いが私たちの初期推定よりも高いか低いか、またはその支払いの時間が私たちの最初の推定と大きく異なる限り、私たちなどは収入利息負債の償却および実際の金利を前向きに調整するだろう。
2023年12月31日と2022年12月31日終了年度の収入利息負債、純活動(単位:千)を表に示す
開始時の収入利子負債 |
|
$ |
|
|
資本化発行コスト |
|
|
( |
) |
利子支出 |
|
|
|
|
支払済み利子 |
|
|
( |
) |
受取利息 |
|
|
( |
) |
利子負債を収入、2022年12月31日現在純額 |
|
|
|
|
利子支出 |
|
|
|
|
支払済み利子 |
|
|
( |
) |
受取利息 |
|
|
( |
) |
利子負債を収入、2023年12月31日現在純額 |
|
$ |
|
支払収入利息#ドル
法律訴訟
通常の業務過程で、私たちは時々クレームと評価の影響を受けるだろう。私たちが責任を負う可能性が高く、金額を合理的に見積もることができる時、私たちはそのような事項のために責任を負うつもりだ。損失可能な範囲が1つしか決定できない場合には、その範囲内で最も可能な金額を計算しなければならない。範囲内の任意の金額が、その範囲内の任意の他の金額よりも良い推定値でない場合、その範囲内の最小金額は計算されるべきである。2023年12月31日まで、私たちは実質的な法的手続きに参加しなかった。
賠償協定
通常の業務過程では、いくつかの事項について、サプライヤー、レンタル者、顧客、および他の当事者に異なる範囲および条項の賠償を提供することができますが、これらに限定されません。また、取締役会のメンバーや一部の役員と賠償協定を締結しており、取締役や上級管理者の身分やサービスによって生じる可能性のある責任を賠償することを求めています。このような賠償協定によると、私たちが未来に支払うことを要求される可能性のある最大の潜在金額は多くの場合無制限だ。私たちはこのような賠償のために何の物質的コストも発生していませんし、今のところ何の賠償要求もありません。
普通株
私たちの普通株は割引や特権がなく、償還できない
110
適応バイオテクノロジー会社は
連結財務諸表付記
2023年12月31日までに以下の会社のために普通株式を予約しました
付与された既発行株式オプションを行使する際に発行可能な株式 |
|
|
|
|
付与された発行制限株式単位が帰属したときに発行可能な株式、及び市場に基づく発行制限株式単位の最高限度額を稼ぐ資格がある |
|
|
|
|
2019年株式インセンティブ計画の下で将来付与可能な株 |
|
|
|
|
従業員が株を購入する計画で後日付与できる株式 |
|
|
|
|
将来のために予約された普通株式総株式を発行する |
|
|
|
我々の2019年株式インセンティブ計画(“2019年計画”)によると、2019年計画によると、2020年1月1日とその後毎年1月1日に発行される株式数は、(A)の少ない者に相当する株式数を毎年増加させることができる
また、我々の従業員株式購入計画(“ESPP”)は、2020年1月1日とその後の毎年1月1日に、我々のESPPに基づいて発行可能な株式数を(A)の最小株式数に相当する毎年増加させることを規定している
2023年1月1日から、2019年計画とESPP備蓄が増加しました
2009年株式インセンティブ計画
私たちは2009年に従業員、取締役、コンサルタントに奨励性と非制限普通株式オプション、その他の株式ベースの奨励金を支給することを規定する株式インセンティブ計画(“2009計画”)を採択した。2009年計画によると、奨励的かつ非制限的な株式オプションの実行権価格は、付与された日の私たちの普通株の公平な市場価値を下回ってはならない。本計画により付与された株式オプションは遅くない
2019年持分インセンティブ計画
2019年は、2019年7月に初公募が終了する前に発効する予定です。2019年計画では、株式オプションやその他の株式ベースの奨励の形で従業員、取締役、コンサルタントに奨励を支給することが規定されている。2019年計画によると、株式オプション取引価格は、1986年国税法第409 a条または第424(A)条の規定に適合しない限り、2019年計画で定義された発効日の株式の公正時価を下回ってはならない。さらに、他の説明がない限り、本計画によって付与された株式オプションは遅くない
2023年12月31日までの1年間、付与可能な株式の変化は以下の通り
|
|
付与可能株 |
|
|
2022年12月31日に付与可能な株 |
|
|
|
|
2019年株式インセンティブ計画準備金引き上げは2023年1月1日から発効 |
|
|
|
|
付与された株式オプション及び制限株式単位及び付与された有資格で稼いだ市場に基づく制限株式単位の最高限度額 |
|
|
( |
) |
没収または満期の株式オプションおよび制限株式単位 |
|
|
|
|
2023年12月31日に付与可能な株 |
|
|
|
|
111
適応バイオテクノロジー会社は
連結財務諸表付記
株式オプション
2023年12月31日までの年間で、2009年計画と2019年計画下の株式オプション活動は以下の通り
|
|
以下の条件を満たす株式 |
|
|
加重平均運動 |
|
|
内在的価値を集める |
|
|||
2022年12月31日現在の未償還株式オプション |
|
|
|
|
$ |
|
|
|
|
|||
付与された株式オプション |
|
|
|
|
|
|
|
|
||||
株式オプションが没収される |
|
|
( |
) |
|
|
|
|
|
|
||
株式オプションが満期になる |
|
|
( |
) |
|
|
|
|
|
|
||
行使した株式オプション |
|
|
( |
) |
|
|
|
|
|
|
||
2023年12月31日現在の未償還株式オプション |
|
|
|
|
$ |
|
|
$ |
|
|||
2023年12月31日に帰属し行使可能な株式オプション |
|
|
|
$ |
|
|
$ |
|
||||
2023年12月31日までの未償還株式オプションの加重平均残存契約期間は
2023年,2022年および2021年12月31日までに年度内に行使された株式オプション総内的価値は$
ドルの中で
限定株単位
2023年12月31日までの年間で、2019年に計画されている限定株式単位活動は以下の通りです
|
|
限定株単位 |
|
|
加重平均付与日 |
|
||
2022年12月31日現在の未帰属制限株式単位 |
|
|
|
|
$ |
|
||
承認された制限株式単位 |
|
|
|
|
|
|||
没収された制限株式単位 |
|
|
( |
) |
|
|
|
|
帰属制限株式単位 |
|
|
( |
) |
|
|
|
|
2023年12月31日現在未発行の非既存限定株式単位 |
|
|
|
|
$ |
|
||
2023年,2022年および2021年12月31日までの年度内帰属制限株式単位の総公平価値は$である
市場に基づく制限株式単位
上記の制限株式単位に加えて、我々の取締役会は2023年3月に市場に基づく制限株式単位が私たちの最高経営責任者と最高科学者に奨励されることを承認した。奨励によって得られる普通株式に基づいて,1株当たり
112
適応バイオテクノロジー会社は
連結財務諸表付記
付与日に付与された株式オプション、制限株式単位及び市場に基づく制限株式単位の公正価値
2023年12月31日、2022年、2021年12月31日までの年間に付与された株式オプションの推定付与日公正価値は、ブラック·スコアーズオプション定価モデルに基づいて以下の仮定の下で推定される
|
|
十二月三十一日までの年度 |
|
|||||||||
|
|
2023 |
|
|
2022 |
|
|
2021 |
|
|||
普通株主公正価値 |
|
$ |
|
|
$ |
|
|
$ |
|
|||
予想期限(年単位) |
|
|
|
|
|
|
||||||
無リスク金利 |
|
|
|
|
|
|
||||||
予想変動率 |
|
|
|
|
|
|
||||||
期待配当収益率 |
|
|
— |
|
|
|
— |
|
|
|
— |
|
ブラック·スコアーズオプション定価モデルを使用して付与された株式オプションの公正価値の決定は、我々の普通株の公正価値の影響を受け、およびいくつかの変数に関する仮定は主観的であり、通常、決定するために判断する必要がある。推定値仮定は以下のように決定される
普通株の公正価値-各普通株の公正価値は、ナスダック全世界精選市場で報告されたように、私たちの普通株の授与日或いは他の関連確定日の終値に基づいている。
所期期限·ASCトピック718に示されるように、従業員および非従業員取締役に付与される株式オプションの期待期間は、“簡略化”方法を使用して決定される報酬--株式報酬なぜなら、私たちはより良い予想期間推定を決定するのに十分な運動歴史がないからだ。この方法では期待期限は株式オプションの帰属日と契約期限終了の間の中点を基準とする.
無リスク金利·我々は、米国財務省のゼロ金利発行に基づくオプション推定モデルにおいて無リスク金利を使用しており、残りの条項は株式オプションの予想条項と類似している。
予想変動率当社の普通株式には十分な取引履歴がないため、予想変動率は、当社の上場取引の業界同業者が、予想期間の推定と一致する期間の履歴変動性を利用することに基づいている。
期待配当収益率-予測可能な未来には現金配当金は支払われないと予想され、したがって、予想配当収益率は
2023年、2022年および2021年12月31日までに年度内に付与された加重平均授受日の1株当たり株式公開価値は$
付与日に付与された制限株式単位の公正価値ナスダック全世界精選市場で報告されたように、私たちの普通株の授与日または他の関連確定日の終値に基づいている2023年まで、2022年および2021年12月31日までに年度内に付与される1株当たり制限株式単位の加重平均授受日公平値は$
2023年12月31日および2022年12月31日までの年間で,市場に基づく制限株式単位の加重平均授与日は1株当たり公平価値を$とする
2023年、2023年、2022年、2021年12月31日終了年度までの株式オプション、限定株式単位と市場ベースの制限株式単位の補償費用を総合業務報告書に列挙すると以下のようになる(千計)
|
|
十二月三十一日までの年度 |
|
|||||||||
|
|
2023 |
|
|
2022 |
|
|
2021 |
|
|||
収入コスト |
|
$ |
|
|
$ |
|
|
$ |
|
|||
研究開発 |
|
|
|
|
|
|
|
|
|
|||
販売とマーケティング |
|
|
|
|
|
|
|
|
|
|||
一般と行政 |
|
|
|
|
|
|
|
|
|
|||
株式に基づく報酬総支出 |
|
$ |
|
|
$ |
|
|
$ |
|
|||
113
適応バイオテクノロジー会社は
連結財務諸表付記
2023年12月31日現在、未確認株式給与支出と残余加重平均確認期間は以下の通り
|
|
認識できない共有に基づいて |
|
|
残り加重平均値 |
|
||
既得株式オプションではない |
|
$ |
|
|
|
|
||
非既得限定株式単位 |
|
|
|
|
|
|
||
市場の非既得制限株式単位に基づく |
|
|
|
|
|
|
||
プロトコルの概要
2017年12月、我々はマイクロソフト社(“マイクロソフト”)と協力協定(“Microsoftプロトコル”)を締結し、単一血液テストに基づく汎用診断を開発するために、全面的なT細胞受容体抗原図を計算した。
マイクロソフトと同時に、標準的な量産価格でマイクロソフトのAzureクラウドサービスを使用し、最低Azure購入要求を$とする単独のプロトコルを締結しました
また、マイクロソフト協定を締結するとともに、マイクロソフトは1ドルの優先株投資を行った
会計概論
マイクロソフト協定の条項は、双方が活動の積極的な参加者であり、大きなリスクとリターンに直面しているので、ASC 808の基準を満たしている。これは活動の商業成功にかかっている。ASC 808は、協調下のアクティビティがどのように指示を提供するかについて説明しておらず、MicrosoftがASC 606におけるクライアントの定義に適合していないと判断する。したがって,それぞれの要素の計算を決定するための他の指導意見が期待される.
私たちは、優先株発行とマイクロソフトAzureクラウドサービスの使用の約束が市場金利と一致する条項で行われていることを確認した。F-1系列転換可能優先株発行の一部として受け取ったすべての対価格は,F-1系列優先株発行の一部として入金される.マイクロソフトAzureクラウドサービスを購入する約束は市場条項に従って行われているので、私たちは7年以内に正常な業務過程で約束を履行したいので、サービス消費期間の費用を記録しました。これらの費用は、それらがサポートする基本的な活動に基づいて統合ビジネスレポートに記録される。
プロトコルの残りの内容は非常に関連しているので、適切な会計適用を決定するために、それらを総合的に評価した。具体的には、双方間の許可権譲渡、マイクロソフトへのデータおよび免疫グループ学、診断およびバイオインフォマティクスの専門知識を提供する約束、およびマイクロソフトが機械学習ソフトウェアおよび関連開発サービスを提供する約束は、各当事者が“マイクロソフト協定”の下での活動を実行するために必要であるため、課金単位として評価すべきであると認定する。
これらの協調活動をASCテーマ845で説明しました非貨幣取引また、連携によってマイクロソフトから受信または提供される資産の価値の変化には重大な不確実性があるため、公正な価値を確実に計測することができないことを決定した。したがって、吾らは、マイクロソフトプロトコルに従って吾等に提供されるか、または吾等によって徴収される権利に関連する非通貨資産または対応する非通貨収入または支出を確認していない。
2022年3月、運営コストを削減し、約をリストラする再編計画を実施しました
114
適応バイオテクノロジー会社は
連結財務諸表付記
本報告に掲げる期間所得税準備金前損失構成は以下のとおりである(千計)
|
|
十二月三十一日までの年度 |
|
|||||||||
|
|
2023 |
|
|
2022 |
|
|
2021 |
|
|||
国内では |
|
$ |
( |
) |
|
$ |
( |
) |
|
$ |
( |
) |
外国.外国 |
|
|
|
|
|
|
|
|
|
|||
所得税未払い準備前の総損失 |
|
$ |
( |
) |
|
$ |
( |
) |
|
$ |
( |
) |
繰延所得税は、財務報告目的のための資産および負債の帳簿金額と所得税目的のための金額との間の一時的な差異の純税影響を反映する。
公表日まで、私たちの繰延税金資産と負債の重要な構成要素は以下の通りです(千計)
|
|
十二月三十一日 |
|
|||||
|
|
2023 |
|
|
2022 |
|
||
繰延税金資産 |
|
|
|
|
|
|
||
純営業損失 |
|
$ |
|
|
$ |
|
||
税金の繰り越しを免除する |
|
|
|
|
|
|
||
条件を満たさない株式オプション |
|
|
|
|
|
|
||
リース負債を経営する |
|
|
|
|
|
|
||
収入を繰り越す |
|
|
|
|
|
|
||
資本化研究と開発 |
|
|
|
|
|
|
||
他にも |
|
|
|
|
|
|
||
繰延税金資産総額 |
|
|
|
|
|
|
||
減算:推定免税額 |
|
|
( |
) |
|
|
( |
) |
繰延税金資産は,推定準備後の純額を差し引く |
|
|
|
|
|
|
||
繰延税金負債 |
|
|
|
|
|
|
||
有形資産と無形資産 |
|
|
( |
) |
|
|
( |
) |
使用権資産 |
|
|
( |
) |
|
|
( |
) |
繰延税金純額 |
|
$ |
|
|
$ |
|
||
ASCトピック740所得税純営業損失(“NOL”)、一時的な差異、信用繰越の税収優遇を資産記録として、経営陣がこれを実現する“可能性が高い”と評価すればよいことが求められている。将来の税金優遇の実現は私たちが繰越期間内に十分な課税収入を生み出すことができるかどうかにかかっている。私たちの経営赤字の歴史のため、管理層は上述した未来の税金優遇による繰延税金資産は現在実現不可能であると考えているため、評価準備を提供している。推定免税額は#ドル増加した
連邦税法は、1986年の国内税法第382節で定義されたように、所有権変更の場合にNOLと信用繰越を使用することに実質的な制限を加えている。したがって、所有権の変化により、私たちがこのような繰越を利用する能力が制限される可能性がある。第382条の2023年6月30日までの所有権変更の分析を完了し、制限をトリガする可能性のある変更を監視していきます。この分析に基づいて、私たちは連邦NOLの使用が永久的に制限されないと予想する。2017年の連邦所得税法の減税と雇用法案によると、2018年および今後数年に発生する連邦NOLは無期限に繰り越すことができるが、このような連邦NOLの控除は年間制限されている。2018年前に生成されたNOLは
115
適応バイオテクノロジー会社は
連結財務諸表付記
我々の所得税準備金の有効税率は、以下の期間の連邦法定税率とは異なる
|
|
十二月三十一日までの年度 |
||||
|
|
2023 |
|
2022 |
|
2021 |
法定料率 |
|
|
|
|||
州税、連邦税収割引を差し引く |
|
|
|
|||
株式ベースの報酬 |
|
( |
|
( |
|
|
永久品 |
|
( |
|
( |
|
( |
単位 |
|
|
|
|||
他にも |
|
|
( |
|
( |
|
評価免除額を変更する |
|
( |
|
( |
|
( |
合計する |
|
|
|
|||
私たちは世界的な無形低税収入を発生時の期間費用に計上する。
私たちは総合財務諸表で、技術的な利点によって、税務状況が審査後にさらに維持される可能性があれば、その状況に影響を与えることを確認した。一ドルの未確認税金の割引があります
提出日の税収割引が確認されていない期初と期末金額の入金は以下の通り(千計)
2020年12月31日残高 |
|
$ |
|
|
2021年の新規プロジェクト |
|
|
|
|
2021年12月31日の残高 |
|
|
|
|
2022年の新規プロジェクト |
|
|
|
|
2022年12月31日の残高 |
|
|
|
|
2023年の新規プロジェクト |
|
|
|
|
2023年12月31日の残高 |
|
$ |
|
2023年、2022年および2021年12月31日までの年間で、不確定な税務状況は
私たちはいかなる確認されていない税金優遇の計算すべき利息と罰金を所得税支出の構成要素として確認した。私たちは
私たちは連邦と特定の州の所得税申告書を提出し、その中で評価に異なる制限法規を提供する。しかし、NOL繰り越しにより、成立以来の基本的なすべての納税年度は依然として連邦と州税務審査を受けている。
次の表は、2023年12月31日、2022年12月31日、2021年12月31日までの年度普通株株主が1株当たり基本純損失と希釈純損失を占める計算を示している(千単位で、株と1株当たりの金額は含まれていない)
|
|
十二月三十一日までの年度 |
|
|||||||||
|
|
2023 |
|
|
2022 |
|
|
2021 |
|
|||
適応バイオテクノロジー会社の純損失によるものです |
|
$ |
( |
) |
|
$ |
( |
) |
|
$ |
( |
) |
適応バイオテクノロジー会社の普通株主に起因する1株当たり純損失の加重平均株式、基本株主及び希釈株主の計算に用いる |
|
|
|
|
|
|
|
|
|
|||
適応バイオテクノロジー会社の普通株株主は1株当たり純損失を占めなければならず、基本と希釈後 |
|
$ |
( |
) |
|
$ |
( |
) |
|
$ |
( |
) |
すべての期間の損失状況を考慮して、普通株株主は1株当たり基本純損失を占めるべきであり、普通株株主は希釈した後の1株当たり純損失と同じであり、すべての潜在的な発行済み普通株を含めることは逆希釈になるからである。
116
適応バイオテクノロジー会社は
連結財務諸表付記
以下の加重平均普通株等価物は、反希釈効果を有するので、2023年、2023年、2022年、2021年12月31日までの年間私たちの普通株主が1株当たり純損失を希釈する計算には含まれていない
|
|
十二月三十一日までの年度 |
|
|||||||||
|
|
2023 |
|
|
2022 |
|
|
2021 |
|
|||
未償還株式オプション |
|
|
|
|
|
|
|
|
|
|||
発行された非既存限定株式単位 |
|
|
|
|
|
|
|
|
|
|||
市場に基づいた限定的な株式単位ではなく最大の利益を稼ぐ資格がある |
|
|
|
|
|
|
|
|
— |
|
||
普通株式承認証を発行した |
|
|
— |
|
|
|
— |
|
|
|
|
|
合計する |
|
|
|
|
|
|
|
|
|
|||
私たちは、ある資格要件に適合する従業員をカバーする賃金延期401(K)計画(“401(K)計画”)を維持する。従業員は最高を守ることができる
117
項目9.Accouとの変更と分岐会計と財務情報開示の専門家
いいえ適用する.
第9条。制御するSとプログラム
情報開示制御とプログラムの評価
最高経営責任者や最高財務責任者を含む経営陣の監督·参加の下、2023年12月31日現在、取引法第13 a-15条の規則に基づいて、制御プログラムやプログラムの設計·動作の有効性を開示することを評価した。この評価に基づき、我々の最高経営責任者と最高財務責任者は、2023年12月31日から有効であると結論した。
経営陣財務報告内部統制年次報告書
我々の経営陣は、取引法第13 a-15(F)条で定義されているように、財務報告の十分な内部統制の確立と維持を担当している。経営陣は、トレデビル委員会後援組織委員会が発表した“内部統制--総合枠組み”(2013年枠組み)に規定されている基準に基づいて、財務報告の内部統制の有効性を評価した。この評価に基づき、経営陣は、財務報告の内部統制を2023年12月31日から有効であり、財務報告の信頼性と公認会計基準に基づいて総合財務諸表を作成する合理的な保証を提供すると結論した。
2023年12月31日現在、財務報告の内部統制の有効性は、独立公認会計士事務所が監査しており、その報告は以下のとおりである。
内部制御の変化
2023年12月31日までの3ヶ月間、私たちは財務報告の内部統制に何の変化もなく、この用語は“取引法”の下のルール13 a-15(F)で定義されており、これは私たちの財務報告の内部統制に大きな影響を与えたり、合理的に大きな影響を与える可能性がある。
118
独立公認会計士事務所報告
適応バイオテクノロジー会社の株主と取締役会へ
財務報告の内部統制については
我々は,トレデビル協賛組織委員会が発表した内部制御-総合枠組み(2013年枠組み)(COSO基準)で確立された基準に基づき,適応バイオテクノロジー会社の2023年12月31日までの財務報告内部統制を監査した。COSO基準に基づき,適応バイオテクノロジー社(当社)は2023年12月31日現在,すべての重要な面で財務報告を効率的に内部統制していると考えられる。
我々はまた、米国上場会社会計監督委員会(PCAOB)の基準に従って、当社の2023年12月31日まで、2023年12月31日と2022年12月31日までの総合貸借対照表を監査し、2023年12月31日までの3年度の関連総合経営報告書、全面赤字、株主権益と現金流量、および関連付記と2024年2月29日に発表した報告書について保留意見を発表した。
意見の基礎
当社経営陣は、効果的な財務報告内部統制を維持し、添付されている“経営陣財務報告内部統制年次報告”における財務報告内部統制の有効性を評価する責任がある。私たちの責任は私たちの監査に基づいて、会社の財務報告書の内部統制に意見を述べることです。私たちはPCAOBに登録されている公共会計士事務所で、アメリカ連邦証券法およびアメリカ証券取引委員会とPCAOBの適用規則と法規に基づいて、私たちは会社と独立しなければなりません。
私たちはPCAOBの基準に従って監査を行っている。これらの基準は、財務報告の有効な内部統制がすべての重要な面で維持されているかどうかを決定するために、合理的な保証を得るために監査を計画し、実行することを要求する。
我々の監査には,財務報告の内部統制を理解すること,重大な弱点があるリスクを評価すること,評価されたリスクテストに基づいて内部統制の設計·運用有効性を評価すること,および状況下で必要と考えられる他のプロセスを実行することが含まれる。私たちは私たちの監査が私たちの観点に合理的な基礎を提供すると信じている。
財務報告の内部統制の定義と限界
会社の財務報告に対する内部統制は、公認された会計原則に基づいて、財務報告の信頼性と外部目的の財務諸表の作成に合理的な保証を提供することを目的としたプログラムである。会社の財務報告に対する内部統制には、(1)合理的で詳細かつ正確かつ公平に会社の資産を反映した取引および処分に関する記録の保存、(2)公認された会計原則に従って財務諸表を作成するために必要な取引が記録されている合理的な保証を提供し、会社の収入および支出は会社の経営陣と取締役の許可のみに基づいて行われる。(三)財務諸表に重大な影響を及ぼす可能性のある不正買収、使用、または処分会社の資産を防止またはタイムリーに発見する合理的な保証を提供する。
その固有の限界のため、財務報告書の内部統制は誤った陳述を防止したり発見できない可能性がある。また,将来的にどのような有効性評価を行うかの予測は,条件の変化により制御不足のリスクが生じる可能性があり,あるいは政策やプログラムの遵守度が悪化する可能性がある.
/S/安永法律事務所
ワシントン州シアトル
2024年2月29日
119
プロジェクト9 B。他にも情報
適用されません。
プロジェクト9 Cです。下型検査阻止に関する外国司法管区の検討
いいえ適用する.
120
部分(三)
プロジェクト10.役員·役員職ICERSと会社管理
表格10-K第10項に要求される資料は、米国証券取引委員会に提出された2024年株主総会依頼書の募集に関する最終依頼書(“2024年依頼書”)に含まれ、引用により本明細書に組み込まれる。
プロジェクト11.行政官E報酬
表格10-K第11項に要求される情報は、2024年の委託書に含まれ、参照されて本明細書に組み込まれる。
プロジェクト12.特定の受益者の保証所有権従業員と経営陣および関連株主について
我々の持分補償計画に関する情報を含むテーブル10-K第12項に要求される情報は、2024年の委託書に含まれ、参照によって本明細書に組み込まれる。
表格10-K第13項で要求される情報は、2024年の委託書に含まれ、参照されて本明細書に組み込まれる。
第14項.元金口座TING料金とサービス
♪the the the表格10-K第14項に要求される情報は、2024年の委託書に含まれ、参照されて本明細書に組み込まれる。
121
部分IV.IV
プロジェクト15.展示品、資金ALIレポート明細書
本文書第2部第8項の連結財務諸表索引を参照表格10-Kの年報.
必要な資料が適用されないため、または添付表の提出を要求するのに十分ではないか、または必要な資料が連結財務諸表または付記に含まれているので、すべての財務諸表の添付表は省略される。
次の展示品索引に記載されている展示品は、本ファイルの一部としてアーカイブ、提供、または統合されて参考になります表格10-Kの年報.
展示品索引
|
|
|
引用で編入する |
|||
展示品 番号をつける |
展示品名 |
アーカイブ済み/搭載済み これがあった 届ける |
表 |
書類番号. |
展示品 |
提出日 |
3.1 |
改訂·再改訂された定款 |
|
8-K |
001-38957 |
3.1 |
7/1/2019 |
3.2 |
付例を改訂および再制定する |
|
8-K |
001-38957 |
3.2 |
7/1/2019 |
4.1 |
7回目の改正と再署名登録者とそのいくつかの株主との間の“投資家権利協定”は,2019年5月30日である |
|
S-1 |
333-231838 |
4.1 |
5/30/2019 |
4.2 |
証券説明書 |
|
10-K |
001-38957 |
4.3 |
2/26/2020 |
10.1 |
Genentech,Inc.と登録業者との戦略的協力とライセンス契約,日付は2018年12月19日 |
|
S-1 |
333-231838 |
10.1 |
5/30/2019 |
10.2 |
マイクロソフト社と登録者間の戦略協力協定、日付は2017年12月11日 |
|
S-1 |
333-231838 |
10.2 |
5/30/2019 |
10.3 |
Illumina,Inc.と登録者との間の主要な販売条項と条件,日付は2019年5月28日である |
|
S-1/A |
333-231838 |
10.3 |
6/17/2019 |
10.4 |
Viking Global Equities LP,Viking Global Equities II LP,VGE III Portfolio Ltd.,Viking Long Fund Master Ltd.と登録者間の添付協定に改訂と再署名され,日付は2019年5月8日であった |
|
S-1 |
333-231838 |
10.5 |
5/30/2019 |
10.5* |
登録者とそのいくつかの行政者との間で改正及び再署名された雇用契約のフォーマット |
|
S-1 |
333-231838 |
10.7 |
5/30/2019 |
10.6* |
登録者とロコン瑞との間で改訂及び再締結された雇用契約のフォーマット |
|
S-1 |
333-231838 |
10.8 |
5/30/2019 |
10.7* |
登録者は、その非従業員取締役毎に再予約された非従業員取締役制御権と協議のフォーマットを変更する |
|
S-1 |
333-231838 |
10.9 |
5/30/2019 |
10.8* |
登録者とそのいくつかの執行者との間の行政離職協定フォーマット |
|
10-Q |
001-38957 |
10.1 |
8/10/2020 |
122
|
|
|
引用で編入する |
|||
展示品 番号をつける |
展示品名 |
アーカイブ済み/搭載済み これがあった 届ける |
表 |
書類番号. |
展示品 |
提出日 |
10.9* |
登録者とその役員及び行政者との間の賠償協定フォーマット |
|
S-1 |
333-231838 |
10.13 |
5/30/2019 |
10.10* |
適応バイオテクノロジー会社の非従業員役員報酬政策 |
|
10-K |
001-38957 |
10.10 |
2/14/2023 |
10.11* |
適応バイオテクノロジー会社2009年株式インセンティブ計画とその奨励協定のフォーマット |
|
S-1 |
333-231838 |
10.15 |
5/30/2019 |
10.12* |
適応バイオテクノロジー会社2019年持分インセンティブ計画とその奨励協定のフォーマット |
|
10-Q |
001-38957 |
10.12 |
8/13/2019 |
10.13* |
非米国参加者向け株式オプション協定形式 |
|
10-K |
001-38957 |
10.16 |
2/24/2021 |
10.14* |
非米国参加者のための限定株式単位プロトコルフォーマット |
|
10-K |
001-38957 |
10.17 |
2/24/2021 |
10.15* |
演技単位契約書及び演技単位授権書フォーマット |
|
10-Q |
001-38957 |
10.1 |
5/4/2022 |
10.16* |
適応バイオテクノロジー会社2019年従業員株購入計画 |
|
S-1/A |
333-231838 |
10.17 |
6/17/2019 |
10.17 |
収入権益購入協定は、2022年9月12日に適応バイオテクノロジー会社、本協定の時々の買い手がOrbiMed Royalty&Credit Opportunities IV、LPと締結し、締結した |
|
8-K |
001-38957 |
10.1 |
9/12/2022 |
10.18 |
2011年7月21日ARE-シアトル有限責任会社が適応TCR会社と締結した賃貸契約は、2011年8月26日第1号修正案、2014年6月30日第2号改正案、2015年11月5日第3号改正案、2015年12月23日第4号改正案、2016年6月6日第5号改正案により改正された |
|
S-1 |
333-231838 |
10.18 |
5/30/2019 |
10.19 |
適応バイオテクノロジー会社とARE-シアトル第11号賃貸契約の第6修正案、日付は2019年8月2日 |
|
8-K |
001-38957 |
10.1 |
8/7/2019 |
10.20 |
適応バイオテクノロジー会社とARE-シアトル第12号有限責任会社の賃貸契約は、2019年8月2日となっています |
|
8-K |
001-38957 |
10.2 |
8/7/2019 |
21.1 |
付属会社名簿 |
|
10-K |
001-38957 |
21.1 |
2/14/2023 |
23.1 |
独立公認会計士事務所の同意 |
X |
|
|
|
|
24.1 |
授権書(署名ページに含まれる) |
X |
|
|
|
|
31.1 |
2002年サバンズ-オキシリー法第302節により可決された1934年証券取引法第13 a-14条又は第15 d-14(A)条に基づいて発行された最高経営責任者証明書 |
X |
|
|
|
|
123
|
|
|
引用で編入する |
|||
展示品 番号をつける |
展示品名 |
アーカイブ済み/搭載済み これがあった 届ける |
表 |
書類番号. |
展示品 |
提出日 |
31.2 |
2002年サバンズ-オキシリー法第302節で可決された1934年“証券取引法”第13 a-14(A)条又は第15 d-14(A)条による首席財務官の証明 |
X |
|
|
|
|
32.1 |
2002年にサバンズ·オクスリ法案第906条で可決された“米国法典”第18編1350条による主要行政官の証明 |
X |
|
|
|
|
32.2 |
2002年サバンズ·オキシリー法第906条で可決された“米国法典”第18編1350条による首席財務官の証明 |
X |
|
|
|
|
97.1* |
適応バイオテクノロジー会社がミス賠償を取り戻す政策 |
X |
|
|
|
|
101.INS |
連結されたXBRLインスタンス文書−インスタンス文書は、そのXBRLタグがイントラネットXBRL文書に埋め込まれているので、相互作用データファイルには表示されない。 |
X |
|
|
|
|
101.書院 |
Linkbase文書を組み込んだインラインXBRL分類拡張アーキテクチャ |
X |
|
|
|
|
104 |
表紙相互データファイル(添付ファイル101に含まれるイントラネットXBRLのフォーマット) |
X |
|
|
|
|
*契約または報酬計画またはスケジュールを管理します。
証券法に基づいて公布されたS-K法規第601項によると、本展示品の一部の内容は漏れており、これらの情報は実質的ではないので、公開開示すれば競争に有害な影響を与える。
項目16.表格10-Kの概要
適用されない.
124
標札題材.題材
1934年の証券取引法第13または15(D)節の要求によると、登録者は、本10-K表年次報告を2024年2月29日にワシントン州シアトル市で正式に許可された以下の署名者が代表して署名することを正式に促した。
適応バイオテクノロジー会社は
|
||
|
|
|
差出人: |
|
/S/チャド·ロビンズ |
|
|
チャド·ロビンズ 最高経営責任者 |
授権依頼書
以下の署名の各人は、その事実代理人チャド?ロビンズを任意及びすべての身分で彼の代わりに指定し、任意及び全ての身分で本10-K表年次報告書の任意の修正に署名し、証拠物及びこれに関連する他の書類と共に米国証券取引委員会に提出することを確認し、上記の事実上の代理人又はその代替者が本表によって行うことができるすべてのことを承認及び確認する。
1934年の証券取引法の要求によると、以下の表格10-Kの年次報告は、以下の登録者代表登録者によって指定された身分及び日付で署名されている。
サイン |
|
タイトル |
|
日取り |
|
|
|
||
/S/チャド·ロビンズ チャド·ロビンズ |
|
取締役CEO兼最高経営責任者 (首席行政主任) |
|
2024年2月29日 |
|
|
|
||
/S/第谷·ピーターソン 第谷·ピーターソン |
|
首席財務官 (首席財務官) |
|
2024年2月29日 |
|
|
|
||
/投稿S/カイル·ピスクル カイル·ピスクル |
|
副社長、首席会計官 (首席会計主任) |
|
2024年2月29日 |
|
|
|
||
/S/ミシェル·グリフィン ミシェル·グリフィン |
|
役員.取締役
|
|
2024年2月29日 |
|
|
|
||
/S/ロバート·ハーシュバーグ ロバート·ハーシュバーグ博士医学博士 |
|
役員.取締役
|
|
2024年2月29日 |
|
|
|
||
/S/ピーター·ノーバート ピーター·ノバート |
|
役員.取締役
|
|
2024年2月29日 |
|
|
|
||
/S/ケイティ·オーウェン ケイティ·オーウェン博士 |
|
役員.取締役
|
|
2024年2月29日 |
|
|
|
|
|
寄稿S/マイケル·ペリーニ |
|
役員.取締役 |
|
2024年2月29日 |
マイケル·ペリニ医学博士 |
||||
|
|
|
|
|
125