
投資家・アナリスト向けイベントシリーズ — 第8巻トランスフォーミング・ミオトニック・ジストロフィーグローバルフェーズ3 HARBOR治験および長期マリーナ・オールのデータ 2024年3月4日ナスダック:RNA | aviditybio.com

2 将来の見通しに関する記述このプレゼンテーションには、かなりのリスクと不確実性を伴う将来の見通しに関する記述が含まれていることを読者に警告します。このプレゼンテーションに含まれる歴史的事実の記述以外のすべての記述は、将来の見通しに関する記述です。将来の見通しに関する記述には、将来の経営成績、事業戦略、進行中の臨床試験の予想時期、設計、実施、進行中の臨床プログラムからのデータ公開時期、臨床試験のデータと結果の特性評価、およびそこから導き出された結論、研究開発計画、AOC 1001、AOC 1020、AOCの計画と予定スケジュールに関する記述が含まれますが、これらに限定されません。1044; 当社製品候補の安全性と耐容性のプロファイル、AOCプラットフォームの可能性、希少疾患の治療における当社の製品候補の能力、成功のタイミングと可能性、期待される製品、製品の承認、将来の事業に関する経営陣の計画と目標、および予想される製品開発努力の将来の成果。場合によっては、読者は将来の見通しに関する記述を「かもしれない」、「する」、「するかもしれない」、「予定」、「予定」、「予想」、「可能」、「意図」、「目標」、「プロジェクト」、「熟考」、「信念」、「見積もり」、「予測」、「可能性」、「継続」などの用語、またはこれらの用語やその他の類似の表現の否定的表現で区別できます。。将来の見通しに関する記述を含めることは、当社の計画のいずれかが達成されることをAvidityが表明したものと見なすべきではありません。実際の結果は、当社の事業に内在し、当社の制御が及ばないリスクと不確実性により、このプレゼンテーションに記載されているものとは異なる場合があります。これには、AOC 1001に関連する部分的な臨床保留を完全に解決できない場合があり、その結果、AOC 1001の臨床開発が遅れる可能性があります。部分的な臨床保留などに関連するデータの追加要求により、大幅な追加費用とタイミング遅延が発生する可能性がありますが、これらに限定されません。部分的な臨床保留に関連してFDAに提供されたデータは、そうではない可能性がありますFDAにとっては満足のいくものです。引き続き利用可能になっているAOC 1001に関連する追加の参加者データは、最新の締め切り時点で作成されたデータと矛盾する可能性があり、既存のデータをさらに分析し、新しいデータを分析すると、その期限の時点で確立されたものとは異なる結論につながる可能性があります。製品候補の予期しない有害な副作用や不十分な有効性により、開発、規制当局の承認、商品化が遅れたり、制限されたりする可能性があります。または、追加の臨床保留、リコール、または製造物責任につながる可能性があります主張; 私たちは開発努力の初期段階にあります。AOCプラットフォームに基づく製品候補の発見と開発に対する私たちのアプローチは実証されておらず、商業的価値のある製品を開発できるかどうかわかりません。製品候補の前臨床研究と臨床試験の成功、初期の臨床試験の結果は必ずしも将来の結果を予測するものではありません。臨床試験の開始、登録、完了が遅れる可能性があります; 前臨床に関連する第三者への依存と臨床試験と製品製造。第三者とのコラボレーションから期待されるメリットを実現できない場合や、既存のコラボレーションが予想より早く終了したり、新しいコラボレーションを形成できなくなったりする場合があります。INDや同様の外国の規制当局への提出物の受理や将来の臨床試験のデザイン案を含む、米国および海外における規制の進展。FDAによるファストトラック指定は、開発、規制上のレビュー、承認プロセスの迅速化につながらない場合があります; 私たちの入手能力と製品候補と専有技術の知的財産保護を維持する。資本資源を予想よりも早く使い果たし、必要な追加資金を調達できない可能性がある。また、SECへの提出書類(2024年2月28日にSECに提出された2023年12月31日に終了した年度のフォーム10-Kの「リスク要因」という見出しを含む)に記載されているその他のリスク、およびその後のSECへの提出書類に記載されています。読者は、これらの将来の見通しに関する記述に過度に依存しないように注意してください。これらの記述は、本書の日付の時点でのみ述べられています。適用法で義務付けられている場合を除き、新しい情報、将来の出来事、状況の変化などの結果として、ここに含まれる将来の見通しに関する記述を公に更新または改訂する予定はありません。すべての将来の見通しに関する記述は、1995年の民間証券訴訟改革法のセーフハーバー条項に基づいて作成されたこの注意書きに完全に当てはまります。このプレゼンテーションには、市場規模や成長に関連して、独立機関や私たちが行った見積もりやその他の統計データ、および業界に関するその他のデータも含まれています。このデータには多くの仮定と制限があり、読者はそのような見積もりを過度に重視しないように注意してください。さらに、当社の将来の業績および当社が事業を展開する市場の将来の業績に関する予測、仮定、および推定には、必然的に高い不確実性とリスクが伴います。これらの要因やその他の要因により、結果は独立機関や当社が行った見積もりで表明されたものと大きく異なる可能性があります。このプレゼンテーションは、有価証券の売却の申し出または勧誘を構成するものではなく、また、そのような州または管轄区域の証券法に基づく登録または資格取得に先立って、そのような申し出、勧誘、または売却が違法となる州または法域における証券の売却があってはなりません。

3 RNA治療薬の提供に革命を起こして人々の生活を大幅に改善するという私たちのビジョン Luke Living with DM1

4 DMD44のAOC 1044〜900人の米国での提供 2024年の提供:3つの希少疾患の3つの臨床プログラムで3つのデータ読み出しDMD44のAOC 1044〜900人、FSHDの1020人の患者、米国の約16,000〜38、00人の患者。2024年第2四半期の参加者の約半数にフェーズ1/2のFORTITUDE予備データが届くと予想しています。DM1の患者数は4万人を超えます 2024年第1四半期の米国のMARINA-OLEデータ 2024年第2四半期にグローバル第3相HARBOR試験の開始に向けて順調に進んでいます 2024年下半期には第1/2 EXPLORE44の患者データを見込んでいます

デイシェア・グローバル第3相HARBORTM試験デザインの5つの目標 • 研究デザインに関する規制合意 • 2024年第2四半期に開始予定 • MARINA-OLETMの長期データを提示 • VHOT、ハンドグリップ、筋力、日常生活活動など、複数の指標における一貫した持続的な改善 • 長期にわたる安全性と忍容性 END-DM1自然史研究のデビューデータは、自然史のデルと比較して病気の進行が逆転していることを示していますパシバート・エテデシランの略語:デル・デシラン(以前はAOC 1001と呼ばれていました)

6 アビディティ管理チームジョン・W・デイ、医学博士、スタンフォード大学医学部神経・小児科教授、神経筋医学部長 G U E S T S P E A K E R スティーブ・ヒューズ医学博士、医学博士、最高医療責任者サラ・ボイス社長兼最高経営責任者 W・マイケル・フラナガン博士最高科学技術責任者ジェフ筋緊張性ジストロフィーを変革する投資家向け広報およびコーポレートコミュニケーション担当グランデ副社長

7 アジェンダ/概要 RNAの提供に革命をもたらす社長兼最高経営責任者サラ・ボイス、フェーズ3へ:HARBORTM試験スティーブ・ヒューズ、医学博士、CMO • MARINA-OLETMの長期有効性と安全性データジョン・W・デイ、医学博士、スタンフォード大学医学部神経・小児科教授、神経筋医学部長 • 人々への配達 Living with DM1スティーブ・ヒューズ、医学博士、CMO閉会の挨拶社長兼最高経営責任者サラ・ボイス、質疑応答セッションアビディティ・マネジメント、スタンフォード大学モデレーター:ジェフ・グランデ、IR/CC担当副社長

8 0 承認された治療法 DM1:患者への著しい負担と満たされていないニーズ:米国では4万人を超えるDM1患者 • 主に骨格、心臓、平滑筋に影響を及ぼす、認識が低く、進行性で、しばしば致命的な神経筋疾患 • 世代から世代へと重症度が増加する • 生活の質に大きな影響 • Del-Desiranは、DM1の根本原因であるロレーン、クリステル、禅のDM1との共生に対処するように設計されています
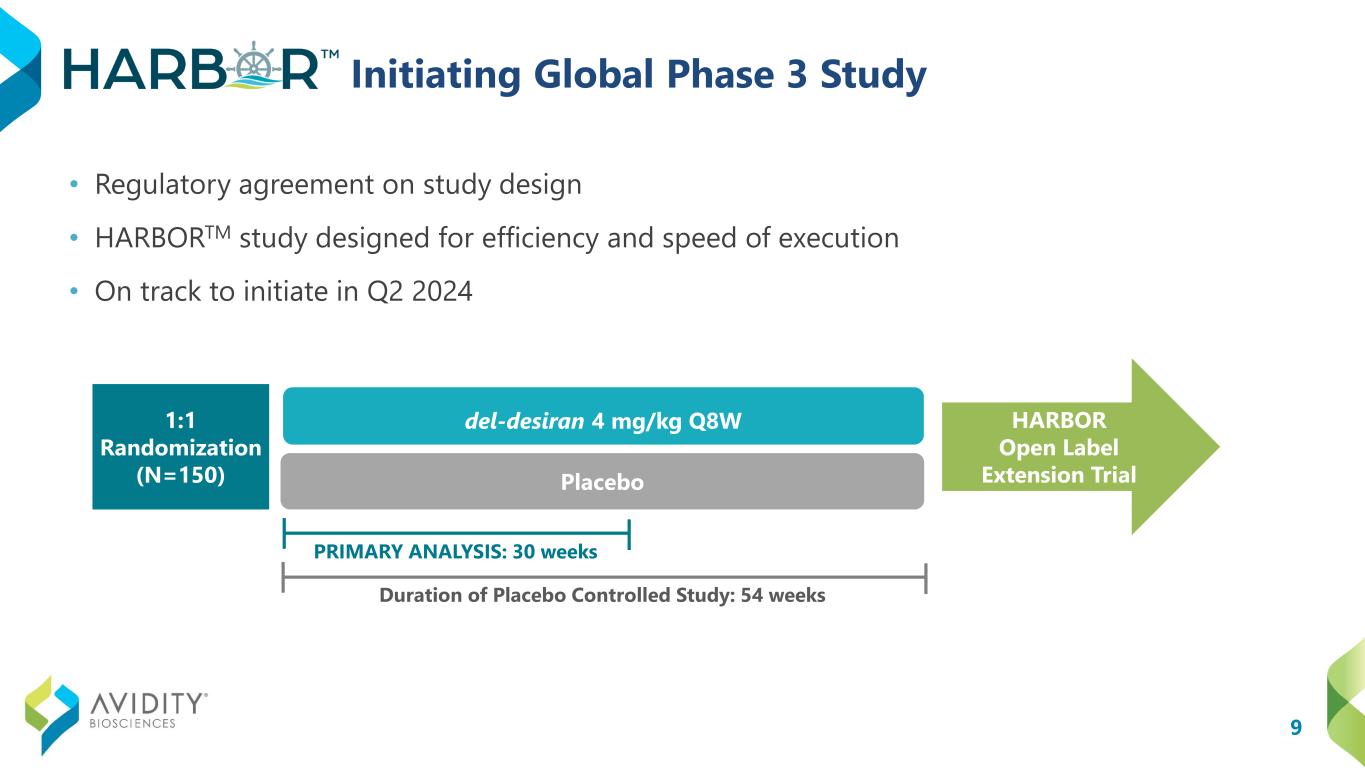
9 グローバル第3相試験の開始 • 研究デザインに関する規制合意 • 効率と実施スピードを重視して設計されたHARBORTM試験 • 2024年第2四半期に開始予定 del-desiran 4 mg/kg Q8W プラセボプラセボ対照試験期間:54週間 HARBORオープンラベル延長試験 1:1ランダム化(N=150)一次分析:30週間
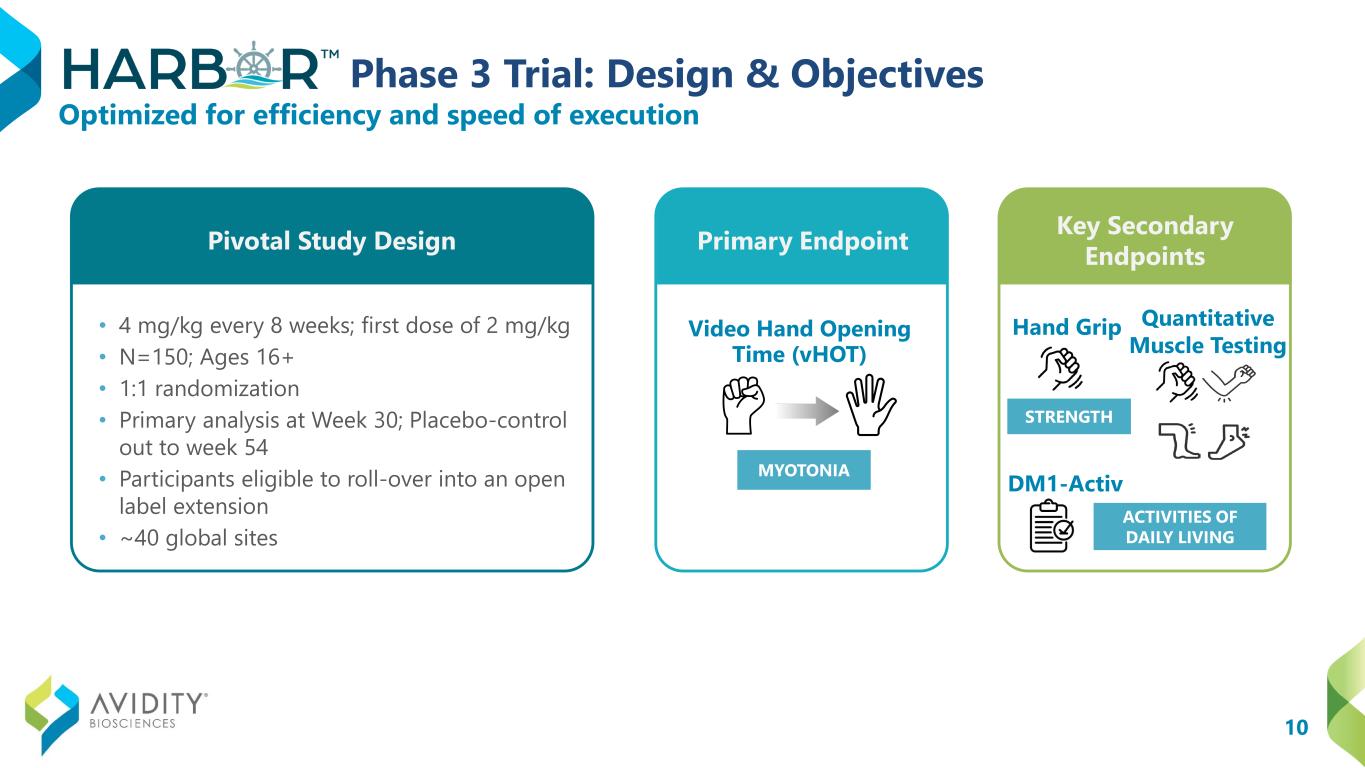
第10相試験:設計と目標 • 8週間ごとに4mg/kg、2mg/kgの初回投与 • N=150、16歳以上、1対1のランダム化 • 30週目に一次分析、54週目までプラセボコントロール • オープンラベルエクステンションへのロールオーバーの対象となる参加者 • 約40のグローバルサイトビデオハンドオープンタイム(VHot)ハンドグリップ定量的筋力検査 DM1-activ 効率と実行速度に最適化されています日常生活における筋力ミオトニア活動ピボタル研究デザイン主要評価項目主要副次評価項目

11 アジェンダ/概要 RNAの提供に革命をもたらす社長兼最高経営責任者サラ・ボイス、フェーズ3へ:HARBORTM試験スティーブ・ヒューズ、医学博士、CMO • MARINA-OLETMの長期有効性と安全性データ John W. Day、医学博士、スタンフォード大学医学部神経・小児科教授、神経筋医学部長 • 人々への配達 Living with DM1スティーブ・ヒューズ、医学博士、CMO閉会の挨拶社長兼最高経営責任者サラ・ボイス、質疑応答セッションアビディティ・マネジメント、スタンフォード大学モデレーター:ジェフ・グランデ、IR/CC担当副社長

ジョン・W・デイ、医学博士、スタンフォード大学医学部神経学、小児科(遺伝学)、病理学教授、神経筋医学部門長 John W. Dayは、スタンフォード大学の神経学、小児科(遺伝学)、病理学の教授であり、神経筋医学部門のディレクターです。デイ博士はミネソタ大学で医学博士号を、アルバート・アインシュタイン医科大学で神経科学の博士号を取得し、シナプス生理学と可塑性を学びました。UCSFで神経学と神経筋トレーニングを終えた後、ミネソタ大学に採用され、神経学、小児科、遺伝学の教授として、ポール・アンド・シーラ・ウェルストーン筋ジストロフィーセンターを設立し、所長しました。2011年、彼はスタンフォード大学に採用され、神経筋医学の総合部門を設立しました。デイ博士は、神経筋疾患の遺伝的原因と多系統的影響を調査し、アンチセンスオリゴヌクレオチドや遺伝子置換療法などの新しい治療法の臨床試験の設計と指導に30年以上携わってきました。12

DM1 13のスペクトルを認識しています
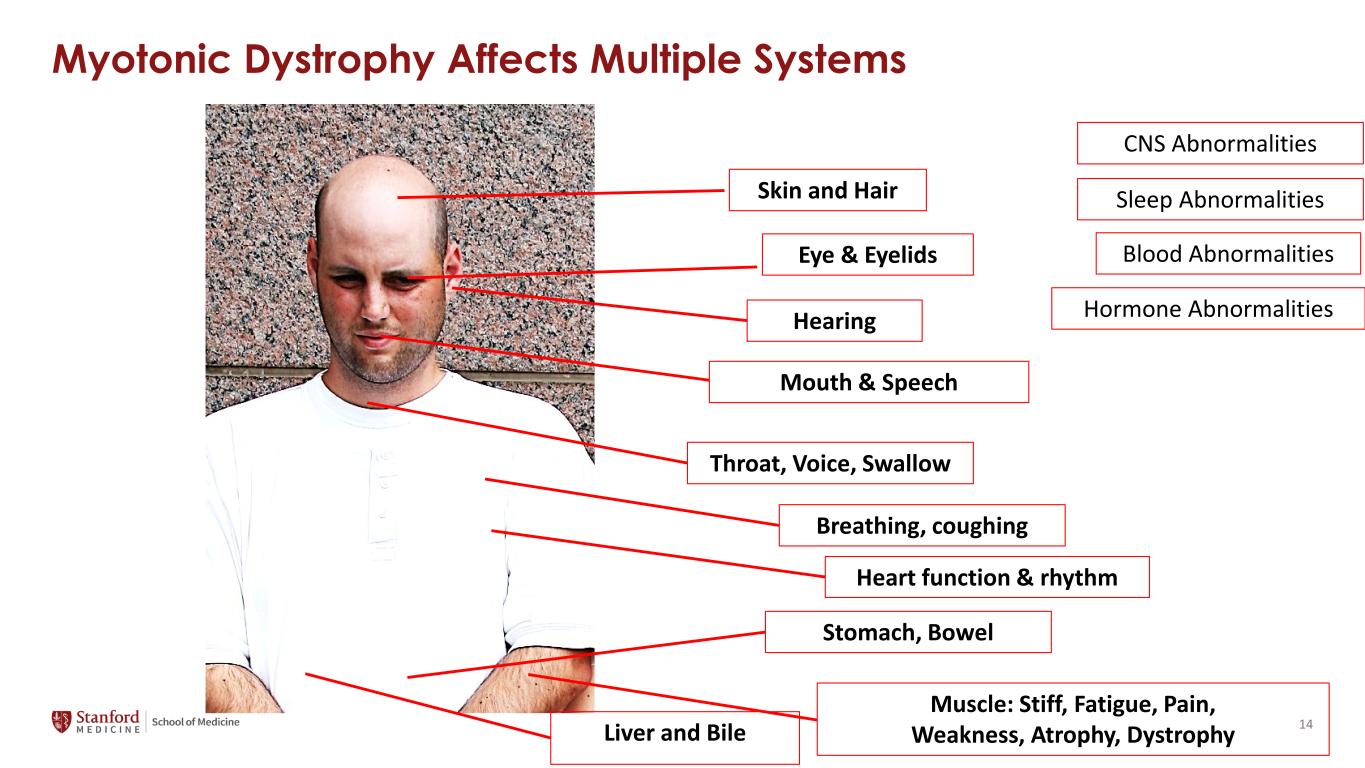
筋緊張性ジストロフィーは複数のシステムに影響を及ぼします目とまぶたの聴覚、口と話、皮膚と毛、声、嚥下呼吸、せき、心機能とリズム胃、腸肝と胆汁筋:こわばり、疲労、痛み、脱力感、萎縮、ジストロフィー、睡眠異常血液異常ホルモン異常 CNS異常 14
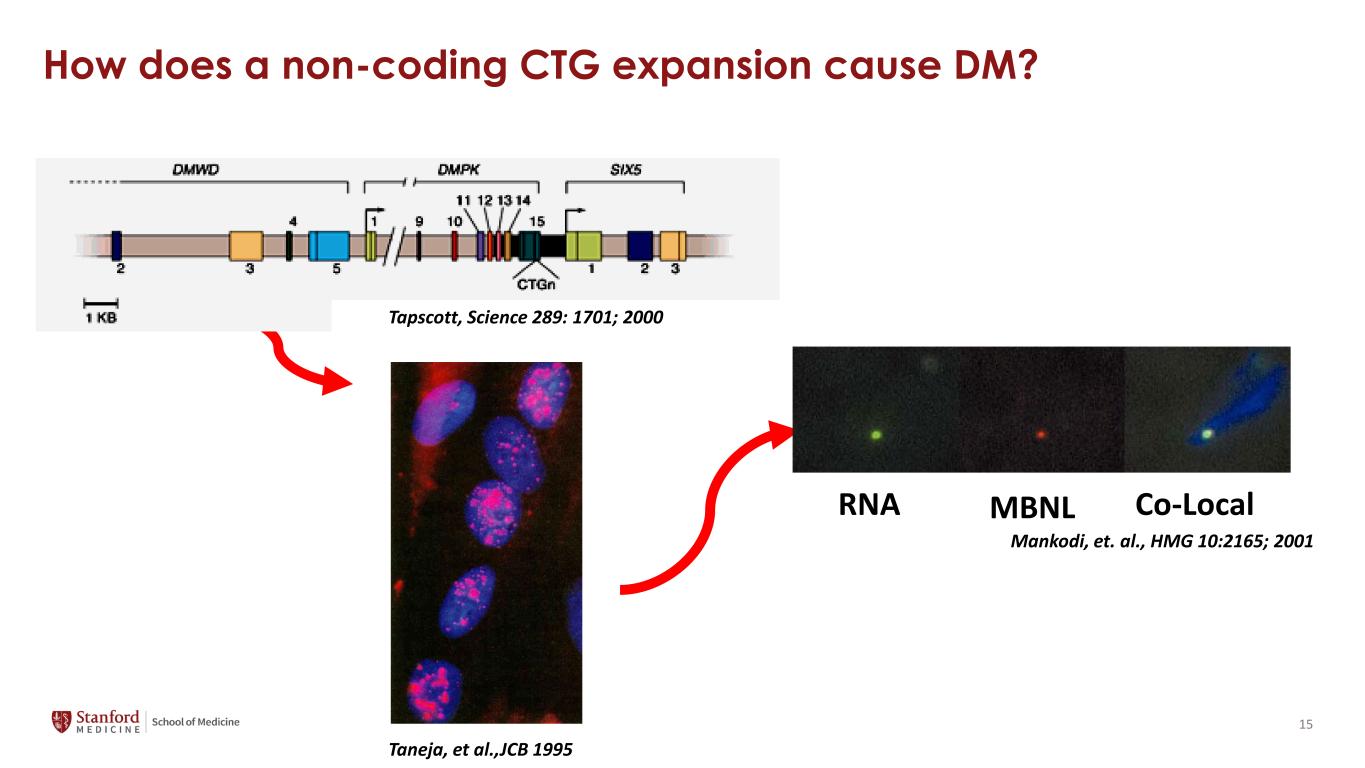
ノンコーディングのCTG拡張はどのようにしてDMの原因になりますか?タネハら。、JCB 1995 RNA MBNL コーローカルマンコディら、HMG 10:2165; 2001 Tapscott、Science 289:1701; 2000 15
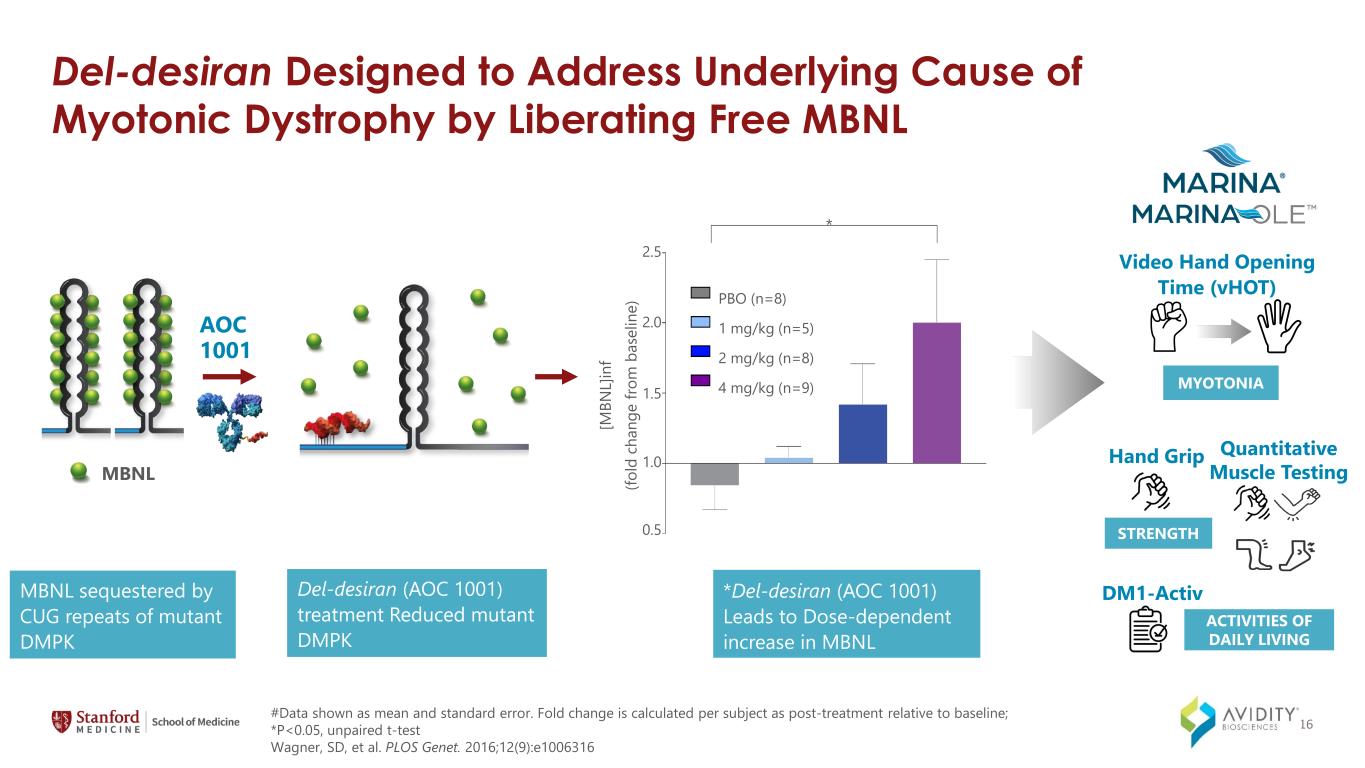
デル・デシランは、無料のMBNL del-Desiran(AOC 1001)治療を解放することにより、筋緊張性ジストロフィーの根本的な原因に対処するように設計されました [M BN L]in f (for ld c ha ng e from m b as el in e) 2.5 2.0 1.5 1.0 0.5 * PBO (n=8) 1 mg/kg (n=5) 2 mg/kg (n=8) 4 mg/kg (n=9) #Data は平均と標準誤差として示されています。倍率変化は、ベースラインを基準にして治療後の被験者ごとに計算されます。* P

DM1 17患者を対象としたMARINA-OLE試験の長期安全性と有効性のデータ
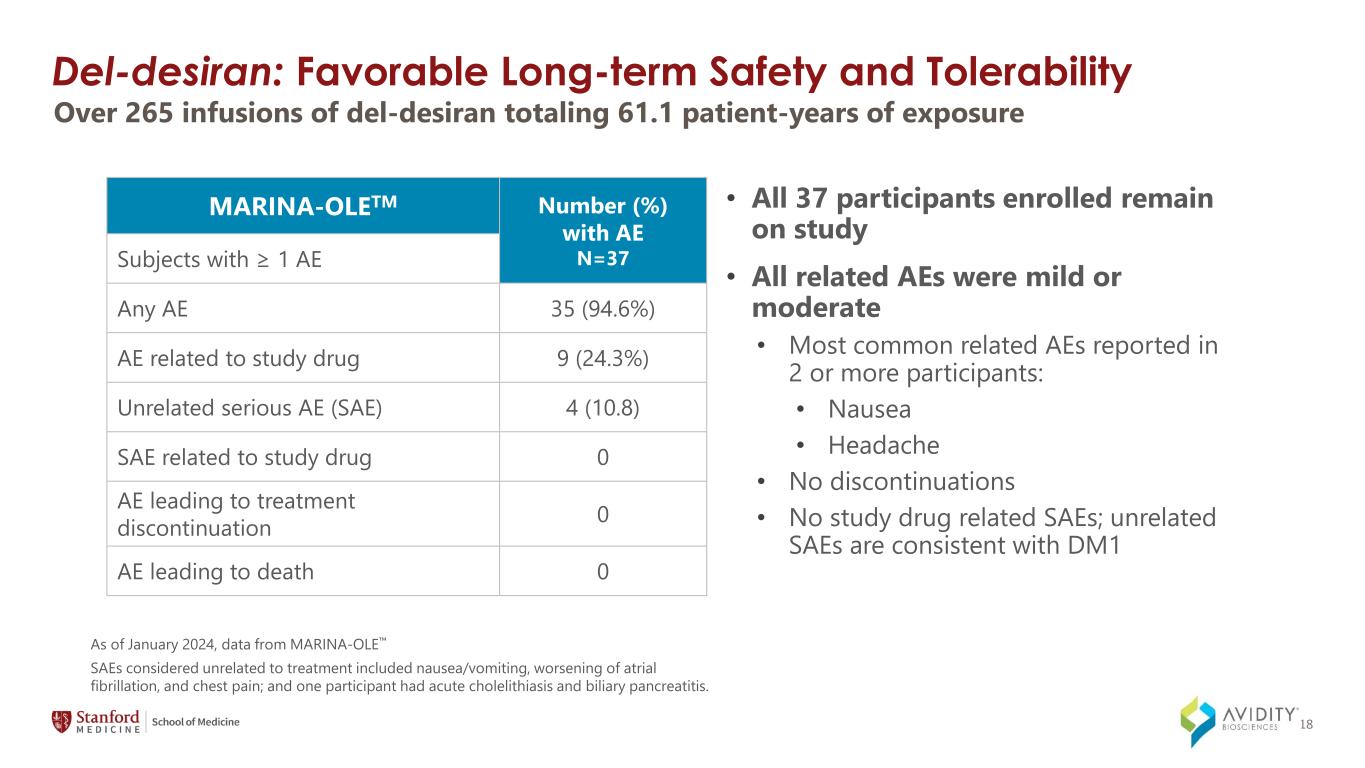
18 del-Desiran:長期にわたる良好な安全性と忍容性 2024年1月現在、MARINA-OLEのデータ • 登録された37人の参加者全員が引き続き治験中 • 関連するAEはすべて軽度または中等度でした • 2人以上の参加者で報告された最も一般的な関連AE:• 吐き気 • 頭痛 • 中止なし、治験薬関連のSAEなし、無関係のSAEは、治療とは無関係と考えられるDM1 SAEと一致しています(吐き気/嘔吐、悪化など)心房細動、胸痛。1人の参加者は急性胆石症と胆道膵炎を患っていました。265回以上のデルデシランの注入、合計61.1患者年の暴露でAE N=37のAEが1歳以上の被験者、治験薬9(24.3%)関連のAE(SAE)4(10.8)治験薬9(24.3%)無関係の重篤なAE(SAE)4(10.8)治験薬に関連するSAE 0 AEが治療の中止につながる 0 AEにつながる 0 AE

19 • DM1患者の疾患進行の理解を深めることを目的とした非介入型NHS • DM1の治療法の開発を支援するために臨床転帰評価に焦点を当てています • 700人の患者、2年間の研究、約20のセンター • 筋緊張性ジストロフィー臨床研究ネットワーク(DMCRN)が設計・運営しています • FDA、MDA、MDFの支援。AvidityはEND-DM1のスポンサー組織の1つです自然史研究:DM1疾患の進行を理解する

20件のEND-DM1データに基づいたMARINA® および第3相HARBOR試験の設計同じエンドポイントの測定済み臨床試験サイトがMARINA® & HARBORの標準治療に基づく現代のデータセットと重複しています END-DM1自然史研究で少なくとも1年間のフォローアップを受けた何百人もの患者今日初めて1年間のデータを提示しました
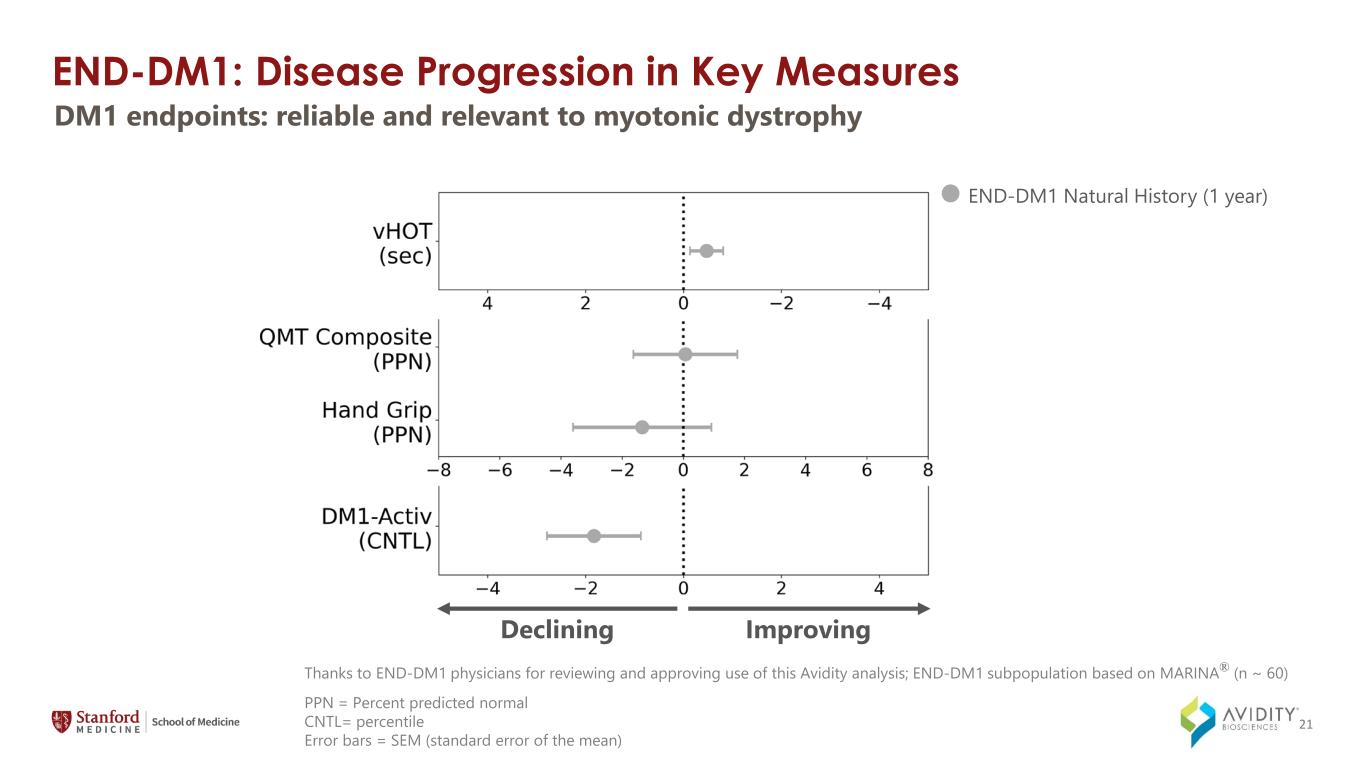
END-DM1:主な対策における疾患の進行 END-DM1自然史(1年)4 mg/kg Q12W(1年)DM1エンドポイントの低下の改善:筋緊張性ジストロフィーとの関連性 PPN = 正常CNTLの予測パーセンタイルエラーバー = SEM(平均の標準誤差)このAviの使用を検討し承認してくれたEND-DM1の医師に感謝しますシティ分析。マリーナ® をベースにしたEND-DM1サブポピュレーション(n ~ 60)21
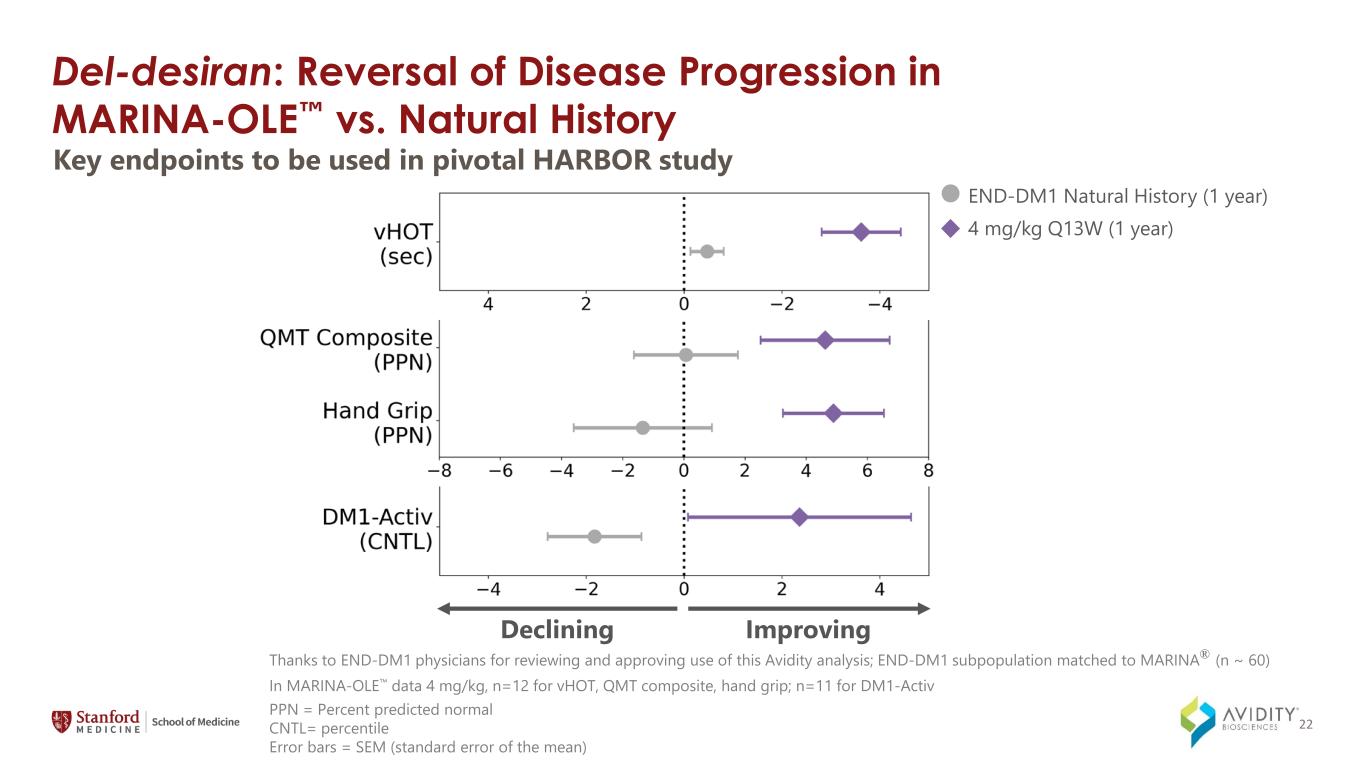
del-Desiran:MARINA-OLEと自然史における病気の進行の逆転PPNの減少の改善 = 正常CNTLの予測率 = パーセンタイルエラーバー = SEM(平均の標準誤差)このアビディティ分析の使用を検討し承認してくれたEND-DM1の医師に感謝します。MARINA®(n)と一致したEND-DM1の亜集団に感謝します。~ 60) MARINA-OLEデータでは 4 mg/kg、VHOT、QMTコンポジット、ハンドグリップの場合はn=12、DM1-Activ END-DM1の場合はn=11 ナチュラルヒストリー (1年) 4 mg/kg Q13W (1年) 22
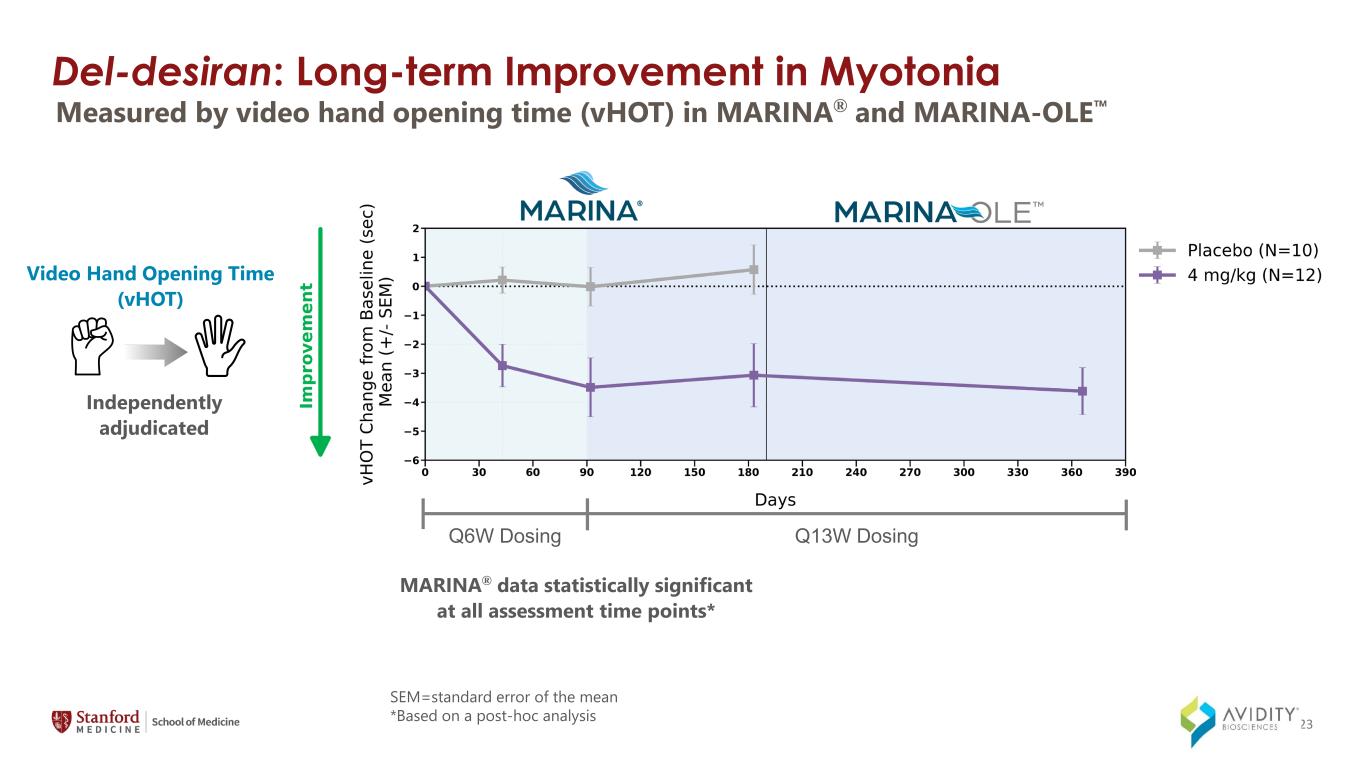
del-Desiran:ミオトニアの長期的な改善MARINA® とMARINA-OLE MARINA® のビデオハンドオープンタイム(VHot)で測定したすべての評価時点で統計的に有意なデータ* ビデオハンドオープニングタイム(VHot)独立判定 Q6Wドージング Q13Wドージング SEM=平均の標準誤差 *事後分析に基づく 23
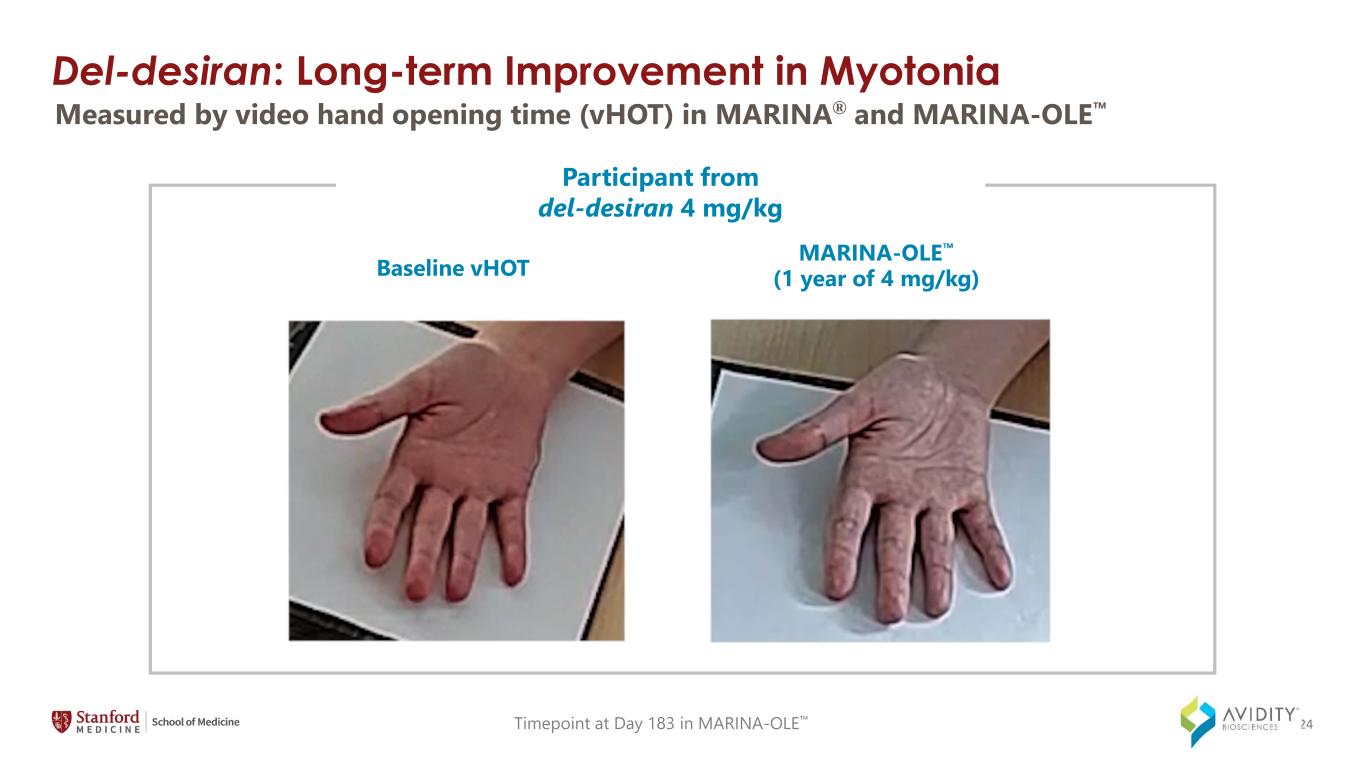
del-Desiran:ミオトニアの長期的改善ベースラインvHot MARINA-OLE(1年4mg/kg)`マリナオレでの183日目のデルデシラン4 mg/kgタイムポイントからの参加者 MARINA® とMARINA-OLE 24のビデオハンドオープンタイム(VHot)で測定しました
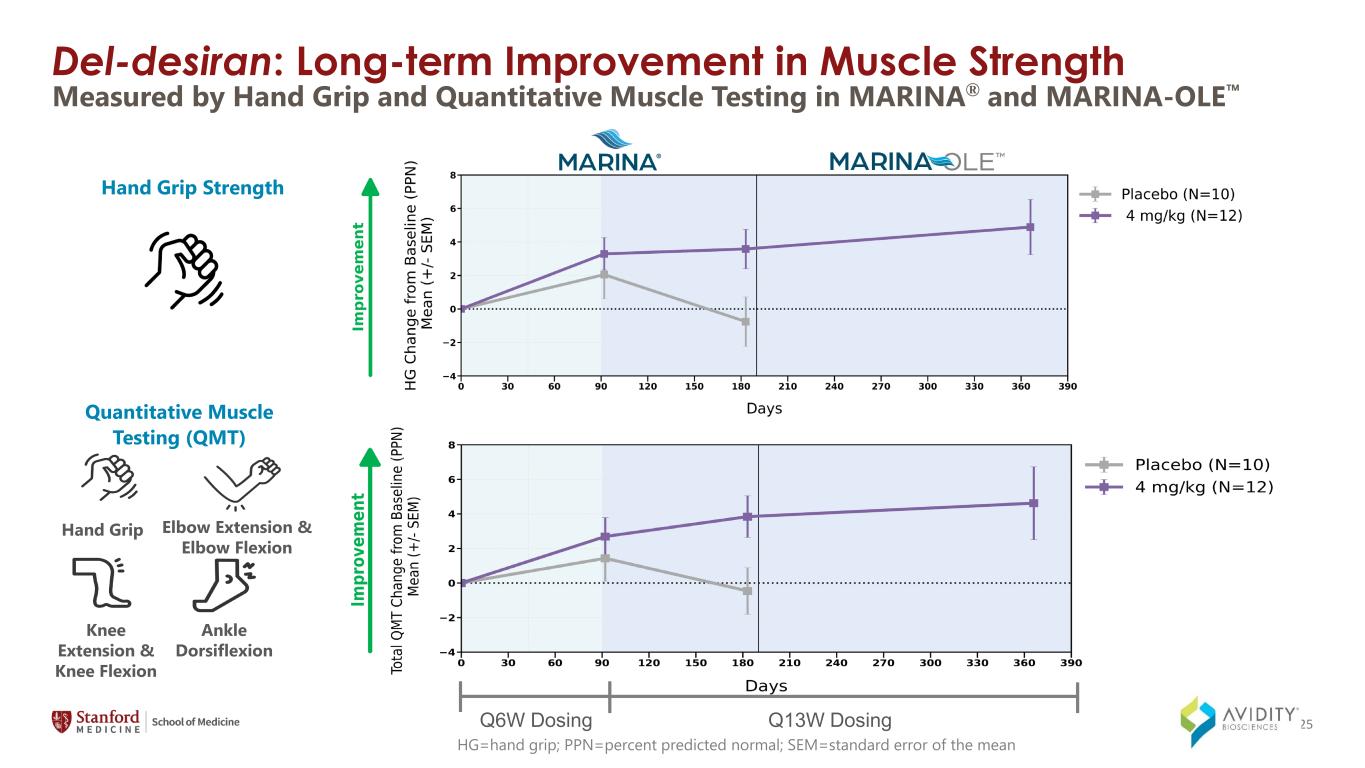
del-Desiran:筋力の長期的改善 HG=ハンドグリップ; PPN=正常予測パーセンテージ; SEM=定量的筋力検査(QMT)平均の標準誤差ハンドグリップ肘伸展と膝屈曲膝伸展と膝屈曲足首背屈ハンドグリップ強度 Q6W投与 Q13W投与ハンドグリップとMARINA® とMARINA-OLE 25での定量的筋力検査
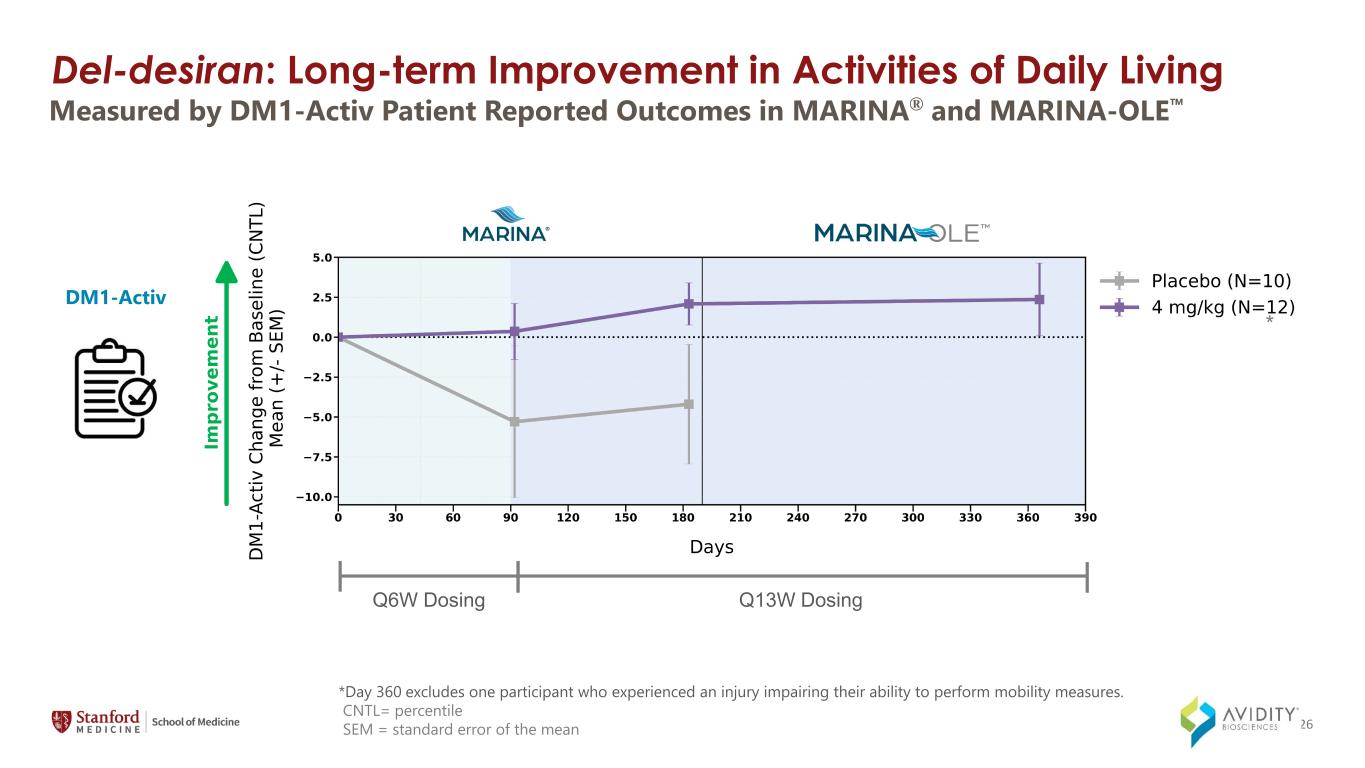
*360日目には、運動能力を損なう怪我をした参加者1名を除きます。CNTL= パーセンタイル SEM = DM1-Activで測定した平均値の標準誤差MARINA® とMARINA-OLE DM1-Activ Q6Wの投与で報告された結果 Q13W投与* 26 del-Desiran:日常生活活動の長期的な改善

27 del-Desiran 4 mg/kg • 長期的に良好な安全性と耐容性を示しました • END-DM1の自然史データと比較して、MARINA® とMARINA-OLEの病勢進行が逆転したことを示しました • 複数の臨床エンドポイントで一貫した持続的な改善が見られました Global HARBOR試験開始 2024年第2四半期のMARINA-OLEデータ要約del-desiranがDM1患者の変革的治療法となる可能性 END-DM1自然史(1年)4ミリグラム/キログラム Q13W(1年)

28 アジェンダ/概要 RNAの提供に革命をもたらす社長兼最高経営責任者サラ・ボイス、フェーズ3へ:HARBORTM試験スティーブ・ヒューズ、医学博士、CMO • MARINA-OLEの長期有効性と安全性データジョン・W・デイ、医学博士、スタンフォード大学医学部神経・小児科教授、神経・小児科教授、神経筋医学部長 • 一緒に暮らす人々への配達 DM1スティーブ・ヒューズ、医学博士、CMO閉会の挨拶社長兼最高経営責任者サラ・ボイス、Q&Aセッションアビディティ・マネジメント&ドクター・デイ、スタンフォード大学モデレーター:ジェフ・グランデ、IR/CC担当副社長

29 患者の経験:del-desiranが彼らの生活に与える影響私はこの薬を6月に始めましたが、最初の点滴を服用してから2週間後に、ポップボトルを開けに行きましたが、それはできませんでした。それはツイストポップのボトルでした... そしてすぐに開きました。私の体力は良くなり、見通しも良くなり、手は機能するようになりました。私にはもっと力があり、伸ばすこともできました。物を開けたり、ドアノブを回したり、もっと難しいものを回したりできました。たとえば、私の二の腕の筋力の方が良かったです。私はもっと上手に歩けました。ネックブレースをいつも着用する必要はありませんでしたし、すべてが大幅に改善されました。「」

30 患者さんの経験:del-desiranが彼らの生活に与える影響研究前は、私はつま先立ちができませんでした。また、運動に戻ってきたので、再びつま先を立てることができました。それで、うまくいけば、ある程度の力をつけることができます。ミオトニア、拳を作っても手を開けません... 問題なく拳を絞って手を開くことができました。私が話すと舌がけいれんしますが、最初の投与以来、その兆候は見られませんでした。「」

31 患者の経験:del-desiranが彼らの生活に与える影響症状が増す前は、私は本当に活発な人だったという事実に、本当に大きな違いがあることに気づきました。注入を数回行った後、私は実際にジムに戻り、トレーナーと一緒に運動を始めることができました。それはすべて、私の機動性が確実に向上したからです。私の可動域も広がりました。私が診断されたとき、治療法も治療法もないと言われたのは驚くべきことだと思います。この研究は私に大きな希望を与えました。それをDM1を持っているコミュニティの他の人々と共有できればいいと思います。「」

32 アジェンダ/概要 RNAの提供に革命をもたらす社長兼最高経営責任者サラ・ボイス、フェーズ3へ:HARBORTM試験スティーブ・ヒューズ、医学博士、CMO • MARINA-OLEの長期有効性と安全性データジョン・W・デイ、医学博士、スタンフォード大学医学部神経・小児科教授、神経・小児科教授、神経筋医学部長 • 一緒に暮らす人々への配達 DM1スティーブ・ヒューズ、医学博士、CMO閉会の挨拶社長兼最高経営責任者サラ・ボイス、Q&Aセッションアビディティ・マネジメント&ドクター・デイ、スタンフォード大学モデレーター:ジェフ・グランデ、IR/CC担当副社長

33 RNA治療薬の提供に革命を起こして人々の生活を大幅に改善するという私たちのビジョン Luke Living with DM1

投資家・アナリスト向けイベントシリーズ — 第8巻トランスフォーミング・ミオトニック・ジストロフィーグローバルフェーズ3 HARBOR治験および長期MARINA-OLEデータに関する質疑応答 2024年3月4日 NASDAQ: RNA | aviditybio.com

投資家・アナリスト向けイベントシリーズ — 第8巻トランスフォーミング・ミオトニック・ジストロフィーグローバルフェーズ3 HARBOR治験および長期マリーナ・オールのデータ 2024年3月4日ナスダック:RNA | aviditybio.com