sgmo-202311022023年11月2日0001001233偽00010012332023-11-022023-11-02 米国
証券取引委員会
ワシントンD.C. 20549
フォーム 8-K
現在のレポート
第13条または第15条 (d) に基づく
1934年の証券取引法の
報告日 (最初に報告されたイベントの日付): 2023年11月2日
サンガモセラピューティクス株式会社
(憲章に明記されている登録者の正確な名前)
| | | | | | | | | | | | | | |
| | | | |
| デラウェア州 | | 000-30171 | | 68-0359556 |
(州またはその他の管轄区域)
法人化) | | (委員会
ファイル番号) | | (IRS) 雇用主
ID番号) |
7000マリーナブルバード, ブリスベン, カリフォルニア94005
(主要行政機関の住所) (郵便番号)
(510) 970-6000
(登録者の電話番号、市外局番を含む)
該当なし
(前回の報告以降に変更された場合、以前の名前または以前の住所)
フォーム8-Kの提出が、次のいずれかの条項に基づく登録者の提出義務を同時に満たすことを目的としている場合は、下の適切なボックスにチェックを入れてください。
| | | | | |
| ☐ | 証券法(17 CFR 230.425)に基づく規則425に基づく書面による通信 |
| | | | | |
| ☐ | 取引法(17 CFR 240.14a-12)に基づく規則14a-12に基づく資料の勧誘 |
| | | | | |
| ☐ | 取引法(17 CFR 240.14d-2 (b))に基づく規則14d-2 (b) に基づく開始前の連絡 |
| | | | | |
| ☐ | 取引法(17 CFR 240.13e-4 (c))に基づく規則13e-4 (c) に基づく開始前の連絡 |
同法第12条 (b) に従って登録された証券: | | | | | | | | | | | | | | |
| | | | |
| 各クラスのタイトル | | トレーディングシンボル | | 登録された各取引所の名前 |
| 普通株式、1株あたり額面0.01ドル | | SGMO | | ナスダック・グローバル・セレクト・マーケット |
登録者が1933年の証券法の規則405(この章の§230.405)で定義されている新興成長企業であるか、1934年の証券取引法の規則12b-2(この章の§240.12b-2)で定義されている新興成長企業であるかをチェックマークで示してください。
新興成長企業☐
新興成長企業の場合は、登録者が取引法第13条 (a) に従って規定された新規または改訂された財務会計基準を遵守するために延長された移行期間を使用しないことを選択したかどうかをチェックマークで示してください。☐
項目 8.01 その他のイベント
SB-525としても知られるGiroctocogene fitelparvovecは、中等度から重度の血友病Aの治療のための遺伝子治療薬候補であり、当社の第1/2相Alta試験と登録第3相AFFINE臨床試験の対象です。私たちは、共同研究者のファイザー社、またはファイザー社とジャイロクトコジーン・フィテルパルボベックを開発しています。私たちとファイザーは、65時のプラットフォームプレゼンテーションで、フェーズ1/2 Alta調査の最新データを発表する予定です。承認された要約の概要は以下にあります。番目の2023年12月11日に開催される米国血液学会年次総会および博覧会。ファイザーは、2024年半ばにジロクトコジーン・フィテルパルボベックを評価する第3相AFFINE試験で極めて重要な結果が出ると予想しています。
ジロクトコゲン・フィテルパルボヴェックの第1/2相ALTA試験の最新の暫定結果の要約
•Altaは、重症血友病Aの成人におけるジロクトコゲン・フィテルパルボベックの安全性と忍容性を評価するための第1/2相単回投与多施設用量範囲試験です。
•重症血友病Aの18歳以上の成人に、4つのコホート(各n = 2)にわたってジロクトコゲン・フィテルパルボベックの4回の段階的投与(9e11、2e12、1e13、および3e13 vg/kg)を注入しました。高用量(3e13vg/kg)コホートは5人の参加者に拡大されました。
•主なエンドポイントには、安全性、循環第VIII因子(FVIII)、活性、FVIII補充療法の使用、出血イベントの頻度が含まれていました。
•研究全体では11人の男性参加者が参加し、3e13-vg/kgの最高用量コホートには5人の参加者がいました。2023年5月19日の締め切り日の時点で、参加者全員が153週間から290週間追跡されています。2人の参加者が156週後に研究を離れました。残りのうち、1人の参加者はまだ4年間(208週間)修了していません。高用量コホート(n = 5)で報告された最も一般的な治療関連の有害事象(AE)は、肝臓酵素の上昇と輸液関連反応、つまりアラニンアミノトランスフェラーゼ(ALT)の増加、n=3 [60.0%])、アスパラギン酸アミノトランス?$#@$ーゼの増加(AST; n = 2 [40.0%])、発熱 (n=3) [60.0%])、および頻脈(n = 2 [40.0%]).
•ジロクトコゲン・フィテルパルボベック注入の約6時間後に発症した低血圧と発熱を経験した最高用量コホートの1人の参加者で、治療関連の重篤な有害事象が報告されました。イベントは治療により完全に解消し、翌日の注入後の退院を遅らせることはありませんでした。
•高用量コホートの参加者の5人中4人で、コルチコステロイドを7日以上摂取する必要があるALTの増加の有害事象が観察されました。ALTの上昇は、FVIII活性の有効レベルを維持しながら、コルチコステロイドの漸減コース(期間中央値:56日、範囲:7〜135日)で管理されました。高用量コホートの参加者は、65週目以降ステロイドを必要とせず、ALT値が正常範囲(フォローアップ:156〜208週間)で、肝臓MRIによる所見は正常です(フォローアップ:104〜208週間)。
•2023年5月19日の締め切り日の時点で、FVIII阻害剤の開発は確認されておらず、血栓性イベントや肝腫瘤も報告されていません。
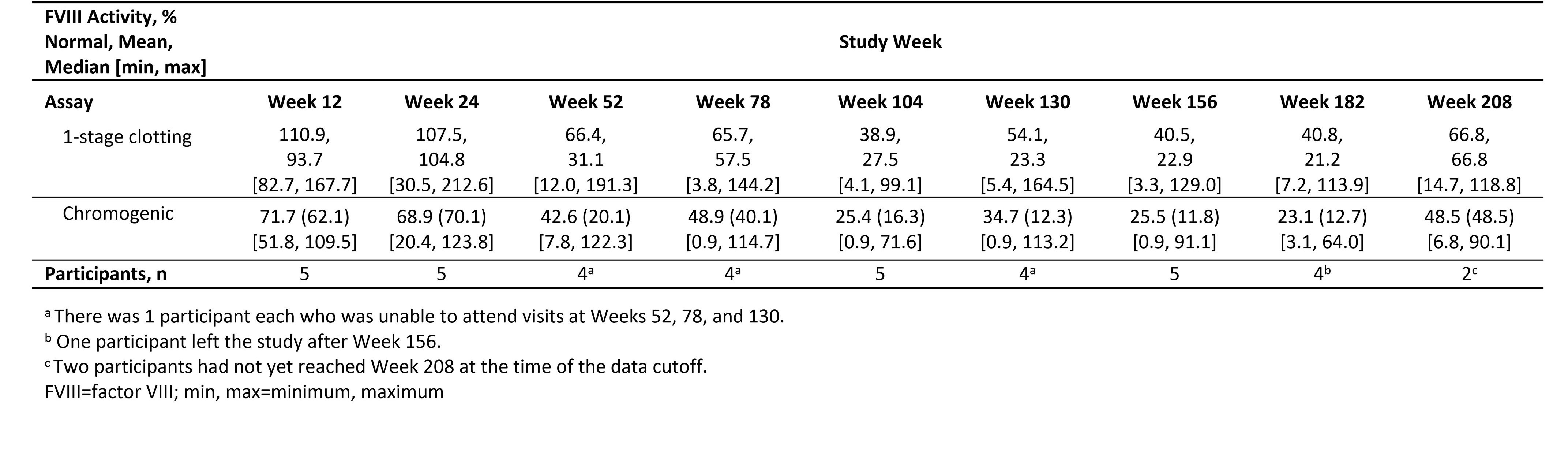
•高用量コホートの5人の参加者のうち、2人は208週目までのデータを入手でき、FVIIIの活動は軽度から正常範囲(下記の表1を参照)に維持され、156週目の結果と一致していました。208週目のデータがない人のうち、2週目には182週目までのデータがありました。1人の参加者はFVIII活性を軽度の範囲(発色分析と1段階アッセイで測定し、それぞれ正常の14.1%と24.1%)で維持しました。もう1人の参加者はFVIII活性が3.1%と7.2%でした。残りの参加者は156週目以降に研究をやめ、FVIIIの活動は穏やかな範囲(11.8%と22.9%)に維持されました。
•高用量コホートでは、年間平均総出血率は [(治験薬注入の3週間後に始まるすべての出血エピソードの数)/(観察期間(年単位))]注入後の最初の1年間は0で、フォローアップの全期間を通して1.2(SD 2.58)でした。このコホートでは、FVIIIの活動レベルが最も低い参加者は合計22件の出血を経験し、そのうち21回は治療が必要でした(8件は外傷性、7件は自発的、6件は不明)。他の4人の参加者は、目的の関節で出血を経験した1人を含め、出血がないか、ごくわずかでした。高用量コホートの参加者は、締め切り日の時点で予防を再開していません。
•重症血友病Aの参加者にジロクトコゲン・フィテルパルボベック遺伝子療法を単回注入しても、注入後約4年間、一般的に良好な耐容性を維持します。持続的なAEがなく、59週目以降の肝機能検査の増加に関連するAEもなく、中等度から正常範囲でFVIIIレベルが上昇します。
表1:ジャイロクトコジーンフィテルパルボベック3e13-vg/kgコホートの1段階および発色分析による第VIII因子活性レベル
署名
1934年の証券取引法の要件に従い、登録者は、登録者に代わってこの報告書に署名させ、正式に権限を与えられた署名者に正式に署名させました。
| | | | | | | | | | | | | | | | | | | | |
| | | | | | |
| | | | サンガモセラピューティクス株式会社 |
| | | |
| 日付:2023年11月3日 | | | | 作成者: | | /s/ スコット・B・ウィロビー |
| | | | 名前: | | スコット・B・ウィロビー |
| | | | タイトル: | | 上級副社長、法務顧問、コーポレートセクレタリー |