| 希少疾患の 治療法の最前線 企業概要 2023年9月 |
| 2 将来の見通しに関する記述 このプレゼンテーションには、1995年の民間証券訴訟改革法の意味における「将来の見通しに関する記述」が含まれています。 製品候補の前臨床および臨床開発、前臨床試験と臨床試験の結果のタイミングと報告、製品候補の規制当局による承認の可能性と時期、 商品化計画、製造および供給計画、資金調達計画、および予測に関するものです。会社の収益とキャッシュポジション。将来の見通しに関する記述を含めることは、 当社の計画のいずれかが達成されることを表明するものと見なすべきではありません。このプレゼンテーションの将来の見通しに関する記述の一部またはすべてが間違っていることが判明する可能性があり、私たちが行う可能性のある不正確な仮定や、既知または未知のリスクや不確実性によって 影響を受ける可能性があります。たとえば、目標、進捗状況、タイミング、結果に関する記述については、新型コロナウイルス関連の混乱の影響を含め、規制当局との 話し合いは、現在の情報に基づいています。COVID-19のパンデミックによる事業への潜在的な影響は本質的に不明であり、自信を持って予測することはできません。また、旅行禁止、 シェルター・イン・プレースオーダー、第三者による事業閉鎖やリソースなど、COVID-19を緩和するための政府当局の取り組みの結果を含め、一般的な政治的および経済的状況への影響のため、実際の結果と業績は を含みますが、これらに限定されません。配分、製造、サプライチェーンの混乱と市販または臨床用 製品への患者のアクセスの制限。COVID-19のパンデミックの影響に加えて、当社の事業に内在するリスクと不確実性のため、実際の結果はこのリリースに記載されているものと大きく異なる場合があります。 には、臨床試験または前臨床研究の結果から製品候補が安全でないまたは効果がないことが示される可能性、 患者を当社の臨床試験に登録することが困難になる可能性、規制当局が以下を含む可能性が含まれますが、これらに限定されません FDA、EMA、MHRA、およびPMDAは、当社製品の承認を付与しない場合や、承認を遅らせたりする場合があります候補者、規制当局による検査が遅れるか成功せず、製品の承認が遅れたり妨げられたりする可能性がある、承認された場合、 ヨーロッパ、日本、米国、その他の地域でのガラフォールドまたはAT-GAAの商品化が成功しない可能性、重篤な副作用や その他の安全上の問題が特定されたために前臨床試験や臨床研究が遅れる可能性、十分な数の臨床製品または市販製品を製造または供給できない可能性があります。また、その可能性 すべての研究と製造を完了するには、追加の資金が必要です。さらに、以前の前臨床試験や臨床試験の結果は、将来の結果を予測できない場合があります。企業財務 ガイダンスと財務目標、およびそのような目標の達成に関する声明。会社の収益とキャッシュポジションの予測に関する記述に関しては、実際の結果は 市場要因と、会社の運営計画と予算計画の実行能力に基づいて異なる場合があります。さらに、将来の見通しに関する記述はすべて、2022年12月31日に終了した年度の Form 10-Kの年次報告書と、2023年6月30日に終了した四半期のForm 10-Qに詳述されているその他のリスクの対象となります。これらの将来の見通しに関する記述( )に過度に依存しないように注意してください。これらの記述は、本書の日付時点でのみ述べられています。すべての将来の見通しに関する記述は、すべてこの注意書きの対象となります。当社は、このニュースリリース リリース日以降の出来事や状況を反映するように改訂または更新する義務を負いません。 非GAAP財務指標 米国会計基準に従って作成された財務情報に加えて、このプレゼンテーションには調整後の財務指標も含まれています。これらの情報は、投資家と経営陣に、業績や傾向に関する 補足情報を提供し、期間間の比較や予測情報の比較を容易にするものです。これらの調整後の財務 指標は非GAAP指標であり、米国会計基準に従って作成された情報に加えて検討すべきですが、それに代わるものではありません。私たちは通常、経営陣が基本業務に影響しないと考えている特定の GAAP項目や、異常項目または非経常項目のGAAP定義を満たさない項目を除外します。他の会社では、これらの 指標をさまざまな方法で定義しているかもしれません。将来の見通しに基づいて非GAAPベースの営業費用の予想を提示する場合、非GAAPベースの予想と対応するGAAP指標との差異の調整は、通常、不当な努力なしには不可能です。これは、 が異常な利益や損失など、関連する将来の期間にGAAP指標から除外される項目について、変動性が高く、複雑で、可視性が低い可能性があるためです。除外項目の変動性は、将来のGAAP業績に重大な、そして潜在的に 予測不可能な影響を与える可能性があります。 |
| 3 二桁の収益 持続的な成長、グローバルな商業インフラ、後期開発能力を備えた、希少疾患に特化したバイオテクノロジー企業 20か国の企業 GALAFOLD & POMBILITI + OPFOLDA 遺伝子治療 プラットフォーム br} タンパク質 エンジニアリング と糖鎖生物学 における の経験を活用 14-18% CER での23年度ガラフォールド の収益成長 非GAAP 収益性 2023年下半期に見込まれる収益性 累計15億ドル- ピークポテンシャル AT-GAA ポンペ病 に関する米国 規制審査中。23年6月30日現在、2億6,600万ドル 現金 、世界クラスの 臨床 開発 能力 |
| 2023 の戦略的優先事項 CER1でガラフォールドの2桁の収益成長を維持 AT-GAA の安全なFDA、EMA、MHRAの承認を受けましょう AT-GAA Advance クラス最高の次世代FabryおよびPompeパイプライン プログラムと機能 収益性への道のりにおいて堅調な財政状態を維持してください 4 1 2 3 4 5 1 CER:固定為替レート。2023年のガラフォールドの収益ガイダンスでは、2022年12月31日現在の実際の為替レートを使用しています |
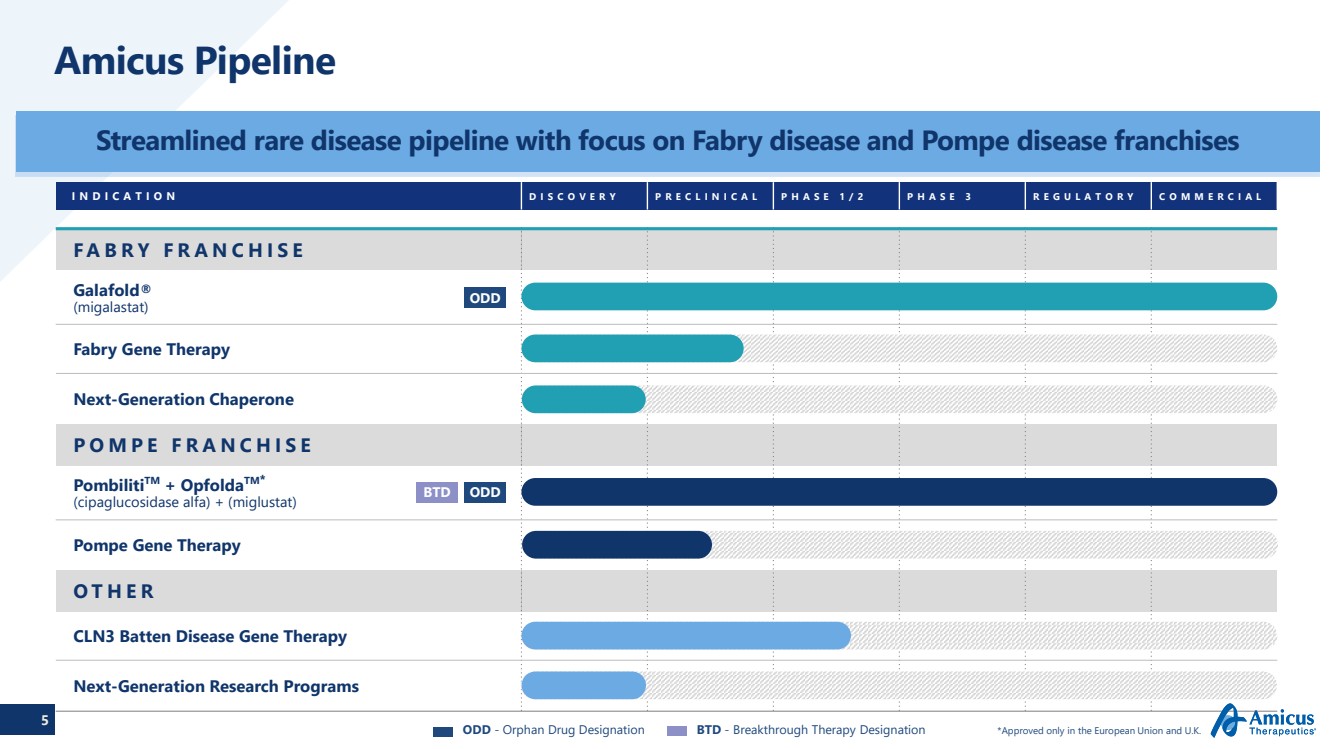
| 5 Amicus Pipeline ファブリー病とポンペ病のフランチャイズに焦点を当てた希少疾患パイプラインの合理化 適応症発見前臨床フェーズ 1/2 フェーズ3 レギュラトリーコマーシャル FABRY FRANCHISE Galafold® (migalastat) ファブリー遺伝子治療 次世代シャペロン POMPE FRANCHISE PombilitiTM + Op foldATM* (シパグルコシダーゼアルファ) + (miglustat) Pompe Gene Therapy OTHER CLN3 バッテン病遺伝子治療 次世代研究プログラム ODD ODD-希少疾病用医薬品指定 BTD-ブレークスルーセラピー指定*欧州連合と英国でのみ承認されています。 |
| 6 Galafold® (migalastat) 継続的な成長 ファブリー病の治療における指導的地位の構築 |
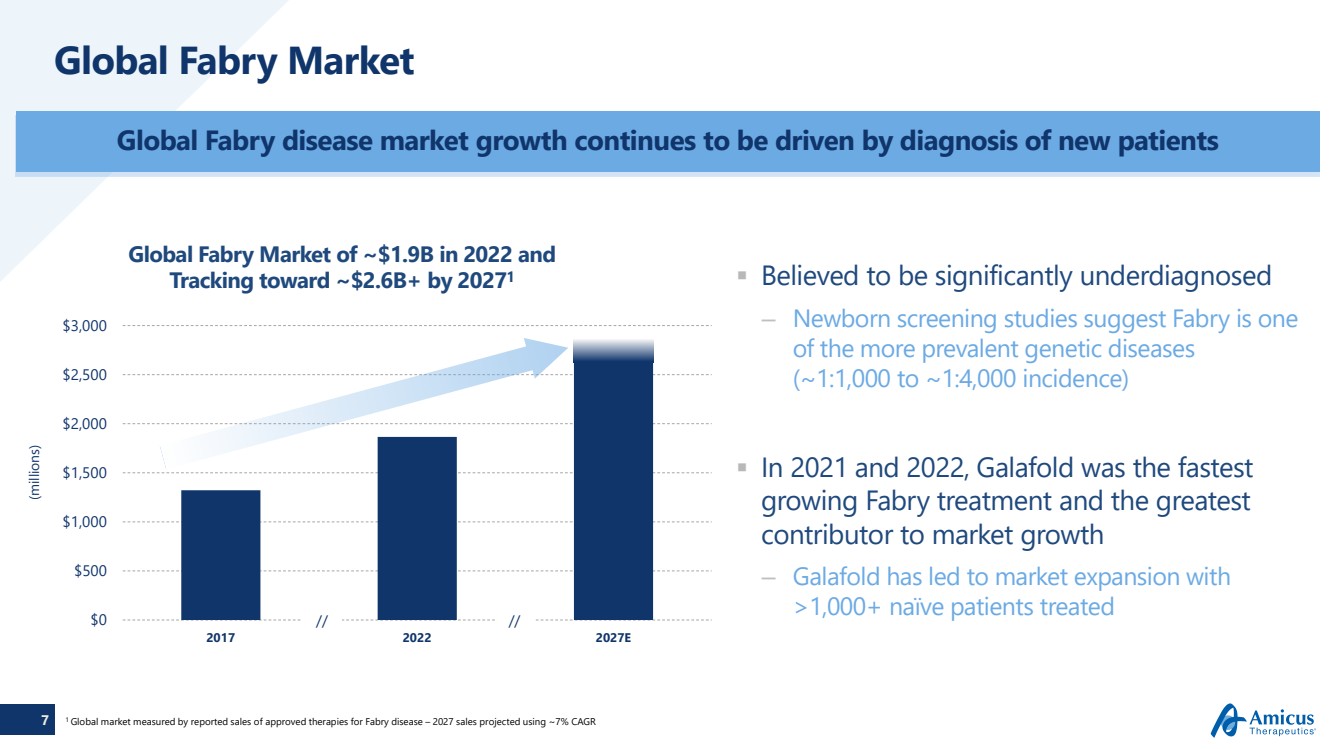
| 7 世界のファブリー市場 は診断がかなり不足していると考えられます — 新生児スクリーニングの研究によると、ファブリーはより蔓延している遺伝病の1つ (発生率約1:1,000〜1:4,000) です。2021年と2022年、ガラフォールドはファブリー治療薬の中で最も急速に成長し、市場の成長に最大の 貢献しました — ガラフォールドは市場をリードしました の治療を受けたナイーブ患者数が1,000人を超えることによる拡大 世界のファブリー病市場の成長は、引き続き新規患者の診断によって牽引されています (数百万) 1 承認されたものの報告された売上高で測定される世界市場ファブリー病の治療法 — 2027年の売上高は、約7%のCAGR で500ドル、1,000ドル、2,000ドル、2,500ドル、3,000ドルと予測されています。2017 2022 2027E 世界のファブリー市場は2022年に約19億ドルに達し、 は20271年までに約26億ドル以上になると予測されています//// |
| 8 2023 ガラフォールドサクセス(2023年6月30日現在) ガラフォールドの成功を踏まえ、指導的地位を活用して継続的な成長を推進 ガラフォールドは、ファブリー病と適応性のある変異と診断されたことが確認された成人に適応されます。ガラフォールド(≥ 10%) で報告された最も一般的な副作用は、頭痛、鼻咽頭炎、尿路感染症、吐き気、発熱でした。米国の処方情報全文など、ガラフォールドに関する追加情報については、 https://www.amicusrx.com/pi/Galafold.pdf をご覧ください。毒素学や投与方法、特別警告、 薬物相互作用、副作用など、ガラフォールドのその他の重要な安全性情報については、EMAのウェブサイト(www.ema.europa.eu)から入手できるガラフォールドの欧州sMPC for Galafoldをご覧ください。 Galafoldは、順応性のある変異体 35-50% Fabry患者 Fabry患者 Galafoldに順応できる、 規制 承認を取得している40か国以上 国 オレンジブック 上場特許 53 Orange Book 上場特許 9,430万ドル 23年第2四半期ガラフォールド 収益 14-18% 2023 ガラフォールド CER での事業成長 での事業成長 の治療を受けた 従順な 患者のシェア |
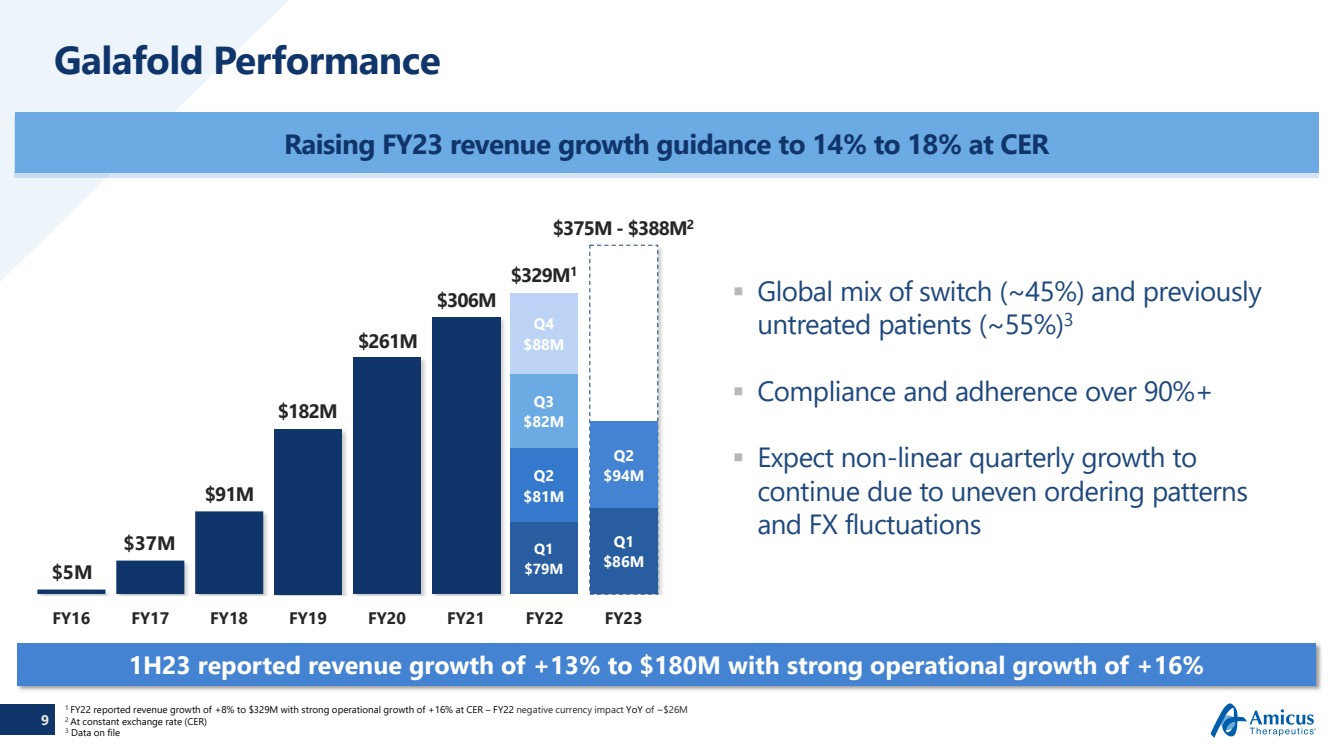
| 9 Galafold Performance CER スイッチのグローバル構成(約45%)と以前 未治療患者(約55%)で23年度の収益成長予想を14%から18%に引き上げ3 コンプライアンスと順守 90%以上の順守注文パターンの不均一な注文パターン と為替の変動により、 の四半期成長は非直線的な伸びを続けると予想しています 2016年度 20会計年度 22会計年度23年度 500万ドル 第1四半期7900万ドル 第2四半期8100万ドル 第3四半期8100万ドル 第4四半期8200万ドル 3,700万ドル 9100万ドル 2億6100万ドル 3億600万ドル 23年上半期の収益は 13% 増加して1億8000万ドルになりました Mは、第1四半期に3億2900万ドルと堅調な事業成長を遂げました 第1四半期には8,600万ドル 3億7,500万ドル-388M2ドル、第2四半期には9400万ドルです 1年の22年度の収益は8%増の3,2900万ドルで、CERでの営業成長は16%と力強い伸びを記録しました。22年度の通貨のマイナスの影響は前年比で約2,600万ドルでした。2 固定為替レート(CER)で 3 登録されているデータ |
| 10 Galafold Global Commercial Momentum(2023年6月30日現在) 患者の強い需要と主要指標に対する業績は、2023年も二桁成長を続けるための基礎を築きました 既存市場への継続的な浸透 診断を受けた未治療集団のさらなる増加 継続的な地域拡大とラベルの拡大 コンプライアンスと順守の維持 償還とアクセスの促進 持続的に 2023年の成長の原動力: |
| 11 Pombiliti®(シパグルコシダーゼアルファ) + Opfolda®(ミグルスタット) ポンペ病患者のための新しい標準治療 を確立する可能性 |
| 12. リソソーム グリコーゲンの蓄積と細胞 機能障害 につながるGAAの欠損は、小児期から成人期までの 人生のさまざまな段階で診断されます。 症状には、進行性の筋力低下、特に骨格筋と呼吸器の 筋力低下が含まれ、時間の経過とともに悪化します。 呼吸不全は の主要な死因です ~5,000-10,000 世界中で と診断された人々; 著しい過少診断 世界全体で約12億ドル以上のPompe ERT 売上1 現在の 標準治療を受けている患者の大多数は、 の晩期発症型ポンペ病(LOPD) 概要 1 2022年12月31日に終了した12か月に基づいています。ソース:サノフィプレスリリース 遅発性ポンペ病は、酵素酸 α-グルコシダーゼ(GAA)の欠乏によって引き起こされる、希少で衰弱性の生命を脅かすリソソーム障害です |
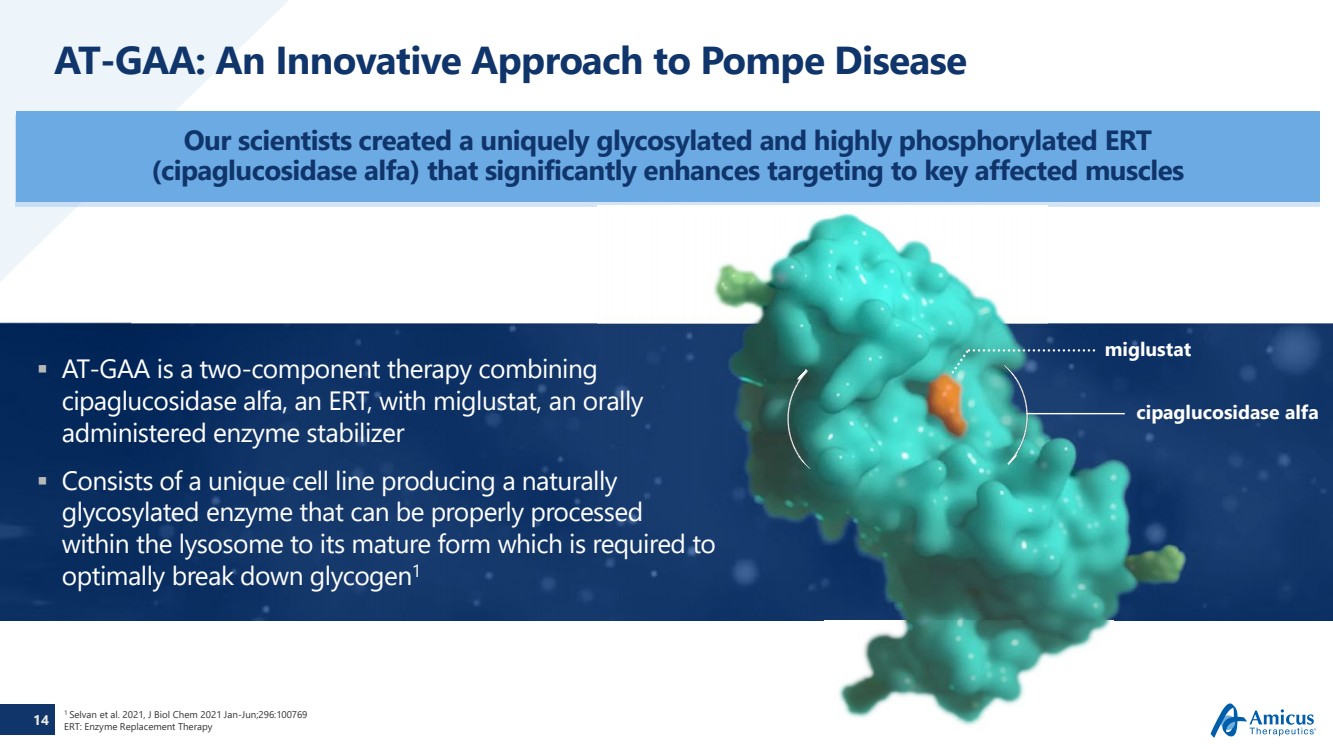
| 13 世界のポンプ市場 世界のポンペ病市場の成長は、引き続き新規患者の診断によって推進されています 世界中の推定3,500〜4,000人のポンペ患者 は、2022年に約12億ドルのERT3グローバルポンプ市場によって治療されており、20271年(百万)までに18億ドル以上になる見込みです。 0ドル 200ドル 400ドル 600ドル 800ドル1,000ドル1,200ドル 400ドル 1,600ドル 1,800ドル 2,000ドル 2017 2022 2027E 1 ポンペ病の承認済み治療法の報告売上高で測定した世界市場 — 2027年の売上高は約8%のCAGR 2を使用して予測されています。2022年度に報告されているように、マーケットマッピングからファイル上のアミカスデータが3件報告されています //// 米国 41% ヨーロッパ 37% その他の国 22% グローバルポンプ市場売上高分割 FY20222 |
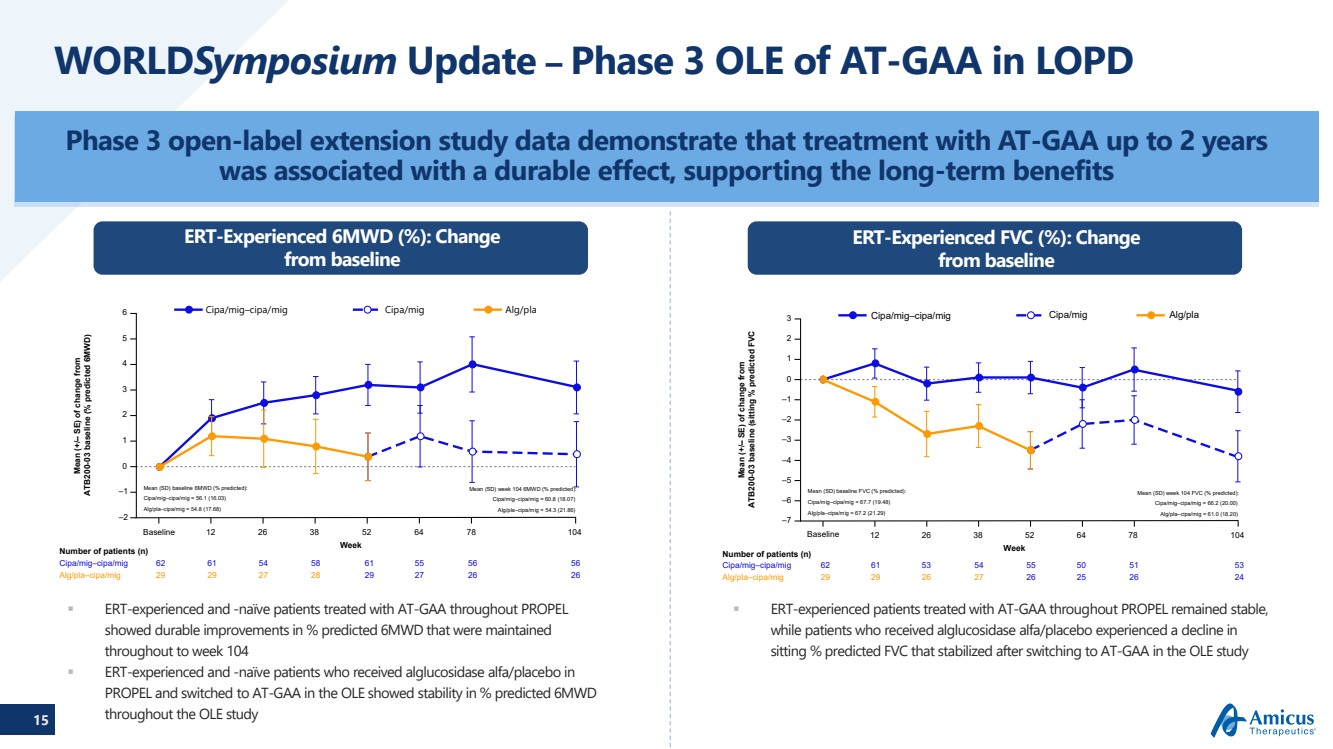
| 14 AT-GAA: ポンペ病への革新的なアプローチ 私たちの科学者たちは、影響を受けた主要な筋肉へのターゲティングを大幅に強化する、独自のグリコシル化および高リン酸化ERT (シパグルコシダーゼアルファ)を開発しました AT-GAAは、 シパグルコシダーゼアルファ(ERT)とミグルスタット(経口投与)を組み合わせた二成分療法です 投与された酵素安定剤 は、天然の グリコシル化酵素を産生するユニークな細胞株で構成されています。この酵素は、リソソーム内で を適切に処理して 、グリコーゲン1を最適に分解するのに必要な成熟型に加工できますシパグルコシダーゼアルファ miglustat 1 セルバン他 2021、J Biol Chem 2021 1月-6月; 296:100769 ERT: 酵素補充療法 |
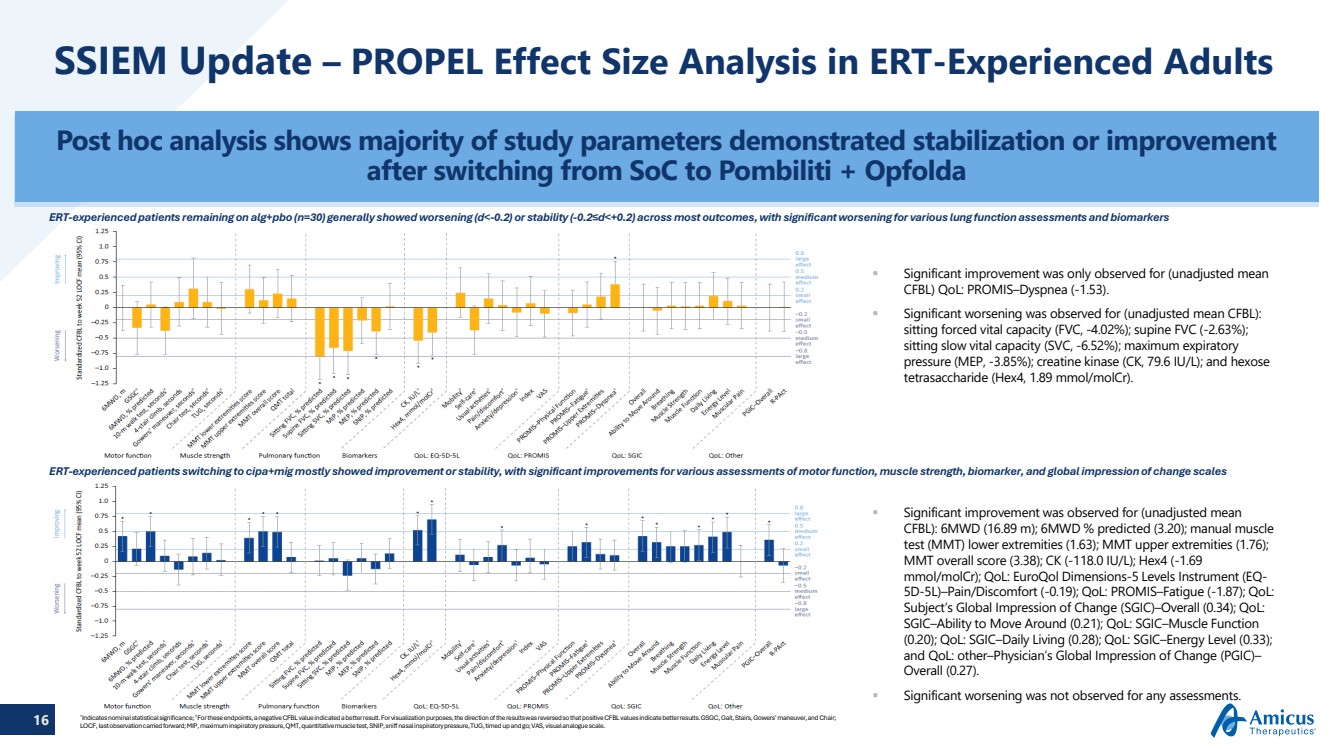
| 15ワールドシンポジウムの最新情報 — LOPD におけるAT-GAAのフェーズ3 OLE(患者数)(n) 平均値(SD)ベースライン6MWD(予測%): CIPA/Mig—CIPA/MIG = 56.1(16.03) ALG/PLA—CIPA/MIG = 54.8(17.68) 平均(SD)週 104 6MMM WD (予測%): CIPA/mig—CIPA/MIG = 60.8 (18.07) alg/PLA—CIPA/MIG = 54.3 (21.86) 6 CIPA/mig—CIPA/MIG CIPA/MIG ALG/PLA ベースライン 週 12 26 38 52 64 78 104 —1 —2 0 1 2 3 4 5 CIPA/mig—CIPA/MIG 62 61 54 58 61 55 56 56 alg/PLA—CIPA/MIG 29 29 27 27 26 ATB200-03ベースラインからの平均変化量(+/— SE)(予測値:6MWD) 平均(SD) ベースラインFVC (予測%): CIPA/mig—CIPA/MIG = 67.7 (19.48) alg/PLA—CIPA/MIG = 67.2 (21.29) SD) FVC第104週平均 (%): CIPA/Mig—CIPA/MIG = 66.2 (20.00) alg/alg/PLA—CIPA/MIG = 61.0 (18.20) —7 —3 —1 0 1 2 3 CIPA/mig—CIPA/MIG CIPA/MIG ALG/PLA —4 —2 —6 週目の患者数 (n) 12 26 52 64 78 104 CIPA/mig—CIPA/MIG 62 61 53 54 55 50 51 53 alg/PLA—CIPA/MIG 29 29 26 27 26 26 26 26 24 ベースライン ATB200-03ベースラインからの平均変化量(+/— SE)(座位%予測FVC FVC )第3相非盲検延長試験のデータによるとAT-GAAによる最長2年間の治療には持続的な効果があり、長期的な効果を裏付けていました PROPEL 全期間にわたってAT-GAAで治療されたERT経験のある未熟な患者は、 にアルグルコシダーゼアルファ/プラセボを投与されたERT経験者で未経験の患者で104週目まで維持された予測6MWDの割合で持続的な改善を示しました。 PROPELとOLEでAT-GAAに切り替えたところ、OLE試験全体を通して予測6MWD の割合が安定していました。 PROPEL全体を通してAT-GAAで治療されたERT経験のある患者は、安定したままでした、 一方、アルグルコシダーゼアルファ/プラセボを投与された患者は 座っている時間が低下しました。一方、OLE研究 ERTエクスペリエンス6MWD(%)では、 の座りが低下したと予測したFVCの割合(%):ベースラインからの の変化(%):ベースラインからの の変化 |
| 16 SSIEMアップデート — ERT経験のある成人を対象としたPROPEL効果量分析 事後分析では、SoCからPombiliti + Opfolda に切り替えた後、研究パラメータの大部分が安定または改善を示したことが示されました 。有意な改善は(未調整平均 CFBL)QOL:Promis—呼吸困難(-1.53)でのみ観察されました。 (調整前の平均CFBL)で有意な悪化が観察されました: 座位強制肺活量(FVC、-4.02%)、仰臥位FVC(-2.63%)、 座位低速肺活量(SVC、-6.52%)、最大呼吸 圧(MEP、-3.85%)、クレアチンキナーゼ(CK、79.6 IU/L)、およびヘキソース 四糖(Hex4、1.89 mmol/molCr)。 (未調整平均 CFBL)で有意な改善が見られました:6MWD(16.89 m)、6MWD予測%(3.20)、手動筋肉 テスト(MMT)(MMT)下肢(1.63)、MMT上肢(1.76)、 MMT総合スコア(3.38)、CK(-118.0 IU/L); Hex4 (-1.69 mmol/molCr); QoL: EuroQol Dimensions-5レベル計測器 (EQ-5D-5L) —痛み/不快感 (-0.19); QoL: 約束—疲労 (-1.87); QoL: 被験者のグローバルな変化の印象(SGIC)—全体(0.34); QoL: SGIC—動き回る能力(0.21); QoL: Sgic—筋肉機能 (0.20); QoL: Sgic—Daily Living (0.28); QoL: SGIC—エネルギーレベル(0.33)、 、QoL:その他—医師の世界的な変化の印象(PGIC)— 全体(0.27)。 どの評価でも有意な悪化は見られませんでした。 ERTを経験した患者(alg+pbo)のまま(n=30)は、一般的に悪化しました(d |
| 17 17 1ファイル グローバル規制状況 規制当局の承認を受け、2023年にはポンペの3大市場に投入される予定です。Pombiliti® + Opfolda® は英国で承認されました。 Pombiliti® + Opfolda® がEUで承認されました 米国食品医薬品局との最近の契約に基づいて、 承認は近日中に予定されています 17 |
| 18件の進行中の臨床研究とアクセスの拡大メカニズム LOPDと乳児発症型ポンペ病(IOPD) 患者を対象とした進行中の臨床研究1 米国、英国、ドイツ、フランス、日本などで 複数の拡張アクセスメカニズムが実施されています 最初の規制当局承認の時点で、ATで ポンペ病を患っている人は約200人です普及研究と アクセス拡大プログラムにわたるGAA 現在、世界中の約75のセンターが臨床試験 とアクセスプログラム に参加しています。継続的ではありますが、科学を進歩させています臨床研究と複数のメカニズムによる アクセスの拡大 1 0歳の子供と青少年 |
| 19 Pombiliti + Opfolda EU Opportunity 注意事項: — Pombiliti®(シパグルコシダーゼアルファ)は、遅発性ポンペ病 (酸性αグルコシダーゼ)の成人の治療に酵素安定剤Opfolda® (ミグルスタット)と組み合わせて使用される長期の酵素補充 療法です [GAA]欠乏) ヨーロッパでは1,300人以上の患者が治療を受けると推定されています1 — 現在Pombiliti + Opfoldaを服用しているEU全域で約60人の患者、 ドイツとオーストリアの約20人を含む ドイツでの開始 — 6か月の「無料価格」期間とAMNOG償還プロセス — 最初の患者が投与され、注入を開始する予定の追加の患者 1 Am マーケットマッピング EU Pompe市場からファイルに保存されているICUSデータは、現在、4億5000万ドル以上の大きな市場機会となっています |
| 20 Pombiliti + Opfoldaの立ち上げがEUで進行中 発売の初期を支援する 経験豊富で情熱的な希少疾患の商業医療機関 発売初期の支援 アクセスと 支払い者との積極的な交流 幅広い患者へのアクセスに焦点を当てる 国別 償還プロセス 償還プロセス 活発な議論 価値を示す 患者の需要 臨床試験 とアクセスの拡大された患者 に最初に焦点を当てた。最初に投与された患者; 複数の 点滴が予定されている すべての試験 への移行とアクセスの拡大に向けて順調に進んでいる90日以内のドイツの患者 KOL と患者 アウトリーチ プロモーションと教育 取り組み 主な治療センターの 医療従事者との既存の関係 最初の30日以内にトップ処方者 の関与 継続的な疾病教育 パフォーマンス |
| 21 企業の展望 患者と 株主に向けた私たちの使命を果たす |
| 財務見通しと収益性への道 事業を構築し、ポートフォリオを進め、収益性を達成するための明確な戦略 22 収益の維持 成長 財務目標の達成 財務目標の達成 の確保 2023年上半期の売上高、 前年比16% 事業成長 2023 ガラフォールド CER Galafoldと AT-GAAの収益 成長指針は前年比14〜18%増で は 、長期的には2桁の力強い成長を牽引すると予想されています。慎重な 経費管理に注力 2023年下半期に収益性1を達成1 1 Amicusの非GAAPベースの予測に基づく現在の事業計画に基づく純利益。これには、AT-GAA規制当局の承認の成功とガラフォールドの継続的な成長が含まれます。非GAAP純利益は、株式ベースの報酬費用、条件付対価の公正価値の変動、減価償却、買収関連収益(費用)、負債の消滅損失、資産の減損損失、リストラ費用、所得税の影響を除いたGAAP純利益と定義しています。 2023 非GAAPベースの営業 経費ガイダンス は、3億3000万ドルから3億5000万ドルです。 |
| 23 大幅な価値成長のポジション 実行に重点を置き、収益性への道のりにおける持続可能な二桁の収益成長の推進 は引き続き できる限り多くの 患者にGalafold® を提供し、 2桁の 営業上の 収益の伸びを維持します と同居する人々 のためのAT-GAAの立ち上げに成功疾患 ファブリー病と ポンペ病における 次世代 遺伝子治療を推進 の希少疾患 のリーダーとして のグローバルな 能力と のインフラをフル活用して の非GAAP を実現20231年下半期の収益性 1 現在の事業計画におけるアミカスの非GAAP純利益の予測に基づいています。これには、AT-GAA規制当局の承認の成功とガラフォールドの継続的な成長が含まれます。非GAAP純利益は、株式ベースの 報酬費用、条件付対価の公正価値の変動、資産の減損損失、減価償却、買収関連収益(費用)、負債の消滅による損失、事業再編費用および所得税の影響を除いたGAAP純利益として定義されます。 |
| 24 成功の真の尺度: 希少疾患を持つ人々の生活への影響 17 2023+ >2,000人の患者* 数千人の患者* YE22 >350人の患者* *臨床および市販の数字はすべて概算です |
| 付録 |
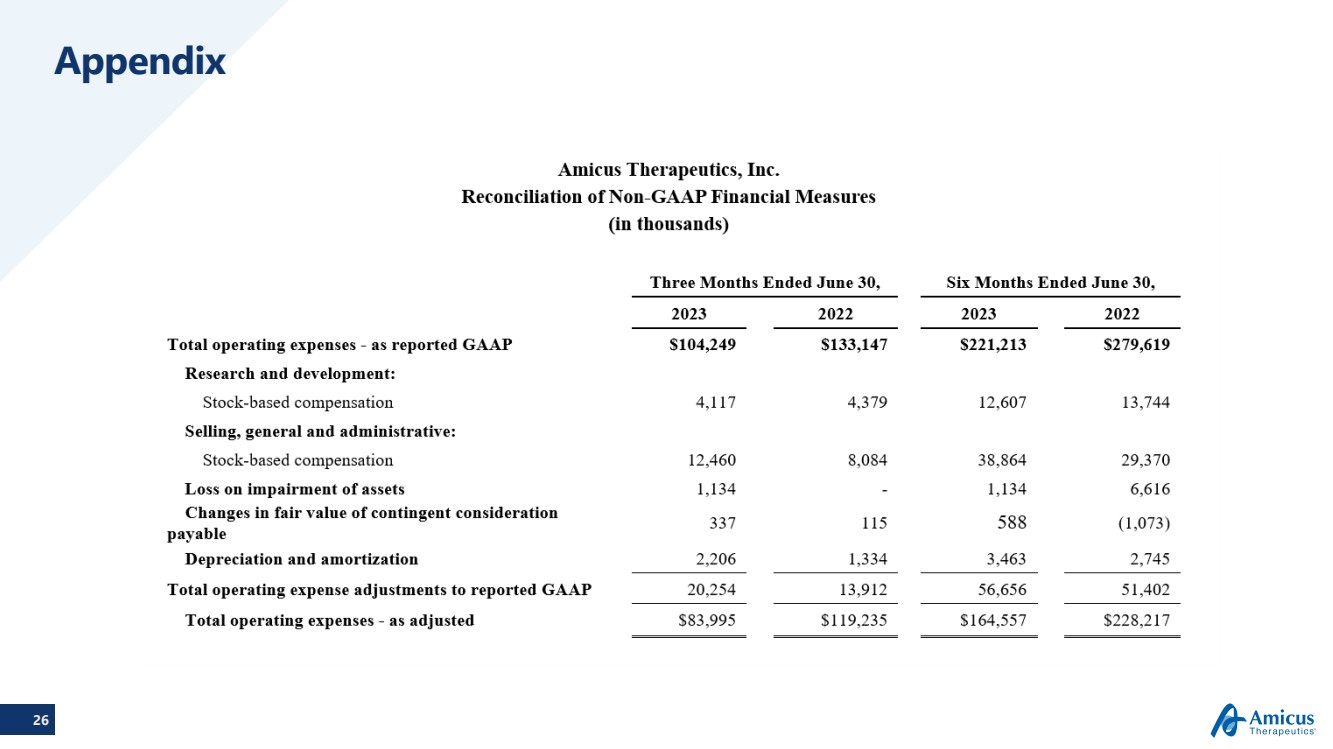
| 26 付録 |
| 2023 2023 環境、社会、ガバナンス(ESG)スナップショット 取締役会 の継続的な改善と の背景、性別、スキル、経験の多様性を約束します。 理事会 独立性 取締役会 取締役会 取締役会 希少な遺伝病への対策 ファーストインクラスまたはクラス最高の は 患者に有意義な利益をもたらします br} 484 グローバル従業員 57% 女性従業員 私たちが奉仕する人物 私たちの使命は、 環境と 持続可能性 の原則を取り入れることで、パートナー と共に持続可能性 を推進することです。すべての 私たちの商用 関係に 治癒の誓約 治療法が見つかるまで、製品収益の一部をその特定の疾患の 研究開発に充ててください。私たち が投資している プログラムには3つの重要な 特徴があります 3 女性 2 退役軍人ステータス 1 アフリカ系アメリカ人 ディレクター多様性 採用率 97% 従業員の能力と専門知識を活用して、パフォーマンスを向上させ、最終的に重要な人材を引き付け、活気づけ、維持する 文化を提供します。 従業員の採用、 エンゲージメント、定着 Pulseの調査によると、従業員は自分の仕事に高い個人的な 満足感を感じ、自分の仕事 と自分がコミュニティに貢献していることに誇りを持っています キャリア開発 は、何をどのように測定するかを測定し、 ミッション重視の行動をロールモデル化した人に報酬を与えています。 事業において、環境 に対する責任を果たし、 持続可能性のベストプラクティスを順守しながら、 の患者さん向けに変革をもたらす医薬品を製造することに尽力しています。 環境 管理 0% アミカス所有の直接製造と 関連の温室効果ガス排出量 ダイバーシティ、エクイティ、および インクルージョン(DEI) は、従業員、コミュニティ、社会に影響を与える、よりインクルーシブな文化を支援することを誓います。 目標は、性別の多様性を維持し、 世界中の従業員全体にわたって多様性を高めることです。 580ボランティア時間 (米国): 22 Amicusが支援する コミュニティプログラム: 79人の患者/19か国 2023年2月までのアクセス拡大: 価格設定PROMISE 割り当てられた拠出金: 2,288,998ドル米国 954,349ドル 慈善寄付 当社の 製品の年間価格を消費者のインフレ率以上に上げることは決してないと約束しています。 |
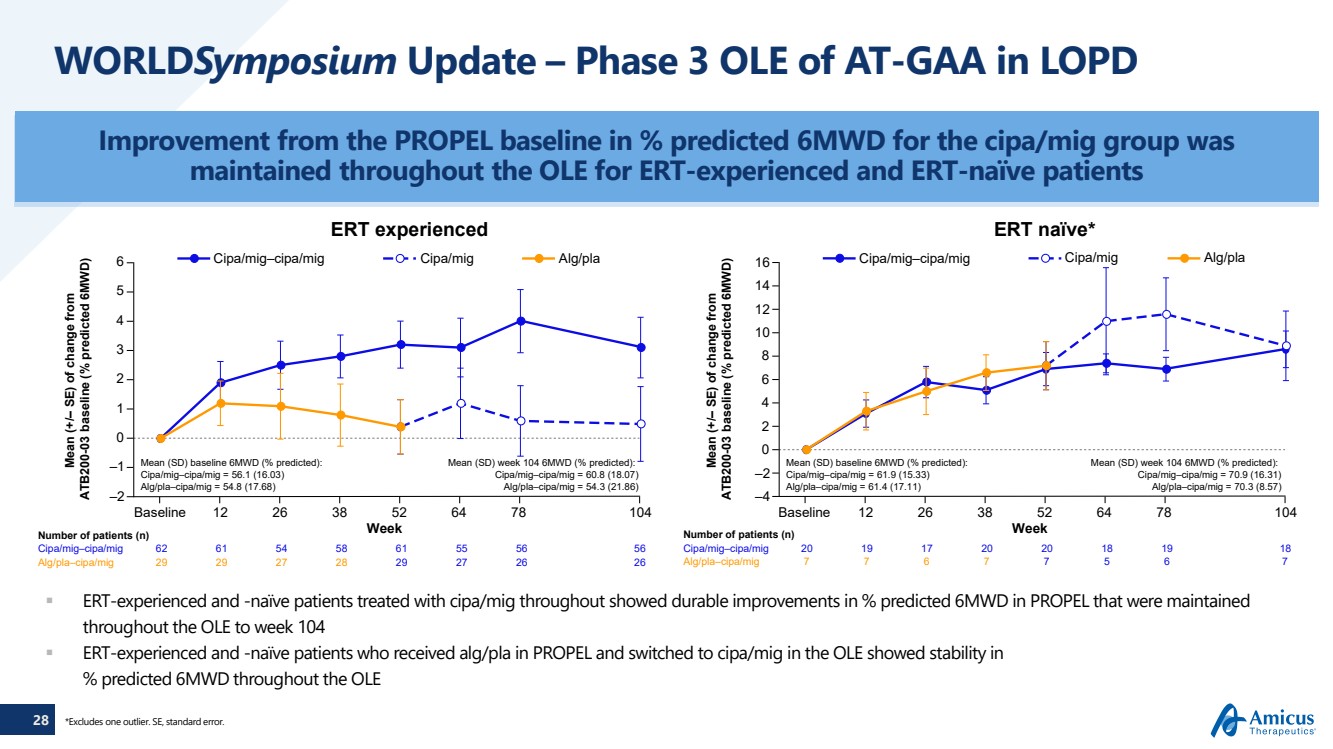
| 28 WorldSymposiumの更新 — LOPD におけるAT-GAAのフェーズ3 OLE PROPELベースラインからの改善。ERTを経験した患者とERT未経験の患者を対象に、cipa/migグループの6MWDがOLE全体にわたって 維持されました ERT経験者で未経験の患者は、全体を通して6MWDの予測率で持続的な改善を示しましたこれは、OLEから104週目まで維持されました。PROPELでalg/plaを投与し、OLEでcipa/migに切り替えたERT経験豊富でナイーブな患者は、OLE全体で %の予測値6MWDが安定していました。} *1つの外れ値を除外します。SE、標準誤差です。 患者数 (n) 平均 (SD) ベースライン 6MWD (予測率): CIPA/mig—CIPA/MIG = 56.1 (16.03) alg/PLA—CIPA/MIG = 54.8 (17.68) SD (SD) 週平均 (SD) 104週平均 6MWD (予測%): CIPA/MIG—CIPA/MIG /mig = 60.8 (18.07) alg/PLA—CIPA/MIG = 54.3 (21.86) 6 CIPA/mig—CIPA/MIG CIPA/MIG ALG/PLA ベースライン 週 12 26 38 64 78 104 患者数 (n) 12 26 38 64 52 78 104 平均 (SD) ベースライン 6MWD (予測%): CIPA/mig—CIPA/MIG = 61.9 (15.33) alg/PLA—CIPA/MIG = 61.4 (17.11) 週平均 (SD) 104週目 6MWD (予測%): CIPA/MIG—cipa/mig = 70.9 (16.31) alg/PLA—CIPA/MIG = 70.3 (8.57) —2 —4 0 2 4 4 6 8 12 10 14 16 —1 —2 0 1 2 3 4 5 CIPA/MIG CIPA/MIG CIPA/MIG ALG/PLA cipa/mig—cipa/mig Alg/PLA cipa/mig—CIPA/MIG 62 61 54 58 55 56 56 29 27 26 26 CIPA/Mig—CIPA/MIG 20 19 17 20 18 18 ALG/PLA—CIPA/MIG 29 27 27 28 alg/PLA—CIPA/Mig 7 7 7 7 7 6 7 {7 7 7 7 7 7 7 7 7 7 — SE( — SE) ATB200-03ベースラインからの変化の平均(+/ — SE)(予測値:6MWD) (予測率:6MWD)) 平均(+/ {{{ — ATB200-03ベースラインからの変化(予測6MWDの割合) ERTが経験したERTナイーブ* |
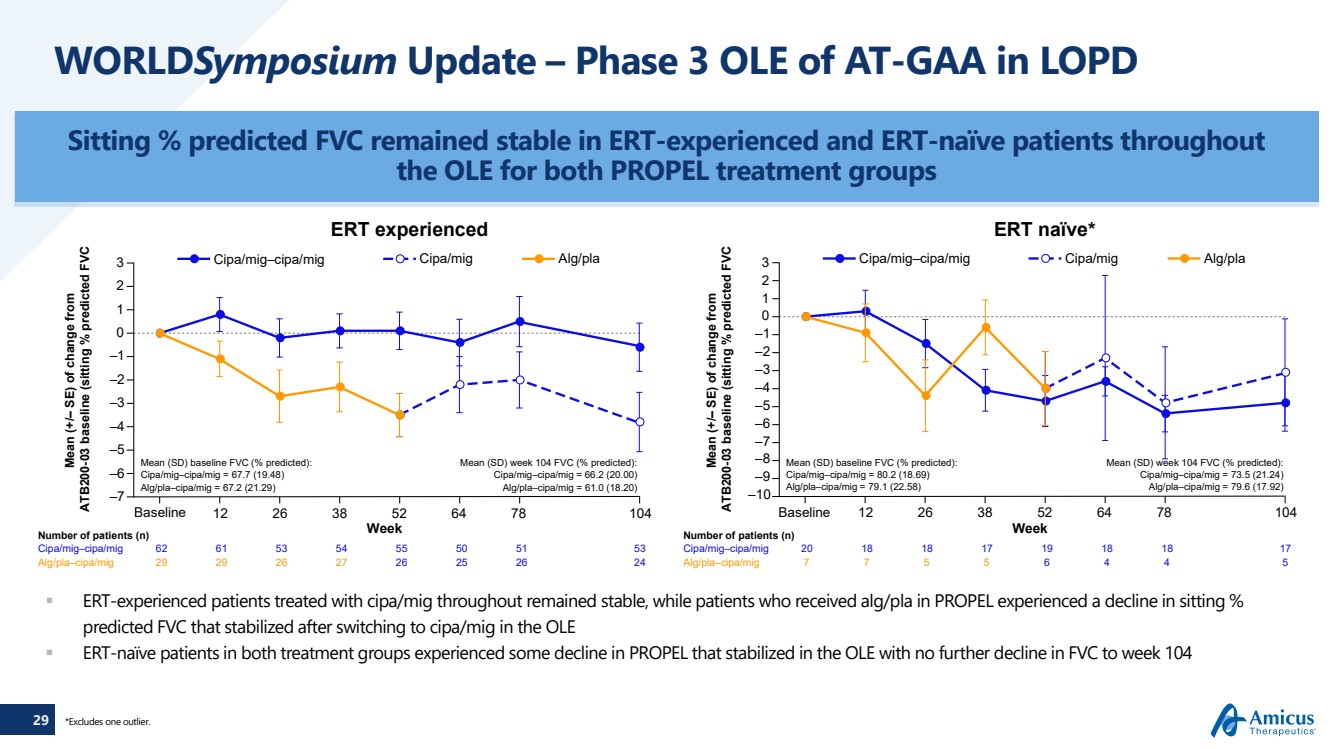
| 29 WorldSymposium Update — LOPD におけるAT-GAAのフェーズ3 OLEは、 全体で、ERT経験のあるERT未経験の患者でFVCが安定していると予測しました。両方のPROPEL治療群 のERT経験患者のOLEは、CIPA/migで治療されたERT経験のある患者のOLEはずっと安定していました。一方、PROPELでALG/PLAを投与された患者は、座位率が低下しました(% )は、FVCを予測しました。OLE でCIPA/migに切り替えた後に安定しました。どちらの治療群でもERT未経験の患者は、PROPELがいくらか低下しましたが、OLEでは安定しましたが、FVCはそれ以上低下しませんでした。104週目までの平均(SD)ベースラインFVC(予測%): CIPA/Mig—CIPA/MIG = 67.7(19.48) alg/PLA—CIPA/MIG = 67.2(21.29) FVC週平均(21.29) FVC週平均(予測%): CIPA/MIG = 66.2(20.00) alg/PLA—CIPA/MIG = 61.0 (18.20) —7 —5 —3 —1 0 1 2 3 CIPA/mig—CIPA/MIG CIPA/MIG ALG/PLA —4 —2 —6 平均(SD)ベースラインFVC(予測%): CIPA/MIG = 80.2(18.69)) alg/PLA—CIPA/MIG = 79.1 (22.58) FVC第104週平均 (SD) (予測%): CIPA/mig—CIPA/MIG = 73.5 (21.24) alg/PLA—CIPA/MIG = 79.6 (17.92) —7 —10 —4 0 —6 —9 —2 1 —2 —1 —5 —8 —1 2 3 チパ/mig —cipa/mig CIPA/MIG ALG/PLA 104 —3 患者数 (n) 週 12 26 38 52 64 78 104 患者数 (n) 週 12 26 38 52 64 78 CIPA/mig—CIPA/MIG 62 61 53 54 55 50 51 53 26 26 24 cipa/mig—cipa/mig 20 18 18 17 19 18 18 17 alg/PLA—CIPA/MIG 29 29 26 27 alg/PLA—CIPA/MIG 7 7 5 5 5 6 4 5 ベースライン ERT 経験豊富な ERT naïve* ( — SE)の ({br)( )( )( ) (SE)は ATB200-03 ベースラインからの変化の平均(+/ — SE) ATB200-03ベースラインからの変更(予測FVC のシッティング率)*1つの外れ値を除外します。 |
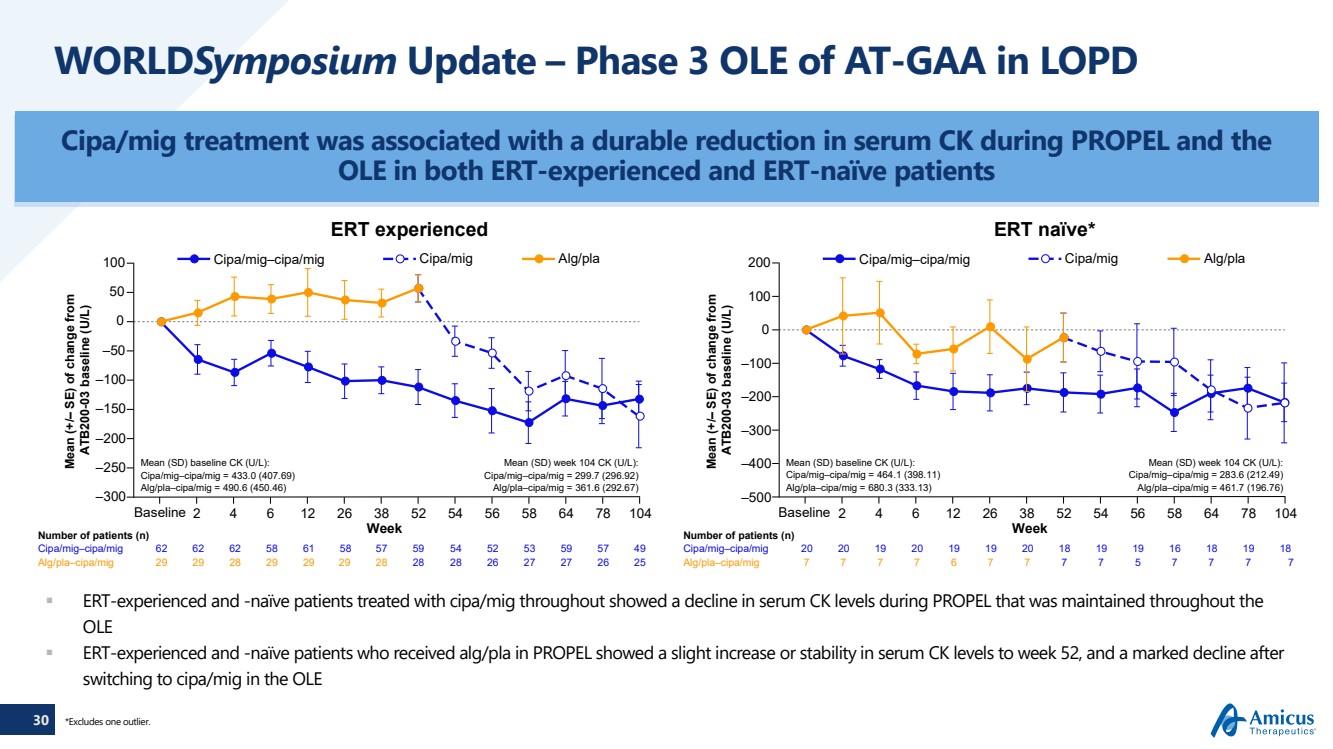
| 30 WorldSymposium Update — LOPD CIPA/MIG治療におけるAT-GAAのフェーズ3 OLEは、PROPEL中の血清CKの持続的な減少と関連しており、ERT経験者とERT未経験患者の両方の OLEは、ずっとCIPA/migで治療されたERT経験者と非ナイブ患者の両方で、PROPEL中の血清CKレベルの低下を示しました。 OLE ERTを経験し、PROPELでalg/plaを投与された患者で、PROPELでalg/plaを投与された患者は、52週目まで血清CKレベルがわずかに上昇または安定し、 でcipa/migに切り替えた後、著しく低下しました。OLE 患者数 (n) 平均 (SD) ベースラインCK (U/L): CIPA/mig—CIPA/MIG = 433.0 (407.69) alg/PLA—CIPA/MIG = 490.6 (450.46) 週平均 (SD) 104 CK (U/L): CIPA/MIG—CIPA/MIG PA/MIG = 299.7 (296.92) alg/PLA—CIPA/MIG = 361.6 (292.67) —300 —250 —200 —150 —50 0 50 50 100 100 100 CIPA/Mig—CIPA/MIG CIPA/MIG ALG/PLA 2 4 6 12 26 38 52 54 56 58 64 78 104 患者数 (n) 平均 (SD) ベースラインCK (U/L): CIPA/MIG—CIPA/MIG = 464.1 (398.11) alg/PLA—CIPA/MIG = 680.3 (333.13) 週平均 (SD) 104週目 CK (U/L): CIPA/MIG = 283.6 (212.49) Alg/pla—cipa/mig = 461.7 (196.76) —400 —500 —300 —100 200 200 200 CIPA/CIPA/MIG CIPA/MIG ALG/PLA 2 4 6 12 26 38 52 54 58 64 104 100 0 CIPA/mig—cipa/mig 62 62 62 58 61 58 57 59 54 52 53 59 57 57 59 57 59 57 59 57 59 57 59 57 59 57 59 57 59 57 59 57 59 57 59 57 59 57 59 57 59 57 59 57 59 57 59 57 59 57 59 57 59 57 59 57 59 57 59 57 59 57 59 57 59 57 59 57 59 57 59 57 59 57 59 57 59 57 59 57 59 57 57 mig—CIPA/MIG 20 20 19 19 19 19 20 19 20 18 19 19 16 18 18 19 18 19 18 19 19 19 19 19 19 19 19 19 19 19 19 19 19 19 19 19 19 19 19 19 19 19 19 19 19 19 19 19 19 19 19 19 19 19 19 19 19 19 19 29 29 29 29 29 29 28 28 28 28 28 26 alg/PLA—CIPA/MIG 7 7 7 7 7 ( — SE) ATB200-03ベースライン(U/L)からの変化の平均値(+/ — SE)) ATB200-03 ベースライン(U/L) からの変化の平均(+/ — SE)1つの外れ値を除外します。 |
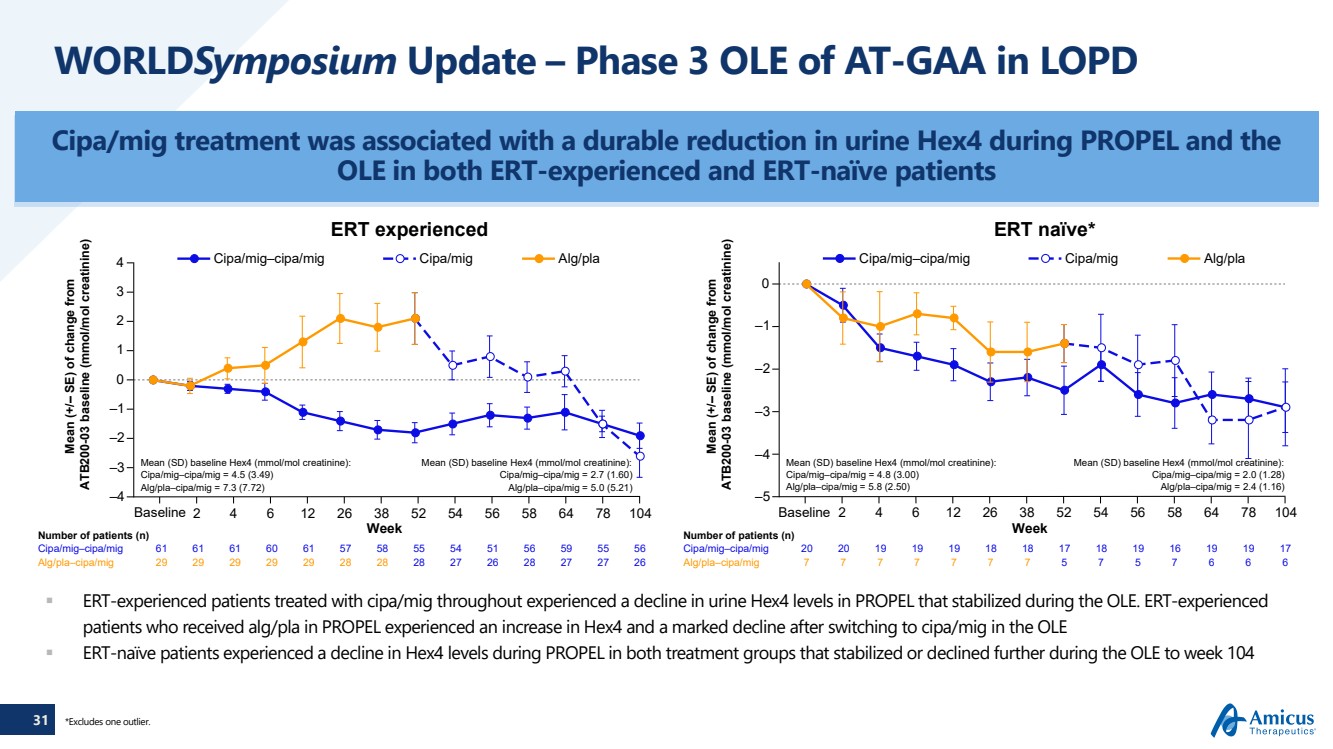
| 31 ERT-experienced patients treated with cipa/mig throughout experienced a decline in urine Hex4 levels in PROPEL that stabilized during the OLE. ERT-experienced patients who received alg/pla in PROPEL experienced an increase in Hex4 and a marked decline after switching to cipa/mig in the OLE ERT-naïve patients experienced a decline in Hex4 levels during PROPEL in both treatment groups that stabilized or declined further during the OLE to week 104 Number of patients (n) Mean (SD) baseline Hex4 (mmol/mol creatinine): Cipa/mig–cipa/mig = 4.5 (3.49) Alg/pla–cipa/mig = 7.3 (7.72) Mean (SD) baseline Hex4 (mmol/mol creatinine): Cipa/mig–cipa/mig = 2.7 (1.60) Alg/pla–cipa/mig = 5.0 (5.21) –4 –3 –2 –1 0 1 2 3 4 Cipa/mig–cipa/mig Cipa/mig Alg/pla Week 2 4 6 12 26 38 52 54 56 58 64 78 104 Number of patients (n) Mean (SD) baseline Hex4 (mmol/mol creatinine): Cipa/mig–cipa/mig = 4.8 (3.00) Alg/pla–cipa/mig = 5.8 (2.50) Mean (SD) baseline Hex4 (mmol/mol creatinine): Cipa/mig–cipa/mig = 2.0 (1.28) Alg/pla–cipa/mig = 2.4 (1.16) –4 –5 –3 –2 –1 0 Cipa/mig–cipa/mig Cipa/mig Alg/pla Week 2 4 6 12 26 38 52 54 56 58 64 78 104 Cipa/mig–cipa/mig 61 61 61 60 61 57 58 55 54 51 56 59 55 56 Cipa/mig–cipa/mig 20 20 19 19 19 18 18 17 18 19 16 19 19 17 Alg/pla–cipa/mig 29 29 29 29 29 28 28 28 27 26 28 27 27 26 Alg/pla–cipa/mig 7 7 7 7 7 7 7 5 7 5 7 6 6 6 Mean (+/ – SE) of change from ATB200-03 baseline (mmol/mol creatinine) Mean (+/ – SE) of change from ATB200-03 baseline (mmol/mol creatinine) WORLDSymposium Update – Phase 3 OLE of AT-GAA in LOPD Cipa/mig treatment was associated with a durable reduction in urine Hex4 during PROPEL and the OLE in both ERT-experienced and ERT-naïve patients Baseline Baseline ERT experienced ERT naïve* *Excludes one outlier. |
| Thank you |