アメリカです
アメリカ証券取引委員会
ワシントンD.C.,20549
表
(マーク1)e
1934年証券取引法第13条又は15条に基づいて提出された年次報告 |
本財政年度末まで
あるいは…。
1934年証券取引法第13条又は15(D)条に基づいて提出された |
手数料書類番号
(登録者の正確な氏名はその定款に記載)
(明またはその他の司法管轄権 会社や組織) |
(税務署の雇用主 識別番号) |
(主にオフィスアドレスを実行) |
(郵便番号) |
登録者の電話番号、市外局番を含む:(
同法第12条(B)に基づいて登録された証券:
クラスごとのタイトル |
|
取引 記号 |
|
登録された各取引所の名称 |
|
|
♪the the the |
||
|
|
♪the the the |
同法第12条(G)に基づいて登録された証券:ありません
登録者が証券法第405条に規定する有名な経験豊富な発行者である場合は、再選択マークで表示してください。はい、そうです☐
登録者がこの法第13又は15(D)条に従って報告書を提出する必要がないか否かを、再選択マークで示す。はい、そうです☐
登録者が(1)過去12ヶ月以内(または登録者がそのような報告を提出する必要があるより短い期間)に1934年の証券取引法第13条または15(D)条に提出されたすべての報告書を再選択マークで示すかどうか、および(2)このような提出要求を過去90日以内に遵守してきた
再選択マークは、登録者が過去12ヶ月以内(または登録者がそのような文書の提出を要求されたより短い時間以内)に、S−T規則405条(本章232.405節)に従って提出を要求した各相互作用データファイルを電子的に提出したか否かを示す
登録者が大型加速申告会社,加速申告会社,非加速申告会社,小さな報告会社,あるいは新興成長型会社であることを再選択マークで示す。取引法第12 b-2条の規則における“大型加速申告会社”、“加速申告会社”、“小申告会社”、“新興成長型会社”の定義を参照されたい。
大型加速ファイルサーバ |
|
☐ |
|
ファイルマネージャを加速する |
|
☐ |
|
|
|
|
|||
|
☒ |
|
規模の小さい報告会社 |
|
||
|
|
|
|
|
|
|
新興成長型会社 |
|
|
|
|
|
|
新興成長型企業であれば、登録者が延長された移行期間を使用しないことを選択したか否かを再選択マークで示し、取引所法第13(A)節に提供された任意の新たまたは改正された財務会計基準を遵守する
登録者が報告書を提出したかどうかを再選択マークで示し、その経営陣が“サバンズ-オクスリ法案”(“米国連邦法典”第15編、第7262(B)節)第404(B)条に基づいてその財務報告の内部統制の有効性を評価したことを証明する。この評価は、その監査報告書を作成または発行する公認会計士事務所によって行われる
証券が同法第12条(B)に基づいて登録されている場合は,登録者の財務諸表が以前に発表された財務諸表の誤り訂正を反映しているか否かを示すチェックマークを適用する☐
これらのエラーのより真ん中に登録者の任意のエンタルピーCER幹部が相関回復期間内に§240.10 D−1(B)に基づいて受信したインセンティブベースの補償に基づいて回復分析を行う必要があるかどうかを再選択マークで示す☐
登録者が空殻会社であるか否かをチェックマークで示す(取引法第12 b-2条で定義されている)。はい、そうです☐違います
登録者の非関連会社が保有する投票権及び無投票権普通株の総時価は、普通株のナスダック資本市場における終値に基づく2022年6月30日には約$
登録者が発行した普通株式数2023年3月30日までに
引用で編入された書類
登録者は,2022年12月31日までの財政年度終了後120日以内に米国証券取引委員会に提出された2023年株主総会の最終委託書に関する部分を,引用により本年度報告の第3部Form 10−Kに組み込む。
カタログ表
|
|
ページ |
|
前向き陳述に関する注意事項 |
1 |
第1部 |
|
|
第1項。 |
業務.業務 |
2 |
第1 A項。 |
リスク要因 |
29 |
項目1 B。 |
未解決従業員意見 |
57 |
第二項です。 |
属性 |
57 |
第三項です。 |
法律訴訟 |
57 |
第四項です。 |
炭鉱安全情報開示 |
57 |
|
|
|
第II部 |
|
|
五番目です。 |
登録者普通株市場、関連株主事項及び発行者による株式証券の購入 |
58 |
第六項です。 |
[保留されている] |
59 |
第七項。 |
経営陣の財務状況と経営成果の検討と分析 |
60 |
第七A項。 |
市場リスクの定量的·定性的開示について |
71 |
第八項です。 |
財務諸表と補足データ |
|
第九項です。 |
会計と財務情報開示の変更と相違 |
97 |
第9条。 |
制御とプログラム |
97 |
プロジェクト9 B。 |
その他の情報 |
98 |
プロジェクト9 Cです。 |
検査妨害に関する外国司法管区の開示 |
98 |
|
|
|
第三部 |
|
|
第10項。 |
役員·幹部と会社の管理 |
99 |
第十一項。 |
役員報酬 |
99 |
第十二項。 |
特定の実益所有者の担保所有権及び経営陣及び関連株主の事項 |
99 |
十三項。 |
特定の関係や関連取引、取締役の独立性 |
99 |
14項です。 |
最高料金とサービス |
99 |
|
|
|
第4部 |
|
|
第十五項。 |
展示·財務諸表明細書 |
100 |
第十六項。 |
表格10-Kの概要 |
103 |
i
前向き陳述に関する警告説明
この10-K表年次報告(“年次報告”)は前向き陳述を含むため、歴史的事実ではない。このような陳述は経営陣の信念と仮定に基づいている。会社はこれらの展望的陳述に反映または暗示された計画、意図、予想は合理的だと考えているが、会社は必ずこれらの計画、意図、あるいは期待を実現または実現することを保証することはできない。展望的な陳述自体が危険、不確実性、そして仮定の影響を受けるだろう。一般に、非歴史的事実の陳述は、会社が可能または仮定した将来の行動、業務戦略、事件または経営結果に関する陳述を含み、前向きな陳述である。場合によっては、これらの陳述は、“信じる”、“推定”、“予想”、“計画”、“予測”、“可能”、“将”、“すべき”、“求める”、“計画”、“予定”、“予想”または“意図”またはこれらの用語の否定またはそれらの変形または同様の用語の前、後、または含むことができる。
前向きな陳述は業績の保証ではない。このような声明はこの合意の日付だけを説明するので、このような声明に過度に依存してはいけない。以下の重要な要素は、会社の将来の業績に影響を与える可能性があり、これらの結果または他の結果は、会社の前向きな陳述における明示的または暗示的な結果とは大きく異なる可能性があることを理解すべきである
実際の結果が本年度報告の前向き陳述によって示唆された結果とは異なる可能性があるこれらの要因および他の要因は、本年度報告でより包括的に記述されているリスク要因“部分。“に記載されているリスク”リスク要因“網羅しているわけではない。新しいリスク要素が時々出現し、私たちはすべてのこれらのリスク要素を予測することができず、会社もこれらのすべてのリスク要素がその業務に与える影響を評価することができない、あるいは任意の要素或いは要素の組み合わせは実際の結果がいかなる前向き陳述に含まれる結果と大きく異なる程度を招く可能性がある。会社または会社を代表して行動することができるすべての人の展望的陳述は、前述の警告的声明によって明確に制限されている。法律の要求がない限り、会社は、新しい情報、未来の事件、または他の理由によるものであっても、いかなる前向きな陳述を公開または修正する義務を負わない。
1
第1部
プロジェクト1.ビジネス
文意が別に指摘されている以外に、本節で言及した“SeaStar Medical”、“会社”、“私たち”、“私たち”あるいは“私たち”はいずれもSeaStar Medical Holding Corporation及び業務合併(本稿で定義するように)後の合併子会社を指すが、業務合併完了前のSeaStar Medical業務に関連するいくつかの歴史情報は除外される。
概要
我々は医療技術会社であり,重要な臓器への過剰炎症の結果を減らすためのプラットフォーム療法を開発している。炎症反応は感染を防ぎ、体内の損傷組織を修復するキーポイントである。炎症の中心は血液やリンパ循環系中の細胞であり,白血球(主に好中球や単球)と呼ばれたり,通常は“膿細胞”とも呼ばれる。正常な炎症反応の中で、好中球は最初に現場に到着した免疫細胞であり、全免疫反応のキーポイントであり、全免疫反応は病原体を殺し、組織修復を促進する。これらの炎症性細胞から放出された化学物質(サイトカイン)は免疫系が外来病原体或いは損傷組織を除去し、免疫反応を増強することを誘発する。もし炎症反応が過度と失調(炎症促進と呼ばれる)、正常な好中球死亡(“アポトーシス”)が遅延する可能性があり、炎症細胞が引き続きサイトカインを産生することを許可し、更に失調した免疫反応を増強し、免疫系を調節するフィードバック機序を変化させる。これは破壊的な過剰炎症を暴走させて身体の他の部位に拡散させ,通常心臓,肺,腎臓,肝臓疾患を含む急性慢性固形臓器機能障害や不全を引き起こす。この高炎症反応は“サイトカイン嵐”とも呼ばれ,高炎症細胞から放出される細胞間通信に関与する小分泌蛋白に対する身体の反応を指す。制御しなければ、サイトカイン嵐は器官損傷、甚だしきに至っては死亡を招く可能性がある。
過去15年間に行われた臨床と臨床前研究に基づいて、同社の技術は炎症促進細胞の活動程度を調節する上で希望を示し、組織損傷を減少し、器官機能の修復と回復を加速することを助ける。この方法が成功すれば,臨床医が集中治療室(ICU)で急性臓器不全を治療する能力を変化させ,入院患者の臓器機能を改善すると信じている。現在,臨床医には過剰炎症の問題を解決するための利用可能な治療法はほとんどなく,確実に存在する選択に対しては,これらの選択は免疫抑制的か,1つのサイトカインのみを対象としている。著者らの技術は現有の抗炎症治療の局限性を克服し、選択的標的活性化好中球と単球の挑戦を解決する潜在力があると信じている。我々は,我々の特許保護と拡張可能な技術プラットフォームを用いて,臓器とは無関係な独自療法を開発し,急性および慢性適応に対応している。
著者らは著者らの独自の選択性細胞遺伝学設備(“SCD”)技術プラットフォームを使用して、最初に腎臓と肺を含むいくつかの急性器官損傷の適応を臨床で検証している。我々が検討しているSCDは,既存の連続性腎臓代替療法(CRRT)システムに容易に統合することを目的とした体外合成膜装置であり,米国各地のICUを含む病院に設置されている。承認され商業化されると、私たちのSCDは最初に小児CRRT群およびCRRTを受けた成人の急性腎臓損傷を対象とする。また,慢性透析や慢性心不全に関連する炎症に対応するためにSCDを開発している。
臨床前、著者らのSCDは各種の動物モデルでテストを行い、急性心筋梗塞、頭蓋内出血、慢性心不全、膿毒症と急性呼吸窮迫症候群を含む。動物モデルは炎症反応と我々のSCDがどのように変化しているかを示している。幅広い市場と適応へのSCD技術の応用を模索していきます 炎症活性化を促進する好中球と単球は急性と慢性適応において疾患の進展或いは重症度を促進する可能性がある。
臨床では安全かつ有効に高炎症を制御することに大きな需要がある。既存の高度炎症治療の選択は、サイトカイン、ウイルス、細菌またはエンドトキシン、サイトカインおよび免疫カスケードに対する薬物を直接吸収することができるコルチコステロイド(免疫抑制)および吸収技術を使用することを含む。活性化好中球または単球は選択的に処理されなかった。140以上の臨床研究の中で、著者らのSCDを用いて児童と成人CRRT急性腎損傷患者のサイトカイン嵐を逆転させた
2
患者の死亡率は50%低下し,60日間生存している患者では透析を必要としている人はいない。この独特な作用機序(好中球と単球を調節する)は成人と小児において一致した臨床結果を示した。著者らのSCDの臨床優勢を考慮して、著者らのSCDは臨床医師が高炎症適応を治療する第一選択治療コースになる可能性があると信じており、それは患者の予後を改善し、生存率を高め、透析への依存を減少し、最終的に医療コストを下げる潜在力があるからである。
2022年12月31日現在,我々のSCDは約170名の成人と小児患者の研究に基づいて使用されている。2022年6月、我々はCRRT急性腎障害(AKI)児童患者に対する人道主義設備免除(HDE)申請を米国食品医薬品局(FDA)に提出した。現在のHDE申請のスケジュールによると、FDAは2023年上半期に私たちのHDE申請の実質的な審査を完了すると予想されていますが、FDAが私たちのHDE申請を承認する保証はありません。さらに、2023年2月9日、CRRTを必要とするAKI成人患者の過剰炎症を減少させるためのSCDの有効性を評価するために、我々の研究装置免除(“IDE”)申請に対するFDAの承認を得た。同社は2023年第2四半期に学生募集を開始する予定で、2023年第4四半期に中期研究結果を生成し、2024年下半期に上場前承認(PMA)申請を提出する予定だ。2022年4月29日、我々は、我々のSCDを用いて成人AKI患者(18歳以上)の免疫調節不全を治療する画期的なデバイス称号(BDD)を取得し、このような試験の規制承認過程を加速させることが予想される。 AKI成人試験を速やかに完了することは保証されないし、AKI成人試験が積極的なデータを生成することは保証されない。これらの実験から積極的な結果を得ることができても,FDAはこの研究を支援するための追加的な実験を要求したり,実験の設計に同意せず,そのような設計の変更や改善を要求したりする可能性がある.
われわれの新しい治療装置は他の適応に応用しやすく,より多くの臨床研究やFDAの承認が必要と信じている。私たちが適応を拡大しようと努力するにつれて、規模経済を利用して生産コストを下げることができると信じています。私たちの拡張可能な製造プロセスは 高度炎症市場で顕著な競争優位を示した。
我々は我々のSCD技術および他の技術のために特許保護を求めてきたが、これらの技術は40件の特許と10件の米国およびいくつかの外国司法管轄区で懸案されている特許出願を含む。これらの特許および特許出願のうち、33件は私たちが独占的に所有し、17件はミシガン大学(UOM)と共同所有している。UOMはすでにUOMが所有するすべての特許とアプリケーションにおける権益のグローバル独占使用料許可を付与している.この許可証は私たちのSCDをすべてのヒト治療適応のために商業化することを可能にする。もっと情報を知りたい場合は“を参照してください”知的財産権“下だ。
適応を拡大することでビジネスや流通戦略を形成し続け,我々の候補製品の発売や特定の患者集団に接触できるように戦略的能力を提供するパートナーとの協力を市場で求めていく予定である。2022年12月27日、Nuwell is,Inc.(“Nuwell is”)と許可および流通協定(“流通協定”)を締結し、この協定に基づいて、Nuwell isを全米でSCD製品を販売および流通する独占流通業者に指定し、FDAの書面許可を得ると、私たちのHDEに従って小児科用製品の販売を申請することができる。取扱契約によると、私たちは前金を受け取り、いくつかのマイルストーンを達成した時にマイルストーン支払いとSCD製品の総売上の特許権使用料を受け取ることになります。流通契約の初期期限は、2022年12月27日から始まり、以下の日の3(3)周年日に終了する:(A)小児科用SCD製品および(B)SCD製品の最初の商業販売のためのFDAの許可を得た、両方の早い日。Dealerプロトコルの期限は自動的に1(1)年延長でき,合計2(2)回延長される.もし重大な違約行為が書面通知後90(90)日以内に是正されなければ、それぞれが流通協定を終了する権利があり、私たちは流通協定に規定されている他の条項に基づいて流通協定を終了する権利があります。
私たちの高度管理チームと取締役会は、医療業界で平均19年を超える経験を有しており、私たちの最初の治療優先分野の医療事務、商業化、流通に関する専門知識を含んでいる。私たちはまた、私たちの技術と製品開発の専門家である尊敬されている科学コンサルタントたちの支持を得ました。
3
企業の歴史
Seastar Medical,Inc.は最初は2007年6月6日にNephrion,Inc.の名で成立した。2007年8月3日、会社名をCytoPherx,Inc.に変更しました。2019年6月19日、会社名をSeaStar Medical,Inc.に変更しました。
2022年10月28日 LMAO、Merge SubとSeaStar Medical、Inc.が2022年4月21日に締結した合併協定と計画(“合併協定”)に基づいて、デラウェア州に位置するLMF Acquisition Opportunities,Inc.(“LMAO”)は一連の取引を完成し、LMF Merge Sub,Inc.とSeaStar Medical,Inc.(“合併子”)とSeaStar Medical,Inc.(“合併子”)の合併を招いた。合併合意の条項により,LMAOとSeaStar Medical,Inc.間の業務合併は合併SubとSeaStar Medical,Inc.合併の影響を受け,SeaStar Medical,Inc.はLMAOの完全子会社として存続する(“業務合併”)。業務合併の完了に伴い、LMAOは“SeaStar医療ホールディングス”(“当社”)と改称した。
私たちの方法は
急性炎症反応は明確な協調順序反応で発生する。好中球は第一反応細胞,次いで単球である。単球が組織に入ると,それらも組織マクロファージに分化する別の配列に従う。まず炎症性マクロファージ,次いでパトロール,修復性マクロファージである。
この複雑な緊密な協調過程は宿主防御と組織修復に重要であるが、身体炎症シグナルと細胞アポトーシスの厳格な制御を受ける必要がある。そうでなければ,制御されていない過剰な炎症により組織や臓器機能が悪化する劣化修復過程がある場合には,さらなる組織破壊が発生する可能性がある。もしこのような過度な全身炎症が深刻で長期的であれば、心血管、呼吸、腎臓、肝臓と神経機能障害を含む多臓器機能不全が発生し、不良な臨床予後を招く可能性がある。従来、可溶性メディエーター標的を遮断する治療法、例えばサイトカインやフリーラジカルは、成功していることが証明されていなかった。細胞を活性化するSCD法は,破壊的でなくても潜在的な変革的治療法であり,一連の急性や慢性炎症性疾患に適していると信じられている。
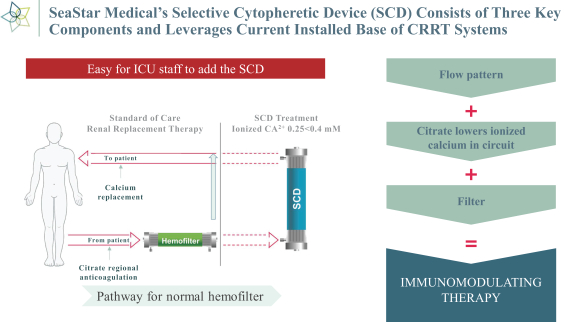
我々のSCDはCRRT体外回路の一部として活性化白血球(好中球と単球)を結合することを目的とした体外合成膜装置である。標準CRRTシステム(局所クエン酸塩を使用して抗凝固)を添加した直後に標準CRRTシステムを添加して放出すると、血液中
4
標準的な血液フィルターは私たちのSCDに入り、装置の繊維に分散されている。低カルシウム環境下でわれわれのSCDを離れると,血液は患者の体内に戻る。

我々のSCDは,活性化好中球および単球の過剰炎症反応を軽減することにより治療的利益を提供する。途切れることなく過剰な炎症反応が多臓器不全(MOF)に進展し,重症患者の発症率も死亡率も増加する。著者らの最初の鉛製品はCRRTを受けた重篤なAKI児童と成人患者に集中した。我々のSCDは現在ICUにおけるCRRTポンプシステムの既存の足跡と,抗凝固剤としての使用と採用が増えている地域クエン酸塩を利用している。クエン酸は体外循環中の遊離イオンカルシウムに結合するために用いられ,好中球や単球に影響を与えるために必要である。“アメリカ医学会雑誌”の2020年の最新の研究により、区域クエン酸塩の抗凝固の使用はヘパリンと同じ死亡率を有するが、領域クエン酸抗凝固は現在、フィルターの寿命を保護する上でより有効であることが証明されている。それは私たちのSCDのための低カルシウム環境を作るために使用され、これは白血球とSCD膜の相互作用に影響し、それによって炎症を減少させる。
行動メカニズム
我々のSCDの作用機序は,1)活性化好中球および単球を我々のSCD生体模倣膜に結合させる,2)我々のSCDにおいて特定のイオンカルシウムレベルを維持することによって,活性化好中球を不活化する,の2つのステップを含む。我々のSCDは,臨床的に承認された局所クエン酸塩抗凝固レジメンを用いてイオンカルシウムレベルを低下させ,回路内の血液閉塞を防止し,活性化した
5
好中球,その後患者に戻した。その後,カルシウムはSCDから患者の血液に注入され,全過程で患者の正常なカルシウムレベルを維持した。
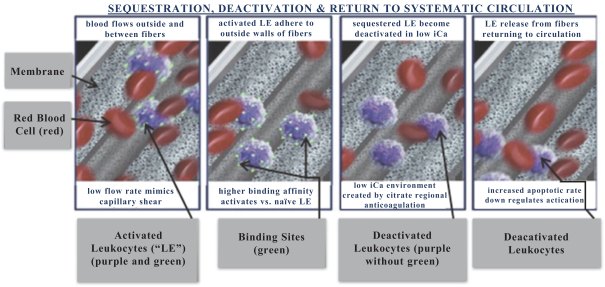
SCDと好中球は
カルシウムは多くの生物過程で重要な役割を果たしている。好中球については,カルシウムはその活動に深い影響を与えることができる。好中球中のカルシウムレベルを低下させることは、好中球のより高いレベルのアポトーシス(不活化)を引き起こすことが明らかにされている。われわれのSCDは最高活性の好中球(高度炎症に関連する)を選択的に結合することを目的としており,低ICA環境では活性化された好中球が不活化され,過剰な炎症を軽減する効果がある。好中球が定常状態の場合,正常な半減期は6−8時間であるが,高度炎症状態では好中球のアポトーシスが遅延し,循環中に活性化する好中球数が増加する。臨床と臨床前研究により,われわれのSCDは最も活性の高い好中球を選択的に隔離·脱活性化し,好中球の動的バランスを回復させることが証明されている。
SCDと単球は
全身炎症と器官特異性損傷における循環単球の作用はますます医療保健専門家に重視されていると信じている。カルシウムは単球活性にも重要な影響を与える。高比率の循環単球亜型(M 1炎症促進とM 2パトロール、修復性)はすでに急性器官損傷と慢性器官機能障害の程度に影響することが証明された。体外では,われわれのSCD膜は低ICA灌流回路でより選択的に血液中の炎症性単球に結合している。この選択的結合はすでに臨床試験で示され、そして炎症性疾患の中で比較的に少ない炎症促進循環単球を引き起こす。我々のSCDはこれらの単球を100%隔離しないことに注目すべきであり,免疫恒常性の維持に重要であるからである。
6
我々のSCDの組織学的評価
われわれのSCDは,患者治療後の顕微鏡下で,白血球が体外循環内の血流経路に沿ってカートリッジの膜外表面に結合していることを示している。結合した白血球は好中球と単球を主とした(以下図1参照)。
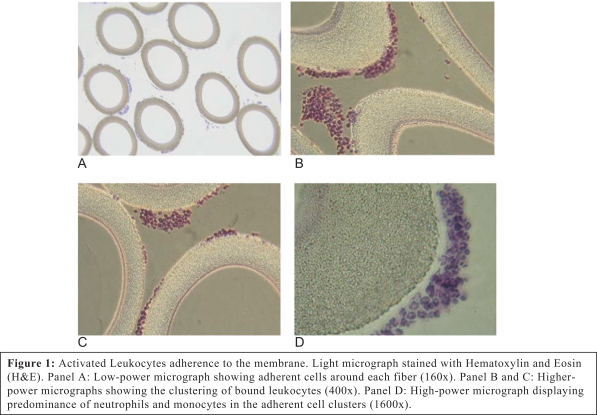
好中球と単球は,従来の血液流路である内壁ではなく,中空糸膜の外壁(下図)に結合することができ,これは血液流動の剪断力の違いによるものである。我々のSCDの絶対力は毛細血管流動と類似しており、好中球と単球に微小環境を提供し、細胞を捕獲と放出できるようにした。

7
私たちの市場のチャンスは
私たちは治療用医療機器会社であり、臨床データを収集し、AKIを有する小児患者における私たちのSCDの使用を要求し、成人AKIにおいて重要なPMA研究を開始することを支援するために、臨床データを収集し、FDAにHDEを提出することを支持するために使用することができる。長期的には,急性呼吸窮迫症候群,慢性透析,心腎症候群,肝腎症候群を含むがこれらに限定されないSCD技術を他の適応に応用する予定である。
急性腎障害での最初の市場機会は
著者らは、AKIはますます医療保健専門家と学術出版物の注目を受けており、これらの出版物はこのような最もよく見られる多臓器症候群が臨床と財務に与える壊滅的な影響を掲示したと信じている。サミュエル·A·シルバー(Samuel A.Silver)とグレン·M·チェルトー(Glenn M Chertow)の2017年の“急性腎障害の経済的結果”と題する研究によると,米国では急性腎障害に関連する病院費は年間54億ドルから200億ドルの間である。
医学的分類では、腎臓は沈黙の殺し屋だ。明らかな症状は出現せず,心臓や肺などの他の主要臓器のように苦痛を受けていることを身体に伝えることもない。例えば,一人では“腎症発作”の痛みを感じず,不可逆的な被害が発生している可能性がある。腎臓はまた、身体および器官の他の部分への曝露の影響(その逆)も回避され、共同治療は通常体系的に考慮されない。
最近全世界一致のAKI診断標準が出現し、リスク、損傷、不全、腎機能喪失と末期腎臓疾患(“RIFLE”)、2004年に導入されたAKI分期と診断ガイドラインの国際共通認識分類、2007年に発売された急性腎損傷ネットワーク(AKIN)分期システム、及び2012年に発表された腎臓疾患:全世界の結果、AKI分期と診断ガイドラインを改善する。これらの源は臨床医師があまり明らかでないAKI二次診断病例の識別、分期、診断と後続記録を改善することを助ける。われわれの最初の市場の重点はCRRTを受けたAKI患者であったが,将来の適応は患者の特徴と診断の改善から利益を得る可能性がある。
そのため,ICU腎臓代替療法への需要が増加している。CRRTは市場最新のAKI透析方式であり,1997年に初めて発売され,Fortune Business Insightsによると,9.86億ドルの世界市場(米国市場3.54億ドル)に増加していると推定されている。2019年までです。収入から計算すると、CRRT市場で最大の2社の事業者はFresenius Medical Care Holdings,Inc.とBaxter Internationalであり、この2社は現在アメリカCRRT市場の80%以上を占めている。
2010年以来、すでに大量のデータを公表してAKIの臨床と財務影響を定量化し、AKI治療“ブーム”を透析から診断、無料治療と薬理学領域に拡張した。病院管理者や政府関係者のAKI影響や負担に対する理解が増加するにつれ,注目度は増加し続けると信じている。ホブソンは“術後急性腎損傷に関連するコストと死亡率”と題する文章の中で、2015年に50,314名の患者(11年を超える)に対して行った研究によると、より厳しい審査を経て、39%の手術後の患者にAKIが出現し、19%の患者が2期あるいは3期のAKIが出現し、1患者あたりの平均増量コストは29,800ドルであった。そのほか、歴史的死亡率は約50%であるため、AKI治療はますます臨床医師、病院と製品メーカーの注目を集めている。
アメリカ連邦機関医療研究と質機関が委託した医療コストと利用プロジェクトによると、AKI患者の人口は毎年平均6.9%増加している。MassicotteとAzarniouchによる2015年の作品“集中治療室における急性腎障害:KDIGO分類と比較して医師が認識したリスク因子と結果”によると,約80%の中·重度AKI症例が診断·記録されておらず,米国AKI患者数が推定された年間600万患者を上回っていることが示唆された。CRRT治療を毎年受けているAKI患者の小児科人口は8000人未満と推定されており,600万AKI患者数と比較してかなり小さいサブセットである。
AKI市場は新しい効果的な解決策を必要とし、病院は引き続き新製品を探し、評価する。1つの製品がAKI領域で成功するためには、それは患者に明確で顕著な臨床利益を実現し、同時に病院の収入と利益を創出するために積極的な財務激励を提供しなければならない。
8
私たちの成長戦略は
著者らの成長戦略の重要な要素は臨床試験による革新と著者らの応用の拡大;医学教育による差別化の実現;業務発展とアウトソーシング許可活動、及び製造パートナーと生産を拡大することを含む。私たちはいくつかのコア成長戦略を採用する予定です
私たちの臨床段階では製品候補は
以下に我々の臨床段階および他の臨床研究におけるSCD候補製品をまとめた。以下のすべての実験と研究はFDAが承認したIDEで行った.
著者らは2022年6月にCRRTを受けた児童急性腎障害患者のSCD治療のためのHDE申請をFDAに提出した。FDAはHDE申請の実質的な審査を2023年上半期までに完了すると予想される。
臨床の進展
SCD 006重点研究(“SCD 006”)設計
FDAが最近付与したBDDにより,SCDによる成人AKI治療の重要な臨床試験が開始されている。この実験(“SCD 006”)は200人の患者で、キー、展望性、マルチセンター、開放的
9
ラベル,ランダム,両腕比較研究は,米国で行われている。SCD 006試験は60日目の死亡率と透析依存性の総合終点を評価することを目的とした。われわれの目標群は病院環境下のICUでAKIを有する成人となり,60日目の死亡率は40%から50%と推定され,生存している人では60日目に透析が必要となる可能性は25%となる。
現在の実験状態
我々は、2023年1月6日にSCD 006 IDEプロトコルをFDAに提出しました。私たちは試験が2023年第2四半期末に登録を開始する予定で、15~18ヶ月以内に登録を完了する予定です。2022年4月29日、我々は、このような試験の規制審査および承認プロセスを加速させるために、我々のSCDを用いて成人AKI患者(18歳以上)の免疫調節障害を治療するBDDを受けた。我々は現在,この試験が2023年末に中期結果が生じ,TOPLINE研究結果が2024年下半期にPMA申請に提出されることを予想している。
IDESによる他の臨床研究はうっ血性心不全の心腎症候群、末期腎症の心筋トン抑制と肝腎症候群である。ミシガン大学ではSCD製品を用いて治療が可能な患者集団を決定するための探索的臨床研究を行っており,将来のどの研究もこれらの研究で収集された予備臨床データに基づくであろう。
臨床研究
我々のSCD 003を除いて,これまでわれわれのすべての臨床研究には無作為対照群はなかった
Aki安全性、死亡率、デバイス完全性研究(中国)(ASAIO Journal 57:426-432,2011)
(2009年1月~2010年4月)
ヒトデ医療は上海華山病院と協力してSCDに関する研究を展開し、中国のタイトルは:二重血濾過装置(DCD)による急性腎不全治療の臨床研究それは.この研究は展望性、非ランダム、介入性研究であり、局部クエン酸塩抗凝固(RCA)のCRRT治療を受けた急性腎不全患者において、SCD治療が入院死亡率に与える影響を評価することを目的とした。7日間にわたる治療を許可した。すべての被験者はSCD治療に加え,CRRT患者の標準集中治療を受けた。
この9名の患者が参加した研究では,病院内のすべての原因による死亡は,国家データセットからの症例マッチング対照と比較して,SCD治療が病院でAKIを有するICU患者の死亡率を低下させることが証明された。研究により、SCD治療群の死亡率は22%であり、病例マッチング対照群の死亡率は78%であった。この向上した生存率は年齢と逐次臓器不全評価(SOFA)採点と関係がないことが証明され、SOFA採点は実験室結果と臨床データに基づいてICU死亡率を予測する採点システムである。この研究の結果,SCDの治療耐性は良好であり,白血球や血小板数を含む血液学的パラメータに有意な影響はなく,有害事象の発生はAKI重症患者のICUで発生することが予想される。
SCD治療を解析した9名の被験者では,好中球減少事件の報告はなく,重篤な有害事象(SAE)の報告もなかった。副作用としては,高カルシウム血症(8例),低カルシウム血症(1例),低リン血症(2例),高ナトリウム血症(1例),血小板減少症(1例)がある。
急性腎不全患者におけるSCDの安全性と有効性を評価するマルチセンター先導性研究(ARF 002)(“透析”第26巻、2013年第5期:616-623期のシンポジウム)(2010年5月~2011年1月)
SCDデバイスのこの先導的研究(ARF-002臨床試験)はSeaStar Medicalによって賛助され、第三者契約研究機関の支持を得た。この研究は7回連続24時間SCD治療後のSCD治療の安全性と有効性を評価することを目的としている。結果をCRRTプラスRCA治療を受けたAKI群の28日目と60日目の全死亡原因の入院死亡率の履歴データと比較した。
10
この研究では35人の成人被験者を募集した。平均年齢は56.3歳で,その71.4%がコーカサス人,22.9%が黒人,5.7%がスペイン系であった。SOFAの平均得点は11.3点であった。60日時のSCD患者の任意の原因による死亡率は31.4%であったが,文献に基づく歴史的看護基準は50%であった。生存しているすべての被験者は60日目に腎臓の回復を観察し,独立透析と定義した。明らかに低い死亡率に基づいて、この初歩的な研究の結果により、歴史看護治療標準と比べ、患者結果は明らかに改善する潜在力があることを表明した。
被験者35名中33名に199回の副作用(AEs)が認められた。この199例の副作用のうち,12例は研究療法に関与している可能性が考えられ,1例は研究療法に関与していると考えられた(研究者による)。これらの症状には,凝固機能欠陥の悪化,低血圧,好中球減少,びまん性血管内凝固(DIC),血小板減少,反復腎不全,低リン血症,高カルシウム血症,貧血と心源性ショックがある。199個の総有害事象のうち,34.7%が軽度と考えられ,60%が経験し,51.8%が経験し,71%が経験し,13.6%が経験し,54%が経験していた。観察された急性腎不全重篤患者群と/或いはICU環境中の副作用。23例の被験者28回のSAE(死亡を含む)を観察した。予期せぬ不良設備の影響はない。この28個のSAEのうち2つは治療に関与している可能性が考えられ(すなわちDICと心源性ショック),強度が重篤であった。28名中7名(25%)が中等度,35名中20%が経験し,21名(75%)が重度,35名中51%が経験していた。以下の表に、研究期間中に遭遇したすべてのSAEおよび各SAEの評価をカテゴリ別に示す
|
|
研究と関係がある |
|
|||||||||||||
重大な不良事件リスト |
|
もちろんいいですよ |
|
|
そうかもしれない |
|
|
そうかもしれない |
|
|
絶対に違う |
|
||||
血液とリンパ系疾患 |
|
|
|
|
|
|
|
|
1 |
|
|
|
2 |
|
||
心臓疾患 |
|
|
|
|
|
|
|
|
1 |
|
|
|
1 |
|
||
胃腸疾患 |
|
|
|
|
|
|
|
|
|
|
|
1 |
|
|||
全身性障害と投与部位の状況 |
|
|
|
|
|
|
|
|
|
|
|
|
||||
感染と侵入 |
|
|
|
|
|
|
|
|
|
|
|
5 |
|
|||
損傷、中毒、プログラム合併症 |
|
|
|
|
|
|
|
|
|
|
|
3 |
|
|||
新陳代謝と栄養失調 |
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|||
筋肉骨格と結合組織疾患 |
|
|
|
|
|
|
|
|
|
|
|
|
||||
神経系疾患 |
|
|
|
|
|
|
|
|
|
|
|
1 |
|
|||
他にも |
|
|
|
|
|
|
|
|
|
|
|
3 |
|
|||
腎臓と尿路疾患 |
|
|
|
|
|
|
|
|
|
|
|
|
||||
呼吸器、胸部、縦隔疾患 |
|
|
|
|
|
|
|
|
|
|
|
8 |
|
|||
血管疾患 |
|
|
|
|
|
|
|
|
|
|
|
|
||||
合計する |
|
|
0 |
|
|
|
0 |
|
|
|
2 |
|
|
|
26 |
|
これは対照、無作為、多中心臨床試験であり、2011年9月に開始され、FDAの承認されたIDEで2013年9月に終了した。この試験では,対照群は標準的なCRRTプラスRCAを受け,SCD治療群は7日間にわたるSCD治療を受けた。この研究はSeaStar Medicalが協賛し,第三者契約研究機関の支持を得た。
この研究の主な目的は,SCDとCRRTを併用した場合,すべての原因による死亡率の60日目の臨床的および統計的改善につながるかどうかを決定することである。副次的目標は,60日目に腎臓代替治療の依存性を評価すること,28日目の死亡率,28日目の人工呼吸器なし日数,および60日目の重篤な膿毒症患者の死亡率を評価することである。
計134名の患者が21の米国医療センターに登録されている。各病院のICUで看護を受けている患者は,CRRTまたはCRRT+SCDを受ける集中治療にランダムに割り当てられている。各参加臨床サイトは、その確立されたRCAレジメンをCRRT+SCD回路(治療群)およびCRRT(対照群)のみに使用する。CRRTで推奨されているカルシウム(ICal)レベル(SCD後測定)
11
SCD血流値は0.25~0.4 mmol/Lの間であり、年齢8~80歳、体重135 kg以上以外、組み入れと排除標準は以前のIDE多センター試験臨床研究と類似している。患者がCRRTを受けることを含むすべての資格基準を満たすと、少なくとも4時間であるが、24時間以下であり、そしてインフォームドコンセントに署名し、被験者は1:1ランダムに区群を設計してランダムに対照群或いは治療群に分け、研究センターと深刻な膿毒症が存在するかどうかによって階層化した。対照群と治療群の死亡率をそれぞれ50%と35%と仮定し、全体の両側0.05レベルの80%分散を用いて344名の患者のサンプル量を計算した。適応設計と中期分析計画は登録された中点(すなわち172名)で行った。また、尿量、血清エラスターゼ、サイトカインレベル及び全治療過程における総絶対白血球、好中球と血小板数を含む対照群と治療群の間のいくつかの探索性バイオマーカーを比較した。
登録期間中の第2四半期には、米国の主要サプライヤーのいくつかのFDAに関連する品質製造問題により、米国で全国的なカルシウム不足が発生した。SCDの機能治療効果は狭い回路内のICA範囲に依存することや,ランダムにSCDに入った患者がICAレベル不足のため有効な治療を受けていないことが懸念されるため,中期分析は134名の患者を登録した後早期に行った。2013年5月24日に登録を一時停止し、研究終点に対するカルシウム不足の臨床的影響を評価した。カルシウム注入液の不足はクエン酸塩注入率を最低に低下させる傾向にあった。そのため、血液循環中のICAレベルはよく推薦した0.25から0.40 mmol/Lの範囲より高く、ベースライン特徴の面では、対照群と治療群の間に有意差がなかった。分析に参加した134名のうち,69名が単独でCRRTを受け,65名がSCD治療を受けた。治療群と対照群60 dの死亡率はそれぞれ39%(27/69)と36%(21/59)であり、統計学的有意差がなかった。対照群と治療群のSAEは統計学的有意差がなかった。また、首席調査員によると、SAEは設備と関係があると考えられているものは一つもない。対照群と治療群の患者は研究方案中に規定した推奨ICA範囲(0.23-0.40 mmol/L)を維持する時間はすべて予想より大幅に低かった。中期分析時にSCD−003レジメンに組み込まれた134人の患者のうち、19人のSCD患者(CRRT+SCD)および31人の対照患者(単独CRRT)は、90%以上の治療時間でこのレジメンの推奨範囲内に維持された。この研究はその後中止された。
対照群と治療群のSAEは統計学的有意差がなかった。この研究では,対照群71例のSAE(63例中40例)とSCD治療群80例(SAE 69例中45例)を報告した。最もよく見られるSAE分類は感染と感染、及び心臓、呼吸系、胸部と縦隔疾患である。また,首席研究者によると,SAEはSCD装置の“肯定”に関与していると考えられているものはないという。意思治療分析では,全体的な不良事象は治療群と対照群の間に差はなかった。以下の表に、研究期間中に遭遇したすべてのSAEおよび各SAEの評価をカテゴリ別に示す
|
|
研究と関係がある |
|
|||||||||||||
重大な不良事件リスト |
|
もちろんいいですよ |
|
|
そうかもしれない |
|
|
そうかもしれない |
|
|
絶対に違う |
|
||||
血液とリンパ系疾患 |
|
|
|
|
|
|
|
|
9 |
|
|
|
|
|||
心臓疾患 |
|
|
|
|
|
|
|
|
15 |
|
|
|
|
|||
胃腸疾患 |
|
|
|
|
|
|
|
|
5 |
|
|
|
|
|||
全身性障害と投与部位の状況 |
|
|
|
|
|
|
|
|
4 |
|
|
|
|
|||
感染と侵入 |
|
|
|
|
|
|
|
|
14 |
|
|
|
|
|||
損傷、中毒、プログラム合併症 |
|
|
|
|
|
|
|
|
1 |
|
|
|
|
|||
新陳代謝と栄養失調 |
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|||
筋肉骨格と結合組織疾患 |
|
|
|
|
|
|
|
|
1 |
|
|
|
|
|||
神経系疾患 |
|
|
|
|
|
|
|
|
6 |
|
|
|
|
|||
他にも |
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|||
腎臓と尿路疾患 |
|
|
|
|
|
|
|
|
1 |
|
|
|
|
|||
呼吸器、胸部、縦隔疾患 |
|
|
|
|
|
|
|
|
13 |
|
|
|
|
|||
血管疾患 |
|
|
|
|
|
|
|
|
7 |
|
|
|
|
|||
合計する |
|
|
0 |
|
|
|
0 |
|
|
|
80 |
|
|
|
0 |
|
12
ICA群と対照群の60日間の死亡率と透析依存性の総合指数を比較すると、SCD群のパーセンテージは16%であり、対照群は58%であった。重篤な有害事象の発生率は治療群と対照群の間に差はなかった。
2014年2月12日、FDAは122名の患者に対して30カ所までの重要な試験を行い、この主要な複合終点を使用するための新しいIDEを承認した。この試験が安全性と有効性基準を満たしていれば、FDAは、上場前の承認と承認を支持することができると述べている。持続可能な注射可能カルシウム不足のため,この臨床試験は2014年に開始されておらず,同社は臨床重点を小児科適応に制限しており,研究規模のため,これらの適応には少ないカルシウムが必要である(小児科研究では15%の患者,キー試験では122名)。
CRRTを必要とする小児AKI患者におけるわれわれのSCD療法の安全性と早期治験(2016年12月と2020年2月)
著者らはRCA持続腎臓代替治療を受けたAKI児童患者におけるSCDの安全性と有効性を評価するために、多センターの展望性先導性研究を行った。この研究の主な目標は,我々のSCDの最大7時間連続24時間治療の安全性を評価することである。第二の目標は,28日目と60日目,最大7回連続24時間SCD治療の全因死亡率と透析依存性に対する治療効果を評価することである。この研究はSeaStar Medicalによって協賛され,第三者契約研究機関の支持を得ている。
16名の患者(男性8名と女性8名)が4つの米国小児科医療センターでこの研究に参加し,2016年12月から2020年2月まで続いた。感染性ショック、横紋筋溶解、肺動脈高圧、溶血性尿毒症症候群、脳脊髄炎、播種性腺ウイルス感染、心臓停止、急性呼吸不全と急性肝不全はICU入院を招く最もよく見られる診断である。
16名中12名(75%)が退院まで生存し(歴史対照群は50%),12名の患者は60日後に透析を必要としなかった(歴史対照群は15%から20%)。この研究では,14名の患者に14回のSAEが発生した。すべてのSAEは設備に関するものではない。この研究では,14名の被験者で47件の有害事象が発生した。以下の表に、研究期間中に遭遇したすべてのSAEおよび各SAEの評価をカテゴリ別に示す
|
|
研究と関係がある |
|
|||||||||||||
重大な不良事件リスト |
|
もちろんいいですよ |
|
|
そうかもしれない |
|
|
そうかもしれない |
|
|
絶対に違う |
|
||||
心臓疾患 |
|
|
|
|
|
|
|
|
|
|
|
4 |
|
|||
胃腸疾患 |
|
|
|
|
|
|
|
|
|
|
|
1 |
|
|||
感染と侵入 |
|
|
|
|
|
|
|
|
|
|
|
1 |
|
|||
新陳代謝と栄養失調 |
|
|
|
|
|
|
|
|
|
|
|
1 |
|
|||
神経系疾患 |
|
|
|
|
|
|
|
|
|
|
|
1 |
|
|||
腎臓と尿路疾患 |
|
|
|
|
|
|
|
|
|
|
|
1 |
|
|||
呼吸器、胸部、縦隔疾患 |
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|||
外科手術と医療プログラム |
|
|
|
|
|
|
|
|
|
|
|
1 |
|
|||
血管疾患 |
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|||
合計する |
|
|
0 |
|
|
|
0 |
|
|
|
0 |
|
|
|
14 |
|
選択的細胞遺伝学装置による急性心筋梗塞または新冠肺炎関連急性呼吸窮迫症候群患者の安全性と有効性を評価する多中心先導研究
(2020年9月~2021年7月)。出版物:危険重病看護探索
22人の被験者が2つの先行医療センターでこの予備研究に参加した。選ばれたすべての患者はコルチコステロイド治療,デキサメタゾンまたはヒドロコルチゾンを受けた。入選した患者の多くもレヒビル治療を受けた。同期対照16例。16名の意思治療(“ITT”)患者は、標準要件が盛り込まれているため、96時間を超えるSCD治療案(“PP”)を受けた
13
少なくとも96時間の治療を希望した。この研究はSeaStar Medicalによって協賛され,第三者契約研究機関の支持を得ている。
われわれのSCD治療開始後60日におけるITT群の死亡率は50%,PP群では31%であった。対照群の死亡率は81%であり,ITT群とPP群より高かった。体外膜酸素化治療を受けた対照群患者は生存していなかったが,ITT治療を受けた患者の44%が生存していた。60日間の透析依存では,ITT群では生存者の60%の腎機能が回復しなかったが,90日後のフォローアップでは,生存者の30%のみが透析支援を必要としていることが示された。
18例の被験者は共に50例のSAEを発生した。注目すべきは,全60日間のフォローアップ期間中に12名の被験者が22例の病院感染と日和見感染を報告したことである。22例の感染中16例はSCD治療後に発生した。現場臨床調査者や独立安全審査委員会の決定によると,これらのSAEはいずれも設備に関連していない。RCA関連不良事象は観察されず、90%の測定回路イオンカルシウム(ICA)値は0.4 mmol/Lより小さく、全身ICA値は臨床方案が要求する正常範囲内であった。2つの循環凝固事象が報告されている:1例は血液透析カテーテル中の凝固,もう1例は血液フィルター中の凝固である。SCD凝固発作の報告はなかった。血小板減少,好中球減少あるいは白血球減少は認められなかった。以下の表に、研究期間中に遭遇したすべてのSAEおよび各SAEの評価をカテゴリ別に示す
|
|
研究と関係がある |
|
|||||||||||||
重大な不良事件リスト |
|
もちろんいいですよ |
|
|
そうかもしれない |
|
|
そうかもしれない |
|
|
絶対に違う |
|
||||
血液とリンパ系疾患 |
|
|
|
|
|
|
|
|
|
|
|
1 |
|
|||
心臓疾患 |
|
|
|
|
|
|
|
|
|
|
|
9 |
|
|||
胃腸疾患 |
|
|
|
|
|
|
|
|
|
|
|
1 |
|
|||
全身性障害と投与部位の状況 |
|
|
|
|
|
|
|
|
|
|
|
3 |
|
|||
肝胆疾患 |
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|||
感染と侵入 |
|
|
|
|
|
|
|
|
|
|
|
22 |
|
|||
損傷、中毒、プログラム合併症 |
|
|
|
|
|
|
|
|
|
|
|
|
||||
新陳代謝と栄養失調 |
|
|
|
|
|
|
|
|
|
|
|
1 |
|
|||
筋肉骨格と結合組織疾患 |
|
|
|
|
|
|
|
|
|
|
|
|
||||
神経系疾患 |
|
|
|
|
|
|
|
|
|
|
|
|
||||
他にも |
|
|
|
|
|
|
|
|
|
|
|
|
||||
腎臓と尿路疾患 |
|
|
|
|
|
|
|
|
|
|
|
|
||||
呼吸器、胸部、縦隔疾患 |
|
|
|
|
|
|
|
|
|
|
|
8 |
|
|||
血管疾患 |
|
|
|
|
|
|
|
|
|
|
|
3 |
|
|||
合計する |
|
|
0 |
|
|
|
0 |
|
|
|
0 |
|
|
|
50 |
|
Seastar Medicalと新冠肺炎の臨床研究の主要な研究員は最近すでに受け入れられ、そして最近同業者が評議した学術定期刊行物“重篤な看護探索”に発表された。
慢性的なアプリケーション
末期腎症患者に対するSCD治療の可能性試験試験(2012年5月から2013年4月)
われわれのSCD治療は,より安定した末期腎症(“ESRD”)慢性血液透析患者群で評価されている。炎症性バイオマーカーの安全性および早期治療効果シグナルを評価するために、15人のESRD患者が入選した。著者らのSCD治療は単球の主要な炎症促進表現型から表現型修復への転換を促進した。
SCD治療やRCA期間中に有害事象やSAEはほとんど認められなかった。13名の患者のうち,4名の患者のSCD治療とRCAが有害事象に関与していた。有害事象は2組ずつ1回の発作からなる
14
発熱、寒気、頭痛、かゆみ、咳、めまい、筋肉痙攣、吐き気、嘔吐と胸痛。標準血液透析治療を受けている患者はこれらの有害事象を経験することが多い。SCD治療に明確に関連する有害事象はなかった。しかし,SCD治療やヘパリン抗凝固は症状や生化学的事象を引き起こす。この列の最初の2人の患者(Pt 1とPt 2)はSCDとヘパリン抗凝固療法を受け,SCD治療4時間後にC反応性蛋白レベルは22から38(Pt 1)および51−132(Pt 2)mg/Lに上昇した。C反応蛋白レベルはSCD治療後1日目に引き続き上昇し,それぞれ93(Pt 1)と147(Pt 2)mg/Lであった。これらの事件のため,SCD治療やヘパリン抗凝固を行う患者はこれ以上募集されていない。以下の表に、研究期間中に遭遇したすべてのSAEおよび各SAEの評価をカテゴリ別に示す
|
|
研究と関係がある |
|
|||||||||||||
重大な不良事件リスト |
|
もちろんいいですよ |
|
|
そうかもしれない |
|
|
そうかもしれない |
|
|
絶対に違う |
|
||||
全身性障害と投与部位の状況 |
|
|
|
|
|
|
|
|
1 |
|
|
|
2 |
|
||
合計する |
|
|
0 |
|
|
|
0 |
|
|
|
1 |
|
|
|
2 |
|
臨床前データの他の適応
われわれのSCDの最初の研究と臨床研究への転換の目標は,AKIやMOFに関連する急性調節失調の全身炎症の治療である。免疫調節治療の広範な応用のため、著者らは臨床前モデルを開発し、著者らのSCDが単一器官組織損傷を改善する治療効果を評価した。
選択的細胞遺伝器による急性腎損傷患者治療の安全性と有効性を評価する多中心無作為対照キー研究(SCD-003-IDEG 090189)(2011年9月から2013年5月)
臨床研究
臨床前データの他の適応
われわれのSCDの最初の研究と臨床研究への転換の目標は,AKIや多臓器不全に関連する急性調節失調の全身炎症の治療である。免疫調節治療の広範な応用のため、著者らは臨床前モデルを開発し、著者らのSCDが単一器官組織損傷を改善する治療効果を評価した。
慢性炎症性疾患
慢性心不全
われわれのSCD治療前の臨床前と臨床評価は,主に臓器機能障害や不全に関連する急性炎症状況に集中している。慢性炎症に関連する臓器機能障害を改善するために免疫調節法を拡大することは変革性である。過去の10年間に、いくつかの新しい薬理学的方法は臨床治療効果を証明できず、これは慢性心不全(CHF)を治療するための新しい、安全な方法を発見する必要性を明らかにした。この点で,われわれのSCDはCHFの臨床前モデルで評価し,CHFの慢性炎症性状態の心臓抑制作用を抑制した。慢性心不全や急性非代償性心不全は慢性全身炎症に関与していると考えられるようになってきている。単球はすでにCHF全身炎症の重要な源と考えられ、心筋細胞の収縮能力の低下を招く可能性がある。
心腎症候群
心腎症候群(CRS)は臨床疾患であり、慢性心不全の充血症状を緩和する治療は腎機能低下の制限を受ける。3分の1に達する急性非代償性慢性心不全患者にはこの疾患が存在し,その発生率は増加しており,米国では毎年100万人が入院していると推定されている。入院すると、これらの患者は、持続的な充血を緩和するために、大量の静脈利尿剤治療を受ける。しかし、利尿剤の使用はよく腎機能の悪化、心不全の進展と死亡を招く。免疫失調は心腎症候群において重要な役割を果たしている。
15
末期腎症慢性血液透析患者の心筋虚血
慢性透析患者の死亡の主要な原因の一つは心血管疾患である。これらの患者の心筋疾患の高発病率と死亡率を改善するために、新しい干与措置を確定とテストする必要がある。慢性血液透析患者において、多種の血液動力学と炎症要素は心臓病のリスクを増加させる。血液透析治療は反復的な虚血イベント或いは心筋トン抑制と関係があり、そして心エコー上の分節性心室壁運動異常と関係がある。このような繰り返しの虚血ストレスは進行性損害を招き、左心室駆出率の低下と心源性突然死のリスクを招く。急性と慢性炎症及びその細胞免疫効果因子が活性化する単球は慢性末期腎症患者の心血管疾患の加速発展の中心である。
ミシガン大学で勉強します
心腎症候群臨床試験
CRS臨床試験は、10人の患者で行われた安全性と有効性用量増加研究であり、CRSの限外ろ過治療とSCD療法の使用が心不全(排尿)機能を改善するかどうかを評価することを目的としている。CRSは予後が暗く、現在の治療が無効な疾患である。この研究では,心臓機能の改善は駆出率で測定されており,駆出率は心臓が収縮するたびに血液が心臓から離れる割合である。腎機能の改善は、血中クレアチニンおよび血中尿窒素(腎機能を評価する2つのよく見られるバイオマーカー)によって測定される。また,他の様々なバイオマーカーも測定する。この研究の成功は,CRS治療を証明する革新的な方法の概念証明が期待できる。初歩的な結果は後続の研究に重要な実行可能性データを提供し、対照無作為臨床試験を行い、著者らのSCDの限外ろ過治療に失敗したCRS患者の臨床治療効果を評価する。
慢性血液透析末期腎症患者の心筋虚血の臨床研究
10名の患者の中で試験的安全性と有効性研究を行い、血液透析患者の心筋トン抑制事件の減少を評価した。主な結果は心エコーで発見された分節性心室壁異常の変化を測定する。初歩的な結果は後続の研究に重要な実行可能性データを提供し、対照無作為臨床試験を行い、SCDの心筋トン抑制血液透析患者に対する臨床治療効果を評価する。
臨床研究
製品開発
我々の第1世代SCDは、FDAによって承認されたポリスルホン中空糸フィルタコアが規制リスクを低下させたため、合成血液フィルタの設計に基づいてきた。第二世代プロトタイプには,治療の一貫した実施を実現するための平端蓋が含まれており,手術規模の拡大に伴い,より適していると予想される。
著者らは現在、未満足の医療需要と製品規格に基づいて価格決定を行うために、異なる臨床適応の変更配置を評価している。
仕入先
私たちは私たちのサプライヤー管理計画を通じて承認と資格を得たサプライヤーからキーコンポーネントを調達します。Fresenius Medical Care North America(“FMCNA”)は現在著者らの小児科急性腎損傷適応に使用されているフィルタのサプライヤーである。2022年3月、私たちはFMCNA付属会社Fresenius USA Marketing,Inc.(“Fusa”)と供給契約(“供給契約”)を締結し、私たちがこれから行う臨床試験および任意の他の臨床試験におけるSCD製品のために、1箱当たり合意された数量でいくつかのフィルタを供給した。フィルタをSCDシステムの一部として緊急使用許可アプリケーションおよび将来のPMAが承認した製品で転売することができる.“供給協定”の初期期限は3年で、2022年3月31日から発効する。いずれか一方は未治癒の実質的な違約または他方の破産により“供給協定”を終了することができる。さらに、いずれか一方の法律顧問が合理的に考える場合、将来の連邦または州法律または法規の任意の変化は、供給の任意の部分を可能にし、いずれか一方は供給協定を終了することができる
16
合意は無効または不正であり、双方とも受け入れ可能な“供給合意”増編で合意することはできない。私たちは特定の第三者請求についてFusaに賠償を提供することに同意した。
私たちは成人と子供のための二番目のソースを開発しており、これは私たちがどんな供給中断もよりよく管理できるようにするだろう。さらに、SCDデバイスを組み立てるために必要なチューブを提供するサプライヤーを見つけましたが、市場でいつでも購入できるので、チューブの追加供給源を決定して確保することができます。
分布
供給協定は、規制機関が私たちのSCD製品候補製品を米国で小児科および成人製品を流通した後の最初の3年以内に優先的に拒否する権利を与える条項を含む。もしこの間、SeaStar Medicalが販売業者を通じてSCDを普及·販売することを選択した場合、SeaStar MedicalはFUSAに優先購入権を提供することが要求され、SeaStar Medicalの米国およびその地域におけるSCD独占販売業者となり、SCDの普及または販売方式はFUSAまたはその付属会社が製造および/または販売するいかなる設備と互換性がないことを前提とする。2022年12月27日、私たちはNuwell isと許可と流通協定を締結した。FDAの書面許可を得たら、私たちのHDE申請に基づいて、Nuwell isを全米でSCD製品を販売し、流通する独占流通業者として指定し、私たちのSCDを小児科に販売します。
第三者精算
医療保険と医療補助サービスセンターの保険範囲と精算を予定しています ("CMS“)と個人支払者は,多くの患者や医療提供者が我々の治療費を支払う鍵となり,特に連続性腎臓代替療法による透析やAKIを含む高炎症性疾患の治療に用いられる。したがって、私たちの製品の将来の販売は、政府当局、個人健康保険会社、他の第三者支払者の精算に大きく依存するだろう。私たちの精算をめぐる戦略は、コード化と支払い経路におけるCMSの一致と一致を実現することに重点を置いている;この両者は、個人支払者源からの最適な精算支払いを実現するために重要である。そこで,協力医療,プライベート支払者,その他の重要な利害関係者を含めた包括的な精算戦略を策定し,すべてのSCD製品の機会に明確かつ持続可能な精算経路を提供することを確保した。
私たちは適切な価格でSCDにMedicareを単独で支払うことを確実にするために規制精算戦略を推進しています。規制戦略には、CMSの政治的および職業的スタッフに保険、支払い、符号化に直接参加させ、その後、FDAの承認を得た後にこれらの分野の正式な申請を提出することが含まれる。CMSが根本的に斬新な製品のカバーと補償の面でどのような決定を下すかを予測することは困難である。参照してください“リスク要因−会社の業務運営に関連するリスク−企業の製品が商業化されることが承認された場合,第三者保険の不足や会社設備への補償が延期または制限される可能性がある.”
知的財産権
私たちは私たちの業務に重要だと思うノウハウを保護するために努力している。私たちはすでに私たちのSCD製品と関連技術、そして任意の未来の製品のために特許保護を求め続けます。特許保護を求めることに加えて、私たちはビジネス秘密に基づいて、私たちの業務が特許保護から保護されているか、あるいは特許保護に適していないと思う側面を保護します。私たちはまた、独自の権利を確立し、保護するために、独自の技術、セキュリティプロトコル、許可プロトコル、および他のプロトコルに依存する。私たちの成功は、私たちのSCD技術と、第三者の固有の権利を侵害することなく運営する能力を含む、私たちの独自技術を保護することに大きく依存します。
個別特許の期限は特許を取得した国の法的期限に依存する。私たちが出願したほとんどの国では,特許期間は非臨時特許出願が提出された最初の日から20年である。アメリカでは特許期間を調整することで延長することができます
17
特許権者が米国特許商標局が特許付与時の行政遅延により得た賠償を賠償する。ある特許の所有者が最終的に別の特許を放棄した場合、米国の特許期限が短縮される可能性がある。
同社は現在18件の発行された米国特許と5つの係属中の米国特許出願を持っている。同社は22件の海外特許を取得しており、5件は外国特許を出願している。同社が発行した特許は2028年に満期になり、最後の特許は2034年に満期になり、免責声明の終了、特許期限の延長、または特許期限の調整は特許期間を短縮または延長することができるが、最終的な特許は2034年に満了する。
次の表は、2022年12月31日までの私たちの特許と特許出願数をまとめています
|
|
付与された特許 |
|
|
処理待ちの申請 |
|
|
|
||||||||||
|
|
アメリカです。 |
|
|
外国.外国 |
|
|
アメリカです。 |
|
|
外国.外国 |
|
|
|
||||
SCD技術(特許シリーズ1−5) |
|
|
16 |
|
|
|
22 |
|
|
|
2 |
|
|
|
5 |
|
|
|
その他の技術(特許第6-10号) |
|
|
2 |
|
|
|
0 |
|
|
|
3 |
|
|
|
0 |
|
|
|
合計する |
|
|
18 |
|
|
|
22 |
|
|
|
5 |
|
|
|
5 |
|
|
|
私たちのSCD技術では、私たちは5つの特許家族の特許と特許出願を持っている。特許シリーズ1における特許と出願は,会社とUOMが共同で所有している.特許シリーズ2−5における特許及び出願は、会社独自所有である。特許シリーズ1-4に開示された発明は、米国政府の援助の下で開発され、“ベハ-ドール法案”の義務に拘束されている。
特許シリーズ1は、白血球を処理し、SCDキットを使用して様々な炎症状態を治療するためのシステムおよび方法、ならびにSCDキットに関する9つの米国特許および1つの係属中の米国特許出願を含む。これらの特許は2028−2031年に満期となり,必要な維持費が支払われたと仮定し,被審査出願が承認されれば2028年に満了する。我々はUOMと共同でカナダ,日本,ニュージーランドで取得した特許と,欧州で出願中の特許を所有している。必要な維持費が支払われていると仮定すると、これらの対応する特許および出願は2028年に満了する。特許シリーズ1の特許および出願は以下のとおりである
18
特許家族1エスペス
管轄権 |
|
状態.状態 |
|
満期になる |
|
題材.題材 |
アメリカです |
|
授与する |
|
2031 |
|
白血球の処理方法及びそれを用いた炎症条件を有する対象の治療方法 |
アメリカです |
|
授与する |
|
2029 |
|
体外循環を受けた被験者の治療法 |
アメリカです |
|
授与する |
|
2029 |
|
末期腎症患者の治療法 |
アメリカです |
|
授与する |
|
2029 |
|
急性腎不全患者の治療法 |
アメリカです |
|
授与する |
|
2029 |
|
膿毒症の治療法 |
アメリカです |
|
授与する |
|
2031 |
|
活性化白血球及び血小板を処理する装置 |
アメリカです |
|
授与する |
|
2029 |
|
急性肺障害及び急性呼吸窮迫症候群の治療法 |
アメリカです |
|
授与する |
|
2029 |
|
活性化血小板を治療するためのシステム |
アメリカです |
|
授与する |
|
2028 |
|
活性化白血球を処理するためのシステム |
アメリカです |
|
未定である |
|
2028* |
|
白血球及び血小板を治療するためのシステム及び方法 |
カナダ |
|
授与する |
|
2028 |
|
白血球を処理するための |
カナダ |
|
授与する |
|
2028 |
|
活性化白血球及び血小板を処理するための装置 |
日本です |
|
授与する |
|
2028 |
|
白血球を処理する装置及び方法 |
日本です |
|
授与する |
|
2028 |
|
活性化白血球を処理するための装置 |
ニュージーランド |
|
授与する |
|
2028 |
|
白血球を処理するための |
ヨーロッパ.ヨーロッパ |
|
未定である |
|
2028* |
|
血小板または白血球を処理する装置 |
香港.香港 |
|
未定である |
|
2028* |
|
血小板または白血球を処理する装置 |
* |
申請が承認された場合、締め切り。 |
|
この特許シリーズは米国連邦政府の援助の下で開発され、“ベハ-ドール法案”に制約されている。 |
UOMとのライセンス契約(改訂された“UOMライセンス協定”)によれば、UOMは、SCD技術プラットフォームで使用されるいくつかの技術(物質組成および使用方法特許を含む)がヒト治療医療機器分野の特許ファミリー1において共通して所有する特許およびアプリケーションの権益を得るために、世界的に特許権使用料を有する独占的許可を付与している。この独占許可については,UOMライセンス契約期間内に,純売上高の1%に相当する特許権使用料と特許費用の補償をUOMに支払うことに同意した.私たちは今までUOMライセンス契約に基づいて支払いも特許権使用料も借りていません。2020年1月1日以来、約12.4万ドルの特許料を支払ってきた。UOMライセンス契約は,我々に何らかの職務調査義務を課し,特定の日までに特定のマイルストーン事件を完了することを要求している.UOMライセンス契約によると,UOMの責任は限られており,使用許可された技術と,その許可を用いた特許および/または技術を用いて創造された製品に関する活動についてUOMを賠償し,損害を受けないようにすることに同意する.事前に終了しない限り、UOMライセンス契約は、(I)すべてのライセンス特許の満了、(Ii)発効日(以下、定義)10周年、または(Iii)最初の商業販売日(以下、定義)7周年まで有効である。他方が合意中の任意の約束または約束に実質的に違反し、90日以内に治癒しない場合、いずれか一方は“計量単位許可協定”を終了することができる。私たちはまた90日前にUOMに合意を終了するように通知することができる。
ファミリー1に共通する特許および特許出願に加えて、他の4つの特許ファミリー(ファミリー2−5)を単独で所有している。特許シリーズ2は、第2世代SCDカセットおよび我々のSCDカセットを用いて白血球を処理する方法の米国特許および出願中の米国特許を含む。この特許は2032年に満期になり,承認された場合,必要な維持費が支払われたと仮定すると,出願は2031年に満了する。オーストラリア、ヨーロッパ、日本はすでに対応する特許を付与しており、ヨーロッパの特許はすでにフランス、ドイツ、イタリア、スペイン、イギリスで検証され、特許出願が待っている
19
カナダです。必要な維持費が支払われたと仮定すると、これらの特許および出願は2031年に満了する。特許シリーズ2の特許および出願状況は以下のとおりである
特許家2エスペス
管轄権 |
|
状態.状態 |
|
満期になる |
|
題材.題材 |
アメリカです |
|
授与する |
|
2031 |
|
白血球や血小板を処理するための薬箱 |
アメリカです |
|
未定である |
|
2031* |
|
白血球または血小板の処置および炎症性疾患の治療方法 |
オーストラリア |
|
授与する |
|
2031 |
|
白血球または血小板を処理するためのカセットおよび炎症条件を有する対象の処理方法 |
フランスでは |
|
授与する |
|
2031 |
|
白血球や血小板を隔離するためのカートリッジ |
カナダ |
|
未定である |
|
2031* |
|
白血球や血小板を処理するためのカートリッジ |
日本です |
|
授与する |
|
2031 |
|
白血球や血小板を処理するための薬箱 |
日本です |
|
授与する |
|
2031 |
|
白血球や血小板を処理するための薬箱 |
* |
申請が承認された場合、締め切り。 |
|
この特許シリーズは米国連邦政府の援助の下で開発され、“ベハ-ドール法案”に制約されている。 |
特許シリーズ3は、2032年に満了する必要な維持費が支払われると仮定して、SCDキットを使用して慢性心不全を治療する方法に関する米国特許を含む。日本には,2032年に満了するために必要な維持費が支払われているとする対応する特許が付与されている。特許シリーズ3の特許および出願は以下のとおりである
特許家族3エスペス
管轄権 |
|
状態.状態 |
|
満期になる |
|
題材.題材 |
アメリカです |
|
授与する |
|
2032 |
|
慢性心不全の治療法 |
日本です |
|
授与する |
|
2032 |
|
慢性心不全の治療装置です |
|
この特許家族は 米連邦政府は資金を提供し、“ベハ-ドール法案”に基づいて義務を負う。 |
特許シリーズ4は、SCDキットを用いて慢性心不全および急性非代償性心不全を治療する方法に関する2つの米国特許を含む。必要な維持費が支払われたと仮定すると、これらの特許は2032年に満期になる。オーストラリアはすでに相応の特許を付与しており、カナダとヨーロッパの特許出願は承認中だ。必要な維持費が支払われていると仮定すると,これらの特許や特許出願が承認されれば,2032年に満期となる。特許シリーズ4の特許および出願は以下のとおりである
20
特許家4:衛士
管轄権 |
|
状態.状態 |
|
満期になる |
|
題材.題材 |
アメリカです |
|
授与する |
|
2032 |
|
急性非代償性心不全患者の心機能向上方法 |
アメリカです |
|
授与する |
|
2032 |
|
慢性心不全患者の心筋機能向上方法 |
オーストラリア |
|
授与する |
|
2032 |
|
急性慢性心不全または慢性心不全被験者の心筋機能を向上させる方法 |
オーストラリア |
|
授与する |
|
2032 |
|
心筋機能を改善し、急性非代償性心不全および慢性心不全に関連する炎症を治療するための方法、キットおよびシステム |
カナダ |
|
未定である |
|
2032* |
|
慢性心不全及び急性非代償性心不全患者の治療のための装置 |
ヨーロッパ.ヨーロッパ |
|
未定である |
|
2032* |
|
慢性心不全または急性非代償性心不全患者を治療するための装置 |
* |
申請が承認された場合、締め切り。 |
|
この特許家族は 米連邦政府は資金を提供し、“ベハ-ドール法案”に基づいて義務を負う。 |
特許シリーズ5は、以下に示すように、米国設計特許3件、欧州共同体設計特許3件、医療機器コネクタに対する3つの英国設計特許を含む
特許家族5
管轄権 |
|
状態.状態 |
|
満期になる |
|
題材.題材 |
アメリカです |
|
授与する |
|
2025 |
|
医療機器用コネクタの設計特許 |
アメリカです |
|
授与する |
|
2024 |
|
医療機器用コネクタの設計特許 |
アメリカです |
|
授与する |
|
2025 |
|
医療機器用コネクタの設計特許 |
イギリス.イギリス |
|
授与する |
|
2034 |
|
医療機器用コネクタの設計特許 |
イギリス.イギリス |
|
授与する |
|
2034 |
|
医療機器用コネクタの設計特許 |
イギリス.イギリス |
|
授与する |
|
2034 |
|
医療機器用コネクタの設計特許 |
ヨーロッパ共同体 |
|
授与する |
|
2034 |
|
医療機器用コネクタの設計特許 |
ヨーロッパ共同体 |
|
授与する |
|
2034 |
|
医療機器用コネクタの設計特許 |
ヨーロッパ共同体 |
|
授与する |
|
2034 |
|
医療機器用コネクタの設計特許 |
我々の他の技術については、他の5つの特許シリーズ(特許シリーズ6−10)の特許および特許出願を独占的に所有しており、以下のように概説される
特許家族6
管轄権 |
|
状態.状態 |
|
満期になる |
|
題材.題材 |
アメリカです |
|
未定である |
|
2040* |
|
移植のためのドナー臓器を準備するための装置及び方法 |
* |
申請が承認された場合、締め切り。 |
21
特許家族7
管轄権 |
|
状態.状態 |
|
満期になる |
|
題材.題材 |
アメリカです |
|
未定である |
|
2040* |
|
レシピエントの体内移植臓器の拒絶反応を低減するための装置及び方法 |
* |
申請が承認された場合、締め切り。 |
特許シリーズ8
管轄権 |
|
状態.状態 |
|
満期になる |
|
題材.題材 |
% |
|
未定である |
|
2041* |
|
サイトカイン放出症候群及び腫瘍溶解症候群の治療装置及び方法 |
* |
申請が承認された場合、締め切り。 |
特許シリーズ9
管轄権 |
|
状態.状態 |
|
満期になる |
|
題材.題材 |
アメリカです |
|
授与する |
|
2027 |
|
体外細胞に基づく腎細胞治療装置及び送達システム |
特許シリーズ10
管轄権 |
|
状態.状態 |
|
満期になる |
|
題材.題材 |
アメリカです |
|
授与する |
|
2031 |
|
腎細胞増殖促進方法 |
特許保護を求めることに加えて、私たちはビジネス秘密や他の機密情報に依存して、私たちの業務が特許保護から保護されているか、あるいは特許保護に適していないと思う側面を保護します。
競争
炎症治療の業界競争は激しく、新しい治療プログラムを開発する会社は巨大な資本と監督管理の挑戦に直面している。我々のSCD製品は臨床段階の設備であるため、私たちは医療業界の支持を確立する追加の挑戦に直面しており、これは人類の臨床研究によって産生される治療データによって駆動される。もし私たちの設備がFDAや他の国の規制機関によって市場進出を許可されれば、資金の豊富な製薬·医療機器会社からの激しい競争に直面する可能性がある。しかも、私たちは競争力を持つために私たちの設備を大規模に生産する必要があるかもしれない。私たちのSCDは市場で効果的に競争できると信じており、持続的な腎臓代替療法を必要とする成人または子供の急性腎臓損傷の治療のために、どのような設備がどこの国でも規制承認されていることを知らない。
米国や国際市場では、医療機器の使用は、政府や個人保険計画など、第三者支払者の精算状況にある程度依存している。医療機器を使用する医療提供者は、一般に、実行中の医療プログラムに関連するコストおよび費用の全部または一部を支払うか、またはそれらの患者ケアサービスを補償するために第三者支払者に依存する。第三者保険の不足や会社設備の精算は採用を延期したり制限したりする可能性があり、市場での競争優位性を損なう可能性がある。
22
販売とマーケティング
現在、顕著な販売やマーケティング能力はありませんが、2022年6月に提出された小児科AKI適応のHDE申請を含むFDAの関連規制の承認を得るために、資源化と商業化努力を積極的に支援しています。2022年12月29日,Nuwell isとHDE審査を受けている小児科SCDについて米国許可と流通協定を締結した。私たちは彼らの既存の販売チームを利用して、彼らのコールポイントは小児科SCDに必要なコールポイントと似ている。私たちは契約を作ったり締結したりして、医学教育と臨床訓練と支援を提供するつもりだ。
政府の監督管理
私たちのSCD製品は多くの監督管理機関によって規制されており、主にFDAと類似の国際規制機関である。これらの機関は,医療機器メーカーに医療機器の開発,テスト,製造,ラベル,マーケティング,貯蔵,流通,広告と販売促進および発売後の監督報告に関する適用法律と法規を遵守することを求めている。SCDは、患者の高炎症性細胞と相互作用し、患者の体内に戻る前に不活化されるカートリッジシステムを含む。著者らのSCDの主要な治療モードは設備がこれらの自己細胞に与える影響及びそれらが適時に患者に戻るため、FDAの生物評価と研究センターは医療設備としての発売前開発、審査と承認の主要な管轄権を持っている。適用された要件を遵守しないことは、警告状の発行、輸入拘禁、強制安全通知、修理/交換/払い戻し行動またはリコール、民事罰金および/または司法制裁、例えば、製品の差し押さえ、禁止、および刑事起訴など、設備および/またはその製造業者に様々な行政制裁を受ける可能性がある。
FDAの上場前承認要求
米国で商業流通されている各医療機器は、免除されていない限り、要求またはFDAのPMAを最初から開始する必要がある510(K)の承認を事前に得る必要があることを求めている。一般に、新しいデバイスが510(K)の許可の下で発売された述語を有する場合、FDAは、新しいデバイスが510(K)の許可の下で発売されることを可能にするであろう。そうでなければ、最初からまたはPMAを開始する必要がある。医療機器は,I類,II類あるいはIII類の3つに分類され,個々の医療機器に関するリスクの程度と,合理的な安全性と有効性保証を提供するために必要な制御程度に依存する。クラスIデバイスは、低リスクデバイスとみなされ、連邦食品、薬物および化粧品法案(“FD&C法案”)の一般的な制御、例えば、偽を混合すること、ブランドエラー、登録および発売、修理、交換または払い戻し、記録および報告、および良好な製造仕様を含む通知に関連する条項によって一般的に制御される。FD&C法案510(K)条によれば、多くのI類機器は上場免除前通知に分類されるため、FDA 510(K)の許可を得ずに商業流通を行うことができる。クラスII設備は一般的な制御を受けながら、合理的な安全と有効性保証を提供するために特別な制御を受けている。特殊な制御は業績標準、上場後の監視、患者登録と/或いは指導文書を含む可能性がある。II類デバイスの多くは、製造業者がFDAに上場前通知を提出することを要求し、これらのデバイスの商業販売を許可することを要求する。FDAが最大のリスクを構成すると考えられるデバイス、例えば、生命を維持する、生命を維持する、または移植可能なデバイスは、クラスIIIに分類される。さらに、FDAが以前に分類されていない、または以前に承認された510(K)デバイスと実質的に等しくないと考えられる新しいデバイスは、デフォルトでIIIクラスとみなされ、FDAが降格するまで(例えば、最初からプロセスを申請することによって)。法規または行政命令によって正式にクラスIIIに分類された高リスクデバイスは、FDAがPMA提出後にデバイスを承認しない限り、米国で販売することはできない。デバイス製造業者がデバイスのリスクが低いことを証明することができる場合、したがって、クラスIまたはクラスIIに分類されるべきである場合、デフォルトでは、クラスIIIの新しいデバイスは、最初からプロセスを申請することによって降格する資格がある可能性があると考えられる。FDAはまた、デバイスを発売後の販売、マーケティング、または他の制限を実施して、安全かつ効率的な方法で使用することを保証することができる。SCDはIII系デバイスに分類されると考えられるため,PMAの提出と承認を受ける。
1984年の“孤児薬物法”によると、まれな疾患は、米国では20万人未満に影響を与える疾患や状況と定義されている。現在、米国では、7000種類のまれな疾患のうち一部のみが承認された治療法が知られている。定義によると、まれな疾患や疾患は少数の患者に発生する。だからそれはすでに
23
FDAが安全性と有効性を合理的に保証する標準を満たすために十分な臨床証拠を収集することは困難である。
この挑戦に対応するために,国会は1990年の“安全医療機器法”に条項を取り入れ,少数(すなわちまれな)人口の疾患や疾患に影響を与える製品のための新たな規制経路を作成し,これが人体機器免除計画である。
人道主義的使用装置(HUD)は、毎年米国で8,000人以下の疾患または状態として現れる患者の治療または診断を支援することを目的とした医療装置である。
HDEはFD&C法案第520(M)条によるHUDに対するマーケティング申請である。HDEは、FD&C法案514および515条の効力要件によって制約されず、いくつかの利益および使用制限によって制限される。
FD&C法案520(M)(6)(A)(I)条によれば、平坦化装置は、HDEの承認を得た後にのみ利益販売を行う資格があり、装置が以下の条件を満たす疾患または状態を治療または診断することが意図されていることを前提とする
HDE申請者のデバイスは、資格基準のうちの1つに適合し、利益を得るためにHUDを販売することを望んでおり、元のHDE申請においてFDAに十分な証明ファイルを提供しなければならない。その設備を売却して利益を稼ぐことを希望するHDE保有者は、最初のHDE申請に申請が提出されていなければ、HUDが資格基準に適合していることを証明するために、補充書類を提出し、十分な証明書類を提供することができる。
販売可能なHDEデバイスの数は、年間流通数(ADN)と呼ばれる数に制限される。FDAがHDE所有者が利益を得るために装置を売却する資格があると判断した場合、FDAはADNを決定し、HDE所有者に通知する。
ADNの計算方法は,毎年個人の治療や診断に必要な合理的な設備数に8000を乗じたものである。例えば、HDEデバイスの予期される用途に応じて、HDEデバイスを使用する典型的な治療コースが、各患者が毎年2つのデバイスを使用する必要がある場合、HDEデバイスのADNは16,000(すなわち、2 x 8000)となる。
1年以内に配信される機器数がADNを超える場合、スポンサーは機器の販売を継続することができるが、この1年間の残り時間で利益を得ることはできない。
私たちは小児科の人々のためにHDEを追求しているので、私たちのSCDは利益を売る資格があると信じている。
上場前の承認ルート
FDAがPMAを要求するIII類デバイスについては,FDAに上場前承認申請を提出しなければならない。上場前の承認申請の流れは510(K)-上場前通知と最初から申請の流れよりもっと広い。PMAの申請は、FDAがこの装置の安全性および有効性を満足的に証明する合理的な証拠を証明するために、技術、臨床前、臨床試験、製造、およびラベルを含むが、これらに限定されない大量のデータサポートを必要とする。
上場前の承認申請を提出した後、FDAは、FDAが審査申請を提出するかどうかを決定するために、実質的な審査を可能にするために、申請が十分に完全であるかどうかを決定するために45日の時間がある。FDAは、出願されたスポンサー(会社)がこの期間中に追加情報に対するFDAの要求を満たすために情報を収集するので、出願の審査に通常より長い時間を要するにもかかわらず、提出された上場前承認申請を審査するために180日間のFDA審査時間を有する。全体的な審査過程の変数が大きく、数年かかるかもしれない。この審査期間内にFDAは
24
資料を補充するか、提供された資料を明確にする。また,FDA以外の専門家コンサルタントグループを集めて申請を審査·評価し,装置の承認についてFDAに提案することも可能である。
FDAは諮問グループ決定に制約されていないにもかかわらず,グループのアドバイスはFDAの全体的な意思決定過程に重要である。また,FDAは通常,品質システム法規(QSR)に適合することを確保するために生産施設の承認前検査を行う。この機関はまた、FDAの規定に適合することを確実にするために、1つまたは複数の臨床場所を検査することができる。
PMA審査が完了した後、FDAは、(I)商業マーケティングを許可し、最初に求められたものよりも範囲が限られている可能性がある1つまたは複数の適応の特定の処方情報を提供するPMAを承認することができ、(Ii)FDAがPMAが承認可能であると考え、FDAがどのような追加情報を必要とするか、または承認前に同意しなければならない承認後の承諾を示す承認可能な書簡を発行することができる。(Iii)承認に必要なステップを概説する承認不可能な手紙を発行するが、これらのステップは、通常、承認可能な手紙のステップよりも煩雑であり、追加の臨床試験を必要とする可能性があり、これらの試験は、しばしば高価で時間がかかり、承認が数ヶ月または数年遅れる可能性があり、または(Iv)出願を拒否する。FDAが承認可能または承認不可能な手紙を発行した場合、出願人は180日の時間で応答し、その後、FDAの審査クロックがリセットされる。
臨床試験
臨床試験はほとんど常に上場前の承認を支持する必要があり,510(K)計画の承認が必要な場合もある。米国では、高リスクデバイスの場合、これらの試験はIDE申請をFDAに提出する必要がある。IDEアプリケーションは、動物および実験室テスト結果のような適切なデータサポートを必要とし、人体上でデバイスをテストすることが安全であり、テストスキームが科学的に合理的であることを示している。特定の研究場所の特定の数の患者に対して、IDEは事前にFDAの承認を得なければならない。試験期間中、スポンサーは調査員の選択、試験モニタリング、報告、記録保存に関するFDAのIDEの要求を守らなければならない。調査者は患者のインフォームドコンセントを得,調査計画や研究案を厳格に遵守し,調査設備の配置を制御し,すべての報告や記録保存要求を遵守しなければならない。IDE申請がFDAや臨床試験現場の適切な機関審査委員会(“IRBs”)の承認を得るまで,重大なリスク機器の臨床試験は開始されない可能性がある。IRBは適切に構成されたグループであり、被験者に関連する医学研究を審査および監督することが正式に指定されており、ヒト研究被験者の権利、安全および福祉を保護するために、研究の修正、または不承認を承認、要求する権利がある。FDAまたは臨床試験が行われている各地点のIRBは、対象のリスクが利点よりも大きいと考えられるか、またはFDAまたはIRBの要求を遵守できないと考えることを含む、様々な理由で臨床試験の承認を随時撤回することができる。試験が完了しても、臨床試験の結果は、装置の安全性および有効性を証明できない可能性があり、曖昧であるか、または製品の承認または許可を得るのに不十分である可能性がある。
アメリカ食品医薬品局の持続的な規制
設備が承認されたり承認されて市場に投入された後も、多くの規制要求が適用される。これらの措置には
25
適応、ラベル、または製造プロセスまたは施設の変更を含む承認されたPMAデバイスのいくつかの変更は、変更を実施するために、新しいPMAまたはPMAサプリメントをFDAと承認して提出する必要がある。PMAの補足は、通常、元のPMAに必要な同じタイプの情報の提出が要求されるが、補足は、一般に、元のPMAがカバーするデバイスの提案変更をサポートするために必要な情報に限定される。FDAはPMAサプリメントを審査する際に原始PMAを審査するのと同様のプログラムと行動を使用する。PMAサプリメントは使用料も提出する必要があり,サプリメントのタイプに依存する。
私たちまたは私たちのサプライヤーが適用される規制要件を遵守できない場合、FDAまたは州当局が法執行行動を取る可能性があり、その中には以下のいずれかの処罰が含まれている可能性があります
さらに、FDAは、すべての陳述が真実で、正確で、誤解性がなく、十分に確認され、かつかなりバランスがとれていることを要求することを含むラベルおよび販売促進活動に要求し、許可された装置を非ラベル用途のために発売することを禁止する。FDAや他の機関は、ラベル外用途の普及を禁止する法律や法規を積極的に実行しており、ラベル外用途を不当に普及させていないことが発見された企業は、巨額の罰金や刑事起訴を含む重大な責任に直面している可能性がある。
新たに発見または開発されたセキュリティまたは有効性データは、新たな警告や禁忌症を増加させることを含む製品のラベルを変更する必要がある場合があり、他のリスク管理措置を実施する必要がある可能性もある。さらに、新しい立法によって生成された要求を含む新しい政府要求が確立される可能性があり、またはFDAの政策が変更される可能性があり、規制部門が私たちが開発している製品の承認または承認を延期または阻止する可能性がある。
医療保健法規
FDAによる医薬品マーケティングの制限に加えて、私たちの運営能力に影響を与える可能性のあるアメリカの医療法律および法規は、連邦詐欺および乱用法律、連邦反リベートおよび虚偽声明法、連邦データプライバシーおよびセキュリティ法律、および医師および他の医療保健専門家および教育病院への支払いおよび/または他の価値移転に関連する連邦透明性法律を含む。多くの州には似たような法律や法規があるが、連邦法律とは大きく異なり、コンプライアンス作業を複雑化させる可能性が高い。例えば、各州には反リベートおよび虚偽請求の法律があり、これらの法律の範囲は類似した連邦法よりも広い可能性があり、支払者が誰であろうと適用される可能性がある。また,健康情報の安全を守る州データプライバシー法は異なる可能性があり,連邦法は先制されない可能性がある。また、いくつかの州はすでに立法を公布し、製薬業者にマーケティングコンプライアンス計画を確立し、州政府に定期報告を提出し、定期的に販売とマーケティング活動を公開開示し、薬品の価格設定に関する情報を報告し、販売代表の登録を要求し、いくつかの他の販売とマーケティング行為を禁止する。これらの法律は私たちに
26
私たちがアメリカで市場承認を得た任意の候補製品に対して、管理とコンプライアンス負担を私たちに押しつけることで、販売、マーケティング、その他の活動を行うことができます。
これらの法律の広範性と利用可能な法定例外状況と安全港の規制範囲が狭いため、私たちのいくつかの商業活動、特に製品候補製品がアメリカで発売された後のいかなる販売とマーケティング活動も許可され、法律の挑戦と法執行行動を受ける可能性がある。私たちの運営が上記の任意の連邦および州法律または私たちに適用される任意の他の政府法規に違反していることが発見された場合、私たちは、損害賠償、罰金、監禁、政府医療計画から除外され、追加の報告義務および監督を含む重大な民事、刑事、行政処罰を受ける可能性があります(これらの法律を遵守しない疑いを解決するために会社の誠実な合意や他の合意の制約を受けた場合)、および私たちの業務の縮小または再編は、いずれも私たちの業務運営能力および私たちの運営結果に悪影響を及ぼす可能性があります。
国会は時々立法を起草し、提出することは、規制された製品の承認、製造、マーケティング、あるいはその精算を規制する法定条項を著しく変える可能性がある。例えば、米国では、2010年に“医療·教育調整法案”によって改正された“患者保護·平価医療法案”は、ある提供者に対する医療保険の精算を減少および/または制限し、米国で販売されている医療機器を製造または輸入する任意のエンティティに2.3%の年間消費税を徴収するが、限られた例外は除外される。2019年12月20日に法律となった更なる総合支出法案に署名し、現在医療機器消費税を永久廃止しています。また、その後の立法で改正された2011年の“予算制御法案”は、2027年の財政年度までに、さらに医療保険を医療サービス提供者に支払う金額が2%減少した。これらの減少はサプライヤーの収入や利益を減少させる可能性があり、これは彼らが新しい技術を購入する能力に影響を与えるかもしれない。また、米国の医療業界は、政府や民間保険会社が、より低いレートを実施し、サービスプロバイダと契約料率を下げることで医療コストを抑制しようとしているため、コストを抑制する傾向を経験している。未来には立法を通じて、政府支払者の私たちの製品に対する支払いを制限するかもしれない。
保証と精算を請け負う
米国や国際市場では、医療機器の使用は、政府や個人保険計画など、第三者支払者の精算状況にある程度依存している。医療機器を使用する医療提供者は、一般に、実行中の医療プログラムに関連するコストおよび費用の全部または一部を支払うか、またはそれらの患者ケアサービスを補償するために第三者支払者に依存する。我々が開発している製品がFDAによって商業化が承認された場合、どのような製品も費用効果があるとみなされない可能性があり、承認されれば、米国や他の国/地域で精算することができない可能性があり、将来の製品を利益に基づいて販売するのに十分ではない可能性がある。衛生技術評価機関の未来の製品に対する評価は第三者支払人の保証決定に大きく影響するだろう。米国での使用が承認されれば,我々が開発したどの製品も主に医療機関が購入し,医療機関は様々な第三者支払者にその施設で患者に提供する医療サービスの費用を徴収することが予想される。支払者は、Medicare計画を管理し、州政府と協力してMedicaid、他の政府計画、個人保険計画を管理するCMSを含むことができる。協力医療に保険と補償を申請する過程は長くて高い。また,連邦医療保険のカバー範囲は,連邦医療保険受益者にとって治療が“合理的かつ必要”であることを証明する能力があるかどうかに基づいている。我々の技術を使用した製品がFDAや他の規制部門の承認や承認を得ても、CMSを含む支払人は、保証や精算を与えない可能性がある。多くの個人支払者は,その保証·補償政策や金額を策定するためのガイドラインとして,CMSが決定した保証決定と支払金額を用いている。しかし,米国の第三者支払者には,医療機器のカバーや精算に関する統一政策はない。そのため、保証範囲と精算範囲は支払人によって異なる。
従業員
2022年12月31日までに、9人のフルタイム従業員がいます。私たちの従業員の中の一人も労働組合代表でもなく、集団交渉協定のカバー範囲もない。
27
利用可能な情報
私たちは、これらの資料を電子的に米国証券取引委員会(“米国証券取引委員会”)に提出または提出した後、合理的で実行可能な範囲で、できるだけ早く私たちのウェブサイト(https://seastarMedical.com)で、または私たちのウェブサイトを通じて、私たちの年間報告、Form 10-Q四半期報告、Form 8-K現在の報告、依頼書、およびこれらの文書のすべての修正を無料で提供します。本ウェブサイトに特に明記されていない限り、当ウェブサイトに掲載されている資料は、参照方法で本ウェブサイトに組み込まれることはない。
さらに、米国証券取引委員会は、報告書、依頼書、および他の発行者に関する情報を含むウェブサイトを維持しており、例えば、これらの発行者は、米国証券取引委員会に電子的に記録されている。このサイトのサイトはwww.sec.govです。
28
第1 A項。リスク要因です
私たちの証券に投資することはリスクと関連がある。あなたが私たちの証券を購入することを決定する前に、上記の“前向きな陳述に関する警告”で議論されたリスクおよび不確実性に加えて、本明細書で説明した具体的なリスクを慎重に考慮しなければならない。これらのリスクのいずれかが実際に発生すれば、私たちの業務、財務状況、流動性、および運営結果に実質的な損害を与える可能性がある。したがって、私たちの証券の市場価格は下落するかもしれません。あなたはあなたの投資の全部または一部を失うかもしれません。さらに、参照によって本明細書に組み込まれた任意の文書に記載されたリスクおよび不確実性は、私たちが直面する唯一のリスクおよび不確実性ではない。私たちは今知らないか、あるいは私たちが現在どうでもいいと思っている他のリスクと不確実性が重大になり、私たちの業務に悪影響を及ぼす可能性がある。
会社の財務状況に関するリスク
Seastar Medicalは設立以来重大な損失が発生しており,予測可能な未来には引き続き重大な損失を被ることが予想される。
同社は医療技術会社であり、主にその主要な候補製品SCDの開発と商業化に力を入れ、小児科と成人AKI適応に用いられている。同社はCRRTを受けたAKI小児患者に対するHDE申請をFDAに提出している。また,2023年2月9日,同社はFDAからIDE申請の承認を得て,CRRTを必要とするAKI成人アレルギー性炎症の減少におけるSCDの有効性を評価する重要な研究を行うことができる。同社は2023年第2四半期に学生募集を開始する予定で、2023年第4四半期に中期研究結果を生成し、2024年下半期にPMA申請を提出する予定だ。しかし,同社がいかなる計画中の臨床試験を適時あるいは完全に完了するかは保証されず,これらの試験に積極的なデータが生じる保証もない。同社がこの試験から積極的な結果を出すことができても、FDAおよび他の規制機関は、この研究を支援するための追加の試験を行うことを要求することができ、または試験の設計に同意せず、そのような設計の変更または改善を要求することができる。これまで、同社は規制部門の承認を得ておらず、その任意のSCD候補製品を商業化または販売することができ、予測可能な未来には、いかなる重大な収入も生じないと予想されている。Seastar Medicalは設立以来重大な純損失を出しており,2022年12月31日と2021年12月31日までの累計損失はそれぞれ9930万ドルと7630万ドルであった。
同社はすでにその大部分の財政資源を研究と開発に応用し、臨床試験と非臨床開発活動を含み、そして監督管理部門のSCD候補製品に対する許可を得た。業務合併が完了して以来、会社は主に証券売却によってその運営に資金を提供しているが、会社はこのような資金を得るために何らかの条件を満たす必要があるため、制限されている。それの未来の純損失の規模は未来の支出の速度と創出能力にある程度依存するだろう。これまで、その候補製品は著しい収入を生じておらず、その候補製品が開発や商業化に成功していない場合、またはマーケティング承認後に収入が不足している場合には、利益を達成することができず、その業務が失敗する可能性がある。たとえ同社が規制部門の承認を得ることに成功しても、米国でその候補製品を販売し、その収入は米国以外の市場の規模、米国以外の規制部門の承認、市場の承認を得て商業成功を得る能力に依存する。
同社は,その研究·開発活動の拡大と規制承認プログラムによる臨床プロジェクトの推進に伴い,引き続き大量かつ増加した費用が発生すると予想している。同社はまた、その製品の潜在的な商業化に備え、上場企業の運営を支援するための追加インフラの作成に関連する費用が増加すると予想している。このような理由から、予測可能な未来には、同社は引き続き重大かつ増加している損失と負のキャッシュフローに見舞われることが予想される。
その会社は何の重大な収入も生じておらず、永遠に利益を上げないかもしれない。
同社が収入を創出し、利益を達成する能力は、その単独またはパートナーとの開発成功、必要な監督管理承認を得、その主要候補製品SCDを商業化する能力に依存する。その製品から収入が得られないと予想されています
29
予測可能な未来における候補者の販売状況。それが将来製品販売から収入を得る能力は、以下の点での成功に大きく依存する
医療機器製品開発に関連する多くのリスクや不確実性のため、同社は、費用を増加させる時間や金額、およびいつ、または利益を達成または維持できるかどうかを予測することができない。さらに、FDAが追加的で予期しない研究を要求した場合、その費用は予想を超える可能性がある。
その候補製品が商業販売に承認されても、同社は任意の承認された候補製品の商業化に関連した巨額のコストが発生すると予想される。小児科AKIを治療するSCD製品候補製品については、会社がFDAによるそのHDE申請の許可を得ても、HDE要求下のいくつかの制限により、毎年販売可能な単位数量が制限されているため、会社がそのSCD装置を販売し、流通する能力は制限され、これは会社が産生する可能性のある収入をさらに制限する。その製品を販売することで収入を得ることができても、同社は利益を上げられない可能性があり、運営を継続するために追加資金が必要かもしれない。
同社の経営歴史は限られているため、その将来の経営業績を予測することは困難である。
同社はFDAや他の規制機関の承認を得ておらず,SCD候補製品を販売できるため,その商業運営履歴は限られている。紹介によると、同社は未来の経営業績を正確に予測する能力が限られており、未来の成長を計画し、それをモデリングする能力を含む多くの不確定性とリスクの影響を受けている。もし同社が監督管理機関の許可を得てSCD候補製品の販売を許可した場合、その将来の収入増加は減速する可能性があり、あるいはその収入は多種の原因によって低下または変動する可能性があり、その製品に対する需要の鈍化、競争の激化、市場需要の変化、新しい科学あるいは技術発展、全体の市場成長の鈍化、より多くの顧客を誘致できなかった、政府機関と保険会社はその製品の補償を受けることができなかった、あるいはいかなる理由でも成長機会を利用することができなかった。これらのリスクおよび不確実性および将来の収入増加に対する同社の仮定が誤っているか、またはこれらのリスクにうまく対応していない場合、またはその業績を正確に予測していない場合、同社の運営および財務結果は、その予想とは大きく異なる可能性があり、その業務が影響を受ける可能性がある。
もし会社が追加融資を受けることができない場合、それはその製品開発計画の延期、減少、またはキャンセルを迫られ、運営を停止させる可能性がある。
臨床前研究や臨床試験を含めた医療機器製品の開発はコストが高い。同社は,その進行中の活動に関する研究や開発費用が大幅に増加し,特にその臨床計画の推進に伴い大幅に増加すると予想している。2022年と2021年12月31日までのヒトデ医療の運営資金はそれぞれマイナス230万ドルと250万ドルであった。同社には現在、その運営を支援し、その計画の規制承認手続きを完了するのに十分な資本がない。その会社は運営を継続するために追加の資本を得る必要があるだろうが、これらの資金は受け入れ可能な条項で獲得できないか、または全く得られないかもしれない。また,取引終了時に大量の債務が発生し,LM Funding America,Inc.(“LMFA”),LMFAOスポンサー(“スポンサー”)とMaxim(“Maxim”)に無担保と保証のある本票を発行することを含め,会社はこれらの融資を返済するのに十分な資金がない可能性がある.会社が追加の資金を得ても、会社は確保を要求されるだろう
30
当該等の本票項目の強制的な支払いは、当社の経営業務による金額を削減します。
2022年8月23日,LMAOおよびSeaStar Medical,Inc.はTumim Stone Capital LLC(“Tumim”)と普通株購入プロトコル(“購入プロトコル”)を締結し,業務合併完了後に最大1,000,000,000ドルの普通株(“普通株”)を購入した。同社はTumimとの1億ドルの株式限度額を利用する能力に一定の条件と制限がある。同社は、(1)コンプライアンス証明書の交付、(2)初期登録宣言の提出、および(3)購入プロトコルに従ってTumimへの普通株式の売却を開始するために、通常の降格意見および負の保証を満たすことを要求されるであろう。これらの条件が満たされると、Tumimの購入は、普通株の取引量に応じて販売できる普通株数の上限と、Tumimのいくつかの実益所有権制限を含む様々な制限および他の制限を受ける。これらの条件のいずれかが満たされていない場合、または制限が発効していない場合、会社はトゥミム株式の全部または一部を使用できない可能性があり、これは会社がその資本需要を満たす能力に悪影響を与え、その業務に重大な悪影響を及ぼす可能性がある。同社は2023年2月現在、これらの長期購入契約から合計190万ドルを受け取っている。しかし、このような資本源は、私たちの普通株の取引量と価格に大きく依存するので、限られているかもしれない。
また、会社は最近、いくつかの条件を満たした場合、元金約980万ドルの転換可能な手形を4回に分けて発行することができる転換可能な手形融資を完了した。2023年3月15日、会社は元金330万ドルの転換可能な手形と最大328,352株の普通株の引受証を発行することで第1弾融資を完了した。しかし、当社が次の株主年次会議でこのような融資に対する株主の承認を得ることを含む、残りの3回の債券の下で追加手形を発行するために必要な条件を満たすことは保証されない。
会社が将来十分な資本を獲得しても、会社は自分の運営を支援し、計画中の規制承認手続きを完了するために追加の資金を調達することを要求され、これらの資金は十分な金額や受け入れ可能な条項で会社に提供できないか、または全く得られない可能性がある。必要な場合や受け入れ可能な条件で追加資本を調達できない場合、会社は要求される可能性がある
当社が十分な額あるいは受け入れ可能な条項で追加資本を調達できない場合、当社はそのSCD候補製品の臨床試験および監督審査手続きを含む開発と商業化を阻止され、これはその業務、運営結果および財務状況に重大な悪影響を与える。
同社はその純営業損失を利用して将来の課税収入を相殺する能力が制限される可能性がある。
2022年12月31日現在、同社の連邦と州(コロラド州、カリフォルニア州、フロリダ州)における所得税の純営業損失(NOL)の繰越はそれぞれ8230万ドルと2890万ドルで、将来的には課税収入の相殺に利用される可能性がある。コロナウイルス援助、救済、経済安全法案改正された2017年減税と雇用法案によると、2017年12月31日以降の納税年度に発生した連邦NOLは無期限に繰り越すことができるが、2020年12月31日以降の納税年度では、このような連邦純営業損失の控除額は課税収入の80%を超えてはならない。2018年前に発生した連邦NOLは20年繰り越すことができますが、課税収入制限を受けません。現行法によると,カリフォルニアのNOLは一般に20年(2020−2021年に発生したカリフォルニアNOLを限られた延期)に繰り越すことができ,課税所得制限を受けない。同社の連邦NOLは2940万ドルを含んでいてもいいです
31
無期限繰り越し、残りの5280万ドル連邦NOLは2027年に始まる異なる年に満期になり、連邦目的に使用される。使用しなければ、カリフォルニア州のNOLは2039年に満期になる。将来の課税収入の不足は、これらのNOLが満期になる前に会社がそれらを使用する能力に悪影響を及ぼすだろう。
一般に、改正後の1986年“国税法”第382節又は同法典によれば、会社は“所有権変更”(同法典第382節及び適用される大蔵省条例で規定されているように)が発生し、その利用変更前のNOLを利用して将来の課税所得額を相殺する能力が制限される。この規則第382条によれば、同社は将来的に所有権変更を経験する可能性があり、これはNOLを用いてその収入を相殺する能力に影響を与える可能性がある。当社はIRC第382条に基づいて所有権変更分析を完了していません。IRC第382条に示される所有権変更が発生したと判定された場合、将来の課税所得額および所得税負債を相殺するために使用することができるNOLおよび研究税収控除繰越額は、重大な制限または撤廃を受ける可能性がある。また,IRC第382条に示す所有権変更を実現した後,このようなNOLや研究税収控除に関する繰延税金資産が大幅に減少する可能性がある。また、同社が将来買収可能な会社のNOLを利用する能力が制限される可能性がある。もう1つのリスクは、法律または法規の変化、例えばNOLの使用停止または他の予見不可能な理由により、企業の既存のNOLが満期になる可能性があるか、または国家税収の目的を含む将来の所得税負担を低減するために使用できない可能性があることである。これらの理由から,当社が利益を実現しても,その貸借対照表に反映されているNOLの大部分を利用できない可能性があり,将来的に当社への納税義務が増加し,その業務,運営業績,財務状況に悪影響を及ぼす可能性がある。
同社の経営歴史は限られているため、その将来の経営業績を予測することは困難である。
同社はFDAや他の規制機関の承認を得ておらず,SCD候補製品を販売できるため,その商業運営履歴は限られている。紹介によると、同社は未来の経営業績を正確に予測する能力が限られており、未来の成長を計画し、それをモデリングする能力を含む多くの不確定性とリスクの影響を受けている。もし同社が監督管理機関の許可を得てSCD候補製品の販売を許可した場合、その将来の収入増加は減速する可能性があり、あるいはその収入は多種の原因によって低下または変動する可能性があり、その製品に対する需要の鈍化、競争の激化、市場需要の変化、新しい科学あるいは技術発展、全体の市場成長の鈍化、より多くの顧客を誘致できなかった、政府機関と保険会社はその製品の補償を受けることができなかった、あるいはいかなる理由でも成長機会を利用することができなかった。これらのリスクおよび不確実性および将来の収入増加に対する同社の仮定が誤っているか、またはこれらのリスクにうまく対応していない場合、またはその業績を正確に予測していない場合、同社の運営および財務結果は、その予想とは大きく異なる可能性があり、その業務が影響を受ける可能性がある。
会社の業務運営に関するリスク
同社にはないし、FDAの承認を得ない可能性もあり、米国や海外でその製品を販売することができる。
同社はFDAのSCD候補製品の販売許可とマーケティングを申請する際に、児童AKI適応のためのHDEと成人AKI適応のための重要な試験を含む様々な挑戦と困難に直面する可能性がある。同社は、SCDが小児科患者を治療する資格があることを証明するために、そのHDE申請を支持する大量の書類の提出を要求された。同社は最近FDAの承認を得てSCE用AKI成人キー試験を行うことができるが,会社が速やかにこの試験を完了できる保証はない,あるいは積極的なデータが発生する保証はまったくない。同社がこの試験から積極的な結果を出すことができても、FDAおよび他の規制機関は、この研究を支援するための追加の試験を行うことを要求することができ、または試験の設計に同意せず、そのような設計の変更または改善を要求することができる。同社はまた、規制承認過程に関する多くの他のリスクに直面しているが、これらに限定されない
32
同社が承認されても、FDAまたは他の規制機関は、高価なまたは重い上場後のテストまたは制御を要求する可能性がある。その将来の製品に対するいかなる遅延も、または維持、承認、または承認を得られなかった場合、会社はこれらの製品から収入を得ることができないか、または利益を達成することができない可能性がある。しかも、FDAと他の規制機関は広範囲な法執行権力を持っている。同社の規制の執行や調査、または他のより厳しい審査は、一部の医師にその製品の使用を勧め、その名声及びその製品の安全性及び有効性に悪影響を及ぼす可能性がある。
製品開発期間中,政府の医療機器政策の変化により,遅延や拒否が発生する可能性がある。FDAは、多くの理由で、PMA出願の承認を延期、制限、または拒否することができる
会社が規制部門のSCDの承認を速やかにあるいは根本的に得ることができなければ、その業務を継続できず、その運営を閉鎖させることができない可能性がある。
同社はHDE経路でFDA承認を求める上で、製品販売から利益を得る能力が制限されることを含むいくつかのリスクがある。
場合によっては、HDEによって承認された製品の販売金額が、デバイスの研究開発、製造、および流通コスト(すなわち、利益のため)を超えることはできない。現在、食品·薬物管理局安全·革新法案によって改正された“食品、薬物および化粧品法”第520(M)(6)(A)(I)条によると、人道主義的使用装置(“HUD”)は、HDEの承認を得た後にのみ利益を得る資格があり、(1)小児科患者または小児科集団で発生した疾患または状態を治療または診断することが意図されており、そのような装置は、小児科患者またはその疾患または状態が発生している小児科群としてマークされている。または(2)小児科患者において発生しない疾患または状況を治療または診断するための、または小児科患者において発生する数は、これらの患者のための装置を開発することが不可能であり、非常に不可能であるか、または安全ではないようにする。HDEによって承認されたデバイスがこの資格基準を満たしていない場合、利益を得るためにデバイスを販売することはできない。2017年のFDA再認可法案の公布に伴い、国会は、2022年10月1日までに免除請求を提出すれば、HUD/HDE収益性の免除を得ることができると規定している。HUD/HDE収益性を免除しなければ、当社の業務、経営業績および財務状況に重大な悪影響を及ぼす。
33
さらに、FDAがその後、PMAまたはHUDまたは同じ適応を有する他の同様のデバイスの510(K)を承認した場合、FDAはHDEを撤回する可能性がある。同様のデバイスがPMA承認または510(K)許可によって合法的に発売されると、関連する疾患または状態を治療または診断するために、HUDがもはや必要とされなくなる可能性があり、したがって、HUDは、FD&C法案520(M)(2)(B)条の要件にもはや適合しない可能性がある。
同社は業務拡大を計画しているが,その成長を効率的に管理できない可能性があり,資源を緊張させ,その業務目標の実現を遅延や破壊してしまう可能性がある。
同社は、FDAとの規制承認手続きを完成させるために、その内部組織インフラの構築と拡大を含む長期業務計画や成長戦略を実施するために、その業務を大幅に拡大する必要があるだろう。同社はまた、様々な戦略パートナー、技術許可者、顧客、製造業者、サプライヤー、コンサルタント、その他の第三者と新たな関係を構築することを要求される。このような拡張とこれらの新しい関係は、会社が既存の管理、運営および財務システムおよびプログラムおよび制御を著しく改善または代替すること、その様々な会社の機能間の協調を改善すること、および管理、訓練、インセンティブ、および増加する従業員基盤を維持することを要求するだろう。これらのステップを実施する時間やコストは、その管理者、システム、資源に大きな圧力を与える可能性があり、特に当時利用可能な財政資源や熟練従業員が限られていれば。当社は、その予想される増加した運営レベルを支援し、その様々な会社の機能を調整するために、その管理、運営、財務システム、プログラム、制御をタイムリーまたは完全に改善することを保証することはできず、予想される増加した従業員基盤を適切に管理、訓練、激励、保持することができることを保証することはできない。その成長戦略を管理できなければ、同社は速やかにその製品を大規模に商業化することができず、その業務は失敗する可能性がある。
同社は最初は単一製品からの収入に依存し、予測可能な未来には限られた数の製品に深刻に依存する。
もし同社がFDAおよび他の規制機関の許可を得た場合、同社は最初にそのSCD製品候補製品が児童および成人AKI患者にもたらす収入に依存し、予測可能な未来に単一または限られた数の製品に深刻に依存する。予見可能な未来に鑑み、当社の業務は単一または限られた数量の製品に依存し、ある特定の製品が市場に歓迎されなければ、当社の販売量、将来性、業務、経営結果、財務状況は重大な悪影響を受ける可能性がある。
もし同社が米国や外国の規制機関の広範な規定を遵守できなければ、その製品の商業化は延期または完全に阻止される可能性がある。
同社のSCD候補製品や研究開発活動は,米国や他の国や地域での開発,テスト,製造,商業化に関する広範な政府法規に制約されている。米国で1つの製品を大規模に購入し、潜在的に使用する準備ができているかどうかは、米国政府が複数の政府機関と協議し、FDA、国家衛生研究院、疾病管理·予防センターを含む。同社のSCDはFDAまたは任意の外国規制機関の規制承認を得ておらず、商業マーケティングや販売を行うことができる。米国や他の国では、FDAや他の政府の規制承認や法規を獲得し、遵守する過程はコストが高く、時間がかかり、不確定であり、予期しない遅延が生じる可能性がある。そのような規制承認を得るには、もしあれば、数年かかるかもしれない。多くの時間と費用がかかったにもかかわらず、規制部門の承認は保証されなかった。他にも、同社は以下のようなリスクと義務に直面している
34
FDAのこれらまたは他の規制要件を遵守しない場合、会社は行政または司法制裁を受ける可能性がある
同社の計画中の臨床試験の成功完了を延期することは、監督部門の許可を得る能力を脅かす可能性がある。
同社の業務の将来性はその完成研究と臨床試験の能力に依存し、成人AKI適応計画のSCDキー試験を含み、満足できる結果を得て、必要な監督管理の許可を得て、そしてそのSCD候補製品の商業化に成功した。同社の臨床試験の完成、試験結果の公表と規制部門の承認を得る能力は、様々な理由で延期される可能性がある
いずれの臨床試験においても重大な遅延が生じたり,計画以上の臨床試験が必要であれば,会社の開発コストが増加する。遅延が深刻である場合、またはその任意の候補製品が安全でないか有効でないことが証明された場合、または規制部門の承認を得ていない場合、会社の財務業績およびその候補製品の商業的見通しが損なわれる。また、同社は適時に臨床試験を完成できず、監督部門の許可を得る能力を危険にさらす可能性がある。
重要材料の第三者サプライヤーの遅延、中断または生産停止、または新材料同定の遅延は、会社がそのSCDデバイスを製造または処理する能力を阻止または遅延させる可能性がある。
供給プロトコルによると、同社は現在、小児科AKI適応のためのSCDデバイスのフィルタを提供するサプライヤーに依存している。現在のサプライヤーがSCDデバイスにフィルタを提供できない場合、またはプロトコルに規定された義務を履行できない場合、会社はその試験を行い、その製品を商業化するのに十分な数のフィルタを得ることができない可能性がある。さらに、会社が制御できない理由により、サプライヤーは、SCDに必要な特定のタイプのフィルタを停止または終了することを決定する可能性があり、この場合、会社は、直ちに入手できない、または全く得られない代替ソースを決定し、確保することを余儀なくされる。会社の既存のサプライヤーからこれらの材料を得ることができない場合、FDAが新しいサプライヤーの審査と承認を行う必要があるかもしれない。他のサプライヤーが所有しているかもしれませんが
35
会社が入手可能な同等の材料は、必要であれば、FDAの任意の代替サプライヤーに対する審査は、入手可能であれば数ヶ月以上かかる可能性がある。必要であれば、会社の重要材料第三者サプライヤーの任意の遅延、中断または生産停止、または新しい材料を鑑定する任意の遅延は、会社がSCDを製造する能力を阻止または延期する。
当社は現在と最近の臨床試験を行うのに十分なSCD在庫があると信じているが,そのSCDの需要が増加する可能性があり,当社はサプライヤーとの合意により現在購入可能なフィルタよりも多くのフィルタを購入する必要がある可能性があり,当社は新たな供給プロトコルの交渉に成功できない可能性がある。もし当社が適時に代替供給源を見つけることができなければ、どのような遅延も当社がSCD需要を満たす能力を制限し、それが行っている臨床試験を遅延させる可能性があり、これはその業務、運営結果と財務状況に重大な悪影響を与える。
同社は医療機器メーカーとの大規模契約の確定と処理について経験が限られている。
SCDおよび任意の他の将来の製品を商業化するために必要な生産レベルを達成するためには、会社は、米国および任意の他の使用国/地域の様々な連邦、州、地方規制機関が規定する製造基準に適合する契約メーカーとの大規模製造合意を確保する必要があるであろう。同社の大規模医療機器製品製造の調整·監督における経験は限られている。会社がその製品を商業化しようとしているため、生産が適時に完成できない可能性があり、商業的に合理的なコストで完成できない可能性があり、製造と制御の問題が生じる可能性がある。また、会社は会社が受け入れられる条項(あれば)でその製品の製造や流通に十分な資金を提供できない可能性がある。もし同社が規制部門の承認を得た後にその製品の製造を監督·援助することに成功しなければ、利益を達成するのに十分な収入を生み出すことができない可能性がある。
同社のSCD製造の困難はその収入や支出に悪影響を及ぼす可能性がある。
同社は現在そのSCDのすべての製造作業をアウトソーシングしている。そのSCDの製造は困難で複雑である。現在の臨床試験ニーズを支援するために,当社はその製品の生産において現行の良好な製造規範(“cGMP”)を遵守し続けていく予定である。当社がSCDをタイムリーに十分に製造·供給できるかどうかは、その第三者メーカーおよびその製品に依存する原材料や供給品を生産する第三者メーカーの絶え間ないかつ効率的な運営に依存している。会社製品の製造は以下の要因の影響を受ける可能性がある
そのSCDの効率的な製造と供給が中断されると、会社は出荷遅延や供給制限に遭遇する可能性がある。いつでも絶え間ない製品供給ができなければ,会社が行っている臨床試験が延期される可能性があり,その業務,運営結果,財務状況に重大な悪影響を及ぼす可能性がある。
36
同社のSCD技術は時代遅れになるかもしれません。
会社のSCD候補製品は、商業化前に新しい科学または技術によって発展した場合、または会社の製品よりも効率的および/またはより経済的な新しい治療法を有する他の人によって淘汰される可能性がある。同社のどのライバルもより効果的な製品を開発することができ、同社の技術を時代遅れにすることになる。さらに、競合他社は、SCDと同様の処理機構を作成しようと試みるFDAの許可されていないいくつかの既存のフィルタを使用することを含む同様の技術、装置、またはデバイスを使用する可能性がある。また,病院環境における新技術や科学的発展は,同社のSCD候補製品を時代遅れにする可能性がある。例えば,SCDはICUにおけるCRRTポンプシステムの既存の足跡に依存し,抗凝固剤として領域クエン酸塩が使用·使用されるようになってきている。これらの分野のさらなる発展は、商業的に実行できない可能性があり、あるいは時代遅れになる可能性があるSCD候補製品を再配置する必要があるかもしれない。最後に、同社がその主要な目標市場で顕著かつ持続的な成長を実現する能力は、病院の浸透、使用、出版、そのSCDの精算地位と医学教育の成功に依存する。新技術に基づく製品と比較して、同社の製品は競争力を維持できない可能性がある。同社が顧客のニーズを満たす製品を販売できなかった場合や、競争相手が発表した新製品に効果的に対応できなかった場合、同社の製品に対する市場の受容度を低下させ、その業務、経営業績、財務状況に悪影響を及ぼす可能性がある。
同社は医療機器業界で激しい競争に直面している。
同社は医療機器業界で多くのアメリカと外国の会社と競争し、その多くの競争相手は同社より多くの財務、人員、運営と研究開発資源を持っている。同社は、複数のライバルがサイトカイン嵐に対応するために、あるいは競争する技術を開発していると考えている。免疫系の治療が進んでおり,SCDの機会が減少する可能性がある。競合他社が以下のいずれかの疾患に対する製品を開発·販売すれば、同社のビジネス機会は減少または消失する
同社がSCDや任意の他の未来製品の開発に成功し、FDAや他の事業化に必要な規制承認を得ても、その製品は他の製品と効果的に競争できない可能性がある。より多くの疾患に関する知識が理解されつつあり,新たな治療技術をもたらす可能性がある。同社の競争相手は、それが開発可能な製品よりも効果的な製品、またはいかなるSeaStar医療製品の前に販売されている製品の開発とマーケティングに成功するかもしれない。同社の競争相手には、完全に統合された製薬·医療機器会社、バイオテクノロジー会社、大学、公共·民間研究機関が含まれている。同社と競争する多くの組織は、より多くの資本資源、より多くの研究開発者や施設、製品開発と規制承認を得る上でのより豊富な経験、およびより強いマーケティング能力を持っている。競合他社がより効果的な感染症や炎症治療法を開発したり、SCDをこのような用途に商業化する前にこれらの治療法を市場に展開したりすると、その製品のための市場吸引力を得ることができない可能性があり、あるいは治療を求める疾患が競合療法によって大きく解決される可能性がある。製薬業界の大企業との競争に成功しなければ、相当な収入や利益は決して生じないかもしれない。
37
当社の製品またはその製品の故障が死亡または深刻なダメージをもたらしたり、促進したりした場合、当社は医療機器報告法規の制約を受け、自発的な是正行動または機関の法執行行動をもたらす可能性がある。
FDA医療機器報告条例によれば、医療機器製造業者は、装置が死亡または重傷をもたらしたか、または死亡または重傷を引き起こす可能性があるか、または死亡または重傷を引き起こす可能性がある方法で故障を起こしたか、または促進する可能性があることをFDAに報告しなければならない。もし会社が規定された時間内にFDAにこれらの事件を報告しなかった場合、あるいは全くなかった場合、FDAは会社に対して法執行行動をとることができる。企業製品に関連する任意のこのような有害事象は、リコールや顧客通知、または検査または法執行行動などの機関行動のような将来の自発的な是正行動をもたらす可能性もある。任意の是正行動は、自発的であっても非自発的であっても、潜在的な訴訟を防止するために、会社が時間と資本を投入し、経営陣の業務運営への関心を分散させ、会社の名声や財務業績を損なう可能性がある。
同社は完全にコントロールできない可能性のある多くの運営や開発活動をアウトソーシングしている。
同社は第三者コンサルタントまたは他のサプライヤーに依存して、臨床試験を行い、その現在の候補製品を製造する大部分の日常的な責任を管理し、実行する。そのため、当社はこれらの第三者の努力の即時性と有効性に依存し続けている。同社の第三者への依存には、SCDの開発、製造、規制承認を支援するキープロバイダおよび第三者サービスプロバイダ、およびその情報技術システムおよび他のインフラの支援が含まれている。その管理チームはこれらのサプライヤーを監督する責任があるが、これらの第三者のいずれかがその契約、法規、その他の義務を履行できなかったり、これらの第三者の業績を深刻に乱す要因が発生した場合、会社の業務、運営結果、財務状況に重大な悪影響を及ぼす可能性がある。現在の新冠肺炎疫病は第三者サプライヤーが会社に必要なサービスを提供する能力を制限する可能性がある。
もし会社が使用した臨床研究機関が適時にその研究に十分な合格者を割り当てることができなければ、或いはその展開した仕事はFDA或いはその他の監督管理機関の要求を完全に満たすことができなければ、会社はその開発仕事を完成する時に重大な遅延とコスト増加に遭遇する可能性がある。当社製品のどのメーカーも、製品の生産量、製品の安定性や賞味期限、品質管理、制御プログラムと政策の十分な性、FDAの規定の遵守、新しい製造プロセスや施設がFDAの承認を必要とするなど、需要を満たすのに十分な新製品を生産する上で困難に直面する可能性がある。いずれかの場合、企業候補製品の開発および商業化は、企業がこのような開発および商業化を単独で継続するのに十分な財政資源または能力がない可能性があるので、延期、削減または終了される可能性がある。
会社またはその請負業者またはサービスプロバイダが法律法規に準拠していない場合、会社または彼らは規制行動の影響を受ける可能性があり、これは、会社がその候補製品および任意の他の将来の候補製品を開発、マーケティングおよび販売する能力に影響を与え、その名声を損なう可能性がある。
会社またはその製造業者または他の第三者請負業者が適用される連邦、州または外国の法律または法規に準拠していない場合、会社は規制行動の影響を受ける可能性があり、これは、SCD候補製品または将来開発されている候補製品の開発、マーケティングおよび販売に成功する能力に影響を与え、その名声を損なう可能性があり、その提案された候補製品の減少または市場に受け入れられない可能性がある。FDAが手紙、現場訪問、学術界或いは生物技術会社への全体的な提案を通じて技術提案或いは証拠を提供しても、臨床製品の製造を極めて労働集約型或いは高価にし、候補製品がコスト効果のある方法で生産できなくなる可能性がある。候補製品の管理モードまたは必要な試験は、候補製品を商業的に不可能にする可能性がある。臨床試験の進行はFDAや臨床試験地点の機関審査委員会や機関生物安全委員会から批判される可能性があり,候補製品の臨床試験を延期したり不可能にしたりする可能性がある。例えば,臨床試験の機関審査委員会は試験を停止したり,候補製品が安全に試験を継続できないと考えたりする可能性がある。これは候補製品の価値や会社の業務、運営結果、財務状況に大きな悪影響を及ぼすだろう。
38
同社の製品が承認されれば,SeaStar Medicalが不正な製品マーケティングや販売促進活動に従事すれば,法執行行動の影響を受ける可能性がある。
FDAの承認を得る前に、同社はその候補製品を普及またはマーケティングしてはならない。承認された後、その宣伝材料および訓練方法は、許可されていないまたはラベル外使用の普及を禁止することを含むFDAおよび他の適用可能な法律法規に適合しなければならない。事業者は,FDAが従事者の医療実践における治療の選択を制限または規範化していないため,ラベル外で同社の製品を使用することができる。しかしながら、FDAが、同社の宣伝材料または訓練が宣伝ラベル外使用を構成していると判断した場合、それは、その研修または宣伝材料を修正すること、または無タイトル手紙、警告手紙、禁止、差し押さえ、民事罰金または刑事罰を含む、会社に監督管理または法執行行動を受けるように要求することができる。他の連邦、州、または外国の法執行機関も行動する可能性があり、会社の宣伝や訓練材料がラベル外使用の宣伝を構成していると考える場合、虚偽精算を禁止する法律のような他の法定機関の巨額の罰金や処罰を招く可能性がある。この場合、会社の名声が損なわれる可能性があり、これにより、その提案の候補製品が減少または市場に受け入れられない可能性がある。また、同社製品のラベル外使用は製品責任クレームのリスクを増加させる可能性がある。製品責任クレームの弁護コストが高く、会社経営陣の注意を分散させ、会社への巨額の損害賠償を招き、会社の名声を損なう可能性がある。
同社は、そのSCDまたはその開発可能な任意の将来の候補製品の臨床開発および製造、販売およびマーケティングを第三者にアウトソーシングおよび依存することを意図しており、その将来の成功は、これらの第三者の努力の即時性および有効性に依存するであろう。
当社は必要な財政及び人力資源が自らそのSCD候補製品或いはその開発可能な任意の他或いは未来の候補製品のためにすべての臨床前及び臨床開発を行い、そのSCD候補製品又はその開発可能な任意の未来候補製品を製造、マーケティング或いは販売する能力もない。同社のビジネスモデルは、その候補製品の臨床、開発、製造、販売とマーケティングの一部または全部をアウトソーシングし、その資本とインフラコストを低減し、その財務状況を潜在的に改善する手段とすることを要求している。その会社の成功はこのようなアウトソーシング供給者の表現にかかっているだろう。もしこれらのサプライヤーが不振であれば、会社候補製品の開発が延期される可能性があり、会社候補製品開発のいかなる遅延もその業務、運営結果、財務状況に重大な悪影響を与える可能性がある。
同社は現在も将来も製品責任リスク,臨床,臨床前責任リスクに直面しており,起訴されれば,これらのリスクは会社に大きな財務負担をもたらす可能性がある。
同社の業務は、潜在的な製品責任や医療機器テスト、製造、マーケティングに固有の他の責任リスクに直面させている。それにクレームをつけることができます。成功した責任クレームまたはそれに対する一連のクレームは、会社の業務、運営結果、および財務状況に重大な悪影響を及ぼす可能性がある。当社は許容可能な条項で十分な製品責任保険(あれば)を獲得または維持できない可能性があり、このような保険は潜在的な責任に十分な保険を提供できない可能性がある。会社が入手可能な任意の製品責任保険範囲を超えるクレームまたは損失は、その業務、運営結果、および財務状況に重大な悪影響を及ぼす可能性がある。
同社のSCD候補製品は医療プログラムに使用可能であり,これらの製品は正確かつ正確な方法で機能しなければならない。もし医療従事者あるいは彼らの患者が当社の製品が設計通りに機能しなかったために損傷を受けた場合、あるいはその製品の設計が不適切であれば、当社は訴訟を受け、重大な補償性と懲罰的賠償を要求する可能性がある。製品責任クレーム、製品リコールと関連する不良宣伝リスクは医療製品のテスト、製造、マーケティングと販売に存在する。同社は一般臨床試験責任保険を獲得しようとしているが,その保険範囲は十分でないか不可能である可能性がある。さらに、会社は許容可能な条項で十分な製品責任保険(あれば)を獲得または維持できない可能性があり、そのような保険は潜在的な責任に十分な保険を提供できない可能性がある。いかなる製品のリコール又は訴訟が会社が獲得する可能性のあるいかなる製品責任保険範囲を超えても、その業務、運営結果及び財務状況に重大な悪影響を与える可能性がある。また、製品リコールはかなりのマイナス影響を与える可能性があります
39
会社の製品や業務を宣伝し、他の将来の候補製品の商業化を禁止または阻止する。
米国の立法あるいはFDA規制改革は会社が監督管理機関のその候補製品に対する承認を獲得し、承認を得た後にその製品を製造、マーケティング、流通させる可能性があり、より困難でコストが高くなる。
国会は時々立法を起草し、提出することは、規制された製品の承認、製造、マーケティング、あるいはその精算を規制する法定条項を著しく変える可能性がある。また、FDAは、FDAの法規やガイドラインを改正または再解釈することが多く、その方式は、会社の業務およびその製品に大きな影響を与える可能性がある。任意の新しい規制または既存の法規の改正または再解釈は、将来の製品のコストを増加させたり、審査時間を延長したりする可能性がある。立法変化が公布されるかどうか,FDAの法規,指導や解釈が変わるかどうか,これらの変化が会社の新製品開発にどのような影響を与える可能性があるかは予測できない。
当社は、厳格かつ変化するプライバシーの法律、法規、基準、データのプライバシーやセキュリティに関する政策、契約、その他の義務を遵守しなければなりません。
当社は、個人情報およびその他の情報(“処理”または“処理”)を収集、受信、記憶、処理、使用、生成、送信、開示、取得、保護、共有し、その業務、法律およびマーケティング目的、および他の業務に関連する目的を運営するために収集された臨床試験に関する情報を含む。
プライバシー、情報セキュリティ、処理に関する多くの連邦、州、地方と国際法律、法規とガイドラインがあり、その数や範囲は変化しており、異なる応用や解釈の影響を受けて一致していない可能性がある。当社は、将来的に上記のいくつかの法律、法規および指導に支配され、将来的には、その外部および内部プライバシーおよびセキュリティ政策、陳述、認証、標準、出版物、枠組み、ならびにプライバシー、情報セキュリティおよび処理に関連する第三者契約義務の条項に制限される可能性がある。
当社がこのような義務を履行または履行できなかったとみなされていない場合は、
また、これらの義務が複雑かつ重い義務を規定していること、およびこれらの義務の解釈や応用に大きな不確実性があることを考慮すると、当社は重大なコストを発生させ、経営陣の注意を移し、その臨床試験を含めてその業務運営を変更し、遵守に努めることが可能であり、その業務、運営結果、財務状況に重大な悪影響を及ぼす可能性がある。
2018年カリフォルニア州消費者プライバシー法案(CCPA)は、米国のますます厳しくなっているデータ保護立法の一例である。CCPAはカリフォルニア住民により大きな権利を与え,彼らの個人情報にアクセスし,削除し,特定の個人情報を共有しないことを選択し,彼らの個人情報がどのように使用されるかに関する詳細な情報を取得することができる.CCPAは違反行為に対する民事処罰と、データ漏洩に対する個人訴権と毎回の違反に対する法定損害賠償を規定しており、金額は100ドルから750ドルまで様々であり、これはデータ漏洩集団訴訟を増加させ、コストの高い法的判決と和解に至ることが予想される。CCPAの臨床試験データに対する免除は限られているにもかかわらず、CCPAや他の類似法律は会社の業務活動に影響を与える可能性があり、具体的にはそれらの解釈に依存する。
40
会社の安全対策や会社の維持を代表する安全対策が損害、制限、または失敗を受けた場合、会社の業務運営は悪影響を受ける。
通常のビジネスプロセスでは、当社は、当社または他の第三者または集団によって所有または制御される個人データ、知的財産権、商業秘密、および独自の商業情報を含む独自、機密および敏感な情報を処理して処理する。当社はこのような敏感な情報を使用し、サービスプロバイダや他の第三者と共有する可能性があります。会社、そのサービスプロバイダ、パートナー、または他の関連第三者が経験したことがある場合、または将来、任意のデータ損失、削除または破壊、不正アクセス;損失、不正取得、開示または機密および敏感な情報を暴露する1つまたは複数のセキュリティイベントが発生した場合、脆弱性問題を解決するための資金の流用、および運営および開発計画における中断、遅延、または中断を含むSeaStar Medicalの業務、運営結果、および財務状態に悪影響を及ぼす可能性がある。
ネットワーク攻撃、インターネットベースの悪意のある活動、およびオンラインとオフラインの詐欺が盛んに行われており、ロシアとウクライナの間の持続的な衝突がサイバー攻撃やサイバーセキュリティ事件を引き起こす可能性があり、私たちの行動に直接的または間接的な影響を与える可能性があることも増加し続けている。従来のコンピュータ“ハッカー”、脅威参加者、ソフトウェア脆弱性、悪意のコード(例えば、ウイルスおよびワーム)、従業員の窃盗または乱用、サービス拒否攻撃(証拠充填など)、脅迫ソフトウェア攻撃の脅威に加えて、複雑な民族国家および民族国家が支持する参加者は、現在も攻撃(高度な持続的脅威侵入を含む)に参加している。会社はまた、ネットワーク釣り攻撃、ウイルス、マルウェアインストール、サーバ障害、ソフトウェアまたはハードウェア障害、データ損失または他のコンピュータ資産、または他の同様の問題を受ける可能性があり、いずれも、そのビジネス、運営結果、および財務状態に重大な悪影響を及ぼす可能性がある。
同社の製品が商業化されることが承認された場合、同社の設備が第三者カバーや補償を欠いている場合、その採用が延期または制限される可能性がある。
米国や国際市場では,医療機器の使用や成功は,政府や個人保険計画などの第三者支払者が精算できるかどうかにある程度依存している。医療機器を使用する医療提供者は、一般に、実行中の医療プログラムに関連するコストおよび費用の全部または一部を支払うか、またはそれらの患者ケアサービスを補償するために第三者支払者に依存する。FDAが同社が開発している製品の商業化を承認した場合、米国や他の国/地域では精算が得られない可能性がある場合や、承認されても、会社の将来の製品(SCDを含む)を利益に基づいて販売するのに十分ではない可能性がある。健康技術評価機関の会社の将来の製品に対する評価は第三者支払人の保証決定に大きく影響する。これらの評価は会社の制御範囲内ではなく、どのような評価も行うことができないか、有利な結果が生じる可能性がある。
米国での使用が承認された場合,同社はSCDを含めて開発された任意の製品を予想し,主に医療機関がその運営予算で購入する。支払者は、医療保険計画を管理し、州政府と協力して医療補助、他の政府計画、個人保険計画を管理する医療保険·医療補助サービスセンター(CMS)を含むことができる。協力医療に保険と逓増補償を申請する過程は長くて高価だ。また,連邦医療保険の保険加入範囲は,同社が連邦医療保険受益者にとって治療が“合理的かつ必要”であることを証明する能力に基づいている。当社のSCD技術を使用した製品がFDAや他の規制部門の承認や承認を得ても、CMSを含む支払者は、保証や精算を与えません。Medicaidのようないくつかの政府計画については、カバー範囲および適切な精算は州によって異なり、いくつかの州のMedicaid計画は、会社の技術システムを使用するプログラム製品に十分な金額を支払わないか、または全く支払わない可能性がある。また,多くの個人支払者は,その引受·償還政策や金額を策定するためのガイドラインとして,CMSが決定した保証決定と支払金額を用いている。しかし,米国の第三者支払者には,医療機器のカバーや精算に関する統一政策はない。そのため、保証範囲と精算範囲は支払人によって異なる。CMSや他の機関が保険の範囲を制限したり、医師や病院の精算支払いを制限したりする場合、これは多くの個人支払者の将来のいかなるSeaStar医療製品の保証と精算決定に影響を与える可能性がある。
41
SCDを含む将来の任意の製品が商業化されることが承認された場合、支払人の精算政策や手続き上の不利な変化は、会社のマーケティングやその製品を販売する能力に影響を与える可能性がある。
過去10年間,医療コストは大幅に上昇し,立法者,規制機関,第三者支払者はコスト低減を提案し続けてきた。第三者支払者は、医療製品やサービスの価格に挑戦し、医療製品やサービスの購入を制御または著しく影響するコスト制御措置を策定することが増えている。
例えば、米国では、2010年に“医療·教育和解法案”(総称して“ACA”と呼ぶ)によって改正された“患者保護·平価医療法案”は、他に加えて、ある提供者への医療保険精算を減少および/または制限している。しかし、2018年12月14日、テキサス州の地方裁判所裁判官は、2017年に公布された非公式名称“2017年減税·雇用法案”の立法の一部として、“個人強制令”が国会で廃止されたため、“平価医療法案”全体が違憲と判断した。また、2021年6月17日、米国最高裁は、ACAが“個人権限”が国会で廃止されたため、全体的に違憲だと弁明する手続き理由に基づく挑戦を却下した。したがって、ACAは“個人許可”なしで依然として有効である
また,米国最高裁が裁決を下す前に,総裁·バイデンは2021年1月28日にACA市場を介して医療保険を受けることを目的とした特殊な保険加入期間を開始し,2021年2月15日から2021年8月15日まで開放された行政命令を発表した。行政命令はまた、特定の政府機関に、医療補助モデルプロジェクトおよび免除計画の再審査、および医療補助またはACAによる医療保険カバー範囲の獲得による不必要な障害をもたらす政策を含む医療補助モデルプロジェクトおよび免除計画の再審査および見直し、医療補助またはACAによる医療保険のカバー範囲を制限する既存の政策およびルールを再検討するように指示する。ACAは未来に司法や国会で挑戦される可能性がある。このような挑戦や訴訟,バイデン政府の医療改革措置がACAや同社の業務にどのように影響するかは不明である。その後の立法で改正された2011年予算制御法案は、2031年の財政年度までに、さらに医療保険を提供者に支払う金額を2%減少させた。しかし,新冠肺炎の救済立法は2020年5月1日から2022年3月31日までの2%の連邦医療保険自動減額を一時停止した。現在の立法によると、医療保険支出の実際の減少幅は2022年の1%から本自動減額の最終年度の3%まで様々になる。これらの減少はサプライヤーの収入や利益を減少させる可能性があり、これは彼らが新しい技術を購入する能力に影響を与えるかもしれない。
また、米国の医療業界は、政府や民間保険会社が、より低いレートを実施し、サービスプロバイダと契約料率を下げることで医療コストを抑制しようとしているため、コストを抑制する傾向を経験している。しかも、議会は追加的な医療改革措置を考慮している。未来には立法を通じて、政府支払人の会社製品に対する支払いを制限するかもしれない。政府はまた新冠肺炎の流行に対応するためにもっと多くの行動をとる可能性がある。また,保険会社などの商業支払者は,医療機器メーカーの製品精算を制限するような政策をとることができる。したがって,SeaStar Medicalの製品やその製品を用いたプログラムや患者看護は,費用便益に応じたレベルで精算されない可能性がある。
同社は、その製品を販売する可能性のある他の国では、精算手続きや政策の不利な変化に関連する類似のリスクに直面している。精算と医療支払いシステムは国際市場で大きく異なる。同社は国際精算承認を得ることができない、あるいは外国支払人の精算政策にいかなる不利な変化も生じ、海外市場でその製品を販売する能力にマイナス影響を与え、その業務、経営業績、財務状況に重大な悪影響を与える可能性がある。
同社はキーパーソンに依存しており、合格者を引き付けることができず、その業務目標を実現する能力を阻害する可能性がある。
会社の成功はキーパーソンの持続的なサービス、特にエリック·スクロフ最高経営責任者にかかっている。これらの人のいずれを失っても、会社の業務、運営結果、財務状況に重大かつ不利な影響を及ぼす可能性がある。会社はまた、その業務計画と成長を全面的に実施するために、高技能の管理、科学、行政人員の採用と採用を要求される
42
戦略です。その業務は専門的な科学性質を持っているため、会社はその合格した科学、技術と管理人員を吸引と維持する能力に高度に依存している。これらの人に対する競争は非常に激しく、会社は将来的により多くの素質の高い人員を引き付け、同化あるいは維持することができないかもしれない。同社は競争力のある価格で合格者を採用してサービスを提供できない可能性があり、特にその限られた財政資源や既定の記録不足による雇用リスクを考慮している。また、会社が米国の他の地域や海外からの人員誘致を要求された場合、その地域への人員移転に関するコストにより、それが困難になる可能性がある。会社が合格した従業員や幹部を引き付けることができない場合、その製品を開発し、規制許可を得ることができず、その業務が倒産する可能性がある。
同社の製品は将来的に製品にリコールされる可能性がある。
FDAと同様の外国政府当局は、設計または製造に重大な欠陥または欠陥がある場合に商業化製品をリコールすることを要求する権利がある。FDAにとって、リコールを要求する権力は、この装置が合理的な可能性があることが深刻な傷害や死亡を招く可能性のある調査結果に基づいていなければならない。設備に何か重大な欠陥が発見されれば、メーカーは自発的に製品をリコールすることができる。FDAは、ある種類のリコールをリコール開始後10営業日以内にFDAに報告することを要求する。健康リスクは受け入れられない、部品故障、故障、製造ミス、設計或いはラベル欠陥或いはその他の欠陥と問題により、政府の強制或いは自発的なリコールが発生する可能性がある。リコール会社のどの製品も管理と財務資源を移転し、会社の名声、業務、経営結果、財務状況に悪影響を与え、企業がコスト効果とタイムリーな方法で製品を生産して顧客の需要を満たす能力を弱める可能性がある。
同社はまた、他のコストを負担することを要求されたり、他の行動を取ったりする責任クレームを受ける可能性があり、その将来の販売および利益創出能力に負の影響を与える可能性がある。会社は、これらのリコールがFDAや他の国の主管当局に報告する必要がなくても、いくつかのリコール記録の保留を要求されている。同社は、これらの製品がFDAや他の国の主管当局に通知する必要がないと考える場合、将来的にその製品に関する自発的なリコールを開始することができる。FDAがその会社の決定に同意しなければ、彼らは同社にこれらの行為をリコールとして報告することを要求することができる。今後のリコール声明は、同社の顧客における名声を損なう可能性があり、その販売にマイナス影響を与える可能性がある。さらに、FDAはリコールが報告されていない状況に対して法執行行動を取るかもしれない。会社は,すべての会社が開始した医療機器の訂正と解体の詳細記録保存要求を遵守することも求められている。
同社の業務は将来の疫病がもたらすリスクの影響を受けている。
全世界の疫病は公衆衛生と経済に巨大な挑戦をもたらし、会社の従業員、患者、コミュニティと業務運営に影響を与え、アメリカと全世界の経済と金融市場にも影響を与えた。
未来の大流行はそのSCD候補製品の発売スケジュールに直接或いは間接的に影響を与える可能性がある。同社は、その業務、臨床試験、製造とサプライチェーンに深刻な影響を与える可能性のある中断に遭遇する可能性がある
43
また、今後の疫病の蔓延は、同社が適時に追加資本を調達する能力にマイナス影響を与え、甚だしきに至っては影響を与えない可能性がある。
将来の大流行が同社の業務に与える影響の程度は、その臨床試験、製造およびサプライチェーンおよび財務状況を含み、将来の事態の発展に依存し、これらの事態の発展は高い不確実性を有し、例えば、疾患の持続的な地理的伝播、大流行の持続時間、米国および他の国の旅行制限や社会的距離、持続的な業務閉鎖または業務中断、および米国および他の国が疾患を制御·治療するための行動の有効性を把握することができない。
同社の少数株主は、その主要株主の陶氏年金基金を含め、その業務に重大な影響を与える可能性がある。
同社にはいくつかの重要な株主がおり、陶氏社員年金計画信託基金と合同炭化物会社社員年金計画信託基金を含むかなりの割合の普通株流通株を持っている。これらの少数の重要株主は、単独または共同行動にかかわらず、合併またはその他の方法で会社またはその資産を売却するなど、取締役の選出および重要な会社取引の承認を含む株主の承認を必要とする事項に大きな影響を与えることができる。このような所有権集中は他の株主が会社を重大に変更することを困難にする可能性があり、会社のコントロール権の変化を遅延、阻止、加速(場合によっては)する可能性があり、普通株の市場価格に不利な影響を与える可能性がある。さらに、これらの重要株主のうちの1つまたは複数は、普通株の全部または大部分を短時間で販売することができ、これは、我々の普通株の取引価格に悪影響を及ぼす可能性がある。
同社の予測経営や財務結果は、同社が開発した仮説や分析に大きく依存している。これらの仮定や分析が正しくないことが証明された場合、同社の実際の運営および財務結果は、その予想を大幅に下回る可能性がある。
同社がこれまで提供してきた予測財務と経営情報は、将来の業績の見積もりを反映している。実際の運営と財務結果が業務発展と一致するかどうか
44
会社の予測に反映される予想と仮定は多くの要素に依存し、その多くの要素は会社の制御範囲内ではなく、含まれているが、これらに限定されない
上記又は他の要因のいずれかの不利な変化は、その大部分が会社がコントロールできるものではなく、会社の業務、経営結果及び財務状況に実質的な悪影響を及ぼす可能性がある。
同社の市場機会の見積もり、業界予測、市場成長の予測は不正確であることが証明されている可能性がある。
本年度報告に含まれる市場機会推定と成長予測は,会社の所在業界や会社が経営しようとしている市場に関する情報を含み,独立した業界や研究機関および他の第三者源が発表した公開情報から得られる。当社は本年度報告書が提供する開示に責任があり、当該等の第三者情報が信頼できると信じているが、当社は当該等の第三者情報を独立して確認していない。また、様々な要因により、会社の業界の将来の業績の予測、仮説、見積もりは不確実性やリスクの影響を受ける。したがって、第三者情報または予測における不正確さは、社内業務計画および投資家分析に依存する仮説に悪影響を及ぼす可能性がある。
会社の知的財産権に関するリスク
当社は第三者が独占的に許可した特許権に依存しており、これらの特許権は終了または失効される。許可側が許可を終了したり、関連特許を維持または強制執行できなかった場合、会社の競争地位は深刻な損害を受ける可能性がある。
同社のSCD技術の開発部分は独占許可の特許権に依存している。例えば、同社はミシガン大学と共同でSCD技術に関連する特許を所有し、独占的に許可している。UOMが会社との許可を終了すれば,共通の特許の独占権利を持つことはなくなり,UOMはUOMの共同所有特許における権益を会社の競争相手に自由に許可することができる.
会社は将来的には、SCD技術または他の技術の開発および商業化に必要ないくつかの第三者特許権および独自技術の許可に依存する可能性がある。企業が商業的に合理的な条項でこれらのライセンスをタイムリーに取得できない場合(あれば)、そのような製品を商業的に開発する能力が制限されたり阻止されたりする可能性がある。これらのライセンスが、すべての関連使用分野および会社がその技術および製品を開発または商業化するすべての地域で主題知的財産権を使用する独占的権利を提供しない場合、会社は、競合他社がこれらの地域で競合製品を開発および商業化することを阻止することができない可能性がある。その会社が必要なライセンスを取得できても、その製品を販売するために巨額の許可料を支払うことが要求される可能性がある。
45
会社の現在または将来の任意のライセンスが何らかの理由で早期に終了された場合、またはそのライセンス者が所有する特許および知的財産権が第三者の挑戦または失敗を受けた場合、会社の研究および商業化努力は実質的な悪影響を受ける可能性がある。その製品を十分に開発·マーケティングするのに要する時間内に、同社のライセンスは継続的に有効ではない可能性がある。ライセンス終了または関連特許および知的財産権が挑戦または失敗した場合、企業が許容可能な条項に従って適切な代替製品を取得または開発することができない可能性がある(あれば)。また,会社が任意の特許許可に応じて必要な金を支払うことができない可能性があり,この場合,許可側は許可を終了する可能性がある.
さらに、会社の許可者は、その許可された、会社業務に依存している、または起訴可能な特許出願を、会社の最適な利益に適合しない方法で起訴することに成功しない可能性がある。また,許可者が許可された特許を維持できない可能性があり,第三者侵害者に対して訴訟を提起しないか,侵害を証明できない可能性があるか,あるいは特許が無効または強制実行不可能な反訴に対して抗弁できない可能性がある.
また、当社が最善を尽くしたにもかかわらず、ライセンス側は、当社が実質的にライセンス契約に違反して許可を終了したと主張することができ、当社は、規制部門による当該ライセンスに含まれるいかなる製品の承認も得られず、その製品を販売することができない。同社のライセンスが終了された場合、または関連特許が予想される市場排他性を提供できなかった場合、競争相手は、規制部門の同じ製品の承認を求め、市場に投入する権利がある。
ライセンス契約によると、知的財産権に関する論争が発生する可能性があります
その会社の許可をめぐる知的財産権の紛争が、許容可能な条項で既存の許可手配の能力を維持することを妨害または損害した場合、同社は、影響を受けた候補製品の開発に成功し、商業化することができない可能性がある。
企業がその製品のために十分な特許保護を得ることができない場合、特許保護の範囲が十分でない場合、または企業がその知的財産権を保護するための特許、商業秘密、および契約条項の組み合わせが不十分である場合、その競争相手は類似または同じ製品を開発して商業化する可能性があり、会社がそのような製品を商業化することに成功する能力は悪影響を受ける可能性がある。
同社の成功は、その製品に含まれる技術の独自の権利を保護する能力、米国および他の国でそのSCD技術に関連する特許保護を取得および保持する能力、およびその業務に重要であると考えられる他の技術を大きく依存する。同社は特許保護、商業秘密法、および秘密保持、秘密およびその他の契約制限に依存して独自技術を保護している。もし会社がその知的財産権を十分に保護していない場合、競争相手はその所有可能ないかなる競争優位性を侵食または否定する可能性があり、これはその業務、運営、財務状況を損なう可能性がある。会社のノウハウを保護するために、そのSCD技術やその業務に重要な他の技術に関する特許保護が米国や海外で求められている。特許出願や承認手続きは高価で
46
時間がかかります。会社は必要または望ましいすべての特許出願を合理的なコストまたはタイムリーに提出して起訴することができないかもしれない。十分な特許および他の知的財産権を保護、取得、維持または延長できない場合、会社がその製品を開発、販売する能力に重大な悪影響を及ぼす可能性がある。このような特許および他の知的財産権の実行、保護、および維持は挑戦的であり、費用が高い可能性がある。
当社は、発行または付与されたいかなる特許も、その後無効および/または実行不可能であることが発見されないことを決定することはできない。同社は、競争相手が競争する製品の開発を防止するために、進行中の特許出願の発行形態が十分な保護を提供することを決定することができない。医療機器技術会社として、複雑な法律や事実に関連して考えられるため、同社の特許地位は確定していない。米国特許商標局(“USPTO”)と外国特許庁が特許を付与する際に採用する基準は,常に統一的または予測可能ではない。例えば、特許を出願可能な主題または医療方法として許容される権利要件の範囲については、世界的に統一された政策はない。したがって、現在未決または将来出願されたいかなる出願からも特許が発行されない可能性がある。そのため、同社は将来のその技術の保護の程度を知らない。そのため、会社特許権の発行、範囲、有効性、実行可能性、商業価値は大きな不確実性を持っている。
発行された特許のみが、そのような特許で主張されている技術を実践する第三者に対して強制的に実行することができる。このような出願が特許を取得しない限り、審査される特許出願は強制的に実行されてはならない。特許性の他の要求が満たされていると仮定し,現在,特許付与が最初に特許出願を提出する側である。しかし、2013年3月16日までに、米国では、特許は最初に発明されて保護を要求された標的の一方に付与されている。科学文献で発表された発見は往々にして実際の発見に遅れており、米国と他の司法管轄区の特許出願は通常、申請18ヶ月後に発表され、時には全く発表されないこともある。したがって、会社は、そのような発明のために特許または係属中の特許出願に請求された最初の発明を行う会社であるか、またはそのような発明のために特許保護を出願した最初の会社であることを決定することができない。
さらに、特許の発行は、その発明性、範囲、有効性、または実行可能性に対して決定的ではないため、会社の特許または係属中の特許出願は、法廷で、または米国特許商標局または外国特許庁によって挑戦される可能性がある。例えば、会社は、第3の方向の米国特許商標局が提出した以前の技術の発行前に提出されたか、または米国または他の場所での異議、派生、再審、当事者間審査または介入手続きのような認可後審査手続きに参加し、その特許権または第三者の特許権に挑戦することができる。このような任意の挑戦において不利な裁決を下すことは、排他性喪失または特許主張の全部または部分的な縮小、無効または実行不能をもたらす可能性があり、これは、企業が他の人の同様の製品の使用または商業化を阻止する能力を制限するか、または会社の特許保護期間を制限する可能性がある。さらに、医療機器の開発、テスト、および規制審査に要する時間を考慮すると、同社の特許は、そのような製品がFDAの承認を得て商業化される前または直後に満了するか、または外国でその製品を販売することが許可される前に満了する可能性がある。
特許出願は、現在および将来の候補製品のすべてまたは一部を保護する特許の発行、または他の競合製品の商業化を効果的に阻止する特許の発行をもたらしてはならない。米国や他国の特許法または特許法解釈の変化は,会社特許の価値を低下させたり,その特許保護範囲を縮小したりする可能性がある。また、外国の法律は米国の法律と同程度や方法で会社の権利を保護しない可能性がある。例えば,欧州特許法は米国特許法に比べて人体治療方法に対する特許性制限が多い。
当社は、そのいくつかの特許および出願が付与されれば、そのSCD技術の独自性を保護するのに役立つと信じているが、このような保護は、この技術の開発中に当社を保護するのに不十分である可能性がある。会社の特許出願が特許として発行されていても、それらの発行形態は、それに意味のある保護を提供し、競争相手がそれと競合することを防止し、または他の方法でいかなる競争優位性を提供してはならない。同社の競争相手は、類似または代替技術または製品を非侵害的に開発することによって、その特許を回避することができるかもしれない。当社の競争相手も承認を求めて、彼ら自身の製品を販売することができます
47
会社の製品です。したがって、会社が有効かつ強制的に実行可能な特許を有していても、これらの特許は、その業務目標を達成するのに十分な競合製品または技術を保護することができない可能性がある。
会社が“ハッジ·ワックスマン法案”や同様の非米国法の保護を受けていない場合、その製品の特許期間を延長するために、その業務、経営結果、財務状況が重大な損害を受ける可能性がある。
特許の有効期限は限られています。米国では、すべての維持費が適時に支払われれば、特許の自然失効時間は、通常、その最初の米国非臨時出願日から20年である。様々な延期があるかもしれないが、特許の有効期限とその提供される保護は限られている。当社の製品やその用途に関する特許を取得しても、特許の有効期限が満了すると、当社は競合製品からの競争に直面する可能性があります。新製品候補製品の開発、テスト、規制審査に要する時間を考慮すると、会社製品を保護する特許は、これらの製品がFDAの承認を得て商業化される前または直後に満期になる可能性がある。したがって、同社の特許組み合わせは、他の会社が同様または同じ製品を商業化することを排除するために、同社に十分な権利を提供していない可能性がある。
FDAが同社の候補製品の上場を承認する期間、期限、要件に基づいて、同社の米国特許が発行された場合、“ハッチ·ワックスマン法”または他の国の類似立法に基づいて限られた特許期間を延長する資格がある可能性がある。しかしながら、同社の特許及び特許出願は、FDAによりIII類機器に分類された医療機器に関連している場合にのみ、“ハッジ·ワックスマン法案”による特許期間の延長を受ける資格がある。したがって、同社の候補製品がクラスIIIデバイスに分類されない場合、それは、そのような承認された製品をカバーする任意の特許出願のために期限を延長することができない。条件を満たしていれば、“ハッジ·ワックスマン法案”は、製品開発およびFDA規制審査中に失われた有効な特許期間の補償として、承認された製品をカバーする特許を最大5年間延長することを可能にする。特許期間の延長は、製品候補承認の日から14年間の残り期間を超えてはならず、承認された製品候補に関する特許を1つだけ延長することができる。しかし、会社が適用の最終期限内に出願できなかった場合、関連特許の満了前に出願できなかった場合、または他の理由で適用の要求を満たしていなかった場合、会社は延期されない可能性がある。また,延期の長さは要求されたものよりも短い可能性がある.
したがって、会社が特許期間の延長を得ることができない場合、またはそのような延長の期間が要求よりも少ない場合、会社はその製品に対して特許権を行使することができる期限が短縮され、競争相手は予想よりも早く上場競争製品の承認を得ることができる可能性がある。そのため、会社の業務、経営業績、財務状況は不利かつ重大な影響を受ける可能性がある。
会社は代償の高い知的財産権訴訟に巻き込まれる可能性があり、管理層の時間と精力の分流を招き、会社に損害賠償金の支払いを要求し、その商業的に入手可能な製品の販売を阻止し、および/またはその製品から実現される利益率を低下させる。
同社のビジネス成功は、第三者の知的財産権および他の独自の権利を侵害することなく、そのSCD技術およびその開発された任意の将来の技術の能力にある程度依存する。
医療機器業界の特徴は,特許や他の知的財産権をめぐる広範な訴訟と行政訴訟である。1つの製品が特許を侵害しているかどうかは、複雑な法律および事実の問題に関連しており、決定はしばしば不確実である。開発中の製品が無意識に既存の特許を侵害している可能性を意識していない会社があるかもしれない。会社の新製品の発売や市場でのより高い知名度の獲得に伴い、会社に対する特許侵害クレームの可能性は競争相手数の増加とともに増加している。
当社に対するいかなる侵害クレームも、法的根拠がなくても、当社に巨額のコストを発生させ、その財務資源に重大な圧力を与え、管理層の核心業務に対する注意を移し、その名声を損なう可能性がある。場合によっては、特許保有会社または他の不利な特許所有者は、関連する製品収入がなく、会社の特許が彼らに対してほとんどまたは全く抑止力がない可能性があると脅したり、訴訟を起こしたりする可能性がある。もし会社がいかなる特許を侵害していることが発見された場合、会社は侵害が発見された場合の故意の3倍の損害賠償金を含む巨額の損害賠償金の支払いを要求される可能性がある。♪the the the
48
会社はまた、裁判所の命令を含めて、権利侵害製品の開発、製造、または商業化を強制的に停止される可能性がある。同社はまた、特許使用料の支払いを要求される可能性があり、ライセンスを取得しない限り、または侵害を回避するためにその製品を再設計することができない限り、その製品の販売を阻止される可能性がある。その会社はライセンスを取得できない可能性があり、合理的な条項でその製品を販売できるようにしたり、ライセンスを取得できない可能性がある。企業が必要なライセンスを取得できなかった場合、またはその技術または製品を任意の必要な変更を行うことができない場合、会社はその1つまたは複数の製品を商業化することができないか、または市場から製品をリコールしなければならない可能性があり、いずれの場合も、その業務、経営業績、および財務状態に重大な悪影響を及ぼすであろう。
競争相手が会社の任意の特許または他の知的財産権を侵害した場合、その権利を実行することは困難であり、時間がかかり、高価である可能性があり、その業務管理に対する管理層の注意をそらすことになる。どんな法執行努力でも、その会社は成功しないかもしれない。さらに、その会社はその知的財産権に対する訴訟、強制執行、または弁護の十分な資源を持っていないかもしれない。
特許庁の訴訟手続中または法廷で疑問視された場合、会社の1つまたは複数の製品に関連する発行された特許は、無効または強制執行できないと認定される可能性がある。
競争相手は会社の特許、商標、または他の知的財産権を侵害する可能性がある。その知的財産権の侵害または不正使用行為に対抗するために、当社は、その知的財産権を強制的に執行するために、第三者に対して法的訴訟を提起することを要求される可能性がある。会社が第三者にクレームを出し、その製品のうちの1つをカバーする特許の強制執行を要求する場合、被告は会社の特許権を無効および/または強制執行できない(これは米国の一般的な慣行である)ことを反訴することができる。
有効性に疑問を提起する理由は、例えば、新規性の欠如、明らかな書面記述の欠如、または実施できないことを含む、特許性に関する1つまたは複数の法定要件を満たしていないと言われている可能性がある。さらに、場合によっては、特許有効性挑戦は、非法定明顕二重特許に基づいている可能性があり、成功すれば、明顕型二重特許に対する権利請求の無効が発見される可能性があり、または明顕二重特許の裁決を排除するための終了免責声明が提出された場合、米国特許商標局によって付与された特許期限調整を含む特許期間の損失をもたらす可能性がある。主張を実行できない理由は,特許起訴に関連する者が起訴中に米国特許商標局に関連情報を故意に隠蔽したり,誤った陳述をしたりした疑惑に基づく可能性がある.
いかなる特許侵害訴訟においても,裁判所は会社の特許の全部または一部を無効または強制的に執行できないと判断する可能性がある。もう1つのリスクは、これらの特許の有効性が支持されても、裁判所がその特許の権利要件を狭く解釈するか、またはその会社の特許請求が論争された発明を含まないことを理由に、その会社が他方が論争された発明を使用することを阻止する権利がないと判断することである。会社の特許に関連する訴訟または訴訟における不利な結果は、他の当事者および他の競争相手に対してその特許を主張する会社の能力を制限する可能性があり、これは、第三者を類似製品の販売から除外する能力を制限または排除する可能性がある。これらの事件はいずれも、会社の業務、経営結果、財務状況に悪影響と実質的な影響を及ぼす可能性がある。
会社が侵害行為を認定しても,裁判所はさらなる侵害活動を禁止する禁止令を発表せず,金銭損害賠償金のみを判決することができ,十分な救済措置ではない可能性がある。また、知的財産権訴訟は大量の開示を必要とするため、会社のいくつかの機密情報は訴訟中に開示によって漏洩される可能性がある。
さらに、第三者は、特定の国の特許庁(米国特許商標局および欧州特許庁を含む)の行政訴訟手続を介して、発行された特許の有効性に疑問を提起することができる。
当社はその特許訴訟は誠実信用の義務に従って行われていると考えているにもかかわらず,特許訴訟期間中に無効かつ強制執行不可能な法的主張を行った結果は予測できない。有効性の問題については、例えば、会社は無効な以前の技術がないと判断することはできないが、それと特許審査員は起訴中にこれを知らない。被告が無効および/または実行不可能な法的主張に勝利した場合、会社は、その1つまたは複数の製品の一部または全部の特許保護を失うであろう。この特許保護の喪失は
49
その業務、経営結果、財務状況。また、知的財産権訴訟は不利な宣伝を招き、会社の名声を損なう可能性がある。
他の当事者たちはその会社の特定の外国特許出願に疑問を提起するかもしれない。そのような当事者のいずれかがその外国特許出願に反対することに成功した場合、会社は特定の司法管轄区域でこれらの特許出願によって提供される保護を得ることができず、他の管轄区の類似特許および関連特許について追加の訴訟に直面する可能性がある。1つの管轄区域で特許保護を失うことは、他の司法管轄区において同一の技術の特許保護を維持する会社の能力に影響を与える可能性がある。
さらに、会社の特許の所有権や発明権に関する紛争が発生する可能性がある。同社はすでに従業員、コンサルタント、協力者と知的財産権譲渡協定を締結しており、独自の特許やアプリケーションを持っていると信じているが、依存する譲渡や他の所有権協定は挑戦される可能性がある。裁判所または行政機関が、その会社がその特定の特許または特許出願を有していない、またはその特定の特許の発明が正しくないと認定した場合、その会社の特許に対する所有権は無効である可能性があり、その技術を開発および商業化する能力は実質的に損なわれる可能性がある。
会社がその商業秘密の機密性を保護できなければ、その技術の価値は不利かつ実質的な影響を受ける可能性があり、その業務は損害を受ける可能性がある。
同社はまた、その技術開発および商業化に参加するすべての従業員、コンサルタント、コンサルタント、契約製造業者、臨床研究者、および他の第三者と秘密保護および秘密保護協定を締結し、その知的財産権および他のノウハウを保護し、いくつかの技術は特許によって保護されていない可能性がある。しかしながら、許可されていない使用または開示または他の合意違反の場合、これらのプロトコルは、強制的に実行できない可能性があり、または会社の商業秘密または他の固有の情報に意味のある保護を提供できない可能性がある。例えば、商業秘密と機密技術は秘密にすることが難しいかもしれない。当社は合理的な措置を講じて商業秘密を保護しているにもかかわらず、それと秘密協定に署名したどちらもその合意に違反し、当社の機密情報を漏洩する可能性がある。
強制執行側が商業秘密を不正に開示したり流用したりする主張は困難であり、高価で時間がかかり、結果は予測できない。したがって,会社は不正開示を行った人に対して任意の法的行動をとる可能性があるにもかかわらず,会社はこのような違反について十分な救済措置を得ることができないかもしれない。また、米国以外の裁判所は米国よりも商業秘密を保護したくないことがある。
会社の任意の商業秘密が競合他社によって合法的に取得または独立して開発された場合、会社は、そのような技術または情報を伝達する第三者または第三者がその技術または情報を使用して会社と競合することを阻止する権利がないであろう。その任意の商業秘密が競争相手に開示される場合、または競争相手によって独立して開発された場合、その業務、経営結果、および財務状況。
会社が現在および将来の技術や製品に関する研究·開発に協力している人は、会社が入手する権利のあるデータやその他の情報を発表する権利がある可能性がある。また,会社は個人や実体を招いてその業務に関する研究を行うことがある.これらの個人またはエンティティが、その研究中に生成されたデータおよび他の情報を公開または他の方法で開示する能力は、いくつかの契約によって制限される。しかし、このような契約条項は会社の機密情報を保護するのに十分ではないか、または十分ではないかもしれない。会社が特許公開前に特許保護を出願していない場合、または会社がそのノウハウおよび他の機密情報を他の方法で秘密にすることができない場合、その特許保護またはその商業秘密情報を保護する能力が脅かされる可能性がある。
50
新技術は、同社の競争相手がより良い製品を開発することを招く可能性があり、それがどのような特許保護を持っている可能性があるかにかかわらず、その製品に対する需要を減少させるだろう。
会社技術に類似した技術研究が急速に行われており,会社や研究機関が会社製品に類似した製品の開発に積極的に参加している。これらの新技術は、会社の技術と比較して開発に成功すれば、顕著な性能や価格優位性を提供する可能性がある。競合他社が新技術に基づく新製品を開発した場合、会社の既存特許又はその保留及び提案された特許出願は、有意義な保護を提供できない可能性がある。
米国政府は連邦政府の資金を用いて開発した会社の発明に対して何らかの権利を行使することができるかもしれない。
米国連邦政府は“特許·商標法改正法”(改正された“ベハ·ドール法案”)に基づき、その財政援助の下で発生した発明に対して何らかの権利を保持している。同社のいくつかの独自特許および特許出願、およびミシガン大学と共同で所有および独占許可されている特許および出願は、米国国立衛生研究院、米国国防総省および/または米国陸軍医学研究および物資司令部の連邦資金を利用して開発されている。したがって、“ベハ·ドール法案”によると、米国政府はSeaStar MedicalをカバーするSCD技術の特許と応用に何らかの権利を有しており、特に本年度報告のタイトルはビジネス--知的財産権特許家1-4に属する。
米国連邦政府は、米国政府によって一部援助された任意の特許権、およびこれらの特許権によって開発された任意の製品または技術に対して、いわゆる“進行権”を含む一定の権利を有する。米国政府の援助の下で新技術を開発する場合、米国政府は、米国政府がこの発明を非商業目的に使用することを許可する非独占的許可を含む、生成された任意の特許のいくつかの権利を得ることができる。これらの権利は、米国政府が第三者に会社の機密情報を開示し、SCD候補製品に関連するいくつかの特許を含む第三者が会社によって許可された特許を使用または使用することを可能にする権利を行使することができる。米国政府が政府援助の技術の実用化を実現できなかったため、健康や安全需要を緩和し、連邦法規の要求を満たしたり、米国工業を優先したりするために行動する必要があると考えている場合、米国政府はそのデモ権利を行使することができる。さらに、そのような発明に対する会社の権利は、そのような発明を含む製品を米国で製造するいくつかの要件によって制約される可能性がある。さらに、会社が政府に発明を開示することができなかった場合、または所定の期間内に特許出願を提出できなかった場合、米国政府は、政府が援助した発明の所有権を得る権利がある可能性がある。
米国政府がこのような進行権を行使する場合、同社はその候補製品を効果的にまたは利益的に開発したり、商業化することができず、さらには実現できない可能性があり、企業の業務、運営結果、財務状況を損なう可能性がある。さらに、会社が所有または許可している任意の知的財産権が、ベハ·ドール法案に従って米国政府または第三者によって取得可能な任意の権利または救済措置によって制約されている場合、これは、会社の知的財産権価値を損なう可能性があり、その業務に悪影響を及ぼす可能性がある。
同社は学術機関と協力し、その研究や開発を加速することもある。同社は連邦資金が共同混合される可能性のあるリスクのあるプロジェクトに学術パートナーを参加させることを回避しようとしているが、ベハ·ドール法案によれば、いかなる共同開発の知的財産権も政府の権利の影響を受けないことは確保できない。会社が将来、その業務に重要かもしれない技術を共同所有している場合、その技術が“ベハ·ドール法案”によって拘束された連邦資金によって全部または部分的に開発されている場合、その技術をカバーする特許を強制的に実行または他の方法で利用する能力は、悪影響および実質的な影響を受ける可能性がある。
米国や他の管轄区特許法の変化は,特許の全体的な価値を低下させ,会社がその製品を保護する能力を損なう可能性がある。
他の医療機器会社と同様に,同社の成功は知的財産権,特に特許に大きく依存している。医療機器業界で特許を獲得し、実施することは技術的な複雑性と法律上の複雑性にも関連するため、コストが高く、時間がかかり、内在的な不確定性を持っている。特許改革
51
2011年9月に法律となった“ライシー·スミス米国発明法”や“ライシー·スミス法案”に署名することを含む米国や他の国の立法は、これらの不確実性やコストを増加させる可能性がある。“ライシー·スミス法案”は米国特許法を多くの重大な改正を行った。これらの条項は、特許出願起訴方法に影響を与える条項を含み、既存技術を再定義し、競争相手により効果的かつ費用対効果的な方法を提供して、例えば、特許付与後および米国特許商標局での当事者間審査手続きを行うことによって、特許の有効性に挑戦する。また、2013年3月から、“ライシー·スミス法案”は、米国の特許制度を“最初の出願”の制度に転換した。Leahy-Smith法案およびその実施は、その発明が特許保護を得ることを難しくし、会社の特許出願をめぐる起訴および発行された特許を実行または保護する不確実性およびコストを増加させる可能性があり、これらのすべては、その業務、運営結果、および財務状態を損なう可能性がある。
米国最高裁判所はいくつかの特許事件に対して裁決を下しており,利用可能な特許保護範囲を縮小するか,場合によっては特許所有者の権利を弱めるかである.また,米国や他国の特許法をより多く改正することを提案しており,採択されれば,会社がそのノウハウを実行する能力に影響を与える可能性がある。国会、米国裁判所、米国特許商標局、および他の国の関連立法機関の将来の行動によれば、特許を管理する法律および法規は変化する可能性があり、それによって、会社が新しい特許を獲得したり、その既存および将来の特許を実行する能力を弱める可能性がある。
知的財産権は会社の競争優位が直面しているすべての潜在的な脅威を解決できるとは限らない。
会社の知的財産権の将来提供の保護程度は不確定であり、知的財産権には限界があるため、その業務を十分に保護できない、あるいは競争優位を維持できない可能性がある。以下の例は例示的である
52
会社の特許保護の獲得·維持は、政府特許機関が適用した様々なプログラム、書類提出、費用支払い、および他の要件を遵守することに依存し、これらの要件に適合しない場合、会社の特許保護は減少またはキャンセルされる可能性がある。
発行された特許の定期維持費は、特許有効期間内にいくつかの段階で米国特許商標局および外国特許代理機関に不足している。米国特許商標局および各種外国政府特許機関はまた、特許出願中にいくつかのプログラム、文書、費用支払い、およびその他の同様の規定を遵守することを要求している。多くの場合、適用された規則に従って滞納金を支払うことによって、または他の方法でミスを是正することができるが、場合によっては、規定を遵守しないことは、特許または特許出願の放棄または失効を招き、関連法ドメインの特許権の一部または全部の喪失をもたらす可能性がある。特許または特許出願の放棄または失効をもたらす可能性のある不正事件には、規定された期限内に公式行動に応答できなかったこと、費用が支払われていなかったこと、および適切に合法化され、正式な文書が提出されなかったことが含まれるが、これらに限定されない。会社またはそのライセンス者が会社製品の特許および特許出願を維持できなかった場合、その競争地位は悪影響を受けるであろう。
ある特許権については、会社は限られた地理的保護しか得られない可能性があり、これは、これらの管轄区域における知的財産権の価値を低下させ、世界的にその知的財産権を実行することを阻止する可能性がある。
世界各国で候補製品特許を申請、起訴、保護する費用は目を引くほど高いだろう。したがって,当社はまだ特許保護を受ける可能性のあるすべての国や地域の管轄区で特許保護を出願していない可能性もある.さらに、特許が付与される前に国および地域の特許出願を放棄することを決定することができ、または特定の司法管轄区で特許が付与された維持費を支払わないことを決定することができる。最後に、各国·地域特許庁の付与手続は独立した手続であり、特定の法域の出願が関連特許庁によって拒絶され、他の出願が承認された場合を招く可能性がある。同様に一般的な場合は、国によって同じ候補製品または技術の特許保護範囲が異なる可能性があることである。
競争相手は会社の技術を使って会社が特許保護を受けていない司法管轄区で自分の製品を開発し、さらに会社に特許保護を持っているが特許執行力はアメリカの地域に比べて侵害製品を輸出することができる。これらの製品はまた、会社が発行または許可された特許または会社の特許または他の知的財産権を有していない場合があり、これらの製品が会社と競合する司法管轄区域内で会社の製品との競争を効果的にまたは阻止するのに不十分である可能性がある。
また、一部の国では米国や欧州の法律と同程度の知的財産権保護を担うことができない。ある外国司法管轄区では、多くの会社が知的財産権の保護と保護に重大な問題に直面している。いくつかの国の法制度は特許と他の知的財産権の強制執行を支持しない。これは、同社がこれらの国でその特許を侵害したり、他の知的財産権を流用したりする行為を阻止することを困難にする可能性がある。例えば、多くの外国国には強制許可法があり、これらの法律によると、特許権者は第三者に許可を付与しなければならない。これらの国では,特許権者の救済措置は限られている可能性があり,このような特許の価値を大幅に低下させる可能性がある。会社またはその任意の許可者が、その業務に関連する任意の特許について第三者に許可を付与することを余儀なくされた場合、その競争的地位が損なわれる可能性があり、その業務、運営結果、および財務状況が悪影響を受ける可能性がある。そのため、会社は米国やヨーロッパ以外のある国/地域で第三者がその発明を実施することを阻止できないかもしれない。競争相手は会社の技術を使って会社が特許保護を受けていない司法管轄区で自分の製品を開発することができる。また、彼らは他の侵害製品を当社に輸出することができます
53
企業がこれらの管轄区域で権利侵害活動を阻止するためにその特許を実行する能力が不足している場合、特許保護がある。
外国司法管区において会社特許権の訴訟を強制的に執行することは、成功するか否かにかかわらず、巨額のコストを招き、その努力及び資源をその業務の他の面から移転させることが可能である。また、会社はその製品の主要市場で知的財産権を保護しようとしているが、その製品を販売したいすべての管轄区域で同様の努力を開始または維持することができない可能性がある。したがって、このような国でその知的財産権を保護するための会社の努力は十分ではないかもしれない。
上場企業に関するリスク
同社は米国上場企業として運営した長期的な経験がなく、サバンズ·オクスリ法案の遵守を含め、上場企業に必要なガバナンス、コンプライアンス、リスク管理、制御インフラや文化を十分に実施できない可能性がある。
同社は米国上場企業としての運営経験を蓄積しており、その中で、同社の幹部は米国上場企業の管理における経験が限られており、法律、規則、法規を遵守する能力が不確定となっている。会社が米国上場企業に適用されるすべての法律、規則、法規を遵守できなかったことは、会社とその管理層を規制審査や制裁を受ける可能性があり、会社の名声や株価を損なう可能性がある。
事業合併が2022年10月に完了するまで、当社はこれまで、サバンズ-オキシリー法案を含む米国上場企業に適用される開示制御や手続き、財務報告の内部統制の確立と維持を要求されていなかった。会社は上場企業に必要な管理、コンプライアンス、リスク管理と制御枠組みと文化を制定し、実施しているにもかかわらず、会社はアメリカ証券取引委員会および/またはその投資家が期待する必要な基準を達成できない可能性がある。会社はまた、プロセスや制御の面でミス、ミス、ミスに遭遇し、上場企業が望む必要な基準を達成できない可能性がある。
米国の公共報告会社として、同社は大量の法律、会計、保険、コンプライアンス、その他の費用を発生させた。当社では、発生する可能性のある追加コスト金額またはそのようなコストの時間を予測または推定することはできません。報告、財務報告の内部統制および会社管理義務を遵守するには、これらの新しい規制要件が満たされることを確実にするために、その管理層メンバーおよびその財務および会計担当者が時間と資源を他の職責から移転する必要がある可能性がある。
必要な管理と制御枠組みを十分に実施できなければ、会社はより大きなリスクに直面し、上場企業に関する規則や要求を守ることができない可能性がある。このような失敗は、投資家の自信を失い、会社の名声を損なう可能性があり、会社証券の市場価格の下落を招く可能性がある。これらの法規の要求を遵守する上で、会社がコンプライアンス評価や任意の必要な救済措置をタイムリーに達成できない可能性があるため、他の挑戦が生じる可能性がある。さらに、規制の変化または増加の複雑さ、会社の経営環境、または他の理由により、現在または将来の制御は不十分であると考えられる可能性がある。
ガバナンスや内部統制政策が不足しているため、エラーや詐欺による誤った陳述や漏れが発生する可能性があり、発見されない可能性があり、必要な文書をタイムリーに提出できず、文書に不正確または誤った情報を含ませる可能性がある。これらの結果のいずれも、米国証券取引委員会の法執行行動、罰金または他の処罰、および会社の名声、業務、財務状況、経営業績、および株価への損害をもたらす可能性がある。
会社はナスダックのすべての上場規則を一貫して守ることができないかもしれない。
上場企業として、当社はナスダック上場規則に制約されています。上場規則の適用要件を満たしていない場合には、その会社がナスダックに上場されず、その株式が停止されたり、後日取られたりする可能性がある。これはさらに、法律または規制手続き、罰金およびその他の処罰、会社の法的責任、会社の株主が株を取引できない可能性があります
54
また、会社の株価、名声、運営と財務状況及び将来の資金調達活動を展開する能力にマイナス影響を与える。
Seastar Medicalはその財務報告の内部統制に重大な欠陥があることを発見した。会社が有効な財務報告内部統制制度を構築·維持できなければ、会社は財務業績を正確かつ適時に報告できない可能性があり、これは会社の業務、経営業績、財務状況に重大な悪影響を及ぼす可能性がある。
会社管理層は財務報告に対する十分な内部統制の確立と維持を担当し、アメリカ公認会計原則に基づいて財務報告の信頼性と外部目的の総合財務諸表の作成に合理的な保証を提供する。当社の経営陣はまた、その内部統制の有効性を評価し、その内部統制を評価することによって発見された任意の変化や重大な弱点を開示しています。重大な欠陥は財務報告内部制御の欠陥或いは欠陥の組み合わせであり、当社の年度或いは中期総合財務諸表の重大な誤報が合理的な可能性があり、適時に防止或いは発見できない。
本年度報告に含まれる連結財務諸表を作成する過程で,SeaStar Medicalは2022年12月31日までの財務報告内部統制に重大な欠陥があることを発見し,その財務会計と報告制御の設計と操作上の欠陥に関連している。具体的には、この重大な欠陥の原因は、財務会計および報告手続きの内部の役割分担の不足であり、取引を連結財務諸表、支払い、および給与システムに記録する上で独立した審査および承認手続きが不足していることである。会社は必要な経験や技能を持つ会計員をより多く雇用することを含む重大な弱点を救済しようとしているが、速やかに救済できるか、あるいは根本的に救済できない保証はない。会社がこの重大な欠陥を是正できなかった場合、連結財務諸表が不正確である可能性があり、適用される財務報告要求を適時に遵守する能力を弱める可能性がある。これらのコンプライアンス問題は、投資家が会社報告の財務情報に自信を失い、会社証券の市場価格変動と下落を招く可能性がある。
以下の9 A項で述べたように、当社は、不合理な努力や費用が発生することなく、2022年12月31日までの財務報告内部統制を評価することができない。したがって、当社には、財務報告の内部統制に関する経営陣の財務規制S-Kコンプライアンス及び開示解釈215.02節に基づく報告は含まれていない。当社は現在、内部制御プログラムを発展·強化する措置を講じていますが、当社の経営陣は、財務報告の内部統制が無効であることや、当社のコントロールが記録、設計、審査のレベルが不十分であること、当社の独立公認会計士事務所が意見を保留していることを報告する可能性があると結論する可能性があります。また,予見可能な将来,報告義務は会社の管理,運営,財務資源,システムに大きな圧力を与える可能性がある。会社はその評価テストと必要な救済をタイムリーに終わらせることができないかもしれない。
社内制御プログラムを記録してテストする過程で、404節の要求を満たすために、会社はその後、その財務報告内部統制上の欠陥を発見する可能性がある。また、企業がその財務報告の内部統制の十分性を維持できなかった場合、これらの基準が時々修正、補充または修正されるため、会社は、財務報告に対して有効な内部統制があると結論を得ることができない可能性がある。当社が有効な内部統制環境を実現し維持できなかった場合、その総合財務諸表に重大な誤報が発生し、その報告義務を履行できなくなり、投資家がその報告した財務情報に自信を失う可能性がある。これは逆に同社が資本市場に参入する機会を制限し、その経営業績を損なう可能性がある。これらの不足点が発見されれば、同社はその前の時期の連結財務諸表の再申告を要求される可能性もある。また、財務報告を無効にする内部統制は、アリババの詐欺リスクや企業資産の乱用リスクを増加させ、ナスダック退市、規制調査、民事や刑事制裁に直面させる可能性がある。これらすべての結果は、会社の名声、業務、経営結果、財務状況、株価に悪影響を及ぼす可能性がある。
55
会社はあなたに不利な時間に未満期株式証明書を償還して、あなたの引受権証を一文の価値もないようにするかもしれません。
当社は、発行された引受証を行使及び満期前の任意の時間に償還する権利があり、株式承認証1部当たりの価格は0.01ドルであり、償還通知が発行される日前の第3の取引日が終了した30取引日以内に、私たちの普通株式の最終報告販売価格は1株当たり18.00ドル(株式分割、株式配当、再編、資本再編などの調整後)を超え、いくつかの他の条件を満たすことを前提としている。株式証明書が私たちが償還できる場合、私たちはすべての適用された州証券法に基づいて対象証券を登録したり、売却資格に適合させることができなくても、償還権を行使することができます。償還されていない引受権証は、閣下に不利になる可能性がある場合には閣下の引受権証を行使し、そのために行使価格を支払うことができます。(Ii)閣下が株式証明書を持ちたい場合には、当時の市価で閣下の引受権証を売却したり、(Iii)名義償還価格を受けて、そのような未償還の株式証明書の償還を要求した場合、名義償還価格はあなたの株式証明書の時価を大きく下回る可能性があります。いかなる個人配給承認株権証も、保証人又はその譲受人が保有することが許可されている限り、当社は償還しません。
私たちは追加資金の不足で損失を受けるかもしれない。
運営に資金を提供し、運営を拡大し、経験者を募集するための運営資金の持続的な需要が予想される。これのために、私たちは株式や債務融資を通じてより多くの資金を調達することを要求されるだろう。しかし、私たちはもしあれば、私たちが優遇された条件で追加的な資本を得ることに成功するという保証はない。もし私たちが成功すれば、条項が有利であっても不利であっても、私たちはこのような融資の条項を遵守できない可能性があり、これは私たちに深刻な責任を負わせるかもしれない。もし私たちが成功しなければ、私たちは(A)コスト削減を開始すること、(B)商業発展機会を放棄すること、(C)債務に資金を提供する時間の延長を求めること、または(D)債権者の保護を求めることが必要になるかもしれない。また、将来的に私たちの株式を売却することは、あなたの株式の所有権と支配権を希釈し、価格は私たちの株式の現在の取引価格を大幅に下回る可能性があります。私たちは資金を集めることができず、私たちが私たちの業務を大幅に削減または完全に終わらせることを要求するかもしれない。私たちは追加的な株式や債務証券を売ることで私たちの現金備蓄を増加させることを求めるかもしれない。転換可能な債務証券または追加の持分証券の販売は、私たちの株主への追加的かつ潜在的な重大な希釈をもたらす可能性がある。債務の発生は債務超過義務の増加を招き、運営や融資契約を招き、私たちの運営や流動性を制限する可能性がある。また、私たちが受け入れ可能な条件で追加資本を得る能力は様々な不確定要素の影響を受ける。
また、運営から十分な現金が発生できなければ、資金源が見つからなければ、資産の全部または一部を売却し、業務統合を行ったり、業務を減らしたり、キャンセルしたりする必要があるかもしれない。利用可能な範囲内で、これらの可能性のある条項は、私たちの株主が深刻に希釈されたり、私たちの株主がわが社でのすべての投資を失ったりする可能性があります。
私たちの管理チームが上場会社を運営する経験は限られています。
わが管理チームの多くのメンバーは、上場会社の運営、上場会社の投資家との相互作用、上場会社に関連する複雑化する法律を遵守する上での経験が限られている。私たちの管理チームは私たちの上場企業への移行を成功的あるいは効果的に管理できないかもしれません。連邦証券法によると、私たちは重大な監督と報告義務、証券アナリストと投資家の持続的な審査を受けています。これらの新しい義務と構成は、私たちの上級管理職に大きな関心を与える必要があり、私たちの業務の日常管理に対する彼らの注意をそらす可能性があり、これは私たちの業務、運営結果、キャッシュフロー、財務状況に悪影響を及ぼす可能性がある。
56
項目1 B。未解決の従業員のコメント。
ない。
項目2.財産
会社の本社はコロラド州デンバー市80216号、ブライトン通り3513号、郵便番号:410です。月別賃貸契約により、本社をレンタルします。私たちはこの不動産が私たちの業務を運営するのに十分だと信じている。
項目3.法的訴訟
時々、私たちは様々なクレームと法的手続きに巻き込まれるかもしれない。私たちは現在、私たちの経営陣が私たちの業務、財務状況、または経営結果に重大な悪影響を及ぼす可能性があると思う法的手続きに参加していません。結果にかかわらず,弁護や和解コスト,管理資源分流などにより,訴訟は我々に悪影響を与える可能性がある。
第4項鉱山安全情報開示
適用されません。
57
第II部
第五項登録者普通株式市場、関連株主事項及び発行者が株式証券を購入する。
市場情報
我々の普通株はナスダック資本市場で取引され、コードはICU(前身はLMAO)である。
所持者
2023年3月25日現在、私たちの普通株の登録株主は13,296,516人です。
記録保持者の数は、その日に我々の帳簿に登録されている実際の所有者の数に基づいて計算され、街の名義で株式を保有する保有者や預託信託会社によって維持されている証券頭証リストで決定された個人、組合、協会、会社または他の実体は含まれていない。
配当政策
今まで、私たちは普通株について何の現金配当金も支払わなかった。私たちの取締役会は時々配当政策を制定するかどうかを考慮するかもしれない。私たちの現在の意図は、私たちの業務運営のために任意の収益を維持することであり、したがって、取締役会は予見可能な未来に配当金を発表しないと予想しています。将来の現金配当金の支払いは私たちの収入と収益(もしあれば)、資本要求、そして全体的な財務状況に依存するだろう。任意の現金配当金の支払いは当社の取締役会が適宜決定します。
最近の未登録証券の売却と収益の使用
パイプ融資
2022年8月23日、合併協定が調印された後、LMAOは3社の機関投資家(“PIPE投資家”)と引受協定を締結し、PIPE投資家は1株10.00ドルで合計700,000株の普通株を引受し、700,000件の引受権証を締結し、総収益は700万ドル(“PIPE融資”)であった。PIPE融資は業務合併が終了しながら完了した。
“証券法”公布の第4(A)(2)条に基づいて、PIPE投資家に発行される普通株は、証券法の規定による免除登録により発行される。
証券法第3(A)(9)条に規定する免除登録によると、B類普通株の自動転換時にA類普通株を発行する場合と、成約時にA類普通株を自動転換する際にA類普通株を発行する場合は、証券法に基づいて登録されていない。
転換可能手形融資
2023年3月15日、当社は1人の機関投資家(“買い手”)と証券購入協定(“証券購入協定”)を締結し、これにより、当社は買い手に高級無担保転換手形(“手形”)を売却および発行することに同意し、4回に分けて完了し、当社の普通株株式に変換することができ、1株当たり0.0001ドル、元金金額は最高約9,800,000ドルおよび自社普通株株式を購入する承認権証(“株式証”)である。2023年3月15日(“予備成約日”)、同社は1,207,729株の普通株に変換できる手形を発行し、初期転換価格は2.70ドル、元金は3,260,869.57ドルであり、株式承認証を発行し、328,352株の普通株を最大購入した。
58
2回目の取引が終了すると、会社は、最大218,901株の普通株式を購入するために、(I)元本金額が2,173,913.04ドルの追加手形および(Ii)追加株式証明書を買い手に発行して販売する。3回目および4回目の取引完了時に、当社はその選択に基づいて、(I)追加手形を買い手に発行および販売することができ、1部当たり元金は2,173,913.04ドルであり、および(Ii)追加株式証明書は、買い手が適用締め切り転換後に発行可能な普通株式株式の25%に相当する普通株式を購入することができる。証券購入契約によると、同社は必ずいくつかの追加条件を満たさなければ、第2、第3及び第4回成約時に追加手形及び追加株式証明書を販売及び発行することができる。これらの付加条件には,会社が証券取引委員会に提出した登録声明の効力,手形の変換および引受証の行使時に発行可能な普通株式の登録,および第3および第4回終値について,会社株主は適用されるナスダック規則に従って19.99%を超える発行および発行済み株式の発行を許可することが含まれるが,これらに限定されない。3回目および4回目の閉鎖が初期閉鎖日から1年以内に発生しない場合、会社が3回目および4回目の閉鎖に影響を与える権利は自動的に終了する。
このロットの債券は元の発行価格で8%割引して発行され、利息率は7%となる。債券は発行後15(15)ヶ月で満期、すなわち2024年6月15日であり、違約事件により満期が加速しない限り有効である。債券は当社が任意の時間に全部または部分的に償還することを適宜決定することができる。最初の成約日に、元の発行割引と買い手弁護士費を差し引いた後、会社は純収益240万ドルを獲得した。
付記には基準と習慣協約と違約事件が記載されている。このような違約事件には、満期不払い、不遵守または履行手形に含まれる契約または合意、違反手形に含まれる任意の重大な陳述または保証、会社の破産または債務返済不能、普通株取引の一時停止、および会社が証券取引委員会に必要な報告を提出できなかったことが含まれるが、これらに限定されない。もしこのような違約事件が発生した場合、任意の治療期間の制約の下で、買い手は償還価格でチケットの任意の部分を償還する権利があり、買い手の選択に応じて一定の金額を普通株式に変換する権利がある。
これらの株式承認証の初期行使価格は1株当たり2.97ドルであり、発行後5(5)年の取引終了前のいつでも行使でき、キャッシュレス行使条項を含む。
手形の転換及びこの等株式証明書の行使時に発行可能な手形、株式証明書及び普通株式株式は、改正された1933年の証券法(“証券法”)に基づいて登録されておらず、証券法により公布された規則例Dに記載されている免除登録に基づいて認可投資家に発行及び売却されている。
発行者による株式証券の購入と関連購入
ない。
第六項です[保留されている]
59
第7項:経営陣の財務状況と経営成果の検討と分析。
以下の議論と分析は、私たちの業務、財務状況、運営結果、流動性、資本源を理解することを目的としています。本年度報告書の他の部分に含まれる会社合併財務諸表と関連説明を組み合わせて本議論を読まなければなりません。業務合併では、SeaStar医療会社が会計買収側に決定した。
歴史的財務分析に加えて、本議論および分析は、“前向きな陳述に関する警告説明”というタイトルで説明されたように、現在の予想に基づく前向きな陳述を含む。本年度報告の他の部分(または参照によって組み込まれる)の“リスク要因”に記載されている要因、リスクおよび不確定要因を含む様々な要因、リスクおよび不確定要因のため、選択されたイベントの実際の結果および時間は、これらの前向き陳述において予想されるものと大きく異なる可能性がある。文意が別に指摘されている以外に、本“経営陣の財務状況と経営結果の討論と分析”で言及されている“SeaStar Medical”、“We”、“Our”と“Company”はSeaStar Medical Holding Corporation及びその合併子会社の業務合併後の業務と運営を意味する。
概要
2022年10月28日、LMAOは一連の取引を完了し、LMF合併子会社とSeaStar Medical,Inc.は合併協定と計画に従って合併を招いた。
同社は医療技術会社であり、重要な器官への過度な炎症の結果を減らすためのプラットフォーム療法を開発した。正常な炎症反応の中で、好中球は最初に現場に到着した免疫細胞であり、全免疫反応のキーポイントであり、全免疫反応は病原体を殺し、組織修復を促進する。炎症反応が過度と失調になると、正常な好中球は死亡を遅延させ、免疫系を調節するフィードバック機序を変化させる可能性がある。これは破壊的な過剰炎症を暴走させて身体の他の部位に拡散させ,通常心臓,肺,腎臓,肝臓疾患を含む急性慢性固形臓器機能障害や不全を引き起こす。この高炎症反応はサイトカイン嵐とも呼ばれ,高炎症細胞から放出される小分泌蛋白に対する身体の反応であり,これらの蛋白は細胞間のコミュニケーションに影響する。制御しなければ、サイトカイン嵐は器官損傷、甚だしきに至っては死亡を招く可能性がある。
著者らは最初に著者らの独自のSCD技術プラットフォームを用いて、腎臓と肺を含むいくつかの急性器官損傷の適応を臨床で検証した。我々の研究SCDは,一般に全米のICUを含む病院に設置されている既存のCRRTシステムに容易に統合することを目的とした体外合成膜装置である。承認され商業化されると、SCDは最初に児童CRRT群およびCRRTを受けた成人の急性腎臓損傷を対象とする。また,慢性透析や慢性心不全に関連する炎症に対応するためにSCDを開発している。
2007年に設立されて以来、私たちは毎年純損失を出している。2022年12月31日と2021年12月31日までの累計赤字はそれぞれ9930万ドルと7630万ドルだった。2022年12月31日と2021年12月31日までの年度の純損失はそれぞれ2300万ドルと460万ドルだった。我々のほとんどの純損失は,我々の研究開発計画に関するコストと我々の運営に関する一般的かつ行政コストによるものである。2022年12月31日まで、追加損失は業務合併と関係があり、長期契約を取得するコスト及び長期オプション派生ツールの公正価値変動を含む。
2022年12月31日と2021年12月31日まで、それぞれ1000万ドルと50万ドルの現金を持っています。
私たちが添付している総合財務諸表は持続経営に基づいて作成されており、正常な業務過程で資産と負債を現金化することを考えています。我々の総合財務諸表には、資産金額の回収可能性や分類や負債分類に関するいかなる調整も含まれておらず、会社が経営を継続できなければ、これらの調整が必要かもしれない。
60
経常赤字,運営資金不足,我々の業務に資金を提供する必要(臨床試験や規制承認費用を含む),および現金備蓄の額は,総合財務諸表が利用可能な日から12カ月間経営を継続する能力があるかどうかに大きな疑いを抱かせる。我々が評価したより多くの情報については、本年度報告書の他の部分に含まれる2022年12月31日現在の監査済み総合財務諸表の付記1を参照されたい。
追加資本に対する私たちの必要性は私たちの開発活動の範囲と費用に部分的に依存するだろう。私たちは今まで商業化された製品の販売から相当な収入を得ていない。私たちが製品収入を作る能力は私たちの製品の成功的な開発と最終商業化にかかっているだろう。その前に、もしあれば、株式または債務の売却、信用手配下の借金、潜在的な協力、他の戦略取引、または政府および他の贈与によって、私たちの業務に融資する予定です。必要な時や受け入れ可能な条件で、私たちは十分な資本を得ることができないかもしれない。もし私たちが資金を調達できなければ、私たちは私たちの研究開発計画や将来の商業化努力を延期、減少、一時停止、停止させることを余儀なくされる可能性があり、これは私たちの業務、将来性、経営業績、財務状況にマイナスの影響を与えるだろう。より多くの情報については、第1部1 A項“リスク要因”を参照されたい。
運営結果の重要な構成要素は
収入.収入
今まで、私たちは商業化された製品の販売から何の収入も得ていない。収入は主に政府と他の寄付金から来ている。私たちは将来的に許可や協力協定や政府や他の贈与の支払いに基づいて収入を創出するかもしれません。私たちの製品が商業化の規制承認を得ていれば、製品販売から収入を得ることもできます。私たちは私たちが作ったどんな収入も四半期の変化によって変動すると予想している。製品の商業化の開発が間に合わなかったり、規制部門の承認を得られなかったりすれば、私たちの将来の収入創出能力や私たちの運営実績や財務状況は大きな悪影響を受けるだろう。
研究と開発費
設立以来、著者らはずっと私たちの研究と開発活動に資源を集中してきて、臨床前研究と臨床試験、及び著者らの製品の監督管理記録に関するプロセスと活動を開発することを含む。追加資金を獲得した場合、私たちは予測可能な未来に私たちの製品を開発し続け、私たちの研究と開発費用をさらに増加させる予定です。
一般と行政費用
一般及び行政支出は主に行政及び財務職務を担当する従業員の給料と関連費用を含み、その中にはこのような従業員の株式給与支出と福祉も含まれている。
その他の重大な一般的および行政的費用には、施設コスト、会計および法的サービスの専門費用、および特許の取得および維持に関連する費用が含まれる。私たちが引き続き私たちの業務を拡大し、発展させることに伴い、私たちは新しい従業員、出張、新しい企業資源計画プラットフォーム、ブランド普及に関連する追加費用を含む私たちの一般的かつ管理費用が増加することを予想します。
長期契約の初期コスト
長期契約の初期コストは主に長期購入プロトコルに関連する対価格を含む。
運営損失と営業利益率
営業損失は会社の毛利から営業費を引いて構成されています。営業利益率とは会社の運営損失がその純売上高のパーセントを占めることです。
61
その他の収入,純額
その他の収入(支出)総額は,純額には,主に我々の転換可能手形による利息に関する利息支出,コロナウイルス援助,救済および経済保障(“CARE”)法案による免除支給小切手保護計画(“PPP”)融資による収益,転換可能手形の早期清算収益,転換可能手形転換オプションに関する派生負債の公正価値変動,および前払い長期合意の長期オプションに関する派生負債の公正価値変動が含まれる。
純損失
純損失には会社の運営損失から他の費用が差し引かれています。
会社の経営業績に影響を与える要素
私たちの業績と未来の成功はいくつかの要素にかかっており、これらの要素は私たちに重大なチャンスをもたらしているが、リスクと挑戦ももたらしていると考えている。より多くの情報については、第1部1 A項“リスク要因”で議論されている要因を含む、本年度報告の他の部分で議論されている要因を参照されたい。
経営成果
2022年12月31日までの年度と2021年12月31日までの年度との比較
次の表は我々の行動成果をまとめたものである.本資料は,本年度報告の他の部分に掲載されている総合財務諸表及び関連付記とともに読まなければならない。
|
|
現在までの年度 |
|
|
|
|
|
|
|
|||||||
|
|
十二月三十一日 |
|
|
変わる |
|
||||||||||
(千ドル) |
|
2022 |
|
|
2021 |
|
|
$ |
|
|
% |
|
||||
収入.収入 |
|
$ |
— |
|
|
$ |
— |
|
|
$ |
— |
|
|
|
— |
|
運営費 |
|
|
|
|
|
|
|
|
|
|
|
|
||||
研究開発 |
|
|
2,819 |
|
|
|
2,766 |
|
|
|
53 |
|
|
|
2 |
% |
一般と行政 |
|
|
6,600 |
|
|
|
1,683 |
|
|
|
4,917 |
|
|
|
292 |
% |
長期契約の初期コスト |
|
|
2,190 |
|
|
|
— |
|
|
|
2,190 |
|
|
|
|
|
総運営費 |
|
|
11,609 |
|
|
|
4,449 |
|
|
|
7,160 |
|
|
|
161 |
% |
運営損失 |
|
|
(11,609 |
) |
|
|
(4,449 |
) |
|
|
(7,160 |
) |
|
|
161 |
% |
その他収入合計 |
|
|
(11,403 |
) |
|
|
(148 |
) |
|
|
(11,255 |
) |
|
|
7605 |
% |
所得税前損失準備 |
|
|
(23,012 |
) |
|
|
(4,597 |
) |
|
|
(18,415 |
) |
|
|
401 |
% |
所得税を支給する |
|
|
1 |
|
|
|
(1 |
) |
|
|
2 |
|
|
|
|
|
純損失 |
|
$ |
(23,013 |
) |
|
$ |
(4,596 |
) |
|
$ |
(18,417 |
) |
|
|
401 |
% |
研究と開発費
次の表は研究開発費の内訳を開示しています
|
|
現在までの年度 |
|
|
|
|
|
|
|
|||||||
|
|
十二月三十一日 |
|
|
変わる |
|
||||||||||
(千ドル) |
|
2022 |
|
|
2021 |
|
|
$ |
|
|
% |
|
||||
臨床試験 |
|
$ |
— |
|
|
$ |
989 |
|
|
$ |
(989 |
) |
|
|
(100 |
)% |
対外サービス |
|
|
1,997 |
|
|
|
1,278 |
|
|
|
719 |
|
|
|
56 |
% |
給与明細と人件費 |
|
|
658 |
|
|
|
353 |
|
|
|
305 |
|
|
|
86 |
% |
他の研究や開発費 |
|
|
164 |
|
|
|
146 |
|
|
|
18 |
|
|
|
12 |
% |
|
|
$ |
2,819 |
|
|
$ |
2,766 |
|
|
$ |
53 |
|
|
|
2 |
% |
62
一般と行政費用
2022年12月31日と2021年12月31日までの年度の一般·行政費はそれぞれ660万ドルと170万ドル。一般と行政費用が490万ドル増加し、すなわち292%増加した理由は、賃金支出が190万ドル増加し、株式信用限度額承諾料が250万ドル増加し、法律費用が20万ドル増加し、保険料が30万ドル増加したからである。
その他の収入(費用)
2022年12月31日と2021年12月31日までの年度のその他の収入(支出)はそれぞれ1140万ドルと20万ドルの支出だった。1,120万ドルの増加は主に長期オプション公正価値変動損失1,020万ドル、転換可能手形派生負債公正価値変動損失60万ドル、及び利息支出が40万ドル増加したためである。
所得税を支給する
Seastar Medicalは2022年12月31日までの年度に2000万ドルの所得税控除を記録し,2021年12月31日までの年度に2000万ドルの所得税優遇を記録した。
会計基準編纂(“ASC”)740−10~30−5によれば、既存の証拠の重みに基づいて、繰延税金資産の一部または全部が現金化できない可能性が高い(すなわち、50%を超える可能性がある)場合、所得税、繰延税金資産は、推定準備金を差し引くべきである。Seastar Medicalは繰延税金資産の潜在的な現金化を確定する時にすべての利用可能な積極と消極的な証拠を考慮し、主に最近の課税収益或いは損失歴史を含む。2022年から2021年までの間に報告された運営損失によると、同社は最近の運営歴史を克服する十分な積極的な証拠がないと結論した。したがって、私たちは、上述したより可能な閾値に基づいて、推定手当が依然として必要だと思う。2022年と2021年12月31日終了年度はそれぞれ2,380万ドルと1,820万ドルの推定手当を記録した。
純損失
海星医療の純損失は2022年12月31日までの1年間で2300万ドルであったが,2021年12月31日までの年度純損失は460万ドルであった。純損失が1,840万ドル増加したのは,主に2022年12月31日までの1年間に一般·行政費用が490万ドル増加し,研究·開発費が10万ドル増加し,長期契約の初期コストが220万ドル増加し,その他の費用が1120万ドル増加したためである。
流動性と資本資源
流動資金源
これまで、私たちは主に株式証券や転換可能な債券を売却することで私たちの業務に資金を提供し、次に政府や他の機関による贈与を行ってきました。設立以来、私たちは深刻な運営損失と負のキャッシュフローを受けた。2022年12月31日と2021年12月31日までの累計赤字はそれぞれ9930万ドルと7630万ドルだった。
2022年12月31日と2021年12月31日まで、それぞれ1000万ドルと50万ドルの現金を持っています。私たちは、私たちの既存の現金が臨床試験費用と資本支出要件を含む私たちの運営に資金を提供するために不足すると予想している。私たちが継続的に経営している企業として継続できるかどうかが疑われると思います。これを超えた運営に資金を提供するためには、追加の資本を調達する必要があり、これは保証されないだろう。これらの状況は,本年度報告書の発表日から1年以内に経営を継続する能力があるかどうかが疑われると結論した。2022年12月31日現在の監査総合財務諸表付記1を参照。
2021年4月、“思いやり法案”により設立された官民パートナーシップにより、10万ドルの融資収益を得た。私たちがローンで得た収入を条件に合った人に使えば、ローンと利息は免除できます
63
賃金、従業員福祉、賃貸料、光熱費を含む他の用途は、その賃金水準を維持する。2021年12月31日までの1年間、10万ドルの購買力平価ローンを免除した。
2021年12月31日までの年間で、主要株主の陶氏年金基金に発行された手形を含む、いくつかの手形購入協定に基づいて合計290万ドルの転換可能な手形を発行した。2022年12月31日までの年間で、陶氏年金基金への元金総額120万ドルの転換手形6枚を含む合計170万ドルの転換可能手形を発行し、未償還優先株を発行した既存所有者に合計170万ドルの転換手形を発行した。転換可能手形の満期日はそれぞれの発行日から一年から三年まで様々です。これらの手形はSeaStar Medicalの無担保債務であり,転換可能手形の借入利息は8.0%であった。取引が終了する直前に、転換手形項の下のすべての元金と課税利息を1株10.00ドルの転換価格で私たちの普通株に変換することができる。
業務統合完了後,PIPE投資の700万ドルの総収益と信託口座の1,000万ドルの収益が主に1,700万ドルの現金を受け取ったが,Maximの繰延費用,法律顧問,譲渡エージェント,コンサルタント,監査師の専門サービス料,承諾費,役員と高級職員保険,長期購入契約売手への前払い合計約1,660万ドルを含む.
業務合併については、800万株を超える株が償還され、総償還額は約9200万ドルだった。我々が受け取った業務合併に関する収益は、1.035億ドルの潜在収益総額をはるかに下回っている(償還されていないと仮定)。株式償還により取引終了時に現金が減少するため、私たちの成長計画、LMAOの業務合併に対する評価について準備した収入と純損失予測及び私たちの流動性(株式証明書所有者が株式証保有者を行使して株式証所有者と会社が株式証から現金収益を得る可能性を含む)にマイナス影響を与えた。
株式引受収益
私たちはその条項に基づいて現金と引き換えに株式承認証を行使する任意の収益を得るつもりだ。すべての現金株式承認証がすべて行使されたと仮定すると,合計約1.85億ドルの現金が得られるが,その等株式証を行使して発行可能な普通株式を売却することから何の収益も得られない.もしいずれの株式承認証が“キャッシュレスベース”で発行された場合、私たちが株式承認証を行使することから得られる現金金額は減少するだろう。将来的には,株式承認証から得られた任意のこのような収益を現金として利用し,一般会社や運営資本用途に利用することが予想され,流動性が増加する。しかし、私たちは権利証所有者が株式承認証を行使する時にのみ、このような収益を受けるだろう。株式承認証の行使、および私たちがその行使から得られる可能性のある任意の収益は、私たちの普通株の価格および株式承認証の行使価格と行使時の私たちの普通株価格との価格差に大きく依存する。権利証所有者が現金と交換するために任意またはすべての株式承認証を行使することを選択することは保証されておらず、以下のような行使は現在発生していないと信じている。本年度報告日現在、私たちは、引受権証を行使する任意の潜在的現金収益を、短期または長期流動資金予測に計上するつもりはありません。私たちは引き続き、私たちの引受権証の有効期間内に引受証を行使する可能性と、引受証を行使する潜在的な現金収益を私たちの流動資金予測に計上するメリットを評価し続ける。
私たちは現金による株式承認証の行使で私たちの業務に資金を提供しないと予想されます。逆に、本年度報告書の他の部分で議論されている主要な現金源に依存して、私たちの運営を支援していきたいと思います。2022年12月31日まで、株式承認証の発行価格は1株当たり11.50ドルで、私たちの普通株の終値は4.10ドルです。したがって、私たちは現在の権証保有者がその権利を行使することはあまり不可能だと思う。株式承認証所有者が引受権証を行使する可能性と、私たちが得る現金収益額は、私たちの普通株の取引価格に依存します。もし私たちの普通株の取引価格が依然として1株11.50ドル以下であれば、私たちの権利証所有者は彼らの権利を行使することがあまりできないと信じている。株式承認証が行使可能後及び満期前にも現金形式で存在することを保証できないため、株式承認証の期限が切れた時には一文の価値もない可能性があり、著者らも何の収益も得られない可能性がある
64
株式承認証を行使したことによる.いずれかの株式承認証が“キャッシュレスベース”で行使された場合、私たちが株式承認証を行使することから得られる現金金額は減少する。
2023年3月15日、会社はある機関投資家と証券購入協定を締結し、協定によると、会社は一連の4種類の高級無担保転換可能手形、元金総額980万ドル、および会社の普通株株式を購入する引受証を発行する。2023年3月15日、同社は第1陣の高級無担保転換可能手形を発行し、金額は330万ドルであり、328,352株の普通株を購入するための引受権証を発行した。優先無担保転換可能手形は8.0%の割引で発行され、年間利息は7.0%で、2024年6月15日に満期になる。優先無担保転換可能手形はいつでも当社が適宜決定して全部または一部を償還することができます。これらの株式承認証の初期行使価格は1株当たり2.97ドルであり、発行日から5年以内に満期となり、キャッシュレス行使条項が含まれている。
2回目の取引が終了すると、会社は、最大218,901株の普通株を購入するために、(I)元本220万ドルの追加手形および(Ii)追加株式証明書を買い手に発行して販売する。3回目および4回目の取引終了時に、当社は、その選択に応じて、(I)追加手形を買い手に発行および販売することができ、元金1部当たり220万ドルであり、(Ii)追加株式証明書は、適用締切手形変換後に発行可能株式の25%に相当する普通株式を購入することができる。証券購入契約によると、同社は必ずいくつかの追加条件を満たさなければ、第2、第3及び第4回成約時に追加手形及び追加株式証明書を販売及び発行することができる。この等の追加条件には、転換手形及び引受証の行使時に発行可能な普通株の登録、及び第3及び第4回収市について、適用されるナスダック規則に基づいて19.99%を超える発行及び発行済み株式の発行を承認するために、当社が米国証券取引委員会に提出する登録声明が有効であるか否かが含まれるが、これらに限定されない。
これらの株式承認証の初期行使価格は1株当たり2.97ドルであり、発行後5(5)年の取引終了前のいつでも行使でき、キャッシュレス行使条項を含む。
2023年3月15日,会社はLMFAチケット,LMFAOチケット,Maximチケットを修正し,期限を2024年6月15日に延長した.はい 当社は、証券購入契約により2回目の成約時に手形を発行して得られた金を受け取った後、手形所持者に総額10万ドルの現金を支払うことに同意した。
2023年3月13日に10万ドルの契約を結びました 米国LM Funding社が発行した年利率7.0%の元票。このチケットは2023年4月13日以降のいつでも即時支払いで、違約金は前払いされていません。同社は2023年3月24日にローンを返済した。
将来の資金需要
(I)FDAの承認を得るために我々のSCD製品の臨床開発を継続したいと考えており,(Ii)規制部門の承認を得て,米国市場で我々の製品を発売し,その後重要な国際市場で我々の製品を発売することを含めて商業化することを希望しているため,我々が行っている活動に関連した巨額の費用が発生すると予想される。私たちはこのような活動に関連した追加資金が必要だ。私たちの将来の短期的かつ長期的な支出需要は、多くの要素に依存するだろう
65
これまで、私たちが私たちの製品を開発して商業化することに成功すれば、株式、債務、信用手配下の借金の売却、または他社との潜在的な協力、他の戦略取引、または政府または他の贈与によって、私たちの運営に資金を提供し続ける予定です。必要な時や受け入れ可能な条件で、私たちは十分な資本を得ることができないかもしれない。
私たちの2022年12月31日までの経営業績と流動性によると、私たちの現金と現金等価物は、業務合併およびPIPE投資から得られた現金と、Tumimとの購入協定および長期購入協定(“FPA”)によって得られる潜在的収益を含むと信じており、2022年12月31日までの監査総合財務諸表日から少なくとも12ヶ月間の運営資本および資本支出需要を満たすには不十分である。また,我々の普通株の取引価格は現在このような株式承認証の行使価格を下回っているため,短期的には株式承認証の行使から現金収益は得られないと予想される.私たちは未来の債務や株式融資取引を通じて私たちの成長に資金を提供する追加の現金を求めている;しかし、私たちが受け入れられる条件で追加的な資本を得ることができる保証はない、あるいは私たちは私たちの運営に資金を提供するのに十分な未来の収入とキャッシュフローを生成するだろう。私たちの運営結果、運営資本、資本支出需要の推定は、私たちの実際の需要とは異なるかもしれません。例えば、私たちの実際の収入が私たちの予想よりも低く、私たちの純運営損失が私たちの予想よりも高く、私たちの現金と現金等価物の減少速度が予想より速い場合、これらの推定を修正する必要があるかもしれません。私たちは現在約束された外部資金源を持っていない。もし私たちが株式または転換可能な債務証券を売却することで追加資本を調達する場合、私たちの株主の所有権権益は希釈され、これらの証券の条項は清算または他の株主権利に悪影響を及ぼす特典を含む可能性がある。債務融資および優先株融資に関与する可能性のある合意には、追加債務、買収または資本支出を招くなど、我々が具体的な行動をとる能力を制限または制限する契約が含まれる。債務融資はまた固定支払義務につながるだろう。もし私たちが必要な時に株式や債務融資や他の手配で追加資金を調達できない場合、私たちは私たちの研究開発計画や将来の商業化努力を延期、減少、一時停止または停止する必要があるかもしれません。これは私たちの業務、見通し、経営業績、財務状況にマイナスの影響を与えます。我々の大量資本要求に関連する追加リスクについては、“リスク要因”の節を参照されたい。
キャッシュフロー
次の表に以下の各時期におけるキャッシュフローの概要を示す
|
|
現在までの年度 |
|
|
|||||
|
|
十二月三十一日 |
|
|
|||||
(千ドル) |
|
2022 |
|
|
2021 |
|
|
||
キャッシュフローデータテーブル: |
|
|
|
|
|
|
|
||
現金総額(使用)/以下の機関によって提供されます |
|
|
|
|
|
|
|
||
経営活動 |
|
$ |
(7,794 |
) |
|
$ |
(5,114 |
) |
|
投資活動 |
|
|
— |
|
|
|
— |
|
|
融資活動 |
|
|
7,331 |
|
|
|
2,817 |
|
|
|
|
$ |
(463 |
) |
|
$ |
(2,297 |
) |
|
経営活動のキャッシュフロー
2022年12月31日までの年間では、経営活動に用いられる純現金は780万ドルだったが、2021年12月31日までの年間は510万ドルだった。業務活動用の現金が270万ドル増加したのは、主に2022年12月31日現在の売掛金と売掛金が増加したためだ。
融資活動によるキャッシュフロー
2022年12月31日までの1年間、融資活動が提供する現金純額は730万ドルで、主に2022年第4四半期の業務合併と関係がある。2021年12月31日までの1年間、融資活動が提供した現金は280万ドルで、主に転換可能な手形の発行から来ている。
66
重要な会計政策と試算
米国公認会計原則に基づいて連結財務諸表と関連開示を作成し、管理層に推定、仮説と判断を要求し、報告の資産と負債額、連結財務諸表の日付のあるいは有資産と負債の開示、及び報告期間内の収入と費用に影響を与える。実際の結果はこれらの推定値と大きく異なる可能性があるが、このような推定値は、管理職が取得可能な最適情報と、管理層の当時の最適判断とに基づいて策定される。
重大な推定には、長期購入プロトコルの長期オプションの推定値、派生負債、株式承認証、および株式ベースの補償費用の金額が含まれる。
長期購入プロトコルの長期オプション
各報告期間において、リスク中性フレームワーク(収益法の特例)にモンテカルロシミュレーションを用いて長期購入プロトコルにおける長期オプションを再計量する。具体的には,将来の株価を幾何ブラウン運動(“GBM”)とする.各シミュレーション経路について、契約条項に基づいて長期購入価値を計算し、その後、期限に一致する無リスク金利で割引する。最後に,転送の値はすべてのシミュレーション経路上の平均現在値として計算される.
転換可能手形派生負債
変換可能なチケット派生負債は、各報告期間において、確率重み付けモデルと、変換価格および変換タイミングに関する仮定とを用いて再計量される。引受オプション負債は、当社の変換可能チケットに含まれる各種割引および各種決済プランに関する確率評価によって計算されたリターンに基づいて推定される。変換可能なチケットの変換のため、変換可能なチケットは、成約時に終了する負債から誘導される。
株式ベースの給与費用
付与された株式オプションの公正価値は、付与された日にBlack-Scholesオプション定価モデルを使用して推定され、このモデルは、以下の仮定を使用することを要求する
予想期間は、オプション付与の付与日と契約終了との間の中点として決定される米国証券取引委員会従業員会計公告第14主題に記載された“簡略化方法”に基づく。株価変動率は、同種の上場企業の類似期限内の推定株価変動率に基づいて推定される。オプション契約期間内の無リスク金利は、付与時に有効な米国債収益率に基づいている。配当収益率はゼロであり、同社が配当金を発表したり支払ったりしたことがなく、予見可能な未来にこのようにする計画もないからだ。
制限株式単位の公正価値の決定は、日会社普通株に付与された価値に基づいている。
新興成長型会社の地位
JumpStart Our Business Startups(“JOBS”)法案の定義によると,我々は新興成長型会社(“EGC”)である。JOBS法案は、EGCの地位を有する会社が、延長された過渡期間を利用して新しい会計基準または改正会計基準を遵守することを許可し、これらの会計基準の採用を民間会社に適用されるまで延期する。私たちは、私たち(I)がもはや新興成長型企業または(Ii)が“雇用法案”に規定されている延長移行期間から撤退することを明確かつ撤回できないまで、この延長された移行期間を使用することを選択し、新しい会計基準または改正された会計基準を遵守できるようにすることを選択した。したがって、上場企業の発効日まで、我々の連結財務諸表は、新たな会計基準や改正された会計基準に適合する企業と比較できない可能性がある。
67
また,JOBS法案が提供する他の免除と減少の報告要求に依存する予定である。私たちはこのような免除に依存するつもりなので、他の事項を除いて、私たちは必要ありません:(I)サバンズ-オキシック法第404条(B)条に基づいて、私たちの財務報告の内部統制制度に関する監査員証明報告書を提供します。(Ii)ドッド·フランクウォール街改革と消費者保護法案による非新興成長型上場企業に要求される可能性のあるすべての報酬開示を提供します。(Iii)上場企業会計監督委員会が採択する可能性のある強制監査会社ローテーションまたは補充監査師報告書が、コア数および総合財務諸表に関する追加資料を提供する任意の規定(監査人議論および分析)を遵守すること、および(Iv)行政職報酬と業績との関連性、および行政総裁報酬と従業員報酬中央値との比較など、いくつかの行政職員報酬に関連する項目を開示する。
雇用法案によると、(I)今回の発行終了5周年後の最初の会計年度の最終日までEGCとなり、(Ii)我々の年間総収入が少なくとも10.7億ドルの会計年度の最終日、(Iii)米国証券取引委員会の規則により“大型加速申請者”とみなされ、非関連会社が少なくとも7.00億ドルの未償還証券を保有する日となる。あるいは(Iv)私たちは過去3年以内に10億ドルを超える転換不能債券を発行した日。
業務合併
2022年10月28日、LMAOは一連の取引を完了し、LMF合併子会社とSeaStar Medical,Inc.が本年度報告でさらに述べた合併協定と計画に基づいて合併を行った。LMAOは“SeaStar医療ホールディングス”と改称した。この業務合併はSeaStar Medicalに相当するとされ,Inc.はLMAOの純資産発行株であり,資本再編を伴う。LMAOの純資産は歴史的コストで報告されています。業務統合前の業務はSeaStar医療会社の業務である。
終値時にSeaStar医療会社に支払うべき株主の総対価格は8,540万ドルであった。対価には、8500万ドルを含む;任意のSeaStar Medical,Inc.の債務を減算すること;SeaStar Medical,Inc.が80万ドルの上限を超える取引費用を差し引くこと;SeaStar Medicalを加えて、Inc.が終値直前に発行および発行された未行使株式証およびオプションの総行使価格を差し引くこと;仮想配当金の基礎となる普通株の価値を減算すること(“終値対価格”)が含まれる。終値はLMAO普通株のみで支払い、1株当たり額面0.0001ドル、1株当たり10ドルの価値があり、終値直前にSeaStar Medical,Inc.の株式保有者に8,540,552株の普通株を発行した。終値時には,LMAOのB類普通株(“B類普通株”)を1対1でA類普通株(“A類普通株”)に自動変換し,1株当たり額面0.001ドル,業務統合後のLMAO定款によりA類とB類普通株を普通株に再分類した。
終値時,SeaStar医療会社が発行·発行した1枚あたりの変換可能手形は自動的にSeaStar医療ホールディングス普通株に変換された。業務合併が発効する前に、SeaStar Medical,Inc.の1株当たり発行および発行された優先株を自動的にSeaStar Medical Holding Corporation普通株に変換し、業務合併に関連するSeaStar Medical,Inc.承認証を行使または交換し、SeaStar Medical,Inc.普通株と交換する。取引終了時には、(I)SeaStar Medical,Inc.行使または交換されない業務合併に関する承認権証はLMAOが負担し、普通株を購入する引受権証に変換され、(Ii)SeaStar Medical,Inc.配当計画下の発行済み普通株式オプションはLMAOが負担して普通株を購入するオプションに変換され、(Iii)SeaStar Medical,Inc.はSeaStar Medical,Inc.の現在の持分計画に従って発行および発行された制限株式単位奨励はLMAO制限株式単位に変換される。
68
契約義務と約束
次の表は、2022年12月31日までの契約義務をまとめています
|
|
合計する |
|
|
少ないです |
|
|
1-3年 |
|
|
3-5年 |
|
|
超過 |
|
|||||
契約義務: |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
LMFA支払手形 |
|
|
968 |
|
|
|
268 |
|
|
|
700 |
|
|
|
— |
|
|
|
— |
|
LMFAO支払手形 |
|
|
2,785 |
|
|
|
0 |
|
|
|
2,785 |
|
|
|
— |
|
|
|
— |
|
マクシム支払手形 |
|
|
4,167 |
|
|
|
— |
|
|
|
4,167 |
|
|
|
— |
|
|
|
— |
|
保険融資 |
|
|
910 |
|
|
|
910 |
|
|
|
— |
|
|
|
— |
|
|
|
— |
|
契約債務総額 |
|
$ |
8,830 |
|
|
$ |
1,178 |
|
|
$ |
7,652 |
|
|
$ |
— |
|
|
$ |
— |
|
長期購入協定
2022年10月17日と10月25日,LMAOおよびSeaStar Medical,Inc.はVella Opportunity Fund SPV LLC−Series 4(“Vella”)とHB Strategy LLC(“HB Strategy”,およびVellaとともに“FPA売り手”)と長期購入契約(“FPA”)を締結した。FPAの条項によると、FPA売り手は、以前に業務合併に関連する償還権に基づいて償還株式を選択した所有者(当該等の購入済み株式、すなわち“循環株式”)から購入することを含む、公開市場ブローカーを介してLMAO又はLMAO連合会社以外の所有者にA類普通株株式を購入する。
FPA売り手は、LMAOの信託口座から直接現金金額(“前払い金額”)を取得し、購入した株式数に1株当たりの償還価格を乗じたものに等しい。FPA売り手はプリペイド金額に加えてLMAOの信託口座から直接返済を受け、仲介人を通じて公開市場で第三者から200,000株のLMAO普通株を購入した。
FPA売り手は、彼らが購入した回収株式(“終了株式”)を適宜売却することができる。当社は売却終了株式から得られた金額が終了株式数にリセット価格(“リセット価格”)を乗じる権利がある。業務合併終了後(“収市”)では,リセット価格は最初は1株10.00ドルであったが,収市後最初のカレンダー月からの毎月最終予定取引日を(A)当時のリセット価格,(B)10.00ドルおよび(C)前月最終10(10)取引日株式の出来高加重平均価格(“VWAP価格”)の最低者に調整したが,5.00ドルを下回らなかった.
FPAの満期日(“満期日”)は,(A)成約3周年,および(B)任意の連続30取引日以内に任意のイベントが発生した後,FPA売手が決定した20取引日のVWAP価格は1株3.00ドルの中で最も早いものを下回る.
満期日には,FPA売手は未売却の循環株数に2.50ドル相当の現金金額を保持する権利があり,FPA売手は未売却の循環株を会社に渡す.
FPA売り手は2022年12月31日現在、売却終了株を売却して得られた000万ドルを会社に支払っている。当社は、FPA売り手が売却終了した株から現金収益を得ることが可能であるが、FPA売り手は、我々普通株の取引価格がリセット価格よりも高くない限り、終了株を売却する動機がない可能性がある。2023年2月10日のリセット価格は1株5.00ドルで、普通株の取引価格が現在のリセット価格以上になる保証はありませんし、その後の適用期間中に当社の普通株の将来の取引価格がリセット価格以上になることも保証されません。この場合,FPA売手は終了した株を売却しない可能性があり,この場合,FPAからいかなる現金収益も得ることができない.また,FPA売手が彼らの株を市場に売却することを決定すれば,我々の普通株の取引価格を大幅に低下させる可能性がある.
69
役員指名協定
保険者と保険者は2022年10月28日に“取締役指名協定”を締結し、保証人に若干の取締役指名権を与え、2人の人を委任または指名することを含めて(状況に応じて)取締役会に入り、当社の第II類取締役を務め、任期は締め切り後しばらくの期間(“取締役指名合意”)である。
持分信用限度額
2022年8月23日、SeaStar Medical,Inc.,LMAOとTumim Stone Capital LLC(“Tumim”)は普通株購入合意を通じて、Tumimに1億ドルに達する普通株を売却する権利があることを規定する株式限度融資計画を達成した。“普通株購入協定”は、いくつかの制限および条件によって制限され、トゥミームに250万ドルの承諾料を支払うことが規定されている。同社は成約時に100万ドルの承諾料を現金で支払った。2022年12月31日現在、会社は承諾料の残り150万ドルの課税費用を記録しており、そのうち100万ドルは新たに発行された普通株で支払う。250万ドルの引受金は、2022年12月31日までの年間総合業務報告書に一般費用および行政費用を記入します。
LMFA支払手形
2022年9月9日、SeaStar Medical,Inc.はLM Funding America,Inc.(“LMFA”)とクレジット協定(“LMFAチケット”)を締結し、この合意によると、LMFAはSeaStar Medical,Inc.に70万ドルまでの融資を提供することに同意し、一般企業用途に使用され、年率は15%である。LMFAチケットからSeaStar Medical,Inc.に支払われたすべての前払いおよび受取利息は,満期日に満了し,LMFA,すなわち(A)2022年10月25日,(B)業務統合完了と(C)統合プロトコル終了の早い日に支払われる.同社は2022年12月31日現在、LMFAチケットにより70万ドルを借り入れている。
2022年10月28日、SeaStar Medical Holding CorporationとLMFAは、LMFAとSeaStar Medical Holding Corporationが2022年9月9日に締結した第1の修正案信用協定を締結し、この協定によると、(I)LMFAチケット下のローンの満期日を2023年10月30日に延長し、(Ii)当社は任意の将来の債務と持分融資から得られた現金収益総額の5.0%をLMFAチケットの未返済残高の支払いに使用する必要があり、(Iii)LMFAチケットの年利率を15%から7%に下げる必要がある。そして(Iv)違約金利は18%から15%に低下した。2022年12月31日以降、期日は2024年6月15日に延期される(付記16)。そこで,当社はLMFAチケットを2022年12月31日までの総合貸借対照表で長期チケットとしている.LMFAの説明には,慣用的な陳述と保証,肯定と否定のチノおよび違約イベントが掲載されている.
また,双方は2022年10月28日に担保合意を締結し,この合意により,SeaStar Medical Holding CorporationはLMFAに実質的にすべての資産および財産の保証権益を付与したが,ある例外を除いて,改訂されたLMFAチケットの担保とした。また,会社は2022年10月28日の保証を締結し,この担保により,SeaStar Medical Holding Corporationは無条件に保証し,LMFAにLMFAチケット項下の未償還元金を支払うことを承諾した。
2022年11月2日、会社はLMFAと30万ドルの追加元票を締結した。このチケットは無利息本券で、2023年3月31日かそれ以降はいつでも支払いを要求しなければなりません。この手形は2023年1月に全額支払われた。
LMFAO支払手形
当社は2022年10月28日、LMFAO保証人LLC(LMAOの保証人および創設株式の唯一の所有者)と元金総額2,785ドルの総合改訂および重述された引受票(“LMFAO手形”)を締結し、改訂および重述(I)LMAOが保証人に発行した元金総額が1,035ドル、日付が2022年7月29日の引受票および(Ii)がLMAOから保証人に発行された元金総額1,750ドルの改訂および重記された引受票(総称して“元手形”)である。LMFAO説明元の説明を,(1)延長期限に改訂する
70
(Ii)プレミアムまたは罰金を支払うことなく、LMFAOチケットの満了に応じた未償還金額を前払いすることを可能にし、(Iii)将来の債務および持分融資から受信した現金収益の総額の20.0%を使用してLMFAOチケットの未償還残高を支払うことを会社に要求するが、最初の500ドルの現金収益は償還する必要がない。2022年12月31日以降、期日は2024年6月15日に延期される(付記16)。そこで,会社は2022年12月31日までの総合貸借対照表においてLMFAOチケットを長期チケットに分類する.LMFAOチケットの年利率は7%であり,慣用的な陳述と保証および肯定と否定の契約を含む.
LMFAOチケットは違約イベントの影響を受け,LMFAOチケットの即時満期と対応の可能性があり,年利率は15.0%である.また、2022年10月28日、双方は、ある例外を除いて、当社のほとんどの資産と財産の担保権益を保証者に付与し、LMFAO手形項における当社の義務を担保する担保契約を締結した。
マクシム支払手形
当社は2022年10月28日にMaximを借主として元金総額420万ドルの約束手形(“Maxim手形”)を締結した。Maxim手形の満期日は2023年10月30日で、どの返済されていない金額も前払いでき、割増や罰金は必要ない。当社が満期日までに債務や株式融資取引から現金収益を得る場合、当社は現金収益総額25.0%に相当する債務を早期に返済しなければなりませんが、この償還義務は当社が受け取った現金収益の前50万ドルには適用されません。2022年12月31日以降、期日は2024年6月15日に延期される(付記16)。そこで、当社は2022年12月31日現在の総合貸借対照表においてMaxim手形を長期手形としている。Maxim債券の利息は年利7.0%である。
Maxim Noteは慣用的な陳述と保証,および肯定と否定の契約を含む.Maxim手形は違約事件の影響を受け、Maxim手形の即時満期と支払いを招く可能性があり、年利率は15.0%である。
保険融資
2022年10月、当社はある貸手と融資協定を締結し、保険証書の一部の保険料に90万ドルの資金を提供した。融資協定の利息は7.35%の年利で満期になる。当社は2023年1月と2023年2月にそれぞれ元金と利息10万元を支払います。
債権者間協議
2022年10月28日、Maxim、LMFA、保証人(総称して“債権者”と呼ぶ)、SeaStar Medical,Inc.及び当社は債権者間合意を締結し、他のLMFA手形、LMFAO手形及びMaxim手形の下での相対権利を設定し、当該等の手形に違約が発生した場合に当社が支払う金を含む。各債権者は,LMFAと保証人にLMFA保証プロトコルと保証人保証プロトコルに規定された担保留置権が付与されたことに同意して認めた.各債権者もMaximのMaxim Note項下の債務が無担保であることに同意し、認めた。
第七A項。市場リスクに関する定量的で定性的な開示。
取引法第12 b-2条の定義によると、我々は小さな報告会社であり、本プロジェクトに要求される情報を提供する必要はない。
71
連結財務諸表索引
独立公認会計士事務所レポート(PCAOB ID: |
73 |
2022年と2021年12月31日までの連結貸借対照表 |
74 |
2022年と2021年12月31日までの総合業務報告書 |
75 |
2022年12月31日と2021年12月31日までの年度転換可能優先株と株主損失総合変動表 |
76 |
2022年12月31日と2021年12月31日までの統合現金フロー表 |
77 |
連結財務諸表付記 |
78 |
72
代表者独立公認会計士事務所のORT
SeaStar医療ホールディングスの株主と取締役会へ
連結財務諸表に対するいくつかの見方
我々は、2022年及び2021年12月31日に添付されたSeaStar Medical Holding Corporation及びその付属会社(総称して“会社”)の総合貸借対照表、及び当該日までの年度までの関連総合経営表、転換可能な優先株及び株主損失変動及びキャッシュフロー、及び関連付記(総称して総合財務諸表と呼ぶ)を監査した。総合財務諸表は,当社の2022年12月31日と2021年12月31日までの総合財務状況,および2022年12月31日までの2年間の各年度の経営結果とキャッシュフローをすべての重要な面で公平に反映しており,米国公認の会計原則に適合していると考えられる。
意見の基礎
これらの連結財務諸表は会社の経営陣が責任を負う。私たちの責任は私たちの監査に基づいて会社の総合財務諸表に意見を発表することです。私たちは米国上場企業会計監督委員会(PCAOB)に登録されている公共会計士事務所であり、米国連邦証券法および米国証券取引委員会とPCAOBの適用規則と法規に基づいて、会社と独立しなければならない。
私たちはPCAOBの基準に従って監査を行っている。これらの基準は、連結財務諸表に重大な誤報がないかどうかに関する合理的な保証を得るために、エラーによるものであっても不正であっても、監査を計画し、実行することを要求する。当社はその財務報告の内部統制を監査することを求められておらず、私たちも招聘されて監査を行っていません。私たちの監査の一部として、財務報告の内部統制を理解することが求められていますが、社内財務報告の内部統制の有効性について意見を述べるためではありません。したがって、私たちはそのような意見を表現しない。
我々の監査には、連結財務諸表の重大な誤報リスクを評価するプログラム、エラーによるものであっても詐欺であっても、これらのリスクに対応するプログラムを実行することが含まれる。これらの手続きは、連結財務諸表中の金額および開示に関する証拠をテストに基づいて検討することを含む。我々の監査には、経営陣が使用する会計原則の評価と重大な見積もり、合併財務諸表の全体列報の評価も含まれています。私たちは私たちの監査が私たちの観点に合理的な基礎を提供すると信じている。
会社の継続経営企業としての継続経営能力に大きな疑いがある
添付されている総合財務諸表の作成仮説会社は引き続き経営を継続する企業となる。総合財務諸表付記1で述べたように、当社はすでに経常的な重大な損失を発生しており、持続経営企業としての持続的な経営能力を大きく疑わせている。付記1は、これらの事項における経営陣の計画も説明しています。連結財務諸表には、このような不確実性の結果によって生じる可能性のあるいかなる調整も含まれていません。
/s/
2023年3月30日
2021年以来、私たちは会社の監査役を務めてきた。
73
Seastar医療ホールディングス
統合された貸借対照表
2022年12月31日と2021年12月31日まで
(単位は千で、1株当たりおよび1株当たりの金額は含まれていない)
|
|
2022 |
|
|
2021 |
|
||
資産 |
|
|||||||
流動資産 |
|
|
|
|
|
|
||
現金 |
|
$ |
|
|
$ |
|
||
その他売掛金 |
|
|
|
|
|
|
||
前払い費用 |
|
|
|
|
|
|
||
流動資産総額 |
|
|
|
|
|
|
||
長期オプション-前払い長期契約、純額 |
|
|
|
|
|
|
||
その他の資産 |
|
|
|
|
|
|
||
総資産 |
|
$ |
|
|
$ |
|
||
負債と株主赤字 |
|
|||||||
流動負債 |
|
|
|
|
|
|
||
売掛金 |
|
$ |
|
|
$ |
|
||
費用を計算する |
|
|
|
|
|
|
||
支払手形 |
|
|
|
|
|
|
||
変換可能チケット-関連側は、割引を差し引いた純額 |
|
|
|
|
|
|
||
転換可能手形派生負債 |
|
|
|
|
|
|
||
流動負債総額 |
|
|
|
|
|
|
||
支払手形 |
|
|
|
|
|
|
||
政府ローン |
|
|
|
|
|
|
||
変換可能手形-関連側は、割引後の純額を控除し、当期分の純額を差し引く |
|
|
|
|
|
|
||
転換可能な手形由来負債、流動分を差し引く |
|
|
|
|
|
|
||
総負債 |
|
|
|
|
|
|
||
|
|
|
|
|
|
|||
株主損(1) |
|
|
|
|
|
|
||
A類普通株--$ |
|
|
|
|
|
|
||
追加実収資本 |
|
|
|
|
|
|
||
赤字を累計する |
|
|
( |
) |
|
|
( |
) |
株主赤字総額(1) |
|
|
( |
) |
|
|
( |
) |
総負債、転換可能優先株、株主損失 |
|
$ |
|
|
$ |
|
||
(1)
付記はこれらの連結財務諸表の構成要素である。
74
Seastar医療ホールディングス
統合された運営説明書
2022年12月31日まで及び2021年12月31日まで年度
(単位は千で、1株当たりおよび1株当たりの金額は含まれていない)
|
|
2022 |
|
|
2021 |
|
||
運営費 |
|
|
|
|
|
|
||
研究開発 |
|
$ |
|
|
$ |
|
||
一般と行政 |
|
|
|
|
|
|
||
前払い契約の初期コスト |
|
|
|
|
|
|
||
総運営費 |
|
|
|
|
|
|
||
|
|
|
|
|
|
|
||
運営損失 |
|
|
( |
) |
|
|
( |
) |
|
|
|
|
|
|
|
||
その他の収入,純額 |
|
|
|
|
|
|
||
利子支出 |
|
|
( |
) |
|
|
( |
) |
その他の収入 |
|
|
- |
|
|
|
|
|
転換可能手形由来負債の公正価値変動 |
|
|
( |
) |
|
|
( |
) |
長期オプション−前払い長期契約公正価値変動 |
|
|
( |
) |
|
|
|
|
回収株の損失 |
|
|
( |
) |
|
|
|
|
その他の費用の合計 |
|
|
( |
) |
|
|
( |
) |
|
|
|
|
|
|
|
||
所得税前損失準備 |
|
|
( |
) |
|
|
( |
) |
|
|
|
|
|
|
|
||
所得税を支給する |
|
|
|
|
|
( |
) |
|
|
|
|
|
|
|
|
||
純損失 |
|
$ |
( |
) |
|
$ |
( |
) |
普通株は基本的に1株当たり純損失と希釈して1株当たり純損失 |
|
$ |
( |
) |
|
$ |
( |
) |
加重平均流通株、基本株及び希釈株(1) |
|
|
|
|
|
|
||
(1)
付記はこれらの連結財務諸表の構成要素である。
75
Seastar医療ホールディングス
統合された転換優先株と株主損失変動表
2022年12月31日まで及び2021年12月31日まで年度
(単位は千で、1株当たりおよび1株当たりの金額は含まれていない)
|
|
転換可能優先株 |
|
|
|
株主損失額 |
|
||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
合計する |
|
||||||||||||
|
|
Bシリーズ優先株 |
|
|
Aシリーズ-1優先株 |
|
|
A-2シリーズ優先株 |
|
|
|
|
|
|
普通株 |
|
|
その他の内容 |
|
|
積算 |
|
|
株主の |
|
||||||||||||||||||||||||
|
|
株式(1) |
|
|
金額 |
|
|
株式(1) |
|
|
金額 |
|
|
株式(1) |
|
|
金額 |
|
|
合計する |
|
|
|
株式(1) |
|
|
金額 |
|
|
実収資本 |
|
|
赤字.赤字 |
|
|
赤字.赤字 |
|
||||||||||||
残高、2021年1月1日 |
|
|
|
|
$ |
|
|
|
|
|
$ |
|
|
|
|
|
$ |
|
|
$ |
|
|
|
|
— |
|
|
$ |
— |
|
|
$ |
|
|
$ |
( |
) |
|
$ |
( |
) |
||||||||
資本再編の遡及応用 |
|
|
( |
) |
|
|
( |
) |
|
|
( |
) |
|
|
( |
) |
|
|
( |
) |
|
|
( |
) |
|
|
( |
) |
|
|
|
|
|
|
|
|
|
|
|
|
— |
|
|
|
|
||||
調整後の残高,期初 |
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
|
|
|
|
|
|
|
|
|
|
( |
) |
|
|
|
||||
株に基づく報酬 |
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
|
— |
|
|
|
— |
|
|
|
|
|
|
— |
|
|
|
|
||
純損失 |
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
( |
) |
|
|
( |
) |
バランス、2021年12月31日 |
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
|
|
|
|
|
|
|
|
|
|
( |
) |
|
|
( |
) |
|||
2022年10月28日の逆資本再編 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
— |
|
|
|
|
|
|
— |
|
|
|
|
||||||||||
オープンカーの改装 |
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
|
|
|
|
— |
|
|
|
|
|
|
— |
|
|
|
|
|||
パイプ融資 |
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
|
|
|
|
— |
|
|
|
|
|
|
— |
|
|
|
|
|||
株に基づく報酬 |
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
|
— |
|
|
|
— |
|
|
|
|
|
|
— |
|
|
|
|
||
純損失 |
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
( |
) |
|
|
( |
) |
バランス、2022年12月31日 |
|
|
— |
|
|
$ |
— |
|
|
|
— |
|
|
$ |
— |
|
|
|
— |
|
|
$ |
— |
|
|
$ |
— |
|
|
|
|
|
|
$ |
|
|
$ |
|
|
$ |
( |
) |
|
$ |
( |
) |
|||
(1)
付記はこれらの総合財務諸表の構成要素である
76
Seastar医療ホールディングス
統合された現金フロー表
2022年12月31日まで及び2021年12月31日まで年度
(千単位で、株や1株当たりの金額は含まれていない)
|
|
2022 |
|
|
2021 |
|
||
経営活動のキャッシュフロー |
|
|
|
|
|
|
||
純損失 |
|
$ |
( |
) |
|
$ |
( |
) |
純損失と経営活動で使用した現金純額の調整 |
|
|
|
|
|
|
||
転換可能な手形を割引して償却する |
|
|
|
|
|
|
||
転換可能手形に関する非現金当算利息 |
|
|
|
|
|
|
||
転換可能手形由来負債の公正価値変動 |
|
|
|
|
|
|
||
長期オプションは価値変動を公平に承諾する |
|
|
|
|
|
|
||
回収株の損失 |
|
|
|
|
|
|
||
PPPローン免除 |
|
|
|
|
|
( |
) |
|
株に基づく報酬 |
|
|
|
|
|
|
||
経営性資産と負債の変動 |
|
|
|
|
|
|
||
その他売掛金 |
|
|
|
|
|
|
||
在庫品 |
|
|
|
|
|
|
||
前払い費用 |
|
|
( |
) |
|
|
|
|
売掛金 |
|
|
|
|
|
( |
) |
|
費用とその他の流動負債を計算しなければならない |
|
|
|
|
|
( |
) |
|
経営活動のための現金純額 |
|
|
( |
) |
|
|
( |
) |
|
|
|
|
|
|
|
||
融資活動によるキャッシュフロー |
|
|
|
|
|
|
||
転換手形を発行して得た金 |
|
|
|
|
|
|
||
資本再編収益 |
|
|
|
|
|
|
||
資本再編成取引コストを支払う |
|
|
( |
) |
|
|
|
|
パイプ投資家の収益 |
|
|
|
|
|
|
||
長期契約払い |
|
|
( |
) |
|
|
|
|
循環株を売却して得た金 |
|
|
|
|
|
|
||
支払手形収益 |
|
|
|
|
|
|
||
支払手形の支払い |
|
|
( |
) |
|
|
|
|
購買力平価ローンの収益 |
|
|
|
|
|
|
||
政府のローンを返済する |
|
|
( |
) |
|
|
|
|
購買力平価ローンを償還する |
|
|
|
|
|
( |
) |
|
融資活動が提供する現金純額 |
|
|
|
|
|
|
||
|
|
|
|
|
|
|
||
現金の純減少 |
|
|
( |
) |
|
|
( |
) |
|
|
|
|
|
|
|
||
期初の現金 |
|
|
|
|
|
|
||
|
|
|
|
|
|
|
||
期末現金 |
|
$ |
|
|
$ |
|
||
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
||
キャッシュフロー情報を補足開示する |
|
|||||||
|
|
|
|
|
|
|
||
所得税の現金を納める |
|
$ |
|
|
$ |
|
||
利子を支払う現金 |
|
$ |
|
|
$ |
|
||
|
|
|
|
|
|
|
||
非キャッシュフロー情報の補足開示 |
|
|||||||
|
|
|
|
|
|
|
||
A-2系列優先株からB系列優先株に転換 |
|
$ |
|
|
$ |
|
||
優先株を普通株に転換する |
|
|
|
|
|
|
||
転換可能手形を普通株式に変換する |
|
|
|
|
|
|
||
売掛金における資本再編成取引コスト |
|
|
|
|
|
|
||
手形における資本再構成取引コスト |
|
|
|
|
|
|
||
転換可能な手形を発行する際の派生負債の価値 |
|
|
|
|
|
|
||
課税料金を非現金方式で転換可能な手形に変換します |
|
|
|
|
|
|
||
転換手形は現金の他の売掛金にあります |
|
|
|
|
|
|
||
付記はこれらの連結財務諸表の構成要素である。
77
Seastar医療ホールディングス
連結財務諸表付記
(千単位で、株や1株当たりの金額は含まれていない)
注1.De業務のスクリプト
業務の組織と記述
Seastar Medical,Inc.は2007年6月にデラウェア州の会社として設立され、コロラド州デンバー市に本社を置いている。同社は主にプラットフォーム医療設備技術の研究、開発と商業化に従事し、異なる患者群の炎症を調節することを目的としている。この技術の主な目標は急性腎障害の治療である。
Seastar Medical,Inc.は製品開発に専念する事業前段階にある。
2022年10月28日、LMF Acquisition Opportunities,Inc.(“LMAO”)の完全子会社LMF Merge Sub,Inc.はSeaStar Medical,Inc.(“業務合併”)と合併し、SeaStar Medical,Inc.はLMAOの完全子会社として存続する(注3参照)。業務合併完了後,LMAOは“SeaStar Medical Holding Corporation”(“当社”,“WE”,“SeaStar Medical”)と改称した。
陳述の基礎
添付されている総合財務諸表は、米国公認会計原則(“米国公認会計原則”)及び米国証券取引委員会(“米国証券取引委員会”)の規則及び規定に従って作成されたものである。連結財務諸表には、同社の完全子会社SeaStar医療会社の合併勘定が含まれている。
すべての重大な会社間取引は合併で除去された。
市場情報を細分化する
その会社は一つの経営部門で運営されているため、本報告ではどの部門情報も開示されていない。
流動資金と持続経営
2022年12月31日までの同社の累積赤字は$
追加資本に対する私たちの必要性は私たちの開発活動の範囲と費用に部分的に依存するだろう。私たちは今まで商業化された製品の販売から相当な収入を得ていない。私たちが製品収入を作る能力は私たちの製品の成功的な開発と最終商業化にかかっているだろう。その前に、もしあれば、株式または債務の売却、信用手配の下での借金、または潜在的な協力、他の戦略的取引、または政府および他の贈与によって、私たちの業務に融資する予定です。必要な時や受け入れ可能な条件で、私たちは十分な資本を得ることができないかもしれない。
もし私たちが資金を調達できなければ、私たちは私たちの研究開発計画や将来の商業化努力を延期、減少、一時停止、停止させることを余儀なくされる可能性があり、これは私たちの業務、将来性、経営業績、財務状況にマイナスの影響を与えるだろう。添付されている総合財務諸表の作成は、同社が引き続き経営を継続する企業であり、このような不確実性の結果による調整は含まれていないと仮定している。この会計ベースは、通常業務過程における会社資産の回収と負債の返済を考慮している。
リスクと不確実性
当社は医療技術業界の早期会社によく見られるリスクに直面しています
78
Seastar医療ホールディングス
連結財務諸表付記
(千単位で、株や1株当たりの金額は含まれていない)
新たな医療技術革新、キーパーソンへの依存、ノウハウの保護、製品責任に限定されない。会社の製品またはサービスが市場に受け入れられることは保証されず、将来のいかなる製品またはサービスが許容可能なコストで開発または配備され、適切な性能特徴を有するか、またはそのような製品またはサービスが成功的にマーケティングされることも保証されない(もしあれば)。これらの要因は、会社の将来の財務業績、財務状況、キャッシュフローに重大な悪影響を及ぼす可能性がある。
同社は現在、将来の大流行がその財務状況と運営に及ぼす具体的な程度、持続時間、あるいは全面的な影響を予測できない。未来の大流行は私たちの臨床前研究を開始し、完成する能力に影響を与える可能性があり、私たちの臨床試験或いは未来の臨床試験を延期し、規制活動を妨害し、或いは私たちの業務と運営に他の不利な影響を与える。
付記2.主要会計政策の概要
予算の使用
アメリカ公認会計原則に基づいて連結財務諸表を作成する際には、管理層は連結財務諸表の日付の資産と負債額及び或いは有資産と負債の開示、及び期間中の収入と支出の報告金額に影響するため、推定、仮説と判断を行わなければならない。重大な推定には、前払い契約の長期オプションの推定値、派生負債、引受権証、税収準備、および株式ベースの補償費用が含まれる。実際の結果はこれらの推定とは異なる可能性があるが,この推定は,経営陣や経営陣がその際に最適な判断で得られた最適な情報に基づいて作成されている.
現金
同社は米国(“米国”)の商業銀行で現金を持っている。連邦預金保険会社が保証し、最高で$に達します
信用リスクが集中する
会社をかなり集中的な信用リスクに直面させる可能性のある金融商品は主に現金です。当社は定期的に金融機関で政府の保険限度額を超える預金を維持することができます。当社は設立以来何の預金赤字も出ていません。
所得税
当社は、統合財務諸表または納税申告書に含まれるイベントの将来の税務結果を予想する繰延税金資産および負債を確認します。繰延税項資産及び負債は、総合財務諸表帳簿額面と資産及び負債の課税基礎との差額に基づいて決定され、当該等の差額に適用される期間に適用される予定の課税収入の制定税率を採用する。繰延税項目の純資産が現金化される可能性が低いと考えられた場合には、推定支出を提供する。
当社は、“会計基準アセンブリ”(ASC)740“所得税”の規定を遵守し、合併財務諸表において、企業が納税申告書を負担しているか、または予想している不確定所得税の確認、開示のための包括的なモデルを提供している。この指導の下で、会社のみが可能である(より大きい)
79
Seastar医療ホールディングス
連結財務諸表付記
(千単位で、株や1株当たりの金額は含まれていない)
公正価値計量
公正価値は、計量日の市場参加者間の秩序ある取引において資産を売却することによって受信された価格または移転負債によって支払われた価格(脱退価格)として定義される。公正価値を計量するための投入は以下の段階に分けられる
第1レベル-同じ資産と負債の活発な市場でのオファー。
第2レベル--他の重要な観察可能な投入(類似資産や負債の見積もり、金利、信用リスクなどを含む)。
第三段階-重大な観察不可能な投入(資産および負債の公正価値を決定する際の会社自身の仮定を含む)。
前払い長期契約の長期オプションおよび変換可能な手形派生負債の公正価値は、公正価値レベルにおいて第3レベルに分類される。
次の表に、2022年12月31日と2021年12月31日までの年間長期オプションと変換可能手形派生負債の変化(単位:千)を示す
|
|
|
|
|
|
|
|
|
||
|
|
|
|
転送オプション |
|
|
転換可能な手形 |
|
||
|
|
|
|
前払いについて |
|
|
導関数 |
|
||
レベル3前転 |
|
|
|
長期契約 |
|
|
負債.負債 |
|
||
残高2020年12月31日 |
|
|
|
$ |
|
|
$ |
|
||
足し算 |
|
|
|
|
|
|
|
( |
) |
|
|
|
|
|
|
|
|
( |
) |
||
残高2021年12月31日 |
|
|
|
|
|
|
|
( |
) |
|
足し算 |
|
|
|
|
|
|
|
( |
) |
|
リサイクル株を売却する |
|
|
|
|
( |
) |
|
|
|
|
|
|
|
|
( |
) |
|
|
( |
) |
|
追加実収資本に再分類する |
|
|
|
|
|
|
|
|
||
残高2022年12月31日 |
|
|
|
$ |
|
|
$ |
|
||
金額$の長期オプション
換算可能な手形派生負債、金額は#ドル
#ドルの派生負債
80
Seastar医療ホールディングス
連結財務諸表付記
(千単位で、株や1株当たりの金額は含まれていない)
派生負債の公正価値変動は、総合経営報告書に変換可能な手形派生負債の公正価値変動に計上される。
これらのツールの短期的な性質のため、前払い費用、売掛金と課税費用の推定公正価値はその公正価値に近い。
株に基づく報酬
ASC主題718によれば、報酬−株式報酬に基づいて、会社は、推定付与日公許可価値に基づいて、必要なサービス期間内に階層的帰属方法で確認された支出である従業員に支給されるすべての株式報酬の報酬支出を確認する。同社は没収が発生した場合に確認することを選択した。株式オプションの公正価値はブラック·スコアーズオプション定価モデルを用いて決定される。オプション定価モデルを用いて日株式オプションを付与する公正価値を決定する際には、会社の普通株式推定値のほかに、経営陣は予想変動率、期待期限、無リスク金利、期待配当を含むいくつかの仮定を行う必要がある。制限株式単位の公正価値は、日本会社に付与された普通株の価値に基づいて推定される(付記12参照)。
業務合併前に、会社普通株は活発な市場が不足していたため、会社は米国公認会計士協会監査および会計実務援助シリーズ:補償として発行された私有会社株式証券の推定値と一致する方法、方法、および仮定を用いて普通株の公正価値を推定した。株式購入の行使価格を決定する際に、当社はすでに当社の授出日の公正価値を考慮している。会社の公正価値は各種の要素によって決定され、これらの要素は会社の財務状況、歴史業績と経営結果、会社の発展段階、会社の研究開発計画の進展、会社がその転換可能な優先株を売却する価格、会社が転換可能な優先株の普通株に対するより高い権利、優遇と特権、生物技術業界の外部市場状況に影響を与える。当社の普通株は市場性に乏しく、流動性事件の将来性、類似会社の初公募株と市場表現の分析、及び最近完成した同業者会社への合併と買収。使用された要素に基づいた主要な仮定の重大な変化は、各推定日における会社の公正価値の違いを招く可能性がある。
研究開発費
研究と開発のための支出は発生時に費用を計上する。外部コストは主に会社の発見と臨床前活動および過程開発と臨床開発活動のために購入した実験室用品の支払いを含む。内部コストには,主に従業員に関する費用,相談費,法規遵守に関する費用が含まれる。将来の研究開発活動のための払戻不可能な商品およびサービス前金は、会社が商品またはサービスを提供している間に資本化され、費用として記録される。
同社は,領収書とその供給,実施,臨床試験を代表するコンサルタントとの契約に基づき,外部研究·開発サービスに関する費用を記録している。
新興成長型会社の地位
当社は2012年のJumpStart Our Business Startups Act(“JOBS法案”)で定義されている“新興成長型会社”です。雇用法案によると、新興成長型企業は、新たなまたは改正された会計基準を遵守するために長い過渡期を利用して、民間企業に適用されるまでこれらの会計基準の採用を延期することができる。当社は、(1)新興成長型企業ではなく、または(2)“雇用法案”に規定されている延長移行期間から明確かつ撤回できないまで、上場企業と非上場企業に対して異なる発効日を有するこの延長された移行期間を使用することを選択した。
81
Seastar医療ホールディングス
連結財務諸表付記
(千単位で、株や1株当たりの金額は含まれていない)
普通株主は1株当たり純損失を占めるべきである
会社の普通株主が1株当たりの基本純損失を占めるべき計算方法は、普通株株主が純損失を当期発行普通株の加重平均株式数で割るべきである。普通株主が1株当たり純損失を占めるべき計算方法は、期間内のすべての潜在的な希釈性普通株等価物を計算することである。これらの潜在普通株の希釈効果は在庫株方法で希釈した1株当たり収益に反映される。
最近発表された未採用の会計基準
2020年8月、財務会計基準委員会(“FASB”)は、実体自己資本の中でツールと契約を変換可能な会計基準(“ASU 2020-06”)を発表した。ASU 2020−06は、負債および権益の特徴を有するいくつかの金融機器に米国公認会計基準を適用することによる複雑さによって決定された問題を解決する。複雑性を処理する際に、ASU 2020-06は、変換可能ツールに関する指導意見と、実体自己株契約の派生商品範囲の例外に関する指導意見を重点的に改訂した。本更新における改訂は、米国証券取引委員会(“米国証券取引委員会”)の届出文書定義に適合する公共商業実体に対して有効であり、米国証券取引委員会の定義に適合する比較的小さい報告会社の実体は含まれておらず、2021年12月15日以降の財政年度から、これらの財政年度内の移行期間を含む。他のすべての実体について、改正案は2023年12月15日以降に開始された財政年度に有効であり、これらの財政年度内の過渡期を含む。早期養子縁組を許可する。JOBS法案によると、会社はASU 2020-06の採用を延期している。したがって、これらの連結財務諸表は、上場企業の発効日に新たなまたは改訂された会計声明を遵守する企業と比較できない可能性がある。
注3.業務合併と資本再編
2022年10月28日、LMAOは一連の取引を完了し、LMF Merge Sub,Inc.とSeaStar Medical,Inc.は付記1で述べたように、合併プロトコルと計画に従って合併した。
米国公認会計原則によると、この業務合併は逆資本再編に計上される。このような会計方法の下で、LMAOは財務報告書で会社を買収するとみなされている。この決定は,主に業務統合後,SeaStar Medical,Inc.の株主が合併後実体の多数の投票権を持ち,SeaStar Medical,Inc.が合併後実体のすべての進行中の業務からなり,SeaStar Medical,Inc.が合併後実体の管理機関の多数からなり,SeaStar Medical,Inc.の上位管理層が合併後実体のすべての高級管理者からなるという事実に基づいている.したがって,会計目的のため,この業務合併はSeaStar Medicalと同等とみなされ,Inc.はLMAOの純資産に株式を発行し,資本再編を伴う。LMAOの純資産は歴史的コストで報告されています。商業権や無形資産は何も記録されていない。業務統合前の業務はSeaStar医療会社の業務である。
業務合併終了時にSeaStar Medical,Inc.が株主に支払う総対価は$である
終値時,SeaStar Medical,Inc.の未償還転換可能手形の1株当たり金額は$である
また閉幕時には
82
Seastar医療ホールディングス
連結財務諸表付記
(千単位で、株や1株当たりの金額は含まれていない)
転換されたVt入って入って
業務統合の一部として$
その他売掛金 |
|
|
|
$ |
|
|
前払い費用 |
|
|
|
|
|
|
費用を計算する |
|
|
|
|
( |
) |
公共株式証責任 |
|
|
|
|
( |
) |
私募配給には責任が必要です |
|
|
|
|
( |
) |
LMFAO支払手形 |
|
|
|
|
( |
) |
マクシム支払手形 |
|
|
|
|
( |
) |
|
|
|
|
$ |
( |
) |
次表は,取引終了直後に発行されたA類普通株の株式と,合併の転換可能な優先株変動表と2022年10月28日現在の株主損失に対する取引の影響をまとめたものである。
|
|
普通株 |
|
|
その他の内容 |
|
||||||
(千ドル) |
|
株 |
|
|
金額 |
|
|
実収資本 |
|
|||
|
|
|
|
|
|
|
|
|
|
|||
SPAC融資 |
|
|
|
|
$ |
|
|
$ |
( |
) |
||
公募株式証負債を持分に分類する |
|
|
— |
|
|
|
|
|
|
|
||
私募株式証債務を株式に再分類する |
|
|
— |
|
|
|
|
|
|
|
||
取引コスト |
|
|
— |
|
|
|
|
|
|
( |
) |
|
2022年10月28日の逆資本再編 |
|
|
|
|
$ |
|
|
$ |
|
|||
付記4.長期購入プロトコル
2022年10月,LMAO,SeaStar Medical,Inc.はVella Opportunity Fund SPV LLC−Series 4およびHB Strategy LLC(“FPA売り手”)と長期調達プロトコル(“FPA”)を確立し,これにより,業務合併前にFPA売り手が購入する
取引終了時に,LMAOがLMAO信託口座からVellaに支払う資金総額は#ドルであった
♪the the theFPA売り手は、回収株式(“終了株式”)の売却を自ら決定することができる。当社は売却終了株式から得られた金額が終了株式数にリセット価格(“リセット価格”)を乗じる権利がある。リセット価格は最初は1株当たり償還価格ですが、根拠は
83
Seastar医療ホールディングス
連結財務諸表付記
(千単位で、株や1株当たりの金額は含まれていない)
月に1回基数は(A)そのときのリセット価格,(B)$である
VWAP価格が$未満であれば
満期対価格は当社が現金または当社がA類普通株で発行した株式で支払い、1株発行価格は30の予定取引日の1日平均VWAP価格に基づく。FPA売り手は、販売されていない回収株式の数を会社に渡す。
2022年12月31日までの年間で
ASC 815デリバティブおよびヘッジによると、当社は、長期購入プロトコル内の長期オプション(I)が独立金融ツールであること、(Ii)デリバティブの定義に適合しないこと、(Iii)自社自身の株式にリンクすること、および(Iv)持分分類の要求に適合しないことを決定した。オプションの公正価値は、総合貸借対照表において資産または負債として長期オプションである前払い契約に計上される。当社は付記2で述べたように、成約時および2022年12月31日までの財務諸表内で長期オプションの公正価値計量を行います。当社は報告期間ごとに長期オプションの公正価値を再計測します。
長期オプション--前払い契約の初期価値は#ドルである
付記5.課税料金
2022年12月31日と2021年12月31日まで、支出には以下の額が含まれる
(千ドル) |
|
2022 |
|
|
2021 |
|
||
承諾料·株式信用限度額を計算する |
|
$ |
|
|
$ |
|
||
ボーナスを計算する |
|
|
|
|
|
|
||
応算利息 |
|
|
|
|
|
|
||
法律性を計算すべきである |
|
|
|
|
|
|
||
役員の報酬を計算する |
|
|
|
|
|
|
||
計画に応じて研究·開発する |
|
|
|
|
|
|
||
その他の措置を講じる |
|
|
|
|
|
|
||
費用総額を計算する |
|
$ |
|
|
$ |
|
||
注6.持分信用限度額
2022年8月、SeaStar Medical,Inc.,LMAOとTumim Stone Capital LLC(“Tumim”)は普通株購入協定を通じてTumimを最高$に売却する権利があることを規定する持分限度融資計画を達成した
84
Seastar医療ホールディングス
連結財務諸表付記
(千単位で、株や1株当たりの金額は含まれていない)
応策余剰$の費用
付記7.支払手形
12月31日の支払手形は以下の通り
(千ドル) |
|
2022 |
|
|
2021 |
|
||
LMFA支払手形 |
|
$ |
|
|
$ |
— |
|
|
LMFAO支払手形 |
|
|
|
|
|
— |
|
|
マクシム支払手形 |
|
|
|
|
|
— |
|
|
保険融資 |
|
|
|
|
|
— |
|
|
支払手形総額 |
|
$ |
|
|
$ |
— |
|
|
LMFA支払手形
2022年9月9日,SeaStar Medical,Inc.はLM Funding America,Inc.(“LMFA”)とクレジットプロトコル(“LMFAチケット”)を締結し,このプロトコルによりLMFAはSeaStar Medical,Inc.に最高$を提供することに同意した
2022年10月28日,SeaStar医療ホールディングスとLMFAはLMFAとSeaStar Medical,Inc.が2022年9月9日に締結した第1修正案信用協定を締結し,この合意により,(I)LMFAチケット下での融資の満期日を延長した
また,双方は2022年10月28日に担保合意を締結し,この合意により,SeaStar Medical Holding CorporationはLMFAに実質的にすべての資産および財産の保証権益を付与したが,ある例外を除いて,改訂されたLMFAチケットの担保とした。また,会社は2022年10月28日の保証を締結し,この担保により,SeaStar Medical Holding Corporationは無条件に保証し,LMFAにLMFAチケット項下の未償還元金を支払うことを承諾した。
2022年11月2日、会社は本チケットを追加しました。金額は#ドルです
LMFAO支払手形
当社は2022年10月28日、LMFAO保証人、LMAO保証人及び創設株式唯一の保有者(“保釣人”)を借入者とし、改訂及び重述された総合元票を締結し、元金総額を$とした
85
Seastar医療ホールディングス
連結財務諸表付記
(千単位で、株や1株当たりの金額は含まれていない)
LMFAO手形は前払いし,割増または罰金を取らない;及び(Iii)会社に使用を要求する
LMFAOチケットは違約イベントの影響を受け,LMFAOチケットの即時満期と支払いを招く可能性があり,利息は
マクシム支払手形
会社とMaximが2022年10月28日に署名した招聘書によると、会社はMaximに#ドル相当の金を支払い、その財務顧問としなければならない
Maxim Noteは慣用的な陳述と保証,および肯定と否定の契約を含む.Maxim手形は違約事件の影響を受け、これはMaxim手形の即時満期と支払いを招く可能性があり、利息は
保険融資
2022年10月、当社はある貸手と融資契約を締結し、保険証書の年間保険料の一部に資金を提供し、金額は#ドルである
86
Seastar医療ホールディングス
連結財務諸表付記
(千単位で、株や1株当たりの金額は含まれていない)
付記8.変換可能手形
ダウ·ジョーンズ指数
同社は陶氏従業員の年金計画信託基金(陶氏手形)に以下の金額の転換可能手形協定(千単位)を発行している
発行する. |
|
|
|
|
成熟性 |
|
日取り |
|
金額 |
|
|
日取り |
|
|
$ |
|
|
|||
|
|
|
|
|||
|
|
|
|
|||
|
|
|
|
|||
|
|
|
|
|||
|
|
|
|
|||
|
|
|
|
|||
|
|
$ |
|
|
|
|
未払い残高の利息は毎年8%の比率で積算される。発行されるたびに、変換機能の公正価値は、変換可能手形から分離され、付記2のような債務割引および派生負債報告として記載される。業務合併が発生した場合、元本加算利息は普通株に変換されます。
複合炭化物手形
同社は、合同炭化物従業員年金計画信託基金(連合炭化物手形)に、以下の金額の転換可能手形協定(千単位)を発行した
発行する. |
|
|
|
|
成熟性 |
|
日取り |
|
金額 |
|
|
日取り |
|
|
|
|
|
|
|
|
|
$ |
|
|
|||
|
|
|
|
|||
|
|
|
|
|||
|
|
|
|
|||
|
|
|
|
|||
|
|
|
|
|||
|
|
|
|
|||
|
|
$ |
|
|
|
|
未払い残高の利息は毎年8%の比率で積算される。発行されるたびに、変換機能の公正価値は、変換可能手形から分離され、付記2のような債務割引および派生負債報告として記載される。業務合併が発生した場合、元本加算利息は普通株に変換されます。
IBTノート
会社は2022年12月31日と2021年12月31日までの年間で、未払い領収書金額を#ドルに変換した
87
Seastar医療ホールディングス
連結財務諸表付記
(千単位で、株や1株当たりの金額は含まれていない)
投資家手形
当社は2022年12月31日および2021年12月31日までの年間で、投資家に交換可能手形を発行し、価格は$とする
上記発行時に記録された割引は、実際の利息法により交換手形の有効期間内の利息支出に償却される。2022年12月31日現在と2021年12月31日現在の債務割引は#ドル
2021年12月31日の変換可能手形および債務割引には、以下が含まれます
|
|
|
|
十二月三十一日 |
|
|
(千ドル) |
|
|
|
2021 |
|
|
ダウ·ジョーンズ指数 |
|
|
|
$ |
|
|
複合炭化物手形 |
|
|
|
|
|
|
IBTとデヴィッドはメモを取って |
|
|
|
|
|
|
投資家手形 |
|
|
|
|
|
|
未償却債務割引 |
|
|
|
|
( |
) |
|
|
|
|
|
|
|
比較的小さな電流部分 |
|
|
|
|
( |
) |
|
|
|
|
$ |
|
|
業務合併の一部として、会社はすべての元本が#ドルの転換可能な手形を変換した
以下に変換後のチケットを示す
(千ドル) |
|
|
|
|
|
|
ダウ·ジョーンズ指数 |
|
|
|
$ |
|
|
複合炭化物手形 |
|
|
|
|
|
|
IBTとデヴィッドはメモを取って |
|
|
|
|
|
|
投資家手形 |
|
|
|
|
|
|
|
|
|
|
$ |
|
|
注9.政府ローンと購買力平価ローン
政府ローン
2020年6月、SeaStar Medical,Inc.は#ドルの融資を受けた
2022年10月17日、会社は小企業管理局に全残高を前払いした#
88
Seastar医療ホールディングス
連結財務諸表付記
(千単位で、株や1株当たりの金額は含まれていない)
購買力平価ローン
2021年4月2日、会社は融資収益#ドルを受け取った
2020年4月、同社は#ドルの融資を受けた
注10.手令
業務合併に先立ち,SeaStar医療会社はSeaStar医療会社の優先株を購入する発行済株式証を有しており,これらの優先株は各種債務融資とともに発行されている。企業合併が発効した後
LMAO初公開の一部として,2021年1月25日の引受権証協定により,業務合併が発効する前にLMAOが発行される
2022年10月28日、当社は個人投資家の公衆株式(“PIPE”)協定を締結し、この合意に基づいて、PIPE投資家は共同で購入した
89
Seastar医療ホールディングス
連結財務諸表付記
(千単位で、株や1株当たりの金額は含まれていない)
同社は2022年12月31日と2021年12月31日に以下の未償還株式証明書を持っている
|
|
十二月三十一日 |
|
|
十二月三十一日 |
|
||
|
|
2022 |
|
|
2021 |
|
||
株主引受権証を公開する |
|
|
|
|
|
|
||
私募株式証明書 |
|
|
|
|
|
|
||
PIPE投資家株式証明書 |
|
|
|
|
|
|
||
Seastar株式証明書 |
|
|
|
|
|
|
||
|
|
|
|
|
|
|
||
注11.優先株、普通株、優先株に転換可能
SeaStar Medical,Inc.は2022年と2021年12月31日までの年間で
Seastar Medical,Inc.の転換可能優先株は対応する合併貸借対照表において一時株式に分類され、転換可能な優先株株主が投票権を持っているため、これはSeaStar Medical,Inc.制御以外のいくつかの事件を引き起こす可能性があり、それによってSeaStar Medical,Inc.は転換可能優先株を償還する義務がある。Seastar Medical,Inc.は転換可能な優先株の帳簿価値をそのような株それぞれの清算優先株に調整しておらず,これらのツールはまだ償還されていないため,SeaStar Medical,Inc.はこれらのツールが償還可能となる可能性は低いと考えている。
業務合併後,当社は発行する権利がある
普通株
会社定款(以下、“定款”と略す)は、普通株式の権利、権力、優先権、特権について以下のように規定する。
投票権
法律に規定または任意の系列優先株のいずれかの指定証明書が別途規定されているほか、普通株式保有者は、当社取締役および他のすべての株主が行動する必要がある事項を選挙する投票権を持っている
配当をする
いかなる優先株発行済み株式所有者が憲章によって享受する権利(ある場合)の規定の下で、普通株式所有者は取締役会が時々適宜発表した配当金(ありあれば)を受け取る権利があり、このような配当金は取締役会が適宜決定して合法的に派遣可能な資金から振り出す権利がある。
清盤·解散·清盤
会社が自発的または非自発的清算、解散、資産分配または清算が発生した場合、普通株式保有者は同等額のすべてを獲得する権利がある
90
Seastar医療ホールディングス
連結財務諸表付記
(千単位で、株や1株当たりの金額は含まれていない)
優先株保有者の権利が満たされ、会社の債務が支払または支出された後、会社は株主に割り当てられた任意のタイプの資産に使用することができる。
優先購入権またはその他の権利
当社の普通株式に適用される優先購入権や債務超過基金条項は存在しません。
優先株
憲章は、優先株が時々1つ以上のシリーズで発行されることができると規定している。当社の取締役会は、各シリーズの株式に適用される投票権(例えば、ある)、指定、権力、特典、相対、参加、選択またはその他の特別な権利およびその任意の資格、制限および制限を決定することを許可されています。私たちは
注12.株ベースの報酬報酬
持分インセンティブ計画--株式オプション
会社取締役会は2019年2月25日にSeaStar Medical,Inc.の2019年株式激励計画(“株式激励計画”と略称する)を採択し、その肝心な従業員と非従業員サービスプロバイダに長期激励を提供した。2022年と2021年12月31日までに
取引終了時には、株式インセンティブ計画が終了し、当社はこの計画に基づいて他の報酬を付与することはありません。しかし、株式インセンティブ計画下の未償還報酬は仮定され、業務合併に関連し続けるだろう。
SeaStar Medical,Inc.普通株またはSeaStar Medical,Inc.優先株のそれぞれのSeaStar医療会社オプション(“SeaStarオプション”)を購入し,企業合併直前に発行されていないものと未行使のものを,普通株を購入するオプションに変換し,額面は$とする
会社取締役会は、株主がSeaStar Medical,Inc.の2022年総合インセンティブ計画(株式インセンティブ計画と略称する)を承認し、そのキー従業員と非従業員サービスプロバイダに長期インセンティブを提供することを承認した
91
Seastar医療ホールディングス
連結財務諸表付記
(千単位で、株や1株当たりの金額は含まれていない)
2022年12月31日と2021年12月31日までの年間オプション活動は以下の通り
|
|
|
|
|
|
|
|
|
|
|
重みをつける |
|
||||
|
|
|
|
|
重みをつける |
|
|
|
|
|
平均値 |
|
||||
|
|
|
|
|
平均値 |
|
|
合計する |
|
|
残り |
|
||||
|
|
|
|
|
トレーニングをする |
|
|
固有の |
|
|
契約書 |
|
||||
(千ドル) |
|
オプション |
|
|
値段 |
|
|
価値がある |
|
|
寿命(年) |
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
2020年12月31日現在の未返済債務 |
|
|
|
|
$ |
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
授与する |
|
|
|
|
$ |
|
|
|
|
|
|
|
||||
没収される |
|
|
( |
) |
|
$ |
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
2021年12月31日現在の未返済債務 |
|
|
|
|
$ |
|
|
$ |
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
合併転換前に没収される |
|
|
( |
) |
|
$ |
|
|
|
|
|
|
|
|||
合併変換で発行された追加オプション |
|
|
|
|
$ |
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
2022年12月31日現在の未返済債務 |
|
|
|
|
$ |
|
|
$ |
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
2022年12月31日までに行使可能なオプション |
|
|
|
|
$ |
|
|
$ |
|
|
|
|
||||
同社は$を確認した
総合業務報告書に記載されているオプションの株式別補償費用は以下のとおりである
(千ドル) |
|
2022 |
|
|
2021 |
|
||
研究開発 |
|
$ |
|
|
$ |
|
||
一般と行政 |
|
|
|
|
|
|
||
合計する |
|
$ |
|
|
$ |
|
||
持分インセンティブ計画--制限株式単位
2022年4月、取締役会は従業員と取締役会メンバー制限株式単位(RSU)を付与し、当該単位により、保有者は合計を獲得する権利がある
業務合併直前に返済されなかったSeaStar Medical,Inc.RSUごとにRSUに変換し,普通株,額面価値$を得る
92
Seastar医療ホールディングス
連結財務諸表付記
(千単位で、株や1株当たりの金額は含まれていない)
2022年12月31日までの年次RSU活動は以下のとおりである
2021年12月31日現在の未返済債務 |
|
|
|
|
|
|
|
|
|
|
|
|
|
授与する |
|
|
|
|
|
|
合併転換前に没収される |
|
|
|
|
( |
) |
マージ変換で発行される追加RSU |
|
|
|
|
|
|
|
|
|
|
|
|
|
2022年12月31日現在の未返済債務 |
|
|
|
|
|
|
|
|
|
|
|
|
|
2022年12月31日から帰属する |
|
|
|
|
|
|
|
|
|
|
|
|
|
2022年12月31日までに買い戻しが必要な株式 |
|
|
|
|
|
|
同社は$を確認した
連結業務報告書に含まれるRSUの在庫別補償費用は以下のとおりである
(千ドル) |
|
2022 |
|
|
2021 |
|
||
研究開発 |
|
$ |
|
|
$ |
|
||
一般と行政 |
|
|
|
|
|
|
||
合計する |
|
$ |
|
|
$ |
|
||
付記13.支払の引受及び又は事項
許可と流通協定
2022年12月27日、当社はある流通業者と許可及び流通協定(“許可協定”)を締結し、この流通業者を米国での普及、宣伝、マーケティング、流通及び販売選択性Cytophertic装置(“SCD”)の独占流通業者に指定した。会社は前金#ドルを受け取った
賃貸契約
同社は共有オフィススペース会員契約の一部であり、いつでもキャンセルすることができる。家賃費用は$
訴訟を起こす
クレーム、評価、訴訟、罰金、罰金および他のソースによって発生したまたは損失のある負債は、負債が発生し、金額が合理的に推定できる可能性が高い場合に記録される。当社は通常業務の過程で起こる法的訴訟に時々巻き込まれる可能性があります。当社は2022年12月31日及び2021年12月31日までに年度に重大な法的訴訟はなく、現在も重大な法律訴訟の保留や脅かされているものはありません。
93
Seastar医療ホールディングス
連結財務諸表付記
(千単位で、株や1株当たりの金額は含まれていない)
注14.所得税
同社は$を記録した
会社所得税準備金の有効所得税税率は連邦法定税率と異なり、以下のようになる
|
|
2022 |
|
2021 |
法定税率で徴収される連邦税 |
|
|
||
州所得税 |
|
|
||
転換可能手形の利子 |
|
( |
|
|
転換可能手形由来負債の公正価値変動 |
|
( |
|
|
他にも |
|
|
( |
|
評価免除額を変更する |
|
( |
|
( |
総有効所得税率 |
|
( |
|
( |
連邦と州所得税の繰延税金資産の重要な構成要素は以下の通りである
|
|
十二月三十一日 |
|
|
十二月三十一日 |
|
||
(千ドル) |
|
2022 |
|
|
2021 |
|
||
繰延税金資産: |
|
|
|
|
|
|
||
純営業損失 |
|
$ |
|
|
$ |
|
||
長期オプション-前払い長期契約、純額 |
|
|
|
|
|
|
||
融資手数料と発起料 |
|
|
|
|
|
|
||
補償すべきである |
|
|
|
|
|
|
||
株に基づく報酬 |
|
|
|
|
|
|
||
第174節研究と開発資本化 |
|
|
|
|
|
|
||
税金控除 |
|
|
|
|
|
|
||
繰延税金資産総額 |
|
|
|
|
|
|
||
推定免税額 |
|
|
( |
) |
|
|
( |
) |
繰延税項目純資産 |
|
$ |
|
|
$ |
|
||
米国公認会計原則によると、会社の一部または全部の繰延税金資産が現金化できない可能性が高い場合、推定準備金を提供しなければならない。同社がその繰延税金資産収益を実現する能力は、将来の課税収入の発生に依存する。将来の利益業務および課税収入の不確実性のため、当社はその繰延税項目の純資産計上全額推定について準備しています。2022年と2021年12月31日終了年度の推定手当純増加額は#ドル
同社の連邦純営業損失は2022年12月31日と2021年12月31日現在$に転換している
その会社は連邦エネルギー信用繰越$を持っている
米国国税法(IRC)第382条及び383条によると、会社の所有権が累計変動を超える場合
94
Seastar医療ホールディングス
連結財務諸表付記
(千単位で、株や1株当たりの金額は含まれていない)
未来.未来今後数年間の課税所得額と所得税負債は大きく制限されたり廃止される可能性がある。また,IRC第382条に示す所有権変更を実現した後,このようなNOLや研究税収控除に関する繰延税金資産が大幅に減少する可能性がある。
不確定税収割引
同社は“可能性が高い”という基準を採用して所得税の所得税優遇が確定していないことを確認し、所得税優遇の尺度を確立している。その会社は所有している
付記15.1株当たり純損失
普通株1株あたりの基本純損失の計算方法は,純損失を当期発行普通株の加重平均で割ったものであり,潜在的な希釈証券は考慮しない。1株当たり純損失の算出方法は,純損失を当期発行普通株と潜在希薄化証券の加重平均で割ったものである。1株当たり純損失を計算する際には、転換可能な優先株と普通株オプションは潜在的な希薄化証券とみなされる。転換可能優先株は参加証券とされているため、証券参加に必要な2段階法に基づいて1株基本と純損失を計上している。当社の参加証券は当社の損失を分担する契約義務を持っていません。したがって、純損失は完全に普通株式株主に起因する。会社は全期間の純損失を報告しているため,希釈後の普通株1株当たり純損失はこれらの時期の普通株1株当たり純損失とほぼ同じである。
以下の希釈可能な証券の加重平均流通株は、これらの株を計上することが逆希釈されるので、本報告に記載されている間に普通株株主が1株当たり純損失を希釈すべき計算範囲内に含まれない
|
|
2022 |
|
|
2021 |
|
||
株主引受権証を公開する |
|
|
|
|
|
|
||
私募株式証明書 |
|
|
|
|
|
|
||
PIPE投資家株式証明書 |
|
|
|
|
|
|
||
Seastar株式証明書 |
|
|
|
|
|
|
||
普通株購入オプション |
|
|
|
|
|
|
||
制限株式単位 |
|
|
|
|
|
|
||
合計する |
|
|
|
|
|
|
||
1株当たり純損失は業務合併及び関連取引関連株式で計算され、株式は2021年1月1日から発行されたと仮定する
95
Seastar医療ホールディングス
連結財務諸表付記
(千単位で、株や1株当たりの金額は含まれていない)
接続する列記された期間を通して,業務との統合の表現が優れていた.
12月31日までの年度: |
|
2022 |
|
|
2021 |
|
||
純損失 |
|
$ |
( |
) |
|
$ |
( |
) |
加重平均流通株-基本 |
|
|
|
|
|
|
||
1株当たりほぼ純損失 |
|
$ |
( |
) |
|
$ |
( |
) |
加重平均流通株-希釈 |
|
|
|
|
|
|
||
薄めて1株当たり純損失 |
|
$ |
( |
) |
|
$ |
( |
) |
注16.後続イベント
2023年1月3日、会社は前金を受け取った$
2023年3月13日、当社は契約を締結しました
2023年3月15日、当社はある機関投資家と証券購入協定を締結し、これにより、当社は一連の4種類の高級無担保転換可能手形を発行し、元金総額は最高$に達する
2023年3月15日,会社はLMFAチケット,LMFAOチケット,Maximチケットを修正し,期限を延長した
2023年3月,VWAPトリガイベントが発生し,長期購入プロトコルはFPA売手が指定した日に満了する可能性があり,FPA売手は適宜決定することができる.これらの総合財務諸表が発表された時点で,FPA売手は長期購入プロトコルの満期日を具体的に説明していない.
2023年1月1日に2023年3月30日同社は#ドルを支払いました
96
項目9.会計·財務開示面の変更と会計士との相違.
ない。
第9条。制御とプログラムです
本プロジェクト9 Aには、本年度報告書添付ファイル31.1および31.2に記載されている“取引所法”第13 a-14条に記載されている我々の最高経営責任者および一時的な財務官の証明に言及されている制御および制御評価の情報が含まれている。
情報開示制御とプログラムの評価
我々の経営陣は、我々の最高経営者及び臨時最高経営責任者を含め、2022年12月31日までの開示制御及び手続(1934年証券取引法(改正“取引法”)第13 a−15(E)条に規定されている)の設計及び運用の有効性を評価し、この評価に基づいて、以下に述べる財務報告内部統制の重大な弱点により、2022年12月31日に我々の開示制御及び手続が無効であると結論した。
規則13 a~15(E)によれば、“開示制御およびプログラム”という用語は、発行者が取引所法案の提出または提出された報告書に基づいて開示を要求する情報が、米国証券取引委員会規則および表によって指定された期間内に記録、処理、集約および報告されることを保証するための発行者の制御および他のプログラムを意味する。開示制御およびプログラムは、発行者が取引所法案に従って提出または提出された報告書に開示を要求する情報が蓄積され、発行者管理者(そのCEOおよび最高財務官を含む)または同様の機能を果たす者に伝達されることを保証するための制御および手順を含むが、必要な開示に関する決定をタイムリーに行うために、これらに限定されない。
経営陣財務報告内部統制年次報告書
経営陣は、財務報告の適切な内部制御の設計、実施、維持を担当し、この用語は、“取引法”ルール13 a~15(F)および15 d~15(F)に定義されている。当社の経営陣はこのような財務報告の内部統制を設計し、あるいはこのような財務報告の内部統制を著者らの監督の下で設計させ、公認会計原則に基づいて財務報告の信頼性と対外財務諸表の作成に合理的な保証を提供する。財務報告書に対する内部統制は、どんなによく設計されていても、内在的な限界がある。したがって,有効と判定されたシステムであっても,財務諸表の作成や列報に合理的な保証を提供することしかできない.また、条件の変化により、財務報告内部統制の有効性は時間の経過とともに変化する可能性がある。
本報告書の他の部分で述べたように、私たちは2022年10月28日に業務統合を完了した。企業合併前にSeaStar Medical,Inc.は民間会社であったため,その制御は取引法ルール13 a−15および15 d−15による設計やメンテナンスを必要としなかった。会社業務後に合併した財務報告の内部統制を設計·実施するためには、管理職やその他の人員が多くの時間と資源を投入する必要があり、継続する必要がある。そのため、私たちの財務報告の内部統制実施と評価フレームワークの設計と持続的な発展は初歩的な段階にある。そのため、経営陣は、不合理な努力や費用を生じることなく、2022年12月31日までの財務報告内部統制を評価することができない。したがって、財務報告の内部統制に関する経営陣のS-Kコンプライアンスおよび開示説明215.02節の内部統制に関する報告は含まれていません。
97
重大な弱点を特定する
本年度報告書に含まれる総合財務諸表を作成する過程で、当社は2022年12月31日までの財務報告内部統制に重大な欠陥があることを発見し、その財務会計と報告制御の設計と操作上の欠陥と関連している。重大な欠陥とは、財務報告の内部統制に欠陥或いは欠陥の組み合わせが存在し、私たちの年度或いは中期財務諸表の重大なミス報告が合理的な可能性があり、適時に防止或いは発見できないようにすることである。具体的には、会社は 財務報告書の内部統制には欠陥があり、実質的に弱い程度まで上昇することが決定された。同社は、最終結論までに複雑な会計取引についてさらなる研究と内部対話を行うために、近いうちに人手を増やすことを決定した。我々が必要な内部制御枠組みを策定するにつれ,会社は全体の内部制御環境を検討し続ける予定である.
財務報告の内部統制の変化
2022年12月31日までの間、取引法ルール13 a-15(F)および15 d-15(F)で定義されているように、財務報告の内部統制に大きな影響を与えなかったか、または合理的に財務報告の内部統制に大きな影響を与える可能性のある変化は発生しなかった。
プロジェクト9 B。その他の情報.
ない。
プロジェクト9 Cです。検査を妨害する外国司法管轄区域を開示する。
適用されません。
98
第三部
プロジェクト10.取締役、上級管理者、および企業管理.
本プロジェクトに要求される情報は、会社が第14 A条に規定する最終委託書を参考にして組み込まれ、当該依頼書は、会社が2022年12月31日までの財政年度終了後120日以内に証券取引委員会に提出される。
私たちは私たちの仕事に関連するすべての高級管理者、役員、従業員に適用される道徳的基準を採択した。私たちの道徳基準は全文私たちのサイトの投資家関係ページに掲示されています。サイトは:https://investors.seastarMedical.com/ガバナンス/ガバナンス-ドキュメント/default.aspxです。
我々は、我々のウェブサイト上で上記で指定されたインターネットアドレスおよび位置にこのような情報を掲示することによって、本道徳規則条項の改訂または放棄に関するForm 8-K第5.05項の任意の開示要件を満たす予定である。
プロジェクト11.役員報酬.
本プロジェクトに要求される情報は、会社が第14 A条に規定する最終委託書を参照するように組み込まれ、当該依頼書は、会社が2022年12月31日までの財政年度終了後120日以内に証券取引委員会に提出される。
プロジェクト12.利益を得たすべての人の保証所有権a経営陣および関連株主について。
本プロジェクトに要求される情報は、会社が第14 A条に規定する最終委託書を参照するように組み込まれ、当該依頼書は、会社が2022年12月31日までの財政年度終了後120日以内に証券取引委員会に提出される。
項目13.特定の関係および関連取引、および取締役独立性.
本プロジェクトに要求される情報は、会社が第14 A条に規定する最終委託書を参照するように組み込まれ、当該依頼書は、会社が2022年12月31日までの財政年度終了後120日以内に証券取引委員会に提出される。
プロジェクト14.主な会計費用とサービス.
本プロジェクトに要求される情報は、会社が第14 A条に規定する最終委託書を参照するように組み込まれ、当該依頼書は、会社が2022年12月31日までの財政年度終了後120日以内に証券取引委員会に提出される。
99
第4部
項目15.物証、財務諸表付表.
(1)本報告書に記載されている財務諸表一覧表は、本年度報告F-1ページの総合財務諸表インデックスを参照し、本項目に参照して組み込まれている。
(2)財務諸表添付表は必要でないか適用されないか、または資料が総合財務諸表またはその付記に含まれているため、これらの付表は省略されている。
(3)展示品
100
展示品索引
|
|
|
展示品 |
|
説明する |
|
|
|
2.1 |
|
合意と合併計画は,期日は2022年4月21日であり,LMF Acquisition Opportunities,Inc.(LMAO),LMF Merge Sub,Inc.とSeaStar Medical,Inc.(添付ファイル2.1を参照して合併したものであり,登録者が2022年4月26日に提出した8−K表)が署名されている。 |
3.1 |
|
SeaStar医療ホールディングスが3回目に改訂·再登録した登録証明書は、2022年10月28日にデラウェア州国務長官に提出された(添付ファイル3.1を参照して登録者が2022年11月4日に提出したタブ8-K)。 |
3.2 |
|
SeaStar医療ホールディングスの定款を改正·再改訂した(登録者が2022年11月4日に提出した表格8−Kは添付ファイル3.2を参照して編入)。 |
4.1 |
|
普通株式証明書サンプル(登録者によって2022年11月4日に提出された表格8−Kは、添付ファイル4.1を参照して組み込まれる)。 |
4.2 |
|
授権書サンプル(添付ファイル4.3に添付)。 |
4.3 |
|
LMAOと大陸株式譲渡と信託会社が2021年1月25日に署名した引受権証協定(登録者が2021年1月28日に提出した8-K表は、添付ファイル4.1を参照して合併する)。 |
4.4 |
|
普通株式引受権証表(登録者が2023年3月16日に提出した添付ファイル4.1から表格8-Kに結合)。 |
4.5 |
|
証券説明(登録者が2023年1月20日に提出した表S−1に“証券説明”の欄に含まれる)。 |
10.1 |
|
改正および再署名された登録権協定は,2022年4月21日であり,LMAO,SeaStar Medical,Inc.とSeaStar Medical,Inc.のある株主間の合意(登録者が2022年4月26日に提出した表格8−Kが添付ファイル10.1を参照して統合されたもの)である。 |
10.2 |
|
投資管理信託協定は、期日が2021年1月25日であり、LMAOと大陸株式譲渡及び信託会社により受託者として達成される(登録者が2021年1月28日に提出した表格8−Kは添付ファイル10.2を参照して登録成立)。 |
10.3 |
|
登録権協定は,2021年1月25日に,LMF Acquisition Opportunities,Inc.,SeaStar Medical,Inc.およびSeaStar Medical,Inc.のある株主によって署名された(登録者が2021年1月28日に提出した8−K表に添付ファイル10.3が引用されている)。 |
10.4 |
|
Seastar Medical Holding Corporation 2022総合インセンティブ計画(登録者が2022年5月16日に提出した表S−4の添付ファイルDを参照して組み込まれる)。 |
10.5 |
|
Seastar Medical Holding Corporation 2022年従業員株式購入計画(登録者が2022年5月16日に提出したS-4表添付ファイルEを参考に統合した)。 |
10.6 |
|
本票は,日付は2022年3月1日であり,LMFAOスポンサー有限責任会社とLMAOとの間の本票である(LMAOは2022年5月19日に米国証券取引委員会の10-Q表に提出される前に添付ファイル10.1として提出される). |
10.7 |
|
修正·再印刷された本チケットは,期日は2022年7月28日であり,LMAOからLMFAOスポンサー有限責任会社に発行される(LMAOは2022年8月1日に米国証券取引委員会に提出され,添付ファイル10.1からForm 8-Kとして提出される). |
10.8 |
|
LMAO、SeaStar Medical,Inc.とある投資家が2022年8月23日に署名した引受契約表(登録者が2022年8月24日に提出したS-4/A表は添付ファイル10.29を参照して統合された)。 |
10.9 |
|
Tumim Stone Capital LLC,LMAOとSeaStar Medical,Inc.の間の普通株購入契約は,2022年8月23日である(登録者が2022年8月24日に提出したS−4/A表は添付ファイル10.30を参照して合併する)。 |
10.10 |
|
Tumim Stone Capital LLC,LMAOとSeaStar Medical,Inc.の間の登録権協定は,2022年8月23日である(登録者が2022年8月24日に提出したS−4/A表は引用添付ファイル10.31により統合されている)。 |
10.11 |
|
SeaStar Medical,Inc.とLM Funding America,Inc.との間の信用協定は,2022年9月9日(登録者が2022年9月13日に提出されたS−4/A表に添付ファイル10.34を参照)である。 |
10.12 |
|
改正及び再署名された登録権協定及び禁売期間免除の第1号改正案は、LMAOとその署名ページに記載されている投資家との間で2022年10月25日に提出される(登録者を参照して2022年11月4日に提出された表8−Kは、添付ファイル10.12を参照して編入される)。 |
101
10.13 |
|
LMAO,SeaStar Medical,Inc.とTumim Stone Capital LLCとの間の手紙プロトコルは,2022年10月28日である(登録者が2022年11月4日に提出した表格8−Kは添付ファイル10.13を参照して統合されている)。 |
10.14 |
|
取締役指名協定は,期日は2022年10月28日であり,LMFAOスポンサーLLCとLMAOの間で署名されている(登録者が2022年11月4日に提出した表格8−Kは添付ファイル10.14を参照して合併した)。 |
10.15 |
|
SeaStar Medical,Inc.とLM Funding America,Inc.の間で2022年10月28日に署名された信用協定第1修正案(登録者が2022年11月4日に提出した表格8−Kは添付ファイル10.15を参照して統合された)。 |
10.16 |
|
修正·再予約された本票は,期日は2022年10月28日であり,SeaStar Medical,Inc.からLM Funding America,Inc.に発行される(添付ファイル10.16を参照して登録者が2022年11月4日に提出された8−K表を参照することにより)。 |
10.17 |
|
セキュリティプロトコルは,期日は2022年10月28日であり,SeaStar Medical,Inc.とSeaStar Medical Holding CorporationからLM Funding America,Inc.に発行されている(登録者が2022年11月4日に提出した8−K表に添付ファイル10.17が引用されている)。 |
10.18 |
|
期日は2022年10月28日の保証であり,SeaStar Medical Holding CorporationからLM Funding America,Inc.に発行される(登録者が2022年11月4日に提出した表格8−Kは添付ファイル10.18を参照して統合された)。 |
10.19 |
|
SeaStar Medical Holding CorporationからLMFAOスポンサーLLCに発行された日付は,2022年10月28日の改訂·再発行された合併本票である(登録者が2022年11月4日に提出した表格8−Kは添付ファイル10.19を参照して合併した)。 |
10.20 |
|
セキュリティプロトコルは,2022年10月28日にSeaStar Medical,Inc.とSeaStar Medical Holding CorporationによってLMFAOスポンサーLLCに発表された(登録者が2022年11月4日に提出したテーブル8−Kは添付ファイル10.20を参照して統合された)。 |
10.21 |
|
保証は,期日は2022年10月28日であり,SeaStar Medical,Inc.がLMFAOスポンサーLLC(引用登録者により2022年11月4日に提出された添付ファイル10.21をForm 8−Kに統合)に発行される。 |
10.22 |
|
本票は,期日は2022年10月28日であり,SeaStar Medical Holding CorporationからMaxim Group LLCに発行された(登録者が2022年11月4日に提出した8−K表は添付ファイル10.22を参照して合併した)。 |
10.23 |
|
債権者間合意は,期日は2022年10月28日であり,Maxim Group LLC,LM Funding America,Inc.,LMFAOスポンサー,LLC,SeaStar Medical,Inc.とSeaStar Medical Holding Corporationが署名された(添付ファイル10.23を参照して合併することにより,会社が2022年11月4日に登録者に提出する8-K表を形成する). |
10.24 |
|
前払い取引確認は,期日は2022年10月26日であり,LMF Acquisition Opportunities,Inc.,SeaStar Medical,Inc.とHB Strategy LLC(登録者が2022年10月27日に提出した表10.1からForm 8−Kを参照して合併したもの)である。 |
10.25 |
|
前払い取引確認は,期日は2022年10月17日であり,LMF Acquisition Opportunities,Inc.,SeaStar Medical,Inc.とVella Opportunity Fund SPV LLC−Series 4(登録者が2022年10月17日に提出した表10.1からForm 8−Kを参照して統合されている)。 |
10.26 |
|
Tumim Stone Capital,LLC,SeaStar Medical,Inc.とSeaStar Medical Holding Corporationとの間の普通株購入協定修正案1は,2022年11月9日である(登録者が2022年11月10日に提出した8−K表は添付ファイル10.1参照により合併)。 |
10.27 |
|
登録権協定第1号改正案は,期日は2022年11月9日であり,Tumim Stone Capital LLC,SeaStar Medical,Inc.とSeaStar Medical Holding Corporationの間で署名されている(登録者が2022年11月10日に提出した表格8−Kは添付ファイル10.2を参照して統合されている)。 |
10.28 |
|
SeaStar Medical Holding Corporationと3 i,LPの間の証券購入契約は,2023年3月15日(登録者が2023年3月16日に提出された表格8−Kが添付ファイル10.1を参照することにより登録成立)である。 |
10.29 |
|
登録権協定は,期日は2023年3月15日であり,SeaStar Medical Holding Corporationと3 i,LPが署名した(登録者が2023年3月16日に提出した表格8−Kは添付ファイル10.2を参照して統合された)。 |
10.30 |
|
高度な無担保変換可能な手形表(登録者が2023年3月16日に提出した表格8−Kは、添付ファイル10.3を参照して組み込まれる)。 |
21.1 |
|
子会社リスト(登録者が2022年11月4日に提出した表21.1~表格8-Kを引用して合併した)。 |
23.1** |
|
海星医療ホールディングス有限会社独立公認会計士事務所同意書 |
102
24.1** |
|
授権書(本文書の署名ページに含まれる)。 |
31.1** |
|
2002年のサバンズ·オキシリー法第302節で可決された1934年の証券取引法第13 a−14(A)及び15 d−14(A)条に基づいて発行された首席執行幹事証明書。 |
31.2** |
|
2002年サバンズ−オキシリー法第302節で可決された1934年証券取引法第13 a−14(A)及び15 d−14(A)条に基づいて首席財務幹事が認証された。 |
32.1** |
|
2002年にサバンズ·オクスリ法案第906条で可決された“米国法典”第18編1350条に規定されている最高経営責任者証明書。 |
32.2** |
|
2002年の“サバンズ-オックススリー法案”906節で採択された“米国法典”第18編1350条による首席財務官の認証。 |
101.INS |
|
連結されたXBRLインスタンス文書−インスタンス文書は、XBRLタグがイントラネットXBRL文書に埋め込まれているので、相互作用データファイルには表示されない。 |
101.書院 |
|
イントラネットXBRL分類拡張アーキテクチャ文書 |
101.カール |
|
インラインXBRL分類拡張計算リンクライブラリ文書 |
101.def |
|
インラインXBRL分類拡張Linkbase文書を定義する |
101.介護会 |
|
XBRL分類拡張ラベルLinkbase文書を連結する |
101.Pre |
|
インラインXBRL分類拡張プレゼンテーションLinkbaseドキュメント |
104 |
|
表紙インタラクションデータファイル(イントラネットXBRL文書に埋め込む) |
+管理契約または補償計画またはスケジュールを示します。
S-K規則601(B)(2)項により,本プロトコルの付表と証拠物は省略されている.任意の漏れたスケジュールおよび/または展示品のコピーは、要求に応じて米国証券取引委員会に提供される。
**関数のアーカイブ
項目16.表格10-Kの概要.
ない。
103
サイン
1934年に改正された証券取引法の要求に基づいて、登録者は正式に許可された次の署名者が代表して本報告に署名することを正式に手配した.
|
|
Seastar医療ホールディングス |
|
|
|
|
|
日付:2023年3月30日 |
|
差出人: |
/s/エリックSlorff |
|
|
|
エリック·スクロフ |
|
|
|
最高経営責任者 (首席行政主任) |
|
|
|
|
日付:2023年3月30日 |
|
差出人: |
/s/Caryl Baron |
|
|
|
カレル·バロン |
|
|
|
臨時首席財務官 (首席財務会計官) |
授権依頼書
このような陳述により、以下の署名者の各々が、Eric Slorff彼または彼女の真の合法的な事実受権者および代理人を構成および任命し、完全な代替および撤回の権力を有し、彼または彼女の名義、場所および代替彼または彼女の任意およびすべての身分で、本テーブル10-Kの本年度報告の任意またはすべての修正を任意およびすべての身分で署名し、すべての証拠物およびそれに関連する他の文書と共に証券取引委員会に提出し、その事実上の債権者および代理人に行われ、実行されなければならない各項目およびすべてのことを完全かつ事柄としての完全な権力および許可を付与することを知っていることを知っている。完全に彼または彼女本人が可能であるか、または自ら行うことができるすべての意図および目的のために、上述した事実代理人および代理人または彼または彼女の1人または複数の代理人が、本条例によるすべてのことを合法的に行うことができるか、またはもたらすことができることを承認および確認する。
本報告書は、改正された1933年の証券法の要求に基づき、次の者によって指定された身分及び日付で次のように署名された。
|
|
|
|
|
名前.名前 |
|
タイトル |
|
日取り |
|
|
|
||
/s/エリックSlorff エリック·スクロフ |
|
取締役CEO兼最高経営責任者 (首席行政主任) |
|
2023年3月30日 |
|
|
|
||
/s/Caryl Baron カレル·バロン |
|
臨時首席財務官 (首席財務会計官) |
|
2023年3月30日 |
|
|
|
||
/s/リック·バーネット リック·バネット |
|
取締役会議長 |
|
2023年3月30日 |
|
|
|
||
/s/Kenneth Van Heel ケネス·ヴァン·ヒル |
|
役員.取締役 |
|
2023年3月30日 |
|
|
|
||
/s/アンドレース·ロボ アンドレース·ロボ |
|
役員.取締役 |
|
2023年3月30日 |
|
|
|
||
/s/エレン·コリンズ エレン·コリンズ |
|
役員.取締役 |
|
2023年3月30日 |
|
|
|
||
/s/ブルース·ロジャース ブルース·ロジャース |
|
役員.取締役 |
|
2023年3月30日 |
|
|
|
||
/s/リチャード·ラッセル リチャード·ラッセル |
|
役員.取締役 |
|
2023年3月30日 |
104