LEGN-2022123120220001801198会計年度誤りE900018011982022-01-012022-12-310001801198Dei:ビジネス連絡先のメンバー2022-01-012022-12-3100018011982022-12-31Xbrli:共有ISO 4217:ドル00018011982021-01-012021-12-3100018011982020-01-012020-12-31ISO 4217:ドルXbrli:共有00018011982021-12-310001801198IFRS-Full:IssuedCapitalMembers2019-12-310001801198IFRS-Full:SharePremiumMembers2019-12-310001801198IFRS-FULL:共有ベースの予約支払いメンバー2019-12-310001801198IFRS-FULL:Reserve OfExchangeDifferencesOnTranslationMember2019-12-310001801198IFRS-Full:RetainedEarningsMembers2019-12-3100018011982019-12-310001801198IFRS-Full:RetainedEarningsMembers2020-01-012020-12-310001801198IFRS-FULL:Reserve OfExchangeDifferencesOnTranslationMember2020-01-012020-12-310001801198IFRS-Full:IssuedCapitalMembers2020-01-012020-12-310001801198IFRS-Full:SharePremiumMembers2020-01-012020-12-310001801198IFRS-Full:IssuedCapitalMembersLEGN:InitialPublicOfferingMember2020-01-012020-12-310001801198IFRS-Full:SharePremiumMembersLEGN:InitialPublicOfferingMember2020-01-012020-12-310001801198LEGN:InitialPublicOfferingMember2020-01-012020-12-310001801198IFRS-Full:SharePremiumMembersLEGN:PrivatePlacementByGenscriptMember2020-01-012020-12-310001801198LEGN:PrivatePlacementByGenscriptMember2020-01-012020-12-310001801198IFRS-FULL:共有ベースの予約支払いメンバー2020-01-012020-12-310001801198IFRS-Full:IssuedCapitalMembers2020-12-310001801198IFRS-Full:SharePremiumMembers2020-12-310001801198IFRS-FULL:共有ベースの予約支払いメンバー2020-12-310001801198IFRS-FULL:Reserve OfExchangeDifferencesOnTranslationMember2020-12-310001801198IFRS-Full:RetainedEarningsMembers2020-12-3100018011982020-12-310001801198IFRS-Full:RetainedEarningsMembers2021-01-012021-12-310001801198IFRS-FULL:Reserve OfExchangeDifferencesOnTranslationMember2021-01-012021-12-310001801198IFRS-Full:IssuedCapitalMembers2021-01-012021-12-310001801198IFRS-Full:SharePremiumMembers2021-01-012021-12-310001801198IFRS-Full:IssuedCapitalMembersLEGN:FollowOnPublicOfferingMember2021-01-012021-12-310001801198IFRS-Full:SharePremiumMembersLEGN:FollowOnPublicOfferingMember2021-01-012021-12-310001801198LEGN:FollowOnPublicOfferingMember2021-01-012021-12-310001801198IFRS-FULL:共有ベースの予約支払いメンバー2021-01-012021-12-310001801198IFRS-Full:IssuedCapitalMembers2021-12-310001801198IFRS-Full:SharePremiumMembers2021-12-310001801198IFRS-FULL:共有ベースの予約支払いメンバー2021-12-310001801198IFRS-FULL:Reserve OfExchangeDifferencesOnTranslationMember2021-12-310001801198IFRS-Full:RetainedEarningsMembers2021-12-310001801198IFRS-Full:RetainedEarningsMembers2022-01-012022-12-310001801198IFRS-FULL:Reserve OfExchangeDifferencesOnTranslationMember2022-01-012022-12-310001801198IFRS-Full:IssuedCapitalMembersLEGN:FollowOnPublicOfferingMember2022-01-012022-12-310001801198IFRS-Full:SharePremiumMembersLEGN:FollowOnPublicOfferingMember2022-01-012022-12-310001801198LEGN:FollowOnPublicOfferingMember2022-01-012022-12-310001801198IFRS-Full:SharePremiumMembers2022-01-012022-12-310001801198IFRS-FULL:共有ベースの予約支払いメンバー2022-01-012022-12-310001801198IFRS-Full:IssuedCapitalMembers2022-12-310001801198IFRS-Full:SharePremiumMembers2022-12-310001801198IFRS-FULL:共有ベースの予約支払いメンバー2022-12-310001801198IFRS-FULL:Reserve OfExchangeDifferencesOnTranslationMember2022-12-310001801198IFRS-Full:RetainedEarningsMembers2022-12-310001801198Legn:LegendBiotechLimitedメンバー2022-01-012022-12-310001801198Legn:LegendBiotechLimitedメンバー2022-12-31Xbrli:純0001801198Legn:レノボ生物科学技術香港有限会社のメンバー2022-01-012022-12-310001801198Legn:レノボ生物科学技術香港有限会社のメンバー2022-12-310001801198LEGN:南京連想生物科技有限公司のメンバー2022-01-012022-12-310001801198LEGN:南京連想生物科技有限公司のメンバー2022-12-310001801198Legn:LegendBiotechアメリカのメンバー2022-01-012022-12-310001801198Legn:LegendBiotech Ireland Limitedメンバー2022-01-012022-12-310001801198Legn:LegendBiotechベルギーBVMember2022-01-012022-12-310001801198Legn:LegendBiotechベルギーBVMember2022-12-310001801198海南伝記生物科学技術有限会社のメンバー2022-01-012022-12-310001801198国際財務報告基準-完全:建築業メンバーIFRS-FULL:ボトムレンジメンバー2022-01-012022-12-310001801198IFRS-Full:TopOfRangeMember国際財務報告基準-完全:建築業メンバー2022-01-012022-12-310001801198IFRS-Full:機器メンバIFRS-FULL:ボトムレンジメンバー2022-01-012022-12-310001801198IFRS-Full:TopOfRangeMemberIFRS-Full:機器メンバ2022-01-012022-12-310001801198LEGN:ComputerAndOfficeEquipmentMembersIFRS-FULL:ボトムレンジメンバー2022-01-012022-12-310001801198IFRS-Full:TopOfRangeMemberLEGN:ComputerAndOfficeEquipmentMembers2022-01-012022-12-310001801198IFRS-Full:車両メンバー2022-01-012022-12-310001801198IFRS-FULL:コンピュータソフトウェアのメンバー2022-01-012022-12-310001801198LEGN:土地賃貸メンバー2022-01-012022-12-310001801198国際財務報告基準-完全:建築業メンバーIFRS-FULL:ボトムレンジメンバー2022-01-012022-12-310001801198IFRS-Full:TopOfRangeMember国際財務報告基準-完全:建築業メンバー2022-01-012022-12-310001801198IFRS-Full:機器メンバIFRS-FULL:ボトムレンジメンバー2022-01-012022-12-310001801198IFRS-Full:TopOfRangeMemberIFRS-Full:機器メンバ2022-01-012022-12-310001801198IFRS-Full:OfficeEquipmentMembersIFRS-FULL:ボトムレンジメンバー2022-01-012022-12-310001801198IFRS-Full:TopOfRangeMemberIFRS-Full:OfficeEquipmentMembers2022-01-012022-12-310001801198LEGN:JansenAgreement MembersLegn:LegendBiotechMembers国:CN2017-12-310001801198LEGN:JansenAgreement Members国:CNLeGn:JansenMember2017-12-310001801198LEGN:JansenAgreement Members2017-12-012017-12-310001801198LEGN:JansenAgreement Members2017-12-310001801198LEGN:指定された製造マイルストーンメンバー2022-01-012022-12-310001801198LEGN:指定された開発マイルストーンメンバー2022-01-012022-12-310001801198LEGN:指定された規制マイルストーンメンバー2022-01-012022-12-310001801198LEGN:NetTradeSalesMilestonesメンバーの指定2022-01-012022-12-3100018011982018-01-012018-12-31LEGN:マイルストーン0001801198LEGN:CARTITUDE 1臨床試験メンバー2019-01-012019-12-310001801198レーガン:CiltaCelMember2020-01-012020-12-310001801198LEGN:CARTITUDE 5臨床試験メンバー2021-01-012021-12-310001801198LEGN:CARTITUDE 5臨床試験メンバー2022-01-012022-12-310001801198LEGN:指定された将来発展のマイルストーンメンバー2022-01-012022-12-310001801198LEGN:ShareOptionAndRestratedStockUnitSchemeMember2022-01-012022-12-310001801198国:アメリカ2022-01-012022-12-310001801198国:アメリカ2021-01-012021-12-310001801198国:アメリカ2020-01-012020-12-310001801198国:CN2022-01-012022-12-310001801198国:CN2021-01-012021-12-310001801198国:CN2020-01-012020-12-310001801198LEGN:その他の国/地域のメンバー2022-01-012022-12-310001801198LEGN:その他の国/地域のメンバー2021-01-012021-12-310001801198LEGN:その他の国/地域のメンバー2020-01-012020-12-310001801198国:アメリカ2022-12-310001801198国:アメリカ2021-12-310001801198国:CN2022-12-310001801198国:CN2021-12-310001801198LEGN:その他の国/地域のメンバー2022-12-310001801198LEGN:その他の国/地域のメンバー2021-12-310001801198LEGN:JanssenAgreement Members国:アメリカ2022-01-012022-12-310001801198LEGN:JanssenAgreement Members国:アメリカ2021-01-012021-12-310001801198LEGN:JanssenAgreement Members国:アメリカ2020-01-012020-12-310001801198レーガン:南京益生生物科学技術有限公司のメンバー2022-01-012022-12-310001801198レーガン:南京益生生物科学技術有限公司のメンバー2021-01-012021-12-310001801198アメリカと非アメリカの領土メンバーは2015-05-272015-05-270001801198アメリカと非アメリカの領土メンバーは2022-01-012022-12-310001801198LEGN:納税前に利益損失納税後支払いと貸記メンバー2022-01-012022-12-310001801198LEGN:納税前に利益損失納税後支払いと貸記メンバー2021-01-012021-12-310001801198LEGN:納税前に利益損失納税後支払いと貸記メンバー2020-01-012020-12-310001801198国:香港2022-01-012022-12-31ISO 4217:香港ドル0001801198国:香港2020-01-012020-12-310001801198国:香港2021-01-012021-12-310001801198国:アメリカ2022-01-012022-12-310001801198国:アメリカ2020-01-012020-12-310001801198国:アメリカ2021-01-012021-12-310001801198STPR:ニュージャージー州2022-01-012022-12-310001801198STPR:ニュージャージー州2020-01-012020-12-310001801198STPR:ニュージャージー州2021-01-012021-12-310001801198国/地域:IE2022-01-012022-12-310001801198国/地域:IE2021-01-012021-12-310001801198国/地域:IE2020-01-012020-12-310001801198国:CN2022-01-012022-12-310001801198国:CN2021-01-012021-12-310001801198国:CN2020-01-012020-12-310001801198国:BE2022-01-012022-12-310001801198レーガン:皆さんありがとうございました2022-01-012022-12-310001801198レーガン:皆さんありがとうございました2021-01-012021-12-310001801198レーガン:皆さんありがとうございました2020-01-012020-12-310001801198IFRS-Full:Gross CarryingAmount MemberIFRS-Full:LandMembers2021-12-310001801198IFRS-Full:Gross CarryingAmount Member国際財務報告基準-完全:建築業メンバー2021-12-310001801198IFRS-Full:レンタル改善メンバーIFRS-Full:Gross CarryingAmount Member2021-12-310001801198IFRS-Full:Gross CarryingAmount MemberIFRS-Full:機器メンバ2021-12-310001801198IFRS-Full:Gross CarryingAmount MemberLEGN:ComputerAndOfficeEquipmentMembers2021-12-310001801198IFRS-Full:車両メンバーIFRS-Full:Gross CarryingAmount Member2021-12-310001801198IFRS−FULL:施工進捗メンバーIFRS-Full:Gross CarryingAmount Member2021-12-310001801198IFRS-Full:Gross CarryingAmount Member2021-12-310001801198IFRS-FULL:累積切り下げと償却メンバーIFRS-Full:LandMembers2021-12-310001801198IFRS-FULL:累積切り下げと償却メンバー国際財務報告基準-完全:建築業メンバー2021-12-310001801198IFRS-Full:レンタル改善メンバーIFRS-FULL:累積切り下げと償却メンバー2021-12-310001801198IFRS-FULL:累積切り下げと償却メンバーIFRS-Full:機器メンバ2021-12-310001801198IFRS-FULL:累積切り下げと償却メンバーLEGN:ComputerAndOfficeEquipmentMembers2021-12-310001801198IFRS-Full:車両メンバーIFRS-FULL:累積切り下げと償却メンバー2021-12-310001801198IFRS−FULL:施工進捗メンバーIFRS-FULL:累積切り下げと償却メンバー2021-12-310001801198IFRS-FULL:累積切り下げと償却メンバー2021-12-310001801198IFRS-Full:LandMembers2021-12-310001801198国際財務報告基準-完全:建築業メンバー2021-12-310001801198IFRS-Full:レンタル改善メンバー2021-12-310001801198IFRS-Full:機器メンバ2021-12-310001801198LEGN:ComputerAndOfficeEquipmentMembers2021-12-310001801198IFRS-Full:車両メンバー2021-12-310001801198IFRS−FULL:施工進捗メンバー2021-12-310001801198IFRS-Full:LandMembers2022-01-012022-12-310001801198国際財務報告基準-完全:建築業メンバー2022-01-012022-12-310001801198IFRS-Full:レンタル改善メンバー2022-01-012022-12-310001801198IFRS-Full:機器メンバ2022-01-012022-12-310001801198LEGN:ComputerAndOfficeEquipmentMembers2022-01-012022-12-310001801198IFRS−FULL:施工進捗メンバー2022-01-012022-12-310001801198IFRS-Full:LandMembers2022-12-310001801198国際財務報告基準-完全:建築業メンバー2022-12-310001801198IFRS-Full:レンタル改善メンバー2022-12-310001801198IFRS-Full:機器メンバ2022-12-310001801198LEGN:ComputerAndOfficeEquipmentMembers2022-12-310001801198IFRS-Full:車両メンバー2022-12-310001801198IFRS−FULL:施工進捗メンバー2022-12-310001801198IFRS-Full:Gross CarryingAmount MemberIFRS-Full:LandMembers2022-12-310001801198IFRS-Full:Gross CarryingAmount Member国際財務報告基準-完全:建築業メンバー2022-12-310001801198IFRS-Full:レンタル改善メンバーIFRS-Full:Gross CarryingAmount Member2022-12-310001801198IFRS-Full:Gross CarryingAmount MemberIFRS-Full:機器メンバ2022-12-310001801198IFRS-Full:Gross CarryingAmount MemberLEGN:ComputerAndOfficeEquipmentMembers2022-12-310001801198IFRS-Full:車両メンバーIFRS-Full:Gross CarryingAmount Member2022-12-310001801198IFRS−FULL:施工進捗メンバーIFRS-Full:Gross CarryingAmount Member2022-12-310001801198IFRS-Full:Gross CarryingAmount Member2022-12-310001801198IFRS-FULL:累積切り下げと償却メンバーIFRS-Full:LandMembers2022-12-310001801198IFRS-FULL:累積切り下げと償却メンバー国際財務報告基準-完全:建築業メンバー2022-12-310001801198IFRS-Full:レンタル改善メンバーIFRS-FULL:累積切り下げと償却メンバー2022-12-310001801198IFRS-FULL:累積切り下げと償却メンバーIFRS-Full:機器メンバ2022-12-310001801198IFRS-FULL:累積切り下げと償却メンバーLEGN:ComputerAndOfficeEquipmentMembers2022-12-310001801198IFRS-Full:車両メンバーIFRS-FULL:累積切り下げと償却メンバー2022-12-310001801198IFRS−FULL:施工進捗メンバーIFRS-FULL:累積切り下げと償却メンバー2022-12-310001801198IFRS-FULL:累積切り下げと償却メンバー2022-12-310001801198IFRS-Full:Gross CarryingAmount MemberIFRS-Full:LandMembers2020-12-310001801198IFRS-Full:Gross CarryingAmount Member国際財務報告基準-完全:建築業メンバー2020-12-310001801198IFRS-Full:レンタル改善メンバーIFRS-Full:Gross CarryingAmount Member2020-12-310001801198IFRS-Full:Gross CarryingAmount MemberIFRS-Full:機器メンバ2020-12-310001801198IFRS-Full:Gross CarryingAmount MemberLEGN:ComputerAndOfficeEquipmentMembers2020-12-310001801198IFRS-Full:車両メンバーIFRS-Full:Gross CarryingAmount Member2020-12-310001801198IFRS−FULL:施工進捗メンバーIFRS-Full:Gross CarryingAmount Member2020-12-310001801198IFRS-Full:Gross CarryingAmount Member2020-12-310001801198IFRS-FULL:累積切り下げと償却メンバーIFRS-Full:LandMembers2020-12-310001801198IFRS-FULL:累積切り下げと償却メンバー国際財務報告基準-完全:建築業メンバー2020-12-310001801198IFRS-Full:レンタル改善メンバーIFRS-FULL:累積切り下げと償却メンバー2020-12-310001801198IFRS-FULL:累積切り下げと償却メンバーIFRS-Full:機器メンバ2020-12-310001801198IFRS-FULL:累積切り下げと償却メンバーLEGN:ComputerAndOfficeEquipmentMembers2020-12-310001801198IFRS-Full:車両メンバーIFRS-FULL:累積切り下げと償却メンバー2020-12-310001801198IFRS−FULL:施工進捗メンバーIFRS-FULL:累積切り下げと償却メンバー2020-12-310001801198IFRS-FULL:累積切り下げと償却メンバー2020-12-310001801198IFRS-Full:LandMembers2020-12-310001801198国際財務報告基準-完全:建築業メンバー2020-12-310001801198IFRS-Full:レンタル改善メンバー2020-12-310001801198IFRS-Full:機器メンバ2020-12-310001801198LEGN:ComputerAndOfficeEquipmentMembers2020-12-310001801198IFRS-Full:車両メンバー2020-12-310001801198IFRS−FULL:施工進捗メンバー2020-12-310001801198IFRS-Full:LandMembers2021-01-012021-12-310001801198国際財務報告基準-完全:建築業メンバー2021-01-012021-12-310001801198IFRS-Full:レンタル改善メンバー2021-01-012021-12-310001801198IFRS-Full:機器メンバ2021-01-012021-12-310001801198LEGN:ComputerAndOfficeEquipmentMembers2021-01-012021-12-310001801198IFRS-Full:車両メンバー2021-01-012021-12-310001801198IFRS−FULL:施工進捗メンバー2021-01-012021-12-310001801198IFRS-Full:Gross CarryingAmount MemberIFRS-FULL:コンピュータソフトウェアのメンバー2021-12-310001801198IFRS-FULL:累積切り下げと償却メンバーIFRS-FULL:コンピュータソフトウェアのメンバー2021-12-310001801198IFRS-FULL:コンピュータソフトウェアのメンバー2021-12-310001801198IFRS-FULL:コンピュータソフトウェアのメンバー2022-12-310001801198IFRS-Full:Gross CarryingAmount MemberIFRS-FULL:コンピュータソフトウェアのメンバー2022-12-310001801198IFRS-FULL:累積切り下げと償却メンバーIFRS-FULL:コンピュータソフトウェアのメンバー2022-12-310001801198IFRS-Full:Gross CarryingAmount MemberIFRS-FULL:コンピュータソフトウェアのメンバー2020-12-310001801198IFRS-FULL:累積切り下げと償却メンバーIFRS-FULL:コンピュータソフトウェアのメンバー2020-12-310001801198IFRS-FULL:コンピュータソフトウェアのメンバー2020-12-310001801198IFRS-FULL:コンピュータソフトウェアのメンバー2021-01-012021-12-310001801198LEGN:コラボレーション資産メンバ2022-12-310001801198LEGN:コラボレーション資産メンバ2021-12-310001801198IFRS-Full:LandMembersLEGN:権限資産使用連携メンバの排除2021-12-310001801198国際財務報告基準-完全:建築業メンバーLEGN:権限資産使用連携メンバの排除2021-12-310001801198国際財務報告基準-完全:建築業メンバーLEGN:コラボレーション資産メンバ2021-12-310001801198IFRS-Full:機器メンバLEGN:コラボレーション資産メンバ2021-12-310001801198LEGN:ComputerAndOfficeEquipmentMembersLEGN:コラボレーション資産メンバ2021-12-310001801198IFRS-Full:LandMembersLEGN:権限資産使用連携メンバの排除2022-01-012022-12-310001801198国際財務報告基準-完全:建築業メンバーLEGN:権限資産使用連携メンバの排除2022-01-012022-12-310001801198国際財務報告基準-完全:建築業メンバーLEGN:コラボレーション資産メンバ2022-01-012022-12-310001801198IFRS-Full:機器メンバLEGN:コラボレーション資産メンバ2022-01-012022-12-310001801198LEGN:ComputerAndOfficeEquipmentMembersLEGN:コラボレーション資産メンバ2022-01-012022-12-310001801198IFRS-Full:LandMembersLEGN:権限資産使用連携メンバの排除2022-12-310001801198国際財務報告基準-完全:建築業メンバーLEGN:権限資産使用連携メンバの排除2022-12-310001801198国際財務報告基準-完全:建築業メンバーLEGN:コラボレーション資産メンバ2022-12-310001801198IFRS-Full:機器メンバLEGN:コラボレーション資産メンバ2022-12-310001801198LEGN:ComputerAndOfficeEquipmentMembersLEGN:コラボレーション資産メンバ2022-12-310001801198IFRS-Full:LandMembersLEGN:権限資産使用連携メンバの排除2020-12-310001801198国際財務報告基準-完全:建築業メンバーLEGN:権限資産使用連携メンバの排除2020-12-310001801198国際財務報告基準-完全:建築業メンバーLEGN:コラボレーション資産メンバ2020-12-310001801198IFRS-Full:機器メンバLEGN:コラボレーション資産メンバ2020-12-310001801198LEGN:ComputerAndOfficeEquipmentMembersLEGN:コラボレーション資産メンバ2020-12-310001801198IFRS-Full:LandMembersLEGN:権限資産使用連携メンバの排除2021-01-012021-12-310001801198国際財務報告基準-完全:建築業メンバーLEGN:権限資産使用連携メンバの排除2021-01-012021-12-310001801198国際財務報告基準-完全:建築業メンバーLEGN:コラボレーション資産メンバ2021-01-012021-12-310001801198IFRS-Full:機器メンバLEGN:コラボレーション資産メンバ2021-01-012021-12-310001801198LEGN:ComputerAndOfficeEquipmentMembersLEGN:コラボレーション資産メンバ2021-01-012021-12-310001801198IFRS-Full:レンタル担当メンバー2021-12-310001801198IFRS-Full:レンタル担当メンバー2020-12-310001801198IFRS-Full:レンタル担当メンバー2022-01-012022-12-310001801198IFRS-Full:レンタル担当メンバー2021-01-012021-12-310001801198IFRS-Full:レンタル担当メンバー2022-12-310001801198IFRS-Full:1年遅れないメンバー2022-12-310001801198IFRS-Full:1年遅れないメンバー2021-12-310001801198LEGN:シリーズAConvertibleRedeemblePferredSharesMember2020-04-160001801198LEGN:シリーズAConvertibleRedeemblePferredSharesMember2020-03-302020-04-160001801198LEGN:シリーズAConvertibleRedeemblePferredSharesMember2020-01-012020-12-310001801198IFRS-FULL:ボトムレンジメンバー2022-01-012022-12-310001801198IFRS-Full:TopOfRangeMember2022-01-012022-12-310001801198LEGN:ライセンスと連携プロトコルのメンバ2021-12-310001801198LEGN:前払いその他売掛金その他資産メンバ2022-12-310001801198LEGN:前払いその他売掛金その他資産メンバ2021-12-310001801198脚部:他の売掛金メンバー2022-12-310001801198LEGN:プリペイドメンバー2022-12-310001801198LEGN:プリペイドメンバー2021-12-310001801198LEGN:財務資産による減価償却コストのメンバー2022-12-310001801198LEGN:財務資産による減価償却コストのメンバー2021-12-310001801198LEGN:金融機関が発行するビジネス紙のメンバー2021-12-310001801198LEGN:金融機関が発行するビジネス紙のメンバー2021-01-012021-12-310001801198通貨:ドル2022-12-310001801198通貨:ドル2021-12-310001801198金種:人民元2022-12-310001801198金種:人民元2021-12-310001801198通貨:ユーロ2022-12-310001801198通貨:ユーロ2021-12-310001801198IFRS-Full:RelatedPartiesMember2022-12-310001801198IFRS-Full:RelatedPartiesMember2021-12-310001801198LEGN:連携収益メンバ2020-12-310001801198LEGN:DifferenceAllowanceInExcessOfRelatedDepreationMember2020-12-310001801198IFRS-Full:RightofuseAssetsMember2020-12-310001801198LEGN:連携収益メンバ2021-01-012021-12-310001801198LEGN:DifferenceAllowanceInExcessOfRelatedDepreationMember2021-01-012021-12-310001801198IFRS-Full:RightofuseAssetsMember2021-01-012021-12-310001801198LEGN:連携収益メンバ2021-12-310001801198LEGN:DifferenceAllowanceInExcessOfRelatedDepreationMember2021-12-310001801198IFRS-Full:RightofuseAssetsMember2021-12-310001801198LEGN:連携収益メンバ2022-01-012022-12-310001801198LEGN:DifferenceAllowanceInExcessOfRelatedDepreationMember2022-01-012022-12-310001801198IFRS-Full:RightofuseAssetsMember2022-01-012022-12-310001801198LEGN:連携収益メンバ2022-12-310001801198LEGN:DifferenceAllowanceInExcessOfRelatedDepreationMember2022-12-310001801198IFRS-Full:RightofuseAssetsMember2022-12-310001801198IFRS-FULL:未使用税金損失メンバー2020-12-310001801198LEGN:差異無形資産償却メンバー2020-12-310001801198LEGN:AcruedExpenseMember2020-12-310001801198IFRS-Full:レンタル担当メンバー2020-12-310001801198LEGN:コスト回収OfResearchedAndDevelopment費用メンバー2020-12-310001801198LEGN:研究·開発メンバー2020-12-310001801198IFRS-FULL:未使用税金損失メンバー2021-01-012021-12-310001801198LEGN:差異無形資産償却メンバー2021-01-012021-12-310001801198LEGN:AcruedExpenseMember2021-01-012021-12-310001801198IFRS-Full:レンタル担当メンバー2021-01-012021-12-310001801198LEGN:コスト回収OfResearchedAndDevelopment費用メンバー2021-01-012021-12-310001801198LEGN:研究·開発メンバー2021-01-012021-12-310001801198IFRS-FULL:未使用税金損失メンバー2021-12-310001801198LEGN:差異無形資産償却メンバー2021-12-310001801198LEGN:AcruedExpenseMember2021-12-310001801198IFRS-Full:レンタル担当メンバー2021-12-310001801198LEGN:コスト回収OfResearchedAndDevelopment費用メンバー2021-12-310001801198LEGN:研究·開発メンバー2021-12-310001801198IFRS-FULL:未使用税金損失メンバー2022-01-012022-12-310001801198LEGN:差異無形資産償却メンバー2022-01-012022-12-310001801198LEGN:AcruedExpenseMember2022-01-012022-12-310001801198IFRS-Full:レンタル担当メンバー2022-01-012022-12-310001801198LEGN:コスト回収OfResearchedAndDevelopment費用メンバー2022-01-012022-12-310001801198LEGN:研究·開発メンバー2022-01-012022-12-310001801198IFRS-FULL:未使用税金損失メンバー2022-12-310001801198LEGN:差異無形資産償却メンバー2022-12-310001801198LEGN:AcruedExpenseMember2022-12-310001801198IFRS-Full:レンタル担当メンバー2022-12-310001801198LEGN:コスト回収OfResearchedAndDevelopment費用メンバー2022-12-310001801198LEGN:研究·開発メンバー2022-12-310001801198国:香港2022-01-012022-12-310001801198国:香港2021-01-012021-12-310001801198国/地域:IE2022-01-012022-12-310001801198国/地域:IE2021-01-012021-12-310001801198IFRS-Full:付録メンバー国:CN2022-12-310001801198IFRS-Full:付録メンバー国:CN2021-12-310001801198IFRS-Full:付録メンバー国:アメリカ2022-12-310001801198IFRS-Full:付録メンバー国:アメリカ2021-12-3100018011982021-05-1300018011982021-05-132021-05-130001801198レーガン:保証期間のメンバー2021-05-130001801198LEGN:A 110 InterestBearingLoansMember2022-12-310001801198LEGN:A 110 InterestBearingLoansMember2022-01-012022-12-3100018011982021-06-1800018011982021-09-1700018011982021-12-1700018011982022-03-1800018011982022-06-1700018011982022-09-1600018011982022-12-160001801198IFRS-FULL:一般共有メンバ2022-12-310001801198IFRS-FULL:一般共有メンバ2021-12-310001801198LEGN:共有資本メンバ2020-12-310001801198LEGN:共有資本メンバ2021-01-012021-12-310001801198LEGN:共有資本メンバ2021-12-310001801198IFRS-Full:IssuedCapitalMembers2022-01-012022-12-310001801198LEGN:共有資本メンバ2022-01-012022-12-310001801198LEGN:共有資本メンバ2022-12-310001801198IFRS-FULL:一般共有メンバ2022-07-290001801198IFRS-FULL:一般共有メンバ2022-07-292022-07-290001801198LEGN:A 2019122520271225メンバー2022-12-310001801198番号:A 2019070120280829メンバー2022-12-310001801198LEGN:A 2019123120281230メンバー2022-12-310001801198LEGN:A 2020070220290701メンバー2022-12-310001801198LEGN:A 2020112920291128メンバー2022-12-310001801198LEGN:A 2021060520300604メンバー2022-12-310001801198LEGN:A 2021090120300831メンバー2022-12-310001801198LEGN:A 202111920301118メンバー2022-12-310001801198支線:A 2022032920310328メンバー2022-12-310001801198支線:A 2022082720310826メンバー2022-12-310001801198番号:A 2023033120320330メンバー2022-12-310001801198番号:A 2023043020320429メンバー2022-12-310001801198LEGN:A 2023050220320501メンバー2022-12-310001801198LEGN:A 2023050520320504メンバー2022-12-310001801198LEGN:A 2023050820320507メンバー2022-12-310001801198LEGN:A 2023051020 320509メンバー2022-12-310001801198LEGN:A 2023051320320512メンバー2022-12-310001801198番号:A 2023063020320629メンバー2022-12-310001801198LEGN:A 2023080220320801メンバー2022-12-310001801198LEGN:A 2019122520271225メンバー2021-12-310001801198番号:A 2019070120280829メンバー2021-12-310001801198LEGN:A 2019123120281230メンバー2021-12-310001801198LEGN:A 2020070220290701メンバー2021-12-310001801198LEGN:A 2020112920291128メンバー2021-12-310001801198LEGN:A 2021060520300604メンバー2021-12-310001801198LEGN:A 2021090120300831メンバー2021-12-310001801198LEGN:A 202111920301118メンバー2021-12-310001801198支線:A 2022032920310328メンバー2021-12-310001801198支線:A 2022082720310826メンバー2021-12-310001801198LEGN:A 2019122520271225メンバー2020-12-310001801198番号:A 2019070120280829メンバー2020-12-310001801198LEGN:A 2019123120281230メンバー2020-12-310001801198LEGN:A 2020070220290701メンバー2020-12-310001801198LEGN:A 2020112920291128メンバー2020-12-310001801198LEGN:A 2021060520300604メンバー2020-12-310001801198LEGN:A 2021090120300831メンバー2020-12-310001801198LEGN:A 202111920301118メンバー2020-12-310001801198LEGN:A 2019112920191209メンバーLEGN:GenscriptGroupメンバー2022-12-310001801198IFRS-FULL:ボトムレンジメンバー2021-01-012021-12-310001801198IFRS-Full:TopOfRangeMember2021-01-012021-12-310001801198IFRS-FULL:ボトムレンジメンバー2020-01-012020-12-310001801198IFRS-Full:TopOfRangeMember2020-01-012020-12-310001801198LEGN:BinomialModelMember2022-12-310001801198LEGN:BinomialModelMemberIFRS-FULL:一般共有メンバ2022-12-310001801198LEGN:BinomialModelMember2022-01-012022-12-3100018011982020-05-262020-05-260001801198LEGN:制限された株式単位メンバ2021-12-310001801198LEGN:制限された株式単位メンバ2022-01-012022-12-310001801198LEGN:制限された株式単位メンバ2022-12-310001801198LEGN:制限された株式単位メンバ2020-12-310001801198LEGN:制限された株式単位メンバ2021-01-012021-12-310001801198LEGN:制限された株式単位メンバ2020-01-012020-12-310001801198LEGN:制限された株式計画メンバー2022-12-310001801198LEGN:制限された株式計画メンバー2022-01-012022-12-310001801198会社名:南京益生生物科技有限公司と江蘇根生物科技有限会社のメンバー2021-01-012021-12-310001801198LEGN:その他の支払·課税料金メンバー2022-01-012022-12-310001801198LEGN:その他の支払·課税料金メンバー2021-01-012021-12-310001801198LEGN:その他の支払·課税料金メンバー2020-01-012020-12-310001801198LEGN:交換可能交換第一選択共有メンバ2020-01-012020-12-310001801198LEGN:交換可能交換第一選択共有メンバ2021-12-310001801198LEGN:他の参加者に支払うことができる2021-12-310001801198LEGN:交換可能交換第一選択共有メンバ2022-01-012022-12-310001801198LEGN:他の参加者に支払うことができる2022-01-012022-12-310001801198LEGN:交換可能交換第一選択共有メンバ2022-12-310001801198LEGN:他の参加者に支払うことができる2022-12-310001801198LEGN:交換可能交換第一選択共有メンバ2020-12-310001801198LEGN:他の参加者に支払うことができる2020-12-310001801198LEGN:交換可能交換第一選択共有メンバ2021-01-012021-12-310001801198LEGN:他の参加者に支払うことができる2021-01-012021-12-310001801198LEGN:交換可能交換第一選択共有メンバ2019-12-310001801198LEGN:他の参加者に支払うことができる2019-12-310001801198IFRS-Full:レンタル担当メンバー2019-12-310001801198LEGN:他の参加者に支払うことができる2020-01-012020-12-310001801198IFRS-Full:レンタル担当メンバー2020-01-012020-12-3100018011982021-09-012021-09-30Utr:SQFT0001801198Legn:南京GenScritBiotechCoLimitedメンバー2022-01-012022-12-310001801198LEGN:江蘇根っこ生物科技有限公司のメンバー2022-01-012022-12-310001801198LEGN:ユニバーサルアメリカ社のメンバー2022-01-012022-12-310001801198LEGN:汎用スクリプトUSAHoldingsIncMembers2022-01-012022-12-310001801198LEGN:GenscritBiotechオランダBVMembers2022-01-012022-12-310001801198LEGN:江蘇益生生物科技有限公司のメンバー2022-01-012022-12-310001801198LEGN:Genscritオランダのメンバー2022-01-012022-12-310001801198LEGN:GenscriptBiotechCorporationメンバー2022-01-012022-12-310001801198LEGN:GenScriptProBioUSAIncMember2022-01-012022-12-310001801198レーガン:南京益生生物科学技術有限公司のメンバー2020-01-012020-12-310001801198Legn:南京GenScritBiotechCoLimitedメンバー2021-01-012021-12-310001801198Legn:南京GenScritBiotechCoLimitedメンバー2020-01-012020-12-310001801198LEGN:江蘇益生生物科技有限公司のメンバー2021-01-012021-12-310001801198LEGN:江蘇益生生物科技有限公司のメンバー2020-01-012020-12-310001801198LEGN:ユニバーサルアメリカ社のメンバー2021-01-012021-12-310001801198LEGN:ユニバーサルアメリカ社のメンバー2020-01-012020-12-310001801198LEGN:汎用スクリプトUSAHoldingsIncMembers2021-01-012021-12-310001801198LEGN:汎用スクリプトUSAHoldingsIncMembers2020-01-012020-12-310001801198LEGN:江蘇根っこ生物科技有限公司のメンバー2021-01-012021-12-310001801198LEGN:江蘇根っこ生物科技有限公司のメンバー2020-01-012020-12-310001801198LEGN:GenScriptProBioUSAIncMember2021-01-012021-12-310001801198LEGN:GenScriptProBioUSAIncMember2020-01-012020-12-310001801198LEGN:Genscritオランダのメンバー2021-01-012021-12-310001801198LEGN:Genscritオランダのメンバー2020-01-012020-12-310001801198LEGN:GenscriptBiotechCorporationメンバーLEGN:FollowOnPublicOfferingMember2022-01-012022-12-310001801198LEGN:GenscriptBiotechCorporationメンバーLEGN:FollowOnPublicOfferingMember2021-01-012021-12-310001801198LEGN:GenscriptBiotechCorporationメンバーLEGN:FollowOnPublicOfferingMember2020-01-012020-12-310001801198LEGN:GenscriptBiotechCorporationメンバーLEGN:FollowOnPublicOfferingMember2021-12-200001801198レーガン:南京益生生物科学技術有限公司のメンバーLEGN:TradeReceivableメンバ2022-12-310001801198レーガン:南京益生生物科学技術有限公司のメンバーLEGN:TradeReceivableメンバ2021-12-310001801198Legn:南京GenScritBiotechCoLimitedメンバー脚部:他の売掛金メンバー2022-12-310001801198Legn:南京GenScritBiotechCoLimitedメンバー脚部:他の売掛金メンバー2021-12-310001801198LEGN:ユニバーサルアメリカ社のメンバー脚部:他の売掛金メンバー2022-12-310001801198LEGN:ユニバーサルアメリカ社のメンバー脚部:他の売掛金メンバー2021-12-310001801198脚部:他の売掛金メンバーLEGN:江蘇根っこ生物科技有限公司のメンバー2022-12-310001801198脚部:他の売掛金メンバーLEGN:江蘇根っこ生物科技有限公司のメンバー2021-12-310001801198脚部:他の売掛金メンバー2021-12-310001801198レーガン:南京益生生物科学技術有限公司のメンバーLEGN:プリペイドメンバー2022-12-310001801198レーガン:南京益生生物科学技術有限公司のメンバーLEGN:プリペイドメンバー2021-12-310001801198LEGN:江蘇益生生物科技有限公司のメンバーLEGN:プリペイドメンバー2022-12-310001801198LEGN:江蘇益生生物科技有限公司のメンバーLEGN:プリペイドメンバー2021-12-310001801198Legn:南京GenScritBiotechCoLimitedメンバーLegn:TradePayablesMembers2022-12-310001801198Legn:南京GenScritBiotechCoLimitedメンバーLegn:TradePayablesMembers2021-12-310001801198LEGN:ユニバーサルアメリカ社のメンバーLegn:TradePayablesMembers2022-12-310001801198LEGN:ユニバーサルアメリカ社のメンバーLegn:TradePayablesMembers2021-12-310001801198Legn:TradePayablesMembersLEGN:江蘇根っこ生物科技有限公司のメンバー2022-12-310001801198Legn:TradePayablesMembersLEGN:江蘇根っこ生物科技有限公司のメンバー2021-12-310001801198レーガン:南京益生生物科学技術有限公司のメンバーLegn:TradePayablesMembers2022-12-310001801198レーガン:南京益生生物科学技術有限公司のメンバーLegn:TradePayablesMembers2021-12-310001801198Legn:TradePayablesMembers2022-12-310001801198Legn:TradePayablesMembers2021-12-310001801198Legn:南京GenScritBiotechCoLimitedメンバーLEGN:他の支払すべきメンバー2022-12-310001801198Legn:南京GenScritBiotechCoLimitedメンバーLEGN:他の支払すべきメンバー2021-12-310001801198LEGN:ユニバーサルアメリカ社のメンバーLEGN:他の支払すべきメンバー2022-12-310001801198LEGN:ユニバーサルアメリカ社のメンバーLEGN:他の支払すべきメンバー2021-12-310001801198LEGN:他の支払すべきメンバーLEGN:江蘇根っこ生物科技有限公司のメンバー2022-12-310001801198LEGN:他の支払すべきメンバーLEGN:江蘇根っこ生物科技有限公司のメンバー2021-12-310001801198LEGN:他の支払すべきメンバーLEGN:江蘇益生生物科技有限公司のメンバー2022-12-310001801198LEGN:他の支払すべきメンバーLEGN:江蘇益生生物科技有限公司のメンバー2021-12-310001801198レーガン:南京益生生物科学技術有限公司のメンバーLEGN:他の支払すべきメンバー2022-12-310001801198レーガン:南京益生生物科学技術有限公司のメンバーLEGN:他の支払すべきメンバー2021-12-310001801198LEGN:GenscritオランダのメンバーLEGN:他の支払すべきメンバー2022-12-310001801198LEGN:GenscritオランダのメンバーLEGN:他の支払すべきメンバー2021-12-310001801198LEGN:他の支払すべきメンバー2022-12-310001801198LEGN:他の支払すべきメンバー2021-12-310001801198LEGN:汎用スクリプトUSAHoldingsIncMembersIFRS-Full:レンタル担当メンバー2022-12-310001801198LEGN:汎用スクリプトUSAHoldingsIncMembersIFRS-Full:レンタル担当メンバー2021-12-310001801198Legn:南京GenScritBiotechCoLimitedメンバーIFRS-Full:レンタル担当メンバー2022-12-310001801198Legn:南京GenScritBiotechCoLimitedメンバーIFRS-Full:レンタル担当メンバー2021-12-310001801198IFRS-Full:売掛金メンバー2022-12-310001801198LEGN:財務資産には前払金その他の売掛金やその他の資産が含まれている2022-12-310001801198IFRS-Full:財務負債公平価値別利益または損失カテゴリメンバー2022-12-310001801198Legn:TimeDepositsMembers2022-12-310001801198LEGN:質抵当預金メンバー2022-12-310001801198LEGN:CashAndCashEquivalentMember2022-12-310001801198LEGN:TradeAndNotesPayablesMember2022-12-310001801198IFRS-FULL:WarrantyContingentLiabilityのメンバー2022-12-310001801198LEGN:財務負債は他の支払·課税料金に含まれています2022-12-310001801198LEGN:CollaborationInterestBearingAdvancedFundingMember2022-12-310001801198IFRS-Full:売掛金メンバー2021-12-310001801198LEGN:財務資産には前払金その他の売掛金やその他の資産が含まれている2021-12-310001801198LEGN:財務資産償却コストメンバー2021-12-310001801198IFRS-Full:レンタル売掛金メンバー2021-12-310001801198Legn:TimeDepositsMembers2021-12-310001801198LEGN:質抵当預金メンバー2021-12-310001801198LEGN:CashAndCashEquivalentMember2021-12-310001801198LEGN:TradeAndNotesPayablesMember2021-12-310001801198IFRS-FULL:WarrantyContingentLiabilityのメンバー2021-12-310001801198LEGN:財務負債は他の支払·課税料金に含まれています2021-12-310001801198LEGN:CollaborationInterestBearingAdvancedFundingMember2021-12-310001801198IFRS-FULL:第1レベル公平価値レベルメンバ2022-12-310001801198IFRS-Full:Level 2 O fFairValueHierarchyMembers2022-12-310001801198IFRS-Full:Level 3 of FairValueHierarchyMembers2022-12-310001801198IFRS-FULL:第1レベル公平価値レベルメンバIFRS-FULL:WarrantyContingentLiabilityのメンバー2022-12-310001801198IFRS-FULL:WarrantyContingentLiabilityのメンバーIFRS-Full:Level 2 O fFairValueHierarchyMembers2022-12-310001801198IFRS-FULL:WarrantyContingentLiabilityのメンバーIFRS-Full:Level 3 of FairValueHierarchyMembers2022-12-310001801198IFRS-FULL:WarrantyContingentLiabilityのメンバー2022-01-012022-12-310001801198IFRS-FULL:WarrantyContingentLiabilityのメンバーIFRS-FULL:ボトムレンジメンバー2022-01-012022-12-310001801198IFRS-Full:TopOfRangeMemberIFRS-FULL:WarrantyContingentLiabilityのメンバー2022-01-012022-12-310001801198IFRS-FULL:第1レベル公平価値レベルメンバIFRS-FULL:WarrantyContingentLiabilityのメンバー2021-12-310001801198IFRS-FULL:WarrantyContingentLiabilityのメンバーIFRS-Full:Level 2 O fFairValueHierarchyMembers2021-12-310001801198IFRS-FULL:WarrantyContingentLiabilityのメンバーIFRS-Full:Level 3 of FairValueHierarchyMembers2021-12-310001801198IFRS-FULL:WarrantyContingentLiabilityのメンバー2021-01-012021-12-310001801198IFRS-Full:CurrencyRiskMember2022-01-012022-12-310001801198IFRS-Full:CurrencyRiskMember2021-01-012021-12-310001801198IFRS-Full:CurrencyRiskMember2020-01-012020-12-310001801198IFRS-Full:CurrencyRiskMemberLEGN:USDollarStrengthensAgainstRMBMembers2022-01-012022-12-310001801198LEGN:USDollarWeakensAgainstRMBMemberIFRS-Full:CurrencyRiskMember2022-01-012022-12-310001801198IFRS-Full:CurrencyRiskMemberLEGN:USDollarStrengthensAgainstEURMembers2022-01-012022-12-310001801198IFRS-Full:CurrencyRiskMemberLEGN:USDollarWeakensAgainstEURMembers2022-01-012022-12-310001801198IFRS-Full:CurrencyRiskMemberLEGN:USDollarStrengthensAgainstRMBMembers2021-01-012021-12-310001801198LEGN:USDollarWeakensAgainstRMBMemberIFRS-Full:CurrencyRiskMember2021-01-012021-12-310001801198IFRS-Full:CurrencyRiskMemberLEGN:USDollarStrengthensAgainstEURMembers2021-01-012021-12-310001801198IFRS-Full:CurrencyRiskMemberLEGN:USDollarWeakensAgainstEURMembers2021-01-012021-12-310001801198IFRS-Full:CurrencyRiskMemberLEGN:USDollarStrengthensAgainstRMBMembers2020-01-012020-12-310001801198LEGN:USDollarWeakensAgainstRMBMemberIFRS-Full:CurrencyRiskMember2020-01-012020-12-310001801198IFRS-Full:CurrencyRiskMemberLEGN:USDollarStrengthensAgainstEURMembers2020-01-012020-12-310001801198IFRS-Full:CurrencyRiskMemberLEGN:USDollarWeakensAgainstEURMembers2020-01-012020-12-310001801198IFRS-Full:LiquidityRiskMemberIFRS-Full:1年遅れないメンバー2022-12-310001801198IFRS-Full:LiquidityRiskMemberIFRS-Full:1年遅れのメンバー2022-12-310001801198IFRS-Full:LiquidityRiskMember2022-12-310001801198IFRS-Full:1年遅れのメンバー2022-12-310001801198IFRS-Full:LiquidityRiskMemberIFRS-Full:1年遅れないメンバー2021-12-310001801198IFRS-Full:LiquidityRiskMemberIFRS-Full:1年遅れのメンバー2021-12-310001801198IFRS-Full:LiquidityRiskMember2021-12-310001801198IFRS-Full:1年遅れのメンバー2021-12-310001801198IFRS-Full:EquityPriceRiskMember2022-12-310001801198IFRS-Full:EquityPriceRiskMember2021-12-31 アメリカです
アメリカ証券取引委員会
ワシントンD.C.,20549
表20-F
(マーク1)
| | | | | |
| o | 1934年証券取引法第12(B)又は(G)条に基づく登録声明 |
あるいは…。
| | | | | |
| x | 1934年証券取引法第13条又は15条に基づいて提出された年次報告 |
本財政年度末まで十二月三十一日, 2022
あるいは…。
| | | | | |
| o | 1934年証券取引法第13条又は15条に基づいて提出された移行報告 |
そこからの過渡期について
あるいは…。
| | | | | |
| o | 1934年証券取引法第13条又は15(D)条に基づいて提出された幽霊会社報告 |
この幽霊会社が報告した事件の日付が必要です
依頼書類番号:001-39307
伝奇生物集団
(登録者の正確な氏名はその定款に記載)
適用されない
(登録者氏名英文訳)
ケイマン諸島
(登録成立または組織の司法管轄権)
伝奇生物集団
綿尾巷2101号
サマセット, ニュージャージー州08873
(主にオフィスアドレスを実行)
Huangに対応するPh.D.
最高経営責任者
伝奇生物集団
綿尾巷2101号
サマセット, ニュージャージー州08873
電話:(737) 317-5050
(会社の連絡先名、電話、電子メールおよび/またはファックス番号および住所)
この法第12条(B)に基づいて登録又は登録される証券:
| | | | | | | | | | | | | | |
| クラスごとのタイトル | | 取引コード | | 登録された各取引所の名称 |
| アメリカ預託株は,1株当たり2株の普通株に相当し,1株当たり額面0.0001ドルである | | LEGN | | ナスダック世界ベスト市場 |
| 普通株、1株当たり0.0001ドル* | | | | ナスダック世界ベスト市場 |
*取引には使用されないが,米国預託株式の登録のみと関係がある。
この法第十二条(G)に基づいて登録又は登録される証券:
ありません
(クラス名)
同法第15条(D)に基づいて報告義務を有する証券:
ありません
(クラス名)
年報で述べた期間終了時までの発行者が属する各種資本または普通株の流通株数を明記する
330,134,480普通株は、1株当たり0.0001ドルの価値があり、2022年12月31日に発行し、発行します
登録者が証券法規則405で定義されている経験豊富な発行者である場合は、再選択マークで示してくださいx はい、そうですo違います。
本報告が年次報告又は移行報告である場合は、登録者が1934年“証券取引法”第13又は15(D)節に基づいて報告を提出する必要がないか否かを勾印で示してくださいoはい、そうですx 違います。
注-上記チェックボックスを選択することは、これらの条項の下で、1934年の証券取引法第13条または15(D)条に基づいて報告書の提出を要求する任意の登録者の義務を解除しない。
再選択マークは、登録者が(1)過去12ヶ月以内(または登録者がそのような報告の提出を要求されたより短い期間)に、1934年の証券取引法第13条または15(D)節に提出されたすべての報告書を提出したかどうか、および(2)過去90日以内にそのような提出要件に適合しているかどうかを示すx はい、そうですo違います。
再選択マークは、登録者が過去12ヶ月以内(または登録者がそのような文書の提出を要求されたより短い時間以内)に、S−T規則405条(本章232.405節)に従って提出を要求した各相互作用データファイルを電子的に提出したか否かを示すx はい、そうですo違います。
再選挙マークで登録者が大型加速申請者、加速申請者、非加速申請者か新興成長型会社かを示す。取引法第12 b-2条の規則における“加速申請者と大型加速申請者”と“新興成長型会社”の定義を参照。
| | | | | | | | | | | | | | |
| 大型加速ファイルサーバ | x | | ファイルマネージャを加速する | o |
| 非加速ファイルマネージャ | o | | 新興成長型会社 | o |
もしある新興成長型会社が米国公認会計原則に従ってその財務諸表を作成した場合、登録者が延長された過渡期間を使用しないことを選択したかどうかをチェック番号で示し、取引所法案第13条(A)に規定されている任意の新しいまたは改正された財務会計基準に適合するo
新たな又は改訂された財務会計基準とは、財務会計基準委員会が2012年4月5日以降に発表したその会計基準編纂の任意の更新を意味する。
登録者が報告書を提出したかどうかを再選択マークで示し、その経営陣が“サバンズ-オキシリー法案”(“米国連邦法典”第15編、第7262(B)節)第404(B)条に基づいてその財務報告の内部統制の有効性を評価したことを証明する。この評価は、その監査報告書を作成または発行する公認会計士事務所によって行われるx
登録者が本文書に含まれる財務諸表を作成する際にどのような会計基盤を使用しているかをチェックマークで示す
| | | | | | | | | | | | | | | | | | | | | | | |
| アメリカは会計原則を公認している | o | | 国際財務報告基準国際会計基準委員会が発表した | x | | 他にも | o |
前の質問に答えたときに“その他”をチェックした場合は、登録者がどの財務諸表項目に従うかをチェックしてくださいoプロジェクト17oプロジェクト18
これが年次報告書である場合は、登録者が空殻会社であるか否かをフックで示してください(取引法第12 b-2条で定義されているように)oはい、そうですx違います。
伝奇生物集団
表格20-F年次報告
カタログ
| | | | | | | | |
| | ページ |
| 第1部 | |
| | |
第1項。 | 役員·上級管理職·コンサルタントの身分 | 6 |
第二項です。 | 割引統計データと予想スケジュール | 6 |
第三項です。 | 重要な情報 | 6 |
第四項です。 | 会社についての情報 | 95 |
プロジェクト4 Aです。 | 未解決従業員意見 | 159 |
五番目です。 | 経営と財務回顧と展望 | 160 |
第六項です。 | 役員、上級管理者、従業員 | 178 |
第七項。 | 大株主と関係者が取引する | 192 |
第八項です。 | 財務情報 | 197 |
第九項です。 | 見積もりと看板 | 197 |
第10項。 | 情報を付加する | 198 |
第十一項。 | 市場リスクの定量的·定性的開示について | 206 |
第十二項。 | 株式証券を除くその他の証券説明 | 206 |
| | |
| 第II部 | |
| | |
十三項。 | 違約、延滞配当金、延滞配当金 | 209 |
14項です。 | 保証所有者の権利と収益使用の実質的な改正 | 209 |
第十五項。 | 制御とプログラム | 209 |
第十六項。 | 保留されている | 211 |
プロジェクト16 A。 | 監査委員会財務専門家 | 211 |
プロジェクト16 B。 | “道徳的規則” | 211 |
プロジェクト16 Cです。 | チーフ会計士費用とサービス | 211 |
プロジェクト16 Dです。 | 監査委員会の上場基準の免除 | 212 |
プロジェクト16 E。 | 発行者および関連購入者が株式証券を購入する | 212 |
プロジェクト16 Fです。 | 登録者の認証会計士を変更する | 212 |
プロジェクト16 Gです。 | 会社の管理 | 213 |
16 H項です。 | 炭鉱安全情報開示 | 213 |
プロジェクト16 I。 | 検査妨害に関する外国司法管区の開示 | 195 |
| | |
| 第三部 | |
| | |
17項です。 | 財務諸表 | 215 |
第十八項。 | 財務諸表 | 215 |
プロジェクト19. | 陳列品 | 215 |
サイン | 218 |
いくつかの情報
本年報20-F表(“年報”)では、説明や文意が別に指摘されているほか、“伝奇生物”はケイマン諸島持株会社の伝説生物を指し、“中国付属会社”は伝奇生物が中国で登録設立された付属会社(以下、“私たち”、“吾等”及び“当社”を意味し、“当社”とは伝奇生物とその総合付属会社を指す。“遺伝子スクリプト”や“遺伝子スクリプト”に言及するとは、我々の大株主であるキングスレー生物科学技術を指す。
私たちの財政年度は12月31日に終わるだろう。ある“財政年度”に言及するとは、当該財政年度12月31日までの財政年度を指す。当社の総合財務諸表は国際会計基準委員会が公布した国際財務報告基準(“IFRS”)に基づいて作成されたものである。私たちはアメリカで公認された会計原則に従って作成された財務諸表を持っていない。
本年報は読者の便宜のために人民元(“人民元”)金額を指定為替レートでドルに換算した。私たちは、本年度報告で言及された人民元またはドルの金額が、任意の特定の為替レートまたは根本的にドルまたは人民元に両替できるかどうかを示しません(場合によっては)。特別な説明を除いて、本年度報告書の人民元はドルに換算され、人民銀行が発表した2022年12月31日までの人民元対1ドルの為替レートで計算される。
本文書に記載されている様々な金額やパーセンテージは四捨五入されているため,本文書に列挙されている表の有意差を説明している可能性がある.本年度報告では、他に説明や文意が指摘されている以外に、以下のように言及されている
•“米国預託株式”とは、米国預託株式のことであり、1株当たり米国預託株式は私たちの2株の普通株式を代表する
•ADRとは、米国預託証明書を証明する米国預託証明書を意味する
•“中国”または“中国”とは、人民のRepublic of Chinaを指し、中国の規則、法律、法規及びその他の法律及び税務事項を記述する場合にのみ、香港特別行政区、マカオ特別行政区及び台湾の規則、法律、法規及びその他の法律及び税務事項を含まないが、本出願で議論されている中国での経営に関する法律及び経営リスクは香港及びマカオにも適用され、“大中国”は香港特別行政区、マカオ特別行政区及び台湾を排除しない
•“普通株”とは、自社の普通株のことで、1株当たり0.0001ドルの価値がある
•“人民元”とは中華人民共和国の法定通貨を意味する
•“A系列優先株”とは、A系列優先株、1株当たり額面$0.0001;および
•“ドル”または“ドル”は米国の法定通貨である。
本年度報告の日までに,我々の組織構造は“第4項であるC社の組織構造情報”を参照されたい
市場、業界、その他のデータ
本年度報告には、これらの市場の推定規模および特定の医療条件の発生率に関するデータを含む、我々の業界、私たちの業務、および候補製品市場の推定、予測およびその他の情報が含まれている。我々は,我々の内部見積りと研究および学術·業界研究,出版物,調査,第三者(政府機関を含む)による研究から,本年度報告に記載されている業界,市場,類似データを得た.いくつかの場合、私たちはこのようなデータの出所を明確に言及しなかった。見積り,予測,予測,市場研究や類似手法に基づく情報自体が不確定要因の影響を受け,実際のイベントや状況は本情報で想定しているイベントや状況とは大きく異なる可能性がある.私たちは私たちが使用した第三者データが信頼できると信じているが、私たちはこのデータを単独で確認していない。また,我々の内部研究は信頼できると信じているが,このような研究は第三者の検証は得られていない.このような情報、予測、見積もりをあまり重視しないように注意してください。
商標とサービスマーク
本年報に登場する“伝説的生物”、連想標識および会社の他の商標またはサービス標識はすべて会社の財産である。便宜上、本年度報告で言及された商標、サービスマーク、および商号は使用されておらず、および他の同様の記号が使用されていないが、このような参照は、適用法に従って、私たちの権利または適用許可者がこれらの商標、サービスマーク、および商号に対する権利を最大限に主張しないことを意味するわけではない。CARVYKTIは米国におけるジョンソンの登録商標である。本年度報告に登場する他社の他の商標,商標,サービスマークは,それぞれの所有者の財産である。私たちは、他の人との関係、または私たちの裏書きやスポンサーを暗示するために、他の会社の商標、サービスマーク、または商号を使用したり、展示したりするつもりはありません。
前向きな陳述に関する警告的声明
本年度報告書には,1995年の個人証券訴訟改革法に適合した前向きな陳述が含まれている。現在と歴史的事実と条件に関する陳述を除いて、すべての陳述は前向き陳述である。このような展望性陳述は私たちの現在の未来事件に対する期待と見方を反映しているが、未来の業績の保証ではない。逆に、それらは、私たちの現在の業務の未来、未来の計画と戦略、私たちの運営結果、および他の未来の条件に対する私たちの信念、期待、仮説に基づいている。展望的な陳述は、本年度報告の複数の場所に現れ、私たちの意図、信念、または現在の予想に関する陳述を含み、これらの陳述は、私たちの運営結果、財務状況、流動性、見通し、成長、戦略、および私たちが経営する業界に関するものである。
前向き記述は、“可能”、“予想”、“予想”、“目標”、“推定”、“計画”、“計画”、“信じる”、“可能性”、“潜在”、“継続”または他の同様の表現によって識別することができる。私たちのこれらの展望的な陳述は主に私たちの現在の未来の事件に対する予想と予測に基づいており、私たちはこれらの事件が私たちの財務状況、経営結果、業務戦略と財務需要に影響を与える可能性があると考えている。これらの前向きな陳述は、以下に関連する陳述を含むが、これらに限定されない
•CARVYKTIを効率的に製造、マーケティング、販売することができます
•CARVYKTIビジネス成功の市場機会と潜在力;
•CARVYKTI治療の潜在的効果;
•私たちの臨床試験は候補製品が受け入れられる安全性と有効性、その他の積極的な結果を証明することができます
•我々が開発可能な候補製品の臨床前研究および臨床試験の時間、進捗および結果は、研究または試験および関連準備作業の開始と完了に関する時間、試験結果の期限、および我々の研究および開発計画を含む
•私たちの製品候補製品の最終規制承認を含む、届出と承認の時間、範囲、可能性を規制する
•ヤンソンバイオテクノロジー社(“ヤンソン”)との協力により、特定のマイルストーンを実現することができる
•私たちは現在の候補製品や計画を開発し推進し臨床試験を成功させることができます
•私たちの製造商業化マーケティング能力戦略
•承認されれば、重点地域と販売戦略を含む候補製品の商業化に関する計画
•より多くの人を雇用し、これらの人々を引き付け、維持し、奨励する能力が必要だ
•私たちの候補製品の市場機会の大きさは、私たちの目標疾患を患っている患者数の推定を含む
•私たちは、私たちの候補製品を第1、第2、または後続治療ラインとして承認し、使用すること、または他の薬剤との併用を期待している
•私たちの競争的地位と既存または可能な競争療法の成功
•臨床試験に組み込まれる患者数の推定は
•私たちの候補製品の有益な特性、安全性、有効性、治療効果
•私たちは規制部門の候補製品に対する承認を得て維持することができる
•私たちが求める可能性のある他の適応も含めて私たちの候補製品をさらに開発する計画について
•私たちの知的財産権状況は、既存の特許条項の拡張、第三者が持っている知的財産権の有効性、私たちが侵害しない、流用しない、または他の方法で第三者の知的財産権を侵害する能力を含む、私たちが開発可能な候補製品のために確立され、維持できる知的財産権保護範囲を含む
•私たちは引き続き第三者に依存して私たちの候補製品に対して追加の臨床試験を行い、臨床前研究と臨床試験のために私たちの候補製品を生産した
•私たちは、私たちの候補製品を開発、製造、または商業化するために必要または必要な任意の協力、許可、または他の手配の有利な条項を獲得して交渉することができる
•承認されれば、私たちが開発する可能性のある候補製品の価格設定と精算
•インフレの結果、これらの情報をタイムリーに得る能力を含む労働力、輸送、および原材料の価格および獲得可能性に関する情報
•為替変動、外国為替規制、定価制限など、海外業務固有のリスクへのリスク開放とその潜在的な影響
•私たちが開発可能な候補製品の市場受容度と臨床的実用性の速度と程度
•我々の重要な情報技術システム、ネットワーク、プロセス、または関連する制御、または当サービス提供者の制御の有効性
•費用、将来の収入、資本需要、追加融資需要の推定
•私たちの財務業績は
•私たちは重要な弱点を補う能力を含む財務報告書の効果的な内部統制の能力を維持し続けている
•税法の変化と解決は追加納税義務または納税事項をもたらす
•私たちの既存の現金と現金等価物は、私たちの将来の運営費用と資本支出需要の期間を支払うのに十分であると予想される
•関税の影響を含む米国または外国の法律法規が会社の運営に与える影響;
•私たちは、新冠肺炎の大流行(緩和措置を含む)、インフレ率の上昇、地政学的緊張、金融機関の失敗および不安定、またはこのような中断の実際または予想影響に関連する需要、供給および運営挑戦を管理する能力を含む、流行病および流行病の影響、例えば新冠肺炎の大流行(緩和措置を含む)の影響を受ける可能性がある。
このような展望的な陳述は様々な危険と不確実性と関連がある。私たちは私たちがこのような展望的陳述で表現された予想が合理的だと信じているが、私たちの予想は後で発見されるかもしれない。多くの重要な要素は、本年度報告“リスク要素”に列挙された要素及びその他の既知と未知のリスクと不確定要素を含み、著者らの実際の結果、業績或いは成果は展望性陳述中の明示或いは暗示の結果、業績或いは業績と大きく異なることを招く可能性がある。また、我々の経営結果、財務状況、流動性が本年度報告に含まれる前向き陳述と一致していても、これらの結果や発展は、後続期間の結果や発展を表すことができない可能性がある。本期間を従来のいずれの期間の結果と比較するかは、任意の将来の傾向や将来の業績の兆候を示すためではなく、特に説明しない限り、履歴データのみとすべきである。あなたは本年度報告書と私たちが参考にした文書をよく読んで、私たちの未来の実際の結果が私たちが予想していたものと大きく違って、さらに悪いかもしれないということを理解しなければならない。私たちはこのような警告声明を通じて私たちのすべての展望的声明を限定する。
本年度報告で行われた前向き陳述は,陳述が行われた日までの事件や情報のみに触れている。法律に別の要求がない限り、私たちは、陳述の日の後、または意外な事件の発生を反映するために、新しい情報、未来のイベント、または他の理由でも、いかなる前向きな陳述を公開更新または修正する義務はない。あなたは本年度報告書と私たちが添付ファイルとして提出した文書を完全に読んで、私たちの未来の実際の結果が私たちが予想していたものと大きく異なる可能性があることを理解しなければなりません。このような危険と不確実性を考慮して、あなたがこのような展望的な陳述に過度に依存しないように注意します。
第1部
項目1.役員、上級管理者、コンサルタントの身分
適用されません。
項目2.見積統計データと予想スケジュール
適用されません。
プロジェクト3.重要な情報
わが国の持株会社構造と中国経営
レノボ生物科学技術はケイマン諸島持株会社であり、中国運営会社ではない。私たちは主にアメリカ、中国、EU(“EU”)にある運営子会社を通じて運営しています。私たちの中国での業務と、私たちの世界の他の場所での業務は、私たちがそこに設立した子会社によって支援されています。私たちアメリカ預託証明書の投資家は私たちの運営子会社の株式証券を持っていません。ケイマン諸島持株会社の株式証券を持っています。会社構造の説明については、“項目4-会社情報-C.組織構造図”を参照されたい
私たちは、私たちの中国における一部の業務や複雑で変化していく中国の法律法規に関連する様々な法律と運営リスクと不確実性に直面している。例えば、私たちは、中国国外で行われている発行や中国以外の個人や実体(“非中国投資家”)が中国に業務を持っている発行者に投資することに関する監督審査や届出要求、反独占規制行動、ネットワークセキュリティ、データプライバシーと遺伝情報の監督に関するリスクに直面している。もし吾らが関連する監督管理規定を遵守できなければ、吾などがある業務を展開し、非中国投資家の投資を獲得したり、中国海外証券取引所に上場する能力にマイナス影響を与える可能性がある。もし吾らが吾らの中国国外での発売や投資に適用されるこのような規制規定を遵守できなければ、中国は吾などの中国付属会社の資産に対して行動する可能性があり、吾などの中国での業務に重大な悪影響を及ぼす可能性がある。したがって、これらのリスクは、私たちの業務と私たちのアメリカ預託証明書の価値に重大な不利な変化をもたらし、投資家に証券を提供または継続する能力を著しく制限、延期、または阻害し、あるいはそのような証券の価値を大幅に低下させる可能性がある
私たちの中国での業務は中国の法律法規によって管轄されている。中国政府当局は私たちの中国での業務に対して重大な監督と裁量決定権を持っており、私たちが中国の法律や法規に準拠していないか、または該当しない可能性がある場合、それは私たちの運営に介入または影響を与える可能性があり、これは私たちの運営および/または私たちのアメリカ預託証明書の価値に重大な不利な変化をもたらす可能性がある。また、中国政府当局は最近、中国国外で行われている発行および/または非中国投資家に対して、中国で業務を行っている発行者への投資により多くの監督と制御を加える意向を示している。このような行動は、私たちの中国付属会社の資産に行動を起こし、それによって私たちの中国での業務に重大な悪影響を与え、投資家への証券の発売または継続を阻害したり、そのような証券の価値を大幅に下落させたりすることを著しく制限、遅延、または阻害する可能性がある。また、私たちの業務に直接向けた全業界法規の施行は、私たちの証券の価値を大幅に低下させる可能性があります。したがって、私たちの株主と私たちの業務は、中国政府当局が取った影響私たちの中国での業務の行動の潜在的な不確実性に直面している
中華人民共和国の法律制度は成文法規に基づく民法制度である.一般法制度と異なり,従来の裁判所判決は参考になるが,その先例価値は限られている。中国はまだ完全に統合された法律体系を構築しておらず、最近公布された法律、規則、法規は中国の経済活動のあらゆる面をカバーするのに十分ではないかもしれない、あるいは中国の監督管理機関と裁判所の大きな解釈を受ける可能性がある。特に、これらの法律、規則、および条例は比較的新しいため、公表された決定の数が限られているため、これらの決定は非前例的な性質を持っており、これらの法律、規則、規則および条例は、それらをどのように実行するかに関する規制機関に重大な裁量権を与えることが多く、これらの法律、規則および条例の解釈と実行は不確実性に関連し、不一致で予測不可能である可能性がある。したがって、未来には私たちの既存の運営が関連された法律に完全に適合していないことが発見されるかもしれない。また、中国の法制度部分は政府政策と内部規則に基づいており、その中のいくつかは適時に公表されていないか、あるいは全く公表されておらず、追跡力を持っている可能性がある。したがって、私たちは違反が発生してから、私たちがこのような政策と規則に違反していることを認識しなければならないかもしれない
最近、中国政府は中国国外で行われている発行および/または非中国投資家に対して中国で業務を持っている発行者の投資により多くの監督と制御を加える意向を表明し、一連の監督管理行動を開始し、証券市場の不法活動に打撃を与え、中国で業務を持っている会社の中国国外での上場に対する監督管理を強化し、新しい措置を講じてネットワーク安全審査範囲を拡大し、反独占法執行を強化することを含む一連の公開声明を発表した。したがって、私たちの業務が直面しているリスクは、中国政府当局の中国子会社の業務と融資活動に対する重大な監督と裁量決定権、複雑かつ発展している中国の法律制度、法律、法規と政府政策の頻繁な変化、法律と法規に関する解釈と実行の不確実性と不一致、規制の承認を得たり、非中国証券取引所に上場したり、いくつかの業務活動を行う届出手続きを完成させる上での不確定性、困難や遅延、および中国政府が最近発表した声明や実施された規制行動に関連するネットワークセキュリティやデータプライバシーのより多くの規制を受け、中国子会社の資産に対する行動を引き起こす可能性がある。これは私たちの中国での業務に重大な悪影響を及ぼす可能性があり、投資家への証券の発売または継続を阻害する能力を著しく制限し、遅延したり、そのような証券の価値を大幅に下落させたりする可能性がある。中国の法律体系および中国の法律法規の解釈と実行における不確実性は、あなたと私たちが利用可能な法的保護を制限する可能性があり、米国の預託証明書を提供または継続する能力を著しく制限、遅延、または阻害し、私たちの業務運営に重大な悪影響を与え、私たちの名声を損なう可能性があり、これはさらに米国の預託証明書の価値を大幅に低下させる可能性がある。
我々の中国での経営リスクの詳細については,“-D.リスク要因−中国でのビジネスに関するリスク”を参照されたい
“外国会社の責任追及法案”
2021年12月16日、上場企業会計監督委員会は、地方当局の職位の原因により、大陸部と香港に本部を置く上場企業会計監督委員会に登録されている会計士事務所中国を完全に検査または調査できないことを決定する報告書を発表した。“外国会社の責任追及法案”(“HFCA法案”と略す)は2020年12月18日に法律に署名した。HFCA法案によると、PCAOBが2021年から3年連続で私たちの監査人を検査あるいは全面的に調査できないと判断した場合、取引所は私たちのアメリカ預託株式を取得することを決定する可能性があり、私たちのアメリカ預託証券はアメリカ国家証券取引所あるいは場外取引市場での取引を禁止する可能性がある
2021年12月2日、米国証券取引委員会は最終改正案を可決し、“米国証券取引委員会法案”の下での開示·提出要求を実施し、この改正案によれば、発行者が公認会計士事務所が発行した監査報告を掲載した年次報告書を提出しており、PCAOBは外国司法管轄区域当局の立場により当該発行者を完全に検査または調査できないと考えている場合、米国証券取引委員会は(I)発行者を“証監会が指定した発行者”と識別し、(Ii)発行者が3年連続で委員会指定の発行者として決定された後、当該発行者に対して取引禁止を実施する。2022年12月29日、総裁·バイデンは“高周波取引法案”の改正を含む“2023年総合支出法案”に署名し、発行者を米国証券取引委員会で発行者の証券に対して初期取引禁止を実施しなければならない初期取引禁止を3年から2年までに減少させ、数年連続で委員会指定の発行者として決定することができる。そのため、発行者が2年連続で証監会指定の発行者として決定されると、米国証券取引委員会は“高頻度取引法案”の規定に基づき、発行者の証券の国家証券取引所と場外取引市場での取引を禁止しなければならない。
2022年8月26日、PCAOBは中国証監会(証監会)と人民財政部Republic of Chinaと“議定書声明”に署名し、PCAOBの開放に向かって大陸部と香港に本部を置く公認会計士事務所の検査と調査に第一歩を踏み出した。2022年12月15日、PCAOBは“米国法”第15章7214(I)(2)(A)条とPCAOB規則6100に基づいてHFCAA確定報告書を発表し、PCAOBがそれについて撤回することはできない
中国大陸部と香港に本部を置く完全公認会計士事務所は、国内関係部門の職に就いているため、検査または調査を行う。これらの裁決を撤回すると同時に、PCAOBは、中国大陸部または香港のどの当局が取った立場により、中国大陸部または香港の監査師に対して検査や調査を行う際にいかなる障害に遭遇した場合、PCAOBは直ちに行動し、HFCA法案とPCAOB規則6100に適合した新しい裁決を発表する必要があるかどうかを再考すると指摘している。
私たちの監査役は、2021年12月31日と2020年12月31日の会計年度まで、独立公認会計士事務所安永華明法律事務所である。PCAOBは安永華明法律事務所がPCAOBが徹底的に検査や調査できない公認会計士事務所の一つであることを確認した
2022年5月4日に最終的に“委員会が認定した発行者”に決定された。我々の監査委員会(I)は、2022年5月3日、安永華明法律事務所が当社の独立公認会計士事務所を辞任することを決定し、2022年6月1日から当社が米国証券取引委員会に提出した財務諸表を監査·財務報告内部統制し、2013年12月31日までの財政年度の当社財務諸表監査と財務報告内部統制の独立公認会計士事務所の招聘を承認した。本年度報告書には2022が含まれており,当社はその後安永法律事務所と招聘状を締結している。しかし,PCAOBが安永華明法律事務所の事実を検査できないことは,投資家のこのような検査のメリットを奪い,我々の証券がHFCA法案によって破棄される可能性がある。また、安永法律事務所との協力はもはや“委員会が認めた発行元”ではない保証はない
安永法律事務所は依然としてPCAOB検査または調査要求時に任意の監査作業の原稿を提示し、検査または調査要求時にPCAOBに任意の関連監査者を提供することができなければならない。安永法律事務所はPCAOB検査や調査要求に関するいかなる法律または専門義務を履行できなかったか、あるいは安永法律事務所がすべての適用された監査基準を遵守できなかったことは、私たちが重大な責任を負うことになったり、HFCA法案によって私たちの証券が外されたりする可能性がある。
PCAOBが2年連続で監査役を検査できない場合、HFCA法案によると、2022年5月4日に米国証券取引委員会によって委員会によって指定された発行者として決定されたため、我々の米国預託証明書が取得される可能性がある私どもの証券退市や当該等証券退市の脅威は、あなたの投資価値に重大な悪影響を及ぼす可能性があります。関連するリスクの詳細な説明については、“-D.リスク要因-中国のビジネスに関連するリスク-PCAOBが2年連続で監査役を検査できない場合、2022年5月4日に米国証券取引委員会委員会によって発行者として決定されたので、我々の米国預託証明書はHFCA法案によって破棄される可能性がある。私たちの証券が退市したり、私たちの証券が退市の脅威にさらされたりする可能性があり、あなたの投資価値に重大かつ不利な影響を与える可能性があります。また,PCAOBは検査を行うことができず,投資家がこの検査から得たメリットを奪っている
われわれの運営は中国当局の許可を得る必要がある
私たちのすべての中国付属会社は国家市場監督管理総局(“国家市場監督管理総局”)の現地対応機関が発行した営業許可証を取得し、取得しなければならない。本年報の日付および吾らの知る限り、私たちの中国付属会社は中国政府当局から中国での業務運営に重要な意義を持つ必要なナンバープレートと許可を取得している。しかし、関連法律法規の解釈と実施、政府当局の法執行実践に不確実性があることを考慮して、中国で業務を展開するために必要なすべての許可証または許可証を取得したことを保証することはできません。
吾らは以前に中国海外証券市場で投資家に証券を発行したことについて、中国の現行の法律、法規及び監督管理規則に基づいて、本年報の日付に基づいて、吾ら及び吾らの中国付属会社:(I)中国証監会の許可を取得しなければならない;(Ii)中国網信弁(“網信弁”)のネットワーク安全審査を受ける必要がある;及び(Iii)吾らの知る限り、吾らはいかなる中国当局に必要な許可を得ていないか、あるいは拒否されている。しかし、中国政府は最近、中国国外で行われている発行および/または非中国投資家に対して、中国で業務を持っている発行者への投資により多くの監督と制御を加える意向を示している。
著者らはずっと中国の監督管理動態に注目し、中国証監会、中国食品薬品監督管理局或いはその他の中国監督管理機関が私たちの中国業務に対する任意の必要な許可或いは承認に注目してきた。しかし、関連法規の要求の解釈と実施には不確定性が存在し、中国の生物製薬業界は厳格な監督管理を受けており、このような法規は変化する可能性がある。したがって、私たちまたは私たちの中国子会社が、絶えず変化する中国の法律と法規に基づいて、私たちの業務運営に関連する追加の承認、許可または許可または追加の届出手続きを得る必要があるかどうか、および私たちがこのような承認、許可証または許可証を取得し、更新することができるかどうか、あるいはそのような届出手続きを適時または根本的に完了することができるかどうかはまだ確定されていない。私たちまたは私たちの中国子会社は、適用される中国の法律や法規を適時または根本的に遵守できなかったり、必要な許可や許可をタイムリーまたは根本的に取得したりすることができず、行政処罰を受ける可能性があり、私たちまたは中国子会社が中国での業務活動を一時停止または終了させる可能性があります。“--D.リスク要因--中国のビジネスに関わるリスク”を見てください
配当金とその他の分配
本年の期日まで、当社はこれまでいかなる現金配当金或いは実物配当金を発表或いは派遣していないし、近いうちに普通株或いはアメリカ預託証明書についていかなる配当金を発表或いは派遣する計画もない。私たちは今
未来のどんな収益もCilta-celの臨床開発に資金を提供し、私たちの製造施設の建設と拡張に資金を提供し、CARVYKTIの商業化に資金を提供し、私たちのパイプラインプロジェクトの開発に資金を提供し、運営資金と他の一般企業用途に資金を提供する.
伝説的な生物は持ち株会社で、自分の業務を持っていない。私たちは私たちの子会社を通じて、私たちの中国子会社を含めて業務を展開している。もし中国政府が中国子会社によるいかなる業務運営も将来的に非中国投資を制限または禁止すべきであると考えた場合、私たちは中国での業務運営を停止することを要求される可能性があり、重大な処罰を受けたり、影響を受けた業務における私たちの権益を放棄させられたりする可能性がある。このような事件は私たちの業務に大きな変化をもたらす可能性があり、私たちの証券の価値も大きく変化し、このような証券の価値が大幅に低下することを含む。私たちは歴史的に運営によって純損失と負のキャッシュフローが発生したため、本年度の報告日まで、私たちはレジェンド生物あるいは投資家に配当金や分配を発表したり、支払ったりする子会社はありません。逆に私たちは主に私たちの協力と許可協定(“Janssen協定”)によると、Janssenから得られた前金とマイルストーン支払い、ならびに有利子借款、公開発行および私募株式証券の収益、およびGenScripからの資本貢献私たちの運営子会社の業務運営に資金を提供します。私たちが金融活動から得たすべての現金純収益はまず伝説的な生物の銀行口座に入金される。伝奇生物口座に入金された資金は、その後、伝奇生物適用子会社を介して各運営子会社に移転し、主に出資や会社間融資によりその運営資金需要を満たす。伝説的生物は、2022年と2021年12月31日までの年間で、このような出資や会社間融資によりそれぞれ340.0ドルと396.6ドルを移転した。私たちは現在、私たちのアイルランド子会社レジェンド生物アイルランド株式会社を伝説生物の財務センターにすることを計画しています。
“中華人民共和国外商投資法”及びその実施細則に基づいて、非中国投資会社が管理する法律枠組みを共同で確立し、非中国投資家は他の適用法律に基づいて、その出資、利益、資本収益、資産処分収入、知的財産権、取得した特許使用料、合法的に獲得した賠償或いは賠償、及び清算して得られた収入を、人民元或いは任意の非中国通貨領域内で自由に中国に調達或いは呼び出し、いかなる単位或いは個人は通貨、金額と頻度の面でこのような移転を不法に制限してはならない。中国会社法及びその他の中国の法律及び法規によると、私たちの中国付属会社は中国の会計基準及び法規に基づいて定められたそれぞれの累積利益から配当金を派遣することしかできない。また、私たちの各中国付属会社は毎年、その基金総額がその登録資本の50%に達するまで、毎年少なくとも10%の累積税引き後オーバーフロー(あればある)をある法定準備基金として保留しなければならない。法定積立金が中国子会社の前の財政年度に発生した損失を補うのに不十分であれば、まず本財政年度の累計税引き後利益を赤字を補うために使用し、それから法定積立金を抽出しなければならない。これらの法定積立金と赤字を補うための累積税引き後利益は配当金として私たちに分配することはできません。我々の中国子会社は適宜中国会計基準に基づいてその税引後利益の一部を自由支配可能備蓄基金に振り込むことができる。“--D.リスク要因--中国でのビジネスに関するリスク--私たちの業務は新たに公布された”外商投資法“と”ネガティブリスト“の重大な影響を受ける可能性がある
人民元は自由に他の通貨に両替できません。そのため、通貨両替に対するいかなる制限も、私たちの中国子会社がその潜在的な未来の人民元収入を利用して私たちに配当金を支払う能力を制限する可能性がある。中国政府は人民元の非中国通貨への両替を規制し、場合によっては中国からの送金通貨の規制も実施している。非中国通貨の供給不足は、私たちのオフショア実体が配当金を支払うか、他のお金を支払うか、または他の方法で私たちの非中国通貨建ての債務を履行するために、私たちのオフショア実体に十分な非中国通貨を送金する能力を制限するかもしれない。人民元は現在“経常項目”で両替でき、“経常項目”には配当金、貿易、サービス関連の非中国外貨取引が含まれているが、“資本項目”の下で両替することはできず、“資本項目”には非中国直接投資と非中国通貨債務が含まれており、岸子会社で獲得する可能性のある融資を含む。現在、我々の中国子会社は、国家外国為替管理局中国(“外管局”)の承認を必要とせず、一定の手続き要件を遵守することを含む、中国以外の通貨を購入して“経常口座取引”の決済に使用することができる。しかし、中国の関係政府当局は、将来的に非中国通貨を購入して経常口座取引を行う能力を制限または撤廃する可能性がある。中国政府は引き続きその資本規制を強化する可能性があり、外管局は経常口座と資本口座に同時に属する国境を越えた取引に対して追加の制限と実質的な審査手続きを実施する可能性がある。いかなる既存および将来の通貨両替制限は、人民元で発生した収入を利用して中国以外の業務活動に資金を提供したり、非中国通貨で私たちの証券保有者に配当金を支払う能力を制限する可能性がある。資本項目下の非中国外国為替取引は依然として制限されており、外管局やその他の関連中国政府当局の承認や登録を得る必要がある。これは私たちが子会社のための債務や株式融資を行うことで非中国通貨を獲得する能力に影響を与える可能性がある。また、アメリカ預託株式保有者は中国を受ける可能性があります
私たちが中国住民企業とみなされている場合、私たちが支払った配当金の税金。リスク要因-中国でのビジネスに関連するリスク-私たちが中国にある子会社から受け取った配当金は、中国の源泉徴収税を支払う必要があるかもしれません。これは、私たちの株主に支払う可能性のある配当金額に重大かつ不利な影響を与える可能性があります“および”第10項追加情報-E.税収-中国税収“です。
A.[保留されている]
B.資本化と負債化
適用されません。
C.収益を提供し使用する理由は
適用されません。
D.リスク要因
私たちの業務と産業は重大な危険に直面している。我々の業務を評価する際には、本年度報告と、以下のリスク要因を含む、米国証券取引委員会に提出された他の文書に記載されているすべての情報を慎重に考慮すべきである。実際に以下のいずれかのリスクが発生すれば、我々の業務、財務状況、経営業績、成長見通しは実質的な悪影響を受ける可能性がある。本年度報告書にはまた、リスクと不確定要素に関する前向きな陳述が含まれている。“前向きな陳述に関する警告声明”を参照してください
リスク要因の概要
以下の要約は,我々が正常な業務活動の過程で直面している重大なリスクについて概説する.要約は完全であると主張するのではなく,本要約の記述に続く包括的なリスク要因議論を参照することで全文を限定する私たちはあなたが完全な危険要素討論をよく読むことを奨励します
私たちの収入と支出は予測が難しく、過去の変化は大きく、多くのリスクと不確定要素のため、未来は引き続き大幅に変動し、その多くは私たちがコントロールできない。したがって、私たちは四半期や年間利益を達成できないかもしれない。私たちの業務、経営結果、財務状況は、以下のいずれかの重大なリスクの重大な悪影響を受ける可能性があります
CARVYKTIや他の候補製品の商業化に関するリスク
•私たちはCARVYKTIのビジネス成功に大きく依存している。もし私たちがCARVYKTIを商業化することに成功しなかったり、商業化の過程で重大な遅延に遭遇したら、私たちの業務は実質的な損害を受けるだろう。
•ビジネス会社として、私たちの経験は限られていて、CARVYKTIや未来の製品の製造、マーケティング、販売は成功しないかもしれないし、予想以上に成功していないかもしれません。
•CARVYKTIと任意の未来製品の商業成功は医師、第三者支払人と医学界の他の人の市場に対する受け入れの程度に依存する。
•もし私たちの製品や任意の未来の製品の市場機会が私たちが思っているより小さい場合、患者を識別して著しい市場シェアを得ることができなければ、私たちの収入は悪影響を受ける可能性があり、私たちの業務は影響を受ける可能性があります。
•臨床試験や商業販売に必要な製品の需要を満たすために、自分の製造インフラを作ることに成功しないかもしれません。
•私たちは以前販売経験がなく、マーケティングと市場アクセス能力が限られていた。私たちは、私たちのビジネスニーズを支援するために、必要な能力やインフラを構築するために、大量の財政·管理資源を投入し続ける予定です。もし私たちがこのような商業能力を作ることができなければ、私たちは私たちの業務を維持するのに十分な収入を生むことができないかもしれない。
•私たちは急速に変化する産業で運営され、激しい競争に直面している。
•潜在的な製品責任リスク。
私たちの業務に関わるリスク
•複雑な治療法の開発と商業化の不確実性により、私たちは実現し、利益を維持する能力は永遠に実現しないかもしれないし、利益を維持することはできないかもしれない。
•私たちの限られた運営の歴史は研究開発に集中してきましたが、将来の見通しを評価するのは難しいです。
•私たちは私たちの候補製品の開発を完了するために追加の資金が必要で、これは全くなければ受け入れられる条項では提供できないかもしれない。
•私たちは製品製造に必要な原材料や重要な出発材料(例えばレンチウイルスベクター)を得ることができず、これらの製品の臨床開発と商業化に悪影響を与え、更に私たちの販売と収益力に悪影響を及ぼす可能性がある。
私たちの候補製品開発に関するリスク
•新たかつ緊急治療のためのバイオ製薬開発過程の不確実性は,臨床試験結果の不確実性や,候補製品が安全性や有効性を示すことができない可能性がある。
•私たちの候補製品に対する規制承認を得たり維持することができないかもしれない。
•われわれの主な研究開発は細胞療法に集中しており,キメラ抗原受容体T細胞(CAR−T)療法とキメラ抗原受容体ナチュラルキラー細胞(CAR−NK)療法を含み,重大な挑戦と障害に直面している新興療法である。
•私たちの候補製品は大量の臨床前研究と臨床試験が必要であり、これは設計と実施が難しいかもしれない。
•我々は臨床試験における患者の募集に依存して候補製品を開発している。
•我々が完全にコントロールできない研究者による臨床試験や研究に関するリスク。
•特定の製品機会は限られた市場機会に直面するかもしれない
•私たちの候補製品に関連した不良副作用や他の安全リスク。
•複雑な細胞療法を作るコストと困難。
私たちの業務運営に関するリスク
•国際事業に関連した経済、政治、規制、そして他の危険。
•業務の拡大とキーパーソンの誘致と維持には潜在的な困難がある。
•潜在的な買収や戦略的協力に関連する危険。
•情報技術システムへの依存。
•政府の各法律法規を守らないいかなる行為も私たちの業務に悪影響を及ぼす可能性がある。
•財務報告の実施と有効な内部統制を維持できなかったことに関連するリスクは、発見された重大な弱点および任意の将来の重大な弱点による任意の影響を含む。
私たちの第三者への依存に関するリスク
•私たちの候補製品の開発、製造、商業化はヤンソンなどの第三者に依存している。
•われわれは第三者の臨床前と臨床試験への依存と,このような第三者が満足できない可能性を示している。
•試薬、専用デバイス、および他の専用材料の利用可能性。
我々の候補製品の規制承認とその他の法的適合性問題に関するリスク
•厳格、複雑と絶えず変化する監督管理枠組みに関連するリスクとコストは、臨床試験法規、発売前法規の要求、定価、精算とコスト制御法規、及び承認製品に対する持続的な法規を含む
•特定の管轄区域の価格規制は私たちの収入と商業化に影響を及ぼす。
私たちの知的財産権に関するリスクは
•私たちは製品の中で知的財産権を獲得、維持、保護、実行する能力、および世界各地の知的財産権の格差と不確実性。
•第三者知的財産権に関するリスクには、知的財産権訴訟に関連する巨大なコストと複雑さが含まれる。
中国でのビジネスに関するリスク
•中国でビジネスをする関連リスクは、中国の広範な監督管理が製薬業界に与える影響を含む
•中国経済に対する政府の高度な参加と、中国の法体系における法的保護の不確実性。
•中国政府当局はいつでも私たちの業務に関与したり、影響したりする可能性があり、これは私たちの業務に重大な変化をもたらし、私たちのアメリカ預託証明書の価値に重大な悪影響を及ぼす可能性がある。
•私たちの大株主と会長の調査に関連した悪影響。
•中国の海外持株会社の中国実体に対する融資と直接投資の監督管理は、私たちの中国運営子会社への融資や追加出資を遅延または阻止する可能性がある。
•中国政府は、中国国外で行われている発行および/または非中国投資家が中国で業務を有する発行者への投資により多くの制御を加える可能性があり、これは、私たちの中国での業務に重大な悪影響を及ぼす可能性があり、投資家への証券提供または継続的な証券提供能力を著しく制限、遅延または阻害し、またはそのような証券の価値を大幅に低下させる可能性がある。例えば、中国の法律によると、中国国外で私たちの株式証券を発行するには、中国証監会や他の政府機関の承認や届出や他の手続きが必要となる可能性があり、必要であれば、このような承認を得るか、またはそのような届出や他の手続きを完了するのにどのくらいの時間がかかるかを予測することはできない。
•PCAOBが2年連続で監査役を検査できない場合,HFCA法案により,2022年5月4日にSECによって委員会で確認された発行者として決定されたため,我々の米国預託証明書が取得される可能性がある。私たちの証券が退市したり、私たちの証券が退市の脅威にさらされたりする可能性があり、あなたの投資価値に重大かつ不利な影響を与える可能性があります。また,PCAOBは検査を行うことができず,投資家がこのような検査から得た利点を奪っている。中国政府の通貨両替の制御は、私たちが収入を有効に利用する能力を制限し、私たちのアメリカ預託証明書の価値に影響を与える可能性がある。
•中国の住民や企業のオフショア投資活動に関する中国の規定は、私たちの行政負担を増加させ、私たちの非中国と国境を越えた投資活動を制限する可能性がある
•米国と中国の間の通貨、経済、政治、環境、社会、貿易紛争。
•米国政府は中国会社に対してより高いレベルの行動をとっており,バイオテクノロジー業界では,米国政府は中国の調達に対するより高いサプライチェーン安全の実施と,中国内部の受給者への技術移転の制限を求めている。
私たちの組織構造に関連するリスクは
•私たちの組織構造は重大な利益衝突を引き起こすかもしれない
•GenScripは私たちの大株主として私たちの大きな統制に影響を及ぼす。
•私たちは制御された会社と外国の個人発行者なので、株主に提供する保護はもっと限られている。
私たちの証券に関するリスクは
•PCAOBが中国の制限により私たちの監査役を十分に検査または調査できない場合、私たちの米国預託証明書は、私たちの前監査人がいる中国で制限が実施されているので、米国の全国的な証券取引所(例えば、ナスダック世界ベスト市場)や米国の場外取引市場での取引のリスクを禁止する
•私たちの業務および財務パフォーマンスが私たちの取引価格の変動を招くこと、および私たちが追加のアメリカ預託証明書または他の証券を発行すれば、私たちのアメリカ預託証明書および普通株が希釈されるリスクを含む、私たちのアメリカ預託証明書の保有に関連するリスク。
CARVYKTIや他の候補製品の商業化に関するリスク
私たちはCARVYKTIのビジネス成功に大きく依存している。もし私たちがCARVYKTIを商業化することに成功しなかったり、商業化の過程で重大な遅延に遭遇したら、私たちの業務は実質的な損害を受けるだろう。
ヤンソン協定によると、私たちは最近cilta-celを商業化し、CARVYKTIの名でアメリカで販売し始めた。CARVYKTIの純貿易売上高は2022年12月31日までの1年間で1兆334億ドルであった私たちはいつCARVYKTIの販売から相当な収入を得るかわかりませんあるいは将来このような収入水準を維持するかどうか。会社として、私たちの成功はCARVYKTIの販売から収入を創出する能力に大きく依存しています。これは多くの要素に依存しますが、これらに限らず、私たちの能力に依存します
•アメリカや他の管轄地域でCARVYKTIの完全な承認を得て維持しています
•CARVYKTIの販売とマーケティング戦略を実行します
•CARVYKTIの持続的かつ成功的な商業化に必要な販売、マーケティング、その他の能力およびインフラの維持と管理;
•CARVYKTIに対する市場の受容度と需要を実現、維持、向上させる
•CARVYKTIの安全性と有効性、および既存および未来の製品と比較した潜在的な優位性と副作用を医学界で確立または展示する
•CARVYKTIの支払者から受け入れ可能な条項で承認されることを確認します
•他の選択と比較して、CARVYKTIを競争力のある価格で提供し、CARVYKTIを販売する際に適切な利益率を達成する能力;
•CARVYKTIタグの追加的な変化に適応し、これらの変化は、他の研究で観察される可能性のある有害事象の結果を含む、CARVYKTIをどのようにマーケティングおよび販売するかに制限を加えるかもしれない
•十分かつタイムリーなCARVYKTI供給を獲得し、将来は私たちの製造能力に関連する要素、新冠肺炎の大流行、地政学的緊張情勢、グローバルサプライチェーンの中断、金融機関の倒産、インフレ上昇とその他の世界事件の不利な影響を受ける可能性がある
•適用される法律と法規の要求を遵守する
•CARVYKTIの販売に必要な国家薬品流通許可証と許可証、および適用法律と法規の要求に適合する薬物警戒システムを維持する;
•専門薬局と手配を維持し、顧客にCARVYKTIを配布し、関連する患者と行政支援サービスを提供する
•CARVYKTIの内部で知的財産権をCARVYKTIに実行し;
•第三者の特許干渉や知的財産権侵害請求を避ける
もし私たちが間に合わないか、あるいはこれらの要素のうちの1つ以上を実現できなければ、その中の多くの要素は私たちがコントロールできない、私たちは販売からできないかもしれませんカビクティこれは私たちの業務の成功に実質的な影響を及ぼすかもしれない。
私たちは臨床試験と商業販売のためにCARVYKTIと私たちの候補製品に対する私たちの要求を満たすために製造能力とインフラを構築することに成功できないかもしれません。そして私たちはCARVYKTIと私たちの候補製品の製造に成功する困難に直面するかもしれません。
AJanssenとの協力の一部として、私たちは米国で商業的に供給されているCARVYKTIに製造施設を設立し、ベルギーで製造能力を確立しており、地域製品の供給を提供し、私たちの世界的な製造カバー範囲を拡大している。私たちはアメリカにも製造施設があり、中国は私たちの臨床試験に臨床材料を提供してくれます。
私たちは世界的にCilta-celの製造を行います。これは、マーケティングの許可を受けた後、私たちが適用された地理的地域で商業化されるにつれて、これらの場所の生産能力を拡大することを要求します。
私たちの製造と商業化戦略は完全に統合された静脈から静脈製品の配送周期を確立することに基づいている。時間の経過とともに、地域や地域的な製造センターを設立し、予想されるビジネスニーズを満たすために主要市場にサービスを提供する予定だ。しかし、私たちはまだ製造施設を建設して、私たちが商業販売数を満たすことができるようにしている。
私たちの長期計画はアメリカ、中国、ヨーロッパに追加的な製造能力を確立することだ。この計画の施行は多くの危険に直面している。例えば,細胞療法製造施設を構築することは複雑な作業であり,知識のある個人が必要である。私たちの内部製造インフラの拡大は、適切な背景を持つ人員を見つけ、従業員や運営施設の訓練を行うことに依存するだろう。もし私たちがこの人たちを見つけることができなければ、私たちは必要な役割を埋めるために外部請負業者やより多くの人員を訓練する必要があるかもしれない。細胞治療経験のある人は少なく、これらの人たちの競争は激しい。
我々自身の商業細胞製造施設を運営することで,臨床試験や商業市場への材料供給の制御を強化し,プロセス変更をより迅速に実施し,より良い長期コスト利益を可能にすることが予想される。しかし、会社として、商業製造施設の設計·運営に関する経験は限られており、私たちの製造能力を決して成功させることはできないかもしれません。私たちがビジネスの足跡を複数の地域に拡張するにつれて、私たちはより多くの製造拠点を設立するかもしれません。これは規制の遅延を招き、あるいはコストが高いことが証明される可能性があります。たとえ私たちが成功しても、私たちの製造業務はコスト超過、意外な遅延、設備故障、労働力不足、自然災害、電力故障、および多くの他の要素の影響を受ける可能性があり、あるいは私たちは計画が発売された要求を満たすために、あるいは未来の潜在的な需要を満たすために十分な生産能力を確立することに成功できないかもしれません。これらのすべては、私たちの製造戦略の期待利益を達成し、私たちの業務に実質的な悪影響を与えることを阻止する可能性があります。
また,細胞治療製品のメーカーは生産過程で困難に遭遇することが多く,特に規模の拡大や初期生産の検証や製品が要求に応じた仕様を確保する上で困難に直面している。これらの問題は生産コストと生産量の困難、品質管理、製品の安定性、品質保証テスト、オペレータミス、合格者不足、及び厳格に実行されている連邦、州と外国法規を遵守することを含む。これらの問題が今後起こらないことは保証されず,既存の資金をタイムリーにあるいは利用して問題を解決あるいは解決できる保証はない.
また,我々の製品や候補製品の出発材料であるT細胞は,患者から調達した後の安定性ウィンドウが限られているため,我々の製造過程の一部として収集や輸送を含めた複雑な物流操作を確立して使用しなければならない。物流と出荷遅延、私たち、私たちの代理、その他の私たちがコントロールできない要素による問題は、天気のように、患者への製品の配送を阻止または遅延する可能性があります。もし私たちの製造過程が満足に実行できなければ、私たちは名声、運営、業務の損害を受けるかもしれない。患者材料の製造過程で複雑なアイデンティティチェーンや保管チェーンを保持することも求められている。アイデンティティチェーンと保護チェーンを維持できないことは不利な患者結果、製品損失或いは監督行動を招く可能性がある。
また、我々の製造過程に必要な原材料サプライチェーンのいかなる重大な中断も、私たちの商業化努力に悪影響を及ぼす可能性がある。私たちは第三者サプライヤーから重要な材料を調達する。私たちの製品と候補製品を生産するためのいくつかの重要な材料のサプライヤーは少ない。私たちはこのような材料の限られた供給を他の市場参加者と争わなければならず、これはコスト増加を招くかもしれない。また、このような出発材料に対するサプライチェーンの制限は、私たちの商業化努力の実行に影響を及ぼす可能性がある。例えば、サプライチェーンの制限により、現在生産できるCARVYKTIの数量が制限されており、限られた供給に対して複雑で挑戦的な流通決定を行うことが求められている。このようなサプライチェーン制限は必然的により広い初期流通から得られる商業的利益を制限するだろう
私たちは現在、強力な製造技術が商業規模に適していると信じており、経済的なコストで商業供給を実現することを予想しています。しかし、私たちはまだ商業規模の製造能力を完全に確立しておらず、そうするのに必要なコストと時間を過小評価したり、私たちの製造過程で実現できる規模経済コストの低下を過大評価したりする可能性がある。最終的にはコストを抑えることができないかもしれません
私たちの製品と候補製品の利益率は私たちの予想と一致したレベルに達し、商業化に関連する投資収益に達するだろう。
CARVYKTIに対する市場の需要を満たすために、私たちとパートナーのJanssenは、私たちの臨床および商業製造能力とインフラを補完するために、第三者契約製造組織(“CMO”)と交渉し、使用を求める初期段階にある。私たちは受け入れ可能な条件やこのようなCMOと合意できないかもしれない。私たちとJanssenは、規制機関がCARVYKTIの製造を許可し、これらのCMOが私たちの製造技術と供給要求の経験を得るのを待つため、私たちの製造技術をこれらのCMOに譲渡するので、開始または参加可能な任意のCMOの計画使用が延期される可能性がある。さらに、私たちとJanssenが開始したか、または接触する可能性のある任意のCMOについて、これらのCMOの生産は、私たちがCARVYKTIを製造するのと同じリスクと不確実性を受けるだろう。私たちやJanssenが運営している施設に比べて、供給の制御が少ない可能性があり、このようなCMO活動のため、CARVYKTIの全体的な商品コストが高い可能性があります。
最後に,CARVYKTIの供給が限られている場合,限られたCARVYKTI供給を重大な患者ニーズに分配する生物倫理的課題に直面する。このような決定は非常に複雑であるため,多くの要因が関与しており,このような分配決定は第三者から疑問視される可能性がある.
ビジネス会社として、私たちの経験は限られていて、CARVYKTIや未来の製品の製造、マーケティング、販売は成功しないかもしれないし、予想以上に成功していないかもしれません。
2022年2月28日にFDAのCARVYKTIの承認を得た後、私たちは協力者のJanssenと共にCARVYKTIの商業化の初期段階にあるプロテアソーム阻害剤、免疫調節剤、および抗CD 38モノクロナル抗体を含む4つ以上の治療を以前に受けた再発性または難治性多発性骨髄腫(MM)の治療に使用するアウディ。CARVYKTIは限られた数の他の司法管轄区域からマーケティング許可を得ているが、米国以外の地域では商業マーケティングを行っていない。
CARVYKTIは私たちが最初に承認された製品であるため、私たちの残りの候補製品はすべて臨床開発中であり、私たちは商業会社としての経験が限られており、バイオ製薬業界の製品商業化会社が直面する多くの挑戦を克服する能力に関する情報も限られている。私たちのビジネス計画を実行するためには、CARVYKTIのマーケティングと販売に成功するほか、単独でまたはパートナーと成功する必要があります
•合格した治療センターと関係を確立し、維持して、これらの治療センターは私たちの製品と任意の未来の製品を受け入れた患者を治療します
•承認された製品を商業化することを計画している各司法管轄区では、CARVYKTIと任意の未来の製品のために十分な価格設定と精算を受ける予定です
•規制当局が我々のパイプラインの他の候補製品と
•CARVYKTIの任意の他の適応および任意の未来製品の臨床試験、マーケティング承認および商業化がコストおよび費用の増加をもたらす場合、支出を管理する。
これらの目標を達成することができなければ、候補製品を開発し、CARVYKTIまたは任意の将来の製品を商業化し、資金を調達し、業務を拡大し、または運営を継続することができないかもしれない。
CARVYKTIと任意の未来製品の商業成功は医師、第三者支払人と医学界の他の人の市場に対する受け入れの程度に依存する。
♪the the the商業広告CARVYKTIと任意の未来製品の成功は医学界、患者と第三者或いは政府支払人が私たちの標的適応に対する新しい治療法、特にCARVYKTIと任意の未来製品を受け入れるかどうかにある程度依存し、それらは医学的に有用で、費用効果が高く、安全であるからである。CARVYKTIと私たちが市場に出す可能性のある任意の他の製品は、医師、患者、第三者支払人、医学界の他の人の市場で受け入れられないかもしれない。これらの製品が十分な受容度に達していなければ、私たちは発生しないかもしれません
巨大な製品収入は、利益を上げることができないかもしれない。CARVYKTIと任意の未来製品に対する市場の受容度は、多くの要素に依存するだろう
•代替療法治療の潜在的治療効果と潜在的優位性
•製品承認ラベルに含まれる任意の制限または警告を含む副作用の流行率および重症度
•ターゲット患者群が新たな療法を試みる意欲と医師がこれらの療法を処方する意欲
•マーケティングと流通支援の実力と競争製品の市場進出のタイミング
•私たちの製品と未来の製品の定価は
•私たちの製品、任意の未来の製品、または競争製品と治療に関する宣伝と
•十分な第三者保険カバー範囲や精算。
1種の潜在的な製品が臨床前と臨床研究において良好な治療効果と安全性を示しても、市場のこの製品に対する受容度はそれが発売された後に知ることができる。私たちの努力、そして私たちのいかなる協力者の努力も、医学界と支払人に私たちの製品のメリットを理解させ、大量の資源を必要とするかもしれないし、永遠に成功しないかもしれない。これらの努力は、私たちの特定の競争相手が販売する従来の技術に必要な資源ではなく、より多くの資源を必要とするかもしれない。これらの要因のいずれも、CARVYKTIまたは任意の将来の製品の不成功または予想以上の成功をもたらす可能性がある。
CARVYKTIや任意の未来製品の市場機会が私たちが思っているより小さい場合、患者を識別して著しい市場シェアを得ることができなければ、私たちの収入は不利な影響を受ける可能性があり、私たちの業務は影響を受ける可能性がある。
我々の予測CARVYKTIまたは任意の未来製品の治療から利益を得る可能性がある人数については推定に基づいている。これらの推定は様々な源から来ており、科学文献、診療所調査、患者基金会或いは市場研究を含み、正しくないことが証明されている可能性がある。さらに、新しい研究は私たちの候補製品の目標疾患の推定発病率または流行率を変えるかもしれない。患者の数は予想よりも少ないか、または識別しにくいかもしれない。
CARVYKTIと私たちが開発している候補製品の潜在的なターゲット群が少ないので、承認された適応内の製品がかなりの市場シェアを得ていても、より多くの適応のマーケティング承認を得なければ、私たちは決して利益を達成しないかもしれない。癌領域では、米国食品医薬品局(FDA)は通常、再発または末期疾患患者のための新しい治療法のみを最初に承認する。例えばFDAのCARVYKTIの承認はプロテアソーム阻害剤、免疫調節剤、および抗CD 38モノクロナル抗体を含む4つ以上の治療を以前に受けた再発性または難治性多発性骨髄腫を有する成人の治療のための方法。多発性骨髄腫の早期治療におけるCARVYKTIの承認を求め,第一線の治療となる可能性が予想されるが,成功する保証はない。
これらの要素のいずれも、CARVYKTIおよび任意の将来の製品の販売から収入を生み出す能力、および私たちが利益を達成し、維持する能力に悪影響を及ぼす可能性があります。したがって、私たちの業務は影響を受けるかもしれない。
私たちは私たちの商業能力を拡大し続けているにもかかわらず、私たちはこれまで販売や流通センターがなく、マーケティングと市場参入能力が限られていた。私たちは、これらの能力やインフラを構築し、商業運営を支援するために、大量の財務·管理資源を投入する予定だ。もし私たちがこれらの商業能力やインフラを構築できなかったり、第三者と合意して私たちの製品や未来の製品をマーケティングして販売することができなければ、私たちは私たちの業務を維持するのに十分な収入を生成できないかもしれません。
私たちはアメリカでの最初のビジネス発売の一部として、私たちの現場チームを拡大し続けていますが、これまで販売や流通経験がなく、マーケティングや市場参入能力が限られていました。CARVYKTIと私たちの開発計画が生み出す可能性のある他の製品の商業化に成功するためには、これらの能力を発展させ、米国、ヨーロッパ、他の地域の商業運営を支援するために、私たちのインフラをさらに拡大し、私たち自身も他の人とも協力する必要がある。CARVYKTIなどの自己CAR−T療法の商業化は資源集約型であり,商業能力に大量の投資が必要である。私たちは現在広範で資金的に十分なマーケティングと販売業務を持っている多くの会社と競争するだろう。もしなければ
マーケティングおよび販売機能を含むこれらの機能を実行するための強力な内部チームまたは第三者の支援がなければ、私たちはこれらのより成熟した会社と成功することができないかもしれない
私たちは現在、CARVYKTIを発売し、マーケティングするために、主にパートナーのJanssenである第三者に深刻な依存を予想しています。JanssenがCARVYKTIを商業化するのに十分な資源を投入しなければ、私たちは私たちの業務を維持するのに十分な製品収入を生成できないかもしれない。
私たちは急速に変化する業界で運営され、激しい競争に直面しており、これは他の人が私たちよりも製品の発見、開発、商業化に成功する可能性がある。
新生物製薬製品の開発と商業化競争は激しく、迅速かつ重大な技術進歩の制約を受けている。我々が開発·商業化する可能性のある現在と将来の候補製品については、大手多国籍製薬会社、バイオテクノロジー会社、専門製薬会社からの競争に直面している。現在,多くの大手製薬やバイオテクノロジー会社が製品をマーケティング·販売したり,癌治療の候補製品を開発したりしている。規模が小さいか早い段階にある会社も重要な競争相手になる可能性があり、特に大手老舗会社との協力で手配されている。潜在的な競争相手はまた、学術機関、政府機関、その他の公共および個人研究機関を含む。臨床探索性試験において良好な臨床治療効果があるため、工学T細胞療法、一般的なリダイレクトT細胞療法と抗体-薬物結合体は多くの生物技術と製薬会社から支持されている。私たちの競争相手は、私たちが開発する可能性のある任意の候補製品よりも効率的で、より効率的にマーケティングおよび販売またはコストの低い技術および製品を開発、取得、または許可することに成功するかもしれません。これは、私たちの候補製品を競争力を失って時代遅れにするかもしれません。
私たちの潜在的なCAR-T細胞療法の競争相手は
•Allgene,Treateutics,Inc.,Autolus Treateutics Plc,Bluebird,BIO,Inc.,百時美施貴宝社,CARsgen Treateutics Holdings Limited,Arcell x,Celyad Oncology,亘喜生物,Innoent Biologics,Poseida Treateutics,Inc.,ノワ製薬およびPrecision Biosciences Inc.;
•学術医学センターはBCMA CAR-T技術の自主開発に取り組んでいる
•他にMMの治療のためにBCMA標的療法を開発した会社には,安進社,Regeneron製薬会社,グラクソ·スミスクライン社,百時美施貴宝社,ジョンソン(我々Cilta−celのパートナーヤンソンの親会社),エバービー,ファイザーがある。
CARVYKTIを除いて、私たちの候補製品はまだ初期開発段階にあります。我々の開発段階計画を持つ競争相手は、FDA、国家医療製品協会(NMPA)、欧州委員会、日本医薬品·医療機器庁(PMDA)または他の同様の規制機関による候補製品のマーケティング承認を迅速に獲得する可能性があり、私たちが市場に参入できる前に、彼らはある製品または特定の適応のための強力な市場地位を確立するかもしれない。
私たちの多くの競争相手は、単独でも、彼らの戦略的パートナーと一緒にも、私たちよりも多くの財力、技術、人的資源を持っている。したがって、私たちの競争相手は治療の承認を得て、広範な市場受け入れを得ることで、私たちよりも成功するかもしれません。これは、私たちの治療を時代遅れにしたり、競争力を欠いたりするかもしれません。バイオテクノロジーと製薬業界の合併と買収は、私たちの数の少ない競争相手により多くの資源を集中させる可能性がある。これらの競争相手はまた合格した科学と管理人員を募集と維持し、臨床研究サイトと臨床研究患者登録を確立し、補充或いは必要な技術を獲得する上で著者らと競争している。規模が小さいかスタートアップ段階にある会社も重要な競争相手になる可能性があり、特に大手や成熟会社との協力で手配する。
もし私たちの競争相手が私たちが商業化する可能性のある任意の製品よりも安全で、より効果的で、副作用が少ない、より便利で安いまたはより安い製品を開発し、商業化すれば、私たちのビジネス機会は-CARVYKTIに関連する機会を含む-減少または除去する可能性がある
私たちに対する製品責任訴訟は、私たちが重大な責任を負い、私たちが開発する可能性のある任意の製品の商業化を制限する可能性があります。
私たちは人体臨床試験で私たちの候補製品をテストすることに関する固有製品責任リスクと、任意の商業化製品に関連するより大きなリスクに直面している。もし私たちが私たちの候補製品や製品に被害を与えるクレームを自己弁護することに成功できなければ、私たちは大きな責任を招くだろう。是非曲直や最終結果にかかわらず、賠償責任は
•私たちの経営陣の資源を減らして、私たちの業務戦略を推進します
•すべての候補製品や私たちが開発する可能性のある製品の需要が減少した
•私たちの名声とメディアの深刻な否定的な関心を損なう
•臨床試験参加者の脱退
•規制当局が調査を開始しました
•製品のリコール、撤回またはラベル付け、マーケティング、または販売促進制限;
•この訴訟を正当化するための巨額の費用
•臨床試験参加者や患者に多額の報酬を支払い
•収入の損失
•私たちが開発する可能性のあるどんな製品も商業化できない。
私たちは現在全部で1,000万ドルの製品責任保険を持っています。各事故の上限は1,000万ドルで、これは私たちが発生する可能性のあるすべての責任をカバーするのに十分ではないかもしれません。CARVYKTIを商業化し、臨床試験を拡大したり、より多くの候補製品を商業化すれば、保険カバー範囲を増やす必要があるかもしれません。保険範囲はますます高くなっています。私たちは可能などんな責任にも対応するために、合理的な費用や十分な金額で保険範囲を維持することができないかもしれない。
私たちの業務に関わるリスク
われわれは成立以来大きな損失を被っており,予見可能な未来にも引き続き重大な損失を被ることが予想される.
我々は2022年12月31日現在と2021年12月31日現在の年度純損失を含めて巨額の純損失を出しており、それぞれ4億463億ドルと4.036億ドルである。2022年12月31日までの累計赤字は9兆665億ドル。私たちは次のような理由で、私たちの純損失が続くと予想している
•我々は,再発と難治性多発性骨髄腫(RRMM)の研究と開発を計画中である
•アメリカ、ヨーロッパ、中国の工場への投資を含む製造能力への投資
•私たちが行っている他の候補製品の臨床開発は
•私たちは研究と開発活動を行っています
•私たちはより多くの候補製品を発見し開発し、臨床製品ラインをさらに拡大した
•臨床試験に成功した任意の候補製品の規制またはマーケティング承認;
•私たちの臨床試験と潜在的な商業化の能力需要を満たすのに十分な数があることを保証するために、内部と外部の製造能力を拡大する
•販売、マーケティング、流通インフラを構築し、規制またはマーケティングの承認を得る可能性のある任意の候補製品を商業化する
•私たちの知的財産権の組み合わせを開発し、維持し、拡大し、保護する
•他の候補品や技術を得ることができます
•より多くの臨床、品質管理、製造者を募集する
•私たちの製品開発を支援し、将来の商業化努力を計画する人を含む、臨床、運営、財務、管理情報システムおよび人員を増加させる
•私たちの世界でのビジネスを拡大し
•追加の法律、会計、投資家関係、その他の上場企業の運営に関する費用が発生する。
これらの純損失はすでに私たちの運営資本、総資産、株主権益にマイナスの影響を与え続けるだろう。私たちの開発と商業化努力に関連する多くのリスクと不確実性のため、私たちはいつ利益を上げることができるか予測できず、私たちは永遠に利益を上げないかもしれない。たとえ私たちが確実に利益を達成したとしても、私たちは四半期や年度の収益性を維持したり向上させることができないかもしれない。私たちは収益性を達成して維持することができません。これは私たちの業務、財務状況、運営結果、キャッシュフローを損なうでしょう。
また、私たちが発生する純損失は、四半期と四半期の間と年度との間で大きく変動する可能性がありますので、製品承認、承認、商業普及、臨床試験、私たちに提起される可能性のある任意の訴訟、協力、許可、または他の合意の実行、およびこれらの合意に基づいて任意のお金を支払うか受け取る時間などの要因により、私たちが業績を運営している期間は、私たちの将来の業績の良い指示ではないかもしれません。私たちの以前の損失と予想された将来の損失は、私たちの運営資本、候補製品の開発に資金を提供する能力、私たちが利益を達成し、維持する能力、そして私たちの普通株のパフォーマンスに悪影響を与え続け、将来的に持続的な経営企業としての私たちの能力に対する大きな疑いを引き起こす可能性がある。
私たちの限られた経営の歴史は、私たちの業務のこれまでの成功度を評価することを困難にするかもしれませんし、私たちの将来の生存能力を評価することも難しいかもしれません。
CARVYKTIがFDAの許可を得た適応以外に、著者らは主に臨床段階の生物製薬会社であり、運営歴史は限られている。組織として、私たちは後期臨床試験の成功、監督管理の承認を得て、私たちの候補製品を商業規模で生産したり、第三者代表を手配したり、商業化に成功するために必要な販売とマーケティング活動を展開したり、販売国が補償を得る上で現れる能力は限られている。私たちは業務目標を達成する過程で予見できない費用、困難、複雑な状況、遅延に遭遇する可能性があります。私たちの運営会社としての短い歴史は、私たちの未来の成功や生存能力のどの評価も重大な不確実性の影響を受けるようにした。もし私たちがこれらのリスクにうまく対応できなかったり、ある時点で研究開発に集中している会社からビジネス活動を支援できる会社に移行できなければ、私たちの業務は実質的な損害を受けることになります。
私たちは私たちの候補製品の開発を完了するために追加の資金が必要になるだろう。これは全くなければ受け入れられる条項では提供できないかもしれない。
私たちは私たちの財政的需要を満たし、私たちの業務目標を達成するために多くの追加資金を必要とするだろう。もし私たちが必要な時に資金を調達できなければ、私たちは私たちの製品開発計画や商業化努力を延期、減少、または完全に停止させることを余儀なくされるかもしれない。
私たちは、私たちの既存の現金と現金等価物が、少なくとも今後12ヶ月の運営費用と資本支出需要に資金を提供できるようにすると信じている。しかし、私たちはCilta-celと私たちの他の候補製品の開発と商業化を達成し、私たちの持続的な運営と他の計画活動に関連するために追加的な資金を調達する必要があるだろう。私たちの将来の資本需要は多くの要素に依存します
•CARVYKTIと私たちが発売許可を得た任意の他の候補製品の商業化活動のコストと時間、製品の製造、マーケティング、販売、および流通;
•私たちの現在の候補製品の実験室テスト、製造及び臨床前と臨床開発の進捗、結果とコスト
•私たちが追求する可能性のある他の候補製品の臨床前開発、実験室テストと臨床試験の範囲、進捗、結果、コスト
•私たちが追求するかもしれない他の候補製品の開発要求は
•将来のライセンス契約によると、私たちは任意のマイルストーンまたは特許使用料の時間と金額を支払う必要があるかもしれない
•より多くの臨床、品質管理、製造者を雇用することを含むインフラ建設のコスト
•私たちの候補製品に対する規制審査のコスト、時間、結果
•私たちはヤンソン協定によって得られた収入金額と、私たちが市場で承認された候補製品の商業販売収入(あれば)、
•特許出願を準備し、提出し、起訴し、私たちの知的財産権を維持し、実行し、知的財産権に関する任意のクレームを弁護するコストと時間;
•上場企業としての運営コスト
•私たちは他の候補製品と技術の程度を得ることができるかもしれない。
Cilta-celを除いて、潜在的な候補製品を決定し、臨床前テストと臨床試験を行うことは時間がかかり、高価で不確定な過程であり、数年を要し、しかも著者らは監督部門の許可を得て製品販売を実現するために必要なデータ或いは結果を永遠に生成できないかもしれない。しかも、私たちの候補製品が承認されれば、商業的成功を得られないかもしれない。これまで、ヤンソンとの協力を通じて、CARVYKTIの販売は限られていました。したがって、私たちは追加的な資金調達に依存して私たちの業務目標を達成し続ける必要があるだろう。私たちは受け入れ可能な条項で十分な追加融資を受けることができないかもしれないし、根本的にできないかもしれない。また、有利な市場条件や戦略的考慮により、現在または将来の運営計画のために十分な資金があると考えても、追加の資本を求めることができる。もし私たちが第三者との協力と許可手配を通じて追加資金を調達すれば、私たちは私たちの技術や候補製品に対するいくつかの権利を放棄しなければならないかもしれません。条項は私たちに不利です。いかなる追加的な資金調達努力も、私たちの経営陣の日常活動への関心を移す可能性があり、承認されれば、現在および将来の候補製品を開発し、それを商業化する能力に悪影響を及ぼす可能性がある。もし私たちが必要な時や魅力的な条件下で資金を調達できなければ、私たちは私たちの研究開発計画や将来の商業化努力を延期、減少、または完全に停止させることを余儀なくされるかもしれない。
われわれの経営業績はインフレの悪影響を受ける可能性がある.
CARVYKTIを商業化し始めるにつれて、私たちの業務はインフレの影響をもっと感じるかもしれません。他の点では、労働力に対する競争がより激しくなっており、CARVYKTIの商業化努力を支援するために従業員を雇用することに伴い、労働コストが増加することが予想される。しかも、インフレとより高いエネルギーコストは原材料と輸送コストの増加を推進するかもしれない。私たちがコスト計画を下げたり、私たちの製品や未来の製品により高い価格を設定することで、いかなるコスト増加も完全に相殺できる保証はありません。もし私たちが一般的に私たちの価格を設定してこれらの増加したコストを十分に相殺することができなければ、あるいはコスト増加と長期インフレが持続すれば、私たちの業務、経営業績、収益性に実質的な悪影響を及ぼすかもしれない。また、いくつかの大口商品市場の変動は私たちの生産コストに大きな影響を与える可能性がある
私たちの候補製品開発に関するリスク
CARVYKTIが2022年2月28日にFDAの承認を得て、限られた数の追加の司法管轄区域のマーケティング許可を得た以外、私たちのすべての候補製品は臨床開発または臨床前開発中である。CARVYKTIと他の候補製品の臨床開発を進め続けることができなければ、規制部門の承認を得られず、最終的に私たちの候補製品を商業化することができなければ、あるいはその過程で重大な遅延に遭遇すれば、私たちの業務は実質的に損害を受けるだろう。
私たちの最初の製品CARVYKTIは2022年2月28日にFDAの承認を得ましたが糖尿病の治療のために大人は罹患しているRRMMプロテアソーム阻害剤、免疫調節剤、および抗CD 38モノクロナル抗体を含む、4つ以上の治療を受けた患者著者らの成功はある程度、早期MM治療シリーズにおけるCARVYKTIの発展を推進し続ける能力に依存する。Janssenと協力して,米国と日本でRRMM患者に対する1 b/2期試験(CARTITUDE−1)を完了し,現在中国でCilta−celのRRMM患者用の第2段階試験(CARTIIFAN−1)を行っている。2019年11月、我々とJanssenは、米国、EU、イスラエルのCilta-cel第2段階多列試験(CARTITUDE-2)に参加し、様々な臨床環境下のMM患者、例えば早期再発患者または第一線治療としての様々な臨床環境下のMM患者の募集を開始した。また,CARTITUDE−4期臨床試験は2020年6月に開始され,米国,EU,オーストラリア,日本,イスラエルを含む約400名の患者を募集した。この臨床試験は,シリル治療難治性MMと標準三連療法による難治性MMの治療を比較している。2023年1月27日,CARTITUDE−4がその主な終点に達したことを発表した:CARTITUDE−4は対照群と比較して無進展生存期間(PFS)で有意に改善した
この研究の最初のあらかじめ指定された中期分析で標準治療を行った。独立したデータ監視委員会の提案の下で、この研究はもう盲目的ではない。2021年8月にCARTITUDE−5期臨床試験を開始し,米国,EU,カナダ,オーストラリア,韓国,日本を含む約650名の患者を募集することを目標とした。この臨床試験では,新たに診断された多発性骨髄腫患者に対してシルチサイ治療と標準三胞胎治療の比較を行っており,造血幹細胞移植を初期治療とする予定はない。また,CARTITUDE−6期臨床試験の案が設計されており,EU,オーストラリア,韓国,イスラエルを含む約750名の患者を募集することを目標としている。この臨床試験では,新たに診断された多発性骨髄腫患者に対するシルチサイ治療と自己幹細胞移植(ASCT)治療の比較を行う。これらまたは任意の他の将来の臨床試験が成功するか、またはより多くの積極的な臨床データが生成されることは保証されず、私たちはFDAまたは他の規制機関からシルタイに対する追加的な上場承認を得ないかもしれない。
Cilta−celに加えて、非ホジキンリンパ腫(NHL)、急性リンパ球性白血病(ALL)、胃癌、食道癌、膵臓癌、結腸直腸癌、肝細胞癌、小細胞肺癌、非小細胞肺癌を含む様々な癌に対する早期自己CAR−T製品候補製品の広範な組み合わせを有する。我々はまた,MMに対するBCMAの同種異体ガンマデルタCAR−T候補製品を開発しており,現在研究者が開始した中国の第1段階臨床試験にある。また,BCMAに対する同種異体CAR−NK候補製品と,臨床前開発中の急性骨髄性白血病(AML)に対するCLL 1/CD 33の同種異体ガンマ増量CAR−T候補品を開発している。私たちの候補製品のこれらまたは任意の他の未来の臨床試験が成功するか、または積極的な臨床データが生成されることは保証されず、私たちはFDAまたは他の規制機関による私たちの任意の候補製品の上場承認を得ないかもしれない。FDAが私たちの候補製品の研究新薬(IND)の申請が適時に発効するか、または全く発効しないことを許可する保証はない。INDなしではアメリカでの臨床試験は許可されません
生物製薬開発は長く、高価で不確定な過程であり、私たちのどの臨床試験のどの段階でも遅延または失敗が生じる可能性がある。もし私たちの候補製品が規制部門の承認を得られなければ、私たちはこれらの候補製品の商業化とマーケティングを行うことができないだろう。私たちの候補製品の開発が成功するかどうかは多くの要素に依存します
•臨床前研究を完成し、そして監督管理の許可を得て、著者らの臨床前段階の計画候補製品のために臨床試験を行う
•私たちの臨床試験で積極的な結果を得て、私たちの候補製品の有効性、安全性、持続性を証明します
•規制部門の候補製品の商業化の承認を得ています
•私たちの候補製品を受け入れられる品質とコストで製造します
•科学者、医療専門家、ビジネス界の人々からなる組織を維持し、発展させ、彼らは私たちの製品と技術を開発し、商業化することができる。
その中の多くの要素は私たちがコントロールできないことであり、臨床テストと監督提出過程を十分に完成するのに要する時間を含む。私たちが規制部門の承認を求めるのに時間と資源がかかっても、私たちの候補製品は規制部門の承認を決して得られないかもしれない。もし私たちがこれらの要素のうちの1つ以上を適時に達成しなかった場合、あるいはこれらの要素に全く到達していなかったり、生物製薬製品の開発成功に影響を与えた他の要素がなければ、私たちは重大な遅延を経験したり、私たちの候補製品を開発することができなくなり、これは私たちの業務に実質的な損害を与えるかもしれない。
我々の独自の次世代細胞作製技術、我々のCAR-TとCAR-NKに対するモジュール化方法、および私たちが候補製品に提供する製造プラットフォームは、重大な挑戦と障害に直面している癌治療の新しい方法を代表している。
著者らは腫瘍生物学と細胞プログラミングにおける著者らの専門知識を利用して、主要な研究と開発努力を著者らのCAR-TとCAR-NK細胞療法に集中し、著者らの未来の成功は著者らの候補製品の成功開発と製造に高度に依存している。最初の製品CARVYKTIを除いて、2022年2月28日にFDAの承認を得ましたプロテアソーム阻害剤、免疫調節剤、および抗CD 38モノクロナル抗体を含む4つ以上の治療を以前に受け、限られた数の他の管轄区域から販売許可を得たRRMMを有する成人の治療のための使用現在、私たちは承認された製品もなく、商業化された製品もない。他の標的治療と同様に、非腫瘍または非標的活動は、開発を延期するか、または特定の候補製品を再設計または放棄することを要求する可能性がある。なぜなら…
細胞療法は細胞免疫療法と癌治療の比較的新しい分野を代表し、私たちの候補製品の開発と商業化は私たちを含む多くのリスクと挑戦に直面させた
•FDA、NMPA、欧州委員会、PMDAと他の規制機関の癌細胞療法における経験が限られているため、私たちの候補製品のために規制されている
•設計ユニットのための一貫性と信頼性のあるプロセスの開発と導入離体する工学細胞を患者に注入し
•私たちのすべての製品を提供しながら、患者に化学療法を行うことは、候補製品の不良副作用のリスクを増加させる可能性があります
•CARVYKTIと私たちの候補製品を製造するための材料を調達する臨床および商業供給;
•不良反応を回避しながら、必要な属性を有するプログラミングモジュールを開発する
•複数のプログラミングモジュールを提供するのに十分な供給が可能なウイルスベクターを作成して取得することと;
•信頼性と一貫性のある担体と電池製造プロセスを作成し
•私たちの臨床研究の拡大募集と私たちが予想しているビジネスニーズに合うように、私たちの候補製品を生産するのに適した製造能力を確立する
•私たちの製造能力を拡大する上で費用対効果を実現し
•私たちの候補製品を安全に管理する合意を作る
•医療従事者を教育して、サイトカイン放出症候群(CRS)に関連する潜在的副作用のような、私たちの細胞技術および私たちの各候補製品の潜在的副作用を理解する
•専門治療センターと協力して総合的な解決策を構築し、通常T細胞治療管理に関連する負担と複雑な後方勤務を軽減する
•販売とマーケティング能力を確立し、必要な規制承認を得た場合、CARVYKTIと私たちの他の任意の候補製品の発売に成功し、それを商業化し、もし私たちが承認された場合、新しい治療法の受け入れに関する市場のリスク;
•任意の承認された候補製品の商業化に関連する新規および個人化療法の保証範囲および第三者支払者からの十分な補償。
私たちは、安全、効果的、拡張可能、または利益のある製品を生成するために、私たちの候補製品、私たちの技術、または他の候補製品の開発に成功できないかもしれない。
さらに私たちの技術は患者細胞の遺伝子改変に関連しているからです離体する私たちは追加的な規制の挑戦とリスクに直面しています
•遺伝子と細胞治療製品の監督管理要求は常に変化し、将来も引き続き変化する可能性がある。これまで、患者の細胞遺伝子修飾に関連するCAR-T細胞治療製品は4種類だけがアメリカで承認され、3種類はEUで承認され、1種類は中国で承認されなかった
•遺伝子配列が患者の染色体に正確に挿入されていない場合、トランスジェニック製品は、リンパ腫、白血病または他の癌、または他の機能異常細胞を引き起こす可能性がある
•我々のウイルスベクターは複製できないが、レトロウイルスまたはレンチウイルスベクターを使用することは、新規または再活性化ウイルスまたは他の感染症の病原株をもたらす可能性があるリスクがある;および
•FDAと欧州委員会は遺伝子療法治療を受けたすべての患者に対して15年間の追跡観察期間を提案しており,我々の候補製品にこのような観察期間を採用する必要があるかもしれない。
さらに,細胞療法安全問題に対する公衆の知覚や認識は,被験者が我々の候補製品の臨床試験に参加する意思や医師が承認した製品を発行する意欲に悪影響を及ぼす可能性がある。医師、病院と第三者支払人は追加の前期コストと訓練を必要とする新製品、技術と治療実践を採用する上でよく行動が遅い。治療センターは細胞治療を管理するために必要な人員や他のインフラの構築を望んでいないか、または投入することができない可能性がある。医者は受け入れたくないかもしれない
研修にはこのような斬新で個性的な療法が採用されており,複雑すぎて適切な訓練がない場合には採用できず,施行しないことを選択する可能性がある。これらや他の要因から,病院や支払者はこのような新しい療法の利点を決定する可能性があり,そのコストを超えないか,あるいはそれを超えない可能性がある。
私たちの未来の成功はCilta-celと私たちの他のパイプラインプロジェクトの規制承認に大きく依存する。私たちのすべての候補製品は大量の臨床前研究と臨床試験が必要で、それから私たちは監督部門の許可を求めて、製品を商業使用に投入することができます。
最初の製品CARVYKTIを除いて、2022年2月28日にFDAの承認を得ましたプロテアソーム阻害剤、免疫調節剤および抗CD 38モノクロナル抗体を含む4つ以上の治療法を受けた成人再発性または難治性多発性骨髄腫については、限られた数の他の司法管轄区域を通じて、規制部門の発売許可を得ていない製品はないそれは.私たちの業務は、CARVYKTIの開発をさらに進める能力があるかどうか、他の管轄地域のCilta-celと他の適応の規制承認を得、私たちの他の候補製品の規制承認を得、CARVYKTIと私たちの他の候補製品を商業化する能力があるかどうかに大きく依存する。米国では、まずFDAの規制承認を得ない限り、候補製品を商業化することはできない;同様に、私たちは米国以外の国で候補製品を商業化することもできない。中国の国家薬品監督管理局、欧州委員会、EUの欧州薬品管理局、日本の薬品監督管理局のような関連司法管轄区の規制機関の規制許可を得なければならない。特定の適応のための任意の候補製品の商業販売の規制承認を得る前に、私たちは、候補製品がこの適応に対して安全かつ有効であることを証明するために、臨床前および臨床研究で収集された大量の証拠を使用して、製造施設、プロセス、および制御が候補製品に関連する規制要件に適合することを証明しなければならない。私たちの任意の候補製品の承認を求める前に、私たちは私たちの臨床試験の設計と私たちの候補製品のために求め、承認を得るために必要な臨床データのタイプと数量についてFDA、NMPA、EMA、PMDA、および他の規制機関と協議する必要がある。
FDA、NMPA、欧州委員会、PMDAとその他の監督管理機関が上場承認を獲得するのに要する時間は予測できないが、通常臨床前研究と臨床試験開始後数年を必要とし、そして多くの要素に依存し、監督機関のかなり大きな適宜決定権を含む。また、承認政策、法規或いは承認を得るために必要な臨床前と臨床データのタイプと数量は候補製品の研究と開発過程で変化する可能性があり、司法管轄区域によって異なる可能性がある。私たちの既存の臨床または臨床前段階の候補製品または任意の未来の候補製品は、監督部門の承認を永遠に得られない可能性がある。
当社の候補製品は、様々な理由でFDA、NMPA、欧州委員会、PMDA、または他の規制機関のマーケティング規制承認を得ることができない可能性があります
•私たちの臨床試験の設計や計画や進行と一致しません
•候補製品がその提案の適応に対して安全かつ有効であることは証明されていない
•臨床試験は承認に必要な統計的意義レベルに達しなかった
•候補製品の臨床的および他の利益がそのリスクよりも大きいことを証明できなかった
•前臨床研究や臨床試験データの説明には同意しません
•私たちの候補製品の臨床試験から収集されたデータが不足しており、生物製品ライセンス申請(“BLA”)または他の提出または規制部門の承認の提出および提出をサポートすることができない
•私たちの工場の製造技術の承認を得られませんでした
•私たちの臨床前および臨床データが承認されるのに十分ではないように、政策または法規の変化を承認する;または
•十分な資金が不足しており、関連する監督管理機関を満足させる方法で臨床試験を完成することができない。
FDA、NMPA、EMA、PMDAまたは同様の規制機関は、承認を支援するための追加の臨床前または臨床データのようなより多くの情報を必要とする可能性があり、追加の臨床前研究、臨床試験、または両方を兼ねたデータの実行を要求すること、または承認および私たちの商業化計画を延期または阻止することができ、または開発計画を放棄することを決定する可能性がある。もし私たちが生産プロセスを変更すれば、追加の臨床試験や他の研究を行う必要があるかもしれません。これはまた、私たちの候補製品の承認を延期または阻止する可能性があります。もし私たちが承認されれば、規制部門は私たちの何でも承認するかもしれない
候補製品の適応は、私たちが要求したもの(最も商業的に有望な適応を承認できなかったことを含む)よりも少なく、処方および流通に警告および制限を加える可能性があり、高価な発売後の臨床試験または他の発売後の承諾の表現に基づいて承認される可能性があり、または候補製品を承認する可能性のあるラベルは、候補製品の商業化に必要または必要なラベル宣言を含まないかもしれない。
Cilta−celはFDAの孤児薬物指定と画期的な治療指定を獲得しているが,優先薬物の使用権を獲得している 我々の発展戦略には、承認の加速または承認の有無など、追加の迅速な承認経路を使用することも含まれているかもしれません。我々の他の候補製品の臨床前と臨床試験結果によると、私たちもこれらの候補製品のためにこのような地位を獲得する可能性がある。私たちの候補製品が突破的な治療、孤児薬、あるいはPrime計画を使用する機会を獲得または維持する資格があるかどうかを確定することはできず、私たちの候補製品の試験から得られた臨床データは任意の迅速な承認計画の資格を得るのに十分であると仮定することはできない。
候補製品がFDA、NMPA、欧州委員会、PMDAまたは他の司法管轄区域の他の同様の規制機関の上場承認を得ることに成功したとしても、任意の承認は、特定の年齢層の使用制限、警告、予防措置または禁忌症に関連する重大な制限を含む可能性があり、または重い承認後の研究またはリスク管理要求の影響を受ける可能性がある。私たちが1つ以上の司法管轄区域で私たちの候補製品のうちの1つに対する規制承認を得ることができない場合、または任意の承認に重大な制限が含まれている場合、私たちは製品を開発し続けたり、候補製品に起因することができる収入を生成するのに十分な資金を得ることができないかもしれない。さらに、私たちの現在または未来の候補製品に対するいかなる規制承認も、一度承認されると、撤回されるかもしれない。
候補製品チャンネルを作るための私たちの努力は成功しないかもしれない。
私たちの戦略の重要な要素の一つは、腫瘍生物学と細胞プログラミングにおける私たちの専門知識と私たちの独自かつモジュール化された細胞プログラミング技術を利用して、より安全で、より効果的と考えられるCAR-TとCAR-NK細胞療法を開発することである。我々の重点は,癌治療のための候補細胞治療製品のパイプラインの開発と,これらの候補製品の臨床開発における進展である。より多くの候補製品を開発するほか、製造技術、装甲戦略、次世代自動車候補製品を含むプラットフォーム技術を開発する予定だ。しかし、私たちは安全で効果的な候補製品を開発できないかもしれないし、他の商業的に利用可能な代替製品と比較して優れているかもしれない。私たちが私たちのパイプラインを確立し続け、次世代候補製品を開発したり、固形腫瘍適応に拡張したりしても、我々が決定した潜在的候補製品は、安全性の欠如、耐性の欠如、抗腫瘍活性の欠如、またはそれらが市場承認を得る可能性がないこと、市場承認を得ることができないこと、または第三者支払者から補償を受ける可能性があることを示す他の製品を含む、臨床開発に適していない可能性がある。私たちが開発過程でこれらの追加候補製品のいずれかを成功的に推進できることを保証することはできません。私たちの研究計画は最初に潜在的な候補製品を決定する上で希望を示す可能性があるが、多くの原因で臨床開発或いは商業化のための候補製品を生成できなかった
•私たちのプラットフォームでは他の候補製品を識別することができないかもしれません
•私たちはより多くの候補製品を獲得または発見するために十分な資源を収集することができないか、またはそれ以上の候補を発見することができないかもしれない
•私たちの候補製品は臨床前や臨床試験では成功しないかもしれません
•さらなる研究では、候補製品は、有効ではないか、または適用されない規制基準に適合していない可能性があることを示す有害な副作用または他の特徴を有することが証明される可能性がある
•競争相手は代替製品を開発し、私たちの候補製品を時代遅れや魅力を低下させるかもしれない
•私たちが開発した候補製品はまだ第三者特許または他の独占権によって保護されているかもしれない
•候補製品の市場は我々の開発計画中に変化する可能性があるため,この候補製品の継続開発は合理的ではない
•候補製品は、許容可能なコストで商業的に量産できないかもしれないし、全くできないかもしれない;
•適用すれば,候補製品は患者,医学界あるいは第三者支払人に安全かつ有効であると受け入れられない可能性がある。
上記のいずれかの事件が発生した場合、1つまたは複数の計画のための開発作業を放棄することを余儀なくされる可能性があり、または他の候補製品を識別、発見、開発、商業化することができない可能性があり、これは私たちの業務に大きな悪影響を与え、運営を停止させる可能性があります。
FDAや他の規制機関の承認を得て、私たちの候補製品を市場に出しても、癌や他の疾患の治療のためにも、どのような候補製品も商業化に成功し、市場に広く受け入れられているか、または他の商業代替製品よりも効果的であることを保証することはできません。また、私たちの財務と管理資源が限られているため、私たちはいくつかの候補製品と特定の疾患に研究計画を集中させる必要がある。したがって、私たちは、実行可能な商業製品または利益の市場機会を利用することができず、他の候補製品または後により大きな商業潜在力を有することが証明される可能性のある他の疾患との追求機会を放棄または延期することが要求されるか、または独占開発および商業化権利を保持することが私たちに有利である場合には、協力、許可または他の特許権使用料配置によって、これらの候補製品に価値のある権利を放棄することが要求される可能性がある。
候補製品の開発や商業化に成功したり、他社と協力したりすることができなければ、将来的に製品収入を得ることができなくなり、私たちの財務状況を深刻に損ない、米国預託証明書の取引価格に悪影響を及ぼす可能性がある。
私たちの臨床前計画は遅延したり、決して臨床試験に入らない可能性があり、これは私たちが適時に規制の承認を得たり、これらの候補製品を商業化する能力に悪影響を与え、これは私たちの業務に悪影響を与えるだろう。
著者らのいくつかの候補製品はまだ臨床前開発段階にあり、臨床前計画失敗のリスクは非常に高い。候補製品の臨床試験を開始する前に、私たちはアメリカのIND申請と中国とEUに基づく臨床試験申請(“CTA”)を含むヒト臨床試験を開始する監督管理許可を得るために、広範な臨床前試験と研究を完成しなければならない。著者らは著者らの臨床前試験と研究の適時な完成或いは結果を確定することができず、FDA、NMPA、PMDA或いは他の監督機関が著者らが提出した臨床計画を受け入れるかどうか、或いは著者らの臨床前試験と研究の結果が最終的に著者らの計画の更なる発展を支持するかどうかを予測することができない。したがって、私たちは私たちが期待しているタイムラインでIND申請または同様の臨床前計画申請を提出できることを保証することができず、IND申請または同様の申請の提出がFDA、NMPA、PMDA、または他の規制機関が臨床試験の開始を許可することを保証することもできない。
臨床試験は設計と実施が困難であり,不確定な結果に触れ,成功しない可能性がある。
人体臨床試験は設計と実施が困難であり、一部の原因はそれらが厳格な監督管理要求を受けているからである。臨床試験の設計はその結果が候補製品の承認を支持するかどうかを確定することができるが、臨床試験設計中の欠陥は臨床試験の進展が良好になるまで明らかにならない可能性がある。組織として、著者らは臨床試験を設計する経験が限られており、監督管理の承認を支持する臨床試験を設計と実行できないかもしれない。臨床試験を行っている生物製品の失敗率は高く,我々の候補製品では,新技術に基づいて患者の状況に応じて設計されているため,失敗率が高い可能性がある。製薬と生物技術業界の多くの会社は後期臨床試験で重大な挫折を経験し、臨床前試験と早期臨床試験においても奮い立つ結果を得た。臨床前と臨床活動から得られたデータは異なる解釈を受ける可能性があり、これは監督部門の承認を延期、制限或いは阻止する可能性がある。また、私たちの候補製品開発中の規制政策の変化を含む多くの要因により、規制の遅延や拒否に遭遇する可能性がある。どのような遅延も、私たちの業務、財務状況、運営結果、および見通しに否定的な影響を及ぼす可能性がある。
臨床前研究或いは臨床試験の成功は未来の臨床試験の結果を予測できないかもしれない。
臨床前研究の結果は必ずしも未来の臨床試験結果を示唆するとは限らず、臨床試験の中期結果も必ずしも最終結果を予測するとは限らない。RRMMが先に完成し,行っているCilta−cel臨床試験から積極的なデータを得ているが,我々は規制部門の承認を求めるために,米国,日本,EU,カナダ,オーストラリア,アルゼンチン,ブラジル,イスラエル,韓国でより多くの臨床試験を行っている。私たちの他の候補製品はまだ初期開発段階にある。このため,これらの候補薬がヒトの期待適応に有効で安全であるかどうかは知られていない。我々の候補製品は臨床開発において期待される安全性と有効性を示すことができないかもしれないが、臨床前研究で積極的な結果が得られたにもかかわらず、
初歩的な臨床試験に成功した。十分な有効性と安全性が決定されなかったことは、候補製品の臨床開発を放棄する可能性がある。
私たちの候補製品は臨床試験における患者登録人数に依存する。われわれが臨床試験で患者を募集する際に困難に遭遇すると,われわれの臨床開発活動は延期されたり,他の悪影響を受けたりする可能性がある。
患者が著者らの候補製品の臨床試験に参加する資格を確定し、参加させることは著者らの成功に重要である。様々な理由から,臨床試験では患者登録の困難に遭遇する可能性がある。プログラムにより速やかに臨床試験を完了し,他の事項を除いて,研究が終了するまで十分な数の患者を募集する能力があるかどうかに依存する。患者の登録は多くの要素に依存している
•プログラムに規定されている患者資格基準
•研究中の病気や状態の患者数
•試用過程における候補製品のリスクと収益を理解すること
•他の既存療法に対する研究中の候補製品の潜在的優位性に対する臨床医および患者の見方は、我々が研究している適応のために承認される可能性のある任意の新薬またはラベルの外でこれらの適応のために使用される可能性のある薬剤を含む
•基準に適合した患者群の規模と性質
•患者と研究場所の距離
•臨床試験の設計
•臨床試験調査員は適切な能力と経験を持つ臨床試験調査員の能力を募集する
•類似療法や他の新しい療法の競争的臨床試験は,T細胞免疫療法には関与していない
•患者の同意を得て維持する能力は
•臨床試験に参加した患者は治療を完了する前に臨床試験から退出するリスクがある。
特に,われわれのいくつかの臨床試験は,非常に小さな集団で発見された特徴を有する患者を募集することを目的としている。他社は多発性骨髄腫やわれわれが検討している他疾患の細胞療法の臨床試験を行っており,患者を募集して研究に参加することを求めており,そうでなければこれらの患者はわれわれの臨床試験に参加する資格がある可能性があり,募集の遅れやわれわれの臨床計画の遅延を招く可能性がある。また,合格臨床研究者の数が限られているため,いくつかの競争相手が使用している同じ臨床試験地点でわれわれのいくつかの臨床試験を行うことが予想され,これらの臨床試験地点で臨床試験を行うことができる患者数をさらに減少させる可能性がある。また、私たちの候補製品はよりよく使われている癌治療法と異なるため、潜在的な患者と彼らの医師は、私たちの臨床試験に参加するのではなく、化学療法や抗体療法などの伝統的な療法を使用する傾向があるかもしれない。
患者登録の遅延は,コスト増加や計画の臨床試験の時間や結果に影響を及ぼす可能性があり,これらの臨床試験の完了を阻止し,候補製品開発を進める能力に悪影響を及ぼす可能性がある。さらに、臨床試験の開始遅延や完成を招く可能性のある多くの要素は、最終的に私たちの候補製品が規制部門の承認を得ることを拒否される可能性もある。
私たちはすでに私たちの候補製品を研究して、調査員で私たちの候補製品を研究し続ける予定です-臨床試験を開始することは,このような試験の進行を完全に制御できないことを意味する。
私たちは現在私たちの候補製品に対して研究者による臨床試験を行っている。また,我々の戦略の一部は,中国の研究者が開始した臨床試験において細胞治療の新たな機会を探索し続けることであり,このような試験は中国国家衛生委員会の監督の下で開始·行われ,医療製品としてではなく医療実践技術として行われている。一般に,米国国家薬品監督管理局はCTAのスポンサーである研究製品メーカーからのCTAのみを受け入れ,審査,拒否または承認することであり,CTAになろうとしている調査者やスポンサーからの医師ではない。NMPAは前者を登録臨床試験,後者を非登録臨床試験に区分しており,通常考慮されていない
メーカーの登録臨床試験申請を審査する際に、研究者によって開始された非登録臨床試験によって生成されたデータ。
しかし、CAR-T療法について、アメリカ国家薬品監督管理局は中国とアメリカに大量の研究者による非登録臨床試験があることを意識し、その薬物評価センターのある審査員は2018年2月と2018年10月にそのサイトで2つの文章を発表し、以下の観点を表明した:(1)主流監督は登録臨床試験の経路に従うが、(2)非登録臨床試験のデータが登録臨床試験に適用される同じ要求に完全に適合すれば、特に製造品質管理、インフォームドコンセント、データ完全性、データ完全性と一致する。データ管理とすべての良好な臨床実践(“GCP”)要求。
したがって,我々が中国の研究者が開始した臨床試験において細胞治療の新たな機会を探索する戦略を継続することにより,NMPAがわれわれの候補製品の研究者からの臨床試験のデータを考慮することを拒否するリスクに直面する可能性があり,(1)登録臨床試験に依存した主流の規制経路に沿っていないこと,あるいは(2)われわれ製品候補製品の非登録臨床試験が登録臨床試験に適用されるのと同じ要求に完全に適合していない可能性があることを懸念し,以下に説明する。
研究者による臨床試験によるリスクは,本節でわれわれが開始した臨床試験に関するリスクと類似している。研究者が始めた試験は臨床データを提供し、私たちの未来の発展戦略に情報を提供するかもしれないが、私たちは試験の方案、管理あるいは進行を完全に制御しているわけではない。したがって,我々は研究者の試験を行う方式に関するリスクに直面しており,我々が中国で行っているどの研究者も臨床試験を開始した臨床データがFDA,EMA,PMDAや中国以外の他の類似規制機関に受け入れられる保証はない。このような研究者が開始した臨床試験の第三者は、私たちの予想されたスケジュールまたは臨床試験規程または適用法規に従って、私たちの臨床試験に対する責任を果たすことができないかもしれない。さらに、これらの試験によるいかなるデータ完全性問題や患者安全問題も私たちがコントロールできるものではないが、私たちの名声に悪影響を与え、私たちの候補製品の臨床と商業の将来性を損なう可能性がある。その他のリスクには、調査者や管理者とのコミュニケーションの困難や遅延、プログラムの遅延、その他の時間の問題、データを解釈する上での困難や分岐がある。第三者研究者は,我々自身が設計した臨床試験と比較して,より実現困難な臨床終点を有する臨床試験を設計したり,臨床試験結果が陰性であるリスクを他の方法で増加させたりする可能性があり,科学的価値があると考えてもこれらの試験を停止することを選択する可能性がある。したがって、私たちはFDA、NMPA、EMAとPMDA、他の類似した規制機関、関連機関審査委員会、道徳委員会、主管国家当局が研究者が開始した試験に関する設計、実施と時間、およびFDA、NMPA、EMAおよびPMDAとのコミュニケーションが制御されておらず、私たちに追加のリスクと不確実性を直面させ、その中の多くのリスクと不確実性は私たちが制御できず、これらのリスクと不確実性の発生は私たちの候補製品の将来性に悪影響を及ぼす可能性がある。
また,われわれが中国で行ったどの研究者による臨床試験の臨床データも,異なる人種,民族,あるいは非中国系患者において類似した結果が生じる保証はない。最後に、中国事件で調査員が起こした裁判と他の裁判で発生したデータの国境を越えた移転は中国の法律によって規制されている。私たちはこのようなデータのすべてまたは一部を他の国に移すことができないかもしれませんが、このようなデータを他の国のさらなる規制適用および報告書を規制する能力に使用することを阻害するかもしれません。
私たちのいくつかの候補製品の市場機会は、以前の治療を受ける資格がない患者または以前の治療を通過できない患者に限られる可能性があり、小さい可能性があり、潜在市場規模の予測は正しくないかもしれない。
癌療法は1線,2線または三線療法と記述されることがあり,FDAは通常最初に最後の線で使用される新しい療法のみを承認する。血液癌が発見された時、彼らは癌を治癒することを目的とした第一線の治療を受ける。これは通常、化学療法、放射線、抗体薬、腫瘍標的小分子、またはこれらの薬剤の組み合わせを含む。また,併用化学療法を行った後,第一線の治療で骨髄移植を増加させることもある。患者の癌が再発した場合、彼らは、より多くの化学療法、放射線治療、抗体薬物、腫瘍標的小分子またはこれらの薬剤の組み合わせ、または骨髄移植を含む二線または三線治療を受けるであろう。一般に,治療線が高いほど治癒の機会は低くなる。三線以上の線では、リンパ腫と骨髄腫治療の目標は腫瘍の成長を制御し、治癒の可能性が大きくないため、患者の生命を延長することである。これらの場合,患者は通常臨床試験に移行される。同様に、私たちの一部の候補パイプライン製品は、以前の治療に失敗した末期または転移性固形腫瘍の治療を目的としている。場合によっては、早期に診断された固形腫瘍は単独で手術治療を行うことができ、化学療法および/または放射線治療を併用することもできる。しかし、より末期或いはより転移した固形腫瘍は通常より治療が困難であり、現在の治療方法はよく十分ではない
多くの患者にとっては。場合によっては、治療の目標は腫瘍の成長を制御し、患者の生命を延長することである可能性がある。
CARVYKTIはFDAの承認を得ており,限られた数の他の管轄地域からマーケティング許可を得ており,MM患者の後期線療法として承認されているが,Cilta−celが早期線療法として承認されることは保証されておらず,我々の他の候補製品も保証されず,承認されても早期線療法のために承認されるであろう。また,早期治療経路の承認を得る前または後に,追加の大型無作為臨床試験を行わざるを得ない可能性がある。
私たちの目標癌患者数の予測と、一線、二線、三線、四線治療を受けることができるこれらの癌患者の亜群の規模、及び誰が私たちの候補製品治療から利益を得る可能性があるかは、私たちの信念と推定に基づいている。これらの推定は様々な源から来ており、科学文献、診療所調査、患者基金会或いは市場研究を含み、正しくないことが証明されている可能性がある。また,新たな研究はこれらの癌の推定発症率や流行率を変える可能性がある。患者数は予想より少ないかもしれない。さらに、私たちの候補製品の潜在的にアドレス指定可能な患者集団は限られているかもしれないし、または私たちの候補製品の治療を受け入れられないかもしれない。潜在的なターゲット層が少ないため、私たちの候補製品がかなりの市場シェアを獲得しても、規制部門のより多くの適応の承認を得なければ、あるいは早期治療シリーズの一部として、私たちは決して相当な収入を得られないかもしれない。
私たちの候補製品に関連する不良副作用や他の安全リスクは、承認を遅延または阻止する可能性があり、臨床試験を一時停止または停止させ、候補製品を放棄し、承認されたラベルの商業イメージを制限すること、または上場承認後の重大な負の結果を招く可能性がある。
我々と他社が行ったCAR−T細胞に関する臨床試験では,最も顕著な急性毒性には,発熱,低血圧,腎機能障害などのCRSに関与すると考えられる症状が含まれている。一部の患者はまた中枢神経系の毒性、或いは意識障害、振戦、脳神経機能障害、てんかん発作、脳症と言語障害などの神経毒性を経験した。最も深刻な副作用はCAR-T細胞によるものであり、いくつかの患者の中で深刻であり、そして生命に危害を及ぼす。生命危険事象は呼吸機能障害と神経毒性と関係がある。深刻かつ生命に危害を及ぼす毒性の多くは細胞注入後の最初の2週間に発生し、通常3週間以内に消失するが、いくつかの患者はCAR-T細胞に関連する臨床試験で死亡し、著者らの臨床試験に含まれている。そのほか、他の患者は治療フォローアップの後期に深刻な不良事件が出現し、例えば細胞減少、感染と神経毒性である。
1期LENGE−2臨床試験では,91.9%の患者にCRSが出現し,9.5%の患者が3段階以上のCRSを出現した。死亡した患者では,任意のレベルの総CAR−T細胞神経毒性が認められた。レベル3以上の神経毒性事件の報告はない。第一段階LEGON−2臨床試験では,34人の死亡が報告されている:28人が疾患進行で死亡し,1人がCRSと腫瘍溶解症候群で死亡し,1人が肺塞栓と潜在的な急性冠症候群で死亡し,1人が後続治療に関連する呼吸不全で死亡し,1人が食道癌で死亡し,2人が感染で死亡した。1 b/2 CARTITUDE−1期臨床試験では、95%の患者がCRSを出現し、5%の患者が3段階以上のCRSを出現した。21.6%の患者は任意のレベルのCAR-T細胞総神経毒性を認め、12.3%の患者はレベル3以上の神経毒性を観察した。1 b/2 CARTITUDE−1段階試験期間中に30例が死亡を報告した:14例は疾患進展,6例は研究者が評価した治療関連有害事象,10例は治療とは無関係な有害事象であった。
われわれの臨床試験には,重症で健康状態が悪化した癌患者が含まれており,他の候補製品のより多くの臨床試験には,健康状態が悪化した類似患者が含まれることが予想される。その中のいくつかの患者は、我々の現在の臨床試験や他の会社や学術機関が行っているCAR−T細胞に関連する臨床試験で観察されたような副作用を経験する可能性があり、患者の疾患が重すぎるため、または患者が候補製品とは無関係な医療問題を経験しているため、私たちの臨床試験において様々な原因で死亡する可能性がある。死亡が私たちの候補製品と関係なくても、これらの死亡は私たちの候補製品の安全性に対する見方に影響を与える可能性がある。
私たちの候補製品または私たちの候補製品と類似していると考えられる他の会社の製品または候補製品による患者の死亡および深刻な副作用は、私たち、機関審査委員会、道徳委員会、FDA、国家薬品監督管理局、薬品監督管理局、または他の監督機関が様々な原因で延期、一時停止、臨床試験の中止を招く可能性がある。もし私たちが開発した任意の候補製品の臨床試験を延期、一時停止、または終了することを選択または要求された場合、その候補製品のビジネスの将来性は
私たちがこの候補製品から製品収入を作る能力を損なわれ、私たちは延期されたり淘汰されたりするだろう。臨床試験で観察された深刻な不良事件は論争のある候補製品に対する市場の受け入れを阻害或いは阻止する可能性がある。これらのすべての状況は私たちの業務、将来性、財務状況、そして経営結果に重大な損害を与える可能性がある。
さらに、市販承認されたCARVYKTIまたは私たちの任意の他の候補製品について、製品または候補製品に起因する副作用が、製品または候補製品の使用を提案または要求する患者の任意の長期追跡観察期間内に、または追加の臨床試験または必要なリスク評価および緩和戦略(“REMS”)の間に、多くの潜在的な重大な負の結果をもたらす可能性があることを、私たちまたは他の人が後に発見した場合、
•規制部門は製品または候補製品の承認を撤回することができる
•規制部門はラベルに警告を追加することを要求するかもしれない
•そのような製品または候補製品がREMSを必要としない場合、私たちは、患者、医療提供者のコミュニケーション計画、および/または安全な使用を保証するための他の要素を配布するために、そのような副作用のリスクを要約するための医薬ガイドラインを含むことができるREMSまたは同様のリスク管理計画を作成する必要があるかもしれない
•私たちは起訴され、患者への傷害に責任を負うかもしれない
•私たちの名声は損なわれるかもしれない。
上記のいずれも、特定の製品または候補製品に対する市場の受容度を達成または維持することを阻止することができ、(承認された場合)、私たちの業務、運営結果、および将来性を深刻に損なう可能性がある。
我々の任意の候補製品の臨床試験が、FDA、NMPA、EMA、PMDAまたは他の同様の規制機関に満足させる安全性および有効性を証明できなかった場合、または他の方法で有利な結果が得られなかった場合、私たちは、候補製品の開発および商業化を完了または最終的に完了できない間に追加のコストまたは経験遅延を生じる可能性がある。
FDA、NMPA、欧州委員会、PMDA、または他の同様の規制機関のマーケティング承認が得られるまで、商業化、マーケティング、普及、または販売されてはならず、開発中の候補製品のこのような承認は決して得られないかもしれない。これらの候補製品がいつ、あるいは人体で有効または安全を証明するかどうかを正確に予測することはできず、監督部門の許可を得る。規制部門が私たちの任意の候補製品の商業販売に対する市場承認を得る前に、私たちの候補製品は各提案された適応において安全かつ有効であることを、長く、複雑で高価な臨床前研究と臨床試験によって証明しなければならない。臨床試験は高価で、設計と実施が困難であり、完成には何年もかかるかもしれないし、結果はまだ確定していない。1つまたは複数の臨床試験の失敗は、臨床発展の任意の段階で発生する可能性がある。
臨床試験の前、期間、または結果として、私たちは多くの予見できない事件に遭遇する可能性があり、これらの事件は、上場許可を得ることを延期または阻止するか、または私たちの任意の候補製品を商業化することを含むかもしれない
•FDA、NMPA、EMA、PMDAまたは他の類似した規制機関は、私たちの臨床試験の数、設計または実施に同意しないかもしれないし、私たちのように臨床試験の結果を説明しないかもしれない
•規制機関または機関審査委員会または道徳委員会は、私たちまたは私たちの調査者が予想される試験場所で臨床試験を開始するか、または臨床試験を行うことを許可してはならない
•私たちは予想される臨床試験場所と受け入れ可能な条項と合意しないかもしれません。これらの条項は広範な交渉が必要かもしれませんし、異なる臨床試験地点の間に有意差があるかもしれません
•私たちの候補製品の臨床試験は否定的または不確実な結果をもたらすかもしれない
•私たちは決定するかもしれないし、監督機関は追加の臨床試験を要求したり、製品開発計画を放棄することを要求するかもしれない
•私たちの候補製品の臨床試験に必要な患者の数は私たちが予想していたより多いかもしれません。これらの臨床試験の登録速度は私たちが予想していたよりも遅いかもしれません。参加者がこれらの臨床試験から退出する割合は、私たちが予想していたよりも高いかもしれません
•私たちの第三者請負業者は、法規の要求を適時に遵守したり、私たちに対する契約義務を履行できなかったり、全く守らなかったりする可能性があります
•監督機関は臨床猶予令を発表する可能性があり、監督機関あるいは機関審査委員会は、監督要求に適合していないことや参加者が受け入れられない健康リスクに直面していることを含む、様々な原因で臨床研究を一時停止または終了することを要求する可能性がある
•私たちの候補製品の臨床試験コストは予想以上に高いかもしれません
•食品薬品監督管理局、国家食品薬品監督管理局、薬品監督管理局、あるいは他の類似した監督機関は、私たちの製造技術や施設を承認できないかもしれない
•候補製品の供給または品質、または候補製品の臨床試験に必要な他の材料が不足しているか、または不十分である可能性がある
•私たちの候補製品は、特にサイトカイン誘導毒性およびT細胞再生障害性疾患のようなヒトにおけるそれらの最初の使用を考慮して、私たちまたは私たちの研究者、規制機関または機関審査委員会が臨床試験を一時停止または終了させることを考慮すると、不良な副作用または他の予期しない特徴を有するかもしれない
•FDA、NMPA、EMA、PMDA或いはその他の類似規制機関の承認政策或いは法規は重大な変化が発生する可能性があり、著者らの臨床データは承認を得るのに十分ではない。
試験結果がFDA、NMPA、欧州委員会、PMDAまたは他の国または司法管轄区域の規制機関にBLA、マーケティング許可申請、新薬申請(“NDA”)または他の同様の申請を承認することができない場合、私たちの候補製品の商業化は大幅に遅れる可能性があり、または追加の試験を行うために多くの追加資源を費やして、私たちの候補製品の潜在的な承認を支援する必要があるかもしれない。
CARVYKTIと私たちの候補製品はすべて生物製剤であり、それらの製造は複雑で、私たちは生産中に困難に直面する可能性があり、特に技術開発或いは私たちの製造能力を拡大する上で困難に直面する可能性がある。もし私たちがこのような困難に直面すれば、商業化と臨床試験に候補製品を提供する能力が延期または停止される可能性がある。
我々はすでに必要な品質のCAR−T細胞を製造する強力な方法を開発しており,我々は処理の不一致を解消するためにウイルス形質導入過程を改善している。私たちは私たちの現在の技術が全面的な商業化に適していると信じている。全面的な商業生産に拡張できると考えられるプロセスを構築しましたが、各製造プロセスは、施設、人員、設備、およびプロセスの設計作業を保証するために、プロセス検証運転の性能を検証しなければなりません。私たちはまだ私たちの候補製品の大多数を商業規模の製造や加工を行っていません。そして私たちの候補製品のどのような製造や加工もできないかもしれません。
他のバイオ製品メーカーと同様に,特に規模の拡大や縮小,生産過程の検証,製造過程の信頼性の確保に困難が生じる可能性がある。これらの問題には、物流や輸送面の遅延や故障、生産コストと生産量の困難、品質管理と製品テスト、オペレータミス、合格者の不足、厳格に実行されている連邦、州と外国法規を遵守できなかったことがある。
さらに、我々が供給する製品または候補製品または製造施設において微生物、ウイルスまたは他の汚染が発見された場合、これらの製造施設は、汚染を調査および修復するために長い間閉鎖する必要があるかもしれない。私たちはあなたにこのような他の私たちが作った問題が未来に起こらないということを保証することはできません。商業製品供給のいかなる遅延や中断も、私たちの商業化計画を延期し、規制審査を招き、私たちの名声を損ない、私たちの収益性を阻害する可能性がある。臨床試験供給のいかなる遅延或いは中断は臨床試験の完成を延期する可能性があり、臨床試験計画の維持に関連するコストを増加し、そして遅延した時間帯に基づいて、著者らは追加費用で新しい臨床試験を開始或いは完全に臨床試験を中止することを要求する。
患者からT細胞を採取し、T細胞をプログラミングすることを含む、患者に自己CAR−T細胞療法を製造および提供することは、患者からT細胞を採取することを含む複雑で総合的なプロセスに関連する離体するCAR-T細胞を増殖させて必要な用量を得、最終的にCAR-T細胞を患者に再注入した。複雑性のため、一般的な生物製剤の製造コスト、特に私たちのCAR-T細胞候補製品は、通常伝統的な小分子化合物よりも高く、製造技術はもっと変わりやすく、しかも困難である
コピーコストが高い。また,われわれの製造過程は製品の紛失や失敗の影響を受けやすく,患者から白血球を採取し,患者材料を生産現場に搬送し,患者材料を貯蔵·処理し,患者材料をCAR−T細胞とともに患者に返送し,最終製品を患者に注入することに関連する物流問題である。他の製造問題は患者の出発材料の差異、細胞成長の不一致、製品特性の変化、製造過程中の中断、設備或いは試薬の故障、設備の設置或いは操作の不適切、及びサプライヤー或いはオペレータの誤りを含む。正常製造プロセスとの微小な偏差でも生産量の低下、製品欠陥、その他の供給中断を招く可能性がある。静脈から静脈供給チェーン内の任意の点で損失、破壊、または他の方法で患者材料を損傷する場合、患者の製造プロセスを再起動する必要がある可能性があり、それによる遅延は、疾患進行のリスクによって患者の予後に悪影響を及ぼす可能性がある。また,我々の製品や候補製品は各特定の患者のために製造されているため,患者から製造施設まで,製造プロセスを介して患者に戻るまでの間に身体鎖を保持する必要がある。このような身分チェーンを維持することは困難で複雑であり、もしこれができなければ、患者の不良結果、製品損失或いは監督管理行動を招き、著者らの製品を市場から撤退することを含むかもしれない。また,候補製品の開発による臨床前から後期までの臨床試験の承認と商業化に伴い,開発計画の様々な面,例えば製造方法,プロセスや結果の最適化に努める過程で変更することが一般的である。これらの変化はこれらの予想される目標を達成できない可能性があるが、これらの変化のいずれも私たちの候補製品の表現を異なり、計画中の臨床試験あるいは他の未来の臨床試験の結果に影響を与える可能性がある。
我々の製造施設はまた,それらが設計どおりに動作していることを証明し,FDA,NMPA,EMA,PMDA,その他の類似規制機関の政府検査を受けるためのデバッグと検証活動が必要である。もし私たちが規制機関が受け入れられる規格に従って製品を生産することができなければ、私たちは私たちの製品を生産するために必要な承認を得ることができないかもしれない。さらに、私たちの施設は、私たちの候補製品が商業的に発表される前または後に政府検査を通過できない可能性があり、これは、規制機関によって発見された任意の欠陥を修復するために必要な追加コストを招く可能性がある。これらの挑戦のいずれも商業製品の供給を中断し、商業化努力を損害する可能性があり、私たちは製品販売の期待を達成できず、臨床試験の完成を延期し、臨床試験を移行あるいは1つ以上の臨床試験を繰り返し、臨床試験コストを増加させ、私たちの候補製品の承認を延期し、私たちの商品コストを増加させ、そして私たちの業務、財務状況、運営結果と成長の将来性に不利な影響を与える必要がある。
T細胞療法を用いた癌患者の治療過程はヒトやシステムリスクの影響を受ける。
自己T細胞療法を用いて癌患者を治療する“静脈対静脈”周期は、一般に、多くのステップおよびヒト参加者を含む約4~6週間を必要とする。まず,臨床現場で患者のリンパ球を分離分離し,製造現場に搬送する。生産現場で現在良好な生産実践(“cGMP”)条件下で、患者のリンパ球は解凍と洗浄され、その後専用の試薬を用いてCD 3陽性T細胞を濃縮した。一夜培養とT細胞活性化後、T細胞はレンチウイルスベクター形質導入技術を用いてCAR遺伝子構造を濃縮したT細胞集団に導入した。T細胞形質導入が完了した後、T細胞は数日増幅され、収穫され、最終的な薬物製品を作製し、その後凍結保存し、患者に使用する。米国と中国では,最終製品のサンプルはいくつかの放出テストを経ており,これらのテストは特定の基準を満たさなければならず,製品放出を輸液に用いることができる。これらの試験は無菌、識別、純度、効力、および他の試験を含む。著者らはT細胞治療過程において厳格な監督管理と品質標準の制約を受けた。私たちの品質管理と保証仕事が成功することを保証することはできませんし、これらの過程の人為的あるいは系統的なミスのリスクが解消されることを保証することもできません。
従来の治療は癌を変化させ,われわれのCAR−T細胞が臨床活動を実現する機会に悪影響を及ぼす可能性がある。
血液病患者は通常猛毒の化学療法を彼らの初期治療として受ける。このような治療は患者から収集したT細胞の活性に影響する可能性があり,CAR−T細胞治療に対する高度な反応を引き起こす可能性がある。患者はまた、以前の治療を受けることができ、腫瘍細胞上で私たちが予想されるプログラムCAR-T細胞製品または候補製品と同じ標的抗原を標的抗原とすることができ、これは、これらの患者の癌細胞の標的タンパク質の低発現または不発現をもたらす可能性がある。したがって,われわれのCAR−T細胞候補製品は癌細胞を認識できない可能性があり,臨床活性を実現できない可能性がある。私たちの主な候補製品Cilta-cel(FDAと欧州委員会のCARVYKTI商標の承認を得ました)この課題に直面しています例えば、MM患者は、Cilta-celを受ける前に、GSK 2857916、AMG-420(安進)およびCC-93269(百時美施貴宝)などのT細胞結合分子を標的とするBCMA、例えばAMG-420(安進)およびCC-93269(百時美施貴宝)、または同様の製品または候補製品などのBCMA標的抗体結合体BCMA-ADCを受けている可能性がある。もし私たちのすべての候補製品が十分な臨床活性レベルに達していなければ、私たちはこの候補製品の開発を停止する可能性があり、これは私たちのアメリカ預託証明書の価値に不利な影響を与えるかもしれない。
私たちは、より利益があるかもしれない、またはより成功する可能性のある候補製品または適応を利用することなく、特定の候補製品または適応を追求するために限られた資源を費やすかもしれない。
私たちの財務と管理資源が限られているため、特定の適応のための研究計画と製品候補に重点を置いています。したがって、私たちは他の候補製品を探す機会を放棄または延期するか、または後により大きな商業潜在力を有することが証明された他の兆候を探す機会を放棄または延期するかもしれない。私たちの資源配分決定は私たちが実行可能な商業製品や利益のある市場機会を利用できないかもしれない。私たちの現在と未来の研究開発計画および特定の適応候補製品への支出はいかなる商業的に実行可能な製品も発生しないかもしれない。もし私たちが特定の候補製品の商業的潜在力や目標市場を正確に評価しなければ、私たちは協力、許可、または他の印税手配によって候補製品に価値のある権利を放棄するかもしれないが、この場合、候補製品の独占開発権と商業化権利を維持することは私たちに有利だ。
私たちの業務運営に関するリスク
米国以外で大量の業務を持っている会社として、私たちの業務は国際業務に関連する経済、政治、規制、その他のリスクの影響を受けている。
EUや中国で大量の業務を持つ会社として、私たちの業務は米国以外で業務を展開する関連リスクの影響を受けている。私たちの多くのサプライヤーと臨床試験の関係はアメリカ以外に位置している。したがって、私たちの将来の業績は様々な要素の影響を受けるかもしれない
•インフレ、特に非アメリカ経済と市場の政治的不安定を含む経済的疲弊
•製品承認の違いと変化する規制要件
•異なる法ドメインは、これらのドメインで動作する自由を保障、維持、または獲得する上で異なる問題をもたらす可能性がある
•知的財産権の保護を減らすことができます
•複数の法域の異なる、複雑で変化する法律、条例、裁判所システム、および様々な外国の法律、条約、条例を遵守することが困難である
•アメリカ以外の規制と税関、関税、貿易障壁の変化
•ドル、ユーロ、人民元などの非米通貨為替レートの変動や通貨規制
•特定の国や地域の政治経済環境の変化
•貿易保護措置、輸出入許可要求、または政府が取った他の制限行動
•ある非アメリカ市場では異なる精算制度と価格規制が行われています
•税法変更による否定的な結果
•例えば、私たちのインセンティブ株式計画に従って付与されたオプションおよび制限株式単位の異なる司法管轄区域における可変税金待遇を含む、居住または海外旅行の従業員のために、税収、雇用、移民、および労働法を遵守する
•労働騒乱がアメリカよりも一般的な国では労働力の不確実性
•非解雇、差別、誤分類、または労働法違反または他の告発された行為に対するクレームを含む、現職または元従業員またはコンサルタントが単独で、または集団訴訟の一部として、私たちに提起された訴訟または行政訴訟;
•異なる労使関係を含む人員配置と国際業務の管理に関する困難
•海外の原材料の供給や製造能力に影響を与える事件による生産不足;
•地政学的行動による業務中断は、戦争やテロ、金融機関の倒産、衛生流行病や地震、台風、洪水、火災などの自然災害を含む。
私たちの中国での業務の他のリスクについては、“リスク要因である中国でのビジネスに関するリスク”を参照されたい。
私たちは私たちの組織の規模を拡大する必要があり、私たちはこのような成長を管理する時に困難に直面するかもしれない。
2022年12月31日現在、約1,390人のフルタイム従業員がいます。私たちの発展と商業化計画の進展および戦略計画の拡大と発展に伴い、私たちの上場企業としての成熟に伴い、私たちの製品開発および現在と計画における将来の商業化努力を支援する人を含む、より多くの管理、運営、財務、その他の人員が必要になると予想される。今後の成長は、経営陣のメンバーにより多くの重大な責任を負わせるだろう
•より多くの従業員を識別し、採用し、統合し、維持し、激励する
•我々の候補製品に対する臨床、FDA、NMPA、EMAおよびPMDA審査プロセスを含む、我々の内部開発作業を効率的に管理する
•私たちの業務、財務、管理制御、報告システム、そして手続きを改善する。
細胞治療経験のある人は少なく、これらの人たちの競争は激しい。私たちの将来の財務業績と候補製品を効果的に商業化する能力は、将来の任意の成長を効果的に管理する能力にある程度依存しており、私たちの経営陣はまた、これらの成長活動を管理するために、不比例な注意を日常活動から移しなければならないかもしれない。
もし私たちが新入社員を雇用することで私たちの組織を効果的に拡大できなければ、私たちは私たちの候補製品のさらなる開発と商業化に必要な任務を成功させることができないかもしれないので、私たちの研究、開発、商業化の目標を達成できないかもしれません。
私たちの組織を拡大するほか、私たちの施設の規模を拡大し、私たちの開発と製造能力を建設しており、これには多くの資本支出が必要です。もしこのような資本支出が予想以上であれば、私たちの財務状況と資本資源に悪影響を及ぼすかもしれない。また、私たちの施設規模の増加が遅れていれば、会社の目標を達成するために組織規模を迅速に拡大する能力を制限する可能性があります。
私たちの将来の成功は、私たちが上級管理職の重要なメンバーを引き留めることができるかどうか、そして合格した人員を誘致、維持、激励できるかどうかにかかっている。
競争の激しい生物製薬業界における著者らの競争能力は私たちの高い素質管理、研究開発、臨床、財務と業務発展人員を吸引と維持する能力に依存する。私たちは私たちの経営陣、科学、医療者に強く依存しており、彼らの誰でもいつでも私たちとの雇用関係を終わらせることができる。私たちは私たちの誰にも“キーパーソン”保険を提供しない。
合格した管理、財務、科学、臨床、商業化、製造及び販売とマーケティング人員を募集と維持することは、著者らの成功の鍵となる。上級管理職のメンバーや他の重要な従業員のサービスを失うことは、私たちの研究開発と商業化目標の実現を阻害し、業務戦略を成功させる能力を深刻に損なう可能性がある。また、私たちの高度管理者やキーパーソンを交換することは困難かもしれませんし、私たちの業界では開発に成功し、規制部門の承認を得て、私たちの候補製品を商業化するために必要なスキルや経験を持っている個人数が限られているので、長い時間がかかるかもしれません。私たちの成功はまた私たちが引き続き高技能の初級、中級と高級管理者及び初級、中級と高級科学と医療人員を吸引、維持、激励できるかどうかにかかっている。この限られた候補者人材バンクから募集する競争は非常に激しく、多くの製薬と生物技術会社の間の類似人員に対する競争を考慮して、私たちは受け入れ可能な条件でこれらの肝心な人員を採用、訓練、維持或いは激励することができないかもしれない。私たちはまた、大学や研究機関から科学や臨床人を募集する競争に直面している。また、私たちは、科学と臨床コンサルタントを含むコンサルタントとコンサルタントに依存して、私たちの研究開発と商業化戦略の制定を助けてくれます。私たちのコンサルタントとコンサルタントは、他のエンティティとの相談やコンサルティング契約で約束があるかもしれません。これは、彼らの私たちに対する利用可能性を制限するかもしれません。もし私たちが引き続き高い素質の人材を誘致し、維持することができなければ、私たちが成長戦略を推進する能力は制限されるだろう。
私たちが将来の買収や戦略協力に従事すれば、これは私たちの資本金要求を増加させ、私たちの株主を希釈し、私たちに債務を発生させたり、負債を抱えたり、他のリスクに直面させてしまう可能性があります
私たちは、当社の業務計画を実行するのに適していると考えられる補完製品、知的財産権、技術、または業務を許可または取得することを含む、様々な買収および戦略的協力を時々評価することができます。潜在的な買収や戦略的協力は多くのリスクをもたらす可能性がある
•業務費と現金需要が増加した
•追加の債務や負債を負担しています
•買収された会社の業務、知的財産権、製品を吸収し、新しい人員の統合に関する困難を含む
•私たちの経営陣の関心を既存のプロジェクトと計画からこのような戦略的パートナーシップ、合併、または買収を求めることに移した
•重要な従業員の保留、キーパーソンの流出、そして私たちがキー業務関係を維持する能力の不確実性
•そのような取引の他方に関連するリスクおよび不確実性は、その当事者およびその既存製品または候補製品の将来性および販売承認を含む;
•買収した技術から十分な収入を得ることができず、買収の目標を達成することができず、関連する買収や維持コストを相殺することさえできない。
また、買収を行えば、希釈証券を発行し、債務を負担または発生させ、巨額の一次費用を発生させ、重大な将来の償却費用を招く可能性のある無形資産を買収することができる。また、適切な買収機会を見つけることができない可能性があり、これは、私たちの業務発展に重要な可能性のある技術や製品を発展させたり、獲得したりする能力を弱める可能性がある。
私たちの内部情報技術システム、あるいは私たちの第三者サプライヤー、協力者、あるいは他の請負業者やコンサルタントのシステムは故障したり、セキュリティホールに遭遇したりする可能性があり、これは私たちの製品開発計画を深刻に中断させ、私たちを規制調査に直面させ、重大な責任を発生させ、私たちをコストが高く、長引く訴訟に直面させ、重大な名声の損害をもたらし、私たちの効果的な業務を運営する能力を妨害する可能性がある。
通常のビジネスプロセスでは、知的財産権、独自のビジネス情報、および健康に関連するデータのような個人情報を含むが、これらに限定されない敏感な情報を収集、格納、および送信する。重要なのは、私たちがこのような敏感な情報の機密性と完全性を維持するために、安全な方法でそうしなければならないということだ。私たちはまた、私たちの運営要素を第三者にアウトソーシングしているので、私たちは多くの第三者サプライヤーと他の請負業者やコンサルタントを管理しています。彼らは私たちの敏感な情報にアクセスすることができます。
私たちの内部情報技術システムおよび私たちの現在および未来の任意の第三者サプライヤー、協力者、および他の請負業者またはコンサルタントのシステムは、社会工学攻撃(ネットワーク釣りによる攻撃を含む)、マルウェア(例えば、ウイルスおよびワーム)、マルウェア(高度な持続的な脅威侵入の結果を含む)、サービス拒否攻撃(例えば、証拠充填)、証拠取得、人員不正行為またはエラー、恐喝ソフトウェア攻撃、サプライチェーン攻撃、ソフトウェアエラー、サーバ障害、ソフトウェアまたはハードウェア障害、データまたは他の情報技術資産の損失、広告ソフトウェア、地震、火災、洪水、テロ、戦争、そして電気通信、電力故障、そして他の似たような脅威。特に、世界各地からの未遂攻撃や侵入の数、強度、複雑性の増加に伴い、セキュリティホールや破壊のリスクは一般的に増加し、特にコンピュータハッカー、外国政府、ネットワークテロリストを含むネットワーク攻撃やネットワーク侵入を介している。また,我々のネットワークにおけるアクセス許可権限を持つ者の意図的または意図的な行動や行動しないため,我々のシステムが破壊されたり中断されたりする可能性がある.私たちはすべての種類の安全脅威を予見できないかもしれないし、これらすべての安全脅威に対して効果的な予防措置を取ることができないかもしれない。サイバー犯罪者が使用する技術はしばしば変化し、発売前に識別されない可能性があり、従来のコンピュータ“ハッカー”、脅威行為者、“ハッカー活動家”、組織的犯罪脅威行為者、人員(例えば、窃盗または乱用によって)、複雑な民族国家および民族国家によって支持される行為者を含む様々なソースから来る可能性がある。
私たちはこれまで、重大なシステム障害、事故、セキュリティホールに遭遇していませんが、このようなイベントが発生し、当社の運営中断または当社のデータまたはアプリケーション、または当社の第三者プロバイダおよび他の協力者、請負業者およびコンサルタントのデータまたはアプリケーションが失われたり、破損したりする場合、私たちのビジネス機密または他の固有情報の損失にかかわらず、当社の開発計画および業務運営中断をもたらす可能性があります
私たちが研究している重大な遅延や挫折、あるいは他の似たような中断。例えば、完成した或いは未来の臨床試験の臨床試験データの紛失は著者らの監督管理の承認作業を遅延させ、著者らのデータの回復或いは複製のコストを著しく増加させる可能性がある。もしどんな中断やセキュリティホールが私たちのデータやアプリケーションを紛失したり破損したり、機密や独自の情報を適切に開示しない場合、私たちは重大な責任を招く可能性があり、私たちの競争地位が損なわれる可能性があり、私たちの名声が損なわれる可能性があり、私たちの候補製品のさらなる開発と商業化が延期される可能性がある。私たちの契約には責任制限が含まれていないかもしれませんが、あっても、私たちの契約における責任制限は、私たちのデータプライバシーとセキュリティ義務に関連する責任、損害、またはクレームから私たちを保護するのに十分である保証はありません。 さらに、私たちの顧客または従業員の個人情報に関する不正アクセス、使用または漏洩を引き起こすこのような事件は、連邦および/または州の違反通知法と外国と同等の法律を遵守させ、強制的な是正措置を迫られる可能性があります。そうでなければ、個人情報のプライバシーおよび安全を保護する法律および法規に基づいて責任を負うことになります。重大なセキュリティホールや中断に関連するコストは巨大である可能性があり、このようなリスクに対して提供されるネットワークセキュリティ保険の制限を超える可能性がある。
第三者サプライヤーと他の協力者、請負業者、コンサルタントの能力は限られています。情報セキュリティアプローチは限られており、これらの第三者には十分な情報セキュリティ対策がない可能性があります。これらの第三者の情報技術システムが中断やセキュリティホールの影響を受ける場合、私たちは重大な責任に直面する可能性があり、このような第三者に対して十分な追跡権がなく、このようなイベントの影響を軽減するために大量の資源を費やし、将来このような性質のイベントの発生を防止するための保護措置を策定し、実施しなければならないかもしれない。第三者サービス提供者がデータプライバシーやセキュリティに関する義務を履行できなかった場合、損害賠償を受ける権利があるかもしれませんが、いかなる賠償も私たちの損害を補うのに十分ではないかもしれません。あるいはそのような賠償を取り戻すことができないかもしれません。
私たちは、データのプライバシーおよびセキュリティに関連する様々な厳格かつ変化する米国および外国の法律、法規、規則、契約義務、政策および他の義務の制約を受ける可能性があり、私たちの第三者サプライヤー、協力者、請負業者またはコンサルタントがプライバシーまたはデータセキュリティに関連する既存または将来の法律および法規を遵守できなかったか、または遵守できなかったことは、民事または刑事罰金または処罰、個人訴訟、他の責任、私たちの業務運営の中断、名声被害および/または不利な宣伝を含む可能性がある。このような法律を遵守または遵守しないことはコストを増加させる可能性があり、それらの使用や採用を制限する可能性があり、そうでなければ、私たちの運営結果や業務に悪影響を及ぼす可能性があります。
通常の業務過程では、我々の商業化および開発活動および当社の従業員に関連する個人データおよび他の敏感な情報を維持して処理し、私たちの商業化および開発活動に関連する独自および機密商業データ、商業秘密、知的財産権、健康情報を含み、私たちの第三者サプライヤー、協力者、請負業者、コンサルタントは私たちを代表してこれらの情報を維持し、処理している。私たちのデータ処理活動は、様々な法律、法規、ガイドライン、業界基準、外部および内部プライバシーおよびセキュリティポリシー、契約要件、およびデータプライバシーおよびセキュリティに関連する他の義務など、多くのデータプライバシーおよびセキュリティ義務の制約を受ける可能性があります。私たち、第三者サプライヤー、パートナー、請負業者、およびコンサルタントは、適用されるデータのプライバシーおよびセキュリティ義務を実際に遵守できないと考えられており、政府の法執行行動(例えば、調査、罰金、処罰、監査、検査および同様の行動)、訴訟(集団訴訟クレームを含む)、追加の報告要件および監督、個人データの処理を禁止すること、個人データの廃棄または使用を命令すること、罰金、会社の役人と大衆の非難、影響を受ける個人の損害クレーム、私たちの名声被害および商業権の喪失、これらはすべて私たちの業務、財務状況、運営結果、または将来性に実質的な悪影響を及ぼす可能性がある。
また、健康関連とデータ保護法律、法規、標準、その他の義務の解釈と応用は依然として不確定であり、常に互いに矛盾し、絶えず変化しているため、これらの法律の範囲と要求は私たちのやり方と一致しない方法で解釈·適用される可能性があり、私たちが変化していくデータ保護規則を遵守する努力は成功しないかもしれない。これらおよび他の任意の適用可能なプライバシーおよびデータセキュリティ法律法規を遵守することは、厳格で時間のかかるプロセスであり、新しいデータ保護ルールの遵守を保証するために追加のメカニズムを確立する必要があるかもしれません。
中国の監督管理部門はすでにデータ保護に関する立法と規制提案を実施し、考慮している。2018年4月2日、中華人民共和国国務院弁公庁は“科学データ管理方法”(“科学データ方法”)を公布し、科学データに対して広義の定義を行い、科学データ管理の関連規則を制定した。“科学データ方法”によると、国家秘密、国家安全、社会公共利益、商業秘密あるいはプライバシーに関連する科学データは、公開共有されてはならない。確かに公開すべきものは、目的、ユーザー資質、秘密条件などの要素を審査し、告知範囲を厳格にコントロールしなければならない。さらにどんな進行でも
少なくとも部分的に中国政府が援助した研究はこの研究者が所属する実体管理のために関連する科学データを提出しなければならず、その後、任意の外国学術定期刊行物にこれらのデータを発表することができる。
2017年6月に施行された“中華人民共和国ネットワークセキュリティ法”は、中国のネットワーク事業者に対する国家レベルのデータ保護を確立し、これには中国国内のすべてのインターネットや他の情報ネットワークを介してサービスを提供する組織が含まれている可能性がある。ネットワークセキュリティ法の傘の下では,多くの法規,ガイドライン,その他の措置がとられる予定である.また、国務院弁公庁などの部門が2021年7月6日に発行した“証券違法活動の厳しい取締りに関する意見”の要求は、“証券海外発行上場に関する守秘とファイル管理の強化に関する規定”の改訂を加速し、データ安全、国境を越えたデータ流動、機密情報管理などの法律法規を完備する。中華人民共和国全国人民代表大会常務委員会が2021年6月10日に公布し、2021年9月1日から施行された“データ安全法”はデータ安全保護の主要な制度枠組みを描き出した。中国人民代表大会は2021年8月20日に公布され、2021年11月1日から施行された“個人情報保護法”は個人情報保護と処理の主要な制度枠組みを描き出した。
“ネットワークセキュリティ審査方法(2021年)”は2021年12月28日に中国民航総局など12の関係部門が発表し、2022年2月15日から施行される。これらの措置は、(一)百万以上のユーザー個人情報を持つ“ネットワークプラットフォーム経営者”が中国以外の国で上場しようとしており、ネットワークセキュリティ審査弁公室にネットワークセキュリティ審査を申請しなければならないこと、(2)中国政府関係部門はある影響或いは国家安全に影響を与える可能性のあるネットワーク製品、サービス或いはデータ処理活動を認定し、ネットワークセキュリティ審査を開始することができることを規定している。
2022年7月7日、CACは、(1)データ処理者が海外でキーデータを提供すること、(2)キー情報インフラ運営者または100万人以上の個人情報を処理するデータ処理者が海外で個人情報を提供すること、(3)データ処理者が前年1月1日から海外で個人情報を提供すること、(3)データ処理者が前年1月1日から海外で個人情報を提供すること、(3)データ処理者が前年1月1日から海外で個人情報を提供すること、(3)データ処理者が前年1月1日から海外で個人情報を提供すること、(3)データ処理者が前年1月1日から海外で個人情報を提供すること、(3)データ処理者が前年1月1日から海外で個人情報を提供すること、(3)データ処理者が前年1月1日から海外で個人情報を提供すること、(3)データ処理者が前年1月1日から海外で個人情報を提供すること、(4)CACに規定されている他のクロスボードデータ伝送セキュリティ評価を申告する必要がある場合。
CACが2021年11月14日に公表した“ネットワークデータセキュリティ管理条例草案”(“データセキュリティ条例草案”)は2021年12月13日に社会に意見を公開し、個人情報100万人以上のデータ処理者を再確認し、大中国以外の他の国で発売しようとしているのは、ネットワークセキュリティ審査を経て、データ処理者が国家安全に影響を与える可能性のあるデータ処理活動を行うべきであり、またネットワークセキュリティ審査を申請しなければならない。データ安全条例草案の要求は、重要なデータを処理する或いは海外で発売されたデータ処理業者は毎年自分で或いは第三者データ安全サービス業者を通じてデータ安全評価を行い、そして現地民航委員会機関に評価報告を提出しなければならない。“データセキュリティ条例”草案は、データ処理活動を広く定義し、収集、記憶、使用、処理、転送、提供、発行、削除、および他の活動を含み、“データセキュリティ条例”草案はまた、データ処理者に対して広い定義を行い、データ処理活動において目的および方法を自律的に決定する個人およびエンティティとして定義する。しかし、“データセキュリティ条例”草案は、どのような場合に“国家安全に影響を与える可能性があるか”を構成している場合についてはさらに述べておらず、正式な採択および発効前にさらに変化する可能性がある。
本年度報告日まで、“ネットワークセキュリティ審査方法(2021年)”と“データ越境移転セキュリティ評価方法”の規則と実施状況は限られており、データセキュリティ条例草案はまだ草案の段階にあり、まだ発効しておらず、中国政府当局はこれらの法律法規の解釈と実行において広範な裁量権を持っている可能性がある。今後の規制改革が私たちのような会社に追加的な制限を加えるかどうかは現在のところ定かではない。私たちは現段階ではデータセキュリティ法規草案の影響を予測することができませんので、ルール制定過程のいかなる進展にも密接に注目して評価します。リリースされたデータセキュリティ条例草案が、私たちのような会社にネットワークセキュリティ審査や他の具体的な行動の承認を要求すれば、このような許可がタイムリーに得られるかどうか、あるいは全く得られない不確実性に直面します。もし私たちがネットワークセキュリティとデータプライバシーの要求をタイムリーにまたは根本的に遵守できなければ、私たちは政府の法執行行動と調査、罰金、処罰、または私たちの不適切なネットワーク業務の一時停止、および他の制裁を受ける可能性があり、これは私たちの業務と運営結果に実質的な悪影響を及ぼす可能性がある。私たちは中国関連のデータ保護法律と法規を遵守するために努力してきて、適用された法律、法規、あるいはガイドラインのいかなる更新も遵守するように努力しています
中国の関係監督部門が発行する.しかし、適用可能なプライバシーやデータセキュリティの法律、法規、ガイドラインをタイムリーにまたは完全に遵守できることを保証することはできません。
また、ある特定の業界の法律法規は中国の個人データの収集、使用、移転に影響を及ぼす。例えば、中国国務院は“人類遺伝資源管理条例”(2019年7月に発効)を公布し、すべて人類遺伝資源に関連する任意の国際協力プロジェクトは、中国国務院科学技術行政部門の許可/届出を経て、そして人類遺伝資源サンプル或いは関連データの任意の輸出或いは国境を越えた移転、或いは非中国実体及びその設立或いは実際に制御している機関に人類遺伝資源情報のアクセスを提供/提供し、追加的に許可、届出とバックアップしなければならない。私たちはあなたに私たちが適用されたすべての人間の遺伝資源関連法規を遵守できるか、または遵守できるということを保証することはできません。これらの法律の解釈と適用は私たちのやり方と一致しない可能性があり、人類の遺伝資源サンプルと関連データを没収し、行政罰金を科す可能性がある。新しい法律法規のさらなる公布と既存の法律法規の改正、解釈、実施にはまだ不確実性があるため、私たちがすべての面でこれらの法規を遵守できることを保証することはできません。私たちは規制されたいかなる機関も違法とみなされ、罰金および/または他の制裁を受けることを命じられるかもしれません。したがって、私たちは関連業務の一時停止や他の処罰に直面することを要求される可能性があり、これは私たちの業務、運営、財務状況に大きな悪影響を及ぼす可能性がある。
データプライバシーとセキュリティに関する新たな提案された法律法規が引き続きあると予想されていますが、これらの将来の法律、法規、基準が私たちの業務にどのような影響を与える可能性があるのかを決定することはできません。新しい法律、既存の法律、法規、基準、その他の義務の改正または再解釈は、追加のコストを発生させ、私たちの業務運営を制限することを要求するかもしれません。健康とデータ保護に関連する法律、法規、標準とその他の義務の解釈と応用は依然として不確定であり、しかも常に互いに矛盾し、絶えず変化しているため、これらの法律の範囲と要求は私たちのやり方と一致しない方法で解釈と適用される可能性があり、私たちが変化するデータ保護規則を遵守する努力は成功しないかもしれない。もしそうであれば、これは政府に罰金や命令を科し、やり方を変更することを要求する可能性があり、これは私たちの業務に悪影響を及ぼす可能性がある。さらに、これらのプライバシー規制は、国/地域によって異なる可能性があり、テストが米国で行われるか、現地の国/地域で行われるかによって異なる可能性があり、私たちの運営または業務実践は、各国/地域でこれらの法規を遵守しない可能性がある。
これらおよび他の任意の適用可能なプライバシーおよびデータセキュリティ法律法規を遵守することは、厳格で時間のかかるプロセスであり、新しいデータ保護ルールの遵守を保証するために追加のメカニズムを確立する必要があるかもしれません。もし私たちまたは私たちの第三者サプライヤー、協力者、請負業者、およびコンサルタントがこのようないかなる法律または法規にも従わなかった場合、私たちは規制調査、巨額の罰金と処罰、名声損害、または私たちの業務慣行の変更を要求される可能性があり、これらはすべて私たちの業務、財務状況、および運営結果に悪影響を及ぼす可能性があります。
2018年5月、ビジネスが増加している欧州経済地域(“EEA”)で一般データ保護条例(“EU GDPR”)が施行された。また、連合王国(The UK)のEU離脱(いわゆるイギリス離脱)により、イギリスはイギリスの“データ保護法”を含むEU GDPRのような立法を実施した。EUおよびイギリスGDPRは、EUまたはイギリス内の個人データの収集、使用、開示、移転、または他の処理を管理します。その他,EUとイギリスGDPRは個人データのセキュリティと国家データ保護当局へのデータ処理義務の通知に要求を加え,個人データ処理に利用可能な限られた範囲の合法的な基礎を構築し,個人データの定義を拡大し,インフォームドコンセントのやり方の変更,臨床試験被験者や調査者のためのより詳細な通知を求めている。しかも、EUとイギリスのGDPRは違反と違反に巨額の罰金を科す。例えば、EU GDPRによれば、会社は、一時的または最終的なデータ処理および他の是正行動の禁止に直面する可能性があり、最大2000万ユーロまたは世界の年収の4%までの罰金、または法的許可によってその利益を表す様々なデータ主体または消費者保護組織によって提起された個人データに関連する個人訴訟を処理することができる。
通常の業務の過程で、私たちは個人データをヨーロッパ経済区、イギリス、その他の司法管轄区域からアメリカや他の国に移すかもしれない。ヨーロッパ経済区、イギリス、その他の司法管轄区はすでに法律を制定し、データの現地化或いは個人データの他の国への移転を制限することを要求している。特に,欧州経済圏やイギリスは,米国や他のプライバシー法が不十分と考えられている国への個人データの転送に大きな制限を与えている.他の司法管轄区域はそのデータ現地化と国境を越えたデータ転送法に対して類似の厳格な解釈を行う可能性がある。現在、法律に従って個人データをヨーロッパ経済区と連合王国からアメリカ、例えばヨーロッパ経済区に移転するための様々なメカニズムがあるが、
イギリスの標準契約条項によると、これらのメカニズムは法的挑戦を受けており、これらの措置を満たしたり依存したりして個人データを合法的に米国に移転できる保証はない。
もし私たちが合法的な方法で個人データをヨーロッパ経済区、イギリスまたは他の司法管轄区域からアメリカに移すことができない場合、あるいは合法的な移転の要求が煩雑すぎる場合、私たちの業務中断または降格、巨額の費用で私たちの業務または全部の業務またはデータ処理活動を他の管轄区域に移す必要があり、より多くの規制行動に直面し、巨額の罰金と処罰、データの転送ができないこと、パートナー、サプライヤーおよび他の第三者との協力、および業務の処理または移転に必要な個人データを禁止することを含む深刻な不利な結果に直面する可能性がある。また,個人データをヨーロッパ経済区やイギリスから他の司法管轄区,特に米国に移転した会社は,規制機関,個人訴訟当事者,活動団体のより厳しい審査を受けることになる。一部の欧州規制機関は、EU GDPRの国境を越えたデータ移転制限に違反した疑いがあるため、いくつかの会社にいくつかのデータの欧州経済地域への移転を一時停止または永久停止するよう命じた。
アメリカでは、連邦と州健康情報プライバシー法、連邦と州安全違反通知法、連邦と州消費者保護法を含む、個人情報の収集、使用、開示と保護を管理する連邦と州プライバシーとデータ安全法律法規が多い。これらの進化し続ける法則のどれもが異なる解釈を受けるかもしれません例えば、1996年に“健康保険携帯性と責任法案”(HIPAA)が公布した条例に基づいて、“経済と臨床健康情報技術法”(HITECH)の改正により、保護された健康情報を構成する個人が健康情報を識別できるプライバシー、伝送、安全に対して具体的な要求が規定された。HIPAA及びその条例を実行することは財務責任と名声損害を招く可能性があり、このような法執行活動に対する反応は大量の内部資源を消費する可能性がある。
また、2018年カリフォルニア消費者プライバシー法(CCPA)は、消費者、商業代表、および従業員の個人情報に適用され、企業にプライバシー通知において具体的な開示を提供し、カリフォルニア住民が特定のプライバシー権を行使する要求を尊重することを要求する。CCPAは、違反行為ごとに最高7500ドルの民事罰金を科すことができ、あるデータ漏洩の影響を受けた個人訴訟当事者が巨額の法定損害賠償を取り戻すことを許可すると規定している。CCPAはいくつかの臨床試験で処理されたデータを免除したが、CCPAはコンプライアンスコストを増加させ、著者らが維持しているカリフォルニア住民の他の個人データに関する潜在的な責任を増加させた。
また、2020年にカリフォルニアプライバシー権法案(“CPRA”)は、個人が個人情報を訂正する新たな権利を増加させることを含むCCPAの要求を拡大し、法律を施行·施行するための新たな規制機関を設立した。バージニア州、コロラド州、ユタ州、コネチカット州などの他の州でも全面的なプライバシー法が可決され、他のいくつかの州および連邦と地方の各レベルでも類似した法律が考えられている。これらの州ではCCPAと同様に臨床試験を背景に処理されたデータも免除されているが,これらの事態はさらにコンプライアンス努力を複雑化させ,我々が依存する第三者としての法的リスクやコンプライアンスコストを増加させている。
米国および海外の多くの法律要件には、私たちまたは私たちの第三者サービスプロバイダが経験した脆弱性による可能性がある個人に特定の個人情報に関連するセキュリティホールを通知する義務があることが含まれている。例えば,米国の全50州とコロンビア特区の法律は,個人情報がデータ漏洩により漏洩した消費者に通知を企業に要求している.これらの法律は一致しておらず、広範囲のデータ漏洩が発生した場合に遵守することは困難であり、費用が高い可能性がある。また、各州は既存の法律を頻繁に改正しており、絶えず変化する監督管理要求に注目することが求められている。契約によると、私たちはまた顧客や他の取引相手にセキュリティホールがあることを通知することを要求される可能性がある。私たちが第三者サービス提供者、請負業者、またはコンサルタントから得られる任意の契約保護は、そのような責任および損失から私たちを十分に保護するのに十分ではないかもしれませんし、私たちはそのような契約保護を実行できないかもしれません。
データプライバシーとセキュリティに関する新たな提案された法律法規が引き続きあると予想されていますが、これらの将来の法律、法規、基準が私たちの業務にどのような影響を与える可能性があるのかを決定することはできません。新しい法律、既存の法律、法規、基準、その他の義務の改正または再解釈は、追加のコストを発生させ、私たちの業務運営を制限することを要求するかもしれません。健康とデータ保護に関連する法律、法規、標準とその他の義務の解釈と応用は依然として不確定であり、しかも常に互いに矛盾し、絶えず変化しているため、これらの法律の範囲と要求は私たちのやり方と一致しない方法で解釈と適用される可能性があり、私たちが変化するデータ保護規則を遵守する努力は成功しないかもしれない。もしそうであれば、これは政府に罰金や命令を科し、やり方を変更することを要求する可能性があり、これは私たちの業務に悪影響を及ぼす可能性がある
さらに、これらのプライバシー規制は、国/地域によって異なる可能性があり、テストが米国で行われるか、現地の国/地域で行われるかによって異なる可能性があり、私たちの運営または業務実践は、各国/地域でこれらの法規を遵守しない可能性がある。
これらおよび他の任意の適用可能なデータプライバシーおよびセキュリティ法律法規を遵守することは、厳格で時間のかかるプロセスであり、新しいデータ保護ルールの遵守を保証するために追加のメカニズムを確立する必要があるかもしれません。もし私たちまたは私たちの第三者サプライヤー、協力者、請負業者、およびコンサルタントがこのようないかなる法律または法規にも従わなかったとみなされなかった場合、私たちは規制調査、巨額の罰金と処罰、名声損害、または私たちの業務慣行の変更を要求される可能性があり、これらはすべて私たちの業務、財務状況、および運営結果に悪影響を及ぼす可能性があります。
新冠肺炎コロナウイルスは著者らの臨床試験を含む著者らの業務に不利な影響を与える可能性がある。
2019年12月、1種の新型コロナウイルス株の新冠肺炎が武漢で中国に出現したことが報告された。それ以来,新冠肺炎コロナウイルスは米国,ヨーロッパ,日本を含めて世界に広がっており,これらの国で計画や臨床試験が行われている。疫病発生と政府が取った対応措置も企業に直接と間接的な重大な影響を与えた。労働力不足が発生したため、サプライチェーンの中断;施設と生産の一時停止;医療サービスと用品などのある商品とサービスに対する需要が急増した。私たちは将来的に私たちの業務や臨床試験に影響を与える中断を経験する可能性があります
•患者を臨床試験に参加させるのは遅延したり困難です
•臨床サイト起動の遅延または困難は、臨床サイト調査員と臨床サイトスタッフを募集する上での困難を含む
•医療資源を臨床試験の進行から移し,われわれの臨床試験場所である病院や臨床試験を支援してくれた病院スタッフを他の場所に移すことを含む
•連邦や州政府、雇用主と他の人が押しつけたり提案したりする旅行制限のため、臨床試験場のモニタリングなどの重要な臨床試験活動を中断した
•従業員資源の制限、そうでなければ、従業員または彼らの家族の病気または従業員が大勢との接触を避けることを望むことを含む、私たちの臨床試験の実施に集中するだろう
•サプライチェーンの中断は、商業販売や臨床試験のための製品の調達に必要な原材料の調達を阻止し、より高価になる可能性がある。
米国以外の地点で行われている臨床試験,特に新冠肺炎コロナウイルスの深刻な影響を受けている国/地域では,これらのリスクに加えて,将来的に以下のような悪影響を経験する可能性がある
•私たちが計画した臨床試験を開始するために地元の監督部門の許可を得ています
•臨床試験に必要な用品や材料の受信を遅延させた
•世界的な輸送中断は臨床試験材料の輸送に影響を及ぼす可能性がある
•新冠肺炎コロナウイルス爆発への対応の一部として,現地法規の変化には臨床試験を行う方式を変更する必要がある可能性があり,予期せぬコスト,あるいは臨床試験を完全に停止する可能性がある。例えば、このような試験を行うことができない主要病院に入ることができない患者の地方評価を可能にするために、いくつかの臨床試験のスキームが修正されている
•従業員資源が限られているか、あるいは政府従業員が休暇を余儀なくされたため、現地の監督機関、道徳委員会および他の重要な機関と請負業者との必要な相互作用が遅延した
•FDAはこれらの影響を受けた地域の臨床試験データの受け入れを拒否した。
新冠肺炎コロナウイルスが著者らの業務と臨床試験に影響する可能性の程度は高度に不確定であり、例えば疾病の最終的な地理伝播、疫病発生の持続時間と社会距離法規、旅行制限、企業閉鎖或いは業務中断、及びアメリカと他の国が取った疾病の抑制と治療行動の有効性を自信に満ちて予測することができない。
業務中断は私たちの将来の収入と財務状況を深刻に損害し、私たちのコストと支出を増加させるかもしれない。
私たちの業務および私たちのサプライヤーとサプライヤーの業務は、地震、電力不足、電気通信故障、金融機関の倒産、水不足、洪水、ハリケーン、台風、火災、極端な天気条件、医療流行病、その他の自然または人為的災害または業務中断の影響を受ける可能性があり、私たちは主にこれらの状況に自己保険を提供します。このような業務中断の発生は、私たちの運営と財務状況を深刻に損害し、私たちのコストと支出を増加させる可能性がある。私たちは現在第三者サプライヤーに依存して、私たちの候補製品を生産して処理して、患者を基礎としています。これらのサプライヤーの運営が人為的または自然災害または他の業務中断の影響を受ける場合、候補製品の臨床供給を得る能力が妨害される可能性がある。
どの地域のテロ、国際敵対行動、そして不安定は私たちの業務に悪影響を及ぼす可能性がある。
テロ、戦争の勃発、または国際敵対行動の存在は、世界経済を損ない、グローバル·サプライチェーンに悪影響を与え、特定の地域に製品を販売したり、これらの地域から物資を購入する能力に悪影響を及ぼす可能性がある。特に、ウクライナの戦争と政治的動揺は私たちの財務状況、運営結果、そしてキャッシュフローに悪影響を及ぼすかもしれない。2022年2月、ロシア軍はウクライナに侵入した。進行中の軍事行動の深刻さと持続時間は非常に予測できないにもかかわらず、ウクライナでのロシアとウクライナの軍事衝突は、欧州での私たちの行動を実質的に混乱させ、および/または彼らのコストを増加させる可能性がある。さらに、ロシアは以前クリミアを併合し、最近ウクライナドネツクとルガンスク地域の2つの分離主義共和国、その後のウクライナへの軍事介入を認め、EU、アメリカ、その他の国がロシア、ベラルーシ、ドネツクとルガンスク地域の2つの分離主義共和国に制裁を科し、追加の潜在的制裁を脅威および/または提案した。ロシアの軍事侵入とそれに伴う制裁は世界経済と金融市場に悪影響を及ぼす可能性があり、それによって私たちの業務、運営、経営業績、財務状況に影響を与える可能性があり、私たちの普通株とアメリカ預託証明書の価格に影響を与える可能性がある。
私たちの財務報告の内部統制には重大な欠陥があることが発見されました。もし私たちが有効な内部制御システムを維持できなければ、将来的にあるいは他の方法でより多くの重大な欠陥が発見される可能性があり、これは私たちの総合財務諸表に重大なミスが発生したり、報告義務を履行できなくなったりする可能性があります
重大な欠陥は財務報告内部統制の欠陥または欠陥の組み合わせであり、私たちの年度または中期財務諸表の重大なミス報告は合理的な可能性があり、適時に防止または発見できないようにする。
2022年10月19日、当社取締役会監査委員会(以下、監査委員会と略す)は、経営陣との会議で関連事実と状況を審議した後、以下の財務諸表に依存しないことを決定した
•当社の2021年12月31日まで、2020年12月31日及び2019年12月31日までの年度の監査財務諸表(“影響を受けた監査財務諸表”);及び
•2022年3月31日現在の中期未監査財務諸表(“影響を受けた未監査財務諸表”)。
我々は、2021年12月31日現在のForm 20−F年度報告書の第1号改正案において、影響を受けた監査済み財務を改正し、再記載し、2023年2月17日現在のForm 6−K/A報告書で影響を受けた未監査財務を改訂し、再記載する。
再記述の結果、2021年12月31日現在、財務報告の内部統制には重大な弱点(2021年の実質的な弱点)が存在し、複雑な合意、特にヤンソン協定の制御の十分な検討と監督の欠如と関連しており、私たちの開示制御と手続きは無効であると結論した。
また、我々が2022年12月31日までの財政年度の財務諸表を監査する際には、2022年12月31日現在、財務報告の内部統制に重大な弱点(“2022年重大弱点”と2021年重大弱点、“重大弱点”)があり、これは、我々の財務報告の流れを支援するキー情報技術(IT)システムの特権と、従来のユーザアクセス·変更管理における無効情報技術汎用制御(ITGC)と関連していると結論した。したがって,関連するプロセスレベルのIT依存制御やアプリケーション制御も無効である.
大きな弱点を解決し、監査委員会の監督の下で、救済措置の実施に取り組んでいます。これらの措置のうちのいくつかは実施されており、他のいくつかは実施中であり、明らかにされた重大な弱点を解決し、我々の全体的な金融統制環境を強化することを目的としている。2021年の重大な弱点を是正するための措置は、(I)ヤンソンプロトコルを含む複雑なプロトコルに対する追加応答性審査および監視制御を実施し、首席財務官および他の上級財務者がキー会計判断および推定、報告および開示を追加的に審査することを含む、(Ii)具体的な持続的な訓練と教育を通じて、既存の財務報告者の能力を拡大し、ヤンソンプロトコルを含む複雑なプロトコルに焦点を当て、国際財務報告基準を適用し、(Iii)適切な国際財務報告会計基準を有するより多くの財務報告者を招聘することを含む。私たちはまた、この修復計画を実行するための私たちの内部資源を支援し、補完するために追加の外部資源を招いた。2022年の重大な欠陥を是正するための措置は、(I)2023年2月に初めて導入されたガバナンス、リスク、およびコンプライアンスツールを使用することによって手動プロセスを動的化すること、(Ii)この機能に従事する人員を増加させることによって、私たちのITコンプライアンス監督を強化すること、(Iii)各制御の原則および要求についてユーザアクセスを重視することを含む、ITGCおよび政策のためのより多くの訓練および認識計画を策定し、(Iv)追加的な審査を増加させることによって審査プロセスを強化すること、および(V)取締役会監査委員会に救済措置に関する最新の状況を定期的に提供することを含む、2022年の重大な欠陥を是正する措置。
我々は重大な弱点を救済しようと努力しているが,我々の適用救済計画が完全に実施され,適用された制御措置が十分に実行されており,新たな実施と強化された制御措置が有効に機能しているとテストにより結論が出るまで,重大な弱点が修復されたとは考えられない.私たちが財務報告に対する私たちの内部統制を評価し、改善し続けるにつれて、私たちはこれらの制御欠陥を解決したり、上記の救済計画を修正したりするために追加的な措置をとるかもしれない。現在、私たちはこれらの努力の成否を予測することができず、救済努力に対する私たちの評価結果を予測することもできない。私たちの努力が実質的な弱点を補う保証はなく、今後これ以上の実質的な弱点が発見されない保証はない。
上場企業として、私たちは財務報告に対して有効な内部統制を行わなければならず、私たちの経営業績と財務状況を正確かつ適時に報告することができる。米国証券法によると、2002年の“サバンズ-オキシリー法案”(以下、“サバンズ-オキシリー法案”)を含め、私たちは報告義務を履行しなければならない。サバンズ·オキシリー法第404条(A)条(“第404(A)条”)は、経営陣に財務報告書の内部統制に対する我々の有効性を毎年評価·報告し、財務報告の内部統制におけるいかなる重大な弱点も見出すことを要求する。サバンズ·オクスリ法第404条(B)条(“第404(B)条”)によると、 私たちの独立公認会計士事務所は、財務報告の内部統制に対する私たちの有効性を示す年間認証報告書の発行を要求されました。♪the the the 以下の基準のルールを管理する サバンズ·オキシリー法404条によると、私たちの経営陣は財務報告書の内部統制を評価しなければならないが、これらは複雑で、大量の文書、テスト、および可能な救済措置が必要だ。これらの厳しい基準は、私たちの監査委員会が提案され、財務報告の内部統制の審査を定期的に更新することを要求する。 重大な弱点が発見された場合、財務諸表のミスを招き、さらに私たちの財務報告のミスや財務報告の遅延を招く可能性があり、これは、私たちの経営業績を再陳述したり、監査人が保留された監査報告を出す必要があるかもしれません。効率的な開示制御と手続きおよび財務報告の内部統制を維持するためには、大量の資源を費やし、重要な管理監督を提供しなければならない。 私たちが適切な内部統制を効果的に維持することは保証されない。
財務報告を効果的に内部統制していると結論できない場合、あるいは私たちの独立監査人が第404(B)条の要求に基づいて財務報告の内部統制の有効性について保留のない報告を提供することを望まないか、または私たちの経営結果に自信を失う可能性があり、私たちのアメリカ預託証明書価格が下落する可能性があり、私たちは訴訟や規制執行行動の影響を受ける可能性がある。さらに、私たちが404条の要求を満たすことができなければ、私たちはナスダック株式市場有限責任会社(“ナスダック”)に上場し続けることができないかもしれない。
私たちは私たちの現金と現金等価物を使用する上で広範な自由裁量権を持っていて、あなたが同意しない方法で投資したり、これらの現金と現金等価物を使用したりすることができます。
私たちの経営陣は、私たちの現金と現金等価物を運用する上で広範な自由裁量権を持っており、私たちの運営業績を改善したり、私たちのアメリカ預託証明書の価値を高めたりすることなく、このような現金と現金等価物を使用することができます。私たちの経営陣がこれらの金額を有効に運用できなければ、財務損失を招く可能性があります
私たちの業務は、私たちのADS価格を低下させ、候補製品と臨床前計画の開発を延期します。私たちの現金と現金等価物を使用する前に、私たちは収入や価値を失わない方法で投資するかもしれない。
私たちの第三者への依存に関するリスク
私たちは既存のパートナーJanssenと他の第三者に依存しており、将来のパートナーに依存して、私たちの候補製品の研究、開発、製造、マーケティングに取り組んでいるかもしれません。
私たちはCilta-celの開発と商業化の面でJanssenと重要な協力を持っている。
私たちは私たちの他の候補製品や開発中の技術のために追加的な協力をするかもしれない。私たちの既存または未来の協力者が私たちの製品の研究、臨床前と臨床開発、製造、またはマーケティングに取り組む資源の時間または数を制御することはできません。私たちの協力者たちは私たちの期待や品質基準に基づいて彼らの義務を履行しないかもしれない。私たちの協力者は、重大な違約または予見できない重大なセキュリティ事件を含む、様々な理由で私たちの既存の合意を終了するかもしれない。Janssenプロトコルが終了すれば、CARVYKTIとCilta-celのさらなる開発の商業化過程で重大な遅延や他の損失に遭遇し、プロトコルによって将来生じることが予想される任意の収入の機会を失い、予測不可能なコストが発生し、私たちの製品、候補製品、および会社全体の名声に損害を与える可能性があります。
市場承認を得るために必要な申請の提出と支援に必要な経験は限られており、この過程で第三者契約研究機関(CRO)に依存する可能性がある。また、私たちの将来のいくつかの候補製品の発売と市場浸透を最適化するために、製薬業界のトップと流通やマーケティング協定を締結する可能性があります。これらの将来パートナーになる可能性のある候補製品については、一旦私たちの製品がマーケティング許可を得たら、私たちは単独で私たちの製品を販売しません。これらの契約を結ぶことに固有のリスクは以下のとおりである
•これらの合意の交渉および実行は長い過程であり、合意の署名を招くことはないかもしれないし、関連する候補製品の開発や商業化を遅らせる可能性がある
•これらの合意は私たちの協力者によってキャンセルされたり更新されないかもしれないし、私たちの協力者は完全に守られないかもしれない
•私たちが許可を与えた場合、私たちは許可候補製品の開発の制御を失った
•この場合、私たちは、私たちのパートナーが製品の商業化のために分配する手段と資源を制限することしかできない
•協力者は、私たちの知的財産権または固有の権利を正確に取得、維持、強制、または保護することができないかもしれないし、または私たちの固有の情報を使用して訴訟を招き、それによって、私たちの固有の情報を危険にさらしたり、潜在的な訴訟に直面させたりする可能性がある。
また、JanssenはCilta-celの開発と商業化に努力することを求められているが、Janssenは、Cilta-celが発売承認された条件と同じまたは類似した条件を治療する可能性のある製品、または潜在的な将来の市場承認のための研究を行っている製品を含む、そのポートフォリオにおける他の製品をCilta-celよりも優先することを求める可能性がある。
さらに、私たちは、製品開発、マーケティング、規制承認、商業化努力などに関連する、私たちの協力者が私たちに生成または報告したデータや他の情報に依存します。パートナーが提供する情報は信頼できると信じていますが、このようなすべてのデータや情報の正確性または完全性を独立して審査または検証することはできません。どんな不正確な点も私たちの業務に悪影響を及ぼす可能性があります。
これらのリスクのいずれかが現実になった場合、または適切なパートナーが見つからなければ、これは私たちの業務、見通し、財務状況、および運営結果に実質的な悪影響を及ぼす可能性がある。
ヤンソン協定によって生成された収入はすでに予測可能な未来に私たちの収入の大きな部分に貢献すると予想されている。
私たちはシリングの開発に関するヤンソン協定を締結した。2018年、楊森から350.0ドルの前金を受け取り、本年度報告の日までに、300.0ドルのマイルストーン支払いを受け取りました。Janssenは計画通りにその義務を履行しないかもしれないし、“Janssen協定”の下での約束の履行を拒否する可能性がある。Janssenの不履行、Janssen協定の早期終了、または私たちは新しいパートナーや代替パートナーを見つけることができず、したがって、私たちの収入、研究開発活動、資金に悪影響を及ぼす可能性があります。これらのリスクのいずれかが現実になれば、これは私たちの業務、見通し、財務状況、経営業績に悪影響を及ぼすだろう。
もし私たちやヤンソンが私たちの予想された時間枠内で私たちの製品開発や商業化目標を達成しなければ、マイルストーンや特許使用料の支払いを受けることができないかもしれません。計画通りに運営できないかもしれません。
私たちはすでに受け取り、ヤンソン協定のいくつかの事前に指定されたマイルストーンを満たした時、私たちは引き続きヤンソンの支払いを受けると予想しています。私たちは現在、私たちの運営に資金を提供するために、Janssenのこのような記念碑的な支払いに大きく依存している。私たちは新しい協力協定を締結するかもしれないし、その中でマイルストーン支払いも規定されている。ヤンソン協定における記念碑的支払いは、通常、様々な臨床、監督、販売、その他の製品開発目標の実現状況に依存する。その中の多くのマイルストーンの成功やタイムリーな達成は私たちがコントロールできるものではなく、一部の理由はこのような活動のいくつかが行われているか、またはJanssenによって行われるからだ。もし私たちやJanssenが適用されたマイルストーンを達成できなかったら、私たちはこのようなマイルストーンの支払いを受けないだろう。このようなマイルストーンの支払いを受けられなかったら、私たちにつながるかもしれません
•いくつかの研究開発プロジェクトを延期、減少、または終了するか、または私たちの長期的な最適な利益に合わない可能性のある短期支出を減らす方法
•追加の株式または転換可能な債券融資で資金を調達することは、私たちの株主を希釈する可能性がある
•協力協定を通じて資金を得ることで、これらの協定は私たちが本来保持する技術または製品に権利を譲渡することを要求するかもしれない
•私たちが異なる状況で得た合意に及ばないかもしれない新しい協力または許可協定に署名すること;および
•戦略的取引や第三者との合弁企業の設立を考慮する。
また、ヤンソン協定によって支払われる任意の潜在的な特許権使用料は、私たちの候補製品の開発成功と商業化にかかっています。しかも、私たちとJanssenは時々Janssen合意の下で特定のマイルストーンを稼いだかどうかについて合意するかもしれない。ヤンソン協定と適用法は、いずれか一方がその義務を履行できなかったことに救済措置を提供しているにもかかわらず、私たちが獲得する権利があると考えられるマイルストーンを得る保証はありません。ヤンソンとのいかなる関連紛争も、ヤンソン合意の終了や他の方法でヤンソンとの協力を損なう可能性があります。
私たちはマイルストーンや特許使用料の支払いを受けることができず、上記のいずれの事件の発生も、私たちの業務、見通し、財務状況、および運営結果に重大な悪影響を及ぼす可能性があります。
Genscriptに依存していくつかのサービスを提供しています。
“第7項-大株主および関連側取引-いくつかの関係および関連側取引-Genscriptとの取引”で述べたプロトコルによると、Genscriptが提供する限られた数のサービスに依存する。私たちはこれらの合意に基づいて私たちにサービスを提供する人員と支援者が私たちの業務を管理して管理することを彼らの第一の責任として、あるいは私たちのためだけに行動することを望んでいない。また,Genscriptは,Genscriptが我々に提供するサービスに同意するのではなく,自分のニーズを優先する可能性があり,あるいは我々の利益ではなく,Genscriptの利益を優先する可能性がある.したがって、この人たちは彼らのすべての時間と資源を私たちに割り当てないだろう。
Genscriptは、彼らが提供してくれたサービスを効率的に管理できず、当社の業務、財務状況、運営結果を損なう可能性があります。
また,Genscriptから内部に移行してこれらのサービスを実行しており,この過程を継続する予定である.もし私たちがこのようなサービスの責任を負う時に十分な財政資源や人員と制度がなければ、私たちは効果的または効率的に成功しないかもしれない
Genscriptからこれらのサービスを移行することは、私たちの業務を混乱させ、当社の財務状況や運営結果に実質的な悪影響を及ぼす可能性があります。これらのサービスの移行に成功したとしても,我々が過渡期にGenscriptから取得したサービスよりも高価または効率が悪い可能性がある.
私たちは将来的に第三者と私たちの候補製品の開発と商業化について協力する可能性があり、これは私たちの創造能力に悪影響を及ぼす可能性があります。
私たちは、第三者と私たちの候補製品の開発と潜在的な商業化についてより多くの協力やパートナーシップを行うことを求めている可能性があります。もし私たちが第三者と予想される開発計画について協力することを求めれば、適切なパートナーを見つけることができない、あるいは商業的に合理的な条項や全く合意できないかもしれない。私たちがJanssenと合意したCilta-celの開発と商業化に関する手配など、私たちの候補製品の開発と商業化のためのパートナーを見つけることに成功しても、私たちのパートナーは私たちの候補製品の開発と商業化のために特化することができる時間と資源の制御は限られているかもしれない。これらのパートナーシップはいくつかのリスクを構成しています
•予算制限、人的資源の不足、戦略的重点の変更などの内部制限のため、パートナーには十分な資源がないか、必要な資源を投入しないことが決定される可能性がある
•パートナーは、私たちの知的財産権が無効または実行不可能、または候補製品が他人の知的財産権を侵害していると考えるかもしれない
•パートナーは、関連費用の支払いまたは任意の収入の分配を含む、適用される協力に基づいて開発および商業化活動を展開する責任に異議を唱えることができる
•パートナーは、協力スケジュール以外に開発された競争力のある製品を追求することを決定することができる
•パートナーは必要な規制承認を得ることができないか、または必要な規制承認を得ることができないかもしれない
•パートナーは、他の候補製品の開発または商業化を支援するために、候補製品の開発または商業化を延期する可能性がある。
したがって、パートナーシップ協定は、最も効果的な方法で、または候補製品の開発、規制承認、または商業化に成功しない可能性がある。いくつかの共同協定は短時間で無断で終了することができる。一度パートナー協定に署名すると、規制部門が候補製品を承認して商業化することはないかもしれない。私たちはパートナーを探すことでも競争に直面している。協力者の目標を達成し、私たちの期待を満たすために新たな協力を得ることができなければ、私たちの候補製品を進めることができないかもしれませんし、意味のある収入が生じないかもしれません。
我々は依存し,引き続き独立した調査者や他の第三者に依存して我々の候補製品の臨床前および臨床試験を行う予定であるが,これらの第三者の表現は,締め切り前にこのような試験を完了できなかったり,適用された法規要件を遵守できなかったりすることを含めて満足できない可能性がある。
私たちは大学、医療機関、戦略パートナーのような独立した研究者と協力者に依存し続け、私たちの臨床前と臨床試験を行う。このような第三者とのプロトコルは、第三者が履行できなかったことを含む様々な理由で終了する可能性がある。もし私たちが代替計画を達成する必要があれば、私たちの製品開発活動は延期されるだろう。
私たちのこれらの第三者の研究開発活動への依存は、これらの活動に対する私たちの統制を減少させるだろうが、私たちの責任を軽減することはない。例えば,我々のすべての臨床試験が試験の全体的な調査計画や案に沿って行われることを確保していきたい。さらに、FDAは、データと報告の結果が信頼性と正確であることを保証し、試験参加者の権利、完全性とセキュリティを保護するために、臨床前と臨床試験結果を行う、記録と報告する規制基準を遵守することを要求し、一般に良好な実験室やり方と良好な臨床やり方と呼ばれる。同様の規制要件は、国際人用医薬品登録技術要求調整理事会(“ICH”)を含む米国以外の地域にも適用される。また,指定された時間範囲でいくつかの行われている臨床試験を登録し,いくつかの完了した臨床試験の結果を政府後援のデータベースに発表することも求められている。もし私たちまたは第三者がそうしなければ、FDAまたは他の規制機関が臨床データに基づく申請、法執行行動、不良宣伝、および民事と刑事制裁の承認を拒否する可能性がある。
さらに、これらの第三者は、他のエンティティと関係がある可能性もあり、その中のいくつかは私たちの競争相手である可能性がある。これらの第三者が規制要件や私たちが規定した規程に従って契約責任を成功的に履行し、予想される期限内に私たちの臨床試験を完了または行うことができない場合、私たちは候補製品のマーケティング承認を得ることができないか、遅延する可能性があり、候補製品の商業化に成功する努力を遅らせることができないか、または遅延する可能性がある。
さらに、私たちの臨床試験の首席研究者は時々私たちの科学顧問や顧問を担当し、このようなサービスのために現金または株式補償を得ることができるかもしれない。これらの関係と任意の関連賠償が知覚または実際の利益の衝突をもたらす場合、またはFDAまたは他の規制機関が、財務関係が試験の解釈に影響を及ぼす可能性があると結論した場合、適用される臨床試験場所で生成されたデータの完全性が問われる可能性があり、臨床試験自体の効用が脅かされる可能性があり、これはFDAまたは他の規制機関の遅延または拒否をもたらす可能性がある。そのような遅延または拒否のいずれも、臨床段階の候補製品または任意の未来の候補製品を商業化することを阻止することができる。
細胞ベースの治療は、試薬、専門設備、および他の特殊な材料の利用可能性に依存し、これらは、私たちが受け入れられない条件または全く得られない可能性がある。これらの試薬、設備、および材料について、私たちは独占的なサプライヤーまたは限られた数量のサプライヤーに依存しているか、または依存する可能性があり、これは私たちが製品を製造して供給する能力を弱めるかもしれない。
私たちの候補製品を製造するためには、私たちの製造過程で化学反応または生物学的反応を引き起こすための物質、および他の特殊な材料および装置が必要となり、その中のいくつかは、商業生物製品の生産を支援するために、資源および経験の限られた小さな会社によって製造または供給される。私たちは現在、私たちの候補製品製造で使用されるいくつかの材料と設備の施設と供給を使用するために限られた数量のサプライヤーに依存している。たとえば,我々は現在,外部CMOの施設や設備および連携内部の補給源を用いて病媒供給を行っている。我々はCMOを用いて生産遅延や供給不足のリスクを増加させ,我々の製造技術をこれらのCMOに譲渡し,彼らは我々の供給需要の面で経験を蓄積したからである。また、私たちは、調達注文に基づいて、hemacare、Miltenyi、白血球分離収集センター、および他のサプライヤーから、私たちの候補製品を生産するために重要な設備および試薬を購入した。私たちのいくつかのサプライヤーは、生物製薬会社がcGMPで生産した商業製品を支援する能力がないかもしれないし、私たちの需要をサポートするのに十分な設備がないかもしれない。私たちもこれらのサプライヤーの多くと供給契約を締結していません。受け入れ可能な条件や供給契約をまったく得られないかもしれません。したがって、私たちは臨床的または商業的製造を支援する重要な材料と設備を得ることができないかもしれない。
これらの試薬、装置、および材料のいくつかについては、私たちは依存しており、将来的には独占的なソースの供給者または限られた数の供給者に依存する可能性がある。これらのサプライヤーのいずれかから製品を調達し続けることができないのは、サプライヤーの規制行動または要求、サプライヤーが経験した不利な財務または他の戦略的発展、労使紛争または不足、意外な需要または品質の問題に影響を与える可能性があり、候補製品の需要を満たす能力に悪影響を及ぼす可能性があり、これは、私たちの製品販売および運営結果、または私たちの臨床試験を行う能力に悪影響および実質的な影響を与える可能性があり、いずれも私たちの業務を深刻に損なう可能性がある。
私たちの製造プロセスの発展と拡大に伴い、私たちはこのプロセスの一部として使用されるいくつかの材料と設備の権利と供給を得る必要があるかもしれない。私たちは商業的に合理的な条項でそのような材料の権利を得ることができないかもしれないし、これらの材料の権利を得ることができないかもしれません。もし私たちがそのような材料を使用したり、適切な代替品を見つけることを避けるために商業的に可能な方法で私たちのプロセスを変えることができなければ、これは私たちの業務に大きな悪影響を与えます。
我々の候補製品の規制承認とその他の法的適合性問題に関するリスク
たとえ著者らが必要な臨床前研究と臨床試験を完成しても、監督管理の審査過程は高価で、時間と不確定であり、私たちが一部或いはすべての候補製品の商業化の許可を得ることを阻止するかもしれない。そのため、いつ、どの地域にあるか、どの地域でも、どの候補製品を商業化するかのマーケティング承認を得ることができません。
私たちの候補製品およびその開発と商業化に関連する活動は、それらの設計、研究、テスト、製造、安全、効果、品質管理、記録保存、ラベル、包装、貯蔵、承認、広告、販売促進、販売、流通、輸入、輸出、および安全および他の発売後の情報の報告を含み、FDA、NMPA、EMA、PMDAおよび他の司法管轄区(EUを含む)の他の同様の規制機関を含む全面的な規制を受けている。上場許可を得られなかった
候補製品は私たちが候補製品を商業化することを阻止するだろう。市場承認を得るために必要な申請を提出して支援する上での経験は限られており、この過程で第三者CROに依存して助けてくれる可能性があります。上場承認を得るためには、広範な臨床前と臨床データ及び各治療適応の支持情報を監督機関に提出し、候補製品の安全性と有効性を確定する必要がある。上場承認を得るためには,製品製造過程に関する情報を規制機関に提出し,規制機関が製造施設を検査する必要がある。私たちの候補製品は効果がないかもしれないし、中程度の効果しかないかもしれないし、あるいは不良または意外な副作用、毒性、または他の特徴があることが証明される可能性があります。これらは私たちの上場承認を阻止するか、または商業用途を阻止または制限するかもしれません。また,上場承認では,製品のラベル付きがその承認の用途を制限する可能性があり,その製品の販売を制限する可能性がある.
米国でも海外でも、上場承認を得る過程は高価であり、承認されれば何年もかかる可能性があり、関連する候補製品のタイプ、複雑さ、新規性を含む様々な要因によって大きく異なる可能性がある。上場承認を得るためには、広範な臨床前と臨床データ及び各治療適応の支持情報を監督機関に提出し、候補製品の安全性と有効性を確定する必要がある。上場承認を得るためには,製品製造過程に関する情報を規制機関に提出し,規制機関が製造施設を検査する必要がある。FDA、NMPA、EMA、PMDAまたは他の規制機関は、私たちの候補製品が安全で有効ではなく、中だけ有効であるか、あるいは不良或いは意外な副作用、毒性或いは他の特徴を有しており、上場承認を得ることができないか、或いは商業使用を阻止又は制限することができないと判断する可能性がある。私たちが最終的に候補製品のために獲得したいかなるマーケティング承認も制限される可能性があり、あるいは制限されたまたは承認された後の約束は、承認された製品が商業的に実行できないようにする可能性がある。
さらに、開発中の市場承認政策の変更、追加法規または法規の変更、または各提出製品申請の規制審査の変更は、申請の承認または拒否の遅延を招く可能性がある。監督管理機関は審査過程中にかなりの自由裁量権を持っており、いかなる申請を受け入れることを拒否することができ、著者らのデータが承認を得るのに十分ではなく、追加の臨床前、臨床或いはその他の研究を行う必要があることを決定することもできる。そのほか、臨床前と臨床試験から得られたデータの異なる解釈は候補製品の上場承認を延期、制限或いは阻止する可能性がある。私たちが最終的に得たどのマーケティング承認も限られているかもしれないし、制限されたり、承認された後の約束は、承認された製品が商業的に実行できないようにすることができる。私たちが最終的に得たどのマーケティング承認も限られているかもしれないし、制限されたり、承認された後の約束は、承認された製品が商業的に実行できないようにすることができる。
もし私たちが承認を得る上で遅延に遭遇した場合、あるいは私たちの候補製品の承認を得られなかったら、私たちの候補製品のビジネスの見通しが損なわれる可能性があり、私たちの収入を作る能力も損なわれるだろう。
EU、日本、中国、その他の国際司法管轄区域で私たちの製品をマーケティングし、販売するためには、単独のマーケティング許可を得て、多くの異なる監督管理要求を守らなければならない。承認手続きは国によって異なり、追加的なテストが含まれるかもしれない。他の場所で承認を得るのに要する時間は、FDAから承認を得るのに要する時間とは大きく異なる可能性がある。米国以外の規制承認過程には、通常、FDA承認の取得に関するすべてのリスクが含まれる。また、米国以外の多くの国では、製品がその国での販売を許可される前に、精算承認を受けなければならないことが求められている。もしあれば、私たちはアメリカ以外の規制機関から直ちに承認されないかもしれない。FDAの承認は、他国又は管轄区域の規制機関の承認を確保するものではなく、米国以外の1つの規制機関の承認も、他の国又は司法管区の規制機関又はFDAの承認を確保することができない。しかし、一つの管轄区域で承認を得ることができなかったことは、他の場所で承認を得る能力に影響を与える可能性がある。私たちはマーケティング承認を申請できないかもしれないし、どの市場でも私たちの製品を商業化するために必要な承認を得ることができないかもしれない。
一つの管轄区域で私たちの候補製品に対する規制承認を獲得し、維持することは、私たちが他の管轄区域で私たちの候補製品の規制承認を得ることに成功するという意味ではない。
1つの管轄区域で私たちの候補製品に対する監督管理承認を獲得し、維持することは、他の任意の管轄区で規制承認を得ることができるか、または維持できる保証はありませんが、1つの管轄区で規制承認を得ることができなかったり、遅延したりすることは、他の管轄区の監督管理承認の流れに悪影響を及ぼす可能性があります。例えば、FDAが候補製品の発売を承認しても、他の司法管轄区の比較可能な規制機関は、候補製品のこれらの国での製造、マーケティング、普及を承認しなければならない。審査手続きは管轄区域によって異なり、異なる要求と行政審査期限に及ぶ可能性があります
1つの司法管轄区で行われる臨床研究は他の管轄区の監督機関に受け入れられない可能性があるため、米国で行われている臨床研究は、追加の臨床前研究または臨床試験を含み、他の司法管轄区の監督当局に受け入れられない可能性がある。アメリカ以外の多くの管轄区域では、製品は定価及び/又は精算承認を受けなければならず、これらの司法管轄区で販売することができる。
米国国外の監督管理の承認を得て、米国国外の監督管理要求を遵守することは、私たちに重大な遅延、困難、コストをもたらす可能性があり、私たちの製品がある国/地域で発売されることを延期または阻止する可能性がある。もし私たちが国際市場の規制要求を遵守できず、および/または適用されたマーケティング承認を得られなければ、私たちの目標市場は減少し、私たちの候補製品の市場潜在力を十分に発揮する能力は損なわれるだろう。
私たちが私たちの候補製品のためにマーケティング承認を得たとしても、私たちの製品に対する承認条項と持続的な規制は、私たちの製品の生産とマーケティングの方法を制限するかもしれません。これらの要求を遵守することは、大量の資源に関連する可能性があり、これは、私たちの収入を創出する能力を深刻に弱めるかもしれません。
候補製品の上場承認を得ても、承認された製品およびその製造業者および営業業者は、製造プロセス、ラベル、包装、流通、有害事象報告、貯蔵、広告、販売促進、サンプリングおよび記録保存を含む持続的な審査および広範な法規要件を受け入れなければならず、REMS計画(FDAがCARVYKTIを承認するための要件である)または同様の外国計画または高価な上場後研究または臨床試験および監督を行って製品の安全性または有効性を監視する潜在的な要件を含む。私たちはまた広告と販売促進に関する要求を守らなければなりません。私たちのすべての候補製品のために、私たちは市場の承認を得ました。処方薬に関する販売促進情報は様々な法律や法規によって制限されており,製品が承認されたラベル中の情報と一致しなければならない。したがって、私たちが開発した未承認の適応や用途のための製品を広めることはできません。さらに、承認された製品の製造業者およびその工場は、品質制御プログラムおよび製造手順がcGMPおよび他の同様の法規および標準に適合することを保証することを含むFDA、NMPA、欧州委員会、PMDAおよび他の規制機関の広範な規制要件を遵守しなければならず、その中には、品質管理および品質保証に関連する要求、および対応する記録および文書保守および報告要件が含まれている。私たちまたは私たちのサプライヤーは、cGMPのコンプライアンスを監視し、確保するために、FDA、NMPA、欧州委員会、PMDAまたは他の規制機関の定期的な抜き打ち検査を受ける可能性がある。
したがって、私たちと私たちのサプライヤーは製造、生産、製品監視、品質管理を含むすべてのコンプライアンス分野に時間、お金、エネルギーを投入し続けます。承認後の規制要件を遵守できなければ、規制機関によって当社製品のマーケティング承認を撤回される可能性があり、将来の製品をマーケティングする能力が制限される可能性があり、利益を達成したり維持したりする能力に悪影響を及ぼす可能性があります。
そのため、承認後の法規を遵守するコストは、私たちの経営業績や財務状況に悪影響を及ぼす可能性があります。
私たちが規制の承認を受けた任意の候補製品は、発売後に市場から制限されたり、リコールされたり、市場から撤退したりする可能性があり、もし私たちが規制要求を守っていない場合、あるいは私たちの候補製品が予期せぬ問題に遭遇した場合、その中のどの製品も承認された場合、処罰を受ける可能性がある。
FDAおよび他の連邦および州機関は、米国司法省(DoJ)と米国以外の同等の規制機関を含み、処方薬に対するすべての要求の遵守を厳格に規制し、承認されたラベルの規定による製品の販売および普及の要求、cGMP要求に応じた製品の生産要求を含む製品マーケティングおよび販売促進に関する要求を含む。FDA、米国司法省、米国以外の同等の規制機関は、私たちの製品承認の適応に基づいて私たちの製品を販売しない場合、または私たちの他のマーケティング声明が虚偽または誤解性と考えられていれば、法執行行動の影響を受ける可能性がある、ラベル外使用に関するメーカーの通信を厳格に制限しています。これらの要件に違反することは、米国連邦食品、薬物および化粧品法案(“食品、薬物および化粧品法案”)および他の法規、米国連邦虚偽声明法案(“虚偽声明法案”)および他の連邦、州または外国医療保健詐欺および乱用法律、ならびに州または外国消費者保護法を含む他の法規に違反すると告発される可能性がある。
私たちはすべての法規要件を遵守することができず、その後、私たちの製品または任意の未来の製品、製造業者または製造プロセスには、以前に未知の不良事件または他の問題が存在することが発見され、様々な結果が生じるかもしれません
•患者が私たちの製品や未来の製品を服用する訴訟と関連しています
•このような製品、製造業者、または製造プロセスの制限;
•このような製品のラベルやマーケティングの制限;
•製品の流通や使用の制限;
•発売後の研究や臨床試験が求められている
•警告状や見出しのない手紙
•この製品を市場から撤退させ
•私たちが提出した保留申請または承認された申請を承認する補充申請を拒否する;
•このような製品をリコールし
•罰金、利益または収入の返還、
•上場承認の一時停止、変更、または撤回;
•進行中の臨床試験を一時停止します
•潜在的な協力者との関係を破壊し
•不利なニュース記事と私たちの名声への損害
•これらの製品の輸出入を許可することを拒否した
•製品を検収する
•民事または刑事処罰を禁令または適用する。
もし私たちまたは任意の未来のパートナーが安全モニタリングや薬物警戒に関する法規的要求、および小児科人のための製品の開発に関する要求を守らなければ、重大な経済的処罰を招く可能性もある。同様に、個人情報の保護に関する規制要件を遵守しないこともまた、重大な処罰と制裁を招く可能性がある。
このような事件が発生した場合、私たちがこのような製品を販売する能力が損なわれる可能性があり、規制要求を遵守するために多くの追加費用が発生する可能性があり、これは私たちの業務、財務状況、および運営結果に悪影響を及ぼす可能性がある。
私たちの従業員、独立請負業者、主要な調査者、コンサルタント、ビジネスパートナー、サプライヤーは、規制基準と要件を遵守しないことを含む、不当な行為またはその他の不適切な活動に従事する可能性があります。
私たちは従業員詐欺や他の不適切な行為、または適用された規制要件を遵守できない危険に直面している。従業員および独立請負業者(例えば、主要な調査者、コンサルタント、商業パートナー、およびサプライヤー)の不正行為は、FDA、NMPA、EMA、PMDAおよび他の同様の規制機関の規定を遵守できなかったこと、これらの規制機関に正確な情報を提供できなかったこと、私たちが確立した製造基準を遵守できなかったこと、医療詐欺および乱用法律を遵守できなかったこと、財務情報またはデータを正確に報告できなかったこと、または許可されていない活動を開示することができなかったことを含む可能性がある。特に、医療業界の販売、マーケティング、その他の商業配置は、詐欺、不正行為、リベート、自己取引、その他の乱用行為を防止するための広範な法律法規によって制約されている。これらの法律法規は、研究、製造、流通、定価、割引、マーケティングおよび販売手数料、販売手数料、顧客インセンティブ計画、および他の商業計画を含むが、これらに限定されない広範な商業活動を制限または禁止することができる。従業員および独立請負業者の不正行為はまた、臨床試験の過程で得られた情報を含むが、これらに限定されない個人識別情報の不適切な使用に関連する可能性があり、これは、規制、民事、行政、および刑事制裁を招き、私たちの名声を深刻に損なう可能性がある。
また、連邦調達法は政府契約に関連する不当行為に実質的な罰を加え、ある請負業者に商業道徳と行為準則を維持することを要求した。従業員および独立請負業者の不正行為を常に識別し、阻止することができるわけではなく、不適切な活動を発見し、防止するための任意の予防措置は、未知または未管理のリスクまたは損失を効果的に制御することができないか、またはそのような法律を遵守できないことによる政府の調査または他の行動または訴訟から私たちを保護することができない可能性がある。私たちにこのような訴訟を提起すれば、これらの訴訟は、重大な民事、刑事および行政処罰、損害賠償、金銭的罰金、利益の返還、監禁、Medicare、Medicaidおよび他の連邦医療計画または他の政府の支援に関与する他の司法管轄区域の医療保険の外から除外される可能性があり、契約損害、名声損害、利益減少および将来の収益減少、法律違反に関する疑惑を解決し、私たちの業務を削減または再編することを含む、当社の信頼協定または他の合意の制約を受ける場合、これらは私たちの運営能力に悪影響を及ぼす可能性があります。
我々の業務運営および米国および他の地域の医療専門家、首席調査者、コンサルタント、顧客および第三者支払者との現在および将来の関係は、直接的または間接的に適用される可能性のあるリベート、詐欺および乱用、虚偽クレーム、医師支払い透明性、健康情報プライバシーおよび安全、および他の医療保健法律および法規の制約を受ける可能性があり、これは私たちを重大な処罰に直面させるかもしれない。
米国や他の地域の医療提供者、医師、第三者支払者は、市場で承認された任意の候補製品を推薦し、処方する上で主な役割を果たすだろう。私たちは現在と未来の医療専門家、主要な調査者、コンサルタント、顧客と第三者支払人の手配は私たちに広範に適用される医療保健法律に直面させるかもしれません。アメリカ連邦反リベート法規を含むが、これらに限定されません (“反リベート規制”)、米国連邦虚偽請求法案、および同様の外国法規は、私たちが販売、マーケティング、および流通、マーケティングの承認を得た任意の候補製品の業務または財務的配置および関係を制限する可能性があります。また、私たちは、アメリカ連邦政府および私たちが業務を展開している州と外国司法管轄区の医師の支払い透明性法律とプライバシーと安全法規の制約を受ける可能性があります。私たちの運営能力に影響を与える可能性のある連邦、州、外国医療保健法は
•リベート条例は、他の事項に加えて、個人の推薦または購入、レンタル、注文または推薦、任意の商品、施設、物品またはサービスを誘導または奨励するために、現金または実物の形態で現金または実物の形態で報酬を請求、提供、受け入れ、または提供することを禁止し、任意の商品、施設、物品またはサービスを注文または推薦することができ、これらの物品、施設、物品またはサービスは、連邦および州医療保健計画(例えば、連邦医療保険および医療補助)に従って全部または部分的に支払うことができる。“報酬”という言葉は価値のあるものを含むと広く解釈されている。この法規は,一方が薬品メーカーである一方で,処方者,購入者,処方管理人の間の手配に適用されると解釈されている。いくつかの法定例外と規制避風港は、起訴や他の規制制裁からいくつかの一般的な活動を保護するが、例外と避風港の範囲は狭く、処方、購入または推薦の報酬を誘導することを目的としていると告発されたやり方が例外または避風港の資格に適合していなければ、審査される可能性がある。特定の適用された法定例外や安全港を規制するすべての要求を満たしていないことは、このような行為自体が“反リベート条例”に規定された不法行為であることを意味するわけではない。代わりに、そのすべての事実と状況の累積審査に基づいて、この手配の合法性を逐案的に評価する。いくつかの裁判所は、報酬の手配に関連する任意の目的が連邦医療カバーの業務への移行を誘導することである場合、反リベート法規に違反すると、法規の意図要件を解釈した
•米国連邦民事および刑事虚偽申告法は、民事通報者または法定訴訟によって強制的に執行可能な“虚偽申告法”および民事通貨罰法を含み、他の事項に加えて、個人または実体を懲罰し、他のほかに、個人または実体を故意に連邦政府に提出または提出させることを処罰し、連邦医療保険および医療補助計画、虚偽または詐欺的な支払いまたは承認クレームを含む、または政府への金銭または財産の支払いまたは移転の義務を履行するために、故意に作成、使用、または虚偽記録または使用をもたらし、または故意に隠蔽またはインフォームドコンセントを適切に回避するために虚偽記録または声明を作成または使用する。連邦政府にお金や財産を支払うか移転する義務を減らす。これらの法律によると、製薬および他の医療保険会社は、価格設定サービス機関に報告された薬品価格を上昇させる疑いがある責任があると判断され、これらの価格設定サービス機関は、逆に連邦医療保険および医療補助販売率を設定するために使用され、顧客に無料製品を提供し、顧客が連邦医療保険計画に課金することが予想される。また、いくつかのマーケティング実践は、ラベル外販売促進を含むことも可能です
虚偽申告法に違反する。また,虚偽請求法によると,製薬業者が政府支払人に直接クレームを提出しなくても,虚偽や詐欺的クレームの提出に“つながる”と考えられていれば責任が問われる可能性がある。連邦政府に虚偽、架空、詐欺的なクレームを出したり、刑事訴訟を起こしたりする可能性もある
•HIPAAは、任意の医療福祉計画をだまし取ろうとする計画またはトリックを知りながら故意に実行または実行しようとする連邦刑法を禁止し、虚偽または詐欺的な口実で、任意の医療福祉計画が所有または保管または制御する任意の金銭または財産を取得し、故意に流用、窃盗または他の方法で合法的な所有者以外の誰に不正に使用するか、または医療福祉計画の任意のお金、資金、証券、保険料、信用、財産または他の資産を故意に乱用し、故意に阻止、阻害、ミスリード、または防止、阻害、ミスリード、遅延または防止しようと試みた、または防止、阻害、ミスリード、遅延または防止しようと試みた。刑事調査員および医療福祉計画に関連する任意の事項への連邦医療犯罪違反に関連する情報または記録の伝達を意図的または遅延させ、故意に、任意のトリック、計画または装置によって重要な事実を偽造、隠蔽または隠蔽するか、または任意の重大な虚偽、架空または詐欺的な陳述または陳述を行うか、または任意の重大な虚偽、架空または詐欺的な陳述または記録を含むことを知っている任意の重大な虚偽または書面を作成または使用することは、医療福祉、プロジェクトまたはサービスの提供または支払いに関連する;
•HITECHによって改正されたHIPAAおよびそのそれぞれの実施条例は、カバーエンティティまたはカバーエンティティのために、個別に識別可能な健康情報を作成、受信、維持、または送信することを表すいくつかのヘルスケア提供者、健康計画および医療情報交換所、およびそれらのそれぞれの“ビジネスパートナー”、ならびに個人が健康情報を識別することができるプライバシー、安全、および送信を保護するためのそのカバーする下請け業者の義務を含む“カバーエンティティ”を規定する。また、他の変化の中で、HITECHは4つの新しい民事罰金等級を設立した;HIPAAを修正し、実体をカバーする商業パートナーに連邦HIPAAの法律を遵守するいくつかの要求を直接責任を負うことができ、そして州総検察長に新しい権力を与え、州住民を代表してHIPAA連邦法律に違反して適切な地区裁判所に民事訴訟を提起し、損害賠償或いは禁止を要求することができ、いかなる成功した訴訟においても、裁判所は適宜訴訟費用と合理的な弁護士費を州に判決することができる
•“食品、薬品および化粧品法”は、他の以外に、薬品、生物製品および医療機器に偽またはブランドを混入することを禁止する
•“米国連邦医師支払陽光法案”は、“医療·教育調整法案”(総称して“ACA”と呼ぶ)およびその実施条例の改正により、ある薬品、機器、バイオ製品および医療用品を規定するメーカーが連邦医療保険、医療補助または児童健康保険計画(例外を除く)で支払うことができる薬品、設備、生物製品および医療用品の年次報告要求を“患者保護および平価医療法案”6002節に基づいて作成し、医師(医師、歯科医、検眼師、足科医、脊医を含むと定義される)に提供される何らかの支払いおよび“価値移転”に関する情報を報告する。他の保健提供者(例えば、勤務看護師や医師アシスタント)と教育病院、ならびに医師およびその直系親族が所有している所有権および投資権益;そして
•同様の州法律法規および外国の法律、例えば州反リベートおよび虚偽請求法は、製薬会社が製薬業界の自発的コンプライアンスガイドラインおよび連邦政府によって公布された関連コンプライアンスガイドラインを遵守すること、または州法律および法規で規定されたコンプライアンス計画を採用すること、または他の方法で医療保健提供者への費用の支払いを制限することを要求する販売またはマーケティング手配および民間保険会社を含む非政府第三者支払者によって償還される医療項目またはサービスに関するクレームに適用可能である。州と外国の法律は薬品製造業者に医者と他の医療保健提供者への支払いと他の方法での価値移転、マーケティング支出或いは薬品価格に関する情報を報告することを要求する;州と地方の法律は薬品販売代表の登録を要求する;そしてある場合の健康情報のプライバシーと安全を管理する州と外国の法律は、その中の多くの法律は互いに大きく異なり、しかもHIPAAは往々にして先制されず、それによってコンプライアンス仕事を複雑化させる。
また,ACAは他の事項に加えて,“反リベート法規”や何らかの医療詐欺を管理する刑事法規の意図要件を改正した。個人や実体はこれ以上法規や法規違反の具体的な意図を理解する必要がない。さらに、ACAは、政府は物品または物品を含むことを主張することができると規定している
虚偽申告法によると、“反リベート条例”違反によるサービスは虚偽または詐欺的申告を構成する。
これらの法律の広汎性、およびそれらの例外的な状況と安全港の狭さのために、私たちの商業活動は1つ以上のこのような法律の挑戦を受けるかもしれない。これらの法律の範囲も執行も不確定であり,現在の医療改革環境の急速な変化の影響を受けている。連邦と州法執行機関は医療保健会社と医療保健提供者の間の相互作用の審査を強化し、これは医療保健業界の一連の調査、起訴、有罪判決と和解を招いた。
我々の内部運営と将来の第三者の業務配置が適用される医療法令に適合することを確保する努力は、多くのコストに関連する。私たちの業務が上記の任意の法律または任意の他の私たちに適用される可能性のある政府法規に違反していることが発見された場合、私たちは損害賠償、罰金、監禁、利益の返還、Medicare、Medicaidおよび他の連邦ヘルスケア計画の参加から除外される可能性があり、契約損害、名声損害、利益減少、および将来の収益減少、当社の誠実な合意または他の合意の制約を受けて、私たちの法律違反に関する疑惑を解決し、私たちの業務を削減または再構成することができ、これらは私たちの業務運営および戦略実施に悪影響を及ぼす可能性があります。私たちがそれと業務を展開することを期待している任意の医師または他の医療提供者または実体(将来の協力者を含む)が適用法に準拠していないことが発見された場合、彼らは政府の医療計画への参加から除外されることを含む重大な刑事、民事または行政制裁を受ける可能性があり、これはまた私たちの業務に影響を与える可能性がある
私たちの候補製品はいくつかの管轄区域で政府の価格規制を受けています。これは私たちの収入に影響を与えるかもしれません。
処方薬価格の上昇を受けて、米国、中国、EU、日本、その他の管轄区の政府はすでに薬品定価のやり方の審査を強化している。米国では,このような審査が最近の国会調査を招き,製品定価の透明性の向上,価格設定とメーカー患者計画との関係の検討,政府計画の製品精算方法の改革を目的とした連邦立法が提案·公布されている。連邦レベルでは、国会指導部は薬品コストを抑制するために新たな立法および/または行政措置を求め続けると表明している。州レベルでは、立法機関は、価格または患者の精算制限、割引、ある製品への参入の制限、およびマーケティングコスト開示と透明性措置を含む、薬品および生物製品の価格を制御するための法規をますます公布し、実施しており、場合によっては、他の国からの輸入と大量購入を奨励することを目的としている。
アメリカ以外、特にEU諸国では、ある薬品の定価と精算は政府によってコントロールされている。これらの国では、製品の上場承認を受けた後、政府当局との定価や補償交渉にかなりの時間がかかる可能性がある。いくつかのEU諸国で保険と精算或いは定価の承認を得るために、私たちは臨床試験を行い、私たちの候補製品のコスト効果を他の利用可能な治療法と比較する必要があるかもしれない。EUのいくつかの加盟国(“EU加盟国”)では、より大きな市場を代表する国を含め、医療製品の衛生技術評価(“HTA”)はますます定価と精算手続きの一般的な部分となっている。HTAプロセスは、単一の国の国家ヘルスケアシステムにおける特定の医療製品の治療、経済、および社会的影響を評価するプログラムである。HTAの結果は、EU個別加盟国の主管当局がこれらの医薬製品の価格設定と補償地位を与えることに影響を与えることが多い。現在、EU加盟国間の定価と補償決定は特定の医薬製品のHTAの影響を受ける程度がそれぞれ異なる。2018年1月31日、欧州委員会は衛生技術評価に関する法規(“HTA法規”)の提案を採択した。HTA条例は、新医薬製品を含む衛生技術の評価におけるEU加盟国の協力を促進し、これらの分野で共同臨床評価を行うEUレベルの協力に基礎を提供することを目的としている。2021年12月にHTA条例が可決され、2022年1月11日に施行された。それは2025年から適用されるだろう。もし私たちの候補製品が精算を受けることができない場合、あるいは範囲や金額が制限されている場合、あるいは定価レベルが満足できなければ、私たちの業務は損害を受ける可能性があります。
米国や他の国が最近公布した立法や将来の立法は、候補製品のために得られる価格に影響を与える可能性があり、候補製品の商業化の難しさとコストを増加させる可能性がある。
アメリカや他の多くの国では、上昇している医療費は政府、患者、健康保険部門の懸念であり、これは法律と法規のいくつかの変化を招き、さらなる発展を招く可能性がある
ヘルスケアおよび健康保険システムに関する立法および規制行動は、CARVYKTIを含む当社および私たちの協力者がマーケティング承認を得る可能性のある任意の製品または候補製品の収益性に影響を与える可能性がある。製薬業にとって重要な意義を持つ医療改革の取り組みの詳細な検討については,“項目4.B.会社情報−業務概要−政府法規−米国法規−医療改革”を参照されたい
例えば,米国では2010年3月にACAが公布され,医療コストの抑制,質の向上,ヘルスケア獲得機会の拡大を目標としており,医療提供方式の変更,保険のある人数の増加,何らかの基本医療サービスを得る機会の確保,上昇している医療費の抑制措置が含まれている。ACAのいくつかの側面は法律と政治的な挑戦を受けている。例えば、2021年6月17日、米国最高裁は、ACAが“個人権限”が国会によって廃止されたため、全体的に違憲であると弁明する手続き理由に基づく挑戦を却下した。また、2022年8月16日には、ACA市場で医療保険を購入した個人への強化補助金を2025年に延長する“2022年インフレ低減法案”(略称“アイルランド共和軍”)に総裁·バイ登が署名した。2025年からアイルランド共和軍は,受益者の最大自己負担コストの著しい低減と新たなメーカー割引計画の作成により,連邦医療保険D部分計画下の“ドーナツ脆弱性”を解消した。ACAは未来に司法や国会で挑戦される可能性がある。これらの挑戦やバイデン政府の医療改革措置がACAにどのように影響するかは不明である。
また,米国は連邦医療保険や他の政府医療計画の精算に影響を与える可能性がある他の連邦医療改革措置を提案し採択した。例えば、2011年の“予算制御法案”によると、国会が追加行動を取らない限り、医療サービス提供者の2023年までの財政年度ごとの医療保険支払い額は2%減少する。現在の立法によると、医療保険支出の実質減幅は2022年の1%から本自動減額の最終年度の4%まで様々になる。また、2012年の“米国納税者救済法”は、いくつかの医療サービス提供者への医療保険支払いを減少させ、政府が提供者に多額の支払いを取り戻す訴訟時効期間を3年から5年に延長した。2015年の“連邦医療保険アクセスとチップ再認可法案”は、持続可能な成長率とも呼ばれる臨床医支払いの法定式の使用を終了し、連邦医療保険に参加する臨床医の報酬を大幅に削減し、品質支払いインセンティブ計画を構築し、品質支払い計画とも呼ばれる。この計画は,高度な代替支払いモード(APM)と功績に基づくインセンティブ決済システム(MIPS)を含む臨床医に2つの参加方式を提供する。APMとMIPSでは、各業績年間に収集された業績データは、支払いを減らす可能性を含む今後数年間の医療保険支払いに影響を与える。連邦医療保険や他の政府医療計画のいずれの精算減少も、個人支払者の支払いのような減少を招く可能性があり、あるいは個人支払者は、その医療計画下での精算を独立して減少させることができる。
また、処方薬や生物製品のコストが上昇していることを受けて、米国政府は薬品定価のやり方の審査を強化した。このような審査は、最近のいくつかの大統領行政命令、国会調査を招き、製品定価の透明性の向上、価格設定とメーカー患者計画との関係の審査、政府計画の製品精算方法の改革を目的とした連邦と州立法を提出し、採択した。例えば、連邦レベルでは、2021年7月、バイデン政府は“米国経済における競争を促進する”という行政命令を発表し、その中には処方薬に対する条項が複数ある。総裁·バイデンの行政命令に応答するため、アメリカ衛生·公衆サービス部は2021年9月9日に高薬価に対応する総合計画を発表し、その中で薬品定価改革の原則を概説し、国会が採用可能な各種の立法政策及び衛生と公衆サービス部がこれらの原則を推進するために取る可能性のある行政行動を示した。また、2020年11月20日、HHSは薬品メーカーのD部分下でスポンサーの値下げを計画する安全港保護を廃止し、法律が値下げを要求しない限り、直接或いは薬局福祉マネージャーを通過する法規を決定した。この規定はまた、販売時点での値下げを反映するための新しい避難港を作成し、薬局福祉マネージャーと製造業者との間のいくつかの固定料金手配のための避難港を作成する。新しい税金還付避難港の実施は2032年1月に延期された。OIGが最終的に2023年1月の発効日までにリベート規則を撤回または修正するかどうかは不明である。他のどんな改革計画が施行される可能性や擁護の意志も不確実だ。さらに、IRAは、医療保険D部分(2026年から)およびB部分(2028年から)でカバーされる少数の模倣薬または生物類似競争相手を有さない単一由来ブランド薬または生物製品の価格について、衛生·公衆サービス部長および製薬会社に交渉することを要求する条項を含む。価格交渉の薬品数は2026年の10種類のD部分薬,2027年の15種類のD部分薬,2028年の15種類のD部分とB部分薬,および2029年以降の20種類のD部分とB部分薬となる。これらの薬剤は,連邦医療保険D部分の総支出が最も高い50種類の薬剤と連邦医療保険B部分の総支出が最も高い50薬剤の中から選択される。交渉価格の上限は法律で定められている
薬物や生物学的要因,具体的な要因を考慮すると,衛生·公衆サービス部部長はこれらの価格を交渉する上で期間限定で考慮しなければならない。アイルランド共和軍はまた、連邦医療保険B部分とD部分にリベートを徴収し、価格上昇幅がインフレを超えたメーカーを処罰した。また、2022年10月14日、バイデン政府は追加の行政命令を発表し、HHS報告書がどのように連邦医療保険と医療補助革新センターをさらに利用して連邦医療保険と医療補助受益者の薬品コストを下げる新しいモデルをテストするかを指示した。
州レベルでは、立法機関は、価格または患者の精算制限、割引、特定の製品参入の制限、マーケティングコスト開示および透明性措置を含む、医薬品および生物製品の価格設定を制御するための法規を立法および実施することが増えており、場合によっては、他の国からの輸入および大量購入を奨励することを目的としている。
私たちは未来の立法や行政行動によって生じる可能性のある衛生改革の措置の可能性、性質、程度を予測することができない。私たちは、将来取る可能性のある医療改革措置は、より厳格なカバー基準とより低い精算を招き、薬品価格に追加の下振れ圧力をもたらす可能性があると予想している。もし私たちまたは私たちの協力者がCARVYKTIを含む任意の承認された製品の十分な保証と精算を獲得または維持できなかった場合、このような製品の収入または販売に実質的な悪影響を及ぼす可能性がある。
2021年12月、欧州議会は、2025年に施行された際に、HTAに対するEU全体の臨床的利益評価を調整することを目的としたHTA条例を採択した。もし私たちがEU加盟国で私たちが開発に成功し、規制承認を得る可能性のある候補製品に対して有利な価格設定と清算の地位を維持できなければ、これらの製品はEUのいかなる予想収入と成長見通しにおいても否定的な影響を受ける可能性がある。
私たちはアメリカとある外国の輸出入規制、制裁、禁輸、反腐敗法、反マネーロンダリング法律法規の制約を受けている。このような法律基準を遵守することは国内と国際市場での私たちの競争能力を弱めるかもしれない。私たちは違反によって刑事責任と他の深刻な結果に直面するかもしれないし、これは私たちの業務を損なうかもしれない。
我々は、米国輸出管理条例、米国税関条例、米国財務省外国資産規制弁公室が実施した様々な経済·貿易制裁条例、1977年に改正された米国反海外腐敗法、米国連邦法典第18編201節に含まれる米国国内賄賂法規、米国旅行法、米国愛国者法、および私たちが活動している国の他の州と国の反賄賂および反マネーロンダリング法を含む輸出規制と輸入法律の制約を受けている。腐敗防止法は広く解釈され、会社およびその従業員、代理人、請負業者、および他の協力者の許可、約束、提供、直接的または間接的に公共または民間部門の受給者に不当なお金または任意の他の価値のあるものを支払うことを禁止する。私たちは、第三者を招いて、アメリカ以外で私たちの製品を販売し、臨床試験を行い、および/または必要な許可、許可証、特許登録、および他のマーケティング承認を得ることができます。私たちは政府機関や政府付属病院、大学、その他の組織の役人や従業員と直接または間接的な相互作用を持っている。私たちは、私たちが明確に権限を持っていなくても、または実際にこれらの活動を理解していなくても、従業員、代理、請負業者、および他の協力者の腐敗や他の不法活動に責任を負わなければならないかもしれない。上記の法律および法規に違反するいかなる行為も、重大な民事および刑事罰金および処罰、監禁、輸出入特権の喪失、資格取り消し、税収の再評価、契約違反および詐欺訴訟、名誉損害、およびその他の結果を招く可能性がある。
もし私たちが環境、健康、安全の法律法規を守らなければ、罰金や処罰を受けたり、私たちの業務を損なう可能性のあるコストが発生するかもしれません。
私たちは多くの環境、健康と安全法律と法規の制約を受けて、それらの研究室の手続きと危険材料と廃棄物の処理、使用、貯蔵、処理と処理を管理する法律と法規を含む。私たちの行動は化学物質と生物学的材料を含む危険な材料の使用に関するものだ。私たちの業務はまた危険な廃棄物製品を発生させるだろう。私たちは一般的に第三者と契約を結び、このような材料と廃棄物を処理する。私たちはこのような材料が汚染や傷害をもたらす危険を除去することができない。もし私たちが危険な材料を使用して汚染や損傷をもたらしたら、私たちはそれによるいかなる損害に責任を負い、いかなる責任も私たちの資源の範囲を超える可能性がある。民事や刑事罰金やこのような法律や法規を遵守しない罰に関する巨額の費用を招く可能性もある。また、中国での私たちの運営については、必要なすべてのセキュリティ関連手続きをタイムリーに完成させておらず、罰金や他の行政処罰を受ける可能性があります。
危険材料の使用により負傷する可能性のある費用や支出に保険を提供しているにもかかわらず、潜在的な責任を負うには不十分である可能性がある。私たちは私たちが生物や危険材料を貯蔵したり処分したりすることで、私たちが提起した環境責任や有毒侵害請求に保険を提供することはできません。
また、現在または未来の環境、健康、安全法律法規を遵守するためには、巨額のコストが生じる可能性がある。このような現行または未来の法律法規は私たちの研究、開発、または生産努力を損なうかもしれない。私たちがこのような法律を守らないことはまた巨額の罰金、処罰、または他の制裁につながるかもしれない。
私たちの知的財産権に関するリスクは
もし私たちの技術や候補製品のために特許保護を獲得して維持することができない場合、あるいは獲得した特許保護範囲が十分でなければ、私たちの競争相手は私たちと類似または同じ技術や生物学的製剤を開発し、商業化する可能性があり、私たちの技術および候補製品を商業化することに成功する能力は損なわれる可能性がある。
私たちの成功は、私たちが製品候補と技術の面でアメリカ、中国、EU、日本、その他の国で特許保護を獲得し、維持する能力に大きくかかっている。我々は,米国,中国,欧州主要国,日本を含む主要製薬市場において,我々の技術や候補製品に関連する特許出願を提出することで,我々の特許地位を保護することを求めている。しかし、私たちの特許組み合わせの発展に伴い、私たちのこのような製品の特許組み合わせは現在主に出願から構成されている。もし私たちが私たちの特許候補製品や技術の特許保護を獲得したり維持したりすることができない場合、あるいは他の方法で私たちの知的財産権を十分に保護していなければ、競争相手は私たちの技術を使用して、私たちが持っている可能性のあるいかなる競争優位性を侵食または否定することができ、これは私たちの業務と利益を達成する能力を損なう可能性がある。
私たちの独自の地位を保護するために、私たちは、私たちの業務に重要な新技術および候補製品に関連して、米国および他の国/地域に特許出願を提出する。特許出願と起訴過程は高価で、複雑で、時間がかかる。私たちはすべての可能な司法管轄区域に合理的なコストで、またはタイムリーにすべての必要または望ましい特許出願を提出し、起訴することができないかもしれない。特許保護を受ける前に、私たちはまた、私たちが研究·開発した申請可能な特許の側面を識別できないかもしれない。私たちの特許または特許出願の準備または提出中に形態的な欠陥が存在する可能性があり、または適切な優先権要件、発明権、特許請求の範囲、または特許期限調整のような欠陥が将来的に生じる可能性がある。任意の既存または将来のライセンシーまたはライセンシーが、任意の特許権の起訴、保守または強制執行において、私たちの意見に完全に協力しないか、または同意しない場合、このような特許権は損害を受ける可能性があり、第三者が競合製品を製造、使用、および販売することを阻止することができない可能性がある。私たちの特許または特許出願の形態または準備中に重大な欠陥がある場合、そのような特許または出願は無効であり、強制的に実行できない可能性がある。また,我々の競争相手は同等の知識,方法,ノウハウを自主的に開発することができる.このような結果のいずれも、私たちが第三者からの競争を阻止する能力を弱める可能性がある。
私たちの特許組合を起訴することはまだ非常に早い段階にある。私たちの特許の大部分の組み合わせは、審査されていない未解決の優先出願と、特許協力条約に基づいて係属中の出願を含む (“PCT”)。優先権出願もPCT出願自体も発行された特許を生成することはできない。対照的に、これらの出願に開示された発明の保護は、審査された出願を介して適用の最終期限内にさらに行われなければならない。優先権とPCT出願の適用締め切りが満了するにつれて、どの国または管轄区域でこれらの出願で主張されている様々な発明のために特許保護を求めるかどうかを決定する必要があり、私たちが保護を求める司法管轄区でのみ特許を申請し、取得する機会があるだろう。
我々は,特許保護を得るのが遅くなるまで,我々の研究開発成果で特許を申請できることを確認できない可能性もある.私たちが持っている特許出願は、発行された特許を生成することができない可能性があり、その権利要件は、現在および将来の米国または他の国/地域における候補製品をカバーする。我々の特許出願は、特許がこのような出願から発行されるまで、その後、発行された特許要件が技術の範囲をカバーする限り、そのような出願で主張された技術を実施する第三者に対して強制的に実行することはできない。
もし私たちが持っている私たちの開発計画や候補製品に関連する特許や特許出願が発表されなかった場合、それらの保護の広さや強度が脅かされている場合、または現在および未来の候補製品に意味のある排他性を提供できなければ、候補製品を商業化する能力を脅かす可能性がある。どんなそのような結果も私たちの業務に否定的な影響を及ぼすかもしれない。
バイオテクノロジーと製薬会社の特許地位は一般的に非常に不確実だ。米国や他の国の特許法や特許法解釈の変化は,我々の特許の価値を低下させたり,我々の特許保護の範囲を縮小したりする可能性がある。しかも、他の国の法律が提供する保護も同じではない。これまで、米国または多くの外国司法管轄区域では、バイオテクノロジーおよび製薬特許によって許容される権利要件の広さに関する一致した政策は出現していない。また,薬物化合物や技術に関する特許権の決定は,通常複雑な法律や事実問題に関連しており,近年多くの訴訟のテーマである。したがって,我々の特許権の発行,範囲,有効性,実行可能性,商業的価値は高い不確実性を持っている.
また、米国特許法の最近の変化は、私たちの特許権の範囲、強度、有効性、実行可能性に影響を与える可能性があり、あるいは私たちが提起したり、私たちに対して提起した私たちの特許権に関する訴訟の性質に影響を与える可能性があります。さらに、米国最高裁判所は近年、いくつかの特許事件に対して裁決を下しているか、場合によっては利用可能な特許保護範囲を縮小するか、場合によっては特許所有者の権利を弱めるかを決定している。我々の将来の特許取得能力に関する不確実性の増加に加えて,このようなイベントの結合は,いったん特許を取得する価値に関する不確実性をもたらしている.米国議会、米国連邦裁判所、米国特許商標局(USPTO)の決定によると、特許を管理する法律·法規は予測不可能な方法で変化する可能性があり、私たちが特許を獲得したり、私たちが将来獲得する可能性のある任意の特許を実行する能力を弱める可能性がある。
私たちは私たちの現在と未来の候補製品に関連する可能性のあるすべての第三者知的財産権を知らないかもしれない。科学文献で発表された発見は往々にして実際の発見に遅れており、米国と他の司法管轄区の特許出願は通常、申請18ヶ月後に発表され、時には全く発表されないこともある。したがって、私たちは、私たちが私たちの特許または係属中の特許出願で保護を要求した最初の発明であるか、または私たちがそのような発明のために特許保護を申請した最初の人であることを確認することができない。同様に、もし私たちが将来どのような特許または特許出願を持つことができるかもしれない場合、私たちまたは適用可能な許可者が、そのような特許または特許出願で主張された発明のために特許保護を申請した最初の人であることを判断しないかもしれない。したがって、私たちの特許権の発行、範囲、有効性、商業価値は何の確定的な予測もできません。さらに、米国または他の場所で第三者による既存技術の発行を受ける前に米国特許商標局に提出されたり、反対、派生、再審査、付与後、当事者間の審査または妨害手続きに巻き込まれたりして、私たちの特許権または他の人の特許権に挑戦する可能性があります。このような提出、訴訟、または訴訟における不利な裁決は、実行不可能または無効な特許権の範囲を縮小、保有する可能性があり、第三者が私たちの技術または候補製品を商業化し、私たちに支払うことなく私たちと直接競争することを可能にしたり、第三者特許権を侵害することなく製品を製造または商業化することができなくなり、これは私たちの業務および運営結果を深刻に損なう可能性があります。最終的な結果が私たちに有利であっても、このような手続きは大量のコストを招く可能性があり、私たちの科学者と経営陣に多くの時間がかかる必要がある。
私たちの未解決および未来の特許出願は、私たちの技術または候補製品の全部または一部を保護するために、または他社が競争相手の技術および製品を商業化することを効果的に阻止するために、特許の発行を招くことができないかもしれない。私たちの特許出願が特許の形で発表されても、それらの発表形態は、競争製品やプロセスの影響を受けないように、競争相手が私たちと競争することを防止し、または他の方法でいかなる競争優位性を提供するのに十分であるように、私たちの業務目標を達成するのに十分である。私たちの競争相手は、彼らが非侵害的な方法で類似または代替技術または製品を開発すれば、私たちの特許を迂回することができるかもしれない。私たちの競争相手は承認を求めて、彼ら自身の製品を販売して、私たちの製品と似ているか、あるいは他の面で私たちの製品と競争するかもしれません。この場合、私たちは訴訟を提起することによって特許侵害を告発することを含む、私たちの特許を擁護および/または主張する必要があるかもしれない。上記のいずれかのタイプの訴訟では、裁判所または他の管轄権を有する機関は、我々の特許が無効であり、および/または強制的に実行できないことを発見することができる。
特許の発行は,その発明性,範囲,有効性または実行可能性に関する決定的な要素ではなく,我々の特許は米国や海外の裁判所または特許庁で挑戦される可能性がある。このような挑戦は、独占的または経営の自由を失うこと、または特許主張の全部または部分的な縮小、無効、または実行できないことをもたらす可能性があり、これは、他人が類似または同じ技術および製品を使用することを阻止するか、またはそれを商業化する能力を制限するか、または我々の技術および製品の特許保護期間を制限する可能性がある。さらに、新製品候補製品の開発、テスト、および規制審査に要する時間を考慮すると、これらの候補製品を保護する特許は、これらの候補製品の商業化前または直後に満了する可能性がある。上記のいずれも私たちの業務に実質的な悪影響を及ぼす可能性がある。
第三者は、私たちが知的財産権を侵害、流用、または他の方法で侵害したことを告発する法的訴訟を提起する可能性があり、その結果は不確実であり、私たちの業務を深刻に損なう可能性がある。
私たちのビジネス成功は、当社の候補製品を開発、製造、マーケティングおよび販売し、当社の独自およびモジュール化CAR-TおよびCAR-NK細胞技術を使用する能力にある程度依存し、第三者の知的財産権および他の独自の権利を侵害、流用または侵害することなく、私たちと私たちの協力者が開発、製造、マーケティング、および販売することにある程度依存する。バイオテクノロジー分野には,T細胞やNK細胞などの免疫細胞の修飾,CAR−TやCAR−NK細胞の生産に関する特許,および我々の競争相手が所有する特許を含む第三者米国および非米国から発行された特許が多く存在する。
第三者は、私たちの競争相手を含めて、Cilta-celを含む私たちの候補製品を主張するかもしれないが、その中のいくつかの特許を侵害している。私たちのこのような特許主張に対して、私たちは有効な防御措置を持つと信じていますが、このような防御措置は成功しないかもしれません。もし私たちの任意の製品がこれらの特許のいずれかを侵害していることが発見された場合、私たちは、そのような製品の開発、製造、マーケティング、販売、および商業化を継続するために、それぞれの特許所有者または(適用される場合)彼らのライセンサーから許可を得ることを要求される可能性がある。しかし、私たちは商業的に合理的な条項や必要な許可証を得ることができないかもしれない。私たちが許可を得ることができても、それは非排他的である可能性があり、許可者と他の第三者が私たちに許可した同じ技術を使用する権利があるように、私たちは大量の許可、印税、および他の費用を支払う必要があるかもしれない。私たちはまた、裁判所の命令、開発、製造、マーケティング、そして適用される製品の商業化を永久的に停止することを余儀なくされる可能性がある。さらに、私たちが任意のこのような特許を自発的に侵害していることが発見された場合、私たちは3倍の損害賠償と弁護士費を含む重大な金銭損害に責任があると判断されるかもしれない。たとえ私たちが最終的に勝訴しても、どんな訴訟でも私たちは大量の財務と管理資源を移転する必要があるかもしれません。そうでなければ、私たちは私たちの業務に投入することができます。
バイオテクノロジーおよび製薬業界には大量の知的財産権訴訟があり、私たちは、米国特許商標局への妨害訴訟を含む、私たちの技術または製品候補製品に関連する知的財産権訴訟または他の対抗性訴訟の一方または脅威になる可能性がある。知的財産権紛争は、特許、他の専有権の使用、許可手配の契約条項を含む多くの分野で発生する。第三者は、既存または将来の知的財産権に基づいて私たちにクレームをつけることができ、私たち自身の特許の組み合わせが抑止力のない競争相手からのクレームをする可能性もある。知的財産権訴訟の結果は不確定要因の影響を受け,これらの不確定要因は事前に十分に定量化できない。他の当事者は、私たちの候補製品や私たちの技術を使用して、彼らが持っている特許主張または他の知的財産権を侵害するか、または私たちが彼らの独自技術を不正に使用したと主張するかもしれない。私たちが現在と未来の候補製品を開発して商業化し続けるにつれて、競争相手は、私たちの技術の侵害、流用、あるいは他の方法で彼らの知的財産権を侵害していると主張するかもしれません。これは、私たちの商業化の成功を阻害するためのビジネス戦略の一部です。将来的には、私たちの任意の1つまたは複数の候補製品の使用または製造に関連する材料、成分、配合、製造方法、または治療方法を必要とするより多くの第三者特許または特許出願があるかもしれない。さらに、私たちは、関連する第三者特許または特許出願を識別できないかもしれないし、または発行された特許の請求項が無効であるか、または私たちの活動によって侵害されていないという結論を誤って導出する可能性がある。特許出願が発行されるまでに数年かかる可能性があるため、第三者が現在処理している特許出願を有する可能性があり、これは、私たちの任意の候補製品が発行された特許を侵害する可能性があるか、またはこれらの第三者が私たちの技術によって侵害されていると主張する可能性がある。
第三者知的財産権クレームに法的根拠がないと考えても,裁判所が侵害,有効性,実行可能性の問題で我々に有利な裁決を下すことは保証されない.もし私たちが第三者の知的財産権を侵害していることが発見された場合、裁判所の命令を含めて、権利侵害の候補製品や製品の開発、製造、または商業化を停止させられる可能性がある。代替的に、権利侵害技術を使用して、他の侵害候補製品の開発、製造、またはマーケティングを継続するために、第三者から許可を得ることを必要または選択することができる。しかし、私たちは商業的に合理的な条項や必要な許可証を得ることができないかもしれない。我々が許可を得ることができても,大量の許可や特許権使用料を支払う必要がある可能性があり,非排他的である可能性があり,我々の競争相手が我々に許可してくれた同じ技術にアクセスできるようにする.さらに、もし私たちが故意に特許を侵害したことが発見された場合、私たちは3倍の損害賠償と弁護士費を含む金銭損害賠償責任を負われる可能性がある。権利侵害行為の発見は、候補製品を商業化することを阻止したり、一部の業務運営を停止させたりする可能性がある。我々が第三者の機密情報や商業秘密を盗用したと主張することは,我々の業務に類似した負の影響を与える可能性がある.成功しても、いかなる権利侵害や流用クレームの弁護も時間がかかり、高価で、私たちの経営陣が行っている業務運営への関心を移しました。また、証券アナリストであれば、公聴会、動議またはその他の一時的な手続きまたは事態の発展の結果を公表する可能性がある
あるいは投資家はこれらの結果が否定的であると考えており、これは私たちのアメリカ預託証明書の価格に実質的な悪影響を及ぼす可能性がある。上記のいずれも私たちの業務に実質的な悪影響を及ぼす可能性がある。
第三者から知的財産権の許可を得る必要があるかもしれませんが、このような許可は得られないかもしれませんし、商業的に合理的な条項では得られない可能性もあります。
第三者は、特許権を含む、我々の候補製品の開発または製造に非常に重要または必要な知的財産権を有することができる。第三者の特許やノウハウを用いて候補製品を商業化する必要があるかもしれませんが、この場合、これらの第三者から許可を得ることが求められます。このようなライセンスは商業的に合理的な条項では得られないかもしれないし、全く得られないかもしれないし、不利な契約条項を受け入れざるを得ないかもしれない。もし私たちが商業的に合理的な条項でそのようなライセンスを得ることができなければ、私たちの業務は損害を受けるかもしれない。
私たちは私たちの特許と他の知的財産権を保護したり強制したりする訴訟に巻き込まれるかもしれないが、これは高価で時間がかかり、成功しないかもしれない。
競争相手は私たちの特許、商標、著作権、または他の知的財産権を侵害するかもしれない。権利侵害や不正使用に対抗するために、費用がかかり、時間がかかる可能性があり、私たちの管理者や科学者の時間と注意力を分散させる権利侵害請求を要求される可能性があります。私たちは侵害者が提起したと思われるいかなるクレームに対しても、私たちが彼らの特許、商標、著作権、または他の知的財産権を侵害していると主張するように、これらの当事者たちに反訴を促す可能性がある。さらに、特許侵害訴訟では、裁判所は、私たちの特許の全部または一部が無効または強制的に執行できないと判断する可能性があり、私たちは他方が関連する発明を使用することを阻止する権利がない。もう一つのリスクは、これらの特許の有効性が支持されても、裁判所がその特許の権利要件を狭く解釈するか、または私たちの特許がその発明を含まないことを理由に、私たちが他方が論争された発明を使用することを阻止する権利がないと判断することである。我々の特許に関連する訴訟または訴訟における不利な結果は、これらの当事者または他の競争相手に対して私たちの特許を主張する能力を制限し、第三者が類似または競合製品を製造および販売する能力を制限または排除する可能性がある。同様に、私たちが商標侵害クレームを主張する場合、裁判所は、私たちが主張する商標が無効または強制執行できないと判断するか、または商標侵害を主張する側が関連商標に対する優先権を有することを主張するかもしれない。この場合、私たちは最終的にこのような商標の使用を中止することを余儀なくされるかもしれない。
いかなる侵害訴訟でも、私たちが得たいかなる金銭的損害賠償も商業的価値がないかもしれない。さらに、知的財産権訴訟は大量の開示を必要とするため、私たちのいくつかの機密情報は訴訟中に開示によって漏洩される可能性がある。さらに、公聴会、動議、または他の一時的な手続きまたは事態の発展の結果が公表される可能性があり、証券アナリストまたは投資家がこれらの結果がマイナスであると考える場合、私たちの米国預託証明書の価格に大きな悪影響を及ぼす可能性がある。しかも、このような侵害クレームを提起し、追及するのに十分な財政的または他の資源があることは保証されず、これらのクレームは通常数年続いて解決される。私たちのいくつかの競争相手は、彼らがより多くの財政資源とより成熟して発展した知的財産権の組み合わせを持っているので、このような訴訟や法的手続きの費用を私たちよりも効率的に負担するかもしれない。私たちが最終的に勝訴しても、このような訴訟の金銭的コスト、およびこのような訴訟の間、私たちの経営陣や科学者の長い間の注意移転は、私たちが訴訟から得たいかなるメリットをも超えるかもしれない。したがって、私たちは努力したにもかかわらず、私たちは第三者の知的財産権の侵害、流用、または成功的な挑戦を防ぐことができないかもしれない。特許訴訟や他の訴訟の開始と継続による不確実性は、市場での競争能力に悪影響を及ぼす可能性がある。
米国、ヨーロッパ、中国の特許法の変化は特許の全体的な価値を低下させ、製品を保護する能力を弱める可能性がある。
米国特許法または特許法解釈の変化は、特許出願をめぐる起訴および発行された特許の実行または弁護の不確実性およびコストを増加させる可能性があり、私たちの特許権の範囲、強度および実行可能性に影響を与える可能性があり、または私たちによって提起されたり、私たちに対して提起された特許権に関連する訴訟の性質に影響を与える可能性がある。特許性の他の要件が満たされていると仮定すると,2013年3月までに,米国では,まず発明により保護された発明を発明した者が特許を取得する権利があり,米国以外では,最初に特許出願を提出した者が特許を取得する権利がある。2013年3月以降“ライシー·スミス米国発明法”によると 2011年9月に公布された“米国発明法”(“米国発明法”)によれば、米国は、第1の発明者提出出願制度に移行し、この制度の下で、他の特許性要件を満たすと仮定して、最初に特許出願を提出した発明者は、要求された発明が第三者が最初に発明したものであるか否かにかかわらず、発明の特許を取得する権利がある。アメリカの発明法には特許方式に影響を与える大きな変化も含まれています
申請は起訴され、特許訴訟に影響を及ぼす可能性もある。これらの措置には、第三者が特許訴訟中に米国特許商標局に以前の技術を提出することを可能にすることと、特許の有効性を攻撃するために、ライセンス後審査を含む米国特許商標局によって管理される認可後手続きとが含まれる各方面間審査と派生手続き。しかしながら、米国発明法およびその実施は、私たちの特許出願をめぐる起訴および私たちが発行した特許の実行または保護の不確実性およびコストを増加させる可能性があり、これらのすべては、私たちの業務、財務状況、運営結果、および見通しに実質的な悪影響を及ぼす可能性がある。
中国では知的財産権法が進化しており,中国では知的財産権保護の整備に努めている。例えば,2021年6月1日に“中華人民共和国特許法改正案”が発効し,条件に適合した革新薬物特許に対して特許延期が行われた。修正案は採択されたが、施行規則とガイドラインはまだ発表されていない。したがって、第三者が所有する特許が延長される可能性があり、これは逆に、侵害リスクに直面することなく、製品を商業化する能力に影響を与える可能性がある。この改正により,特許権者は特許期間を延長する出願を提出することができる。このような延期の長さはいずれも不確実だ。もし私たちが長期的に商業化を延期することを要求されれば、技術進歩を発展させ、新製品を発売する可能性があり、これは私たちの製品を競争力を失う可能性がある。中国の知的財産権法の他の変化が私たちの知的財産権保護にマイナスの影響を与えないことも保証できない。
他の国と同じように、ヨーロッパ諸国の知的財産権法も進化している。例えば、統一特許と統一特許裁判所は2023年6月1日に運用を開始し、すべての参加する欧州諸国の薬品特許構造に不確実性をもたらす。私たちはこの新しい特許と裁判所システムにおける特許の実行可能性を保証することができず、新しい特許集中化の挑戦に直面しており、これは特許が参加加盟国間で実行できなくなり、ヨーロッパでの特許の組み合わせに新たなリスクをもたらす可能性がある。私たちはヨーロッパの知的財産権法の他の変化が私たちの知的財産権保護に否定的な影響を与えないということを保証できない。
私たちの候補製品のために特許保護を受けることができても、このような保護の有効期間(あれば)は限られており、第三者が私たちと似ているか、または同じ製品や技術を開発し、商業化することができ、私たちの特許権が満期になった後に直接私たちと競争することができ、任意の製品または技術を商業化することに成功した能力は実質的に悪影響を受けるだろう。
特許の有効期間と提供される保護は限られている。例えば、米国では、すべての維持費が直ちに支払われる場合、特許の自然失効時間は、通常、その最初の米国非一時出願日から20年である。私たちが承認された候補製品のための特許保護に成功したとしても、それは模倣薬や生物類似薬からの競争に直面する可能性がある。模倣薬または生物類似薬の製造業者は、法廷または特許庁において、私たちの特許の範囲、有効性、または実行可能性に挑戦する可能性があり、私たちはこれらの知的財産権を成功的に実行または守ることができない可能性があり、したがって、関連製品を独占的に開発またはマーケティングすることができない可能性があり、これは、製品の任意の潜在的販売に重大な悪影響を及ぼすであろう。
新製品候補製品の開発、テスト、および規制審査に要する時間を考慮すると、これらの候補製品を保護する特許は、これらの候補製品の商業化前または直後に満了する可能性がある。したがって、私たちの特許と特許出願は、他の人が私たちと似ているか同じ製品を商業化することを排除するために、私たちに十分な権利を提供していないかもしれない。特定の特許期間の延長を受ける資格があると考えても、米国のFDAやUSPTO、他の国/地域のどの同等の規制機関も含めて、このような延長が利用可能かどうかの評価に同意することはできません。これらの機関は、私たちの特許延長の承認を拒否するか、あるいは私たちが要求したよりも限られた延長を承認することができるかもしれません。私たちの候補製品の未定特許出願が発表されれば、“ビジネス-知的財産権”に記載されている異なる日に満了する予定です。私たちの特許出願が満期になったら、私たちは潜在的な競争相手にこれらの特許権を主張することができなくなり、これは私たちの業務、財務状況、運営結果、将来性に大きな悪影響を及ぼすだろう。
私たちの候補製品は予想よりも早く生物類似製品からの競争に直面するかもしれません。
私たちが規制部門の承認を得ることに成功しても、私たちの競争相手よりも早く候補製品を商業化しても、私たちの候補製品は生物類似製品からの競争に直面する可能性がある。米国では,我々の候補製品はバイオ製品としてFDAによって規制されており,BLA経路に基づいてこれらの候補製品の承認を求める予定である。2009年バイオ製品価格競争と革新法案 (“BPCIA”)は、生物学的類似性および交換可能な生物学的製品を承認するための簡明な道を開いた。簡略化された規制経路は、生物類似体と既存ブランド製品との類似性に基づいて、それを“交換可能”な生物類似体として指定することを含む、FDAのための生物類似生物製品を審査および承認する法的権威を確立する。BPCIAによると、生体類似製品の申請は最初のブランド製品のみとされている
法案に基づいて承認される。この法律は複雑であり、FDAはまだ説明して施行している。したがって、その最終的な影響、実施、そして意味には不確実性がある。FDAがBPCIAを実施するためのこのようなプロセスをいつ完全に採用するかは不明であるが、どのようなプロセスも、私たちの候補製品の将来のビジネス見通しに重大な悪影響を及ぼす可能性がある。
もし私たちの任意の候補製品がBLAによって生物製品として承認された場合、私たちが得られる可能性のあるいかなる排他性も、国会の行動または他の理由によって短縮される可能性があり、またはFDAは私たちの候補製品を競争製品の参考製品とみなさないで、これは予想よりも早く模倣薬または生物学的類似競争のための機会を作るかもしれない。さらに、承認されると、生物類似製品が私たちのいずれかの参考製品をどの程度置換するか、その方法は非生物製品の伝統的な模造薬代替に類似しており、これはまだ発展中のいくつかの市場と規制要素に依存するかどうかは不明である。また,競争相手は生物類似の承認手順を放棄し,自分の臨床前研究と臨床試験を完了した後に完全なBLAを提出することを決定することができる。この場合、BPCIAによっては、その製品が承認された直後に競合他社がその製品を販売することを阻止する資格がある可能性のある排他性はない。
ヨーロッパでは、欧州委員会は、過去数年間に発表された生物類似承認に関する一般的かつ特定の製品カテゴリに関するガイドラインに基づいて、いくつかの生物類似製品のマーケティング許可を承認した。ヨーロッパでは、競争相手は革新生物製品の承認を支持するデータを参考にすることができるが、革新製品が承認されてから10年後にのみ発売されることができる。この10年前の8年間に、マーケティング許可保持者が1つまたは複数の新しい治療適応の承認を得、これらの新しい治療適応が既存の療法と比較して有意な臨床的利益をもたらす場合、この10年間の市場排出期間を11年に延長することができる。また、会社は他の国で生物類似製品を開発する可能性があり、承認されれば、これらの製品は私たちの製品と競争する可能性がある。
もし競争相手が私たちの候補製品を参考にする生物模倣薬のマーケティング許可を得ることができれば、もし承認されれば、このような製品はこのような生物模倣薬の競争を受ける可能性があり、それに伴う競争圧力と潜在的な不利な結果である。これらの競争力のある製品は、私たちの候補製品が承認される可能性のあるすべての指標で直ちに私たちと競争するかもしれない。
私たちは、私たちまたは私たちの従業員、コンサルタント、コンサルタントの流用、誤った使用、または彼らの商業秘密または他の知的財産権を開示した、または私たち自身の知的財産権の所有権であることを要求する第三者のクレームを受けるかもしれません。
私たちの多くの従業員、コンサルタント、そしてコンサルタントは現在または以前、私たちの競争相手や潜在的な競争相手を含む大学や他のバイオテクノロジーや製薬会社に雇われています。
私たちは、私たちの従業員、コンサルタント、およびコンサルタントが、私たちのために働いているときに第三者の固有情報またはノウハウを使用しないことを保証するために努力しているが、私たちまたはこれらの個人は、商業秘密または他の固有情報を含む任意のそのような個人の元雇用主の知的財産権を無意識にまたは他の方法で使用していると告発される可能性がある。将来的には、私たちはまた、その個人がそのスポーツ禁止またはスポーツ禁止協定の条項に違反しているという疑惑を受けるかもしれない。このような潜在的なクレームを弁護するためには、訴訟を提起する必要があるかもしれない。
また、私たちの政策は、知的財産権開発に参加する可能性のある私たちの従業員と請負業者が合意に署名し、このような知的財産権を私たちに譲渡することを要求することですが、これらの従業員と請負業者は合意に違反し、開発された知的財産権を彼らの所有にすることを要求する可能性があります。
私たちの譲渡協定は自動的に実行されないか、違反される可能性があるかもしれません。私たちは私たちの知的財産権の所有権を決定するために、第三者にクレームを出したり、私たちが提起したクレームを弁護したりすることを余儀なくされる可能性があります。このようなクレームは、私たちの業務、財務状況、運営結果、および見通しに実質的な悪影響を及ぼす可能性があります。
もし私たちがこのようなクレームを起訴したり、弁護することができなければ、金銭的損害賠償を支払う以外に、私たちは貴重な知的財産権や人員を失う可能性がある。裁判所は、これらの技術または機能が以前の雇用主の商業秘密または他の固有情報を含むか、または由来する場合、私たちの候補製品に重要な技術または機能を使用することを禁止することができる。このようなクレームの起訴や抗弁に成功したとしても、訴訟は巨額の費用を招く可能性があり、経営陣の注意を分散させる可能性がある。さらに、どんな訴訟や脅威も、私たちが従業員を雇ったり、独立サービス会社と契約を結ぶ能力に悪影響を及ぼす可能性があります
仕入先。さらに、キーパーソンや彼らの仕事の成果の損失は、製品を商業化する能力を阻害したり阻止したりする可能性がある。
私たちは私たちの特許権と他の知的財産権の発明権または所有権のクレームに疑問を受けるかもしれない。
私たちは通常、私たちの従業員、コンサルタント、外部科学協力者、協賛研究者、その他のコンサルタントと秘密と知的財産権の分配協定を締結します。しかし、このような合意は遵守されないかもしれないし、知的財産権を効果的に私たちに割り当てられないかもしれない。例えば、論争は、私たちの技術および製品候補製品の開発に参加するコンサルタントまたは他の人の義務衝突に起因する可能性がある。訴訟は、これらと他の挑戦在庫または所有権のクレームに対抗するために必要かもしれない。もし私たちがこのようなクレームを弁護することができなければ、金銭損害賠償を支払うことに加えて、貴重な知的財産権、例えば貴重な知的財産権の独占所有権や使用権を失う可能性がある。このような結果は私たちの業務に実質的な悪影響を及ぼすかもしれない。私たちがこのようなクレームを弁護することに成功しても、訴訟は巨額のコストを招き、経営陣や他の従業員の注意を分散させる可能性がある。
私たちが獲得する可能性のあるどの商標も侵害されたり、成功的に挑戦されたりして、私たちの業務に損害を与える可能性があります。
私たちは商標に依存して、私たちが発売を許可された候補製品を私たちの競争相手の製品と区別したい。私たちはまだ私たちの候補製品のために商標を選択していないし、私たちの候補製品のための登録商標を申請する過程も始まっていない。私たちが商標を選択して登録を申請すると、私たちの商標申請は承認されないかもしれない。第三者は私たちの商標申請に反対するか、または他の方法で商標の使用に挑戦するかもしれない。もし私たちの商標が成功的に挑戦されれば、私たちは私たちの製品ブランドを再形成することを余儀なくされるかもしれません。これはブランド認知度の喪失を招き、広告と新しいブランドをマーケティングするために資源を投入する必要があるかもしれません。私たちの競争相手は私たちの商標を侵害するかもしれないが、私たちは私たちの商標を実行するのに十分な資源がないかもしれない。
さらに、私たちは、米国で臨床段階の候補製品または任意の他の候補製品と共に使用される任意の固有名が、登録または出願が商標として登録されているか否かにかかわらず、FDAの承認を受けなければならないことを計画している。FDAは通常、他の製品名と混同される可能性を評価することを含む、提案された製品名を検討する。FDAが私たちが提案した任意の独自製品名に反対する場合、私たちは、適用商標法に適合し、第三者の既存の権利を侵害せず、FDAのために受け入れられる適切な独自製品名を決定するために、多くの追加リソースを必要とするかもしれません。
もし私たちが私たちの商業秘密の機密性を保護できなければ、私たちの商業と競争の地位は損なわれるだろう。
私たちの技術や製品候補のための特許や商標保護を求めるほか、特許を取得していないノウハウ、技術、その他の独自の情報を含む商業秘密に依存して、私たちの競争地位を維持しています。ビジネス秘密と技術的ノウハウを保護することは難しいかもしれない。私たちは、私たちの従業員、会社協力者、外部科学協力者、CRO、契約製造業者、コンサルタント、コンサルタント、および他の第三者のような、これらの秘密にアクセスする権利のある当事者と秘密協定を締結することによって、私たちのビジネス秘密および他のノウハウを保護することを求めています。私たちはまた私たちの従業員とコンサルタントと秘密と発明または特許譲渡協定を締結します。私たちは私たちが可能であるか、または私たちの商業秘密またはノウハウとプロセスに接触したすべての当事者とこのような合意に到達したことを保証することができない。このような努力にもかかわらず、どちらも合意に違反し、私たちのビジネス秘密を含む私たちの固有の情報を漏洩する可能性がある。私たちの知的財産権の無許可使用と開示を規制することは困難であり、私たちは私たちの知的財産権を保護するために私たちが取った手順が有効かどうかも分からない。しかも、私たちはこのような違反のすべてについて十分な救済措置を得ることができないかもしれない。強制執行側が商業秘密を不正に開示したり流用したりする主張は困難であり、高価で時間がかかり、結果は予測できない。しかも、米国国内外のいくつかの裁判所は商業秘密をあまり望んでいないか、または保護したくない。
また,我々の競争相手や他の第三者は,我々のビジネス秘密に相当する知識,方法,ノウハウを独立して開発することができる.競争相手や他の第三者は私たちの製品を購入し、私たちの技術開発から得られた競争優位性の一部または全部をコピーすることができますが、私たちはこれらの技術に対して特許保護を持っていません。もし私たちの任意の商業秘密が競争相手または他の第三者によって合法的に取得または独立して開発された場合、私たちは彼らまたは彼らが交流する人がこの技術を使用することを阻止する権利がないだろう
私たちと競争している情報ですもし私たちの任意の商業秘密が競争相手または他の第三者に漏洩された場合、または競争相手または他の第三者によって独立して開発された場合、私たちの競争地位は損なわれるだろう。
私たちは世界各地で私たちの知的財産権を保護できないかもしれない。
世界各国で候補製品特許を出願、起訴、擁護する費用は目を引くほど高く、米国以外のいくつかの国での知的財産権は米国ほど広くないかもしれない。場合によっては、私たちはアメリカ以外で特定の技術の特許保護を受けることができないかもしれない。また、いくつかの外国の法律は知的財産権の保護の程度はアメリカの連邦や州法律に及ばず、私たちが確かに特許保護を求めている司法管轄区でも同様である。したがって、私たちは、米国以外のすべての国または地域で私たちの発明を実施することを阻止することができないかもしれません。私たちが確かに特許保護を求めている司法管轄地域であっても、または私たちの発明を使用して製造された製品をアメリカまたは他の管轄地域で販売したり、輸入したりすることはできません。
競争相手は私たちが特許保護を申請していない管轄区域で私たちの技術を使用して自分の製品を開発し、さらに他の侵害製品を私たちが特許保護を持っている地域に輸出することができるが、法執行力はアメリカに及ばない。これらの製品は私たちの候補製品や臨床前プロジェクトと競争するかもしれませんが、私たちの特許や他の知的財産権は彼らの競争を効果的にまたは阻止するのに十分ではないかもしれません。
多くの会社は外国の管轄区域の知的財産権の保護と保護に重大な問題に直面している。特定の国の法律制度、特に特定の発展途上国の法律制度は、特許、商業秘密、および他の知的財産権保護、特にバイオテクノロジー製品に関する保護の強制執行を支持しておらず、これは、私たちの特許侵害を阻止したり、全体的に私たちの独占権を侵害したりして競争製品を販売することを困難にするかもしれない。
外国の管轄区域で私たちの特許権を強制的に執行する訴訟手続きは、巨額のコストを招き、私たちの努力と注意を私たちの業務の他の側面から移転させる可能性があり、私たちの特許が無効または狭義に解釈されるリスクに直面する可能性があり、私たちの特許出願を発表できないリスクに直面させ、第三者からのクレームを引き起こす可能性がある。私たちは私たちが起こしたどんな訴訟でも勝てないかもしれないし、判決された損害賠償や他の救済措置(もしあれば)は商業的な意味がないかもしれない。したがって、私たちが世界各地で私たちの知的財産権を実行する努力は、私たちが開発または許可した知的財産権から顕著なビジネスメリットを得るのに十分ではないかもしれません。
私たちの特許保護の獲得と維持は、政府特許機関によって提出された様々なプログラム、書類提出、費用支払い、および他の要求を遵守することに依存し、これらの要求に適合しなければ、私たちの特許保護は減少またはキャンセルされる可能性がある。
発行された特許の定期維持費および年会費は、特許有効期間内にいくつかの段階で米国特許商標局および米国以外の特許代理機関に支払われなければならない。米国特許商標局および各種外国政府特許機関は、特許出願過程において、いくつかのプログラム、文書、費用支払い、およびその他の同様の規定を遵守することを要求する。多くの場合、適用規則に従って滞納金を支払うか、または他の方法で不注意を是正することによって失効を是正することができるが、場合によっては、規定を遵守しないことは、特許または特許出願が放棄または失効され、関連法ドメインの特許権の一部または全部の喪失をもたらす可能性がある。特許または特許出願が放棄または失効される可能性のある規定を遵守しないイベントは、規定された期限内に公式行動に応答することができなかったこと、費用を支払わなかったこと、および適切に合法化されず、正式な文書を提出することを含む。もし私たちが私たちの製品や候補製品をカバーする特許と特許出願を維持できなければ、私たちの競争相手は市場に入る可能性があり、これは私たちの業務を損なうだろう。
知的財産権はすべての潜在的な脅威を解決できるとは限らない。
私たちの知的財産権が提供する未来の保護の程度は不確定であり、知的財産権には限界があるため、私たちの業務を十分に保護できないか、あるいは競争優位性を維持することができるかもしれない。例えば:
•他の人は、私たちが同様の技術を開発または利用する可能性のある任意の候補製品と同様の製品を製造することができるかもしれないが、これらの製品は、私たちが現在または将来所有または許可する可能性のある特許請求の範囲内ではない
•私たち、または任意の未来のライセンスパートナーまたは協力者は、私たちが現在または将来所有または許可している発表された特許または係属中の特許出願に含まれる発明を最初にした会社ではないかもしれない
•私たち、または未来のライセンスパートナーまたは協力者は、私たちまたは彼らのいくつかの発明をカバーする最初の特許出願ではないかもしれない
•他の人は私たちの知的財産権を侵害することなく、類似または代替技術を開発したり、私たちの任意の技術を複製したりすることができる
•私たちが未解決の特許出願または私たちが将来所有する可能性のある特許出願は、発行された特許を招くことができないかもしれない
•私たちが権利を持っている発行された特許は、私たちの競争相手による法的挑戦を含む無効または強制執行不可能と認定される可能性があります
•私たちの競争相手は特許権のない国で研究や開発活動を行い、これらの活動から学んだ情報を利用して競争力のある製品を開発し、私たちの主要な商業市場で販売するかもしれません
•私たちは他の特許を申請できるノウハウを開発しないかもしれない
•いくつかの商業秘密またはノウハウを保護するために、私たちは特許を出願しないことを選択することができ、第三者はその後、これらの知的財産権をカバーする特許を提出する可能性がある。
これらの事件のいずれかが発生した場合、私たちの業務、財務状況、運営結果、および見通しに実質的な悪影響を及ぼす可能性がある。
中国でのビジネスに関するリスク
文意が別に指摘されているほか、本節の“中国で商売をするリスク”で言及されている“外国”とは、中国以外の国や地域を指す
中国の医薬業界は高度な監督管理を受けており、これらの法律法規は変化する可能性があり、これは私たちの薬品の承認と商業化に影響を与える可能性がある。
私たちが中国に提供している研究開発業務と製造施設の主な部分は 中国に位置し、私たちはこれが臨床、商業、そして規制の優位性を与えていると思う。中国の医薬業界は政府の全面的な監督管理を受けており、新薬の審査、登録、製造、包装、許可とマーケティングを含む。現在の中国における我々の業務活動に適用される規制要求の検討については、本年度報告における“会社情報−業務概要−政府規制−中国規制”を参照されたい。例えば、中国人類遺伝資源を使用する国際協力プロジェクトは、“ヒトゲノム条例”が規定している場合を除いて、関連科学技術部門の許可を受ける必要がある。実際の操作のいくつかの制限は私たちの制御範囲を超えているため、私たちは中国人類遺伝資源法律法規に要求されたすべての承認をタイムリーにあるいは根本的に獲得したことを保証することはできません。私たちは規制の傾向に注目しており、関連する規制機関の承認を申請している。このような承認を得られなかったことは、関連する国際協力プロジェクトが管理当局によって一時停止される可能性があり、罰金やその他の処罰を招く可能性があり、いくつかのCROとの合意の違約となる可能性もある。中国の法律法規によると、中国の人類遺伝資源を利用した国際科学研究協力プロジェクトでは、中国の人類遺伝資源を輸送、郵送または携帯することが計画されており、政府主管部門の輸出証明を得なければならない。中国の人類遺伝資源輸出証明は税関手続きの要求である。関連する輸出活動でこのような輸出証明書を獲得できなかったことは、政府当局がこのような活動を一時停止させ、不法に収集と保存された人類の遺伝資源と非法で得られた所得を没収し、このような実体とその責任者の商業活動に罰金と制限を科し、関連する輸出活動が犯罪となれば、甚だしきに至っては刑事責任を招く可能性がある。私たちが中国の人類遺伝資源を中国から輸出することは保証されず、いつも関連する承認を得ることができる。
また,中国の関連法律法規によると,動物での実験には実験動物の許可証を用いる必要がある。この要求を完全に守ることができなかった行為は、私たちの実験データを無効にする可能性がある。さらに、我々のパートナーに対して、nhcおよび他の管理機関が中国細胞治療研究者を管理することによって開始された臨床試験を遵守しない既存または未来の法律法規を遵守しない行為は、政府の処罰、関連活動の一時停止、または規定違反を招く可能性がある
責任です。このような法律および法規を遵守または遵守しないことは、研究者によって開始されたこれらの臨床試験および研究開発活動のコストを増加、制限し、著しい遅延をもたらす可能性があり、これはまた、私たちの業務、運営、および将来性に実質的な悪影響を及ぼす可能性がある。しかし、私たちは私たちの協力者をコントロールすることができず、NHCや他の管理当局の要求に従うように強要することもできない。したがって、私たちの協力者が法律で規定された任意の必要な登録や届出手続きが直ちに完了するか、または根本的に達成できないということを保証することはできません。
近年、中国の医薬業界に関する監督管理の枠組みは重大な変化が発生し、私たちはそれが引き続き重大な変化が発生することを予想している。このような変更や修正は、私たちの業務のコンプライアンスコストを増加させたり、中国での候補製品の開発や商業化の成功を遅延させたり、現在中国で薬物の研究開発や製造に及ぼすメリットを減少させたりする可能性があります。中国当局は製薬業界の法律を執行する際にますます警戒されており、私たちまたはパートナーが適用された法律や法規を遵守できなかったり、必要な許可や許可を取得して維持できなかったりすることで、中国での業務活動が一時停止または終了され、さらに行政処罰を受ける可能性がある。私たちの戦略と方法は中国政府の規制政策と一致していると信じているが、私たちの戦略と方法が引き続き一致していることを保証することはできない。
中国の既存または将来の人間の遺伝資源管理に関連する法律法規を遵守しない場合、民事、行政または刑事罰金または処罰、個人訴訟、他の責任、および/または負の宣伝を含む可能性がある政府の法執行行動を招く可能性がある。このような法律を遵守または遵守しないことは、著者らの臨床研究と研究開発活動のコストを増加、制限し、顕著な遅延を招く可能性があり、そうでなければ、私たちの運営結果、業務と将来性に重大な不利な影響を与える可能性がある。
中国の人類遺伝資源管理に関連する法律法規は急速に変化しており、予見可能な未来において、その実行状況はまだ確定していない可能性がある。1998年6月10日、科学技術部と衛生部は共同で“人類遺伝資源管理暫定方法”を発表し、中国で人類遺伝資源の保護と利用規則を制定した。中国の大多数の規制機関や他の規制機関はHGR立法に集中しており、条例草案について積極的に公衆の意見を求めてきた。2015年、MOSTはHGRに関する指導意見を発表し、HGR管理の立法努力を強化した。2019年5月、“ヒト遺伝資源管理条例”(“HGR条例”と略称する)が制定された。国務院は2019年6月10日に“HGR条例”を公布し、2019年7月1日から施行した。
“障害者権利条例”は、非中華人民共和国単位、個人或いはそれを基礎に設立或いは実際にコントロールされた単位或いは“外国人”が中国国内で中国の人体成長ホルモンを採集、保存することを禁止し、或いは中国の人体成長ホルモンを国外に提供することを禁止し、臨床診断と治療、血液採取と提供サービス、不法活動の調査、覚せい剤検査と葬儀サービスなどの目的の器官、組織と細胞の採集と保存は、他の関連法律法規に従って行う必要がある。“条例”は外国人が中国河北原子炉を有限に使用することを許可し、“科学研究活動”を行い、中国の科学研究機関、高等学校、医療機関或いは企業と協力しなければならず、総称して“中国実体”と呼ばれる。このような活動はMOSTの承認を経なければならず,承認申請は外国籍者と関係中国実体が共同で提出しなければならない。承認要求の唯一の例外は器官、組織或いはヒトゲノム、遺伝子或いはその他の遺伝物質を構成する細胞などの中国HGR材料に関連しない臨床試験国際協力であり、総称して中国HGR材料と呼ばれる。しかし,このような臨床試験協力はMOSTにあらかじめ登録されていなければならない。HGR条例の規定をどのように解釈して実行するかについては、依然として大きな不確実性がある。外国実験室或いは外商投資実験室短期保存実験室検査サンプルも中国HGRを保存すると解釈される可能性があるため、大多数の申請、承認或いは事前登録プログラムの影響を受ける。
2020年10月17日、全国人民代表大会常務委員会は“中華人民共和国生物安全法”(以下、“生物安全法”と略称する)を公表し、2021年4月15日から施行された。新法律は“生物安全条例”の生物安全資源の収集、保存、利用と対外提供に関する審査または事前登録要求を再確認した。新法律の公布は、中国政府が中国の生物安全を保護し、国家の生物安全を維持する約束をさらに明らかにした。
“HGR条例”および“生物安全法”を含む既存または将来のHGR法律および法規に準拠せず、罰金、関連活動の一時停止、および関連するHGRの没収、およびこれらの活動を展開することによって生じる収益、または責任違反を含む罰を受ける可能性がある。ストーリーが深刻な場合は、職場とその担当者が一定期間あるいは永久に中国の遺体の収集、保存、使用、出国などの活動を禁止することができる。また、関連活動があれば、刑事責任を招く可能性があります
犯罪を構成する。既存または将来のHGR法律および法規に従って、すべての申請、承認、または事前登録プロセスを常に完了できる保証はありません。
私たちは江蘇省鎮江市税関密輸局、人民Republic of Chinaあるいは税関管理局が行った調査や調査の悪影響を受けるかもしれません。私たちの大株主と私たちの会長に関連しています。鎮江市人民検察院または検察院は調査の審査を終了し、私たち、私たちの高級管理者、取締役または従業員に告発されていないことを知っているが、当局または他の政府当局が将来、私たちまたは私たちの役員、高級管理者または従業員に制裁、罰金、規制行動を含む刑事、民事または行政救済措置を取らないことは保証されず、これは私たちに悪影響を及ぼす可能性がある。
私どもの大株主GenScripも私どもの会長兼取締役役員の張方亮博士も調査の対象となっております。吾らは中国の法律下の輸出入法規違反の疑いがある調査であり、主にGenScripの2020年6月の初公開前の輸出入活動を対象としており、当時私たちはGenScripの付属会社であり、張博士はGenScripの主席兼最高経営責任者であった。調査開始時、張博士は私たちの会長兼最高経営責任者で、彼は調査に関する職を辞めた。
2022年5月、GenScripはその上場が所在する香港連合取引所の文書を通じて、検察は調査の審査を終了し、どの個人も実体もこれによって刑事告発を受けないと発表した。2022年8月、張博士は再び取締役第二類取締役に任命され、取締役会議長に選出された。
調査は我々の米国預託証明書や普通株の価格に悪影響を与えていると考えられる。管理局または検察が私たち、私たちの上級職員、従業員または役員に対して取った任意のさらなる行動、またはそれによって引き起こされる任意の告発または行政処罰は、私たちの名声を損なう可能性があり、または私たちの既存のパートナーJanssenおよび他の第三者が既存の合意および潜在的なパートナーを終了させ、他のパートナーを探すことにつながり、これらは、私たちの業務、財務状況、経営業績、および私たちのアメリカ預託証明書および普通株の価格に負の影響を与えるだろう。
中国経済は多くの点で大多数の先進国の経済と異なり、より高いレベルの政府参加、市場経済の持続的な発展、より高いレベルの外貨規制、そしてより効率的な資源配置を含む。
中国経済は1970年代末以来著しい成長を経験しているが、地理的にも経済の各部門の間でも成長は不均衡である。中国政府は経済成長を奨励し、資源配置を誘導する様々な措置を実施した。これらの措置は中国経済全体に利益を与えることを目的としているが、私たちにマイナスの影響を与える可能性もある。例えば、私たちの業務、財務状況、経営結果は、中国政府の資本投資のコントロールや私たちの法規に適用される変化によって悪影響を受ける可能性があります。
中国経済は中央計画経済からより市場化された経済へと転換してきた。中国政府は1970年代末から市場力を利用した経済改革を強調する措置を実施してきたが、中国政府は引き続き産業政策を実施することで業界の発展を調節する上で重要な役割を果たしている。中国政府はまた、資源配置、外貨債務の支払い制御、通貨政策の制定、特定の業界や会社に優遇待遇を提供することで、中国の経済成長を重大な制御を行っている。
中国の法制度には不確実性が含まれており、これはあなたと私たちが得ることができる法的保護を制限するかもしれない。
1979年、中華人民共和国政府は経済事務を全面的に管理する法律法規体系を公布し始めた。過去40年間の立法全体効果は中国の各種形式の外商投資に対する保護を著しく強化した。我々の中国子会社は中国外商投資企業に適用される法律法規の制約を受けている。特に、それらは外国企業の製薬企業における所有権と運営を管理する中国の法律、規則、法規の制約を受けている。これらの法律や法規は変化する可能性があり、それらの解釈と実行には不確実性があり、これは私たちと私たちの投資家が得ることができる法的保護を制限するかもしれない。また、新しい法律の公布、既存の法律の改正やそれなどの法律の解釈や実行、あるいは中国の法律、規則と法規が先制された地方性法規を含む、中国の法律制度の将来の発展の影響を予測することはできない。
また、中華人民共和国の法律制度は成文法規に基づく民法制度である。一般法制度と異なり,従来の裁判所判決は参考になるが,その先例価値は限られている。中国はまだ完全に統合された法律体系を構築しておらず、最近公布された法律、規則、法規は中国の経済活動のあらゆる面をカバーするのに十分ではないかもしれない、あるいは中国の監督管理機関と裁判所の大きな解釈を受ける可能性がある。特に、これらの法律、規則、および条例は比較的新しいため、公表された決定の数が限られているため、これらの決定は非前例的な性質を持っており、これらの法律、規則、規則および条例は、それらをどのように実行するかに関する規制機関に重大な裁量権を与えることが多く、これらの法律、規則および条例の解釈と実行は不確実性に関連し、不一致で予測不可能である可能性がある。したがって、未来には私たちの既存の運営が関連された法律に完全に適合していないことが発見されるかもしれない。また、中国の法制度部分は政府政策と内部規則に基づいており、その中のいくつかは適時に公表されていないか、あるいは全く公表されておらず、追跡力を持っている可能性がある。したがって、私たちは違反が発生してから、私たちがこのような政策と規則に違反していることを認識しなければならないかもしれない。
中国のいかなる行政訴訟と裁判所訴訟も長引く可能性があり、巨額のコストと資源の分流と管理注意力の移転をもたらす可能性がある。中国の行政·裁判所当局は法定·契約条項の解釈·実施に重大な適宜決定権を持っているため、行政や裁判所訴訟の結果および我々が享受している法的保障レベルを評価することは、より発達した法制度よりも難しい可能性がある。これらの不確実性は、私たちが締結した契約を実行する能力を阻害し、私たちの業務、財務状況、および運営結果に実質的な悪影響を及ぼす可能性があります。
また、中国政府は最近、中国国外で上場する中国企業の監督管理を強化する計画を発表した。2021年7月6日に発表された“証券違法違反活動の厳しい取締りに関する意見”要求:
•データ安全、国境を越えたデータ流動と機密情報管理の監督管理を強化し、関連規定を改訂し、中国国外に上場する中国会社のデータ安全と情報安全方面の責任を明確にする
•海外上場企業に対する監督管理を強化し、海外上場会社の株式融資と上場に対する監督管理を強化する
•中国証券法の域外適用。
“証券違法行為への厳しい打撃に関する意見”が最近発表されているため,その解釈や実施には大きな不確実性がある。中国政府は関連法律、規則と法規を公布し、中国国外で上場している中国企業に追加と重大な義務と責任を適用し、データ安全、国境を越えたデータの流動と中国の証券法の遵守に関連することができる。これらの新しい法律、規則と法規とその解釈と実施が私たちにどのように影響するかどうかはまだ確定されていないが、その中には、私たちが中国国外で株式証券を発行することで外部融資を得る能力がマイナス影響を受ける可能性がある。
中国政府当局はいつでも私たちの業務に関与したり、影響したりする可能性があり、これは私たちの業務に重大な変化をもたらし、私たちのアメリカ預託証明書の価値に重大な悪影響を及ぼす可能性がある
中国政府は私たちの業務行為に対して重要な監督と裁量権を持っており、政府が適切だと思う場合に私たちの運営に介入したり、影響を与えたりして、規制、政治、社会目標をさらに実現する可能性がある。中国政府は最近、ある業界(例えば教育やインターネット業界)に重大な影響を与える新しい政策を発表したが、将来私たちの業界に関する法規や政策が発表されることを排除することはできず、中国当局の許可を求めて中国で業務を継続することが要求される可能性があり、これは私たちの業務、財務状況、経営業績に悪影響を与え、ADSの価値に悪影響を与え、その価値が大幅に低下する可能性がある。また、中国政府が最近発表した声明は、政府が中国で重要な業務を持っている会社の海外市場での発行と、私たちのように中国で業務を持っている発行者の外国投資の監督と制御を強化する意向があることを示している。中国政府がこのような行動をとると、中国が私たちの中国子会社に対して行動する可能性があり、顕著な制限、遅延、あるいは阻害を招く可能性がある 我々は、投資家に証券を提供または継続する能力、またはそのような証券価値の大幅な低下を招く能力を提供する。
あなたは法律手続きを履行したり、外国の判決を実行したり、中国で外国の法律に基づいて私たちまたは私たちの経営陣に訴訟を提起することが困難になるかもしれません。中国国外の監督管理機関やあなたも中国の調査や証拠収集が難しいかもしれません。
私たちはケイマン諸島の法律登録に基づいて設立された免除会社だ。私たちは中国で大量の業務を展開し、私たちの大量の資産も中国に位置している。また、私たちの多くの上級管理職や役員は中国内部に大きく住んでいますが、その中のいくつかは中国公民です。したがって、あなたは私たちや中国内部の人たちに法的手続き書類を送るのが難しいかもしれない。アメリカ連邦証券法に基づいて私たちとその上級管理者や取締役に対する民事責任条項がアメリカ裁判所で得られた判決をアメリカ裁判所で執行することも難しいかもしれません。また、ケイマン諸島や中国の裁判所が、米国または任意の州証券法の民事責任条項に基づいて米国の裁判所が下した我々またはそのような人々に対する判決を認めたり執行したりするかどうかにも、不確実性がある。
“中華人民共和国民事訴訟法”は外国判決の承認と執行について規定した。中国裁判所は“中華人民共和国民事訴訟法”の要求に基づいて、中国と判決所在国が締結した条約に基づいて、あるいは司法管轄区域間の対等原則に基づいて、外国判決を認め、執行することができる。中国と米国にはいかなる条約やその他の形式の書面もなく、外国の判決を相互に認め、執行することを規定している。また、“中華人民共和国民事訴訟法”によると、中国の裁判所が外国判決が中国の法律の基本原則や国家主権、安全または公共利益に違反していると判断した場合、中国裁判所は私たちまたは私たちの役員や高級職員に対して外国判決を執行しないだろう。したがって、中国の裁判所がどのような根拠で米国の裁判所が下した判決を執行するかどうかは定かではない。
あなたや中国以外の規制機関も中国を調査したり証拠を収集することが難しいかもしれません。例えば、中国の事件では、中国国外あるいは他の方法で外国実体に対して監督調査や訴訟を行うために必要な情報、文書、材料を得るためには、重大な法律やその他の障害が存在する。中国当局は他の国や地域の証券監督管理機関と規制協力メカニズムを構築し、国境を越えた監督管理を実施することができるが、相互かつ実務的な協力メカニズムが不足している場合には、このような米国証券監督管理機関との規制協力は効率的ではない可能性がある。また、2020年3月に施行された“中国証券法”第177条によると、中国国外の証券監督管理機関は中国国内で直接調査や証拠取得活動を行ってはならない。そのため、中国証券監督管理機関の主管部門と関係部門の同意を得ず、いかなる部門と個人も中国海外の各方面に証券業務活動に関する文書と資料を提供してはならない。第百七十七条に基づく規則の詳細な説明や実施はまだ公表されていないが、中国国外の証券監督機関は中国内部で直接調査や検証活動を行うことができず、自分の利益を保護する上での困難をさらに増加させる可能性がある。
私たちは制限されるかもしれないし、私たちの科学データを海外に移すことはできない。
2018年3月17日、中華人民共和国国務院弁公庁は“科学データ方法”を公布し、科学データに対して広義の定義を行い、科学データ管理の関連規則を制定した。“科学データ管理方法”によると、中国国内企業が国家秘密に関連する任意の科学データは、必ず政府の許可を得て、国外或いは外国側に移転することができる。また、少なくとも部分的に中国政府が援助した研究を行う研究者は、当該研究者が所属する実体の管理のために関連科学データを提出しなければならず、その後、いかなる外国の学術定期刊行物にもこのようなデータを発表することができる。現在,“国家秘密”という言葉は明確に定義されていないため,科学データ(我々が中国内部で行った臨床前研究や臨床試験の結果)を海外に送信したり,中国にいる外国のパートナーに送信したりする際には,常に承認を得ることは保証されていない。
もし私たちが適時に必要な承認を得ることができない場合、あるいは根本的にできなければ、候補製品の研究·開発が阻害される可能性があり、これは私たちの業務、経営業績、財務状況、見通しに実質的な悪影響を及ぼす可能性がある。関連政府当局が我々の科学データ転送が“科学データ措置”の要求に違反していると判断すれば、これらの政府当局の具体的な行政処罰を受ける可能性がある。
米国と国際貿易政策の変化、特に中国に関する政策変化は、我々の業務や経営業績に悪影響を及ぼす可能性がある。
アメリカ政府が最近発表した声明と取ったいくつかの行動は、いくつかの製造された製品に数回の関税を課すことを含む、アメリカと国際貿易政策の潜在的な変化を招く可能性がある
中国にいます。最近、中国と米国はそれぞれ関税を課しており、これはより多くの貿易障壁が出現する可能性があることを示している。新しい関税(または他の新しい法律や法規)が採用されるかどうか、新しい関税がどの程度採用されるか、またはそのような行動が私たちまたは私たちの産業にどのような影響を与えるかは不明だ。私たちが候補製品を商業化し始める時、いかなる不利な政府の国際貿易政策、例えば資本規制や関税は、私たちの薬品の需要、私たちの薬品の競争地位、科学者と他の研究開発者の採用、薬品開発に関連する原材料の輸出入、あるいはある国で私たちの薬品を販売することを阻止する可能性があります。任意の新しい関税、立法および/または法規が実施される場合、または既存の貿易協定が再交渉される場合、または特に米国政府が最近の米中国貿易緊張のために報復貿易行動をとる場合、これらの変化は私たちの業務、財務状況、および運営結果に悪影響を及ぼす可能性がある。
私たちが中国にある付属会社から受け取った配当金は中国の源泉徴収税を払わなければならないかもしれません。これは株主に支払う可能性のある配当金額に重大かつ不利な影響を与える可能性があります。
“中華人民共和国企業所得税法”は企業を住民企業と非住民企業に分ける。中国企業所得税法では、非住民投資家に支払う配当金(I)は中国に機関や営業地点が設立されていない、あるいは(Ii)中国に設立機関や営業地点があるが、関連収入は設立や営業地点と有効な関係がなく、このような配当金が中国国内から来ている限り、20%の所得税税率が適用されると規定されている。中国国務院は“中華人民共和国企業所得税法実施条例”によりこの税率を10%に引き下げた。また、香港と大陸部の二重租税回避手配によると、中国は (“二重租税回避手配”)、及び国家税務総局が2009年2月に発表した“租税条約配当規定の執行に関する若干の問題に関する通知” “二重租税回避手配”(“二重租税回避手配”)によると、例えば香港住民企業が中国から配当を取得する直前の12ケ月間に、いかなる時間にもこの会社が25%を超える持分を持っていれば、配当に関する10%源泉徴収項目は5%に減少し、しかし中国の関連税務機関は二重租税回避手配及びその他の中国法律下のいくつかの条件と規定に符合するかどうかを適宜決定することができる。
もし私たちの英領バージン島子会社と私たちの香港付属会社が非住民企業とみなされ、私たちの香港付属会社は二重租税回避手配によって香港住民企業とみなされ、中国主管税務機関によって関連条件と要求に符合すると認定された場合、その中国子会社が私たちに支払う香港付属会社の配当金は二重租税回避手配の下で5%の所得税税率に減額される可能性がある。しかし、“税務条約配当規定の執行に関する若干の問題に関する通知”によると、中国の関連税務機関が適宜認定すれば、会社は主に税収によって駆動される構造や手配から利益を受け、当該中国税務機関は税収優遇を調整することができる。また、2018年4月1日から発効した税収条約における実益所有者に関する問題に関する国家税務総局の公告によると、場合によっては、会社は条約下の実益所有者と定義することができず、二重租税回避手配の下で上記5%の減税所得税率を享受する権利がない。もし中国企業所得税法の規定に基づいて、吾らは吾らが中国付属会社から受け取った任意の配当について所得税を納めなければならない場合、あるいは中国政府当局が吾などの香港付属会社が主に税務駆動の構造や手配を受けて所得税税率を下げる利益を得たと認定した場合、私などが株主に支払う可能性のある配当金額(あればある)に重大な悪影響を与えることになる。
中国企業所得税法に基づいて吾等を中国の“住民企業”とすれば、吾ら及び吾等の非中国株主は不利な税務結果を負担しなければならない可能性があり、吾等の業務、財務状況及び経営業績は重大な悪影響を受ける可能性がある。
“中国企業所得税法”とその実施規則によると、中国国外に“事実上の管理機関”を設立した企業は“住民企業”とみなされ、その全世界の収入は25%の税率で企業所得税を納めることになる。実施細則は、“事実上の管理機関”を、企業の業務、生産、人員、会計、財産を全面的かつ実質的にコントロールし、全面的に管理する機関と定義する。2009年、国家税務総局は、海外に登録された中国制御企業の“事実上の管理機関”が中国に設置されているかどうかを決定するための特定の基準が規定されている“国家税務総局第82号通告”という通知を発表した。
本通知は、中国企業または中国企業グループによって制御されるオフショア企業にのみ適用され、中国または非中国個人によって制御されるオフショア企業には適用されないが、この通知で提出された基準は、“事実上の管理機関”テキストをどのように適用してすべての企業の税務住民の身分を決定するかに関する国家税務総局の一般的な立場を反映している可能性がある
オフショア企業。中国税務総局第82号通告によると、中国企業または中国企業グループがコントロールするオフショア登録企業は、その“事実上の管理機関”が中国に設置されているため、中国税務住民とみなされ、以下のすべての条件を満たす時にのみ、その全世界収入に従って中国企業所得税を納付する:(I)日常経営管理の主要な場所は中国にある;(Ii)当該企業の財務と人的資源事項に関する決定はすでに中国国内の組織或いは人員によって行われ、或いはその承認を経なければならない。(Iii)企業の主要資産、会計帳簿および記録、会社印鑑、および取締役会および株主決議は、中国に位置または保存されている;および(Iv)投票権を有する取締役会メンバーまたは上級管理者の少なくとも50%は、中国に常住している。
私らは、中国税務について言えば、当社は中国住民企業ではないと信じている。しかし、企業の税務住民身分は中国の税務機関の決定に依存し、“事実上の管理機関”という言葉に関する解釈には依然として不確定性がある。中国税務機関が企業所得税について吾などを中国住民企業と認定すれば、吾らは非住民企業株主(米国預託証明書所持者を含む)に支払われた配当金から10%の税金を源泉徴収することを要求される可能性がある。また、米国預託証明書または普通株を売却または処分する収益が中国国内からのものとみなされる場合、非住民企業株主(私たちの広告所持者を含む)は、10%の税率で中国税を納付しなければならない可能性がある。また、吾等が中国住民企業とみなされ、吾等の非中国個人株主(吾等の広告所持者を含む)に支払われた配当金と、当該等の株主が米国預託証明書又は普通株を譲渡して生じた任意の収益があれば、20%の税率で中国税を納付することができ、配当金については、当該等の配当金を源に控除することができる。どの中国の納税義務も適用された税金条約によって減少することができる。しかし、当社が中国住民企業とみなされていれば、当社の非中国株主がその税務居住国と中国との間のいかなる税務協定の利益を享受できるかどうかは不明である。このような税金は、私たちのアメリカ預託証明書または普通株に対する任意の投資収益を減少させる可能性がある。
“住民企業”分類の適用に不確実性があるほか、中国政府がより厳しい税収要件やより高い税率を適用するために、税収法律、規則、法規を改正または改正しないことを保証することはできません。このような変化は私たちの財務状況と経営結果に実質的な悪影響を及ぼす可能性がある。
政府の通貨両替の制御は、私たちが収入を有効に利用する能力を制限し、私たちのアメリカ預託証明書の価値に影響を与えるかもしれない。
中国政府は人民元の外貨両替を規制し、場合によっては中国の送金通貨に対して規制を実施している。私たちの現在の会社の構造の下で、私たちのケイマン諸島持株会社は私たちの中国子会社に配当金を支払い、将来可能な任意の現金と融資需要に資金を提供するかもしれません。中国の現行の外国為替法規によると、経常項目の支払いには、利益分配、利息支払い及び貿易やサービスに関する外国為替取引が含まれており、ある手続の要求に適合した場合には、外国為替局が事前に承認する必要がなく、外貨で支払うことができる。具体的には、既存の外国為替制限により、外管局の事前承認を受けていない場合には、我々が中国の中国子会社の運営により発生した現金をわが社への配当金の支払いに用いることが可能である。しかし、人民元を外貨に両替し、外貨建ての銀行ローンを返済するなど、中国から資本支出を送金するには、関係政府部門の承認や登録を受ける必要がある。そのため、私たちは外管局の許可を得たり、外管局の登録を完了したりして、私たちの中国子会社が運営している現金を使って人民元以外の通貨でそれぞれ中国以外の実体の債務を返済したり、人民元以外の通貨で中国以外の他の資本支出を支払うことができます。
最近中国が人民元が弱くなって大量の資本が流出したことを受けて、中国政府はより厳しい外国為替政策を実施し、海外直接投資を含む重大な対外資本流動の審査を強化した。外管局は、資本口座に属する国境を越えた取引を規制するために、より多くの制限と厳格な審査手続きを設定した。当社のように当該などの保険証書の監督管理を受けている株主は、適用された海外直接投資申告や承認規定にタイムリーまたは完全に適合できなかった場合、中国の関係当局の処罰を受ける可能性がある。中国政府は今後、経常口座取引の外貨使用を適宜制限することができる。もし外国為替規制システムが私たちの外貨需要を満たすのに十分な外貨を得ることを阻止すれば、私たちの株主に外貨配当金を支払うことができないかもしれません。
為替レートの変動は私たちの経営業績にマイナス影響を与える可能性があります。
人民元の米ドルやその他の通貨に対する価値は変動する可能性があり、中国の政治経済条件の変化や中国の外貨政策などの要素の影響を受ける可能性がある。2010年6月以来、人民元対ドルレートはずっと変動しており、変動幅が大きく、意外なこともある。2015年11月30日、IMF執行取締役会は、特別引出権を構成するバスケット通貨の5年間定期審査を完了した (“特別引出権”)は、2016年10月1日から人民元が自由に使用可能な通貨として決定され、ドル、ユーロ、円、ポンドとともに第5の通貨として特別引出権通貨バスケットに組み入れられることを決定した。2016年第4四半期以降、ドルの高騰と中国の資本流出を背景に、人民元は大幅に値下がりした。外国為替市場の発展、金利自由化と人民元国際化の進展に伴い、中国政府は将来さらなる為替制度改革を発表する可能性があり、将来人民元の対ドルレートが大幅に切り上げたり値下がりしたりしないことを保証することはできません。将来の市場力や中国や米国政府の政策が人民元の対ドルレートにどのように影響するかを予測することは難しい。
人民元の大幅な上昇は私たちの業務にマイナス影響を与える可能性がある。例えば、私たちの業務がドルを人民元に変換する必要がある程度では、人民元の対ドル高は私たちが転換から得た人民元金額に悪影響を与えるだろう。逆に、私たちが私たちの人民元をドルに両替し、私たちの普通株やアメリカ預託証明書の配当金や他の商業目的のために支払うことを決定すれば、ドルは人民元の上昇が私たちが利用できるドル金額にマイナス影響を与えるだろう。
中国が提供できるヘッジオプションは非常に限られており、為替レート変動への開放を減らすために非常に限られている。本年の日付まで、当社は外貨両替リスクを低減するためにいかなるヘッジ取引も行っていません。将来的にヘッジ取引を行うことになるかもしれませんが、これらのヘッジの可用性と有効性は制限される可能性があり、私たちは私たちのリスクを十分にヘッジできず、ヘッジすることさえできないかもしれません。また、私たちの通貨為替損失は中国の外貨規制規定によって拡大される可能性があり、これらの規定は人民元を外貨に両替する能力を制限しています。
中国住民と企業のオフショア投資活動に関する中国の規定は私たちの行政負担を増加させ、私たちのを制限するかもしれません 国境を越えた投資活動、中国国外での私たちの投資活動、そして私たちの中国での投資。もし吾らの中国住民や企業株主が当該等の法規に基づいて必要な申請や提出書類を提出できなければ、吾等は当該等の株主に利益を分配できない可能性があり、中国の法律に基づいて法的責任を負わなければならない可能性がある。
2014年7月、外匯局は“国内住民の海外投融資と特殊目的担体往復投資外貨管理に関する問題に関する通知”を発表した (“外匯局第37号通達”)は、“中国住民の海外特殊目的融資と往復投資外貨管理に関する問題に関する通知”(“外匯局第75号通達”)に代わっている。外管局第37号通達は、中国個人と中国法人実体を含む中国住民に、その直接或いは間接的なオフショア投資活動について外管局或いはその現地支店に登録することを要求した。外管局第37号通達は、中国住民の株主のために適用され、将来可能な任意の海外買収に適用される可能性がある。
外管局第37号通書によると、外管局37号通達が実施される前に、オフショア特殊目的担体に対して直接または間接投資を行っている中国住民 (“特殊目的機関”)は、外国為替局またはその現地支店にそのような投資を登録しなければならない。また、特殊目的機関である直接又は間接株主であるいかなる中国人住民も、基本情報又は重大事件の任意の変化を反映するために、外国為替局現地支店に当該特殊目的機関に関する登録を更新しなければならない。当該特殊目的会社のいずれかの中国住民株主が所定の登録又は更新登録を行うことができない場合、当該特殊目的会社の中国における子会社は、その利益又は減資、株式譲渡又は清算により得られた金を当該特殊目的会社に割り当てることを禁止することができ、当該特殊目的会社は、中国における子会社への追加出資を禁止することもできる。2015年2月、外国為替局は“直接投資外貨管理政策のさらなる簡略化と改善に関する通知”を発表した ("“外国為替局通知13”は、海外直接投資及び対外直接投資の外国為替登録申請は、“外国為替局第37号通知”の要求を含むものは、外国為替局ではなく、条件に適合する銀行に提出しなければならない。条件に適合する銀行は、外国為替局の監督の下で申請を審査し、登録を受理しなければならない。
私たちは私たちのすべての実益が人の身分を持っていることを知らないかもしれない。彼らはみんな中国の住民だ。私たちの知る限りでは、私たちの実益所有者の一部は、外管局第37号通告を守らなかった
その後の実行ルールが時間どおりまたはまったく実行されないのは,彼らが制御できないためである場合がある.しかし、私たちは私たちの実益をすべての人たちを統制することができず、外部管理局第37号通達と後続の施行規則を遵守するように強要することもできない。したがって、私たちはあなたに、外管局第37号通達といかなる修正案に基づいて要求された任意の登録が直ちに完了するか、または全く完成しないということを保証することができません。当社の中国住民実益所有者が外管局通告37及び後続実施規則に基づいてその外貨登録を登録又は改訂することができなかった場合や、当社の将来の中国住民実益所有者が外管局通告37及び後続実施規則に記載されている登録手続きを遵守できなかった場合、当該等の実益所有者又は吾等の中国付属会社に罰金及び法的制裁を科す可能性がある。関連規定を登録または遵守できなかったことも、中国子会社に追加資本を提供する能力を制限し、私たちの中国子会社が私たちに配当金を分配する能力を制限する可能性がある。
これらのリスクは私たちの業務、財務状況、そして経営結果に実質的な悪影響を及ぼすかもしれない。
また、これらの外国為替と対外投資に関連する法規とその解釈と実施は絶えず変化しているため、関連政府当局がこれらの法規をどのように解読、改訂、実施するか、未来の任意のオフショア或いは国境を越えた投資と取引に関する法規をどのように解読、改訂し、実施するかは不明である。例えば、私たちの外国為替活動に対して、配当送金や外貨借款など、より厳しい審査·承認を行うことができ、これは私たちの財務状況や経営業績に悪影響を及ぼす可能性があります。私たちはあなたに私たちが適用されるすべての外国為替と対外投資関連法規を遵守できるか、または遵守できるということを保証することはできません。また、中国国内の会社を買収することを決定した場合、私たちまたはその会社の所有者(場合によっては)が必要な承認を得たり、外国為替規制要件の必要な届出や登録を完了することができることを保証することはできません。これは私たちが買収戦略を実施する能力を制限し、私たちの業務や将来性に悪影響を及ぼす可能性がある。
中国の海外持株会社の中国実体に対する融資と直接投資の監督管理は、私たちの中国運営子会社への融資や追加出資を遅延または阻止する可能性がある。
私たちの中国運営付属会社であるオフショア持ち株会社として、吾らは私たちの中国付属会社に融資や追加出資を提供することができますが、適用される政府の登録と承認規定に適合しなければなりません。
私たちが私たちの中国子会社に発行したいかなるローンも、中国の法律によって外商投資企業とみなされ、法定限度額を超えてはならず、現地外国為替局に登録しなければならない。
私たちはまた出資方式で私たちの中国子会社に資金を提供することにしたかもしれない。中国の外商投資企業に関する規定によると、これらの出資は国家工商行政管理局あるいは現地の関係部門に登録しなければならない。また、中国政府は外貨の人民元への両替とその収益の使用を制限している。2015年3月30日、外匯局は“外商投資企業の外国為替資金決済管理方法の改革に関する通知”を発表した (“国家外国為替管理局第19号通知”)は、2015年6月1日から施行され、従来のいくつかの外管局規定に代わっている。外匯局はさらに、“資本項目の外貨決済管理政策の改革規範化に関する通知”を発表した 2016年6月9日に施行された“国家外国為替管理局第16号通知”(以下、“通知”と略称する)は、“国家外国為替管理局第19号通知”の若干の規定を改正した。“国家外国為替管理局第19号通知”及び“国家外国為替管理局第16号通知”によると、外商投資会社の外貨登録資本を人民元資本に換算した流動及び使用が規範化されており、業務範囲が別途許可されていない限り、人民元資本をその経営範囲を超えた業務に使用したり、関連側以外の他の人に融資を提供したりしてはならない。適用される通告や規則に違反すると、“外国為替管理条例”に規定されている巨額の罰金を含む厳しい処罰を受ける可能性がある。これらの通告は私たちが中国子会社に資金を移転する能力と速度を制限するかもしれない。2019年10月23日、外管局は“国境を越えた貿易投資の円滑化のさらなる利便化に関する通知”を発表した (“安全書簡28”)は、同日に施行される。外匯局第28号通知は、非投資性外商投資企業に対して資本金で国内株式投資を行う制限を撤廃することを通知した。非投資性外商投資企業が決済で取得した資本金で国内株式投資を行う場合、被投資先は規定に従って国内再投資登録手続きを行い、“資本口座--決済口座”を開設し、相応の資金を受け取るべきである。このような安全通達の制限と手続きの要求があるにもかかわらず、私たちの中国付属会社は外貨登録資本から両替した人民元資金を使用することができ、その正常な業務過程及び業務範囲内でいかなる活動を行うことができ、運営に資金を提供する必要があり、国内会社への株式投資を含む。
中国法規が海外持ち株会社の中国実体に対する融資と直接投資に対して提出した様々な要求を受けて、私たちはすでに必要な政府登録を完了し、関連する政府の要求を満たすことができるか、あるいは直ちに必要な政府の承認を得ることができるか、あるいは既存あるいは未来の私たちの中国子会社への融資または私たちの未来への出資を根本的に保証することができます
私たちの中国付属会社まで。もし吾等が当該等の登録を完了しなかった場合や当該等の承認を得られなかった場合、私たちが中国業務に資金を提供する能力はマイナスの影響を受ける可能性があり、これは私たちの流動資金及び業務に資金を提供し、業務を拡張する能力に重大な悪影響を与える可能性がある。
中華人民共和国従業員の持株計画又は株式オプション計画の登録又は届出要求に関する規定を遵守できなかった場合、計画参加者又は私たちは罰金及びその他の法律又は行政処罰に直面する可能性がある。
適用される法規と外管局の規則によると、中国公民は、中国国外で上場している上場企業の従業員の持株計画や株式オプション計画に参加するように、外管局に登録し、いくつかの他の手続きを完了しなければならない。2012年2月、外匯局は“国内個人が海外上場会社の株式激励計画に参加することに関する問題に関する通知”あるいは“株式オプション規則”を発表し、外為局が2007年3月に発表した“国内個人が海外上場会社の従業員の持株計画或いは株式オプション計画に参加する外国為替管理申請手続き”に代わった。株式オプション規則によると、中国住民が中国国外に上場する上場企業の任意の株式インセンティブ計画に参加するように、資格を有する中国国内代理店は、当該参加者を代表して外国為替局に申請を提出し、当該株式インセンティブ計画について安全に登録し、当該参加者が保有する株式又は株式の行使又は売却に関する外国為替購入について承認を受けなければならない。同等に参加した中国住民は、株式の売却や海外上場企業から派遣された配当金により得られた外貨収入は、当該等の参加者に分配される前に、中国が代理設立及び管理する中国集団外貨口座に全額振り込まなければならない。当社及び当社の株式オプション又はその他の株式に基づくインセンティブ措置を付与された中国住民従業員は、株式オプション規則を遵守しなければならない。しかし、私たちは私たちの中国人住民参加者を統制することができず、彼らに安全登録を守るように強要することもできない。
したがって、私たちはあなたに安全な登録項目の下の任意の必要な登録がタイムリーに完了するか、または全く完成しないということを保証することができません。もし私たちまたは私たちの中国住民参加者がこれらの規定を遵守できなかった場合、私たちおよび/または私たちの中国住民参加者は罰金と法的制裁を受ける可能性がある。また、安全登録を完了できなかったことは、私たちの中国住民参加者が私たちの持分インセンティブ計画に基づいてお金を支払うか、それに関連する配当金や販売収益を受け取る能力を制限するか、あるいは私たちが中国にいる外商独資企業に追加資本を注入する能力を制限し、私たちの外商独資企業が私たちに配当金を分配する能力を制限するかもしれない。私たちはまた規制面の不確実性に直面しており、これは中国の法律に基づいて私たちの役員や従業員のために追加の株式インセンティブ計画を実施する能力を制限するかもしれない。
また、国家税務総局は“簡政放権、放管結合、サービス最適化の若干の措置の更なる深化に関する通知”を発表し、市場主体の活力を育成と刺激した “通知”は2021年10月に発表され、株式(持分)激励計画を実施することを要求する企業は、持分激励を実施することを決定した翌月15日以内、或いは実施したがまだ完成していない持分激励計画に対して、海外企業従業員に持分激励を提供する国内企業を含み、2021年末までに主管税務機関に持分激励報告表などの材料を報告する。しかしながら、この通知は新たに発行されたため、その解釈および実際の実行には依然として大きな不確実性が存在する。したがって、私たちは、通知や他の規制によって要求される任意の登録または届出が直ちに完了するか、または完全に達成できないことを保証することができません。もし私たちまたは私たちの参加者がこのような規定を遵守できなかったら、私たちおよび/または私たちの参加者は罰金と他の法的制裁を受けるかもしれない。
中国の法律によると、中国国外で私たちの株式証券を発行するには、中国証監会や他の政府機関の承認や届出や他の手続きが必要となる可能性があり、必要であれば、このような承認を得るか、またはそのような届出や他の手続きを完了するのにどのくらいの時間がかかるかを予測することはできない。
2006年8月8日、中国証監会など6つの監督管理機関は“外国投資家の国内企業のM&Aに関する規定”を発表した 2006年9月8日に施行され、2009年6月22日に改正された(“M&A規則”)。 その他の事項を除いて、M&A規則は、中国国外で上場するために設立され、中国会社或いは個人がコントロールするオフショア特殊目的機関は、その証券が中国国外の証券取引所に上場する前に、中国証監会の許可を得なければならないと規定している。この規定の適用状況はまだ明確ではない。吾らの中国法律顧問はすでに吾らに、彼らの中国現行の法律に対する理解によると、私たちが初の公募を行う際に、M&A規則に基づいて中国証監会の承認を必要としない。私たちの中国付属会社の所有権構造は、M&A規則で定義された海外機関がどの中国国内会社の株式や資産を買収するのではなく、直接投資によって構築されているからである。しかし、中国の法律顧問は、中国の法律と法規の解釈と適用には不確実性があると教えてくれました
中国政府が最終的に我々の中国法律顧問の上記の意見に反しない観点をとることは保証されない
また、このほど発表された“証券違法行為の厳しい取締りに関する意見”は、中国で業務のある会社の海外上場に対する監督管理を強化し、“国務院の株式有限会社の海外発行上場に関する特別規定”の改正を規定していることを強調した。これらの意見の解釈と実行にはまだ不確実性があり、将来的にはこれらの意見についてさらなる解釈や細則が発表される可能性があり、これは私たちに追加的な要求をするかもしれない。
2023年2月17日、証監会は“国内会社の海外証券発行上場試行管理方法”(“海外上場試行方法”)を発表し、2023年3月31日から施行する。“海外上場試行方法”によると、(一)国内会社は直接或いは間接的に海外で株式証券を発行或いは上場し、届出手続きを履行し、そして中国証監会に関連情報を報告しなければならない。(二)海外企業が同時に次の2つの条件を満たす、海外での上場と上場は、国内会社の間接発行とみなされる:(一)海外会社の最近の会計年度に監査された総合財務諸表中の総合収入、利益、総資産または純資産の50%以上が国内会社に帰属し、(2)その業務の重要な構成要素が中国で行われ、その主要な営業場所が中国国内にある場合のうちの1つに適用される。あるいは経営管理を担当する高級管理者の多くは中国公民や住民である。(3)中国国内会社が中国国外市場で間接的に証券を発行·上場することを求めている場合、同社は主要な国内経営実体を指定して中国証監会へのすべての届出手続きを担当しなければならない。会社が株式の初公開または海外市場での上場を申請した場合は、申請してから3営業日以内に中国証監会に届出書類を提出しなければならない。発行者はその上場証券を発行する海外同一市場で後続発行を行う場合は、後続発行が完了してから3営業日以内に中国証監会に届出書類を提出しなければならない。中国国内の会社が届出手続きを完了していない、あるいは重大な事実を隠したり、届出書類の中で重要な内容を偽造したりした場合、改正、警告、罰金などの行政処罰を受ける可能性があり、その持株株主、実際のコントロール者、直接責任者、その他の直接責任者も警告、罰金などの行政処罰を受ける可能性がある。
しかし、“海外上場試行方法”は新しく公布されたため、“海外上場試行方法”の解読、適用と実行状況はまだ不明である今のところ確定していない海外で発売される当社の証券発行には試案が適用されますもし私たちの未来のいかなる後続発行あるいは任意の他の融資活動が海外上場試行方法に基づいて中国証監会に届出手続きを提出する必要があれば、私たちがこのなどの承認を得ることができるかどうか、あるいはそれなどの届出手続きを完成することができるかどうかはまだ確定していない。現段階で中国証監会の最新届出要求をめぐる重大な不確定性を考慮して、私たちはあなたに保証することはできません。私たちは適時に記録を完成し、関連する新しい規則を完全に守ることができます。
しかも、私たちはあなたに未来に公布されたどんな新しい規則や規定が私たちに追加的な要求をしないということを保証できません。もし未来に吾らの中国国外での発行に中国証監会或いは他の監督機関或いはその他の手続きの承認及び届出が必要であることを確定した場合、“ネットワークセキュリティ審査方法”及び“データセキュリティ条例草案”によるネットワークセキュリティ審査を含み、吾等が当該等の承認を取得するか又はどのくらいの時間を必要とするか又は当該等の届出手続きを完了するかは確定されず、いかなる当該等の承認又は届出は撤回又は拒否されることができる。例えば吾等が取得できなかったり遅延したりして吾等の中国国外での発売について当該等の承認を取得したり、当該等の届出手続きを完了したり、あるいは吾等がいかなる当該等の承認又は届出を取得しても撤回され、吾等は吾等の中国国外での発売について中国証監会の承認又は届出又は他の政府の許可を求めることができなかったため、中国証監会又は他の中国監督管理機関の制裁を受けることになる。これらの監督管理機関は、私たちの中国での業務に罰金と処罰を加え、私たちの中国以外の配当能力を制限し、私たちの中国での経営特権を制限し、私たちが中国国外で株式を発行して得られたお金を中国に送金することを延期または制限するか、あるいは私たちの業務、財務状況、経営業績と将来性、および私たちの上場証券の取引価格に大きな悪影響を与える可能性のある他の行動をとるかもしれない。
M&Aルールや他の中国法規は、非中国投資家が中国会社を買収するために複雑な手続きを設けており、これにより中国を買収することで成長を実現することが難しくなる可能性がある。
M&A規則及び合併と買収に関する関連法規と規則は追加の手続きと要求を確立し、非中国投資家の合併と買収活動を更に時間と複雑にする可能性がある。M&A規則は商務部に要求する 非中国投資家が中国国内企業のコントロール権変更取引を制御する、例えば(一)重要な業界に関連し、(二)国家経済安全に影響を与える可能性がある要素に関連する;あるいは(三)この取引は有名な商標或いは中国の老舗を持つ国内企業の制御権の変更を招き、事前に中国商務部に通知しなければならない(“商務部”)。中国企業又は住民が中国国外で設立又はコントロールしている会社が国内の関連会社を買収する場合は、商務部の承認を受けなければならない。
全人代常務委員会が公布した“独占禁止法” (“全国人民代表大会”)は2007年8月に改訂され、2022年6月に改訂され、2022年8月に施行された。独占禁止法は、いくつかのハードルがトリガされた場合、任意の合併、株式または資産買収、または契約または他の方法で(影響力を提供することを含む)支配権を獲得した場合、SAMRに事前に通知しなければならない。特定の出来高の敷居を持つ当事者に集中していると考えられる取引は,SAMRが清算しなければ完了しない。
また、商務部が2011年8月に発表した“海外投資家の国内企業M&Aに関する安全審査の実施細則”は、国家安全業界に関連する外国投資家のM&Aは商務部の厳格な審査を受けるべきであり、委託代理や契約制御による取引の手配を含む安全審査を迂回しようとする活動を禁止すべきであることを明らかにした。また、国家発展·改革委員会、商務部が2020年12月19日に発表した“外商投資安全審査方法”あるいは新しい安全審査方法に基づいて、外商投資安全審査作業メカニズムを構築し、外商投資安全審査業務を組織、調整、指導する。新設外商投資は新しい“安全審査方法”の規定条件に符合する場合、外国投資家或いは国内の関係者は審査工作機関に報告し、安全審査許可を取得した後に擬設外商投資を行うことができる。しかし、新たな安全審査措置が新たに発表されたため、その解釈や実践における実施には依然として大きな不確実性が存在する。将来、私たちは補完的な業務を買収することで私たちの業務を発展させるかもしれない。上述の条例とその他の関連規則の要求を遵守してこのような取引を達成するのは時間がかかる可能性があり、国家外国為替管理局、商務部或いは国家発改委或いはその地方対応機関の承認を得ることを含む任意の必要な承認手続きは、私たちがこのような取引を完了する能力を遅延或いは抑制する可能性がある。
商務省や他の政府機関が将来、私たちの理解とは逆の解釈を発表したり、このような安全審査の範囲を拡大したりする可能性を排除することはできませんが、この場合、今後の中国での買収は、ターゲットエンティティとの契約制御手配による買収を含め、密接に審査または禁止される可能性があります。私たちが将来買収を通じて事業を拡大したり、市場シェアを維持したり拡大したりする能力は、それによって実質的で不利な影響を受けるだろう。
私たちと私たちの株主は、中国住民企業の株式の間接譲渡、中国に帰属して設立された非中国会社の資産あるいは非中国会社が所有する中国にある不動産に関する不確定性に直面している。
2015年2月、国家税務総局は“非税住民企業の間接譲渡財産の若干の企業所得税問題に関する公告”を発表した (“SAT公告7”)。Sat公告7は、その税務管轄権を、オフショア譲渡外国中間持株会社による他の課税資産の移転に関する取引に拡大する。また、SAT公告7は合理的な商業目的を評価するために明確な基準を提供し、グループ内部の再編と公開証券市場を通じて株式を売買するために安全港を導入した。Sat公告7も課税資産の外国譲渡人や譲渡者(又は他に譲渡費用の支払いを義務付けられている者)に挑戦をもたらしている。2017年10月、国家税務総局は“国家税務総局の非住民企業所得税に関する源の事前提出に関する公告”を発表した (“衛星37号公報”)は、2017年12月1日から施行される。“37号公報”はさらに、非住民企業所得税の代理徴収のやり方と手順を明らかにした。非住民企業は持株会社の持分を処分することで間接的に課税資産を譲渡するものであり,間接譲渡に属するものであり,非住民企業は譲渡先,譲渡先あるいは直接課税資産を持つ中国単位として,関係税務機関に申告することができる。実質的に形式よりも重い原則によると、持ち株会社が中国国外に合理的なビジネス目的がなければ、設立の目的は
減税、租税回避、または中華人民共和国の税収を延期する目的。そのため、公開市場で売買されている米国預託証券株式を譲渡するほか、当該等の間接譲渡による収益は中国企業所得税を支払う必要がある可能性があるが、譲渡者又は譲渡金を支払う責任がある他の者は、適用された税金を源泉徴収する責任があり、現在10%の税率で中国住民企業の株式を譲渡している。譲渡先が税金を代理納付しておらず、譲渡先が税金を納めていない場合、譲渡側と譲り受け側はいずれも中国税法の処罰を受ける可能性がある。
私たちは、オフショア再編、私たちのオフショア子会社の株式の売却、投資のような、中国の課税資産の過去と未来の取引に関する報告およびその他の影響の不確実性に直面している。もし当社がこのような取引の譲渡先であれば、当社は申告義務や納税を負担するかもしれません。もし当社がこのような取引の譲渡先であれば、SAT公告7および/または公告37により、当社は源泉徴収義務を負うかもしれません。
PCAOBが2年連続で監査役を検査できない場合、HFCA法案によると、2022年5月4日に米国証券取引委員会によって委員会によって指定された発行者として決定されたため、我々の米国預託証明書が取得される可能性がある。私たちの証券が退市したり、私たちの証券が退市の脅威にさらされたりする可能性があり、あなたの投資価値に重大かつ不利な影響を与える可能性があります。また,PCAOBは検査を行うことができず,投資家がこのような検査から得た利点を奪っている。
米国上場企業の監査役及びPCAOBに登録されている会計士事務所として、2021年及び2020年度12月31日までの監査報告を発行する独立公認会計士事務所安永華明会計士事務所は、米国の法律に基づいてPCAOBの定期検査を受け、米国の法律及び専門基準に適合しているか否かを評価する。PCAOB検査は被検査会社の監査プログラムや品質制御プログラム中の欠陥を発見することができ、これらの欠陥は検査過程の一部として解決し、将来の監査品質を向上させることができる
近年、米国の立法者や規制機関は、新興市場に本部を置いたり、新興市場に大量の業務を持っている会社の関連リスクを懸念しており、中国を含む。特に,議員たちは独立監査師がPCAOB検査を受けられない会社が直面しているリスク増加を強調している。現在国家の法律で保護されている監査やその他の情報取得に対する米国の持続的な関心の一部として、2020年12月18日、米国の総裁は法律にする“高周波取引法案”に署名した。2021年11月5日、米国証券取引委員会は“外国会社責任追及法案”に基づいてPCAOB規則6100を承認し、取締役会の決定を決定した。ルール6100は、米国国外に位置する1つまたは複数の当局がとる立場のために、司法管轄区に位置する公認会計士事務所を検査または調査することができないかどうかを決定するための枠組みをPCAOBに提供する。2021年12月2日、米国証券取引委員会は“高頻度取引法案”を実施する最終規則を採択した
2021年12月16日、PCAOB規則6100によって構築された枠組みに基づいて、PCAOBは地方当局の職位の原因により、大陸部と香港に本部を置くPCAOB公認会計士事務所中国を完全に検査または調査できないことを決定する報告書を発表した中国監査委員会の検査が不足しているため、監査委員会は中国に設置された独立監査会社の監査と品質制御プログラムを定期的に評価することができない PCAOB検査の監査員よりも,PCAOBが監査員を検査できなければ,このような監査員の監査プログラムや品質制御プログラムの有効性を評価することは困難である。 そのため、投資家はその監査師がPCAOB検査を受けない発行者報告の財務情報と手順及び財務諸表の品質に対する自信が低い可能性がある。
HFCA法案は、米国以外の司法管轄区域当局が適用した制限により、完全に検査または調査できない米国証券取引委員会にその監査報告が監査役によって用意された米国上場企業リストを識別し、維持することを要求する。HFCA法案はまた、米国証券取引委員会が識別した上場企業(I)に文書を提出し、その会社がPCAOB検査を制限する司法管轄区域内の政府実体によって所有または制御されていないことを証明し、(Ii)その米国証券取引委員会届出書類の中でPCAOBがその監査会社を検査できないという事実について何らかの追加開示を行う。米国以外の司法管区の政府実体が会社の株式の割合を保有しているか否か、米国以外の司法管区の政府実体が会社に対して持株権を有しているか否か、会社取締役会のいずれかの中国共産党メンバーの氏名、及び会社の組織文書(いずれかのこのような定款のテキストを含む)に中国共産党規約が含まれているか否か。HFCA法案は当初、発行者が3年連続で米国証券取引委員会が確認した会社のリストにとどまることを規定していた
同社は米国の全国的な証券取引所、例えばナスダックの世界的な精選市場、あるいは米国の場外取引市場での取引を禁止する
2022年12月29日、総裁·バイデンは“2023年総合支出法案”に署名した, 他の事項に加えて、同法案は、発行者が米国証券取引委員会が発行者の証券に対して初期取引禁止を実施しなければならないまで、証監会が指定した発行者と連続して識別される年数を3年から2年に減少させる“証券取引委員会法案”を改正した。そのため、発行者が2年連続で証監会指定の発行者として決定されると、米国証券取引委員会は“高頻度取引法案”の規定に基づき、発行者の証券の国家証券取引所と場外取引市場での取引を禁止しなければならない。
2022年8月26日、PCAOBは中国証券監督管理委員会と人民財政部Republic of Chinaと“議定書声明”に署名し、PCAOBを開放して大陸部と香港に本部を置く公認会計士事務所の検査と調査に第一歩を踏み出した。“議定書声明”はPCAOBにその検査と調査の事務所、監査活動および潜在的な違反行為を選択する完全な自由裁量権を与え、PCAOB検査員と調査者がすべての情報を含む完全な監査作業の底稿を確認し、PCAOBに必要に応じて情報を保持させるための手続きを制定した。さらに、“コンシェルジュ声明”は、PCAOBがPCAOBの検査または調査の監査に関連するすべての者と直接面談し、彼らの証言を聞くことを可能にする。2022年12月15日、PCAOBは“米国法典”第15章7214(I)(2)(A)条とPCAOB規則6100に基づいてHFCAA認定報告を発表し、PCAOBの裁定を撤回した、すなわち国内の関係当局の職位のため、中国大陸部と香港に本部を置く完全登録会計士事務所を検査または調査することができなかった。これらの裁決を撤回すると同時に、PCAOBは、中国大陸部または香港のどの当局が取った立場により、中国大陸部または香港の監査師に対して検査や調査を行う際にいかなる障害に遭遇した場合、PCAOBは直ちに行動し、HFCA法案とPCAOB規則6100に適合した新しい裁決を発表する必要があるかどうかを再考すると指摘している。
私たちの監査役は2021年12月31日と2020年度12月31日までの安永華明法律事務所独立公認会計士事務所であり、本年度報告書に含まれる2021年12月31日現在の会計監査報告書を発表した。PCAOBは安永華明会計士事務所がPCAOBが全面的に検査や調査できない公認会計士事務所の一つであることを確認し、2022年5月4日に最終的に“委員会認定発行者”に決定した。我々の監査委員会(I)は、2022年5月3日、安永華明法律事務所が当社の独立公認会計士事務所を辞任することを決定し、2022年6月1日から当社が米国証券取引委員会に提出した財務諸表を監査·財務報告内部統制し、2013年12月31日までの財政年度の当社財務諸表監査と財務報告内部統制の独立公認会計士事務所の招聘を承認した。本年度報告書には2022が含まれており,当社はその後安永法律事務所と招聘状を締結している。しかし、安永法律事務所と協力することで、私たちが“委員会が認める発行元”ではなくなる保証はありません
安永法律事務所は依然としてPCAOBの任意の検査または調査要求に応じて任意の監査作業の原稿を提供することができ、PCAOBの検査または調査要求時にPCAOBに任意の関連する監査者を提供することができなければならない。安永法律事務所はPCAOB検査や調査要求に関するいかなる法律または専門義務を履行できなかったか、あるいは安永法律事務所がすべての適用された監査基準を遵守できなかったことは、私たちが重大な責任を負うことになったり、HFCA法案によって私たちの証券が外されたりする可能性がある。
HFCA法案の公布および米国監督管理機関の中国監査情報の取得を増加させるための任意の追加ルール制定努力の影響は、私たちを含む影響を受けたアメリカ証券取引委員会登録者に投資家の不確実性をもたらす可能性があり、私たちのアメリカ預託証明書の市場価格は重大な悪影響を受ける可能性がある。伝説生物が依然として米国証券取引委員会が認定した会社である限り、伝説生物が“高周波取引法案”と“高周波取引法案”の要求に応えるためのいかなる行動にも、伝説生物が追加の法律、会計、その他の費用を招く可能性があり、これは巨額である可能性がある。
私たちの業務は新たに公布された“外商投資法”と“ネガティブリスト”の大きな影響を受ける可能性がある
2019年3月15日、全国人民代表大会は“外商投資法”を発表し、2020年1月1日から施行され、中国の現行の3部の外商投資を規範化する法律に取って代わった。外商投資法は外商投資主体に中国国内主体と同等の待遇を与えるが、国務院が公表した“ネガティブリスト”で制限または禁止と認定されている業界を経営する外商投資主体は除外する。私たちはケイマン諸島持株会社で、私たちの中国子会社の南京聯想と海南聯想は現在
外商投資実体。伝説的海南は2021年10月に設立された。本年報の日付では、連想海南は中国で実質業務に従事していない。
商務部、発改委が発表した最新版“ネガティブリスト”、すなわち“外商投資参入特別管理措置(ネガティブリスト)(2021年)”または“ネガティブリスト”は、2022年1月1日から施行される。ネガティブリストは、外国がヒト幹細胞或いは遺伝子診断と治療技術の開発と応用を禁止することを規定している。
本年度報告が発表された日まで,ネガティブリストに記載されている“ヒト幹細胞や遺伝子診断と治療技術”の範囲は公式には説明されておらず,この規定の適用状況は不明である。商務部と国家発改委が発表した“2022年外商投資奨励産業目録(2022年)”(“2022年奨励産業目録”)は2023年1月1日から施行され、その中で、外商投資を禁止する領域以外に、外商投資細胞治療薬物の開発と生産を奨励することが規定されている。また,2021年12月3日,CDEは“遺伝子治療製品非臨床研究と評価技術ガイドライン(試行)”(“遺伝子治療製品技術ガイドライン”)と“遺伝子修飾細胞治療製品非臨床研究技術ガイドライン(試行)”(“遺伝子修飾細胞治療製品技術ガイドライン”)を発表し,発表日から施行した。“遺伝子治療製品技術ガイドライン”の規定は、遺伝子組換え細胞治療製品以外の遺伝子治療製品に適用し、CAR-T細胞治療製品などの遺伝子組換え細胞治療製品は“細胞治療製品研究と評価技術ガイドライン(試行)”によって制定された“遺伝子修飾細胞治療製品技術ガイドライン”を参照すべきである。
連想南京はCAR-T細胞療法の研究開発に従事している。南京連想は現在開発中のCAR-T細胞療法は、ヒト幹細胞或いは遺伝子診断と治療に関連していないため、ネガティブリスト下の“ヒト幹細胞或いは遺伝子診断と治療技術”のクラスに属するべきではないと考えている。また、関連政府部門は、南京連想が現在従事しているCAR-T細胞療法の研究開発が外商投資産業政策の要求に符合することを実証した。著者らは中国法律顧問君と法律事務所から、南京レノボホールディングスはCAR-T細胞療法の研究開発においてすでにすべての重要な方面で中国の法律法規を遵守し、そしてすでに中国監督管理機関のすべての重大な政府の許可と許可を得たことを知った。しかし、吾らはすでに吾らの中国法律顧問から、中国の法律及び法規の解釈及び応用について不確定要素が存在し、中国政府が最終的に吾等の観点及び吾等の中国法律顧問の上記の意見に反しない観点をとることを保証することはできないと伝えている。我々のいずれかの中国子会社が研究·開発しているCAR-T細胞療法または他の技術が、中国関連規制機関によってネガティブリスト下の“ヒト幹細胞または遺伝子診断および治療技術”のカテゴリーに属するとみなされた場合、中国子会社は、このようなCAR-T細胞療法または他の技術の研究または開発に従事することを禁止される。この場合、私たちは中国子会社への投資をやめなければならないかもしれないし、私たちの中国子会社を中国国内実体と私たちの可変権益実体に再編することを考えなければならないかもしれない。我々の中国子会社もこのような技術の研究や開発から得られた収入を没収せざるを得ない可能性がある。これらのすべての状況は私たちの業務、将来性、財務状況、そして経営結果に重大な損害を与える可能性がある。
私たちの賃貸物件の権益に欠陥があるかもしれません。私たちの賃貸物件の権利は挑戦されるかもしれません。これは私たちの業務に重大な妨害を与えるかもしれません。私たちのレンタル契約が登録されていないので、私たちは罰金を科されるかもしれない。
中国では、私たちは第三者から私たちが運営するためのいくつかの場所を借りた。すべてのレンタル者が私たちの賃貸物件に有効な所有権証明書や転貸許可を提供できることを保証することはできません。中国の関連法律及び法規によると、レンタル人が当該等の物件が不正に建設された場合や検査やその他の原因で業権証明書を取得できなかった場合、当該等の賃貸契約は無効とみなされる可能性があるため、吾等は関連物件の転出を要求される可能性がある。また、もし私たちのレンタル者が物件の所有者ではなく、彼らが所有者またはそのレンタル者の同意を得なければ、私たちのレンタル契約は無効になる可能性があります。このような状況が発生した場合、私たちは所有者または賃貸物件を所有する権利のある当事者と賃貸契約を再交渉する必要があるかもしれませんが、新しい賃貸契約の条項は私たちにあまり有利ではないかもしれません。あるいは新しい賃貸契約の条項が達成されていない場合、関連物件を空ける必要があるかもしれません
中国の法律によると、すべての賃貸契約は現地の住宅当局に登録されなければならない。私たちはまだ関連政府部門に私たちのいくつかのレンタル協定を登録していない。これらの要求の登録を完了できなかったことは、私たちの大家さん、レンタル人、そして私たちを潜在的な罰金に直面させるかもしれません。
労働コストの増加や中国のより厳しい労働法律·法規の施行は、私たちの業務や私たちの収益性に悪影響を及ぼす可能性がある。
近年、中国全体の経済と中国の平均賃金水準は向上しており、引き続き増加することが予想される。近年、私たち従業員の平均賃金水準も向上している。私たちは賃金と従業員福祉を含めて私たちの労働コストが増加し続けると予想する。
また,従業員との労働契約,指定政府機関への年金,住宅積立金,医療保険,労災保険,失業保険,生育保険など様々な法定従業員福祉についても,より厳しい規制要求を受けている。社会保険の納付や住宅積立金の納付義務に関する法律法規を含めて、労働に関するすべての法律法規を遵守しているか、または遵守できることを保証することはできません。私たちは適用された中国法規の要求に従って私たちのすべての従業員の住宅積立金を全額支払っていません。私たちは従業員の供給を補充することを要求されるかもしれません。私たちの財務状況と経営業績は不利な影響を受けるかもしれません
私たちのアメリカ預託証明書の市場価格と私たちの業務はアメリカ商務部の実体リストの重大な影響を受けるかもしれません。
2021年12月16日米国商務省工業·安全保障局 国際清算銀行(“国際清算銀行”)は、米国以外の特定の人(企業、研究機関、政府および民間組織、個人および他のタイプの法人を含む)のリストを含む40エントリの37個のエンティティをそのエンティティリストに追加する最終ルールを発表し、これらの人は、特定の物品の輸出、再輸出および/または譲渡の特定の許可要件によって制約される。米国商務省が2021年12月16日に発表したプレスリリースによると、国際清算銀行の行動は“中華人民共和国が軍事応用のためのバイオテクノロジーやその他の技術の開発と配備に努力し、人権を侵害する努力が米国の国家安全と外交政策にとって持続的な脅威となる”ことをある程度解決するためである。国際清算銀行の最終規則に基づいてエンティティリストに追加された40個のエントリのうち、34個は中国に位置し、その中の12個はバイオテクノロジーエンティティ(すなわち、1つのバイオテクノロジーエンティティ及びその11個の研究機関)である。私たちは国際清算銀行の行動によって解決を求めるいかなる活動にも参加しないと考えているが、私たちが将来実体リストに登録されない保証はない。
中国と米国の関係が悪化すれば、私たちの業務、経営業績、財務状況は不利な影響を受ける可能性がある。
近年、米国と中国は通貨、経済、政治、環境、社会などの問題で何度も重大な相違が発生しており、将来的に両国関係が悪化する可能性がある。政治条件の変化や中国と米国の関係状況の変化は予測困難であり、我々の業務、経営業績、財務状況に悪影響を及ぼす可能性がある。政治的または貿易関係のどんな悪化も私たちの業務を損なう可能性がある。中国とアメリカの関係のいかなる変化が米国と中国で資金を獲得したり、効率的に業務を展開する能力にどのような影響を与える可能性があるかは予測できません。
また、米国と中国の間のいかなる政治的あるいは貿易紛争も、私たちの業務と直接関連しているかどうかにかかわらず、投資家が私たちのアメリカ預託証明書を保有したり購入したりすることを招き、それによって私たちのアメリカ預託証明書の取引価格の下落を招く可能性がある。さらに、中国は通貨、経済、政治、環境、または社会問題において任意のより厳しい規則または規定を採用しており、特に米国関係に関連する問題では、私たちの業務、財務状況、または将来性を損なう可能性がある。
私たちの組織構造に関連するリスクは
我々は適用されるナスダック上場規則が指す“制御された会社”であるため、ある会社の管理要求を遵守する資格を免除する資格がある。もし私たちがこのような免除に依存し続ける場合、あなたはこのような要求に制約された会社の株主に同じ保護を受けることができないだろう。
Genscriptは2022年12月31日現在,我々が発行した普通株の大部分の投票権を支配している.したがって、私たちはナスダック上場規則が指す“制御された会社”を適用する。これらの規則によると、役員選挙の投票権の50%以上が個人、グループ、または他の会社が保有する会社は“制御された会社”である。私たちがまだ“制御された会社”である限り、私たちは以下の要求を含むいくつかの会社の管理要求を守らないことを選択することができます
•取締役会の多くは独立役員で構成されている
•指名委員会、会社管理委員会、報酬委員会の年間業績評価を行った
•私たちには指名と会社管理委員会があり、完全に書面の定款を持つ独立役員で構成されている
•委員会の趣旨と責任を処理する;
•私たちは完全に独立した役員で構成された報酬委員会を持ち、その委員会の目的と責任を述べた書面規約を作成した。
私たちはこの免除を使用して、私たちは未来にこのような免除のすべてまたは一部を使用し続けるつもりだ。したがって、ナスダックのすべての会社の管理要求に制約されている会社の株主に対しては、同じ保護を受けることができないかもしれません。
GenScripは私たちのかなりの割合の普通株式を保有し続け、株主の承認が必要な事項に大きな制御を加えることができるだろう。
GenScripは現在私たちの大株主で、私たちの取締役会のメンバー10人のうち3人がGenscriptの従業員です。したがって,Genscriptはこの所有権の地位によって我々に大きな影響を与え,大きな制御を加えることができる.例えば、Genscriptおよびその株主は、株式インセンティブ計画に従って私たちの従業員に株式を発行すること、私たちの組織ファイルを修正すること、または任意の合併、合併、資産の売却、または他の重大な会社取引を承認することを含む取締役選挙、株式発行を制御することができるかもしれない。GenScripの利益はいつも私たちの会社の利益や他の株主の利益と一致していないかもしれません。それはあなたが同意しないかもしれない方法でその投票権と他の権利を行使することができますか、または私たちの他の株主の最適な利益に合わないかもしれません。また,Genscriptの管理層や所有権が変化する可能性があり,我々の会社の利益や他の株主の利益に合わないようにGenscriptの利益に影響を与える可能性がある.Genscriptが私たちの大量の株式を保有し続ける限り、それは私たちの決定を強力に影響し、効果的に制御し続けるだろう。
私たちの組織と所有権構造は重大な利益衝突をもたらすかもしれない。
私たちの組織と所有権構造は多くの関係に関連しており、これらの関係は、私たちと私たちの米国預託証明の少数株主との間のいくつかの利益の衝突を招く可能性があり、一方、Genscriptとその株主との間の利益の衝突を引き起こす可能性があります。我々の取締役や従業員の一部はGenscriptの株式を持っているため,彼らの利益はGenscriptの利益と一致する可能性があり,つねに我々の会社の利益や我々の他の株主の利益と一致しているわけではないかもしれない.さらに、当社の他の株主は、当社の取締役や役員のGenscript所有権を見ることができないかもしれませんが、この所有権は、買収、処置、希釈、または他の方法によって随時変化する可能性があります。私たちの役員や上級管理職の所有権のどんな変化もこのような所有者の利益に影響を及ぼす可能性があります。
また,Genscriptのある係り先とプロトコルする側である.GenScripとその株主は、私たちのいくつかの役員と従業員を含み、私たちまたは私たちの普通株主の少数株主の利益とは異なる利益を持っている可能性があります。GenscriptまたはGenscriptの任意の他の子会社との間の任意の重大な取引は、事前に監査委員会の承認を得ることを要求する関連側取引ポリシーに準拠します。もし私たちがこのような利益衝突を適切に処理できなければ、私たちの名声と追加資金を調達する能力、および取引相手が私たちとビジネスをする意欲にマイナスの影響を与える可能性があり、これらはすべて私たちの業務、財務状況、運営結果、およびキャッシュフローに悪影響を及ぼす可能性がある。 Genscriptの関連先とのプロトコルのさらなる情報については,“項目7-大株主と関連側取引”を参照されたい.
上場企業の結果として、コストが発生しており、追加コストが発生し続けることが予想され、内部制御プログラムやコーポレートガバナンス構造を遵守できない可能性があります。
上場企業として、私たちに課せられた要求を守るために、私たちが民間会社として発生していない巨額の法律、保険、会計、その他の費用を負担し続ける予定です。増加した費用は私たちが業務の他の分野でコストを下げる必要があるかもしれない。しかも、私たちの取締役会、管理職、そして行政者たちは追加的な任務を遂行する必要がある。例えば、私たちは、証券法に規定されている義務に基づいて、定期的に公開されている報告書を作成·配布するすべての内部·外部コストを負担する。私たちは、変化する法律、法規、基準を遵守するために資源に投資し続けるつもりです。このような投資は一般的かつ行政費用の増加を招き、管理職の時間と注意を分散させる可能性があります
研究と開発活動から利益を得る。これらの法律、条例、基準はしばしば異なる解釈があり、多くの場合、特殊性が不足しているため、規制機関と理事機関が新しい指導意見を提供するにつれて、それらの実践における適用は時間の経過とともに変化する可能性がある。これは、コンプライアンス事項、法執行手続きの持続的な不確実性、および開示およびガバナンス慣行を継続的に修正するために必要なより高いコストをもたらす可能性があり、これは、私たちの業務、財務状況、運営結果、および将来性に重大な悪影響を及ぼす可能性がある。
私たちは外国の個人発行者として資格があるので、米国の委託書ルールの制約を受けず、米国内の上場企業の報告よりも詳細で頻繁ではないことを許容する“取引法”の報告義務に制約されています。
我々は現在、取引法に基づいて報告されており、外国の個人発行者の地位を持つ非米国会社である。私たちは“取引法”に規定されている外国の個人発行者の資格に適合しているため、(I)“取引法”に基づいて登録された証券募集依頼書、同意書、または許可の条項を含む“取引法”に適用される米国国内上場企業に適用されるいくつかの条項の制約を受けない。(I)“取引法”では、株式所有権および取引活動に関する公開報告書の提出を内部者に要求する条項、および短時間で取引から利益を得る内部者の責任、(Iii)“取引法”に規定された規則は、監査されていない財務及び他の指定された情報を含むForm 10-Q四半期報告を提出するか、又は指定された重大なイベントが発生した場合に現在のForm 8-K報告を提出するように米国証券取引委員会に要求する。また、外国人個人発行者は、各事業年度終了後120日までにForm 20−F年次報告書を提出する必要はなく、加速提出者である米国内発行者は、各事業年度終了後75日以内にForm 10−K年次報告書を提出することが要求される。
外国の個人発行者もFD規定の制約を受けず、発行者が重大な情報を選択的に開示することを防止することを目的としている。上記の理由により、外国のプライベート発行者ではない株主に提供される同等の保護が得られない可能性がある。
もし私たちが外国の個人発行者の地位を失ったら、私たちは外国の個人発行者の要求よりも詳細で広い米国内発行者の要求に適用される“取引法”報告書や他のアメリカ国内発行者の要求を遵守することが要求されるだろう。私たちはまたアメリカ証券取引委員会とナスダックの様々な規則に基づいて私たちの会社のガバナンスのやり方を変えることを要求されるかもしれません。米国証券法によると、米国内の発行者に適用される報告書の要求を遵守することが要求されれば、私たちが直面している規制やコンプライアンスコストは、外国の個人発行者として発生するコストよりもはるかに高くなる可能性がある。したがって、私たちは外国の個人発行者の地位を失うことは、私たちの法律と財務コンプライアンスコストを増加させ、いくつかの活動を非常に時間的で高価にするだろうと予想している。また、米国国内発行者に適用される規制を遵守することが要求されれば、取締役や上級管理者責任保険を獲得することがより困難かつ高価になり、低減された保証範囲の受け入れや大幅な保証コストの発生が要求される可能性があると予想される。このような規制はまた私たちが合格した取締役会のメンバーを引き付けて維持することをもっと難しくするかもしれない。
外国の個人発行者として、私たちは会社の管理問題にいくつかのナスダック会社の上場基準とは大きく異なる母国のやり方を採用することを許可された。我々がナスダック社の上場基準を完全に遵守している場合に比べて、これらのやり方は株主の保護が少ない可能性がある。
私たちは私たちが特定の会社統治事項でケイマン諸島の会社法に従うことを可能にするナスダック社の管理規則の条項に依存する権利がある。これにより、ナスダックに上場している米国企業に適用されるコーポレートガバナンス要件とは大きく異なるいくつかのコーポレートガバナンス実践に従うことができる。例えば、私たちの母国ケイマン諸島のコーポレートガバナンス実践は、私たちの取締役会の大多数のメンバーが独立取締役で構成されることを要求しているわけではなく、指名やコーポレートガバナンス委員会を実施する必要もありません。現在、私たちの取締役会は大多数の独立取締役で構成されており、指名と会社管理委員会がありますが、もし私たちが外国の個人発行者免除に依存すれば、私たちの取締役会の大部分は独立取締役で構成されていない可能性がありますので、より少ない取締役会メンバーが独立した判断を行使し、取締役会のわが社の経営陣に対する監督レベルが低下する可能性があります。
ケイマン諸島の法律で規定されている株主権利は米国の法律規定とは異なるため、あなたは自分の株主権利を保護することが困難かもしれません。
私たちはケイマン諸島の法律登録に基づいて設立された株式会社です。当社の会社事務は、当社の組織定款大綱及び細則、ケイマン諸島会社法(改正)及びケイマン諸島一般法によって管轄されています。ケイマン諸島法律によると、株主が私たちの役員に対して行動する権利、私たちの小株主の行動、そして私たちの役員の私たちの受託責任はケイマン諸島普通法の管轄を大きく受けています。ケイマン諸島の一般法の一部は,ケイマン諸島の比較的限られた司法判例およびイングランドの一般法に由来しており,イングランド裁判所の裁決はケイマン諸島の裁判所に説得力があるが,拘束力はない。私たちの株主の権利とケイマン諸島の法律の下での私たちの役員の受託責任はアメリカのある司法管轄区域の法規や司法前例のように明確ではありません。特に、ケイマン諸島の証券法システムはアメリカほど発達していない。ケイマン諸島と比較して、米国のいくつかの州、例えばデラウェア州は、より完全な会社法機関と司法解釈を持っている。また、ケイマン諸島会社は米連邦裁判所で株主派生訴訟を起こす資格がないかもしれない。
ケイマン諸島免除会社の株主、例えば、ケイマン諸島法律によれば、一般的な権利は、会社の記録(これらの会社が採択した組織定款大綱及び定款細則及び任意の特別決議、並びにこれらの会社の担保及び担保登録簿を除く)又は株主リストの写しを取得する権利がない。ケイマン諸島会社登録処部長は、任意の人が費用を払った後に調べるために、当社の現取締役(及び(適用される)当社の現取締役候補)のリストを提供しなければなりません。我々の上場後のメモと組織規約の細則によると、私たちの取締役は私たちの株主がどのような条件でわが社の記録を閲覧できるかを決定する権利がありますが、これらの記録を私たちの株主に提供する義務はありません。これは、株主が発議するために必要な任意の事実を決定するために、または依頼書競争について他の株主に依頼書を募集するために必要な情報を得ることを困難にする可能性がある。
ケイマン諸島のある会社のガバナンスのやり方は、米国などの他の管轄区に登録されている会社への要求とは大きく異なる。外国の個人発行者として、私たちはナスダック上場規則に基づくいくつかの企業統治事項で母国のやり方に従うことを許可された。現在、私たちはどの会社の統治問題でも母国の接近に依存するつもりはない。しかし、もし私たちが未来に自国のやり方に従うことを選択すれば、私たちの株主が獲得した保護は、アメリカ国内の発行者に適用される規則や法規を下回る可能性がある。
上記の理由により、我々の経営陣、取締役会メンバー、または我々の持株株主がとる行動に対して、公衆株主が自分の利益を保護することの難しさは、米国に登録されている会社またはナスダック社のガバナンス規則に完全に拘束されている会社である公衆株主よりも難しい可能性がある。ケイマン諸島会社法(改正された)の規定と、米国で登録設立された会社及びその株主に適用される法律との間の重大な違いに関する議論は、本年度報告書に従って提出された添付ファイル2.5を参照されたい。
私たちが改訂して再記述した組織定款大綱や定款細則の条項は、私たちの株主が私たちの経営陣を交代しようとしていることを阻止または挫折させ、私たちの持株権獲得の努力を阻害する可能性があり、したがって、私たちのアメリカ預託証明書の市場価格はより低くなる可能性がある。
私たちの組織定款大綱や定款細則には、あなたや他の株主が支配権の変更が有利だと思っていても、第三者がわが社の支配権を獲得したり買収しようとすることは難しいという規定があります。例えば、私たちの取締役会は、優先株を含む可能性がある最大1,000,000株の追加カテゴリの株を発行する権利があります。取締役会は、他のカテゴリの株式の価格、権利、特典、特権、および制限を決定することができ、私たちの株主がさらに投票したり、行動したりする必要はありません。このような株の発行は支配権変更取引を延期または阻止する可能性がある。したがって、私たちのアメリカ預託証明書の市場価格と私たちの株主の投票権と他の権利は不利な影響を受ける可能性がある。他の種類の株を発行することは、他の株主が議決権制御権を失う可能性がある。
私たちの定款には、反買収の効力を持つ可能性のある他の条項も含まれています
•私たちの3種類の役員のうち、毎年1種類だけが選挙で生まれています
•株主は理由がある場合にのみ取締役を罷免する権利がある
•株主は書面の同意の下で行動してはならない
•株主は事前に指名役員に通知したり、年次株主総会の審議のために提案を提出しなければならない。
これらの規定は潜在的な買収提案を阻害する可能性があり、制御権変更取引を延期または阻止する可能性がある。これらは、あなたの最大の利益に合致する可能性のある取引を含む、他の人の買収要約を阻止する効果もあるかもしれません。これらの条項はまた、私たちの経営陣の変動を阻止したり、投資家が私たちのアメリカ預託証明書に支払う価格を制限したりする可能性があります。
追加資本を調達することは、私たちの所有者に希釈をもたらし、私たちの運営を制限するか、または私たちの技術または候補製品に対する権利を放棄することを要求するかもしれない。
将来的には,臨床試験,商業化努力,研究·開発活動の拡大,上場企業の運営に関するコストなど,我々の計画運営を継続するために多くの追加資本が必要となる可能性が予想される。これまで、私たちが相当な製品収入を生み出すことができれば、私たちは証券発行、債務融資、協力と許可協定、研究支出の任意のまたは組み合わせを通じて、私たちの現金需要を満たす予定です。もし私たちが証券を発行することで資金を調達すれば、このような売却はまた私たちの既存の株主の重大な希釈を招く可能性があり、新しい投資家は私たちのアメリカ預託証明書または普通株式保有者よりも優先的な権利、優遇、特権を得ることができる。
もし私たちが株式または転換可能な債務証券を売却することで追加資本を調達すれば、私たちのアメリカ預託証明書の保有者は希釈され、これらの証券の条項は清算または他の私たちの株主権利に悪影響を及ぼす特典を含む可能性がある。債務融資および優先持分融資(実行可能であれば)は、固定支払義務をもたらす可能性があり、追加債務を発生させる能力を制限する条項を受け入れることを要求される可能性があり、特定の流動性または他の比率を維持させたり、配当金の支払いを制限したり、買収する能力を制限したりすることができる。
もし私たちが第三者との協力、戦略連合またはマーケティング、流通または許可手配を通じてより多くの資金を調達する場合、私たちは、私たちの技術、将来の収入源、研究計画、または候補製品に対する貴重な権利を放棄するか、または私たちに不利になる可能性のある条項でライセンスを付与することを要求されるかもしれない。さらに、私たちはまた、より早い段階で協力者や他の人との手配を通じて資金を求めることを要求されるかもしれない。そうでなければ望ましい。もし私たちが研究支出を通じて資金を調達すれば、私たちはいくつかの要求によって制限されるかもしれません。これは私たちが資金を使用する能力を制限したり、研究開発情報を共有することを要求するかもしれません。もし私たちが必要な時に株式や債務融資を通じてより多くの資金を調達できない場合、私たちは私たちの製品開発や将来の商業化努力の延期、制限、減少、または将来の商業化努力の延期、制限、または第三者開発とマーケティングのより自分で開発とマーケティングを望む候補製品の権利を与えることを要求されるかもしれない。これらまたは他の任意の方法で追加資本を調達することは、私たちの業務および私たちの株主の持株または権利に悪影響を及ぼす可能性があり、私たちの米国預託証明書の市場価格の下落を招く可能性がある。
私たちの証券に関するリスクは
私たちのアメリカ預託証明書の取引価格は変動するかもしれません。
私たちのアメリカ預託証明書の取引価格はずっと高度に変動し続ける可能性があり、様々な要素の広範な変動を受ける可能性があり、その中のいくつかの要素は取引量が限られていることを含む制御できない。一般的な株式市場,特にバイオ製薬会社の市場は極端な変動を経験しており,この変動は特定の会社の経営業績とは無関係であることが多い。このような変動により、投資家はその米国預託証明書を米国預託証明書またはそれより高い価格で売ることができない可能性がある。“リスク要因”の節と本年度報告の他の部分的に議論された要因に加えて、これらの要因には、以下のような要因が含まれる
•CARVYKTIの製造と商業化
•私たちの計画と将来の臨床試験の開始、登録、または結果
•私たち、協力者、または競争相手のテストおよび臨床試験の陽性または陰性結果または遅延;
•重要な科学者や管理職を失ってしまいました
•アメリカ、中国などの国の規制や法律の発展状況
•競争力のある製品や技術の成功
•規制当局が私たちの臨床試験や製造業者に取った不利な行動
•私たちの候補製品および臨床前計画に適用される法律または法規の変化または発展
•医療支払い制度の構造を変え
•協力者や製造業者やサプライヤーとの関係を変えます
•私たちの候補製品やCAR-T細胞の安全性への懸念
•私たちの競争相手や製薬業界全体の発表について
•経営業績の実際または予想変動
•証券アナリストの財務推定や提案を変更する
•潜在的な買収、融資、協力、または他の会社の取引
•私たちは他の候補製品の結果を発見、開発、取得、または許可するために努力している
•私たちのアメリカ預託証券のナスダックでの取引量は
•私たち、私たちの上級管理職のメンバーと取締役、または私たちの株主は、私たちのアメリカ預託証明書または普通株を売却したり、将来このような売却が起こる可能性があることを期待しています
•米国や中国の経済、政治、市場状況、金融市場の全体的な変動
•比較可能な会社、特にバイオ製薬業界で経営している会社の株式市場価格と取引量が変動している
•私たちと私たちのビジネスに対する投資家の一般的な見方は
•他の事件と要素、その多くは私たちがコントロールできない。
これらと他の市場と業界要素は、私たちのアメリカ預託証明書の市場価格と需要を大幅に変動させる可能性があり、私たちの実際の経営業績にかかわらず、これは投資家がアメリカ預託証明書に支払う価格でそのアメリカ預託証明書を販売することを制限または阻止し、他の方法で私たちのアメリカ預託証明書の流動性に負の影響を与える可能性がある。また,株式市場,特にバイオ製薬会社は,極端な価格や出来高変動を経験しており,これらの変動はこれらの会社の経営業績に関係なくあるいは比例しないことが多い。
一部の株式取引価格が変動している会社は証券集団訴訟の対象となっている。私たちは一方としてのいかなる訴訟も、正当な理由の有無にかかわらず、不利な判決を招く可能性がある。私たちはまた不利な条件で訴訟を解決することに決定するかもしれない。
このような負の結果は、巨額の損害賠償または罰金の支払い、私たちの名声を損なう、または私たちのビジネス慣行に悪影響を及ぼす可能性があります。訴訟を弁護するためには高価で時間がかかり、私たちの管理職の関心と私たちの資源を分散させるかもしれない。さらに、訴訟過程において、公聴会、動議、または他の一時的な手続きまたは事態の発展を否定的に発表する結果がある可能性があり、これは、我々の米国預託証明書の市場価格に負の影響を与える可能性がある。
私たちの業務が良好であっても、私たちの普通株やアメリカ預託証明書を大量に売却することは、私たちのアメリカ預託証明書の市場価格を大幅に低下させる可能性がある。
私たちの大量の普通株式やアメリカ預託証明書はいつでも公開市場で販売される可能性があります。もし私たちの株主が公開市場で私たちの普通株やアメリカ預託証明書を大量に売却したり、市場が私たちの株主が私たちの普通株やアメリカ預託証明書を売却しようとしていると思っていれば、私たちのアメリカ預託証券の市場価格は大幅に低下する可能性があります。
さらに、いくつかの普通株式所有者またはその譲受人は、いくつかの条件に適合する場合には、その株式をカバーする1つまたは複数の登録声明(または提出すれば有効である)を提出するか、またはその株式を自己または他の株主のために提出することができる登録声明に組み込む権利がある。これらの株式は転売登録されると、公開市場で自由に販売することができる。これらの追加株式が公開市場で販売されている場合、またはそれらが売却されると考えられている場合、私たちの米国預託証明書の取引価格が低下する可能性がある。
私たちのアメリカ預託証明書の保有者は私たちの株主よりも少ない権利を持っており、彼らの権利は信託機関を通じて行使されなければならない。
当社の米国預託証券保有者は当社の株主と同じ権利を持っておらず、預金契約の規定に基づいて関連する普通株に対する投票権のみを行使することができます。米国預託証券保有者は、米国預託証明書に代表される普通株式に付随する投票権を行使するために、受託管理人またはその代名人をその代表とする。株主総会が開催されたとき、閣下がアメリカ預託証明書を開催すれば、閣下が閣下のアメリカ預託証明書に関する普通株を撤回することを許可し、閣下がいかなる特定事項に投票するかを許可するために、閣下は十分な株主総会の通知を受けないかもしれません。私たちはすべての商業的に合理的な努力を尽くして、信託銀行が適時にアメリカ預託株式保有者に投票権を拡張させることを促進しますが、アメリカ預託株式保有者が適時に投票材料を受け取り、信託銀行に投票を指示することを保証することはできません。そして、米国預託株式保有者または仲介人、取引業者、または他の第三者を通じて米国預託証明書を持っている人は投票権を行使する機会がないかもしれません。さらに、保管人は、いかなる採決指示、いかなる採決方法、または任意のそのような採決を実行できなかった効果に対しても責任を負わないであろう。したがって,我々の米国預託証明書保持者は彼らの投票権を行使できない可能性があり,そのような米国預託証明書がその保持者の要求に応じて投票しなければ,追徴権がない可能性がある.また、米国預託株式の保有者は株主総会を開催することができない。
米国預託証明書保持者は預金協定に基づいて提出されたクレームについて陪審裁判を行う権利がない可能性があり、これはどのような訴訟においても原告に不利な結果を暗示している可能性がある。
吾等の株式を代表する米国預託証明書を管理する預金協定では、米国預託証明書の所有者及び実益所有者は、預金協定、吾等の株式又は米国預託証明書又はそれによって行われる取引(連邦証券法により提出された請求を含む)により生じる又は関連する任意の法律手続において、法律を適用することが許容される最大範囲内で吾等又は委託者に対して陪審裁判を行う権利を放棄することができない。もしこの陪審裁判免除条項が法律で禁止されている場合、訴訟は依然として陪審裁判の預金協定の条項によって行われることができる。私たちが知っている限り、連邦証券法によると、陪審裁判の免除の実行可能性はまだ連邦裁判所によって最終的に裁かれていない。しかしながら、預金協定を管轄するニューヨーク州法律によれば、通常、預金協定の下で生じる事項に対して非排他的管轄権を有する陪審員免審条項がニューヨーク州裁判所またはニューヨーク州連邦裁判所によって強制的に執行されることができると信じており、このような法律が適用される。陪審裁判免除条項を執行するかどうかを決定する時、ニューヨーク裁判所と連邦裁判所は、一方の当事者が陪審員裁判によって裁判される権利を故意に放棄するために、陪審裁判免除条項の可視性が十分に突出しているかどうかを考慮するであろう。私らは、預金協定、吾等の株式及び米国預託証明書及びそれに基づいて行われる取引はいずれもそうであると信じている。さらに、ニューヨーク裁判所は、実行可能な相殺または反クレームが詐欺または債権者の不注意に基づく担保が保証者の要求に基づいて担保を清算することができなかったように聞こえることを阻止するために、陪審裁判免除条項を強制的に執行することはなく、または故意に権利侵害クレームを請求した場合(契約紛争に対して)、これらは預金協定、私たちの株式または米国預託証明書、またはそれによって予想される取引には適用されないと考えられる。預金協定又は米国預託証明書のいかなる条件、規定又は規定は、米国預託証明書を構成するいかなる所有者又は実益所有者又はわれわれ又は信託機関が連邦証券法のいかなる規定を遵守することを放棄しない。もし米国預託証明書の所持者又は実益所有者が預金契約、吾等の株式又は米国預託証明書又はそれに基づいて行う取引について吾等又は受託保管人に申索を提出する場合、当該所持者又は実益所有者は当該等の申立索について陪審裁判を行う権利がない可能性があり、これは吾等及び/又は受託保管者に対する訴訟を制限及び阻止することができる。預金協定に基づいて私たちおよび/または委託者に訴訟を提起する場合、適用される初審裁判所の裁判官または裁判官によってのみ審理される場合、これは、異なる民事手続きに従って行われ、任意のこのような訴訟において原告に不利になる可能性のある結果を含む陪審裁判とは異なる結果を示唆する可能性があり、具体的には、クレームの性質、そのようなクレームを審理する裁判官または裁判官、および聴聞場所に依存する。
米国預託証明書所有者に普通株式を提供することが違法または非現実的である場合、米国預託証明書所有者は、そのような米国預託証明書に代表される普通株の割り当てまたはその任意の価値を取得することができない。
私たちは現在、普通配当金を発表または支払いする計画はありませんが、もし私たちがいかなる配当金を発表して支払う場合、アメリカ預託証明書の受託者は、私たちの普通株式または他の預金証券から受け取った現金配当金または他の分配をアメリカ預託証明書所持者に支払うことに同意し、その費用と費用を差し引くことに同意しました。アメリカ預託証明書保持者は、そのアメリカ預託証明書に代表される私たちの普通株式数の割合でこれらの分配を獲得します。しかし、預金協定に規定されている制限により、米国預託証明書保持者に流通を提供することは不法または非現実的である可能性がある。このような分配によって得られた米国預託証券、普通株、または他の証券の発行を米国証券法に基づいて登録する義務はない。私たちはまた、米国預託証明書、普通株式、権利、または他の何かを米国預託証明書保持者に割り当てることを可能にする他の行動を取る義務はない。これはアメリカの預託証明書の所有者が普通株式や何も受け取っていないかもしれないということを意味します
それらをこれらの所有者に提供することが不正または非現実的であれば、これらの所有者から価値を得ることができる。このような制限はアメリカの預託証明書の価値に悪影響を及ぼすかもしれない。
米国預託株式保有者が将来の任意の株式発行に参加する権利が制限される可能性があり、これにより、保有者の持分が希釈される可能性がある。
私たちは時々私たちの証券を購入する権利を含めて私たちの株主に権利を割り当てるかもしれない。しかし、1933年の証券法(“証券法”)下の権利や権利関連証券を登録しない限り、米国の米国預託株式保有者に権利を提供することはできません。また、預金契約によれば、口座開設銀行は、権利およびどの関連証券が証券法に基づいて登録されているか、またはこれらの権利および任意の関連証券を米国預託株式保有者に配布して証券法による登録を免れない限り、米国預託株式保有者に権利を提供しない。私たちはこのような権利や証券について登録声明を提出する義務がないし、その登録声明を発効させるために努力する義務はない。しかも、私たちは証券法に基づいて登録免除を確立することができないかもしれない。保管人が権利を割り当てない場合、保管者プロトコルに従って、それは可能な場合にこれらの権利を販売することができ、またはこれらの権利の失効を許可することができる。そのため、米国預託証明書保持者は私たちの株式発行に参加できず、希釈に遭遇する可能性がある。
私たちは予測可能な未来に私たちのアメリカ預託証明書や普通株に現金配当金を支払わないと予想されているので、資本付加価値(あれば)は私たちのアメリカ預託証明書と普通株式保有者の唯一の収益源になり、これらの保有者は決して彼らの投資から見返りを得ないかもしれない。
私たちは過去に普通株の配当金を発表したり支払ったりしたことがありません。現在、私たちは私たちの未来の収益を維持するつもりで、もしあれば、私たちの業務の発展と成長に資金を提供します。したがって、私たちの普通株式とアメリカ預託証明書の保有者はこれらの証券への投資に依存して配当収入を提供してはいけない。当社の取締役会は完全な情動権を持って配当金を派遣するかどうかを決定しますが、ケイマン諸島の法律のある制限を受けなければなりません。すなわち、当社は利益または当社の株式割増帳内の信用からのみ配当金を支払うことができ、常に規定しています。いずれの場合も、当社が正常な業務過程で満期になった債務を支払うことができない場合、当社は配当金を支払うことができません。また、私たちの組織規約の大綱と定款の細則によると、私たちの株主は一般決議を通じて配当を発表することができますが、いかなる配当も私たちの取締役会が提案した金額を超えてはいけません。私たちの取締役会が配当金を発表して支払うことを決定しても、将来の配当の時間、金額、形式(あれば)は、私たちの将来の経営業績とキャッシュフロー、私たちの資本要求と黒字、私たちが子会社から得た割り当て金額(あれば)、私たちの財務状況、契約制限、取締役会が関連していると思う他の要素に依存します。したがって、私たちのアメリカ預託証明書と普通株の資本付加価値(あれば)は、これらの証券保有者の予測可能な未来における唯一の収益源となる。このような要素は私たちのアメリカ預託証明書の価値を損なうかもしれない。
もし私たちが受動的な外国投資会社に分類されたり、受動的な外国投資会社に分類されたりすれば、私たちのアメリカの株主はしたがって不利な税金結果を受ける可能性がある。
一般的に、任意の納税年度において、私たちの総収入の少なくとも75%が受動的収入である場合、または私たちの資産価値の少なくとも50%が、受動的収入を生成するための資産または現金を含む受動的収入を生成するために保有する資産に起因することができる場合、米国連邦所得税目的のための受動的外国投資会社(“PFIC”)と同定される。これらのテストについては、受動的収入には、配当金、商品および証券取引の利息収益、受動的収入を生じる資産処分の収益が損失を超える部分(一時投資による株式発行で調達された資金から得られた金額を含む)、および貿易または業務を積極的に展開することに関連する関係者から受信された賃貸料および特許権使用料以外のレンタル料および特許権使用料が含まれる。私たちがPFICと同定された場合、私たちのアメリカ株主は、資本収益ではなく、私たちの普通株式またはアメリカ預託証明書を売却する実現収益を一般収入とすること、米国保有者が私たちの普通株式またはアメリカ預託証明書から受け取った配当金に適した優遇率を失うこと、および私たちの株式または米国預託証明書を分配して販売する収益に対して利息費用を受け取ることを含む不利な税金結果を受ける可能性がある。
個人資産投資会社としての私たちの地位は、私たちの収入の性質と構成と、私たちの資産の性質、構成と価値に依存します(これは各資産の公正な市場価値によって決定されるかもしれません。営業権価値と持続的な経営価値は、私たちのアメリカ預託証明書の市場価値を参考にして決定されているかもしれません。これは不安定かもしれません)。私たちの地位はまた、私たちが業務で初めて公募株、後続発行、その他の資金調達活動を利用して得られた現金の速度にある程度依存するかもしれません。私たちの運営履歴と私たちの収入構成と資産推定値によると、営業権を含めて、2022年12月31日までの納税年度がPFICだとは思いません。国税局が私たちの結論に同意する保証はなく、国税局が私たちの立場に挑戦することに成功しない保証もない。どの課税年度にもPFICかどうかを決めるのは事実だからです
個々の課税年度終了後に毎年決定される決定は,いずれの課税年度においても,本課税年度を含めてPFICとみなされるか否かは保証されない。したがって,我々の米国法律顧問は,2022年12月31日までの納税年度のPFIC地位については何の意見も発表せず,本納税年度や将来の納税年度のPFIC地位の期待にも何の意見も発表しない。
私たちがPFICに分類されれば、適用される税収結果も、上述した米国の株主が有効な適格選挙基金(“QEC”)選挙を行うことができれば税収結果とは異なるだろう。現在、米国の株主にQEC選挙を行うために必要な情報は米国の株主に提供されない見通しだ。潜在的な投資家たちはQEC選挙が行われないと仮定しなければならない。
米国人が米国預託証明書に代表される普通株を含む少なくとも10%の普通株式を所有しているとみなされた場合、その保有者は不利な米国連邦所得税の結果の影響を受ける可能性がある。
Genscriptは私たちの50%以上の株式を所有しており、1つ以上のアメリカ会社の50%以上の株式を持っているため、私たちと私たちのいくつかの非米国子会社は、米国連邦所得税目的の“制御された外国企業”とみなされる可能性があります。米国の株主(以下“重大な所得税考慮事項--米国連邦所得税考慮事項”参照)が、米国預託証明書代表の普通株式を含む少なくとも10%の普通株式価値または投票権を有する(直接、間接的、または建設的)とみなされる場合、米国所有者は、私たちおよびそれが制御対象とされている外国会社の各非米国子会社に対する“米国株主”とみなされる可能性がある。制御された外国会社の米国株主は、米国の課税収入に比例して割り当てられた“F支部収入”、“世界無形低税収入”、および制御された外国会社の米国財産への投資を毎年報告することを要求される可能性があり、その制御された外国会社がいかなる分配を行っているかにかかわらず、さらに、制御された外国会社の株式を売却または交換することで収益を実現する米国の株主は、資本収益ではなく、そのような収益の一部を配当収入に分類することを要求される可能性がある。支配された外国企業の場合、米国の株主である個人は通常、何らかの減税や外国税収控除を受けることは許されず、米国会社の米国株主はそうすることを許可される。上記の報告書や納税義務を遵守するために必要となる可能性のある情報をどの米国の株主にも提供する保証はありません。これらの申告義務を守らないと巨額の罰金に直面する可能性があり、申告すべき年度のアメリカ連邦所得税申告書の訴訟時効を阻止する可能性があります。アメリカの保有者は彼らの税務顧問に相談して、これらの規則が私たちのアメリカ預託証明書への投資における潜在的な応用を理解しなければならない。
将来の税法の変化はわが社に実質的な悪影響を与え、わが株主の純利益を減少させる可能性がある。
会社の税務処理は、税務法律、法規、条約の変化やその解釈、考慮されている税収政策の取り組みと改革、および私たちの管轄区域の税務機関のやり方の影響を受けています。我々が事業を展開している多くの国では、経済協力開発機構(OECD)の税ベース侵食と利益移転プロジェクト、Shift、プロジェクト、欧州委員会の国家援助調査、その他の取り組みなど、税法が改正されることが予想される。このような変動は、限定される訳ではないが、営業収入、投資収入、受信された配当金、または(特定の源泉徴収の場合)支払いに対する配当課税を含むことができる。OECDは、基数侵食と利益移転プロジェクトの産物として、顧客所在地に応じて大型多国籍企業の全世界利益を市場司法管轄区に再分配することと、世界最低税率を導入することを含む一連の改革措置を公表した。一括計画の多くの提案された措置は、異なる司法管轄区の国内税収立法を改正する必要がある。米国では、“2022年インフレ率低減法案”は他の規定を除いて、ある大企業の帳簿収入に15%の最低税率を徴収し、ある会社の株式買い戻しに1%の消費税を徴収する。将来どのような税制改革が提案され、公布されるか、あるいはこれらの変化が私たちの業務にどのような影響を与えるかは予測できませんが、これらの変化は、それらが税収立法、法規、政策または実践に組み込まれていれば、私たちの財務状況および私たちが業務を展開している国の将来の全体的または有効な税率に影響を与え、私たちの株主の税引後リターンを減少させ、税務コンプライアンスの複雑さ、負担、コストを増加させる可能性があります。
税務機関はいくつかの税収に対する私たちの立場と結論に同意しない可能性があり、それによって意外なコスト、税収、あるいは予想された利益を達成できない可能性がある。
税務機関は私たちが取った税金の立場に同意しないかもしれないが、これは税金負担の増加を招くかもしれない。例えば、アメリカ国税局や他の税務機関は、私たちの会社間の手配と私たちの関連会社との間の税収分配に基づいて、私たちの収入分配に疑問を提起し、
譲渡定価政策は、私たちの知的財産権開発に関する支払い金額を含む。同様に、税務当局は、私たちが課税関係が確立されていないと考えている司法管轄区域で納税し、国際税務条約によると、このような関連は一般に“常設機関”と呼ばれ、成功すれば、この断言が1つ以上の司法管轄区での予想納税義務を増加させる可能性があると断言することができる。税務機関は私たちが重大な所得税債務、利息、罰金を支払うべきだと思うかもしれないが、この場合、私たちはこの評価に異議を唱える可能性があると予想される。このような評価に異議を唱えるには長い時間とコストがかかる可能性があり,評価に異議を唱えることが成功しなければ,その影響は適用された場合に予想される実際の税率を上げる可能性がある.
株式研究アナリストが私たち、私たちの業務、または私たちの市場に不利な研究や報告を発表すれば、私たちのアメリカ預託証明書の価格と取引量が低下する可能性がある。
私たちのアメリカ預託証券の取引市場は、株式研究アナリストが発表した私たちと私たちの業務に関する研究と報告の影響を受けるだろう。私たちはアナリストや彼らの報告書に含まれている内容と意見に対して何の統制権もない。1つ以上の株式研究アナリストが私たちのアメリカ預託証券格付けを引き下げたり、私たちに不利な他のコメントや研究を発表したりすれば、私たちのアメリカ預託証券の価格が低下する可能性がある。1つ以上の株式研究アナリストが私たちの報告書を停止したり、私たちに関する報告書を定期的に発表できなかった場合、私たちのアメリカ預託証明書に対する需要が減少する可能性があり、これは逆に私たちのアメリカ預託証明書の取引価格や取引量を低下させる可能性がある。
米国預託証明書所持者はその米国預託証明書を譲渡する際に制限される可能性がある。
あなたのアメリカ預託証明書は預かり人の帳簿に譲渡することができます。しかしながら、いずれの場合も、適用される米国証券法を遵守することを前提として、受託者は、職責を履行する誠意のために、または私たちの合理的な書面要求の下で、必要または適切であると考えられる場合には、その譲渡帳簿を随時または時々閉鎖することができる。さらに、私たちの帳簿または委託者の帳簿が閉鎖されたとき、または法律または任意の政府または政府機関の任意の要求、または預金協定の任意の規定または任意の他の理由によって、いつでもそうすることが望ましいと考えられる場合、受託者は、米国預託証明書の交付、譲渡または登録を拒否することができる。
私たちは証券訴訟の影響を受けるかもしれませんが、これは高価で、経営陣の注意をそらすかもしれません。
我々の米国預託証券の市場価格は変動している可能性があり、過去に株式市場価格の変動を経験した会社は証券集団訴訟の影響を受けたことがある。私たちは未来にこのような訴訟の目標になるかもしれない。私たちに対する証券訴訟は巨額のコストを招き、私たちの経営陣の注意を他の業務から移す可能性があり、これは私たちの業務を深刻に損なう可能性があります。
項目4.会社に関する情報
A.会社の歴史と発展
私たちの法定名称はレノボバイオテクノロジー会社で、私たちの商業名はレノボバイオテクノロジー会社です。当社は二零一五年五月二十七日にケイマン諸島で免除会社に登録され、ケイマン諸島会社法により有限責任を負います。レノボ生物科学技術はケイマン諸島持株会社であり、中国運営会社ではない。私たちは主にアメリカ、中国、EUにある運営子会社を通じて運営しています。私たちの中国での業務と、私たちの世界の他の場所での業務は、私たちがそこに設立した子会社によって支援されています。
次の図は、当社の親会社ケイマン諸島ホールディングス、子会社、合併の付属実体を含む今年度の報告日までの当社の構造を示しています
私たちの主な実行事務室はニュージャージー州サマーセット郡綿尾巷2101号にあります。郵便番号:08873、電話番号は(737)3175050です。当社の登録先はハニス信託(ケイマン)有限会社、4これは…。ケイマン諸島大ケイマン諸島KY 1-1002号郵便ポスト10240号教会南街103番地ハーバーズスクエア1階です。私たちのアメリカでのプロセスサービス代理はニュージャージー州サマーセット郡綿尾巷2101号レノボ生物科学技術会社の最高経営責任者黄穎博士、郵便番号:08873です
2022年、2021年、2020年12月31日までの年間、私たちの資本支出はそれぞれ7,030万ドル、4,450万ドル、5,000万ドルです。このような支出は主に不動産、工場と設備、そして無形資産を含む。研究開発計画の推進と事業拡大に伴い、私たちの資本支出は短期的に絶対値が増加すると予想されます。私たちは2023年の資本支出が私たちの手元の現金と現金同等物から来ると予想している。これらの資本支出は主にアメリカ、EU、中国で行われ、私たちの主要な製造と研究開発施設は現在これらの地域に位置している。
SECは,SECに電子的に提出されたレポート,依頼書,情報宣言,その他の発行者に関する情報を含み,www.sec.gov上でアクセス可能なサイトを保持している.私たちはwww.LegendBiotech.comで会社のサイトを維持している。当社または他のサイトに掲載されているか、または本サイトから取得可能な資料は、本年度報告の一部を構成していません。
B.業務の概要
われわれは主に世界的な臨床段階生物製薬会社であり,腫瘍学や他の適応の新しい細胞療法の発見,開発,製造,商業化に取り組んでいる。私たちはアメリカ、中国、ヨーロッパに約1,390人の従業員を持っており、私たちは差別化された技術、世界的な開発と製造戦略、専門知識が、需要を満たしていない適応に対する次世代細胞療法を産生、テスト、製造する能力を提供してくれた。我々の主要候補製品ciltalabagene autolucelあるいはcilta−cel(我々のLegend−2試験ではlcar−B 38 Mと呼ぶ)は,我々が戦略パートナーであるJanssenと共同開発した多発性骨髄腫(MM)の治療のためのCAR−T細胞療法である。これまでに得られた臨床試験の結果
Cilta-celは再発性と難治性多発性骨髄腫(“RRMM”)患者に深度と持続性の抗腫瘍反応を提供する潜在力があり、しかも安全性が制御可能であることを証明した。
2022年2月28日、Cilta-celは、プロテアソーム阻害剤、免疫調節剤、および抗CD 38モノクロナル抗体を含む4つ以上の治療を受けたCARVYKTI商標で米国食品医薬品局(FDA)によって許可された再発または難治性多発性骨髄腫の成人患者の治療に使用された。CARVYKTIの米国での発売を支援するために、販売、マーケティング、運営インフラを構築しました。2022年5月25日、欧州委員会は、プロテアソーム阻害剤(PI)、免疫調節剤(IMiD)、および抗CD 38抗体を含むRRMMを有する成人を治療するためのCARVYKTIの条件付きマーケティング許可を承認し、最後の治療において疾患の進行を示した。2022年9月26日、厚生労働省は、成人再発性または難治性多発性骨髄腫の治療のためのCARVYKTIの使用を許可し、B細胞成熟抗原(BCMA)に対するCAR陽性T細胞注入療法を有さない患者、および免疫調節剤、プロテアソーム阻害剤および抗CD 38モノクロナル抗体を含む3つ以上の治療を受けた患者、および多発性骨髄腫は最近の治療後に反応または再発しない、の2つの条件を満たす患者に限定される。
Cilta-celはFDAによって画期的な治療の称号を与えられ、薬物を優先しています (“Prime”)、欧州医薬品局(“EMA”)の加速評価、およびCDEの画期的な治療指定。2021年1月人用医薬品委員会は (“CHMP”)、EMAは、マーケティング許可申請を加速的に評価する要求を受けた。米国食品薬品監督管理局、欧州委員会、日本厚生労働省、スイススイス医療グループ、韓国食品薬品安全部はシルタイを孤児薬として承認した。
2022年6月4日、著者らはCARTITUDE-1臨床試験の最新結果を公表し、RRMM治療におけるシクロホスファミドの作用を研究し、この結果は2022年ASCO年会で公表され、同時に臨床腫瘍学雑誌に発表された。
われわれの1 b/2 CARTITUDE−1期試験では,RRMM患者97名の長期結果が98%と高い総有効率(ORR)を示し続けた。27.7カ月のフォローアップ期間を経て,シルトセル治療を受けた患者の83%が厳しい完全応答(SCR)を得ており,報告の67%のSCR率を上回り,中央値は約1年であった。また95%の患者が非常に良い部分応答を得ました (“VGPR”)、またはそれ以上です。中位無進展生存率(PFS)と中位総生存率(OS)は達成されていないが,27.7カ月のPFS率は54.9%,27.7カ月のOS率は70.4%であった。微小残留病(“MRD”)を評価可能な61名の患者のうち,91.8%の患者が10−5の閾値でMRD陰性であった。MRD持続陰性少なくとも6カ月と12カ月の患者27カ月のPFS率はそれぞれ73%と78.8%であった。比較的長期的なデータでは,中央値の約1年間のフォローアップ以来,新たなCRSイベントの報告はないことが示されている。27.7カ月の中位フォローアップ期に1例の新しいパーキンソン病バイタルサインと症状が観察され、以前は運動と神経認知治療-緊急有害事象(AEs)と呼ばれていた。本年度報告日現在,患者状況は安定しており,機能は正常であり,SCR中である。我々はまた,2022年の各種科学大会で我々の第2段階多列CARTITUDE−2試験の新たな結果を発表した。CARTITUDE-2試験は、異なる臨床環境下でMM患者を治療するシルチゲームの安全性と有効性を評価することを目的としている。この試験Aキューの最新データは、2022年国際骨髄腫協会(IMS)年次総会で発表された。コホートAは20例のドナドアミン耐性の進行性多発性骨髄腫患者に対してセラチゼイの治療効果と安全性研究を行った。長い中央値17.1ケ月のフォローアップにおいて、患者は早期と深さの反応を経験し、安全性は制御可能であり、CARTITUDE-1試験と一致した。ORRは95%であり、その90%の患者は完全緩和(CR)以上に達し、95%の患者はVGPR以上に達している。初回緩解の中位期間は1カ月,最適反応に達した中位期間は2.6カ月であった。15カ月のPFS率は70%であった。
CARTITUDE−2試験B群の最新データは第64回米国血液学会(ASH)年次総会で発表された。B群は19名のPIとIMIDの予備治療を受けた後早期に再発した患者を含み、IMIDは自己幹細胞移植(“ASCT”)と定義されてから12ケ月以内に進展し、或いはASCTを受けていない患者に対して抗MM治療を開始した。データによると、早期と深い反応は管理可能な安全概況を持っている。18ヶ月の中央フォローアップ期間において、OORは100%であり、そのうちの90%の患者がCRまたはそれ以上に達し、100%の患者がVGPRまたはそれ以上に達している。初回反応の中位時間は0.95カ月,最適反応の中位時間は5.09カ月であった。18カ月のPFSと18カ月のOS金利はそれぞれ83%と83%であった。
CARTITUDE-2試験Cグループの最新データも第64回ASH年次総会で発表された。キューCは、プロテアソーム阻害剤(PI)、免疫調節薬(IMiD)、抗CD 38モノクロナル抗体(MAb)、および非細胞BCMA標的治療(抗体-薬物結合体(ADC)または二重特異性抗体(BsAb))を接触したことのある20人の患者を含む。18カ月の中位フォローアップ期間では,全キューのORRは60%であった
ADCおよびBsAbに曝露された患者であって、55%の患者がVGPRに到達するか、またはそれ以上である。全キューでは,中位有効時間は12.3カ月,中位PFSは9.1カ月であった
CARTITUDE−2キューA,B,Cに見られるセキュリティプロファイルは,先にCARTITUDE−1から報告されたデータと一致する。A群の95%の患者がCRS,B群の84%の患者がCRS,C群の60%の患者がCRSを発生し,これらの患者の多くは1/2級であり,平均発症期間は輸液後7~8日,中位持続時間は約3~5.5日であった。
また,われわれの第3段階試験CARTITUDE−4は,シセとポマドアミン,ポチゾミとデキサメタゾン(PVD)あるいはダラマミド,ポアメタゾンとデキサメタゾン(DPD)による再発性とレナドアミン難治性多発性骨髄腫(DPD)の治療効果を評価し,試験の1回目にあらかじめ指定した中期分析では,標準治療と比較してPFSが統計学的に有意に改善したことが第3段階試験の主な終点であった。独立したデータ監視委員会の提案の下で、この実験は盲目を解除された。
CAR-T細胞療法は癌免疫療法の一形態であり、患者のT細胞を改造することによって腫瘍細胞表面抗原を認識し結合するCARを発現し、癌細胞を破壊するために活性化される。CAR-T細胞療法はすでにある血液病患者を治療する革命性と潜在的な治療方法になっている。2017年、FDAは最初の2種類のCAR-T細胞療法KymriahとYescartaを許可し、これまでこれらの製品は部分再発或いは難治性B細胞悪性腫瘍に対して強力な治療効果を示した。
CAR-T細胞療法の発展は各領域で著しい進展を得て、いくつかの挑戦を克服し、理想的な腫瘍抗原標的を選択し、有効と選択的に腫瘍細胞を殺傷するCAR構造を設計し、検証された臨床前モデルが不足して人類の安全性と有効性を予測し、及び製薬製品に必要な高品質と再現性を有する細胞療法を製造する能力が不足している。しかも、地域と世界的なビジネスニーズを満たすことは依然として挑戦だ。
著者らはCAR−T細胞治療開発に関する挑戦を克服することをめぐって当社を設立し、早期発見、効率的な臨床翻訳、製造と商業化に関する内部の専門知識を含む完全に統合された全世界の細胞治療能力を配備することにより、著者らの次世代CAR-T候補製品パイプラインを患者に提供した。我々は,我々の内部で産生された抗体を用いて,我々のCAR−T特異的機能スクリーニング能に加えて,T細胞に1つまたは複数の腫瘍抗原結合部位を増加させている。我々と臨床医との関係や,彼らが中国一流病院で研究者による臨床試験を行う能力を利用することにより,正式な試験新薬なしに発見研究と患者との差を埋めることを求めている (IND)国家医療製品管理局がイノベーションを奨励する一部として (“NMPA”).我々は臨床医や病院と協力し,国際基準に基づいてこれらの試験を行い,将来のグローバル規制申告とパートナー関係を支援する。この戦略により,候補製品を大量の需要を満たしていない患者群に迅速に押し上げることができる。異なる地域で予想されるビジネスニーズを満たすために、私たちはアメリカ、EU、中国に製造工場を設立しています。また、私たちの製品が承認されれば、アメリカ、ヨーロッパ、アジアの癌患者を独立させたり、パートナーを通じて私たちの製品を広く使用したりすることを求めます。以上より,われわれが完全に統合した方法は,CAR−T細胞療法の使用を迅速に拡大することができると信じている。
我々の主要製品cilta-celはBCMAに対する自己CAR-T細胞療法であり、BCMAはMMを含む多くの血液系悪性腫瘍に高度に発現するタンパク質である。自己体細胞は患者自身の細胞を指す。FDAがCARVYKTIを承認した後、著者らは引き続きCilta-celを開発し、MMの治療を更に改善することを期待している。MMは1種の高度侵襲性疾患であり、全世界のすべての血液系悪性腫瘍の約10%を占め、血液系悪性疾患死亡の20%を占める。米国癌協会は,2020年に米国で32,270例の多発性骨髄腫症例と12,830例の死亡例が追加されると予想している。世界的に2018年には159,985例の多発性骨髄腫新症例が推定されている。既存の治療法にはモノクロナル抗体,プロテアソーム阻害剤,免疫調節剤があり,2018年の総売上高は約180億ドルであった。しかし,多発性骨髄腫は依然として治癒できず,最終的に再発し治療に難治性を生じる。例えば、少なくとも3つの以前の治療を受け、免疫調節薬およびプロテアソーム阻害剤の両方に無効な患者では、平均総生存期間(MOS)はわずか13カ月である。大量の前治療や難治性多発性骨髄腫患者の群では,承認された治療法のOORは30%以下であることが報告されている。したがって,高度に満たされていない需要が存在し,長い間効果を改善できる治療法が必要であると考えられる。
シルゼルはMM治療を変える潜在力があると信じている。われわれが中国で行った第1段階臨床試験の結果からLEGUS−2と呼び,RRMM患者に対するシルチゲームの第2段階登録試験を中国で行っており,これをCARTIFAN−1と呼ぶ。CARTIFAN−1の既存データに基づき,2022年12月に中国の薬物評価センターに新薬申請(NDA)を提出した。
我々のパートナーであるJanssenとともに,2021年3月にCilta−cel Biologicsライセンス申請(“BLA”)の転がり提出をFDAに完了し,2021年4月にEMAにCiltaマーケティング許可申請を提出し,2021年12月に日本医薬品·医療機器庁(“PMDA”)にCilta NDAを提出した。FDAは2022年2月28日に糖尿病の治療のためのCARVYKTIというシクロホスファミドを承認しました再発または難治性多発性骨髄腫を有する成人患者は、プロテアソーム阻害剤、免疫調節剤、および抗CD 38モノクロナル抗体を含む4つ以上の治療を前に受けている。 2022年5月25日欧州委員会は、再発および難治性多発性骨髄腫の成人患者を治療するためのCARVYKTIの条件付きマーケティング許可を承認し、これらの患者は、免疫調節剤、プロテアソーム阻害剤、および抗CD 38抗体を含む少なくとも3つの治療を受け、最後の治療において疾患の進展を示した。2022年9月26日、厚生労働省は、成人再発性または難治性多発性骨髄腫の治療にCARVYKTIを許可し、BCMAに対するCAR陽性T細胞注入療法がない患者、免疫調節剤、プロテアソーム阻害剤および抗CD 38モノクロナル抗体を含む3つ以上の治療を受けた患者、および多発性骨髄腫は最近の治療後に反応または再発しない、の2つの条件を満たす症例に限定されている。
私たちが最初の規制提出を支援するために行われている試験に加え、シルゼルをMMの早期治療法として評価するための複数の臨床試験を行っている。2019年11月、私たちと戦略パートナーのJanssenは、米国、EU、イスラエルで合計約160人の患者をシルベンチの2期多列試験に参加し始め、これをCARTUDE-2と呼び、早期再発患者や治療の第一線として様々な臨床環境下のMM患者に使用している。これらの結果に基づき,規制機関の同意後に規制承認を提出することを潜在的に支援するために,これらの患者群における我々の調査を拡大することを模索する予定である。また,CARTITUDE−4期臨床試験は,米国,ヨーロッパ,オーストラリア,日本,韓国,イスラエルの約400名の患者を含み,2021年10月に登録を完了した。この臨床試験は,シルチレースと標準三連療法によるRevlimid難治性MMの治療効果を比較している。2023年1月27日,CARTITUDE−4が主な終点に達したことが発表され,検討の最初の事前に指定された中期分析では,標準療法と比較してCARTITUDE−4がPFSで統計的に有意に改善したことが示された。独立したデータ監視委員会の提案の下で、この実験は盲目を解除された。また,2021年8月にCARTITUDE−5期臨床試験を開始し,米国,ヨーロッパ,カナダ,オーストラリア,韓国,日本を含む約650名の患者を募集することを目標とした。この臨床試験では,新たに診断された多発性骨髄腫患者に対してシルチサイ治療と標準三胞胎治療の比較を行っており,造血幹細胞移植を初期治療とする予定はない。
私たちは楊森と全世界の協力関係を構築し、その上で、私たちはすべての地区の開発、生産と商業化コストと損益を折半したが、しかし大陸中国、香港マカオ台湾或いは大区中国を除いて、大陸、香港マカオ台湾或いは大区で、私たちは70%の開発、生産と商業化コストを負担し、そして70%の税前損益を保留或いは負担する。私たちは2018年にJanssenから3.5億ドルの前金を受け取り、2022年12月31日までに300.0ドルのマイルストーン支払いを追加した
Cilta−celに加えて、非ホジキンリンパ腫(NHL)、急性リンパ球性白血病(ALL)、胃癌、食道癌、膵臓癌、結腸直腸癌、肝細胞癌、小細胞肺癌、非小細胞肺癌を含む様々な癌に対する早期自己CAR−T製品候補製品の広範な組み合わせを有する。我々はまた,MMに対するBCMAの同種異体ガンマデルタCAR−T候補製品を開発しており,現在研究者が開始した中国の第1段階臨床試験にある。また私たちは同種異体を開発しています
BCMAに対するCAR-NK候補製品および急性骨髄性白血病(AML)に対するCLL 1/CD 33の同種ガンマDelta CAR-T候補製品。次の表に私たちの候補製品ルートをまとめました。
私たちはHuang博士が指導して、彼は私たちの最高経営責任者と取締役会のメンバーで、彼は最近取締役の社長とアメリカ銀行証券会社のバイオテクノロジー株研究主管で、彼のキャリアの初期には、彼は先霊雅(現在のメルク)の首席科学者であり、私たちの最高財務官Lori Macomberでもあります。私たちは生物製薬薬の発見、開発、商業化の面で豊富な経験を持つチームを結成した。
私たちの戦略
我々の目標は,細胞療法のグローバルリーダーとなり,癌の治療を進めることである。この目標を達成するための戦略は以下のとおりである
•登録試験を通じてCilta−celを推進し、世界MM治療の承認を得たそれは.Cilta−celは深く持続的な抗腫瘍反応を産生し,RRMM患者の生存率を向上させることが証明されたと信じている。Cilta−celは2022年にFDAの承認,欧州委員会の条件付き承認,および日本厚生労働省の承認を得た。これらの承認は末期患者に対するものであるが,早期患者を含む多発性骨髄腫の臨床開発を積極的に行い,潜在的に第一線の治療とする予定である。
•私たちのグローバル臨床開発戦略を利用することで、私たちのルートを迅速に推進します。我々は,我々の技術ノウハウ,発見と臨床専門知識,および臨床研究者や治療センターとの深い関係を継続して利用し,細胞治療の新たな機会を探る予定である。私たちは続ける予定です
我々が研究者による臨床試験を得る機会を得たことを利用して,これらの試験は国際基準に基づいて行われ,中国での候補製品を促進し,米国でIND応用を行う候補製品を選択した。著者らの全世界臨床開発戦略は著者らが効率的かつ低コストでこれらの個別候補製品の患者への治療潜在力を迅速に評価できるようにした。われわれは,臨床データを中国から他の管轄区に移行する際に法律や規制上の挑戦に直面しているが,最も有望と考えられる候補製品を迅速に世界登録臨床試験に進めることができると信じている。著者らはまた、研究者が始めた試験で十分な結果が得られなかった候補製品を抽出し、最適化し、潜在的に著者らの目標市場のいくつかの臨床開発リスクを下げることができる。
•細胞治療分野での私たちの世界的なリードを維持して拡大する。私たちは細胞治療分野のリーディングカンパニーであると信じていますが、承認されれば、世界中の患者に私たちの製品を使用する機会を提供するために、私たちのグローバル業務を拡大していきたいと思います。私たちは、中国での効率的かつ費用対効果のある臨床開発戦略を利用し、私たちの技術キットを拡大することができるように、異なる地域でリードした人材を採用することを計画しており、これらの技術は、改善された細胞療法を迅速に開発するためにシステム的な方法をとることができると信じている。我々は,米国,ヨーロッパ,中国,日本などの主要市場のさらなる規制承認を支援するためのCilta−celの臨床キー試験を行っている。私たちはまた、市場参入、医療保健提供者の訓練、病院認証、精算、製造、および患者とプロバイダの支援を含む、私たちの製品販売のあらゆる面を支援するための全世界の商業チームを構築するつもりだ。
•私たちの製造能力を拡大する。私たちが米国でJanssenと協力している製造施設は現在、アメリカとEU市場にCARVYKTIを供給しており、もし私たちが他の国で承認されれば、このような施設を使用して他の国に供給する予定です。私たちの試験の臨床材料は私たちのアメリカ機関と私たちの中国の機関が提供します。我々は,我々の米国工場の商業規模製造能力をさらに拡大し,欧州·米国市場の商業·臨床供給を満たすためにベルギーに製造施設を建設し,より多くの市場で提供することが可能であると考えている。また,Janssenについては,我々の臨床·商業供給製造施設を補完するための第三者CMOの使用を接触·求めている初期段階である
•私たちを第一選択のグローバルパートナーにしてください著者らの全世界ネットワークと戦略はパイプライン候補患者の臨床概念検証を加速することに役立つ。また、私たちの中国における強力な影響力を通じて、中国の主要な世論リーダー、衛生政策専門家、リード医療機関、現地の世界的製造業との深い関係、及び中国法規に対する深い理解と経験を通じて、私たちは有利な地位にあり、非中国会社の利益が潤沢であるが複雑な中国市場を制御するのを助ける第一選択のパートナーになることができる。私たちはヤンソンとの世界的な協力が、Cilta-celの開発と潜在的な商業化に証明を提供し、私たちの第一選択のグローバルパートナーとしての潜在力を証明したと信じている。
癌とCAR−T細胞治療の背景
癌は世界で2番目に大きな死因です単一細胞の基本細胞機能が突然変異し、細胞分裂と成長が増加すると、癌が発生する。T細胞は免疫系の重要な構成部分であり、感染病原体と癌細胞の浸潤から身体を防御することを担当する。T細胞受容体により,T細胞は癌細胞を認識·除去することができる。しかし,癌細胞はT細胞認識から逃れる機序を進化させ,他のT細胞監視から逃れる機序を確立することができる。癌免疫治療は免疫反応を増強し、操作して癌により有効に対抗することを目的とした治療策略である。
細胞療法をとる ACTは免疫細胞を患者に注入し,これらの細胞を攻撃して癌細胞を破壊することを目的とした癌免疫療法である。多くの場合,これらの免疫細胞は自己由来であるか,あるいはそれらを再投与した同一患者から分離される。これらの単離された細胞は数量的に拡張することができ、特定の増殖因子、サイトカイン、ケモカインまたは抗原によって刺激されることができ、あるいは遺伝子改変によっていくつかの腫瘍を認識し、破壊することができる。
CAR-T細胞とTCR-T細胞は2種類の最もよく見られる工学細胞であり、それらはキメラ抗原受容体或いは自然産生T細胞受容体(TCR)を発現し、患者の腫瘍上の抗原を識別する。他の免疫細胞タイプは、NK細胞を含むCAR構造を発現するように改変されてもよい。人工合成したCARはモノクロナル抗体の特異性とT細胞の細胞毒性と免疫監視機能に結合し,癌細胞が過剰に発現する細胞表面蛋白の細胞外抗原に結合し,主要な組織適合性複合体がT細胞の活性化に依存しないようにした。CD 19はリンパ腫癌細胞に過剰発現する抗原である。抗CD 19 CAR-T細胞療法は非常に強い治療効果を示し、ある場合には選択性再発に対して治癒潜在力がある
あるいは難治性B細胞悪性腫瘍は、最終的にFDAが2017年に第1回CAR-T療法、KymriahおよびYescartaを承認した。
CAR−Tの発展とCAR−NK細胞療法の挑戦
この領域は進展しているにもかかわらず,CAR−TとCAR−NK細胞療法の開発にはいくつかの重要な挑戦が存在している。
•適切な腫瘍抗原標的を選択しますCAR-TまたはCAR-NK細胞が認識する抗原標的は膜結合細胞表面蛋白である。正常組織における分布は限られており、腫瘍中の過剰或いは均一発現、及び脱落或いは内化の不足は標的抗原と関連する重要な要素であり、細胞治療を発展させる時に標的の選択を考慮する必要がある。標的抗原の正常組織への発現は標的上/腫瘍外毒性のリスクを増加させるが、腫瘍細胞の脱落或いは内化による発現減少或いは損失は治療効果を低下させる可能性がある。
•最適な車の構造を設計しますCAR構造の特性はCAR-TとCAR-NK細胞治療の全体的な成功に重要である。抗原結合ドメインの親和性と柔軟性は腫瘍特異性識別を増強する中で重要であり、細胞活性化過程中の共刺激はT細胞の新陳代謝、生存と機能を調節する。CAR-TとCAR-NK細胞治療のよく見られる副作用の1つは、その標的抗原に遭遇した時に細胞が過剰活性化することである。このような過剰活性化はサイトカイン放出症候群(CRS)を引き起こし,高レベルの炎症性サイトカインによる生命を脅かす疾患である。したがって,最適な自動車構造を設計するには有効性と安全性のバランスをとる必要がある.
•臨床前から臨床への転換:有効な臨床前モデルが不足し、人類の安全性と有効性を予測し、CAR-TとCAR-NK細胞治療製品の有効な開発にかなりの障害を提供した。現在、臨床前動物モデルは人体免疫システム、腫瘍微小環境と正常組織中の標的抗原の分布を概括できることは少ない。従来のCAR−TやCAR−NK細胞治療研究にはいくつかの動物モデルが用いられてきたが,それらの多くは臨床治療効果を実現する障害を反映しておらず,潜在的な生命に危害を及ぼす毒性も予測できない。
•製造の複雑さ:個々の患者から収集した細胞の多様性により,細胞療法の製造は困難である。自己CAR−TとCAR−NK製造のカスタマイズ性質を考慮すると,限られた規模経済を実現することができる。これらの要素は臨床翻訳と患者の接触が限られている。さらに、高いコスト、および場合によっては、製造中の高い失敗率は、CAR−TおよびCAR−NK細胞療法のスケーラビリティを制限し続ける。異なる地域の細胞療法生産に対する監督管理は異なり、全世界範囲内で能力を拡大したい薬物開発者に追加の複雑性をもたらした。
私たちの方法は
我々は,細胞治療開発に関する挑戦を克服することをめぐって当社を設立し,早期発見,効率的な臨床翻訳,製造,商業化における内部の専門知識を含め,我々の完全に集積された全世界の細胞治療能力を展開することにより,我々の次世代候補製品パイプラインを患者にもたらした。我々は,我々の内部で産生された抗体を用いて,我々のCAR−TやCAR−NK特異的機能スクリーニング能に加えて,免疫細胞に1つまたは複数の結合部位を増加させている。著者らは発見研究と患者治療の間の差を埋めることを求め、著者らと中国の臨床医師の長期関係と彼らの専門知識を利用して、中国の一流病院で研究者による臨床試験を行い、迅速に候補製品を大量の需要を満たしていない患者群に普及させる。様々な地域の予想されるビジネスニーズを満たすために、米国に製造工場を設立し、EUと中国に製造工場を設立している。また,第三者CMOの使用状況を評価し,ビジネスニーズを満たすことを支援する.また、私たちの製品が承認されれば、私たちの製品を世界的に癌患者に広く提供することを求めます。アメリカ、ヨーロッパ、アジアを含めて。以上より,われわれの包括的な統合方法は,患者では満たされていない大きなニーズを満たすために,細胞療法の使用を迅速に拡大することができると信じている。
技術力
2014年に運営を開始して以来,細胞療法の変革の潜在力を認識してきた。私たちは専門家チームと技術を作りましたこれらの技術は改善された細胞療法を迅速に開発できるようにシステム的な方法をとることができると信じています多くの技術分野が細胞治療や関連分野に対する我々の方法を支えている。
内部抗体とCARスクリーニング能
CAR−TとCAR−NK細胞療法は腫瘍細胞を認識·殺傷する能力がかなり異なる。他の多くの人によって開発された早期候補製品は、CAR-TおよびCAR-NKアプリケーションに特化して設計されていない可能性がある許可内の抗体に依存する。これに対し,我々は最適な特性を持つ抗体断片を認識できるようにする高スループットスクリーニング技術を開発し,特定のCAR構造に対して抗原結合ドメインとリンカーを最適化することができるようにした。これにより,最も興味のある腫瘍細胞を標的とするCAR構造を効率的に標的とするCAR構造を選択と優先的に選択し,正常細胞を保持することができる。著者らは臨床前研究と早期臨床研究において、抗原結合ドメインの適切な選択は全体の抗腫瘍活性の重要な決定要素であることを証明した。また,我々の内部抗体生成に加え,我々のCAR−T特定機能スクリーニング能力を加えることは,内部パイプライン計画を拡張し,急速に発展した細胞治療発展パターンと同期するのに役立つと信じている。
多抗体開発プラットフォーム及び多重特異的結合方法
CAR-TまたはCAR-NKアプリケーションにおける所与の目標のための最適な結合剤を最大限に決定するために、ラクダおよびマウスからの単一ドメイン抗体および完全なヒト抗体を含む複数の内部抗体開発プラットフォームを有する。
我々の主要候補製品cilta−celについては,ラクダから我々自身の抗原結合ドメインを分離して特徴付けることを選択した。大アルパカは、重鎖および軽鎖ドメインからなるより伝統的な抗体と比較して、より高い抗原結合効力を有するユニークな単一ドメイン抗体を含む高度に多様な抗体を産生する。これらの小さな単ドメイン抗体は細胞膜に近い抗原部位にもアクセスできるが,大きな従来の抗体はこれらの部位に物理的に接触できない可能性がある。
我々の技術は,同じ抗原または多抗原特異的CAR構造に対するポリエピトープ抗体を効率的に産生する可能性がある。ラクダ単一ドメイン抗体の小さいサイズは、同一の抗原または異なる抗原の2つ以上の抗原結合ドメインに対するCARSを効率的に構築することができる。この技術を用いて,BCMA上の2つのエピトープに対するラクダ単一ドメイン抗体の作製に成功し,Car構築した有毛細胞に応用した。
グローバル臨床発展戦略
著者らは全世界の臨床開発戦略を採用し、臨床を通じて著者らの候補製品を迅速に改善することを目的とした。特に,我々は中国思想指導者との深い関係を利用して概念検証研究を行っており,これらの研究により,我々の臨床開発計画の設計により有効に情報を提供し,何らかの臨床開発リスクを潜在的に低下させることができると信じている。われわれは臨床データを中国から他の管轄区に移す際に法律や規制面の挑戦に直面しているが,この方法は有益であると信じている。中国の研究者が始めた試験で候補製品に対して初歩的な人体テストを行うことにより、著者らは単一の候補製品の治療潜在力を迅速に評価し、効率的かつ費用効果のある方法でこれらの候補製品を改善することができ、これにより、私たちは将来性のある候補製品を迅速に決定し、それらを中国、アメリカ、ヨーロッパと日本の登録臨床試験に推進することができる。また、米国、EU、中国における私たちの製造施設に投資し続け、製品普及、医療提供者研修、医療·科学交流を含む私たちの製品販売を支援するためのビジネス能力を発展させていきたいと思います。
私たちの専門知識と中国細胞療法規制環境とアメリカの重大な差異の理解を考慮して、私たちは中国以外の会社或いは中国以外の実体から作成或いは制御した会社が中国の遺伝子組換え細胞を用いて科学研究を行う第一選択パートナーになる可能性がある。相談後、科学顧問委員会と倫理委員会の監督の下で、中国の臨床医は彼らの病院で実験的細胞療法の臨床試験を開始することができ、NMPAが正式なIND申請を承認する必要がなく、これはNMPAが革新を奨励する一部である。我々は臨床医師や病院と協力し,国際基準に基づいて研究者による試験を行い,将来のグローバル規制申告とパートナー関係を支援する。この方法で私たちは
病人です。著者らはまた、中国の主要なオピニオンリーダー、監督機構、機構審査委員会、倫理委員会と細胞療法の臨床発展の加速と監督に参与する関連実体と関係を築いた。
著者らは中国でCAR-T細胞療法を開発した最先端の会社の一つであり、国家薬品監督管理局の許可を得た最初のCAR-T細胞療法IND申請を得た。私たちも中国で初めてCAR−T臨床試験を行った人です。我々は305人を超える研究者からなる強力なグローバル研究チームを構築し、潜在的な細胞標的を識別し、広範な候補製品の組み合わせを作成し、評価した。この専門知識を確立することは、中国内部の主要な調査員とパートナーを引きつけた。
レノボ2号試験は4つの一流の大型病院で行われており,これらの病院は毎年数百万人の患者を治療し,医療と医学教育を一体化して運営する大学に関係している。中国だけでは,2018年に新規癌症例430万例,癌死亡290万例と推定されている。その中の80%の患者は地区と省レベルの病院で治療を受け、著者らはその中の多くの病院と協力した。これらの病院は用量、調節方案、不良事件(例えばCRS)の管理においてこれらの治療法を用いて患者を治療する臨床経験は、潜在的な臨床候補者の初の人体テストにとって貴重な資源であると信じている。
研究者によって開始された臨床試験に参加する患者は、通常、複数の以前の治療案に失敗しており、任意の代替案が不足している。これらの臨床試験の中から、臨床医師は詳細なバイオマーカーデータ、細胞反応概況と臨床反応を収集し、治療方案の改善を助け、そして私たちと共有して、私たちの候補製品の優勢と劣勢を理解する。我々は,これらの早期臨床試験のデータを用いて有望な候補製品を推進し,適切なときに他の候補製品を改善する。これらのデータを用いて無効な候補製品や生物学的仮定を識別し,注目範囲を縮小し,不必要な費用や時間を回避することができるようにした.
臨床·ビジネス段階の製造専門知識
私たちは臨床、製造、ビジネスを組み立てました CAR-Tプロセス開発および商業化経験が豊富なチームであり、多くの人が市場におけるCAR-T製品の商業発表および製造供給において直接経験を有する。われわれは目下良好な生産実践がある 私たちはアメリカのコンプライアンス製造工場と私たちの試験に臨床材料を供給する中国工場、そして私たちはアメリカにある工場で、アメリカ市場の製品も商業的に供給しています。私たちはまた連合に製造施設を設立して、未来の供給のための準備をする。
これらの施設を構築する過程で,我々は大きな努力をし,製造安定性,施設設計,高品質者の雇用,製造可能性を考慮した細胞療法設計に関する明確なプログラムを構築した。これらの努力は,我々の厳格な製造インフラや深い業界の専門知識に加えて,強力な製造プロセスを開発することができ,細胞治療候補製品の開発においてサイクルのさらなる短縮とコスト低減が可能であると信じている。
私たちの番組
Cilta-celは多発性骨髄腫を治療します
Cilta−celは,我々が開発しているMMを治療するCAR−T細胞療法である。第1段階のヒト臨床試験(LEGON−2)では,74名のRRMM患者がLCAR−B 38 M CAR−T細胞の治療を受けている。平均フォローアップ時間は47.8ケ月、OORは87.8%、CR率は73%であった。中位有効期間は23.26カ月,中位PFSは18カ月であった。中央値オペレーティングシステムには達していない.Legend−2のすべての患者が予想される有害事象を報告し,91.9%の患者がCRSを報告し,9.5%の患者が3段階以上のCRSを報告している。1例の患者は任意のレベルの総CAR-T細胞神経毒性を観察した。レベル3以上の神経毒性事件の報告はない。第一段階LEGON−2臨床試験では,34人の死亡が報告されている:28人が疾患進行で死亡し,1人がCRSと腫瘍溶解症候群で死亡し,1人が肺塞栓と潜在的な急性冠症候群で死亡し,1人が後続治療に関連する呼吸不全で死亡し,1人が食道癌で死亡し,2人が感染で死亡した。
国際骨髄腫ワーキンググループ(IMWG)のMMに対する統一反応標準に基づいて、患者に対して測定を行い、彼らがCR、VGPR或いは部分緩和(PR)に達するかどうかを確定する
標準はすでに許可された骨髄腫薬物の登録研究に応用されている。IMWG統一反応標準は骨髄腫治療方案の治療効果を評価し、そして臨床試験中の治療策略間の治療効果を比較することを許可し、下表に示す反応に対する厳格な定義、及び詳細の改善と臨床試験中の不一致解釈の分類を明らかにするために用いられる。
IMWGのCR、VGPR、PRと安定型疾患(“SD”)に対する標準の概要は以下の通りである。
| | | | | |
| |
| クロム.クロム | •血清と尿中の陰性免疫固定 •軟部組織形質細胞腫の消失や • |
| |
| |
| VGPR | •血清や尿単クローン蛋白(“M−蛋白”)は免疫固定により検出できるが,電気泳動法や電気泳動法では検出できない •≥血清M蛋白と尿M蛋白レベルを90%低下させる |
| |
| |
| 印刷機 | •≥血清M蛋白を50%低下させながら24時間尿M蛋白を90%低下させるか •もし血清と尿中のM蛋白が測定できない場合、罹患と影響を受けていない遊離軽鎖との差をM蛋白標準の代わりに50%低下させる必要があり、もし血清光分析も測定できなければ、M蛋白の代わりに形質細胞50%が必要であり、ベースライン骨髄形質細胞パーセンテージが30%であることを前提とする •これらの基準に加えて,ベースライン上に存在すれば,軟部組織形質細胞腫の大きさ(Spd)を50%縮小する必要がある |
| |
| |
| はっきりしている | •CR、VGPR、PRまたは進行性疾患の基準を満たしていない |
| |
Janssenと協力して,Cilta−celの中国のRRMM患者における第2段階試験(CARTIFAN−1)と米国と日本のRRMM患者における1 b/2段階試験(CARTITUDE−1)を行っている。CARTITUDE-1フェーズ1 b/2登録試用版の登録が完了しました。CARTITUDE-1試験の1 b段階では、主な終点は安全性を決定し、推奨される第2段階用量を決定することであり、第2段階部分では、主要終点はORRによる治療効果の評価である。二次終点は、治療効果、持続時間および効果開始時間、無進展生存期間、総生存期間、薬物動態学および薬効学マーカーおよび抗JNJ-4528抗体の存在を含む。米国では97名の患者が1 b/2 CARTITUDE−1期共同試験でシルチゲームの治療を受けている。27.7カ月の中央値フォローアップ(2022年1月11日までのデータ)では,全体応答率は98%であり,時間の経過とともにさらに深まり,83%のSCR比率を顕著に示した。さらに、95%の患者がVGPRまたはそれ以上の非常に良い部分応答を得た。中位PFSと中位OSは達成されていないが,27.7カ月のPFS率は54.9%,27.7カ月のOS率は70%であった.微小残留病と評価された61人の患者のうち (“MRD”)、10歳で91.8%の人がMRD陰性-5閾値を切る。MRD持続陰性少なくとも6カ月と12カ月の患者27カ月のPFS率はそれぞれ73%と78.8%であった。最もよく見られる血液学的副作用は白血球減少(95.9%)、血小板減少(79.4%)、白血球減少(61.9%)とリンパ細胞減少(53.6%)である。特に興味のある有害事象については,比較的長期的なデータでは,中央値の約1年間のフォローアップ以来,新たなCRSイベントは報告されていない。27.7カ月の中位フォローアップ期に新たなパーキンソン病バイタルサインと症状が認められ,従来は運動や神経認知治療−緊急脳梗塞と呼ばれていた。本年度報告日現在,患者状況は安定しており,機能は正常であり,SCR中である。
Cilta−celはすでにFDAの突破的治療指定、Prime指定、EMAの加速評価とCDEの突破的治療指定を獲得した。2021年1月、CHMPはまた、マーケティング許可申請の加速評価の要求を受け入れた。米国食品医薬品局、欧州委員会、日本厚生労働省、スイススイス医療グループ、韓国食品医薬品安全保障部は、シルタを孤児薬として承認した。Cilta-celは2022年2月28日にFDAによって承認されたCARVYKTI商標を取得したプロテアソーム阻害剤、免疫調節剤、および抗CD 38モノクロナル抗体を含む4つ以上の治療を以前に受けた再発性または難治性多発性骨髄腫を治療するための成人患者それは.2022年5月25日、欧州委員会は、PI、IMIDおよび抗CD 38抗体を含む少なくとも3つの治療を受け、最後の治療において疾患の進行を示す再発および難治性MMの成人を治療するためのCARVYKTIの条件付きマーケティング許可を承認した。開ける
2022年9月26日、厚生労働省は、CARVYKTIが再発性または難治性多発性骨髄腫の治療に使用されることを許可し、BCMAに対するCAR陽性T細胞注入療法を有さない患者、および免疫調節剤、プロテアソーム阻害剤および抗CD 38モノクロナル抗体を含む3つ以上の治療を受けた患者、および多発性骨髄腫が最近の治療後に反応または再発しない、の2つの条件を満たす症例に限定される。2022年12月、中国の疾病管理センターにRRMM治療の報告書を提出した。
今までに受け取った臨床結果により、Cilta-celは安全性制御可能なRRMM患者に深さと持続的な抗腫瘍反応を提供する潜在力があることを表明した。私たちはまだ新冠肺炎の大流行でシクロホスファミドに関するいかなる臨床試験も停止していない。また,米国や中国では製造施設が正常に稼働しており,患者,医師,医療センターが患者の登録や患者への投与を準備していれば,全力で支援していきたい。著者らはまた、医師と医療センターとの定期的なコミュニケーションを含む患者計画の受診を監視し、緩和措置を確定するための新冠肺炎運営チームを構築した
2017年、私たちはヤンソンと世界的な協力を達成し、中国大中華区を除くすべての地域の開発、生産、商業化コストおよび損益を共同で負担し、私たちは70%の開発、生産、商業化コストを負担し、70%の税引前利益または損失を保留または負担した。私たちは2018年にJanssenから3.5億ドルの前金を受け取り、2022年12月31日までに300.0ドルのマイルストーン支払いを追加した。
多発性骨髄腫の研究背景
MMは現在1種の治愈できない血液癌であり、骨髄から始まり、その特徴は形質細胞と呼ばれる抗体産生白血球の過剰増殖である。MMは第三種の最もよく見られる血液癌であり、すべての血液病病例の約10%を占め、血液系悪性腫瘍死亡の20%を占める。2018年、アメリカ新規多発性骨髄腫25,962例、死亡13,648例;ヨーロッパ新規多発性骨髄腫48,297例、死亡30,860例;中国新規多発性骨髄腫20,066例、死亡14,655例。米国癌協会は,2021年には米国で約34920例の多発性骨髄腫症例が新たに増加し,約12410例の死亡が予想されると予測している。
米国では多発性骨髄腫と診断された人の多くは年齢65歳以上であり,1%未満の症例のみが35歳以下の人で確定診断されている。現在利用可能な治療法の下で、MMの5年生存率は約55.6%である。多発性骨髄腫の治療選択は疾患の侵襲性と患者全体の健康によって異なる。
新たに診断された身体健康状態の良好な活動期疾患患者は通常大量の化学療法を受け,自己造血幹細胞移植を行う (“HSCT”)。移植が選択またはHSCT患者がCRを得られなかった場合、標準的な看護は全身化学療法を含む。過去10年間に、新規免疫調節剤(例えば、百時美施貴宝(Bristol-Myers Squibb)で販売されているレナドアミン(Lenalidomide))およびモノクロナル抗体(例えば、Daratumab(Janssenが販売しているDarzalex))とプロテアソーム阻害剤(bortezomibおよびcarfizomibの販売名Veladeを含む)の発売に伴い、MMの治療構造は著しく変化した。2018年,MM治療薬の世界での売上高は約180億ドルであり,その63%が米国にある。
これらの重大な進展を得たにもかかわらず、患者が1種以上の治療薬物を受けても、多発性骨髄腫は治愈できない。患者は通常3~5本の線の治療を受けているが,すべての有効な治療案を使い切った後,最終的に腫瘍再発を経験する。少なくとも3つの以前の治療を受け、免疫調節薬およびプロテアソーム阻害剤の両方に無効な患者のMOSは13カ月のみであり、CD 38標的モノクロナル抗体および1つまたは複数のプロテアソーム阻害剤および/または1つまたは複数の免疫調節薬が無効な患者のMOSは12カ月未満であった。大量の前治療や難治性多発性骨髄腫患者の群では,承認された治療法のOORは30%以下であることが報告されている。
新たに出現した治療方法は、MM細胞上の特定の抗原を標的とする一連の候補製品を含み、抗体-薬物結合体およびT細胞活性化剤およびCAR-T細胞療法などの再配向T細胞療法をさらに含む。最近進展しているにもかかわらず,満たされていないニーズが多く,改善と持続効果を提供できる療法が必要であると考えられる。
BCMA
BCMAは通常B細胞に発現するタンパク質であり,B細胞上でその機能は生存を支持する受容体である。形質細胞には高レベルのBCMAが認められ,形質細胞は大量の抗体を産生·分泌する特殊なB細胞である。BCMAはMMを含む多くの血液系悪性腫瘍に過剰発現している。
BCMAの組織分布は,転写レベルの定量分析により,BCMAは通常リンパ球にのみ発現し,身体の他の組織には発現しないことが示唆された。形質細胞腫或いはMM腫瘍において、BCMAの発現レベルは正常組織より数百から数千倍高く、BCMAをMMに対する第一選択の治療薬物にした。
米国国立衛生研究院の主要研究者による第三者試験の公表詳細報告によると,RRMM患者24名のうち,抗BCMA CAR−T細胞治療を用いたORRは58%,最高用量9 x 106 CAR−T細胞/kgを受けた16名中ORRは81%であった。これらの結果は抗BCMA CAR-T細胞がRRMMの治療に発揮可能な作用に初歩的な証拠を提供した。これらの初歩的な結果をもとに,次世代CAR−T細胞療法を開発する機会があると信じている。
私たちの解決策Cilta-celは
Cilta−celはBCMAの構造分化に対する自己CAR−T細胞療法である。大アルパカから分離した抗BCMAの単ドメイン抗体を用いてCilta Car構造を設計した。次いで、2つのBCMA結合ドメインVH 1およびVH 2を4-1 BBタンパク質のT細胞共刺激ドメイン(CD 137とも呼ばれる)およびCD 3 Zeta鎖に連結してCAR構築物を形成する。
Cilta-cel自動車構造
毛包のCAR構造は2つの抗原結合領域を有する
同種抗原二重結合ドメインCAR
Cilta−celは以下の作用機序により多発性骨髄腫患者に利点を提供すると考えられる
•2つの抗原結合ドメインがより高い結合親和性を利用した概念であるCARと腫瘍抗原間の2つの接触点は、いずれかの抗原の単一接触点に比べて結合の可逆性がはるかに小さい
•二重抗原結合ドメインはまたCARを異なる分子上でエピトープを架橋させ、それによって免疫シナプス中のより多くのCARSの凝集を促進し、T細胞を活性化し、T細胞の下流シグナル強度を増加させ、それによってCAR-Tの全体機能を増強することができる
•抗原部位を独立に認識する抗原結合ドメインを含むことは、スイッチ標的結合比率の増加を招くことができ、それによってより高い特異性を産生し、それによって脱標的効果を減少させる。
著者らは臨床前研究を行い、BCMA CAR(BCMA CAR 001とBCBR 002)と二重結合BCMA CAR(BCBR 003)を単結合した抗腫瘍殺傷効果を比較した。以下に示すように、この研究のデータは、同じ標的比(E/T 5:1)において、BCMAを発現する細胞系において、二重接着剤を含むCARの抗腫瘍殺傷活性が、1つの接着剤のみを含むCARよりも優れていることを示している。
臨床前データは二重接着剤BCMA CARがより高い特定の細胞殺傷活性を有することを示した
単一接着剤BCMA乗用車
完成臨床結果図例−2(中国)
Legend-2は中国が展開した最初の人類研究者が始めた1期研究であり、LCAR-B 38 M CAR-T細胞の安全性を評価し、再発或いは難治性多発性骨髄腫患者に初歩的な概念検証治療効果を提供することを目的とした。この研究の患者登録は2016年に始まり,中国の4つの学術サイトに合計74名の患者が蓄積された。この4つの学術サイトのデータはこれまで2022年の“血液学と腫瘍学雑誌”に発表されている。中央値47.8ケ月のフォローアップにおいて、CRを獲得した患者の全体MPFS中央値は18ケ月と28.16ケ月であった。記者はまだMOSに連絡していない。この研究では,LCAR−B 38 MはBCMA標的CAR−T療法の他の安全報告と一致した安全性の概要を示している。CRSや細胞減少症は本研究で最も多く観察された副作用であり,長期フォローアップデータ収集が行われている。
現在行われている臨床開発
2018年3月,我々は中国で多センターによる検証的臨床試験CARTIFAN−1の承認を得た。FDAが2018年5月にIND提出を承認した後,JanssenとCARTITUDE−1,CARTITUDE−2,CARTITUDE−4,CARTITUDE−5試験を行っている。
CARTIFAN-1(中国)
我々はRRMM患者を募集して1つの重要な2期試験に参加しており、私たちはCARTIFAN-1と呼ばれ、中国の8つの地点に関連している。この実験の主な終点はORRである.2022年12月、我々はCARTIFAN-1の既存データに基づいて、中国のCDEにCDAを提出した。
CARTITUDE-1(アメリカと日本)
JanssenとともにCilta−cel 1 b/2期臨床試験の患者登録が完了し,米国の17地点と日本の4地点をカバーし,97名の患者が米国の1 b/2段階試験で用量治療を受けた。この97名の患者の前治療に失敗した中央値は6個(前治療の範囲は3−18個)であった。すべての患者は免疫調節薬物、プロテアソーム阻害剤と抗CD 38治療を受け、99%の患者は最後の第一線の治療に無効であった。CARTITUDE−1試験の1 b期部分では,主な終点は安全性の決定と投与量の決定であり,第2段階部分では主要終点はORRによる治療効果の評価である。二次終点は、治療効果、持続時間および効果開始時間、無進展生存期間、総生存期間、薬物動態学および薬効学マーカーおよび抗JNJ-4528抗体の存在を含む。CARTITUDE−1試験では,分離後にシクロホスファミドとフルダラビンの1日1回のシクロホスファミドとフルダラビンリンパ郭清術を受けた。シプロフロキサシンの中央投与量は0.71×10であった6 CAR+生T細胞/kg(範囲:0.51-0.95 x 106).
われわれはすでにCARTITUDE−1試験2期の一部患者の募集を完了し,1 b/2期CARTITUDE−1共同研究の最新結果を2022年ASCO年次総会で公表し,同時に臨床腫瘍学誌に発表した。
2022年1月11日まで(平均27.7カ月フォローアップ),97名のRRMM患者は引き続き98%の高ORRを示し,そのうち83%の患者はSCR,MPFSとMOSに達したが,27.7カ月のPFS率は54.9%,27.7カ月のOS率は70%であった。微小残留病またはMRDを評価できる61人の患者のうち、91.8%の患者が10歳でMRD陰性であった-5閾値を切る。MRD持続陰性少なくとも6カ月と12カ月の患者27カ月のPFS率はそれぞれ73%と78.8%であった。比較的長期的なデータでは,中央値の約1年間のフォローアップ以来,新たなCRSイベントの報告はないことが示されている。27.7カ月の中位フォローアップ期に新たなパーキンソン病バイタルサインと症状が認められ,従来は運動や神経認知治療−緊急脳梗塞と呼ばれていた。本年度報告日現在,患者状況は安定しており,機能は正常であり,SCR中である。
*2022年米国臨床腫瘍学会(ASCO)年次総会で発表され、2022年6月3日から7日まで、米国イリノイ州シカゴおよび仮想。
結論的に,これらの結果は,推奨された第2段階用量でCilta−celが制御可能な安全性を有し,大量の予備治療されたRRMM患者において早期,深く,持続的な反応を提供できることを示していると考えられる。
CARTITUDE−1の結果によると,試験1 b段階と第2段階の奏効率観察を含め,Cilta−cel BLAをFDAスクロールに提出する作業は2020年12月に開始され,2021年4月に完了した。Cilta-celマーケティング許可申請は2021年4月にEMAに提出され、NDAは2021年12月にPMDAに提出される。
CARTITUDE-2(アメリカ、ベルギー、フランス、ドイツ、オランダ、スペイン、イスラエル)
我々とJanssenは2019年11月にJNJ−4528の米国,ヨーロッパ,イスラエルでの多列開放ラベル第2段階試験に患者を募集し,CARTITUDE−2と呼ぶ。CARTITUDE−2は以下の6つのキューからなり,約157名の患者が登録されている
•まず1~3コース後にセファロスポリンで進行性MM患者を治療する
•一線治療後早期再発の多発性骨髄腫患者の治療
•プロテアソーム阻害剤,免疫調節療法,ダラツマブおよび抗BCMA治療に失敗したRRMM患者の治療
•セセロとレナドアミンの併用による造血幹細胞移植後完全に緩和されなかった多発性骨髄腫
•新たに診断された多発性骨髄腫患者の治療には,移植には計画がない
•新診断の多発性骨髄腫標準危険疾患患者の治療
この試験の各列の主な終点は、治療1年後のMRD陰性患者のパーセンテージである。各キューの結果に基づいて、規制機関の同意後に規制承認を提出することを潜在的に支援するために、これらの患者集団における私たちの調査の拡大を模索する予定である。我々はまた、MM患者の追加的な需要が満たされていないことを評価するために、より多くのキューを含むようにCARTITUDE-2を拡張する能力がある。Janssenと協力して,2022年の主要医学会議でCARTITUDE−2試験のより多くのデータを示す予定である。
A群の試験は20例のレナドアミン無効の進展性多発性骨髄腫患者に対する治療効果と安全性を評価し、これらの患者は1-3つの以前の治療方案を経た。2022年1月まで(中位フォローアップ時間17.1ケ月)、OORは95%、CR或いはそれ以上の率は90%であった。初回緩解の中位期間は1.0カ月,最適反応の中位期間は2.6カ月であった。中位有効時間(DOR)は達成されず,15カ月のPFS率は70%であった。すべてのMRD評価サンプルが10-5閾値に達した患者(n=16)はMRD陰性であった。≥中の20%の患者は好中球減少、血小板減少、貧血、リンパ球減少と白血球減少を含む血液学的副作用が出現した。95%の患者がCRSを発症し、30%の患者がCAR T細胞神経毒性を発症した。3人の患者(15%)は免疫効果細胞関連神経毒性症候群(ICANS)を出現した。運動や神経認知治療,突発的有害事象やパーキンソン病は認められなかった。4例の患者は毛包点滴後に死亡した:1例は新冠肺炎で死亡し(治療に関連して)、1例は膿毒症で死亡し(治療と関係なく)、2例は進行性疾患で死亡した
*国際骨髄腫協会(IMS)年次総会で発表された;2022年8月25日から27日まで、カリフォルニア州ロサンゼルス。
この試験のBコホートは19例の第一線治療後早期再発のMM患者のシルチゲーム使用の有効性と安全性を評価した。2022年6月まで(中央値は18カ月)、総有効率は100%であり、その中の90%の患者は完全な緩和を実現した。初回反応の中位時間は0.95カ月,最適反応の中位時間は5.09カ月であった。MRDを評価可能な15名の患者のうち,14名(93.3%)は10歳でMRDは陰性であった-5臨界点です。約20%の患者で観察された血液治療緊急有害事象(TEAES)には,好中球減少症,血小板減少症,貧血,リンパ球減少症,白血球減少症がある。CRS 16例(84.0%),ICAN 1例であった。1例の患者は注腸後38日目に運動と神経認知TEAEsが出現した。
*第64回米国血液学会(ASH)年次総会で発表;2022年12月10日から13日まで、米ロサンゼルスニューオーリンズ
試験したC群は、PI、IMiD、mAbおよび非細胞BCMA標的治療(ADCまたはBsAbを含む)を受けた20名の患者のシルチゲーム使用の有効性と安全性を評価した。2022年6月(平均18カ月間のフォローアップ)まで、ADCおよびBsAbに曝露された全キュー患者のOORは60%であり、その中に55%以上のVGPR患者が含まれていた。全キューでは,中位有効時間は12.3カ月,中位PFSは9.1カ月であった.MRD評価可能な10人の患者10人のうち-5閾値は,7例(70%)がMRD陰性であった。約20%の患者に認められた血液学的TEAEには,好中球減少症,血小板減少症,貧血,
リンパ球減少と白血球減少。12例(60%)の患者はCRSが発生し、4例の患者はICANが発生した。運動や神経認知治療の緊急AEs,MNTs/パーキンソン病症例は認められなかった。
 *第64回米国血液学会(ASH)年次総会で発表;2022年12月10日から13日まで、米ロサンゼルスニューオーリンズ
*第64回米国血液学会(ASH)年次総会で発表;2022年12月10日から13日まで、米ロサンゼルスニューオーリンズ
CARTITUDE-4(オーストラリア、オーストリア、ベルギー、デンマーク、フランス、ドイツ、イタリア、イスラエル、日本、大韓民国、オランダ、ポーランド、スペイン、スウェーデン、イギリス、米国)
われわれとJanssenは400名の患者の無作為開放ラベル3期試験を行っており,1~3つの以前の一連の治療を受けたRevlimid難治性MM患者をCARTITUDE−4と呼ぶ。患者は1:1ランダムな割合で標準治療(研究者はポアマイド/ポタゾミ/デキサメタゾンまたはダラトモノクロナル/ポアメタゾン/デキサメタゾンの間で選択)または単回シルセール治療を受ける。この実験の主な終点は進展のない生存だ。2023年1月27日,CARTITUDE−4がその主要終点に達したことが発表され,本研究の最初のあらかじめ指定された中期分析では,標準治療と比較してPFSが統計的に有意に改善したことが示された。独立したデータ監視委員会の提案の下で、この実験は盲目を解除された。
CARTITUDE-5(アルゼンチン、オーストラリア、オーストリア、ベルギー、ブラジル、カナダ、チェコ共和国、デンマーク、フィンランド、フランス、ドイツ、ギリシャ、ハンガリー アイルランド、イタリア、イスラエル、日本、大韓民国、オランダ、ノルウェー、ポーランド、ポルトガル、ロシア連邦、スペイン、スウェーデン、 スイスイギリスアメリカ)
われわれとJanssenは新たに診断されたMM患者650名のランダム,開放ラベル,全世界,マルチセンター,3期試験を行っており,CARTITUDE−5と呼ぶ。患者はランダムに1:1に分けられVRD誘導の標準看護を受けレレミテとデキサメタゾンを維持またはVRD誘導、その後単回投与(維持しない)。この実験の主な終点は進展のない生存になるだろう。
CARTITUDE-6(オーストラリア、ベルギー、チェコ、ギリシャ、イスラエル、日本、コラ共和国、オランダ、ノルウェー、スペイン、スイス、スウェーデン、アメリカ、連合王国)
ヨーロッパの骨髄腫ネットワークと協力することで (“EMN”)、我々とJanssenは、新たに診断されたMM患者750名において、ランダム、開放ラベル、全世界、マルチセンター、3期試験を行い、シルセル治療および自己幹細胞移植治療を比較する予定である。EMNは研究のスポンサーになることが予想される。この研究をEMN 028と呼び,これをCARTITUDE-6と呼ぶ.試験の二重主要終点はPFSと12ケ月持続したMRD陰性CRであり、次世代シークエンシングによって決定された(少なくとも10-5閾値)。
CARTITUDE-6のINDは2022年11月14日にFDAに提出され、受信された。その後、FDAは、米国INDの下での研究の継続を可能にする条件として、追加のセキュリティデータを提供することを要求し、主に、提案された用量およびスケジュールおよび提案された誘導スキームをサポートするために追加のセキュリティデータを要求することを含む。このような論評に基づいて、私たちとヤンソンは、EUでの少なくとも1つの施設の建設が完了すると、INDを撤回し、他の国でCARTITUDE-6を継続することを決定した。これらの他の国で行われている研究は、FDAが要求する追加のセキュリティデータを生成し、これらのデータは、INDをFDAに再提出するための基礎として使用されることが予想される。
アメリカで行われている他の1期臨床試験は
2022年11月にFDAはLB 2102の臨床開発を継続することができるIND申請を承認したことを発表し,LB 2102は広範な小細胞肺癌(SCLC)を治療するための成人患者の研究性自己CAR−T療法である。LB 2102は、Delta様リガンド3(DLL-3)を選択的に標的にするように設計されており、このリガンドは、小細胞肺癌、大細胞神経内分泌癌、いくつかの他の神経内分泌腫瘍およびいくつかの前立腺癌を含む様々な悪性腫瘍に高度に限定されている。DLL−3も腫瘍の成長、遊走、浸潤に関連している。第一段階は人類初の開放ラベル臨床研究であり、広範期小細胞肺癌患者とLCNEC患者におけるLB 2102の安全性と初歩的な治療効果を評価し、そして第二段階の推薦投与量を決定することを目的とした。
2022年6月にFDAは米国での第1段階臨床試験評価LB 1908のIND申請を承認したと発表した。LB 1908は研究中の自己CAR−T療法であり,高親和性VHH抗体によりClaudin 18.2を選択的に標的とし,再発あるいは難治性胃癌,食道癌(胃−食道境界を含む)あるいは膵癌の治療に用いられる。Claudin 18.2は密着結合タンパク質であり、通常これらの癌サブタイプの患者に発現される。第一段階は初のヒト開放ラベル多中心臨床研究であり、LB 1908の安全性と耐性を確定し、そして第二段階の推薦投与量を確定し、初歩的な治療効果を評価することを目的としている。
中国で行われている他の研究者による臨床前プロジェクトは
Cilta-cel以外に、著者らは自家と同種異体を含む広範な候補製品の組み合わせがあり、臨床前と臨床開発の異なる段階にある様々な癌に対して、いくつかの研究者が開始した試験中の癌を含む。我々は研究者から開始された臨床試験のデータを使用して、どの候補製品がより広範な臨床試験に入るかを決定する予定である
自己CAR−T製品候補臨床開発
われわれは,中国の再発と難治性進行肝細胞癌患者において一期単腕開放マーカー研究を行っているGPC 3に対する自己CAR−T療法を評価している。
我々は、中国で行われている開放ラベル研究者による1期単一腕試験において、進行性固形腫瘍(進行胃癌および非胃癌を含む)患者のためのclaudin 18.2に対する自己CAR−T療法を評価している。2022年6月にFDAは米国での第1段階臨床試験評価LB 1908のIND申請を承認したと発表した。“プロジェクト4.会社に関する情報−B.業務概要−我々の計画−米国で行われている他の第1段階臨床試験”を参照
2022年11月、FDAはLB 2102の臨床開発を継続することができるIND申請を承認したことを発表し、LB 2102は広範期小細胞肺癌(SCLC)成人患者を治療するための研究性自己CAR−T療法である。“プロジェクト4.会社に関する情報−B.業務概要−我々の計画−米国で行われている他の第1段階臨床試験”を参照
オープンタグ研究者による1期単腕臨床試験であるCD 19,CD 20およびCD 22に対する自己CAR−T療法を評価している中国に再発難治性B細胞リンパ腫を合併したオープンタグ研究者による1期単腕臨床試験であるCD 19,CD 20およびCD 22に対する自己CAR−T療法を評価している難治性B細胞急性リンパ球性白血病を再発した。
同種異体CAR−TとCAR−NK候補製品の臨床開発
再発や難治性多発性骨髄腫患者で開始された1期,単腕,開放マーカーの研究であるBCMAに対する同種異体ガンマデルタ(γδ)T細胞製品候補薬を評価している。
再発または難治性多発性骨髄腫患者の1期,単腕,開放マーカーに対する研究であるBCMAに対する同種異体CAR−NK細胞候補製品を評価している
われわれは,再発または難治性急性骨髄性白血病(AML)患者のためのオープンタグ研究者による1期単腕試験であるCD 33およびCLL−1に対する同種異体ガンマデルタ(γδ)T細胞療法を評価している
Janssen Biotech,Inc.との協力と許可協定。
2017年12月、Cilta-celを世界規模で開発·商業化する協力·許可協定(“ヤンソン協定”)をヤンソンと締結した。
ヤンソン協定によると、私たちはヤンソンに世界独自のcilta-celの共同開発と商業化のライセンスを付与した。我々と楊森は全世界発展計画と全世界商業化計画に基づいて、全世界範囲で協力して多発性骨髄腫を治療するシルゼルを開発と商業化する。
楊森は世界規模ですべての臨床試験を行うことを担当し、私たちのアメリカのチームと大中国のチームが参加します。私たちは大中華区の中国のための監督管理活動を行い、定価の許可と予約販売を獲得し、ヤンソンは世界の他の地区のための監督管理活動を行い、定価の審査と予約販売を獲得する。私たちとヤンソンは世界のすべての国で開発、生産と商業化コストおよび税前損益を均等に分担するが、大中国を除いて、私たちとヤンソンのコスト分担と損益分担はそれぞれ私たちの70%とヤンソンの30%になるだろう。
Janssenに許可されたライセンスと他の権利の代価として、Janssenは私たちに350.0ドルの前払いを支払い、私たちはJanssenから13.5億ドルまでの追加マイルストーン支払いを受ける資格がある。13.5億ドルのうち、双方が臨床開発計画を修正することに同意したため、最大2.8億ドルを受け取ることはできないかもしれません
決定は当初の計画通りに特定の裁判を行わないことにつながった。私たちは以前次のような記念碑的な支払いを受けました
•2019年1月、2019年9月、2020年1月はそれぞれ2500万ドル、3000万ドル、3000万ドルであり、我々のCARTITUDE-1臨床試験で指定された数の患者の投与量によると、
•2019年9月のマイルストーン支払いは、CARTITUDE-1臨床試験で指定された数の患者の応答データ読み取りを受信するための2500万ドルであり、OORが少なくとも50%であることを示している
•2021年1月にFDAとのBLA前会議を完了するために支払われた7500万ドルの記念碑的支払いは、米国で初めてCilta-celの上場申請を承認するために使用された
•2021年7月にEMAに提出されたマーケティング許可を受けるために支払われた1500万ドルのマイルストーン支払い
•2022年2月のマイルストーン支払い5000万ドルは、日本のPMDAにセキュリティプロトコルを提出し、私たちのCARTITUDE-5臨床試験で特定の数の患者を募集し、
•記念碑的な支払いは、2022年4月の間に、米国のマシュマロ商業化承認を受けたことに関連する5000万ドル。
また、特定の製造マイルストーンを実現し、2.1億ドルに達し、特定の貿易純販売マイルストーンを実現するための1.25億ドルのマイルストーン支払いを取得する資格があり、特定の未来の開発と規制マイルストーンを実現するために7.15億ドルに達する
また、私たちの協力が最初の利益年度を経験する前に、どの年も協力する予定の運営資金が5,000万ドル以下であれば、私たちはJanssenから前金を得る権利がある。この場合、Janssenが私たちに提供してくれた前払い金額は、協力年度の運営資本が5000万ドルを超えることに相当する。いかなる例年の前金総額も1.25億ドルを超えてはならず、いつでも未払いの前払い総額は2.5億ドルを超えてはならない。未償還前払金は“ウォール·ストリート·ジャーナル”が発表したロンドン銀行間同業借り換え金利(LIBOR)に2.5%を加算した。Janssenは、私たちが協力した税引前利益から分けられた前金と利息から回収する権利があり、いくつかの制限を受けた場合、協力および許可協定に従って私たちに支払わなければならないマイルストーンの支払いから回収する権利がある。私たちは、私たちの深刻な合意違反のため、統制権を変更したり、Janssenが協力と許可協定を終了したりしない限り、前金や利息を返済する他の義務はありません。私たちはいつでも自発的にその時返済されていない前払いまたは関連する利息の任意の部分を自ら決定することができます。2022年12月31日現在、同等立て替え金と利息の未返済元金総額はそれぞれ約250.0ドルと1,090万ドルである。LIBORの金融サービス業での使用停止に伴い、新たな金利計算方法を採用するためにJanssenプロトコルを改正することをJanssenと検討し始めている。
“ヤンソン協定”の有効期間内に、“ヤンソン協定”が許可される以外、私たちもヤンソンもciltcelを開発または商業化することはできない。さらに、“ヤンソン協定”が発効してから20年に及ぶ間、私たちおよびJanssenは、“ヤンソン協定”に準拠しない限り、BCMAの治療MMに対する任意のCAR-T細胞療法を単独で、または第三者と協力して開発または商業化してはならないが、合併、買収、許可内、または同様の取引のいくつかの例外を除いてはならない。
Cilta-celがまだ販売されている限り、ヤンソン協定は引き続き効果的になるだろう。私たちまたはJanssenは、他方の重大な違約行為が治癒されていないため、90日の通知後にJanssenプロトコルを終了することができます。Janssenはまた、(I)180日に吾等に通知した場合に無断で“Janssenプロトコル”を全部終了するか、または(Ii)予測不可能な重大なセキュリティイベントが発生した場合に全てのプロトコルを終了するように吾等に通知することもできる。いかなる終了後も、私たちはJanssenの知的財産権に基づいてJanssenに賠償することなく、独立してCilta-celを開発し、商業化する権利があるだろう。
楊森協定については、吾らは二零二年二月二十八日に仮製品供給協定(“IPSA”)を締結し、この合意に基づき、吾らは世界(大中国を含まない)で楊森に臨床及び商業用途に応用する注腸を提供する。IPSAによると、Janssenは製品の生産と供給に必要な総コストに基づいて、供給された製品の譲渡価格を支払います。しかし,最終的には,ヤンソン協定によると,製品の商業供給と臨床供給のコストは,我々とヤンソンがそれぞれ“許容費用”と“開発コスト”として均等に分担される。IPSAは、2023年6月30日まで、またはヤンソン協定に従って設立された共同製造委員会(“JMC”)によって決定された代替日まで有効である。IPSAはまた
ヤンソン協定が満了または終了した場合、終了する。私たちはIPSAの代わりにJanssenと製品供給協定を結ぶ予定だ。
原材料.原材料
私たちは現在、細胞、化学品、水、サイトカイン、担体、核酸、抗体、媒体、血清、緩衝液など、私たちの候補製品を生産するために必要ないくつかの生物学的材料を専門的な第三者から調達している。私たちはサービス協定を通じてこのような原材料を獲得し、体系的に長期供給契約を締結しなかった。しかし、私たちの各サプライヤーは多くの潜在的な長期代替品を持っているため、競争力のある価格設定が実現されたと信じている。一般的に、私たちが購入した主要な生物原料と出発原料の価格は安定しているか、あるいは限られた範囲で変動している。ある程度、価格変動の影響を受けていますが、私たちは通常、候補製品の早期開発段階のため、短期的にコスト増加を転嫁できないと予想されています。
商業化する
我々は、CARVYKTIの米国での商業化を支援するために、販売、マーケティング、運営インフラを構築している。Janssenとの協力と許可協定によると、私たちは米国全体の商業化作業の50%を実行することを選択する権利があります(Janssenが独占的な実行権を持ついかなる活動も含まれていません)。Janssenは双方が合意した商業化計画に基づき、米国と中国を除くすべての国でCiltcelを商業化する。もし私たちが中国大中華区でCilta-celを発売すれば、私たちはそこで商業化努力をリードし、楊森はそこで総商業化努力の30%までを選択する権利があり、私たちが独占的に行う権利がある活動は含まれていない。私たちの候補製品を開発段階から市場承認段階に押し上げるにつれて、各候補製品のいくつかのビジネス戦略を評価します。これらの戦略には,我々の外部販売組織をさらに拡大し,他の薬物開発会社と共同マーケティング協力協定を締結したり,他の薬物開発会社に製品をライセンスしたりすることが含まれる可能性がある。
知的財産権
知的財産権は私たちの分野と全体的なバイオテクノロジー分野で必須的だ。我々は、特許権を求め、維持し、守ることにより、内部開発、第三者から取得された特許権であっても、第三者から取得された特許権であっても、我々の業務発展に重要なビジネス的意義を有するノウハウ、発明、改善を保護し、強化することを求める。孤児薬の指定,開発·審査の加速,データ独占性,市場独占性,特許期限延長などによる規制保護も求めている。
私たちはすでに私たちの臨床候補とプラットフォーム技術のためにアメリカと国際的に特許保護を求めている。2022年12月31日まで、私たちは世界で43件の発表された特許と549件の未解決特許出願を持っていて、私たちの開発プラットフォーム、商業製品、臨床製品、臨床前製品をカバーしています。このような出願は特許の発行につながらない可能性があり,確かに特許が発行されていても,このような特許の形態は我々の製品に意味のある保護を提供しない可能性がある.私たちはまた私たちの業務発展に必須的かもしれない商業秘密に依存している。商業秘密は保護することが難しく、私たちに限られた保護を提供することしかできない。
私たちは、既存および新しい臨床候補、ならびに新しいプラットフォームおよびコア技術を支援するために、より多くの特許出願を提出する予定だ。私たちのビジネス成功は、私たちの現在および未来の候補製品の獲得と維持、およびこれらの製品を開発および製造するための方法の特許保護および商業秘密保護にある程度依存し、これらの特許を第三者の挑戦から保護し、他人の独占権を侵害することなく運営されるであろう。私たちが第三者が私たちの製品を製造、使用、販売、提供、または輸入することを阻止する能力は、これらの活動をカバーする効果的かつ強制的に実行可能な特許または商業秘密の下で当社が所有する権利の程度に依存する。私たちは、私たちの任意の保留特許出願または未来に提出された任意の特許出願に特許を付与するかどうかを決定することができず、将来私たちに付与される可能性のある任意の特許が、私たちの候補製品、発見計画、およびプロセスを保護する上で商業的に有用であることを保証することはできない。このリスクおよび私たちの知的財産権に関するより包括的なリスクについては、第3.d項を参照されたい。“リスク要因--私たちの知的財産権に関連するリスク”
個別特許の期限は特許を取得した国の法的期限に依存する。私たちが出願したほとんどの国では,米国を含め,特許期間は非臨時特許出願が提出された最初の日から20年である。米国では,特許期間の延長は特許期限調整によって延長することができ,特許権者が米国特許商標局の行政遅延による損害を補償することになる (“USPTO”)
特許の審査及び付与、又は以前に提出された特許のために特許が最終的に放棄された場合、又は特許権者が出願を遅延させた場合、短縮することができる。米国では,FDAが承認した薬物をカバーする特許期限も特許期間を延長する資格があり,FDA規制審査中に失われた特許期限の補償として特許期限の回復を可能にしている。ハッジ-ワックスマン法は特許期間を特許満了後最大5年間延長することを許可している。特許期間の延長の長さは,薬物が規制審査を受ける時間の長さと関係がある。1つの特許の残り期間は、製品が承認された日から14年を超えてはならず、承認された薬物に適した特許を延長することしかできず、承認された薬物、その使用方法、またはその製造方法に関する請求項を延長することしかできない。欧州や他の外国司法管区にも同様の規定があり、承認された薬物をカバーする特許の期限を延長する。将来、私たちの製品がFDAの承認を得たら、私たちはこれらの製品の特許出願のために特許期間を延長する予定です。私たちは、任意の管轄区域で取得可能な任意の発行された特許のために特許期間の延長を求めることを計画していますが、米国のFDAを含む適用当局は、このような延長を承認すべきかどうか、および承認されれば、そのような延長の長さの評価に同意することに同意します。我々の知的財産権に関連するリスクに関するより多くの情報は、第3.d項を参照されたい。“リスク要因--私たちの知的財産権に関連するリスク”
場合によっては、一時的または優先特許出願として、中国特許庁(CNIPA)を含む米国特許商標局または世界各地の他の特許機関に直接特許出願を提出する。対応する非一時的特許出願は、一時的または優先的出願日の12ヶ月以内に提出されなければならない。我々は,我々の一時的または優先的な特許出願に関連する非一時的な特許出願をタイムリーに提出する予定であるが,このような特許出願が競争優位性を提供してくれる特許の発行につながるかどうかは予測できない.
私たちは非臨時出願と特許協力条約を提出します (“PCT”)は,より早く提出された仮出願又は優先権出願の優先権日利益の出願(例えば,適用)を有することを要求する。PCT制度は、特許出願の最初の優先日の後12ヶ月以内に単一出願を提出することを許可し、すべてのPCT加盟国を指定し、これらの国の後にPCTによって出願された国際特許出願に基づいて国家特許出願を出願することができる。PCT検索機関は、特許性検索を実行し、申請料を生成する前に外国国出願の成功機会を評価するために使用することができる拘束力のない特許性意見を発表する。PCT出願は特許として発行されていないが、出願人が国家段階出願を介して任意の加盟国で保護を求めることを可能にしている。特許出願の第1の優先権の日から2年半の期限が終了したとき、PCTのどの加盟国も直接国家出願を通過することができ、または場合によっては欧州特許機関のような地域特許組織を介して単独の特許出願を出願することができる。PCTシステムは費用を遅延させ、国/地域特許出願の成功機会の限られた評価を可能にし、出願が出願の最初の2年半以内に放棄された場合に大量の節約を実現した。
すべての特許出願について、私たちは具体的な状況に基づいて特許請求戦略を決定するつもりだ。私たちはいつも弁護士の提案と私たちのビジネスモデルと需要を考慮するつもりだ。私たちは、私たちのノウハウおよび任意の製品のすべての有用なアプリケーションを保護し、これらのアプリケーションが戦略的価値を有することを前提として、既存技術および製品のために発見されたすべての新しいアプリケーションおよび/または用途を保護することを要求する特許出願の提出を求めている。我々は、既存の特許庁規則及び規定に基づいて、私たちのプロセス及び組成のために最大のカバー面及び価値を追求するために、特許出願の数及びタイプ、並びに未解決及び発表された特許出願を絶えず再評価する。また、特許訴訟中には、私たちの知的財産権および業務ニーズを満たすためにクレームが修正される可能性がある。
特許保護を得る能力およびこのような保護の程度は、従来技術の範囲、発明の新規性および非顕著性、および特許法実施要件を満たす能力を含む多くの要因に依存することを認識している。さらに、特許出願において要求されるカバー範囲は、特許発行前に大幅に縮小することができ、特許発行後であっても、その範囲を再解釈またはさらに変更することができる。したがって、私たちは私たちの未来の任意の候補製品や私たちの技術プラットフォームのために十分な特許保護を獲得または維持することができないかもしれない。私たちが現在求めている特許出願が任意の特定の司法管轄区域で特許として発行されるかどうか、または任意の発行された特許の権利主張が競争相手の影響を受けないように十分な特許保護を提供するかどうかを予測することはできない。私たちが持っているどんな特許も第三者によって挑戦され、回避され、無効に発表される可能性がある。
特許保護に加えて、私たちは商標登録、商業秘密、ノウハウ、他の独自情報、および持続的な技術革新に依存して、私たちの競争的地位を発展させ、維持しています。私たちは、私たちの業務において特許保護から保護されているか、または特許保護に適していないと考えられる側面を保護し、保護し、独自の情報の機密性を維持することを求めている。私たちは、当社の従業員やコンサルタントと契約を締結することを含む、当社の独自情報およびビジネス秘密を保護する措置をとっていますが、第三者は、実質的に同じ独自の情報および技術を独立して開発したり、他の方法で私たちのビジネス秘密を取得したり、当社の技術を開示したりすることができます。したがって、私たちは私たちの商業秘密を意味的に保護することができないかもしれない。私たちの政策は
私たちの従業員、コンサルタント、外部科学協力者、賛助研究者、および他のコンサルタントが、私たちとの雇用またはコンサルティング関係を開始する際に秘密協定を実行することを要求します。これらの合意は、個人と私たちとの関係中に開発または開示された当社の業務または財務に関するすべての機密情報は、特定の場合を除いて第三者に開示されてはならないことを規定している。私たちと従業員の合意はまた、従業員が私たちに雇われた過程で構想されたすべての発明または従業員が私たちの機密情報を使用することによって生成されたすべての発明が私たちの固有財産であることを規定している。しかしながら、このようなセキュリティプロトコルおよび発明譲渡プロトコルは違反される可能性があり、このような違反に対応するための十分な救済措置がない可能性がある。しかも、私たちのビジネス秘密は競争相手に知られたり独立して発見されるかもしれない。私たちのコンサルタント、請負業者、または協力者が、私たちのために働いているときに他人が所有している知的財産権を使用する場合、関連またはそれによって生じる商業秘密、ノウハウ、および発明の権利について議論が生じる可能性がある。我々の知的財産権に関連するリスクに関するより多くの情報は、第3.d項を参照されたい。“リスク要因--私たちの知的財産権に関連するリスク”
私たちのようなバイオテクノロジー会社の特許地位は通常不確実であり、複雑な法律、科学、および事実の問題に関連している。私たちのビジネス成功はまた第三者の独占権を侵害しないことにある程度依存するだろう。第三者特許は、私たちの開発または商業戦略、または私たちの製品またはプロセスを変更し、許可を得たり、いくつかの活動を停止することを要求するかもしれません。私たちは、任意のライセンス契約に違反したり、将来の製品を開発または商業化するために必要な独自の権利の許可を得ることができず、私たちに実質的な悪影響を及ぼす可能性があります。もし第三者が米国で準備して提出した特許出願も権利の技術を要求する場合、私たちは発明の優先権を決定するために、米国特許商標局の干渉または派生プログラムに参加しなければならないかもしれない。詳しくは“プロジェクト3.D.リスク要因-私たちの知的財産権に関するリスク”を参照されたい
市場独占性を拡大するために使用可能な場合、私たちの戦略は、現在または予想される開発プラットフォーム、技術コア要素、および/または臨床候補対象に関連するかもしれない追加の知的財産権を得ることである。
会社が持っている知的財産権
私たちは2016年8月に提出された発表されたPCT申請と、2017年8月に提出されたCilta-cel BCMA候補製品に関連する発表されたPCT申請を持っている。この2つのPCTは、米国、大中華区中国(大陸と香港)、イエメン、サウジアラビア、カタール、オマーン、バーレーン、エジプト、アラブ首長国連邦、ヨーロッパ、韓国、ブラジル、カナダ、チリ、コロンビア、コスタリカ、ユーラシア、イスラエル、インド、日本、メキシコ、フィリピン、ウクライナ、ベトナム、マレーシア、南アフリカ、シンガポール、オーストラリア、ニュージーランドを含む複数の司法管轄区域の特許カバー範囲を取得するために102件の国家段階出願を提出した。2022年12月31日現在、Cilta-celに関する28件のライセンス特許(米国特許4件、中国特許3件、オーストラリア特許3件、日本特許3件、南アフリカ特許2件を含む)を取得している。もし発行されれば、これらの申請が発行された構成事項クレームは2036年と2037年に期限が切れると予想される。
Cilta-cel BCMA標的CAR-T細胞による多発性骨髄腫の治療について、著者らは2021年12月に提出したPCT出願、2022年11月に提出されたPCT出願、2022年5月に提出されたPCT出願、2022年2月に米国で提出された臨時特許出願、及び2022年11月に米国で提出された臨時特許出願を有している。ジェイソンは私たちのこのような申請書の共同申請者だ。発行されれば,これらの出願から発行される構成事項クレームは2041年,2042年,2043年に満了する予定である
我々のClaudin 18.2候補製品については、2020年に提出され、米国、ヨーロッパ、大中国、日本などの重要な司法管轄区域で全国段階に入っている米国以外のPCT申請を持っている。もし発行された場合、本出願が発行する事項構成クレームは2040年に満了する予定です。
我々のCD 19/CD 20/CD 22候補製品については、2021年7月に提出された4つの米国海外特許出願を有しており、これらの出願は2023年に国家段階に入る。発行された場合、本出願が発行する事項構成クレームは2041年に満了する予定です。
CD 33/CLL-1候補製品については、2021年3月に米国、大中国、欧州、カナダ、オーストラリアを含む2つの米国以外の特許出願と2019年9月に提出された係属中のPCT出願を2つ持っています。もし発行されれば、これらの申請が発行された構成事項クレームは2039年に満了する予定だ。
我々のGPC−3候補製品については,2020年2月に提出され,米国,ヨーロッパ,大中国,日本などの主要な司法管轄区で国の段階に入っているPCT特許出願を有している。もし発行されれば、これらの申請が発行された構成事項クレームは2040年に満了する予定だ。
我々のDDL 3候補製品については、2020年7月に提出され、米国、ヨーロッパ、大中国、日本などの主要な司法管轄区域で国家段階に入っているPCT特許出願を持っている。もし発行されれば、これらの申請が発行された構成事項クレームは2040年に満了する予定だ。
我々のGamma Delta T-cell BCMA候補製品については、2020年12月に提出されたPCT特許出願と、2020年4月に提出されたPCT特許出願とを有しており、いずれも米国、ヨーロッパ、大中国、日本などの重要な司法管轄区域で国家段階に入っている。
製造業
細胞療法の製造と患者への提供は複雑,総合的な過程に関与している。細胞療法の商業成功には信頼性、拡張可能と経済的な製造技術が必要である。我々は大量の資源を投入してプロセス開発と製造を行い,プロセスロバスト性を最適化し,細胞療法候補製品開発の失敗率を低下させ,我々の単位製造コストを低減し,規制機関の候補製品の承認を得た後,地域と地球規模を迅速に実現できるようにしている。
私たちが米国でJanssenと協力している製造施設は現在、アメリカとEU市場にCARVYKTIを供給しており、もし私たちが他の国で承認されれば、このような施設を使用して他の国に供給する予定です。私たちの試験の臨床材料は私たちのアメリカ機関と私たちの中国の機関が提供します。私たちは、私たちのアメリカ工場の商業規模製造能力をさらに拡大し、ヨーロッパとアメリカ市場の商業供給を満たすためにベルギーに製造施設を建設し、より多くの市場で提供することが可能であると考えています。また,Janssenについては,我々の臨床·商業供給製造施設を補完するための第三者CMOの使用を接触·求めている初期段階である。
私たちは、私たちのすべての候補製品を製造するのに適した汎用プラットフォームを提供するために、システム化された製造方法を採用している。このプラットフォームは、並列処理を可能にし、制御された環境において経済コストで商業供給に拡張することができる。著者らはウイルス伝達過程を改善し、処理不一致を最小限に抑え、失敗率を下げることを支援した。また、私たちの製造と物流プロセスは、出荷中に製品の完全性を維持し、出荷を正確に追跡し、追跡することを目的としています。
私たちの製造と商業化戦略は完全に統合された製品配送サイクルを必要とする。我々の細胞療法の早期開発段階では,米国,中国,ヨーロッパで商業化に適した製造プラットフォームプロセスと製造能力を持つことが競争優位であると信じている。時間が経つにつれて、地域製造能力を拡大し、CMOと交渉し、商業化が予想される製品需要を満たすことが予想される。私たちの施設は拡張しやすいように設計されているため、Cilta細胞と新しい管路計画に対する期待される将来の臨床と商業の需要を満たすことができると信じている。
私たちは、私たちが拡張可能な強力な製造プロセスと、私たちのノウハウと業界の経験豊富なチームは、潜在的な競争相手にとって挑戦的であり、複製コストも高いと信じている。
競争
CARVYKTIは標準看護治療以外に,バイオ製薬会社,学術研究機関,政府機関および公共·民間研究機関が開発した新しい療法と競争し,どの将来の製品も競争する。
ノワールとKiteはFDAの承認を得た最初の自己T細胞療法である。2017年8月、ノワールはFDAの許可を得て、Kymriahを商業化し、難治性或いは少なくとも2回再発した急性Bリンパ球性白血病(ALL)の児童と若者の治療に使用した。2018年5月、KymriahはFDAの承認を得て、再発或いは難治性びまん性大B細胞リンパ腫(DLBCL)の治療に使用した。2017年10月、KiteはFDAの承認を得てYescartaを商業化し、Yescartaは再発または難治性大B細胞リンパ腫および濾胞性リンパ腫の成人患者の治療に使用された最初のCAR-T細胞候補製品である。Kiteはまた別の市販の自己CAR-T製品Tecartusがあり、再発性或いは難治性マントル細胞リンパ腫(MCL)或いは再発性或いは難治性B細胞前駆体急性リンパ球性白血病(ALL)の成人患者に適している。2021年、百時美施貴宝
SquibbはJuno Treeutics/Celgeneの買収によりFDAによる抗CD 19 CAR−T療法Breyanzi(Liso−cel)の承認と,ブルーバード生物会社と協力した初の抗BCMA CAR−T療法Abecma(ide−cel)を獲得した。
細胞療法は臨床試験で良好な治療効果があるため,既存と新たにこれらの療法を開発した会社からの競争がますます激しくなることが予想される。
私たちの潜在的なCAR-T細胞療法の競争相手は
•BCMAに対する多発性骨髄腫に対する細胞療法を開発した会社は,異遺伝子治療会社,Autolus治療会社,ブルーバード生物会社,百時美施貴宝社,CARsgen治療ホールディングス,Arcell x,Celyad Oncology,亘喜生物,InnoventBiologics,ポセイダ治療会社,ノワ製薬と精密会社である 生物科学会社
•学術医学センターはBCMA CAR-T技術の自主開発に取り組んでいる
•他にBCMA標的療法療法を開発したMM治療会社には,安進社,Regeneron製薬会社,グラクソ·スミスクライン社,百時美施貴宝社,ジョンソン社(Cilta−celのパートナーヤンソン社の親会社),エバービー社,ファイザー社がある。
この点で、我々のCilta−celパートナーJanssenは、BCMAおよびCD 3の既製のT細胞配向に対する二重特異性抗体であるTecvalyi(teclistamab-cqyv)のために、2022年10月にFDAによって承認された。
また,試験地点,われわれの試験登録者数,我々が狙っているもの,将来的に照準を合わせる可能性のある疾患など,細胞療法を開発している多くの会社と競合している。また,アジアでの開発に専念している細胞療法会社と競争する可能性がある。
さらに、私たちのビジネス成功は、私たちと私たちの協力者が、私たちの製品および任意の未来の候補製品を開発、製造、マーケティングおよび販売する能力に依存し、第三者の知的財産権および他の固有の権利を侵害、流用、または他の方法で侵害することなく、私たちの独自およびモジュール化されたCAR-T細胞技術を使用する。バイオテクノロジー分野には,CAR−T細胞療法分野や,我々の競争相手が所有または制御する特許を含む多くの第三者米国および非米国から発行された特許が存在する。しかも、バイオテクノロジー分野の特許侵害疑惑もしばしば発生している。第三者は、私たちの競争相手を含めて、Cilta-celを含む私たちの候補製品を主張するかもしれないが、その中のいくつかの特許を侵害している。私たちのどのような特許主張に対しても、私たちは有効な抗弁を持つと信じていますが、このような抗弁は成功しないかもしれません。私たちに対する特許侵害クレームは成功する可能性があり、損害賠償責任を負い、大量の許可、使用料、その他のお金を支払うこと、あるいは開発、製造、マーケティング、商業化侵害製品の開発を停止することを要求します。さらに、もし私たちが候補製品のために特許保護を獲得して維持することができない場合、あるいは取得されたまたは許可された特許保護の範囲が十分でない場合、またはそのような特許保護の有効性が脅かされた場合、競争相手のために市場に参入する機会を作ることができないかもしれないし、他社が私たちと協力して製品や技術を開発することを阻止する可能性があり、これらはいずれも私たちの競争地位を損なうことになり、私たちの候補製品を商業化することに成功する能力を弱める可能性があるからだ。
私たちの多くの競争相手は、単独あるいはパートナーと協力しても、研究開発、臨床前試験、臨床試験、製造とマーケティング方面の財力と専門知識はすべて私たちよりずっと多い。将来の協力とM&Aは、より少ない数の競争相手に資源をさらに集中させる可能性がある。
もし私たちの競争相手が私たちが開発する可能性のある製品よりも安全で、より効果的で、副作用が少なく、より効率的で便利で、より安価な製品を開発·商業化すれば、私たちのビジネス潜在力は減少または解消されるかもしれない。私たちの競争相手も私たちよりも早くFDAや他の規制機関からその製品の承認を得ることができ、これは私たちの競争相手が私たちが市場に入る前に強力な市場地位を確立したり、私たちの開発をもっと複雑にしたりする可能性がある。著者らのすべてのプロジェクトの成功を影響する重要な競争要素は有効性、安全性、製造成功と患者参入である可能性がある。
これらの競争相手はまた臨床試験のために類似の合格科学と管理人材バンク、場所と患者集団、及び著者らの計画のために補充或いは必要な技術を奪い合う可能性がある。
政府の監督管理
アメリカの法規
FDAと連邦、州と地方の各レベル及び国外の他の監督管理機関は著者らが開発している生物製品の研究、開発、テスト、製造、品質管理、輸出入、安全、有効性、ラベル、包装、貯蔵、流通、記録保存、承認、広告、販売促進、マーケティング、承認後の監視と承認後の報告などの方面に対して広範な監督管理を行った。私たちは、第三者請負業者と共に、私たちが研究したい、または承認を求めることができるかもしれない国/地域規制機関の様々な臨床前、臨床、および商業承認要件を満たすことが要求されるだろう。
米国では、FDAは“連邦食品、薬物と化粧品法”及びその実施条例とその他の法律に基づいて生物製品を規制し、生物製品については、“公衆衛生サービス法”を含む。私たちの候補製品は生物製品としてFDAによって規制されている。生物製品は米国で発売される前に,米国食品·薬物管理局のBLAと許可証を提出する必要があり,承認となった。最初の製品CARVYKTIを除いて、2022年2月28日にFDAの承認を得ましたプロテアソーム阻害剤、免疫調節剤、および抗CD 38モノクロナル抗体を含む4つ以上の治療を以前に受けた再発性または難治性多発性骨髄腫を治療するための成人患者私たちの候補製品はFDAの承認を得てアメリカで発売されませんでした。製品開発、臨床試験、承認過程中または承認後のいつでも、適用されるFDAまたは他の要求を遵守しなければ、行政または司法制裁を受ける可能性がある。これらの制裁には、FDAが未解決の申請の承認を拒否すること、承認された申請を一時停止または撤回すること、警告状、製品のリコール、製品の差し押さえ、製造または流通の完全または部分的な一時停止、禁止、罰金、民事罰、または刑事起訴を含むことができる。
FDAがバイオ製品候補製品が米国で発売される前に必要とされるプログラムは、一般に以下のような態様を含む
•FDAの良好な実験室のやり方に基づいて臨床前実験室テストと動物研究を完成する(“プロス”)法規制
•臨床試験が開始される前に発効しなければならず、毎年更新されるか、または大きな変化が生じたときに更新されなければならないINDをFDAに提出する
•試験の前に、各臨床場所の独立機関審査委員会(“IRB”)または道徳委員会の承認 すでに始まっている
•提案された候補生物製品の期待適応に対する安全性と有効性を決定するために、十分かつ良好に制御された人体臨床試験を行った
•重要な臨床試験から十分なデータが得られた場合、BLAを準備してFDAに提出する
•FDAはBLAを受信してから60日以内に再審申請を受けることを決定した
•適用されれば、FDA諮問委員会の審査が満足的に完了する
•CGMPのコンプライアンスを評価し、施設、方法、および生物製品の持続的な安全性、純度および効力を維持するのに十分な制御を確保し、良好な臨床実践またはGCP法規のコンプライアンスを評価するために、FDAの生産推奨製品の1つまたは複数の製造施設の承認前検査を満足的に完了させる
•FDAは、米国で使用される特定の適応の製品の商業マーケティングを可能にするためにBLAを審査および承認する。
臨床前と臨床発展
米国で最初の候補製品の臨床試験を開始する前に,IND申請をFDAに提出しなければならない。IND申請はFDAが研究用新薬製品のヒトへの輸送·管理を許可する請求である。IND申請の中心焦点は臨床研究の全体的な研究計画と方案である。IND出願はまた、製品の毒性学、薬物動態学、薬理学的および薬効学的特徴を評価する動物およびインビトロ研究結果、化学、製造および制御情報、および研究製品の使用を支援するための任意の利用可能なヒトデータまたは文献を含む。INDはヒト臨床試験が始まる前に発効しなければならない。IND自動
FDAが30日以内に提案された臨床試験に対して安全懸念または問題を提起しない限り、FDAが受領してから30日後に発効する。INDスポンサーが30日間でFDAの懸念を満足に解決できなければ、INDは臨床的に放置される可能性がある。INDスポンサーおよびFDAは、INDがFDA承認および臨床試験を開始する前に、任意の未解決の問題または問題を解決しなければならない。したがって,INDの提出はFDA認可による臨床試験の開始につながる可能性があり,そうでない可能性もある。
臨床試験は、GCPに従って合格した研究者の監督の下でヒト被験者に研究製品を服用することを含み、すべての研究被験者に任意の臨床研究への参加についてインフォームドコンセントを提供することを含む。臨床試験は,研究目標を詳細に説明し,安全性をモニタリングするためのパラメータと評価する有効性基準のシナリオで行った。一般に、製品開発中に行われる各後続の臨床試験および任意の後続のレジメン修正は、既存のINDに個別に文書を提出しなければならない。また,臨床試験を推奨する各地点の独立IRBは,その地点で臨床試験を開始する前に任意の臨床試験の計画とそのインフォームドコンセントを審査·承認しなければならず,完成まで研究を監視しなければならない。規制当局、IRB、またはスポンサーは、対象が受け入れられない健康リスクに直面していることを発見すること、または試験がその目標を達成する可能性が低いことを含む、様々な理由で臨床試験を随時一時停止することができる。いくつかの研究はまた、臨床研究スポンサーによって組織された独立した合格専門家グループの監督を含み、このグループはデータ安全監視委員会(DSMB)と呼ばれ、この委員会は研究中のあるデータへのアクセスに基づいて、研究が指定されたチェックポイントで提案すべきかどうかについてアドバイスを提供する。Dsmbが被験者に受け入れられない安全リスクがあると判断した場合、または他の理由に基づいて、有効性が証明されていなければ、臨床試験の中止を推奨することができる。現在行われている臨床研究や臨床研究結果を公的登録機関に報告することに関する要求もある。
BLAの承認を得るために,ヒト臨床試験は通常3つの重複可能な連続段階に分けて行われる。
•段階1-研究製品は、健康なヒト対象または標的疾患または状態を有する患者に最初に導入される。これらの研究は、人体内での製品の安全性、用量耐性、吸収、新陳代謝と分布、および用量増加に関連する副作用をテストし、可能な場合に有効性の早期証拠を得ることを目的としている。腫瘍学的適応のために開発された研究製品では,第一段階試験は通常重篤あるいは生命にかかわる疾患を有する患者で行われ,他の治療代替案はない。
•第二段階-初期治療効果、最適用量および用量計画を評価し、可能な不良副作用および安全リスクを決定するために、特定の疾患または状態の限られた患者集団のための製品を研究する。より大規模かつより高価な3期臨床試験を開始する前に、複数の2期臨床試験を行って情報を得ることができる。深刻なまたは生命を脅かす疾患を有し、利用可能な治療法を有さない患者のいくつかの適応については、積極的な利益リスクプロファイルが示されている場合、第2段階試験のデータからBLA承認を得ることができる。
•第三段階-製品を拡大した患者群に研究し、用量を更に評価し、臨床治療効果の統計的に意義のある証拠を提供し、そして更に安全性をテストし、通常複数の地理的に分散した臨床試験地点で行われる。これらの臨床試験は研究製品の全体的なリスク/収益比率を確定し、製品の承認に十分な基礎を提供することを目的としている。
臨床試験と同時に、会社は追加の動物研究を完成させ、候補製品の生物学的特性に関する追加情報を開発することができ、cGMP要求に基づいて商業量産製品の過程を最終的に決定しなければならない。製造過程は高品質の候補製品ロットを持続的に生産できる必要があり、特に最終製品の特性、強度、品質と純度をテストする方法を開発しなければならない、あるいは生物製品に対しては、安全、純度、効力の試験方法を開発しなければならない。また,適切な包装を選択·テストし,候補製品が賞味期限内に受け入れられない変質が生じないことを証明するために安定性研究を行わなければならない。
場合によっては、FDAは、製品が承認された後に追加の臨床試験を自発的に実施して、製品に関するより多くの情報を得ることを要求する可能性がある。このようないわゆる第4段階研究は“法案”を承認する条件かもしれない。
BLA提出と審査
すべての適用された法規要件に基づいて必要なすべてのテストが成功したと仮定すると,製品開発,非臨床研究,臨床試験の結果はBLAの一部としてFDAに提出され,その製品を1つまたは複数の適応の市場に使用することの承認が求められる。BLAは,否定や曖昧な結果や積極的な発見,製品の化学,製造,制御,アドバイスのラベルなどに関する詳細な情報を含む関連する臨床前および臨床研究から得られたすべての関連データを含まなければならない。BLAを提出するには、免除または免除が適用されない限り、FDAに相当な申請使用料を支払う必要がある。
元のBLAが提出されると、FDAは、申請を提出することができるかどうかを決定するために60日の時間を有する。FDAが申請表面に欠陥があると判断した場合、全面審査の可能性を排除し、FDAは審査申請を受け入れず、スポンサーに提出拒否の書簡を発行する可能性がある。FDAが申請を提出することができると判断した場合、FDAは、出願を受けてから10ヶ月以内に審査基準申請を行うことを目標としているか、または申請が優先審査資格を満たしている場合、FDAが提出申請を受けてから6ヶ月以内に審査基準申請を行うことを目標としている。標準審査および優先審査では、補足情報または明確化に対するFDAの要求は、審査プロセスを著しく延長することができる。FDAは、製品が安全で、純粋かつ有効であるかどうか、およびその製造、加工、包装、または保持されている施設が、製品の持続的な安全、純度および効力を保証するための基準に適合しているかどうかを決定するためにBLAを審査する。FDAは諮問委員会を招集し,審査申請について臨床的知見を提供する可能性がある。BLAを承認する前に、FDAは通常、製品を生産する1つまたは複数の施設を検査する。FDAは、製造プロセスおよび施設がcGMP要件に適合していることを決定し、要求された仕様の下で製品が一貫して生産されることを保証するのに十分でない限り、申請を承認しないであろう。さらに、BLAを承認する前に、FDAは、GCPに適合することを確実にするために、通常、1つまたは複数の臨床場所を検査する。FDAが申請、製造プロセス、または製造施設が受け入れられないと判断した場合、提出された文書において欠陥を決定し、追加の試験または情報の提供を要求することが多い。任意の要求された補足情報が提出されたにもかかわらず、FDAは最終的に、その申請が承認された規制基準を満たしていないと決定する可能性がある。
FDAがBLAを評価し、商業製品および/またはその薬物を生産する製造施設を検査した後、FDAは承認状または完全な返信を発行することができる。承認書は、製品の商業マーケティングを許可し、特定の適応に関する具体的な処方情報を提供する。完全な返信は、FDAがBLAで発見されたすべての欠陥を記述するが、FDAが申請をサポートするデータが承認をサポートするのに不十分であると判断した場合、FDAは、必要な検査、試験提出された製品バッチ、および/または提案されたラベルを最初に検討することなく、完全な返信を発行する可能性がある。完全な返信を発行する際に、FDAは、BLAがより多くの情報の提供または明確化を要求することを含む、BLAが承認された条件であるように、申請者がとる可能性のある行動を提案する可能性がある。適用される規制基準を満たしていない場合、FDAは、製品の安全性または有効性を監視するために、追加の試験または情報を要求し、および/または上場後の試験および監視を要求するBLAの承認を延期または拒否することができる。
1つの製品が規制部門の承認を受けた場合、このような承認は特定の適応が付与され、製品が発売される可能性のある指定用途の制限をもたらす可能性がある。FDAはまた,提案されたラベルの変更,十分な制御や仕様の作成,承認後のセキュリティ対策などを条件に承認することも可能である.例えば、FDAがCARVYKTIを承認したように、FDAは、製品のメリットがそのリスクよりも大きいことを確実にするために、BLAのリスク評価および緩和戦略(“REMS”)計画を承認する可能性がある。REMSは、製品に関連する既知または潜在的に深刻なリスクを管理し、そのような薬剤の安全な使用を管理することによって、患者がこれらの薬剤を継続的に得ることを可能にするための安全戦略であり、制限された分配方法、患者登録、および他のリスク最小化ツールのような薬物ガイドライン、医師のコミュニケーション計画、または安全使用を保証する要素を含むことができる。承認されると、発売前と上場後の要求に対する遵守が保たれていない場合、あるいは製品が市場に進出した後に問題が発生した場合、FDAは製品承認を撤回する可能性がある。FDAは、製品の商業化後の安全性と有効性をさらに評価し、監視するために、1つまたは複数の第4段階上場後の研究および監視を要求することができ、これらの発売後の研究の結果に基づいて製品のさらなる販売を制限する可能性がある。
開発と審査計画を加速する
FDAは合格した候補製品に一連の迅速な開発と審査計画を提供した。高速チャネル計画は、特定の基準に適合した新製品の審査プロセスを加速または促進することを目的としている。具体的には、新製品が深刻または生命に危険な疾患や状況を治療し、その疾患または状況が満たされていない医療需要を満たす潜在力を示す場合、迅速なチャネル指定を受ける資格がある。高速チャネル指定は,製品と研究中の特定の適応の組合せに適している.高速チャネル製品のスポンサーは製品開発中にFDA審査チームと頻繁に交流する機会があります
また,BLAが提出されると,その製品は優先審査を受ける資格がある可能性がある。高速チャネル製品もローリング審査の条件に適合する可能性があり、この場合、FDAは、完全な出願を提出する前にBLAの審査部分をスクロールして考慮することができ、スポンサーがBLA部分を提出するスケジュールを提供した場合、FDAはBLAの部分を受け入れることに同意し、スケジュールが許容可能であると判断し、スポンサーはBLAの第1の部分を提出する際に任意の必要な使用料を支払うことができる。
深刻または生命に危害を及ぼす疾患または状態を治療することを目的とした製品も、その開発と審査を加速するために、突破的な治療指定を受ける資格がある可能性がある。初歩的な臨床証拠が、1つの製品が1つまたは複数の臨床的に重要な終点で既存の治療法よりも実質的な改善を示す可能性があることを示す場合、例えば、臨床開発早期に観察された実質的な治療効果が示された場合、製品は画期的な治療指定を得ることができる。この指定には、高速チャネル計画のすべての機能と、第1段階で開始されたより密集したFDA相互作用および指導と、高度な管理者の参加を含む製品開発および審査を加速する組織約束とが含まれる。
迅速なチャネル指定および/または画期的な治療指定を有する製品を含むFDA承認された生物学的製品に提出された任意のマーケティング申請は、優先審査および加速承認のようなFDAの審査および承認プロセスを加速することを意図した他のタイプの計画の資格に適合する可能性がある。市場で販売されている製品と比較して、製品が重篤な疾患や状況の治療、診断または予防において著しく改善される可能性がある場合、優先審査を受ける資格がある。新分子実体を含む製品について、優先審査指定は、FDAが60日申請後6ヶ月以内に上場申請に行動することを目標としていることを意味する(標準審査は10カ月)。
さらに、深刻または生命を脅かす疾患または状態の治療における安全性および有効性について研究された製品は、臨床的利益を合理的に予測する可能性のある代替終点に有効であるか、または不可逆的な発病率または死亡率よりも早く測定することができる臨床終点に有効であると判断され、病状の重症度、希少性または流行率、および代替治療を利用可能または不足し、不可逆的な発症率または死亡率または他の臨床的利益への影響を合理的に予測することを考慮すると、加速承認を得ることができる。承認を加速する条件として、FDAは通常スポンサーに十分かつ良好な制御を行う上場後の臨床研究を要求し、不可逆的な発病率或いは死亡率或いは他の臨床利益に対する期待影響を検証と記述する。また、FDAは現在、承認を加速させる条件として宣伝材料を事前承認することを求めており、製品商業発売の時期に悪影響を及ぼす可能性がある。
FDAは2017年に新しい再生医学高度治療法を確立しました (“rmat”)は、その実施“21世紀治療法”の一部として、2016年12月に署名して法律となった。RMAT指定計画は、21世紀の治療法案の要求、すなわちFDAが、細胞療法、治療組織工学製品、ヒト細胞および組織製品、またはそのような治療法または製品を使用する任意の組み合わせ製品として定義されるRMATの資格に適合し、審査を加速することを目的としているが、限られた例外的な状況であるが、(2)深刻なまたは生命に危険な疾患または状態を治療、修正、逆転または治癒することを目的としている;および(3)このような疾患または状態の満たされていない医療需要を満たす可能性があることを示す予備臨床証拠を示す。RMAT指定は、高速チャネルや画期的な治療指定と同様に、FDAとのより頻繁な会議の開催、候補製品の開発計画の検討、スクロール審査および優先審査の資格の有無を含む潜在的な利点を提供する。RMAT認証が付与された製品も、長期的な臨床的利益を合理的に予測する可能性のある代替物または中間終点に基づいて、またはより多くの場所に拡張することによって加速承認を得ることを含む、大量の場所から取得されたデータに依存する資格がある。承認が得られると、適切なとき、FDAは、臨床証拠、臨床研究、患者登録、または電子健康記録のような他の真の証拠源を提出することによって、より大きな検証データセットを収集することによって、または承認前にすべての治療を受けた患者を承認後に監視することによって、加速承認の下で承認後の要求を満たすことを可能にすることができる。
高速チャネル指定、画期的な治療指定、優先審査、加速承認、およびRMAT指定は、承認の基準を変更することはないが、開発および/または承認プロセスを加速する可能性がある。
孤児薬名
孤児医薬品法によれば、FDAは、米国で20万人未満の影響を与える稀な疾患または疾患を治療するための医薬または生物学的薬剤を孤児として指定することができ、または米国で20万人を超える影響を与える場合、そのような疾患または疾患を治療するための医薬または生物学的薬剤の開発および提供のコストを米国での医薬品または生物学的薬剤の販売から回収することができる合理的な期待がない。BLAを提出する前に,指定孤児薬を申請しなければならない。FDAで承認されました
FDAは、孤児薬の名称、治療剤の模倣薬の識別情報、およびその潜在的な孤児の使用を開示する。孤児薬物の指定は、規制審査または承認過程においていかなる利点も伝達されず、規制審査または承認過程の持続時間を短縮することもない。
孤児薬物指定を有する製品がその後、このような指定された疾患に対するFDAの最初の承認を得た場合、この製品は、孤児薬物の独占的承認(または排他性)を得る権利があり、これは、FDAが完全なBLAを含む他の出願を承認しない可能性があり、限られた場合、例えば孤児薬物に対する排他性を有する製品に対する臨床的利点を示さない限り、7年以内に同じ生物適応を販売する可能性があることを意味する。孤児薬物の排他性は、FDAが同じ疾患または条件のために異なる薬剤または生物学的薬剤を承認することを阻止しないか、または異なる疾患または条件のための同じ薬剤または生物学的薬剤を使用することを阻止しない。孤児薬物を指定する他の利点は、いくつかの研究の税金相殺およびBLA申請料の免除を含む。
指定された孤児薬物が孤児が指定された適応よりも広い用途で承認された場合,孤児薬物の排他性を得ることはできない。さらに、FDAが指定された要求に重大な欠陥があると後に判断した場合、または製造業者がこのような稀な疾患または疾患患者の需要を満たすのに十分な数の製品を保証できない場合、米国での独占営業権を失う可能性がある。
承認後に要求する
我々は、FDAによって製造または流通を許可されたどの製品も、記録保存、有害事象報告、定期報告、製品サンプリングおよび流通、ならびに製品広告および販売促進に関連する要件を含むFDAによって普遍的かつ持続的に規制されている。承認後、承認された製品の大多数の変更は、新たな適応または他のラベル宣言を追加するなど、FDAの事前審査および承認を経なければならない。継続的なユーザ料金要求もあり,この要求に基づいて,FDAは承認されたBLAで決定された製品ごとの年間計画費用を評価する.生物製造業者とその下請け業者は、FDAとある州機関に彼らの機関を登録し、FDAと特定の州機関の定期的な抜き打ち検査を受けて、cGMPのコンプライアンスを理解しなければならない。これは、私たちと私たちの第三者製造業者にいくつかの手続きと文書要求を加えている。製造プロセスの変更は厳しく規制されており,変更の重要性により,FDAが事前に承認して実施する必要がある可能性がある。FDAの規定はまた、cGMPから外れた状況を調査·是正し、私たちと私たちが使用を決定する可能性のある任意の第三者メーカーに報告することを要求している。そのため、メーカーは生産と品質管理の分野で時間、お金、精力をかけ続け、cGMPやその他の法規遵守性を維持しなければならない。
規制要件や基準が守られていない場合、あるいは製品発売後に問題が発生した場合、FDAは承認を撤回する可能性がある。その後、製品には、予期しない深刻度または頻度の不良事象、または生産プロセス、または法規要件を遵守できなかったことを含む、以前に未知の問題が存在することが発見され、新しいセキュリティ情報を追加するために承認されたラベルの改訂を招く可能性がある;新しい安全リスクを評価するために発売後研究または臨床研究を実施すること、またはREMS計画に従って流通制限または他の制限を実施することが可能である。他の他の潜在的な結果には
•製品の販売または製造を制限し、市場から製品を完全に撤退させるか、または製品をリコールすること
•承認後の臨床研究には罰金、警告状、放置を科す
•FDAは、承認されるべき出願の承認または承認された出願の追加を拒否するか、または既存の製品の承認を一時停止または撤回する
•製品が差し押さえられたり、差し押さえられたり、FDAが製品の輸出入を許可することを拒否したり;
•民事または刑事処罰を禁令または適用する。
FDAは生物製品のマーケティング、ラベル、広告、販売促進を厳格に規制している。1社は承認されたラベルと一致する安全性と有効性、純度、効力に関する声明しか提出できない。FDAと他の機関は非ラベル用途の普及を禁止する法律法規を積極的に施行している。これらの要求を守らないことは、否定的な宣伝、警告状、改正広告、および潜在的な民事と刑事罰を招く可能性がある。医師は、製品ラベルに記載されていない使用のための合法的に入手された製品の処方、および我々が試験およびFDAによって承認された用途とは異なる使用を行うかもしれない。このようなラベル外の使用は医学専門科でよく見られる。内科医は,この非ラベル使用は多くの患者の最適な治療法であると考えているかもしれない
状況は多種多様である.FDAは医者が治療を選択する時の行動を規範化しない。しかし、FDAは製品ラベルの外使用問題に対する製造業者のコミュニケーションを制限した。
生体模倣薬と参考製品の排他性
“患者保護·平価医療法案”“衛生保健·教育和解法案”改正 (総称してACAと呼ぶ)2010年に法律に署名し、“2009年生物製品価格競争と革新法案”という副題を含む FDAによって承認された参照生物学的製品と類似したまたは交換可能な生物学的製品のための短い承認経路を作成する(“BPCIA”)。
生物類似性、即ち製品の高度な類似が要求され、しかも安全性、純度と効力の面で生物製品と参考製品の間に臨床的に意義のある差異がなく、分析研究、動物研究と臨床研究によって証明することができる。互換性は、製品が基準製品生物と類似していなければならず、任意の所与の患者において参照製品と同じ臨床結果を生成することができることを証明しなければならず、複数回投与された製品の場合、安全リスクを増加させることなく、または参照生物の独占使用と比較して治療効果のリスクを低下させることなく、以前の投与後に生物および参照生物を交互にまたは交換することができることを証明しなければならない。生物製品がもっと大きく、よくもっと複雑な構造に関連する複雑性、及びこのような製品を製造する技術は、FDAがまだ制定している簡略化審査経路の実施に対して重大な障害を構成した。
BPCIAによると,生物類似製品の申請は参考製品が初めて許可を得た日から4年後にFDAに提出される。また,FDAは参考製品が初めて許可を得た日から12年以内に生物類似製品を承認する可能性がある。この12年間の独占期間内に、FDAが完全なBLAを承認した場合、出願人自身の臨床前データと、競合製品の安全性、純度、および効力を証明するために、十分かつ良好に制御された臨床試験からのデータとが含まれており、別の会社は、参照製品の競合バージョンを販売する可能性がある。BPCIAはまた、交換可能な製品として承認された生物模倣薬のためのいくつかの排他的期限を設けている。この時点で,FDAが“交換可能”と考えている製品が,実際に国家薬剤法に管轄されている薬局にどの程度取って代わられるかは不明である。
BPCIAは複雑であり、FDAによって解釈され、実施され続けている。また、政府の提案は12年間の参考製品専門期間を短縮しようとしている。BPCIAの他の面では,そのいくつかがBPCIAの排他的条項に影響を与える可能性があり,最近の訴訟のテーマでもある.そのため,BPCIAの最終実施と影響は重大な不確実性の影響を受ける。
他の医療法とコンプライアンス要件
製薬会社は連邦政府およびそれらが業務を展開している州と外国司法管轄区当局の追加医療監督と法執行を受けている。このような法律は、誘導または見返りとして、個人を紹介するか、または任意の連邦医療計画に従って費用を直接または間接的に支払うことができる物品またはサービスを購入または推薦するために、個人およびエンティティが、知られている場合および意図的な場合に報酬を請求、受け入れ、提供または支払うことを禁止する米国連邦反バックル法規を含むが、これらに限定されない。“民事虚偽精算法”を含む連邦民事および刑事虚偽精算法であって、他の事項に加えて、連邦医療保健プログラムおよびそれに相当する刑事法を含む連邦政府への虚偽または詐欺的な支払いまたは承認精算申請の提出または提出を禁止する“民事通貨処罰法”であって、他のほかに、連邦医療保健計画下で提供される項目およびサービスの支払い精算に虚偽または詐欺的なクレームを提供するために、個人または実体が虚偽または詐欺的な虚偽記録または報告書を作成、使用または使用することを禁止する連邦民事および刑事虚偽精算法、1996年の連邦医療保険可携帯性および責任法 追加の連邦刑法を制定し、(1)任意の医療福祉計画を詐欺の計画またはトリックを実行または実行しようとしていることを知り、故意に禁止している(2)虚偽または詐欺的な言い訳、陳述または約束によって、任意の医療福祉計画が所有または保管または制御している任意の金銭または財産を得ること、(3)任意のトリック、計画または装置によって重要な事実を偽造、隠蔽または隠蔽すること、および(4)医療福祉計画に関連する任意の事項について任意の重大な虚偽、架空または詐欺的な陳述または陳述を行うことを禁止する“HIPAA”)。医療福祉、プロジェクトまたはサービスの交付または支払いに関連する重大な虚偽、架空または詐欺的陳述または記録を含むことを知り、2009年に“経済および臨床健康情報技術法案”によって改正された任意の重大な虚偽または文書を作成または使用するか、または使用することができる また、HIPAAがカバーするエンティティ、そのビジネスパートナー、およびそのカバーされた下請け業者に対して、プライバシー、セキュリティ、および個人識別可能な健康情報の送信に関するいくつかの要求を提出し、米国連邦医師が日光法案を支払う法案
連邦医療保険、医療補助または児童健康保険計画に従って支払いを受けることができるいくつかの薬品、機器、生物製品、および医療用品メーカーは、透明性を向上させるために、そのような法律で定義された医師への支払い(直接および間接)または他の価値移転に関する情報を毎年連邦政府に報告することが要求される いくつかの他の医療保健専門家、例えば、勤務看護師と医師アシスタント、ならびに教育病院、ならびに医師およびその直系親族が持つ所有権と投資権益、ならびにアメリカ各州と外国法律の上述の各連邦法律に対する等価物は、場合によっては、これらの法律は互いに大きく異なり、同じ効果を持たない可能性があり、それによってコンプライアンス仕事を複雑化させる可能性がある。もし私たちの運営がこのような法律または任意の他の適用可能な政府法規に違反していることが発見された場合、私たちは、MedicareおよびMedicaidまたは他の国または司法管轄区域のような同様の計画、違反、返却、監禁、契約損害、名声損害、利益減少、および私たちの業務の削減または再編に関する告発を解決するために、民事、刑事および行政処罰、損害賠償、罰金、MedicareおよびMedicaidまたは他の国または司法管轄区域の同様の計画を含むが、これらに限定されない重大な処罰を受ける可能性がある。
保証と精算を請け負う
著者らが監督管理の許可を得た任意の薬品或いは生物製品のカバー範囲と精算状態に対して、重大な不確定性が存在する。任意の製品の販売は、連邦、州と外国政府医療保健計画、商業保険とホスト医療組織、および第三者支払人のこの製品に対する清算レベルなど、第三者支払者のこの製品に対する保証範囲にある程度依存する。提供されるべき補償範囲と金額に関する決定は個々の計画に基づいて行われる。米国の第三者決済者には統一された薬品保証と精算政策がないため、支払先によって薬品引受と精算政策が大きく異なる可能性がある。保険の獲得と精算に重大な遅延が発生する可能性があり、保険と精算を確定する過程はよく時間がかかり、高価であるため、これは私たちの製品を使用するためにそれぞれの支払人に科学と臨床支持を提供することを要求し、保険或いは十分な精算を保証することができない。政府当局と第三者支払人が私たちの薬品の保険や精算についてどのように決定するか予測するのは難しい。医師の監督下で管理されている製品については、このような薬物が高い価格に関連することが多いため、保険および適切な補償を得ることは特に困難である可能性がある。また,製品自体やその製品を使用した治療やプログラムは単独では精算できない可能性があり,医師の使用に影響を与える可能性がある。
また、米国政府、州立法機関、外国政府は価格制御、カバー範囲と補償の制限及び模造薬代替の要求を含むコスト制御計画を継続して実施している。第三者支払者は安全性と有効性を疑問視するほか、医療製品やサービスの価格に挑戦し、医療の必要性を審査し、薬品や生物製品、医療機器と医療サービスの費用効果を審査することが増えている。価格制御及びコスト制御措置、並びに既存の制御及び措置を講じている司法管区において、より限定的な政策をとることにより、任意の製品の販売をさらに制限することが可能となる。いかなる製品の第三者精算または第三者支払者が製品を保証しないと決定したかを減らすことは、医師の使用や患者のその製品に対する需要を減少させる可能性がある。
医療改革
米国や一部の外国司法管轄区は医療システムを変更するために一連の改革提案を検討しているか、公布されている。医療コストのコントロール、質の向上或いは参入拡大を既定の目標とし、医療保健システムの変革を推進することは重大な意義がある。アメリカでは、製薬業はずっとこれらの努力の重点であり、連邦と州立法計画の重大な影響を受けており、薬品と生物製薬製品の価格設定、カバー範囲と精算を制限するための立法措置、特に政府が援助する医療保健計画の下で、政府が薬品価格の制御を強化することを含む。
2010年3月、ACAは法律に署名し、米国政府と民間保険会社が医療保健に資金を提供する方式を大きく変え、製薬業に大きな影響を与えた。ACAは、製薬および生物技術業界に特殊な重要性を有するいくつかの条項を含み、連邦医療計画登録を管理する条項を含むが、これらに限定されない、新しい方法であって、この方法に基づいて、製造業者が医療補助薬品バックル計画の下で吸入、注入、点滴、移植または注射された薬物のリベートを計算し、連邦医療計画における製薬会社の販売シェアに基づいて年会費を計算する新しい方法。ACAが公布されて以来、司法、国会、行政部門はACAのいくつかの方面に挑戦し、将来的にACAに対してより多くの挑戦と修正案を提出することが予想される。例えば、2020年に連邦支出計画は永久に廃止され、2020年1月1日から発効し、ACA強制対高-
コスト雇用主が後援する医療保険と医療機器税は,2021年1月1日から健康保険会社税も廃止された。また,税法が公布され,他の事項を除いてACA個人が医療保険を購入する規定を守らないことに対する罰則が撤廃された。2021年6月17日、米国最高裁は、ACAは全体的に違憲であり、“個人権限”が国会で廃止されたため、プログラム理由に基づく挑戦を却下した。また、2022年8月16日、総裁·バイデンはACA市場で医療保険を購入した個人への増強補助金を2025年計画年に延長することを含むアイルランド共和軍法案に署名した。2025年からアイルランド共和軍は,受益者の最大自己負担コストの著しい低減と新たなメーカー割引計画の作成により,連邦医療保険D部分計画下の“ドーナツ脆弱性”を解消した。ACAは未来に司法や国会で挑戦される可能性がある。これらの課題や任意の追加的な医療改革措置がACAや我々の業務にどのように影響するかは不明である
ACAが公布されて以来、会計年度ごとに提供者に支払われる連邦医療保険総額の2%の減少、およびいくつかのタイプの医療保険提供者に支払われるお金の減少など、他の立法変化も提案され、採択され、追加の国会行動が取られない限り、これらの変化は2031年まで有効である。現在の立法によると、医療保険支出の実際の下げ幅は2022年の1%から最高4%まで様々になる。
また、処方薬や生物製品価格の上昇を受けて、米国政府は薬品定価のやり方の審査を強化した。このような審査は、最近のいくつかの大統領行政命令、国会調査を招き、製品定価の透明性の向上、価格設定とメーカー患者計画との関係の審査、政府計画の製品精算方法の改革を目的とした連邦と州立法を提出し、採択した。例えば、連邦レベルでは、2021年7月、バイデン政府は“米国経済における競争を促進する”という行政命令を発表し、その中には処方薬に対する条項が複数ある。総裁·バイデンの行政命令に応答するため、アメリカ衛生·公衆サービス部は2021年9月9日に高薬価に対応する総合計画を発表し、その中で薬品定価改革の原則を概説し、国会が採用可能な各種の立法政策及び衛生と公衆サービス部がこれらの原則を推進するために取る可能性のある行政行動を示した。また、“2022年インフレ率低減法案”(以下、“アイルランド共和法”)には、医療保険D部(2026年から)とB部(2028年から)でカバーされている少数の模倣薬や生物類似競争相手のいない単一由来ブランド薬や生物製品の価格について、厚労省大臣と製薬会社に交渉するよう求める条項が含まれている。価格交渉の薬品数は2026年の10種類のD部分薬,2027年の15種類のD部分薬,2028年の15種類のD部分とB部分薬,および2029年以降の20種類のD部分とB部分薬となる。これらの薬剤は,連邦医療保険D部分の総支出が最も高い50種類の薬剤と連邦医療保険B部分の総支出が最も高い50薬剤の中から選択される。この法律は特定の薬物や生物の交渉価格上限を規定しており,衛生·公衆サービス部部長がこれらの上限価格を交渉する際に考慮しなければならない要因を規定している。アイルランド共和軍はまた、連邦医療保険B部分とD部分にリベートを徴収し、価格上昇幅がインフレを超えたメーカーを処罰した。また、2022年10月14日、バイデン政府は追加の行政命令を発表し、HHS報告書がどのように連邦医療保険と医療補助革新センターをさらに利用して連邦医療保険と医療補助受益者の薬品コストを下げる新しいモデルをテストするかを指示した。州レベルでは、立法機関は、価格または患者の精算制限、割引、特定の製品参入およびマーケティングコスト開示の制限、および透明性措置を含む薬品の価格設定を制御するための法規を立法し、実施してきており、場合によっては、他の国からの輸入および大量購入を奨励することを目的としている。私たちは衛生改革の計画が続くと予想している
“欧州連合(EU)規約”
アメリカと同様に、EUで開発されている生物製品の研究、開発、テスト、製造、品質管理、輸出入、安全、有効性、ラベル、包装、貯蔵、流通、記録保存、承認、広告、販売促進、マーケティング、承認後の監視と承認後の報告は、一連の影響を受ける複雑な法律、規則、法規の制約を受けている
EUの医薬製品開発
EUでは、医薬製品の開発は通常臨床前実験室と動物試験及び臨床試験を含む。EUの発売前の審査要求を満たすには通常長年の時間が必要であり、実際の所要時間は製品或いは疾病のタイプ、複雑性と意外性によって大きく異なる可能性がある。
臨床前試験は実験室評価と動物研究を含み、この製品の特性と潜在的な薬理、薬物動態学と毒性を評価する。臨床前試験の実施は良好な実験室操作規範(“GLP”)を含むEUと国家の法規と要求に符合しなければならない。
EUの臨床試験は,米国のように,適用される法規,良好な臨床実践(GCP)を遵守し,試験目標と安全性と有効性基準をモニタリングするためのパラメータを詳細に説明するためのプロトコルでなければならない。EUでは、患者の検査に関する各合意およびその後の合意改正は、新たな臨床試験申請(CTA)の一部として関連規制機関に提出され、1つまたは複数の道徳委員会および国家主管当局に提出されて審査されなければならない。アメリカと同様にマーケティング許可申請を支援するための臨床試験を展開しています 通常は3つの連続段階で行われる.
2022年1月31日,EU第536/2014号条例(臨床試験条例)は,従来の第2001/20指令(臨床試験指令)を廃止し,代替した (“テロ対策条約”)とEU加盟国(“EU加盟国”)の関連国が立法を行うことはEUに完全に適用されている。CTRは臨床試験の許可を調整と簡略化し、不良事件報告プログラムを簡略化し、臨床試験に対する監督を改善し、そしてその透明性を増加させることを目的としている。具体的には、すべてのEU加盟国に直接適用されるCTRは、単一の入口点である“EUポータル”である臨床試験情報システム(CTIS)を介して簡略化された申請手続き、申請のための準備および提出された単一の文書セット、および簡略化された臨床試験スポンサー報告プログラムを導入する。臨床試験申請を評価する統一プログラムが採用されており,このプログラムは2つに分類されている。第1部評価は,EU加盟国の主管当局を参考に試験スポンサーが選択したものであり,EU加盟国で科学的に協調されていると考えられる臨床試験に関連している。そして、この評価報告書は、その審査のために、裁判を行うすべてのEU加盟国の主管当局に提出されるだろう。二番目の部分はEU加盟国に関する各主管当局と道徳委員会によってそれぞれ評価される。個別のEU加盟国はその領土で臨床試験を行うことを許可する権限を保持している
CTRはCTDにより認可された臨床試験の過渡期を予見した。CTDによって許可された2023年1月31日までの臨床試験は、CTR適用開始後3年以内にCTDに従って継続することができる(2025年1月31日まで)。2023年1月31日または後に提出される予備臨床試験出願は、CTRに規定された要件を満たさなければならない
CTRによると,国家主管当局(“NCA”)が臨床試験が適用の要求に従って行われていないと判断した場合,あるいは臨床試験患者に対して受け入れられないリスクとなっている場合には,随時臨床試験の一時停止や永久停止を命じたり,他の制裁を加えたりすることができる。道徳委員会はまた,臨床試験が適用の要求を守れなかったために一時的または永久的に停止したり,他の条件を加えたりすることを要求することができる。
EU臨床試験情報の開示
EUでは,CTRはスポンサーに医薬製品開発に関するデータ,特に臨床試験情報の公開開示を求めている。これらのデータは伝統的に秘密商業情報(CCI)とみなされているが、EUが採用した政策によると、マーケティング許可申請においてEMAに提出された臨床研究データは、臨床前データおよび患者レベルデータを含み、公開開示の影響を受ける可能性がある。CTRは、個人データまたはCCIを保護する理由で秘密にされていない限り、臨床試験申請に含まれる情報およびCTIにアップロードおよび格納されたすべての関連文書を公開してアクセス可能である透明性の一般的な原則を確立し、これは、EU加盟国間の評価報告書作成に関する機密通信を保護するために必要であるか、またはEU加盟国による臨床試験を効果的に監視することを確保するために必要である。もしすべてを圧倒する公共利益が存在することを開示すれば、この秘密例外は覆されるかもしれない。臨床試験に関するデータや文書の公表は特定のスケジュールで行う。関連スケジュールはEMAによって作成され、文書と臨床試験の分類に基づいて決定される。そのほか、臨床試験の発起人は初歩的な臨床試験申請を提出する時にいくつかの書類の公表を延期することを申請することができる。公表延期申請は正当な理由に基づいており、合理的な提案延期期限を含まなければならない。公表を延期する申請は関連EU加盟国の承認を受けなければならない。
また、閲覧文書に関する第1049/2001号条例、または“閲覧文書条例”、および文書閲覧に関するEUの政策0043は、EUの利害関係者が環境保護局が保有しているいくつかの情報を含む文書の閲覧を要求する要求をEU関係者に提出する権利があることを規定している。ただ非常に限られた情報だけがこのような開示要求から免除される。これらの例外は-したがって-EUではCCIの保護および保護された個人データを含む狭義に解釈されるだろう。しかし、当局がすべてを圧倒する公共利益を開示すると結論した場合、CCI保護は提供されない。欧州連合裁判所判例法
(以下、“CJEU”と称する)も確認されており、臨床および臨床前データを掲載した文書については一般的な秘密推定はなされておらず、これらの文書は、上場許可申請を支援するために環境管理専門家に提供されている。
EUマーケティング許可
EUでは、医薬製品はマーケティングの許可を得た後にのみ商業化されることができる。EEAまたはEEA国のEFTA支柱にも同様の規則が適用される (ノルウェーアイスランドリヒテンシュタイン)会社は集中プログラム、分散プログラム、相互認識プログラムを通じて上場許可申請を提出することができる。会社はまた、国家マーケティング許可を提出し、担当NCAによって発行され、それぞれの国家領土のみをカバーすることができる。
欧州経済地域全体で有効な製品マーケティング許可をEUで取得するためには、出願人は、欧州市場管理局が管理する中央プログラムまたはEU加盟国主管当局が管理するプログラムのうちの1つ、分散プログラム、国家手続き、または相互承認プログラムに従ってマーケティング許可申請を提出しなければならない。マーケティング許可は連合に設立された申請者にのみ付与されることができる。
中央手続きは欧州委員会によってすべてのEU加盟国に有効な単一マーケティング許可を付与することを規定している。(EC)第726/2004号条例によれば、いくつかのタイプの製品は、(I)いくつかのバイオテクノロジープロセスに由来する薬剤、(Ii)孤児医薬品に指定された製品、(Iii)HIV/エイズ、癌、神経変性疾患、糖尿病、自己免疫疾患および他の自己免疫機能障害およびウイルス疾患を治療するための新しい活性物質を含む集中管理手順を実行しなければならない。遺伝子治療,体細胞治療,組織工学製品を含む高度な治療薬製品(ATMP)では,集中化プログラムも強制的である。対照的に、他の疾患を治療するための新しい活性物質を含む製品、または重大な治療、科学的または技術的革新を構成すると考えられる製品、またはその集中認可プロセスがEU患者の利益に適合する製品については、集中化プロセスが任意である。
中央手続きの下で、環境保護局の人は薬品委員会(“委員会”)で製品を評価し、環境保護局を代表して医療製品の安全性、有効性、品質について意見を提出した。 CHMPはまた、既存のマーケティング許可の修正または拡張を評価するなど、いくつかの許可後および保守活動を担当する。CHMPは各加盟国の国家薬品管理局が指名した専門家からなり,そのうちの1人が評価調整作業の調査委員に任命され,できれば別の委員会のメンバーが共同調査委員を務めることになる
EUの中央手続きによれば、マーケティング許可出願を評価する最長期限は210日であり、マーケティング許可申請者がCHMP質問に回答したときに追加の情報または口頭解釈を提供する時間を含まない。このプロセスは、通常、より多くの情報を必要とするので、プログラムスケジュール内のクロック停止をトリガするため、より長い時間を要する。審査期間終了時に、CHMPは欧州委員会に意見を提供する。もし意見が有利なら、欧州委員会は決定を採択してマーケティング許可を付与するかもしれない。マイナス意見があれば、会社はマイナス意見を受け取った日から15日以内に申請の再審を要求することができる。そして,同社はCHMPに再検査を要求する詳細な理由を60日間提供した。これらの情報を提供する60日以内に、CHMPはその意見を再検討しなければならない。欧州委員会はほとんどの場合CHMPの提案に従っている。
特殊な場合、公衆衛生の観点、特に治療革新の観点から、満たされていない医療需要に対する医薬製品に対する重大な利益が期待される場合、CHMPは加速評価を許可することができる。CHMPが加速評価の要求を受けた場合、210日間の制限時間は150日(クロックポーズを含まない)に減少する。しかしながら、CHMPが加速評価を行うのにもはや適していないと考える場合、集中プログラムの標準期限に回復することができる。私たちはEMAの確認を受けて、私たちの製品証明書は加速評価を行う資格があります。
原則として、上場許可の初期有効期間は5年である。マーケティング許可は、EMAまたは最初に販売許可を許可したEU加盟国の主管当局による医薬製品のリスク-収益バランスの再評価に基づいて5年後に更新することができる。リスク−収益バランスは,その品質,安全性,有効性に関する科学的基準に基づいている。応援するために
上場授権書を申請する時、上場授権書保持者はEMA或いは主管当局に電子汎用技術文書(“ECTD”)の総合バージョンを提供し、製品の品質、安全と効果に関する最新のデータを提供しなければならず、マーケティング授権書を授与してから導入されたすべての変化を含み、少なくともマーケティング授権書が失効する前の九ヶ月前である。欧州委員会またはEU加盟国の主管当局は、薬物警戒に関する正当な理由に基づいて、上場許可の延長期間をさらに5年間延長することを決定することができる。その後最終的に更新されると、上場許可の有効期限は無期限となる。いかなる許可の後も、許可が失効してから3年以内に薬品が実際にEU市場(集中マーケティング許可のために使用される)またはEU加盟国の市場(いわゆる日没条項)に許可されていない場合。
ATMPは遺伝子治療製品、体細胞治療製品と組織工学製品を含む。遺伝子治療医薬製品のような生存可能なヒト組織または細胞を含む製品のEUにおける販売許可は、ATMPに関する(EC)1394/2007号法規によって管轄され、この法規は、欧州議会および欧州理事会の(EC)第2001/83命令と組み合わされ、この命令は、一般に医療製品共同体コードと呼ばれる。(EC)第1394/2007号条例は、遺伝子治療薬製品、体細胞治療薬製品、および組織工学製品の許可、監督および薬物警戒に関する具体的な規則を制定する。先進治療薬物のメーカーはEMAにその製品の品質、安全性と有効性を証明しなければならず、EMAは発売許可申請について意見を提供しなければならない。ATMPに対しては,CHMPは高度治療委員会(“CAT”)と任意の必要な科学的評価について協議し,その科学的意見を策定しなければならない。欧州委員会はEMAによって提供された意見に基づいてマーケティング許可を承認または拒否する
細胞ベースの製品はまた、ヒト組織および細胞への寄付、調達、試験、加工、保存、貯蔵および分配に関する欧州議会および欧州理事会の2004年3月31日の品質および安全基準を設定する指令(“組織および細胞指令”)に適合しなければならない。本指令は,細胞ベースの医薬製品を製造するための細胞を調達する際に適用しなければならない条件と品質要件を述べている。EU加盟国は“組織と細胞指針”を自国の法律に変えた。しかし、組織や細胞指針に対する様々な解釈が登場し、個別のEU加盟国の国家執行立法に反映されており、これは異なるやり方を招いている。
EU適応経路
EMAには,患者が高度な医療ニーズの下で早期かつ漸進的に薬物を獲得することを可能にする適応経路方法がある。この目標を達成するために、例えば、重篤な疾患を有する小集団を識別することを含むいくつかの方法が想定され、これらの集団では、薬物の利益-リスクバランスが有利である可能性があり、または適切な場合には、臨床試験データをサポートするために実世界のデータをより多く利用することが考えられる。適応経路概念は主に医療需要の高い地域の治療に適用され,これらの地域では伝統的な経路でデータを収集することは困難であり,大型臨床試験は薬物から利益を得ることが不可能な患者を不必要に暴露する。この接近は既存のEUの法的枠組み内ですでに準備された規制手続きに基づいている。その中には条件付きマーケティング許可が含まれている。
EUでは、必要なすべてのセキュリティおよび有効性データが得られていない場合、欧州委員会は条件付きマーケティング許可を承認する可能性がある。以下のすべての基準に適合することが証明された場合、欧州委員会は、医薬製品に条件付きマーケティング許可を付与することができる:(I)利益-リスクバランスが正である;(Ii)製品が市場で直ちに発売される利点が依然として追加データを必要とするという事実に固有のリスクを超えていると考えられる場合、(Iii)申請者は許可後に全面的なデータを提供することができる可能性が高く、(Iv)この医薬製品は未満足の医療需要を満たしている。条件付きマーケティング許可は、失われたデータを生成するために、またはセキュリティ対策を増加させることを保証するために、満たされるべき条件に依存する。それの有効期間は1年で、すべての関連条件が満たされるまで毎年更新しなければならない。任意の未解決の研究が提供されると、条件付きマーケティング許可は、従来のマーケティング許可に変換することができる。しかしながら、EMAが設定された時間枠内で条件が満たされず、欧州委員会の承認を得ない場合、マーケティング許可は更新を停止する。このプログラムはまた,将来性のある薬物開発中のデータのスクロール審査と組み合わせて,その評価をさらに加速させることができる
“特別な場合”では、出願人が、製品が許可され、特定の手順に従った後であっても、正常な使用条件下での治療効果および安全性に関する包括的なデータを提供できないことを証明することができれば、上場許可を承認することもできる。これらのことは,特に予想される適応では非常にまれであり,当時の科学的知識状況では,網羅的な情報を提供することは不可能である場合や,データを生成することが一般的に受け入れられている倫理原則に違反する可能性がある場合である。条件付きマーケティングライセンスと同様に、特別な場合に付与されたマーケティングライセンスは、
稀な疾患または満たされていない医療需要を治療するための医薬製品を許可することが意図されているが、出願人は、標準的なマーケティング許可を付与するために必要な完全なデータセットを持っていない。しかしながら、条件付きマーケティング許可とは異なり、特別な場合には、許可を申請する出願人は、その後、欠落したデータを提供する必要はない。“特殊な場合”の上場許可は最終的に付与されるが、毎年薬品のリスク-収益バランスを審査し、リスク-収益比がもはや有利でなければ、マーケティングライセンスを撤回する。
EMA特典プラン
EUでは、満たされていない医療需要に対して、重大な公共衛生利益を有する革新製品に対して、いくつかの加速開発と審査計画を獲得する資格がある可能性がある。この中には、米国の画期的な治療指定のようなインセンティブを提供するPrime計画が含まれている。Primeは、満たされていない医療ニーズに対する医療製品開発へのEMAの支援を強化するための自発的な計画である。条件に適合する製品は、満たされていない医療需要が存在する場合(EUには満足できる診断、予防または治療方法がない、または、ある場合、新しい医療製品は既存の治療法よりも大きな治療利点を提供する)でなければならず、それらは、新しい治療方法を導入することによって、または既存の方法を改善することによって、満たされていない医療需要を満たす可能性を示さなければならない。Primeの称号を持つ候補製品のスポンサーは、EMAと早期かつ積極的な対話を行うことを含むが、臨床試験設計と他の開発計画要素について頻繁に討論し、ファイルを提出した後にマーケティング許可申請の評価を加速する可能性があることを含むが、利益を得る
我々の製品証明書はPrime計画のアクセス権限を取得し,加速評価を行う資格があることを確認した.
EUの承認後の要求
マーケティング許可を付与した後、マーケティング許可の所有者は、マーケティング許可の条件として課せられた許可後効果研究(“PAES”)または許可後セキュリティ研究(“PASS”)の義務、または教育計画または制御されたアクセス計画のような他のリスク最小化措置(“RMMS”)のような製品の製造、マーケティング、販売促進、および販売に関連する一連の承認後の要求を遵守することを要求される可能性があり、これらの措置は、EU加盟国によって異なる場合がある。米国と同様に、医薬製品の販売許可保持者とメーカーはすべてヨーロッパ薬品管理局、欧州委員会、および/または個別のEU加盟国の主管監督機関の全面的な監督管理を受けている。上場許可所持者は薬物警戒システムを構築·維持し,薬物警戒に従事する資格のある個人を指定し,このシステムの監督を担当しなければならない。主な義務は深刻な副作用が疑われる報告を加速させ、安全更新報告書を定期的に提出することを含む。さらに、ある会社が加速承認経路によって製品の元のマーケティング許可を得た場合、同社は通常、完全なマーケティング許可をサポートする臨床的利益を検証および説明するために、上場後の検証性試験を行うことを要求される。成功しなかった発売後の研究やこのような研究を完成させなかったことは、製品のマーケティング許可を撤回させる可能性がある
すべての新しいマーケティング許可申請は、企業が実施するリスク管理システムを記述し、製品に関連するリスクを防止または最大限に低減するための措置を記録したリスク管理計画またはRMPを含まなければならない。規制部門はまた、上場許可の条件として特定の義務を規定することができる。このようなリスク最小化措置または認可後の義務は、追加の安全監視、PSURsのより頻繁な提出、または追加の臨床試験または通過を含むことができる。
また、上場承認後、不良事件報告書と定期報告書を提出する必要がある。欧州委員会またはNCA(状況に応じて)はまた、承認製品の影響を監視するため、または製品の流通または使用を制限する可能性のある承認条件に条件を適用するために、上場後テスト、いわゆる第4段階テスト、リスク評価および緩和策および監視を要求する可能性がある。また,承認された後,品質管理および製造,包装,ラベルプログラムは適用されるcGMPに適合しなければならない.医薬製品メーカー及びそのある下請け業者は定期的な抜き打ち検査を受け、検査人員は検査期間中に生産施設を監査し、cGMPに適合する状況を評価する。例えば、マーケティング許可所有者が規制基準を遵守できなかった場合、最初のマーケティング許可の後に問題が発生した場合、または後に以前に認識されていなかった問題が発見された場合、マーケティング許可は一時停止、変更、または撤回されることができる。そのほか、EUは薬品偽造を打撃し、薬品貿易が厳格にコントロールされることを確保するために、厳格な規則を発表した
医薬製品の広告と販売促進はEUとEU加盟国の医薬製品の普及、医療専門家との相互作用に関する法律の制約を受けている (“HCP”)、誤解性および比較広告、および不公平な商業行為。EU立法は医薬製品の広告と販売促進の一般的な要求を規定しているが、詳細はEU加盟国が制定した法規によって管理されており、各国は異なる可能性がある。例えば,適用される法律要件は,医薬製品に関する宣伝材料や広告が製品に適合する“製品特性要約”である (“SmPC”)は,主管当局によって承認され,販売許可と関係がある.SmPCは,医師に安全かつ有効な製品の使用に関する情報を提供するファイルである。SmPCに該当しない販促活動はラベル外とされ、EUでは禁止されている。連合はまた消費者に直接向けた処方薬製品の広告を禁止する。
さらに、規則は、これらのプレゼント、金銭的利益または実物利益が高価ではなく、医薬または薬局業務に関連しない限り、HCPにプレゼント、金銭的利益または実物利益を贈呈することを禁止する。同様に、厳格な規則はキャンペーンでのおもてなしにも適用される。これらの規則に基づいて、一連の業界基準が発表され、時々個別のEU加盟国で発効された国家法律が発表され、フッ化炭化水素企業への不当な支払いや他の価値移転、および一般的に広範な販売促進性質を持つ可能性のある誘因を打撃する。歴史的に見ると、製薬会社は反腐敗と類似調査の目標であり、メディアが広く注目している目標でもあり、これらの会社に巨額の罰金、イメージ、その他のコストをもたらすことがある。
データのプライバシーとセキュリティ
最後に、ヨーロッパ経済地域とイギリスでは非常に厳しいデータプライバシー要件が適用される。特に、“(EU)2016/679号条例”(“EU一般データ保護条例”)とイギリス“一般データ保護条例”(以下、“イギリスGDPR”)は、個人データの制御者や処理者に、特定、明確、合法的な目的で個人データを収集し、その等の目的に一致した方法で個人データを処理する原則を遵守することを含む厳しいデータ保護義務を課している。収集および処理される個人データは、十分に相関しなければならず、収集および処理の目的に関連することはできない。EUとイギリスのGDPRはまた、個人データは安全に保有しなければならず、適切な保護レベルを確保するために何らかのステップが取られない限り、適用された場合にヨーロッパ経済地域またはイギリス以外の地域に移転してはならないと規定している。EUおよび英国GDPRはまた、適切なセキュリティレベルを確保するために、個人データを処理する会社に適切な技術的措置を実施することを要求しており、これは、処理された個人データの種類、最新の技術、実施コストおよび処理の性質、範囲、背景および目的、ならびに自然人の権利および自由の可能性および深刻性が異なるリスクなどの異なる要因に依存する可能性がある。さらに、EUおよび英国GDPRは、個人データを処理する会社が、要求に応じてデータ主体の苦情および要求に応答することを含むデータ主体を保護する権利を保証するために、十分な記録、政策、安全、訓練、および管理フレームワークを有することを保証するためのいくつかの組織ステップをとることを要求する。例えば、EUおよび英国GDPRは、どのような条件下で有効な処理同意を得ることができるかを規定し、敏感な個人データ(例えば、健康データ)を大規模に処理する際にデータ保護官を任命し、欧州経済地域全体またはイギリス全体でデータ漏洩通知を強制的に規定し、サービスプロバイダまたはパートナーと契約する際に追加的な義務を課すことを規定することをデータ主体に詳細に開示することを要求する。さらに、会社が“特殊カテゴリ”の個人データ(患者の健康または医療情報、遺伝子情報および生体識別情報を含む)を処理、制御、または他の方法で使用する場合には、より厳しいルールが適用され、企業が法的にこれらのデータの処理を許可される場合および方法をさらに制限する。EUやイギリスのGDPRの要求や欧州経済圏諸国の関連国データ保護法を守らないと、2000万ユーロ(イギリスGDPRによる1750万ポンド)までの罰金や、会社の前会計年度の世界年収の4%を、金額の高い者を基準にする可能性がある。
EUの定価と精算
通常、政府は薬品の定価と精算を密接に監督し、製品が精算されるかどうかを決定し、精算された場合、大きな自由裁量権があることが多い。連合では、様々な国の価格設定と補償プログラムの差が大きい。いくつかのEU諸国では、補償価格が合意される前に、医薬製品は商業化できない。他の国は、特定の候補製品の費用対効果を現在利用可能な治療法と比較するための追加的な研究を要求するかもしれない--いわゆる衛生技術評価 精算または定価承認を得るために(“HTA”)。例えば、いくつかのEU加盟国は、製品の具体的な価格を承認するか、または製品を市場に投入する会社の収益性を直接または間接的に制御する制度をとることができる。他のEU加盟国は会社が自分の製品価格を固定することを許可したが、処方量を監視と制御し、医師に指導を発表して処方を制限した。最近、多くのEU加盟国は製薬会社が提供することを要求された割引金額を増加させた。各国が医療支出を管理しようとするにつれて、このような努力は続くかもしれない。全体的には,医療コスト,特に処方薬の下り圧力が大きくなっている。そのため、新製品の国家市場進出にますます高い壁が設けられている
政治、経済、規制の発展は定価交渉をさらに複雑化させる可能性があり、補償を受けた後、定価交渉は継続される可能性がある。EU加盟国が使用する参考価格と平行貿易(低価格と高価な加盟国間の裁定)はさらに価格を下げることができる
政府当局との価格交渉は私たちの製品の商業化を延期するかもしれない。多くの国の支払者は、他国の価格を参考にし、これらの参考価格を利用して自分の価格を制定し、強制値下げとリベートを含む様々なコスト制御措置を使用する。このような国際的な寄せ集めの価格規制は国によって価格が違うかもしれません。私たちの製品は価格の低い市場から国境を越えた貿易を行うかもしれません。交渉が価格を達成した後でも、各国はそうすることができ、時間の経過とともに価格や他の譲歩を要求したり、要求したりすることが多い。
EUのデータ排他性と市場排他性
EUでは、マーケティング許可を得た革新医薬製品(すなわち参考製品)は通常8年間のデータ独占権と他の2年間の市場独占権を獲得する。データ専門期間後発薬或いは生物類似製品の許可申請者は、参考製品が初めてEUで許可を得た日から8年以内に参照製品ファイルに含まれる臨床前と臨床試験データに依存することを防止する。追加の2年間の市場専門期間内に、模倣薬または生物学的に類似した製品の許可申請を提出することができ、参照製品のデータを参照することができる。しかし、市場の排他的な期間が終わるまで、いかなる模倣薬や生物類似製品も発売できない。この10年の最初の8年間に、マーケティング許可保持者が1つまたは複数の新しい治療適応の許可を得た場合、10年全体の期間を最大11年に延長することができ、許可前の科学的評価期間中に、これらの適応は、既存の治療法と比較して有意な臨床的利益をもたらすことができると考えられる。
EUでは、生物模倣薬、即ち参考薬品と類似しているが模倣薬の定義に符合しない生物医薬製品に対して、特殊な制度がある。このような製品に対しては、上場許可申請を支持するために、適切な臨床前或いは臨床試験結果を提供しなければならない。EMAのガイドラインは、異なるタイプの生物学的製品に提供される補足データのタイプおよび数を詳細に示す。
EUの孤児薬品指定と排他性
第141/2000条例(欧州委員会)第3条によれば、スポンサーが(1)製品が生命または慢性衰弱に危険な疾患であることを診断、予防または治療するためのものであること、(2)申請したとき、そのような疾患がEUで10,000人以下のうちの5人に影響を与えるか、または(B)製品に孤児身分によるメリットがない場合、その製品はEUで十分な見返りを生じず、投資が合理的であることを証明することができる場合、その製品はEU委員会によって孤児に指定されることができる。ならびに(3)このような疾患を満足できる診断、予防または治療する方法がEU市場で販売されていないこと、またはそのような方法が存在する場合、製品は、条例(欧州委員会)847/2000によって定義されるように、そのような疾患の影響を受ける人に大きな利益をもたらすであろう
EUでは、孤児に指定された申請は、マーケティング許可申請を記入する前のいつでも提出することができる。孤児薬品指定は申請者に費用減免、方案援助、集中マーケティング許可手続きへの進入などの激励措置を得る権利がある。
上場許可を得ると,孤児に指定された薬品は承認された治療適応の10年間の専営権を得る権利がある。この間、EMAは、別のマーケティング許可申請を受け入れることができないか、またはマーケティング許可を承認するか、または同じ適応の類似製品のマーケティング許可を10年間延長する申請を受け入れることができない。 合意した小児科調査計画(PIP)にも適合する孤児薬品については,市場排出期間を2年間延長した。小児科研究はEUでの市場排他性だ。いかなる補充保護証明書も孤児の症状に関する小児科研究によって延期してはならない。孤児薬品指定は規制審査と承認過程でいかなる利点も伝達することはなく、監督審査と承認過程の持続時間を短縮することもない。
5年目の終わりにその製品が基準を満たしていないと確定すれば、10年の市場独占経営権は6年に減らすことができます その上で、それは既存の証拠によって証明できることを含む孤児医薬製品の称号を獲得し、もし原始医薬製品の利益が十分に高ければ、市場排他性を維持するのに十分な理由にならない、あるいは疾病の流行率が法律のハードルを超えていることを含む。また、(I)第2の出願人は、(I)第2の出願人が、その製品が類似しているが、より安全であることを証明することができる場合、10年間の任意の期間において、同じ孤児に示された類似製品に販売許可を付与することができる
(Ii)出願人は、孤児医薬製品を第2回申請することに同意するか、または(Iii)元孤児医薬製品の製造業者は、十分な数の孤児医薬製品を供給することができない。
EU補充保護証明書
EUでは、追加保護証明書(“SPC”)を使用して、規制審査中に失われた特許保護を補償するために、特許期間を最大5年に延長することができる。許可証はすべての国に基づいて申請されて承認されなければならない。
EUの小児科適応に対する追加保護
EUでは、新しい医薬製品を開発する会社は、EMAの小児科調査計画(PIP)に同意しなければならず、EMAが申請者の要請に応じて延期または免除を許可しなければならない(例えば、関連疾患または状態が成人でのみ発生するので)このようなPIPに基づいて小児科臨床試験を行わなければならない。マーケティング許可保持者がすでに許可された医薬製品のために新たな適応、薬物形態、または投与経路を増加させようとしている場合、PIP要求も適用される。上場許可申請はPIPによる小児科臨床試験の結果を含まなければならず、適用免除或いは延期が許可されていない限り、この場合、小児科臨床試験は遅い時期に完成しなければならない。PIPに基づいてすべての合意された研究と措置が行われると、製品は6ヶ月のSPC延期を取得する資格があり、承認時に有効であれば、あるいは孤児医薬製品に対しては、上述したように孤児市場を2年間排他的に延長する。この小児科報酬の配布は、特定の条件に依存し、特に、(I)出願人は、PIPに含まれるすべての措置を遵守していることを証明し、(Ii)SMPCおよび適切な包装チラシは、PIPによる研究結果を反映し、(Iii)この製品は、すべてのEU加盟国で許可されている。小児科群における研究の奨励は,合意されたPIPによる情報が小児科適応の認可を招くことができなかったことを考慮しないことができる。
“中華人民共和国条例”
中国では、私たちはますます複雑になっている法律と規制環境で運営されている。私たちは私たちの業務のあらゆる面に影響を与える様々な中国の法律、規則、法規に支配されている。本部分では,我々の業務や運営に関連していると考えられる主な中国の法律,規則,法規について概説した。
“中華人民共和国薬品管理条例”
序言:序言
中国は生物製品を含む薬品の開発、審査、製造と流通を厳格に規制している。適用される具体的な監督管理要求は薬品が国内で製造された中国製造と完成品であるか、それとも国外で製造され、完成品で中国体内に輸入されたのかに依存し、輸入薬品、及び薬品の承認或いは“登録”カテゴリと呼ばれる。輸入と国産薬物については、中国は発売許可申請を提出する前に、通常監督部門が中国薬品監督管理局が中国で臨床試験を行うことを許可し、中国の臨床試験データを提出する必要がある。国内で生産された薬品については,中国の工場で薬品生産許可証を持つことも求められている。
2017年、薬品監督体制は新たな重大な改革時期に入った。2017年10月、国務院弁公庁、中共中央弁公庁は共同で“審査評価審査制度改革の深化による薬品医療機器の革新奨励に関する意見”あるいは“革新意見”を通達した。この改革と最近の他の改革の下での加速計画とその他の優勢は、薬品メーカーがまず中国で上場許可を求め、国内で生産し、腫瘍学などの高度に優先する疾病領域で薬物を開発することを奨励する。
“革新意見”が提出した監督管理改革を実行するため、全人代と国家薬品監督管理局はずっと薬品と業界を規範化する根本的な法律、法規と規則を改正しており、その中には“中華人民共和国薬品管理法”と呼ばれるフレーム的な法律が含まれている (“DAL”)。DALは全国人民代表大会常務委員会が1984年9月20日に発表し、最後の修正は2019年8月26日、2019年12月1日から施行された。DALは国務院が発表したDAL実施条例と呼ばれる高層法規によって実施されている。国家薬品監督管理局は自分のDALを更に実施する法規がある;CTA、上場審査と承認後の修正と継続を管理する主要な法規は薬品登録と呼ばれる
監督管理 (“DRR”).“DRR”は国家薬品監督管理局によって2005年2月28日に公表され、前回の改訂後のDRRは2020年7月1日から発効した。国家薬品監督管理局はすでに2018年と2019年にいくつかの通知と提案された法規を発表して改革を実施しているが、革新意見の多くの改革の実施細則はまだ決定と発表されていないため、監督管理の変化の実施詳細はいくつかの面でまだ確定していない。
規制当局と最近の政府再編
中国では、国家薬品監督管理局は薬品と企業の主要な監督管理機関である。この機関は元中国食品薬品監督管理局に基づいて設立された (“中国食品薬品監督管理局”)は、政府再編の一部としている
中国食品薬品監督管理局と同様に、国家薬品監督管理局は依然として主要な薬品監督機構であり、中国食品薬品監督管理局と同じ法律、法規、規則とガイドラインを実行し、それは薬品のライフサイクルのほとんどの肝心な段階を監督し、非臨床研究、臨床試験、発売審査、生産、広告と販売促進、流通と薬物警戒(即ち発売後の安全報告義務)を含む。CDEは依然としてNMPAに属し、各薬物と生物応用に対して技術評価を行い、安全性と有効性を評価する。
国家衛生委員会(以前の名称は:衛生部と国家衛生·計画出産委員会)であり、中国の主要な医療保健監督機関である。それは医療機関の運営を監督し、その中のいくつかの機関も臨床試験場所であり、病院と他の医療従事者の免許を監督する。NHCは薬品精算において重要な役割を果たしている。そのほか、NHC及びその省級或いは省級以下の地方対応機関は公立医療機関の薬品の集中入札と調達過程を監督と組織し、公立病院及びその薬局はこれらの過程を通じて薬品を獲得する。
また、2018年の再編の一部として、中国政府は国家医療保障管理局を設立し、国が支援する保険計画下の精算を重点的に監督している。
非臨床研究
アメリカ国家薬品監督管理局は臨床前データに輸入と国産薬物の登録申請を支持することを要求した。DRRの規定により、非臨床安全性研究は必ず“非臨床実験室良好な実験室操作管理方法”に符合しなければならない。2003年8月6日、国家薬監局は“非臨床実験室良好検査管理方法”を公布し、2017年7月27日に改訂を行い、非臨床研究の質を高め、そして良好な実験室実践を開始した。NMPAは2023年1月19日に新しく改訂された“非臨床実験室良好実験室操作管理方法”を発表し、2023年7月1日から施行した。国家薬品監督管理局が2007年4月16日に発表した“非臨床実験室良好実験室操作規程認証管理方法に関する通知”によると、国家薬品監督管理局は全国非臨床研究機構の認証を担当し、地方省級医療製品管理部門は非臨床研究機構の日常監督を担当する。国家薬監局は評価機構の組織管理、研究者、設備と施設及び非臨床薬物プロジェクトの運営と管理を通じて、この機関が薬物非臨床研究に従事する資格があるかどうかを決定する。すべての関連要求を満たせば、国家薬監局は“良好な実験室操作規範証明書”を発行し、この証明書も国家薬監局のウェブサイトで公表される。
1988年11月14日に国家科学委員会が公布し、2011年1月8日、2013年7月18日と2017年3月1日に改訂された“実験動物事務管理規定”に基づいて、1997年12月11日に国家科学委員会、国家品質技術監督局が共同で発表した“実験動物良好行為管理方法”、2001年12月5日に科学技術部などの監督部門が発表した“実験動物証明書管理方法(試行)”である。実験動物の使用と飼育は一定の規定を遵守すべきであり,動物で実験を行うには“実験動物使用許可証”を持つ必要がある。
登録カテゴリ
国家薬品監督管理局と研究開発と承認を行う前に、申請者はその候補製品の登録種別を決定する必要があり(最終的には国家薬品監督管理局に確認する必要がある)、これはその臨床試験とマーケティング応用の申請要求を決定する。
“薬品発売登録条例”によると、薬品発売登録申請は3種類に分けられ、即ち漢方薬、化学薬物と生物製品である。その中、化学薬品の登録申請は革新化学薬品、改良化学新薬、模倣薬などによって分類され、生物製品の登録申請は革新生物製品、改良生物製品、発売生物製品(生物類薬物を含む)などによって分類される。
国家薬監局は2020年6月29日に“生物製品の登録類別と申告資料の要求”を発表し、2020年7月1日から施行し、元の治療性生物製品の種類を代替し、治療性生物製品を3種類に分類すべきであることを規定し、その中のI類はまだ世界各地で発売されていない治療性生物製品であり、II類は改良された新型治療性生物製品を指し、III類はすでに中国国内外で発売された治療性生物製品である。
加急プロジェクト
革新を奨励する優先的な評価と承認計画
2009年以来、国家薬品監督管理局はいくつかの迅速な審査と承認メカニズムを採用し、ここ数年に革新を奨励するための追加迅速プロジェクトを創立した。これらの加速プロジェクトの申請は、登録パッケージと共に提出することができ、または登録提出がCDEによって審査を受けた後に提出することができる。国家薬品監督管理局が2017年12月21日に発表した“薬品革新優先審査審査承認の奨励に関する意見”は、革新薬物が快速チャンネルCTA或いは薬品登録経路を獲得することを明らかにした。“薬品革新優先審査承認の奨励に関する意見”は国家薬品監督管理局が2020年7月7日に発表した“突破的治療薬物評価プログラム(試行)”などの3つの文書の公告に取って代わられ、この3つの文書はそれぞれ“突破的治療薬物評価プログラム(試行)”、“薬品発売条件審査申請審査承認手続き(試行)”、“薬品発売優先審査手続き(試行)”などである。出願人が、生命または生活の質に深刻な影響を及ぼす疾患の予防および治療に使用され、有効な予防および治療手段がないか、または既存の治療方法と比較して顕著な臨床的利点を有することを示す画期的な治療薬プログラムを、第1段階および第2段階の臨床試験中および一般的に第3段階の臨床試験の開始よりも遅くないことを可能にする。また,薬品の発売許可を申請する際には,臨床価値が明らかな薬品については,申請者は優先審査審査承認手続きを申請することができる。
これらの迅速なプロジェクトのうちの1つに採用された場合、申請者は全体の審査承認過程においてCDEの審査員とより頻繁かつタイムリーなコミュニケーションを行い、審査と承認を加速し、より多くの機関資源を得る権利がある。
国家薬品監督管理局はまた、早期中国臨床試験データ或いは国外で許可された臨床データのみに基づいて、ある薬物に対して条件付きの許可を行うことを許可した。承認後、出願人は1つ以上の上場後の研究を行う必要があるかもしれない。当施設では,生命にかかわる疾患の満たされていない臨床的ニーズを満たす薬剤や孤児適応を治療する薬剤のために行われている。2018年、NMPAおよびNHCは、CDEに指定された過去10年間に米国、EU、および日本で承認された薬剤のための条件付き承認計画を確立し、これらの薬剤は、(1)孤児適応、(2)生命に危険な疾患を治療する薬剤、有効な治療または予防方法がない、および(3)生命を脅かす疾患を治療する薬剤のうちの3つの基準を満たし、他の承認された治療法と比較して明らかな臨床的優位性を有する。
国家薬品監督管理局はこれまでの臨床試験と薬品上場登録の承認加速に関する改革を取り入れ、薬品の発売登録を加速する4つのプログラム、即ちプログラムを発売した
先駆的治療薬、条件付き承認手続き、優先審査審査承認手続き、特別審査手続き:
•画期的な治療薬のプログラム:生命の質に深刻な影響を与える疾患又は疾患を予防及び治療するための革新的薬物又は新薬を改良するための薬物臨床試験中に、他に有効な予防及び治療方法がなければ、又は革新薬又は改善された新薬が既存の治療方法と比較して明らかな臨床的優位性を有することを証明する十分な証拠があれば、出願人は、画期的な治療薬の適用手続きを申請することができる。
•条件付き審査手続き:薬品の臨床試験期間中に、以下の状況の1つの薬品があり、条件付きで上場登録を許可することができる:(一)有効な治療方法がない生命に危害を及ぼす疾病を治療する薬品は、その臨床試験はすでに治療効果データがあり、臨床価値を予測できる;(2)公衆衛生が必要な薬品であり、その臨床試験はすでに治療効果データがあり、臨床価値を予測できる。(Iii)重大な突発的公衆衛生事象が必要とされる他のワクチン、または評価によれば、利益がリスクよりも大きい場合、NHCは必要と考えられる他のワクチンである。
•優先審査手続き:薬品の発売登録時に、明らかな臨床価値を有する薬品は優先審査手続きを申請することができ、(一)臨床で必要だが不足している薬品、革新薬品と重大伝染病の予防と治療、珍しい病気の改良新薬を含む;(二)小児科の生理特徴に符合する薬品の新品種、剤形と規格;(三)疾病予防と治療に必要なワクチンと革新ワクチン;(四)突破的な治療薬品のプログラムに入った薬品;(五)条件付き審査基準に適合する薬品;(六)“国家薬品監督管理局”が規定するその他の優先審査状況。
•特別審査手続き:突発公共衛生事件が脅威或いは発生した時、国家薬品監督管理局は法に基づいて突発公共衛生事件中の予防と治療が必要な薬品に対して特別審査を実施することを決定することができる。特別審査手続きに組み入れられた薬品は、疾病予防制御の特殊な需要に応じて、一定の期限と範囲内で使用を制限することができる。
臨床試験と上場承認
臨床研究を完成した後、スポンサーは通常中国で臨床試験を行って初めて新薬を登録することができる。今回の申請に必要な書類と資料要求は登録種別によって決定される。国家薬品監督管理局はすでに一連の措置を取ってCTAを承認する効率を高め、また“薬品臨床実践品質管理条例”或いは中華人民共和国GCPに対する監督と実行を大幅に強化し、データの完全性を確保した。
試行審査
中国で行われている新薬登録臨床試験は,届出管理の薬品臨床試験機関で承認されて行わなければならない。輸入薬については,この薬物が世界のどこでも承認されていない限り,試験前に中国国外の承認証明を提供する必要がある。発展を支持する独立中国試験以外に、輸入薬品申請者は全世界の試験開始時に中国にサイトを構築することができ、国際マルチセンター試験(IMCT)の一部とすることができる。国内で生産された薬物は中国国外では承認要求を受けず,従来のやり方とは異なり,国家薬品監督管理局は最近これらの薬剤もIMCTによる開発を許可することを決定した。
2015年、国家薬品監督管理局は新薬臨床試験のすべての段階(通常は3段階)に対して包括承認を発表し始め、段階ごとに承認を発表するのではない。いくつかのタイプの新製品候補については、CTAは他の申請よりも優先され、単独の高速キューで承認を待つ可能性がある。
米国国家薬品監督管理局は現在、新薬臨床試験制度を採用しており、60営業日後、申請者はCDEの反対意見を何も受けていなければ、試験を継続することができる。中国では試験点の数を拡大し,臨床試験点認証プログラムを通知プログラムに変更している。
薬物臨床試験登録
DRRによると、薬物の臨床試験は承認され、生物学的同等性試験を提出しなければならない。薬品臨床試験は必ず“薬品臨床試験規範”に符合しなければならず、すでに規定に従って記録を完成し、関連規定に符合する薬品臨床試験機関で行わなければならない。2013年9月6日、国家薬品監督管理局は“薬品臨床試験情報プラットフォーム公告”を発表し、すべて国家薬品監督管理局の許可を経て中国で行われた臨床試験は、上述した国家薬品監督管理局に報告した臨床試験以外、すべて臨床試験登録を完成し、そして薬物臨床試験情報プラットフォームを通じて試験情報を発表すべきである。出願人は、臨床試験の承認を得てから1ヶ月以内に試験事前登録を完了し、試験の唯一の登録番号を取得し、第1の被験者が試験に参加することを登録する前にいくつかの後続情報の登録を完了しなければならない。臨床試験の承認を得てから1年以内にも上記の事前登録と登録許可を得ていない場合は,出願人は説明を提出しなければならず,3年以内にもプログラムが完了していない場合は,臨床試験承認は自動的に廃止される。
人類遺伝資源承認
2015年7月2日、科学技術部は“人類遺伝資源サンプリング、採集、取引、出力或いは中国審査行政許可事項サービスガイドライン”を発表し、その中で、非中国投資の発起人が臨床試験で人類遺伝資源をサンプリング採集するのは、中国人類遺伝資源管理所のオンラインシステムを通じて報告すべきであると規定した。2017年10月26日、科学技術部は“人類遺伝資源の行政審査の最適化に関する通知”を発表し、中国薬品の商業化サンプリングによる人類遺伝資源の採集の審査を簡略化した。中華人民共和国国務院は“人類遺伝資源管理条例”(以下は“条例”と略称する)を発表し、2019年7月1日から施行した。“人類遺伝資源条例”は中国人類遺伝資源の収集、保存、利用と対外提供に対して規範化を行った。この規定によると,“ヒト遺伝資源”にはヒト遺伝資源材料と情報が含まれている.ヒト遺伝資源材料とは,ヒトゲノム,遺伝子などの遺伝物質を含む器官,組織,細胞などの遺伝物質である。人間遺伝資源情報とは、データのような人間の遺伝資源材料から生成された情報である。科学技術部は国家レベルの人類遺伝資源管理を担当し、省級政府科学技術行政部門は地方レベルの人類遺伝資源管理を担当する。非中国実体、非中国個人及びそれによって設立或いは実際に制御された実体は、中国の人類遺伝資源(器官、組織、細胞とその他のヒトゲノムと遺伝子の遺伝物質を含む)を収集或いは保存してはならない)、或いは国外で人類遺伝資源を提供すると同時に、彼らが中国の人類遺伝資源の使用を禁止し、彼らがすでに中国の関係政府機関の許可を得たか、或いは関係政府機関と中国実体に国際協力を行って記録した限りである。HGR条例は中国と非中国が持つ実体間の研究協力に関する承認要求を正式に規定している。新規定によると,臨床機関が中国のヒト遺伝資源を用いて臨床試験を行う際には,ヒト遺伝資源を中国以外の地域に輸出することには触れず,新たな通知制度(従来の事前承認方式とは逆)を実施する。
生物安全法
2020年10月17日、全人代常務委員会は“人民Republic of China生物安全法”を採択し、2021年4月15日から施行された(“生物安全法”)。“生物安全法”はHGRと生物資源の安全監督管理を含む中国の生物安全関連活動を規範化するための完全な制度を確立した。“生物安全法”は中国がその“生物安全法”に対して主権を持つことを明確に宣言し、さらに“生物安全条例”を認め、中国案中の非中国実体に対して中国の“生物安全法”が確立した基本的な監督管理原則と制度を利用することを認めた。“生物安全法”は中国最高立法機関が通過した法律であり、中国の生物安全の主要な監督機関である科学技術部にもっと大きな監督管理権力と自由裁量権を与え、中国の生物安全の全体的な監督管理構造は変化し、更に厳格かつ複雑になると予想される。“生物安全法”を遵守しない要求は、罰金、関連活動の一時停止、関連HGRの没収、これらの活動の展開によって生じる収益を含む処罰を受ける。
2022年3月21日、科学技術部は“人類遺伝資源管理条例実施細則草案(意見募集稿)”(“実施細則草案”)を発表し、上流からHGR材料を採集し、下流までHGR材料及びその由来データを開発と対外に提供するすべてのHGR関連活動(“HGRデータ”)に対して厳格な審査を行った。実施細則草案は、業務の詳細を提供し、過去数年間に“人類健康責任条例”の発効後に発生した問題を明らかにすることを目的としている。実施細則草案に基づき,マーケティング目的を獲得するための臨床研究
中国の薬品と医療機器の許可は、HGR材料の輸出に触れなければ、もしHGR材料が場所によって収集され、臨床試験方案で規定された場所或いは陸上第三者実験室で処理された場合、科学技術部に報告しなければならない(事前承認ではない)。実施規則の草案は、重要な遺伝子ファミリーに関するHGRデータ、特定の領域のHGRデータ、および500人以上のエクソン群配列決定およびゲノム配列決定情報を外部で提供または開示するように、HGRデータを公開的に提供または利用する必要がある場合を列挙する。
非中華人民共和国データに対する試験免除と受け入れ
アメリカ国家薬品監督管理局は臨床試験とデータに対する要求を減少する可能性があり、具体的には薬物と現有のデータに依存する。国家薬監局は試験の全部または一部の免除を承認し、その要求に応じた早期データを含む海外で生成されたデータ(世界的な研究の一部でなくても)を受け入れることを示している。2018年7月6日、国家薬品監督管理局は“外国薬の臨床試験データの受け入れに関する技術指導原則”を発表した (“指導原則”)は“革新的意見”の実施細則の一つである。指導原則に基づき、非中華人民共和国臨床試験データは必ず真実性、完全性、正確性とトレーサビリティの要求を満たさなければならず、しかもこれらのデータは国際人用薬品登録技術要求調整会議GCP下の関連要求に符合しなければならない (“無形文化遺産”)スポンサーは被験者グループの潜在的に意味のある人種差に注意しなければならない。
国家薬品監督管理局は現在正式に許可されていることと、その前身機関が過去のケースに基づいて、中国以外で許可された薬物を中国で条件的に承認することを許可し、中国内部で事前承認の臨床試験を行う必要がない。具体的には、2018年10月23日、国家薬品監督管理局と国家薬品監督管理局は“海外臨床に必要な新薬審査プログラム”を発表し、その中に最近10年以内にアメリカ、EU或いは日本で許可された薬物を許可するプログラムを設置した:1)孤児疾患の治療、2)中国で有効な治療或いは予防がない深刻な生命に危害を及ぼす疾患の予防或いは治療、3)深刻な生命に危害を及ぼす疾患の予防或いは治療、かつ中華人民共和国で許可されていない薬物は明らかな臨床優勢を持っている。申請者はリスク緩和計画の構築を要求され、薬物発売後に中国で試験を完成することが要求される可能性がある。
臨床試験の流れと良好な臨床実践
DRRによると,臨床試験にはI,II,IIIとIV相臨床試験および生物同等性試験がある。薬物の特徴と研究目標に基づいて、研究内容は臨床薬理研究、探索性臨床試験、検証性臨床試験と発売後の研究を含むべきである。国家薬監局は中国の臨床試験の異なる段階で倫理委員会の許可を得なければならず、中華人民共和国のGCPに適合しなければならないことを要求した。国家食品薬品監督管理局は中国のGCP遵守状況を評価するために検査を行い、重大な問題が発見されたらCTAを中止する。
臨床試験の質を高めるため、中国食品薬品監督管理局は2003年8月6日に“中国臨床試験規範”を発表し、2020年4月23日に更に改訂し、2020年7月1日から施行した。臨床試験の質と被験者の安全を確保するため、中華人民共和国GCPは中国臨床試験の設計と実施に対して全面的かつ実質的な要求を提出した。特に,中国のGCPは研究対象の保護を強化し,臨床試験で採取した生物試料の制御を強化している。中国のGCPは、スポンサーは臨床試験関連の原因で負傷或いは死亡した人体被験者の医療費用と相応の賠償を負担しなければならないと規定している。保証人、調査人は直ちに人体主体に賠償金或いは賠償金を支払わなければならない。“革新意見”に基づいて、薬物臨床試験機関の認可に対して届出管理を実行する。臨床試験の進行は中華人民共和国のGCPを遵守しなければならず,案は研究地点ごとの倫理委員会の承認を得なければならない。新しく改訂されたDAL、及び国家薬品監督管理局と国家薬品監督管理局は2019年11月29日に共同で公布し、2019年12月1日から施行した“薬品臨床試験機構管理条例”に基づいて、薬品臨床試験機関に対して届出管理を実施した。薬物臨床試験に関連する生物サンプルのみを分析する実体は届出を必要としない。
新薬申請(NDA)と承認
“薬品上場登録条例”によると、申請者は薬剤学、薬理学、毒理学と薬物臨床試験の関連研究を完成し、薬品の品質標準を確定し、商業規模の生産技術を確認し、そして主管国家薬品監督管理局が指定した専門技術機関による検証と検査を受ける準備をした後、CDEに薬品発売登録申請を提出することができる。CDEは組織薬学,医療などの技術者がその安全性,有効性,品質を全面的に審査する
出願人が提出した出願書類、専門技術機関によるチェックや検査結果等に基づいて、薬品の制御可能性等を評価する。総合審査結論が肯定的である場合は、当該薬品の発売を承認し、薬品承認文番号、上場授権者、メーカーの情報を含む薬品登録証を発行する。
2015年8月9日に公表された“薬品と医療機器設備審査審査承認制度の改革に関する意見”によると、国務院は“薬品上場授権者メカニズムの試験展開に関する政策”を公表した。
新しく改訂された“薬品上場授権書”によると、薬品上場許可書保有者のメカニズムの下で、薬品登録証を取得した企業と研究開発機構はすべて薬品上場授権書の保有者になる資格があり、この薬品上場授権書保有者は“薬品上場授権書”の規定に従って薬品の非臨床実験室研究、臨床試験、生産と流通、発売後の研究及び薬品不良反応のモニタリング、報告と処理を担当する。薬品発売許可所持者は代理工生産企業を招聘して生産を行うことができるが、代行生産企業は必ず許可を得なければならず、薬品経営許可証を持つ薬品経営企業を招聘して経営活動に従事することができる。国務院医療製品管理部門の許可を経て、薬品発売許可保持者は薬品の発売許可を譲渡することができ、譲受人は品質管理、リスク防止と責任補償能力を持ち、薬品の安全、有効と品質制御可能を確保し、薬品の発売許可保持者の義務を履行しなければならない。
製造と流通
新たに改訂されたDALとDALの実施方法によると、中国国内のすべての薬品生産施設は現地の薬品監督管理部門が発行した適切な“生産範囲”を持つ“薬品生産許可証”を取得しなければならない。この免許証は五年ごとに更新しなければなりません。2004年8月5日に公表され、2020年7月1日から施行された最新改訂された“薬品生産監督管理方法”によると、上場許可所持者が代理工生産機構を通じて薬品を生産しない場合は、国家薬品監督管理局の省級対口部門に薬品生産許可証を申請し、国家薬品監督管理局の検査とその他の監督を受けなければならない。
同様に、販売、輸入、輸送と貯蔵或いは流通活動を行うためには、会社は現地の薬品監督機関から適切な“流通範囲”を持つ“薬品流通許可証”を取得し、5年ごとに継続しなければならない。
中国は薬品の流通を制御する“2枚の領収書制度”を形成した。2枚の発券制は一般的に流通チェーン全体で領収書を発行してはいけないことを要求し、1枚はメーカーからディーラーに発行し、もう1枚はディーラーからエンドユーザー病院に発行する。これは、製造業者からその完全所有または制御された流通業者、または輸入医薬品からその独占流通業者に、または流通業者からその完全または制御された子会社(または完全または制御子会社間)に請求書を販売する製品を含まない。しかし、この制度は依然として、企業が複数の流通業者を使用して中国のより大きな地理的地域に入る選択を大きく制限している。2枚の領収書制度を遵守することは製薬会社が公立病院調達プロセスに参加する前提条件となり、現在中国の大部分の医療保健は公立病院が提供している。2発制を実施できなかったメーカーやディーラーは入札過程に参加する資格を失う可能性がある。
規格外のメーカーもブラックリストに登録される可能性があり、地元の公立病院に薬品を販売してはいけない。
2枚の領収書制度は最初に11の総合医療改革試験に参加した省で実施されたが、この計画はほとんどの省に拡張されており、これらの省には独自の計画規則がある。
ヒト細胞療法
2003年3月20日、アメリカ国家薬監局は“人体細胞療法研究及び製剤品質管理技術ガイドライン”を発表し、人体細胞療法の研究にいくつかの原則を設定した。
国家薬品監督管理局が2007年7月10日に発表し、2007年10月1日から施行した“ヒト細胞治療及びその製品は生物製品に属する”に基づいて、生物製品の申請は新薬申請過程として提出しなければならない。
2009年3月2日、衛生部は“医療技術臨床応用管理方法”を発表し、2009年5月1日から施行し、細胞免疫治療は第三種類の医療技術に属することを規定し、その臨床応用は衛生部の付加規定に適用する。2009年5月、衛生部は初めて臨床応用を許可する三種類の医療技術目録を公表し、即ち細胞免疫治療技術は三種類の医療技術が臨床応用を許可する三種類の医療技術と規定し、そして2015年6月29日に“三種類の医療技術参入承認の臨床応用の廃止に関する通知”によって廃止された。“臨床申請の三種類の医療技術参入許可の取り消しに関する仕事に関する通知”も三種類の医療技術の臨床申請の承認を取り消した。
2017年11月30日、中国食品薬品監督管理局は“薬品登録受理審査ガイドライン(試行)”の通知を公表し、治療性生物製品の臨床試験の申請と治療性生物製品の生産発売応用、その規定を適用した。2017年12月18日、中国食品薬品監督管理局は“細胞治療製品研究と評価技術指導原則(試行)”を公布し、薬物研究、開発と登録としての細胞治療製品の研究と評価を規範と指導した。
CDEが2021年2月10日に発表した“免疫細胞治療製品の臨床試験技術ガイドライン(試験)”(“臨床試験技術ガイドライン”)は、CAR-Tは免疫細胞治療製品として、遺伝子治療製品の性質を持っていると規定している。“臨床試験技術ガイドライン”の内容は強制的ではなく、その目的は免疫細胞療法製品の臨床試験中のいくつかの技術問題について提案と提案を提供することであり、免疫細胞療法製品の監督管理性質或いは分類を確定することではない。2021年12月3日、CDEは“遺伝子治療製品非臨床研究と評価技術ガイドライン(試行)”、“遺伝子治療製品非臨床研究技術ガイドライン(試行)”、“遺伝子修飾細胞治療製品技術ガイドライン”を発表し、発表日から施行した。“遺伝子組換え細胞治療製品技術ガイドライン”は“細胞治療製品研究と評価技術ガイドライン(試行)”に基づいて制定され、CAR-T細胞治療製品などの遺伝子組換え細胞治療製品の非臨床研究と評価を規範と指導することを目的としている。CDEは2022年1月29日に“キメラ抗原受容体T細胞(CAR-T)治療製品の発売承認臨床リスク管理計画技術ガイドライン”を発表し、発表の日から施行し、CAR-T治療製品の上場承認臨床リスク管理計画の起草作業を規範と指導した
発売後監督
新しく改訂されたDALによると、薬品発売許可所持者はDALの規定に従って薬品に関連する副作用のモニタリング、報告と処理を担当しなければならない。上場許可所持者、薬品生産企業、薬品経営企業と医療機関は定期的にその生産、販売、使用した薬品の品質、治療効果と副作用を検査しなければならない。副作用が疑われる症例については,直ちに薬品監督管理部門と衛生行政主管部門に報告すべきである。薬品の発売許可所持者は直ちに販売を停止し、薬品経営企業と医療機関に販売、使用を停止し、販売済みの薬品をリコールし、品質問題或いはその他の安全上の危険がある薬品に対して、適時にリコール情報を公告しなければならない。
医薬製品の広告と販売促進
中国は承認された薬品広告に対して厳格な制度がある。未承認の薬品は広告宣伝をしてはいけません。広告の定義は非常に広く、エンドユーザに製品を直接または間接的に紹介する任意のメディアであってもよい。広告と他の種類の販売促進との間には明確な限界がない。
各薬品広告は現地の薬品監督管理部門の許可を得なければならず、許可された広告内容は、再申請して承認されておらず、変更してはならない。処方薬の広告を求める企業はNMPAとNHCが共同で許可した医学定期刊行物にしか広告を行わず、しかも処方薬の広告は医療と製薬専門家が読むためにのみ提供されることを明記すべきである
薬品広告は厳しい内容制限を受け,医師や病院の推薦や有効性保証を禁止している。この薬の承認以外の内容を含む広告
文書、ラベル外の内容は、禁止されている。虚偽広告は、エンドユーザーが民事訴訟を起こし、罰金を含む行政責任を負う可能性がある。広告以外にも,薬品情報を伝達する非販売促進サイトは,現地の薬品監督機関の単独承認手続きを通過しなければならない。
製品責任
中華人民共和国製品品質法 1993年2月22日に全国人民代表大会常務委員会が公表した“製品品質法”は、それぞれ2000年7月8日、2009年8月27日と2018年12月29日に改正され、製品品質監督管理に関する主要な法律である。製品品質法により,メーカーはその生産した製品の品質に責任を負わなければならず,販売者はその販売する製品の品質を確保する措置を講じなければならない。製品欠陥による人身傷害又は財産損害は,欠陥製品自体を除いてメーカーが賠償責任を負うべきであるが,メーカーは(一)製品が販売されていないこと,(二)製品販売時に傷害又は損害を与える欠陥が存在しないこと,又は(三)製品を販売する際の科学技術レベルで欠陥を検出できないことを証明することができる。製品に欠陥があるため他人の人身被害や財産損失をもたらすのは、販売者の責任である。売り手が欠陥製品の製造業者やサプライヤーを指定していない場合は、賠償しなければならない。製品欠陥による人身被害や財産損失の場合は、生産者又は販売者に賠償を請求することができます。
1986年4月12日に全国人民代表大会が公布し、2009年8月27日に改正された“中華人民共和国民法通則”によると、欠陥製品が他人の財産損失或いは人身損傷を引き起こす場合は、生産者と販売者が共同で責任を負わなければならない。“中華人民共和国侵害責任法”に基づく “侵害責任法”は2009年12月26日に全国人民代表大会常務委員会によって公布され、2010年7月1日から施行され、製品欠陥により他人に損害を与えた場合は、侵害責任を負わなければならないと規定されている。他人の損害をもたらした製品欠陥は販売者に責任を負うことができ、販売者は権利侵害責任を負わなければならない。被害者側は、損害を与えた瑕疵製品のメーカー又は販売者に賠償を請求することができる。2020年5月28日に公布され、2021年1月1日から施行された“中華人民共和国民法典”は、“中華人民共和国民法通則”と“侵害行為法”に合併し、2021年1月1日から施行された。“中華人民共和国民法典”の権利侵害法に関する規定は“中華人民共和国民法通則”と“侵害法”とほぼ一致している。
商業賄賂
賄賂に関する刑事調査や行政訴訟に関連する製薬会社は、それぞれの省級衛生·計画出産行政部門が“商業賄賂不良記録”に登録されている。衛計委が2013年12月25日に公表し、2014年3月1日から施行した“薬品購入販売業界が商業賄賂不良記録を確立する規定”に基づいて、省衛生計生行政部門は“商業賄賂不良記録を確立する実施方法”を制定した。医薬企業あるいはその代理人が一度に“商業賄賂不良記録”に登録されたのは、不良記録が公表された日から2年以内に、調達入札過程に参加したり、現地の省級地区にある公立医療機関にその製品を販売することを禁止する。医薬会社又はその代理人が5年以内に2回又は2回以上“商業賄賂不良記録”に登録されている場合は、当該不良記録が公表された日から2年以内に、調達入札過程に参加したり、中国のすべての公立医療機関にその製品を販売することを禁止する。
知的財産権保護を監督する
非特許排他性新薬監視期間
薬品監督管理局の実施条例によると、国家薬品監督管理局は公衆の健康を保護する目的で、承認の日から生産を許可した新薬に対して5年間の行政監視期間を実施し、新薬の安全性を持続的にモニタリングすることができる。監視期間内に、国家薬品監督管理局は、同じタイプの薬物に対する別の申請者の別のCTAを承認しないだろう。2020年7月、新しいDRRが施行され、5年間の監視期間がそれに応じて廃止される。
また,CDEは2020年7月2日に“生物製品登録受付と審査ガイドライン”を発表し,このガイドラインの付録IIにより,同一タイプの治療性生物製品のモニタリング期間の記述も削除した。
規制データ保護
“革新意見”はまた革新者を保護する監督管理データ保護制度の構築に基礎を築いた。この保護は、革新薬、革新的治療生物製剤、孤児疾患を治療する薬剤、小児科薬、および特許挑戦に成功した薬剤の他の種類の薬剤の未開示臨床試験データに適用される。
2018年4月25日、国家薬品監督管理局は“薬学研究データ保護実施条例”の意見募集稿を発表し、革新小分子薬物の監督管理データ保護期限を6年とし、革新治療性生物製品の監督管理データ保護期限を12年とした;小児科と孤児薬物は承認の日から6年間同時に実施する。完全な保護条項は、中国のローカル試験またはマルチセンター試験地点、および中国と他の国で同時に提出されたマーケティング申請に依存する必要がある。中国で提出された書類は、海外で提出された書類が最長6年に達すると、その期限は1~5年に短縮される。中国で提出された意見が6年を超えた後、海外で提出された意見は保護されない可能性がある。
特許に関する保護特許と連動する
“革新的意見”はまた、後続の出願人がその出願に関連する特許を指定することを要求され、出願後の指定された期限内に関連する特許保有者(イノベーターを含む)に関連する特許保有者を通知し、彼らが自分の権利を保護するために訴訟を提起することを可能にする、革新者を保護する特許連動制度の基本要素を述べている。このシステムは、イノベーターが任意の訴訟を提起している間、潜在的な侵害の後続申請を継続して審査するようにNMPAに要求するであろう。しかしながら、国家特許商標局は、後続の出願に有利な後続の出願を承認しなくてもよいし、より短い時間を基準として、後続の出願の後続の出願を承認しなくてもよい。この改革は規制を施行する必要があるだろう。
特許期間を延長する
2020年10月17日に全人代常務委員会が発表した特許法に基づき、2021年6月1日から施行され、国務院特許行政部門は特許権者の請求に基づいて、中国が上場を許可した新薬の関連発明特許の特許期限を延長する。有償展示期間は5年を超えず,新薬承認発売後の総有効特許期間は14年を超えない。
商標
1982年8月23日に全国人民代表大会常務委員会が公布し、1993年2月22日、2001年10月27日、2013年8月30日と2019年4月23日に改正され、2019年11月1日から施行された“中華人民共和国商標法”によると、登録商標の有効期限は10年で、登録日から計算される。引き続き使用する場合は,登録者は商標満了前12ヶ月以内に更新手続きをしなければならない。登録者がそうしなければ、6ヶ月の猶予を与えることができる。1回の継続登録の有効期間は10年であり,当該商標の前の有効期間が満了した日から計算する。期限が満了して継続しない場合は,登録商標を抹消する.工商行政管理機関は法律に基づいて登録商標専用権を侵害する行為を調査する権利がある。刑事犯罪の疑いがある場合は,直ちに司法機関に移送して法に基づいて決定しなければならない.
ドメイン名
ドメイン名は情報産業部が2004年11月5日に発表した“中国インターネットドメイン名管理方法”の保護を受け、2004年12月20日から施行され、工業と情報化部が発表した“インターネットドメイン名管理方法”に取って代わられる (以下、工信部と略す)は、2017年8月24日から施行され、2017年11月1日から施行される。工信部は中国インターネットドメインの管理を担当する主要な監督管理機関である。ドメイン登録は関連規定により設立されたドメイン名サービス機関によって処理され,登録に成功した後,出願人はドメイン名保持者となる.
精算と定価
中国の国家医療保険プランは1998年に国務院が発表した“国務院の都市従業員基本医療保険プランの構築に関する決定”に基づいて採択された
都市のすべての使用者は従業員を基本医療保険計画に加入させなければならない。保険料は雇用主と従業員が共同で支払う。2007年、国務院は“国務院の都市住民基本医療保険試験の展開に関する指導意見”を公布し、試験地区の都市住民は自発的に都市住民の基本医療保険に参加することができ、都市従業員ではない。国家医療保険計画の参加者及びその雇用主は(ある場合)月ごとに保険料を納付しなければならない。計画参加者はNRDLに含まれる薬品コストの全部または一部を清算する資格がある。NRDLに記載されている薬品は臨床で必要な、安全、有効、価格が合理的で、使用が便利で、十分な数量の薬品でなければならない。
薬品がNRDLに組み入れられることを影響する要素はこの製品が中国で大量に使用され、通常臨床処方に使用されているかどうか、及びこの製品が一般公衆の基本医療需要を満たすために重要であると考えられているかどうかを含む。2016年以来,特に臨床価値の高い革新的な薬物や大病治療薬が考えられてきた。また、中国人人力資源·社会保障部も、NRDLへの組み入れと引き換えに、値下げと引き換えに、臨床的要求が高く、有効であることが証明された高価な薬物メーカーと交渉してきた。最新バージョンのNRDLは2023年に発表され、2023年1月13日に実施される。
政府価格規制
2015年5月4日、国家発改委など6部委員会は“薬品価格改革の推進に関する意見”を発表し、政府が規定した大多数の薬品の最高小売価格を廃止し、政府医療保険基金が精算した薬品、特許薬品、その他のいくつかの薬品を含む。政府は主に統一的な調達メカニズムを確立し、医療保険精算標準を調整し、医療と定価のやり方に対する監督管理を強化することによって価格を制御し、以下に述べる。
集中調達と入札
現行の規定によると、政府の所有或いは国有或いは持株企業のすべての公立医療機関は集中オンライン調達プロセスを通じて薬品を調達しなければならない。国家の基本的な薬物目録上の薬品も例外があり、必ず自分の調達規則、及び中央政府の特別に規制された薬品、例えば有毒、放射性、麻酔薬品と漢方薬を守らなければならない。
集中調達プログラムは省レベルあるいは市レベルの政府機関が公開入札を行う形式をとる。集中入札手続きは通常年に1回行われる。入札は専門家データベースからランダムに選択した委員会によって評価される.委員会のメンバーは一連の要素に基づいて入札を評価し、入札価格、製品品質、臨床有効性、製品安全、技術レベル、メーカーの資質と名声、アフターサービスと革新を含むがこれらに限定されない。
国務院弁公庁が2019年1月に印刷配布した“国家組織薬品集中調達使用試験方案に関する通知”によると、11の試験都市は模造薬ブランドから薬品を抽出して薬品集中調達を行う。入選薬品は品質と効果の一致性によって評価されなければならない。この政策は患者の薬品コストを下げ、企業の取引コストを下げ、機構の薬品使用を規範化し、薬品の集中調達と定価制度を完備することを目的としている。今回の集中調達は、中国調達リストの薬品生産が許可されたすべての企業に向けて開放された。薬品の臨床効果、副作用とロット安定性を考慮し、その一致性は評価の主要な標準であり、同時にサプライヤーの生産能力と安定性も考慮する。
その他中華人民共和国国家級と省級法律法規
本節において“中華人民共和国その他の国家レベル及び省級法律法規”における“外国”とは、文意が別に説明されていない限り、中華人民共和国以外の国又は地域を意味する
国、省、市レベルの政府が管理する多くの他の法律と法規によると、私たちは法規を変える必要があります。その中のいくつかの法規は現在、あるいは私たちの業務に適用される可能性があります。例えば、法規は、患者医療情報の機密性を制御し、どのような場合に患者医療情報を私たちのデータベースに発行することができるか、または第三者に発行することができる。プライバシーがあります
臨床試験中の人体被験者も法規によって保護されている。例えば、症例報告表は、ヒト対象の名前の開示を避けなければならない。
プライバシーとデータセキュリティ保護
これらの機密を管理する患者の医療情報開示や使用の法律法規は,医療データ転送の制限を含めて将来的により厳しくなる可能性がある
科学的データ
2018年3月、国務院弁公庁は“科学データ管理方法”を公布し、科学データに対して広義の定義と科学データ管理の関連規則を行った。“科学データ管理方法”によると、国家秘密、国家安全、社会公共利益、商業秘密とプライバシーに関連する科学データは秘密にすべきであり、公開すべきものは、使用目的、使用者資格、秘密条件などを審査し、接触者の範囲を厳格にコントロールすべきである。中国国内の企業は対外交際と協力の中で国家秘密に関する科学データを提供する前に、政府の承認を受けなければならない。法人単位は主管部門の許可を得た後,規定に従って関連手続きを行い,ユーザと秘密保持契約を締結しなければならない.また、中国政府が援助した研究を一部或いは全部行う研究者は、いかなる外国学術定期刊行物に関連する科学データを発表する前に、関連する科学データを提出して、当該研究者の所属実体が管理するために提出しなければならない。
個人情報
“中華人民共和国民法”によると、個人情報は法律で保護されている。他人の個人情報を取得する必要がある組織や個人は合法的に情報を取得し,情報の安全を確保し,他人の個人情報を不正に収集,使用,加工,転送してはならず,他人の個人情報を不正に売買,提供,配布してはならない.また、個人情報の処理は、合法性、適切性、必要性の原則に従うべきである。全人代常務委員会は2021年8月20日に公布され、2021年11月1日から施行された“個人情報保護法”で、個人情報の保護と処理の主要な制度枠組みを描き出した。個人情報保護法は,個人情報の処理と法的責任を詳細に規定しており,個人情報の範囲や個人情報を処理する方式,個人情報処理規則の制定,個人が個人情報を処理する際の権利や処理者の義務を含んでいる.個人情報保護法は,個人情報の不正処理に対する処罰にも力を入れている
データ安全です
2016年11月7日、中国全国人民代表大会常務委員会は“中華人民共和国ネットワークセキュリティ法”を公布し、2017年6月1日から施行され、ネットワーク事業者が業務とサービスを提供する際には、ネットワークセキュリティを維持する義務を履行しなければならないと規定した。ネットワーク事業者は、適用された法律またはそのユーザと締結された協定の規定に違反して、それが提供するサービスとは無関係な個人情報を収集したり、その個人情報を収集または使用してはならず、CIIOは、中国国内で収集および生成されたすべての個人情報および重要なデータを中国に格納することを要求される
2021年6月10日、全人代常務委員会は中国“データ安全法”を公布した (“データ安全法”)は,2021年9月1日から施行される。“データ安全法”はデータ活動に従事する単位と個人に対してデータ安全とプライバシー義務を規定し、経済社会発展におけるデータの重要性、及びデータの改ざん、廃棄、漏洩、不正取得或いは使用が国家安全、公共利益或いは個人或いは組織の合法的権益に与える損害程度に基づいて、データ分類と階層保護制度を導入した。“データセキュリティ法”はまた、国家安全に影響を与える可能性のあるデータ活動に対して国家安全審査手続きを規定している。
“ネットワークセキュリティ審査方法”は2021年12月28日に中国民航総局など12の関係部門によって発表され、2022年2月15日から施行される。“ネットワークセキュリティ審査方法”は,(一)首席情報官がネットワーク製品とサービスを購入し,ネットワークプラットフォーム経営者のデータ処理活動に影響を与え,あるいは国家セキュリティに影響を与える可能性があるものは,ネットワークセキュリティ審査を行うべきである,(二)百万以上のユーザ個人情報を持つネットワークプラットフォーム経営者が大中国以外の国で上場しようとしている場合は,ネットワークセキュリティ審査事務室にネットワークセキュリティ審査を申請しなければならないと規定している
CACは2022年7月7日に“データ越境移転安全評価方法”を発表し、2022年9月1日から施行された。“データ越境移動安全評価方法”では、データ処理者は、(1)データ処理者が海外でキーデータを提供すること、(2)CIIOまたは100万人以上の個人情報を処理するデータ処理者が海外で個人情報を提供すること、(3)データ処理者が前年1月1日から海外で個人情報を計10万人または1万人の敏感な個人情報を提供すること、のうちの1つを申請すべきであると規定されている。(4)CACに規定されている他のクロスボードデータ伝送セキュリティ評価を申告する必要がある場合。
“中華人民共和国外商投資管理条例”
外商の中国への投資活動は、主に“外商投資産業指導目録”に従って実行される (“目録”)は、商務部、国家発改委が公表し、時々改訂する。商務部、発改委は2021年12月27日に2022年1月1日から施行された“外商投資参入特別管理措置(ネガティブリスト)(2021年)”を発表し、施行した。ネガティブリストはさらに産業制限と禁止産業の2つのサブカテゴリに分類される。ネガティブリスト以外の業界は一般的に外商独資企業の設立を許可する。ネガティブリストにおける制限業界については、一部の業界は株式または合弁企業に限定されており、場合によっては、中国のパートナーはこのような合弁企業の中で多数の株式を保有することを要求されている。外国人投資家は投資カテゴリーが禁止されている業界に投資してはいけない。“目録”に入っていない業界は一般的に外商投資に開放されており、中国の他の法規が明確に制限されていない限り。2021年1月27日に発効した“外商投資奨励産業目録(2020)”あるいは“2020年奨励産業目録”は、外商投資が禁止されている領域を除いて、外商投資細胞治療薬物の開発と生産を奨励することを規定している。
2019年3月15日、全人代は“中華人民共和国外商投資法”を可決した 2020年1月1日から施行される“外商投資法”は、中国の外商投資に関する3つの旧規則、すなわち“中華人民共和国合弁経営企業法”、“中華人民共和国合作経営企業法”、“外商独資企業法”、及びその実施細則と付属法規に代わっている。“外商投資法”は投資保護と公平競争の観点から、外国投資の参入、促進、保護と管理のために基本的な枠組みを確立した。外商投資法によれば、“外商投資”とは、外国の1つまたは複数の自然人、経営主体または他の組織(“外国投資家”と総称する)が中国国内で直接または間接的に行う投資活動を意味し、(一)外国投資家個人または他の投資家と中国国内に外国投資企業を設立すること、(2)外国投資家が中国国内で企業の株式、株式、資産またはその他の類似権益を取得すること、(三)外国投資家単独又は他の投資家と中国国内で新たな建設プロジェクトに投資する;(四)法律、行政法規、国務院が規定する他の投資方式。外商投資法は外商投資実体に中国国内実体と同じ待遇を与えるが、ネガティブリストでは“制限されている”または“禁止されている”とみなされている業界経営の外商投資実体は除外される。
2019年12月26日、国務院は“外商投資法実施細則”を公布し、2020年1月1日から施行した。実施細則はさらに明確にし、国家は外商投資を奨励し、促進し、外国投資家の合法的な権益を保護し、外商投資管理を規範化し、引き続き外商投資環境を最適化し、より高いレベルの開放を推進する。
2019年12月30日、商務部と商務部は共同で“外商投資情報申告方法”を発表し、2020年1月1日から施行した。“外商投資情報申告方法”によると、外国投資家が中国で投資活動を展開している場合は、ビジネス主管部門に投資情報を報告しなければならない。
M&A規則
商務部、国務院国資委員会、国家統計局、国家工商総局、中国証監会、国家外匯局は2006年8月8日に共同で発表し、2009年6月22日に商務部が改訂したM&A規則に基づいて、(一)非外商投資企業登録資本の株式または引受を購入すること、(2)外商投資企業が非外商投資企業の資産を購入·経営することを含む。(三)外国投資者が非外商投資企業の資産を購入することと、これらの資産を利用して外商投資企業を設立してこのような資産を経営することは、いずれもM&A規則を適用すべきである
特に国内会社、企業又は自然人が設立又は制御する海外会社の名義で中国国内の国内会社、企業又は自然人を買収する場合は、承認を申請しなければならない。
従業員株インセンティブ計画に関する規定
2012年2月15日、外為局は“株式オプション規則”を発表した。株式オプション規則及び関連規則及び規則に基づいて、中国に1年以上連続して住んでいる中国公民或いは非中国公民、例えば海外上場公衆会社の任意の株式激励計画に参与する場合、少数の例外状況を除いて、国内合資格代理人(この海外上場会社の中国付属会社であることができる)を通じて外匯局に登録し、そしていくつかの手続きを完成しなければならない。当社及びその従業員は、中国公民又は中国に1年以上連続して居住し、当社の株式激励計画に参加する場合、この規定に制約される。また、SATは従業員の株式オプションや制限株に関する通知を発表した。この等通告によると、中国で働いている従業員は、購入権或いはその制限的な株式帰属を行使すれば、中国個人所得税を支払う必要がある (“個人所得税”)。海外上場会社の中国子会社は、従業員の株式購入又は制限性株式に関する書類を関係税務機関に提出し、当該等の従業員がその株式オプション又は制限株式に関連する個人所得税を源泉徴収する義務がある。もし従業員が関連する法律、法規或いは法規に従って個人所得税を納付或いは源泉徴収していない場合、中国子会社は税務機関或いはその他の中国政府機関の処罰に直面する可能性がある。
外国為替管理に関する規定
1996年1月29日に国務院が公表した“中華人民共和国外貨管理条例”は、それぞれ1997年1月14日と2008年8月5日に改正され、中国外貨管理の主体条例である。“中華人民共和国外国為替管理条例”によると、経常項目の支払い、例えば利益分配と貿易及びサービスに関連する外国為替取引は、外貨支払いが可能であり、外国為替局の事前承認を必要とせず、特定の手続きの要求に符合する。対照的に、人民元を外貨に両替して中国から送金して外貨ローンの返済などの資本支出を支払う場合には、関係政府部門や指定銀行の承認や登録を受ける必要がある。
現行の規定によると、外商投資企業の資本金と外商投資企業が決済によって獲得した人民元資金は、企業の経営範囲を超えた金の支払いまたは関連法律法規で禁止されている金の支払いに直接または間接的に使用されてはならない。関連する法律法規が別途規定されていない限り、非関連者に融資を行うことができる場合、および/または非自己用不動産の購入に関連する費用を支払うことができるが、不動産企業を除く。
2017年に新規定を発表し、外国為替流入政策の制限を緩和し、貿易投資の利便化レベルをさらに向上させ、国境を越えた取引と国境を越えた資本流動の真実性と適合性審査を強化する。
2019年、外匯局は外匯局第28号通知を発表し、非投資性外商投資企業に対して資本金で国内株式投資を行う制限を撤廃した。非投資性外商投資企業が決済で取得した資本金で国内株式投資を行う場合、被投資先は規定に従って国内再投資登録手続きを行い、“資本口座--決済口座”を開設し、相応の資金を受け取るべきである。
安全通告37番
2014年7月、外管局はこれまでの“国家外国為替管理局第75号通知”に代わって“国家外貨管理局第37号通知”を発表した。外管局第37号通達は、中国個人と中国法人実体を含む中国住民に、その直接或いは間接的なオフショア投資活動について外管局或いはその現地支店に登録することを要求した。外管局第37号通達は、中国住民の株主のために適用され、将来可能な任意の海外買収に適用される可能性がある。
外管局第37号通書によると、外管局37号通達が実施される前に、オフショア特殊目的担体に対して直接または間接投資を行っている中国住民 (“特殊目的機関”)は、外国為替局またはその現地支店にそのような投資を登録しなければならない。また、特殊目的機関である直接又は間接株主であるいかなる中国人住民も、基本情報又は重大事件の任意の変化を反映するために、外国為替局現地支店に当該特殊目的機関に関する登録を更新しなければならない。当該特殊目的会社の中国住民株主が規定に従って登録又は更新登録を行っていない場合は、当該特殊目的会社が中国の子会社にその利益又は任意の分配を禁止することができる
SPVへの減資、持分譲渡または清算、およびSPVの中国子会社への追加出資も禁止されることができる。2015年2月、外管局は“外匯局第13号通知”を発表した。“外匯局第13号通知”によると、外商直接投資と対外直接投資の外国為替登録申請は、外国為替局第37号通知が要求した外国為替登録を含め、外国為替局ではなく条件に適合する銀行に提出しなければならない。条件を満たした銀行は外国為替局の監督の下で申請を審査して登録を受理しなければならない.
配当金分配に関する規則
外商投資企業の中国における配当分配を管理する主要な法律、規則と法規は、1993年に公布され、2018年最後に改正された“中華人民共和国会社法”と2020年1月1日に施行された“外商投資法とその実施条例”である。これらの要求に基づき、外商投資企業は中国の会計基準と法規に従って決定された累積利益(あれば)から配当金しか支払わない。中国の会社は毎年少なくともそれぞれの累計税引後利益の10%を一定の資本積立金とし、これらの積立金の総額が企業登録資本の50%に達するまで支出しなければならない。前のいくつかの会計年度のいかなる損失を相殺する前に、中国会社はいかなる利益も分配してはならない。前会計年度に留保された利益は、本会計年度の分配可能利益とともに分配することができる。
労働法と労働契約法
1994年7月5日に全人代常務委員会が公表し、2018年12月29日に最後に改正された“中華人民共和国労働法”と2007年6月29日に全人代常務委員会が公表し、2012年12月28日に改正された“中華人民共和国労働契約法”によると、使用者は常勤従業員と書面労働契約を締結しなければならない。すべての雇用主たちは地域の最低賃金基準を守らなければならない。使用者は全面的な管理制度を構築し、職業健康と安全管理制度を含む従業員の権利を保護し、従業員に職業訓練を提供し、職業傷害を防止し、そして使用者に潜在従業員の仕事説明、仕事条件、場所、職業危害と安全生産状況及び報酬などの条件を如実に通知することを要求しなければならない。“中華人民共和国労働契約法”と“中華人民共和国労働法”に違反し、もしストーリーが深刻であれば、罰金及びその他の行政と刑事責任を科すことができる。
社会保険と住宅積立金に関する規定
また、全国人民代表大会常務委員会が2010年10月28日に公表し、2018年12月29日に改正された“中華人民共和国社会保険法”、1999年1月22日に国務院が公表し、2019年3月24日に改正された“社会保障基金徴収暫定条例”、1999年4月3日に国務院が公表し、2002年3月24日と2019年3月24日にそれぞれ改正された“住宅積立金管理条例”によると、使用者は私たちの中国子会社のように、従業員に養老保険、失業保険、生育保険、労災保険、医療保険、住宅積立金などの福祉計画を提供しなければならない。これらの金は地方行政当局に支払われており,いずれの雇用主も納付していない場合は罰金を科され,所定の期限内に赤字額を支払うよう命じられている。
企業所得税に関する規定
2008年1月1日から施行され、2017年2月24日と2018年12月29日にそれぞれ改正された“中華人民共和国企業所得税法”によると、内資と外商投資企業の所得税率はいずれも25%であるが、一部の例外を除く。“中華人民共和国企業所得税法”の若干の規定を明確にするため、国務院は2007年12月6日に“企業所得税法実施細則”を公表し、2019年4月23日に改正施行した。“中華人民共和国企業所得税法”と“中華人民共和国企業所得税法実施細則”によると、企業は“住民企業”と“非住民企業”に分けられる。中国国内に設立された企業のほか、中国国外に設立された“実際の管理機関”が中国に設置された企業は“常駐企業”とみなされ、その全世界の所得税率は25%に統一されている。また、中国企業所得税法では、非住民企業とは外国の法律に基づいて設立された実体であり、その“事実上の管理機関”は中国国内にはないが、中国に機関や営業場所が設置されているか、あるいは中国に機関や営業場所が設立されていないが、その収入源は中国国内から来ていると規定されている。
“中華人民共和国企業所得税法実施細則”は、2008年1月1日から、非中国住民企業投資家に申告した配当金は、中国国内に機関又は営業地点が設立されていないか、又は中国国内に機関又は営業地点が設立されていないが、関連機関又は場所がある場合は、一般的に10%の所得税率が適用されると規定している
このような配当金が中国国内から来た場合、収入は業務成立や営業場所と有効な関連がない。中国と非中国株主のいる司法管轄区間の税収協定によると、配当金の所得税は減免することができる。
世界の他の地域の規制
米国や中国以外の他の国では,臨床試験,薬物許可,定価,精算の要求は国によって異なる。すべての場合,臨床試験はGCP要求と適用の法規制要件および“ヘルシンキ宣言”起源の倫理原則に従って行われなければならない。
民事責任の強制執行
本節で“民事責任強制執行”と題する“外国”とは,文意が別に説明されていない限り,中華人民共和国とケイマン諸島以外の国を指す
ケイマン諸島に登録されていますケイマン諸島免除会社としての利点を利用しています
•政治と経済の安定
•効果的な司法システム
•有利な税制
•外国為替規制や通貨制限はありません
•専門とサポートサービスを提供します
しかし、ケイマン諸島で会社を設立することにもいくつかの不利な点がある。これらの欠点は、これらに限定されるものではない
•ケイマン諸島の証券法システムは米国に比べてあまり発達しておらず、これらの証券法が投資家に提供する保護は米国よりもはるかに少ない
•ケイマン諸島の会社はアメリカ連邦裁判所で訴訟を起こす資格がないかもしれない。
私たちの構成文書には規定がありませんが、私たち、私たちの上級管理者、役員と株主の間の紛争は、アメリカ証券法による紛争を含めて、仲裁を行わなければなりません。
私たちの特定の資産と業務は中国に位置している。私たちの一部の取締役はアメリカ以外の管轄区の国民あるいは住民で、彼らの資産はアメリカ以外にあるかもしれません。したがって、株主は、米国内でこれらの人々に法的手続き文書を送達することが困難であるか、または米国または米国の任意の州証券法の民事責任条項による判決を含む、米国裁判所で取得された判決を我々または彼らに対して実行することが困難である可能性がある。
ケイマン諸島法律顧問Maplesとケイマン諸島法律顧問Calder(シンガポール)LLPと私たちの中国法律顧問Junhe LLPはそれぞれケイマン諸島と中国の裁判所が
•米国裁判所が米国または米国の任意の州証券法の民事責任条項に基づいて下した、われわれまたはわれわれの役員または上級管理者に対する判決を承認または執行すること;または
•米国または米国のいずれの州の証券法に基づいて各司法管区でわれわれまたはわれわれの役員または上級管理者に対して提起されたオリジナル訴訟を受理する。
証券法民事責任条項に基づいて米国裁判所から得られた判決がケイマン諸島裁判所によって懲罰的または懲罰的と判定されるかどうかについては、ケイマン諸島法律には不確実性がある。もしそのような判決が下されれば、ケイマン諸島裁判所はケイマン諸島会社に対する判決を認めたり実行しないだろう。ケイマン諸島の裁判所はこのような判決が懲罰的判決か懲罰的判決かについて判決を下していないため,これらの判決がケイマン諸島で実行可能かどうかは定かではない。Maples&Calder(シンガポール)LLPは、ケイマン諸島は米国連邦や州裁判所から得られた判決を強制的に執行していないが、このような司法管轄区で得られた対人判決は、新たにすることなく、通常法に基づいてケイマン諸島裁判所で認められ、実行されることを教えてくれた
ケイマン諸島大裁判所では、外国の債務判決が提起された訴訟について紛争の是非を審査し、このような判決を下した
•管轄権のある判決を下した管轄権のある外国裁判所によって与えられる
•債務者の判定には、具体的な積極的な義務(違約金を支払うこと、または特定の義務を履行する義務)を規定する
•最終的で決定的なものです
•税金、罰金、罰則とは関係がない
•何らかの方法で得られなかったし、自然正義やケイマン諸島公共政策に違反した強制執行でもない。
君と法律事務所はさらに、“中華人民共和国民事訴訟法”は外国判決の承認と執行を規定していることを教えてくれた。中国裁判所は“中華人民共和国民事訴訟法”の要求に基づいて、中国と判決所在国が締結した条約に基づいて、あるいは司法管轄区域間の対等原則に基づいて、外国判決を認め、執行することができる。中国と米国やケイマン諸島にはいかなる条約や他の形式の互恵関係もなく、相互承認と外国判決の執行を規定している。また、“中華人民共和国民事訴訟法”によると、中国の裁判所が外国判決が中国の法律の基本原則や国家主権、安全又は社会公共利益に違反していると判断した場合、私たち又は我々の役員及び上級管理者に対して外国判決を執行することはない。そのため、中国の裁判所が米国やケイマン諸島裁判所が下した判決をどのような根拠で執行しているかは定かではない。中国民事訴訟法によると、外国の株主は中国の法律に基づいて論争について中国の会社に訴訟を提起することができ、彼などが中国と十分な関係を構築できることを前提としており、中国の裁判所が司法管轄権を持ち、そして他の手続きの要求を満たすために、原告は事件と直接の利益がなければならないこと、及び具体的なクレーム、事実根拠と訴訟根拠がなければならないことを含む。しかし、外国株主は私たちのアメリカ預託証明書や普通株を持っているだけで、中国と十分な関係を築くことは難しい。
また、吾らがケイマン諸島の法律に基づいて登録成立したため、米国の株主は中国の法律に基づいて中国で吾などを提訴することは困難であるが、米国の株主は吾などを持つ米国の預託証明書や普通株だけでは中国との連絡を確立することは困難であり、中国の裁判所が中国の民事訴訟法の規定に基づいて司法管轄権を持つようになる。
施設
私たちの主な実行オフィスは現在ニュージャージー州サマーセット郡綿尾巷2101号に位置しています。郵便番号:08873ここで、伝説生物アメリカ会社は約32,039平方フィートのオフィス空間と53,332平方フィートの倉庫空間を含む約85,371平方フィートの施設を持っています。私たちはかなりの部分の倉庫空間のリフォームを完了し、GMP生産空間となり、私たちのパイプの開発と潜在的な商業化に使用されている。私たちは私たちの既存の施設が適切で十分で、私たちの現在の需要を満たすことができると信じている。もし私たちが従業員を増やしながら新しい施設を増やしたり、既存施設を拡大したりする必要があれば、私たちの業務のどのような拡張も収容するための適切な追加空間があると信じています
C.組織構造図
以下の図は、本年度報告日までの当社の構造を説明し、親会社、子会社、合併の付属実体を含む
D.財産·工場·設備
主な執行事務室
私たちの主な実行オフィスは現在ニュージャージー州サマーセット郡綿尾巷2101号に位置しています。郵便番号:08873ここで、伝説生物アメリカ会社は約32,039平方フィートのオフィス空間と53,332平方フィートの倉庫空間を含む約85,371平方フィートの施設を持っています。我々は最近,かなりの倉庫空間をGMP製造空間に改修する作業を完了した。私たちは私たちの既存の施設が適切で十分で、私たちの現在の需要を満たすことができると信じている。もし私たちが従業員を増やしながら新しい施設を増やしたり、既存施設を拡大したりする必要があれば、私たちの業務のどのような拡張も収容するための適切な追加空間があると信じています。
より多くのアメリカの施設は
私たちはアメリカで以下の追加施設をレンタルまたは予想しています
•私たちの研究機関はニュージャージー州ピスカットウェイ騎士橋路10号にあります郵便番号08854 Genscriptの子会社から約22,000平方フィートをレンタルしました
•私たちはJanssenと賃貸契約を締結し、このレンタルによると、Janssenからニュージャージー州ラリタンにある約106,000平方フィートのGMP製造工場をレンタルする予定です。この賃貸契約は、私たちがヤンソン協力と許可協定に従って施設を引き継ぐ未来の日に施行されるだろう。CARVYKTIはこの工場で生産されています
EU.EU
私たちはEUで以下の施設をレンタルまたは予想しています
•Janssenは現在ベルギーのゲントで2つの工場を借りており、この2つの工場は主にGMP生産に使用される。これらの施設はそれぞれ約180,900平方フィートと30,000平方フィートで建設中である。私たちはJanssenの協力と許可協定に基づいてこのような施設を接収したので、これらの施設は私たちにレンタルされ、将来の日付から発効することが予想される。完成すれば、私たちはこれらの施設をCARVYKTIを製造するために使用する予定だ。
•私たちはベルギー根特有の行政事務施設で、約4500フィートをレンタルします。
•私たちはアイルランドダブリンに研究と行政施設を持っていて、私たちはそこで約8300平方フィートを借りた。
中華人民共和国
南京では、江蘇省南京市江寧高新区月華路以北、前徳路以西に約5万平方メートルの建物を持ち、現在GMP製造工場を建設している。また、中国では、オフィススペース、倉庫、実験室作業、GMP製造のためのいくつかの施設をレンタルしています
| | | | | | | | | | | |
| 住所.住所 | 賃貸期限が切れる | リース面積 | 所用の使用 |
1ST, 2発送する, 3研究開発と4これは…。南京市江寧区龍綿大道568号南京生命科学城6号棟 | 2026年12月31日 | 3592平方メートル | オフィスとGMP製造 |
3研究開発, 4これは…。と5これは…。南京生命科学城3号棟 | 2023年5月30日 | 2,038平方メートル | オフィスと実験室 |
4これは…。南京市江寧区京郵路33号産学研総合ビルA座 | 2024年7月23日 | 2940.67平方メートル | オフィス |
4これは…。南京市江寧区京郵路33号産学研総合棟E座 | 2025年12月31日 | 7250平方メートル | 実験室 |
1ST南京市江寧区永渓路28号5号棟* | 2025年6月30日 | 1000平方メートル | オフィスと実験室 |
1STそして3研究開発南京市江寧区京郵路33号産学研総合ビルB座 | 1STフロア:2024年8月25日;3研究開発フロア:2024年9月14日 | 1279.8平方メートル | 貨物倉庫 |
| 南京市江寧区京郵路33号産学研総合棟B座3階 | 2024年9月14日 | 1334.28平方メートル | 研究室とオフィス |
プロジェクト4 Aです。未解決従業員意見
適用されない
プロジェクト5.ビジネスと財務審査と展望
以下の財務状況と経営結果の検討と分析、および私たちの総合財務諸表と本年度報告書の他の部分に関する付記を読むべきです。この議論は、特に、本年度報告における“展望的陳述に関する警告声明”のタイトルに記載されているように、特に、我々の将来の経営結果または財務状況、業務戦略、および将来の経営の計画および管理目標に関する情報、特にリスクおよび不確定要因に関する前向きな陳述を含む。私たちの業務を評価する際には、私たちの実際の結果が展望性陳述で予測された結果と大きく異なる重要な要素をもたらす可能性があることを議論するために、“第3.D.項目のリスク要因”で提供される情報も慎重に考慮しなければならない。
概要
われわれは主に世界的な臨床段階生物製薬会社であり,腫瘍学や他の適応の新しい細胞療法の発見,開発,製造,商業化に取り組んでいる。私たちはアメリカ、中国、ヨーロッパに約1,390人の従業員がいて、私たちは差別化された技術、世界の開発と製造戦略と専門知識が私たちに次世代電池を生産、テスト、製造する能力を提供してくれました
高度な需要を満たしていない適応に対する治療。著者らの主要な候補製品ciltalagene autolucelあるいはcilta-cel(我々のLegend-2試験ではlcar-B 38 Mと呼ばれる)は、著者らが戦略パートナーのJanssenと共同開発したキメラ抗原受容体T細胞(“CAR-T”)療法であり、MMの治療に用いられている。これまでに得られた臨床試験の結果、cilta-celは安全性制御可能な状況下で再発と難治性多発性骨髄腫(“RRMM”)患者に対して深刻で持続的な抗腫瘍応答の潜在力を有することが明らかになった。
著者らの主要な候補製品ciltalabagene autolucel或いはcilta-celは著者らが戦略パートナーJanssen Biotech,Inc.(“Janssen”)と共同開発したCAR-T細胞療法であり、多発性骨髄腫(MM)の治療に用いられる。今までに得られた臨床試験結果により、Cilta-celは再発性或いは難治性多発性骨髄腫(“RRMM”)患者に深度と持続性の抗腫瘍反応を提供し、しかも安全性制御可能であることが示唆された。2022年2月28日、米国食品医薬品局(FDA)は、プロテアソーム阻害剤、免疫調節剤、および抗CD 38モノクロナル抗体を含む、プロテアソーム阻害剤、免疫調節剤、および抗CD 38モノクロナル抗体を含む、4つ以上の治療レジメンを経験した成人RRMMの治療のための我々の製品CARVYKTI(cilta-cel)を承認した。CARVYKTIは私たちが最初に衛生当局の許可を得た製品だ。
設立以来、私たちは重大な運営損失が発生した。2022年と2021年12月31日までの年度の純損失はそれぞれ446.3ドルと4.036億ドルだった。2022年12月31日まで、私たちは累計966.5ドルの損失を出しました。私たちは予測可能な未来に巨額の費用と運営損失が続くと予想している。私たちは持続的な活動に関連する費用が大幅に増加すると予想しています
•RRMMを治療するためのRRMM治療の研究と開発を継続して行っている
•アメリカ、ヨーロッパ、中国のインフラへの投資を含む私たちの製造能力に投資し続けています
•私たちが行っている他の候補製品の臨床開発を続けています
•私たちが行っている研究と開発活動を続けています
•より多くの候補製品の発見と開発を求め、私たちの臨床製品ラインをさらに拡大した
•臨床試験に成功した候補製品のために規制またはマーケティング承認を求める
•私たちの臨床試験と潜在的な商業化の能力需要を満たすのに十分な数があることを確実にするために、内部と外部製造能力を拡大し続ける
•販売、マーケティング、流通インフラを構築し、規制またはマーケティングの承認を得る可能性のある任意の候補製品を商業化する
•私たちの知的財産権の組み合わせを開発し、維持し、拡大し、保護する
•他の候補製品や技術を買収したり許可したり
•より多くの臨床、品質管理、製造者を招聘する
•私たちの製品開発および計画の将来の商業化努力を支援する人員を含む、臨床、運営、財務、および管理情報システムおよび人員を増加させる
•私たちの世界でのビジネスを拡大し
•追加の法律、会計、投資家関係、その他の上場企業の運営に関する費用が発生する。
私たちはJanssenと協力して
2017年12月、私たちはヤンソンと協力·許可協定(“ヤンソン協定”)に署名し、世界的にcilta-celを開発し、商業化した。
ヤンソン協定によると、私たちはヤンソンに世界独自のcilta-celの共同開発と商業化のライセンスを付与した。我々と楊森は全世界発展計画と全世界商業化計画に基づいて、全世界範囲で協力して多発性骨髄腫を治療するシルゼルを開発と商業化する。
楊森は世界規模ですべての臨床試験を行うことを担当し、私たちのアメリカのチームと大中国のチームが参加します。私たちは規制活動を担当し、定価の承認と予約販売を受ける大中国、ヤンソンは監督活動を担当する
定価の承認を得て、世界の他の地域のために販売を予約します。私たちとヤンソンは世界のすべての国で開発、生産と商業化コストおよび税前損益を均等に分担するが、大中国を除いて、私たちとヤンソンのコスト分担と損益分担はそれぞれ私たちの70%とヤンソンの30%になるだろう。
Janssenに許可された許可証と他の権利を考慮して、Janssenは私たちに前金とマイルストーン支払いを支払って、私たちはまだ追加のマイルストーン支払いを受ける資格があるJanssenがJanssenの協力と許可協定に従って私たちに支払った前金とマイルストーン支払い、およびJanssenがこの合意に従って私たちに支払う可能性のある将来のマイルストーン支払いの説明については、“項目4.会社に関する情報−B−ビジネス概要−Janssen Biotech,Inc.との協力とライセンス契約.”
また、私たちの協力が最初の利益年度を経験する前に、どの年も協力する予定の運営資金が5,000万ドル以下であれば、私たちはJanssenから前金を得る権利がある。この場合、Janssenが私たちに提供してくれた前払い金額は、協力年度の運営資本が5000万ドルを超えることに相当する。いかなる例年の前金総額も1.25億ドルを超えてはならず、いつでも未払いの前払い総額は2.5億ドルを超えてはならない。未償還前払金は“ウォール·ストリート·ジャーナル”が発表したロンドン銀行間同業借り換え金利(LIBOR)に2.5%を加算した。Janssenは、私たちが協力した税引前利益から配当された前金と利息から回収する権利があり、いくつかの制限を受けた場合、Janssen協定に従って私たちに支払われなければならない記念碑的支払いから回収する権利がある。当社の統制権の変更やJanssenが私たちの深刻な合意違反のためにJanssen協定を終了しない限り、前金や利息を返済する義務はありません。私たちはいつでも自発的にその時返済されていない前払いまたは関連する利息の任意の部分を自ら決定することができます。2022年12月31日現在、同等立て替え金と利息の未返済元金総額はそれぞれ約250.0ドルと1,090万ドルである。LIBORの金融サービス業での使用停止に伴い、新たな金利計算方法を採用するためにJanssenプロトコルを改正することをJanssenと検討し始めている。
世界経済状況
世界の経済状況は依然として不確定であり、私たちは引き続き新冠肺炎の疫病、露烏戦争、金融機関の倒産と不安定、上昇するインフレ率に関連する影響を含むマクロ経済状況の影響を監視し続けている。
経済状況の変化、サプライチェーン制限、物流挑戦、労働力不足、ロシア-ウクライナ戦争、および各国政府と中央銀行が取った措置、特に新冠肺炎の流行に対応するための措置は、より高いインフレを招き、これはコスト上昇を招き、金利上昇を含む財政と通貨政策の変化を招く。 アメリカと中国の製品製造は続いています。現在、私たちは私たちの材料サプライチェーンへの実質的な影響を経験しておらず、インフレと金利上昇の影響も受けていない。適切な安全対策として、より多くの特定の原材料と消耗品が貯蔵されている。私たちはすべての必要な材料のための強力な調達戦略を制定しており、大きな影響はないと信じています。
また,中国では,2022年12月31日までの1年間に新冠肺炎の中断を経験しているが,我々の業務に実質的な影響を与えないと考えられる。 新冠肺炎の未来の著者らの業務に対する影響、経営結果と財務状況は依然として不確定性が存在し、影響の程度は多くの絶えず変化する要素に依存し、しかしこれらに限定されない:新冠肺炎の規模と持続時間、新冠肺炎ワクチンとその他の医療サービス流通の発展と進度、期待した回復速度、及び政府と企業の疫病に対する反応。状況が大幅に悪化すれば、我々の業務、経営業績、財務状況は重大かつ不利な影響を受ける可能性がある。私たちは疫病の持続的な発展が私たちの財務状況と経営業績に与える影響を引き続き監視し、評価し、相応の反応を行う
経済状況のこれらの変化が継続している場合、またはそれらの深刻性が増加すれば、短期的にはさらなる経済不確実性や資本市場の変動を招き、私たちの運営に負の影響を与える可能性がある。これらのマクロ経済状況がこれまで私たちの財務状況や運営結果に実質的な影響を与えてきたとは考えられないが、近い将来、労働力コストや研究開発コストを含む運営コストが影響を受ける可能性があり(特にインフレ率が上昇し続ける場合)、サプライチェーン制限、新冠肺炎とロシアとウクライナとの持続的な衝突に関する結果、従業員の可用性および賃金上昇が含まれており、これは私たちの運営資金資源が追加的な圧力に直面する可能性がある
私たちの運営結果の構成要素は
収入.収入
今まで、私たちの収入には主にヤンソン協定によって受け取った前金とマイルストーン支払いによって生じた許可収入が含まれています。2022年、Janssenとの提携は、CARVYKTIの製品販売からコラボレーション収入を生成し始めます。私たちが製品の収入と利益を創出する能力は、私たちが開発に成功し、規制の承認を得て、Cilta-celと私たちの他の候補製品を商業化する能力にかかっている。
運営費
研究と開発費
研究と開発費用には、主に私たちの研究活動に関するコストが含まれています
•給与、福祉、株式ベースの給与費用を含む人員費用;
•第三者が行った研究費を援助し
•臨床前研究および臨床試験材料を設計、開発および製造するための実験室用品および非資本設備の購入費用;
•顧問料
•規制活動に関連する費用には、規制機関に支払う届出費用が含まれている
•賃貸料、減価償却および修理費用を含む施設コスト;
•私たちの第三者許可協定に基づいて許可を維持する費用。
研究·開発コストは発生時に費用を計上する。製造、臨床前研究および臨床試験のようないくつかの活動のコストは、通常、特定の任務を達成する進捗の評価に基づいて、私たちのサプライヤーおよび協力者が提供してくれた情報およびデータを使用して確認される。
私たちは一般的に開発計画全体で従業員、コンサルタント、そしてインフラ資源を使用する。我々は、これらのコストを私たちのB細胞成熟抗原(BCMA)計画またはすべての他の非BCMA計画に分配することによって、アウトソーシング開発コストを追跡するが、私たちは、特定の候補製品または臨床前計画に人員コスト、他の内部コスト、または外部コンサルタントコストを割り当てることはない。2022年と2021年12月31日までの年間で,我々の総研究開発費はそれぞれ210.9ドルと204.4ドルであり,我々のBCMA計画,および他のすべての非BCMA計画のための総研究開発費はそれぞれ124.7ドルと108.9ドルであった
2022年12月31日から2022年12月31日まで、我々の候補製品や臨床前計画の開発を研究·推進するために、約11億ドルの研究開発費が発生している。予測可能な未来には、私たちの臨床前計画と候補製品の推進を求めるにつれて、私たちの研究開発費が増加すると予想される。現在、私たちは、私たちの候補製品開発を完成させるために必要な努力の性質、時間、および見積もりコストを合理的に推定または知ることができない。私たちもいつ(あれば)私たちの候補製品の販売から大量の現金純流入が始まるか予測できません。これは、このような候補製品の開発に関連する多くのリスクおよび不確実性に起因しており、以下のような不確実性を含む
•臨床試験の登録に成功しました
•適切なセキュリティプロファイルを構築すること
•商業製造能力を確立するか、または第三者製造業者との手配を行う
•関連規制部門の上場承認を受けた
•承認されれば、単独でも他の会社とも協力して候補製品を商業化する
•私たちの候補製品のために特許と商業秘密保護および規制排他性を獲得し、維持する
•承認後の製品の持続的に許容可能なセキュリティプロファイル;および
•重要な研究開発者を引き留める。
我々の任意の候補製品の開発に関連するこれらの変数のいずれかの結果の変化は、候補製品の開発に関連するコスト、タイミング、および生存能力を著しく変化させるであろう。
行政費
行政費用には、主に、給与、福祉、株式ベースの給与費用を含む行政、財務、会計、業務発展、情報技術、法律、人的資源機能者の費用が含まれる。行政費用には、研究開発費に含まれていない会社の施設コスト、知的財産権や会社事務に関する法律費用、会計やコンサルティングサービス費用も含まれています。
将来的には、RRMMの治療を行っているシルタイの研究および開発、および他の候補製品の臨床前および臨床試験の開始および継続を含む、持続的な研究および開発活動を支援するための管理費用が増加することが予想される。私たちが初めて公募した後、私たちの会計、監査、法律、規制、投資家と広報、コンプライアンス、役員と高級社員保険のコストが増加し、私たちが上場企業のインフラを強化し続けるにつれて、これらのコストは引き続き増加すると予想されます。
販売と流通費用
販売および流通費用には、主に私たちのビジネス活動に関連するコストが含まれ、株式給与、出張費用、求人費用、スポンサー料、およびCiltacelマーケティングおよび開発に関連する外部機関に支払われる相談料を含む従業員の給料および関連コストが含まれています。
他の収入と収益
その他の収入と収益には、財務収入、公正価値損益によって変動する金融資産の公正価値収益、政府贈与、外国為替収益、賃貸料収入が含まれる。
収入確認
前払い費用
ヤンソン協定では、前払いは単一の履行義務に割り当てられている。楊森が支払った350.0ドルの前払い費用は、2017年の契約開始時に取引価格に含まれ、2018年に知的財産権(技術移転サービスを含む)の履行義務が完了したときに確認される。2018年、私たちは全額350.0ドルの前払い費用を受け取りました
一里塚払い
マイルストーン支払いは可変対価格形式を表し、取引価格に計上される範囲は、可変対価格に関する不確実性がその後解決された場合、確認された累計収入が大きく逆転しない可能性が高い。マイルストーン支払いを含む各スケジュールの開始時に、マイルストーンが実現される可能性が高いと考えられるかどうかを評価し、可能な金額法を用いて取引価格に含まれる金額を推定する。累積収入が大きく逆転しない可能性が高い場合、関連するマイルストーン価値は取引価格に含まれる。規制承認など,我々の制御範囲内ではない記念碑的支払いは,これらの承認を受けるまで実現されない可能性が高い.私たちはこの評価における特定のマイルストーンを実現するために、科学、臨床、監督管理、商業と他の克服しなければならないリスクなどの要素を評価した。累積収入が大きく逆転しない可能性が高いかどうかを決定する際には,かなりの判断が必要である。その後の各報告期間が終了すると、すべての制限されたマイルストーンの実現確率を再評価し、必要に応じて全体の取引価格の推定値を調整する
いくつかの記念碑的支払いは、技術移転サービスを含む知的財産権許可を交付するために、ヤンソン協定内の単一履行義務に割り当てられる。我々は2018年に初期取引価格に含まれるマイルストーン許可収入5000万ドル、すなわち義務履行の年を確認しました
そのため、国際財務報告基準第15号契約で確認された累積収入は大きな逆転が生じない可能性が高い。5000万ドルのマイルストーン費用は2019年に私たちによって全額受け取りました。
また、指定された製造マイルストーンを実現するための1.25億ドルまでのマイルストーン支払いを取得する資格があり、指定された将来の開発と規制マイルストーンの実現に4.35億ドル、指定された貿易純売上のマイルストーンを実現するための2.1億ドルを追加する資格がある。その後の開発、製造、規制マイルストーンは、2018年に満たされた知的財産権ライセンス(技術移転サービスを含む)の履行義務に関連しているため、IFRS 15契約によって確認された累積収入が大きな逆転が生じない可能性が高い期間に十分に確認される。印税確認制限によりマイルストーンが実現された場合、販売のマイルストーンに基づく収入を確認します。私たちは残りのマイルストーンの達成が大きな不確実性を持っており、関連するマイルストーン支払いは取引価格に含まれていないと評価した。
JanssenがJanssen協定に基づいて私たちに支払った前金とマイルストーン支払いおよび将来可能なマイルストーン支払いに関する説明J本協定によれば、アンソンは私たちに情報を提供する可能性がありますので、“項目4.会社に関する情報-B.業務概要-ヤンソンバイオテクノロジー会社との協力および許可協定”を参照してください
知的財産権許可証
ライセンスが他の承諾と異なるかどうかを評価する際には,連携パートナーの研究,開発,製造,商業化能力,一般市場での専門知識の可用性などを考慮する。さらに、私たちは、ライセンスの価値が未履行のコミットメントに依存するかどうか、他のプロバイダが残りのコミットメントを提供することができるかどうか、および残りのコミットメントから分離して識別できるかどうかを考慮することによって、取引相手が残りのコミットメントを受けることなく許可から利益を得ることができるかどうかを考慮する。私たちは、約束が一定期間内に行われるか、またはある時点で履行されるかを決定するために、ライセンスを付与する約束の性質を評価する。我々は、許可が付与された時点で存在する我々の許可を使用する権利を表す技術移転サービスを含む“ヤンソン協定”における単一の履行義務であることを評価する。ライセンス収入は、ライセンス使用権制御権がお客様に譲渡されたときに確認されます。
収入の協力コスト
協調収入コストは,我々が発生したコストと我々が比例して分担した協調収入コストを含むCARVYKTIの販売に関連している.収入の協働コストには、販売在庫コスト、製造コスト、生産に起因することができる他のコスト、および超過および古い在庫、または品質規格に適合しない在庫のような在庫の削減が含まれる。
研究開発コスト
すべての研究費は発生時に損益表とその他の包括収益を計上した。
使用または販売可能にするために無形資産を完成させる技術的可能性、資産を完成させる意図、および資産を使用または販売する能力、資産が将来の経済効果をどのようにもたらすか、プロジェクトを達成する資源の利用可能性、および開発中に支出を確実に測定する能力を証明することができる場合にのみ、新製品候補製品を開発するためのプロジェクトに発生する支出が資本化および繰延される。これらの基準を満たしていない候補製品開発支出は発生時に計上される
株式ベースの報酬
当社は株式購入計画及び制限性株式単位(“RSU”)計画を推進し、当社の運営成功に貢献した合資格参加者に奨励及び奨励を提供することを目的としている。私たちの従業員と取締役は株式支払いの形で報酬を得ることができ、従業員は株式決済ツールまたは株式決済取引の対価格としてサービスを提供することができる
従業員と株式決済取引を行うコストは、付与された日の公正価値によって計量される。株式オプションの公正価値は二項モデルで決定され,各RSUの公正価値は
吾らの株式に基づいて授出日に関する市価を決定する。詳細は本年度報告総合財務諸表付記27および付記28を参照されたい
株式決済取引のコストは、相応の権益が増加するとともに、従業員福祉支出において業績及び/又はサービス条件を満たす期間に確認する。帰属日までの各報告期間終了時に確認された権益決済取引累積支出は、帰属期間が満了した程度を反映し、最終的に帰属する権益ツール数の最適な推定値を吾等に反映する。ある期間損益表に計上された費用または貸方は,その期間中と期末に確認された累積費用の変動を表す
付与日を決定する際には,サービスや業績条件は考慮されないが,条件を満たす可能性は,最終的に付与される株式ツール数の最適な推定の一部として評価する
私たちは、付与日の公正価値に基づいて、従業員および取締役に付与された株式オプションおよび他の株式ベースの奨励を測定し、その奨励が必要なサービス期間(通常は対応する奨励の帰属期間)内に推定没収された相応の補償支出を差し引くことを確認する。一般的に、業績帰属条件を含む株式オプションを発行し、参加者が取締役会が設定したいくつかの業績目標を達成できない場合は没収されます
パフォーマンスおよび/またはサービス条件を満たしていないため最終的に付与されていない報酬については、いかなる費用も確認されません
A.経営実績
2022年12月31日までと2021年12月31日までの財政年度比較
次の表は、2022年12月31日と2021年12月31日までの財政年度の運営結果をまとめたものである
| | | | | | | | | | | | | | | | | |
| 財政年度が終わる 十二月三十一日 | | 分散.分散 |
| 2022 | | 2021 | |
| (単位:千) |
| 総合運営レポートデータ: | | | | | |
| 収入.収入 | | | | | |
| 許可証収入 | 50,000 | | | 65,402 | | | (15,402) | |
| 協力収入 | 66,677 | | | — | | | 66,677 | |
| その他の収入 | 328 | | | 3,424 | | | (3,096) | |
| 総収入 | 117,005 | | | 68,826 | | | 48,179 | |
| 運営費用: | | | | | |
| 収入の協力コスト | (65,363) | | | — | | | (65,363) | |
| 研究開発費 | (335,648) | | | (313,346) | | | (22,302) | |
| 行政費 | (80,631) | | | (46,961) | | | (33,670) | |
| 販売と流通費用 | (93,417) | | | (102,542) | | | 9,125 | |
| 他の収入と収益 | 12,049 | | | 3,059 | | | 8,990 | |
| その他の費用 | (9,823) | | | (9,132) | | | (691) | |
| 株式証負債の公正価値損益を認める | 20,900 | | | (6,200) | | | 27,100 | |
| 融資コスト | (10,796) | | | (900) | | | (9,896) | |
| 税引き前損失 | (445,724) | | | (407,196) | | | (38,528) | |
| 所得税(費用)/控除 | (625) | | | 3,614 | | | (4,239) | |
| 本年度の赤字 | (446,349) | | | (403,582) | | | (42,767) | |
収入.収入
許可証収入
2022年12月31日までの1年間のライセンス収入は5,000万ドルですが、2021年12月31日までの1年間、ライセンス収入は6,540万ドルです。この1,540万ドル削減の要因は,2022年12月31日までの1年間に,“ヤンソン協定”に基づき,世界開発計画が実現したマイルストーンの性質とスケジュールを概説したためである。
協力収入
2022年12月31日までの年度連携収入は6670万ドルであったが,2021年12月31日までの年度はゼロであった。6670万ドル増加しましたヤンソン協定に関連したCARVYKTIの米国でのビジネス開始によるものである。
その他の収入
その他の収入は2022年12月31日現在で30万ドルであるが、2021年12月31日現在の事業年度は340万ドルである。この310万ドルの減少は、2022年に発生した許可と特許使用料収入の減少によるものであり、2022年12月31日までの年度内に南京ProBio生物技術有限会社及びその付属会社にある特許を許可することに関連している
運営費
収入の協力コスト
2022年12月31日までの年度の連携収入コストは6540万ドルであるが,2021年12月31日までの年度はゼロである。この6,540万ドルの増加は、主に米国でヤンソン協定の一部としてCARVYKTIを発売したことによる販売コストのシェアによるものである
研究と開発費
2022年12月31日までの年間研究開発支出は3兆356億ドルだったが、2021年12月31日までの年間研究開発支出は3億133億ドルだった。この2,230万ドル増加の要因は,2022年12月31日までの1年間に,2つの研究新薬(IND)申請を提出し,米国の第1段階臨床開発に準備を開始したため,早期治療系のCilta−celの研究と開発活動および我々のパイプライン支出が増加したためである。
行政費
2022年12月31日までの年度の行政費用は8060万ドルであるのに対し,2021年12月31日までの年度の行政費用は4700万ドルである。この3360万ドルの増加は、事業拡張を促進するために補助行政機能を拡大したためだ。この成長は,主に情報技術インフラとキングスレー生物科学技術分離の最終段階(“遺伝子スクリプト”や“遺伝子スクリプト”)を実施し,ネットワークセキュリティやプライバシーの強化,候補製品の製造施設を支援するために必要なITインフラを構築する必要があるためである
販売と流通費用
2022年12月31日までの年間販売·流通費は9340万ドルだったが、2021年12月31日までの年度は1.025億ドルだった。910万ドル減少した理由は商業活動に関連した費用の減少だ
他の収入と収益
2022年12月31日までの年間その他の収入·収益は1200万ドルであるのに対し、2021年12月31日までの年度は310万ドルである。この890万ドルの増加は、主に2022年12月31日までの年間利息収入、政府贈与、公正価値に基づいて損益を計上した金融資産の公正価値収益の増加によるものである。
その他の費用
2022年12月31日現在の年度別支出は980万ドルであるのに対し,2021年12月31日現在の年度別支出は910万ドルである。70万ドル増加したのは主に為替損失によるものだ
融資コスト
2022年12月31日までの年間財務コストは1080万ドルであるが、2021年12月31日までの年間財務コストは90万ドルである。9,900万ドルの増加は主に前借り資金の利息によるものであり、前借り資金はJanssenがJanssen協定に基づいて資金を提供し、元金と適用利息からなる利息借款である。ヤンソン協定の条項によると、2022年12月31日まで、私たちは増額130.3ドルを選択した
株式証負債の公正価値損益を認める
2022年12月31日までの年度の権証負債公正価値収益は2,090万ドルであり,2021年5月に私募取引により機関投資家に発行された権証の公正価値が変化し,発行日の初期公正価値が8,170万ドルであったためである。また、普通株は私募取引で同一機関投資家に売却される。この権利証は金融負債として評価され、2022年12月31日現在の公正価値は6700万ドルである。
所得税(費用)/控除
2022年12月31日までの年間所得税支出は60万ドルだが、2021年12月31日までの年間所得税控除は360万ドル。
2021年12月31日までと2020年12月31日までの財政年度比較
次の表は、2021年12月31日と2020年12月31日までの財政年度の運営結果をまとめたものである
| | | | | | | | | | | | | | | | | |
| 財政年度が終わる 十二月三十一日 | | 分散.分散 |
| 2021 | | 2020 | |
| (単位:千) |
| 総合運営レポートデータ: | | | | | |
| 総収入 | 68,826 | | | 75,000 | | | (6,174) | |
| 運営費用: | | | | | |
| 研究開発費 | (313,346) | | | (232,160) | | | (81,186) | |
| 行政費 | (46,961) | | | (23,134) | | | (23,827) | |
| 販売と流通費用 | (102,542) | | | (49,571) | | | (52,971) | |
| 他の収入と収益 | 3,059 | | | 6,119 | | | (3,060) | |
| その他の費用 | (9,132) | | | (346) | | | (8,786) | |
| 株式証負債の公正価値損失を認める | (6,200) | | | — | | | (6,200) | |
| 転換可能優先株の公正価値損失 | — | | | (79,984) | | | 79,984 | |
| 融資コスト | (900) | | | (4,209) | | | 3,309 | |
| 当期損失 | (407,196) | | | (308,285) | | | (98,911) | |
| 所得税控除 | 3,614 | | | 41,912 | | | (38,298) | |
| 本年度の赤字 | (403,582) | | | (266,373) | | | (137,209) | |
収入.収入
2021年12月31日現在の年度収入は6880万ドルであるのに対し、2020年12月31日現在の年度収入は7500万ドルである。この620万ドル削減の要因は、2021年12月31日までの1年間に、“ヤンソン協定”下のグローバル開発計画で概説されたマイルストーンの性質と実現時期により、マイルストーン確認の収入が減少したためである。2021年12月31日現在、CARVYKTIの製品販売から何の収入も得ていません
運営費
研究と開発費
2021年12月31日までの年間研究開発支出は3億133億ドルだったが、2020年12月31日までの年間研究開発支出は2兆322億ドルだった。この8,110万ドルの増加は,主に早期治療シリーズにおけるcilta−cel研究と開発活動と,2021年12月31日までの1年間の非BCMA研究·開発活動への持続的な投資によるものである。
行政費
2021年12月31日までの年度の行政費用は4700万ドルであるのに対し,2020年12月31日までの年度の行政費用は2310万ドルである。この2,390万ドルの増加は、主に、GenScripから離脱し続けているため、持続的な業務拡張と内部能力構築を促進するために行政支援機能を拡張したためである
販売と流通費用
2021年12月31日現在の年間販売·流通費は1.025億ドルであるのに対し、2020年12月31日現在の年度は4960万ドルである。5,290万ドル増加した要因は、米国でCilta-celを発売したビジネス準備活動に関するコスト増加である
他の収入と収益
2021年12月31日までの年間その他の収入·収益は310万ドルであるのに対し、2020年12月31日までの年度は610万ドルである。300万元の減少は、主に平均金利の低い定期預金の利息収入の減少と、政府助成金の減少によるものだ。
その他の費用
2021年12月31日までの年度別支出は910万ドルであるのに対し,2020年12月31日までの年度別支出は30万ドルである。880万ドル増加した主な原因は為替損失と資産処分損失だ。
融資コスト
2021年12月31日までの年度の財務コストは90万ドルで、主に前借り資金の利息が含まれており、前借り資金はJanssenがJanssen協定に基づいて資金を提供する利息借款であり、元金と当該元金の適用利息からなる。2020年12月31日までの年度の財務コストが420万ドルであるのは、転換可能な償還可能優先株(“Aシリーズ優先株”)を発行する融資コストが、2020年6月に初公開を終えて普通株に転換したためである。
株式証責任の公正価値損失を認める
2021年12月31日までの年間で、株式証負債の公正価値損失が620万ドルであったのは、2021年5月に私募取引により機関投資家に発行された権利証の公正価値が変化し、この権利証の発行日における初期公正価値が8170万ドルであったためである。また、普通株は私募取引で同一機関投資家に売却される。権利証は金融負債と評価され、2021年12月31日現在の公正価値は8790万ドル。
転換可能優先株の公正価値損失
2020年12月31日までに,Aシリーズ優先株公正価値変動による一次非現金費用8,000万ドルを報告した。2020年6月に米国での初公開発売を完了した後、発行されたAシリーズ優先株をすべて当社の普通株に変換し、すべて計上すべきですが支払われていない配当は当社の普通株として決済されます。 上場後、著者らはAシリーズのすでに発行された優先株がないため、2021年にこのような公正価値損失はなかった。
所得税控除
所得税控除は2021年12月31日までの年間360万ドルですが、2020年12月31日までの年間所得税控除は4190万ドルです。
肝心な会計政策
我々の総合財務諸表は、国際会計基準委員会が発表した国際財務報告基準(“IFRS”)に基づいて作成された。私たちの連結財務諸表を作成する際には、資産、負債、コスト、費用報告金額に影響を与える推定、仮説、判断を行う必要があります。私たちの推定と仮定は歴史的経験と他の私たちが当時の状況で合理的な要素だと考えている。私たちは持続的な基礎の上で私たちの推定と仮定を評価する。私たちの実際の結果はこのような推定とは違うかもしれない。私たちの最も重要な会計政策は次のようにまとめられる。我々の他の重要な会計政策の説明については、本年度報告書に含まれる総合財務諸表付記2.4を参照されたい。
収入確認
前払い費用
ヤンソン協定では、前払いは単一の履行義務に割り当てられている。楊森が支払った350.0ドルの前払い費用は、2017年の契約開始時に取引価格に含まれ、2018年に知的財産権(技術移転サービスを含む)の履行義務が完了したときに確認される。2018年、私たちは全額350.0ドルの前払い費用を受け取りました
一里塚払い
マイルストーン支払いは可変対価格形式を表し、取引価格に計上される範囲は、可変対価格に関する不確実性がその後解決された場合、確認された累計収入が大きく逆転しない可能性が高い。マイルストーン支払いを含む各スケジュールの開始時に、マイルストーンが実現される可能性が高いと考えられるかどうかを評価し、可能な金額法を用いて取引価格に含まれる金額を推定する。累積収入が大きく逆転しない可能性が高い場合、関連するマイルストーン価値は取引価格に含まれる。規制承認など,我々の制御範囲内ではない記念碑的支払いは,これらの承認を受けるまで実現されない可能性が高い.私たちはこの評価における特定のマイルストーンを実現するために、科学、臨床、監督管理、商業と他の克服しなければならないリスクなどの要素を評価した。累積収入が大きく逆転しない可能性が高いかどうかを決定する際には,かなりの判断が必要である。その後の各報告期間が終了すると、すべての制限されたマイルストーンの実現確率を再評価し、必要に応じて全体の取引価格の推定値を調整する
いくつかの記念碑的支払いは、技術移転サービスを含む知的財産権許可を交付するために、ヤンソン協定内の単一履行義務に割り当てられる。2018年の初期取引価格に含まれるマイルストーン許可収入5,000万ドルは、この年に履行義務が履行されており、IFRS 15契約で確認された累計収入が大きく逆転しない可能性が高いことを確認しました。5000万ドルのマイルストーン費用は2019年に私たちによって全額受け取りました。
また、指定された製造マイルストーンを実現するための1.25億ドルまでのマイルストーン支払いを取得する資格があり、指定された将来の開発と規制マイルストーンの実現に4.35億ドル、指定された貿易純売上のマイルストーンを実現するための2.1億ドルを追加する資格がある。その後の開発、製造、規制マイルストーンは、2018年に満たされた知的財産権ライセンス(技術移転サービスを含む)の履行義務に関連しているため、IFRS 15契約によって確認された累積収入が大きな逆転が生じない可能性が高い期間に十分に確認される。印税確認制限によりマイルストーンが実現された場合、販売のマイルストーンに基づく収入を確認します。私たちは残りのマイルストーンの達成が大きな不確実性を持っており、関連するマイルストーン支払いは取引価格に含まれていないと評価した。
JanssenがJanssen協定に基づいて私たちに支払った前金とマイルストーン支払いおよび将来可能なマイルストーン支払いに関する説明J本協定によれば、アンソンは私たちに情報を提供する可能性がありますので、“項目4.会社に関する情報-B.業務概要-ヤンソンバイオテクノロジー会社との協力および許可協定”を参照してください
知的財産権許可証
ライセンスが他の承諾と異なるかどうかを評価する際には,連携パートナーの研究,開発,製造,商業化能力,一般市場での専門知識の可用性などを考慮する。さらに、私たちは、ライセンスの価値が未履行のコミットメントに依存するかどうか、他のプロバイダが残りのコミットメントを提供することができるかどうか、および残りのコミットメントから分離して識別できるかどうかを考慮することによって、取引相手が残りのコミットメントを受けることなく許可から利益を得ることができるかどうかを考慮する。私たちは、約束が一定期間内に行われるか、またはある時点で履行されるかを決定するために、ライセンスを付与する約束の性質を評価する。我々は、許可が付与された時点で存在する我々の許可を使用する権利を表す技術移転サービスを含む“ヤンソン協定”における単一の履行義務であることを評価する。ライセンス収入は、ライセンス使用権制御権がお客様に譲渡されたときに確認されます。
研究開発コスト
すべての研究費は発生時に損益表とその他の包括収益を計上した。
使用または販売可能にするために無形資産を完成させる技術的可能性、資産を完成させる意図、および資産の使用または売却を達成する能力、資産がどのように将来の経済効果をもたらすか、プロジェクトを達成する資源の利用可能性、および開発中に支出を確実に測定する能力を証明することができる場合にのみ、新製品候補製品を開発するためのプロジェクトによって発生する支出が資本化および繰延される。これらの基準を満たしていない候補製品開発支出は発生時に計上される
株式ベースの報酬
株式オプション計画とRSU計画を実施し、私たちの運営成功に貢献した合格参加者にインセンティブと報酬を提供することを目的としています。私たちの従業員と取締役は株式支払いの形で報酬を得ることができ、従業員は株式決済ツールまたは株式決済取引の対価格としてサービスを提供することができる
従業員と株式決済取引を行うコストは、付与された日の公正価値によって計量される。株式購入の公正価値は当社が二項モデルを採用して決定したが、各購入株式単位の公正価値は吾がそれぞれ与えた日の株式市価を参考にして決定した。詳細は本年度報告総合財務諸表付記26および付記27を参照されたい
株式決済取引のコストは、相応の権益が増加するとともに、従業員福祉支出において業績及び/又はサービス条件を満たす期間に確認する。帰属日までの各報告期間終了時に確認された権益決済取引累積支出は、帰属期間が満了した程度を反映し、最終的に帰属する権益ツール数の最適な推定値を吾等に反映する。ある期間損益表に計上された費用または貸方は,その期間中と期末に確認された累積費用の変動を表す
付与日報酬の公正価値を決定する際には、サービス表現条件は考慮されないが、条件を満たす可能性は、最終的に付与される権益ツール数の最適な推定の一部として評価される。決裁に付加された他の条件はいずれも,関連するサービス要求がなく,非帰属条件とみなされる.非帰属条件は、裁決の公正価値に反映され、サービスおよび/または業績条件がない限り、裁決の費用の即時支払いをもたらす
以下の表に用いたモデルの入力を示す
| | | | | | | | | | | |
| 十二月三十一日までの年度 |
| 2022 | | 2021 |
| オプションの期待寿命 | 10 | | 10 |
| 予想変動率 | 73.0% - 87.1% | | 73.2%-76.4% |
| 無リスク金利 | 0.52% - 3.11% | | 0.03%-1.72% |
| 配当率 | 0 | % | | 0 | % |
私たちは、付与日の公正価値に基づいて、従業員および取締役に付与された株式オプションおよび他の株式ベースの奨励を測定し、その奨励が必要なサービス期間(通常は対応する奨励の帰属期間)内に推定没収された相応の補償支出を差し引くことを確認する。一般的に、業績帰属条件を含む株式オプションを発行し、参加者が取締役会が設定したいくつかの業績目標を達成できない場合は没収されます
私たちは、私たちの普通株の公正価値、私たちの株式オプションの実行権価格、比較可能な会社の歴史変動性に基づく普通株予想変動率、私たちの株式オプションの予想条項、私たちの株式オプションの期待期限に近い一定期間の無リスク金利、帰属後の失敗率、私たちの期待配当率を使用した二項オプション定価モデルを用いて各株式オプション付与の公正価値を推定した
発表されたがまだ発効していない国際財務報告基準
当社の連結財務諸表に適用される最新の会計声明の説明については、本年度報告における当社の連結財務諸表の付記2.3を参照されたい。
B.流動性と資本資源
流動資金源
設立以来、私たちは重大な運営損失を受けた。予見可能な未来には,我々の研究計画や候補製品の臨床前と臨床開発に伴い,巨額の費用と運営損失を招くことが予想される。現在と将来の研究計画と候補製品のためにより多くの臨床試験と臨床前研究を行うため、契約製造組織(“CMO”)と臨床試験と臨床前研究を支援する契約を締結し、私たちの知的財産権の組み合わせを拡大し、私たちの運営に一般と行政支援を提供するため、私たちの研究開発および一般と管理費用は増加すると予想される。したがって、私たちは私たちの運営に資金を提供するための追加の資本が必要であり、私たちは追加の持分や債務融資、協力、許可手配、または他の出所を通じてこれらの資金を得ることができるだろう。
最初の製品CARVYKTIを除いて、2022年2月28日にFDAの承認を得ましたプロテアソーム阻害剤、免疫調節剤、および抗CD 38モノクロナル抗体を含む、4つ以上の治療を受けた成人RRMMの治療のための使用現在、承認された製品は何もありませんし、他の製品の販売から何の収入も得ていません。設立から2022年12月31日まで、私たちの運営資金は主に:
•Genscriptから390万ドルの出資があります
•Aシリーズの優先株を売った毛収入は1兆605億ドルでした
•Janssenは、私たちの協力と許可協定に基づいて、6.5億ドルの前金とマイルストーン支払いを支払います
•米国初公開株の純収益は4.501億ドルで、Genscriptと別の1200万ドルの私募を行った
•2021年5月、投資家への私募·発行関連権証の純収益は3億ドル
•2021年12月に完成したアメリカの預託証明書公開純収益3.234億ドル
•ヤンソン協定によるとヤンソンは2億5千万ドルの前金を提供しています
•我々が2022年7月に完成した米国預託証券公開純収益は3兆776億ドル。
2022年12月31日現在、会社は約7.873億ドルの現金と現金等価物、約5400万ドルの定期預金、約1億856億ドルの公正価値で損益に計上された金融資産を持ち、累計9億664億ドルの赤字を計上している。
私たちのいくつかの子会社は、中国で非中国資本企業に登録されている子会社を含み、その積立金がその登録資本の50.0%に達するまで、少なくとも10.0%の税引後利益を一般積立金に計上しなければならない。中国法規によると、非中国投資企業は中国会計基準と法規に従って確定した累積利益(例えばある)から配当金を支払うことしかできない。前のいくつかの会計年度のいかなる損失を相殺する前に、中国会社はいかなる利益も分配してはならない。前会計年度に留保された利益は、本会計年度の分配可能利益とともに分配することができる。私たちは現在、私たちの中国付属会社にこのような配当金を送って私たちの業務に資金を提供することを要求していませんが、もし私たちが将来追加の流動資金源が必要であれば、このような制限は私たちの流動資金や資本資源に重大な悪影響を及ぼす可能性があります。詳しくは“第4.B項-業務概要-政府法規-中華人民共和国法規-その他の中華人民共和国国家レベルと省級法規-株利分配に関する法規”を参照されたい
キャッシュフロー
次の表に我々のキャッシュフローの概要を示す
| | | | | | | | | | | | | | | | | |
| 2013年12月31日までの年度 |
| 2022 | | 2021 | | 2020 |
| (単位:千) |
| 経営活動のための現金純額 | (201,281) | | | (198,465) | | | (223,005) | |
| 投資活動のための現金純額 | (77,092) | | | (194,983) | | | (24,169) | |
| 融資活動が提供する現金純額 | 377,976 | | | 626,663 | | | 618,879 | |
| 現金と現金等価物の純増加 | 99,603 | | | 233,215 | | | 371,705 | |
経営活動
2022年12月31日現在、経営活動で使用されている現金純額は201.3ドルで、主に非現金項目調整、経営資産と負債変化および現金項目調整後の税引き前純損失4.457億ドルによるものだ。非現金プロジェクトには、主に820万ドルの財務収入、1080万ドルの財務コスト、1020万ドルの物件および工場設備減価償却費用、250万ドルの無形資産償却費用、570万ドルの使用権資産減価償却、2090万ドルの権証負債公正価値収益、920万ドルの為替損失、3430万ドルの株式決済株式補償費用が含まれる。経営資産と負債の変化には、主に売掛金が5,030万ドル減少し、主な理由は、2つの記念碑的な支払いを受け、前払金、その他の売掛金、その他の資産が5,060万ドル増加し、他の非流動資産が370万ドル減少し、協力在庫が860万ドル増加し、繰延政府贈与が620万ドル増加し、貿易支払いが2,590万ドル増加し、他の支払·売掛金項目が1.659億ドル増加し、他の非流動負債が増加(20万ドル)することである。現金プロジェクトには、主に受け取った財務収入560万ドルと受け取った所得税370万ドルが含まれており、これは前年に支払われた所得税申告書の返金である。
2021年12月31日までの1年間で、経営活動に用いられた現金純額は1兆985億ドルであり、これは主に非現金プロジェクト調整後の税引き前純損失3.614億ドルおよび営業資産と負債の変化によるものである。非現金プロジェクトは、主に株式証明負債の公正価値損失620万ドルと株式決済の株式ベース報酬支出2020万ドルを含む。経営資産と負債の変化は主に売掛貿易売掛金の2,460万ドルの減少を含み、主な原因は7,500万ドルのマイルストーン支払いを受け、実現されたマイルストーン支払いの5,000万ドルの増加と年内の売掛金使用料収入の増加4,000,000ドルの相殺である;主に支払い協力費用の増加、他の支払·売掛金プロジェクトの増加により1.407億ドル、前払、その他の売掛金およびその他の資産が3,000,000ドル増加する。
2020年12月31日現在の年度、経営活動で使用されている現金純額は2.23億ドルで、非現金プロジェクト調整後の税引前純損失2.125億ドルと、営業資産と負債の変化が主な原因となっている。非現金プロジェクトは主に8,000万ドルの転換可能な優先株の公正価値損失から来た。営業資産と負債の変化には、主に一里塚支払いを受けたことで増加した貿易売掛金4500万ドルが含まれる。
投資活動
2022年12月31日までの年度の投資活動のための現金純額は7,710万ドルで、主に物件、工場と設備2,090万ドルの購入、無形資産130万ドルの購入、協力資産1,480万ドルを前払いし、公正価値に応じて損益純による金融資産1.85億ドルを購入したが、定期預金が1.136億ドル減少し、償還コストで計算された金融資産3,000万ドルと現金が130万ドルの投資収入を受け取ったことで部分的に相殺された。
2021年12月31日までの年度の投資活動のための現金純額は1.95億ドルで、主に物件、工場、設備4,220万ドルの購入、無形資産320万ドルの購入、パートナーに協力資産170万ドルを前払いし、償却コストで計算した金融資産2,980万ドルの購入と定期預金2.981億ドルを購入したが、定期預金が1.8億ドル減少した部分で相殺された。
2020年12月31日までの投資活動のための現金純額は2,420万ドルであり,主に物件,工場,設備2,630万ドルの購入,無形資産4,000,000ドルの購入,パートナーへの協業使用権資産1,950万ドルの前払い,定期預金5,000万ドルの購入,回収された7,560万ドルの定期預金から相殺される
融資活動
2022年12月31日までに、融資活動が提供する現金純額は3.78億ドルで、主に7月に後続公開発売の普通株を発行して得られた純額3.776億ドル、株式購入を行使して得られた金290万ドルを含み、一部は賃貸支払元金部分260万ドルで相殺される。
2021年12月31日までの年度まで、融資活動が提供する現金純額は6.267億ドルで、主に12月に普通株を発行して後続公開発売のために得られた金の純額3.234億ドル、5月に機関投資家に普通株式及び株式承認証を発行して得られた金3.00億ドル、及び株式購入を行使して得られた金460万ドルを含み、一部は140万ドルのリース支払元金によって部分的に相殺される。
2020年12月31日までの年間、融資活動が提供する現金純額は6.189億ドルで、主に2020年3月と4月にAシリーズ優先株を売却して得られた1億505億ドルと1,000万ドルを含み、GenScrip私募発行普通株で得られた1,200万ドルを含み、私たちはアメリカで初めて株式を公開発売および行使して得られた純額4.501億ドルと株式購入権行使による150万ドルを得たが、260万ドルの賃貸支払いと250万ドルの転換償還優先株支払い部分に相殺できる。
経常支出ではない
2022年、2021年、2020年12月31日までの年間、私たちの資本支出はそれぞれ7,030万ドル、4,450万ドル、5,000万ドルです。このような支出は主に財産、工場、設備、そして協力資産を含む。
2022年と2021年12月31日まで、資本支出に対する私たちの約束はそれぞれ約2,660万ドルと2,590万ドルで、主に実行可能で法的拘束力のある契約に使用され、使用する固定または最低サービス、固定、最低または可変価格規定、および契約下での行動の大まかな時間を含むすべての重要な条項を指定する。私たちは2023年の資本支出が私たちの手元の現金と現金同等物から来ると予想している。これらの資本支出は主にアメリカと中国で行われ、私たちの主要な研究開発施設は現在アメリカに位置している。
資金需要
次の表には、2022年12月31日までの契約義務と約束を示しています
| | | | | | | | | | | | | | | | | | | | | | | | | | | | | |
| 少ないです 1年 | | 1~3 年.年 | | 3~5個 年.年 | | 超過 5年間 | | 合計する |
| (単位:千) |
| レンタル義務 | $ | 3,994 | | | $ | 5,928 | | | $ | 5,003 | | | $ | 12,303 | | | $ | 27,228 | |
| 資本約束 | $ | 16,745 | | | $ | 5,961 | | | — | | | — | | | $ | 22,706 | |
| 合計する | $ | 20,739 | | | $ | 11,889 | | | $ | 5,003 | | | $ | 12,303 | | | $ | 49,934 | |
これには資本約束と、ニュージャージー州、アイルランド、中国の施設運営賃貸契約の下での私たちの満期支払いが含まれている。
上の表の承諾額は、使用する固定または最低サービス、固定、最低または可変価格規定、および契約に基づいて行動する大まかな時間を含むすべての重要な条項を規定する強制実行可能かつ法的拘束力のある契約に関連している。この表には、重大な処罰を受けることなく、私たちがキャンセルできる合意下の義務は含まれていない
私たちはまた正常な業務過程で契約研究機関(“CRO”)と撤回可能な契約を締結し、臨床試験、臨床前研究、製造と運営目的のための他のサービスと製品に使用する。
私たちは私たちが行っている活動に関連する費用が増加することを予想して、特に私たちが候補製品の臨床試験を研究、開発、継続、あるいは開始し、マーケティング承認を求める時に。さらに、FDAがCARVYKTIを承認した後、このような販売、マーケティング、製造、および流通は潜在的なパートナーの責任ではないので、計画販売、マーケティング、製造、流通に関連する巨額の商業化費用が発生することが予想される。例えば、私たち自身の施設に投資するほか、1つ以上のCMOと協定を締結することで、私たちの製造能力やインフラを補完したいと思います。また、私たちは上場企業の運営に関連した追加コストが発生すると予想される。したがって、私たちは私たちの持続的な業務と関連した多くの追加資金を得る必要があるだろう。もし私たちが必要な時や魅力的な条件下で資金を集めることができなければ、私たちは私たちの研究開発計画や将来の商業化努力を延期、減少または廃止することを余儀なくされるだろう。
新冠肺炎の流行とインフレ、およびそれによる経済的不確実性を含むマクロ経済状況の結果は、将来の流動性および資本資源に悪影響を及ぼす可能性があり、現金需要は以下に説明する多くの要因の時間および程度によって変動する可能性があるが、現在、私たちの既存の現金と現金等価物は、少なくとも今後12ヶ月の運営費用および資本支出需要に資金を提供することができると予想されている。私たちの将来の資本需要は多くの要素に依存します
•製品発見、臨床前研究と臨床試験の範囲、進展、結果とコスト
•私たちの研究開発プロジェクトの範囲、優先順位、数量
•私たちの候補製品に対する規制審査のコスト、時間、結果
•私たちが有利な条件で協力を確立し維持する能力があれば
•ヤンソン合意と私たちが達成した任意の他の協力協定に基づいて、マイルストーンまたは支払いをトリガする他の事態が発生した
•協力協定によると、臨床試験費用の補償程度(あれば)を返済する権利がある
•特許出願を準備し、提出し、起訴し、私たちの知的財産権を維持し、実行し、知的財産権に関するクレームを弁護するコスト;
•他の候補品や技術をどの程度得ることができるか
•商業生産の製造手配のコストを確保すること
•もし私たちが規制機関の承認を得て私たちの候補製品をマーケティングする場合、販売とマーケティング能力の契約を確立または締結するコスト。
Cilta-celに加えて、私たちは幅広い初期候補製品の組み合わせを持っている。潜在的な候補製品を決定し、臨床前研究と臨床試験を行うことは時間がかかり、高価かつ不確定な過程であり、長年を必要とし、私たちは決して必要なデータ或いは結果を生成せず、市場の許可を得て、このような候補製品の製品販売を実現することができるかもしれない。しかも、私たちの候補製品が承認されれば、商業的成功を得られないかもしれない。私たちの商業収入は、もしあれば、全然なければ、何年も商業化できないと予想される候補製品を販売します。したがって、私たちは追加的な資金調達に依存して私たちの業務目標を達成し続ける必要があるだろう。私たちは受け入れ可能な条項で十分な追加融資を受けることができないかもしれないし、根本的にできないかもしれない。
これまで、相当な製品収入を生み出すことができれば、株式発行、債務融資、協力、戦略連合、許可手配の組み合わせで現金需要を満たす予定です。株式または転換可能な債務証券を売却することで追加資本を調達すれば、私たちのアメリカ預託証明書の保有者は
これらの証券の条項は、清算または私たちの株主権利に悪影響を及ぼす他の特典を含む可能性がある希釈されるだろう。債務融資が可能であれば、追加債務を招く、資本支出を行う、または配当を宣言するなど、私たちが具体的な行動をとる能力を制限または制限する契約を含むいくつかの合意が含まれる可能性がある。
もし私たちが追加的な協力、戦略連合、または第三者との許可手配を通じて資金を調達すれば、私たちは私たちの技術、将来の収入源、研究計画、または候補製品に対する貴重な権利を放棄しなければならないかもしれないし、私たちに不利になる可能性のある条項で許可を与えなければならないかもしれない。もし私たちが必要な時に株式や債務融資を通じてより多くの資金を調達できなければ、私たちは私たちの製品開発や将来の商業化努力を延期、制限、減少または終了することを要求されるか、あるいは私たちが開発とマーケティングをより望んでいた開発とマーケティングの権利を与えることができるかもしれない。
ヤンソン協定によると、私たちの協力が最初の利益年度を経験する前に、どの年も協力する予定の運営資金が5,000万ドル以下であれば、私たちはJanssenから前金を得る権利がある。この場合、Janssenが私たちに提供してくれた前払い金額は、協力年度の運営資本が5000万ドルを超えることに相当する。いかなる例年の前金総額も1.25億ドルを超えてはならず、いつでも未払いの前払い総額は2.5億ドルを超えてはならない。未償還前払金は“ウォール·ストリート·ジャーナル”が発表したロンドン銀行間同業借り換え金利(LIBOR)に2.5%を加算した。Janssenは、私たちが協力した税引前利益から配当された前金と利息から回収する権利があり、いくつかの制限を受けた場合、Janssen協定に従って私たちに支払われなければならない記念碑的支払いから回収する権利がある。当社の統制権の変更やJanssenが私たちの深刻な合意違反のためにJanssen協定を終了しない限り、前金や利息を返済する義務はありません。私たちはいつでも自発的にその時返済されていない前払いまたは関連する利息の任意の部分を自ら決定することができます。2022年12月31日現在、このような前払いと利息の未返済元金総額はそれぞれ約2.5億ドルと1090万ドルである。LIBORの金融サービス業での使用停止に伴い、新たな金利計算方法を採用するためにJanssenプロトコルを改正することをJanssenと検討し始めている。
C.研究開発、特許、ライセンスなど
我々の研究開発活動と支出および特許およびライセンスのすべての詳細は“プロジェクト4.B-会社情報”に掲載されている—本年度報告の“業務概要”及び“プロジェクト5−運営及び財務回顧及び展望”部分
D.トレンド情報
本年度報告の他の部分(第5.a項-経営業績“及び”第5.b項-流動資金及び資本資源“を含む)に述べた以外に、当社等は、いかなる傾向、不確定要因、需要、承諾又はイベントが自社の収入、持続的な経営収入、収益性、流動資金又は資本資源に重大な悪影響を及ぼす可能性があるか、又は自社報告の財務情報が必ずしも将来の経営結果又は財務状況を反映するとは限らないことを知らない
E.肝心な会計見積もり
我々の重要会計政策の説明については、重要な会計判断及び見積もりを含み、本年度報告その他の部分の総合財務諸表付記2及び3を参照されたい。
項目6.役員、上級管理職、従業員
A.役員と上級管理職
次の表には、2023年3月1日現在の私たちの現職役員と役員に関するいくつかの情報を示しています
| | | | | | | | | | | | | | |
| 名前.名前 | | 年ごろ | | ポスト |
| 行政員 | | | | |
| Huang、博士。 | | 50 | | 取締役CEO兼最高経営責任者 |
| Lori Macomber公認会計士 | | 52 | | 首席財務官 |
| 非従業員取締役 | | | | |
| 張方亮、博士。 | | 58 | | 取締役会議長 |
| Ye(サリー)Wang M.S. | | 54 | | 役員.取締役 |
| Li·朱博士。 | | 73 | | 役員.取締役 |
| 季暁慧医学博士博士。 | | 61 | | 独立役員 |
| コラソン·D·サンダース博士 | | 66 | | 独立役員 |
| 邱偉民会計士 | | 47 | | 独立役員 |
| パトリック·キャシー博士 | | 67 | | 独立役員 |
| Li、医学博士 | | 66 | | 独立役員 |
| トーマス·ハイマン | | 67 | | 独立役員 |
行政員
Huang博士2020年9月から私たちのCEOを務め、2019年7月から2022年5月まで私たちの最高財務責任者を務めています。Dr.Huangは2022年2月以来、個人持株会社広達治療有限公司の取締役メンバーであった。私たちに加入する前に、Dr.Huangは2014年8月から2019年7月までアメリカ銀行証券会社で取締役社長兼バイオテクノロジー株式研究主管を務め、そこで彼が指導したアナリストチームは30社以上のバイオテクノロジー会社をカバーし、安進、ギレド、セル建、生物遺伝など、広範な治療領域をカバーした。Dr.Huangは2007年からバイオテクノロジーアナリストで、米国銀行証券会社に入社する前に、富国銀行(Wells Fargo)(前身は美聯銀行)、スイス信用(Credit Suisse)、グリチェル(Gleacher)、バークレイズ銀行(Barclays)で働いていた。ウォール街に入る前、Dr.Huangは先霊雅(Schering-Plough)(現在はメルク社)の首席科学者だった。化学研究部では,心血管や中枢神経系治療分野の小分子薬物発見に焦点を当てている。彼は複数の特許と同業者評議出版物の共著者でもある。Dr.Huangはコロンビア大学生物有機化学博士号を持っている。Dr.Huangはコロンビア大学商学院と中国科学技術大学資優青年専門クラスにも通っていた。2021年12月、Dr.Huangは取締役の第1種取締役に任命された。
Lori Macomber公認会計士2022年5月以来、私たちの首席財務官を務め、Macomberさんは私たちの首席財務官と首席会計官を務めてきました。マッコバーさんはこれまで2021年3月から2022年5月まで私たちの副財務総裁を務め、2019年9月から2021年3月まで私たちのサプライチェーン財務と主計長総裁の副総裁を務めてきました。私たちに参加する前に、Macomberさんは2018年3月から2019年9月まで航空宇宙と国防業界をリードする部品とシステムサプライヤーAmetek PDSの業務部門総監を務め、2017年4月から2018年2月までCello Healthの米国首席財務官兼財務総監を務めました。これまでMacomberさんは複数のポストを担当していたが、最近のポストはEli Lilly&Companyの財務サイト担当上級副総裁で、2010年5月から2017年4月まで。Macomberさんはペンシルバニア州立大学の会計学学士号を持ち、公認会計士だ。
非従業員取締役
張方亮、博士2022年8月以来、私たちの取締役と取締役会長を務めてきました。張博士は2022年12月から遺伝子スクリプト会社役員の執行役員を務めており,これまで2022年5月から2022年12月まで遺伝子スクリプト会社取締役の非執行役員を務めていた。 これまで、2015年から2020年までの間にGenScrip会長兼取締役幹部を務めていた 彼はGenscriptグループ内のいくつかの会社の社長も務めている。 2002年、彼は他人と共同でGenScripグループを設立し、GenScripになるまで複数のグループ会社の取締役を務めてきた
GenScripが2015年に初めて公募した会社再編によると、グループ会社の持ち株会社。2015年,張博士は同社を設立し,GenScripの子会社としてGenScripの業務目標を拡大し,一連の免疫療法を研究,製造,商業化した。張博士は2015年から2020年11月まで私たちの取締役会長を務め、2020年8月から2020年9月まで私たちのCEOを務めています。2018年、張博士は中国医療サミットで年度人物を受賞し、医療分野における彼の貢献と重大な影響を表彰した。GenScripを創設する前に,張博士は1995−2002年の間に先霊雅の首席科学者を務め,そこで大統領賞を受賞した。張博士はデューク大学生物化学博士号、南京大学修士号、成都地質学院学士号を持っている。
葉莉·王M.S.,2015年5月から取締役会長を務め、2020年11月から2022年8月まで取締役会長を務めている。王さんは2014年4月から2017年11月までキングスッド首席運営官を務め、2009年からキングスッド取締役会のメンバーを務め、2017年12月からキングスッドの総裁を務め、キングスッドの戦略と全体運営管理を担当している。彼女は2002年にGenscriptグループを共同設立し,GenscriptがGenscriptグループ会社のホールディングスになるまで,Genscript Corporationで様々な管理職を務めてきた.キングス捷に加入する前に、深セン市福田環境保護監視所で環境モニタリングエンジニアを務めていた。王さんは南京GenBest企業管理センターのパートナーであり、仁修基金会有限公司の役員と総裁でもある。王さんは武漢大学の修士号、ブリッジポート大学のコンピュータ科学修士号、中国ヨーロッパ国際商学院の幹部MBAの学位を持っている。
Li·朱博士は2020年11月以来私たちの役員として働いてきました。朱博士は2020年11月からGenscriptの首席戦略官を務めている。朱博士はこれまで、2010年から2017年2月までキングズド戦略副総裁を務め、2017年2月から2019年7月までキングズド首席戦略官を務め、2019年7月から2020年11月までキングスッド顧問を務めてきた。遺伝子科学技術会社に入社する前に、朱博士は1990年から2000年までClontech実験室会社で分子生物学取締役を務めた。朱博士は酵母抗体発見に専念するバイオテクノロジー会社であり、2000年から2005年まで総裁と最高経営責任者を務めたGenetastix Corporation,Inc.を創立した。朱博士はその後、中国の生物技術会社で働き、2006年から2008年まで国泰生物科学技術株式有限公司研究部副主任総裁を務め、2009年から2009年まで八重歯生物医薬科学技術(上海)有限公司総裁副主任を務めた。朱博士は2020年11月以来遺伝子科学技術会社の取締役を務めてきた。朱博士は東中国師範大学の生物学学士号とスタンフォード大学分子生物学と免疫学博士号を持っている。
季暁慧医学博士博士2020年5月以来私たちの役員として働いてきました。紀万昌は現在Elpiscience BiopPharmticals,Inc.のCEO兼会長を務めており,2017年6月にヒトと共同設立した臨床段階免疫療法会社である。2017年1月から2019年12月までの間に担当した礼来アジアベンチャー企業(Lilly Asia Ventures,LAV)のリスクパートナーも務めている。これに先立ち、紀万昌博士は2013年から2016年12月までF.Hofmann-La Roche Ltd.でアジアと新興市場業務発展グローバル主管兼副総裁を務めた。紀万昌博士のキャリアはP&G製薬から始まり、1997年から2007年まで薬品の研究開発と業務発展を担当した。2008年、彼は上海でPharmaLegacy実験室を共同創立し、管理し、最高経営責任者を務めた。2008年から2013年にかけて、中国生命科学遺産ビジネスリーダーコミュニティBayHelix Groupの取締役会のメンバーを務めた。紀万昌博士は中国医科大学医学博士号、イギリスシェフィールド大学博士号、シカゴ大学工商管理修士号を持っている。
Corazon Sanders Ph.D2020年5月以来私たちの役員として働いてきました。サンダース博士は2019年12月からAltruBio Inc.(F/k/a AbGenology Holdings Inc.)分子テンプレート会社の取締役会メンバーである。2020年3月から現在まで、百済神州さんは2020年8月から勤め、Ultragenyx製薬会社は2021年6月から在任する。サンダース博士はこれまで2018年3月から2019年11月までCelgene首席医療官オフィスの戦略顧問を務めてきた。これまでサンダース博士はジュノ治療実行委員会のメンバーであり,開発運営実行副総裁を務め,2017年1月から2018年3月まで戦略運営,定量科学,生物サンプル,臨床運営を担当していた。2009年から2017年にかけて、サンダース博士は遺伝子泰克/羅氏末期投資組合委員会のメンバーを務め、2012年から2017年まで、遺伝子泰克/羅氏末期臨床運営グローバル責任者を務めた。サンダース博士はフレッド·ハッチンソンがん研究センターの取締役会メンバーも務め、2022年から新たに設立されたフレッド·ハッチンソン研究センター顧問委員会の合同議長を務めてきた。サンダース博士は統計学学士と修士号を持ち、優れた成績でフィリピン大学を卒業し、ペンシルバニア大学ウォートン博士プロジェクトで統計学修士と博士号を取得した。
邱偉民公認会計士2020年5月以来私たちの役員として働いてきました。邱氏は2021年10月から嘉嘉国際有限公司の首席財務官を務めている。その前に、彼はHSBC銀行の非執行副議長だった
2016年から2019年12月にかけて、AMTD Groupで戦略開発、企業融資、投資機能を指導した。2011年から2016年3月まで、安永中国法律事務所でパートナーを務め、リスクコンサルティング会社の中国南方市場主管を務め、大中国地区の顧客にサービスを提供し、そこで財務、管理、商業問題についてコンサルティングを提供した。2006年から2011年まで、彼はプロティビティ上海有限会社で取締役と深セン事務所の責任者を務め、主に会社の全面管理を担当した。1997年から2006年まで、彼は普華永道と安達信会社で働いており、最近担当したポストはリスクコンサルティング業務の高級マネージャーである。游さんは2021年6月から2022年4月までの間に教育サービス会社の中国通識教育集団有限公司の役員を務めた。邱氏はアメリカ公認会計士、香港会計士組合のベテラン会員及び香港内部監査師学会登録内核員である。Yauさんは、米オレゴン大学レンデクイストビジネススクールの会計学学士号と、西北大学ケロッグ管理学院と香港科技大学が共同で行ったEMBA号を取得している。
パトリック·キャシー博士は2020年12月以来私たちの役員として働いてきました。キャシー博士は2005年からデューク·国立大学医学院研究部高級副院長とデューク大学ジェームズ·B·デューク薬理学と癌生物学教授を務めてきた。キャシー博士はデューク大学医学センター分子癌生物学と生化学アシスタント教授も務め、1990年以来この職を務めている。彼はデューク化学生物学センターの創始者でもあり、これはデューク大学の科学者からなる組織であり、基本化学原理を生物学及び疾病と治療基礎の研究と訓練に応用することに取り組んでいる。キャシー博士はオグスタナ大学の生物と化学学士号、ブランディス大学の生化学博士号を持ち、ダラスのテキサス大学西南医学センターでポストドクターの仕事をしている。
Li、医学博士。2022年8月以来、私たちの取締役として働いてきました。毛博士は現在SciClone製薬会社の首席医療官を務めており、2022年6月以来この職を務めている。これまで,毛博士は2021年5月から2022年6月まで中国生物製薬株式会社の首席医療官,2021年3月から2021年4月まで麗宗生物最高経営責任者,2018年11月から2021年3月までXcovery Holdings,Inc.最高経営責任者を務めていた。2018年3月から2021年3月まで、毛博士はベータ製薬有限会社で高級副総裁兼首席医療官を務め、2016年6月から2018年2月まで、毛博士はジョンソン社で総裁副主任を務めていた。また,2004年から2009年3月までMDアンダーソン癌センターで教授を務め,2009年3月から2016年6月までボルチモアメリーランド大学で教授を務めた。2018年4月から2021年3月まで、毛博士は深セン証券取引所に公開上場しているベータ製薬有限公司の取締役会メンバーも務めている。毛先生は南京医科大学の医学博士号を持っている。毛博士はまたジョン·ホプキンス大学医学院で癌遺伝学のポストドクター研究を終えた。
トーマス·J·ハイマン2022年8月以来、私たちの取締役として働いてきました。ハイマンさんは、2015年から2019年9月までの間に、世界的なヘルスケア企業ジョンソン·ベンチャー·グループの社長を務め、1992年から2015年までの間、ジョンソン·メディカル·グループのグローバル業務開発担当者を務めていました。また、ヘイマンは2008年から2016年まで製薬会社ヤンソン製薬会社の最高経営責任者を務めていた。ハイマンさんは、2020年12月から製薬専門会社OptiNose,Inc.の取締役を務め、2020年6月からバイオテクノロジー会社アクロ治療会社の取締役を務め、2021年6月からバイオ製薬会社インビオ社(前身:Adagioセラピー社)の取締役を務め、2022年9月からバイオテクノロジー会社ヒリオ治療会社の取締役を務める。ハイマンさんは、ベルギーのルモール大学を卒業し、法学の修士号を取得しました。彼は引き続きスイスのジュネーブで国際法大学院生の課程を専攻し、ベルギーのアントワープ大学で工商管理大学院生の課程を専攻した。
家族関係
私たちのどんな役員や役員の間にも家族関係はありません。
B.補償する
役員および行政職の報酬
2022年12月31日までの年間で、役員と非従業員取締役に合計2,144,854.82ドルの現金と福祉を支払った。2022年12月31日までの年間で、非従業員取締役に362,500ドルを支払いました。われわれの新任の非従業員取締役Tomas HeymanさんとLi毛博士は、2022年12月31日までに、それぞれ30,000株の普通株式を購入し、普通株式1株当たり23.27ドルおよび
2032年8月1日の満期日と18,656株普通株の制限株式単位奨励は、彼らが私たちの取締役会メンバーに選出されたことと関係がある
我々の取締役会はすでに非従業員役員報酬政策を採用しており、この政策によると、我々の各取締役が、当社の従業員でなければ、あるいはどのエンティティと関連していても、そのエンティティ利益は、我々が発行している普通株式の5%以上、すなわち紀万昌博士、サンダース博士、キュンテン華さん、キャシー博士、ハイマンさん、毛博士であれば、我々の取締役会や取締役会に在籍していることにより、報酬を得る資格があることになります。条件を満たしたすべての役員は私たちの取締役会に勤めていて、年間75,000ドルの現金事前招聘金を得ることができます。監査委員会の議長と給与委員会の議長は毎年それぞれ25000ドルと20000ドルを追加的に獲得する。すべての年間現金補償金額は、サービスを提供する四半期ごとの前30日以内に均等四半期分割払いで前払いしなければなりません。
取締役会に新たに加入した合資格取締役1人には30,000株の普通株式を購入する選択権が付与され、そのうちの5分の1の株式は授出日1周年に帰属し、残りの株式はその後4回に分けて平均年間分割払いで帰属するが、帰属日が適用される前に取締役サービスを継続しなければならない。取締役会に新たに加入した合資格取締役1人当たり、制限株単位の奨励を受け、奨励数は200,000ドルの普通株に相当し、付与日の米国預託証明書の終値の半分に相当する。
また、各株主総会当日に、合資格の取締役1人当たりが会議後も取締役株主を継続すれば、200,000ドル相当の普通株に相当する制限株式単位賞を授与され、取締役が授出日の市価の半分で割る。監査委員会の議長と給与委員会の議長は、それぞれ70,000ドルを授与日の米国預託証券の終値の半分で割った追加制限株単位の奨励を受ける。我々の非従業員役員報酬政策に基づいて付与された制限株式単位奨励は、付与日の1周年に3分の1に帰属し、残りの株式は、適用された帰属日が取締役としてサービスを継続するまで、その後四半期ごとに8回均等に帰属する。
我々の上級管理者や取締役に株式インセンティブを付与することに関するより多くの情報は、項目6.Bを参照されたい。役員、上級管理者、そして従業員の報酬持分インセンティブ計画。当社は、退職金、退職その他の同様の福祉を当社の行政者及び取締役に提供するために、いかなる資金も予約又は蓄積していません。
雇用協定と賠償協定
私たちは私たちのすべての幹部と雇用協定を持っていて、私たちのすべての幹部は標準的な知的財産権譲渡、競業禁止、秘密協定に署名し、それぞれの雇用協定で修正した 各行政人員もすでに同意し、張志軍博士は撤回できない依頼書に基づいて株式購入権を行使して発行したいかなる普通株に対して投票権を持っている。各合意の具体的な条項は以下のとおりである.
会社の最高経営責任者Huang博士と締結された雇用協定を改訂して再署名します
改訂および再記述された採用合意条項によると、Dr.Huangの年間基本給は700,000ドルであるが、Dr.Huangは適宜年間現金配当を得る資格があり、Dr.Huang当時の基本給(“最高経営責任者目標金額”)の75%(“最高経営責任者年間ボーナス”)を目標としている。2023年3月、取締役会はDr.Huangの年間基本給を71.5万ドルに引き上げることを許可し、2023年4月2日から発効した。Dr.Huangが最高経営責任者年次ボーナスを獲得する資格があるかどうかは、取締役会が全権決定した取締役会による個人と会社の業績目標達成状況の評価に基づいている。
雇用協定の条項によると、Dr.Huangの採用は自由であり、私たちはいつでも終わらせることができる。もし我々(雇用プロトコルの定義による)やDr.Huang(雇用プロトコルの定義による)が制御権変更に関係なくDr.Huangの雇用関係を理由なく終了したり,Dr.Huangが正当な理由(雇用プロトコルの定義による)で雇用関係を終了したりすると,Dr.Huangは以下の解散費福祉を獲得し,適用された源泉徴収税金(以下,最高経営者非中投離職福祉と呼ぶ)を差し引く資格がある:
•通常の給料手続きでDr.Huang当時の基本給を18ヶ月間支払う
•Dr.Huangが解任された前年の年間ボーナスを支払い,解任発効日(“最高経営責任者解任の日”)まで支払われていなければ,適用した会社業績指標の実現状況および個人指標の平均値から計算する
この業績年度前2年以内のHuangの個人業績評価(“最高経営責任者の前年度ボーナス”)を適用します
•終了日当時のDr.Huang最高経営責任者の目標金額の比例部分は、サービスや業績指標や格付けが確立または達成されたかどうか(会社でも個人でも)(“CEOの比例ボーナス”)は考慮されていない
•Dr.Huangとその家族が“コブラ法案”の下で18ヶ月に及ぶ持続健康保険(“最高経営責任者コブラ支払い”)の支払いまたは精算
•雇用契約を締結する際の既存株式奨励について、全額付与を加速する
•雇用契約を締結した後にDr.Huangの任意の株式奨励を付与する可能性がある場合、Dr.Huangが保有する任意の株式奨励は、Dr.Huang退職後18ヶ月の間に帰属すべき部分を加速しなければならず、このような当時帰属していなかった株式奨励は直ちに付与され、業績に基づく要求を考慮することなく、完全に行使可能または没収できないものとなるべきであるが、任意の適用された会社の業績目標を達成することが前提である
•雇用契約締結後にDr.Huangの任意の株式奨励が付与される可能性がある場合、Dr.Huangが所有する任意の株式奨励のうち、Dr.Huangが契約を終了した日から18ヶ月以内に帰属すべき部分は、その時点で帰属していない株式奨励が直ちに帰属し、完全に行使可能であるように、実施を加速すべきである。
•没収してはならず、業績に基づく要求は何も考慮していないが、適用される会社の業績目標を達成した場合にのみ、
•株式オプションの終了後の行権期間は、Dr.Huang終了日から18ヶ月に延長されることができる
•国が認可したプロバイダと提供する再就職サービスや12カ月の幹部研修サービスは、年会費は最大40,000ドル(“CEO研修サービス”)に達する。
雇用契約によると、私たちがDr.HuangまたはDr.Huangを理由なく解雇し、コントロール権変更発効日の3ヶ月前またはコントロール権変更が発効してから18ヶ月以内に退職した場合、Dr.Huangは以下の解散費福祉を獲得し、適用される源泉徴収税を引く権利がある(“最高経営責任者国投離職福祉”、非中投会社の離職福祉と一緒に、“最高経営責任者退職福祉”:
•通常の給料手続きで24ヶ月間その時点の基本給を支払う
•CFOの前年度ボーナスの支払いは、終了日にまだ支払われていない場合
•最高経営責任者は比例してボーナスを支給した
•終了日に発生した年間CEOの目標金額の2倍を支払う
•CEOコブラが支払いました
•Dr.Huangが保有するすべての持分奨励の速度を加速し、このような当時帰属していなかった株式奨励を直ちに付与し、終了した日から業績に基づく要求を考慮することなく、完全に行使可能または没収できないようにすべきである
•株式オプションの引受または転換オプションの終了後の権利期間は、終了日から18ヶ月に延長されなければならない
•最高経営責任者コーチサービス部です。
最高経営責任者の離職金を支払う条件は、Dr.Huangが署名し、私たちに有利なクレームを全面的に解除することを含む退職協定を提出したことだ。雇用契約によると、Dr.Huangが解雇されたり、Dr.Huangが正当な理由なく辞任した場合、Dr.Huangは最高経営責任者の退職給付を受けないだろう。
私たちの最高財務責任者Lori Macomberさんと修正して雇用協定に再署名しました
改正および追記されたMacomberさんとの雇用協定条項によると、Macomberさんの年間基本給は320,000ドルで、Macomberさんは適宜年間現金ボーナスを得る資格があり、その当時の基本給(“CFO目標金額”)の35%(“CFO年間ボーナス”)を目標としている。2023年3月、私たちの取締役会はMacomberさんの年間基本給を40万ドルに引き上げ、2023年4月2日から発効し、CFO目標を彼女の当時の基本給の45%に増やすことを許可した。Macomberさんが最高財務官年間ボーナスを獲得する資格があるかどうかは、伝説的な生物の表現、業務状況、および任意の適用可能なボーナス計画の条項に基づいて、取締役会報酬委員会が要求する範囲内で、取締役会または報酬委員会が最高経営責任者の提案に基づいて策定した業績目標の達成状況に基づいている。
雇用協定の条項によると、Macomberさんの雇用は自由であり、私たちはいつでも終わらせることができる。Macomberさんの雇用が理由なく終了された場合(雇用契約の定義に従って)、あるいはMacomberさんによって十分な理由(雇用合意の定義による)で終了された場合、Macomberさんは以下の解散費給付を受け、適用された源泉徴収税を差し引く資格があります(“CFO非CIC退職福祉”)
•通常の賃金支給手続きに従ってMacomberさんの現在の12ヶ月の基本賃金を支払います
•Macomberさんが退職する1年前に稼いだ年間ボーナスを支払い、解雇日までに支払われていない場合は、適用される会社の業績指標の実現状況に基づいて計算し、個人指標については、Macomberさんのその業績年度前の2年間の個人業績格付け平均値に基づいて計算する(“CFO前年ボーナス”)
•Macomberさんは、サービスまたは業績指標や格付けが確立または達成されたかどうかにかかわらず、終了日の年間目標金額のうち比例して計算された部分である(“最高財務官が比例して計算されたボーナス”);
•Macomberさんとその養育者が“コブラ法案”の下で12ヶ月に及ぶ持続健康保険の支払いまたは返済
•雇用契約を締結する際の既存株式奨励について、全額付与を加速する
•雇用契約を締結した後にMacomberさんに付与される可能性のある任意の持分奨励については、Macomberさんが退職した日後12ヶ月間に帰属すべき任意の持分奨励の部分を加速し、このような当時付与されていなかった持分奨励を直ちに付与し、業績に基づく要求を考慮することなく、完全に行使可能または没収できないようにしなければならないが、適用された会社の業績目標を実現することを前提としている
•株式オプションの終了後の行使期間は、Macomberさんの終了日から12ヶ月に延長されることができる
•国で認められているプロバイダが提供する再就職サービスまたは12ヶ月間の幹部研修サービス(“CFOトレーニングサービス”)。
雇用契約によると、マコーバーさんの雇用が伝説的な生物によって無断で中止された場合、あるいはマコーバーさんが十分な理由で退職した場合、コントロール権変更の発効日までの3ヶ月以内でもその後18ヶ月以内でも、マコーバーさんは以下の解散費給付を受け、適用される源泉徴収税を引く権利があります(“首席財務官の離職福祉”、非中投会社の離職福祉、“首席財務官退職福祉”)
•通常の給料手続きで18ヶ月分の現在の基本給を支払う
•最高財務官の前年のボーナスは、終了日に支払われていなければ
•CFOは比例してボーナスを支給する
•支払い終了日のその年のCFO目標額の1.5倍
•Macomberさんとその養育者が“コブラ法案”の下で18ヶ月に及ぶ持続健康保険の支払いまたは返済
•Macomberさんが所有していたすべての持分奨励の速度を速めなければならない。それは、このような当時付与されていなかった持分奨励が直ちに授与され、終了した日から業績に基づく要求を考慮することなく、完全に行使可能または没収できないようにすべきである
•引受または転換オプションの、株式オプション終了後の権利期間は、終了日から18ヶ月に延長される
•首席財務官コーチサービス部です。
最高財務官の退職福祉の支払いは、Macomberさんが署名し、私たちに有利な全面的なクレーム解除を含む退職協定を提出してくれることに依存します。雇用協定によると、Macomberさんが解雇されたり、Macomberさんが正当な理由なしに退職した場合、MacomberさんはいかなるCFO退職給付も受けないだろう。
賠償協定
ケイマン諸島の法律は、ケイマン諸島裁判所がこのような規定が公共政策に違反していると考えない限り、例えば民事詐欺や犯罪結果について賠償を提供するなど、会社の組織定款大綱や定款細則が高級管理者や役員に対して賠償を行う程度を制限していない。当社の組織規約では、当社は、当社の高級社員又は取締役がその職責、権力、権限又は適宜決定権を執行又は履行する際に招いた一切の訴訟、法的手続、費用、損失、損害又は責任を賠償するが、当該等の者の不誠実、故意の違約又は詐欺以外の理由により、又はその職責、権力、権限又は適宜決定権を実行又は履行する過程において、任意の費用、支出、支出を含む取締役又はその上級職員がケイマン諸島又は他の地方のいずれの裁判所においても当社又はその事務に関連する任意の民事訴訟について抗弁(成功するか否かにかかわらず)による損失又は責任。この行為基準は一般的にデラウェア州会社が許可するデラウェア州会社の行為基準と同じだ。
また、私たちは、組織規約に規定されている以外の追加賠償を提供するために、私たちのすべての役員や役員と賠償協定を締結しました。これらの合意に基づき,私らは役員や役員が取締役や当社幹部として招致を行うことで招いた何らかの法的責任や支出について,彼などに弁済することに同意することができる。
持分激励計画
株式購入計画
2017年12月2日、私たちの株主は、私たちの株式オプション計画、または株式オプション計画を承認し、この計画によれば、私たちの取締役会が承認すれば、条件を満たす参加者にオプションを付与することができます。株式購入計画の主な条項は以下の通り記載されている。
株式オプション計画は株式オプションの付与を規定しており,米国の参加者にとってはインセンティブオプションと非法定オプションを付与することで代表される.インセンティブオプションは私たちの職員たちと私たちの子会社の職員たちにしか与えられない。その他のすべてのオプションは、当社の従業員および取締役、Genscriptおよびその子会社の従業員および取締役に付与される可能性がありますが、適用される法律に適合しなければなりません。
初期株式購入計画の規模は20,000,000株であり、株式購入計画が承認された時の著者らの法定株式の10%に相当する。株式購入計画及び吾等が締結可能な任意の他の株式購入計画に基づいて、すべての授権及び行使されていない未行使の購入権を行使する場合、発行可能な普通株の総数上限は、当社の法定株式の30%を超えてはならない。任意の12ヶ月の期間内に、任意の参加者に購入権(行使された、解約および行使されていない購入権を含む)を行使して発行および発行される普通株式の総数は、一般に当社が発行した法定株式の1%を超えてはならない。
2022年12月31日まで、オプションは9,179,778株の普通株をカバーし、加重平均行権価格は
1株当たり流通株7.14ドル、3,041,266株普通株は依然として未来のオプション付与に用いることができる。
行政です。当社の取締役会は、当社の株式購入計画を管理し、それに株を購入する合資格者及び株式購入の時間を付与することを決定し、各購入持分の条項及び条件(購入持分規程の株式数、購入株権の使用価格(あれば)、及び購入持分が帰属及び行使可能な時間を含む)、購入持分の帰属又は行使を加速する時間、及び我々の株式購入計画及び当該計画に基づいて付与された株購入権の条項を解釈及び解釈する権利がある。Genscriptの取締役および従業員に付与されるいくつかの支出は、Genscriptの独立した取締役および/またはGenscriptの株主によって承認される必要があります。
選択肢です。株式購入計画によって付与された購入株の行使価格は、授出日の普通株の公平な市価を下回らない。株式購入計画条文に符合する場合、取締役会は株を購入する他の条項を決定し、任意の帰属及び実行可能性規定、株式購入使用価格の支払い方法、株式購入期限及びサービス終了後に引き続き株購入期間を行使することができる。
資本構造の変化。私たちの資本構造に特定のタイプの変化、例えば株式分割または逆株式分割が発生した場合、購入持分計画によって付与された各未行使株式購入に含まれる株式数および行使価格は適切に調整される。
計画は修正または終了する。取締役会はいつでも株式購入計画を改訂することができるが、Genscriptに適用される香港聯交所の上場規則及びいくつかの改訂規定に制限されなければならず、この等の改訂はGenscript株主の許可を得なければならない。いかなる改正も、以前に授出または許可された株式購入条項に悪影響を与えるように、一般に、当時購入持分計画によって授受された株式規約のすべての株式額面の少なくとも4分の3の承認を得なければならない。株式購入計画は2027年12月21日に終了し、その日までに取締役会で終了する可能性がある。
限定株インセンティブ計画2020限定株計画
2020年5月26日、我々の株主は、我々の2020年限定株式計画、すなわちRSU計画を承認し、この計画によれば、我々の取締役会が承認すれば、条件を満たす参加者に制限株式及び制限株式単位を付与することができる。以下にRSU計画の具体的な条項を示す.
RSU計画は制限株と制限株式単位(奨励と呼ぶ)を付与することを規定している。適用される法律により、当社の従業員、コンサルタント、取締役、Genscriptの他の子会社の従業員、コンサルタント、取締役が受賞する可能性があります。
RSU計画により付与されたすべての奨励により,発行可能株式総数の上限は11,000,000株である.2022年12月31日現在、発行された制限株式単位は、3,386,305株の普通株を含み、7,613,695株の普通株は、将来的にRSU計画に従って付与することができる。
行政です当社の取締役会又はその報酬委員会(管理人)は、当社のRSU計画を管理し、奨励を受ける資格者及び時間、各奨励を決定する条項及び条件(奨励を受けるべき株式数及び奨励付与時間を含む)、奨励が付与可能な時間を速める権利があり、我々のRSU計画の条項及びその計画に基づいて付与された奨励を解釈及び解釈する権利がある。
資本構造の変化私たちの資本構造に特定のタイプの変化、例えば株式分割または逆株式分割が発生した場合、発行可能な株式総数およびタイプ、任意の未完了報酬の条項および条件(任意の適用可能な業績目標または基準を含むがこれらに限定されない)、および任意の未完了報酬の付与または使用価格が適切に調整される。
修正または終了管理人は、RSU計画を終了、修正、または修正することができるが、条件は、(A)適用法または証券取引所規則を遵守するために必要かつ適切な範囲内で、会社が必要な方法および必要な程度で株主の任意の修正の承認を得なければならないことであり、会社が母国のやり方に従うことを決定しない限り、(B)会社が母国のやり方に従うことを決定しない限り、RSU計画の任意の修正(I)株式数を増加させるには株主の承認を得る必要があるということである
(Ii)補償委員会がRSU計画の期限を延長することを可能にするか、または(Iii)福祉の大幅な増加または資格要件の変化をもたらす。一般に、参加者が事前に書面で同意することなく、RSU計画の終了、修正、または修正は、RSU計画によって以前に付与された任意の賞に実質的な悪影響を与えてはならない。
C.取締役会の慣例
取締役会
私たちの取締役会は十人の役員で構成されています。取締役は取締役になる資格があるためにわが社のどの株式も持つ必要はありません。取締役は、彼または彼女の利害関係のある任意の契約または任意の提案された契約または予定投票について投票することができ、もし彼または彼女がそうした場合、彼または彼女の投票は計算されなければならず、彼または彼女は、そのような契約または提案された契約または手配を審議する任意の取締役会議に定足数を計上することができ、条件は、(A)当該取締役が最初に契約または手配を締結することを考慮した取締役会会議でその利益の性質を声明しており、もし彼または彼女が当時彼または彼女の利益の存在を知っていた場合、または(B)契約または手配が関連者との取引である場合、取引は監査委員会によって承認された。取締役は、会社が調達又は貸借した金、住宅ローン又は押記その業務、(既存又は将来の)財産資産及び未納株式又はその任意の部分のすべての権力、並びに債権証、債権株式証、債券又はその他の証券を発行することができ、直接又は会社又は任意の第三者としての任意の債権、債務又は義務の付属保証を行使することができる。私どもの非執行役員はいずれもサービス契約を締結していません。このサービス契約はサービス終了時の福祉を規定しています。ナスダックの上場要求に従って、海外私募発行者として、私たちは母国の管理要求及びその下のいくつかの免除に頼ることができ、ナスダックの管理要求に頼るのではない。しかし、私たちの取締役会は役員の独立性を検討した。各取締役の要求及び提供された取締役の背景、雇用状況及び関係(家族関係を含む)に関する資料によると、当社取締役会は、取締役10名のうち6名が米国証券取引委員会及びナスダック現行規則で定義されている“独立取締役”とすることを決定した。このような決定を下す際に、私たちの取締役会は、どの取締役が私たちと実質的な関係があるかどうかを考慮しており、彼らが職責を履行する際に独立した判断能力を行使することに影響を与える可能性がある
ナスダック上場規則によると、1社の投票権の50%以上を1つのエンティティが保有する会社は“持株会社”とみなされている。制御された会社は、取締役会に過半数の独立取締役がいなければならないか、または完全に独立した報酬、指名、およびコーポレートガバナンス委員会を有することを要求するナスダックのコーポレートガバナンス規則を遵守する必要はない。ナスダック上場規則の定義によると、私たちは“持ち株会社”です。
私たちは“制御された会社”免除に依存し続けています。私たちは多数の独立した役員を持つ必要はありません。私たちの報酬委員会と私たちの指名と会社管理委員会は完全に独立した取締役で構成される必要はありません。これらの委員会は年間業績評価を受ける必要もありません。したがって、あなたはすべての証券取引所の規則に制約された会社の株主によって同じ保護を受ける必要はありません。外国の個人発行者と制御された会社の免除は、監査委員会の独立的な要求を修正しないだろう。
役員の職責
ケイマン諸島の法律によると、私たちの役員は私たちの最高の利益を実現するために、誠実で誠実な行動の受託責任を持っている。私たちの役員も、彼らが実際に持っているスキルを行使する責任があり、かなり慎重な人が似たような状況で慎重で勤勉であることを示しています。私たちに対する注意義務を履行する際には、私たちの取締役は、私たちが改訂し、再記述した組織定款大綱と定款細則を遵守することを確実にしなければならない。もし私たちの役員の責任が違反されたら、株主は損害賠償を請求する権利があります。
当社の取締役会の職権には、以下のようなものがある
•当社の業務を経営·管理する
•契約と取引で私の会社を代表します
•私の会社に弁護士を指名した
•上級管理職を選抜する
•従業員の福祉と年金を提供します
•会社の財務と銀行口座を管理します
•最高経営責任者の業績を評価し、その報酬水準を決定する
•当社の借金権力を行使し、当社の財産を抵当に入れる
•株主総会又は当社が改訂及び再記載された組織定款大綱及び細則に付与された任意の他の権力を行使する。
役員および行政職の任期
我々が改訂·再記述した組織定款大綱と定款細則によると、我々の取締役会は3つのカテゴリに分類され、各カテゴリは可能な限り取締役会全体を構成する取締役総数の3分の1で構成され、3年間の任期をずらす。毎回の株主周年大会において、任期満了の取締役後継者の任期は、当選と取締役資格取得日から、選挙後の第3回年次会議で後継取締役を選出して取締役資格を得るまで、または取締役が以前に免職、辞任または死去するまでである。私たちの取締役は以下の3つに分類されます
•第一に、王野、季暁慧、Huang、トーマス?ハイマンからなり、任期は2024年に我々の年次株主総会で満了する
•2つ目はパトリック·ケイシー遊恵民張方亮で構成されています2025年に私たちの年間株主総会で任期が満了します
•第三に,Li·朱,コラゾン·D·サンダースとLi·毛からなり,彼らの任期は2023年に我々の年次株主総会で満了する。
我々が改訂·再記述した組織定款大綱と定款細則の規定は、取締役会の多数のメンバーが承認した決議を通過して初めて、許可された取締役数を変更することができる。取締役数の増加により増加した任意の取締役職は、各レベルが可能な限り3分の1の取締役で構成されるように、この3つのレベルに割り当てられる。
私たちの取締役会は3つのレベルに分かれており、3年間の任期を交錯させ、私たちの経営陣の交代や統制権の変更を延期または阻止する可能性があります。
取締役は、以下の場合、取締役ではなくなる:(一)破産または債権者とのいかなる手配または和解、(2)精神的に不健全であることが発見されたこと、(3)会社の辞任を書面で通知すること、(4)特別な許可を受けずに取締役会会議を欠席すること、(3)3回連続して取締役会会議を欠席し、取締役会決議を罷免すること、(5)第3回改正及び回復定款の他の規定により免職されること。あるいは(Vi)任意の法律や成文法則の任意の条文に基づいて命令される.私たちの官僚たちは取締役会選挙によって選出され、取締役会によって適宜決定される。
取締役会と管理委員会
私たちの取締役会は監査委員会、報酬委員会、指名、そして会社管理委員会を設立した。私たちはすべての委員会の規定を採択した。各委員会のメンバーと機能は以下のとおりである。 さらに実行委員会を立ち上げました会社の業務及び運営に関する意思決定について、会社行政総裁に意見を提供する。
監査委員会
私たちの監査委員会は季暁慧、コラソン·D·サンダース、遊維民フィリップで構成されている。邱さんは我々の監査委員会の議長である.邱さんは、米国証券取引委員会の適用規則に規定されている監査委員会の財務専門家基準を満たしている。セダン博士、サンダース博士、チュンテン華さんは、上場規則第5605条(A)第2条に記載されている独立ナスダック条件を満たし、取引所法第10 A−3条に記載の独立基準を満たしています。
監査委員会は私たちの会計と財務報告の流れと私たちの財務諸表の監査を監督する。他の事項を除いて、私たちの監査委員会は責任を負う
•独立監査人を選択し
•独立監査人が従事することを可能にする事前承認監査および非監査サービス
•独立監査人の報告を毎年審査し、監査会社の内部品質制御プログラム、最近の独立監査師の内部品質管理審査または同業者審査で提起された任意の重大な問題、独立監査師とわが社とのすべての関係を説明する
•内部監査機能の職責、予算、報酬、および人員構成を検討する
•独立監査人と共に任意の監査問題や困難、および経営陣の対応を検討する
•進行中のすべての関連者取引を検討して承認する
•管理職および独立監査人と年次監査された財務諸表を審査し、検討する
•経営陣と独立監査人と会計原則と財務諸表の列報に関する主要な問題を審査し、討論する
•経営陣または独立監査員が重大な財務報告問題と判断について作成した報告書を審査する
•経営陣と収益プレスリリースを検討し、アナリストや格付け機関に提供する財務情報と収益指針
•管理職や独立監査人と一緒に規制と会計措置および表外構造が私たちの財務諸表に与える影響を検討する
•経営陣や内部監査人とリスク評価とリスク管理に関する政策を検討した
•当社が使用するすべての重要な会計政策および慣行に関する独立監査人の報告、国際財務報告基準で管理層と議論されるすべての財務情報の代替処理方法、および独立監査人と管理職との間の他のすべての書面コミュニケーション材料を適時に検討します
•私たちの従業員から受け取った会計、内部会計制御または監査事項に関する苦情、および私たちの従業員が問題のある会計または監査事項について提出した秘密、匿名提出の懸念を受信、保留、処理するためのプログラムを確立する
•取締役会が監査委員会に不定期に処理を依頼した他の事項
•管理職、内部監査人、独立監査人と定期的に会議を開く。
報酬委員会
私たちの報酬委員会は季暁慧、コラソン·D·サンダース、王葉で構成されている。季昇林博士は私たちの報酬委員会の議長だ。季博士およびサンダース博士はいずれも“取締役上場規則”第5605(A)(2)条で指摘されている“独立ナスダック”の条件を満たしている。
他の事項を除いて、私たちの報酬委員会は責任を負う
•私たちの全体的な報酬政策を検討し、評価し、必要に応じて修正します
•役員と関連高級管理者の業績を審査·評価し、関連高級管理者の報酬を決定する
•私たちの高官との採用協定を審査して承認します
•私たちの奨励的な報酬計画と株式に基づく報酬計画に基づいて、関連する高級管理者のための業績目標を設定します
•条項に基づいて私たちの株式報酬計画を管理し、
•取締役会は給与委員会に処理を委託する他の事項を定期的に明確にしない。
指名と会社管理委員会
私たちの指名と企業管理委員会は王野、遊恵民、そしてパトリック·Caseyで構成されている。
王さんは私たちが指名して会社統治委員会の議長です。
他の事項を除いて、指名と会社管理委員会が責任を負う
•指名者を選抜して取締役会に推薦し、株主選挙または取締役会が任命する
•毎年私たちの取締役会と一緒に私たちの取締役会の現在の構成を審査して、独立性、知識、技能、経験と多様性などの特徴を含む
•取締役会会議の頻度と構造について提案し、取締役会の各委員会の運営を監督する
•定期的に会社ガバナンスの法律と実践の重大な発展及び私たちの法律と法規の遵守状況について私たちの取締役会に提案し、すべての会社の管理事項と任意の必要な救済行動について取締役会に提案します。
実行委員会
2022年8月に実行委員会を設立しました会社の業務及び運営に関する意思決定について、会社行政総裁に意見を提供する。実行委員会は会社の最高経営責任者であるHuang博士、会社の財務責任者のローリー·マッコンバー博士、会社の副総裁兼総法律顧問のマーク·ハリソン、会社の技術運営高級副総裁のリーズ·ゴソンと会社の首席科学官兼業務発展主管の方国偉博士から構成されている。
取締役会の多様性
次の表は、本年度報告日までの取締役会の多様性に関するいくつかの情報を提供します
| | | | | | | | | | | | | | |
| 取締役会-多様性-マトリックス |
| 役員総数 | 10 |
| 女性は | 男性 | -ではない 2桁上げ | ありません
開示する
性別 |
| 第1部:性別同意 | |
| 役員.取締役 | 2 | 8 | 0 | 0 |
| | | | |
第2部:以下のいずれかのカテゴリーの取締役数: |
| アフリカ系アメリカ人や黒人 | 0 | 0 | 0 | 0 |
| アラスカ原住民あるいは原住民 | 0 | 0 | 0 | 0 |
| アジア人 | 2 | 6 | 0 | 0 |
| スペイン系やラテン系 | 0 | 0 | 0 | 0 |
| ハワイ先住民や太平洋島民 | 0 | 0 | 0 | 0 |
| 白 | 0 | 2 | 0 | 0 |
| 2つ以上の人種や民族 | 0 | 0 | 0 | 0 |
| LGBTQ+ | 0 |
| 障害者 | 0 |
2022年3月31日までの取締役会の多様性に関する情報は、2021年12月31日までの年次報告Form 20−Fの第1号改正案を参照されたい。
D.従業員
2022年12月31日現在、私たちには約1,390人の従業員がおり、そのうち136人が博士号および/または医学学位を持っている。この約1390人の従業員のうち、305人が研究·開発活動に従事し、残りは業務開発、財務、情報システム、施設、人的資源、行政支援、または他の業務機能に従事している。私たちのすべての職員たちは集団交渉協定の制約を受けない。私たちは私たちが従業員と仲がいいと思う。
表示された日付ごとに、以下のような数の従業員が行政や研究開発に従事しています。
| | | | | | | | | | | |
| 12月31日まで |
| 2022 | | 2021 |
| 機能: | | | |
| 一般と行政 | 175 | | 121 |
| 研究開発 | 305 | | 371 |
| 販売とマーケティング | 57 | | 60 |
| 他の人は | 850 | | 519 |
| 合計する | 1,387 | | 1,071 |
| 地理的位置: | | | |
| アメリカです | 739 | | 475 |
| アジア太平洋 | 563 | | 582 |
| ヨーロッパ.ヨーロッパ | 85 | | 14 |
| 合計する | 1,387 | | 1,071 |
E.株式所有権
当社取締役及び上級管理職の持株状況については、“6.B項取締役、上級管理者及び従業員の報酬”及び“7.A項大株主及び関連側取引である大株主”を参照されたい
項目7.大株主と関連者取引
A.大株主
2022年12月31日までに、330,134,480株の普通株流通株があります。特に明記されている以外に、2022年12月31日までの私たちの普通株式の実益所有権情報を以下の表に示します
•私たちの役員や幹部は
•全体として私たちのすべての役員と行政は
•私たちが知っているすべての実益は私たちの普通株の5%以上を持っている
別の説明がない限り、表に記載されている人員の営業住所は伝奇生物会社であり、住所はニュージャージー州サマセット郡綿尾巷2101号、郵便番号:08873である
米国証券取引委員会の規則と規定に基づいて受益権属を決定する。ある人の実益所有株式数とその人の所有率を計算する際には、任意のオプションの行使、株式承認証、または他の権利の転換、または任意の他の証券を含む、2023年1月31日から60日以内に取得する権利を有する株式を計算する。しかし、このような株式は他の人の所有権パーセンテージ計算に含まれていない。
| | | | | | | | | | | |
| 普通数量 実益株 持っている | | パーセント 株 有益な 持っている |
5%以上の株主: | | | |
キングスレー生物技術は(1) | 174,497,556 | | 52.9 | % |
AquaPoint L.P(2) | 30,320,000 | | 9.2 | % |
FMR有限責任会社(3) | 30,283,156 | | 9.2 | % |
高槻投資管理有限公司(4) | 20,273,234 | | 6.1 | % |
管理職と役員: | | | |
Huang、博士。(5) | 75,316 | | * |
Lori Macomber M.S.(6) | 111,878 | | * |
張方亮、博士。(7) | 1,067,386 | | * |
Ye(サリー)Wang M.S(8)(2) | 16 | | * |
季暁慧医学博士博士(9) | 31,376 | | * |
コラソン·D·サンダース博士(10) | 31,376 | | * |
邱偉民会計士(11) | 31,376 | | * |
Li·朱博士 | — | | * |
パトリック·キャシー博士(12) | 19,960 | | * |
| Li、医学博士 | — | | * |
| トーマス·ハイマン | — | | * |
すべての現執行幹事と役員(11人) | 1,368,684 | | * |
*実益を代表して私たちの総流通株の1%未満の株式を持っています。
1.これらの情報は、2022年2月14日に米国証券取引委員会に提出されたキングスレー生物科学技術の付表13 G/Aに完全に基づいており、2022年12月31日までの利益所有権を報告している。別表13 G/A報告は、この等持株には、(I)2020年6月に初公開発売を完了する前にGenScripが保有する169,680,000株の普通株、(Ii)吾等の初公開発売と同時に完了した私募取引でGenScripに発行された1,043,478株普通株、および(Iii)2021年12月に完成した後続発売に等しいために購入した2,250,000株米国預託株式を含み、725,922株普通株を減少させ、香港連結所規則に従って株主に普通株を割り当てることを指す。Genscriptの住所はケイマン諸島ケイマン諸島KY 1-1002大ケイマン諸島郵便ポスト10240ポスト南教堂街103番地ハーバープラザ4階です
2.これらの情報は、AquaPoint L.P.が2022年2月14日に米国証券取引委員会に提出された13 G/A付表に完全に基づいており、同社は2022年12月31日までの利益所有権を報告している。付表13 G/Aは、これらの株式には、AquaPoint L.P.が保有する30,320,000株の普通株が含まれていると報告している。AquaPoint L.P.の住所は、ケイマン社センター、病院路27号、郵便ポスト1748号、ジョージ城KY 1-1109、ケイマン諸島である。AquaPoint L.P.-FSD 157 of 220610(DDJ)事件に関するケイマン諸島大法院(“裁判所”)の判決(“裁判所”)によると,AquaPoint L.P.は裁判所が指定した共同公式清算人の監督の下で清盤を行っている.したがって,清算が完了する前に,AquaPointの判決により,AquaPoint L.P.登録所有者である30,300,000株の普通株のすべての投票権と処分権は連合公式清算人が所有する.AquaPoint L.P.の住所はR&H Trust Co.Ltd.,郵便ポスト897,向風1号,漕艇会事務公園,大ケイマン諸島西湾路,KY 1−1103,ケイマン諸島である。
3.本情報は,FMR LLCとそのある子会社と付属会社が2022年2月9日に米国証券取引委員会に提出した付表13 Gに完全に基づいており,FIAM LLC,IA,Fidelity Institution Asset Management Trust Company BK,Fidelity Management&Research Company LLC*IA,Fidelity Management Trust Company BK(総称してFMR記者と呼ぶ)を含み,2022年12月30日までの実益所有権を報告している。付表13 G報告によると、FMR記者は30,283,156株の普通株に対して唯一の投票権と処分権を持っている。FMR記者の住所はマサチューセッツ州ボストンSummer Street 245号、郵便番号:02210。アビゲイル?P?ジョンソンは取締役の一員であり、FMR LLCの会長兼最高経営責任者でもある。アビゲイル·P·ジョンソンを含むジョンソン家族のメンバーは、FMR LLC Bシリーズ議決権普通株の主要所有者であり、FMR LLC投票権の49%を占めている。ジョンソンファミリーグループと他のBシリーズ株主はすでに株主投票合意に達しており、この合意によると、すべてのBシリーズの投票権のある普通株は、Bシリーズの投票権のある普通株の多数票で投票される。したがって,1940年の“投資会社法”によると,投票権のある普通株と実行株主投票合意により,ジョンソンファミリーのメンバーはFMR LLCに関するホールディンググループを構成していると見なすことができる。
4.本情報は,高槻投資管理有限公司(以下HOM)が2022年2月14日に米国証券取引委員会に提出した13 G/A付表のみに基づいており,2022年12月31日現在の実益所有権を報告している。付表13 G/Aは、HHLR Advisors,Ltd.が保有する1,400,000株の普通株式およびLGN Holdings Limited(“LGN”)が保有する18,873,234株の普通株式(10,000,000株関連株式承認証を含む)を含むことを報告している。LGNはHillhouse Investment Management V,Ltd.が全額所有しており,後者の唯一の株主はHillhouse Fund V,L.P.(“ファンドV”)である.基金Vは彼が管理する。彼が管理する基金。彼はLGNの持つ普通株の唯一の実益所有者とみなされ,その普通株の投票権および投資権を完全に制御している.HHLR Fund,L.P.(“HHLR”)はHHLR FundおよびYHG Investment,L.P.(“YHG”,彼,LBN,HHLRおよびHHLR Fund,“高報告者”)とともにそれぞれ唯一の投資管理人を務めている。HHLRはここでHHLR FundとYHGが持つ普通株の実益所有者とみなされ,その投票権と投資権を制御する.HHLRとHISは共同制御下にあり、いくつかの政策、人員、資源を共有する。各高報告者の住所はケイマン諸島大ケイマン諸島西湾路漕艇会事務公園迎風3号棟122番オフィス、郵便番号:KY 1-9006
5.Dr.Huangが直接保有する5,653株の米国預託証券(11,306株普通株に相当)からなる。Dr.Huangはこれに対して処分権を持っているが投票権はない2023年4月1日までに行使可能な32,005株の米国預託証券(64,010株普通株に相当)を買収するオプションも含む。
6.Macomberさんが直接保有する7,606株の米国預託証明書(15,212株普通株に相当)からなる。また,2023年4月1日までに行使可能な48,333株の米国預託証券(96,666株普通株に相当)を購入するオプションも含まれており,マッコバーはこれに対して処分権を持っているが,投票権はない。
7.1,067,386株から2023年1月31日までの普通株からなり、張博士は撤回不可能な依頼書に基づいて当該等普通株に対して投票権を有し、この委託書は当該等普通株発行に基づく購入権行使後に発効し、その登録所有者が公開市場販売中に売却した当該等普通株について終了する。張勇は香港証券取引所上場会社の金斯瑞生物科学技術の株主であるが、金斯瑞生物科学技術が持っている普通株に対して投票権や処分権はない。AquaPoint L.P.を含まない30,300,000株の普通株
すべての人(“AquaPoint株式会社”)を登録することです。AquaPoint社が清算を完了する前に、AquaPoint社の判決によると、AquaPoint社の株に関するすべての投票権と処分権は共同公式清算人が持っている。清算が完了すると、張博士はAquaPointの株式を実益することはないだろう。注釈2を参照されたい。
8.家族信託により,王さんとその家族はAquaPoint L.P.32.98%の株式を保有しており,AquaPoint L.P.の一般パートナーは我々の大株主キングスレー生物科学技術の筆頭株主Genscript Corporationである。王雪紅はAquaPointの株に対して投票権や処分権を持っていない。AquaPoint社が清算を完了する前に、AquaPoint社の判決によると、AquaPoint社の株に関するすべての投票権と処分権は共同公式清算人が持っている。注釈2を参照されたい。
9.季博士が直接保有している9,688株の米国預託証明書(19,376株普通株に相当)からなる。2023年4月1日までに行使可能な6,000株の米国預託証券(12,000株普通株に相当)のオプションも含まれており、紀万昌はこれに対して処分権を持っているが、投票権はない。
10.サンダース博士が直接保有する9,688株の米国預託証明書(19,376株普通株に相当)からなる。サンダースは2023年4月1日までに行使可能な米国預託証券6000株(1.2万株普通株に相当)を買収するオプションも含み、サンダースは処分権を持っているが、投票権はない。
11.邱さんが直接保有している米国預託証券9,688株(普通株式19,376株に相当)を含む。また、2023年4月1日に行使可能な米国の保有株式6,000株(普通株式12,000株に相当)の買収オプションも含まれており、特にさんなどは処分権を保有しているが投票権はない。
12.Casey博士が直接保有している6,845株の米国預託証明書(13,690株普通株に相当)からなる。2023年4月1日までに行使可能な3,000株の米国預託証券(6,000株普通株に相当)のオプションも含まれており、キャシー博士は処分権を持っているが、投票権はない。
私たちの主要株主は他の株主とは違う投票権を持っていない。
2022年12月31日現在、私たちの発行済み普通株(米国預託証明書形式の普通株を含む)のうち130,007,028株は登録されている3つの保有者が保有しており、2022年12月31日現在の私たちが発行した普通株の39.4%を占めていると推定される。実際の保有者数は、その普通株式または米国預託証明書がブローカーおよび他の著名人によって街頭名義で保有されている実益所有者を含むこれらの記録保持者数を超える。この数の登録所有者には、その株式が他のエンティティが信託形式で保有する可能性のある所有者も含まれていない。
B.関係者取引
以下は、私たちが2022年1月1日から締結または参加した関連側取引の説明であり、これらの取引において、私たちの当時の任意の取締役、役員、または取引時に5%を超える投票権を有する証券の任意のカテゴリの所有者、または彼らの任意の直系親族が、直接的または間接的な重大な利益を有することになる。
我々の大株主Genscriptとの取引は
GenScripは私たちの大株主で、2022年12月31日現在、約52.9%の発行済み普通株を持っています。以下にGenscriptと達成した他の取引の概要を示す.我々の業務戦略の発展と実行にともない,Genscriptが提供できる資源や専門知識を利用することができるGenscriptとの類似や他の取引を継続していく可能性が予想される.我々が将来的にGenscriptと達成した任意の取引は、以下に述べる関連者取引ポリシーに従って評価され、承認されるであろう。
主な製品、サービス、関連協定
主製品とサービス契約
伝説的生物米国社は2022年10月1日、GENSCRIPTの子会社GENSCRIPT米国社と主製品·サービス協定(“マスタ·サービス協定”)を締結した。すべての材料とサービス
我々(我々の任意の子会社を含む)は、通常の業務中にキングスジャー(その任意の連結会社、レジェンド生物及び当社の子会社を除く)から購入した(伝説生物とキンスジャーとの間の他の合意に従って購入された任意の関連サービス又は材料を含む)は、主製品及びサービス契約の範囲に属し、その制約を受ける。これらのサービスおよび材料は、(I)遺伝子合成、プラスミド調製、オリゴマー合成、ポリペプチド、タンパク質発現、試薬抗体、GMPプラスミドおよびウイルスベクター、生物学的発見および開発、および他のカスタマイズサービスに関連するサービス、および(Ii)タンパク質検出および細胞分離および活性化に関連する材料を含む。双方は、“主製品及びサービス契約”の下の個別作業説明書に基づいて追加製品及びサービス契約を締結することができる。2022年の間に,我々は本プロトコルによる費用のために約150万ドルを積算した.マスタ製品およびサービスプロトコルの初期期限は1年であり、いずれか一方が早期に終了しない限り、最大2つの追加の1年間期間を自動的に延長する。協定によると、伝説的な生物の1日当たりの購入総額は730万ドルを超えてはならない。
研究開発技術サービス協定
2020年1月、南京連想と遺伝子科学技術(“南京遺伝子”)の子会社南京遺伝子生物科学技術有限会社は技術サービス協定を締結し、協定によると、遺伝子遺伝子はDNAシークエンシング、オリゴヌクレオチド合成、遺伝子合成、プラスミド調製及びその他の分子生物学技術サービスを含む研究開発活動の材料準備に関連するサービスを提供する。本プロトコルは2022年10月1日にメイン製品とサービスプロトコルに置き換えられ、その後、メイン製品とサービスプロトコルに従ってこれらのサービスが実行されます。2022年には、“主製品·サービス協定”が発効する前に、本協定の下の金を支払うために約260万ドルの支出を累計した。
化学、製造、制御プロジェクト
2021年11月、南京聯想と遺伝子科学技術の子会社である江蘇遺伝子生物科技有限公司は技術サービス契約を締結し、この契約に基づいて、遺伝子遺伝子はプラスミドとレンチウイルスベクターに関連する化学、製造と制御(CMC)サービスを提供する。本プロトコルは2022年10月1日にメイン製品とサービスプロトコルに置き換えられ、その後、メイン製品とサービスプロトコルに従ってこれらのサービスが実行されます。2022年には、“主製品·サービス協定”が発効する前に本協定に基づいて支払われた金のために、累計約900,000ドルを支出します。
国際製品供給と物流サービス協定
2022年2月、南京レノボとキングスッド(“キングスッド米国”)の子会社キングスッド米国社は年間調達協定を更新し、この合意に基づき、キングスッドは試薬、酵素、キット、媒体、ヌクレオチド、消耗品および研究開発活動のための商業化細胞、身体組織と血清および関連する国際物流サービスを提供してくれた。本プロトコルは2022年10月1日にメイン製品とサービスプロトコルに置き換えられ、その後、メイン製品とサービスプロトコルに従ってこれらのサービスが実行されます。2022年には、主製品およびサービス協定が発効する前に本協定に基づいて金を支払うために、累計約500,000ドルを支出します。
主サービス協定
2020年1月、伝説生物アメリカ会社は遺伝子スクリプトアメリカ会社とメインサービス契約を締結し、このプロトコルによると、著者らは遺伝子スクリプト会社から試薬と消耗材を購入し、遺伝子スクリプト会社は私たちにいくつかの遺伝子配列測定サービスを提供してくれた。本プロトコルは2022年10月1日にメイン製品とサービスプロトコルに置き換えられ、その後、メイン製品とサービスプロトコルに従ってこれらのサービスが実行されます。2022年には、“主製品·サービス協定”が発効する前に、本プロトコルの下の金の支払いに約300,000ドルの費用を積算しました。
ProBio独占許可協定
吾らは南京ProBio Biotech株式会社(“ProBio”)と2021年8月18日に独占許可協定を締結し、この合意に基づき、吾らはProBio及びその共同所属会社に特定の特許及び関連技術下の独占許可を付与し、ProBioが吾等に150万ドルの支払いとその合意日から2年間以内にCDMOサービスの形で吾等に150万ドルのCDMOサービスを提供することに同意した。この協定によると、ProBioはProBioによって生成された任意の収入のために10.0%の印税を支払う責任がある
ProBioはこのような特定の特許と関連したノウハウを第三者に再許可する。2022年の間に,本プロトコルにより約33万ドルの特許使用料収入を確認した
“政務サービス協定”
二零二年一月、レノボ南京支社が設立され、Genscript南京社と政府事務サービス枠組み協定を締結し、合意に基づいて、Genscriptは政府機関及び機関との関係の構築と維持、政府支出の申請、及び中央管理の政府事務に対する協力、コンサルティング及び支援サービスを提供する。この協定の予定期限は2025年12月である。2022年の間,我々は本プロトコルによる費用のために約140万ドルを積算した.
サービスに応じて協議する
2020年1月、南京聯想と金斯捷南京公司は代理支払い協定を締結し、この合意に基づき、連想南京は伝奇生物と金斯捷に同時にサービスを提供するいくつかのサプライヤーに南京聯俊達を代表して支払った金を支払った。これらのサービスには、国内運航、エンジニアリング保守、ソフトウェア許可(マイクロソフトの企業ソフトウェア許可を含む)、電気代および廃棄物費、ITサービス、郵便サービス、人的資源訓練、安全、セルフサービス、およびその他の関連サービスが含まれています。この協定の予定期限は2025年12月である。2022年の間に,我々は本プロトコルにより累計約175万ドルの費用を支払い,そのうち約525,000ドルはマイクロソフトの企業ソフトウェアライセンスに関係している.
ITサービス協定
伝奇生物アメリカ有限公司、伝奇生物アイルランド有限公司と南京伝奇生物有限公司はそれぞれGenscriptの子会社と情報技術支援と応用関連支援サービス協定に調印した。2022年の間に,我々は本プロトコルによる費用のために約13万ドルを積算した.これらの協定のすべては2022年9月から12月までの間に終了または満了する。
施設
ビスカットウェイ伝説的生物米国会社はテナントとして、Genscript USA Holdings,Inc.と2022年1月1日から発効し、ニュージャージー州ピスカタビルに約22,000平方フィートの施設を建設する賃貸契約を締結した。レンタル契約によると、Genscriptに以下の金額のレンタル料を支払うことに同意しました。2022年、毎月35,844ドル、2023年、毎月36,919ドルです。さらに、(I)建物およびその周囲地域に対する不動産税、(Ii)死傷および責任保険、(Iii)清掃、景観美化、除雪、および同様の費用の分配を含むGenscript公共地域維持費用の支払いに同意した。私たちは、レンタル契約の12ヶ月前に毎月Genscriptに18,589.39ドルを支払い、レンタルプロトコルの後の12ヶ月に毎月19,309.11ドルを公共エリアメンテナンス費用の予定として支払うことに同意しました。これらの支払いは実際の公共地域維持費用と年間精算され、伝説的な生物が要求する任意の追加支払いはこれらの計画支払いの最高20%を超えない。本賃貸契約は2023年12月31日に満了します。条件は、レンタル契約を2年間延長することを選択できることです。
動物施設レンタルとサービス契約-Genscript南京社と締結した動物施設レンタル契約の一方です 私たちは南京で1,000平方メートルの動物飼育場をレンタルした。中国では、費用は約51,000元/月(7,393ドル/月、人民元6.9元の1ドルに対する換算率、すなわち2022年12月31日の為替レート)(付加価値税を含む)に基づいている。レンタル契約は2025年6月に満期になります。 また、私たちは2021年4月に金斯傑南京会社と動物技術サービス協定を締結し、2022年1月にこの協定を更新し、この協定に基づいて、キングスダー南京会社は私たちに施設運営、動物調達、検疫、動物飼育と看護及び動物試験コンプライアンスサービスを提供してくれた。動物技術サービスプロトコルによると,2022年の間にGenscriptに約120万ドルを支払い,このプロトコルの予定期限は2024年12月31日である
ダブリン2018年、Tango Medc SLUと賃貸契約を締結しました。この協定によると、アイルランドダブリンで約8,300平方フィートの施設をレンタルし、毎月約13,000ユーロ(ユーロ)の費用をかけています。本レンタル期間は2018年8月から2028年8月までです。GenScripは私たちのこのレンタル契約の義務を保証した。
ROFRと共同販売プロトコル
2020年3月と2020年4月に、新規投資家に1株7.792ドルで合計20,591,629株のAシリーズ優先株を発行·売却し、総収益は1兆605億ドルだった。Aシリーズ優先株の売却については,2020年3月30日にGenscript,AquaPoint L.P.と新投資家と優先購入権と共同販売契約を締結した。合意によれば、GenscriptおよびAquaPoint L.P.(I)優先購入権を付与して、潜在的譲受人に提示された同じ価格および同じ条項および条件で譲渡された普通株と、(Ii)新投資家第2優先購入権を提案して、優先購入権に従って購入されなかった吾などの普通株の全部または一部を購入することを提案することができる。新しい投資家が権利を二次的に拒否させることができない場合、その投資家は同じ条項と条件でこのような販売に参加する権利がある。
役員および行政に株式引受権を付与する
私たちは私たちの特定の役員と幹部に株式オプションを授与した。取締役および指定役員に付与された株式オプションについては、“6.B.取締役、上級管理職、および従業員の報酬--取締役および役員の報酬”を参照されたい。“プロジェクト6.B役員、上級管理職、従業員--報酬--雇用契約、賠償協定”
雇用協定と賠償協定
私たちは私たちのすべての幹部と雇用協定を締結し、私たちのすべての幹部と役員と賠償協定を締結しました。より多くの情報は“プロジェクト6.B.取締役、上級管理者、従業員--報酬--雇用協定と賠償協定”を参照されたい
関係者取引の政策と手順
2020年5月27日、関連者取引の識別、審査、承認または承認のための政策·手順を規定する関連者取引政策を採択した。本保険証書は、関連者または関係者から商品やサービスを購入または関連者に購入することを含む、吾らおよび関係者がかつてまたは参加する任意の取引、手配または関係をカバーしており、当該関係者は、当該等の取引、手配または関係において重大な権益、債務および債務保証を有しているが、証券法の下でS-K条例第404項に規定されているいくつかの例外を除く。私たちの監査委員会の定款は、監査委員会は、関連者の取引を審査し、承認するか、または承認しないと規定している。そのような取引を審査及び承認する際には、我々の監査委員会は、取引の目的、他の出所の同種製品又はサービスの有無、取引の条項が公平な取引の条項と一致しているか否か、管理層が提案した関係者取引に対する提案、及び関係者の取引における権益の程度など、すべての関連事実及び状況を適宜考慮する。
C.専門家と弁護士の利益
適用されません。
項目8.財務情報
A.連結報告書およびその他の財務情報
“プロジェクト18財務諸表”をご覧ください
法律と行政訴訟
私たちは時々様々な請求と、私たちの業務に関連した請求の法的手続きを扱うかもしれない。私たちは現在、私たちの経営陣が私たちの業務に重大な悪影響を及ぼす可能性があると思う法的手続きに参加していません。結果にかかわらず,弁護や和解コスト,管理資源分流などにより,訴訟は我々に悪影響を与える可能性がある。
配当政策
当社の取締役会は配当金を派遣するかどうかを適宜決定する権利がありますが、当社が改訂及び再記述した組織定款の大綱及び細則、及びケイマン諸島の法律のいくつかの規定を遵守しなければなりません。また、私たちの株主は一般決議で配当を発表することができますが、いかなる配当も私たちの取締役会が提案した金額を超えてはいけません。この2つの場合、すべての配当金はケイマン諸島の法律によって制限されており、すなわち、当社は利益または当社の株式割増口座の信用から配当金を支払うことしかできず、これが当社が債務を返済できない場合には、債務が分配または配当支払い日に続く通常の業務過程で満了するため、いかなる場合も配当金を支払うことができないと規定されている。私たちが配当金を派遣することを決定しても、配当の形式、頻度、金額は私たちの未来の運営と収益、資本要求と黒字、一般的な財務状況、契約制限、取締役会が関連すると考えられる他の要素に依存するかもしれない
私たちは現在予測可能な未来に私たちの普通株にどんな現金配当金を支払う計画もない。私たちは現在、私たちの業務を運営し、拡大するために、利用可能な資金と将来の任意の収益の大部分(すべてでなければ)を保留するつもりだ。
もし吾らが吾等の普通株についていかなる配当金を支払うならば、吾らは米国預託証明書に関連する普通株に関する配当金を当該等の普通株登録者である信託銀行に支払い、その後、信託銀行は米国預託株式保有者が保有する米国預託株式米国預託株式関連普通株比率で米国預託株式保有者に関連金を支払うことになり、これに対応する手数料及び支出を含む預金契約の条項を遵守しなければならない。“プロジェクト12.D.株式証券以外の証券説明--米国預託株式”を参照。私たちの普通株の現金配当金(あれば)はドルで支払います
B.重大な変化
適用されません
項目9.見積もりとリスト
A.割引と発売詳細
私たちのアメリカ預託証明書は“LEGN”のコードで発売され、ナスダック世界ベスト市場で取引されています
B.配送計画
適用されません。
C.市場
私たちのアメリカ預託証明書は2020年6月5日からナスダック全世界でベスト市場で取引され、取引コードは“LEGN”です
D.売却株主
適用されません。
E.薄めにする
適用されません。
F.債券発行の支出
適用されません。
項目10.補足情報
A.株本
適用されません。
B.定款の大綱および定款細則を組織する
当社はケイマン諸島登録免除を受けて設立された有限責任会社であり、当社の事務は当社の組織定款大綱及び細則、ケイマン諸島会社法(改正)及びケイマン諸島普通法(以下、会社法(改正)と呼ぶ)によって管轄されている。吾等当社が2020年5月29日に初めて米国証券取引委員会に提出したF-1表(文書番号333-238232)(改訂済み)では、当社の3回目の改訂及び再改訂された組織定款大綱及び定款細則の記述を引用方式で当社の登録説明書に盛り込む。当社の株主は2020年5月26日に特別決議案で当社の3つ目の改訂及び改訂された組織定款の大綱及び細則を採択し、当社の米国預託証明書に代表される普通株の初公開発売完了後に発効します。
当社の改訂及び再記述された組織定款大綱及び定款細則、及び会社法(改訂された)の重大な条文概要については、当社普通株の重大な条項に触れていれば、本年報に沿ってアーカイブされている添付ファイル2.5を参照されたい
C.材料契約
正常業務過程中および本年度報告において“第4項.当社に関する情報”、“第5項.経営と財務回顧及び展望”、“第6項.取締役、高級管理者と従業員”、“第7.B項.関連側取引”又はその他の部分で述べた以外に、吾らは他の重大な契約を締結していない。
D.外国為替規制
“4.b.会社情報-業務概要-政府規則-中華人民共和国法規-その他の中華人民共和国国家レベルと省級法律法規-外国為替管理条例”を参照。そして“第4.B項会社情報-業務概要-政府法規-中華人民共和国法規-その他中華人民共和国国家級と省級法律法規-株式分配に関する法規”
E.税収
以下は,我々の米国預託証明書と普通株への投資に関するケイマン諸島,人民Republic of China,米国連邦所得税結果の一般的な要約である.議論の目的は、任意の特定の潜在的な買手に法律または税務アドバイスを提供すると解釈されるべきでもない。議論は、本年度報告日までに発効する法律およびその関連解釈に基づいており、これらのすべての法律または解釈は変化する可能性があり、または異なる解釈があり、遡及効力を有する可能性がある。米国の州や地方税法には触れず、ケイマン諸島、人民Republic of China、米国以外の司法管轄区の税法にも触れない。あなたは私たちのアメリカ預託証明書と普通株の買収、所有、処分の結果について税務コンサルタントに相談しなければなりません。
ケイマン諸島の税金
ケイマン諸島には現在、利益、収入、収益または付加価値に基づいて個人や会社に課税されておらず、相続税や相続税の性質の税収もない。
ケイマン諸島政府が徴収した他のいかなる税金も、印紙税がケイマン諸島司法管轄区域内で署名された文書や署名後にケイマン諸島の管轄範囲内で署名された文書に適用される可能性がない限り、私たちにとって実質的ではないだろう。ケイマン諸島はわが社またはわが社によって支払われたいかなる金にも適用される二重課税条約の締約国ではない。ケイマン諸島には外国為替規制や通貨制限がない。
当社の普通株及びアメリカ預託証明書に関する配当及び資本の支払いはケイマン諸島で納税することはなく、当社の普通株或いはアメリカ預託証明書所有者に配当金或いは資本を支払う際にも源泉徴収する必要はなく、当社の普通株或いはアメリカ預託証明書を売却して得られる収益もケイマン諸島の所得税或いは会社税を支払う必要がありません。
当社普通株または当社普通株に関する譲渡文書を発行するには印紙税を支払う必要がありません。
アメリカ連邦所得税がアメリカの保有者に与える重大な影響
以下の議論は、米国保有者の我々の米国預託証明書の所有権と処置に関連する重大な米国連邦所得税の結果を説明する(以下に定義する)。本検討は、今回発売された米国預託証明書を購入し、当該米国預託証明書を資本資産として保有する米国保有者に適用され、同等米国預託証明書は、1986年に改正された米国国税法第1221節又はこの準則の意味を満たす。本議論は“規則”に基づいており、この規則に基づいて公布された米国財務省条例とその行政と司法解釈に基づいており、これらはすべて本条例の発効日に発効し、これらはすべて変化する可能性があり、追跡力がある可能性がある。本議論は、米国連邦所得税のすべての結果に関連するものではなく、これらの結果は、特定の米国連邦所得者の特別な状況に関連する可能性があり(例えば、法典451(B)条に規定されているいくつかの収入が財務諸表に計上されるべき時間の影響)、または米国連邦所得税法によって特別に扱われる米国の保有者(例えば、いくつかの金融機関、保険会社、証券取引業者およびトレーダー、または米国連邦所得税目的のために通常その証券を市価で計算する個人、免税実体、退職計画、規制された投資会社、不動産投資信託基金)に関するものではない。ある前にアメリカ市民または住民が、アメリカ預託証明書を“国境を越えて”、“ヘッジ”、“転換取引”、“合成証券”あるいは総合投資の一部として持っている人、アメリカ預託証明書を補償支払いとして受け取る人、ドル以外の“機能通貨”を持っている人、直接、間接的あるいは投票または価値を通じて私たちの10%以上の株式を持っている人に帰属し、収益を蓄積してアメリカ連邦所得税から逃れる会社、組合企業と他の直通実体と手配は、組合企業に分類され、アメリカ連邦所得税の目的に適合する。このような直通実体の投資家)もあります本議論は、いかなる米国州や地方または非米国の税収結果にも触れず、米国連邦遺産、贈与、または代替最低税収結果にも触れない。
本議論で使用される用語“米国所有者”とは、米国預託証明書の実益所有者、すなわち米国連邦所得税について、(1)米国市民または住民の個人であり、(2)米国、その任意の州またはコロンビア特区の法律または法律の下で作成または組織された会社(または米国連邦所得税において会社の実体とみなされる)を意味する。(3)その収入は、その出所にかかわらず、米国連邦所得税の遺産を納付しなければならない;または(4)信託(X)は、米国内の裁判所がその管理を主な監督を行使することができ、1つまたは複数の米国人が、そのすべての重大な決定を制御する権利があるか、または(Y)適用される米国財務省法規に基づいて、米国連邦所得税目的国内信託とみなされることを選択した
米国連邦所得税目的によって組合企業の実体とみなされる場合、または米国預託証明書の保有を手配する場合、米国預託証明書への投資に関連する米国連邦所得税の結果は、その実体または手配および特定のパートナーの地位と活動に部分的に依存する。任意のこのようなエンティティまたは手配は、それおよびそのパートナーが米国預託証明書を購入し、所有し、処分するために適用される米国連邦所得税結果について、自分の税務コンサルタントに相談しなければならない。
アメリカ預託証明書に投資することを考慮した人は彼ら自身の税務顧問に相談し、アメリカ預託証明書の購入、所有と処分に関連する特殊な税収結果を理解し、アメリカ連邦、州と地方税法及び非アメリカ税法の適用性を含む。
受動型外国投資会社の結果
一般に、米国国外で設立された会社は、任意の課税年度において、(1)総収入の少なくとも75%が“受動的収入”(“PFIC収入テスト”)であるか、または(2)平均の少なくとも50%の資産が受動的収入を生成する資産であるか、または受動的収入を生成するために保有する資産(“PFIC資産テスト”)であり、受動的外国投資会社またはPFICとみなされる。この目的のために、受動的収入は、一般に、配当金、利息、特許使用料、レンタル料、および受動的収入を生成する売却または交換財産の収益を含む。受動的収入を生成または生成するために保有される資産は、通常、現金が運営資本として保有されていても、または公開発行によって調達されても、現金、有価証券、および受動的収入を生成する可能性のある他の資産を含む。一般に、非米国会社が個人投資会社であるか否かを決定する際には、少なくとも25%の権益(価値計算)を直接または間接的に所有する各会社の収入および資産の割合が考慮される。
私たちの個人資産投資会社としての地位は、私たちの収入の性質と構成と、私たちの資産の性質、構成と価値に依存します(これは各資産の公正な市場価値によって決定されるかもしれません。営業権価値と持続的な経営価値は、私たちのアメリカ預託証明書の市場価値を参考にして決定され、ADSの市場価値は不安定かもしれません)。私たちの地位は、私たちが業務で初めて公募株(IPO)や他の資金調達活動を利用して得た現金の速度にもある程度依存するかもしれない。我々の運営履歴および我々の収入と資産推定値(営業権を含む)の予測構成から,2022年12月31日までの納税年度はPFICとは考えられない。国税局がわれわれの結論に同意することは保証できないが,国税局は成功しない
私たちの地位に挑戦する。PFICとしての我々の地位は,個々の納税年度(本納税年度を含む)が終了した後に毎年行われる事実集約型決定である。したがって,我々の米国法律顧問は,2022年12月31日までの納税年度のPFIC地位については何の意見も発表せず,本納税年度や将来の納税年度のPFIC地位の期待にも何の意見も発表しない。
米国預託証明書所持者が米国預託証明書を所有する任意の課税年度内の米国預託証明書所持者である場合、米国預託証明書所持者は、“米国預託証明書超過割当制度”に基づいて、以下の事項について、追加の税額および利息費用を負担することができる:(1)課税年度内に支払われる割当額が、前の3課税年度に支払われた平均年間割当額の125%を超えるか、または(2)米国預託証明書保持者に継続しているか否かにかかわらず、販売、交換またはその他の処置(質権を含む)で確認された任意の収益。PFIC超過割当制度によれば、このような分配または収益の税収は、米国保有者が米国預託証明書を保持している間に比例的に分配または収益を分配することによって決定される。本課税年度(すなわち分配または収益確認が発生した年度)および我々がPFICの第1課税年度までのいずれかの年度に分配した金額は,本課税年度の一般収入として納税する。他の課税年度に割り当てられた額は、個人や会社に適用される最高限界税率で当該等課税年度ごとの一般収入に課税され、その税項に通常税金の少納に適用される利息料金が追加される。
もし私たちがアメリカの保有者がアメリカの預託証明書を持っている任意の年度のPFICであれば、私たちはアメリカの預託証明書の保持者の資格の要求に適合しなくなり、そしてアメリカの保有者がアメリカの預託証明書について“売却と見なす”選択をしなければならない。そうでなければ、アメリカの保有者がアメリカの預託証明書を持っている間、私たちは通常、この保有者からアメリカの預託証明書の所有者とみなされ続けなければならない。選択すれば、米国の保有者は、私たちがPFICになる資格がある最後の納税年度の最後の日にその保有するADSを公平な市場価値で売却するとみなされ、このような売却で確認された任意の収益はPFIC超過分配制度によって課税される。売却された選挙後、米国保有者の米国預託証明書は、その後PFICにならない限りPFICの株とはみなされない。
いずれの課税年度内にも、米国株主が米国預託証明書を持つPFICであり、我々の非米国会社子会社もPFIC(すなわち、より低いレベルのPFIC)であれば、米国所有者は、より低いレベルのPFIC株式を所有する割合金額(価値で計算される)とみなされ、PFIC超過割当制度によるより低いレベルのPFICの分配およびより低いレベルのPFICを売却する株の収益を課税し、たとえ米国所有者がこれらの分配または処置の収益を受けなくても、これらの分配または処置の収益を受けることはない。各アメリカの所有者はPFICルールが私たちの非アメリカ子会社に適用されることについて税務コンサルタントに相談することをお勧めします。
もし我々がPFICであれば,米国所持者はPFICの超過分配制度に基づいて分配あるいはADSで確認された収益を納税することはなく,その米国所有者が我々のADSのために有効な“時価ベース”を選択していることを前提としている。米国の保有者にとっては、時価ベースの選挙は“販売可能な株”にしか適用されない。私たちのアメリカ預託証明書が依然としてナスダック全世界の精選市場に上場し、定期的に取引している限り、私たちのアメリカ預託証明書は適切な株です極小の数は、カレンダー四半期ごとに少なくとも15日。時価ベースの選択が発効すれば、米国保有者は、米国保有者がその課税年度終了時に保有する米国預託証明書の公平な市場価値が当該等預託証明書の調整税ベースを超える部分を、その課税年度ごとの一般収入とするのが一般的である。米国の保有者は毎年、このような米国預託証明書の調整税額がその公平な市場価値を超える部分を普通損失として考えているが、先に計上された収入の金額が市価選択によって差し引かれた普通損失を超えている部分に限られている。米国保有者の米国預託証明書における納税基盤は、時価選挙で確認された任意の収入や損失を反映するように調整される。当社がPFCのための任意の課税年度において、米国預託証明書を売却、交換、または他の方法で処分する任意の収益は、一般収入とみなされ、このような売却、交換または他の処置からの任意の損失は、最初に一般損失(以前に計上された収入のいずれかの時価で計算された純収益の範囲)とみなされ、その後、資本損失とみなされる。
我々がPFICでないいかなる課税年度についても,時価ベースの選挙はADSには適用されないが,PFICとなるいかなる後続納税年度に対してもADSは有効である。そのような選挙は私たちが将来組織したり買収したりする可能性のある非米国子会社には適用されないだろう。したがって、私たちが将来組織または買収する可能性のある任意の低いレベルのPFICについては、米国の保有者はADSに対して時価ベースの選挙を行ったにもかかわらず、PFIC超過流通制度に基づいて納税を継続する可能性がある。
もし私たちがPFICであれば、適用される税収結果も、上述した米国所有者が有効な合格選挙基金(“QEF”)選挙を行うことができれば税収結果とは異なるだろう。現在、米国の保有者がQEF選挙を行うために必要な情報を米国の保有者に提供することは望んでいない。潜在的投資家たちはQEF選挙が行われないと仮定しなければならない。
PFIC投資家である米国人は、通常、米国財務省が要求する可能性のある情報を含むIRS Form 8621に年次情報申告書を提出することを要求される。IRS表8621を提出できなかった場合、米国連邦所得税に処罰を加え、訴訟時効を延長する可能性がある。
PFICに関するアメリカ連邦所得税規則は非常に複雑だ。潜在的な米国保有者がPFIC地位がADSの購入、所有権と処置に与える影響、PFICへの投資の結果、ADSに関連する任意の選択、およびPFICのADSの購入、所有権および処置に関連する米国国税局情報報告義務について彼ら自身の税務コンサルタントに相談することを強く促す。
分配する
“第8.A項.総合報告書および他の財務情報である配当政策”の節で述べたように、私たちは予測可能な将来、私たちの米国預託証明書保持者に配当金を発表したり、支払うことはないと予想される。しかしながら、予想とは逆の分配を行った場合、上記“第10.E.付加情報-税金-受動外国投資会社結果”の項目の議論によれば、ADSの分配に関する米国所有者は、一般に、米国保有者が現在および/または累積収益および利益(米国連邦所得税原則に従って決定された)における米国保有者の比例シェアを実際にまたは建設的に受信した場合に、このような分配の毛額を配当金として含めることが要求される。もし米国の保有者が受け取った分配が、配当金ではなく、現在および累積収益および利益における米国所有者の割合を超えている場合、それはまず免税資本リターンとみなされ、米国保有者の米国預託証明書の調整税ベースを低下させる(しかし、ゼロ以下ではない)。米国保有者の米国預託証明書を超える調整税基が割り当てられていれば、残りの部分は資本利益として課税される。私たちはアメリカ連邦所得税の原則に従って私たちの収入と利益を会計処理しないかもしれないので、アメリカの保有者はすべての分配が配当金として彼らに報告されることを期待すべきだ。
配当金とされる米国預託証明書の分配は通常、米国以外の源からの収入を構成し、外国の税収控除に使用され、通常は受動的なカテゴリ収入を構成する。いくつかの複雑な条件と制限により、ケイマン諸島の米国預託証明書に対する任意の分配源泉徴収の税金は、米国保有者の連邦所得税義務を相殺する資格がある可能性がある。アメリカの外国税収控除を確定することに関する規則は複雑で、アメリカの保有者は彼らの税務顧問に相談し、彼らの特定の状況下で外国税収控除があるかどうか、および支払われたまたは源泉徴収された任意の外国税収の分額控除(外国税収控除の代わり)を要求する可能性があるかどうかを知るべきである。
通常配当金とされている米国預託証明書の分配は、一般的に会社株主が米国会社から取得した配当金について“受け取った配当金”を差し引くことを許可する資格には適合しない。ある要求を満たせば、“適格外国会社”が支払う配当金は、一般的に一般的な収入に適用される限界税率ではなく、低下した資本利益税税率に従って非会社アメリカ株主に課税される資格がある。非米国会社(配当金を支払う課税年度または前の課税年度にPFICに分類された会社を除く)は、一般に適格外国会社とみなされる:(A)米国との包括的な税金条約のメリットを享受する資格がある場合、米国財務大臣は、この条約は本規定について好ましいと考えており、この条約には情報交換規定が含まれているか、または(B)米国の既定の証券市場でいつでも取引可能な株式支払いのいずれかの配当金である。私たちのアメリカ預託証明書はナスダック世界の精選市場に上場すれば、通常アメリカの成熟した証券市場でいつでも取引できると考えられています。各アメリカの保有者はその税務顧問に問い合わせ、その特定の状況に応じて低減された配当税率を得ることができるかどうかを知ることを提案する。
アメリカの預託証明書を売却、交換、または他の方法で処分する
上記の“10.E.付加情報-税収-受動的外国投資会社結果”の項目の議論によると、米国の保有者は一般に、米国預託証明書を売却、交換、または他の方法で処分する際に、米国連邦所得税の資本収益または損失を確認し、その金額は達成されたものに等しい(即売却、交換または他の処置における現金金額に、受信した任意の財産の公平な市場価値)および米国預託証明書における米国保有者の調整税ベース。このような資本収益または損失は、一般に、非会社の米国保有者に対して低い税率で納税されるか、または販売、交換または他の処置の日に、米国預託証明書保持者が1年を超える米国預託証明書を保有する場合、長期資本損失である。非会社アメリカ保有者のいかなる資本収益も長期資本収益でなければ、通常所得税率で課税される。資本損失の控除額
制限されています。米国の預託証明書を売却または他の方法で処理することから確認された任意の収益または損失は、一般に、米国の外国税控除目的のために米国国内源から得られる収益または損失である。
医療保険税
個人、遺産、または信託に属するいくつかの米国所有者は、その収入がいくつかのハードルを超え、通常、その全体または一部の純投資収入に3.8%の税をかけなければならず、その中には、彼らの総配当収入および米国預託証明書の販売の純収益が含まれている可能性がある。もしあなたが個人、遺産、または信託基金のアメリカの所有者であれば、この連邦医療保険税がアメリカの預託証明書を所有して処分する上での収入と収益に適用されるかどうかを知るために、税務コンサルタントに相談することを奨励します。
情報報告とバックアップ減納
米国保有者は、米国国税局表8938(指定外国金融資産報告書)を含む、米国国税局に米国預託証明書投資に関するいくつかの米国情報報告書申告書を提出するように要求される可能性がある。上述したように、“10.E.付加情報--税金--受動的外国投資会社の結果”の節では、PFICの株主である米国の保有者一人ひとりが、何らかの情報を含む年間報告書を提出しなければならない。米国預託証明書に100,000ドルを超える米国所有者は、IRSフォーム926(米国財産譲渡者が外国会社に返却)を提出し、この支払いを報告することを要求される可能性がある。要求された情報報告を守れなかった米国の保有者は重大な処罰を受ける可能性がある。これらの要求に加えて、米国の保有者は、FinCEN報告書114(外国銀行および金融口座報告書)を毎年米財務省に提出することを要求される可能性がある。したがって、米国の所有者は、これらと他の米国預託証明書の買収に適用可能な報告書について、彼らの米国税務顧問に相談することを要求することを奨励する。
米国預託証明書を売却または処分する配当金および収益は、米国保有者が免除の基礎を確立しない限り、米国国税局に報告することができる。保有者が(1)正確な米国納税者識別番号を提供できない場合、または他の方法で免税ベースを確立する(通常、米国国税局テーブルW−9上)、または(2)いくつかの他のカテゴリの人に記載されている場合、バックアップバックルは、報告を必要とする金額に適用される可能性がある。しかし、会社であるアメリカの保有者は、通常、これらの情報報告書と予備源泉徴収規則から除外される。予備源泉徴収は付加税ではありません。米国の保有者が米国国税局に必要な情報をタイムリーに提供した場合、予備源泉徴収規則に従って源泉徴収された任意の金額は、通常、米国所有者としての米国連邦所得税義務の返金または相殺が許可される。
アメリカの保有者は予備源泉徴収税と情報報告規則について彼ら自身の税務顧問に相談しなければなりません。
各潜在投資家は投資家自身の状況に基づいて、アメリカ預託証明書に投資してITに対して発生した税務結果について自分の税務顧問に相談しなければならない。
中華人民共和国の税収
“中国企業所得税法”とその実施規則によると、中国国外に設立されているが、中国内部に“実際の管理機関”がある企業は、中国企業所得税については、住民企業を納税するとみなされ、その全世界の収入は統一された25%税率で企業所得税を徴収するのが一般的である。“中華人民共和国企業所得税法実施細則”は、事実上の管理機関を、企業の業務、生産、人員、会計及び財産に対して全面的、実質的な制御及び全面的な管理を行う機関と定義する。2009年4月、国家税務総局は、海外で登録設立された中国持株企業の“事実上の管理機関”が中国にあるかどうかを決定するための特定の基準が規定されている国家税務総局第82号通知を発表した。本通知は、中国企業または中国企業グループによって制御されるオフショア企業にのみ適用され、中国または非中国個人によって制御されるオフショア企業には適用されないが、通知に提出された基準は、すべてのオフショア企業の税務住民の地位を決定する際に“事実上の管理機関”テキストをどのように適用すべきかという国家税務総局の一般的な立場を反映している可能性がある。中国税務総局第82号の通達によると、中国企業または中国企業グループがコントロールするオフショア登録企業は、以下のすべての条件を満たす場合、(1)日常経営管理の主要所在地は中国にある;(2)企業の財務と人的資源に関する決定は中国に位置する組織或いは人員が行う或いは承認された場合、中国に“事実上の管理機関”が設置されているため、中華人民共和国住民とみなされる。(Iii)企業の主要資産、会計帳簿および記録、会社印鑑、取締役会および株主決議は、中国に位置または保存されている;および(Iv)投票権を有する取締役会メンバーまたは上級管理者の少なくとも50%は、中国に常住している。
吾らは、中国税務については、吾らは中国住民企業とみなされるべきではなく、(I)吾らは中国以外で登録が成立し、かつ中国企業や中国企業グループによって制御されているわけではない、および(Ii)吾などは上記のすべての条件を満たしていないと考えている。しかし、企業の税務住民身分は中国の税務機関の決定に依存し、“事実上の管理機関”という言葉に関する解釈には依然として不確定性がある。中国の税務機関が最終的に違う見方をしないという保証はない。
もし中国税務機関が企業所得税について吾などを中国住民企業と認定した場合、吾らの全世界の収入は25%の企業所得税を徴収することができ、吾などの普通株やアメリカ預託証明書に対応する非住民企業所有者の任意の配当は中国内部からの収入と見なすことができるため、適用される所得税条約が別途規定されていない限り、10%の源泉徴収税を払わなければならない(あるいは非住民個人所有者にとっては20%である)。また、非住民企業株主(我々の米国預託株式保有者を含む)が我々の普通株式または米国預託証明書を売却する際に実現される資本収益は、中国国内からの収入とみなされる可能性があるので、適用される所得税条約が別途規定されていない限り、10%の所得税(非住民個人株主または米国預託株式保有者の場合は20%)を納付しなければならない。もし当社が中国住民企業とみなされていれば、当社の非中国株主がその税務居住国と中国との間のいかなる税務協定の利益を享受できるかどうかは不明である。3.D項を参照されたい。リスク要因--中国でビジネスをすることに関連するリスク--中国企業所得税法によれば、私たちが中国の“住民企業”に分類されれば、私たちと私たちの非中国株主は不利な税収結果を受ける可能性があり、私たちの業務、財務状況、経営業績は重大な悪影響を受ける可能性がある
F.配当金と支払代理人
適用されません。
G.専門家の発言
適用されません。
H.展示された書類
私たちは取引法の情報要求に制約され、アメリカ証券取引委員会に報告書やその他の情報を提出することを要求された。米国証券取引委員会は、そのEDGARシステムを用いて米国証券取引委員会に電子届出を行った登録者の報告、依頼書、情報声明、その他の情報を含むウェブサイトをwww.sec.govに掲載している
我々は証券法405条の規則で定義されている“外国個人発行者”であり、米国証券取引委員会の米国国内発行者に対する同じ要求を受けない。取引法によると、我々の報告義務は、米国内の報告会社の報告義務よりもいくつかの点で詳細で少ない。したがって、私たちはアメリカ国内発行者がアメリカ証券取引委員会に提出したのと同じ報告書を提出しない。
我々はまた、米国証券取引委員会または米国証券取引委員会に電子的に提出された文書を電子的に提出した後、合理的で実行可能な範囲内で、私たちのウェブサイトの投資家関係ページ上で、これらの報告書の任意の修正、およびいくつかの他の米国証券取引委員会届出書類を含む、当社の年報およびForm 6-K報告書のテキストをできるだけ早く無料で提供する。私たちの投資家関係ページの住所はwww.Investors.LegendBiotech.comそれは.当社のサイトに掲載されている資料は参考に本年報に組み込まれていません。
本年度報告書で言及された伝説的生物の任意の契約または他の文書については、このような参照は、必ずしも完全ではなく、実際の契約または文書のコピーを取得するために、本年度報告書を参照することによって組み込まれた証拠を参照しなければならない
I.子会社情報
適用されません。
J. 証券所持者への年次報告
表6−K報告の証拠物として,証券保持者に電子フォーマットで提供される年次報告を提出する予定である。
プロジェクト11.市場リスクに関する定量的かつ定性的開示
私たちの現金はいつでも利用できる営業口座と中短期預金と証券に保管されています。これらの証券は元本保証されており、金利変動の悪影響を受けない。したがって、市場金利の変化は私たちの現金残高に大きな影響を与えないだろう。
Janssenとの私たちの協力と許可協定によると、私たちがJanssenから受け取った前金はLIBORに2.5%の金利で利息を計算します。したがって、ロンドン銀行の同業借り換え金利の変化は、私たちのキャッシュフローに変動をもたらす可能性がある。例えば、2022年12月31日現在のJanssenが返済していない元金総額2.5億ドルによると、LIBORは毎年0.5%(50ベーシスポイント)増加し、会社は毎年130万ドルの利息を追加支払うことになる。LIBORの金融サービス業での使用停止に伴い、JanssenとJanssenプロトコルの改正を検討し、新たな金利計算方法を採用しています。
インフレは一般的に労働コストと臨床試験費用を増加させることで私たちに影響を及ぼす。2022年12月31日と2021年12月31日までの年間では、インフレは我々の業務、財務状況や運営結果に実質的な影響を与えないと考えられる。
私たちはまた私たちがどんな重大な外貨為替レートの危険に直面しているとも思わない。
第12項.持分証券以外の証券の説明
A.債務証券
適用されません。
B.株式証明書と権利を認める
2021年5月に、吾らはある機関投資家と引受合意を締結し、私募方式で20,809,850株の普通株を発売し、購入価格は1株当たり14.41625ドルであり、米国預託株式28.8325ドル(“パイプ発売”)に相当し、引受合意により、吾らもパイプ発売と同時に、機関投資家に行使可能な引受権証を発行·販売することに同意し、合計で最大10,000,000株の普通株を発行した。この株式承認証は2021年5月19日から行使可能であり、その全部または一部の行使可能価格は普通株1株当たり20ドルであり、米国預託株式40ドルに相当し、この日の2周年記念日まで行使可能となる。引受権証を行使する際に発行可能な10,000,000株普通株は、2021年7月13日に施行されたF-3表登録声明に基づいて登録されています。2022年12月31日現在、権証はまだ全部または一部行使されていない。
C.その他の証券
適用されません。
D.アメリカ預託株
JPMorgan Chase Bank,N.A.(“JPMorgan”)は,我々の米国預託証明書のホスト機関として,米国預託証明書を登録·交付する.各アメリカ預託株式は、私たちが受託者(受託者の代理として)の指定された数の株式に保管する所有権を代表します。すべてのアメリカ預託株式は2つの普通株式を代表する。米国預託株式と株式の割合は、米国預託証券形式の改訂を受ける可能性がある(これは、米国預託証券形式で予想される費用が生じる可能性がある)。預かり人のオフィスはニューヨークマディソン通り三八三号十一階、NY一零一七九にあります。
当社、預託証明書所持者、本人は米国預託証明書所持者及び他のすべての米国預託証明書所持者として、及び米国預託証明書で時々証明される米国預託証明書権益のすべての実益所有者間の預託協定は、米国預託証明書所持者の権利及び預託証明書の権利と義務を列挙する。ニューヨーク州法律は預金協定とアメリカ預託証明書を管轄している。預金協定の写しは本年度報告の証拠物として,参考として本報告に組み込まれる。
私たちに支払った費用とお金を係の人に預ける
私たちの受託者はアメリカの預託証明書所持者が受託者に支払ういくつかの費用を私たちと分担することに同意します。私たちは、適用されるアメリカの税金を差し引いた後、ホスト機関が私たちと共有する費用は約30万ドルだと予想している。
信託銀行は、米国預託証明書を発行された各者から料金を請求することができるが、これらに限定されないが、株式預金の発行、株式割り当て、権利およびその他の割り当てに関連する発行、吾等によって発表された配当金または株式分割による発行、または合併、証券交換または任意の他の影響を及ぼす米国預託証券または既存証券の取引またはイベントに応じた発行、および保管されている証券を抽出するために提出された米国預託証明書または任意の他の理由によって米国預託証明書がキャンセルまたは減少された者毎に、米国預託証券100部(またはその任意の部分)を発行、またはその一部を受け取るか、それに基づいて株式100部毎に株式を提供または選択的に割り当てることができる。場合によります。保管者は、そのような費用を支払うために、入金前に株式分配、権利および/または他の分配について受信した十分な証券および財産を(公開または私的販売によって)販売することができる(公開または私的販売によって)販売することができる。
米国預託証明書所有者、実益所有者、株式の預け入れまたは抽出のいずれか一方、米国預託証明書の引渡しのいずれか一方、および/または米国預託証明書を発行されたいずれか一方(吾等によって発表された配当金または株式分割または米国預託証明書または入金証券に関する株式交換または米国預託証明書の分配を含むがこれらに限定されないが)も、次の追加費用を発生しなければならない
•預金契約によれば、保有する米国預託株式の任意の現金分配または提供される任意の選択的現金/株式配当金について、アリペイを保有するごとに0.05ドル以下の費用が徴収される
•米国預託株式毎の毎日例年(またはその一部)は、管理者によって提供されるADR管理サービスのために0.05ドル以下の総費用を受け取ることができる(各例年の定期的にADR所持者に受け取ることができ、この費用は、各例年に設定された1つまたは複数の記録日からADR保持者に徴収され、次の後続の規定で説明される方法で支払われるべきである)
•受託者および/またはその任意の代理人(受託者を含むが、これらに限定されないが、米国の預託証明書保持者を代表する外国投資に関する法律または条例の遵守によって発生する費用、課金および支出の精算費用、これらの費用、課金および支出は、株式または他の既存証券のサービスまたは他の既存証券(既存証券を含むが、これらに限定されないが含まれる)、既存証券の交付またはその他の受託者またはその委託者またはその委託者に関連する法律に関連する費用に関連する。規則または規則(これらの料金および料金は、保管者によって決定された1つまたは複数の記録日に比例してADR所持者を評価し、そのようなADR所持者に請求書を発行することによって、または1回または複数回の現金配当または他の現金分配からそのような費用を差し引くことによって、保管者によって自己決定されるべきである)
•証券割当費用(または割り当てに関連する証券販売費用)は、米国預託証明書の署名および交付手数料に相当し、米国預託株式当たりの米国預託証券発行手数料0.05ドルであり、このような米国預託証明書の発行および交付は、このような証券(すべてのこのような証券を株式とみなす)の入金によって徴収されるべきであるが、信託銀行は、これらの証券またはこれらの証券を売却して得られた現金純額を、当該証券を取得する権利のある米国預託証明書保持者に分配する
•株式譲渡やその他の税金やその他の政府の料金
•あなたの要求によって生成された株式の保管または交付、米国預託証明書、または証券の保管に関連する電報、電送およびファックス送信および交付費用;
•預託された証券の預け入れ又は引き出しに関する任意の適用登録簿に入金された証券の譲渡又は登録費用を登録すること;
•受託者は、預金契約書の下の任意の公開および/または個人証券販売を指導、管理および/または実行するための任意の部門、支店、または付属機関の費用を提供する
配当金の支払いやその他の現金分配と他の会社の行動を含む各種預金証明書取引の管理を容易にするために、預託機関はモルガン大通銀行(以下“銀行”と呼ぶ)及び/又はその関連会社の外貨両替部門と即時外貨取引を行い、外貨をドルに両替することができる。いくつかの通貨の場合、外国為替取引は、主要な身分で銀行または付属機関と(状況に応じて)締結される。他の通貨については、外国為替取引は独立したローカル委託者(または他の第三者ローカル流動資金提供者)によって直接管理され、本業またはその任意の関連会社は、そのような外国為替取引の一方ではない
外国為替取引に適用される外国為替レートは、(A)公表された基準為替レート、または(B)第三者ローカル流動資金提供者によって決定される為替レートであり、それぞれの場合、プラスまたはマイナス(場合に応じて)となる。ホスト機関は、その通貨に適用される為替レートおよび利差(ある場合)を、www.adr.comの“開示”ページ(または後続のページ)上で開示する。このような適用される為替レートおよび利益差は可能である(かつ、信託銀行、当行、またはそのどの関連会社も、その為替レートがないことを保証する義務はない)とは異なる
どのような比較可能な取引が他の顧客と達成されたか、または当行またはその任意の関連会社が外国為替取引当日に関連通貨で外国為替取引を行う為替レートおよび利益範囲であるか。さらに、外国為替取引の実行時間は現地市場の動態によって異なり、これには規制要求、市場時間、外国為替市場の流動性、または他の要素が含まれる可能性がある。また、当行およびその関連会社は、このような活動が預託管理人、私たち、所有者または実益所有者に与える影響を考慮することなく、適切と考えられる方法で市場に保有するポジションに関するリスクを管理することができる。適用される利益差は、当行及びその付属会社がリスク管理或いはその他のヘッジ関連活動によって獲得或いは招く可能性のあるいかなる損益を反映していない。
それにもかかわらず、私たちが信託銀行にドルを提供する限り、当行またはその任意の関連会社は、本明細書で説明する外国為替取引を実行しない。この場合、係の人は私たちから受け取ったドルを配布するだろう
適用される為替レート、適用される価格差、外国為替取引の実行状況に関するより多くの詳細は、ホスト機関によってADR.com上で提供される。米国預託証明書所有者および実益所有者は、米国預託証明書または米国預託株式またはその中の権益を保有または所有しているが、吾らはそれぞれ、米国預託証明書が時々開示する外国為替取引に適用される条項が、預金協定に基づいて実行される任意の外国為替取引に適用されることを認め、同意する。
私たちと係の者との間で時々合意された合意によると、私たちは、委託者及びその任意の代理人(受託者を除く)の他のすべての費用及び費用を支払います。
保管人が費用、料金、支出を徴収する権利は、保管者契約の終了後も有効であり、保管人の辞任または更迭が発効する前に発生した費用、料金、および支出に適用されなければならない。
上記の料金や料金は、吾等が保管者と合意した後に随時改訂することができる。
受託者は、吾等が係の者と時々達成した条項及び条件に基づいて、ADR計画について徴収する固定金額又は一部の管財料又はその他の条項を吾等に提供することができる。米国預託証明書の発行とログアウト費用は,株への入金や抽出目的で米国預託証明書を渡した投資家またはその代理の仲介機関に直接受け取る。保管人は、投資家に分配する費用を受け取り、分配された金額からこれらの費用を差し引くか、または分配可能な財産の一部を売却して費用を支払う。 受託者は、現金分配から控除されるか、または投資家に直接課金するか、または投資家を代表する参加者の帳簿課金システムアカウントに課金することによって、ホストサービス年会費を受け取ることができる。保管人は一般的にアメリカの預託証明書所持者に割り当てられた金から借金を相殺します。しかしながら、割り当てが存在せず、管理者が不足金をタイムリーに受信していない場合、管理者は、これらの費用および費用の支払いが完了するまで、不足した費用および支出を支払っていないADR所持者にさらなるサービスを提供することを拒否することができる。保管人が適宜決定し、保管人が保管者契約に基づいて借りたすべての費用及び料金を予め支払わなければならない(又は)保管人が借金を申告したときに支払わなければならない。
第II部
プロジェクト13.配当金の滞納および配当金の滞納
適用されません。
プロジェクト14.所有者を保証する権利および収益の使用を実質的に修正する
答え:適用できません。
B.適用されません。
C.は適用されません。
D.は適用されない.
E.は適用されない.
F.は適用されない
プロジェクト15.制御とプログラム
A.制御とプログラムを開示する
我々の経営陣は、最高経営責任者及び最高財務官の参加の下、取引所法案第13 a-15(B)条の要求に基づいて、本年度報告がカバーする期間終了までの開示制御及び手順(取引所法案第13 a-15(E)条を定義する)の有効性を評価した。この評価に基づき、我々の経営陣は、財務報告に対する内部統制が不十分であるため、2022年12月31日現在、財務報告の内部統制が不十分であるため、以下の“-経営陣の財務報告内部統制年次報告”に記載されている大きな弱点によるものであると結論したこれらの大きな弱点にもかかわらず経営陣が出した結論は審査されました本年度報告に掲載された財務諸表は国際財務報告基準に従って各期間の財務状況、経営業績及び現金流量を列記し、各重要な方面でかなりの程度の反映がある。
B.経営陣財務報告内部統制年次報告書
会社経営陣は、“取引法”ルール13 a-15(F)に定義されている財務報告の十分な内部統制の確立と維持を担当している。経営陣は、最高経営責任者と財務責任者の参加の下、2022年12月31日までの財務報告内部統制の有効性を評価した。経営陣の評価は、テレデビル委員会後援組織委員会が発表した“内部統制--総合枠組み(2013)”(“2013フレームワーク”)の枠組みに基づいている。
この評価に基づき、経営陣は、2022年12月31日現在、以下に述べる重大な弱点により、会社の財務報告に対する内部統制が無効であると結論した。
その固有の局限性のため、財務報告の内部統制は誤った陳述を防止或いは発見できない可能性があり、財務報告の信頼性と財務諸表の作成に合理的な保証を提供するしかない。また,将来的にどのような有効性評価を行うかの予測は,条件の変化により制御不足のリスクが生じる可能性があり,あるいは政策やプログラムの遵守度が悪化する可能性がある.
独立公認会計士事務所安永会計士事務所は、2022年12月31日現在の社内財務報告内部統制報告において、本報告に含まれる社内財務報告内部統制の有効性を監査している。テキスト項目15(C)の段落を参照されたい。
2022年12月31日までの大きな弱点
これまでに開示されたように、私たちは、2021年12月31日現在、財務報告の内部統制に実質的な弱点(すなわち2021年の実質的な弱点)があることを発見してきた。PCAOBが制定した基準によると、重大な欠陥は財務報告内部制御の欠陥或いは欠陥の組み合わせであるため、合理的な可能性があるため、著者らの年度財務諸表の重大な誤報は適時に防止或いは発見されない。私たちは複雑な計画に対する十分な審査と監督管理、特にその唯一の協力と許可協定の不足という重大な弱点を発見した我々の救済措置が進められているため,経営陣は2022年12月31日現在,重大な弱点を救済と見なすことはできないと結論した。
また,我々の2022年12月31日までの財政年度の監査では,我々の財務報告プロセスを支援するキー情報技術(“IT”)システムの特権や通常のユーザアクセスや変更管理における無効情報技術一般制御(“ITGC”)に関連した内部統制における大きな弱点(“2022年重大弱点”)が発見された。したがって,関連するプロセスレベルのIT依存制御やアプリケーション制御も無効である.情報技術の重大な弱点は、我々の財務諸表や開示に重大な誤報を招くことはなく、これまでに発表された財務業績も変化していない。
これらの重大な弱点を救済するための救済計画を策定しており、我々が講じている重大な弱点を救済する手順のさらなる情報については、以下の“財務報告内部統制の重大な弱点の救済”を参照されたい。関連する制御措置が十分に長時間実行され、管理層がテストによってこれらの制御措置が有効に動作する前に、上記のような重大な弱点が存在すると結論付けた。
C.独立公認会計士事務所認証報告
F-4ページ“プロジェクト18.財務諸表”に掲載されている独立公認会計士事務所安永会計士事務所の報告を参照。
D.財務報告の内部統制の変化
以下に述べることに加えて、本年度報告がカバーする期間において、財務報告の内部統制(取引所法案第13 a-15(F)条参照)に大きな影響を与えるか、または合理的に我々の財務報告の内部統制に大きな影響を与える可能性のある変化は発生しない。
2021年の財務報告の内部統制の重大な欠陥を補う
上記2021年の重大な弱点を確定した後、監査委員会の監督の下で、管理層はこの重大な弱点を解決するために救済作業に取り組んでいる。以下に概説する救済作業は、明らかにされた重大な弱点を解決し、我々の全体的な財務制御環境を強化することを目的として実施または行われている。このような点で私たちの措置には
•協力および許可プロトコルを含む複雑なプロトコルに対して、最高財務官および他の高級財務者によるキー会計判断および推定、報告および開示の追加審査を含む、情勢に応じたより多くの審査および監視制御を実施する
•“国際財務報告基準”の応用において具体的な持続的な訓練と教育を行うことによって、協力と許可協定を含む複雑な合意に重点を置き、既存の財務報告者の能力を拡大する
•適切な国際財務報告基準会計経験を持つ財務報告者をより多く採用する
この救済計画の実行を支援するために、会社はまた、会社の既存の内部資源を支援し、補完するために追加の外部資源を招聘した。
2022年の財務報告の内部統制の重大な欠陥を補う
上記2022年の重大な弱点を特定した後、監査委員会の監督の下、経営陣はこの重大な弱点を解決するための救済作業に取り組んでいる。以下に概説する救済作業は、明らかにされた重大な弱点を解決し、我々の全体的な財務制御環境を強化することを目的として実施または行われている。このような点で私たちの措置には
•2023年2月に初めて導入されたガバナンス、リスク、コンプライアンスツールを用いて、手動プロセスの自動化を実現します
•この機能に従事する人をより多く増やすことで、私たちの情報技術コンプライアンス監視を強化します
•情報技術制御および政策のために、各制御の原則と要求について、ユーザ参入に重点を置いた教育を行うこと、(4)より多くの審査を増加させることによって審査プロセスを強化すること、および情報技術制御および政策のためのより多くの訓練および認識向上方案を実施すること
•取締役会監査委員会に救済措置の最新状況を定期的に通報する。
上記の努力が全面的に実施され、実行される場合には、上記の重大な弱点を効果的に補い、財務報告に対する内部統制を強化すると信じている。私たちが財務報告に対する私たちの内部統制を評価し、改善しようと努力するにつれて、私たちはこれらの制御欠陥を解決したり、上記の救済計画を修正したりするための他の措置をとるかもしれない。しかし、私たちはあなたに私たちがいつこのような弱点を修復するのか、私たちはまた追加的な行動が必要かどうかを確認することができない。私たちはこのような重大な弱点の救済作業が2023財政年度が終わるまでに完了すると予想する。
新冠肺炎の大流行に対する行動:
新冠肺炎が大流行したため、2022年12月31日までの1年間、私たちはアメリカとある国際地点で公衆衛生当局の指導、現地の現地避難令、その他の政府の制限に基づいて、在宅勤務の手配を実施した。私たちは、私たちの制御環境、運営手順、データへの影響を軽減するために、財務報告プロセスと業務連続性計画を検討しました
プロジェクト16.保留
プロジェクト16 A。監査委員会財務専門家
当社取締役会は、独立取締役(ナスダック証券市場規則第5605(A)(2)条及びナスダック証券取引法第10 A-3条に記載されている基準)及び当社監査委員会の邱偉民を監査委員会財務専門家とすることを決定し、その定義はForm 20-F第16 A(B)項を参照されたい
プロジェクト16 B。道徳的準則
適用された連邦証券法とナスダック規則によると、私たちは私たちの役員、上級管理者、従業員に適用されるビジネス行動と道徳基準を採択した。私たちのビジネス行動と道徳基準は私たちのサイトで見つけることができますHTTPS://LegendBiotech.com/Complianceそれは.私たちは、本規則の任意の修正またはその要求に対するいかなる免除も、私たちのウェブサイトで開示されると予想している。当サイトに含まれている、または当サイトを介してアクセス可能な情報は、本年度報告書に引用的に組み込まれません。
プロジェクト16 Cです。チーフ会計士費用とサービス
安永法律事務所と安永華明法律事務所が指定期間中に提供するいくつかの専門サービスの費用総額を表に示す。次の期間、吾らは安永法律事務所や安永華明法律事務所に何の他の費用も支払わなかった
安永法律事務所は2022年5月以来、独立監査役を務めてきた。2020年から2022年5月まで、安永華明法律事務所が独立監査役を務めています。
| | | | | | | | | | | |
| ここ数年で私たちは終わりました 十二月三十一日 ドル‘000ドル |
| 2022 | | 2021 |
料金を審査する1 | 6,990 | | | 2,250 | |
監査関連費用2 | 58 | | | 67 | |
| 合計する | 7,048 | | | 2,317 | |
1.監査費用“とは、安永法律事務所と安永華明法律事務所が我々の年間財務諸表を監査するために提供する専門サービス、および米国証券取引委員会に提出された書類およびその他の法定および規制届出書類に協力して審査するために提供される専門サービスが、各会計年度に徴収または徴収される費用の総額を意味する
2.“監査関連費用”とは、我々の主要監査人が提供する保証及び関連サービスに列挙されている各会計年度において、監査又は財務諸表審査の表現に合理的に関連しているが、“監査費用”の項で報告されていない費用総額をいう
監査委員会があらかじめ承認した政策と手続き
現在、私たちの独立公認会計士である安永会計士事務所が提供する監査サービスは、私たちの監査委員会の承認を得なければなりません。
2022年12月31日までの年度中に、安永会計士事務所及び安永華明法律事務所(何者適用による)が吾等に提供するすべての非監査関連費用のサービスは、我々の監査委員会がS−X規則第2-01条第(C)(7)(I)(C)段落に規定する事前承認要求の最低限の例外状況に基づいて承認する。
プロジェクト16 Dです。免除監査委員会は上場基準を遵守する
適用されません
プロジェクト16 E。発行者および関連購入者が株式証券を購入する
適用されません
プロジェクト16 Fです。登録者の認証会計士を変更する
a.独立公認会計士事務所を退職する
安永華明会計士事務所(“安永華明会計士事務所”)は中国人民Republic of China(“中国”)上海に位置し、2020年から当社の独立公認会計士事務所を務める。
2022年5月3日、審査手続きを経て、取締役会監査委員会(“監査委員会”)は、安永会計士事務所が独立公認会計士事務所を辞め、会社が米国証券取引委員会(“米国証券取引委員会”)に提出した財務諸表と財務報告内部統制を監査し、2022年6月1日に6-K表形式で米国証券取引委員会に2022年第1四半期の財務業績を提出した日から発効することを決定した。EYHMが辞任した後、我々は、以前に発表された2021年12月31日までの年次報告書のForm 20-F財務諸表に依存すべきではなく、2021年12月31日までのForm 20-F年次報告書を修正して、我々の財務諸表(“20-F/A”)を再記述する予定であると評価し、結論付けた。20-F/Aについて、私たちはEYHMを再稼働させた。改正日が2023年2月17日のエラーが連結財務諸表に与える影響を除いて、2021年12月31日現在のEYHMおよび2022年3月31日現在の会計年度監査報告(以下、EYHM監査報告と略す)は、2023年2月17日に米国証券取引委員会に提出された20−F/A文書に含まれている。EYHM監査報告書はまた、“総合財務諸表付記2.2に記載されているように、会社が2021年12月31日に統合財務諸表を再列記して、誤った陳述を是正する”と指摘する個別の段落を含む。EYHM
監査もしました 会社の 内部.内部 制御する 財務的に これを報告する 2021年12月31日、テレデビル委員会後援組織委員会が発表した内部統制·総合枠組み(2013年枠組み)で決定された基準と2022年3月31日の報告書によると、実質的な疲弊の影響を除いて反対意見を表明した。
2021年12月31日および2020年12月31日までの財政年度内、および2023年2月17日までのその後の移行期間において、会計原則または慣例、財務諸表開示または監査範囲またはプログラムの任意の事項(第16 F(A)(1)(Iv)項からForm 20−Fおよびその関連指示によって定義されるように)、EYHMとは何の相違もなく、EYHMが満足できる解決が得られなければ、EYHMがこれらの年次総合財務諸表に関する報告書で言及されたテーマに言及することになる。“報告すべき事項”は、20−F/Aレポートで報告された財務報告の内部統制に重大な弱点があることを除いて発生していない(表20−Fの16 F(A)(1)(V)項に記載されている)。
EYHMは米国証券取引委員会に手紙を送り、EYHMに関する会社の声明に同意すると表明した。この手紙のコピーは、本年度報告書の添付ファイル16.1としてアーカイブされます。
b.新しい独立公認会計士事務所
2022年5月3日、監査委員会の審査手順及び第16 F項(A)の一部で述べた安永辞任の決議に基づき、監査委員会は米国にある安永会計士事務所(“安永米国”)を自社の独立公認会計士事務所に委任することを許可し、当社が2022年12月31日までの財政年度の財務諸表及び財務報告書の内部統制を監査し、その後安永米国と招聘状を作成した。
2021年12月31日と2020年12月31日までの財政年度内に、2022年5月3日までのその後の移行期間内に、当社または当社を代表するいかなる者も、以下の事項について安永米国と協議していない:(I)完了したか、または行う予定の特定の取引に会計原則を適用するか、または会社の財務諸表で提出される可能性のある監査意見のタイプ、および安永米国は、当社が会計、監査または財務報告問題について決定する際に考慮する重要な要素ではないと考えている書面報告または口頭提案;または(Ii)属分岐(表格20-F第16 F(A)(1)(Iv)項およびその関連指示によって定義されるように)に属する任意の事項、または報告すべき事象(表格20-F第16 F(A)(1)(V)項に記載されている)のいずれかの事項).
プロジェクト16 Gです。会社の管理
ナスダック上場規則は会社管理要求にいくつかの緩和措置を含み、アメリカなどの外国の個人発行者が“母国”の会社管理実践に従うことを許可し、ナスダック上場規則に他に適用される会社管理基準ではない。大多数のナスダック社のガバナンス規則を自発的に遵守することが予想されるが、以下の限られた免除を利用することを選択する可能性がある
•特定の重大な事件が発生した場合、監査されていない財務および他の指定された資料を記載したテーブル10-Qの四半期報告またはグリッド8-Kの現在の報告書の提出を免除する
•第16条規則の制約を受けず、この規則は、内部者がその証券所有権および取引活動について公開報告書を提出し、内部者が短時間で取引から利益を得る責任を規定することを要求する
•免除は、4営業日以内に任意の免除役員および上級管理者の商業行為および道徳基準の決定を開示することを要求する国内発行者のナスダック上場規則に適用される
•株主が株式オプション計画を承認することを含む、特定の証券発行が株主の承認を得なければならない要求を免除する
•私たちの監査委員会は、表格20-F 7.B.項で定義されているように、すべての“関連者取引”に対して審査と監督責任の要求を免除する
•完全に独立した取締役会で構成され、その委員会の目的と責任を説明する書面規約がある報酬委員会の要求を免除する
•取締役の指名者が我々の取締役会によって選択または推薦されるか、または(1)我々の取締役会を構成する独立取締役の多数の独立取締役が投票するか、または(2)独立取締役のみからなる委員会が、正式な書面または取締役会決議(適用される場合)によって指名過程を解決するという要求の制限を受けない。
また、私たちはナスダック上場規則で定義されている“制御された会社”、すなわち単一エンティティが50%以上の投票権を持っている会社です。制御された会社は、取締役会に過半数の独立取締役がいなければならないか、または完全に独立した報酬、指名、およびコーポレートガバナンス委員会を有することを要求するナスダックのコーポレートガバナンス規則を遵守する必要はない。
私たちは依存し、引き続き“制御された会社”免除に依存しています。私たちは必要なく、時々多数の独立した役員を持っていないかもしれません。私たちの報酬委員会と私たちの指名と会社管理委員会は完全に独立した取締役で構成されていません。これらの委員会は年間業績評価を受けないでしょう。したがって、私たちの株主はすべての証券取引所の規則に拘束されている会社の株主と同じ保護を受けないでしょう。現在、私たちの取締役の多くは独立していますが、私たちの報酬委員会と指名と会社統治委員会は完全に独立した取締役で構成されているわけではありません。外国の個人発行者と制御された会社の免除は、監査委員会の独立的な要求を修正しないだろう
16 H項です。炭鉱安全情報開示
適用されません。
プロジェクト16 I。検査妨害に関する外国司法管区の開示
2021年12月31日と2020年12月31日の会計年度まで、監査役は独立公認会計士事務所EYHMである。安永は,2021年12月31日までの財政年度のForm 20−F年報(以下,“2021年年報”と略す)と,その後の2021年年報の第1号改正案及び2021年12月31日までの財政年度の監査報告について監査報告を出している 本年度報告書に含まれています。PCAOBは以前,EYHMをPCAOBが全面的に検査や調査できない公認会計士事務所の1つとして決定していたため,同社は2022年5月4日にHFCAA下の“委員会が決定した発行者”と決定した
当社は中国のどの中央、省級あるいは地方政府が一部の持分を所有しているわけではなく、中国のどの政府実体も当社が持株権を持っているわけではない。我々の取締役会メンバーはいずれも中国共産党(“CCP”)の役人ではなく、我々の定款大綱や定款にもCCP定款や定款テキストは何もない。上場企業会計監督委員会(“PCAOB”)は、中国当局の立場のため、我々の独立監査師の全面的な検査や調査を行うことができないことを決定した。
我々の監査委員会(I)は2022年5月3日にEYHMの独立公認会計士事務所を辞任することを決定し、当社が2022年6月1日に米国証券取引委員会の財務諸表及び財務報告内部統制に提出し、2022年6月1日に発効することを監査し、(Ii)米国にあるEYUSを自社の独立公認会計士事務所として招聘することを許可し、2022年12月31日までの財務諸表監査及び財務報告内部統制を担当し、その後EYUSと招聘状を作成する。2022年12月15日、PCAOBは“米国法典”第15章7214(I)(2)(A)条とPCAOB規則6100に基づいてHFCAA認定報告を発表し、PCAOBの裁定を撤回した、すなわち国内の関係当局の職位のため、中国大陸部と香港に本部を置く完全登録会計士事務所を検査または調査することができなかった。HFCAAのさらなる情報については,“項目3−キー情報−外国会社責任追及法案”と“項目16 F−登録者認証会計士の変更”を参照されたい
第三部
プロジェクト17.財務諸表
“プロジェクト18.財務諸表”を参照
プロジェクト18.財務諸表
伝説的生物及びその子会社の連結財務諸表は本年報の末尾に掲載されている。
プロジェクト19.展示品
展示品索引
(引用で組み込む)
| | | | | | | | |
展示品 番号をつける | | 書類の説明 |
| | |
| 1.1*** | | 第三次改正及び再改訂現行有効登録者組織覚書及び定款(2020年5月29日に米国証券取引委員会に提出された登録者登録声明F−1表(書類番号333−238232)添付ファイル3.2を参照して本明細書に組み込む) |
| | |
| 2.1*** | | 普通株式登録者証明書サンプル(2020年5月29日に米国証券取引委員会に届出された登録者F−1表(文書番号333−238232)の添付ファイル4.1を本明細書に組み込む) |
| | |
| 2.2*** | | 登録者とモルガン大通銀行との間の預金契約表として(本稿では、登録者が2020年5月29日に米国証券取引委員会に提出したF-1表登録声明(第333-238232号文書)添付ファイル4.2を参照して編入) |
| | |
| 2.3*** | | 米国預託株式を証明する米国預託証券フォーマット(F-1表添付ファイル4.2(第333-238232号文書)に掲載され、2020年5月29日に米国証券取引委員会に提出) |
| | |
2.4*** | | 証券取引法第12節に登録された証券説明(これに合わせて、2022年3月31日に米国証券取引委員会に届出された登録者20-F表(文書番号001-39307)添付ファイル2.5を参照) |
| | |
| 2.5*** | | LGN Holdings Limitedと登録者との間の引受契約は、2021年5月13日である(本稿では、登録者が2021年7月2日に米国証券取引委員会に提出されたF-3表登録声明(文書番号333-257625)添付ファイル10.1)を引用する |
| | |
| 2.6*** | | 購入登録者普通株の引受権証(これに合わせて、2021年7月2日に米国証券取引委員会に提出された登録者F-3表(書類番号333-257625)添付ファイル10.2参照) |
| | |
| 4.1*** | | 伝説的生物米国会社、伝奇生物アイルランド株式会社とヤンソン生物科学技術会社との間の協力と許可協定は、2017年12月21日に改訂された(2020年5月29日に米国証券取引委員会に提出された登録者登録声明F-1表(文書番号333-238232)の添付ファイル10.1を参照して本明細書に組み込む) |
| | |
| 4.2*** | | 登録者とその執行者及び取締役の各々との間の賠償協議表(参照登録者により2020年5月29日に米国証券取引委員会の登録者F−1表に提出された(書類番号333−238232)添付ファイル10.2が本明細書に組み込まれる) |
| | |
| | | | | | | | |
4.3+*** | | 登録者とHuangとの間で改訂および再署名された雇用協定は、2022年8月3日に施行される(本明細書では、2022年8月4日に米国証券取引委員会の登録者報告書6-K表(文書番号001-39307)の添付ファイル10.1を参照して本明細書に組み込まれる) |
| | |
4.4+*** | | 改正され再署名された雇用協定は、登録者、伝説的生物米国会社、Lori Macomberによって署名され、2022年9月28日に施行される(合併は、2022年10月3日に米国証券取引委員会に提出された登録者報告6-K表(文書番号001-39307)の添付ファイル10.1参照) |
| | |
| 4.5+*** | | 株式購入計画(委託書、授出通知書、発行通知書及び株式購入契約及び投資申告書を含む)(2020年5月29日に米国証券取引委員会に提出された登録者登録説明書F-1表(第333-238232号文書)添付ファイル10.5を本明細書に組み込む) |
| | |
| 4.5*** | | 伝説的生物米国会社とGenscript USA Holding,Inc.との間のリース契約は、2018年2月8日である(本稿では、2020年5月29日に米国証券取引委員会に提出された登録者F−1表登録声明(文書番号333−238232)の添付ファイル10.6を参照して本明細書に組み込む) |
| | |
4.7+*** | | 2020年の株式制限計画(限定株奨励協議フォーマットを含む)は、2020年8月28日に改訂される(本文は、2020年9月4日に米国証券取引委員会に提出された登録者S-8表登録説明書(第333-239478号文書)添付ファイル10.2を参照して編入) |
| | |
4.7***^ | | 伝説的生物米国会社とヤンソン製薬会社との間の一時供給協定は、2022年2月28日(登録者を引用して2022年3月31日に米国証券取引委員会に提出された20−F表(文書番号001−39307)の添付ファイル4.7を参照して本明細書に組み込む) |
| | |
| 4.8**** | | 非従業員役員報酬政策 |
| | |
| 4.9***^ | | 伝説的生物米国会社とヤンソン製薬会社が2022年7月7日に署名した仮供給協定の第1号改正案(登録者を引用して2022年7月13日に米国証券取引委員会に提出された6−K表報告書(文書番号001−39307)の99.1号添付ファイルが本明細書に組み込まれる) |
| | |
| 4.10*** | | 伝説的生物米国会社とヤンソン製薬会社が2022年10月17日に署名した仮供給協定の第2号改正案(これに合併し、参照登録者は2022年11月22日に米国証券取引委員会に提出された6−K表報告(文書番号001−39307)の添付ファイル10.1) |
| | |
| 4.11*** | | 伝説的生物米国会社とヤンソン製薬会社が2022年11月16日に署名した仮供給協定の改正案第3号(これに合併し、参照登録者は2022年11月22日に米国証券取引委員会に提出された6−K表報告(書類番号001−39307)の添付ファイル10.2) |
| | |
4.12* | | 2018年2月26日現在のレジェンド生物米国社、レジェンド生物アイルランド株式会社とヤンソンバイオテクノロジー社との間の協力·許可協定の改正案第1号。 |
| | |
4.13* | | 2018年12月10日、レジェンド·バイオ·アメリカ社、レジェンド·バイオテクノロジー株式会社、ヤンソンバイオテクノロジー社との間の協力·ライセンス協定改正案3。 |
| | |
4.14* | | 2020年11月30日にレジェンド生物米国社、レジェンド生物アイルランド株式会社とヤンソンバイオテクノロジー会社との間の協力·許可協定修正案5 |
| | |
4.15*^ | | 2020年12月7日にレジェンド生物米国社、レジェンド生物アイルランド株式会社とヤンソンバイオテクノロジー会社との間の協力·許可協定改正案6。 |
| | |
4.16*^ | | 2021年7月26日伝説的生物米国社、伝説生物アイルランド有限会社、ヤンソン生物技術会社とヤンソン製薬会社との間の協力と許可協定改正案第7号。 |
| | |
| | | | | | | | |
4.17*^ | | 2021年11月11日伝説的生物米国社、伝説生物アイルランド株式会社、ヤンソンバイオテクノロジー会社、ヤンソン製薬会社との間の協力と許可協定改正案8。 |
| | |
4.18*^ | | 2022年7月7日伝説的生物米国社、伝奇生物アイルランド株式会社、ヤンソン生物技術会社とヤンソン製薬会社との協力と許可協定第9号改正案。 |
| | |
8.1 | | 登録者の主な付属会社リスト |
| | |
| 11.1*** | | 登録者商業行為と道徳基準(これに合わせて、2020年5月29日に米国証券取引委員会に提出された登録者F−1表(文書番号333−238232)添付ファイル99.1)を参照) |
| | |
12.1* | | 2002年サバンズ·オキシリー法第302条に基づいて発行されたCEO証明書 |
| | |
12.2* | | 2002年サバンズ·オキシリー法第302条に基づいて発行された最高財務官証明書 |
| | |
13.1** | | 2002年サバンズ·オキシリー法第906条に基づいて発行された最高経営責任者証明書 |
| | |
13.2** | | 2002年サバンズ·オキシリー法第906条に基づいて発行された首席財務官証明書 |
| | |
15.1* | | 独立公認会計士事務所安永会計士事務所の同意を得ました。 |
| | |
| 15.2* | | 独立公認会計士事務所安永華明法律事務所の同意を得た |
| | |
| 15.3** | | 表格20-F第16 I(A)項に基づいて提出された“外国会社責任追及法案”に関する書類 |
| | |
16.1* | | 安永華明有限責任会社の独立公認会計士事務所変更に関する書簡は、期日は2023年3月30日。 |
| | |
| 101* | | 以下の資料は伝奇生物会社がiXBRL(内連拡張可能商業報告言語)形式で作成したForm 20.F報告書から抜粋した:(1)総合損益及びその他の全面収益表、(2)総合財務状況表、(3)総合権益変動表、(4)総合キャッシュフロー表、(5)総合財務諸表付記。 |
| | |
| 104* | | 表紙相互データファイル(添付ファイル101に含まれるイントラネットXBRLのフォーマット) |
*本年度レポートと一緒にテーブル20-Fで提出します。
**本年次報告書は、テーブル20-F形式で提供されます
*前に提出されました
+管理契約または補償計画を示す
^米国証券取引委員会によって公布されたS-K法規第601(B)(10)(Iv)項によれば、本展覧会のいくつかの部分は、いずれも実質的ではないので、開示されている場合は競争に損害を与えるため、編集されている。登録者は、米国証券取引委員会の要求に応じて、編集されていない本展覧会のコピーを提供することに同意する。
サイン
登録者は、それが20-F表を提出するすべての要求に適合し、本年度報告書に署名するために以下の署名者を正式に手配し、許可したことを証明する。
| | | | | |
| 伝奇生物集団 |
| |
| /s/Huangに対応 |
| 名前:Huang |
| 肩書:CEO |
| |
日付:2023年3月30日 | |
伝奇生物集団
連結財務諸表索引
| | | | | |
| ページ |
独立公認会計士事務所レポート(PCAOB ID:42) | F-2 |
独立公認会計士事務所レポート(PCAOB ID:1408) | F-6 |
| 監査された連結財務諸表 | |
年度までの総合損益表その他包括収益表2022年12月31日, 2021そして2020 | F-7 |
会計年度総合財務状況表2022年12月31日そして2021 | F-8 |
同年度までの総合権益変動表2022年12月31日, 2021そして2020 | F-9とF-8 |
年度までの連結現金フロー表2022年12月31日, 2021そして2020 | F-10とF-11 |
年度までの総合財務諸表付記2022年12月31日, 2021そして2020 | F-13戦闘機F-65戦闘機 |
独立公認会計士事務所報告
伝説的な生物会社の株主と取締役会へ
財務諸表のいくつかの見方
当社は、添付されている伝奇生物会社(当社)の2022年12月31日現在の総合財務状況表、2022年12月31日現在の関連総合損益表及びその他の包括収益表、2022年12月31日現在の年度権益及びキャッシュフロー変動表及び関連付記(総称して“総合財務諸表”と呼ぶ)を監査している。総合財務諸表は,すべての重要な点において,会社が2022年12月31日に発表した財務状況と,2022年12月31日までの年度の経営結果とキャッシュフローを公平に反映しており,国際会計基準委員会が発表した国際財務報告基準に適合していると考えられる。
また、米国上場企業会計監督委員会(PCAOB)の基準に基づき、テレデビル委員会後援組織委員会が発表した“内部統制-総合枠組み(2013枠組み)”で確立された基準に基づき、2022年12月31日までの財務報告内部統制を監査し、2023年3月29日に発表された報告に反対意見を示した。
意見の基礎
これらの財務諸表は会社の経営陣が責任を負う。私たちの責任は私たちの監査に基づいて会社の財務諸表に意見を発表することです。私たちはPCAOBに登録されている公共会計士事務所で、アメリカ連邦証券法およびアメリカ証券取引委員会とPCAOBの適用規則と法規に基づいて、私たちは会社と独立しなければなりません。
私たちはPCAOBの基準に従って監査を行っている。これらの基準は、財務諸表に重大な誤報がないかどうかに関する合理的な保証を得るために、エラーによるものであっても不正であっても、監査を計画し、実行することを要求する。我々の監査には、財務諸表の重大な誤報リスクを評価するプログラム、エラーによるものであれ詐欺であっても、これらのリスクに対応するプログラムを実行することが含まれています。これらの手続きは、財務諸表中の金額および開示に関連する証拠をテストに基づいて検討することを含む。我々の監査には、経営陣が使用する会計原則の評価と重大な見積もり、財務諸表の全体列報を評価することも含まれています。私たちは私たちの監査が私たちの観点に合理的な基礎を提供すると信じている。
重要な監査事項
以下に述べる重要な監査事項とは、監査委員会に伝達または要求が監査委員会に伝達された当期財務諸表監査によって生じる事項である:(1)財務諸表に対して重大な意義を有する勘定または開示に関するものであり、(2)特に挑戦的で主観的または複雑な判断に関するものである。重要監査事項の伝達は、総合財務諸表に対する私たちの全体的な意見をいかなる方法でも変えることはなく、以下の重要な監査事項を伝達することによって、重要な監査事項またはそれに関連する勘定または開示について個別の意見を提供することはない。
| | | | | | | | |
| | Janssen Biotech,Inc.との協力と許可協定。 |
| | |
| 関係事項の記述 | | 総合財務諸表付記2で述べたように、当社はヤンソン生物科学技術会社(“ヤンソン”)と協力及び許可協定(“協力協定”)を締結している。提携協定によると、同社はJanssenにCilta-celの開発·商業化を世界的に独占的に許可した。人民Republic of Chinaを除いて、当社と楊森平はCARVYKTIのすべての収入、費用と利益を分けた。 監査同社の協力協定は挑戦的であり、権威ある会計指導を適用するためには重大な判断が必要である。会社は協力契約に適用される権威ある指導を決定する上で,連携収入,連携収入コスト,連携在庫,連携資産リースに関する指導を含む重大な判断を行っている。 |
| | |
| 私たちが監査でどのようにこの問題を解決したのか | | 当社の監査プログラムテスト会社は、契約協定の読み取り及び改訂、重要な条項の識別に対する管理層の完全性、及び顧客の識別を含む合意条項及び改正関連会計の影響を評価することを含む協力協定の権威ある指導の適用状況をテストする。また、経営陣の権威的な指針の選択と応用の適切性とその会計政策の決定と一致性を評価し、記録された金額と会社の会計政策と関連文書との一致性を比較した。
|
/s/ 安永法律事務所
2022年以来、私たちは会社の監査役を務めてきた。
イセリンニュージャージー州
2023年3月29日
独立公認会計士事務所報告
伝説的な生物会社の株主と取締役会へ
財務報告の内部統制については
私たちは、トレデビル委員会発足組織委員会が発表した“内部統制-総合枠組み”で確立された基準に基づいて、伝説生物の2022年12月31日までの財務報告内部統制を監査した(2013年の枠組み) (COSO標準)。以下に述べる重大な弱点が制御基準目標の実現に及ぼす影響により,伝説的生物会社(当社)は2022年12月31日までCOSO規格に基づいて財務報告に有効な内部統制を維持していないと考えられる。
重大な欠陥とは、財務報告の内部統制に欠陥或いは欠陥の組み合わせが存在し、当社の年度或いは中期財務諸表の重大な誤報が合理的な可能性があり、適時に防止或いは発見できないようにすることである。以下のような重大な弱点が明らかになり、経営陣の評価に組み込まれている。管理層は制御面の重大な弱点を発見し、これは複雑な手配に対する十分な審査と監視制御の不足と関係があり、特に会社の独占的な協力と許可プロトコル、及び会社の財務報告の流れを支持する肝心な情報技術システムの特権と通常のユーザーのアクセスと変更管理領域の情報技術の一般制御に関する制御を含み、関連する流れレベルの情報技術依存制御と応用制御を含む
米国上場企業会計監督委員会(PCAOB)の基準に従って、添付されている当社の2022年12月31日までの総合財務状況表、2022年12月31日までの関連総合損益表、その他の全面収益表、権益と現金流量の変化、および関連付記を監査しました。2022年の総合財務諸表の監査に適用される監査テストの性質、時間、範囲を決定する際には、これらの重大な弱点が考慮されており、本報告は2023年3月29日の報告に影響を与えず、この報告について保留されていない意見を発表している。
意見の基礎
当社経営陣は、効果的な財務報告内部統制を維持し、添付されている“経営陣財務報告内部統制年次報告”における財務報告内部統制の有効性を評価する責任がある。私たちの責任は私たちの監査に基づいて、会社の財務報告書の内部統制に意見を述べることです。私たちはPCAOBに登録されている公共会計士事務所で、アメリカ連邦証券法およびアメリカ証券取引委員会とPCAOBの適用規則と法規に基づいて、私たちは会社と独立しなければなりません。
私たちはPCAOBの基準に従って監査を行っている。これらの基準は、財務報告の有効な内部統制がすべての重要な面で維持されているかどうかを決定するために、合理的な保証を得るために監査を計画し、実行することを要求する。
我々の監査には,財務報告の内部統制を理解すること,重大な弱点があるリスクを評価すること,評価されたリスクテストに基づいて内部統制の設計·運用有効性を評価すること,および状況下で必要と考えられる他のプロセスを実行することが含まれる。私たちは私たちの監査が私たちの観点に合理的な基礎を提供すると信じている。
財務報告の内部統制の定義と限界
会社の財務報告に対する内部統制は、公認された会計原則に基づいて、財務報告の信頼性と外部目的の財務諸表の作成に合理的な保証を提供することを目的としたプログラムである。会社の財務報告に対する内部統制には、(1)会社の資産の取引および処分の記録を合理的かつ詳細かつ正確に反映する記録を保存することに関連する政策および手順、(2)公認された会計原則に基づいて財務諸表を作成するために取引が必要とされる合理的な保証を提供すること、および会社の収入および支出が会社の管理職および取締役の許可のみに基づいて行われるための合理的な保証を提供すること、および、企業の収入および支出が会社の管理職および取締役の許可のみに基づいて行われること、の政策および手続きが含まれる。(3)財務諸表に重大な影響を与える可能性のある不正買収、使用または処分会社の資産を防止またはタイムリーに発見することについて合理的な保証を提供する。
その固有の限界のため、財務報告書の内部統制は誤った陳述を防止したり発見できない可能性がある。また,将来的にどのような有効性評価を行うかの予測は,条件の変化により制御不足のリスクが生じる可能性があり,あるいは政策やプログラムの遵守度が悪化する可能性がある.
/S/安永法律事務所
イセリンニュージャージー州
2023年3月29日
独立公認会計士事務所報告
伝説的な生物会社の株主と取締役会へ
財務諸表のいくつかの見方
当社は、添付されている伝説的生物(“御社”)を2021年12月31日までの総合財務状況表、2021年12月31日までの両年度の各年度の関連総合損益表及びその他の全面収益表、権益及びキャッシュフロー変動表及び関連付記(総称して“総合財務諸表”と呼ぶ)を監査している。総合財務諸表は,すべての重要な点で,会社が2021年12月31日に発表した財務状況と,2021年12月31日までの2年度の経営結果とキャッシュフローを公平に反映しており,国際会計基準委員会が発表した国際財務報告基準に適合していると考えられる。
意見の基礎
これらの財務諸表は会社の経営陣が責任を負う。私たちの責任は私たちの監査に基づいて会社の財務諸表に意見を発表することです。私たちはPCAOBに登録されている公共会計士事務所で、アメリカ連邦証券法およびアメリカ証券取引委員会とPCAOBの適用規則と法規に基づいて、私たちは会社と独立しなければなりません。
私たちはPCAOBの基準に従って監査を行っている。これらの基準は、財務諸表に重大な誤報がないかどうかに関する合理的な保証を得るために、エラーによるものであっても不正であっても、監査を計画し、実行することを要求する。我々の監査には、財務諸表の重大な誤報リスクを評価するプログラム、エラーによるものであれ詐欺であっても、これらのリスクに対応するプログラムを実行することが含まれています。これらの手続きは、財務諸表中の金額および開示に関連する証拠をテストに基づいて検討することを含む。我々の監査には、経営陣が使用する会計原則の評価と重大な見積もり、財務諸表の全体列報を評価することも含まれています。私たちは私たちの監査が私たちの観点に合理的な基礎を提供すると信じている。
/安永華明法律事務所
私たちは2020年から2022年まで当社の監査役を務めています。
上海、人民のRepublic of China
2022年3月31日、連結財務諸表に対する訂正誤りの影響を除いて、その日付は2023年2月17日
伝奇生物集団
合併損益表とその他の包括収益表
2022年まで、2022年、2021年および2020年12月31日まで年度
| | | | | | | | | | | | | | | | | | | | | | | |
| 備考 | | 2022 | | 2021 | | 2020 |
| | | ドル、000ドル
除
1株当たりのデータ | | ドル、000ドル
除
1株当たりのデータ | | ドル、000ドル
除
1株当たりのデータ |
| 収入.収入 | 5 | | | | | | |
| 許可証収入 | | | 50,000 | | | 65,402 | | | 75,000 | |
| 協力収入 | | | 66,677 | | | — | | | — | |
| その他の収入 | | | 328 | | | 3,424 | | | — | |
| 総収入 | | | 117,005 | | | 68,826 | | | 75,000 | |
| 収入の協力コスト | | | (65,363) | | | — | | | — | |
| 他の収入と収益 | 5 | | 12,049 | | | 3,059 | | | 6,119 | |
| 研究開発費 | | | (335,648) | | | (313,346) | | | (232,160) | |
| 行政費 | | | (80,631) | | | (46,961) | | | (23,134) | |
| 販売と流通費用 | | | (93,417) | | | (102,542) | | | (49,571) | |
| その他の費用 | | | (9,823) | | | (9,132) | | | (346) | |
| 株式証負債の公正価値損益を認める | | | 20,900 | | | (6,200) | | | — | |
| 転換可能優先株の公正価値損失 | | | — | | | — | | | (79,984) | |
| 融資コスト | 7 | | (10,796) | | | (900) | | | (4,209) | |
| 税引き前損失 | 6 | | (445,724) | | | (407,196) | | | (308,285) | |
| 所得税(費用)/控除 | 8 | | (625) | | | 3,614 | | | 41,912 | |
| 本年度の赤字 | | | (446,349) | | | (403,582) | | | (266,373) | |
| なぜなら: | | | | | | | |
| 親会社の普通株保有者 | | | (446,349) | | | (403,582) | | | (266,373) | |
| 親会社の普通株主は1株当たりの損失を占めるべきだ | 9 | | | | | | |
| 基本的な情報 | | | (1.40) | | | (1.43) | | | (1.13) | |
| 薄めにする | | | (1.40) | | | (1.43) | | | (1.13) | |
| その他総合収益 | | | | | | | |
| その後、損益の他の包括的収益に再分類することができる: | | | | | | | |
| 為替差異: | | | | | | | |
| 渉外業務翻訳のコミュニケーションの違い | | | 9,807 | | | 5,215 | | | 4,078 | |
| 今後の期間で損益に再分類できる他の総合収益純額 | | | 9,807 | | | 5,215 | | | 4,078 | |
| 今年度の税額控除後のその他の全面的な収入 | | | 9,807 | | | 5,215 | | | 4,078 | |
| 本年度の総合損失総額 | | | (436,542) | | | (398,367) | | | (262,295) | |
| なぜなら: | | | | | | | |
| 親会社の普通株保有者 | | | (436,542) | | | (398,367) | | | (262,295) | |
付記は総合財務諸表の構成要素である。
伝奇生物集団
合併財務状況表
2022年、2022年、2021年12月31日まで
| | | | | | | | | | | | | | | | | | | | |
| 備考 | | 2022年12月31日 | | 2021年12月31日 | |
| | | ドル‘000ドル | | ドル‘000ドル | |
| 非流動資産 | | | | | | |
| 財産·工場·設備 | 10 | | 105,168 | | | 102,506 | | |
| 財産·工場·設備の前払金 | | | 914 | | | 2,168 | | |
| 使用権資産 | 13 | | 55,590 | | | 38,283 | | |
| 定期預金 | 19 | | — | | | 4,705 | | |
| 無形資産 | 11 | | 3,409 | | | 4,684 | | |
| 協業プリペイドリース | 13 | | 65,276 | | | 12,121 | | |
| 他の非流動資産 | 12 | | 1,487 | | | 5,148 | | |
| 非流動資産総額 | | | 231,844 | | | 169,615 | | |
| 流動資産 | | | | | | |
| 協業在庫 | 15 | | 10,354 | | | 1,749 | | |
| 売掛金 | 16 | | 90 | | | 50,410 | | |
| 前払金、その他の入金、その他の資産 | 17 | | 61,755 | | | 13,852 | | |
| 公正価値に基づいて損益する金融資産 | 34 | | 185,603 | | | — | | |
| 余剰コストで計量された金融資産 | 18 | | — | | | 29,937 | | |
| 質入れ預金 | 19 | | 1,270 | | | 1,444 | | |
| 定期預金 | 19 | | 54,016 | | | 163,520 | | |
| 現金と現金等価物 | 19 | | 786,031 | | | 688,938 | | |
| 流動資産総額 | | | 1,099,119 | | | 949,850 | | |
| 総資産 | | | 1,330,963 | | | 1,119,465 | | |
| 流動負債 | | | | | | |
| 貿易応払い | 20 | | 32,893 | | | 7,043 | | |
| その他の支払及び課税項目 | 21 | | 184,109 | | | 123,558 | | |
| 政府支出 | 24 | | 451 | | | 304 | | |
| 賃貸負債 | 13 | | 3,563 | | | 911 | | |
| 税金を納めるべきだ | | | 9,772 | | | 9,488 | | |
| 株式証法的責任 | 23 | | 67,000 | | | 87,900 | | |
| 流動負債総額 | | | 297,788 | | | 229,204 | | |
| 非流動負債 | | | | | | |
| 協力利息前払い資金 | 25 | | 260,932 | | | 120,462 | | |
| 長期賃貸負債 | 13 | | 20,039 | | | 1,593 | | |
| 政府支出 | 24 | | 7,659 | | | 1,866 | | |
| 他の非流動負債 | | | 233 | | | 396 | | |
| 非流動負債総額 | | | 288,863 | | | 124,317 | | |
| 総負債 | | | 586,651 | | | 353,521 | | |
| 株権 | | | | | | |
| 株本 | 26 | | 33 | | | 31 | | |
| 埋蔵量 | 29 | | 744,279 | | | 765,913 | | |
| 普通株主権益総額 | | | 744,312 | | | 765,944 | | |
| 総株 | | | 744,312 | | | 765,944 | | |
| 負債と権益総額 | | | 1,330,963 | | | 1,119,465 | | |
付記は総合財務諸表の構成要素である。
伝奇生物集団
合併権益変動表
| | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | |
| 親会社に所属する持分所有者 | | |
| 共有
資本 | | 共有
高級* | | 株式を基礎とする
補償する
備蓄* | | 外国.外国
貨幣
訳す
備蓄* | | 保留する
収益/収益
(累計)
損失)* | | 合計する
株権 |
| ドル‘000ドル | | ドル‘000ドル | | ドル‘000ドル | | ドル‘000ドル | | ドル‘000ドル | | ドル‘000ドル |
| 2020年1月1日まで | 20 | | | 3,908 | | | 1,976 | | * | (4,429) | | | 149,848 | | | 151,323 | |
| 本年度の赤字 | — | | | — | | | — | | | — | | | (266,373) | | | (266,373) | |
| その他の全面的な損失: | | | | | | | | | | | |
| 渉外業務翻訳のコミュニケーションの違い | — | | | — | | | — | | | 4,078 | | | — | | | 4,078 | |
| 本年度の総合損失総額 | — | | | — | | | — | | | 4,078 | | | (266,373) | | | (262,295) | |
| 転換可能優先株を普通株に転換する | 2 | | | 240,432 | | | — | | | — | | | — | | | 240,434 | |
| 普通株を初公開発行するために発行コストを差し引く | 4 | | | 450,081 | | | — | | | — | | | — | | | 450,085 | |
| GenSCRIPT私募に関する普通株を発行する | — | | | 12,000 | | | — | | | — | | | — | | | 12,000 | |
| 購入権を行使する | 1 | | | 1,885 | | | (422) | | | — | | | — | | | 1,464 | |
| 持分決算持分報酬費 | — | | | — | | | 4,760 | | | — | | | — | | | 4,760 | |
| 2020年12月31日まで | 27 | | | 708,306 | | * | 6,314 | | * | (351) | | * | (116,525) | | * | 597,771 | |
| 本年度の赤字 | — | | | — | | | — | | | — | | | (403,582) | | | (403,582) | |
| その他の全面的な損失: | | | | | | | | | | | |
| 渉外業務翻訳のコミュニケーションの違い | — | | | — | | | — | | | 5,215 | | | — | | | 5,215 | |
| 本年度の総合損失総額 | — | | | — | | | — | | | 5,215 | | | (403,582) | | | (398,367) | |
| 機関投資家指向増発に関する普通株を発行する | 2 | | | 218,298 | | | — | | | — | | | — | | | 218,300 | |
後続の公開発行のために普通株を発行し,純額
発行コスト | 2 | | | 323,438 | | | — | | | — | | | — | | | 323,440 | |
| 購入権を行使する | | | 6,089 | | | (1,447) | | | — | | | — | | | 4,642 | |
| 既存限定株式単位の再分類 | | | 5,323 | | | (5,323) | | | — | | | — | | | — | |
| 持分決算持分報酬費 | | | | | 20,158 | | | — | | | — | | | 20,158 | |
| 2021年12月31日まで | 31 | | | 1,261,454 | | * | 19,702 | | * | 4,864 | | * | (520,107) | | * | 765,944 | |
| 本年度の赤字 | — | | | — | | | — | | | — | | | (446,349) | | | (446,349) | |
| その他の全面的な損失: | | | | | | | | | | | — | |
| 渉外業務翻訳のコミュニケーションの違い | — | | | — | | | — | | | 9,807 | | | — | | | 9,807 | |
| 本年度の総合損失総額 | — | | | — | | | — | | | 9,807 | | | (446,349) | | | (436,542) | |
後続の公開発行のために普通株を発行し,純額
発行コスト | 2 | | | 377,641 | | | — | | | — | | | — | | | 377,643 | |
| 購入権を行使する | — | | | 4,070 | | | (1,141) | | | — | | | — | | | 2,929 | |
| 既存限定株式単位の再分類 | — | | | 13,850 | | | (13,850) | | | — | | | — | | | — | |
| 持分決算持分報酬費 | — | | | — | | | 34,338 | | | — | | | — | | | 34,338 | |
| 2022年12月31日まで | 33 | | | 1,657,015 | | * | 39,049 | | * | 14,671 | | * | (966,456) | | * | 744,312 | |
*これらの準備口座には#ドルの総合備蓄が含まれている744.3百万ドル765.9百万ドルとドル597.72022年、2021年、2020年12月31日の総合財務状況表の百万ドル
伝奇生物集団
統合現金フロー表
2022年まで、2022年、2021年および2020年12月31日まで年度
| | | | | | | | | | | | | | | | | | | | | | | |
| 備考 | | 2022 | | 2021 | | 2020 |
| | | ドル‘000ドル | | ドル‘000ドル | | ドル‘000ドル |
| 経営活動のキャッシュフロー | | | | | | | |
| 税引き前損失 | | | (445,724) | | | (407,196) | | | (308,285) | |
| 以下の項目を調整する | | | | | | | |
| 財政収入 | 5 | | (8,182) | | | (971) | | | (2,930) | |
| 融資コスト | 7 | | 10,796 | | | 900 | | | 4,209 | |
| 財産·工場·設備の減価償却 | 10 | | 10,173 | | | 8,139 | | | 6,234 | |
| 財産·工場·設備の損失を処分する | 6 | | 481 | | | 974 | | | 55 | |
| 無形資産の償却 | 11 | | 2,476 | | | 1,379 | | | 192 | |
| 使用権資産減価償却 | 13 | | 5,743 | | | 4,399 | | | 3,507 | |
| 公正価値(収益)/株式証負債損失を認める | 23 | | (20,900) | | | 6,200 | | | — | |
| 転換可能優先株の公正価値損失 | | | — | | | — | | | 79,984 | |
| 公正価値に応じて損益変動により計量された金融資産の公正価値収益 | 5 | | (593) | | | — | | | (47) | |
| 外貨為替損失/(収益)、純額 | | | 9,159 | | | 4,867 | | | (66) | |
| 持分決算持分報酬費 | | | 34,338 | | | 20,158 | | | 4,760 | |
| 繰延の政府支出 | 24 | | (307) | | | (295) | | | (114) | |
| | | (402,540) | | | (361,446) | | | (212,501) | |
| 貿易売掛金減少/(増加) | | | 50,320 | | | 24,590 | | | (45,000) | |
| (追加)/前払金、その他の入金、およびその他の資産の削減 | | | (50,614) | | | (2,966) | | | 3,366 | |
| その他非流動資産の減少/(増加) | | | 3,661 | | | (1,175) | | | (3,973) | |
| 連携在庫(増加)/減少 | | | (8,605) | | | 51 | | | (643) | |
| 政府から資金を受け取りました | 24 | | 6,180 | | | 80 | | | 2,452 | |
| 貿易未払い増加/(減少) | | | 25,850 | | | 1,805 | | | (4,348) | |
| その他の支払·課税項目の増加 | | | 165,883 | | | 140,747 | | | 26,932 | |
| その他非流動負債の増加/(減少) | | | (163) | | | (158) | | | 554 | |
| 質入れ預金の純額が増加する | | | (15) | | | (1,060) | | | (128) | |
| 運営に使われている現金 | | | (210,043) | | | (199,532) | | | (233,289) | |
| 所得税を納めた | | | — | | | — | | | (278) | |
| 受取利息収入 | | | 5,580 | | | 652 | | | 3,366 | |
| 所得税を徴収した | | | 3,709 | | | 557 | | | 7,391 | |
| 賃貸払いの利息 | | | (527) | | | (142) | | | (195) | |
| 経営活動のための現金純額 | | | (201,281) | | | (198,465) | | | (223,005) | |
付記は総合財務諸表の構成要素である。
伝奇生物集団
合併現金フロー表(継続)
2022年まで、2022年、2021年および2020年12月31日まで年度
| | | | | | | | | | | | | | | | | | | | | | | |
| 注意事項 | | 2022 | | 2021 | | 2020 |
| | | ドル‘000ドル | | ドル‘000ドル | | ドル‘000ドル |
| 投資活動によるキャッシュフロー | | | | | | | |
| 家屋·工場·設備を購入する | | | (20,927) | | | (42,197) | | | (26,254) | |
| 無形資産を購入する | | | (1,348) | | | (3,207) | | | (4,029) | |
| 協力者に協力資産を前払いする | | | (14,810) | | | (1,708) | | | (19,493) | |
| 公正価値で損益により計量された金融資産を購入する | | | (285,000) | | | (50,000) | | | (22,682) | |
| 金融資産から受け取った現金を引き出し,公正価値に応じて損益で計量する | | | 99,990 | | | 50,081 | | | 22,682 | |
| 金融資産の引き出しから受け取った現金は剰余コストで計量する | | | 30,000 | | | — | | | — | |
| 投資収益の現金収入 | | | 1,252 | | | — | | | 47 | |
| 財産·工場·設備を処分して得た収益 | | | — | | | 4 | | | 1 | |
| 定期預金の付加額 | | | (369,971) | | | (298,107) | | | (50,000) | |
| 定期預金が減る | | | 483,617 | | | 180,000 | | | 75,559 | |
| 抵当預金減少 | | | 105 | | | — | | | — | |
| 余剰コストで計量された金融資産を購入する | | | — | | | (29,849) | | | — | |
| 投資活動のための現金純額 | | | (77,092) | | | (194,983) | | | (24,169) | |
| 融資活動によるキャッシュフロー | | | | | | | |
| 関連先の前払い現金を償還する | 32 | | — | | | — | | | (4) | |
| 転換可能な優先株収益 | | | — | | | — | | | 160,450 | |
| 普通株を初公開して得られた収益は,発行コストを差し引く | | | — | | | — | | | 450,085 | |
| GenSCRIPT私募に関する普通株式取得金を発行する | | | — | | | — | | | 12,000 | |
| 普通株を発行して後続公開発行の収益に用い,発行コストを差し引く | | | 377,643 | | | 323,440 | | | — | |
| 機関投資家のための普通株及び私募に関する引受権証を発行して得られた金 | | | — | | | 300,000 | | | — | |
| 持分を行使して得た金 | | | 2,929 | | | 4,642 | | | 1,464 | |
| 転換可能な優先株発行の支出を支払う | | | — | | | — | | | (2,514) | |
| 賃貸支払いの元金部分 | | | (2,596) | | | (1,419) | | | (2,602) | |
| 融資活動が提供する現金純額 | | | 377,976 | | | 626,663 | | | 618,879 | |
伝奇生物集団
合併現金フロー表(継続)
2022年まで、2022年、2021年および2020年12月31日まで年度
| | | | | | | | | | | | | | | | | | | | | | | |
| 注意事項 | | 2022 | | 2021 | | 2020 |
| | | ドル‘000ドル | | ドル‘000ドル | | ドル‘000ドル |
| 現金および現金等価物の純増加 | | | 99,603 | | | 233,215 | | | 371,705 | |
| 為替レート変動の影響,純額 | | | (2,510) | | | 34 | | | 620 | |
| 年初現金および現金等価物 | 19 | | 688,938 | | | 455,689 | | | 83,364 | |
| 年末現金および現金等価物 | 19 | | 786,031 | | | 688,938 | | | 455,689 | |
| 現金および現金等価物残高分析 | | | | | | | |
| 現金と銀行残高 | | | 841,317 | | | 858,607 | | | 506,073 | |
| 差し引く:質抵当預金 | | | 1,270 | | | 1,444 | | | 384 | |
| 定期預金 | | | 54,016 | | | 168,225 | | | 50,000 | |
| 財務状況表に記載されている現金と現金等価物 | 19 | | 786,031 | | | 688,938 | | | 455,689 | |
| 現金フロー表に記載されている現金と現金同等物 | | | 786,031 | | | 688,938 | | | 455,689 | |
付記は総合財務諸表の構成要素である。
伝奇生物集団
連結財務諸表付記
2022年まで、2022年、2021年および2020年12月31日まで年度
1. 企業情報
伝説的な生物会社は2015年5月27日免除された会社としてケイマン諸島“ケイマン諸島会社法”に基づいて限られた責任を負う。当社の登録住所はケイマン諸島ジョージシティ南教堂街103番地ハーバーズスクエア10240郵便ポスト.
伝説的な生物は投資持株会社です。同社の子会社は主に腫瘍学や他の適応の新規細胞療法の発見,開発,製造,商業化に従事している。
伝説的生物の最終持株会社当社取締役会は、ケイマン諸島のある会社がアメリカ合衆国に登録設立されたGenscript Corporation(“Genscript Corp”)であるとしている。
子会社に関する情報
| | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | |
| 会社 | | 場所と期日
のです。
法団に成立する | | 普通版発行
株式/払込持分
資本 | | 持分パーセント
応占利息
会社へ | | 元金
活動する |
| | | | | | 直接パーセント | | 間接率% | | |
| 伝奇生物有限公司(“BVI伝奇”) | | 英領バージン諸島2015年6月2日 | | ドル | 80,000,000 | | | 100 | | | — | | | 投資持株 |
| レジェンド生物香港有限公司(“レノボ香港”) | | 香港、2015年6月3日 | | ドル | 80,000,000 | | | — | | | 100 | | | 投資持株 |
| 南京連想生物科学技術有限公司(“連想南京”) | | 中国*2014年11月17日 | | ドル | 162,500,000 | | | — | | | 100 | | | 生命科学研究製品の製造と販売;性能と研究開発サービスの販売 |
| 伝説的生物アメリカ社(“伝説的アメリカ”) | | アメリカデラウェア州2017年8月31日 | | — | | | — | | | 100 | | | 生命科学製品の製造と販売;生命科学研究と開発の業績 |
| 伝説的生物アイルランド株式会社(“伝説アイルランド”) | | アイルランド、2017年11月13日 | | — | | | — | | | 100 | | | 生命科学製品の製造と販売;生命科学研究と開発の業績 |
| レジェンド·バイオベルギー社(“伝説的ベルギー”) | | ベルギー2021年6月23日 | | ドル | 2,423,693 | | | — | | | 100 | | | 生命科学製品の製造と販売 |
| 海南伝記生物科学技術有限公司(“海南伝記”) | | 中華人民共和国2021年10月25日 | | — | | | — | | | 100 | | | 一般と行政事務 |
**人民Republic of China(“中華人民共和国”または“中国”)は、香港特別行政区中国(“香港”)を含む。
2.1 準備の基礎
当社及びその付属会社(総称して“当社”)の総合財務諸表は、国際会計基準委員会が公布した国際財務報告基準(“IFRS”)に基づいて作成され、この基準はすべての基準及び解釈を含む
公正価値によって計量された金融資産と金融負債を除いて、総合財務諸表はすべて歴史コストに従って作成される。総合財務諸表はドル(“ドル”)に示されており、他に説明がある以外は、すべての価値が最も近い千元に四捨五入されている。
強固な基礎
総合財務諸表には、当社が2022年12月31日までの3年度の各年度の財務諸表を含む。子会社とは、会社によって直接または間接的に制御されるエンティティ(構造化エンティティを含む)を指す。当社が被投資先への参加の可変リターンを直面または獲得する権利があり、被投資先への権限(すなわち、会社が現在被投資先の関連活動を指導する能力がある)によってこれらのリターンに影響を与える能力がある場合には、統制権が実現される。
各付属会社の財務諸表は当社の報告期間と同じであり、一致した会計政策を用いて作成されている。子会社の業績は、会社が支配権を獲得した日から合併し、支配権が終了した日まで合併を続ける。
損益およびその他の全面収益または損失の各部分は当社の親会社の持分所有者に帰属します。当社間の取引に関するすべてのグループ内の資産と負債、権益、収入、費用、キャッシュフローは合併時にすべてログアウトします。
2.2 会計政策と開示の変化
2022年に発効した新国際財務報告基準、改訂、解釈は当社の総合財務諸表に大きな影響を与えていない。
2.3 発表されたがまだ発効していない国際財務報告基準
発表されていないが発効していない新しい指針は、会社の総合財務諸表に大きな影響を与える見通しだ。
2.4 重要会計政策の概要
公正価値計量
当社は各報告期末に公正価値損益によってその金融資産を計量し、公正価値によって株式証負債を計量した。公正価値とは、計量日に市場参加者間の秩序ある取引において資産を売却することによって受信された価格または負債を移転して支払う価格を意味する。公正価値計量の基礎は、資産の売却または負債の移転の取引が資産または負債の主要市場で発生すると仮定すること、または主要市場がない場合、資産または負債の最も有利な市場で発生すると仮定することである。主または最も有利な市場は会社が入ることができるものでなければならない。資産または負債の公正価値は、市場参加者が資産または負債の価格を設定する際に使用する仮定を使用して測定され、市場参加者の行為がその経済的最適な利益に適合することを前提としている
非金融資産の公正価値計量は、資産を最高かつ最適な方法で使用することによって、または資産を最高かつ最適な方法で使用する別の市場参加者に売却することによって、市場参加者が経済的利益を生成する能力を考慮する。
当社は,公正な価値を計量するのに十分なデータがある場合に適用する推定技術を採用し,関連する観察可能な投入を最大限に使用し,観察できない投入を最大限に削減している。
財務諸表の中で公正価値を計量或いは開示するすべての資産と負債はすべて公正価値計量全体に対する重要な最低レベル投入に基づいて、公正価値階層構造の中で以下のように分類される
レベル1-アクティブ市場における同じ資産または負債に基づく見積もり(調整されていない)
第2レベル−公正価値計測に重要な意味を持つことが直接または間接的に観察される最低レベル投入に基づく推定技術
第3レベル−公正価値計測に重要な意味を持つ最低レベル投入が観察されないことに基づく推定技術
財務諸表において恒常的に確認された資産および負債について、当社は、各報告期間の終了時に分類(公正価値全体の計量に重要な最低レベル入力に基づいて)を再評価することにより、階層構造における各レベル間に移行が発生したか否かを決定する。
非金融資産減価準備
減値の兆候がある場合、または資産(契約資産および金融資産を除く)の年間減値テストを行う必要がある場合、その資産の回収可能金額を推定する。資産の回収可能金額は、資産または現金生成単位の使用価値およびその公正価値から処置コストを差し引いた高い者であり、その資産が他の資産または資産群と実質的に独立した現金流入を生じない限り、個別資産によって決定され、この場合、回収可能金額は、資産が属する現金生成単位のために決定される。
1つの資産の帳簿金額がその回収可能金額を超えた場合にのみ、減価損失が確認される。使用価値を評価する際には,現在の市場の貨幣時間価値と資産特有リスクの評価を反映した将来のキャッシュフローを税前割引率を用いて現在値に割引する。減値損失は,減価資産機能と一致する費用種別で発生した期間の損益を計上する.
以前に確認された減価損失がもはや存在しないか、または減少した可能性があることを示す兆候があるかどうかを決定するために、各報告期間の終了時に評価が行われる。もしそのような兆候があれば、回収可能な金額を推定する。以前に確認された営業権以外の資産の減価損失は、当該資産の回収可能金額を決定するための推定値が変化した場合にのみ変化するが、(いかなる減価償却/償却を差し引いても)確定すべき帳簿金額を超えない場合にのみ、打ち消すことができる違います。この資産の減価損失は数年前に確認された。当該等減値損失のインパルスを計上して減値損失が生じた期間の損益を計上する。
関連先
以下の場合、一方は会社と関連があるとみなされる
(a)当事者は一人またはその人の家族の親密なメンバーであり、その人は
(i)当社には支配権または共同支配権があります
(Ii)会社に大きな影響を与える
(Iii)当社の主な管理者または当社の親会社のメンバーです
あるいは…。
(b)当事者は次のいずれかの条件を満たすエンティティである
(i)その実体は当社と同じ会社のメンバーである
(Ii)1つのエンティティは、別のエンティティ(または別のエンティティの親会社、子会社または同系子会社)の共同または合弁企業である
(Iii)この実体は当社と同じ第三者の合弁企業である
(Iv)1つのエンティティは第3のエンティティの合弁企業であり、もう1つのエンティティは第3のエンティティの関連企業である
(v)当該エンティティは、当社又は当社に関連するエンティティの従業員の利益のために設立された退職後福祉計画である
(Vi)このエンティティは、(A)項に列挙された人員によって制御または共同制御される
(Vii)(A)(I)項に記載の人が、エンティティに重大な影響を与えるか、またはエンティティ(またはエンティティの親会社)の鍵管理者のメンバーであるか
(Viii)エンティティまたはその所属会社の任意のメンバーは、会社または親会社にキー管理者サービスを提供する。
財産·工場·設備および減価償却
建設中の工事以外に、物件、工場及び設備はコスト(或いは推定値)から減価償却及びいかなる減価減価損失を引いて帳簿を作成する。1つの財産、工場、および設備のコストは、その購入価格と、その所望の用途のために資産をその動作状態および位置に持っていく任意の直接課税コストとを含む
物件、工場及び設備の運用開始後に発生した支出、例えば修理及び保守は、通常発生期間を損益表及びその他の全面収益に計上する。確認基準を満たした場合には、重大検査の支出を資産の帳簿金額に資本化し、代替とする。例えば、物件、工場及び設備の重要部分は一定期間ごとに交換する必要があり、当社はこのような部分を特定の耐用年数を有する個別資産として確認し、それに応じて減価償却を行う
減価償却は資産の推定耐用年数内で直線的に計算され、方法は以下の通りである
| | | | | |
| 永久保有土地 | 未減価償却 |
| 家を建てる | 39至れり尽くせり50年.年 |
| 賃借権改善 | 賃貸期間または資産年限の短い者 |
| 機械と設備 | 5至れり尽くせり15年.年 |
| コンピュータとオフィス機器 | 3至れり尽くせり5年.年 |
| 輸送設備 | 10年.年 |
1つの財産、工場及び設備の部分が異なる使用寿命を有する場合、この項のコストは、合理的な基準に従って各部分間に割り当てられ、部分毎に個別に減価償却される。少なくとも財政年度終了時には、耐用年数や減価償却方法を審査し、適切な場合に調整する。
最初に確認された任意の重要部分を含む財産、工場、および設備であって、販売時またはその使用または処置が将来の経済的利益をもたらさない場合に確認を取り消されることを特徴とする財産、工場および設備。資産終了確認年度の損益表と他の包括収益表で確認された任意の処分または廃棄損益は、関連資産の販売収益純額と帳簿価値との差額である。
建設工事とは、設置中の設備で、コストからいかなる減価損失を引いても申告し、減価償却をしないことを指す。コストにはインストールの直接コストが含まれる。建設工事が竣工して使用可能な場合は、新たに適切な種類の財産、工場、設備に分類する。
無形資産
単独で買収した無形資産は,初期確認時にコストで計測される.無形資産の使用寿命は限られていると評価された。有限年限を有する無形資産はその後、利用可能な経済年限内に償却し、無形資産が減値可能であることを示す兆候がある場合に減値評価を行う。耐用年数の限られた無形資産の償却期限と償却方法は、少なくとも財政年度終了時に審査を行う。
無形資産は、次のような有用な経済年限で直線的に償却される
研究開発コスト
すべての研究費は発生時に損益表とその他の包括収益を計上した。
企業が使用または販売のために無形資産を完成させる技術的実行可能性、資産を完成させる意図およびその使用または売却を達成する能力、資産がどのように将来の経済効果をもたらすか、プロジェクトを達成するための資源の利用可能性、および開発中に支出を確実に測定する能力を証明することができる場合にのみ、新製品候補製品を開発するためのプロジェクトによって発生する支出は資本化および繰延される。これらの基準を満たしていない候補製品開発支出は発生時に計上される。
賃貸借証書
当社は契約開始時に契約がレンタルであるか含まれているかを評価します。契約が一定期間内に確定された資産の使用権を価格と交換するように制御した場合、契約はレンタルであるか、またはレンタルを含む。
テナントとしての会社
短期賃貸および低価値資産賃貸を除いて、当社はすべての賃貸に対して単一確認および計量方法を採用している。当社は、リース金を支払うリース負債と、対象資産の使用権を代表する使用権資産を確認します。会社は各構成要素の相対的な独立価格に基づいて契約中の対価格を賃貸と非レンタル構成要素に分配することを選択した。
(a)使用権資産
使用権資産はリース開始日(すなわち対象資産が使用可能な日)に確認される。使用権資産は、コストに応じて任意の減価償却および任意の減価損失を差し引いて計量し、リース負債の任意の再計量に基づいて調整する。使用資産コストには、確認されたリース負債額、生成された初期直接コスト、および有効日または前に支払われた賃貸支払いから受信された任意のレンタル報酬が差し引かれることが含まれる使用権資産は、リース期間および資産の推定耐用年数のうち短いものを直線的に減価償却する
| | | | | |
| 借受地 | 50年.年 |
| 家を建てる | 39至れり尽くせり50年.年 |
| 賃借権改善 | 賃貸期間または資産年限の短い者 |
| 機械と設備 | 5至れり尽くせり15年.年 |
| コンピュータとオフィス機器 | 3至れり尽くせり5年.年 |
賃貸資産の所有権が賃貸期間終了時に当社に移転したり、コストが購入選択権の行使を反映している場合は、減価償却は資産の推定耐用年数に応じて計算される。
(b)賃貸負債
レンタル負債は、レンタル開始日にレンタル期間内に支払われたリース支払いの現在値を確認する。賃貸支払いは、固定支払い(実質固定支払いを含む)から任意の受取賃貸報酬を減算すること、指数またはレートに依存する可変賃貸支払い、および残存価値保証に応じて予想される支払い金額を含む。賃貸支払いには、当社が行使する購入選択権の使用価格を合理的に決定することと、レンタル終了の罰金を支払うことも含まれる(レンタル期限が会社がレンタル終了の選択権を行使することを反映している場合)。指数またはレートに依存しない可変リース支払いは、支払いをトリガするイベントまたは条件が発生している間に料金として確認される。レンタル期間には、経営陣が当社が行使する任意のレンタル継続期間を合理的に決定するための評価が含まれています。
賃貸支払いの現在値を計算する際には、当社はレンタル開始日の逓増借入金金利を使用しており、レンタルに隠れている金利が確定しにくいためです。発効日後、賃貸負債額を増加させて利息の増加を反映させ、支払われる賃貸支払いを減少させる。また、賃貸負債の帳簿金額が変動し、リース期限の変化、賃貸支払いの変化(例えば、指数や料率の変化により将来のリース支払いの変化)、または購入対象資産のオプションの評価が変化した場合、賃貸負債の帳簿価値を再計測する。
(c)短期賃貸借契約
当社は短期借約確認免除をその短期賃貸契約に適用しており,この等短期賃貸は発効日からリース期間が12カ月以下で購入選択権を含まない借約である。
短期レンタルのレンタル支払いはレンタル期間中に直線原則で料金として確認されます。
レンタル人としての会社
当社がレンタル者を務めている場合、当社はレンタル開始時(またはレンタル改訂がある場合)に各レンタルをレンタル経営または融資リースに分類します。
当社が資産所有権に付随するほとんどのリスクとリターンを移転しない賃貸は、経営リースに分類されます。賃貸料収入は賃貸期間内に直線法で入金され,その経営性質から損益表その他の全面収益に計上される。交渉および運営リースによる初歩的な直接コストを手配し,賃貸資産の帳簿金額を計上し,賃貸期間内に賃貸料収入と同じ基準で確認した。
協業資産を借りる
ヤンソン合意の条項と条件に基づき、当社とそのパートナーはその協力のための資産を購入し、関連コストを分担する。当社は国際財務報告基準第16号の共同手配に関する指針を採用して、類推的に協力レンタルと協力レンタルの会計処理を行った。
会社のパートナーが当該資産を所有し、かつ、提携合意の条項及び条件に基づいて、会社のパートナーからパートナーへのリースが存在する場合、会社は、パートナーからパートナーにリースされた資産シェアの使用権資産及びリース負債を確認する。通常、連携して共同指導委員会(“JSC”)や他のガバナンス委員会を通じて資産の使用を指導し、使用資産から実質的にすべての経済的利益を得る権利がある。当社がリース開始前に支払った賃貸金は、他の非流動資産に前払い賃貸料として記録され、レンタル開始時に使用権資産に再分類される。
会社が資産を所有し、かつ提携合意の条項や条件に基づいて、会社が提携に対するリースが存在する場合、会社は提携している資産にリースする融資リースを確認する。この場合、当社が共同でコントロールしている資産シェアは、物件、工場、設備に計上され、前金、その他の売掛金、その他の資産の総合財務状況表でパートナーの資産中のシェアとしてレンタルされなければならない。
当社が賃貸金の支払いに主な責任がある場合、当社はそのシェアではなく、協力を代表して締結した賃貸の全リース責任を確認します。会社が協力の主な事業者として賃貸契約の唯一の署名者である場合、状況はそうかもしれない。関連使用権資産が提携に転貸した場合、融資転貸は後で確認します。
投資や他の金融資産
初期認識と測定
金融資産は初期確認時に分類し、その後余剰コストで計量し、損益を通じて公正価値を計上する。
最初に確認した場合の金融資産の分類は,金融資産の契約キャッシュフローの特徴と,会社がこれらの資産を管理するビジネスモデルに依存する.重大融資部分を含まない売掛金や当社がすでに実際の便宜をとって重大融資部分の影響を調整しない以外、当社は最初にその公正価値に基づいて金融資産を計量し、もし金融資産が公正価値に基づいて損益を計上しなければ、取引コストに従って計量する。重大な融資成分や当社が実際に便宜的な売掛金を申請したことを含まず、以下の“収入確認”政策に基づき、国際財務報告基準第15号に基づいて定められた取引価格を計量する
1つの金融資産を剰余コストによって分類し、計量するためには、元金を返済していない元金と利息(“SPPI”)のみに支払うキャッシュフローを生成する必要がある。業務モデルにかかわらず、キャッシュフローがSPPIではない金融資産はすべて公正価値によって損益による分類と計量を行う。
当社が金融資産を管理する業務モデルとは、その金融資産をどのように管理してキャッシュフローを生成するかということです。ビジネスモデルは、キャッシュフローが収集契約キャッシュフローからか、金融資産を売却するか、両者を兼ねているかを決定している。余剰コスト別に分類·計量された金融資産を1つの業務モデルで保有し、契約キャッシュフローを収集するために金融資産を保有することを目的とする
通常の方法で金融資産を購入および売却するすべての取引は、取引日、すなわち会社が資産の購入または売却を承諾した日に確認される。通常の購入または販売とは、市場法規または慣行が一般的に決定された期間内に資産を交付することを要求する金融資産を購入または売却することを意味する。
後続測定
償却コストに応じて計量された金融資産(債務ツール)
償却コストによって計量された金融資産はその後、実際の利息法を用いて計量し、減価を計算すべきである。資産が確認解除、修正または減値された場合、損益は損益表および他の包括収益表で確認される。
計量金融資産 公正価値に応じて損益を計上する
公正価値に応じて損益により計量された金融資産は財務状況表に公正価値で勘定され、公正価値純変動は損益表とその他の全面収益で確認される
当社は損益により公正価値に計量された金融資産を通貨市場基金から構成し、貨幣市場基金は公正価値レベルで第1級に分類される
金融資産は再確認しない
以下の場合、1つの金融資産(または適用される場合、1つの金融資産の一部または同様の金融資産の一部)は、主にキャンセル確認される(すなわち、企業の総合財務状況表から削除される)
•資産からキャッシュフローを取得する権利が満期になった;または
•当社は、当該資産からキャッシュフローを受け取る権利を譲渡したか、または“伝達”スケジュールに従って、受信したキャッシュフローを第三者に全数支払う義務を負い、および(A)当社が当該資産の実質的にすべてのリスクおよびリターンを移転したか、または(B)当社は当該資産の実質的なすべてのリスクおよびリターンを移転も保持していないが、当該資産の制御権を移転した。
当社が資産からキャッシュフローを受け取る権利を譲渡したり、送達手配を締結したりする場合、当社は、資産所有権をどの程度保持しているかのリスクおよびリターンを評価します。会社が資産のすべてのリスクやリターンを移転または保持していない場合、資産の支配権も移転していない場合、会社が継続的に参加している範囲で、会社は移転した資産を確認し続ける。この場合、当社は関連負債も確認しました。移転された資産と関連負債は、会社が保持している権利と義務を反映した基準で計量される。
譲渡資産を担保形式で継続的に参加する資産の原始帳簿金額と、当社が返済を要求される可能性のある最高対価格金額のうち低い者を計量する。
金融資産減価準備
当社は、公正価値に応じて損益に保有しているすべての債務ツールの予想信用損失準備(“ECL”)を確認していない。ECLは,契約満期に応じた契約キャッシュフローと会社が予想して受信したすべてのキャッシュフローとの差額に基づいて,元の有効金利の近似値で割引する.期待されるキャッシュフローは、保有する担保または契約条項の構成要素としての他のクレジット増強によって生成されるキャッシュフローを含むことが予想される。
一般的な方法
ECLの認識は2段階に分けられる.最初に確認されてから信用リスクが著しく増加していない信用リスク開放については,今後12カ月以内に発生する可能性のある違約事件(12カ月ECL)による信用損失にECLを提供する。最初に確認されて以来信用リスクが著しく増加している信用リスク開放については,違約時間(終身ECL)にかかわらず,リスク開放残寿命内に予想される信用損失準備金を用意する必要がある。
報告日ごとに、当社は、金融商品の信用リスクが初期確認以来大幅に増加しているか否かを評価する。評価を行う際に、当社は報告日に当該金融商品に違約が発生するリスクと初期確認日に当該金融商品に違約が発生するリスクを比較し、不当なコスト或いは努力がない場合に得られる合理的かつ支持可能な資料を考慮し、歴史と展望性資料を含む。
契約支払いが90日を超えた場合、会社は契約違反金融資産とみなされるだろう。しかし、場合によっては、社内または外部情報が、当社が保有するいかなる信用向上を考慮する前に未返済の契約金額を全額受け取ることが不可能であることを示す場合もあり、当社は金融資産を違約と見なす可能性もある。契約キャッシュフローを回収する合理的な期待が存在しない場合、金融資産はログアウトされる。
余剰コストによって計量した金融資産は一般的な方法で減値を提案し、以下の段階でECLを計量する必要があるが、以下に詳述簡略化方法を採用した売掛金及び契約資産は除外する。
第1段階−初回確認以来信用リスクが著しく増加していない金融商品,その損失準備金の計算金額は12カ月のECLに相当する
第2段階--初回確認以来信用リスクは著しく増加しているが信用被害金融資産ではない金融商品であり、その損失準備金の計算金額は生涯ECLに等しい
ステップ3--報告日がクレジット減値の金融資産(ただし、クレジット減価を購入または生成する金融資産ではない)であり、その損失計上の計量金額は、生涯ECLに等しい。
簡略化方法
重大融資部分を含まない貿易売掛金や契約資産について、あるいは当社が重大な融資部分の影響を調整しない実際の便宜策をとった場合、当社はECLを計算する際に簡略化方法を採用する。簡略化方法では,当社は信用リスクの変化を追跡するのではなく,報告日ごとに終身ECLにより損失準備金を確認する。当社はその歴史的信用損失経験に基づく準備行列を構築し、債務者と経済環境の特定の前向き要因に基づいて調整を行った。
金融負債
初期認識と測定
すべての金融負債は最初に公正価値で確認され、融資および借入金および支払いについては、直接取引コストの純額を占めるべきであることが確認された。
会社の財務負債には、貿易売掛金、その他の売掛金、株式承認債務、協力利息前払い資金、リース債務が含まれる。
後続測定
償却コストで計量された金融負債(ローンと借金)
最初に確認した後、アモーティでの計量協力利息の前払い資金zコストは、有効金利法を用いて、割引の影響が重要でない限り、この場合、それらはコスト順に示される。収益も損失も確認されましたz負債が再確認されない場合は、損益表及びその他の包括収益表に計上するz有効金利で償却しますz変化の過程です
アモールティz対外債務コストの算出方法は、買収の任意の割引又は割増、及び実金利構成要素としての費用又はコストを考慮することである。有効金利の償却z減価償却損益表やその他の包括収益表の財務コストを計上する。
協業在庫
連携在庫には,製造済みの完成品,製造中の物品,および当社の提携パートナーに販売する商品に関する製造過程で使用する材料が含まれている.完成品とは、品質発表を待っている完成品のことです。品質発表後、製品は会社の協力パートナーに納品され、顧客に配信されます
協同在庫はコストと協同在庫の可変現純値の中で低い者を基準とする。コストは先進的な先出しに基づいて決定され、製品と完成品については、コストには直接材料、直接人工、適切な割合の管理費用が含まれる。換金可能な算入値は、共同して顧客に製品を販売する推定販売価格に基づいて、完了および処理によって生成された任意の推定コストを減算する
当社は古く、移動が遅い、または欠陥のある在庫記録準備金です。臨床前と臨床プロジェクトのための製品の連携在庫コストは,在庫が臨床前または臨床に特化した場合に研究開発費を計上する。当社は、前金、その他の売掛金及びその他の資産に、自社パートナーに購入して納入した在庫に関する売掛金、及び当社がその提携パートナーから補償を受ける権利がある生産過程で発生した在庫コストの金額を記録する。
現金と現金等価物
総合現金流動量表について言えば、現金と現金等価物は手元現金と普通預金、及び短期高流動性投資を含み、これらの投資は随時既知の数量の現金に変換することができ、価値変化のリスクは大きくなく、買収時の原始期限は3ヶ月であり、必要に応じて返済すべき銀行貸越を差し引くことは会社の現金管理の構成部分である。
総合財務状況表については、現金および現金等価物は、預金および性質が現金に類似した資産を含む手元および銀行現金を含み、用途は制限されない。
定期預金
定期預金とは、買収時に銀行に入金され、満期日が3ヶ月を超える現金のことです。定期預金の受け取り予想が1年を超えた場合、定期預金は非流動資産として列報される。
条文
過去の事件により現在の債務(法律または推定)が生じ、将来の資源流出が債務を返済する必要が高い可能性が高い場合には、債務の額を確実に見積もることができれば、1つの規定を認める
割引の影響が重大であれば、支出確認のための金額は、報告期間終了時に債務返済に必要と予想される将来の支出の現在値である。時間経過による割引現在値の増加は損益表やその他の包括収益表の財務コストに計上される。
所得税
所得税には当期税と繰延税が含まれている。損益以外で確認された項目に関する所得税は損益以外で確認することができ、他の全面収益で確認することもでき、直接権益で確認することもできる。
流動税務資産及び負債は、報告期間末までに公布又は実質公布された税率(及び税法)に基づいて、当社の経営所の国の解釈及び慣例を考慮し、予想通りに税務機関に回収又は支払うことができる金額を計量する。
繰延税項は、財務報告のために、報告期末資産及び負債の課税基礎とその帳簿金額との間のすべての一時的な差異について、負債法により準備される。
繰延税金負債はすべての課税の一時的な差として確認されなければなりませんが、以下の場合は除外します
•非企業合併の取引において、営業権または資産または負債の初期確認による繰延税金負債は、取引時に会計利益にも、課税損益にも影響を与えない
•付属会社投資に関する課税課税一過性差額については,一時的な差額を抑制できる時間であり,このような一時的な差額は予見可能な将来に打ち切られない可能性が高い。
繰延税金資産は、控除可能なすべての一時的な差異、未使用の税金の繰越、および任意の未使用の税金損失として確認されます。繰延税金資産の確認範囲は、課税利益を得る可能性があり、相殺可能な一時的な差異、および未使用の税収控除と未使用の税収損失の繰越であるが、以下の場合を除く
•一時的な差異を相殺できる繰延税金資産は、非企業合併の取引において最初に1つの資産または負債を確認したものであり、取引時に会計利益にも課税損益にも影響を与えない
•付属会社投資に関する一時的な差異を差し引くことができる場合には,繰延税項資産は,一過性の差が予想される将来に戻る可能性があり,一時的な差異を相殺するための課税利益がある場合にのみ確認される。
繰延税金資産の帳簿金額は、各報告期間の終了時に審査され、繰延税金資産の全部または一部が使用できる十分な課税利益がなくなる可能性がない場合には減少する。未確認の繰延税金資産は、各報告期間末に再評価され、繰延税金資産の全部または一部を回収できる十分な課税利益がある可能性がある範囲で確認される。
繰延税項資産及び負債は、報告期間末に公布された又は実質的に公布された税率(及び税法)に基づく資産現金化又は負債清算期間の税率計量に適用される。
繰延税項資産及び繰延税項負債は、当社が法に基づいて強制執行可能な権利を有して当期税項資産及び当期税項負債を相殺する場合にのみ、繰延税項資産及び繰延税項負債は、同一税務機関が同一の課税実体又は異なる課税実体に徴収する所得税に関連し、この等の税項は、当期税金項目の負債及び資産を純額で決済することを目的としているが、同時に資産及び清算負債を償還し、大量の繰延税項又は負債を回収することが期待される今後の期間内に、繰延税項資産及び繰延税項負債は相殺される。
政府支出
贈与を受け、すべての付加条件を遵守することが合理的に保証されている場合、政府贈与はその公正価値で確認される。贈与金が支出項目に関係している場合は,その補償しようとしている費用支出期間中に,システムによって収入と確認される。
資産に関連するものが付与された場合、公正価値は繰延収益帳に記入され、関連資産の予想使用年数内に均等年次分割払いの方法で損益表および他の全面収益表に計上される。
協力手配
同社は製薬やバイオテクノロジーパートナーと協力取り決めを結び、この計画によると、同社はそのパートナーにライセンスを付与し、その候補製品の1つをさらに開発して商業化することができる。同社はまた、その協力計画に基づいて研究、開発、製造、商業活動を行うことができる。これらの契約の下での考慮事項には、前金、開発および規制マイルストーン、商業販売マイルストーン、およびその他の支払い、費用精算、および利益共有が含まれる可能性があります
複数の要素を含む連携スケジュールに対して,会社は契約開始時に連携要素がサプライヤーと顧客の関係を反映しているかどうかを決定するため,属するかどうかを決定する
IFRS 15.協力手配の要素は、双方が活動の積極的な参加者であり、このような活動の重大なリスクとリターンに直面する共同経営活動に関連しており、顧客との手配ではなく、IFRS 15の範囲内でもない。手配中に顧客とは異なる異なるバンドル商品やサービスについては、この会計単位の確認と計量は他の権威ある会計文献に基づくべきであり、あるいは適切な権威ある会計文献がなければ、合理的、合理的かつ一致して適用される会計政策を選択すべきである
もし会社がそのパートナーが特定の活動および関連支払いの顧客ではないと結論した場合、例えばいくつかの協力研究、開発、製造、および商業活動は、会社が基礎費用の位置を報告し、そのパートナーから費用の減少として費用を支払う。当社の協力者が研究開発、製造または商業化関連活動を行う場合、当社はその協力者がこのような費用を発生している間、当社が精算義務のある協力者費用の一部を費用(例えば研究開発費や販売と流通費用などは、場合によります)として確認します
ヤンソン協定
2017年12月、当社はヤンソン社と協力·許可協定(“ヤンソン協定”)を締結し、Cilta-celを世界的に開発·商業化した。ヤンソン協定によると、私たちはヤンソンに世界独自のcilta-celの共同開発と商業化のライセンスを付与した。我々と楊森は全世界発展計画と全世界商業化計画に基づいて、全世界範囲で協力して多発性骨髄腫を治療するシルゼルを開発と商業化する。
楊森は世界規模ですべての臨床試験を行うことを担当し、私たちのアメリカのチームと大中国のチームが参加します。私たちは大中華区の中国のための監督管理活動を行い、定価の許可と予約販売を獲得し、ヤンソンは世界の他の地区のための監督管理活動を行い、定価の審査と予約販売を獲得する。私たちとヤンソンは世界各国で開発、生産と商業化コストおよび税前損益を平均的に分担しているが、大中国を除いて、そのコスト分担と損益分担は70%は私たちと30Janssenの割合は
JanssenはJanssenにライセンスと他の権利を与える代価として#ドルを前払いしました350.01000万ドルで最高の追加$を得る資格があります1.35Janssenは1000億ドルの記念碑的支払いを支払った。ドルの中で1.3520億ドルは最高ではないかもしれません280双方はわれわれの臨床開発計画の修正に同意したため,当初の計画通りに何らかの試験を行わないことにした。
楊森協定については、吾らは二零二年二月二十八日に仮製品供給協定(“IPSA”)を締結し、この合意に基づき、吾らは世界(大中国を含まない)で楊森に臨床及び商業用途に応用する注腸を提供する。IPSAによると、Janssenは製品の生産と供給に必要な総コストに基づいて、供給された製品の譲渡価格を支払います。しかし,最終的には,ヤンソン協定によると,製品の商業供給と臨床供給のコストは,我々とヤンソンがそれぞれ“許容費用”と“開発コスト”として均等に分担される。IPSAは、2023年6月30日まで、またはヤンソン協定に従って設立された共同製造委員会(“JMC”)によって決定された代替日まで有効である。ヤンソンプロトコルが満了または終了した場合、IPSAも終了する。IPSAの代わりにヤンソンと製品供給協定を結びたいです
収入確認
取引先と契約した収入
会社は国際財務報告基準第15号に基づいて収入を確認した取引先と契約した収入(国際財務報告基準第15号)。国際財務報告基準第15号によると、貨物又はサービスの支配権が顧客に移転した場合、顧客との契約からの収入が確認され、その金額は、会社がそのような貨物又はサービスの対価格と交換する権利があることを反映している。IFRS 15の範囲に属すると考えられるプロトコルの収入確認を決定するために,当社は,(I)契約を確定する,(Ii)契約における履行義務を決定する,(Iii)取引価格を決定する,(Iv)取引価格を契約に割り当てる履行義務,および(V)エンティティが履行義務を履行する際に収入を確認する,の5つのステップを実行する.
契約がIFRS 15の範囲内にあると決定されると、会社は契約開始時に契約を評価して、それがどのような履行義務を交付しなければならないか、およびこれらの履行義務のうちのどれを決定しなければならないかを決定する
まったく違います。以下の2つの基準が満たされる場合、顧客に約束された貨物またはサービスは異なり、(A)顧客は単独で、または顧客がいつでも利用可能な他のリソースと共に貨物またはサービスから利益を得ることができ、(B)エンティティが顧客に貨物またはサービスを譲渡する承諾は、契約内の他の承諾とは別に識別することができる。
当社は譲渡契約で約束された貨物またはサービスにより予想される対価格金額に基づいて取引価格を決定します。考慮事項は、固定された、可変であってもよく、または両方であってもよい。契約中の対価格に可変金額が含まれている場合、会社は、貨物またはサービスを顧客に移転するために、取得する権利があると推定される。可変対価格は契約開始時に推定され、その後可変対価格に関する不確実性が解決されるまで制限され、確認された累積収入金額は重大な収入逆転が発生しない可能性が高い。このような契約は一般的に重要な資金調達部分を含まない。
会社が承諾した貨物やサービスの統制権を譲渡することで義務を履行した場合にのみ、会社は収入を確認する。制御権の移行は時間の経過とともに発生することができ,ある時点で発生することも可能である.履行義務が以下の基準のうちの1つを満たす場合、履行義務は、時間の経過とともに履行される:(I)取引相手が会社の契約を履行する際に会社の履行によって提供される利益を同時に獲得し、消費するか、または(Ii)会社の履行は、取引相手が資産作成または増強時に制御する資産を創造または増強する。
財やサービスの制御権が相手側に移動した場合,ある時点で義務履行に割り当てられた取引価格部分が収入として確認される.履行義務が時間の経過とともに履行されると,その履行義務に割り当てられた取引価格部分は,義務履行時に収入として確認される。収入を確認するために、当社は適切な進捗計測方法を採用しています。同社は各報告期間終了時に進捗指標を評価し、必要に応じて業績指標と関連収入確認を調整する。
契約書は、契約仕様や要求の変化に適応するために修正することができる。契約修正が新たに生じた場合、または既存の強制的に実行可能な権利および義務が変更された場合、契約修正が存在する。契約修正に新たな履行義務が生じ、かつ価格の増加が契約の具体的な事実や状況に応じて調整されたこのような新たな履行義務に関連する貨物·サービスの独立販売価格に近い場合には、改正は単独の契約とみなされる。
契約修正が別個の契約として計算されていない場合、残りの貨物またはサービスが契約修正の日または以前に移転された貨物またはサービスと異なる場合、会社は、既存の契約を終了し、新しい契約を作成するように、契約修正の日に譲渡されていない約束貨物またはサービス(残りのコミットメント貨物またはサービス)を前向き会計処理する。契約改正後に発生した取引価格変化について、取引価格の変化が修正前に約束された可変対価格金額に起因する場合、当社は、修正前契約で決定された履行義務に取引価格変化を割り当てる。
残りの貨物又はサービスが明確でないため、契約修正の日に部分的に履行される単一履行義務の一部を構成する場合、会社は契約修正を既存契約の一部とみなす。この場合、契約修正が取引価格に与える影響、及び実体が契約履行義務を完全に履行する上で進展したことの測定は、契約修正の日の収入の調整(収入の増加又は減少)(収入の調整は累積追跡に基づいて行われる)であることが確認される。
許可と協力収入
知的財産権許可
会社の知的財産権許可の付与を含む協力手配について、会社は、許可付与が手配に含まれる他の履行義務とは異なるかどうかを考慮する。ライセンスが他の承諾と異なるかどうかを評価する際に、会社は協力パートナーの研究、開発、製造、商業化能力、関連専門知識の一般市場での可用性などの要素を考慮する。さらに、当社は、ライセンスの価値が未履行のコミットメントに依存するか否か、他のサプライヤーが残りのコミットメントを提供することができるか否か、および残りのコミットメントから分離して識別できるか否かを考慮することにより、取引相手が残りのコミットメントを受けることなく、その予期される目的のためにライセンスから利益を得ることができるかどうかを考慮することができる。同社の評価によると
ライセンスは、技術移転サービスを含み、ヤンソン協定の単一履行義務であり、許可を付与する際に私たちの許可を使用する権利を代表する。ライセンス収入は、ライセンス使用権制御権がお客様に譲渡されたときに確認されます。
一里塚払い
マイルストーン支払いは可変対価格形式を表し、取引価格に計上される範囲は、可変対価格に関する不確実性がその後解決された場合、確認された累計収入が大きく逆転しない可能性が高い。一里塚支払いを含む各項目の手配開始時に、当社はマイルストーンが実現可能であると考えられているかどうかを評価し、可能な金額法を用いて取引価格に含まれる金額を推定する。規制承認のような会社の統制範囲内ではない記念碑的支払いは、これらの承認を受ける前に、実現されない可能性が高いと考えられる。同社の評価の要因には、この評価における特定のマイルストーンを達成するために、科学、臨床、規制、商業、および他の克服しなければならないリスクが含まれている。累積収入が大きく逆転しない可能性が高いかどうかを決定する際には,かなりの判断が必要である。その後の各報告期間が終了した時点で、当社はすべての制限されたマイルストーンの実現確率を再評価し、必要に応じて全体の取引価格の推定を調整する。
当社が契約項下の累積収入に重大な収入逆転が生じない可能性が高いと判断できない場合、当社は関連する可変対価格を制限し、取引価格から除外します。その後の各報告期間が終了した時点で、当社はすべての制限されたマイルストーンの実現確率を再評価し、必要に応じて全体の取引価格の推定を調整する
特許権使用料支払い
以下のいずれかの場合が発生した場合にのみ、会社は、知的財産権許可の交換のための販売ベースのマイルストーン支払いを約束した収入を確認する
(a)その後発生した販売
(b)分配された部分または全部は、販売された特許使用料の履行義務に基づいて履行された(または部分的に履行されている)。
ヤンソン協定
同社は顧客(Janssen)とライセンスと連携協定を締結した。契約の条項には、前払い費用を返還しないことが含まれています350.0特定の製造マイルストーン、特定の開発マイルストーン、特定の規制マイルストーンと特定の貿易純売上マイルを実現するために支払う百万ドルとマイルストーン支払い125.0百万、$215.0百万、$800.0百万ドルとドル210.0それぞれ100万ドルです当社は、技術移転サービスを含む知的財産権許可証の譲渡という明確な履行義務があると評価している。当社はこの履行義務は他の協力活動とは異なり、ライセンスには独立した価値があるため、当社はこれ以上研究開発や他の協力活動に参加しないと考えている。契約開始時に、会社の推定取引総価格は#ドルに制限されています400.0前払い費用を含めて百万ドルです350.0百万ドルとマイルストーンで払います50.0百万ドルです。取引価格は契約における単一履行義務に割り当てられる
前払い費用
ヤンソン協定では、前払いは単一の履行義務に割り当てられている。前払い費用は$350.02017年の契約開始時の出来高には100万ドルと2018年に知的財産権交付の単一履行義務を完了し,技術移転サービスを含めて確認した。♪the the the$350.0百万前払い費用は当社は2018年に全面的に受け取りました。
一里塚払い
いくつかの記念碑的支払いは、技術移転サービスを含む知的財産権許可を交付するために、ヤンソン協定内の単一履行義務に割り当てられる。頭文字をとる二つ記念碑的支払い総額は$50.0百万ドルは2017年の契約開始時に取引価格を計上し、2018年の単一履行義務完了時に確認します。そして2019年にはまた1つ追加されました二つ記念碑的支払い$60.0CARTITUDE-1臨床試験における特定の数の患者の用量トリガーのマイルストーンが達成されると、取引価格には100万ドルが含まれている。2020年には追加マイルストーンが$に支払われます75.0毛包の臨床発展に関連する研究成果は100万部に達した。2021年には三つ追加マイルストーン支払い総額は$65.0EMAへのマーケティング許可の提出,CARTITUDE−5臨床試験で特定数の患者を募集し,衛生部が製品の薬品承認申請を提出することで100万件の成果を得た労働党a日本の福祉と。2022年、追加マイルストーン支払いは$50.0日本では,PMDAにセキュリティプロトコルを提出することにより,同社のCARTITUDE−5臨床試験で特定数の患者を募集し,米国でCilta−celの商業化承認を得て1.8億ドルの売上を実現している。
2022年12月31日現在、この合意に基づき、会社の将来の契約マイルストーン残り支払総額は$です1,050.0100万ドルは、様々な開発、規制、製造、純貿易販売のマイルストーンを実現するために使用される。より具体的には、未来の契約マイルストーンは#ドルを含む125.0具体的な製造マイルストーンを実現するための百万ドルです60.0具体的な発展のマイルストーンを実現するための百万ドル655.0具体的な規制のマイルストーンと$を実現するために百万ドル210.0具体的な貿易販売純額マイルストーンを実現するために100万ドルを支払います。同社の発展計画や研究進展は時々変化する可能性があり、将来の契約マイルストーンを実現する不確実性を増加させる。その会社はドルを信じない280.0残りの百万ドル1,050.0その後の協力者との発展計画の変化によると、100万件の契約マイルストーン支払いを受ける資格がある。また、同社は、残りのすべての契約マイルストーンの実現には大きな不確実性があり、関連するマイルストーン支払いは取引価格に含まれていないと評価している。プロトコルに記述されたトリガイベントが発生すると、マイルストーンが実現される。
利益共有
人民Republic of Chinaを除いて、当社と楊森平はCARVYKTIのすべての地域での販売利益を分け、当社が保留または負担している香港特別行政区、マカオ特別行政区、台湾(“大中国”)は含まれていない70税金前の利益や損失の割合。大中国を除くすべての地域で、ヤンソンは顧客と販売取引を行う担当者であるため、当社はヤンソンで販売を完了し、顧客に製品を納入している間、比例して協力貿易の純売上高の一部を確認している。大中国を除く当社のすべての地域における協力貿易純売上高シェアは、協力収入、損益表、その他の全面収益で確認されています。監督管理機関の承認を経て、大中国の製品販売収入は損益表やその他の全面収益の中で製品販売内で確認され、当社は顧客への販売の元本となるからだ
協力活動
ヤンソン協定には、知的財産権許可のほか、会社とそのパートナーによる共同開発、製造、ビジネス活動も含まれている。当社とそのパートナーはいずれもこのような活動の積極的な参加者であり,そのような活動の重大なリスクやリターンに直面しているため,このような活動とその関連考慮事項はIFRS 15の範囲内ではない
製品販売
販売貨物の収入は,貨物制御権を顧客に渡す際に確認し,通常貨物交付時に確認する.現在まで、同社は何の製品販売も発生していない。我々の協働純貿易売上高におけるシェアは,Janssenが顧客との販売取引の主体であり,連携収入では損益表やその他の包括収益で確認されている。
収入の協力コスト
連携収入コストは,自社で発生したコストと当社が比例して分担した連携収入コストを含むCARVYKTIの売却に関連している。収入の協働コストには、販売在庫コスト、製造コスト、生産に起因することができる他のコスト、および超過および古い在庫、または品質規格に適合しない在庫のような在庫の削減が含まれる
その他の収入
利息収入は実際の利息法を用いて計上して確認し、金融商品の期待使用年数或いは短い期間(例えば適用)に適用して金融資産の帳簿純値を正確に割引して未来の現金収入の比率を推定する。
株式ベースの支払い
当社は株式購入計画及び制限株式単位計画(“RSU計画”)を推進し、当社の経営成功に貢献した合資格参加者に奨励及び奨励を提供することを目的としている。当社従業員及び取締役は株式支払形式で報酬を受け取り、従業員及び取締役は権益ツール(“株式決済取引”)の対価としてサービスを提供する。
従業員と株式決済取引を行うコストは、付与された日の公正価値によって計量される。株式購入の公正価値は二項モデルによって決定され、各購入株式単位の公正価値は当社の株式の各授出日の市価を参考にして決定され、関連の更なる詳細は総合財務諸表に付記27及び28に掲載されている。
株式決済取引のコストは、相応の権益が増加するとともに、従業員福祉支出において業績及び/又はサービス条件を満たす期間に確認する。帰属日までの各報告期間終了時に確認された権益決済取引の累積費用は、帰属期間が満了した程度と、最終的に帰属する権益ツール数に対する当社の最適な推定とを反映する。ある期間の計上または貸記損益は,その期間期初めと期末に確認された累積費用の変動を表す.
付与日を決定する際には、サービスおよび業績条件は、付与された公正価値を考慮していないが、条件を満たす可能性は、最終的に帰属する株式ツール数に対する当社の最適な推定の一部と評価される
パフォーマンスおよび/またはサービス条件が満たされていないために最終的に付与されていない報酬については、違います。料金は確認されました。
他の従業員福祉
退職金計画
当社は大中華区中国及び香港で経営する付属会社の従業員が現地市政府が運営する中央退職金計画に参加しなければならない。これらの子会社は中央年金計画に一定の割合の賃金コストを支払うことを要求されている。拠出金は中央年金法の規則に従って支払う際に利益または損失を記入する。
固定払込計画
アメリカにいる従業員は私たちが始めた固定支払計画に参加する資格があります。固定納付計画は、従業員が指定されたガイドラインに基づいて税引前に報酬の一部を納付することを可能にする。私たちは従業員の支払いの一定の割合を一定の上限に一致させる。
外貨取引
これらの連結財務諸表はドルで表され、ドルは会社の機能通貨です。当社の各子会社は自分のビットコインを決定し、各エンティティの連結財務諸表に含まれる項目はそのビットコインを用いて計量します
実体機能通貨以外の通貨建ての取引は、取引日の即時為替レートを適用することにより、当該機能通貨で記録される。本報告で述べた期間終了時には、機能通貨以外の通貨建ての通貨資産と負債を適用して報告した期間終了時の現在為替推定値を機能通貨とする。これらの外貨リスコアリングによる収益と損失は純収益で確認されている。非貨幣に分類される外貨建て取引は歴史的現物為替レートを用いて測定される。
外貨換算
中国及びヨーロッパに設立されたいくつかの付属会社の機能通貨はドル以外の通貨である。報告期間末までに、これらの実体の資産と負債は報告期間末の現行レートでドルに換算され、その損益表は期間の平均レートでドルに換算される。
これにより発生した為替差額は他の全面収入で確認され、外貨換算準備金に蓄積される。海外業務を処分する際には、当該特定海外業務に関連する他の全面収益の構成要素が純収益で確認される。
総合キャッシュフロー表については、中国およびヨーロッパに設立された付属会社のキャッシュフローは、キャッシュフロー日のレートでドルに換算されている。中国やヨーロッパに設立された会社が年間によく出現する経常現金流量は,年間加重平均レートでドルに換算されている。
予算の使用
会社の総合財務諸表を作成するには、経営陣に判断、推定及び仮定を要求し、これらの判断、推定及び仮定は、収入、費用、資産及び負債の報告金額及びそれに付随する開示、及び負債の開示に影響を与える。これらの仮定および推定された不確実性がもたらす可能性のある結果は、将来影響を受ける資産または負債の帳簿価値を大きく調整する必要があるかもしれない。
世界経済状況
世界経済状況は依然として不確定であり、同社は新冠肺炎の流行、ロシア-ウクライナ戦争、金融機関の失敗と不安定、上昇するインフレ率に関連する影響を含むマクロ経済状況の影響を監視し続けている。
経済状況の変化、サプライチェーン制限、物流挑戦、労働力不足、ロシア-ウクライナ戦争、および各国政府と中央銀行が取った措置、特に新冠肺炎の流行に対応するための措置は、より高いインフレを招き、これはコスト上昇を招き、金利上昇を含む財政と通貨政策の変化を招く。 アメリカと中国の製品製造は続いています。現在、当社はインフレと金利上昇によって私たちの材料サプライチェーンに実質的な影響を与えていません。適切な安全対策として、より多くの特定の原材料と消耗品が貯蔵されている。同社は、必要なすべての材料のための強力な調達戦略を策定しており、大きな影響はないと信じている。
また,中国では,2022年12月31日までの年度内に当社は新冠肺炎の中断を経験しているが,このような中断は我々の業務に実質的な影響を与えないと考えられる。 新冠肺炎の未来の著者らの業務に対する影響、経営結果と財務状況は依然として不確定性が存在し、影響の程度は多くの絶えず変化する要素に依存し、しかしこれらに限定されない:新冠肺炎の規模と持続時間、新冠肺炎ワクチンとその他の医療サービス流通の発展と進度、期待した回復速度、及び政府と企業の疫病に対する反応。状況が大幅に悪化すれば、会社の業務、経営業績、財務状況は重大な悪影響を受ける可能性がある。その会社は
疫病の持続的な発展がその財務状況と経営成果に与える影響を引き続き監視と評価し、相応の反応を行った
経済状況のこれらの変化が継続している場合、またはそれらの深刻性が増加すれば、短期的にはさらなる経済不確実性や資本市場の変動を招き、私たちの運営に負の影響を与える可能性がある。当社はこれらのマクロ経済状況がその財務状況やこれまでの経営業績に実質的な影響を与えるとは考えていないが、近い将来(特にインフレ率が上昇し続ける場合)、当社はサプライチェーン制限、新冠肺炎に関連する結果、ロシアとウクライナ間の持続的な衝突、および従業員の可用性と賃金上昇によってその運営コストに影響を与える可能性があり、労働コストや研究開発コストを含む当社の運営資金資源に追加の圧力を与える可能性がある。
3. 重大会計判断と見積もり
判断
当社の会計政策を適用する過程で、見積もりに関する判断に加えて、経営陣は、連結財務諸表で確認された金額に最も大きな影響を与えると判断した
取引先と契約した収入
当社は、契約履行義務と顧客との契約収入を推定する可変対価格を決定する方法に重大な影響を与えると判断し、特にヤンソン協定による歴史会計:
(i)契約の履行義務を確定する
以下の2つの基準が満たされる場合、顧客に約束された貨物またはサービスは異なり、(A)顧客は単独で、または顧客がいつでも利用可能な他のリソースと共に貨物またはサービスから利益を得ることができ、(B)エンティティが顧客に貨物またはサービスを譲渡する承諾は、契約内の他の承諾とは別に識別することができる。当社はヤンソン協定により、ライセンスが異なることができることを確認しました。Janssenプロトコル下のライセンスが顧客に独立した価値があるかどうかを評価する際に、会社は、提携パートナーの研究、製造および商業化能力、関連する専門知識の一般市場での可用性などを考慮し、お客様がライセンスから独立して利益を得ることができることを示している。当社は、知的財産権許可と技術移転サービスが単一の履行義務を構成していると認定している。知的財産権許可と技術移転は高度に依存しており,区別することはできない.技術移転は、顧客が使用許可証を取得し、そこから利益を得る能力に必須的だ。技術移転サービスを含む譲渡許可証の約束は、契約の背景で異なる。技術移転サービスを含む知的財産権ライセンスは、契約において個別に決定することができ、他の協力活動とは別に譲渡されなければならない。ライセンスは、組合せを代表して出力されるサービスと統合される入力ではなく、技術移転サービスを含む。各指導委員会の準備と出席および協力活動(例えば共同開発)への参加は,臨床試験の協力と規制機関のこの技術の承認を得るためであるが,許可証や技術は修正されない。さらに、ライセンスは、技術移転サービスを含み、ライセンスおよび技術移転サービスの送達は、将来提供されるこれらの活動に依存しないので、共同委員会および他の協調活動と高度に依存または高度に関連していないので、これらの活動と相互に依存または相互に関連していない。
ライセンス(技術移転サービスを含む)がある時点でまたは時間とともに顧客に転送されているかどうかを判断する際に、会社は、会社が顧客に許可を付与する承諾の性質が、会社の知的財産権にアクセスまたは使用する権利を提供することであると考えられる。当社は、Janssenプロトコル下のライセンスがライセンス付与および技術移転を行う時点に存在するので、当社はライセンスを使用する権利を提供する(形態および機能に関して)、すなわち顧客がライセンスを使用し、利益を得ることができる時点である。この許可証はすでに開発され、癌患者候補者に積極的な効果を与えている。次のステップは,制御されモニタリングされた環境で再臨床試験を行うことである。
ヤンソン協定によると、当社は手配中の唯一の履行義務であるため、すべての取引価格を知的財産権許可に割り当てている
(Ii)推定変数の考慮を決定する方法
特定の契約にはマイルストーン支払いが含まれており、これは可変価格を引き起こすだろう。可変対価を見積もる際には、当社は期待値方法や可能金額法を採用し、どの方法で獲得する権利のある対価格額を予測する必要があります。会社は、最も可能な金額法はマイルストーン支払いの可変対価格を推定する適切な方法であり、この方法は会社が獲得する権利のある可変対価格の金額をよりよく予測しているからだと確定した。
任意の変動対価格を取引価格に計上する前に、当社は変動対価の額が制限されているかどうかを考慮します。同社の評価の要因には、この評価における特定のマイルストーンを達成するために、科学、臨床、規制、商業、および他の克服しなければならないリスクが含まれている。
不確定度を見積もる
将来に関する主な仮定や報告期末推定不確実性の他の主要源には重大なリスクがあり、次の財政年度内の資産や負債の帳簿金額の重大な調整を招く可能性があり、詳細は以下の通りである。
非金融資産減価準備
当社は、すべての非金融資産(使用権資産を含む)が各報告期間末に減値指標があるかどうかを評価します。帳簿額面が回収できない可能性があることを示す指標がある場合、非金融資産に対して減値テストを行う。資産や現金発生単位の帳簿価値がその回収可能金額を超えた場合,減値は減値となり,回収可能金額はその公正価値から処分コストおよび使用価値を差し引いた高い金額となる。公正価値から処分コストを差し引いた計算は、同様の資産の公平な取引における拘束的販売取引または観察可能な市場価格から処分資産の増分コストを差し引いたデータに基づく。使用価値計算を行う際には,管理層は資産や現金発生単位の予想将来のキャッシュフローを推定し,適切な割引率を選択してこれらのキャッシュフローの現在値を計算しなければならない.列挙されたすべての期間の減値指標はない.
繰延税金資産
繰延税項資産は未使用税項損失および一時的な差を差し引くことができることが確認されているが,課税利益が損失や一時的な差を相殺するために利用できる可能性があることを前提としている。経営陣は、将来の課税利益の可能な時間とレベル、および将来の税務計画戦略に基づいて、確認可能な繰延税金資産金額を決定するために重大な判断を下す必要がある。それらが実際に利用した結果は異なるかもしれない。さらに詳細は、総合財務諸表付記22に記載されている。
株式証法的責任
権利証負債の公正価値は二項モデルで決定された。評価モデルの使用は,管理層が選定したモデルの投入を何らかの仮定することを要求する.経営陣は比較可能な会社株の歴史的変動率から予想変動率を推定した。無リスク金利は、残存期限が権証の期待寿命に近い国債収益率曲線金利に基づく。これらの入力変数の変化は権証の公正価値に影響を与える.さらに詳細は、総合財務諸表付記23および付記34に記載される。
株式ベースの報酬
当社が付与した株式購入権の公正価値は二分木モデルを用いて見積もる.評価モデルの使用は,管理層が選定したモデルの投入を何らかの仮定することを要求する.経営陣は比較可能な会社株の歴史的変動率から予想変動率を推定した。満期日はオプション期待寿命を決定するための基礎である。無リスク金利は国債収益率曲線金利に基づいており,その残存期限は付与された日に仮定した期待寿命に近似している。これらの入力変数の変化は、株式ベースの報酬に関する費用金額に影響を与える。株式に基づく奨励確認のすべての補償費用は、推定没収額を差し引いた純額です。同社はオプション没収の歴史分析に基づいて罰金率を推定している。実際の没収が見積もりの没収と異なる場合、補償費用を調整する必要があるかもしれません。さらに詳細は、総合財務諸表付記27および付記28に記載される。
4. 運営細分化市場情報
国際財務報告基準8細分化市場を運営する会社の構成要素に関する内部報告に基づいて運営部門を決定し、首席運営決定者は、部門に資源を割り当て、その業績を評価するために、これらの部門を定期的に審査する必要がある。会社取締役会は会社の主要経営決定者であり、資源配分や業績評価のために取締役会に報告する情報には離散的な運営部門財務情報が含まれておらず、取締役たちは会社全体の財務業績を審査した。そのため,運営部分に関するさらなる情報は提供されていない.
地理情報
(a)外部顧客からの収入
| | | | | | | | | | | | | | | | | |
| 2022 | | 2021 | | 2020 |
| ドル‘000ドル | | ドル‘000ドル | | ドル‘000ドル |
| アメリカ合衆国 | 116,602 | | | 65,402 | | | 75,000 | |
| 中国 | 328 | | | 3,424 | | | — | |
| 他にも | 75 | | | — | | | — | |
| 合計する | 117,005 | | | 68,826 | | | 75,000 | |
上記の収入情報は顧客の位置に基づいている。
(b)非流動資産
| | | | | | | | | | | |
| 十二月三十一日
2022 | | 十二月三十一日
2021 |
| ドル‘000ドル | | ドル‘000ドル |
| アメリカ合衆国 | 114,426 | | | 103,648 | |
| 中国 | 54,510 | | | 50,800 | |
| 他にも | 62,908 | | | 10,462 | |
| 合計する | 231,844 | | | 164,910 | |
上記非流動資産情報は、資産所在地に基づいて、非流動定期預金を含まない。
主要顧客に関する情報
収入は5ドルです116.7百万、$65.4百万ドルとドル75.02022年,2022年,2021年および2020年12月31日までの年度の百万ドルは,それぞれ単一顧客への販売およびヤンソン合意によるものである。収入は5ドルです0.32022年12月31日までの年間は400万ドル3.4南京ProBioバイオテクノロジー株式会社とその関連会社は,2021年12月31日までの年間で,ある特許の独占ライセンスによる独占許可と販売による使用料に基づいて3.8億ユーロの収入を生み出した。
5. 収入、その他の収入、収益
収入の分析は以下のとおりである
| | | | | | | | | | | | | | | | | |
| 2022 | | 2021 | | 2020 |
| ドル‘000ドル | | ドル‘000ドル | | ドル‘000ドル |
| 収入.収入 | | | | | |
| 知的財産権の許可 | 50,000 | | | 65,402 | | | 75,000 | |
| 協力収入 | 66,677 | | | — | | | — | |
| その他の収入 | 328 | | | 3,424 | | | — | |
| 117,005 | | | 68,826 | | | 75,000 | |
知的財産権許可の収入はある時点で確認される。知的財産権許可の収入はマイルストーン支払いに関する可変対価格であり、これらの支払いは数年前に制限されているが、マイルストーンが実現した場合に取引価格を計上する可能性が高い。“ヤンソン協定”開始時に知的財産権許可に割り当てられた金額は#ドルであった400.0アメリカと非アメリカの領土はいずれも100万ドルで$に更新されました650.02022年12月31日まで。協力収入には協業純取引売上高に占める割合が含まれており、このうちJanssenが元本で販売しているのは顧客である
その他の収入は、南京ProBio生物技術有限会社及びその関連会社のある特許の独占許可及び関連する後続販売ベースの使用料と関係がある
| | | | | | | | | | | | | | | | | |
| 2022 | | 2021 | | 2020 |
| ドル‘000ドル | | ドル‘000ドル | | ドル‘000ドル |
| 他の収入と収益 | | | | | |
| その他の収入: | | | | | |
| 財政収入 | 8,182 | | | 971 | | | 2,930 | |
| 政府支出* | 2,434 | | | 1,736 | | | 3,072 | |
| 他にも | 88 | | | 35 | | | 4 | |
| 総収入 | 10,704 | | | 2,742 | | | 6,006 | |
| | | | | |
| 収益: | | | | | |
| 外貨両替収益純額 | — | | | — | | | 66 | |
| 公正価値に応じて損益変動により計量された金融資産の公正価値収益 | 603 | | | — | | | 47 | |
| 他にも | 742 | | | 317 | | | — | |
| 総収益 | 1,345 | | | 317 | | | 113 | |
| その他の収入と収益の合計 | 12,049 | | | 3,059 | | | 6,119 | |
*この金額は、企業の業務を支援するために地方政府当局から得られた補助金だと言っています。このような政府の贈与には未履行の条件と他の事項がない。
6. 税引き前損失
当社の税引き前損失は、以下の費用を計上したものです
| | | | | | | | | | | | | | | | | | | | |
| | 2022 | | 2021 | | 2020 |
| | ドル‘000ドル | | ドル‘000ドル | | ドル‘000ドル |
| 従業員福祉支出(役員報酬を含む): | | | | | | |
| 給料と賃金 | | 147,385 | | | 105,751 | | | 70,682 | |
| 年金支給計画(供出計画を定義) | | 5,057 | | | 2,257 | | | 640 | |
| 持分決算持分報酬費 | | 34,338 | | | 20,158 | | | 4,760 | |
7. 融資コスト
| | | | | | | | | | | | | | | | | |
| 2022 | | 2021 | | 2020 |
| ドル‘000ドル | | ドル‘000ドル | | ドル‘000ドル |
| 賃貸負債利息 | 527 | | | 142 | | | 195 | |
| 協力利息前払い資金 | 10,269 | | | 758 | | | — | |
| 転換優先株を発行する費用 | — | | | — | | | 4,014 | |
| 合計する | 10,796 | | | 900 | | | 4,209 | |
8. 所得税
当社は、当社及びその付属会社の登録及び運営所が管轄区域で発生又は取得した利益について、実体に応じて所得税を納付しなければならない。
ケイマン諸島
ケイマン諸島の現行法によると、当社は収入や資本利益について納税する必要はありません。同社が会社間手形に源泉徴収税を課すのは取るに足らないことだ
英領バージン諸島
英領バージン諸島(“英領バージン諸島”)の現行法によると、英領バージン諸島で運営する子会社は所得税や資本利益税を納める必要がない。また、英領バージン諸島に登録設立された会社子会社が株主に配当金を支払う際には、違います。源泉徴収税がかかります。
香港.香港
香港現行税法によると、香港で経営する付属会社は2段階の利得税税率で徴収しなければならない。最初の香港ドル2,000,000(2021年および2020年:香港ドル2,000,000)の課税利益は8.25%(2021年および2020年:8.25%)、残りの課税利益は16.5%(2021年および2020年:16.5%)。香港税法によると、香港付属会社の海外収入は所得税の納付を免除することができるが、香港国内の配当金の送金も税金を前納する必要はない。
アメリカ合衆国
米国現行税法によると、米国で経営する付属会社は#%の税率で連邦税を納めなければならない21%(2021年および2020年:21%)、州税率は9%(2021年および2020年:9%)、含まれていません2.5%ニュージャージー州追加料金は、ニュージャージー州NOLの使用時間が予想されるためである。♪the the the2.5%ニュージャージー州追加料金は2023年12月31日に満了します。会社のアメリカ実体が非アメリカ住民企業に支払う配当金は一致しなければならない30%源泉徴収税は、それぞれの非米国住民企業の会社の管轄区域が米国と税金条約または手配がない限り、源泉徴収税率を低下させるか、または源泉徴収税を免除することを規定している。
アイルランド
アイルランド現行法によると,アイルランドで経営する子会社は以下の税率で企業所得税(CIT)を納付しなければならない12.5%(2021年および2020年:12.5%)の課税取引収入。いかなる非取引収入も以下の税率でCITを徴収しなければならない25%(2021年および2020年:25%)。アイルランド社が行った分配には源泉徴収配当税がかかり,税率は252022年(2021年と2020年:25%)と、多くの免除が提供されます。
偉大な中国
“中華人民共和国Republic of China企業所得税法”と関連規定(“企業所得税法”)によると、大中国地区で経営する子会社は、25課税所得額の%です。2022年、2022年、2021年、2020年12月31日までの年間で、適用される所得税税率は25%です。当社の中国実体が非中国住民企業に支払う配当金、利息、レンタル料又は特許権使用料、及び当該等の非住民企業投資家が資産を処分する収益(当該等の資産の純資産を差し引く)は適用されなければならない10%CIT、すなわち源泉徴収税であり、関連する非中国住民企業の登録司法管轄区域が中国と税収条約または手配を締結しない限り、源泉徴収税率を下げるか、または源泉徴収税を免除することが規定されている。
ベルギー
ベルギーの現行法律によると、ベルギーで運営する子会社は以下の税率で企業所得税を徴収しなければならない25課税取引収入の1%ですベルギー会社の配当分配に源泉徴収配当税を徴収し,税率は 30%と、多くの免除が提供されます。
他の地方が課税すべき割増税項は、すでに当グループが経営している司法管轄区の現行税率で計算されている。
| | | | | | | | | | | | | | | | | |
| 2022 | | 2021 | | 2020 |
| ドル‘000ドル | | ドル‘000ドル | | ドル‘000ドル |
| 現在のアメリカ合衆国は | 224 | | | 211 | | | (4,548) | |
| 現在-他の場所では | 401 | | | 416 | | | 383 | |
| 延期(付記22) | — | | | (4,241) | | | (37,747) | |
| 本年度の税費/(相殺)総額 | 625 | | | (3,614) | | | (41,912) | |
当社及びその大部分の子会社が所在する国·地域(又は管轄区域)は、法定税率で税前損失の税費/(相殺)と有効税率による税の支出/(相殺)との入金を以下のように適用する
| | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | |
| 2022 | | | | 2021 | | | | 2020 | | |
| ドル‘000ドル | | % | | ドル‘000ドル | | % | | ドル‘000ドル | | % |
| 税引き前損失 | (445,724) | | | | | (407,196) | | | | | (308,285) | | | |
アメリカ連邦と州の法定混合所得税税率で28.1%(2021年および2020年:28.1%) | (125,293) | | | 28.1 | | | (114,463) | | | 28.1 | | | (86,659) | | | 28.1 | |
| 他の国と地域の税率差の影響 | 15,129 | | | (3.4) | | | 15,027 | | | (3.7) | | | 35,062 | | | (11.4) | |
| 信用を研究開発する | (24,970) | | | 5.6 | | | (954) | | | 0.2 | | | (15,643) | | | 5.1 | |
| 国の金利の変化 | (107) | | | — | | | — | | | — | | | — | | | — | |
| 支出の影響を差し引くことはできない | 1,829 | | | (0.4) | | | 2,298 | | | (0.6) | | | 383 | | | (0.1) | |
| 未確認の税収損失と相殺可能な一時的な違い | 131,194 | | | (29.4) | | | 102,481 | | | (25.2) | | | 26,040 | | | (8.4) | |
| オプション所得税割引 | 2,668 | | | (0.6) | | | (9,532) | | | 2.3 | | | (442) | | | 0.1 | |
| 前年は実際に成長しました | — | | | — | | | — | | | — | | | — | | | — | |
| 不確定税収状況 | — | | | — | | | — | | | — | | | — | | | — | |
| 利子前払税 | — | | | — | | | — | | | — | | | — | | | — | |
| 他の人は | 175 | | | — | | | 1,529 | | | (0.4) | | | (653) | | | 0.2 | |
| 会社の実際の税率で計算される税金/(割引) | 625 | | | (0.1) | | | (3,614) | | | 0.9 | | | (41,912) | | | 13.6 | |
9. 親会社の普通株主は1株当たりの損失を占めるべきだ
1株当たりの基本損失額の計算は、今年度の親会社普通株保有者に帰属する損失に基づいている318,083,913, 281,703,291そして236,305,234それぞれ2022年,2022年,2021年および2020年12月31日までに年度発行される。
1株当たりの収益額を希釈する計算は、親会社の普通株株主が今年度の赤字を占めるべきであることに基づいて計算される。計算に用いた普通株加重平均は,基本1株当たり収益を計算する際に使用する年内に発行された普通株数と,すべての希釈性潜在普通株が普通株として行使されたと仮定した場合に無料で発行される普通株加重平均である。
二零一二年十二月三十一日現在、二零二年、二零二一年及び二零二年十二月三十一日までに年次償却事項について記載されている1株当たりの基本損失金額は調整されていない。なぜなら、株式購入権、RSU及び株式承認証負債が記載されている1株当たりの基本損失金額に対して逆償却作用があるためである。
1株当たりの基本損失と赤字の計算根拠は以下のとおりである
| | | | | | | | | | | | | | | | | |
| 2022 | | 2021 | | 2020 |
| ドル‘000ドル | | ドル‘000ドル | | ドル‘000ドル |
| 収益.収益 | | | | | |
| 親会社の普通株主は損失を占め,基本的な1株当たりの収益を計算するために用いなければならない | (446,349) | | | (403,582) | | | (266,373) | |
| | | | | | | | | | | | | | | | | |
| 株式数 |
| 2022 | | 2021 | | 2020 |
| 株 | | | | | |
| 基本1株当たり収益を計算するための年間発行普通株の加重平均 | 318,083,913 | | 281,703,291 | | 236,305,234 |
10. 財産·工場·設備
| | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | |
| 永久保有権
土地 | | 建物.建物 | | 賃借権改善 | | 機械設備
そして
装備 | | 電気計算機
そしてオフィスは
装備 | | 交通輸送
装備 | | 建設
進行中です | | 合計する |
| ドル‘000ドル | | ドル‘000ドル | | ドル‘000ドル | | ドル‘000ドル | | ドル‘000ドル | | ドル‘000ドル | | ドル‘000ドル | | ドル‘000ドル |
| 2022年12月31日 | | | | | | | | | | | | | | | |
| 2022年1月1日 | | | | | | | | | | | | | | | |
| コスト | 2,889 | | | 16,011 | | | 20,908 | | | 35,251 | | | 2,977 | | | 45 | | | 41,367 | | | 119,448 | |
| 減価償却累計 | — | | | (1,360) | | | (3,503) | | | (10,432) | | | (1,633) | | | (14) | | | — | | | (16,942) | |
| 帳簿純額 | 2,889 | | | 14,651 | | | 17,405 | | | 24,819 | | | 1,344 | | | 31 | | | 41,367 | | | 102,506 | |
| 2022年1月1日現在、減価償却累計額を差し引く純額 | 2,889 | | | 14,651 | | | 17,405 | | | 24,819 | | | 1,344 | | | 31 | | | 41,367 | | | 102,506 | |
| 足し算 | — | | | 1,732 | | | 522 | | | 583 | | | 34 | | | — | | | 14,346 | | | 17,217 | |
| 処置する | — | | | — | | | — | | | (122) | | | (14) | | | — | | | (406) | | | (542) | |
| 本年度は減価償却を計上する | — | | | (988) | | | (2,566) | | | (5,818) | | | (797) | | | (4) | | | — | | | (10,173) | |
| 取引所再調整 | — | | | — | | | (1,164) | | | (1,802) | | | (32) | | | (3) | | | (839) | | | (3,840) | |
| 振替 | — | | | 27,332 | | | 1,970 | | | 10,110 | | | 872 | | | — | | | (40,284) | | | — | |
| 2022年12月31日現在、減価償却累計額を差し引く純額 | 2,889 | | | 42,727 | | | 16,167 | | | 27,770 | | | 1,407 | | | 24 | | | 14,184 | | | 105,168 | |
| 2022年12月31日: | | | | | | | | | | | | | | | |
| コスト | 2,889 | | | 45,075 | | | 21,974 | | | 42,576 | | | 3,638 | | | 41 | | | 14,184 | | | 130,377 | |
| 減価償却累計 | — | | | (2,348) | | | (5,807) | | | (14,806) | | | (2,231) | | | (17) | | | — | | | (25,209) | |
| 帳簿純額 | 2,889 | | | 42,727 | | | 16,167 | | | 27,770 | | | 1,407 | | | 24 | | | 14,184 | | | 105,168 | |
| | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | |
| 永久保有権
土地 | | 建物.建物 | | 賃借権改善 | | 機械設備
そして
装備 | | コンピュータ、固定装置
そしてオフィスは
装備 | | 交通輸送
装備 | | 建設
進行中です | | 合計する |
| ドル‘000ドル | | ドル‘000ドル | | ドル‘000ドル | | ドル‘000ドル | | ドル‘000ドル | | ドル‘000ドル | | ドル‘000ドル | | ドル‘000ドル |
| 2021年12月31日 | | | | | | | | | | | | | | | |
| 2021年1月1日 | | | | | | | | | | | | | | | |
| コスト | 2,889 | | | 11,210 | | | 11,887 | | | 25,841 | | | 3,281 | | | 44 | | | 27,811 | | | 82,963 | |
| 減価償却累計 | — | | | (817) | | | (1,854) | | | (6,514) | | | (1,426) | | | (10) | | | — | | | (10,621) | |
| 帳簿純額 | 2,889 | | | 10,393 | | | 10,033 | | | 19,327 | | | 1,855 | | | 34 | | | 27,811 | | | 72,342 | |
| 2021年1月1日現在、減価償却累計額を差し引く純額 | 2,889 | | | 10,393 | | | 10,033 | | | 19,327 | | | 1,855 | | | 34 | | | 27,811 | | | 72,342 | |
| 足し算 | — | | | — | | | — | | | 1,603 | | | 7 | | | — | | | 37,269 | | | 38,879 | |
| 処置する | — | | | — | | | (859) | | | (177) | | | (77) | | | — | | | — | | | (1,113) | |
| 本年度は減価償却を計上する | — | | | (543) | | | (1,833) | | | (4,967) | | | (792) | | | (4) | | | — | | | (8,139) | |
| 取引所再調整 | — | | | — | | | 123 | | | 358 | | | 10 | | | 1 | | | 45 | | | 537 | |
| 振替 | — | | | 4,801 | | | 9,941 | | | 8,675 | | | 341 | | | — | | | (23,758) | | | — | |
| 2021年12月31日現在、減価償却累計額を差し引く純額 | 2,889 | | | 14,651 | | | 17,405 | | | 24,819 | | | 1,344 | | | 31 | | | 41,367 | | | 102,506 | |
| 2021年12月31日: | | | | | | | | | | | | | | | |
| コスト | 2,889 | | | 16,011 | | | 20,908 | | | 35,251 | | | 2,977 | | | 45 | | | 41,367 | | | 119,448 | |
| 減価償却累計 | — | | | (1,360) | | | (3,503) | | | (10,432) | | | (1,633) | | | (14) | | | — | | | (16,942) | |
| 帳簿純額 | 2,889 | | | 14,651 | | | 17,405 | | | 24,819 | | | 1,344 | | | 31 | | | 41,367 | | | 102,506 | |
11. 無形資産
| | | | | |
| ソフトウェア |
| ドル‘000ドル |
| 2022年12月31日 | |
| 2022年1月1日 | |
| コスト | 6,402 | |
| 累計償却する | (1,718) | |
| 帳簿純額 | 4,684 | |
| 2022年1月1日までの累計償却純額 | 4,684 | |
| 足し算 | 1,264 | |
| 処置する | (6) | |
| 年内に償却する | (2,476) | |
| 取引所再調整 | (57) | |
| 2022年12月31日までの累計償却純額 | 3,409 | |
| 2022年12月31日 | |
| コスト | 7,505 | |
| 累計償却する | (4,096) | |
| 帳簿純額 | 3,409 | |
| 2021年12月31日 | |
| 2021年1月1日 | |
| コスト | 3,186 | |
| 累計償却する | (334) | |
| 帳簿純額 | 2,852 | |
| 2021年1月1日現在、累計償却純額 | 2,852 | |
| 足し算 | 3,207 | |
| 年内に償却する | (1,379) | |
| 取引所再調整 | 4 | |
| 2021年12月31日までの累計償却純額 | 4,684 | |
| 2021年12月31日 | |
| コスト | 6,402 | |
| 累計償却する | (1,718) | |
| 帳簿純額 | 4,684 | |
12. 他の非流動資産
| | | | | | | | | | | |
| 十二月三十一日
2022 | | 十二月三十一日
2021 |
| ドル‘000ドル | | ドル‘000ドル |
| 付加価値税(“付加価値税”)は払い戻すことができる | — | | | 4,080 | |
| 前払い費用 | 1,092 | | | 1,068 | |
| 賃借金を受け取る | 395 | | | — | |
| 合計する | 1,487 | | | 5,148 | |
13. 賃貸借証書
テナントとしての会社
同社は土地と建物を賃貸する賃貸契約を持っている。建物(駐車スペースを含む)のレンタル期限は一般的です2そして10何年もです。一度に金を支払って,所有者から賃貸土地を買収し,リース期間を50年もあれば違います。進行中の支払いはこのような賃貸土地の条項に基づいて行われるだろう。他の建物や部屋のレンタル条項は一般的に12か月または開始日から始まり、購入オプションは含まれていません。当該グループはその短期借約に対して短期賃貸契約を適用して免除を確認する。連携資産とは、当社がJanssenから連携にレンタルした資産シェアであり、Janssen代表がJanssen協定に関連する資産を共同購入したものである。建設中の連携資産は,投入時にJanssenから連携にリースされ,連結財務諸表では連携前払いリースに分類される。
(a)使用権資産
| | | | | | | | | | | |
| 十二月三十一日
2022 | | 十二月三十一日
2021 |
| ドル‘000ドル | | ドル‘000ドル |
| 借受地 | 4,357 | | | 4,862 | |
| 賃貸建築物 | 23,016 | | | 2,324 | |
| 協働資産 | 28,217 | | | 31,097 | |
| 合計する | 55,590 | | | 38,283 | |
本年度の会社使用権資産の帳簿価値および変動状況は以下のとおりである
| | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | |
| リース非協働資産 | | 賃貸借協力資産 | | |
| 賃借権
土地 | | 建物.建物 | | 建物.建物 | | 機械設備
そして
装備 | | 電気計算機
そしてオフィスは
装備 | | 合計する |
| ドル‘000ドル | | ドル‘000ドル | | ドル‘000ドル | | ドル‘000ドル | | ドル‘000ドル | | ドル‘000ドル |
| 2022年12月31日 | | | | | | | | | | | |
| 2022年1月1日までの使用権資産 | 4,862 | | | 2,324 | | | 19,907 | | | 11,174 | | | 16 | | | 38,283 | |
| 足し算 | — | | | 23,163 | | | — | | | 298 | | | — | | | 23,461 | |
| 減価償却累計 | — | | | — | | | — | | | — | | | — | | | — | |
| 取引所再調整 | (408) | | | (3) | | | — | | | — | | | — | | | (411) | |
| 使用権資産減価償却 | (97) | | | (2,468) | | | (1,412) | | | (1,761) | | | (5) | | | (5,743) | |
| 2022年12月31日までの使用権資産 | 4,357 | | | 23,016 | | | 18,495 | | | 9,711 | | | 11 | | | 55,590 | |
| 2021年12月31日 | | | | | | | | | | | |
| 2021年1月1日までの使用権資産 | 4,851 | | | 3,158 | | | 21,311 | | | 10,201 | | | 21 | | | 39,542 | |
| 足し算 | — | | | 678 | | | 7 | | | 2,517 | | | — | | | 3,202 | |
| 賃貸借変更 | — | | | (59) | | | — | | | (53) | | | — | | | (112) | |
| 取引所再調整 | 112 | | | (62) | | | — | | | — | | | — | | | 50 | |
| 使用権資産減価償却 | (101) | | | (1,391) | | | (1,411) | | | (1,491) | | | (5) | | | (4,399) | |
| 2021年12月31日までの使用権資産 | 4,862 | | | 2,324 | | | 19,907 | | | 11,174 | | | 16 | | | 38,283 | |
(b)賃貸負債
賃貸負債は以下のとおりである
レンタル開始日に、当社はレンタル支払いの現在価値で計量されたレンタル負債がレンタル期間内に支払われることを確認しました。
| | | | | | | | | | | |
| 2022 | | 2021 |
| ドル‘000ドル | | ドル‘000ドル |
| 1月1日帳簿金額 | 2,504 | | | 3,373 | |
| 足し算 | 23,703 | | | 678 | |
| 賃貸借変更 | — | | | — | |
| 処置する | — | | | (68) | |
| 年内確認の利子増加 | 527 | | | 142 | |
| 支払い | (3,123) | | | (1,561) | |
| 取引所再調整 | (9) | | | (60) | |
| 12月31日帳簿金額 | 23,602 | | | 2,504 | |
| 分析結果は以下のとおりである | | | |
| 現在の部分 | 3,563 | | | 911 | |
| 非流動部分 | 20,039 | | | 1,593 | |
| 合計する | 23,602 | | | 2,504 | |
(c)レンタルに関する損益で確認された金額は以下の通りです
| | | | | | | | | | | |
| 2022 | | 2021 |
| ドル‘000ドル | | ドル‘000ドル |
| 賃貸負債利息 | 527 | | | 142 | |
| 使用権資産減価償却費用 | 5,743 | | | 4,399 | |
| 短期レンタルに関する費用 | 1,132 | | | 182 | |
| 損益で確認した総金額 | 7,402 | | | 4,723 | |
リース負債の満期分析は、財務諸表付記35に開示される。リース現金流出総額は財務諸表付記31(C)に開示される。
レンタル人としての会社
当社はヤンソン合意に基づいて所有している資産を提携会社に貸します。これらは融資リースであり、会社は2022年12月31日と2021年12月31日までの年度に些細な融資収入を確認した。
2022年12月31日、2022年12月31日および2021年12月31日に、テナントと締結した取消不可経営賃貸契約に基づいて、当社の未来期間の未割引最低賃貸支払い売掛金は以下の通り
| | | | | | | | | | | |
| 2022 | | 2021 |
| ドル‘000ドル | | ドル‘000ドル |
| 融資リース: | | | |
| 1年以内に | 583 | | | 94 | |
14. 転換可能優先株
2020年3月30日と2020年4月16日、当社は共同で発表します20,591,629Aシリーズ転換可能優先株(“Aシリーズ優先株”)は独立第三者に売却され、価格は#ドル7.7921株当たり、総購入コストは$160.5百万ドルです
すべてのAシリーズ優先株は当社普通株に変換され、すべて計上されていますが支払われていない配当は2020年6月に条件を満たす初公募株の場合は普通株形式で決済されます。公正価値損失$80.0転換時の公正価値の変化により、2020年12月31日までの会計年度に1000万ユーロを記録した。
15. 協業在庫
| | | | | | | | | | | |
| 十二月三十一日
2022 | | 十二月三十一日
2021 |
| ドル‘000ドル | | ドル‘000ドル |
| | | |
| 原料.原料 | 6,989 | | | 1,749 | |
| 製品の中で | 690 | | | — | |
| 完成品 | 2,675 | | | — | |
| 協業在庫合計 | 10,354 | | | 1,749 | |
同社の在庫準備金は#ドルです5.32022年12月31日までに会社は違います。2021年12月31日までの在庫準備金。当社の2022年12月31日までの在庫備蓄は、主に期限切れ材料と、品質規格を満たしていないいくつかのロットまたは単位製品に関連し、共同販売コストを計上しています。
16. 売掛金
| | | | | | | | | | | |
| 十二月三十一日
2022 | | 十二月三十一日
2021 |
| ドル‘000ドル | | ドル‘000ドル |
| 売掛金 | 90 | | | 50,410 | |
その会社とその顧客との取引条件は主に売掛です。信用限度額は45至れり尽くせり60何日ですか。当社は未払い売掛金を厳格にコントロールし、管理層が期限を過ぎた残高を定期的に審査することを求めている。売掛金は利息を計算しません。同社の信用リスクは$に集中している50.0百万(または)99.22021年12月31日現在、単一顧客は、許可と協力協定により満期となった貿易売掛金の%)
2022年、2022年、2021年12月31日まで、予想される信用損失は取るに足らない。
17. 前払金、その他の入金、その他の資産
| | | | | | | | | | | |
| 十二月三十一日
2022 | | 十二月三十一日
2021 |
| ドル‘000ドル | | ドル‘000ドル |
| 受取利息 | 1,517 | | | 230 | |
| その他売掛金 | 41,324 | | | 837 | |
| 賃借金を受け取る | 188 | | | 94 | |
| 所得税を払い戻す | 1,003 | | | 4,712 | |
| 付加価値税は税金の払い戻しができる | 1,396 | | | 2,264 | |
| 繰り上げ返済する | 16,327 | | | 5,715 | |
| 合計する | 61,755 | | | 13,852 | |
会社の他の入金に含まれる会社の関連先の受取金は#ドルです0.32022年12月31日、2022年12月31日、2021年12月31日(注32)。2022年12月31日現在、2022年12月31日および2021年12月31日まで、当社関連先に前払いする金額は#ドルです0.3百万ドルとドル1.2百万ドル(付記32)。
上記の資産はいずれも期限を超えていないか減価されていない。上記残高に記載されている金融資産は、最近違約履歴のない入金に係る。上記の大部分の残高は12ヶ月以内に決済されており、延滞歴史はない。当社は、上記の売掛金が2022年、2022年及び2021年12月31日に予想される信用損失は取るに足らないと推定している。
18. 余剰コストで計量された金融資産
| | | | | | | | | | | |
| 十二月三十一日
2022 | | 十二月三十一日
2021 |
| ドル‘000ドル | | ドル‘000ドル |
| 余剰コストで計量された金融資産 | — | | | 29,937 | |
償却コストで計量された金融資産は、ある金融機関が発行した元本#ドルの商業手形と関係がある30.03.5億割引収益率は0.5年利率1年期日は2022年6月1日である。
19. 現金と現金等価物、定期預金と質権預金
| | | | | | | | | | | |
| 十二月三十一日
2022 | | 十二月三十一日
2021 |
| ドル‘000ドル | | ドル‘000ドル |
| 現金と現金等価物 | 841,317 | | | 858,607 | |
| 差し引く:質抵当預金 | (1,270) | | | (1,444) | |
| 定期預金 | (54,016) | | | (168,225) | |
| | | |
| 現金と現金等価物 | 786,031 | | | 688,938 | |
| | | |
| ドルで値段を計算する | 727,160 | | | 681,025 | |
| 人民元で値段を計算する | 21,472 | | | 5,875 | |
| ユーロで値段を計算する | 37,399 | | | 2,038 | |
| | | |
| 現金と現金等価物 | 786,031 | | | 688,938 | |
当社は人民元(“人民元”)建ての現金及び現金等価物を$とする21.5百万ドルとドル5.9それぞれ2022年、2022年と2021年12月31日の総合財務状況表に百万元を列挙した。人民元は自由に他の通貨に両替することはできないが、“大中国外貨管理条例”と“決済管理条例”の規定により、会社は外国為替業務を許可した銀行を通じて人民元を他の通貨に両替することができる。
2022年12月31日までの質抵当預金は質抵当であり、当社の1つのサプライヤーに保証書を発行し、クレジットカード融資に使用する。2021年12月31日現在の質抵当預金は質抵当であり、当社のサプライヤーとクレジットカード施設に銀行引受手形を発行するために使用される。
銀行の現金は1日の銀行預金金利をもとに、変動金利で利息を稼ぐ。銀行残高は信用の良い銀行に保管されており、最近は違約の歴史がない。現金と現金等価物の帳簿価値はその公正価値に近い。
20. 貿易応払い
| | | | | | | | | | | |
| 十二月三十一日
2022 | | 十二月三十一日
2021 |
| ドル‘000ドル | | ドル‘000ドル |
| 貿易応払い | 32,893 | | | 7,043 | |
貿易請求金は利息を計算しません。通常は30日間条項です。
2022年、2022年、2021年12月31日現在、対応会社の関連先の金額は、会社の貿易未払いに含まれており、金額は$です1.2百万ドルとドル2.4百万ドル(付記32)。
21. その他の支払及び課税項目
| | | | | | | | | | | |
| 十二月三十一日
2022 | | 十二月三十一日
2021 |
| ドル‘000ドル | | ドル‘000ドル |
| 賃金総額を計算すべきである | 21,892 | | | 19,207 | |
| 費用を計算する | 127,390 | | | 81,364 | |
| その他の支払い | 10,960 | | | 16,867 | |
| 協調資産の対応 | 22,852 | | | 5,605 | |
| その他課税額 | 1,015 | | | 515 | |
| 184,109 | | | 123,558 | |
その他の支払いは利息ではなく、必要に応じて返済しなければなりません。
2022年12月31日現在、2022年12月31日および2021年12月31日現在、当社の他の対応金に計上されている当社関連先金は$2.5百万ドルとドル3.3百万ドル(付記32)。
22. 税金を繰延する
2022年12月31日と2021年12月31日までの繰延税金負債と資産変動状況は以下の通り
繰延税金負債
| | | | | | | | | | | | | | | | | | | | | | | |
| 協力収入 | | 超過減価償却の差額準備 | | 使用権資産 | | 合計する |
| ドル‘000ドル | | ドル‘000ドル | | ドル‘000ドル | | ドル‘000ドル |
| 2021年1月1日 | (28,211) | | | (6,672) | | | (159) | | | (35,042) | |
| 今年度の損益計算書に計上された繰延税金 | 14,086 | | | (1,964) | | | 159 | | | 12,281 | |
2021年12月31日現在の繰延税金負債総額 | (14,125) | | | (8,636) | | | — | | | (22,761) | |
| 2022年1月1日 | (14,125) | | | (8,636) | | | — | | | (22,761) | |
| 今年度の損益計算書に計上された繰延税金 | 14,125 | | | 885 | | | (114) | | | 14,896 | |
2022年12月31日現在の繰延税金負債総額 | — | | | (7,751) | | | (114) | | | (7,865) | |
繰延税金資産
| | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | |
| 将来の課税利益の損失を相殺するために使える | | 無形資産償却差額 | | 費用を計算する | | リース責任 | | R&D費用のコスト回収 | | 信用を研究開発する | | 合計する |
| ドル‘000ドル | | ドル‘000ドル | | ドル‘000ドル | | ドル‘000ドル | | ドル‘000ドル | | ドル‘000ドル | | ドル‘000ドル |
| 2021年1月1日 | 15,081 | | | 5,342 | | | 608 | | | 165 | | | — | | | 9,605 | | | 30,801 | |
年度損益表から差し引かれた繰延税金 | 5,367 | | | (4,286) | | | 649 | | | (165) | | | — | | | (9,605) | | | (8,040) | |
2021年12月31日現在の繰延税項目総資産 | 20,448 | | | 1,056 | | | 1,257 | | | — | | | — | | | — | | | 22,761 | |
| 2022年1月1日 | 20,448 | | | 1,056 | | | 1,257 | | | — | | | — | | | — | | | 22,761 | |
年度損益表から差し引かれた繰延税金 | (20,448) | | | 194 | | | 2,192 | | | 120 | | | 3,046 | | | — | | | (14,896) | |
2022年12月31日までの繰延税項目総資産 | — | | | 1,250 | | | 3,449 | | | 120 | | | 3,046 | | | — | | | 7,865 | |
同社が香港で発生した税務損失は$である1.92022年に百万ドル(2021年:ドル)38.0千ドル)で、赤字が発生した会社の将来の課税利益を無期限に相殺することができる。
当社が大区中国で発生した税額損失は$である90.92022年に百万ドル(2021年:ドル)91.8百万)は5損失が発生した会社の将来の課税利益を相殺するための年度
その会社がアイルランドで発生した税金損失は#ドルだ118.62022年100万ドル(2021ドル)82.9百万ドル) 持ち帰ってもいいもの1会社の課税利益を相殺するために無期限に繰り越した.
その会社がアメリカ合衆国で発生した税金損失は#ドルだった149.92022年に百万ドル(2021年:ドル)226.6百万ドル) これらの資金は損失が発生した会社の将来の課税利益を無期限に相殺することができる。
繰延税金資産は当該等税項目の損失について確認されていません。課税利益が当該等税項損失を相殺することができるはずがないと考えられるからです。
報告年度内に、次の項目は繰延税金資産を確認していません
| | | | | | | | | | | |
| 2022 | | 2021 |
| ドル‘000ドル | | ドル‘000ドル |
| 差し引くことができる一時的な違い | 190,133 | | | 15,420 | |
| 税損 | 966,542 | | | 609,200 | |
| 合計する | 1,156,675 | | | 624,620 | |
繰延所得税資産は、将来課税利益により関連税項利益を実現する可能性がある程度で、繰越税項損失であることが確認された。繰延税金資産は上記の項目について確認されていません。これらの項目を相殺するための課税オーバーメリットがある可能性は低いと考えられるからです。
“中華人民共和国企業所得税法”によると、a10中国大中華区に設立された外商投資企業が外国投資家に申告した配当金には、%の源泉徴収税が徴収される。この要求は2008年1月1日から施行され、2007年12月31日以降の収益に適用される。大中国と外国投資家の司法管轄区域の間に税収条約があれば、低い事前提出税率を適用することができる。当社に対して適用される料率は10%です。そのため、当社は中国大区に設立された付属会社から派遣された配当金について、2008年1月1日から1日までに発生した収益について税金を前納する責任がある。
2022年12月31日現在、2022年12月31日と2021年12月31日まで、大中国の子会社違います。留保収益を分配することができる。
アメリカ税法によると、会社のアメリカ実体はアメリカの非住民企業に支払う配当金です30税金を前納します。米国と外国投資家の管轄区域の間に税収条約があれば、より低い源泉徴収税率を適用することができる。当社に対して適用される料率は5%です。そのため、同社は米国に設立された子会社に割り当てられた配当金に源泉徴収する責任がある。
2022年12月31日及び2021年12月31日に、米国の子会社違います。留保収益を分配することができる。
23. 株式証法的責任
2021年5月13日、当社は機関投資家と引受契約を締結し、契約及び販売に関する20,809,850当社普通株、額面$0.00011株当たり、私募では、買い取り価格は$14.41625普通株式1株(“パイプ発行”)。パイプ発行の総収益は$である300.0百万ドルです。引受契約によると、当社も株式承認証(“株式承認証”)を発売すると同時に株式承認証(“株式承認証”)を発行及び販売することに同意し、行使可能な総金額は20%に達する10,000,000普通株式(このような取引はパイプライン発行とともに、単に“取引”と呼ぶ)。同等取引は2021年5月21日(“成約日”)に完了した。株式承認証は全部或いは部分的に行使でき、使用価格は#ドルである20.0すべての普通株式は、締め切りの2年前のいつでも
株式承認証は財務負債として入金され、株式承認証は所有者が選択して決済できる純株式である可能性があるからである。株式証券負債の公正価値評価は#ドルであった81.7百万ドル、取引が完了した時に確認します。2022年12月31日まで、株式承認証の公正価値はドルと評価された67.0百万ドルです。公正価値収益$20.9公正価値の変化により,2022年12月31日までの年度の損益は百万元を記録した。経営陣は、2022年12月31日までの年間で、当社自身の信用リスクに大きな変化はなく、負債の公正価値変動を証明するとしている。
株式証券負債の変動状況は以下のとおりである
| | | | | | | | | | | |
| 2022 | | 2021 |
| ドル‘000ドル | | ドル‘000ドル |
| 期初残高 | 87,900 | | | — | |
| 株式証責任の発行 | — | | | 81,700 | |
| 株式証負債の公正価値(収益)/損失を認める | (20,900) | | | 6,200 | |
| 期末残高 | 67,000 | | | 87,900 | |
24. 政府支出
| | | | | | | | | | | |
| 2022 | | 2021 |
| ドル‘000ドル | | ドル‘000ドル |
| 繰延の政府支出 | 8,110 | | | 2,170 | |
| 現在のところ | 451 | | | 304 | |
| 当面ではない | 7,659 | | | 1,866 | |
贈与金は、ある施設の支出を補償するために自治体当局から得た補助金に関連し、繰延収入口座に記入される。贈与は、関連資産の予想使用年限内の他の収入および収益に使用される。同グループはまた、現地政府当局から一定の財政補助金を受け、現地企業を支援している。このような政府の贈与には未履行の条件と他の事項がない。これらの政府の贈与は受け取った時に他の収入と収益で確認される。
25. 協力利息前払い資金
| | | | | | | | | | | | | | | | | |
| 効き目がある
利子
率 | | 成熟性 | | 十二月三十一日
2022 |
| % | | | | ドル‘000ドル |
| 当面ではない | — | | | | | — | |
| 協力者からの融資 | 7.98 | | | 具体的な期日はない | | 260,932 | |
協力者と締結された許可及び連携協定によると、ある運営条件が満たされた場合、会社は協力者から資金前払いを受ける権利がある。そのため、同社は元金#ドルの初期資金前払いを獲得した17.32021年6月18日、元金600万ドルの第2の前金53.12021年9月17日、元金300万ドルの第3回前払い49.32021年12月17日、元金400万ドルの第4回前払い5.32022年3月18日、元本50億ドルの第5回前払い60.92022年6月17日、元金600万ドルの第6回前払い60.52022年9月16日は100万ドルで、元金は7回目の前払いです3.62022年12月16日、提携者に支払うべき同じ額の他の支払(総称して“前払い”と呼ぶ)をそれぞれ減らすことによって、600万ドルを支払うことができる。
これらの資金前払は,協力者が資金を提供する利息借款と記載されており,元金から構成され,元金は#ドルである250.0百万と利息が適用され,累算総額は$に達する10.9このような元金に百万ドルです。各借金の金利は、“ウォール·ストリート·ジャーナル”が四半期領収書満期日または次の営業日(満期日が週末や祝日に当たる場合)に報道されたドルロンドン銀行間同業借り換え金利(LIBOR)の平均年率に基づいている250基点は、会社が当該等の借金を申請した日から日数として算出する。7回の前借り金はそれぞれ2021年6月18日、2021年9月17日、2021年12月17日、2022年3月18日、2022年6月17日、2022年9月16日および2022年12月16日から利上げを開始した。
許可及び協力協定の条項によれば、協力者は、協力計画の最初の利益年度の会社税前利益から前払総額及びその利息を回収することができるそしてヤンソン協定に基づいて当社に支払うべきマイルストーン支払いですが、いくつかの制限を受けなければなりませんそれは.会社の経営陣は,協力者は1年以内に融資を回収しないと予想している
当社も1年以内に立て替え金の返済を期待していないため、このローンは長期負債とされている。
26. 株と株の割増
株
| | | | | | | | | | | |
| 十二月三十一日
2022 | | 十二月三十一日
2021 |
| ドル‘000ドル | | ドル‘000ドル |
| 許可: | | | |
2,000,000,000$の株0.0001どれも | 200 | | | 200 | |
| 配布され、全額支払いされました | | | |
330,134,480 (2021: 308,456,852)普通株$0.0001どれも | 33 | | | 31 | |
当社の株式および株式割増変動状況の概要は以下の通りである
| | | | | | | | | | | | | | | | | | | | | | | |
| 量
既発行株 | | 共有
資本 | | 共有
割増価格 | | 合計する |
| | | ドル‘000ドル | | ドル‘000ドル | | ドル‘000ドル |
| 2020年12月31日と2021年1月1日 | 266,010,256 | | 27 | | | 708,306 | | | 708,333 | |
| | | | | | | |
| 機関投資家指向増発に関する普通株を発行する | 20,809,850 | | 2 | | | 218,298 | | | 218,300 | |
| 後続の公開発行のために普通株を発行し,発行コストを差し引く | 17,231,150 | | 2 | | | 323,438 | | | 323,440 | |
| 購入権を行使する | 4,056,380 | | — | | | 6,089 | | | 6,089 | |
| 限定株帰属の再分類 | 349,216 | | — | | | 5,323 | | | 5,323 | |
| | | | | | | |
| 2021年12月31日と2022年1月1日に | 308,456,852 | | 31 | | | 1,261,454 | | | 1,261,485 | |
| | | | | | | |
| 後続の公開発行のために普通株を発行し,発行コストを差し引く | 18,722,000 | | 2 | | | 377,641 | | | 377,643 | |
| 購入権を行使する | 2,040,580 | | — | | | 4,070 | | | 4,070 | |
| 限定株帰属の再分類 | 915,048 | | — | | | 13,850 | | | 13,850 | |
| | | | | | | |
| 2022年12月31日 | 330,134,480 | | 33 | | | 1,657,015 | | | 1,657,048 | |
注:2022年7月29日、当社は以下のように後続公開を完了しました18,722,000普通株、合計$21.50普通株ごとに純収益$を受け取ります377.6100万ドル、関連発行コストを差し引いて$24.9百万ドルです。
27. 株式オプション案
当社は、当社の経営成功に貢献した合資格参加者に奨励及び奨励を提供することを目的とした株式購入計画(“同計画”)を実施します。この計画の合資格参加者は、当社取締役(独立非執行役員を含む)及び当社の任意のメンバー会社の従業員を含む。この計画は2017年12月21日に施行され、他にキャンセルや改訂がない限り有効になります10その日から数年。この計画には業績帰属条件が設けられており、参加者が取締役会が設定したいくつかの業績目標を達成できなかった場合、その計画は没収されることができる。
株式オプションは、いかなる投票権も付与されない、または配当金または分配に参加する権利を付与しない年内、同計画の未償還株式購入権は以下の通り
| | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | |
| 2022 | | 2021 | | 2020 |
| 重みをつける
平均値
トレーニングをする
値段 | | 量
オプション | | 重みをつける
平均値
トレーニングをする
値段 | | 量
オプション | | 重みをつける
平均値
トレーニングをする
値段 | | 量
オプション |
| 1株当たりドル | | ’000 | | 1株当たりドル | | ’000 | | 1株当たりドル | | ’000 |
| 1月1日 | 2.8970 | | | 9,529 | | 1.9353 | | | 14,241 | | 0.9273 | | | 18,013 |
| 年内に発送する | 19.4468 | | | 2,265 | | 15.4774 | | | 595 | | 15.6128 | | | 679 |
| 今年度中に没収される | 4.2888 | | | (573) | | 2.9987 | | | (1,251) | | 0.9963 | | | (2,769) |
| 年内に行われる運動 | 1.8032 | | | (2,041) | | 1.3346 | | | (4,056) | | 1.0131 | | | (1,682) |
| 十二月三十一日 | 7.1370 | | | 9,180 | | 2.8970 | | | 9,529 | | 1.9353 | | | 14,241 |
| 12月31日に行使できます | 2.8705 | | | 3,281 | | 1.4334 | | | 2,828 | | 1.0703 | | | 4,619 |
2022年以内に株式購入権を行使する日の加重平均株価は$22.58131株当たり(2021年:$18.4846, 2020: $14.9131).
本報告で述べた期間終了時点で、行使されていない株式オプションの行権価格と行権期間は以下のとおりである
| | | | | | | | | | | | | | |
| 2022年12月31日 | | |
量
オプション.000 | | 行権価格*
ドル
1株当たり | | 運動周期 |
| 2,875 | | 0.5 | | | 2019/12/25 – 2027/12/25 |
| 1,248 | | 1.0 | | | 2019/07/01 – 2028/08/29 |
| 271 | | 1.0 | | | 2019/12/31 – 2028/12/30 |
| 1,393 | | 1.5 | | | 2020/07/02 – 2029/07/01 |
| 201 | | 11.5 | | | 2020/11/29 – 2029/11/28 |
| 90 | | 11.5 | | | 2021/06/05 – 2030/06/04 |
| 322 | | 16.3 | | | 2021/09/01 – 2030/08/31 |
| — | | 13.6 | | | 2021/11/19 – 2030/11/18 |
| 410 | | 14.1 | | | 2022/03/29 – 2031/03/28 |
| 165 | | 19.0 | | | 2022/08/27 – 2031/08/26 |
| 740 | | 18.4 | | | 2023/03/31 - 2032/03/30 |
| 750 | | 18.2 | | | 2023/04/30 - 2032/04/29 |
| 80 | | 18.4 | | | 2023/05/02 - 2032/05/01 |
| 40 | | 18.4 | | | 2023/05/05 - 2032/05/04 |
| 80 | | 18.4 | | | 2023/05/08 - 2032/05/07 |
| 200 | | 18.4 | | | 2023/05/10 - 2032/05/09 |
| 15 | | 19.7 | | | 2023/05/13 - 2032/05/12 |
| 240 | | 27.5 | | | 2023/06/30 - 2032/06/29 |
| 60 | | 23.3 | | | 2023/08/02 - 2032/08/01 |
| 9,180 | | | | |
| | | | | | | | | | | | | | |
| 2021年12月31日 | | |
量
オプション.000 | | 行権価格*
ドル
1株当たり | | 運動周期 |
| 4,054 | | 0.5 | | | 2019/12/25 – 2027/12/25 |
| 1,849 | | 1.0 | | | 2019/07/01 – 2028/08/29 |
| 382 | | 1.0 | | | 2019/12/31 – 2028/12/30 |
| 1,822 | | 1.5 | | | 2020/07/02 – 2029/07/01 |
| 332 | | 11.5 | | | 2020/11/29 – 2029/11/28 |
| 90 | | 11.5 | | | 2021/06/05 – 2030/06/04 |
| 385 | | 16.3 | | | 2021/09/01 – 2030/08/31 |
| 20 | | 13.6 | | | 2021/11/19 – 2030/11/18 |
| 430 | | 14.1 | | | 2022/03/29 – 2031/03/28 |
| 165 | | 19.0 | | | 2022/08/27 – 2031/08/26 |
| 9,529 | | | | |
| | | | | | | | | | | | | | |
| 2020年12月31日 | | |
量
オプション.000 | | 行権価格*
ドル
1株当たり | | 運動周期 |
| 5,393 | | 0.5 | | | 2019/12/25 - 2027/12/25 |
| 4,317 | | 1.0 | | | 2019/07/01 - 2028/08/29 |
| 540 | | 1.0 | | | 2019/12/31 - 2028/12/30 |
| 2,868 | | 1.5 | | | 2020/07/02 - 2029/07/01 |
| 444 | | 11.5 | | | 2020/11/29 - 2029/11/28 |
| 90 | | 11.5 | | | 2021/06/05 - 2030/06/04 |
| 569 | | 16.3 | | | 2021/09/01 - 2030/08/31 |
| 20 | | 13.6 | | | 2021/11/19 - 2030/11/18 |
| 14,241 | | | | |
*配当又は配当発行又は自社株の他の類似変動がある場合には、購入株式の行使価格が調整される可能性がある。香港聯交所のいくつかのメンバー会社が遵守しなければならない香港聯通所の上場規則によると、当社は2019年11月29日から2019年12月9日までの間に授受される購入権の行使価格をドルに調整する11.50一株ずつです。この調整を行うと同時に、当社は影響を受けて株式を購入した従業員1人に現金金額を支払うことに同意し、株式購入時に調整された行権価格と元の権利価格との差額を代表する。
2022年12月31日までに年度内に譲渡された株式の公平な価値は$27.2百万ドル12.010各)(2021年:$5.7百万、$9.4972020年:ドル6.7百万、$9.817それぞれ)。会社は株式承認支出が#ドルであることを確認した10.7百万ドル(2021年:ドル)2.4百万ドル2020年ドル1.92022年12月31日までの年度内)。
本期間に付与された株式決済株式購入の公正価値は二項モデルを用いて推定され、このオプションを付与する条項と条件を考慮する以下の表に用いたモデルの入力を示す
| | | | | | | | | | | | | | | | | |
| 2022 | | 2021 | | 2020 |
| 配当率(%) | — | | | — | | | — | |
| 期待変動率(%) | 73.0% - 87.1% | | 73.2% -76.4% | | 73.0% - 87.2% |
| 無リスク金利(%) | 0.52% - 3.11% | | 0.03% - 1.72% | | 0.07%- 0.91% |
| オプションの期待寿命 | 10 | | 10 | | 10 |
予想株価収益の標準偏差で測定した変動率は、同業界の比較可能な上場企業の統計分析に基づいている。加重平均株価は1ドルです19.44682022年12月31日までの年度内に株式購入公正価値推定モデルに使用する。
2022年12月31日現在、当社は9,179,778この計画によるとまだ株式購入権を行使していない。当社の現在の資本構造によると,まだ行使されていない株式購入権を全部行使することで発行につながる9,179,778会社の追加普通株、追加配当金$918株の割増#ドルです65.5100万ユーロ(未発行費用)。
これらの財務諸表を承認する日に会社は9,179,778株式購入計画の下でまだ行使されていない株購入権は,約50%を占める2.8当社がこの日発行した株式の割合を占めています。
28. 限定株単位
会社はRSU計画を実行し、会社の運営成功に貢献した合資格参加者に奨励と奨励を提供することを目的としている。この計画の合資格参加者は、当社取締役(独立非執行役員を含む)及び当社の任意のメンバー会社の従業員を含む。RSUは2020年5月26日に施行される予定で、別途キャンセルや改訂がない限り、10その日から数年。RSU計画には業績帰属条件があり、参加者が取締役会が設定したいくつかの業績目標を達成できない場合、その計画は没収されることができる。
2022年、2022年、2021年、2020年12月31日までの年度の未返済債務単位数の変動状況は以下の通り
| | | | | | | | | | | |
| 2022 |
| 量
RSU | | 重みをつける
平均値
授与日
公正価値 |
| ’000 | | ドル/単位 |
| 1月1日現在の未返済金 | 2,601 | | 15.1808 | |
| 年内に発送する | 2,200 | | 20.5695 | |
| 年内に帰属する | (915) | | 15.1354 | |
| 今年度中に没収される | (500) | | 17.3746 | |
| 12月31日現在の未返済金 | 3,386 | | 18.3704 | |
| | | | | | | | | | | |
| 2021 |
| 量
RSU | | 重みをつける
平均値
授与日
公正価値 |
| ’000 | | ドル/単位 |
| 1月1日現在の未返済金 | 1,113 | | 15.3409 | |
| 年内に発送する | 2,133 | | 15.0120 | |
| 年内に帰属する | (349) | | 15.2420 | |
| 今年度中に没収される | (296) | | 14.4913 | |
| 12月31日現在の未返済金 | 2,601 | | 15.1808 | |
資源割当て単位によって計画された未償還単位の加重平均残存契約期間は7.86そして8.16それぞれ2022年、2022年、2021年12月31日まで。
付与株式の公正価値は、自社株式のそれぞれの授出日の市価に基づいて計算される。
2022年12月31日現在,期間内に付与された買い戻し単位の公正価値は$である45.3百万ドル20.570各会社はRSU費用が#ドルであることを確認しました23.6百万ドルです。
2021年12月31日までの年度中に付与された買い戻し単位の公正価値は$である32.0百万ドル15.012各会社はRSU費用が#ドルであることを確認しました17.8百万ドルです
二零年十二月三十一日までの年度、期間内に付与された買い戻し先の公正価値は17.5百万ドル15.364各会社はRSU費用が#ドルであることを確認しました2.9百万ドルです。
これらの財務諸表を承認する日に会社は3,386,305RSU計画で返済されていないRSUは約1.0当社がこの日発行した普通株式の割合を占める。
29. 埋蔵量
本年度および例年の当社備蓄金の額とその変動を総合財務諸表の総合権益変動表に示した。
外貨換算準備金には、経営財務諸表をドル以外の機能通貨で換算したすべての為替差額が含まれています。
中国の法律及び法規によると、当社の中国付属会社はいくつかの純資産を配当、ローン又は立て替えの形で当社に譲渡してはならない。制限された純資産には、当社の中国子会社の実納資本と備蓄資金が含まれ、総額は$81.8百万ドルとドル71.92022年、2022年、2021年12月31日まで、それぞれ100万人。
30. 合併現金フロー表に付記する
(a)主に非現金取引
当社は2022年,2022年および2021年12月31日までに,協力利息前借り資金に非現金および追加金を増加させた$130.3百万ドルとドル119.7協力者に他の支払いを差し引くことで受け取った100万ドル。
2022年12月31日および2021年12月31日までの当社の非現金および公正価値収益は20.9百万ドルと非現金公正価値損失6.2株式承認債務は1.5億ドルである。
2021年12月31日まで、当社は非現金前払い$を持っています1.5南京ProBio生物技術有限会社と江蘇GenScript ProBio生物技術有限会社は研究開発サービスを100万ドル交換した。
2022年、2022年、2021年、2020年12月31日までの年度、会社の使用権資産に対する非現金増加は$23.2百万、$0.7百万ドルとドル0.5百万ドル賃貸負債は$23.7百万、$0.7百万ドルとドル0.5三百万ドルで、それぞれ建物のレンタル手配に使われます。
本グループは、2022年、2022年、2021年および2020年12月31日までの年度までに、パートナーへのリース資産の他の支払金および計上項目には、パートナーへの前払いリースの非現金増加を含む26.501000万ドル7.6百万ドルとドル5.2それぞれ100万ドルで、不動産、工場と設備の非現金増加を他の支払いと応算項目に入れた#ドル5.1百万、$6.7百万ドルとドル8.6それぞれ100万ドルです
2020年12月31日までの当社の非現金公正価値損失は80.0百万株転換可能な優先株を償還できる。
(b)融資活動による負債変動
| | | | | | | | | | | | | | | | | |
| オープンカー
償還可能である
優先株 | | その他は支払うべきです
関連先 | | 賃貸負債 |
| ドル‘000ドル | | ドル‘000ドル | | ドル‘000ドル |
| 2022年1月1日 | — | | | — | | | 2,504 | |
| 賃貸負債の増加 | — | | | — | | | 23,703 | |
| 融資キャッシュフローの変化 | — | | | — | | | (2,596) | |
| 処置する | — | | | — | | | — | |
| 利子支出 | — | | | — | | | 527 | |
| 支払済み利息は、運営キャッシュフローに分類されます | — | | | — | | | (527) | |
| 外国為替動向 | — | | | — | | | (9) | |
| 2022年12月31日 | — | | | — | | | 23,602 | |
| 2021年1月1日 | — | | | — | | | 3,373 | |
| 賃貸負債の増加 | — | | | — | | | 678 | |
| 融資キャッシュフローの変化 | — | | | — | | | (1,419) | |
| 処置する | — | | | — | | | (68) | |
| 利子支出 | — | | | — | | | 142 | |
| 支払済み利息は、運営キャッシュフローに分類されます | — | | | — | | | (142) | |
| 外国為替動向 | — | | | — | | | (60) | |
| 2021年12月31日 | — | | | — | | | 2,504 | |
| 2020年1月1日 | — | | | 4 | | | 6,085 | |
| 賃貸負債の増加 | — | | | — | | | (437) | |
| 融資キャッシュフローの変化 | 160,450 | | | (4) | | | (2,602) | |
| 利子支出 | — | | | — | | | 195 | |
| 支払済み利息は、運営キャッシュフローに分類されます | — | | | — | | | (195) | |
| 転換可能優先株の公正価値損失 | 79,984 | | | — | | | — | |
| 普通株に転換する | (240,434) | | | — | | | — | |
| 外国為替動向 | — | | | — | | | 327 | |
| 2020年12月31日 | — | | | — | | | 3,373 | |
(c)リース現金流出総額
キャッシュフロー表に記載されているレンタル現金の流出総額は以下の通りです
| | | | | | | | | | | | | | | | | |
| 2022 | | 2021 | | 2020 |
| ドル‘000ドル | | ドル‘000ドル | | ドル‘000ドル |
| 経営活動中に | 527 | | | 142 | | | 195 | |
| 融資活動では | 2,596 | | | 1,419 | | | 2,602 | |
| 短期賃貸借契約 | 1,132 | | | 182 | | | 69 | |
| 合計する | 4,255 | | | 1,743 | | | 2,866 | |
31. 引受金とその他の事項
(a)資本約束
同社は年末に次のような資本約束を持っている
| | | | | | | | | | | | | | | | | |
| 2022 | | 2021 | | 2020 |
| ドル‘000ドル | | ドル‘000ドル | | ドル‘000ドル |
| 建設中の工事 | 22,706 | | | 25,897 | | | 33,637 | |
(b)あるいは損失がある
2021年9月、ある元従業員は、性別と誤りによって差別され、いわゆる保護活動に従事したことで完全に解雇されたと主張する連想米国会社に対する仲裁を米国仲裁協会に提起することを選択した。この元従業員はレノボに約1ドルの賠償金を要求しました3.0賃金損失、株式損失、名声損害、精神的苦痛、その他の関連損失に対して100万ドル賠償するといわれている。
経営陣は、この元従業員の上記の説は根拠がなく、積極的に弁護しようとしていると考えている。プログラムの早い段階では、管理層は上記クレームの最終結果を予測することができず、全てであっても部分であっても、これにより損失を招く可能性がある(あれば)。そのため、経営陣や法律顧問は、現時点では合理的に可能な損失額や手配を見積もることはできないとしている。したがって、財務諸表にはどんな負債も準備されていない。
(C)リースまたは事項
Janssenとレンタル契約を締結しました。このレンタルによって、私たちは約レンタルを予定しています106,000ヤンソンはニュージャージー州ラリタンの平方フィート製造工場にあります。 このリースは,米国食品医薬品局が我々のCilta−cel生物製品許可証申請の将来の日付を発効させてリース契約として記録することを施設移行日と呼ぶ。 Janssenと協力して運営しているこの施設については、CARVYKTIの発売をサポートするために、製造、品質、情報技術、流通能力に投資していきます。
32. 関係者取引
| | | | | | | | |
| 会社 | | 関係.関係 |
| 南京金思睿生物科技有限公司(前身は南京金思瑞生物科技有限公司) | | 最終持株会社が支配する会社 |
| 江蘇金思達生物科技有限公司。 | | 最終持株会社が支配する会社 |
| GenScripアメリカ社は | | 最終持株会社が支配する会社 |
| GenScrip USAホールディングスInc | | 最終持株会社が支配する会社 |
| GenScript Biotech.B.V. | | 最終持株会社が支配する会社 |
| 南京益生生物科学技術有限公司。 | | 最終持株会社が支配する会社 |
| 江蘇金斯普生物科技有限公司。 | | 最終持株会社が支配する会社 |
| GenScripオランダ | | 最終持株会社が支配する会社 |
| キングスレー生物科学技術(“遺伝子シナリオ”) | | 最終持株会社が支配する会社 |
| 遺伝子スクリプトProBioアメリカ社は | | 最終持株会社が支配する会社 |
(a)総合財務諸表に記載されている他の詳細な取引を除いて、当社は年内に関連側と以下の取引を行った
(i)関連側に特許の許可を付与する:
| | | | | | | | | | | | | | | | | |
| 2022 | | 2021 | | 2020 |
| ドル‘000ドル | | ドル‘000ドル | | ドル‘000ドル |
| 南京益生生物科学技術有限公司。 | — | | | 3,019 | | | — | |
この取引は南京ProBio生物技術有限会社及びその付属会社にある特許を独占的に許可することによって生まれた。
(Ii)関連側の売上に基づく印税:
| | | | | | | | | | | | | | | | | |
| 2022 | | 2021 | | 2020 |
| ドル‘000ドル | | ドル‘000ドル | | ドル‘000ドル |
| 南京益生生物科学技術有限公司。 | 328 | | | 405 | | | — | |
この取引の収入は、南京ProBio生物技術有限会社及びその付属会社にある特許を独占的に許可することに関する販売ベースの使用料から来ている。
(Iii)関連先から購入:
| | | | | | | | | | | | | | | | | |
| 2022 | | 2021 | | 2020 |
| ドル‘000ドル | | ドル‘000ドル | | ドル‘000ドル |
| 南京金思達生物科学技術有限公司。 | 6,174 | | | 9,615 | | | 4,162 | |
| 江蘇基恩思特ProBio生物技術有限公司 | 1,306 | | | 334 | | | — | |
| GenScripアメリカ社は | 1,028 | | | 786 | | | 424 | |
| GenScrip USAホールディングスInc | 380 | | | — | | | — | |
| 南京益生生物科学技術有限公司。 | 237 | | | 21 | | | — | |
| 江蘇金思特生物科技有限公司 | 51 | | | 146 | | | 41 | |
| 遺伝子スクリプトProBioアメリカ社は | 8 | | | — | | | — | |
| GenScripオランダ | 5 | | | 6 | | | — | |
| 合計する | 9,189 | | | 10,908 | | | 4,627 | |
これらの取引は,関連先と合意した価格や条項に基づいて行われる.
(Iv)共有サービス:
南京遺伝子生物科学技術有限会社は、2022年、2022年、2021年および2020年12月31日までの年間に、いくつかの会計、法律、情報科学技術および行政共有サービスを当社に提供し、代償は$とする1.6百万、$1.6百万ドルとドル3.3それぞれ100万ドルです
(v)サービス契約終了補償料:
| | | | | | | | | | | | | | | | | |
| 2022 | | 2021 | | 2020 |
| ドル‘000ドル | | ドル‘000ドル | | ドル‘000ドル |
| 江蘇金思達生物科技有限公司。 | — | | | 2,666 | | | — | |
2021年5月、当社と江蘇遺伝子生物科技有限公司が合意した和解合意に基づき、当社は実験室施設設計と建設に関するサービス協定を終了したため、賠償費用を発生させた。
(Vi)後続の公開発行から資金を集め,発行コストを差し引く
| | | | | | | | | | | | | | | | | |
| 2022 | | 2021 | | 2020 |
| ドル‘000ドル | | ドル‘000ドル | | ドル‘000ドル |
| キングスレー生物技術は | — | | | 84,600 | | | — | |
購入したGenScrip4,500,000普通株は,米国預託証券の形で2021年12月20日に後続公開の一部として発行され,価格は公衆に発行された普通株と同じである(付記26)。
(Vii)賃貸契約担保
2018年、アイルランド伝奇はダブリンの第三者とコピー物件賃貸契約を締結し、レンタル期間は2018年から2028年8月まで。GenScripは、レンタル契約下でのアイルランドのレノボ娯楽の支払い義務に保証されており、いかなる価格も提供していない。
(b)関連先との不明残高:
年末までの会社とその関連先の残高は以下の通り
(i)関係者が支払うべき金
| | | | | | | | | | | |
| 十二月三十一日
2022 | | 十二月三十一日
2021 |
| ドル‘000ドル | | ドル‘000ドル |
| 売掛金 | | | |
| 南京益生生物科学技術有限公司。 | 90 | | | 409 | |
| | | | | | | | | | | |
| 十二月三十一日
2022 | | 十二月三十一日
2021 |
| ドル‘000ドル | | ドル‘000ドル |
| その他売掛金 | | | |
| 南京金思達生物科学技術有限公司。 | 321 | | | 243 | |
| GenScripアメリカ社は | 16 | | | 19 | |
| 江蘇根思特生物科技有限公司 | 3 | | | — | |
| 合計する | 340 | | | 262 | |
| | | | | | | | | | | |
| 十二月三十一日
2022 | | 十二月三十一日
2021 |
| ドル‘000ドル | | ドル‘000ドル |
| 繰り上げ返済する | | | |
| 南京益生生物科学技術有限公司。 | 251 | | | 274 | |
| 江蘇基恩思特ProBio生物技術有限公司 | 21 | | | 925 | |
| 合計する | 272 | | | 1,199 | |
(Ii)関係者の都合で。
| | | | | | | | | | | |
| 十二月三十一日
2022 | | 十二月三十一日
2021 |
| ドル‘000ドル | | ドル‘000ドル |
| 貿易応払い | | | |
| 南京金思達生物科学技術有限公司。 | 935 | | | 2,301 | |
| GenScripアメリカ社は | 134 | | | 46 | |
| 江蘇金思特生物科技有限公司 | 93 | | | 1 | |
| 南京益生生物科学技術有限公司。 | 21 | | | 22 | |
| 合計する | 1,183 | | | 2,370 | |
| | | | | | | | | | | |
| 十二月三十一日
2022 | | 十二月三十一日
2021 |
| ドル‘000ドル | | ドル‘000ドル |
| その他の支払い | | | |
| 南京金思達生物科学技術有限公司。 | 2,435 | | | 3,293 | |
| GenScripアメリカ社です。 | 58 | | | 50 | |
| 江蘇根思特生物科技有限公司 | 7 | | | — | |
| 江蘇金スキットProBio生物技術有限公司 | 4 | | | — | |
| 南京益生生物科学技術有限公司 | 3 | | | — | |
| GenScripオランダ | 1 | | | — | |
| 合計する | 2,508 | | | 3,343 | |
| | | | | | | | | | | |
| 十二月三十一日
2022 | | 十二月三十一日
2021 |
| ドル‘000ドル | | ドル‘000ドル |
| 賃貸負債 | | | |
| GenScrip USAホールディングスInc | 427 | | | — | |
| 南京金思達生物科学技術有限公司。 | 205 | | | 286 | |
| 合計する | 632 | | | 286 | |
借入金金利は賃貸負債を除いて増加している5.14%和7.94返済すべき割合が超過する5年内に、他のすべての関連側残高は担保がなく、必要に応じて返済し、利息を免除する。
(Iii)会社の重要な管理職の報酬:
| | | | | | | | | | | | | | | | | |
| 2022 | | 2021 | | 2020 |
| ドル‘000ドル | | ドル‘000ドル | | ドル‘000ドル |
| 持分決算持分報酬費 | 3,582 | | | 2,907 | | | 529 | |
| 短期従業員福祉 | 2,170 | | | 1,942 | | | 1,733 | |
| 解雇料 | — | | | — | | | 774 | |
| 合計する | 5,752 | | | 4,849 | | | 3,036 | |
33. カテゴリー別の金融商品
各報告期間終了時の金融商品ごとの帳簿金額は以下のとおりである
2022年12月31日まで
金融資産
| | | | | | | | |
| 金融資産価格は
原価を償却する | 金融資産価格は
利益や損失で価値を実現する |
| ドル‘000ドル | ドル‘000ドル |
| 売掛金 | 90 | | — | |
| 前払金、その他の入金、その他の資産に含まれる金融資産(付記17) | 43,029 | | — | |
| 公正価値に応じて損益により計量された金融資産 | — | | 185,603 | |
| 定期預金 | 54,016 | | — | |
| 質入れ預金 | 1,270 | | — | |
| 現金と現金等価物 | 786,031 | | — | |
| 合計する | 884,436 | | 185,603 | |
金融負債
| | | | | | | | | | | |
| 財務負債
償却後のコストで計算する | | 金融
負債を公平に承諾する
価値がある |
| ドル‘000ドル | | ドル‘000ドル |
| 貿易応払い | 32,893 | | | — | |
| 株式証法的責任 | — | | | 67,000 | |
| その他売掛金及び売掛金項目に掲げる金融負債(付記21) | 10,960 | | | — | |
| 協力利息前払い資金 | 260,932 | | | — | |
| 賃貸負債 | 23,602 | | | — | |
| 合計する | 328,387 | | | 67,000 | |
2021年12月31日まで
金融資産
| | | | | |
| 金融資産
償却後のコストで計算する |
| ドル‘000ドル |
| 売掛金 | 50,410 | |
| 前払金、その他の入金、その他の資産に含まれる金融資産(付記17) | 1,067 | |
償却コストで計算された金融資産
| 29,937 | |
| 賃借金を受け取る | 94 | |
| 定期預金 | 168,225 | |
| 質入れ預金 | 1,444 | |
| 現金と現金等価物 | 688,938 | |
| 合計する | 940,115 | |
金融負債
| | | | | | | | | | | |
| 財務負債
償却後のコストで計算する | | 金融
負債を公平に承諾する
価値がある |
| ドル‘000ドル | | ドル‘000ドル |
| 貿易応払い | 7,043 | | | — | |
| 株式証法的責任 | — | | | 87,900 | |
| その他売掛金及び売掛金項目に掲げる金融負債(付記21) | 16,867 | | | — | |
| 協力利息前払い資金 | 120,462 | | | — | |
| 賃貸負債 | 2,504 | | | — | |
| 合計する | 146,876 | | | 87,900 | |
34. 金融商品の公正価値と公正価値レベル
管理層は、現金および現金等価物、質抵当預金、定期預金、前払いに含まれる金融資産、その他の売掛金およびその他の資産、その他の売掛金、貿易売掛金および金融負債の公正価値は、主にこれらのツールの短期満期日によってその帳簿に近いと評価した。
当社の財務マネージャーをはじめとする財務部は、金融商品の価値計量を公正に決定する政策とプログラムを担当しています。財務部は財務マネージャーに直接仕事を報告します。各報告日において、財務部門は、金融商品価値の変動を分析し、推定値への適用の主な投入を決定する。財務マネージャーは推定値を検討して承認した。年間財務報告を行うために、推定過程と結果を年に1回取締役と検討する。
金融資産および負債の公正価値は、強制販売または清算販売ではなく、意思のある当事者間の現在の取引で交換可能な金額でこのツールによって計上される。
以下の表は、同社の金融商品の公正価値計量レベルを説明した
公正な価値で計量された資産:
| | | | | | | | | | | | | | | | | | | | | | | |
| 2022年12月31日まで | | | | | | | |
| 公正価値計量使用 | | |
| 引用する
値段
活動状態にある
市場
(レベル1) | | 意味が重大である
観察できるのは
入力
(レベル2) | | 意味が重大である
見えない
入力
(レベル3) | | 合計する |
| ドル‘000ドル | | ドル‘000ドル | | ドル‘000ドル | | ドル‘000ドル |
| 公正価値に基づいて損益する金融資産 | 185,603 | | | — | | | — | | | 185,603 | |
公正な価値で計量された金融資産は通貨市場基金を含む
公正な価値で計量された負債:
| | | | | | | | | | | | | | | | | | | | | | | |
| 2022年12月31日まで | | | | | | | |
| 公正価値計量使用 | | |
| 引用する
値段
活動状態にある
市場
(レベル1) | | 意味が重大である
観察できるのは
入力
(レベル2) | | 意味が重大である
見えない
入力
(レベル3) | | 合計する |
| ドル‘000ドル | | ドル‘000ドル | | ドル‘000ドル | | ドル‘000ドル |
| 株式証法的責任 | — | | | 67,000 | | | — | | | 67,000 | |
以下の表に、権証負債公正価値推定のための二項モデルの投入を示す
| | | | | |
| 2022年12月31日 |
| 対象株式価格 | $24.96 | |
| 波動率 | 62.3 | % |
| 無リスク金利 | 3.8% - 4.7% |
| 配当をする | 0 | % |
| | | | | | | | | | | | | | | | | | | | | | | |
| 2021年12月31日まで | | | | | | | |
| 公正価値計量使用 | | |
| 引用する
値段
活動状態にある
市場
(レベル1) | | 意味が重大である
観察できるのは
入力
(レベル2) | | 意味が重大である
見えない
入力
(レベル3) | | 合計する |
| ドル‘000ドル | | ドル‘000ドル | | ドル‘000ドル | | ドル‘000ドル |
| 株式証法的責任 | — | | | 87,900 | | | — | | | 87,900 | |
以下の表に、権証負債公正価値推定のための二項モデルの投入を示す
| | | | | |
| 2021年12月31日 |
| 対象株式価格 | $23.31 | |
| 波動率 | 70.5 | % |
| 無リスク金利 | 0.58 | % |
| 配当をする | 0 | % |
2022年、2022年、2021年及び2020年12月31日までの年度まで、第1級と第2級の間に公正な価値計量移転がなく、金融資産及び金融負債が第3級の間で移転或いは転出することもない。
35. 金融リスク管理目標と政策
同社の主要な金融商品には、現金および現金等価物、質抵当預金、定期預金、償却コストに応じて計量された金融資産、前払い、他の売掛金およびその他の資産、および他の売掛金および売掛金項目に含まれる金融負債が含まれる。これらの金融商品の主な目的は会社の運営のための資金調達だ。同社には、貿易売掛金や貿易売掛金など、様々な他の金融資産や負債があり、これらの資産や負債は直接その業務から来ている。
当社の金融商品が発生する主なリスクは、金利リスク、外貨リスク、信用リスク、流動性リスクである。取締役会は、これらのリスクを管理する政策を検討し、同意し、これらの政策を以下のように概説する。
金利リスク
2022年12月31日、当社の金利変動リスクは、主に当社が総合財務諸表付記25に開示した低利クッション金と関係がある。2022年12月31日、経営陣は金利のいかなる合理的な変動も前借り資金の利息支出に大きな影響を与えないと考えている。したがって、金利リスクに対する敏感な分析は行われなかった。
外貨リスク
その会社には取引通貨のリスクがある。このようなリスクは,経営単位が単位機能通貨以外の通貨で販売または購入することに由来する。大ざっぱに0.32022年(2021年と2020年:54%和ゼロ)当社の売上高は、売却を行う経営実体の本位貨幣以外の貨幣で価格化されている。
2022年、2022年、2021年および2020年12月31日までに、会社は違います。未返済外貨長期外貨契約。現在、会社はその外貨変動のリスクの開放を求めるつもりはない。しかし、経営陣は経済情勢や会社の外国為替リスク状況を監視し、今後必要なときに適切なヘッジ措置を考慮する。
次の表は、報告期間末に、他のすべての変数が不変のままである場合、会社の税引前損失(通貨資産と負債の公正価値の変化による)のユーロ(“ユーロ”)と人民元対ドルレートが合理的に変化する可能性があることに対する敏感性を示している。
| | | | | | | | | | | |
| 増加/
(減少)
この速度は
外国.海外
貨幣 | | 減少/
(増加)
赤字状態にある
税引き前 |
| % | | ドル‘000ドル |
| 2022年12月31日までの年度 | | | |
| 米ドルを人民元に両替すれば強いです | 5 | | | 1,314 | |
| もし米ドルが人民元に弱くなったら | (5) | | | (1,314) | |
| ドルがユーロに両替したら強いです | 5 | | | (1,441) | |
| もしドルがユーロに両替したら弱いです | (5) | | | 1,441 | |
| 2021年12月31日までの年度 | | | |
| 米ドルを人民元に両替すれば強いです | 5 | | | 1,215 | |
| もし米ドルが人民元に弱くなったら | (5) | | | (1,215) | |
| ドルがユーロに両替したら強いです | 5 | | | (3,086) | |
| もしドルがユーロに両替したら弱いです | (5) | | | 3,086 | |
| 2020年12月31日までの年度 | | | |
| 米ドルを人民元に両替すれば強いです | 5 | | | 678 | |
| もし米ドルが人民元に弱くなったら | (5) | | | (678) | |
| ドルがユーロに両替したら強いです | 5 | | | (817) | |
| もしドルがユーロに両替したら弱いです | (5) | | | 817 | |
信用リスク
同社は公認と信用の良い第三者とのみ取引している。同社の政策は、信用条件で取引を希望するすべての顧客が信用検証プログラムを受けることだ。また、売掛金残高は継続的にモニタリングされており、会社の不良債権リスクは大きくない。関連業務実体ではない本位貨幣建ての取引については、信用制御主管の具体的な承認なしに、当社は信用条項を提供しません。
当社の他の金融資産の信用リスクは、現金及び現金等価物、質抵当預金、余剰コストで計量された金融資産及びその他の売掛金を含み、取引相手の違約により発生し、最大リスクは当該等のツールの帳簿金額に等しい。当社の売掛金及びその他の売掛金による信用リスクのさらなる定量化に関するデータは、それぞれ総合財務諸表付記16及び17に開示されている。
同社は公認と信用の良い第三者とのみ取引を行うため、担保を必要としない。信用リスクの集中は債務者が管理する。当社は売掛金について何らかの集中的な信用リスクが存在し、これらのリスクは総合財務諸表付記16に開示されている。
流動性リスク
同社は経常的流動性計画ツールを使用してその資金不足のリスクを監視している。このツールは、その金融投資および金融資産(例えば、売掛金や他の金融資産)の満期日および予想される業務キャッシュフローを考慮する。
本報告で述べた期間が終了した場合、契約未割引支払いに基づいて計算される会社の財務負債の満了状況は以下のとおりである
| | | | | | | | | | | | | | | | | |
| 2022年12月31日まで | | | | | |
| 1以下
年.年 | | 1を超える
年.年 | | 合計する |
| ドル‘000ドル | | ドル‘000ドル | | ドル‘000ドル |
| 貿易応払い | 32,893 | | | — | | | 32,893 | |
| その他の支払及び課税項目 | 10,960 | | | — | | | 10,960 | |
| 株式証法的責任 | 67,000 | | | — | | | 67,000 | |
| 協力利息前払い資金 | — | | | 260,932 | | | 260,932 | |
| 賃貸負債 | 3,966 | | | 23,193 | | | 27,159 | |
| 合計する | 114,819 | | | 284,125 | | | 398,944 | |
| | | | | | | | | | | | | | | | | |
| 2021年12月31日まで | | | | | |
| 最初の月より低い
年.年 | | 1を超える
年.年 | | 合計する |
| ドル‘000ドル | | ドル‘000ドル | | ドル‘000ドル |
| 貿易応払い | 7,043 | | | — | | | 7,043 | |
| その他の支払及び課税項目 | 16,867 | | | — | | | 16,867 | |
| 株式証法的責任 | 87,900 | | | — | | | 87,900 | |
| 協力利息前払い資金 | — | | | 120,462 | | | 120,462 | |
| 賃貸負債 | 911 | | | 1,708 | | | 2,619 | |
| 合計する | 112,721 | | | 122,170 | | | 234,891 | |
注:許可と協力協定の条項により、協力者は、協力計画の最初の利益年度の会社税前利益シェアから前金総額とその利息を回収することができますそしてヤンソン協定に基づいて当社に支払うべきマイルストーン支払いですが、いくつかの制限を受けなければなりませんそれは.会社の経営陣は、協力者は1年以内に融資を回収できないと予想している。
資本管理
会社資本管理の主な目標は、会社が持続的な経営企業としての持続的な経営能力を保障し、その業務を支援し、株主価値を最大化するために良好な信用格付けと健康な資本比率を維持することである。
当社はその資本構造を管理し、経済状況の変化と標的資産のリスク特徴に基づいて調整している。資本構造を維持または調整するために、会社は株主に配当金を支払い、株主に資本を返却したり、新株を発行したりするように調整することができる。当社はいかなる外部から課せられた資本要求にも制約されません。本報告書で説明されている間、資本管理の目標、政策、または手続きは何の変化もない。
同社はレバレッジ率を用いて資本をモニタリングし、レバレッジ率は総負債を総資産で割ったものだ。毎年年末の負債比率は以下の通り
| | | | | | | | | | | |
| 十二月三十一日
2022 | | 十二月三十一日
2021 |
| ドル‘000ドル | | ドル‘000ドル |
| 総負債 | 586,651 | | | 353,521 | |
| 総資産 | 1,330,963 | | | 1,119,465 | |
| 伝動比 | 44 | % | | 32 | % |
36. 連結財務諸表を承認する
連結財務諸表は2023年3月28日に取締役会の許可を得て発表された.
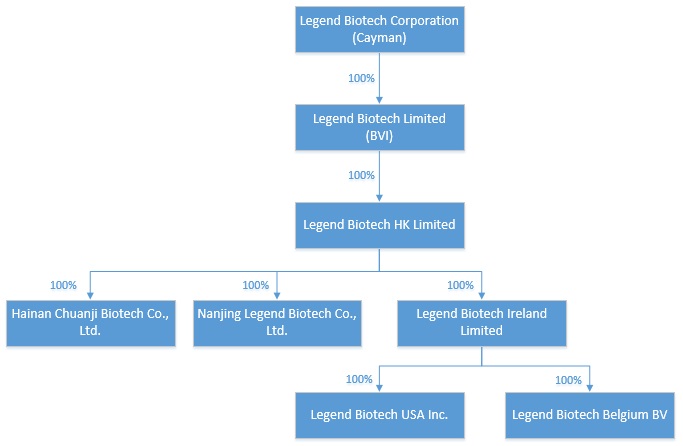












 *第64回米国血液学会(ASH)年次総会で発表;2022年12月10日から13日まで、米ロサンゼルスニューオーリンズ
*第64回米国血液学会(ASH)年次総会で発表;2022年12月10日から13日まで、米ロサンゼルスニューオーリンズ