アメリカ アメリカ
証券取引委員会
ワシントンD.C.,20549
表
あるいは…。
あるいは…。
あるいは…。
手数料ファイル番号
(登録者がその定款に明記されている氏名)
は適用されない
(登録者名を英語に翻訳)
(会社の司法管轄権
(主に実行オフィスアドレス )
電話:
+
電子メール:
(会社の連絡先名、電話、メールアドレス、住所)
この法第12条(B)に基づいて登録又は登録される証券:
| クラスごとのタイトル | 取引 個の記号 |
登録された各取引所の名称 | ||
| トロント証券取引所 |
同法第12条(G)に基づいて登録又は登録される証券:なし
ACT第15条(D)条により報告義務を有する証券 :なし
年次報告に係る期間終了までの発行者の各種資本または普通株の流通株数 :2022年12月31日までの普通株式。
は、登録者が証券法ルール405で定義されている経験豊富な発行者であるか否かをチェックマークで表す。はい。☐
この報告が年次報告または移行報告である場合、登録者が1934年の証券取引法第
13または15(D)節に従って報告を提出する必要がないかどうかを決定するためにマークをチェックしてください。はい。☐
再選択マークは、登録者が、(1)過去12ヶ月以内(または登録者がそのような報告の提出を要求された短い期間内)に、1934年の証券取引法第13または15(D)節に提出されたすべての報告書を提出したかどうか、および(2)
が過去90日以内にそのような提出要件に適合しているかどうかを示す
再選択マークは、登録者が過去12ヶ月以内に(または登録者がそのような文書の提出および発行を要求されたより短い時間以内に)ルールS−T(本章232.405節)405条に従って提出および発行を要求する各相互作用データファイルを電子的に提出したかどうかを示す
登録者が大型加速ファイルサーバ,加速ファイルサーバ,非加速ファイルサーバであるか新興成長型会社であるかをチェックマークで示す.取引法第12 b-2条の規則における“加速申請者”、“大型加速申請者”、“新興成長型会社”の定義を参照されたい。(1つを選択):
大型
加速ファイルサーバ加速ファイルサーバ☐
もし 一家が米国公認会計原則に基づいて財務諸表を作成する新興成長型会社であれば、登録者 が延長された過渡期間を使用しないことを選択したかどうかをチェック番号で表す場合、取引法第13(A)節に提供される任意の新しいまたは改正された財務会計基準 を遵守する
新しいまたは改訂された財務会計基準とは、財務会計基準委員会が2012年4月5日以降に発表されたその会計基準の編纂の任意の更新を意味する。
登録者が報告書を提出したか否かを再選択マークで示し、その経営陣が“サバンズ-オキシリー法案”(“米国法典”第15編7262(B)節)第404(B)条に基づいてその財務報告の内部統制の有効性を評価したことを証明する
証券が当該法第12(B)条に基づいて登録されている場合は、届出書類に含まれる登録者の財務諸表が以前に発表された財務諸表の誤り訂正を反映しているか否かをチェックマークで示してください
これらのエラーのより真ん中に再記述があるかどうかをチェックマークで示すことは、登録者の任意の幹部が関連する回復中に受信したインセンティブベースの報酬を§240.10 D−1(B)に従って回復分析する必要があるかどうかを示す
登録者が本文書に含まれる財務諸表を作成する際にどのような会計基盤を使用しているかをチェックマークで示す
アメリカ☐
国際会計基準委員会☒
前の質問に回答する際に“その他”をチェックした場合は、登録者がどの財務諸表項目に従うかを選択することをチェックマークで示してください。プロジェクト17プロジェクト18☐
これが年次報告である場合は、登録者が空殻会社であるか否かをチェックマークで示してください(“取引所規則”第12 b-2条で述べたように)。はい。☐
デモベース
一般情報
本文がまた言及されている以外に、本年度報告20-F表のすべての“会社”、“Aeterna Zentaris”、“Aeterna”、“We”、“Our”または類似語またはフレーズに言及されている言葉は、いずれもAeterna Zentaris Inc.およびその子会社を指す。本Form 20-F年次報告では,“$”と“U.S.$”への引用とは米国(“U.S.”)を指す.ドル、“カナダ元”はカナダ元、“ユーロ”と“ユーロ”はユーロ、“GB”はポンドを意味する。別の説明がない限り、本年度報告の20−Fテーブルに含まれるすべての情報は、2022年12月31日から提供される。
本“Form 20−F”年次報告書はまた、我々の製品および候補製品と競合する可能性のある製品または候補製品に関するいくつかの情報を含み、これらの情報は、主に、このような潜在的競争製品および候補製品を開発するbr社によって開示されており、Aeterna Zentarisによって独立して検証されていない。
前向き陳述に関する特別説明
本“Form 20-F年次報告”と本文で引用した文書は、“1995年の米国個人証券訴訟改革法”の安全港条項に基づいて作成された“前向きな陳述”を含み、現在の未来の事件に対する私たちの期待を反映している。歴史的事実の陳述を除いて、本20-F表年次報告 中の“重要な情報-リスク要因”のタイトル下のすべての陳述は前向き陳述であり、 これらの陳述は、年度情報テーブルではなく、カナダ関連証券監督機関に提出されるものであり、米国証券取引委員会(“米国証券取引委員会”)に提出されるものでもなく、これらの陳述 は、私たちが予想し、信じているか、または予想するか、または将来発生する可能性のある活動、事件、または発展に関連する。私たちの前向きな陳述は、会社の将来展望と予想される事件または結果と関係がある可能性があり、会社の財務状況、業務戦略、成長戦略、予算、運営、財務結果、税収、配当、計画、目標に関する陳述を含むことができる。具体的には、会社の未来の業績、将来性或いは機会に関する陳述はすべて前向きな陳述である。場合によっては、前向き表現は、“計画”、“予想”または“予期しない”、“予算”、“計画”、“推定”、“予測”、“意図”、“予想”、“予期しない”または“信じている”、またはそのような言葉およびフレーズの変形またはいくつかの行動、イベントまたは結果“可能”、“可能”、“将”、“可能”、“可能”を述べるような前向き用語を使用することによって識別することができる“Will”または“Will Be Take”、“発生”または“Be Be Good”またはこれらの語または他の類似した意味の語や用語の否定。
本文に含まれる経営、財務状況或いはキャッシュフローの予想結果に関するいくつかの展望性陳述は財務展望を構成する可能性がある。このような陳述は,将来の事件の仮定に基づいており,本報告日の経済状況,提案された行動案および経営陣の既存関連資料の評価に基づいている。当社の経営陣は、本公告日までの財務展望を承認しました。本稿に含まれるこのような財務展望情報 は、本稿開示以外の他の目的で使用されてはならないことに注意されたい。
展望性(Br)陳述は、本年度報告日までの会社の意見と推定に基づいており、それらは既知と未知のリスク、不確定性、仮説およびその他の要素の影響を受け、これらの要素は実際の結果、活動レベル、業績または 成果を招く可能性があり、このような前向き陳述の明示または暗示の内容とは大きく異なるが、これらに限定されないリスク要因“およびアンド:DETECT試験に対するアイトナーの期待(DETECT試験における被験者の登録、Macimorelin成長ホルモン刺激試験の適用、およびDETECT試験の完了を含む);Aeternaは、NMOSDおよびパーキンソン病の治療を決定および特徴化するための臨床前研究を行うAIM生物製剤に基づく開発候補の期待、および選択された候補のための製造プロセスの開発に対する期待;関連するパーキンソン病モデルにおける評価に対するAeternaの期待;クイーンズランド大学ではその後の研究者が開始した臨床試験を行い,MacimorelinはALS治療の潜在療法であることを評価し,Aeternaは臨床前開発計画を策定している;Aeternaは本格的な臨床前開発AEZS−150を開始し,可能なIND申告に備えてAEZS−150の初のヒト臨床研究を行い,Novo NorDisk Healthcare AGのライセンスプロトコルに関連する影響を終了した。
| 2 |
展望性 陳述は、既知および未知のリスクおよび不確定要素、ならびに本明細書に記載された実際の結果、業績または成果と展望性 情報の明示または暗示をもたらす可能性のある他の未来の結果、業績または達成とは大きく異なる要素を含む。このようなリスクと不確実性には、欧州連合とアメリカの小児科臨床試験の成功に対するMacrilen(Macimorelin)の依存、DETECT試験の開始が延期される可能性がある、または規制部門の許可を得ることができない可能性があり、DETECT試験で予想される数の被験者を登録できない可能性があり、DETECT試験の結果がCGHDにおける規制承認を支持しない可能性がある。クイーンズランド大学で行われているまたは計画中のMacimorelin臨床前研究または私たちが開発している他の製品の結果は成功しないかもしれないし、人体臨床試験への推進を支持していない可能性があります;私たちは現在計画されている運営を継続するために資金と資金を獲得しています;私たちは現在計画されている運営を継続する能力に大きく依存しています;私たちは現在Macrilen(Macimorelin)と関連する外部許可手配および資金と資源を獲得し続けて製品を商業化することに成功しています;私たちはノバノルド株式会社との許可協定の終了後に新しい許可協定または同様の手配を締結する能力に大きく依存しています。新冠肺炎の世界的流行による世界的な不安定と私たちの計画中の業務に対する潜在的な影響;私たちは他の製薬会社と外部許可、開発、製造、マーケティング、流通協定を締結し、これらの協定を発効させる能力;および私たちの普通株をナスダック資本市場(“ナスダック”)やトロント証券取引所(“トロント証券取引所”)に上場させる能力を継続している。
これらの リスク要因は、会社のリスク要因に影響を与える可能性のある完全なリストを表すものではない。しかし、このような要素と仮定は慎重に考慮されなければならない。これらおよび他の要因に関するより詳細な情報は、本年度報告の20−Fテーブルおよび参照によって本明細書に組み込まれた他の文書における“リスク要因”の項目に含まれる。
しかし、私たちは、私たちが米国証券取引委員会に提出または提供するForm 6-K報告書と、SEDARウェブサイトwww.sedar.comで提出された他の公開開示で関連テーマについて行われた任意のさらなる開示を確認することをお勧めします。
会社は実際の結果と展望性陳述に含まれる結果が大きく異なる重要な要素を招く可能性があることを確定しようとしているが、他の要素による結果は予想、推定或いは予想の結果と大きく異なる可能性がある。その中の多くの要素は私たちの統制範囲を超えている。このような陳述が正確であることが証明されることは保証されない。実際の結果と未来の事件はこのような陳述の中で予想されているものと大きく異なる可能性があり、特に持続的かつ持続的に発展する新冠肺炎疫病及び世界経済への影響及び会社の業務に対する不確定な影響を考慮するためである。したがって、読者は前向きな陳述に過度に依存してはいけない。適用される証券法の要求を除いて、会社は本文に含まれるいかなる前向き陳述も更新することを承諾しない。新しい要素が時々出現し、会社はすべてのこれらの要素を予測できない、あるいは各要素が会社の業務に与える影響を事前に評価して、あるいは任意の要素或いは要素の組み合わせは実際の結果が任意の前向き陳述に含まれる結果と大きく異なる程度 を招く可能性がある。
| 3 |
カタログ表
一般情報
| ページ 責任 | |||
| 第1部 | |||
| 第 項1. | 役員·上級管理職·コンサルタントの身分 | ||
| A.役員と上級管理職 | 6 | ||
| B.コンサルタント | 6 | ||
| C.核数師 | 6 | ||
| 第 項2. | 割引統計データと予想スケジュール | ||
| A.見積統計 | 6 | ||
| B.方法と予想スケジュール | 6 | ||
| 第 項3. | 重要な情報 | ||
| A. [保留されている] | 6 | ||
| B.資本化と負債 | 6 | ||
| C.報酬を提案し使用する理由 | 6 | ||
| D.リスク要因 | 6 | ||
| 第 項. | 会社についての情報 | ||
| A.会社の歴史と発展 | 29 | ||
| B.業務概要 | 30 | ||
| C.組織構造 | 44 | ||
| D.財産と装置 | 44 | ||
| 項目 4 A. | 未解決従業員意見 | 45 | |
| 第 項5. | 経営と財務回顧と展望 | ||
| A.経営実績 | 45 | ||
| B.流動資金、キャッシュフロー、および資本資源 | 51 | ||
| C.研究開発、特許、ライセンスなど。 | 54 | ||
| D.トレンド情報 | 54 | ||
| E.キー会計推定数 | 55 | ||
| 第 項6. | 役員、上級管理者、従業員 | ||
| A.役員と上級管理職 | 56 | ||
| B.補償 | 59 | ||
| C.取締役会の慣例 | 74 | ||
| D.従業員 | 76 | ||
| E.株式所有権 | 76 | ||
| 第 項7. | 大株主と関係者が取引する | ||
| A.主要株主 | 76 | ||
| B.関連者取引 | 77 | ||
| C.専門家と弁護士の利益 | 77 | ||
| 第 項8. | 財務情報 | ||
| A.連結レポートおよびその他の財務情報 | 77 | ||
| B.重大な変化 | 77 | ||
| 第 項9. | 見積もりと看板 | ||
| A.特典と発売詳細 | 77 | ||
| B.分配計画 | 78 | ||
| C.市場 | 78 | ||
| D.売却株主 | 78 | ||
| E.希釈 | 78 | ||
| F.債券発行費用 | 78 | ||
| 4 |
| 第 項10. | 情報を付加する | ||
| A.株 | 78 | ||
| B.組織覚書と規約 | 78 | ||
| C.材料契約 | 89 | ||
| D.外国為替規制 | 94 | ||
| E.課税 | 94 | ||
| F.配当金と支払代理人 | 101 | ||
| G.専門家の発言 | 101 | ||
| H.展示された書類 | 102 | ||
| 一、付属情報 | 102 | ||
| 第 項11. | 市場リスクの定量的·定性的開示について | 102 | |
| 第 項12. | 株式証券を除くその他の証券説明 | ||
| A.債務証券 | 103 | ||
| B.株式承認証及び権利 | 103 | ||
| C.その他の証券 | 103 | ||
| D.アメリカ預託株式 | 103 | ||
| 第II部 | |||
| 第 項13. | 違約、延滞配当金、延滞配当金 | 104 | |
| 第 項14. | 保証所有者の権利と収益使用の実質的な改正 | 104 | |
| 第 項15. | 制御とプログラム | 104 | |
| 第 項16 A。 | 監査委員会財務専門家 | 105 | |
| 16 B項目. | 道徳的規則 | 106 | |
| 第 項16 C. | チーフ会計士費用とサービス | 106 | |
| 第 項16 D. | 監査委員会の上場基準の免除 | 107 | |
| 16 E項目. | 発行者および関連購入者が株式証券を購入する | 107 | |
| 16 F項目. | 登録者の認証会計士を変更する | 107 | |
| 第 項16 G. | 会社の管理 | 107 | |
| 16 H項目. | 炭鉱安全情報開示 | 107 | |
| 第 項16 i | 検査妨害に関する外国司法管区の開示 | 107 | |
| 第三部 | |||
| 第 項17. | 財務諸表 | 107 | |
| 第 項18. | 財務諸表 | 107 | |
| 第 項19. | 陳列品 | 156 | |
| 5 |
第 部分I
| 第 項1 | 役員·上級管理職·コンサルタントの身分 |
| A. | 役員brと上級管理職 |
は適用されない.
| B. | 顧問.顧問 |
は適用されない.
| C. | 監査役 |
は適用されない.
| 第 項2 | 割引統計データと予想スケジュール |
| A. | 見積 統計データ |
は適用されない.
| B. | 方法 と予想スケジュール |
は適用されない.
| 第 項3 | 鍵 情報 |
| A. | (保留) |
| B. | 資本化と負債 |
は適用されない.
| C. | 報酬の提供と使用の原因 |
は適用されない.
| D. | リスク要因 |
私たちの証券に投資することは高いリスクと関連がある。投資決定を下す前に、以下に述べるリスクと、本年度報告に含まれる他のすべての情報をよく考慮しなければなりません。実際に以下のいずれかのリスク が発生した場合、我々の業務、見通し、財務状況、または経営結果は、これらのリスクのいずれかの重大な悪影響を受ける可能性がある。私たちは今知らないか、あるいは私たちが現在どうでもいいと思う他のリスクもまた私たちの業務運営を損なう可能性がある。上記のいずれかのリスクにより、私たち証券の取引価格は下落する可能性があり、あなたは投資の全部または一部を損失する可能性があります。本年度報告書 にはリスクと不確実性に関する前向きな陳述も含まれている。いくつかの要因により、以下に言及するリスクを含むため、私たちの実際の結果は、これらの前向き陳述で予想される結果と大きく異なる可能性がある。本年度報告に含まれる前向き 陳述は,我々が本年度報告発表の日に得た情報に基づいており,引用統合された文書中のすべての前向き陳述 は,このような文書の発行日ごとに得られた情報に基づいている.私たちは、証券規制要件が適用されない限り、新しい情報、未来のイベント、または他の理由で、このような前向きな陳述を更新または変更する義務がないことを否定します。
| 6 |
私たちの業務に関するリスク
リスクファクターの概要
以下に我々の業務が直面しているリスク要因の概要を示す.次のリストは詳細ではなく、投資家はこの“リスク要因”の部分を完全に読むべきだ。私たちが直面しているリスクは
| ● | 私たちの普通株がナスダックあるいはトロント証券取引所から撤退することはその市場価格と流動性に影響を与える可能性があります |
| ● | 私たちbrは受動的な外国投資会社かもしれません。これは不利な税金結果を招くかもしれません |
| ● | アメリカ税法によると、私たちの純営業損失は限られているかもしれません |
| ● | 私たちの権利計画は会社の統制権の変更を阻止するかもしれない |
| ● | Br新冠肺炎の経済効果は私たちの普通株の市場価格に影響する可能性がある |
| ● | バイオ製薬会社への投資は一般的に投機的とされている |
| ● | 商業化されていないか、またはMacrilen(Macimorelin)許可を得られていないことに関するリスク |
| ● | 私たちの収入と支出は大きく変動している可能性があり、財政的期待に達していないかもしれない |
| ● | Macrilen(Macimorelin)小児科適応の臨床試験計画が完成しなかったことは,我々の運営に影響を及ぼす可能性がある |
| ● | Macrilen戦略第三者関係に依存しています |
| ● | 私たち はMacrilen(Macimorelin)のさらなる外部許可手配に成功できないかもしれない |
| ● | 私たちは重要な早期臨床前計画を開始しました |
| ● | 私たちは大量の追加融資が必要かもしれないし、私たちは十分な資本を得ることができないかもしれない |
| ● | 私たちは今も将来も政府の私たちの製品に対する持続的な規制を受けるだろう |
| ● | 上場 Macrilen(Macimorelin)の承認は制限または撤回される可能性がある |
| ● | 医療改革は製品のビジネス成功を阻害し、私たちの業務に影響を与える可能性がある |
| ● | もし私たちが医療詐欺や法律乱用の方法で医療従事者と交流すれば、私たちは民事または刑事罰を受ける可能性がある |
| ● | Macrilen(Macimorelin)が市場に認められなければ、私たち は相当な収入を生み出すことができないかもしれない |
| ● | 私たち は特定の製品や適応を追求するために限られた資源を使うかもしれませんが、より成功する可能性のある他の製品や適応を利用することはできません |
| ● | 私たちは私たちが発表し、予想された時間範囲で私たちの予想された発展目標を達成できないかもしれない |
| ● | もし私たちがMacrilenのために受け入れ可能な価格や十分な精算を得ることができなければ、私たちの収益能力は弱まるだろう |
| ● | 我々の目標市場の競争は激しく、他社の開発はMacrilen (マカロニ)や私たちの未来のいかなる製品も競争力を失う可能性がある |
| ● | 私たち は私たちの知的財産権 によってMacrilen(Macimorelin)のために十分な保護を受けることができないかもしれない |
| ● | 私たちは他人の知的財産権を侵害するかもしれない |
| ● | 特許訴訟は高価で時間がかかり、私たちに責任を負わせるかもしれない |
| ● | 私たちは現在または未来の製品のために商標登録を得ることができないかもしれない |
| 7 |
| ● | 私たちは第三者に依存して臨床試験を監督していますこれらの第三者は満足できないかもしれません |
| ● | 臨床試験中のいかなる困難または遅延は、私たちのコスト増加、br遅延、あるいは私たちの収益能力を制限し、私たちのビジネスの将来性に不利な影響を与える可能性がある |
| ● | FDAと他の外国の同業者は米国以外からの臨床試験のデータを受け入れない可能性があり,この場合,我々の開発計画が延期され,我々の業務に実質的な被害を与える可能性がある |
| ● | 業務を展開する際には、安定して一致した原料供給と原材料に依存している |
| ● | 製品の生産と供給に依存する第三者が満足に実行できないことは、供給不足を招く可能性があると予想される |
| ● | 私たちは技能人材に対する激しい競争に直面しており、肝心な人員の流失や多くの人員を引き付けることができないことは私たちがbr運営を展開する能力を弱める可能性がある |
| ● | 私たちは未来に訴訟を受けるかもしれない |
| ● | 私たち は製品責任クレームのリスクに直面して、私たちは十分な保険カバー範囲がないかもしれません |
| ● | 私たちの子会社債権者の債権は一般に私たちおよび私たち債権者と株主の債権より優先されています |
| ● | 私たちのカナダの会社とドイツの存在により、アメリカの投資家は私たちに不利な判決を得て実行することが難しいかもしれない |
| ● | 私たちは私たちが将来いつでも私たちが財務報告書の内部統制に有効であることを報告できるという保証はない |
| ● | 私たちは財務報告の内部統制に重大な欠陥があるかもしれません。これは私たちの普通株の価格に重大な悪影響を及ぼすかもしれません |
| ● | 私たちのbrは環境法によって制約され、環境救済義務の制約を受ける可能性があります。 これらの義務の影響は私たちの業務に実質的な悪影響を及ぼす可能性があります |
| ● | 私たちは外貨変動によって損失を受ける可能性があります |
| ● | 立法行動、新しい会計声明、より高い保険料は、私たちの将来の財務状況や経営業績に悪影響を及ぼす可能性があります |
| ● | データbrのセキュリティホールは私たちの運営を混乱させ、私たちの運営結果に悪影響を及ぼす可能性があります |
| ● | 私たちの株価は大きく変動していますこれは私たちがコントロールできない要素かもしれません |
| ● | 私たちは近い将来に配当するつもりはない |
| ● | 将来の証券発行とヘッジ活動は私たちの普通株の取引価格を下げるかもしれません |
| ● | ある財政年度の6月30日に海外個人発行者の資格を失ったら、1934年の証券取引法の国内報告制度の遵守を要求され、追加の法律、会計、その他の費用が生じる可能性があります |
| ● | 当社の定款には“空白小切手”の優先株条項が含まれており、わが社への買収を延期または阻害する可能性があります |
| ● | 維権株主の行動は私たちの業務に否定的な影響を及ぼすかもしれない。 |
| 8 |
私たちの普通株はナスダックあるいはトロント証券取引所から撤退するかもしれません。これはその市場価格と流動性に影響を与えるかもしれません。もし私たちの普通株がbrによって整理されたら、投資家は彼らの普通株を処理することが難しいかもしれない。
私たちのbrの普通株は現在ナスダックとトロント証券取引所で発売されており、コードは“AEZS”です。私たちは持続的な上場要求を満たして、私たちの普通株がナスダックとトロント証券取引所で上場することを維持しなければならない。上場継続のため、ナスダックは上場証券が1株1ドル以上の最低終値を維持することを要求した。
2021年7月28日、吾らはナスダック上場資格審査員(“本スタッフ”)から手紙を受け取り、当社に手紙日前の最後の30営業日に、当社の普通株の終値が1株1.00ドルを下回ったことを通知したため、吾らはナスダック上場規則第5550(A)(2) (“購入価格ルール”)に規定されている引き続きナスダック上場の要求に適合しなかった。ナスダック上場規則第5810(C)(3)(A)条によると、2022年1月24日まで180暦の猶予期間を得たが、2022年1月26日には、入札価格規則を遵守していることを証明するために、180暦の延長を許可された。入札価格ルールを再遵守するために、当社は2022年7月21日から逆株式分割(株式合併とも呼ばれる)を実施し、合併前普通株25株当たり1株合併後普通株 を基礎としている。最低購入価格要求に加えて、ナスダックの持続上場規則 は、(I)株主資本が少なくとも250万ドル、 (Ii)上場証券の時価(我々の証券の1日当たりの終値に私たちの未償還証券総数brを乗じた)が少なくとも3500万ドルであるか、または(Iii)継続的に運営される純収益(直近の財政年度または過去3財政年度のうちの2つの財政年度)のうち少なくとも50万ドルを満たすことを要求する。
私たちは受動的な外国投資会社かもしれませんが、これはアメリカの投資家に不利な税金結果をもたらすかもしれません。
不利な米国連邦所得税規定は,受動外国投資会社(“PFIC”)株を直接または間接的に保有する“米国保有者”に適用される。米国連邦所得税の場合、(I) の総収入の少なくとも75%が“受動的収入”である場合、または(Ii)私たちの資産平均価値の少なくとも50%が、営業権 (年間四半期平均値に基づく)を含む場合、受動的収入を生成する資産または受動的な収入を生成するために保有する資産に起因することができる場合、PFICに分類される。
私たちが課税年度であるかどうかを決定するPFICは、複雑な米国連邦所得税ルールの適用にある程度依存し、これらのルールは異なる解釈を受ける可能性がある。このことは疑いの余地はないが,2022納税年度ではPFIC ではなく,2023納税年度でもPFICになる可能性は低いと信じている。PFICの地位は我々の納税年度全体の収入,資産,活動および我々の時価に基づいているため,納税年度が終了するまで2023納税年度にPFICと同定されるかどうかは特定できない。PFICの地位を確定するテスト は多くの不確定要素の影響を受ける。これらのテストは年に1回行われており,将来の収入,資産 とその決定に関する活動を正確に予測することは困難である.また,我々普通株の市場価格が変動する可能性があるため, 市場価格はPFICとみなされるかどうかの決定に影響する可能性がある。どの納税年度(私たちの2023納税年度を含む)でもPFICとみなされない保証はありません。
米国保有者が普通株を保有するいかなる課税年度内にもPFICであれば,米国保有者がその普通株を保有している後続のすべての年度内に,PFIC身分の敷居要求を満たさなくても,米国保有者とみなされ続けるPFIC である。したがって、私たちは現在のbr(またはいかなる未来)の納税年度にPFICを構成しないことも保証できませんし、国税局(IRS)が私たちのPFICの地位について私たちのいかなる決定も疑問視しないことを保証することはできません。PFICの定性的は、アメリカの保有者に不利なアメリカ連邦所得税の結果をもたらす可能性がある。特に、いくつかの選挙がなければ、アメリカの保有者は通常、通常の所得税税率でアメリカ連邦所得税を納付し、可能な利息費用を加えて、私たちの普通株を処分する収益と、私たちのいくつかの分配を得る必要がある。いずれの課税年度にPFICとみなされれば,米国保有者は課税年度ごとに“時価ベース”の普通株を選択し,普通株価値の増加に基づいて一般収入を確認することができる。
また、米国の保有者は“適格選挙基金”(“QEF”)選挙を行うことでPFICルールの不利な税収結果を緩和することができるが、QEFに適用される記録保存要求を満たす保証はなく、QEF選挙を行うために米国所有者がQEF選挙を行うために必要な我々の収入に関する情報を提供する保証もない。
| 9 |
会社がPFICであれば、アメリカの保有者は通常アメリカ国税局に年次情報申告書を提出することを要求されます(IRS表8621で情報受動型外国投資会社または合格選挙基金の株主申告PFIC株主は、その普通株式所有権に関連する米国連邦所得税または情報申告書の提出を要求される。この届出要求 は、PFICにおける米国所有者の権益に適用される任意の予め存在する報告要求に対する補足である(この要求 は影響しない)。
米国国税法第382条によると、米国連邦所得税の目的で、我々の純営業損失は限られている可能性がある。
純営業損失(“NOL”)のある会社が改正された“1986年米国国税法”(“規則”)382節で指摘された“所有権変更”を経験した場合、同社はこのような“変更前”NOLを用いて所有権変更後に生じる収入を相殺することが制限される可能性がある。このような制限は、所有権変更の日までに“固有”されたいくつかの損失または減額(すなわち、所有権変更の前の期間に起因することができるが、税務目的に計上されていない)にも適用され、その後確認される。所有権変更は、一般に、(I)1つ以上の“5%株主”の所有権移転に関連する場合、または(Ii) “株式構造変化”に関連し、その結果、“テスト期間”(通常は試験日の3年前)において、1つ以上の5%株主が所有する会社株パーセンテージ(価値ベース)が、これらの 株主が所有する会社株の最低パーセンテージよりも50ポイント以上増加する。一般に,このような変化が生じると, 社がそのNOL繰り越しや何らかの他の税務属性を利用する能力は年次制限され, は以下のようになる.このようなNOL繰越や税務属性の未使用部分は毎年繰り越しているが、今後数年間同様の制限を受けている。所有権変更が州NOL繰り越しに与える影響は州によって異なる可能性がある。これまでの所有権変更,あるいは今回の発行過程または後に所有権変更が発生した場合,NOLを使用する能力は本規則382節の制限を受ける可能性がある.将来的に私たちの株式所有権の変更は、そのいくつかは私たちの制御範囲内ではなく、本規則第382条による所有権変更を招く可能性があります。最近の立法では,今後数年,特に2021年12月31日以降に開始される納税年度にNOLを控除する能力を要求するいくつかの制限が増加しており,課税収入の80%に相当する控除限度額とNOL繰越控除の制限が含まれている。このような理由で、私たちは利益を達成しても、NOLの大きな部分を使うことができないかもしれない。
会社の制御権変更に係る取引を防ぐ
2019年5月8日から、株主は当社の権利計画を再承認し、取締役会と会社株主に追加の 時間を提供して、会社への任意の能動的買収要約を評価し、株主価値の最大化 を実現するために、適切な場合に他の代替案を求める。配当計画によると、現在発行されている普通株を発行する毎に、1つの権利が発行され、時々発行される可能性のある各追加の普通株のために権利が発行される。配当計画は顕著な逆買収効果をもたらす可能性がある。割当計画は、我々の株を買収した人の所有権権益を大幅に希釈する可能性があるため、会社の支配権変更を延期、阻止、阻止する効果がある可能性がある。
大流行、流行病あるいは伝染病爆発の経済影響は私たちの運営あるいは私たちの普通株の市場価格に不利な影響を与える可能性がある。
公衆衛生危機、例えば大流行、流行病或いは類似の爆発は、“新冠肺炎”と呼ばれる新型コロナウイルス株を含み、 は私たちの運営或いは私たちの普通株の市場価格に不利な影響を与える可能性がある。新冠肺炎が私たちの運営に与える影響程度或いは私たちの普通株の市場価格は未来の発展に依存し、これらの発展は高度な不確定性があり、自信に満ちて予測できない、国際的にもアメリカ、カナダ或いはドイツ国内でも、疫病発生の持続時間、出現する可能性のある新冠肺炎の重症度に関する新しい情報、及びウイルスの制御或いはその影響を治療する行動などを含む。しかし、新冠肺炎はすでに により世界と各国の取引市場の大幅な変動を招いた。
| 10 |
新冠肺炎の伝播は、私たちの臨床試験活動と私たちのサプライチェーンを中断する可能性があることを含む、私たちの運営に影響を与える可能性があります。例えば、新冠肺炎の大流行におけるオミック変異体の増加は、小児期成長ホルモン欠乏症の診断のための第三段階の臨床試験のサイト起動と患者登録遅延を検出するために使用されています。また、米国の成人成長ホルモン欠乏症診断活動の遅延により、ノワノード社のMacrilenの米国での販売活動が影響を受ける可能性がある。また、隔離が患者の流動を阻害したり、医療サービスを中断したりすると、新冠肺炎の大流行により、一部の患者が私たちの試験に参加したくないことや臨床試験案を遵守できない可能性があり、臨床試験を行う能力や臨床試験結果を適時に発表する能力を遅らせることになり、規制部門の許可を得て候補製品を商業化する能力を遅らせる可能性がある。伝染病の伝播は、新冠肺炎を含み、私たちのサプライヤーが適時或いは根本的にコンポーネント或いは原材料を渡すことができない可能性もある。また、病院は人手を減らし、何らかの治療を減らしたり、延期したりして、伝染病の伝播に対応する可能性がある。このようなイベントは、一定期間の業務中断をもたらす可能性があり、運営を減少させる場合、医師または医療提供者は、私たちの臨床試験に参加したくない可能性があり、いずれも、私たちの業務、財務状態、または運営結果に大きな影響を与える可能性がある。アメリカ、カナダあるいはドイツでの新冠肺炎の著しい伝播は広範な健康危機を招き、各国経済、私たちがサービスする市場、私たちの業務及び私たちの普通株の市場価格に不利な影響を与えた。
バイオ製薬会社への投資は一般的に投機的とされている。
生物製薬業界の会社の将来性は不確定であり、この業界の性質がこの業界の会社はよく長い開発時間、広範な資本要求、迅速な技術発展と主に科学と技術要素に基づく高度な競争を経験したからである。これらの要因には、技術および製品が特許および他の保護を得る可能性、技術開発を商業化する能力、および政府の承認を得てテスト、製造、マーケティングを行う能力が含まれる。したがって、バイオ製薬会社への投資は投機的資産とみなされなければならない。
もし私たちがMacrilen(Macimorelin)を商業化したり許可を得たりすることに成功しなかったら、あるいは私たちがそうしている過程で大きな遅延があったら、私たちの業務は実質的な損害を受け、会社の未来と生存能力が脅かされるかもしれない。
私たちの主要製品Macrilen(Macimorelin)はアメリカ食品·薬物管理局と欧州委員会が許可した最初の経口テストであり、慢性萎縮性心臓病患者の診断に使用することができ、現在私たちは他の製品は何もありません。私たちはヨーロッパとアメリカの大学とのネットワークを日和見的に利用することに集中し、私たちはこれが異なる適応の革新開発候補に重要な機会を提供し、稀或いは孤立した適応と小児科応用の潜在力に重点を置くと信じている。我々はこれまでに,視神経脊髄炎スペクトル障害(NMOSD) とパーキンソン病(PD),原発性副甲状腺機能低下症と筋萎縮性側索硬化症(ALS)を含む複数の適応を含むこの増加するチャネルを確立するためにbr協定に署名した。
我々 は,米国,カナダ,欧州経済区,イギリス,韓国でMacrilen(マカロニ)の開発,製造,登録,商業化の許可協定を行う側である。私たちはイスラエルとパレスチナの権力機関、トルコ、いくつかの非EUバルカン諸国で商業化された流通協定の締約国であるMacrilen(マカロニ)である。私たちは世界的な範囲で許可と流通機会を探索し続けている。
上述したように、2022年8月26日、同社はMacrilenの米国とカナダでのすべての権利を再獲得することを発表し、これまで Novoは開発と商業化許可協定を終了し、270日間の通知期間をトリガした。当社は米国とカナダにおけるMacrilenのすべての選択を積極的に模索しているにもかかわらず、当社がMacrilenの米国とカナダでの権利について類似した合意や任意の合意に到達できる保証はありません。
Macrilenのビジネス成功は、以下の要因を含むが、これらに限定されないいくつかの要因に依存する
| ● | 外国の監督管理機関の許可を受けた | |
| ● | EUのキー市場でMacrilenの価格設定と補償について交渉することに成功した | |
| ● | 合格した第三者サプライヤーと契約を結び、Macrilen(Macimorelin)を生産することに成功した | |
| ● | 私たちの製品のための適切な流通とマーケティングインフラと手配を開発します |
| 11 |
| ● | Brを発売し、この製品の商業販売を増加させる | |
| ● | Macrilenを第三者に権限を与えること; | |
| ● | 医療界、患者、第三者支払者のこの製品に対する受容度。 |
もし私たちがこれらの要素のいずれかを達成できなければ、私たちの業務、財務状況、運営結果は実質的な影響を受ける可能性があります。
私たちの収入と支出は変動が大きい可能性があり、財務予想に達しなかった場合は、証券アナリストや投資家を失望させ、私たちの普通株や他の証券の価格や価値を低下させる可能性がある。
私たち は運営赤字の歴史があります。私たちの収入と支出は過去に変動し続け、未来は変動し続けるかもしれない。これらの 変動は私たちの普通株の株価や私たちの他の証券の価値を低下させる可能性がある。私たちの収入と支出の変動を引き起こす可能性のあるいくつかの要素は、以下の要素を含むが、これらに限定されない
| ● | 現在または未来の協力者投資がMacrilen(Macimorelin)を商業化するために必要な資源のタイミングと意欲; | |
| ● | 米国食品医薬品局(FDA)、欧州医薬品局(EMA)、欧州委員会(“EC”)や他の機関は、Macrilen(Macimorelin)の小児科適応を延期または阻止する可能性があり、これは私たちの普通株の株価に影響を与える可能性がある | |
| ● | 規制当局が提出して承認した時間 | |
| ● | ライセンス料収入の性質と時間 | |
| ● | 未来の訴訟の結果 | |
| ● | 海外通貨変動; | |
| ● | 最近の新冠肺炎発生の影響は、ウイルス伝播の影響を制御する努力を強化することを含み、これまでは他の以外に隔離と旅行制限が含まれていた | |
| ● | 合意に達した時間と、現在または未来の許可パートナーから受信されたマイルストーン支払い ;および | |
| ● | Macrilen(Macimorelin)を生産するサプライヤーと新しい合意を締結できなかったか、または既存のプロトコルが満了または終了しました。 |
我々の収入と支出の変動により,我々の運営結果を定期的に比較することは必ずしも我々の将来の業績を示すとは限らないと考えられる.今後のある時期には、私たちの収入と支出は証券アナリストや投資家の予想よりも高いか低いかもしれない。この場合、私たち普通株の株価と私たちの他の証券の価値は大幅に変動したり低下したりする可能性がある。
Macrilen(Macimorelin)の小児科臨床試験計画を成功させることができない場合,あるいはこのような臨床試験 の完了時間が予想よりも長くなれば,任意の関連業務戦略を実行する能力は悪影響を受けるであろう。
もし私たちがサイトとの契約を決定し、および/または小児科臨床試験計画中にMacrilen(マルクレリン)の登録を遅延させると、私たちの開発計画に追加のコストと遅延が生じ、経済的に効率的またはタイムリーな方法で私たちの臨床試験を完成させることができないかもしれない。また、多国籍研究を行うことは、米国やカナダ以外の国の事件に影響を受けるため、別のレベルの複雑さやリスクを増加させる。また,われわれが行った臨床試験の陰性や不確実な結果や不良医療事象は,臨床試験を繰り返しあるいは中止せざるを得ない可能性がある。また,子供の新陳代謝問題は成人とは異なる。したがって,可能な時間範囲で小児科臨床試験(あれば)を完成させることはできないかもしれない。われわれまたはわれわれの契約研究機関(“CRO”)が計画的に臨床試験を行うのに十分な数の患者を募集することが困難であれば,進行中の臨床試験を延期または終了する必要があるかもしれない。
| 12 |
臨床試験は政府の監督機関と機関審査委員会の持続的な監督を受けており、他の要求以外にも必要である
| ● | 複数の国および司法管轄区域からのこれらの機関およびその関連法規、法規およびガイドラインの要求を満たす | |
| ● | インフォームドコンセントの要求を満たす | |
| ● | 機関審査委員会の要求を満たす; | |
| ● | Brの良好な臨床実践の要求を満たす。 |
我々 は現在,第三者との何らかの戦略関係に依存してMacrilen (Macimorelin)を開発,製造,許可することに依存しており,将来的にMacrilen(Macimorelin)の開発,製造,許可について協力する可能性がある.
私たちと第三者との調整は私たちに期待された利益を提供できないかもしれないし、私たちを多くのリスクに直面させるかもしれない。
現在、私たちは様々なパートナーに依存してイギリス、EU、韓国でMacimorelinを商業化している。以上のように,ノルドとの許可プロトコルが終了した後, 社はMacrilenのすべての権利を再獲得する.私たちの潜在的収入の大部分は、マイルストーンとMacrilen(Macimorelin)販売の特許権使用料を含むか、支払いを含む。私たちがこの協力の下で得ることが可能な記念碑的および特許権使用料収入は、これらの側がMacrilen(マカロニ)の発売、マーケティング、販売に成功する能力に依存する。もし彼らが十分な時間と資源を投入して私たちと協力していなければ、私たちはこの手配の潜在的な商業利益を実現できないかもしれません。私たちの運営結果は実質的な悪影響を受ける可能性があります。
我々 のこれらの関係や他の潜在的第三者への依存は多くのリスクをもたらす.私たちはこのようなプロトコルの期待収益 を実現できないかもしれませんし、どちらか一方が私たちの収入を最大化するように義務を果たしているかどうかも決定できません。これらの合意は、いくつかの物質的権利を第三者に譲渡することを要求する可能性もあります。このような合意はいくつかの追加的な危険をもたらすだろう。以下の任意のイベントまたは他のイベントが発生すると、Macrilen(Macimorelin)の商業化が延期または損害される可能性があります:
| ● | 場合によっては、第三者は、我々の同意または承認を必要とすることなく、本プロトコルの下での権利および義務を他の第三者に譲渡することができる | |
| ● | 第三者は経済的な理由や他の理由で経営を停止する可能性がある | |
| ● | 私たちはこのようなプロトコルを更新できないかもしれません | |
| ● | 第三者がMacrilen(Macimorelin)の商業化に重要な意味を持つ可能性のある知的財産権を正確に維持または守ることができない可能性がある | |
| ● | 第三者は、利益衝突、業務戦略の変化、または他の 問題に遭遇する可能性があり、これらの問題は、彼らが私たちの義務を履行する意思または能力に悪影響を及ぼす可能性がある(例えば、製薬会社は従来、合併と統合後にその優先順位を再評価してきたが、この業界ではよく見られてきた) | |
| ● | 遅延または商業バッチ拡大が達成されていないか、または現在の原材料サプライヤーまたは製品製造業者の変更(私たちまたはサプライヤーまたは製造業者による変更にかかわらず)は、臨床研究を延期する可能性がある。Macrilen(Macimorelin)の規制提出と商業化そして | |
| ● | 私たちは第三者との間で紛争が発生する可能性があり、Macrilen(Macimorelin)の生産や商業化の遅延や中止を招き、訴訟や仲裁を招き、時間も高価になる可能性がある。私たちや私たちの株主の利益のためではなく、第三者が自分の利益のために行動することを招いたりする。 |
| 13 |
また,第三者は,我々が彼らと締結した各プロトコルの条項に基づいて,様々な理由で我々と彼らとの合意を終了することができる.1つまたは複数のプロトコルが終了した場合、私たちはMacrilen(Macimorelin)の製造および商業化のために追加のリソースを投入する必要があるだろう。
Macrilenの追加発行許可を達成できないかもしれませんTM(Macimorelin)割引条項とbr}の条件では、そうでなければ、私たちはそうすることを大幅に遅延させるかもしれません。
私たちの製品開発と商業化戦略の一部として、Macrilen(Macimorelin)の外部許可機会と、ノとノッド、Consilient Health、MegaPharm Ltd.,ER Kim PharmPharmticalsブルガリアEOODとNK MEDITECH Ltd.との既存のライセンス契約と商業化協定を評価しています。第三者とMacimorelinについて協力することを選択すれば、Macimorelinの協力スケジュールを優遇的な条項と条件で交渉することができないかもしれません。もし任意の パートナーがMacimorelinの商業化に成功しなかった場合、私たちの業務、財務状況、運営結果は不利な影響を受ける可能性がある。
私たちは重要な早期臨床前計画を開始しました
2021年の全過程で,潜在療法に関する4つの新たな臨床前開発プロジェクトの許可を得ており,これらすべての項目は,それらが重要な個別市場機会を代表する潜在力に基づいて我々の開発プロセスに追加されている。これらの臨床前開発計画は早期開発段階にあり,これらの潜在的な製品は規制部門の承認を得ておらず,どの国/地域でも商業使用や販売が可能であるため,製品販売は何の収入ももたらさない。私たちの任意の候補製品の開発を完了するためには、大量の追加投資が必要になるだろう。まず臨床前と臨床試験を完成して、それから私たちの潜在製品は私たちが確定した市場で使用することができます。私たちはどんな製品も開発できないかもしれないし、監督部門の承認を得ることができない、臨床試験に入ることができない、あるいはいかなる製品を商業化することができないかもしれない。私たちの潜在的な製品開発努力が、brが有効で、適用された規制基準に符合し、必要な監督管理の承認を得て、合理的なコストで生産でき、あるいは市場に受け入れられることを証明するかどうかはわかりません。私たちはまた、販売、許可料、または関連する印税が、製品の商業化過程で行われた任意の投資を回収することを許可しているかどうかを知らない。我々が現在開発している候補製品は少なくとも今後数年以内には商業的に可能ではないと予想され,候補製品を商業化する過程で予見できない困難や遅延に遭遇する可能性がある。しかも、私たちの潜在的な製品は効果がないかもしれないし、副作用につながる可能性がある。
私たちの候補製品は臨床結果が陽性の場合に規制部門の承認を得るために多くの資金が必要です。我々の候補製品にそのような資金を提供することは困難である可能性があり、または公開またはプライベート市場で、またはパートナー関係によって調達されることは不可能である。資金やパートナー関係 を得ることが容易でなければ,我々の候補製品の開発は著しく遅延したり完全に停止したりする可能性がある.開発の延期や停止を宣言することは私たちの株価に悪影響を及ぼすかもしれません。
私たち は多くの追加融資が必要かもしれないし、私たちは十分な資金を得ることができないかもしれない。
私たちの商業化努力を支援するために多くの追加資金が必要かもしれませんし、計画中のbr臨床試験と規制承認を行うために追加資金が必要かもしれません。私たちの手元にある既存の現金は、私たちが予想している今後12ヶ月の運営と資本支出需要を満たすのに十分であると信じていますが、近い将来運営から顕著な収入が発生しないと予想されています。しかも、私たちは現在約束された資金源を持っていない。
我々は、公的または個人融資、他の製薬会社との協力、または他のソースからより多くの資金を調達しようと試みることができるが、市場による証券の発行および発行に限定されない。私たちが受け入れられる条項 で追加資金を得ることができないかもしれない。もし私たちが合理的な条項で十分な資金を得ることができなければ、私たちは私たちの製品開発計画を延期、減少、またはキャンセルしたり、私たちが受け入れた条項より下で資金を得る必要があるかもしれない。追加資本が株式証券を売却することによって、または交換可能または行使可能な株式証券に変換することによって調達された場合、これらの証券を発行することは、我々の株主への希薄化をもたらす。さらに、債務融資または配当優先株の発行は、そのような債務の元本および利息を支払うために、またはそのような優先株の配当金を支払うために、私たちの将来の運営キャッシュフローの大部分(もしあれば)をもたらす可能性があり、私たちの運営および私たちが何らかの支出および/または追加債務を発生させる能力に制限を加える可能性があり、これは、競争圧力や景気後退の影響を受けやすいかもしれない。
| 14 |
私たちの未来の資本需要は巨大で、私たちの現在の予想を超えるかもしれません。これは多くの要素に依存しますが、以下の要素に限定されません
| ● | 未来の製品臨床試験の変更持続時間と結果 | |
| ● | 規制承認を求める上で意外な遅延や進展が見られた | |
| ● | 特許請求の範囲の準備、提出、起訴、維持および実行に要する時間およびコスト; | |
| ● | 私たちの業務発展と商業化戦略を実施する際に思わぬbr発展に遭遇した | |
| ● | 商品化された製品を潜在的に私たちの製品の組み合わせに追加します | |
| ● | 未来の訴訟の結果 | |
| ● | 協力者とさらなる 手配を行う(あれば). |
また、世界経済と市場状況、そして信用と資本市場の将来の発展は、私たちが将来的により多くの資金を調達することをより困難にするかもしれない。
私たちのbrは、規制部門から後者の許可を得ても、私たちの製品と候補製品に対する政府の厳しい規制を受け続けている。
Macrilen(Macimorelin)と私たちの候補製品の製造、マーケティング、販売は厳しく持続的な規制を受けており、Macrilen(Macimorelin)が食品·薬物管理局と欧州委員会の上場承認を得ても、厳格で持続的な規制を受けるだろう。このような規制を遵守することは高価であり、大量の財務と管理資源を消費するだろう。例えば,欧州共同体によるMacimorelinの承認は,我々が発売後の後続研究を行うことに同意し,その製品の安全性や有効性を監視することを条件としている.また,臨床試験期間よりも使用患者数が多く,範囲が広いため,承認後に使用される臨床経験が拡大するため,承認前の臨床試験期間中に観察されなかったり予想されたりする副作用や他の問題が生じる可能性がある。この場合、規制機関は、製品が販売される可能性のある適応を制限したり、製品の規制承認を撤回したりすることができる。
私たち と私たちの契約製造業者は、私たちの現在または未来の製品を生産する際に、適用される現行の良好な製造規範(GMP) 法規および他の法規を遵守することを要求されるだろう。これらの規定には、品質保証に関する要求と、厳格な記録と文書の相応の維持が含まれている。製造施設はbrの承認を経なければならず,製品の商業生産に利用し,規制機関のその後の定期検査を受けることができる。また、製造方法の材料変更や原材料サプライヤーの変更には、さらなる規制審査と承認が必要です。
もし私たちまたは任意の未来のマーケティング協力者または契約製造業者が適用された法規要件を遵守できなかった場合、罰金、製品のリコールまたは差し押さえ、および関連する宣伝要件、禁止、生産の全部または一部の一時停止、民事処罰、以前に付与された監督管理許可、警告または命名されていない手紙の一時停止または撤回、新製品または承認された補充剤の承認を拒否する保留上場申請、マーケティング申請の撤回、政府医療計画からの除外、輸出入禁止または制限、および/または刑事起訴および処罰を含む制裁を受ける可能性がある。これらの処罰のいずれも、製品の販売促進、マーケティング、または販売を延期または阻止する可能性がある。
| 15 |
Macrilenが市場の承認を得た場合でもTM(Macimorelin)、このような製品承認が制限されたり撤回されたりする可能性があります。 規制要求が変化する可能性があります。
2017年12月20日、FDAはAGHD患者 の診断に用いられるMacrilen(Macimorelin)の米国上場を許可し、2019年1月16日、欧州委員会はMacimorelinの欧州での発売を許可し、AGHDの診断に用いた。規制部門は一般的に特定の適応の製品を承認するだろう。限られた適応が承認されれば,この制限はその製品の潜在市場規模を縮小する.製品が承認されると、規制機関は持続的な審査と定期的な検査を行う。私たちの運営とやり方は、アメリカ政府と、私たちが業務や活動を展開している任意の他の国/地域の政府の規制と審査を受けています。その後、以前未知の問題または安全問題 および/または知らない場合または知らない場合に国内または海外の法律を遵守しないことが発見され、様々な不良結果を招く可能性があり、その中には、承認製品の承認または拒否、警告または無タイトル手紙、罰金、禁止、民事処罰、リコールまたは差し押さえ製品および関連宣伝要求、生産の完全または部分的な一時停止、輸入または輸出禁止または制限、政府がマーケティング申請の更新を拒否する、マーケティング申請の完全な撤回、刑事起訴および処罰が含まれている。以前に付与された規制承認を一時停止または撤回し、承認された製品を市場から撤回し、および/または政府医療計画から除外する。このような規制の強制執行は、承認された製品に直接的かつ負の影響を与える可能性があるが、新薬または承認された補充剤を承認する任意の未解決の上場申請に悪影響を及ぼす可能性もある。
私たちの業界は高度に規制されているため、規制機関は様々な理由で、許可者や協力者の業務やマーケティング活動に関連した法執行行動をとる可能性がある。
一定期間ごとに、新しい立法が採択されて法律となり、FDA、EU、その他の衛生当局が規制する製品の承認、製造、マーケティングの法定条項を著しく変える可能性がある。また、衛生機関は、私たちの業務に大きな影響を与える可能性がある方法で法規やガイドラインを改正または再解釈することが多い。さらなる立法改正が公布されるかどうか,あるいは法規,指導や解釈が変更されるかどうか,およびそのような変更の影響(あれば)は予測できない.
医療改革措置は、製品のビジネス成功を阻害または阻止し、私たちの業務に悪影響を及ぼす可能性がある。
製薬·バイオテクノロジー会社の業務見通しや財務状況は、政府や第三者支払者が医療コストをコントロールしたり低減したりする努力の影響を受けている。米国政府や他の政府は医療改革の推進と医療コストの低減に大きな興味を示している。政府が講じたいかなる改革措置も,米国や国際的なMacrilen(Macimorelin) や政府機関や他の第三者支払者が提供する精算金額を含む医療製品やサービスの価格設定に大きな圧力を与える可能性がある。もしMacrilen (Macimorelin)の精算が私たちの予想を大幅に下回ったら、私たちの収入見通しは実質的で不利な影響を受けるかもしれない。
米国および他の司法管轄地域では、米国または国際的な医療製品およびサービス定価、他の国/地域からの医薬品の再輸入(他の国/地域でより低い価格で販売される)、および政府機関または他の第三者支払者から得られる精算金額に関する提案など、医療システムを変更するための立法および規制の多くの提案が継続されることが予想される。また、薬品、特に特殊薬品の定価は米国議会が注目してきた話題であり、公聴会が行われ、米国の総裁を含む政界人が発言した話題でもある。また、米国では個別州でも薬品の価格決定の透明性を高めるための立法や法案が可決され、薬品の価格設定に影響を与える可能性がある。このような薬品価格の審査がMacrilen(Macimorelin)の未来の価格にどのように影響するかは保証されない。
| 16 |
♪the the the“患者保護と平価医療法案”と“2010年医療·教育負担能力調整法案”(総称して“ACA”と呼ぶ)は、私たちのような専門的なバイオ製薬会社を含む多くのヘルスケア会社に大きな影響を与えている。しかしながら、ACAのいくつかの態様は、行政、司法、および国会によって挑戦されているので、ACAの未来は不確定である。2021年6月、米国最高裁は、原告がACAを攻撃する資格がない最低基本保険条項が違憲であることを理由として、ACA実行時の被告の行為により被害を受けたことを証明しなかったため、ACAへの挑戦を却下した。他のこのような訴訟やバイデン政府の医療改革努力がACAやわれわれの業務にどのように影響するかは不明である。
追加では,2007年食品医薬品局改正法案FDAにより強い上場後権限を与え、上場後の研究と臨床試験の要求、新しいセキュリティ情報に基づくラベル変更及びFDA承認のリスク評価と緩和策を遵守する権限を含む。FDAがこの権限を行使することは、製品開発、臨床試験、および規制承認中の遅延またはコストの増加をもたらす可能性があり、これは、新たな承認後の規制要件の遵守に関連するコストを増加させ、承認された製品の販売または流通に対するFDAの潜在的制限を増加させる可能性がある。
もし私たちまたは私たちの許可者が医療詐欺または法律違反の方法で製品をマーケティングしたり、医療従事者と相互作用したりすれば、私たちまたは私たちの許可された人は、政府の医療保健計画への参加から除外されることを含む民事または刑事罰を受ける可能性がある。
製薬会社として、私たちは医療サービスを提供せず、Medicareから直接支払いを受けたり、Medicareに直接支払いを受けたりしないにもかかわらず、私たちの現在の製品のMedicaidまたは他の国または第三者支払人、アメリカ連邦と州医療保健法律法規、および詐欺や乱用に関連するいくつかのEU規制および政府機関は現在も将来も私たちの業務に適用される。私たちと私たちのライセンス所持者は、私たちがマーケティング参入を求めることができる国/地域と、アメリカ連邦政府と私たちが業務を展開している州に位置するEU規制機関や政府機関の医療詐欺や乱用規制を受けています。
私たちの許可された人の運営能力に影響を与えるか、または影響を与える可能性のある法律は、関係者および意図的な場合に、brの返品時に任意の医療項目またはサービスの購入、レンタルまたは注文を誘導または注文するため、またはMedicare、Medicaid、または他の連邦援助された医療計画に従って精算可能な任意の医療項目またはサービスの購入、レンタルまたは注文を手配することを禁止する連邦ヘルスケア計画のバックオフ法規を含む。本法規は薬品メーカーと処方者、購入者と処方管理人の間の手配に適用される。多くの法定例外と規制避風港保護のいくつかのよく見られる活動があるが、例外と避風港の範囲は非常に狭く、処方、購入或いは推薦を誘導するための報酬 に関連するやり方は例外或いは 避難港の資格を満たしていなければ、審査を受ける可能性がある。
連邦虚偽クレーム法は、虚偽クレームの提出を意図的に連邦政府に提出するか、または虚偽クレームを得るために意図的にまたは虚偽陳述を引き起こすことを禁止する。これらの法律によると、製薬会社は様々な疑いのある販売促進やマーケティング活動で起訴され、例えば顧客に製品を無料で提供し、顧客が製品のために連邦計画の請求書を発行し、価格設定サービスに上昇した平均卸売価格 を報告し、連邦計画によって販売率を設定し、ラベル外販売促進活動に参加し、非保証のためのラベル外用途のためにMedicaidにクレームを提出し、Medicaid薬品返却計画に誇張された最適価格情報を提出することが予想される。
1996年“健康保険移行性と責任法案”医療保健事項に関する医療詐欺や虚偽陳述も禁止されている。医療詐欺法規は、個人支払者を含む任意の医療福祉計画を詐欺する計画を故意に実行することを禁止する。上述した直ちに言及された虚偽陳述法規は、医療福祉、プロジェクトまたはサービスの交付または支払いに関連する重大な事実を故意に偽造、隠蔽または隠蔽すること、または任意の重大な虚偽、架空、または詐欺的陳述を行うことを禁止する。
また,最近では連邦や州政府が医師に支払う費用の規制を強化する傾向が見られている。ACAは2010年に“医師支払い陽光法案”を可決し、薬品、機器、生物製品および医療用品のメーカーに新しい要求を提出し、薬品、器械、生物製品および医療用品のメーカーに医療保険、医療補助または児童健康保険計画(いくつかの例外を除く)で支払い、毎年医療保険と医療補助サービスセンター(CMS)に医師(医師、歯科、検眼師、足科医師および脊医を含むと定義される)や教育病院への支払いまたは他の“価値移転”に関する情報を報告することを要求した。 および適用されるメーカーと共同購入組織は、毎年CMSに 医師(上述した)およびその直系親族が持っている所有権と投資権益、およびこのような医師 所有者およびその直系親族に支払われたお金または他の“価値移転”を報告する。メーカーは毎年90日目の日 の前に政府にこれらのデータを報告するように要求されている。
| 17 |
ほとんどの州でも、これらの連邦法律に類似した法規や法規があり、医療補助や他の州計画に基づいて精算するプロジェクトやサービスに適用され、あるいは、いくつかの州では、支払者が誰であろうと適用される。また、いくつかの州には全面的なコンプライアンス計画を採用することが法的に要求されている。例えば,カリフォルニア州の法律によると,製薬会社は2003年4月の総監察長室の製薬メーカーに対するコンプライアンス計画ガイドラインや改訂された“PhRMAとヘルスケア専門家との相互作用指針”を遵守しなければならない。いくつかの州はまた、私たちが医師および他の医療提供者に支払うプレゼント、補償、br、および他の報酬を追跡して報告することを要求する。
コンプライアンス計画は,これらの法律違反による調査·起訴のリスクを低減することができるが,これらのリスクを完全に解消することはできない。私たちまたは私たちのライセンシーがこれらの法律に違反する行為は、たとえ私たちが弁護に成功しても、私たちが巨額の法的費用を発生させ、名声を損なうことを招き、私たちの経営陣の業務運営に対する注意をそらす可能性があります。また、EU政府や規制機関、適用される米国連邦と州の法律を実現し、維持するコストが高くなる可能性がある。
これらの法律の広さと安全港の狭さのため、私たちのいくつかの商業活動は1つまたは複数のこのような法律の挑戦を受けるかもしれない。ACAはまた、連邦反リベート法規、虚偽クレーム法律と医療詐欺法規に対していくつかの重要な改正を行い、反リベートと医療詐欺法規中の意図要求を弱化させ、政府或いは通報者がこのような詐欺と乱用違反行為を告発しやすくする可能性がある。個人や実体は本法規を実際に理解したり、この法規に違反する具体的な意図を持っている必要はなくなった。また、“反リベート法”の規定は、虚偽クレーム法規について、政府は連邦反リベート法規違反による物品或いはサービスを含むクレームが虚偽或いは詐欺的クレームを構成することを主張することができる。さらに、ACAは詐欺と乱用違反に対する処罰を増加させる。もし私たちの過去、現在、または将来の業務が上記の任意の法律または私たちに拘束された他の同様の政府法規に違反していることが発見された場合、私たちは重大な民事、刑事と行政処罰、損害賠償、罰金、監禁、brを政府が援助する医療計画(例えばMedicareおよびMedicaid)から除外され、私たちの業務の縮小または再編を受ける可能性があり、これらはいずれも私たちの業務運営能力に悪影響を与え、私たちの財務業績に悪影響を及ぼす可能性がある。
もしMacrilen(Macimorelin)が市場の承認を得られなければ、私たちは相当な収入を得ることができないかもしれない。
市場がMacrilen(Macimorelin)を受け入れるかどうかは、以下の要因を含むが、これらに限定されない多くの要因に依存する
| ● | 臨床効果と安全性を示しています | |
| ● | どんな副作用の流行率や重症度も | |
| ● | 製品の承認されたラベルに含まれる制限または警告; | |
| ● | 我々の目標に対する適応の代替治療またはテストの有用性 ; | |
| ● | 現在または代替治療および試験と比較して、Macrilen(Macimorelin)の利点および欠点; | |
| ● | 関連マニュアルにおけるMacrilenTM(Macimorelin)の分類および記述; | |
| ● | 許容可能な価格および適切な第三者補償を提供すること; | |
| ● | Macrilen(Macimorelin)のマーケティングと流通方法の有効性。 |
もしMacrilen(Macimorelin)が医師、患者、医療支払者、医学界の他の人の市場の承認を得なければ、彼らはMacrilen(Macimorelin)を受け入れたり使用しないかもしれないが、私たちがMacrilen(Macimorelin)から大量の収入を得る能力は制限され、私たちの財務状況は実質的な悪影響を受ける可能性がある。また、私たちがコア市場と既存の地理市場をさらに浸透させたり、私たちの業務を新しい市場に拡張することに成功したりすれば、Macrilen(Macimorelin)の販売増加と私たちの経営業績は否定的な影響を受ける可能性がある。
| 18 |
私たちのコア市場と私たちが競争している既存の地理市場をさらに浸透させることができますか、あるいは私たちの業務をヨーロッパ、アジア、あるいは他の国の他の国に拡張することに成功して、多くの要素の影響を受けて、その多くの要素は私たちがコントロールできません。Macrilen (Macimorelin)は商業化に成功すれば、現在主要な製薬会社と他のバイオテクノロジー会社によって販売されているいくつかの薬物、療法、製品とテストと競争する可能性がある。Macrilen(Macimorelin)は、他社が現在開発している新製品やMacrilen(Macimorelin)よりも安い製品と競争する可能性もある。コア市場と既存の地理市場で市場浸透率を増加させる私たちの努力が必ず成功する保証はありません。私たちのbrができなかったことは、私たちの経営業績に悪影響を与え、私たちの普通株の株価を下落させる可能性があります。
我々 は限られた資源をかけて特定の製品や適応を追求する可能性があり,他のより成功する可能性のある製品や適応を利用することはできない.
私たち は現在、Macrilen(Macimorelin)の特定の適応と私たちの4つの臨床前計画に集中しています。 したがって、私たちはMacrilen(Macimorelin)の他の潜在的な適応を探す機会を放棄または延期する可能性があり、これはより大きな成功の可能性があるか、またはより大きなビジネス潜在力を持っていることが証明される可能性があります。Macrilen(マルクレリン)のために新たな候補品を探したり,代替適応を探す研究プロジェクトには大量の技術,財力,人的資源が必要である。これらの活動を継続すると,最初は潜在的な候補品や適応を識別する上で希望を示す可能性があるが,br}はさらなる臨床開発のための候補品や適応は生じない。
私たち は私たちが発表して予想された時間範囲で私たちの予想された開発目標を達成できないかもしれない。
我々 は、目標を設定し、 臨床試験の開始、登録および予想完了、予想される規制提出および承認日、および製品発表の時間 のような、私たちの成功に重要な目標を達成する時間について公開声明を行うことができる。任意の臨床試験の遅延或いは失敗、規制審査過程に固有の不確実性、及び私たちの任意の製品或いは候補製品を商業化するのに十分な製造或いはマーケティング手配を実現する上での遅延などの要素により、これらの活動の実際の時間は大きく異なる可能性がある。私たちが計画的に規制申請を提出したり、規制承認を得ることは保証されないし、Macrilen(Macimorelin) や私たちの未来の任意の候補製品の発売スケジュールに従うことができる保証もない。もし私たちがこのようなマイルストーンのうちの1つ以上を計画的に達成できなければ、私たちの普通株の株価は下落するかもしれない。
もし私たちがMacrilen(Macimorelin)のために受け入れ可能な価格や十分な精算を得ることができなければ、私たちの収益能力は弱化されるだろう。
私たちまたは私たちのライセンシーがMacrilen(Macimorelin)を商業化することに成功した能力は、私たちまたは彼らの受け入れ可能な価格を得る能力に大きく依存し、患者が第三者支払者(例えば、政府や個人保険計画)から補償を受ける可能性に大きく依存する。これらの第三者支払人はよく会社に価格に基づいて所定の割引を提供することを要求し、彼らは薬品と他の医療製品の価格に挑戦するようになってきている。Macrilen(Macimorelin) は費用効果があると考えられない可能性があり、患者は私たちまたは私たちの許可者 を競争に基づいて私たちの製品を販売することができないか、または十分ではないかもしれない。Macrilen(Macimorelin)の特典精算料率を協議できない可能性があります。 不利な定価や精算条件は、第三者によるMacrilen (Macimorelin)の使用を誘導する能力を弱める可能性もあります。
| 19 |
さらに、第三者支払者が様々な方法で医療コストを制御または低減する持続的な努力は、私たちのビジネス機会を制限し、任意の関連収入および利益を減少させる可能性がある。私たちは、政府統制のような提案を実施することが継続されると予想する。医薬品、特に特殊薬品の定価は、公聴会が行われた米議会が注目してきた話題であり、米国総裁を含む政界人が講演した話題でもある。具体的には、米国議会が最近何度か調査を行い、薬品定価の透明性の向上、価格決定とメーカー患者計画との関係の審査、政府が薬品精算方法を改革するための法案を提出した。また,米国では州レベルの薬品定価改革が行われており,製薬会社のマーケティングや薬品販売の方式や価格に影響を与える。また,第三者支払者はその安全性と有効性を疑問視するほか,価格,医療の必要性の検査,医療薬品や医療サービスのコスト効果の審査に挑戦することが増えている。このような薬品定価の審査がどのように製品或いは孤児薬品或いは薬品の未来の定価に影響を与えるかを保証することはできない。さらに、管理医療の日々の重視は、医薬品および生物製薬製品の価格設定に圧力をかけ続けるであろう。コスト制御計画は、私たちまたは任意の既存または潜在的なパートナーが製品の価格を受け取ることができ、br}が私たちの収益性に悪影響を及ぼす可能性がある。さらに、米国、カナダ、および他の多くの国/地域では、処方薬およびバイオ医薬品の一部または全部の価格設定および/または収益性が政府によって規制されている。
もし私たちまたは私たちの許可者がMacrilen(Macimorelin)の受け入れ可能な価格や十分な精算レベルを得ることができなければ、Macrilen(Macimorelin)の販売は不利な影響を受けるだろうし、Macrilen(Macimorelin)は商業的に実行可能な市場がないかもしれない。
我々の目標市場の競争は激しく、他社の開発はMacrilen(Macimorelin)や私たちの未来の任意の製品 を競争力を失う可能性がある。
生物製薬分野では競争が激しい。この業界の他社が開発した新製品は、Macrilen (Macimorelin)や私たちの将来のどの製品も競争力を失ったり、競争力を著しく低下させたりする可能性があります。競争相手はMacrilen(Macimorelin)や私たちの未来の任意の製品と競争するために製品や技術を開発してテストしている。これらの競合製品のいくつかは、Macrilen(マカロニ) または私たちの将来の任意の製品と比較して、または予期される効果を達成するために完全に異なる方法または方法を有する可能性がある。時間の経過とともに,製薬やバイオ製薬会社および学術研究機関からの競争が激化していくことが予想される。私たちの多くの競争相手と潜在的な競争相手は私たちよりも強力な製品開発能力と財務、科学、マーケティング、人材を持っています。
私たち は私たちの知的財産権を通じてMacrilen(Macimorelin)のために十分な保護を受けることができないかもしれない。
私たちはMacrilen(Macimorelin)を開発して製造する際に私たちの独自の情報に大きく依存している。私たちの成功は、特許、商業秘密、商標、その他の知的財産権を通じて私たちの競争的地位を保護する能力に大きく依存しています。私たちはすでに多くの国と地域で特許と商標出願を提出し、出願しています。未解決の特許出願は特許の発行を招くことはない可能性があり、Macrilen(Macimorelin)に関連する追加発行の特許を得ることができない可能性がある。
一部の国の法律は知的財産権の保護の程度はアメリカとカナダの法律に及ばない。多くの会社は外国の管轄区域でこのような権利を保護し、守る際に重大な問題に直面している。多くの国では,ヨーロッパを含むある国では,強制許可法があり,これらの法律により,特許権者は第三者に許可を強制的に付与される可能性がある。また、多くの国は政府機関や政府請負業者に対する特許の実行可能性を制限している。これらの国/地域では,特許所有者の救済措置が限られている可能性があり,特許の価値を大幅に低下させる可能性がある.また,特定の国の法制度,特にある発展途上国の法制度は,特許や他の知的財産権保護を積極的に実行することに賛成せず,侵害行為を阻止·防止することが困難になっている。
私たちの特許は挑戦、縮小、失効、強制執行または回避される可能性があり、これは競争相手の類似製品の販売を阻止する能力を制限したり、Macrilen(マルクレリン)に対する私たちの特許保護期間を制限したりするかもしれない。米国や他の国/地域特許法や特許法解釈の変化 は,我々の知的財産権の価値を低下させたり,Macrilen(Macimorelin)に対する我々の特許保護範囲を縮小したりする可能性がある.私たちに発行または発行されるMacrilen(Macimorelin)特許は、私たちにどんな競争優位性も提供してくれないかもしれませんし、似たような技術を持つ競争相手から私たちを保護してくれないかもしれません。また、製品が私たちと非常に似ている第三者は、代替設計やプロセスによって私たちの特許を回避するかもしれません。私たちは使用方法、製造方法、および/または新しい処方に依存して、私たちが開発している化合物および任意の最終製品を保護しなければならないかもしれません。これらの製品は、主張する化合物と同じ保護を提供しないかもしれませんそれ自体が.
| 20 |
さらに、私たちの特許は特許訴訟で第三者の挑戦を受ける可能性があり、これは生物製薬業界でますます一般的になっている。私たちが知らないいくつかの既存技術は、特許請求の範囲の有効性または実行可能性に影響を及ぼす可能性があるかもしれない。我々が知っているかもしれないが,クレームの有効性や実行可能性に影響を与えるとは考えられない既存技術があるが,最終的には がクレームの有効性や実行可能性に影響を与える可能性があることが分かった。我々の特許が挑戦されたときに裁判所によって有効または強制執行可能であると判断される保証はなく,競争相手の技術や製品が裁判所に我々の特許を侵害していると認定される保証はない.私たちが付与した特許はまた、米国の許可後の手続きおよび米国以外のいくつかの国/地域の反対または無効な手続きで挑戦され、撤回される可能性があります。また、私たちは特定の特許の一部の期限の放棄を要求される可能性があります。これらの訴訟のbrはコストが高いかもしれませんが、私たちの努力は成功しないかもしれません。それによって、アメリカでの特許地位が損なわれる可能性があります。
私たちはまた私たちの知的財産権を保護するために商業秘密とノウハウに依存している。もし私たちが私たちの独自の情報とノウハウの機密性を保護できなければ、私たちの技術と製品の価値は悪影響を受けるかもしれない。私たちは、従業員、コンサルタント、外部科学協力者、および賛助されたbr研究者に、他のコンサルタントと秘密保護協定を締結することを要求することによって、私たちの非特許固有の情報を保護しようとしています。これらの合意は、個人と私たちとの関係の過程で開発または個人に開示されるすべての機密情報は、特定の場合を除いて第三者に開示されてはならないことを規定している。私たちの職員たちの場合、合意は、個人が雇用されている間に構想されたすべての技術が私たちの固有財産であることを規定している。許可されていないか、または私たちの固有の情報を開示する場合、これらの合意は、意味のある保護または十分な救済措置を提供できない可能性がある。さらに、第三者は、私たちと実質的に類似した独自の情報および技術を独立して開発したり、他の方法で私たちのビジネス秘密を取得したりすることも可能である。私たちが独自の情報やノウハウの機密性を保護できなければ、競争相手 は、これらの情報を利用して私たちの製品や技術と競争する製品を開発する可能性があり、これは私たちの業務に悪影響を及ぼす可能性があります。
第三者と締結されたライセンス契約により,我々 は現在何らかの特許や技術を使用する権利がある.私たちが1つまたは複数の許可プロトコルを遵守できなかった要求は、このような合意の終了を招く可能性があり、これは、関連する開発計画を終了させ、その計画または特定の市場での私たちの投資を完全に損失させる可能性がある。いくつかの許可内特許でbrと主張される発明は、米国政府の援助の下で行われる可能性があり、米国政府の権利によって制約される可能性があり、そのような許可内の技術を採用する候補製品 の商業化または製造を求める場合、追加の要件を満たす必要がある可能性がある。
このような要素のため、私たちは私たちの知的財産権に依存して市場でMacrilen(Macimorelin)を保護することができないかもしれない。
私たち は他人の知的財産権を侵害するかもしれない。
私たちのビジネス成功は、第三者特許や他の知的財産権を侵害することなく運営する能力に大きく依存しています。私たちが私たちの製品や方法が侵害を発見される可能性があることを知らない特許が存在するかもしれない、あるいは私たちが侵害していないが最終的に侵害が発見される可能性があることを知って信じている特許が存在するかもしれない。さらに、特許出願 およびその基本的な発見は、特許が発行されるまで、場合によっては秘密にされている。特許の発行には数年かかる可能性があるので、私たちが知らない現在承認されている出願が存在する可能性があり、これらの出願は、私たちの製品または技術が発行された特許 を侵害していることを発見する可能性がある。さらに、まだ公表されていない申請には、現在、私たちの製品または技術に関するクレームは含まれていないかもしれませんが、今後起草されたクレームの支援を提供しており、発行されれば、私たちの製品または技術の侵害が発見される可能性があります。
もし私たちが第三者の知的財産権を侵害したり告発されたりすれば、私たちの業務に悪影響を及ぼすだろう。第三者 は、これらの特許または特許出願を米国および海外で所有または制御することができる。これらの第三者は私たちまたは私たちの協力者にクレームをつけるかもしれません。これは私たちに巨額の費用を発生させ、勝訴すれば、巨額の損害賠償金を支払うことになるかもしれません。さらに、私たちまたは私たちの協力者に特許侵害訴訟を提起した場合、私たちまたは彼らは、訴訟の対象となる製品または候補製品の研究、開発、製造、または販売の停止または延期を余儀なくされる可能性がある。
| 21 |
バイオ製薬業界は大量の特許を生み出しており、私たちを含む業界参加者は、どの特許が様々なタイプの製品をカバーしているのかを常に明確にしているわけではない。特許のカバー範囲は裁判所の解釈にかかっており、解釈はいつも一致しているわけではない。他方の特許または他の知的財産権を侵害または侵害する場合、私たちは合理的なコストで許可手配を達成したり、他の手配をすることができない可能性がある。ライセンスや代替技術を取得できない場合は、私たちの製品の発売が遅れたり、私たちまたはパートナーや協力者が製品の製造や販売を禁止したりする可能性があります。
特許訴訟は高価で時間がかかり、私たちに責任を負わせるかもしれない。
もし私たちが任意の特許訴訟、妨害、異議、再審、または他の行政訴訟に巻き込まれれば、私たちはこれに関連した巨額の費用を発生する可能性が高く、私たちの技術と管理者の努力は著しく分散されるだろう。また、訴訟における不利な裁決は私たちに重大な責任を負わせる可能性がある。
私たち は私たちの現在または未来の製品のために商標登録を得ることができないかもしれない。
私たちは、Macrilen(Macimorelin)を含む、米国を含む異なる司法管轄区で商標登録申請を提出しました。私たちはMacimorelinのために他の可能な商標申請を提出するかもしれません。私たちの任意の商標が他の場所に登録されるか、または任意の登録または未登録商標を使用することが市場で競争優位をもたらすことは保証されない。
私たちは第三者に依存して私たちの臨床試験を行い、監督し、監督しているが、これらの第三者の表現は満足できないかもしれない。
著者らはCRO、医療機関と臨床研究者のような第三者に依存して合格した患者を募集し、そして著者らの臨床試験を行い、監督と監督する。これらの第三者の臨床開発活動への依存は,これらの活動の制御を減少させた。しかし,これらの第三者への依存は,我々の臨床試験がGCPガイドラインやINDがFDAに提出した出願や同様の外国規制文書に含まれる研究計画や案に従って行われることを確実にすることを含む規制責任を解除することはできない。さらに、これらの第三者は の他のエンティティと関係がある可能性があり、その中のいくつかは私たちの競争相手である可能性がある。また,彼らは計画どおりに活動を遂行しないかもしれないし,法規の要求や我々の試験設計に基づいて我々の臨床前研究や臨床試験を行わない可能性がある。これらの第三者がその契約責任を成功裏に履行できなかった場合、または予期された最終期限内に完了できなかった場合、私たちの製品のために規制部門の承認を得て商業化する努力は延期または阻止される可能性がある。
我々 は、我々の候補製品 を開発することを含むが、これらに限定されないいくつかの候補製品 を含む第三者に依存して我々の業務に関連する様々な機能を実行する。私たちはこのような関係に対する依存性に多くの危険をもたらす。
私たちが行っているか計画中の臨床試験の開始または完了、または終了または一時停止のいかなる困難または遅延は、私たちのコスト増加、遅延、または私たちの創造能力を制限し、私たちのビジネスの将来性に悪影響を及ぼす可能性があります。
私たちの候補製品の臨床試験を開始する前に、臨床開発を許可するために必要なINDまたは同様の規制文書の一部として、臨床前研究の結果およびその他の情報をFDAまたは同様の外国規制機関に提出しなければならない。FDAまたは同様の外国の監督管理機関は、任意の候補製品に対して追加の臨床前研究 を要求する可能性があり、その後、任意のINDまたは同様の規制申請に基づいて臨床試験を開始することを可能にすることができ、これは、br}遅延を招き、私たちの臨床前開発計画のコストを増加させる可能性がある。CGHDまたは任意の他の候補製品を診断するためのMacimorelinを評価するための検出試験 の開始または完了中の任意のこのような遅延は、我々の製品開発コスト に深刻な影響を与える可能性がある。
| 22 |
また,海外での臨床試験は,われわれが行っている検査試験のように,余分なリスクをもたらし,われわれの臨床試験の完了を遅らせる可能性がある。これらのリスクには,外国に登録された患者が医療サービスや文化的慣習の違いにより臨床案を遵守できなかったこと,外国規制計画に関連する追加行政負担の管理,戦争を含むこのような外国関連の政治的·経済的リスクがある。例えば,2022年には,ロシアがウクライナに侵入したため,ロシアとウクライナでの検査試験活動が停止し,試験計画患者総数の約25を占め,試験完了予想の遅延を招いた。これらの国/地域 の代わりに、迅速な検査試験の完了を確保するために、同社は第2のCROを招いて4つの新しい国/地域(アルメニア、スロバキア、ギリシャ、トルコ)に検査場所を確立した。臨床試験申請が行われているが,ロシアのウクライナ侵入はこの地域で何らかの試験を行う能力に影響し,これまでの試験の遅延を招いている。これは私たちの臨床試験および/または臨床結果分析の完了を阻害する可能性があり、これは私たちの業務に実質的な損害を与える可能性がある。
われわれ は世界的にMacimorelinの検出試験を行っており,米国以外で将来の臨床試験を行う可能性がある。しかし,FDAは他の外国と同等の機関がこのような実験のデータを受け入れない可能性があり,この場合,我々の開発計画が延期され,我々の業務に実質的な被害を与える可能性がある.
具体的には、ロシアとウクライナを含む2つのCROを米国以外の場所で検査試験を行った。ロシアが2022年2月にウクライナに侵入したため、ウクライナとその周辺地域の臨床試験地点が停止された。また、米国とその欧州同盟国は、地域禁輸、全面封鎖制裁、ロシアの主要金融機関に対する他の制限など、ロシアに対して重大な新たな制裁を実施した。ロシア,ウクライナの一部地域,その地域の他の地域で臨床試験を行う能力は制裁法の適用に制限されており,代替試験場所を探すことが求められており,開発コストが増加し,候補製品の臨床開発が遅れている。これらのすべてのことが,われわれの臨床開発計画の実行を阻害する可能性があり,われわれの業務に実質的な損害を与える可能性がある。
業務を展開する際、私たちは安定して一貫した具材と原材料供給に依存している。
私たちの契約製造業者または私たちの許可者が、将来、現在の条項に類似したまたは根本的に割引されていない条項で、私たちの既存のサプライヤーまたは任意の他のサプライヤーから製品を購入することができることを保証することはできません。ある原材料や原料の供給が中断されたり、私たちがそれらのために支払った価格が大幅に上昇して、私たちの業務、財務状況、流動性、経営業績に重大な悪影響を及ぼす可能性があります。
製品の生産と供給に依存する第三者が満足に職責を果たすことができず、供給不足を招く可能性があると予想される。
私たちは第三者にMacrilenを生産して供給することに依存している。私たちはまた特定の供給義務を持っているか、または持っているかもしれない に対して私たちの既存で潜在的なライセンス所有者たちは、Macrilen(Macimorelin)のマーケティングを担当しているか、または担当するだろう。成功するためには、Macrilen(Macimorelin)は、品質管理や規制の要求に応じて商業的な量産を行わなければならない。 代替サプライヤーを導入することで、常に安定した供給を確保し、このようなリスクを最小限に抑えることを目標としているが、Macrilen(Macimorelin)やその生産に使用される材料を生産できる契約メーカーやサプライヤーの数は限られている。もし私たち自身がこれをできなかったり、第三者がMacrilen (Macimorelin)や材料を製造したり供給したりすることができなかったり、商業的に合理的な条項でそうすることができなかったら、私たちは私たちの許可者を通じてMacrilen(Macimorelin) を商業化することができないかもしれない。第三者製造商会に依存してリスクをもたらし、もし私たちが自分で製品を製造すれば、私たちは第三者に依存して法規を遵守することを含むリスクの影響を受けません。第三者は私たちがコントロールできない要素によって製造協定に違反する可能性があり、第三者はそれ自身の業務優先順位に従って合意を終了または更新しないかもしれませんが、これは私たちにとってコストが高く不便です。
私たち は技術者に対する激しい競争に直面しており、肝心な人の流失や多くの人を引き付けることができないことは私たちの運営能力を弱める可能性があります。
私たちbrは私たちの経営陣と臨床、監督、科学スタッフに高度に依存しており、彼らのサービスを失うことは私たちの目標を達成する能力に悪影響を及ぼす可能性がある。合格した管理者及び臨床、科学と監督者を募集と維持することは著者らの成功に重要である。私たちの人員数の減少は、重要な能力やスキルにおける常勤従業員の冗長性を解消し、外部コンサルタントや第三者により多く依存することを求めています。私たちは従業員の報酬をそのサービスの完全な競争力を維持するために必要な程度に高めることができず、これは私たちの従業員の留任リスクを増加させます。バイオ製薬分野の合格者に対する競争は非常に激しく、私たちが合格したbrを維持し続けることができなければ、私たちの外部コンサルタントと積極的な関係を維持することができなければ、私たちは私たちの戦略と運営目標 を実現できないかもしれません。
| 23 |
私たちは未来に訴訟を受けるかもしれない。
正常業務の過程で、私たち は時々訴訟の側になる可能性があります。法的訴訟を監視·防止することは,価値の有無にかかわらず,我々の管理職の時間がかかり,内部資源を完全に業務活動に集中させる能力に影響を与える.また、このような活動に関連する法的費用やコストが高い可能性があり、将来的に判決を受けたり、重大な金銭損害クレームについて和解したりする可能性がある。私たちの利益に違反する決定は、重大な損害賠償の支払いを招き、私たちのキャッシュフロー、運営結果、財務状況に重大な悪影響を及ぼす可能性があります。
いかなる訴訟に対しても、私たちの保険は私たちを清算しないかもしれないし、あるいは抗弁や結審時に受ける可能性のある費用や損失を精算するのに十分ではないかもしれません。任意の保険が請求に適用される前に満たされる必要がある大量の自己保険留保費用、未精算の法的費用、または任意の訴訟における不利な結果を含む巨額の訴訟コストは、私たちの業務、運営実績、または財務状況に悪影響を及ぼす可能性があります。
私たちは製品責任クレームのリスクに直面していて、私たちは十分な保険範囲を獲得できないかもしれません。
Macrilen(Macimorelin)の販売と使用は、製品責任クレームと関連する負の宣伝のリスクに関連するだろう。製品br患者、ヘルスケア提供者、または製薬会社や販売、購入、または使用している他の人は、私たちに直接責任クレームを出す可能性があります。私たちは保険方式で私たちの責任リスクを管理しようと努力している。私たちは私たちの臨床前と臨床研究に責任保険と製品責任保険を提供します。しかし、非常に重大な法的費用の可能性のある保険範囲を含む十分かつ負担可能な保険範囲を獲得または維持する能力がないか、または維持することができない可能性があり、十分な保険範囲がなければ、私たちに対するいかなるクレームも、私たちの業務、財務状況、または運営結果に重大な悪影響を及ぼす可能性がある。
私たちbrは持株会社であり、私たちの子会社債権者の債権は、通常、私たちおよび私たちの債権者と株主の債権よりも優先されます。また、ドイツの法律によると、私たちの主要運営子会社AEZSドイツ会社の流動性不足や負債が過重であれば、破産手続きの制約を受ける可能性がある。
Aeterna Zentarisは持ち株会社で、私たちの非現金資産の大部分は私たちの子会社の株式です。AEZSドイツ、私たちの主要な運営子会社、本社はドイツフランクフルトに設置されて、私たちの大部分の知的財産権を持っています。Aeterna Zentaris は持株会社であるため、私たちの債権者に対する債務は、私たちの子会社に属するすべての既存および未来の債務から構造的に、追加的または他の債務および/または義務を生じる可能性がある。したがって、私たちの権利および私たちの債権者が任意の子会社の資産分配に参加する権利brは、その子会社が清算または再編された場合、またはその子会社に関連しているか、またはその子会社の破産または破産手続きに関連する任意の場合に、したがって、私たちの証券保有者がこれらの資産に参加する権利は、当該子会社の債権者の優先債権によって制限される。私たちがこのような子会社に対して公認債権を持っている可能性のある債権者の範囲内で、もし私たちの債権が保証されているか、または私たちの保有する債権者よりも優先的であれば、私たちの債権は依然として私たちの子会社の債権者の優先債権に支配されます。
私たちの証券の所有者は私たちの子会社の債権者ではありません。私たちの子会社の資産に対する債権は、これらの運営子会社における私たちの所有権br権益から来ます。我々子会社の債権者の債権は、通常、私たち自身の所有権権益債権ではなく、このような子会社の資産よりも優先されるので、私たちの証券の所有者よりも優先される。我々の子会社の債権者は、時々一般債権者、貿易債権者、従業員、保証債権者、税務機関、および担保を持つ債権者を含む可能性がある。したがって、私たちまたは私たちの財産または任意の子会社に関連する停止、解散、清算または再編、または破産、資本不担保または債権者保護手続きが発生した場合、私たちの証券所有者が得ることができる価値を保証することはできません。また、私たちの子会社の私たちへのどんな分配も、私たちの子会社が運営している司法管轄区の通貨移転によって制限される可能性があります。
| 24 |
私たちの主な運営子会社AEZSドイツを管理するドイツの法律では、取締役管理者がAEZSドイツ社が倒産したと結論した場合、管理者はドイツの法律の規定に基づいて当該子会社に対して破産手続きを提起する義務があり、AEZSドイツ社の流動性不良や債務が重すぎるためである。
私たちのカナダの会社とドイツの存在により、アメリカの投資家は私たちに不利な判決を得て実行することが難しいかもしれない。
私たちはカナダの法律によって存在する会社です。私たちの多くの役員や上級管理職はカナダの住民や他の方法でアメリカ以外に住んでいます。彼らの資産の全部または大部分と私たちの資産の大部分はアメリカ外にあります。したがって、私たちは代理がアメリカで伝票手続きを送達することを指定していますが、米国の投資家は、これらの役員や上級管理職を提訴することは困難かもしれないし、連邦証券法や米国の他の法律の民事責任条項に基づいて米国裁判所が得た判決を執行することも困難である可能性がある。投資家は、外国裁判所(I)が我々またはこのような取締役に対する訴訟で米国裁判所が獲得した判決を執行すると仮定してはならない。米国連邦証券法または米国内の任意の州の証券法または“青空”法律の民事責任条項に基づく上級管理者または専門家、または(Ii) は、最初の訴訟において、米国連邦証券法または任意のこのような州証券または“青空”法律に基づいて、私たちまたはそのような取締役、上級管理者または専門家に対して責任を執行する。
適用されたカナダ証券法と米国の“サバンズ-オキシリー法案”によると、私たち は様々な内部統制報告書の要求に制約されています。私たちは未来のいつでも財務報告書の内部統制に有効であることを報告できる保証はありません。
上場企業としてアメリカを守らなければなりません2002年サバンズ·オクスリ法案(“第404節”) および国立機器52-109-発行者が年度と中間申告書類に開示した情報の証明カナダ証券管理人 。どんな年でも、私たちは私たちの内部統制評価、テスト、そして救済行動の完了時間、またはそれらが私たちの運営に及ぼす影響を決定することができない。このプロセスを完了すると、適用される米国証券取引委員会と上場企業会計監督委員会(米国)に基づいて、異なる深刻度の制御欠陥を決定することができる。規則制度。上場企業としては、他の事項以外にも、内部制御の重大な弱点や変化を構成する制御欠陥 、あるいは合理的に財務報告の内部制御に重大な影響を与える可能性のある制御欠陥を報告しなければならない。“重大な欠陥” は、我々の年間または中期連結財務諸表の重大なミス報告が合理的である可能性があり、 が直ちに防止または発見できないように、財務報告内部制御の欠陥または欠陥の組み合わせである。もし私たちが第404条の要求やカナダの同様の要求を遵守できなかった場合、あるいは私たちが重大な欠陥を報告した場合、私たちは規制機関の制裁を受ける可能性があり、投資家は私たちの合併財務諸表に自信を失うかもしれません。もし私たちがこのような重大な欠陥を是正できなければ、連結財務諸表は正確ではないかもしれません。
私たちは財務報告の内部統制に重大な欠陥がある可能性があり、これは私たちの普通株の価格に重大な悪影響を与える可能性があります
財務報告に対する内部統制は財務報告の信頼性と公認会計原則に基づいて外部財務諸表を作成するために合理的な保証を提供することを目的とした過程である。Brの制御および手続きを開示することは、証券監督機関に提出された報告において、会社が開示を要求する情報が適時に記録され、処理され、まとめられ、報告され、その最高経営者および最高財務官を含む会社の経営陣に蓄積され、開示を要求する決定をタイムリーに行うことを保証することを目的としている。会社はすでに資源を投入して、その開示制御システムと財務報告の内部制御に対して記録と分析を行った。財務報告及び財務諸表作成の信頼性については、設計及び運用がどんなに良好であっても、絶対的な保証ではなく、合理的な保証しか提供できない制御システムを提供する。
| 25 |
我々 は広範な環境法規に制約されており,このような安全や関連法律法規に基づいて環境救済義務を負うことが可能である。これらの債務の影響および会社がこれらの債務に効果的に対応する能力は、私たちの業務、財務状況、キャッシュフロー、経営業績に重大な悪影響を与え、私たちの普通株の時価低下を招く可能性がある。
私たちのbrは、アメリカ、カナダ、ドイツの一連の連邦、州、省と地方の環境法律法規の制約を受けています。私たちが製品を生産と販売したり、他の方法で業務を経営している国では、環境、安全事項、化学品規制と製品安全に関する法規です。他の事項に加えて、これらの要件は、環境への汚染物質、危険物質、および廃棄物の排出を含む、材料の運搬、製造、輸送、貯蔵、使用および処理の規制を含む。我々の正常な業務過程において、このような物質および廃棄物は環境中に排出される可能性があり、これはbr環境または財産損害または人身傷害をもたらす可能性があり、汚染土壌および地下水に関する救済義務、潜在的な損害クレーム責任または社会的または名声被害、および他の同様の悪影響を負わせる可能性がある。いくつかのbr法によると、汚染が私たちによるものであっても、不動産の前の居住者によるものであっても、他の人によるものであっても、私たちがゴミを送る第三者の場所によるものであっても、私たちのある物件の汚染を修復する必要があるかもしれない。
近年、すべての会社の運営は環境保全に関するますます厳しい法律や法規によって制約されています。 そのような立法と規制は複雑で、絶えず変化している。現行の法律や法規の変更やその実行、あるいは私たちの施設での汚染の発見など、将来的に発生するイベントは、他の事項に加えて、いくつかの排出源に追加の制御装置を設置し、私たちの製造プロセスを変更し、現在このような清掃を行う必要がない施設で土壌や地下水汚染 を修復するか、またはそのような変化によって引き起こされる、またはそれに関連する社会的期待または関心brを満たす行動をとる必要があるかもしれない。このような追加的なコンプライアンスまたは救済義務br、またはそのような社会的期待または懸念に応答するコストは非常に高い可能性があり、私たちの業務、財務状態、キャッシュフロー、および運営結果に重大な悪影響を及ぼす可能性があり、私たちの普通株式および/または債務証券の時価縮小を招く可能性がある。
私たちは外貨変動によって損失を受ける可能性があります。
多くの場合、私たちの業務は私たちのビットコインや私たちの子会社のビットコイン以外の通貨を使って行われます。 貨幣値の変動は私たちの通貨為替損失を招く可能性があります。私たちは現在為替レートの危険に対するヘッジ戦略を採用していない。私たちは私たちがドル、ユーロ、カナダドルと他の通貨の間の為替レートの不利な変動のために損失を受けないという保証がない。
立法行動、新しい会計声明、より高い保険費用は、私たちの将来の財務状況や運営結果に悪影響を及ぼす可能性がある。
財務会計基準または会計基準実施の変化 は、不利な、意外な収入または費用変動 を招き、私たちの財務状況または経営業績に影響を与える可能性がある。新しい声明と声明に対する異なる解釈はすでにより頻繁に出現しており、将来も出現することが予想され、私たちは将来的に私たちの会計政策を変更することを要求されるかもしれない。変化するコーポレート·ガバナンスと公開開示法規、特に財務報告に関する内部統制を遵守することは、追加費用を招く可能性がある。コーポレートガバナンスや公開開示に関連して変化していく法律、法規、基準 は、私たちのような会社に不確実性をもたらしていますが、この不確実性は保険コストの上昇をもたらしています。
データ セキュリティホールは、私たちの運営を乱し、私たちの運営結果に悪影響を及ぼす可能性があります。
私たちのネットワークセキュリティとデータ回復措置、および私たちと契約した第三者の措置は、コンピュータウイルス、ネットワーク攻撃、侵入、および不正な改ざんによるコンピュータシステムによる同様の中断を防ぐのに十分ではないかもしれません。私たちが電子的に保存している任意の固有および機密情報(研究または臨床データを含む)の流用、窃盗、破壊、または任意の他のタイプのセキュリティホールは、私たちの運営中断を招く可能性があり、私たちの臨床活動と業務運営が実質的に妨害される可能性があり、第三者の法的クレームに直面させる可能性があります。さらに、私たちはサイバー攻撃や侵入の原因を修復するために多くの資源が必要かもしれない。このような中断は私たちの業務、運営業績、財務状況に実質的な悪影響を及ぼす可能性がある。さらに、当施設への任意の侵入または侵入は、当社の独自および機密情報(研究または臨床データを含む)を盗用、窃盗、破壊、または任意の他のタイプのセキュリティホールにもたらし、または私たちの研究開発設備および資産の破損をもたらし、私たちの業務、運営結果、および財務状況に大きな悪影響を及ぼす可能性があります。
| 26 |
私たちの業務は臨床活動や従業員に関する個人情報を扱っています。これらの情報を使用することは、製品の開発と従業員の管理を含む、私たちの運営と革新に重要だ。EUの一般データ保護法規のような新しい法規と変化する法規は、将来的に私たちのデータ管理をより厳格に審査する可能性がある。重要かつ敏感なシステムおよび情報を保護できない他のネットワーク攻撃または他の行為は、私たちの名声を損なう可能性があり、訴訟を起こしたり、規制制裁を招いたりする可能性があり、これらはすべて私たちの財務状況および運営結果に重大な影響を与える可能性がある。
私たちの普通株に関するリスク
私たちの株価の変動は大きく、これは私たちがコントロールできない要素のせいかもしれない。
私たちの推定値と株価自己が初めて上場した後の取引が始まって以来、まずカナダにいて、それからアメリカでは、現在あるいは歴史的財務業績、資産価値、帳簿価値あるいは多くの伝統的な株式価値測定基準に基づく基準とは意味のある関係がありません。
2022年1月1日から2022年12月31日までの間、我々の普通株のナスダックでの終値は1株3.02ドルから10.50ドルであり、トロント証券取引所での終値は1株4.05カナダドルから12.75カナダドルである。2023年3月22日まで、私たちのナスダックでの普通株価格は2.60ドルで、トロント証券取引所での普通株価格は3.65カナダドルです。私たちの株価は私たちの業務の事態発展に直接影響を受ける可能性があり、私たちがコントロールできない、あるいは私たちとは関係のない事態の影響を受ける可能性もあります。株式市場、特にバイオ製薬業界は、投資家の感情の急激な変化の影響を受けやすい。バイオ製薬業界の会社の株価や取引量は、経営業績に関係なく、あるいは経営業績に比例しない方式で激しく変動する可能性がある。我々の株価と取引量は、以下の要因を含むが、これらに限定されない一連の要因に基づいて変動する可能性がある
| ● | 現在または将来の第三者サプライヤーおよびライセンサー側の動的 ; | |
| ● | Macrilen(Macimorelin)に関する臨床試験と制御進展 | |
| ● | 私たちが期待している臨床試験の開発または商業化スケジュールを遅延させます | |
| ● | 技術、法規、または他の事項に関する私たちの公告 ; | |
| ● | 要人は着任したり離任したりした | |
| ● | 米国、カナダ、および他の国/地域では、私たちの候補製品および競争相手製品に影響を与える政府または規制措置 ; | |
| ● | 特許または独自の権利に関する紛争の開発または関連; | |
| ● | 収入や支出の実際の変動や予想変動 | |
| ● | 新興成長型とバイオ製薬業界の一般市場状況と変動; と | |
| ● | 米国や海外の経済状況は、新冠肺炎による不安定さを含む。 |
著者らは同時にナスダックとトロント証券取引所で上場することは各種の要素によって価格変動性を増加させる可能性があり、これらの要素は私たちの普通株を売買する能力の違い、異なる資本市場の市場状況の違い及び取引量の違いを含む。しかも、低い取引量は私たちの普通株の価格変動性を増加させるかもしれない。あっさりした取引市場は私たちの普通株の株価変動を株式市場全体をはるかに超える可能性がある。
私たちは近い将来に配当するつもりはありません。
Br日まで、私たちはまだ私たちの普通株式の任意の配当金を発表したり支払ったりしていません。したがって、私たちの普通株または私たちの任意の他の証券への投資収益は未来の任意の付加価値に依存するだろう。私たちの普通株や他の証券の価値が上昇する保証はなく、株主がそれらを購入する価格が変わらない保証さえありません。
| 27 |
将来の証券発行とヘッジ活動は私たちの普通株の取引価格を下げるかもしれません。
株式オプションの行使および引受権または他の転換可能な証券または発行可能な証券を含む任意の追加または将来の発行可能な証券または転換可能な証券は、私たちの既存の株主の利益を希釈し、私たちの普通株の取引株価を大幅に低下させる可能性がある。
私たちのbrは、オプションまたは株式証明書を行使する際の義務を履行するために、私たちの運営および業務戦略に資金を提供することを含む、様々な理由で株式証券を発行する可能性があります。私たちの株式オプション計画は、通常、その時点で発行された普通株式総数の11.4%に相当する、任意の所与の時間に行使可能な最大普通株数の既発行株式オプションを持つことを許可しています。
また、私たち普通株の株価は、他の投資ツールをより魅力的に私たちの株式に参加する方法と、私たちの証券のヘッジや裁定取引活動に発展する可能性がある投資家が証券を売却する可能性のある影響を受ける可能性があります。このようなヘッジや裁定は逆に私たちの普通株の取引株価に影響を及ぼす可能性がある。
ある財政年度の6月30日に海外個人発行者資格を失った場合、1934年の証券取引法の国内報告制度の遵守を要求され、追加の法律、会計、その他の費用が生じる可能性があります。
私たちの現在の外国個人発行者としての地位を維持するためには、(1)私たちの普通株式の大部分はアメリカ住民が直接または間接的に所有してはならない、または(2)(A)私たちの幹部と取締役の多くはアメリカ市民または住民であってはならない、(B)私たちの資産の50%以上はアメリカに位置することができず、(C)私たちの業務は主にアメリカ以外の地域で管理されなければならない。
2022年、私たちの経営陣は、私たちが外国人個人発行者であることを決定した様々な事実や状況を年次評価し、上記の状況に基づいて、私たちの経営陣は、確定日まで、2022年6月30日までのbr、私たちは依然として外国個人発行者であることを決定しました。
しかし、私たちが2023年または今後の財政年度に外国の個人発行者になるという保証はない。
いずれかの財政年度の6月30日に外国人個人発行者の資格を失った場合、1934年の証券取引法や米国国内発行者に適用される他の要求を遵守することが求められるであろう。これらの要求は、外国民間発行者への要求よりも詳細で広い。私たちはまた様々なアメリカ証券取引委員会規則やナスダック上場基準に基づいて私たちのコーポレートガバナンスを改革することを要求されるかもしれません。私たちにとって、アメリカ証券法を遵守してアメリカ国内発行者に適用される報告書は、私たちにとっての規制とコンプライアンスコストが、外国の個人発行者としての歴史的に生じるコストよりも高い可能性があることを要求しています。したがって、今後ある時点で外国の個人発行者の地位を失う可能性があることが予想され、私たちの法律、財務報告、会計コンプライアンスコストが増加する可能性があり、このような場合に私たちの法律、財務報告、会計コンプライアンスコストがどのくらい増加する可能性があるかを推定することは困難である。
わが社の定款には“空白小切手”の優先株条項が含まれており、わが社への買収を延期または阻害する可能性があります。
私たちの改訂された会社定款細則は数量を問わない“空白小切手”優先株の発行を許可し、 は株主の承認を必要とせずに当社の取締役会によって発行することができ、清算、配当、その他の権利を含む可能性があり、私たちの普通株などと同じあるいはbr}を優先することができる。また、我々は、株主 が取締役会への指名を提案する人選を含む株主年次会議への提出を承認するための事前通知手順を我々の継続文書に実施している。これらの規定は、単独でも共同実施でも、敵意の買収や制御権の変更や私たちの経営陣の変動を延期または阻害する可能性がある。私たちの持続文書の制御権の変更を延期または阻止する条項は、私たちの株主がその普通株からプレミアムを得る機会を制限する可能性があり、一部の投資家が私たちの普通株に支払いたい価格に影響を与える可能性もあります。
| 28 |
維権株主の行動は私たちの業務に否定的な影響を及ぼすかもしれない。
過去数年間、生物製薬業界の多くの会社に対して代理競争が開始された。エージェント競争に直面すると, 我々は競合に応答できない可能性があり,我々の業務を中断する.たとえ私たちが成功しても、私たちのbr業務はエージェント競争の悪影響を受ける可能性がある
| ● | 維権株主の代理権競争と他の行動に応答することは高価で時間がかかる可能性があり、私たちの運営を乱し、管理層と従業員の注意をそらす可能性がある | |
| ● | 任意のエージェント権競争の潜在的な結果の感知不確実性は、私たちが潜在的な買収、協力、または許可内の機会を達成することができず、合格者と業務パートナーを誘致および維持することをより困難にする可能性がある | |
| ● | もし私たちの経営陣とは異なる具体的な議題を持っている個人や私たちの取締役会の他のメンバーが任意の代理競争によって私たちの取締役会に選ばれたら、このようなbr選挙は、私たちの戦略計画を効果的かつタイムリーに実施し、私たちの株主のために価値を創造する能力に悪影響を及ぼす可能性がある。 |
| 第四項です。 | 会社に関する情報 |
| A. | 会社の歴史と発展 |
Eeterna Zentaris Inc.は1990年9月12日に設立されカナダ商業会社法(“CBCA”) は,CBCAに管轄され続けている.私たちの登録住所はカナダオンタリオ州ドレンド市ドレンド湾街222号Suite 3000、M 5 K、1 E 7 c/o Norton Rose Fulbright Canada LLPです。サウスカロライナ州サマービルに別の事務所を設置して、住所は29486です。私たちの電話番号は(843900-3223)、ウェブサイトはWww.zentaris.com.
2004年5月私たちはAeterna Zentaris Incと改名しました2022年7月15日に1株25株合併(逆株式分割)を完了し、これまで2015年11月17日に100株合併(逆株分割)を完了した。私たちの普通株は2015年11月20日にナスダックとトロント証券取引所で合併と調整取引を開始した。
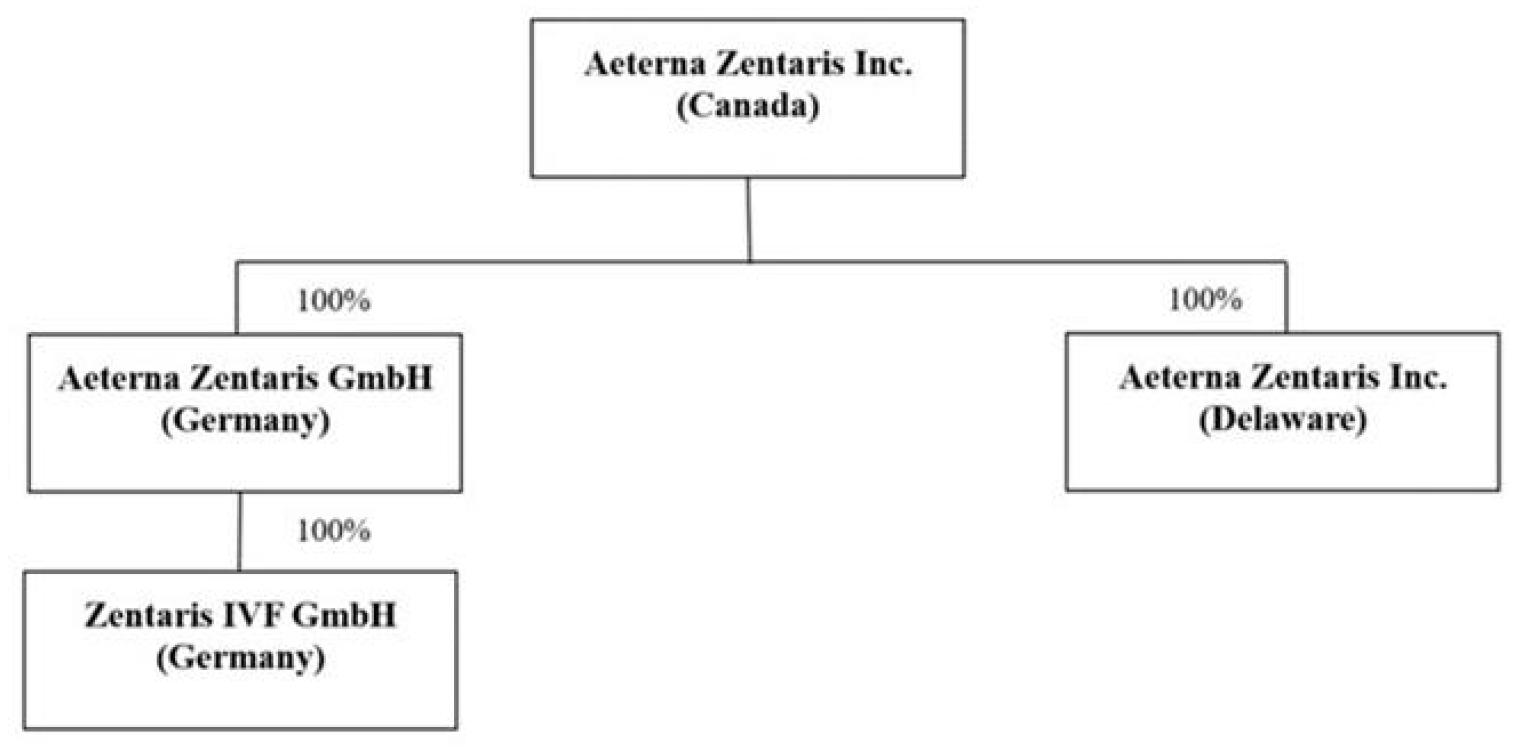
私たちは現在3つの完全な直接と間接子会社を持っています:Aeterna Zentaris GmbH(“AEZSドイツ”)は、ドイツの法律に基づいて登録されています。ドイツの法律に基づいて登録されています。Zentaris IVF GmbH、AEZSドイツ社の直接完全子会社、本社はドイツのメーン川のほとりフランクフルトにあり、ドイツの法律に基づいて登録されています。そしてAeterna Zentaris,Inc.、一家はデラウェア州に登録され、アメリカサウスカロライナ州チャールストンに事務所を設置している実体です。
| 29 |

私たちの普通株はナスダックとトロント証券取引所で取引され、取引コードは“AEZS”です。
私たちのアメリカでの流れとアメリカ証券取引委員会事務代理は私たちの完全子会社、アイトナーZentaris、Inc.,サウスカロライナ州サマービル、315 Sigma Drive、Summerville、29486にあります。
最近の発展
会社に関連する最新の事件と発展の完全な記述については、“プロジェクト4.B.-業務概要”(以下)を参照されたい。
| B. | 業務 の概要 |
Aeterna Zentarisは専門のバイオ製薬会社で、治療と診断テストの商業化と開発に従事している。同社の主導製品Macrilen(Macimorelin)は米国食品医薬品局(FDA)と欧州医薬品局(EMA)が承認した第1種であり,成人成長ホルモン欠乏症患者の診断のための唯一の経口試験でもある。Macimorelinは現在Macrilenの商標で米国で販売されており,Novoとのライセンス契約や改訂されたライセンスプロトコル(総称して“Novo修正案”)により,NovoはMacrilen(Macimorelin)の開発,製造,登録,商業化の独占許可を得ており,米国やカナダの成人や小児成長ホルモン欠乏症の診断に用いられている,以下に述べる。2022年8月26日、当社はNovoがNovo修正案を終了する権利を行使したと発表した。270日間の通知期間の後、アイトナーは2023年5月23日に米国およびカナダでMacrilen のすべての権利を再獲得する。
他のグローバル市場については、Consilient Health Limited(“Consilient Health”または“CH”)と独占ライセンス契約を締結し、ヨーロッパ経済圏とイギリスでMacimorelinを商業化している。欧州諸国·地域の商業化は2022年第2四半期に始まった。2023年3月15日,当社の同意により,Consilient Healthは譲渡 協定を締結し,現在のマカロニのヨーロッパ経済区およびイギリスで商業化されている許可プロトコルをAtnahs Pharma UK Limited(“Pharmanovia”)に譲渡し,当社はPharmanoviaと独占供給 プロトコルを締結し,これにより,当社はPharmanoviaに許可製品を提供することに同意した。私たちはMegaPharm Ltd.と商業化と供給協定を締結しており、同社は規制部門の承認を求め、その後、イスラエルとパレスチナの権力機関でMacimorelinを商業化する計画を立てている。我々は韓国PharmBioの子会社NK Meditech Ltd.(“NK”)と許可と供給協定を締結し、2021年11月30日から発効し、ER Kim PharmPharmticalsブルガリア EOOD(“ER-Kim”)と流通と商業化協定を締結し、2022年2月1日から発効した。NKとのプロトコルは、韓国でAGHDやCGHDを診断するためのMacimorelinの開発と商業化に関連しており、ER-Kimとのプロトコルは、トルコや一部の非EUバルカン諸国の子供や成人成長ホルモン欠乏症を診断するためのMacimorelinの商業化に関連している。私たちはまた、Macimorelinの臨床成功と注目される安全性を利用してCGHDを診断するための化合物を開発しており、満足されていない重要な需要分野である。同社はアジアや世界の他の地域で商業化するMacimorelinのビジネス発展機会を積極的に求めている。
| 30 |
同社は治療資産の開発にも取り組んでおり,最近では臨床前管路 を構築し,複数の適応の中で満たされていない医療ニーズを潜在的に解決し,まれあるいは孤立した適応に重点を置き,潜在的な小児科用途を有している。これまでに,NMOSD,PD,原発副甲状腺機能低下症,ALSを含む一連の適応にこのパイプラインを構築する協定に署名してきた。
Macrilen (Macimorelin)
Macrilen(Macimorelin)は新型経口胃腸促進成長ホルモン受容体アゴニストであり、グレリン受容体(Ghsr−1 a)と結合することにより成長ホルモンの分泌を刺激し、内分泌学的にも腫瘍学的適応にも潜在的な用途がある。Macrilen(Macimorelin) は米国食品·薬物管理局によって孤児薬として承認され,成長ホルモン欠乏症の診断に用いられている。
Macrilen(Macimorelin)はaghdを診断する製品の競争相手として主に内分泌学者による診断テストであり,これらのテストは食品や薬物管理局の承認を得ていないにもかかわらず。GHDの最も一般的な診断テストは
| ● | インスリン耐性試験(ITT)は、高い感受性と特異性を有するため、AGHDを評価するゴールドスタンダードとされてきた。しかし、ITTは患者と医者に不便をもたらし、静脈投与(“IV”)、 はある患者、例えば冠状動脈性硬化症或いはてんかん患者である。正確な結果を得るためには患者が低血糖を経験する必要があるからだ。一部の内科医師は完全低血糖を招くことはなく、故意に正確性を損害し、患者の安全性と快適性を増加させる。また、ITTの管理には、医師が2~4時間のテスト中に患者を密接に監視することに関連する追加費用が含まれている。テストは救急設備があり患者が迅速に入院できる環境で行わなければならない。br}ITTは心血管疾患、てんかん発作障害や脳癌の病歴などの併存疾患を有する患者には適していない。安全を考慮して高齢者が弱い患者もいます | |
| ● | グルカゴン刺激試験(GST)は内分泌学者によって比較的安全であると考えられているが,この試験の作用機序は不明である。また,このテストには最大3時間から4時間 を要した.3分の1までの患者で副作用が生じ,最も一般的なのは試験中と試験後に嘔気が出現することである。このテストは筋肉注射(“IM”)です。 | |
| ● | 成長ホルモン放出ホルモン−アルギニン刺激試験(“GHRH+ARG”)は,オフィス環境で実行しやすい試験であり,良好な安全性を有しているが,ITTやGSTに比べて管理コストが高いと考えられている。GHRH+ARGは がITTの最適な代替案となることが提案されているが,GHRH+ARGは米国では利用できなくなった。この テストは静注により行われた。 |
経口Macrilen(Macimorelin)は現在使用されている成長ホルモン欠乏症試験よりも便利で簡単な方法を提供しており,これらのすべての試験には 静脈または即時注射が必要である。また、Macrilen(Macimorelin)は既存の診断テストよりも有利な安全性を示す可能性があり、その中のいくつかはいくつかの患者集団(例えば糖尿病または冠状動脈性硬化症患者)に適していない可能性があり、様々な副作用を示しているが、Macrilen(Macimorelin)はこれまでこのような副作用が出現していない。これらの因子は成長ホルモン欠乏症検出の使用を制限する可能性があり,Macrilen(Macimorelin)を成長ホルモン欠乏症を評価する第一選択品とする可能性がある。Macrilen(Macimorelin)はITTに代わる可能性が高く,内分泌学者がAGHDを評価する第一選択方法となっていると考えられる
| ● | 患者の血糖降下を必要としないので、ITTよりも安全で便利である | |
| ● | Macrilen(Macimorelin)は経口投与されるが、ITTはインスリンを静脈内投与する必要がある | |
| ● | Macrilen (Macimorelin)はITTよりも信頼できるテストであり、評価可能なテスト結果をもたらした | |
| ● | Macrilen (Macimorelin)は再現性が高い |
| 31 |
| ● | Macrilen(Macimorelin)を用いてAGHDを評価することは,ITTよりも時間がかかり,手間がかかる | |
| ● | 評価は病院のような環境ではなく,医師のオフィスで行うことができる。 |
Macrilen(マルクレリン)が全面的に市場に投入された後,米国では年間約15,000−20,000回のAGHD検出が行われると信じている。また、米国疾病管理·予防センターが発表した情報、異なる科学出版物、ヒューロン、TVG、Navigant Researchによると、米国のAGHD評価の総潜在市場は年間28,000~43,000回のテストの範囲内であり、外傷性脳損傷(“TBI”)を受けた患者の評価は含まれていないと推定される。脳外傷患者では、GHDがしばしば発生し、認知後遺症や生活の質の低下を招く可能性がある。発表された研究結果によると,約10%から35%の脳損傷患者にGHDが発生する可能性がある。これらのデータはGHDテストの巨大なアップリンク可能性をサポートしている。
Macimorelin 発展の歴史
以下は,我々が開発したMacrilen(Macimorelin)の履歴要約である
2017年から現在まで
| ● | 2017年1月4日,トップデータの分析により,Macrilen(Macimorelin)の確認性 期臨床試験は共通の主要 の終点の一つに達しなかったことを発表した。検討案では,主要奏効率変数の両側95%信頼区間の下限が75%以上であれば,Macrilen(Macimorelin)を用いてAGHDを評価することに成功すると考えられる。70%以上の割合はITTの“肯定的”と一致している。推定された負のプロトコルの割合は成功基準を満たしているが、推定された肯定的なプロトコルのbrパーセントは成功結果の基準に達していない。したがって、 結果は所定の同等基準を満たしておらず、この基準は、 否定同意および肯定的同意の割合の両方が成功しなければならないことを要求する。 | |
| ● | 2017年2月13日,主要データベースであるオリジナルデータを検討したところ,Macrilen(Macimorelin)がFDA登録を支援する を示し,登録を継続する予定であると結論した。 公告は,我々が結論を出すための根拠となる事実を述べている.当社は2017年3月末にFDAと面会し、この立場を検討した。 | |
| ● | 2017年3月7日我々は,小児科委員会急診科がMacrilen (マキシロリン)に対する小児科調査計画に同意し,会社が提出書類 を提出するまで小児科調査計画を延期できることに同意したことを発表した。マーケティング許可を求めるマーケティング許可申請 は、Macrilen(Macimorelin)を用いてAGHDを評価する。 | |
| ● | FDAは2017年7月18日、2017年12月30日の処方薬使用料改定日を提供してくれた。 | |
| ● | 2017年11月27日、環境保護局はMacrilen(Macimorelin)のMAA申請を受けた。 | |
| ● | 2017年12月20日、米国食品·薬物管理局は先天性巨大結腸患者の診断のためのMacrilen(Macimorelin)の発売許可を許可した。 | |
| ● | 2018年1月16日、会社はAEZSドイツ社を通じてライセンス契約を締結し、 の開発、製造、登録、Macrilen(Macimorelin)の米国とカナダにおける商業化の規制とサプライチェーンサービス は以下のとおりである。 | |
| ● | “臨床内分泌学と代謝誌”2018年8月第103巻第8号では,Macrilenからのキー3期データ®(Macimorelin)検証性試験は、Jose M.Garcia,MD,PhDらによって発表され、タイトルは‘Macimorelin as a Diagnotics Test for Adult GH Define’(Macimorelinは成人成長ホルモン欠乏の診断試験として)。 |
| 32 |
| ● | 2018年11月19日,我々はEMAの人用医薬品委員会(“CHMP”) が積極的な意見を採択し,Macimorelinが上場許可を得ることを提案したことを発表した。 | |
| ● | 2019年1月16日、私たちは欧州委員会がMacimorelinの上場許可を承認したと発表した。 | |
| ● | 2019年12月18日米国臨床内分泌学者協会(“AACE”)と米国国内分泌学会(“ACE”)は新たな“成人と患者成長ホルモン欠乏症管理ガイドライン”(“ガイドライン”)(“ガイドライン”)を発表したと発表した。AACE/ACE 2019年ガイドラインは、従来のGHSTと比較して、Macimorelinを“より短く、より簡単な代替案”として決定した。 | |
| ● | 2020年1月28日,最初の小児科研究の患者募集に成功し,Macimorelinを成長ホルモン刺激試験として小児成長ホルモン欠乏症(GHD)の評価に用いたことを発表した。 | |
| ● | 2020年4月6日,小児成長ホルモン欠乏症(CGHD)の初の小児科研究の陽性結果を発表し,Macimorelinを成長ホルモン刺激試験として評価した。 | |
| ● | 2020年4月7日,欧州医薬品局(EMA)は,AEZSによる会社の小児科研究計画(PIP)の修正要請 Macimorelinを受け入れることを決定したと発表した。 | |
| ● | 我々は2020年6月25日に、美嘉製薬有限公司とMacrilenのイスラエルとパレスチナ権力機関の商業化について独占販売と関連の品質協定を達成したと発表した。 | |
| ● | 2020年7月22日、私たちはMacimorelinに関する2つの特許出願を提出した。この2つの特許出願はいずれもMacimorelinの発明に関連しており,Macimorelinは小児患者の成長ホルモン欠乏を診断する方法である。 | |
| ● | 2020年11月16日,我々は完全子会社を通じて,ノボノルド生物製薬有限公司(NNBL)とMacimorelin開発と商業化に関する既存ライセンス協定改正案を締結したと発表した。修正案は、(I)更新された供給協定を反映し、(Ii)NNBL特許権の共同所有権権益を付与し、(Iii)小児科臨床試験の責任を修正するために、元の許可協定の具体的な条項と条件を部分的に修正する。および(4)AEZSへの支払い。 | |
| ● | 私たちは2020年12月7日に、マシモレリンをヨーロッパとイギリスで商業化する独占許可協定をConsilient Health Ltd.と締結したと発表した。 | |
| ● | 2021年5月13日,我々の重要な第3段階安全性と有効性研究 AEZS−130−P 02(検出試験)の開始を発表し,Macimorelinが小児期発症の成長ホルモン欠乏症(CGHD)の診断に用いられた。 | |
| ● | 2022年1月31日、我々のパートナーであるルキン社、地域専門製薬会社は、トルコ、セルビア、アルバニアを含む8カ国·地域でMacrilenを流通·販売する独占協定に署名したことを発表した。 | |
| ● | 2022年3月21日,我々は進行中の重要な段階3安全性と有効性研究AEZS−130−P 02(検出試験)の最新情報を提供し,サイト活性化と患者登録が新冠肺炎の大流行の影響を受け続けていることに注目した。また,ロシアの侵入により,ウクライナとロシアの臨床試験地点で中止される予定であった。 | |
| ● | 2022年4月19日、欧州特許庁は、EU 27カ国および他の欧州非EU諸国においてMacimorelinの知的財産権保護を提供する特許を発行したと発表した。 | |
| ● | 2022年5月25日、Ghryvelin(Macimorelin)が現在、ヨーロッパ各地の医療専門家に提供されていることを発表しました。 | |
| ● | 2022年8月29日、Aeterna Zentarisは、ノボノルドヘルスケア株式会社が、改訂された開発および商業化許可協定を終了する権利を行使したと発表した。Novoの270日間の通知期間の後、Eeternaは、この製品に対する米国およびカナダのすべての権利を再取得する。 |
| 33 |
Macrilen臨床計画
2020年1月28日,小児GHD評価の最初の小児科研究の患者募集として小児成長ホルモン刺激試験Macimorelinの完成に成功したことを発表した。この研究は,AEZS−130−P 01(“研究P 01”)は,われわれの小児科調査計画(“PIP”)においてEMAとMacimorelinがGHD診断として合意した2つの研究の中で第1項である。Macimorelinはグレリン作動薬であり、経口活性小分子であり、下垂体の循環系への成長ホルモンの分泌を刺激する。P 01研究の目標は、小児科患者に安全に使用することができ、最終的にGHDがないと診断された対象の成長ホルモン濃度を有意に上昇させることができる用量を確立することである。研究P 01から得られた推奨用量は,診断の有効性と安全性について重要な第2研究P 02で評価される。研究P 01は国際多センター研究であり、ハンガリー、ポーランド、ウクライナ、セルビア、ベラルーシ、ロシアで行われている。P 01は開放ラベル、グループ比較、用量増加試験であり、マキモレリンの安全性、耐性と薬物動態学/薬効学(“PK/PD”)を調査し、2~18歳のCGHD疑い児童患者の中で、マキモレリン0.25、0.5と1.0 mg/kgを単回経口投与した後、酢酸マキモレリンの耐性と薬物動態学/薬効学(“PK/PD”)を調査することを目的とした。この研究の3つのコホートで合計24名の小児科患者を募集した。研究方案によると、すべての登録された患者はスクリーニング期間が成功した後に4回の研究訪問を完成した。訪問1と訪問3では、研究地点の現地慣例に基づいて刺激性成長ホルモン刺激試験を行った。訪問2では、Macimorelinテストを行い、Macimorelin溶液を経口投与した後、所定の時間に血液サンプルを採取してPK/PD評価を行った。訪問4は研究終了時の安全フォローアップ訪問である。
P 01研究の最終研究結果は2020年第2四半期に発表され,CGHDにMacimorelinを用いた安全性と耐性が陽性データと,成人研究予想範囲で観察されたPK/PDデータが示唆された。
2020年4月7日、会社はEMAが私たちが最初に2017年3月に承認したPIP修正要請を受け入れることを決定したと発表し、その中に2つの小児科研究を行い、研究大綱の中で関連する重要な要素を定義した。EMAのこの決定は,世界的に統一されたテスト検証研究案,特にP 02研究を支援しており,欧州でも米国でも受け入れられることを期待していると信じている。
2020年末には臨床安全性と有効性研究の開始段階に入り,AEZS−130−P 02(“検出−試験”), はMacimorelinのCGHDの診断を評価した。DETECT試験は開放ラベル、単用量、多中心、および多国の研究であり、全世界で約100人の被験者を募集する予定であり、その中の少なくとも40人の思春期前の被験者と40人の思春期の被験者は、少なくとも25人の被験者が米国に登録されると予想される。成功すれば、この研究設計は潜在的な独立テスト を支持するのに適していると予想される。また、Novo修正案によると、NovoとEeternaは、Aeterna関連予算内部労働コストの返済を含む960万ドル(900万ユーロ)までの検出·試験費用を支援することに同意した。すべての共同承認された外部検査試験費用は960万ドル(900万ユーロ)を超え、NovoとAeternaによって二等分される。2021年4月22日、この臨床試験に関連する米国FDA調査性新薬出願が発効した(参照:Https://Clinicaltrials.gov/ct 2/show/NCT 04786873) ,2021年5月13日,米国で最初の臨床サイトを開設することを発表した。
2022年1月26日、同社は、オミック変種の新冠肺炎疫病における上昇により、同社はサイト起動と患者登録に避けられない遅延に遭遇したと発表した。私たちのチームは、より多くの臨床サイトを起動·稼働させるために努力してきました。私たちの目標は、勢いを確立し、この研究をゴールラインを越えながら、可能な限り対応することです。私たちは、ロシアがウクライナに侵入したため、これらの国の臨床試験活動を2022年2月に休止した契約研究組織(CRO)を招聘して、アメリカとロシアとウクライナを含む多くのヨーロッパ諸国で検査試験を行っています。したがって,これまで両国の臨床サイトには患者が入選していなかった。ロシアのウクライナ侵攻は私たちがこの地域で裁判をする能力に影響を及ぼす。
| 34 |
2022年8月26日、同社は米国とカナダ地域におけるMacrilenの全権利を再獲得することを発表し、これまでNovoは開発と商業化許可協定を終了し、270日間の通知期間を引き起こした。Novoは引き続き、アイトナー関連の予算内部の人件費の精算を含む960万ドル(900万ユーロ)までの資金を検出·試験費用に提供し続ける。960万ドル(900万ユーロ)から1050万ドル(980万ユーロ)を超える任意の追加検出-試験費用はNovoとEeternaによって二等分される。その会社はMacrilenのすべての選択を積極的に探索している。
同社は2023年1月17日、非アクティブなbrの国/場所の交換と追加の臨床研究組織(CRO)の採用により、登録者数が増加することを強調する最新の業務報告書を提供した。現在、4つの新しい国(アルメニア、スロバキア、ギリシャ、トルコ)は検査臨床試験の応用活動を行っており、2023年上半期に臨床試験の許可を得る予定である。学生募集は2023年末に完成する予定だ。新冠肺炎とロシアのウクライナ侵攻により、管理層が現在推定しているMacrilenの小児科臨床開発に関連する遅延 と予想以上のコストの影響は以下でさらに検討する。
Macimorelin 臨床前計画:グレリン作動薬は筋萎縮性側索硬化症(Lou Gehrig病)の治療に開発されている
2021年1月13日、私たちはクイーンズランド大学と材料譲渡協定を達成し、マキモレリンによるALS治療の臨床前と臨床研究の評価を行うためにマキモレリンを提供した。筋萎縮性側索硬化症は稀な進行性神経系疾患であり、主に随意運動を制御する神経細胞に影響し、歩行、話すと咀嚼などの運動を制御できない。ALS患者の多くは呼吸不全で死亡し,通常確定診断後3−5年以内に死亡する。筋萎縮性側索硬化症を治癒する方法はなく,疾患の進行を阻止あるいは逆転する有効な治療法もない。グレリンは広範な生物学的作用を有するホルモンであり,成長ホルモン放出を刺激することで最も有名であり,ALS治療の新たな証拠であることが示されている。グレリンアゴニストとしてmacimorelinはALS治療の潜在力を有していることを本研究協力で評価した。
クイーンズランド大学の研究者はこのような臨床研究を行うための支持的支出を申請している。2022年7月、同社はオーストラリアブリスベンクイーンズランド大学(UQ)の商業化会社UniQuest Pty Ltdと研究とオプション許可協定を締結し、ALS治療の潜在療法としてMacimorelinの開発を推進した。同社はALSに適した代替処方の開発に実質的な進展を遂げ,この適応におけるMacimorelinの治療潜在力を証明するためにトランスジェニックマウスALSモデルにおけるAEZS−130の評価を継続している。私たちの次の措置は、進行中の毒理学と安全性研究を完成させ、長期治療を支持し、概念検証を実現可能な後、次の計画開発を検討するために、規制機関と科学的な提案を提供することを含む。
Macimorelin 商業化計画
Novo は現在、アイテニン先天性心臓病の診断のためにMacrilenの商標で米国でMacrilenを販売しており、最近では、アイトナー特許権と商標所有権に関するNovoの追加権利を付与することに同意し、Macrilenを小児科適応症(“小児科適応症”)として使用している診断の開発計画に関するアイトナーとNovoの間のいくつかの責任を修正する。小児科適応に関する開発活動に関する費用の補償としてNovo による総対価格の提供が決定され,Novoは会社に払い戻し不可能な610万ドル(500万ユーロ)を前払いすることが規定されており,特許権使用料の低減を含め,最初のNovoとの合意から会社が獲得した500万ドルの小児科マイルストーン費用を免除する将来の支払い義務が改正された。
特許使用料の減少により、当社はMacrilenの年間純売上高を15%から8.5%に引き下げ、最高4,000万ドルに達し、Macrilenの年間純売上高が4,000万ドルを超えることに対して15%の特許使用料を決定することに同意しました。
“Novo修正案”の終了後、Novo修正案の条項によると、Novoは2023年5月23日までの270日間の通知期間内にその義務を継続しなければならない。その会社はMacrilenのすべての選択を探索するために努力する予定だ。
| 35 |
2020年12月7日、当社はConsilient Health Limited(“CH”または“Consilient”) とMacimorelinのヨーロッパ経済区およびイギリスでの商業化について独占許可協定を締結した。2021年12月、イギリス保健省と社会保障部は価格を承認し、CHが同社に226ドル(20万ユーロ)の定価マイルストーンを支払うことをトリガした。ドイツでは2022年6月15日に価格が承認され、CHが会社に支払う2番目の226ドル(20万ユーロ)の定価マイルストーン を引き起こした。私たちは2022年第1四半期にConsilientに初のMacimorelin(Ghryvelin)を出荷した。Consilientは同時にイギリス、スウェーデン、デンマーク、フィンランド、ドイツ、オーストリアでこの製品を発売した。より多くの連合国は未解決の払い戻し交渉をフォローするだろう。2022年4月19日、欧州特許庁は、イギリスやトルコのようなEU 27カ国および他の欧州非EU諸国に、成人の成長ホルモン欠乏症の診断のためのマキモレリン(Ghryvelin;Macrilen)の知的財産権保護を提供したと発表した。2023年3月15日、Consilient Healthは、現在ヨーロッパ経済地域とイギリスでマカロニ商業化を行っているライセンス契約をAtnahs Pharma UK Limited(“Pharmanovia”)に譲渡する譲渡協定を締結した。br社はPharmanoviaと独占供給協定を締結し、これにより、会社はPharmanoviaに許可製品を提供することに同意した。
著者らは2020年6月25日に、著者らはイスラエルの有力な生物製薬会社MegaPharm Ltdと独占販売と関連する品質協定を締結し、Macimorelinはイスラエルとパレスチナの権力機関で商業化し、AGHD患者の診断とCGHDの臨床開発に用いることを発表した。合意条項によると、MegaPharm 有限会社はイスラエルとパレスチナ権力機関でMacimorelinの登録を販売することを担当し、会社 は関連する知的財産権の製造、製品供給、品質保証と制御、規制支援と維持を担当する。2021年6月、兆豊製薬有限公司はイスラエル衛生部に申請を提出し、2022年11月に承認されたMacimorelinのイスラエルでの使用をイスラエル規制機関に許可するよう求めた。
私たちは韓国PharmBioの子会社NK Meditech Ltd.(“NK”)と許可と供給協定を締結し、2021年11月30日から発効し、ER Kim PharmPharmticalsブルガリアEOOD(“ER-Kim”)と流通と商業化協定を締結し、2022年2月1日から発効した。NKとのプロトコルは、AGHDおよびCGHDの診断のためのMacimorelin を韓国で開発および商業化することに関連し、ER-Kimとのプロトコルは、トルコおよびいくつかの非EUバルカン国の子供および成人成長ホルモン欠乏症を診断するためのMacimorelinの商業化に関する。
チャネル 拡張機会
副甲状腺ホルモン(DC-PTH)融合ポリペプチドの遅延除去:慢性副甲状腺機能低下症の潜在的治療
2021年3月11日,当社はイギリスのシェフィールド大学と,まず慢性副甲状腺機能低下症(“副甲状腺機能低下症”)の治療の可能性をAeternaが検討するヒト使用分野に係るPTH融合ポリペプチドの知的財産権 について独占ライセンス契約を締結した。シェフィールド大学と締結された独占特許および独自技術許可協定の条項によると、Aeternaは、特許出願に含まれるすべての人間用途を許可する前払い現金支払いと、特定の開発、規制および販売マイルストーンを達成する際に支払われるマイルストーン支払いと、これらの製品の純売上のより低いビット数の特許使用料brと、再許可に関連するいくつかの対処費用とを含む世界的にPTH融合ポリペプチドを開発、製造、商業化する権利を取得する。エトナーは許可された製品のさらなる開発、製造、承認、商業化を担当するだろう。Aeternaはまた、Aeternaによって助成されたいくつかの研究活動を研究契約に基づいてシェフィールド大学に招聘し、その結果はAeternaに付与されたライセンスの範囲に含まれる。
シェフィールド大学の研究者はポリペプチドの血清除去時間を延長する方法を開発しており,同社はHypoPT治療法の開発に応用している。副甲状腺機能低下は副甲状腺ホルモンレベルが異常に低いあるいは存在しない孤児疾患であり,米国の100,000人あたりの罹患率は37人,デンマークは22人,ノルウェーは9.4人,イタリアは5.3から27人である。標準的な治療法はカルシウム補充とビタミンD補充である。シェフィールド大学と協議した後、エトナーはそのDC−PTH計画の主要候補としてAEZS−150を選択した。AEZS−150は開発中であり,成人慢性副甲状腺機能低下症に毎週治療オプションを提供している。最近の進展は,副甲状腺機能低下症のラットモデルにおいてシェフィールド大学以前の体内データの検証·複製に成功したことと,会社の契約開発·製造組織とともにAEZS−150の製造プロセスを持続的に開発することであり,AEZS−150を発現する細胞系の主細胞バンクとより大規模なGMP生産に適したプロセス の確立に向かって進んでいる。私たちの次の措置はシェフィールド大学と協力して開発候補者を深く表現することです体外培養そして体内にある);AEZS-150を発現する細胞株のための一次細胞バンクを確立し、AEZS-150の臨床前開発を正式に決定し、第1のヒト臨床研究を行うために可能なIND申請に準備する。
| 36 |
目的生物製剤:標的、高度特異的な自己免疫調節療法、視神経脊髄炎スペクトル障害とパーキンソン病の治療に用いる
2021年1月、エテナーはドイツのヴェルツブルク大学と独占特許許可および研究協定を締結し、NMOSDの潜在的治療のためのAIM生物製品を開発、製造、商業化する世界的な権利を持っている。また、会社はヴェルツブルク大学病院のJoerg Wischhuen教授とボストンマサチューセッツ工科大学総病院の神経免疫学者Michael Levy博士を顧問として招聘し、炎症性中枢神経系疾患、神経系自己免疫性疾患とNMOSD領域で科学的な支持と提案を提供した。2021年9月、同社はヴェルツブルク大学と追加の独占ライセンスを締結し、パーキンソン病の潜在的治療の早期臨床前開発を行った。2022年5月12日、同社は、α-Synuclein特異的AIMバイオ製品を用いた治療が運動機能を改善する傾向を示し、制御性T細胞を有意に誘導し、黒質ニューロンを救命する革新的なパーキンソン病マウスモデルの臨床前陽性結果を発表した。これらのデータは,2022年5月6日から10日までオレゴン州ポートランドで開催された米国免疫学者協会の年次活動IMMUN LOGY 2022で公表されている。2022年6月13日、同社は両国でNMOSD治療の概念検証を実現したと発表した体外培養マウスモデルでも同様である。これらの発見は,2022年6月10日から13日までギリシャアテネで開催された第13回国際自己免疫大会で発表された。2022年10月、同社はボストンマサチューセッツ州総合病院(MGH)とMichael Levy博士とbr研究開発協定を締結し、臨床前のbr}を行った体外でそして体内にあるNMOSDの研究である。
目的生物製品は妊娠期の1つの自然過程に基づいて、それは母体免疫システムの一部の外来胎児抗原に対する免疫原性耐性を誘導する。胎児蛋白は加工され、ある免疫抑制の主要な組織適合性複合体I類分子上に現れ、この耐性を誘導する。自己免疫疾患では,免疫系が誤解され,身体自身のタンパク質を目指している。AIM Biologicsを用いることにより,このタンパク質に対する耐性の回復を目指し,自己免疫疾患の治療を目指している。
NMOSDは水チャンネル蛋白4に対する自己免疫性疾患であり、主に視神経と脊髄に発見されている。この失明や麻痺をきたす疾患の罹患率は100,000人あたり0.7−10人であり,ヨーロッパの祖先に比べてアジア人やアフリカ人の方がよく見られ,女性の流行率は男性の9倍である。NMOSDは常に生命を脅かす再発の中で進展し、大量のステロイドと血漿置換を用いて積極的に治療する。われわれの臨床前計画には,NMOSDの治療のための既存の概念検証データ の拡張が含まれている体外培養そして体内にあるAIM生物製品に基づく開発候補;br}および選択された候補に基づく製造プロセス開発を選択するために評価される。
パーキンソン病は1種の神経系疾患であり、通常は運動問題と関係があり、緩慢かつ迅速な進展形式を有する。それは全世界の1000万人に影響を与える二番目によく見られる神経変性疾患である。パーキンソン病の特徴はニューロン内封入体が主にα−シヌクレイン(α)であり,ドパミン産生細胞の死亡に関与していることである。ドパミン作動薬はパーキンソン病症状を治療する主要な薬物であるが,現在のところ疾患の進行を予防あるいは遅延させる薬物療法はないため,短電パルス脳深部刺激などの代替療法が研究されている。潜在的なパーキンソン病治療薬としてAIM生物製品を開発するために,アイトナーは革新的な動物モデルを利用して,α−A 53 T−α−シヌクレインパーキンソン病マウスのシヌクレイン特異的T細胞により神経を退化させることを計画しており,このモデルは最近ヴェルツブルク大学の研究者によって発表されている体外培養そして体内にあるパーキンソン病の潜在的治療のための抗原特異的AIMバイオ製品候補分子の試験。
| 37 |
細菌ワクチンプラットフォーム:経口活性、弱毒化生細菌ワクチンプラットフォーム、コロナウイルスとクラミジア細菌などのウイルスと細菌に対する潜在的な応用を有する
過去2年間、新冠肺炎ワクチンの構造は引き続き深刻な変化が発生した。すでに高効率ワクチンが使用可能であり、ますます多くの治療方案が同時に承認されたか、あるいは後期開発段階にあり、あまり致命的ではないウイルス変異体が伝播しており、これらはすべて任意の早期新冠肺炎ワクチン計画に関連する財務リスクを増加させている。我々が資源を慎重に使用することを確保するために,会社のワクチン開発計画の早期段階と世界情勢の変化を考慮して,エテナーは新冠肺炎やクラミジアワクチンプラットフォームをさらに開発しないことを決定した(このプラットフォームは会社の新冠肺炎計画で使用されているワクチンプラットフォームと同じプラットフォームに基づいている)。そのため、同社はまた、このワクチンプラットフォーム技術に関するヴェルツブルク大学との既存の許可協定を終了することを選択した。
地理的エリア
私たちの競争の主な地理的地域の記述は、過去3年間に私たちが収入した地理および分類内訳を含めて、今年度の財務諸表の付記25(支部情報)に今年度の20-Fレポート第17項に記載されている。
季節性
専門的なバイオ製薬会社として、同社はそのいかなる製品やサービスも季節的とは考えていない。
原材料 材料
原材料と供給品は通常数量が十分で、私たちの業務需要を満たすのに十分です。私たちまたは私たちの許可者は販売された薬品を第三者 メーカーに依存するだろう。ある原材料や原料の供給が中断されたり、私たちがそれらのために支払った価格が大幅に上昇して、私たちの業務、財務状況、流動性と経営業績に重大な悪影響を及ぼす可能性があります。
“薬品開発条例”
一般的に。 アメリカ、カナダ、ヨーロッパとその他の国の政府当局は薬品の臨床前と臨床試験、br製造、ラベル、貯蔵、記録保存、広告、販売促進、輸出、マーケティングと流通などの方面に対して広範な監督管理を行った。米国,EU諸国,その他の国の法律によると,われわれの臨床試験は良好な臨床実践(GCP)ガイドラインおよび新薬(IND)申請や同様の外国監督提出に含まれる研究計画や案に基づいて行われることを確保する義務がある。以下は、主要市場で私たちの主要政府法規に影響を与える簡単な要約であり、私たちは、これらの市場で私たちの製品をマーケティングし、および/または、私たちが買収または許可した製品または私たちが販売促進権を獲得した製品を普及させるつもりです。
アメリカですアメリカでは、FDAの薬物評価と研究センター(“CDER”)は改正された1938年の連邦食品、薬物と化粧品法案(“FDCA”)、公衆衛生サービス法と他の連邦法規と条例に基づいて、薬品を厳格に審査した。米国で新薬製品をマーケティング·販売するためには、まずそれをテストし、これらのテストを通じてCDER証拠を送信して、この薬剤が予期される用途に使用されることが安全かつ有効であることを証明しなければならない。大多数の症例において、これらのテストは広範な臨床前、臨床と実験室テストを含む。CDER医師、統計学者、化学者、薬理学者と他の科学者からなるチームは同社のデータを審査し、ラベルを提出した。この独立して偏らない審査が、1つの薬剤の健康利益がその既知のリスクよりも大きいと決定した場合、薬剤の販売が許可される。CDER自体は薬物を試験しないが,薬物の質,安全性,有効性基準については限られた研究が行われている。新薬または上場申請を承認する前に、FDAは薬物の開発業者(“スポンサー”)、そのCROおよび/またはその臨床試験場所に対して承認前検査を行うことができ、臨床、安全性、品質管理および他の規制された活動が特定の非臨床毒理学研究のGCPまたは良好な実験室規範(GLP)に適合することを確保することができる。GMPに適合した製造プロセスや製品を生産するための製造施設もFDAの継続検査を受けなければならない。FDAはまた、承認された製品の効果を監視するために、または製品の商業アプリケーションを制限する可能性のある任意の承認に条件を適用するために、検証性試験、発売後試験、および/または追加の監視を要求することができる。承認されると、医薬品または生物製品のラベル、広告、販売促進、マーケティング、および流通は、FDAの法規的要件に適合しなければならない。
| 38 |
FDAが最終的に新しい生物或いは薬物を承認するために必要な第一段階は臨床前研究を完成することを含み、スポンサーは動物に新薬の毒性をテストしなければならない。多様な種を用いて調査および/または研究されている化合物の安全性と有効性に関する基本情報を収集した。FDAは一連の現在のGLP法規と呼ばれる法規及び連邦法規第21部分Dサブ章中の法規要求に基づいて臨床前研究を監督する。スポンサーがこれらの規定に違反した場合、FDAは、スポンサーにこれらの研究の複製を要求することができ、またはスポンサーに対して法執行行動または以下にさらに説明する処罰をとることができる。スポンサーは、その後、薬物の成分および製造、および人体上で薬物を試験する計画を含むIND申請を予備試験の結果に基づいてFDAに提出する。FDAは提案された研究(臨床試験)が人体を不合理な傷害リスクに置かないことを保証するためにIND を審査した。FDAはまた が十分なインフォームドコンセントと人間主体が十分に保護されているかどうかを検証している。
スポンサーがIND申請を提出した後、FDAがこの展望的研究を審査する時間があるように、30(30)日待たなければならない。FDAが問題を発見すれば,臨床放置を命じて調査を延期したり,研究中に問題が発生した場合に臨床試験を中断することができる。IND申請が発効した後,スポンサーは人体臨床試験を開始することができる。スポンサー は通常3つの連続段階に分けて人体臨床試験を行うが,この3段階が重なる可能性がある。第1段階試験では、スポンサーは、主に1剤または多剤の安全性である少量の患者または健康ボランティア(通常は20~80人の健康ボランティア)で製品を試験する。この段階の目標は,薬物の最も一般的な副作用が何であるか,薬物がどのように代謝·排泄されているかを決定することである。第1段階研究で許容できない毒性が認められなければ,第2段階研究を開始する。第2段階では,スポンサー は安全性に加えて,第1段階試験よりやや大きい患者群におけるこの製品の治療効果を評価した。第2段階研究の対象数は通常数十人から約300人まで様々である.この段階は、ある疾患または状態を有する人に薬物が有効であるかどうかの初歩的なデータを得ることを目的としている。第2段階の終了時に、FDAとスポンサーは、第3段階の大規模研究をどのように行うかについて合意しようとしている。
第2段階で有効性の証拠が示された場合、第3段階研究が開始される。第3段階試験は、一般に、拡大した集団における追加の安全性試験および臨床効果(約疾患または疾患を有するボランティア300~3,000人)が、地理的に分散された試験地点br}を有する。スポンサーは,各臨床試験が開始される前に,臨床計画や“案”をFDAに提出し,試験に参加する機関の承認を添付しなければならない。FDAはいつでも臨床試験の一時的または永久的な停止を命令することができる。
癌候補製品の場合、最初の人体テストは、健康なボランティアではなく、疾患患者に行われる可能性がある。これらの患者はすでに目標疾患に悩まされているため、このような研究は伝統的に第二段階の研究で得られた結果を提供する可能性がある。したがって,これらの研究は一般に2段階を組み合わせているため“段階1/2”研究と呼ばれる.患者が最初の人体試験に参加して1/2期研究を行っても,スポンサーは通常1期と2期研究で得られたすべてのデータを得る責任がある。
スポンサーは臨床前と臨床試験の結果,製品製造や成分に関する詳細な情報をFDAに提出しなければならないが,形式は新薬申請(“NDA”)または生物製品ライセンス申請(“BLA”)である。1年以上を要する可能性のあるプロセスにおいて、FDAは、新規化合物が特定の適応に対して安全に有効であることを示すのに十分なデータがあり、他の適用要件を満たしていると考えられる場合、薬剤または生物学的薬剤の発売を承認するのに十分なデータを有する。この承認過程に要する時間 は,提出文書の質と提出された研究報告 と,この化合物の疾患に関する治療改善への潜在的な貢献を含む複数の変数に依存する。
FDA 提供激励措置例えば、孤児薬物指定または小児科専有権。孤児薬物指定は、米国で200,000人未満に影響を及ぼす稀な疾患または障害を安全かつ効率的に治療、診断または予防するためにFDA孤児医薬製品事務室から付与された、または200,000人を超えるが、治療薬の開発およびマーケティングのコストを回収できないと予想される新薬または生物製品である。この薬剤が適応を指定するために最初に許可された薬剤である場合、または優れた安全性、br}治療効果、または患者ケアへの大きな貢献を示す場合、指定は、以前に同じ適応指定を受けた他の同種の薬剤ではなく、スポンサーに7年間の米国市場排他期brを提供する。成長ホルモン欠乏症を評価するためのMacrilen(Macimorelin)の孤児薬名を得た。
1984年の“薬品価格競争と特許期限回復法”(“ハッジ-ワックスマン法”)によれば、新たに承認された薬品および適応は、法定の非特許データ独占期から利益を得ることができる。ハッジ·ワックスマン法“は、新しい化学物質(NCE)秘密保持協定の承認を得た最初の申請者に、同じ活性医薬成分または活性部分を含む任意の他の薬剤が以前に承認されなかったことを意味する5年間のデータ排他性 を提供する。“ハッジ·ワックスマン法案”の保護は、別の完全なセキュリティ協定の提出または承認を阻止しないにもかかわらず、このようなセキュリティ協定申請者は、安全性および有効性を証明するために、自身の臨床前かつ十分な、制御された良好な臨床試験を行うことを要求される。
| 39 |
ハッジ-ワックスマン法“はまた、505(B)(2)条の既存の薬剤の新しい適応、剤形、投与経路または強度に関する出願、またはBr}の新しい用途のための出願を含む新しいNDAの承認のための3年間のデータ排他性を提供し、FDAがスポンサーが提供またはスポンサーが支援する新しい臨床研究が承認申請に重要であると判断した場合、br}を含む。この独占性は臨床研究独占性と呼ばれることがあり,スポンサーが安全性と有効性を証明するために十分な制御良好な臨床試験を行っていれば,この独占性は別の申請の承認を阻止することもなく,承認された薬物製品を含まない排他的保護変更を承認する後発薬を阻止することもない。
薬品または生物製品のラベル、広告、販売促進、マーケティングおよび流通はFDA法規のbr要求に適合しなければならない。適用された要求を遵守しないことは、FDAが生産および出荷を停止することを要求する可能性があり、場合によっては、メーカーは製品をリコールしたり、差し押さえ、禁止、刑事起訴を含む法執行行動を取ったりする可能性がある。これらの失敗は、FDAが製品のマーケティング承認を撤回することにもつながる可能性がある。要求を満たしてFDAに料金 を払えば,製品は市場に残ることができ,更新プログラムはない.
カナダ。 カナダでは,カナダ衛生局治療製品局はカナダ連邦当局であり,人間用の薬物や医療機器の管理を担当している。市場の許可を得る前に、スポンサーは製品の安全性、有効性と品質が“食品と薬品法”及びその他の法律法規の要求に符合することを証明するために、実質的な科学的証拠を提供しなければならない。カナダの薬品開発と販売に対する要求 は米国とほぼ類似しており,上記のようになっている。
EUですEUでは、集中認可手順(CP)または国家認可手続きを使用して医薬品を許可することができる。欧州連合はすでに欧州医薬品局が調整したヒト薬物承認の集中的な手続きを実施しており、これはEUおよびアイスランド、リヒテンシュタイン、ノルウェーで有効な欧州委員会が発行した単一のマーケティング許可を招いた。HIV/エイズ、癌、糖尿病、神経変性疾患、自己免疫疾患、他の免疫機能障害、ウイルス性疾患、または孤児br医薬製品として指定された新しい活性物質を含むヒト医薬製品の場合、集中手順を実行しなければならない。また,バイオテクノロジー過程や遺伝工学からの製品タイプにもCPが必要である。これらのカテゴリに属さない医薬品の場合、関連する薬剤が重大な治療、科学的または技術的革新である限り、またはその許可が公衆の健康に有利である限り、出願人は、集中販売許可出願をEMAに提出することを選択することができる。
いくつかのEU諸国/地域に2種類の許可医薬製品の国家経路があり、集中プログラムの範囲に属さず、国家マーケティング許可を招く研究薬物製品に適用される
| ● | 分散した プログラム.分散したプログラムを使ってスポンサーは、1つ以上のEU諸国で同時に許可を申請することができます。brは、どのEU諸国でも許可されておらず、集中プログラムの強制範囲に属さない薬品を申請することができます。関連された各会員国によってそれぞれ が付与されるだろう。プログラムを相互認識する。相互認識手続きでは、EU加盟国の国家手続きに基づいて、薬品はまずその加盟国で許可される。その後、関連国が国家マーケティング許可正本の有効性を認めることに同意したプログラムにおいて、他のEU諸国/地域 にさらなるマーケティング許可を求めることができる。 | |
| ● | 国 プログラム。1つの国/地域でのみ単独で承認を求める場合、販売許可申請は、その加盟国の主管当局に直接提出される。 |
| 40 |
アメリカと同様にEMAは激励措置孤児薬の開発や小児科用に使用されている。EUでは、10,000人に5人の病気が孤児の称号を与えられている。この指定があれば,スポンサーは延長された市場排他性 (10年)と費用減免の恩恵を受けることになる。
小児科条例は小児科発展を許可し、補充保護証明書を6ケ月延長した。
EUマーケティング許可の有効期間は5年で、MAH申請後に更新することができます。更新後、承認は永久的に有効です
ビジネス運営条例
人間の薬品メーカーのマーケティング、販売促進と定価のやり方及びメーカーが調達業者と処方者と相互作用する方式 は各種のアメリカ連邦と州法律の制約を受けて、連邦反リベート法規と 虚偽クレーム法案、及びリベート、虚偽クレーム、不公平貿易やり方と消費者保護を管理する州法律、及び他の国/地区の類似法律を含む。米国では,これらの法律は司法省(DoJ),衛生·公衆サービス部監察長事務室,連邦貿易委員会,人事管理事務室,州総検事長などによって実行されている。過去数年間、FDA、米国司法省、他の多くの機関は製薬会社に対する法執行活動を増加させ、法執行活動の機関間協調を強化した。
米国では,生物製薬や医療機器メーカーは,勤務医や教育病院への任意の価値移転を記録し,衛生·公衆サービス部(HHS)にこのようなデータを開示することを要求されている。医師や教育病院に価値移転を報告していない民事罰のほか,メーカーが故意に虚偽の陳述をしたり,このような報告から情報を排除したりすれば,刑事罰を受ける。バイオ製薬会社および医療機器会社の支払いデータは、衛生·公衆サービス部によって公開されたサイトに公開されている。詐欺と乱用調査員、業界評論家とメディアのこのようなデータへのより多くのアクセスは人々の報告実体との協力に対する関心を引き起こし、そして重要に機会を提供し、新薬の開発と科学情報の交換における著者らの協力の重要な性質を強調する。この全国的な支払い透明性努力に加え、自発的な行動基準(例えば“PhRMAと医療保健専門家との相互作用規則”および“処方薬消費者広告に関するPhRMAの指導原則”)の維持に対する業界の約束と、厳格な内部訓練およびコンプライアンス努力は、既存の法律法規と相互補完し、道徳的協力および真の製品コミュニケーションの確保を助けるであろう。
カナダ研究型製薬会社協会(“Rx&D”)は“利害関係者支援透明性ガイドライン”を採択し,メンバー会社に定期的にウェブサイトと年次報告書を介して直接援助したすべての利害関係者のリストを開示することを求めた。“利害関係者”という言葉は、Rx&Dの“道徳実践規則”において“衛生保健専門家”を含むように定義されている。EUでは,欧州製薬工業·協会連合会(EFPIA)が採択した医療専門家や組織への移転価値の開示コードは,br}EFPIAの全メンバーが2016年から保健専門家や医療組織への移行の価値を開示し,br}2015年の関連移転を含むことを求めている。各メンバー会社は、(I)支払いまたは他の価値移転を受けた医療専門家および協会の名前、ならびに(Ii)移転の金額または価値、ならびに関係タイプを記録して開示することを要求されるであろう。
当社の業務運営に関する規制リスクに関するより多くの情報は、“プロジェクト3 D”を参照されたい。リスク要因です“
知的財産権 特許
我々は,特許,商業秘密,技術ノウハウの組み合わせにより,我々の主要薬物や候補薬物の化合物,製造プロセス,成分,医療用途方法を保護することを求めている。私たちの特許の組み合わせは、約6つの所有および許可内の特許シリーズを含む(米国、ヨーロッパ、および他の司法管轄区域で発行され、付与されているか、または承認を待っている)。バイオテクノロジーと製薬業界会社の特許地位は高度に不確定であり、複雑な法律と事実問題に関連している。したがって、私たちは、私たちの任意の特許出願が許容される可能性のあるクレーム範囲(もしあれば)を予測することもできませんし、私たちが許可する任意の特許の実行可能性を予測することもできません。 は“3.D.項目のリスク要因-私たちの知的財産権を介して私たちの製品に十分な保護を提供できないかもしれません”を参照してください
| 41 |
特許 は、特許出願又は付与された日及び特許保護を受けた各国/地域の特許の法的期限に応じて延長される。特許提供の実際の保護は国によって異なり,これは特許の種類,そのカバー範囲,その国の法的救済措置に依存する。米国では,FDA承認された薬物をカバーする特許の特許期間も延長する資格があり,これによりFDA規制審査過程で失われた特許期間の補償 として特許期間の回復を可能にしている。“ハッジ·ワックスマン法”は、特許期間が特許満了後最大5年間の延長を可能にし、特許が満期になり、FDAが機密協定を承認していない場合、特許権者は5年以内に年間臨時延期出願を提出することができる。特許期間の延長時間の長さは,薬物規制審査を受ける時間の長さと関係がある。特許延期は,特許の残期限を製品承認日から合計14年間延長することはできず,承認された薬物に適用される特許を1つ延長することしかできない。
ヨーロッパや他の外国司法管轄区域にも同様のbr条項があり、承認薬物をカバーする特許の有効期限を延長する。しかし、これらのbr司法管轄区では、一時的な延期は存在せず、特許が満期になる前に上場を許可しなければならない。将来的には、米国以外ではこれらの製品のための特許期間の延長が予想されます。このような特許期限の延長は承認される可能性がありますが、このような特許期限 が米国、ヨーロッパ、または他の管轄区域で延長される正確な時間長は予測できません。もし私たちがより長い時間で製品特許の特許期間を延長することができなければ、私たちは利益を達成したり維持することができないかもしれません。これは私たちのビジネスに悪影響を与えます。
特許保護に加えて、我々の製品は、NCE独占性または新しい処方独占性のような“孤児薬物条例”に含まれる市場排他性条項またはFDA法案の小児科独占性条項または他の条項から利益を得ることができる。br}孤児医薬品法規は、製薬およびバイオテクノロジー会社が、まれな疾患の治療のための薬物brを開発および生産することを奨励し、現在、米国患者が200,000人未満の疾患として定義されているか、または米国の200,000人を超えるが、実際にスポンサーが純利益を生じないことが予想される疾患に影響を与える。これらの規定によると、孤児薬を指定したメーカーは税収優遇を求めることができ、FDAが指定孤児製品の保有者がFDAの承認を受けた孤児製品の7年間の市場排他期を初めて承認する。米国では、FDAは、スポンサーが子供または青少年の集団で指定された試験を行う許可された薬剤に追加のデータ保護を付与する権利がある。許可された場合、この小児科専門権は、これらの保護が満了していない限り、6ヶ月のデータ保護期間および任意の関連特許の有効期間を追加的に提供する。私たちはまた、EUのような他の地域の市場排他性 を利用することを求めることができる。私たちの任意の候補薬物が米国、EU、または任意の他の地域でこのような孤立した薬物指定、小児科独占特許、NCE独占特許、または任意の他の市場独占特許を獲得することは保証されず、特定の国または地域でのこのような薬物の規制承認を得て、いかなる市場独占保護の資格を得る資格があるbr}であることも保証されない。
Macrilen (Macimorelin):
フランス国立科学研究センター(CNRS)とライセンス側としてAEZSドイツとの独占ライセンス契約に基づき,我々 はMacimorelinの世界的権利を持っている。CNRSへの純売上高特許権使用料の支払い義務は2022年に満期となる。Macrilen は,ライセンスプロトコルに基づいて米国とカナダで商業化許可されたMacimorelinの承認商標である.
以下の特許および特許出願はMacimorelinに関連している:
| ● | 米国特許第8,192,719号は、複方マキモレリンの経口投与および試料中の成長ホルモンのレベルを測定し、評価することを含む、ヒトまたは動物の下垂体関連成長ホルモン欠乏症を評価する方法を含む試料中の成長ホルモン含量 は成長ホルモン欠乏症を示した。この特許は2027年10月に満期になるだろう。 |
| 42 |
| ● | 欧州特許第1,984,744号は、Macimorelinの経口投与によって下垂体に関連するGHDを評価する方法をカバーしている。この特許は2027年2月に満期になるだろう。 | |
| ● | 日本特許第4,852,728号は、Macimorelinを経口投与することにより下垂体に関連するGHDを評価する方法をカバーしている。この特許は2027年2月に満期になるだろう。 | |
| ● | 欧州特許1,289,951によれば、ドイツ、イギリス、フランス、イタリア、スペイン、オランダ、デンマークは、5年間の補足保護証明書(SPC)出願を承認している。 |
ドイツAEZSの発明家は、Macimorelinを含む組成物を用いて成人GHDを評価する発明を発明した。
| ● | 関連する米国仮特許出願シーケンス番号62/607,866は2017年12月19日に提出され、シーケンス番号62/609,059は2017年12月21日に提出された。両方とも同じであり、 は、組成物を含むMacimorelin を経口投与することと、1~2つの投与後サンプルを収集することとを含むGHDを評価する方法を対象とする。 | |
| ● | 非仮米国出願15/993,507は2018年5月30日に提出され、この2つの仮出願の優先権 が作成された。関連する米国特許10,288,629は2019年5月14日に付与され、2038年5月30日に満期になる。特許協力条約PCT/EP/2018年/085622号出願は12月18日に提出された。GHDを評価する方法は、成分を含むMacimorelin を経口投与するステップと、1つまたは2つの投与後サンプルを採取するステップとを含み、PCT申請 は、3つの投与後サンプルを用いてGHDの同様の方法を評価することをさらに含む。2022年2月24日欧州特許出願18827044.1を審査した後Macimorelin含有組成物を経口投与し、投与後の1つまたは2つの試料を採取することを含む、“成長ホルモン欠乏症を評価する方法”という欧州特許が認可された。この特許は2022年3月23日に欧州特許公報 に公開される。ヨーロッパ特許はヨーロッパ共同体によって承認されたラベルに基づいて、成人GHD診断のためのMacimorelinの使用をカバーしている。この欧州特許は12のヨーロッパ諸国で検証されている。29個のヨーロッパ諸国で、この特許は国有化された。 |
ドイツAEZSの発明者は、Macimorelinを含む組成物を用いて小児GHDを評価する発明を発明した。本発明は、成長ホルモン分泌を誘導するのに十分な量のMacimorelinを投与した後、約15~約100分の範囲で対象から取得し、各血液試料の成長ホルモンレベルを測定し、そのレベルを単一の閾値と比較してGHD診断を行うことを含む方法に関する。本発明の方法は、独立試験である。
| ● | 米国は2020年7月22日にシリアル番号63/054,889に関する仮申請を提出し,Macimorelinを用いた児童成長ホルモン欠乏の評価を求めた。 | |
| ● | 番号17/375,709の非仮米国出願は2021年7月14日に提出され,その名は“Macimorelinを用いて小児成長ホルモン欠乏症を評価する”と呼ばれ,仮申請の優先順位が決定された。 | |
| ● | 文書番号PCT/EP 2020/070691の国際PCT出願は2020年7月22日に提出された。PCT申請に基づいて、適時にいくつかの国家申請を提出した。 |
| 43 |
特許出願 はパイプ拡張機会に関連しており,AEZSドイツとライセンス者間の個別特許とライセンスプロトコルによって保護されている。
| ● | 副甲状腺ホルモン融合ポリペプチドの遅延除去による成人副甲状腺機能低下症の治療 | |
| ● | 我々の許可側は2017年4月27日に巻頭番号GB 1706781.0の優先特許出願をシェフィールド大学に提出した。特許出願は、副甲状腺機能低下症および骨粗鬆症の治療における受容体ポリペプチドを含む長時間作用性副甲状腺ホルモン様融合ポリペプチドおよびその使用を提供する。副甲状腺ホルモン融合ポリペプチド“国際特許出願は、PCT/GB 2018/051120である2018年4月27日に出願された。16/608,611の米国特許出願が2019年10月25日に提出され、2020年5月28日にUS 2020/0164033 A 1として発表された。関連する米国特許US 11,344,607は2022年5月31日にライセンスを取得した。 |
目的生物製品:標的、高度に特異的な自己免疫調節療法
| ● | 我々の許可側ヴェルツブルク大学は,2017年5月23日に特許番号EP 17172444.6の優先特許出願を提出した.本発明は、定義されたポリペプチドと、非古典的MHCクラス1 b分子の1つ以上のドメインを含むタンパク質、またはMHCクラス1 b分子とその受容体との相互作用を妨害する分子との組み合わせの標的免疫調節作用に関する。PCT/EP 2018/063100番号の国際PCT出願 は、2018年5月18日に提出され、標的治療のためのMHCクラス1 b分子とポリペプチドとの組み合わせ と命名された。この出願は、2018年11月29日にWO 2018/215340 A 1として発表された。届出番号16/615,188の米国国申請は2019年11月20日に提出され、2020年5月21日にUS 2020/0157175 A 1の名称で発表された。 | |
| ● | 我々の許可側ヴェルツブルク大学は2022年3月24日に特許番号EP 22164161.6の優先特許出願を提出した。この特許出願は,視神経脊髄炎スペクトル障害(NMOSD)を治療する新しい方法として,MHC Ibを介した水チャネル蛋白4(AQP 4)特異的免疫抑制に対する治療蛋白を提供している。 | |
| ● | 我々の許可側ヴェルツブルク大学は2022年3月24日に特許番号EP 22164123.6の優先特許出願を提出した。本発明は、MHCクラスIb分子とポリペプチド抗原との組み合わせによるパーキンソン病の治療用途に関する。 |
| C. | 組織構造 |
当社の会社構造、私たちの直接·間接子会社の登録司法管轄区域、および2022年12月31日現在、これらの子会社で保有している株式パーセント は、タイトル“4.A.当社の歴史と発展”の下のグラフを参照してください。
| D. | 財産 と設備 |
私たちの登録住所はカナダトロントにあります。私たちの最大の事務所はドイツのフランクフルトにあり、サウスカロライナ州のサマービルにはもう一つの事務所があります。私たちには不動産は何もありません。当社は2022年9月30日から、その所有者と共にドイツ子会社の既存建築賃貸契約を1年プラス6ヶ月延長する通知に同意し、2024年3月31日まで継続している。
次の表に2022年12月31日までの私たちの主要施設に関する情報を示します。
| 位置 | 空間を使用する | 正方形 素材 | 興味のあるタイプ | |||
| サウスカロライナ州サマーヴェルシグマ通り315号、郵便番号:29486 | 占有管理 | 168 | 賃借権 | |||
Weismülerstr. 50 D-60314 ドイツのマイン川のほとりフランクフルト |
管理、研究開発、業務開発、行政のためにbrを占有する | 7,319 | 賃借権 |
私たちは私たちの既存の施設が私たちの持続的な需要を満たすのに十分だと信じている。
| 44 |
| プロジェクト 4 A | 未解決 従業員意見 |
は要りません。
| 五番目です。 | 運営 と財務回顧と展望 |
主な発展
| A. | 経営実績 |
連結財務状況データレポート
| 12月31日の として、 | ||||||||||||
| 2022 | 2021 | 2020 | ||||||||||
| (単位:千) | $ | $ | $ | |||||||||
| 現金 と現金等価物 | 50,611 | 65,300 | 24,271 | |||||||||
| 取引 およびその他の入金およびその他の流動資産 | 4,648 | 5,447 | 3,322 | |||||||||
| 在庫品 | 229 | 73 | 21 | |||||||||
| 制限された 現金等価物 | 322 | 335 | 338 | |||||||||
| 財産 と設備 | 216 | 192 | 179 | |||||||||
| その他 非流動資産 | — | 8,755 | 8,874 | |||||||||
| 総資産 | 56,026 | 80,102 | 37,005 | |||||||||
| 売掛金(Br)および未払い負債と所得税対応 | 3,936 | 2,787 | 2,322 | |||||||||
| 準備されている現在のbr部分 | 45 | 34 | 92 | |||||||||
| 繰延収入の現在 部分 | 2,949 | 4,815 | 2,193 | |||||||||
| レンタル負債 | 179 | 161 | 184 | |||||||||
| 非金融 非流動負債(1) | 13,141 | 19,319 | 19,003 | |||||||||
| 総負債 | 20,250 | 27,116 | 23,794 | |||||||||
| 株主権益 | 35,776 | 52,986 | 13,211 | |||||||||
| 総負債と株主権益 | 56,026 | 80,102 | 37,005 | |||||||||
(1) 主に従業員の未来の福祉、繰延収益、繰延収入の非当期部分と準備金から構成される。
最近の会計声明
国際財務報告基準(Br)は発表されたが発効していない公告
いくつかの新しい会計基準、会計基準修正案、解釈が発表されており、2022年12月31日の報告期間については強制的ではなく、会社によって事前に採用されていない。これらの基準、改訂、または解釈は、現在または未来の報告期間内にエンティティに実質的な影響を与えず、予測可能な未来の取引に実質的な影響を与えないと予想される。
金融リスク要因と他のツール
我々は、2022年と2021年12月31日まで、および2022年、2021年および2020年12月31日までの監査総合財務諸表付記24において、信用リスク、流動性リスク、市場リスクを含む金融商品に発生するリスクの性質と程度、およびこれらのリスクをどのように管理するかを説明した本年度報告書の表20−Fの第17項− “財務諸表に含まれる.
| 45 |
運営結果
損失表と包括損失情報を統合する
3か月まで 十二月三十一日 | 年限 終わり 十二月三十一日 | |||||||||||||||||||
| (単位:千) | 2022 | 2021 | 2022 | 2021 | 2020 | |||||||||||||||
| $ | $ | $ | $ | $ | ||||||||||||||||
| 収入.収入 | 2,485 | 956 | 5,640 | 5,260 | 3,652 | |||||||||||||||
| 運営費用 | ||||||||||||||||||||
| 販売コスト | 51 | 18 | 157 | 90 | 2,317 | |||||||||||||||
| 研究開発 | 4,425 | 1,863 | 12,506 | 6,574 | 1,506 | |||||||||||||||
| 販売、 一般と管理 | 2,012 | 2,206 | 8,230 | 7,267 | 5,893 | |||||||||||||||
| 修正住宅賃貸収益 | — | — | — | — | (219 | ) | ||||||||||||||
| 無形資産減価 | 584 | — | 584 | — | — | |||||||||||||||
| 営業権減価 | 7,642 | — | 7,642 | — | — | |||||||||||||||
| その他の資産の減価 | 124 | — | 124 | — | (139 | ) | ||||||||||||||
| 運営費総額 | 14,838 | 4,087 | 29,243 | 13,931 | 9,358 | |||||||||||||||
| 運営損失 | (12,353 | ) | (3,131 | ) | (23,603 | ) | (8,671 | ) | (5,706 | ) | ||||||||||
| 外貨レート変動による収益 (損失) | (98 | ) | 257 | 879 | 215 | 572 | ||||||||||||||
| 権証負債の公正価値変動 | — | — | — | — | 1,147 | |||||||||||||||
| その他 財務コスト | — | — | (3 | ) | (21 | ) | (736 | ) | ||||||||||||
| 純財務収入(コスト) | (98 | ) | 257 | 876 | 194 | 983 | ||||||||||||||
| 所得税前損失 | (12,451 | ) | (2,874 | ) | (22,727 | ) | (8,477 | ) | (4,723 | ) | ||||||||||
| 収入 税金の払い戻し | — | (20 | ) | — | 109 | (395 | ) | |||||||||||||
| 純損失 | (12,451 | ) | (2,894 | ) | (22,727 | ) | (8,368 | ) | (5,118 | ) | ||||||||||
| 基本 と希釈して1株当たり損失 | (2.56 | ) | (0.63 | ) | (4.68 | ) | (1.82 | ) | (3.11 | ) | ||||||||||
収入.収入
我々は,顧客とのライセンス·連携協定(ライセンス料,マイルストーン収入,特許権使用料),開発サービスの提供,ある活性薬剤成分の販売(“原料薬”),半製品と完成品 およびあるサプライチェーン活動から収入を得ており,これらの活動には,主に顧客と締結された基礎契約に規定されている原料薬の量産に関する安定性研究や開発活動の監督または監督支援サービスが含まれている。
| 12月31日までの3ヶ月間 | ||||||||||||||||
| (単位:千) | 2022 | 2021 | 変わる | 変わる | ||||||||||||
| $ | $ | $ | % | |||||||||||||
| 収入.収入 | ||||||||||||||||
| 許可証料 | 873 | 361 | 512 | 142 | % | |||||||||||
| サービスを開発する | 1,526 | 528 | 998 | 189 | % | |||||||||||
| 印税収入 | 44 | 21 | 23 | 110 | % | |||||||||||
| サプライチェーン チェーン | 42 | 46 | (4 | ) | -8 | % | ||||||||||
| 総収入 | 2,485 | 956 | 1,529 | 160 | % | |||||||||||
2022年12月31日までの3カ月間の総収入は250万ドルであり,2021年同期の100万ドルに比べて150万ドル増加したのは,主にライセンス料が50万ドル増加したことと,Novoとの開発サービスが100万ドル増加したためである。
| 12月31日までの12ヶ月間 | ||||||||||||||||
| (単位:千) | 2022 | 2021 | 変わる | 変わる | ||||||||||||
| $ | $ | $ | % | |||||||||||||
| 収入.収入 | ||||||||||||||||
| 許可証料 | 1,704 | 1,670 | 34 | 2 | % | |||||||||||
| サービスを開発する | 3,617 | 3,337 | 280 | 8 | % | |||||||||||
| 製品販売 | 57 | — | 57 | 100 | % | |||||||||||
| 印税収入 | 101 | 68 | 33 | 49 | % | |||||||||||
| サプライチェーン チェーン | 161 | 185 | (24 | ) | -13 | % | ||||||||||
| 総収入 | 5,640 | 5,260 | 380 | 7 | % | |||||||||||
2022年12月31日までの12カ月間の総収入は560万ドルだったが、2021年同期は530万ドルと30万ドル増加したが、これは主にNovoとの開発サービスが30万ドル増加したためである。
| 46 |
研究開発費
次の表は、指定された時間帯で発生した研究開発費(金額は千単位ですが、 パーセントは含まれていません):
| 12月31日までの四半期 、 | ||||||||||||||||
| (単位:千) | 2022 | 2021 | 変わる | 変わる | ||||||||||||
| $ | $ | $ | % | |||||||||||||
| Macrilen (Macimorelin)小児科試験(DETECT−TRAIL)直接研究開発費 | 1,297 | 526 | 771 | 147 | % | |||||||||||
| AEZS-130直接研究開発費 | 1,004 | 143 | 861 | 602 | % | |||||||||||
| DC−PTH 直接研究開発費 | 697 | 63 | 634 | 1,006 | % | |||||||||||
| パーキンソン病直接研究開発費 | 155 | 171 | (16 | ) | -9 | % | ||||||||||
| 新冠肺炎は研究開発費を直売する | 222 | 137 | 85 | 62 | % | |||||||||||
| NMOSD 直接研究開発費 | 320 | 106 | 214 | 202 | % | |||||||||||
| クラミジア感染直接研究開発費 | 295 | 108 | 187 | 173 | % | |||||||||||
| 追加のbr計画の直接研究開発費 | 27 | 249 | (222 | ) | -89 | % | ||||||||||
| 直接研究開発費総額 | 4,017 | 1,503 | 2,514 | 167 | % | |||||||||||
| 従業員に関する費用 | 311 | 335 | (24 | ) | -7 | % | ||||||||||
| 施設、減価償却、その他の費用 | 97 | 25 | 72 | 288 | % | |||||||||||
| 合計する | 4,425 | 1,863 | 2,562 | 138 | % | |||||||||||
2021年12月31日までの四半期と比較して,2022年12月31日までの四半期の研究開発費が260万ドル増加したのは,主に直接研究開発費が250万ドル増加したためである。直接研究開発費 には、試験を検出する契約研究機関、契約メーカー、コンサルタントなど、第三者との手配に基づいて発生する費用が含まれる。2022年12月31日までの四半期に直接研究開発費総額が250万ドル増加したのは,DETECT試験のコストが80万ドル増加したことと,我々が大学と協力した新たな臨床前プロジェクトの費用が170万ドル増加したためである。また,同社は2022年12月31日までの四半期に新冠肺炎とクラミジアワクチン試験の開発を中止した。これまで資本化されていたこの2つの試験に関連するライセンス前払いは212ドルであり、以下に述べるように完全に減少している。
2022年第4四半期、会社が患者を募集して検査試験に参加する数は著しく増加し、コストは前年より増加し、当時会社は主に検査試験中の患者登録のためにテストサイト を構築することに集中した。DETECT試験以外に、同社はその大学研究パートナーと協力して命名の臨床前プロジェクトを積極的に展開している。前年と比較して,これらのプロジェクトの支出増加は主にこれらのプロジェクトの推進,特に2021年に許可されたAEZS−150とDC−PTHプロジェクトによるものである。
| 47 |
次の表は、指定された時間帯で発生した研究開発費(金額は千単位ですが、 パーセントは含まれていません):
| 12月31日までの年間 、 | ||||||||||||||||
| (単位:千) | 2022 | 2021 | $ 変更 | 変わる | ||||||||||||
| $ | $ | $ | % | |||||||||||||
| Macrilen (Macimorelin)小児科試験(DETECT−TRAIL)直接研究開発費 | 3,818 | 3,244 | 574 | 18 | % | |||||||||||
| AEZS-130直接研究開発費 | 2,514 | 230 | 2,284 | 993 | % | |||||||||||
| DC−PTH 直接研究開発費 | 1,999 | 154 | 1,845 | 1,198 | % | |||||||||||
| パーキンソン病直接研究開発費 | 657 | 171 | 486 | 284 | % | |||||||||||
| 新冠肺炎は研究開発費を直売する | 527 | 712 | (185 | ) | -26 | % | ||||||||||
| NMOSD 直接研究開発費 | 637 | 453 | 184 | 41 | % | |||||||||||
| クラミジア感染直接研究開発費 | 623 | 146 | 477 | 327 | % | |||||||||||
| 追加のbr計画の直接研究開発費 | 262 | 486 | (224 | ) | -46 | % | ||||||||||
| 直接研究開発費総額 | 11,037 | 5,596 | 5,441 | 97 | % | |||||||||||
| 従業員に関する費用 | 1,199 | 839 | 360 | 43 | % | |||||||||||
| 施設、減価償却、その他の費用 | 270 | 139 | 131 | 94 | % | |||||||||||
| 合計する | 12,506 | 6,574 | 5,932 | 90 | % | |||||||||||
R2021年12月31日までの年度と比較して,2022年12月31日までの年間研究·開発費は590万ドル増加し,主に直接研究·開発費が540万ドル増加したためである。直接研究開発費には、検査試験の契約研究機関、契約メーカー、 やコンサルタントなど、第三者との手配で発生した費用が含まれている。2022年12月31日までの年度,直接研究開発費総額が540万ドル 増加したのは,主にDETECT試験のコストが600万ドル増加したことと,我々が大学と協力した新たな臨床前プロジェクトに関する費用が480万ドル増加したためである。2022年には、同社は新たな臨床サイトの開設を加速し、検査試験に参加する患者の募集を開始したのに対し、2021年には患者の募集を開始していない。DETECT試験に加え,同社では年間を通して6つの臨床前プロジェクトを実行しており,前年の6つの臨床前プロジェクトが許可されているのとは対照的である。最後に,同社は2022年12月31日までの四半期に新冠肺炎とクラミジアワクチン試験の開発を中止した。この2つの試験に関連する以前に資本化されたライセンス前払い212ドルは完全に減少しており、以下ではさらに議論される。
2021年12月31日までの年度と比較して,従業員に関する支出が2022年に40万ドル増加したのは,主に我々の研究開発チームが2名の上級メンバーを増加させたためである。
2021年と比較して、施設、減価償却、その他の費用は2022年に10万ドル増加し、主により高い相談や他のサービス関連費用から来ている。
| 48 |
販売、一般、管理費用
| 12月31日までの3ヶ月 | ||||||||||||||||
| (単位:千) | 2022 | 2021 | 変わる | 変わる | ||||||||||||
| $ | $ | $ | % | |||||||||||||
| 給料 と福祉 | 882 | 869 | 13 | 1 | % | |||||||||||
| 保険 | 420 | 406 | 14 | 3 | % | |||||||||||
| 専門費用 | 222 | 310 | (88 | ) | -28 | % | ||||||||||
| 相談料 | 89 | 184 | (95 | ) | -52 | % | ||||||||||
| その他 オフィスと一般料金 | 399 | 437 | (38 | ) | -9 | % | ||||||||||
| 販売、一般と行政費用の合計 | 2,012 | 2,206 | (194 | ) | -9 | % | ||||||||||
2022年12月31日までの3ヶ月間、私たちの販売、一般、行政費用の総額は200万ドルだったが、2021年の同時期は220万ドルで20万ドル減少した。この低下は主に専門費が10万ドル低下したことと相談費が10万ドル低下したためである。
| 12月31日までの12ヶ月間 | ||||||||||||||||
| (単位:千) | 2022 | 2021 | 変わる | 変わる | ||||||||||||
| $ | $ | $ | % | |||||||||||||
| 給料 と福祉 | 2,994 | 2,525 | 469 | 19 | % | |||||||||||
| 保険 | 1,678 | 1,040 | 638 | 61 | % | |||||||||||
| 専門費用 | 1,163 | 1,207 | (44 | ) | -4 | % | ||||||||||
| 相談料 | 682 | 688 | (6 | ) | -1 | % | ||||||||||
| その他 オフィスと一般料金 | 1,713 | 1,807 | (94 | ) | -5 | % | ||||||||||
| 販売、一般と行政費用の合計 | 8,230 | 7,267 | 963 | 13 | % | |||||||||||
2022年12月31日までの12ヶ月間、私たちの販売、一般、行政費用の総額は820万ドルだったのに対し、2021年の同時期は730万ドルと100万ドル増加した。この増加は主に賃金と福祉が50万ドル増加し、保険費用が60万ドル増加したが、他のオフィスや一般費用は10万ドル減少したためだ。
営業権と無形資産の減価
| 12月31日までの3ヶ月 | ||||||||||||||||
| (単位:千) | 2022 | 2021 | 変わる | 変わる | ||||||||||||
| $ | $ | $ | % | |||||||||||||
| 営業権減価 | 7,642 | — | 7,642 | 100 | % | |||||||||||
| 無形資産減価 | 584 | — | 584 | 100 | % | |||||||||||
| 8,226 | — | 8,226 | 100 | % | ||||||||||||
| 12月31日までの12ヶ月 | ||||||||||||||||
| (単位:千) | 2022 | 2021 | 変わる | 変わる | ||||||||||||
| $ | $ | $ | % | |||||||||||||
| 営業権減価 | 7,642 | — | 7,642 | 100 | % | |||||||||||
| 無形資産減価 | 584 | — | 584 | 100 | % | |||||||||||
| 8,226 | — | 8,226 | 100 | % | ||||||||||||
同社は2022年12月31日までの四半期に新冠肺炎とクラミジアワクチン試験の開発を中止した。この2つの試験に関連する以前に資本化されたライセンス前払い212ドルは完全に減少している。また,当社の年間営業権減価評価の一部として,営業権に割り当てられた現金発生単位グループ(“CGU”)の回収可能金額は,公正価値から販売コスト(“FVLCD”)モデルを引いて決定した。FVLCDは市場方法に基づいて決定し、市場データに由来し、市場参加者からの当社 がこのグループのCGUを販売して受け取ることができる価格に関する資料を含む。当社の評価によると、当社グループCGUの回収可能金額 は帳簿価値を下回っているため、その営業権および無形資産はそれぞれ減値費用7,642ドルおよび372ドルに計上されており、当社が総合財務諸表を審査して付記11で述べたように。
| 49 |
純財務収入(コスト)
2022年12月31日までの3ヶ月間の純財務コストは10万ドルであったが、2021年12月31日までの3ヶ月間の純財務収入は30万ドルであった。これは主に外貨収益(赤字)が30万ドル減少したためです。 2022年12月31日までの12ヶ月間、私たちの純財務収入は90万ドルでしたが、2021年同期は20万ドルと70万ドル増加しました。これは主に外貨 の貨幣種の変化による収益が70万ドル増加したためである.
純損失
2022年12月31日までの3ヶ月間に、総合純損失1,250万ドル、または普通株1株当たり2.56ドル(基本と希釈後)を報告し、2021年12月31日までの3ヶ月間の総合純損失290万ドル、または普通株1株当たり(基本と希釈後)0.63ドルの損失を報告する。純損失が960万ドル増加したのは,主に総運営費が1,080万ドル増加したことと,純財務収入(コスト)が30万ドル減少したことが収入150万ドル増加によって相殺されたためである。
Fあるいは2022年12月31日までの12ヶ月間、総合純損失2270万ドル、または普通株1株当たり4.68ドル(基本と希釈後)を報告し、2021年12月31日までの年度総合純損失840万ドル、または普通株(基本と希釈後)1.82ドルの損失を報告する。純損失が1,430万ドル増加したのは,主に運営費が1,530万ドル増加したためであるが,上記のように収入総額は30万ドル増加し,純財務収入は70万ドル増加し,この増加を相殺した。
選定された 四半期財務データ
| 3ヶ月まで ヶ月 | ||||||||||||||||
| (単位:千、1株当たりデータを除く) | 2022年12月31日 | 2022年9月30日 | 2022年6月30日 | 2022年3月31日 | ||||||||||||
| $ | $ | $ | $ | |||||||||||||
| 収入.収入 | 2,485 | 1,860 | (222 | ) | 1,517 | |||||||||||
| 純損失 | (12,451 | ) | (3,420 | ) | (4,216 | ) | (2,640 | ) | ||||||||
| 1株当たり純損失 (基本と希釈後)(2) | (2.56 | ) | (0.70 | ) | (0.87 | ) | (0.54 | ) | ||||||||
| 3ヶ月まで ヶ月 | ||||||||||||||||
| (単位:千、1株当たりデータを除く) | 2021年12月31日 | 2021年9月30日 | 2021年6月30日 | 2021年3月31日 | ||||||||||||
| $ | $ | $ | $ | |||||||||||||
| 収入.収入 | 956 | 1,052 | 1,584 | 1,668 | ||||||||||||
| 純損失 | (2,894 | ) | (1,932 | ) | (2,084 | ) | (1,458 | ) | ||||||||
| 1株当たり純損失 (基本と希釈後)(1) | (0.63 | ) | (0.40 | ) | (0.43 | ) | (0.38 | ) | ||||||||
| (1) | 1株当たり純損失は報告期間ごとの加重平均流通株数に基づいており、この数字は四半期によって異なる可能性がある。そのため、四半期1株当たり純損失金額の合計は年間1株当たり純損失に等しくない可能性がある。 |
歴史 運営と純損失の四半期業績は予測可能な傾向を反映した経常的収入或いは支出モードと見なすことができず、これは主に私たちの収入のいくつかの構成部分が非日常的な性質を持っており、純財務収入と為替損益の四半期変化は予測できないからである。
| 50 |
| B. | 流動性キャッシュフロー資源 |
流動性 と資本資源
Br社管理資本の目標は,十分な流動資金を確保し,研究開発コスト,販売費用,一般と行政費用および運営資金需要に資金を提供することである。過去数年間、私たちは公開と私募株式発行と発行を通じて資金を集め、許可と協力手配、これらの手配から得られた対価格と株式発行の収益はずっと私たちのものです流動性の主な源です当社の資本管理目標は往期と変わらない。配当に関する政策は,会社の製品開発組合を推進するために必要な活動を支援するために現金を保持し,出現可能な適切なビジネス機会brを求める際に求められるものである。当社はいかなる規制機関や他の外部源に加えられたいかなる資本要求も制約されません。
キャッシュフロー
次の表に我々が示した期間の統合キャッシュフロー要約(千単位)を示す
| 12月31日までの年間 、 | ||||||||||||
| (単位:千) | 2022 | 2021 | 2020 | |||||||||
| $ | $ | $ | ||||||||||
| 現金と現金等価物--年明け | 65,300 | 24,271 | 7,838 | |||||||||
| 経営活動用の現金 | (13,680 | ) | (8,581 | ) | (4,129 | ) | ||||||
| 融資活動が提供するキャッシュフロー | (118 | ) | 51,037 | 20,468 | ||||||||
| 投資活動が提供するキャッシュフロー | (12 | ) | (658 | ) | 56 | |||||||
| 現金と現金等価物に及ぼす為替レート変動の影響 | (879 | ) | (769 | ) | 38 | |||||||
| 現金 と現金等価物-年末 | 50,611 | 65,300 | 24,271 | |||||||||
操作 活動
2022年12月31日までの12カ月間、経営活動で使用された現金総額は1370万ドルだったのに対し、2021年同期の経営活動で使用された現金は860万ドルだった。運営活動支出は510万ドル増加したが、これは主に研究開発および一般と行政費用の増加によるものである。
活動に資金を提供する
2022年12月31日までの12カ月間、融資活動用の現金総額は10万ドルだったのに対し、2021年同期の融資活動用現金は5100万ドルだった。2021年2月、同社は1回の融資を完了し、3100万ドルの純資金brを提供し、2021年全体で3510万ドルの権利証を行使し、会社に2000万ドルの収益をもたらした。
投資 活動
2022年12月31日までの12カ月間、投資活動に用いられた現金総額は10万ドルだったのに対し、2021年同期の投資活動で提供された現金は70万ドルだった。70万ドルの前年比低下は、2021年にいくつかの許可協定に従って大学に支払われた前払いによるものである。
| 51 |
財源が十分かどうか
設立以来,同社は製品の開発と共同普及に多大な費用を費やしてきた。我々の現在の業務の重点は,Macrilenのさらなる治療用途の研究,パイプライン開発活動の拡大,利用可能な地域でMacimorelinの商業化 をさらに拡大し,持続的な臨床試験コストに資金を提供することである。そのため,当社は過去数年間毎年経営損失を出し,負のキャッシュフローを生じていたが,2018年12月31日までの年度を除き,当時当社は米国とカナダでMacrilen成人適応許可証を販売することで収入を得ていた。会社brは、臨床前と臨床開発を通じてその候補製品を推進し、監督部門の承認を求め、任意の承認された候補製品の商業化を追求するため、予測可能な未来に巨額の費用と運営損失が生じると予想している。我々の研究開発コストは,我々が計画している研究開発活動によって増加すると予想される.
2022年12月31日現在、会社は累計3.52億ドルの赤字を計上している。2022年12月31日までの1年間で、会社の純損失は2,270万ドル、運営キャッシュフローはマイナス1,370万ドルだった。私たちは私たちの現在の手元の現金が私たちの今後12ヶ月の予想運営と資本支出需要を満たすのに十分だと信じている。私たちは主に手元の現金を通じて私たちの未来の運営と資本支出に資金を提供する予定だ。また、私たちの手元の既存の現金は、今後12ヶ月と2025年の私たちの予想される運営と資本支出需要を満たすのに十分であると信じています。私たちは間違っていることが証明される可能性があるという仮定に基づいて、私たちは予想よりも早く資本資源を枯渇させるかもしれません。 私たちはまた、許可証内や他の候補製品を買収するための追加の資本が必要になるかもしれません。
私たちの財務資源がどのくらいの間私たちの運営を支持するのに十分な予測は展望的な 陳述であり、リスクと不確定要素に関連し、実際の結果は多種の要素によって大きく異なるかもしれない。私たちの将来の資本需要は予測が難しく、多くの要素に依存するだろう
| ● | 私たちが確立する可能性のある他の任意の協力、許可、および他の手配の条項および時間; | |
| ● | 著者らは現在と未来の潜在候補製品の臨床前研究と臨床試験の開始、進展、スケジュールと完成、新冠肺炎が著者らが行っていると計画中の研究と開発に与える影響を含む | |
| ● | 私たちは規制承認要件についてFDAと一致している | |
| ● | Br新冠肺炎が食品と薬物管理局などの主要な政府機関の運営に与える影響は、私たちの現在の候補製品或いは任意の未来の候補製品の開発を延期する可能性がある | |
| ● | 私たちが求めている候補製品の数量と特徴は | |
| ● | 規制承認の結果、時間、コスト | |
| ● | 規制要求の変化による可能性のある遅延 ; | |
| ● | 私たちの持続的な成長のコストとタイミングを支援するために新入社員を募集する | |
| ● | 特許出願の提出及び起訴、並びに特許請求の執行及び弁護に係る費用; | |
| ● | 知的財産権に関する任意のクレームの提起と起訴および知的財産権に関するクレームの執行と弁護の費用; | |
| ● | 不満と潜在的な訴訟に対応して自分を弁護する費用 | |
| ● | 私たちの候補製品のための臨床および商業用品を調達するコストと時間; と | |
| ● | 私たちは他の候補製品や技術の範囲を得ることができるかもしれない。 |
契約義務と約束
以下は、2022年12月31日までの契約義務の概要です
| サービス業と製造業 | 研究開発 契約書 |
合計して | ||||||||||
| $ | $ | $ | ||||||||||
| 1年未満 | 9,250 | 1,577 | 10,827 | |||||||||
| 1-3年 | 1,362 | 218 | 1,580 | |||||||||
| 4-5年 | 29 | — | 29 | |||||||||
| 5年以上 | — | — | — | |||||||||
| 10,641 | 1,795 | 12,436 | ||||||||||
| 52 |
2021年には、会社は開発パートナーと内部許可や同様の手配を含む様々な合意に調印した。このようなプロトコル は、一般に、会社 が処罰を受けることなく、これらのプロトコルを終了する権利があるにもかかわらず、開発、発表、または収入マイルストーンの段階に達したときに支払うことを会社に要求することができる特定の製品の販売量、法規、または他のマイルストーンに達した場合、br社は38,458ドルまでの費用を支払う必要があるかもしれない。
事件があったり
通常の運営過程では、会社は、契約終了および従業員関連事項およびその他の事項など、様々なクレームおよび法的手続きに関連する可能性がある。
関連する締約国取引と表外手配
私たちの経営陣との雇用協定や賠償協定以外には、関連者との取引は何もありません。
2022年12月31日まで、私たちは特別な目的実体または任意の他の表外手配に何の権益もありません。
リスク要因と不確実性
私たちの証券に投資することは高いリスクと関連がある。本MD&Aや関連連結財務諸表に含まれる他の情報に加えて、投資家に以下のリスクを慎重に考慮するよう促すプロジェクト 3,D.--“リスクファクター”この20-F表の年次報告では、我々の業務に重大な影響を与える可能性のある様々なリスクが検討されている。私たちは現在知らないか、あるいは現在重要ではないと考えているリスクと不確実性は、私たちの業務、経営業績、財務状況に実質的な損害を与え、あなたの投資の完全な損失を招く可能性もあります。
キー会計見積もりと判断
我々の2022年と2021年12月31日までの総合財務諸表および2022年、2021年および2020年12月31日までの年度の総合財務諸表は、国際会計基準委員会が発表した国際財務報告基準に基づいて作成されている。
我々の重要な会計見積もりと判断の詳細な議論は、我々が監査した合併財務諸表の付記3 を参照2022年と2021年12月31日まで,および2022年,2021年,2020年12月31日までの年度本年度報告表格20-F第17項“財務諸表” に掲載されています。重要な会計推定および判断とは、財務諸表を作成する際に、他のbrの仮定がなされた場合、報告の結果が大きく異なる可能性があるために、管理層が重大な判断および/または推定を行う必要があることを意味する。これらの推定は私たちの資産、負債、収入、費用、そして関連開示に影響を及ぼす報告書の金額。過去の経験、期待、現在の傾向、および経営陣が連結財務諸表を作成する際に関連する他の要因に基づいていると判断、推定および仮定する。A実際の 結果はこれらの見積り値と大きく異なる可能性がある.
経営陣は、総合財務諸表が国際財務報告基準に従って公平に列記されることを確実にするために、会社の会計政策、仮説、推定、判断を定期的に審査する。会計推定の改訂は、改訂推定の期間及び任意の影響を受けた将来の期間で確認される。
会社が総合財務諸表を作成する時に作成した最も重要な会計推定と仮定 は:契約修正、許可証と多要素協力手配の会計、営業権減値、従業員の未来の福祉と研究開発費用を含む。
| 53 |
| C. | 研究開発、特許、ライセンスなど。 |
私たちの過去3年間の研究開発政策の説明については、本プロジェクトの冒頭の“プロジェクト4.B.業務概要”と“主な発展” を参照してください。過去4年間、私たちの研究開発活動は以下の通りです
| ● | 2018年にMacrilenTM(Macimorelin)の小児科適応P 01研究を開始し,Novoは70%の費用を支払った | |
| ● | 2021年に検査試験が開始され、Novoはすべての費用に資金を提供し、最大960万ドル(900万ユーロ)に達する。960万ドル(900万ユーロ)から1050万ドル(980万ユーロ)を超える追加コストは、2023年5月までNovoと同社によって二分される。そして | |
| ● | 私たちのbrパイプライン活動には臨床前作業が含まれている。 |
| D. | トレンド 情報 |
以下および本年報の他の部分に開示されている場合を除いて、当社はいかなる傾向、不確定要素、需要、承諾またはbr}事件が当社の純収入、持続的な経営収入、収益力、流動資金、brまたは資本資源に重大な影響を与える可能性があり、あるいは報告された財務情報が必ずしも将来の経営業績や財務状況を反映するとは限らない。
Aeterna は現在,その鍵となる3期安全性と有効性研究AEZS−130−P 02(“検出試験”)を行い, macimorelinをCGHD診断に用いている。2歳から18歳以下に成長ホルモン欠乏症が疑われる児童と青少年 が含まれる。この研究にはヨーロッパと北米の約100人の被験者が含まれ、少なくとも40人の被験者が思春期前にあり、40人の被験者が思春期状態にあると予想される。再現性データを得るために,Macimorelin成長ホルモン刺激試験(“GHST”)を2回行い,対照:アルギニン(IV)とクロニジン(経口)の2種類の標準GHSTを用いた。2021年4月22日,この臨床試験に関連する米国FDA調査性新薬申請が発効した。アメリカとヨーロッパの最初の臨床サイトはすでに開放されて患者を募集した。ヨーロッパでは,国家臨床試験承認手続きや現場起動活動が行われている。現在、著者らは持続的な新冠肺炎疫病によるウェブサイトの活性化と登録遅延を密接に監視し、予想試験完了日への潜在的な影響を軽減している。
会社は、他の 市場におけるMacimorelinの商業化パートナーを確保するために、業務発展交渉を継続している。これまでに合意した合意に加え、アイトナーは最近NK Meditech Ltdとライセンス契約を締結し、 は韓国でMacimorelinの開発と商業化の許可協定に調印し、 はErKim PharmPharmticalsと流通協定 ブルガリアEOODを締結し、トルコといくつかのバルカン国でMacimorelinを商業化する。
潜在的パーキンソン病治療薬であるAIM生物製品の開発について,イタイナーは革新的な動物モデルを用いて,パーキンソン病マウスにおけるα−A 53 T−α−シヌクレイン特異的T細胞の神経変性を研究する計画であり,このモデルは最近ヴェルツブルク大学の研究者によって発表された。
次のステップ 手順−NMOSD
| ● | AIM生物製品に基づく開発候補を選択するために、インビトロおよびインビボ評価を行った。 | |
| ● | 選定した候補者のために プロセス開発を製造する. |
次はパーキンソン病です
| ● | パーキンソン病の潜在的治療に用いられる抗原特異的AIM生体分子を設計し生産した。 | |
| ● | 関連するパーキンソン病モデルで体外と体内評価を行った。 |
シェフィールド大学と協議した後、エトナーはそのDC−PTH計画の主要候補としてAEZS−150を選択した。AEZS-150は、成人原発性副甲状腺機能低下症に潜在的な新しい治療選択を提供することを目的として開発されている。
| 54 |
次のステップ ステップDC-Pth
| ● | シェフィールド大学と協力し,開発候補 (体外と体内)を深く表現した。 | |
| ● | 製造プロセスを開発する。 | |
| ● | AEZS−150の臨床前開発を正規化し,潜在的なIND申請に備えて,第1のヒト臨床研究を行う |
エテナーは,既存の診断用Macimorelinの臨床前や臨床データに加えて,構築されたサプライチェーンを利用してこの開発を支援する可能性がある。代替製剤は現在も開発されており,成人成長ホルモン欠乏症(AGHD)診断のための既存の経口溶液のさらなる選択として承認されている。
Next Steps−Macimorelin潜在的治療として(ALS)
| ● | クイーンズランド大学と協力し,特定疾患の動物モデルにMacimorelinを用いた概念検証研究を行った。 | |
| ● | 代替レシピを評価する. | |
| ● | 臨床前発展計画を決定する |
過去2年間、新冠肺炎ワクチンの構造は引き続き深刻な変化が発生した。すでに高効率ワクチンが使用可能であり、ますます多くの治療方案が同時に承認されたか、あるいは後期開発段階にあり、あまり致命的ではないウイルス変異体が伝播しており、これらはすべて任意の早期新冠肺炎ワクチン計画に関連する財務リスクを増加させている。我々が資源を慎重に使用することを確保するために,会社のワクチン開発計画の早期段階と世界情勢の変化を考慮して,エテナーは新冠肺炎やクラミジアワクチンプラットフォームをさらに開発しないことを決定した(このプラットフォームは会社の新冠肺炎計画で使用されているワクチンプラットフォームと同じプラットフォームに基づいている)。そのため、同社はまた、このワクチンプラットフォーム技術に関するヴェルツブルク大学との既存の許可協定を終了することを選択した。
金融リスク要因と他のツール
金融商品からのリスクのオープンな性質と程度、信用リスク、流動性リスク、市場リスク(株価リスク)、およびこれらのリスクをどのように管理するか、見てみましょう注意事項24当社の2022年と2021年12月31日まで、および2022年、2021年および2020年12月31日までの年度監査総合財務諸表。
本年度報告書20-F表の一部として提出された連結財務諸表は、“第17項--財務諸表”の下に記載されている。
| E. | キー会計試算 |
上述の“流動性、キャッシュフローと資本資源--肝心な会計推定と判断”項目5.bを参照。
| 55 |
第br項6.役員、上級管理者、および従業員
| A. | 役員brと上級管理職 |
次の表には、2022年12月31日現在の取締役と会社の上級管理職の情報を示しています
| 氏名と居住地 | Eeterna Zentarisを用いた定位 | |
ニコラ·アンマー ドイツ黒森市 |
首席医療官総裁臨床開発部高級副主任 | |
エドワーズピーター·Gです アメリカオハイオ州 |
役員.取締役 | |
エグベルトキャロライン アメリカテキサス州 |
取締役、取締役会長 | |
Gagnon, ギルス カナダケベック州 |
役員.取締役 | |
Gerlach、 Matthias ドイツ黒森市 |
社長製造とサプライチェーン上級副社長 | |
ガンサー、エクハド ドイツ黒森市 |
総裁業務発展と連盟管理上級副総裁;取締役ドイツAEZS取締役 | |
ジュリアーノ·フラタ カナダケベック州 |
最高財務官総裁上級副総裁 | |
ポーリーニクラウス ドイツ黒森市 |
社長、取締役CEO;管理役員ドイツAEZS | |
テピン デニス カナダケベック州 |
役員.取締役 | |
Teifel、マイケル ドイツ黒森市 |
上級副総裁非臨床開発首席科学者 |
以下は私たち一人一人の役員と役員の概要です。
Nicola Ammerは2021年1月に我々の上級副総裁,臨床開発と首席医療官に任命された。彼女は私たちの幹部です。Ammer博士はAEZSドイツフランクフルト事務所に常駐し,2002年にCRO業務の製薬薬環境で彼女のキャリアを開始し,各ポストで臨床研究開発のすべての経験を蓄積し,臨床運営役員を含むますます多くの責任を担っている。彼女は2015年3月にAEZSドイツ会社に入社し、臨床取締役プロジェクトを担当し、2016年1月に臨床開発担当に就任した。彼女は製薬分野で豊富なスキルを持ち,成人適応のMacimorelin臨床開発計画の成功に大きく貢献している。Ammer博士はエソン大学で学業を終えた後,1995年に医師免許を取得した。彼女は2004年にミンスター大学から医学博士号を授与され、2009年にデュイスブルク-エッセン大学に薬学修士号を授与された。
ピーター·G·エドワーズは2020年5月15日に取締役会に加入し、監査委員会と指名、管理、報酬委員会のメンバーである。エドワーズは現在Aziyo Biologicsの総法律顧問だ。エドワーズさんは、2017年1月から2019年1月まで、セラニス社執行副社長兼法律顧問を務めています。エドワーズ以前はバクスターから剥離したバイオ製薬会社Baxalta Inc.の執行副総裁と総法律顧問であり,2015年6月から2016年7月までBaxaltaがShire plcと合併していた。これまでは、2013年7月から2015年6月まで世界の専門製薬会社美楽美社の上級副総裁兼総法律顧問を務め、2010年5月から2013年6月までCoviden plcから剥離する前に同社の副総裁と総法律顧問を務めていた。彼は2007年6月から2010年4月までベルギーブリュッセルで蘇威製薬執行副総裁兼総法律顧問を務め、2005年10月から2007年6月までアメリカで蘇威製薬の高級副総裁と総法律顧問を務めた。これまで、彼はメットラー·トレド社と礼来社で責任が増している内部職を務めていた。エドワーズさんは、1990年に彼のキャリアを開始しました。彼はミズーリ州カンザスシティSok,Hardy&Bacon L.L.P.オフィスのアシスタントでした。エドワーズさんは楊百ガム大学の法学博士号を優秀な成績で取得しました。
| 56 |
キャロライン·エグベルトは2012年8月から取締役会の取締役を務め、2016年5月から取締役会長を務めてきた。彼女はまた指名、管理、そして報酬委員会のメンバーだ。ミシガン州とワシントンD.C.で弁護人を務めた後、テキサス州ヒューストンにあるSolvay America,Inc.(Solvay)(化学と製薬会社)に入社した。ソルヴィの20年間のキャリアの中で、彼女は人力資源部副主任総裁、ソルヴィ管理サービス会社総裁、全世界人的資源主管とグローバル道徳とコンプライアンス部高級執行副総裁などのポストを務めた。蘇威在任中、彼女は7つの子会社で取締役会のメンバーを務め、子会社の会長を務めていた。2010年の退職後、彼女はコンサルティング会社であるCreative Solutions for Executionsを設立し、会社のガバナンス、道徳、コンプライアンス、組織発展、役員報酬、戦略的人的資源に関する専門知識を提供した。彼女はワシントン州ジョージワシントン大学の生物科学学士号とワシントン州シアトル大学の法学博士号を持っています。彼女もワシントンD.C.にあるジョージシティ大学医学院とイリノイ州シカゴにある西北大学医学院の薬理学博士候補でもある。彼女は依然としてミシガン州弁護士協会とワシントンD.C.コロンビア特別区弁護士協会の活躍のメンバーだ。
Gilles Gagnonは2020年1月1日に取締役会に加入し、監査委員会と指名、管理と報酬委員会のメンバーである。ガグノンは現在、バイオテクノロジー会社Ceapro Inc.の最高経営責任者兼CEO総裁である。これまで、彼はエトナーZentaris社のCEO兼社長です。過去35年間、ガグノンさんは衛生分野、特に病院環境や製薬業界で働いていました。複数の国際委員会·戦略諮問委員会にさんが参加した。彼はカナダの研究に基づく製薬会社(Rx&D−現在はInnovative Medicine Canada)の取締役会に9年間勤め,バイオ製薬業界のメンバーを代表し,Rx&Dのカナダ生物協力計画を創始した。彼は現在Ceapro Inc.の総裁兼CEOを務めている。 彼はカナダ革新医学最高経営責任者委員会のメンバーだ。彼は取締役認証企業で、トロント大学ロートマン管理学院の取締役教育計画を完成させ、バイオ製薬業界の私営や上場企業の複数の取締役会に勤務していた。
マティアス·グラッチは2014年6月に製造運営部副総裁に任命され、2018年1月に製造·サプライチェーン副総裁に任命された。彼は私たちの執行役員です。2011年12月から2014年5月まで、彼は私たちの副総裁で、薬物化学 です。Gerlach博士はAEZSドイツ社のフランクフルト事務所で働き、1997年に製薬業界でキャリアを開始した。2001年1月にわが社に入社し、彼のキャリアの中で製品商業化により薬物化学や臨床前開発分野でますます多くの責任を担ってきた。彼は豊富な科学と商業技能を持ち、革新、薬物開発と管理の面で長期的な成功記録があり、そしてMacimorelinがアメリカで成人適応の商業化に成功するために重要な貢献をした。Gerlach博士は1994年にフランクフルトのジョン·ウォルフガン·ゲーテ大学で化学証書を取得し,1997年にジョン·ウォルフゴン·ゲーダー大学から合成有機化学博士号を授与された。
エクハルト·ゲンザーは2020年1月にアイトナーZentaris株式会社取締役の取締役社長に任命され、上級副総裁は2021年に業務発展と連盟管理部門の責任者に任命された。Guenther博士は製薬業界で25年を超える経験を有しており,腫瘍学や内分泌学など様々な適応分野の薬物発見や開発に深い知識と専門知識を有している。また、彼のキャリアの中で、彼は研究協調、プロジェクト管理、知的財産権、業務発展の面で豊富な経験を得た。ドイツのハーラー·ウィテンベグマーティン·ルーサー大学有機化学博士号を取得した後、1985年にマグデブルク·ファルブルク大学で工業生活を開始した。1990年、フランクフルトのASTA Medica株式会社に入社し、そこで薬物化学系で働いていた。ASTA Medica在任中、Guenther博士は生物技術会社ZentarisがASTA Medicaから剥離する準備と実行に積極的に参与した。2002年にエトナー·ゼタリスが設立された後,薬物発見と臨床前研究を担当する総裁副主任に任命された。2008年、彼は総裁連合管理と知的財産権副総裁に昇進し、2014年にアイトナーZentaris社の業務発展副総裁に昇進した。Guenther博士はConsilient Health、MegaPharm Ltd.,先霊製薬、ソウェイ、益力多本砂、Hikma PharmPharmticalsと国薬持株A-Thinkを含む大中型国際製薬会社との多くの研究開発と許可協定の開始と実行を担当している。Guenther博士はドイツのフランクフルトで働いています。
| 57 |
ジュリアーノ·ラフラタは2022年1月に私たちの最高財務官上級副総裁に任命された。彼は高度な金融専門家で、製薬、バイオ製薬、金融サービス分野で20年以上の専門経験を持っている。彼のキャリアの中で、彼は公共と民間部門に勤め、広範な金融活動を指導し、管理する面で豊富な経験を蓄積し、M&A取引、会社発展、監査、会計と行政機能を含む。Aeterna Zentarisに加入する前に、La Frattaさんは、財務副総裁を務めたCellCarta(Caprion Biosciences)で財務副社長を務め、CellCartaはカナダモントリオールに本社を置く私募株式所有の専門的な臨床研究開発組織実験室である。La FrattaさんはCellCartaに加入する前にIMS Canada Health(現Iqvia)とCato Researchで様々な職務を担当していた。彼のキャリアは徳勤から始まり、カナダとアメリカの異なる業界会社(製薬業界を含む)の高級監査役である。La Frattaさんは、コンコルディア大学で会計学の学士号を取得し、公認会計士の資格を有しています。
クラウス·ポーリーニ博士は2019年10月に社長兼当社の最高経営責任者に任命されるとともに、わが取締役会の取締役でもある。Paulini博士はドイツフランクフルトAEZSドイツ支社に常駐し、2019年7月に取締役社長に任命され、2018年2月に総裁品質·監督部副主任に任命された。Paulini博士は1997年にASTA Medica AGで製薬業界でのキャリアを開始した。Zentarisが設立されASTA Medicaから剥離された場合,彼は積極的な役割を果たし,会社で様々な職務を担当し,西トロードのプロジェクト責任を含めて責任が大きくなってきた。2010年と2019年の品質保証担当期間中、Paulini博士は研究開発段階で薬物化学グループの担当者を務めるMacrilen/Macimorelin− を含む我々の多くの臨床開発プロジェクトを管理することに成功した。その豊富な経験と知識によって、彼は著者らの薬品と臨床開発プロジェクトに成功した監督と貴重な投入を提供し、成功とコンプライアンスの結果を確保し、最終的にアメリカFDAとEMAの監督許可を得た。ポーリーニ博士は博士号(Ing博士)を取得した。ASTA Medica AGに加入する前に、1993年にドイツのダムシュタット工業大学で化学専攻を専攻し、その後のストラスクライド大学(スコットランドグラスゴー)とJ.W.ゲーテ大学(ドイツフランクフルト)博士後奨学金中に薬物化学/薬物発見を専攻した。
デニス·ターピンは経験豊富な専門幹部と公認会計士(CPA)であり、金融と資本市場取引、業務発展とM&Aの面で豊富な経験を持ち、その中で20年以上生物製薬業界で働いている。何 は現在専門バイオ製薬会社EndoCeutics,Inc.の総裁兼最高経営責任者である。 これまでEndoCeutics,Inc.で副総裁、特別プロジェクトを務めてきた。特平さんは、2016年2月から2018年6月までの間、ケベック港務局副総裁兼最高財務責任者を務めていました。2007年から2015年まで、特平さんはAeterna Zentarisの上級副総裁兼最高財務責任者(br};2007年から1996年まではAeterna Zentarisで様々な財務職を務めている。これまで1988年から1996年までCopers Lybrand(現普華永道)税務部門で取締役 を務め、1985年から1988年まで監査役を務めていた。テピンさんはケベック州ラバル大学で会計学の学士号を取得しました。彼は1985年に会計免許を取得し、1987年にフランチャイズ会計士になった。
Michael Teifelは有力な業界幹部であり、彼のキャリアは20年以上を越え、内分泌学と腫瘍学を含む多くの治療領域に関連している。彼は研究を臨床開発に転換する上で豊富な経験を持っている。彼のキャリアの中で、彼は小分子薬物、ポリペプチド、標的療法と生物製品の非臨床開発計画の設計と実施、および全世界の登録候補薬物の持続的な非臨床評価において特殊な専門知識を獲得した。Teifel博士はAeterna Zentarisに入社し,工業的に異なる職を務め,薬理学,薬物動態学,毒理学,翻訳科学における役割が大きくなってきている。彼はロー氏診断会社で輸送システム/非ウイルス遺伝子療法分野でのキャリアを開始した。1999年、Teifel博士は共同創業者としてドイツのマーティンスレイドにあるバイオテクノロジースタートアップ会社ミュンヘンバイオテクノロジーに入社した。薬理学と毒理学の責任者として、新しい血管標的技術の評価と非臨床開発を担当し、抗腫瘍診断と治療を開発した。2004年,Teifel博士はAeterna Zentarisで最初の任期を開始し,そこで臨床前開発·翻訳研究分野でいくつかの職を務めた。彼のアイデンティティでは,他を除いて,Macimorelinの米国とEUの適応AGHDに登録されている非臨床アーカイブの準備を担当している。2019年,Teifel博士はAeterna Zentarisを離れ,オランダのウデレ支のCleara Biotechで非臨床研究開発に従事した。Cleara Biotech変換科学の担当者として,抗老化薬の研究を年齢関連疾患や進行癌に変換する臨床前開発を担当している。2021年5月、彼はAeterna Zentarisに再加入し、上級副総裁非臨床開発兼首席科学官を務めた。Teifel博士はドイツのダムシュタット工業大学の生物学の学位と博士号を持っています。
| 58 |
上記の任意の人の間には家族関係もなく、任意の顧客、大株主、サプライヤー または他の人といかなる手配を締結することもなく、上記のいずれかの人を取締役または行政総裁に選ばせた。各取締役の任期は当社の次期株主周年総会または正式に後継者を選出または委任するまでです。
マザーボード 多様性
次の表は,本年度報告日までの取締役会の多様性に関するいくつかの情報を表 20−Fの形で提供している。
| マザーボード 多様性マトリックス | ||||
| 主にオフィスがある国·地域: | カナダ | |||
| 外国の個人発行業者 | はい、そうです | |||
| 母国法によると、情報開示は禁止されています | 違います。 | |||
| ガイド総数 | 5 |
| 女性は | 男性 | 非 バイナリ | もしかして
ないの 開示する 性別 | |||||||||||||
| 第1部:性別同意 | ||||||||||||||||
| 役員.取締役 | 1 | 4 | — | — | ||||||||||||
| 第2部:人口統計的背景 | ||||||||||||||||
| 自国の管轄区に勤務している人数が不足している個人 | — | — | — | — | ||||||||||||
| LGBTQ+ | — | — | — | — | ||||||||||||
| 人口統計の背景を明らかにしていませんか | — | — | — | — | ||||||||||||
| B. | 補償する |
私たちの役員と役員は通常自国通貨で報酬を支払います。他に説明がない限り、本稿に含まれるすべての報酬情報はドルで表され、取締役または上級管理職の報酬がドル以外の通貨で支払われている場合、金額は、以下の年度の平均為替レートによってこの人の国の通貨からドルに変換された:2022年12月31日までの財政年度:ユーロ1.000=1.053ドル、1.000=0.759ドル。:2021年12月31日までの財政年度:ユーロ1.000=1.182ドル、カナダドル1.000=0.797ドル、2020年12月31日までの財政年度:ユーロ1.000=1.140ドル、カナダドル1.000=0.745ドル。
外部役員報酬
我々従業員ではない取締役会メンバー(我々の“外部取締役”)に支払われる報酬は、(I)取締役会及びその委員会に最も合格した者を吸引·保持することを目的としており、(Ii)外部取締役の利益を我々株主の利益と一致させ、(Iii)取締役外部に有効なbrになるためのリスク及び責任に適切な補償を提供することを目的としている。この報酬は、ノミネート、管理および報酬委員会(“NGCC”)が取締役会に提案している。 NGCCは現在、3人の外部役員から構成されており、各取締役はそれぞれ独立取締役で、Carolyn Egbertさん(主席)、Peter G.Edwardsさん、Gilles Gagnonさんである。
取締役会はNGCCの正式な許可を通過しました。この許可は私たちのサイトで取得することができます。URLは:Wwwww.zentaris.comそれは.NGCCの任務規定は、他の事項以外に、それは取締役会に協力して私たちの会社管理問題に対する方法を制定し、新しい取締役会の有名人を提出し、取締役会とその委員会、そのそれぞれの 議長と個人取締役の有効性評価を監督し、取締役報酬について取締役会に提案し、そして著者らの会社管理実践の中で指導役を務める。
| 59 |
固定器
私たちのbr外部取締役は毎年採用金を獲得しており、金額は取締役会で担当するポストに依存します。年間採用金は四半期ごとに私たちの外部役員に支払われます。取締役以外の一人一人は同値な自国通貨支払いを受け、法律の要求を適用する任意の控除または控除を控除する。
| 報酬タイプ: | 毎月のノルマ 2022年 | 年度ノルマ 2022年 | ||||||
| 取締役会が議長を招聘する | — | 80,000 | ||||||
| 取締役会のメンバーが採用者を採用する | — | 50,000 | ||||||
| 監査委員会議長ロケータ | — | 30,000 | ||||||
| 監査委員会のメンバー採用者 | — | 7,500 | ||||||
| NGCC 椅子固定器 | — | 15,000 | ||||||
| NGCC メンバーロケータ | — | 5,000 | ||||||
| 指導委員会固定器 | 6,500 | — | ||||||
すべての取締役が取締役会や委員会会議に出席することによる出張費やその他の自己負担費は精算されます。財政年度内に、外部役員が取締役会に加入した場合、採用金は比例して分配される。
傑出した賞
次の表には、2022年12月31日までの取締役以外のすべての賞を示しています
| オプションに基づく 報酬 | 株式に基づく報酬 | |||||||||||||||||||||||||||||||||||
| 名前.名前 | 発行日 (mm-dd-yyyy) | オプションを行使していない証券数 (#) | オプション 練習 値段 ($) | オプション の有効期限 (mm-dd-yyyy) | 未行使の値 お得なオプション オプション(1) ($) | 発行日 (mm-dd-yyyy) | 帰属された株式または株式単位数 (#) | まだ帰属していない株式奨励の市場 または支払い価値(2) ($) | 市場 または未支払いまたは分配された既得株奨励の支払価値(2) ($) | |||||||||||||||||||||||||||
| エドワーズピーター | — | — | — | — | — | 05/15/2020 | 1,200 | — | 3,816 | |||||||||||||||||||||||||||
| — | — | — | — | — | 05/05/2021 | 2,800 | — | 8,904 | ||||||||||||||||||||||||||||
| — | — | — | — | — | 08/03/2022 | 20,000 | — | 63,600 | ||||||||||||||||||||||||||||
| 05-10-2016 | 400 | 87.00 | 05-09-2023 | — | — | — | — | — | ||||||||||||||||||||||||||||
| 12-06-2016 | 314 | 86.25 | 12-06-2023 | — | — | — | — | — | ||||||||||||||||||||||||||||
| 08-15-2017 | 2,400 | 51.25 | 08-15-2024 | — | — | — | — | — | ||||||||||||||||||||||||||||
| エグベルトキャロライン | — | — | — | — | — | 05/08/2018 | 920 | — | 2,926 | |||||||||||||||||||||||||||
| — | — | — | — | — | 05/22/2019 | 1,200 | — | 3,816 | ||||||||||||||||||||||||||||
| — | — | — | — | — | 05/15/2020 | 1,200 | — | 3,816 | ||||||||||||||||||||||||||||
| — | — | — | — | — | 05/15/2021 | 2,800 | — | 8,904 | ||||||||||||||||||||||||||||
| — | — | — | — | — | 08/03/2022 | 20,000 | — | 63,600 | ||||||||||||||||||||||||||||
| Gagnon, ギルス | — | — | — | — | — | 05/15/2020 | 1,200 | — | 3,816 | |||||||||||||||||||||||||||
| — | — | — | — | — | 05/19/2021 | 2,800 | — | 8,904 | ||||||||||||||||||||||||||||
| — | — | — | — | — | 08/03/2022 | 20,000 | — | 63,600 | ||||||||||||||||||||||||||||
| テピン デニス | — | — | — | — | — | 05/19/2021 | 2,800 | — | 8,904 | |||||||||||||||||||||||||||
| — | — | — | — | — | 08/03/2022 | 20,000 | — | 63,600 | ||||||||||||||||||||||||||||
(1) 財政年度末“行使されていない現金オプション価値”の計算方法は,本年度(2022年12月31日)ナスダック普通株最終取引日の終値は3.18ドルであり,オプションの行使価格 に未行使のオプション数を乗じたものである.
(2) 当社がナスダックの普通株を使用した本年度(2022年12月31日まで)の最終取引日の終値は3.18ドルであった。
| 60 |
取締役会が2016年3月29日に採択され、株主が2016年5月10日に承認した当社の第2回改訂で再記述された株式オプション計画(“株式オプション計画”)の詳細は“株式オプション計画概要”、 取締役会が2018年3月27日に可決し、株主が2018年5月8日に承認した当社長期インセンティブ計画の詳細は“長期インセンティブ計画概要”を参照されたい。
外部役員報酬合計
下表は、2022年12月31日までの財政年度内に外部役員に支払われる総報酬(すべての金額をドルで示す)をまとめたものである。私たちの外部役員は通常自国通貨で報酬を支払います。GagnonさんとTurpinさんの給与はカナダドルです。エグベルトとエドワーズの報酬はドルです。
| 名前.名前 | 稼いだ費用 (1) ($) | 株式を基礎とする 賞.賞(2) ($) | オプションに基づく 報酬 ($) | 非持分インセンティブ計画報酬 ($) | 年金 価値 ($) | 他の報酬はすべて ($) | 合計する ($) | |||||||||||||||||||||
| エドワーズピーター | 69,750 | 100,400 | — | — | — | — | 170,150 | |||||||||||||||||||||
| エグベルトキャロライン | 102,000 | 100,400 | — | — | — | — | 202,400 | |||||||||||||||||||||
| Gagnon, ギルス | 55,615 | 100,400 | — | — | — | — | 156,015 | |||||||||||||||||||||
| テピン デニス | 76,517 | 100,400 | — | — | — | — | 176,917 | |||||||||||||||||||||
| (1) | 2022年12月31日までの財政年度では、取締役として提供されたサービスを支払うために、全外部取締役に合計303,882ドルの費用を支払った。 は,自己払い費用の精算や2022年に付与された株式とオプションによる報酬の価値 は含まれていない. | |
| (2) | 表示された金額 は付与日のDSU価値(5.02ドル)を表す.授与日の一株の価値は、先日の最終取引日のナスダックの普通株の終値を授与するためである。 |
役員報酬
以下では、2022年に私たちの“指定役員”に支払われた報酬に関する情報を開示します。2022年、私たちの“指名された幹部”のリストは以下の通りです
| ● | クラウス·ポーリーニ博士は、2019年10月4日から総裁兼最高経営責任者を務め、2019年7月から管理役員AEZSドイツ社を担当している | |
| ● | さん ジュリアーノ?ラ?フラタは、2022年1月24日から最高財務官上級副総裁を務めている | |
| ● | 社長製造とサプライチェーンの副社長マルティアス·グラッハ博士、社長ビジネス開発とアライアンス管理副社長、役員AEZSドイツの責任者エクハルト·ガンサーさん;Nicola Ammer夫人と臨床開発上級副社長さん;非臨床開発上級副社長兼首席科学官Michael Teifelさん、彼らは“私たち一時間”の最高報酬の役員です。 |
| 61 |
報酬 議論と分析
報酬理念と目標
私たちの取締役会はNGCCを通じて、総現金報酬と総直接報酬を含む競争力のあるパーセンタイル値で をグループ化する市場をベースにした当社の役員報酬計画を確立しました。NGCCは以下の方式で高業績の高級管理者を誘致、激励と維持し、優秀な業績を奨励と奨励し、幹部の利益を著者らの株主の利益と一致させることを目的とした報酬計画を構築した
| ● | 比会社において同じまたは測定可能な類似の職に就くことができる幹部と競合する報酬を得る機会を役員に提供する; | |
| ● | 役員に株式インセンティブ報酬計画に参加する機会を提供する | |
| ● | 役員報酬を私たちの会社の目標と一致させ | |
| ● | 重要な職場での高い素質の人材を吸引し、維持する。 |
報酬 要素
私たちの役員報酬は現地と全国市場の小型バイオ製薬会社の50%を対象としており、固定と可変の2つの部分から構成されている。可変部分は株式と非持分インセンティブ計画を含む。 各報酬部分は異なる機能にサービスすることを目的としているが、すべての要素は特定の、競争的な運営と会社目標を確立し、従業員がこれらの目標を達成するレベルに基づいて従業員に財務 インセンティブを提供し、会社と個人業績の最大化を実現することを目的としている。
私たちの現在の役員報酬計画は、(I)基本給、(Ii)個人と会社の業績に関連する年間ボーナス、の4つの基本的な構成要素から構成されている。(Iii)株式オプションを含む株式インセンティブは、以前、2016年3月29日に取締役会が採択し、2016年5月10日にAeterna Zentaris株主によって承認された第2回改正および再記載された株式オプション計画(“株式オプション計画”)に基づいて付与されており、現在は、取締役会が2018年3月27日に通過し、2018年5月8日にAeterna Zentaris株主によって承認された会社長期インセンティブ計画(“長期インセンティブ計画”)に基づいて付与されており、この計画は、我々の取締役の利益のために設立されている。取締役会または国家調整委員会は、時々指定されたいくつかの幹部および他の参加者 ;(4)他の補償要素は、福祉、追加手当、退職福祉 を含む。
基本給 。基本給は株価にかかわらず、私たちの役員に安定した収入を提供することを目的としている。個人基本給を決定する際には、NGCCは、役員職の範囲、役員に関する能力や経験、および留任リスクを含む可能性がある個別の状況を考慮する。NGCCは,会社の目標の実現状況や,役員の個人表現も考慮する.
短期的、非持分的奨励的報酬私たちの短期非持分インセンティブ報酬計画は、役員ごとに目標現金ボーナスを設定し、役員の基本給のパーセンテージで表示しています。上級管理職に支払われる現金ボーナス額 は,その年度に決定した年間業績目標の実現に取締役会が貢献している程度に依存している。年度業績目標は、具体的な運営、臨床、監督、財務、商業、会社目標 であり、私たちの製品ラインを推進し、私たちのビジネス努力の成功を促進し、私たちの財務状況を改善することを目的としています。年度業績目標は、会社戦略年度審査の一部として、財政年度終了時に設定されています。業績目標は、単一の役員のために制定されたものではなく、機能分野別に策定されており、その多くの目標は、私たちの総裁と最高経営責任者、最高財務官(または最高財務官)および他の幹部(私たちが指定した幹部を含む)によって実行されるか、またはそれらの役割に属する。現金ボーナスの支給はNGCCと取締役会の承認を得,各人の表現およびわが社レベルでの全体表現の評価 に基づく必要がある。個人業績の決定は数学計算を用いた定量的な措置には触れず,数学計算では個々の個人業績目標にデジタル重みが与えられている。逆に、NGCCの個人業績の決定 は、特定の幹部がその目標を実質的に達成したかどうかの主観的判断、あるいは私たちの成功に重要であると考えられる会社の目標の面で基準超過やパフォーマンスが良くないことである。
| 62 |
役員長期持分報酬計画。私たちの役員報酬の長期部分は完全に長期インセンティブ計画に基づいており、この計画は役員の貢献と彼らの職責に基づいていくつかの株式ベースの奨励を発行することを可能にする。取締役会は2014年12月に、各任命された幹部 がオプションを獲得して、私たちの普通株を買収する資格があり、その価値はBlack-Scholesオプション定価 モデルに基づいており、その賃金の指定倍数に等しい株式オプションを付与する政策を採択した。総裁とCEOの指定倍数は1.5である。 互いに指定された実行社長の指定倍数は0.75である。留任を奨励し,我々の持続的成長戦略の策定と成功に管理の重点を置くためには,株式オプションは3年以内に付与され,上位3分の1の株式オプションは授与日1周年にbr}が付与される。2018年に長期インセンティブ計画を採用して以来、株式オプション以外の配当奨励タイプ(限定株式単位(“RSU”)、 DSU、その他のタイプを含む)を拡大しました。
その他 形式の補償私たちの幹部従業員福祉計画はまた生命保険、医療保険、歯科保険と障害保険を含み、範囲と方式はすべての他の従業員と同じで、給与システムの福祉計画に加入するか、追加のbrパーセンテージ補償によって自分で個人保険証書に加入する。これらの福祉や追加福祉は,生命科学業界における同等の北米組織の同等のポストと比較して全体的な競争力を持つことを目的としている。私たちはまた北米の従業員の退職計画のために支払います。アメリカとカナダの従業員の毎年の最高支払い金額は19,500ドルです。私たちアメリカとカナダの従業員の支払い金額はそれぞれアメリカ国税局とカナダ税務署による私たちの最高賃金の従業員の支払いによって制限されています。フランクフルトで働いている従業員;ドイツも雇用主が従業員年金基金に納めたいくつかのお金から利益を得ている。私たちの管理者は、任命された管理者を含めて、他のすべての従業員と同程度かつ方法でこのような雇用主供出計画に参加する資格がある。
位置を定める
NGCCは自分の独立顧問を招聘し、役員報酬問題についてアドバイスを提供する権利がある。NGCC は外部情報およびアドバイスに依存する可能性があるが、すべての役員報酬に関する決定は、NGCCの提案に基づいて取締役会が行ったものであり、任意の外部報酬コンサルタントが提供する情報およびアドバイス とは異なるまたは異なる可能性のある要因および考慮要因を反映している可能性があり、これらの情報およびアドバイスは時々保持される可能性がある。
2022年に、国家給与調整委員会は、市場競争力のある報酬機会を提供する目標を達成したかどうかを決定するために、取締役報酬計画を基準評価する報酬コンサルタントを招聘した。報酬コンサルタントは、その結論を出した私たちの規模および/または発展段階に相当する会社と、私たちの競争相手の他社から報酬データを収集します。一部は報酬顧問の提案に基づいており、NGCCは取締役会の許可を得て取締役会メンバーの事前招聘費と委員会主席の報酬に対していくつかの変更を行う。
リスク役員報酬計画評価
取締役会はNGCCによる報酬方法の実施を監督し、これらの報酬方法は一部の役員報酬を著者らの短期と長期業績および各幹部の業績とリンクさせ、このような報酬方法に関連する優勢とリスクを考慮した。また、取締役会は、株主価値の創造を奨励し、短期的および長期的な業績と各役員の業績とのバランスを反映させることを目的とした報酬政策の策定を監督している。NGCCは、全体的に我々の役員報酬計画に関するリスク概念を考慮している。
基本給は、株価にかかわらず、幹部に安定した収入を提供するために一定の額であり、したがって、冒険行為を奨励または奨励せず、それによって他の重要な業務、運営、商業または臨床指標またはマイルストーンを損害する。可変報酬要素(年間ボーナスと株式ベースの奨励)は、短期、中期、長期業績を奨励することを目的としています。短期業績については、具体的な運営目標や会社目標の実現時間やレベルに応じて適宜の年間ボーナスを付与することができ、NGCCはこれらの目標は挑戦的だと考えていますが、不必要や過度な冒険を奨励していません。私たちのボーナスは通常年間業績に基づいていますが、各上級管理者の最高ボーナスは予め定められており、一人当たりの総報酬機会の一部しか占めていません。特別な場合、特定の幹部 は、その最高予め定められた金額または目標ボーナス金額を超えるボーナスを得る可能性がある。最後に、役員報酬の大部分は株式奨励の形で提供され、役員の利益と株主の利益をさらに一致させることを目的としている。NGCCは、これらの報酬は、報酬の最終価値が私たちの株価とリンクしているので、不必要または過度な冒険行為を奨励しないと考えており、長期インセンティブ報酬計画下の報酬であれば、通常 は、長期株価パフォーマンスに関連する顕著な価値 を有することを保証するために、中長期帰属スケジュールから制限される。
NGCCは、可変報酬要素(年間ボーナスおよび株式ベースの報酬)が総報酬に占める割合 は、私たちの役員が優れた短期、中期、および長期会社の業績を創出するのに十分であり、固定報酬要素(基本給)も、役員が不必要または過度のリスクを負担することを阻止するのに十分であると考えている。NGCCと取締役会は通常、個人の業績と彼らが当時の状況で適切だと思う任意の他の要素に基づいて年間ボーナスと株式ベースの奨励を調整する権利がある。必要または適切な場合、このような要因は、ある実行幹事が前年に負う可能性のあるリスクの程度を含むことができる。
このような状況に基づいて、NGCCは、当社の役員報酬計画に関連するいかなる重大な悪影響を及ぼす可能性のある具体的なリスクも発見していません。NGCCは、私たちの役員報酬計画は、不必要または過度な冒険行為を奨励したり奨励したりしないと考えている。
私たちの役員、役員、および従業員が私たちの普通株に関連する派生証券を購入、販売、または他の方法で取引することを禁止します。派生証券とは、その価値が証券価格によって変動する証券である。Br派生証券の例は、私たちの普通株の引受証、私たちの普通株上のコールまたはコールオプション、および個別に配置された派生取引、例えば、決定性を向上させるために前払いされた可変長期契約、株式交換、セットまたは外国為替基金単位を含む金融商品を含み、役員報酬または役員報酬として付与された私たちの株式証券市場値の低下をヘッジまたは相殺することを目的としている。当社の普通株を買収するオプションおよび株式オプション計画または長期インセンティブ計画に基づいて発行される他の持分ベースの奨励は、そのために発行された派生証券ではない。
2022年補償
基本給 。私たちの給与計画の主な内容は基本賃金だ。競争力のある基本給は合格幹部を引き留めるために必要な要素だと思います。NGCCは,個人基本給を決定する際に,役員職の範囲,役員に関する能力や経験 および留任リスクを含む個別状況を考慮する。NGCCはわが社の目標の実現状況や,役員の個人表現も考慮している.
| 63 |
短期的、非持分的奨励的報酬取締役会はNGCCの提案に基づき、2022年の以下の業績目標を採択した
| 目標 | 結果 | |
リスク分析と緩和オプションを含む企業発展分析と戦略計画の提供3月の国防総省会議の前に。 |
8月末のH 2の発展(NNの通知)に鑑み,新たな商業化パートナーを探すことが急務である。 | |
| 私たちのキャッシュ滑走路に関する開発プロジェクトの費用 を計画して予測するためのツールを維持します。 | 潜在戦略選択の評価が行われています。 は優先順位に従って開発プロジェクトを実行し、費用を監視·調整し続けています。 | |
| マシモレリンを新しい市場にタイムリーかつ効果的に投入するためにすべての活動を支持する。 | Macimorelinでは,韓国での臨床研究を必要とせず,イスラエルの承認を得た。供給準備が進行中です。 | |
| 詳細な投資家関係計画を制定し、改善案を確定して、ナスダックコンプライアンス要求を満たすことを確保し、退市を避ける | 市場感情の全体的な変化(リスクに注目)は,適切な切り上げは許されない | |
2022年にbrのタイムリーな臨床研究/測定可能なマイルストーンを有する研究を行い,2023年にMacimorelinを追跡承認する小児科適応を確保する。 |
特定の状況下で、この挑戦的な目標は主に持続的な新冠肺炎疫病、ウクライナ戦争と総支出の慎重な管理などの外部要素によって実現されたものではない。
Novoに関する変化を考慮して、第3四半期から第4四半期まで緩和活動を開始するしかない | |
| マキモレーリン原料薬のコストを削減する | 実現されました。 は治療と全体的な収益性のビジネス選択として重要です。 | |
| 開発計画が軌道に乗ることを確保し、少なくとも1つのプロジェクトは2023年上半期に臨床開発段階に入る | 世界的な供給と物流情勢は2022年通年で悪化している。私たちは慎重に行動して、現金を保存しながら、できるだけ早く進展を確実にしなければならない。
積極的な体内治療効果データがあれば,2023年末までにALSプロジェクトを臨床に投入する機会がある(2023年第1四半期末の決定点 )。 | |
が新しいCFOにシームレスに移行することを確保し,統合する.より効率的で費用効果のある機能を実現するために、財務組織を評価し、縮小または再編成することが可能である |
新しい最高財務官は、財務業務を引き継ぐことと、厳しい環境で部門を再編することでよくやっています。 目標は達成されました。 |
長期株式報酬
2022年12月31日までの財政年度について、取締役会は2022年1月10日に1人の従業員に合計2,000件の株式オプションを付与することを許可し、行権価格は8.88ドルだった。
株式オプション計画概要
私たちは持続的なサービスの役員、高級管理者、従業員、サプライヤーを誘致し、維持するために株式オプション計画を策定し、彼らは激励され、私たちの成功を確保するために努力します。取締役会は完全に株式オプション計画を解釈する権利があり、 は適用される規則と法規を確立し、株式オプション計画の管理に必要又は有用であると考えられるすべての他の決定を下し、このような解釈、規則、規則及び決定が のすべての証券取引所と見積システムの規則及びすべての関連する証券法規に適合することを前提としている。
| 64 |
2022年12月31日現在、株式購入計画により返済されていないオプションは5,030件で、すべての発行済みおよび発行済み普通株の約0.1% を占めている。長期インセンティブ計画に従って普通株式を発行可能な提案数は、任意の所与の時間の発行済み株式および発行済み普通株の11.4%に固定され、その際に株式オプション計画によって付与された株式オプション発行可能な普通株数 を減算する。長期インセンティブ計画の完全な説明については、以下を参照されたい。2021年12月31日現在、 は493,195株の普通株が割り当てられておらず、将来株式オプション計画に基づいてオプションを付与することができる;しかし、会社 は株式オプション計画に基づいていかなる新しい株式オプションを発行するつもりはなく、 長期激励計画に従って任意の未来株式オプションを発行する。
最近完成した財政年度株式オプション計画の焼失率は以下のとおりである
| 株式 オプション計画 | ||||||||||||
| 年末 | オプションが付与されました | 加重平均 未償還株 | やけど率 (1) | |||||||||
| 2022年12月31日 | — | 4,855,766 | 0 | % | ||||||||
| 2021年12月31日 | — | 4,596,980 | 0 | % | ||||||||
| 2020年12月31日 | — | 1,643,327 | 0 | % | ||||||||
| (1) | 年度焼損率を百分率で表し,計算方法は株式オプション計画により付与された証券数 を適用会計年度の加重平均未償還証券数 で割る |
株式オプション計画によれば、(I)私たちのすべての証券ベースの補償スケジュールに基づいて、いつでも内部者に発行することができ、または任意の年以内に発行されることができる証券の数は、私たちが発行および未償還証券の10%を超えてはならず、(Ii)株式オプション計画に従って付与される資格を有する任意の個人は、発行された普通株式および発行された普通株式の5%以上を購入するオプションを保有してはならない。また、(I)任意の年内に、私たちのすべての証券ベースの報酬スケジュールに基づいて、株式オプション計画に基づいて利益を受け取る権利がある任意の外部取締役に付与されたオプションの公正価値の合計が100,000ドルを超えないことは、NGCCによって決定され、(Ii)証券ベースの報酬スケジュールに基づいて、株式オプション計画に基づいて利益を得る権利があるすべての外部取締役に発行される証券総数は、発行済み証券および未償還証券の1%を超えてはならない。
株式オプション計画に従って付与されたオプション は、その付与日(“外部満期日”)の後、最長7年または10年以内の任意の時間に行使することができ、具体的には、付与日に依存する。取締役会またはNGCC(場合に応じて) は、株式オプション計画に従って株式オプションを付与する特定の参加者を適宜指定し、このような各オプション付与に含まれる普通株式数、付与日、各オプションの使用価格、外部満期日 およびこれに関連する任意の他の事項を決定する。普通株購入価格は、オプション付与日前の最終取引日のナスダックでの普通株の終値を下回ってはならない。株式オプション計画に基づいて付与されるオプションは、3年以内(毎年3分の1、付与日から計算)又は取締役会又はNGCC(場合によって決定される)が確定した場合には、同等の割合で を付与しなければならない。参加者は,遺言又は適用された遺産及び相続法に基づいてそのオプション(又はその中の任意の権益)を譲渡してはならないが,遺言で譲渡してはならない。
取締役会または国家調整委員会が別の決定がない限り、参加者は株式オプション計画下のオプションを行使する権利がなくなった:(I) 参加者が上級管理職または従業員が退職または自発的に退職した場合、直ちに雇用を終了し、参加者が取締役または私たちの子会社の非従業員である場合、その参加者が関連取締役会のメンバーではない日である。(Ii)役員または従業員の参加者が死去により雇用を中止された日から6ヶ月、参加者が取締役以外の者である場合、その参加者が死去により理事局のメンバーでなくなった日から6ヶ月である。(Iii)参加者が上記(I)または(Ii)項以外の理由(参加者の障害、長期疾患、退職または早期退職を含むがこれらに限定されない)のために雇用を終了した日からの90日間(br};および(Iv)参加者がサービス提供者である場合、参加者が任意の理由または理由によりサービス提供者として行動しなくなった日から30日(それぞれ“早期満了日”)である。
| 65 |
株式オプション計画はまた、1つ以上のオプションの満期日(早期満期日または外部満期日を問わず) が“閉鎖期間”期間または我々が規定した閉鎖期間の直後の7営業日以内に発生した場合、 満期日を閉鎖期間の最終日後の7営業日まで自動的に延長することを規定している。前述したように、“販売禁止期間”とは、会社政策に基づいて証券取引を制限する期間をいう。
もし (I)私たちが任意の他のエンティティ(私たちの完全子会社を除く)との合併、合併または合併の要約を受け入れる場合、またはbr}私たちのすべてまたは実質的なすべての資産を売却することができるかもしれない他のエンティティ(私たちの完全子会社を除く);(Ii) 私たちは通常の形式の支持協定に署名し、この合意に基づいて、取締役会は買収要約を支持することに同意し、私たちの株主 はその普通株をこの買収要約に提出することを提案する。または(Iii)その時点で発行された普通株式の50%を超える保有者がすべての普通株式所有者に買収要約を提出して、当時発行された普通株および発行済み普通株をすべて購入する場合、いずれの場合も、すべての発行済み普通株は直ちに帰属し、吾等はさらなる行動をとる必要はない。その後、各参加者は、締め切り(定義は後述)の後10日以内の任意の時間に、その日付の取引終了後を含むが含まれないすべてのオプションを行使する権利がある。10日間の期間が満了した後、参加者は、均等権または同等のオプションを行使するすべての権利(例えば、行使されていない)に対して自動的にbr}を終了し、もはやいかなる効力または効果も有さない。“締め切り”とは、(X)合併、販売または許可取引の締め切り(上記(I)項のように)、(Y)買収要約の初回満期日(上記(Ii)条の場合は要人の諸条件に適合または放棄)、または(Z)50%を超える当時発行された普通株式を保有する所持者が に買収要約を提出したことを公開発表した日を意味する。
株式オプション計画は、各取締役会と我々の株主の承認を得て、必要なすべての規制承認を受けた後にのみ、計画を以下のように修正することができると規定している
| ● | 株式オプション計画3.2節(内部人に付与可能なオプション数の制限を規定している)に対する任意の 修正は許容効果がある.無株主が正式に開催された株主総会で“利害関係無投票”について株主承認を得た場合には、株式オプション計画で3.2節で禁止されている任意のオプションを付与する | |
| ● | 株式オプション計画下で発行可能な証券数の任意の修正(ただし、株式分割、合併、または再分類のようないくつかの調整が許可されている場合を除く) | |
| ● | 株式オプション計画に従って付与された任意のオプションの譲渡または譲渡を許可する任意のbr}改正が可能であるが、遺言または遺産および相続による適用法は除外される | |
| ● | は現金や証券で支払うキャッシュレス行使機能を追加しているが、株式オプション計画備蓄から対象証券の数を全額差し引くことは提供されていない | |
| ● | 繰延または制限株式単位成分または任意の他の条項を増加させることにより、従業員は、現金対価格を受け取っていない場合に証券を取得する | |
| ● | は、参加者が“内部者”であるか否かにかかわらず、任意の参加者を尊重し、 は、株式分割、合併、または再分類のようないくつかの許可された調整に関連しない限り: | |
| ● | オプション付与後の任意のオプション価格の任意の 引き下げ;または | |
| ● | オプションを異なる条項でキャンセルし、オプションを再付与する任意の行動; | |
| ● | オプション期間は、その外部満期日後に参加者への任意の 延長(“中断 期間”の範囲内で延長されることを除く) | |
| ● | 株式オプション計画に従って付与されたオプション価格決定方法の任意の 修正; | |
| ● | 任意の形態の経済援助を増加させるか、または従業員により有利な経済援助条項を任意の修正すること;および | |
| ● | 取締役会、株主、規制部門が承認した上記の改正条項の任意の 改訂が必要です。 |
| 66 |
株式オプション計画は、取締役会の承認を得て、すべての必要な規制承認を受けた後、株式オプション計画を以下のように修正することができるが、株主承認を必要としないことも規定されている
| ● | “内務”または文書的性質の修正または株式オプション計画の規定の明確化; | |
| ● | オプションの任意の帰属期限に関する改訂 ; | |
| ● | 任意の参加者に対してオプションを期限前まで延長した後の修正案 ,または任意の“非内部者”参加者に対してオプションを外部満期日を超えるまで延長する修正案 ; | |
| ● | 普通株式分割または合併、再分類、株式配当金の支払いによる発行可能普通株数または発行済み普通株の行権価格を調整する 私たちの株主に比例して特別現金または非現金分配を支払い、このような分配が私たちの株主の承認を得て、適用法による資本再編を行うことを前提としています。再編成または任意の他のイベントは、発行済みオプションを比例的に公平に調整するとともに、すべての発行済み普通株に応じて調整する必要がある | |
| ● | 株式オプション計画の終了または終了;および株式オプション計画条項に基づいて株主の承認を必要としない他の修正はない。 |
長期インセンティブ計画の概要
長期インセンティブ計画の目的は、(I)研修、経験、能力を有する管理職および他の人員およびキーサービスプロバイダを誘致し、維持することによって、私たちの長期的な財務的利益と成長を促進すること、(br}は、彼らが私たちの業務の成功に大きな貢献をできるようにすること、(Ii)成長に関連するインセンティブ措置によって管理者を激励すること、および(Iii)会社の株式の機会を増加させることによって、参加者の利益を私たちの株主の利益と一致させることである。
NGCCは長期インセンティブ計画の管理者(“管理者”)である。取締役会は、NGCCの代わりに、または補完するために、いつでも長期インセンティブ計画の管理人を務めることができる。長期奨励計画には別の規定があるほか、管理人は長期奨励計画の条項に基づいて資格を合わせた個人に奨励を付与し、奨励の種類と奨励に含まれる株式数を決定し、奨励の行使用価格と期限を含む報酬の条項と条件を決定し、長期奨励計画の目的と意図を実現するために、他のすべての必要または適切な行動をとる。
長期インセンティブ計画への参加は一般に、外部取締役を含むすべての幹部、従業員、その他の個人に開放されている。しかしながら、当社またはその任意の付属会社に提供されるサービスは、融資取引または自社証券市場の普及および維持に限定されており、長期インセンティブ計画に参加する資格はない。会社に約サービスを提供することを受けた将来の役員,従業員,他のサービスプロバイダも長期インセンティブ計画 に参加することができる。
長期インセンティブ計画は、株式オプション、株式付加価値権(“SARS”)、株式奨励、株式 単位奨励、業績株、現金業績単位、繰延株式単位、および他の株式ベースの奨励を付与することを許可し、各奨励は個別に付与することができ、または他の奨励と共に付与することができる。
長期インセンティブ計画に基づいて発行可能な普通株の最大数は、任意の所与の時間に発行された普通株式の11.4% から、当時株式オプション計画によって付与された株式オプションで発行可能な普通株式数を減算する。 長期インセンティブ計画における未発行奨励は133,920株であり、2022年12月31日現在のすべての発行済み普通株と発行済み普通株の約2.8%を占める。2022年12月31日現在、長期インセンティブ計画により、414,620株の普通株が分配されておらず、将来の普通株での決算の奨励に用いることができる。株式 オプション計画の完全な説明については、上記を参照されたい。
| 67 |
LTIPの最近完成した財政年度の燃焼率は以下のとおりである
| LTIP | ||||||||||||
| 年末 | 賞を授与する | 加重平均 未償還株 | やけど率 (1) | |||||||||
| 2022年12月31日 | 82,000 | 4,855,876 | 1.7 | % | ||||||||
| 2021年12月31日 | 34,400 | 4,596,980 | 0.7 | % | ||||||||
| 2020年12月31日 | 12,000 | 1,643,327 | 0.7 | % | ||||||||
| (1) | 年度 焼損率は百分率で表され,計算方法はLTIPにより付与された証券数 を適用した 年度未償還証券の加重平均数で割る。 |
私たちのすべての証券ベースの補償スケジュールによると、いつでも内部者に発行することができ、または任意の年以内に発行される証券の数 は、私たちが発行した証券および発行された証券の10%を超えることはできず、いかなる単一参加者も、時々私たちが発行した普通株式の5%以上のオプションを購入することを持ってはならない。
いずれの年も、長期インセンティブ計画に従って福祉を受ける権利のある外部取締役のいずれかに付与されたオプションの公正価値は、私たちのすべての証券ベースの報酬スケジュールに基づいて合計100,000ドルを超えることができず、これはNGCCによって決定される;私たちのすべての証券ベースの報酬スケジュールによれば、任意の年の間、私たちのすべての証券ベースの報酬スケジュールに基づいて、長期インセンティブ計画に従って福祉を得る権利があるすべての外部取締役が発行することができる証券の総数は、発行された証券および未償還証券の1%を超えることはできない。
以下の規定又は奨励協定に規定されている場合を除いて、長期奨励計画に基づいて付与される各報酬(株式で支払うことができない業績単位を除く)は、(I)各株式オプション又はSARが付与された日から12ヶ月の最短帰属期間、(Ii)株式、株式単位、業績 株の毎回の奨励を受ける最短帰属期間又は最短制限期間によって制限される。非従業員br取締役に付与された株式形式で支払われた業績単位および他の株式ベースの報酬(“全価値奨励”)は、最短12ヶ月の制限を受け、付与された日からカウントされ、(Iii)非従業員取締役に付与された参加者 の各全価値奨励は、付与された日から12ヶ月の最短制限期間 を受け、このような奨励の帰属又は制限が失効した場合、業績目標に対する満足状況に基づいており、最短制限期間は、付与された日から36ヶ月であり、比例分割であっても使い捨て分割払いであっても、このような報酬の付与または制限失効 が、参加者の特定のサービス要求に対する満足状況に完全に基づいている場合(このような 全価値報酬が付与された日の前12ヶ月以内に付与または失効しないことを前提とする)。業績奨励の付与が業績目標を満たすことを条件とした場合、業績期間は12ヶ月のbr持続時間未満であってはならないが、このような奨励は追加的な最低制限期間を必要としない。最短帰属期間または最短制限期間 は、参加者の死亡または障害または制御権変更の場合には適用されない。長期インセンティブ計画によれば、最低 の帰属期間または最低制限期限を考慮することなく、発行総額が長期インセンティブ計画の場合の株式プールの最大5%まで発行される報酬を付与することができる。
SARとは,プロトコルに規定された1株あたりの基本価格を付与したうえでSARを行使した日であり,指定された数の株に相当する公平な市価(定義は後述)の超過支払い を得る権利がある.法律が別途規定されていない限り、各特別行政区の基本価格は、付与日普通株公平市価の100%を下回ってはならず、特別行政区の期限は付与日から10年を超えてはならない。管理署長の適宜決定権により、特別行政区を行使する際に支払われる金は、現金、株式、または両者の組み合わせであってもよい。“公平市価”とは、当日の普通株の正常市場時間帯の正式な終値を決定することである。
長期奨励計画によって付与された奨励は、管理人が別の決定がない限り、いかなる方法でも譲渡、期待、販売、譲渡、譲渡、質権または財産権負担を行うことができない。しかし、この制限は、適用奨励協定に規定されている奨励関連普通株譲渡制限が失効した日後に受信された普通株には適用されない。
| 68 |
適用インセンティブプロトコルに規定されているまたは署長が他の方法で決定され、上述した最短許可期間または最短制限期間によって制限されることに加えて、サービス終了時(長期報酬計画に定義されているように):
| ● | 株式 オプションまたは株式付加価値権は、株式オプションまたは株式付加価値権が付与および行使できない範囲で失われる; | |
| ● | 適用された制限期間内に、当時制限されていた制限株と任意の課税されたが支払われていない配当金は没収される | |
| ● | 適用される延期期間または没収条件を適用する部分期間、または が普通株式またはRSU、履行株式または履行単位に関連する現金を交付する任意の他の条件を満たしていない場合、すべての履行株式、その後、延期または制限されたパフォーマンス単位およびRSU、ならびにそのようなRSUに関連する任意の他の計算されるが、支払われていない配当等価物は没収されるべきである。 |
もし 会社の制御権が変更された場合(長期インセンティブ計画で定義されているように)、未完了の報酬は、まだ存在するまたは後任のエンティティまたはその親会社によって継続、負担、または報酬の代替が規定されない限り、制御権変更の発効時間 で終了する。ライセンス契約が別途規定されていない限り、会社の統制権変更により終了した授賞は以下のように発生する
| ● | 株式オプションおよび特別引出権は、付与されているか否かにかかわらず完全に行使可能であり、これらの報酬の所有者は、制御権が変更される直前にこれらの報酬を行使することが許可される | |
| ● | 制限された は時間的に帰属する在庫とRSU(すなわち業績目標達成の制限を受けない) は制御権が変更される直前に完全に帰属し,RSUは適用法に従って実行可能な場合にできるだけ早く決済する | |
| ● | 業績目標実現状況 に基づいて付与された制限された 株、RSU、業績株式と業績単位は目標業績 業績目標レベルによって完全に帰属と儲けられる。目標報酬を制御権変更の日から100%にする。また,適用法により,実行可能な場合にRSUと履行単位をできるだけ早く解決する.長期インセンティブ計画は、以下の日付の中で最も早い日で終了する:(I)長期インセンティブ計画によって付与されたすべての報酬はすべて完了または終了し、任意の株式の発行が許可されていない最も早い日 長期的なインセンティブはまだ新しい報酬の下で与えられます又は(Ii) 改正及び再記載された長期インセンティブ計画10周年の日には、我々の株主が を承認する。 |
管理人は、長期インセンティブ計画を修正、変更、または終了することができるが、参加者の同意なしに、以前に付与された報酬に対して、参加者の権利を実質的に損なういかなる修正、変更または終了を行ってはならないが、当社の普通株が上場または取引を受ける任意の証券取引所または市場の適用法律または規則を遵守するために、または会社または参加者が不利な税金または会計結果を受けることを防止するためには、この限りではない。しかしながら、いずれの場合も、我々の株主の承認を得ず、 は、(I)長期インセンティブ計画における参加者の計上すべき利益を大幅に増加させること、(Ii)長期インセンティブ計画または参加者によって発行可能な株式数を増加させること、(Iii)長期インセンティブ計画に参加する資格を大幅に拡大すること、(Iv)株式オプションおよびSARS再定価を禁止する禁止令を廃止または修正すること、を行うことができない。(V)最長期間の延長、または株式オプションおよびSARSによって許容される最低行権価格またはベース価格の低減、(Vi)増発または追加オプションの発行を禁止する規定の修正、(Vii) 長期インセンティブ計画における改訂条項の修正、または(Viii)長期インセンティブ計画を改訂し、10%以上の内部者参加制限を廃止または超える。
| 69 |
優れた オプションによる報酬と株式ベースの報酬
次の表は、2022年12月31日までに指定された役員に授与されたすべての賞を示しています
| オプションに基づく 報酬 | 株式に基づく報酬 | |||||||||||||||||||||||||||
| 名前.名前 | 発行日 (mm/dd/yyyy) |
オプションを行使していない証券数 (1) (#) |
オプション 行使価格 ($) |
オプション の有効期限 (mm/dd/yyyy) |
行使されていない現金オプションの価値 (2) ($) |
発行日 | まだ帰属していない株式または株式単位数 (#) |
市場 や支出 まだ付与されていない株式奨励の値 ($) |
市場 または未支払いまたは分配された既得株奨励の支払価値 ($) |
|||||||||||||||||||
ポーリーニクラウス |
12/06/2016 | 100 | 86.25 | 12/06/2023 | — | — | — | — | — | |||||||||||||||||||
| 08/15/2019 | 1,000 | 53.75 | 08/15/2026 | — | — | — | — | — | ||||||||||||||||||||
| 11/11/2019 | 1,400 | 25.75 | 11/11/2026 | — | — | — | — | — | ||||||||||||||||||||
| 12/14/2020 | 1,400 | 9.15 | 12/14/2027 | — | — | — | — | — | ||||||||||||||||||||
| 12/17/2021 | 4,000 | 10.51 | 12/17/2028 | — | — | — | — | — | ||||||||||||||||||||
| ジュリアーノ·ラフラタ | 1/10/2022 | 2,000 | 8.88 | 01/10/2029 | — | — | — | — | — | |||||||||||||||||||
| Gerlach、 Matthias | 12/06/2016 | 600 | 86.25 | 12/06/2023 | — | — | — | — | — | |||||||||||||||||||
| 12/04/2019 | 800 | 21.75 | 12/04/2026 | — | — | — | — | — | ||||||||||||||||||||
| 12/14/2020 | 1,000 | 9.15 | 12/14/2027 | — | — | — | — | — | ||||||||||||||||||||
| 12/17/2021 | 2,000 | 10.51 | 12/17/2028 | — | — | — | — | — | ||||||||||||||||||||
ガンサー、エクハド |
11/08/2016 | 16 | 87.50 | 11/08/2023 | — | — | — | — | — | |||||||||||||||||||
| 12/06/2016 | 400 | 86.25 | 12/06/2023 | — | — | — | — | — | ||||||||||||||||||||
| 12/04/2019 | 1,000 | 21.75 | 12/04/2026 | — | — | — | — | — | ||||||||||||||||||||
| 12/14/2020 | 1,000 | 9.15 | 12/14/2027 | — | — | — | — | — | ||||||||||||||||||||
| 12/17/2021 | 2,000 | 10.51 | 12/17/2028 | — | — | — | — | — | ||||||||||||||||||||
ニコラ·アンマー |
12/06/2016 | 400 | 86.25 | 12/06/2023 | — | — | — | — | — | |||||||||||||||||||
| 12/04/2019 | 1,000 | 21.75 | 12/04/2026 | — | — | — | — | — | ||||||||||||||||||||
| 12/14/2020 | 1,000 | 9.15 | 12/14/2027 | — | — | — | — | — | ||||||||||||||||||||
| 12/17/2021 | 2,000 | 10.51 | 12/17/2028 | — | — | — | — | — | ||||||||||||||||||||
| Teifel、マイケル | 12/17/2021 | 2,000 | 10.51 | 12/17/2028 | — | — | — | — | — | |||||||||||||||||||
| (1) | 未行使オプション関連証券数は、2022年12月31日までのすべての未償還奨励を代表する。 |
| (2) | 財政年度末に行使されなかった現金オプション価値は、ナスダック普通株の財政年度最終取引日(12月31日)の終値との差額に基づいて計算される。2022年)は3.18ドル,オプションの行権価格, に未行権のオプション数を乗じた. |
2022年12月31日現在、私たちが任命した幹部は株式ベースの報酬を何も受けていない。
奨励計画奨励−年内に帰属または稼いだ価値
次の表は、2022年12月31日までの財政年度中に、任命された幹部1人当たりの報酬プランの奨励価値を示している
オプションに基づく 奨励−年内帰属の価値(1) | 株式に基づく報酬−年内帰属の価値 | 非持分インセンティブ計画報酬−年内に稼ぐ価値(2) | ||||||||||
| $ | $ | $ | ||||||||||
| ポーリーニクラウス | — | — | 45,561 | |||||||||
| ジュリアーノ·フラタ | — | — | 31,192 | |||||||||
| Gerlach、 Matthias | — | — | 24,370 | |||||||||
| ガンサー、エクハド | — | — | 19,072 | |||||||||
| ニコラ·アンマー | — | — | 23,310 | |||||||||
| Teifel、マイケル | — | — | 23,310 | |||||||||
| (1) | オプションが帰属日に行使されていれば現金化可能な合計ドル価値を表す は、ナスダック普通株のその帰属日の終市価格と使用価格との差に基づいている。ナスダック普通株の帰属日の終値が行権価格を下回る場合、ドルは達成されたとみなされる。 | |
| (2) | 2022年にはPaulini博士、Gerlach博士、Guenther博士、Ammer博士が2022年に2021年関連の活動でボーナスを獲得し、2022年に2022年に関連活動で2023年にボーナスを獲得する。 |
| 70 |
集計表 給与表
以下に示すbr報酬集計表は、2022年12月31日、2021年、2020年12月31日までの各財政年度において、任命された各役員が様々な身分で提供されるサービスにより得られた報酬情報を示している。次の表のすべての金額をドル ドルで表します。AuldさんとLa Frattaさんの現金はカナダドルで支払われた。Paulini博士、Guenther博士、Gerlach博士、Teifel博士、Ammer博士に支払われたすべての現金はユーロだ。
集計表 給与表
| 非持分インセンティブ計画報酬(1) | ||||||||||||||||||||||||||||||||||||
| 氏名 と主要職務 | 年.年 | 賃金.賃金 ($) | に基づく報酬を共有する ($) | オプション に基づく報酬 ($) | 年間奨励計画 ($) | 長期インセンティブ計画 ($) | 年金.年金 価値がある ($)(2) | 登録退職貯蓄計画/401 K口座への入金 ($) | 全額補償する ($) | |||||||||||||||||||||||||||
| ポーリーニクラウス(3)総裁と行政長官 | 2022 | 319,614 | — | — | 45,561 | — | 218,798 | — | 583,972 | |||||||||||||||||||||||||||
| 管理 | 2021 | 374,496 | — | 35,298 | 162,530 | — | 213,700 | — | 786,024 | |||||||||||||||||||||||||||
| 取締役AEZドイツ | 2020 | 306,086 | — | 9,503 | 183,580 | — | 292,983 | — | 792,152 | |||||||||||||||||||||||||||
| “友情は長く続く”レスリー | 2022 | 17,116 | — | — | — | — | — | — | 17,116 | |||||||||||||||||||||||||||
| 社長副上級 | 2021 | 163,038 | — | — | — | — | — | — | 163,038 | |||||||||||||||||||||||||||
| 最高財務官 | 2020 | 166,834 | — | — | — | — | — | — | 166,834 | |||||||||||||||||||||||||||
| ジュリアーノ·ラフラタ 最高財務官上級副社長 | 2022 | 208,262 | — | 14,944 | 31,192 | — | — | 12,921 | 267,319 | |||||||||||||||||||||||||||
| ガンサー、エクハド 上級副総裁商業発展と連合 | 2022 | 223,359 | — | — | 19,072 | — | (146,455 | ) | — | 95,976 | ||||||||||||||||||||||||||
| 管理 管理 | 2021 | 238,737 | — | 17,649 | 67,021 | — | 5,019 | — | 328,426 | |||||||||||||||||||||||||||
| 取締役AEZドイツ | 2020 | 218,966 | — | 6,788 | 85,460 | — | 97,937 | — | 409,151 | |||||||||||||||||||||||||||
| Gerlach、
Matthias 上級副総裁 | 2022 | 200,316 | — | — | 24,370 | — | (247,820 | ) | — | (23,135 | ) | |||||||||||||||||||||||||
| 総裁 製造業 | 2021 | 203,276 | — | 17,649 | 55,319 | — | 16,314 | — | 292,558 | |||||||||||||||||||||||||||
| サプライチェーンと | 2020 | 185,379 | — | 6,788 | 70,810 | — | 14,827 | — | 277,803 | |||||||||||||||||||||||||||
| ニコラ·アンマー 首席医療官と | 2022 | 173,724 | — | — | 23,310 | — | (29,047 | ) | — | 167,987 | ||||||||||||||||||||||||||
| 総裁副上級 | 2021 | 182,787 | — | 17,649 | 53,191 | — | 2,400 | — | 256,027 | |||||||||||||||||||||||||||
| 臨床発展 | 2020 | 154,512 | — | 6,788 | 64,880 | — | 2,266 | — | 228,446 | |||||||||||||||||||||||||||
| Teifel、マイケル 首席科学官と | 2022 | 153,558 | — | — | 23,310 | — | (139,729 | ) | — | 37,138 | ||||||||||||||||||||||||||
| 総裁副上級 | 2021 | 157,510 | — | — | — | — | 1,007 | — | 158,517 | |||||||||||||||||||||||||||
(1) 非持分インセンティブ計画報酬には現金ボーナスが含まれています。2022年の間に、Paulini博士、Gerlach博士、Guenther博士、Ammer博士はそれぞれ2021年に支給された2021年関連活動のボーナスを獲得し、2023年に2022年に関連活動に支給されるボーナスbrを獲得する。
(2) Paulini博士とGuenther博士は、Unterstützungskasse Degussa e.V.が1999年12月31日までにAEZSドイツ社(またはその前身)に雇用された従業員のための固定拠出年金計画であるDUPK(以下の定義)に参加している。DUPKには,資金のある多雇用者による支払い計画の間接義務と,資金のない直接固定福祉計画義務がある。Gerlach博士は、Unterst≡tzungskasse Degussa e.V.保守による固定拠出年金計画RUK 1(以下の定義)に参加した。Ammer博士は、Unterst≡tzungskasse Degussa e.V.によって維持されるRUK 2(以下の定義)に参加した。年金価値は、任命された各執行官の年金負債の2021年12月31日から2022年12月31日までの変化を表す。2022年、割引率精算は、2021年の1.1%から2022年の3.75%に大幅に増加すると仮定し、すなわち は年金福祉計画債務の推定に用いられる。何人かの指名された実行幹事にとって、これにより年金価値が低下します 表を参照してください
| 71 |
(3) ポーリーニ博士は取締役有限会社の取締役社長や役員役員を務めている間何の報酬も得られませんでした。
前表に示したオプション報酬のbr価値は,先日の最終取引日のナスダック普通株の終値にその日のブラック·スコアズ係数とそのbrの日に付与された株式オプション数を乗じたものである.2022年について、ブラック·スコアズ推定モデルは、期待寿命5.72年、予想変動率115.75%、無リスク年利1.59%、期待配当収益率0%の仮定に基づいてオプションを推定した。先日ブラック·スコアーズオプション定価モデルに適用された仮定については、2021年現在、2020年と2019年12月31日までの年度および2020年、2019年および2018年12月31日までの年度の総合財務諸表を参照されたい。当社はこのようなオプションの公正価値を最も正確に反映しているため、ブラック·スコイルズ推定値モデルを採用している。次の表にオプションベースのbr報酬の価値と対応するブラック-スコアズ係数を示す:
| 付与日 | 付与された値 | ブラック·スコルス係数 | ||||||
| 2016年11月9日 | $ | 87.50 | 80.35 | % | ||||
| 2016年12月6日 | $ | 86.25 | 80.57 | % | ||||
| 2016年12月16日 | $ | 95.00 | 80.68 | % | ||||
| 2017年8月15日 | $ | 51.25 | 78.86 | % | ||||
| 2018年4月2日 | $ | 36.50 | 77.57 | % | ||||
| 2018年6月22日 | $ | 52.75 | 80.86 | % | ||||
| 2019年8月15日 | $ | 53.75 | 79.22 | % | ||||
| 2019年11月11日 | $ | 26.25 | 67.13 | % | ||||
| 2019年12月4日 | $ | 21.75 | 68.01 | % | ||||
| 2020年12月14日 | $ | 9.15 | 74.19 | % | ||||
| 2021年12月17日 | $ | 10.50 | 83.94 | % | ||||
| 2022年1月10日 | $ | 8.88 | 84.14 | % | ||||
CEOの報酬
私たちの総裁とCEOの報酬 は私たちの役員報酬政策(br“役員報酬”の節で述べた)によって管轄され、総裁とCEOは他の役員とともに私たちのすべてのインセンティブ計画に参加する。
Paulini博士の総収入は2022年12月31日までの財政年度で583,972ドルで、45,561ドルの奨励金が含まれている。
2022年12月31日までの財政年度について、取締役会は長期インセンティブ計画に基づいてPaulini博士に株式オプションを付与することを承認していない。
株式オプション計画の完全な説明については、“役員長期持分報酬計画-株式オプション計画概要”を参照されたい。長期インセンティブ計画の完全な説明については、“役員長期持分報酬計画である長期インセンティブ計画の概要”, を参照されたい。
退職金や退職などの福祉
私たちが任命したAEZSドイツ社に雇われたすべての幹部は固定拠出年金計画に参加した。このような年金計画の条項は以下の通りだ。
| 72 |
Degussa 年金(“DUPK”)
Paulini博士とGuenther博士は、Unterstützungskasse Degussa e.V.メンテナンスによる固定拠出年金計画は、1999年12月31日までにAEZSドイツ会社(またはその前身)に雇用された従業員に適用されるDUPKに参加した。 DUPKには、資金のある多雇用主納付計画による間接的な義務と、直接的な未確定資金の福祉計画 義務が含まれている。
DUPKの基金多雇用者納付分によると、AEZSドイツ社と従業員の支払いは従業員の前年の総賃金に基づいて計算される。従業員はその月平均賃金の2%を貢献しているが、ドイツのAEZS 貢献額は従業員貢献の1.784倍である。納付は社会保障納付の分担上限 に限られる。2022年、社会保障納付分担上限は月7666ドル(7275ユーロ)となる。したがって、従業員は毎月最大153.32ドル(145.50ユーロ)、AEZSドイツ社は毎月最大273.52ドル(259.57ユーロ)を納めている。
DUPKの資金支援のない固定福祉部分によれば,従業員は社会保障納付評価上限(“補足年金”)を超える 従業員賃金に資金支援がなく,会社貸借対照表に年金福祉義務として示されている部分の将来の年金を追加申告することができる。補足年金 は、社会保障納付評価の上限のパーセントである架空の賃金ピークの1.25%に相当する。また,br}従業員は年間クリスマス福祉(“クリスマス福祉”)を受ける権利があり,額はサービス年度ごとに最終的に年金の月収の1.4%を計算でき,社会保障納付評価上限の制限を受けている。従業員の納付 とAEZSドイツの納付は月ごとに年金基金に移行し,AEZSドイツの納付は賃金とともに を計算して年金支払準備金とする。民間年金提供者が約束した年金を支払わないか、支払うことができない場合、約束された年金給付を従業員に支払う責任がある。従業員は、雇用期間中の納付に基づいて年金 を取得し、法定退職年齢に達した後に、AEZSドイツ社でその年齢まで働いているか否かにかかわらず、補充年金とクリスマス福祉 を得る。すべての 直接年金義務および繰延補償からの年金義務が含まれており,当社の年金福祉義務に計上されている。
Rück gedeckte Unterstützungskasse 1(“RUK 1”)
Gerlach博士はUnterstützungskasse Degussa e.V.によって維持された固定納付年金計画RUK 1に参加した。RUK 1によると、ドイツAEZS はGerlach博士の月収総収入の2.4%に貢献し、Gerlach博士は月総収入の2%に貢献した。 支払いは社会保険納付分担上限に限定される.しかし、AEZSドイツ社は、社会保険納付評価の上限を超える賃金の一部に、その月賃金総額の18%に相当する追加支払いを提供している。2022年、社会保障納付分担上限は月7,666ユーロ(7,275ユーロ)となる。そのため、AEZSドイツ社は毎月最大1,844.48ドル(1750.41ユーロ)(18%の追加寄付を含む)、Gerlach博士は毎月最大153.32ドル(145.50ユーロ)を寄付している。この2つの支払いはいずれも月給会計で計算され、月ごとに救済基金に移されている。民間年金提供者が約束した年金支払いをしていないか、支払うことができない場合、Gerlach博士に約束された年金給付を支払う責任がある。Gerlach博士は、彼がAEZSドイツ社でその年齢まで働いているかどうかに関係なく、法定退職年齢に達した後の勤務期間の納付に基づいて年金を得る。
Rück gedeckte Unterstützungskasse 2(“RUK 2”)
Ammer博士はUnterstützungskasse Degussa e.V.が維持する固定拠出年金計画RUK 2に参加した。RUK 2によると、AEZS ドイツはAmmer博士の月総収入の2.4%に貢献し、Ammer博士は彼女の月総収入の3%に貢献した。納付 は社会保険納付分担上限に限定される.2022年、社会保障納付分担上限は月7,666ユーロ(7,275ユーロ)となる。そのため、AEZSドイツ社は毎月最大183.98ドル(174.60ユーロ)、アンマー博士は毎月最大229.98ドル(218.25ユーロ)を寄付している。この2種類の納付金はいずれも月給計算で計算され、月ごとに救済基金に転入する。民間年金提供者が約束した年金を支払うことができないか、または支払うことができない場合、私たちはAmmer博士に約束された年金給付を支払う責任がある。Ammer博士は、彼女がAEZSドイツ社でその年齢まで働いているかどうかに関係なく、法定退職年齢に達した後の勤務期間の納付に基づいて年金を得る。
| 73 |
次の表には、DUPKに参加する各指定幹部の以下の情報が含まれており、DUPKは会社唯一の福祉計画であり、明確な福祉構成要素を持っている
| ● | 2022年12月31日までの貸記サービス年限 ; | |
| ● | 2022年12月31日と65歳の正常退職時に計上または稼ぐべき年間福祉と、 | |
| ● | A 2021年12月31日から2022年12月31日までの間の債務の入金。 |
| 年数 | 年間福祉
支払額(元)(2) | 開ける 提示する の値 定義されている | 補償性の | -ではない | 終業する 提示する の値 定義されている | |||||||||||||||||||||||
| 名前.名前 | 貸方に記入する サービス.サービス (#)(1) | 年末に | 65歳の時に | 利益 義務 ($)(3) | 変わる ($)(4) | 補償性の 変わる ($)(5) | 効果がある 債務 ($)(3) | |||||||||||||||||||||
| ポーリーニクラウス | 25 | 72,863 | 90,349 | 1,275,359 | 218,798 | (140,813 | ) | 1,353,345 | ||||||||||||||||||||
| ガンサー、エクハド | 32 | 48,643 | 48,643 | 1,228,378 | (146,455 | ) | (135,625 | ) | 946,298 | |||||||||||||||||||
| Gerlach、 Matthias | 22 | 12,236 | 25,378 | 467,544 | (247,820 | ) | (51,622 | ) | 168,102 | |||||||||||||||||||
| Teifel、マイケル | 18 | 14,834 | 14,834 | 396,134 | (141,864 | ) | (43,737 | ) | 210,532 | |||||||||||||||||||
| ニコラ·アンマー | 8 | 2,269 | 4,895 | 65,352 | (29,047 | ) | (7,216 | ) | 29,089 | |||||||||||||||||||
(1) 2022年12月31日までの入金サービス年限は、AEZSドイツ社の実サービス年限に対応する。
(2) 任命された実行幹事ごとに、2022年12月31日に支払われる年間給付額は、任命された実行幹事が2022年12月31日に雇用終了後に65歳から受給する権利がある年金である。任命された実行主任ごとに、65歳で支払われるべき年間福祉は、65歳時の推定貸金サービスを反映するために、2022年12月31日に支払われるべき年間福祉が増加する。
(3) 現在値は、当社の総合財務諸表に開示されている退職金負債を決定する際に用いられる精算仮定と方法に基づいて、示された日までの退職金負債の推定価値である。 過去には、十分な資料が不足しているため、ある退職金福祉計画が固定供出計画として入金されており、当社は当該等の退職金 福祉計画に関する定義された福祉債務、計画資産、コストを比例して計上できていない。2021年、会社はより多くの情報を取得し、固定福祉義務や計画資産における割合シェアの計上を開始した。改正された会計処理方法を反映するために、指定実行幹事毎の固定福祉債務期間の初期現在値を調整した。
(4) 補償的変化とは、任命された実行幹事毎に、2021年12月31日から2022年までの間の年金負債の変化をいう。
(5) 報告金額の計算に用いる精算仮説及び方法は、当社が付記15に開示した2022年及び2021年の連結財務諸表及び国際財務報告基準に規定されている計算すべき福祉負債及び年間費用を算出するための精算仮説及び方法と同様である。推定金額を決定するための方法および仮定は、他の発行者と使用する方法および仮定とは異なる であるため、異なる発行者間の数字は直接比較できない可能性がある。上に示したすべての 金額は仮定に基づいており,時間とともに変化する可能性のある契約権利を表す.
| C. | 取締役会 実践 |
私たちのbr条項は、私たちの取締役会は最低5(5)名から最大15(15)名の取締役で構成されなければならないと規定しています。取締役は当社の株主が毎年選挙して選出されるが、取締役は時々1人以上の取締役を委任することができ、このように委任された取締役総数は前回の株主周年大会で選ばれた取締役数の3分の1以下であることが条件となる。当選した各取締役は、そのポストが早期に離任しない限り、次の株主周年総会が終了またはその後継者が正式に選挙または任命されるまで在任を継続する。私たちは私たちの独立役員とサービス協定を持っていません。
プロジェクト6 Aを参照。私どもの取締役と会社の上級管理職ごとのサービス期限に関する情報です。
取締役会常務委員会
私たちのbr取締役会は監査委員会とNGCCを設立した。
| 74 |
監査委員会
監査委員会は取締役会がその監督責任を履行するように協力する。監査委員会は財務報告の流れ、br}内部制御システム、監査の流れ、及び私たちは法律法規と私たちの道徳行為準則を遵守する流れを監督します。職責を履行する際、監査委員会は取締役会、管理職、非常勤監査人と有効な仕事関係を維持する。その職責を効果的に履行するために、各委員会メンバーは、委員会メンバーの詳細な職責と、私たちの業務、運営、リスクを理解するだろう。
監査委員会の機能は監督であり、その定款に規定された職責と権力(本年度報告書20-F表の添付ファイル11.3参照)を持っているが、委員会には責任計画や監査を行う責任もなく、私たちの財務諸表が完全で正確で、公認された会計原則に適合しているかどうかを決定する責任もなく、内部統制や手続きを維持する責任もない。
監査委員会の現メンバーはデニス·ターピン(議長)、ピーター·G·エドワーズ、ギルス·ガニーオン。
NGCC
当社とその付属会社の役員の報酬はNGCCが取締役会に提案します。NGCCは(I)取締役会の会社管理問題の策定に協力する方法を担当し、(Ii)新しい取締役会指名者を推薦し、(Iii)取締役会とその委員会を監督し、それぞれの議長と個人取締役の有効性評価、および(Iv)取締役会メンバーの指名と役員報酬および私たちのコーポレートガバナンス実践において指導役を務めることについて取締役会に提案する。それはまたすべての合理的な措置を取って の適切な人力資源政策、プログラムと制度を確保して、例えば採用と保留政策、能力と業績 の指標と測定基準、訓練と発展計画及び市場に基づく競争的な報酬と福祉構造を確保して、私たちは業務目標を実現するために必要な人員の素質を吸引、激励し、維持することができるようにする。NGCCはまた、取締役会が私たちの執行と高度管理メンバーの採用、保留、発展、評価、報酬、およびbr}後継計画に関連する職責を履行することに協力します。
したがって、NGCCは、彼らの任命および終了の条項および条件を含む高官の任命を提案し、彼らの報酬を提案し、役員の報酬政策および慣行に関連するリスク識別および管理を監視することを含む、私たち高官の業績評価を検討することを提案する。取締役会はNGCCメンバーを含み、CEOの会社戦略、目標、業績目標を審査し、これらの目標と目標の実現状況に基づいてその業績と報酬を評価し、評価する。
NGCCは、私たちが置かれている業界、監督と競争環境はバランスのとれたリスク負担レベル を必要とし、専門生物製薬会社幹部の業績予想を促進し、実現する必要があることを認識した。NGCCは、我々の役員報酬計画は、役員が不適切または不合理なリスクを負担することを奨励すべきではないと考えている。この点で、NGCCは、役員報酬の一部を我々の短期および長期業績および各役員の業績に適切に関連付ける報酬方法を実施することを提案し、このような報酬方法に関連するbr}優位性とリスクを考慮する。NGCCはまた,株主価値の創造を奨励することを目的とした報酬政策の策定を担当しており,我々の短期的かつ長期的な業績と各幹部とのバランス を反映している。
国家調整委員会は現在、Carolyn Egbertさん(議長)、Peter G.Edwardsさん、Gilles Gagnonさんによって構成されており、彼らは皆独立している。NGCCのメンバー集団は、そのタスクを遂行するために必要な知識、経験、背景を持っていると取締役会は考えている:
| 75 |
| D. | 従業員 |
2022年12月31日までに、私たちは21人の在職従業員がいて、そのうち17人はドイツのフランクフルトに常駐しています。また,1人の従業員が米国におり,他の3人の在職従業員はそれぞれケベック,ニューブランクス,カナダオンタリオ州で働いている。
私たちの現在の従業員は以下の活動に従事している:(I)6人は研究開発、監督事務と品質保証の仕事に従事している;(Ii)6人は商業運営と業務発展に従事している;(Iii)9人は財務と会計を含む各種行政機能に従事している。私たちはどんな販売代表も雇っていません。2021年12月31日まで、私たちは17人の在職従業員がいて、そのうち16人はドイツのフランクフルトに常駐しています。しかも、私たちはアメリカに従業員がいて、私たちの前の首席財務官はカナダのトロントにいた。
我々 は,従業員と秘密保持,忠誠,競業禁止,譲渡雇用期間中に開発されたすべての知的財産権の合意 を締結した.
| E. | 所有権を共有する |
次の表は、2023年3月22日までに当社の現職役員と指定された役員が提供してくれた会社の普通株式と株式オプションの所有権に関する情報を示しています
| 名前.名前 | 所有または保有する普通株式数 | パーセント(1) | 保有株式オプション数: (2) | 現在行使可能なオプション 番目 | ||||||||||||
| ニコラ·アンマー | — | — | 4,400 | 2,734 | ||||||||||||
| エグベルトキャロライン | 1,276 | * | 3,114 | 3,114 | ||||||||||||
| エドワーズピーター·Gです | — | — | — | — | ||||||||||||
| Gagnon, ギルス | — | — | — | — | ||||||||||||
| Gerlach、 Matthias | — | — | 4,400 | 2,734 | ||||||||||||
| ガンサー、エクハド | — | — | 4,416 | 2,750 | ||||||||||||
| ポーリーニクラウス | 4,200 | * | 7,900 | 4,768 | ||||||||||||
| テピン デニス | 4,821 | * | — | — | ||||||||||||
| Teifel、マイケル | — | — | 2,000 | 667 | ||||||||||||
| ジュリアーノ·フラタ | — | — | 2,000 | — | ||||||||||||
| 合計する | 10,297 | — | 28,230 | 16,767 | ||||||||||||
* 1%未満
| (1) | 2023年3月22日現在の4,855,876株発行普通株に基づく | |
| (2) | オプション満期日及び行権価格に関する情報は、“未完了オプションベース報酬及び株式ベース報酬”というタイトルの表を参照されたい。 |
| 第 項7 | 大株主と関係者が取引する |
| A. | 大株主 |
私たち は他の会社や任意の外国政府によって直接または間接的に所有または制御されているわけではない。米国証券取引委員会およびカナダ証券規制機関に提出された文書 によると、2023年3月22日現在、以下に述べる以外に、私たちの普通株式を直接または間接的に所有または制御または指揮する個人または実体 はなく、それに付随する投票権 は、私たちのすべての普通株式(私たちは主要株主と呼ぶ)の5%を超える。
| 76 |
大株主持株率の変化
私たち 2017年は大株主がいません。2018年,J.Goldman&Co.,L.P.J.,Goldman Capital Management,Inc.とJay G.Goldman(総称して“ゴールドマン”)は5%を超える発行済み普通株を買収して主要株主となったが,2020年2月14日に米国証券取引委員会に提出されたスケジュール13 Gのみにより,2019年12月31日現在,ゴールドマン·サックスは5%を超える普通株の実益所有者ではなくなった.2020年2月18日、停戦資本マスターファンド株式会社は、私たちの発行済み普通株の5%以上を買収して当社の大株主となりましたが、2021年2月16日にアメリカ証券取引委員会に提出された第13 Gスケジュールのみに基づいて、2020年12月31日現在、実益が5%を超える私たち普通株を保有していません。2020年7月1日、Intrasastal Capital LLCは、発行済み普通株の5%以上を買収して主要株主となったが、2022年2月11日に米国証券取引委員会に提出されたスケジュール13 Gのみに基づいて、2021年12月31日現在、実益が5%を超える私たち普通株を保有していない。2020年7月2日,Lind Global Macro Fund,LPは5%を超える発行済み普通株を買収して大株主となったが,2022年2月11日に米国証券取引委員会に提出されたスケジュール13 Gのみにより, 2021年には実益が5%を超える我々普通株を保有しなくなった。2023年3月22日まで、私たちには大株主はいない。
アメリカの株主
我々の譲渡エージェントが提供してくれた情報の審査によると,2023年3月22日現在,我々の普通株は14名の登録所有者であり,そのうち2名の登録住所は米国であり,合計で発行された普通株の約99%を保有している.私たちの普通株の実益所有者の数は記録保有者の数よりはるかに多いと信じています。私たちの普通株の大多数はブローカーの“街名”で保有されているからです。
| B. | 関連する 側取引 |
“第10項-付加情報”で述べたように、我々の経営陣との雇用契約や賠償協定以外には、関連者との取引は何も存在しない。
| C. | 専門家や法律顧問の興味は |
は要りません。
| 第 項8. | 財務情報 |
| A. | 合併の レポートとその他の財務情報 |
本年度報告書20-F表の一部として提出された連結財務諸表は、“第17項--財務諸表”の下に記載されている。
| B. | 重大な変化 |
本年度報告がForm 20−F形式で他の地方に含まれる年次連結財務諸表の日から大きな変化はなかった。
| 第 項9. | 割引と発売 |
| A. | 割引 とリスト詳細 |
適用されないが、第9 A条第4項を除く。私たちの普通株はナスダックとトロント証券取引所に上場しています。コードはAEZSです。次の表は、当社の普通株の2022年12月31日までのナスダックとトロント証券取引所での終値の高値と最低点を示している
| 77 |
| ナスダック (ドル) | TSX (カナダ元) | |||||||||||||||
| 高 | ロー | 高 | ロー | |||||||||||||
| 2020 | 36.00 | 7.50 | 46.75 | 9.75 | ||||||||||||
| 2021 | 83.50 | 9.00 | 106.25 | 16.00 | ||||||||||||
| 2022 | 10.50 | 3.02 | 12.75 | 4.05 | ||||||||||||
| 第4四半期 | 4.34 | 3.02 | 5.84 | 4.05 | ||||||||||||
| 第3四半期 | 6.00 | 3.69 | 7.50 | 5.07 | ||||||||||||
| 第2四半期 | 9.25 | 4.25 | 11.75 | 5.50 | ||||||||||||
| 第1四半期 | 10.50 | 8.25 | 12.75 | 10.25 | ||||||||||||
| 2021 | 83.50 | 9.00 | 106.25 | 16.00 | ||||||||||||
| 第4四半期 | 19.25 | 9.00 | 24.00 | 11.38 | ||||||||||||
| 第3四半期 | 22.00 | 14.75 | 27.50 | 19.00 | ||||||||||||
| 第2四半期 | 28.50 | 20.75 | 35.50 | 25.50 | ||||||||||||
| 第1四半期 | 83.50 | 12.75 | 106.25 | 16.00 | ||||||||||||
| 2020 | 36.00 | 7.50 | 46.75 | 9.75 | ||||||||||||
| 第4四半期 | 11.00 | 7.50 | 14.00 | 9.75 | ||||||||||||
| 第3四半期 | 13.75 | 8.50 | 18.25 | 11.50 | ||||||||||||
| 第2四半期 | 29.25 | 11.25 | 42.75 | 16.50 | ||||||||||||
| 第1四半期 | 36.00 | 10.50 | 46.75 | 14.75 | ||||||||||||
| B. | 流通計画 |
は適用されない.
| C. | 市場 |
私たちの普通株はナスダックとトロント証券取引所で取引され、コードは“AEZS”です。
| D. | 売却株主 |
は適用されない.
| E. | 薄めにする |
は適用されない.
| F. | 発行費用 |
は適用されない.
| 第 項10. | その他 情報 |
| A. | 株式 資本 |
は要りません。
| B. | 覚書と会社規約 |
私たちのbrは、CBCAによって再記述された定款(“重述の定款”)と が2012年10月2日、2015年11月17日と2019年5月9日(重述の定款とともに、“定款”)によって改訂された定款および2013年3月21日に改訂·重述された定款(“定款”)の制約を受けている。私たちの文章はすでにカナダ会社に記録されています。会社番号は264271-9です。このような条項は宣言の目的を含まず、私たちが展開する可能性のある業務に何の制限も加えないだろう。
| 78 |
株主権利を検査する
CBCAによると、株主は私たちが登録した株主リストのコピーを得る権利がある。株主リストを取得するために、株主は、CBCAによって許可されるbrの目的のためにのみ使用される宣言を含む宣誓書を提供しなければならない。これらの許容される目的は、私たちの株主の投票に影響を与えるように努力すること、私たちの証券を買収する要約、私たちの事務に関連する任意の他の事項を含む。私たちは株主リストを提供するために合理的な費用を受け取る権利があり、上記の誓約書を受け取ってから10日以下にこのリストを交付しなければならない。
CBCAによると、株主はある会社の記録を調べる権利があり、著者らの定款と定款、議事録と株主決議を含む。株主は私たちの取締役の議事録と決議を調べる法的権利がありません。私たちの株主は私たちのいくつかの財務情報を得る権利があります。CBCAは、証券法を適用して提出を要求した年度·四半期財務諸表に加えて、年次株主総会のたびに監査された比較年度財務諸表 を提出することを求めている。また、株主は、私たちの各子会社と任意の他の会社の実体の財務諸表を審査する権利があり、これらの実体の勘定は私たちの財務諸表に統合されています。
役員.取締役
我々が持たなければならない最小コントローラ数は5(5),最大数は15(15)である.CBCAによると、私たちの役員のうち少なくとも25%がカナダ住民でなければなりません。取締役になるためには、一人は自然人でなければならず、満18歳になり、精神が健全で、破産せず、またどの裁判所も彼の取締役を務めることを禁止することはできない。これらの条項、細則、CBCAはすべて取締役に対していかなる強制退職要求も提出しなかった。
取締役は取締役を選挙する必要がある年次会議で多数票で選出され、任期は後継者選挙までですが、辞任や死亡やその他の理由で欠員した場合は除外します。当社の定款の規定を満たしている場合には、すべての取締役がまだ取締役に就く資格があれば、再任に立候補することができます。取締役会は一定期間ごとに交代するのではなく、年に1回選挙される。
私たちの定款や文章では取締役が株主でなければならないと規定されていません。
取締役は取締役会や取締役会がその権力を付与する可能性のある委員会が時々決定した報酬を得る権利がある。国家役員委員会の認可によると、この委員会は少なくとも多数の独立取締役からなり、取締役の報酬について取締役会に提案することを担当している。独立役員の法定人数がない場合には、取締役が自分の報酬を議決して承認することを許可する。
“条例”は,取締役契約側であり,取締役幹部あるいはその中で重大な権益を持つ任意の者であり,吾などと締結あるいは締結しようとする重大な契約や取引あるいは締結しようとする重大な契約や取引の当事側であれば,“条例”の規定の方式で吾などにその権益の性質や程度を開示しなければならず,あるいはその権益を取締役会議事録に登録することを要求し,たとえ当該契約が吾などの正常な業務活動に関係していても, 取締役や株主承認を必要としないことを規定している。総裁または任意の取締役の要求に応じて、利益衝突状態にある取締役は、取締役会がこの件を議論している間に会議を離れなければならない。CBCAは、契約または取引がない限り、そのような取締役が契約または取引を承認する任意の決議案への投票を禁止する
| ● | 主に私たちの役員や私たちの付属会社の役員、役員、従業員または代理である彼または彼女の報酬に関係しています | |
| ● | 取締役の責任は中国商務部が許可した賠償または保険を受けるかどうか | |
| ● | 私たちの支店のメンバーです。 |
CBCAは取締役会が私たちを代表することができます株主の許可なしに
| ● | 私たちの信用でお金を借ります | |
| ● | 私たちの借金を発行したり再発行したり売却したり | |
| ● | 誰もが義務を果たすことを保証するために、私たちに代わって保証します | |
| ● | 担保、担保、質権、または他の方法で私たちのすべてまたは任意の財産の保証権益を作成し、私たちの任意の義務を保証するために、所有またはその後に得られた財産を保証します。 |
| 79 |
株主は我々の定款や定款(あるいは合意した株主合意によって)でこのような権力を制限する能力があるが,このような制限はない.
CBCAは、任意の目的のために、私たちの任意の株主、取締役、上級管理者または従業員または関連会社のbrまたはその連絡先に保証を提供することを禁止し、または私たちまたは私たちの関連会社によって発行されるまたは発行された株式を購入する目的または株式の購入に関連する目的を購入するために誰にも保証を提供することを禁止し、合理的な理由があれば、私たちが保証を提供した後、満期債務を支払うことができない、または私たちの資産が担保または担保の形で可変現価値 を保証することを保証する。保証を提供した後、私たちのすべてのカテゴリの負債と法定資本の合計よりも少なくなります。これらの借金権力は私たちの規約や条項によって異なる可能性があります。しかし、私たちの規定と条項はこのような借金の権限に対するいかなる制限やbrの変化も含まない。
牛熊証によると,我々の役員は我々の業務や事務を管理·管理し,牛熊証,細則および細則によって権限を行使するすべての権力と権力を行使する.CBCAによると、私たちの役員と上級管理者の一般的な職責はbrが誠実かつ誠実に行動し、私たちの最適な利益を実現し、合理的で慎重なbr人員が類似の状況で行使する慎重、勤勉、技能を行使することである。これらの義務に違反するいかなる行為も、私たちと私たちの株主が受託責任に違反して責任を負う可能性があります。また、CBCAのいくつかの規定に違反して、配当金の不当な支払いや株式の不当な購入または償還を含めて、このような行動を許可した取締役には、任意の不当な支払いまたは分配の金額について責任を負わせる責任があります。
私たちの付例では、取締役会は時々取締役会のいくつかの委員会から取締役会の任意の権力を委任し、取締役会の任意の権力をそのような委員会に譲渡することができるが、取締役会の委員会がCBCAによって行使する権利は除外される。したがって、取締役会には、監査委員会と指名、管理および報酬委員会、またはNGCCの2つの常設委員会がある。
銀監会の規定の制限を遵守する場合、私たちの附例規定は、法律で規定されているすべての範囲内で、取締役または私たちの請求に応じて行動するか、または取締役役員として行動する人を賠償しなければならない。私たちは、現在またはかつて株主または債権者であった取締役の役員、および彼または彼女の後継者および法定代表者を含み、訴訟を結んだり、判決を履行するために支払う費用を含み、訴訟を結んだり、判決を履行するために合理的に招いた任意の民事費用、損失、課金、およびbr支出を含む。(A)彼または彼女が私たちの最高の利益のために誠実に行動し、(B)刑事または行政訴訟または訴訟で罰金によって強制的に執行される限り、彼または彼女は、(A)彼または彼女が私たちの最高の利益のために行動し、(B)刑事または行政訴訟または訴訟で罰金によって強制的に執行される限り、彼または彼女はその行為が合法であると信じる合理的な理由がある。
私たちのbr取締役は、通常の業務中に私たちまたは私たちがコントロールする任意の会社のために任意の責任を負う任意の取締役または他の人を時々賠償する権利があり、担保権または任意の他の物権を設定することによって、私たちのすべてまたは一部の動産または不動産を品質管理することによって、その取締役または他の人がいかなるbr損失から保護することができる。
また、様々な役員と高官の賠償協定に基づいて、ある費用、利息、判決、罰金、罰金、法定義務、専門費用と採用費、その他の任意の性質や種類の費用、利息、判決、罰金、法定義務、専門費用と手付金とその他の費用について、私たちドイツ子会社の取締役と高級会社の上級管理者および取締役社長に対して無害な賠償と保存を行うことに同意します。このような任意のコスト、有料、専門費用とその他の費用が合理的であることを前提としています(総称して“費用”と呼ばれます) および補償を受ける側が取締役サービスとして被ったり発生したりするすべての費用です。会社(またはその付属会社)の上級管理者または従業員 は、会社(またはその付属会社)の取締役高級管理者または従業員として、承諾、許可、許可、または黙認された任意の、事項、行為、または事柄として行われる。
| 80 |
株 大文字
我々の認可株式構造は、以下のカテゴリの無限数の株式(すべてのカテゴリ無名義 または額面):普通株;および第1優先株(“第1優先株”)および第2優先株 (“第2優先株”、および第1優先株、および第1優先株)、 を連続的に発行することができるカテゴリの無限数の株式を含む。2023年3月22日までに4,855,876普通株 が発行されました。今まで優先株は発行されていません。私たちはまた株式引受証を発行し、ある株式融資を通じてbrに関連する普通株を買収した。
普通株 株
普通株式保有者は、保有する普通株式1株につき全株主総会で1票を投じる権利があるが、特定種別株式の株主のみが投票権を有する会議は除外する。また、私たちの取締役会が普通株式で発表した場合、保有者は配当金を得る権利がある。最後に、普通株式保有者は、私たちの事務を清算、解散、または終了する時に、自発的でも非自発的でも、私たちの残りの財産を得る権利がある。株主は、発行されたすべての株式と発行された株が全額支払われており、評価する必要がないため、さらなる資本催促の責任を負わない。
優先株 株
第1および第2の優先株は、各カテゴリに固有の権利および特権と共に発行することができる。優先株の保有者は、一般に株主総会の通知を受けたり、株主総会に出席したり、株主総会で投票する権利がない。第一優先株の保有者は、第二優先株、普通株又は任意の他の種類の株式に優先的かつ優先的に所有する権利を有する者が、当社の株式のうち第一優先株よりも低い他の種類の株式の配当に参加し、また、われわれの清算の場合、解散又は清算の際に私たちの財産を分配するか、又は株主の間に私たちの全又は一部の資産を分配し、金額は、当該等流通株について支払われる対価格の価値に相当し、われわれの発行及び払込済み株式に記入し、平等に基づいて、それぞれが保有する当該等の株式に対する債権金額の割合で算出する。第二優先株の所有者は、普通株又は当社株式のうち第二優先株よりも低いレベルの任意の他の種類の株式の保有者が参加する任意の優先株の優先株及び優先株を有する権利があり、われわれが清算する場合、われわれの解散又は清算の際に、われわれの財産分配、又は私たちの全又は一部の資産の株主への分配、金額は、このような流通株について支払われた対価格価値に等しく、われわれの発行及び払込持分に記入し、平等な基礎の上で、それぞれが保有する当該等の株式の請求額に応じて決定される。
私たちのbr取締役会は時々追加の優先株シリーズを設立と発行することを規定するかもしれないが、任意の優先株 を発行するにはCBCA下の取締役の一般的な責任、すなわち誠実かつ誠実に行動して、私たちの最適な利益 の実現を期待し、そして合理的で慎重な人が類似の状況で行使する慎重、勤勉と技能を行使しなければならない。
株式承認証
私たちは株式証の説明を認めます付注17--持分、株式承認証とその他の資本を参照して、 に至る本年度報告表20-F第17項に記載されている監査された総合財務諸表。
株主行動
CBCAは、裁判所の許可を得て、私たちの株主は私たちの名義で私たちを代表して訴訟を提起することができ、私たちを代表して訴訟を弁護したり、訴訟を停止したりすることができると規定している。このような訴訟を承認するために,CBCAは,裁判所 は,我々の取締役が申請に関する十分な通知を受けていることを確信しなければならず,株主は善意に基づいて行動しており,訴訟を起こすことは我々の最良の利益に合致しているようであると規定している。
| 81 |
株主権利計画
当社取締役会は、2019年3月29日に改訂·再記載された当社株主権利計画を承認し、株主が2019年5月8日に開催された年次株主総会と特別総会で承認、承認と確認(“権利計画”と略す)を承認した。当社が2016年に最初に実施した株主権利計画を修正し、再記述し、当社のすべての株主が任意の買収要約または他の方法で当社の制御権を買収する際に公平に扱われることを可能な限り確保するために、brを実施した。
権利計画の目標と背景
割当計画の基本的な目標は、買収要約を提出する際に株主価値最大化 を実現し、株主に買収要約に参加する平等な機会を提供するために、我々の取締役会と株主に十分な時間を提供して、我々の能動的な買収 を評価し、取締役会に代替案を探索·開発することである。
以下に述べるように、買収要約を提出した潜在的な買収者が“入札を許可する”方法で買収を行うことを奨励することは、買収要約が公平を促進するためのいくつかの最低基準を満たすか、または我々の取締役会の同意を得ることを要求する。買収要約がこれらの最低基準に達しず、かつ配当計画が取締役会に放棄されていない場合、株式計画は、普通株保有者(買収側を除く)が市場より大幅に割引された価格で追加普通株を購入することができ、普通株を買収する人が持ち株を大幅に希釈するリスクに直面することができると規定している。
権利計画要約
以下は“権利計画”の主な条項の要約であり,要約全文はその中の条項 を参照する.本要約において他に定義されていない大文字用語は、“権利計画”におけるそのような用語の意味を有するべきである。権利計画草案は、以下のウェブサイトで調べることができる:www.zenataris.com、www.sedar.com、およびwww.sec.gov。
本要約の目的および権利計画では、用語“NI 62−104”は、国家文書62−104−を意味する接収入札と発行者入札現在のように、現行のように有効または時々修正、再制定または置換され、確実性を向上させるための任意の後続文書を含む任意の後続文書を含むことができるように、カナダ証券監督機関によって採択される。
権利計画の操作
株式供給計画の条項によると、午後5:01に1株当たり普通株を発行して1項の供株を発行した。2016年3月29日(記録的時間 )。さらに、記録時間 の後、分離時間(以下のように定義する)、および満了時間(以下のように定義する)の前に発行された各追加の普通株式について1つの権利を発行する。当該等の権利の初期 行使価格は分割時に決められた普通株市価(定義は以下の文を参照)に 5を乗じたに等しいが、いくつかの反ダンピング調整(“行使価格”)を経なければならず、分割前に行使してはならない。反転事件(定義は後述)が発生すると、各権利はその所有者( 購入者または株式供給計画条文に従って権利が失効または無効になった任意の他の者を除く)に、br}吾等に株式取得日(以下、定義参照)後8取引日営業時間終了時に発効する普通株を購入する権利があり、br}吾等に行使価格を支払った後、br}吾等に合計市価を購入することは、取引完了またはその等の転売事件が発生した日に行使価格の2倍の普通株に等しいが、いくつかの逆希釈調整規定の制限を受ける必要がある。
市場価格の定義
市場価格は、一般に、決定されなければならない任意の所与の日に、普通株として連続して20取引日(すなわち、普通株が取引されるトロント証券取引所または別の証券取引所または全国証券見積システム(ナスダックグローバル精選市場、ナスダックグローバル市場、およびナスダック資本市場を含む)として決定されなければならない確定性を向上させるための取引日)の出来高加重平均価格で定義され、決定日直前の取引日を含む。特定の例外的な状況によって制限される。
| 82 |
権利取引
分割時間(または権利終了または満期より早い時間)の前に、これらの権利は、普通株と共に取引され、普通株と同じ株式または発行された任意の普通株に関する証券登録事項によって を表す。権利は、分立時間から後、満期時間前に権利証明書によって証明され、普通株式とは別に取引される。これらの権利は、投票権または配当権のような普通株式に付随する任意の権利を伴わない。
分離時間
権利は、付属普通株から分離され、以下の場合が最初に発生してから8営業日目の営業終了時(“分離時間”) 行使:
| (1) | 誰かが買収者となった事実を公開発表する最初の日(“株式買収日”) ;および | |
| (2) | 任意の者(吾等又は吾等のいずれかの付属会社を除く) 買収要約又は株式交換要約の開始日又は初めて意向を公表する日 は、買収要約が引き続き許可要約又は競争的許可要約の要求を満たしていれば(場合によって決まる)、買収要約又は株式交換要約は20%を超える発行済み普通株を買収するが、買収要約又は競争許可要約は除外することを許可する。 |
分割時間は取締役会が時々決定した比較後の時間であってもよいが、いずれかの当該等の買収要約が分割時間前に満了したり、分割時間前にキャンセルされたり、終了したり、他の方法で撤回されたりすることができ、当該等の買収要約に基づいて保管されている証券が引受及び支払いされていない場合、分割が行われたことがないとみなされ、取締役会が権利 計画をある特定の転売事件に適用することを放棄することを決定した場合、当該転売事件に関する分割時間は発生しないとみなされる。
から分割時間後および満期時間前に、各権利の所有者は、私などに使用価格 を支払った後に普通株を購入する権利がある。
反転イベント
1人の人(“買収者”)(その人と共同または一致して行動する他の人を含む)は、発行された普通株の20%を超える株式を買収し、買収を許可し、競合して買収を許可するか、または株式供給計画に記載された他のいくつかの限られた場合に買収することを“転売事件”と呼ぶのではない。
満期時間前に放棄されていない投機イベントが発生した場合(以下の“放棄及び償還” を参照)、その後、各権利(買収者が保有しているか、又は買収者が保有しているとみなされる権利を除く)は、株式取得日後の第8取引日の取引終了時に保有者に購入させ、行使価格を支払い、他の方法で株式計画の条項に従ってその権利を行使する権利を有する。取引が完了または発生した日には、市場総価格が行使価格の2倍に等しい普通株式数 は、執行価格の現金金額に相当する(供株計画で述べたいくつかの反ダンピング調整に制限される)。
入札者は我々の株主(“販売禁止者”)と販売禁止許可プロトコルを締結することができ,このような株主は入札者の共同会社や共同経営会社ではなく,入札者と共同あるいは一致して行動するわけでもなく,これにより,このなどの株主は買収入札(“禁売価格”)にその普通株(“禁売価格”) を提供することに同意し,入札者は販売価格に応じて保管された普通株を実益として所有しているとはみなされない.このようなプロトコルは、販売禁止要約よりも大きな対価格を株主に提供するか、または販売禁止要約よりも予想以上の株式を売却する権利があることを規定する条項を含む必要がある(許可された販売禁止プロトコルは、ロックカプセル下の株式数を超えて7%以下を要求することができることを前提とする)。
| 83 |
許可された販売禁止プロトコルは,別の取引の対価格が販売禁止入札の対価格よりも指定された金額よりも高いことを要求する可能性がある.指定された金額は7%以上ではいけません。確実性を向上させるために、販売禁止プロトコル が優先購入権を含むことを可能にするために、または入札者が別の買収要約または取引においてより高い価格を一致させる機会があるように、優先購入権を含むか、または別の買収要約または取引中に権利 を行使して普通株を引き下げることを妨げることがない限り、一定期間の遅延(または他の同様の制限)を要求することができる。
権利計画は、私たちと大衆に許可されたいかなる販売禁止協定を提供することを要求する。販売許可契約の定義はまた、許可販売禁止合意に基づいて、“手切れ金”、“追加”費用、罰金、費用またはその他の総金額が、(I)販売禁止価格の下で支払われるべき総費用の2.5%を超えてはならないこと、および(Ii)販売禁止者が別の買収契約または取引によって受信した対価の価格または価値の50%を超えてはならないことを規定している。被販売者が普通株を売却禁止株に入金するか、または直前に入札した普通株を撤回して、その普通株を別の買収要約に入金するか、または別の取引をサポートすることができない場合、禁断者が支払うことができる。
許容 入札要求
入札を許可する 要求は以下のものを含む
| 1. | 買収入札は買収入札通告の形で行わなければならない | |
| 2. | 買収要約は,入札者ではなく,どこに住んでいるすべての普通株式所有者にも同じ条項と条件で発行しなければならない; | |
| 3. | 買収要約は、要約入札による普通株の受け入れまたは支払いを許可してはならない |
| a) | NI 62-104によれば、関連する買収入札日後105日以上の営業終了前、または(第5セクション(NI 62-104の入札機構)の任意の要求の免除を受けない)接収入札の最短時間内に、入札を受信するには、証券保管のための開放された最短時間を維持しなければならない | |
| b) | 取引終了時にのみ、普通株(および/または権利計画に定義されている“変換可能証券”)が初めてこの買収要約に従って引受または支払いされ、発行された普通株および変換可能証券は株主が を保有するが、他の購入者、入札者、入札者の関連会社または共同経営会社、入札者と共同または一致して行動する人、任意の従業員福祉計画、繰延利益共有計画は含まれていない。(I)当時発行された普通株式および(Ii)変換可能証券を行使する際に発行可能な普通株の合計の50%以上を占め、買収要約に基づいて入金または提出されるか否かを示す株式参加計画または信託は、(I)当時発行された普通株および(Ii)が転換可能な証券を行使する際に発行可能な普通株の合計の50%以上を占め、買収要約に従って入金または提出され、撤回されていない、我々の従業員または任意の子会社の従業員の利益のための株式参加計画または信託 |
| 4. | 買収要約は、買収要約が撤回されない限り、買収要約に従って普通株および/または変換可能証券の取引が終了する前の任意の時間 を許可しなければならない | |
| 5. | 買収要約は、買収および支払いの前に普通株および/または変換可能証券が撤回されることを許可しなければならない | |
| 6. | 上記の条項3.b)に規定されている要求を満たせば,入札者はこの事実を公開しなければならず,買収カプセルは公表日から10日以上普通株の保証金や入札に対して開放状態を維持しなければならない. |
| 84 |
許容入札は、すべての非入札者が所有する発行された普通株に対する入札である必要はなく、すなわち、許可入札は部分入札であってもよい。 割当計画は、許可入札が存在する場合に競争的許容入札(“競争的許可入札”) を行うことも許可する。競争許可入札は、上記(Br)条第(3.a)項に規定する要求以外のすべての許可入札の要求を満たさなければならず、競争許可入札を構成する接収入札の日後、NI 62-104の規定により、最低初期預金期間の最終日の取引が終了する前に、当該入札に従って提出または格納された普通株の引受または支払いを許可してはならず、この接収入札は、NI 62-104による証券格納のために開放されたままでなければならない。しかし、 が入札許可入札条件を満たした買収要約は、当該買収要約が“入札許可要約”の定義の任意またはすべての前述の規定を満たさなくなった場合、および当該買収要約に基づいて普通株および/または変換可能証券の任意の買収を買収し、当該買収要約が入札許可要約にならなくなる前に行われる任意の普通株および/または変換可能証券買収を含む場合には、入札許可要約ではなくなるべきである。“許可された入札買収”(権利計画によって定義されたような)ではないだろう。
免除と両替
取締役会は、反転イベントが発生する前に、すべての普通株式所有者に買収要約を発行することにより発生した買収要約による特定の反転イベント の希釈効果を放棄することができる。この等免除は、買収要約が満了する前に買収要約通告方式ですべての普通株式所有者に発行された買収要約 で発生した任意の他の投機事件の放棄とみなされるべきである。
取締役会は、大多数の独立株主(または個別時間発生後、権利保持者であるが、権利計画の規定により無効な権利または個別時間前に独立株主以外の他の人が所有する権利を除く)の承認を受けて、放棄されていない反転イベントが発生する前の任意の時間に、各0.00001カナダドルの価格で当時のすべてのがすべての未償還権利を償還することを選択することができる。配当計画で提供される に応じて適切に調整する(“償還価格”)。非許可買収要約または 競争的許可買収要約が分割時間発生後および反転事件が発生する前に撤回または他の方法で終了する場合、取締役会は、普通株式保有者の同意を得る必要がなく、または償還後直ちに普通株式記録保持者に供株計画下の権利 を再発行することを選択することができる。このような権利の償還および再発行後、供株計画のすべての条文は、分立時間が発生していないように適用され、分立時間は発生していないとみなされ、吾らは当時発行された普通株式の所有者brに置換権利を発行したとみなされる。
権利計画修正案
権利計画は、権利計画の有効性を維持するために、任意の文書または印刷エラーを訂正するために、または権利計画の下で適用される任意の法律、法規または規則の任意の変化によって必要な修正を行うために、普通株式または権利保持者の承認なしに修正されてもよい。分割時間前に、吾らは普通株式保有者の事前同意を経て、株式供給計画の任意の条文を改訂、変更または削除し、取締役会が誠意に基づいて必要または適切と考える任意の変更を実施することができる。権利保持者が事前に同意した場合、私たちは、分離時間の後および満了時間の前の任意の時間に、権利計画の任意の規定を修正、変更、または削除することができる。
希釈から を保護する
使用価格、権利行使時に購入可能な証券の数および性質、および発行された権利の数 は、配当、分割、合併、再分類または発行された普通株の他の変化が発生し、普通株式所有者に比例的に割り当てられ、権利所有者の利益を適切に保護するために調整される必要がある他の場合に株式を希釈することを防止するために時々調整される可能性がある。
| 85 |
取締役会の受託責任
Br権利計画は、私たちの最大利益と株主の最大利益のために取締役会が正直に行動する責任を減損または軽減しないだろう。取締役会は引き続き責任と権限を持ってこのような行動を取り、私たちの株主に適切と思われる提案をするだろう。
投資コンサルタントの免除条項
ファンドマネージャー、投資コンサルタント(完全に管理されている口座に対して)、信託会社(受託者と管理人として行動)、 その業務は基金管理の法定機関および登録年金計画の管理人を含み、彼らがグループ買収要約の一部でない限り、投機事件をトリガすることはない。
用語.用語
権利計画は(I)終了時期;及び(Ii)当社が2023年に開催する株主総会及びその後第3回株主総会(当該等株主周年総会毎に“再確認 会議”)当日(“満期期間”)が満了するが、当該等株主周年総会では、権利計画は再確認又は再確認のために再確認されていない(“満期時間”)を基準とする。
株主権利の変更に必要な操作
私たちの株主の権利を変更するために、私たちは変更を発効させるために私たちの条項を修正しなければならない。このような改正は、正式に開催された特別会議で発行済み株式3分の2と発行済み株式保有者の承認を得る必要があるだろう。いくつかの改正に対しては,株主はCBCAによって当該等の改正細則の決議案に異議を唱える権利があり,当該決議案が可決されて吾らがこの等の改正を実施すると,株主はその株式の公平な価値を支払うことを要求する権利がある。
開示株式所有権
一般に、カナダで適用される証券法規によれば、誰又は会社が実益が発行者の議決権証券、発行者の議決権証券又は両者の組み合わせを所有又は直接又は間接的に制御又は指揮する場合、発行者のすべての未代償及び議決権証券に付随する10%以上の投票権が付随する場合は、内部者に属し、内部人になった日から10日以内に所定の形で報告書を提出し、当該人に対する任意の直接又は間接実益所有権、制御又は指示を開示しなければならない。発行者の証券を申告する。
また,カナダの証券法規では,持株変更の報告発行者の内部者は報告書を提出しなければならず, 報告は変更発生日から5日以内に提出しなければならないと規定している。
“取引法”第 13節は、“取引法”第 条第12条に基づいて登録された株式類証券の5%を超える受益所有権(この用語は“取引法”の下の規則 13 d-3で定義される)を取得した者に対して報告要求を行う。私たちの普通株はこのように登録されています。一般的に、これらの人は、取引法第13節に規定する情報を含む利益所有権報告書を買収後10日以内に米国証券取引委員会に提出しなければならない。この情報 は,証券の発行者や証券取引の各取引所にも送信される必要がある.
会社規約は株式所有権の開示を要求しない。
株主総会
株主周年大会は毎年開催され、財務諸表と報告、選挙取締役、委任査定師及び認可取締役会がその報酬を決定し、株主総会が適切に に提出する可能性のある他の事務を処理することを目的とする。任意の年次会議は、特別会議が審議及び処理可能な任意の事項を審議及び処理するための特別会議を構成することもできる。定款によると、私たちのCEOや私たちの総裁は株主総会を開催する権利がある。
| 86 |
CBCAは,議決権を発行した株式の5%以上を持つ所有者は,我々の取締役に申請書に述べた目的で 株主総会を開催することを要求できることを規定している.限られた場合には,株主総会が開催され会議通知が出されたこと,あるいは要求に関する主な目的が,吾らや吾などの役員,上級社員や株主への個人不満 を是正することを明確にしない限り,取締役はその要求を受けた後,株主総会を開催しなければならない.取締役が請求を受けてから21日以内に株主総会が開催されていない場合は, のどの請求に署名した株主も株主会議を招集することができ,株主がbr会議で別途決議がない限り,株主が申請,開催,株主総会の開催により合理的に発生した費用を精算する.
CBCAはまた,限られた場合を除いて,株主総会でその決議について投票する権利のあるすべての株主が署名した書面決議は,株主総会で採択された決議と同様に有効であると規定している.
株主年次総会や特別総会に出席する株主数は定足数であり,株主総会に出席する人数 にかかわらず,持株者数が発行済み議決権株式の少なくとも10%を占める株主が自ら出席するか,当社定款に基づいて代表を出席させることを前提としている。CBCA、私たちの定款、または私たちの定款の要求または私たちの株式のあるカテゴリの株主がカテゴリ別に投票することを許可する場合、任意の会議の定足数は、そのカテゴリ流通株の10%を代表する1人以上の人となる。
毎回の株主周年大会や特別総会の時間および場所に関する通知 は,毎回の株主総会日 までに21日以上,50日を超えないように,各取締役,監査役および会議で投票する権利のある株主に送付しなければならない.任意の株主,取締役または監査人の住所が我々の帳簿に現れていない場合,通知は通知を送信した者に送信される可能性があり,その株主,取締役または監査人の住所に迅速に到達する可能性が最も高いと考えられる.牛熊証の運用により譲渡又はbrのいずれかの他の方法で任意の株式を取得する者は、株式に関する各通知に拘束されなければならないが、当該等通知は、その氏名及び住所を自社登録簿に記入する前に、その通知を発行する際にその氏名が登録簿にある者に発行されるものである。財務諸表及び計数師の報告の審議、取締役の選挙及び現監査師の再委任以外に、株主総会の通知は業務の性質を詳しく述べなければならず、株主は大会に提出する任意の特別決議案或いは定款について合理的な判断を行うことができ、そしてそのテキスト を明らかにしなければならない。
我々の 附則には事前通知条項(“事前通知要求”)が含まれている.事前通知規定は、以下の場合に適用される:(br}当社株主は、以下の規定により取締役会メンバーを指名していない): (A)CBCAの規定による会議要求、または(B)CBCAの規定による株主提案 を適用する。
その他の事項に加えて,株主は取締役を選挙する年度または特別株主総会の前に取締役指名通知brを提出し,株主 が通知に含まれた情報を有効にしなければならないという締め切りが決定されたことをあらかじめ通知する.年次株主総会であれば,年次会議日までに30日以上65日を超えないように通知しなければならないが,年次会議の開催日 が年度会議日を初めて公表してから50日以内に開催されていれば,通知は10日の会議終了時に遅くなくてもよいこれは…。このような公開発表の翌日に。株主特別会議(年次会議でもない)であれば、15日の事務終了前にお知らせしなければなりませんこれは…。最初に特別会議の日付が発表された翌日。
取締役会は事前に要求された任意の要求を放棄することを適宜全権することができる。
| 87 |
証券所有権の制限
カナダの法律、私たちの条項、あるいは定款は非住民が私たちの普通株を保有または投票する権利を制限しませんが、 “カナダ投資法”(“投資法”)。
“投資法”は、任意の非カナダ人(“投資法”の定義による)が既存のカナダ業務の制御権 (“投資法”の定義に従って)を獲得することを要求し、開業前審査申請又は開業後 通知をカナダ革新、科学及び経済発展部に提出しなければならない。
本文書が発表された日まで、非国有企業を審査する世界貿易機関加盟国の投資家がカナダの非文化企業の支配権を直接買収するハードルは、資産価値が12.87億カナダドルを超える企業である。非国有企業の“貿易協定投資家”(“投資法”の定義による)に対して、カナダの非文化企業の支配権を直接買収することを審査するハードルは19.31億カナダドルを超える企業資産価値である。世界貿易機関加盟国と貿易協定投資家の企業価値審査のハードルはすべて年度の国内総生産の増加とリンクし、毎年相応の調整を行っている。上場企業の場合、カナダ企業資産の“企業価値”は、その実体の時価にその負債(その経営負債を含まない)を加えて現金と現金等価物を引いたものに等しい。
したがって、投資法によれば、私たちの資産の企業価値が指定された審査のハードルを超えた場合にのみ、世界貿易機関加盟国投資家または貿易協定投資家(米国投資家を含む)である非カナダ人(私たちの普通株または私たちの全部または実質的にすべての資産を買収することによって)が私たちの支配権を審査することができる。
支配権を得ることが検討可能な取引である場合、投資法は、関連大臣が審査後に信納または信納買収がカナダに純利益をもたらす可能性があるとみなされない限り、審査可能な取引 を実施することを一般的に禁止する。
1つのエンティティを買収する多数の議決権を有する権益は、そのエンティティに対する“制御権”を獲得するとみなされる。 1つの会社が所有する議決権株式に添付されている議決権総数の多数に満たないが3分の1以上を買収するか、または当該会社が議決権を有する株式の付属議決権総数のうち同等の不可分の所有権権益を買収する は、当該会社の制御権の買収が確定できない限り、買収時には、会社 は実際には買収者が議決権付き株式を所有することによって制御されないと推定される。1社の議決権を有する株式を買収する総投票権の3分の1未満 は、同社への支配権を獲得するとはみなされず、国有企業投資に関するある裁量権によって制限されている。以下に説明する“国家安全”審査に関連するものを除いて、私たちの普通株に関連するいくつかの取引は、“投資法”の制約を受けない
| ● | ある人は証券取引業者または取引業者としてその正常な業務過程で私たちの普通株を買収する; | |
| ● | 融資または他の財政援助のための保証を実現するための私たちの買収または制御、および“投資法”の規定に関するいかなる目的のためにも私たちを買収またはコントロールするのではなく、買収が“銀行法”、“協力信用協会法”、“保険会社法”または“信託およびローン会社法”に基づいて承認される必要がある場合、および | |
| ● | 合併、合併、合併または会社再編によって私たちを買収したりコントロールしたりして、私たちの議決権のある権益を持つことで、私たちの事実上の最終的な直接または間接制御は変わらない。 |
“投資法”の国家安全制度によると、連邦政府はまた、“カナダですべてまたは一部の業務を展開する実体 ”を買収または部分的に設立するために、より範囲の広い非カナダ人の投資を適宜審査することができる。関連する試練は、非カナダ人のこのような投資が“国家安全を損なう”かどうかだ。革新、科学、経済発展大臣は広範な自由裁量権を持っており、投資家がカナダ人ではないかどうかを決定することができるため、国家安全審査を受ける可能性がある。国家安全理由に基づく審査は連邦政府が自ら決定し、結審前または結審後に行うことができる。
| 88 |
源泉徴収要件を除いて、カナダにはいかなる法律、政府法令、あるいは法規が資本の輸出入を制限することもなく、いかなる法律、政府法令あるいは法規もなく、私たちが非住民の普通株式所有者に配当金あるいは他の支払いを支払うことに影響を与える。
| C. | 材料 契約 |
以下は、本協定が発効した当社唯一の有効な重大な合意(通常のビジネスプロセスで締結されたいくつかの合意を含まない)である
| ● | 米国とカナダのライセンス契約(以下に述べる); | |
| ● | Consilient Healthと締結されたライセンスプロトコル(以下に述べる). |
アメリカとカナダのライセンス契約
2018年1月16日、会社はAEZSドイツ社を介してStrongbridgeとライセンス契約を締結し、米国とカナダでMacrilen(Macimorelin)の開発、製造、登録、商業化を行い、現金支払い2,400万ドル (“2018年合意”)を受け取った。
2018年12月19日から、StrongbridgeはカナダのMacrilen(Macimorelin)と米国のMacrilen(Macimorelin)での権利をNovoに売却し、NovoはStrongbridgeのMacrilen Macrilen(Macimorelin)現場組織を現地契約力として米国で普及させることに同意し、最長3年に達する。本サービス協定は2019年12月1日から終了します。
2020年11月16日、当社は完全子会社付属会社を通じてNovoとMacimorelinの開発と商業化について、既存の許可協定を改訂(“改訂”) することを発表した。元のライセンス契約の条項によると、Novoは米国とカナダでMacimorelinを商業化する独占的権利を付与される。Novoは現在米国でMacrilenの商標でMacimorelinを販売しており,AGHDの診断に用いられている。この修正案は、2018年の協定 を以下のように修正することを目的としている
| ● | 双方間の酢酸マキモレリン原料薬供給に関する最新の供給スケジュールを反映した | |
| ● | Eeterna特許権および商標に対するNovoの共同所有権の付与; | |
| ● | 小児科適応に対する双方の臨床試験の責任(100%費用補償、最大900万ユーロ、および改正案ごとに費用の50%を超え、2018年の合意における総費用は70%を超える)を修正した | |
| ● | 将来の支払い義務、すなわち特許使用料の低減と、FDAが承認した小児科適応を免除する会社の将来の規制マイルストーン支払いを改正する。 |
U修正案によると、Eeternaは米国とカナダ以外の地域でMacimorelinを使用するすべての権利を維持し続けているが、NovoはEeternaに610万ドル(500万ユーロ)を前払いすることに同意し、同社は2020年12月にこの金を受け取る。改正案によると、年間純売上高が4,000万ドル以下の製品については、Aeternaが米国とカナダから取得した印税を15%から8.5% に引き下げ、年間純売上高が4,000万ドルを超えるMacimorelinについては15%以上に返還する。また,FDAが小児科適応を承認した後,NovoはEeternaの500万ドルの可変支払いを免除された。修正案によると、NovoとAeternaは、Aeternaが単独で契約研究機関(CRO)と協力してキー研究P 02を行うことに同意した。開発活動がEeternaに移行したことから,NovoはEeternaに返済する必要があるP 02研究臨床試験費用の割合をコストの70%から100%に調整し,最高900万ユーロ(約1090万ドル)に達する。外部共同承認されたP 02試験費用が900万ユーロを超える追加費用はNovoとEeternaによって二等分されるだろう。さらに、共同指導委員会の権利と責任についていくつかの修正が行われた
| 89 |
修正案によると、両社は米国とカナダのマキモレリンの開発と商業化に関する活動を共同指導委員会を通じて緊密に調整し続け、双方はある分野で意思決定権を持っている。Novo はまた、AeternaがMacimorelinに所有している米国とカナダ特許および商標の共通所有権を取得するが、いくつかの終了イベントが発生した場合に、これらの特許の共通所有権 をAeternaに譲渡することが要求される。
また、米国の規制機関がCGHDの診断にMacimorelinを承認した後、NovoがカナダでMacimorelin を商業化していないと判断した場合、Eeternaはカナダ(米国ではないが)でMacimorelinの権利を独占的に許可することを選択することができる。第三者に売る。修正案はまた、成功すれば、EeternaはP 02研究の結果を使用してEeternaが規制 の承認を求めることを支持する権利があり、ヨーロッパとNovo、アメリカ、カナダに許可された2つの国と地域以外の他の地域にMacimorelinの協力機会を求めるために努力し続けていることを確認した。
改正案によると、Macrilen(マカロニ)が特許保護されている限り、会社は純売上高が4,000万ドル以下のbr}に対して8.5%の印税を徴収する権利があり、純売上高が4,000万ドルから7,500万ドルの場合には15%の印税を得る権利があり、純売上高が7,500万ドルを超える18%の印税を受ける権利がある。 Macrilen(マカロニ)は米国やカナダの特許保護が終了した後、会社はその国の純売上高に対して5%の印税を徴収する権利がある。
また、会社は、以下のビジネスマイルストーン事件が初めて実現した後、Novoから一括払いを取得する
| ● | 400万ドル年間純売上高2500万ドルを達成しました | |
| ● | 1000万ドルで5000万ドルの年間純売上を達成しました | |
| ● | 2000万ドルで1億ドルの年間純売上を達成しました | |
| ● | 4,000万ドルで2億ドルの年間純売上高と | |
| ● | 1億ドル、5億ドルの年間純売上高を達成した。 |
改正案は、米国とカナダの規定印税期限が終了した時点で満期になり、会社が付与した許可証はこれらの国/地域で取り消すことができない、全額支払い、永久、免除となる。Macrilen(Macimorelin)に関するセキュリティ問題があれば、米国でMacrilen(Macimorelin)の規制承認(恒久的とされる)を撤回すれば、許可者は修正案を終了し、270日前に書面通知を出す権利がある。あるいは、会社が違反条項の書面通知を受けてから90(90)日以内に改訂条項に対する実質的な違反を是正できなかった場合、会社は改訂を終了する権利があります。許可された人が改正条項に重大に違反したが、違反通知を受けてから90(90)日以内に是正できなかった場合、会社は改訂を中止する権利があります。違反がカナダに関連している場合、会社はカナダに関する修正案を終了する権利しかない。違反が米国に関連している場合、会社は修正案の全内容を終了する権利がある。Novoが修正を早期に終了した場合、またはNovoの重大な違反によって会社が終了した場合、共同所有権は会社に返却されます。
改正案には、秘密および秘密、陳述と保証、賠償、紛争解決などに関する慣例規定が含まれている。その修正案はスイスの法律によって管轄されている。
Novoは2022年8月26日、Novo修正案の終了通知を当社に提供した。Novo修正案の条項によると、270日間の通知期間(“通知期間”)が終了した後、2023年5月23日に発効する。終了後, 社はNOVO改正案によりNovoに付与された権利とライセンスを会社に返還し,会社はMacrilenの臨床開発と将来の商業化を継続するすべての権利を再獲得する。終了通知の後、および270日間の通知期間内に、Novoは、960万ドル(900万ユーロ)以下のすべての検出試験費用に資金を提供し続け、960万ドル(900万ユーロ)から1050万ドル(980万ユーロ)を超える任意の追加の検出試験費用は、Novoおよび会社によって二分される。
| 90 |
ヨーロッパ経済圏とイギリス許可証協定
2020年12月7日,当社はConsilient Health Limited(“CH”)とMacimorelin(“ライセンス製品”)の欧州経済区およびイギリスでの商業化について独占ライセンス契約(“CH ライセンス契約”)を締結した。
CHライセンス契約の条項によると、CHは、2021年1月に受信された120万ドル(br}(100万ユーロ)の払戻不能、貸切不可の前金を会社に支払うことに同意する。同社には、合意された価格設定や精算パラメータに関する規制マイルストーン、純販売マイルストーン、および特許権使用料がMacimorelinの純売上高の10%~20%から様々(場合によっては減少する場合がある)、またはCHによって記録された再許可収入を含む追加の対価格を得る資格がある。また、2020年12月7日に、当社はCHと独占供給協定を締結し、これにより、当社は第三者メーカーが10年間製造する特許製品をCHに提供することに同意したが、 (“CH供給協定”)を継続しなければならない。
ライセンス製品の商業化権利を考慮すると、CHは、以下に述べるいくつかのマイルストーンに同意する
一度に 支払い(返却不可かつクレジット不可)
| ● | ライセンス契約発効日後30(30)日に100万ユーロを支払います |
小児科(Br)は監督管理支払いを使用する(払い戻しができず、しかも貸記できない)
| ● | 欧州委員会の小児科使用に対する最初のマーケティング許可を得て、金額は500,000ユーロです。 |
規制されたbr支払い(払い戻し不可と貸付け不可)
| ● | フランス、ドイツ、イタリア、スペイン、イギリスで定価と精算承認を受けた後、毎回テストされた価格: | |
| ● | 300ユーロ以上:各国20万ユーロ; | |
| ● | 250ユーロから300ユーロ:各国10万ユーロ; | |
| ● | フランス、ドイツ、イタリア、スペイン、イギリスの平均精算価格は300ユーロを超え、500,000ユーロに達した。 |
ビジネスマイルストーン(返金しないと記帳しない)
| ● | 年間純売上高は400万ユーロ、支払いは25万ユーロ | |
| ● | 年間純売上高は600万ユーロ、40万ユーロを支払う | |
| ● | 年間純売上高は800万ユーロに達し、60万ユーロを支払う | |
| ● | 年間純売上高は1000万ユーロに達し、100万ユーロを支払う。 |
印税
| ● | 10.0%で、年間純売上高は200万ユーロに達した | |
| ● | 純売上高は200万ユーロから300万ユーロの12.5% ; | |
| ● | 純売上高は300万ユーロから400万ユーロの15.0% ; | |
| ● | 20.0% ,純売上高は400万ユーロを超えています。 |
| 91 |
再許可印税収入
| ● | 10.0%純売上に対して特許権使用料を徴収する以外の任意の形態の対価格 |
許可製品が許可協定によってカバーされる任意の国/地域の有効なクレーム範囲内にある限り、(Ii)許可協定によってカバーされる任意の国/地域の許可製品の商業化のために同様の排他性を提供する任意の規制マーケティング排他期間または他の法定指定が満了した場合、許可は依然として完全に有効である。または(Iii) カバーエリアの国/地域とライセンス製品別に分類されたライセンス製品は、それぞれの国/地域で初めて商業販売日(長い期間を基準とする)後10(10)年以内に更新することができる。場合によっては、許可者はライセンスを終了する権利がある。
雇用 とサービス契約
私たちのbrまたは私たちの子会社は、私たちのbrが任命した各幹部と雇用協定を締結しており、場合によっては制御権変更協定も締結されています。
クラウス·ポーリーニ
私たち はKlaus Paulini博士と雇用協定を締結し、2019年10月4日から発効(“雇用協定”) で、当社の最高経営責任者を務めています。当社はまた、AEZSドイツ社とクラウス·ポーリーニ博士を通じて、AEZSドイツ社の取締役社長を務めることについて、2019年7月26日から発効するサービス協定(“サービス協定”)を締結した。雇用協定では,Paulini博士(“幹部”)にAEZSドイツ社取締役社長としてのサービス報酬を含む260,000ユーロの初期基本給を支払うことが規定されている。また、雇用協定によると、私は2019年11月に行政人員に35,000件の株式オプションを初歩的に付与した。サービス協定の条項 によると、執行者は取締役会またはNGCCの適宜決定権に基づいてその後に付与された株式オプション、年間ボーナスを得ることができるが、NGCCの決定と承認を経て、雇用主が後援する年金計画に参加することができる。
もし我々が無断で役員の雇用を中止すれば,役員は300,000ユーロ相当の解散費を得る権利がある.
雇用協定は一般的な秘密、知的財産権、そして非けなす条項を含む。
“雇用協定”については、“原因”による雇用終了は、(限定される訳ではない)(I)役員が何らかの詐欺、窃盗、公金流用、または他の類似した性質の犯罪を実施した場合、および(Ii)役員が職責を履行する際に深刻な不正行為または故意の不注意を犯した場合を含む。
レスリー:友情は長く続いています
我々は、2018年9月24日から発効する諮問協定(“諮問協定”)を首席財務官上級副総裁の女性と締結した。コンサルティング協定では、Auldさん(“コンサルタント”) が毎月最大120時間の特定のサービスを提供することが規定されています。コンサルタントの報酬は1時間150カナダドル(プラスHST)(“基本料金”)となる。また,コンサルタントは1往復あたり最大8(8)時間の旅行時間を獲得し,1時間あたり150カナダドルのレートで計算される。
便宜上、いずれも30(30)日以内に書面通知を出した後、本相談プロトコルを終了することができます。コンサルタントが諮問協定のいかなる条項に実質的に違反または履行しない場合も、相談合意 を直ちに終了し、コンサルタントの死亡後または双方の同意を経て直ちに終了することができる。終了した場合、コンサルタントは、終了発効日前に、支払われていない基本料金および発生した費用の補償を得る権利がある。
Brコンサルティング協定は、コンサルタントが、エラー分類に関連する費用を含む、相談プロトコルまたはサービスによって発生したすべてのクレーム、費用、責任、損害、費用、および費用を賠償することを規定しています。
| 92 |
Auldさんが締結した諮問協定は2022年3月31日に施行された。
ジュリアーノ·ラフラタ
AEZS Inc.は20022年1月に財務兼首席財務官(CFO)ジュリアノ·ラ·フラタ、上級副総裁と雇用協定を締結した。雇用契約の条項によると,La Frattaさんは,その基本給の5%に相当するRRSP を獲得する。
もし私たちが理由なくその役員の雇用関係を終了すれば、その役員はそのサービス年限に基づいて解散費を得る権利がある。2022年12月31日末には、同幹部は137,500カナダドル相当の解散費を得る権利がある。
AEZS は2022年11月18日にLa Frattaさんと制御権変更協定を締結した。“制御権変更” (制御権変更プロトコルで定義されるような)が発生すれば、La Frattaさんは得る権利があります:
| ● | 彼の雇用協定に規定されているすべての債務 | |
| ● | 基本賃金の18ヶ月分の解散費に相当します | |
| ● | は、制御権変更が発生した年の年間ボーナスの金額に相当する | |
| ● | コントロール権変更が発生した当年の目標年間ボーナスに応じて、年間ボーナスの1.5倍に相当する金額を支払う | |
| ● | 現金金額は、会社がその保険の健康福祉を提供するために支払う年間保険コストの1.5倍に相当する |
すべての 未完了のオプションは,制御権変更後に自動的に付与される.
マティアス Gerlach
ドイツAEZSは2001年1月に総裁製造とサプライチェーン副総裁Gerlach博士と雇用協定を締結した。雇用協定の条項によると、Gerlach博士は法定退職年齢に達した後に年金を受け取ることになり、AEZSドイツ社でその年齢まで働いているかどうかに関係なく、金額はAEZSドイツ社で働いている間の支払いに基づく。
エクハルト·ガンサー
ドイツAEZS ドイツは1990年に総裁業務発展と連盟管理副総裁Guenther博士と雇用協定を締結した。雇用協定の条項によると、Guenther博士は法定退職年齢に達した後に年金を受け取り、AEZSドイツ社でこの年齢まで働いているかどうかにかかわらず、金額はAEZSドイツ社で働いている間の資金に基づく。
ニコラ·アンマー
AEZS ドイツは2015年4月にAEZS首席医療官Ammer博士と上級副総裁臨床開発会社と雇用契約を締結した。雇用契約の条項によると、Ammer博士は法定退職年齢に達した後に年金を受け取り、AEZSドイツ社でこの年齢まで働いているかどうかに関係なく、金額はAEZSドイツ会社で働いている間の支払いに基づく。
| 名前.名前 | 終了条項 条項 値 ($)(1) (2) | |||
| ニコラ·アンマー | — | |||
| ジュリアーノ·フラタ | 101,338 | |||
| Gerlach、 Matthias | — | |||
| ガンサー、エクハド | — | |||
| ポーリーニクラウス | 321,969 | |||
| (1) | 終了値トリガイベントは、財政年度終了の最終営業日(2022年12月31日)に発生すると仮定します。 |
| (2) | 適用される場合、取得/未使用休暇の価値 および対応する費用精算金額は含まれておらず、雇用終了に関する“逓増”支払いとはみなされないからである。 |
| 93 |
| D. | Exchange 制御 |
カナダ には外国為替規制制度がない。外国からの借金や配当金、利息、特許使用料や類似支払、管理費、ローンの返済、貿易債務の決済や資本の送金に為替制限はありません。
| E. | 税収 |
以下の要約は一般性のみを持ち,いかなる 特定の所有者に対する法律や税務提案としても解釈されるべきではない.したがって、持株者は彼らの特殊な状況を考慮して、彼ら自身の税務顧問に普通株に投資する税務結果に関する提案を相談することを提案する。
材料カナダ所得税の考慮事項
以下の要約は、普通株式保有者に適用されるカナダ連邦所得税の主な考慮事項を説明し、改正されたカナダ連邦所得税法(R.S.C.1985)(“税法”)について、すべての関連する 回において、当社と取引され、当社と関連がなく、その普通株を資本財産として保有する( “所有者”)について説明する。税法の場合、普通株式は、一般に、所有者が証券取引または取引を行う過程でそのような普通株を保有しているか、またはその所有者が1つまたは複数の取引の性質とみなされる取引において当該普通株を保有または買収しない限り、所有者の資本財産としてみなされる。
本要約は,(I)時価計算規則で税法で定義された“金融機関”,(Ii)税法で“特定金融機関”と定義された所有者,(Iii)税法で“租税回避投資”と定義された権益,(Iv)税法に基づいて選択された機能的通貨報告,(V)すでに“派生長期合意”に到達する保有者には適用されない.普通株式の場合、または(Vi)税法によって定義された配当賃貸手配または税法で定義された配当賃貸手配の一部として普通配当金を取得する会社。この人たちは彼ら自身の税務顧問に相談しなければならない。
本明細書で議論されていない他のbr注意事項は、カナダに住む会社の所有者に適用される可能性があり、税法の目的については、普通株の買収を含む取引または一連の取引または事件の一部として、カナダに住む会社と一定の距離を維持していない取引になっているか、またはなっている。1つの非住民またはグループの非住民によって制御され、税法212.3節の“外国付属会社ダンピング”規則によると、互いに一定の距離を保つことができない。この保有者たちは普通株を買収した結果について彼らの税務顧問に相談しなければならない。
本要約は、税法及びその公布された法規(以下、“条例”と略称する)の現在の条項及びカナダ税務局(CRA)が現在公表している行政政策及び評価慣行に対する会社の理解に基づいている。税法と法規のすべての提案修正案も考慮されており、 は本条例の施行日前に財務大臣によって公布された(“税収提案”)であり、このようなすべての税金提案 が現在の提案に従って実行されると仮定する。税金提案が提案の形態または完全に提案の形態で公布されることは保証されない。本要約は、立法、法規、司法または行政行動または解釈によっても、省、br}地方、地域、または外国の税金考慮要因にも関連しないCRAの法律または行政または評価実践または政策のいかなる変化も考慮または予想されない。
税法の目的に対して、すべての金額は、配当金、調整後のコスト基数と処分収益を含み、通常はカナダドルで確定しなければならない。外貨建ての金額は税法によって決定された為替レート を使ってカナダ通貨に変換しなければなりません。保有者が普通株に関連する任意の資本収益または任意の資本損失の金額はカナダレート変動の影響を受ける可能性がある。
| 94 |
所有者 非カナダ住民
以下で議論する は,すべての関連時間に適用され,税法については,カナダ住民でもカナダ住民ともみなされず,また,カナダで業務や一部の業務を経営しているまたは普通株を保有している所有者 (“非住民所有者”)ともみなされない。なお、本議論は、カナダや他の地方で保険を受けたり、保険業務を受けているとみなされる保険会社には適用されない。
普通株式を処分する
非住民所有者は、一般に、当該非住民 所有者が普通株式を処分する際に現金になる任意の資本収益について税法に基づいて納税することはなく、当該等の株式が処分時に非住民所有者の“カナダ課税財産” (税法の定義により)を構成し、所得税条約又は条約を適用するbr条項に基づいて、当該収益は納税を免除されない。普通株が処分時に指定された証券取引所(現在はナスダックとトロント証券取引所を含む)に上場している限り、普通株は通常、非住民所有者の課税カナダ財産を構成しない。(A)処分直前60ヶ月の間のいつでも、(I) (A)非住民所有者、(B)非住民保有者が一定の距離を置いて取引していない者を除いて、 および(C)非住民所有者または(B)前記者の直接または間接 は、1つまたは複数の共同企業によって会員権益を保有し、当社の任意のカテゴリまたはシリーズ株式の25%以上の発行済み株式を所有する;および(Ii)当社の株式公平時価の50%を超える直接的または間接的には、カナダに位置する不動産、“カナダ資源財産”(税法参照)、“木材資源 財産”(税法の定義参照)、または任意の当該財産のオプション、権益または民法権利のうちの1つまたは任意の組み合わせ に由来し、これらの財産の存在または(B)普通株が他の方法で非住民 保有者とみなされるカナダ課税財産とみなされる。
課税 カナダ財産(かつ税法で定義された“条約保護財産”ではない)を構成または構成またはみなされる普通株については、非住民所有者の資本収益(または資本損失)は、一般に“カナダ住民所有者-普通株処分”というタイトルで記述された 方式で計算される。普通株がナスダック、トロント証券取引所、または他の“公認証券取引所”(定義税法参照)に上場を停止した場合、カナダ課税財産に属する普通株を処分する非住民 保有者は、普通株が処分されている非住民 保有者の“条約によって保護された財産”でない限り、税法116節の要求を満たすことを要求される可能性がある(定義税法参照)。
非住民普通株はカナダ課税財産の保有者は自分の税務顧問に相談しなければならない。
普通配当金の課税
当社は、非住民所有者への支払または貸記とみなされる配当金を25%の税率でカナダの源泉徴収税を納付しなければならない。適用される税務条約または条約の条項に基づいて減額しなければならない。改正されたカナダ-米国税条約(1980)(“条約”)によると、配当実益所有者である非住民配当金保有者に支払われる源泉徴収税率は、本条約については、米国に居住し、本条約の利益を享受する権利を有する会社(“米国所有者”)は、一般に配当総額の15%に限られている(例えば、米国所有者が実益で当社の少なくとも10%の議決権を有する株式を有する会社であれば、br}米国所有者の5%である)。非住民所有者は自分の税務顧問に相談しなければならない。
カナダに住むbrを持つ人
以下では、任意の関連時間に税法についてカナダに居住する普通株式保有者(“カナダ所有者”)に適用されるか、または とみなされる一般株式保有者に適用する。場合によっては、普通株式のあるカナダ所有者は、資本財産としての資格を満たしていない可能性があり、場合によっては、税法第39(4)項に規定する撤回不可能な選択を行うことによって、カナダ所有者が所有する普通株式および他のすべての“カナダ証券”(例えば、税法で定義されているbr})を資本財産と見なすことができる。カナダ人所有者は、彼らの特定の場合、税法39(4)項による選挙が実行可能であるかどうかおよび/または望ましいかどうかを知るために、自分の税務コンサルタントに相談しなければならない。
| 95 |
普通配当金の課税
税法によると、普通株が受け取ったか、または受け取ったとみなされる配当金はカナダ所有者の収入に計上される。個人(特定の信託を除く)であるカナダの保有者が受信したか、または受信されたとみなされるこのような配当金 は、課税カナダ会社株について税法で受信された配当金の合計および配当相殺規則 を遵守する。一般的に、会社が税法の規定に基づいて配当金を“合格配当金”(税法の意味に適合する)に指定すると、その配当金は増強された総和と配当税相殺 を享受する資格がある。会社が配当金を合格配当金に指定する能力が制限される可能性がある。会社であるカナダ 保有者は、その収入を計算する際にそのような配当金を含むことが要求され、通常、その課税所得額を計算する際にそのような配当金の金額を差し引く権利がある。場合によっては、税法第55条第2項は、カナダ会社所有者が受領した課税配当金を処分収益又は資本収益と見なすことができる。カナダの株主が“個人会社”または“主体会社”(税法で定義されているように)に属する場合、税法第IV部の規定により、所持者の課税所得額を計算する際に、普通株が受け取ったか、または受け取ったとみなされる配当金について払戻可能な税金を支払う責任がある。
普通株式を処分する
カナダの株主が普通株を処分するか、または普通株を処分するとみなされると、通常、資本収益(または資本 損失)が発生し、その額は、株式を売却して得られた収益が任意の合理的な処分コストを差し引いて株主の株式調整コストベースを超える(または下回る)額に相当する。このような資本収益(または資本損失)は、後述する“資本利益と資本損失税”に記載されている処理方式で処理される。
追加の は税金の払い戻しができます
“カナダ制御民間会社”(この用語は税法で定義されている)であるカナダ所有者は、以下に定義する“課税資本利益”の金額を含む、いくつかの投資収入に追加的な払戻可能な税金を支払う責任がある可能性がある。
資本利益と資本損失の課税
一般に、カナダ所有者が1つの課税年度に実現した任意の資本収益(“課税資本収益”)の半分は、所持者の同年度の収入に計上される。税法の規定によると、カナダの保有者が1つの課税年度に実現した任意の資本損失(“許容資本損失”)の半分 は、保有者がその年度に実現した課税資本収益からbrを差し引かなければならず、課税資本収益を超える許容資本損失は、前の3つの納税年度のいずれかで転換して控除することができ、またはその後の任意の納税年度に繰越し、その年度に実現された課税資本収益の純額からbrを差し引くことができる。会社であるカナダ所有者が普通株式を処分又は処分することにより実現された任意の資本損失の金額は、税法で規定された範囲及び場合には、当該普通株式(又は普通株が置換された株式)から受信したか、又は受信した配当額とみなされることができる。会社が組合企業のメンバーまたは信託の受益者であり、brが組合企業または信託会社を介して直接または間接的に普通株を所有している場合には、類似した規則も適用される。
代替最低税額
個人であるカナダ所有者によって達成された課税資本収益および受信された課税配当金 (信託を含むが、特定の指定された信託を含まない)は、最低税額に代わる責任を生じる可能性がある。
| 96 |
材料:アメリカ連邦所得税の考慮事項
以下の議論は、米国の保有者(以下のように定義する)に適用される普通株の購入、所有、処分に適用される重大な米国連邦所得税結果の要約であるが、すべての潜在的な米国連邦収入 税収への影響の完全な分析ではない。本要約は,1986年に改正された“国税法”(以下,“法典”と略す),それに基づいて公布された“米国財務省条例”,米国国税局の裁決と,その日から発効する司法判断に基づいている。これらはすべて変化する可能性があり,遡及効力を持つ である可能性があり,異なる解釈である可能性がある.本要約は、いかなる提案立法の潜在的な影響も議論せず、不利であっても有益であってもよい。 任意の提案された立法が採択されると、遡及的に適用することができる。本要約は、国税局に対して拘束力がなく、国税局が本要約の持つ立場とは異なるまたは逆の立場をとることも排除しない。
この要約は、米国連邦所得税のすべての態様に関連するものではなく、これらの態様は、特定の米国連邦所得税保有者の具体的な状況に関連する可能性がある(例えば、米国所有者は、“基準”に基づいて純投資収入に代替最低税または連邦医療保険納付税を徴収する)、または米国連邦所得税法の特殊な規則によって制約される可能性のある所有者を含む
| ● | 株、証券、または通貨取引業者 ; | |
| ● | 時価会計方法を用いた証券トレーダー | |
| ● | 銀行や金融機関 | |
| ● | 保険会社 ; | |
| ● | 規制された投資会社 ; | |
| ● | 不動産投資信託基金 | |
| ● | 免税組織 ; | |
| ● | 退職計画、個人計画、個人退職口座、繰延納税口座 | |
| ● | 共同企業または米国連邦所得税の他の直通エンティティおよびそのパートナーまたはメンバー; | |
| ● | ヘッジまたは転換取引または他の総合的またはリスク低減取引の一部として普通株を保有する者 ; | |
| ● | “規則”の外国籍条項に拘束されているか、または制限されている可能性のある者; | |
| ● | 機能通貨はドルではない人 | |
| ● | 私たちのすべてのカテゴリが議決権を持つ株式の総投票権の10%以上、または私たちのすべてのカテゴリの株式の総価値の10%以上を直接、間接的にまたは推定します。 |
本要約は、当社の株式承認証を保有、行使、または処分する税務結果についても言及しない。同社が以下に説明するPFICである場合、その株式証明書の米国所有者は不利な税収規則の制約を受け、これを株式証の時価計算のbrまたはQEF選挙に類認することはできないであろう。米国権証所持者は、会社がPFICに分類された場合を含む、会社の権利証を保有、行使または処分する米国連邦所得税結果についてその税務顧問に相談しなければならない。
この要約は、米国の所有者に適用される州、現地または外国の法律、相続税、または贈与税のいずれにも適用されることについては議論しない。なお、本議論は、普通株を資本資産として保有する米国の保有者に限定される。本要約では、“米国株式保有者”とは、普通株の実益所有者を意味するか、または米国連邦所得税については、
| ● | アメリカの個人市民や住民は | |
| ● | 米国連邦所得税目的のために、米国、その任意の州またはコロンビア特区法律内、または法律に基づいて設立または組織された会社または他のエンティティ; | |
| ● | その収入は、その出所にかかわらず、米国連邦所得税の遺産を納めなければならない | |
| ● | (A)米国内の裁判所が、このような信託の管理行使を主に監督することができ、1つまたは複数の“米国人”(本規則でいう)が、信託のすべての実質的な決定を制御する権利がある場合、(br}または(B)米国連邦所得税については、有効な選挙が効果的に米国人とみなされる。 |
| 97 |
組合企業または米国連邦所得税によって組合企業に分類された他のエンティティまたは普通株を保有するように手配されている場合、パートナーの米国連邦所得税待遇は、一般に、パートナーの地位およびパートナーの活動に依存するであろう。本要約は、このようなパートナーに対する税務結果については言及しない。このようなパートナーは共同企業が普通株を購入、所有し、処分する税収結果について自分の税務顧問に相談しなければならない。
米国の所有者は、以下の税収結果について、その特定の状況および任意の州、地方、外国または他の税法(贈与法および遺産税法を含む)について、自分の税務顧問に相談しなければならない。
もし私たちが受動的な外国投資会社(“PFIC”)の結果なら
外国企業は、任意の課税年度においてPFICに分類され、br社およびいくつかの子会社が適用される“透視規則”による収入および資産を考慮した後、(I)その総収入の少なくとも75%が“受動的収入”であるか、または(Ii)その資産の平均四半期価値の少なくとも50%が、受動的収入を生成する資産または受動的収入を生成するために保有される資産であることができる。受動的収入は、一般に、配当金、利息、レンタル料、および特許使用料 (貿易またはビジネスを積極的に展開することから得られるいくつかのレンタル料および特許使用料を含まない)、年金、および受動的収入を生成する資産収益を含む。一方の非米国会社が価値で別の会社の少なくとも25%の株を持っていると計算すると、PFICテストでは、非米国会社は別の会社の資産の割合シェアを持っているとみなされ、直接 が他の会社の収入の割合シェアを獲得しているとみなされる。
Br社は2015納税年度のPFICと考えているが,2016−2022納税年度のPFICではない。しかし、当社の資産の公正時価 は普通株の市場価格によって大きく決定される可能性があり、普通株の市場価格が変動する可能性があり、当社の収入と資産の構成は、当社がどのようにどのように、どのような融資取引で調達した任意の現金をどのように迅速に使用するかの影響を受ける。したがって,当社が2022課税年度または将来のいずれの課税年度においてもPFICに分類されないことは保証されない。アメリカの保有者は会社のPFIC地位について彼らの税務顧問に相談しなければならない。
米国所有者が普通株式を所有するいかなる課税年度内に、当社がPFICに分類される場合、米国所有者は、いくつかのbr選挙(以下に述べる時価およびQEF選挙を含む)がない場合、通常、以下の点に関する不利なルールを遵守する(br}当社がPFICに分類され続けるか否かにかかわらず):(I)いかなる“超過割り当て”(通常、1つの納税年度に米国所有者が受信した普通株式割り当ては、以前の3つの納税年度に米国所有者が受信した平均年間割り当ての125%を超え、または(br}が短い場合、米国所有者の普通株式保有期間)および(Ii)普通株の売却または他の処置によって達成された任意の収益を超える。
これらの不利なルール(A)によれば、超過分配または収益は、米国の保有者の保有期間内に比例して分配される。(B)本課税年度及び当社がPFICに分類される第1の課税年度までのいずれかの課税年度に割り当てられたbr}金額を一般収入として課税し、(C)当社がPFICに分類された他の課税年度毎の金額を当該年度適用納税者種別の有効最高税率 に課税し、当該等の他の納税年度の課税項目について利子費用を徴収する。会社ではないアメリカの保有者 は、支払われたどのような利息も“個人利息”と見なすことを求められており、これは差し引くことができない。
米国 保有者は、普通株が“販売可能”であることを前提として、普通株を時価で選択することで、上記の不利なルールを部分的に回避することができる。普通株が“適格取引所”または適用される米財務省法規が指す他の市場で“定期取引”されていれば、普通株は取引可能である。そのため、普通株は、その取引期間中の任意のカレンダー年度内に定期的に取引されると考えられるが、カレンダー四半期ごとに少なくとも15日は最低数で取引される。普通株は現在ナスダックに上場し、 は合格取引所を構成している;しかし、普通株が合格取引所で時価計算選挙を行う時に通常取引とみなされることは保証されない。普通株がナスダックで正常に取引されていない場合、またはナスダックから退市し、上記必要な期間内に他の合格取引所で取引されていない場合、時価ベースの選挙はない。
| 98 |
時価選択を行う米国の保有者は,課税年度ごとの毛収入に,米国保有者の普通株の納税年度終了時の公正時価が米国普通株調整後の課税ベースを超えた金額を含まなければならない。当選した米国保有者は、米国保有者が普通株で調整した納税基礎が普通株の納税年度終了時の公平時価を超える部分について一般損失控除を申請することもできる。しかし、この減額は、以前に収入に含まれていた任意の時価での純収益に限定される。時価計算で選択した米国の保有者は、通常、このような時価での選択によって毛収入を計上するか、控除されることが許可された金額を反映するために、通常、米国保有者の普通株における納税ベースを調整する。普通株の実際の売却または他のbr処分の収益は普通収入とみなされ、普通株の売却または他の方法で処分することによる任意の損失は普通損失とみなされるが、これまでに収益に計上された任意の時価純収益を限度とする。
米国で保有者が普通株のいずれかの課税年度を所有しているが、時価建ての選択を行う前に、会社がPFICに分類される場合、上記の不利なPFICルールは、選択された年度に確認された任意の時価収益に適用される。そうでなければ、時価ベースの選択は、選択された納税年度およびその後のすべての納税年度に発効する。アメリカ国税局の同意なしに、普通株が流通を停止しない限り、br選択権を取り消すことはできません。この場合、選択権は自動的に終了します。
当社がPFICに分類されている場合、普通株の米国保有者は、通常、当社が任意の直接または間接子会社に所有している株を所有しているとみなされ、これらの直接または間接子会社もPFICであり、当社がこのような子会社の株式を自社に分配·処分する上で同様の不利なルールを遵守する。PFICにも分類されている当社のどの子会社の株も時価ベースの選挙は許されていません。アメリカの保有者は彼らの税務顧問に相談して、時価建て選挙の可用性と手続きを知るべきだ。
場合によっては、PFICの株主は、QEFを選択することによって、利息料金および上述した他の不利なPFIC結果を回避することができ、現在、PFIC未分配収入におけるシェアに課税される。QEFに適した記録保存要求を満たし,要求した米国所有者にQEFルールに基づいてこのような米国保持者に報告 を要求する情報を提供するように努力する.しかし,会社が記録保存要求を満たしたり,米国の保有者が報告すべき情報を提供したりする保証はない.
米国の持株者がその普通株式保有期間に開始した最初の納税年度にQEF選挙をタイムリーに効率的に行うbr}は、通常、その普通株に関する上述した不利なPFIC結果の影響を受けない。逆に、タイムリーかつ有効なQEF選挙を行った米国人保有者 は、(A)会社の純資本収益、長期資本利益として当該米国所有者に課税すること、および(B)会社の一般収益を一般収入として当該米国所有者に課税することを含む米国連邦所得税を当該米国所有者に比例して納付する。一般に,“純資本収益”は(1)長期純資本収益 を(2)短期純資本損失で割ったものであり,“普通収益”は(A)“収益と利益”を (B)純資本収益で割ったものである。
当社についてタイムリーかつ効率的なQEF選挙を行うbr米国所有者は、一般に(A)米国所有者が以前にQEF選挙により収入に計上された“収入と利益”を代表する免税分配 を得ることができ、(B)QEF選挙によって収入に含まれるか、または免税分配として許可されたbr}金額を反映するために、米国所有者の普通株式における課税ベースを調整することができる。さらに、QEF選挙を行った米国の保有者は、通常、普通株または他の課税処分の資本収益または損失を確認する。
QEF選挙は株主単位で行われる.良質教育基金選挙が行われると、良質教育基金選挙を行う課税年度およびその後のすべての課税年度に適用され、良質教育基金選挙が失効または終了しない限り、あるいはアメリカ国税局は良質教育基金選挙の撤回に同意する。また,米国の保有者がQEFを選択すれば,QEF選挙は会社がPFICではない納税年度内に有効(適用しないにもかかわらず) を継続する。
| 99 |
会社がPFICに分類され、その後分類されなくなった場合、米国所有者は選択することができ(“売却”とみなす)、米国連邦所得税の目的で会社の納税年度の最終日にその米国所有者の普通株式を売却したとみなされる。売却選択をした米国の保有者は、会社の普通株を持つことで を停止することをPFICを持つ株とみなす。しかしながら、売却選択とみなされる結果として確認された報酬は、上記の不利なルールによって制約され、損失は確認されない。
もし会社が毎年米国の所有者である個人私募株式投資会社である場合、米国所有者は、一般株式の分配および売却によって達成された任意の収益に関するIRS Form 8621の年間情報申告書を提出することを要求される。
さらに、会社がPFICである場合、米国持株者は、通常、その普通株式所有権に関する年間情報申告書を米国国税局に提出する必要がある(br}IRS Form 8621においても、PFIC株主に米国連邦所得税または情報申告書を提出することを要求する)。
米国の所有者は、適用可能なPFIC制度と、この制度によって彼らが負担する可能性のあるいかなる報告義務についても彼らの税務コンサルタントに相談しなければならない。
配当をする
上述したPFICルールに適合することを前提として、会社は、現在または累積収益および利益(米国連邦所得税の目的に応じて決定される)から支払われる任意の分配から、その支払いされた任意のカナダ源泉徴収税について減額する前に、通常、外国由来配当収入として米国所有者に課税され、一般に、会社brが控除されることが一般的に許容される配当収入を享受する資格がない。
当期と累積収益と利益の分配 を超えると米国 保有者の普通株における調整税ベースの範囲で資本の免税返還とみなされ,その後資本収益とみなされる。しかし、会社はアメリカ連邦所得税の原則に基づいてその収益と利益を計算するつもりはない。したがって、米国所有者は、br社から行われる任意の分配は、通常、米国連邦所得税目的配当金とみなされることを期待すべきである。アメリカの保有者は会社から得られた任意の分配の適切なアメリカ連邦所得税処理について自分の税務顧問 に相談しなければならない。
会社がPFICとみなされる納税年度またはそれに続く納税年度に不正者米国株主に支払う配当金 は,通常長期資本利益に適用される特別減税税率を享受する資格がない。他のすべての課税対象のbr年度には、ある条件を満たす限り、会社が支払う配当金は、通常長期資本利益に適用される特別減税税率で非会社米国保有者に課税されなければならない。(最短保有期間要件を含む)。当社 は2020納税年度のPFICではないと考えています。しかし,当社が2021年にPFICに分類されない保証はないため,米国所有者が2021年または2022年に支払う配当金の比率 (あれば)の低減を要求できる保証はない。より詳細な議論については、上記のタイトル“重要な米国連邦所得税考慮事項--”私たちが受動型外国投資会社の税収結果であれば“小節を参照してください。
Brの現行法によると、会社は非カナダ投資家に配当金を支払うには一般的に25%のカナダ源泉徴収税を支払う必要がある。 はカナダ-米国税収条約(“br条約”)に基づいて福祉を受ける資格のある米国人所有者の源泉徴収税率が最高15%に引き下げられる(米国所有者が実益が会社の少なくとも10%の議決権株式を有する会社であれば5%)に適用される。米国の保有者が受け取った配当金がカナダにある米国の永久機関と効果的に関連している場合、この低減された源泉徴収率は適用されないだろう。米国連邦所得税については、米国のbr所持者は会社から源泉徴収されたカナダ税を受け取ったとみなされ、カナダ税務当局に源泉徴収されたbr税が支払われている。この規則の結果として、米国の保有者が配当金を支払うことにより米国連邦所得税総収入に計上された配当収入金額は、米国の保有者がその支払いについて会社から実際に受け取った(または受け取る)現金金額よりも大きい可能性がある。
| 100 |
ある制限を受けた場合、米国の保有者は通常、米国の保有者の選挙で米国連邦所得税の責任を免除する権利があり、あるいはその米国連邦の課税所得額を計算する際に会社が控除したカナダ所得税を差し引く権利がある。この選択は年ごとに行われ、米国の保有者が1年以内に納めたすべての外国税(直接納付でも源泉徴収でも)に適用される。外国税収控除限度額について言えば、会社が支払う配当金は通常“受動カテゴリ収入”バスケット中の外国 源収入を構成する。外国の税収免除規則は複雑で、アメリカの保有者はその特定の状況下で外国の税収控除を受けることができるかどうかについて彼らの税務顧問に相談しなければならない。
カナダドルで支払われた配当金は、当該カナダドルが当時実際にドルに両替されていたか否かにかかわらず、米国所有者(実際または建設的に)が配当金を受信した日の有効為替レートで計算されたドル金額を米国所持者の総収入に計上する。受信したカナダドルが受信した日にドルに両替されていない場合、米国所有者は、受信した日のドル価値に等しいカナダドル課税基礎を有する。カナダドルの収益または損失は、通常、米国由来の一般収入または米国所有者のbr損失である。
会社は一般的に何の配当も派遣せず、予見可能な未来にも何の配当も支給しない。
普通株の売却、交換又はその他の課税処分
上述したPFICルールによれば、米国の保有者は、通常、米国連邦所得税目的の資本収益または損失を確認し、売却、交換、または他の課税処分において達成された金額と、普通株式における米国所有者の調整課税ベースとの間の差額に等しい(ある場合)に、通常株式を売却、交換または他の課税処分に処理する際に、米国所有者は通常株式における調整課税ベースとの間の差額を確認する。
米国の保有者の普通株式における保有期間が1年を超える場合、このbr}資本収益または損失は長期資本収益または損失となる。資本損失の控除には制限がある。いかなる収益や損失も通常、米国からのものであり、米国の外国税免除目的に使用される。
情報br報告とバックアップ控除
米国内または米国の支払人または米国の中間者によって支払われる配当金および普通株を売却または処分することによって生じる収益は、通常、適用法規の要求に基づいて米国国税局および米国所有者に報告されなければならない。米国の保有者が正確な納税者識別番号を適切な方法でタイムリーに提供できなかった場合、またはそのような予備源泉徴収要件を遵守または免除できなかった場合、予備源泉徴収税はこれらの支払いに適用される可能性がある。いくつかの米国の保有者 は、本明細書に記載された情報報告または予備源泉徴収要件によって制限されない。アメリカの保有者は彼らの税務顧問に問い合わせて、予備の源泉徴収税を免除する資格を獲得し、免税の手続きを確立することを理解しなければなりません。
バックアップ源泉徴収税は付加税ではありません。アメリカ国税局に必要な情報をタイムリーに提供すれば、アメリカの保有者は通常、そのアメリカ連邦収入から返金またはbrの源泉徴収金額を免除する納税義務を得ることができる。会社は源で税金を代理徴収する責任を負っている。
いくつかの例外的な状況および将来の指導によって制限されない限り、“個人を指定する”または“国内エンティティを指定する”(米国国税局表8938の説明で定義されている)米国保有者は、米国国税局テーブル8938において、米国人保有者が非米国個人(例えば、当社のような)で発行した株式または証券におけるbr権益を毎年報告しなければならない。アメリカの持株者はその買収、所有或いは処分普通株が発生する可能性のある情報報告義務についてその税務顧問に相談しなければならない。
| F. | 配当 と支払いエージェント |
は要りません。
| G. | 専門家発言 |
は要りません。
| 101 |
| H. | 展示されている文書 |
以上のように年次株主総会で監査された総合年次財務諸表を提出するほか、改正された1934年の証券取引法の情報要求を遵守しなければならない。これらの要求に基づき,我々は米国証券取引委員会に報告書やその他の情報を記録し,提供する.これらの資料は、本20−F表年次報告書と本報告書の証拠物とを含み、米国証券取引委員会公共資料室で閲覧·コピーすることができ、住所はワシントンD.C.20549号、住所はワシントンD.C.20549、N.E.F Street 100 F Streetである。 公衆は米国の米国証券取引委員会に電話し、米国証券取引委員会公共資料室の運用情報を取得することができる。 米国証券取引委員会公共資料室の運営情報を取得することができる。 米国証券取引委員会はまた、www.sec.gov上でウェブサイトを維持しており、 が米国証券取引委員会の登録者に電子的に提出された報告書、依頼書、その他の情報を含む。私たちが米国証券取引委員会に提出した年次報告書や他のいくつかの情報は というサイトで取得することができる。さらに、私たちが提出した資料は、www.sedar.comのウェブサイトでアクセス可能なカナダ証券管理人の電子届出システム(SEDAR)で調べることができる。本材料には,2023年に6−K表形式で米国証券取引委員会に提出されるbr株主年次総会の管理情報通書が含まれており,取締役や上級管理者の報酬や債務,証券の主要所有者などの情報が提供されている。より多くの財務情報は、2022年12月31日までの年度監査年度財務諸表に提供され、MD&Aがこれらのレポートに関連するレポートは、本年度レポート20-Fの他の部分に含まれています。これらのファイルはSEDAR(www.sedar.com)やEdga(www.sec.gov)でもアクセス可能である.
| I. | 子会社 情報 |
は要りません。
| 第 項11. | 市場リスクの定量的·定性的開示について |
公正価値
当社はその金融商品を“分担コストで計算する金融資産”と“分担コストで計算する財務負債”の2種類に分類している。
| ● | 会社が余剰コストで計算した金融資産は現金及び現金等価物、貿易及びその他の受取金及び制限性現金等価物を含む | |
| ● | 超過コストで計算される財務負債には、売掛金と売掛金、賃貸負債が含まれている。 |
上記のすべての金融商品の帳票価値は,その短期満期日によってその公正価値に近いか,あるいは は当該などのツールの現行金利と比較すると,市場金利に相当する.
ブラック-スコアーズ推定値方法は公正価値を計算する際に投入を使用し、IFRS 13で定義されているように、公正価値を計量するための投入を優先順位付けする階層構造を構築した。同じ資産または負債については,この階層構造はアクティブ市場における未調整の見積りに最高優先度(1レベル計測)を与え,観察できない投入に最低優先度(3レベル計測)を与える.
財務リスク要因
以下に、信用リスク、流動性リスク、外国為替リスク、および当社がこれらのリスクをどのように管理するかを含む、当社が金融商品に発生するリスクの性質と程度を開示する。
| (a) | 信用リスク |
信用リスクとは、顧客や金融商品の取引相手がその契約義務を履行できなかった場合、意外な損失が発生するリスクのことです。当社は定期的に信用リスクの開放をモニタリングし、この開放による損失の可能性を低減する措置を講じています。当社の現在の信用リスクの開放は、表の償却コストで計算されている金融資産に関連しています。会社 が保有する利用可能な現金額は、いつでも既知の額の現金に変換することができ、その現金残高を投資レベル格付けが少なくとも“P-2”または同等格付けの金融機関 に預けることができる。この情報は、独立した格付け機関によって提供され(ある場合)、ない場合、会社は、その現金を信頼性の良い金融機関に投資することを保証するために、公開された財務情報を使用する。合理的な回復期待がないという兆候があると、このような金融資産はログアウトされるが、法執行活動が必要だ。
| 102 |
2022年12月31日現在、売掛金に含まれる3つの取引相手の売掛金総額は約403ドル(2021-932ドル)であり、このうちゼロドル(2021-55ドル)は期限を超えており、減額されたと考えられ、全額支出されている。
通常、会社は顧客が売掛金に担保や他の保証を提供する必要はないが、信用は信用を評価した後に発行される。また、同社はすべての顧客に対して継続的な信用審査を行い、予想される信用損失を決定する。その上で、同社は2022年12月31日現在、br業務に関連するすべての未払い金と未払い金を準備している。
信用リスクの最大リスク開放は、当社の総合財務状況表で確認された金額とほぼ同じです。
| (b) | 流動性リスク |
流動性 リスクとは、会社が満期財務義務を履行できないリスクである。当社はその資本構造を管理することでこのリスク を管理し,キャッシュフローを期待したうえで当社の現金と現金等価物のスクロール予測を監視している。
経営陣は,会社計画の研究開発活動,販売費用,一般と行政費用および運営資金需要を考慮し,会社の手元には今後12カ月間の債務を履行するのに十分な現金があると結論した。同社はその研究·開発活動を拡張し、現金供給状況に応じて必要に応じてそうする能力がある。同社は2022年12月31日現在、現金および現金等価物50,611ドルを持っているが、その製品および技術を研究開発、商業化、製造するための追加の資本資源を必要としている。
リース負債を除いて、会社のすべての財務負債は流動負債であり、決済日は1年以内と予想される。
| (c) | 外貨リスク |
ビットコインの実体としてユーロを使用する
Br社はユーロを本位貨幣とする海外業務に投資し、外貨リスクに直面している。2022年12月31日現在、ドル対ユーロレートが10%上昇または低下すれば、他のすべての変数が不変のままである場合、2022年12月31日までの年度の純損失 は約823ドル(2021-300ドルと2020-110ドル)減少または増加する。
| 第 項12. | 株式証券を除く他の証券説明 |
| A. | 債務証券 証券 |
は要りません。
| B. | 株式承認証 と権利 |
は要りません。
| C. | その他 証券 |
は要りません。
| D. | アメリカ預託株 |
は適用されない.
| 103 |
第 第2部分
| 第 項13. | 違約、配当金滞納、滞納 |
ない。
| 第 項14. | 材料保持者権利の修正と収益の使用を保証する |
ない。
| 第 項15. | 制御 とプログラム |
最高経営責任者と最高財務責任者を含む経営陣の監督と参加の下で、2022年12月31日までの開示統制と手続きの有効性を評価した。私たちの開示制御および手続き は、1934年の証券取引法に基づいて提出または提出された報告書で開示を要求した情報が、米国証券取引委員会の規則および表に指定された期間内に記録、処理、集約および報告されることを保証し、そのような情報が蓄積され、最高経営者および最高財務官を含み、必要な開示に関する決定をタイムリーに行うことを確実にすることを目的としている。
どのような制御およびプログラムも、設計や操作がどんなに良くても、予想される制御目標を達成する合理的な保証を提供することしかできない。管理層は、可能な制御とプログラムの費用対効果関係を評価する際に、その判断を運用しなければならない。今回の評価によると、最高経営責任者と財務責任者は、これらの開示制御およびプログラムは2022年12月31日から有効であると結論した。
経営陣財務報告内部統制年次報告書
私たちの経営陣は財務報告書の十分な内部統制を確立して維持する責任がある。我々の財務報告に対する内部統制は、国際会計基準委員会が発表したIFRSに基づいて財務報告の信頼性と外部目的の財務諸表の作成に合理的な保証を提供することを目的とした過程である。
私たちの財務報告に対する内部統制は、(I)Aeterna Zentaris資産の取引および処置を合理的かつ詳細かつ正確に反映するための記録の維持に関する政策と手順と、(Ii)IFRSに基づいて財務諸表を作成するために必要な取引記録の合理的な保証を提供し、会社の収支は会社の管理層の許可のみに基づいて行われる。および(Iii)財務諸表に重大な影響を与える可能性のある不正買収、使用または処分会社の資産の防止またはタイムリーな発見について合理的な保証 を提供する。
その固有の限界のため、財務報告書の内部統制は誤った陳述を防止したり発見できない可能性がある。また,将来的に任意の有効性評価を行う予測は,条件の変化により制御不足のリスクが生じる可能性があり, や政策やプログラムの遵守度が悪化する可能性がある.
救済材料の弱点
2021年12月31日までの年次報告Form 20−Fにおける第15項である“制御とプログラム”と,2022年までに我々が提出した四半期ごとのMD&で開示したように,管理層は重大な弱点を構成する制御欠陥 を発見した。重大な欠陥とは財務報告内部制御の制御欠陥或いは制御欠陥の組み合わせであり、 は著者らの中期或いは年度連結財務諸表或いは関連開示の重大な誤報が合理的な可能性があり、適時に防止或いは発見できない可能性がある。
| 104 |
“国際財務報告基準”での許可と協力協定および関連収入確認の会計処理の審査制御を設計·実施できなかったためである。具体的には、我々の審査制御設計は不十分であり、複雑な収入手配の収入確認会計分析に対して十分な審査と評価を行うことができない。これは、私たちが以前に発表した2021年3月31日、2021年6月30日、2021年9月30日までの四半期と年初から現在までの簡素化中期総合財務諸表を再記述し、合意の収入確認に関連している。したがって、経営陣は上述したような重大な弱点があると判断した。
2022年には、上で議論した重大な欠陥を解決し、財務報告に対する私たちの内部統制を改善するための救済計画を実行しました。私たちの救済活動は
| ● | 2022年1月に新しい首席財務官を採用し、2022年9月に新しい会社財務総監を採用し、収入確認分野およびより広い国際財務報告基準分野で必要な知識および経験を有する外部専門家のサービスを利用することを含む、十分な技術知識および訓練を有する新しいリソースまたは追加資源を増加させることによって、私たちの収入確認および財務報告制御 を強化する。 | |
| ● | これらの取引を交渉および実行する際に、任意の会計影響を有する事項をタイムリーに処理することを保証する許可および協力協定など、適切な財務および会計担当者の審査戦略および複雑な取引に関連する有効な内部統制を設計および実施すること; | |
| ● | 重要な判断または分析を適用する必要がある取引を含むすべての非通常の取引を確保し、適切なレベルの徹底的な研究を経て、適切な会計および財務者(必要に応じて第三者テーマの専門家を含む)によって十分な記録を行うことを保証し、このような記録は、会社の首席財務担当者によってタイムリーに承認される。 |
我々は,上記のような重大な欠陥を解決するために新たに策定された政策,プログラム,制御活動をテストした.したがって,2022年12月31日からこの重大な欠陥が修復されたと考えられる.
財務報告内部統制変更
上記のような重大な弱点を救済するための行動を達成する以外に、2022年12月31日までの年度中に、財務報告の内部統制に大きな影響を与えたり、合理的に財務報告の内部統制に大きな影響を与える可能性のある変化はありません。
我々の経営陣は、2022年12月31日までの財務報告内部統制、すなわち今年度の20-Fレポートに含まれる期間が終了したことを評価した。経営陣は、トレデビル委員会後援組織委員会が発表した“内部統制--総合枠組み(2013年)”で決定された基準に基づいて評価を行った。我々の財務報告に対する経営陣の内部統制の評価によると、経営陣は、2022年12月31日まで、財務報告の内部統制に有効であると結論した。
| 第 項16 A。 | 監査委員会財務専門家 |
当社の取締役会では、我々には少なくとも1人の監査委員会財務専門家がいることが決定されています(第16 A~20-F表(B)段落の定義参照)。 監査委員会財務専門家の名前は、監査委員会会長Dennis Turpinさんです。表表第20-F(D)段(br}16 A)によれば、監査委員会財務専門家として特定された特平さんは、(I)特平さんをいかなる目的の“専門家”とするか、この指定により改正された1933年“証券法”第11条の目的(br};(Ii)により特平さんに課された職務、義務、又は責任を問わず、監査委員会及び取締役会のメンバーとして負う責務、義務又は責任を超えるものを含む。)または(Iii)監査委員会または取締役会の任意の他のメンバーの責務、義務または責任に影響を与える。監査委員会の他の現メンバーはPeter G.EdwardsとGilles Gagnonであり、彼らはDennis Turpin(議長)と独立しており、この用語はナスダック上場基準に定義されている。彼らそれぞれの教育背景や勤務経験の説明については、“第6項--役員、上級管理職、従業員”を参照されたい。
| 105 |
| 16 B項目. | 道徳基準 |
2017年12月16日、取締役会は“行為と商業道徳基準”を採択し、2018年1月1日から当時の“道徳行為準則”に代わった。“行動と商業道徳基準”は2018年1月24日に改正された。行為と商業道徳基準 は、これまでの道徳行為準則に基づいて拡張され、会社とその従業員が医療業界のメンバーとして担う具体的な義務を含む、会社のすべての従業員と取締役の予想される行為のより多くの詳細な情報を提供した。私たちは、私たちの道徳的行動基準および財務および/または会計違反または詐欺行為に違反する可能性のある懸念を報告するために、秘密および匿名のコミュニケーションチャネルを提供するために、独立した第三者供給者を選択した。改訂された“道徳的行動基準”のコピーは、添付ファイル11.1としてForm 20-Fの形態で本年度報告書に組み込まれ、当社のウェブサイトwww.zentaris.comの投資家-コーポレートガバナンスオプションカードの下で取得することもできる。道徳的行動基準“は、表20-F 16 B項(B)項で定義された”道徳的行動基準“ である。道徳的行動基準は、私たちの最高経営責任者、最高財務官、最高会計官または財務総監、または同様の機能を履行する者を含む、すべての従業員、役員、および上級管理者に適用され、会計事務における誠実さ、利益衝突、および適用される法律および法規の遵守に関する具体的な条項を含む。2014年12月4日、当社取締役会は“取締役会メンバーの商業行為と道徳基準”を採択し、本年度報告20-F表の添付ファイル11.2として参考に組み込んだ。もし私たちの会社の秘書に要請すれば、私たちは本部にこれらのファイルを無料で提供します。住所はサウスカロライナ州サマービル29486,315 Sigma Drive, です。
| 第 項16 C. | 依頼人 会計士費用とサービス |
(すべての 金額はドルで表される)
同社の現在の監査役は安永会計士事務所です。安永法律事務所は会社の監査役に任命され、2021年3月25日から発効した。
| (a) | 監査費用 |
2022年12月31日までの財政年度中に、会社の主要会計士である安永会計士事務所は、会社年度連結財務諸表の監査および法定·監督文書に関するサービスに390,571ドルを支払った。2021年12月31日までの財政年度中に、会社の主要会計士である安永会計士事務所は242,986ドルの費用を支払い、監査会社の年度総合財務諸表のために、法定·監督文書に関するサービスを提供する。
| (b) | 監査に関する費用 |
2022年12月31日までの財政年度内に、当社の主要会計士である安永会計士事務所はゼロドルの監査費用或いはbr法律法規が要求していない証明サービスを受け取り、提案取引についての会計相談、審査募集定款と目論見説明書の付録に用いられ、これに関連する常習同意書と慰め状を提供することを含む。2021年12月31日までの財政年度内に、当社の主要会計士である安永会計士事務所は、法律や法規が要求しない監査や目撃サービスのためにゼロドルを支払い、提案された取引についての会計相談、目論見書と目論見説明書の補充材料を審査し、これに関連する慣用的な同意と慰め状を渡すことを含む。
| (c) | 税 手数料 |
2022年12月31日までの財政年度中、会社の主要会計士である安永会計士事務所の税務コンプライアンス、税務計画、税務相談に関するサービスに関する請求書は15,646ドルである。2021年12月31日までの財政年度において、会社の主要会計士である安永会計士事務所の税務コンプライアンス、税務計画、税務相談におけるサービス料金は45,054ドルである。
| 106 |
| (d) | すべての その他の費用 |
2022年12月31日までの財政年度中に、会社の主要会計士である安永法律事務所は、監査費用、監査関連費用、税費を計上していないサービスにゼロドルの請求書を発行した。2021年12月31日までの財政年度中に、会社の主要会計士である安永会計士事務所は、監査課金、監査関連費用、税費を計上していないサービスのために3987ドルの請求書を発行した。
| (e) | 監査委員会の承認前政策と手順 |
適用されるカナダ証券法規によると、私たちの監査委員会が非監査サービスの採用について具体的な政策と手続きを取ったかどうかを開示し、これらの政策と手続きの概要を準備しなければならない。監査委員会定款(本20-F年度報告添付ファイル11.3に引用して組み込むことにより、監査委員会は、すべての監査採用費用と条項を承認し、外部監査師が非監査サービスを提供する政策を審査し、必要に応じてこのようなサービスの事前承認枠組みを審査する責任がある。監査委員会はその議長がこのような非監査費用を事前に承認することを許可した。議長の事前承認は、このような事前承認後の最初の予定会議で監査委員会に提出される。
2022年および2021年12月31日までの各年度中、私たちの非常勤原子力師は審査委員会の承認を必要とする非審査サービスを提供していません。
| 第 項16 D. | 免除監査委員会の上場基準 |
ない。
| 16 E項目. | 発行者と関連購入者が株式証券を購入 |
ない。
| 16 F項目. | 登録者認証会計士の を変更する |
会社の外部監査サービスを全面的に審査した後、監査委員会は2022年12月31日までの財政年度に監査サービスを提供する提案を求めた。監査委員会は、会社の外部監査サービスを全面的に審査した後、2021年12月31日までの財政年度に監査サービスを提供する提案を求めた。寄せられた提案を精査し、すべての関連要因を適切に考慮した後、監査委員会は、普華永道会計士事務所ではなく、取締役会提案委員会が安永会計士事務所を当社の2021年12月31日までの財政年度の監査人とすることを提案した。安永会計士事務所は会社監査役に任命され、普華永道会計士事務所は会社監査師を辞任し、2021年3月25日から発効した。
過去2年間、独立監査人の報告書には不利な意見や免責声明が含まれていないか、または不確実性、監査範囲、または会計原則の面で保留意見または修正が存在する。
| 第 項16 G. | 会社管理 |
私たちのbrは全体的にナスダックの会社管理要求を遵守しているが、以下の記述と題する“私たちの普通株はナスダックあるいはトロント証券取引所から退市する可能性があり、これはその市場価格と流動性に影響を与える可能性がある”と題するリスク要素 は除外されている。もし私たちの普通株が取得されれば、投資家は上記3.D項の普通株を処分することが困難になる可能性がある“と述べた。私たち は、私たちの普通株式保有者会議に関するナスダックの法定人数が、このような発行済み株式の33 1/3% の要求を下回らないことを満たしていません。我々の規約では,任意の株主総会の定足数には,発行された議決権株式の少なくとも10% が含まれている。私たちは、私たちの定款に規定されている法定人数がCBCA(私たちが管理する会社法規)の要求に適合し、議決権を有する株式取引の母国取引所トロント証券取引所の規則にも適合するので、ナスダックのこの定足数要件の免除を受ける。適用された現在のナスダック要求によると、私たちは過去にナスダックに外部弁護士の手紙を提供し、これらのやり方が私たちの自国の法律によって禁止されていないことを証明した。
| 16 H項目. | 鉱山安全開示 |
ない。
| 項目 16 i | 検査阻止に関する外国司法管轄区域を開示する |
は適用されない.
第 第3部分
| 第 項17 | 財務諸表 |
財務諸表がページに表示される[108]至れり尽くせり[155].
| 第 項18. | 財務諸表 |
は適用されない.
| 107 |
Eeterna Zentaris Inc.
連結財務諸表
2022年と2021年12月31日まで,2022年,2022年,2020年12月31日まで年度
| 独立公認会計士事務所レポート(PCAOB ID: |
109 |
| 前身独立公認会計士事務所報告(PCAOB ID: |
111 |
| 合併財務状況表 | 112 |
| 合併株主権益変動表 | 113 |
| 統合損失表と包括損失表 | 114 |
| 統合現金フロー表 | 115 |
| 連結財務諸表付記 | 116 |
| 108 |
独立公認会計士事務所報告
Br社の株主と取締役会へ
Eeterna Zentaris Inc.
財務諸表に対する意見
添付のAeterna Zentaris Inc.(当社)2022年12月31日現在,2022年と2021年までの総合財務諸表,2022年12月31日までの2年度の株主権益,赤字と全面赤字およびキャッシュフローに関する総合財務変動表,および関連付記(総称して“総合財務諸表”と呼ぶ)を監査した。総合財務諸表は、国際会計基準委員会が発表した国際財務報告基準(IFRS)に基づき、すべての重要な面で、当社の2022年12月31日、2022年および2021年12月31日までの財務状況、および2022年12月31日までの各年度の財務業績とキャッシュフローを公平に反映していると考えられる。
意見を求める根拠
これらの財務諸表は会社経営陣が担当しています。私たちの責任は私たちの監査に基づいて会社の財務諸表に意見を発表することです。私たちはアメリカ上場企業会計監督委員会(PCAOB)に登録されている公共会計士事務所であり、アメリカ連邦証券br法律およびアメリカ証券取引委員会とPCAOBの適用規則と法規に基づいて、私たちは会社と独立しなければならない。
私たち はPCAOBの基準に従って監査を行います。これらの基準は、財務諸表に重大な誤報がないかどうかに関する合理的な保証を得るために、エラーによるものであっても不正であっても、監査を計画し、実行することを要求する。会社 はその財務報告の内部統制を監査する必要はなく、私たちを招いて監査を行うこともありません。私たちの監査の一部として、財務報告の内部統制を知る必要がありますが、社内財務報告の内部統制の有効性について意見を述べるためではありません。したがって、私たちはそのような観点を表現しなかった。
我々のbr監査には、財務諸表の重大な誤報のリスクを評価するための実行プログラムが含まれており、エラーによるものであっても詐欺であっても、これらのリスクに対応するプログラムを実行する。これらの手続きは、財務諸表中の金額および開示に関連する証拠をテストに基づいて検討することを含む。我々の監査には、評価に使用される会計原則と経営陣による重大な推定と、連結財務諸表の全体列報を評価することも含まれている。私たちは私たちの監査が私たちの観点に合理的な基礎を提供すると信じている。
重大監査事項
以下に述べる重要な監査事項とは、当期に財務諸表を監査する際に生じる事項であり、この事項は、監査委員会に伝達または要求されたものである:(1)財務諸表に対して重大な意義を有する勘定又は開示に関するものであり、(2)特に挑戦性、主観性又は複雑性に係る判断である。重要監査事項の伝達は、連結財務諸表に対する私たちの全体的な意見をいかなる方法でも変えることはなく、以下の重要な監査事項を伝達することによって、重要な監査事項またはそれに関連する勘定または開示に関する個別的な意見を提供することもない。
| 109 |
| 営業権減価 | |
| イベント記述 | 総合財務諸表に付記されている2、3および11に開示されているように、当社は、少なくとも年に1回の営業権減価テストを行うか、または割り当てられた営業権が割り当てられたグループの営業権が減少する可能性があることを示す兆候がある。減値は、このグループの現金付加価値税単位の帳簿額面(分配された営業権を含む)がその回収可能金額を超えているかどうかを評価することによって決定され、この回収可能金額は公正価値から販売コスト(“FVLCD”)と使用価値(“VIU”)の両方の中で高い者を引いて決定される。当社は2022年12月31日までに、その商誉計について減価費用を提案し、金額は760万ドルである。管理層は、VIUよりも高いと決定されたFVLCDモデルに基づいてCGUグループの回収可能数を決定した。FVLCDは市場方法に基づいて決定し、市場データに由来し、市場参加者からの当社がこのグループのCGUを販売する際に受け取ることができる価格に関する資料を含む。VIUは5年間をカバーするキャッシュフロー予測を用いて決定し,推定された税前割引率を用いて現在値に割引した。
|
我々 は,経営陣が適切な方法を決定するための重大な判断と,キャッシュフロー単位集団の回収可能金額を推定するための仮定 のために,キャッシュフロー単位グループの営業権減値を重要な監査事項として確認した.
| |
| 監査でこの問題をどのように処理するか | 営業権減価テストの推定回収可能金額をテストするために、我々の監査プログラムには、管理職の準備を取得する分析が含まれており、我々の評価専門家の協力の下で、回収可能な金額推定を作成するための管理職の評価方法が含まれている。我々は,推定されたFVLCDを支援文書と利用可能な市場データと比較し,そのグループのCGUを販売する際に市場参加者から得られる価格に関する情報を含む.また,経営陣のVIUモデルを取得し,履歴データ,現在のプロトコル,市場情報と比較することにより,経営陣のキャッシュフロー予測に関する推定と仮定の合理性を評価した。我々の評価専門家の助けを借りて,一連の独立した推定値を作成することで割引率をテストし,これらの推定値を経営陣が選択した割引率と比較する. |
/s/
私たち は2021年以来当社の監査役を務めています。
2023年3月22日
| 110 |

独立公認会計士事務所報告
Aeterna Zentaris Inc.取締役会と株主に。
財務諸表に対する意見
吾らは、関連付記(総称して総合財務諸表と呼ぶ)を含む2020年12月31日までの年度株主権益、損失及び全面損失及び現金流量の総合報告書を審査した。 吾らは、総合財務諸表は、各社の2020年12月31日までの年度の経営業績及び現金流量を各重大な面で公平に反映しており、国際会計基準委員会が公布した国際財務報告基準に適合しているとしている。
意見を求める根拠
これらの合併財務諸表は会社経営陣が担当しています。私たちの責任は、私たちの監査に基づいて会社の連結財務諸表に意見を発表することです。私たちは公的br社会計監督委員会(米国)(PCAOB)に登録されている公共会計士事務所であり、米国連邦証券法および米国証券取引委員会とPCAOBの適用規則と法規に基づいて、私たちは会社と独立しなければならない。
我々はPCAOBの基準に基づいてこれらの連結財務諸表を監査します。これらの基準は、合併財務諸表に重大なミスがないかどうかを合理的に決定するために、エラーによるものであっても不正であっても、監査を計画し、実行することを要求しています。当社は必要とせず、財務報告書の内部統制を監査する必要もありません。私たちの監査の一部として、財務報告の内部統制を知る必要がありますが、会社財務報告の内部統制の有効性について意見を述べるためではありません。したがって、私たちはそのような意見を表現しない。
我々のbr監査には,連結財務諸表の重大な誤報リスクを評価するプログラム,エラーによるものであっても詐欺であっても,これらのリスクに対応するプログラムを実行することが含まれる.これらの手続きは、連結財務諸表中の金額および開示に関する証拠をテストに基づいて検討することを含む。私たちの監査には、評価に使用される会計原則と経営陣による重大な推定と、連結財務諸表の全体列報を評価することも含まれています。私たちの監査は私たちの意見に合理的な基礎を提供していると思います。
/s/ 普華永道会計士事務所
特許専門会計士、公認会計士
カナダトロント
2021年3月24日
付記16で述べた逆株式分割を反映するように調整した場合を除いて、日付は2023年3月22日である。
私たち は1993年から2021年まで当社の監査役を務めています。
普華永道有限責任会社
カナダオンタリオ州トロント、ヨーク街18号普華永道ビル2600室、郵便番号:M 5 J 0 B 2
電話:+1 416 863 1133,電話:+1 416 365 8215
“普華永道” とはオンタリオ州の有限責任組合会社普華永道のことである。
| 111 |
Eeterna Zentaris Inc.
合併財務状況表
2022年12月31日と2021年12月31日まで
(単位:千ドル)
| 2022 | 2021 | |||||||
| $ | $ | |||||||
| 資産 | ||||||||
| 現在の資産 | ||||||||
| 現金と現金等価物(付記6) | ||||||||
| 貿易 とその他の売掛金(付記7) | ||||||||
| 在庫品 | ||||||||
| 所得税 課税税金 | ||||||||
| 前払い料金その他流動資産(付記8) | ||||||||
| 流動資産合計 | ||||||||
| 非流動資産 | ||||||||
| 制限 現金等価物(注6) | ||||||||
| 財産と設備(注9) | ||||||||
| 無形資産の識別が可能(付記10) | ||||||||
| 商誉 (付記11) | ||||||||
| 非流動資産合計 | ||||||||
| 総資産 | ||||||||
| 負債.負債 | ||||||||
| 流動負債 | ||||||||
| 支払すべき と課税負債(付記12) | ||||||||
| 予備 (付記13) | ||||||||
| 所得税 課税税金(付注22) | ||||||||
| 繰延収入 (付記5) | ||||||||
| 賃貸負債(付記14) | ||||||||
| 流動負債合計 | ||||||||
| 非流動負債 | ||||||||
| 繰延収入 (付記5) | ||||||||
| 延期 収益(付記10) | ||||||||
| 賃貸負債(付記14) | ||||||||
| 従業員 未来福祉(付記15) | ||||||||
| 予備 (付記13) | ||||||||
| 非流動負債合計 | ||||||||
| 総負債 | ||||||||
| 株主権益 | ||||||||
| 株本(注: 16) | ||||||||
| 株式承認証 | ||||||||
| その他 資本(注18) | ||||||||
| 赤字.赤字 | ( | ) | ( | ) | ||||
| その他の総合損失を累積 | ( | ) | ( | ) | ||||
| 株主権益合計 | ||||||||
| 総負債と株主権益 | ||||||||
承諾 (付記27)
後続事件(付記28)
付記はこれらの連結財務諸表の構成要素である。
取締役会の承認を経て
| /s/ キャロライン·エグベルト | /s/ デニス·ターピン | |
キャロライン·エグベルト 取締役会議長 |
デニス·ターピン 役員.取締役 |
| 112 |
Eeterna Zentaris Inc.
合併株主権益変動表
2022年、2021年、2020年12月31日までの年度
(単位:千ドル)
| 株式 資本 | 株式承認証 | その他 資本 | 赤字.赤字 | 累計 その他総合収益(損失) | 合計する | |||||||||||||||||||
| $ | $ | $ | $ | $ | $ | |||||||||||||||||||
| 残高 -2020年1月1日 | ( | ) | ( | ) | ||||||||||||||||||||
| 純損失 | ( | ) | ( | ) | ||||||||||||||||||||
| その他 全面赤字: | ||||||||||||||||||||||||
| 外貨通貨換算調整 | ( | ) | ( | ) | ||||||||||||||||||||
| 固定福祉計画損失の精算と固定福祉負債純額の再計量(付記15) | ( | ) | ( | ) | ||||||||||||||||||||
| 全面損失 | ( | ) | ( | ) | ( | ) | ||||||||||||||||||
| 株式承認証を株式に再分類する(付記17) | ||||||||||||||||||||||||
| 普通株式と引受権証を発行し、取引コストを差し引く(付記16) | ( | ) | ||||||||||||||||||||||
| 株式ベースの報酬コスト | ||||||||||||||||||||||||
| 残高 -2020年12月31日 | ( | ) | ( | ) | ||||||||||||||||||||
| 純損失 | ( | ) | ( | ) | ||||||||||||||||||||
| その他 全面赤字: | ||||||||||||||||||||||||
| 外貨通貨換算調整 | ||||||||||||||||||||||||
| 固定福祉計画損失の精算と固定福祉負債純額の再計量(付記15) | ( | ) | ( | ) | ||||||||||||||||||||
| 全面損失 | ( | ) | ( | ) | ||||||||||||||||||||
| 普通株式と引受権証を発行し、取引コストを差し引く(付記16) | ||||||||||||||||||||||||
| 持分権行使 (付記17) | ( | ) | ||||||||||||||||||||||
| 権証行使時の権証発行原価振込(付記17) | ( | ) | ||||||||||||||||||||||
| 繰延株単位を行使する | ( | ) | ( | ) | ||||||||||||||||||||
| 株式ベースの報酬コスト | ||||||||||||||||||||||||
| 残高 -2021年12月31日 | ( | ) | ( | ) | ||||||||||||||||||||
| 純損失 | ( | ) | ( | ) | ||||||||||||||||||||
| その他 全面赤字: | ||||||||||||||||||||||||
| 外貨通貨換算調整 | ( | ) | ( | ) | ||||||||||||||||||||
| 固定福祉計画の精算収益と固定福祉負債純額の再計量(付記15) | ||||||||||||||||||||||||
| 全面損失 | ( | ) | ( | ) | ( | ) | ||||||||||||||||||
| 株式ベースの報酬コスト | ||||||||||||||||||||||||
| 残高 -2022年12月31日 | ( | ) | ( | ) | ||||||||||||||||||||
付記はこれらの連結財務諸表の構成要素である。
| 113 |
Eeterna Zentaris Inc.
統合損失表と包括損失表
2022年まで、2021年および2020年12月31日まで年度
(単位:1株当たり千ドル、1株当たりのデータは含まれていない)
| 12月31日までの年間 、 | ||||||||||||
| 2022 | 2021 | 2020 | ||||||||||
| $ | $ | $ | ||||||||||
| 収入 (付記5と25) | ||||||||||||
| 料金 (付記19) | ||||||||||||
| 販売コスト | ||||||||||||
| 研究開発 | ||||||||||||
| 販売、 一般と管理 | ||||||||||||
| 修正住宅賃貸収益 | ( | ) | ||||||||||
| 無形資産減価 (付記10) | ||||||||||||
| 営業権減価 (付記11) | ||||||||||||
| その他資産減額(付記7) | ( | ) | ||||||||||
| 運営費総額 | ||||||||||||
| 運営損失 | ( | ) | ( | ) | ( | ) | ||||||
| 外貨レート変動による収益 | ||||||||||||
| 権証負債公正価値変動 (付記17) | ||||||||||||
| その他 財務コスト | ( | ) | ( | ) | ( | ) | ||||||
| 純財務収入 | ||||||||||||
| 所得税前損失 | ( | ) | ( | ) | ( | ) | ||||||
| 収入 税金の払い戻し(費用)(付記22) | ( | ) | ||||||||||
| 純損失 | ( | ) | ( | ) | ( | ) | ||||||
| その他 全面赤字: | ||||||||||||
| その後、損益に再分類される可能性のある項目 : | ||||||||||||
| 外貨通貨換算調整 | ( | ) | ( | ) | ||||||||
| 損益に再分類されない項目 : | ||||||||||||
| 福祉計画の精算収益(損失)の確定と福祉負債の純確定の再計量 | ( | ) | ( | ) | ||||||||
| 全面損失 | ( | ) | ( | ) | ( | ) | ||||||
| 基本1株当たり損失と希釈後の1株当たり損失(付記26) | ( | ) | ( | ) | ( | ) | ||||||
| 重み 平均流通株数(基本と希釈) | ||||||||||||
付記はこれらの連結財務諸表の構成要素である。
| 114 |
Eeterna Zentaris Inc.
統合されたキャッシュフロー表
2022年、2021年、2020年12月31日までの年度
(単位:千ドル)
| 12月31日までの年間 、 | ||||||||||||
| 2022 | 2021 | 2020 | ||||||||||
| $ | $ | $ | ||||||||||
| 経営活動のキャッシュフロー | ||||||||||||
| 純損失 | ( | ) | ( | ) | ( | ) | ||||||
| プロジェクト は現金と現金等価物に影響を与えない: | ||||||||||||
| 繰延収入償却 | ( | ) | ( | ) | ||||||||
| 株式ベースの報酬コスト | ||||||||||||
| 再構成と他の費用のために を準備する | ( | ) | ( | ) | ||||||||
| 無形資産減価 (付記10) | ||||||||||||
| 営業権減価 (付記11) | ||||||||||||
| その他の資産の減価 | ( | ) | ||||||||||
| 減価償却と償却 | ||||||||||||
| 従業員の未来福祉 | ||||||||||||
| 修正住宅賃貸収益 | ( | ) | ||||||||||
| 権証負債の公正価値変動 | ( | ) | ||||||||||
| 取引権証発行コストは、財務コストとして支出される | ||||||||||||
| 処分財産と設備収益 | ( | ) | ( | ) | ||||||||
| 賃貸負債利息増加 | ( | ) | ||||||||||
| 純為替差額 | ( | ) | ( | ) | ||||||||
| その他 非現金項目 | ||||||||||||
| 所得税を払い戻す | ( | ) | ( | ) | ||||||||
| 経営資産と負債変動(付記21) | ||||||||||||
| 純額 経営活動で使用した現金 | ( | ) | ( | ) | ( | ) | ||||||
| 融資活動のキャッシュフロー | ||||||||||||
| 普通株式と引受権証を発行して得られる収益(付記16) | ||||||||||||
| 取引コスト | ( | ) | ( | ) | ||||||||
| 株式承認証の行使と繰延株式単位による収益 | ||||||||||||
| 繰延収益収益 | ||||||||||||
| レンタル債務の支払い | ( | ) | ( | ) | ( | ) | ||||||
| 融資活動が提供する現金純額 | ( | ) | ||||||||||
| 投資活動のキャッシュフロー | ||||||||||||
| 無形資産を購入する | ( | ) | ||||||||||
| 財産と設備を購入する | ( | ) | ( | ) | ||||||||
| 処分財産と設備の収益 | ||||||||||||
| (減少) 制限的現金等価物の増加 | ( | ) | ( | ) | ||||||||
| 投資活動が提供する現金純額 | ( | ) | ( | ) | ||||||||
| 現金と現金等価物に及ぼす為替レート変動の影響 | ( | ) | ( | ) | ||||||||
| 現金と現金等価物純変化 | ( | ) | ||||||||||
| 現金と現金等価物--年明け | ||||||||||||
| 現金 と現金等価物-年末 | ||||||||||||
付記はこれらの連結財務諸表の構成要素である。
| 115 |
Eeterna Zentaris Inc.
連結財務諸表付記
2022年12月31日までと2021年12月31日現在
2022年、2021年、2020年12月31日
(単位:千ドル、1株当たりと1株当たりのデータを除いて、別途明記されている)
1. 業務の概要
業務概要
Aeterna Zentaris(“会社”または“Aeterna”)は専門的なバイオ製薬会社で、治療と診断テストの商業化と開発に従事している。同社の主導製品であるMacrilen(Macimorelin)は,米国食品·薬物管理局と欧州医薬品局が承認した第1種であり,成人成長ホルモン欠乏症患者の診断のための唯一の経口試験である。Macrilenは現在,会社がノボノルドヘルスケア株式会社(“ノとノッド”)と締結した2023年5月までのライセンス契約(“NOVO修正案”)を介して米国で販売されており,Consilient Healthcare Inc.(“Consilient”または“CH”)とGhryvelinの商標 でイギリスやヨーロッパで販売されている。同社は治療資産の開発にも力を入れており,最近すでに臨床前管路を構築し,複数の適応の未満足医療需要を潜在的に満たすために,小児科応用の潜在力を持つまれあるいは孤立適応に重点を置いている。
新冠肺炎とロシアのウクライナ侵攻の影響
新冠肺炎変異体の影響とロシアのウクライナへの侵入は、引き続き私たちの検出試験中のサイト起動と患者登録の遅延 をもたらし、アメリカとGhryvelinのヨーロッパでのMacrilenの販売活動に影響を与える可能性がある。我々の検出試験ではこれらの遅延により,検出試験は現在2023年遅くまで続くが,前期末は2022年末まで続く予定である。新冠肺炎やロシアのウクライナ侵攻に関連する遅延はこの計画の追加コストを招き、DETECT-TRANSEの完成推定コストを増加させた。同社は今後しばらくの間、新冠肺炎の流行とロシアのウクライナ侵攻の影響を監視し、brの判断、推定、会計政策、合併財務諸表で確認された金額に対するこれらの影響を評価する。実際の結果はこれらの推定値とは異なる可能性があり,このような違いは実質的である可能性がある.
報告 エンティティ
添付の連結財務諸表は、Aeterna Zentaris Inc.のアカウントを含み、このエンティティはカナダ商業会社法その全資付属会社(“当グループ”)。Aeterna Zentaris Inc.は本グループの最終親会社である.会社は現在、ドイツフランクフルトに本社を置くAeterna Zentaris GmbH(“AEZSドイツ”)、ドイツフランクフルトに本社を置くAEZSドイツの完全子会社Zentaris IVF GmbH、米国デラウェア州に登録され、米国サウスカロライナ州サマービルに事務所を設置しているAeterna Zentaris,Inc.の3つの完全子会社を持っている。
当社登録事務所はカナダオンタリオ州トロント郵便ポスト53号、湾街222号、3000軒の部屋、カナダオンタリオ州M 5 K 1 E 7に位置しています。
Br社の普通株はトロント証券取引所とナスダック資本市場に上場している。
デモベース
(A) コンプライアンス宣言
2022年と2021年12月31日までの総合財務諸表および2022年、2021年および2020年12月31日までの総合財務諸表は、国際会計基準委員会(“IFRS”)が発表した国際財務報告基準に基づいて作成されている。
| 116 |
Eeterna Zentaris Inc.
連結財務諸表付記
2022年12月31日までと2021年12月31日現在
2022年、2021年、2020年12月31日
(単位:千ドル、1株当たりと1株当たりのデータを除いて、別途明記されている)
これらの合併財務諸表は2023年3月22日に会社取締役会の承認を得た。
“国際財務報告基準”に基づいて財務諸表を作成するには、ある重要な会計推定を使用し、会社の会計政策を適用する際に管理層の判断力を行使する必要がある。高度な判断や複雑さに関連する分野 および当社の連結財務諸表に重要な意味を持つ分野を想定·推定し、付記 3−キー会計推定·判断で検討した。
(B) 計測ベース
連結財務諸表は歴史的コスト慣行に基づいて作成されている。
(C) 統合原則
これらの合併財務諸表は、当社が50%以上の投票権を直接または間接的に保有する任意のエンティティ または当社がそれに対して制御権を行使する任意のエンティティを含む。会社がエンティティに参加するために直面したり、可変リターンを得る権利がある場合、会社はそのエンティティを制御し、そのエンティティへの権力によってそのリターンに影響を与える能力がある。エンティティ は,制御権が当社に移管された日から合併に含まれ,販売されているどのエンティティも制御権が終了した日から合併から除外される.すべての会社間残高と取引は合併時に流されます。
(D) 外貨
本グループ実体の財務諸表に含まれる項目 は、実体経営が置かれている主要経済環境の通貨(“機能通貨”)で計量され、当該通貨は自社及びその米国子会社Aeterna Zentaris,Inc.のドル、及びそのドイツ子会社のユーロ(“ユーロ”又は“ユーロ”)である。
ドイツ子会社の資産と負債は期末レートでユーロ残高から換算され、運営結果 はその期間を平均レートで換算したユーロ金額から換算された。これにより生じた換算調整は累計 株主権益内の他の全面損失に計上される。
外貨取引使用ベース 取引日の為替レートは本位貨幣に換算されます。このような取引の決済と非本位通貨建ての貨幣資産と負債の転換による為替損益は合併損失表と総合損失表で確認された。
2. 重要会計政策の概要
以下に記載する会計政策は、このような総合財務諸表に記載されているすべての年度に適用されてきたが、本グループのすべての実体もこのような会計政策を踏襲してきた。
現金 と現金等価物
現金 及び現金等価物は、手元に制限されていない現金及び銀行での残高、及び短期利息預金、例えば通貨市場口座を含み、いつでも既知の額の現金に両替することができ、br}価値変動の軽微なリスクの影響を受け、買収の日から満期日は3ヶ月以下である。
| 117 |
Eeterna Zentaris Inc.
連結財務諸表付記
2022年12月31日までと2021年12月31日現在
2022年、2021年、2020年12月31日
(単位:千ドル、1株当たりと1株当たりのデータを除いて、別途明記されている)
在庫品
在庫 は、コストまたは可変現純値のうちの低いもので推定されます。コストは先進的な方法で決定された。会社のbr政策は時代遅れの在庫とコストベースを減記してその予想を超える可変現純値の在庫である。準備金の増加は販売コスト中の費用と記す。FDA承認されていない候補製品については,臨床試験で使用した在庫を生産時に記録し,開発(R&D)コスト と記録した。FDAで承認された製品については,臨床試験で使用した在庫が臨床試験包装在庫のために支出されている。承認後に発生したすべての直接製造コストを在庫に計上します。2022年12月31日と2021年12月31日まで、すべての在庫は製品と関係がある。
制限された 現金等価物
制限されたbr現金等価物には銀行預金が含まれており,これらの預金は長期経営賃貸義務の保証に関係しており,現在の目的に利用できない会社のクレジットカード項目にも関係している。
財産 と設備
財産と設備項目 は減価償却累計と減価償却費用を差し引いたコストで入金されます。減価償却は、以下の方法、年率、期間を用いて計算します
| 方法 | 年率と期限 | |||
| 装備 | ||||
| コンピュータ 装置 |
統合損失表と総合損失表に記録された減価償却 費用は,関連財産や設備項目に関する適切な機能費用種別に割り当てられる。
資産を使用する権利は、初期リース負債、レンタル開始日または前に支払われる賃貸支払い、初期直接コスト、および回復義務からリースインセンティブを減算することを含むコストで計量される。使用権資産はその後、償却コストによって計量される。この等資産は資産使用年数及び賃貸期間中の短い者は直線的に減価償却し、br}の任意の累積減価損失を減算し、レンタル負債の任意の再計量に基づいて調整する。レンタル期間には、1つのオプションがカバーする期間が含まれており、会社がそのオプションを行使すると合理的に判断した場合、そのオプションを延長する。
識別可能な無形資産
識別可能な
使用寿命の限られた無形資産には,業務統合によって行われている研究開発,特許,商標,許可を得た
技術,および会社の第三者Macimorelinメーカーに位置する系列化装置の権利がある.企業合併で買収している研究開発
は買収日に公正価値で確認されている。特許および商標は、特許出願および商標登録に関連する専門費用を含み、製品マーケティングおよび製造目的
のためのコストを含み、関連政府支出、減価損失、および累積償却を差し引く。限られた使用寿命を有する識別可能無形資産
は、資産が使用可能なときから直線的に
資産の推定使用寿命を償却し、その範囲は至れり尽くせり
| 118 |
Eeterna Zentaris Inc.
連結財務諸表付記
2022年12月31日までと2021年12月31日現在
2022年、2021年、2020年12月31日
(単位:千ドル、1株当たりと1株当たりのデータを除いて、別途明記されている)
または支払いがある
会社は コスト累積法により単独で獲得した無形資産(例えば許可内技術)のまたは可変支払いを計算する。あるいは対価格は資産を初期確認する際に考慮せず,発生時に最初に記録された資産コストを計上する.
商誉
商誉(Br)は、被買収側の任意の非持株権益の確認金額を含み、買収日に買収された確認可能資産純分と負担された負債の公正価値を減算する譲渡対価としての公正価値を確認する。初期確認後、営業権はコストから累積減価損失を差し引いて計量される。業務合併で得られた営業権 は、合併の相乗効果から利益を得ることが予想される現金発生単位(“CGU”)グループに割り当てられる。
長期資産減価
イベントや環境変化が資産の帳簿価値が回収できない可能性があることを示す場合には、減価償却または償却された財産および設備および寿命が限られている識別可能な無形資産項目 をそれぞれ言及して減価を検討しなければならない。 償却すべきでない無形資産は、その帳簿価値が回収できない可能性があることを示す兆候がある場合にテストを行い、 または少なくとも年に1回行われる。管理層は、資産がbr}減少する可能性があることを示す兆候があるかどうかを各報告日に評価する必要がある。この表示があれば,資産の回収可能金額とその帳簿価値を比較し,資産の帳簿金額がその回収可能金額を超えた金額について減価損失を確認する.回収可能金額は,資産の公正価値から売却コストと使用価値の両方を引いたものである.減値を評価するために,資産は単独でキャッシュフローまたはCGUを識別できる最低レベルでグループ化される.特定資産やCGUの使用価値を決定する際には,現在の市場の貨幣時間価値と資産特有のリスクを反映した現在の市場評価の税前割引率を用いて将来のキャッシュフローをその現在値に割引する.
もし最近の減値テスト日以来、減価資産の回収可能金額を決定するための推定数字が変わった場合、すでに減値を受けた物件と設備及び識別可能な有限年限無形資産項目 が減値を戻す可能性があるかどうかを審査する。しかしながら、先の減価損失償却により増加した資産帳簿金額は、元の減価が発生していない場合に決定すべき帳簿金額(減価償却または償却を差し引く) を超えてはならない。
営業権 は償却を行わず、毎年またはより頻繁に減値テストを行い、商業権が割り当てられたCGUグループ が減値する可能性があることを示す兆候があれば。営業権減価の査定方法は、現金付加価値グループの帳簿価値(割り当てられた営業権を含む)が現金付加価値グループの回収可能金額を超えているかどうかを評価することであり、即ち公正価値から販売コストと現金付加価値グループの使用価値の両方の中で高い者である。公正価値から販売コストを引くのは市場方法によって決定され、市場データに基づいて決定され、市場参加者が当社が当社グループCGUを売却して受け取ることができる価格に関する資料を提供することを含む。使用価値は、上級管理職が承認した5年間の財務予算におけるキャッシュフロー予測に基づいて決定される。将来の現金流量は税前割引率によってその現在値に割引されると推定され、この割引率は現在の市場の貨幣時間価値に対する評価とそのグループのCGU特有のリスク を反映している。このグループCGUの帳票金額(割り当てられた営業権を含む)がその回収可能金額を超えた場合,減値損失の金額は超過した金額に等しいことが確認される.商誉に関する減価損失は総合損失表と全面損失表に記録されており,その後は流されない。
条文
準備は当社に対する負債を表しており、その金額や時間はまだ確定していません。会社が過去の事件により現在の法律や推定義務を負っている場合には,義務を履行するために資源を流出させる必要があり,金額を確実に見積もることができれば,準備を確認する。将来の営業損失の計上は確認されていません。
| 119 |
Eeterna Zentaris Inc.
連結財務諸表付記
2022年12月31日までと2021年12月31日現在
2022年、2021年、2020年12月31日
(単位:千ドル、1株当たりと1株当たりのデータを除いて、別途明記されている)
激務とされるいかなる契約についても規定されている。契約項目の義務を履行する避けられないコストが契約予想に応じて得られる経済的利益を超えていれば、契約は重くなる。激務契約準備金は、契約終了の予想費用と契約を継続して履行する予定純費用の両方のうち低い者の現在値で計量される。現在値は予想される未来の現金流量に基づいて決定され、将来の現金流量は現在の市場の貨幣時間価値と特定の負債リスクの評価を反映した税引き前金利で割引される。割引のキャンセルは財務コストで確認されます。
賃貸借証書
契約開始時に、会社は契約がレンタルであるか、またはレンタルを含むかどうかを評価する。リースとは、価格の交換のために、合意された一定期間内に決定された資産の使用を制御する権利を付与する契約である。当社は、確定した資産を直接使用する権利があり、その使用から実質的にすべての経済的利益を得る権利がある場合、契約が確定した資産の使用制御権を伝達しているかどうかを評価する。当社はリース開始日に使用権資産とリース負債 を確認します。
レンタル負債は、最初にレンタル期間内にレンタル支払いを無効にすることができない現在値で計量し、レンタル隠れ金利 で割引します。この金利が決定できない場合には、企業の逓増借款金利、または企業 が類似した経済環境下で類似した条項および条件で類似価値の資産を得るために必要な借金金利を使用する。賃貸支払いには、固定支払いと、レンタル報酬を受け取る任意のレートを指数または減算するような可変支払いとが含まれる。
賃貸負債はその後、実際の利息法に従って償却コストで計量し、将来の賃貸支払いが指数または金利の変化によって変化し、当社の残存価値保証の下で支払うべき金額の推定値が変化するか、または当社が購入、延期、または選択権を行使するかどうかの評価を変更する際に再計量する。賃貸負債を再計量する際には、使用権資産の帳簿金額に応じて調整し、損失表と全面損失表に任意の差を記録する。
同時に、会社がリース修正を単独のリースとして会計処理する場合、(A)1つ以上の対象資産の使用権を増加させることによりリースの範囲を拡大することと、(B)レンタルの対価格増加 が範囲が拡大した独立価格に相当する金額と、特定の契約の状況を反映するためにその独立価格の任意の適切な調整とを行う場合がある。当社が契約改訂入金を新規賃貸契約とすると,独立借約 の入金方式は上述した新規賃貸と同様である。
当社が賃貸改訂を独立賃貸と見なしていない場合、賃貸負債は、(A)使用権資産の帳簿金額を減算して、賃貸範囲を縮小するためのリース変更の一部または全部を反映するように再計量され、合併損失および全面赤字報告書には、賃貸終了に関する任意の損益の一部または全部が記録されるか、または(B)他のすべてのレンタル使用権が変更された資産に応じて調整される。
短期賃貸と低価値資産リースに関する支払い は,統合された 損失表と全面損失表で直線的に料金として確認されている.
退職後福祉
ドイツでは,一部の資金と無資金の固定収益多雇用主年金計画,すなわちDUPK年金計画とRUK 1990年と2006年の年金計画(“年金福祉計画”)と資金のない退職後福祉計画がある。退職·障害僧が扶養者年金を受けるために支払われる年金には、年金義務準備金が規定されている。Br社はまた一部の従業員に固定払込計画を提供している。
| 120 |
Eeterna Zentaris Inc.
連結財務諸表付記
2022年12月31日までと2021年12月31日現在
2022年、2021年、2020年12月31日
(単位:千ドル、1株当たりと1株当たりのデータを除いて、別途明記されている)
固定給付年金計画やその他の離職後福祉については,定期年金純支出は四半期精算 は予想単位クレジット法を用いて決定した。従業員が獲得する年金や他の福祉のコストは,割引率,年金福祉増加率,従業員退職時の予想年齢,将来の報酬の期待 率を含む何らかの 仮説を適用することで決定される。
従業員未来福祉負債は、推定された将来の現金流出を良質社債の金利を用いて割引することによって決定され、この良質社債は、福祉の通貨建てで決定され、 の満期日条項は、関連する将来の福祉負債の条項とほぼ同じであることが確認される。福祉債務の現在値を決定する際に生じる精算損益は,税項を差し引いた他の全面損失で確認するとともに,精算損益が発生した当年総合財務状況表の赤字で再分類され,後続期間の総合損益表と総合損失表に循環していない。
固定支払計画については,費用は合併損失表と包括損益表に発生した,すなわち,関連従業員サービスを提供している間の費用として記録されている。
金融商品
当社はその金融商品を,公正価値で損益を計算する金融資産(“FVTPL”),公平価値で損益を計算する財務負債,償却コスト別の財務資産,償却コスト別の財務負債および公正価値で他の全面収益で抽出された財務資産(“FVTOCI”)に分類した。
FVTPLの財務 資産
FVTPLの財務資産は最初に公正価値で入金され、財務資産を発行する直接占有取引コスト は損失表と全面損失表の中に並ぶべきである。FVTPLが保有する金融資産の公正価値変動による実現済みと未実現損益 は発生期間の損益表と全面損失表に計上されている。2022年12月31日と2021年12月31日まで、会社はFVTPLに金融資産を何も持っていない。
FVTPLの財務負債
この等 金融負債は初歩的に公正価値で確認し、金融負債が直接占めるべき取引コスト を発行して損益表及び全面損益表の中に列挙する。FVTPLで計測することを要求する金融負債は報告日ごとに を再計測し,公正価値変動は損失表と全面損失表で報告する。2022年12月31日と2021年12月31日まで、会社はFVTPLで財務負債を何も持っていない。
償却コストで計算した財務資産
ビジネスモデルの目標がbr契約キャッシュフローを収集するために金融資産を保有し、資産の契約キャッシュフローが元金および利息の支払いのみを含む場合、金融資産は剰余コストで計量される。分担コストで計算した財務資産は満期日に流動或いは非流動資産に分類し、初歩的に公正価値で確認し、その後償却コストから任意の減値を引いて入金する。
| 121 |
Eeterna Zentaris Inc.
連結財務諸表付記
2022年12月31日までと2021年12月31日現在
2022年、2021年、2020年12月31日
(単位:千ドル、1株当たりと1株当たりのデータを除いて、別途明記されている)
償却コストで計算した財務負債
余剰コストに分類された財務負債は、最初に公正価値から直接取引コストを引いて確認すべきである。初歩的な確認後、コストはその後、実金利法を用いて償却コストで計量し、利息支出 は実際の収益率で確認した。実金利は、金融負債の予想年限、又は適切な場合には、より短い期間、推定された将来の現金支払いに対して割引を行う金利である。利息増加は総合損失表の利息支出 に計上される.
FVTOCIの財務 資産
FVTOCIの持分ツールへの投資 は最初に公正価値と増分取引コストによって確認された。その後,FVTOCIの金融資産 は公正価値で計測され,公正価値変動による損益はこの等損益が発生している間は他の全面損失で を確認した。2022年12月31日と2021年12月31日まで、会社はFVTOCIに金融資産を何も持っていない。
償却コスト別に金融資産減価 を提案する
当社は売掛金に対応して簡略化方法を採用しており、金融資産の期待寿命内に違約する可能性を考慮して、生涯予想信用損失計上を使用することができる。12ヶ月のECLは、レポート日の後1年以内に発生する可能性のあるデフォルトイベント のみを考慮します。会社は準備行列を用いて貿易売掛金のECLを計算する。準備行列は最初に当社の歴史上観察された違約率に基づいて、その後、新しい前向きな情報に基づいて評価と更新を行った。
株式 資本
普通株式 は株式に分類される.普通株式の発行に直接起因する増分コストは、任意の税金の影響を差し引いて株式から差し引かれることが確認されている。
会社は株式決済の株式報酬計画を実施し、同計画によると、会社は取締役、高級管理者、従業員、その他の協力者が提供するサービスを受け、会社の株式ツールの対価格とする。当社は公正価値に基づく方法ですべての形態の株式ベースの報酬を計算します。株式オプションの公正価値は、帰属期間内に付与されると予想される報酬数の推定を含むBlack-Scholes オプション定価モデルを使用して付与される日に決定される。帰属期間内にバッチ的に 購入権(階層帰属と定義する)が付与された場合、当社は毎期を単独の 購入株権付与とみなす。株式補償支出は、帰属中に確認されるか、または特定の帰属条件を満たすときに確認され、 は、他の資本に記入される。当社が株式オプションを行使するために受け取ったいかなる代価も株式に記入します。株式ベースの報酬の任意の他の資本部分は、株式発行時に株式に移行する。
当社は繰延株式単位を当社従業員又は上級社員でない取締役会メンバーに付与します。所有者が当社の取締役でなくなり、株式決済ツールとみなされる前に、DSUは償還されることができない。DSUはDSU協定の条項に基づいて、DSUが付与された直後に帰属する。配給単位の占有価値は授受時の株価時価をもとに,株式ベースの補償支出は一般項目で確認され,行政支出は総合損失および全面損失表で確認されるべきである。償還時に、各DSUは1株会社の普通株brに交換することができ、適用される保有税を含まない。会社が受け取ったDSUの行使に関連するいかなる対価格も株式に記入する。株式報酬の任意の他の資本部分は、株式発行時に株式 に移行する。
| 122 |
Eeterna Zentaris Inc.
連結財務諸表付記
2022年12月31日までと2021年12月31日現在
2022年、2021年、2020年12月31日
(単位:千ドル、1株当たりと1株当たりのデータを除いて、別途明記されている)
収入 確認
会社の収入は、顧客と締結された許可および協力協定(許可料、マイルストーン収入、特許権使用料)、開発サービスの提供、ある活性薬物成分(“原料薬”)、半製品と完成品の販売、およびいくつかのサプライチェーン活動から来ており、これらの活動は主に顧客と締結された基本契約br}に規定されている原料薬の量産に関する監督または監督支援サービスを含む。
会社は“国際財務報告基準第15号”の規定を適用した取引先と契約した収入(“国際財務報告基準15”)は、単一で包括的な収入確認基準のセット。IFRS 15は、顧客と締結されたすべての契約に適用されるが、他の標準範囲内の契約は除外される。IFRS 15は、約束された商品またはサービスの制御権が顧客に譲渡されると、収益がフレームワークによって確認され、その金額は、これらの商品またはサービスと交換するために、エンティティが獲得する権利が予想される対価格を反映する5段階フレームワークを規定する。異なる商品およびサービスが、異なるバンドルパケットが識別されるまで、他の約束された商品またはサービスと組み合わされると決定される。会社は契約義務ごとに取引価格(会社 が約束した貨物やサービスについて交換する権利があることを期待している対価格金額)を割り当て,個々の履行義務を履行する際に関連収入 を確認する.各契約の取引価格に対する会社の推定には、各報告期間の終了時に を再評価する権利があると予想されるすべての可変対価格が含まれる。同じ顧客と同時にまたはほぼ同時に2つ以上の契約を締結した場合、会社は、これらの契約が単一の手配とみなされるべきかどうかを決定するために、契約を評価する。
取引価格は相対的に独立した販売価格で履行義務の間に分配され,適用される収入 確認基準は個々の履行義務に適用される.独立販売価格は、調整後の市場評価方法、期待コスト利益率方法、または残差法を含むがこれらに限定されない方法で推定することができます。 義務を履行する独立販売価格を決定するには重大な判断が必要です。
社は,ある時点または時間とともに総合履行義務を履行しているかどうかを決定する判断を適用し,かつ,時間とともに履行される履行義務については,収入を確認するのに適した適切な進捗測定方法 を決定するのに適している.当社は報告期間ごとに進捗指標を評価し,進捗変化指標 に関する推定数に基づいて収入確認に応じて調整している。当社の見積進捗指標の変動 は累積追跡基準に従って会計推定変動として入金され、調整期間内の総合損失及び全面赤字報告書に入金される。
許可証料
会社の知的財産権の許可が合意で決定された他の約束または履行義務 とは異なると判定された場合、許可が顧客に譲渡され、顧客が許可を使用して利益を得ることができる場合、会社は、許可に割り当てられた払戻不可能な前払い費用の収入を確認する。ライセンスが他のコミットメントと異なるかどうかを評価する際に、会社は、パートナーが残りのコミットメントを受信せずにライセンスからその予期される用途から利益を得ることができるかどうかを考慮し、ライセンスの価値が実行されていない約束に依存するかどうか、残りのコミットメントを提供することができるかどうか、および残りのコミットメントから分離して識別することができるかどうかを考慮する。他の承諾と合併するライセンスについては、会社は、合併履行義務の性質およびライセンスが合併履行義務における主要な承諾であるか否かを判断することを利用して、合併履行義務 が一定期間またはある時点で履行されているかどうかを決定し、時間が経過すれば、収入を確認する目的で進行を測定するための適切な方法である。
| 123 |
Eeterna Zentaris Inc.
連結財務諸表付記
2022年12月31日までと2021年12月31日現在
2022年、2021年、2020年12月31日
(単位:千ドル、1株当たりと1株当たりのデータを除いて、別途明記されている)
サービスを開発する
評価には,サービスが が異なるか,互いに依存していないか,または互いを大きく修正しないかを決定するために,会社が開発サービスを提供する約束を含む手配 が含まれており,そうであれば,顧客にサービスを提供する際にサービスを単独の履行義務として入金する.そうでなければ、開発サービスが区別できないと判定された場合、そのようなサービスは、基本ライセンスを含む履行義務に追加される。他の承諾と結合した開発サービスに対して,会社は合併履行義務の性質 を評価して,合併履行義務が一定期間内かある時点で履行されているかを決定する.当社では,判断 を用いて収入を確認することを目的として進展を測る適切な方法を決定しており,これは通常, によるコストのような投入措置である。
マイルストーン支払い
マイルストーン支払いを含む任意の契約を顧客と締結する際に、会社はマイルストーンに達する可能性があると判断し、最も可能な金額法を用いて取引価格に含まれる金額を推定します。会社が大きな収入逆転が起こらない可能性が高いと結論した場合、関連するマイルストーン支払いは取引価格に含まれる。マイルストーン は、会社や許可者がコントロールする範囲内での支払い、例えば規制承認ではなく、通常、これらの承認を受けるまでは実現不可能であると考えられています。そして,取引価格は相対 独立販売価格で契約履行義務ごとに割り当てられ,会社は契約項下の履行義務 を履行する際に収入を確認する.その後の各報告期間終了時に、当社はマイルストーンを実現する可能性と任意の関連制限を再評価し、必要に応じて累積追跡原則に基づいて全体の取引価格の見積もりを調整します。
印税払い
販売ベースの印税(販売レベルに基づくマイルストーン支払いを含む)を含む手配について、およびライセンスが印税に関連する主要項目とみなされた場合、会社は、(A)関連販売が発生した場合、 または(B)印税の一部または全部が割り当てられた履行義務が履行されたか、または部分的に履行されたときに収入を確認する。
製品販売
同社はMacrilenを含むいくつかの原料薬と半製品の販売収入を確認したTMこのような 物品をそのクライアントに渡した後.
サプライチェーン収入 チェーン収入
サプライチェーンサービスは固定料金で契約を締結し、一定期間提供される。同社はサービスのパフォーマンスモデルを最も代表するため、直線的に収入 を確認した。
サービスを提供すると同時に,会社は下請け業者の何らかの直接コストと,その顧客から直接回収できる他の費用を発生させる.これらの直接コストの回収可能金額は、会社が顧客にサービスを移転する前に制御し、これらの手配において依頼者として機能するため、会社の運営費用に含まれる。
| 124 |
Eeterna Zentaris Inc.
連結財務諸表付記
2022年12月31日までと2021年12月31日現在
2022年、2021年、2020年12月31日
(単位:千ドル、1株当たりと1株当たりのデータを除いて、別途明記されている)
契約コスト
回収コストが期待される場合、会社は顧客との契約の増分コストを資産として確認し、任意の資本化された契約コストは、資産に関連する貨物またはサービスの顧客への移行に一致するシステムベースで償却される。実際の便宜策として、確認すべき資産の償却期間が1年以上である場合、会社は、取得契約の増額コスト を発生時の費用として確認する。これまで、会社は顧客との契約によっていかなる増分コストも発生していない。
契約書 修正
契約修正は、“国際財務報告基準”第15条において、契約当事者によって承認された契約範囲または価格(または両者)の変化として定義され、契約修正などである。契約修正とは、契約当事者が既存の強制的に実行可能な権利および義務を生成するために、新しいまたは変更するための修正を承認することをいう。事実および状況に基づいて、当社は、(A)単独の契約として、(B)既存の契約を終了して新しい契約を作成する、または(C)上記処理の組み合わせとして、のうちの1つで契約修正を会計処理する。契約範囲が異なる承諾商品またはサービスの増加によって拡大し、契約価格が増加した対価格金額が、追加の承諾商品またはサービスに対する会社の独立販売価格を反映している場合、契約修正は別個の契約として計上されるべきである。契約修正が別個の契約とみなされず、残りの貨物またはサービスが契約修正当日または以前に譲渡された貨物またはサービスと異なる場合、会社は、契約修正 を既存の契約を終了し、新しい契約を作成するとみなさなければならない。契約修正 が単独の契約とみなされず、残りの貨物またはサービスが独立していない場合、会社は、契約修正 を既存の契約の付加内容として、累積追跡に基づく収入調整として会計処理を行う。
所得税 税
所得税損益税には当期税と繰延税が含まれている。税項は損益で確認されているが、他の全面赤字であることが確認されたり、権益で直接確認されたbr項の収入や費用の変動によっても直接他の全面赤字で確認または直接権益で確認することができる。経営陣は定期的に税務法規の適用について説明しなければならない状況について申告表の立場を評価し、適切な場合には予想に応じて税務機関に支払うべき金額に基づいて準備を行う。
当期所得税費用は、報告日 までに当社子会社で経営及び課税所得国が公布又は実質公布した税率及び法律に基づいて計算される。
繰延所得税は、総合財務諸表内の資産および負債の計税基準とその帳簿額面との間に生じる一時的な差異(適用すれば、外国付属会社および連合会社からの未送金収益に関する一時的な差異 を除いて、投資が存続期間上基本的に恒久的であれば、および初歩的な確認営業権に関する一時的な差異 を除く)、および本グループ内で使用されていない税項損失または研究開発が返却できない税項控除確認を行う。繰延所得税brは、報告日までに公布されたか、または実質的に公布された税率および法律に基づいて決定される。
繰延所得税資産は、将来課税利益が一時的な差額の相殺に利用できる可能性がある場合にのみ確認される。
繰延 法に基づいて強制執行可能な権利が存在して当期税項資産を当期税金項目負債と相殺し、しかも繰延所得税資産と負債は同じ税務機関が同一の課税実体或いは異なる課税実体から徴収した所得税と関係があり、しかも純額で残高を決済することを意図している場合、繰延所得税と資産は相殺する。
| 125 |
Eeterna Zentaris Inc.
連結財務諸表付記
2022年12月31日までと2021年12月31日現在
2022年、2021年、2020年12月31日
(単位:千ドル、1株当たりと1株当たりのデータを除いて、別途明記されている)
Br社は、不確定な税収状況や他の問題に関連して各税務機関に支払う可能性のある税金に準備金を提供します。準備金は、会社がその納税申告で得た税収割引があるかどうか、および税収割引に関連する任意の潜在的または有有事項を解決した後に達成される可能性があるかどうかを決定することに基づいています。
政府援助
政府援助計画から受け取った又は受け取るべき額は、研究開発のための贈与及び払戻可能な投資税収控除を含み、国際会計基準第20条に基づいて入金されなければならない政府補助金の採算と政府援助の開示、 政府援助を受ける金額およびすべての付加条件が遵守されることが合理的に保証されている場合に確認する。この金額が研究や開発コストなどの支出項目に関係していれば,システムに基づいて収入として確認し,補償しようとするコストを削減する.1つの資産に贈与された場合、それは、その資産の帳簿金額を減少させ、その後、減価償却費用によって、減価償却資産使用年限内の収入として確認される。
研究開発費
コストは発生時に費用を計上することを検討する.開発コストは発生時に費用を計上するが,延期基準を満たすコストは除外し,この場合,コストは資本化し,推定受益期間内に運営に償却する。本報告で述べたいずれの期間も,開発コストは 資本化されていない。
基本 1株当たり純損失は今年度発行された普通株の加重平均を用いて計算される。
希釈後の1株当たり純損失は,年内に発行された普通株の加重平均に希釈普通株等価物の影響 を加えて計算したものであり,例えば株式オプション,株式承認証,類似ツールである。オプション、株式承認証及び類似ツールに関する株式数は在庫株式方法で計算する。1株当たりの純損失を希釈することは1株当たりの基本純損失に等しく、当社は赤字状態にあるため、オプションと引受権証を含むすべての証券は逆赤字となる。
3. 重要な会計見積もりと判断
国際財務報告基準に基づいて連結財務諸表を作成するには、管理層が会社の資産、負債、収入、費用と関連開示報告金額に影響を与える判断、推定と仮定 を行う必要がある。 と仮説は、歴史的経験、期待、現在の傾向、および経営陣が当社の連結財務諸表を作成する際に関連する他の要因に基づいていると判断、推定します。
経営陣は定期的に会社の会計政策、仮説、推定、判断を審査し、br}総合財務諸表が国際財務報告基準に従って公平に報告されることを保証する。会計推定の改訂は、改訂推定の期間及び任意の影響を受けた将来の期間で確認される。
重要な 会計推定と仮定は、重大なリスクが重大な調整をもたらす推定と仮定であり、通常、本質的に不確定で変化する可能性のある事項または結果に適用される。そのため、経営陣は、将来の事件は予測や予想とは異なることが多く、予想は常に調整が必要だと戒めている。
以下では、当社が総合財務諸表を作成する際に作成した最も重要な会計見積もりと仮定について検討する。
| 126 |
Eeterna Zentaris Inc.
連結財務諸表付記
2022年12月31日までと2021年12月31日現在
2022年、2021年、2020年12月31日
(単位:千ドル、1株当たりと1株当たりのデータを除いて、別途明記されている)
契約修正の会計処理
“Novo修正案”および“Novo修正案”が2022年8月26日に受信した“Novo修正案”終了通知は、付記5--“ライセンス、供給および流通手配”で定義され、議論され、“国際財務報告基準”第15条の規定に基づいて修正として決定され、許可協定範囲の任意の変化を評価すること、残りの商品またはサービスが修正前に譲渡された商品またはサービスとは異なるかどうかを評価することを含む管理層に重大な判断を要求する。また、取引価格変化の一部が、修正前に約束された可変対価格金額 に起因するかどうかを評価する。本プロトコルに適用される判断または仮定のいかなる変化も、当社の収入および繰延収入に大きな影響を与える可能性があります。
ライセンス と複数の要素を含む連携スケジュール
会社は、Macimorelinの異なる地域での許可、開発、供給、流通に関する許可と供給協定を締結した。各合意は、特定の条項または条項を含むことができ、管理層は、適切な会計処理の達成を保証するために、IFRS 15に従ってこれらの条項または条項を詳細に分析する必要がある。契約には、払い戻し不可能な前払いおよび許可費用(Br)、開発サービスの提供、商業化前および商業化後のマイルストーン支払い、そのようなライセンス契約から得られた将来の製品販売の印税、および供給スケジュールが含まれる場合がある。管理層は、各合意を分析して重大な判断を行い、同時刻又は同時刻に締結された契約が単一手配として入金されるべきか否かを決定し、契約の全ての部分がIFRS 15に適用されるか否かを決定して、すべての履行義務を決定し、履行義務が異なるか否か、又は履行義務を他の承諾された貨物及びサービスと統合すべきか否かを決定し、相対的に独立した販売価格に基づいて取引価格を決定し、合併の履行義務がある時点で満たされるか否か、及び時間とともに満たされる履行義務 について、収入を確認するために採用された進行を測る適切な方法。 に適用された判断や仮定の任意の変化は、会社の収入や繰延収入に大きな影響を与える可能性がある。
営業権減価
営業権に関連する年間減価評価は、経営陣が回収可能な金額、すなわち資産の公正価値から処分コストと使用価値を差し引いた高い者を推定することを要求する。経営陣は、公正価値の使用から売却コストを差し引くと、高い推定回収可能価値をもたらすことを決定した。その総合純資産の帳簿価値と公正価値から売却コストを引いて比較した。この計算によると、経営陣は営業権が減値されたと判断した(付記11参照)。
従業員の未来福祉
従業員の将来の福祉に関する費用や債務を決定する際には、債務の割引率 ,年金福祉成長率、従業員退職時の予想年齢、および将来の報酬の予想比率 などの仮定を用いる必要がある。従業員の将来の福祉に関するコストや債務の決定には様々な仮定が必要であるため,精算推定には固有の計量不確実性が存在する。実際の結果は,上記の仮定に基づいて推定した結果とは異なる である.より多くの情報は付記15--従業員未来福祉 に含まれている。
研究と開発は費用を計算しなければならない
財務諸表作成過程の一部として、経営陣は、会社の研究開発費に関する費用を含めて計算すべき費用を試算する必要がある。このプロセスは、未締結契約および調達注文を検討することと、当社を代表して提供されるサービスを決定するために、当社が請求書を受信していない場合、または他の方法で実際のコストを通知する場合に、提供されるサービスレベルおよびサービスによって生じる関連コストを推定することとを含む。サービスの実際の履行時間または努力の程度が管理層の推定値と異なる場合、会社は、それに応じて を計算または前払い費用残高を調整する。実際に発生した金額 と実質的な差はないと予想されているにもかかわらず、提供されるサービスの状態や時間の推定が提供サービスの実態や時間と異なる場合、会社は任意の特定の時期に高すぎるまたは低すぎる金額を報告する可能性がある。
| 127 |
Eeterna Zentaris Inc.
連結財務諸表付記
2022年12月31日までと2021年12月31日現在
2022年、2021年、2020年12月31日
(単位:千ドル、1株当たりと1株当たりのデータを除いて、別途明記されている)
4. 最近の会計声明
新しいbr基準や解釈は採用されていない
いくつかの新しい会計基準、会計基準の改正、解釈は発表されているが、2022年12月31日の報告期間内に強制的ではなく、当社によって事前に採択されていない。これらの基準、改訂、または解釈は、現在または未来の報告期間内にエンティティに実質的な影響を与えず、予測可能な未来の取引に実質的な影響を与えないと予想される。
5. 収入.収入
収入分解
会社は、経時的および以下のカテゴリのある時点での貨物およびサービス譲渡から収入を得る:
| 12月31日までの年間 、 | ||||||||||||
| 2022 | 2021 | 2020 | ||||||||||
| $ | $ | $ | ||||||||||
| 許可証料 | ||||||||||||
| サービスを開発する | ||||||||||||
| 製品販売 | ||||||||||||
| 印税 | ||||||||||||
| サプライチェーン チェーン | ||||||||||||
収入
は約$
ライセンス、 供給と流通手配
NOVO ノドヘルスケア会社−Macrilen−アメリカとカナダ
2018年1月16日、当社はStrongbridgeアイルランド株式会社(“Strongbridge”)とライセンス契約を締結し、Macrilen(Macimorelin)の米国とカナダでの商業化に開発、製造、登録、規制、サプライチェーンサービスを提供し、(I)成人適応(“成人適応”)に関する使用権ライセンス、(Ii)将来FDAが承認する小児科適応のライセンス(“小児科適応”)を規定している。(Iii)EMAおよびFDAによって許可された小児科臨床試験(“検出試験”)に人為的に提出されることが許可された費用の70%は、共同指導委員会(“PIP”)の監督の下でbr}社によって行われる;および(Iv)一時的な供給スケジュールである。2018年1月、会社は現金支払いを受け取りました$
| 128 |
Eeterna Zentaris Inc.
連結財務諸表付記
2022年12月31日までと2021年12月31日現在
2022年、2021年、2020年12月31日
(単位:千ドル、1株当たりと1株当たりのデータを除いて、別途明記されている)
2020年11月16日、当社はNovo とMacimorelinの開発及び商業化について既存のライセンス協定の改正(“Novo改正案”)を締結した。
Novo修正案によると、Eeternaは米国とカナダ以外のすべての権利を保持し続けているが、NovoはEeternaにドルを前払いすることに同意した
改正された条項によると、Novoはまた、AeternaがMacimorelinに所有している米国とカナダ特許と商標の共同所有権 を付与されているが、いくつかの終了事件が発生した場合、これらの特許の共通所有権をAeternaに譲渡することが要求される。
経営陣 は,当社がこれまでNovoに許可していた米国とカナダ特許と商標の共同所有権を付与する改正は,関連利益が高度に依存しており,改正前に既存のライセンス契約によって付与されたライセンス適応と相互に関連しているため,明確な履行義務ではないことを決定している。
また、米国の規制機関がCGHDの診断にMacimorelinを承認した後、NovoがカナダでMacimorelin を商業化していないと判断した場合、Eeternaはカナダ(米国ではないが)でMacimorelinの権利を独占的に許可することを選択することができる。第三者に売る。Novo修正案はまた、成功すれば、EeternaがDETECT実験の結果を使用して、2つの許可国、米国、カナダ以外の他の地域でMacimorelinの協力機会を求めるために、Eeternaが規制承認と持続的な努力を求める権利があることを確認した。
修正前分析
契約開始時に、2ドルの総割引キャッシュフローの分析によると、
ライセンス契約によると、当社はPIP項下の融資手配を国際財務報告基準第11号下の協力手配と見なし、発生コストの削減に領収書を計上している。2020年に同社は許可された人に$を発行しました
| 129 |
Eeterna Zentaris Inc.
連結財務諸表付記
2022年12月31日までと2021年12月31日現在
2022年、2021年、2020年12月31日
(単位:千ドル、1株当たりと1株当たりのデータを除いて、別途明記されている)
分析 修正後
2020年11月16日、同社は既存のライセンス契約のNovo修正案を発表し、前金を受け取った$
“国際財務報告基準”第11号に要求されているように,小児科関連の開発活動の事実や状況が変化したことから,Novo改正案によりNovoに付与された権利と責任が実質的に変化した−経営陣 は,これらの活動の分類が変わるべきかどうかを再評価した。経営陣の結論は、“Novo修正案”の当事者たちが関連活動を共同でコントロールしなくなったということだ。したがって,IFRS 11により,小児科適応開発活動はbrに計上されなくなり,小児科適応開発サービスに関する逓増履行義務は小児科許可証と合併し,収入を確認した。Novo修正案では他の追加的な履行義務が確定されていない。
先の分析により、管理層は修正後の取引総価格を$と決定した
終了通知
Novoは2022年8月26日、Novo修正案の終了通知を当社に提供した。Novo修正案の条項によると、270日間の通知期間(“通知期間”)が終了した後、2023年5月23日に発効する。終了後,
社はNOVO改正案によりNovoに付与された権利とライセンスを会社に返還し,会社はMacrilenの臨床開発と将来の商業化を継続するすべての権利を再獲得する。Novoは、通知終了後および270日間の通知期間全体にわたって、Novo修正案の条項に基づいて、最大で
ドルに達するすべての検出-試験費用に資金を提供し続ける
社は,終了通知は会計目的で契約の修正であると結論している。当社はさらに、終了通知を受けた後、通知期間内に履行された残りの商品及びサービスを
の異なる商品及びサービスと見なしているため、契約修正は前向き会計処理を行う必要があると判断した。Novo終了通知を受けた日までに,同社は小児科適応に関する許可料総額を$と確認した
| 130 |
Eeterna Zentaris Inc.
連結財務諸表付記
2022年12月31日までと2021年12月31日現在
2022年、2021年、2020年12月31日
(単位:千ドル、1株当たりと1株当たりのデータを除いて、別途明記されている)
サプライチェーン·チェーン·スケジュール
ライセンス契約の中期供給スケジュールでは,会社はMacrilen (マカロニ)を生産する原料を過渡期に供給することに同意し,価格は“原価価格”で設定されており,利益率は何もない。当社は製造原料の独立販売価格がそのコストであると考えているが,これはNovoが他のサプライヤーから同じ商品を調達できる金額とほぼ同じであるからである。2019年11月、NovoはAEZSドイツ社と契約を締結し、安定性研究(支援サービス)を提供する監督およびいくつかの原料薬の量産および納入を含むサプライチェーンサービスを提供する。
Consilient Healthcare Limited-Macimorelin-EUとイギリス
2020年12月7日,当社はConsilient Health Limited(“CH”)とMacimorelin(“ライセンス製品”)の欧州経済区およびイギリスでの商業化について独占ライセンス契約(“CH ライセンス契約”)を締結した。
“CHライセンス契約”の条項によると、CHは、当社に払戻不可、貸記不可の前金$を支払うことに同意します
CHプロトコルに関連する
取引の総価格は$である
Br社は調整後の市場評価方法を用いて,取引価格を成人と小児科適応の許可プロトコルと供給プロトコルの総合的な履行義務に割り当てている。収入はCHに供給される許可製品単位に基づく産出方法を用いて 時間で確認される.“CHプロトコル”によると,当社がCHに供給する総単位は現在の予測と予想される市場需要の推定に基づいているため,産出方法を用いて収入を確認する際に重要なbr}判断となる.
2021年12月、イギリスの衛生·社会保健省は値札を承認し、これが$を引き起こした
2022年5月に価格がドイツで承認され、これが$を引き起こしました
2022年12月31日現在,CHプロトコルにより,会社の未履行または一部未履行の履行義務に割り当てられた取引価格総額は$である
| 131 |
Eeterna Zentaris Inc.
連結財務諸表付記
2022年12月31日までと2021年12月31日現在
2022年、2021年、2020年12月31日
(単位:千ドル、1株当たりと1株当たりのデータを除いて、別途明記されている)
2022年12月31日までの年間で、会社は$を確認しました
NK Meditech Limited-Macimorelin-韓国
当社はNK Meditech Limited(“NK”)とライセンス契約を締結し、2021年11月30日から発効し、これにより、当社はNK独占権利を付与し、韓国(“韓国”)および朝鮮民主主義人民共和国(“朝鮮”)(場合によっては)に独占商業化(マーケティング、販売および要約販売を含む)Macimorelin(“NKライセンス協定”)を独占的に商業化する。
NK許可契約の条項によると、NKは当社に返却不可、貸記不可の前金$を支払うことに同意しました
また、2021年11月30日から、当社はNKと独占供給協定を締結し、これにより、当社は10年の間、NKにマキモレリンを供給することに同意したが、継続する必要がある(“NK供給協定”)。
管理層
は、NK許可プロトコルに関する取引総価格を$と決定した
顧客契約に関する負債
社は、以下の顧客の契約に関する繰延収入残高を確認しました
| 2022年12月31日 | ||||||||||||
| 現在のところ | 当面ではない | 合計する | ||||||||||
| $ | $ | $ | ||||||||||
| ノとノド医療 | ||||||||||||
| Consilient Healthcare Limited | ||||||||||||
| NK 医療科技有限公司 | ||||||||||||
| 2021年12月31日 | ||||||||||||
| 現在のところ | 当面ではない | 合計する | ||||||||||
| $ | $ | $ | ||||||||||
| ノとノド医療 | ||||||||||||
| Consilient Healthcare Limited | ||||||||||||
| NK 医療科技有限公司 | ||||||||||||
| 132 |
Eeterna Zentaris Inc.
連結財務諸表付記
2022年12月31日までと2021年12月31日現在
2022年、2021年、2020年12月31日
(単位:千ドル、1株当たりと1株当たりのデータを除いて、別途明記されている)
6. 現金と現金等価物
| 十二月三十一日 | ||||||||
| 2022 | 2021 | |||||||
| $ | $ | |||||||
| 手元の現金と銀行の残高 | ||||||||
| 期限が3か月を超えない生息預金 | ||||||||
社が制限している現金等価物は#ドル
7. 貿易その他売掛金
| 十二月三十一日 | ||||||||
| 2022 | 2021 | |||||||
| $ | $ | |||||||
| 取引売掛金 | ||||||||
| 付加価値税 | ||||||||
| その他 売掛金 | ||||||||
2022年12月31日までの年間で,会社は他の売掛金に#ドル減記を記録した
8. 前払い費用と他の流動資産
| 十二月三十一日 | ||||||||
| 2022 | 2021 | |||||||
| $ | $ | |||||||
| 保険料前払い | ||||||||
| プリペイド開発 | ||||||||
| 他にも | ||||||||
| 133 |
Eeterna Zentaris Inc.
連結財務諸表付記
2022年12月31日までと2021年12月31日現在
2022年、2021年、2020年12月31日
(単位:千ドル、1株当たりと1株当たりのデータを除いて、別途明記されている)
9. 財産と設備
会社の財産と設備の構成要素 を以下にまとめる.
| コスト | ||||||||||||||||||||
| 装備 | コンピュータ 装置 | 建物を使う権利 | 車両を使用する権利 | 合計する | ||||||||||||||||
| $ | $ | $ | $ | $ | ||||||||||||||||
| 2021年1月1日 | ||||||||||||||||||||
| 足し算 | ||||||||||||||||||||
| 家屋賃貸契約を修正する | ||||||||||||||||||||
| 処置する | ( | ) | ( | ) | ( | ) | ||||||||||||||
| 為替レート変動影響 | ( | ) | ( | ) | ( | ) | ( | ) | ( | ) | ||||||||||
| 2021年12月31日 | ||||||||||||||||||||
| 足し算 | ||||||||||||||||||||
| 賃貸借契約の修正 | ||||||||||||||||||||
| 処置する | ( | ) | ( | ) | ( | ) | ||||||||||||||
| 為替レート変動影響 | ( | ) | ( | ) | ( | ) | ( | ) | ( | ) | ||||||||||
| 2022年12月31日 | ||||||||||||||||||||
| 減価償却累計 | ||||||||||||||||||||
| 装備 | コンピュータ 装置 | 建物を使う権利 | 車両を使用する権利 | 合計する | ||||||||||||||||
| $ | $ | $ | $ | $ | ||||||||||||||||
| 2021年1月1日 | ||||||||||||||||||||
| 処置する | ( | ) | ( | ) | ( | ) | ||||||||||||||
| 減価償却 | ||||||||||||||||||||
| 為替レート変動影響 | ( | ) | ( | ) | ( | ) | ( | ) | ( | ) | ||||||||||
| 2021年12月31日 | ||||||||||||||||||||
| 処置する | ( | ) | ( | ) | ( | ) | ||||||||||||||
| 減価償却 | ||||||||||||||||||||
| 為替レート変動影響 | ( | ) | ( | ) | ( | ) | ( | ) | ( | ) | ||||||||||
| 2022年12月31日 | ||||||||||||||||||||
| 金額を携帯する | ||||||||||||||||||||
| 装備 | コンピュータ 装置 | 建物を使う権利 | 車両を使用する権利 | 合計する | ||||||||||||||||
| $ | $ | $ | $ | $ | ||||||||||||||||
| 2021年12月31日 | ||||||||||||||||||||
| 2022年12月31日 | ||||||||||||||||||||
2022年9月30日、同社は所有者と共同で、ドイツ子会社の既存ビル賃貸契約を1年プラス6ヶ月延長する通知に同意し、2024年3月31日まで継続し、建物使用権資産を修正し、金額は$とした
| 134 |
Eeterna Zentaris Inc.
連結財務諸表付記
2022年12月31日までと2021年12月31日現在
2022年、2021年、2020年12月31日
(単位:千ドル、1株当たりと1株当たりのデータを除いて、別途明記されている)
10. 無形資産を識別することができる
当社が認識できる無形資産の帳簿価値の変動状況の概要は以下のとおりである。
| 2022年12月31日 | 2021年12月31日 | |||||||||||||||||||||||
| コスト | 累計償却 | の値を持つ | コスト | 累計償却 | の値を持つ | |||||||||||||||||||
| $ | $ | $ | $ | $ | $ | |||||||||||||||||||
| 残高 -年明け | ( | ) | ( | ) | ||||||||||||||||||||
| 足し算 | ||||||||||||||||||||||||
| 償却する | ( | ) | ( | ) | ( | ) | ( | ) | ||||||||||||||||
| 無形資産減価 | ( | ) | ( | ) | ||||||||||||||||||||
| 為替レート変動影響 | ( | ) | ( | ) | ( | ) | ( | ) | ||||||||||||||||
| 残高 -年末 | ( | ) | ( | ) | ||||||||||||||||||||
2021年に会社は$を増加させた
同社は2022年12月31日までの年度中に新冠肺炎とクラミジアワクチン試験の開発を中止した。従来
はこの2つの試験に関するライセンス前払いを$に資本化していた
シトロペプチド
2021年8月10日、同社はメルクKGaA(“メルク”)の子会社ARES Trading SAと、会社が所有するシトラペプチド(注射用シトロレックス)商標について商標維持·譲渡選択権協定を締結し、シトロペプチドは黄体ホルモン放出ホルモン拮抗薬であり、不妊症治療を受ける女性の体外受精計画(“シトロペプチド協定”)が承認された。同社は2013年に許可·供給協定(LSA)を通じてCetrotieのすべての活動をメルク社に移転した。
セトロティ協定によると、当社は、LSA期限(現在2029年5月(“譲渡日”)の終了時にセトロティ商標の任意およびすべての権利(“オプション”)を取得するためにメルクに独占選択権を付与し、その際、会社はbrの約束に従って、セトロティ商標のすべての権利と権益および所有権をメルクに譲渡する。譲渡の日に商標を譲渡することは販売を構成し,その後,会社はCetrotie商標に関連するいかなる所有権または義務も所有しなくなる。
メルク社は選択権を獲得した対価格として、同社に合計$を支払うことに同意した
| 135 |
Eeterna Zentaris Inc.
連結財務諸表付記
2022年12月31日までと2021年12月31日現在
2022年、2021年、2020年12月31日
(単位:千ドル、1株当たりと1株当たりのデータを除いて、別途明記されている)
シトラペプチド関連商標の帳簿価値はゼロドル,会社が受け取った収益は$であった
11. 商誉
| 十二月三十一日 | ||||||||
| 2022 | 2021 | |||||||
| $ | $ | |||||||
| 残高 -期初 | ||||||||
| 営業権の減価 | ( | ) | ||||||
| 為替レート変動影響 | ( | ) | ( | ) | ||||
| 残高 -期末 | ||||||||
会社が減値指標を評価する際には,他の要因に加えて,その時価と帳簿価値との関係も考慮する。2022年12月31日現在、当社の時価はその株主持分の帳簿価値を下回っており、営業権減値とCGUグループ資産減値が出現する可能性があることを示した。2022年12月31日までに、このグループの現金付加価値税単位の回収可能金額は、公正価値から処分コスト(“FVLCD”)
モードを引いて決定される。FVLCDは市場方法に基づいて決定し、市場データに由来し、市場参加者からの当社がこのグループのCGUを販売して受け取ることができる価格に関する資料
を含む。使用した推定技術の投入により、公正価値計量は2級公正価値に分類される。経営陣は、使用中の価値による推定回収可能価値はFVLCDよりも低いと判断した。当社の評価によると、当社グループCGUの回収可能金額は帳簿価値を下回っているため、その営業権と無形資産に減値費用#ドルを計上しています
12. 売掛金と売掛金
| 十二月三十一日 | ||||||||
| 2022 | 2021 | |||||||
| $ | $ | |||||||
| 貿易 は帳簿を払わなければならない | ||||||||
| 開発コストを計算すべきだ | ||||||||
| 従業員福祉 | ||||||||
| 給与明細税とその他の法定債務 | ||||||||
| その他 課税負債 | ||||||||
| 136 |
Eeterna Zentaris Inc.
連結財務諸表付記
2022年12月31日までと2021年12月31日現在
2022年、2021年、2020年12月31日
(単位:千ドル、1株当たりと1株当たりのデータを除いて、別途明記されている)
13. 条文
| 十二月三十一日 | ||||||||
| 2022 | 2021 | |||||||
| $ | $ | |||||||
| 残高 -期初 | ||||||||
| 食糧の使用 | ( | ) | ( | ) | ||||
| 規定中の を変更する | ||||||||
| 割引撤廃と為替変動の影響 | ( | ) | ( | ) | ||||
| 残高 -年末 | ||||||||
| 減算: 現在の部分 | ||||||||
| 非現在 部分 | ||||||||
2013年、当社は、付記br 10で議論されているCetrotie活動に関連するいくつかの取消不可能な契約の準備を確認し、これらの契約は重いと考えられている。重い契約に関する規定は、推定される避けられない将来の使用料の現在値と、シトロペプチドの知的財産権に関連する特許コストである。
14. 賃貸負債
| 十二月三十一日 | ||||||||
| 2022 | 2021 | |||||||
| $ | $ | |||||||
| 残高 -期初 | ||||||||
| 足し算 | ||||||||
| 利子 は他の融資コストとして純損失を計上する | ( | ) | ( | ) | ||||
| レンタル債務に対する支払い | ( | ) | ( | ) | ||||
| レンタル責任の修正 | ||||||||
| 為替レート変動影響 | ( | ) | ||||||
| 残高 -年末 | ||||||||
| 当期賃貸負債 | ||||||||
| 非流動賃貸負債 | ||||||||
Br社とその大家は,ドイツ子会社の既存建築賃貸契約を1年プラス6カ月延長する通知に合意し,2024年3月31日まで継続し,賃貸負債を修正し,金額は$とした
2022年12月31日までの将来のレンタル支払いは以下の通りです
| $ | ||||
| 1年未満 | ||||
| 1-3年 | ||||
| 合計する | ||||
| 137 |
Eeterna Zentaris Inc.
連結財務諸表付記
2022年12月31日までと2021年12月31日現在
2022年、2021年、2020年12月31日
(単位:千ドル、1株当たりと1株当たりのデータを除いて、別途明記されている)
15. 従業員未来福祉
同社はドイツで資金と資金のない固定福祉多雇用者年金計画と資金のない離職後福祉計画の一部を持っている。これらの計画は、終身支給された年金水準を保証する形でメンバー(またはその生存家族)に福祉を提供する最終賃金年金計画である。提供される福祉水準はメンバーのサービス年限と退職前の最後の数年の給料に依存する。
これらのbr計画はドイツの就業法によって管轄されており、通常、インフレの増加やセットに対応するために、各計画の最終賃金支払いが3年ごとに調整されることが求められている
年金負債はインフレの増加または一連の調整によって
から
過去には、固定福祉義務、計画資産、当該などの年金に関連するコストにおける当社の割合分を計算するための十分な情報がなかったため、ある年金福祉計画は固定払込計画
に計上されていた。2021年、当社はより多くの情報を取得し、固定福祉債務と計画資産に占める割合シェアを開始し、総額は#ドルとなった
| 138 |
Eeterna Zentaris Inc.
連結財務諸表付記
2022年12月31日までと2021年12月31日現在
2022年、2021年、2020年12月31日
(単位:千ドル、1株当たりと1株当たりのデータを除いて、別途明記されている)
従業員の将来の福祉義務に関する会社が福祉義務を計算すべきであるbrの変化をまとめた
| 十二月三十一日 | ||||||||||||||||
| 2022 | 2021 | |||||||||||||||
| 年金.年金 | 他にも | |||||||||||||||
| 福祉計画 | 福祉計画 | 合計する | 合計する | |||||||||||||
| $ | $ | $ | $ | |||||||||||||
| 計画負債変更 | ||||||||||||||||
| 残高 -期初 | ||||||||||||||||
| 現在のサービスコスト | ||||||||||||||||
| 利息 コスト | ||||||||||||||||
| 財務仮説変更による精算収益 | ( | ) | ( | ) | ( | ) | ( | ) | ||||||||
| 多雇用主計画に関する過去のサービスコスト | ||||||||||||||||
| 現在の将来の年金増加資金の仮定を変えることによる精算損失 | ||||||||||||||||
| 福祉を支払いました | ( | ) | ( | ) | ( | ) | ( | ) | ||||||||
| 為替レート変動影響 | ( | ) | ( | ) | ( | ) | ( | ) | ||||||||
| 残高 -期末 | ||||||||||||||||
| 変更計画資産中の | ||||||||||||||||
| 残高- 期初 | ||||||||||||||||
| 2021年12月31日までの計画資産列報 | ||||||||||||||||
| 利息 計画資産収入 | 120 | — | 120 | — | ||||||||||||
| 雇用主は支払い | ||||||||||||||||
| 従業員 貢献 | ||||||||||||||||
| 福祉を支払いました | ( | ) | ( | ) | ||||||||||||
| 計画資産再計測 | ( | ) | ( | ) | ||||||||||||
| 為替レート変動影響 | ( | ) | ( | ) | ( | ) | ||||||||||
| 残高 -期末 | ||||||||||||||||
| 未支出計画の純負債 | ||||||||||||||||
| 援助計画された純負債 | ||||||||||||||||
| 従業員の将来福祉を確認した純額 | ||||||||||||||||
| 確認金額 : | ||||||||||||||||
| 純損失 | ||||||||||||||||
| 福祉計画を決定する精算収益(損失)とその他の総合(収益)損失における純確定収益負債の再計量 | ( | ) | ||||||||||||||
| 139 |
Eeterna Zentaris Inc.
連結財務諸表付記
2022年12月31日までと2021年12月31日現在
2022年、2021年、2020年12月31日
(単位:千ドル、1株当たりと1株当たりのデータを除いて、別途明記されている)
2022年12月31日現在、多雇用主年金計画資産における会社の割合は以下の通り
| 十二月三十一日 | ||||||||
| 2022 | 2021 | |||||||
| $ | $ | |||||||
| 株式(Br)ツール(一級) | ||||||||
| 債務 ツール(レベル1) | ||||||||
| 現金と現金等価物(一級) | ||||||||
| 不動産 (レベル3) | ||||||||
| その他 (レベル3) | ||||||||
会社の福祉義務を決定するために適用される重要な精算仮定は以下のとおりである
| 年金福祉計画 | その他 福祉計画 | |||||||||||||||||||||||
| 12月31日までの年間 、 | 12月31日までの年間 、 | |||||||||||||||||||||||
| 精算 仮定 | 2022 | 2021 | 2020 | 2022 | 2021 | 2020 | ||||||||||||||||||
| % | % | % | % | % | % | |||||||||||||||||||
| 割引率 | ||||||||||||||||||||||||
| 年金給付が増加する | ||||||||||||||||||||||||
| 報酬増加幅 | ||||||||||||||||||||||||
将来の死亡率に関する仮定
は,ドイツが公表した統計データと経験に基づいて精算提案により決定された。これらの仮説は退職者の平均残存寿命(年単位)に変換される
| 十二月三十一日 | ||||||
| 2022 | 2021 | 2020 | ||||
| 年.年 | 年.年 | 年.年 | ||||
| 報告期間終了時退職 : | ||||||
| 男性 | ||||||
| 女性は | ||||||
2022年12月31日までの仮定によると、支給される予定の未割引年金給付は以下の通り
合計する $ | ||||
| 2023 | ||||
| 2024 | ||||
| 2025 | ||||
| 2026 | ||||
| 2027 | ||||
| その後… | ||||
固定福祉義務の加重平均期限は
| 140 |
Eeterna Zentaris Inc.
連結財務諸表付記
2022年12月31日までと2021年12月31日現在
2022年、2021年、2020年12月31日
(単位:千ドル、1株当たりと1株当たりのデータを除いて、別途明記されている)
以下の仮定で2022年期間に変化があれば,会社の年金福祉義務への影響を$とする
| 仮に | 増す | 少量を減らす | ||||||
| 変更
の割引率 | ( | ) | ||||||
| 年俸率を変更する | ( | ) | ||||||
| 年金料率の変更仮定
| ( | ) | ||||||
| 死亡率を1年に変更します | ( | ) | ||||||
会社が固定払込計画として計算した固定収益計画の総費用は約
$
ライセンス
Br社は数量を問わない普通株(投票権と参加株)を持ち、額面がなく、無限数の優先株、第1級、第2級株を持ち、シリーズ発行が可能で、種類ごとに特定の権利と特権を持ち、額面がない。
株主権利計画
2019年5月8日から、株主は、取締役会および会社株主に追加時間を提供して、会社に対する任意の能動的買収要約 を評価し、株主価値最大化を実現するために適切な場合に他の代替案を求める会社の株主権利計画(“権利計画”)を再承認した。配当計画によると、現在発行されている普通株を発行する毎に、権利が発行され、時々発行される可能性のある各追加の普通株のために1つの権利が発行される。
| 発行済みで返済されていません | 普通株 株 | 金額 | ||||||
| # | $ | |||||||
| 残高 -2019年12月31日 | ||||||||
| 普通株を発行し,取引コストを差し引く | ||||||||
| 残高 -2020年12月31日 | ||||||||
| 普通株を発行し,取引コストを差し引く | ||||||||
| 権証の行使は,行使時に発行コストを差し引いた純額 | ||||||||
| 繰延株式単位演習 | ||||||||
| 残高 -2021年12月31日 | ||||||||
| 残高 -2022年12月31日 | ||||||||
2022年7月15日、株主と取締役会は定款の改正を承認し、実現した株式
社普通株の合併(逆分割)。会社の発行済み株式オプション,未償還株式権証,引受権証も反映するように調整されている
| 141 |
Eeterna Zentaris Inc.
連結財務諸表付記
2022年12月31日までと2021年12月31日現在
2022年、2021年、2020年12月31日
(単位:千ドル、1株当たりと1株当たりのデータを除いて、別途明記されている)
2021
2021年2月19日、会社は引受公開を完了した普通株価格は$普通株1株当たり、
総収益を$とする保険割引、手数料、発売費用を差し引く$(“2021年2月融資”)。会社はまた、引受業者と配給代理(“引受業者”)に30日間の超過配給選択権
を付与して、最も多く購入する追加普通株、価格は$普通株式1株(“引受業者選択権”).
また、会社は関連する引受権証を発行しました
2021年2月22日、引受業者は引受業者選択権を行使して受領する普通株式交換会社総収益
$それは.引受業者の選択権を行使したとき,引受業者はまた別のものを受け取った
2021年2月の融資に関する総収益総額は$現金取引コストを差し引く$
2020
2020年2月21日、同社は登録直接発売を完了した普通株、買い取り価格は$1株当たり、 は市場によって価格を設定します。また、投資家の権利証の使用価格は#ドルです1株当たり普通株と仲買人 引受権証の発行権価格は$1株当たり普通株。会社が今回の発行から得た現金純額は合計 $それは.総収益は$$に割り当てられました帰属公正価値と余剰毛収入$に基づく保証責任株式に割り当てられています1ドルの取引コスト株式及び引受権証の相対公正価値に応じて を分配する。株式の公正価値は分配された取引コストを差し引いた権益内に入金される。1ドルの取引コスト株式証明書に割り当てられた負債は総合損失表では費用 と全面損失と記されている。
2020年7月7日、同社は以下の公募株を完成させた単位,価格は$単位ごとに、会社にもたらす純現金収益
$それは.各単位は、1株の普通株(または同値な普通株)と、1株の普通株を購入するための投資家引受権証とを含む。全体的に言えば普通株投資家株式証の行使価格は$である満期寸前の1株
株式承認証は株式に分類されるため、総収益は#ドルとなる$に割り当てられました株とドルその相対公正価値に基づく引受権証
1ドルの取引コスト
| 142 |
Eeterna Zentaris Inc.
連結財務諸表付記
2022年12月31日までと2021年12月31日現在
2022年、2021年、2020年12月31日
(単位:千ドル、1株当たりと1株当たりのデータを除いて、別途明記されている)
2020年8月5日に、当社は証券購入契約を完了しました普通株、買い取り価格は$普通株
株で計算する。今回発行された総収益は#ドルですそれは.また、当社は購入者に未登録の引受権証を発行し、
で最も多く購入します
17. 株式承認証
2022年、2021年、2020年12月31日までの年度の権証活動状況は以下の通り
| 番号をつける | 重み 平均行権価格 | 金額 | ||||||||||
| # | $ | $ | ||||||||||
| 2019年12月31日 | ||||||||||||
| 授与する | ||||||||||||
| 権証負債の持分の再分類 | ||||||||||||
| 2020年12月31日 | ||||||||||||
| 授与する | ||||||||||||
| 鍛えられた | ( | ) | ( | ) | ||||||||
| 取引コストを配当金に分配する | ||||||||||||
| 2021年12月31日 | ||||||||||||
| 2022年12月31日 | ||||||||||||
権証負債の持分の再分類
会社が発表しました
2020年6月16日から、当社は当該等株式証の普通株式を登録声明で登録し、株式承認証上のキャッシュレス行使選択権を1対1で廃止する。そのため、2020年6月16日現在、株式証負債は公正価値に応じてBlack-Scholesオプション定価モデルを用いて再計量し、損失金額を再計量し、合併損失表と総合損失表で確認した。株式証明書の帳簿価値はその後、株式証負債から権益内の他の資本 に再分類される。
| 143 |
Eeterna Zentaris Inc.
連結財務諸表付記
2022年12月31日までと2021年12月31日現在
2022年、2021年、2020年12月31日
(単位:千ドル、1株当たりと1株当たりのデータを除いて、別途明記されている)
その会社はまた発行した
権利証の公正価値はBlack-Scholesオプション定価モデルを用いて推定される。ブレイク·スコイルズ推定値モデルで用いた重み付き平均は以下のように仮定される
| 12月31日までの年間 、 | ||||||||
| 2021 | 2020 | |||||||
| 期待配当収益率 | % | % | ||||||
| 期待変動 | % | % | ||||||
| 無リスク 年率 | % | % | ||||||
| 期待寿命(年) | ||||||||
| 加重平均株価 | $ | $ | ||||||
| 重み 平均行権価格 | $ | $ | ||||||
これらの株式認証の期待変動率は履歴変動率に基づいて決定され,期待寿命は発行日からの 満期時間に基づいて決定される.
18. 他の資本
2018年年次株主総会及び株主特別総会において、会社株主は、取締役会が最大発行を許可する2018年長期インセンティブ計画(LTIP)を承認した任意の所与の時間に、取締役会が付与時に決定した行使用価格で条件を満たす個人に発行された発行済みおよび発行された普通株式総数
は、株式オプション、株式付加権、株式奨励、繰延株式単位(“DSU”)、業績株、br}業績単位、および他の株式ベースの奨励を上限とする。LTIPは,会社にサービスを提供する役員,役員,従業員,他の協力者の株式オプション計画(“株式オプション計画”)に代わっている.LTIPにより付与されたオプションは,付与日後7年後に満期
を発行し,3年以内に付与され,付与日後1年から開始される.会社取締役会は2014年3月20日に株式オプション計画を改訂し、会社株主は2016年5月10日に株式オプション計画を承認、承認、確認した。2014年改正前の株式オプション計画により付与されたオプションは最長期限
の後に満期になる
株 オプション
社は,市場で普通株を購入して株式オプションの行使を決済するのではなく,新普通株を発行することで行使した株式オプションを決済する.
| 144 |
Eeterna Zentaris Inc.
連結財務諸表付記
2022年12月31日までと2021年12月31日現在
2022年、2021年、2020年12月31日
(単位:千ドル、1株当たりと1株当たりのデータを除いて、別途明記されている)
2022年12月31日までの年間給与支出は$
| 番号をつける | 重み 平均行権価格(ドル) | 番号をつける | 重み 平均行権価格(加元) | |||||||||||||
| # | $ | # | $ | |||||||||||||
| 2019年12月31日 | ||||||||||||||||
| 授与する | — | |||||||||||||||
| 取消·没収 | ( | ) | — | |||||||||||||
| 期限が切れる | ( | ) | ( | ) | ||||||||||||
| 2020年12月31日 | ||||||||||||||||
| 授与する | — | |||||||||||||||
| 期限が切れる | ( | ) | — | |||||||||||||
| 2021年12月31日 | ||||||||||||||||
| 授与する | — | |||||||||||||||
| 取消·没収 | ( | ) | — | |||||||||||||
| 期限が切れる | ( | ) | — | |||||||||||||
| 2022年12月31日 | ||||||||||||||||
2023年1月17日、年末後、会社は承認長期投資協定下の株式オプション。株式オプションは$で行使される 1株あたりには期限がありますそして.
次の表は、報酬有効期間内の株式ベースの報酬コストを決定するために、Black-Scholesオプション定価モデルに適用される仮定または加重平均パラメータを示す。
| 12月31日までの年間 、 | ||||||||||||
| 2022 | 2021 | 2020 | ||||||||||
| 期待配当収益率 | % | % | % | |||||||||
| 期待変動 | % | % | % | |||||||||
| 無リスク 年率 | % | % | % | |||||||||
| 期待寿命(年) | ||||||||||||
| 加重平均株価 | $ | $ | $ | |||||||||
| 重み 平均行権価格 | $ | $ | $ | |||||||||
| 重み 平均授権日公正価値 | $ | $ | $ | |||||||||
これらの株式オプションの期待変動率は履歴変動率を用いて決定され,期待寿命は過去に発行されたオプションの加重平均寿命を用いて決定される.
| 145 |
Eeterna Zentaris Inc.
連結財務諸表付記
2022年12月31日までと2021年12月31日現在
2022年、2021年、2020年12月31日
(単位:千ドル、1株当たりと1株当たりのデータを除いて、別途明記されている)
| オプション 未完了 | 行使可能オプション | |||||||||||||||||||||||
| ドル株式オプション価格範囲 | 番号 (#) | 加重 平均残余契約期間 (年) | 重み 平均行権価格 ($) | 番号 (#) | 加重 平均残余契約期間 (年) | 重み 平均行権価格 ($) | ||||||||||||||||||
| から | ||||||||||||||||||||||||
| 至れり尽くせり | ||||||||||||||||||||||||
| 至れり尽くせり | ||||||||||||||||||||||||
| 至れり尽くせり | ||||||||||||||||||||||||
| から | ||||||||||||||||||||||||
延期の 個のシェア単位
2022年12月31日までの年間給与支出は$ (2021 – $2020年には-ドル)、販売、一般 と管理費用を計上します。12月31日までの年度におけるDSUの活動は以下のとおりである
| 12月31日までの年間 、 | ||||||||||||
| 2022 | 2021 | 2020 | ||||||||||
| # | # | # | ||||||||||
| 残高 -年明け | ||||||||||||
| 授与する | ||||||||||||
| 鍛えられた | ( | ) | ( | ) | ||||||||
| 残高 -年末 | ||||||||||||
| 146 |
Eeterna Zentaris Inc.
連結財務諸表付記
2022年12月31日までと2021年12月31日現在
2022年、2021年、2020年12月31日
(単位:千ドル、1株当たりと1株当たりのデータを除いて、別途明記されている)
19. 本質的費用
| 12月31日までの年間 、 | ||||||||||||
| 2022 | 2021 | 2020 | ||||||||||
| $ | $ | $ | ||||||||||
| 今年度は在庫品を支出しました | ||||||||||||
| 時代遅れの在庫に備えて | ||||||||||||
| 第三者研究開発 | ||||||||||||
| 給料、給料、福祉 | ||||||||||||
| 専門家 と相談料 | ||||||||||||
| 保険 | ||||||||||||
| 株に基づく報酬 | ||||||||||||
| ソフトウェア とITサービス | ||||||||||||
| 減価償却と償却 | ||||||||||||
| マーケティング、コミュニケーション、投資家の関係 | ||||||||||||
| 営業権の減価 | ||||||||||||
| その他の資産の減価 | ( | ) | ||||||||||
| 無形資産減価 | ||||||||||||
| 旅行、飲食と娯楽 | ||||||||||||
| オフィス、レンタル料と電信料 | ||||||||||||
| 許可証料 | ||||||||||||
| 他にも | ( | ) | ||||||||||
| 修正住宅賃貸収益 | ( | ) | ||||||||||
20. 鍵管理の補償
主な経営陣には、会社役員、最高経営責任者、最高財務官、首席科学者、首席医療官が含まれる。キー経営陣に与えられた報酬の概要は以下の通り
| 12月31日までの年間 、 | ||||||||||||
| 2022 | 2021 | 2020 | ||||||||||
| $ | $ | $ | ||||||||||
| 給料 と短期福祉 | ||||||||||||
| 相談料 | ||||||||||||
| 退職後福祉 | ||||||||||||
| 株に基づく報酬 | ||||||||||||
当社とその上級管理者との間で締結されている雇用契約の大部分には終了条項が含まれており、この条項によると、会社が無断で高級管理者の雇用を終了したり、支配権変更後にその雇用を終了したりすれば、高級管理者は支払うべき福祉を得る権利がある。離職福祉は、通常、合意された適用基本給と奨励報酬の倍数に基づいて計算され、場合によっては他の福祉額に基づいて計算される。
| 147 |
Eeterna Zentaris Inc.
連結財務諸表付記
2022年12月31日までと2021年12月31日現在
2022年、2021年、2020年12月31日
(単位:千ドル、1株当たりと1株当たりのデータを除いて、別途明記されている)
21. キャッシュフロー情報を補足開示する
| 12月31日までの年間 、 | ||||||||||||
| 2022 | 2021 | 2020 | ||||||||||
| $ | $ | $ | ||||||||||
| 経営資産と負債の変化 : | ||||||||||||
| 貿易 とその他の入金 | ( | ) | ||||||||||
| 在庫品 | ( | ) | ( | ) | ||||||||
| 前払い料金と他の流動資産 | ( | ) | ( | ) | ( | ) | ||||||
| 支払すべき負債 | ||||||||||||
| 課税所得税 | ( | ) | ||||||||||
| 繰延収入 | ||||||||||||
| 再構成と他の費用のために を準備する | ( | ) | ||||||||||
| 従業員の未来福祉 | ( | ) | ( | ) | ( | ) | ||||||
22. 所得税
2022年、2021年、2020年12月31日までの年度の当期と繰延所得税回収(費用)の重要な構成要素は以下のとおりである
| 12月31日までの年間 、 | ||||||||||||
| 2022 | 2021 | 2020 | ||||||||||
| $ | $ | $ | ||||||||||
| 現在の所得税の払い戻し | ( | ) | ||||||||||
| 繰延税: | ||||||||||||
| 一時的な分岐の発生と逆転 | ||||||||||||
| 未確認納税資産の変更 | ( | ) | ( | ) | ( | ) | ||||||
| 合計 所得税の払い戻し | ( | ) | ||||||||||
当社は時々税務監査を受けています。当社はその届出の立場が適切で支持可能であると考えているが、何らかの事項は定期的に税務機関から疑問視されている。当社はその税務支出が十分であると考えているが、税務監査及び任意の関連論争の最終決定は歴史所得税の準備及び課税項目と大きな違いがある可能性がある。br}2020年、AEZSドイツ社は2013~2016課税年度の税務監査を受けた。税務機関は2022年12月31日と2021年12月31日までにこの3年間の監査を終了した。その後各年度も監査されておらず、当社は#ドルを計上しています
| 148 |
Eeterna Zentaris Inc.
連結財務諸表付記
2022年12月31日までと2021年12月31日現在
2022年、2021年、2020年12月31日
(単位:千ドル、1株当たりと1株当たりのデータを除いて、別途明記されている)
カナダ連邦と省の合併企業所得税税率と所得税支出の入金は以下の通りである
| 12月31日までの年間 、 | ||||||||||||
| 2022 | 2021 | 2020 | ||||||||||
| カナダ連邦と省の法定所得税税率の合計 | % | % | % | |||||||||
| 12月31日までの年間 、 | ||||||||||||
| 2022 | 2021 | 2020 | ||||||||||
| $ | $ | $ | ||||||||||
| 所得税 合併法定所得税率に基づく還付 | ||||||||||||
| 未確認納税資産の変更 | ( | ) | ( | ) | ( | ) | ||||||
| 株式発行コスト | ||||||||||||
| 営業権減価の恒久的な差額に起因することができます | ( | ) | ||||||||||
| 投資税収相殺満期の影響 | ( | ) | ( | ) | ( | ) | ||||||
| 提出された返品調整に備えてください | ||||||||||||
| 株式証負債公正価値純変化の永久的な違いによるものとすることができる | ||||||||||||
| 株式ベースの報酬コスト | ( | ) | ( | ) | ( | ) | ||||||
| 海外子会社の法定所得税率差 | ||||||||||||
| 不確定な税務状況 | ( | ) | ||||||||||
| 他にも | ( | ) | ||||||||||
| ( | ) | |||||||||||
所得税前損失 は当社の税務管轄範囲以下の通りである
| 12月31日までの年間 、 | ||||||||||||
| 2022 | 2021 | 2020 | ||||||||||
| $ | $ | $ | ||||||||||
| ドイツ | ( | ) | ( | ) | ( | ) | ||||||
| カナダ | ( | ) | ( | ) | ( | ) | ||||||
| アメリカ アメリカ | ( | ) | ( | ) | ( | ) | ||||||
| 所得税前損失合計 | ( | ) | ( | ) | ( | ) | ||||||
| 149 |
Eeterna Zentaris Inc.
連結財務諸表付記
2022年12月31日までと2021年12月31日現在
2022年、2021年、2020年12月31日
(単位:千ドル、1株当たりと1株当たりのデータを除いて、別途明記されている)
繰延税金資産と負債の重要な構成要素は以下のとおりである
| 十二月三十一日 | ||||||||
| 2022 | 2021 | |||||||
| $ | $ | |||||||
| 繰延納税資産 | ||||||||
| 営業損失の繰り越し | ||||||||
| 無形資産 | ||||||||
| 繰延納税義務 | ||||||||
| 売掛金 | ||||||||
| 支払すべき負債 | ||||||||
| 財産 と設備 | ||||||||
| 繰延収入 | ||||||||
| 他にも | ||||||||
| 繰延納税資産(負債)、純額 | ||||||||
未確認の繰延税金資産と損失の重要な構成要素は以下のとおりである
| 十二月三十一日 | ||||||||
| 2022 | 2021 | |||||||
| $ | $ | |||||||
| 未確認の繰延税金資産 | ||||||||
| 繰延収入と他の支出 | ||||||||
| 営業損失の繰り越し | ||||||||
| 資本 は損失を繰り越す | ||||||||
| 高度教育 池(&E) | ||||||||
| 未使用税収控除 | ||||||||
| 従業員の未来福祉 | ||||||||
| 財産 と設備 | ||||||||
| 無形資産 | ||||||||
| 株式発行費用 | ||||||||
| 他にも | ||||||||
| 未確認の繰延税金資産 | ||||||||
繰延所得税資産は、一時的な差異と将来の課税利益を押し出すことで関連税収割引を実現する範囲で確認されている。現在予測されている将来の課税利益と一時的な差に基づく償却会社は、将来の収益は繰延税金資産を相殺するのに十分ではなく、未確認の繰延税金資産残高$があると考えている
| 150 |
Eeterna Zentaris Inc.
連結財務諸表付記
2022年12月31日までと2021年12月31日現在
2022年、2021年、2020年12月31日
(単位:千ドル、1株当たりと1株当たりのデータを除いて、別途明記されている)
2022年12月31日までの会社累計非資本損失総額は$
| カナダ | ||||||||
| 連邦制 | 省級 | |||||||
| $ | $ | |||||||
| 2028 | ||||||||
| 2029 | ||||||||
| 2030 | ||||||||
| 2031 | ||||||||
| 2032 | ||||||||
| 2033 | ||||||||
| 2034 | ||||||||
| 2035 | ||||||||
| 2036 | ||||||||
| 2037 | ||||||||
| 2038 | ||||||||
| 2039 | ||||||||
| 2040 | ||||||||
| 2041 | ||||||||
| 2042 | ||||||||
Br社の研究開発投資税収は約$の払い戻しはできません
| アメリカ アメリカ | ||||
| $ | ||||
| 2028 | ||||
| 2029 | ||||
| 2034 | ||||
| 2035 | ||||
| 2036 | ||||
| 2037 | ||||
| 無期限 | ||||
| 無期限 | ||||
| 無期限 | ||||
| 無期限 | ||||
繰越の営業損失や申請した税収控除は税務機関の審査と可能な調整を受ける可能性がある。未登録納税資産のその他控除可能な一時的差額は時間制限を受けないが,株式発行費用を除くと,これらの費用 は5年以内に償却することができる。
| 151 |
Eeterna Zentaris Inc.
連結財務諸表付記
2022年12月31日までと2021年12月31日現在
2022年、2021年、2020年12月31日
(単位:千ドル、1株当たりと1株当たりのデータを除いて、別途明記されている)
23. 資本管理
会社管理資本の目標は,十分な流動資金を確保し,研究開発コスト,販売費用,一般とbr管理費用および運営資金需要に資金を提供することである。付記24で述べたように、過去数年間、当社は公募株式を公開発売および発行することにより資金を調達し、その流動資金の主な源としている。会社の資金管理目標 は往期と変わらない。配当に関する政策は、会社の製品開発組合を推進するために必要な活動に資金を提供するための資金を維持し、出現可能な場合に適切なビジネス機会を求めるために現金を保持することである。
会社はいかなる規制機関または任意の他の外部源によって適用されるいかなる資本金要求の制約も受けない。
24. 金融商品と金融リスク管理
2022年と2021年12月31日現在の財務資産と負債は以下のとおりである。
| 2022年12月31日 | 償却コストで計算した財務資産 | 償却コストで計算した財務負債 | ||||||
| $ | $ | |||||||
| 現金 と現金等価物 | ||||||||
| 貿易 とその他の入金 | ||||||||
| 制限された 現金等価物 | ||||||||
| 支払すべき負債 | ||||||||
| レンタル責任 | ||||||||
| 2021年12月31日 | 償却コストで計算した財務資産 | 償却コストで計算した財務負債 | ||||||
| $ | $ | |||||||
| 現金 と現金等価物 | ||||||||
| 貿易 とその他の入金 | ||||||||
| 制限された 現金等価物 | ||||||||
| 支払すべき負債 | ||||||||
| レンタル責任 | ||||||||
付加価値税のような非契約性資産及び負債は、政府が定める法定要求により生じ、金融資産又は金融負債の定義に適合しないため、貿易その他の売掛金及び売掛金から除外される。
公正価値
IFRS 13,公正価値計量(“国際財務報告基準第13号”)は、公正価値を計量するための投入を優先順位付けする階層構造を構築した。 この階層構造は、同じ資産または負債の活発な市場の未調整オファーに最高優先度(第1レベル計量) を与え、観察できない投入に最低優先度(第3レベル計量)を与える。
| 152 |
Eeterna Zentaris Inc.
連結財務諸表付記
2022年12月31日までと2021年12月31日現在
2022年、2021年、2020年12月31日
(単位:千ドル、1株当たりと1株当たりのデータを除いて、別途明記されている)
“国際財務報告基準”13で議論された投入レベルは、
レベル 1-アクティブ市場における同じ資産または負債の未調整見積もり。
第2のレベル-第1のレベルにおける見積以外の直接(すなわち、 価格)または間接(すなわち、価格から)を含む資産または負債が観察可能な投入。
第3レベル-資産または負債の投入は、観察可能な市場データ(観察不可能な投入)に基づいているわけではない。
財務リスク要因
以下に、信用リスク、流動性リスク、外国為替リスク、および当社がこれらのリスクをどのように管理するかを含む、当社が金融商品に発生するリスクの性質と程度を開示する。
(A) 信用リスク
信用リスクとは、顧客や金融商品の取引相手がその契約義務を履行できなかった場合、意外な損失が発生するリスクのことです。当社は定期的に信用リスクの開放をモニタリングし、この開放による損失の可能性を低減する措置を講じています。当社の現在の信用リスクの開放は、表の償却コストで計算されている金融資産に関連しています。会社 が保有する利用可能な現金額は、いつでも既知の額の現金に変換することができ、その現金残高を投資レベル格付けが少なくとも“P-2”または同等格付けの金融機関 に預けることができる。この情報は、独立した格付け機関によって提供され(ある場合)、ない場合、会社は、その現金を信頼性の良い金融機関に投資することを保証するために、公開された財務情報を使用する。合理的な回復期待がないという兆候があると、このような金融資産はログアウトされるが、法執行活動が必要だ。
2022年12月31日現在,売掛金に含まれる3つの取引相手の売掛金総額は約#ドルである
通常、会社は顧客が売掛金に担保や他の保証を提供する必要はないが、信用は信用を評価した後に発行される。また、同社はすべての顧客に対して継続的な信用審査を行い、予想される信用損失を決定する。その上で、同社は2022年12月31日現在、br業務に関連するすべての未払い金と未払い金を準備している。
信用リスクの最大リスク開放は、当社の総合財務状況表で確認された金額とほぼ同じです。
(B) 流動性リスク
流動性 リスクとは、会社が満期財務義務を履行できないリスクである。付記23に示すように、当社は予想キャッシュフローをもとに、当社の現金および現金等価物のスクロール予測を監視することにより、その資本構造を管理してこのリスクを管理する。
経営陣は,会社計画の研究開発活動,販売費用,一般と行政費用および運営資金需要を考慮し,会社の手元には今後12カ月間の債務を履行するのに十分な現金があると結論した。同社はその研究·開発活動を拡張し、現金供給状況に応じて必要に応じてそうする能力がある。その会社は$を持っています
| 153 |
Eeterna Zentaris Inc.
連結財務諸表付記
2022年12月31日までと2021年12月31日現在
2022年、2021年、2020年12月31日
(単位:千ドル、1株当たりと1株当たりのデータを除いて、別途明記されている)
リース負債を除いて、会社のすべての財務負債は流動負債であり、決済日は1年以内と予想される。賃貸負債の満期分析は付記14に開示されている
(C)外国為替リスク
ビットコインの実体としてユーロを使用する
25. 市場情報を細分化する
会社は運営部門つまりバイオ製薬部門です
地理情報
地理的地域別収入 は、社外顧客または許可された人の居住が許可されている国/地域に応じて地理的地域に割り当てられており、具体的には以下の通りである
| 12月31日までの年間 、 | ||||||||||||
| 2022 | 2021 | 2020 | ||||||||||
| $ | $ | $ | ||||||||||
| スイス | ||||||||||||
| アイルランド | ||||||||||||
| デンマーク | ||||||||||||
| 他にも | ||||||||||||
非流動資産は、限定的な現金等価物、使用権資産、財産およびデバイス、識別可能無形資産、他の資産 および営業権(2021年のみ)を含み、地理的領域によって以下のように細分化される
| 十二月三十一日 | ||||||||
| 2022 | 2021 | |||||||
| $ | $ | |||||||
| ドイツ | ||||||||
| カナダ | ||||||||
| アメリカ アメリカ | ||||||||
| 154 |
Eeterna Zentaris Inc.
連結財務諸表付記
2022年12月31日までと2021年12月31日現在
2022年、2021年、2020年12月31日
(単位:千ドル、1株当たりと1株当たりのデータを除いて、別途明記されている)
| 12月31日までの年間 、 | ||||||||||||
| 2022 | 2021 | 2020 | ||||||||||
| $ | $ | $ | ||||||||||
| 純損失 | ( | ) | ( | ) | ( | ) | ||||||
| 基本 と希釈加重平均流通株数 | ||||||||||||
| プロジェクト はその逆希釈作用により、1株当たりの純損失の計算には含まれていない | ||||||||||||
| 株式 オプションとDSU | ||||||||||||
| 株引受権証 | ||||||||||||
27. 支払いを引き受ける
本報告で述べた期間終了時に契約したが負債と確認されなかった重大な支出は以下のとおりである
| サービス業と製造業 | 研究開発 契約書 | 合計して | ||||||||||
| $ | $ | $ | ||||||||||
| 1年未満 | ||||||||||||
| 1-3年 | ||||||||||||
| 4-5年 | ||||||||||||
| 5年以上 | ||||||||||||
当社は2021年に、内部許可や同様の手配を含む様々な協定を開発パートナーと締結した(付記10)。このようなbr協定は、開発、発表、または収入マイルストーンの段階に達したときに会社に支払うことを要求する可能性があるが、会社は通常、処罰されずにこれらの合意を終了する権利がある。その会社は高い$を支払う必要があるかもしれない
28. 後続事件
2023年3月15日、会社の同意の下、Consilient Healthは、欧州経済地域とイギリスの現在のマカロニ商業化許可協定をAtnahs Pharma UK Limited(“Pharmanovia”)に譲渡する譲渡協定を締結した。同じく2023年3月15日にPharmanoviaと独占供給協定を締結し、これにより、会社はPharmanoviaに許可製品を提供することに同意した。
29. 比較的数字の再分類
総合財務状況表、総合損益表、全面損益表のいくつかの比較可能な金額及びこれらの総合財務諸表の付記は本年度に採用した列報方式に適合するように再分類された。
| 155 |
物品 19.展示品
添付ファイル インデックス
| 1.1 | 登録者が再記載した会社登録証明書と重記の会社定款(2011年5月25日に証監会に提出された登録者6-K表報告添付ファイル99.2参照) | |
| 1.2 | 登録者改訂証明書及び改訂定款(添付ファイル99.2を参照して登録者が2012年10月3日に証監会に提出した表格6-K報告に組み込む) | |
| 1.3 | 登録者改訂証明書及び改訂定款(登録者が2015年11月17日に証監会に提出した表格6−Kの報告添付ファイル99.1参照) | |
| 1.4 | 登録者第1条改正及び再記載(登録者が2013年3月22日に証監会に提出した2012年12月31日までの財政年度20−F表年次報告添付ファイル1.3参照) | |
| 2.1 | 権利代理人として登録者とカナダ計算機株式信託会社との間の株主権利計画協定を改訂·再署名し、日付は2019年5月8日(添付ファイル99.2を参照して登録者が2019年5月9日に委員会に提出した表格6-K報告書に編入) | |
| 2.2 | 連結所第12条に基づいて登録された証券説明 | |
| 4.1 | 登録者が2回目の改訂と再作成した株式オプション計画(登録者が2014年3月21日に証監会に提出した2013年12月31日までの財政年度20−F表年次報告書の添付ファイル4.1) | |
| 4.2 | 登録者2018年長期インセンティブ計画(2018年5月8日に委員会に提出された登録者S−8表添付ファイル4.7編入を参照) | |
| 4.3 | ライセンス·譲渡契約は、2018年1月16日にAeterna Zentaris GmbHとStrongbridgeアイルランド株式会社によって締結されました(登録者が2018年1月19日に委員会に提出した6-Kフォーム報告書の添付ファイル99.2を参照して統合されます) | |
| 4.4 | 株式証明書プロトコル表(登録者が2019年9月20日に証監会に提出した表格6-K報告添付ファイル99.1を参照) | |
| 4.5 | 登録者とMaxim Group LLC間の配給代理プロトコルは、2019年9月20日となる(登録者が2019年9月20日に委員会に提出したテーブル6-K報告の添付ファイル99.2を参照して合併する) | |
| 4.6 | 登録者とある機関投資家との間の証券購入契約表は、日付が2019年9月20日である(登録者が2019年9月20日に証監会に提出した表格6-K報告の99.3号添付ファイルを参照) | |
| 4.7 | 投資家株式証明書表(参考登録者が2020年2月21日に証監会に提出した表格6-K報告添付ファイル99.1) | |
| 4.8 | 配給代理人授権書表(登録者が2020年2月21日に証監会に提出した表格6−K報告の添付ファイル99.4を参照して合併) | |
| 4.9 | 普通株式引受権証表(登録者が2020年6月30日に証監会に提出したF-1表登録説明書添付ファイル4.5参照) | |
| 4.10 | 事前出資株式証表(登録者が2020年6月30日に証監会に提出した表F-1登録説明書添付ファイル4.6) | |
| 4.11 | 配給代理人授権書表(参考登録者が2020年6月30日に証監会に提出した登録者登録説明書F−1表の添付ファイル4.7) | |
| 4.12 | 投資家株式証明書表(登録者が2020年8月5日に証監会に提出した表格6-K報告添付ファイル99.1を参照) | |
| 4.13 | 配給代理人授権書表(登録者が2020年8月5日に証監会に提出した表格6-K報告添付ファイル99.5参照) | |
| 4.14 | Aeterna Zentaris GmbHとノとノド生物製薬有限会社が2020年11月16日に署名した改訂協定。(引用登録者が2020年11月16日に証監会に提出した表格6-K報告書の添付ファイル99.1) | |
| 4.15 | Aeterna Zentaris GmbHとConsilient Health Ltd.によって署名され、2020年12月7日に施行される許可協定(登録者が2020年12月7日に委員会に提出した6-K表報告書の添付ファイル99.1を参照することにより統合される) | |
| 4.16 | 登録者とH.C.Wainwright&Co.が2021年2月14日に署名した婚約状。 | |
| 4.17 | ノドとノドは2020年11月16日に改訂協定(“合意”)を早期に終了した | |
| 8.1 | 登録者の子会社 |
| 156 |
| 11.1 | 登録者の行為規則と商業道徳(参考登録者が2018年3月28日に証監会に提出した2017年12月31日までの財政年度20−F表年次報告書の添付ファイル11.1) | |
| 11.2 | 取締役会メンバーの商業行為及び道徳規則(参考登録者が2015年3月17日に証監会に提出した2014年12月31日までの財政年度20-F表年次報告添付ファイル11.2) | |
| 11.3 | 登録者監査委員会規約(登録者が2015年3月17日に証監会に提出した2014年12月31日までの20−F表年次報告添付ファイル11.3参照) | |
| 12.1 | 2002年サバンズ·オキシリー法第302条認証首席執行幹事によると | |
| 12.2 | 2002年サバンズ·オキシリー法第302条に基づく認証首席財務幹事 | |
| 13.1 | 2002年サバンズ·オキシリー法案第906条に基づく“米国法典”第18編第1350条首席執行幹事の証明 | |
| 13.2 | 2002年サバンズ·オキシリー法第906条で可決された“米国法典”第18編1350条による首席財務官の証明 | |
| 15.1 | 安永法律事務所が同意した | |
| 15.2 | 普華永道有限責任会社は同意した |
添付ファイル インデックス
101. INS XBRLを連結したインスタンスドキュメント
101. 連結SCH XBRL分類拡張アーキテクチャ
101. イントラネットCAL XBRL分類拡張アーキテクチャ計算リンクライブラリ
101. イントラネットDEF XBRL分類拡張アーキテクチャ定義リンクライブラリ
101. イントラネット研究所XBRL分類拡張アーキテクチャタグLinkbase
101. インラインPre XBRL分類拡張アーキテクチャプレゼンテーションリンクライブラリ
104表紙インタラクションデータファイル(イントラネットXBRL文書に埋め込む)
| 157 |
サイン
登録者は、それが20-F表を提出するすべての要求に適合し、本年度報告書に署名するために署名者を代表して正式に手配され、許可されたことを証明する。
| Eeterna Zentaris Inc. | |
| /s/ クラウス·ポーリーニ | |
| クラウス·ポーリーニ | |
| 社長 とCEO |
日付: 2023年3月22日
| 158 |