
アメリカです
アメリカ証券取引委員会
ワシントンD.C.,郵便番号:20549
表
1934年証券取引法第13条又は15条に基づいて提出された年次報告 |
本財政年度末まで
あるいは…。
1934年証券取引法第13条又は15条に基づいて提出された移行報告 |
移行期になります 至れり尽くせり .
依頼書類番号:

(登録者の正確な氏名はその定款に記載)
|
||
(明またはその他の司法管轄権 会社や組織) |
|
(税務署の雇用主 識別番号) |
|
|
|
|
||
(主にオフィスアドレスを実行) |
|
(郵便番号) |
(
(登録者の電話番号、市外局番を含む)
同法第12条(B)に基づいて登録された証券:
|
|
|||
(クラス名) |
|
(取引コード) |
|
(登録所の取引所名) |
同法第12条(G)により登録された証券:なし
登録者が証券法規則405で定義されている経験豊富な発行者である場合は、再選択マークで示してください。はい、そうです ☐
登録者がこの法第13節または第15節(D)節に基づいて報告を提出する必要がないかどうかを再選択マークで示す。はい、そうです ☐
再選択マークは、登録者が(1)過去12ヶ月以内(または登録者がそのような報告の提出を要求されたより短い期間)に、1934年の証券取引法第13条または15(D)節に提出されたすべての報告書を提出したかどうか、および(2)過去90日以内にそのような提出要件に適合しているかどうかを示す
再選択マークは、登録者が過去12ヶ月以内(または登録者がそのような文書の提出を要求されたより短い時間以内)に、S−T規則405条(本章232.405節)に従って提出を要求した各相互作用データファイルを電子的に提出したか否かを示す
登録者が大型加速申告会社,加速申告会社,非加速申告会社,小さな報告会社,あるいは新興成長型会社であることを再選択マークで示す。取引法第12 b-2条の規則における“大型加速申告会社”、“加速申告会社”、“小申告会社”、“新興成長型会社”の定義を参照されたい。
大型加速ファイルサーバ |
|
☐ |
|
|
☒ |
|
新興成長型会社 |
|
☐ |
|
非加速ファイルサーバ |
|
☐ |
|
規模の小さい報告会社 |
|
|
|
|
|
新興成長型企業であれば、登録者が延長された移行期間を使用しないことを選択したか否かを再選択マークで示し、取引所法第13(A)節に提供された任意の新たまたは改正された財務会計基準を遵守する。
登録者が報告書を提出したかどうかを再選マークで示し、その経営陣が“サバンズ·オクスリ法案”(“米国法典”第15編7262(B)節)第404(B)条に基づいて、その監査報告書を作成または発表する公認会計士事務所の財務報告内部統制の有効性を評価した。
証券が同法第12条(B)に基づいて登録されている場合は,登録者の財務諸表が以前に発表された財務諸表の誤り訂正を反映しているか否かを示すチェックマークを適用する。 ☐
これらのエラーのより真ん中に登録者の任意のエンタルピーCER幹部が相関回復期間内に§240.10 D−1(B)に基づいて受信したインセンティブベースの補償に基づいて回復分析を行う必要があるかどうかを再選択マークで示す。 ☐
登録者が空殻会社であるか否かをチェックマークで示す(同法第12 b-2条で定義される)。はい、そうです
ナスダック世界精選市場の報告によると、2022年6月30日までの財期最終営業日普通株の終値によると、非関連会社が保有する登録者普通株の総時価は約$である
2023年3月1日までに
引用で編入された書類
登録者は,Orthofix Medical Inc.2022年度株主総会に関連する最終委託書の一部を委員会に提出し,引用により本年度報告の第3部に組み込む。
Orthofix医療会社です。
2022年12月31日までの年間表10-K
カタログ表
|
|
|
|
ページ |
第1部 |
|
|
|
|
第1項。 |
|
業務.業務 |
|
4 |
第1 A項。 |
|
リスク要因 |
|
26 |
項目1 B。 |
|
未解決従業員意見 |
|
58 |
第二項です。 |
|
属性 |
|
58 |
第三項です。 |
|
法律訴訟 |
|
58 |
第四項です。 |
|
炭鉱安全情報開示 |
|
58 |
第II部 |
|
|
|
|
五番目です。 |
|
登録者普通株市場、関連株主事項及び発行者による株式証券の購入 |
|
59 |
第六項です。 |
|
保留されている |
|
60 |
第七項。 |
|
経営陣の財務状況と経営成果の検討と分析 |
|
61 |
第七A項。 |
|
市場リスクの定量的·定性的開示について |
|
74 |
第八項です。 |
|
財務諸表と補足データ |
|
75 |
第九項です。 |
|
会計と財務情報開示の変更と相違 |
|
75 |
第9条。 |
|
制御とプログラム |
|
75 |
プロジェクト9 B。 |
|
その他の情報 |
|
78 |
プロジェクト9 Cです。 |
|
検査妨害に関する外国司法管区の開示 |
|
78 |
第三部 |
|
|
|
|
第10項。 |
|
役員·幹部と会社の管理 |
|
79 |
第十一項。 |
|
役員報酬 |
|
79 |
第十二項。 |
|
特定の実益所有者の担保所有権及び経営陣及び関連株主の事項 |
|
79 |
十三項。 |
|
特定の関係や関連取引、取締役の独立性 |
|
79 |
14項です。 |
|
チーフ会計士費用とサービス |
|
79 |
第4部 |
|
|
|
|
第十五項。 |
|
展示品と財務諸表の付表 |
|
80 |
第十六項。 |
|
表格10-Kの概要 |
|
85 |
前向きに陳述する
本年度報告には、1934年“証券取引法”(以下、“取引法”と略す)第21 E節及び1933年“証券法”(改正)第27 A節の意味に適合する展望的陳述が含まれており、これらの陳述は、我々の現在の信念、仮説、予想、推定、予測及び予測に基づいており、我々の業務及び財務見通しに関連している。場合によっては、前向きな陳述は、“可能”、“会議”、“すべき”、“予想”、“計画”、“予想”、“信じ”、“推定”、“プロジェクト”、“意図”、“予測”、“潜在的”または“継続”または他の同様の用語によって識別することができる。前向きな陳述は、以下の態様に関する陳述を含むが、これらに限定されない
これらの展望性陳述は未来の業績の保証ではなく、予測困難なリスク、不確定性、推定と仮説に関連している。私たちが作った任意またはすべての前向き陳述は誤りであることが証明される可能性があり(私たちが作ったまたは他の不正確な仮定のため)、私たちの実際の結果および結果は、これらの前向き陳述で表現されたものとは大きく異なる可能性がある。実際の結果が大きく異なる可能性のある潜在的リスクおよび不確定要因は、第1部1 A項“リスク要因”の下、第2部第7項“経営陣の財務状況および経営結果の議論および分析”および本年度報告の他の部分、ならびに本年度報告を参照して組み込まれた任意の他の文書に記載されているリスクおよび不確実性を含むが、これらに限定されない。あなたはこのような展望的な陳述のいずれかに過度に依存してはいけない。さらに、いかなる前向きな陳述も、別の明確な声明が異なる日に発表されない限り、本プレスリリースの発表日にのみ発表される。我々は,前向き陳述を更新する義務を負わず,本プレスリリースの日以降に発生した状況やイベント,新情報,その他の原因によるものであっても,更新前向き陳述の責任を負わないことを明確に示している.
商標
便宜上、本年度報告では、私たちの商標や商号に言及する際には使用および記号は使用されていませんが、このような言及は、適用法に基づいて私たちの権利を最大限に主張するいかなる指示もないと解釈されるべきではありません。
第1部
I項目1。 業務.業務
本年度報告において、用語“私たち”、“Orthofix”および“会社”は、いずれもOrthofix Medical Inc.およびその合併子会社および付属会社の合併業務を意味し、文意が別に指摘されていない。
会社の概要
我々が最近SeaSpineホールディングス(“SeaSpine”)と合併した後,新たに合併したOrthofix−SeaSpine組織は世界有数の脊柱と整形外科会社であり,全面的な生物製剤,革新的な脊柱ハードウェア,骨成長療法,専門整形外科解決策とリードした手術ナビゲーションシステムを有している。我々の製品は直接·間接販売代表·在庫流通業者を通じて世界約68カ国·地域で販売されている。
私たちはテキサス州のルイスビルに本部を置き、カリフォルニア州のカールスバッドとイタリアのヴェローナに主要な事務所を設置して、脊柱と生物製剤の製品革新と外科医師教育に集中して、重点は整形外科の製品革新、生産と医学教育です。私たちの世界的な研究開発、商業と製造の足跡はまた、カリフォルニア州オーウェン、カナダトロント、カリフォルニア州森ビル、ペンシルベニア州ウェイン、ペンシルバニア州オリーブ支社、イギリスメデンヘード、ドイツミュンヘン、フランスパリとブラジルサンパウロの工場と事務所も含まれています。
同社は1987年にキュラソーで設立され、前身は“Orthofix International N.V.”だった。2018年には,クラッソからデラウェア州への組織管轄権変更(“馴化”)を完了し,我々の名称を“Orthofix Medical Inc.”に変更した。したがって、私たちはデラウェア州の法律に基づいて存在する会社だ。
我々とSeaSpineの合併は2023年1月5日に完了し,取引完了後,SeaSpineはOrthofixの完全子会社として継続している。Orthofixは合併後の会社構造における会社親実体としてナスダック上で取引を継続し,コードは“OFIX”である.親会社は遅れて名称を変更し、それまでは、親会社は引き続きOrthofix Medical Inc.と呼ばれています。他に説明がない限り、本年度報告第1項“業務”というタイトルで開示されている情報とは、合併後の会社を指します。しかし、ここで述べた財務結果は、統合に影響を与えることなく、Orthofixと独立して関連しているため、SeaSpineの結果は含まれていない。我々の2023年3月31日までの財政四半期のForm 10-Q四半期報告から、今後の文書はOrthofix-SeaSpine合併組織の結果を反映する。
利用可能な情報とOrthofixサイト
我々が米国証券取引委員会(“米国証券取引委員会”)に提出した文書は、我々の10-K表年次報告、10-Q表四半期報告、現在の8-K表報告、株主総会依頼書、任意の登録声明、およびそれなどの報告書の改訂を含み、米国証券取引委員会または米国証券取引委員会に提出された後、合理的で実行可能な範囲内でできるだけ早く私たちのウェブサイトで無料で閲覧することができる。本年報には、当社サイトに掲載されている資料や当社サイトに関する資料は含まれていませんので、ご参考までに。私たちのサイトはwww.oreofix.comにあります。私たちのアメリカ証券取引委員会の申告書類もアメリカ証券取引委員会のウェブサイトwww.sec.govで調べることができます。
業務の細分化
歴史的には,Orthofixは2つの報告部門であるGlobal SpineとGlobal Orthopedicsでこの業務を管理しており,この2部門はそれぞれOrthofix 2022年の総純売上高の77%と23%を占めている。次のグラフは、Orthofixの製品販売とマーケティングサービス費用を含む2022年12月31日、2021年12月31日、2020年12月31日までの各年度の純売上高を示している。上述したように、これらの金額にはSeaSpineの純売上は含まれていない。
4
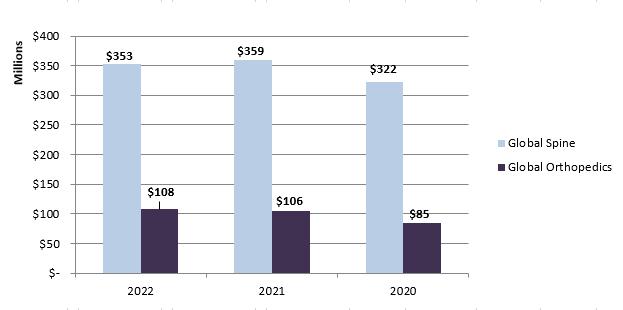
SeaSpineは従来1つの運営部門として業務を管理してきたが,報告された収入は,(I)生物製剤(従来Orthobiologicsと認められていた)と(Ii)脊柱インプラントとイネーブル技術の2つの製品種別に分類されてきた。本年度報告については,SeaSpineの履歴業務記述は単独の部分として本業務部門の議論に含まれている.SeaSpineとの合併が2023年1月5日に完了した後、2023年第1四半期に新合併会社の運営管理方式に基づいて報告部門を再評価する予定です。
我々の報告可能な業務部門とある地理情報に関する財務情報は、本年報第II部第7項“経営層の財務状況と経営結果の検討と分析”、及び本年報第8項総合財務諸表付記16に掲載されている。
全世界脊椎
Global Spine領域では,脊柱疾患や創傷患者の生活の質を回復するための埋め込み型医療機器,生物製剤,その他の再生解決策を提供している。著者らは多種の治療解決方案を提供し、唯一無二に多種の治療モード、例えば機械、生物と電磁モードを融合し、期待される臨床結果を実現する。
世界脊椎戦略
著者らの全世界脊柱領域における戦略は有機と無機革新、医師協力及び専門的かつ高業績の商業販売ルートと協力パートナー関係を構築することによって、業務成長を推進することである。成長計画には
5
世界の脊椎主要製品
全世界脊柱報告部門は主に3つの主要な製品カテゴリーから構成され、i)骨成長療法、ii)脊柱インプラント、及びiii)生物製品。以下、これらの製品カテゴリの各々についてさらに説明する
骨成長療法
骨成長療法製品の種類の中で、著者らは市場をリードする骨融合を増強する骨成長刺激設備の製造、流通と支持サービスを提供する。これらIII系医療機器は補助的な非侵襲的治療と考えられ,頚椎と腰椎の融合成功率を向上させ,癒合していない非脊柱や付属器骨折(“骨不連”)を治療することも可能である。著者らの製品の組み合わせ中のいくつかの設備は著者らの特許パルス電磁場(“PEMF”)技術を使用し、その安全性と有効性は科学文献中の基本的な作用機序データ及び一次無作為対照臨床試験からの公開データの支持を得た。私たちは製品グループの新しいメンバーが私たちの低強度パルス超音波(“LIPUS”)を使用することを刺激し、この技術も強力な基礎科学と出版された臨床文献の支持を得た。OrthofixはPEMFとLIPUS技術を同時に提供する唯一のメーカーである。私たちはほとんどアメリカでしかこれらの製品を販売していません。流通業者と直売代表を使って医療提供者と彼らの患者に私たちの設備を提供します。
脊柱インプラント
脊柱インプラント製品のカテゴリでは、著者らは脊柱外科手術のための運動保護と固定インプラント製品の組み合わせを設計、開発、販売している。脊椎製品を販売するために流通業者と販売代表ネットワークを通じて世界で販売しています 脊柱ケアを提供する施設は,病院,外来手術センター,外来病院を含む。
生物製品
Biologics製品分類において、著者らは一連の製品と組織形式を提供し、医師が各種の脊柱と整形疾患の治療に成功できるようにした。我々は主に独立流通業者と販売代表からなるネットワークを介して、脊柱看護機関と外科医にMTF Biologics(“MTF”)が提供する組織形態を販売する。我々はMTFとのパートナー関係により、Virtuos Lyoggraph、三一エリート、FiberFuse Advanced、FiberFuse帯状およびいくつかの他の筋肉骨格欠陥の組織形態を独占的に販売し、骨融合を増強することができる。また,合成材料由来の再生可能な非組織バイオソリューションを販売している。OPUS BAとOpus MG Setは我々の現在の合成,生物製品を代表する。
以下の表と議論は、商標名によって当社の主要Global Spine製品を決定し、それらの主な応用を説明します
製品 |
|
主な応用 |
|
|
|
骨成長療法製品 |
|
|
|
|
|
頚椎椎体融合治療 |
|
PEMF非侵襲的頚椎融合術は骨成長を促進する |
|
|
|
脊柱脊柱融合治療 |
|
PEMF非侵襲性腰椎融合術は骨成長を促進する |
|
|
|
生理骨癒合療法 |
|
PEMF非侵襲的付属器骨癒合療法による骨不連骨折骨成長促進 |
|
|
|
加速時間 |
|
Lipus癒合療法はいくつかの新鮮な橈骨遠位端と脛骨骨幹骨折の骨成長を促進するために用いられる |
|
|
|
脊柱インプラント製品 |
|
|
|
|
|
M 6-C人工頚椎椎間板 |
|
頚椎椎間板変性により損傷した間盤の代わりに開発された次世代人工椎間板;人工粘弾性核と繊維輪をその設計に組み込むことにより、自然椎間板の解剖構造を模倣した唯一の人工頚椎 |
|
|
|
M 6-L人工腰椎間板 |
|
開発した新世代人工腰椎椎間板は、腰椎椎間板変性により損傷した間盤の代わりに使用することができる |
6
|
|
人工粘弾性核と線維輪をその設計に組み込むことで天然椎間板の解剖構造を模倣する(米国では提供されていない) |
|
|
|
火鳥/火鳥NXG脊柱固定システム |
|
後方腰椎融合術に埋め込まれた棒、横棒、モジュール化椎弓根ねじからなるシステム |
|
|
|
Forza XP Expanble Spacerシステム |
|
チタン膨張性スペーサーシステムは後路腰椎間融合術(PLIF)と経孔腰椎間融合術(TLIF)に用いられ,拡張後の腰椎を原位置で充填できる大きな移植片窓を有することが特徴である |
|
|
|
Forza PEEK/チタン複合材料(“PTC”)ガスケットシステム |
|
後路腰椎間帯3 D印刷の多孔質チタン終板は骨成長を促進でき、ポリエーテルエーテルケトン(PEEK)コアは画像特徴を維持することができる |
|
|
|
Forza Spacerシステム |
|
PLIFおよびTLIF手術におけるPEEK椎間装置の使用 |
|
|
|
フォーザTi Spacerシステム |
|
PLIF及びTLIF手術のための全3 D印刷チタン装置 |
|
|
|
百夫長枕後頚胸(POCT)システム |
|
チタン合金またはコバルトクロムからなる各種非無菌使い捨て部品からなる多成分システムであって、外科医が脊柱移植構造を構築することを可能にする |
|
|
|
フェニックス低侵襲脊柱内固定システム |
|
後路胸腰椎融合術のためのFirebird脊柱固定システムの多軸拡張復位ねじ体 |
|
|
|
Construx Mini PTC Spacerシステム |
|
頚椎前路椎間に3 D印刷した多孔質チタン終板を移植することは、骨成長とPEEKコアを促進し、画像特徴を維持することができる |
|
|
|
Construxミニチタンガスケットシステム |
|
全3 D印刷チタン質頚椎前路椎間隔壁システム |
|
|
|
Cetra頚椎前路鋼板システム |
|
頚椎前路鋼板システムは、直感的なロック機構を有する低輪郭鋼板、大きな植骨窓、高さのネジ角度、および簡略化された内固定を提供する |
|
|
|
Janusセンターライン固定ネジ |
|
火鳥脊柱固定システムの1つの補充は、従来の椎弓根スクリューと比較して、より多くの内側から外側軌跡までの皮質骨購入を実現し、外科医に正中線入路の選択を提供することを目的としている |
|
|
|
孤星首立 |
|
患者の解剖学的破壊を減少させ、解剖学的輪郭を維持しながら、伝統的または低侵襲な頚椎前路髄核摘出および融合術に生物力学的強度を提供することを目的とした独立したスペーサシステム |
|
|
|
ONE PIECE LL SA PTC PEEK間隔システム |
|
独立した前路腰椎間融合術(ALIF)であり、3 D印刷の多孔質チタン終板を用いて、骨成長とPEEKコアを促進し、画像特徴を維持することができる |
|
|
|
天鷹側方椎間融合システムと側板システム |
|
外科医師に1つの完全な解決方案を提供して腰椎側方椎体間融合術を実行し、これは1種の脊柱融合術であり、外科医師は患者側から手術入路を用いて椎間板隙間に入り、妨害の構造と組織は比較的に少ない |
|
|
|
火鳥SI |
|
骨齢成熟患者の仙腸関節断裂の固定のための低侵襲ねじシステム |
|
|
|
7
生物製品技術 |
|
|
|
|
|
Viuos Lyograft |
|
脊柱および整形手術のための、室温、すなわち使用可能、成形可能な形態で提供される、初の棚安定で完全な自己移植代替品 |
|
|
|
三位一体エリート |
|
脊柱融合または骨融合手順の成功を助けることを目的とした、手術において使用される、生細胞を有する完全に成形可能な同種移植片 |
|
|
|
光ファイバヒューズ高級 |
|
松質骨と脱灰皮質骨繊維の混合物からなり、血管再建、細胞成長及び新骨形成のための天然ステントを創出した同種異体骨 |
|
|
|
光ファイバヒューズストリップ |
|
鉱化した松質骨と脱灰した皮質線維からなるプレキャスト同種異体骨は,骨癒合に理想的な基質を提供する |
|
|
|
O-Genesis接ぎ木交付 |
|
無菌·使い捨ての形態で提供される骨移植送達システム |
|
|
|
OPUS MGセット |
|
欠損箇所でその場で硬化させる注射可能で成形可能かつ生体適合性の骨空洞充填剤 |
|
|
|
作品BA |
|
抗圧縮性、完全に吸収可能かつカスタマイズしやすい特徴を有する合成骨伝導ステントであって、一連の臨床応用に用いることができる合成骨伝導ステント |
|
|
|
伝統的な脱灰骨基質(“DBM”) |
|
すぐに使用可能で流動可能なDBMパテ |
骨成長療法−脊柱療法−
著者らは脊柱応用に用いられる骨成長治療設備は人体自身の手術後の自然癒合機序を刺激することによって骨成長を促進し、そしてある脊柱融合手術の成功率を高めることを目的としている。これらの非侵襲的携帯機器は,医師が処方した家庭治療計画の一部として利用することを目的としている。
われわれはSpinalSTimとCervicalSTim装置の2種類の脊柱融合治療装置を提供する。われわれの刺激製品はPEMF技術を用いて,術後骨組織の成長を促進し,癒合する部位の外部に置くことを目的としている。研究データによると、著者らのPEMFシグナルは鉱化を誘導し、脊柱融合部位で新たな再生過程を刺激する。一部の脊柱融合患者は融合部位の周囲で新しい骨の強固な融合を実現できないリスクは更に大きい。これらの患者は、一般に、喫煙、肥満または糖尿病などの1つまたは複数の危険因子を有し、または彼らの手術は、修復失敗の融合、または1回の手術で複数の椎体を融合させることに関連する。これらの患者に対して,術後骨成長治療は融合成功の可能性を著しく増加させることが証明されている。
SpinalSTim装置は1種の非侵襲性脊柱融合刺激システムであり、脊柱を治療するための腰部区域を設計した。この装置は、PEMF信号を生成するためにノウハウおよび波長を使用する。アメリカ食品と薬物管理局(FDA)はすでにSpinalSTimシステムを脊柱融合の補助設備として許可し、融合成功の可能性を増加させ、そして手術後少なくとも9ケ月として脊柱融合に失敗した非手術治療を救う。
我々のCervicalSTim製品は依然として市場で唯一のFDAが許可した骨成長刺激剤であり、頚椎融合手術の補助装置に指定されている。未融合のハイリスク患者に適しています
SpinalSTimとCervicalSTimシステムは,STIM OnTrackと呼ばれるモバイルデバイスアプリケーションを付加している.このモバイルアプリケーションは率先して発売された機能を含み、医師が患者の処方治療方案に対する遵守状況と患者報告の結果測定基準を遠隔で見ることができる。STIM OnTrackツールは、スマートフォンや他のモバイルデバイスと一緒に使用するために設計されており、患者が彼らの処方に従うのを助けることができ、毎日治療警告やデバイスがカレンダーを使用している。このアプリは無料で、Androidとアップルアプリで購入できます。
骨成長療法−整形外科療法−
われわれのPhysioSTim骨癒合療法製品に用いたPEMF技術は,われわれの脊椎刺激器で用いられている技術と類似している。主な違いは,PhysioSTim装置が添付ファイルの骨に使用するために設計されていることである。
骨の再生能力は多くの骨折を数ケ月以内に自然癒合させる。しかし、ある危険要素が存在する場合、いくつかの骨折は癒合できない或いは癒合が遅く、それによって“骨不連”を招く。伝統的に、整形外科医師は外科手術によるこのような骨不連状況を治療し、通常は骨折固定装置を持つ骨移植、例えば骨板、ねじ釘或いは
8
髄内棒。これらは“侵襲的”治療の例である。我々の特許PhysioSTim骨癒合療法製品は、低レベルのPEMF信号を使用して、身体の自然治癒過程を非侵襲的に活性化することを目的としている。これらの設備は解剖学的設計を経て、配置、患者の移動性、広範囲の治療区域をカバーする能力を容易にする。
われわれのSpinalSTimやCervicalSTimシステムと同様に,PhysioSTim装置はSTIM OnTrackモバイルアプリケーションを搭載しており,治療骨が患者につながっていない医師が処方治療案や患者報告結果の遵守状況を遠隔で確認·評価できるようにしている。
AccelSTim装置は骨不連癒合を改善し、指定された新鮮骨折の癒合を加速することができる安全かつ有効な非手術治療方法を提供する。この装置はLIPUS波により骨の自然癒合過程を刺激して骨折部に到達する。
脊柱インプラント−運動保護ソリューション−
著者らのM 6-C頚椎とM 6-L腰椎人工椎間板は脊柱退行性椎間板疾患を治療するための患者である。M 6椎間板は、設計に人工粘弾性核および線維輪を添加することによって、天然椎間板解剖学的構造を模倣するFDAによって承認された唯一の人工椎間板である。天然の椎間板のように、このような独特な構造は、移植レベルでの制振を可能にし、脊柱がその組み合わせの複雑な運動中に移行する時に制御可能な運動範囲を提供する。この2種類の頚椎椎間板はすべて欧州委員会CEマーカーの許可を得て、2019年2月、著者らはFDAの許可を得て、M 6-C人工頚椎は単節頚椎変性患者の治療に応用した。著者らは2019年に制御市場を通じてM 6-C人工頚椎を発表し、外科医に広範な訓練と教育課程を提供した。M 6-C椎間板はすでに著者らのリードする脊柱移植装置になり、ここ数年に著者らの成長に重大な貢献をした。また、M 6-C人工頚椎に対するアメリカ二級研究設備免除(“IDE”)研究を開始し、現在進行中である。
脊柱インプラント−脊柱固定解決策
著者らは広範なインプラントを提供し、主に頚部、胸と腰椎融合手術に用いられる。これらのインプラントは、金属から作られるか、PEEKと呼ばれる熱可塑性化合物から作られる。私たちが提供するほとんどのインプラントはチタン金属で作られている。火鳥脊柱固定システム、フェニックス低侵襲脊柱固定システムとCenturion POCTシステムは後方融合過程に移植された一連の棒、交差コネクタとねじである。Firebirdモジュール化と前装脊椎固定システムは開放型或いは低侵襲腰椎後路融合術に設計されている。我々の鋼板、棒とねじ固定オプションを補充するため、著者らはPillarとForza製品線の中で完全な頚椎と胸腰椎チタン合金とPEEK椎体間設備の組み合わせを提供した。著者らは最近、頚椎のConstrux Miniチタンと腰椎後路移植のためのForzaチタンの2種類の新しい3 D印刷椎間解決策を発売した。この胴体間製品の組み合わせは、2つの独立した装置LonestarとPillar SAと、Construx Mini PTCシステムとを含み、これは、現在市販されている他のプラズマスプレーオプションよりも良い選択を提供する新規なチタン複合ガスケットである。一般的ではないプログラムで使用される特製板材やネジも提供する。
生物製品−再生溶液
我々が販売している良質な生物組織には,Viguos Lyograftと三一エリート組織形式があり,骨中の固有増殖因子と生細胞を温存した皮質−松質同種移植である。それらは外科手術において筋肉骨格欠陥を治療し、骨再建と修復を行うために用いられる。これらの同種移植片は、自己移植片の収穫が追加の手術手順および修復手術に関連する患者の不快感のリスクを増加させることが証明されているので、実行可能な自己移植片プログラムの代替を提供することを意図している。Virtuos Lyograftの独特な点は、それは同類製品の中で初めて開発された、棚が安定した完全な自己骨移植代替品であり、室温、即ち使用し、成形可能な形式で脊柱と整形手術を提供できることである。
FiberFuse Advanced組織は、骨含有量に影響を与えることなく、利他的エリート製品と類似した処理特性を有する組織形態である。繊維技術を利用して、松質骨が提供する内向き成長の利点を有し、より広範な外科応用範囲を満たすために製品を拡張した先進的な脱鉱骨製品を提供した。FiberFuseストリップはFiberFuse Advancedの予備成形同種異体移植形式であり、鉱化松質骨と脱鉱の皮質繊維から構成され、骨癒合に理想的な基質を提供する。従来のDBM 1種の即時使用、流動可能な脱鉱骨泥であり、臨床体験に影響を与えることなく経済的に効率的な選択を提供した。
私たちはMTFと協力することで、Virtual os、三一エリート、FiberFuse Advanced、FiberFuse Bar、Legacy DBM、およびいくつかの他のティッシュのためのマーケティング費用を受け取ります。MTFは組織を処理し、在庫を維持し、そして病院、手術センターと他の看護場所に領収書を発行し、サービス料を受け取り、これらの費用は顧客が購入注文を通じて提出する。私たちはVicuosとリバースエリートティッシュを世界で独占販売する権利を持っており、米国でFiberFuse AdvancedとFiberFuse帯状ティッシュを販売する独占的な権利を持っている。
9
合成された生物の解決策に対して,Opus BAとOpus mg Setを提供する.OPUS BAは合成生物活性溶液であり、水和と柔軟性が容易である。厳選した3種類の成分は骨成長に理想的な環境を創造し、早期合成骨移植の基礎の上に創立した。OPUS MG SETは注射可能で成形可能で生体適合性のある骨空洞充填剤であり,欠損部で原位置で硬化する。
これまで、私たちの生物製品は主にアメリカ市場で提供されていましたが、一部の原因は他の国でアメリカ人体寄付組織の提供を制限しています。
世界の脊柱未来製品の応用
私たちは依然として、将来の新技術の商業化努力を支援するために、複数の内部開発を非常に積極的に行っている。これらの新技術は頚椎と胸腰椎解剖に同時に適用される。さらに、インプラント、生物学的製剤、および他の新興技術を我々の脊柱製品の組み合わせに添加するために、外部許可および買収機会を積極的に評価している。新たな内部開発技術と未確定な外部買収の貢献が将来の成長の主な駆動力になると予想している。
著者らの骨成長治療業務において、著者らは維克森林大学健康科学、香港中文大学とカリフォルニア大学サンフランシスコ校の研究に参与し、そこで、科学者たちは動物と細胞研究を行い、著者らのPEMFシグナルの骨、軟骨、半月板、神経と癒合効果に対する作用機序を確定した。これらの努力を通じて、いくつかの研究はすでに同業者評議の定期刊行物に発表された。その他の知見以外に、これらの研究は骨かさぶた形成と骨強度、半月板と神経損傷修復及び組織再生と癒合に参与する細胞の増殖と分化に対するPEMFの積極的な影響を示した。また,これまでクリーブランドクリニック,香港中文大学,ペンシルバニア大学との研究では,Orthofixの新たなPEMF波形の表現やプレゼンテーションが許可されており,様々な新たな応用や適応の信号最適化のための道が広がっていると信じている。このような臨床前データの収集,その他の臨床データは,われわれの再生刺激解決策の新たな臨床適応機会を代表している可能性がある。また,M 6−C人工頚椎に対する米国二次集積開発環境研究を開始した。
世界整形外科
全世界の整形外科報告部分は肢体奇形矯正と複雑な肢体再建の製品と解決策を提供し、重点的に創傷、小児科と足首手術における使用である。この報告部門は専門的に外部と内部固定矯正製品の設計、開発とマーケティングに従事し、これらの製品は結合してデジタル技術を完全な患者の治療経路にサービスできるようにした。私たちはグローバル流通業者と販売代表ネットワークを介して病院、ヘルスケア組織、ヘルスケア提供者にこれらの製品を販売します。
グローバル整形外科戦略
著者らの全世界整形外科報告領域における戦略は引き続き先駆的な肢体再建と奇形矯正プログラム解決方案を提供し、患者全体の治療経路を解決することである。
この細分化された市場における私たちの主な戦略は
10
世界の整形外科フォーカス製品
Global Orthopedicsは全面的な肢体再建と複雑な奇形矯正技術を提供する。著者らは革新と低侵襲の四肢解決方案を提供し、外科医師が患者の生活の質を高めることを助け、すべての年齢層の患者の生涯骨格と関節健康需要を満たすことを目的とした。そのほか、著者らの機能が完備した製品ラインは小児科、肢体再建、創傷と足首専門科に内固定と外固定解決方案を提供する。
私たちの骨折修復解決策は特定の解剖領域のために設計された各種の設備を含む。これらの装置の基本理念は十分な安定性を提供し、早期機能回復を許可し、それによって患者の生活の質を高めることである。我々の目標は,再現可能な結果を得るために,簡単で標準化された方法を実現できる装置を提供することである.
私たちの創傷製品は全面的な即時使用、無菌、各種の解剖部位のために設計されたインプラントキットを含む。
以下の表と議論は、商品名によって主要なGlobal Orthopedics製品を決定し、それらの主な応用を説明した
製品 |
|
主な応用 |
|
|
|
TrueLok |
|
外固定フレームは外科医が設計した軽量外固定システムであり、創傷、肢体延長と奇形矯正のために使用され、円形リングと患者の肢体を中心とする半円形外部支持からなり、交差、緊張した鋼線と半釘によって骨に固定されている |
|
|
|
TrueLok六足システム(“TL-HEX”) |
|
創傷と奇形矯正のための六足外固定システムとその関連ソフトウェアは,先に開発したTrueLokフレームワークを補完するための3次元骨セグメント再位置決めモジュールとして設計されている。このシステムは円形と半円形外部支持からなり,鋼線と半ピンで骨に固定され,6本の支柱で相互に接続され,外部支持の多平面調整が可能である。リングの位置は迅速に調整することができ、3次元空間において骨セグメントの再配置を行うために、正確な増分で徐々に調整することもできる |
|
|
|
TrueLok EVO |
|
手術中および術後看護において、医師が骨解剖をより良く評価することができるように、明確な放射可視化を実現するための放射透明リングおよび支柱を有するモジュール化円形外固定システム |
|
|
|
Fitbone髄内肢延長術 |
|
低侵襲手術によって骨に移植された大腿骨および脛骨の肢体延長のための髄内延長システムであって、伸張プロセスを管理する外部遠隔測定制御装置を含み、FDAによって許可された小児科適応を有する唯一の髄内肢体延長システムである、髄内延長システム |
|
|
|
小児科製品組合 |
|
私たちの小児科解決策には、小児科と骨折および奇形を有する若者に特化した一連の製品と資源が含まれている。私たちは患者の旅の360度の処理を通じて、治癒過程のすべての段階を治療するための専門的なツールを提供しました:側枝、教育ゲーム、ソフトウェアアプリケーション、術後管理のための患者アプリケーション
私たちの小児科解決策の組み合わせには 我々の弾性釘MJ-flexおよび青少年のための硬質髄内釘Agile Nailを含む、創傷および肢体再建のための完全な一連の釘システム −銀河固定小児科システム; |
11
|
|
−8ディスクガイド成長システム(“8ディスク”)および8ディスクガイド成長システム+(“8ディスクプラス”); -JuniOrtho電気めっきシステム |
|
|
|
Galaxy固定システム |
|
一時的および決定的な上肢および下肢骨折固定のためのロッドシステム。このシステムは、簡略化された治具の組み合わせを組み合わせ、レバーおよびレバーへのピンの接続能力を有し、肩、肘および手首のための特定の解剖学的ユニットを含む完全な応用範囲を提供する。最新バージョンのGalaxy Geminiには、手術プロセスをより良く簡略化するための汎用治具および他の更新が含まれています |
|
|
|
Galaxy肩固定 |
|
上腕骨近位部骨折治療のユニークな解決策 |
|
|
|
足首後足釘(“Ahn”) |
|
より大きな骨欠損とより複雑な後足病理を解決するための修復オプションを含む後足融合の差別化解決策 |
|
|
|
Gビーム融合収束システム |
|
このシステムは、足部と足首応用の末期奇形と創傷再建の特殊な需要を満たすことを目的としており、例えばCharcot、内側および/または外側柱融合、矯正性骨切り手術、および足中と後脚関節融合が必要である |
|
|
|
アカデミー賞 |
|
関節置換術を修復するための超音波動力手術システム |
|
|
|
外固定器 |
|
外固定は,われわれの肢延長システム,ProCallus,X Caliber,Pennig,放射線透過性手首固定器,踵骨固定器を含む |
|
|
|
8皿と8皿を加える |
|
1つ目は現在も市場をリードしている小児科患者の成長板の段階的矯正システムです |
|
|
|
LRS高度肢体再建システム |
|
骨かさぶたを使用して、単焦点延長および奇形矯正を含む様々な手順で骨を延長する肢体延長および奇形矯正のための外固定解決策であって、その多焦点プログラムは、骨輸送、異なる部位の同時圧縮および伸張、二焦点延長および矯正奇形の短縮を含む、外固定解決策 |
|
|
|
OrthoNextデジタルプラットフォーム |
|
JuniOrtho鋼板システムとFitbone髄内肢体延長システムのために開発したデジタルプラットフォームソフトウェアは、外科医が正確に奇形矯正と骨切り位置を計画でき、そしてインプラントと解剖関係を可視化できるようにした |
著者らは成人と児童に肢体修復と奇形矯正の内外固定解決策を提供した。私たちの骨折修復製品は骨折を安定させるための固定装置を含み、それが癒合するまで。これらの装置があれば,簡単で複雑な骨折パターンを治療し,奇形矯正を実現することができる。
外固定
外固定装置は骨折を固定するために用いられ、複雑骨折、関節付近骨折及び既知の危険因子或いは合併疾患を有する患者に理想的な治療方法を提供する。この治療は低侵襲であり,骨の外部操作を可能にし,最終的な骨アライメント(復位)を得て保持する。骨は癒合するまでこのように固定されている。外固定ステントは比較的に小さい程度の微動(動力化)を許可し、それによって骨折部位の血液流動を促進し、骨癒合過程を加速する。外固定フレームは,明確な治療前に骨折を安定させるために,複雑な創傷症例に一時的に使用することも可能である。これらの場合,迅速な骨折安定を提供することは,救命や保肢手術において重要である。
私たちが提供したほとんどの製品は無菌包装を採用しており、これは簡略化と即ち製品セットに対する需要、特にタイミングで重要な創傷応用に満足している。
我々の外固定装置には,TrueLok,TL−HEX,TrueLok Evo,Galaxy,Galaxy Gemini固定システム,LRS高度肢体再構成システムがある。
12
内固定
内固定装置は,一般に釘と呼ばれる長棒や骨にネジで固定された鋼板からなる。釘と鋼板には異なる大きさがあり,治療が必要な骨に依存する。人の腕や足(例えば,上腕骨,大腿骨または脛骨)を骨折した長骨の髄管に釘を挿入する。あるいは,鋼板をネジで手首,臀部や足骨折などに固定する。我々内の固定デバイスの例としては,Chimaera,Ahn,G-BEAM Fusion Beamingシステムがある.
2020年3月に買収したFITBONE髄内肢体延長システムは大腿骨と脛骨の肢体延長に内部選択を提供し、Orthofixに市場で最も完全な肢体再建製品の組み合わせを提供した。我々は引き続きFITBONE技術プラットフォームに投資し、外科医により多くの奇形矯正解決策を提供する。
骨折を治療する以外に、著者らは先天性骨格疾患を治療するための設備、例えば角度奇形(例えば児童の脚部屈曲)、退行性疾患と過去の創傷による疾患を設計、製造、流通している。この分野で提供される製品の一例は、八板プラス誘導成長システムである。
海刺
SeaSpineの業務の重点は脊柱疾患患者を設計、開発と商業化治療する手術解決方案である。著者らは全面的な生物製剤と脊柱移植物解決策の組み合わせ、及び手術ナビゲーションシステムを持ち、神経外科医と整形外科脊柱外科医が腰椎、胸椎と頚椎で融合手術を行うために必要な各種の製品の組み合わせを満たす。この広範な組み合わせは,これらの外科医の“完全な解決策”の要求を満たすために不可欠であると信じている。
SeaSpineは従来,(I)生物製品(従来Orthobiologicsと考えられていた)と(Ii)脊柱インプラントとイネーブル技術の2つの製品種別の収入を報告してきた。著者らのBiologics製品は一連の先進的と伝統的な骨移植代替品を含み、各種の整形外科手術後の骨融合率を高めることを目的とし、脊柱、寛骨部と四肢手術を含む。著者らの脊柱インプラントとイネーブル技術製品の組み合わせは一連の広範な製品と画像誘導手術解決方案を含み、退行性、低侵襲手術(“MIS”)と複雑な脊柱奇形手術中の脊柱融合を促進する。SeaSpineの生物科学と脊柱インプラント、ソフトウェアと先進光学製品開発における専門知識は外科医師の顧客に差別化された製品の組み合わせと完全な解決方案を提供し、患者の融合需要を満たすことができるようにした。
海刺戦略
SeaSpine事業における我々の目標は,生物製剤分野における我々の市場地位を向上させ,脊柱インプラントや画像誘導手術市場のリーダーとなるために,我々の業務規模を拡大し続けることである。私たちの目標を達成するために、私たちは以下の戦略に投資している
海嶺主力製品
SeaSpineは主に2つの主要な製品カテゴリによって代表され、i)生物製品とii)脊柱インプラントとエネルギー技術。以下、これらの製品カテゴリの各々についてさらに説明する
13
生物製品
我々のBiologics製品は整形外科や歯科手術に用いられ,広範な骨移植代替品からなり,骨再生の重要な要因を解決することを目的としている。骨移植代替物は天然生物蛋白と合成材料からなる。それらは脊柱融合手術に必要な自家骨移植の数を減少させることを目的としている。その設計により,骨移植代替品は患者自身の骨組織を完全に代替し,自己移植と呼ぶか,あるいは患者の骨移植材料と骨移植代替品を組み合わせることで体積を拡大することができる。我々のBiologics製品の組み合わせには,繊維と粒子に基づくDBM,コラーゲンセラミック基質,脱鉱同種松質骨,合成骨空洞充填物がある。一連の外科用途のための繊維、パテ、ペースト、ストリップ状、および吸収性メッシュのDBMを含む様々な形態の生物製品を提供する。
脊柱移植とエネルギー技術
著者らの脊柱インプラントとイネーブル技術製品の組み合わせは、脊柱減圧、整列、安定と画像誘導手術解決方案のための広範な製品シリーズを含み、脊柱全体の広いスペクトル使用のための手術ナビゲーションシステムを設計した。このような製品は通常腰椎、胸椎と頚椎領域の退行性、低侵襲と複雑な脊柱奇形手術の融合を促進するために用いられる。著者らの製品は矢状面(前から後まで)で十分な脊柱バランスと側貌を回復することにますます集中しており、著者らは脊柱変性或いは奇形手術患者の生活の質を改善する重要な要素であると信じている。
次の表と討論は商品名によって私たちのSeaSpineの主要製品を決定し、それらの主な応用を説明しました
製品 |
|
主な応用 |
|
|
|
生物製品 |
|
|
|
|
|
Accell骨基質 |
|
治癒早期に骨タンパク質のバイオアベイラビリティの低下を増加させる開放構造分散DBMであって、従来のDBMに結合したときに、繊維および粒子形態が、治癒を促進するために成長因子の2相放出を提供する、開放構造分散DBM |
|
|
|
OsteoStrand Plus/OsteoStrand |
|
100%脱灰骨繊維製品ラインは、改善された導電性マトリックスを提供しながら、最大化骨誘導含有量によって融合を促進および支援することを目的としており、OsteoStrand Plusは、我々の独自のAccell骨マトリックスと結合している |
|
|
|
Evo 3/Evo 3 c DBMパテ |
|
高度なDBMパテは,従来のDBMSをAccellと組み合わせ,動揺チップを使用または使用しない。 |
|
|
|
OsteoTorrent/OsteoTorrent C |
|
先進的なDBMパテは、Accell骨基質と顆粒DBMを結合し、松質チップを持っていると持たない;乾燥状態で包装と滅菌して、製品の骨誘導潜在力、賞味期限の安定性と賞味期限を高める |
|
|
|
メッシュ中の骨切りやバラストDBMを吸収できる |
|
DBM含有量を最大化しながら、移植片の配置を簡略化し、移植片の移動を防止することを目的とした担体を含まない100%DBMを含む吸収性メッシュ |
|
|
|
OsteoStruxとMozaik |
|
コラーゲンとβ−tCPを混合して骨再生を形成する骨伝導材料;パテとストライプ状の2種類の配置が選択可能である |
|
|
|
脊柱インプラントとエネルギー技術製品 |
||
|
|
|
Reef−to,Reef−TA,Reef−Th椎間装置 |
|
ナノ金属表面技術を用いたPEEK椎間装置、PLIFとTLIF手術に用いられる |
|
|
|
VU aPOD PRIMEナノ金属とサンゴ礁−A体間装置 |
|
ナノ金属表面技術を用いたPEEK椎間装置ALIF手術用 |
|
|
|
14
漕艇会ナノ金属側方システム |
|
側方アプローチで脊柱を融合することができる全面側方腰椎間システム |
|
|
|
カンブリア紀ナノ金属体間装置 |
|
頚椎前方融合のための椎間装置 |
|
|
|
海岸線頚椎前路独立システム、暗礁地形を持つナノ金属を特徴とする |
|
頚椎前方融合術における広範な解剖、手術状況、または骨を解決するために、手術中の柔軟性を最大化することを目的としたモジュール化鋼板および椎間装置 |
|
|
|
波形 |
|
頚椎前路、経椎間隙、腰椎外側及び関節突起間融合術における三次元印刷椎間融合器の応用 |
|
|
|
探索者から拡張可能な体間設備システムまで |
|
相補的な前方凸および平行拡張インプラントオプションを有する拡張可能な椎間装置システム |
|
|
|
Northstar OCT頚椎後方固定システム |
|
新型器械と解剖学的に設計したインプラントの脊柱固定システムを用いて、複雑な頚椎手術における手術の流れを改善することを目的とした安全かつ有効な解決策を提供する |
|
|
|
海軍大将頚椎前路鋼板システム(ACP) |
|
強度、輪郭と構造剛性の間の最適なバランスを達成することを目的とした全面的かつ完全な頚椎前方鋼板システム |
|
|
|
マリナー後方固定システム |
|
椎弓根ねじシステム、開放手術と管理情報システム手術と成人奇形手術に適し、モジュール化ねじ技術とセット器械を用いて、手術に必要なトレイの数を減少させ、外科医に様々な術中選択を提供し、腰椎後路固定を促進する |
|
|
|
新港管理情報システム |
|
小切開および経皮経路のための2つの棒搬送オプションを提供する小切開輪郭のための拡張フラップを有するMIシステム |
|
|
|
Mariner管理情報システム後方固定システム |
|
MISシステムは、ロッド導入と還元のための低輪郭、堅固なタワー、および超強靭なモジュール化拡張舌を有し、強力な器具圧縮と分散脊柱を提供することができる |
|
|
|
デトナ奇形システム |
|
複雑な脊柱奇形手術システム、複数のロッドオプションと直感的器具を有する拡張クリップ片面と多軸ネジを使用して、外科医の好みに適応可能な汎用システムを作成する |
|
|
|
デイトナ小サブシステム |
|
このシステムは解剖学的制限により低い輪郭構造を必要とする比較的小さい患者の標準から複雑な奇形症例を解決することを目的としている |
|
|
|
水夫脚修正システム |
|
以前の融合を効果的に修正し、延長することを目的としたMariner後方固定システムの添付ファイル |
|
|
|
7 D技術を用いたFlashナビゲーション(脊柱) |
|
開放式とマイクロ開放式脊柱後路手術のための機械視覚ナビゲーションプラットフォームは、独自の可視光技術と先進的なソフトウェアアルゴリズムを使用して、脊柱手術に迅速、高効率、コスト効果と無放射の解決策を提供する |
|
|
|
7 D技術を用いたFlashナビゲーション(経皮) |
|
Flashナビゲーションプラットフォームに対して価値のある増強を行い、経皮脊柱手術を解決した;カメラに基づく技術と7 D機械視覚アルゴリズムを結合し、脊柱プラットフォームと同じ迅速、正確かつ高効率な手術流れを維持し、同時に経皮脊柱後路手術に画像と関係のない解決方案を提供した |
|
|
|
7 D技術を用いたFlashナビゲーション(首) |
|
7 D機械視覚技術を利用して頭蓋骨手術を行うFlashナビゲーションプラットフォーム上のモジュール;可視光技術は完全に非接触ワークフローを可能にし、患者自身の解剖構造を使用して数十万個の仮想基準を取得し、ほぼ任意の手術位置でほぼ即時の頭蓋骨皮膚または頭骨位置合わせを生成することを可能にする |
15
技術を発揮する
著者らの機械視覚フラッシュナビゲーションプラットフォームは各種の脊柱後路手術に応用され、変性、奇形、腫瘍、創傷と改修手術を含む。このプラットフォームは、情報システム/経皮技術、マイクロ開放技術、または開放技術を管理するために使用することができる。この技術はまた脳神経外科に全面的な脳プラットフォームを提供した。
我々は7 D技術を採用した革新的なフラッシュナビゲーションシステムは可視光、機械視覚カメラと知能ソフトウェアアルゴリズムを利用して数秒以内に3 D画像を作成し、手術ナビゲーションに使用する全面的なナビゲーションプラットフォームを提供した。この斬新な技術は外科医の仕事の流れを中断することなく、外科ナビゲーションに迅速な画像再構築を提供し、手術中の患者、外科医と手術室スタッフへの放射線暴露を除去することができる。
私たちの脊柱モジュールはフラッシュメモリナビゲーション製品の組み合わせでリードしており、世界で104個以上のインストールを持っています。2022年、著者らは更に脊柱モジュールを強化し、事前計画機能を増加し、そしてハードウェアとソフトウェアの増強を通じてMariner後路固定システム、Mariner MIS後路固定システムとNorthstar OCT頚椎後路固定システムを完全にプラットフォームに統合した。私たちはまた2022年に私たちの商業Flash経皮脊柱モジュールを発表し、低侵襲脊柱手術をナビゲーションした。この応用は新しい機器と結合し、脊柱ナビゲーション市場の重要な構成部分を解決し、Flashナビゲーションプラットフォームを完備し、病院と外来手術センターにとって貴重な改善である。脊柱モジュールと経皮モジュールのさらなる増強と新機能が開発されており,2023年に発売される予定である。
脊柱に集中したこれらの新製品に加えて、フラッシュメモリナビゲーション製品の組み合わせには、頭蓋骨手術のための頭蓋骨モジュールも含まれている。この技術は1種の完全非接触式のワークフローを使用し、患者自身の解剖構造を用いて数十万個の仮想基準を獲得し、ほとんど任意の手術姿勢で瞬時に皮膚或いは頭骨に頭蓋骨登録を行うことができる。新しい開発も進行中であり、2023年に発売される予定であり、7 D技術を利用して更に脳応用を拡大し、神経危篤看護市場に入り、フラッシュEVD(“屋外ドレナージ”)を発売し、これは1種の移動ベッドサイドナビゲーションシステムであり、迅速かつ確実にEVDを置くことを目的としている。
SeaSpine未来製品の応用と開発
私たちの未来の成功と収入増加を推進し続ける能力は、私たちが過去数年に示したように、似たようなリズムを維持し、新しいものと次の世代の製品を発売できるかどうかにかかっていると信じている。私たちは引き続き差別化された新製品を積極的に開発して、これらの製品は私たちが新しい市場に入ることができ、私たちが不足している市場を代表する上でもっと競争力を持つことができると信じています。
我々は次世代フラッシュ経皮モジュールとフラッシュメモリ脊柱モジュールを発売し,我々の事前計画ソフトウェアを追加的に増強し,椎間プログラムをナビゲートする枠組みを開発する予定である。著者らはまたFlash EVDを発売する予定であり、これは小型移動ベッドサイドナビゲーションシステムであり、迅速かつ確実にEVDを置き、初めて神経危篤看護市場に入ることによって、著者らの総目標市場を拡大することを目的としている。
製品開発
私たちの主な研究開発機関はテキサス州のルイビル、カリフォルニア州のカールスバッド、カナダのトロントとイタリアのヴェローナにあります。
私たちは研究開発機構を持っていて、製品開発と臨床事務計画を通じて私たちの脊柱インプラント、生物製剤、整形インプラントと外固定デバイス及び機械視覚画像誘導革新製品の組み合わせを推進することに取り組んでいる。私たちの製品開発は、外科医、私たちのエンジニア、私たちのメカニック、そして私たちの監督者の間の協力を含む統合されたチーム方法を採用しています。著者らはまた、有力な病院研究機関とある非営利組織(例えばMTF Biologics、外科医とその他の顧問)と協力し、著者らの製品と治療法に対して長期的な科学計画と変化を行った。私たちが販売しているいくつかの製品はこれらの協力によって開発されました。また、私たちは定期的に科学と医学界から新製品や製品の改善の提案を受けており、その中のいくつかの提案は私たちが医師や第三者と譲渡または許可協定を締結した。
私たちの脊柱と整形外科製品について、私たちの製品開発チームは設計外科医と協議して、製品設計を制定し、その後、私たちの機械師はプロトタイプを製造して、私たちの施設で私たちのプロトタイプ開発とテスト操作をテストします。我々は広範な技術を用いて,顧客の複雑な工程要求を満たすことができるようにした.開発過程の一部として、外科医の私たち内部の身体実験室試験製品の移植は、外科医と患者のニーズを満たすための新製品の設計に役立ちます。我々のチームは,製品テストの結果に応じて必要に応じてプロトタイプを改良または再設計し,設計-プロトタイプ-テスト開発サイクルの高速な反復を実行することを可能にした.私たちの臨床と監督者は私たちの製品工学者と並行して仕事をして、
16
私たちの製品の規制許可。これらの製品開発は,外科医の顧客とその患者のニーズに応じた解決策を提供できると信じている。
脊柱と整形外科製品開発の流れと同様に、私たちのソフトウェアエンジニア、製品マネージャー、設計外科医は私たちの脊柱インプラントと生物製剤製品ラインを私たちの機械視覚フラッシュナビゲーションシステムと完全に統合しようと努力している。これには、退行性、複雑性、改訂性と脊柱奇形プログラムを含む各種プログラムの需要を満たすために、特定のソフトウェアモジュール、機能と追跡機器を設計することが含まれる。また,7 D技術を様々な成人や小児科整形外科応用に統合する機会を模索している。
生物製品に対して、著者らは私たちの革新的な生物製品技術のために生産ラインを開発し、脊柱領域と一般整形外科応用における特定のプログラムの要求を満たすと同時に、引き続き骨形成潜在力を高める予定である。我々は従来のDBMとセラミック基材製品種別の新製品配合を研究している。我々の生物製品研究開発チームは生物材料科学と次世代技術を市場に出す上で豊富な経験を持っている。
2022年、2021年、2020年、私たちの研究開発支出はそれぞれ4910万ドル、4960万ドル、3910万ドルです。
特許、商業秘密、譲渡、許可証
私たちは特許、商業秘密、譲渡および許可協定、および秘密保護協定の組み合わせによって私たちの独自の知的財産権を保護します。我々は大量の米国と外国特許を有し,多くの未決特許出願を有し,第三者が保有する特許の許可権を持っている。私たちの主要製品はその販売されている主要市場で特許を取得しました。私たちはどの特許の期限が私たちの知的財産権状況に大きな影響を及ぼす可能性があるとは思わない。医療機器業界の特徴は特許数が多く,特許侵害告発訴訟が頻繁であることである。特許訴訟は複雑な事実と法的問題に関連する可能性があり、その結果は不確実だ。私たちの成功は私たちの競争相手と潜在的な競争相手を含む他人の特許を侵害しないことにある程度かかっている。私たちは私たちの製品が他の側の特許と独占権を侵害しないように最善を尽くしていますが、私たちの製品と方法は私たちの競争相手が持っている特許によってカバーされるかもしれません。これらのリスクのさらなる検討については、本年度報告“リスク要因”というタイトルの項目1 Aを参照されたい
私たちは、従業員、コンサルタント、他の当事者と締結された秘密と秘密協定に依存して、商業秘密やその他のノウハウをある程度保護しています。
私たちのいくつかの製品について、私たちは第三者から異なる期限の譲渡または許可を得ます。私たちは通常、このような譲渡によって権利を得ることができるかもしれません。一括払いまたはライセンス者に売上高の一定の割合を支払う手配と交換することができます。しかし、私たちへの譲渡は一般的に撤回できないかもしれないが、このような計画が私たちが受け入れられる条項で提供され続けることを保証することはできないし、根本的にはできない。私たちの許可と譲渡協定の条項の長さは様々で、指定された年限から製品特許の有効期限あるいは製品の経済寿命まで様々です。これらの協定は,一般に重大な違約が発生した場合に特許権使用料と停止権を支払うことを規定している.
コンプライアンスと道徳的計画
私たちの基本方針は最高の道徳と法律基準に従って業務を展開することです。私たちは、私たちのCEOと取締役会コンプライアンス委員会に直接報告する包括的なコンプライアンスと道徳的計画を持っています。この計画の目的は、私たちの国内と国際業務において合法的で道徳的なビジネス実践を促進することである。その目的は、米司法省(“米司法省”(“企業コンプライアンス計画評価”(2020年6月更新))、監察長事務室(HCCA-OIG“コンプライアンス計画の有効性を測定する:資源ガイド”)および米国量刑委員会(“有効コンプライアンス·道徳計画”(2014年11月))に規定されている基準に基づいて、適用される連邦、州、現地の法律に違反する行為を防止·発見することである。この計画の主な内容は次の通りです
17
政府の監督管理
FDAと他の規制機関による製品の分類と承認
私たちの研究、開発と臨床プロジェクト、そして私たちの製造とマーケティング業務は、アメリカと他の国の広範な規制を受けています。最も注目すべきは、私たちがアメリカで販売しているすべての製品は、FDAによって施行され、施行された連邦食品、薬物、化粧品法案(FDCA)、公衆衛生サービス法によって制限されていることだ。私たちの製品と施設をカバーする規制は国によって違う。規制当局の承認や許可を得るのに要する時間も国によって異なる。
適用免除が適用されない限り、私たちが米国で商業流通する各医療機器は、販売前通知(“510(K))許可、届出、承認販売前承認申請(”PMA“)またはFDAのいくつかの他の承認によってカバーされる。FDAは医療機器を3つのカテゴリの1つに分類しており,この3つのカテゴリは通常FDAが承認すべきタイプを決定している。リスクが低いと考えられるデバイスはクラスIに分類され、中リスクを構成すると考えられるデバイスはクラスIIに分類され、最大リスクを構成すると考えられるデバイスはクラスIIIに分類され、これらのデバイスは、合理的な安全性および有効性保証を提供するためにより多くの規制制御を必要とするか、または510(K)の許可を得ていたデバイスとは異なると考えられるデバイス(以下に述べる)がクラスIIIに分類される。私たちの脊柱インプラントおよびグローバル整形外科製品は、多くの場合、私たちの7 DフラッシュナビゲーションシステムはクラスIIに分類され、そのいくつかの添付ファイルはクラスIに分類されています。私たちの骨成長療法製品とM 6-C人工頚椎は現在クラスIIIに分類され、PMAプロセスを介してアメリカでの商業流通が許可されています。しかしながら、FDAの専門家グループは、FDAが骨成長刺激デバイスをクラスIIIデバイスからクラスIIデバイスに再分類し、特別な制御を行うことを提案している。この事態の更なる検討については,本年度報告“リスク要因”という見出しの項目1 Aを参照されたい
私たちが開発、製造、流通、販売している医療機器はFDAと多くの他の連邦、州と外国政府機関によって厳格に規制されている。FDA承認および他の規制承認を得て医療機器を開発·販売するプロセス、特にFDAから承認されるプロセスは、高価で時間がかかる可能性があり、そのような承認が直ちに承認されるかどうかは保証されない。我々の製品の製造·販売はすべての必要な許可と承認を得ており、これらの製品は適用されるFDAや他の重要な規制要件に実質的に適合していると信じているが、これらの要求を遵守し続けることができる保証はない。
2017年、欧州連合(“EU”)EU医療機器条例(“MDR”(理事会条例2017/745)を採択し、その中で医療機器のマーケティングと販売に対して厳格な要求を提出し、新しい品質システムと発売後の監督要求を含む。この法規は2023年3月に改正され,2021年5月までに承認されたすべての医療機器(欧州医療機器指令による)に追加的な要求を満たすための過渡期が提供され,ある機器については2027年12月に延長され,高リスク機器については2028年12月,中低リスク機器については延長された。この過渡期の後,EUで販売されているすべての医療機器は,これらの新たな要求に応じて認証を行う必要がある。この規定は私たちが追加的な要求に対する遵守を維持するために、過渡期とこれからも巨額の費用を負担することを要求する。規制の要求を満たすことができなければ,EUや他のEUが医療機器登録を要求している国の業務を利用したり依存したりすることに悪影響を及ぼす可能性がある。
EUでは,我々の製品はMDRで定義された医療機器ではなく,脱灰骨材料を含むヒト由来の組織を含んでいる。欧州議会やEU理事会2001/83/EC指令で定義されている医療製品でもありません。今日、EUが人間由来組織を含む製品を管理する法規(適用すれば)はEU加盟国によって異なります。統一的な監督管理枠組みとEUの先進治療薬物に対する提案的な監督管理が不足しているため、EUのヒト由来細胞或いは組織に基づく医療製品の審査過程は広く、長く、高価で予測できない可能性がある。
ある国とEUは動物原料を含む製品を規制する規制を発表した。規制当局は特に牛海綿状脳症(BSE)を引き起こす病原体に感染した材料に注目している。これらの規定は脊柱用の生体材料製品に影響を与えます。これらの製品には牛から抽出された材料が含まれています
18
組織します。我々の製品が安全であり、原因となる可能性のある物質が含まれていないことを保証する措置を取っているにもかかわらず、私たちの製品を含む動物原料を含む製品は、プリオンウイルスが伝播する可能性があることが懸念されているため、追加的な規制を受ける可能性があり、さらには特定の国でも禁止される可能性がある。重大な新しい法規、私たちの製品に対する禁止、あるいは狂牛病の爆発のために牛原性製品の使用を停止することは、私たちの業務または私たちの業務拡大能力に実質的な悪影響を及ぼす可能性がある。“リスク要因-法律法規を守らないことに関連するリスク-私たちのいくつかの製品には動物由来の物質が含まれており、追加的な規制を受ける可能性がある”と見られる
我々のBiologics製品カテゴリでは,骨修復と再建のための組織を販売しており,ブランド名は三一エリートであり,我々の同種骨基質は生存可能な細胞を含む松質骨と脱鉱皮質骨成分からなる。また、著者らはFiberFuseというブランド名の脱鉱皮質繊維技術、脊柱融合のための構造的同種異体移植片と羊膜を提供し、羊膜は天然の組織バリアである。これらの同種移植片はFDAのヒト細胞、組織および細胞と組織ベースの製品(“HCT/P”)によって規制されており、医療設備、生物或いは薬物としてではない。これらの組織はFDAによって最も少ない操作の組織として管理され、FDAの“良好な組織実践”法規によって保護され、この法規は同種異体移植過程のすべての段階をカバーしている。私たちのサプライヤーが適用される規制要件を満たし続ける保証はなく、これらの要件が私たちの業務に悪影響を及ぼす可能性のある方法で変化しない保証もありません。また、これらの製品が引き続き私たちに提供される保証はなく、適用される規制基準が満たされているか、あるいは変わらないという保証もない。さらに、人体組織や骨格由来の製品は、ある行政的または安全な理由で時々リコールされ、1回または複数回のこのようなリコールの影響を受ける可能性がある。
我々の同種移植片解決策(HCT/Ps)に加えて,人工合成され,FDAによって医療機器として規制されている他の生物製剤製品も販売·流通されており,特にOpus BAとOpus MG合成移植片シリーズである。FDAによって規制されている補助技術も提供し,医療設備として臨床で我々の骨移植選択を提供することを支援している。これらの製品は第三者メーカーから来て、第三者メーカーは製品の供給中断を避けるために十分な在庫を維持していると信じています。
ヒト組織(脱灰骨組織)から抽出した製品も生産している。国内で生産されたHCT/PはFDCAによって規制されている生物製品、医療機器或いは薬物の定義に属する可能性がある。これらの生物、器械または薬物HCT/Pは、発売前の承認またはFDAの承認を含む、HCT/Pに特化した要求および生物製品、器械または薬物に適した要求に適合しなければならない。
公衆衛生サービス法第361条は、伝染病の導入、伝播又は伝播を防止するためにFDAに法規を発行することを許可する。361個のHCT/Pとして規制されているHCT/Pは、FDAに施設を登録し、製品、組織ドナー資格のスクリーニングとテスト、加工、貯蔵、ラベル、およびHCT/Pを配布する際の良好な組織実践、必要なラベル情報、厳格な記録保存、および有害事象報告を含む製品、組織ドナー資格のスクリーニングとテスト、加工、貯蔵、ラベル、および配布時の良好な組織実践に制約されている。
アメリカティッシュ銀行協会(AATB)はすでにティッシュ銀行の操作基準を発表した。認証は自発的であるが,これらの基準を遵守することはAATB認証となる組織機関の要求である.しかも、アメリカのいくつかの州にも独自の組織銀行規制がある。私たちはカリフォルニア州、フロリダ州、ニューヨーク州、メリーランド州、その他の特定の許可または登録が必要な州でAATB認証と許可を取得し、あるいは組織銀行業務許可証を持っています。
ある人体器官および組織を購入して移植に使用することは、皮膚および関連組織を含む価値のある人体器官の譲渡を禁止する“国家臓器移植法”(NOTA)の制限を受けるが、人体組織および皮膚の除去、輸送、インプラント、加工、保存、品質管理および貯蔵に関連する合理的な費用の支払いを許可する。私たちはそれらを回収、貯蔵、輸送して私たちに提供してくれた寄付人体組織に関する費用を組織銀行に精算する。我々の価格構造には、組織の加工、保存、品質管理および貯蔵に関連するいくつかのコスト、マーケティングおよび医学教育費用、および組織加工技術の開発に関連するコストに加えて、組織回収および輸送に関連する費用を補償するために組織銀行に支払う金額が含まれている。Nota Payment手当は、製品定価で回収可能なコストと費用を制限し、将来の収入と収益力を減少させるために解釈されるかもしれません。
上記事項に関連するいくつかのリスクのさらなる説明については、本年度報告“リスク要因”というタイトルの項目1 Aを参照されたい
他の製品や製造法規は
設備が市場に投入された後、多くの規制要求が引き続き適用される。これらの規制要件は、製品の発売と登録、品質システム法規(QSR)、製造過程のすべての面で厳格な設計、テスト、制御、文書、および他の品質保証手続きに従うようにメーカーに要求する第三者製造業者を含み、ラベル法規と政府は製品の普及を禁止している
19
未承認、未承認またはラベル外の用途または適応;承認が安全性または有効性に著しく影響する可能性があり、または我々が承認したデバイスのうちの1つの予期される用途に重大な変化を構成する製品修正;我々PMAが承認したデバイスのうちの1つの安全性または有効性に影響を与える製品修正を承認すること;医療デバイス有害事象報告条例は、そのデバイスが死亡または深刻なダメージをもたらす可能性がある場合、FDAおよび他の外国政府機関に報告すること、またはデバイスまたは同様のデバイスの故障が再び発生した場合、死亡または深刻なダメージの障害を引き起こす可能性があることを製造業者に要求する。承認後の研究承諾を含む承認後の制限または条件;公衆の健康を保護するために、または装置のための追加の安全および有効性データを提供するために必要に応じて適用される上場後監督法規;FDAのリコール権限は、この権力に基づいて、特定の条件下で、管理法律および法規に違反した製品を市場から回収するようにデバイス製造業者に命令することができ、自発的なリコールに関連する規定、および通知を修正または除去することができる。
私たちと私たちのいくつかのサプライヤーはまた、FDAのQSRおよび他の国際法規を遵守するかどうかを決定するために、FDAと欧州通知機関の発表と抜き打ち検査を受けた。FDAが私たちまたは私たちのいくつかのサプライヤーが適用された法規に準拠していないことを発見した場合、その機関は、公開警告状からより厳しい制裁まで、例えば、私たち、私たちの官僚、私たちの従業員、または私たちのサプライヤーに罰金と民事処罰を科すことができます。私たちの製品の整理または承認の遅延または拒否;FDAまたは他の規制機関が、私たちの製品または私たちの第三者サプライヤーを承認した製品の撤回または一時停止、製品のリコールまたは差し押さえ、生産中断、経営制限、禁止、および刑事起訴です。FDAの検査を除いて,我々のすべての製造施設は年次通知機関の検査を受けなければならない。
また,米国以外の政府当局も医療機器の規制が厳しくなってきている。私たちの製品は将来アメリカの非政府機関によってもっと厳しく規制されるかもしれません。追加的な規制は、米国でも国際的にも、私たちの業務や運営に実質的な悪影響を及ぼす可能性がある。上記規制要件に関連するいくつかのリスクの説明については、本年度報告書の“リスク要因”というタイトルの第1 A項を参照されたい
認証要求
我々の子会社Orthofix US LLCはすでに医療保健認証委員会(“ACHC”)の認可を受け,耐久医療機器,義足,装具と用品(“DMEPOS”)に関する医療供給プロバイダサービスを提供している。ACHCは民間非営利企業であり、すでにISO 9001:2000標準認証を通過し、家庭看護とコミュニティサービス提供者によって開発され、会社の業務運営と患者看護の質の改善を助けることを目的としている。認証は通常1つの自発的な活動であり、即ち医療保健組織はその内部政策、プロセスと患者看護サービスを国家標準に符合するために同業者に提出し、国家標準に符合するが、連邦医療保険と医療補助サービスセンター(CMS)はDMEPOSサプライヤーに認証を要求する。認証を得ることにより,Orthofix US LLCは,より高いレベルの能力を維持するために努力していることを示しており,その製品,サービス,顧客満足度の面で優れたものを目指したいと信じている。
第三者支払人要求
私たちの製品は、Medicare、Medicaid、およびTricare、または個人保険計画および医療ネットワークを含む政府計画のような第三者支払者によって精算される可能性があります。第三者支払者が、患者に提供される装置やプログラムで使用される装置が適用される支払基準を満たしていないと判断した場合、または保険加入者の医療保険給付が限られている場合には、精算を拒否することができる。また,非政府第三者決済者は,医療の必要性や我々の製品やサービスのための価格に挑戦することが多くなってきている。連邦医療保険計画は,その競争的入札計画を実施することにより,あるDMEPOSプロジェクトに対して新たな支払いメカニズムを継続して実施する予定である。骨成長治療設備は現在この競争的入札過程を免除している。
医療詐欺と濫用を規制する法律
私たちの販売およびマーケティング行為はまた、連邦反リベート法規や連邦医師自己推薦法(“スタック法”と呼ばれる)、民事虚偽請求法案と1996年の健康保険携行性と責任法案(“HIPAA”)など、複数の医療詐欺や乱用行為を規制する米国の法律によって制約されており、医療保健と保険を規制する多くの州法律である。これらの法律は米国衛生·公衆サービス部(HHS)内の監察長事務室、米国司法省、その他の連邦、州、地方機関によって執行されている。他の事項に加えて、これらの法律および他の法律は、一般に(I)患者の紹介または購入、注文または推薦の代わりに、連邦医療計画(MedicareおよびMedicaidを含む)によって精算された任意の項目またはサービスを提供することを禁止し、(Ii)連邦医療計画に提出された支払い申請は真実でなければならないことを要求し、(Iii)その情報を受信する権利のない人への保護された医療情報の送信を禁止し、(Iv)特定の政府許可および許可を維持することを要求する。
20
健康情報の機密性を守る法律
米国連邦および州法律は、特定の健康情報の機密性、特に医療記録などの個別に識別可能な情報を保護し、保護された情報の使用および開示を制限している。連邦レベルで、衛生と公衆サービス部はHIPAAに基づいて健康情報プライバシーと安全規則を公布した。これらの規則は、研究およびその他の目的のための衛生情報の使用と開示を管理することによって衛生情報を保護する。HIPAA“保証実体”は、HIPAAのこのような“保護された健康情報”に関する規定を遵守できず、連邦法律に違反し、民事と刑事罰を受ける可能性がある。カバーされたエンティティは、私たちのように、クレームを健康計画に送信することを含む、特定の電子取引に従事するヘルスケアプロバイダ(いくつかの販売デバイスまたはデバイスのプロバイダを含む)を含む。したがって、我々がアクセス、収集、分析、および他の方法で使用および/または開示する健康情報は、HIPAAによって制限された保護された健康情報を含む。上述したように、多くの州の法律はまた健康情報のセキュリティを扱っている。このような法律はHIPAAに先制されるとは限らず,特にHIPAAよりもプライバシー保護を大きく与える州法である.これらの州の法律は通常、健康情報に影響を与える不正行為に適用できる独自の罰則条項を持っている。
EU内では、“一般保障資料規則”(以下、“一般保障資料規則”と呼ぶ)には複数の規定が含まれており、その中には、資料当事者と監督当局が資料規定違反を発見した場合が含まれており、資料当事者と監督当局に直ちに通知し、規定違反者に巨額の罰金を科しなければならない場合がある。国際的には、一部の国はまた、現地サーバ上にその市民の個人識別データを保存し、これらのデータの送信または処理を制限することを要求する法律を採択している。
これらの法律と法規は、私たちが個人データ、保護された健康情報、そして私たちの情報技術システムを使用して管理する方式に影響を及ぼす。それらはまた私たちが地理的境界を越えて移動し、保存し、データにアクセスする能力に影響を及ぼすだろう。これらの要求を遵守するためには、業務慣行を変更し、私たちの運営を複雑化させ、複雑性と追加的な管理と監督需要を増加させる必要があるかもしれません。これらはまた,我々の臨床研究活動や臨床データ転送や使用に関連する製品供給を複雑化させる可能性がある。
“平価医療法案”の医師料金陽光条項
“平価医療法案”(第6002節)(“陽光法案”)の医師支払陽光条項は、贈り物や飲食などの実物移転価値を含む医師および教育病院に支払う費用を米国政府に公開開示することを要求する。サンシャイン法案はまた、規定を守らないことに対する処罰を規定している。サンシャイン法案は3月31日に年次報告書を提出することを要求していますST前の年に起こった価値移転のカレンダー年。
2018年には,“患者とコミュニティオピオイドの回復と治療を促進する物質使用−疾患予防法案”(“支援法案”)が法律に署名された。“支援法案”は、医師アシスタント、勤務看護師、臨床看護師専門家、登録看護師麻酔科医および登録助産師への支払いおよび他の価値移転を含む“陽光法案”に規定された報告義務を拡大する。これらの拡大した報告義務は2022年報告書の支払いに有効であり,2021年から追跡支払いを開始する。“陽光法案”または“支持法案”に違反した行為は民事罰金を受けるだろう。
法案拡大を支援する陽光法案のほか、マサチューセッツ州やバーモント州の透明性法律など、他の国際的かつ個別州の透明性法律の遵守を求めている。
販売、マーケティング、流通
私たちは直売代表、販売代理、流通業者からなる広範な販売ネットワークを持っている。この構築された販売ネットワークは、新製品を紹介し、既存製品の販売を拡大するプラットフォームを提供してくれる。私たちの製品は世界約68カ国·地域に販売されている。
市場と製品種別の細分化を報告する
歴史的には,Orthofixは2つの報告部門−Global SpineとGlobal Orthopedicsで業務を管理しており,この2部門はそれぞれ2022年の総純売上高の77%と23%を占めている。これに対し,SeaSpineは従来,その業務を1つの運営部門として管理してきたが,報告された収入は,(I)生物製剤(従来Orthobiologicsと呼ばれていた)と(Ii)脊柱インプラントとイネーブル技術の2つの製品種別に分類されてきた。SeaSpineとの合併が2023年1月5日に完了した後、私たちは
21
2023年第1四半期に新合併会社の運営管理方式に基づいて我々の報告部門を再評価する予定です。
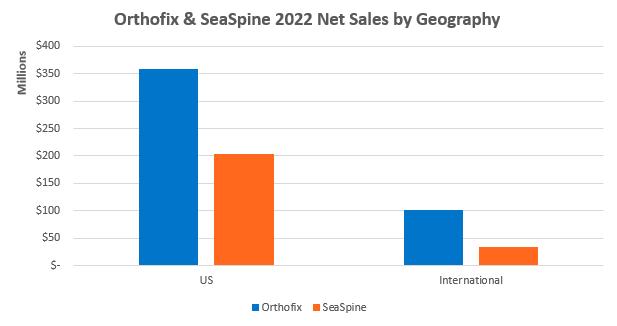
販売ネットワーク
私たちのアメリカでの販売ネットワークは通常直売代表と独立流通業者で構成されています。具体的には各製品の種類に依存します。このような独立流通業者たちは一つ以上の製品カテゴリーの製品を販売するようになっている。著者らの骨成長療法製品分類は直接販売代表と独立流通業者からなる混合流通ネットワークの支持を大きく得ているが、著者らの脊柱インプラント、生物製品と整形外科販売組織は主に地域と地区の業務マネージャーから構成され、彼らは独立流通業者と販売エージェントからなる広範なネットワークを監督することを担当している。
私たちは、アメリカの直販チームで私たちのEnabling Technologies製品の組み合わせをマーケティングすることによって、私たちの独立販売エージェントと協力して、資本の効率的な方法で資本販売を実現するか、またはシステムおよびコンポーネントをアカウントに入れて、私たちの脊椎および/またはバイオ製品製品の長期収入約束と交換します。
米国では、我々は通常、私たちの生物製品および脊柱インプラントおよび整形外科インプラントアセンブリを病院および独立販売エージェントに委託または貸与し、その後、病院および独立販売エージェントによって病院に渡されて外科手術を行うか、または大量ユーザーの病院に残して複数の手術のために使用する。これらのデバイスは、一般に、使い捨てデバイスおよびインプラントを含む手術を完了するために必要なデバイスを含む。
私たちは成長の潜在力の大きい地域で流通関係を作ることに集中しています。これらの地域では、私たちのパートナーは私たちの製品を独占的に提供しますが、私たちの製品は臨床市場に向けられていません。長期的に見れば、これらのより排他的な協力関係は、私たちがこれらの地域でより速く、より費用対効果的な成長を達成できると信じている。私たちはまた、私たちの独立した販売エージェントの足跡の拡大を支援するために、より多くの機器設備やマーケティングや教育に投資し続ける予定です。
アメリカ以外では、私たちはある市場で直売代表を雇用し、独立した在庫流通業者と契約を結び、彼らは私たちから直接私たちの製品を購入し、独立して販売します。私たちの独立販売ネットワークを支援するために、販売と製品の専門家がいて、彼らは定期的に独立販売業者に訪問し、訓練と製品支援を提供しています。
マーケティングと製品教育
私たちは主に医者、病院、外来手術センター、統合医療サービスシステムと他の調達組織にマーケティングと販売しています。
著者らはAdvaMed道徳基準(“AdvaMed基準”)とMedTechヨーロッパ道徳商業実践準則(“MedTech準則”)に符合する医師と販売専門家のための全面的かつ専門的な訓練シンポジウムを開催することを通じて、私たちの販売チームと販売拡張努力を支持した。我々は定期的に複数の場所で多言語教育シンポジウムを開催しており,仮想的に行うことも可能である.そのため,テキサス州ルイビル,カリフォルニア州カールスバッド,ペンシルベニア州ウェインに位置する実体操身体訓練実験室の能力を利用して,外科医や販売代理の訓練機会を増加させた。私たちはまたイタリアのヴェローナとラテンアメリカの違う場所で対面訓練を行った。研修と教育は外科医が私たちの製品と技術を熟知し、患者の予後を改善するのに役立つと信じている。近年,これらの対面や仮想製品教育シンポジウムには,世界各地から数千人の外科医が参加しており,専門家からの様々な講座やプレゼンテーションやワークショップが含まれている。
22
私たちはまた、手術手順を概説する材料を含む、印刷、ビデオ、およびマルチメディアフォーマットを使用して、様々な言語で、私たちの顧客、販売者、および販売業者のためのマーケティングおよびトレーニング材料を作成します。私たちは私たちのすべての販売者に、直接であっても独立であっても、広範な製品、政策、コンプライアンス訓練を受けて、私たちの基準、政策、適用法律を遵守することを保証しなければならない。
競争
全世界の脊柱、生物製薬、整形外科と画像誘導手術市場の競争は激しい。私たちはこれらの市場で、大型多国籍医療機器会社からの脊柱と整形外科部門、脊柱と整形外科に完全または主に集中している老舗会社、製品革新に専念する小型新興会社の激しい競争に直面している。これらの競争相手は、新しい技術を市場に投入し、私たちの製品と直接競争するか、または私たちの製品を時代遅れまたは競争力を持たない可能性のある潜在的な製品の優位性を持つ技術および技術ライセンスを得ることに集中している。
我々の骨成長療法製品種別は,主にZimmer Biomet,DJO Global,Bioventusが販売している類似製品と競合している。我々のバイオ製薬,エネルギー技術と脊柱インプラント市場における主要な競争相手は,Alphatec Spine,Baxter,B.Braun,BrainLab,Bioventus,Cerapedics,DePuy Synths Spine(ジョンソン社),Globus Medical,美敦力,NuVasive,Stryker,Surgalign,XTANT Medical,ZimVieおよび様々な小さな公共·民間会社である。Global Orthopedics装置では,我々の主な競争相手はDePuy Synths,Zimmer Biomet,Stryker,Smith&Nephew,OrthoPediatricsを含む.
私たちは、製品機能(例えば、使いやすさ、多機能性、コストおよび患者受容性)および付加価値サービス(例えば、STIM OnTrackモバイルアプリケーション、HEX Rayソフトウェア、OrthoNext術前計画および私たちの医学教育サービス)に集中することによって、私たちの競争地位を強化すると信じている。私たちは価格だけに基づいた競争を避けるために努力している。全体的なコストと医療効果、革新、信頼性、付加価値サービスと訓練は私たちの製品の市場で最も一般的な競争方式であり、私たちは私たちの競争が有効であると信じている。
製造と供給源
一般的に、私たちの業務に重要な原材料は多様なソースから簡単に得ることができる。品質保証、可用性、または費用効果のため、いくつかの構成要素と原材料は1つのサプライヤーからしか得られない。私たちとサプライヤーとの関係は材料費用や遅延なしに置き換えることはできません。私たちとサプライヤーとの関係は書面契約によって管理され、通常は供給契約です。これらの合意は、私たちがこのようなサプライヤーに部品や原材料を注文する流れ(このプロセスは、調達注文に基づいて、または四半期または年度予測に基づいて、場合によっては最低金額の購入を要求する)と、そのような部品や原材料の購入に関する費用を規定しています。これらの協定は,いずれも品質保証,検査,適用法律を遵守する権利を概説し,ビジネス合意と考えられる習慣賠償条項を含んでいる。これらの合意のすべては私たちの正常な業務過程で締結されたものであり、金額と重要性はどうでもいいし、私たちの業務が依存する契約でもない。また、特定の部品や材料が一定期間使用できなくても、私たちの生産が深刻な妨害を受けないように、十分な部品と原材料の在庫を維持するように努力しています。
脊柱と整形外科製品
私たちは通常私たちの骨成長刺激、脊柱インプラントと整形外科製品を設計、開発、組み立て、テストと包装し、相当部分の部品と器具の製造を下請けします。私たちのいくつかの重要な原材料は単一の供給源から得られたが、私たちはこれらの材料に代替源があると信じている。しかも、私たちは製品の流れが中断されないように十分な在庫供給を維持すると信じている。歴史的に、私たちは生産計画を満たすために必要な材料を得る上で困難に直面していない。
私たちの製品は現在アメリカ、カナダ、イタリアで生産と組み立てられています。私たちの工場はすべての実質的な側面でFDAとアメリカ以外のすべての関連規制機関の要求に適合していると信じています。私たちが受けた法律の説明については、副題“会社コンプライアンスと道徳計画”と“政府規制”の下の項目1“業務”を参照してください。私たちは私たちの各下請け業者を積極的に監督して、製造と品質標準及び製品規格の適合性を維持します。
生物製品
私たちのほとんどの生物製品は人や牛組織から抽出された物質を含んでいる。私たちはFDA登録とAATBで承認された組織ライブラリから私たちの原材料のみを調達します。ドナーは組織ライブラリがFDAとAATBの要求に基づいてスクリーニング、テストと処理を行う。またすべてのドナーはアメリカ食品医薬品局に規定されている細菌やウイルスの検査を受ける前に
23
原材料は私たちに追加加工されて配布された。私たちは各ドナーと一緒に組織庫から医療役員の原材料安全性認証を受けた。追加的な安全保証として、私たちの品質保証微生物学者が入力された骨と血清学的試験記録をスクリーニングした後にのみ、各骨を製造過程に放出する。私たちの製造過程で、骨粒子は私たちの独自のプロセスと最終滅菌を経た。このプロセスは、我々のDBM製品の安全性と有効性をサポートすることを目的としています。
我々のコラーゲンセラミック基質製品に使用されているコラーゲンは,ニュージーランドで24カ月未満の牛の深屈筋腱のみに由来している。世界保健機関は狂牛病伝播の相対リスクによって異なるタイプの牛組織を分類する。深屈筋腱は狂牛病伝播のリスクが最も低いクラス(例えば,牛乳と同じクラス)であることから,狂牛病を引き起こす病原体(Prionと呼ばれる誤ったフォールディングタンパク質)を含むリスクは無視できると考えられる。
著者らはまたMTF Biologicsと協力し、顧客に異体骨移植解決方案(Hct/Ps)を提供し、各種の脊柱、整形外科とその他の骨修復需要を満たす。MTF Biologicsは顧客が望むドナーのスクリーニング、加工、品質基準を提供する。MTFとのパートナー関係は、Virtual os Lyoggraph、三一エリート、FiberFuseとFiberFuse帯状製品、およびいくつかの他の組織形態を独占的にマーケティングすることを可能にし、Opus BAとOpus MGシリーズ合成生物製品の非独占営業権を持っている。
人的資本資源
著者らが業務を管理する重要な人力資本目標はトップレベルの人材を誘致、育成と維持することを含み、同時に多様性、公平性と包摂性の原則と実践を私たちの核心価値観に溶け込ませることを含む。
従業員
2022年12月31日現在、私たちは世界に1092人の従業員を持っている。このうち、786人が米国に雇用され、306人が他の非米国場所に雇用された。私たちのイタリア人従業員との関係は、金属機械工業界の労働関係の強制的な最低基準を規定する国家集団労働協定の条項によって管轄されています。2022年12月31日現在、私たちのイタリア人従業員は227人です。私たちは他のいかなる集団交渉協定の締約国でもない。
SeaSpineとの合併が2023年1月5日に完了した後,我々は世界に約1,734名の従業員を有し,そのうち1,371名の従業員は米国におり,363名の従業員は他の非米国地域にいる。
報酬と福祉
ハイレベル人材の誘致、育成と維持は著者らの人力資本目標の重要な構成部分であるため、私たちは競争力のある報酬と福祉方案を提供し、従業員の健康と健康を優先することを求めている。私たちが提供する全面的で競争力のある健康計画のほかに、私たちの従業員は、会社に一致する401(K)退職計画、従業員株式購入計画、仮想医師相談、従業員健康提唱者、会社が提供する基本生命保険と障害福祉企業健康計画、ある場所の現場フィットネスセンター、有給育児休暇、従業員援助計画、柔軟な支出口座、健康貯蓄口座、現地従業員割引計画を得ることができる。私たちの革新者とBeyondおよびBeyond奨励計画を通じて、私たちは私たちの従業員を表彰し、奨励し、これらの従業員は私たちが患者の生活を改善するために変革的な解決策を提供する使命を体現している。
人材育成
私たちは、成功は私たちの従業員に投資し、私たちの従業員が私たちの使命と価値観と一致することを確実にすることから来たと信じている。この目標を達成するために、私たちは時間と資源を投入して、従業員が私たちの業務、業界、製品に慣れるのを助ける。私たちは新しく採用された従業員のために強力な入社計画を立て、私たちの製品の組み合わせと会社の歴史を全面的に概説した。私たちは私たちの従業員と販売代表を訓練して、私たちの製品治療の潜在的な医療条件を含む私たちの業務を理解してもらうことに重点を置いています。また、私たちは、彼らが職業発展過程で最善を尽くすことができるように、発展、指導、参加、そして健康と健康の分野で私たちのチームを支援するために努力している。2022年には、私たちの第2年度夏休み実習計画を完成させることに成功し、80%の参加実習生が多様性基準に適合している。また、2022年には、2021計画から募集した実習生を従業員指導者とマッチングさせ、2021年のリーダーシップ卓越と加速計画(LEAP)の最初のキューを継続し、2023年には少なくとも25%の少数派が参加する第2のキューを開始する予定です。
24
多様性と包括性
私たちは多様性を促進し、公平で包容的な文化を育成、育成、保護するために努力している。多様性の価値を抱き、私たちの生活や仕事のコミュニティを反映することを目的とした、私たちのMoving 4 ward計画などの計画を通じて、すべての従業員に平等かつ公平な機会を提供する約束を示すことを求めています。また、私たちはOrthofix女性ネットワークを誇りに思ってサポートしており、女性に相互学習とわが社や業界で成長する機会を提供するプロジェクトです。この年、私たちは黒人歴史月、マーティン·ルーサー·キングなどを記念することで、様々な声を従業員に広めた。日、女性歴史月、アジア太平洋系アメリカ人伝統月、LGBTQ誇り月、6月19日とスペイン系伝統月。私たちは従業員の違いを抱きしめて奨励し、多様性、公平、包容が真のグローバル化、変革的な業務の構築に役立つことを知り、私たちの力の源泉になり続けるだろう。この信念に基づき、当社は“採用、リーダー、多様化と包括的なチームの育成”という研修を全社的に導入し、新たな採用訓練に取り入れています。私たちの目標は2023年末までに、すべての採用マネージャー、指導者、面接官がこの訓練を完成させることだ。
健康と安全
私たちの職員たちの安全を促進して保護することは優先順位だ。健康と安全問題は私たちの組織全体が共同で負う責任だ。過去数年間、私たちはこれらの問題で絶えず発展して、私たちの新冠肺炎疫病期間中の労働力の需要を満たす。従業員の安全リスクは彼らの役割によって異なり、私たちはそれに応じて私たちの安全努力を調整することを求めている。私たちは定期的に従業員の敬業度調査を通じて従業員の気持ちを測定し、調査結果と行動項目を従業員と共有している。
コミュニティ
私たちは寄付、資金調達、学院や大学との教育パートナーシップ、地域コミュニティの発展を通じて様々な慈善団体を支援しています。数年来、著者らは退役軍人支持団体、食品と住宅建設組織及び健康に関連する機関のために資金を集め、人々の認識を高めた。2022年には、コミュニティボランティアを奨励するための企業目標を年次インセンティブ計画に追加しました。この計画の下で、私たちの従業員は私たちのコミュニケーション目標を超えて、コミュニティ外展計画に1,988時間貢献した。私たちは私たちの生活と仕事の世界各地のコミュニティで命を寄付し、ウクライナ、テキサス州スコットランド児童マナー病院、献血活動、食品貯蔵室、その他の慈善活動を支援することを誇りに思っています。
25
Iプロジェクト1 A。 リスク要因
本年度報告書および添付ファイルに含まれる他の情報に加えて、以下に説明するリスクも慎重に考慮しなければなりません。このような危険は私たちが直面する可能性のある唯一の危険ではない。私たちは今知らないか、あるいは私たちが現在どうでもいいと思う他のリスクもまた私たちの業務運営を損なう可能性がある。本年度報告書にはまた、リスクと不確定要素に関する前向きな陳述が含まれている。いくつかの要因の影響により、私たちの実際の結果は、これらの前向き陳述で予想される結果と大きく異なる可能性があり、これらの要因は、以下または本年度報告において他の場所で直面するリスクを含む。私たちの普通株に投資することは高いリスクに関連しており、これらのリスクや不確定要素が発生した場合、私たちの普通株の取引価格は下落する可能性があり、あなたは投資の一部または全部を損失する可能性があります。別の説明がない限り、本年報第1 A項“リスク要因”項で開示された資料は、合併後の合併後の会社と関係がある。
リスク要因の概要
本節では、正常な商業活動の過程で私たちが直面している多くの危険について概説する。この要約には、あなたにとって重要である可能性のあるすべての情報は含まれていません。要約および本節の後、および本報告の他の場所でのリスクのより詳細な議論を読むべきです。
26
27
私たちが最近完成したSeaSpine合併に関するリスク
合併は、ある販売業者、顧客、OrthofixまたはSeaSpineが参加する他のプロトコルにおける制御権または他の条項の変化を引き起こす可能性があり、合併後の会社の業務および合併完了後の運営結果に悪影響を及ぼす可能性があります。
統合は、OrthofixやSeaSpineが参加するいくつかのプロトコルにおける制御権や他の条項を変化させる可能性があります。OrthofixやSeaSpineがこれらの条項の免除について交渉できない場合、取引相手は、合意の終了または金銭損害賠償または平衡法の救済措置を含む合意下の権利および救済措置を行使することができる。OrthofixとSeaSpineが同意や免除について交渉できても,取引相手はこのような免除のための費用を要求したり,OrthofixやSeaSpineにあまり有利でない条項で合意を再交渉することを求めたりする可能性がある.上記又は類似の事態発展は、合併後の会社の業務や合併完了後の経営業績に悪影響を及ぼす可能性がある。
合併に関連する不確実性は、管理職や他のキーパーソンの流失を招く可能性があり、合併完了後の合併後の会社の将来の業務や運営に悪影響を及ぼす可能性がある。
私たちは上級管理職や他の重要な従業員の経験と業界知識に基づいて私たちの業務計画を実行します。合併完了後、合併後の会社の成功は、合併後の会社がOrthofixとSeaSpineのある重要な管理者と従業員を維持する能力にある程度依存する。合併の結果、取引完了後、既存および将来の従業員は、彼らの役割が不確定に遭遇する可能性があり、これは、重要な経営陣や他のキーパーソンを誘致または維持する能力に悪影響を及ぼす可能性がある。また,OrthofixやSeaSpineの前に自分の従業員を引き付けたり引き留めたりできるように,合併後の会社がキー管理者や他のキー従業員を引き付けることができる保証はない.
株主訴訟は私たちの業務と運営に否定的な影響を及ぼすかもしれない。
それぞれ2022年11月17日、2022年11月21日、2022年12月13日に、SeaSpine当時の株主が米ニューヨーク南区地域裁判所と米デラウェア州地域裁判所にSeaSpineと当時のSeaSpine取締役会メンバーを起訴したという。また、2022年12月13日、Orthofix当時の株主といわれる一人が、Orthofixと当時のOrthofix取締役会メンバーをニューヨーク南区アメリカ地方裁判所に起訴した。起訴状は、取引法第14(A)節及びその公布された第14 a-9条及び取引法第20(A)節に提出されたクレームに基づいて、2022年11月8日に米国証券取引委員会に提出されたS-4表登録声明の重大な不完全及び誤解性を招くことを招くか、又は2022年11月23日に米国証券取引委員会に提出された付表14 Aの最終委託書に重大な不完全かつ誤解性がある疑いがある。他の救済措置で、原告は合併を禁止しようと努力した。この4つのすべての訴訟はもう原告によって自発的に却下された。2022年11月19日、SeaSpineの2人の異なる株主の弁護士が要求状を出し、類似した主張をした。2022年11月23日、SeaSpine当時の株主といわれるもう一人の弁護士は、取引法第14(A)節及びその公布された規則14 a-9及び取引法第20条(A)に基づいて同様の疑惑を提起し、合併禁止を求める類似の告発を連邦裁判所に提出した。また、2022年11月15日と2022年12月20日, Orthofix当時の2人の異なる株主の弁護士は,Orthofixの弁護士に要求状を出し,Orthofixに対する連邦裁判所申し立て草案と,取引法第14条(A)条とその公布された規則14 a-9と取引法第20(A)条に類似したクレームを出したOrthofix取締役会メンバーを添付し,合併禁止を求めた.2022年12月14日と2022年12月22日、Orthofixの株主とされる他の2人の弁護士は、Orthofixの弁護士に類似した告発を含む要求状を出した。これらの訴訟の最終結果は正確に予測できないにもかかわらず、OrthofixとSeaSpineはこれらの疑惑に根拠がないと考え、これらの行動を有力に弁護しようとしている。
証券集団訴訟やデリバティブ訴訟は、通常、合併合意に達した会社に対して提起される。将来的にはOrthofix、SeaSpine、Merge Subおよび/またはOrthofixおよび/またはSeaSpineの役員および上級管理者に対して合併に関するより多くの訴訟を提起するかもしれない。OrthofixおよびSeaSpineは、抗弁クレームに関連する費用金額またはそのような訴訟に関連する可能性のある任意の他の責任を含む、すでに提起されているか、または提起可能な任意の訴訟の結果を保証することができない。原告のクレームが勝訴するか否かにかかわらず、このタイプの訴訟は巨額の費用を招き、経営陣の注意力や資源を分散させる可能性があり、OrthofixやSeaSpineの業務運営に悪影響を及ぼす可能性がある。
合併後の会社はOrthofixとSeaSpineの業務統合に成功できない可能性があり、合併の期待的なメリットを実現できません。
28
合併の成功はある程度合併後の会社がOrthofixとSeaSpineの業務を合併と統合することに成功できるかどうかに依存し、そして予想される収益を実現し、協同効果、コスト節約、革新と技術機会及び合併による運営効率を含むが、合併は既存の顧客、サプライヤーと従業員の関係に実質的な破壊を与えることはなく、顧客の損失或いは注文減少による収入減少を招くこともない。合併後の会社が予想される時間枠内でこれらの目標を達成できない場合や、予想される収益をまったく実現できない場合や、達成するには予想よりも長い時間がかかる可能性があり、合併後の会社の普通株の価値が低下する可能性がある。合併は追加的で予見できない費用をもたらす可能性があり、合併後の会社は合併の予想される利益の一部またはすべてをタイムリーにまたは根本的に実現できない可能性がある。
合併が完了して以来、私たちは複数の統合活動を成功させてきたが、私たちの残りの統合活動はうまくいかないかもしれない。両社の統合は実質的な挑戦をもたらす可能性があるが、これらに限定されない
その中の多くの要素は私たちの制御範囲内ではなく、その中のいずれの要素も遅延、コスト増加、期待収入の減少とその他の不利な影響を招く可能性があり、これは合併後の会社の財務状況、運営結果とキャッシュフローに重大な影響を与える可能性がある。また,ある業務の統合には大量の管理資源が投入される必要があり,日常業務に対する管理層の注意を一時的に分散させる可能性がある.統合過程での従業員たちの不確実性と重点の不足はまた私たちの業務を混乱させる可能性がある。
また、SeaSpineは2021年5月に7 D Surgical,Inc.との統合を完了し、SeaSpine業務と7 D Surgicalの統合はまだ進行中であり、(A)買収から期待される利益がすべて達成できない可能性があること、(B)私たちまたは7 D Surgicalの業務に予期せぬ悪影響を及ぼす可能性があること、および/または予想される投資リターンを実現できない可能性があることを含む。(C)7 D Surgicalビジネスに関連するクレームまたは債務の影響を受ける可能性があり、SeaSpineは、7 D Surgicalを買収する前に、いくつかの負債、欠陥、または他の状況の規模を識別または評価できない可能性がある。そして(D)7 D Surgicalは米国上場企業基準に適合した内部制御インフラを維持する必要がなく,このような制御やプログラムを実施する際に大量のコストが発生し,実施中に予期しない遅延や挑戦に遭遇する可能性がある。7 D Surgicalが行われている統合は、OrthofixおよびSeaSpineビジネス統合の複雑さおよび関連する挑戦を増加させる可能性があり、これは、OrthofixおよびSeaSpineを完全にまたは完全にまたは予期される時間範囲内で統合を達成することをより困難にすることができる。
合併会社が合併完了後に複雑な運営を効率的に管理していなければ、合併後の会社の将来の業績は悪影響を受ける可能性がある。
合併完了後、合併後の会社の業務規模はSeaSpineやOrthofixの現在の業務規模を大きく上回る。統合後の会社がこの拡張業務を成功的に管理する能力は,OrthofixとSeaSpine業務の統合だけでなく,合併後の業務とそれに関連する経営陣の設計や戦略的取り組みの能力に部分的に依存する
29
それに伴いコストと複雑性が増加する。合併後の会社が業務統合に成功することは保証されず、予想される運営効率、コスト節約、現在予想されている合併による他のメリットを実現する保証もない。
我々は,統合およびOrthofixとSeaSpine業務の統合完了に関連した巨額の費用を予想している。
私たちは、OrthofixとSeaSpineが合併に関連する大量のプロセス、政策、プログラム、運営、技術、システムを統合するために、統合を完了するために巨額の支出を発生させる。これらの費用の大部分は取引や施設やシステム合併費用に関する非日常的な費用となる。合併後の会社は、取引完了後にトリガされる可能性のある制御権変更または他の条項、および/または顧客注文の損失または減少を含む第三者契約の下で追加のコストまたは業務損失を生じる可能性があり、特定の重要な管理者および従業員を維持するコストも生じる可能性がある。OrthofixやSeaSpineは合併後の業務の統合計画の策定に関する取引費やコストも発生し,これらの計画の実行は余分な意外なコストや時間遅延を招く可能性がある.これらの取引に関連する増分コストは、合併後の企業が予想している重複コストを除去し、業務統合に関連する他の効率を実現することによって節約されるコスト、特に短期的には、および重大な意外なコストが発生した場合を超える可能性がある。各方面がコントロールできない要素はこれらの費用の総額や時間に影響を与える可能性があり、その中の多くの費用の性質を正確に見積もることは困難である。
合併完了後の合併後の会社普通株の市場価格は、合併完了前にOrthofix普通株やSeaSpine普通株価格に影響する要素とは異なる影響を受ける可能性がある。
合併完了後、従来のOrthofix普通株式保有者と従来のSeaSpine普通株式保有者は現在合併後の会社の普通株式保有者である。OrthofixとSeaSpineの業務が異なるため,経営結果や合併後の会社普通株の価格は将来的にOrthofixとSeaSpineの独立会社としてのそれぞれに影響を与える要因とは異なる影響を受ける可能性がある。合併後の会社はより多くのリスクと不確実性に直面し、OrthofixもSeaSpineもこれらのリスクや不確実性の影響を受けていない可能性がある。そのため、合併完了後、合併後の会社株の市場価格が大幅に変動する可能性がある。
合併後の会社普通株の市場価格は、いくつかのOrthofixおよび/またはSeaSpine株主による彼らのポートフォリオの調整を含む合併によって低下する可能性がある。
OrthofixやSeaSpine業務統合に関する運営コスト節約が実現されていなければ,Orthofixの財務状況に予期せぬ負の影響を与えたり,合併に関する取引コストが予想以上に高ければ,合併後の会社普通株の市場価格は合併により低下する可能性がある.合併後の会社が財務或いは業界アナリストの予想程度に迅速に或いは達成できなかった場合、或いは取引が合併後の会社の財務状況、経営結果或いはキャッシュフローに与える影響が財務或いは業界アナリストの予想と一致しなければ、市場価格も低下する可能性がある。
また、合併完了後に合併後の会社普通株を売却することは、その普通株の市場価格を低下させる可能性がある。Orthofixは,合併終了前に発行されたSeaSpine普通株の数に応じて,合併中のSeaSpine普通株の保有者に合計約1600万株のOrthofix普通株を発行した。歴史上のSeaSpine株主は、合併で獲得する合併後の会社普通株の株式を保有しないことを決定する可能性がある。また、特定のOrthofix株主、例えば彼らが個別発行者が持っている株が制限された基金は、合併完了後に彼らの普通株を売却することを要求される可能性がある。合併後の会社普通株を売却すると合併後の会社普通株の市場価格が低くなる可能性があります。
これらの事象のいずれも、(I)合併後の会社が株式または株式関連証券を売却することを困難にすること、(Ii)合併後の会社の所有権権益を希釈すること、および/または(Iii)合併後の会社の普通株の価格に悪影響を及ぼすことを可能にする。
30
私たちの法律と規制環境に関するリスク
有効な内部統制システムを維持できない場合や、財務報告の内部統制に重大な弱点を発見することができなければ、財務結果を正確に報告したり、詐欺行為を発見することができない可能性があり、これは私たちの業務と私たちの普通株の取引価格を損なう可能性がある。
効果的な内部統制は私たちが信頼できる財務報告書を作成するために必要であり、私たちの財務詐欺防止のための努力も重要だ。私たちは私たちの内部統制の設計と動作の有効性を定期的に評価することを要求された。数年前に起きたように、このような評価は、私たちの内部統制を強化、修正、または変更することが必要であり、望ましいと結論を出すかもしれない。経営陣は定期的に私たちの内部統制の有効性を評価しているが、これらの統制はいつも効果的ではない。内部制御の有効性には固有の限界があり,談合,管理凌駕,人為的判断のミスを含む.そのため,制御プログラムは業務リスクを解消するのではなく削減を目指している.また,時間の経過とともに,我々の業務や経営構造の変化により,従来の有効な内部制御が不十分になる可能性があり,これらの制御の十分性を評価し,必要に応じてこれらの制御を更新する措置をとることができない可能性がある.有効な内部統制システムを維持できない場合や、経営陣や独立公認会計士事務所が私たちの内部統制に大きな弱点があることを発見した場合、信頼できる財務報告書を作成したり、詐欺を防止することができない可能性があり、これは私たちの財務状況や経営業績を損なう可能性があり、投資家の自信喪失や株価下落を招く可能性があります。
我々は“反海外腐敗法”(“FCPA”)や他の類似した反賄賂法律の制約を受けており、このような法律に違反するいかなる行為も私たちに不良な結果をもたらす可能性がある。
非米国司法管区では、“反海外腐敗法”や同様の反賄賂法は、会社及びその中間者が業務の獲得又は保留を目的として外国政府関係者に不正な金を支払うことを一般的に禁止している。“海外腐敗防止法”はまた、会社資金が贈賄やその他の不正支払いに移行されることを防ぐために、米国の上場実体とその外国付属会社に対して会計基準と要求を実施している。政府が支援する医療システムは世界各地で主導的な地位を占めているため,我々は米国以外の多くの顧客関係が政府実体と構築されているため,このような反賄賂法の制約を受けている。
ここ数年来、アメリカと非アメリカの監督管理機関はすべて医療機器業界に対する監督、法執行、検査と政府調査を強化し、アメリカ政府の“反海外腐敗法”に対する監督と実行を強化した。包括的なグローバル医療コンプライアンス計画が実施されているにもかかわらず、私たちは将来、より多くの規制、法執行、検査、政府当局の調査を受ける可能性がある。
米国または海外で適用される法律および法規義務を遵守できないいかなる行為も、個人の監禁、罰金および処罰、輸出特権の剥奪、CE合格証明書の一時停止または撤回、貨物の差し押さえ、特定の商業活動の制限、返還およびその他の救済措置、私たちの運営中断、および深刻な管理を含む重大な刑事、民事および行政処罰を含む様々な方法で私たちに悪影響を及ぼす可能性がある。また、適用される法律や法規義務を遵守できなかったことは、私たちの流通や販売活動を中断させる可能性があります。国際売上高のいかなる低下も、私たちが私たちの国際市場をさらに開発できなかったことは、私たちの業務、経営結果、財務状況に実質的な悪影響を及ぼす可能性がある。
私たちは連邦と州医療詐欺、虐待、反自己転換法の制約を受けており、これらの法律を完全に遵守していないと判断されれば、実質的な処罰に直面する可能性がある。
連邦と州政府の医療詐欺と規制の乱用は私たちの業務に影響を及ぼす。私たちの業務に適用される可能性のある医療詐欺と乱用法律は、
31
連邦と州政府機関および個人通報者はこれらの法律に基づいて調査と法執行活動を大幅に増加させた。これらの法律に違反した行為は、民事と刑事罰、損害賠償、罰金、私たちの業務を削減または再編し、あるいは連邦、非米国、または州医療計画から除外されるだろう。私たちは、私たちの販売とマーケティング実践、顧客割引手配、および医療専門家との相互作用を構築する際に非常に慎重で、これらの法律と法規を遵守するために非常に慎重であるにもかかわらず、政府関係者が私たちのやり方が規則に合わないと断言しないか、あるいは政府の監督管理機関や裁判所が私たちの解釈と一致した方法でこれらの法律や法規を解釈することを保証することはできない。調査が成功しなかったり、全面的に展開されていなくても、私たちはかなりの時間と資源をかけて自己弁護するかもしれません。私たちが違反に従事する可能性のある断言は、既存および潜在的な顧客における私たちの名声および私たちの業務、財務状況、および運営結果に実質的な悪影響を及ぼすかもしれません。
第三者の精算政策、コスト制御措置、医療改革は、私たちの製品需要に悪影響を与え、製品を販売する能力を制限する可能性があります。
私たちの製品の販売を維持し、増加させることは、アメリカ国内外の第三者支払者が十分な保証範囲と精算を提供することに依存します。私たちの製品は、私たちが直接販売したり、独立販売代表によって顧客や私たちの独立流通業者に販売され、病院、医療提供者、患者によって購入されます。これらの製品は、Medicare、MedicaidおよびTricare、または個人保険計画、管理医療組織、および医療ネットワークを含む政府計画のような第三者支払者によって精算されることができる。アメリカと国際医療サービスの主要な第三者支払者は引き続き医療コストのコントロールに努力し、ますます多くの医療製品とサービスの政策と価格に挑戦し、価格監督管理、競争定価、カバーと支払い政策、治療の比較有効性、技術評価と管理型医療手配を含む医療コストの増加を制限する措置をすでに或いは実施する可能性がある。私たちの製品の清算範囲を廃止、減少、または実質的に修正する医療政策の発展は、私たちの製品を販売する能力に影響を与える可能性があります。また、第三者支払者は、患者に提供またはプログラムで使用される設備や製品が適用される支払い基準を満たしていないと判断した場合、または保険加入者の医療保険福祉が限られている場合には、通知せずに保険または精算をキャンセルまたは減少させることができる、我々の製品を使用するプログラムに関する保険範囲および精算政策を継続的に検討·改訂していく。
例えば,過去,米国の主要な全国的第三者保険会社は頚椎融合術に使用されている生体機械設備(例えば脊柱融合器)の保証範囲(全例あるいは大多数の症例から限られた適応に減少)を低下させており,これらの設備は植骨よりも有効であることは証明されていない。また,ある保険会社は腰椎融合に対する保険範囲が限られており,他の保険会社は将来類似した保険決定をとる可能性がある。精算を制限することは、私たちの製品を購入することをより困難にし、患者が私たちの製品を得る機会を大幅に減少させる可能性がある。また、政府当局が第三者の引受·精算に影響を与える立法や法規を制定し続けると、民間または公共保険会社がわが製品や保険の範囲を得る機会が減少し、販売や利益に大きな悪影響を及ぼす可能性がある。
CMSはその実施中の連邦医療保険計画において、定期的に医学研究文献を審査し、文献がどのように連邦医療保険群の中のいくつかのプログラムと治療法を解決するかを確定する。これらの情報がわが製品の連邦医療保険カバー政策に及ぼす可能性のある影響は不明であるが,それによる行動が我々の製品の連邦医療保険カバー範囲を制限しない保証はない。私たちや私たちの流通業者が未来にこれらや他の手続きに関連した重大な精算問題に遭遇しないという保証はない。
法律の要求に基づき,CMSはMedicare計画によって支払われた選定DMEPOSプロジェクトの競争的入札計画の実施に努め続けている。この計画では、連邦医療保険料率は、指定された地理的地域における特定製品の入札金額に基づいており、連邦医療保険費用スケジュール金額ではない。骨成長刺激製品は現在この競争的入札プログラムの影響を受けない。私たちはどの業務のどの製品が最終的に影響を受ける可能性があるか予測できないし、入札過程がいつ私たちの業務に拡張される可能性があるかどうかを予測することもできません。入札計画の実施が私たちのいくつかの製品の販売に悪影響を与えない保証はありません。
国際販売については,市場受け入れの程度は主流医療支払いシステムにおけるカバー範囲や精算状況にある程度依存する可能性がある。国際市場の精算と医療支払いシステムは国によって異なる。アメリカと同じように、私たちの製品は特定の国際市場で適時に保証と精算承認を得ることができないかもしれません。しかも、私たちが特定の国の保険と補償の承認を受けても、私たちはそれのためにかなりの費用を発生させるかもしれない。このような保険および承認を得ることができなかったことは、このような故障が発生した国際市場での製品の市場受容度に悪影響を与え、このような保険および承認を得ることに関連する費用は、このような保険および承認を得るメリットを超える可能性がある。
32
世界的に、私たちの製品はイギリス、ドイツ、フランス、イタリアのような多くの国に販売されています。これらの国は公共援助の医療システムを持っています。このようなシステムによって支援される病院が私たちの製品を購入する能力は公共予算制限にある程度依存する。このような制限の増加は私たちの販売と売掛金に実質的な悪影響を及ぼす可能性がある。
政府機関や他の第三者支払者が我々の製品を使用するプログラムの保証範囲および/または精算を減少させ続ける場合、私たちの業務、運営結果、財務状況は実質的な悪影響を受ける可能性がある。また、現在と将来の支払いシステムでは、私たちの製品のコストがプログラムの総コストに十分に計上されているかどうかを確認することができませんので、私たちの製品に対して実行されるプログラムが費用効果のあるレベルで精算されるか、あるいは全く精算されないかを決定することはできません。
私たちと私たちのいくつかのサプライヤーは広範な政府によって規制されるかもしれません。これは私たちのコストを増加させ、私たちのマーケティングや製品を販売する能力を制限するかもしれません。
私たちが製造·販売している医療機器はFDAと多くの他の連邦、州、外国政府機関によって厳格に規制されている。これらの機関は医療機器の開発,承認,分類,テスト,製造,ラベル,マーケティング,販売を管理している。同様に、特定のカテゴリの健康情報の使用および開示は、健康情報のプライバシーおよび安全を保護する政府当局によって実施され、実行される連邦および州法律によって制限される可能性がある。本条例の説明については、“政府条例”の副題下の第1項“業務”を参照されたい
いずれの医療機器も米国や他の国で発売される前に、通常、米国FDAを含む政府当局の承認または許可を得る必要がある。将来、アメリカや外国政府が、私たちの業務、財務状況、運営結果、またはキャッシュフローに実質的な悪影響を及ぼす法規を実施するかどうかは予測できません。
FDAの承認と承認を得て医療機器を開発·販売する過程は、コストが高く、時間がかかる可能性があり、このような承認または承認がタイムリーに承認できない(あれば)リスクに直面している。FDAが新設備の審査時間を延長する場合、規制プロセスは新製品のマーケティングを延期または禁止し、大量の追加コストをかける可能性がある。さらに、FDAは、承認または承認されたデバイスの規制カテゴリをより高い規制カテゴリからより低い規制カテゴリに変更する権利があるか、またはHCT/Pを再分類する権利があり、両方の場合は、私たちのデバイスをマーケティングまたは販売する能力に実質的な悪影響を及ぼす可能性がある。
しかも、私たちは広範囲な記録と報告書を行わなければならない。例えば、連邦医療機器報告法規要件は、装置が死亡または深刻な傷害をもたらす可能性があるか、または再発時に死亡または深刻な傷害をもたらす可能性が高い障害が発生したことを合理的に示す証拠がある限り、FDAに情報を提供しなければならない。
私たちと私たちのいくつかのサプライヤーはまた、FDAのQSRおよび他の規制に適合するかどうかを決定するために、FDAの発表および発表されていない検査を受けている。ドナー回収組織または組織銀行を含めて、生体材料製品の買収または加工が適用されるFDA法規または他の関連法律法規に適合していないと主張することを含む、私たちまたは私たちのサプライヤーに告発することができるかもしれない。そのような告発は、規制機関や他の当局が私たちまたは私たちのサプライヤーを調査したり、他の行動を取ったり、あるいは私たちまたは私たちの産業に否定的な宣伝をもたらす可能性があるかもしれない。もしFDAが告発や他の理由で私たちを調査し、FDAが適用された法律や法規を遵守していないと結論した場合、またはFDAが私たちの任意の医療機器が無効または健康に不合理なリスクを構成していると結論した場合、その機関は、公開警告状からより厳しい制裁まで、私たち、私たちの役人、私たちの従業員または私たちのサプライヤーへの罰金や民事処罰、このような行動の意外な支出の解決または弁護、私たちの製品の整理または承認の遅延、または拒否;FDAまたは他の規制機関は、私たちの製品または私たちの第三者サプライヤーの製品を撤回または一時停止し、製品のリコールまたは差し押さえ、生産中断、運営制限、禁止、および刑事起訴を許可する。FDAはまた、私たちが製造または流通している任意の医療機器の費用の修理、交換、または払い戻しを要求する権利がある。FDAはまたアメリカ司法省に起訴を提案するかもしれない。FDAは、適用要件を遵守できなかった任意の通知または通信について, あるいはいかなる不利な監督管理行動による負の宣伝または製品責任クレームは、私たちの新しい実験室テスト、業務戦略、財務状況、運営結果またはキャッシュフローの開発に重大な悪影響を及ぼす可能性がある。
私たちは適用された規制に対する供給者たちの持続的なコンプライアンスをほとんど統制できない。彼らが遵守しないことは、罰金および民事処罰、生産停止、一時停止または新製品の承認または承認の遅延、製品の差し押さえまたはリコール、または製品の承認または承認の撤回を含む規制行動および他の責任に直面させるかもしれない。
また,米国以外の政府機関の医療機器の規制はますます厳しくなっており,我々の製品は将来的には米国非政府機関のより厳しい規制を受ける可能性がある。アメリカか非アメリカか
33
将来実施される可能性のある政府法規は、私たちの業務と運営に実質的な悪影響を及ぼすかもしれない。欧州委員会(“EC”)は,メーカーが遵守しなければならない欧州医療機器指令により,各国の医療機器の制御法規を調整した。これらの新規定によると、製造工場は“通知機関”からの全面的な品質保証認証を取得しなければ、EUメンバー国内で製品を販売することができる。この認証は、メーカーが認証された工場の製品に“CE”マークを押すことを可能にする。EU法規でカバーされているCEマークを持たない製品はEU内で販売や流通することはできません。私たちは現在すべての既存の製造施設が認証を受けています。
また、スイスとEUの間で完全な相互承認合意が達成される前に、スイスは第3国とみなされるだろう。しかし、同社はスイスの新しい法律に基づいてスイスにいくつかの重要な製品の登録を求めている。イギリスはまたイギリスの離脱と関連した似たような活動を展開した。
医療機器業界の規制は,我々の医療機器の販売や市場での競争の仕方に影響を与える可能性がある。
FDA、アメリカ衛生·公衆サービス部監察長弁公室、アメリカ司法省とその他の監督機関は積極的に法規を実行し、FDAの許可或いは許可されていない用途のための医療機器の普及を禁止した。承認または承認の適応以外に1つの装置を使用することを“ラベル外”と呼ぶ。医師は、FDAが医療実践における医師の治療の選択を制限または規範化していないので、ラベル外の使用のために私たちの製品を処方するかもしれない。しかし、規制機関が、私たちの販売促進材料、訓練または活動が非ラベル使用の不適切な宣伝を構成していると判断した場合、監督管理機関は、警告状、禁止、差し押さえ、民事罰金、および/または刑事罰を含む監督管理法執行行動を取るように私たちに要求することができる。私たちの政策は、私たちの製品のラベル外販売促進に対する声明や活動とみなされることを避けることですが、どの規制機関も同意せず、ラベル外の販売促進活動に従事しており、虚偽の声明を提出する可能性があると結論した可能性があります。また,ラベル外で我々の製品を使用することは患者の受傷リスクを増加させ,製品責任クレームのリスクを増加させる可能性がある。さらに、FDAが私たちの1つまたは複数の製品修正にFDAの新たな承認または承認を必要としない決定に疑問を提起した場合、私たちはコンプライアンス行動、処罰、または禁止の影響を受ける可能性がある。
FDAのグループは、FDAが骨成長刺激装置をクラスIII装置からクラスII装置に再分類することを提案し、これは、将来の製品カテゴリにおける私たちの競争を増加させ、将来のこのような製品の販売に悪影響を及ぼす可能性がある。
我々は市場をリードする骨成長刺激プラットフォームを持ち,FDAが承認した唯一の頚椎適応と,患者の処方遵守と臨床結果の改善を支援するための唯一のモバイルデバイスAPP添付ファイル,STIM OnTrack 2.1を有している。肩袖引き裂きなどの分野での適応を拡大するためにIDE研究にも投資しています。我々の骨成長療法製品は現在III類装置に指定されている。米国では、クラスIIIデバイスはFDAの最も厳しい医療機器承認手続きを通過しなければならない。提案された新しいカテゴリが合理的な安全性と有効性保証を提供するために十分な規制制御を持っている場合にのみ、FDAはデバイスの分類を変更することができる。
2020年9月,FDAの整形外科·リハビリテーションチームは,骨成長刺激装置をIII系装置からII類装置に再分類し,“特殊制御”を行い,患者の安全と治療効果を確保することを提案した。これらの提案された特殊な制御措置は、このような設備は厳格な臨床研究を受け入れ、そして任意の新製品に対して発売後の監督を行わなければならないことを含む。これは、任意の新製品が承認または承認された装置と“基本的に同じ”ことを示す他の特殊な制御および第2の一般的な要求の追加となるであろう。
専門家グループの提言は,これらのデバイスに対するPMA系臨床データの重要性を正確に認識しているため,メーカーは承認中に信頼できる臨床データを提出し,これらのデバイスの患者に対する安全性と有効性を確保することが求められ続けていると考えられる。著者らは,他の骨成長刺激剤メーカーとともに,FDAが提案した規則制定に対する応答意見を提出し,専門家グループの提案,すなわち骨成長刺激剤製品を承認あるいは承認する前に,強力な臨床データ,および発売後の監督要求を強調した。
長期的に見れば、競争相手が私たちの設備の効果に相当する技術を作り出すことができれば、提案された再分類は彼らの市場進出能力を増強する可能性があり、これは私たちの製品を追加的な競争に直面させ、未来のこれらの製品の販売にマイナスの影響を与える可能性がある。
私たちはアメリカの医療改革計画の影響を受け続けている。
“衛生保健と教育調整法”(あるいは総称して“ACA”と呼ぶ)によって改正された“患者保護と平価医療法”は、近年、医療保健が両国政府から資金を提供する方式にいくつかの重大な変化が発生している
34
民間保険会社もありますACAは影響が深く、医療保険のカバー範囲を拡大し、品質を高め、時間の経過とともにコストを下げることを目的としている。他の事項を除いて、ACA:
アメリカ政府機関はACAの条項を修正するために努力し続けている。例えば、CMSは各州が医療補助拡張計画をカバーする人に仕事の要求を加えることを許可し始め、保険会社に対するいくつかの連邦補助金は終了し、いくつかの完全なACA福祉を提供しない短期保険計画は期限の延長が許可された。その中のいくつかの変化はアメリカの裁判所で挑戦されているので、それらの長期的な影響はまだ確定していない。このような変化する連邦構造はアメリカ医療業界に積極的な影響もあれば、消極的な影響もあり、連邦法律の各種条項及びこれらの法律の潜在的な改正或いは廃止が最終的にどのようにこの業界に影響するかについては、依然として大きな不確定性がある。反腐敗条約のある条項の範囲と効果の面で持続的に存在する不確実性は契約遵守コストを高くする。ACAまたは他のこのような法律の将来の任意の変化は、その性質に応じて、リベート、価格または医療製品およびサービスの価格上昇幅に影響を与える可能性があり、または報告および開示が必要であり、任意の製品の販売および利益を達成する能力を維持または増加させることに悪影響を及ぼす可能性がある。私たちは未来のどんな規則や法的変化の時間や影響を予測することができない。しかしながら、製品の精算の減少や医療プログラム量の減少を招くいかなる変化も、私たちの業務、財務状況、および運営結果に実質的な悪影響を及ぼす可能性がある。
私たちが業務を経営しているいくつかの司法管轄区で、私たちは違う税関と輸出入規則の制約を受けています。
私たちは世界の多くの違う国に私たちの製品を輸出入します。外国政府の規制はますます厳しくなり、ますます一般的になってきており、私たちは外国政府当局によってより厳しい規制を受けるかもしれない。多くの法的制限は、場合によっては、米国企業が特定の国の個人または実体に直接または間接的に商品、技術、またはサービスを販売することを禁止する。また、これらの法律は、私たちの販売とマーケティング実践を組織し、海外で製品登録を行う際に慎重であることを要求している。このような規定を遵守する費用は高い。
私たちの製品の輸出入は、異なる税関と輸出入規則と法規を持つ司法管轄区域内で運営されている子会社と第三者に関連しています。これらの司法管轄区の税関当局は、それぞれの税関法と条約のいくつかの面に基づいて、税関と製品輸送に関する輸出入規則の処理方式に疑問を提起することができる。もし私たちが私たちの税関と輸出入の分類方法を弁護することに成功できなければ、私たちは追加の関税、罰金、または罰金を徴収されるかもしれません。これは私たちの収益性に悪影響を及ぼすかもしれません。
また、国際貿易における米国や外交政策の変化も、私たちの業務にマイナス影響を与える可能性がある。私たちが販売したり、私たちの製品と競争している特定の製品に関税やその他のこのような費用を設定したり増加させたりすることは、私たちの業務または私たちの運営結果に悪影響を及ぼすかもしれません。
私たちの業界の販売とマーケティング実践は連邦と州政府機関が審査を強化する対象となってきた。
医療機器業界のいくつかの主要な業界協会AdvaMed(アメリカ)、Eucomed(ヨーロッパ)、MEDEC(カナダ)とMTAA(オーストラリア)は道徳規範手本を公布し、そのメンバー(と非メンバー会社)が異なる地区でその製品を普及させる時に遵守すべき標準を規定した。私たちはすでにこれらの協会が公布した政策と手続きと一致したコンプライアンス政策と手続きを実施し、私たちの販売とマーケティング実践政策について私たちの販売とマーケティング担当者の訓練を行った。それにもかかわらず、私たちの業界の販売とマーケティング実践は連邦と州政府機関のより厳格な審査を受けてきており、この傾向は続くと信じており、顧客と他の私たちの業務に重要な関係を維持する能力に影響を与える可能性がある。
例えば、州と連邦の2級はいくつかの主要設備会社が医療専門者を維持する検察審査と政府監督に対して、医療設備会社がどのように医療専門人員を顧問として保留するかを制限した。様々な病院組織、医学会および業界協会は、医療専門家と医療機器会社との関係を詳細に開示すること、または贈り物やビジネス食事のようないくつかのマーケティングおよび販売方法を禁止または制限することを要求する可能性がある独自のやり方を確立している。さらに、ACAおよびいくつかの州法律は、特定の財務関係、プレゼント、および他の特定の医療専門家および教育病院に支払われる報酬を詳細に開示することを要求しており、これらの宣伝環境は、私たちとの関係に悪影響を及ぼす可能性がある
35
顧客と製品設計や研究への参加に対する意見を求める能力。法律、規則および法規、または私たち自身または第三者が相互作用を禁止または制限する政策によって、あるいは医療専門家と業界との間のいかなる相互作用も汚染されていると考える人が増えているため、私たちは他の状況と同じ方法や程度で、あるいは私たちの医療専門顧客と付き合うことができない可能性があり、これは、顧客のニーズを理解し、これらの需要を満たすフィードバックを私たちの開発計画に組み込む能力に悪影響を及ぼす可能性がある。もし私たちが私たちの医師顧客とその患者の需要を満たす新製品を開発し、商業化することができなければ、私たちの製品は市場に広く受け入れられないかもしれないし、根本的にはないかもしれません。これは私たちの業務、運営結果、財務状況にマイナスの影響を与えます。
私たちは危険材料と関連した要求を受けており、これは私たちに大きな適合性や他の費用をもたらすかもしれない。
私たちの研究、開発、そして製造プロセスは特定の危険材料の制御された使用に関するものだ。例えば,我々の同種骨組織処理は廃棄物を発生させる可能性があり,米国では医療廃棄物に分類されている。しかも、私たちはまた危険な材料を使用する可能性のある施設をレンタルする。上記の理由から、私たちは危険材料と特定の廃棄物を使用、製造、貯蔵、運搬、処理、救済、処分する際に、連邦、州、外国と現地の法律と法規を遵守しなければならない。
我々が危険材料を処理·処分する手続きは現在有効な適用法に適合していると信じているが,これらの材料による意外な汚染や傷害のリスクを解消することはできない。また,いくつかの環境法律や法規によれば,このような汚染が我々によるものでなくても,我々の過去や現在の施設や第三者廃棄物処理場の任意の汚染に関するすべての費用を負担することができる。事故が発生した場合、州や連邦または他の適用当局は、これらの材料の使用を制限し、私たちの業務運営を中断する可能性があります。さらに、事故や環境排出が発生した場合、または以前の操作(私たちが買収した物件の以前の所有者や事業者を含む)による汚染が発見された場合、整理義務、損害、罰金を負う可能性があり、任意の関連責任は私たちの資源範囲を超える可能性があります。もしこのような予期しない費用が大きいなら、これは私たちの財務状況と運営結果を深刻に損なうかもしれない。私たちは危険材料の使用に関する環境クレームを専門的に引き受けていない。
私たちのビジネスや産業に関するリスクは
新冠肺炎疫病はすでに著者らの運営、サプライチェーン、製造、製品需要、製品流通、顧客とその他の商業活動に実質的な不利な影響を与える可能性がある。
この新型コロナウイルスは2019年末に発見され,それによる疾患は新冠肺炎と呼ばれ,医療市場や米国や国際経済の大きな中断を招き,この中断は長く続く可能性がある。コロナウイルスの2020年の急速な伝播と2021年のウイルスの変種による大流行の持続,各国政府や個人側がこの大流行の伝播を抑制するための措置と,このウイルスに対する一般的な懸念は,我々の多くの製品の需要に悪影響を与え続け,我々の業務に負の影響を与え続ける可能性がある。特に、私たちの多くの製品は選択的医療手続きを減らすことに特に敏感だ。2020年、2021年、2022年の一部の時間で、私たちの製品のマーケティングと販売市場は選択的な医療プログラムを何度も一時停止または減少させ、これは私たちの業務、キャッシュフロー、財務状況と運営結果にマイナスの影響を与えた。
Alpha発表後にフィードバックを収集する時間が予想より長くなれば,選択的手術の延期は製品発表の遅延を招く可能性がある。また,通常我々の製品を使用している施設は再開放できない可能性があり,あるいは再開放しても,患者は外来外科センターのようなリスクの低い施設で手術を行うことを選択する可能性があり,我々の製品はこのような施設で承認されない可能性があり,我々の製品がこのような施設で使用されることをタイムリーにまたは全く承認できない可能性がある。
米国でも他の市場でも,新冠肺炎の大流行の未来の軌跡はまだ不確定であり,特に未来変異の性質やワクチンがこのような未来変異の重篤な疾患の不確実性を予防できるかどうかである。
これらの異なる不確実性を考慮すると,選択的手順の鈍化が2023年以降の業務にどの程度影響を与え続けるかは不明である。著者らは新冠肺炎が著者らの業務に与える影響は様々な要素に依存すると予想し、(I)追加症例波と未来変種の規模、長さと毒性、(Ii)新冠肺炎ワクチンの持続分布、治療効果、改善と公衆受容度、(Iii)患者の診療所と病院訪問の快適度、及び(Iv)新冠肺炎患者の治療が必要なため病院容量が緊張した場合、選択性手術は更に減速する程度である。
36
選択性手術への影響以外に、疫病は著者らの能力及び著者らの第三者サプライヤー、メーカー、販売業者と顧客が肝心な従業員を維持する能力に負の影響を与える可能性があり、そして著者ら及びその複雑な業務を運営するために必要な熟練者の持続的なサービスと可用性を確保する。もし私たちの管理層または他の人員、あるいは私たちの第三者サプライヤー、メーカー、流通業者および顧客の管理層または他の人員が疫病の負の影響を受け、彼らの仕事の職責を履行できない場合、私たちは製造業務、販売活動、研究と製品開発活動、規制作業の流れ、臨床開発計画および他の重要な商業および会社の機能の遅延または一時停止に遭遇する可能性がある。また,我々と従業員との関係は,新冠肺炎への対応により中断される可能性がある。著者らは労働市場が全体的に緊迫しており、競争が日々激しくなっていることを観察し、これはある程度新冠肺炎疫病による労働力不足と対応措置であり、その中には他の雇用主が提供する昇給と業界従業員の自発的な流失が含まれており、第三者サプライヤー、メーカー、流通業者と顧客を含む。
これらすべての要素を合わせると、私たちの業務、財務状況、経営結果に重大な悪影響を及ぼす可能性がある。
新冠肺炎の流行と関連するサプライチェーンと原材料の中断、ロシアとウクライナの間の持続的な衝突、およびこれに対する世界的な反応は、私たちのグローバル業務と私たちのサプライチェーンの運営に持続的な実質的な影響を与える可能性があり、これは私たちの業務業績や財務状況に悪影響を及ぼす可能性がある。
私たちは限られた数量の供給者たちに依存して特定の製品や部品を製造または供給する。私たちのサプライチェーンが中断されたり、重要な供給やコンポーネントの世界的な不足がある場合、私たちは、著しい追加コストおよび/または重大な遅延を生じることなく、他のソースから生産能力を増加させたり、代替または二次ソースを開発することができない可能性があります。例えば、新冠肺炎の疫病は全世界の半導体チップが不足しており、私たちのいくつかの製品は半導体チップを使用している。この不足は主にメーカーが大流行期間中に生産停止や減速を経験したことによるもののようであり、正常な生産能力を回復するためにはいくつかの財政四半期あるいはそれ以上の時間がかかるかもしれない。また、キー原材料供給の制限は、半導体チップや他の部品不足の持続を招く可能性もある。このような状況が続く場合、またはより多くの不足が生じる場合、特により長期的には、このようなコンポーネントを調達し、いくつかの製品を生産する能力に悪影響を及ぼす可能性があり、または、より容易に入手可能なコンポーネントに組み込むために影響を受けた任意の製品を再設計する必要がある可能性があり、追加の規制テストおよび承認が必要となる可能性がある。したがって、私たちの1つまたは複数のサプライヤーが特定の場所または特定の材料または構成要素に関連する任意の中断が私たちの業務に影響を与える場合、私たちの業務は深刻な影響を受ける可能性がある。
ロシアとウクライナの間の持続的な衝突は、米国と他の国家政府がロシアに制裁を科し、世界市場に大きな変動と混乱をもたらした。この衝突の短期的または長期的な影響を予測することはできないが、さらなる制裁、経済および政治的安定の不確実性、インフレ率およびエネルギー価格の上昇、サプライチェーンの挑戦、および通貨レートおよび金融市場への悪影響を含むことができるが、これらに限定されない。また、米政府は、衝突への対応として、米国のロシアへの制裁が米国会社に対するサイバー攻撃の脅威を増加させる可能性があると報告している。これらの増加した脅威は,我々の情報技術システムやネットワークのセキュリティ,および我々のデータのセキュリティ,可用性,完全性にリスクを与える可能性がある.衝突の現在の範囲の著しいエスカレートやさらなる拡大、あるいは世界市場への関連破壊は、私たちの行動結果に重大な悪影響を及ぼす可能性がある。
医療産業の統合が価格優遇の需要をもたらす場合、またはグループ調達組織(“GPO”)や同様のエンティティが私たちをサプライヤーから除外した場合、私たちの業務は悪影響を受ける可能性がある。
医療コストが過去10年間で大幅に上昇したため、立法者、監督機関、第三者支払人はこれらのコストを抑制するために多くの措置と改革を開始した。そのため,管理型医療組織の発展に伴い,調達意思決定と業界統合をまとめることで医療コストを抑える傾向が見られ,これらすべてがより費用対効果のある医療療法の提供を重視している。例えば:
37
医療産業の統合に伴い、業界参加者に製品やサービスを提供する競争がより激しくなり続けている可能性がある。これは、GPO、独立配信ネットワーク、および大きな単一アカウントがそれらの市場力を利用して調達決定を強化し続け、より大きな製造業者がその広範な製品を使用して独占的な配置を確保するために、より大きな価格設定圧力およびいくつかの仕入先を重要市場から除外し続ける可能性がある。GPOが私たちをサプライヤーリストから除外すれば、私たちの純売上高は不利な影響を受ける可能性があります。市場需要、政府規制、第三者清算政策、社会的圧力が世界の医療業界を変え続けることは、私たちの製品価格にさらなる下振れ圧力を加える可能性があると予想される。
また、複数の製品フランチャイズ権を持つ最大設備会社は、大量割引と長年の手配を提供することによって、フランチャイズ権を利用して顧客と広範な契約を締結する努力を強化し、これらの割引と長年の手配は、これらの顧客との接触を阻止したり、価格競争を困難にしたりする可能性がある。
私たちの経営する業界は競争が激しいです。他の人たちの新しい開発は私たちの製品や技術を競争力を失ったり時代遅れにするかもしれない。
医療機器業界は競争が激しい。私たちは大量の会社と競争して、その中の多くの会社は私たちより多くの財務、製造、マーケティング、流通、技術資源を持っています。私たちの多くの競争相手は私たちと競争したり、私たち自身より優れた製品と技術を開発することができるかもしれません。私たちの競争相手はまた、より強力な知的財産権の組み合わせ、より広範な脊柱外科製品の供給とより広範な臨床データによって支持される製品、より確立された流通ネットワーク、医師との強固な関係、私たちが販売している製品と類似した製品の知名度と識別しやすい商標、医療保健提供者および支払人とのより多くの関係の構築、FDAおよび他の規制許可または製品承認および製品増強の獲得と維持におけるより豊富な経験、および私たちよりも豊富な製品発売、マーケティング、および販売経験を持つ可能性がある。私たちの多くの競争相手は特定の製品に集中したり、特定の細分化市場に集中したりして、全体的な市場地位を高めることを難しくしています。競争相手は私たちの製品よりも良い製品を頻繁に発売したり、私たちの製品よりも良い製品を主張したり、私たちの既存または計画中の製品の代替品であり、市場混乱を引き起こす可能性もあり、私たちの製品と競争製品の優位性を区別することが困難になる可能性がある。また、複数の新製品と競争相手の参入は、私たちのいくつかの競争相手に定価戦略を採用させる可能性があり、これは私たちの製品の定価と脊柱市場の全体的な価格設定に不利な影響を与える可能性がある。
また、競争相手よりも低コストまたは性能の良い新製品の開発や発売に成功したり、競合他社と同等の割引の支払いや他のビジネス条項を我々の製品の購入者に提供することもできない可能性がある。私たちの競争相手に関するより多くの情報を知るためには、“競争”の副題下の項目1“業務”を参照してください
また,我々が競争している脊柱や整形外科医療機器業界は,急速かつ重大な技術変革を経験しており,その特徴は。私たちは技術の進歩に伴い、競争が激化すると予想する。他社が開発した新技術や製品が市場に導入されることが多く、これは私たちの製品や技術を競争力を失ったり、時代遅れにしたりする可能性がある。
私たちが製品を販売することに成功する能力は、消費者の製品に対する受容度だけでなく、独立した第三者の製品に対する受け入れ度にも依存する。
私たちが私たちの製品を成功的にマーケティングできるかどうかは、独立した第三者(病院、医師、他の医療提供者と第三者支払人を含む)と患者の製品に対する受け入れの程度にある程度依存する。市場は私たちのすべての製品を受け入れる必要があり、他の事項以外に、私たちは直ちに監督部門の承認および/または承認を得る必要があります
38
私たちは私たちの製品を医師の顧客と支払人に提供し、これは私たちが臨床データを収集し、および/または臨床研究を行うことを要求することができる;私たちの医師の顧客とその従業員が私たちの製品を正確に使用することを効果的に教育し、訓練すること;アメリカ国内外で、連邦医療保険と医療補助計画の下で、個人支払者から、私たちの製品のカバー範囲と適切な精算を獲得し、維持することを要求することができる;神経内科医と整形外科脊柱医師に集中した独立した販売代理と在庫流通業者ネットワークを吸引し、保留し、有効なマーケティング戦略を制定し、私たちの製品の独自の地位を保護することを含み、十分な量の良質な製品を一貫して生産し、需要を満たす。これらの活動の各々および市場が私たちの現在および未来の製品の受け入れに必要な他の活動を達成するためには、協調または新しい製造または撮像技術を使用することに固有のリスク、例えば、追加処理(一般に3 D印刷と呼ばれる)または先進的な光学技術および機械バージョンベースの位置合わせアルゴリズムを含む重大なリスクがある。私たちの任意の製品に関する予期しない副作用や否定的な宣伝は、病院の承認を維持したり、医師、管理型看護提供者、および他の小売業者、顧客、および患者の受け入れ能力を維持したりすることに悪影響を及ぼすかもしれません。
臨床研究費用は高く、広範な監督管理を受けており、その結果、私たちの候補製品の主張を支持しないかもしれない、あるいは副作用の発見を招く可能性がある。
新製品や既存製品の新適応の開発や既存製品の修正を行う際には,臨床前試験,臨床研究あるいは他の臨床研究を行ったり賛助したりする可能性がある。私たちはいくつかの製品に対して発売後の臨床研究を行って、それらの性能或いは最適な使用に関する情報を収集しています。これらの臨床研究から収集されたデータは、最終的に、これらの製品または将来の製品の追加の市場許可または承認をサポートするために使用される可能性がある。もし私たちのすべての新製品が発売前の臨床研究を必要とするならば、これらの研究費用は高く、結果自体は不確定であり、それらはFDAを含むアメリカと海外の多くの政府当局の広範な監督と審査を受け、もし連邦資金に関連する場合、あるいは研究者或いはウェブサイトが連邦保証に署名した場合、人類研究保護事務室とアメリカ国立衛生研究院の更なる監督管理を受ける。例えば、臨床研究はFDA法規、現地法規及び総称して“良好な臨床実践”と呼ばれる原則と標準に符合しなければならない。適用された法規を遵守しないことは、罰金、処罰、研究の一時停止を含む規制や法律実行行動を招く可能性があり、データを無効にし、FDAが提出した文書を支援するために使用できなくなる可能性もある
私たちの未来のどの発売前の臨床研究が計画通りに完成しても、彼らの結果が私たちの候補製品および/または提案された声明を支持するかどうか、あるいはFDAや外国当局と通知機関が彼らが生成したデータの解釈と結論に同意するかどうかを決定することはできない。臨床前研究と早期臨床研究の成功は後の臨床研究も成功することを確保できず、著者らも後の研究結果が早期或いは以前の研究結果を重複することを確定できない。臨床研究過程では、私たちの候補製品が提案の指定用途に対して安全かつ有効であることを証明できない可能性があり、これは、ある候補製品を放棄し、他の候補製品の開発を延期する可能性がある。私たちの臨床研究のいかなる遅延や終了も、私たちが提出した製品申請を延期し、最終的に候補製品を商業化し、収入を創出する能力を延期する。我々の上場製品の臨床研究に登録されている患者も,現在候補製品プロファイルにない不良副作用を経験する可能性があり,そうであれば,これらの発見は市場受容度の低下を招く可能性があり,我々の業務,運営結果,財務状況に実質的かつ不利な影響を与える可能性がある。
そのほか、新冠肺炎の大流行は私たち或いは他の人が私たちのある製品の臨床研究を開始、進行或いは継続する能力を制限或いは制限する可能性がある。このような研究の遅延と中断は、FDA拡大や他の規制部門のわが製品の承認または承認の遅延を招く可能性がある。
もし著者らが臨床研究と協力に頼って臨床前開発を行った第三者が契約要求或いは期待通りに仕事を行っていなければ、著者らは監督管理許可、承認或いはCE適合性証明書を得ることができず、著者らの製品を商業化することもできないかもしれない。
私たちは常に第三者、例えば契約研究機関、医療機関、臨床研究者と契約実験室に依存して、臨床研究とその他の開発活動を助けなければならない。これらの第三者が彼らの契約義務の履行に成功しなかった場合、適用された法規義務を遵守した場合、または予想される最終期限内に完了した場合、またはこれらの第三者が交換する必要がある場合、または彼らが取得したデータの品質または正確性が臨床規程、適用された法規要件、または他の理由を遵守できなかった場合、私たちの臨床前開発活動および臨床研究は延長、延期、一時停止または終了される可能性がある。この場合、私たちは私たちの製品のために規制許可/承認またはCE合格証明書をタイムリーに得ることができないかもしれません。あるいはそれを商業化することに成功して、私たちの業務、経営業績、将来性は実質的で不利な影響を受ける可能性があります。
39
私たちの同種異体骨移植と細胞同種異体骨移植は私たちを何らかのリスクに直面させ、私たちの業務を乱すかもしれない。
私たちの生物製品業務はヒト身体ドナーからの同種移植組織を販売しており、私たちがこれらの組織を販売する能力は、私たちのサプライヤーが寄付されたヒト身体組織を引き続き獲得できるかどうかに依存し、サプライヤーはその処理方法において高い基準を維持している。このようなドナーの供給量は本質的に予測不可能であり,時間の経過とともに変動する可能性がある。同種移植組織はFDAのHCT/P規制モードで管理されており、医療設備、生物或いは薬物としてではない。FDAが将来のある日に移植組織を再分類しないことは保証されず、この製品を人体組織から医療設備に再分類することは、私たちまたはその製品のサプライヤーに悪影響を与える可能性があり、上場前の承認または承認を要求し、追加の発売後の監督管理要求を遵守することによって、私たちはこの業務をより難しく、あるいは高価に展開することができる。
また、移植のためにある人体器官と組織を調達することは“国家臓器移植法”(以下“国家臓器移植法”と呼ぶ)の制約を受け、この方法は皮膚と関連組織を含む価値のある人体器官の譲渡を禁止しているが、人体組織と皮膚の除去、輸送、移植、加工、保存、品質管理と貯蔵に関連する合理的な費用の支払いを許可している。もし私たちが価値のある代価で人体組織の売却や譲渡に関するNOTAの禁止に違反していることが発見された場合、私たちは刑事法執行制裁を受ける可能性があり、これは私たちの運営結果に実質的で不利な影響を与えるかもしれない。
EUとその他の国は統一的な監督管理枠組みと先進的な治療薬物の提案された監督管理が不足しているため、EUの人類由来細胞或いは組織に基づく医療製品の審査過程は広く、冗長で、高価で予測できないかもしれない。その他の面で、私たちのいくつかの生物製品はEU加盟国の法規によって管轄され、これらの法規はHCT/Pの寄付、調達、テスト、コード、追跡可能性、加工、保存、貯蔵と配布を管理している。これらのEU加盟国の法規には、登録、上場、ラベル、不良事件報告、および検査と実行に関する要求が含まれている。いくつかのEU加盟国は新しい冠肺炎とドナーのスクリーニングに関連する新しい要求を含む独自の組織銀行法規を持っている。どのEU加盟国でも私たちの製品に関する様々な規定を遵守しないことは、私たちの製品がその会員国で禁止されたり、私たちに法執行行動を提起されたりする可能性があり、これは私たちの業務、運営結果、そして財務状況に実質的な悪影響を及ぼすかもしれない。
ドナーから組織を回収する不適切な方法や寄付組織が疾病を伝播する不利なメディア報道やその他の負の宣伝は、人々のいくつかの製品に対する広範な受け入れを制限する可能性がある。
米国と国際上の不当あるいは不法組織回収のやり方に関する不利な報告や、処理しない組織が疾病伝播を招く事件は、未来の組織寄付の速度と市場の人体組織を含む技術に対する受容度に影響を与える可能性がある。また,負の宣伝は潜在ドナーの家族が組織を営利団体加工業者に寄付したくなくなる可能性がある。たとえば,身体部位の不正採取の疑いがある例や,不正採取の影響を受けた人体組織製品を販売している会社によるリコールが報道されている。このような報告書と他の報告書は私たちの組織再生事業に否定的な影響を及ぼすかもしれない。
私たちのいくつかの製品は動物由来の材料を含んでおり、追加的な規制を受けるかもしれない。
私たちのいくつかの製品は牛組織から抽出された材料を含んでいる。食品、医薬品、および医療機器を含む動物由来の材料を含む製品は、メディアおよび規制機関によって審査されている。規制当局はこれらの材料を通じて動物から人間に病気を伝播する可能性を懸念している。過去数年間、西欧は動物由来製品の公衆審査が特に厳しく、主に狂牛病を引き起こす病原体に感染した材料が心配され、摂取あるいは移植されると、人類克雅病の変種を招く可能性があり、これは最終的に致命的な疾患であり、現在知られていない治療法である。カナダや米国で発見された狂牛病症例は北米の意識を高めた。
我々の製品を含む動物由来の物質を含む製品は、感染症または他の病原体が伝播する可能性が懸念されるため、追加的な規制を受ける可能性があり、さらには特定の国でも禁止される可能性がある。重大な新規定、又は我々製品の禁止は、我々の業務又は私たちの業務拡大能力に実質的な悪影響を及ぼす可能性がある。
ある国,例えば日本,中国,台湾,アルゼンチンでは,われわれのコラーゲン製品は狂牛病症例が発生していない国からのアキレス腱を用いて加工しなければならないことが規定されている。私たちの製品に使われているコラーゲン原料はニュージーランドから来ています。我々のサプライヤーはすでに米国、EU、日本、台湾、中国、アルゼンチンを含むいくつかの国の許可を得ており、これらの国で販売されている製品にこのコラーゲン原料を使用することができる。狂牛病例のない国から合格した腱由来のコラーゲン原料を得ることができなければ
40
当社のコラーゲン製品を特定の国で販売することは許可されておらず、これは私たちの業務、運営結果、および財務状況に実質的な悪影響を及ぼす可能性があります。
私たちは新製品を市場に出すことに成功できないかもしれません。私たちの製品のために開発される市場機会は私たちが予想しているほど大きくないかもしれません。
競争力を維持し、維持するためには、私たちの製品を引き続き改善し、新製品を開発し、私たちの製品を新市場に投入し、技術進歩に成功する必要があります。そうすることは技術的に挑戦的で、重大な危険と不確実性に関するものだ。我々は計画を行ったにもかかわらず,新製品(製品増強を含む)を開発·発売する過程は本質的に複雑で不確実であり,リスクに関連している。私たちの新しい製品や既存製品の強化または修正の成功は、私たちが能力があるかどうかを含むいくつかの要素に依存するだろう
また、競争相手は、より効率的で、製造コストが低く、価格がより競争力のある製品を開発したり、私たちの製品の前にビジネスに投入する準備をしたりすることができる。競争相手が新製品を発売することは、私たちの製品の値下げを招き、利益が減少したり、市場シェアを失ったりする可能性があり、私たちの製品を時代遅れにしたり、競争力を失ったりする可能性がある。
これらのリスクは私たちの製品の未来の純売上を予測し予測することを難しくさせる。競争相手の前に技術的かつ商業的に実行可能な新製品を一貫して開発し、既存製品を強化したり修正したりすることができなければ、私たちの見通しは実質的で不利な影響を受ける可能性がある。また、私たちの製品(新製品を含む)のために開発される市場機会が私たちが予想しているほど大きくなければ、私たちの業務成長能力に悪影響を及ぼす可能性があります。
また重要なのは、私たちは新製品の発売と既存製品の強化や修正を真剣に管理しなければならないということだ。潜在的な顧客が新しい、強化された、または改善された製品が利用可能になるまで購入を延期する場合、これは私たちの販売に負の影響を与える可能性がある。また、私たちが新しい製品や改善された製品に移行すると、過剰または時代遅れの在庫があれば、時代遅れの在庫の利益率が減少し、ログアウトし、私たちの運営結果が影響を受ける可能性があります。
FDAが将来の製品の510(K)の承認または上場前の承認を与えることが保証されないか、または同等の外国規制機関が外国に同等の承認を与えることは保証されず、将来の製品が必要な承認または承認を得ることができなければ、私たちの業務成長能力に悪影響を及ぼすだろう。
一般的に、適用免除が適用されない限り、医療機器や機器またはその適応の修正は、FDAの発売前に承認または発売前に承認されなければ、米国で発売されなければならない。過去には、私たちはこのような承認を得ていたが、将来的には承認や承認をタイムリーに得ることができず、さらには成功できないかもしれない。FDAおよび同様の外国規制機関から新製品の承認または許可を得るか、または既存製品を強化または修正するプロセスが可能である:
41
私たちの新製品のいくつかは発売前にFDA 510(K)の承認または発売前の承認申請またはPMAが必要です。510(K)の許可を得た装置の任意の修正は、重大な設計および製造変更を含む、その安全性または有効性に著しく影響を与える可能性がある場合、またはその予期される用途、設計、または製造に重大な変化を構成するであろう場合、新しい510(K)の許可を必要とするか、またはPMAの承認を得る必要がある場合がある。同様に,PMAが承認した製品の修正には,PMA付録の提出と承認が必要となる可能性がある.FDAは、製造業者がこれらの決定を行うのを容易にするために、510(K)の承認およびPMA承認を評価するためのデバイス修正のガイドラインを発行した新しい510(K)またはPMAが必要かどうかを最初に決定することを各メーカーに要求する。しかしながら、FDAは、新しい許可または承認が必要かどうかに関する私たちの決定に同意しない可能性がある任意のそのような決定を審査することができる。我々は、510(K)の許可を得たいくつかの製品を修正し、FDAガイドに対する私たちの理解に基づいて、いくつかの変更は新しい510(K)許可を必要としないことを決定した。FDAが私たちの決定に同意せず、新たな510(K)許可またはPMA承認を求めて承認された製品を修正することを要求した場合、私たちはマーケティングを停止したり、私たちの製品を流通させなければならないかもしれません。承認または承認されるまで、修正された製品をリコールする必要があるかもしれません。巨額の規制罰金または処罰を受ける可能性があります。私たちの新製品は、承認や承認を得る上での重大な遅延、または承認または承認を得られなかった場合、業務の能力拡大に重大かつ不利な影響を与えることになります。
米国以外では、承認または承認手続きは国によって異なる可能性があり、追加の製品テストと検証、および追加の行政審査期限が関連する可能性があります。他国で承認または承認を得るのに要する時間は、FDAの承認または承認を得るのに要する時間とは異なる可能性がある。他の国の規制過程には、私たちがアメリカで直面しているすべてのリスクと、他のリスクが含まれているかもしれない。一方の国の有利な規制行動は、他の国で有利な規制行動をとることを確保することはできないが、1つの国では規制許可や承認を得ることができなかったり、遅延したりすることは、他の国の規制過程に悪影響を及ぼす可能性がある。他の国で承認または承認を得ることができなかったか、または承認または承認を得る上でいかなる遅延や挫折が生じても、我々の製品を含めて、すべての要求の適応で承認または承認を得ることができない可能性があることを含む、当社の業務に大きな悪影響を与え、製品の使用を制限し、製品販売に悪影響を及ぼす可能性がある。
ヨーロッパ経済地域(“EEA”)では、EEAで販売されている医療機器の適合性評価を行う通知機関に通知しなければなりません。例えば、私たちの品質システムを大きく変更したり、私たちの設備を重大に変更したりしなければなりません。そして、通知機関は、この変化を評価し、製品が基本的な要求または設備の使用条件に適合しているかどうかを確認する。評価が有利であれば,通知機構は新たなCE適合性証明書や既存のCE適合性証明書の付録を発行することができる.そうでなければ、私たちはEEAで適用された製品をマーケティングし、販売し続けることができないかもしれません。これは私たちの業務、運営結果、財務状況に大きな悪影響を及ぼす可能性があります。
FDAと外国規制機関による新製品(既存製品の修正を含む)に必要な承認や承認がタイムリーに得られるかどうかは確認できません。新製品の承認や承認を速やかに得ることができなければ、我々の財務状況や経営業績に重大かつ不利な影響を与えることになる。
私たちの業務を発展させるために、著者らは医者に対して適切な教育と訓練を行い、彼らに著者らの製品の独特な特性、利益、安全性、臨床治療効果とコスト効果を理解させる必要がある。
私たちの製品を受け入れるかどうかはある程度私たちが医学界を教育する能力があるかどうかに依存し、彼らに私たちの製品が代替製品、プログラムと治療法と比較した独特の特徴、利益、安全性、臨床治療効果と費用効果、及び(Ii)医師を訓練して私たちの製品を正確に使用し、実施することを理解させる。新しく発売された製品や製品を新市場に導入する場合、特に、例えばアメリカでM 6-C人工頚椎を発売します。私たちは医師と販売専門家が参加する専門研修セミナーを通じて、私たちの販売チームや販売業者を支援しています。私たちはまた、手術手順を概説する材料を含む、印刷、ビデオ、およびマルチメディアフォーマットを使用して、様々な言語で販売者および販売業者のためのマーケティング材料を作成します。医師により多くの高度な訓練を提供し、“先進医学規範”と“医療技術規範”に符合するため、著者らは複数の場所で定期的に多言語教育シンポジウムを開催した。しかし,医師に必要な時間と精力を投入して適切な訓練を行うように説得することは挑戦的であり,医学界の教育や医師の適切な訓練への努力は成功しない可能性がある。私たちの製品を使わない医師は、以下のような理由で迷ってしまうかもしれません
42
もし医者が適切な訓練を受けていなければ、彼らは私たちの製品を乱用または無効にする可能性があり、これは患者の結果が満足していない、患者の負傷、負の宣伝、あるいは私たちに対する訴訟を招く可能性がある。また、私たちの製品について医学界を教育できなかったことは、私たちの製品に対する市場の受け入れ能力を弱めるかもしれません。
また、私たちは、影響力のある医師が私たちの製品の推薦と支援が市場の受け入れと採用に重要だと信じている。もし私たちがこれらの医者の支持を得なかったり、長期データが私たちの製品を使用するメリットを示していなければ、医者は私たちの製品を使用しないかもしれません。もし私たちが医者に私たちの製品の利点を信じるように説得できなければ、私たちは私たちの販売を維持したり、増加させることができないかもしれませんし、利益を達成したり維持することもできません。
これに関連して、私たちは医師の訓練方法がFDAおよび他の国および第三国で制定された適用法規に従って行われていると信じているが、FDAまたは他の規制機関が私たちの訓練構成が私たちの製品に貼られていないCEマークやFDA承認のラベルに含まれていない予想される用途や宣伝を促進すると判断した場合、彼らは私たちの訓練を修正したり、警告状、禁止、差し押さえ、民事罰金、刑事罰を含む規制された法執行行動を受けるように要求することができる。
臨床研究が私たちの製品単独と競争製品に対する安全性と有効性を証明しない限り、私たちの製品の販売または私たちの販売価格は悪影響を受ける可能性があります。
一般的に、私たちはアメリカで販売されている製品の510(K)の製造、マーケティング、販売の許可を得ており、ヨーロッパ経済区で販売されている製品にCEマークを貼り付ける権利があります。これまで、510(K)許可、CEマーカー、または他の国/地域における製品登録を支援するために、新しい臨床データを生成することが要求されていない。しかし、EU医療機器法規は2021年5月に以前の医療機器指令に代わり、いくつかの発売前と発売後のデータを提出して、私たちのCEマークを維持することを要求した。また,我々は最近MEDDEV 2.7.1改訂版4により,我々のどの製品システムが臨床データを提出する必要があるかの分析を完了し,欧州委員会の医療機器の臨床評価に対する指導意見を述べた。したがって,われわれが臨床的価値を提供するビジョンと一致するために,我々のある市場製品のために臨床データを収集し始めていることは“リスク因子”の節でより全面的に述べられている。
一部はより費用対効果のある治療を提供することを日々重視しているため、私たちの顧客の購入決定はますます臨床データに基づいて、これらのデータは私たちの製品の価値或いは他の製品に対するわが製品の有効性を証明した。臨床研究を行うのは高価で時間がかかり、結果も確定しない。上記の“臨床研究費用が高く、広範な監督管理を受けており、その結果、著者らの候補製品声明を支持しないか、或いは副作用の発見を招く可能性がある”を見た。私たちは臨床研究を援助しないことを選択するかもしれませんし、援助できないかもしれません。私たちのすべての製品の効果的な競争に必要なデータを生成することができます。一部の原因は私たちの製品の組み合わせの広さです。現在、私たちはすべての製品に対してこのような臨床研究を行いたくありません。リスク調整に基づいて収益がコストを超えることが予想される場合にのみそうします。しかし,我々が1つ以上の製品を選択して支援することができても,そのような研究は成功しない可能性がある。私たちが生成したデータは私たちの既存のデータと一致しない可能性があり、悪い安全性や有効性を示すかもしれません。これは私たちの製品への需要を減らし、将来の販売に悪影響を及ぼす可能性があります。神経内科医および整形外科脊柱医は、競合製品の安全性および有効性をサポートするより強力なまたは任意の臨床データがあれば、私たちの製品を使用することができない可能性がある。もし私たちが私たちの製品の安全性と有効性を支持する臨床データを生成したくない場合、私たちの業務、運営結果、財務状況は実質的な悪影響を受ける可能性があります。
43
また,将来の患者研究や臨床経験は,我々の製品を用いた治療は患者の結果を改善できないことを示している可能性がある
2009年の“アメリカ回復と再投資法案”の成立に伴い、アメリカ衛生·公衆サービス部の医療研究と品質部門はすでに有効性研究を比較し、ある疾病と疾病の治療における異なる薬物、医療機器とプログラムの有効性を決定するために支出を獲得した。私たちのいくつかの製品や私たちの製品と一緒に実行されるプログラムはこのような研究のテーマになるかもしれない。この研究が我々の業務にどのような影響を与える可能性があるかは不明である。また,将来の研究や経験は,我々の製品を用いた治療が患者の結果を改善していないこと,あるいは改善した患者の結果が当初予想されていたよりも小さいことを示している可能性がある。このような結果は、私たちの製品に対する需要を減少させ、第三者支払者の持続可能な精算に影響を与え、予想される収入を達成する能力を著しく低下させ、製品を市場から撤退させ、収益性を維持または向上させることを阻止する可能性がある。さらに、将来の結果と経験が、私たちの製品が意外または深刻な合併症や他の予見できない負の影響をもたらす場合、私たちは重大な法的責任、否定的な宣伝、名声の損害に直面する可能性があり、私たちの製品の売上は大幅に低下する可能性があり、これらはすべて私たちの業務、財務状況、運営結果に実質的な悪影響を与えるだろう。脊柱医療機器市場は特に潜在的な製品責任クレームが出現しやすく、これらのクレームは脊柱外科手術プログラム用医療機器と製品のテスト、製造と販売に固有のものである。
私たちは情報技術システムの中断の悪影響を受ける可能性があり、これは私たちのキャッシュフロー、経営業績、財務状況に悪影響を及ぼす可能性があります。
私たちの運営は私たちの主要な業務機能をすべてカバーしている私たちの情報技術システムに依存します。私たちはこのような情報技術システムに依存して在庫を管理し、補充し、顧客の注文をタイムリーに記入し、私たちのすべての製品やサービスの販売活動を調整し、私たちの行政活動を調整します。私たちの情報技術システムが任意の長時間にわたって重大な中断(例えば、私たちのトラフィックの意外な増加、停止、またはサービス遅延によるシステム容量制限)が発生した場合、在庫および用品の受信または顧客注文を満たす遅延を招き、私たちの顧客サービスおよび関係に悪影響を及ぼす可能性がある。我々のシステムは,自然や人為的なイベントの破壊や中断,あるいはコンピュータウイルス,物理的あるいは電子的な侵入,およびインターネットに影響を与える類似の破壊を受ける可能性がある.このような遅延、問題、あるいはコストが私たちのキャッシュフロー、経営業績、財務状況に実質的な悪影響を与えないことは保証されない。
私たちの業務規模と範囲が拡大するにつれて、私たちの情報技術システムとインフラの信頼性と完全性を維持しながら、私たちの情報技術システムとインフラを改善し、向上させる必要がある。私たちの情報技術システムやインフラの拡張は、業務量が増加する前に大量の財務、運営、技術資源を投入する必要があるかもしれません。業務量が増加する保証はありません。現在も将来も、我々の情報技術システムおよび情報技術または新技術のどのようなアップグレードにも、これらのアップグレードまたは新技術の統合を支援するために、我々の管理および資源が我々のコア業務から移行することが要求される。私たちの経営陣がこれらのアップグレードにかかる時間と資源、サービス中断、または任意の新しいまたはアップグレードされた技術(およびこれに関連する顧客問題)のインストールによる遅延、または任意の新しいまたはアップグレードされた技術が私たちのデータ信頼性に与える影響は、私たちのキャッシュフロー、経営業績、財務状況に実質的な悪影響を与えない保証はありません。
我々の業務の大部分は単一の企業資源計画(“ERP”)プラットフォーム上で動作している.我々の国際業務を効率的に管理するためには,我々の企業資源計画システム,内部電子情報,通信システム,および第三者からのシステムや支援サービスに大きく依存する.これらのシステムのいずれも、電力または電気通信中断、コンピュータハッカー攻撃、または他の一般的なシステム障害の影響を受ける。将来の買収も異なる企業資源計画システム上で動作する可能性があり、新たに買収した業務や会計機能を統合する上で困難に直面する可能性がある。我々のERPシステムのアップグレード或いは拡張の困難、或いは私たちの情報処理に影響を与える全システム或いは局部故障は私たちのキャッシュフロー、経営業績と財務状況に不利な影響を与える可能性がある。
私たちは、ネットワーク攻撃、データ漏洩、または恐喝ソフトウェア攻撃の障害または損害の悪影響を受ける可能性があり、これは、私たちの業務に悪影響を及ぼす可能性があります。
私たちは、電子情報の処理、送信、および記憶、および顧客、サプライヤー、医療支払者、および他の第三者との相互作用を含む情報技術システムによって私たちの業務操作を実行します。他の医療機器会社と同様に,我々の情報技術システムの規模と複雑さは,ネットワーク攻撃,悪意の侵入,崩壊,破壊,データプライバシーの喪失,恐喝ソフトウェア攻撃,あるいは他の重大な中断を容易にする.私たちの情報システムは
44
大量の資源を持続的に投入して、既存のシステムを維持、保護と強化し、新しいシステムを開発し、情報処理技術の持続的な変化、絶えず発展するシステムと監督管理標準、患者と顧客に関連する財務或いは個人情報の日々増加する需要、及び絶えず変化する顧客モードを保護する必要がある。
例えば、第三者は、患者に関連するデータを取得し、私たちの製品の性能を破壊したり、私たちの固有の情報にアクセスするために、私たちの製品に侵入しようと試みるかもしれません。コンピュータに感染し、身代金を払ってロックを解除するまでユーザのアクセスを制限するマルウェアである恐喝ソフトウェアの攻撃を受ける可能性もある。ネットワーク攻撃、侵入、または他の侵入から当社の情報技術システムおよびデータの完全性を維持または保護することができず、不正に患者データおよび個人識別情報へのアクセス、知的財産権の窃取または他の流用資産の行為、または他の方法で私たちの機密または独自の情報を危険にさらし、私たちの運営を妨害し、私たちの業務、財務状況、および運営結果に重大な悪影響を及ぼす可能性があります。
アメリカでは、連邦と州のプライバシーと安全法律は、患者の医療記録と他の健康情報を含む個人情報の機密性を保護することを要求している。ヨーロッパでは、データ保護指令はEUの個人情報を管理することを要求しており、違反が発生した場合、GDPRは私たちの世界収入の4%までの罰金を科す可能性がある。国際的には、一部の国では、現地サーバ上でその市民の個人識別データを保存することを要求する法律も採択されており、これらのデータの送信や処理を制限する可能性がある。2020年1月に施行される“カリフォルニア消費者プライバシー法”(以下、“消費者プライバシー法”と略す)も遵守しなければならない。2020年11月、カリフォルニア州はCCPAに基づいて消費者プライバシー権を拡大し、GDPRとより緊密に結合させる“カリフォルニアプライバシー権法案”(CPRA)を可決した。CPRAは2023年1月1日に施行され,2022年1月1日以降に収集された情報に適用される。CCPAやCPRAなどの法案は、保険会社のために新たなデータプライバシー義務を創出し、その情報を開示しない権利を選択することを含むカリフォルニア住民に新たなプライバシー権を提供している。CCPAはまた、特定のデータ漏洩に対して法定損害賠償を有する個人訴権を作成し、それにより、データ漏洩に関連するリスクを潜在的に増加させる。カリフォルニアの立法機関がCPRAをどのように追加的に修正するか、あるいはどのように説明するのかは不明だ。私たちは、私たちが規制を適用する期待を達成し、これらの規則を遵守する持続的なコストは私たちの業務に重要ではないが、新しい法規のために重要になるかもしれないと信じている。私たちがこれらの規定を守ることができる保証はありません, または、重大なデータ漏洩を回避するか、または適用されるデータプライバシー法規に準拠できないことによってもたらされる可能性のある負の名声および他の影響は、いずれも、私たちのビジネス、財務状態、または運営結果に重大な悪影響を及ぼす可能性がある。
近年、世界各地の会社が電信為替“釣り”攻撃の急増を目撃しており、これらの攻撃は従業員をだまして会社の銀行口座のお金を犯罪者の銀行口座に振り込もうとしている。場合によっては、会社はこのような比較的簡単な攻撃で数百万ドルを損失し、これらの資金は往々にして取り戻すことができない。我々は従業員にこれらのタイプの攻撃を認識し,適切な予防措置をとるように訓練しているが,近年攻撃者が使用する技術の複雑さが向上しており,我々に対する成功した攻撃は大量の資金損失を招く可能性がある.
サイバー攻撃のリスクに対する保険を持っているにもかかわらず、このような事件に関連する責任が保険カバー範囲の制限を超えないか、またはそのような保険が合理的で商業的に許容可能な条項で提供され続けることを保証することもできない。将来的に十分な保険範囲を維持するコストが大幅に増加すれば、我々の経営業績は実質的な悪影響を受ける可能性がある。
気候変動の実際的な影響や気候変動に対応するための法律、法規、または市場措置は、私たちの運営や運営結果に悪影響を及ぼす可能性がある。
時間の経過とともに、気候変化による天気パターンの変化は、ハリケーン、竜巻、地震、野火、干ばつ、極端な温度または洪水のようないくつかの不利な気象条件および自然災害の頻度、深刻さまたは持続時間を増加させることが予想され、すべての状況は、より深刻な業務およびサプライチェーンの中断を招く可能性があり、私たちの製品と施設、ならびに病院、医療施設および他の顧客のインフラに損害を与え、労働力供給を減少させ、原材料とコンポーネントのコストを増加させる。気候変動は、我々の製品需要や治療の医療条件のある人の数に実質的な影響を与えないことが予想されるが、気候変化は、ウイルスや空気伝播疾患の伝播などの影響をもたらす可能性もあり、病院や他の医療施設および/またはサプライチェーンに圧力を与え、業務を展開する選択的手術市場を混乱させるような予測不可能な事件を引き起こす可能性がある。さらに、気候変動に対する公衆の関心は、気候変動の影響を軽減するための新しい法律または規制要件をもたらす可能性があり、その中には、より厳しい環境法律および法規によって、または既存の法律および法規をより厳格に実行することが含まれている可能性がある。これらの発展はコンプライアンスコストの増加を招く可能性があり、原材料調達、製造運営、私たちの製品流通に悪影響を与え、私たちの運営と運営結果に悪影響を及ぼす可能性がある。
45
もし私たちの任意の製造、開発、あるいは研究施設が損傷し、および/または私たちの製造プロセスが中断すれば、私たちは供給中断、収入損失に遭遇する可能性があり、私たちの業務は深刻な損害を受ける可能性があります。
我々の製造、開発または研究施設の損傷または業務運営の中断については、自然災害(例えば、地震、野火および他の火災または極端な天気)、停電、通信中断、許可されていない進入、または他の事件(例えば、インフルエンザまたは他の健康流行病(例えば、新冠肺炎大流行))を含み、一部または全ての製品の開発および製造を一定期間停止させる可能性がある。私たちが維持しているこれらの施設の財産損失および業務中断保険は、この場合のすべての損失をカバーできない可能性があり、将来的に許容可能な条項で保険を更新したり、合理的な費用で保険を更新したり、そのような保険を受けることができない可能性があります。もし私たちの施設が損傷したら、交換が難しいかもしれませんし、修復や交換のために大量の準備時間が必要かもしれません。特に、カリフォルニア州オーウェンの工場で私たちのいくつかの生物製品を生産しています。この施設のいかなる損傷も、これらの製品の需要を適時に満たす能力に悪影響を及ぼす可能性があります。高度な慎重さから、2020年10月、シルヴィラドール大火の脅威により、私たちは一部の生物製品の完成品在庫をオーウェン工場からカールスバッドオフィスに移転し、この大火はカリフォルニア州オーランド県の人員を避難させた。私どもの業務運営の中断は、当社の仕入先の施設損傷や業務運営中断による可能性があります。例えば、私たちのオーウェン工場で“クリーンルーム”滅菌を維持するために必要な使い捨て物品や他の材料を得ることができない場合、私たちはその工場で製品を生産し続けることができないかもしれない, どの製品が私たちの総収入の大きな部分を占めていますか。私たちの製造業務および市場需要能力を満たすいかなる重大な中断も、当社の独立販売エージェントや在庫流通業者や医師顧客を含む重要な利害関係者が、より信頼性の高い製品源に移行しているため、私たちの販売および収入に悪影響を及ぼす可能性があります。
私たちの多くの製品は第三者メーカーに依存している。
私たちは第三者メーカーと契約を結び、医療機器業界の多くの他の会社のように、私たちの多くの製品を生産します。もし私たちまたはそのようなメーカーが生産や納品計画を満たしていなければ、このような製品を販売する能力に悪影響を及ぼす可能性があります。また、私たちが直接製品を製造しても第三者メーカーを利用しても、材料不足と損傷、労働力の停止、製品のリコール、製造欠陥とその他の類似事件は生産を延期し、適時に新製品を市場に出す能力を抑制します。例えば,リバースエリートとリバース進化同種移植片の供給はヒト身体ドナーからのものであり,これらの組織を販売する能力はMTFが寄付されたヒト身体組織を獲得し続けるかどうかに依存し,彼らは処理方法において高い基準を維持し続けている。
私たちは限られた数の第三者サプライヤーに依存して加工活動、部品、原材料を行い、これらのサプライヤーのいずれかを失ったり、彼らは私たちの品質と他の要求を満たす十分な材料供給を提供することができなくて、私たちの業務を損なう可能性があります。
外部サプライヤー、その中のいくつかは独占サプライヤーで、私たちの生物製剤と脊柱インプラント製品を生産するために必要な製品、原材料と部品を提供してくれます。私たちは、特定の製品、原材料、またはコンポーネントが一定期間利用できない場合、サプライヤーがISOまたは他の認証を失ったこと、または以下のリスク要因の下で説明された任意の中断を含む、当社の生産が深刻な妨害を受けないように、十分な製品、原材料、およびコンポーネント在庫を維持するために努力している:もし私たちの任意の製造、開発または研究施設が損傷し、および/または私たちの製造プロセスが中断された場合、私たちは供給中断、収入損失を経験する可能性があり、私たちの業務は深刻な損害を受ける可能性がある。例えば、私たちの一定数の製品はチタンを必要とし、チタンは第三者サプライヤーから来た。このような製品に必要なチタンは直接ロシアからのものではないが、現在ロシアとウクライナに関連する地政学的事件はより広範なチタンサプライチェーンに負の影響を与えており、それに関連する或いはそれによって発生した地政学的事件と要素は制裁を実施することを含み、私たちの現地供給源が直ちに私たちにチタンを供給する能力にマイナス影響を与える可能性がある。さらに、私たちのいくつかのサプライヤーは、MDRに従うのではなく、EUで彼らの製品を提供することを停止することを選択するかもしれません。これは、これらの製品のための代替供給源を探すことを要求します。私たちの生産中のどのような中断も、私たちの名声、業務、財務状況、運営結果を損なう可能性があります。
私たちは代替供給源があると信じているにもかかわらず、多くの場合、私たちのサプライヤーを交換することは非現実的または困難かもしれない。例えば、FDAまたは他の外国規制機関が受け入れ可能な他の供給者から同様のサービスまたは製品を得ることは困難である可能性があり、これらの供給者は、許容可能なコストで適切な供給量を提供することができる。また、もし私たちが私たちの製品のいくつかのサービスやコンポーネントを新しいサプライヤーに移行することを要求された場合、これらの代替サプライヤーが提供するサービス、コンポーネント、または材料を使用することは、私たちの運営を変更する必要があるかもしれません。もし私たちが製品のキーコンポーネントのメーカーの交換を要求された場合、私たちは、新しいメーカーの施設、プログラム、運営が私たちの品質と適用された規制要件に適合しているかどうかを検証しなければなりません。これは、私たちが製品を適時に製造する能力をさらに阻害する可能性があります。新しいサプライヤーへの移行は時間がかかり高価かもしれません
46
私たちの運営や製品交付が中断される可能性があり、私たちの製品の性能仕様に影響を与える可能性があり、あるいはこれらのシステムの設計を修正することが要求されるかもしれません。
もし私たちがどんな理由でも私たちの品質と他の要求を満たすのに十分な数の脊柱インプラント製品、原材料、またはコンポーネントをタイムリーに得ることができない場合、私たちは新しいまたは代替的な供給源が見つかって資格を得るまで、十分な数の製品を生産することができないかもしれません。したがって、私たちは顧客を失う可能性があり、私たちの名声は損なわれる可能性があり、私たちの業務は影響を受ける可能性があります。また、私たちの製造と互換性がないか、私たちが知らない部品や原材料の中で是正されていない欠陥やサプライヤーの変化は、私たちの製品を製造する能力を損なう可能性があります。
また、2012年の医療機器使用料改正案や他の医療機器条項を含むFDASIAによると、すべての米国や外国メーカーは、米国で販売するためにFDA機関登録と完全な医療機器リストを持っていなければならない。私たちの施設は実質的にこれらの要求に適合していると信じているが、外国契約メーカーから製品を調達している。私たちのいくつかの外国契約製造業者は適用された要求を守らず、FDAに登録しないことを選択するかもしれない。この場合、私たちは適用要件に適合する他の外国契約製造業者がいるかどうかを確認する必要がある。もしこのような外国契約メーカーが私たちの製品の独占サプライヤーであれば、私たちは別のサプライヤーを見つけることができない可能性があります。
また、私たちはアメリカ組織銀行協会の認証を得た少数の組織バンクに依存して人体組織を供給し、これは私たちの骨移植の代替品である生物製品の重要な構成要素である。これらの源から組織を得ることができなかった場合、またはこれらの源を直ちに処理することができなかった組織は、生物製品の需要を効果的に満たす能力を妨害するであろう。人体組織を生物製品に加工することは労働集約型であり、安定した供給流を維持することは挑戦的である。そのほか、死亡率の季節的変化により、私たちの生物製品に使用されるいくつかの希少組織は特に供給が需要に追いつかない場合がある。各国政府が新冠肺炎で追加のドナー検査を要求すれば、組織供給を緊張させる可能性もある。私たちは私たちがサプライヤーから得た人体組織が現在のレベルで供給されるか、あるいは私たちの需要を満たすか、あるいは他の認可された組織ライブラリと商業的に合理的な条項を交渉することに成功することができるだろう。
もし私たちが私たちの独立販売代表と流通業者ネットワークを維持して拡大できなければ、私たちは私たちの収入を維持したり増加させることができないかもしれない。
私たちは独立した販売代表と流通業者を通じて多くの国で私たちの製品を販売しています。通常、私たちの独立販売代表と流通業者はそれぞれの地域で私たちの製品を販売する独占的な権利を持っています。もし私たちの独立販売代表や流通業者が私たちの製品を十分に宣伝、マーケティング、販売できなければ、私たちの売上は大幅に減少するかもしれません。私たちは独立販売代表や流通業者との合意期間はそれぞれ異なり、一般的には1年から10年まで様々です。私たちの標準流通契約の条項によると、もし他方に重大な違約が発生した場合、双方は契約を終了する権利があり、もしディーラーが合意した販売目標に達していない場合、あるいは時間通りに支払うことができなければ、私たちは通常契約を終了する権利がある。私たちと独立販売代表または流通業者との既存の関係を終了することは、ビジネス的に許容可能な代替流通スケジュールが制定されるまで、私たちのビジネスに悪影響を及ぼす可能性があります。また、私たちは、世界的に不況や災害に比例しない影響を受けている可能性のある地域で業務を展開しており、既存または将来の売掛金が回収できない可能性があるリスクを担っており、これらの流通業者や病院が業務中断に遭遇した場合、継続的な売掛金や倒産の支払いを停止している。
また、私たちは地理的に分散した流通ネットワークを管理し、このネットワークを構成する独立販売代表と流通業者を維持する方面で巨大な挑戦とリスクに直面しており、私たちが新製品を発売し、既存製品に対してマーケティングに力を入れることに伴い、私たちはマーケティングと販売努力の範囲を拡大し、新しい独立販売代表と販売業者を募集する必要があるかもしれない。独立した販売代表と流通業者は脊柱看護実践、脊柱損傷と疾病及び脊柱健康などの各領域で豊富な技術専門知識を持つ必要があり、彼らは最高生産性を実現するために訓練と時間が必要である。私たちは合格した独立販売代表と流通業者を引き付けたり維持したりすることはできないかもしれませんし、割引や商業合理的な条項で彼らと協定を締結することもありません。これは、限定される訳ではないが、我々の既存の製品の組み合わせに存在する欠陥または差、独立販売代表および販売業者サービスの激しい競争、または代表または流通業者が受ける可能性のある制限的契約に関連する破壊、および潜在的な訴訟および関連費用を含む多くの要因によるものである可能性がある。私たちはまた、私たちと長年協力してきた独立販売代表や流通業者が意外に離脱した状況に直面するかもしれない。私たちがより多くの合格した独立販売代表や流通業者と協定を締結しても、新しい販売代表や流通業者は通常、完全な運営効率を達成するのに6~12ヶ月かかり、彼らは私たちが予想しているように迅速に収入を発生させ、必要な資源を投入して私たちの製品を効果的にマーケティングし、販売することはできないかもしれない, 最終的に私たちの製品を販売することに成功しました私たちの成功は私たちが採用、訓練、維持を続ける能力があるかどうかに大きくかかっている
47
合格した独立販売代表と流通業者を激励した。もし私たちが国内や国際で私たちの販売やマーケティング能力を拡大することができなければ、新しい独立販売代表や流通業者を十分に訓練していなければ、あるいは私たちの販売ネットワークが高い回転率を経験していれば、私たちの製品を十分に商業化できないかもしれないし、根本的にできないかもしれません。これは私たちの業務、運営結果、財務状況に悪影響を及ぼすでしょう。
また、私たちの独立販売代表と流通業者は私たちの従業員ではないので、私たちは彼らの活動に対する統制が限られており、通常私たちは彼らと独占的な関係を構築しない。もし彼らのうちの1つ以上が競争相手に保留されていれば、独占的であっても非独占的であっても、彼らは私たちから私たちの競争相手に業務を移すことができ、これは私たちの販売に実質的な悪影響を及ぼすかもしれない。
私たちは私たちの高度な管理チームに頼っている。
私たちの成功は私たちの高度な管理チームのメンバーのスキル、経験、表現にかかっており、彼らは私たちの運営の管理と私たちの業務戦略の実施に重要です。私たちの上級管理チームは重要な人保険を持っておらず、1人以上の重要な幹部を失うことは私たちの運営に実質的な悪影響を及ぼすかもしれない。また、私たちの上級管理チームのどんな変動も、私たちの経営業績やキャッシュフローに悪影響を及ぼす可能性があります。
競争のために、私たちは重要な従業員を引き付け、維持し、激励しなければならない。もし私たちがそれができなければ、私たちの運営結果に悪影響を及ぼすかもしれない。
競争のために、私たちは管理、技術、販売、マーケティング、研究開発、財務、情報と技術及び他の異なる背景、経験と技能を代表する支持的な職の従業員を含む幹部と他の肝心な従業員を誘致、維持し、激励しなければならない。合格した幹部、エンジニア、技術者と販売代表を募集と維持することは私たちの業務に重要であり、医療機器業界の経験豊富な従業員に対する競争は非常に激しいかもしれない。私たちのブランドと名声、そして多様で包括的な労働環境を維持して、私たちのすべての従業員がすくすくと成長できるようにすることは、私たちが従業員を募集し、維持する能力にとって非常に重要だ。もし私たちの採用がそんなに成功しなければ、あるいは私たちが高技能労働者や重要な指導者を引き留めることができなければ、私たちが成功した製品やサービスを開発して提供する能力は悪影響を受ける可能性がある。
また、キースタッフの交代は困難で高価で長引く過程である可能性があり、退職従業員のすべての責任を負うことができる他のスタッフはいないかもしれません。私たちの業界の会社間の適格人材に対する競争は非常に激しく、特に重要なポストの競争は、私たちが合格人材を競争する多くの組織がわが社よりも多くの財政や他の資源、そして異なるリスク状況を持っており、それらをより魅力的にすることができるかもしれない。私たちのすべての従業員は、私たちの管理者を含めて、予告なく、いつでも彼らの私たちの雇用関係を終了することができます。もし私たちが必要に応じて高い素質の人材を誘致して維持することができなければ、私たちは私たちの財務や他の目標を達成できないかもしれない。
合格した幹部と肝心な従業員を吸引、維持、激励するために、私たちは従業員の株式オプションと制限的な株式単位のような株ベースの奨励を利用している。いくつかの報酬は時間の経過に応じて付与され、他のいくつかの報酬は、業績または市場に基づくいくつかの条件の達成に基づいて付与される。普通株価格の表現で評価すれば、このような株式奨励の価値は上昇せず、もはや価値のメリットとみなされなくなり、私たちが従業員を引きつけ、維持し、激励する能力は不利な影響を受ける可能性があり、これは私たちの運営結果にマイナス影響を与える可能性があり、および/または現金や他の形態の給与支出を増加させる必要がある。
また、今後の内部成長は、私たちの経営陣に大きな追加責任をもたらす可能性があり、成長を効率的に管理するために、より多くの従業員を確定、採用、維持、インセンティブ、統合する必要があるだろう。もし私たちがこのような成長を効果的に管理できなければ、私たちの支出は予想よりも増加するかもしれないし、私たちは私たちの目標を達成できないかもしれないし、私たちの収入を創出および/または増加させる能力は弱まるかもしれない。
私たちの業務は国際販売や運営に関連する経済、政治、規制、その他のリスクの影響を受けている。
私たちは多くの国で私たちの製品を販売しているので、私たちの業務は国際業務の展開に関連するリスクの影響を受けています。国際業務の純売上高は引き続き私たちの総純売上高の大部分を占めると予想しています。また、私たちのいくつかの製造施設とサプライヤーはアメリカ以外に位置しています。したがって、私たちの将来の業績は様々な要素の影響を受ける可能性があります
48
私たちの知的財産権に関するリスクは
私たちは私たちの能力に依存して私たちの知的財産権と所有権を保護するが、私たちはこれらの資産を秘密にしたり、保護されていることを確実にすることができないかもしれない。
私たちの成功は、私たちの現在と未来の技術と製品を保護し、私たちの知的財産権を守る能力に大きくかかっている。もし私たちが私たちの知的財産権を十分に保護できなければ、競争相手は私たちの製品と似ているか、または私たちと直接競争する製品を製造して販売するかもしれない。私たちはすでに私たちの技術に関する多くの特許を取得しており、私たちは特許出願を提出し、引き続き提出される予定で、これらの特許出願は、米国を含む各国の新しい開発技術や製品の保護を求めている。米国のいくつかの特許出願は、特許が発表されるまで秘密にされている。発見の公表は実際の発見より数ヶ月遅れることが多いので、私たちは最初の発明や私たちの発見について特許出願を提出した会社ではないかもしれません。さらに,米国特許商標局には大量に蓄積された特許出願があり,特許出願を承認または拒否するのに数年かかる可能性がある。私たちのいかなる特許出願や、私たちに発行または許可された既存または未来の特許についても特許を発行しないかもしれませんし、私たちの製品に十分な保護または競争優位性を提供しないかもしれません。発行された特許は私たちの競争相手によって挑戦され、無効に宣言され、または回避されるかもしれない。また、私たちの特許権は、私たちの競争相手が私たちの製品と似ているか、機能的に同じ製品を開発、使用、または商業化することを阻止しないかもしれません。また、私たちの研究製品について特許を発行しなければ、これらの製品に関する情報を秘密にすることができないかもしれません。さらに、私たちの任意の製品に関連する特許が失効または失効すれば、私たちは新しい市場参入者によるより大きな競争に直面する可能性がある。
私たちはまた、ビジネス秘密、非特許専門知識、および持続的な技術革新に依存しており、私たちは、譲渡者、ライセンシー、サプライヤー、従業員、およびコンサルタントと秘密保護協定を締結することによって、これらの技術革新を部分的に保護している。このような合意は違反される可能性があり、違反が発生すれば、十分な救済措置がないかもしれない。知的財産権の所有権や秘密保護協定の適用性または実行可能性について議論される可能性がある。さらに、私たちの商業秘密とノウハウは私たちの競争相手に知られたり独立して開発されるかもしれない。
49
契約措置に加えて、私たちは物理的および技術的セキュリティ措置を使用して、私たちの固有の情報の機密性を保護しようと努力している。例えば、許可アクセス権限を有する従業員や第三者がビジネス秘密を盗用した場合、このような措置は、我々の固有情報を十分に保護できない可能性がある。私たちの安全対策は、従業員やコンサルタントが私たちのビジネス秘密を盗用して競争相手に提供することを阻止できないかもしれませんが、このような不正行為に対する追跡権は、私たちの利益を十分に保護するための十分な救済措置を提供できないかもしれません。許可されていない当事者たちはまた、複製や逆工事をしようとするかもしれないし、私たちは独自の製品のいくつかの側面だと思う。強制執行側が商業秘密を不正に開示したり流用したりする主張は困難であり、高価で時間がかかる可能性があり、結果は予測できない。
私たちは、従業員、コンサルタント、またはコンサルタントとの間の合意が無効になったり、以前または競争していた譲渡契約義務と衝突したりする第三者のクレームに直面する可能性があり、これらの合意は、彼らが知的財産権を私たちに譲渡することを要求し、これは、私たちが開発した知的財産権に関する所有権紛争を引き起こすか、またはそのような知的財産権の商業的価値を取得する能力を発展させ、妨害する可能性がある。所有権紛争を解決するためには訴訟が必要かもしれません。もし私たちが成功しなければ、私たちは特定の知的財産権の使用を禁止されるかもしれません。またはその知的財産権上の私たちの独自の権利を失う可能性があります。どんな結果も私たちの業務と競争の地位を損なう可能性がある。
また、いくつかの外国の法律は、もしあれば、アメリカの法律のように私たちの知的財産権を保護しないかもしれない。私たちのいくつかの発行された特許と出願されている特許はアメリカにしかないので、私たちは他の国で対応する特許保護範囲が不足している。したがって、私たちは競争相手が他の国で私たちのいくつかの製品と似たような製品を販売することを阻止できないかもしれない。
もし私たちが私たちの技術的な特許を獲得し、保護し、実行することができなければ、私たちの商業秘密を保護することができなければ、この能力は私たちの業務、運営結果、財務状況に実質的な悪影響を及ぼすかもしれない。
第三者は私たちが彼らの独占権を侵害していると主張し、私たちのいくつかの製品を製造して販売することを阻止するかもしれない。
私たちの成功は、米国および外国における私たちの運営能力、すなわち他人の特許および独自の権利を侵害することなく運営され、侵害が発生したときに第三者が保有する特許または独自の権利の適切な許可を得る能力にある程度依存する。
医療機器業界では新製品の製造,使用,販売においてすでに多くの訴訟が発生している。このような訴訟は第三者特許または独占権の有効性と侵害性に関するものだ。私たちは第三者の特許または独自の権利の侵害に関する疑いを弁護することを要求されるかもしれない。他の事項を除いて、このような訴訟はすべて可能です
医療機器業界内の特許および知的財産権紛争は、通常、譲渡、許可または同様の手配によって解決されるが、これらの手配に関連するコストは高く、長期的な特許料の支払いを含む可能性がある。したがって、司法や行政訴訟で不利な裁決を下したり、必要な譲渡や許可を得られなかったりすると、大量の損害賠償(判決された損害賠償の3倍まで増加することができる)および/または巨額の印税を支払わなければならない可能性があり、特定の製品の製造または販売を阻止したり、許可を得たり、侵害を回避するために製品を再設計することができない限り、これらの製品を販売するコストを増加させる可能性があります。このような許可は合理的な条項で提供されない可能性があり、もしあれば、他人の知的財産権を侵害しないように私たちの製品を再設計できる保証もありません。もし私たちが必要なライセンスを取得できなかった場合、あるいは私たちの製品や技術を必要な変更をしなければならない場合、私たちは既存製品を市場からリコールしなければならないかもしれないし、私たちの1つまたは複数の製品を商業化できないかもしれません。これらはすべて私たちの業務、運営結果、および財務状況に実質的な悪影響を及ぼす可能性があります。
また、私たちの製品は第三者の独占権を侵害しているため、私たちは一般的に私たちの顧客と販売代表を賠償します。第三者は私たちの顧客や販売代表に権利侵害を請求するかもしれない。このようなクレームは、このようなクレームの是非にかかわらず、私たちの顧客または販売代表を代表して、長引く費用の高い訴訟を開始または弁護する必要があるかもしれない。これらのクレームのいずれかが成功すれば、以下の会社を代表して損害賠償金を支払うことを余儀なくされる可能性がある
50
私たちの顧客や販売代表または彼らが使用している製品のためのライセンスを取得する必要があるかもしれない。もし私たちが商業的に合理的な条項ですべての必要な許可を得ることができなければ、私たちの顧客は私たちの製品の使用を停止させることを余儀なくされるかもしれない。
もし私たちが訴訟や他の手続きを通じて私たちの知的財産権を保護または実行しようとするなら、これは私たちに多くの時間とお金がかかるかもしれないし、結果はまだ確定していない。
私たちの知的財産権を保護または実行するために、私たちは、侵害訴訟、異議訴訟、または他人の固有の権利を侵害していないと裁判所が宣言すること、または彼らの権利が無効であるか、または実行できないことを第三者に対して開始または抗弁しなければならないかもしれない。私たちは私たちの知的財産権を実行したり、私たちの知的財産権を挑戦から保護するのに十分な資源がないかもしれない。私たちが勝訴しても、訴訟コスト、管理や他の資源の移転を含めて、私たちの収益性に影響を与え、私たちの財務資源に大きな圧力を与える可能性があります。
私たちが知的財産権を行使する能力は私たちが侵害行為を検出する能力にかかっている。その製品で使用されているコンポーネントを宣伝しない侵害者を発見することは困難かもしれない.さらに、競争相手または潜在的な競争相手の製品侵害の証拠を得ることは困難または不可能である可能性がある。医療機器業界の特徴は特許数が多く,特許侵害告発訴訟が頻繁であることである。知的財産権侵害と許可手配をめぐる当事者たちの告発が手紙を交換することは珍しくない。また,医療機器会社の特許地位は,我々の特許地位を含め,複雑な法律や事実問題に関与している可能性があるため,我々がすでにあるいは獲得可能な任意の特許主張の範囲,有効性,実行可能性は確定的に予測できない。
私たちは、私たち、私たちの従業員、または私たちの独立販売代理または在庫流通業者が、私たちの競争相手のいわゆるビジネス秘密を誤って使用または開示したり、私たちの競争相手との競争禁止または入札合意に違反したりするという告発を受けるかもしれない。
私たちの多くの従業員は、私たちの競争相手や潜在的な競争相手を含めて、他の医療機器会社に雇われています。場合によっては、私たちに参加する前に。また、私たちの多くの独立販売代表や流通業者は、競争相手の製品を販売したり、過去に販売したりしたことがある。私たちは、私たち、私たちの従業員、または私たちの独立販売代表または流通業者が、前の雇用主または競争相手の商業秘密または他の固有の情報を意図的に、意図的に、または他の方法で使用または漏洩した疑いの影響を受けるかもしれない。さらに、私たちは、私たちが従業員または独立販売代理を奨励/協力することが、彼または彼女の入札禁止または入札協定の条項に違反することを引き起こす可能性があるという疑惑を受けているかもしれない。このような疑いに対抗するために訴訟を提起する必要があるかもしれない。訴訟は高価で時間がかかり、経営陣の注意と資源を私たちの業務から移すかもしれない。私たちが勝訴しても、訴訟費用は私たちの収益性に影響を及ぼすかもしれない。もし私たちが勝たなければならない場合、私たちが支払わなければならないかもしれないいかなる損害賠償に加えて、私たちは貴重な知的財産権や従業員、独立販売代表、または流通業者を失う可能性がある。このような訴訟やその脅威が、私たちが重要な従業員、販売代表、または流通業者を採用し、維持する能力に悪影響を与えないことは保証されない。
訴訟や製品責任に関するリスク
私たちは製品や他の責任クレームの影響を受けるかもしれません。これらのクレームは保険範囲内ではない可能性があり、巨額の費用を支払うことを要求するかもしれません。
私たちはこのようなクレームが有効であるかどうかにかかわらず、製品責任と他の責任クレームの固有のリスクとそれに関連する否定的な宣伝に直面している。脊柱手術は出血、神経損傷、麻痺、甚だしきに至っては死亡を含む深刻な合併症の極めて大きなリスクに関連する。また、もし神経外科医と整形外科脊柱外科医師が私たちの製品を使用する上で十分な訓練を受けていない場合、彼らは私たちの製品を誤用或いは無効に使用する可能性があり、これは患者の不満な結果或いは患者の負傷を招く可能性がある。私たちは製品責任訴訟の対象になる可能性があり、コンポーネントの故障、故障、製造欠陥、設計欠陥、或いは製品関連リスク或いは製品関連情報を十分に開示していないことによる不安全状況或いは患者の負傷を告発する。また、同種異体インプラントと人体組織修復と治療技術の開発は疾病を人類の受容者に伝播させる特別なリスクをもたらす可能性があり、どのような伝播も私たちに対する製品責任のクレームを招く可能性がある。
製品責任クレームの弁護コストは高く、私たちの経営陣の注意を分散させ、もし私たちが弁護に成功しなければ、私たちへの巨額の金銭賠償や費用の高い和解を招く可能性がある。さらに、私たちの1つ以上の競争相手に対する成功した製品責任クレームは、私たちに対するクレームを招くか、あるいは私たちが似たようなクレームを受けやすいという印象を与える可能性があります。私たちに提起されたいかなる製品責任クレームも、正当な理由の有無にかかわらず、結果が十分に追及されているか否かにかかわらず、私たちの製品に対する需要の減少、私たちの名声が損なわれていること、重大な訴訟費用、製品のリコール、収入損失、新製品や候補製品を商業化することができないこと、そして私たちの製品に対する否定的な宣伝を招く可能性がある。どれも既存の顧客と潜在的な顧客の間での私たちの名声と
51
私たちの業務、財務状況、そして経営結果。また、いくつかの製品をリコールすることは、製品責任クレームの結果であるか否かにかかわらず、重大なコストと顧客損失を招く可能性がある。
私たちは製品責任保険の金額と範囲を維持し、私たちは合理的で十分だと思う。しかしながら、製品責任または他のクレームが私たちの保険カバー範囲を超えないことを保証することはできず、このような保険が合理的で商業的に許容可能な条項で提供され続けるか、または全く不可能であることを保証することはできない。成功した製品責任クレームは私たちの保険カバー範囲の制限を超えて、私たちが大量のお金を支払う必要があるかもしれませんし、私たちの財務状況に実質的な悪影響を及ぼすかもしれません。また、いくつかの製品をリコールすることは、製品責任クレームの結果であるか否かにかかわらず、重大なコストと顧客損失を招く可能性がある。
私たちの保険証書は高くて、私たちをいくつかのリスクから保護するだけで、これらのリスクは私たちに多くの未保険の責任を負わせるだろう。
私たちは私たちの業務が直面しているか、直面する可能性のあるすべての種類のリスクに保険をかけていません。私たちが維持するいくつかの保険書には製品責任保険、役員と高級管理者責任保険、財産保険と労災賠償保険が含まれています。しかし、私たちは私たちを損失から守るために合理的な費用、十分な金額、または範囲で保険範囲を維持できるかどうか分からない。将来的に十分な保険範囲を維持するコストが大幅に増加すれば、我々の経営業績は実質的な悪影響を受ける可能性がある。たとえ保険があっても、請求金額は私たちの保険範囲を超えるかもしれません。あるいは保険条項によっては、保険範囲から除外される可能性があります。いかなる重大な未保険債務も私たちが大量の費用を支払う必要があるかもしれません。これは私たちの現金状況と経営業績に悪影響を与えます。
潜在的買収,投資,資産剥離に関するリスク
新しい事業機会(買収を含む)を探し、追求し、実施する努力は成功しない可能性があり、私たちの業務に悪影響を及ぼす可能性があります。
私たちの成長は私たちが新しいビジネス機会を識別、追求し、実施する能力に大きく依存し、これらの新しいビジネス機会は私たちの製品供給、能力、地理的位置を拡大し、私たちは他の医療機器会社とこれらの機会を競争する。私たちがこのような機会を探す努力は、主に新業務、製品または技術の潜在的な買収、許可手配、商業化手配、および第三者との他の取引に集中している。私たちは私たちの戦略基準や私たちまたは私たちの株主が受け入れられるビジネス機会を決定できないかもしれない。私たちが受け入れ可能なビジネスチャンスを見つけることができても、私たちはタイムリーに、または費用効果的な方法で(または根本的に)そのようなビジネスチャンスを追求または実施することができない可能性があり(または買収または他の取引の場合、そのような買収または他の取引を完了することはできない)、私たちはそのようなビジネスチャンスの予想される利益を達成できないかもしれない。もし私たちが新しいビジネス機会を発見し、追求し、実施できなければ、私たちの業務成長能力に悪影響を及ぼすだろう。
さらに、新たなビジネス機会(特に買収)を求めて実施することは、多大なコストを伴う可能性があり、特に特定の製品または技術を開発またはマーケティングする企業として、特に特定の地理的地域で運営されている企業としての経験が限られている場合には、我々の業務にリスク、不確実性、および中断をもたらす可能性がある。我々は、新たな業務、製品または技術を効率的に統合することができない可能性があり、または、買収または他の事業機会に関連する巨額の費用(例えば、買収資産の償却または資産減価費用)を生じる可能性があり、これは、私たちの業務、財務状況、および運営結果に悪影響を及ぼす可能性がある。新たに取得された技術または製品は、商業販売の前に、臨床試験およびFDAおよび適用される外国規制機関の承認を含む追加の開発作業が必要となる可能性があり、このような追加的な開発作業は、巨額の費用がかかり、最終的には成功しない可能性がある。上述したリスクに加えて、任意の国境を越えた買収または取引は、異なる文化および言語にわたる業務統合に関連するリスク、通貨リスク、および特定の国に関連する特定の経済、政治、および規制リスクを含む独自のリスクに関連する可能性がある。私たちが買収に関連した追加株式について言えば、これは私たちの既存の株主を希釈するかもしれない。
さらに、他のヘルスケア事業を買収することにより、買収された業務に関連する意外な業務不確実性、規制および他のコンプライアンス事項または法的責任のリスクに直面する可能性があり、買収された業務の販売者は、これらの業務に保険(または十分な保険)を提供できない可能性があり、または保険(または十分な保険)を得ることができない可能性があり、または賠償が最終責任を支払うのに不十分である可能性がある。
私たちはスイスの民間会社に1000万ドル以上の投資とローンを提供して、私たちの投資を回収できないかもしれない。
2020年10月、著者らはNeo Medical SAと協定を締結し、Neo Medical SAは個人持株のスイス医療技術会社であり、脊柱手術のために新世代製品(“Neo Medical”)を開発した。我々とNeo Medicalとの協力は,彼らと頸部プラットフォームを共同開発し,一度に使用する無菌パッケージソリューションを展開することであり,増加を目指している
52
斬新な設備設計と技術を通じて手術室の効率を高め、手術時間とコストを減少し、患者の予後を改善し、感染率を低下させる。これらの機器は外科環境のために設計されており、救急病院、外来病院と外来手術センターを含む。著者らとNeo Medicalの合意に基づき、著者らはまたあるアメリカの顧客にNeo Medicalの胸腰椎手術解決方案を独占的に流通する。
これらの手配により,Neo Medical 500万ドルの優先株を購入し,転換可能な融資プロトコルに基づいてNeo Medicalに460万スイスフラン(発行日まで500万ドル)の融資を提供した。このローンの年利率は8%で、どちらか一方からNeo Medicalの追加優先株に変換することができる。この期間に他の方法で優先株に変換されていない場合、ローンとすべての課税利息は2024年10月に満期になって支払います。2021年10月、当社はNeo Medical追加ローンに60万スイスフラン(発行日現在70万ドル)を追加融資する追加転換可能ローン協定(“追加転換可能ローン”)を締結した。2022年1月、会社は追加の転換可能な融資をNeo Medicalに変換する優先株を選択した。
Neo Medicalは私たちが優先株とローンを購入した収益を使用してその持続的な運営に資金を提供している。しかし,Neo Medicalの業務が最終的に成功する保証はない。したがって、私たちは最終的に私たちが購入した優先株のいかなる価値も回収できないかもしれないし、/または私たちの融資金額を回収できないかもしれない。
私たちは巨額の費用を発生させたり、処分活動に関連した負債を維持するかもしれない。
私たちは時々販売、許可、譲渡、または他の方法で私たちが所有する資産、子会社株または個別製品、製品ライン、または技術にはもはや適していないと思うかもしれません。その中のいくつかは実質的である可能性があります。このような活動は私たちがこのような努力からコストと支出を発生させる可能性があり、その中のいくつかは巨大かもしれない。これは、例えば、創設資産が処分されたとしても、処分された資産や財産に関連する負債を保持することにもつながる可能性がある。これらの費用と支出はいつでも発生する可能性があり、私たちの運営結果に実質的な影響を与える可能性がある。
私たちの財務業績と融資需要に関連するリスク
私たちの四半期の経営業績は変動する可能性があります。
過去、私たちの四半期の経営業績は大きく変動していた。私たちの今後の四半期の経営業績は大幅に変動する可能性があり、私たちは多くの要素によって損失が出るかもしれません。その中の多くの要素は私たちがコントロールできません。これらの要素には
53
また、いくつかの要因の影響により、売上高と毛利益は、異なる四半期および四半期ごとに大きく変化する可能性がありますが、これらに限定されません
当社の営業権、無形資産および固定資産は潜在的な減価の影響を受けなければなりません。当社はすでに重大な営業権減価費用に計上しており、もし私たちの余剰営業権または無形資産が減価された場合、将来の収益に追加費用を計上する必要があるかもしれません。
私たちの資産の大部分は商業権、無形資産、そして固定資産で構成されている。最近買収された無形資産を含むこれらの資産減価を決定すれば、これらの資産の帳簿価値が減少する可能性がある。
私たちのほとんどの無形資産と固定資産は限られた耐用年数を持っていて、その耐用年数内に直線的に償却したり減価償却したりします。このような無形資産推定利用可能年数に関する基本的な仮定は少なくとも年に1回分析され,事件や状況により資産の帳簿価値が回収できない可能性がある場合に分析されることが多い。必要であれば、このようなどんな変化も屋台を加速させることで調整されるだろう。イベントや状況変化が資産の帳簿価値を回収できない可能性があることを示す場合には、将来のキャッシュフローの見積もりに基づいて、無形資産の減値をテストします。状況の変化は、私たちの無形資産および/または営業権の帳簿価値が回収できない可能性があることを示している可能性があり、これらの要素は、株価および時価の低下、私たちの業界の成長速度の鈍化、将来の販売のより新しい技術や競争製品の導入、または私たちの業務の収益性に影響を与える他の重大な不利な事件を含む可能性がある。使用年数の限られた無形資産を保有する減値をテストする際に、資産をキャッシュフローが個別に識別可能な最低レベルにグループ化する。1つの無形資産が減値とみなされる場合、減値金額は、その資産の帳簿価値が公正価値を超える部分に等しい。
営業権は少なくとも年に1回減価テストが行われなければならない。私たちの年間営業権減価テストの一部として、私たちは毎年第4四半期に私たちの2つの報告単位の潜在的な営業権減値を審査し、事件や状況が発生した場合、減少が存在する可能性が高い場合、私たちはこの2つの報告機関をよりよく検討します。2021年第4四半期に、著者らは全世界の整形外科の名声の全面的な減値を記録した。これは1180万ドルの減価費用を招き、これは買収に関連する償却·総合経営報告書の再計量に反映されている。もし実際の結果が仮説と違っていれば
54
営業権や無形資産計算で使用される推定であれば、将来の減価や償却費用が生じる可能性があり、これは私たちの財務状況や運営業績に悪影響を及ぼす可能性がある。
私たちは外貨為替レートと関連した危険に直面している。
私たちのいくつかの収入、運営費用、資産と負債は外貨建てであるため、私たちは外国為替リスクの影響を受け、これは私たちの運営と報告の業績に悪影響を及ぼすかもしれない。私たちが発生した費用や確認されたドル以外の通貨の純売上については、ドル価値に対するこれらの外貨のどんな変化も、私たちの利益の低下や競争相手に対する私たちの製品の競争力を低下させる可能性があります。外貨建ての流動資産が外貨建ての流動負債より大きいか少ない限り、潜在的な外貨リスクがあります。2022年期間の為替変動は、米国以外の純売上高に1050万ドルの悪影響を与えている。非ドル収入と支出を合わせることで外貨開放を管理することを求めているが、為替変動は将来の運営業績に実質的な悪影響を及ぼす可能性がある。このようなリスクを最小限に抑えるために、私たちは時々通貨ヘッジを行うかもしれない。
また、ドルで私たちの製品を購入している外国人顧客にとって、ドルとこれらの顧客が業務を行っている通貨との為替レート変動は、現地通貨に対してドルが値上がりした外国人顧客が私たちの製品の需要に悪影響を及ぼす可能性がある。国際業務の収益をドルに変換して米国で使用することも課題をもたらし、資金の所在国以外に資金を移す問題や、通常の売掛金支払い周期の長い外国で売掛金を回収することの困難さがある。
私たちの世界的な業務は私たちを税務リスクに直面させるかもしれない。
私たちはアメリカと多くの外国司法管轄区で税金を払わなければならない。私たちは私たちの納税義務を評価するために税法の重要な判断と説明をしなければならない。政治的·経済的条件により、管轄区域によって税法や税率が大きく変化する可能性がある。私たちの有効所得税税率は、税法の変化、異なる税務管轄区域の収益の組み合わせの変化、私たちの繰延税金資産と負債推定値の変化、元の推定値より低い価格で株式権を付与すること、歴史実体分類選挙及び税務監査による問題の解決の不利な影響を受ける可能性がある。
2022年から、2017年の減税·雇用法案は、発生年に研究開発支出を直ちに差し引く選択肢を廃止し、納税者に5年以内にこのような支出を償却することや、米国以外で発生したこのような支出を15年以内に償却することを要求している。この要求は、米国、イタリア、カナダで研究開発を行う際の現金納税義務や有効税率に大きな影響を与える可能性がある。
私たちの一部の子会社は、他のOrthofix子会社に直接製品を販売したり、他のOrthofix子会社にマーケティングと支援サービスを提供したりします。これらの会社間販売·支援サービスは、異なる税率の管轄区域で運営されている子会社に関するものであり、複雑な所得税法規の現在の解釈に基づいて、各管轄区の適切な収入分配を決定しなければならない。これらの管轄区域の税務機関は、私たちがこのような会社間取引の処理方式に疑問を提起するかもしれない。もし私たちが会社間取引の処理を弁護することに成功しなければ、私たちは追加の税金負担、利息、または罰金を受けるかもしれません。これは私たちの収益性に悪影響を及ぼすかもしれません。
私たちは私たちのほとんどの財産を担保にした3.00億ドルの保証された循環信用計画を維持している。
2019年10月に、吾らはいくつかの全額付属会社(総称して“借り手”)と2つ目の改訂された信用協定(“改訂された信用協定”)を締結した。改訂された信用協定は2024年10月25日に期限が切れた3.00億ドルに保証循環信用手配があることを規定し、以前の1.25億ドルの保証循環信用手配を改訂と再記述した。2022年12月31日または本協定の日まで、信用手配には未返済の金額はありませんが、将来的にはこの手配を利用する可能性があります。
当社のいくつかの付属会社(総称して“保証人”と呼ぶ)は、改訂された信用協定項下の任意の債務の償還を保証しなければならない。改訂された信用協定に関連する責任は借り手及び各保証人が実質的にすべての個人財産資産の質抵当とし、売掛金、預金口座、知的財産権、投資財産及びそれぞれの付属会社の在庫、設備及び持分を含む。
改訂された信用協定は、当社が追加債務を招くこと、追加留置権を付与または許可すること、投資および買収を行うこと、他社との合併または合併、資産の処分、配当金および割り当て、二次債務の支払い、および関連取引を行う能力の制限を含む慣用的なプラスおよび負の契約を含む。しかも、修正された信用協定には財務的なチノが含まれていて、私たちは総合的な基礎の上で、任意のことを要求します
55
財務四半期、総純レバー率は3.5~1.0を超えず(重大買収後は4財政四半期を超えず、この比率は4.0~1.0に増加することができる)、利息カバー率は少なくとも3.0~1.0である。改訂された信用協定はこのようなローンの常習違約事件も含まれているが、一旦このような違約事件が発生すると、常習救済権利に符合する場合、このローン項目の下のすべての未返済ローンは融資者の承諾を加速及び/或いは終了することができる。
私たちは条約を遵守し、2022年12月31日(とそれまでの時期)に違約事件はないと考えている。しかし、私たちは私たちが未来の財政四半期にこのような財政協約を履行できるということを保証できない。これができなければ、このような合意下での違約事件を招く可能性があり、このとき融資の下で大量の資金を抽出した場合、私たちの財務状況に大きな悪影響を及ぼす可能性がある。
私たちは高いレベルの在庫を維持しなければならない。これは私たちの大量の資源を消費し、私たちのキャッシュフローを減少させるかもしれない。
私たちは顧客の需要を満たすために大量の在庫レベルを維持しているため、在庫過剰、古い、賞味期限が切れるリスクに直面しています。私たちの多くの脊柱移植製品はセットになっています。各セットは、医師が患者の必要に応じて適切な脊柱インプラントを選択することができるように、大量の異なるサイズの構成要素を含む。典型的な手術では、セット内のすべてのインプラントが使用されるわけではなく、したがって、セット内に配置されたいくつかのサイズのインプラントまたは在庫を補充するために購入したいくつかのサイズのインプラントは、使用可能になる前に時代遅れになる可能性がある。さらに、私たちの製品を効果的にマーケティングするためには、しばしば、冗長な製品および異なるサイズの製品を確保することを含む脊柱インプラントおよび器具を含む、病院および独立した販売エージェントに委託装置を提供しなければならない。また、私たちの生物製品は賞味期限があります。一年から五年まで様々です。これらの製品は使用する前に期限が切れているかもしれません。もし私たちの大部分の在庫が過剰、時代遅れ、または期限切れとされれば、在庫減値費用に関するコストと、このような在庫交換に要するコストのため、私たちの収益やキャッシュフローに重大な悪影響を及ぼす可能性があります。また、私たちがますます新製品と製品システムを発売するにつれて、私たちは古い製品と製品システムを蚕食するかもしれません。これは過度で時代遅れの料金を悪化させる可能性があります。
私たちは将来的に私たちの資本需要を満たしたり、日和見買収を行うための追加融資が必要になるかもしれませんが、このような融資は全くなければ優遇的な条件で提供されないかもしれません。
私たちは将来的に私たちの資本需要を満たしたり、日和見買収を行うために追加的な融資が必要になるかもしれない。資本と信用市場は極端な変動や混乱を経験する可能性があり、これは借り手や投資家に不確実性と流動性の問題をもたらす可能性があり、もしあれば、有利な条件で必要な追加融資を得ることができないかもしれない。もし私たちが受け入れ可能な条項で十分な資金を得ることができない場合、私たちは製品の開発や強化に成功したり、競争圧力に対応することができないかもしれません。いずれも私たちの業務、運営結果、および財務状況に悪影響を及ぼす可能性があります。もし私たちが債券を発行したり、信用手配を行ったりすることで資金を調達すれば、私たちの業務は制限された契約によって制限されるかもしれません。
一般リスク
私たちの株価はずっと変動していて、変動し続けるかもしれません。これは私たちの株の未来の価格を予測しにくくするかもしれません。
投資家は最近或いは歴史的傾向に依存して未来の株価、財務状況、経営業績或いはキャッシュフローを予測すべきではない。他の医療機器会社と同様に、私たちの株価は変動する可能性があり、メディアや投資界の投機、報道または感情、私たちまたは私たちの競争相手が新しい、計画中または考慮している製品、サービス、技術革新、買収、資産剥離または他の重大な取引を発表する可能性があります;私たちの四半期の財務業績および投資界の推定または私たちが提供する財務見通しとの比較;私たちの競争相手の財務業績と商業戦略;私たちまたは私たちの業界の研究報告書の出版または証券アナリストの提案または研究報告の撤回に関する変化;税法を含む私たちの業務の法律または法規の変化に影響を与える。会計基準、政策、ガイドライン、解釈または原則の変化、脅威または実際の訴訟または政府調査、ならびにインフレ、爆発、流行病、地政学的緊張または衝突、または他のマクロ経済動態による市場変動または低迷。一般的または業界固有の市場状況または株式市場表現、または私たちの表現とは無関係な国内または国際マクロ経済および地政学的要因も我々の株価に影響を与える可能性がある。
また,株式市場,特に医療機器会社の株は,極端な価格や出来高変動を経験しており,これらの変動はこれらの会社の経営業績に関係なくあるいは比例しないことが多い。これは投資家がいつでも彼らの株を売却することを制限または阻止する可能性があり、そうでなければ、私たちの普通株の流動性に悪影響を及ぼす可能性がある。証券会社の集団訴訟は往々にして会社全体が一定の変動期を経て提起される
56
市場と会社証券の市場価格。私たちに訴訟を提起すれば、非常に大きな費用を招き、私たちの経営陣の関心と資源を分散させ、私たちの業務、財務状況、経営結果を損なう可能性があります。
私たちは上場企業に関連する法律や法規を遵守するために大量の資源を費やし、コンプライアンスを維持できなかったいかなる行為も、規制機関の審査を受け、投資家が私たちの会社に自信を失ってしまう可能性があり、これは私たちの業務を損ない、私たちの株価に実質的な悪影響を与える可能性がある。
2010年のドッド·フランクウォール街改革と消費者保護法と2002年のサバンズ-オックススリー法案の条項、および米国証券取引委員会とナスダック株式市場で採択された関連規則と法規を含む上場企業の法律と法規に影響を与え、私たちの会計、法律、財務コンプライアンスコストを増加させ、いくつかの活動をより時間とコストを高くする。私たちは私たちがこれらの法律と法規を遵守することによって生じる可能性のあるコスト総額や時間を合理的な正確性で予測したり推定することはできない。
私たちはまたアメリカ証券取引委員会法規の制約を受けて、この法規は私たちの製品に特定の鉱物が含まれているかどうかを確認することを要求して、法規ではそれを“衝突鉱物”と呼び、含まれていれば、このような衝突鉱物がコンゴ民主共和国からか隣国からのものかを決定するために、私たちのサプライチェーンを広く調査します。これらの規定を遵守することは私たちのコストを増加させ、私たちの経営陣やサプライチェーンの人員には非常に時間がかかり(私たちのサプライヤーにとっても同様)、遵守し続けるには引き続き多くの資金と時間が必要になると予想されます。また、私たちの任意の開示が市場から“負の”とみなされると、顧客が私たちの製品の購入を拒否する可能性があります。さらに、製品、プロセス、または供給源を任意に変更することを決定した場合、追加のコストを招く可能性があり、これは私たちの業務、財務状況、および運営結果に悪影響を及ぼす可能性があります。
私たちの改正と再記述された法律は、特定の裁判所を、私たちの株主によって開始される可能性のある特定の訴訟の唯一のおよび独占的なフォーラムとして指定し、これは、私たちの株主が有利な司法フォーラムを得ることを制限し、私たちとの紛争を処理する能力を制限するかもしれない。
私たちが書面で代替裁判所を選択することに同意しない限り、法的に許容される最大範囲内で、私たちが書面で代替裁判所を選択することに同意しない限り、私たちが改正して再記述する付例規定は、(A)デラウェア州衡平裁判所(または、デラウェア州衡平裁判所が主題管轄権を欠いている場合、デラウェア州高級裁判所、または、デラウェア州衡平裁判所およびデラウェア州上級裁判所に主題管轄権がない場合、米国デラウェア州地方裁判所)および任意の州(または、適用される場合は米国デラウェア州地方裁判所、連邦)控訴裁判所は、以下の事件の唯一および専属裁判所でなければならない:(I)当社が提起した任意の派生訴訟、訴訟または法的手続き、(Ii)任意の現職または前任役員、役員または他の従業員または株主がわが社または当方の株主に負う受託責任クレームの任意の訴訟、訴訟または法的手続き、またはこのような受託責任違反行為に協力して教唆することを主張する任意の訴訟、(Iii)私たちまたは任意の取締役、役員、役員に対して、または他の従業員は、“デラウェア州会社法”または当社(登録証明書または添付例)の任意の規定に従って、任意の権利、義務または救済措置を強制的に実行することを求め、(Iv)DGCLは、デラウェア州衡平裁判所に管轄権を与える任意の訴訟、訴訟または手続き、または(V)私たちまたは私たちの現職または前任取締役、上級職員、従業員または株主のための内部事務原則によって管轄される任意の訴訟、訴訟または手続きを主張する, すべての事件において、裁判所は、被告に指名された不可欠な当事者に対して属人管轄権(このような任意の不可欠な当事者がデラウェア州またはそのような裁判所で属人管轄権を有することに同意することを含む)、および(B)米国連邦地域裁判所は、1933年の証券法(改訂本)に基づいて訴因を提起する任意の訴えを解決するための独占的なフォーラムでなければならない。これらの規定は株主が司法裁判所の能力を獲得することを制限する可能性があり、当該株主はこれらの規定が管轄する紛争について司法機関を求めることを好むかもしれない。
環境、社会、企業統治(“ESG”)法規、政策、規定は、私たちのサプライチェーンをより複雑にし、私たちと顧客との関係に悪影響を及ぼす可能性があります。
環境と社会リスクに対する管理は日々重要視されている。私たちの多くの顧客は支払者または流通業者であり、彼らは、そのサプライヤーまたは製造業者が遵守しなければならないESG条項を含む調達ポリシーを採用しているか、またはそのような条項および条件にそのような条項を含めることを求めている可能性がある。ますます多くの医療機器業界参加者は、責任ある商業連合のような自発的なESGグループまたは組織にも参加する。私たちのサプライチェーンの複雑さと私たちの製品のいくつかのコンポーネントのアウトソーシング製造を考慮すると、これらのESG条項や措置は変化する可能性があり、予測できないかもしれません。私たちにとっては守りにくく、コストも高いかもしれません。もし私たちが私たちのサプライヤーにこのような政策や規定を遵守させることができない場合、顧客は私たちに製品を購入することを停止し、私たちに法的行動をとるかもしれません。これは私たちの名声、収入、運営結果を損なう可能性があります。
57
私たちのサービスは、企業市民権およびESG事項および/またはそのような事項に対する私たちの報告に否定的な影響を受ける可能性があります。
一部の投資家、顧客、消費者、および他の利害関係者はますます企業市民と持続可能な発展問題に注目している。私たちはこのような問題について責任を持って行動しないと思われるかもしれない。私たちの業務はこのような事件の否定的な影響を受けるかもしれない。このような問題、または関連する企業市民および持続可能な開発の問題は、私たちの業務に実質的な悪影響を及ぼす可能性がある。
I項目1 B。 未解決従業員意見
ない。
ITEM 2。 属性
私たちは私たちの業務を支援するために不動産をレンタルしたり所有しています。私たちが私たちの業務に重要だと思う不動産を以下に列挙する。私たちの施設は私たちの現在の需要を満たすことができ、私たちは必要な時に受け入れ可能な条件でこのようなレンタル契約を更新したり、代替施設を見つけることができると信じています。
施設 |
|
位置 |
|
おおむね |
|
|
所有権 |
|
製造·倉庫·配送·研究開発·立地 |
|
テキサス州ルイビル |
|
|
140,000 |
|
|
レンタルする |
生物学的製剤と脊柱インプラントの設計、開発、マーケティング、検査 |
|
カリフォルニア州カールスバッド |
|
|
82,000 |
|
|
レンタルする |
ある生物製品の製造と流通は |
|
カリフォルニア州オーウェン |
|
|
70,000 |
|
|
レンタルする |
製造、倉庫、配送、開発、 |
|
カリフォルニア州サニービル |
|
|
25,000 |
|
|
レンタルする |
脊柱インプラントの設計と身体訓練実験室の立地 |
|
ペンシルバニア州ウェイン |
|
|
3,700 |
|
|
レンタルする |
Enabling Technologies製品の設計、開発、マーケティング |
|
カリフォルニア州トロント |
|
|
9,200 |
|
|
レンタルする |
開発、部品製造、品質管理、 |
|
イタリアのヴェローナ |
|
|
38,000 |
|
|
持っている |
Orthofix製品国際配送センター |
|
イタリアのヴェローナ |
|
|
18,000 |
|
|
レンタルする |
Orthofix製品機械工場 |
|
イタリアのヴェローナ |
|
|
9,000 |
|
|
レンタルする |
イギリスの販売管理·流通·行政施設 |
|
イギリスのメデンヘイデ |
|
|
5,580 |
|
|
レンタルする |
ブラジルの販売管理·流通·行政施設 |
|
ブラジルサンパウロ |
|
|
22,000 |
|
|
レンタルする |
フランスでの販売管理·流通·行政施設 |
|
アルクイル、フランス |
|
|
8,500 |
|
|
レンタルする |
ドイツでの販売管理·流通·行政施設 |
|
ドイツのオットブルン |
|
|
18,300 |
|
|
レンタルする |
私たちの生産施設はFDAに登録されている。私たちの施設はその品質体系法規に適合することを確実にするためにFDAの検査を受けている。FDA検査状況のさらなる情報については、“項目1.企業−政府法規”を参照されたい
第三項です。 法律訴訟
法律手続きを行うべき重大事項の説明については、本年報第8項総合財務諸表付記13を参照されたい。
ITEM 4. 炭鉱安全情報開示
適用されません。
58
第II部
ITEM 5。 登録者普通株市場、関連株主事項及び発行者による株式証券の購入
私たちの普通株の市場
私たちの普通株はナスダック世界の精選市場で取引され、コードは“OFIX”です。2023年3月1日現在、私たちは493人の普通株式保有者がいます。私たちの普通株式の保有者の多くは“巷”や実益所有者であり、彼らの株式は銀行、ブローカー、他の金融機関が保有している。私たちの普通株の2023年3月1日の終値は20.18ドルです。次の表は最近の二つの財政年度の私たちの普通株の最高と最低販売価格を示しています。
|
|
高 |
|
|
ロー |
|
||
2021 |
|
|
|
|
|
|
||
第1四半期 |
|
$ |
48.50 |
|
|
$ |
39.34 |
|
第2四半期 |
|
|
45.96 |
|
|
|
39.23 |
|
第3四半期 |
|
|
43.30 |
|
|
|
36.35 |
|
第4四半期 |
|
|
39.98 |
|
|
|
28.65 |
|
2022 |
|
|
|
|
|
|
||
第1四半期 |
|
$ |
35.83 |
|
|
$ |
29.75 |
|
第2四半期 |
|
|
34.89 |
|
|
|
23.54 |
|
第3四半期 |
|
|
25.93 |
|
|
|
19.11 |
|
第4四半期 |
|
|
20.87 |
|
|
|
14.33 |
|
配当をする
私たちは過去に私たちの普通株の保有者に配当金を支払ったことがなく、今も予測可能な未来に配当金を支払うつもりはない。しかも、私たちが修正した信用協定によると、私たちは場合によっては配当金を支払う能力が制限されている。私たちは現在、私たちのすべての合併収益を維持し、私たちの業務の持続的な成長に資金を提供するつもりだ。
将来的に子会社から受け取った配当金で普通株式所有者に配当金を支払うことにした場合、現行税率によると、このような金額に追加の源泉徴収税と所得税を支払う必要があるかもしれない。
株式報酬計画情報
私たちの持分補償計画に関する情報は、ここに本報告書の第3部第12項に組み込まれています。
最近売られている未登録証券
2022年第4四半期には、改正された1933年証券法(“証券法”)に基づいて登録されていない証券は何も発行されていない。
[パフォーマンスチャート]
以下の業績グラフは、“募集材料”とみなされないか、または米国証券取引委員会に“入金されている”とみなされず、第14 A又は14 C条の制約を受けず、取引所法案第18節の責任も負わない。これらの情報は、参照によってこれらの情報が明確に組み込まれていない限り、1933年の証券法または取引法に従って提出されたいかなる文書にも含まれているとはみなされない。
59
以下の図は、過去5年間の普通株式累積総リターンの年間パーセンテージ変化を、ナスダック総合指数とナスダック指数(SIC 3840-3849米国と外国)の株式会社の累積総リターンと比較したものである。本報告では、2017年12月31日に関連発行者の株に100ドルを投資し、受信した配当金が直ちに増発株に投資されると仮定した。このグラフは,表示された会計年度において1年ごとに行われる100ドルの初期投資の価値を示している。本分析と今後の分析では,CRSP指数データが利用できなくなったため,ナスダック総合指数はCRSPナスダック株式市場(米国と外国社)指数に代わった。CRSP指数は2022年までにデータに含まれている。

ITEM 6。保留されている
60
ITem 7。 経営陣の財務状況と経営成果の検討と分析
以下、我々の財務状況及び経営結果の検討及び分析は、本年度報告の他の部分の“前向き陳述”と、我々の総合財務諸表とその付記と一緒に読まなければならない。以下の議論と分析は、私たちのこの2年間の前年比パフォーマンスの比較を含む、2022年と2021年の財務業績に集中しています。私たちの2020年度の具体的な議論と分析、および私たちの2021年と2020年の財務業績の前年比比較は、第2部に位置し、第7項-管理層は、2022年2月25日に米国証券取引委員会に提出された10-K表年次報告において、財務状況と経営成果の検討と分析を行うことができ、この報告は、私たちのウェブサイトwww.oreofix.comと米国証券取引委員会のウェブサイトwww.sec.govで調べることができる。
SeaSpineと合併する
2022年10月10日,我々はSeaSpineホールディングス(“SeaSpine”)と合併協定と計画を締結し,SeaSpineは脊柱疾患の外科的解決策に専念する世界的な医療技術会社である。2023年1月5日、取引が完了し、取引が完了した後、SeaSpineはOrthofixの完全子会社として継続した。合併は2023年に完了したため、SeaSpineの2022年12月31日までの歴史的財務業績は運営実績に含まれていない。そのため、以下のタイトルは“経営業績”という情報はOrthofixの独立した財務業績のみに触れている。しかし、合併は私たちの未来の経営業績と財務状況に大きな影響を及ぼすだろう。例えば、統合は、持続的な相乗効果を達成するための巨額の費用をもたらすことが予想され、これは、製品ラインの合理化、従業員解散費、および留置費用、統合プロセスおよび情報技術システムの専門費用、および他の費用に関連する可能性がある。我々の2023年3月31日までの財政四半期のForm 10-Q四半期報告から、今後の文書はOrthofix-SeaSpine合併組織の結果を反映する。合併の他の議論については、本年報第8項総合財務諸表付記22を参照されたい。
実行要約
新しく合併したOrthofix-SeaSpine組織は世界をリードする脊柱と整形外科会社であり、全面的な生物製剤、革新的な脊柱ハードウェア、骨成長療法、専門整形外科解決方案とリードした手術ナビゲーションシステムを持っている。その製品は世界約68カ国·地域に販売されている。
私たちはテキサス州のルイスビルに本部を置き、カリフォルニア州のカールスバッドとイタリアのヴェローナに主要な事務所を設置して、脊柱と生物製剤の製品革新と外科医師教育に集中して、重点は整形外科の製品革新、生産と医学教育です。私たちの世界的な研究開発、商業と製造の足跡はまた、カリフォルニア州オーウェン、カナダトロント、カリフォルニア州森ビル、ペンシルベニア州ウェイン、ペンシルバニア州オリーブ支社、イギリスメデンヘード、ドイツミュンヘン、フランスパリとブラジルサンパウロの工場と事務所も含まれています。
61
2022年の注目すべき財務業績には、
経営成果
次の表は、私たちの総合経営報告書のいくつかの項目を示しており、純売上高の割合を占めています
|
|
十二月三十一日までの年度 |
|
|||||||||
|
|
2022 |
|
|
2021 |
|
|
2020 |
|
|||
純売上高 |
|
|
100.0 |
|
|
|
100.0 |
|
|
|
100.0 |
|
販売コスト |
|
|
26.8 |
|
|
|
24.7 |
|
|
|
25.1 |
|
毛利 |
|
|
73.2 |
|
|
|
75.3 |
|
|
|
74.9 |
|
販売とマーケティング |
|
|
49.7 |
|
|
|
47.6 |
|
|
|
50.3 |
|
一般と行政 |
|
|
17.4 |
|
|
|
14.9 |
|
|
|
16.7 |
|
研究開発 |
|
|
10.6 |
|
|
|
10.7 |
|
|
|
9.6 |
|
買収に関連した販売と再計量 |
|
|
(1.6 |
) |
|
|
3.9 |
|
|
|
(0.2 |
) |
営業収入(赤字) |
|
|
(2.9 |
) |
|
|
(1.8 |
) |
|
|
(1.5 |
) |
純収益(赤字) |
|
|
(4.3 |
) |
|
|
(8.3 |
) |
|
|
0.6 |
|
報告別市場別純売上高
次の表は主要製品別と報告書別に純売上高を提供している
|
|
|
|
|
|
|
|
|
|
|
百分率変化 |
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
2022/2021 |
|
|
2022/2021 |
|
|
2021/2020 |
|
|
2021/2020 |
|
|||||||
(ドル、千単位) |
|
2022 |
|
|
2021 |
|
|
2020 |
|
|
すでに報告した |
|
|
不変貨幣 |
|
|
すでに報告した |
|
|
不変貨幣 |
|
|||||||
骨成長療法 |
|
$ |
187,247 |
|
|
$ |
187,448 |
|
|
$ |
171,396 |
|
|
|
-0.1 |
% |
|
|
-0.1 |
% |
|
|
9.4 |
% |
|
|
9.4 |
% |
脊柱インプラント |
|
|
109,546 |
|
|
|
115,094 |
|
|
|
94,857 |
|
|
|
-4.8 |
% |
|
|
-4.0 |
% |
|
|
21.3 |
% |
|
|
20.8 |
% |
生物製品 |
|
|
56,381 |
|
|
|
56,421 |
|
|
|
55,482 |
|
|
|
-0.1 |
% |
|
|
-0.1 |
% |
|
|
1.7 |
% |
|
|
1.7 |
% |
全世界脊椎 |
|
|
353,174 |
|
|
|
358,963 |
|
|
|
321,735 |
|
|
|
-1.6 |
% |
|
|
-1.4 |
% |
|
|
11.6 |
% |
|
|
11.4 |
% |
世界整形外科 |
|
|
107,539 |
|
|
|
105,516 |
|
|
|
84,827 |
|
|
|
1.9 |
% |
|
|
11.0 |
% |
|
|
24.4 |
% |
|
|
21.3 |
% |
純売上高 |
|
$ |
460,713 |
|
|
$ |
464,479 |
|
|
$ |
406,562 |
|
|
|
-0.8 |
% |
|
|
1.5 |
% |
|
|
14.2 |
% |
|
|
13.5 |
% |
62
全世界脊椎
Global Spineは、以下の製品カテゴリを提供します
2022年は2021年と比較して
純売上高は580万ドル下がって1.6%減少した
世界整形外科
Global Orthopedicsが提供した製品と解決策は,医師が肢体再建や脊柱とは無関係な奇形矯正に関連する様々な整形外科疾患の治療に成功することを可能にした。Global Orthopedicsは流通業者と販売代表ネットワークを介してその製品を世界的に流通させ,病院や保健提供者に整形外科製品を販売している。
2022年は2021年と比較して
純売上高は200万ドル、報告ベースでは1.9%、不変通貨ベースでは11.0%増
毛利
|
|
|
|
|
|
|
|
|
|
|
百分率変化 |
|
||||||||
(ドル、千単位) |
|
2022 |
|
|
2021 |
|
|
2020 |
|
|
2022/2021 |
|
|
2021/2020 |
|
|||||
純売上高 |
|
$ |
460,713 |
|
|
$ |
464,479 |
|
|
$ |
406,562 |
|
|
|
-0.8 |
% |
|
|
14.2 |
% |
販売コスト |
|
|
123,544 |
|
|
|
114,914 |
|
|
|
101,889 |
|
|
|
7.5 |
% |
|
|
12.8 |
% |
毛利 |
|
$ |
337,169 |
|
|
$ |
349,565 |
|
|
$ |
304,673 |
|
|
|
-3.5 |
% |
|
|
14.7 |
% |
毛利率 |
|
|
73.2 |
% |
|
|
75.3 |
% |
|
|
74.9 |
% |
|
|
-2.1 |
% |
|
|
0.4 |
% |
2022年は2021年と比較して
毛利益は1,240万ドル減少し、減少幅は3.5%
63
販売とマーケティング費用
|
|
|
|
|
|
|
|
|
|
|
百分率変化 |
|
||||||||
(ドル、千単位) |
|
2022 |
|
|
2021 |
|
|
2020 |
|
|
2022/2021 |
|
|
2021/2020 |
|
|||||
販売とマーケティング |
|
$ |
228,810 |
|
|
$ |
221,318 |
|
|
$ |
204,434 |
|
|
|
3.4 |
% |
|
|
8.3 |
% |
純売上高のパーセントを占める |
|
|
49.7 |
% |
|
|
47.6 |
% |
|
|
50.3 |
% |
|
|
2.1 |
% |
|
|
-2.7 |
% |
2022年は2021年と比較して
販売とマーケティング費用は750万ドル増加しました
一般と行政費用
|
|
|
|
|
|
|
|
|
|
|
百分率変化 |
|
||||||||
(ドル、千単位) |
|
2022 |
|
|
2021 |
|
|
2020 |
|
|
2022/2021 |
|
|
2021/2020 |
|
|||||
一般と行政 |
|
$ |
79,966 |
|
|
$ |
69,353 |
|
|
$ |
67,948 |
|
|
|
15.3 |
% |
|
|
2.1 |
% |
純売上高のパーセントを占める |
|
|
17.4 |
% |
|
|
14.9 |
% |
|
|
16.7 |
% |
|
|
2.5 |
% |
|
|
-1.8 |
% |
2022年は2021年と比較して
一般と行政費用は1060万ドル増加します
研究開発費
|
|
|
|
|
|
|
|
|
|
|
百分率変化 |
|
||||||||
(ドル、千単位) |
|
2022 |
|
|
2021 |
|
|
2020 |
|
|
2022/2021 |
|
|
2021/2020 |
|
|||||
研究開発 |
|
$ |
49,065 |
|
|
$ |
49,621 |
|
|
$ |
39,056 |
|
|
|
-1.1 |
% |
|
|
27.1 |
% |
純売上高のパーセントを占める |
|
|
10.6 |
% |
|
|
10.7 |
% |
|
|
9.6 |
% |
|
|
-0.1 |
% |
|
|
1.1 |
% |
2022年は2021年と比較して
研究開発費は60万ドル減少しました
64
買収に関連した販売と再計量
|
|
|
|
|
|
|
|
|
|
|
百分率変化 |
|
||||||||
(ドル、千単位) |
|
2022 |
|
|
2021 |
|
|
2020 |
|
|
2022/2021 |
|
|
2021/2020 |
|
|||||
買収に関連した販売と再計量 |
|
$ |
(7,404 |
) |
|
$ |
17,588 |
|
|
$ |
(499 |
) |
|
|
-142.1 |
% |
|
|
-3624.6 |
% |
純売上高のパーセントを占める |
|
|
-1.6 |
% |
|
|
3.9 |
% |
|
|
-0.2 |
% |
|
|
-5.5 |
% |
|
|
4.1 |
% |
2022年は2021年と比較して
買収に関連する償却と再計量は2,500万ドル減少
営業外収入
|
|
|
|
|
|
|
|
|
|
|
百分率変化 |
|
||||||||
(ドル、千単位) |
|
2022 |
|
|
2021 |
|
|
2020 |
|
|
2022/2021 |
|
|
2021/2020 |
|
|||||
利子支出,純額 |
|
$ |
(1,288 |
) |
|
$ |
(1,837 |
) |
|
$ |
(2,483 |
) |
|
|
-29.9 |
% |
|
|
-26.0 |
% |
その他の収入(費用) |
|
|
(3,150 |
) |
|
|
(3,343 |
) |
|
|
8,381 |
|
|
|
-5.8 |
% |
|
|
-139.9 |
% |
営業外収入と支出は主に利息収入と支出、外貨為替レート変動による取引損益、私たちのある個人持株会社の株式に関連する公正価値の変化及びある転換可能な債務投資確認の信用損失を含む。為替損益は主に私たちのいくつかの海外子会社が貿易と会社間の売掛金または売掛金(最も明らかにドル)を持っており、その機能通貨ではないからである。
2022年は2021年と比較して
利子支出は正味50万ドル減少した
その他の収入(支出)は20万ドル増
所得税費用
|
|
|
|
|
|
|
|
|
|
|
百分率変化 |
|
||||||||
(ドル、千単位) |
|
2022 |
|
|
2021 |
|
|
2020 |
|
|
2022/2021 |
|
|
2021/2020 |
|
|||||
所得税支出 |
|
$ |
2,043 |
|
|
$ |
24,884 |
|
|
$ |
(2,885 |
) |
|
|
-91.8 |
% |
|
|
-962.5 |
% |
実際の税率 |
|
|
-11.5 |
% |
|
|
-184.4 |
% |
|
|
784.0 |
% |
|
|
172.9 |
% |
|
|
-968.4 |
% |
2022年は2021年と比較して
所得税の純支出は2,280万ドル減少した
65
本年度報告第8項に記載されている総合財務諸表付記20には、各年度の実税率の入金が記載されている。
細分化市場回顧
過去,我々の業務は2つの報告部門で管理されていた:Global SpineとGlobal Orthopedics。業務を分部別に管理するための主な指標はEBITDAである(本年報第8項に掲載されている総合財務諸表付記16ではさらに説明されている)。
SeaSpineとの合併が2023年1月5日に完了した後、2023年第1四半期に新合併会社の運営管理方式に基づいて報告部門を再評価する予定です。その時、私たちはまた私たちが決定した部門の利益指標を再評価するつもりだ。したがって,次の報告分部情報は,2022年12月31日までの年度の運営を管理するための我々の2つの履歴報告分部に基づいて作成される.
以下の表でEBITDAと所得税前損失を照合した
|
|
十二月三十一日までの年度 |
|
|||||||||
(ドル、千単位) |
|
2022 |
|
|
2021 |
|
|
2020 |
|
|||
全世界脊椎 |
|
$ |
60,649 |
|
|
$ |
58,014 |
|
|
$ |
63,036 |
|
世界整形外科 |
|
|
(4,037 |
) |
|
|
3,374 |
|
|
|
(4,993 |
) |
会社 |
|
|
(44,011 |
) |
|
|
(31,691 |
) |
|
|
(25,382 |
) |
EBITDA合計 |
|
|
12,601 |
|
|
|
29,697 |
|
|
|
32,661 |
|
減価償却および償却 |
|
|
(29,019 |
) |
|
|
(29,599 |
) |
|
|
(30,546 |
) |
営業権の減価 |
|
|
— |
|
|
|
(11,756 |
) |
|
|
— |
|
利子支出,純額 |
|
|
(1,288 |
) |
|
|
(1,837 |
) |
|
|
(2,483 |
) |
所得税前損失 |
|
$ |
(17,706 |
) |
|
$ |
(13,495 |
) |
|
$ |
(368 |
) |
流動性と資本資源
2022年12月31日現在、現金、現金等価物、制限現金は5070万ドルですが、2021年12月31日までは8780万ドルです。
|
|
2011年12月31日までの年度 |
|
|
|
|
||||||
(ドル、千単位) |
|
2022 |
|
|
2021 |
|
|
変わる |
|
|||
経営活動の現金純額 |
|
$ |
(11,538 |
) |
|
$ |
18,475 |
|
|
$ |
(30,013 |
) |
投資活動の現金純額 |
|
|
(24,534 |
) |
|
|
(23,013 |
) |
|
|
(1,521 |
) |
融資活動の現金純額 |
|
|
(78 |
) |
|
|
(3,621 |
) |
|
|
3,543 |
|
為替レート変動が現金と制限現金に及ぼす影響 |
|
|
(997 |
) |
|
|
(815 |
) |
|
|
(182 |
) |
現金、現金等価物および限定的現金の純変化 |
|
$ |
(37,147 |
) |
|
$ |
(8,974 |
) |
|
$ |
(28,173 |
) |
次の表は自由キャッシュフローを示しており、これは非公認会計基準財務指標であり、その計算方法は経営活動の純現金から資本支出を差し引くことである。
|
|
2011年12月31日までの年度 |
|
|
|
|
||||||
(ドル、千単位) |
|
2022 |
|
|
2021 |
|
|
変わる |
|
|||
経営活動の現金純額 |
|
$ |
(11,538 |
) |
|
$ |
18,475 |
|
|
$ |
(30,013 |
) |
資本支出 |
|
|
(23,160 |
) |
|
|
(19,592 |
) |
|
|
(3,568 |
) |
自由キャッシュフロー |
|
$ |
(34,698 |
) |
|
$ |
(1,117 |
) |
|
$ |
(33,581 |
) |
経営活動
経営活動のキャッシュフローは3,000万ドル減少
66
私たちの二つの主な運営資金口座は売掛金と在庫です。2022年12月31日現在、売掛金当日売上高は62日であるのに対し、2021年12月31日は58日である(第4四半期売掛金純売上高と期末売掛金計算を使用)。2022年12月31日現在、在庫回転率は1.2倍であるのに対し、2021年12月31日は1.4倍である。
投資活動
投資活動からのキャッシュフローは150万ドル減少しました
融資活動
融資活動のキャッシュフローは350万ドル増加しました
信用手配
2019年10月25日、吾らは2つ目の改訂及び再署名された信用協定(“改訂された信用協定”)を締結し、5年間の3億ドルの保証付き循環信用手配を提供した。改正された信用協定の期限は2024年10月25日であり、これまでの1.25億ドルの保証循環信用手配を改訂し、再確認した。
改訂されたクレジット協定の下の借金は、運営資金および他の一般会社用途(株式買い戻し、買収許可、および配当金および他の割り当ての許可を含む)として使用することができる。改訂信用協定項での借入金は,過去12カ月で確認されたEBITDAレベルによって制限される可能性がある。
2022年12月31日現在、改正された信用協定によると、未返済の借金はありません。しかし、2023年1月3日には、合併に関連するいくつかの費用に資金を提供することを含む、3.0億ドルの保証循環信用手配の下で3,000万ドルを借金しました。また、2023年3月3日に1500万ドルを借り入れた。信用手配に関するその他の資料は、本年報第8項総合財務諸表付記11を参照されたい。
また、2022年12月31日現在、イタリアの550万ユーロ(630万ドル)の信用限度額に未返済の借金はありません。この無担保信用限度額は、イタリアで借金をする際に決定された金利借金の選択権を提供してくれる。
SeaSpineは2022年12月31日までに全国協会富国銀行(Wells Fargo Bank)に3000万ドルの信用手配を持ち,2025年7月に満期となる予定である。合併終了日までに、SeaSpineは信用手配の下で2700万ドルの未返済借金を持っている。合併と関連して、2023年1月5日に、すでに信用協定項の下で元金、利息及び費用に関するすべての未返済債務を返済し、信用協定項の下のすべての適用の承諾を終了した。
他にも
関連又は事項のある資料は、本年度報告第8項連結財務諸表付記13を参照されたい。
67
軍団革新有限責任会社の資産買収
2022年12月29日、我々は米国に本部を置く医療機器技術会社Legion Innovation,LLCと技術譲渡と特許権使用料協定を締結し、特定の資産の知的財産権を獲得した。対価格として、2023年1月に20万ドルを支払いましたが、追加の支払いは将来の商業化と収入ベースのマイルストーンにかかっています。
CGBio株式会社許可と流通契約
2022年7月30日、私たちはCIBio有限会社(“CIBio”)と独占許可と流通協定を締結し、CGBioは革新的な合成骨移植開発業者である。この協定はアメリカとカナダで臨床前と臨床研究、商業化、普及、マーケティングとNovosis組換えヒト骨形態発生蛋白-2(rhBMP-2)骨成長材料と他の未来の組織再生解決方案を販売する独占的な権利を与える。対価格として,CTGioに140万ドルの前金を支払い,具体的な開発マイルストーンの実現状況に応じて追加金を支払った
脊柱動力学の獲得と価格の比較があります
Spinal Kineticsを買収する一部の代価として、私たちは6000万ドルまで支払うか、マイルストーンの支払いに同意する。そのうちの一つの記念碑的な支払いは1500万ドルで、FDAがSpinal KineticsのM 6-C人工頚椎の満期を承認し、2019年に実現し、支払いした。2021年には合計1500万ドルの収入ベースのマイルストーン支払いを実現し、いくつかの純販売目標を達成した後にこの支払いを支払った。
残りのマイルストーン支払いは収入ベースのマイルストーン支払いで、金額は3000万ドルで、買収した人工ディスクの将来販売に関係している。2022年12月31日現在、2023年4月30日の最終期限までにこのマイルストーンが達成されないことが予想されるため、この対価格負債の公正価値はゼロに決定された。この事項のさらなる検討については,本年度報告第8項総合財務諸表付記12を参照されたい。
Igea S.p.A独占許可と流通協定
2021年4月,イタリア骨·軟骨刺激システムメーカーと流通業者Igea S.p.A(“Igea”)と独占許可と流通協定(“ライセンス契約”)を締結した。ライセンス契約の条項によると、私たちは米国とカナダでIGEA製品を販売する独占的な権利を持っている。ライセンス契約の対価格として、私たちは最大400万ドルを支払うことに同意し、そのうちの50万ドルは2021年に支払い、いくつかの支払いはFDAのマイルストーンの実現にかかっている。
2022年5月、同社はFDAの買収技術の承認を得て、350万ドルまたは対価格マイルストーン債務をトリガした。このうち、150万ドルは2022年に支払い、100万ドルは他の流動負債に計上し、100万ドルは2022年12月31日までの他の長期負債に計上しなければならない。
関係者取引
2021年2月、私たちは、私たちのCEOの妻、元社長、最高経営責任者のジョイン·セブセクによって部分的に所有され、制御された医療機器技術会社と技術移転と特許権使用料協定を締結し、これにより、1,000万ドルまでの代価で特定の資産の知的財産権を獲得しました。対価格は、510(K)の許可を得るか、またはいくつかの純販売目標を達成することなど、複数のマイルストーンに依存する、署名時に支払われる100万ドルおよび900万ドルを含むか、または対価格である。この取引の追加検討については、本年度報告第8項総合財務諸表付記17を参照されたい。
Neo医療投資と転換可能なローン
2020年10月、吾らはスイスの私営医療科学技術会社Neo Medical SA(“Neo Medical”)と転換可能な融資協定(“転換可能融資”)を締結し、460万スイスフランをNeo Medical(発行日500万ドル)に貸し出した。このローンの利息は8.0%で、半年ごとに満期になります。転換可能なローンは2024年10月に満期になる;しかし、Neo Medicalの制御権が満期になる前に変化した場合、転換可能なローンはこの事件の発生時に直ちに満期になるべきである。
新冠肺炎とコロナウイルス援助,救済と経済安全法(CARE法案)の流動性と資本資源への影響
2020年4月、CARE法案の一部として、CMS加速と前金計画から1,390万ドルの資金を獲得し、新冠肺炎の影響を受けたサービスプロバイダとサプライヤーのキャッシュフローを増加させた。2021年4月、連邦医療保険は25%の医療保険支払いを回収し始め、そうでなければ提出されたクレームによってプロバイダやサプライヤーに不足してしまう。2022年3月、補償は医療保険支払いの50%に増加した。したがって、これらの時間帯では、全額支払いを受けるのではなく、
68
新たに提出されたクレームでは、2022年に完了するまで、加速および前払い案の下の未清算残高から返金金額を差し引く。
SeaSpineとの合併による潜在的義務に関する開示
SeaSpineは2022年12月1日、Lattus Spine LLCと独占許可と流通協定を締結した。(“Lattus”)特定の手術器具の永久ライセンスを取得する。SeaSpineは対価格として前払い許可料を支払い,最初のいくつかの機器を購入した。追加支払いは、買収資産のその後の純販売に依存し、その大部分は買収資産の将来の純販売に基づいており、会社は普通株を発行することでこれらの支払いの一部に資金を提供することを選択することができる。
SeaSpineとその流通業者との間の流通業者協定によると、合併の結果、会社は流通業者の選択に応じて流通業者の特定の資産を購入する義務がある。これが発生した場合、取引の買収価格は、(I)420万ドルまたは(Ii)ディーラーが支配権変更前の特定期間内に稼いだ手数料の100%となり、その買収価格は株式で支払われる。
未送金外貨収入
2022年12月31日現在、送金されていない外国収入は2700万ドル。当社の外国子会社への投資は依然として無期限ですが、重大な追加納税義務が生じない範囲では、当社はこれらの収益の一部を定期的に国内に送金する可能性があります。
契約義務
私たちの業務の結果として、私たちはいくつかの契約義務の制約を受けて、大量の現金が必要です。我々の重大な契約義務は、i)Spinal Kineticsの買収に関連するまたは対価格設定があること、ii)上述したような特定の資産買収に関連するまたは相対的な義務があること、iii)経営リースおよび融資リース義務、およびiv)不確定な税務状況を含むが、これらに限定されない。
価格設定(付記12及び17)、リース責任(付記9)及び不確定税務状況(付記20)のさらなる説明がある場合は、本年報第8項総合財務諸表付記を参照されたい。
表外手配
2022年12月31日現在、私たちは、私たちの財務状況、財務状況、収入または支出、運営結果、キャッシュフロー、流動性、資本支出または資本資源に対して、私たちの財務状況、財務状況、収入または支出に現在または未来の影響を与える可能性がある表外手配を持っていないか、または合理的に投資家に重要な意義を持っている。しかも、私たちは会社の注文の在庫が実質的だとは思わない。
肝心な会計見積もり
私たちの経営業績の検討は連結財務諸表と付記に基づいています。これらのレポートを作成する際には、財務諸表の日までに報告された資産および負債額、または有資産および負債の開示、および報告期間内の報告の収入および支出に影響を与える推定および仮定を行う必要がある。歴史的経験や経営陣が当時の状況で合理的と考えていた様々な他の仮定に基づいて、これらの推定を評価し続けている。実際の結果は,これらの見積り値と大きく異なる場合がある.
私たちは以下に説明する見積もりが私たちの総合財務諸表を作成する際に最も重要だと信じている。私たちは取締役会監査委員会と一緒にこのような重要な会計推定値を検討した。
収入確認
収入を確認する過程は私たちの特定の収入源に対する重大な仮定と判断に関するものだ。収入確認政策は“鍵となる会計見積もり”であり,見積もりを策定するための仮定の変化が純売上高,毛利,営業収入,EBITDA,純収入を含むキー財務指標に大きな影響を与える可能性があるからである。
骨成長療法の収入は主にアメリカから来ており、第三者支払人取引と卸売収入を含む。
69
我々の刺激製品の販売に関連する第三者支払者(商業保険会社、健康維持組織、第一選択提供者組織、例えばMedicareを含む)からの収入については、刺激製品が患者に適合し、患者に受け入れられ、第三者支払者が要求するすべての適用書類を取得したときに収入を確認する。これらの第三者支払者が支払う金額は、通常、固定または許可された精算料率に基づいている。これらの収入は予想または事前に承認された返済率で入金され、任意の契約手当を差し引いたり調整したりする。一部の請求書は第三者支払者によって審査され、調整される可能性がある。
卸売収入は我々の骨成長刺激器を医師や他の医療提供者に直接販売することに関連している。卸売り収入は、積み込みと購入注文の確認を受けたときに確認する、つまり顧客が約束した貨物に対するコントロール権を獲得した場合である。
生物製品の収入は主にアメリカから来ており、主にMTFの協力手配と関係がある。私たちは独占グローバル営業権を持っていて、MTFが取り扱う製品に基づいてMTFの営業費を徴収します。MTFはこれらの手配における要因と考えられているため,製品を顧客に出荷して購入確認注文を受けた場合には,これらのマーケティングサービス費用を純額で確認する.
脊柱インプラントと全世界整形外科会社の製品は世界各地に分布しており、アメリカでの販売は主に商業収入と商業販売と在庫流通業者の手配によって得られた国際販売を含む。
商業収入は主に病院の顧客に私たちの脊柱インプラントと全世界の整形外科製品を販売することから来ている。これらの製品が使用され、病院から確認調達注文を受けた場合には、商業収入を確認する。
在庫流通業者は私たちの製品を購入して、病院のような顧客に直接転売します。在庫流通業者からの収入は、積み込みと購入確認注文を受けたときに確認され、これは、流通業者が承諾貨物の制御権を獲得したときである。取引価格は私たちと在庫流通業者の歴史収集経験に基づいて推定されます。この百分率ビットは、各在庫流通業者に決定され、取引価格を計算するために使用される。販売コストも、製品統制権が顧客に移管されたときの記録、すなわち私たちの履行義務が履行されたときにもあります。
期待信用損失準備と契約手当
売掛金の最終入金を試算する過程は、重大な仮定と判断に関連する。売掛金の契約年限、未払い売掛金の帳簿齢及びこれらの売掛金推定契約年限の歴史入金、核販売と支払人返済経験を確定することは、期待信用損失準備金と契約手当の確定に関する推定過程の構成部分である。売掛金は四半期ごとに分析を行い、期待信用損失準備金と契約手当の十分性を評価する。期待信用損失推定準備の改訂は販売とマーケティング費用内の不良債権支出の調整に計上される。契約手当の改定は純売上高の調整に計上されている。これらは定期的に実際の収集経験に基づいて見積りをテストする.また、予想される信用損失推定を作成する際には、地理的位置と顧客タイプによって私たちの売掛金を分析します。
私たちの信用損失準備金は顧客の信用リスクを補うのに十分だと信じています。しかし、2022年12月31日まで、私たちの信用損失準備金が10%変化すれば、販売とマーケティング費用の増加または60万ドルの減少につながります。また、私たちは、顧客の信用リスクに対応するための契約手当の推定を確立するのに十分であると信じているが、2022年12月31日現在、契約手当準備金の10%変化は、純売上高の増加または30万ドルの減少につながると信じている。我々の信用損失準備と契約手当推定は“肝心な会計推定”であり、推定のための仮定の変化は純売上高、毛金利、営業収入、EBITDA、純収入と売掛金を含む重要な財務指標に重大な影響を与える可能性があるからである。
在庫免税額
超過、緩やかな移動と古い在庫の備蓄は在庫コストと市場価値の間の差額に基づいて計算され、新製品の投入周期、全体の製品ライフサイクル、需要と市場状況の予測の仮定と判断に基づいている。もし私たちの製品に対する需要が減少すれば、製品の生産が過剰かそれ以上になります
70
在庫が時代遅れになったら、在庫備蓄の増加を要求されるかもしれません。これは販売コストと毛利益を増加させます。私たちは在庫減記に対する私たちの開放を定期的に評価する。市場価値を決定するために使用されるか、または需要を予測するための条件または仮定が変化する場合、将来的に追加の在庫調整が必要となる可能性がある。私たちの在庫準備は“キー会計見積もり”であり、見積もりを作成するための仮定の変化は、毛利、営業収入、EBITDA、純収入、在庫を含む重要な財務指標に重大な影響を与える可能性があるからだ。
無形資産の価格計算
我々の無形資産には、主に特許、取得または開発の技術、進行中の研究開発(“IPR&D”)、顧客関係、商号、商標、許可手配が含まれる。私たちは業務合併や資産買収によって生じる無形資産の推定値について重大な判断を下します。企業合併で獲得した知的財産権研究開発活動のための無形資産は,関連プロジェクトが完了または放棄されるまで,無限の生命期を持つとみなされている。関連プロジェクト終了時には、買収した知的財産権研究開発の予想使用寿命内に償却したり、プロジェクトが成功せず、将来代替用途がない場合に買収した知的財産権研究開発の費用を償却する。
我々の割引キャッシュフロー推定モデルでは,将来の経営結果の予測に関する大きな判断が必要であり,無形資産の推定値を決定する必要がある。主に,買収された無形資産の期待使用寿命,個々の無形資産に関する予想キャッシュフロー,買収された知的財産権研究開発プロジェクトの推定成功確率,および予想成長率と割引率を仮定した。計画または仮定の重大な変更は、これらの資産の回収可能性に影響を与え、減値をもたらす可能性がある。これらの推定のための仮定の変化は、営業収入、EBITDA、純収入を含む重要な財務指標に大きな影響を与える可能性があるため、無形資産の推定値は“キー会計推定”である。
商誉
私たちの営業権は企業合併から得られた純資産のコストが公正な価値を超えていることを代表します。企業合併によって生じる営業権と無形資産の価値を決定する際には、取得された有形および無形資産の純資産値の公正価値に購入価格を分配するために、会計推定と判断を広く使用する必要がある。
著者らは少なくとも毎年営業権に対して減値テストを行い、潜在的な減値指標が存在すれば、毎年2回のテストの間でテストを行う。これらの指標には,売上高,収益あるいはキャッシュフローの著しい低下,あるいはビジネス環境の重大な不利な変化が含まれている。使用される推定および仮定のため、評価営業権の減少は、高度な判断に関するものである。このような見積もりと仮説の重大な変化は、営業収入、EBITDA、純収入を含む主要な財務指標に重大な影響を与える可能性があるため、減値評価に関連する見積もりと仮定が重要であると考えられる。
2021年第4四半期、年間営業権減値分析の一部として、営業権の数量化評価を行った。その各報告単位の公正価値を推定した後、著者らは全世界の整形外科報告単位の公正価値がその純資産の帳簿価値より低いことを確定した。これにより世界の整形外科会社の売上高は1180万ドルの全額減値を記録し、これは買収に関連する償却と再計量に反映されている。評価で得られた結論は、全世界の脊柱営業権に減値指標がないことである。
2022年第4四半期に、我々は年間営業権減価分析に対して定性評価を行い、減値費用は発生しなかった。この定性分析は報告部門特有のすべての関連要素を考慮し、マクロ経済条件、業界と市場考慮要素、全体財務業績及び関連実体の具体的な事件を含む。我々の定性的評価の一部として,減値可能性を評価する量子化要因を含め,減値が発生していないわけではない可能性が高いと結論した.
収益法と市場法から得られた公正価値加重平均値を用いて報告単位ごとの公正価値を推定した。公正価値計測は,市場では観察できない重大な投入に基づいており,主な仮定には,我々が予測した将来の純売上高と支出,端末成長率,適用割引率,報告単位ごとに会社レベルの費用を割り当てることが含まれているが,これらに限らない。これらの仮定の重大な変化は公正価値の大幅な上昇或いは低下を招く可能性があり、更に商業権が損なわれるかどうかに関する最終結論に影響する可能性がある。
公正価値計量
71
公正価値は、計量日市場参加者間の秩序ある取引において、資産または負債が元金または最も有利な市場で負債を譲渡するために課金または支払いされる価格(脱退価格)として定義される。2022年12月31日と2021年12月31日まで、公正な価値で記録された2つの最も重要な項目は、(I)Spinal Kineticsの買収に起因するか、または対価および(Ii)Neo Medicalとの転換可能な融資協定を含む。
またはSpinal Kineticsの買収に関連する将来の潜在的マイルストーン支払いを含む対価格があり、最大6000万ドルに達し、2023年4月30日までに支払わなければならない。これらの記念碑的支払いには,(I)FDAマイルストーンに達した1500万ドルと,(Ii)M 6−C人工頚椎とM 6−L人工腰椎未来販売に関する4500万ドルにのぼる収入ベースの記念碑的支払いがある。FDAのマイルストーンは2019年に実現され、そのうちの1つは収入ベースのマイルストーンが2021年に実現し、1500万ドルが支払われた。
2022年12月31日現在、我々は確率加重キャッシュフロー分析に基づいて余剰収入マイルストーンの公正価値を推定し、この分析は著者らの人工頚椎の歴史純売上高と2023年4月30日までのこのような人工頚椎の予想純売上高に基づいている。2022年12月31日現在,残りマイルストーンの推定公正価値はゼロであり,2023年4月30日までにマイルストーンが実現される可能性は低いと考えられるからである。
前の時期に、私たちはモンテカルロシミュレーションを使用して、収入ベースのマイルストーン支払いの残りの公正な価値を推定した。この公正価値計測は,市場では観察されない重大な投入に基づいており,主な仮定には,我々が予測した運動保存製品の将来の純売上高,適用の割引率,予測収入の潜在変動性の仮定がある。これらの仮定の大きな変化は、各期間の公正価値の大幅な上昇または低下をもたらす可能性がある。
著者らはオプション定価モデルと確率加重割引キャッシュフローモデルを用いて、Neo Medicalと達成した転換可能なローン合意の公正価値を推定した。公正価値計量は市場では観察できない重大な投入に基づいており、その中の重大な観測不可能投入は適用の割引率、隠れ変動率、償還或いは転換の可能性と予想時間、及びNeo Medicalによる企業価値の推定を支持する予測キャッシュフローを含む。このような仮定の重大な変化は公正な価値の大幅な上昇や低下を招く可能性がある。他の投入が不変の場合、株式割引率コストが2%増加すると転換可能ローンの公正価値が10万ドル減少し、株式割引コストが2%減少すると転換可能ローンの公正価値が20万ドル増加すると仮定する。
私たちの公正価値計量は1種の“肝心な会計推定”であり、推定のための仮定の変化は営業収入、EBITDAと純収入を含む重要な財務指標に重大な影響を与える可能性があるからである。
訴訟や負債があります
我々は時々、製品責任、人身傷害、特許及び知的財産権、健康及び安全、並びに雇用及びヘルスケア規制事項を含む訴訟、調査及び訴訟の当事者又は目標となり、これらの事項は正常な業務過程で処理され、弁護される。これらの訴訟、調査、または訴訟は大量のクレームに関連する可能性があり、私たちの名声と顧客基盤に悪影響を及ぼす可能性もある。私たちはこのような訴訟、調査、あるいは訴訟につながる可能性のある責任のために様々な責任保険計画を維持していますが、私たちはこのような責任の大部分のために自ら保険をかけています。
債務が発生し、金額を合理的に見積もることができる可能性が高い場合、私たちはこのような請求に応じます。損失が可能かどうか或いは合理的な可能性の評価、及び損失或いは損失範囲が合理的に推定されるかどうかは、往々にして未来の事件に対する一連の複雑な判断に関連する。私たちが評価に考慮する要素は、既存の法律手続き、調査およびクレームの性質、主張または可能性、または損害または損失(合理的に評価可能であれば)、事件の進展、既存の法律および前例、法律顧問および他のコンサルタントの意見または観点、このような訴訟における米国政府およびその機関の参加状況、類似事件における私たちの経験および他社の経験、評価時に把握した事実、および私たちが訴訟、調査またはクレームにどのように応答または応答するつもりかを含む。個別訴訟,調査,クレームの進展に伴い,これらの要因の評価は時間とともに変化する可能性がある。私たちが現在合理的に損失可能な範囲を合理的に推定できない事項について、この決定を促進する要素は、(I)求められている損害賠償が不確定であること、または調査が提起された民事または刑事訴えに現れていないこと、(Ii)事項が早期段階にあること、(Iii)事項が新しいまたは未解決の法的理論に関連しているか、または大量または不確実な実際または潜在的な事件または当事者に関連していることを含む。および/または(Iv)は、最終的に交渉および和解によって解決される可能性のある事項について政府または他の当事者と議論するが、損失または損失範囲を合理的に推定できると考えられる程度には至っていない。この場合私たちは
72
このような問題のスケジュールや最終解決には,可能な最終損失,罰金,罰金または業務影響(あれば)が含まれていると考えられる.
クレームに関する事実や状況の変化は、準備金推定期間中の我々の記録または改訂準備金推定期間の経営結果やキャッシュフローに実質的な影響を与える可能性がある。私たちの保険範囲と準備金は現在推定されているリスクの開放をカバーするのに十分だと信じていますが、記録準備金や既存の保険範囲を超える負債が生じない保証はありません。訴訟およびまたは有負債は“キー会計推定”であり、推定のための仮定の変化は、営業収入、EBITDA、純収入を含む重要な財務指標に大きな影響を与える可能性があるからである。
税務の件
私たちと私たちのすべての子会社はそれぞれの管轄区域内で適用される税率で課税されます。私たちの所得税支出、有効税率、繰延税金資産、繰延税金負債は利益による司法管轄区域によって異なります。さらに、私たちのいくつかの子会社は、私たちの他の子会社に直接製品を販売したり、私たちの他の子会社に行政、マーケティング、支援サービスを提供したりします。これらの会社間販売·支援サービスは、異なる税率の管轄区域で運営されている子会社に関するものである。これらの司法管轄区の税務機関は居住地基準、譲渡定価条項、あるいはそれぞれの税法の他の方面によって私たちの待遇に疑問を提起するかもしれません。これは私たちの総合税率と条項に影響を与えるかもしれません。
私たちが時々従事している取引では、税金の結果は不確実性の影響を受けるかもしれない。私たちは適用された会計基準に基づいてこれらの不確定な税務状況を計算する,これは取引の推定税金結果を評価する時に重要な判断を下す必要がある。我々は、既存の証拠の重みが、技術的利点を評価した後、税務立場が任意の関連する控訴または訴訟手続きを解決することを含む監査において維持される可能性が高いことを示すかどうかを判断することによって、納税申告書において採択されたまたは意図された税収的立場を評価する。私たちは税金割引を最終和解後に達成可能な50%以上の最大金額として測定した。私たちは、事実や状況の変化、税法の変化や解釈、監査における問題の効果的な解決、新しい監査活動などの要素を考慮するために、私たちの所得税を定期的に再評価します。このような確認または計量の変化は、財務諸表に大きな影響を与える可能性がある税収割引の確認または追加的な課税準備をもたらすであろう。
もしある繰延税金資産が予測可能な将来に現金化できない可能性が高い場合、私たちは繰延税金資産を計量する際に推定準備を確立する。この過程は、現在の税金負債を予測し、純営業損失と税金相殺繰越を含む今後の繰延税金資産と負債を推定しなければならないため、重大な判断を下す必要がある。評価に免税額が必要かどうかを評価する際には,最近の経営業績,繰越年度の課税収入可獲得性,課税一過性差の将来の引抜き,将来の課税収入予測(引越一時的差額は含まない),およびすべての慎重で実行可能な税務計画策を考える。
税務事項は“キー会計見積もり”に属し、見積もりを作成するための仮定の変化が純利益を含むキー財務指標に重大な影響を与える可能性があるからだ。
株式ベースの報酬
我々はBlack-Scholes推定モデルを用いてサービス型株式オプションの公正価値を計算した.この価値は実際に没収されたサービス期間を差し引いて費用として確認される。付与オプションの予想期間は、付与された帰属および満期条項、現在の未償還オプションおよび行使または満期オプションの従業員履歴行使行為、私たち普通株式の履歴変動性、および従業員の平均サービス年限を含む一連の要因に基づいて推定される。無リスク金利は一定の米国債安全金利に基づいて決定され、その契約期間はオプション付与の期待期限に近い。私たちは株の歴史変動率に基づいて期待変動率を推定する。
我々はモンテカルロ推定方法を用いて市場に基づく制限株式単位の公正価値を計算する.この価値は必要なサービス期間内に費用として確認され,没収が発生した場合に調整される。私たちが奨励公正価値を推定するためのモンテカルロ方法は、市場状況が満たされない可能性を含む。
業績に基づく制限株式単位の公正価値は,(I)付与日の終値と(Ii)期待が履行期間終了時に帰属する株式単位数に基づいて計算される.この価値は費用が超過していることが確認された
73
帰属の可能性があるとみなされる期間から派生する必要なサービス期間が付与される。帰属確率は予測された財務結果に基づいて評価され、重大な判断が必要である。
適切な公正価値モデルを確定し、従業員の株式奨励の公正価値を計算するには推定と判断が必要である。私たちの株式ベースの給与は“キー会計見積もり”であり、公正価値推定或いは必要なサービス期限を制定するための仮定の変化は、毛利益、営業収入、EBITDAと純収入を含む重要な財務指標に重大な影響を与える可能性があるからである。
非公認会計基準財務指標
特定のプロジェクトを含まない非公認会計基準財務措置を提供することは、投資家により大きな透明性を提供し、上級管理職がその財務および運営決定に使用する情報をより透明にすると考えられる。我々の業務運営の業績と潜在的な傾向に関する情報を補完するための上位管理層を投資家に提供することは,歴史的な運営実績との比較を容易にし,我々の運営戦略の有効性を内部で評価するために重要であると考えられる.これらの非GAAP財務指標を開示することはまた私たちの基本経営業績を業界の他の会社と比較するのに役立ち、これらの会社も非GAAP財務指標を用いてGAAP結果を補充する。
本年度報告で使用された非GAAP財務計量は分析ツールとして局限性がある可能性があり、単独で考慮したり、GAAP財務計量の代替として考慮すべきではない。これらの非公認会計基準の財務措置の使用に関連するいくつかの制限は、キャッシュフローに実質的な影響を与える可能性のある経済コストを反映する項目を排除することである。同様に、株式給与支出のようないくつかの非現金支出は、キャッシュフローに直接影響を与えないが、公認会計基準下の総報酬コストの一部に属する。
不変貨幣
不変貨幣は非公認会計原則の測定基準であり、前年比可能期間の外貨為替レートを用いて計算され、可比為替レートで純売上高を表す。不変貨幣は多種のGAAP指標に用いることができるが、管理層は外貨為替レートの変化の影響を受けることなく、不変貨幣を最もよく使用して純売上高を分析する。
EBITDA
EBITDAは,利息収入(費用),純額,所得税,減価償却,償却前の収益(任意の営業権減価の影響を含む)を差し引くと定義されている。EBITDAは,我々の首席運営決定者が業務を管理する際に用いる主な指標である.
自由キャッシュフロー
自由キャッシュフローは1種の非公認会計基準の財務計量であり、その計算方法は経営活動の純現金から資本支出を差し引くことである。自由キャッシュフローは、私たちの正常な業務運営(資本支出を含む)がどれだけの現金を発生または使用するかを評価する重要な指標である。経営陣はその資本効率とキャッシュフロー計画の進捗状況を測る指標として自由キャッシュフローを使用している。
ITEM 7 Aです。 市場リスクの定量的·定性的開示について
私たちが行っている業務運営の一部として、私たちは特定の市場リスクに直面している。主なリスクの開放には金利変化と外貨変動が含まれる。これらのリスク開放は、販売、販売コスト、運営コスト、融資コスト、現金と短期投資の収益に影響する可能性がある。私たちはこのような危険を管理するために適切な状況で派生金融商品を使用することができる。しかし、私たちのリスク管理政策は私たちが持っていないことを許さないし、私たちが取引や投機目的でデリバティブや他の金融投資をすることも許さない。
私たちは私たちの循環信用手配に関連する金利リスクに直面して、循環信用手配は保証のある隔夜融資金利(SOFR)を基礎として変動金利で利息を計算し、適用された借入保証金を加えて、あるいは基本金利(改訂信用協定の定義参照)に適用される借入保証金を加える。したがって、他の要素が不変であると仮定すると、金利の変化は通常債務の公平な市場価値に影響を与えないが、確かに未来の収益とキャッシュフローに影響を与える。2022年12月31日現在、改正された信用協定に関連する未返済残高は何もないため、現在このリスクは最小である。
74
しかし、2023年1月3日、私たちは、合併に関連するいくつかの費用の資金提供を含む運営資金目的のために、循環クレジット手配の下で3,000万ドルを借金しました。また、2023年3月3日に1500万ドルを借り入れた。
我々の売掛金に関する信用リスク集中は限られており,我々の顧客が地理的に分散しているため,エンドユーザはいくつかの業界で多様化していると考えられる.これらの顧客が経営する地域のグローバル経済状況及び/又は現地経営及び経済状況の変化、又は他の要因は、これらの売掛金残高の将来の現金化に合理的に影響を与える可能性がある。
私たちの外貨の開放は為替レートの変動から来て、主にドル対ユーロ、ブラジルレアル、オーストラリアドル、スイスフランあるいはポンドの為替レートです。我々の子会社(または会社自体)がその機能通貨以外の通貨で取引を行う場合、取引通貨リスクの影響を受ける。当社は2022年12月31日までに、経営報告書および総合収益(赤字)で外貨損失330万ドルを記録しました。
我々はまた、グローバル業務の結果を期間ごとに変動する為替レートをドルに換算することによる通貨リスクに直面している。2022年12月31日までの年間では、外貨建ての国際売上高に相当するドルが悪影響を受けているが、2021年12月31日までの年度では、ドルが我々の国際業務のすべての外国機能通貨の毎月の外貨為替レート変動によりドルが有利な影響を受けている。私たちが選定された外国市場で私たちの製品を流通·生産し続けることに伴い、将来的にこれらの市場での活動に関連する販売とコストは引き続き適用される外貨建てで価格を計算し続けることが予想され、為替変動が私たちの経営業績に大きな影響を与える可能性がある。本年度の純売上高と営業収入の外貨為替レート変化に対する敏感性を決定するための分析を行った。私たちの国際業務のすべての外貨に対してドルが10%値下がりすれば、純売上高は900万ドル増加し、営業収入は80万ドル増加すると確信しています。もしドルが私たちの国際業務のすべての外貨に対して10%上昇すれば、純売上高は900万ドル減少し、営業収入は80万ドル減少する。
ITEM 8。 財務諸表と補足データ
本年度報告F-1ページ“連結財務諸表索引”を参照。
ITem 9. 会計と財務情報開示の変更と相違
ない。
ITEM 9 Aです。 制御とプログラム
情報開示制御とプログラムの評価
本年報で述べた期間の終了時には、経営陣(総裁、最高経営責任者、財務責任者を含む)の監督·参加の下で、我々の開示制御およびプログラムの設計および動作の有効性を評価した。この評価に基づき、我々の総裁と最高経営責任者兼最高財務官は、本年度報告に係る期間が終了するまで、我々の開示制御および手続きが有効であると結論した。
財務報告の内部統制に関する経営陣の報告
会社経営陣は、財務報告書の十分な内部統制の確立と維持を担当する(この用語は、取引法第13 a-15条(F)条に定義されている)。当社の財務報告に対する内部統制は、(I)合理的で詳細かつ正確かつ公平に当社の資産を反映した取引および処置の記録を維持することに関連している;(Ii)米国公認会計基準に基づいて財務諸表を作成するために取引が必要とされることを保証するために合理的な保証を提供し、当社の収入および支出は、当社の管理層および取締役の許可のみに基づいて行われる、という政策および手順を含む。および(Iii)財務諸表に重大な影響を及ぼす可能性のある不正買収、使用または処分について、当社の資産を防止または適時に発見することについて合理的な保証を提供する。
75
財務報告の内部統制は米国公認会計原則に基づいて会社管理層と取締役会に合理的な保証を提供し、外部目的の信頼できる財務諸表を作成することを確保することを目的としている。いかなる内部制御の内在的限界のため、どんなによく設計されていても、誤った陳述が発生する可能性があり、予防や発見できない。したがって、財務報告を効率的に内部統制しても、財務諸表の作成に合理的な保証を提供するしかない。また、財務報告の内部統制の有効性の評価は特定の日に行われ、今後の期間の持続的有効性は、条件の変化により制御が不十分になる可能性があり、あるいは政策やプログラムを遵守する程度が低下する可能性がある。
本年度報告書の作成と届出について、会社経営陣は、総裁、最高経営責任者、最高財務官を含み、テレデビル委員会後援組織委員会が発表した“内部統制-総合枠組み(2013年)”(COSO基準)に基づいて、2022年12月31日までの財務報告内部統制の有効性を評価した。その評価によると、会社経営陣は、2022年12月31日現在、財務報告に対する社内統制は指定された基準に基づいて有効であると結論している。
安永会計士事務所は、本報告の後に発表された我々の財務報告書の内部統制の有効性に関する監査報告書を発表した。
財務報告の内部統制の変化
2022年第4四半期、財務報告の内部統制に大きな影響を与えたり、合理的に財務報告の内部統制に大きな影響を与える可能性のある変化はありません。
76
独立公認会計士事務所報告
Orthofix Medical Inc.の株主と取締役会へ
財務報告の内部統制については
我々は,トレデビル委員会後援組織委員会が発表した内部統制−総合枠組み(2013年枠組み)(COSO基準)で確立された基準に基づき,Orthofix Medical Inc.2022年12月31日までの財務報告内部統制を監査した。COSO基準によると,Orthofix Medical Inc.(当社)は2022年12月31日現在,すべての重要な面で財務報告に対して有効な内部統制を行っていると考えられる。
また、米国上場企業会計監督委員会(PCAOB)の基準に従って、2022年12月31日現在と2021年12月31日までの総合貸借対照表、2022年12月31日までの関連総合経営報告書と全面収益(損失)表、2022年12月31日現在の3年度の株主権益とキャッシュフローの変化および関連付記と2023年3月6日までの報告を監査し、保留のない意見を示した。
意見の基礎
当社経営陣は、効果的な財務報告内部統制を維持し、添付されている“経営陣財務報告内部統制報告”に掲載されている財務報告内部統制の有効性を評価する責任がある。私たちの責任は私たちの監査に基づいて、会社の財務報告書の内部統制に意見を述べることです。私たちはPCAOBに登録されている公共会計士事務所で、アメリカ連邦証券法およびアメリカ証券取引委員会とPCAOBの適用規則と法規に基づいて、私たちは会社と独立しなければなりません。
私たちはPCAOBの基準に従って監査を行っている。これらの基準は、財務報告の有効な内部統制がすべての重要な面で維持されているかどうかを決定するために、合理的な保証を得るために監査を計画し、実行することを要求する。
我々の監査には,財務報告の内部統制を理解すること,重大な弱点があるリスクを評価すること,評価されたリスクテストに基づいて内部統制の設計·運用有効性を評価すること,および状況下で必要と考えられる他のプロセスを実行することが含まれる。私たちは私たちの監査が私たちの観点に合理的な基礎を提供すると信じている。
財務報告の内部統制の定義と限界
会社の財務報告に対する内部統制は、公認された会計原則に基づいて、財務報告の信頼性と外部目的の財務諸表の作成に合理的な保証を提供することを目的としたプログラムである。会社の財務報告に対する内部統制には、(1)合理的で詳細かつ正確かつ公平に会社の資産を反映した取引および処分に関する記録の保存、(2)公認された会計原則に従って財務諸表を作成するために必要な取引が記録されている合理的な保証を提供し、会社の収入および支出は会社の経営陣と取締役の許可のみに基づいて行われる。(三)財務諸表に重大な影響を及ぼす可能性のある不正買収、使用、または処分会社の資産を防止またはタイムリーに発見する合理的な保証を提供する。
その固有の限界のため、財務報告書の内部統制は誤った陳述を防止したり発見できない可能性がある。また,将来的にどのような有効性評価を行うかの予測は,条件の変化により制御不足のリスクが生じる可能性があり,あるいは政策やプログラムの遵守度が悪化する可能性がある.
/S/安永法律事務所
テキサス州ダラス
March 6, 2023
77
ITEM 9 Bです。 その他の情報
2023年3月3日、会社はそれぞれジョアン·セブセクとダグラス·ライスと移行協定を締結した。シェブゼッカーさんは現在会社のCEOを務めており、2023年1月5日にSeaSpineホールディングスとの合併が完了する前に、同社の社長兼CEOを務めています。ライスさんは現在、合併前に同社の最高財務責任者を務めていた統合活動を支援している。
シェブゼクさんとの引継ぎ合意に基づき、双方は、ゼブゼッカーさんが2023年株主総会(現在は2023年6月に予定されている)で取締役再任に立候補しないことに同意し、その際、執行主席や取締役会のメンバーとしてのサービスを終了し、2023年7月5日まで非執行役員として雇用を継続する方針である。協定では、シェルブセクは現在の年間基本給を引き続き受け取り、2023日に例年の雇用された部分で比例計算された2023日の例年の現金ボーナスを受け取り続け、年間基本給の105%に相当することが規定されている。この合意はSerBousekさんと当社の間の支配権変更と解散料合意の条項に基づき,統合の結果,SerBousekさんが“CIC期間の十分な理由”を所有していることから,SerBousekさんが2023年7月5日に雇用関係を終了することを示しており,SerBousekさんによって当該制御権変更と解散料合意に基づく“CIC期十分理由”が終了したと考えられる。同協定はまた、セブセクさんが未償還株式オプションを行使する期間を、終了後24ヶ月から48ヶ月に延長することを規定しています。
双方は、ライスさんとの移行協定に基づき、2023年6月30日まで、同社の雇用関係を終了するまで、従業員として移行サービスを継続することで合意した。協定では、ライスは2023年6月30日までに、2023年の年間基本給や年間現金インセンティブ計画ボーナス機会ではなく、6.5万ドルの月費を得ることが規定されている。この合意は、ライスさんと当社との間の支配権変更と解散料合意の条項に基づき、合併によりライスさんが“CIC期間中の十分な理由”を有していたことから、ライスさんが2023年6月30日まで在任していた場合、その日における解雇は、その支配権変更及び解散料協議の下の“CIC期間”内に当社によって理由なく終了されたとみなされることを明らかにした。同協定では、ライスさんが未償還株式オプションを行使する期間を、終了後24ヶ月から48ヶ月に延長することも規定されている。
SerBousekさんとレスさんとの締結の移行プロトコルの記述は完全ではありませんが、これらのプロトコルの全文を参照して、それぞれ本ファイルの添付ファイル10.70と10.71アーカイブとして添付され、参照によって本明細書に組み込まれています。
プロジェクト9 Cです。 検査妨害に関する外国司法管区の開示
ない。
78
第三部
表格10−K第10,11,12,13および14項に要求された資料は本年度報告で省略し,本年度報告に含まれる財政年度終了後120日以内に最終依頼書または本年度報告の改訂本で提出する。
ITem 10。 役員·幹部と会社の管理
我々の最終委託書において、又は本年度報告に含まれる会計年度終了後120日以内の本年度報告修正案において、“取締役情報”、“第16条(A)実益所有権報告適合性”及びその他の可能なタイトルで、第10項役員報酬に関する情報を提供する。この情報は、参照によって本プロジェクト10に組み込まれる。
ITEM 11. 役員報酬
私たちの最終委託書または本年度報告書に含まれる会計年度終了後120日以内の本年度報告修正案では、第11条の役員報酬に関する情報を提供し、いずれも“役員報酬”というタイトルで提供され、その中の他の場所で提供される可能性がある。この情報は、参照によって本プロジェクト11に組み込まれる。
ITEM十二。 特定の実益所有者の担保所有権及び経営陣及び関連株主の事項
我々は、最終委託書又は本年度報告でカバーされる会計年度終了後120日以内の本年度報告修正案において、“特定の実益所有者及び管理層及び関連株主の証券所有権”及び“持分補償計画情報”のタイトルの下、及びその中の他の場所において、第12条の特定の実益所有者、我々の取締役及び幹部の私たちの証券所有権に関する情報、並びに私たちの持分補償計画に関する情報を提供する。この情報は、参照によって本プロジェクト12に組み込まれる。
ITem十三。 特定の関係や関連取引、取締役の独立性
我々の最終委託書において、または本年度報告がカバーする財政年度終了後120日に遅れない本年度報告修正案において、“何らかの関係および関連取引”、“取締役独立性”、および可能な他のタイトルの下で、13項に関連する取引および取締役独立性に関する情報を提供する。この情報は、参照によって本条項13に組み込まれる。
ITEM 14. チーフ会計士費用とサービス
我々の最終委託書又は本年度報告に含まれる会計年度終了後120日以内の本年度報告修正案において、“首席会計士費用及びサービス”というタイトルの下、及びその中の他の場所において、第14項に関連する主要会計士料金及びサービスに関する情報を提供する。この情報は、参照によって本プロジェクト14に組み込まれる。
79
第4部
ITEM十五。 展示·財務諸表明細書
(A)表10-Kレポートの一部として提出された書類
以下の書類は、本年度報告の10-Kフォームの一部として提出される
この表の10-K第F-1ページの“連結財務諸表インデックス”を参照されたい。
明細書は必要ではなく、必要な資料が存在しないか、金額が明細書の提出を要求するのに十分ではないため、または必要な情報が合併財務諸表または付記に含まれているからである。
展示品 |
|
説明する |
|
|
|
2.1 |
|
Orthofix Medical Inc.,Orca Merge Sub Inc.とSeaSpine Holdings Corporationとの間の合併協定と計画は,期日は2022年10月10日である(自社日が2022年10月11日の8−K表の証拠として提出され,引用により本明細書に組み込まれる)。 |
|
|
|
2.2 |
|
合意と合併計画は,Blackstone Medical,Inc.,Summit Development,Inc.とSpinal Kinetics,Inc.が2018年3月15日に署名された(会社が2018年3月31日までのForm 10−Q四半期報告の証拠として提出し,引用により本明細書に組み込む)。 |
|
|
|
3.1 |
|
Orthofix Medical Inc.社登録証明書(同社の日付が2018年8月1日である8-Kフォームの現在の報告の証拠として提出され、参照によって本明細書に組み込まれる)。 |
|
|
|
3.2 |
|
改訂および再記述されたOrthofix Medical Inc.規約は、2022年10月10日から改訂および再記載される(2022年10月11日に同社が現在報告している8−K表の証拠品として提出され、引用によって本明細書に組み込まれる)。 |
|
|
|
4.1 |
|
株式証明書表(2018年8月1日に会社が現在報告している8-K表の証拠品として提出され、参照により本明細書に組み込まれる)。 |
|
|
|
4.2 |
|
1934年証券取引法第12条に基づいて登録された登録者証券記述(会社が2019年12月31日現在の年次報告書10−K表の証拠品として提出し、引用により本明細書に組み込む)。 |
|
|
|
10.1 |
|
Orthofix Medical Inc.,Orthofix Inc.,Orthofix Spinal Implants Inc.,Orthofix International B.V.,Orthofix III B.V.およびOrthofix Medical Inc.のある子会社は保証人として,貸手であるいくつかの銀行や他の金融機関,および行政代理人であるモルガン大通(JPMorgan Chase,N.A.)の間で2019年10月25日に署名された第2回改訂と再署名されたクレジット協定(2019年11月1日に提出された会社として現在8−Kレポートの証拠物として,引用により本明細書に組み込まれる)。 |
|
|
|
10.2* |
|
2023年3月1日、Orthofix Medical Inc.,Orthofix US LLC,OrthofixオランダB.V.とOrthofix Medical Inc.のある子会社との間の第2次改正と再署名された信用協定の第1改正案は、保証人として、融資者であるいくつかの銀行や他の金融機関、および行政代理であるモルガン大通である。 |
|
|
|
10.3 |
|
改訂·再署名されたマトリックス商業化協力協定は、Orthofix US LLCと筋骨格移植基金社の間で2022年2月7日に締結された(会社が2022年12月31日までの会計年度のForm 10−K年度報告の証拠として提出され、参照により本明細書に組み込まれる)。 |
|
|
|
10.4 |
|
SeaSpine Orthopedics CorporationとPcoMed,LLCとの間の供給合意は,2021年3月1日である(SeaSpineホールディングスが提出した2021年3月31日までの四半期報告Form 10−Qの証拠として引用により本明細書に組み込まれる)。 |
|
|
|
80
10.5* |
|
AR Industrial No.1 Ltd.とOrthofix Inc.が2009年2月10日に締結したレンタル契約。 |
|
|
|
10.6* |
|
AR Industrial No.1 Ltd.とOrthofix Inc.が2009年4月13日に締結した賃貸契約第1修正案。 |
|
|
|
10.7* |
|
AR Industrial No.1 LtdとOrthofix Inc.が2010年5月12日に締結した賃貸契約第2修正案。 |
|
|
|
10.8* |
|
AR Industrial No.1 Ltd.Orthofix Inc.と2017年12月21日に締結された賃貸契約第3修正案。 |
|
|
|
10.9* |
|
AR Industrial No.1 Ltd.とOrthofix Inc.が2018年3月13日に締結した賃貸契約第4修正案。 |
|
|
|
10.10* |
|
AR Industrial No.1 Ltd.Orthofix Inc.と2019年1月3日に締結された賃貸契約第5修正案。 |
|
|
|
10.11* |
|
Lake Midas LLCとSpinal Kinetics,Inc.の間の標準賃貸契約は,2015年4月16日である。 |
|
|
|
10.12* |
|
Lake Midas LLCとSpinal Kinetics LLC(前身はSpinal Kinetics,Inc.)との間の標準賃貸契約の第1改正案日付は2022年3月4日。 |
|
|
|
10.13 |
|
SeaSpine Orthopedics CorporationとSkinMedica,Inc.の間の賃貸契約は、2015年7月8日である(SeaSpine Holdings Corporationによって2015年9月8日に現在の報告書として8-K表の証拠が提出され、参照によって本明細書に組み込まれる)。 |
|
|
|
10.14 |
|
Monch RRC Properties,LPとIsotis Orthobiologics,Inc.の間の標準工業/商業単テナント賃貸ネットワークは,2022年6月1日(SeaSpine Holdings Corporation 2022年6月30日までの四半期10−Q表の四半期報告の証拠物として提出され,参照により本明細書に組み込まれる)。 |
|
|
|
10.15 |
|
Orthofix Medical Inc.第2次改訂と再改訂された株式購入計画は,その第1号改正案により改正された(同社が2020年12月31日までの財政年度10−K表の年次報告書の証拠品として提出し,引用により本明細書に組み込む)。 |
|
|
|
10.16 |
|
Orthofix Medical Inc.第2次改正及び再改訂された株式購入計画の第2号修正案(会社が2021年6月21日に提出した8−K表の現在の報告書の証拠として提出され、参照により組み込まれる)。 |
|
|
|
10.17 |
|
Orthofix Medical Inc.は、2012年長期インセンティブ計画を改訂し、再改訂した(会社が2018年12月31日会計年度までのForm 10−K年度報告の証拠として提出し、引用により本明細書に組み込む)。 |
|
|
|
10.18 |
|
Orthofix Medical Inc.改訂·再改訂された2012年長期インセンティブ計画(会社が2020年6月8日に提出した現在の8−K表報告の証拠として引用により本明細書に組み込む)。 |
|
|
|
10.19 |
|
Orthofix Medical Inc.改正および再確認された2012年長期インセンティブ計画修正案2(会社が2021年6月21日に提出した8−Kフォームの現在の報告書の証拠として提出され、参照によって組み込まれる)。 |
|
|
|
10.20 |
|
Orthofix Medical Inc.改正および再改訂された2012年長期インセンティブ計画修正案3(会社が2022年6月7日に提出した8-K表の現在の報告書の証拠として提出され、参照によって組み込まれる)。 |
|
|
|
10.21 |
|
Orthofix Medical Inc.改正と再策定された2012年長期インセンティブ計画(会社が2022年12月31日までの財政年度10-K表年次報告の証拠物として、引用により本明細書に組み込む)下の従業員業績株式単位合意表(2022年付与)。 |
|
|
|
10.22 |
|
Orthofix Medical Inc.改訂·再策定された2012年長期インセンティブ計画(2019年12月31日現在の会社年次報告10-K表の証拠物として、引用により本明細書に組み込む)下の従業員業績株式単位プロトコル表(2016-2021年付与)。 |
|
|
|
10.23* |
|
Orthofix Medical Inc.改正と再起動による2012年長期インセンティブ計画下での時間に基づく従業員制限株式単位付与協定(2023年付与)の形式。 |
|
|
|
10.24 |
|
Orthofix Medical Inc.改訂·再策定された2012年長期インセンティブ計画(会社が2022年12月31日までの財政年度10-K表年次報告の証拠物として、本明細書に引用して組み込む)下の時間ベースの帰属従業員制限株式単位付与協定(2018-2022年付与)。 |
|
|
|
10.25* |
|
Orthofix Medical Inc.改正と再策定による2012年長期インセンティブ計画下での時間に基づく従業員非制限株式オプション協定(2023年付与)の形式。 |
|
|
|
81
10.26 |
|
Orthofix Medical Inc.改訂および再作成された2012年長期インセンティブ計画(会社が2016年7月8日に提出した現在の8-Kフォームの証拠として提出され、参照によって本明細書に組み込まれる)下の時間ベースの従業員非制限株式オプション協定の付与テーブル。 |
|
|
|
10.27 |
|
Orthofix Medical Inc.改訂および再署名された2012年長期インセンティブ計画-2014年7月から2016年6月まで(時間の帰属に基づく)従業員非限定株式オプション協定表(会社が2014年9月30日までの10-Q表四半期報告書の証拠として提出し、参照によって本明細書に組み込む)。 |
|
|
|
10.28 |
|
Orthofix Medical Inc.改正され再改訂された2012年長期インセンティブ計画(2014年前付与)(会社が2012年12月31日までの財政年度10-K表年次報告書の証拠として提出し、引用により本明細書に組み込む)下の従業員無保留株式オプション協定表。 |
|
|
|
10.29* |
|
Orthofix Medical Inc.改正と見直しによる2023年長期インセンティブ計画下の非従業員取締役限定株式単位協定(2023年付与)の表。 |
|
|
|
10.30 |
|
Orthofix Medical Inc.改正および再策定された2012年長期インセンティブ計画(2017年8月7日に提出された会社10-Q表の証拠として提出され、本明細書に引用して組み込まれる)下の非従業員取締役限定株式単位合意表(2017-2022年付与)。 |
|
|
|
10.31 |
|
Orthofix Medical Inc.改正と再策定による2012年長期インセンティブ計画下での時間ベース付与非従業員取締役無制限株式オプション協定の形式(初期贈呈金)(2016年7月8日に提出された会社の現在の報告書の8-K表の証拠として提出され、参照によって本明細書に組み込まれる)。 |
|
|
|
10.32 |
|
Orthofix Medical Inc.改正され再改訂された2012年長期インセンティブ計画(会社が2012年12月31日までの財政年度10−K表年度報告の証拠物として、引用により本明細書に組み込む)下の非従業員取締役非限定株式オプション合意表。 |
|
|
|
10.33 |
|
Jon SerBousekの従業員インセンティブ制限株式単位協定(2019年8月5日に提出された会社S-8表の証拠として提出され、参照により本明細書に組み込まれる)。 |
|
|
|
10.34 |
|
Jon SerBousekの従業員インセンティブ非限定株式オプション協定(2019年8月5日に提出された会社S-8表の証拠として提出され、参照によって本明細書に組み込まれる)。 |
|
|
|
10.35 |
|
Orthofix International N.V.およびBradley R.Masonが2013年3月13日に署名した誘因として非限定的株式オプション協定を付与した(2013年3月13日に提出された会社の現在の8-Kレポートの証拠として提出され、参照によって本明細書に組み込まれる)。 |
|
|
|
10.36 |
|
Orthofix Medical Inc.SeaSpine従業員研修計画(会社が2023年1月4日に提出したS-8表登録声明(登録番号:333-269116)の添付ファイル4.3として提出され、参照によって本明細書に組み込まれる)。 |
|
|
|
10.37 |
|
Orthofix Medical Inc.SeaSpine従業員インセンティブ計画-株式単位付与協定(会社2023年1月4日に提出されたS-8表登録声明(登録番号333-269116)として添付ファイル4.4が提出され、参照によって本明細書に組み込まれる)。 |
|
|
|
10.38 |
|
Orthofix Medical Inc.SeaSpine従業員に提供されるインセンティブ計画である非適格株式オプション付与協定(同社が2023年1月4日に提出したS−8表(登録番号:333−269116)の登録声明として添付ファイル4.5が提出され、参照により本明細書に組み込まれる)。 |
|
|
|
10.39 |
|
SeaSpineホールディングスは、2015年インセンティブ奨励計画(2016年3月30日現在改訂·再起動)を改訂·再策定した(2023年1月10日提出の会社S-8表の証拠として提出され、引用により本明細書に組み込まれている)。 |
|
|
|
10.40 |
|
“SeaSpine Holdings Corporation第1修正案”は、2015年奨励計画を改正し、再改訂した(会社が2023年1月10日に提出したS-8表の証拠品として提出され、参照によって本明細書に組み込まれる)。 |
|
|
|
10.41 |
|
SeaSpine Holdings Corporation第2改正案は、2015年奨励計画を改正し、再決定した(会社が2023年1月10日に提出したS-8表の証拠品として提出され、参照によって本明細書に組み込まれる)。 |
|
|
|
10.42 |
|
“海嶺ホールディングス2015年インセンティブ奨励計画改正案”(会社が2023年1月10日に提出したS-8表の証拠として提出され、引用により本明細書に組み込まれる)。 |
|
|
|
82
10.43 |
|
SeaSpine Holdings Corporation 2015インセンティブ奨励計画下の株式オプション付与通知および株式オプションプロトコル表(行使終了後3ヶ月の行使期間)(SeaSpine Holdings Corporationが2016年6月7日に証監会に提出したS-8表登録声明の証拠物として、参照によって本明細書に組み込まれる)。 |
|
|
|
10.44 |
|
SeaSpine Holdings Corporation 2015インセンティブ奨励計画(終了後1年の期間)における株式オプション付与通知および株式オプション協定の表(SeaSpine Holdings Corporationが2015年6月1日に委員会に提出した修正案第2号からForm 10への証拠として提出された表10は、参照により本明細書に組み込まれる)。 |
|
|
|
10.45 |
|
SeaSpine Holdings Corporation 2015インセンティブ奨励計画下の制限株式付与通知および制限株式奨励協定の表(SeaSpine Holdings Corporationが2016年6月7日に証監会に提出したS-8表登録声明の証拠物として、参照によって本明細書に組み込まれる)。 |
|
|
|
10.46 |
|
SeaSpine Holdings Corporation 2015インセンティブ奨励計画下の制限株式単位報酬通知および制限株式単位報酬プロトコルの表(SeaSpine Holdings Corporation 2016年12月31日までの年間報告Form 10−Kの証拠品として、参照により本明細書に組み込まれる)。 |
|
|
|
10.47 |
|
SeaSpine Holdings Corporation 2015インセンティブ奨励計画(2018年2月1日以降に付与された奨励)における制限株式単位奨励通知および制限株式単位奨励協定の表(2017年12月31日現在の年次報告10−K表の証拠物としてSeaSpine Holdings Corporationにより提出され、参照により本明細書に組み込まれる)。 |
|
|
|
10.48 |
|
SeaSpine Holdings Corporation 2015インセンティブ奨励計画における制限株式単位報酬通知および制限株式単位奨励プロトコル表(2020年1月1日以降に付与された報酬)(SeaSpine Holdings Corporationの2019年12月31日までの年次報告Form 10−Kの証拠物として、本明細書に組み込まれる)。 |
|
|
|
10.49 |
|
SeaSpine Holdings Corporation 2015年インセンティブ奨励計画(2018年6月6日以降に上級指導者チームメンバーに付与された奨励)に基づく株式オプション付与通知および株式オプション協定の表(SeaSpine Holdings Corporation 2018年6月30日現在のForm 10-Q四半期報告の証拠品として提出され、参照により本明細書に組み込まれる)。 |
|
|
|
10.50 |
|
SeaSpine Holdings Corporation 2015年インセンティブ奨励計画(2018年6月6日以降の非上級指導者チームメンバーへの奨励)における株式オプション付与通知および株式オプションプロトコル表(SeaSpine Holdings Corporationの2018年6月30日までの四半期報告Form 10-Qの証拠として提出され、参照により本明細書に組み込まれる)。 |
|
|
|
10.51 |
|
SeaSpine Holdings Corporationの下の年間インセンティブ計画は、2019年1月1日に改訂された2015年インセンティブ計画が改訂された(SeaSpine Holdings Corporation日付が2021年1月28日である現在の報告8−K表の証拠として提出され、引用により本明細書に組み込まれる)。 |
|
|
|
10.52 |
|
SeaSpine Holdings Corporation 2018年雇用誘因奨励計画(会社が2023年1月10日に提出したS-8表の証拠品として提出され、参照によって本明細書に組み込まれる)。 |
|
|
|
10.53 |
|
SeaSpine Holdings Corporation 2018年雇用誘因報酬計画下の制限株式単位奨励通知表および制限株式単位奨励協定(SeaSpine Holdings Corporation 2018年6月30日までの四半期報告Form 10-Qの証拠品として、本明細書に組み込まれる)。 |
|
|
|
10.54 |
|
SeaSpineホールディングス2018年雇用誘因奨励計画下の株式オプション付与通知と株式オプションプロトコル表(上級指導者チームメンバーの付与)(SeaSpineホールディングス社の2018年6月30日までの四半期報告Form 10-Qの証拠品として、参考に組み込む)。 |
|
|
|
10.55 |
|
SeaSpine Holdings Corporation 2018年雇用誘因奨励計画下の株式オプション付与通知および株式オプションプロトコル表(非上級指導者チームメンバーの付与)(SeaSpine Holdings Corporation 2018年6月30日までのForm 10-Q四半期報告の証拠品として、参考に組み込む)。 |
|
|
|
10.56 |
|
SeaSpineホールディングスは、2020年の雇用誘因奨励計画(会社が2023年1月10日に提出したS-8表の証拠として提出し、引用により本明細書に組み込む)。 |
|
|
|
83
10.57 |
|
SeaSpine Holdings Corporation 2020雇用誘因奨励計画における制限株式単位報酬通知および制限株式単位報酬プロトコルテーブル(SeaSpine Holdings Corporation 2020年6月30日までの四半期報告Form 10−Qの証拠物として、本明細書に組み込まれる)。 |
|
|
|
10.58 |
|
SeaSpineホールディングスの2020年雇用インセンティブ奨励計画下の株式オプション付与通知と株式オプションプロトコル表(上級指導者チームメンバーへの奨励)(SeaSpineホールディングスによる2020年6月30日までの四半期報告Form 10−Qの証拠品として、参考に組み込む)。 |
|
|
|
10.59 |
|
SeaSpine Holdings Corporation 2020年雇用インセンティブ奨励計画(非上級指導者チームメンバーに付与する奨励計画)下の株式オプション付与通知と株式オプション協定の表(SeaSpineホールディングスが2020年6月30日までのForm 10-Q四半期報告の証拠品として提出し、参照により本明細書に組み込む)。 |
|
|
|
10.60 |
|
Orthofix Medical Inc.とその役員および上級管理者との間の賠償プロトコル表(2023年1月5日に提出された会社の現在の8−K表の証拠として提出され、参照によって本明細書に組み込まれる)。 |
|
|
|
10.61 |
|
Orthofix Medical Inc.とその役員と上級管理者との間の賠償協定テーブル(2018年4月23日に提出された会社S-4フォーム登録声明(登録番号333-24407)添付ファイル10.1参照により統合)。 |
|
|
|
10.62 |
|
ブラッドリー·R·メイソンとOrthofix Medical Inc.が2019年2月25日に署名した移行·退職協定(会社が2018年12月31日までの財政年度Form 10−K年度報告の証拠として提出し、引用により本明細書に組み込む)。 |
|
|
|
10.63 |
|
Orthofix Medical Inc.およびJon Serbousekが2019年11月1日に署名した“制御およびサービス変更協定”(2019年11月1日に提出された会社の現在の8-Kフォーム報告書の添付ファイルとして提出され、参照によって本明細書に組み込まれる)。 |
|
|
|
10.64 |
|
Orthofix Medical Inc.とKevin Kennyが2019年11月1日に署名した“制御権変更と制御権変更協定”(2019年12月31日現在の10−Kフォーム年次報告の証拠として提出され、参照により本明細書に組み込まれる)。 |
|
|
|
10.65 |
|
Orthofix International N.V.とダグ·ライスが2016年11月1日に締結した改訂された“制御権変更と所有権変更協定”(会社が2016年12月31日までの財政年度Form 10−K年度報告の証拠物として引用により本明細書に組み込む)。 |
|
|
|
10.66 |
|
Orthofix International N.V.とキンバリーEltingが2016年11月1日に締結した“制御権変更と制御権変更協定”(会社が2016年12月31日までの会計年度のForm 10−K年度報告の証拠物として引用により本明細書に組み込む)。 |
|
|
|
10.67 |
|
会社とキース·C·バレンティンとの間の招待状(会社が2023年1月5日に提出した8-K表の証拠として提出され、引用により本明細書に組み込まれる)。 |
|
|
|
10.68 |
|
会社とJohn J.Bostjancicとの間の招待状(会社が2023年1月5日に提出した8-Kフォームの証拠として提出され、参照によって本明細書に組み込まれる)。 |
|
|
|
10.69 |
|
会社とパトリック.L.Keranとの間の重要な手紙(2023年1月5日に提出された会社の現在の報告Form 8-Kの証拠として提出され、引用によって本明細書に組み込まれる)。 |
|
|
|
10.70* |
|
Orthofix医療会社とジョイン·セブセクが2023年3月3日に署名した移行協定。 |
|
|
|
10.71* |
|
Orthofix医療会社とダグ·ライスが2023年3月3日に署名した移行協定。 |
|
|
|
21.1* |
|
子会社リスト。 |
|
|
|
23.1* |
|
独立公認会計士事務所が同意します。 |
|
|
|
31.1* |
|
ルール13 a−14(A)/15 d−14(A)首席実行幹事の認証。 |
|
|
|
31.2* |
|
細則13 a-14(A)/15 d-14(A)首席財務幹事の証明。 |
|
|
|
32.1* |
|
第1350条最高経営責任者証明書及び最高財務官証明書。 |
84
|
|
|
101.INS |
|
相互接続されたXBRLインスタンス文書−インスタンス文書は、そのXBRLタグがXBRL文書に埋め込まれているので、対話型データファイルに表示されない。 |
|
|
|
101.SCH* |
|
インラインXBRL分類拡張アーキテクチャ文書. |
|
|
|
101.CAL* |
|
インラインXBRL分類はリンクベース文書を計算する. |
|
|
|
101.DEF* |
|
インラインXBRLソートはLinkbase文書を定義する. |
|
|
|
101.LAB* |
|
XBRL分類ラベルLinkbase文書を連結する. |
|
|
|
101.PRE* |
|
LinkbaseドキュメントをインラインXBRL分類でプレゼンテーションする. |
|
|
|
104 |
|
表紙対話データファイル(添付ファイル101に含まれるイントラネットXBRLのフォーマット)。 |
*本テーブルの10-Kに従って提出されます。
テキストの一部を編集して括弧付きスター番号で置き換えることにより,本展覧会ではいくつかの実質的でないプライベートや機密部分が省略されている.
第十六項。 表10-Kの概要
ありません
85
サイン
1934年“証券取引法”第13又は15(D)節の要求に基づいて、登録者は、正式に許可された以下の署名者がその代表を代表して本報告に署名することを正式に手配した。
|
|
|
|
Orthofix医療会社です。 |
||
|
|
|
|
|
||
日付:2023年3月6日 |
|
|
|
差出人: |
|
/s/キース·バレンティン |
|
|
|
|
名前: |
|
キース·バレンティン |
|
|
|
|
タイトル: |
|
社長と取締役CEO |
|
|
|
|
|
|
|
日付:2023年3月6日 |
|
|
|
差出人: |
|
/s/John Bostjancic |
|
|
|
|
名前: |
|
ジョン·ボスターヤンシッチ |
|
|
|
|
タイトル: |
|
首席財務官 |
本報告は、1934年の証券取引法の要求に基づき、以下の登録者によって登録者として指定日に署名された。
名前.名前 |
|
タイトル |
|
日取り |
|
|
|
|
|
/s/キース·バレンティン キース·バレンティン |
|
社長と取締役CEO (首席行政主任) |
|
March 6, 2023 |
|
|
|
|
|
/s/John Bostjancic ジョン·ボスターヤンシッチ |
|
首席財務官 (首席財務会計官) |
|
March 6, 2023 |
|
|
|
|
|
キャサリン·ブルジク キャサリン·ブルジク |
|
取締役会首席独立取締役 |
|
March 6, 2023 |
|
|
|
|
|
/s/ジョイン·セブセク ジョイン·セブセク |
|
取締役、取締役会執行議長 |
|
March 6, 2023 |
|
|
|
|
|
/s/Stuart Essig スチュアート·エシガー |
|
役員.取締役 |
|
March 6, 2023 |
|
|
|
|
|
ジェイソン·ハンナ ジェイソン·ハンノン |
|
役員.取締役 |
|
March 6, 2023 |
|
|
|
|
|
ジョン·ヘニマンIII ジョン·ヘニマンIII |
|
役員.取締役 |
|
March 6, 2023 |
|
|
|
|
|
/s/ジェームズ·シンリッジ |
|
役員.取締役 |
|
March 6, 2023 |
ジェームズ·シンリッジ |
||||
|
|
|
|
|
/s/Sheta Singh Maniar |
|
役員.取締役 |
|
March 6, 2023 |
シュヴィータ·シンガー·マニアール |
||||
|
|
|
|
|
/s/マイケル·ポールチ |
|
役員.取締役 |
|
March 6, 2023 |
マイケル·ポールチ |
|
|
|
|
|
|
|
|
|
86
Orthofix医療会社です。
財務諸表に対する経営陣の責任説明
Orthofix Medical Inc.の株主へ:
経営陣は本年度報告書に掲載されている総合財務諸表及び関連資料の作成を担当している。総合財務諸表には、経営陣の推定と判断に基づく額が含まれており、米国で一般的に受け入れられている会計原則に基づいて作成されている。株主の報告書に提出された他の財務情報は、連結財務諸表中の情報と一致する。
当社には会計及び内部制御制度が設けられており、合理的なコストで合理的な保証を提供し、資産が無許可使用や処分によって損失を被ることがないようにし、財務記録の信頼性を確保し、財務諸表の作成及び資産に対する責任を維持する。書面政策、責任分担の組織構造の提供、合格者の慎重な選別と訓練により、これらの制度が強化された。
当社は独立公認会計士の安永法律事務所を招聘し、アメリカ上場会社会計監督委員会の監査基準に基づいて合併財務諸表を監査し、意見を提出する。これらの基準には,内部統制制度の評価と取引のテストが含まれており,その意見を支持するために必要な程度である.
取締役会は、その監査委員会を介して経営陣と我々の独立公認会計士と定期的に面会することにより、各人がそれぞれの責任を果たすことを確保し、内部統制及び財務報告に関する事項を検討する。安永法律事務所は監査委員会に完全かつ自由に接触することができる。
ジェームズ·シンリッジ
監査委員会議長
キース·バレンティン
社長と取締役CEO
ジョン·ボスターヤンシッチ
首席財務官
87
Orthofix医療会社です。
I連結財務諸表のNDX
|
ページ |
|
|
連結財務諸表索引 |
|
F-1 |
|
独立公認会計士事務所報告(PCAOB ID: |
|
F-2 |
|
2022年と2021年12月31日までの連結貸借対照表 |
|
F-4 |
|
2022年、2021年、2020年12月31日までの総合営業と全面収益(赤字)レポート |
|
F-5 |
|
2022年12月31日現在、2021年12月31日と2020年12月31日までの総合株主権益変動表 |
|
F-6 |
|
2022年12月31日現在、2021年12月31日と2020年12月31日までの連結現金フロー表 |
|
F-7 |
|
連結財務諸表付記 |
|
F-8 |
|
F-1
R独立公認会計士事務所報告
Orthofix Medical Inc.の株主と取締役会へ
財務諸表のいくつかの見方
我々はすでにOrthofix Medical Inc.(当社)の2022年12月31日と2021年12月31日までの連結貸借対照表、関連する総合経営報告書と全面収益(赤字)を監査しました 2022年12月31日までの3年度の株主権益及びキャッシュフロー変動及び関連付記(総称して“総合財務諸表”と呼ぶ)。総合財務諸表は、すべての重要な面で、2022年12月31日、2022年12月31日、2021年12月31日までの会社の財務状況、および2022年12月31日までの3年度の経営結果とキャッシュフローを公平に反映しており、米国公認会計原則に適合していると考えられる。
また、米国上場企業会計監督委員会(PCAOB)の基準に基づき、テレデビル委員会後援組織委員会が発表した“内部統制-総合枠組み(2013枠組み)”で確立された基準と、2023年3月6日までの報告に基づき、2022年12月31日までの財務報告内部統制を監査し、保留のない意見を発表した。
意見の基礎
これらの財務諸表は会社の経営陣が責任を負う。私たちの責任は私たちの監査に基づいて会社の財務諸表に意見を発表することです。私たちはPCAOBに登録されている公共会計士事務所で、アメリカ連邦証券法およびアメリカ証券取引委員会とPCAOBの適用規則と法規に基づいて、私たちは会社と独立しなければなりません。
私たちはPCAOBの基準に従って監査を行っている。これらの基準は、財務諸表に重大な誤報がないかどうかに関する合理的な保証を得るために、エラーによるものであっても不正であっても、監査を計画し、実行することを要求する。我々の監査には、財務諸表の重大な誤報リスクを評価するプログラム、エラーによるものであれ詐欺であっても、これらのリスクに対応するプログラムを実行することが含まれています。これらの手続きは、財務諸表中の金額および開示に関連する証拠をテストに基づいて検討することを含む。我々の監査には、経営陣が使用する会計原則の評価と重大な見積もり、財務諸表の全体列報を評価することも含まれています。私たちは私たちの監査が私たちの観点に合理的な基礎を提供すると信じている。
重要な監査事項
以下に述べる重要な監査事項とは、監査委員会に伝達または要求が監査委員会に伝達された当期財務諸表監査によって生じる事項である:(1)財務諸表に対して重大な意義を有する勘定または開示に関するものであり、(2)特に挑戦的で主観的または複雑な判断に関するものである。重要監査事項の伝達は、総合財務諸表に対する私たちの全体的な意見をいかなる方法でも変えることはなく、以下の重要な監査事項を伝達することによって、キー監査事項またはそれに関連する勘定または開示に関する個別的な意見を提供することはない。
F-2
在庫超過と古い備蓄 |
|
関係事項の記述 |
2022年12月31日現在、会社の在庫残高は1.002億ドルで、経営陣の在庫過剰と古い備蓄に対する見積もり純額となっている。統合財務諸表付記5に記載されているように、管理層は、古い要因または他の要因により在庫コストを回収できないことを決定するために、その在庫価値を現金化可能値に調整する。これらの決定を下すために、管理層は、将来の需要を推定して、適切な在庫備蓄を決定し、これらの在庫の帳簿価値をそれに応じて調整して、コストまたは換金可能純値のより低い者を反映する。
監査管理層は、推定された製品需要、製品ライフサイクルの長さ、および新製品の市場受容度の評価に要する時間を含む仮説の変化に敏感であるため、在庫過剰および古い備蓄の推定に対して高度な主観性を有する。これらの仮定は在庫過剰と古い備蓄の測定に大きな影響を及ぼす。 |
私たちが監査でどのようにこの問題を解決したのか |
在庫過剰と古い備蓄の計量と推定に関する重大な誤報リスクを処理した制御措置の設計を評価し,制御措置の操作有効性をテストした。例えば、企業が在庫過剰と旧備蓄を推定する流れの制御、在庫過剰および古い備蓄を推定するためのモデルの管理層の審査および承認、このモデルのデータ入出力および管理層のモデルに対する定性的な調整をテストした。 在庫過剰と古い備蓄残高をテストするために、上記の重大な仮定と品質調整の評価、会社が分析に使用する基礎データを含む監査プログラムを実行した。我々の監査プログラムには、テストモデルで使用されている基礎データの完全性と正確性が含まれており、これらのデータが現在の状況を表すかどうかを評価する。我々は、経営陣の推定の歴史的正確性を評価し、仮説変化による在庫過剰と古い備蓄の変化を評価するために、重大な仮説に対して敏感な分析を行った。 |
/s/
2002年以来、私たちは同社の監査役を務めてきた。
March 6, 2023
F-3
Orthofix医療会社です。
C2022年12月31日現在と2021年12月31日現在の連結貸借対照表
(ドル、千円、額面データは除く) |
|
2022 |
|
|
2021 |
|
||
資産 |
|
|
|
|
|
|
||
流動資産 |
|
|
|
|
|
|
||
現金と現金等価物 |
|
$ |
|
|
$ |
|
||
売掛金、準備金純額#ドルを差し引く |
|
|
|
|
|
|
||
棚卸しをする |
|
|
|
|
|
|
||
前払い費用と他の流動資産 |
|
|
|
|
|
|
||
流動資産総額 |
|
|
|
|
|
|
||
財産·工場·設備·純価値 |
|
|
|
|
|
|
||
無形資産、純額 |
|
|
|
|
|
|
||
商誉 |
|
|
|
|
|
|
||
その他長期資産 |
|
|
|
|
|
|
||
総資産 |
|
$ |
|
|
$ |
|
||
負債と株主権益 |
|
|
|
|
|
|
||
流動負債 |
|
|
|
|
|
|
||
売掛金 |
|
$ |
|
|
$ |
|
||
融資リース負債の当期分 |
|
|
|
|
|
|
||
その他流動負債 |
|
|
|
|
|
|
||
流動負債総額 |
|
|
|
|
|
|
||
融資リース負債の長期部分 |
|
|
|
|
|
|
||
その他長期負債 |
|
|
|
|
|
|
||
総負債 |
|
|
|
|
|
|
||
(注13) |
|
|
|
|
|
|
||
株主権益 |
|
|
|
|
|
|
||
普通株$ |
|
|
|
|
|
|
||
追加実収資本 |
|
|
|
|
|
|
||
利益を残す |
|
|
|
|
|
|
||
その他の総合損失を累計する |
|
|
( |
) |
|
|
— |
|
株主権益総額 |
|
|
|
|
|
|
||
総負債と株主権益 |
|
$ |
|
|
$ |
|
||
付記はこれらの総合財務諸表の不可分の一部である。
F-4
Orthofix医療会社です。
C合併経営と全面収益報告書(赤字)
2022年12月31日まで,2021年12月31日と2020年12月31日までの年度
(ドル、単位は千で、1株および1株当たりのデータは含まれていない) |
|
2022 |
|
|
2021 |
|
|
2020 |
|
|||
純売上高 |
|
$ |
|
|
$ |
|
|
$ |
|
|||
販売コスト |
|
|
|
|
|
|
|
|
|
|||
毛利 |
|
|
|
|
|
|
|
|
|
|||
販売とマーケティング |
|
|
|
|
|
|
|
|
|
|||
一般と行政 |
|
|
|
|
|
|
|
|
|
|||
研究開発 |
|
|
|
|
|
|
|
|
|
|||
買収に関連した販売と再計量 |
|
|
( |
) |
|
|
|
|
|
( |
) |
|
営業(赤字) |
|
|
( |
) |
|
|
( |
) |
|
|
( |
) |
利子支出,純額 |
|
|
( |
) |
|
|
( |
) |
|
|
( |
) |
その他の収入,純額 |
|
|
( |
) |
|
|
( |
) |
|
|
|
|
所得税前(赤字) |
|
|
( |
) |
|
|
( |
) |
|
|
( |
) |
所得税の割引 |
|
|
( |
) |
|
|
( |
) |
|
|
|
|
純収益(赤字) |
|
$ |
( |
) |
|
$ |
( |
) |
|
$ |
|
|
|
|
|
|
|
|
|
|
|
|
|||
普通株1株当たり純収益(損失): |
|
|
|
|
|
|
|
|
|
|||
基本的な情報 |
|
$ |
( |
) |
|
$ |
( |
) |
|
$ |
|
|
薄めにする |
|
|
( |
) |
|
|
( |
) |
|
|
|
|
普通株式加重平均: |
|
|
|
|
|
|
|
|
|
|||
基本的な情報 |
|
|
|
|
|
|
|
|
|
|||
薄めにする |
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|||
税引き前その他全面収益 |
|
|
|
|
|
|
|
|
|
|||
債務証券の未実現収益 |
|
|
|
|
|
( |
) |
|
|
|
||
貨幣換算調整 |
|
|
( |
) |
|
|
( |
) |
|
|
|
|
税引き前その他全面収益 |
|
|
( |
) |
|
|
( |
) |
|
|
|
|
その他総合収益(赤字)項目に関する所得税収益(費用) |
|
|
— |
|
|
|
|
|
|
( |
) |
|
その他総合収益(損失)、税引き後純額 |
|
|
( |
) |
|
|
( |
) |
|
|
|
|
総合収益(赤字) |
|
$ |
( |
) |
|
$ |
( |
) |
|
$ |
|
|
付記はこれらの総合財務諸表の不可分の一部である。
F-5
Orthofix医療会社です。
2022年12月31日まで,2021年12月31日と2020年12月31日までの年度
(ドル、千単位) |
|
量 |
|
|
ごく普通である |
|
|
その他の内容 |
|
|
保留する |
|
|
積算 |
|
|
合計する |
|
||||||
2019年12月31日 |
|
|
|
|
$ |
|
|
$ |
|
|
$ |
|
|
$ |
( |
) |
|
$ |
|
|||||
採用後の累積効果調整 |
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
( |
) |
|
|
— |
|
|
|
( |
) |
純収入 |
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
|
|
|
— |
|
|
|
|
||
その他の総合収益、税引き後純額 |
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
|
|
|
|
||
株式ベースの給与費用 |
|
|
— |
|
|
|
— |
|
|
|
|
|
|
— |
|
|
|
— |
|
|
|
|
||
普通株式を発行し,純額 |
|
|
|
|
|
|
|
|
|
|
|
— |
|
|
|
— |
|
|
|
|
||||
2020年12月31日 |
|
|
|
|
$ |
|
|
$ |
|
|
$ |
|
|
$ |
|
|
$ |
|
||||||
純損失 |
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
( |
) |
|
|
— |
|
|
|
( |
) |
その他総合損失、税引き後純額 |
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
( |
) |
|
|
( |
) |
株式ベースの給与費用 |
|
|
— |
|
|
|
— |
|
|
|
|
|
|
— |
|
|
|
— |
|
|
|
|
||
普通株式を発行し,純額 |
|
|
|
|
|
|
|
|
|
|
|
— |
|
|
|
— |
|
|
|
|
||||
2021年12月31日 |
|
|
|
|
$ |
|
|
$ |
|
|
$ |
|
|
$ |
- |
|
|
$ |
|
|||||
純損失 |
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
( |
) |
|
|
— |
|
|
|
( |
) |
その他総合損失、税引き後純額 |
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
( |
) |
|
|
( |
) |
株式ベースの給与費用 |
|
|
— |
|
|
|
— |
|
|
|
|
|
|
— |
|
|
|
— |
|
|
|
|
||
普通株式を発行し,純額 |
|
|
|
|
|
|
|
|
|
|
|
— |
|
|
|
— |
|
|
|
|
||||
2022年12月31日 |
|
|
|
|
$ |
|
|
$ |
|
|
$ |
|
|
$ |
( |
) |
|
$ |
|
|||||
付記はこれらの総合財務諸表の不可分の一部である。
F-6
Orthofix医療会社です。
Cキャッシュフロー表統合レポート
2022年12月31日まで,2021年12月31日と2020年12月31日までの年度
(ドル、千単位) |
|
2022 |
|
|
2021 |
|
|
2020 |
|
|||
経営活動のキャッシュフロー |
|
|
|
|
|
|
|
|
|
|||
純収益(赤字) |
|
$ |
( |
) |
|
$ |
( |
) |
|
$ |
|
|
純収益を経営活動の現金純額に調整する |
|
|||||||||||
減価償却および償却 |
|
|
|
|
|
|
|
|
|
|||
営業権の減価 |
|
|
— |
|
|
|
|
|
|
— |
|
|
リース資産、債務コスト、その他の資産の償却経営 |
|
|
|
|
|
|
|
|
|
|||
期待信用損失準備金 |
|
|
|
|
|
|
|
|
|
|||
所得税を繰延する |
|
|
|
|
|
|
|
|
|
|||
株式ベースの給与費用 |
|
|
|
|
|
|
|
|
|
|||
投資証券推定の利子と損失 |
|
|
( |
) |
|
|
( |
) |
|
|
|
|
価格の公正価値変動があるかもしれない |
|
|
( |
) |
|
|
( |
) |
|
|
( |
) |
他にも |
|
|
|
|
|
|
|
|
( |
) |
||
経営性資産と負債の変動,買収の影響を差し引く |
|
|
|
|
|
|
|
|
|
|||
売掛金 |
|
|
( |
) |
|
|
( |
) |
|
|
|
|
棚卸しをする |
|
|
( |
) |
|
|
|
|
|
( |
) |
|
前払い費用と他の流動資産 |
|
|
( |
) |
|
|
( |
) |
|
|
|
|
売掛金 |
|
|
|
|
|
|
|
|
|
|||
その他流動負債 |
|
|
|
|
|
|
|
|
|
|||
契約責任(付記15) |
|
|
( |
) |
|
|
( |
) |
|
|
|
|
支払うか掛け値がある |
|
|
— |
|
|
|
( |
) |
|
|
— |
|
その他の長期資産と負債 |
|
|
( |
) |
|
|
( |
) |
|
|
( |
) |
経営活動の現金純額 |
|
|
( |
) |
|
|
|
|
|
|
||
投資活動によるキャッシュフロー |
|
|
|
|
|
|
|
|
|
|||
企業を買収する |
|
|
— |
|
|
|
— |
|
|
|
( |
) |
不動産·工場·設備の資本支出 |
|
|
( |
) |
|
|
( |
) |
|
|
( |
) |
無形資産資本支出 |
|
|
( |
) |
|
|
( |
) |
|
|
( |
) |
投資証券を購入する |
|
|
— |
|
|
|
( |
) |
|
|
( |
) |
資産買収やその他の投資 |
|
|
( |
) |
|
|
( |
) |
|
|
( |
) |
投資活動の現金純額 |
|
|
( |
) |
|
|
( |
) |
|
|
( |
) |
融資活動によるキャッシュフロー |
|
|
|
|
|
|
|
|
|
|||
循環信用手配からの収益 |
|
|
— |
|
|
|
— |
|
|
|
|
|
循環信用手配を償還する |
|
|
— |
|
|
|
— |
|
|
|
( |
) |
普通株式を発行して得た金 |
|
|
|
|
|
|
|
|
|
|||
株式の減納に関する支払い |
|
|
( |
) |
|
|
( |
) |
|
|
( |
) |
支払うか掛け値がある |
|
|
— |
|
|
|
( |
) |
|
|
— |
|
融資リース義務に関する支払い |
|
|
( |
) |
|
|
( |
) |
|
|
( |
) |
債務発行費用やその他の融資活動を支払う |
|
|
( |
) |
|
|
( |
) |
|
|
( |
) |
融資活動の現金純額 |
|
|
( |
) |
|
|
( |
) |
|
|
|
|
為替レート変動が現金と制限現金に及ぼす影響 |
|
|
( |
) |
|
|
( |
) |
|
|
|
|
現金、現金等価物および限定的現金の純変化 |
|
|
( |
) |
|
|
( |
) |
|
|
|
|
年初の現金、現金等価物、制限現金 |
|
|
|
|
|
|
|
|
|
|||
年末現金、現金等価物、制限現金 |
|
$ |
|
|
$ |
|
|
$ |
|
|||
|
|
|
|
|
|
|
|
|
|
|||
年末現金、現金等価物、制限現金の構成 |
|
|||||||||||
現金と現金等価物 |
|
$ |
|
|
$ |
|
|
$ |
|
|||
制限現金 |
|
|
— |
|
|
|
— |
|
|
|
|
|
年末現金、現金等価物、制限現金 |
|
$ |
|
|
$ |
|
|
$ |
|
|||
これらの総合財務諸表を構成する構成要素を付記する
F-7
Orthofix医療会社です。
N連結財務諸表のOTES
1.業務と届出根拠
業務記述
Orthofix医療会社とその子会社(“会社”)は最近SeaSpineホールディングス(“SeaSpine”)と合併した後、世界をリードする脊柱と整形外科会社であり、全面的な生物製剤、革新的な脊柱ハードウェア、骨成長療法、専門整形外科解決方案とリードする外科ナビゲーションシステムを持っている。その製品は世界68カ国·地域に販売されている。
同社はテキサス州ルイビルに本部を置き、カリフォルニア州カールスバッドとイタリアのヴェローナに主要な事務所を設置し、脊柱製品革新と外科医師教育に集中し、重点は整形外科の製品革新、生産と医学教育である。合併後の会社の世界的な研究開発、商業、製造業務には、カリフォルニア州オーウェン、カナダトロント、カリフォルニア州サニービル、ペンシルベニア州ウェイン、ペンシルベニア州オリーブ支社、イギリスメデンヘド、ドイツミュンヘン、フランスパリ、ブラジルサンパウロの工場や事務所も含まれる。
SeaSpineとの合併は2023年1月5日に完了し,取引完了後,SeaSpineはOrthofixの完全子会社として継続した。SeaSpineとの合併に関するより多くの議論については、付記22を参照されたい。Orthofixは,統合後の会社構造における会社親実体として,ナスダック上で“OFIX”のコードで取引を継続する.合併後の会社は遅れて命名され、それまでOrthofix Medical Inc.の名称で命名され続ける。同社の2022年12月31日現在の財務諸表には、報告期間終了後に発生するため、SeaSpineの財務状況や業務は含まれていない。
陳述の基礎
連結財務諸表には、当社及びその完全子会社の財務諸表が含まれている。すべての会社間口座と取引は合併でキャンセルされた。我々が総合財務諸表を作成するために採用した会計政策と方法の資料については、適用される場合は、以下の各付記を参照されたい。
脚注 |
|
脚注参考 |
ビジネスとプレゼンテーションの基礎 |
|
1 |
重大会計政策 |
|
2 |
最近採用された会計基準、最近発表された会計公告、最近の法律変化 |
|
3 |
買収する |
|
4 |
棚卸しをする |
|
5 |
財産·工場·設備 |
|
6 |
無形資産 |
|
7 |
商誉 |
|
8 |
賃貸借証書 |
|
9 |
その他流動負債 |
|
10 |
長期債務 |
|
11 |
価値の計量と投資を公平にする |
|
12 |
引受金とその他の事項 |
|
13 |
株主権益 |
|
14 |
収入確認と売掛金 |
|
15 |
業務細分化情報 |
|
16 |
買収に関連した販売と再計量 |
|
17 |
株式ベースの報酬 |
|
18 |
固定払込計画と繰延補償 |
|
19 |
所得税 |
|
20 |
1株当たりの収益 |
|
21 |
後続事件 |
|
22 |
F-8
2.重大な会計政策
アメリカ公認会計原則(“アメリカ公認会計原則”)に基づいて財務諸表を作成する際、管理層は財務諸表日の資産及び負債額、或いは有資産及び負債の開示、及び報告期間内の収入及び支出の報告金額に影響するため、推定と仮定を行わなければならない。私たちは、契約手当、予想信用損失準備、在庫、無形資産推定値、営業権、公正価値計量、訴訟、または負債、所得税、および株式ベースの報酬に関する推定を含むこれらの推定値を継続的に評価する。我々は過去の経験,未来予想,その他当時の状況に属すると考えられる合理的な関連仮定に基づいて推定し,その結果は資産や負債の帳簿価値を判断する基礎を構成しているが,このような資産や負債の帳簿価値は他の出所から容易に見られるわけではない。実際の結果はこれらの推定とは異なる可能性がある。
以下は、他の脚注には記載されていない我々の連結財務諸表で使用される会計政策および方法の検討である。
市場リスク
正常な業務過程で、会社は金利変化や外貨変動の影響を受ける。同社の目標は、このような変動が収益やキャッシュフローに与える影響を制限することだ。この目標を達成するために、同社は非ドル建ての収入と支出のバランスを求めている。
米国以外の業務の財務諸表は通常現地通貨で保存されている。株主権益を除いて、すべての外貨建て貸借対照表口座は年末レートでドルに換算され、収入と支出項目は年内の平均為替レートに換算される。外貨換算による損益は株主権益の累計その他全面収益(損失)分に計上される。取引性外貨損益は、会社間業務による損益を含め、他の費用、純額、損失#ドルを計上する
金融商品と信用リスク集中
会社を集中的な信用リスクに直面させる可能性のある金融商品には、主に現金、現金等価物、売掛金が含まれる。一般に、現金は大型金融機関に保管されており、現金等価物は高流動性の通貨市場基金から構成されている。同社は顧客に対して継続的な信用評価を行い、一般に担保を必要とせず、予想される信用損失のために準備金を保留する。当社は,売掛金に関する信用リスク集中は限られており,顧客が地理的に分散しているため,エンドユーザが多様化していると考えている。
現金、現金等価物、制限された現金
当社はすべての原始期限が三ヶ月以下の高流動性投資を現金等価物と見なしています。
2019年9月、約1ドル
12月31日までの年間で現金収入や現金支払いが生じていない投資活動2022年、2021年、2020年には、企業総合キャッシュフロー表の投資活動現金には含まれていない項目が含まれています
(ドル、千単位) |
|
2022 |
|
|
2021 |
|
|
2020 |
|
|||
キャッシュフロー情報の追加開示: |
|
|
|
|
|
|
|
|
|
|||
非現金投資活動: |
|
|
|
|
|
|
|
|
|
|||
資産買収で得られた無形資産 |
|
$ |
|
|
$ |
— |
|
|
$ |
|
||
購入日に確認したものや掛け値がある |
|
|
— |
|
|
|
— |
|
|
|
|
|
F-9
広告費
広告費用は発生時に費用を計上する。広告費用は販売とマーケティング費用に含まれ、総額は#ドルです
研究と開発費用、協力手配を含む
研究と開発支出は発生時に計上される。当社とMTF Biologics(“MTF”)との連携手配に関する支出は,関連プロトコルの条項に基づいて計上される。同社は$を確認した
2020年10月、当社は新世代脊柱外科製品を開発したスイスのプライベートホールディングスNeo Medical SA(“Neo Medical”)と共同開発協定を締結し、双方が頚椎手術のための使い捨て器具を共同開発することを含む。本プロトコルについては、当社は特定の製品開発に関する可変コストの支払いを担当しています。この協力計画による研究と開発費用は合計#ドルである
3.最近採用された会計基準、最近発表された会計公告、および最近の法律の変化
最近採用された会計基準
会計基準更新(ASU)2021-10-政府援助(特別テーマ832):企業実体による政府援助状況の開示
2021年11月、財務会計基準委員会(FASB)は、取引の性質、取引に関連する条項および条件、および取引の影響を受ける財務諸表行プロジェクトに関する情報をエンティティに提供することを要求することにより、政府援助の透明性を向上させるためのASU 2021-10を発表した。当社は2021年12月31日までの年度にこの基準を早期に採用することを自発的に選択し、前向きである。この基準を採用することは,当社が2020年にコロナウイルス援助,救済および経済安全法案(“CARE法案”)に基づいて受け入れた政府援助による既存開示に大きな影響を与えることはない。
ASU 2019-12を採用し、所得税会計を簡略化
2019年12月、FASBはASC 740における一般原則のいくつかの例外を除去することにより、所得税会計の複雑さを低減するASU 2019−12を発表した所得税それは.また、ASUは米国公認会計原則を簡略化し、“混合”税制会計に関する要求を修正し、営業権計税基礎の増加がいつ業務合併の一部とみなされるべきか、いつ単独取引とみなされるべきかの要求を増加させた。会社はこのASUを有効に採用した
ASU 2016-13により、“金融商品·信用損失”(特別テーマ326):“金融商品信用損失の計量”及び後続修正案
2016年6月、FASBは、予想される信用損失および他の変化に基づいて、売掛金を含む特定のタイプの金融商品の信用損失を推定することが要求されるASU 2016-13(その後、ASUにおいてさらにこれを明らかにする)を発表した。会社は本ASUを採用しています
ASU 2017-04、無形資産-営業権およびその他(テーマ350)を採用:営業権減価テストの簡略化
FASBは2017年1月、仮想的な購入価格配分によって営業権減価を測定することを要求する以前の営業権減価テストの第2ステップを廃止したASU 2017-04を発表した。ASU 2017-04年度の規定によると、営業権減値損失は現在、報告単位の帳簿価値がその公正価値を超えているが、記録された営業権金額を超えないで計量されている。会社はこのASUを有効に採用した
F-10
ASU 2018-13を通じて、公正価値計量(テーマ820):開示枠組み-公正価値計量開示要求の変化
2018年8月、FASBは、公正価値階層構造の第1レベルと第2レベルとの間で転送される金額および理由のようないくつかの開示をキャンセルし、第3レベル計量に対する新たな開示要求を追加したASU 2018-13を発表した。会社はこのASUを有効に採用した
ASU 2018-15、無形資産-営業権とその他の内部使用ソフトウェア(サブテーマ350-40):サービス契約としてのクラウド手配で発生した実施コストの計算
2018年8月、FASBは、サービス契約であるホスト手配における実施コストを資本化する要求を、内部使用ソフトウェアの開発または取得による実施コスト資本化の要求と一致させたASU 2018−15を発表した。サービス契約のホスト手配であるサービス要素の計算は,今回の更新における改訂の影響を受けない.会社はこのASUを有効に採用した
ASU 2020-04を採用し、為替レート改革を参考に(テーマ848)
FASBは2020年3月、ロンドン銀行間の同業借り換え金利ではなく、予想される市場移行による潜在的な財務報告負担を軽減するための臨時オプション指導を提供するASU 2020-04を発表した。2022年12月31日までにいくつかの基準を満たす場合、新しい指導意見は、米国公認会計原則を契約修正、ヘッジ会計、および他の参照為替レート改革の影響を受ける取引に適用するために、オプションの便宜的かつ例外を提供する。会社はこのASUを有効に採用した
最近発表された会計公告
主題.主題 |
|
マニュアル説明 |
|
発効日 |
|
会社評価の現状 |
顧客との契約から契約資産と契約負債を計算する(ASU 2021-08) |
|
取得者は、顧客との収入契約の会計処理を管理する主題606に基づいて、企業合併で得られた契約資産及び負債を確認及び計量することを要求する。このガイドラインは、発効日または後に発生した買収に前向きに適用され、早期採用が許可される。 |
|
2023年1月1日 |
|
同社は現在、このASUがその連結財務諸表に及ぼす影響を評価している。 |
契約販売制限を受けた持分証券公正価値計測(ASU 2022-03) |
|
テーマ820“公正価値計量”における契約制限された持分証券の公正価値の計量に関する指導意見を明らかにし、この条項は持分証券の売却を禁止し、契約販売制限された持分証券に対して新たな開示要求を提出した。その中のいくつかの条項は遡及的に適用され、他の条項は未来に適用されるだろう。 |
|
2024年1月1日 |
|
同社は現在、このASUがその連結財務諸表に及ぼす影響を評価している。 |
最近の法律変化
新冠肺炎とコロナウイルス援助、救済と経済安全法(“CARE法案”)
2020年3月、CARE法案は、2019年のコロナウイルス病(“新冠肺炎”)の大流行の影響を受けた個人、家庭、企業に緊急援助と医療保健を提供し、米国経済に一般的な支援を提供することを目的とした連邦法に入った。 その他の事項に加えて,CARE法には,雇用者側の社会保障金の支払い延期に関する規定と,条件を満たす内装物件の税収減価償却方法の技術的修正に関する規定がある。“CARE法案”は,合併業務報告書ごとに当社が報告した所得税費用/福祉に影響を与えない
F-11
2021年12月31日と2020年12月31日までの年度。CARE法案はまた、他の様々な計画を通じて会社に財政救済を提供しており、各計画は以下でより詳細に説明されている。
2020年4月に同社はドルを受け取りました
2020年4月、当社はドルを自動的に受け取りました
また、“CARE法案”の一部として、当社は“CARE法案”が連邦法に署名された後、2020年の残り時間内にすべての雇用主の社会保障賃金税の支払いを延期することを許可しました
2021年総合支出法案(“総合支出法案”)
2020年12月27日、“総合支出法案”が正式に連邦法となった。総合支出法案は、会社の2021年12月31日までの年間所得税支給に実質的な影響を与えていない。
“2021年米国救援計画法案”(“米国救援計画”)
2021年3月11日、“米国救援計画”が連邦法に入った。米国の救援計画には2027年から役員報酬を差し引くことに関する条項が含まれている。米国の救援計画は、会社が2021年12月31日までの年度簡明総合財務諸表に影響を与えなかった。
4.買収
FITBONE資産購入契約
はい当社はドイツの個人持株会社ヴィテンスタインSE(“ヴィテンスタイン”)と資産購入協定(“購入協定”)を完了し,大腿骨と脛骨の肢体延長に使用するためにFITBONE髄内延長システムに関連する資産を$で買収した
総代理店買収
2020年7月には医療機器流通業者の資産を1ドルで買収しました
上記で議論した買収済み買収価格配分
(ドル、千単位) |
|
FITBONE |
|
|
割り当てをする |
|
総代理店買収 |
|
|
割り当てをする |
||
買収した資産 |
|
|
|
|
|
|
|
|
|
|
||
棚卸しをする |
|
$ |
|
|
|
|
$ |
— |
|
|
|
|
その他長期資産 |
|
|
— |
|
|
|
|
|
— |
|
|
|
無形資産 |
|
|
|
|
|
|
|
|
|
|
||
取引先関係 |
|
|
|
|
|
|
|
|
||||
発達した技術 |
|
|
|
|
|
|
— |
|
|
適用されない |
||
現在行われている研究と開発(“IPR&D”) |
|
|
|
|
|
|
— |
|
|
適用されない |
||
商号 |
|
|
|
|
|
|
— |
|
|
適用されない |
||
集結した労働力 |
|
|
— |
|
|
適用されない |
|
|
|
|
||
取得した確認可能資産総額 |
|
$ |
|
|
|
|
$ |
|
|
|
||
負担的負債 |
|
|
— |
|
|
|
|
|
— |
|
|
|
商誉 |
|
|
|
|
|
|
|
— |
|
|
|
|
譲渡対価の公正価値総額 |
|
$ |
|
|
|
|
$ |
|
|
|
||
F-12
5.在庫
在庫はコストまたは推定可変動純値の中で低い者の値で、超過、古い、または減価項目を提出した後、管理層が定期的に審査·更新する。イタリアにある会社の製造工場内部や契約製造により調達や生産を手配した在庫については,コストは加重平均ベースで決定されており,これは先進先出し(FIFO)手法とほぼ同じである。テキサス州とカリフォルニア州にある会社の製造工場で調達または生産された在庫については,内部でも契約製造手配でも標準コストが在庫を評価するために用いられており,標準コストは先進先出法の実際のコストに近い。状況がコストが変化したことを示す場合、経営陣は少なくとも毎年またはより頻繁に標準コストを検討する。
製品と完成品には材料、人工、生産管理費用が含まれている。現場在庫および委託在庫とは、製品に含まれる第三者顧客(例えば、流通業者および病院など)の即時販売可能な完成品在庫を、会社が独立して販売する代表によって所有または位置する完成品在庫を意味する。以前に実地/委託在庫と報告されていた在庫は完成品に再分類され,今期の新聞に適合するようになった。
|
|
十二月三十一日 |
|
|||||
(ドル、千単位) |
|
2022 |
|
|
2021 |
|
||
原料.原料 |
|
$ |
|
|
$ |
|
||
製品の中で |
|
|
|
|
|
|
||
完成品 |
|
|
|
|
|
|
||
棚卸しをする |
|
$ |
|
|
$ |
|
||
当社は経営陣が古いやその他の要因でコストを回収できないと考えている程度まで在庫価値を調整しています。これらの決定を下すために、管理層は、各製品の将来の需要の推定を使用して適切な在庫備蓄を決定し、これらの在庫の帳簿価値を対応して調整して、コストを反映するか、または換金可能な純価値の低い者を推定する。
6.財産、工場、および設備
財産、工場と設備が企業合併の一部として獲得された場合、コスト或いは見積もり公正価値から減価償却累計を減算する
これらの資産の耐用年数は一般的に以下のとおりである
|
|
年.年 |
建物.建物 |
|
|
工場と設備 |
|
|
計器計器 |
|
|
コンピュータソフト |
|
|
家具と固定装置 |
|
当社は毎年これらの資産の耐用年数を評価しています。減価償却は資産の耐用年数によって直線的に計算される。賃貸改善減価償却は、賃貸期間または資産使用年数のうち短いもので計算される。減価償却費用総額は$
保守·メンテナンスおよび小規模更新·改善の支出はそれぞれの資産の寿命を延長することなく、発生時に費用を計上する。更新と改善のためのすべての他の支出は資本化されている
F-13
|
|
十二月三十一日 |
|
|||||
(ドル、千単位) |
|
2022 |
|
|
2021 |
|
||
コスト |
|
|
|
|
|
|
||
建物.建物 |
|
$ |
|
|
$ |
|
||
工場と設備 |
|
|
|
|
|
|
||
計器計器 |
|
|
|
|
|
|
||
コンピュータソフト |
|
|
|
|
|
|
||
家具と固定装置 |
|
|
|
|
|
|
||
建設中の工事 |
|
|
|
|
|
|
||
融資リース資産 |
|
|
|
|
|
|
||
不動産·工場·設備,毛額 |
|
|
|
|
|
|
||
減価償却累計 |
|
|
( |
) |
|
|
( |
) |
財産·工場·設備·純価値 |
|
$ |
|
|
$ |
|
||
会社はアプリケーション開発段階で内部使用ソフトウェアに関するシステム開発コストを資本化している.予備プロジェクト活動と実施後活動に関する費用は発生時に費用を計上する。内部使用ソフトウェアはその推定耐用年数内に直線的に償却され、耐用年数は一般的に3%から3%の間であると推定される
長期資産は、毎年、または減少を示す可能性のあるイベントまたは状況の変化が発生するたびに減少値を評価する。評価については、当社は、その長期資産と他の資産および負債とを識別可能なキャッシュフローの最低レベルでグループ化し、その資産が他の資産および負債とは独立したキャッシュフローを生じないことを前提としている。当該資産又は資産グループ別の帳簿価値が当該資産グループ別の使用及び最終処分による未割引キャッシュフローを超える場合、当社は確定した期間に帳簿価値を公正価値に減記する。
当社は一般に長期資産の公正価値を将来のキャッシュフローを推定する現在値として決定しています。資産に関する将来のキャッシュフローの推定を決定する際には、当社は、資産グループの将来の収入貢献、コスト構造、および残存利用可能寿命の推定および仮定を使用する。代替仮説を用いることは,キャッシュフローの推定,割引率,代替推定残存可能寿命を含み,異なる減値計算を招く可能性がある。
7.無形資産
無形資産をコストまたは企業合併の一部として買収する場合は、見積もり公正価値から累積償却を差し引いて入金する。当該等資産は資産の使用年数に応じて直線的に償却されており、当社は当該等資産が提供する経済的利益モデルと実質的に一致していると信じている。
|
|
|
|
十二月三十一日 |
|
|||||
(ドル、千単位) |
|
加重平均販売期間 |
|
2022 |
|
|
2021 |
|
||
コスト |
|
|
|
|
|
|
|
|
||
特許 |
|
|
$ |
|
|
$ |
|
|||
発達した技術 |
|
|
|
|
|
|
|
|||
知的財産権研究開発 |
|
|
|
|
|
|
|
|||
取引先関係 |
|
|
|
|
|
|
|
|||
許可証とその他 |
|
|
|
|
|
|
|
|||
商標-限られて生きている |
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|||
累計償却する |
|
|
|
|
|
|
|
|
||
特許 |
|
|
|
$ |
( |
) |
|
$ |
( |
) |
発達した技術 |
|
|
|
|
( |
) |
|
|
( |
) |
取引先関係 |
|
|
|
|
( |
) |
|
|
( |
) |
許可証とその他 |
|
|
|
|
( |
) |
|
|
( |
) |
商標-限られて生きている |
|
|
|
|
( |
) |
|
|
( |
) |
|
|
|
|
|
( |
) |
|
|
( |
) |
無形資産、純額 |
|
|
|
$ |
|
|
$ |
|
||
F-14
買収した知的財産権の研究開発とは、まだ技術実行可能性に達していない買収研究開発資産に割り当てられた公正な価値である。企業合併において、買収に割り当てられた知的財産権研究開発の公正価値は、買収した技術を商業的に実行可能な製品に開発する余剰コストを推定し、プロジェクトによる収入を推定し、純現金流量を現在値に割引することによって決定される。買収を評価するための知的財産権研究開発の収入とコスト予測は、開発資産の成功確率に応じて適宜減少する。また、予想収入は関連する市場規模と成長要因、技術の予想傾向及び会社とその競争相手が新製品を発売する性質と予想時間を考慮した。純現金流量を現在値に換算するための比率は,プロジェクトの発展段階や予測に用いられる経済推定数における不確実性に見合っている。買収後に知的財産権の研究開発をさらに開発する任意の未来のコストはすでに発生した研究開発費用に計上されている。
関連する研究·開発事業を完了または放棄する前に、知的財産権研究開発資産は無期限資産とされている。資産が無期限存続とされている間は、償却しないが、減価テストを行う。欠陥テストは、少なくとも年に1回行われるか、または潜在的欠陥を示す可能性のあるトリガイベントが発生したときに行われる。開発が完了した場合(通常、販売製品の規制承認を得た場合に発生する)、関連資産は、開発された技術に再分類され、これらの資産が提供する経済的利益を最も反映する指定された耐用年数内に償却される。
無形資産の償却費用は#ドルです
(ドル、千単位) |
|
償却する |
|
|
2023 |
|
$ |
|
|
2024 |
|
|
|
|
2025 |
|
|
|
|
2026 |
|
|
|
|
2027 |
|
|
|
|
その後… |
|
|
|
|
有限寿命無形資産総額、純額 |
|
$ |
|
|
生きている無限無形資産、純額 |
|
|
|
|
無形資産、純額 |
|
$ |
|
|
8.営業権
同社は少なくとも年に1回営業権減価テストを行っている。指標や状況変化が存在すれば減値が存在する可能性があることを示しており,会社はより頻繁にテストを行う.これらの指標は、他にも、売上高、収益またはキャッシュフローの低下、またはビジネス環境の重大な不利な変化を含む。当社は報告単位レベルで営業権の減価を評価し、報告単位レベルは運営部門または運営部門の一レベル以下と定義されている。
次の表は現在までの営業権帳簿純価値を示しています2022年12月31日および2021年12月31日、これらの残高は、2021年12月31日から報告可能なセグメントで行われる前転:
(ドル、千単位) |
|
2021年12月31日 |
|
|
減損する |
|
|
貨幣換算調整 |
|
|
2022年12月31日 |
|
||||
全世界脊椎 |
|
$ |
|
|
$ |
— |
|
|
$ |
— |
|
|
$ |
|
||
世界整形外科 |
|
|
|
|
|
|
|
|
( |
) |
|
|
|
|||
商誉、毛利 |
|
$ |
|
|
$ |
— |
|
|
$ |
( |
) |
|
$ |
|
||
減価損失を累計する |
|
|
( |
) |
|
|
— |
|
|
|
|
|
|
( |
) |
|
営業権は,累積減価損失後の純額を差し引く |
|
$ |
|
|
$ |
— |
|
|
$ |
— |
|
|
$ |
|
||
2021年第4四半期、同社はその営業権を数量化評価した。当社では,収益法と市場法(すべての第3級公正価値計測)から得られた公正価値加重平均値を用いて報告単位ごとの公正価値を推定している。その各報告単位の公正価値を推定した後、当社はその全世界の整形外科報告単位の公正価値がその純資産の帳簿価値よりも低いことを確定した。これは全世界の整形外科の名誉を全額#ドル減少させた
F-15
再測定しますこの金額は、それぞれ、会社の2022年12月31日と2021年12月31日までの累計営業権減額損失総額を表している。評価で得られた結論は
2022年第4四半期に、当社はその年度の営業権減値分析に対して定性評価を行い、減値に至っていない。この定性分析は報告部門特有のすべての関連要素を考慮し、マクロ経済条件、業界と市場考慮要素、全体財務業績及び関連実体の具体的な事件を含む。
9.賃貸証書
会社は契約を開始時にレンタルになる資格があるかどうかを決定します。同社のレンタルは主に施設、車両、設備、およびいくつかの契約製造協定に関連している。リース資産は当社がリース期間内に対象資産を使用する権利を表し、リース負債はリースによるリース金の支払い義務を表す。リース資産および負債は、開始日にレンタル期間内にレンタル支払いの現在値を確認します。当社の借款は暗黙的な金利を提供していないため、当社の逓増借款金利は、開始日に得られる情報に基づく割引率として使用され、賃貸支払いの現在値を決定する。リース資産はまた、支払い済みのプリペイドの影響を含み、任意のレンタルインセンティブの影響によって減少する。
当社は貸借対照表上で短期賃貸(リース期間が12ヶ月以下の賃貸)の貸借対照または賃貸資産を確認しない。逆に、どの短期レンタル支払いもレンタル期間内に直線的に確認された料金です。今期の短期賃貸費用は私たちの短期賃貸の約束を合理的に反映しています。
すべての種類のレンタルについて、当社はレンタルと非レンタルコンポーネントを単一レンタルコンポーネントに統合します。可変リース支払いはリース負債から除外され、債務が発生している間に確認される。また、レンタル条項には、会社が選択権を行使することを合理的に決定した場合に、リース契約を延長または終了する選択権が含まれている場合があります。
以下の日までの会社のレンタル組合の概要2022年12月31日と2021年12月31日は、次の表のようになります
(ドル、千単位、レンタル期間と割引率を除く) |
|
分類する |
|
2022年12月31日 |
|
|
2021年12月31日 |
|
||
資産 |
|
|
|
|
|
|
|
|
||
賃貸借契約を経営する |
|
|
$ |
|
|
$ |
|
|||
融資リース |
|
|
|
|
|
|
|
|||
リース資産総額 |
|
|
|
$ |
|
|
$ |
|
||
負債.負債 |
|
|
|
|
|
|
|
|
||
現在のところ |
|
|
|
|
|
|
|
|
||
賃貸借契約を経営する |
|
|
$ |
|
|
$ |
|
|||
融資リース |
|
融資リース負債の当期分 |
|
|
|
|
|
|
||
長期の |
|
|
|
|
|
|
|
|
||
賃貸借契約を経営する |
|
|
|
|
|
|
|
|||
融資リース |
|
融資リース負債の長期部分 |
|
|
|
|
|
|
||
リース総負債 |
|
|
|
$ |
|
|
$ |
|
||
|
|
|
|
|
|
|
|
|
||
加重平均残余レンタル期間 |
|
|
|
|
|
|
|
|
||
賃貸借契約を経営する |
|
|
|
|
|
|
||||
融資リース |
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
||
加重平均割引率 |
|
|
|
|
|
|
|
|
||
賃貸借契約を経営する |
|
|
|
|
% |
|
|
% |
||
融資リース |
|
|
|
|
% |
|
|
% |
||
F-16
レンタル料金の構成は以下のとおりである
(ドル、千単位) |
|
2022年12月31日までの年度 |
|
|
2021年12月31日までの年度 |
|
|
2020年12月31日まで年度 |
|
|||
融資リースコスト: |
|
|
|
|
|
|
|
|
|
|||
使用権資産の償却 |
|
$ |
|
|
$ |
|
|
$ |
|
|||
融資リース負債利息 |
|
|
|
|
|
|
|
|
|
|||
リースコストを経営する |
|
|
|
|
|
|
|
|
|
|||
短期賃貸コスト |
|
|
|
|
|
|
|
|
|
|||
可変リースコスト |
|
|
|
|
|
|
|
|
|
|||
総賃貸コスト |
|
$ |
|
|
$ |
|
|
$ |
|
|||
レンタルに関する補足キャッシュフロー情報は以下のとおりである
(ドル、千単位) |
|
2022年12月31日までの年度 |
|
|
2021年12月31日までの年度 |
|
|
2020年12月31日まで年度 |
|
|||
賃貸負債の金額を計上するための現金 |
|
|
|
|
|
|
|
|
|
|||
レンタル経営からの経営キャッシュフロー |
|
$ |
|
|
$ |
|
|
$ |
|
|||
融資リースの運営キャッシュフロー |
|
|
|
|
|
|
|
|
|
|||
融資リースによるキャッシュフロー |
|
|
|
|
|
|
|
|
|
|||
賃貸義務と引き換えに使用権資産 |
|
|
|
|
|
|
|
|
|
|||
賃貸借契約を経営する |
|
|
|
|
|
|
|
|
|
|||
融資リース |
|
|
— |
|
|
|
|
|
|
|
||
以下の日までの会社の残り賃貸負債の概要2022年12月31日、詳細は以下の通り
(ドル、千単位) |
|
運営中です |
|
|
金融 |
|
||
2023 |
|
$ |
|
|
$ |
|
||
2024 |
|
|
|
|
|
|
||
2025 |
|
|
|
|
|
|
||
2026 |
|
|
|
|
|
|
||
2027 |
|
|
|
|
|
|
||
その後… |
|
|
|
|
|
|
||
賃貸負債未割引価値合計 |
|
|
|
|
|
|
||
差し引く:利息 |
|
|
( |
) |
|
|
( |
) |
賃貸負債現在価値 |
|
$ |
|
|
$ |
|
||
|
|
|
|
|
|
|
||
賃貸負債の流動部分 |
|
$ |
|
|
$ |
|
||
賃貸負債の長期部分 |
|
|
|
|
|
|
||
リース総負債 |
|
$ |
|
|
$ |
|
||
F-17
10.その他流動負債
|
|
十二月三十一日 |
|
|||||
(ドル、千単位) |
|
2022 |
|
|
2021 |
|
||
費用を計算する |
|
$ |
|
|
$ |
|
||
給料、ボーナス、手数料及び関連する税金を支払うべきです |
|
|
|
|
|
|
||
採点者手数料を払わなければならない |
|
|
|
|
|
|
||
法律費用と和解費用を計算する |
|
|
|
|
|
|
||
対価格負債があります |
|
|
|
|
|
|
||
短期経営賃貸負債 |
|
|
|
|
|
|
||
非所得税に対処する |
|
|
|
|
|
|
||
事前支払い計画を加速します |
|
|
— |
|
|
|
|
|
その他の支払い |
|
|
|
|
|
|
||
その他流動負債 |
|
$ |
|
|
$ |
|
||
11.長期債務
2019年10月25日、当社とそのいくつかの全額付属会社(総称して当社、“借り手”と呼ぶ)を借り手とし、当社のいくつかの主要な付属会社を保証人とし、行政代理であるモルガン大通銀行(“JPMorgan”)及びいくつかの貸手側と2つ目の改訂された信用契約(“改正信用協定”)を締結した。 改正された信用協定は$を規定している
2020年4月、会社の現金状況と新冠肺炎の発生による最初の不確実性の期間中に財務柔軟性を維持する予防策として、会社は#ドルの借金を完了した
改訂された信用協定の下の借金は、運営資金および当社およびその付属会社の他の一般的な会社用途(配当金およびその他の割り当ての買収および許可の支払いを含む)として使用することができる。この施設はドルで提供され、最高で$に達する
この融資メカニズムでの借入金は変動金利で利下げされ、借り手の選択に応じて、変動金利はSOFRに適用される保証金を加えた範囲となる
当社のいくつかの既存及び未来の主要付属会社(総称して“保証人”)は、改訂された信用協定項下の借り手の債務の償還を保証しなければならない。借款人及び各保証人は改訂された信用協定に対する責任を、実質的にすべての動産の質抵当で保証する
F-18
借入者及び各保証人の資産は、売掛金、預金口座、知的財産権、投資財産、在庫、設備及びそれぞれの子会社の株式を含む。
改訂された信用協定は、当社に対する追加債務の発生、追加留置権の付与または許可、投資および買収、他の会社との合併または合併、資産の処分、配当金および割り当て、二次債務の支払い、および関連取引を行う能力の制限を含む慣用的なプラスおよび負の契約を含む。また、改訂された信用協定には財務契約が記載されており、当社は任意の財政四半期の最終日に、総合的な基礎の上で総純資産率を超えないように維持することを要求している
融資を受けながら、会社は#ドルを支払った
同社は未使用のイタリアの信用限度額ユーロを持っている
会社は利息に関する現金#ドルを支払った
12.価値計測と投資を公平にする
公正価値は、計量日市場参加者間の秩序ある取引において、資産または負債が元金または最も有利な市場で負債を譲渡するために課金または支払いされる価格(脱退価格)として定義される。公正な価値で計量された当社の非金融資産と負債は、現在の報告期間内に減値された任意の長期資産または秩序取引において可視価格で計量された権益証券を含む。この権威ガイドはまた、公正な価値を測定するために使用されることができる3つのレベルの投入を説明する
レベル1: |
活発な市場における同じ資産と負債の見積もり |
|
|
第2レベル: |
同資産と負債の活発な市場見積もり以外の観察可能な投入 |
|
|
第3レベル: |
観察できない投入は、その中で市場データが少ないか、全くないか、これは報告実体に自分の仮説を立てることを要求します |
同社の金融商品には、現金等価物、売掛金、売掛金、長期保証債務、販売可能な債務証券、株式証券、または対価格および繰延補償計画債務が含まれる。これらのツールの短期満期日により,現金等価物,売掛金,売掛金の帳簿価値は公正価値に近い。当社の担保付き循環信用手配は変動金利を採用しているため、長期債務の帳簿価値は公正価値に近いとされている。
F-19
会社が販売可能な債務証券、株式証券、または対価格および繰延補償計画負債は、公正な価値に応じて恒常的に記録された唯一の金融商品であり、具体的には以下の通りである
(ドル、千単位) |
|
てんびん |
|
|
レベル1 |
|
|
レベル2 |
|
|
レベル3 |
|
||||
資産 |
|
|
|
|
|
|
|
|
|
|
|
|
||||
Neo医療転換ローン協定 |
|
$ |
|
|
$ |
— |
|
|
$ |
— |
|
|
$ |
|
||
ネオ医療優先株証券 |
|
|
|
|
|
— |
|
|
|
|
|
|
— |
|
||
骨生物株証券 |
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
— |
|
その他の投資 |
|
|
|
|
|
— |
|
|
|
— |
|
|
|
|
||
合計する |
|
$ |
|
|
$ |
— |
|
|
$ |
|
|
$ |
|
|||
負債.負債 |
|
|
|
|
|
|
|
|
|
|
|
|
||||
脊柱運動学や考えがあります |
|
|
— |
|
|
$ |
— |
|
|
$ |
— |
|
|
$ |
— |
|
繰延補償計画 |
|
|
( |
) |
|
|
— |
|
|
|
( |
) |
|
|
— |
|
合計する |
|
$ |
( |
) |
|
$ |
— |
|
|
$ |
( |
) |
|
$ |
— |
|
(ドル、千単位) |
|
てんびん |
|
|
レベル1 |
|
|
レベル2 |
|
|
レベル3 |
|
||||
資産 |
|
|
|
|
|
|
|
|
|
|
|
|
||||
Neo医療転換ローン協定 |
|
$ |
|
|
$ |
— |
|
|
$ |
— |
|
|
$ |
|
||
ネオ医療優先株証券 |
|
|
|
|
|
— |
|
|
|
|
|
|
— |
|
||
骨生物株証券 |
|
|
|
|
|
|
|
|
— |
|
|
|
— |
|
||
その他の投資 |
|
|
|
|
|
— |
|
|
|
— |
|
|
|
|
||
合計する |
|
$ |
|
|
$ |
|
|
$ |
|
|
$ |
|
||||
負債.負債 |
|
|
|
|
|
|
|
|
|
|
|
|
||||
脊柱運動学や考えがあります |
|
$ |
( |
) |
|
$ |
— |
|
|
$ |
— |
|
|
$ |
( |
) |
繰延補償計画 |
|
|
( |
) |
|
|
— |
|
|
|
( |
) |
|
|
— |
|
合計する |
|
$ |
( |
) |
|
$ |
— |
|
|
$ |
( |
) |
|
$ |
( |
) |
会社繰延補償計画負債の公正価値は、公開市場でいつでも入手可能な投入または公開上場市場から入手可能な情報に基づいて決定され、そのため、会社はこの負債を二次金融商品に分類した。
Neo医療転換ローン契約と株式投資
2020年10月1日,会社はNeo Medicalの優先株を1ドルで購入した
2021年10月に、当社は追加の交換可能株ローン協定(“追加交換可能株ローン”)を締結し、これにより、当社はNeo Medicalに追加のスイスフランローンを提供した
株式証券は他の長期資産に計上され、投資とみなされ、その公正価値は簡単に確定できない。そこで,当社はコストから任意の減値を減算し,同一発行者の同じまたは類似した投資の秩序取引に見られる価格変化による変化を加えたり減算したりしてこの投資を計測する。
次の表にNeo Medical優先株証券投資に対する当社の帳簿価値を示すDecember 31, 2022, and 2021:
F-20
(ドル、千単位) |
|
2022 |
|
|
2021 |
|
||
Neo Medical優先株証券の1月1日の公正価値 |
|
$ |
|
|
$ |
|
||
融資を優先株証券に転換する |
|
|
|
|
|
— |
|
|
他の収入で確認された外貨再計量、純額 |
|
|
— |
|
|
|
|
|
他の収入(費用)で確認された未実現収益,純額 |
|
|
— |
|
|
|
|
|
Neo Medical優先株証券の12月31日の公正価値 |
|
|
|
|
|
|
||
Neo Medical優先株証券の累計収益は実現していない |
|
|
|
|
|
|
||
転換可能な融資の公正価値計量に使用されるいくつかのより重要な観察不可能な入力は、適用可能な割引率、隠れ変動率、償還或いは転換の可能性と予想時間、及びNeo Medicalによる企業価値の推定を支持する予測キャッシュフローを含む。他の投入が一定のままである場合、これらの仮定の変化は、変換可能融資の公正価値に大きな変化をもたらす可能性がある。もし転換可能なローンの余剰コストがその推定公正価値を超えた場合、この証券は減価とみなされ、信用損失を確認するために評価を行わなければならない。信用損失による減値は損益表で確認したが,他の要因による減値は他の全面収益(損失)で確認した。2022年12月31日まで会社が所有しています
下表は転換可能なローンの期初と期末残高の入金を提供し、公正価値に応じて重大な観察不可能な投入(第3級)計量を使用する
(ドル、千単位) |
|
2022 |
|
|
2021 |
|
||
1月1日Neo医療転換可能ローンの公正価値 |
|
$ |
|
|
$ |
|
||
足し算 |
|
|
— |
|
|
|
|
|
利子純額で確認した利息 |
|
|
|
|
|
|
||
他の収入(費用)で確認された外貨再計量、純額 |
|
|
( |
) |
|
|
( |
) |
他の全面収益(赤字)で確認された未実現収益(赤字) |
|
|
|
|
|
( |
) |
|
追加の転換可能な融資を優先株証券に転換する |
|
|
( |
) |
|
|
— |
|
Neo医療転換可能ローンの12月31日の公正価値 |
|
|
|
|
|
|
||
Neo医療転換ローン12月31日の償却コストベース |
|
|
|
|
|
|
||
次の表は、変換可能なローンの推定値で使用されるいくつかの重要な仮定に関する定量化情報を提供しています2022年12月31日:
(ドル、千単位) |
|
2022年12月31日までの公正価値 |
|
|
観測不可能な入力 |
|
見積もりをする |
|
||
Neo医療転換ローン |
|
$ |
|
|
株式原価割引率 |
|
|
% |
||
|
|
|
|
|
隠れ波動率 |
|
|
% |
||
F-21
骨生物株証券
2022年8月までに、同社は骨生物会社(“骨生物”)の普通株の投資を持っており、同社は骨生物学製品の開発業者である。2021年までに、株式証券は骨生物の取引量が非常に限られているため、公正な価値を決定しにくい投資とされている。そこで,当社はコストから任意の減値を減算し,同一発行者の同じまたは類似した投資の順序取引に見られる価格変化による変化を加えたり減算したりして投資を計測する。
2021年、骨生物は単位の公開発行を完了し、各単位は1株の普通株と1部の普通株購入権証からなる。そのため,骨生物の普通株はナスダック(株式コード:BBLG)で取引が活発である。普通株はその後、活発な市場で同じ資産オファーであるため、同社はこの投資が公開発行後の第1級公正価値計量を代表すると結論した。そのため、会社は公正価値記録によってこの投資を記録し、公正価値変動記録は上場後の他の収入(費用)純額内に記録されている。
以下の表に12月31日までの各年度に確認された公正価値変動を示す2022, 2021, and 2020:
(ドル、千単位) |
|
2022 |
|
|
2021 |
|
|
2020 |
|
|||
骨生物株1月1日の持分証券 |
|
$ |
|
|
$ |
— |
|
|
$ |
|
||
公正価値調整とその他の収入(費用)で確認された減価,純額 |
|
|
( |
) |
|
|
|
|
|
( |
) |
|
株式証券を売却して得た収益 |
|
|
( |
) |
|
|
— |
|
|
|
— |
|
12月31日の骨生体株式証券 |
|
$ |
— |
|
|
$ |
|
|
|
— |
|
|
その他の投資
その他の投資とは、公正な価値によって記録された他の資産及び投資であり、当該等の資産及び投資は個別の基礎の上で重大な開示とはみなされない。これらの資産の公正価値は,確率重み付き現金フローモデルのような重大な観察不可能な投入に基づいており,会社に自分の仮説を立てることが求められる.そこで、当社はこれらの資産を三級金融資産に分類します。この残高は2022年12月31日現在、他の流動資産に帰属しているが、2021年12月31日現在、この残高は他の長期資産に分類されている。
値段が合うかもしれない
同社は2018年にSpina Kineticsの買収に関連するまたは対価格義務があることを確認した。Spina Kineticsまたは将来達成可能なマイルストーン支払いを含む価格があります。最高で$までです
会社は2023年4月30日にこのマイルストーンに到達しないと予想されているため、2022年12月31日まで、収入に基づくマイルストーンの残りSpine Kineticsや価格の推定公正価値がゼロになることに起因する。推定された公正価値は、選任プロセスの予想時間および数、およびこれらのプロセスが将来の収入に及ぼす影響など、2022年12月31日までに管理職が行った仮定を反映している。公正価値のいかなる変動も買収に関連する償却と再計量に営業費用を計上する。
(ドル、千単位) |
|
2022 |
|
|
2021 |
|
||
1月1日の脊髄運動学あるいは考慮 |
|
$ |
|
|
$ |
|
||
買収に関する償却と再計量で確認された公正価値の減少 |
|
|
( |
) |
|
|
( |
) |
支払い済み |
|
|
— |
|
|
|
( |
) |
12月31日の脊柱動力学あるいは考慮事項 |
|
|
— |
|
|
$ |
|
|
F-22
13.支払いの引受およびまたは事項
あるいは事項保険証書があります
当社はいくつかの未解決の法律訴訟、調査またはクレームの計上費用を記録しており、これらの訴訟、調査またはクレームは債務が発生している可能性が高く、損失金額は合理的に見積もることができる。当社は、計上すべき金額の法的訴訟、調査、クレームに関する事態の発展、および損失を可能にしたり、合理的に四半期ごとに推定したりするいかなる事態にも影響を及ぼす可能性があると評価しています。損失があったり、不可能であったり、合理的に見積もることができない場合、当社は損失を計上すべきではない。しかしながら、損失(または計算すべき項目を超える追加損失)が少なくとも合理的な可能性および実質的である場合、このような合理的な推定が可能であれば、当社は、可能な損失または損失範囲の合理的な推定を開示する。もし会社が可能な損失や損失範囲を合理的に推定できない場合は、開示する。また、法的費用が他に直接関連するコストは発生時に費用を計上する。
以下の各段落で述べた事項を除いて、正常な業務過程において、当社は時々様々な訴訟に触れ、いくつかの他のまたはある事項の影響を受ける可能性がある。当社は,このような事項に関するいかなる損失も,起こりうる損失や損失範囲については,個別や全体にかかわらず無関係であると信じている。
イタリアの医療機器返済(“IMDP”)
2015年、イタリア議会はイタリア国家ヘルスケアシステムに商品やサービスを提供する実体の規則を発表した。この法律の重要な条項は、イタリアの医療機器会社に、医療機器支出が地域の最高上限を超えた場合にイタリア政府に支払うことを要求する補償措置である。会社が支払いを要求された金額は支出の割合に相当し、地域最高上限を超えている。
イタリア保健省は2022年第3四半期、イタリアの各地域·省に2015年12月31日から2018年12月31日までの年間支出超過の返済を求めるガイドラインを提供した。指導意見を受けて以来,複数の地域や省が同社を含む影響を受けた医療機器会社に支払いを要求している。同社は法的行動をとっており、このような措置の合法性に異議を唱えている。
当社はIMDPの見積もりコストを販売·マーケティング費用として会計処理し、現在の事実と状況に応じて負債を定期的に再評価している。したがって、同社が記録した費用は#ドルとなる
14.株主権益
配当をする
同社は従来、その普通株保有者に配当を支払ったことがない。改訂された信用協定によると、当社のいくつかの付属会社はいくつかの場合に配当金を派遣する能力が制限されている。会社が将来的に子会社から受け取った配当金で普通株式保有者に配当金を支払うことを決定した場合、現行税率によると、会社は子会社から受け取ったこのような金額に追加の源泉徴収税と所得税を支払う必要があるかもしれない。
F-23
その他の総合収益を累計する
その他の総合収益(赤字)の累積には、外貨換算調整と債務証券の売却可能な未実現収益(赤字)が含まれる。同社の政策は、他の総合収益(赤字)の累計で確認された項目に関する所得税の影響をポートフォリオ方式で公表することだ
(ドル、千単位) |
|
貨幣 |
|
|
Neo医療転換ローン |
|
|
その他の投資 |
|
|
その他を累計する |
|
||||
2019年12月31日の残高 |
|
$ |
( |
) |
|
$ |
— |
|
|
$ |
— |
|
|
$ |
( |
) |
その他総合収益 |
|
|
|
|
|
|
|
|
— |
|
|
|
|
|||
所得税 |
|
|
— |
|
|
|
( |
) |
|
|
— |
|
|
|
( |
) |
2020年12月31日残高 |
|
$ |
|
|
$ |
|
|
$ |
— |
|
|
$ |
|
|||
その他総合損失 |
|
|
( |
) |
|
|
( |
) |
|
|
— |
|
|
|
( |
) |
所得税 |
|
|
— |
|
|
|
|
|
|
— |
|
|
|
|
||
2021年12月31日の残高 |
|
$ |
( |
) |
|
$ |
|
|
$ |
— |
|
|
$ |
— |
|
|
その他全面収益(赤字) |
|
|
( |
) |
|
|
|
|
|
|
|
|
( |
) |
||
所得税 |
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
— |
|
2022年12月31日の残高 |
|
$ |
( |
) |
|
$ |
|
|
$ |
|
|
$ |
( |
) |
||
15.収入確認と売掛金
収入確認
当社は、(1)双方の承認と承諾、(2)双方の権利の決定、(3)支払条項の決定、(4)契約が商業的実質を有する、(5)と可能な対価格収集可能性、の場合に契約を会計処理する。会社の契約には1つ以上の履行義務が含まれているかもしれない。1つの契約に1つ以上の履行義務が含まれている場合、当社は、各履行義務の背後で約束された貨物またはサービスの観察可能な独立販売価格に基づいて、総取引価格を各履行義務に割り当てる。約束された商品またはサービスの制御権が顧客に転送されると、会社は収入を確認し、これは、通常、積み込み、交付、または使用後のある時点で発生し、その金額は、約束された商品またはサービスと交換するために、会社が獲得する権利が期待される対価格を反映する。貨物やサービスの対価格反映契約で規定されている任意の固定額,割引などの任意の可変対価格の推定数は,可変対価格に関する不確実性が解決された後,確認された累積収入が大きく逆転しない可能性が高いことが条件である.
以下の各節で重要製品別に会社の収入確認政策を検討する:
骨成長療法
骨成長療法の収入は主にアメリカから来ており、第三者支払人取引と卸売収入を含む。
骨成長療法収入の最大部分は第三者支払者によるものである。これには商業保険会社、健康維持組織、第一選択提供者組織と政府支払人、例えば連邦医療保険が含まれる。製品が患者に装着され患者に受け入れられ,第三者支払者が要求したすべての適用文書が取得された場合には,収入が確認される。第三者支払者が支払う金額は、通常、固定または許可された支払率に基づく。これらの収入は予想または事前に承認された返済率で入金され、任意の契約手当を差し引いたり調整したりする。一部の請求書は第三者支払者によって審査され、調整される可能性がある。
卸売収入は同社の骨成長刺激器を耐久医療設備サプライヤーに直接販売することと関係がある。卸収入は通常、出荷と購入注文の確認を受けたときに確認され、これは顧客が約束した貨物統制権を獲得したときである。
F-24
生物製品
生物製品の収入は主にアメリカから来ており、主にMTFの協力手配と関係があり、この計画は2032年12月31日まで続く。この手配によると、同社は骨修復と再建のための組織を、利他的進化と利他的エリートのブランドで販売している。プロトコル条項によれば、MTFは組織源を探し、同種移植を作成し、パッケージを作成し、組織を顧客に渡すために加工される。同社はViguos Lyograftとリバースエリートティッシュの独占グローバル販売権を持ち、米国でFiberFuse Advanced、FiberFuseストリップ、およびある他のティッシュを独占的にマーケティングする権利を持ち、ある他の製品に対して非独占営業権を持ち、総売上高に応じてMTFから営業費を徴収する。MTFはこれらの手配中の主要債務者とされているため,当社は製品を顧客に出荷して購入確認注文を受けた後,純売上高でマーケティングサービス料を確認している。
脊柱インプラントと全世界整形外科
脊柱インプラントおよび全世界整形外科会社の製品は世界各地に分布しており、アメリカでの販売は主に商業販売と商業販売と在庫流通業者から手配された国際販売を含む。
商業収入は主に病院の顧客に同社の脊柱インプラントと全世界の整形外科製品を販売することから来ている。これらの製品が使用され、病院から購入確認注文を受けた場合、顧客は制御権を取得し、収入を確認する。
脊柱インプラントと全世界整形外科製品カテゴリの他の収入は在庫流通業者からであり、これらの流通業者は同社の製品を購入し、それを直接病院などの顧客に転売する。在庫流通業者の手配については、会社の方針は、出荷確認と調達注文を受けたときに収入を確認し、流通業者が約束した貨物統制権を獲得したときである。収入確認の取引価格は、会社と在庫流通業者の履歴収集経験から推定されています。
製品販売とサービス料の市場普及
次の表は、製品販売とマーケティングサービス料を含む今年度までの各年度の純売上高を示しているDecember 31, 2022, 2021, and 2020.
|
|
12月31日までの年度 |
|
|||||||||
(ドル、千単位) |
|
2022 |
|
|
2021 |
|
|
2020 |
|
|||
製品販売 |
|
$ |
|
|
$ |
|
|
$ |
|
|||
マーケティングサービス料 |
|
|
|
|
|
|
|
|
|
|||
純売上高 |
|
$ |
|
|
$ |
|
|
$ |
|
|||
製品販売は主に骨成長療法、脊柱インプラントと全世界整形外科製品の販売を含む。マーケティングサービス料は生物製品組織の総売上高によってMTFから徴収され、全世界の脊柱報告部門における生物製品の種類のみと関係がある。MTFから受け取ったマーケティングサービス料は$です
収入には付加価値税や他の地方税、会社間販売、貿易割引は含まれていません。顧客に発送された製品の輸送や運搬コストは販売コストに含まれている
売掛金及び関連引当金
支払い条件は、会社のお客様のタイプや場所、提供される製品やサービスによって異なります。領収書発行と満期支払いの間の期限は重要ではありません。
T会社の予想信用損失準備とは、過去の事件、現在の状況及び将来の経済状況の合理的かつ支援可能な予測を考慮した後、実体が売掛金の契約期間内に徴収されないと予想される売掛金償却コスト基礎部分である。
F-25
売掛金の最終入金を推定する過程は、いくつかの仮定と判断に関連する。売掛金の契約年限、未払い売掛金の帳簿齢及びこれらの売掛金推定契約年限の歴史入金、核販売と支払人返済経験を確定することは、期待信用損失準備金と契約手当の確定に関する推定過程の構成部分である。売掛金は四半期ごとに分析を行い、期待信用損失準備金と契約手当の十分性を評価する。期待信用損失推定準備の改訂は販売とマーケティング費用内の不良債権支出の調整に計上される。契約手当の改定は純売上高の調整に計上されている。これらは定期的に実際の収集経験に基づいてテストを行うと予想される.また、予想信用損失推定を作成する際に、同社は地理的位置と顧客タイプによってその売掛金を分析した。
以下の表は,当社の年度までの予想信用損失準備変化の詳細を提供しているDecember 31, 2022, and 2021:
|
|
12月31日までの年度 |
|
|||||
(ドル、千単位) |
|
2022 |
|
|
2021 |
|
||
信用損失準備期初め残高を予想する |
|
$ |
|
|
$ |
|
||
当期予想信用損失準備金 |
|
|
|
|
|
|
||
手当やその他の費用から差し引かれた押し売り |
|
|
( |
) |
|
|
( |
) |
為替レート変動の影響 |
|
|
( |
) |
|
|
( |
) |
信用損失準備期末残高 |
|
$ |
|
|
$ |
|
||
同社は毎年、あるイタリアの公立病院の売掛金を販売し、現金調達速度を加速させている。2022、2021、2020年にはその会社はユーロを売っています
契約責任
その会社の契約債務は主に前金#ドルと関連がある
2020年10月1日、米国の総裁は“2021年継続支出法案及びその他の延期法案”に署名し、この計画から資金を獲得した提供者やサプライヤーに対する医療保険加速·前払い計画のいくつかの補償条項を緩和した。2021年4月医療保険回収開始
次の表は、2022年12月31日および2021年12月31日までの年間における加速および前払い計画に関する会社契約負債の変化の詳細を提供します
|
|
12月31日までの年度 |
|
|||||
(ドル、千単位) |
|
2022 |
|
|
2021 |
|
||
契約負債期間の初め残高 |
|
$ |
|
|
$ |
|
||
純売上高で確認した補償 |
|
|
( |
) |
|
|
( |
) |
契約負債期末残高 |
|
$ |
— |
|
|
$ |
|
|
その他契約資産
会社の契約資産は、売掛金(“その他の契約資産”)を含まず、主に特定の流通業者に支払い、契約を取得し、特定の地域の顧客に接触し、会社の製品を独占的に販売する利益を提供することを含む。他の契約資産は他の長期資産に含まれ、総額は#ドルである
F-26
その他の契約資産は関連契約期間内に直線的に償却します
16.ビジネス細分化情報
2022年12月31日まで会社の運営は以下のように管理されている
SeaSpineとの合併が2023年1月5日に完了した後、同社は2023年第1四半期に新合併会社の運営管理方式に基づいて報告部門を再評価する予定だ。その際、会社は決定した部門の利益指標も再評価する。したがって,次の報告分部情報は,2022年12月31日までの年度の運営を管理するための会社の2つの履歴報告分部に基づいて作成される。
全世界脊椎
全世界の脊柱報告部分は3つの主要な製品種別を提供する:骨成長療法、脊柱インプラントと生物製品。
骨成長療法製品の種類の製造、流通と市場をリードする骨成長刺激設備の支持サービスを提供し、骨融合を増強する。これらIII系医療機器は補助的な非侵襲的治療と考えられ,頚椎と腰椎の融合成功率を向上させることができ,癒合していない非脊柱骨折(骨不連)に対する治療でもある。この製品種別は,流通業者と販売代表を用いて病院,医療提供者,患者にその機器を販売しており,主に米国である。
脊柱インプラント製品の種類は広範な脊柱外科手術に使用される運動保護と固定インプラント製品の組み合わせを設計、開発とマーケティングする。脊柱インプラント会社は、流通業者と販売代表からなるグローバルネットワークを通じてその製品を流通し、病院と医療保健提供者に脊柱製品を販売する。
Biologics製品分類は一連の再生製品と組織形式を提供し、医者が各種の脊柱と整形疾患の治療に成功できるようにした。この製品種別は,会社再生組織のマーケティングに特化し,独立流通業者や販売代表のネットワークを介して病院やヘルスケア提供者に組織を配布し,主に米国である。MTFとの協力関係により、同社はViguos Lyoggraph、三位一体進化会社、FiberFuse Advanced社、FiberFuseストリップ会社とある他の筋肉骨格欠陥組織形式を独占的に販売し、骨融合を強化することができる。
世界整形外科
全世界の整形外科報告部門が提供した製品と解決策は医師が脊柱とは関係のない各種の整形外科疾患の治療に成功できるようにした。この報告部門は骨折修復、奇形矯正と骨再建プログラムのための整形外科製品の設計、開発とマーケティングに専門的に従事している。Global Orthopedicsはグローバル流通業者と販売代表ネットワークを介してその製品を流通し,病院や保健提供者に整形外科製品を販売する。
会社
会社活動は会社の運営費用と活動からなり,これらの費用や活動は必ずしも両報告部門で確認できるとは限らない。
次の表に主要製品種別と報告細分化市場別の純売上高を示す
F-27
|
|
十二月三十一日までの年度 |
|
|||||||||||||||||||||
|
|
2022 |
|
|
2021 |
|
|
2020 |
|
|||||||||||||||
(ドル、千単位) |
|
純売上高 |
|
|
パーセント |
|
|
純売上高 |
|
|
パーセント |
|
|
純売上高 |
|
|
パーセント |
|
||||||
骨成長療法 |
|
$ |
|
|
|
% |
|
$ |
|
|
|
% |
|
$ |
|
|
|
% |
||||||
脊柱インプラント |
|
|
|
|
|
% |
|
|
|
|
|
% |
|
|
|
|
|
% |
||||||
生物製品 |
|
|
|
|
|
% |
|
|
|
|
|
% |
|
|
|
|
|
% |
||||||
全世界脊椎 |
|
|
|
|
|
% |
|
|
|
|
|
% |
|
|
|
|
|
% |
||||||
世界整形外科 |
|
|
|
|
|
% |
|
|
|
|
|
% |
|
|
|
|
|
% |
||||||
純売上高 |
|
$ |
|
|
|
% |
|
$ |
|
|
|
% |
|
$ |
|
|
|
% |
||||||
次の表は報告部門別にEBITDAを示しており,これは会社を管理する際に使用する主な指標である
|
|
十二月三十一日までの年度 |
|
|||||||||
(ドル、千単位) |
|
2022 |
|
|
2021 |
|
|
2020 |
|
|||
全世界脊椎 |
|
$ |
|
|
$ |
|
|
$ |
|
|||
世界整形外科 |
|
|
( |
) |
|
|
|
|
|
( |
) |
|
会社 |
|
|
( |
) |
|
|
( |
) |
|
|
( |
) |
EBITDA合計 |
|
|
|
|
|
|
|
|
|
|||
減価償却および償却 |
|
|
( |
) |
|
|
( |
) |
|
|
( |
) |
営業権の減価 |
|
|
— |
|
|
|
( |
) |
|
|
— |
|
利子支出,純額 |
|
|
( |
) |
|
|
( |
) |
|
|
( |
) |
所得税前損失 |
|
$ |
( |
) |
|
$ |
( |
) |
|
$ |
( |
) |
次の表は報告書の段落ごとに減価償却と償却を示しています
|
|
十二月三十一日までの年度 |
|
|||||||||
(ドル、千単位) |
|
2022 |
|
|
2021 |
|
|
2020 |
|
|||
全世界脊椎 |
|
$ |
|
|
$ |
|
|
$ |
|
|||
世界整形外科 |
|
|
|
|
|
|
|
|
|
|||
会社 |
|
|
|
|
|
|
|
|
|
|||
合計する |
|
$ |
|
|
$ |
|
|
$ |
|
|||
地理情報
以下のデータには、地理的目的地別の純売上高が含まれる
|
|
十二月三十一日までの年度 |
|
|||||||||
(ドル、千単位) |
|
2022 |
|
|
2021 |
|
|
2020 |
|
|||
アメリカです。 |
|
$ |
|
|
$ |
|
|
$ |
|
|||
イタリア |
|
|
|
|
|
|
|
|
|
|||
ドイツ |
|
|
|
|
|
|
|
|
|
|||
イギリス.イギリス |
|
|
|
|
|
|
|
|
|
|||
フランス |
|
|
|
|
|
|
|
|
|
|||
ブラジル |
|
|
|
|
|
|
|
|
|
|||
他の人は |
|
|
|
|
|
|
|
|
|
|||
純売上高 |
|
$ |
|
|
$ |
|
|
$ |
|
|||
F-28
次の表に報告部門と合併会社ごとの地理的位置別の純売上高を示す
|
|
十二月三十一日までの年度 |
|
|||||||||
(ドル、千単位) |
|
2022 |
|
|
2021 |
|
|
2020 |
|
|||
全世界脊椎 |
|
|
|
|
|
|
|
|
|
|||
アメリカです。 |
|
$ |
|
|
$ |
|
|
$ |
|
|||
国際的に |
|
|
|
|
|
|
|
|
|
|||
全世界の脊椎総数 |
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|||
世界整形外科 |
|
|
|
|
|
|
|
|
|
|||
アメリカです。 |
|
$ |
|
|
|
|
|
|
|
|||
国際的に |
|
|
|
|
|
|
|
|
|
|||
世界整形外科 |
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|||
統合された |
|
|
|
|
|
|
|
|
|
|||
アメリカです。 |
|
|
|
|
|
|
|
|
|
|||
国際的に |
|
|
|
|
|
|
|
|
|
|||
純売上高 |
|
$ |
|
|
$ |
|
|
$ |
|
|||
以下のデータには、地理的地域別の不動産、工場、設備が含まれている
(ドル、千単位) |
|
2022 |
|
|
2021 |
|
||
アメリカです。 |
|
$ |
|
|
$ |
|
||
イタリア |
|
|
|
|
|
|
||
ドイツ |
|
|
|
|
|
|
||
イギリス.イギリス |
|
|
|
|
|
|
||
ブラジル |
|
|
|
|
|
|
||
他の人は |
|
|
|
|
|
|
||
合計する |
|
$ |
|
|
$ |
|
||
17.買収に関連する償却と再計量
買収に関連する償却·再計量には、(1)企業合併または資産買収によって得られた無形資産に関する償却、(2)任意の関連または対価格配置の再計量、(3) 買収された知的財産権研究開発資産に関する確認コストは、買収時に直ちに確認され、及び(Iv)先に確認された業務合併に関する営業権減値である
|
|
十二月三十一日までの年度 |
|
|||||||||
(ドル、千単位) |
|
2022 |
|
|
2021 |
|
|
2020 |
|
|||
価格の公正価値変動があるかもしれない |
|
$ |
( |
) |
|
$ |
( |
) |
|
$ |
( |
) |
無形資産の償却を獲得した |
|
|
|
|
|
|
|
|
|
|||
買収した知的財産権の研究開発 |
|
|
|
|
|
|
|
|
— |
|
||
世界の整形外科の名誉減価 |
|
|
— |
|
|
|
|
|
|
— |
|
|
合計する |
|
$ |
( |
) |
|
$ |
|
|
$ |
( |
) |
|
CGBio株式会社許可と流通契約
2022年7月30日、同社はCIBio有限会社(“CIBio”)と独占許可と流通協定(“許可協定”)を締結し、CGBioは革新的な合成骨移植植物開発業者である。この協定は同社に米国とカナダで臨床前と臨床研究、商業化、普及、マーケティング、Novosis組換えヒト骨形態発生蛋白-2(rhBMP-2)骨成長材料と他の未来組織再生解決方案を販売する独占的な権利を与えた。価格として、同社はCGBioに#ドルを前払いすることに同意した
F-29
取引記録資産購入に分類された場合、またはマイルストーンに関連する対価格価値は、適用事項または関連事項を解決し、対価格または対価格を支払う際に確認される。これは1ドルです
軍団革新有限責任会社の資産買収
2022年12月29日、当社は米国に本社を置く医療機器技術会社Legion Innovation,LLCと技術譲渡と特許権使用料協定を締結し、これにより当社はある資産の知的財産権を獲得した。対価格として、会社は#ドルを支払うことに同意しました
Igea S.p.A資産買収
当社は2021年4月にイタリア骨および軟骨刺激システムメーカーおよび流通業者Igea S.p.A(“Igea”)と独占許可および流通協定(“ライセンス契約”)を締結した。ライセンス契約の掛け値として、同社は最高$を支払うことに同意しました
2022年5月、同社はFDAの買収技術の承認を得て、1ドルの対価格マイルストーン義務をトリガした
関連側資産買収
当社は2021年2月に、当社の執行主席夫人及び前総裁兼最高経営責任者Jon SerBousekが部分的に所有·制御している医療機器技術会社と技術譲渡及び特許権使用料協定を締結し、これにより当社は$に達する
価格には#ドルが含まれています
この取引は、会社監査·財務委員会の承認を得て、監査·財務委員会が取引の交渉を直接監督する。SerBousekさんはこのような議論から除外され、取引の交渉や評価にも参加しなかった。SerBousekさんはまた、企業が取得した技術開発および商業化活動に関する監督から除外され、企業と取引相手との関係に関連するその他のすべての事項から除外され続けています
F-30
18.株式ベースの報酬
2022年12月31日と2021年12月31日に、会社は株式オプションと奨励計画、および株式購入計画を持っている。
2012年長期インセンティブ計画
取締役会は2018年4月23日に改訂·再改訂された二零一二年長期インセンティブ計画(“二零一二年長期インセンティブ計画”)を採択し、その後株主の承認を得た。2012年LTIP規定では、当社の普通株株式を購入するオプション、株式奨励(限定株、非制限株式および株式単位を含む)、株式付加価値権、業績に基づく奨励、およびその他の持分ベースの奨励が付与されている。当社のすべての従業員と当社の付属会社及び連合会社の従業員はすべて資格に符合し、2012年の長期税務優遇によって奨励を受けることができる。また、当社とその付属会社と共同経営会社にサービスを提供する当社の非従業員取締役、コンサルタント、コンサルタントは、2012年の長期投資普及計画に基づいて奨励を受けることができる。2012 LTIPによって付与された報酬は
激励計画
2013年に同社は最大の買収を授与しました
2019年8月、当社は新しいユニバーサル脊柱総裁を任命し、その後総裁兼最高経営責任者に昇進した。当社に雇われた誘因として,その個人は株式オプションを付与され,最も多くの獲得を獲得した
積み荷計画
改正された2回目の改訂及び改訂された株式購入計画(“株式購入計画”)は、その計画に参加し、賃金減額により普通株を獲得した会社及びその付属会社の合資格従業員及び取締役(役員を含む)に会社普通株を発行することを規定している。
各購入期間内に、資格に適合する従業員は
この計画の補償性質により、当社は総合経営報告書に関連する株式補償費用を記録した。報酬費用はブラック·スコアーズ推定モデルを用いて試算し,その価値は計画期間中に費用であることを確認した。2022年12月31日まで株式購入計画に基づいて予約して発行する株式の総数は
F-31
株式ベースの給与費用
株式ベースの給与支出は、従業員の現金給与と連結経営報告書の同一行に計上される。
|
|
十二月三十一日までの年度 |
|
|||||||||
(ドル、千単位) |
|
2022 |
|
|
2021 |
|
|
2020 |
|
|||
販売コスト |
|
$ |
|
|
$ |
|
|
$ |
|
|||
販売とマーケティング |
|
|
|
|
|
|
|
|
|
|||
一般と行政 |
|
|
|
|
|
|
|
|
|
|||
研究開発 |
|
|
|
|
|
|
|
|
|
|||
合計する |
|
$ |
|
|
$ |
|
|
$ |
|
|||
|
|
十二月三十一日までの年度 |
|
|||||||||
(ドル、千単位) |
|
2022 |
|
|
2021 |
|
|
2020 |
|
|||
株式オプション |
|
$ |
|
|
$ |
|
|
$ |
|
|||
時間に基づく制限株式報酬及び株式単位 |
|
|
|
|
|
|
|
|
|
|||
業績に基づく/市場に基づく制限株式単位 |
|
|
|
|
|
|
|
|
|
|||
株購入計画 |
|
|
|
|
|
|
|
|
|
|||
合計する |
|
$ |
|
|
$ |
|
|
$ |
|
|||
この支出に関連した所得税の割引は#ドルだ
株式オプション
時間に基づく株式オプションの公正価値はブラック·スコアーズ推定値モデルを用いて決定され,この価値はサービス期間内に費用として確認され,サービス期間は通常4年であり,実際に没収される。当社が各年度までに授受した株式の公正価値を決定する際に採用した仮説要約2022年12月31日、2021年12月31日、2020年12月31日は、次の表に示すとおりです。当社は2022年に時間に基づく株式オプションを付与していません。
|
|
十二月三十一日までの年度 |
|
|||||||||
|
|
2022 |
|
|
2021 |
|
|
2020 |
|
|||
仮定: |
|
|
|
|
|
|
|
|
|
|||
予想期限(年単位) |
|
|
— |
|
|
|
|
|
||||
予想変動率 |
|
|
— |
|
|
|
|
|
||||
無リスク金利 |
|
|
— |
|
|
|
|
|
||||
配当率 |
|
|
— |
|
|
|
— |
|
|
|
— |
|
加重平均授権日公正価値 |
|
|
— |
|
|
$ |
|
|
$ |
|
||
付与されたオプションの予想期限は、報酬の帰属および満期条項、現在の未償還オプションおよび行使されたまたは満了したオプションの従業員履歴行使行為、および従業員の平均サービス年数を含む一連の要因に基づいて推定される。予想変動率は同社普通株の歴史変動率に基づいている。無リスク金利は固定された米国債安全金利に基づいて決定され、その契約期限はオプションの期待期限に近い。
F-32
会社株オプション計画までの状況概要2022年12月31日と2021年12月31日、および2022年12月31日までの1年間の変化は以下の通り
|
|
オプション |
|
|
重みをつける |
|
|
重みをつける |
|
|||
2021年12月31日現在の未返済債務 |
|
|
|
|
$ |
|
|
|
|
|||
授与する |
|
|
— |
|
|
$ |
- |
|
|
|
|
|
鍛えられた |
|
|
( |
) |
|
$ |
|
|
|
|
||
没収または期限切れ |
|
|
( |
) |
|
$ |
|
|
|
|
||
2022年12月31日に返済されていません |
|
|
|
|
$ |
|
|
|
|
|||
すでに帰属しており,2022年12月31日に帰属する予定である |
|
|
|
|
$ |
|
|
|
|
|||
2022年12月31日に行使できます |
|
|
|
|
$ |
|
|
|
|
|||
2022年12月31日まで付与され、確認される予定のオプションに関する未償却補償支出は#ドルである
時間に基づく制限株式報酬及び株式単位
時間に基づく制限株式報酬と株式単位の補償費用は、付与された日に市場価格で計量された公正価値を代表し、帰属期間中に直線ベースで確認される。これは、通常、
2017年から毎年非従業員役員に手当を支給する形で
2022年12月31日,2021年12月31日と2020年12月31日までの年間で,時間に基づく制限的株式奨励と株式単位の公正価値の合計はい$です
業績と市場に基づく限定的な株式単位
当社のある発行された限定株式単位は、業績に基づく既存条件または市場に基づく既存条件を含む。
業績に基づく制限株式単位の公正価値は、付与日の終値に基づいて計算される。この価値は必要なサービス期間内に費用として確認され,それらが帰属可能とされている期間から実際に没収される。帰属確率は,予測収益と財務結果に基づいて評価される.
市場に基づく制限株式単位の公正価値は、付与された日にモンテカルロ推定方法を使用して決定され、帰属後制限の任意の割引は、Chaffeモデルを使用して推定される。モンテカルロ法は市場状況が満たされない可能性を推定値に入れている。この価値は帰属期間中に直線的に確認され,実際に没収された純額を差し引く。
F-33
2022年、2021年および2020年12月31日までの年間において、帰属および決算の業績および/または市場に基づく制限株式単位の公正価値の合計は$である
12月31日現在、時間ベース、業績ベース、および/または市場に基づく制限株式単位の状況要約に基づいて、2022年と2021年、および2022年12月31日までの1年間の変化は以下の通り
|
|
時間に基づく制限株 |
|
|
パフォーマンスベースおよび/または市場ベース |
|
||||||||||
|
|
株 |
|
|
重みをつける |
|
|
株 |
|
|
重みをつける |
|
||||
2021年12月31日現在の未返済債務 |
|
|
|
|
$ |
|
|
|
|
|
$ |
|
||||
授与する |
|
|
|
|
$ |
|
|
|
|
|
$ |
|
||||
仲直りしなければならない |
|
|
( |
) |
|
$ |
|
|
|
— |
|
|
$ |
— |
|
|
キャンセルします |
|
|
( |
) |
|
$ |
|
|
|
( |
) |
|
$ |
|
||
2022年12月31日に返済されていません |
|
|
|
|
$ |
|
|
|
|
|
$ |
|
||||
19.確定した払込計画と繰延補償
固定払込計画
Orthofix US LLCは、ほぼすべての米国のフルタイム従業員をカバーする固定納付計画(“401(K)計画”)を開始した。401(K)プログラムは、参加者に最大の貢献を可能にする
2020年4月、会社の現金状況の増加と財務柔軟性の維持の予防策として、新冠肺炎疫病の最初の不確実性に対応するため、会社は2020年度の残り時間内に401(K)Match計画を一時停止した。401(K)Matchは、2021年1月に回復する予定である。
同社はまた、最低サービス要求を満たす国際従業員のための固定払込計画を実施している。会社の2022年12月31日,2021年12月31日,2020年12月31日までの年間におけるこのような寄付金はい$です
繰延補償計画
イタリア法によると、私たちのイタリア子会社はその従業員を代表して、雇用終了時に支払われる繰延補償を計算しなければならない。繰延報酬の累積額は、従業員の現在の年間報酬の一パーセントに年間費用を加算して計算される。解雇された場合に代理人に支払われる退職補償金も延滞補償金に計上されなければならない。これは国の契約で規定されており、ほぼ等しい
F-34
20.所得税
未計上所得税準備金の収入(赤字)には、以下のことが含まれる
|
|
十二月三十一日までの年度 |
|
|||||||||
(ドル、千単位) |
|
2022 |
|
|
2021 |
|
|
2020 |
|
|||
アメリカです。 |
|
$ |
( |
) |
|
$ |
( |
) |
|
$ |
|
|
アメリカではない |
|
|
|
|
|
( |
) |
|
|
( |
) |
|
所得税前収入 |
|
$ |
( |
) |
|
$ |
( |
) |
|
$ |
( |
) |
所得税の支出には以下の内容が含まれる
|
|
十二月三十一日までの年度 |
|
|||||||||
(ドル、千単位) |
|
2022 |
|
|
2021 |
|
|
2020 |
|
|||
アメリカです。 |
|
|
|
|
|
|
|
|
|
|||
現在のところ |
|
$ |
|
|
$ |
( |
) |
|
$ |
( |
) |
|
延期する |
|
|
|
|
|
|
|
|
( |
) |
||
|
|
|
|
|
|
|
|
|
( |
) |
||
アメリカではない |
|
|
|
|
|
|
|
|
|
|||
現在のところ |
|
|
|
|
|
|
|
|
|
|||
延期する |
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|||
所得税支出 |
|
$ |
|
|
$ |
|
|
$ |
( |
) |
||
米国連邦法定税率で算出された所得税の計上と、当社の12月31日までの年間有効税率との差2022、2021、および2020は、以下からなる
|
|
2022 |
|
|
2021 |
|
|
2020 |
|
|||||||||||||||
(ドル、千円、百分率を除く) |
|
金額 |
|
|
パーセント |
|
|
金額 |
|
|
パーセント |
|
|
金額 |
|
|
パーセント |
|
||||||
アメリカの法定連邦所得税率 |
|
$ |
( |
) |
|
|
% |
|
$ |
( |
) |
|
|
% |
|
$ |
( |
) |
|
|
% |
|||
アメリカ連邦福祉の州税を差し引くと |
|
|
( |
) |
|
|
|
|
|
( |
) |
|
|
|
|
|
|
|
|
( |
) |
|||
外国の税率差、源泉徴収税が含まれています |
|
|
|
|
|
( |
) |
|
|
|
|
|
( |
) |
|
|
( |
) |
|
|
|
|||
評価免税額,純額 |
|
|
|
|
|
( |
) |
|
|
|
|
|
( |
) |
|
|
|
|
|
( |
) |
|||
外国収入を含めて純額 |
|
|
|
|
|
( |
) |
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
研究単位 |
|
|
( |
) |
|
|
|
|
|
( |
) |
|
|
|
|
|
( |
) |
|
|
|
|||
税収割引が確認されていない場合は、和解後の純額を差し引く |
|
|
( |
) |
|
|
|
|
|
( |
) |
|
|
|
|
|
( |
) |
|
|
|
|||
持分補償 |
|
|
|
|
|
( |
) |
|
|
|
|
|
( |
) |
|
|
|
|
|
( |
) |
|||
役員報酬 |
|
|
|
|
|
( |
) |
|
|
|
|
|
( |
) |
|
|
|
|
|
( |
) |
|||
値段が合うかもしれない |
|
|
( |
) |
|
|
|
|
|
( |
) |
|
|
|
|
|
( |
) |
|
|
|
|||
その他、純額 |
|
|
|
|
|
( |
) |
|
|
|
|
|
( |
) |
|
|
( |
) |
|
|
|
|||
所得税費用(福祉)/有効税率 |
|
$ |
|
|
|
( |
)% |
|
$ |
|
|
|
( |
)% |
|
$ |
( |
) |
|
|
% |
|||
当社は税金に関する現金を合計で支払う(受領または払い戻し))、百万、$
F-35
当社の繰延税金資産と負債は以下の通りです
|
|
十二月三十一日 |
|
|||||
(ドル、千単位) |
|
2022 |
|
|
2021 |
|
||
無形資産と商業権 |
|
$ |
|
|
$ |
|
||
在庫と関連備蓄 |
|
|
|
|
|
|
||
販売貨物の繰延収入とコスト |
|
|
|
|
|
|
||
その他課税項目と準備金 |
|
|
|
|
|
|
||
補償すべきである |
|
|
|
|
|
|
||
期待信用損失準備金 |
|
|
|
|
|
|
||
純営業損失と税収減免繰り越し |
|
|
|
|
|
|
||
研究開発資本化 |
|
|
|
|
|
— |
|
|
賃貸負債 |
|
|
|
|
|
|
||
その他、純額 |
|
|
|
|
|
|
||
繰延税金資産総額 |
|
|
|
|
|
|
||
推定免税額 |
|
|
( |
) |
|
|
( |
) |
繰延税金資産は,推定準備後の純額を差し引く |
|
$ |
|
|
$ |
|
||
税金を前納する |
|
|
( |
) |
|
|
( |
) |
財産·工場·設備 |
|
|
( |
) |
|
|
( |
) |
リース資産を使用する |
|
|
( |
) |
|
|
( |
) |
繰延税金負債 |
|
|
( |
) |
|
|
( |
) |
繰延税項目純資産 |
|
$ |
|
|
$ |
|
||
|
|
|
|
|
|
|
||
報告は以下のとおりである |
|
|
|
|
|
|
||
繰延所得税資産(その他の長期資産に帰属) |
|
|
|
|
|
|
||
繰延所得税負債(他の長期負債に計上) |
|
|
( |
) |
|
|
( |
) |
繰延税項目純資産 |
|
$ |
|
|
$ |
|
||
当社は従来、その総合貸借対照表において繰延所得税資産を独立および独立した項目としてきたが、推定免税額の確認によりその資産の重要性が低下したため、当社は他の長期資産に組み入れるためにこの残高を再分類した。そのため、前年の残高は今期の列報に適合するように再分類された。
当社は貸借対照法を用いて所得税を計算し、この方法の下で、繰延税項資産と負債が資産と負債の財務報告と所得税基礎との間の一時的な差異及び営業損失と信用繰越による予想将来の税収結果を確認する。繰延税金資産及び負債は、この等プロジェクトの年間の現行税率計量の実現が期待される。税法と税率の変化はこのような変化が公布された期間に記録されている。ある繰延税金資産が予測可能な将来に現金化できない可能性が高い場合、当社は評価準備を設立する。
推定値の減少は主に純営業損失の繰越及び国内及びいくつかの海外司法管轄区の一時的な差異によるものである。推定免税額は純増加#ドル
同社は連邦純営業損失を#ドルに繰り越している
F-36
のですどのお金ですか
未送金の外貨収入は#ドルです
既存の証拠の重みが、技術的利点の評価により、税務状況が監査で維持される可能性が高いことを示している場合、当社は不確定税収状況の利益を記録している。税金優遇の基準は
同社の未確認税収割引は1ドルです
12月31日終了年度に税収優遇総額(利息や罰金を含まない)の入金が確認されていない2022年と2021年は以下のようになる
(ドル、千単位) |
|
2022 |
|
|
2021 |
|
||
1月1日までの残高 |
|
$ |
|
|
$ |
|
||
今年度の税収の増加 |
|
|
|
|
|
|
||
前年は税収が増加した |
|
|
|
|
|
|
||
前年の納税状況を決算する |
|
|
( |
) |
|
|
— |
|
法規の有効期限が満了する |
|
|
( |
) |
|
|
( |
) |
12月31日までの残高は |
|
$ |
|
|
$ |
|
||
会社およびその子会社は、米国連邦司法管轄区、ある州と外国司法管轄区(イタリアを含む)および会社が業務を展開している他の司法管轄区に所得税申告書を提出する。連邦と州税務申告の訴訟時効は2019年までの数年以内に閉鎖される。主要外国税務申告管轄区域に関する訴訟時効は2018年までの数年以内に閉鎖される。同社はどの州や地方や外国の検査がその財務諸表に実質的な影響を与えるかどうかを合理的に決定することができず、これらの税務検査の解決時間を予測することもできない。
二十一1株当たり収益(EPS)
ある時期に没収できない配当金または配当等価物の権利の非既得限定株式報酬(参加証券と呼ばれる)が存在するため、当社は2段階法を使用して基本的な1株当たり収益を計算する。基本1株当たり収益は,それぞれ年度内に発行された普通株の加重平均を用いて計算される。償却1株当たり収益は、それぞれ年度内に発行された普通株及び普通株等値株式の加重平均で計算され、在庫株式法或いは2種類法の中で割増程度が高い者を採用する。基本株式と希釈株式との差は、主に普通株同値株式からのものであり、いくつかの発行済み購入株権の行使を仮定し、従業員および取締役に帰属付与された制限株式またはいくつかまたは発行可能株式の要件を満たすと仮定することによる希薄化効果に相当する(付記18参照)。
F-37
2022年12月31日、2021年12月31日、2020年12月31日までの3年間の毎年基本的な1株当たり収益と減額1株当たり収益を計算する際に、純収入に対して重大な調整を行っていない
|
|
十二月三十一日までの年度 |
|
|||||||||
|
|
2022 |
|
|
2021 |
|
|
2020 |
|
|||
加重平均普通株式-基本 |
|
|
|
|
|
|
|
|
|
|||
希釈証券の影響: |
|
|
|
|
|
|
|
|
|
|||
未行使株式オプションと従業員株購入計画 |
|
|
— |
|
|
|
— |
|
|
|
|
|
帰属していない時間に基づく制限株式単位 |
|
|
— |
|
|
|
— |
|
|
|
|
|
加重平均普通株式-希釈後 |
|
|
|
|
|
|
|
|
|
|||
いくつありますか
22.後続事件
SeaSpineホールディングスと合併する
2022年10月10日、当社はOrthofixの完全子会社Orca Merge Sub Inc.(“合併子会社”)と脊柱疾患手術解決策に専念するグローバル医療技術会社SeaSpineと合併協定および合併計画(“合併協定”)を締結した。2023年1月5日に取引が完了し、Merge SubはSeaSpineと合併してSeaSpine(“合併”)に組み込まれ、SeaSpineは取引完了後も存続している会社とOrthofixの完全子会社となる。2022年12月31日までに、当社は約
合併の結果,締め切り直前に発行·発行されたSeaSpine普通株1株当たり収受権に変換される
今回の合併は、Orthofixが米国公認会計原則に基づいて業務合併を会計処理する買収方法によるSeaSpineの買収とされている。したがって、Orthofixは会計目的で買収側とみなされている。買収先を決定する際には,OrthofixとSeaSpineは,取引の構造や合併合意で考慮されている他の行動,未償還の株式所有権と市場価値,合併後の会社取締役会の構成およびOrthofixとSeaSpineの相対規模を考慮している.
買収日までに、合併に関する総推定公正対価には、以下のようなものが含まれる
(ドル、千元、株や1株当たりの価格は含まれていない) |
|
|
|
|
株式対価格: |
|
|
|
|
SeaSpine普通株式と交換するためにOrthofix普通株式を発行します |
|
|
|
|
Orthofix 2023年1月4日現在の1株当たり終値 |
|
$ |
|
|
SeaSpine普通株と引き換えに発行された株式の見積公正価値 |
|
$ |
|
|
未返済のSeaSpine持分奨励と引き換えに発行されたOrthofix株式オプションとRSUの推定公正価値 |
|
|
|
|
合計して価格を公平に見積もる |
|
$ |
|
|
統合協定によると、SeaSpineの未償還持分報酬(株式オプションおよび制限株式単位を含む)は、Orthofixの報酬として交換される。その会社は発行した
F-38
購入掛け値をつける。残りの推定公正価値は、報酬に関連する残りのサービス期間内に補償費用として記録される。
総合財務諸表の発表日まで、当社は総推定公正価値の対価格による純資産の買収と余剰営業権の公正価値の初歩的な分配を決定しているが、このような分配はまだ最終的に確定されていない。 買収された資産と負担する負債に対する買収価格の予備配分は、2023年3月31日までの四半期報告Form 10-Qで報告されるが、この配分は、買収された資産と負担した負債の推定値に依存し、買収日から1年以内に完了する予定である。
合併に関連して、2023年1月5日に買収が完了した後、Orthofixは直ちにSeaSpineを代表して期日が2018年7月27日の改正と再署名された信用協定下のすべての元金、利息および費用に関する未償還債務を返済し、その中でSeaSpineとProject Maple Leaf Holdings ULCを保証人として、SeaSpine Orthopedics Corporation,SeaSpine,Inc.,ISOTIS Sales LLC,ISOTIS Orthobiologics,Inc.,Theken Spine,LLC,SeaSpine Orthopedics Intermediate CoD,IngSA Surgical 7.この協定の下でのすべての適用約束を終了します。
また、2023年1月3日、同社は$を借入した
F-39