pcrx-202212310001396814誤り2022会計年度Http://Fasb.org/us-GAAP/2022#Account StandardsUpdate 20 2006メンバーP 0 D317.4037.34130.0373413P 6 M00013968142022-01-012022-12-3100013968142022-06-30ISO 4217:ドル00013968142023-02-24Xbrli:共有00013968142022-12-3100013968142021-12-31ISO 4217:ドルXbrli:共有0001396814アメリカ-公認会計基準:製品メンバー2022-01-012022-12-310001396814アメリカ-公認会計基準:製品メンバー2021-01-012021-12-310001396814アメリカ-公認会計基準:製品メンバー2020-01-012020-12-310001396814US-GAAP:RoyaltyMember2022-01-012022-12-310001396814US-GAAP:RoyaltyMember2021-01-012021-12-310001396814US-GAAP:RoyaltyMember2020-01-012020-12-310001396814PCRX:コラボレーション許可とマイルストーン収入のメンバー2022-01-012022-12-310001396814PCRX:コラボレーション許可とマイルストーン収入のメンバー2021-01-012021-12-310001396814PCRX:コラボレーション許可とマイルストーン収入のメンバー2020-01-012020-12-3100013968142021-01-012021-12-3100013968142020-01-012020-12-310001396814アメリカ-アメリカ公認会計基準:普通株式メンバー2019-12-310001396814US-GAAP:AdditionalPaidInCapitalMembers2019-12-310001396814アメリカ-公認会計基準:前払いメンバーを保留2019-12-310001396814アメリカ公認会計原則:他の総合収入メンバーを累計2019-12-3100013968142019-12-310001396814アメリカ-アメリカ公認会計基準:普通株式メンバー2020-01-012020-12-310001396814US-GAAP:AdditionalPaidInCapitalMembers2020-01-012020-12-310001396814PCRX:変換可能上位ノード2022メンバーUS-GAAP:AdditionalPaidInCapitalMembers2020-01-012020-12-310001396814PCRX:変換可能上位ノード2022メンバー2020-01-012020-12-310001396814PCRX:移行可能な高度な注意事項2025メンバーUS-GAAP:AdditionalPaidInCapitalMembers2020-01-012020-12-310001396814PCRX:移行可能な高度な注意事項2025メンバー2020-01-012020-12-310001396814アメリカ公認会計原則:他の総合収入メンバーを累計2020-01-012020-12-310001396814アメリカ-公認会計基準:前払いメンバーを保留2020-01-012020-12-310001396814アメリカ-アメリカ公認会計基準:普通株式メンバー2020-12-310001396814US-GAAP:AdditionalPaidInCapitalMembers2020-12-310001396814アメリカ-公認会計基準:前払いメンバーを保留2020-12-310001396814アメリカ公認会計原則:他の総合収入メンバーを累計2020-12-3100013968142020-12-310001396814アメリカ-アメリカ公認会計基準:普通株式メンバー2021-01-012021-12-310001396814US-GAAP:AdditionalPaidInCapitalMembers2021-01-012021-12-310001396814アメリカ公認会計原則:他の総合収入メンバーを累計2021-01-012021-12-310001396814アメリカ-公認会計基準:前払いメンバーを保留2021-01-012021-12-310001396814アメリカ-アメリカ公認会計基準:普通株式メンバー2021-12-310001396814US-GAAP:AdditionalPaidInCapitalMembers2021-12-310001396814アメリカ-公認会計基準:前払いメンバーを保留2021-12-310001396814アメリカ公認会計原則:他の総合収入メンバーを累計2021-12-310001396814US-GAAP:AdditionalPaidInCapitalMembersSRT:累計調整有効期限調整メンバ2021-12-310001396814アメリカ-公認会計基準:前払いメンバーを保留SRT:累計調整有効期限調整メンバ2021-12-310001396814SRT:累計調整有効期限調整メンバ2021-12-310001396814アメリカ-アメリカ公認会計基準:普通株式メンバー2022-01-012022-12-310001396814US-GAAP:AdditionalPaidInCapitalMembers2022-01-012022-12-310001396814PCRX:変換可能上位ノード2022メンバーUS-GAAP:AdditionalPaidInCapitalMembers2022-01-012022-12-310001396814PCRX:変換可能上位ノード2022メンバー2022-01-012022-12-310001396814アメリカ公認会計原則:他の総合収入メンバーを累計2022-01-012022-12-310001396814アメリカ-公認会計基準:前払いメンバーを保留2022-01-012022-12-310001396814アメリカ-アメリカ公認会計基準:普通株式メンバー2022-12-310001396814US-GAAP:AdditionalPaidInCapitalMembers2022-12-310001396814アメリカ-公認会計基準:前払いメンバーを保留2022-12-310001396814アメリカ公認会計原則:他の総合収入メンバーを累計2022-12-310001396814PCRX:変換可能な上位ノード2025メンバー2022-01-012022-12-310001396814PCRX:変換可能な上位ノード2025メンバー2021-01-012021-12-310001396814PCRX:変換可能な上位ノード2025メンバー2020-01-012020-12-310001396814PCRX:変換可能上位ノード2022メンバー2021-01-012021-12-310001396814PCRX:変換可能上位ノード2024メンバー2022-01-012022-12-310001396814PCRX:変換可能上位ノード2024メンバー2021-01-012021-12-310001396814PCRX:変換可能上位ノード2024メンバー2020-01-012020-12-310001396814米国-GAAP:SalesRevenueNetMembersアメリカ公認会計基準:製品集中度リスクメンバー2022-01-012022-12-31PCRX:製品0001396814US-GAAP:顧客集中度リスクメンバー2022-01-012022-12-31PCRX:お客様0001396814US-GAAP:顧客集中度リスクメンバー米国-GAAP:SalesRevenueNetMembersPCRX:大顧客メンバー2022-01-012022-12-31Xbrli:純0001396814US-GAAP:顧客集中度リスクメンバー米国-GAAP:SalesRevenueNetMembersPCRX:大顧客メンバー2021-01-012021-12-310001396814US-GAAP:顧客集中度リスクメンバー米国-GAAP:SalesRevenueNetMembersPCRX:大顧客メンバー2020-01-012020-12-310001396814US-GAAP:顧客集中度リスクメンバー米国-GAAP:SalesRevenueNetMembersPCRX:Second LargestCustomerMembers2022-01-012022-12-310001396814US-GAAP:顧客集中度リスクメンバー米国-GAAP:SalesRevenueNetMembersPCRX:Second LargestCustomerMembers2021-01-012021-12-310001396814US-GAAP:顧客集中度リスクメンバー米国-GAAP:SalesRevenueNetMembersPCRX:Second LargestCustomerMembers2020-01-012020-12-310001396814PCRX:ThirdLargestCustomerMemberUS-GAAP:顧客集中度リスクメンバー米国-GAAP:SalesRevenueNetMembers2022-01-012022-12-310001396814PCRX:ThirdLargestCustomerMemberUS-GAAP:顧客集中度リスクメンバー米国-GAAP:SalesRevenueNetMembers2021-01-012021-12-310001396814PCRX:ThirdLargestCustomerMemberUS-GAAP:顧客集中度リスクメンバー米国-GAAP:SalesRevenueNetMembers2020-01-012020-12-310001396814US-GAAP:顧客集中度リスクメンバー米国-GAAP:SalesRevenueNetMembersPCRX:3つの大きな顧客メンバー2022-01-012022-12-310001396814US-GAAP:顧客集中度リスクメンバー米国-GAAP:SalesRevenueNetMembersPCRX:3つの大きな顧客メンバー2021-01-012021-12-310001396814US-GAAP:顧客集中度リスクメンバー米国-GAAP:SalesRevenueNetMembersPCRX:3つの大きな顧客メンバー2020-01-012020-12-310001396814US-GAAP:顧客集中度リスクメンバー米国-GAAP:SalesRevenueNetMembersPCRX:クライアント外部ユーザメンバ2022-01-012022-12-310001396814US-GAAP:顧客集中度リスクメンバー米国-GAAP:SalesRevenueNetMembersPCRX:クライアント外部ユーザメンバ2021-01-012021-12-310001396814US-GAAP:顧客集中度リスクメンバー米国-GAAP:SalesRevenueNetMembersPCRX:クライアント外部ユーザメンバ2020-01-012020-12-310001396814PCRX:ComputerEquipmentAndSoftwareMemberSRT:最小メンバ数2022-01-012022-12-310001396814PCRX:ComputerEquipmentAndSoftwareMemberSRT:最大メンバ数2022-01-012022-12-310001396814アメリカ-GAAP:家具と固定機器のメンバー2022-01-012022-12-310001396814SRT:最小メンバ数アメリカ-GAAP:機械とデバイスのメンバー2022-01-012022-12-310001396814SRT:最大メンバ数アメリカ-GAAP:機械とデバイスのメンバー2022-01-012022-12-31PCRX:細分化市場0001396814SRT:累積有効期限調整バランスメンバを採用する2021-12-310001396814アメリカ-公認会計基準:前払いメンバーを保留SRT:累積有効期限調整バランスメンバを採用する2021-12-310001396814US-GAAP:AdditionalPaidInCapitalMembersSRT:累積有効期限調整バランスメンバを採用する2021-12-310001396814米国-GAAP:返品·許可メンバーの販売2019-12-310001396814PCRX:予約セールPayDiscountメンバー2019-12-310001396814PCRX:一括警報サービス料メンバー2019-12-310001396814PCRX:ボリューム回収および記憶容量に応じた課金メンバの使用を可能にする2019-12-310001396814PCRX:政府応答を許可するメンバー2019-12-310001396814米国-GAAP:返品·許可メンバーの販売2020-01-012020-12-310001396814PCRX:予約セールPayDiscountメンバー2020-01-012020-12-310001396814PCRX:一括警報サービス料メンバー2020-01-012020-12-310001396814PCRX:ボリューム回収および記憶容量に応じた課金メンバの使用を可能にする2020-01-012020-12-310001396814PCRX:政府応答を許可するメンバー2020-01-012020-12-310001396814米国-GAAP:返品·許可メンバーの販売2020-12-310001396814PCRX:予約セールPayDiscountメンバー2020-12-310001396814PCRX:一括警報サービス料メンバー2020-12-310001396814PCRX:ボリューム回収および記憶容量に応じた課金メンバの使用を可能にする2020-12-310001396814PCRX:政府応答を許可するメンバー2020-12-310001396814米国-GAAP:返品·許可メンバーの販売2021-01-012021-12-310001396814PCRX:予約セールPayDiscountメンバー2021-01-012021-12-310001396814PCRX:一括警報サービス料メンバー2021-01-012021-12-310001396814PCRX:ボリューム回収および記憶容量に応じた課金メンバの使用を可能にする2021-01-012021-12-310001396814PCRX:政府応答を許可するメンバー2021-01-012021-12-310001396814米国-GAAP:返品·許可メンバーの販売2021-12-310001396814PCRX:予約セールPayDiscountメンバー2021-12-310001396814PCRX:一括警報サービス料メンバー2021-12-310001396814PCRX:ボリューム回収および記憶容量に応じた課金メンバの使用を可能にする2021-12-310001396814PCRX:政府応答を許可するメンバー2021-12-310001396814米国-GAAP:返品·許可メンバーの販売2022-01-012022-12-310001396814PCRX:予約セールPayDiscountメンバー2022-01-012022-12-310001396814PCRX:一括警報サービス料メンバー2022-01-012022-12-310001396814PCRX:ボリューム回収および記憶容量に応じた課金メンバの使用を可能にする2022-01-012022-12-310001396814PCRX:政府応答を許可するメンバー2022-01-012022-12-310001396814米国-GAAP:返品·許可メンバーの販売2022-12-310001396814PCRX:予約セールPayDiscountメンバー2022-12-310001396814PCRX:一括警報サービス料メンバー2022-12-310001396814PCRX:ボリューム回収および記憶容量に応じた課金メンバの使用を可能にする2022-12-310001396814PCRX:政府応答を許可するメンバー2022-12-310001396814SRT:最小メンバ数2022-01-012022-12-310001396814SRT:最大メンバ数2022-01-012022-12-310001396814PCRX:ExPARELメンバー2022-01-012022-12-310001396814PCRX:ExPARELメンバー2021-01-012021-12-310001396814PCRX:ExPARELメンバー2020-01-012020-12-310001396814PCRX:ZILRETTAMメンバー2022-01-012022-12-310001396814PCRX:ZILRETTAMメンバー2021-01-012021-12-310001396814PCRX:ZILRETTAMメンバー2020-01-012020-12-310001396814PCRX:Ioveraメンバー2022-01-012022-12-310001396814PCRX:Ioveraメンバー2021-01-012021-12-310001396814PCRX:Ioveraメンバー2020-01-012020-12-310001396814PCRX:ブピバカイン脂質注射剤徐放剤メンバー2022-01-012022-12-310001396814PCRX:ブピバカイン脂質注射剤徐放剤メンバー2021-01-012021-12-310001396814PCRX:ブピバカイン脂質注射剤徐放剤メンバー2020-01-012020-12-310001396814PCRX:Flexion治療薬IncMember2021-11-192021-11-190001396814PCRX:Flexion治療薬IncMemberPCRX:RestratedStockUnitsMoneyStockOptionsAndCommonStockMember2021-11-192022-12-310001396814PCRX:Flexion治療薬IncMember2021-11-190001396814PCRX:2.5億人のメンバーにおけるZILRETTASSの成果2021-11-190001396814SRT:シーン予測メンバPCRX:2.5億人のメンバーにおけるZILRETTASSの成果2021-11-192030-12-310001396814PCRX:ZILRETTASS販売実績3.75億メンバー2021-11-190001396814PCRX:ZILRETTASS販売実績3.75億メンバーSRT:シーン予測メンバ2021-11-192030-12-310001396814PCRX:5億名のメンバーのうちZILRETTASSの販売実績2021-11-190001396814PCRX:5億名のメンバーのうちZILRETTASSの販売実績SRT:シーン予測メンバ2021-11-192030-12-310001396814PCRX:FDAApprovalOfFX 201メンバー2021-11-190001396814PCRX:FDAApprovalOfFX 301メンバー2021-11-190001396814PCRX:Flexion治療薬IncMemberアメリカ-アメリカ公認会計基準:普通株式メンバー2022-01-012022-12-310001396814PCRX:Flexion治療薬IncMemberアメリカ-アメリカ公認会計基準:普通株式メンバー2022-12-310001396814PCRX:Flexion治療薬IncMemberアメリカ-アメリカ公認会計基準:普通株式メンバー2021-11-192021-11-190001396814PCRX:Flexion治療薬IncMember米国-GAAP:制限株式単位RSUメンバー2021-11-192021-11-190001396814PCRX:Flexion治療薬IncMemberアメリカ公認会計基準:債務メンバー2021-11-190001396814PCRX:Flexion治療薬IncMember2022-12-3100013968142021-11-192022-12-310001396814PCRX:Flexion治療薬IncMember米国-GAAP:技術的権利の発達したメンバー2021-11-192021-11-190001396814PCRX:Flexion治療薬IncMember米国-公認会計基準:投入割引率を測るメンバー米国-GAAP:IncomeApproachValuationTechnologiesメンバー米国-GAAP:技術的権利の発達したメンバー2021-11-192021-11-190001396814米国-GAAP:InProcessResearchAndDevelopmentMembersPCRX:Flexion治療薬IncMember2021-11-192021-11-190001396814米国-GAAP:InProcessResearchAndDevelopmentMembersPCRX:Flexion治療薬IncMemberアメリカ公認会計基準:評価技術割引現金流量メンバー米国-公認会計基準:投入割引率を測るメンバー2021-11-192021-11-190001396814PCRX:Flexion治療薬IncMember2022-01-012022-12-310001396814PCRX:Flexion治療薬IncMember2021-01-012021-12-310001396814アメリカ-GAAP:機械とデバイスのメンバー2022-12-310001396814アメリカ-GAAP:機械とデバイスのメンバー2021-12-310001396814アメリカ-公認会計基準:リース改善メンバー2022-12-310001396814アメリカ-公認会計基準:リース改善メンバー2021-12-310001396814PCRX:ComputerEquipmentAndSoftwareMember2022-12-310001396814PCRX:ComputerEquipmentAndSoftwareMember2021-12-310001396814アメリカ-GAAP:家具と固定機器のメンバー2022-12-310001396814アメリカ-GAAP:家具と固定機器のメンバー2021-12-310001396814アメリカ-アメリカ公認会計基準:建設中のメンバー2022-12-310001396814アメリカ-アメリカ公認会計基準:建設中のメンバー2021-12-310001396814アメリカ-アメリカ公認会計基準:建設中のメンバーPCRX:科学センターキャンパスと熱漁師のメンバー2022-12-310001396814アメリカ-GAAP:機械とデバイスのメンバー2022-01-012022-12-310001396814アメリカ-公認会計基準:リース改善メンバーアメリカ-GAAP:非アメリカのメンバー2022-12-310001396814アメリカ-公認会計基準:リース改善メンバーアメリカ-GAAP:非アメリカのメンバー2021-12-310001396814PCRX:SkyePharmaHoldingIncMember2021-01-012021-12-310001396814PCRX:UponFirstCommercial SaleInMajorEUCountryメンバー2021-12-310001396814PCRX:UponAnnualNetSalesReachingDollar 5.00百万Threshold Members2022-03-310001396814PCRX:Flexion治療薬IncMember2021-11-192022-12-310001396814米国-GAAP:技術的権利の発達したメンバー2022-12-310001396814米国-GAAP:技術的権利の発達したメンバー2022-01-012022-12-310001396814US-GAAP:クライアント関係メンバ2022-12-310001396814US-GAAP:クライアント関係メンバ2022-01-012022-12-310001396814米国-GAAP:InProcessResearchAndDevelopmentMembers2022-12-310001396814米国-GAAP:技術的権利の発達したメンバー2021-12-310001396814米国-GAAP:技術的権利の発達したメンバー2021-01-012021-12-310001396814US-GAAP:クライアント関係メンバ2021-12-310001396814US-GAAP:クライアント関係メンバ2021-01-012021-12-310001396814米国-GAAP:InProcessResearchAndDevelopmentMembers2021-12-310001396814PCRX:UponAnnualNetSalesReachingDollar 5.00百万Threshold Members2021-12-310001396814米国-GAAP:SecuredDebtメンバーPCRX:TermLoanBFacilityDue 2026メンバー2022-12-310001396814米国-GAAP:SecuredDebtメンバーPCRX:TermLoanBFacilityDue 2026メンバー2021-12-310001396814PCRX:変換可能な上位ノード2025メンバー2022-12-310001396814PCRX:変換可能な上位ノード2025メンバーアメリカ公認会計基準:非安全債務メンバー2022-12-310001396814PCRX:変換可能な上位ノード2025メンバーアメリカ公認会計基準:非安全債務メンバー2021-12-310001396814PCRX:変換可能上位ノード2024年5月2022-12-310001396814PCRX:変換可能上位ノード2024年5月アメリカ公認会計基準:非安全債務メンバー2022-12-310001396814PCRX:変換可能上位ノード2024年5月アメリカ公認会計基準:非安全債務メンバー2021-12-310001396814PCRX:変換可能上位ノード2022メンバーアメリカ公認会計基準:非安全債務メンバー2022-12-310001396814PCRX:変換可能上位ノード2022メンバーアメリカ公認会計基準:非安全債務メンバー2021-12-310001396814アメリカ公認会計基準:非安全債務メンバー2022-12-310001396814アメリカ公認会計基準:非安全債務メンバー2021-12-310001396814米国-GAAP:SecuredDebtメンバーPCRX:TermLoanBFacilityDue 2026メンバー2021-12-010001396814米国-GAAP:SecuredDebtメンバーPCRX:TermLoanBFacilityDue 2026メンバー2021-01-012021-12-310001396814米国-GAAP:SecuredDebtメンバーPCRX:TermLoanBFacilityDue 2026メンバー2022-06-302022-06-300001396814米国-GAAP:SecuredDebtメンバーPCRX:TermLoanBFacilityDue 2026メンバーSRT:シーン予測メンバ2025-12-312025-12-310001396814米国-GAAP:SecuredDebtメンバーPCRX:TermLoanBFacilityDue 2026メンバーSRT:シーン予測メンバ2026-12-070001396814米国-GAAP:SecuredDebtメンバーPCRX:TermLoanBFacilityDue 2026メンバー2022-01-012022-12-310001396814PCRX:TermLoanBFacilityDue 2026メンバー2022-12-310001396814PCRX:TermLoanBFacilityDue 2026メンバーSRT:最小メンバ数US-GAAP:SecuredOvernightFinancingRateSofrOvernightIndexSwapRateRateメンバー2022-01-012022-12-310001396814PCRX:TermLoanBFacilityDue 2026メンバーUS-GAAP:SecuredOvernightFinancingRateSofrOvernightIndexSwapRateRateメンバー2022-01-012022-12-310001396814アメリカ公認会計基準:基本比率メンバーPCRX:TermLoanBFacilityDue 2026メンバーSRT:最小メンバ数2022-01-012022-12-310001396814PCRX:TermLoanBFacilityDue 2026メンバーSRT:最小メンバ数PCRX:FederalReserve BankOfNYRateMember2022-01-012022-12-310001396814アメリカ公認会計基準:基本比率メンバーPCRX:TermLoanBFacilityDue 2026メンバー2022-01-012022-12-310001396814PCRX:変換可能な上位ノード2025メンバーアメリカ公認会計基準:非安全債務メンバー2020-07-310001396814PCRX:変換可能な上位ノード2025メンバーアメリカ公認会計基準:非安全債務メンバー2020-07-012020-07-310001396814PCRX:変換可能上位ノード2022メンバーアメリカ公認会計基準:非安全債務メンバー2020-07-310001396814PCRX:変換可能上位ノード2022メンバーアメリカ公認会計基準:非安全債務メンバー2020-07-102020-07-100001396814PCRX:変換可能な上位ノード2025メンバーアメリカ公認会計基準:転換可能債務メンバー2022-01-012022-12-310001396814PCRX:変換可能な上位ノード2025メンバーPCRX:DebtConversionTermsBusinessDayすぐ優先2月320月2022-10-012022-12-31PCRX:取引日0001396814PCRX:変換可能な上位ノード2025メンバー2022-10-012022-12-310001396814PCRX:変換可能な上位ノード2025メンバー2020-07-310001396814PCRX:変換可能な上位ノード2025メンバーアメリカ公認会計基準:非安全債務メンバー2022-01-012022-12-310001396814PCRX:変換可能な上位ノード2025メンバーPCRX:DebtRedemptionTermsOnor AfterAugust 12023メンバー2022-10-012022-12-310001396814PCRX:変換可能な上位ノード2025メンバーアメリカ公認会計基準:転換可能債務メンバー2022-12-310001396814PCRX:変換可能な上位ノード2025メンバーアメリカ公認会計基準:転換可能債務メンバーSRT:累積有効期限調整バランスメンバを採用する2022-01-010001396814PCRX:変換可能な上位ノード2025メンバーアメリカ公認会計基準:転換可能債務メンバーSRT:累積有効期限調整バランスメンバを採用する2022-01-012022-01-010001396814PCRX:変換可能上位ノード2024メンバーアメリカ公認会計基準:非安全債務メンバーPCRX:Flexion治療薬IncMember2017-05-310001396814PCRX:変換可能上位ノード2024メンバーPCRX:Flexion治療薬IncMember2017-05-020001396814PCRX:変換可能上位ノード2024メンバー2021-12-062022-01-060001396814PCRX:変換可能上位ノード2024メンバーPCRX:Flexion治療薬IncMember2021-12-060001396814PCRX:変換可能上位ノード2024メンバーアメリカ公認会計基準:非安全債務メンバー2022-01-070001396814PCRX:変換可能上位ノード2022メンバーアメリカ公認会計基準:非安全債務メンバー2017-03-132017-03-130001396814PCRX:変換可能上位ノード2022メンバーアメリカ公認会計基準:非安全債務メンバー2017-03-130001396814PCRX:変換可能上位ノード2022メンバーアメリカ公認会計基準:非安全債務メンバー2020-07-100001396814PCRX:変換可能上位ノード2022メンバーアメリカ公認会計基準:非安全債務メンバー2022-04-012022-04-010001396814アメリカ-アメリカ公認会計基準:普通株式メンバー2022-04-012022-04-010001396814PCRX:変換可能上位ノード2024メンバーPCRX:Flexion治療薬IncMember2017-05-022017-05-020001396814アメリカ-アメリカ公認会計基準:横ばい報告金額公正価値開示メンバー2022-12-310001396814アメリカ-公認会計基準:公正価値入力レベル1メンバーUS-GAAP:EstimateOfFairValueFairValueDisclosureMember2022-12-310001396814アメリカ-公認会計基準:公正価値入力レベル2メンバーUS-GAAP:EstimateOfFairValueFairValueDisclosureMember2022-12-310001396814アメリカ-公認会計基準:公正価値投入レベル3メンバーUS-GAAP:EstimateOfFairValueFairValueDisclosureMember2022-12-310001396814米国-GAAP:SecuredDebtメンバーPCRX:TermLoanBFacilityDue 2026メンバーアメリカ-アメリカ公認会計基準:横ばい報告金額公正価値開示メンバー2022-12-310001396814アメリカ-公認会計基準:公正価値入力レベル1メンバー米国-GAAP:SecuredDebtメンバーPCRX:TermLoanBFacilityDue 2026メンバーUS-GAAP:EstimateOfFairValueFairValueDisclosureMember2022-12-310001396814米国-GAAP:SecuredDebtメンバーPCRX:TermLoanBFacilityDue 2026メンバーアメリカ-公認会計基準:公正価値入力レベル2メンバーUS-GAAP:EstimateOfFairValueFairValueDisclosureMember2022-12-310001396814米国-GAAP:SecuredDebtメンバーアメリカ-公認会計基準:公正価値投入レベル3メンバーPCRX:TermLoanBFacilityDue 2026メンバーUS-GAAP:EstimateOfFairValueFairValueDisclosureMember2022-12-310001396814PCRX:変換可能な上位ノード2025メンバーアメリカ公認会計基準:非安全債務メンバーアメリカ-アメリカ公認会計基準:横ばい報告金額公正価値開示メンバー2022-12-310001396814アメリカ-公認会計基準:公正価値入力レベル1メンバーPCRX:変換可能な上位ノード2025メンバーアメリカ公認会計基準:非安全債務メンバーUS-GAAP:EstimateOfFairValueFairValueDisclosureMember2022-12-310001396814PCRX:変換可能な上位ノード2025メンバーアメリカ-公認会計基準:公正価値入力レベル2メンバーアメリカ公認会計基準:非安全債務メンバーUS-GAAP:EstimateOfFairValueFairValueDisclosureMember2022-12-310001396814PCRX:変換可能な上位ノード2025メンバーアメリカ-公認会計基準:公正価値投入レベル3メンバーアメリカ公認会計基準:非安全債務メンバーUS-GAAP:EstimateOfFairValueFairValueDisclosureMember2022-12-310001396814PCRX:変換可能上位ノード2024メンバーアメリカ公認会計基準:非安全債務メンバー2022-12-310001396814PCRX:変換可能上位ノード2024メンバーアメリカ公認会計基準:非安全債務メンバーアメリカ-アメリカ公認会計基準:横ばい報告金額公正価値開示メンバー2022-12-310001396814アメリカ-公認会計基準:公正価値入力レベル1メンバーPCRX:変換可能上位ノード2024メンバーアメリカ公認会計基準:非安全債務メンバーUS-GAAP:EstimateOfFairValueFairValueDisclosureMember2022-12-310001396814アメリカ-公認会計基準:公正価値入力レベル2メンバーPCRX:変換可能上位ノード2024メンバーアメリカ公認会計基準:非安全債務メンバーUS-GAAP:EstimateOfFairValueFairValueDisclosureMember2022-12-310001396814アメリカ-公認会計基準:公正価値投入レベル3メンバーPCRX:変換可能上位ノード2024メンバーアメリカ公認会計基準:非安全債務メンバーUS-GAAP:EstimateOfFairValueFairValueDisclosureMember2022-12-310001396814PCRX:変換可能な上位ノード2025メンバーSRT:最大メンバ数2022-01-012022-12-310001396814米国-公認会計基準:株式証券メンバー2020-12-310001396814PCRX:変換可能ノードの受信メンバー2020-12-310001396814米国-公認会計基準:株式証券メンバー2021-01-012021-12-310001396814PCRX:変換可能ノードの受信メンバー2021-01-012021-12-310001396814米国-公認会計基準:株式証券メンバー2021-12-310001396814PCRX:変換可能ノードの受信メンバー2021-12-310001396814米国-公認会計基準:株式証券メンバー2022-01-012022-12-310001396814PCRX:変換可能ノードの受信メンバー2022-01-012022-12-310001396814米国-公認会計基準:株式証券メンバー2022-12-310001396814PCRX:変換可能ノードの受信メンバー2022-12-310001396814PCRX:TELABioMembers2021-01-012021-12-310001396814アメリカ公認会計基準:副次的事件メンバー2023-02-012023-02-280001396814PCRX:FlexionとMyoscienceAcquisitionMembers2022-12-310001396814PCRX:FlexionとMyoscienceAcquisitionMembers2021-12-310001396814PCRX:Flexion AcquisitionMember2021-11-300001396814PCRX:Flexion AcquisitionMember2022-08-310001396814PCRX:Flexion AcquisitionMember2021-11-012021-11-300001396814PCRX:Flexion AcquisitionMember2021-11-012021-12-310001396814PCRX:Flexion AcquisitionMember2022-01-012022-12-310001396814SRT:重み平均メンバPCRX:ContingentConsiderationMemberアメリカ-公認会計基準:公正価値投入レベル3メンバー米国-公認会計基準:投入割引率を測るメンバーPCRX:Flexion AcquisitionMember2022-12-310001396814SRT:重み平均メンバPCRX:ContingentConsiderationMemberアメリカ-公認会計基準:公正価値投入レベル3メンバーPCRX:Flexion AcquisitionMemberPCRX:入力確率OfSuccessOfRegulatoryMilestonesメンバーを測定する2022-12-310001396814SRT:重み平均メンバPCRX:ContingentConsiderationMemberアメリカ-公認会計基準:公正価値投入レベル3メンバーPCRX:Flexion AcquisitionMemberPCRX:入力確率OfSuccessOfRegulatoryMilestonesメンバーを測定する2021-12-310001396814SRT:重み平均メンバPCRX:ContingentConsiderationMemberアメリカ-公認会計基準:公正価値投入レベル3メンバーPCRX:Flexion AcquisitionMemberPCRX:入力確率OfPaymentDueToLikelihodOfAchievementMemberを測定2022-12-310001396814SRT:重み平均メンバPCRX:ContingentConsiderationMemberアメリカ-公認会計基準:公正価値投入レベル3メンバーPCRX:Flexion AcquisitionMemberPCRX:入力確率OfPaymentDueToLikelihodOfAchievementMemberを測定2021-12-310001396814SRT:重み平均メンバPCRX:ContingentConsiderationMemberアメリカ-公認会計基準:公正価値投入レベル3メンバーPCRX:入力確率OfSuccessInRegulatoryApprovalMemberを測定するPCRX:Flexion AcquisitionMember2022-12-310001396814SRT:重み平均メンバPCRX:ContingentConsiderationMemberアメリカ-公認会計基準:公正価値投入レベル3メンバーPCRX:入力確率OfSuccessInRegulatoryApprovalMemberを測定するPCRX:Flexion AcquisitionMember2021-12-310001396814PCRX:Flexion AcquisitionMember2022-12-310001396814PCRX:Flexion AcquisitionMember2021-12-310001396814PCRX:MyoscienceAcquisitionMembers2019-04-012019-04-300001396814PCRX:MyoscienceAcquisitionMembers2022-12-310001396814PCRX:MyoscienceAcquisitionMembers2022-01-012022-12-310001396814PCRX:MyoscienceAcquisitionMembers2021-01-012021-12-310001396814PCRX:MyoscienceAcquisitionMembers2020-01-012020-12-310001396814PCRX:ContingentConsiderationMemberアメリカ-公認会計基準:公正価値投入レベル3メンバーPCRX:MeasurementInputExspectedMilestonePaymentMemberPCRX:MyoscienceAcquisitionMembers2022-12-310001396814PCRX:MyoscienceAcquisitionMembers2021-12-310001396814PCRX:ContingentConsiderationMember米国-公認会計基準:投入割引率を測るメンバーPCRX:Flexion AcquisitionMemberSRT:最小メンバ数2022-12-310001396814PCRX:ContingentConsiderationMember米国-公認会計基準:投入割引率を測るメンバーPCRX:Flexion AcquisitionMemberSRT:最大メンバ数2022-12-310001396814PCRX:ContingentConsiderationMemberPCRX:Flexion AcquisitionMemberPCRX:MeasurementInputExspectedMilestonePaymentMemberSRT:最小メンバ数2022-12-310001396814PCRX:ContingentConsiderationMemberPCRX:Flexion AcquisitionMemberSRT:最大メンバ数PCRX:MeasurementInputExspectedMilestonePaymentMember2022-12-310001396814PCRX:ContingentConsiderationMember2020-12-310001396814PCRX:ContingentConsiderationMember2021-01-012021-12-310001396814PCRX:ContingentConsiderationMember2021-12-310001396814PCRX:ContingentConsiderationMember2022-01-012022-12-310001396814PCRX:ContingentConsiderationMember2022-12-310001396814米国-公認会計基準:資産認可証券メンバー米国-GAAP:ShortTermInvestmentsメンバー2022-12-310001396814米国-GAAP:ビジネス紙のメンバー米国-GAAP:ShortTermInvestmentsメンバー2022-12-310001396814アメリカ-公認会計基準:アメリカ政府機関債務証券メンバー米国-GAAP:ShortTermInvestmentsメンバー2022-12-310001396814アメリカ-GAAP:アメリカReasuryNotesSecuritiesMembers米国-GAAP:ShortTermInvestmentsメンバー2022-12-310001396814米国-GAAP:ShortTermInvestmentsメンバー2022-12-310001396814アメリカ-公認会計基準:アメリカ政府機関債務証券メンバーPCRX:LongTermInvestmentsメンバー2022-12-310001396814アメリカ-GAAP:アメリカReasuryNotesSecuritiesMembersPCRX:LongTermInvestmentsメンバー2022-12-310001396814PCRX:LongTermInvestmentsメンバー2022-12-310001396814米国-公認会計基準:資産認可証券メンバー米国-GAAP:ShortTermInvestmentsメンバー2021-12-310001396814米国-GAAP:ビジネス紙のメンバー米国-GAAP:ShortTermInvestmentsメンバー2021-12-310001396814米国-公認会計基準:社債証券メンバー米国-GAAP:ShortTermInvestmentsメンバー2021-12-310001396814米国-GAAP:ShortTermInvestmentsメンバー2021-12-310001396814US-GAAP:顧客集中度リスクメンバーアメリカ公認会計基準:売掛金メンバーPCRX:主要顧客OneMember2022-01-012022-12-310001396814PCRX:主な顧客2人のメンバーUS-GAAP:顧客集中度リスクメンバーアメリカ公認会計基準:売掛金メンバー2022-01-012022-12-310001396814US-GAAP:顧客集中度リスクメンバーアメリカ公認会計基準:売掛金メンバーPCRX:主なお客様4名のメンバー2022-01-012022-12-310001396814US-GAAP:顧客集中度リスクメンバーアメリカ公認会計基準:売掛金メンバーPCRX:主要顧客OneMember2021-01-012021-12-310001396814PCRX:主な顧客2人のメンバーUS-GAAP:顧客集中度リスクメンバーアメリカ公認会計基準:売掛金メンバー2021-01-012021-12-310001396814US-GAAP:顧客集中度リスクメンバーアメリカ公認会計基準:売掛金メンバーPCRX:主な顧客3人のメンバー2021-01-012021-12-310001396814US-GAAP:顧客集中度リスクメンバーアメリカ公認会計基準:売掛金メンバーPCRX:主なお客様4名のメンバー2021-01-012021-12-310001396814米国-GAAP:累計純未現金投資GainLossMembers2019-12-310001396814米国-GAAP:累積換算調整メンバー2019-12-310001396814米国-GAAP:累計純未現金投資GainLossMembers2020-01-012020-12-310001396814米国-GAAP:累積換算調整メンバー2020-01-012020-12-310001396814米国-GAAP:累計純未現金投資GainLossMembers2020-12-310001396814米国-GAAP:累積換算調整メンバー2020-12-310001396814米国-GAAP:累計純未現金投資GainLossMembers2021-01-012021-12-310001396814米国-GAAP:累積換算調整メンバー2021-01-012021-12-310001396814米国-GAAP:累計純未現金投資GainLossMembers2021-12-310001396814米国-GAAP:累積換算調整メンバー2021-12-310001396814米国-GAAP:累計純未現金投資GainLossMembers2022-01-012022-12-310001396814米国-GAAP:累積換算調整メンバー2022-01-012022-12-310001396814米国-GAAP:累計純未現金投資GainLossMembers2022-12-310001396814米国-GAAP:累積換算調整メンバー2022-12-3100013968142021-06-012021-06-300001396814米国-公認会計基準:従業員株式オプションメンバー2022-01-012022-12-310001396814米国-GAAP:制限株式単位RSUメンバー2022-01-012022-12-3100013968142022-06-012022-06-300001396814PCRX:StockIncentivePlan 2011メンバー2022-12-310001396814PCRX:StockIncentivePlan 2011メンバー2022-01-012022-12-310001396814PCRX:入社計画2014年メンバー2022-12-310001396814PCRX:入社計画2014年メンバー2022-01-012022-12-310001396814PCRX:EmployeStockPurche ePlanEPSP 2014メンバー2022-12-310001396814PCRX:EmployeStockPurche ePlanEPSP 2014メンバー2022-01-012022-12-310001396814米国-GAAP:販売コストメンバー2022-01-012022-12-310001396814米国-GAAP:販売コストメンバー2021-01-012021-12-310001396814米国-GAAP:販売コストメンバー2020-01-012020-12-310001396814米国-公認会計基準:研究·開発費メンバー2022-01-012022-12-310001396814米国-公認会計基準:研究·開発費メンバー2021-01-012021-12-310001396814米国-公認会計基準:研究·開発費メンバー2020-01-012020-12-310001396814アメリカ-公認会計基準:販売一般と管理費用メンバー2022-01-012022-12-310001396814アメリカ-公認会計基準:販売一般と管理費用メンバー2021-01-012021-12-310001396814アメリカ-公認会計基準:販売一般と管理費用メンバー2020-01-012020-12-310001396814米国-公認会計基準:従業員株式オプションメンバー2021-01-012021-12-310001396814米国-公認会計基準:従業員株式オプションメンバー2020-01-012020-12-310001396814米国-GAAP:制限株式単位RSUメンバー2021-01-012021-12-310001396814米国-GAAP:制限株式単位RSUメンバー2020-01-012020-12-310001396814アメリカ公認会計基準:従業員ストックメンバー2022-01-012022-12-310001396814アメリカ公認会計基準:従業員ストックメンバー2021-01-012021-12-310001396814アメリカ公認会計基準:従業員ストックメンバー2020-01-012020-12-3100013968142019-01-012019-12-310001396814米国-公認会計基準:従業員株式オプションメンバー2022-12-310001396814米国-GAAP:制限株式単位RSUメンバー2019-12-310001396814米国-GAAP:制限株式単位RSUメンバー2020-12-310001396814米国-GAAP:制限株式単位RSUメンバー2021-12-310001396814米国-GAAP:制限株式単位RSUメンバー2022-12-310001396814SRT:最小メンバ数アメリカ公認会計基準:従業員ストックメンバー2022-01-012022-12-310001396814SRT:最大メンバ数アメリカ公認会計基準:従業員ストックメンバー2022-01-012022-12-310001396814SRT:最小メンバ数アメリカ公認会計基準:従業員ストックメンバー2021-01-012021-12-310001396814SRT:最大メンバ数アメリカ公認会計基準:従業員ストックメンバー2021-01-012021-12-310001396814SRT:最小メンバ数アメリカ公認会計基準:従業員ストックメンバー2020-01-012020-12-310001396814SRT:最大メンバ数アメリカ公認会計基準:従業員ストックメンバー2020-01-012020-12-310001396814PCRX:ConversionPremiumOn 2022注意メンバー2022-01-012022-12-310001396814PCRX:ConversionPremiumOn 2022注意メンバー2021-01-012021-12-310001396814PCRX:ConversionPremiumOn 2022注意メンバー2020-01-012020-12-310001396814米国-公認会計基準:従業員株式オプションメンバー2022-01-012022-12-310001396814米国-公認会計基準:従業員株式オプションメンバー2021-01-012021-12-310001396814米国-公認会計基準:従業員株式オプションメンバー2020-01-012020-12-310001396814アメリカ-GAAP:高齢者の注意事項メンバー2022-01-012022-12-310001396814アメリカ-GAAP:高齢者の注意事項メンバー2021-01-012021-12-310001396814アメリカ-GAAP:高齢者の注意事項メンバー2020-01-012020-12-310001396814米国-GAAP:制限株式単位RSUメンバー2022-01-012022-12-310001396814米国-GAAP:制限株式単位RSUメンバー2021-01-012021-12-310001396814米国-GAAP:制限株式単位RSUメンバー2020-01-012020-12-310001396814アメリカ公認会計基準:従業員ストックメンバー2022-01-012022-12-310001396814アメリカ公認会計基準:従業員ストックメンバー2021-01-012021-12-310001396814アメリカ公認会計基準:従業員ストックメンバー2020-01-012020-12-310001396814アメリカ-公認会計基準:会計基準更新202006年メンバーアメリカ-GAAP:高齢者の注意事項メンバー2022-01-012022-12-310001396814米国-GAAP:国内/地域メンバー2022-12-310001396814アメリカ-公認会計基準:研究メンバー米国-GAAP:国内/地域メンバー2022-12-310001396814アメリカ-公認会計基準:州と地方法律法規のメンバー2022-12-310001396814アメリカ-公認会計基準:研究メンバーアメリカ-公認会計基準:州と地方法律法規のメンバー2022-12-310001396814アメリカ-公認会計基準:外国人メンバー2022-12-310001396814米国-GAAP:国内/地域メンバーSRT:シーン予測メンバ2023-12-310001396814米国-GAAP:国内/地域メンバーSRT:シーン予測メンバ2024-12-310001396814米国-GAAP:国内/地域メンバーSRT:シーン予測メンバ2025-12-310001396814米国-GAAP:国内/地域メンバーSRT:シーン予測メンバ2028-12-310001396814米国-GAAP:国内/地域メンバーSRT:シーン予測メンバ2027-12-310001396814米国-公認会計基準:資本損失繰越メンバー2022-01-012022-12-310001396814PCRX:ForeignNetDeferredTaxAssetメンバー2022-01-012022-12-310001396814PCRX:RabbiTrustメンバー2022-01-012022-12-310001396814PCRX:RabbiTrustメンバー2021-01-012021-12-310001396814PCRX:AcquisitionRelatedFeesMembers2022-01-012022-12-310001396814PCRX:AcquisitionRelatedFeesMembers2021-01-012021-12-310001396814PCRX:AcquisitionRelatedFeesMembers2020-01-012020-12-310001396814米国-公認会計基準:その他の再構成メンバー2022-01-012022-12-310001396814米国-公認会計基準:その他の再構成メンバー2021-01-012021-12-310001396814米国-公認会計基準:その他の再構成メンバー2020-01-012020-12-310001396814PCRX:Flexion治療薬IncMember2020-01-012020-12-310001396814米国-GAAP:InProcessResearchAndDevelopmentMembers2022-01-012022-12-310001396814米国-GAAP:InProcessResearchAndDevelopmentMembers2021-01-012021-12-310001396814米国-GAAP:InProcessResearchAndDevelopmentMembers2020-01-012020-12-310001396814PCRX:ライセンス契約を終了するメンバー2022-01-012022-12-310001396814PCRX:ライセンス契約を終了するメンバー2021-01-012021-12-310001396814PCRX:ライセンス契約を終了するメンバー2020-01-012020-12-310001396814PCRX:NuanceBiotechCo.Ltd.メンバー2022-01-012022-12-310001396814PCRX:NuanceBiotechCo.Ltd.メンバー2021-01-012021-12-310001396814PCRX:NuanceBiotechCo.Ltd.メンバー2020-01-012020-12-310001396814PCRX:DepoCyteMember2022-01-012022-12-310001396814PCRX:DepoCyteMember2021-01-012021-12-310001396814PCRX:DepoCyteMember2020-01-012020-12-310001396814PCRX:Flexion AcquisitionMemberPCRX:LegalFeesメンバー2022-01-012022-12-310001396814PCRX:Flexion AcquisitionMemberPCRX:LegalFeesメンバー2021-01-012021-12-310001396814PCRX:Flexion AcquisitionMember2021-11-192021-11-190001396814PCRX:Flexion AcquisitionMember2021-01-012021-12-310001396814PCRX:NuanceBiotechCo.Ltd.メンバー2021-01-012021-12-310001396814PCRX:DepoCyteMember2019-11-012019-11-300001396814PCRX:DepoCyteMember2020-01-012020-12-310001396814PCRX:EUの研究室のメンバー2021-06-012021-06-300001396814PCRX:発展成果とビジネスマイルストーンのメンバーPCRX:EUの研究室のメンバー2021-01-012021-12-310001396814PCRX:DePuySyntheSalesIncMemberPCRX:協同推進プロトコルのメンバー2020-01-012020-12-310001396814PCRX:Aratana治療IncMembersPCRX:発展成果とビジネスマイルストーンのメンバー2012-12-310001396814PCRX:Aratana治療IncMembers2022-01-012022-12-310001396814PCRX:FortisMember2020-10-012020-10-310001396814アメリカ-GAAP:サービスメンバー2022-12-310001396814米国-GAAP:公共施設在庫未加工材料メンバー2022-12-310001396814PCRX:マーケティングスポンジ製品会員アメリカ公認会計基準:副次的事件メンバー2023-01-010001396814PCRX:香港医薬テノール有限会社会員2020-01-012020-12-310001396814PCRX:香港医薬テノール有限会社会員PCRX:発展成果とビジネスマイルストーンのメンバー2022-12-310001396814PCRX:香港医薬テノール有限会社会員PCRX:発展成果とビジネスマイルストーンのメンバーアメリカ公認会計基準:副次的事件メンバー2023-01-310001396814PCRX:発展成果と規制マイルストーンのメンバーPCRX:Flexion治療薬IncMemberPCRX:GeneQuineMember2017-02-280001396814PCRX:発展成果と規制マイルストーンのメンバーPCRX:Flexion治療薬IncMemberPCRX:GeneQuineMember2017-02-012017-02-28
アメリカです
アメリカ証券取引委員会
ワシントンD.C.,20549
表10-K
| | | | | |
| (マーク1) | |
| ☒ | 1934年証券取引法第13条又は15条に基づいて提出された年次報告 |
本財政年度まで:十二月三十一日, 2022
あるいは…。 | | | | | |
| ☐ | 1934年証券取引法第13条又は15条に基づいて提出された移行報告 |
そこからの過渡期について
依頼書類番号:001-35060
Pacira生物科学社は
(登録者の正確な氏名はその定款に記載)
| | | | | |
| デラウェア州 | 51-0619477 |
(明またはその他の司法管轄権
会社や組織) | (税務署の雇用主
識別番号) |
| |
| ケネディ通り西五四零一号室、八九零号室 |
| タンパ、 | フロリダ州 |
| 33609 |
| (主要行政事務室の住所と郵便番号) |
| |
| (813) | 553-6680 |
| (登録者の電話番号、市外局番を含む) |
同法第12条(B)に基づいて登録された証券: | | | | | | | | | | | | | | |
| クラスごとのタイトル | | 取引記号 | | 各取引所名
それに登録されている |
| 普通株は一株当たり0.001ドルの価値があります | | PCRX | | ナスダック世界ベスト市場 |
同法第12条(G)に基づいて登録された証券:ありません
登録者が証券法規則405で定義されている経験豊富な発行者である場合は、再選択マークで示してくださいはい、そうです x No o
登録者がこの法第13節または第15節(D)節に基づいて報告を提出する必要がないかどうかを再選択マークで示す。はい、そうですo 違います。 x
再選択マークは、登録者が(1)過去12ヶ月以内(または登録者がそのような報告の提出を要求されたより短い期間)に、1934年の証券取引法第13または15(D)節に提出されたすべての報告書を提出したかどうか、および(2)過去90日以内にそのような提出要件に適合しているかどうかを示すはい、そうです x No o
再選択マークは、登録者が過去12ヶ月以内(または登録者がそのような文書の提出を要求されたより短い時間以内)に、S−T規則405条(本章232.405節)に従って提出を要求した各相互作用データファイルを電子的に提出したか否かを示すはい、そうです x No o
登録者が大型加速申告会社,加速申告会社,非加速申告会社,小さな報告会社,あるいは新興成長型会社であることを再選択マークで示す。取引法第12 b-2条の規則における“大型加速申告会社”、“加速申告会社”、“小申告会社”、“新興成長型会社”の定義を参照されたい。
| | | | | | | | | | | |
| 大型加速ファイルサーバ | ☒ | ファイルマネージャを加速する | ☐ |
| 非加速ファイルサーバ | ☐ | 規模の小さい報告会社 | ☐ |
| | 新興成長型会社 | ☐ |
新興成長型企業である場合は、登録者が延長された移行期間を使用しないことを選択したか否かを再選択マークで示し、取引所法案第13(A)節に規定する任意の新たな又は改正された財務会計基準を遵守するo
登録者が報告書を提出したかどうかを再選択マークで示し、その経営陣が“サバンズ-オクスリ法案”(“米国連邦法典”第15編、第7262(B)節)第404(B)条に基づいてその財務報告の内部統制の有効性を評価したことを証明する。この評価は、その監査報告書を作成または発行する公認会計士事務所によって行われる。はい、そうですx No o
証券が同法第12条(B)に基づいて登録されている場合は,登録者の財務諸表が以前に発表された財務諸表の誤り訂正を反映しているか否かを示すチェックマークを適用するo
これらのエラーのより真ん中に再記述があるかどうかをチェックマークで示すには、登録者の任意の実行幹事が関連回復中に受信した報酬ベースの補償を2240.10 D-1(B)節に従って回復分析する必要があるo
登録者が空殻会社であるか否かをチェックマークで示す(取引法第12 b-2条で定義されている)。はい、そうです☐ No x
ナスダック世界選りすぐり市場2022年6月30日に報告された普通株終値によると、登録者の非関連会社が保有する登録者議決権株の総時価は1株約58.3ドルで、登録者が最近完成した第2四半期の最終取引日となる1.9十億ドルです。各取締役幹部(及びその関連会社)及び発行された普通株の10%以上又は登録者が支配的な個人が保有する普通株は除外されたと考える。他の目的に対して,このような関連地位の決定は必ずしも決定的な決定であるとは限らない.
2023年2月24日まで45,952,450登録者の普通株式は1株当たり0.001ドルで発行された。
引用で編入された書類
この10-K表年次報告の第3部は、登録者が2023年株主総会に提出する委託書のいくつかの情報を引用しており、この依頼書は、登録者が2022年12月31日までの財政年度終了後120日以内に証券取引委員会に提出される。
リスク要因の概要
本リスク要因の要約は、当社の業務、財務状況、運営結果、または将来性に最も重要なリスクを含みます。本要約に記載されているリスクおよび以下に記載されていないリスクの包括的な議論を参照第I部,第1 A項リスク要因本年度報告で。
·私たちの成功は、主にExPARELを商業化する能力にかかっている®(ブピバカインリポソーム注射用懸濁液)およびジレッタ® (トリアムシノロンアセトニド徐放性注射用懸濁剤)。
·EXPARELおよびZILRETTAの商業化に成功した我々の努力は、多くの内部および外部課題に直面している。
·合理的な価格設定条項で提供された製品を実現し、十分な第三者支払者のカバーおよび補償レベルを維持できない場合、私たちの製品の商業的成功は深刻に阻害される可能性があります。
·他の製薬、医療機器、バイオテクノロジー会社からの激しい競争に直面しています
·任意の承認された製品の規制承認は、その臨床的安全性および有効性が証明された特定の適応および条件、およびそのような承認適応を遵守できなかった疑いに関連するリスクに限定される。
·効果的なマーケティングおよび販売能力を確立し、維持することができない場合、または第三者と合意して製品をマーケティングおよび販売することができない場合。
·EXPAREL、ZILRETTA、ioveraの多くの基本サービスをサードパーティに提供することに依存しています®そして私たちが商業化している他のどんな製品も第三者の事実に依存するだろう
·私たちの組織の規模を拡大し、販売チームを効率的に管理する必要があるかもしれません。この成長を管理することは困難になるかもしれません。
·キーパーソンを引き付けることができなければ、効率的に業務を管理することができません。
·私たちが直面する可能性のある潜在的な製品責任が開放されています。
·私たちは十分な数量、許容可能な品質、価格レベルで私たちの製品を生産することができなかったか、CGMPを完全に守ることができませんでした(以下のように定義します)。
·当社の製造業務を拡大するか、第三者にアウトソーシングする必要がある場合があります。
·十分な数の製品を生産し続けることができません。
·Thermo Fisherとの共同制作や他のプロトコル(以下のように定義)は、予期せぬ費用や遅延に及ぶ可能性があります。
·EXPAREL、ZILRETTA、iOVERA°の生産に必要な特定の原材料および装置をサードパーティにタイムリーに提供することに依存します。
·私たちの将来の成長は、製品を識別、開発、取得、許可する能力にある程度依存します。
·私たちは研究開発に大量の投資を行いましたが、これらの投資が成功しなければ、私たちの業務、財務状況、運営結果に実質的な悪影響を及ぼす可能性があります。
·私たちの業務では危険材料を使用しており、環境法律や法規を守らなければなりません。
·システム障害のリスク。
·私たちが将来達成する可能性のあるどんな協力計画も成功しないかもしれない。
·私たちの試験の費用、持続時間、および不確実な結果、私たちの試験が私たちの医薬製品または医療機器の安全性および有効性を証明できなかった場合、規制部門の承認を阻止または著しく遅らせる可能性があります。
·私たちは、契約研究機関、臨床研究者、および臨床サイトに依存して患者を募集し、他の第三者に依存して試験を管理し、関連データ収集および分析を実行することもあります。
·様々な組織が発表したガイドラインや提案は、当社の製品への需要や使用を減らす可能性があります。
·時間およびリソースの損失または意外な損失をもたらす可能性がある定期訴訟
·規制または法執行機関が、私たちが私たちの製品の“ラベル外”の使用を推進または過去に促進していると判断した場合。
·私たちは、規制部門の任意の候補製品の承認を得ることができない場合がありますし、彼らの承認は様々な理由で延期される可能性があります。
·承認プロセスを規制し、これは、重大な遅延、意外または追加コスト、および他の予見不可能な要因、および私たちが商業化できる製品のタイプおよび用途の制限をもたらす可能性があります。
·規制当局は、当社の製品または任意の候補製品に副作用があると認定する可能性があります。
·医療業務に関連する連邦、州、外国の法律法規を守らなければ、重大な処罰に直面する可能性があります。
·当社の製品の設計、開発、製造、供給、流通は高度に規制されており、技術が複雑です。
·私たちと私たちの製品が受ける幅広い規制要件を守ることができませんでした。
Pacira生物科学社は| 2022 Form 10-K |1ページ
·政府または第三者支払者がEXPAREL、ZILRETTA、iOVERA、または任意の将来の製品に十分な保険および支払いレートを提供できない場合、または病院またはASC(以下で定義する)の場合、より安価な代替療法の使用を選択する。
·EXPARELやZILRETTAなどの医薬品やiovera°などの医療機器製品の安全性を懸念している。
·当社のpMVL(以下に定義する)製品をカバーする特許および特許出願は、当社のpMVL薬物送達技術に含まれる薬物の特定の注射製剤、プロセスおよび使用に限定され、私たちの候補製品の市場機会は、活性成分自体および競合他社が開発する可能性のある他の処方および送達技術およびシステムの特許保護の欠如によって制限される可能性がある。
·我々の特許および特許出願は、主に冷媒で冷却された特定の手持ち式低温針装置と、これらの低温装置を用いて神経組織を凍結治療する方法に限定されている
·私たちの専有権が保護され、すべての特許が最終的に満期になることを保証することはできません。
·第三者の知的財産権侵害で起訴されたら。
·私たちの従業員が元雇用主のいわゆる商業機密を誤って使用または開示したと告発される可能性があります。
·私たちの債務を返済するには大量の現金が必要ですが、私たちの業務には巨額の債務を支払うのに十分なキャッシュフローがないかもしれません。
·私たちのクレジットプロトコルおよびIndentures(それぞれ以下に定義されています)は、私たちおよびいくつかの子会社に重大な運営および財務的制限を加えており、ビジネスチャンスの利用を阻止する可能性があります
·必要な資金を調達し、債券の転換を現金で決済する能力がないかもしれません(後述)、または根本的な変化が発生した場合に債券を買い戻すことができますが、将来の債務は、債券を変換する際に現金を支払う能力を制限したり、債券を買い戻す能力を制限したりすることができます。
·私たちの債務は、当社の業務、財務状況、および経営結果、および当社の信用協定および手形に基づいて支払い義務を履行する能力に悪影響を及ぼす可能性があります。
·現在の負債水準は高いにもかかわらず、より多くの債務のリスクを負う可能性がある。
·当社の定款書類やデラウェア州法律の条項は逆買収効果をもたらす可能性があり、買収が株主に有利であっても、買収が当社の株主に有利になることを阻止し、現在の経営陣を交換または更迭しようとすることを阻止する可能性があります。
·私たち普通株の価格は大きな変動や変動の影響を受ける可能性があります。
·予測可能な未来に普通株に配当金を支払わないつもりです。
·将来的に公開市場で私たちの普通株を販売または発行することは、私たちの普通株の市場価格を下げる可能性があります。
·証券を発行することでより多くの資金を調達することは、既存の株主に希釈され、貸借および許可手配による資金調達は、私たちの業務を制限したり、所有権を放棄することを要求する可能性があります。
·伝染病の大流行、流行または爆発(例えば、新冠肺炎の大流行、またはこのような事件に対する恐怖)。
·個人およびビジネス情報のプライバシーやセキュリティを維持できませんでした。
·上昇するインフレは、材料、労働力、サービスなどに関するコストを増加させる。
·環境、社会、企業統治問題に関するリスクに直面する可能性があります。
·私たちが設立以来受けた大きな損失と、将来的にはより多くの損失を受ける可能性があります。
·営業権または無形資産の帳簿価値の重大な減価は、当社の運営結果や財務状況に悪影響を及ぼす可能性があります。
·追加資金が必要かもしれませんが、必要なときに資金を集めることができないかもしれません。これは、製品開発計画や商業化努力を延期、減少、またはキャンセルさせることになります。
·当社の四半期運営実績の潜在的な大幅な変動。
·買収された会社と企業の業務や人員の統合に成功できず、期待される相乗効果やこのような買収のメリットを実現することができません。
·我々は、ZILRETTAのビジネス成功と、PaciraとFlexionのトラフィックをタイムリーかつ効率的に統合することによって節約されるコストに大きく依存するFlexion買収の利点を達成することができない(以下のように定義する)。
·私どもの純営業損失繰越と研究開発税収控除の使用が制限されています。
·データプライバシーと法律法規の変化、特にヨーロッパとカリフォルニア州。
·サイバーセキュリティの脅威や事件に関するリスク。
·世界的な気候、極端な天気条件、水資源供給が大きく変化している。
·私たちの国際業務は、多くの、時に衝突する法律と規制要件に直面しています。
Pacira生物科学社は| 2022 Form 10-K |2ページ目
Pacira生物科学社は
表格10-Kの年報
2022年12月31日までの年度
カタログ | | | | | | | | |
| | | ページ番号 |
リスク要因の概要 | 1 |
カタログ表 | 3 |
前向き陳述に関する注意事項 | 4 |
| | |
第1部 | | 5 |
第1項。 | 業務.業務 | 5 |
第1 A項。 | リスク要因 | 35 |
項目1 B。 | 未解決従業員意見 | 68 |
第二項です。 | 属性 | 68 |
第三項です。 | 法律訴訟 | 68 |
第四項です。 | 炭鉱安全情報開示 | 68 |
| | |
第II部 | | 69 |
五番目です。 | 登録者普通株市場、関連株主事項及び発行者による株式証券の購入 | 69 |
第六項です。 | 保留されている | 70 |
第七項。 | 経営陣の財務状況と経営成果の検討と分析 | 70 |
第七A項。 | 市場リスクの定量的·定性的開示について | 81 |
第八項です。 | 財務諸表と補足データ | 81 |
第九項です。 | 会計と財務情報開示の変更と相違 | 81 |
第9条。 | 制御とプログラム | 81 |
プロジェクト9 B。 | その他の情報 | 82 |
プロジェクト9 Cです。 | 検査妨害に関する外国司法管区の開示 | 82 |
| | |
第三部 | | 82 |
第10項。 | 役員·幹部と会社の管理 | 82 |
第十一項。 | 役員報酬 | 82 |
第十二項。 | 特定の実益所有者の担保所有権及び経営陣及び関連株主の事項 | 82 |
十三項。 | 特定の関係や関連取引、取締役の独立性 | 82 |
14項です。 | チーフ会計士費用とサービス | 82 |
| | |
第4部 | | 83 |
第十五項。 | 展示·財務諸表明細書 | 83 |
第十六項。 | 表格10-Kの概要 | 86 |
Pacira BioSciences,Inc.|2022 Form 10-K|3ページ目
前向き陳述に関する注意事項
本Form 10-K年次報告(“年次報告”)および我々が行った他のいくつかの通信には、1934年証券取引法(“取引法”)第21 E節(“取引法”)および1995年個人証券訴訟改革法の意味に適合する展望的な陳述が含まれているが、これらに限定されない:柔軟な買収(以下のように定義される)とそのコストと収益、私たちの成長と将来の経営結果と傾向、私たちの戦略、計画、目標、予想(財務またはその他)と意図、将来の財務結果および成長潜在力。債務返済に関する私たちの計画、予想される製品の組み合わせ、開発計画、特許条項、製品開発、戦略連盟、知的財産権を含む。この目的のために、歴史的事実ではないいかなる陳述も前向きな陳述とみなされなければならない。私たちは、前向き陳述の識別を助けるために、“信じる”、“予想”、“計画”、“推定”、“予想”、“予定”、“可能”および同様の表現をよく使用する。私たちはあなたに私たちの推定、仮定、そして予想が正しいことが証明されるということを保証できません。様々な重要な要素のため、実際の結果は展望性陳述によって示された結果と大きく異なる可能性があり、これらの要素は、業務が成功的に統合できないリスクのような買収に関連するリスクを含み、このような統合は予想よりも困難で、より時間的または高価である可能性があり、または取引の予想利益は起こらないかもしれない;Flexion(以下のように定義される)およびその製品の将来の機会および計画に関連するリスク, Flexionおよびその製品の予想財務パフォーマンスの不確実性を含む;もし私たちが財務アナリストや投資家が期待しているように、財務アナリストまたは投資家が予想している程度にFlexion買収の予想利益を達成しなければ、私たちの普通株の市場価格は下落する可能性がある;選択的手術、私たちの製造とサプライチェーン、世界とアメリカまたはアメリカ、経済状況(インフレと金利上昇を含む)および私たちの業務は、私たちの収入、財務状況、キャッシュフロー、運営結果の影響を含む。EXPARELの商業化を支援する販売と製造努力に成功しました®(ブピバカインリポソーム注射用懸濁液)、ZILRETTA®(トリアムシノロンアセトニド徐放性注射用懸濁剤)およびiovera®EXPAREL、ZIERRETTAおよびIOVERA°の市場受容率と程度;EXPAREL、ZIERA°の潜在的市場の規模と成長、およびこれらの市場にサービスを提供する能力;EXPAREL、ZILRETTAおよびIOVERA°をより多くの適応と機会に拡大し、EXPAREL、ZIERA°の任意の関連臨床試験のタイミングと成功、EXPAREL、ZIERRETTAおよびIOVERA°のビジネス成功;米国食品·薬物管理局、FDA、新薬補充申請と前通知に関する成功タイミング;私たちが考えている問題は、ヨーロッパ医薬品局(EMA)、マーケティング許可申請(MAA)の関連タイミングと成功、私たちの特許多カプセルリポソーム(PMVL)薬物送達技術を利用して、より多くの候補製品の計画を評価、開発、追求すること、私たちの製品の他の管轄区域での商業化承認、既存または潜在的なpMVLベースの製品の臨床試験を支持すること、私たちの商業化とマーケティング能力、カリフォルニア州サンディエゴにおけるEXPARELの生産能力拡張プロジェクトの能力、イギリスのスウィンデンでZILRETTA資本プロジェクトを成功させる能力、任意の訴訟の結果、Flexionまたは任意の未来の買収を既存のビジネスに統合する能力に成功したこと、私たちの繰延税金資産の回収可能性;または対価格支払いに関する仮定;および第1部分である第1 A項で議論された要因リスク要因.
本年度報告書に含まれる前向き陳述は、本年度報告の提出日までの私たちの観点を代表します。重要な要素は、私たちの実際の結果が展望性陳述で表明または示唆した結果と大きく異なる可能性があるため、後続の事件と発展は私たちの観点を変化させることが予想される。法律の適用に別の要求がある以外に、私たちは新しい情報、未来の事件、または他の理由でいかなる前向きな陳述を更新または修正することを意図しているか、または修正する義務があり、読者は展望的な陳述を本年度の報告書の提出日以降の任意の日付が私たちの観点を代表すると見なしてはならない。
これらの前向き陳述は既知および未知のリスク、不確定性および他の要素に関連し、私たちの実際の結果、活動レベル、業績または成果はこれらの陳述と明示的または暗示的なものとは大きく異なる可能性がある。これらの要素は、項目1 Aで議論され言及された事項の第1の部分を含むリスク要因.
Pacira BioSciences,Inc.|2022 Form 10-K|4ページ
第1部
プロジェクト1.ビジネス
参考文献
Pacira BioSciences,Inc.はデラウェア州会社であり,我々カリフォルニアの運営子会社Pacira PharmPharmticals,Inc.のホールディングスである.2007年3月,SkyePharma Holdings,Inc.(現在Vectura Group plcの子会社)やSkyePharmma(yeSkPharma買収)からPacira PharmPharmticals,Inc.を買収した.2019年4月には、民間医療技術会社MyoScience,Inc.(“MyoScience買収”)を買収し、2021年11月には、上場バイオ製薬会社Flexion Treateutics,Inc.またはFlexion(“Flexion買収”)を買収した。文意に加えて、本年度報告で言及されている“Pacira”、“私たち”、“会社”、“私たち”、“私たち”は、Pacira生物科学会社、デラウェア州の会社とその子会社を意味する。
企業情報
我々は2006年12月にデラウェア州に設立され、名称は青色買収会社であり、2007年6月にPacira,Inc.と改名した。2010年10月、私たちはPacira PharmPharmticals,Inc.,2019年4月、私たちはPacira BioSciences,Inc.と改名しました。私たちの主な実行オフィスと会社の本社はフロリダ州タンパ市にあります。
商標とサービスマーク
パッシラ®ExPAREL®、ZILRETTA®Iovera°®PACIRAロゴおよびPACIRAが本年度報告に登場する他の商標またはサービスマークは、PACIRAの財産であり、本報告の各部分で初めて使用される場合には、記号を含むようにしてください。
本年度報告書には、他社の他の商号、商標、サービスマークが含まれており、これらの名称は、または記号を持っている場合もあれば、ない可能性もある。これらの標識がないことは、それぞれの全員が適用法に基づいてそのような商標に対する権利を最大限に主張しないことを意味するわけではない。私たちは、他の会社の商標または商号を使用して、これらの会社またはこれらの会社といかなる裏書き、賛助、または他の関係を構築することを示唆してはならない。
概要
著者らは,非オピオイドの疼痛管理に取り組み,可能な限り多くの患者に非オピオイド選択を提供する上で業界トップにあり,オピオイドが救急療法としての役割のみを再定義した。著者らはまた、心電嵐、慢性疼痛と痙攣などの交感神経系の衰弱状況に対応するための革新的な干与措置を開発している。著者らは一連の独特、安全、同類の最も良い製品を推進しており、各種の治療領域をカバーしており、急性手術後の痛み、急性と慢性骨関節炎、痛み、痙攣と星状神経節ブロックを含む。3つの商業的な非オピオイドがありますExPAREL®術後疼痛治療のために現在承認されている長時間作用性局所鎮痛剤;ZILRETTA;®(トリアムシノロンアセトニド徐放性注射懸濁剤)、徐放性、関節内またはIA(関節内を指す)、膝関節炎疼痛の治療のためのコルチコステロイド注射;®正確で制御可能な用量の冷温度を使用して、標的神経の即時、長時間効果、薬物のない疼痛制御を行う新規な手持ち式装置である。
戦略.戦略
我々が非オピオイド疼痛管理と再生健康解決策の面で世界的にリードしている目標を実現するために、私たちは三つの戦略を進めている
•私たちがオピオイドを含まない商業資産の使用を拡大する。COVIDの大流行とオピオイド類薬物危機はオピオイド類薬物代替品に対する需要を悪化させた。米国では、EXPARELは、局所または局所手術後の鎮痛を産生するために浸透、野ブロック、および角間腕神経叢ブロックのために許可されている唯一のオピオイドを含まない長時間作用性局所および領域鎮痛剤である。米国では、EXPARELは6歳以上の小児科患者への浸透も許可されている。ヨーロッパでは、EXPARELは腕神経叢ブロックや大腿神経ブロックとして承認され、成人手術後の痛みの治療や、6歳以上の成人や小児の術後中小傷による身体痛の治療に用いられている。EXPARELの長時間作用域と神経ブロックを用いた麻酔駆動の術後疼痛管理は,複雑で苦痛な手術を外来看護地に移行させることができる。ZILRETTAは第一種であり、唯一の徐放関節内療法であり、三ケ月以内に主に骨性関節炎の膝関節痛を緩和することができ、そしてヒアルロン酸(HA)と多血小板血漿(PRP)、注射或いはその他の早期介入治療の代替品になる可能性がある。Iovera°システムを使って
Pacira BioSciences,Inc.|2022 Form 10-K|5ページ
医療保健提供者は1種の革新的な無薬物神経ブロックを用いて麻酔と高周波アブレーションを代替することができる。Iovera°システムもZILRETTAの高度補完であると考えられる。私たちの現在のビジネス機会に加えて、私たちはラベル拡張活動を推進している。EXPARELでは,最近われわれのラベルを拡張し,陽窩の坐骨神経ブロックおよび内転筋管の大腿神経ブロックを含め,FDAは2023年下半期に“処方薬使用者費用法案”(PDUFA)に基づいて行動する予定であるsNDAを提出した。6歳以下の患者に対するEXPAREL臨床開発計画も進めている。ZILRETTAについては,肩関節骨関節炎の3期研究と2型糖尿病の4期研究を開始する予定である。Iovera°では,慢性下腰痛や脊柱手術に用いられる新たなiovera°Smart Tipsを開発している。けいれんを治療する方法としてiovera°の登録研究を開始する予定である。
•私たちの臨床段階のパイプラインは、満たされていない多くの需要分野で進められている。我々はすでにPCRX-201の一期研究を完成し、PCRX-201は新しいIA遺伝子治療候補製品であり、膝骨性関節炎疼痛の治療に使用する抗炎症性タンパク質インターロイキン1受容体アンタゴニスト(IL-1 ra)を産生することができる。納得できるPCRX-201第一段階の治療効果と安全性データに基づいて、著者らは調査者と協力し、FDAに会議を開催し、膝蓋骨関節炎の将来の制御経路、及び再生医学高度療法(RMAT)の指定を討論することを計画している。私たちはまた、私たちの独自の多嚢胞リポソーム(PMVL)技術を利用した私たちの臨床段階資産パイプラインを推進している。PMVL担体基質は微小な球状脂質基粒子からなり,これらの粒子は多くの非同心の内部水腔からなるハニカムからなり,内部水腔内には被覆された活性物質が含まれている。各チャンバは、隣接するチャンバから脂質膜によって分離されている。注射後,脂質膜の侵食や組換えに伴い,pMVL粒子は比較的長い時間で活性物質を放出した。われわれは,デキサメタゾン−pMVLによる下腰痛治療の第1段階研究(“PCRX−401”),高用量ブピバカイン−pMVLを5日間以上持続させる鎮痛の第1段階研究(“PCRX−501”),および髄腔内鎮痛のためのExPARELの第1段階研究を開始しようとしている。
•戦略投資、内部許可または買収を組み合わせた方法で相互補完性革新資産を獲得する。ExPAREL,ZILRETTA,iovera°とわれわれのpMVL薬物送達技術はオピオイド流行に対応するために堅固な基礎を提供していると信じている。これらの固有資産に基づいて,筋骨格や慢性疼痛の分野にも投資した。我々は,膝と脊柱の連続ケアと慢性疼痛に重点を置いたこの2つの重要な領域を進めていく予定である。私たちは一連の戦略投資を使用して、将来性の高い早期プラットフォームを支持し、内部許可或いは買収取引を使用して、神経痛経路における患者の旅を改善するための革新的なパイプを構築している。
オピオイドの流行
オピオイド依存症は米国で流行しており,米国疾病コントロール·予防センター(CDC)は,2022年3月までの12カ月間に10.7万人を超える米国人が薬物過剰で死亡したと報告しており,2年前に報告された統計データより44%に躍進している。報告されているすべての薬物過剰死のうち,3分の2以上がオピオイドに関与しており,その中で合成オピオイドが死亡者数増加の主な駆動因子である。
2018年,新たな研究によると,肩袖修復や股関節置換から膝置換やカフ胃切除術など4種類のよく見られる手術の痛みの緩和に役立つオピオイド100~200粒近くを受けていることが示された。そのほか、整形外科手術患者の4分の1は毎日90 mg或いはそれ以上のモルヒネに相当するオピオイドが処方され、疾病管理センターはこれらの投与量はこのように大きく、患者は服薬過剰の高リスクに直面している。2017年の報告によると,検査を受けた7種類の整形外科や軟部組織手術では,患者1人当たり平均82オピオイドを処方し,術後疼痛のコントロールを支援している。手術患者の9%近くが2017年に新たな持続使用者となり,術後少なくとも3~6カ月間これらのオピオイドを服用し続けていることが明らかになった。膝関節置換術や結腸切除術を受けた患者では,新たにオピオイドを持続投与した患者はそれぞれ15%と17%上昇した。また,女性がオピオイドを持続的に使用する可能性は男性より40%高く,オピオイドを継続的に使用している人では,女性が男性より15%多く処方されている。これらの発見は報告から来ています米国の非依存性:オピオイド過剰処方の米国における影響分析2016年に裁決された医療·薬局のクレームデータの分析に基づくQuintilesIMS。
LPGAスポンサー
2023年2月には,女子プロゴルフ協会(LPGA)と長年の協賛関係を構築し,iovera°をLPGAの公式非オピオイド疼痛管理パートナーとすることを発表した。協賛の目的は、非オピオイド疼痛管理選択が米国オピオイドの流行を抑制する上で発揮する作用に対する関心を引き起こすことである。著者らは様々なLPGA選手権で活動を開催し、非オピオイド介入措置の有用性に対する認識と教育を高め、ファンに毎年9月に紫色の服を着ることを奨励し、この月はオピオイド意識月と公認されている。
Pacira BioSciences,Inc.|2022 Form 10-K|6ページ
製品の組み合わせと候補製品ルート
次の表は、現在の製品の組み合わせと候補製品ライン、および今後12~18ヶ月の予想マイルストーンをまとめています
Pacira BioSciences,Inc.|2022 Form 10-K|7ページ
私たちの商業製品は
ブピバカインリポソーム注射懸濁剤
EXPARELは2011年10月にFDAの承認を得、2012年4月に米国で商業化された。米国では,EXPARELは現在6歳以上の患者で単回浸透に用いられて術後局所鎮痛を産生し,成人では間角間腕神経叢神経ブロックに術後局所鎮痛に用いられている。他の神経ブロックの安全性と有効性は確立されていない。2020年11月、欧州委員会(EC)はEXPARELを腕神経叢遮断薬或いは大腿神経遮断薬として成人手術後の疼痛の治療に応用し、成人と6歳以上の児童の手術後の中小傷口の身体疼痛の治療に野戦遮断薬として使用することを許可した。私たちはイギリスでEXPARELを発売し、2021年11月にEUまたはEU諸国を選択した。2011年に初めて承認されて以来,1200万人を超える患者がEXPARELの治療を受けている。
EXPARELはブピバカインからなり,アミド系局所麻酔薬であり,われわれのpMVL投与技術に封入し,時間の経過とともにブピバカインを提供して鎮痛時間を延長する。EXPARELは安全かつ有効な長時間作用非オピオイド術後鎮痛剤に対する重大な医学的需要を満たし,オピオイド最小化戦略に重要な役割を果たしていると考えられる。ExPARELは回復のために設計されており、オピオイドの使用が最も少なく、方法は:(I)手術部位に的確な局所鎮痛を提供する;(Ii)時間の経過に従ってブピバカインを確実に放出して鎮痛時間を延長する;(Iii)回復を阻害する可能性のあるカテーテルとポンプの需要を除去する;および(Iv)長期的な鎮痛を提供し、同時にオピオイドに対する需要を減少させる。
私たちの2022年のEXPARELの製品純売上高は5.369億ドルです。ExPARELの製品純売上高は,2022年,2021年,2020年12月31日までの年間で,それぞれ総収入の81%,94%,96%を占めている。2022年百分率の大きな変化は、2021年11月にFlexion買収を完了した後、ZILRETTA製品の純売上高の年間年間を確認したためである。
トリアムシノロンアセトニド徐放注射懸濁剤
ZILRETTAは2017年10月にFDAの承認を得て、まもなく米国で発売された。ZILRETTAは第一種であり,骨性関節炎膝関節痛患者に対する徐放関節内療法でもある。ZILRETTAは特許の徐放マイクロスフェア技術を用いて、トリアムシノロンアセトニド(TAと略称する)を徐々に持続的に膝部に放出し、約3ケ月持続し、これはよく使われ、直ちに放出されるコルチコステロイドであり、12週間以内に痛みを著しく緩和することができ、一部の患者の痛み緩和は16週間持続可能である。
2021年11月のFlexion買収の完了に伴い、ZILRETTAを私たちのビジネス製品に追加します。ZILRETTAの製品純売上高は12月31日までの1年間で1.055億ドル2022それは.2021年、ZILRETTAの製品純売上高は1270万ドルであることを確認しました2021年11月19日から2021年12月31日までのFlexion買収の終了後期限。
♪the the the Ioveraシステム
Iovera°システムは、標的神経に正確な制御用量の寒冷温度を生成するための、FDAによって承認された非オピオイド手持ち式凍結鎮痛装置である。米国でFDA 510(K)認証を受け,EUでCEマーカーを取得し,カナダでの疼痛遮断のための発売が許可されている。IOVERA°系は非オピオイドとしてEXPARELとZILRETTAの高度補充であり,非薬物神経ブロックを用いて損傷や手術部位から脳に伝達される疼痛信号を遮断し,痛みを軽減する。90日間にわたる膝関節炎に関連する痛みや症状を緩和するためにも使用されている。2022年、2021年、2020年12月31日までのiovera°製品の純売上高はそれぞれ1,530万ドル、1,620万ドル、880万ドルです。
ExPAREL臨床的メリット
EXPARELは弾性ポンプを介して輸送されるブピバカインに代わることができ,長時間作用術後疼痛治療のマルチモードレジメンの基礎となると信じられている。我々の臨床データに基づいてEXPAREL:
•持続的な局所的または局所的な鎮痛を提供します
•出来合いのレシピです
•必要な体積を達成するために生理食塩水や乳酸リンガー溶液と容易に膨張した
Pacira BioSciences,Inc.|2022 Form 10-K|8ページ
•既存の角間腕神経叢ブロック、野ブロックと浸透投与技術を利用した
•様々な手術部位の治療を促進する。
EXPARELはオピオイドの需要を減少する長期効果術後疼痛治療方案の重要な構成部分であると考えられる。われわれの3期と4期の臨床研究の臨床データおよび遡及性健康結果研究のデータに基づき,EXPARELはオピオイドの使用を有意に減少させるとともに,術後疼痛管理を改善した。
3期内痔切除術試験ではEXPAREL:
•EXPAREL治療を受けた患者の鎮痛剤(オピオイド)の回復時間を15時間に延期し、プラセボ治療を受けた患者を1時間に延期した
•術後72時間以内にオピオイド救急薬を必要としない患者の割合は28%に有意に増加したが、プラセボ群は10%であった
•術後72時間のオピオイド使用量はプラセボと比較して45%減少した
•プラセボと比較して術後24時間無痛患者の割合が増加した。
われわれの3期試験では,上肢手術としての角間腕神経叢ブロック,EXPAREL:
•オピオイド総消費量78%減少(p
•プラセボと比較して疼痛スコアは46%低下した(p
•EXPARELを受けることを許可した患者の13%が術後48時間以内に無オピオイドを維持した(p
われわれの第3段階試験では,全膝関節置換術(TKA)を受けた患者では,内転筋管の大腿神経ブロックとしてEXPAREL:
•塩酸ブピバカインと比較して術後96時間の累積疼痛スコアは有意に低下した(p
•副次的なゴールに達し,術後96時間でオピオイド使用量は統計学的に有意に減少した(p
われわれの第3段階試験では,陰嚢切除術を受けた患者では,月国窩部の坐骨神経ブロックとしてExPAREL:
•塩酸ブピバカインと比較して術後96時間の累積疼痛スコアは有意に低下した(p
•副次的なゴールを達成し,術後96時間でオピオイド使用量は統計学的に有意に減少した(p
EXPARELは患者の満足度と予後を高めることができる。EXPAREL:
•マルチモード術後疼痛レジメンの一部として使用されるときに、高価で使用困難な送達技術を必要とせずに、弾性ポンプのようなブピバカインの作用時間を延長するために、または患者自己制御鎮痛(PCA)によって投与されるオピオイド薬を提供すること;
•患者が弾性ポンプと自己制御鎮痛システムによって制限されることを減少させることは、これは比較的に早い下部の障害であり、感染を含むカテーテルに関連する問題を引き起こす可能性がある
•術後早期疼痛管理の維持を促進することは,集中治療室にかかる時間を減少させる可能性がある。
主なEXPAREL市場
EXPARELによる術後回復,あるいはERASの増強は,オピオイドの術後疼痛管理を節約する礎となり,多くの複雑で苦痛な整形外科プログラムを23時間滞在環境に移行させることができるようになっている。
Pacira BioSciences,Inc.|2022 Form 10-K|9ページ
整形外科
EXPARELは多種の整形外科手術に応用され、関節再建、肩、脊柱、四肢手術と寛骨骨折を含む。
今後数年で関節形成術総数は急速に増加することが予想され,これらの手術は入院病院から外来看護場所に大量に移行するためである。EXPARELによる地域鎮痛は,増強したERAS経路におけるマルチモード疼痛管理レジメンの一部として,このような外科的遊走を支持している。EXPARELの全関節置換術における臨床と経済効果はすでに臨床研究で証明されており、EXPARELの使用はオピオイドの消費を著しく減少させ、痛みを有効にコントロールし、回復時間を短縮し、当日退院し、患者の満足度が高い。
EXPARELはますます多くの脊柱手術に採用されており、多モード疼痛管理解決方案の重要な構成部分として、手術後の迅速な回復とオピオイドへの依存を減少させ、オピオイド薬物は数十年来ずっと脊柱手術後の疼痛制御の大黒柱である。2つの重要な患者群は脊柱市場を推進している:第一に、児童病例、例えば青少年脊柱側弯患者、彼らは高侵襲性手術を受けており、最近までオピオイドによる痛みの治療を受けている;第二に、成年退行性患者、彼らは通常オピオイド類薬物に耐性があり、すでに何度も背部手術を受けたことがあるかもしれない。これらの成年退行性患者はオピオイドに対してすでに耐性があるため、術後の痛みの管理は挑戦性があるかもしれないが、EXPARELを使用することによって、医療保健提供者は非オピオイド薬物方法を用いて彼らの痛みをコントロールすることができ、そして実行可能な情況下で、手術干与と患者の特徴に基づいて、多くの歴史上の入院プログラムを23時間の入院環境に移すことができる
EXPARELは腕神経叢ブロック投与として著者らの業務の重要かつ増加している部分である。ExPAREL腕神経叢ブロックは上腹部の痛みを覆い,肩袖,肩関節形成術,肘関節,手首と手部手術に用いられる。他の地域ブロックと同様に,われわれの麻酔科医は腕叢ブロックを用いた強い優位性を見ており,古いポンプやカテーテルを交換することで手術を外来環境に移行させることができ,これらのポンプやカテーテルは常に変位し,手術を23時間の看護場所で行うことができない。また,支払者や自己保険雇用主が各種手術の入院看護から外来看護への転換を推進し続けるにつれ,EXPAREL精算は改善されてきた。
腹部と結腸直腸
各種体幹ブロックが出現し,腹部や結腸直腸手術に用いられている。横腹筋平面あるいはTAPと脊柱起立平面ブロックはEXPARELが腹部と脊柱手術に長時間効果的な疼痛制御を提供し、これらのプログラムの23時間設置への移行を支持する重要な市場である。EXPARELフィールドブロックは,各種腹部や結腸直腸手術増強回復レジメンの基礎となる拡大使用が重要な成長原動力となり続けることが予想される。
女性の健康
女性では,非オピオイドによる鎮痛の需要が著しく増加している。女性のオピオイド依存症は驚くべき速度で増加しており,女性が術後新たなオピオイド持続使用者となる可能性は男性より40%高いことが示唆されている。女性の健康は依然として重要な成長源であり、麻酔駆動のEXPARELに基づくTAPと胸筋ブロックはすでに帝王切開、腹部形成術、婦人科腫瘍学、乳房切除術と乳房再建術の制度的プロトコルになっているからである。
心臓外科
開放手術でも低侵襲手術でも,心胸郭手術は最も苦痛な手術型の一つとされている。したがって,オピオイドは広く使用されているが,不十分であることが多い。術後疼痛コントロール不良により40%もの患者に慢性持続性疼痛が出現し、10%を超える患者は術後にオピオイドを持続的に使用した。区域麻酔方法はずっと発展しており、EXPARELは胸部硬膜外麻酔の代わりに、術後長期鎮痛を産生する代替方法となっている。
Pacira BioSciences,Inc.|2022 Form 10-K|10ページ
小児科学
2021年3月、FDAは、6歳以上の患者を単剤浸透に使用し、術後局所鎮痛を産生するために、我々のsNDA拡張EXPARELタグを承認した。EXPARELはFDAが許可した第一種であり、唯一の長時間効果の局部鎮痛剤であり、わずか6歳の児童群に適用される。2022年11月,EMAの人用薬品委員会(CHMP)と薬品·保健製品監督機関(MHRA)はEXPARELの適応拡大のマーケティング認可を許可し,6歳および6歳以上の児童を中小手術創術後の身体痛を治療する現場ブロックとして利用した。
オピオイド、短時間局部麻酔薬とカテーテルに基づく装置はずっと小児科手術後の疼痛治療の歴史的支柱であり、安全上の危険が存在するにもかかわらず、児童の研究は限られている。成人に基づく疼痛管理方法のリスクや合併症は小児で拡大する可能性があり,50%の児童が手術後に病院で重度の痛みが出現し,20%の児童が術後12カ月後に慢性疼痛が出現したと報告している。
ExPARELは小児術後疼痛管理の看護パラダイムを再定義しており,市場で唯一臨床的に証明されている安全代替案として,6歳以上の小児術後疼痛コントロールの長時間作用,非オピオイドに用いられている。米国では毎年約100万例の小児科手術がある。私たちは有名な思想指導者と協力しており、彼らはEXPARELに基づく方案を新しい看護標準として構築するために最適な実践の迅速な移転を提供している
第三臼歯手術
第三臼歯抜歯(智歯)はアメリカで最もよく見られる歯科手術の一つであり、毎年500万人もの患者が抜歯手術を受けている。口腔手術は,第三臼歯の抜歯を含み,特定の痛みや不快期に関与しており,伝統的にオピオイドを処方している。医療補助データベースの大型レビューでは,280万人の手術抜歯を受けた患者のうち,120万−約42%−術後7日間にオピオイドが処方され,1患者あたりに割り当てられたモルヒネmg当量の中央値は120 mgであった。EXPARELの第三臼歯抜去術後のオピオイド処方への影響に関する研究では,EXPAREL治療を受けていない患者と比較して,EXPAREL治療を受けた患者から処方されるオピオイド(充填を含む)が有意に減少した。この研究はブピバカインリポソームの第三臼歯抜去術後のオピオイドへの影響の回顧性横断面研究発表されました口腔顎顔面外科雑誌2021年7月。この回顧分析では,2012年から2018年までの間に第三臼歯抜歯術を受けた600名の患者のデータを振り返った。EXPAREL治療を受けた300名の患者の非識別データとEXPAREL浸透を受けていない300名の患者のデータを比較した。この分析には2つの外来口腔外科センターからのデータが含まれている。EXPAREL治療群の患者受け入れ:
•非EXPAREL群と比較して再灌流を含むオピオイドは59%(P)減少した
•追加のオピオイド処方は非EXPAREL群に比べて少ない(3.3%の患者は継続薬が必要であり,7.7%の患者は継続薬が必要)
2017年9月,我々は米国口腔顎顔面外科協会(AAOMS)の支援のもと,米国をリードする多様な医療福祉会社の一つである安泰(Aetna)と協力することを発表した。この国の計画は,EXPARELを用いて長期的な非オピオイド術後疼痛コントロールを提供することにより,抵抗性第三臼歯抜歯患者に分配されるオピオイド数を少なくとも50%減少させることを目指している。安泰には現在EXPARELのコストが含まれており,この製品の使用訓練が完了した外科医による影響を受けた第三臼歯抜歯の被覆費用となっている。
2022年9月、著者らはグループ調達組織SEV VI REDET調達解決方案或いはSEV VI REDETと共同で計画を開始し、サプライヤーのパートナー関係を通じて志を同じくする歯科組織に競争優勢を創造し、サプライチェーンの価値と効率を推進し、口腔顎顔面外科手術を受けた患者にもっとEXPARELを獲得する機会を提供し、範囲は第三臼歯と全口から義歯とインプラントまで抜歯した。この協力はSEV≡REDETが患者の結果を改善し、オピオイド曝露とその関連リスクを減少させる目標を推進し、米国の1,800以上の歯科診療所に包括的な製品訓練とPACIRAの入社支援を含むExPARELを容易に得る機会を提供した。
ZILRETTAの臨床的メリット
ZILRETTAは常用ステロイドTAと特許の徐放マイクロスフェア技術を結合し、関節により長い治療濃度と持続的な鎮痛効果を与える。
Pacira BioSciences,Inc.|2022 Form 10-K|11ページ
その鍵と他の臨床試験の優位性から,ZILRETTAは米国で数百万人の安全かつ有効に膝関節炎の痛みを緩和する必要がある患者の重要な治療選択であると考えられるZILRETTAを承認するキー3期試験では,ZILRETTAは12週間以内に膝関節炎の痛みを有意に軽減し,一部の患者の痛みは16週間以内に緩和されたZILRETTAは臨床試験で提供した鎮痛幅と持続時間はすべて臨床意義があり、その鎮痛幅は今までOA臨床試験で見られた最大の鎮痛幅の一つである。これらの試験では,治療に関連する有害事象の全体的な頻度はプラセボで観察されたものと類似しており,薬物に関する重篤な有害事象は報告されていない。ZILRETTAの安全性と有効性,市場で初めて唯一の徐放コルチコステロイドであることから,ZILRETTAは第一選択コルチコステロイドとなる可能性があると考えられる。2021年9月、アメリカ整形外科協会(AAOS)はその根拠に基づく臨床実践ガイドラインを更新し、ZILRETTAは伝統的な速放コルチコステロイドではなく、患者の予後を改善できることを発見した。
Iovera°臨床的メリット
Iovera°による膝骨性関節炎の治療に成功した臨床データが増えている。手術干与は通常膝骨性関節炎患者の最後の手段である。1つの研究では,多くの膝骨性関節炎患者がiovera°治療を受けた後,150日間にわたる疼痛が緩和された。
初歩的な調査の結果、オピオイドは減少していることが分かった
•PERシナリオ分析では,1日のモルヒネ当量消費量は72時間で有意に低下した(P
•Iovera°治療を受けた患者が術後6週間にオピオイドを服用する可能性ははるかに少ない。対照群の術後6週にオピオイドを服用した人数は凍結鎮痛群の3倍であった(14%比44%,P
•Iovera°群患者の72時間後の疼痛採点はベースライン疼痛採点より明らかに低下した(p
これらのデータは,iovera°がTKAを受けた患者にとって臨床的意義のある非オピオイド代替品であることを検証し,iovera°は任意の必要な手術介入前に一連の重要な製品属性を介して患者に非オピオイド鎮痛制御を提供する機会を提供すると信じている
•Iovera°は安全かつ有効であり,すぐに痛みを緩和し,時間の経過とともに神経再生し,痛みは数カ月持続する
•Iovera°は繰り返し可能である
•Iovera°技術は周囲の組織に被害を与えない
•Iovera°は、一度に使用するプログラム固有の知的提示を有する便利なハンドヘルドデバイスである
•超音波ガイドや解剖ランドマークを用いてiovera°を正確に提供することができる。
2021年9月、AAOSはその根拠に基づく臨床実践ガイドラインを更新し、除神経治療-凍結神経剥離術を含む-膝関節痛を軽減し、膝関節症候性骨関節炎患者の機能を改善する可能性があると報告した。
骨性関節炎市場
骨性関節炎は最もよく見られる関節炎である。退行性関節疾患とも呼ばれ、手、臀部、膝に最もよく発生する。骨性関節炎では関節内の軟骨が分解し始め,底層骨が変化し始めた。このような変化は一般的に発展が遅く、時間の経過とともに悪化する。骨性関節炎は痛み、硬直、腫脹を招く。場合によっては、機能低下や障害を引き起こすこともあります-一部の人は日常的な仕事や仕事をすることができなくなります。米国疾病コントロール·予防センターのデータによると、米国では3250万人を超える成人が骨性関節炎を患っている。
関節炎財団のデータによると,症状を有する膝骨性関節炎の生涯リスクは45%であった。症状のある膝骨性関節炎の罹患率は加齢とともに増加し,55歳から64歳までの膝関節骨性関節炎の年間発症率が最も高かった。米国では1400万人が症状のある膝骨性関節炎を有しており,そのうち200万人近くが45歳以下である。手術干与は通常膝骨性関節炎患者の最後の手段である。
ZILRETTAを我々の製品に添加することにより,現在臨床医に柔軟性を提供し,患者因子や好み,医師訓練,看護場所,精算の考慮に応じて,ZILRETTAやiovera°を有する無薬物神経遮断薬を用いて個性化されたOA膝関節疼痛治療を行うことができる。
Pacira BioSciences,Inc.|2022 Form 10-K|12ページ目
ラベルと世界的な拡張活動
ExparEL
•下肢神経ブロック2022年9月,われわれはEXPARELを単用量神経ブロックとして下肢術後区域鎮痛の2つの3期登録研究に用いた陽性TOPLINE結果を発表した。第1の研究では,ExPARELがTKA患者内転筋管内の大腿神経ブロックとしての作用を評価し,主な終点に達し,0から96時間の累積疼痛スコアが塩酸ブピバカインと比較して統計学的に有意に低下したことを示した(p
•小児科です。一期薬物動態研究を開始し,その後EXPAREL単剤浸透ラベルの6歳以下を含む患者への拡大を支援する登録研究を開始する予定である。成功すれば,この研究は米国とEUにおけるEXPARELタグの拡張を支持すると予想され,小児科環境におけるEXPARELの神経ブロックとしての規制戦略も検討している。
•星状神経節ブロック現在、EXPARELを星状神経節遮断薬として難治性心室性不整脈の治療に応用し、心臓直視手術後の心房細動の予防に応用する多中心登録研究が計画されている。私たちは重要なオピニオンリーダーからなる指導委員会、すなわちKOLと、地域麻酔と星状神経節塊の面で協力して、最終的な研究設計の決定を支援している。星状神経節ブロックを含むようにEXPARELタグを拡張した規制戦略についてFDAと一致した後,登録試験を継続する予定である。EXPARELを用いた星状神経節ブロックは数日間持続し,心室性や心房性不整脈患者では満たされていない重大な需要を解決すると信じている。
•世界が拡大しています私たちはヨーロッパとラテンアメリカ市場を世界拡張の優先順位に置いた。ヨーロッパではEXPARELが成人術後痛を治療する腕神経叢ブロックや大腿神経ブロック,成人中小型手術創の体幹術後痛を治療するための野戦ブロックとして承認され,2022年11月には6歳または6歳以上の小児を野戦ブロックとし,中小型手術創の術後体痛の治療に用いることが許可されている。私たちはイギリスでEXPARELを発売し、2021年第4四半期にEU諸国を狙った。ラテンアメリカでは、Eurofarma実験室S.A.またはEurofarmaとEXPARELを開発し、商業化するためのDealerプロトコルを締結した。Eurofarmaはアルゼンチン、ブラジル、コロンビア、メキシコを含むラテンアメリカ19カ国および地域におけるマーケティングおよび流通EXPARELの独占的権利を持っている。また、Eurofarmaは、これらの国におけるEXPARELの規制届出を担当し、ブラジルでの承認を求める申請を最近提出した。私たちは印税を獲得し、いくつかの事件の実現によって触発された規制と商業に基づくマイルストーン支払いを得る資格がある。
ZILRETTA
ZILRETTAの徐放プロファイルも肩部の骨性関節炎疼痛に有効な治療を提供する可能性があると信じており,2023年にZILRETTAによる肩骨関節炎治療の第3段階試験を開始する予定である。また,2型糖尿病患者に対する4期研究を計画している。肩研究,糖尿病研究ともにZILRETTAを即時放出TAと比較した。
Iovera°
2022年には、次世代iovera°手持ち装置を発売しました。この装置はより効率的で、使いやすく、耐久性があると信じています。われわれは,ある手術のために新たなiovera?Smart Tipsを開発し,慢性下腰痛や脊柱手術の内側分枝ブロックの治療のための特定のヒントを開発している。ブランドの範囲を拡大することも求めています
Pacira BioSciences,Inc.|2022 Form 10-K|13ページ
けいれんの治療は,iovera°の重要な長期的機会であると考えられる。また、私たちは2022年に契約販売チームを通じてEUでiovera°の販売を開始します。
臨床発展計画
PCRX-201
Flexion買収の一部として、PCRX-201は私たちのポートフォリオに追加された。PCRX-201は新型のIA遺伝子治療候補製品であり、膝関節炎の疼痛の治療に用いられる抗炎症性タンパク質IL-1 raを産生することができる。納得できるPCRX-201第1段階の治療効果と安全性データに基づいて、著者らは調査者と協力し、FDAに会議を開催し、膝蓋骨関節炎の将来の制御経路、およびRMATの指定を討論することを計画している。
PMVLに基づく臨床計画
著者らのpMVL薬物送達技術プラットフォームが急性、亜急性と慢性疼痛応用に対してすでに証明された安全性、柔軟性とカスタマイズ可能性に対して、著者らはいくつかのpMVLに基づく製品が臨床開発を行っている。これらの候補の臨床前研究と実行可能性研究のデータに基づいて、著者らは3つの臨床開発方案を優先した:(I)PCRX-401、1種の下腰痛を治療するデキサメタゾン-pMVL;(Ii)PCRX-501、1種の高効率ブピバカイン-pMVL、より持続的な鎮痛(20.0 mg/ml)と(三)EXPARELに用い、鞘内鎮痛(13.3 mg/ml)に用いた。2023年上半期にEXPARELの髄腔内鎮痛の第1段階研究の後半を開始する予定である。
PCRX−301
PCRX−301は現地管理ナトリウムであるV1.7フォラピッドと呼ばれる腐食防止剤であって、感温性ヒドロゲル中での放出を延長するように配合されている腐食防止剤。PCRX−301の最初の開発は、末梢鎮痛剤としての下肢神経遮断薬の術後疼痛の管理を支援するためである。2022年9月、完成した第1段階研究の結果に基づいて、プラセボと比較して臨床的治療効果が乏しいこと、およびヒドロゲル配合に問題があるため、PCRX-301のさらなる開発を中止することにした。
外部革新
我々の内部臨床プロジェクトとともに,我々の業務開発チームはEXPAREL,ZILRETTA,iovera°の補完であり,今日呼びかけられている外科や麻酔受容者の大きな興味を引き起こしている革新的な買収目標を求めている。著者らは戦略投資、内部許可と買収取引の組み合わせを利用して、神経痛経路における患者の旅を改善するための革新的なパイプを構築している。我々が将来性の高い早期プラットフォームを支持するために行った戦略投資は以下のようにまとめられる
| | | | | | | | | | | |
| 会社 | 発展段階 | プラットフォーム技術記述 | 潜在的治療領域 |
| CarthroniX,Inc. | フェーズ1-準備完了 | CX-011は、関節内注射として、IL-6サイトカインを媒介することによって関節変性を緩和することを目的としたgp 130の小分子調節剤である | 膝蓋骨関節炎 |
| Genascence社は | フェーズ1 b-準備完了 | アデノ関連ウイルス(AAV)に基づく遺伝子治療は,インターロイキン1受容体拮抗薬(IL−1 ra)を関節標的細胞に輸送することができる | 膝蓋骨関節炎 |
| GQ生物治療有限会社 | 臨床前 | 補助依存アデノウイルス(HDAd)による遺伝子療法により,DNAを関節や椎間板中の標的細胞に輸送することができる | 膝骨性関節炎と退行性間盤疾患(DDD) |
| 脊柱生物製薬有限責任会社 | 第3段階 | 形質転換成長因子−β1(形質転換成長因子−β1)に結合して下方制御を誘導する7アミノ酸鎖ペプチド、形質転換成長因子β−1、SB−01 | 退行性間盤疾患(DDD) |
販売とマーケティング
私たちは私たちの販売とマーケティング組織を設立し、私たちの製品を商業化した。われわれの主な目標は,麻酔科医,外科医,薬剤師,医師普及者(医師アシスタント,看護師従事者,登録看護師を含む)の疼痛管理意思決定に影響を与える医療従事者である。
Pacira BioSciences,Inc.|2022 Form 10-K|14ページ
私たちの現場チームは販売代表、顧客マネージャー、科学と医療事務員、清算と市場参入専門家からなり、彼らは疼痛管理における非オピオイドの使用を拡大するための一連の活動を展開している
•臨床治療効果および安全性、健康結果を示す出版物および要約、ならびに評論文章を提供する
•病院スタッフ、例えば麻酔科医、外科医、品質担当者、薬剤師、幹部と登録看護師と協力し、薬物利用或いは薬物使用評価と健康結果研究に経路と資源を提供し、著者らの病院顧客に回顧と展望性分析を提供し、彼ら自身の病院データを用いてオピオイドに基づく術後疼痛制御の真のコストを証明した
•KOLとコンサルティング委員会と協力して、ベストプラクティスと私たちの製品を使ったガイドラインとプロトコルのテーマを解決し、私たちの内科医、外科医、麻酔科医、薬剤師と登録看護師の顧客の教育と訓練需要を満たす
•教育措置を展開し、例えば英才センター方案;指導方案;オピオイド非処方とERAS疼痛方案と予測モデル、患者看護を強化する;インタラクティブフォーラム;適切な時に公共関係、宣伝パートナーシップと公共事務努力の患者教育プラットフォーム;ネットワークに基づく訓練と仮想起動方案;
•医療保健提供者と協力して、手術と骨性関節炎患者の疼痛知識と管理を改善し、重点はオピオイドリスクと非オピオイド薬物代替品であり、そして著者らの地方医療チームに全システムのパートナーシップに参加させ、全国オピオイド薬物の流行に対応し、目標はオピオイド薬物代替戦略の最適化と最適化を重点とした術後疼痛管理代替方案の研究である
•精算の促進と病院外来や外来外科センター,あるいはASC,看護場所へのプログラムの移行を促進する。
パチラ訓練施設
私たちは二つの訓練施設を維持して運営しています。一つはフロリダ州タンパで、もう一人はテキサス州ヒューストンにあります。これらのサイトの建設には単一の目標がある:最適なやり方技術に関する教育を促進し、急性疼痛を効果的に管理し、オピオイドに対する需要を減少または除去しながら。これらの施設は臨床医師に柔軟で最先端の環境を提供し、相互作用、着手で最新と最も革新的な地元、地域と現場のブロック方法を指導し、痛みを管理し、患者の看護を改善し、そして患者が23時間の入院環境に移動できるようにする。
フロリダ州タンパ市
2020年10月、私たちはタンパ市にパチラ革新訓練センターを開設した。著者らはこの施設を設計し、臨床医師が最新の局部、区域と現場ブロック止痛方法をよりよく理解することを助けるためである。タンパの穴は医療保健提供者に比類のない訓練環境を提供し、患者のオピオイド類薬物への接触を減少或いは除去するために努力した。タンパのPITは一連の全方位の教育活動を支持し、臨床医師の疼痛コントロールとオピオイド暴露の最新の現地、地区と現場ブロック方法に対する理解を促進する。私たちの主な行政事務室と会社の本社もタンパ市に設置されています。
タンパの修理ステーションは約13,000平方フィートであり、最先端の技術とオーディオ/ビデオ機能を搭載し、7つの超音波スキャンステーションを備えたシミュレーション実験室を含むいくつかの異なる訓練空間を備えている;高さ4.5フィート、幅24フィートの液晶ディスプレイビデオ壁を有する講演ホールは、現場、仮想、さらには世界的なデモをサポートするための講演室と、単一または複数の司会者とコンテンツを中継することを目的とした緑スクリーン放送スタジオを含む。
我々のEXPARELプロジェクトのほかに,新しいユーザーがタンパ坑でiovera°管理を行う最適実践技術を研修するシンポジウムを開催している。これらの実験室は医療保健専門家が指導し、授業と手訓練を含み、超音波と末梢神経刺激を用いた現場モデル神経スキャンと識別を含む。
タンパのPITも国家麻酔提供者組織が自分のシンポジウムと訓練課程を開催して医療保健提供者を教育する場所であり、この組織に対して何の費用も徴収しない。
ヒューストン、テキサス州
2023年1月、私たちはテキサス州ヒューストンに2つ目の訓練機関であるヒューストンパチラ革新訓練センターを開設した。この19,000平方フィートの最先端の施設には125席の適応講演室が搭載されており、同じ液晶を採用しています
Pacira BioSciences,Inc.|2022 Form 10-K|15ページ
タンパ鉱坑のビデオ壁、1つの放送スタジオ、濡れたと乾燥した実験室空間を展示し、身体と他のインタラクティブスタジオを使用する。1つのシミュレーション実験室には8台の先進的な超音波機器が搭載されており、人工知能と3-Dトレーニングソフト、専門的な医療照明と天井内カメラが搭載されている。ヒューストンの整備ステーションは私たちの医師のチャンピオンを育成し、オピオイド節約疼痛管理の最前線に維持したいコミュニティ臨床医師の核心である。この新しい研修施設があれば、EXPAREL、ZILRETTA、iOVERAプロジェクトを主催する能力と能力を倍増させます。
DePuy Synths Sales Inc.
2020年7月には,ジョンソンファミリー社のデップ·シンディス販売会社やデップ·シンディス社と共同普及協定を結び,EXPARELを用いた整形外科手術を米国でマーケティング·普及させることを発表した。協力は2017年1月に始まり、2021年1月に終了した。この間,DePuy Synths現場代表はPacira現場とチームワークし,EXPARELの整形外科環境における使用と教育を支援した。DePuy Synthsと協力して整形外科手術プログラムを支援するほか、Paciraの現場代表は依然としてEXPARELの全体顧客マネージャーと軟組織外科医、麻酔科医とASCのビジネスリーダーである。この協力により,EXPARELの使用が著しく拡大し,一連の整形外科プログラムにおけるオピオイド節約案における役割を強固にした。著者らが協力を終了することにしたのは、整形外科実践が入院歴から外来環境に変化し、麻酔駆動の地域的方法がますます重要な役割を果たしているからである。私たちの現場チームはこの持続的に増加している市場にサービスを提供した。
その他の合意
屈曲習得
2021年11月19日に、吾らは2021年10月11日の合併合意および合併計画(“Flexion合併合意”)(“Flexion合併合意”)に基づいてFlexion買収を完了し、買収側は私たちの中の米国デラウェア州会社およびPacira(“買い手”)の完全資本付属会社Oyster Acquisition Company Inc.およびFlexionを含む。Flexion普通株に対する入札オファーに成功した後、買い手はFlexionと合併してFlexionに組み込まれ、FlexionはPaciraの完全子会社として存続する。合併が完了した後、私たちはFlexionをPacira治療会社と改名した。膝屈曲治療の一部としてZILRETTAが得られ,膝骨性関節炎痛の治療に用いられる唯一の徐放性IA(関節内)注射である。ZILRETTAは非オピオイドであり,特許マイクロスフェア技術を用いて疼痛緩和を提供している。ZILRETTAを著者らの革新的な非オピオイド薬物製品の組み合わせに加えることは直接に著者らの使命に符合し、即ちできるだけ多くの患者にオピオイド代替品を提供し、神経疼痛経路の医療需要を満たす。
初歩的には、買収事項の総費用は約5.788億ドルであり、(I)Flexion株主および決済制限株式単位およびいくつかの株式購入に支払われた現金4.485億ドル、(Ii)現金支払いは吾らが負担していないFlexion債務8,510万ドルを含む;および(Iii)Flexion買収事項とともにFlexion株主およびいくつかの持分奨励所有者に発行されたあるいは価値権に関連するまたは対価は公正価値4520万ドルを推定する。私たちは手元の現金で買収価格の現金部分に資金を提供し、価格は潜在的なマイルストーン支払いの見積もり公正価値によって調整されるかもしれない。2022年12月31日までに、特定の規制および商業マイルストーンに達した場合、これらまたは価値のある権利は合計3兆723億ドルになる可能性がある。詳細については、付記5を参照されたい屈曲習得12を追加して金融商品私たちの連結財務諸表はここに含まれています。
MyoScience買収
2019年4月、私たちはMyoScienceの買収を完了した。総対価格には、1.2億ドルの初期現金支払い、取引完了後の購入価格調整と賠償義務のための100万ドルを引いたもの、総額1.0億ドルに達するものやマイルストーンの支払いが含まれており、うち4300万ドルは2022年12月31日に使用できる。節目を実現した期日は2023年12月31日です。統合が完了した後,MyoScienceをPacira CryoTech,Inc.と改名する.MyoScienceが買収したことや価格の詳細については、付記12を参照されたい金融商品私たちの連結財務諸表はここに含まれています。
研究開発基金
研究開発基金(RDF)との合意によると、私たちは、ある製品から収入の低い桁の特許権使用料をRDFに支払うことを要求されています
Pacira BioSciences,Inc.|2022 Form 10-K|16ページ
協定はまだ効果的だ。RDFには、私たちの破産または非債務に関連する未治癒の重大な違約行為を終了する権利があり、または譲渡された特許権の有効性に直接または間接的に反対または論争する場合。
我々の米国特許番号11,033,495は2021年6月15日に発行された。その後,RDFは,この特許の発行は,我々が合意に基づいて負担する印税義務を2041年に延長すると主張している.私たちは同意せず、協定下の特許権期間は2021年12月24日に終了し、私たちの米国特許番号9,585,838が満了したと説明した。本合意に対する解釈に食い違いがあるため,2021年12月,米国ネバダ州地方裁判所に宣言的判決訴訟を起こした(21-cv-02241).訴訟は、私たちが2021年12月24日以降に私たちのEXPAREL製品に関するRDFの特許権使用料を借りないことを裁判所に声明することを要求する。訴訟が未解決の期間中は,抗議中のRDFに特許権使用料を支払い続けるが,この行動の結果を予測することはできない.
Aratana治療会社は
2012年12月、Elanco Animal Health,Inc.またはAratanaの完全子会社Aratana Treateutics,Inc.と独占許可、開発と商業化協定および関連供給協定を締結した。合意に基づき、動物用ブピバカイン注射懸濁剤製品の開発および商業化のための再許可を付与する限られた権利を含むAratanaに独占印税許可を付与した。2016年8月FDAの獣医センター(CVM)がNocitaを承認しました®犬頭蓋十字靭帯手術後の局所鎮痛として(NocitaはAratanaの登録商標である)ブピバカインリポソーム注射懸濁液。2018年8月,CVMはNocitaのタグを拡張し,末梢神経ブロックとして用い,猫甲切除後の局所術後鎮痛を提供した。2019年6月、クラウドサーバはNocitaの10 mlボトルサイズを承認した。Aratanaは2016年にブピバカイン注射用懸濁剤製品の購入を開始した。
私たちはビジネスマイルストーンを達成した後、4000万ドルまでの奨励金を得る資格がある。Aratanaは、米国で行われているいくつかの純売上高のために2桁の等級版税を支払う必要があります。製品が外国の規制機関によって米国以外の地域での販売が許可された場合、Aratanaはこのような純売上について2桁の等級版税を支払うことを要求されます。動物健康指標の非特許競争者がある司法管轄区域またはAratanaに入って、場合によっては第三者に特許料を支払わなければならない場合、印税料率は一定のパーセント低下するであろう。
いずれも,(1)他方の破産事件に関与しているが,所定の時間内に解除されていない,(2)他方は合意に深刻に違反し,所定の治癒期間内に治癒していない,または(3)合意の規定の最低年収に達していない,のいずれかを終了する権利がある,これらはすべて所定の通知の下で行われている。私たちは、以下の理由で合意を終了するかもしれない:(I)Aratanaは、協定の下で満了した任意のお金を支払うことができなかった;(Ii)Aratanaは、特定の管轄区域でその管轄区域に関する規制の承認を得ることができなかった、または(Iii)Aratanaは、規制の承認を得てから一定時間以内に各国でその最初の商業販売を達成できなかった。これらは、指定された通知の下で行われた。Aratanaは、(I)動物健康指標の非特許競争者が進入したときに、個々の国または(Ii)が任意の時間に国/地域に基づいて許可協定を終了することができるが、米国およびEUのいずれの国を除いても、これらは指定された通知の下で行われることができる。双方の同意によって、双方はまた許可協定を終了することができる。もし私たちが供給協定を終了すれば、許可協定は自動的に終了するだろう。ライセンス契約が終了した場合、製品のすべての権利は(管轄区域に従って)終了し、私たちに返却されます。その条項によって早期に終了しない限り、ライセンス契約の有効期間は2033年7月までであり、その後、Aratanaはいくつかの要求に応じて合意をさらに5年間延長する権利がある。
ヨーロッパ農場実験室株式会社
2021年6月、ラテンアメリカでEXPARELを開発し、商業化するEurofarmaと流通協定を締結した。合意条項によると、Eurofarmaはアルゼンチン、ブラジル、コロンビア、メキシコを含むラテンアメリカ19カ国でマーケティングおよび流通EXPARELの独占的権利を獲得した。Eurofarmaは最近ブラジルでの承認を求める申請を提出した。さらに、Eurofarmaはこれらの国でのEXPARELの規制準備を担当している。私たちはEurofarma未来EXPARELの商業化に基づく特許権使用料を取得し、特定の規制や商業活動の実現によって触発された記念碑的な支払いを得る資格もある。
Verve医療製品会社です。
2021年7月,Verve Medical Products,Inc.とカナダでiovera°を流通するライセンス契約を締結した。私たちは2021年第4四半期にカナダでiovera°の販売を開始した。
Pacira BioSciences,Inc.|2022 Form 10-K|17ページ
重要な取引先
2022年12月31日までの一年に、私たちは三つの卸売業者がいて、それぞれ私たちの総収入の10%以上を占めています:紅衣主教健康会社、マケソン製薬会社、アメリカベルゲン健康会社、それらはそれぞれ私たちの総収入の31%、23%と22%を占めています。これらの卸は直運計画に従ってEXPARELの注文を処理している。EXPARELはエンドユーザに直接渡されるが,卸は実際に製品を所有していない.2022年12月31日までの1年間、ZILRETTAまたはiovera°のお客様は、私たちの総収入の10%以上を占めていません。
製造·研究施設
内部施設
カリフォルニア州サンディエゴの工場でExPARELとIOVERA°ムーブメントを生産しています。私たちはまた、私たちのEXPARELとIOVERA°製造施設、そしてこれらの施設の5マイルの範囲に位置する多用途の研究開発、製造、オフィス施設を持っています。この3つの建物を科学センターキャンパスと呼んでいます合わせて約19.5万平方フィートです我々の製造施設は定期的に検査を受け,FDA,EMA,MHRA,環境保護局(EPA)の承認を得ている。
私たちは第三者サプライヤーから原材料と部品を購入してEXPAREL、ZILRETTA、iovera°を製造します。多くの場合、代替供給源は利用可能であり、場合によっては代替供給源への切り替えに時間がかかり、我々の候補製品の生産遅延をもたらす可能性がある。サプライヤーは私たちが必要な時や商業的に合理的な条件下でこれらの原材料を私たちに販売しないかもしれません。私たちはサプライヤーからこれらの原材料を得ることを直接制御することもできません。原材料不足に関連するリスクを抑えるために、重要な原材料の十分な供給を維持し、追加の供給源を適宜決定するように努力している。
すべての製品の製造、初期製品の発表と安定性テストは私たちと私たちの製造パートナーが現在の良好な製造規範またはCGMPに基づいて行います。
私たちは科学中心園区にあるEXPAREL製造工場は5エーカー、敷地は約84,000平方フィートです。それは製薬研究開発と製造施設としてカスタマイズされている。この施設の活動は,ExPARELバルク製品とそのボトル/充填,微生物と品質管理試験,製品貯蔵,分析方法の開発と開発製品の製造を専用ライン上で製造することである。私たちの科学センターパークのEXPAREL製造能力を拡大しており,EXPARELへの需要が増加することが予想されるからである。
私たちは90,000平方フィートの混合用途の研究開発、製造、オフィス施設が私たちのEXPAREL製造施設に隣接し、2020年に私たちの仕様を満たすために全面的に改修しました。私たちはこの工場ですべてのiovera°携帯電話を生産している。このビルはまた、実験室と必要な建築インフラを含み、より多くの商業製品の適応と新しいパイプライン製品の調合、分析テスト、臨床と過程開発活動を支持するため、科学センターに関連する研究開発活動と一般と行政機能を収容している。私たちの早期臨床製品生産のためのパイロット工場キットはこの建物内にあり、未来にはもっと多くの拡張空間がある。
私たちの科学センターパークが運営する主要なCGMP倉庫として、主に生産材料を貯蔵するための約21,000平方フィートの倉庫があります。常温と低温CGMP倉庫貯蔵を含み,原料をサンプリングするための品質制御クリーンルームを有している。
我々のpMVL製品の流通は,EXPARELを含み,コールドチェーン流通が必要であるため,製品は指定された温度範囲で保持しなければならない。我々は,製造からエンドユーザへの配信までの継続温度監視フローを検証した.
共同制作施設
Thermo Fisher科学医薬サービス会社
2014年4月、Thermo Fisherと戦略共同生産協定、技術移転とサービス協定、製造·供給協定(“EXPAREL製造·供給協定”)を締結し、EXPARELを協力して製造した。Thermo Fisherはいくつかの技術移転活動と建築サービスを担当しています
Pacira BioSciences,Inc.|2022 Form 10-K|18ページ
Thermo Fisherのイングランドスウィンデン工場を用意し、2つの専用スイートでEXPARELを生産する必要がある。EXPARELの製造に必要な設備をThermo Fisherに提供し,Thermo Fisherが実現したいくつかの技術移転と建設マイルストーンに基づいてThermo Fisherに費用を支払った。私たちはまたThermo Fisherのいくつかの象徴的な費用と追加サービスを精算する。2019年2月、EXPARELの商業生産が最初のThermo Fisherスイートで行われていることを発表しました。私たちは現在、Thermo Fisher工場でのEXPAREL製造能力を2倍以上に増加させた2つ目のより大規模な専用キットを使用している。私たちは2021年8月に2セット目のスイートルームでEXPARELの商業生産を開始した。
EXPAREL製造および供給プロトコルの初期期限は、FDAが最初の製造キットを承認した日から10年で、2018年5月に受け取りました。Thermo Fisherに製造キットの運営費用とThermo Fisher製EXPAREL数量を支払います。私たちはまたThermo Fisherが私たちを代表して行った購入、いくつかの象徴的な費用、追加サービスを精算します。規制当局がEXPARELを米国または私たちの総売上の80%を占める他の市場から撤回させた場合、1ヶ月前に本合意の終了を通知したり、便宜上18~24ヶ月の通知を提供したりすることができます(FDA承認日後の年数によります)。他方が違約または破産すれば、いずれも“EXPAREL製造および供給プロトコル”を終了することができる。
Flexion買収に先立ち、FlexionとThermo Fisherは2015年7月に製造および供給協定(“ZILRETTA製造および供給協定”)と、私たちのEXPARELスイートがあるイングランドのスウィンデンの同じThermo Fisher工場でZILRETTAを生産することに関連する技術移転およびサービス協定を締結した。Thermo Fisherは,何らかの譲渡活動や建築サービスを担うことに同意し,専用製造キットでZILRETTAを商業製造する施設の準備をしている。Flexionは、Thermo FisherにZILRETTAを製造するために必要ないくつかのデバイスおよび材料を提供する。私たちは毎月Thermo Fisherにこのような活動の費用を支払い、いくつかの材料、設備、雑費、追加サービスをThermo Fisherに精算します。
Flexion買収の一部として、ZILRETTA製造および供給プロトコルの初期期限は2027年10月に満了すると仮定しています。私たちは毎月Thermo Fisherに生産職場運営の基本費用を支払い、商業需要からZILRETTA 1本当たり製品費用を支払うと予測している。私たちはまた、Thermo Fisher代表が私たちが購入した材料と設備、いくつかの象徴的な費用、追加サービスを精算します。ZILRETTA製造および供給プロトコルは、このプロトコルの満了または終了まで完全に有効に維持されるであろう。規制機関がZILRETTAを米国または私たちの総売上の80%を占める他の市場から撤退させた場合、私たちは1ヶ月前に本合意の終了を通知するか、便宜上24ヶ月の通知を提供することができます。他方が違約または破産した場合、いずれか一方はZILRETTA製造および供給協定を終了することができる。ZILRETTA製造契約を終了した後(Thermo Fisherが製造マイルストーンに達していない場合やThermo Fisherの違約により終了した場合を除き)、Thermo Fisherの製造設備の除去に関する費用および指定の上限を超えないThermo Fisherの終了費用を支払う義務があります。
カーライル社
2020年1月には,Carlisle Companies,Inc.またはCarlisle(前身はProvidien Device Assembly,LLC)と製造·供給協定(“Carlisle協定”)を締結し,Carlisleがメキシコティワーナにある工場でiovera?Smart Tipsを生産することに協力した。カーライル協定の初期期限は5年だ。カーライル協定によると、私たちはカーライルが提供したiovera?Smart Tipsの金額に基づいて料金を支払います。2022年4月からすべてのiovera°Smart Tipsは現在カーライル製である。
カーライル協定はいずれか一方が1年前に無断で書面で通知した後に終了することができる。Iovera°が市場から撤退するか、またはこれ以上私たちが販売しない場合、私たちは30日前にカライル協定を終了することを書面で通知することができる。一方が約束を破ったり破産したりすれば、どちらも“カーライル協定”を終了することができる。
知的財産権と排他性
私たちは、特許、商業秘密、ノウハウ、規制排他性、開示に対する契約制限によって、私たちの製品、私たちの候補製品、および私たちの技術を保護することを求めています。以下に説明する特許および出願は、我々の既存および開発されている製品の組み合わせによって提供される様々なカバー範囲を強調するためにのみ使用されることに留意されたい。
Pacira BioSciences,Inc.|2022 Form 10-K|19ページ
特許と特許出願
私たちは、私たちのノウハウ、発明、改善に関連する米国および外国特許出願を提出することによって、私たちの製品および候補製品の独自の地位を保護することを求めており、これらの特許出願は、私たちの業務発展に非常に重要である。2022年12月31日現在、pMVL薬物送達技術の各方面に関する特許及び特許出願は13ファミリーを超え、ioveraが使用する技術の各態様に関連する特許及び特許出願は29ファミリーを超えている。ZILRETTAによって使用される技術の様々な態様に関する一連の特許および特許出願がある。特許は多くの国で発行されており、北米、ヨーロッパ、日本市場に重点を置いている。これらの実用特許の有効期限は、より早く提出された非仮出願よりも優先されることが要求されない限り、非臨時出願の日から20年であるのが一般的である。私たちのいくつかの満期のアメリカ特許の有効期限は17年で、授与日から計算されます。以下に述べるように、pMVL薬物送達技術の最後の現在発行されている特許は2041年に満了し、ZILRETTAの最後の現在発行されている特許は2031年に満了し、iovera?技術の最後の実用特許は2040年に満了する。
私たちのpMVLとpMVL製品の特許と特許出願
2021年6月,米国特許商標局(USPTO)はEXPARELに関連する米国特許番号11,033,495を発行した。この特許はブピバカイン多カプセルリポソームの製造、改良された製造プロセスによって製造されたEXPARELクレーム成分。2021年11月、米国特許商標局は、それぞれEXPAREL製造プロセスおよびEXPAREL成分の改善を主張する米国特許第11,185,506号および11,179,336号を発表した。2022年3月から9月までの間に、EXPARELの製造プロセスの改善に関連する6つの製品および個々の製品の米国特許を取得し、2041年に追加の特許保護を提供した。USPTOは2022年3月にEXPAREL成分を要求する米国特許第11,278,494号を発表した。2022年4月、米国特許商標局は、製造プロセスの改善を要求するEXPAREL組成物およびEXPAREL組成物の製造をそれぞれ要求する米国特許11,304,904および11,311,486号を発表した。2022年6月、米国特許商標局は、製造プロセスの改善を求めてEXPAREL組成物を製造する米国特許11,357,727号を発行した。2022年8月,USPTOはEXPARELバッチ組成物を要求する米国特許11,426,348号を発行した。USPTOは2022年9月にEXPARELバッチ組成物を要求する米国特許11,452,691号を発行した。
2021年と2022年に発行されたすべての8特許の満期日は2041年1月22日である。米国特許番号11,033,495,11,179,336,11,278,494,11,304,904,11,311,486,11,357,727,1426,348および11,452,691は現在FDAの承認された薬物製品とその治療同等性評価(“オレンジブック”)。また、我々は最近、2023年に適時に発表される米国特許商標局からEXPAREL特許に対する補助金通知を受けた。発表された後、私たちはこの特許をオレンジブックに提出するつもりだ。発売後,Orange Bookは合計9件のEXPAREL特許を有し,各特許の満期日は2041年1月22日である。
私たちはまた、EXPARELおよび他のpMVLベースの製品を製造するための一連の米国および外国特許を持っている。このプロセスはより大規模な生産とより低い製造コストを含む多くの利点を提供する。発行された8つのアメリカ特許があります。この方法および装置を要求する特許は遅くとも2033年11月に満了する。特許のうちの1つは,このようなプロセスで製造された製品であり,2031年4月に満了すると主張している。2022年12月31日現在、我々は中国で4つのライセンス特許を有しており、1つはヨーロッパで許可されており、1つは日本で許可されており、1つはイスラエルで許可されており、機器の使用方法および機器自体を含む代替プロセスの様々な側面を保護している。
2022年2月、EXPARELを星状神経節ブロックとして使用し、電気嵐を含む不整脈の治療に関する臨時申請を提出した。2022年10月には,デキサメタゾンリン酸ナトリウム−pMVL製品の物質組成,製造プロセス,治療法に関する米国と特許協力条約(PCT)出願を提出した。そのほか、著者らは1種の高効率ブピバカイン-pMVL製品の物質組成、製造過程と治療方法に関連するアメリカ申請とPCT申請を提出した。
ZILRETTAの特許と特許出願
米国特許商標局はZILRETTAに合成物質特許を発行し,特許期間は2031年までである。米国特許商標局はまた,ZILRETTAの製造と使用方法について2つの特許を発行し,特許期限は2031年までである。50種類以上のステロイドやポリ乳酸−グリコール酸(PLGA)製剤の効果を試験·観察することを含むZILRETTA配合の基礎となる大量のオリジナル作業を行うためには,多くの専門知識と努力が必要である。私たちは、正確な薬物放出状況に関連する秘密を含む、ZILRETTA製造過程に関連する広範な技術的ノウハウおよび商業秘密は、有意義な進入障害であると信じている。
Pacira BioSciences,Inc.|2022 Form 10-K|20ページ
私たちは3つの米国ZILRETTA特許と対応する外国特許と特許出願を持っており、物質の組成、製造方法、使用方法をカバーしている。私たちのアメリカでのZILRETTA特許は2031年に満期になるだろう。ZILRETTA物質成分発明はいくつかの独特な発見の結果であり、これらの発見は狭義の薬物負荷規格、ポリマーの特定の放出曲線、特定のポリマーの重量と比率及び用量範囲で観察された臨床治療効果と関係がある。ZILRETTAの物質組成と使用方法に対する米国特許はFDAオレンジブックに記載されている。ZILRETTAのような物質組成物に対する米国特許と、それらを製造して使用する2つの方法があり、特許期間は2031年までである。
2022年、私たちはパキスタンで特許を取得し、米国、オーストラリア、カナダ、中国、ヨーロッパ、香港、インドネシア、インド、イスラエル、日本、マレーシア、メキシコ、ニュージーランド、パキスタン、フィリピン、ロシア連邦、サウジアラビア、シンガポール、南アフリカ、韓国、台湾、ウクライナの特許を含む世界的な知的財産の組み合わせをさらに拡大しました。これらの外国特許は,物質の組成,製造方法,ZILRETTAを用いた方法をカバーしており,上記米国の保護と同様の範囲である。
我々はまた,西南研究院(SWRI)が所有するライセンス内知的財産権を有しており,ZILRETTAを製造するための独自微小球製造技術をカバーしたSWRI特許の独占的権利を獲得した。これらの特許は2025年に満期になる予定だ。
Ioveraの特許と特許出願
米国で発行された特許はiovera°技術の様々な面で広いカバー範囲を提供してくれた。例えば、我々が最初に提出したいくつかの特許は、単針および針アレイを有する手持ち式低温装置の構造的態様、取り外し可能な組織貫通針プローブ、溶融シリコン管流体輸送経路、低温装置を用いた凍結治療方法、および交換可能な針プローブを使用する方法をカバーする。これらの特許は2025年から2032年の間に満期になるだろう。痛みの治療に特化したシステムおよび方法の重要な特許シリーズは、使い捨ての針、特殊な針サイズおよび形状を含む、広範かつ可変な低温デバイス特徴およびそれを使用して疼痛管理を行う方法を提供する。この一連の特許は2025年から2028年の間に満期になるだろう。もう一つの重要な特許ファミリーは、関節機能および硬直、骨関節炎、後頭神経痛、痙攣、神経腫、および他の神経圧迫適応を含む低温装置治療の様々な適応を広く開示し、カバーし、2033年から2037年に満了する。
さらに、iovera?技術の他の重要な側面に関するいくつかの特許と出願されている特許がある。例えば、プローブフィルタシステムに関する特許は2033年に満了し、スマート先端技術の特許は2034年から2037年の間に満了する。他の特許および出願は、不動態化先端の針を使用する方法と、神経刺激器と組み合わせて神経を位置決めする低温装置の側面をカバーしており、これらの特許および出願は2035年から2038年に満了する。現在商業化され開発されている次世代技術をカバーする8つの新しい実用·設計特許ファミリーがあり、これらの特許は北米、ヨーロッパ、日本、中国、ブラジル市場で発表または発表を待っており、これは、他の会社がこのような現在商業化されている次世代低温設備を使用することを阻止し、少なくとも2040年までの公共事業特許および2046年の設計特許を必要とする可能性がある。
また,2022年には電気嵐を含めたiovera°を星状神経節ブロックとして用いた不整脈の管理に関するいくつかの仮申請を提出した。
PCRX-201
2017年12月、Flexionは、BQ Bio Treateutics GmbH(GeneQuine BioTreateutics GmbH)からPCRX-201のグローバル権利を買収し、ベイラー医学院が所有するいくつかの基礎特許、特許出願、および他の独自の権利の直接独占許可を含み、これらの特許は、PCRX-201のヒトアプリケーションの使用に関連している。これらの特許は、PCRX−201が骨性関節炎を治療する物質組成および使用方法を実質的にカバーする。2019年、米国特許商標局は、骨性関節炎の治療におけるPCRX−201の物質組成および使用方法をカバーした米国第10,301,647号特許を発行し、2033年1月まで有効である。また、PCRX−201に関連するベイラー特許は欧州で発行され、満期日は2032年、オーストラリア、カナダ、中国、インド、日本、ユーラシア大陸で発行され、満期日は2033年である。私たちはPCRX-201に関連する米国ベラー特許出願を起訴し続けている。さらに、私たちは、ヒト骨性関節炎の治療におけるPCRX-201の物質組成および有効用量をカバーし、承認されれば、2040年までの保護を提供する予定であるブラジル、中国、ヨーロッパ、日本、および米国でPCT出願に基づく国家段階に入っている。
我々には、PCRX-201による変性間盤疾患(DDD)の治療に関する米国出願とPCT出願とがあり、承認されれば、2042年までの保護が提供されることが予想される
Pacira BioSciences,Inc.|2022 Form 10-K|21ページ
他の知的財産権
我々のPCT出願は,トリブロックコポリマー成分(1つ以上のPLGA−ポリエチレングリコール−PLGAトリブロックコポリマー)で調製されたアミノアミド系麻酔薬(リドカイン,ブピバカインおよびロビカイン)の物質組成,使用方法および製造方法をカバーしており,変換および承認されれば2042年までの保護が提供される予定である。
ビジネス秘密と独自の情報
ビジネス秘密は,我々のpMVLに基づく製品(EXPARELを含む)やパイプ,ZILRETTAおよびiovera°を保護する上で重要な役割を果たしており,特許や法規を超えた排他的な保護を提供している。PMVLに基づく製品とiovera°製品の拡大と商業化生産は,プロセス,カスタマイズ設備およびプロセス中および放出分析技術に関連しており,これらの技術は我々にとって唯一無二であると考えられる。我々のpMVL製造手順の肝心な方面に必要な専門知識と知識を理解するためには、伝統と非伝統エマルジョン加工及び伝統製薬生産方面の知識を理解する必要があり、同時に無菌製造によるすべての挑戦を理解する必要がある。ZILRETTAはまた、ZILRETTAにおけるTA処方のPLGAマイクロスフェアに関連するいくつかの処方および製造技術に関するカスタマイズ装置および独自プロセスを使用して、その正確な薬物放出状態に関連する技術を含む製造を行う。Iovera?システムはカスタマイズ製造技術により,自給式手持ち式低温設備に必要な精度と緊急公差を提供することができる。さらに、iovera?デバイスは、凍結治療中のデバイス動作のための独自のソフトウェアをさらに含む。
私たちは、従業員、コンサルタント、および他のコンサルタントが、雇用または採用開始時に独自の情報および秘密協定に署名することを要求する、私たちのビジネス秘密およびノウハウを含む当社の固有情報を保護することを求めています。これらの合意は、一般に、我々との関係過程で開発または開示されたすべての機密情報を秘密にしなければならず、特定の場合でなければ、第三者に開示してはならないと規定している。私たちの従業員の場合、協定は一般的に、法的に許可された範囲内で、私たちのために従事している仕事、私たちの財産、または私たちの業務に関連するすべての発明、および雇用中に構想または完成した発明は、私たちの固有の財産でなければならないと規定している。適切な場合、私たちが私たちのコンサルタントと達成した合意は、一般に同様の発明義務分配も含む。さらに、私たちは私たちの機密データや材料を受け取った第三者の秘密協定を得る必要がある。
競争
製薬業界は競争が激しく、迅速で重大な技術変革の影響を受けている。私たちの競争相手には大手多国籍製薬会社、老舗バイオテクノロジー会社、専門製薬会社、後発薬会社などの組織があります。私たちの多くの競争相手は、より多くのビジネス資源、より多くの研究開発者、およびより広範なマーケティングと製造組織のような、私たちよりも多くの財務および他の資源を持っている。そのため、これらの会社が上場承認を得る速度は私たちより速いかもしれません。彼らの製品を開発、販売、マーケティングする上でもっと効果的かもしれません。規模が小さいか早い段階にある会社も重要な競争相手になる可能性があり、特に大手老舗会社との協力で手配されている。
ExparEL
私たちの競争相手は、EXPARELまたは現在パートナーによって販売または開発されている、または私たちが開発する可能性のある他の任意の製品よりも効果的またはより安価な技術および医薬製品の開発、買収または独占ライセンスに成功する可能性があり、これは、私たちの製品を時代遅れにし、競争力を持たないかもしれない。我々が開発·商業化したどの製品も,有効性,安全性,管理·交付の利便性,価格,政府や他の第三者支払者が精算できるかどうかをもとに競争することが予想される
ExPARELは類似適応を有する成熟製品と競合している。術後鎮痛に使用可能な競争製品はモルヒネ、フェンタニル、度冷丁と水素モルヒネなどのオピオイド薬物を含み、それぞれはいくつかの製造業者から獲得することができ、その中のいくつかは特許製品として新しい投与システムを使用することができる。ケトロール酸は、非ステロイド性抗炎症薬、または非ステロイド性抗炎症薬と呼ばれ、米国でもいくつかのメーカーが提供しており、非ステロイド性抗炎症薬Caldolor(注射用イブプロフェン)は、成人の疼痛および発熱の治療のためにFDAによって承認されている。ExPARELはまた、ブピバカイン、マカイン、ロビカイン、他の麻酔薬/鎮痛剤などの現在市販されている非オピオイド薬と競合しており、これらのすべての製品も術後疼痛の治療に使用され、経口錠剤、注射剤形、または新しい投与システムの形態で提供されている。新しい注射可能な非ステロイド抗炎症薬、新しいオピオイド、既存の新しい製剤を含む急性疼痛を治療するためのより多くの製品を開発することができます
Pacira BioSciences,Inc.|2022 Form 10-K|22ページ
オピオイドと非ステロイド抗炎症薬,長時間作用局所麻酔薬と新たな化学物質,各種オピオイドと非ステロイド抗炎症薬の代替投与形態。現在,EXPARELは,数日間ブピバカインを提供するためのエラストマーポンプやカテーテル装置,および他の承認された鎮痛剤のラベル外組み合わせ(“カクテル”と呼ぶ)とも競合しており,これらの薬剤は複合薬局によって併用され,疼痛制御の持続時間の延長を図っている。
ZILRETTA
速放ステロイドとヒアルロン酸注射剤は現在市場でZILRETTAと直接競争している2種類のIA製品である。幹細胞やPRP注射も利用可能であるが,これらは患者の組織や血液から現場で準備する必要があり,対照臨床試験で疑わしい効果が生じている。これらは最小限に操作された自己療法であるため,不要であり,FDAの審査や承認も得られていない。このため,彼らは通常支払人の精算を受けることはなく,患者は自腹を切ってこれらの治療を受けなければならない。また,米国寛骨膝外科医協会(AAHKS)は幹細胞およびPRP注射を含む生物療法による末期股関節や膝関節関節炎の治療を推奨していないことを示す立場声明を発表した。
Iovera°
医療機器業界の競争は激しく,迅速かつ重大な技術変革の影響を受けている。冷凍治療疼痛管理領域、特に絶えず増加している業界は、人々がオピオイド類薬物の痛みへの関心がますます多くなっているため、これは迅速に台頭する市場を創造し、そして人々のオピオイド類薬物代替品に対する興味を日々増加させている。私たちの分野の多くの競争相手は、より多くのビジネス資源、より多くの研究開発者、およびより広範なマーケティングと製造組織のような、私たちよりも多くの財務および他の資源を持っている。そのため、これらの会社が上場承認を得る速度は私たちより速いかもしれません。彼らの製品を開発、販売、マーケティングする上でもっと効果的かもしれません。凍結治療疼痛管理分野の様々な小型や早期会社の台頭も重要なライバルであることが証明されている可能性があり,特に大手成熟会社と協力していれば。
我々の競争相手は絶えず試験を行い,新たな製品や方法を開発し,疼痛管理市場の占領を図っている。彼らはiovera?システムよりも効率的でコストが低いかもしれない技術を独占的に開発し、獲得することに成功するかもしれないが、これはiovera?システムを時代遅れにし、競争力に欠けるかもしれない。したがって、私たちは革新を続け、私たちの初級市場でマーケティングを強化することは重要だ。我々が開発·商業化したどの製品も,有効性,安全性,管理·交付の利便性,価格,政府や他の第三者支払者が精算できるかどうかをもとに競争することが予想される。
痛みを治療する薬物製品のほかに、iovera°は末梢神経をアブレーション或いは退化させる医療設備と競争し、関節痛、神経痛と骨性関節炎疼痛などの特徴を治療する。競合する製品は、凍結治療装置および冷却無線周波数アブレーション装置などの他の装置を含み、これらの装置は、疼痛信号を伝達する末梢神経を遮断または劣化させることができる。Avanos Medical,Inc.は米国でこれらの医療機器を販売しています。私たちの1つ以上の競争相手は、痛みを治療するために他の非オピオイドまたは完全に異なる方法を開発することも可能です。
政府の監督管理
アメリカでは、処方薬と医療機器製品はFDAの広範な発売前と発売後の監督管理を受けており、連邦食品、薬物と化粧品法案(FDCA)及びその実施条例によるこのような製品の研究、開発、テスト、製造、流通、安全性、有効性、承認、ラベル、貯蔵、記録保存、報告、広告と普及などの方面の監督管理を含む。米国以外では、処方薬や医療機器製品は、類似機関(EUとイギリスのEMAとMHRA、およびカナダとラテンアメリカの当局を含む)、法律、法規によって規制されている。適用される規制要件を遵守しないことは、承認保留申請の拒否、承認撤回、警告状、臨床抑留、民事または刑事罰、製品のリコールまたは差し押さえ、禁止、禁止の取り消し、生産の一部または全部の一時停止、または市場からの製品の撤回につながる可能性がある。どんな機関や司法法執行行動も会社に重大な悪影響を及ぼす可能性がある。
環境を規制する
製薬業
米国では、一般的に、FDAは、以前に承認された薬物の新しい用途を含めて、その後、米国で発売されるために、任意の新薬を承認しなければならない
Pacira BioSciences,Inc.|2022 Form 10-K|23ページ
•FDAの“良好な実験室操作規程”に従って臨床前実験室と動物試験及び調合研究を完成した
•ヒト臨床試験が米国で承認されない前に発効しなければならない研究用新薬またはINDのヒト臨床試験申請をFDAに提出する
•各臨床試験が開始される前に、各臨床試験場所で独立した機関審査委員会またはIRBによって承認される
•FDAの良好な臨床実践またはGCPに基づいて、各予期される用途に対する提案された医薬製品の安全性および有効性を決定するために、十分かつ制御されたヒト臨床試験を行う
•技術検証、品質製品の排出と安定性を完了する
•FDAに新薬申請またはNDAを提出する
•CGMP要件に適合することを評価し、施設、方法、および薬物の特性、品質、および純度を維持するのに十分な施設、方法、および制御を保証するために、製品の1つまたは複数の製造施設の承認前検査を良好に完了させる
•適用されれば、FDA諮問委員会の審査が満足的に完了する;
•NDAに対するFDAの審査と承認。
臨床前と臨床テストと承認過程は大量の時間、精力と財力を必要とし、著者らはFDAが適時に私たちのいかなる候補製品を承認するかどうかを確定することができない。臨床前試験は製品の化学、調合と安定性の実験室評価、及び動物毒性の評価研究を含む。前臨床試験の結果は,製造情報,分析データ,提案された臨床試験案やその他の情報とともに,IND申請の一部としてFDAに提出された。INDはFDA受信後30日に自動的に発効し,FDAが臨床試験の進行やヒト研究対象の不合理な健康リスク曝露などの懸念から臨床試験を一時停止しない限り。この場合,INDスポンサーやFDAは臨床試験開始前に未解決の問題を解決しなければならない。したがって,IND提出自体はFDA認可による臨床試験の開始を自動的に招くわけではない。また,FDAは製品開発期間中に行った後続臨床試験ごとに既存のINDを修正することを求めている。また,臨床試験が予定されている各地点をカバーするIRBは,当センターの臨床試験が開始される前に,任意の臨床試験の計画および被験者のインフォームドコンセント情報を審査·承認しなければならない。IRBはまたそれが完了するまで臨床試験を監視しなければならない。FDA、IRB、またはスポンサーは、対象または患者が許容できない健康リスクに曝露されていることを発見することを含む、様々な理由で臨床試験を随時一時停止することができる。私たちはまた、変化するビジネス目標および/または競争環境に応じて臨床試験を一時停止または終了することができる。
臨床試験は、GCP要求に応じて、合格した研究者の監督の下で、候補製品を健康ボランティアまたは研究中の疾患を有する患者に投与することであり、すべての研究対象に任意の臨床試験に参加することを要求するインフォームドコンセントを含む。臨床試験のスポンサーは一般に米国国立衛生研究院(NIH)が維持しているサイト(www.Clinicaltrials.gov)に登録し,キー発見とパラメータを報告しなければならない。秘密協定の提出と承認のために、人体臨床試験は通常、以下の3つの上場前順序段階で行われ、この3つの段階は重複または合併する可能性がある
•第一段階:スポンサーは最初に限られた人々の中で臨床試験を行い,患者でも健康ボランティアでも,候補製品の安全性,用量耐性,吸収,代謝,分布,排泄と臨床薬理学をテストし,可能であれば有効性の早期証拠を得た。深刻または生命を脅かす疾患のためのいくつかの製品の場合、特に製品がそれ自体の毒性によって健康ボランティアに道徳的に服用できない可能性がある場合、最初の人体試験は、通常、特定の疾患を有する患者にのみ行われる
•第二段階:スポンサーは一般的に限られた患者群で臨床試験を行い、可能な副作用と安全リスクを確定し、この製品の特定の標的適応に対する治療効果を初歩的に評価し、そして用量耐性、最適投与量と用量計画を確定する。スポンサーは、より大規模かつより広範な3期臨床試験を開始する前に情報を得るために、複数の2期臨床試験を行うことができる。
•第3段階:その中に拡大対照試験と非対照試験が含まれ、肝心な臨床試験を含む。第2段階評価が製品の用量範囲の有効性および製品の安全プロファイルの受容可能性を示す場合、スポンサーは、薬物の全体的な利益およびリスクバランスを評価するために必要な追加情報を得るために、より大きな患者集団で第3段階の臨床試験を行い、ラベルを作成するために十分な基礎を提供する。
Pacira BioSciences,Inc.|2022 Form 10-K|24ページ
いくつかの臨床試験は、データ安全監視委員会または委員会と呼ばれる臨床試験スポンサーによって組織された独立した合格専門家グループによって監督される可能性がある。このグループは,実験のあるデータへのアクセスにより,許可試験が指定されたチェックポイントで行えるかどうかを決定する.1つの新薬が臨床試験を完成し、FDAの承認を得る過程は数年かかる可能性があり、大量の資源が必要である。申請を提出すれば,FDAがNDAを審査·承認する保証はない。また、スポンサーは、NDA承認後に薬物の安全性または有効性をさらに評価し、新たなデータおよび最適実践投与技術を生成するために、FDAの要求に応じて承認後の臨床試験を行うか、または行うことができる。承認後の適応研究は通常4期臨床試験と呼ばれる。
他の国では、薬物承認と臨床試験の要求は似ているが、各規制機関は異なる政策、手続き、プロセスを持っており、私たちはそれぞれの製品を販売する市場でこれらの政策、手続き、プロセスを遵守しなければならない。私たちの製品の承認や使用が他の管轄区域で同じであることも保証されない。例えば、EXPARELはヨーロッパでは成人術後疼痛の治療に許可されていますが、米国FDAではこの適応は承認されていません。しかし、下肢手術大腿神経ブロックの第3段階臨床試験としてのEXPARELの陽性結果に基づいて、2023年1月にsNDAをFDAに提出し、内転筋管の大腿神経ブロックと窩窩での坐骨神経ブロックを含めたEXPARELのラベルの拡張を求めており、PDUFAにおけるFDAの作用日は2023年下半期と予想されています。
医療機器
アメリカでは、1976年にFDCAに対する“医療機器修正案”及びその後の修正案は医療機器の設計、製造とマーケティングを規範化した。510(K)の承認要求の形態で通知を提出する必要がある医療機器は、FDAの審査および承認を経なければならず、その後、マーケティングを開始することができる。510(K)の許可を申請するためには、医療機器が以前に許可され、合法的に販売された510(K)の医療機器と実質的に等しいことを証明することができなければならない。医療機器は安全性と有効性研究、次いで発売前承認、あるいはPMAを含む広範な臨床テストが必要であり、特定の手術適応を申請する。FDAの品質体系法規、あるいはQSRと呼ばれ、私たちの製品設計と製造過程のために標準を制定し、ある記録を維持することを要求し、FDAが私たちの施設を検査することを規定した。私たちの製品を製造して販売する時にも、国、地方、外国政府のいくつかの要求は守らなければならない。510(K)除去の新しい適応は、必要とされる場合もあり、臨床試験を必要としない場合もある。Iovera°タグをけいれん治療を含めた臨床試験に拡張し,2023年に開始する予定である。
審査と承認の流れ
製薬業
すべての適用された法規要求に基づいてすべての要求されたテストが成功したと仮定し,スポンサーは製品開発,臨床前研究,臨床試験の結果をFDAに提出し,NDAの一部として,その製品を1つまたは複数の適応の市場に使用することの承認を求めた。NDAはまた,製品の薬理,化学,製造,制御,提案のラベルなどに関する広範な情報を含まなければならない。さらに、505(B)(2)出願は、出願に参照される薬剤をカバーし、第三者研究を行うFDAオレンジブックに記載された各特許の特許証明を含まなければならない。いくつかの薬物の場合、規制機関は、リスク評価および緩和戦略、すなわちREMSを必要とする可能性があり、その中には、投与ガイド、医師のコミュニケーション計画、または配布および使用の制限、例えば、誰が薬を処方することができるか、またはどこで配布または投与することができるかの制限を含むことができる。現在,FDAはEXPARELのREMSを要求していないが,EMAやMHRAは要求している。
FDAが実質的な審査の提出を受ける場合、FDAは通常、既定の時間枠に基づいてNDAを審査する。PDUFAによると、FDAは1つの2段階分類システムを通じてNDA審査時間の目標を確立した:優先審査と標準審査。優先審査の指定とは、治療において大きな進展を得ること、または現在十分な治療法がない場合に治療を提供することによって、満たされていない医療ニーズを満たす薬剤である。標準審査は優先審査資格を満たしていないすべての申請に適用される。FDAは、提出後12ヶ月以内(60日目の提出日後10ヶ月)にNDAの標準審査を完了し、提出後8ヶ月以内(60日目の出願日後6ヶ月)に優先審査を完了することを目標としている。SNDAについては,FDAは提出後10カ月以内に標準審査を完了し,提出後6カ月以内に優先審査を完了することを目標としている。FDAは、より多くの情報を提供すること、または明確にすること、諮問委員会会議を手配することが困難であること、REMSまたはFDAの仕事量に関する交渉を要求するため、審査プロセスがこれらの目標完了日の後に延長される可能性があるが、一般に、PDUFAによれば、FDAは、これらの要因が存在するにもかかわらず、目標時間枠内で審査を完了すべきである。FDAは、審査、評価、および提案申請の承認のために諮問委員会に申請を提出することができる。諮問委員会の提案はFDAを制限しないが、FDAは一般的にそのような提案に従う。
Pacira BioSciences,Inc.|2022 Form 10-K|25ページ
PDUFAにより,セキュリティプロトコル申請者は提出時に巨額のセキュリティプロトコル使用料を支払わなければならない.また,承認された処方薬製品のメーカーは,EXPARELやZILRETTAに対して行ったように年間計画費用を支払わなければならない。
秘密協定を承認する前に、FDAは製品を生産する1つまたは複数の施設を検査するだろう。FDAは、製造プロセスおよび施設がCGMP要件に適合していることを決定し、要求された仕様の下で製品が一貫して生産されることを保証するのに十分でない限り、申請を許可しないであろう。さらに、FDAは、通常、GCPに適合することを確実にするために、NDAを承認する前に1つまたは複数の臨床場所を検査する。
FDAがNDAおよび製造施設を評価した後、それは、申請の審査期間が完了したことを示すために、承認書または完全な応答手紙またはCRLを発行することができ、この申請は承認の準備ができていない。CRLは、通常、提出中の不足点を列挙し、FDAが申請を再検討するために、大量の追加のテストまたは情報を必要とする可能性がある。このような補足情報を提出しても,FDAはNDAが承認基準を満たしていないことを最終的に決定する可能性がある。臨床試験のデータは常に決定的ではなく,FDAによるデータの解読は我々とは異なる可能性がある。FDAがREMS計画を要求する場合、それは、投与方法、患者登録、および他のリスク最小化ツールのような薬物ガイドライン、医師コミュニケーション計画、または安全な使用を保証する要素を含むことができる。FDAはまたNDAを承認することができ、条件は提案されたラベルを変更し、1つ以上の上場後の研究或いは臨床試験を行うことを承諾し、十分な制御と規範を制定することを含む発見された製造欠陥を是正することを含む。もしこのような欠陥がFDAによって満足的に解決された場合、FDAは通常承認書を発行するだろう。この薬物の商業マーケティングを許可し、特定の適応の具体的な処方情報を提供する。
米国以外では、具体的な規制手順のスケジュールが異なるにもかかわらず、一般的な原則は同じであり、患者登録およびリスク最小化ツールを含む他の要求が必要となる可能性のあるREMS計画を含むが、これらに限定されない。
医療機器
米国では,医療機器を市場に出す許可は通常2つの方法のうちの1つで得られる。第1のアプローチは、発売前通知(510(K)プロセス)であり、新しいデバイスがすでに合法的に発売された医療デバイスと実質的に等しいことを証明する必要がある。第2のアプローチはPMAであり,医療機器がその期待用途に対して安全かつ有効であることを証明する独立した証明が必要である。一般に、プロジェクト管理プロトコルは、より長い時間範囲を必要とし、510(K)プログラムによって許可される費用よりもはるかに高い可能性がある。デバイスが510(K)承認フローに適合していないと判定された場合、PMAをFDAに提出しなければならない。PMAは技術、臨床前と臨床試験、製造とラベルを含むが、この装置の安全性と有効性を証明する合理的な証拠を含み、FDAを満足させるために、大量のデータの支持を受けなければならない。
510(K)の承認を得るためには、提案された装置が以前に承認され、合法的に発売された510(K)装置、または1976年5月28日以前に商業流通中にあった装置と実質的に同等であることを証明する上場前通知をFDAに提出しなければならず、FDAはPMAの提出を要求していない。Iovera°の前身装置が510(K)の許可を初めて得たのは2009年3月であり、当時MyoScienceの重点は美容アプリケーション(すなわち顔しわ除去)であった。MyoScienceは2014年に疼痛管理に重点を置き、それ以来多くの進展を遂げ、iovera°およびその後のiovera°製品ラインの増加をサポートするために、他の510(K)計画の提出と承認を招いた。
デバイスが510(K)の許可またはPMA承認を取得した後、変更または修正することができる。その安全性または有効性に深刻な影響を与える可能性のある修正、またはその予期される用途に大きな変化をもたらす可能性のある任意の修正は、新たな承認または承認が必要となる。規制は、製造業者がいつ特定の改正をFDAに通知する必要があるかを最初に決定する。FDAはすでにガイドライン草案を発表しており、最終的に決定されて実施されれば、製造業者は合法的に販売されている設備の変更のために多くの新しい許可を求める必要があるだろう。FDA審査製造業者は、工場監査中に510(K)またはPMAを提出して修正の決定を行う。
第五百五十五条第二項新薬出願
医薬品の場合、FDA承認を得るための代替経路として、特に以前にFDA承認を受けた医薬品の修正については、出願人は、FDCA第505(B)(2)条に従って秘密協定を提出することができる。第505条(B)(2)条は、1984年に“医薬品価格競争及び特許期限回復法”(“ハッジ·ワックスマン法”とも呼ばれる)の一部として公布され、申請者又は出願人のための臨床前及び/又は臨床試験ではない場合からの機密協定の提出を少なくとも部分的に承認することを可能にする。FDAはFDCA第505条(B)(2)条を解釈する
Pacira BioSciences,Inc.|2022 Form 10-K|26ページ
出願人がFDA以前に承認された製品の安全性及び有効性に関する調査結果に依存することを可能にする。FDAはまた、以前に承認された製品との任意の変化をサポートするために、追加の臨床試験または測定を行うことを企業に要求する可能性がある。次に、FDAは、参照製品のすべてまたは一部が承認されたラベル適応および第505条(B)(2)の出願人が求めた任意の新しい適応について新製品候補を承認することができる。
第505条(B)(2)条に従って提出された出願は、参照製品に適用される任意の非特許専有期間によって制限され、これは、FDAが実質的な審査を完了し、薬剤が承認されるべきであると判断したとしても、505(B)(2)出願の承認を延期する可能性がある。さらに、505(B)(2)出願は、参照製品をカバーするFDAオレンジマニュアルに記載されている任意の特許の特許証明を含む必要がある。505(B)(2)出願人が適用される上場特許の満了前に承認を得ることを求める場合,505(B)(2)出願人は,参照製品の特許権者及び秘密協定保持者に通知を出さなければならない。特許所有者または秘密保持者が通知後45日以内に特許侵害訴訟を提起した場合、505(B)(2)出願は30ヶ月以内に承認を得ることができず、または505(B)(2)出願人が勝訴するまで、両者はより早い者を基準とする。505(B)(2)出願人が特許侵害訴訟で敗訴した場合、FDAは、特許が満了するまで、任意の時期の小児科排他性を加えて505(B)(2)の出願を許可しない可能性がある。
将来私たちの候補製品に提出される任意の秘密協定では、FDCAによって許可される開発と承認経路に従う予定であり、これらの候補製品のビジネス機会を最大化すると信じています。
承認後に要求する
製薬業
承認された後、NDAスポンサーは薬品の発売、記録保存、製造、マーケティング活動、製品のサンプリング、流通と年度報告などの方面の全面的な要求を守らなければならない。また,有害事象は速やかにFDAに報告しなければならず,FDAは有害事象を能動的に探す薬物警戒計画を規定している。有害事象とは,患者の医療製品の使用に関するいかなる不良体験である。深刻な不良事件とは死亡を招き、生命に危害を及ぼす或いは入院或いは障害などを招く不良事件である。これらのイベントが、問題のある薬物が新しいセキュリティ信号を有することを示す場合、製品または追加のREMSのラベルに安全宣言を追加する必要がある可能性がある。さらに、他の薬物で発見された有害事象は、私たちが追加的な安全措置を遵守し、私たちのラベルに警告を含まなければならないことを意味するかもしれない。米国以外の規制機関にも似たような報告や薬物警戒義務がある。
承認後に新しいセキュリティ問題が発見された場合、FDAは、新しいセキュリティ情報を反映するために承認されたラベルを修正するようにNDAスポンサーに要求することができ、新しいセキュリティ情報を評価し、新しい発見のリスクを低減するためにREMS計画を実施するために発売後研究または臨床試験を行うことができる。FDAはまた、商業化された承認製品の効果を監視するための第4段階試験および監督計画を含む承認後試験を要求する可能性があり、FDAはこれらの上場後計画の結果に基づいて製品のさらなる販売を阻止または制限する権利がある。薬品は承認された適応とFDA承認のラベルの規定でしか販売できない。さらに、適応、ラベル、または製造プロセスまたは施設の任意の変化を含む薬物を修正する場合、FDAは、新しいまたは追加のNDAに対するFDAの承認を提出し、取得することを要求することができ、これは、追加のデータの開発または追加の臨床前研究および臨床試験を必要とするかもしれない。
また、薬品メーカーと生産と流通許可薬品に参加する他の実体はFDAと州機関にその機関を登録し、CGMP要求に適合することを確保するために、FDAとこれらの州機関の定期的な抜き打ち検査を受けなければならない。製造プロセスの変更は厳しく規制されており,通常FDAが事前に承認して実施する必要がある。FDAの法規はまた,CGMPから外れた任意の状況を調査·是正し,我々と我々が使用することが可能な任意の第三者メーカーに対して報告や文書要求を行うことを要求している.
FDAが承認後に、製品が適用可能な規制要件に適合していないと判断した場合、または受け入れられないセキュリティリスクを構成する場合、FDAは、NDA承認の一時停止または撤回を開始することを含む他の規制行動をとる可能性がある。その後、予想されていない深刻度や頻度の不良事象、または製造過程、または法規要件を遵守できなかったことを含む、以前の未知の製品問題が発見され、他のものを除いて、以下のようになる可能性がある
•製品の販売や製造を制限し、市場から製品を完全に撤回したり、製品をリコールしたりする
•承認後の臨床試験には罰金、警告状、一時停止を科す
Pacira BioSciences,Inc.|2022 Form 10-K|27ページ
•FDAは、承認されるべき出願または承認された出願の追加申請を拒否するか、または製品ライセンスの承認を一時停止または撤回する
•製品を差し押さえたり、差し押さえたり、製品の輸出入を許可することを拒否したりする
•民事または刑事処罰を禁令または適用する。
FDAは市場に投入された製品のマーケティング、ラベル、広告、販売促進を厳格に規制している。これらの規定には、消費者向け広告、業界スポンサーの科学的および教育活動、インターネットに関連する販売促進活動、ラベル外販売促進の基準および制限が含まれる。医師は非ラベル用途の処方を出すことができるが,メーカーは承認されたラベルの規定に基づいて承認の適応を宣伝することしかできない。FDAはFDCAの下で非常に広範な実行権を有しており,これらの規定を遵守しないと警告状の発行,FDA標準との偏差の是正を実体に指示すること,将来の広告や販売促進材料がFDAの承認を事前に得なければならないこと,州と連邦民事·刑事調査·起訴を要求することを含む罰を受ける可能性がある。
そのほか、処方薬製品の流通は“処方薬販売法”(PDMA)の制約を受け、この法案は連邦一級で薬品と薬品サンプルの流通を管理し、各州の薬品流通業者に対する登録と監督管理に最低基準を設定した。PDMAも州法も処方薬製品サンプルの分配を制限し,処方薬の分配を追跡する薬物スペクトルを含む分配中の責任を確保することが求められている。
医療機器
FDAは広範囲な発売後と規制義務を持っており、私たちは守らなければならない。私たちはQSRと他の規制を遵守するかどうかを確認するためにFDAの抜き打ち検査を受けた
医療機器が市場に投入された後、多くの監督管理要求を満たす必要がある。これらの措置には限定されるものではない
•QSRは、製品設計および製造プロセス全体にわたって厳格な設計、テスト、文書、および他の品質保証手順に従う第三者製造業者を含むことを要求する
•ラベル規制およびFDAは、未承認、未承認、またはラベル外用途のための製品の普及を禁止すること;
•医療機器報告法規は、製造業者が、その装置が死亡または重傷または障害を引き起こす可能性がある場合にFDAに報告することを要求し、故障が再び発生した場合、死亡または重傷を引き起こす可能性がある。
規制要件を遵守しないことは、FDAが法執行行動をとることを招く可能性があり、その中には、以下のいずれかの制裁が含まれている可能性がある
•製品の販売や製造を制限し、市場から製品を完全に撤回したり、製品をリコールしたりする
•承認後の臨床試験には罰金、警告状、一時停止を科す
•以前に承認された510(K)計画または他の承認を取り消すことができる
•FDAは、承認されるべき出願または承認された出願の追加申請を拒否するか、または製品ライセンスの承認を一時停止または撤回する
•製品の差し押さえ、差し押さえ、あるいは製品の輸出入を許可しないことを拒否した
•民事または刑事罰の命令または適用を禁止する;または
•私たちが製造または流通した任意の医療機器のコストを修理、交換、および/または返却することを要求します。
もしこのような事件のいずれかが発生すれば、私たちの業務に実質的な悪影響を及ぼす可能性がある。
国際規則
アメリカの法規以外に、私たちは各種の外国法規の制約を受けて、これらの法規は私たちの臨床試験と私たちの製品の商業販売と流通を管理しています。私たちの製品がfdaの承認を得たかどうかにかかわらず、私たちは臨床試験や発売を開始するために、外国の比較可能な監督管理機関の承認を得なければならない
Pacira BioSciences,Inc.|2022 Form 10-K|28ページ
これらの国の製品。承認手続きや要求は国によって異なり、時間はFDA承認に要する時間よりも長いか短い可能性がある
例えば、ヨーロッパでは、承認を求める製品タイプによって、薬品発売審査、製品審査と承認後の監督管理の流れにはいくつかの軌道がある。集中手続きの下で、ある会社は環境管理協会に申請を提出した。マーケティング申請は米国のNDAに類似しており,EMAの専門家科学委員会CHMPによって評価されている。もし中国食品薬品監督管理局が発売申請が品質、安全と治療効果の要求に符合すると確定すれば、それはヨーロッパ共同体に有利な意見を提出する。CHMPの意見は拘束力がないが、通常ヨーロッパ共同体に採択されている。欧州共同体が承認したマーケティング申請はすべてのEU加盟国で有効であり、MHRAの承認を得た。すべての生物製品、孤児薬品と神経退行性疾患の新しい治療法は集中的なプログラムが必要であり、ある他の製品は、それらの重大な治療、科学或いは技術革新を構成する製品を含み、このようなプログラムを採用することもできる。
FDA、EMA、MHRAの承認と同様に、もしあれば、追加の規制承認をタイムリーに得ることができないかもしれない。また、米国と同様に、製品製造、マーケティング、または流通に関する要求のような承認された規制要件は、ヨーロッパ、イギリス、カナダ、ラテンアメリカで承認された任意の製品に適用され、これらの義務を遵守しなければ、任意の製品を商業化することに成功する能力に重大な悪影響を及ぼす可能性がある。
ヨーロッパとアメリカの法規に加えて、イギリス、カナダ、ラテンアメリカおよびEXPAREL、ZILRETTA、IOVERA°または任意の他の未来の製品が承認された任意の他の司法管轄区域の臨床試験、製品承認、および商業流通法規を遵守します。
第三者支払者は保証と精算を請け負う
私たちの製品と候補製品の商業成功は、連邦、州、そして個人レベルの第三者支払者が保険と補償を提供するかどうかにある程度依存するだろう。政府支払人計画は、MedicareとMedicaid、私営医療保険会社と管理医療計画を含み、製品や治療法が医学的に不適切または不必要であることが確定された場合、全部または一部の保証または精算を拒否する可能性がある。また,第三者支払者は,特定のプログラム,医療機器,薬物治療のカバー範囲や精算金額を制限することでコストを抑制しようとしている。米国議会や州立法機関は、コストを抑えるための措置を時々提案し、採択することで、製品を十分に高い価格で販売する能力に影響を与え、適切な投資リターンを実現する可能性があり、これは私たちの運営結果に実質的な影響を与えるだろう。
2010年3月、オバマ総裁は、“医療·教育負担能力調整法案”(“平価医療法案”と総称する)によって改正された“患者保護·平価医療法案”に署名し、医療保険の許容性を拡大し、医療支出の増加を減少または制限し、詐欺や乱用に対する救済措置を強化し、医療保健·医療保険業界の新たな透明性要求を増加させ、医療業界に新たな税費を徴収し、追加の医療政策改革を実施することを目的とした包括的な法律である。報告を容易にするために,“平価医療法案”は“メーカー平均価格”の定義を改正し,製薬業者がカバーする外来薬に対する各州の医療補助薬品払い戻し額を増加させる可能性がある。“平価医療法案”はまた新しい連邦医療保険D部分保証切欠き割引計画を構築し、この計画によると、薬品メーカーは保証間隔期間内に条件を満たす受益者に適用ブランド薬品交渉価格の50%の販売時点割引を提供することに同意しなければならず、メーカーの外来薬として連邦医療保険D部分保証の条件に組み込まれている。また、コンプライアンスに影響を与える大量の新しい条項が公布されており、これは私たちと医療従事者の業務やり方を修正する必要があるかもしれない。“平価医療法案”の一部として拡大されたこのような政府計画は340 B薬品定価計画であり,医療補助に参加する製薬業者が衛生·公共サービス部部長と薬品定価協定,すなわちPPAを締結することを要求している, そして、製造業者に割引を340 B薬品定価計画がカバーするエンティティに拡大することを要求した。340億ドルの医薬品価格設定計画は、米国経済の最も脆弱な患者集団に接触することができる財源の希少な実体をカバーすることを目的としている。国会は“平価医療法案”の廃止を含む医療に関する立法イニシアティブをいくつか提案している。平価医療法案に変化があるかどうかは不明である。平価医療や他の新しい法律が私たちの業務にどの程度影響を与えるかはまだ定かではない。しかし,このような法律は薬品定価に圧力をかけ続ける可能性があり,特に連邦医療保険計画の下では,我々の規制負担や運営コストを増加させる可能性もあるようである。また,今後数年で政府医療計画がより多く変更される可能性があり,我々の製品の成功に大きな影響を与える可能性がある。
2022年12月,2023年総合支出法案の一部として,総裁·バイデンは非オピオイド防止国家添加法案に署名し,連邦認可であり,医療保険に非オピオイドの返済を要求する費用である
Pacira BioSciences,Inc.|2022 Form 10-K|29ページ
ASCや病院外来(HOPD)環境で行われているすべての手術で使用されている製品,例えばEXPAREL。具体的には、NOPAIN法案は、(I)ヒトオピオイド受容体に作用せず、術後疼痛を軽減するため、または術後局所鎮痛を産生するためのすべての非オピオイド薬、および(Ii)術後疼痛の治療または軽減または術後または局所鎮痛を産生するためのすべての装置を提供するための精算を含む。NOPAIN法により補償を受ける資格がある任意の薬物或いは装置は、術中オピオイドの使用或いは臨床試験で処方されたオピオイドの数を減少或いは回避する能力があることを証明しなければならない、或いは同業者評議定期刊行物に発表されたデータを通じて。医療保険·医療補助サービスセンター(CMS)はNOPAIN法案の実施に時間を要し,2025年1月から施行される見通しである。
政府と第三者支払者が十分な保険と補償を提供できなければ、私たちの製品の適正性が影響を受ける可能性があります。また,米国では管理式医療への重視が増加しており,医薬品や医療機器の価格設定への圧力が増加していくと予想される。一部の第三者支払者は,新たな設備や革新的な設備や薬物療法の保証範囲をあらかじめ承認しておくことを要求し,そのような治療法を用いた医療提供者に精算したり,精算金額を制限したりする。引受政策と第三者支払人の精算料率は随時変化する可能性がある。私たちの製品が有利な保証と精算状態を得ても、将来的にはあまり有利ではない保証政策や精算料率が実施される可能性があります。
国際市場では,精算や医療保険支払い制度は国によって異なり,多くの国で特定製品や治療法に価格上限が設定されている。私たちの製品が医学的に合理的であることは保証できません。特定の適応が必要で、私たちの製品が第三者支払者によって費用効果があると思われる保証はありません。また、第三者支払人の精算政策が私たちの販売製品の収益力に悪影響を与えないように、十分な精算レベルを持っている保証はありません。
マーケティングとデータ独占性
FDCA下の市場排他性条項は、他の会社の秘密協定を引用することを求める他の会社のいくつかの申請の提出または承認を延期する可能性がある。出願人によるまたは賛助された新しい臨床研究が承認申請に重要である場合、FDAは、既存の薬剤の新しい適応、用量、または剤形を含む新しいまたは補足的なNDAを承認するために、米国に3~5年の市場排他性を付与することができる。FDAが以前に同じ活性部分を含む他の新薬を承認していなければ,薬物は新しい化学実体であり,活性部分は薬物物質の作用を担う分子やイオンである。排他的期間内に、FDAは、出願人が承認のために必要なすべてのデータを合法的に参照する権利を有していない場合、FDAは、薬剤の別のバージョンのために別の会社に提出された簡略化された新薬出願またはANDAまたは第505(B)(2)条のNDAを受け入れない可能性がある。しかしながら、このような出願は、イノベーターNDA所有者がFDAに列挙した特許のうちの1つの特許の無効または未侵害の証明を含む場合、4年後に提出することができる。FDCAはまた、NDAに3年間の市場排他性、または既存のNDAの補充を提供し、申請者が行ったり賛助したりする新しい臨床研究(バイオアベイラビリティ研究を除く)がFDAによって承認申請に重要であると考えられている場合、例えば既存の薬物の新しい適応、用量または強度である。また、FDCA第505 A条によれば、FDAの書面による請求に応じて、米国で6ヶ月間の市場独占経営権を得ることができる, スポンサーは,承認された薬物の小児科群における使用に関する要求された情報を提出し,機関はその情報を受け入れる。この6ヶ月の小児科専門期間は、独立した専門期間ではなく、医薬製品が取得する資格のある任意の既存特許または非特許専門期間に添加される。過去,我々のEXPAREL臨床試験計画によると,FDAはEXPARELに3年間の市場独占経営権を付与し,この独占経営権は2014年10月に満期となった。欧州では、メーカーはマーケティング許可を得た後、8年間のデータ独占経営権と他の2年間の市場独占経営権を取得する資格があり、合計10年間の監督独占経営権がある。
製造要求
私たちはFDAのCGMP要求と他の国の似たような規制を守らなければならない。CGMP規定には、人員、建物および施設、設備、アセンブリおよび薬品容器および封口の制御、生産およびプロセス制御、包装およびラベル制御、保有および分配、実験室制御、記録および報告、ならびに返品または回収された製品に関する要件が含まれる。我々の製品の製造施設はCGMP要求に適合しなければならず,FDAや他の権威機関が承認前の検査に満足させるためには,それらを用いて我々の製品を生産することができる。私たちと私たちが雇用したり、私たちと協力したりする任意の第三者メーカーも、私たちの製品をテストして製造する際に使用する手続きや操作を含むFDAや他の権威機関の定期的な施設検査を受けて、私たちが適用される法規に適合しているかどうかを評価しなければならない。これらと他の法律と規制要件を守らないと、メーカーは警告状、製品の差し押さえまたはリコール、禁止、同意法令を含む可能な法律または規制行動に直面するだろう
Pacira BioSciences,Inc.|2022 Form 10-K|30ページ
生産作業に重大な制限または一時停止を実施し、民事と刑事処罰を科す。製品または製品苦情の不良経験を報告しなければならず、ラベルを変更したり、製品を除去したりすることによって市場制限を実施することになる可能性がある。規制要件の遵守が維持されていない場合、または承認後に製品の安全性または有効性に関する問題が生じた場合、製品承認は撤回される可能性がある。
販売とマーケティングに関する規定
私たちは、リベート法や虚偽申告法を含む、ヘルスケアの“詐欺と乱用”に関する様々な連邦や州法に支配されている。逆引き落とし法は、一般に、特定の薬品または器具の処方を購入または発行することを含む、任意の報酬を生成するために、処方薬または医療機器製造業者が誘致、提供、受け入れ、または支払うことを禁止する。これらの法律の具体的な規定はそれぞれ異なるにもかかわらず、それらの範囲は通常広く、これらの法律が特定の業界実践にどのように適用されるかを明らかにするための法規、指導意見、または裁判所判決はないかもしれない。したがって、私たちの接近は逆リベートや似たような法律の挑戦を受けるかもしれない。虚偽請求法は、虚偽または詐欺的な精算薬、プログラムまたはサービスのクレーム、またはクレームによって提供されていない項目またはサービスに対するクレーム、または医療上不必要な項目またはサービスに対するクレームを第三者支払者(MedicareおよびMedicaidを含む)に第三者に提出することを禁止する。これらの法律によると、私たちの製品販売やマーケティングに関する活動が審査される可能性があります。詐欺や法律違反行為は、罰金や民事罰金を含む刑事または民事制裁を受ける可能性があり、連邦医療計画(連邦医療保険や医療補助を含む)から除外される可能性がある。米国では,連邦や州当局は製薬や医療機器業界におけるこれらの法律の執行状況にますます注目しており,個人はこれらの法律の違法行為を積極的に告発し,連邦民事虚偽クレーム法案に基づいて政府を代表して訴訟を起こしてきた。もし私たちがこのような法律に関する告発を受けたり、これらの法律に違反したと判断されたら、私たちの業務は損害を受けるかもしれない。
連邦政府と各州はすでに法律と法規を公布し、薬品と医療機器メーカーの販売とマーケティングのやり方を規範化した。法律法規は、一般に、製造業者と医療提供者との間の財務的相互作用を制限するか、または政府および公衆にそのような相互作用を開示することを要求する。これらの法律には,連邦医師支払い法,あるいは“陽光”条項が含まれており,平価医療法案の一部として2010年に公布された。陽光条項は、ある政府計画に基づいて製品を精算する薬品および医療機器メーカーに適用され、これらのメーカーは、医師およびいくつかの他の保健従事者または教育病院に支払われたいくつかのお金を連邦政府に毎年開示(再開示)するように要求する。州の法律はまた、薬品と医療機器の価格設定情報とマーケティング支出の開示を要求するかもしれない。このような法律には曖昧な要求が多く含まれている。法律とその実施の不明確性を考慮して、私たちの通報行為は関連連邦と州法律法規の処罰条項の制約を受ける可能性がある。米国以外では,他の国では医療提供者との財務的インタラクションを開示する要求が実施されており,より多くの国ではこのような法律が考慮または施行される可能性がある。
再生医学高度療法
21世紀の一部としてST世紀治療法は、議会がRMATの称号を作成するためにFDCAを改正した。RMATの指定は再生医学高度療法の有効な開発と審査の加速を促進することを目的としており、これらの療法は深刻な或いは生命に危害を及ぼす疾患或いは状況の治療、修正、逆転或いは治癒を目的としている。RMATは、細胞療法、遺伝子療法、治療用組織工学製品、ヒト細胞および組織製品、および任意のそのような治療法または製品を使用する組み合わせ製品を含む。スポンサーは、INDの提出と同時にまたはその後の任意の時間に再生医学高度療法を指定することをFDAに要求することができる。例えば、PCRX−201のRMAT称号をFDAに申請することが意図されている。FDAは60個のカレンダー日が標準に符合するかどうかを確定し、初歩的な臨床証拠があるかどうかを含むことにより、深刻或いは生命に危害を及ぼす疾病或いは状況を解決する可能性のある満たされていない医療需要を表明した。再生医学先進療法のバイオ製品ライセンス申請(BLA)は、代理または中間エンドポイントを介して優先審査または加速承認を得る資格がある可能性があり、これらの代替または中間エンドポイントは、長期臨床利益を合理的に予測するか、または大量の臨床試験地点から得られたデータに依存する可能性がある。このような指定の利点はまた、承認の加速を支援するために、FDAと早期に相互作用し、任意の潜在的な代替または中間終点を議論することを含む。加速承認を獲得し、承認された後に要求される再生医学先進療法は、臨床証拠、臨床研究、患者登録或いはその他の真実の証拠源を提出することによって、これらの要求を満たすことができる, 例えば、電子健康記録、より大きな検証データセットを収集すること、または承認前に、そのような治療を受けたすべての患者を承認した後に監視すること。
医療プライバシーと安全法
私たちは制限されているか、あるいは私たちのマーケティング活動は“健康保険携帯性と責任法”または“HIPAA”とその実施条例の制限を受ける可能性があり、この条例はいくつかの“保険を受ける実体”(医療保健)のための統一的な基準を確立している
Pacira BioSciences,Inc.|2022 Form 10-K|31ページ
医療サービス提供者,医療計画,医療情報交換所)は,ある電子医療取引の進行を管理し,保護された医療情報の安全とプライバシーを保護する。2009年の“米国回復·再投資法案”(American Recovery And ReInvestment Act)は、通常、HIPAAのプライバシーとセキュリティ基準の全面的な拡張を含む経済刺激計画と呼ばれ、この基準は“経済·臨床健康情報技術法案”と呼ばれ、2010年2月に発効した。他の事項に加えて、HITECHは、保護された健康情報を受信または取得し、サービスを提供する独立請負者またはエージェントを表す、HIPAAのプライバシーおよびセキュリティ基準を“ビジネスパートナー”に直接適用する。HITECHはまた、実体、商業パートナー、および可能な他の人に適用される民事と刑事罰を増加させ、州総検察長に新たな権力を与え、連邦裁判所に民事訴訟を提起し、連邦HIPAA法を実行するために損害賠償または禁令を要求し、連邦民事訴訟の提起に関連する弁護士費と費用を求めることができる。
環境問題
我々の研究開発プロセスと製造プロセスは危険材料と化学品の制御使用に関連し、薬物残留を含む廃棄物製品を産生する。私たちは連邦、州、地方の法律と法規を受けて、危険な材料と廃棄物の使用、製造、貯蔵、処理と処分を管理し、薬物残留に関連する材料と廃棄物を含む。私たちは適用された環境法規を遵守していると信じていますが、このような法規を完全に遵守できなかったことは、罰、罰金、および/または制裁の適用につながる可能性があり、これは私たちの業務に実質的な悪影響を及ぼす可能性があります。未来にも私たちが今予測できない環境問題が発生する可能性がある。
廃棄物の削減,水回収,省エネルギー設備の可能な限りの使用などの重要なやり方で持続可能な足跡の改善に努めている。私たちのポイントは意識を高め、従業員に内部消耗品や自然資源の使用を減らすように教育することです。しかも、私たちは私たちの製造施設と会社のオフィスで広範な回収と廃棄物管理計画を持っている。例えば、私たちの内部製造施設では、紙製品、アルミニウム缶、ガラス、電子製品、プラスチックの使用と回収の問題を解決し、回収不可能な物品と効率的な水管理を責任を持って処分しています。
ネットワーク·セキュリティ
私たちはリスクに基づくネットワークセキュリティプログラムを実行し、私たちの情報の機密性、完全性、可用性を保護するために努力しています。我々は,階層的手法を用いてネットワーク攻撃を防御.検出し,外部パートナー関係を利用して脅威に関する情報を取得し,有効にするために我々の保護機構を調整し続ける.全従業員は毎年情報セキュリティ訓練(データ保護や詐欺意識を含む)を受けており、最先端の技術を用いてシステムの異常行動を監視している。事故が発生すると、法律顧問を含む複数の職能部門のメンバーで構成された安保事故反応チームが招集される。さらに、私たちは調査と緩和費用の支払いを支援するためのネットワーク保険を提供する。
私たちは一般的な攻撃を防ぐことができる多くの統制措置を持っているにもかかわらず、いくつかの攻撃はまだ効果的かもしれない。私たちの統制はこのような攻撃を検出し、分類し、根絶することを目的としている。過去3年間、既知の重大な違反はなく、このような違反を調査する費用もなかった。
企業公民権
著者らは,非オピオイドの疼痛管理に取り組み,可能な限り多くの患者に非オピオイド選択を提供する上で業界トップにあり,オピオイドが救急療法としての役割のみを再定義した。私たちは社会的責任と良い会社管理原則に努力している。私たちの取締役会は業界リーダーで構成されており、彼らは豊富な商業と科学的指導経験を持っている。私たちは自分が最高の基準を遵守することを要求し、私たちの商業行為と道徳基準はこの約束を支持する商業実践と行為原則を反映している。私たちは患者と従業員の福祉、環境、そして私たちの生活と仕事のコミュニティに深く投入した。私たちは責任ある方法で私たちの製品とパイプラインプロジェクトを運営し、管理し、適用される法律、規則、法規を遵守するように努力しています。
2021年と2022年には,ホンジュラス,ガーナ,ザンビア,グアテマラ,エクアドル,メキシコ,インドの慈善医療任務をEXPARELを寄付することにより支援し,必要な患者の手術支援を支援し,ルイジアナ州立大学オピオイド最小化イニシアティブを支援し,今後3年間で毎年非営利小児病院にEXPARELを寄付することを約束した。
Pacira BioSciences,Inc.|2022 Form 10-K|32ページ
人力資本
Paciraの核心的価値観
著者らは尊敬業と才能あふれる専門チームであり、オピオイド減少策略による患者の予後改善に集中している。私たちは高尚な道徳基準、患者に対する揺るぎない約束と透明なコミュニケーションの上に設立された組織である。私たちは私たちの周りの世界を改善し、患者、家族、コミュニティ、社会の生活に意味のある変化をもたらす原動力と願いがある。
私たちがしていることを支える6つの核心的価値観は
•病人彼らの安全と福祉はいつも私たちの最優先順位です
•人々は:私たち最大の資産
•激情私たちは私たちがしていることに情熱を持っています
•考えてみる私たちの考えは寛大に共有されています
•トラスト信頼を築くことが重要です
•チームワーク私たちのビジネス成功の基盤は
企業持続可能な開発報告書
2023年1月、当社のサイトで初の企業持続可能な開発報告書を発表しました。企業社会責任報告には、私たちの従業員、私たちの文化、患者と製品の安全、私たちのコミュニティに対する約束、オピオイド薬物節約計画及び私たちの会社の管理と道徳に関する情報が含まれている。以上、当社の企業社会責任報告の目的に言及したが、企業社会責任報告に記載されている資料や自社サイトに掲載されている任意の他の資料を引用して本年度報告に組み込むべきでもないと見なすべきでもない。
総奨励
人材を誘致し、維持するために、私たちはすべての従業員に提供する広範な福祉を維持し、私たちの401(K)退職計画と各支払期間の雇用主支払いに一致する計画、従業員株式購入計画、柔軟な支出口座、医療、歯科と視力ケア計画、医療保健と家族介護貯蓄口座、生命保険、短期と長期障害保険証書、有給休暇、有給病気休暇、有給会社休暇を含む。また、著者らは各種の長期と短期激励措置を通じて顕著な価値創造を奨励する従業員を奨励し、表彰プラットフォーム、年間業績ボーナス、株式オプション、制限株式単位、長期業績現金激励を含む。私たちはまた私たちの幹部に雇用主と一致した繰延賃金計画に参加する機会を提供する。私たちは職員たちが地域社会にフィードバックし、毎年ボランティアに1日の有給休暇を提供することを奨励する。私たちは定期的に私たちの奨励計画に対して基準テストを行い、必要に応じて調整して、私たちの総奨励に競争力があることを保証します。私たちはすべての職員たちに公平で最低生活水準の賃金を提供するために努力している。
人材管理
私たちは未来のリーダーの成長と発展を育成することで、彼らに多くの投資を行った。私たちは定期的に私たちの新興人材を評価し、識別し、正式な計画を通じて彼らの発展を支援し、私たちの潜在力の高いリーダーに対する授業訓練、幹部訓練、指導計画、“360度フィードバック”調査を含む。私たちのこのようなプロジェクトに参加した多くの指導者たちは組織内でより高いレベルの地位に昇進するだろう。私たちは従業員在任中に彼らのフィードバック意見を求めて、組織文化を形成し、私たちの人員戦略に情報を提供することに力を入れている。私たちは、従業員に私たちの初歩的な経験に対するフィードバックを求め、成功した入社を確保し、組織への同化と私たちの使命に貢献する能力を加速させるために、新しい採用調査を行った。私たちは従業員の流動率と従業員の敬業度などの指標を追跡し、留任と退職面接を行い、私たちの人材戦略が私たちの目標に合っていることを確保して、即ちトップレベルの人材を誘致、育成、維持し、私たちの未来のリーダーと管理者とする。また、著者らはすべての従業員に対して年間中と年間業績評価を行い、定期的に業績を確保し、目標の進展と専門発展について討論を行った。空いているポストの最適候補者を決定して採用する際に一致した方法が採用されることを確保し、現場および仮想環境におけるキースキルトレーニングと、人事管理者管理スキルトレーニング、プロジェクト管理およびコミュニケーショントレーニングを含む、私たちの学習プラットフォームを介して提供されるオンライン授業を提供するために、面接官に的確な選抜トレーニングを提供する。
Pacira BioSciences,Inc.|2022 Form 10-K|33ページ
従業員の福祉、健康、安全
Paciraは私たちの従業員とその家族の全体的な福祉に努力している。私たちは、個人のニーズを満たし、従業員とその家族が健康な生活を送るのを助けるための一連の福祉を提供しています。これには、私たちの従業員とその家族の健康を維持し、彼らの医療コストを下げ、ストレスを軽減するために、健康、富、仕事、生活の分野で全体的な福祉を促進する様々なツールが含まれている。例えば,無料の生体認識スクリーニング,従業員支援計画またはEAPを提供し,ストレス管理や他のEAP福祉に関する対面やネットワークシンポジウム訓練を開催し,心理的健康アクセスを含む遠隔医療を提供し,従業員およびその家族が医療システムを制御するのを支援する健康提唱者サービス,活動挑戦などを提供する。私たちは、適切なワーク/ライフバランスを実現するために、遠隔勤務機会、柔軟な労働時間、および削減された勤務時間を含む、条件に適合した従業員のための柔軟な作業スケジュールを提供します。これらに限定されないが、有給育児休暇福祉、短期および長期障害中に資産保護を支援する保険、生命保険および予期せぬ死亡および肢解除保険、貯蓄、債務および他の金融テーマに関する金融教育シンポジウム、様々な製品およびサービスの割引、および新たなまたは健康維持活動に従事する奨励を含む財務的健康を保護する福祉も提供される。また私たちは私たちの核心的価値観に基づく承認計画を維持しています祝賀の意それを通じて、私たちは、私たちの患者やコミュニティのために意味のある変化をするためにお互いに努力し、共有された文化を作ることを認識しています。この文化では、誰もが私たちの核心的な価値観を実践し、維持する責任があります。
私たちは正式な環境健康と安全(EHS)計画を持っている。私たちの政策はすべての人が安全で健康な職場を得る権利があるということだ。事故予防、従業員の健康と運営効率は品質、生産とコストに直接関連していることを認識している。Paciraは従業員の健康を守るように施設を運営し,運営の環境への影響を最小限に抑えている。
多様性公平性包括性
私たちは、誰もが自分の背景、観点、経験が歓迎され、重視されていると感じる包容的な文化を意識的に育成することに取り組んでいる。私たちは私たちの共同体と集団目標を支持するために信頼と透明性を促進するためにお互いに責任を問う。私たちの多様性、公平、包摂的なビジョンを支持するために、私たちは戦略と長年の路線図を制定し、教育と訓練を優先順位にし、世界の労働と人権政策を制定した。私たちの幹部チームと上級指導者たちは無意識の偏見と包括的なリーダーシップ訓練を受けた。私たちは州勤務銀行に私たちの求人情報をリストし、それらをコミュニティが参加する退役軍人、少数民族、女性、そして多様な組織に配布します。私たちは私たちの人員の流れを評価して、私たちが異なる人材を誘致、発展、抜擢し、維持していることを確保するために努力している。
2018年には,Paciraのすべての同僚に開放された従業員資源グループであり,リーダー的価値観の促進,コミュニティ支援の育成,職業発展やネットワーク機会による女性の地位向上に専念したP.O.W.E.R.(私たち女性の卓越と結果を追求するための準備)を設立した。2020年に私たちは機能を越えた多様で公平で包括的な従業員理事会を設立しました 顧問委員会として、私たちの会社の多元化、公平、包摂的な戦略措置を指導、提唱、告知、伝達する従業員からなり、リーダーシップ発展、多元化採用、文化とコミュニケーションの4つの重要な分野を中心に構成されている。
従業員
2022年12月31日現在、715人の従業員がおり、そのうち713名がフルタイム、2名がアルバイトです。13人のイギリス人従業員を除いて、私たちのすべての従業員はアメリカにいる。私たちは労働組合の代表者が一人もいなくて、私たちは私たちの現在の職員たちが仲がいいと思う。
利用可能な情報
私たちの会社のサイトはwww.pacira.comにあります。我々は、“取引法”の要求に基づき、米国証券取引委員会または米国証券取引委員会に報告書やその他の情報を提出し、米国証券取引委員会のサイトwww.sec.govで閲覧することができる。当社のウェブサイトを通じて、当社の年間報告書、Form 10-Q四半期報告書、Form 8-K現在の報告書、委託書、および取引所法案第13(A)および15(D)条に基づいて提出または提供されたこれらの報告書の任意の修正を無料で提供します。私たちがアメリカ証券取引委員会に電子的に提出したり、このような報告書を提出したりした後、合理的で実行可能な範囲でできるだけ早く当社のウェブサイトを介してこれらの報告を提供します。また、当社のサイトを使用して、当社の業務、製品開発計画、ガバナンスに関する情報を発表することが多く、投資家が私たちのサイト、特に“投資家”や“ニュース”の部分の情報を私たちの情報源として使用することを奨励しています。以上のように当社サイトの内容に言及することは目的ではなく、当社サイト上の資料を参考に本年報に格納すべきでもないが、当社年報に掲載されている当社サイトのアドレスは非アクティブテキスト参照のみであり、当社サイトのアクティブリンクとなるつもりはない。
Pacira BioSciences,Inc.|2022 Form 10-K|34ページ
第1 A項。リスク要因
本年度報告の他の情報を除いて、以下のいずれの要因も、当社の業務、財務状況、運営結果、または将来性に大きなマイナス影響を与える可能性があります。このような危険のため、私たちの普通株の取引価格は下がるかもしれない。この部分には前向きな陳述が含まれている。あなたは本年度報告書の1ページ目からの展望的陳述の資格と制限の説明を参考にしなければならない。このような危険要素はわが社が直面している唯一の危険ではない。私たちは今知らないか、あるいは私たちが現在どうでもいいと思っている他のリスクと不確実性は、私たちの業務、財務状況、または将来の業績に大きな悪影響を及ぼす可能性もあります。
我々の製品や候補製品の開発と商業化に関するリスク
私たちの成功は主にExPARELとZILRETTAを商業化することに成功した能力にかかっている。
私たちは2011年10月28日にFDAの承認を得て2012年4月に商業化された主導的な製品EXPARELを開発·商業化するために多くの精力と財力を投入した。EXPARELはEU(イギリスを含む)の承認を得た。2020年11月16日。2022年にはEXPARELの売上が私たちの総収入の81%を占め、EXPARELの売上高は予見可能な未来でも第一になると予想されています。2021年11月にFlexionの買収を完了した後、私たちはZILRETTAを私たちの製品グループに追加し、2022年には私たちの総収入の16%を占めます。私たちの成功は主にEXPARELとZILRETTAを効率的に商業化し続ける能力にかかっている。EXPARELとZILRETTAから効果的に収入を得ることができるかどうかは、私たちの能力にかかっています
•私たちのマーケティングと販売活動、EXPARELとZILRETTAを普及させるための他の手配を通じて、EXPARELとZILRETTAの市場ニーズをさらに創造します
•合格した販売チームを訓練、配置、支援します
•EXPARELがかなりの数のターゲット病院とASCsで処方承認を得ることを確認します
•管理機関の要求に応じて、商業需要を満たすために、十分な数のEXPARELおよびZILRETTAを許容可能な品質および価格レベルで生産する
•卸売業者および流通業者との合意を合理的な商業条項で実行し、維持すること
•EXPARELおよびZILRETTAの適切なレベルの保険および補償を商業健康計画および政府健康計画から得る
•規制の遵守を維持すること
•EXPARELとZILRETTAを用いた追加適応と地域拡張の規制承認を得る
•私たちのサプライチェーン全体が効率的に一致してお客様にEXPARELとZILRETTAを提供することを保証します
•EXPARELとZILRETTAに対する私たちの特許保護と規制の排他性を維持して擁護します。
EXPARELやZILRETTAの販売から得られた収入のどの中断も、当社の運営結果や財務状況に重大で不利な影響を与えます。
EXPARELとZILRETTAの商業化に成功した私たちの努力は、多くの内部的かつ外部的な課題に直面しており、これらの課題をタイムリーに克服できなければ、私たちの将来の収入と利益は実質的な悪影響を受ける可能性がある。
EXPARELは2012年から商業的な薬物である。私たちは引き続き大量の時間と資源を使って私たちの販売チームを訓練して、医者、病院、ASCsがEXPARELを使用するように説得する上で信頼性と説得力を持たせます。また、私たちの潜在的な顧客にEXPARELに関する一致と適切な情報を伝達することを確実にするために、販売者を訓練しなければなりません。私たちの販売チームを効果的に訓練し、医療や販売文献を含む有効な材料を提供することができなければ、潜在的な顧客EXPARELのメリットとリスクとその適切な管理を告知して教育するのを助けることができれば、EXPARELの商業化に成功する努力は脅かされる可能性があり、これは私たちの将来の収入と利益に実質的な悪影響を与える可能性がある。
我々の広範な内部努力に加えて,EXPARELの商業化には我々が制御できない多くの第三者がEXPARELを使用し続ける必要がある.これらの第三者には医師と病院薬学·治療委員会(“P&T委員会”)が含まれている。一般に,病院でEXPARELを販売することが試みられる前に,EXPARELは病院P&T委員会の承認を得なければ,当院の承認薬物リストや処方リストに追加されなければならない。病院のP&T委員会は通常,薬物処方データの審査と医療従事者への施設内の適切な薬物使用の推奨を含む施設内の薬物使用に関するすべての事項を管理している
Pacira BioSciences,Inc.|2022 Form 10-K|35ページ
スタッフです。P&T委員会は病院での会議の頻度が大きく異なり,P&T委員会はしばしば彼らの意思決定過程を支援するための追加的な情報を必要とする。したがって、私たちは処方箋の承認を得ることで大きな遅延に直面するかもしれない。また,病院薬剤師は,EXPARELをその施設に購入するコストが薬局全体の予算に悪影響を及ぼすことが懸念され,EXPARELを処方に加える努力をボイコットしたり,EXPARELの使用制限を実施したり,外科医や麻酔科医がコストを抑えるために選択したコスト量の使用を奨励したりする可能性がある。十分な速度で十分なP&T委員会から必要な承認を得て、EXPARELの病院販売を最適化する保証はありません。病院のEXPAREL処方の承認を得ても,医師はEXPARELを処方して商業化に成功させなければならない。
EXPARELがより広い市場で認められなければ、私たちがその販売から得る収入は限られるだろう。EXPARELに対する市場の受け入れ度は、他のいくつかの要因にも依存する
•EXPAREL目標適応看護基準の変化は、私たちが提起できる任意のクレームのマーケティング影響を減少させる可能性がある
•EXPAREL投与の相対的有効性、利便性、および使いやすさ;
•EXPARELに関連する有害事象の発生率と重症度;
•治療コストと経済効果と臨床効果の比較は,絶対値からも代替療法の観点からも
•保険会社や他の医療支払者や、連邦医療保険や医療補助を含む政府医療計画、十分な保険や補償があるかどうか、第三者
•ExPARELマーケティングおよび流通の範囲および実力;
•EXPARELが病院環境において疼痛の治療に使用されているいくつかの製品を含む、代替療法と比較した安全性、有効性および他の潜在的利点、ならびに代替療法の獲得性;
•規制機関によって適用されるか、または私たちは、強制的リスク評価および緩和戦略または自発的リスク管理計画の一部としての配布および使用制限に同意する。
EXPARELおよび病院またはASC市場で開発、許可または買収される可能性のある任意の候補製品を効果的に普及および販売できるかどうかは、競争力のある価格で製品を生産し、したがってその製品を病院の処方によって受け入れられる能力と、十分な第三者保険または精算を得る能力を含む価格設定と費用効果にも依存するだろう。我々はまた,許容可能な安全性と有効性を証明する証拠と,比較的便利で管理しやすい証拠が必要である.私たちの候補製品に関連する任意の期待または予期しない副作用の流行率と重症度によって、市場受容度はさらに制限される可能性がある。
また、我々が承認したEXPARELタグには、競合製品よりも安全または効率的なEXPARELの宣言は含まれておらず、競合製品よりもEXPARELの優れた宣伝も許可されていません。また,安価な非特許形態の術後疼痛管理製品の獲得性も,医師,患者,第三者支払者のEXPARELの受け入れを制限する可能性がある。EXPARELが医師,患者,第三者支払者でより広い受け入れ度を得ることができなければ,EXPARELから有意な収入が生じない可能性があり,利益を上げ続けることはないかもしれない。
ZILRETTAは、米国患者の膝骨性関節炎疼痛の治療にのみ許可されている。ZILRETTAの成功した商業化は多くのリスクに直面している。ZILRETTAに対する市場の受け入れ度は、一連の要因に依存する
•臨床試験の有効性と安全性
•実際の世界の証拠の影響を証明する能力
•製品の発売タイミングと市場を競争する
•製品のための製品ラベルと臨床適応を承認します
•医師、医学界、患者はこの製品を安全かつ有効な治療方法である
•既存の低コストの非特許代替療法から安全性と有効性を区別する能力;
•患者が製品に処方、投与、起動を容易にする
•代替療法に対する製品の潜在的および知覚的利点または価値;
•任意の同様の非特許治療を含む代替治療に関連する治療費用;
•製品の購入と決済の経済性と私たちが提供する割引とリベート
Pacira BioSciences,Inc.|2022 Form 10-K|36ページ
•第三者支払者と政府当局が定価を支援するための保険と適切な補償
•副作用の発生率と重症度
•販売とマーケティング努力の有効性。
ZILRETTAが医師、患者、第三者支払者でより広く受け入れられなければ、ZILRETTAから有意義な収入を得ることができない可能性があり、私たちの業務、財務状況、運営結果が影響を受ける可能性がある。
もし私たちが合理的な価格設定条項で私たちが提供する可能性のあるいかなる製品にも十分な第三者支払者のカバーと補償レベルを達成し、維持できなければ、その製品の商業的成功は深刻に阻害されるかもしれない。
ZILRETTAは医師が管理する製品であるため,医師に患者に使用する前にZILRETTAの在庫を購入して管理することを要求する。患者にZILRETTAを施行した後のみ,医師は適用された第三者支払者(例えば連邦医療保険や健康保険会社)からZILRETTAの精算を受けることができる。これはいわゆる“購入と請求書”過程だ。医師は精算を受ける前に,請求書を購入して発行する製品コストの財務リスクに直面しているため,精算への懸念が医師のその製品使用の決定に影響を及ぼす可能性がある。ZILRETTAの将来の成長は、第三者支払者(商業支払者、連邦医療保険および医療補助のような政府医療計画を含む)、および管理医療機関が提供する保険および十分な補償に依存する。EXPAREL精算はASC設定において同様の考慮事項に従っている。
自分の病状を治療するために処方薬を処方した患者は,通常,その処方薬に関する費用の全部または一部を第三者支払者によって精算する。保証範囲と第三者支払者の十分な精算は製品の受け入れ度に重要である。カバー範囲の決定は臨床および経済基準に依存する可能性があり、より成熟またはより低コストの治療代替物が使用可能になった場合、またはその後利用可能な場合、これらの基準は薬物製品に不利である。これによるEXPARELやZILRETTAの精算支払率が不十分である可能性があり,あるいは患者が受け入れられないほど受け入れられないほど高い共同支払いが必要である可能性がある。EXPARELとZILRETTAの保証範囲や精算が得られない場合、または限られたレベルに限られていれば、EXPARELおよびZILRETTAの商業化に成功できない可能性があり、業務、運営結果、財務状況に実質的な悪影響を及ぼす可能性があります。
私たちは他の製薬、医療設備、そしてバイオテクノロジー会社からの激しい競争に直面している。もし私たちが効果的に競争できなければ、私たちの経営業績は影響を受けるだろう。
製薬、医療機器と生物技術業界の競争は激しく、迅速と重大な技術変革の影響を受けている。私たちの主な競争相手は大手多国籍製薬や医療機器会社、老舗バイオテクノロジー会社、専門製薬や後発薬会社などの組織です。私たちの多くの競争相手は私たちより多くの財政と他の資源、例えばより多くの研究開発者、より広範なマーケティング、流通、販売と製造組織と経験、より広範な臨床試験と監督管理経験、知的財産権の起訴に関する専門知識、及び人員と技術などの開発資源を獲得する。したがって、これらの会社は私たちよりも早く規制部門の承認を得ることができ、彼らの製品を販売し、マーケティングする上でより効果的かもしれない。規模が小さいか早い段階にある会社も重要な競争相手になる可能性があり、特に大手老舗会社との協力で手配されている。私たちの競争相手は、EXPAREL、ZILRETTA、IOVERA°または私たちが現在開発している、または私たちが開発、許可または買収する可能性のある任意の候補製品よりも効果的または安価な技術、医薬品、および医療機器の開発、買収または独占に成功する可能性があり、これは、私たちの製品を時代遅れで競争力がない、またはEXPAREL、ZIELRETTA、IOVERA°または私たちの任意の候補製品のビジネス機会を深刻に損なう可能性がある。
これらの要因により、私たちの競争相手は特許保護または他の知的財産権を獲得する可能性があり、これはEXPAREL、ZILRETTA、IOVERA°または私たちの任意の候補製品のための他の適応を開発するか、またはそれを商業化する能力を制限するかもしれない。私たちの競争相手はまた、私たちよりも安全で、より効果的で、より有用で、あるいはコストの低い薬物や医療機器を開発し、彼らの製品を製造し、マーケティングする上で、私たちよりも成功するかもしれない。
ExPARELは類似適応を有する成熟製品と競合している。術後鎮痛に使用可能な競争製品はモルヒネ、フェンタニル、度冷丁と水素モルヒネなどのオピオイド薬物を含み、それぞれはいくつかの製造業者から獲得することができ、その中のいくつかは特許製品として新しい投与システムを使用することができる。ケトロラックは非ステロイド性抗炎症薬であり,米国でもいくつかのメーカーから購入可能であり,非ステロイド性抗炎症薬Caldolor(注射用イブプロフェン)はFDAによって成人疼痛や発熱の治療に許可されている。ExPARELはまた、ブピバカイン、マカイン、ロビカインおよび他の麻酔薬/鎮痛剤など、現在市販されている非オピオイド製品からの競争に直面しており、これらのすべての製品も術後疼痛の治療に使用され、経口錠剤、注射剤形、または新しい投与システムの形態で提供されている。ExPARELはまた、数日間ブピバカインを提供することを目的としたエラストマーポンプおよびカテーテル装置、ならびに他の承認された鎮痛剤の非ラベル組み合わせ(“カクテル”と呼ばれる)と競合し、これらの薬剤は、複合薬局によって併用され、疼痛制御の持続時間の延長を試みている。新しい注射可能な非ステロイド性抗炎症薬、新しいオピオイド、新しいオピオイドを含む急性疼痛の治療にもっと多くの製品を開発することができます
Pacira BioSciences,Inc.|2022 Form 10-K|37ページ
現在利用可能なオピオイドと非ステロイド抗炎症薬,長時間作用局所麻酔薬と新たな化学物質,各種オピオイドと非ステロイド抗炎症薬の代替投与形態である。EXPARELは,ブピバカインを数日以内に提供しようとするエラストマーバッグやカテーテル装置とも競合している
ZILRETTAは,即時放出ステロイドおよびHA含有製品および幹細胞およびPRP注射と競合している。速放TAや他の注射可能な速放ステロイドは現在IAが骨性関節炎痛を治療する基準であり,模倣形で提供されているため,ZILRETTAの定価に比べて相対的に安価である。これらの非特許ステロイドは安定した市場地位を有しており,医師,医療支払者,患者に精通している。臨床試験で実証され、延長された鎮痛効果はZILRETTAが臨床意義と高度に有効な選択であることを表明していると信じているが、著者らは他の臨床試験中あるいは発売後の環境中で医師と患者がこのような解釈を支持し続けない商業製品を使用した経験からデータを得る可能性がある。
Ioveraシステムは、疼痛信号を伝達する末梢神経を遮断または変性する冷却無線周波数アブレーション装置のような凍結治療装置および他の装置と競合する。
任意の承認された製品に対する規制承認は、臨床的安全性および有効性が証明された特定の適応および条件に限定され、このような承認適応を遵守できなかった疑いは、私たちの販売努力を制限し、私たちの業務に実質的な悪影響を及ぼす可能性がある。
処方薬や医療機器のマーケティング、ラベル、広告、販売促進活動を厳格に規範化する。これらの規定には、消費者向け広告、業界スポンサーの科学的および教育活動、インターネットに関連する販売促進活動、ラベル外販売促進の基準および制限が含まれる。与えられたいかなる規制承認は適切な監督管理機関が製品の安全かつ有効であると考えている特定の疾病と適応に限られている。例えば,FDAが承認したEXPARELタグには産科子宮頸部傍ブロック麻酔の適応は含まれていない。新処方にはFDA承認が必要であるほか,任意の承認製品の新適応にもFDA承認が必要である。もし私たちの製品や候補製品に対する規制部門の任意の予想される将来の適応の承認を得ることができなければ、私たちは製品を効果的にマーケティングし、販売する能力が低下する可能性があり、私たちの業務は不利な影響を受ける可能性がある。
例えば、米国およびヨーロッパでは、医師は、製品ラベルに記載されていない使用のための医薬品、医療機器、または治療処方を選択し、一般的に許可することができ、臨床試験において試験され、規制機関によって承認された使用とは異なるが、製品を普及させる能力は、FDA、EMAまたはMHRAによって特に承認された適応に限定される。これらの“ラベル外”の使用は医学専門科でよく見られ、異なる場合にはいくつかの患者に対する適切な治療を構成する可能性がある。規制当局は一般的に治療を選択する際の医師の行動を規制しないだろう。しかし、規制機関は、非ラベル使用問題における製薬と医療機器会社のコミュニケーションを制限している。米国では、最近の裁判所の裁決は、あるラベル外の販売促進活動が米国憲法第1改正案によって保護されている可能性があることを示しているにもかかわらず、どのような保護の範囲も不明である。もし私たちの販売促進活動がFDAの規定やガイドラインに適合していなければ、私たちはこれらの当局の警告や法執行行動を受けるかもしれない。さらに、FDAが販売促進や広告に関連するルールやガイドラインを遵守していない場合、FDAが警告状や無見出しの手紙を発行し、許可された製品を一時停止または市場から撤回し、罰金や民事罰金の実施を要求するか、または資金の返還、運営制限、禁止または刑事起訴を招く可能性があり、これらのいずれも私たちの名声や業務を損なう可能性がある。
効果的なマーケティングと販売能力を確立し、維持することができない場合、あるいは第三者と合意して私たちの製品をマーケティングして販売することができなければ、追加の製品収入を生み出すことができないかもしれません。
私たちは医薬製品のマーケティング、販売、流通のために、私たちの商業インフラを建設し続けている。私たちの製品を効果的に商業化し続けるためには、私たちのマーケティング、販売、流通能力を確立し続けなければならない。私たちの販売チームと関連するコンプライアンス計画を創立し、発展させ、訓練して、私たちの製品をマーケティングするのは高価で時間がかかります。もし私たちが私たちのマーケティングや販売インフラをさらに発展させることに成功できなければ、私たちはアメリカ以外にも私たちの製品を商業化することに成功し続けることができないかもしれません。これは私たちが追加製品収入を作る能力を制限します。
私たちの内部マーケティングと販売努力に加えて、第三者流通業者と、ある地域でEXPARELを普及·販売する協定を締結しました。例えば,我々は以前DePuy Synthsと共同普及協定を達成し,米国でEXPARELを用いた整形外科手術をマーケティングと普及させ,2021年1月にこの合意を終了した。また、2020年3月、Flexionは香港泰諾製薬有限公司と江蘇泰諾製薬有限公司とZILRETTAの大中国地区での開発と商業化(製造を除く)について独占許可協定を達成した。2022年7月には、本ライセンス契約に関する書簡をHK Tainnooに提出し、双方がライセンス契約の終了を決定し、2023年1月にHK Tainnooに1,300万ドルの解約金を支払った。詳細については付記20を参照されたい引受金とその他の事項私たちの統合まで
Pacira BioSciences,Inc.|2022 Form 10-K|38ページ
本書類に掲載されている財務諸表。これらの流通業者と販売促進者が私たちの製品を成功的にマーケティングして普及させることは保証されない。
私たちは将来、ある国で私たちの製品を商業化し、販売するための第三者流通業者との手配を含む、より多くの流通手配を求めることができるかもしれない。流通業者の使用は、これらの流通業者を含む一定のリスクに関連する
•私たちの製品を効果的に流通したり支持したりしていません
•彼らの在庫、私たちの製品を使用する口座の数量、あるいは私たちの製品に対する苦情に関する正確またはタイムリーな情報は提供されていません
•私たちに対する義務を果たすことができなかった
•米国または外国の管轄地域で拘束されている法律法規を遵守していない
•彼らの販売を減らしたり、私たちの製品を普及させる努力を減らしたり、あるいは
•行動を止める。
このような失敗はいずれも売上高の低下を招く可能性があり、これは私たちの業務に悪影響を及ぼすだろう。
私たちは第三者に依存してEXPAREL、ZILRETTA、IOVERA°に多くの基本サービスを提供し、私たちが商業化している他のどんな製品も第三者に依存します。もしこれらの第三者の表現が予想に合わなかったり、法律や法規の要求に従わなかったりすれば、EXPAREL、ZILRETTA、iovera°を商業化する能力に大きく影響し、規制部門の制裁を受ける可能性がある。
私たちは、販売および流通EXPAREL、ZILRETTA、iovera°に関する様々な機能を履行するために、第三者サービスプロバイダと合意を締結しており、これらの重要な側面は私たちの直接制御下ではありません。これらのサービスプロバイダは、顧客サービスサポート、倉庫および在庫計画サービス、流通サービス、契約管理、および記憶容量に応じた課金処理サービス、売掛金管理および現金アプリケーションサービス、財務管理および情報技術サービスに関連するキーサービスを提供する。また、私たちの完成品在庫は、2つのサービスプロバイダがメンテナンスする3つの倉庫に保存されています。私たちはこれらのサプライヤーと私たちにサービスを提供する他の第三者サプライヤーに大きく依存して、私たちの製品在庫を彼らに委託して面倒を見て処理することを含みます。これらの第三者サービス提供者が適用される法律法規を遵守できなかった場合、予想される期限までに完了できなかった場合、または他の方法で私たちに対する契約義務を履行しなかった場合、またはその施設で有形または自然損害に遭遇した場合、商業的需要を満たすために製品を納入する能力は深刻な損害を受けることになります。また,第三者を招いて有害事象報告,セキュリティデータベース管理,我々の候補製品に関する医療情報要求,関連サービスに関する様々な他のサービスを提供してくれる可能性がある。もしこのようなサービスプロバイダが維持しているデータの品質や正確性が不足していれば、私たちは規制制裁を受けるかもしれない。
我々はpMVLに基づく製品の流通は,EXPARELを含み,第三者がコールドチェーン流通を提供する必要があるため,製品は指定された温度で保持しなければならない。もし私たちのコールドチェーン流通中に問題が発生した場合、私たちが指定された温度範囲で私たちの製品または候補製品を維持できなかったためであっても、私たちのあるディーラーやパートナーが製品または候補製品の温度を維持できなかったために、製品または候補製品が偽に混合されて使用できない可能性がある。私たちは私たちの製品に限られた在庫と貨物保険をかけました。しかし、私たちの保険カバー範囲は私たちを清算しないかもしれないし、私たちが受ける可能性のある費用や損失を清算するのに十分ではないかもしれない。これは私たちの業務、財務状況、運営結果、そして名声に実質的な悪影響を及ぼすかもしれない。
私たちは私たちの組織の規模を拡大し、私たちの販売チームを効果的に管理する必要があるかもしれません。私たちは成長を管理する上で困難に直面するかもしれません。
2022年12月31日まで、私たちは715人の従業員を持っている。私たちはEXPAREL、ZILRETTA、IOVERA°または私たちの任意の候補製品、または私たちが買収した製品の運営と販売を管理するために、私たちの人的資源を拡張する必要があるかもしれない。私たちの既存の管理、人員、システム、そして施設は未来の成長を支援するのに十分ではないかもしれない。また、医薬と医療機器企業間の人材競争により、私たちは将来合格者を募集し、維持することができない可能性があり、特にマーケティング職では、これができなければ、私たちの未来の製品収入と業務業績に重大なマイナス影響を与える可能性がある。私たちは私たちの運営、成長、様々なプロジェクトを効果的に管理する必要があります
•EXPAREL、ZILRETTA、iovera°を商業化し、適切な制度、政策、およびインフラを構築して組織を支援する効果的な商業組織の採用と訓練を継続する
•販売店やビジネスパートナーと効果的な関係を確立し、維持して、私たちの製品を普及して販売していきます
Pacira BioSciences,Inc.|2022 Form 10-K|39ページ
•私たちの流通業者、パートナー、サプライヤー、コンサルタント、および他のサービスプロバイダがその契約義務を成功裏に履行し、質の高い結果を提供し、予想される最終期限内に完了することを確実にする
•私たちの開発や臨床試験を効率的に管理しています
•私たちの製造能力を拡大し、Thermo FisherとCarlisleとの共同生産スケジュールを効率的に管理します
•私たちのライセンシーと他の第三者に対する私たちの契約義務を履行し続ける
•私たちの業務、財務、管理制御、報告システム、そして手続きを引き続き改善します。
私たちはこれらの任務をより広い範囲で成功させることができないかもしれないので、私たちの発展と商業化目標を達成できないかもしれない。しかも、このような任務は私たちの行政と業務インフラに圧力を与えるかもしれない。もし私たちが私たちの成長を効果的に管理できなければ、私たちの製品販売とそれによって生じる収入は否定的な影響を受けるだろう。
もし私たちが重要な人員を引きつけて維持できなければ、私たちは私たちの業務を効果的に管理できないかもしれない。
生物技術、製薬、医療機器とその他の企業及び大学、非営利研究組織と政府実体の間の合格人材に対する激しい競争のため、特にフロリダ州タンパ、カリフォルニア州サンディエゴ、ニュージャージー州北部とテキサス州ヒューストン及びその周辺地域では、私たちは合格した管理者と商業、科学と臨床人員を吸引或いは維持することができないかもしれない。私たちが必要な人員を引き付けて維持することができなければ、私たちの業務目標を達成するための制限があるかもしれません。これらの制限は、私たちの開発目標の実現、追加資本を調達する能力、そして私たちが業務戦略を実施する能力を深刻に阻害します。
近年、私たちの業界の管理職の流出率は高い。私たちは私たちの製品とpMVL薬物送達技術の開発と製造専門知識、及び私たちの高級管理職のあるメンバーの商業化専門知識に高度に依存している。特に、私たちは私たちの高度な管理チームのスキルとリーダーシップに強く依存している。もし私たちがこれらの重要な従業員のうちの1人以上を失ったら、私たちが業務戦略を成功させる能力は深刻な損害を受ける可能性がある。キー従業員の交換は困難かもしれませんし、私たちの業界では開発に成功し、監督管理の承認を得て製品を商業化するために必要な技能と経験を持っている個人の数が限られているので、長い時間がかかるかもしれません。この限られた人材バンクから募集する競争は非常に激しく、私たちはより多くのキーパーソンを募集、訓練、維持、あるいは激励することができないかもしれない。
管理、商業、科学と臨床人員を含む高技能人材の競争は非常に激しく、特にフロリダ州タンパ、カリフォルニア州サンディエゴ、ニュージャージー州北部とテキサス州ヒューストンおよびその周辺地域である。私たちが運営している地理的地域外で従業員を募集できるように遠隔勤務手配を許可していますが、私たちは経験して-合格者を探したり募集したりする困難を経験しているかもしれません。特に成長戦略を追求する過程で。私たちは私たちの既存の政策と一致した給与や弾力的な水準でこのような人々を採用したり維持したりすることができないかもしれない。私たちは彼らが競争力を維持することを確実にし、私たちが市場条件が許可されていると思う時にそれらを向上させるために、私たちの報酬水準を定期的に検討する。競争や労働力不足に対応するために、既存の給与水準をさらに向上させる必要があるかもしれません。これは、私たちの運営コストを増加させ、利益率を低下させます。また、持続的な労働力不足、熟練労働力の不足、売上増加或いは労働力コストの上昇は、持続的な新冠肺炎疫病或いは一般マクロ経済要素によるものであり、コスト増加を招く可能性があり、これは私たちの全体業務を有効に運営する能力にマイナス影響を与え、私たちの運営結果と財務状況に他の不利な影響を与える可能性がある。私たちと競争する多くの会社は私たちよりも多くの資源を持っており、より魅力的な雇用条件を提供できるかもしれない。特に、求職者が就職決定を行う際には、特に私たちの業界では、その雇用に関連する任意の株式報酬の価値を得ることができることが多い。私たちの普通株価格のいかなる重大な変動も、私たちの高技能技術者の能力を引き付けたり維持したりすることに悪影響を及ぼす可能性があります, 財務·マーケティング担当者。
私たちは潜在的な製品責任のリスクに直面しています。もし私たちのクレームが成功すれば、EXPAREL、ZILRETTA、IOVERA°または私たちが開発する可能性のある任意の候補製品に重大な責任を負い、それらの商業化を制限しなければならないかもしれません。
EXPAREL、ZILRETTA、IOVERA°、臨床試験で開発、許可または買収可能な任意の候補製品を使用して、規制部門の許可を得た任意の製品を販売することは、製品責任クレームのリスクに直面させます。消費者、ヘルスケア提供者、または私たちの製品を使用、管理、または販売する人は、私たちに製品責任を請求するかもしれません。私たちは過去にこのようなスーツの一部だったが、未来はまたそうなるかもしれない。もし私たちがこのようなクレームを自己弁護することに成功できなかったら、私たちは重大な責任を負うだろう。是非曲直や最終結果にかかわらず、賠償責任は
•私たちの製品および/または候補製品の需要の減少による収入損失
•私たちのビジネス的名声や財務的安定を損なうことは
•関連する訴訟の費用は
Pacira BioSciences,Inc.|2022 Form 10-K|40ページ
•患者や他のクレーム者に巨額のお金の報酬を提供し
•経営陣の注意をそらす
•臨床試験参加者の脱退および臨床試験場所または臨床計画全体の可能性の終了;および
•私たちの製品および/または候補製品を商業化することはできない。
私たちはすでに私たちの製品と臨床試験のために限られた製品責任保険を獲得しました。年間総保証限度額は1,000万ドルです。しかし、私たちの保険範囲は私たちを補償しないかもしれないし、他の当事者に対する私たちの賠償義務を含めて、私たちが受ける可能性のあるいかなる費用や損失を補償するのに十分ではないかもしれない。さらに、保険範囲はますます高くなっており、将来的には、私たちが責任による損失から守るために、許容可能な条件、合理的な費用、または十分な金額で保険範囲を維持することができないかもしれない。私たちは、規制部門が開発している候補製品を承認したときに追加の商業製品を販売することを含む保険カバー範囲を拡大するつもりですが、発売が許可された製品のために商業的に合理的な商品責任保険を得ることができないか、あるいは全く得られないかもしれません。予期せぬ副作用を有する薬物や医療機器に基づく集団訴訟では,多額の判決が下されることがある。成功した製品責任クレームや一連の私たちに対するクレームは私たちの普通株の価格を下落させる可能性があり、もし判決が私たちの保険範囲を超えたら、私たちの現金残高を減少させ、私たちの業務に悪影響を及ぼすかもしれません。
もし私たちが十分な数量と受け入れ可能な品質と価格レベルで私たちの製品を生産できない場合、あるいはCGMP規定を完全に守ることができなければ、私たちはこれらの製品の商業化を延期したり、市場の需要を満たすことができず、潜在的な収入を失う可能性がある。
我々の製品の製造には大量の専門知識と資本投資が必要であり、先進的な製造技術、プロセス制御と専門的な加工設備の使用を含む。私たちはCGMPに関するFDAの法規を含む連邦、州、そして外国の法規を遵守しなければならない。これらの法規はFDAがその施設検査計画と私たちが業務を展開している他の司法管轄区の同様の規制機関によって実行されている。これらの要求は、他にも、品質管理、品質保証、および記録およびファイルの維持を含む。FDAまたは同様の外国規制機関は、いつでも新しい基準を実施したり、私たちの製品の製造、包装、またはテストの既存の基準の解釈および実行を変更したりすることができる。もし私たちまたは私たちの製造パートナーが適用された法規を遵守できなかった場合、罰金と民事処罰、生産停止、製品の差し押さえまたはリコール、操作制限、同意法令の実施、製品の承認または刑事起訴の修正または撤回を招き、私たちの製品の供給を制限することになります。製品の生産と流通後に発見された任意の製造欠陥や誤りは、高価なリコールプログラム、再入荷コスト、私たちの名声に対する損害、および可能な製品責任クレームを含む重大な結果を招く可能性がある。
FDAは、FDAのQSRを含むいくつかの規定を遵守することを医療機器メーカーに要求し、この規定は、定期的な監査、設計制御、品質管理テストおよび文書プログラム、ならびに苦情評価および調査を必要とする。医療製品開発,製造,販売に関する法規が進化しており,将来的には変化する可能性がある。
市場ニーズを満たすために必要な商業数量の製品をタイムリーにまたは根本的に生産できない場合、または製品製造の適用法を遵守できなければ、私たちの名声とビジネスの見通しが損なわれ、潜在的な収入を損失し、このような問題を解決するために多くの時間と資源が必要になるかもしれない。
私たちは私たちの製造業務を拡大したり、これらの業務を第三者にアウトソーシングする必要があるかもしれない。
EXPAREL、ZILRETTA、iOVERA°に対する将来の顧客のニーズに応えることに成功するためには、既存の商業製造施設を拡大したり、大規模な商業製造能力を確立したりする必要があるかもしれません。また,われわれの薬物開発パイプラインの増加と成熟に伴い,臨床試験や商業製造能力により大きな需要がある。したがって、私たちは生産コストを下げることができるように、私たちの製造技術を改善し続けなければならない。私たちは商業成功に必要なコストや数量で私たちの薬品および/または医療機器を生産することができないかもしれない。
カリフォルニア州サンディエゴの科学センターパークでEXPAREL生産のために内部製造能力を構築または他の方法で拡大し,Thermo Fisherのイングランドスウィンデン工場でEXPARELとZILRETTAの共同生産能力を提供し,大きな前期固定コストに直面させた。もし市場の私たちの製品に対する需要が私たちの拡大した製造能力と一致しなければ、私たちはこれらのコストを相殺したり、規模経済を実現することができないかもしれません。私たちの経営業績は高い運営費用によって悪影響を受けるかもしれません。あるいは、私たちの製品需要が私たちの予想を超えていれば、私たちの施設はより高い生産量をサポートするのに十分ではない可能性があり、これは私たちの顧客関係と全体的な名声を損なう可能性があります。私たちがこのような過剰な需要を満たす能力はまた、私たちが追加資本を調達し、私たちの製造業務を効果的に拡大する能力にかかっているかもしれない。
Pacira BioSciences,Inc.|2022 Form 10-K|41ページ
また,EXPARELとZILRETTAを製造するための設備の調達時間は長い納期を要する。したがって、私たちは、EXPARELまたはZILRETTAの生産に必要な製造設備調達の潜在的遅延に関連するイベントを含む、私たちの生産能力拡張プロジェクトに関連する遅延、追加または予期しないコスト、および他の不利なイベントに遭遇する可能性がある。
私たちの内部製造施設を拡大することに加えて、私たちは第三者と供給、製造、包装、テストおよび/またはストレージEXPAREL、ZILRETTA、IOVERA°または私たちの候補製品の配置、例えば私たちとThermo FisherとCarlisleの製造計画を達成する可能性があります。このような手配を達成するためには,テストやコンプライアンス検査,規制機関の承認および我々の製品生産に必要なプロセスや施設の開発が必要である。このような計画はまた追加的な危険と関連があり、その中の多くの危険は私たちの統制範囲内ではない。このようなリスクには、生産中断や遅延、製造された製品が私たちの要求に適合していないこと、このような第三者メーカーがCGMP法規や他の法規要件を遵守していないこと、私たちの知的財産権と製造プロセスの保護、私たちの複雑な製造プロセスのコントロールを失うこと、私たちのビジネスニーズを満たすことができないこと、イギリスのスウェンデンのThermo Fisher工場で私たちの製造プロセスを構築するために必要な巨額の資本支出など、第三者製造プロセスの構築に関連する財務リスクが含まれています。
もし私たちが適時に実現して満足できる生産量と品質を維持できなければ、私たちの内部製造能力を通じても、契約メーカーとの手配を通じても、私たちと顧客との関係や私たちの名声は損なわれる可能性があり、私たちの収入は低下するかもしれない。
私たちは十分な数の製品を生産し続けることができず、顧客やパートナーへの供給中断を招く可能性があり、これは私たちの業務や運営結果に実質的な悪影響を及ぼす可能性がある。
EXPARELは現在カリフォルニア州サンディエゴの工場で生産されている;EXPARELとZILRETTAは現在イギリスのスウィンデンのThermo Fisher工場で生産されているが、iovera°は現在カリフォルニア州サンディエゴにある工場とメキシコティワーナーのCarlisle工場で生産されている。これらの工場はEXPAREL,ZILRETTA,ioveraの生産を現在世界で唯一許可している工場である。私たちの製品は、製造過程で修復しなければならない問題やFDAなどの外国規制機関による検査によって一時的または長期的に生産停止になる可能性があり、これは私たちの業務、財務状況、運営結果に大きな悪影響を及ぼす可能性があります。
カリフォルニア州サンディエゴの工場、イギリスのスウィンデンのThermo Fisher工場、メキシコのティワーナのCarlisle工場も地震、洪水、火災やその他の業務中断を含む自然災害や人為的災害のリスクに直面している。また、私たちはサンディエゴ、イギリス、メキシコの製造拠点で限られた財産と業務中断保険を獲得してくれた。しかし、私たちの保険カバー範囲は私たちを清算しないかもしれないし、私たちが受ける可能性のある費用や損失を清算するのに十分ではないかもしれない。私たちの現在の製造システムに悲劇的な事件や故障が発生すれば、EXPAREL、ZILRETTA、またはIOVERA°の要求を満たすことができる保証はありません。もし私たちが新しい製造業者またはサプライヤーの交換または追加を要求された場合、このプロセスは、FDAおよび/または同等の外国規制機関の承認を事前に得る必要がある可能性が高く、非常に時間がかかり、費用がかかる可能性が高い。もし私たちが私たちの工場でEXPAREL、ZILRETTA、またはIOVERA°製品を十分に生産し続けることができなければ、私たちの顧客とパートナーへのこれらの製品の供給の中断を招き、これらの取引相手に対する私たちの契約義務に違反する可能性があります。
私たちとThermo Fisherとの共同制作と他の合意は思わぬ費用と遅延を伴うかもしれない。
私たちはThermo Fisherと共同生産協定、技術移転とサービス協定、製造と供給協定を締結した。これらの合意に基づき、Thermo Fisherは、イングランドのスウェンデンの施設で、2つの専用製造キットでEXPARELを生産するためのいくつかの技術移転活動および建築サービスを担当し、第1のキットは2018年5月にFDAの承認を得、2019年2月に商業生産を開始する。2021年8月、2セット目のEXPARELがFDAの承認を得て商業化生産を開始した。その他の事項を除いて,Thermo Fisherと合意し,これらのキットでEXPARELを製造するために必要なプロセス設備を提供した。
Flexionを買収する前に、FlexionとThermo FisherはZILRETTAの製造と供給契約およびZILRETTAの技術移転とサービス協定を締結し、私たちのExPARELスイートルームがあるイングランドのスウェンデンの同じThermo Fisher工場でZILRETTAを生産することに関連している。Thermo Fisherは,何らかの譲渡活動や建築サービスを担うことに同意し,専用製造キットでZILRETTAを商業製造する施設の準備をしている。Flexionは、Thermo FisherにZILRETTAを製造するために必要ないくつかのデバイスおよび材料を提供する。
Thermo Fisher工場はEXPARELとZILRETTAを生産·製造する前に規制部門の承認を得る必要がある。Thermo Fisherに関連した追加資本支出を予想し予算しましたが
Pacira BioSciences,Inc.|2022 Form 10-K|42ページ
EXPARELおよびZILRETTAのスイートルームの場合、Thermo Fisherスイートルームがその規制承認を維持していない場合(または将来必要となる可能性のある任意の追加的な規制承認を得られない場合)、これは、私たちの業務、財務状況、および運営結果に実質的な悪影響を及ぼす可能性がある。
さらに、これらの合意による生産は他のリスクに関連しており、その中の多くのリスクは私たちがコントロールできません、例えば、生産中断や遅延、完成品が私たちの要求に適合していない規格、Thermo FisherがCGMP法規や他の規制要件を遵守できなかったこと、私たちの知的財産権と製造プロセスを保護すること、私たちの複雑な製造プロセスが制御を失うこと、そして私たちの商業需要を満たすことができません。
EXPAREL、ZILRETTA、IOVERA°の生産に必要な特定の原材料と設備を第三者にタイムリーに提供することに依存しています。連続性と品質を提供するためにこれらの第三者関係を積極的に管理していますが、私たちがコントロールできないイベントは、これらの商品やサービスを完全にまたは部分的に失敗させる可能性があります。このようなどんな失敗も私たちの財政状況と運営に実質的な悪影響を及ぼすかもしれない。
私たちの製品を生産するために、私たちは違うサプライヤーからある原材料と設備を購入します。ある材料の調達にはかなりの準備時間がかかるかもしれません。私たちがこのような材料を調達する能力も物流サプライヤーに依存します。もし私たちが必要な原材料や設備をタイムリーに調達できない場合、あるいは私たちの規格に合わない材料を受け取ることができない場合、私たちは製造過程で遅延に遭遇する可能性があり、これは私たちの運営結果や財務状況に実質的かつ不利な影響を与え、お客様やパートナーの私たちの製品に対する需要を満たすことができません。さらに、私たちは製造過程で使用されるいくつかの材料と設備にいくつかの単一の供給源を提供する。仕入先の資格を増やしたり、サプライヤーを交換したりする必要があれば、巨額のコストを負担し、私たちの製品に対する需要を満たすのに十分な生産レベルを維持できないかもしれません。さらに、我々と第三者サプライヤーはCGMP法規を含む連邦、州、外国の法規を遵守しなければならず、適用法規や政府機関が必要な許可を提供できない行為は、私たちの製品をタイムリーかつ競争力を持って生産し、商業化する能力を損なう可能性があり、これは製品販売の減少と収入の低下を招く可能性がある。
新冠肺炎の全世界的な影響が続くにつれて、私たちはより多くの中断を経験する可能性があり、これは私たちのサプライチェーンに深刻な影響を与える可能性があり、これは私たちの臨床試験と商業化努力を乱すだろう。もし私たちのサプライヤーが私たちの合意の下での義務を履行できない場合、あるいはタイムリーに貨物やサービスを渡すことができなければ、私たちは私たちの製品に対する商業的な需要を満たし続けたり、私たちの候補製品の開発を推進する能力が損なわれる可能性があります。また、新冠肺炎ワクチンの生産に必要な原材料と供給は政府の委託注文の支援を受けており、これは私たちのサプライヤーが私たちの製品に重要な原材料を供給する能力に影響を与えている。
サプライチェーンの中断は、製品製造とグローバル物流を中断し、製品コストを増加させる可能性がある。
私たちは国際運航によっていくつかの原材料を受け取り、私たちの製品を違う地理市場に輸送します。輸送遅延は私たちが私たちの製品を輸送したり、原材料を受け取るためにもっと高価な迅速貨物輸送方法を使用する可能性がある。持続的な新冠肺炎の流行と関連政府の行動も出荷遅延を招いた。2022年12月31日までの1年間に、一時閉鎖や労働者不足による引上げ前期を含む原材料獲得の引上げ前期増加を経験した。また、世界的なインフレはすでに高い運賃増加を悪化させ、このインフレは運賃をさらに増加させ続ける可能性がある。私たちの製品を十分に生産し、タイムリーに顧客に出荷できないと、潜在的な収入損失、顧客の需要を満たすことができない、卸売業者を含む顧客との関係が緊張する可能性があります。原材料や設備を十分に調達できなかったり、生産してタイムリーに私たちの製品を顧客に出荷できなかったりすると、潜在的な収入損失を招き、顧客の需要を満たすことができず、卸売業者を含む私たちの顧客と緊張してしまう可能性があります。私たちはこのような影響を緩和するために行動しているにもかかわらず、2023年には世界的な物流課題の影響を受ける可能性がある。
私たちの運営はグローバルサプライチェーンに依存しており、サプライチェーン制限やインフレ圧力の影響は私たちの運営業績に悪影響を及ぼす可能性があります。
著者らの運営はずっと供給チェーンの制限と原材料不足の影響を受け、材料コストの増加、納期の延長と貨物輸送コストの増加を招く可能性があり、一部の原因は新冠肺炎の疫病、不確定な経済環境とマクロ経済傾向である。また、現在または将来の政府政策はインフレリスクを増加させる可能性があり、これは我々の業務に必要な原材料や部品コストをさらに増加させる可能性がある。同じように、貨物コストが引き続き増加すれば、私たちのサプライヤーは私たちに価格を上げることを要求するかもしれない。もし私たちが値上げや他の措置を通じてサプライチェーン制限やインフレ圧力の影響を緩和できなければ、私たちの運営業績と財務状況はマイナスの影響を受ける可能性がある。様々な措置でサプライチェーン制限を緩和しようと努力しているにもかかわらず、近い将来、これらの制限が私たちの業務の収入や運営コストのスケジュールに与える影響を予測することはできません。原材料供給不足とサプライチェーン制限、コスト上昇を含み、ますます増加する需要を満たす能力に負の影響を与え続ける可能性があり、これは逆に私たちの純売上高に影響を与える可能性がある
Pacira BioSciences,Inc.|2022 Form 10-K|43ページ
収入と市場シェア。新冠肺炎に関連する状況のいかなる悪化,為替レートの変動およびインフレ圧力の持続的な存在に伴い,情勢は不安定であることが予想される。
私たちの未来の成長は私たちが可能な製品を識別、開発、獲得する能力にある程度依存しており、もし私たちが関連する候補製品を識別、開発、取得、許可したり、それらを私たちの業務に統合することができなければ、私たちの成長機会は限られるかもしれない。
我々の業務戦略の重要な部分は,我々の病院市場への関心と戦略的適合性を持つと考えられる製品,業務あるいは技術を開発,買収あるいは許可することであり,一連の候補製品の開発を継続することである。しかし、これらの業務活動は、多くの経営と財務リスクをもたらすかもしれない
•重大な資本支出
•このような開発、買収または許可された製品または技術の開発活動に資金を提供することが困難または資金を得ることができない
•新製品の開発、買収または許可を支払うために発生する巨額の債務または希釈発行された証券;
•買収された製品、業務、または技術を私たちの業務に統合することに成功し、このような買収から予想される利益と協同効果を実現する
•私たちの業務を混乱させ、私たちの経営陣の時間と注意を移す
•予想以上の開発、買収、またはライセンス内および統合コスト
•未知の借金への開放
•買収された企業の業務および人員を私たちの業務および人員と合併する困難およびコスト
•買収された企業の鍵となる従業員を引き止めることはできません
•私たちの経験が限られているか直接経験のない市場に入ることは難しい
•複数の製品開発計画を管理することは困難である
•新製品の開発や臨床失敗に成功できない。
私たちは、製品、業務、技術の開発、買収、または許可を決定し、実行し、既存のインフラに統合するために限られた資源しかありません。私たちは、公共および民間研究組織、学術機関、政府機関を含む、より大きな製薬·医療機器会社や他の競争相手と競争する可能性があり、新たな協力と許可機会の構築に努力している。これらの競争相手は、私たちよりも多くの財務資源、研究開発者、施設を持っている可能性があり、新しい機会を識別し評価する上でより強い専門知識を持っている可能性がある。私たちは許容可能な条項や他の理想的な候補製品を成功的に見つけたり許可したりすることができないかもしれない。私たちは現在の候補製品を開発したり、それを商業化することでも成功しないかもしれない。このような努力は大量の財政や人的資源を投入する必要がある可能性があり,いかなる資源の移転もEXPAREL,ZILRETTAやiOVERA?の販売を拡大できないように我々の管理を混乱させる可能性がある。また、未完成の潜在的な開発、買収に資源を投入することができるかもしれませんが、そうでなければ、このような努力の予想されるメリットを実現できないかもしれません。
私たちは研究開発に大量の投資を行い、成功しない投資は私たちの業務、財務状況、運営結果に重大な悪影響を及ぼす可能性がある。
私たちが競争する業界の特徴は、迅速な技術変革、顧客需要の変化、頻繁な新製品の発売と増強、絶えず発展する業界標準と新しい交付方法である。競争力を維持するために、私たちはすでに研究と開発に大きな投資を続ける予定だ。もし私たちが新たで強化された製品や技術を開発できなければ、広く採用されていない製品や技術に集中したり、私たちがサポートしていない競争力のある新製品や技術が広く受け入れられたりすれば、私たちの製品への需要が減少する可能性がある。研究開発投資の増加或いは成功しない研究開発努力は私たちのコスト構造と製品需要の逸脱を招く可能性があり、これは私たちの財務業績に負の影響を与える。
私たちの業務は危険材料の使用に関連しており、私たちは環境法律と法規を守らなければならない。これは高価かもしれないし、私たちの業務方式を制限しているかもしれない。
私たちの製造活動は、私たちの製品の構成要素、候補製品、および他の危険化合物を含む、危険材料の制御された貯蔵、使用、および処置に関する。私たちは使用、製造、貯蔵、処理、放出と処置、そしてこれらの危険物質への曝露について連邦、州、地方法律法規によって制限されている
Pacira BioSciences,Inc.|2022 Form 10-K|44ページ
材料です。このような法律法規に違反することは巨額の罰金と処罰を招くかもしれない。私たちがこれらの材料を処理して処分する安全手続きはこれらの法律法規が規定する基準に符合すると信じているが、これらの材料の意外な汚染や傷害、あるいは意外にこれらの法律法規を遵守できなかったリスクを除去することはできない。もし事故が発生したり、これらの法律法規を遵守できなかった場合、連邦、州、地方当局はこれらの材料の使用を制限し、私たちの業務運営を中断する可能性があります。また,現在未知であっても未来の放出によるものであっても,任意の汚染の調査や清掃に関する潜在的な重大な責任を負う可能性がある。
私たちが将来達成する可能性のあるどんな協力計画も成功しない可能性があり、これは私たちの候補製品を開発し、商業化する能力に悪影響を及ぼすかもしれない。
私たちのビジネスモデルは、私たちの製品をアメリカや海外で商業化し、たまに製薬やバイオテクノロジー会社と協力して、他の国で私たちの製品を開発したり、商業化したりすることを求めています。したがって、私たちは今後選択的に協力計画に到達するかもしれない。私たちが未来に達成したどんな協力計画も成功しないかもしれない。私たちの協力計画の成功は私たちの協力者の努力と活動に大きく依存するだろう。協力者は一般に、彼らがこれらの協力計画の仕事と資源に適用されることを決定する上で大きな裁量権を持っている。
協力手配各方面間の臨床開発と商業化問題における相違は開発過程の遅延或いは適用候補製品の商業化を招く可能性があり、場合によっては、協力手配を終了することもある。もし双方が最終決定権を持っていなければ、このような相違は解決しにくいかもしれない。
製薬および/または医療機器会社および他の第三者との協力は、一般に、他方によって終了または終了が許可される。このような終了や満了は私たちの財務に悪影響を与え、私たちの商業的名声を損なう可能性がある。
臨床試験は高価で、時間がかかり、結果は確定せず、早期研究と試験の結果は未来の試験結果を予測できないかもしれない。臨床試験は,我々の薬物製品や医療機器の安全性と有効性を証明できない可能性があり,規制部門の承認を阻止または著しく遅らせる可能性がある。
私たちの任意の薬物製品や医療機器を商業化することが承認される前に、厳格に制御された臨床試験から科学的に適切かつ統計的に信頼できる証拠を用い、FDAと他の規制機関に満足させ、すべての製品が安全かつ有効であることを証明しなければならない。すべての医薬製品について,その有効性を証明し,その安全性を全過程で監視する必要がある。臨床試験費用は高価であり,完成までに数年かかる可能性があり,その結果自体も不明である。もしこのような発展が成功しなければ、私たちの業務と名声は損なわれ、私たちの株価は不利な影響を受けるだろう。
我々のすべての薬品や医療機器製品は開発過程に固有の失敗リスクを容易にしている。新薬と医療機器製品の臨床試験は監督部門の承認を得るのに十分であり、費用が高く、完成するのに数年かかる。私たちは私たちが計画した時間枠で臨床試験を成功させることができないかもしれないし、完全に達成できないかもしれない。臨床試験中あるいは臨床試験過程のため、私たちは多くの予見できない事件に遭遇する可能性があり、これらの事件は私たちが監督部門の許可を得たり、私たちの製品を商業化することを延期したり阻止したりする可能性がある。また,われわれの製品の臨床前研究と早期臨床試験の結果は必ずしも後期臨床試験の結果を予測できるとは限らない。後期臨床試験はすでに初歩的な臨床テストに合格したにもかかわらず、1つの製品が安全かつ有効であることを証明できないかもしれない。我々の製品の臨床試験から収集したデータが有望であると信じていても,これらのデータは規制機関の承認を支持するには不十分である可能性がある。臨床前と臨床データは異なる方法で解釈することができ、著者らが完成した臨床試験による結果はいかなる未来の臨床試験が成功するか或いは以前の試験が産生した結果と一致することを保証できない。
したがって、規制機関は、私たちまたは私たちのパートナーとは違う方法でこれらのデータを解釈することができ、これは規制承認を延期、制限、または阻止する可能性がある。規制機関、私たちの機関審査委員会、私たちの契約研究組織、あるいはCRO、あるいは私たち自身は、私たちの薬物製品と医療機器の臨床試験を一時停止または終了するかもしれません。私たちの医薬製品や医療機器の臨床試験を完了したり、規制部門の許可を得て私たちの任意の薬品や医療機器を販売する上でのいかなる失敗や重大な遅延も、私たちの業務と名声を深刻に損なう可能性があります。私たちが監督部門の許可を得ても、私たちの薬品と医療機器製品は後に悪影響を示す可能性があり、それらの広範な使用を制限または阻止する可能性があり、監督管理機関がそれらの承認を撤回、一時停止、あるいは制限することを招き、あるいはこれらの薬品または医療機器製品から派生した製品を市場からリコールさせる可能性がある。
Pacira BioSciences,Inc.|2022 Form 10-K|45ページ
私たちの契約研究機関への依存は私たちの薬物開発の遅延と追加コストを招くかもしれない。
われわれはCROに依存して,協力者なしに開発された候補薬剤を選択して臨床前試験と臨床試験を行う可能性がある。もし私たちが臨床試験および臨床試験を行うCROまたは私たちの協力者または許可者を招いて期限前に完了できなかった場合、適切な手順に従っていない、または私たちと私たちのCROとの間に衝突が生じた場合、私たちの臨床前試験および臨床試験は予想よりも長い時間を必要とする可能性があり、延期されるか、または終了される可能性がある。もし私たちがCROの代わりに私たちの任意の臨床前試験や臨床試験を実行することを余儀なくされれば、もしあれば、適切な有利な条件の代替品を見つけることができないかもしれない。臨床前試験または臨床試験を実行するために他のCROを見つけることができても、試験または臨床試験における任意の重大な遅延は、顕著な追加支出をもたらす可能性があり、これは私たちの運営結果に悪影響を及ぼす可能性がある。このような事件はまた、規制部門の私たちの候補薬物の承認を延期したり、製品を商業化する能力を延期したりする可能性がある。
著者らは臨床研究者と臨床サイトに依存して患者を募集して著者らの臨床試験に参加し、時々他の第三者に依存して試験を管理し、関連データの収集と分析を実行するため、著者らはコントロールできないコストと遅延に直面する可能性がある。
われわれは臨床研究者や臨床サイトに依存して患者を募集し,第三者によって我々の試験を管理し,関連するデータ収集や分析を行うこともある。しかし,臨床試験を行う臨床サイトがわれわれの臨床試験に投入される可能性のある資源の数や時間を制御できない可能性がある
私たちの臨床研究者は十分な合格患者を募集できないため、私たちの臨床試験は延期または終了される可能性がある。患者の入選は多くの要素に依存し、患者群の大きさ、試験方案の性質、患者と臨床場所の距離及び試験の資格標準を含む。もし私たちの臨床研究者と臨床サイトが私たちの臨床試験で十分な数の患者を募集できなかった場合、あるいは私たちの計画されたスケジュールに従って彼らを募集できなかった場合、私たちは増加したコスト、遅延、あるいは試験終了に直面する可能性があり、これは規制部門の候補製品の承認を得ることを延期または阻止する可能性がある
著者らは臨床研究者と臨床サイトと臨床テストと試験管理サービスについて達成した合意はこれらの各方面に大きな責任を与え、もしこれらの各方面が期待通りに表現できなければ、これは著者らの臨床試験の遅延或いは終了を招く可能性がある。例えば,我々のいずれの臨床試験サイトもFDA承認GCPに準拠できなかった場合,これらのサイトで収集したデータを使用できない可能性がある。これらの臨床研究者、臨床サイト、または他の第三者がその契約義務または義務を履行していない場合、または予期された期限内に達成できなかった場合、または彼らが得た臨床データの品質または正確性が、彼らが私たちの臨床計画または他の理由を遵守できなかった場合、私たちの臨床試験は延長、延期または終了される可能性があり、私たちは規制機関の候補製品の承認を得ることができないか、または商業化に成功できない可能性がある。
私たちは周期的な訴訟の影響を受けており、これは時間と資源の損失や予期しない費用を招く可能性がある
私たちは時々私たちの業務に関連した訴訟で自分自身を弁護するように要求される。訴訟自体の不確実性のため、私たちはこのような訴訟の最終結果を正確に予測することができない。付記20を参照引受金とその他の事項私たちの法律手続きに関する情報は、私たちの連結財務諸表を参照してください。これらまたは他の訴訟における不利な結果は、私たちの業務、財務状況、および運営結果に悪影響を及ぼす可能性があります。また、将来のいかなる重大な訴訟も、その是非にかかわらず、経営陣の私たちの運営への関心を移し、巨額の法的費用を招く可能性がある。しかも、もし私たちの株価が変動すれば、私たちは未来にもっと多くの証券集団訴訟に巻き込まれるかもしれない。いずれの訴訟も巨額のコストを招き、私たちの業務を成功させるために必要な経営陣の注意と資源を移す可能性がある。
私たちの法律手続きに関するより多くの情報は、付記20を参照されたい引受金とその他の事項私たちの連結財務諸表はここに含まれています。
様々な組織が発表したガイドラインや提案は、私たちの製品への需要や使用を減らす可能性があります。
政府機関は私たちと私たちの製品と候補製品に直接適用される法規とガイドラインを公布する。さらに、専門協会、実践管理団体、個人健康および科学財団、および他の組織は、特定の製品または製品カテゴリについて、医療および患者コミュニティに論文、ガイドラインまたはアドバイスを時々発表することができる。政府機関またはこれらの他の団体または組織の提案は、使用、用量、投与経路、および付随療法の使用などの事項に関連する可能性がある。製品を認めない、製品の限界または不足を示唆するか、または患者およびヘルスケア提供者が準拠する看護基準として競合製品または代替製品を使用することを提案するアドバイスまたはガイドラインは、私たちの任意の製品の使用を減少させるか、または採用することをもたらす可能性があり、これは、私たちの業務、財務状態、および運営結果に悪影響を及ぼす可能性がある。
Pacira BioSciences,Inc.|2022 Form 10-K|46ページ
リスクを規制する
もし規制や法執行機関が私たちが私たちの製品を普及または過去に普及させていると判断すれば、私たちの業務は実質的な悪影響を受ける可能性がある。
処方薬や医療機器のマーケティング、ラベル、広告、販売促進活動を厳格に規範化する。これらの規定には、消費者向け広告、業界スポンサーの科学的および教育活動、インターネットに関連する販売促進活動、ラベル外販売促進の基準および制限が含まれる。これらの規定によれば、会社は、医薬品または医療機器を“非ラベル”用途、すなわち製品ラベルと一致しない用途、およびFDA、EMA、MHRAまたは他の規制機関によって承認された用途とは異なる用途に使用してはならない。例えば,FDAが承認したEXPARELタグには産科子宮頸部傍ブロック麻酔の適応は含まれていない。新しい処方または設備増強に必要なFDA承認に加えて、承認された製品の任意の新しい適応もFDA承認を必要とする。もし私たちの製品や候補製品に対する規制部門の任意の予想される将来の適応の承認を得ることができなければ、私たちは製品を効果的にマーケティングし、販売する能力が低下する可能性があり、私たちの業務は不利な影響を受ける可能性がある。
例えば、医師は、製品ラベルに記載されていない使用のための医薬品および/または医療機器の処方を選択し、一般的に許可することができ、臨床試験において試験され、規制機関によって承認された使用とは異なるが、製品を普及させる能力は、FDAまたは他の規制機関によって承認された適応に限定される。“ラベル外”の使用は医学専門科でよく見られ、異なる場合にはある患者に対する適切な治療を構成する可能性がある。規制当局は一般的に治療を選択する際の医師の行動を規制しないだろう。しかし、規制機関は、非ラベル使用問題における製薬と医療機器会社のコミュニケーションを制限している。最近の裁判所の裁決は、あるラベル外の販売促進活動が米国憲法第1改正案によって保護されている可能性があることを示しているにもかかわらず、このような保護の範囲は不明である。また,我々の製品は我々が考えている薬品や医療機器の承認適応と一致していると宣伝しているにもかかわらず,規制機関は同意しない可能性がある。もし規制機関が私たちの販売促進活動が彼らの規定やガイドラインに適合していないと判断した場合、私たちはこれらの機関の警告や法執行行動を受けるかもしれない。さらに、販売促進や広告に関するルールやガイドラインを遵守していない場合、規制機関が警告状や無見出しの手紙を出し、許可された製品を一時停止したり、市場から撤回したり、罰金や民事罰金の実施を要求したり、資金の返還、経営制限、禁止、刑事起訴につながる可能性があります。これらはいずれも私たちの名声や業務を損なう可能性があります。
例えば、2014年9月、EXPARELのいくつかの普及に関連したFDA処方薬普及オフィス(OPDP)から警告状が寄せられた。私たちは、FDAの懸念を直ちに解決し、私たちの業務へのさらなる妨害を最小限に抑えるための行動を取った。しかし、最終的に2015年9月、私たちは2人の独立した医師と連邦裁判所に訴訟を起こし、FDAと他の政府の被告を起訴し、彼らは私たちの合法的な権利を行使し、EXPARELに関する真実かつ非誤解性情報を伝達しようとした。起訴状は、FDAが2014年9月に受け取った警告状と、EXPARELに関する真実かつ非誤解的な発言を制限する規定が“行政手続法”および米国憲法第1改正案および第5改正案に違反しているという私たちの信念について概説している。この訴訟は、承認された適応に適合し、FDA承認の重要な試験を支援するEXPARELの普及を可能にするために、声明および禁止救済を求めている。2015年12月15日、FDAが2014年9月の警告状を“撤回状”で正式に撤回したことを発表し、FDAとPaciraは訴訟について友好的な解決策を達成した。この問題の解決策の一部として,FDAはEXPARELがその重要な試験で検討されている手術に限らず,様々な手術への応用が広く承認されていることを明らかにした。FDAはまたEXPARELのラベル補充を承認し、さらにEXPARELは任意の特定の手術タイプまたは部位に限定されず、EXPARELの適切な用量および投与は、様々な患者および手術特定の因子に基づくことを明らかにした, 重要な痔切除術試験の72時間前にはプラセボと比較してEXPARELが有意な治療効果が認められ,一定の投与割合が認められればEXPARELはブピバカインと混合して使用可能であった。警告書とラベル補充は当時承認された浸透適応のみであり,その後2018年4月に承認された角間腕神経叢ブロック適応には適用されなかった。私たちとFDAは未来の相互作用で、当事者たちが公開的で率直で公平な方法で相互に処理することに同意する。
2015年4月、EXPARELに関連するマーケティングや販売促進実践に関する幅広い文書の提示を求める米司法省、米ニュージャージー州地域検事室から召喚状を受け取った。2020年7月,我々は正式に和解合意に達し,米国司法省,米国衛生·公衆サービス部,各州総検事長,個人原告(“原告”)のすべての未解決調査とクレームを解決した。この協定はEXPAREL販売とマーケティングに関する5年間の調査を終了した。様々な和解協定に基づいて、私たちは世界的に350万ドルの和解を支払った。和解協定の一部として
Pacira BioSciences,Inc.|2022 Form 10-K|47ページ
いかなる不正行為もないことを認め、原告の告発を明確に否定する。米司法省が2015年4月に出した召喚状による調査を終了することが保証された。
将来のいかなる規制行動が私たちの製品販売に影響を与えるかどうかは予測できません。このような行動が最終的に有利に解決されても、私たちの販売は名声や他の側面の懸念によって影響を受ける可能性があります。私たちは将来FDAや他の規制機関から警告状を受け取ったり、他の規制行動の影響を受けないという保証はない。上述したように、いかなる規制違反や違反に対する告発も、私たちの名声および業務に重大な悪影響を及ぼす可能性がある。
私たちは、規制部門の任意の候補製品の承認を得ることができないかもしれないし、FDAが505(B)(2)条の解釈に対する成功した挑戦を含む様々な理由で承認を延期する可能性があり、これは私たちの業務や財務状況に実質的な悪影響を及ぼすだろう。
私たちのどの候補製品についても、私たちはFDA規制の承認を得る努力で遅延に遭遇する可能性があり、このような承認が延期されない保証もなく、FDAが最終的にこれらの候補製品を承認する保証もない。FDAの長期的な立場は、機関が505(B)(2)申請の承認をサポートするために以前のセキュリティまたは有効性調査結果に依存する可能性があることであるが、この政策は過去に議論され、挑戦されてきた。FDAの政策が行政上または法廷で成功的に挑戦された場合、私たちの候補製品の安全性と有効性を証明する完全なデータパケットが含まれている完全なNDAによって、私たちの製品の承認を求める必要があるかもしれません。これは時間がかかり、高価で、私たちの業務および財務状況に実質的な悪影響を及ぼすでしょう。
2011年10月28日にEXPAREL NDAが承認された条件の一つとして,FDAは小児科患者におけるEXPARELの応用を検討し,発売後の要求として検討することが求められている。私たちは試験スケジュールに同意しましたが、そこで連続小児科患者亜群を検討します。2019年12月,われわれは6歳から17歳までの心血管あるいは脊柱手術を受けた児童に対して局所鎮痛を行う拡張薬物動態と安全性研究の積極的な結果を発表した。これらの積極的な結果は,2021年3月にFDAが承認したsNDA申請に基礎を築いた。また,0歳から6歳以下の児童の他の小児科学習義務を明らかにするためにFDAとEMAと交渉している。これらの実験は高価で時間がかかり、提出案とデータのスケジュールとFDAとEMAと合意された完了スケジュールを満たす必要があり、これらのスケジュールを満たす上で延期される可能性がある。我々はこれらの実験を行うことが求められており,科学的あるいは財務的な観点からも,これらの実験を行うコストや潜在的利益には根拠がないと考えられている.これらの小児科試験を行わない場合や適用の締め切りまでに完了できない場合には,制裁の実施を招く可能性があり,他に警告状の発行や差し押さえや禁止の実施を含む。詳細については付記20を参照されたい引受金とその他の事項私たちの連結財務諸表はここに含まれています。
Iovera°および任意の他の潜在的な医療機器については、新製品を発売したり、既存製品を修正したりする前に、FDAまたは他の規制機関の承認または承認を受けなければならない。規制承認過程は、私たちが商業化できる製品のタイプや用途に重大な遅延、意外または追加コスト、その他の予測不可能な要素と制限をもたらす可能性があり、これらの要素はいずれも私たちの業務や財務状況に重大な悪影響を及ぼす可能性がある。
米国では、新しい医療機器、または既存の医療機器の新しい用途、声明、または重大な修正を販売することができる前に、私たちは通常、FDAおよびいくつかの他の規制機関の承認または承認を最初に得なければならない。アメリカ以外の多くの外国司法管轄区も許可を得る必要があり、或いはある標準に符合して、医療機器或いはその他の製品を発売することができる。監督管理許可と承認を得て医療設備を市場に投入する過程はコストが高く、時間がかかる可能性があり、厳格な臨床前と臨床テストに関連し、製品を変更する必要があり、或いは製品の指定用途が制限されることを招く。もし可能であれば、このような許可と承認がタイムリーに承認される保証はない。さらに、医療機器が承認または承認されると、新たな承認または承認が必要となる可能性があり、その後、医療機器を修正し、そのラベルを変更するか、または他の用途に押し出すことができる。医療機器は、1つまたは複数の特定の予期される用途のために許可され、非ラベル用途のための器具を普及させることは、政府の法執行行動をもたらす可能性がある。さらに,医療機器に予見不可能な問題やその応用に関する問題が生じるため,製品承認や許可が撤回または制限される可能性がある。規制承認手続きは、製品純売上高の実現遅延(あれば)、私たちが市場に出す可能性のある製品タイプ、またはその指定された用途の大量の追加コストおよび制限をもたらす可能性があり、いずれも、私たちの業務、運営結果、財務状況、およびキャッシュフローに大きな悪影響を及ぼす可能性があります。
規制当局は私たちの製品や私たちの任意の候補製品に不良な副作用があると判断するかもしれない。
臨床試験で発見された不良副作用によって新製品候補製品の安全性が懸念された場合、規制機関は、薬剤または医療機器の承認を拒否するか、または製品が最終決定を下すかどうかを承認する前に、より多くのデータまたは情報を提供することを要求することができる。私たちの製品あるいは任意の候補製品による副作用はまた私たちの製品ラベルに不利な情報を含み、流通や使用制限を実施し、発売後の研究あるいは実施を要求する可能性があります
Pacira BioSciences,Inc.|2022 Form 10-K|48ページ
リスク評価および緩和策は、FDAまたは他の規制機関の任意またはすべての目標適応に対する規制承認を拒否、一時停止または撤回し、EXPAREL、ZILRETTA、iovera°または任意の候補製品の販売を商業化し、収入を生成することを阻止する。
例えば,これまでに完成したEXPAREL臨床試験で観察された副作用には,嘔気や嘔吐がある。また,EXPARELに属する薬物種別は高用量の神経系や心血管毒性に関与している。私たちは、これらの副作用および他の副作用が将来観察されないか、または規制機関がこれらの副作用または他の懸念のために追加的な試験を要求するか、またはより厳しいラベル制限を実施することを要求しないかを決定することができない。EXPARELの活性成分はブピバカインであり,ブピバカインの注入は関節軟骨の破壊や軟骨溶解に関与している。EXPARELの臨床試験では軟骨溶解は認められなかったが,将来この副作用が認められないとは考えられない。
EXPAREL、ZILRETTA、IOVERA°または私たちの任意の候補製品が承認された後、もし私たちまたは他の人が、そのような製品が以前に未知の副作用を引き起こすことを後に発見した場合、既知の副作用が過去よりも頻繁または深刻である場合、またはそのような製品またはそのような製品と類似していると考えられる任意の意外な安全信号を検出した場合:
•規制部門は、不利なラベル宣言、特定の警告、または禁忌症(ブロック警告を含む)の追加を要求することができる
•規制部門は、製品の承認を一時停止または撤回するか、または製品を市場から出荷することを要求することができる
•規制部門は製品の流通や使用に制限を加えることができる
•私たちは製品の投与方法を変更し、追加の臨床試験を行い、製品を再調製し、製品のラベルを変更したり、製造施設の再承認を得たりすることを要求されるかもしれない
•この製品の売上高は予想売上高より大幅に低下する可能性がある
•私たちは政府の調査、製品責任クレーム、そして訴訟を受けるかもしれない
•私たちの名声は損なわれるかもしれない。
これらの事件のいずれも、私たちの製品または任意の候補製品が市場受容度を獲得または維持することを阻止し、私たちの商業化コストと支出を大幅に増加させる可能性があり、これは逆に販売からの大量の収入を遅延または阻止する可能性がある。
もし私たちが医療業務に関連する連邦、州、外国の法律法規を守らなければ、私たちは重大な処罰に直面するかもしれない。
私たちと私たちの顧客は連邦政府と私たちが業務を展開する可能性のある州と外国政府によって広く規制されています。アメリカでは、私たちの業務能力に直接または間接的に影響を与える法律には、
•連邦反バックル法は、誰もが知っている間に故意に報酬を請求、提供、受け入れ、または提供することを禁止している--直接または間接的に現金または実物の形態で個人の紹介を誘導するか、または連邦医療保険や医療補助などの連邦保健プログラムに従って支払うことができる貨物またはサービスを提供または手配することを禁止する
•他の医療保険の法律および法規は、私たちの顧客が提供するサービスの保証範囲と支払い要求を規定しており、このような支払いの金額を含む
•“連邦虚偽請求法”は、虚偽または詐欺的支払い請求を政府に提出するか、または提出した個人および実体に民事および刑事責任を適用する
•保健福祉、物品またはサービスの提供または支払いに関連する重大な事実を故意に偽造、隠蔽または隠蔽または隠蔽すること、または任意の重大な虚偽陳述を行うことを禁止する連邦虚偽陳述法
•様々な州の法律は、州医療の精算や他の計画に似たような要求と責任を課している。
もし私たちの業務が上記の任意の法律法規に違反していることが発見された場合、または私たちまたは私たちの顧客が受けている任意の他の法律または政府法規が発見された場合、私たちは民事および刑事罰、損害賠償、罰金、連邦医療保険および医療補助計画から除外され、私たちの業務を削減または再構築することができます。同じように、もし私たちの顧客が適用された法律を守らないことが発見されたら、彼らは制裁を受けるかもしれないし、これは私たちに否定的な影響を及ぼすかもしれない。どんな処罰、損害賠償、罰金、縮小、あるいは再編は私たちの業務に不利な影響を与えます
Pacira BioSciences,Inc.|2022 Form 10-K|49ページ
私たちの業務を運営する能力と私たちの財務業績に影響を及ぼす。私たちがこれらの法律に違反した行為は、たとえ私たちが弁護に成功しても、巨額の法的費用を招き、私たちの経営陣の業務運営への注意を移し、私たちの名声を損なう可能性があります。
私たちの製品の設計、開発、製造、供給と流通はすべて厳格な監督管理を受けており、技術が複雑です。
私たちの製品の設計、開発、製造、供給と流通はすべて厳格な監督管理を受けています。私たちは私たちの第三者サプライヤーと共に、FDAと外国規制機関のすべての適用規制要件を守らなければならない。また、我々の製品を製造、保存、流通するための施設は、適用される法規に適合するかどうかを決定するために、規制機関の検査を随時受ける。
我々の製品を生産および供給するための製造技術および施設は、事前に得られる可能性のある規制承認を含むCGMPおよび他のFDA、EMAおよびMHRA法規に適合しなければならない。また,Thermo FisherやCarlisle工場の製造キットを含む我々の既存製造施設の任意の拡張や任意の新しい製造施設の導入も,CGMPや他のFDA,EMA,MHRA法規に適合する必要がある。これらの要求を守るためには、私たちの共同生産パートナーやサプライヤーと共に、生産、記録保存および品質保証と制御に時間、お金、エネルギーを投入して、私たちの製品が適用される規格と他の安全、効果、品質要求に適合することを保証しなければなりません。また,我々は我々の共同制作パートナーやサプライヤーとともに,FDA,EMA,MHRA,他の規制機関から抜き打ち検査を受けた.
私たちの製品の製造、供給、流通に適用される法規および他の法律要件を遵守しないいかなる行為も、救済措置(例えば、リコール)、民事と刑事処罰、および私たちの製品の製造、供給、流通の遅延を招く可能性があります。
私たちの製品の設計、開発、製造、供給、流通は非常に複雑です。もし私たちが将来高度に複雑な規格で私たちの製品を生産できなければ、私たちは製品の交換、巨額のコストと費用、供給制限あるいはその他の是正措置の影響を受けるかもしれません。
もし私たちと私たちの製品が受ける広範な規制要求を守らなければ、これらの製品は制限されたり、市場から撤退したりするかもしれません。私たちは罰を受けるかもしれません。
EXPAREL、ZILRETTA、iOVERA°と私たちの候補製品のテスト、製造、品質管理、ラベル、安全、有効性、広告、販売促進、貯蔵、販売、流通、輸入、輸出、マーケティングなどは、米国と世界各地の政府当局によって広く規制されている。私どもの製品と候補製品についての品質管理と製造プログラムはCGMPに適合しなければなりません。FDA,EMA,MHRAを含むがこれらに限定されず,CGMPに適合するかどうかを評価するために製造施設を定期的に検査する。FDA、EMA、MHRA、または他の政府機関によって施行された法律を遵守できなかったか、または将来私たちと協力する可能性のある任意の契約製造業者がこれらの法律を遵守できなかったことは、他の事項を除いて、以下のいずれかの場合を招く可能性がある
•製品のリコールや差し押さえ
•市場から承認された製品を一時停止または撤回する
•生産が中断する
•顧客や医療界の名声への懸念
•経営制限
•警告状
•禁令
•承認された製品の輸入または輸出を拒否する者;
•私たちが提出した保留申請または承認された申請を承認する補充申請を拒否する;
•ある管轄区域で申請または補充を許可することを拒否する
•法令に同意する
•臨床試験を一時停止または終了します
•罰金やその他の罰金
•刑事告発
•予想外の支出。
Pacira BioSciences,Inc.|2022 Form 10-K|50ページ
政府または第三者支払者がEXPAREL、ZILRETTA、iovera°または任意の将来の製品に十分な保証範囲および支払率を提供できない場合、または病院またはASCがより安い代替療法を使用することを選択した場合、私たちの収入および利益の見通しは制限されるだろう。
国内外の市場では、私たちの既存製品と任意の未来の製品の販売は保証範囲と第三者支払人の精算にある程度依存するだろう。このような第三者支払者には,連邦医療保険や医療補助などの政府医療項目,管理型医療保健提供者,個人健康保険会社,その他の組織がある。カバー範囲の決定は臨床と経済標準に依存する可能性があり、より成熟或いはより低コストの治療代替物がすでに利用可能であるか、あるいはその後利用可能な場合、これらの標準は新薬製品に不利である。保険が承認されたと仮定すると、それによる精算支払率が十分高くない可能性がある。特に,多くの米国病院やASCは,彼らが行っているいくつかの手術や他の治療法では,プログラムごとに固定的な精算額を得ている。この金額は病院やASCに基づく実際の費用ではない可能性があるので、これらのサイトは、私たちの候補製品よりも安い療法を選択するかもしれません。病院およびASCは、EXPAREL、ZILRETTA、iovera°または私たちが開発、許可または買収する可能性のある任意の候補製品の精算を単独で得る可能性があるが、承認されれば、これらの限られた病院およびASCの財務資源は、他の療法および薬物からの競争に直面するであろう。著者らは発売後の研究を行い、任意の未来の製品のコスト効果を証明し、病院、ASC、その他の目標顧客及び第三者支払い者を満足させる必要があるかもしれない。そのような研究は私たちが多くの管理時間、財政、そして他の資源を投入する必要があるかもしれない。私たちの未来の製品は最終的に費用効果があると思われないかもしれない。十分な第三者保険や精算が得られない可能性があり、製品開発投資の適切なリターンを実現するために十分な価格レベルを維持することができる。
第三者決済者は,海外でも国内でも,政府のものでも商業的でも,ますます複雑な方法を開発して医療コストを抑えている。例えば、340 B薬品定価計画は医療補助に参加する製薬業者が衛生と公衆サービス部部長とPPAを締結することを要求する。PPAによると、メーカーは特定のプロバイダが購入した保険外来薬に先端割引を提供することに同意し、これらの薬物は“保険実体”と呼ばれ、アメリカで最も脆弱な患者群にサービスを提供する。このようなカバーエンティティの任意の拡大または医療補助フィードバック式の変更は、必要な340 B割引の増加をもたらし、それにより、収入漏れの増加をもたらす可能性がある。
また,第三者支払者は,我々の製品精算の適応や状況を,適切と考えられるものよりも少ない適応や場合に制限する可能性がある.また,米国では,第三者支払者の間に薬品や医療機器製品の保険や精算に関する統一政策はない。そのため,支払者によって薬品のカバー範囲や精算が大きく異なる可能性がある。
また,連邦,州,外国政府が医療コストを低減または抑制するための新たな立法を提案し,採択することにより,将来の保険·精算は米国や国際市場でより多く制限される可能性があると考えられる。私たちの製品や私たちが規制承認を受けた候補製品の第三者保険·精算は、米国や国際市場で十分に補償されたり、十分な補償が得られない可能性があり、これは私たちの業務、運営結果、財務状況、見通しに悪影響を及ぼす可能性があります。
EXPARELやZILRETTAなどの医薬品や医療機器製品(例えばiovera°)の安全性に対する公衆の懸念は、我々のラベルに不利な情報を含むか、または追加コストが生じる可能性のある他の活動を要求する可能性がある。
ある薬品の安全リスクに関する事件が広く宣伝されているため、FDA、国会議員、政府責任局、医療専門家と公衆は潜在的な薬品と医療機器の安全問題に関心を提出した。これらの事件は、医薬品および医療機器製品の撤回をもたらし、医薬品および医療機器製品の使用をさらに制限するラベルを改訂し、承認された後の医薬品または医療機器製品の流通を制限する可能性があるリスク管理計画を確立した。2007年の食品医薬品局修正案、またはFDAAAは、FDAに著しく拡大された権限を付与し、その大部分は、承認前および承認後の医薬品および医療機器製品の安全性を向上させることを目的としている。特に、FDAAAは、FDAが他の事項に加えて、承認後の研究および臨床試験を行うことを要求し、新しいセキュリティ情報を反映するために製品タグを強制的に変更し、現在承認されているいくつかの薬物および医療機器を含むいくつかの薬物および医療機器のリスク評価および緩和戦略を要求する。FDAAAは連邦政府の臨床試験登録や結果データベースも著しく拡大しており,臨床試験に対する政府の監督が著しく増加することが予想される。FDAAAによると、新しい法律に違反したこれらおよび他の条項に違反した会社は、大量の民事罰金、および他の規制、民事、刑事罰を受ける。薬物安全問題に対するより多くの関心はFDAが著者らの臨床試験のデータを審査する際により慎重な方法をとることを招く可能性がある。臨床試験のデータは,特に安全性の面でより厳しい審査を受ける可能性がある, これはFDAまたは他の規制機関が追加の臨床前研究または臨床試験を要求する可能性をより可能にするかもしれない。FDAまたは任意の他の規制機関がEXPAREL、ZILRETTAまたはIOVERA°の追加の臨床または臨床前データを提供することを要求する場合、これらの製品の適応
Pacira BioSciences,Inc.|2022 Form 10-K|51ページ
承認された用量は限られている可能性があり、または特定の警告または用量制限がある可能性があり、EXPAREL、ZILRETTAまたはIOVERA°を商業化する努力は悪影響を受ける可能性がある。
知的財産権に関するリスク
我々のpMVL製品をカバーする特許および特許出願は,我々のpMVL薬物送達技術に含まれる薬物の特定の注射製剤,プロセスおよび用途に限られており,我々の候補製品の市場機会は,活性成分自体および競争相手が開発する可能性のある他の配合および輸送技術およびシステムの特許保護の欠如によって制限される可能性がある。
ExPARELにおける有効成分はブピバカインである。ブピバカイン分子自体の特許保護はすでに満期になり、汎用即時放出製品はすでに発売された。したがって、必要な規制承認を得たライバルは、ライバルが私たちのpMVL薬物送達技術に封入された薬物開発の任意のプロセス、使用または処方特許を侵害しない限り、EXPARELと同じ有効成分の製品を提供することができる。
例えば,EXPARELの代替投与システムを用いたFDA承認の長時間効果点滴可能なブピバカイン製品の少なくとも1つが市販されていることが知られている。この製品はEXPARELと類似しており,ブピバカインの有効期限も延長しているため,われわれのpMVL薬物送達技術と比較して,まったく異なる薬物送達システムを用いてこの臨床結果を実現している。
EXPARELの同じ分野の製品をカバーする特許および特許出願数は、ライバルが我々の特許および特許出願に含まれない可能性のある競合処方の開発を求め、販売することが可能であることを示している。競争相手が長期的に開発·商業化できるが我々の特許範囲内ではないブピバカイン代替製剤であれば,EXPARELのビジネス機会は深刻な被害を受ける可能性がある。
例えば、EXPARELがFDAの承認を得たため、1つまたは複数の第三者が製品の特許に挑戦する可能性があり、これは、関連する特許主張の一部または全部を無効にするか、または強制的に実行できない可能性がある。例えば、第三者がブピバカインを含む模倣薬製品のためにANDAを提出し、私たちまたは私たちによる研究に完全にまたは部分的に依存している場合、第三者は、(I)FDAのオレンジブックにEXPARELのNDAに関する特許情報が記載されていないこと、(Ii)Orange Bookに記載されている特許が期限切れであることをFDAに証明するように要求されるであろう。(Iii)に記載された特許は、まだ満了していないが、特定の日に満了し、特許の満了後に承認を求めるか、または(Iv)に記載された特許が無効であるか、または第三者の模倣薬製品の製造、使用または販売によって侵害されることはない。新製品がEXPARELオレンジ書に記載されている特許またはこのような特許を侵害しない無効な認証を第4項認証と呼ぶ。第3の方向FDAが第4項の認証を提出した場合、第三者のANDAがFDAによって届出を受けた場合、第4項の認証の通知も我々に送信しなければならない。そして、私たちは通知で決定された特許を守るために訴訟を提起するかもしれない。通知を受けてから45日以内に特許侵害訴訟を提起し、30ヶ月または特許満了の日、訴訟が和解に達し、または裁判所が侵害訴訟において第三者に有利な裁決を下すまで、FDAが第三者のANDAを承認することを自動的に阻止する。もし私たちが規定された45日間以内に特許侵害訴訟を起こさなければ, 第三者のANDAは30ヶ月間の滞在に制限されないだろう。知的財産権を実行または擁護する訴訟や他の手続きはしばしば非常に複雑で、非常に高価で時間がかかる可能性があり、コア業務に対する私たちの管理職の注意を分散させ、不利な結果を招く可能性があり、第三者が私たちの製品と競争することを阻止する能力に悪影響を及ぼす可能性がある。
2021年10月、私たちは、米国特許番号11,033,495(‘495特許)の満了前に米国でEXPARELの模造バージョン(266 mg/20 ml)を製造および販売するために、米国特許番号11,033,495(’495特許)の満了前に米国でEXPARELを製造および販売するための第4段落の認証を有するANDAをFDAに提出したことを通知する通知書を受け取った。
2021年11月、我々は、eVenusおよびその親会社に対する特許侵害訴訟を米国ニュージャージー州地域裁判所(21-cv-19829)に提起し、“495特許を侵害した”と主張した。これはeVenus ANDAの最終承認を30ヶ月間自動的に延期することを触発する。2022年1月6日、eVenusは、eVenusが提出したANDA文書に記載された製品の製造、販売、または要約によって侵害されていないと主張する反訴答弁を提出した。
2021年12月、私たちは、‘495特許が満了する前に米国で非特許バージョンのEXPAREL(133 mg/10 ml)の製造および販売を求める第4のセグメント認証を含むeVenusにそのANDAの修正案を提出したことを通知する第2の通知書を受信した。通知書では、eVenusはまた、米国第11,179,336号特許(‘336号特許)の満了前に米国でEXPARELの模造バージョン(266 mg/20 mlおよび133 mg/10 ml)の製造および販売を求める第4段落の認証をFDAに提出したことを示している。EVenusは、通知書において、‘495特許および’336特許の両方が無効であり、および/または侵害されていないとさらに主張している。
Pacira BioSciences,Inc.|2022 Form 10-K|52ページ
2022年2月、我々は米国ニュージャージー州地域裁判所(22-cv-00718)において、eVenusおよびその親会社に対して、133 mg/10ミリリットルのANDA製品が“495および”336特許を侵害すると主張し、266 mg/20 mlのANDA製品が336特許を侵害すると主張した。この申請は133 mg/10ミリリットルANDA製品の2回目の自動30ヶ月の最終承認延期をトリガした。
このような訴訟はまだ初期段階にあり、現在私たちはその結果を予測できない。
我々が有するiovera製品をカバーする特許および特許出願は、主に特定の手持ち式低温針デバイスに限定され、これらのデバイスは、冷媒によって冷却され、低温デバイスを用いて神経組織を凍結治療する方法に限定される。私たちの候補製品に対して、私たちの市場機会は、競争相手が開発する可能性のある低温設備、使用方法、他の凍結治療技術とシステムの特許カバー率差によって制限される可能性がある。
Iovera°低温装置は、交換可能な冷媒カートリッジを備え、内部供給管を介して交換可能な針の針腔に冷媒を搬送し、針を冷却し、周囲の標的神経組織を冷却するコンパクトで独立した手持ち装置である。特定の凍結治療法や疼痛治療をカバーする特許も取得しており,iovera°低温装置を用いた最適な治療を提供している
様々な代替設計や方法をカバーするのに十分な幅広い特許を持っているにもかかわらず,我々の大部分の特許カバー範囲はiovera?設備と使用方法に対してカスタマイズされている.したがって、競争相手は私たちの多くの特許を迂回して設計しようと努力するかもしれない。例えば,競争相手は自給自足の手持ち設備ではない低温システムや,異なるメカニズムで低温治療を提供する低温システムを開発していることが知られている。ライバルはまた、我々の特許でカバーされていない凍結治療装置および方法、例えば、非特許の基本凍結治療システムまたは他の神経圧迫治療のための凍結鎮痛の開発および販売を試みることができる。
競争相手が我々の特許範囲外の代替設計や方法を開発·商業化できれば,iovera°のビジネス機会は深刻な被害を受ける可能性がある。
また,iovera°最初の特許家族計画は2025年に満了し,競争相手に我々の早期技術をコピーするための扉を開いた。この早期の特許シリーズは主に治療に集中しており,iovera°に重点を置いて注目されている美容欠陥ではないが,基礎技術はまだ十分に関連しているため,明らかな重複が存在する。
最後に、1つまたは複数の第三者は、iovera製品をカバーする特許に挑戦することができ、これは、関連する特許請求の範囲の一部または全部を無効にするか、または強制的に実行できない可能性がある。知的財産権を保護または実行する訴訟や他の手続きはしばしば非常に複雑で、非常に高価で時間がかかる可能性があり、コア業務に対する私たちの管理層の注意を分散させ、不利な結果を招く可能性があり、第三者が私たちの製品と競争することを阻止する能力に悪影響を及ぼす可能性がある。
私たちの独占権を保護することは難しくて高価なので、私たちは彼らの保護を保障できないかもしれないし、すべての特許は最終的に満期になるかもしれない。
私たちのビジネス成功は、EXPAREL、ZILRETTA、IOVERA°、私たちのpMVL薬物送達技術、および私たちが開発、許可または買収する可能性のある任意の候補製品、ならびにそれらを製造するための私たちの方法の特許保護および商業秘密保護の獲得および維持にある程度依存し、これらの特許および商業秘密を第三者の挑戦から保護することに成功するであろう。私たちは効果的で強制的に実行可能な特許または商業秘密がカバーされている範囲内でのみ、私たちの技術が第三者の許可されていないことから保護することができる。
製薬、医療機器と生物技術会社の特許地位は非常に不確定である可能性があり、複雑な法律と事実問題に関連し、重要な法律原則はまだ解決されていない。これまで、米国は製薬、医療機器、またはバイオテクノロジー特許によって許容される権利要求の広さについて一致した政策を制定していない。米国以外の特許状況や政策はさらに不確定である。米国や他の国の特許法や特許法解釈の変化は,我々の知的財産権の価値を低下させる可能性がある。したがって、私たちは、私たちの特許または第三者特許において許容または実行される可能性のある特許請求の範囲の広さを予測することができない。
法的手段は限られた保護しか提供できず、私たちの権利を十分に保護できないか、あるいは私たちの競争優位性を獲得または維持することができるかもしれないので、未来の私たちの所有権の保護の程度は不確定だ。例えば:
•私たちはすべての未解決の特許出願および発行された特許をカバーする最初の発明ではないかもしれない
•私たちはこれらの発明のために特許出願をした最初の会社ではないかもしれません
Pacira BioSciences,Inc.|2022 Form 10-K|53ページ
•他の会社は、類似または代替技術を独立して開発したり、私たちの任意の候補製品または技術を複製したりすることができる
•すべての係属中の特許出願が発行された特許を生成しない可能性がある
•私たちの候補製品をカバーする発行された特許は、商業的に実行可能な活性製品に基礎を提供しないかもしれないし、競争優位性を提供してくれないかもしれないし、保護しようとしていた技術を保護するのに十分な範囲や実力がないかもしれないし、第三者の挑戦を受ける可能性がある
•他の人は私たちの特許の範囲を超えた競争力のある製品を生産するために、私たちの特許主張を中心に設計されるかもしれない
•他の特許を申請できるノウハウを開発しないかもしれません
•他人の特許は私たちの業務に悪影響を及ぼすかもしれない;または
•競争相手は私たちの特許を侵害するかもしれないが、私たちは私たちの特許を実行するのに十分な資源がないかもしれない。
米国における特許出願は、その最も早い有効出願日後少なくとも18ヶ月以内に秘密に維持されている。したがって、私たちは、私たちが最初の発明または最初の申請EXPAREL、ZILRETTA、iovera°、私たちのpMVL薬物送達技術、または私たちが開発、許可、または買収する可能性のある任意の候補製品の特許出願の会社であることを決定することはできない。もし第三者が私たちの候補製品や同様の発明に関連する米国特許出願を提出した場合、私たちは米国特許商標局が発表した干渉訴訟に参加して、米国における発明の優先権を決定しなければならないかもしれない。これらの訴訟のコストは高い可能性があり、私たちの努力は成功しない可能性があり、それによって私たちの米国特許地位に重大な悪影響を与える可能性がある。さらに、私たちの業務に影響を与えるすべてのアメリカおよび外国特許または公表の出願を決定していないかもしれませんが、私たちの薬品や医療機器を商業化する能力を阻止することによっても、私たちの薬品や医療機器市場に影響を与える類似技術をカバーすることによっても。
さらに、いくつかの国には、多くのヨーロッパ諸国を含み、人間を治療する方法に対する特許主張は付与されておらず、これらの国では、私たちの候補製品を保護するための特許保護が全くない可能性がある。特許が発行されても、私たちはこれらの特許の主張が有効で実行可能であることを保証することはできず、競争製品に対する重大な保護を提供してくれたり、私たちにとって商業的価値を持っていることはできません。さらに、私たちは通常、私たちが特許製品を製造、製造、使用、または販売しようとしている国で特許を申請しているが、最終的に特許保護が必要なすべての国を正確に予測することはできないかもしれない。もし私たちがそのような国で特許出願をタイムリーに提出しなかったら、私たちは後でそうすることを禁止されるかもしれない。私たちの外国特許出願によって発行された特許は、私たちのアメリカ特許と同じカバー範囲を持つことを保証できません。
私たちのいくつかの古い特許は期限が切れています。EXPARELについては、EXPAREL配合を保護する欧州および米国特許が2018年に満了した。EXPARELの既存処方特許は2013年11月に満了した。EXPARELの既存処方特許は2013年に米国で満期になり、カナダ、ドイツ、フランス、スペイン、イタリア、イギリスの同種の配合特許は2014年に満期になった。欧州では、メーカーはマーケティング許可を得た後、8年間のデータ独占経営権と他の2年間の市場独占経営権を取得する資格があり、合計10年間の監督独占経営権がある。私たちの最初のiovera°特許シリーズは2025年に満了する予定だ。EXPAREL、ZILRETTA、IOVERA°をカバーする特許が満期になると、私たちは模倣薬競争から保護するためにビジネス秘密にもっと依存するだろう。
私たちはまた、特に特許保護が適切でないか、または得ることが不可能だと思う場合に、ビジネス秘密に基づいて私たちの技術を保護する。しかし、商業秘密は保護することが難しい。私たちは秘密と秘密協定を通じて私たちのビジネス秘密を保護するために合理的に努力していますが、私たちの許可者、従業員、コンサルタント、請負業者、外部科学協力者、および他のコンサルタントは、意図的にまたは故意に競争相手に私たちの情報を開示するかもしれません。私たちの商業秘密を無許可に使用したり、第三者が私たちの商業秘密を不正に取得して使用した疑いを強制したりすることは高価で時間がかかり、結果は予測できない。また、他国の商業秘密法は米国のように保護作用を持っていない可能性がある。そのため、米国以外の裁判所は商業秘密を保護したくない場合がある。また,我々の競争相手は同等の知識,方法,ノウハウを自主的に開発することができる.
わが社や製品名に関する商標権を保護するために、私たちは商標によって私たちの商標を保護します。私たちはすでにアメリカ特許商標局に“PACIRA”、“EXPAREL”、“ZILRETTA”、“iOVERA°”マークを登録しました。第三者は、私たちのある商標がその商標と困惑していると主張するかもしれないが、このようなクレームやFDAまたは他の規制機関が商標をタイムリーに登録できなかったり、異議が私たちの候補製品のための新しい名前を選択させたりする可能性があり、これは、追加費用を発生させたり、製品の商業化を延期したりする可能性がある。
EXPAREL、ZILRETTA、iOVERA、私たちのpMVL薬物伝達技術、または私たちが開発、許可または買収する可能性のある任意の候補製品の特許、商業秘密および/または商標保護を取得または維持できない場合、第三者は私たちの固有の情報を使用するかもしれません。これは、市場での競争能力を弱化させ、私たちの収入を創出し、収益を維持する能力に悪影響を及ぼす可能性があります。
Pacira BioSciences,Inc.|2022 Form 10-K|54ページ
もし私たちが第三者の知的財産権侵害を起訴されたら、これは高価で時間がかかり、どんな訴訟の不利な結果も私たちの業務を損なうだろう。
EXPAREL、ZILRETTA、iovera°、当社のpMVL薬物送達技術、または私たちが開発、許可、または買収する可能性のある任意の候補製品を開発、製造、マーケティングおよび販売する能力は、第三者の独占権の侵害を回避する能力に依存します。第三者が所有する大量の米国や外国から発行された特許および出願されている特許は,疼痛管理や癌治療の一般分野に存在し,我々の目標市場における大量の化合物,配合,医療機器の使用をカバーしている。特許権に関連する特許または他の訴訟に固有の不確実性のため、私たちおよび私たちの許可者は、第三者の知的財産権クレームを正当化することに成功できない可能性があり、これは私たちの運営結果に大きな悪影響を及ぼす可能性がある。どんな訴訟の結果にもかかわらず、訴訟を弁護するのは高価で、時間がかかり、経営陣の注意を分散させるかもしれない。さらに、特許出願が発行されるまでに数年かかる可能性があるため、我々が知らない現在の係属中の出願が存在する可能性があり、EXPAREL、ZILRETTA、またはiOVERA°が発行された特許を侵害する可能性がある。EXPAREL、ZILRETTA、またはIOVERA°が無意識に侵害される可能性がある既存の特許も存在する可能性がある。
バイオテクノロジー,バイオ製薬,医療機器業界では,特許や他の知的財産権に関する訴訟が多く行われている。もし第三者が私たちが彼らの製品や技術を侵害したと主張すれば、私たちは多くの問題に直面するかもしれません
•権利侵害や他の知的財産権クレームは、正当な理由の有無にかかわらず、訴訟を起こすのは高価で時間がかかる可能性があり、経営陣のコア業務に対する注意力を移転する可能性がある
•もし裁判所が私たちの製品が競争相手の特許を侵害したと判定した場合、私たちは過去の侵害行為に大量の損害賠償金を支払う必要があるかもしれない
•裁判所は特許所有者が私たちに特許を付与しなければ、私たちの製品を販売することを禁止して、これは必要ではありません
•特許所有者が許可を提供する場合、私たちは私たちの特許に巨額の使用料を支払うか、または交差許可を付与しなければならないかもしれない
•私たちのプロセスを再設計して、権利を侵害しないようにすることは不可能かもしれないし、大量の支出と時間を必要とするかもしれない。
私たちは私たちの従業員がその前の雇用主によって言われた商業機密を間違って使用したり開示したりしたと告発されるかもしれない。
バイオテクノロジー、製薬、医療機器業界でよく見られるように、私たちが雇った個人は以前、私たちの競争相手や潜在的な競争相手を含む他のバイオテクノロジー、製薬、医療機器会社に雇われていた。現在、私たちに対するクレームが解決されていないにもかかわらず、私たちは、これらの従業員または私たちが意図していない、または他の方法でその前の雇用主の商業秘密または他の固有情報を使用または漏洩するというクレームを受ける可能性がある。このような疑いに対抗するために訴訟を提起する必要があるかもしれない。これらのクレームを弁護することに成功しても、訴訟は巨額のコストを招き、経営陣の注意を分散させる可能性がある。
私たちの財務状況、債務、普通株に関連するリスク
私たちの借金を返済するには大量の現金が必要で、私たちは私たちの巨額の債務を支払うのに十分なキャッシュフローがないかもしれない。
当社には、定期融資(以下のように定義される)、2025年満期の0.750%転換可能優先手形(または2025年手形)、2024年満期のFlexion 3.375変換可能優先手形またはFlexion 2024年手形、および2025年手形(各チケットは以下に述べる)と共に元本を支払う能力、または2025年手形またはFlexion 2024年手形(例えば、適用される)の任意の変換について現金支払いを行う能力が、我々の将来の表現に依存し、当社が元金を支払う能力、利息を支払う能力、または当社の債務再融資を行う能力があるかどうかは、私たちの将来のパフォーマンスに依存します。競争と他の私たちがコントロールできない要素。私たちの業務は将来的に運営から十分なキャッシュフローを生み出して債務返済や必要な資本支出を行うことができないかもしれません。もし私たちがそのようなキャッシュフローを生成できない場合、私たちは資産の売却、再編債務、または煩雑または高度に希釈される可能性のある条項で追加の株式を取得するような1つまたは複数の代替案を取ることを要求されるかもしれない。私たちが債務を再融資する能力は資本市場と私たちの現在の財務状況に依存するだろう。私たちはこのような活動のいずれにも従事できないかもしれないし、理想的な条件でこれらの活動に従事することができないかもしれません。これは私たちの債務不履行をもたらす可能性があります。
2021年12月7日、私たちは行政代理と初期融資者であるノースカロライナ州モルガン大通銀行と信用協定(“信用協定”)を締結した。クレジット協定は、基本的に私たちの所有および任意の付属会社によって保証される3.75億ドルの単一前払い定期ローンBローン(“定期ローン”)を提供する
Pacira BioSciences,Inc.|2022 Form 10-K|55ページ
信用協定に記載されているいくつかの例外状況によると、保証人の資産は2026年12月7日に満期になる
2020年7月10日に元金総額4.025億ドルの2025年債券の私募を完了し、2025年債券について2025年契約を締結した。債券金利は固定されており、年利0.750厘、半年ごとに配当され、それぞれ毎年2月1日および8月1日に配当される。2025年に発行される債券は2025年8月1日に満期になる。
2017年5月2日、Flexionは元金総額2.013億ドルのFlexion 2024手形を発行し、Flexion 2024手形の補充として契約、またはFlexion 2024手形契約を締結し、2025 IndentureとともにIndenturesを締結した。Flexex 2024年債の固定利息率は年利3.375厘で、半年ごとに配当され、それぞれ毎年5月1日および11月1日に配当される。Flexion買収の結果として、Flexion 2024債券の保有者は、Flexion買収に関連するいくつかの転換および買い戻し権利を得る権利がある。根本的な変化会社がFlexion 2024債券を通知·購入する要約が2022年1月に満期になった後、Flexion 2024債券の未償還元金総額は860万ドルである。詳細については付記11を参照されたい債務私たちの連結財務諸表はここに含まれています。さらに、Flexion買収の結果として、以下でより詳細に説明するように、任意の未来の変換権は、任意の未来のイベントの発生に依存して、Flexion 2024手形契約項下のこのような変換権を生成する。折れ曲がった2024年期債券は2024年5月1日に満了する。
2022年12月31日現在、我々の総合総負債は7.08億ドルで、その中には4.025億ドルの2025年債券未償還元金、2.999億ドルの定期融資の未返済元金、860万ドルのFlexION 2024年債券未償還元金が含まれている。付記11を参照債務私たちの連結財務諸表にはより多くの情報が含まれている。また、我々の子会社には負債(貿易支払、会社間負債、所得税関連負債は含まれていません)はありません。
私たちの信用協定と契約はそれぞれ私たちと私たちのいくつかの子会社に重大な運営と財務制限を加えて、これは私たちがビジネスチャンスを利用することを阻止するかもしれません。これらの制限的な契約に違反することは、信用協定および/または契約の下で私たちの契約を違約させる可能性があり、私たちの貸手は私たちの資産の担保償還権をキャンセルすることができます。
私たちの信用協定は私たちが特定の財政的契約を維持することを要求する。もし私たちの経営業績が低下すれば、私たちがこのような財務条約を履行する能力に否定的な影響を及ぼすかもしれない。もし私たちがこのような制限的な契約に違反した場合、貸手は私たちに資金を提供することを拒否したり、信用協定の下で返済されていない借金の返済を加速させることができる。私たちは約束を破った時にこのような債務を返済するのに十分な資金がないかもしれないし、貸金人から違約免除を受けることができないかもしれない。私のように債務を返済することができなければ、貸手は吾らの資産について破産手続きや催促手続きを起動することができ、これらはすべて信用協定によって吾などの債務を保証することができる。
信用協定及び契約にもいくつかの制限的な契約が掲載されており、制限及びある場合は吾などの能力を禁止している:追加債務或いは優先株の発行を招く;吾などの普通株について配当金の支払い及び他の分配或いは償還或いは買い戻しを行う;いくつかの資本支出及び投資を行う;債務或いは債務を保証する;いくつかの保留権を設立する;吾などの連合会社と取引を締結する;及びいくつかの合併、合併或いはその他の再編取引を締結する。これらの制限は、私たちの将来の融資の獲得、追加債務の発生または保証、特定の留置権の発生、関連会社との取引、特定の資産の譲渡または売却、買収または必要な資本支出、私たちの業務または全体経済の潜在的衰退を受けること、運営を展開すること、または可能なビジネスチャンスを他の方法で利用する能力を制限する可能性があり、これらのいずれも、私たちの競争相手に対して競争上不利になる可能性がある。私たちが未来に発生する可能性のある任意の債務の条項はもっと限定的な契約を含むかもしれない。私たちはあなたに私たちが将来このような条約を遵守し続けることができると保証することはできません。もし私たちがそうできなければ、私たちは貸金人から免除を受けて、そして/またはこの条約を修正することができます。私たちは上記の制限的な契約や私たちの債務の他の条項を守れず、違約事件を招く可能性があり、違約を治癒または免除しなければ、満期日までにこれらの借金を返済することを要求される可能性があります。私たちがこれらの借金をあまり優遇しない条件で再融資を余儀なくされたり、これらの借金を再融資できなければ、私たちの経営業績や財務状況は悪影響を受ける可能性があります。
吾らには、債券を決済して必要な現金金額を両替したり、債券に重大な変動が発生した場合に債券を買い戻す能力がない可能性がありますが、今後の負債は、債券を両替する際に現金を支払う能力を制限したり、債券を買い戻す能力を制限したりする能力がないかもしれません。
債券保有者は、債券に重大な変動が発生した場合には、その元金100%に等しい買い戻し価格で、別途加算および未払い利息(あれば)を要求する権利がある。私たちは現金、普通株式、または両方の任意の組み合わせで元金を支払うことを選択する権利がある。私たちは現金で元金を支払うつもりですが、債券を転換する際には、1,000元ごとに現金を払わなければなりません
Pacira BioSciences,Inc.|2022 Form 10-K|56ページ
両替の手形は最低$1,000で、毎日の両替価値の合計を加えます。しかし、私たちは十分な利用可能な現金を持っていないかもしれないし、私たちがそれのために渡された手形や変換された手形を買い戻すことを要求された時に融資を受けることができるかもしれない。信用協定限度額-及び吾等が締結する可能性のある任意の信用手配又は他の合意は、吾等が債券の重大な変動や転換時に現金を支払う能力を制限する可能性がある。また、私たちが債券を買い戻したり、債券を変換する際に現金を支払う能力は、法律、規制機関、または私たちの将来の債務に関する合意によって制限される可能性があります。吾らは,契約要求買い戻し手形を適用した場合に手形を買い戻すことができなかった場合や,後日手形を変換する際に支払うべき現金を契約規定で支払うことができなかった場合には,適用契約項下の違約行為を構成する.契約を適用した場合の違約や根本的な変化自体も、私たちの信用協定や未来の債務協定での違約を招く可能性があります。適用される通知又は猶予期間の後に関連債務の返済を加速させる場合には、債務の償還及び債券の買い戻し、又は転換債券の際に現金を支払うのに十分な資金がない可能性がある。
私たちの債務は、私たちの業務、財務状況、経営結果、および私たちの信用協定と手形に基づいて支払い義務を履行する能力に悪影響を及ぼす可能性があります。
2022年12月31日現在、我々の総合総負債は7.08億ドルで、その中には4.025億ドルの2025年債券未償還元金、2.999億ドルの定期融資の未返済元金、860万ドルのFlexION 2024年債券未償還元金が含まれている。付記11を参照債務私たちの連結財務諸表にはより多くの情報が含まれている。信用協定や契約に含まれる限度額の規定の下で、私などは時々大量の追加債務を招く可能性がある。もし私たちがそうすれば、私たちの債務水準と関連した危険が増加するかもしれない。具体的には、私たちの債務水準は重要な結果をもたらすかもしれない
·債務上の義務を履行しにくくした
·将来の運営資本、資本支出、買収、または他の一般会社の目的を支援するための追加資金を得る能力を制限する
·将来の運営資本、資本支出、買収、または他の一般会社の目的のために利用可能なキャッシュフローを減少させるために、他の目的ではなく債務返済のために必要なキャッシュフローの大部分が求められている
·一般的に不利な経済的および工業的条件下での私たちの脆弱性を増加させる
·いくつかの借金の金利が可変であるため、金利を上昇させるリスクがある
·他のレバレッジ率の低いライバルに比べて劣勢になる
·貸出コストを増加させ、
·ビジネスの変化を計画し、競争する業界の変化に対応するための当社の柔軟性を制限します。
さらに、私たちが債務超過義務を履行できない場合、または私たちの債務を管理する合意に含まれる財務および他の負の契約を遵守できない場合、私たちは債務の全部または一部を再融資し、重要な戦略資産を不利な価格で売却し、追加の債務を生成したり、普通株式または他の株式証券を発行したりすることを要求される可能性がある。任意の所与の時間に、私たちは私たちが受け入れられる条項で私たちの債務を再融資し、資産を売却し、追加債務を生成したり、私たちの需要を満たすのに十分な株式証券を発行することができないかもしれない。もし私たちが株式証券を発行することでより多くの資金を集めることができれば、この発行はまた私たちの株主の持分を希釈することになるだろう。私たちは債務を返済したり、債務を再融資することができず、私たちの業務、財務状況、あるいは経営業績に実質的な悪影響を及ぼす可能性があります。また、私たちの債務義務は、私たちが生産能力、技術または他の業務分野で必要な投資を行う能力を制限する可能性があり、これは私たちの業務、財務状況または経営業績に実質的な悪影響を及ぼす可能性があります。
これらの要素のいずれも、私たちの業務、財務状況、運営結果、および私たちの債務義務を履行する能力に悪影響を及ぼす可能性がある。
私たちの現在の負債水準にもかかわらず、私たちはより多くの債務を発生させる可能性があり、これは私たちの上述した財務状況のリスクを増加させるかもしれない。
私たちは未来に多くの追加債務を招くかもしれない。私たちの既存債務を管理するいくつかのプロトコルは、追加債務の発生と、いくつかのタイプの他の取引を行うための制限を含むが、これらの制限は、様々な財務条件を遵守することを含むいくつかの制限および例外的な状況によって制限される。既存の債務道具の規定を遵守して生成された追加債務は巨大かもしれない。私たちの現在の債務レベルで新たな債務が増加すれば、前のリスク要因に記載された大量のレバレッジリスクが増加するだろう。
2022年12月31日現在、私たちの総合総負債は7.08億ドルで、その中には4.025億ドルの未返済2025年手形元金、2.969億ドルの定期ローン元金、860万ドルが含まれています
Pacira BioSciences,Inc.|2022 Form 10-K|57ページ
屈曲2024年債の未償還元金。付記11を参照債務当社の総合財務諸表を参照して、当社の負債に関するより多くの資料を取得してください。
私たちの憲章文書やデラウェア州法律のいくつかの条項は反買収効果がある可能性があり、買収が私たちの株主に有利であっても、買収が私たちの株主に有利であっても、私たちの株主が現在の経営陣を交換または更迭しようとするのを阻止するかもしれない。
我々の会社登録証明書と我々の定款の条項、およびデラウェア州会社法(DGCL)の条項を再記述することは、第三者が私たちを買収したり、私たちを買収するコストを増加させたりすることを難しくするかもしれません。そうしても、株主がその株からプレミアム取引を受ける可能性があることを含めて、株主に利益を与えます。これらの規定には
•“空白小切手”優先株の発行を許可し、その株式を株主の承認なしに発行できるように設定することができる
•株主が書面の同意の下で行動することを禁止し、すべての株主の行動が私たちの株主会議で行われなければならないことを要求する
•株主が株主特別会議を開催する能力を廃止する
•取締役会への指名又は株主総会で行動可能な事項の事前通知要求を行うことを規定する。
これらの規定は、株主が責任を持って私たちの経営陣に命じられた取締役会のメンバーを交代させることを難しくし、株主が現在の経営陣を交代または罷免しようとしていることを挫折または阻止する可能性がある。また、DGCL第203条の制約を受けており、この条項は、一般に、デラウェア州会社が株主が利害関係のある株主になった日から3年以内に、このような取引が我々の取締役会の承認を得ない限り、その株主と広範な業務合併に従事することを禁止している。この規定は、我々の株主が望むものであっても、我々の株主に有利であるかにかかわらず、制御権変更を遅延または防止する効果がある可能性がある。
私たちの普通株価格は大きな変動と変動の影響を受けるかもしれない。
私たちの株価は大きく変動しています。2011年2月3日、つまり私たちの普通株取引の初日から2023年2月27日まで、私たちの株式の取引価格は1株6.16ドルから121.95ドルまで様々です。
私たちの株価は様々な要因で大きく変動する可能性があります
•EXPAREL、ZILRETTA、IOVERA°のビジネス成功;
•私たちの製品候補製品や競争相手の臨床試験結果
•私たちの製品または候補製品に適用される法律または法規の変化または発展
•競争力のある製品や技術を導入し
•私たちが大衆に提供した財政的予測を達成できなかったか、またはそれを超えることができなかった
•四半期の経営業績の実際または予想変化
•投資界の予想と予測を達成できなかったか、またはそれを超えることができなかった
•公衆、立法機関、規制機関、投資界の製薬と医療機器業界に対する見方
•規制上の懸念や政府の行動
•全体的な経済と市場状況と米国株式市場の全体的な変動、および全体的な政治、健康と経済状況、経済減速、衰退、インフレ、金利上昇、信用市場の引き締めなどのマクロ経済発展の影響
•金利上昇と米国株式市場への一般的なマイナス影響
•私たちの製造供給源の発展について
•特許または他の独占権に関連する紛争または他の事態の発展;
•重要な科学技術者や管理者の増減
•私たちは製品や業務や技術に投資しています
•債権、株式、または転換可能な証券を発行する
•同じ会社の市場予想が変化しています
Pacira BioSciences,Inc.|2022 Form 10-K|58ページ
•変化する投資家の環境、社会、企業統治問題に対する期待と懸念
•“リスク要因”の節で述べた他の要因。
また,株式市場,特に製薬やバイオテクノロジー会社の市場は,極端な価格や出来高変動を経験しており,これらの変動はこれらの会社の経営業績に関係なくあるいは比例しないことが多い。私たちの実際の経営業績にかかわらず、広範な市場と業界要素は私たちの普通株の市場価格にマイナス影響を与える可能性がある。私たちの株価の変動は私たちの株の取引価格に悪影響を及ぼすかもしれません。
予測可能な未来に、私たちは私たちの普通株に配当金を支払うつもりはない。
私たちは私たちの普通株式に対するどんな配当金も発表したり支払ったりしたことがない。私たちは現在、私たちの未来の収益を維持し、私たちの業務の将来の発展と拡張に資金を提供するつもりですので、予測可能な未来には、私たちの普通株に現金配当金は何も支払わないと予想されます。将来の配当金の支払いは、私たちの取締役会が適宜決定し、私たちの財務状況、経営結果、資本要求、将来の融資ツールに含まれる制限、適用法律の規定、および私たちの取締役会が関連すると思う他の任意の要素に依存します。
将来的に公開市場で私たちの普通株を販売または発行することは私たちの普通株の市場価格を下げるかもしれません。
未来に、私たちは資金を集めるためにもっと多くの普通株を売るかもしれない。限られた場合を除いて、私たちは、転換可能または交換可能な証券、または普通株を受け入れる権利を表す証券を含む追加の普通株の発行を制限しない。私たちの未償還オプションの行使、私たちに帰属する制限株式単位、または他の方法を含めて、私たちの普通株式または転換可能証券の追加株式を発行し、私たちの普通株株主の所有権利益を希釈します。また、当社の株式の5%以上を保有する株主は、公開市場で大量の株式を売却する可能性があり、これは私たちの普通株の市場価格にも影響を与える可能性があります。将来の私たちの普通株の販売や発行規模を予測することもできませんし、私たちの普通株の市場価格に与える影響も予測できません。大量の普通株の発行および/または売却、またはそのような発行および/または売却が発生する可能性があるとの見方は、私たちの普通株の市場価格に悪影響を及ぼす可能性があり、追加株式または債務証券を売却または発行することで資金を調達する能力を弱める可能性がある。
証券発行による追加資金調達は既存の株主に希釈され、貸借や許可手配による資金調達は、私たちの業務を制限したり、所有権の放棄を要求したりする可能性があります。
ある程度、私たちは株式証券を発行することで追加資本を調達し、私たちの既存株主の所有権は希釈されるだろう。もし私たちが許可手配を通じてより多くの資金を調達する場合、私たちの潜在的な製品またはノウハウの潜在的に価値のある権利を放棄するか、または私たちに不利な条項で許可を付与する必要があるかもしれない。私たちが達成したどんな債務資金調達も私たちの運営を制限する契約と関連があるかもしれない。このような制限条約は、追加借款の制限、私たちの資産使用に対する具体的な制限、および私たちの留置権の作成、配当金の支払い、株式の償還、または投資を行う能力の禁止を含むことができる。
インフレ駆動の変化を含むが、インフレ駆動の変化に限らず、私たちの顧客や私たちと業務往来のある他の人の支出や財務健康に悪影響を及ぼす可能性があり、これは私たちの財務状況、経営業績、キャッシュフローに悪影響を及ぼす可能性がある。
現在と将来の世界経済状況とインフレの不確実性は、患者の医療手続きの延期またはキャンセルを招く可能性がある。私たちの財務成功は全世界と特定の市場の全体的な経済状況の変化に非常に敏感であり、これらの変化は衰退の経済周期、より高い金利、より高い燃料と他のエネルギーコスト、労働力コストの増加、資産価値の低下、インフレ、大口商品価格の上昇、失業率の上昇、消費者債務レベルの上昇、より高い税率と他の税法の変化、公衆衛生問題、例えば新冠肺炎の疫病、あるいはその他の経済要素を含む、いくつかの影響は、コストインフレを含み、私たちは2022年に経験し、2023年に継続的に経験する予定である
もし世界経済と金融市場の状況が悪化したり、長い間疲弊を維持したりすれば、以下の要素などは私たちの財務状況、経営業績、キャッシュフローに重大な悪影響を及ぼす可能性がある
•外貨の対ドルレートの変化。
•消費者支出の鈍化は、私たちが新しい顧客と既存の顧客への販売を維持或いは増加できず、患者の数量を減少させ、製品注文の減少或いは製品注文の遅延或いは卸売顧客のキャンセルを招く可能性があり、これらは直接全体の経済変動、在庫管理困難、より高い割引と製品利益率の低下の影響を受ける。
•私たちの顧客、製品供給者、および他のサービスプロバイダが得ることができる流動性または信用の減少。
Pacira BioSciences,Inc.|2022 Form 10-K|59ページ
•もし私たちの顧客が流動資金の減少に遭遇した場合、私たちは製品注文の減少、顧客注文のキャンセル増加、および/または顧客の支払い期限を延長する必要がある場合があり、これは私たちの売掛金残高がもっと大きく、入金遅延、キャッシュフローの減少、催促費用の増加、そして私たちの売掛金が支払いできないリスクを増加させる可能性があります。
•もし私たちが値上げや他の措置を通じてサプライチェーン制限やインフレ圧力の影響を緩和できなければ、私たちの運営業績と財務状況はマイナスの影響を受ける可能性がある。また、製品の価格を上げることができても、消費者はこのような値上げに否定的に反応する可能性があり、これは私たちのブランド、名声、販売などに実質的な悪影響を及ぼす可能性がある。
上記のいくつかの場合は、医療保険カバー面が低いこと、および/または消費者自信を抑制することをもたらす可能性もあり、いずれも、いくつかの顧客が私たちの製品を購入する能力を制限し、いくつかのオプションの医療プログラムへの消費者の支出を短期的および中期的に減少させる可能性がある。
米連邦準備委員会(Federal Reserve)は最近、インフレへの懸念に応え、再び利上げする可能性があると何度も利上げしている。金利上昇は、政府支出の減少や金融市場の変動に加え、経済不確実性を増加させ、消費者支出にマイナス影響を与える可能性もある。同様に、ウクライナの持続的な戦争は世界資本市場を極度に動揺させ、グローバルサプライチェーンやエネルギー市場を混乱させるなど、さらなるグローバル経済結果が生じ続けると予想される。このような変動や中断は、私たちの業務または私たちが依存する第三者に悪影響を及ぼす可能性がある。政治的動揺や戦争の結果を含む株式市場や信用市場が悪化した場合、任意の必要な債務や株式融資をタイムリーに入手しにくくしたり、優遇条件で獲得したり、コストが高くなったり、希釈作用があったりする可能性がある。インフレ率の上昇は、労働力や従業員福祉コストを含め、私たちのコストを増加させることで、私たちに悪影響を与え続ける可能性があります。また、より高いインフレやマクロ不安や不確実性も、私たちの顧客に悪影響を及ぼす可能性があり、これは私たちの製品への需要を減らす可能性があります。
累積的には、私たちは設立以来大きな損失を被っており、将来的により多くの損失を招く可能性がある。
これまで,我々は主にEXPARELの開発と商業化に専念し,その後iovera°とZILRETTAを買収してきた。2022年、2021年、2020年12月31日までの会計年度では、純収益はそれぞれ1590万ドル、4200万ドル、1億455億ドルだった。2022年12月31日までの累計赤字は1兆488億ドル。他の事項を除いて、従来の損失は株主権益や運営資本に悪影響を与えていた。我々はEXPARELのビジネス発表に備えて大量の商業化前費用を発生させ,大量の販売,マーケティング,製造費用,EXPAREL,ZILRETTA,iOVERA°商業化に関する持続開発費用も発生している。したがって、私たちは2015年まで利益を上げておらず、2020年まで再び利益を上げなかった。医薬品や医療機器の開発や商業化に関連する多くのリスクや不確実性により,将来の損失の程度を予測することはできない。
私たちの営業権や無形資産の帳簿価値の重大な減価は私たちの経営業績と財務状況にマイナスの影響を与える可能性があります。
私たちの総資産の大部分は商業権と他の無形資産だ。アメリカ公認会計原則によると、私たちは私たちの営業権と無期限無形資産の減価を評価しなければならない。営業権は償却されないが、少なくとも毎年、または潜在的な減値が存在することを示すトリガイベントが発生した場合に減値テストが行われる。耐用年数を定めた無形資産は、その推定耐用年数内に直線的に償却し、累積償却後のコストを差し引いて入金される。寿命不定の無形資産は償却せず、少なくとも毎年、または潜在的な減値の存在を示す可能性のあるトリガイベントが発生した場合に減値テストを行う。減価費用は帳簿価値がその公正価値を超えた場合に確認する。2022年12月31日現在、我々の販売権の帳簿価値は1.632億ドルであり、累計償却後の無形資産の帳簿価値を差し引いて5.405億ドルである。これらの資産の帳簿価値が現在の推定公正価値を超える場合、これらの資産は減値とみなされ、これは、私たちの経営報告書を非現金費用に計上することになり、これは実質的である可能性がある。減値をもたらす可能性のあるイベントおよび条件は、将来の収入またはキャッシュフロー予測の仮定の変化、私たちの普通株市場価格の持続的な低下、競争の激化または市場シェアの喪失、古い、製品寿命内の売上または収益力の重大な損失をもたらす製品声明、マクロ経済状況の悪化、または予想結果と比較した財務業績の低下を含むが、これらに限定されない。
例えば、2022年には、肩痛の治療のためのZILRETTAの買収に関連する研究開発のための無形資産関連2,610万ドルの減価費用が確認されており、2022年第4四半期に開示された事実や状況によって推進されており、これらの事実や状況は、この無形資産の公正価値の減少が収入予測に影響を与える臨床試験の完了時期が遅いなどの要因によって推進されていることを示している。より多くの情報については付記9を参照されたい商誉と無形資産私たちの連結財務諸表はここに含まれています。さらに進む
Pacira BioSciences,Inc.|2022 Form 10-K|60ページ
私たちの名誉と無形資産の将来の公正な価値の仮定の変化は、将来に追加の減価費用をもたらす可能性があり、これは重大かもしれない。
私たちは追加の資金が必要かもしれないし、必要な時に資金を集めることができないかもしれません。これは私たちの製品開発計画や商業化努力を延期、減少、またはキャンセルさせます。
病院やASC環境で使用される製品を開発·商業化し,臨床試験を行い,アウトソーシング製造関係を構築し,我々が開発可能な薬物や医療機器の製造·マーケティングに成功したことは高価である。追加資本を集める必要があるかもしれません
•私たちの業務に資金を提供し続けます
•EXPAREL、ZILRETTA、iovera°を商業化するために、より多くの人を募集し、ビジネスインフラを構築しようと努力している
•CGMPに基づいて私たちの製品を資格鑑定、アウトソーシング、または追加の商業規模生産を確立します
•許可を得て他の候補品を開発し
•私たちの手形と定期融資を再融資します。
私たちは私たちの業務を継続したり、私たちのすべての目標を達成するための十分な財政資源を持っていないかもしれないが、これは私たちがこれらの目標の一部または全部を延期、削減または廃止する必要があるかもしれない。私たちの未来の資金需要は多くの要素に依存するだろうが、これらに限定されない
•ビジネス組織販売、マーケティング、および流通ExPAREL、ZILRETTA、およびioveraのコストを維持する
•EXPAREL、ZILRETTA、IOVERA°の商業化に成功した
•EXPAREL、ZILRETTA、IOVERA°を生産して、EXPAREL、ZILRETTA、IOVERA°を生産するために当社の製造施設を拡大することを含む十分な数のコストと時間を生産し、
•私たちは、IND、NDA、SDNDA、または510(K)の発売前に通知された進捗とコストを提出する準備ができており、規制承認申請の可能性を支援するために追加の臨床試験を行う必要があるかもしれない
•私たちの製品および候補製品に関連する任意の特許主張および他の知的財産権のコストを提出、起訴、弁護、および実行することは、私たちの許可者がそうしたくない場合、またはそうできない場合、私たちが支出を要求される可能性のある任意のこのようなコストを含む
•競争の技術と市場発展の影響
•私たちが構築する可能性のある任意の協力、許可、共同普及、または他の計画の条項と時間;
•私たちは、iovera°の様々な特許を侵害しているマーケティングブピバカイン徐放リポソーム注射剤、長時間作用トリアムシノロンアセトニド注射剤または冷凍鎮痛器の後発薬バージョンを求める挑戦から、私たちの特許権または規制排他性を守るために訴訟を提起することを要求されるかもしれない。
将来の資本需要はまた、追加の補充業務、製品、技術にどの程度買収または投資するかにかかっている。
私たちの製品から十分な収入を生み出すことができない限り、公開または私募株式発行、債務融資、株式オプション行使、特許使用料、協力および許可手配、および私たちの現金と投資残高で稼いだ利息収入によって、将来の現金需要に資金や補充を提供する予定です。必要であれば、私たちは受け入れ可能な条件で追加資金を提供するかどうか、あるいは根本的にできないかどうかを確認することができない。十分な資金がなければ、私たちは私たちの1つまたは複数の開発計画または商業化努力を延期、縮小、または廃止することを要求されるかもしれない。
私たちの四半期の経営業績は大きく変動するかもしれません。
私たちの経営業績は四半期変動の影響を受けると予想されています。私たちの経営業績は様々な要素の影響を受けるだろう
•EXPAREL、ZILRETTAおよびIOVERA°に対する基礎病院およびASCの需要レベルおよびエンドユーザ購入モード
•私たちの既存のExPAREL、ZILRETTA、IOVERAの製造施設を維持し、それらの製造能力を拡大し、
Pacira BioSciences,Inc.|2022 Form 10-K|61ページ
•私たちは、他の協力、許可、流通、製造、または同様の手配を実行し、これらの手配に基づいて支払いまたは受信可能な支払い時間を実行する
•私たちの将来の開発計画に関連した費用レベルの変化
•私たちが巻き込まれる可能性のある製品責任や知的財産権侵害訴訟
•EXPAREL、ZILRETTA、IOVERA°または競争相手候補製品に影響を与える規制動向、訴訟および調査;
•ウクライナ戦争、経済減速、景気後退、インフレ、金利上昇、信用市場の引き締めが私たちの業務に与える影響など、全体的な政治、健康と経済状況のようなマクロ経済発展の影響。
もし私たちの四半期や年度の経営業績が私たちの投資家や証券アナリストの予想を下回れば、私たちの普通株の価格は大幅に低下するかもしれません。また、私たちの経営業績のどの四半期や年度の変動も、私たちの普通株の価格を大幅に変動させる可能性があります。私たちの財務業績を四半期比較することは必ずしも意味があるわけではなく、私たちの将来の業績としての指標に依存すべきではないと考えられます。
買収された会社や企業の業務や人員の統合に成功できない可能性があり、このような買収の期待される相乗効果やメリットを実現できない可能性もある。
時々、私たちは会社の買収や会社のいくつかの業務を完成させるかもしれませんが、統合困難や他の挑戦のため、このような買収の期待収益を達成できない可能性があります。例えば、2019年4月にMyoScienceの買収を完了し、2021年11月にFlexionの買収を完了しました。
任意の買収の成功は、すべてまたは部分的に予想される相乗効果を達成することができるかどうか、および買収される事業が既存の業務と統合される他のメリットを達成する能力があるかどうかにある程度依存するであろう。統合過程は複雑で高価で時間がかかるかもしれない。私たちが買収したビジネスを統合する際に直面する可能性のある困難は
•統合業務の業務計画および合併または生産能力の拡大を計画的に実行できず、適用された場合には、
•私たちが買収した会社と企業の重要な従業員、顧客、サプライヤーの意外な損失
•私たちが買収された会社や企業の基準、プロセス、プログラム、内部統制を私たちの運営と一致させる上で意外な問題があります
•新製品と工芸の開発を調整する
•私たちの行動の範囲、地理的多様性、複雑さを増加させる
•経営陣の関心を他の業務から移す
•私たちや私たちが買収された会社と企業の既存の業務関係に悪影響を与えています
•法律法規を適用する意外な変化
•私たちが買収された会社や企業の業界や運営に固有のリスクは
•予期せぬ費用と負債
•私たちが買収された会社や企業の技術、製品、市場に慣れていないかもしれません
•私たちが買収された会社や企業の運営、技術、製品、システムを吸収する上での他の困難。
MyoScience、Flexion、または任意の他の買収された会社および業務が、特許および商標侵害クレーム、違法行為、商業紛争、税収、および他の既知または未知のタイプの債務によって予期以上の責任を負う場合、買収された会社および業務の職務調査中に過小評価または発見されていない負債が存在する可能性がある。適用される買収関連協定によると、買収された会社や事業の負債に関する損害賠償を取り戻すために、請求権または追跡権が限られていない可能性がある。
私たちは、買収された各会社および事業、ならびにPaciraの歴史的に達成された、または別々に達成される可能性のある収入、収益、または運営効率レベルを維持または向上させることができないかもしれない。また、買収された会社や事業の統合は、順調に、成功したり、予想されるコストや時間の範囲で達成できない可能性があります。もし私たちが統合過程で困難に直面した場合、あるいは買収された会社または企業の業務が悪化した場合、買収された会社および企業が予想していたコスト節約、成長機会、その他の相乗効果
Pacira BioSciences,Inc.|2022 Form 10-K|62ページ
完全に実現されていないかもしれないし、全く実現されていないかもしれないし、達成するには予想よりも長い時間が必要かもしれない。上記のようないかなるリスクが発生した場合、私たちの業務、財務状況、経営業績、キャッシュフローは実質的な悪影響を受ける可能性があり、私たちは投資家やアナリストの期待に達することができないかもしれない;私たちの株価はそれによって下落するかもしれない。
私たちがFlexionを買収する利点を達成できるかどうかは、ZILRETTAのビジネス成功と、PaciraとFlexion業務をタイムリーかつ効率的に統合することによって節約されるコストに大きく依存する。
私たちがFlexion買収収益を達成する能力は、ZILRETTAを商業化することに成功した能力に大きく依存する。Paciraとの合併はZILRETTAの成長と成功を加速させないかもしれない。医療提供者がZILRETTAの採用率を増加させることに成功しなければ、私たちの販売は悪影響を受ける可能性があり、私たちの業務や財務状況は影響を受ける可能性がある。
また,我々がFlexionを買収する利点を実現できるかどうかは,PaciraとFlexion業務をタイムリーに効率的に統合することで節約されるコストに大きく依存する.PaciraとFlexionが業務を統合する過程は、キーマンの損失、キー顧客の損失、キーサプライヤーの損失、製品、サービスおよび関連資産、および内部統制を私たちの業務運営に統合すること、および販売、マーケティング、および行政機能の統合における予期しない問題を含む、予期せぬコストおよび遅延に遭遇する可能性がある。PaciraとFlexionの業務をタイムリーかつ効率的に統合できなければ、私たちの運営結果は悪影響を受ける可能性があり、私たちの業務は影響を受ける可能性がある。また、統合がタイムリーで効果的であっても、両社の業務統合や相乗効果に期待されるコスト節約を永遠に実現できない可能性がある。
私たちの純営業損失の繰越と研究開発税収控除の使用は制限されます。
私たちは大量の連邦と州の純営業損失、あるいはNOL、繰り越し、そして連邦と州の研究と開発税収は繰越を免除します。私たちのNOL繰越と研究開発税収控除は期限が切れて使用されない可能性があります。私たちの連邦と州NOL繰り越しはそれぞれ2032年と2028年に満期になります。もし私たちがそれまでそれらを使用していなければ。2017年12月31日以降に発生した任意の連邦NOLについては、無期限の寿命を有しており、その使用は課税収入の80%に制限される。アメリカでなければNOLは満期になりません。また、国税法382と383節の規定によると、私たちは3年以内に50%を超える所有権の累積変化を経験したので、将来的にいくつかのNOLと信用繰越を使用してそれぞれ課税収入または税金を相殺する能力が制限される。この等所有権変動は,2000年7年に当社株を初めて買収したことと,二零一年二月に初公開発売を完了し,その他の融資取引を完了したことによる累積所有権変動によるものである。また、2021年11月19日にFlexion買収を完了し、これも所有権変更を引き起こした。これらの所有権の変化により、私たちは今後毎年課税収入や税収のNOL繰り越しを相殺し、税収控除の金額が制限されることを検討することができる。このような年間制限は,NOLや研究税収控除が満期になる前に使用を著しく減少させる可能性がある。したがって、私たちは、私たちの連結財務諸表で満期になる可能性のある未使用のNOLと税金控除のメリットを確認していません。
一般リスク因子
大流行、流行病或いは伝染性疾患(例えば新型コロナウイルス(新冠肺炎)の大流行)の爆発、あるいはこのような事件に対する恐怖は、私たちの業務、経営業績と財務状況に実質的な悪影響を与える可能性がある。
現在の新冠肺炎の大流行または他の公衆衛生危機を含む流行病、流行病または伝染病の発生が発生した場合、人員不足、コスト膨張および輸送遅延、および顧客支払いの遅延を含むが、我々の収入およびキャッシュフローに限定されないが、もたらす可能性のある販売低下、製造問題、サプライチェーン問題を含むが、人員不足、コスト膨張および輸送遅延を含むが、これらに限定されない実質的な悪影響を及ぼす可能性がある。例えば、2020年の間、私たちの製品の純売上高は新冠肺炎疫病のマイナス影響を受けており、原因は公衆衛生指導と政府指令による選択的外科手術のスケジュールが大幅に延期または一時停止されたからである。2020年4月,選択的手術制限が州ごとに廃止され,我々の製品純売上高は2020年6月に前年比増加を回復した。しかし、新冠肺炎ワクチンが現在広く獲得できるようになり、多くの制限は緩和されたが、新冠肺炎デルタ変異病例の地区の急増、人員不足及び看護チームが大量のプログラムが蓄積した疲労を処理するため、選択性手術市場は2021年8月と9月に追加の大流行に関連する挑戦に直面している。2021年12月、新冠肺炎オミック変異は選択的プログラムと手術者の配備に対する政府のいくつかの制限を促進し、この挑戦は2022年1月から緩和された。また、新冠肺炎ワクチンの生産に必要な原材料と供給は政府の委託注文の支援を受けており、これは私たちのサプライヤーが私たちの製品に重要な原材料を供給する能力に影響を与えている。 これらの挑戦は最近沈静化し始めているが,待機手術市場が正常化するのにどのくらい時間がかかるかは不明であり,新冠肺炎変異菌株やその他の原因で待機手術が再制限されるかどうかも不明である。著者らは未来の制限及び外科コミュニティの回復或いは正常手術の再定義にどのように影響するかを知らず、政府の制限、機構、患者或いは臨床決定或いは一般経済条件によるものである。政府の規制や行動により、新たなまたは長期的な一時停止の選択的手術はわが製品の純売上高を低下させるだろう。さらに、新冠肺炎の大流行による健康への懸念や負の経済状況により、患者および臨床医は選択的手続きをキャンセルまたは延期したり、他の方法で医療を回避したりする可能性がある
Pacira BioSciences,Inc.|2022 Form 10-K|63ページ
これは患者数と収入の減少を招き、これは長い間続くかもしれない。
業務中断には、私たちの製品のメリットを理解し、典型的な販売活動を実行するように教育するために、私たちの従業員チームへの妨害や制限が含まれている可能性があります。例えば、持続的な新冠肺炎疫病は、私たちの販売代表が医療保健環境(病院とASCを含む)内で個人的な相互作用を通じて顧客と医療専門家に接触する能力に著しく影響を与える。多くの州の再開業に伴い,我々の販売代表は遠隔勤務とともに,すべての看護場所で対面参加努力を更新し,医師室やASCにより多く注目することができる。さらに、私たちの製造施設または私たちのサプライヤーおよび契約製造業者の施設(およびそれによって生産または私たちの製品に与える影響)またはそのような施設を一時的に閉鎖する任意の場合は、私たちの製品の出荷または生産遅延をもたらす可能性があります。お客様が業務やキャッシュフローの中断に遭遇した場合、売掛金の入金遅延や困難に遭遇する可能性があります。私たちの施設または従業員、私たちの顧客、私たちのサプライヤー、または私たちの契約製造業者の任意の持続的な影響および業務中断は、当社のキャッシュフロー、販売、および経営業績に悪影響を及ぼす可能性があります。
疫病により、私たちの遠隔作業の従業員数は大幅に増加し、遠隔作業手配の延長とその後再び職場に入る時間の延長は、運営リスクをもたらし、私たちの業務連続性計画に圧力を与え、生産性および/または協力に負の影響を与え、従業員のクレームを引き起こしたり、他の方法で私たちの業務に悪影響を与えたりする可能性がある。そのほか、新冠肺炎の疫病は新しい或いは修正の流れ、プログラムと制御措置が必要である可能性があり、私たちの商業環境の変化に対応する。私たちは、政府当局の要求や、私たちの従業員、顧客、および業務パートナーの利益に最も適合していると思う状況に応じてさらに行動するかもしれません。これらの措置が新冠肺炎によるリスクを緩和するのに十分かどうかはまだ確定できない。
そのほか、新冠肺炎の疫病は全世界のマクロ経済の不確定性をもたらし、消費者支出とサプライチェーンを混乱させ、各種の全世界の運航遅延と港の渋滞を招き、そして金融市場の著しい変動と混乱をもたらした。
結局、新冠肺炎や他の公衆衛生危機が引き続き私たちの業務に影響を及ぼす可能性の程度は予測困難であり、感染の速度、有効な予防措置と可能な治療法の開発と実施、選択的手術に対する政府の制限および他の制限の範囲、隔離/社会距離および他の措置による旅行や他の活動、有効なワクチンの普及と公衆に受け入れられる時間、これらの要素に対する大衆の反応など、多くの制御できない要素に依存するであろう。
新冠肺炎が著者らの業務、収入と運営結果に与える影響程度は未来の発展に依存し、これらの発展は高度な不確定性を持ち、絶えず変化し、予測できない。これには出現する可能性のある新冠肺炎の重症度、新冠肺炎の世界各地での伝播と拡散、疫病発生の持続時間及び新冠肺炎の抑制或いはその影響に対応するための行動などの新しい情報が含まれている。
環境、社会、および企業統治またはESG問題は、私たちの業務、財務状況、および運営結果に悪影響を与え、私たちの名声を損なう可能性があります。
一部の投資家、顧客、消費者、従業員、立法者、監督機関(例えば、アメリカ証券取引委員会)と他の利害関係者は、特に気候に関連するリスクに注目することを含む持続可能な発展問題にますます注目している。また、上場企業のESG実践に関連する公衆利益と立法圧力は増加し続けている。もし私たちのESG実践が規制要件を満たすことができない場合、あるいは投資家、顧客、消費者、従業員または他の利害関係者の環境管理、地域コミュニティへの支援、取締役会と従業員の多様性、人的資本管理、従業員の健康と安全実践、製品品質、サプライチェーン管理、会社の管理と透明性などの分野で責任ある企業市民が絶えず変化する期待と基準が、私たちの名声、ブランド、従業員の保留率は負の影響を受ける可能性があり、私たちの顧客とサプライヤーは引き続き私たちとビジネスをしたくないかもしれない。
私たちは時々市場参加者および私たちの顧客およびサービスパートナーに特定のESGイニシアティブおよび目標を伝達する。私たちが行う任意の企業責任開示は、様々な社会的および道徳的問題、会社管理、環境コンプライアンス、持続可能性、従業員の健康と安全実践、人的資本管理、製品品質、サプライチェーン管理、および従業員の包括性と多様性に関する私たちの政策、実践、イニシアティブ、目標を含むことができる。私たちは、私たちのESG計画を改善および実施するために大きな努力をしているが、前述の各当事者は、このような開示、私たちのESG実践、または私たちが採用、実施、および/または開示する速度に満足していない可能性がある。私たちのESG実践が投資家または他の利害関係者の持続的な発展の期待および基準に適合していない場合、またはESG問題に対する関心に適切に応答していないと考えられるか、または適切に対応していないと考えられる場合、法的要求があるか否かにかかわらず、利害関係者および消費者の名声に損なわれる可能性があり、私たちの業務および財務状況は実質的かつ不利な影響を受ける可能性がある。私たちもかもしれません
Pacira BioSciences,Inc.|2022 Form 10-K|64ページ
追加の費用を生成するか、または利害関係者の期待および基準を監視し、私たちの目標と約束を達成するために追加の資源が必要です。
データプライバシーおよび保護法令の変化、特にヨーロッパおよびカリフォルニア州では、またはこのような法律法規を遵守できないいかなる行為も、私たちの業務および財務業績に悪影響を及ぼす可能性があります。
我々は、個人データの収集、記憶、処理、使用、開示、伝送、およびセキュリティに関する法律および法規を含む、プライバシー、データ保護、およびデータセキュリティに関する世界的に変化し発展する様々な法律および法規に支配されている。プライバシーやデータ保護法に対する各国の解釈や適用が異なる可能性があり,不一致や衝突の要求が生じる可能性があるため,大きな不確実性がある.これらの法律は、私たちの付属会社間の情報伝達、および第三者サプライヤーとの取引に適用されます。
例えば、EUは2016年5月に包括的な一般データプライバシー法規、略称GDPRを採択し、2018年5月に当時のEUデータ保護指令と関連する国別立法に代わった。GDPRは、その使用、保護、およびデータを格納する人が、それ自身に関するこのようなデータを訂正または削除する能力を含む、個人および敏感なデータを処理するための新しい要件を満たすことを要求する。GDPR要求を守らないことは、世界の総収入4%までの罰金を招く可能性がある。
また、カリフォルニア州消費者プライバシー法案(CCPA)は2020年1月に施行され、カリフォルニアに住む従業員や消費者の個人情報を処理、開示、削除する新たな責任を与えられている。CCPAは、カリフォルニアがCCPA違反の潜在的な巨額の罰金を評価し、違反行為に対する損害賠償を求めるために、個人に集団訴訟を提起する権利を与えることを許可する。我々はまた,CCPAに対する修正案であるカリフォルニアプライバシー権法案に関するより厳しいプライバシー法規を実施した.
また、最近いくつかの会社が広範なサイバー攻撃を受けていることを受けて、米国の立法者や規制機関は新たな、より強力なサイバーセキュリティ規則を提案している。GDPR、CCPA、および他のプライバシーおよびデータ保護法を遵守する努力は、時間とともに増加する可能性があり、いくつかのビジネス実践を修正する必要があるかもしれない大きなコストと挑戦をもたらす可能性があります。これらの世界各地との同様の取り組みは、当社のサーバを開発、実施、または保護するコストを増加させる可能性があり、改善された技術により多くのリソースを割り当てることで、私たちの情報技術およびコンプライアンスコストを増加させることが求められています。また、データセキュリティ事件やプライバシー侵害に関する規制部門の法執行行動や調査が増加し続けている。より限定的な法律、規則、法規、または将来の法執行行動または調査を公布することは、重大な規制処罰および重大な法的責任または既存または将来のデータプライバシー法律法規の違反につながる可能性のある訴訟を遵守することなく、私たちの業務コストまたは制限を増加させることによって私たちに影響を与える可能性があります。
もしシステムが故障したら、私たちの業務と運営は影響を受けるだろう。
セキュリティ対策が実施されているにもかかわらず、我々の内部コンピュータシステムは、コンピュータウイルス、人為的エラー、許可されていないアクセス、自然災害または人為的災害、意図的な破壊行為、テロ、戦争およびネットワーク、電気通信、および電気故障の破壊を受けやすい。私たちの運営を中断させるシステムの故障、事故、セキュリティホールは、私たちの製造運営や製品開発計画の実質的な中断を招く可能性があります。例えば、私たちの製品の完成した臨床試験中の臨床試験データの紛失は私たちの監督管理の承認作業を遅延させ、データを回復或いは複製するコストを著しく増加させる可能性がある。任意の中断またはセキュリティホールが、私たちのデータまたはアプリケーションの損失または破損をもたらし、または機密または独自の情報を適切に開示しない場合、私たちは、責任、名声の損害、および私たちのビジネス運営の損害を招く可能性があります。
私たちはサイバーセキュリティの脅威と事件と関連した危険に直面している。
我々は,他の人がインターネットを介して不正なアクセスを試みたり,マルウェアを我々の情報技術やITシステムに導入しようとしたりすることが多い.悪意のあるハッカーおよび内部脅威(従業員および第三者サービス提供者を含む)、または私たちの物理施設に侵入する侵入者を含む個人または組織は、時々私たちのソフトウェア、ネットワーク、およびサービスに不正にアクセスしようとする。私たちはまた、私たちのネットワークまたはデータセンターにアクセスしようとする悪意のある攻撃者の目標になる可能性があります。私たちの業務、製品、従業員、サプライヤー、および顧客に関連する独自の情報を盗み取ること、私たちまたは私たちのサプライヤー、顧客、または他の人のシステムおよびサービスを中断すること、またはそのようなシステムおよびサービスの支配権を回復するために身代金を要求すること。このような試みは、含まれるが、これらに限定されない−ソーシャルエンジニアリングまたは“ネットワーク釣り”の試み、サービス攻撃およびマルウェア(ウイルス、トロイの木馬およびキーボード記録プログラムを含む)を拒否する数および技術的複雑性が増加しており、成功すれば、私たちおよび任意の影響を受ける様々な態様が、独自または機密情報を紛失または乱用するか、または私たちのビジネス運営(私たちの製造トラフィックを含む)を中断するリスクに直面する。当社のITインフラストラクチャには、第三者が提供するサービスも含まれており、これらのサービスプロバイダのシステムや製品が破壊され、私たちのシステムおよび当社の独自または機密情報のセキュリティに影響を与える可能性があります。もし私たちまたは私たちのサービスプロバイダのシステムが深刻に破壊され、私たちの名声を損なう可能性があり、収入損失や機密データが乱用される可能性があり、私たちはこのような問題を解決するために巨額の費用を発生させるかもしれない。
Pacira BioSciences,Inc.|2022 Form 10-K|65ページ
個人やビジネス情報のプライバシーやセキュリティを維持しなければ、顧客や従業員における私たちの名声を損なう可能性があり、大量の追加コストが発生し、訴訟の対象となる可能性があります。
顧客と従業員の個人情報を受信、保持、送信し、これらの情報を第三者プロバイダに依頼し、活動を実行してくれるクラウドサービスプロバイダを含む。我々のトラフィックは、支払いを許可する情報を含む暗号化された機密情報を公共ネットワーク上で安全に送信することに依存する。我々のセキュリティシステムが損害を受けた場合、または私たちのハードウェアまたはソフトウェアまたはサプライヤーの欠陥が顧客または従業員の情報を許可されていない人によって取得された場合、顧客および他の人における私たちの名声および私たちの運営、運営結果、財務状況および流動性に悪影響を与え、訴訟、政府行動、または処罰をもたらす可能性がある。さらに、脆弱性は私たちの運営を混乱させ、情報システムのセキュリティに多くの追加資源を使うことを要求するかもしれない。
私たちが運営しているすべての国と州や地方では、私たちの業務のデータの使用は国と州や地方レベルで規制されている。プライバシーや情報セキュリティの法律や法規が変化し,これらの法律や法規を遵守することはコスト増加を招く可能性があり,その原因には他にもシステム変化や新しいプログラムの開発が含まれている.もし私たちまたは私たちと情報を共有する人がこれらの法律や法規を守らなければ、私たちの名声は損なわれる可能性があり、将来の業務損失を招く可能性があり、私たちは遵守しないために追加の法的リスクに直面する可能性がある。
個人やビジネス情報を保護し、私たちの情報技術ネットワークへのアクセスを確保するための投資を継続するためのセキュリティ対策と制御措置があります。しかしながら、外部当事者の行為、従業員のミス、内部または外部違反、または他の理由により、これらの措置は破壊される可能性があるため、不正な当事者は、私たちのデータシステムにアクセスし、商業および個人情報を流用する可能性がある。許可されていないアクセスを取得し、サービスを無効にしたり、システムを破壊したり、またはシステムを破壊するための技術がしばしば変化し、直ちに侵入の兆候が生じない可能性があるため、これらの技術を予測し、それらをタイムリーに発見または対応し、または十分な予防措置を実施することができない可能性がある。このような違反や不正アクセスは、重大な法的および財務的リスクをもたらし、私たちの名声を損なう可能性があり、私たちの業務および運営結果に悪影響を及ぼす可能性があります。
世界的な気候の重大な変化、極端な天気条件、利用可能な水、および他の気候関連のリスクは、私たちの業務や運営に悪影響を及ぼす可能性がある。
気候変化、嵐、または他の極端な気象条件および/または給水挑戦が、私たちの運営または私たちのサプライヤー、流通業者、および顧客の運営に悪影響を及ぼす場合、私たちの業務は悪影響を受ける可能性があります。ますます多くの科学的証拠と公衆の懸念は、温室効果ガスの排出と促進の人類活動がすでに世界の気温と天気パターンの重大な変化をもたらし続け、嵐と他の天気事件、酷暑、ハリケーン、野火と洪水の頻度或いは深刻さを増加させることを示している。このような状況は予測できませんが、もしこのような状況が私たちの生産場所に影響を与えたり、私たちの第三者原材料サプライヤー、私たちの製造設備、あるいは私たちの流通業者の生産計画を含めて生産計画を変更したりすると、EXPAREL、ZILRETTAまたはIOVERA°が私たちの顧客やパートナーに供給される中断に遭遇したり、私たちの原材料や包装材料のコストや可用性に悪影響を及ぼす可能性があります。私たちの顧客の運営中断はまた私たちの製品需要に悪影響を及ぼす可能性があります。気候変動対策の法規制はコンプライアンスの増加や水やエネルギーコストに関する製造コストの増加を招く可能性がある。
気候変化、自然災害(例えば、地震、野火、ハリケーン、竜巻、津波または他の不利な天気イベントおよび気候条件)およびその結果および影響は、原材料の獲得可能性、製造コストの増加、私たちの製造業務生産性への中断、消費者の選好または支出優先順位の変化、およびエネルギー不足、過去も将来も私たちの運営や私たちのサプライヤー、他のサプライヤーまたは顧客の運営を損害または妨害し、あるいは経済的不安定を招き、私たちの運営業績や財務状況に負の影響を与える可能性がある。さらに、いくつかの災害は私たちの一般保険証書の保証範囲内にない可能性があり、これは重大な取り返しのつかない損失を招く可能性がある。世界各地の多くの政府や他の規制機関は気候変動の影響を軽減するための法規を制定している。もし私たち、私たちのサプライヤー、または私たちのサプライチェーンの他の人がこれらの法律と法規を遵守することを要求された場合、または私たちが気候への影響を減少または軽減するために追加の自発的なステップを取ることを選択した場合、私たちはエネルギー、生産、輸送、原材料コストの増加、資本支出の増加、または保険料と賠償免除額の増加を経験し、すべてが私たちの運営に悪影響を及ぼす可能性がある。また、管轄区域間の不一致の規制は、私たちがこのような法律法規を遵守するコストにも影響を及ぼす可能性がある。将来の気候変動立法、法規または業界基準、およびいかなる国際条約や協定の潜在的な影響に対するいかなる評価も不確定である。なぜなら、私たちが業務を展開している国では、潜在的な規制変化の範囲が広いからである。
Pacira BioSciences,Inc.|2022 Form 10-K|66ページ
私たちの国際業務は私たちに時々衝突する多くの法律と法規の要求を直面させ、これらの要求を守ることは費用が高く、時間がかかる可能性があり、これらの規定に違反することは私たちの業務や運営に不利な影響を与えるかもしれない。
医薬品や医療機器マーケティング、製品責任、反腐敗、データ保護とプライバシー、コンプライアンス、税収、会計·財務報告、労働法、賃金と工数基準、労働関係、人権など様々な問題において、私たちは多くの法律要求の制約を受け、時に衝突している。私たちの業務のグローバル化は、様々な法律要求を遵守することが高価で、時間がかかり、大量の資源を必要とするため、様々な法規や法律を遵守する難しさとコストを増加させる可能性がある。私たちの業務展開中にこれらの規定に違反する1つ以上は、私たちおよび/または私たちの従業員に対する巨額の罰金、法執行行動、または刑事制裁を招き、業務を禁止し、私たちの名声を損なう可能性があります。
これらの法律や規制要件に加えて、国際的な業務展開には固有のリスクが存在するが、これらに限定されない
•異なるまたはより厳格なプライバシー、データ保護、データローカライズ、および他の法律は、特定の国で収集されたいくつかのタイプのデータをその国で格納および/または処理しなければならないように、私たちの製品、サービス、および運営を変更することを要求することができる
•地理的距離、言語、文化の違いにより、我々の海外業務を開発、整備し、同時に管理することは困難である
•厳しい地方労働法律法規
•利益送金と外貨両替制限
•自然災害、戦争とテロ行為、突発的な公衆衛生事件を含む地政学的事件は、これに対する私たちの管轄区域各国政府の異なる反応を含む
•輸出入条例
•米国の“海外腐敗防止法”、イギリスの“反賄賂法”、その他の司法管轄区域で政府関係者や他の第三者への贈賄を禁止する法律法規を遵守する
•反独占と競争規制
•世界の港の在庫や渋滞に関する遅延を含む、製造、輸送、および製品の配送に関する遅延
•距離、エネルギー価格、インフレ、または他の要因により輸送コストが増加した
•潜在的な不利な税収の発展
•貿易障壁や貿易法規の変化
•ウクライナ戦争、経済不安定、弾圧または人権問題を含むが、これらに限定されない政治的または社会的動揺
•他の政府法規や地域法律の遵守を要求することと関連した危険。
また、私たちの輸出入活動は税関の法律法規によって制限されており、これらの法律法規は複雑で、私たちが業務を展開する法律管轄区域内ではそれぞれ異なる。私たちは予防措置を取ったにもかかわらず、私たちは税関の法執行において統制ミスが起こらないことを確実にすることができない。私たちは現在税関当局の監査を受けている。税関の法律や法規を守らない行為は、米国または外国政府の税関監査で発見される可能性があり、あるいは税関当局が私たちの関税処理方法に同意しない可能性があり、このような行為は巨額の罰金と処罰を招く可能性があり、これは私たちの業務や財務業績に悪影響を及ぼす可能性がある。しかも、アメリカ貿易法の改正は私たちの業務に悪影響を及ぼすかもしれない。これらの変化と他国の貿易法のいかなる変化も追加的なコンプライアンスコストと義務を増加させ、遵守しないことで巨額の罰金と罰に直面させる可能性がある。これらや他の外国法制度を遵守することは、私たちの業務や運営結果に実質的な悪影響を及ぼす可能性がある。また、グローバル企業として、米国の“海外腐敗防止法”やイギリスの“反賄賂法”を含む、政府の腐敗対策を目的とした外国や米国の法律法規の制約を受けている。これらの法律と法規に違反すると罰金と処罰を招く可能性があります;私たち、私たちの役員、私たちの上級管理者、または従業員に刑事制裁を実施し、私たちの業務展開を禁止し、私たちが1つ以上の国/地域で私たちの製品とサービスを提供する能力;そして私たちのブランドと私たちの経営業績に実質的なマイナス影響を与えます。米国の“海外腐敗防止法”やイギリスの“贈収賄法”など、これらの外国とアメリカの法律·法規の遵守を確保するための政策や手続きが実施されているにもかかわらず、私たちの従業員は保証されていません, 業務パートナーやエージェントは私たちの政策に違反しないだろう。
Pacira BioSciences,Inc.|2022 Form 10-K|67ページ
項目1 B。未解決従業員意見
ない。
項目2.財産
カリフォルニア州サンディエゴの科学センターパークには合計約19.5万平方フィートの施設が三つあります。これらの施設を研究開発,製造,一般と行政目的,在庫と原材料の貯蔵に用いた。EXPARELとiovera°携帯電話を生産する製造工場および私たちのハイブリッド用途研究開発物件賃貸契約は2030年6月に満期になり、私たちの倉庫賃貸契約は2030年8月に満期になります。♪the the theタンパのPacira革新と訓練センターフロリダ州タンパに位置する約13,000平方フィートの施設は全方位の教育活動を支持し、臨床医師の痛みのコントロールとオピオイド暴露の減少或いは除去に対する最新の現地、地域と現場ブロック方法に対する理解を促進する。私たちの主な行政事務室と会社の本社もタンパ市にあり、私たちの賃貸契約は2026年12月に満期になります。♪the the theヒューストン派ヒラ革新訓練センターテキサス州ヒューストンに位置する約19,000平方フィートの施設はタンパの修理ステーションに似ているが、人工知能、3-D訓練ソフトウェアと専門的な医療照明と天井カメラ、湿気と乾燥した実験室空間、125席を収容できる報告室も搭載されている。ヒューストン鉱山のレンタル契約は2027年10月に満期になる。
また、私たちはニュージャージー州パシパニに行政、商業、業務発展事務所を設置し、2028年3月に満期になった賃貸契約によると、私たちはそこに約53,000平方フィートの面積を持っています。Flexion買収の一部として、2025年4月に満期になった賃貸契約に基づいて、マサチューセッツ州バーリントンの約42,000平方フィートのオフィス空間をレンタルし、2024年2月に満期になった賃貸契約に基づいて、マサチューセッツ州ウォーベン約5,300平方フィートの実験室空間を部分的に転貸すると仮定し、現在完全に転貸している。
私たちは科学センターパーク、Thermo Fisher、Carlisleサイトの研究開発と製造施設を信じています(後述)プロジェクト1-ビジネス以上)は,我々のビジネスやパイプ開発ニーズを満たすのに十分である.また、従業員を増やし、地理的市場を拡大しながら、EXPAREL、ZILRETTA、IOVERA°の需要が増加すれば、必要に応じて適切な追加または代替空間を提供して、私たちの業務のこのような拡張を満たすことができると信じています。
項目3.法的訴訟
第3項.法律訴訟の資料については、付記20を参照してください引受金とその他の事項私たちの連結財務諸表はここに含まれています。
プロジェクト4.鉱山安全情報開示
適用されません。
Pacira BioSciences,Inc.|2022 Form 10-K|68ページ
第II部
項目5.登録者普通株式市場、関連株主事項、発行者による株式証券の購入
私たちの普通株はナスダック世界ベスト市場に上場して取引され、株式コードは“PCRX”です。2023年2月27日現在、私たちは11人の普通株式保有者がいます。記録保持者の数は,我々の譲渡代理帳簿に登録されている実所有者数に基づいて計算され,“街頭名簿”の株式保有者の数が大幅に増加していることは反映されておらず,その株式は銀行,ブローカー,他の金融機関が登録保有している.
[パフォーマンスチャート]
次の図は2017年12月29日,すなわち2017年の最終取引日であり,Pacira BioSciences,Inc.,ナスダック総合指数,ナスダックバイオテクノロジー指数,標準プル製薬ベスト指数各100.00ドルへの投資価値を示している。含まれる3つの指数は比較に供するだけであり、管理層がこれらの指数が私たちの普通株の相対表現を評価する適切な指標であると考えることを必ずしも反映しているわけではない。すべての業績は配当金の再投資(あれば)を想定し、12月31日まで計算するST一年ごとです。我々普通株の歴史的株価表現とこの表現図に示す指数は,必ずしも未来の株価表現を示しているとは限らない.
5年間累計総収益の比較
Pacira BioSciences Inc.,ナスダック総合指数では
ナスダックバイオテクノロジー指数と標準プール製薬ベスト指数
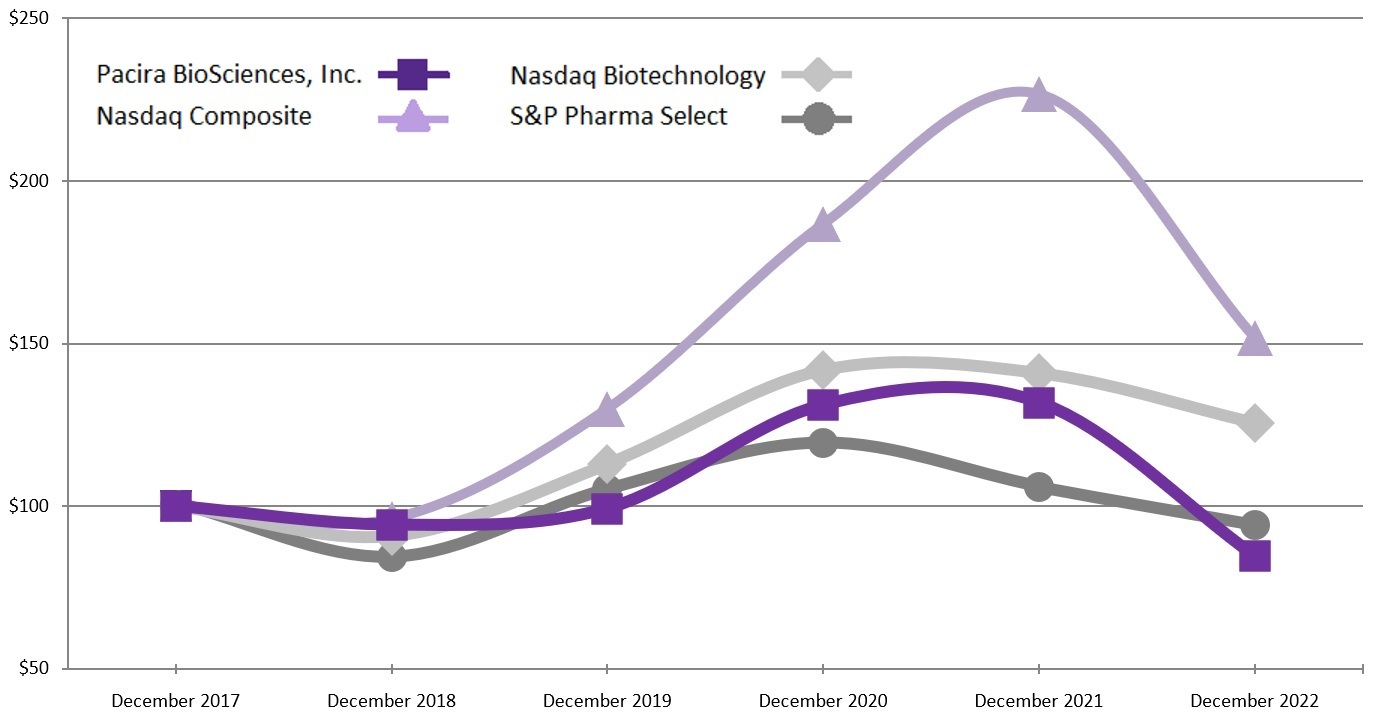
| | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | |
| 12月31日までの累積総リターン |
| 2017 | | 2018 | | 2019 | | 2020 | | 2021 | | 2022 |
| 太平洋生物科学会社(PCRX) | $ | 100.00 | | | $ | 94.24 | | | $ | 99.23 | | | $ | 131.08 | | | $ | 131.81 | | | $ | 84.58 | |
| ナスダック総合指数(^IXIC) | $ | 100.00 | | | $ | 96.12 | | | $ | 129.97 | | | $ | 186.69 | | | $ | 226.63 | | | $ | 151.61 | |
| ナスダックバイオテクノロジー指数(^NBI) | $ | 100.00 | | | $ | 90.68 | | | $ | 112.81 | | | $ | 141.78 | | | $ | 140.88 | | | $ | 125.52 | |
| 標準プール製薬ベスト指数(^SPSIPH) | $ | 100.00 | | | $ | 84.29 | | | $ | 105.16 | | | $ | 119.45 | | | $ | 106.02 | | | $ | 94.15 | |
配当政策
私たちは私たちの普通株式に対するどんな配当金も発表したり支払ったりしたことがない。私たちは現在、任意の未来の収益を維持し、私たちの業務の将来の発展と拡張に資金を提供するつもりですので、予測可能な未来には、私たちの普通株に現金配当金を支払うことはないと予想されます。将来の配当金の支払い(あれば)は、私たちの取締役会が適宜決定し、私たちの財務状況、経営結果、資本要求、私たちの債務を管理する合意に含まれる制限、適用法律の規定、および私たちの取締役会が関連すると思う他の任意の要素に依存します。
Pacira BioSciences,Inc.|2022 Form 10-K|69ページ
プロジェクト6.保留
プロジェクト7.経営陣の財務状況と経営成果の検討と分析
経営陣の財務状況及び経営結果の検討及び分析は、米国公認会計原則(すなわち公認会計原則)と米国証券取引委員会(米国証券取引委員会)の規則及び規定に基づいて作成された我々の総合財務諸表に基づいている。私たちは一つの部門で私たちの財政情報を運営して報告する。以下,当社の財務状況及び経営成果に関する検討は,本年度報告の他の部分とともに読み,当社の総合財務諸表及び以下の総合財務諸表の付記を含む第IV部, プロジェクト15本年度報告します。この討論には重大な危険と不確実性に関する前向きな陳述が含まれている。多くの要因で“リスク要因” in 第1部, 第1 A項それは.この年間報告書で、私たちの実際の結果は、このような前向きな陳述で予想されているものとは大きく異なるかもしれない。定義された用語のいくつかは第1部本年度報告書の一部。
本年度報告のこの部分は,2022年と2021年の年次比較,および2022年と2021年のプロジェクトに関する他の議論を検討した。“米国証券取引委員会”が許可を規定している場合には、2020年12月31日までの年度(本年度報告書で我々の合併財務諸表がカバーする3年度のうち最初の1つ)についての議論を省略した。“経営陣の2021年と2020年の財務状況と経営成果の全面的な議論と分析”および2020年プロジェクトの他の議論は第II部, 第七項, 2021年12月31日までの年次報告書は,2022年2月28日に米国証券取引委員会に提出されるアメリカ証券取引委員会サイトwww.sec.govとわが社のサイトwww.pacira.comで入手できます。上記の当社サイトへの引用は意図せず、当社サイト上の情報を参考に本年報に格納すべきではなく、当社サイトアドレスが非能動的なテキスト参照のみであることが含まれており、当社サイトへのアクティブリンクとするつもりはない。
概要
Paciraは我々が非オピオイド管理に取り組んでいる業界の先駆者であり,可能な限り多くの患者に非オピオイド選択を提供し,オピオイドの役割を再定義し,救援治療のみとしている。著者らはまた、心電嵐、慢性疼痛と痙攣などの交感神経系の衰弱状況に対応するための革新的な干与措置を開発している。長期効果のある局所鎮痛剤実験は®(ブピバカインリポソーム注射可能懸濁液)は2012年4月に商業的に発売された。EXPARELは我々独自のpMVL薬物送達技術を利用して,薬物分子構造を変化させることなく薬物をカプセル化し,必要な時間内に放出する。米国では、EXPARELは、局所または局所手術後の鎮痛を産生するために浸透、野ブロック、および角間腕神経叢ブロックのために許可されている唯一のオピオイドを含まない長時間作用性局所および領域鎮痛剤である。米国では、EXPARELは6歳以上の小児科患者への浸透も許可されている。ヨーロッパでは、EXPARELは腕神経叢ブロックや大腿神経ブロックとして承認され、成人手術後の痛みの治療や、6歳以上の成人や小児の術後中小傷による身体痛の治療に用いられている。2011年に初めて承認されて以来,1200万人を超える患者がEXPARELの治療を受けている。私たちは卸または直接私たちに注文したことによってEXPARELをエンドユーザーに直接出荷し、卸は何の製品も持っていません。2021年11月にFlexion Treateutics,Inc.(“Flexion買収”)を買収することにより,ZILRETTAを買収した®トリアムシノロンアセトニド徐放注射懸濁剤(トリアムシノロンアセトニド徐放注射懸濁剤)は第一種であり、唯一の徐放関節内療法であり、三ケ月以内に主にOA膝関節疼痛を緩和することができ、そしてヒアルロン酸(HA)と多血小板血漿(PRP)、注射或いはその他の早期干与治療の代替品になる可能性がある。MyoScience,Inc.(“MyoScience買収”))2019年4月ioveraを買収しました®標的神経に正確で制御可能な凝縮温度アプリケーションを提供するための手持ち式凍結鎮痛装置であり、エンドユーザに直接販売する。ExPAREL,ZILRETTAとIOVERA°システムは長時間作用,非オピオイドによる疼痛緩和の高度に相補的な製品である。
我々は、EXPAREL、ZILRETTA、IOVERA°の使用を引き続き他のプロセスで拡大し、私たちの早期の製品候補パイプラインの推進、EXPAREL、ZILRETTA、IOVERA°および他の候補製品の規制活動の推進、EXPAREL、ZILRETTAおよびIOVERA°の販売とマーケティング資源への投資、EXPAREL、ZILRETTAおよびIOVERA°の製造能力の拡大と向上、製品、業務、技術への投資、法務の支援を希望する。
Pacira BioSciences,Inc.|2022 Form 10-K|70ページ
屈曲習得
2021年11月、私たちはFlexion合併協定に従ってFlexionの買収を完了し、この合意によると、Flexionは私たちの完全子会社となり、ZILRETTAを私たちの商業製品に添加し、ZILRETTAは1種の非オピオイドコルチコステロイドであり、特許マイクロスフェア技術を採用して延長した鎮痛効果を提供する。ZILRETTAを著者らの革新的な非オピオイド薬物製品の組み合わせに加えることは直接に著者らの使命に符合し、即ちできるだけ多くの患者にオピオイド代替品を提供し、神経疼痛経路の医療需要を満たす。
総コスト5.788億ドルは、Flexion普通株1株8.50ドルに相当する予備支払い4.283億ドル、制限株式単位および現金株式オプションを決済するために2,020万ドルの支払い、Flexion債務の8,510万ドルの支払い、およびFlexion買収と同時に発行された価値ある権利(CVR)の公正価値に相当する4,520万ドルまたは有償を含む。Flexion合併協定はFlexion普通株ごとに1株の非流通株CVR、及びあるFlexion株権が1株当たり1回のCVRを奨励することを規定する。2030年12月31日までにいくつかのマイルストーンに達した場合、各CVRはFlexion株主にFlexion普通株1株当たり8.00ドルに達するか、またはマイルストーン支払いを得る権利がある。Flexionを買収した日、吾らは、それぞれの適用マイルストーンに達すると、CVR所持者に合計3億802億ドルの追加支払いが可能になると予想している。各報告期間において、関連する事項または問題が解決されるまで、Flexity買収に関連するまたは価格の公正な価値が再推定されるであろう。詳細については、付記5を参照されたい屈曲習得私たちの連結財務諸表はここに含まれています。
最近のハイライト
•2023年1月に我々のsNDAをFDAに提出し,拡張EXPARELラベルを求め,月窩の坐骨神経ブロックと内転筋管の大腿神経ブロックを含め,FDAは2023年下半期に“処方薬使用者費用法案”に基づいて行動する予定である。SNDAは2つの成功した3期研究の支持を得ており,この2つの研究では,塩酸ブピバカインと比較して術後96時間で疼痛コントロールとオピオイド消費の統計的有意な減少を実現している。
•2023年1月、私たちはヒューストンに2つ目の革新訓練センターを開設した。この最先端の施設は,125席の適応講演室,放送スタジオ,身体や他のインタラクティブ職場のための乾湿実験室空間,人工知能訓練ソフトを備えた先進的な超音波機器を備えている。この訓練センターは医師の思想指導者とコミュニティ臨床医師を育成する核心であり、彼らはオピオイド非疼痛管理の最前線を維持することを望んでいる。
•2022年11月,EMAのCHMPとMHRAはいずれもEXPARELの適応拡大のマーケティング認可を許可し,6歳および6歳以上の小児を中小手術創からの術後身体痛を治療する現場遮断薬として使用した。承認は,脊柱や心臓手術を受けた小児患者のEXPAREL浸透に基づく第3段階Play研究の結果である。全体的な結果は成人患者の薬物動態と安全性と一致し、投与量4 mg/kgで安全問題は認められなかった。EMAの承認は全27のEU加盟国およびアイスランド、ノルウェー、リヒテンシュタインに適用され、MHRAの承認はイギリスにも適用される。ExPARELは最初に2020年11月にEUとイギリスの承認を得て、成人術後の痛みを治療する腕神経叢ブロックや大腿神経ブロック、成人手術後の中小傷口の身体痛を治療するための現場ブロックとして使用された。
•2022年10月,米国特許商標局は特許11,452,691号を発行した。この特許は化学成分特許であり,期日は2041年1月22日である。この特許は現在FDAのオレンジマニュアルに含まれており、8番目に列挙された特許だ。同社はまた、EXPARELのプロセス別製品特許である米国特許出願に対する米国特許商標局から補助金通知を受けた。発表後、Paciraはオレンジブックに発売するためにこの特許を提出するだろう。
新冠肺炎コロナウイルスの大流行と世界経済情勢
2020年初めから、私たちの収入とサプライチェーンはずっと新冠肺炎疫病に関連する挑戦の影響を受けており、その中には公衆衛生指導と政府指示による選択性手術のスケジュールを大幅に延期或いは一時停止することを含む。大流行期間中、ワクチンと治療法の採用及び選択性手術に対する制限が減少したため、影響程度は軽減されたが、大流行に関連するいくつかの業務と人員配置挑戦は依然として存在している。選択性手術市場が正常化するのにどのくらいの時間がかかるかは不明であり、未来の新冠肺炎変異体或いはその他の原因で再び選択性手術を制限するかどうかも不明である。疫病と全世界の経済状況の直接と間接的な影響はすでに私たちの業務、財務状況と経営結果に負の影響を与える可能性がある。これらの影響には長期的なインフレと金利上昇が含まれているかもしれません
Pacira BioSciences,Inc.|2022 Form 10-K|71ページ
お客様と仕入先およびより長い納期や十分な材料供給が確保できません。状況は依然として動態的であり、迅速で実質的な変化が起こる可能性がある。私たちが予見できない他の否定的な影響も出るかもしれない。このような影響の性質や程度は将来の事態の発展に依存し,これらの事態の推移は高度に不確実であり,予測もできない.
私たちは引き続き状況を積極的に監視し、連邦、州、または地方当局が提案した措置、あるいは私たちの患者、従業員、パートナー、サプライヤー、株主、および利害関係者の利益に最も適合すると思う措置を実施する。会社が直面している新冠肺炎の大流行又は任意の他の未来の大流行、流行病又は伝染性疾病の発生に関連するリスクに関する説明は、参照されたい第1 A項. “リスク要因この年間報告書にあります。
経営成果
2022年と2021年12月31日終了年度比較
収入.収入
製品純売上高には,(I)米国,EU,英国におけるEXPARELの売上,(Ii)ZILRETTAの米国での売上,(Iii)米国,カナダ,EUにおけるiovera°の売上,(Iv)主に獣医用ブピバカインリポソーム注射懸濁剤の売上と特許権使用料,(V)許可料およびマイルストーン支払いが含まれている
次の表は、百分率変化(千単位のドル金額)を含む私たちの年の収入に関する情報を提供します | | | | | | | | | | | | | | | | | |
| | 十二月三十一日までの年度 | | パーセント増加/(減少) |
| | 2022 | | 2021 | |
| 製品純売上高: | | | | | |
| ExparEL | $ | 536,899 | | | $ | 506,515 | | | 6% |
ZILRETTA(1) | 105,517 | | | 12,683 | | | 100% + |
| Iovera° | 15,258 | | | 16,162 | | | (6)% |
| ブピバカインリポソーム注射用懸濁剤 | 6,476 | | | 3,606 | | | 80% |
| 製品純売上合計 | 664,150 | | | 538,966 | | | 23% |
| 特許権使用料収入 | 2,673 | | | 2,442 | | | 9% |
| 協力許可と記念碑的な収入 | — | | | 125 | | | (100)% |
| 総収入 | $ | 666,823 | | | $ | 541,533 | | | 23% |
(1)ZILRETTAの製品純売上高は、2021年12月31日までの1年間、2021年11月19日からの期間、すなわちFlexion買収日に起因することができる。
ExPARELは2021年に比べて2022年の製品純売上高が6%増加したが,これは主に薬瓶総容量が5.5%,単位総販売価格が3.6%増加したためであるが,この部分はEXPAREL薬瓶サイズの販売組み合わせと主に340 B薬品定価や他の戦略パートナーへの参加による毛純調整増加によって相殺されている。EXPARELに対する需要が引き続き増加しているにもかかわらず、主にASCと麻酔科医がEXPAREL長時間作用区域方法の使用を拡大し、マルチモードオピオイド最小化策略の基礎として、入院患者がプログラムを23時間看護場所に移すことができるようにしたが、新冠肺炎変異症例の地域急増、人員不足と看護チームの疲労、及び経済とインフレの消費者自信に対する圧力により、選択性手術市場は依然として大流行後の挑戦に直面している。EXPARELの使用率が大流行前のベースラインレベルに対する選択的外科手術の全体的な低下を依然として上回っているのは,外来や緊急手術の使用率が増加しているためである。
2021年11月のFlexion買収の結果としてZILRETTAを買収した。2022年12月31日と2021年12月31日の年度までに、製品の純売上高はそれぞれ1.055億ドルと1270万ドルであることを確認しました。2021年12月31日までの1年間で、製品純売上高は2021年11月19日から、すなわちFlexion買収の終了日となった
2021年に比べて2022年のiovera°の製品純売上高が6%低下したのは,主に第1世代iovera°製品から第2世代iovera°製品への移行の遅れと,ある地域での精算政策の短期的な変化によるものである。TKA手術や慢性疼痛治療において最大のニーズは,TKA術前の疼痛緩和,特に軽度から重度の膝骨性関節炎を有する患者であることが示唆された。
2022年、ブピバカインリポソーム注射懸濁剤収入は2021年より80%増加し、その関連特許使用料は9%増加したが、これは主に獣医が注文した瓶サイズの販売組み合わせによるものである。
Pacira BioSciences,Inc.|2022 Form 10-K|72ページ
政府が再び患者の選択的手術を受けることを一時停止或いは望まないのは、持続的な新冠肺炎疫病と経済状況(インフレを含む)が消費者医療選択に与える影響が頭から離れないため、私たちの未来のEXPAREL、ZILRETTAとIOVERA°の販売に影響を与える。
販売原価
商品を販売するコストとは、主に生産、包装、顧客に製品を渡すコストを指す。これらの費用には、労働力、原材料、製造管理費用、占有コスト、施設減価償却、特許権使用料支払い、品質管理、工事が含まれる。
次の表は、百分率変化(千単位のドル金額)を含む、示された年の貨物販売コストと毛率の情報を提供します | | | | | | | | | | | | | | | | | |
| | 十二月三十一日までの年度 | | パーセント増加/(減少) |
| | 2022 | | 2021 | |
| 販売原価 | $ | 199,295 | | | $ | 140,255 | | | 42% |
| 毛利率 | 70% | | 74% | | |
2021年と比べ、2022年の毛金利は4ポイント低下した。原因は在庫備蓄の増加、ある機械と設備の加速減価償却がその将来の経済効果を確定していないこと、およびZILRETTAは調達会計によって固定資産と在庫を公正価値に増加させたが、前の時期の計画外停止部分によって相殺されたからである。
研究と開発費
研究開発費には,主に臨床試験や関連外部サービスに関するコスト,製品開発,その他の研究開発コストがあり,EXPAREL,ZILRETTA,IOVERA°のための新たなデータを生成するための試験,株式による報酬費用が含まれている。臨床と臨床前開発費用は臨床人員費用、第三者による臨床試験、毒理学研究、材料と用品、データベース管理とその他の第三者費用を含む。製品開発と製造生産能力拡張費用には、プロセス開発と製品候補者、設備、材料、請負業者コスト、私たちの製造能力の著しい拡大に関する開発コスト、および私たちの研究空間の施設コストが含まれています。規制費用およびその他の費用には、未承認製品および適応に関する規制活動、医療情報費用、および関係者が含まれる。株式ベースの報酬支出は、株式オプション付与、制限株式単位報酬、および我々従業員株式購入計画(ESPP)のコストに関する。
次の表は、百分率変化(千単位のドル金額)を含む、私たちの示した年の研究開発費の内訳を提供します | | | | | | | | | | | | | | | | | |
| | 十二月三十一日までの年度 | | パーセント増加/(減少) |
| | 2022 | | 2021 | |
| 臨床と臨床前発展 | $ | 45,615 | | | $ | 24,138 | | | 89% |
| 製品開発と製造能力の拡張 | 24,635 | | | 19,352 | | | 27% |
| 規制やその他 | 7,953 | | | 6,590 | | | 21% |
| 株に基づく報酬 | 6,594 | | | 5,465 | | | 21% |
| 研究と開発費用総額 | $ | 84,797 | | | $ | 55,545 | | | 53% |
| 総収入のパーセントを占める | 13% | | 10% | | |
2021年に比べ、2022年の研究開発総支出は53%増加した。
2022年の臨床·臨床前開発費が2021年より89%増加したのは,持続費用と2つのEXPAREL下肢神経ブロック試験が完了し,バルーン切除術とTKAに用いられており,製品開発候補製品としての屈曲獲得と毒理学研究の一部である。前年は新冠肺炎の大流行に関連した臨床試験遅延の影響を受けたが,今年度は内部拡大の候補製品パイプラインおよびFlexting買収の結果を含み,OA用IA遺伝子治療候補薬PCRX−201の持続費用を含む
2021年と比較して,2022年の製品開発と製造生産能力拡張支出が27%増加したのは,主にカリフォルニア州サンディエゴにある科学センターパークのEXPAREL製造能力が著しく拡大したためである。
Pacira BioSciences,Inc.|2022 Form 10-K|73ページ
2022年の規制およびその他の費用は、EUのEXPAREL小児科提出書類と米国のsNDAを支持するために2021年より21%増加し、私たちは2023年1月にFDAにこの文書を提出し、内転筋管の大腿神経ブロックと月窩の坐骨神経ブロックを含むようにEXPARELのラベルを拡張することを求めた。
2022年の株式ベースの報酬が2021年より21%増加したのは、主に研究開発者の未償還株式奨励額が増加したためだ。
私たちは2023年の研究開発コストが2022年より少し低くなると予想し、重点はZILRETTA、iovera°、PCRX-201とPCRX-401である。ZILRETTAの徐放プロファイルは肩部の骨性関節炎疼痛に有効な治療を提供できると信じており、ZILRETTAによる肩性関節炎治療の3期試験を開始する予定である。著者らはまた、2型糖尿病患者におけるZILRETTAのOA膝関節安全性研究と痙攣患者のiovera°を調査する3期試験を開始し、PCRX-401のIND申請を提出して、下腰痛治療の1期試験を開始する予定である。
販売、一般、行政費用
販売とマーケティング費用は、主に私たちの販売チームと、私たちの販売、マーケティング、医療と科学事務運営を支持する人員の報酬と福祉、私たちの製品の健康結果効果を宣伝することに関する費用、プロバイダレベルの市場参入と患者精算支援、顧客教育計画への投資を含む。一般的および行政的費用には、承認された製品および適応に関連する法律、財務、規制活動、コンプライアンス、情報技術、人的資源、業務発展、実行管理、および他の支援者の報酬および福祉が含まれる。それはまた法律、監査、税務、そしてコンサルティングサービスの専門的な費用を含む。株式ベースの報酬支出は、株式オプション付与、RSU報酬、および私たちのESPPのコストに関する。
次の表は、表示された年内の販売、一般、および行政費用の情報を提供し、百分率変化(千単位のドル金額)を含む | | | | | | | | | | | | | | | | | |
| | 十二月三十一日までの年度 | | パーセント増加/(減少) |
| | 2022 | | 2021 | |
| 販売とマーケティング | $ | 144,996 | | | $ | 111,022 | | | 31% |
| 一般と行政 | 73,989 | | | 57,433 | | | 29% |
| 株に基づく報酬 | 35,531 | | | 30,890 | | | 15% |
| 販売、一般、行政費用の合計 | $ | 254,516 | | | $ | 199,345 | | | 28% |
| 総収入のパーセントを占める | 38% | | 37% | | |
2021年と比較して、2022年の販売、一般と行政費用総額は28%増加した。
2021年に比べて2022年の販売·マーケティング費が31%増加したのは、2021年11月にFlexion買収を完了した後、ZILRETTAとiovera°を支持する販売チームが拡大し、EXPARELの欧州での契約販売チームに全員を配備したためである。増加した費用にはZILRETTAの患者精算支援費用も含まれている。オピオイドや術後疼痛管理の影響に関する教育イニシアチブや計画,非オピオイド治療選択を理解することを患者に教育するための全国提唱活動を含む,我々の製品へのマーケティング投資を継続している。また,引き続き臨床医研修に投資し,タンパの整備所でEXPARELとIOVERA°を使用した。ZILRETTAは著者らの商業製品の組み合わせに参加し、臨床医師に2種類の独特なOA治療選択を提供し、患者看護の個性化を実現した。
2021年と比較して、2022年の一般·行政費用が29%増加したのは、2021年11月のFlexion買収による行政支援コスト、統合期間中の移行費用、知的財産権保護を含む法的コスト、および欧州市場への拡張のための追加的な支援が原因である。
2021年と比較して、株式ベースの報酬は2022年に15%増加し、主に販売、一般、管理者の未償還株式奨励数および株式ベースの報酬支出が加速したためである。
Pacira BioSciences,Inc.|2022 Form 10-K|74ページ
無形資産の償却を取得した
下表は、百分率変化(千ドルの金額)を含む年間に購入された無形資産の償却状況をまとめたものである
| | | | | | | | | | | | | | | | | |
| 十二月三十一日までの年度 | | パーセント増加/(減少) |
| 2022 | | 2021 | |
| 無形資産の償却を取得した | $ | 57,288 | | | $ | 13,553 | | | 100% + |
2022年はFlexion買収完了後初の年間であるため、買収された無形資産の償却は2022年に2021年より大幅に増加する。私たちはZILRETTAのために、膝関節炎の痛みを治療するための開発技術の無形資産を獲得し、この資産は約10年間の使用寿命内に償却される。詳細については、付記5を参照されたい屈曲する 買収して私たちの連結財務諸表に含まれている。
買収に関連する費用(収益)、減価その他
次の表は、Flexion買収、MyoScience買収、ビジネスプロトコル、終了コスト、および他の活動に関連する年間のコストをまとめています(千ドルで) | | | | | | | | | | | | | | | | | |
| 十二月三十一日までの年度 | | パーセント増加/(減少) |
| 2022 | | 2021 | |
| 買収に係る費用 | $ | (18,231) | | | $ | 39,911 | | | 適用されない |
| 得られた進行中の研究と開発の減価 | 26,134 | | | — | | | 適用されない |
| 他にも | 3,000 | | | 3,000 | | | —% |
| 買収に関連する費用(収益)、減価その他 | $ | 10,903 | | | $ | 42,911 | | | (75)% |
2022年、1820万ドルの買収関連収益を確認した。これらの収益は、主に、Flexion統合プロトコルによって実現可能または対価格の適用期間の予測を調整することと、2023年12月31日(これらのマイルストーンの満期日を達成する)前にMyoScienceまたは対価マイルストーンに達する可能性が低下する可能性があることによる買収または対価負債の減少によるものである. これらの収益は、解散費および従業員に関連する他のコスト、法律および他の専門費用、第三者サービス、およびFlexion買収に関連する他の使い捨て費用によって部分的に相殺される。詳細については、付記12を参照されたい金融商品18を付記して買収に関連する費用(収益)、減価その他私たちの連結財務諸表はここに含まれています。
2021年には、3990万ドルの買収関連費用を確認しました。これらの費用は、主に解散費と他の従業員関連のコスト、投資銀行、法律および他の専門費用、第三者サービス、およびFlexion買収に関連する他の使い捨て費用によって推進される。これらの費用は、MyoScienceの買収に関連する、または価格に関連する公正な価値変化の収益によって部分的に相殺される。
2022年には,これまでの帳簿価値がその公正価値を超えた金額に基づいて,ZILRETTAに関する買収のための無形資産の開発に2,610万ドルの減値を確認し,肩の骨性関節炎痛の治療に用いた。注9を参照商誉と無形資産もっと多くの情報を知ります。
2022年には、ライセンス契約の終了に関する300万ドルの費用を確認しました。付記20を参照引受金とその他の事項私たちの連結財務諸表にはより多くの情報が含まれている。2021年、私たちはNuance Biotech Co.Ltdと共同で私たちの開発と商業化協定を中止して、中国ExPARELの開発と商業化を推進することに同意した。なぜなら、実行可能な監督ルートが不足して、私たちの知的財産権を十分に保護し、模倣薬のリスクから保護することができ、これは300万ドルの解散コストを招いた
Pacira BioSciences,Inc.|2022 Form 10-K|75ページ
その他の費用、純額
次の表は、百分率変化(千ドルの金額)を含む、示された年の他の費用純額の情報を提供します | | | | | | | | | | | | | | | | | |
| | 十二月三十一日までの年度 | | パーセント増加/(減少) |
| | 2022 | | 2021 | |
| 利子支出 | $ | (39,976) | | | $ | (31,750) | | | 26% |
| 利子収入 | 4,542 | | | 896 | | | 100% + |
| | | | | |
| その他、純額 | (11,288) | | | (2,666) | | | 100% + |
| その他の費用の合計 | $ | (46,722) | | | $ | (33,520) | | | 39% |
その他の総支出は、2022年に2021年より39%増加した。
利息支出が26%増加したのは、2021年12月に締結された3.75億ドルの定期融資によるものだ。この成長は、2022年に会計基準を採用して更新(またはASU 2020-06)するため、2022年に関連する債務割引償却がなく、私たちの2.375転換可能優先手形が2022年4月1日に満期になるか、2022年4月1日に満期になるため、この成長は部分的に相殺された。ASU 2020-06を採用した詳細については、注釈2を参照されたい重要な会計政策の概要私たちの連結財務諸表にあります。私たちは2022年12月に定期ローンのために5000万ドルの元金を前払いし、また940万ドルの四半期元金を支払い、2023年にさらに前払いする予定だ。詳細については付記11を参照されたい借金を抱え私たちの連結財務諸表にあります。
全体の投資残高とより高い金利により、2022年の利息収入は2021年より大幅に増加した。
2022年の他の純支出には1,000万ドルの株式投資減価が含まれる。2021年の他の純支出には、株式売却投資を含む260万ドルの赤字が達成された。
所得税(福祉)費用
次の表は、パーセント変化(千単位のドル金額)を含む年間の私たちの所得税(福祉)支出の情報を提供します | | | | | | | | | | | | | | | | | |
| | 十二月三十一日までの年度 | | パーセント増加/(減少) |
| | 2022 | | 2021 | |
| 所得税(福祉)費用 | $ | (2,607) | | | $ | 14,424 | | | 適用されない |
| 実際の税率 | (20)% | | 26% | | |
我々は2022年12月31日までの会計年度に260万ドルの所得税優遇を記録し、2021年12月31日現在の会計年度に1440万ドルの所得税支出を記録した。2022年12月31日までの年度の有効税率は(20%)%であり、米国の法定税率21%とは異なり、非課税または対価格公正価値収益、SkyePharmaマイルストーン支払いの課税可能利息と税収控除があるが、資本損失繰越と差し引くことができない幹部給与の評価手当部分に相殺されるからである。2021年12月31日までの年度の実質税率は26%で、米国の法定税率21%とは異なり、これは資本損失繰越に記録されている控除不可費用と推定手当により、株式に基づく報酬控除と税収控除によって一部が相殺されたためである。
流動性と資本資源
2006年の設立以来、私たちは大部分の現金資源をEXPAREL開発と商業化に関連する製造、研究開発と販売、一般と行政活動に投入してきた。また、2021年11月には、Flexion買収の一部としてZILRETTAを買収し、MyoScience買収の一部として2019年4月にiovera°を買収した。私たちは主にExPARELとZILRETTAのビジネス成功に依存している。私たちの運営資金は主に転換可能な優先手形と他の債務、普通株の売却、製品販売と協力許可、マイルストーン収入の収益から来ています。2022年12月31日現在、我々の累計赤字は1兆488億ドル、現金および現金等価物と売却可能投資は3.259億ドル、運営資本は3.506億ドル
私たちの手元の現金と売却可能な投資は私たちの短期流動資金需要を満たすのに十分であり、必要であれば他の融資源を得ることができると予想している。
2020年3月、新型肺炎の大流行に対応するため、コロナウイルス援助、救済、経済安全(CARE)法案が法律に署名された。その他の事項を除いて、CARE法案は、企業の流動性を増加させるための何らかの措置をとることを許可している
Pacira BioSciences,Inc.|2022 Form 10-K|76ページ
例えば、雇用主賃金税の納付を延期し、従業員を維持するための税収控除、その他の規定を提供する。私たちは2020年12月31日までの年間特定雇用者賃金税280万ドルの支払いを延期する条項の恩恵を受け、それぞれ2021年12月と2022年12月に140万ドルを送金した。私たちは2022年12月にFlexion買収を完了する前に受け取ったFlexion福祉として60万ドルを外貨で出した。
キャッシュフローの概要
次の表は、2022年12月31日と2021年12月31日までの年間私たちの経営、投資、融資活動のキャッシュフロー(単位:千)をまとめています | | | | | | | | | | | | | | |
| | | 十二月三十一日までの年度 |
| キャッシュフローデータ統合レポート: | | 2022 | | 2021 |
| 提供された現金純額(使用): | | | | |
| 経営活動 | | $ | 145,274 | | | $ | 125,717 | |
| 投資活動 | | (225,185) | | | (20,790) | |
| 融資活動 | | (401,528) | | | 380,694 | |
| 現金および現金等価物の純増加 | | $ | (481,439) | | | $ | 485,621 | |
経営活動
2022年、運営活動が提供する純現金は1兆453億ドルだったが、2021年には1兆257億ドルだった。1,960万ドルの増加は、ZILRETTAおよびEXPARELの製品純売上高の増加によるものであり、これらの純製品売上高は2021年11月にFlexion買収の一部として買収されたが、既存および新規買収を支援する製品および候補製品のすべての運営費用項目の増加、毛金利のやや低下、利息支払いの増加によって相殺される。
投資活動
2022年、投資活動のための現金純額は2.252億ドルで、1.501億ドルの売却投資購入(満期日を除く)、2021年第4四半期にSkyePharmaからPacira PharmPharmticals,Inc.を買収した3200万ドルまたは対価格マイルストーン支払い、カリフォルニア州サンディエゴの科学センターパークに位置するEXPAREL生産能力拡張プロジェクトの製品および設備充填ラインから購入した固定資産3010万ドル、および1300万ドルの株式および債務投資を含み、外部補充開発段階の製品候補製品のために使用される。
2021年、投資活動のための現金純額は2,080万ドルであり、これは主にFlexion買収に関連する買収価格の対価格の4.2億ドルの現金部分と、4590万ドルの資本支出が、主にカリフォルニア州サンディエゴにある科学センターパークの新たな200リットルEXPAREL生産能力拡張プロジェクトの設備に使用されているためである。これらの現金の使用は、Flexion買収に関連する買収価格対価格の現金部分を支払うための4.572億ドルの売却可能な投資部分によって相殺される。
融資活動
2022年、融資活動に使用される現金純額は4.015億ドルで、Flexion買収のトリガとなるFlexion 2024債券保有者購入要約に対する1.926億ドルの元金償還、2022年4月1日満期の2022年債券の1.57億ドル、および5,000万ドルの元金前金を含む7810万ドルの定期融資元金支払いが含まれ、一部は株式オプションを行使する2,440万ドルの収益と、我々のESPPが普通株を発行した300万ドルによって相殺される。
2021年、融資活動が提供する現金純額は3.807億ドルで、その中には3.592億ドルの定期融資純収益、2380万ドルの株式オプション行使収益、および我々のESPPによる株式発行の280万ドルが含まれている。MyoScience証券保有者にも支払いまたは対価格があり、そのうち520万ドルが融資活動に分類されており、これはMyoScienceを買収する際の確認に基づいている。
株式融資
2006年12月設立から2022年12月31日まで、普通株や他の株式証券を公開発行することで3兆445億ドルの純収益を集めた。
Pacira BioSciences,Inc.|2022 Form 10-K|77ページ
債務
2026年の定期ローンBローン
2021年12月に、吾らは3.75億ドルの定期融資を締結し、このローンは当社及び任意の付属保証人のほとんどの資産を抵当にし、2026年12月7日に満期になる予定であるが、信用協定に掲載されているいくつかの例外状況に制限されなければならない。当社は代替基準金利借入や定期基準借入を選択することができます。各定期ローン借款は予備基本金利借入金であり、予備基本金利(信用プロトコルの定義参照)に相当する変動年利で利息を計算し、金利下限は1.75%プラス6.00%である。各定期ローン借款は定期基準借入金であり、(I)調整された定期SOFR金利(定義は信用プロトコル参照)プラス(Ii)7.00%の変動年利建て利息である。
クレジット協定は、(I)任意の財政四半期の最終日に決定された第1留置権正味レバー率を1.75~1.00以下維持すること、および(Ii)流動資金がいつでも少なくとも1.5億ドルであることを要求する。信用協定はまた、慣例の肯定と否定契約、金融契約、陳述と保証、違約事件、およびその他の条項を含む。当社は2022年12月31日現在、信用協定下のすべての財務契約を遵守している。
2022年12月31日現在、私たちは定期ローンの下で2兆969億ドルの未返済借金があります。私たちは2022年12月に定期ローンのために5000万ドルの元金を前払いし、また940万ドルの四半期元金を支払い、2023年にさらに前払いする予定だ。付記11を参照債務私たちの連結財務諸表は、定期融資についてさらに議論するためにここに含まれている。
2025年変換可能優先チケット
2020年7月には、2025年債券元金総額4.025億ドルの私募を完了し、2025年債券について契約を締結した。2025年に発行される債券固定率は年利0.750厘で、半年ごとに配当され、毎年2月1日と8月1日に配当される。2025年に発行される債券は2025年8月1日に満期になる。2022年12月31日現在、2025年債の未償還元金は4.025億ドル。付記11を参照債務さらに議論するために、私たちの連結財務諸表。
2024年変換可能優先チケット
2021年11月、Flexion買収の一部として、Flexion 2024債券の元金総額を2.013億ドルと仮定する。Flexex 2024年発行の債券の満期日は2024年5月1日、無担保、年利3.375厘、半年ごとに配当され、日付はそれぞれ毎年5月1日および11月1日である。2022年1月、Flexion 2024債券を買い戻した元金総額は1兆926億ドルだった。Flexion 2024手形の未償還元金は2022年12月31日現在860万ドルである。付記11を参照債務さらに議論するために、私たちの連結財務諸表。
将来の資本需要
私たちは、私たちの既存の現金と現金等価物、販売可能な投資、および製品販売から受け取った現金は、私たちの運営費用、資本支出要求、および私たちの定期ローンと債券の利息と元本を支払うのに十分であり、今後12ヶ月間の私たちの債券の任意の転換に資金を提供すると信じています。私たちの将来の運営現金と資本需要の使用は、以下の要素を含むが、これらに限定されない多くの展望的要因に依存する
•Flexion買収に関連する潜在的なFlexionマイルストーン支払いのコストと時間は、ある規制と商業マイルストーンに達すると、総金額は3兆723億ドルに達する可能性がある。2022年9月にPCRX-301のさらなる開発を正式に停止することが決定するまで、総金額は4.255億ドルだった。注5を参照屈曲習得そして、付記12、金融商品より多くの情報を取得するために、私たちの連結財務諸表を参照してください
•潜在的に残っているマイルストーンの費用と時間をMyoScienceセキュリティホルダーに支払うコストと時間は、ある規制とビジネスマイルストーンに達すると、4300万ドルに達する可能性がある。付記12を参照金融商品より多くの情報を取得するために、私たちの連結財務諸表を参照してください
•新冠肺炎の大流行の影響と全世界の経済状況、一時停止の待機手術の数量と遅延、臨床試験、準備時間の延長、十分な材料供給が確保できないこと及びインフレが材料コストに与える影響を含む
•債券保有者は、債券の転換時間と程度、および私たちの定期融資の元本と利息支払い時間を選択する
Pacira BioSciences,Inc.|2022 Form 10-K|78ページ
•信用協定の条項に基づいて、私たちの定期ローンの変動金利の時間と影響を増加させる
•コストと私たちは引き続きEXPAREL、ZILRETTA、IOVERA°商業化の能力を米国以外に含めて拡大することに成功した
•カリフォルニア州サンディエゴの科学センターパークでのEXPAREL生産能力拡張プロジェクトや、イギリスのスウィンデンのThermo Fisher工場でのZILRETTA資本プロジェクトを含む、私たちの製造施設のコストと時間を拡大して維持します
•既存の協定による追加投資を含む追加戦略投資の費用およびタイミング
•法律や規制の問題に関する費用
•インフレが私たちの製品コスト、サプライチェーン、運営費用、業務戦略に与える影響
•FDAおよびEMAがEXPAREL承認条件として必要な追加の小児科試験を含む、我々の製品のための追加の臨床試験のコスト
•他の候補製品の開発と商業化コスト
•私たちの従業員福祉計画によると、将来の支払いのコストと時間は、私たちの現金長期インセンティブ計画および非合格繰延報酬計画を含むが、これらに限定されない
•私たちは製品、業務、そして技術の程度を買収または投資する。
私たちは私たちの未来の運営と資本需要を満たすために追加の債務や株式融資が必要かもしれない。私たちは約束された外部資金源を持っておらず、もしあれば、許容可能な条件で追加的な持分や債務融資を得ることができないかもしれない。特に、資本市場の混乱や負の経済状況、特に新冠肺炎の大流行を背景に、資本獲得を阻害する可能性がある。
契約義務
2022年12月31日現在、返済されていない転換可能な優先手形が2つあり、このうち2024年5月に満期になった2024年手形元金総額は860万ドル、2025年8月期の2025年手形元金総額は4.025億ドル。債券の残り利息は940万ドルで、このうち330万ドルが2023年に満期になると推定されている。返済されていない元金は2億969億ドル、2023年と2024年の契約元金はそれぞれ3750万ドル、2025年と2026年の元金はそれぞれ4220万ドルと1億797億ドルの定期融資がある。現在の金利によると、定期ローンの残り利息は約1.154億ドル。
正常な業務過程において、著者らは製造、研究開発と会社活動のために各種のレンタル協定を締結し、財務会計基準委員会会計基準に基づいてテーマ842を編集する規定に基づいて、これらの協定は通常経営性賃貸に分類される賃貸借証書それは.2022年12月31日まで、私たちの最低純約束は9380万ドルで、うち1400万ドルは2023年に満期になる。詳細は付記8を参照してください賃貸借証書私たちの連結財務諸表はここに含まれています。
また、2022年12月31日まで、私たちの代行サービスに対する最低取消不可契約は約7,330万ドルであり、そのうちの1,830万ドルは1年以内に満了し、残りの5,500万ドルは1年から3年以内に満了する。2022年12月31日現在、ある原材料に対する最低取消不能契約は約520万ドルと約束されており、そのうち270万ドルは1年以内に満期になり、残りの250万ドルは1年から2年以内に満期になる。2022年12月31日の後、私たちはまた280万ドルの最低撤回不可能なマーケティング賛助契約を締結し、そのうちの90万ドルは1年以内に満期になり、残りの190万ドルは1年から2年以内に満期になる。
Flexion買収の一部として、すべての規制とビジネスマイルストーンが満たされれば、潜在的な支払い金額は3兆723億ドルに達する。2022年9月にPCRX-301のさらなる開発を正式に停止することが決定するまで、総金額は4.255億ドルだった。詳細については、付記5を参照されたい屈曲習得私たちの連結財務諸表はここに含まれています。MyoScience買収の一部として、ある規制とビジネスマイルストーンを実現した後、2022年12月31日までに、4300万ドルに達する潜在的なマイルストーン支払いを得ることができる。MyoScience記念碑的な達成期間は2023年12月31日に終了する。
Pacira BioSciences,Inc.|2022 Form 10-K|79ページ
肝心な会計見積もり
私たちの経営陣は、私たちの財務状況と経営結果の議論と分析は、アメリカ公認会計原則に基づいて作成された財務諸表に基づいています。これらの財務諸表の作成は、財務諸表の日付に影響を与える報告された資産および負債額、または資産と負債、ならびに報告期間内に報告された収入および支出の推定を行うことを要求します。私たちは、収入確認、または有価価値、無形資産減価、在庫コスト、負債および計算項目、臨床試験費用、株式ベースの報酬および繰延税金資産推定値に関する推定および判断を含む、私たちの推定と判断を継続的に評価する。私たちの推定は歴史的経験、契約条項、そして私たちがこのような状況で適切だと思う他の要素に基づいている。異なる仮定または条件では、実際の結果は、これらの推定値とは異なる可能性がある。
私たちの重要な会計政策は付記2でより十分な議論があります重要会計政策の概要私たちの連結財務諸表はここに含まれています。我々は、総合財務諸表を作成する際に、以下の会計政策を採用しており、その中には重大な判断と推定が含まれている可能性がある。
収入確認
販売製品の収入は、返品手当、即時支払い割引、サービス料、政府リベート、数量リベート、ストレージ容量別使用料金を差し引いた純額です。これらの準備金は、関連販売によって稼いだ金額または請求された金額の推定に基づいている。これらの金額は可変対価格とみなされ,可能金額法を用いて販売時の取引価格の減少が推定され確認されたが,収益は除外され,期待値法に基づいている.会社はこれらの見積金額を取引価格に計上しており,このような取引確認の累積収入が大きく逆転しない可能性が高いこと,あるいは可変対価格に関する不確実性が解決される可能性が高いことを前提としている。その中のいくつかの項目の計算は、管理層が販売データ、履歴返品データ、契約、法定要求、その他の将来知っている可能性のある関連情報に基づいて推定する必要がある。このような規定の十分性は四半期ごとに検討される。もし私たちの評価、経験、あるいは判断が未来の結果の正確な推定でなければ、私たちの運営結果は影響を受ける可能性がある。私たちが推定した感度はプロジェクトによって異なる。記録すべき項目と最終決済との間の時間遅延により、記憶容量別の使用課金および政府計画に関する推定は、最大の調整リスクがある。歴史的には、これらの推定数を調整して実際の結果や更新の予想を反映することは重要ではない。
2022年、2022年、2021年、2020年12月31日終了年度までの販売関連手当と応募項目活動概要に付記4を参照収入.収入私たちの連結財務諸表はここに含まれています。
値段が合うかもしれない
買収後、私たちは公正価値によって各期間のあるいは価格を計量し、公正価値変動は総合経営報告書で買収に関連する費用(収益)、減値その他であることを確認した。または対価格の変化は、推定売上高の仮定実現および時間、販売商品のコスト、規制承認の変化による可能性がある。新しい情報がない場合,公平価値の変化は,時間の経過とともにマイルストーンが実現可能な影響を反映している.
次の表には、価格マイルストーンを推定する際に使用される重要な仮定が含まれています
| | | | | | | | |
| 仮に | | 使用時までの屈曲範囲
2022年12月31日 |
| 割引率 | | 14.90% to 15.10% |
| 規制のマイルストーンを実現するためにお金を支払う確率 | | 0% to 12.50% |
| 規制の節目に達する年が予想されています | | 2030 |
2022年12月31日現在、Flexion買収または対価格関連の最高潜在的支払い金額は3.723億ドル。仮定の変更は計算された金額に実質的な影響を与える可能性がある.さらに、予測された収入年間成長率は、私たちのビジネスマイルストーンに関連しているか、または価格評価における重要な仮定がある。予測された年間成長率10%増加の影響は、2022年12月31日までにFlexion買収に関連した、または対価負債の価値を580万ドル増加させると仮定している。割引率が100ベーシスポイント増加した影響は、2022年12月31日現在のFlexion買収関連や対価負債の価値を140万ドル減少させると仮定する。
Pacira BioSciences,Inc.|2022 Form 10-K|80ページ
最近の会計公告
注3を参照最近の会計公告私たちの連結財務諸表はここで最近の会計声明をさらに検討することを含む。
第七A項。市場リスクの定量的·定性的開示について
私たちの現金等価物と投資活動の主な目標は、元本を維持しながら、リスクを著しく増加させることなく、私たちが投資から得た収入を最大化することです。私たちは社債、商業手形、資産支援証券、米国国債、他の政府機関手形に投資しており、これらは公正価値で報告されている。このような証券は金利リスクと信用リスクの影響を受ける。これは現在の金利の変化が投資元金の変動を招く可能性があることを意味する。例えば、私たちが当時の金利で発行された固定金利の証券を持っていて、金利が後に上昇すれば、私たちの投資の公正価値は下がると予想されます。金利が100ベーシスポイント上昇したと仮定すると、我々が売却できる証券の2022年12月31日の公正価値は約130万ドル減少する。
私たちの2025年債券の公正価値は私たちの普通株式公正価値と金利変動の影響を受ける。2022年12月31日現在、2025年債券の公正価値は1,000ドル当たり元金908ドルと推定されている。付記11を参照債務私たちの総合財務諸表は、固定金利で利息を計上する2025年手形についてさらに議論するためにここに含まれています。2022年12月31日現在、2025年債の元本総額は4.025億ドル、2024年債の元本残高は860万ドル。Flexion買収の結果として、注釈11でより詳細に説明されているように、債務当社の総合財務諸表によると、2024年手形の任意の未来転換権は、2024年手形の契約項の下でこのような転換権を生成する任意の未来事件に制限されなければならない。
発行時、この定期ローンは元金3.75億ドルの単一前払い定期ローンを提供し、2026年12月7日に満期になる予定だ。各定期ローン借款は予備基本金利借入金であり、予備基本金利(信用プロトコルの定義参照)に相当する変動年利で利息を計算し、金利下限は1.75%プラス6.00%である。各定期ローン借款は定期基準借入金であり、(I)調整された定期SOFR金利(定義は信用プロトコル参照)プラス(Ii)7.00%の変動年利建て利息である。2022年12月31日現在、私たちは定期ローンの下で2兆969億ドルの未返済借金があります。金利が100ベーシスポイント上昇すると仮定すると、2022年12月31日までの1年間で利息支出は約360万ドル増加する。
私たちは外国の管轄区域で運営されているいくつかのサプライヤーとパートナーと合意した。大きな取引は主にドル建てで、通貨レートの変化に応じて年次調整を行う。
また、私たちの売掛金は主に4つの大型薬品卸売業者に集中しています。不履行または不払いが発生した場合、我々の財務状況、運営結果、または純キャッシュフローに実質的な悪影響を及ぼす可能性がある。
項目8.財務諸表と補足データ
本プロジェクトに要求される総合財務諸表は、独立公認会計士事務所の報告とともに、本年度報告のF−1ページから開始する。
項目9.会計·財務開示面の変更と会計士との相違
ない。
第9条。制御とプログラム
情報開示制御とプログラムの評価
我々は、取引法の下のルール13 a-15(E)および15 d-15(E)において定義されている開示制御プログラムおよびプログラムに準拠して、取引法に従って提出または提出された報告書で開示を要求する情報が、米国証券取引委員会規則および表で指定された期間内に記録、処理、集約および報告され、これらの情報が蓄積され、私たちの経営陣に伝達されることを保証し、必要な開示に関する決定をタイムリーに行うために、我々のCEO、会長、および最高財務官を含む、開示制御プログラムおよびプログラムを遵守する。
彼らの2022年12月31日までの評価によると、私たちのCEO、会長兼財務官は、私たちの開示制御と手続きは2022年12月31日から有効であると結論した。
Pacira BioSciences,Inc.|2022 Form 10-K|81ページ
財務報告の内部統制に関する経営陣の報告
我々の財務報告に対する内部統制は、財務報告の信頼性と公認会計基準に基づいて外部目的の財務諸表の作成に合理的な保証を提供することを目的とした過程である。我々の経営陣は、“取引法”ルール13 a-15(F)および15 d-15(F)に定義されている財務報告の十分な内部統制の確立と維持を担当している。私たちの経営陣は、CEO、会長、財務責任者を含む監督と参加の下で、経営陣は内部統制--統合フレームワーク(2013)テレデビル委員会(COSO)が主催して組織委員会が発表した。評価結果によると、我々の経営陣は、財務報告書に対する内部統制が2022年12月31日から有効であると結論した
2022年12月31日までの財務報告内部統制の有効性は、2022年12月31日までの財務報告内部統制の有効性について保留のない意見を発表した独立公認会計士事務所ピマウェイ会計士事務所が監査します。
財務報告の内部統制の変化
私たちの経営陣は、2022年12月31日までの四半期に、買収したFlexity業務の内部統制を既存の統制に統合します。Flexion業務を統合するために強化または実施されている制御に加えて、2022年12月31日までの四半期内に、財務報告の内部統制に大きな影響を与えたり、合理的に財務報告の内部統制に大きな影響を与える可能性のある変化はありません。
プロジェクト9 B。その他の情報
ない。
プロジェクト9 Cです。検査妨害に関する外国司法管区の開示
ない。
第三部
プロジェクト10.取締役、上級管理者、および企業管理
本プロジェクトが要求する情報は,我々の2023年度株主総会の依頼書に含まれ,引用により本報告に組み込まれる。
プロジェクト11.役員報酬
本プロジェクトが要求する情報は,我々の2023年度株主総会の依頼書に含まれ,引用により本報告に組み込まれる。
プロジェクト12.特定の実益所有者および経営陣および株主の保証所有権に関する事項
本プロジェクトが要求する情報は,我々の2023年度株主総会の依頼書に含まれ,引用により本報告に組み込まれる。
第13項:特定の関係及び関連取引、並びに取締役独立性
本プロジェクトが要求する情報は,我々の2023年度株主総会の依頼書に含まれ,引用により本報告に組み込まれる。
プロジェクト14.チーフ会計士費用とサービス
本プロジェクトが要求する情報は,我々の2023年度株主総会の依頼書に含まれ,引用により本報告に組み込まれる。
Pacira BioSciences,Inc.|2022 Form 10-K|82ページ
第4部
項目15.物証、財務諸表付表
(a)本年度報告10−Kフォームの一部として提出された書類:
一財務諸表
合併貸借対照表
連結業務報告書
総合総合収益表
株主権益合併報告書
統合現金フロー表
連結財務諸表付記
我々の独立公認会計士事務所ピマウェイ会計士事務所の上記財務諸表及び財務報告内部統制に関する報告は、本年度報告の10−K表に含まれる。彼らの同意は添付ファイル23.1本年度報告の表格10−K。
独立公認会計士事務所報告
(2)別表
必要ではない、適用されない、または情報が連結財務諸表または関連付記に含まれるので、すべての財務諸表の添付表は省略される。
(3)展示品
本年度報告はForm 10−Kの形で以下の証拠を提出または引用した。
Pacira BioSciences,Inc.|2022 Form 10-K|83ページ
展示品索引 | | | | | | | | | | | | | | | | | | | | | | | | | | |
| | | | 引用で法団として成立する |
展示品
番号をつける | | 説明する | | 表 | | 展示品 | | 日取り
保存済み |
2.1 | | 協定と合併計画は,日付は2019年3月4日であり,Pacira PharmPharmticals,Inc.,PS Merge,Inc.,MyoScience,Inc.とFortis Advisors LLCが証券保有者代表として署名された。♪゚ | | 8-K | | 2.1 | | 3/5/2019 |
2.2 | | Flexion治療会社、Pacira生物科学社、Oyster買収会社が署名した合併協定と計画は、2021年10月11日である。 | | 8-K | | 2.1 | | 10/12/2021 |
3.1 | | 会社登録証明書の改訂と再予約。 | | 8-K | | 3.1 | | 2/11/2011 |
3.2 | | 2019年4月9日に改正された“会社登録証明書改正案”。 | | 8-K | | 3.1 | | 4/9/2019 |
3.3 | | 二番目に、添付例を修正して再設定する。 | | 8-K | | 3.2 | | 4/9/2019 |
4.1 | | 普通株式株式を証明する証明書サンプル。 | | 10-Q | | 4.1 | | 5/2/2019 |
4.2 | | 債券(2025年満期の0.750%転換優先手形を含む)は、日付が2020年7月10日であり、登録者と受託者である全国協会(旧富国銀行、全国協会)のコンピュータ株式会社信託との契約である。 | | 8-K | | 4.1 | | 7/10/2020 |
4.3 | | 契約(2024年満期の3.375%が優先手形に変換可能な形式を含む)は,日付は2017年5月2日であり,Flexion Treeutics,Inc.と受託者であるComputerShare Corporation Trust,National Association(前身はWells Fargo Bank,National Association)である | | 10-K | | 4.4 | | 2/28/2022 |
4.4 | | First Supplemental Indentureは,2021年11月19日にFlexion Treeutics,Inc.と受託者であるComputerShare Corporation Trust,National Association(前Wells Fargo Bank,National Association)によって署名された。 | | 10-K | | 4.5 | | 2/28/2022 |
4.6 | | 証券説明。 | | 10-K | | 4.3 | | 2/21/2020 |
10.1 | | 2011年の株式インセンティブ計画を改訂し、再策定しました* | | 8-K | | 10.1 | | 6/11/2021 |
10.2 | | 法定株式オプション協定形式ではなく、2022年2月1日までに付与された改正·再改訂された2011年株式インセンティブ計画に適用される。* | | 8-K | | 10.3 | | 6/4/2014 |
10.3 | | 改正·再改訂された2011年株式インセンティブ計画によると、2022年2月1日以降に付与される非法定株式オプション協定(従業員)のフォーマット | | 10-K | | 10.3 | | 2/28/2022 |
10.4 | | 改正·再改訂された2011年株式インセンティブ計画によると、2022年2月1日以降に付与される非法定株式オプション協定(非従業員取締役)のフォーマット。* | | 10-K | | 10.4 | | 2/28/2022 |
10.3 | | 改訂·改訂された2011年株式インセンティブ計画下の制限株式単位奨励協定(従業員)のフォーマット。* | | 10-Q | | 10.6 | | 7/30/2015 |
10.4 | | 改正·再編成された2011年株式インセンティブ計画下の制限株式単位奨励協定(非従業員取締役)のフォーマット。* | | 10-Q | | 10.7 | | 7/30/2015 |
10.5 | | 2014年インセンティブ計画。* | | 10-Q | | 10.1 | | 5/1/2014 |
10.6 | | 2014年の従業員の株式購入計画を改訂し、再策定しました* | | 8-K | | 10.1 | | 6/10/2022 |
10.7 | | 登録者と研究開発基金との間の譲渡協定は,日付は1994年2月9日,2004年4月15日に改訂された。 | | S-1/A | | 10.4 | | 12/3/2010 |
10.8 | | 2007年1月8日、SkyePharma,Inc.と登録者との間の株式購入協定。 | | S-1/A | | 10.5 | | 12/3/2010 |
10.9 | | 登録者とDavid書局の間の雇用協定* | | S-1/A | | 10.21 | | 12/3/2010 |
10.10 | | 2013年3月13日登録者とDavid書局との間の幹部採用協定の改正案第1号。* | | 8-K | | 99.3 | | 3/18/2013 |
10.11 | | 登録者とDavid協定が2015年6月30日に署名した役員採用協定第2号改正案。* | | 10-Q | | 10.2 | | 7/30/2015 |
10.12 | | 登録者とクリスチャン·ウィリアムズが2012年11月29日に締結した雇用契約。* | | 10-Q | | 10.2 | | 4/30/2015 |
10.13 | | 2013年3月13日登録者とクリスチャン·ウィリアムズとの間の雇用協定の改正案第1号 | | 10-Q | | 10.3 | | 4/30/2015 |
Pacira BioSciences,Inc.|2022 Form 10-K|84ページ
| | | | | | | | | | | | | | | | | | | | | | | | | | |
| | | | 引用で法団として成立する |
展示品
番号をつける | | 説明する | | 表 | | 展示品 | | 日取り
保存済み |
10.14 | | 登録者とクリスチャン·ウィリアムズが2015年6月30日に署名した雇用協定第2号改正案。* | | 10-Q | | 10.5 | | 7/30/2015 |
10.15 | | 登録者とチャールズ·A·ラインハルトとの幹部採用協定は、2016年5月2日であった。* | | 10-Q | | 10.1 | | 8/4/2016 |
10.16 | | 登録者とMax Reinhardtが2019年6月19日に締結した役員採用契約。* | | 10-Q | | 10.1 | | 5/7/2020 |
10.17 | | 登録者とロイ·ウィンストンが2017年4月24日に締結した役員採用協定。* | | 10-Q | | 10.2 | | 5/7/2020 |
10.18 | | 登録者とその役員と上級管理職との間の賠償協定フォーマット。* | | S-1/A | | 10.32 | | 1/13/2011 |
10.19 | | 登録者と統合商業化ソリューション会社が2011年8月25日に締結した商業アウトソーシングサービス協定 | | 10-Q | | 10.1 | | 8/25/2011 |
10.20 | | 登録者と統合商業化ソリューション会社が2013年8月1日に署名した“商業アウトソーシングサービス協定第1改正案” | | 10-Q | | 10.1 | | 10/31/2013 |
10.21 | | 登録者と統合商業化ソリューション会社が2014年8月25日に署名した“商業アウトソーシングサービス協定第2修正案” | | 10-Q | | 10.1 | | 10/30/2014 |
10.22 | | 登録者と統合商業化ソリューション会社が2015年4月29日に署名した“商業アウトソーシングサービス協定第3改正案” | | 10-Q | | 10.1 | | 7/30/2015 |
10.23 | | 登録者と統合商業化ソリューション会社との間の商業アウトソーシングサービス協定の第四乃至第十一項改正案 | | 10-Q | | 10.3 | | 5/7/2020 |
10.24 | | Pacira BioSciences,Inc.繰延給与計画。* | | 8-K | | 10.1 | | 6/11/2020 |
10.25 | | Pacira BioSciences,Inc.繰延補償計画修正案第1号* | | | | | | |
10.26 | | Pacira BioSciences,Inc.長期インセンティブ計画。* | | 8-K | | 10.1 | | 12/7/2020 |
10.27 | | 2014年4月4日、登録者とPatheon UK Limitedとの間で署名された戦略共同制作協定 | | 10-Q | | 10.1 | | 7/31/2014 |
10.28 | | 登録者とPatheon UK Limitedとの間で2014年4月4日に締結された製造及び供給協定 | | 10-Q | | 10.2 | | 7/31/2014 |
10.29 | | 登録者とPatheon UK Limitedとの間で2014年4月4日に締結された技術移転及びサービス協定 | | 10-Q | | 10.3 | | 7/31/2014 |
10.30 | | 登録者とゲイリー·ペスが2012年4月3日に署名した改正および再署名の諮問協定。* | | 10-Q | | 10.1 | | 5/9/2012 |
10.31 | | 登録者とゲイリー·ペスが2012年8月17日に締結した第2次改正および再署名の諮問協定。* | | 10-Q | | 10.1 | | 11/1/2012 |
10.32 | | 登録者とゲイリー·ペスが2013年9月11日に署名した“諮問協定第3修正案”。* | | 10-Q | | 10.3 | | 10/31/2013 |
10.33 | | 登録者とゲイリー·ペスが2015年11月25日に署名した“諮問協定第4修正案”。* | | 10-K | | 10.57 | | 2/25/2016 |
10.34 | | 登録者とデニス·マクロフリンが2017年5月29日に署名した役員採用協定。* | | 10-Q | | 10.1 | | 5/2/2019 |
10.35 | | または2021年11月19日にPacira BioSciences,Inc.および米国株譲渡によって信託会社LLCによって署名される価値のある権利協定。 | | 8-K | | 10.1 | | 11/19/2021 |
10.36 | | クレジット協定は,2021年12月7日にPacira BioSciences,Inc.,時々の貸手,行政代理人であるノースカロライナ州モルガン大通銀行によって署名された | | 8-K | | 10.1 | | 12/9/2021 |
10.37 | | 2015年7月31日、Flexion治療会社とPatheon UK株式会社との間の製造·供給協定は、これまで改訂されてきた | | 10-K | | 10.36 | | 2/28/22 |
10.38 | | 2015年7月31日、Flexion治療会社とPatheon UK株式会社との間の技術移転とサービス協定は、これまで改訂されてきた | | 10-K | | 10.37 | | 2/28/22 |
Pacira BioSciences,Inc.|2022 Form 10-K|85ページ
| | | | | | | | | | | | | | | | | | | | | | | | | | |
| | | | 引用で法団として成立する |
展示品
番号をつける | | 説明する | | 表 | | 展示品 | | 日取り
保存済み |
10.39 | | Flexion治療会社とPatheon UK株式会社との間の製造·供給協定の付状は、日付が2020年4月8日である | | 10-K | | 10.38 | | 2/28/22 |
10.40 | | 登録者とジョナサン·スロネンが2020年5月4日に締結した役員採用協定。* | | 10-Q | | 10.1 | | 5/4/2022 |
21.1 | | 登録者の付属会社。* | | | | | | |
23.1 | | ピマウェイ有限責任会社は同意した。* | | | | | | |
31.1 | | 取引所法令第13 a-14条に基づいて行政総裁及び議長を証明する。* | | | | | | |
31.2 | | 取引所法令第13 a-14(A)条による首席財務官の証明。* | | | | | | |
32.1 | | 米国法第18編第1350条の規定に基づき、2002年の“サバンズ·オックススリー法案”第906条の規定により、最高経営責任者、会長、財務責任者を認証する。** | | | | | | |
| | | | | | | | |
| 101.INS* | | XBRLインスタンスドキュメントを連結します。* | | | | | | |
| 101.SCH* | | XBRL分類アーキテクチャドキュメントを内部接続します。* | | | | | | |
| 101.CAL* | | インラインXBRL分類はリンクベース文書を計算します* | | | | | | |
| 101.LAB* | | XBRL分類ラベルLinkbaseドキュメントを連結します。* | | | | | | |
| 101.PRE* | | インラインXBRL分類はLinkbaseドキュメントを実演します。* | | | | | | |
| 101.DEF* | | XBRLソート拡張を連結してLinkbaseドキュメントを定義します* | | | | | | |
| 104* | | 表紙対話データファイル(添付ファイル101に含まれるイントラネットXBRLのフォーマット)。 | | | | | | |
*アーカイブをお送りします。
**関数で提供されます。
*管理契約または補償計画またはスケジュールを示します。
エンタルピーは、一部の部分の機密処理を要求または承認し、これらの部分は省略され、秘密処理要求に基づいて米国証券取引委員会に個別に提出される。
S-K規則第601(B)(10)条によれば、展示品の一部は省略されている。漏れた資料(I)は大きな意味を持たないことや,(Ii)公開開示すれば当社に競争被害を与える可能性がある。
#改正された1934年証券取引法S-K条例第601(B)(2)項によると、いくつかの付表は省略されている。会社は要求があれば、米国証券取引委員会に任意の漏れたスケジュールのコピーを提供することを約束した。
##S-Kルール601(A)(5)項に従って、表および証拠品が省略されています。会社は証券取引委員会に任意の漏れたスケジュールと証拠品のコピーを追加提供することを要求しなければならないと約束した。
項目16.表格10-Kの概要
ない。
Pacira BioSciences,Inc.|2022 Form 10-K|86ページ
| | |
サイン |
|
1934年“証券取引法”第13又は15(D)節の要求に基づいて、登録者は、次の署名者が代表して本報告書に署名することを正式に許可した。 |
| | | | | | | | | | | | | | |
| | | | Pacira生物科学社は
/s/Davidスタック |
| 日付: | 2023年2月28日 | 差出人: | | デヴィッドスタック CEO兼会長 |
| | |
本報告は、1934年の証券取引法の要求に基づき、以下の者によって登録者として指定日に署名された。 |
| | | | | | | | | | | | | | |
| サイン | | タイトル | | 日取り |
| | | | |
| /s/Davidスタック | | 取締役、CEO兼会長
(首席行政主任) | | 2023年2月28日 |
| デヴィッドスタック | | | | |
| | | | |
| チャールズ·A·ラインハルト,III | | 首席財務官
(首席財務官) | | 2023年2月28日 |
| チャールズ·A·ラインハルト,III | | | | |
| | | | |
| /s/Lauren Riker | | 上級副社長、金融学
(首席会計主任) | | 2023年2月28日 |
| ローレン·レイク | | | | |
| | | | |
| /s/Laura BREGE | | 役員.取締役 | | 2023年2月28日 |
| ララ·ブレガー | | | | |
| | | | |
| クリストファー·J·クリスティ | | 役員.取締役 | | 2023年2月28日 |
| クリストファー·J·クリスティ | | | | |
| | | | |
| /s/Mark Froimson | | 役員.取締役 | | 2023年2月28日 |
| マーク·フロイムソン | | | | |
| | | | |
| /s/イフォン·グリンストリット | | 役員.取締役 | | 2023年2月28日 |
| エフォン·グリンストリット | | | | |
| | | | |
| /s/Mark KRONENFELD | | 役員.取締役 | | 2023年2月28日 |
| マーク·クロナンフィールド | | | | |
| | | | |
| /秒/ゲイリー·ペス | | 役員.取締役 | | 2023年2月28日 |
| ゲイリー·ペス | | | | |
| | | | |
| /s/Andreas Wicki | | 役員.取締役 | | 2023年2月28日 |
| アンドレアス·ウィキ | | | | |
| | | | |
| ポール·ヘイスティングス | | 役員をリードする | | 2023年2月28日 |
| ポール·ヘイスティングス | | | | |
Pacira BioSciences,Inc.|2022 Form 10-K|87ページ
Pacira生物科学社は
表格10-Kの年報
2022年12月31日までの年度
連結財務諸表索引 | | | | | | | | | | | | | | |
| | | | ページ番号 |
独立公認会計士事務所報告 | F-2 |
| 監査役の名前: | ピマウェイ会計士事務所 | | |
| 監査役位置: | ニュージャージー州ショットヒルズ | | |
| 監査役事務所ID: | 185 | | |
2022年と2021年12月31日までの連結貸借対照表 | F-4 |
2022年·2021年·2020年12月31日までの総合業務報告書 | F-5 |
2022年,2021年,2020年12月31日までの総合総合収益表 | F-6 |
2022年まで、2021年、2020年12月31日まで年度株主権益総合レポート | F-7 |
2022年、2021年、2020年12月31日までの統合現金フロー表 | F-8 |
連結財務諸表付記 | F-10 |
Pacira BioSciences,Inc.|2022 Form 10-K|第F-1ページ
独立公認会計士事務所報告
株主や取締役会に
Pacira生物科学社:
連結財務諸表と財務報告の内部統制に関する意見
Pacira BioSciences,Inc.とその子会社(当社)の2022年12月31日までと2021年12月31日までの連結貸借対照表,2022年12月31日までの3年間の各年度の関連総合経営表,全面収益,株主権益とキャッシュフロー,および関連付記(総称して総合財務諸表と呼ぶ)を監査した。私たちはまた、会社が2022年12月31日までの財務報告の内部統制、根拠を監査しました内部統制--統合フレームワーク(2013)テレデビル委員会が主催して委員会が発表された。
上記の総合財務諸表は、すべての重要な点において、会社の2022年12月31日と2021年12月31日までの財務状況、および2022年12月31日までの3年間の毎年の経営結果と現金流量を公平に反映しており、米国公認会計原則に適合していると考えられる。また、2022年12月31日現在、当社はすべての重要な面で財務報告に対する有効な内部統制を維持しており、その根拠は内部統制--統合フレームワーク(2013)トレデビル委員会は組織委員会を後援して配布している
意見の基礎
当社の経営陣は、これらの総合財務諸表の作成、財務報告の有効な内部統制の維持、財務報告の内部統制の有効性の評価を担当しており、添付の管理層財務報告内部統制報告に含まれている。私たちの責任は、会社の連結財務諸表について意見を発表し、私たちの監査に基づいて会社の財務報告内部統制に意見を発表することです。私たちは米国上場企業会計監督委員会(PCAOB)に登録されている公共会計士事務所であり、米国連邦証券法および米国証券取引委員会とPCAOBの適用規則と法規に基づいて、会社と独立しなければならない。
私たちはPCAOBの基準に従って監査を行っている。これらの基準は、連結財務諸表に重大なミスがないかどうか、エラーによるものであっても詐欺であっても、すべての重大な点で財務報告に対する有効な内部統制が維持されているかどうかを決定するために、合理的な保証を得るために監査を計画し、実行することを要求する。
我々の連結財務諸表の監査には、連結財務諸表の重大な誤報リスクを評価するプログラム、エラーによるものであっても詐欺であっても、これらのリスクに対応するプログラムを実行することが含まれる。これらの手続きは、連結財務諸表中の金額および開示に関する証拠をテストに基づいて検討することを含む。我々の監査には、経営陣が使用する会計原則の評価と重大な見積もり、合併財務諸表の全体列報の評価も含まれています。我々の財務報告の内部統制の監査には、財務報告の内部統制を理解すること、重大な弱点があるリスクを評価すること、評価されたリスクテストに基づいて内部統制の設計と運営有効性を評価することが含まれる。私たちの監査はまた、私たちがこのような状況で必要だと思う他の手続きを実行することを含む。私たちは私たちの監査が私たちの意見に合理的な基礎を提供すると信じている。
財務報告の内部統制の定義と限界
会社の財務報告に対する内部統制は、公認された会計原則に基づいて、財務報告の信頼性と外部目的の財務諸表の作成に合理的な保証を提供することを目的としたプログラムである。会社の財務報告に対する内部統制には、(1)合理的で詳細かつ正確かつ公平に会社の資産を反映した取引および処分に関する記録の保存、(2)公認された会計原則に従って財務諸表を作成するために必要な取引が記録されている合理的な保証を提供し、会社の収入および支出は会社の経営陣と取締役の許可のみに基づいて行われる。(三)財務諸表に重大な影響を及ぼす可能性のある不正買収、使用、または処分会社の資産を防止またはタイムリーに発見する合理的な保証を提供する。
Pacira BioSciences,Inc.|2022 Form 10-K|第F-2ページ
その固有の限界のため、財務報告書の内部統制は誤った陳述を防止したり発見できない可能性がある。また,将来的にどのような有効性評価を行うかの予測は,条件の変化により制御不足のリスクが生じる可能性があり,あるいは政策やプログラムの遵守度が悪化する可能性がある.
重要な監査事項
以下に述べる重要な監査事項は、監査委員会が監査委員会に伝達または要求する当期総合財務諸表監査によって生じる事項を指すことである:(1)総合財務諸表に対して大きな意味を有する勘定または開示に関するものであり、(2)私たちが特に挑戦的で主観的または複雑な判断に関するものである。重要な監査事項の伝達は、総合財務諸表に対する私たちの全体的な意見をいかなる方法でも変えることはなく、以下の重要な監査事項を伝達することによって、重要な監査事項またはそれに関連する勘定または開示について個別の意見を提供することもない。
開発中の無形減価準備の評価
総合財務諸表付記5及び付記9に記載されているように、当社は年ごとに無期限無形資産減価テストを行い、任意の事件又は状況変化が当該無期限無形資産の公正価値がその額面よりも低いことを示したときに行われる。公正価値は割引キャッシュフローモデルを用いて推定した。同社は2022年に2610万ドルの減価費用を記録しており,ZILRETTAの進行中の研究開発(IPR&D)に関係している。
私たちは知的財産権研究開発無形資産減価費用の評価を重要な監査事項として決定した。公正価値を推定するためのある仮定を評価する際に主観性が高いため、この無形資産を評価する公正価値計量は複雑であり、監査師の重大な判断が必要である。特に,公正価値計測は,経営層の収入予測や割引率仮定に非常に敏感である。これらの仮定の変化はこの無形資産の公正価値に大きな影響を及ぼすかもしれない。また,評価会社の割引率に関する監査は,専門技能や知識を持つ評価専門家を用いることに関連している。
以下は私たちがこの重要な監査問題を解決するために実行した主な手続きだ。著者らは設計を評価し、会社がその知的財産権研究開発無形資産の公正価値を決定するためのプロセスに関するいくつかの内部制御の運営有効性をテストした。これには,予測収入と割引率の仮定の作成に関する制御が含まれている.我々は、予測収入の将来の収入増加率を決定するための会社を評価し、それらを相関および信頼性が評価された業界データと比較する方法である。公開されている市場データの投入を利用して,割引率の独立した見積りの作成に協力し,結果を会社の割引率仮説と比較する専門技能と知識を持つ推定専門家を招待した.
Flexityの獲得に関連するまたは対価格負債の公正価値計量
総合財務諸表付記5および12に記載されているように、会社は、買収日にその推定公正価値に従って、Flexion治療会社(Flexion)の買収に関連するまたは対価負債があることを確認した。または、価格負債公正価値の後続の変動が変動期間の総合業務表に記録されている。同社は観察不可能な投入とモンテカルロシミュレーションに基づく確率重み付き現金フロー法を用いて公正価値を推定している。2022年12月31日現在、柔軟または価格の公正価値は2,810万ドルである。
Flexionの買収に関連する商業および規制マイルストーンに関連する、または対価格負債の公正な価値計量の評価が重要な監査事項であることを確認します。評価または対価格負債の公正な価値計量には監査人の重大な判断が必要であり、モデルで使用されているいくつかの仮定は観察できない投入を持ち、高度な主観性を持っているからである。特に、公正価値計量は管理層の収入、推定確率とある商業と監督管理マイルストーン、波動性と割引率の実現に関する時間の予測に非常に敏感である。また,会社の変動率や割引率の評価に関する監査は,専門技能や知識を持つ評価専門家を用いることに関連している。
以下は私たちがこの重要な監査問題を解決するために実行した主な手続きだ。著者らは商業と規制マイルストーンの実現に関連する、あるいは対価格負債がある会社の公正価値計量プロセスに関するいくつかの内部制御の設計を評価し、その運営効果をテストした。これが
Pacira BioSciences,Inc.|2022 Form 10-K|第F-3ページ
何らかのマイルストーン,波動性,割引率の実現に関する予測収入,推定確率,タイミングの仮定の作成に関する制御が含まれている.著者らは会社モデルで使用されている予測収入といくつかの商業と監督管理マイルストーンの仮定を評価し、それらを相関と信頼性が評価された履歴データ、業界基準と他の第三者市場データと比較することである。我々は,公開市場データの情報を利用して割引率と変動率仮説の独立した見積りの作成に協力し,結果を会社の割引率と変動率仮説と比較する専門技能と知識を持つ推定専門家を招聘した.
| | | | | | | | |
| /s/ピマウェイ法律事務所 | | |
| | |
| 2015年以来、当社の監査役を務めてきました。 | |
| | |
| ショットヒルズニュージャージー州 | |
| 2023年2月28日 | | |
Pacira BioSciences,Inc.|2022 Form 10-K|第F-4ページ
Pacira生物科学社は
合併貸借対照表
(単位は千で、1株当たりおよび1株当たりの金額は含まれていない) | | | | | | | | | | | |
| | 十二月三十一日 |
| 2022 | | 2021 |
| 資産 | | | |
| 流動資産: | | | |
| 現金と現金等価物 | $ | 104,139 | | | $ | 585,578 | |
| 短期的には投資を売ることができる | 184,512 | | | 70,831 | |
| 売掛金純額 | 98,397 | | | 96,318 | |
| 在庫、純額 | 96,063 | | | 98,550 | |
| 前払い費用と他の流動資産 | 15,223 | | | 14,771 | |
| 流動資産総額 | 498,334 | | | 866,048 | |
| 非常時には投資を売ることができる | 37,209 | | | — | |
| 固定資産、純額 | 183,512 | | | 188,401 | |
| 使用権資産、純額 | 70,877 | | | 76,410 | |
| 商誉 | 163,243 | | | 145,175 | |
| 無形資産、純額 | 540,546 | | | 623,968 | |
| 繰延税金資産 | 160,309 | | | 153,364 | |
| 投資やその他の資産 | 27,170 | | | 21,987 | |
| | | |
| 総資産 | $ | 1,681,200 | | | $ | 2,075,353 | |
| | | |
| 負債と株主権益 | | | |
| 流動負債: | | | |
| 売掛金 | $ | 15,220 | | | $ | 10,543 | |
| 費用を計算する | 89,785 | | | 127,555 | |
| 賃貸負債 | 9,121 | | | 7,891 | |
| 転換可能優先手形、純額 | — | | | 350,466 | |
| | | |
| 長期債務の当期分,純額 | 33,648 | | | 24,234 | |
| | | |
| | | |
| 所得税に対処する | — | | | 429 | |
| 流動負債総額 | 147,774 | | | 521,118 | |
| 転換可能優先手形、純額 | 404,767 | | | 339,267 | |
| 長期債務、純額 | 251,056 | | | 335,263 | |
| 賃貸負債 | 64,802 | | | 71,727 | |
| | | |
| 値段が合うかもしれない | 28,122 | | | 57,598 | |
| その他負債 | 9,669 | | | 19,972 | |
| 総負債 | 906,190 | | | 1,344,945 | |
引受金及び又は有事項(付記20) | | | |
| 株主権益: | | | |
優先株、額面$0.001; 5,000,000ライセンス株;ありません2022年12月31日及び2021年12月31日に発行及び未返済 | — | | | — | |
普通株、額面$0.001; 250,000,000ライセンス株;45,927,790そして44,734,308それぞれ2022年12月31日及び2021年12月31日に発行及び発行された株式 | 46 | | | 45 | |
| 追加実収資本 | 924,095 | | | 942,091 | |
| 赤字を累計する | (148,751) | | | (211,895) | |
| その他の総合収入を累計する | (380) | | | 167 | |
| 株主権益総額 | 775,010 | | | 730,408 | |
| 総負債と株主権益 | $ | 1,681,200 | | | $ | 2,075,353 | |
連結財務諸表の付記を参照。
Pacira BioSciences,Inc.|2022 Form 10-K|第F-5ページ
Pacira生物科学社は
連結業務報告書
(千単位で、1株当たりを除く) | | | | | | | | | | | | | | | | | |
| | 十二月三十一日までの年度 |
| | 2022 | | 2021 | | 2020 |
| 収入: | | | | | |
| 製品純売上高 | $ | 664,150 | | | $ | 538,966 | | | $ | 426,614 | |
| 特許権使用料収入 | 2,673 | | | 2,442 | | | 3,033 | |
| 協力許可と記念碑的な収入 | — | | | 125 | | | — | |
| 総収入 | 666,823 | | | 541,533 | | | 429,647 | |
| 運営費用: | | | | | |
| 販売原価 | 199,295 | | | 140,255 | | | 117,328 | |
| 研究開発 | 84,797 | | | 55,545 | | | 59,421 | |
| 販売、一般、行政 | 254,516 | | | 199,345 | | | 193,516 | |
| 無形資産の償却を取得した | 57,288 | | | 13,553 | | | 7,866 | |
| 買収に関連する費用(収益)、減価その他 | 10,903 | | | 42,911 | | | 5,166 | |
| 総運営費 | 606,799 | | | 451,609 | | | 383,297 | |
| 営業収入 | 60,024 | | | 89,924 | | | 46,350 | |
| その他(費用)収入: | | | | | |
| 利子収入 | 4,542 | | | 896 | | | 4,629 | |
| 利子支出 | (39,976) | | | (31,750) | | | (25,671) | |
| 債務損失を繰り上げ返済する | — | | | — | | | (8,071) | |
| その他、純額 | (11,288) | | | (2,666) | | | 2,852 | |
| その他の費用の合計 | (46,722) | | | (33,520) | | | (26,261) | |
| 所得税前収入 | 13,302 | | | 56,404 | | | 20,089 | |
| 所得税の割引 | 2,607 | | | (14,424) | | | 125,434 | |
| 純収入 | $ | 15,909 | | | $ | 41,980 | | | $ | 145,523 | |
| | | | | |
| 1株当たり純収益: | | | | | |
| 普通株1株当たりの基本純収入 | $ | 0.35 | | | $ | 0.95 | | | $ | 3.41 | |
| 希釈して普通株当たり純収益 | $ | 0.34 | | | $ | 0.92 | | | $ | 3.33 | |
| 加重平均発行された普通株式: | | | | | |
| 基本的な情報 | 45,521 | | | 44,262 | | | 42,671 | |
| 薄めにする | 46,538 | | | 45,630 | | | 43,682 | |
連結財務諸表の付記を参照。
Pacira BioSciences,Inc.|2022 Form 10-K|第F-6ページ
Pacira生物科学社は
総合総合収益表
(単位:千) | | | | | | | | | | | | | | | | | |
| | 十二月三十一日までの年度 |
| | 2022 | | 2021 | | 2020 |
| 純収入 | $ | 15,909 | | | $ | 41,980 | | | $ | 145,523 | |
| その他総合(赤字)収入: | | | | | |
| 投資は赤字純額,税引き後純額を実現していない | (662) | | | (180) | | | (3) | |
| 外貨換算調整 | 115 | | | 29 | | | (1) | |
| その他総合損失合計 | (547) | | | (151) | | | (4) | |
| 総合収益 | $ | 15,362 | | | $ | 41,829 | | | $ | 145,519 | |
連結財務諸表の付記を参照
Pacira BioSciences,Inc.|2022 Form 10-K|第F-7ページ
Pacira生物科学社は
合併株主権益報告書
2022年まで、2021年および2020年12月31日まで年度
(単位:千) | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | |
| | 普通株 | | その他の内容
支払い済み
資本 | | 積算
赤字.赤字 | | 積算
他にも
全面的に
収入(損) | | 合計する |
| | 株 | | 金額 | | | | |
| 2019年12月31日の残高 | 41,908 | | | $ | 42 | | | $ | 753,978 | | | $ | (399,398) | | | $ | 322 | | | $ | 354,944 | |
| 株式オプションの行使 | 1,428 | | | 2 | | | 45,227 | | | — | | | — | | | 45,229 | |
| 既得制限株式単位 | 239 | | | — | | | — | | | — | | | — | | | — | |
| 従業員の株式購入計画に基づいて発行された普通株 | 62 | | | — | | | 2,546 | | | — | | | — | | | 2,546 | |
| 株に基づく報酬 | — | | | — | | | 39,920 | | | — | | | — | | | 39,920 | |
| 2022年に転換可能な優先チケットの権益部分無効(付記11) | — | | | — | | | (33,089) | | | — | | | — | | | (33,089) | |
2025年に発行された転換可能優先手形の権益部分は、繰延税の純額#ドルを差し引く20,450(注11) | — | | | — | | | 64,619 | | | — | | | — | | | 64,619 | |
| その他全面赤字(付記13) | — | | | — | | | — | | | — | | | (4) | | | (4) | |
| 純収入 | — | | | — | | | — | | | 145,523 | | | — | | | 145,523 | |
| 2020年12月31日残高 | 43,637 | | | 44 | | | 873,201 | | | (253,875) | | | 318 | | | 619,688 | |
| 株式オプションの行使 | 732 | | | 1 | | | 23,833 | | | — | | | — | | | 23,834 | |
| 既得制限株式単位 | 310 | | | — | | | — | | | — | | | — | | | — | |
| 従業員の株式購入計画に基づいて発行された普通株 | 55 | | | — | | | 2,811 | | | — | | | — | | | 2,811 | |
| 株に基づく報酬 | — | | | — | | | 42,246 | | | — | | | — | | | 42,246 | |
| その他全面赤字(付記13) | — | | | — | | | — | | | — | | | (151) | | | (151) | |
| 純収入 | — | | | — | | | — | | | 41,980 | | | — | | | 41,980 | |
| 2021年12月31日の残高 | 44,734 | | | 45 | | | 942,091 | | | (211,895) | | | 167 | | | 730,408 | |
| 2020-06会計基準更新後に転換可能な優先手形の資本部分を負債に再分類(付記3) | — | | | — | | | (96,468) | | | 47,235 | | | — | | | (49,233) | |
| 株式オプションの行使 | 690 | | | 1 | | | 24,386 | | | — | | | — | | | 24,387 | |
| 既得制限株式単位 | 331 | | | — | | | — | | | — | | | — | | | — | |
| 従業員の株式購入計画に基づいて発行された普通株 | 71 | | | — | | | 2,954 | | | — | | | — | | | 2,954 | |
| 株に基づく報酬 | — | | | — | | | 48,092 | | | — | | | — | | | 48,092 | |
| 2022年転換優先手形変換後普通株式発行(付記11) | 102 | | | — | | | 3,040 | | | — | | | — | | | 3,040 | |
| その他全面赤字(付記13) | — | | | — | | | — | | | — | | | (547) | | | (547) | |
| 純収入 | — | | | — | | | — | | | 15,909 | | | — | | | 15,909 | |
| 2022年12月31日の残高 | 45,928 | | | $ | 46 | | | $ | 924,095 | | | $ | (148,751) | | | $ | (380) | | | $ | 775,010 | |
連結財務諸表の付記を参照。
Pacira BioSciences,Inc.|2022 Form 10-K|第F-8ページ
Pacira生物科学社は
統合現金フロー表
(単位:千) | | | | | | | | | | | | | | | | | |
| | 十二月三十一日までの年度 |
| | 2022 | | 2021 | | 2020 |
| 経営活動: | | | | | |
| 純収入 | $ | 15,909 | | | $ | 41,980 | | | $ | 145,523 | |
| 純収入と経営活動が提供する現金純額を調整する: | | | | | |
| 税金を繰延する | (7,945) | | | 10,872 | | | (126,613) | |
| 固定資産減価償却と無形資産償却 | 91,501 | | | 28,548 | | | 19,908 | |
| 債務発行原価償却 | 4,400 | | | 2,754 | | | 2,156 | |
| 債務割引償却 | 2,807 | | | 23,152 | | | 18,254 | |
| 固定資産処分損益 | 193 | | | (10) | | | 22 | |
| 債務損失を繰り上げ返済する | — | | | — | | | 8,071 | |
| 株に基づく報酬 | 48,092 | | | 42,246 | | | 39,920 | |
| 価格の変動があります | (29,476) | | | (989) | | | 5,204 | |
| 当座無期限無形資産減価 | 26,134 | | | — | | | — | |
| 投資減価準備 | 10,000 | | | — | | | — | |
| 投資とその他の営業外収益損失(収益)純額 | 92 | | | 2,673 | | | (1,618) | |
| 経営性資産と負債変動状況: | | | | | |
| 売掛金純額 | (2,079) | | | (10,434) | | | (5,516) | |
| 在庫、純額 | 2,486 | | | (4,467) | | | (6,353) | |
| 前払い費用と他の資産 | (2,699) | | | 1,142 | | | (739) | |
| 売掛金 | 6,272 | | | (10,262) | | | (3,312) | |
| 課税費用と所得税の支払 | (19,857) | | | 5,451 | | | (5,999) | |
| その他負債 | (556) | | | (104) | | | (2,467) | |
| 支払うか掛け値がある | — | | | (6,835) | | | (9,409) | |
| | | | | |
| 経営活動が提供する現金純額 | 145,274 | | | 125,717 | | | 77,032 | |
| 投資活動: | | | | | |
| Flexion Treateutics,Inc.(買収した現金を差し引く) | — | | | (420,042) | | | — | |
| 固定資産購入状況 | (30,076) | | | (45,866) | | | (37,801) | |
| | | | | |
| 売却可能な投資を購入する | (387,685) | | | (611,488) | | | (546,516) | |
| 投資を売ることができる販売 | 237,576 | | | 1,068,736 | | | 307,870 | |
| 支払うか掛け値がある | (32,000) | | | (4,000) | | | — | |
| 株式売却投資 | — | | | 9,057 | | | — | |
| 株式購入と債務投資 | (13,000) | | | (17,187) | | | (1,160) | |
| 投資活動のための現金純額 | (225,185) | | | (20,790) | | | (277,607) | |
| 融資活動: | | | | | |
| 株式オプションを行使して得られる収益 | 24,387 | | | 23,844 | | | 45,218 | |
| 従業員の株式購入計画に基づいて普通株の収益を発行する | 2,954 | | | 2,811 | | | 2,546 | |
| 2026年12月期の定期融資B融資の収益 | — | | | 363,750 | | | — | |
| 2025年の転換優先手形の債務分 | — | | | — | | | 314,708 | |
| 2025年に転換可能な優先手形の配当金の一部 | — | | | — | | | 87,792 | |
| 2022年の転換可能優先手形の償還 | (156,960) | | | — | | | (176,793) | |
| 2022年に転換可能な優先手形の株式部分の廃棄 | — | | | — | | | (33,089) | |
| 返済2024年転換優先手形 | (192,609) | | | — | | | — | |
| 2026年12月満期の定期ローンBローンを返済する | (78,125) | | | — | | | — | |
| 債務発行と融資コストの支払い | (1,175) | | | (4,546) | | | (12,487) | |
| 支払うか掛け値がある | — | | | (5,165) | | | (5,591) | |
| | | | | |
| 融資活動が提供した現金純額 | (401,528) | | | 380,694 | | | 222,304 | |
| 現金および現金等価物の純増加 | (481,439) | | | 485,621 | | | 21,729 | |
| 現金と現金等価物、年明け | 585,578 | | | 99,957 | | | 78,228 | |
| 現金と現金等価物、年末 | $ | 104,139 | | | $ | 585,578 | | | $ | 99,957 | |
連結財務諸表の付記を参照。 |
Pacira BioSciences,Inc.|2022 Form 10-K|第F-9ページ
| | | | | | | | | | | | | | | | | |
Pacira生物科学社は 合併現金フロー表(継続) (単位:千) |
| 十二月三十一日までの年度 |
| 2022 | | 2021 | | 2020 |
| キャッシュフロー情報の追加: | | | | | |
| 利子を支払う現金 | $ | 33,295 | | | $ | 6,996 | | | $ | 7,205 | |
| 所得税をお支払いの現金は、返金後の純額を差し引かれます | $ | 7,398 | | | $ | 3,221 | | | $ | 2,417 | |
| 非現金投資と融資活動: | | | | | |
| 2022年に転換可能な優先手形に転換した普通株式を発行する | $ | 3,040 | | | $ | — | | | $ | — | |
| 売掛金および売掛金に含まれる固定資産 | $ | 5,888 | | | $ | 6,828 | | | $ | 9,288 | |
| 対価格負債の純増加額もあります | $ | — | | | $ | 45,241 | | | $ | — | |
連結財務諸表の付記を参照。
Pacira BioSciences,Inc.|2022 Form 10-K|第F-10ページ
カタログ表
Pacira生物科学社は
連結財務諸表付記
注1-業務説明
Pacira BioSciences,Inc.とその子会社(総称して“会社”あるいは“Pacira”)は,非オピオイド疼痛管理に取り組み,可能な限り多くの患者に非オピオイド薬物選択を提供し,オピオイドの役割を再定義して救急療法のみの業界の先頭である。同社はまた、心電嵐、慢性疼痛、痙攣などの交感神経系の衰弱状況に対応するための革新的な干与措置を開発している。会社の長時間作用局所鎮痛剤EXPAREL® (ブピバカインリポソーム注射可能懸濁剤)は2012年4月に米国で商業的に発売され、2021年11月に一部のヨーロッパ諸国およびイギリスまたはイギリスで承認された。EXPARELは、薬物分子構造を変化させることなく薬物を被覆し、必要な時間内にそれらを放出することができる同社独自の多嚢胞リポソームまたはpMVL薬物送達技術を使用する。2021年11月、同社はFlexion Treateutics、Inc.またはFlexionを買収し、ZILRETTAを追加した®(トリアムシノロンアセトニド徐放性注射懸濁剤)それらの製品組み合わせを添加する。ZILRETTAは第一種であり、骨性関節炎または膝痛の治療に用いられる唯一の徐放性関節内注射(指関節内注射)でもある。詳細については、付記5を参照されたい屈曲習得それは.2019年4月、会社はiovera°を追加しました® MyoScience、Inc.またはMyoScienceを買収することで提供される商業製品。Iovera°システムは手持ち式冷凍鎮痛装置であり、目標神経を正確かつ制御可能な凝縮温度に応用する。
Paciraは同様の業界や段階の企業と同じリスクに直面していますが、大きな企業からの競争に限らず、三つこれらの要素には、製品への依存、限られた数量の卸売業者への依存、限られた数量の生産拠点への依存、新技術革新への依存、キーパーソンへの依存、第三者サービスプロバイダと単一ソースサプライヤーへの依存、ノウハウの保護、政府条例の遵守、およびネットワークセキュリティに関連するリスクがある。
新冠肺炎コロナウイルスの大流行と世界経済情勢
2020年初め以来、同社の収入とサプライチェーンは、公衆衛生指導と政府指示による選択的外科手術のスケジュールの大幅な延期または一時停止を含む新冠肺炎の大流行に関連する挑戦の影響を受けてきた。大流行期間中、ワクチンと治療法の採用及び選択性手術に対する制限が減少したため、影響程度は軽減されたが、大流行に関連するいくつかの業務と人員配置挑戦は依然として存在している。選択性手術市場が正常化するのにどのくらいの時間がかかるかは不明であり、未来の新冠肺炎変異体或いはその他の原因で再び選択性手術を制限するかどうかも不明である。疫病と全世界の経済状況の直接と間接的な影響はすでに会社の業務、財務状況と経営結果に負の影響を与える可能性がある。これらの影響には、長期インフレや金利上昇が会社の顧客やサプライヤーに与える影響や、より長い納期や十分な材料供給が確保できないことが含まれる可能性がある。状況は依然として動態的であり、迅速で実質的な変化が起こる可能性がある。また、会社が予見できない他の否定的な影響も発生する可能性がある。このような影響の性質や程度は将来の事態の発展に依存し,これらの事態の推移は高度に不確実であり,予測もできない.
注2-重要会計政策の概要
列報根拠と合併原則
これらの連結財務諸表は、米国公認会計原則と米国証券取引委員会(米国証券取引委員会)の規則に基づいて作成されている。当社の完全子会社の勘定はこれらの連結財務諸表に含まれています。すべての会社間の残高と取引はすでに合併中に販売されている。以前に発表された財務諸表を何らかの再分類し、現在の列報方式に適合させた。
予算の使用
公認会計基準に従って財務諸表を作成するには、財務諸表の日付を開示するか、資産および負債があるか、ならびに報告中に報告された収入および支出金額を含む、資産および負債報告金額に影響を与える推定および仮定を使用する必要がある。他の事項に加えて、推定数は、収入確認、購入価格分配、株式ベースの補償、在庫コスト、株式投資減価、長期資産、営業権および他の無形資産、負債および課税項目、対価格、および繰延税金資産の推定値を含むか、またはあるか、および繰延税金資産の推定値に使用される。会社のキー会計見積もりは、会社の総合財務状況も経営結果も最も重要な見積もりであり、応用時に管理層が最も困難で、最も主観的あるいは最も複雑な判断を行う必要があり、これは通常、本質的に不確実な事項の影響を推定する必要があるからである。この問題をめぐる様々な要因の不確実性によって
Pacira BioSciences,Inc.|2022 Form 10-K|第F-11ページ
カタログ表
Pacira生物科学社は
連結財務諸表付記
連結財務諸表の作成に推定数や判断数を用いると、実際の結果はこれらの推定数と異なる可能性がある。
取引先と契約した収入
同社の収入源は、(I)米国、EUまたはEUおよびイギリスでのEXPARELの販売、(Ii)ZILRETTAの米国での販売、(Iii)iovera?米国、カナダおよびEUでの販売、(Iv)動物のブピバカインリポソーム注射懸濁剤の販売および特許権使用料、(V)許可料およびマイルストーン支払いを含む。特許使用料収入は同社の協力許可協定から得られる。注4を参照収入.収入そして、会社と顧客契約収入に関する会計政策に関する更なる情報を取得する。
協力許可と記念碑的な収入
その会社の協力協定は通常、その会社の製品のライセンスに関するものだ。提携プロトコルに従って収入がいつ確認されるかを決定する際には、企業は、顧客がライセンスから利益を得ることができるかどうか、およびライセンスがプロトコル内の他の履行義務から分離されているかどうかに応じて、ライセンスが異なるかどうかを評価しなければならない。ライセンスが異なる場合、企業は、顧客がライセンスにアクセスまたは使用する権利があるかどうかをさらに評価しなければならず、ライセンスの機能が時間とともに実質的に変化することが予想されるかどうかに依存する。ライセンスが実質的に変化しないと予想される場合、収入はライセンスが提供された時点で確認されるだろう。ライセンスが実質的に変化すると予想される場合、収入はライセンス期限内に確認されるだろう。
マイルストーン支払いの収入確認はマイルストーン支払いをめぐる事実と状況にかかっている。開発ベースのマイルストーン(例えば、規制承認を得る)など、非販売指標に基づくマイルストーン支払いは、可変対価格を表し、任意の制限の場合に取引価格に含まれる。記念碑的な支払いが将来の発展に関係していれば、確認のタイミングは歴史的経験と第三者の結果に対する重要性に依存する。販売の敷居に達したときに受け取ったマイルストーン支払いについては、マイルストーン支払いの収入が実際の販売または販売に関する業績義務が履行されたときに確認される。
特許権使用料収入
特許使用料は、特許使用料が主に供給契約に関連しているため、特定の制限がない限り、会社の商業パートナーに販売する際に収入として推定され、確認される。特許使用料は,同社の獣医用ブピバカインリポソーム注射懸濁剤製品の販売に基づいて計算した。
大顧客集中度
同社は直運計画によりEXPARELの販売を計画しており,この計画により,注文は卸(amerisourceBergen Health Corporation,Cardinal Health,Inc.およびMcKesson製薬会社を含む)で処理されているが,製品出荷は病院,外来手術センター,個人医師などの個人口座に直接送信されている。同社は外来外科センターや医師にもEXPARELを直接販売している。同社は主に専門流通業者とある専門薬局にZILRETTAを販売し、その後ZILRETTAを医師、診療所とある医療センター或いは病院に転売する。同社はまた、医療提供者や仲介機関(団体調達組織やGPOなど)と直接契約を結んでいる。同社はその動物用ブピバカインリポソーム注射可能懸濁液を米国の第三者ライセンス取得者に販売し,エンドユーザにiovera°を直接販売した。
次の表には当社の収入の割合が含まれています三つ各時期の最大の卸売業者の紹介: | | | | | | | | | | | | | | | | | |
| | 十二月三十一日までの年度 |
| | 2022 | | 2021 | | 2020 |
| 最大卸売業者 | 31 | % | | 31 | % | | 31 | % |
| 第二卸売業者 | 23 | % | | 28 | % | | 31 | % |
| 第三卸売業者 | 22 | % | | 26 | % | | 25 | % |
| 合計する | 76 | % | | 85 | % | | 87 | % |
2022年12月31日までの年度はZILRETTA製品の純売上高の最初の年間を含む。会社は2021年11月19日からZILRETTAの製品純販売収入、すなわちFlexion買収の日付(本稿で定義したように)を確認した。
Pacira BioSciences,Inc.|2022 Form 10-K|第F-12ページ
カタログ表
Pacira生物科学社は
連結財務諸表付記
アメリカ以外からの収入比率は12022年12月31日までと2021年12月31日までの年間総収入の割合を占める。同社は2021年第4四半期にEUとイギリスでEXPARELの販売を開始し、カナダでiovera°を販売している。その会社は所有している違います。2020年12月31日までの会計年度では、米国以外からの収入がある。
研究と開発費
研究と開発支出は発生時に計上される。これには内部および外部コストが含まれており,その大部分は契約研究組織を含む第三者に開発活動がアウトソーシングされている.臨床試験費用は契約に定められたサービス期間内に積算し,作業レベルや実費の継続審査に必要な調整を行う。研究と開発費用はビジネスパートナーの補償を差し引いて掲載されています。
所得税
当社は貸借対照法を用いて所得税を計算します。繰延税金資産および負債は、既存の資産および負債の帳簿金額とそのそれぞれの税ベースとの間の基礎差による将来の税金項目の影響を推定することによって確認することができる。税金資産及び負債を繰延して税率計量を策定し、その等の一時的な差額を回収又は決済する予定の年度の課税収入に適用されることが予想される。繰延税金資産を予想現金化金額に減少させるために、必要に応じて評価準備を設ける
当社は、その総合経営報告書において、所得税(未確認税収割引に関する所得税を含む)に対して利息と罰金(あれば)を計上し、所得税支出の構成要素としている。
株に基づく報酬
同社の株式報酬には、従業員、コンサルタント、非従業員取締役に株式オプションおよび制限株式単位を付与すること、従業員が従業員の株式購入計画に参加する機会を含む。これらの計画に関連する費用は、会社の総合経営報告書において、適用される帰属条項又は発売期間の長さに基づいて稼いだ公正価値に基づいて確認される。
付与された株式オプションと従業員株式購入計画株式オプションの推定公正価値を計算する際には、会社はブラック-スコアーズオプション推定モデルまたはブラック-スコアモデルを用い、授与日会社の普通株の終値を除いて、公正価値を推定するためには、以下の変数を考慮する必要がある
•オプションの所期
•予想変動率
•配当を期待する
•無リスク金利
当社はその履歴変動率データを用いて期待オプション期間内の予想変動率を決定する。同社はその株式オプション活動の履歴データに基づいて期待される用語を使用している。無リスク金利は、米財務省のゼロ金利債券の暗黙的な収益率に基づいており、期限はオプションの予想期限に見合っている。会社の普通株の配当収益率はゼロと推定されているが、会社は設立以来何の配当金も発表したり支払ったりしていないし、予見可能な未来にそうするつもりもないからだ。また、その債務を管理する協定によると、同社が将来的に配当金を発表して支払う能力が制限される可能性がある。当社は報告期間ごとの没収状況を見積もるのではなく、贈与没収が発生した場合に記録します。
現金と現金等価物
すべての購入時満期日が90日以下の高流動性投資は現金等価物とみなされる。現金等価物には、会社の債務証券、資産支援証券、通貨市場基金が含まれる。2022年12月31日現在、通貨市場基金の帳簿価値は42.6百万ドルです。2021年12月31日現在、通貨市場基金の帳簿価値は223.0100万ドル商業手形は$19.0100万ドルと資産支援証券は$2.6百万ドルです。2022年12月31日と2021年12月31日までの帳簿価値は公正価値に近い。
Pacira BioSciences,Inc.|2022 Form 10-K|第F-13ページ
カタログ表
Pacira生物科学社は
連結財務諸表付記
短期と非流動は投資を売却することができます
短期売却可能投資には、クレジットカードの売掛金、投資レベルの商業手形、社債、国債を担保とした資産保証証券、および外国実体が米国で発行した他のドル建て債券が含まれており、これらの債券の満期日は3ヶ月を超えているが、1年未満である。非当期売却可能投資には、満期日が一年を超える会社や政府機関債券が含まれている。当社は、購入時にその投資種別を評価し、資産負債表ごとに当該等を見直し、売却可能な証券を保有する意向を評価することを含む。会社の投資政策はその投資に最低信用品質標準と最高期限制限を設定し、資本、流動性と合理的なリターン率を保護する。その会社はその投資を販売可能なものに分類した。販売可能な証券は現在の市場推定値を基礎として、公正価値によって記録されている。証券売却可能な未実現保有収益と損失(信用損失を除く)は純収益(損失)には含まれず,実現までに他の全面(損失)収入を累積する単独構成要素として報告されている。総合経営報告書の利子収入を損益計上し、特定の確認方法を用いて証券売却コストを決定することが実現されている。当社は信用損失が存在するか否かを評価し、確実に信用損失が存在すれば、公正価値が償却コストより小さい金額に基づいて合併経営報告書において信用損失を確認する。
棚卸しをする
在庫には販売され分配される製品、原材料、製品が含まれている。在庫はコストの中で低い者に記載されており、材料、人工と間接費用、あるいは現金化可能な純価値に関する金額を含み、先進的な先出し(“FIFO”)方法で決定されている。同社は定期的に在庫を審査し、時代遅れ、移動が遅い、あるいは他の方法では販売できない在庫を確定し、在庫コストが回収できないと予想される場合に備えを立てている。
固定資産
固定資産はコスト、減価償却、償却純額で入金される。事件や状況の変化がある資産の額面が回収できない可能性があることを示すたびに、当社はその物件、工場及び設備資産の減値を審査する。
固定資産減価償却はその推定耐用年数内に直線的に提案されている。同社はこれらの実要因、経済要因、業界傾向に関連する有用な寿命を定期的に評価している。財産や設備の計画用途が変化した場合、これらの資産に割り当てられる耐用年数は短縮される必要があり、将来的に減価償却費用が加速されることが確認される可能性がある。レンタル改善は、使用年数または関連する残りのレンタル期間のうち短い時間を推定して直線法で償却する資産別の使用寿命は以下のとおりである | | | | | | | | |
| 資産種別 | | 使用寿命 |
| コンピュータ装置及びソフトウェア | | 1至れり尽くせり3年.年 |
| オフィス家具と設備 | | 5年.年 |
| 製造と実験室装置 | | 5至れり尽くせり10年.年 |
資産廃棄債務
当社には、当該等のリース契約が終了した場合に、レンタル空間を元の状態に戻すといういくつかのリース契約による契約義務がある。当社は予想される将来のキャッシュフローの現在値に基づいて、その資産廃棄債務(ARO)を対応する資本資産とともに記録し、金額はAROの推定公正価値に相当する。その後の期間、会社はAROをその全価値に統合する費用を記録した。各ARO資本資産は関連固定資産の減価償却期間内に減価償却を行う。
賃貸借証書
同社は、そのリース契約の開始時に使用権またはROU資産と賃貸負債を確認します。リースは開始時に評価を行い、それらが経営的賃貸または融資リースに分類されるべきかどうかを決定する。経営リースに関するリースコストは直線法で確認し,融資リースのリースコストは実際の利息法でリース期間で確認した。当社には融資リースは何もありません。確認すべきROU資産およびリース負債額賃貸支払タイプ、レンタル期間、および
Pacira BioSciences,Inc.|2022 Form 10-K|第F-14ページ
カタログ表
Pacira生物科学社は
連結財務諸表付記
借入金利を逓増する。可変レンタル支払いは開始時に含まれておらず、レンタル支払いが変動している間に確認します
同社は、総合キャッシュフロー表でROU資産を純償却し、他の負債における賃貸負債元金を削減することを選択した。
レンタル期間は契約期間をもとに、行使する任意の継続選択権または停止権を合理的に決定することによって調整される。逓増借款金利は、当社が想定しているような経済環境下での類似期限内に担保方式で支払われる金利です。
買収する
企業合併では、買収会計方法は買収した資産と負担した負債を買収日にそれぞれの公正価値で記録することを要求しているが、いくつかの例外がある。企業合併で取得した資産と負担または事項が発生した負債は、一般に公正価値で確認される。公正価値が決定されることができる場合、資産または負債が確認され、公正価値が確定できない場合、いかなる資産または負債も確認されない。公正価値は、計量日市場参加者間の秩序ある取引において、資産または負債が元金または最も有利な市場で負債を譲渡するために徴収または支払いされる交換価格(“脱退価格”)として定義される
買収された進行中の研究·開発、またはIPR&Dは、公正な価値で確認され、買収されたIPR&Dに代替の将来的な用途があるか否かにかかわらず、最初に無期限の無形資産として記述される。買収した純資産が会計買収法下の業務を構成していなければ、その取引は資産買収に計上され、営業権を確認しない。資産買収では、買収された知的財産権研究·開発に割り当てられ、他の将来用途のない金額が買収日に費用として記録されている。
買収価格(移転対価格)が買収された純資産の推定公正価値を超える任意の部分は営業権に計上されている。取引コストと再編被買収会社のコストは発生時に費用を計上する。買収された業務の経営結果は買収終了後に会社の総合財務諸表に反映される。
値段が合うかもしれない
買収後、当社は報告期間ごとに公正価値の計量または価格設定があり、公正価値変動は総合経営報告書で買収に関する費用(収益)であることを確認した。または対価格の変化は、推定売上高の仮定実現および時間、販売商品のコスト、規制承認の変化による可能性がある。新しい情報がない場合、公正価値の変化は、マイルストーンの実現または終了に経過した時間を反映し、予想される支払い期間を計上する。
商誉
営業権とは、買収価格が企業合併で買収した純資産の推定公正価値を超え、償却しないことであるが、少なくとも毎年、あるいは潜在的な減値が存在することを示す可能性のあるトリガイベントが発生した場合に減値テストを行う。
無形資産
耐用年数を定めた無形資産は、その推定耐用年数内に直線的に償却し、累積償却後のコストを差し引いて入金される。存在期間が不定な無形資産は、少なくとも毎年減値テストを行うか、または潜在的な減値の存在を示す可能性のあるトリガイベントが発生した場合に減値テストを行う。減価費用は帳簿価値がその公正価値を超えた場合に確認する。
株式投資
当社が保有する株式証券投資は、いつでも公正な価値を特定することができず、コストから任意の減値を引いて確認し、類似投資の秩序取引に見られる価格変動によるいかなる変動も加えたり、減算したりすることができる。
Pacira BioSciences,Inc.|2022 Form 10-K|第F-15ページ
カタログ表
Pacira生物科学社は
連結財務諸表付記
長期資産減価準備
イベントや環境変化が1つの資産の帳簿金額を回収できない可能性があることを示すたびに、管理層は長期資産(固定資産および有限寿命無形資産を含む)の減値を審査する。保有·使用する資産の回収可能性は,資産の帳簿価値と資産予想による将来の未割引現金流量を比較することで測定した。このような資産は減値とみなされ,確認すべき減値は資産の帳簿価値が資産公正価値を超える金額で計測される.
1株当たりのデータ
普通株1株当たり基本純収益(損失)の算出方法は、普通株株主が適用可能(帰属可能)の純収益(損失)を、その期間に発行された普通株の加重平均株式数で割る。
普通株式1株当たりの純利益(損失)の計算方法は、普通株株主の利用可能(帰属可能)純収益(損失)を当期発行普通株と希釈性普通株の加重平均株式数(あれば)で割る。潜在的普通株には,発行済み株式オプションを行使する際に発行可能な普通株株式,帰属が予想されるRSU,会社員株購入計画(在庫株使用方法)によって購入予定の普通株株式,IF変換方法を用いて転換可能優先手形を変換する際に発行可能な潜在普通株がある.IF−転換法により,希釈後の普通株当たり純収益(損失)の計算を調整し,当社が期間ごとの初日に転換可能優先手形を転換したように調整した。分子の調整は,税引後に転換可能優先手形に関する利子支出を再計上するためである。
外貨?外貨
当社の海外子会社の貸借対照表口座はドル以外の機能通貨を使用し、それぞれの貸借対照表日の為替レートを用いて換算します。収入と支出は一年間の日歴月あたりの平均為替レート換算を使います。換算調整は、連結財務諸表において、他の全面(損失)収入を累積する構成要素と記す。外貨両替の収益または損失は連結業務報告書に他の純額を記入する。
細分化市場報告
同社は単一企業として管理と運営を行い、非オピオイド疼痛管理と再生健康ソリューションの開発、製造、マーケティング、流通と販売に集中している。会社は単一の管理チームによって管理され、その組織構造と一致し、最高経営責任者である会社の経営意思決定者は、統一的なレベルで資源を管理し、分配する。したがって,当社はその業務を以下のように考えている1つは報告可能な運営部門は、その業績を評価し、資源を割り当て、運営目標を設定し、その将来の財務業績を予測する。
注3-最近の会計声明
最近採用された会計公告
2020年8月、財務会計基準委員会(FASB)は会計基準更新(ASU,2020-06)を発表した債務--転換債務および他のオプション(主題470-20)および派生ツールおよびヘッジを伴うエンティティ自身の権益の契約(主題815-40)、この条項は、個別計算を必要とする変換可能債務ツールの数を、(I)債務の不明確かつ密接に関連し、派生ツールの定義に適合し、派生ツールの会計例外範囲に適合しない変換可能な特徴を有する変換可能債務ツール、および(Ii)実収資本として割増された発行された転換可能債務ツールに制限される。また,新たな指針では,希釈後の1株当たり収益計算には在庫株方法ではなくIF−転換法を用いることが求められている。同社は新たなガイドラインを採用することを選択し、2022年1月1日に完成していない取引に適用される改正後の遡及移行方法を採用している。そのため、2022年1月1日から、当社は単独で株式においてその転換可能債券に組み込み変換機能を提供することはない。代わりに、その会社はその転換可能な債務ツールを完全に債務として入金した。また、2022年1月1日から、会社は以前に記録された転換可能債務割引の利息支出を記録しない。2022年1月1日現在、簡明総合貸借対照表への影響は純債務を約1ドル増加させている64.9百万ドル、累積赤字はドル減少します47.2100万ドルで追加の実収資本が減少しました96.5100万ドル、繰延税金負債が減少#ドル15.7百万ドルです。
Pacira BioSciences,Inc.|2022 Form 10-K|第F-16ページ
カタログ表
Pacira生物科学社は
連結財務諸表付記
注4-収入.収入
当社の収入源の詳細は付記2を参照重要会計政策の概要それは.会社はEXPARELやZILRETTA以外の他の源を販売する収入がその総合収入の主要な源であるとは考えていない。したがって、以下の開示はEXPARELやZILRETTAの製品純売上に関する収入に限られる
製品純売上高
同社は直運計画によりEXPARELの販売を計画しており,この計画によると,卸はエンドユーザー(すなわち病院,外来手術センター,保健提供者オフィス)での製品注文に基づいて注文を処理している。EXPARELはエンドユーザに直接渡されるが,卸は実際に製品を所有していない.同社は主に専門流通業者と専門薬局にZILRETTAを販売し、その後ZILRETTAを医師、診療所とある医療センター或いは病院に転売する。同社はヘルスケア提供者やGPOなどの仲介機関とも直接契約を結んでいる。製品収入は、貨物の制御権を顧客に移転することを承諾したときに確認され、金額は、これらの貨物を移転することと交換するために、会社が獲得する権利があると予想されている対価格を反映している。EXPARELとZILRETTAの収入は、製品が顧客に渡されたときに記録されます。
販売製品の収入は、返品手当、即時支払い割引、サービス料、政府リベート、数量リベート、ストレージ容量別使用料金を差し引いた純額です。これらの準備金は、関連販売によって稼いだ金額または請求された金額の推定に基づいている。これらの金額は可変対価格とみなされ,可能金額法を用いて販売時の取引価格の減少が推定され確認されたが,収益は除外され,期待値法に基づいている.会社はこれらの見積金額を取引価格に計上しており,このような取引確認の累積収入が大きく逆転しない可能性が高いこと,あるいは可変対価格に関する不確実性が解決される可能性が高いことを前提としている
合格した政府医療保健提供者に徴収される費用と割引とは、他の顧客から徴収された価格よりも低い価格で合格した退役軍人事務部病院と340 B実体に製品を販売することを契約が約束したことによる推定義務である。340 B薬品割引計画は、米国連邦政府が1992年に作成した計画であり、計画に参加した薬品製造業者に、より低い価格で条件を満たす医療保健組織および保証実体に外来薬品を提供することを要求する。顧客は条件を満たした実体から製品支払いと法定販売価格との差額を受け取る。準備金は関連収入が確認された同期間に設立され、製品収入と貿易売掛金の純額が減少した。返金金額は通常、合格した政府医療提供者に販売する際に顧客が決定し、会社は通常、顧客が販売を通知してから数週間以内にこのような金額の信用限度額を発行する。記憶容量別使用課金準備金には、企業が合格医療提供者に売却されると予想される機器のクレジット限度額と、顧客が申請したが会社がクレジット額を発行していない記憶容量別使用課金が含まれる。
その中のいくつかの項目の計算は、管理層が販売データ、履歴返品データ、契約、法定要求、その他の将来知っている可能性のある関連情報に基づいて推定する必要がある。このような規定の十分性は四半期ごとに検討される。
次の表は、2022年、2022年、2020年12月31日までの年間会社のEXPARELに関する販売関連手当と課税項目および2022年12月31日と2021年12月31日までの年間ZILRETTAの活動概要(単位:千)を提供しています
Pacira BioSciences,Inc.|2022 Form 10-K|第F-17ページ
カタログ表
Pacira生物科学社は
連結財務諸表付記
| | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | |
| 返品手当 | | 即時支払割引 | | サービス.サービス
費用.費用 | | 一括返却とストレージ容量別の課金 | | 政府の税金の払い戻し | | 合計する |
| 2019年12月31日の残高 | $ | 540 | | | $ | 962 | | | $ | 1,486 | | | $ | 1,816 | | | $ | — | | | $ | 4,804 | |
| 規定 | 794 | | | 8,541 | | | 6,437 | | | 12,345 | | | — | | | 28,117 | |
| 支払い/調整 | (311) | | | (8,496) | | | (6,755) | | | (12,561) | | | — | | | (28,123) | |
| 2020年12月31日残高 | 1,023 | | | 1,007 | | | 1,168 | | | 1,600 | | | — | | | 4,798 | |
| 規定 | 3,095 | | | 10,388 | | | 10,112 | | | 17,101 | | | 1,139 | | | 41,835 | |
| 支払い/調整 | (757) | | | (10,217) | | | (7,644) | | | (15,207) | | | (378) | | | (34,203) | |
| 2021年12月31日の残高 | 3,361 | | | 1,178 | | | 3,636 | | | 3,494 | | | 761 | | | 12,430 | |
| 規定 | 1,390 | | | 11,145 | | | 16,866 | | | 48,890 | | | 1,641 | | | 79,932 | |
| 支払い/調整 | (3,060) | | | (11,136) | | | (17,309) | | | (46,932) | | | (1,616) | | | (80,053) | |
| 2022年12月31日の残高 | $ | 1,691 | | | $ | 1,187 | | | $ | 3,193 | | | $ | 5,452 | | | $ | 786 | | | $ | 12,309 | |
協力許可と記念碑的な収入
当社の協力許可とマイルストーン収入確認政策は付記2で検討されている重要会計政策の概要
売掛金
売掛金の多くは製品販売から来ており、卸売業者、病院、外来外科センター、専門流通業者、専門薬局と個人医師の未収金額を代表する。支払い条件は普通ゼロ至れり尽くせり97取引の日から数日間であるため、重大な融資部分はない
契約義務を履行する
履行義務は、契約において、1種のユニークな貨物またはサービスを顧客に移転することを承諾する約束であり、会計基準編纂またはASC,606における会計単位である。契約の取引価格は、それぞれ異なる履行義務に割り当てられ、義務履行時に収入として確認される
契約開始時に、同社は、顧客との契約で約束された貨物を評価し、顧客に異なる貨物を譲渡する毎の承諾の履行義務を決定する。個別履行義務を決定する際には、会社は契約で約束されたすべての貨物を考慮し、顧客契約で明確に規定されているものでも、ビジネス慣行に慣れていることから示唆されている。同社の顧客との契約は、単一の履行義務を表す個別の独自製品の譲渡を要求している。同社の製品販売における履行義務は,EXPARELとZILRETTAの交付時に顧客に制御権を移譲することである時点で履行されている。当社は、支配権は交付時に譲渡されたと考えており、顧客は資産に対して法定所有権を持っており、資産の実際の占有権は譲渡されており、顧客は資産の所有権に対して重大なリスクとリターンを持っているが、当社は当時支払いを受ける権利があった。
仕分け収入
以下の各時期の製品販売純額分類状況(単位:千)を示す | | | | | | | | | | | | | | | | | |
| 十二月三十一日までの年度 |
| 2022 | | 2021 | | 2020 |
| 製品純売上高: | | | | | |
| ExparEL | $ | 536,899 | | | $ | 506,515 | | | $ | 413,338 | |
| ZILRETTA | 105,517 | | | 12,683 | | | — | |
| Iovera° | 15,258 | | | 16,162 | | | 8,817 | |
| ブピバカインリポソーム注射用懸濁剤 | 6,476 | | | 3,606 | | | 4,459 | |
| 製品純売上合計 | $ | 664,150 | | | $ | 538,966 | | | $ | 426,614 | |
Pacira BioSciences,Inc.|2022 Form 10-K|第F-18ページ
カタログ表
Pacira生物科学社は
連結財務諸表付記
会社は2021年11月19日からZILRETTAの製品純販売収入、すなわちFlexion買収の日付(本稿で定義したように)を確認した。
注5-屈曲習得
屈曲治療会社
2021年11月19日、会社はFlexion(“Flexion買収”)を買収し、筋肉骨格疾患患者の治療のための新しいローカル療法の発見、開発に専念し、商業化し、2021年10月11日までに当社、Oyster Acquisition Company Inc.,当社のデラウェア州会社と完全子会社(“買い手”)およびFlexionが署名した合意および合併計画(“Flexion合併協定”)に基づいて、最も一般的な関節炎関節炎から開始した。Flexion普通株株式への入札要約に成功した後、Flexion合併プロトコルの条項とデラウェア州会社法第251(H)条によると、買い手はFlexionと合併してFlexionに組み込まれ、Flexionは当社の完全子会社として存続する。合併完了後、同社はFlexionをPacira治療会社と改称した。
Flexion買収の総対価格は約ドルである578.8(I)$を含む百万ドル448.5Flexion株主に支払う現金百万ドルは、限定的な株式単位および現金株式オプションを決済するための現金百万ドル;(Ii)$85.1会社が負担していない柔軟な債務の現金は百万ドルと(Iii)ドルを支払う45.2買収時にFlexion株主及びいくつかの株式奨励所有者がFlexion買収に同時に発行した或いは価値のある権利或いはCVRに関する推定或いは代償百万元がある。価格はいくつかの潜在的なマイルストーン支払いの実現状況に応じて調整されるかもしれない。買収時には、同社は最高で追加で$を支払うことができると推定しています380.22030年12月31日までに各適用のマイルストーンを実現すれば、CVR所持者に合計100万ドルを支払うことができ、以下のようになる
(i) $1.00CVRによると、ZILRETTAの毎年の純売上高は初めて$以上となった250.0百万
(ii) $2.00CVRによると、ZILRETTAの毎年の純売上高は初めて$以上となった375.0百万
(Iii)$3.00CVRによると、ZILRETTAの毎年の純売上高は初めて$以上となった500.0百万
(iv) $1.00米国食品医薬品局(FDA)が臨床段階遺伝子治療候補製品PCRX-201の生物製品ライセンス申請(BLA)を承認した後、各CVR;および
(v) $1.00FDAが候補製品PCRX−301を研究するための新薬出願またはNDAを承認した後、CVRに従って。2022年9月、完成した第1段階研究の結果、同社はPCRX-301のさらなる開発を中止することを決定した。
Flexion買収の総対価は$578.8百万ドル(1株当たりの金額を除く)が含まれています
| | | | | | | | |
| 購入価格対価格の公正価値 | | 金額 |
| 成約時に支払う購入対価格の公正価値: | | |
Flexion普通株すべての流通株に対する現金対価(50,392ドルで購入した普通株8.501株当たり) | | $ | 428,333 | |
| RSUと現金株式オプションの決済のために支払われた現金対価格 | | 20,153 | |
| | |
| | |
| 屈曲債務返済のための現金 | | 85,118 | |
| | 533,604 | |
| | |
| CVRの公正価値 | | 45,241 | |
| 総掛け値を買う | | $ | 578,845 | |
同社は買収会計方法を用いてFlexion買収に対して会計計算を行ったため、2021年11月19日の買収日から、同社はすでに買収した資産、負担した負債と経営結果をその総合財務諸表に組み入れた
Pacira BioSciences,Inc.|2022 Form 10-K|第F-19ページ
カタログ表
Pacira生物科学社は
連結財務諸表付記
購入した資産と負担した負債に移行する対価格の最終配分が完了した次の表に、買収日の純資産買い取り価格の推定公正価値における柔軟買収価格の分配状況(千計)を示す | | | | | | | | | | | | | | | | | | | | |
| | 購入日に確認した金額 (以前と同じ) (報道済み)(a) | | 測算期調整(b) | | 購入日に確認した金額
(調整後) |
| 買収した資産 | | | | | | |
| 現金と現金等価物 | | $ | 113,562 | | | $ | — | | | $ | 113,562 | |
| 短期的には投資を売ることができる | | 11,153 | | | — | | | 11,153 | |
| 売掛金 | | 32,838 | | | — | | | 32,838 | |
| 棚卸しをする | | 29,667 | | | — | | | 29,667 | |
| 前払い費用と他の資産 | | 4,852 | | | — | | | 4,852 | |
| 固定資産 | | 23,307 | | | — | | | 23,307 | |
| 繰延税金資産 | | 58,015 | | | (16,906) | | | 41,109 | |
| 使用権資産 | | 6,585 | | | — | | | 6,585 | |
| 無形資産を識別することができる | | 480,000 | | | — | | | 480,000 | |
| 知的財産権研究開発 | | 61,000 | | | — | | | 61,000 | |
| 総資産 | | $ | 820,979 | | | $ | (16,906) | | | $ | 804,073 | |
| 負担的負債 | | | | | | |
| 売掛金 | | $ | 9,794 | | | $ | — | | | $ | 9,794 | |
| 費用を計算する | | 22,746 | | | 1,162 | | | 23,908 | |
| 収入を繰り越す | | 10,000 | | | — | | | 10,000 | |
| 賃貸負債 | | 6,585 | | | — | | | 6,585 | |
| その他負債 | | 1,187 | | | — | | | 1,187 | |
| 長期債務 | | 201,450 | | | — | | | 201,450 | |
| 総負債 | | 251,762 | | | 1,162 | | | 252,924 | |
| 買収の確認可能純資産総額 | | 569,217 | | | (18,068) | | | 551,149 | |
| 商誉 | | 9,628 | | | 18,068 | | | 27,696 | |
| 移転の総対価 | | $ | 578,845 | | | $ | — | | | $ | 578,845 | |
(A)会社が2021年12月31日までの年次報告Form 10-Kで報告したように。
(B)当社が2022年に支払う税務研究及び買収前の支出を完了し、一部は見積もり備蓄の発行によって相殺される。
買収の確認可能無形資産と知的財産権研究開発資産は、多期超過収益法(収益法)を用いて市場参加者の観点から推定される。識別可能な有限寿命無形資産ZILRETTAは膝骨性関節炎の痛みを治療する開発技術であり、ドルの価値がある480.0百万ドルと有用な寿命9.7何年もです。割引率は17.5%は、この技術の公正価値を計算するために使用されます。IPR&D資産はZILRETTAを用いた肩骨性関節炎疼痛の治療に関連し、#ドルの価値がある60.0百万ドルです。この資産の予想キャッシュフローは、開発成功と商業化の可能性に応じて調整され、18.0%.
購入価格が取得された識別可能な純資産の公正価値を超えることが営業権である。この善意は主にZILRETTAとiovera°とExPARELを安全かつ有効な非オピオイド系薬物マルチモード鎮痛方案として結合した価値、及び合併操作の協同効果によるものである。取得された商標権と無形資産は納税時に控除されてはいけない
付記9を参照してください商誉と無形資産18を付記して買収に関連する費用(収益)、減価その他、Flexion買収に関連したより多くの情報を取得する。
Pacira BioSciences,Inc.|2022 Form 10-K|第F-20ページ
カタログ表
Pacira生物科学社は
連結財務諸表付記
監査されていない業務の予備的概要
次の表は,Flexion買収が2020年1月1日に発生したように,2021年12月31日と2020年12月31日までの未監査の予定運営概要を示しているこれらの予想情報は、買収が2020年1月1日に発生すれば、会社の実際の結果が何になるかを意味するものではなく、今後のどの時期の予想結果も示すことができない(千計、1株当たり金額を除く)
| | | | | | | | | | | | | | |
| | 十二月三十一日までの年度 |
| | 2021 | | 2020 |
| 総収入 | | $ | 630,942 | | | $ | 515,199 | |
| 純損失 | | (67,264) | | | (19,711) | |
| 基本と希釈後の1株当たり純損失を予想する | | $ | (1.52) | | | $ | (0.46) | |
| | | | |
監査を受けていない予備財務情報は会計買収法を用いて作成し、当社の歴史財務情報とFlexionに基づいて作成した。備考財務情報の概要は主に以下の備考調整を反映する:
•株式ベースの補償および買収に関連する他の補償費用を含む、2021年12月31日および2020年12月31日までの年間から買収に関する取引手数料およびコストを差し引く
•Flexion 2021年12月31日までの年間繰延税金資産の既存推定額の減少準備による所得税収益の確認
•Flexionの利息支出とドル関連の繰延融資コストの償却85.1未負担の百万の債務
•Flexityの現金を買収するための会社の利息収入を調整する
•在庫増加の価値に関する販売商品の追加コスト;
•開発された技術無形資産の追加償却費用
•Flexion固定資産の追加減価償却;
•FlexionのROU資産の追加レンタル費用。
また、上記のすべての調整は適用された税務影響に基づいて調整された。
注6-在庫品
在庫純額の構成は以下の通り(千で計算) | | | | | | | | | | | |
| | 十二月三十一日 |
| | 2022 | | 2021 |
| 原料.原料 | $ | 39,810 | | | $ | 36,337 | |
| 製品の中で | 28,853 | | | 35,182 | |
| 完成品 | 27,400 | | | 27,031 | |
| 合計する | $ | 96,063 | | | $ | 98,550 | |
Pacira BioSciences,Inc.|2022 Form 10-K|第F-21ページ
カタログ表
Pacira生物科学社は
連結財務諸表付記
注7-固定資産
主要カテゴリ別にまとめた固定資産純資産額には、以下が含まれる(千単位) | | | | | | | | | | | |
| | 十二月三十一日 |
| | 2022 | | 2021 |
| 機械と設備 | $ | 118,684 | | | $ | 117,264 | |
| 賃借権改善 | 61,302 | | | 59,740 | |
| コンピュータ装置及びソフトウェア | 15,360 | | | 13,197 | |
| オフィス家具と設備 | 2,420 | | | 2,883 | |
建設中の工事(1) | 103,226 | | | 80,557 | |
| 合計する | 300,992 | | | 273,641 | |
| 減算:減価償却累計 | (117,480) | | | (85,240) | |
| 固定資産、純額 | $ | 183,512 | | | $ | 188,401 | |
(1) ドルの上昇幅22.7建設中の100万ドルは、カリフォルニア州サンディエゴにある科学センターパークのEXPAREL生産能力拡張プロジェクトや、イギリスのスウェンデンにあるThermo Fisher Science Pharma ServicesサイトのZILRETTA資本プロジェクトなど、会社の製造施設の拡張進展と関係がある。 |
資産種別別の耐用年数に関する情報は、付記2、重要会計政策の概要を参照されたい。
2022年12月31日現在、2021年と2020年12月31日までの減価償却費用は34.2百万、$15.0百万ドルとドル12.0それぞれ100万ドルです当社は2022年、2021年および2020年12月31日までの年間で、利息を$に資本化します4.1百万、$3.9百万ドルとドル2.4それぞれ100万ドルです2022年に同社は加速しました10.5その将来の経済効果が確定していないいくつかの機械と設備の減価償却費用は百万ドルである。
総固定資産純額は、2022年12月31日と2021年12月31日まで、リース改善と米国国外に位置する製造プロセス設備を含み、金額は$44.7百万ドルとドル65.4それぞれ100万ドルです
2022年12月31日と2021年12月31日まで、同社のAROは$3.3百万ドルとドル2.4その総合貸借対照表の計上すべき支出および他の負債にそれぞれ百万ドルを計上し、いくつかの賃貸契約終了後に賃貸空間を元に戻す関連費用を支払う。
Pacira BioSciences,Inc.|2022 Form 10-K|第F-22ページ
カタログ表
Pacira生物科学社は
連結財務諸表付記
注8-賃貸借証書
同社はカリフォルニア州サンディエゴの科学センターパークにあるEXPARELとiovera°携帯電話製造施設を含むすべての施設をレンタルしている。同社はまた,Thermo Fisher Science Pharma Servicesとイギリスのスウェンデンに位置する製造施設を用いた埋め込み賃貸契約を締結している。関連する毎月の基本費用の一部は相対的に公正な価値によってレンタル構成要素に分配された
施設の運営リースコストには、公共エリアメンテナンスや他の一般的な運営費用、保険や不動産税などのレンタルや非レンタル部分の実行可能コストが含まれている総運営リースコストは以下の通り(千単位): | | | | | | | | | | | | | | | | | | | | |
| | 十二月三十一日までの年度 |
| リースコストを経営する | | 2022 | | 2021 | | 2020 |
| 固定リースコスト | | $ | 13,949 | | | $ | 11,976 | | | $ | 10,055 | |
| 可変リースコスト | | 1,988 | | | 1,722 | | | 2,096 | |
| 転貸収入 | | (253) | | | — | | | — | |
| 合計する | | $ | 15,684 | | | $ | 13,698 | | | $ | 12,151 | |
経営リースに関する補足キャッシュフロー情報は以下の通り(千計): | | | | | | | | | | | | | | | | | | | | |
| | 十二月三十一日までの年度 |
| | 2022 | | 2021 | | 2020 |
| レンタル負債経営のための現金は、レンタルインセンティブ後の純額を差し引かれます | | $ | 14,357 | | | $ | 12,709 | | | $ | 14,347 | |
| 賃貸義務と引き換えに記録された使用権資産 | | $ | 3,324 | | | $ | 8,692 | | | $ | 42,191 | |
重み付き平均残存賃貸期間と加重平均割引率の要約は以下のとおりである | | | | | | | | | | | | | | |
| | 十二月三十一日 |
| | 2022 | | 2021 |
| 加重平均残余レンタル期間 | | 6.83年.年 | | 7.77年.年 |
| 加重平均割引率 | | 7.05% | | 6.96% |
2022年12月31日現在、会社の経営賃貸負債満期日は以下の通り(千計) | | | | | | | | |
| 年.年 | | 未納最低返済額合計 |
| 2023 | | $ | 14,022 | |
| 2024 | | 13,928 | |
| 2025 | | 13,078 | |
| 2026 | | 12,814 | |
| 2027 | | 12,586 | |
| その後… | | 27,350 | |
| 将来のレンタル支払総額 | | 93,778 | |
| 差し引く:推定利息 | | (19,855) | |
| リース負債総額を経営する | | $ | 73,923 | |
Pacira BioSciences,Inc.|2022 Form 10-K|第F-23ページ
カタログ表
Pacira生物科学社は
連結財務諸表付記
注9-商業権と無形資産
商誉
会社の営業権は2007年にSkyePharma Holding,Inc.(現在Vectura Group plcの子会社)あるいはSkyePharmaからPacira PharmPharmticals,Inc.(“SkyePharmaを買収”)、2019年にMyoScienceを買収し、2021年にFlexionを買収することに由来する当社の営業利益の帳簿価値の変動概要は以下の通り(千計) | | | | | | | | |
| | 帳簿価値 |
| 2020年12月31日残高 | | $ | 99,547 | |
| SkyePharmaを買収して得たマイルストーンによる名声 | | 36,000 | |
| Flexionの買収による営業権 | | 9,628 | |
| 2021年12月31日の残高 | | 145,175 | |
| Flexity買収に関する見積期間調整による営業権(付記5) | | 18,068 | |
| 2022年12月31日の残高 | | $ | 163,243 | |
SkyePharmaの買収は財務会計基準141の声明に基づいて計算された企業合併の会計処理買収の日に発効するGAAP規格である。SkyePharmmaの買収について、同社はEXPARELを含むDepoBupivacaine製品に何らかの記念碑的な支払いを支払うことに同意した。2021年第4四半期にSkyePharmaのため、会社は残りの2つのマイルストーンを実現しました:$4.02021年第4四半期にイギリス、フランス、ドイツ、イタリア、またはスペインで初めて商業販売されたときに支払われた100万ドル32.0年間純売上高は百万ドルに達した500.0このお金は2022年第1四半期に支払われた。これらの記念碑的な支払いはSkyePharmma買収の補完とされているため、商標として記録されている
Flexion買収時、会社が記録した営業権総額は$9.6百万ドルです。Flexion買収日から1年間、試算期間は$に調整されます18.1事実と状況が買収日前に存在していたため、百万ドルが営業権に計上された。このような調整は主に税務研究と買収前の費用を達成することだ。取得された商標権と無形資産は納税時に控除されてはいけない。
無形資産
無形資産純資産には、Flexion買収から開発された技術と知的財産権の研究開発、MyoScience買収から開発された技術と顧客関係があり、以下のようにまとめられる(千ドル単位)
| | | | | | | | | | | | | | | | | | | | | | | | | | |
| 2022年12月31日 | | 毛収入
帳簿価値 | | 積算
償却する | | 目に見えない
資産、純額 | | 加重平均
有用な寿命 |
| 発達した技術 | | $ | 590,000 | | | $ | (84,376) | | | $ | 505,624 | | | 10年5ヶ月 |
| 取引先関係 | | 90 | | | (34) | | | 56 | | | 10年.年 |
| 有限寿命無形資産総額、純額 | | 590,090 | | | (84,410) | | | 505,680 | | | |
| 買収した知的財産権の研究開発 | | 34,866 | | | — | | | 34,866 | | | |
| 無形資産総額,純額 | | $ | 624,956 | | | $ | (84,410) | | | $ | 540,546 | | | |
| | | | | | | | |
| 2021年12月31日 | | 毛収入
帳簿価値 | | 積算
償却する | | 目に見えない
資産、純額 | | 加重平均
有用な寿命 |
| 発達した技術 | | $ | 590,000 | | | $ | (27,097) | | | $ | 562,903 | | | 10年5ヶ月 |
| 取引先関係 | | 90 | | | (25) | | | 65 | | | 10年.年 |
| 有限寿命無形資産総額、純額 | | 590,090 | | | (27,122) | | | 562,968 | | | |
| 買収した知的財産権の研究開発 | | 61,000 | | | — | | | 61,000 | | | |
| 無形資産総額,純額 | | $ | 651,090 | | | $ | (27,122) | | | $ | 623,968 | | | |
2022年12月31日までと2021年12月31日までの無形資産償却費用は57.3百万ドルとドル13.6それぞれ100万ドルです2022年費用の増加はZILRETTAに関する年間償却の結果であり,ZILRETTAは2021年11月に膝屈曲買収の一部であり,膝関節炎痛の治療に用いられている。
Pacira BioSciences,Inc.|2022 Form 10-K|第F-24ページ
カタログ表
Pacira生物科学社は
連結財務諸表付記
これらの無形資産の帳簿総額は変わらないと仮定すると、将来推定される有限寿命無形資産の償却費用は#ドルとなる57.32023年から2030年まで37.42031年には100万ドルです7.92032年には100万ドルです2.22033年には100万に達する。
当社は毎年無期限無形資産の減値を審査し,無期限無形資産の帳簿価値が回収できない事件や状況変化に直面していることを示す評価を行っている。ZILRETTAが買収した肩骨性関節炎痛に対するIPR&Dの年次減値評価は,2022年12月31日までに2022年12月31日までに回復可能性テストにより比較した60.0割引キャッシュフローモデルを通じて資産帳簿価値百万ドルと公正価値を比較した33.9百万ドルは新しい事実と状況に基づいている。公正価値の変化は主に遅い臨床試験の完成スケジュールが収入予測に影響するなどの要素である。減価$26.12022年12月31日までの年度の総合経営報告書のうち、百万元が買収関連費用(収益)、減値及びその他の項目で確認されたのは、以前の額面が更新後の公正価値を超えた金額で計算される。
付記10-費用を計算する
計算すべき費用には、以下の項目が含まれる | | | | | | | | | | | |
| | 十二月三十一日 |
| | 2022 | | 2021 |
| 販売費用、一般費用、行政費用を計算しなければなりません | $ | 11,927 | | | $ | 12,063 | |
| 研究と開発費用を計算すべきである | 4,065 | | | 5,480 | |
| その他は営業費用を計算します | 14,959 | | | 14,912 | |
報酬と福祉 (1) | 26,198 | | | 45,491 | |
終業料(2) | 13,000 | | | — | |
| | | |
課税税(3) | 3,400 | | | 35,298 | |
| 応算利息 | 8,941 | | | 5,358 | |
| 返品と卸サービス料 | 7,295 | | | 8,953 | |
| 合計する | $ | 89,785 | | | $ | 127,555 | |
(1)給与·福祉は2021年12月31日現在#ドルを含む18.4Flexion買収に関連した解散費は100万ドルである。
(2)付記20を参照引受金とその他の事項もっと多くの情報を知ります。
(3)2021年12月31日現在、特許権使用料には$が含まれている32.02021年第4四半期にSkyePharmaに支払った百万ドルの記念碑的支払いは、年間純売上高ドルを実現しました500.0同社のDepoBupiacaine製品はEXPARELを含め、100万ドルの価値がある。このマイルストーンは2022年第1四半期に発生した。注9を参照商誉と無形資産もっと情報を知っています.
注11-債務
当社の未済債務の帳簿価値の概要は以下の通りです(千計)
| | | | | | | | | | | |
| 十二月三十一日 |
| 2022 | | 2021 |
| 2026年12月期の定期ローンBローン | $ | 284,704 | | | $ | 359,497 | |
0.7502025年8月に期限が切れた換算優先手形の割合 | 396,126 | | | 330,627 | |
3.3752024年5月に満期になった変換可能優先チケットの割合 | 8,641 | | | 201,249 | |
2.3752022年4月期の転換可能優先手形の割合(1) | — | | | 157,857 | |
| 合計する | $ | 689,471 | | | $ | 1,049,230 | |
(1)2022年に発行された債券(以下、定義)は2022年4月1日に満期となった。
Pacira BioSciences,Inc.|2022 Form 10-K|第F-25ページ
カタログ表
Pacira生物科学社は
連結財務諸表付記
定期ローンBローン
二零二一年十二月、当社は行政代理及び初期融資者であるモルガン大通銀行と定期融資信用協定(“信用協定”)を締結した。信用協定に基づく定期融資(“定期融資”)は3%割引と、#ドルの元金単一のプリペイドローンBローンを可能にします375.0当社および各付属保証人のほとんどの資産を抵当にした。いくつかの条件の規定の下で、当社は、いつでも1回または複数回、1つまたは複数の新しい定期融資カテゴリを追加することができ、および/または1つまたは複数の増分定期融資を申請することによって、任意の既存カテゴリの融資元金金額を増加させることができる。定期ローンの純収益は約#ドル363.8元の発行割引$を差し引いた百万ドル11.2百万ドルです。
定期融資の総債務構成は以下のとおりである(単位:千): | | | | | | | | | | | |
| 十二月三十一日 |
| 2022 | | 2021 |
| 2026年12月に満期となる定期ローン | $ | 296,875 | | | $ | 375,000 | |
| 繰延融資コスト | (3,919) | | | (4,443) | |
| 債務割引 | (8,252) | | | (11,060) | |
| 債務総額、債務割引と繰延融資コストを差し引く | $ | 284,704 | | | $ | 359,497 | |
| | | |
| | | |
| | | |
| | | |
定期ローンは2026年12月7日に満期になり、四半期ごとに元金1ドルの返済を要求する9.42022年6月30日から$に増加14.12025年12月31日から100万ドル、残りのバルーン支払いは約$137.5満期の百万ドル。当社は、(I)当社の任意の財政年度に存在する超過現金流量(信用協定の定義を参照)、及び当該財政年度の高級担保レバレッジ率(信用協定の定義参照)がいくつかの所定の限度額を超える(Ii)非一般課程資産売却及び事故の純収益(信用協定の定義を参照)及び(Iii)債務を発行して得られた金(クレジット協定下の許可債務を除く)から元金を強制的に前払いしなければならない。定期ローンの繰り上げ返済罰金は2最初のローン年度の%と利息を加えて全額支払います22つ目のローン年度には13番目のローン年度は%で、その後はなくなりました。事前返済罰は、一般に、超過キャッシュフローにより満期になった早期返済など、信用協定項下の強制的な早期返済義務には適用されない。当社は2022年12月31日までに予定通り元金$を支払いました28.1合計百万ドルになります。また、2022年12月31日までの年間で、当社は#ドルを追加前払いしました51.0100万ドルで1ドルも含まれています50.0元金は100万ドル減少し1.0その繰延融資コストの一部として記録されている百万早期返済罰金は、予想される利息支出に計上される。
定期融資要求会社は,その他の事項を除いて,(I)任意の財政四半期の最終日に決定された第1留置権純レバー率が高くない1.751.00までおよび(Ii)流動資金はいつでも少なくとも$である150.0百万ドルです。融資期間には、慣用的な肯定と否定契約、金融契約、陳述と担保、違約事件、その他の条項も含まれる。当社は2022年12月31日現在、信用協定下のすべての財務契約を遵守している。
当社は定期基準借入または予備基準金利借入を選択することができます。定期基準借入金は調整後期限SOFR金利(信用協定の定義参照)変動年利で利下げ(受け)75基点下限に適用の限界を加える700基点。予備基本金利借款基本金利を使用して決定された可変年利利息(受け)175基点下限)は、(I)この日に発効する最優遇金利(クレジット協定の定義参照)、(Ii)NYFRB金利(クレジットプロトコル参照)プラスに等しい50基点または(Iii)クレジット協定で定義されているように、調整後の期限SOFR金利を追加する100基点は,ある例外的な場合を除いて別途適用されるものである600基点。2022年12月31日現在、定期借款下の借入金はすべて定期基準借入金で構成されており、金利は10.78%.
2025年満期の転換可能優先手形
2020年7月に会社は方向性増発を完了し、資金を募集して402.5元金総額は百万ドルである0.7502025年に満期された転換可能優先手形の割合、または2025年手形について、2025年手形についてComputerShare Corporation Trust,N.A.(前身はWells Fargo Bank,N.A.)または2025 Indentureについて契約を締結する。2025年に発行される債券は、固定資産率は0.750年利%は,半年ごとに支払い,2月1日に延滞するST八月一日とST2021年2月1日から、毎年。2025年に発行される債券は2025年8月1日に満期になる
Pacira BioSciences,Inc.|2022 Form 10-K|第F-26ページ
カタログ表
Pacira生物科学社は
連結財務諸表付記
2025年債の債務総額は以下の通り(千で計算) | | | | | | | | | | | |
| 十二月三十一日 |
| 2022 | | 2021 |
0.7502025年8月に期限が切れた換算優先手形の割合 | $ | 402,500 | | | $ | 402,500 | |
| 繰延融資コスト | (6,374) | | | (7,155) | |
| 債務割引 | — | | | (64,718) | |
| 債務総額、債務割引と繰延融資コストを差し引く | $ | 396,126 | | | $ | 330,627 | |
| | | |
| | | |
| | | |
| | | |
2025年債発行による純額は約$390.0百万ドル、手数料と会社が支払った発売費用を差し引いた。会社は2025年に債券を発行して得られた純額の一部をドルの買い戻しに使う185.0当時未返済の元金の総額は百万ドルだった2.3752022年に私的協議の取引で満期になった転換可能な優先手形の割合、総額は$211.1百万の現金(課税利息を含む)。同社の取引コストは約$である12.52025年債発行に関連した百万ドルを利子支出に償却する5年制2025年債券の期限
所有者は、2025年2月3日前の営業日営業終了直前のいつでも、以下の場合、(I)任意のカレンダー四半期(かつ、このカレンダー四半期期間のみ)、会社の普通株式の最後の報告販売価格が少なくとも20以下の期間内の取引日(連続の有無にかかわらず)30前のカレンダー四半期の最終取引日に終了した連続取引日以上130適用される取引日ごとの株式交換価格の割合5人-次のイベント直後の営業日5人連続取引日期間(“精算期間”)は,算定期間の取引日ごとに,1,000ドルあたりの手形元金の取引価格(“2025年契約”と定義)を下回っている98(I)当社が最近公表した普通株販売価格の積の%と当該取引日毎の換算率と、(Iii)自社の全部またはほぼすべての資産の合併または売却を含む指定された会社事項の発生、または(Iv)当社が2025年債の償還を要求した場合、償還日直前の営業日の営業時間が終了するまで。2022年12月31日までのカレンダー四半期では、転換条件が満たされていない。
2025年2月3日以降、2025年8月1日までの第2の予定取引日の取引が終了するまで、保有者は2025年債を随時転換することができる。
転換後、保有者は2025年の債券の元本金額と任意の残りの転換価値を受け取り、これらの価値は1株当たりの出来高加重平均価格に基づいて計算される40観察期間内の連続取引日(2025年契約でより全面的に記述されているように)。元本と超過転換価値については、保有者は会社の選択に応じて、現金、会社普通株または現金と会社普通株の組み合わせを得ることができる。2025年債券の予備為替レートは1,000元当たり元金13.9324株で、初期両替価格1,000ドルに相当する71.78一株の会社普通株です。転換率は場合によっては調整されるが、任意の計算および未払い利息については調整されない。2025年債券の予備交換株価プレミアムは約32.5%から終値$54.172020年7月7日、すなわち会社が2025年債の非公開発行定価の日に、会社普通株のナスダック世界選りすぐり市場での1株当たり収益。
2022年12月31日現在、2025年債券の市場価格は1,000ドル当たり元金908ドルである。転換すると、保有者はすべての未来の利息支払い、いかなる未返済の応算利息、株価がさらに値上がりする可能性を放棄する。転換請求を受けた後、2025年契約の条項に基づいて2025年債券の決済金を支払う。もしすべての2025年に発行された債券がすべて転換すれば、会社は$を返済しなければならない402.5現金と普通株の任意の組み合わせの元本価値と任意の転換プレミアム(当社が選択)。
2023年8月1日までに、会社は2025年債を償還しない可能性がある。2023年8月1日またはその後日(ただし、すべての未返済の2025年債を償還する場合は、遅くはありませんこれは…。満期直前の予定取引日)には、会社普通株の最終報告販売価格(2025年契約と定義)が少なくとも達成されていれば130当時有効な変換価格の割合は、少なくとも(I)に適用される20任意期間の取引日(連続するか否かにかかわらず)30(I)当社が償還通知日の直前の取引日及び(Ii)当社が償還通知日の直前の取引日に関する連続取引日を発行するまで。償還価格は(I)の和になる100償還されている2025年債券元金の%は、別途(Ii)を加算して計算及び未払い利息を含めて支払う(ただし含まれていない)
Pacira BioSciences,Inc.|2022 Form 10-K|第F-27ページ
カタログ表
Pacira生物科学社は
連結財務諸表付記
償還日。また、償還2025年期手形は、“完全に根本的な変化”(2025年契約で定義されているように)を構成し、場合によっては、償還に関連してこれらの手形を変換すると、そのような手形に適用される換算率が増加する場合がある。2025年に発行された債券は債務超過基金は設けられていない。
もし会社がある条件を満たしている場合、“2025年契約”で定義されているように根本的に変化した場合、2025年債券保有者は、2025年債券の全部または一部を現金で買い戻すことを要求することができ、買い戻し価格は100購入した2025年期債券元金の%に、基本変動買い戻し日(ただし含まない)の応計及び未払い利息を加算する。また、2025年8月1日までに重大な変更が発生した場合、当社はそのチケットを転換することを選択した所持者の為替レートを上げる場合もあります。
2025年債券は当社の一般的な無担保債務であり、支払権はその全債務よりも優先されるが、2025年手形の返済権は2025年手形に明確に従属しているが、支払権は自社の無担保債務と等しい。2025年債の支払権も、実際には、当該債務等の担保を提供する資産価値を限度とし、かつ、当社子会社に構造的に従属する任意の債務又は他の債務(貿易売掛金を含む)であれば、当社の任意の担保債務を下回っている。
2025年手形は現在、会社が2022年12月31日までの総合貸借対照表で長期債務に分類されているが、このような負債の将来の両替性とそれによって生じる貸借対照表の分類は、四半期報告日ごとにモニタリングされ、会社普通株の規定された測定期間の市場価格に基づいて分析される。2025年手形の所有者が、所定の計量期間内の任意の時間に2025年手形を転換する権利がある場合、2025年手形は流動債務とみなされ、このように分類される。
2022年1月1日までに、従来のASC 470-20によると、転換やその他のオプションを持つ債務転換可能な債務ツールの負債と資本部分とを別々に計算するためのエンティティであって、変換時に発行者の経済的利息コストを反映する変換可能な債務ツールの全部または一部が現金で決済される可能性があるエンティティ。この手形の負債部分の過去の推定方式は,類似した変換不可能手形の発行日における市場金利を反映している.負債部分の初期帳簿価値は#ドルである314.7百万は使っています5.78借入金利を%とする。#ドルの持分部分87.8転換選択権を代表する百万ユーロは、2025年手形の額面から負債部分の公正価値を差し引くことで決定され、発行日に総合貸借対照表に追加実収資本を計上する。株式部分は過去に2025年期手形負債部分の割引とみなされていた5年制2025年債券の期限は実質金利法を採用する
ASC 470-20はASU 2020-06に由来し、2022年1月1日から改訂され、単独計算と債務不明確と密接に関連する組み込み式転換特徴の要求を取り消し、これらの特徴は派生商品の定義に符合し、派生商品会計と発行された転換可能債務ツールの範囲例外に符合せず、これらのツールの保険料記録は資本で支払う。2022年1月1日から、2025年債券割引帳簿額面は64.7100万ドルが淘汰されました1.7繰延融資コストは百万ドル増加し、追加の実収資本、累積赤字と繰延税金資産から相殺される。ASU 2020-06を採用した詳細については、注釈3を参照されたい重要な会計政策の概要.
2025年債券にはいかなる財務や経営契約も含まれておらず、会社の配当金の支払い、他の債務の発行、証券の発行または買い戻しに対するいかなる制限も含まれていない。2025年債には、何らかの違約事件が発生すると、2025年債の100%元本および未払い利息が自動的に満期になって支払うことが含まれる2025年債に関する慣例違約事件が含まれている。
Flexion買収から想定される2024年満期の転換可能優先手形
Flexionの買収に先立ち,Flexionは2017年5月に合計ドルの債券を発行した201.3百万ドルの元金3.375%が2024年に満了する転換可能優先チケット(“Flexion 2024チケット”)は、日付が2017年5月2日の契約(“元Flexion Indenture”)に基づいて、FlexionとComputerShare Corporation Trust,N.A.(前Wells Fargo Bank,N.A.)を受託者(“Flexion受託者”)とし、日付を2021年11月19日とする第1の補足契約(“最初の補足Flexion Indenture”、元のFlexion Indenture,“Flexion Indenture”)を補助する。Flexion 2024手形の満期日は2024年5月1日で、無担保で、計算すべき利息は3.375年利%は、半年ごとに支給され、日付は毎年5月1日と11月1日です。Flexion買収時には、元本は当社が負担し、公正価値で入金されます。
Pacira BioSciences,Inc.|2022 Form 10-K|第F-28ページ
カタログ表
Pacira生物科学社は
連結財務諸表付記
Flextion 2024年手形の転換時には、その所持者ごとの選択の下で、各Flexon 2024年手形は、Flexionの選択に従って現金、Flexionの普通株またはそれらの組み合わせに変換することができ、変換率は$1,000 Flex2024年手形あたりの元金約37.3413株のFlexion普通株であり、これは約$の初期転換価格に対応する26.781株当たりFlexionの普通株。Flexion買収の結果として、通知(定義は後述)に関連して、Flexion 2024債券の所有者は、以下に述べるように、Flexion買収に関連するいくつかの転換および買い戻し権利を得る権利がある。さらに、Flexion買収の結果として、以下でより詳細に議論されるように、任意の未来の転換権は、任意の未来の事件の発生に依存して、Flexion義歯項下のこのような転換権を生成する。
二零二一年十二月六日、Flexion買収事項及びFlexion Indentureにより、FlexionはFlexion 2024債券保有者に基本的な変更会社の通告及び要約購入(“この通知”)を提供し、そして発行されていないすべてのFlexion 2024債券を現金で買い戻すことを提出し、買い戻し価格は現金と同じである100買い戻しのFRANSION 2024債券本金額の%は、2022年1月7日(ただし含まない)の課税及び未払い利息を別途加算するが、当該等の債券に記載されている条項及び条件規定の制限を受けなければならない。購入要約は2022年1月6日のニューヨーク時間午後5時に期限が切れます。
いかなる所有者も通知条項に基づいてその買い戻し権利を行使していない場合は,その所持者が指屈曲契約によって発行した屈指2024手形に関連する転換権を保持する.Flexion買収による基本的な変動および全体の基本的な変動(Flexion Indentureの定義を参照)によってFlexion 2024債券を転換する場合、Flexion 2024債券の1,000元あたりの元金は(I)$に両替できる317.40現金及び(Ii)37.3413CVRは、37.3413の転換率に基づいて、ニューヨーク市時間2022年1月7日午後5:00までである。代替的に、所有者は、そのFlexion 2024チケットを保持することができ、Flexity 2024チケットは、Flexity 2024チケットの利息支払いを受け取る権利があり、Flexion Indentureによって生成される可能性のある任意の将来の両替権利を行使する権利を含む、その既存の条項の規定の下で返済されないであろう。
2022年1月7日、買収要約が満期になった後、会社はドルを受け入れた192.6有効入札済み(および有効撤回されていない)の屈曲2024年債元金総額は百万元である。通知に関連する曲げられた2024チケットの変換はない。2022年12月31日現在、未返済元金残高は$8.6百万ドルです。
2022年満期の転換可能優先手形
2017年3月、会社は方向性増発を完了し、資金を募集した345.0元金の総額は百万元である2.3752022年満期の転換可能優先手形の割合、または2022年の手形、2022年の手形について契約を結ぶ。2022年に発行される債券の固定利息率は2.375年利%は、半年ごとに支払い、4月1日に延滞しますST十月一日とST一年ごとです。2020年7月に、会社は2025年の債券発行で得られた純額の一部を買い戻しに使用する$185.02022年債の元本総額は百万元で、個人合意取引方式で行われ、総額は211.1百万の現金(課税利息を含む)。2022年債の一部買い戻しの結果8.12020年12月31日までの年度の早期返済債務は百万元の損失を計上している。
2022年債の総債務構成は以下の通り(単位:千): | | | | | | | | | | | |
| | 十二月三十一日 |
| | 2022 | | 2021 |
2.3752022年4月期の転換可能優先手形の割合 | $ | — | | | $ | 160,000 | |
| 繰延融資コスト | — | | | (223) | |
| 債務割引 | — | | | (1,920) | |
| 債務総額、債務割引と繰延融資コストを差し引く | $ | — | | | $ | 157,857 | |
2022年4月1日、2022年債券が満期になり、会社は余剰元金残高を清算する$160.0100万ドルをプレミアムに換算します4.8現金で100万ドル払う156.9100万ドルを発行しています101,521会社の普通株は、追加の実収資本を増加させた$3.0百万ドルです。
Pacira BioSciences,Inc.|2022 Form 10-K|第F-29ページ
カタログ表
Pacira生物科学社は
連結財務諸表付記
利子支出
以下の表に列報期間中に確認された利息支出総額(千ドル単位)を示す | | | | | | | | | | | | | | | | | |
| 十二月三十一日までの年度 |
| 2022 | | 2021 | | 2020 |
| 契約とその他の利子支出 | $ | 36,880 | | | $ | 9,759 | | | $ | 7,650 | |
| 債務発行原価償却 | 4,400 | | | 2,754 | | | 2,156 | |
| 債務割引償却 | 2,807 | | | 23,152 | | | 18,254 | |
資本化利息その他(付記7) | (4,111) | | | (3,915) | | | (2,389) | |
| 合計する | $ | 39,976 | | | $ | 31,750 | | | $ | 25,671 | |
| | | | | |
| 総債務の実利率 | 5.47 | % | | 6.66 | % | | 7.15 | % |
ASU 2020-06を採用して2022年1月1日に施行された後、会社は2022年手形と2025年手形に関する転換可能な債務割引を廃止し、これらの割引は最初に株式で確認された組み込み変換機能の相殺として記録された。2022年1月1日から、会社は以前に記録された転換可能債券割引の利息支出を記録することはなく、これらの割引は変換可能機能に起因することができる。以前転換機能に割り当てられていた繰延融資コストは未返済債務に再分配された。ASU 2020-06を採用した詳細については、注釈3を参照されたい重要な会計政策の概要.
付記12-金融商品
公正価値計量
公正価値は、秩序ある取引において資産を売却するか、または元金または最も有利な市場で負債を移動させて得られる価格として定義される。公正価値計量の一致性と比較可能性を高めるために、財務会計基準委員会は三級階層構造を構築し、公正価値を計量する時に観察可能な投入を最大限に使用し、使用が観察できない投入を最大限に減少することを要求した。公正価値計測の3つのレベルは
•レベル1:資産または負債が計量された日に得られる活発な市場オファー(調整されていない)。公正価値階層構造は1レベル投入最高優先度を与える.
•第2レベル:投入の観察可能価格に基づいて,これらの投入は活発な市場オファーはなかったが,市場データの実証を得た。
•第3レベル:市場データが少ない場合やない場合に使用される観察不可能な入力。公正価値階層構造は、最低優先度を第3レベル投入に割り当てる。
これらの項目の短期的な性質により,現金および現金等価物,売掛金および売掛金を含む金融商品の帳簿価値はそれぞれの公正価値に近い.同社の転換可能優先手形の公正価値は,これらの手形の場外取引市場(第2級)の市場見積を利用して計算される.当社の買収関連又は対価のある公正価値は、公正価値に応じて恒常的に報告されています(第3級)。いつでも公正価値を決定することができない交換可能手形の帳簿金額は可視取引の減値或いは上方或いは下方調整によって調整されていないが、1つの株式投資は2022年12月31日までの年度に完全に減少した
Pacira BioSciences,Inc.|2022 Form 10-K|第F-30ページ
カタログ表
Pacira生物科学社は
連結財務諸表付記
2022年12月31日現在、会社の金融資産と負債の帳簿価値と公正価値は以下の通り(千計)
| | | | | | | | | | | | | | | | | | | | | | | | | | |
| | 携帯する
価値がある | | 公正価値計量使用 |
| | | レベル1 | | レベル2 | | レベル3 |
| 公正な価値で日常的に計量された金融資産と金融負債: | | | | | | | | |
| 金融資産: | | | | | | | | |
| 株式投資 | | $ | 15,877 | | | $ | — | | | $ | — | | | $ | 15,877 | |
| 受取転換可能な手形 | | $ | 5,315 | | | $ | — | | | $ | — | | | $ | 5,315 | |
| 財務負債: | | | | | | | | |
| 買収に関連しているか,あるいは掛け値がある | | $ | 28,122 | | | $ | — | | | $ | — | | | $ | 28,122 | |
| | | | | | | | |
| 余剰コストで計量された財務負債: | | | | | | | | |
| 2026年12月期の定期ローンBローン | | $ | 284,704 | | | $ | — | | | $ | 292,422 | | | $ | — | |
0.7502025年までに換算可能な優先手形の割合 (1) | | $ | 396,126 | | | $ | — | | | $ | 365,269 | | | $ | — | |
3.3752024年満期の変換可能優先チケットの割合(2) | | $ | 8,641 | | | $ | — | | | $ | 8,641 | | | $ | — | |
(1) ナスダック世界ベスト市場によると、同社の普通株の終値はドルだ38.612022年12月31日の1株当たり収益、換算価格は$71.78一株ずつです。2022年12月31日、持ち株価格が株価を上回ったため、転株条件はまだ達成されていない。2022年12月31日に満期となる2025年債の最高転換プレミアムは約5.6100万株の会社普通株は、ある事件の転換率が増加しないと仮定する。
(2)“屈曲2024”紙幣に関係する。詳細については付記11を参照されたい債務.
いくつかの資産及び負債は、公正価値に応じて非日常的な基礎に計量され、業務合併で取得した資産及び負債及び長期資産が含まれており、減価とみなされたり、販売待ち資産に再分類されたりすれば、公正価値で確認される。このような場合の公正な価値は第3レベルの投入を使用して決定されるだろう。
公正な価値に応じて恒常的に計量された金融資産と負債
株式と転換可能手形投資
同社は株式と転換可能な手形投資の形式で、臨床と臨床前段階の個人持株生物技術会社に対して戦略投資を行った以下の投資は、容易に決定可能な公正価値を有さず、コストから減値(ある場合)に、同じまたは同様の投資の観察可能な価格変化(千単位で)を加算または減算する
| | | | | | | | | | | | | | | | | | | | |
| | 株式投資 | | 転換可能な受取手形 | | 合計する |
2020年12月31日残高 | | $ | 12,802 | | | $ | — | | | $ | 12,802 | |
| 購入 | | 12,967 | | | 4,220 | | | 17,187 | |
| 剥離投資 | | (11,642) | | | — | | | (11,642) | |
| 外貨調整 | | — | | | (88) | | | (88) | |
2021年12月31日の残高 | | 14,127 | | | 4,132 | | | 18,259 | |
| 購入 | | 11,750 | | | 1,250 | | | 13,000 | |
| 減損する | | (10,000) | | | — | | | (10,000) | |
| 外貨調整 | | — | | | (67) | | | (67) | |
2022年12月31日の残高 | | $ | 15,877 | | | $ | 5,315 | | | $ | 21,192 | |
年末までに年度を終える2022年12月31日、1つの株式投資減価$10.0100万ドルを他の純額に記録しています連結業務報告書にあります。
Pacira BioSciences,Inc.|2022 Form 10-K|第F-31ページ
カタログ表
Pacira生物科学社は
連結財務諸表付記
2021年12月31日までの年間で,会社は持分投資を売却し,現金収益純額は$とした9.1100万ドルで損失を達成したことを確認します2.6連結業務報告書には他の純額の100万ドルを記入する。剥離株式投資の公正価値は一級投入を基礎とする。
2023年2月、同社は$を投資した4.0百万ドルの受取転換手形です。
買収に関連しているか,あるいは掛け値がある
会社はFlexion買収とMyoScience買収に関連しているか、または対価格が確認されています。金額は$です28.1百万ドルとドル57.6それぞれ2022年12月31日と2021年12月31日まで。付記5を参照してください屈曲する 採掘する18を付記して買収に関連する費用(収益)、減価その他、より多くの情報を得るために。
当社のまたは有価債務は、その推定公正価値に基づいて入金され、関連または問題が解決される前に、各報告期間内に再評価される。当社では,観察不能投入とモンテカルロシミュレーションに基づく確率重み付き現金フロー法を用いて,価格の公正価値を計測している。これらの投入には、適用される推定確率と、特定の商業および規制マイルストーンを実現する時間と、収入およびコストの推定予測と、将来の支払い現在値を推定するための割引率とが含まれる。重大な変化は、関連する商業および規制イベントを達成する可能性を増加または減少させ、そのようなイベントを達成するのに必要な時間を短縮または延長するか、または推定予測を増加または減少させる可能性がある
2021年11月、当社はFlexionへの買収を完了し、Flexion株主とある株権奨励所有者にCVR関連または対価格を発行し、総金額は$に達することができる372.3特定の規制と商業マイルストーンに到達すれば、100万ユーロに達するだろう。以前の総金額は#ドルでした425.5会社が2022年9月にPCRX-301のさらなる開発を正式に停止することが決定するまで、すでに100万ドルがあった。当社のマイルストーン支払い義務は、2030年12月31日までに実現されるマイルストーンに限られ、60年度業績四半期終了の日数。Flexion買収に関連する買収価格の対価格の一部として、会社は#ドルの対価格を記録しているか、またはある45.2100万ドル、これは規制とビジネスマイルストーンを達成するための会社の潜在的な成果を表している。Flexionを買収した日から2021年12月31日まで、会社は追加のドルを記録した1.2百万の借金この1年の一段落した 2022年12月31日会社は#ドルの収益を記録しました18.3これは主に,連結業務報告書に買収に関する収益として入金されている弾力性や対価格融資期の近未来予測を調整したためである。2022年12月31日、加重平均割引率は15.0%です。期日までに残りの規制マイルストーンを完成させる支払い確率は12.52022年12月31日152021年12月31日。支払い確率の低下は,満期日までに実現される可能性が低下したためである50%から100%臨床試験研究の時間が改訂されたため、規制承認の成功確率が向上しました25%から15%です。2022年12月31日と2021年12月31日現在、Flexion買収に関連するまたは対価負債が$であることが確認された28.1百万ドルとドル46.4それぞれ100万ドルです
2019年4月、会社は合意および合併計画の条項に基づいてMyoScienceの買収を完了し、合意および合併計画は規定されているか、またはマイルストーンの支払い総額は$に達する100.0特定の規制と商業マイルストーンを達成した上で、100万ユーロに達した。当社のマイルストーン支払い義務は、2023年12月31日までに実現されるマイルストーンに限られ、60年度業績四半期終了の日数。2022年12月31日現在、支払い待ちの最大潜在的マイルストーン支払いは$です43.0百万ドルです。2022年12月31日まで、当社は対価収益を確認または有償としています11.22023年12月31日(残りのマイルストーンを実現する期限)までにMyoScienceに到達したり、審議マイルストーンがある可能性が低下したりするため、MyoScienceや審議マイルストーンの実現確率が低下する
当社は2021年12月31日および2020年12月31日までに買収に関する収益を$で確認した2.2100万ドルと買収に関連する費用$5.2これは,それぞれ規制マイルストーンに達する確率と将来予測を改訂した結果であり,これらの予測は総合経営報告書に買収に関する費用(収益)に含まれているためである。2022年12月31日に、まだ達成されていない規制マイルストーンの成功確率はゼロそれは.MyoScience買収に関連する、または対価格負債に関連する公正価値は、2022年12月31日および2021年12月31日までに評価されたゼロそして$11.2それぞれ100万ドルです
Pacira BioSciences,Inc.|2022 Form 10-K|第F-32ページ
カタログ表
Pacira生物科学社は
連結財務諸表付記
次の表には、会社または価格評価に使用される主な仮定が含まれています | | | | | | | | | | |
| 仮に | | 使用時までの屈曲範囲
2022年12月31日 | | |
| 割引率 | | 14.9%から15.1% | | |
| 規制のマイルストーンを実現するためにお金を支払う確率 | | 0%から12.5% | | |
| 規制の節目に達する年が予想されています | | 2030 | | |
当社が第3段階で計量して公正価値で記録した場合や価格変動がある場合は以下の通り(千で計算) | | | | | | | | |
| | あるいは条件がある
考慮事項
公正価値 |
| 2020年12月31日残高 | | $ | 28,346 | |
| Flexity買収に関連しているか、または割引があります | | 45,241 | |
| 価値調整と付加価値を公正に承諾する | | (989) | |
| 支払われた金額または満期金額と相殺される | | (15,000) | |
| 2021年12月31日の残高 | | 57,598 | |
| 価値調整と付加価値を公正に承諾する | | (29,476) | |
| 2022年12月31日の残高 | | $ | 28,122 | |
売却可能な投資
短期投資には、クレジットカードの売掛金を担保とした資産保証証券、投資レベルの商業手形、満期日が3ヶ月を超えるが1年未満の会社、連邦機関、政府債券が含まれる。非流動投資には期限が一年を超えているが三年未満の連邦機関債券が含まれている。会社短期·非流動投資の未実現純損益(信用損失を除く)は他の総合(損失)収益に列報されている。2022年12月31日現在、会社のすべての短期および非流動投資は、販売可能な投資に分類され、観察可能な投入を有する標準業界モデルを使用して公正な価値で計量される二次ツールとして決定されている。商業手形の公正価値は、3ヶ月期の米国国庫券金利を観察可能な入力として使用する標準的な業界モデルに基づいて測定される。資産支援証券と社債の公正価値は主に同じ発行の取引データによって計量或いは実証されているが、関連取引活動は十分に頻繁ではなく、一級投入或いは比較可能証券の投入と見なすのに十分ではない。購入時に、すべての短期および非流動投資は、標準プールによってA級またはそれ以上の格付けに評価された。
Pacira BioSciences,Inc.|2022 Form 10-K|第F-33ページ
カタログ表
Pacira生物科学社は
連結財務諸表付記
以下は、同社の2022年12月31日と2021年12月31日の投資概要(単位:千)である
| | | | | | | | | | | | | | | | | | | | | | | | | | |
2022年12月31日投資: | | コスト | | 毛収入
実現していない
収益.収益 | | 毛収入
実現していない
損 | | 公正価値
(レベル2) |
| 現在: | | | | | | | | |
| 資産支援証券 | | $ | 6,836 | | | $ | — | | | $ | (3) | | | $ | 6,833 | |
| 商業手形 | | 134,423 | | | 23 | | | (386) | | | 134,060 | |
| | | | | | | | |
| アメリカ連邦機関債券 | | 41,971 | | | — | | | (337) | | | 41,634 | |
| アメリカ政府債券 | | 2,003 | | | — | | | (18) | | | 1,985 | |
| 小計 | | 185,233 | | | 23 | | | (744) | | | 184,512 | |
| 現在ではない | | | | | | | | |
| | | | | | | | |
| | | | | | | | |
| | | | | | | | |
| アメリカ連邦機関債券 | | 22,783 | | | 2 | | | (66) | | | 22,719 | |
| アメリカ政府債券 | | 14,499 | | | — | | | (9) | | | 14,490 | |
| 小計 | | 37,282 | | | 2 | | | (75) | | | 37,209 | |
| 合計する | | $ | 222,515 | | | $ | 25 | | | $ | (819) | | | $ | 221,721 | |
| | | | | | | | | | | | | | | | | | | | | | | | | | |
2021年12月31日投資: | | コスト | | 毛収入
実現していない
収益.収益 | | 毛収入
実現していない
損 | | 公正価値
(レベル2) |
| 現在: | | | | | | | | |
| 資産支援証券 | | $ | 3,182 | | | $ | — | | | $ | — | | | $ | 3,182 | |
| 商業手形 | | 57,533 | | | 80 | | | (2) | | | 57,611 | |
| 社債 | | 9,936 | | | 102 | | | — | | | 10,038 | |
| | | | | | | | |
| | | | | | | | |
| | | | | | | | |
| | | | | | | | |
| | | | | | | | |
| | | | | | | | |
| | | | | | | | |
| 合計する | | $ | 70,651 | | | $ | 182 | | | $ | (2) | | | $ | 70,831 | |
2022年12月31日現在、売却可能な投資は何もなく、その償却コストを大きく下回っている。
その会社はその受取利息を売却可能な投資と分けて確認することを選択した。2022年と2021年12月31日に、前払い費用と他の流動資産で確認された受取利息は#ドルです0.8百万ドルとドル0.1それぞれ100万ドルです
信用リスク
会社を集中的な信用リスクに直面させる可能性のある金融商品には、主に現金と現金等価物、短期的および非流動的な売却可能な投資および売掛金が含まれる。当社は高信用品質の金融機関と現金と現金等価物を保持しています。このような金額は連邦保険の限度額を超えるかもしれない。
2022年12月31日までに三つ卸はそれぞれ会社の売掛金の10%以上を占めている34%, 19%和18%です。2021年12月31日までに四つ卸はそれぞれ会社の売掛金の10%以上を占めている30%, 20%, 17%和11%です。その会社の卸に関する情報をもっと知りたいのですが、注2を参照してください重要な会計政策の概要それは.ExPARELおよびZILRETTAの収入は、主に、通常大量の現金資源を有する主要な卸売業者および専門流通業者からのものである。同社はライセンスに基づいてその顧客に対して継続的な信用評価を行い、通常担保を必要としない。当社の売掛金の信用損失準備は、歴史的支払いモデル、現在と推定された将来の経済状況、売掛金の帳簿年齢とそのログアウト履歴に基づいて維持されています。同社は2022年12月31日と2021年12月31日まで注釈売掛金の信用損失に対応して任意の準備を行う必要があると考えられる。
Pacira BioSciences,Inc.|2022 Form 10-K|第F-34ページ
カタログ表
Pacira生物科学社は
連結財務諸表付記
注13-株主権益
普通株
その会社は最も多く発行する権利がある250,000,000普通株、その中で45,927,790そして44,734,308それぞれ2022年12月31日と2021年12月31日に発行され返済されていない。
優先株
その会社は最も多く発行する権利がある5,000,000優先株株違います。優先株は2022年12月31日または2021年に発行または発行される。
その他の総合収入を累計する
以下の表に本報告に示した期間中の会社累計その他総合(赤字)収入残高の変化(千単位)を示す
| | | | | | | | | | | | | | | | | | | | |
| | 純収益を実現していない
売却可能な投資から | | 未実現外貨換算 | | その他の総合収入を累計する |
| 2019年12月31日の残高 | | $ | 322 | | | $ | — | | | $ | 322 | |
| 投資は純損失を実現していない | | (3) | | | — | | | (3) | |
| 外貨換算調整 | | — | | | (1) | | | (1) | |
| | | | | | |
| 2020年12月31日残高 | | 319 | | | (1) | | | 318 | |
投資は赤字純額,税引き後純額を実現していない(1) | | (180) | | | — | | | (180) | |
| 外貨換算調整 | | — | | | 29 | | | 29 | |
| | | | | | |
| 2021年12月31日の残高 | | 139 | | | 28 | | | 167 | |
投資は赤字純額,税引き後純額を実現していない(1) | | (662) | | | — | | | (662) | |
| 外貨換算調整 | | — | | | 115 | | | 115 | |
| | | | | | |
| 2022年12月31日の残高 | | $ | (523) | | | $ | 143 | | | $ | (380) | |
(1)$控除0.2百万ドルとドル0.12022年12月31日までと2021年12月31日までの年度はそれぞれ百万円の税収割引を受ける。
付記14-在庫計画
株式激励計画
当社が改訂して再記述した2011年株式インセンティブ計画、または2011年計画は、最初に2011年6月に取締役会を通過し、株主の承認を経て、2014年6月、2016年6月、2019年6月、2021年6月に改訂された。2021年6月の改正と会社株主の承認により、計画に基づいて株式奨励として発行される普通株式数が増加しました1,500,000株式です。
2011年計画では、奨励的株式オプション、非法定株式オプション、制限株式奨励、およびその他の株式ベースの奨励を付与することが可能になる。2014年4月、会社役員会も2014年インセンティブ計画を採択した。
会社の株式オプション付与の行権価格は,会社普通株の授与日の終値に等しく,通常ある10年間契約期間と増額(通常超過4年自己授権日から、当社は時々異なる帰属条項で株式購入権を授与することができ、非従業員取締役を付与することを含む)。会社は従業員と非従業員取締役にもRSUを授与し,一般に増分形で授与する4年付与された日から,非従業員取締役に付与されたこのような付与は除く。同社は普通株式のライセンスを使用しているが発行されていない株式を使用して、これらの計画に基づいて負担する義務を履行している。
従業員株購入計画
当社が改訂及び再予約した従業員の株購入計画は、最初に2014年4月に取締役会で採択され、2014年6月に当社の株主の許可を得て、2022年6月に改訂及び再記述された。2022年6月の改正案と再記載は、この計画に基づいて売却可能な普通株式数を増加させた500,000最初に提供された500,000株式です。ESPPの目的は
Pacira BioSciences,Inc.|2022 Form 10-K|第F-35ページ
カタログ表
Pacira生物科学社は
連結財務諸表付記
資格のある従業員は割引価格で会社の普通株を購入し、既存の従業員を維持と激励し、新しい人材を誘致するのを助ける。ESPPで最も多いのは1,000,000普通株は販売できます。ESPPは2032年6月に満了する。ESPPは、“米国国税法”(IRC)第423節で指摘された“従業員株式購入計画”に適合することを目的としている。参加者がカレンダー年度内に購入可能な株の最高公平時価は$25,000. 六-毎月の入札期間は、毎年1月1日から7月1日までです。発売期間中、合資格の従業員は、6月30日と12月31日(又は発売期間の最終取引日)に会社普通株を購入することを選択する機会がある。1株あたりの買い入れ価格は等しい85当社の普通株は発売日または購入日(低い者を基準)の公平市価の%に相当します。2022年12月31日までの年間で71,301株はESPPで購入して発行された。
次の表には、2022年12月31日の会社の株式インセンティブ計画に関する情報が含まれています | | | | | | | | | | | | | | | | | | | | |
| 株式激励計画 | | 贈られた賞を保留する | | 賞.賞
発表されました | | 授与可能な賞 |
| 2011年計画 | | 14,431,701 | | | 13,858,585 | | | 573,116 | |
| 2014年インセンティブ計画 | | 175,000 | | | 36,076 | | | 138,924 | |
| 合計する | | 14,606,701 | | | 13,894,661 | | | 712,040 | |
| | | | | | |
| 従業員株購入計画 | | 保留株
購入に用いる | | 株
購入した | | 利用可能な株
購入に用いる |
| ESPP | | 1,000,000 | | | 480,350 | | | 519,650 | |
株に基づく報酬
株式オプションとRSUの補償費用は,直線料金帰納法により必要なサービス期間に確認された報酬の推定付与日公正価値から計算される.ESPPストックオプションの補償費用は、ESPP株の推定付与日公正価値と購入可能な付与日株式数とに基づいており、これは、発売期間の長さにおいて直線料金帰属方法で料金として確認される。
会社が2022年、2022年、2021年、2020年12月31日までの年度総合経営報告書で確認した株式ベースの報酬支出は以下の通り(千計) | | | | | | | | | | | | | | | | | | | | |
| | | 十二月三十一日までの年度 |
| | | 2022 | | 2021 | | 2020 |
| 販売原価 | | $ | 5,967 | | | $ | 5,891 | | | $ | 5,589 | |
| 研究開発 | | 6,594 | | | 5,465 | | | 5,211 | |
| 販売、一般、行政 | | 35,531 | | | 30,890 | | | 29,120 | |
| 合計する | | $ | 48,092 | | | $ | 42,246 | | | $ | 39,920 | |
| | | | | | |
| 株式ベースの報酬は | | | | | | |
| 株式オプション | | $ | 26,800 | | | $ | 25,980 | | | $ | 26,749 | |
| RSU | | 20,310 | | | 15,335 | | | 12,266 | |
| ESPP | | 982 | | | 931 | | | 905 | |
| 合計する | | $ | 48,092 | | | $ | 42,246 | | | $ | 39,920 | |
| | | | | | |
| 関連所得税割引 | | $ | 10,219 | | | $ | 8,989 | | | $ | 8,578 | |
Pacira BioSciences,Inc.|2022 Form 10-K|第F-36ページ
カタログ表
Pacira生物科学社は
連結財務諸表付記
以下の表は、2019年12月31日から2022年12月31日までの株式オプション活動および関連情報をまとめたものです | | | | | | | | | | | | | | | | | | | | | | | |
| 量
株式オプション | | 重みをつける
平均値
相場(1株) | | 加重平均
残り
契約書
期限(年) | | 骨材
内在的価値
(単位:千) |
| 2019年12月31日現在返済しておりません | 6,706,378 | | | $ | 42.80 | | | 7.05 | | $ | 50,652 | |
| 授与する | 1,502,803 | | | 47.50 | | | | | |
| 鍛えられた | (1,428,111) | | | 31.67 | | | | | $ | 34,227 | |
| 没収される | (426,925) | | | 42.08 | | | | | |
| 期限が切れる | (119,027) | | | 71.71 | | | | | |
| 2020年12月31日現在返済していません | 6,235,118 | | | 45.98 | | | 6.97 | | $ | 102,955 | |
| 授与する | 890,277 | | | 60.27 | | | | | |
| 鍛えられた | (732,117) | | | 32.56 | | | | | $ | 23,967 | |
| 没収される | (278,233) | | | 46.46 | | | | | |
| 期限が切れる | (64,505) | | | 80.31 | | | | | |
| 2021年12月31日現在の未返済債務 | 6,050,540 | | | 49.32 | | | 6.59 | | $ | 81,407 | |
| 授与する | 1,061,630 | | | 59.99 | | | | | |
| 鍛えられた | (689,464) | | | 35.37 | | | | | $ | 23,983 | |
| 没収される | (113,506) | | | 54.97 | | | | | |
| 期限が切れる | (36,206) | | | 79.90 | | | | | |
| 2022年12月31日に返済されていません | 6,272,994 | | | $ | 52.38 | | | 6.28 | | $ | 2,011 | |
| 2022年12月31日に行使できます | 4,224,921 | | | $ | 50.51 | | | 5.17 | | $ | 1,997 | |
| 帰属しており、2022年12月31日に帰属する予定です | 6,272,994 | | | $ | 52.38 | | | 6.28 | | $ | 2,011 | |
2022年12月31日までにドル45.4未帰属株式オプションに関する未確認報酬コスト総額は、加重平均中に確認されると予想される2.6何年もです。同社の株式オプションの最大満期日は10年授与の日から効力を発揮する
2022年,2021年および2020年12月31日までに年度に授出された購入権の加重平均公正価値は25.60, $26.74そして$22.40それぞれ1株です付与された株式オプションの公正価値は、ブラック·スコアモデルを用いて以下の加重平均仮定の下で推定される | | | | | | | | | | | | | | | | | | | | |
| | | 十二月三十一日までの年度 |
| ブラック·スコアーズ加重平均仮定 | | 2022 | | 2021 | | 2020 |
| 期待配当収益率 | | ありません | | ありません | | ありません |
| 無リスク金利 | | 1.37% - 4.17% | | 0.43% - 1.21% | | 0.22% - 1.60% |
| 予想変動率 | | 45.1% | | 49.1% | | 53.5% |
| オプションの所期 | | 4.92年.年 | | 5.36年.年 | | 5.36年.年 |
Pacira BioSciences,Inc.|2022 Form 10-K|第F-37ページ
カタログ表
Pacira生物科学社は
連結財務諸表付記
次の表は、2019年12月31日から2022年12月31日までの会社のRSUイベントと関連情報をまとめています | | | | | | | | | | | | | | | | | |
| | 量
限定株単位 | | 重みをつける
平均補助金
期日が公正価値(1株あたり) | | 骨材
内在的価値
(単位:千) |
| 2019年12月31日に帰属していない | 631,141 | | | $ | 41.87 | | | $ | 28,591 | |
| 授与する | 665,476 | | | 48.70 | | | |
| 既得 | (239,085) | | | 41.91 | | | |
| 没収される | (100,079) | | | 44.43 | | | |
| 2020年12月31日に帰属していません | 957,453 | | | 46.34 | | | $ | 57,294 | |
| 授与する | 446,450 | | | 60.81 | | | |
| 既得 | (309,779) | | | 45.16 | | | |
| 没収される | (138,847) | | | 50.67 | | | |
| 2021年12月31日に帰属していません | 955,277 | | | 52.85 | | | $ | 57,479 | |
| 授与する | 621,149 | | | 60.11 | | | |
| 既得 | (331,196) | | | 50.25 | | | |
| 没収される | (95,768) | | | 56.00 | | | |
| 帰属しておらず、2022年12月31日に帰属する予定です | 1,149,462 | | | $ | 57.26 | | | $ | 44,381 | |
2022年12月31日までにドル52.7RSUに帰属していないことに関する未確認補償費用総額の百万ドルは#年の加重平均期間中に確認されると予想される2.9何年もです。会社のRSUの最大帰属日は4年授与の日から効力を発揮する.付与されたRSUの公正価値は、授与された日の会社普通株の終値に等しい。
付与されたESPPストックオプションの公正価値は、ブラック·スコイルモデルを用いて以下の加重平均仮定の下で推定される | | | | | | | | | | | | | | | | | | | | |
| | 十二月三十一日までの年度 |
| ブラック·スコアーズ加重平均仮定 | | 2022 | | 2021 | | 2020 |
| ESPP株式オプション公正価値 | | $15.26 - $15.86 | | $15.16 - $15.23 | | $11.02 - $17.54 |
| 期待配当収益率 | | ありません | | ありません | | ありません |
| 無リスク金利 | | 0.22% - 2.52% | | 0.50% - 0.90% | | 0.14% - 1.57% |
| 予想変動率 | | 39.5% | | 37.0% | | 44.9% |
| ESPPストックオプションの期待期限 | | 61か月 | | 61か月 | | 61か月 |
Pacira BioSciences,Inc.|2022 Form 10-K|第F-38ページ
カタログ表
Pacira生物科学社は
連結財務諸表付記
付記15-1株当たり純収益
潜在普通株は、それらが逆希釈されている限り、希釈後の1株当たり純収益の計算から除外される。同社が今年度の純損失を報告すれば、希釈後の1株当たり純損失を計算する際には、希釈可能な証券は何も計算しない。付記11で述べたように、債務会社は、2025年の債券転換時に満期になった元金総額を現金で支払う権利があり、そうするつもりだ
ASU 2020-06は2022年1月1日に可決され、企業にIF変換方法を用いて転換可能債務の潜在的希薄化株式数の計算を要求した。IF−転換法により,希釈後の普通株当たり純収入の計算は,会社が届出期間の初日に転換可能債務を転換したように調整されている。分子を調整するのは税引後に転換可能債務に関する利息支出を再計上するためである。分母の調整は期初仮定変換可能株式数を反映している.ASU 2020-06の採用についての詳細は、注3を参照されたい最近の会計公告それは.当社は2021年12月31日および2020年12月31日までに、在庫株方法を用いて転換可能債務の償却株式を計算する。
次の表は、2022年、2022年、2021年、2020年12月31日終了年度までの普通株1株当たりの基本と希釈純収入の計算(1株当たり額を除く)を示している
| | | | | | | | | | | | | | | | | |
| | 十二月三十一日までの年度 |
| | 2022 | | 2021 | | 2020 |
| 分子: | | | | | |
| 純収入-基本収入 | $ | 15,909 | | | $ | 41,980 | | | $ | 145,523 | |
| | | | | |
| | | | | |
| | | | | |
| | | | | |
| | | | | |
| 分母: | | | | | |
| 加重平均発行済み普通株式-基本 | 45,521 | | | 44,262 | | | 42,671 | |
| 希釈証券の計算: | | | | | |
| | | | | |
| 株式オプションの希釈効果 | 787 | | | 1,030 | | | 783 | |
| RSUの希釈効果 | 226 | | | 298 | | | 227 | |
| 2022年債に対する割増転換の役割 | — | | | 38 | | | — | |
| ESPP購入オプションの希釈効果 | 4 | | | 2 | | | 1 | |
| 加重平均普通株式発行-希釈後 | 46,538 | | | 45,630 | | | 43,682 | |
| 1株当たり純収益: | | | | | |
| 普通株1株当たりの基本純収入 | $ | 0.35 | | | $ | 0.95 | | | $ | 3.41 | |
| 希釈して普通株当たり純収益 | $ | 0.34 | | | $ | 0.92 | | | $ | 3.33 | |
次の表は、これらの潜在的株の影響を含む期間が逆希釈されているので、未償還の株式オプション、RSU、ESPP購入オプション、および転換可能優先手形をまとめており、これらのオプションは、これらの潜在的株の影響を含む期間中に逆希釈されている(千単位)ので、これらのオプションは、普通株当たりの償却収益の計算から除外される | | | | | | | | | | | | | | | | | |
| | 十二月三十一日までの年度 |
| | 2022 | | 2021 | | 2020 |
| 株式オプション加重平均 | 2,821 | | | 2,141 | | | 4,237 | |
転換可能優先手形(1) | 6,206 | | | — | | | — | |
| 加重平均RSU数 | 417 | | | 116 | | | 99 | |
| 加重平均ESPP購入オプション | 7 | | | 13 | | | 16 | |
| 合計する | 9,451 | | | 2,270 | | | 4,352 | |
(1)転換可能優先手形は、1ドルごとに2022年12月31日までに反償却となる5.1百万IF変換方法は、ASU 2020-06年度の税引後に転換可能債務に関連する利息支出を再追加する分子に調整される。
Pacira BioSciences,Inc.|2022 Form 10-K|第F-39ページ
カタログ表
Pacira生物科学社は
連結財務諸表付記
付記16-所得税
所得税前収入(損失)および関連税(利)費は以下の通り(単位:千): | | | | | | | | | | | | | | | | | |
| 十二月三十一日までの年度 |
| 2022 | | 2021 | | 2020 |
| 所得税前収入(損失): | | | | | |
| 国内では | $ | 21,068 | | | $ | 64,751 | | | $ | 17,000 | |
| 外国.外国 | (7,766) | | | (8,347) | | | 3,089 | |
| 所得税前総収入 | $ | 13,302 | | | $ | 56,404 | | | $ | 20,089 | |
| | | | | |
| 当期税額: | | | | | |
| 連邦制 | $ | — | | | $ | — | | | $ | (6) | |
| 状態.状態 | 5,309 | | | 3,533 | | | 1,185 | |
| 外国.外国 | 29 | | | 19 | | | — | |
| 当期税額総額 | $ | 5,338 | | | $ | 3,552 | | | $ | 1,179 | |
| 繰延税金: | | | | | |
| 連邦制 | $ | (2,781) | | | $ | 12,554 | | | $ | (99,164) | |
| 状態.状態 | (5,164) | | | (1,682) | | | (27,449) | |
| | | | | |
| 繰延税金総額 | $ | (7,945) | | | $ | 10,872 | | | $ | (126,613) | |
| | | | | |
| 所得税費用総額 | $ | (2,607) | | | $ | 14,424 | | | $ | (125,434) | |
米国連邦法定税率で計算される所得税(福祉)費用と所得税の計上は以下のとおりである(千ドル単位) | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | |
| | 十二月三十一日までの年度 |
| | 2022 | | 2021 | | 2020 |
| 金額 | | 税率.税率 | | 金額 | | 税率.税率 | | 金額 | | 税率.税率 |
| 税引前収入に適用されるアメリカの法定税率 | $ | 2,793 | | | 21.00 | % | | $ | 11,845 | | | 21.00 | % | | $ | 4,219 | | | 21.00 | % |
| 州税 | (448) | | | (3.37) | % | | 2,154 | | | 3.82 | % | | 632 | | | 3.15 | % |
| 外国税 | 248 | | | 1.86 | % | | (651) | | | (1.15) | % | | 639 | | | 3.18 | % |
| 役員報酬 | 1,267 | | | 9.53 | % | | 719 | | | 1.27 | % | | 765 | | | 3.81 | % |
| 評価免除額を変更する | 2,871 | | | 21.58 | % | | 3,695 | | | 6.55 | % | | (130,150) | | | (647.87) | % |
| 株に基づく報酬 | (1,795) | | | (13.49) | % | | (2,144) | | | (3.80) | % | | (216) | | | (1.08) | % |
| 税金控除 | (2,542) | | | (19.11) | % | | (1,690) | | | (3.00) | % | | (1,591) | | | (7.92) | % |
| 利子支出 | (3,477) | | | (26.14) | % | | — | | | — | % | | — | | | — | % |
| 値段が合うかもしれない | (3,841) | | | (28.88) | % | | 247 | | | 0.44 | % | | — | | | — | % |
| | | | | | | | | | | |
| 差し引かれない費用 | 1,164 | | | 8.75 | % | | 1,929 | | | 3.42 | % | | 149 | | | 0.74 | % |
| 埋蔵量 | 984 | | | 7.40 | % | | (738) | | | (1.31) | % | | 1,539 | | | 7.66 | % |
| 転換債 | — | | | — | % | | — | | | — | % | | (1,048) | | | (5.22) | % |
| | | | | | | | | | | |
| 他にも | 169 | | | 1.27 | % | | (942) | | | (1.67) | % | | (372) | | | (1.84) | % |
| 所得税(福祉)費用と有効税率 | $ | (2,607) | | | (19.60) | % | | $ | 14,424 | | | 25.57 | % | | $ | (125,434) | | | (624.39) | % |
Pacira BioSciences,Inc.|2022 Form 10-K|第F-40ページ
カタログ表
Pacira生物科学社は
連結財務諸表付記
繰延税項は、財務報告目的のために資産及び負債として記録された金額と所得税目的で記録された比較可能金額との差額の税収影響を反映している。各報告日において、会社は、積極的であっても消極的であっても、繰延税金資産の将来の現金化に対する見方に影響を与える可能性のある新しい証拠を考慮するであろう。二零年十二月三十一日までに、当社は十分な確実な証拠があると認定し、当社は1ドルの国内繰延税を支払う可能性が高いと結論した126.6100万ドルは現金化可能で、したがって、国内推定手当は釈放される。税収優遇が実現できない可能性が高いため、当社はその海外繰延税項目の純残高に対して全額推定手当を維持している。
当社の2022年12月31日と2021年12月31日までの繰延税金資産と負債の重要な構成要素は以下の通りです(千計) | | | | | | | | | | | |
| | 十二月三十一日 |
| | 2022 | | 2021 |
| 繰延税金資産: | | | |
| 純営業損失が繰り越す | $ | 151,495 | | | $ | 174,203 | |
| 連邦と州の信用限度額 | 23,098 | | | 35,414 | |
| 課税項目と準備金 | 19,979 | | | 29,691 | |
| 株に基づく報酬 | 27,473 | | | 24,545 | |
| 収入を繰り越す | — | | | 2,430 | |
| 在庫備蓄 | 4,889 | | | 572 | |
| 他にも | 11,036 | | | 2,441 | |
| 繰延税金資産総額 | 237,970 | | | 269,296 | |
| 繰延税金負債: | | | |
| 減価償却および償却 | (54,743) | | | (81,418) | |
| 転換可能優先手形割引 | 13 | | | (15,521) | |
| 繰延税金負債総額 | (54,730) | | | (96,939) | |
| 繰延税金資産、繰延税金項目負債純額 | 183,240 | | | 172,357 | |
| 減算:推定免税額 | (22,931) | | | (18,993) | |
| 繰延税項目純資産 | $ | 160,309 | | | $ | 153,364 | |
2022年12月31日現在、会社の連邦純営業損失(NOL)と連邦税収控除繰越総額は$571.8百万ドルとドル16.6それぞれ100万ドルですこの会社は州NOLと州税控除金を持っています518.0百万ドルとドル6.5当社の年間国家分担係数の変化により、この数字は毎年変化する可能性があります。連邦と州NOLはそれぞれ2032年と2028年に満期になるだろう。同社の非アメリカ税収NOLは$です6.52022年12月31日は100万人。アメリカでなければNOLは満期になりません。
当社の所有権の累計変動が超過したため50%3年以内に、IRC第382条および383条によれば、企業が特定のNOL、税金属性、およびクレジット繰越を使用して課税所得または税金を相殺する能力が制限される。この等所有権変動は,2007年に初めて当社株を買収したことと,当社が2021年に初公開発売,その他の融資取引およびFlexion買収を完了したことによる累積所有権変動によって触発されたものである.これらの所有権の変動により会社は$と推定しています516.2100万連邦NOLは年間制限されており、提供可能な数は以下の通りと推定されます。$32.62023年には100万台の価値があります32.52024年には百万ドル32.42025年には100万ドルです28.32026年には100万ドルと6.92027年以降は100万に達するだろう。
米国会計基準第740条によると、当社は、現金化不可能と判断された繰延税金資産に推定値を設定する準備をしている。これらの判断は、税収計画戦略を含む各税務管区の将来の収入の予測に基づいている。各報告期間内に、当社は繰延税金資産の現金化の可能性を評価し、その評価準備の調整が適切であるかどうかを決定する。同社の推定手当は#ドル純増加した3.9百万ドルとドル16.52022年12月31日までと2021年12月31日までの年度はそれぞれ100万ドル。本年度の当社の推定免税額の純増加は#ドルを含む2.5アメリカ資本損失のための百万ドルは0.9Flexion買収状態属性のための百万ドルと$0.5100万ユーロは外国繰延税金純資産を差し引く。当社は海外繰延税項目純資産の全額評価維持に引き続き備えており、海外損失に関する税務優遇が償還できない可能性が高いためだ
Pacira BioSciences,Inc.|2022 Form 10-K|第F-41ページ
カタログ表
Pacira生物科学社は
連結財務諸表付記
はい2022その会社は$を記録しました2.7未確認の税金割引、またはUTBを減らして、$3.7100万ドルはFlexionが得た税金控除のすべての減少です0.2前年の税金控除とドル関連の百万ドルの増加0.8年内に保有する税収控除に関する百万ドル。12月31日のUTBの負債は2022はい$です6.3百万ドルです2022年12月31日までの1年間における会社の違反建築面積の変化の概要は以下の通り(単位:千)
| | | | | | | | |
| | 識別できない
税収割引 |
| 2020年12月31日までの残高 | | $ | 6,076 | |
| | |
| | |
| | |
| 前年のポストを減らす | | (1,355) | |
| 今年度のポストの増加 | | 4,300 | |
| 2021年12月31日の残高 | | 9,021 | |
| | |
| | |
| | |
| 前年のポストを減らす | | (3,526) | |
| 今年度のポストの増加 | | 827 | |
| | |
| 2022年12月31日の残高 | | $ | 6,322 | |
12月31日現在、2022年、2021年、2020年までの違約金は、その後確認されれば、実際の所得税率に有利な影響を与える。
当社は管轄区域の追加評価税の可能性を定期的に評価し、必要に応じて新しい資料や発展に基づいてその違例建築備蓄金を調整する。当社の税収繰越免除により、この準備金は当社の繰延税金資産の減価として記録されており、いかなる潜在的な不足も納税義務を招くことはありません。そのため、2022年、2021年、2020年12月31日までの年間所得税支出では利息や罰金は確認されていない。
現在、同社は2019年から2022年まで米国国税局(IRS)の監査を受け、2018年から2022年まで州税務管区の監査を受けている。しかし、米国国税局または各州は、まだ監査を受ける必要がある年に利用されるように、閉鎖年によるNOLを審査·調整することができる。同社が以前提出した所得税申告書は現在アメリカ国税局や州税務機関の監査下にありません。
付記17-従業員福祉計画
401(K)計画
会社の401(K)計画はIRC第401(K)条下の延期賃金スケジュールである。401(K)計画によれば、計画に参加した米国人従業員は、401(K)計画において定義され、会社の取締役会によって決定された適宜割合一致(IRCで許容される最高金額まで)に適合する税引前収入の一部の支払いを延期することができる。同社は$を確認した3.4百万、$2.8百万ドルとドル2.9それぞれ2022年,2021年,2020年12月31日までの年度内に,401(K)適宜試合に関連補償費用100万ドルを支払う。
給与繰延計画
2020年6月、会社取締役会は会社の延期補償計画、略称DCPを採択した。当社は、改正1974年の“従業員退職所得保障法”と改正された1986年IRCに基づいて、資金のない繰延補償計画を構成し、それを無資金の繰延補償計画と解釈·管理する予定であり、この計画によると、条件を満たす参加者は、現在の補償の受信を延期することを選択することができる。該当する参加者には、当社が指定した役員を含む当社厳選された経営陣と高給社員が含まれています。DCPによれば、DCP管理者が作成する可能性のある任意の最低および最高延期要求に基づいて、参加者は、彼らの基本賃金および年間報酬を延期することを選択することができる。選択的延期に加えて、DCPは、会社が参加者に一致およびいくつかの他の自由に支配可能な寄付を提供することを可能にする。同社は資産をラビ信託基金に貢献し、資金を蓄積し、DCPに基づいて福祉を支払う。ラビ信託に保有されている資金は、DCP参加者に福祉を支払うために使用されなければならないが、会社が倒産または債務を返済できない場合を除き、この場合、彼らは会社債権者の債権の対象となる。同社は$を確認した0.32022年12月31日までの年間DCP情状酌量に関する補償費用は百万ドルと0.22021年12月31日と2020年12月31日までの年間100万ドル。ラビ信託基金が保有する資産の帳簿価値は、2022年12月31日と2021年12月31日現在でDCP負債とほぼ等しく、残高は#ドルである4.3百万ドルとドル2.6それぞれ100万ドルです引き比信託資産は他の資産に格納され、DCP負債は総合貸借対照表の他の負債に分類される
Pacira BioSciences,Inc.|2022 Form 10-K|第F-42ページ
カタログ表
Pacira生物科学社は
連結財務諸表付記
現金長期インセンティブ計画
2020年12月、会社取締役会は、2021年から、予め定められた目標業績目標に専念する現金長期インセンティブ計画、すなわちLTIPを採択した。LTIPは,例年1月1日から12月31日までの適用実績期間ごとに何らかの業績目標を達成した場合に応じて,参加者に現金報酬を提供する.奨励額は0%から225目標現金報酬の%は、純収入と調整後の利息、税項、減価償却および償却前収益(EBITDA)と、標準プル製薬精選業界指数構成会社に対する会社の株価表現に基づく相対総株主リターン補正係数との2つの同等の重みに基づく財務指標の実現に基づくことができる。これらの指標のパフォーマンス期限は1年1つ追加します3年出演期間が終わった後の時間は帰属する。2022年12月31日及び2021年12月31日まで、当社は確認しました1.0百万ドルとドル1.2LTIPでの関連報酬支出はそれぞれ100万ドルであり,これらの支出は2021年の業績期間と関係がある。2021年の業績年度の収入は2025年1月に参加者に支払われる3年制授権期間が終わる。2022年の業績期間中は何の額も稼いでいない。2022年12月31日と2021年12月31日までに2.2百万ドルとドル1.2百万ドルは、それぞれ総合貸借対照表の他の負債に計上される。
付記18-買収に関連する費用(収益)、減価その他
2022年12月31日、2021年、2020年12月31日までの年度買収に関する費用(収益)、減価、その他の費用の概要は以下の通り(千計) | | | | | | | | | | | | | | | | | |
| 十二月三十一日までの年度 |
| 2022 | | 2021 | | 2020 |
| 解散費関連費用 | $ | 4,494 | | | $ | 26,371 | | | $ | — | |
| 買収関連費用 | 1,032 | | | 10,963 | | | — | |
| その他の買収費用 | 5,719 | | | 3,566 | | | 150 | |
| 買収に関連する総費用 | 11,245 | | | 40,900 | | | 150 | |
| 柔軟か割引があります | (18,292) | | | 1,174 | | | — | |
| MyoScienceか割引があります | (11,184) | | | (2,163) | | | 5,204 | |
| 得られた知的財産権研究開発の減価 | 26,134 | | | — | | | — | |
| 許可協定を中止する | 3,000 | | | — | | | — | |
| 微妙生物科学技術有限会社協定解約費 | — | | | 3,000 | | | — | |
| DepoCyt(E)の使用停止 | — | | | — | | | (188) | |
| 買収に関連する費用(収益)、減価その他 | $ | 10,903 | | | $ | 42,911 | | | $ | 5,166 | |
屈曲習得
同社は買収に関連するコストとその他のコストが#ドルであることを確認した11.2百万ドルとドル40.22022年12月31日と2021年12月31日までの年間では、主に解散費、法的費用、第三者サービス、Flexion買収に関連する他の使い捨て費用に用いられる。注5を参照屈曲習得もっと多くの情報を知ります。
2021年11月19日、会社はFlexion買収に関連する買収価格の対価格の一部として、1件または対価格$を記録した45.2100万ドルは、規制と販売に基づくマイルストーンを達成した同社の潜在的な成果を表している。2022年12月31日まで、当社は対価収益を確認または有償としています18.3それや価格の公正価値が減少したため、100万ユーロの損失が生じた。買収の日から2021年12月31日まで、当社は対価を計上しますか$1.2百万ドルです。付記12を参照金融商品当社あるいは対価のある公正価値計測方法および主な仮定に関する資料を理解した。
MyoScience買収
会社は掛け値収益#ドルを確認したり持っています11.2百万ドルとドル2.22022年と2021年12月31日終了年度はそれぞれ100万ドルと対価格料金#ドル5.22020年12月31日までの1年間で付記12を参照金融商品方法、または価格公正価値計量に使用される重要な仮定および公正価値変動に関するより多くの情報を得るために使用される。
Pacira BioSciences,Inc.|2022 Form 10-K|第F-43ページ
カタログ表
Pacira生物科学社は
連結財務諸表付記
同社は買収に関する費用とその他の費用#ドルを確認した0.7百万ドルとドル0.22021年12月31日と2020年12月31日までの年間で,それぞれMyoScience買収に関する一度の給付終了と費用に関係している。
得られた知的財産権研究開発の減価
2022年12月31日までの年間減値は$26.1ZILRETTAが買収した肩の痛みの治療のためのIPR&D無形資産の100万ドルは、その以前の帳簿価値#ドルによって確認された60.0百万ドルは公正価値を超えています33.9百万ドルです。注9を参照商誉と無形資産もっと多くの情報を知ります。
許可協定を中止する
会社が確認した費用は#ドルです3.02022年12月31日までの1年間で、ライセンス契約終了に関する費用は100万ドル。付記20を参照引受金とその他の事項もっと多くの情報を知ります。
ノーランス生物科学技術有限公司です。
2018年6月、会社は中国の専門製薬会社Nuance Biotech Co.Ltd.またはNuanceと合意し、ExPARELの中国での開発と商業化を推進した。契約条項によると、同社はNuanceがEXPARELを開発し、それを商業化する独占的権利を付与した。2021年4月、当社とNuanceは、解散コスト$を含む、当社の知的財産権を後発医薬品製品のリスクから十分に保護するための実行可能な規制経路が不足しているため、共同で合意を終了することに同意した3.02021年12月31日までの年間で
DepoCyt(E)中止
2018年4月,当社はそれぞれMundiPharma International Corporation LimitedおよびMundiPharma Medical Company(総称して“MundiPharma”と呼ぶ)からの供給終了プロトコルおよび流通プロトコル(およびその後改訂されたすべての関連プロトコル)の正式通知を受けた。2019年11月、会社はMundiPharmaと和解し、5.3DepoCyt(E)の生産停止に関する百万ドルの支払いは、以前に計上されていた。
その会社は#ドルの収益を記録した0.22020年12月31日までの年間で,DepoCyt(E)製造活動が2017年6月に関連する百万ドルを停止した。先に述べたDepoCyt(E)とはDepoCytである®アメリカとカナダやDepoCyteの背景で議論すると®連合の背景の下で議論する時。
付記19-ビジネスパートナーや他の合意は
Thermo Fisher科学医薬サービス会社
2014年4月、当社はThermo Fisherと戦略共同生産協定、技術移転とサービス協定(“EXPAREL技術移転とサービス協定”)および製造·供給協定を締結し、EXPARELの生産に協力した。EXPAREL技術移転およびサービス協定の条項によると、Thermo Fisherは、2つの専用スイートでEXPARELを生産するために、イングランドのスウィンデンにある工場を準備するために、いくつかの技術移転活動および建築サービスを負担することに同意した。同社はThermo FisherからEXPARELを購入する契約を、FDAが1軒目の部屋を承認したことから2018年5月に行った。2019年2月に商業化生産を開始します。同社は現在、2つ目のより大規模な専用製造キットを利用している。これらの合意に基づき、同社は毎月Thermo Fisherに基本料金を支払う。本契約は、最長2年の通知を出して契約を終了しない限り、2028年5月に満了します(会社はThermo Fisherで重大な違約が発生した場合は契約を終了します)
Flexion買収に先立ち、FlexionとThermo Fisherは2015年7月に製造と供給協定と技術移転とサービス協定を締結し、会社EXPARELスイートがあるイングランドのスウィンデンの同じThermo Fisher工場でZILRETTAを生産することに関連した。Thermo Fisherは,何らかの譲渡活動や建築サービスを担うことに同意し,専用製造キットでZILRETTAを商業製造する施設の準備をしている。Flexionは、Thermo FisherにZILRETTAを製造するために必要ないくつかのデバイスおよび材料を提供する。同社は製造キット運営の基本費用を毎月Thermo Fisherに支払い、商業需要からZILRETTA 1本当たり製品1本当たりの費用を支払うと予測されている。同社はまた、その名義で購入した材料や設備、特定の名義費用、追加サービスをThermo Fisherに精算している。会社がThermo Fisherでない限り
Pacira BioSciences,Inc.|2022 Form 10-K|第F-44ページ
カタログ表
Pacira生物科学社は
連結財務諸表付記
指定されたマイルストーンやThermo Fisherが違約した場合、会社はThermo Fisherの製造設備の除去に関する費用と、指定の上限を超えないThermo Fisherの終了費用を支払う義務がある。
ヨーロッパ農場実験室株式会社
2021年6月、同社はEurofarma社またはEurofarma社とEXPARELをラテンアメリカで開発し、商業化するDealer契約を締結した。合意条項によると、Eurofarmaはアルゼンチン、ブラジル、コロンビア、メキシコを含むラテンアメリカ19カ国でマーケティングおよび流通EXPARELの独占的権利を獲得した。さらに、Eurofarmaはこれらの国でのEXPARELの規制準備を担当している。その会社は1ドルを受け取った0.3場合によっては部分的に返金可能な100万元の前払いは、Eurofarmaの将来の製品の商業化に基づいて印税を獲得し、特定の規制や商業事件の実現によって触発された記念碑的支払いを得る資格もある。同社は$を確認した0.12021年12月31日までの年間で,その合併運営報告書における連携許可と記念碑的収入は100万ドルである。
Verve医療製品会社です。
2021年7月、同社はVerve Medical Products,Inc.とカナダでiovera°を流通するライセンス契約を締結した。同社は2021年第4四半期にカナダでiovera°の販売を開始した。
ディプイ·シンディス販売会社
2017年1月、会社はジョンソングループ傘下のDePuy Synths Sales,Inc.またはDePuy Synthsと共同普及協定を達成し、米国でExPARELを整形外科手術にマーケティングと普及させることを発表した。Depuy Synths現場代表は関節再建、脊柱、運動医学、創傷と頭蓋顔面(CMF)手術に専門的に従事し、EXPARELの病院手術室と外来手術センターでの教育範囲と頻度を拡大することで、会社の現場チームと協力して補充した。
2020年7月、当社はDePuy Synthsに通知し、共同販売促進協定は2021年1月2日に終了します。会社が記録した契約終了に関する費用は#ドルです8.82020年12月31日までの年間で,販売,一般,行政費に記録されている費用は100万ユーロである。
Aratana治療会社は
2012年12月、同社はElanco Animal Health,Inc.またはAratanaの完全子会社Aratana Treateutics,Inc.と世界的な許可、開発、商業化協定を締結した。協定によると、同社は、獣医用ブピバカイン注射懸濁剤製品の開発および商業化のための再許可を付与する限られた権利を含むAratanaに独占特許使用料許可を付与した。プロトコルにより,AratanaはFDAの承認を得て開発され,獣医手術でこの製品を使用して術後痛をコントロールすることができる。同社はAratanaから合計$を超えない資格を持っている40.0ビジネスのマイルストーンを達成した上で100万ドルに達した。Aratanaは、米国で行われているある純売上高のために会社に2桁の分級特許権使用料を支払う必要がある。製品が外国規制機関によって米国以外で販売されることが承認された場合、Aratanaはこのような純売上について会社に2桁の等級別特許権使用料を支払うことを要求される。動物健康指標の非特許競争者がある司法管轄区域またはAratanaに入って、場合によっては第三者に特許料を支払わなければならない場合、印税料率は一定のパーセント低下するであろう。その条項によって早期に終了しない限り、許可協定の有効期間は2033年7月までであり、その後、Aratanaは合意を1回延長する権利がある5年制期限は,特定の要求によって制限される.
Aratanaは2016年にブピバカイン注射用懸濁剤製品の購入を開始し,Nocitaを商標として販売している®(Aratanaの登録商標)獣医用。
付記20-引受金とその他の事項
法律訴訟
当社は特許、製品責任、政府調査に関する訴訟を含む、その正常な業務過程における法的訴訟に再び巻き込まれる可能性がある。以下に述べる以外に、当社は現在、それが重大であると考えられる法的手続きに参加しておらず、その業務、経営業績、財務状況、またはキャッシュフローに重大な悪影響を及ぼす可能性があると考えられる当社の係属中または脅威に対する訴訟も知られていない。
Pacira BioSciences,Inc.|2022 Form 10-K|第F-45ページ
カタログ表
Pacira生物科学社は
連結財務諸表付記
MyoScienceマイルストーン訴訟
2020年8月、会社とその子会社Pacira CryoTech,Inc.(“Pacira CryoTech”)はデラウェア州衡平裁判所に訴訟を提起し、MyoScience前証券所有者代表として富通顧問有限公司(“Fortis”)と他のある被告に対してのみ訴訟を提起し、MyoScience買収の合併協定(“MyoScience合併協定”)のいくつかの条項(“MyoScience合併協定”)について、特にMyoScience合併協定下のあるマイルストーン支払いに関連する条項について宣言的判決を求めた。また、当社とPacira CryoTechは、MyoScience合併協定の項におけるマイルストーン支払いに関する受託責任に違反することと、MyoScience合併協定および被告との何らかの他の合意に違反することについて、他の被告に一般的、特殊、補償的損害賠償を求めることを他の被告に要求する。2020年10月、富は当社とPacira CryoTechに答弁と反訴を行い、MyoScience合併協定に基づいて何らかの記念碑的な支払いを取り戻すことを要求した。これらのマイルストーンの総残存価値は$30.0100万ドル弁護士費がかかります当社は富通の反クレームには根拠がないと考え、すべてのクレームに対して有力な抗弁を行うつもりである。その会社は現在この行動の結果を予測できない。
EVenus薬学研究所訴訟
2021年10月、同社は、米国特許番号11,033,495(‘495特許)の満了前にEXPARELの模倣バージョン(266 mg/20 ml)を製造および販売するために、米国特許番号11,033,495(’495特許)の発行を求める第4段落認証を有する簡略化新薬出願(ANDA)をFDAに提出したことを通知する通知書を受信した。
2021年11月、同社は、eVenusおよびその親会社に対する特許侵害訴訟を米国ニュージャージー州地域裁判所(21-cv-19829)に提起し、“495年の特許を侵害した”と主張した。これはeVenus ANDAの最終承認を30ヶ月間自動的に延期することを触発する。2022年1月6日、eVenusは、eVenusが提出したANDA文書に記載された製品の製造、販売、または要約によって侵害されていないと主張する反訴答弁を提出した。
2021年12月、会社は、eVenusにANDA修正案および第4段落の認証を提出したことを通知し、‘495特許が満了する前に米国で非特許バージョンのEXPAREL(133 mg/10 ml)を製造および販売することを求める第2の通知書を受信した。通知書では、eVenusはまた、米国第11,179,336号特許(‘336号特許)の満了前に米国でEXPARELの模造バージョン(266 mg/20 mlおよび133 mg/10 ml)の製造および販売を求める第4段落の認証をFDAに提出したことを示している。EVenusは、通知書において、‘495特許および’336特許の両方が無効であり、および/または侵害されていないとさらに主張している。
2022年2月、同社はeVenusおよびその親会社に対して米国ニュージャージー州地域裁判所(22-cv-00718)に2回目の特許侵害訴訟を提起し、133 mg/10ミリリットルのANDA製品が“495および”336特許を侵害し、266 mg/20 mlのANDA製品が336特許を侵害すると主張した。この申請は133 mg/10ミリリットルANDA製品の2回目の自動30ヶ月の最終承認延期をトリガした。
このような訴訟はまだ初期段階であり、会社は現在その結果を予測できない。
研究開発基金
研究開発基金(RDF)との合意によると、プロトコルに従って会社に割り当てられたいくつかの特許が依然として有効である限り、会社は、ある製品から収入を得るより低い桁の特許使用料をRDFに支払わなければならない。RDFは、会社の破産または資本不履行に関連する未治癒の重大な違約行為を終了する権利があり、または譲渡された特許権の有効性に直接または間接的に反対または疑問視する権利がある。同社の‘495特許は2021年6月15日に発行された。その後,RDFは,この特許の発行は,同社が合意に基づいて負担する特許使用料義務を2041年に延長すると主張している。同社は,同協定で規定されている特許使用料期限は2021年12月24日に締め切り,米国特許番号は9,585,838であるとしている。合意の解釈に食い違いがあったため、同社は2021年12月、米ネバダ州地方裁判所に布告的判決訴訟を起こした(21-cv-02241)。訴訟は、同社が2021年12月24日以降にEXPAREL製品の特許権使用料をRDFに支払うべきではないと裁判所に発表した。訴訟が未解決の期間中,会社は抗議されたRDFに特許権使用料を支払い続けるが,会社はこの行動の結果を予測できない。
Pacira BioSciences,Inc.|2022 Form 10-K|第F-46ページ
カタログ表
Pacira生物科学社は
連結財務諸表付記
購入義務
その会社は約ドルを持っている73.3契約製造サービスの最低、キャンセルできない契約引受百万ドルと5.22022年12月31日現在、ある原材料を購入する最低でキャンセルできない契約は100万ドルと約束されている。2022年12月31日以降、当社は追加でドルを締結しました2.8マーケティング支援のための最低でキャンセルできない契約は百万ドルに達した。
その他の引受金とその他の事項
許可協定を中止する
2020年3月、Flexionと香港泰諾薬業有限会社及び中国石家荘薬業有限会社の付属会社江蘇泰諾薬業有限公司はZILRETTAの大中国(大陸部中国、香港、マカオ及び台湾からなる)の開発と商業化について独占許可協定を締結した。合意条項によると、香港のテノールはFlexionに前金を支払った10.02020年12月31日までの年間で繰延収入を記録し,2021年12月31日までである。その会社には最高可達$を取得する資格がある32.5独占許可協定によると、開発、規制、商業販売マイルストーンの支払い総額は100万ドル。香港テノールはZILRETTAの大中華区における中国の臨床開発、製品登録と商業化を担当している。当社は香港テノールのすべての臨床及び商業活動のためのZILRETTAの製造及び供給を独占的に担当しています。ライセンス契約で合意された価格設定および最低購入量要件を含む製品製造および供給に関する条項は、最後に決定されたことのない個別供給プロトコルによってカバーされる
当社は2022年7月に香港テノールに通知を提出し、許可協定を終了する意向を示した。2022年12月31日までにドル13.0連結貸借対照表の課税費用には100万ドルが記録されている。これは1ドルです13.0ライセンス契約の終了に関連した100万ドルはその後、2023年1月に支払われる。
小児科試験約束
EXPAREL承認の条件の一つとして,FDAは小児科患者へのEXPARELの応用,小児科環境における神経ブロックの管理としてのEXPARELの検討を求めている。同社は成人の適応が承認されるまで必要な小児科試験の延期を許可された。同様に、欧州では、欧州医薬品局(EMA)と小児科調査計画について合意しており、EUでマーケティング許可申請(MAA)を提出するための前提条件となっている。イギリスはEUを離脱したにもかかわらず、合意した小児科計画はイギリスに適用される。
2019年12月、同社は6~17歳で心血管または脊柱手術を受けた児童に対する局所鎮痛拡張薬物動態と安全性研究(“PLAY”)の積極的な結果を発表した。これらの積極的な結果は,米国に補充新薬申請やsNDAを提出し,EUとイギリスに第二類変種の基礎を提出し,EXPARELラベルの使用範囲を拡大し,6歳以上の患者を単剤浸透に用いて術後局所鎮痛を産生することである。同社は2021年3月、FDAが米国sNDAの提出を承認したことを発表した。EMAと医薬品·保健品規制機関(MHRA)はまだ第2の変化を検討している。同社はFDA,MAAとMHRAと協力しており,その残りの小児科のために規制経路を決定することを約束している。
マイルストーンの支払いがあります
付記5を参照してください屈曲する 採掘する12を付記します金融商品はFlexion買収およびMyoScience買収に関連する潜在的またはマイルストーン支払いに関する情報が理解されます。
PCRX-201
PCRX−201は、付記5で説明したように、Flexion買収の一部として会社のポートフォリオに追加されている屈曲する 採掘するそれは.Flexionを買収する前に、Flexionは2017年2月にGQ Bio Treateutics GmbH(前身はGeneQuine BioTreateutics GmbH)と合意し、遺伝子治療製品候補製品PCRX-201の全世界権利を買収した。合意の一部として総額は最高$に達する56.0いくつかの発展と規制のマイルストーンを実現する時、最高#ドルを含む数百万ドルの支払いが満期になるかもしれません4.5第2段階概念検証臨床試験を開始することにより,概念検証に成功した後,最高で余分に得ることができる51.5百万ドルの開発と世界的な規制はマイルストーン支払いを承認した。
Pacira BioSciences,Inc.|2022 Form 10-K|第F-47ページ



