cmps-2022123100018165902022会計年度虚像P 3 Y0.250.7500018165902022-01-012022-12-3100018165902022-06-30ISO 4217:ドル00018165902023-02-22Xbrli:共有00018165902022-12-3100018165902021-12-310001816590CMPS:一般共有メンバ2021-12-31ISO 4217:ポンドXbrli:共有0001816590CMPS:一般共有メンバ2022-12-310001816590CMPS:遅延共有メンバ2021-12-310001816590CMPS:遅延共有メンバ2022-12-3100018165902021-01-012021-12-3100018165902020-01-012020-12-31ISO 4217:ドルXbrli:共有0001816590CMPS:一般共有メンバ2019-12-310001816590CMPS:一般共有メンバ2020-12-310001816590CMPS:遅延共有メンバ2019-12-310001816590CMPS:遅延共有メンバ2020-12-310001816590米国-GAAP:転換可能な第一選択株メンバー2019-12-310001816590CMPS:ConvertibleAPferredStockMember2019-12-310001816590CMPS:ConvertibleBPferredStockMember2019-12-310001816590CMPS:一般共有メンバアメリカ-アメリカ公認会計基準:普通株式メンバー2019-12-310001816590CMPS:遅延共有メンバアメリカ-アメリカ公認会計基準:普通株式メンバー2019-12-310001816590US-GAAP:AdditionalPaidInCapitalMembers2019-12-310001816590アメリカ公認会計原則:他の総合収入メンバーを累計2019-12-310001816590アメリカ-公認会計基準:前払いメンバーを保留2019-12-3100018165902019-12-310001816590CMPS:ConvertibleBPferredStockMember2020-01-012020-12-310001816590CMPS:一般共有メンバアメリカ-アメリカ公認会計基準:普通株式メンバー2020-01-012020-12-310001816590US-GAAP:AdditionalPaidInCapitalMembers2020-01-012020-12-310001816590米国-GAAP:転換可能な第一選択株メンバー2020-01-012020-12-310001816590CMPS:ConvertibleAPferredStockMember2020-01-012020-12-310001816590CMPS:遅延共有メンバアメリカ-アメリカ公認会計基準:普通株式メンバー2020-01-012020-12-310001816590アメリカ公認会計原則:他の総合収入メンバーを累計2020-01-012020-12-310001816590アメリカ-公認会計基準:前払いメンバーを保留2020-01-012020-12-310001816590米国-GAAP:転換可能な第一選択株メンバー2020-12-310001816590CMPS:ConvertibleAPferredStockMember2020-12-310001816590CMPS:ConvertibleBPferredStockMember2020-12-310001816590CMPS:一般共有メンバアメリカ-アメリカ公認会計基準:普通株式メンバー2020-12-310001816590CMPS:遅延共有メンバアメリカ-アメリカ公認会計基準:普通株式メンバー2020-12-310001816590US-GAAP:AdditionalPaidInCapitalMembers2020-12-310001816590アメリカ公認会計原則:他の総合収入メンバーを累計2020-12-310001816590アメリカ-公認会計基準:前払いメンバーを保留2020-12-3100018165902020-12-310001816590CMPS:一般共有メンバCMPS:A 2021受賞メンバーアメリカ-アメリカ公認会計基準:普通株式メンバー2021-01-012021-12-310001816590CMPS:A 2021受賞メンバーUS-GAAP:AdditionalPaidInCapitalMembers2021-01-012021-12-310001816590CMPS:A 2021受賞メンバー2021-01-012021-12-310001816590CMPS:一般共有メンバCMPS:A 2020 AwardMemberアメリカ-アメリカ公認会計基準:普通株式メンバー2021-01-012021-12-310001816590CMPS:A 2020 AwardMemberUS-GAAP:AdditionalPaidInCapitalMembers2021-01-012021-12-310001816590CMPS:A 2020 AwardMember2021-01-012021-12-310001816590CMPS:一般共有メンバアメリカ-アメリカ公認会計基準:普通株式メンバー2021-01-012021-12-310001816590US-GAAP:AdditionalPaidInCapitalMembers2021-01-012021-12-310001816590アメリカ公認会計原則:他の総合収入メンバーを累計2021-01-012021-12-310001816590アメリカ-公認会計基準:前払いメンバーを保留2021-01-012021-12-310001816590CMPS:一般共有メンバアメリカ-アメリカ公認会計基準:普通株式メンバー2021-12-310001816590CMPS:遅延共有メンバアメリカ-アメリカ公認会計基準:普通株式メンバー2021-12-310001816590US-GAAP:AdditionalPaidInCapitalMembers2021-12-310001816590アメリカ公認会計原則:他の総合収入メンバーを累計2021-12-310001816590アメリカ-公認会計基準:前払いメンバーを保留2021-12-310001816590CMPS:一般共有メンバアメリカ-アメリカ公認会計基準:普通株式メンバー2022-01-012022-12-310001816590US-GAAP:AdditionalPaidInCapitalMembers2022-01-012022-12-310001816590CMPS:一般共有メンバCMPS:A 2020 AwardMemberアメリカ-アメリカ公認会計基準:普通株式メンバー2022-01-012022-12-310001816590CMPS:A 2020 AwardMemberUS-GAAP:AdditionalPaidInCapitalMembers2022-01-012022-12-310001816590CMPS:A 2020 AwardMember2022-01-012022-12-310001816590アメリカ公認会計原則:他の総合収入メンバーを累計2022-01-012022-12-310001816590アメリカ-公認会計基準:前払いメンバーを保留2022-01-012022-12-310001816590CMPS:一般共有メンバアメリカ-アメリカ公認会計基準:普通株式メンバー2022-12-310001816590CMPS:遅延共有メンバアメリカ-アメリカ公認会計基準:普通株式メンバー2022-12-310001816590US-GAAP:AdditionalPaidInCapitalMembers2022-12-310001816590アメリカ公認会計原則:他の総合収入メンバーを累計2022-12-310001816590アメリカ-公認会計基準:前払いメンバーを保留2022-12-310001816590米国-GAAP:IPOメンバー2021-05-012021-05-310001816590CMPS:米国の預金者共有メンバー米国-GAAP:IPOメンバー2021-10-0800018165902021-10-082021-10-08Xbrli:純0001816590CMPS:AtTheMarketOfferingMember2022-12-142022-12-140001816590CMPS:AtTheMarketOfferingMember2022-12-140001816590米国-GAAP:IPOメンバー2022-12-3100018165902019-08-282019-08-28ISO 4217:ポンド0001816590米国-GAAP:デバイス構成員2022-01-012022-12-310001816590アメリカ-GAAP:OfficeEquipmentMembersSRT:最小メンバ数2022-01-012022-12-310001816590SRT:最大メンバ数アメリカ-GAAP:OfficeEquipmentMembers2022-01-012022-12-310001816590アメリカ-GAAP:家具と固定機器のメンバー2022-01-012022-12-31CMPS:地域00018165902021-01-010001816590CMPS:UnitedKingdomResearchAndDevelopmentTaxCreditRegimeSmallor MediumSizedEnterprisesSMEメンバー2022-01-012022-12-310001816590CMPS:UnitedKingdomResearchAndDevelopmentTaxCreditRegimeMember2022-01-012022-12-31ISO 4217:ユーロ0001816590アメリカ公認会計基準:転換可能債務メンバー2019-12-310001816590アメリカ公認会計基準:転換可能債務メンバー2020-01-012022-12-310001816590アメリカ公認会計基準:転換可能債務メンバー2022-12-310001816590漢方医:DelixTreateuticsIncMember2020-03-062020-03-060001816590漢方医:DelixTreateuticsIncMember2020-03-060001816590米国-GAAP:デバイス構成員2022-12-310001816590米国-GAAP:デバイス構成員2021-12-310001816590アメリカ-GAAP:OfficeEquipmentMembers2022-12-310001816590アメリカ-GAAP:OfficeEquipmentMembers2021-12-310001816590アメリカ-GAAP:家具と固定機器のメンバー2022-12-310001816590アメリカ-GAAP:家具と固定機器のメンバー2021-12-310001816590アメリカ公認会計基準:レンタルとレンタル改善メンバー2022-12-310001816590アメリカ公認会計基準:レンタルとレンタル改善メンバー2021-12-310001816590アメリカ公認会計基準:転換可能債務メンバー2020-04-170001816590CMPS:ConvertibleBPferredStockMember2020-04-172020-04-170001816590CMPS:ConvertibleBPferredStockMember2020-04-170001816590CMPS:一般共有メンバ2020-01-012020-12-310001816590CMPS:米国の預金者共有メンバー米国-GAAP:IPOメンバー2020-09-222020-09-220001816590CMPS:米国の預金者共有メンバー米国-GAAP:IPOメンバー2020-09-220001816590米国-GAAP:IPOメンバー2020-09-222020-09-220001816590CMPS:一般共有メンバ2021-05-042021-05-040001816590CMPS:一般共有メンバ2021-05-192021-05-190001816590米国-GAAP:IPOメンバー2021-05-042021-05-190001816590CMPS:一般共有メンバ2022-01-012022-12-31漢方医:投票0001816590CMPS:一般共有メンバCMPS:A 2021受賞メンバー2021-01-012021-12-310001816590CMPS:一般共有メンバCMPS:A 2020 AwardMember2021-01-012021-12-310001816590CMPS:A 2017持分インセンティブ計画メンバー2021-01-012021-12-310001816590CMPS:A 2017持分インセンティブ計画メンバー2022-01-012022-12-310001816590CMPS:一般共有メンバ漢方医:A 2021メンバー2022-01-012022-12-310001816590漢方医:A 2022メンバーCMPS:一般共有メンバ2022-01-012022-12-310001816590アメリカ公認会計基準:従業員ストックメンバー2022-01-012022-12-310001816590アメリカ公認会計基準:従業員ストックメンバー2021-01-012021-12-310001816590SRT:最小メンバ数米国-公認会計基準:従業員株式オプションメンバーCMPS:A 2017持分インセンティブ計画メンバー2022-01-012022-12-310001816590SRT:最大メンバ数米国-公認会計基準:従業員株式オプションメンバーCMPS:A 2017持分インセンティブ計画メンバー2022-01-012022-12-310001816590CMPS:OptionsGrantedBeever 6月30日米国-公認会計基準:従業員株式オプションメンバーCMPS:A 2017持分インセンティブ計画メンバー2022-01-012022-12-310001816590米国-GAAP:共有による補償補償TracheOneMember米国-公認会計基準:従業員株式オプションメンバーCMPS:A 2017持分インセンティブ計画メンバー2022-01-012022-12-310001816590米国-公認会計基準:従業員株式オプションメンバーCMPS:A 2017持分インセンティブ計画メンバー2022-01-012022-12-310001816590米国-GAAP:制限株式単位RSUメンバーCMPS:A 2017持分インセンティブ計画メンバー2022-01-012022-12-310001816590CMPS:付与日6月30日米国-公認会計基準:従業員株式オプションメンバーCMPS:A 2017持分インセンティブ計画メンバー2022-01-012022-12-310001816590CMPS:付与日6月30日米国-公認会計基準:従業員株式オプションメンバーUS-GAAP:共有ベースの補償報酬送信2人のメンバCMPS:A 2017持分インセンティブ計画メンバー2022-01-012022-12-310001816590米国-GAAP:共有による補償補償TracheOneMemberCMPS:付与日6月30日米国-GAAP:制限株式単位RSUメンバーCMPS:A 2017持分インセンティブ計画メンバー2022-01-012022-12-31CMPS:一日0001816590米国-公認会計基準:従業員株式オプションメンバーCMPS:A 2017持分インセンティブ計画メンバー2022-12-310001816590アメリカ公認会計基準:従業員ストックメンバー2022-12-310001816590アメリカ公認会計基準:従業員ストックメンバー2021-10-012021-10-010001816590CMPS:A 2020 ShareOptionPlanMembers2020-09-012020-09-300001816590CMPS:一般共有メンバCMPS:A 2020 ShareOptionPlanMembers2020-09-300001816590CMPS:A 2020 ShareOptionPlanMembers2022-12-310001816590米国-GAAP:制限株式単位RSUメンバー2022-12-310001816590CMPS:A 2020 ShareOptionPlanMembers2022-01-012022-12-310001816590CMPS:ShareBasedPaymentArrangementVestingConditionOneMemberCMPS:A 2020 ShareOptionPlanMembers2022-01-012022-12-310001816590CMPS:ShareBasedPaymentArrangementVestingConditionTwoMemberCMPS:A 2020 ShareOptionPlanMembers2022-01-012022-12-310001816590CMPS:A 2020 ShareOptionPlanMembersCMPS:ShareBasedPaymentArrangementVestingConditionThreeMember2022-01-012022-12-310001816590CMPS:非従業員メンバー2021-01-012021-12-310001816590CMPS:非従業員メンバー2020-01-012020-12-310001816590CMPS:一般共有メンバCMPS:A 2022入社付与オプション受賞メンバー2022-08-010001816590CMPS:一般共有メンバCMPS:A 2022入社付与オプション受賞メンバー2022-08-012022-08-010001816590CMPS:一般共有メンバ2020-12-310001816590CMPS:一般共有メンバ2021-01-012022-12-310001816590CMPS:一般共有メンバ2022-12-310001816590米国-公認会計基準:制限された株式メンバー2022-01-012022-12-310001816590米国-公認会計基準:制限された株式メンバー2021-01-012021-12-310001816590米国-公認会計基準:制限された株式メンバー2020-01-012020-12-310001816590米国-GAAP:制限株式単位RSUメンバー2020-12-310001816590米国-GAAP:制限株式単位RSUメンバー2021-01-012021-12-310001816590米国-GAAP:制限株式単位RSUメンバー2021-12-310001816590米国-GAAP:制限株式単位RSUメンバー2022-01-012022-12-310001816590米国-GAAP:制限株式単位RSUメンバー2020-01-012020-12-310001816590CMPS:一般共有メンバ米国-公認会計基準:従業員株式オプションメンバー2020-12-3100018165902020-12-312020-12-310001816590CMPS:一般共有メンバ米国-公認会計基準:従業員株式オプションメンバー2021-12-3100018165902021-12-312021-12-3100018165902022-12-312022-12-310001816590米国-公認会計基準:研究·開発費メンバー2022-12-310001816590アメリカ-公認会計基準:一般と行政費用メンバー2022-12-310001816590米国-公認会計基準:従業員株式オプションメンバー2022-01-012022-12-310001816590米国-公認会計基準:従業員株式オプションメンバー2021-01-012021-12-310001816590米国-公認会計基準:従業員株式オプションメンバー2020-01-012020-12-310001816590米国-公認会計基準:研究·開発費メンバー2022-01-012022-12-310001816590米国-公認会計基準:研究·開発費メンバー2021-01-012021-12-310001816590米国-公認会計基準:研究·開発費メンバー2020-01-012020-12-310001816590アメリカ-公認会計基準:一般と行政費用メンバー2022-01-012022-12-310001816590アメリカ-公認会計基準:一般と行政費用メンバー2021-01-012021-12-310001816590アメリカ-公認会計基準:一般と行政費用メンバー2020-01-012020-12-310001816590米国-GAAP:共有による補償補償TracheOneMemberCMPS:A 2022入社付与オプション受賞メンバー2022-08-012022-08-010001816590CMPS:A 2022入社付与オプション受賞メンバーUS-GAAP:共有ベースの補償報酬送信2人のメンバ2022-08-012022-08-010001816590CMPS:IncreasesToIncomeTaxProvisionMember2022-01-012022-12-310001816590CMPS:IncreasesToIncomeTaxProvisionMember2021-01-012021-12-310001816590CMPS:IncreasesToIncomeTaxProvisionMember2020-01-012020-12-310001816590漢方医:臨床試験申請メンバーに増加2022-01-012022-12-310001816590漢方医:臨床試験申請メンバーに増加2021-01-012021-12-310001816590漢方医:臨床試験申請メンバーに増加2020-01-012020-12-310001816590漢方医:臨床試験申請メンバーに減らす2022-01-012022-12-310001816590漢方医:臨床試験申請メンバーに減らす2021-01-012021-12-310001816590漢方医:臨床試験申請メンバーに減らす2020-01-012020-12-3100018165902019-01-012019-12-310001816590CMPS:UnvestedRefintedShareUnitsMember2022-01-012022-12-310001816590CMPS:UnvestedRefintedShareUnitsMember2021-01-012021-12-310001816590CMPS:UnvestedRefintedShareUnitsMember2020-01-012020-12-310001816590CMPS:不安定な通常の共有メンバ2022-01-012022-12-310001816590CMPS:不安定な通常の共有メンバ2021-01-012021-12-310001816590CMPS:不安定な通常の共有メンバ2020-01-012020-12-310001816590米国-公認会計基準:従業員株式オプションメンバー2022-01-012022-12-310001816590米国-公認会計基準:従業員株式オプションメンバー2021-01-012021-12-310001816590米国-公認会計基準:従業員株式オプションメンバー2020-01-012020-12-310001816590CMPS:共有オプションのメンバー2022-01-012022-12-310001816590CMPS:共有オプションのメンバー2021-01-012021-12-310001816590CMPS:共有オプションのメンバー2020-01-012020-12-310001816590CMPS:私たちのスタッフは2022-08-310001816590CMPS:私たちのスタッフは2022-08-012022-08-310001816590漢方医:SohoLondonUKMember2021-07-310001816590漢方医:SohoLondonUKMember2021-07-012021-07-310001816590漢方医:SohoLondonUKMember2022-01-012022-12-310001816590漢方医:DenmarkHillLondonUKMember2022-06-210001816590漢方医:DenmarkHillLondonUKMember2022-01-012022-12-31 アメリカです
アメリカ証券取引委員会
ワシントンD.C.,20549
表10-K
⊠1934年証券取引法第13条又は15条に基づいて提出された年次報告
本財政年度末まで十二月三十一日, 2022
あるいは…。
☐1934年証券取引法第13条又は15条に基づいて提出された移行報告
_から_への過渡期
依頼書類番号:001-39522
羅針盤経路会社
(登録者の正確な氏名はその定款に記載)
| | | | | |
| イングランドとウェールズ | 適用されない |
(明またはその他の司法管轄権
会社や組織) | (税務署の雇用主
識別番号) |
ブロドウィック街33番地
ロンドン.ロンドンW 1 F 0 DQ
イギリス.イギリス
(主な執行機関住所、郵便番号)
+1 (716) 676-6461
(登録者の電話番号、市外局番を含む)
同法第12条(B)に基づいて登録された証券:
| | | | | | | | | | | | | | |
| クラスごとのタイトル | | 取引記号 | | 登録された各取引所の名称 |
アメリカ預託株式は1株当たり普通株に相当し,額面は1株当たり0.008 GBである | | 中成薬 | | ナスダック世界ベスト市場 |
同法第12(G)条により登録された証券:なし。
登録者が証券法規則405で定義されている経験豊富な発行者である場合は、再選択マークで示してください。はい。☐違います。 ☒
登録者が法案第13節又は第15(D)節に基づいて報告書を提出する必要がない場合は,複選マークで示してください。はい。☐違います。 ☒
再選択マークは、登録者が(1)過去12ヶ月以内(または登録者がそのような報告の提出を要求されたより短い期間)に、1934年の証券取引法第13条または15(D)節に提出されたすべての報告書を提出したかどうか、および(2)過去90日以内にそのような提出要件に適合しているかどうかを示すはい、そうです ☒ No ☐
再選択マークは、登録者が過去12ヶ月以内(または登録者がそのような文書の提出を要求されたより短い時間以内)に、S−T規則405条(本章232.405節)に従って提出を要求した各相互作用データファイルを電子的に提出したか否かを示すはい、そうです ☒ No ☐
登録者が大型加速申告会社,加速申告会社,非加速申告会社,小さな報告会社,あるいは新興成長型会社であることを再選択マークで示す。取引法第12 b-2条の規則における“大型加速申告会社”、“加速申告会社”、“小申告会社”、“新興成長型会社”の定義を参照されたい。
| | | | | | | | | | | |
| 大型加速ファイルサーバ | ☐ | ファイルマネージャを加速する | ☐ |
| 非加速ファイルサーバ | ☒ | 規模の小さい報告会社 | ☒ |
| | 新興成長型会社 | ☐ |
新興成長型企業であれば、登録者が延長された移行期間を使用しないことを選択したか否かを再選択マークで示し、取引所法第13(A)節に提供された任意の新たまたは改正された財務会計基準を遵守する
登録者が報告書を提出したかどうかを再選択マークで示し、その経営陣が“サバンズ-オクスリ法案”(“米国連邦法典”第15編、第7262(B)節)第404(B)条に基づいてその財務報告の内部統制の有効性を評価したことを証明する。この評価は、その監査報告書を作成または発行する公認会計士事務所によって行われる☐
証券が同法第12条(B)に基づいて登録されている場合は,財務諸表が虚偽であるかどうかをフックで示す
申告書類に記載されている登録者の情報は、以前に発表された財務諸表の誤り訂正を反映している
これらのエラーのより真ん中に再記述があるかどうかをチェックマークで示すことは、登録者の任意の実行幹事が関連回復中に受信した報酬ベースの補償を回復分析する必要があるかどうかを示す
to §240.10D-1(b). ☐
登録者が空殻会社であるか否かをチェックマークで示す(取引法第12 b-2条で定義されている)。はい、違います☒
2022年6月30日現在,すなわち最近完成した第2財期の最終営業日であり,登録者の非関連会社が保有する普通株総時価は#ドルである247.2百万ドルです。この計算は、何らかの他の目的で特定の人が登録者であることを決定する付属会社を反映していない。
登録者は42,763,8162023年2月22日までに発行された普通株
引用で編入された書類
登録者2023年年次株主総会依頼書の内容の一部は、本明細書で参照されるように本年度報告の第3の部分に組み込まれ、表10−Kは本明細書で説明される範囲内にある。このような依頼書は,登録者が2022年12月31日までの財政年度の120日以内に証券取引委員会に提出される。
カタログ
| | | | | | | | |
第1部 |
第1項。 | 業務.業務 | 7 |
第1 A項。 | リスク要因 | 64 |
項目1 B。 | 未解決従業員意見 | 133 |
第二項です。 | 属性 | 133 |
第三項です。 | 法律訴訟 | 133 |
第四項です。 | 炭鉱安全情報開示 | 133 |
第II部 |
五番目です | 登録者普通株市場、関連株主事項及び発行者による株式証券の購入 | 134 |
第六項です。 | [保留されている] | 134 |
第七項。 | 経営陣の財務状況と経営成果の検討と分析 | 135 |
第七A項。 | 市場リスクの定量的·定性的開示について | 151 |
第八項です。 | 財務諸表と補足データ | 151 |
第九項です。 | 会計と財務情報開示の変更と相違 | 151 |
第9条。 | 制御とプログラム | 151 |
プロジェクト9 B。 | その他の情報 | 152 |
プロジェクト9 Cです。 | 検査妨害に関する外国司法管区の開示 | 152 |
第三部 |
第10項。 | 役員·幹部と会社の管理 | 153 |
第十一項。 | 役員報酬 | 153 |
第十二項。 | 特定の実益所有者の担保所有権及び経営陣及び関連株主の事項 | 153 |
十三項。 | 特定の関係や関連取引、取締役の独立性 | 153 |
14項です。 | チーフ会計士費用とサービス | 153 |
第4部 |
第十五項。 | 展示と財務諸表明細書 | 154 |
第十六項。 | 表格10-Kの概要 | 156 |
| サイン | F-26 |
前向き陳述に関する特別説明
本年度報告における10-K表は、1933年“証券法”(改正)第27 A節又は“証券法”及び改正された1934年“証券取引法”(又は“取引法”)第21 E節で定義された前向き陳述を含む。展望的陳述は一般的に未来の事件や私たちの未来の財務や経営業績と関連がある。本Form 10-K年度報告書に含まれる歴史的事実に関する陳述には、我々の戦略、将来の運営、財務状況、予想収入および損失、予想コスト、見通し、計画、管理目標に関するすべての陳述が前向きに述べられている。場合によっては、“可能”、“そう”、“はず”、“予想”、“計画”、“予想”、“可能”、“意図”、“目標”、“プロジェクト”、“考慮”、“信じる”、“推定”、“予測”、“潜在的”または“継続”などの言葉または他の類似語の否定を含むので、前向きな陳述を識別することができる。本10-K報告書に含まれる前向き陳述および意見は、本10-K報告書が発表された日までに我々の経営陣が得ることができる情報に基づいており、これらの情報はこのような陳述の合理的な基礎を構成していると考えられるが、このような情報は限られているか不完全である可能性があり、私たちの陳述は、入手可能なすべての関連情報について詳細な調査または審査が行われていることを示すものと解釈されてはならない。本年度報告におけるForm 10−Kに関する前向きな陳述は、以下に限定されるものではない
•我々はCOMP 360ヌードカバーキノコ療法の時間、進展と結果を研究し、試験或いは研究の開始と完成時間及び関連する準備に関する声明を含む 我々の3期合意改定への期待,FDAと検討している結果,われわれの難治性うつ病(TRD)3期臨床計画の完成時間,試験結果が出現する時間帯,およびわれわれの研究·開発計画を含む
•私たちの費用、資本需要、追加資金調達の需要と能力の推定
•COMP 360裸蓋キノコ療法の成功に依存しています
•記録と承認の時間、範囲、または可能性を規制する
•COMP 360ヌードゲラリン治療に合格した患者集団の大きさへの期待は、商業用途のために承認されれば、
•私たちは第三者臨床サイトで試験を行う能力と、適切な資格のセラピストが臨床試験でCOMP 360ヌードカバーキノコ療法を実施する能力を識別し、訓練した
•ビジネスモデルやビジネス戦略を実施することができますCOMP 360ヌードカバーキノコ療法を研究しています
•現在の主要なTRD、神経性拒食症、創傷後ストレス障害(PTSD)ではなく、COMP 360の新しい適応を識別することができる
•私たちは研究中のCOMP 360ヌードカバーキノコ療法の管理を強化するために、デジタル技術の能力を識別、開発、または取得した
•私たちは私たちの技術と薬物開発候補を利用して他の満足されていない精神健康需要の分野で新しい幻覚化合物を推進することができます
•私たちは英才センターの設立と維持能力と精神衛生研究と革新センターの目標を達成する能力を成功させました
•私たちのビジネス化マーケティング能力戦略
•承認されれば、COMP 360ヌードカバーキノコ療法の価格、カバー範囲、精算を研究しています
•私たちの製造方法とプロセスの拡張性と商業可能性は
•われわれが検討しているCOMP 360裸蓋キノコ療法,特に裸蓋キノコ療法による市場受容率と臨床的効用の速度と程度
•私たちは協力や戦略的関係を確立したり維持したり、追加の資金を得る能力を持っています
•研究におけるCOMP 360ヌードカバーキノコ療法の潜在的利益への期待と私たちの治療法
•私たちの規制機関のフィードバック、開発経路の規制、制御物質法の指定への期待
•現在または将来の許可者またはパートナーとCOMP 360をカバーする知的財産権の保護範囲を確立し、維持することができる
•私たちは第三者の知的財産権やノウハウを侵害、流用、または他の方法で侵害することなく、私たちの業務を運営することができます
•イングランドとウェールズ、その他の管轄区域の法律と法規によると、アメリカの規制動向
•私たちの競争相手や業界に関する発展と予測
•我が国の財務報告の内部統制の有効性
•私たちは合格した従業員とキーパーソンの能力を引きつけて維持します
•世界金融、経済、地政学的事件が私たちの業務に与える影響は、株式市場の変動、金利とインフレの激化と変動、為替変動、特にポンドの対ドルレートの変動を含む
•公衆衛生危機の影響、新冠肺炎の大流行といかなる新しい新冠肺炎変種あるいは 私たちの業務または運営の任意の前述または他の態様への任意の将来の緩和措置および現在または未来の経済的影響;
•1986年に改正された国内税法によると、現在および今後の間、規制された外国企業、クロロフッ化炭素会社、受動的外国投資会社または民間投資会社に分類されるかどうか
•米国預託証券の将来の取引価格および証券アナリストはこれらの価格への影響を報告している。
私たちはあなたに、上記のリストには、この10-Kテーブルで行われたすべての前向きな陳述が含まれていない可能性があることを想起させます。
あなたは未来の事件の予測として前向きな陳述に依存してはいけません。これらの陳述は行われた日付だけを説明しているからです。本年度報告に含まれる展望的な陳述は主に私たちの現在の未来の事件と傾向の予想と予測に基づいており、これらの事件と傾向は私たちの業務、財務状況、運営結果、将来性に影響を与える可能性があると考えられる。これらの前向き表現に記述されたイベントの結果は、本年度報告第I項第1 A項の“リスク要因”の節と、米国証券取引委員会または米国証券取引委員会に提出された他の文書に記載されているリスク、不確定要因、および他の要因の影響を受ける。しかも、私たちの運営環境は競争が激しく、変化が迅速だ。新しいリスクと不確定要素は時々出現し、私たちは本年度報告10-K表の展望性陳述に影響を与える可能性のあるすべてのリスクと不確定要素を予測することができない。前向き表現に反映された結果、イベント、および状況が達成または発生することを保証することはできません。実際の結果、イベント、または状況は、前向き表現に記載されているものとは大きく異なる可能性があります。米国証券法に別の要求がない限り、私たちは、そのような陳述日後の事件または状況を反映するために、または予期または予期された事件の発生を反映するために、その後、任意の前向きな陳述を修正する義務がない
私たちの業務に関する重大なリスクの概要
私たちの業務は多くのリスクと不確実性の影響を受けており、あなたは私たちの業務を評価する際にこれを認識しなければならない。これらのリスクと不確定要素は含まれているが、これらに限定されない
•私たちは臨床段階の精神健康看護会社で、設立以来すでに重大な損失が発生している。私たちは予測可能な未来に損失が予想され、永遠に利益を達成したり維持したりすることができないかもしれない
•私たちは私たちの研究におけるCOMP 360ヌードカバーキノコ療法の開発と商業化を達成するために多くの追加資金を必要とする。我々がより多くの資金を調達する能力は、マクロ経済状況や米国や世界各地の信用·金融市場の中断や変動の悪影響を受ける可能性がある。必要に応じて、または有利な条件下で追加資金を得ることができない場合、私たちのいくつかまたはすべての製品発見、治療開発、研究操作、または商業化努力を延期、制限、または終了させること、または私たちが自分で開発およびマーケティングしたい製品または候補治療薬を開発およびマーケティングする権利を付与することができるかもしれない
•追加資本の調達は、私たちの普通株式および米国預託証明書の保有者を希釈し、私たちの業務を制限するか、またはCOMP 360または任意の将来の候補治療薬の権利を放棄することを要求するかもしれない
•われわれの研究におけるCOMP 360裸蓋キノコ療法の成功開発に依存している。COMP 360が臨床試験の成功や規制部門の承認を得ることは保証できませんこれはその商業化に必要です
•COMP 360は、私たちが将来開発する可能性のある任意の候補治療薬であり、承認された場合、私たちの製品が販売される可能性のある司法管轄区域の制御物質法律および法規を遵守しなければならず、これらの法律および法規を遵守しない場合、またはこれらの法律および法規を遵守するコスト、またはこれらの法律および法規の変化が、臨床開発中にも承認後でも、私たちの財務状況に悪影響を及ぼす可能性がある。さらに、COMP 360の審査中に、任意の承認前に、米国食品医薬品局またはFDAおよび/または他の規制機関は、COMP 360が乱用または誤用の可能性があるかどうかに関するデータを含む追加のデータを必要とする可能性があり、これは、承認および任意の可能な再配置プロセスを延期する可能性がある
•COMP 360には制御物質が含まれており、これらの物質を使用することは公衆の議論を引き起こす可能性がある。COMP 360、特に裸蓋キノコに基づく療法の否定的な宣伝や公衆の見方、あるいは私たちが現在または将来的に裸蓋キノコを使用する研究療法は、これらの治療法の成功に悪影響を及ぼす可能性がある
•臨床薬物開発は長く高価な過程であり、不確定なスケジュールと不確定な結果を持っている。もしCOMP 360ヌードカバーキノコ療法または任意の将来の候補療法の臨床試験が延長または延期された場合、私たちまたは私たちの現在または未来の協力者は必要な規制の承認を得ることができないかもしれないので、私たちの研究におけるCOMP 360ヌードカバーキノコ療法または任意の未来の候補療法を商業化することはできなくなり、これは私たちの業務に悪影響を与えるだろう
•COMP 360ヌードカバーキノコ療法と私たちが開発する可能性のある任意の未来の候補療法は深刻な不良、不良、あるいは受け入れられない副作用がある可能性があり、発売承認を延期または阻止する可能性がある。COMP 360ヌードマスク療法または任意の将来の候補療法の開発中または承認後にそのような副作用が発見された場合、私たちは、そのような候補療法の開発を放棄する必要があり、任意の承認されたラベルのビジネスイメージが制限される可能性があり、または他の重大な負の結果の影響を受ける可能性がある
•中枢神経系に対する薬物の研究開発は特に困難であり、これは人々がなぜ薬物がいくつかの患者に対して積極的な作用があるのか、他の患者に対して積極的な作用がないのかを予測し理解することを困難にする
•私たちはこれまで候補療法を商業化したことがなく、私たちの治療法を商業化することに成功したり、適切な協力者と協力したりするために必要な専門知識、人員、資源が不足しているかもしれない
•私たちの研究におけるCOMP 360ヌードカバーキノコ療法または任意の未来の候補療法の将来のビジネス成功は、医療専門家、患者、医療保険支払者、衛生技術評価機関、および医学界全体の私たちの潜在療法に対する市場参入と受け入れの程度に依存する
•私たちの業務および商業化戦略は、任意の承認された治療を提供する第三者治療サイトを識別、同定、準備、認証、およびサポートする能力に依存する。これができなければ、私たちの商業化の見通しは制限され、私たちの業務、財務状況、経営業績は損なわれるだろう
•われわれは現在,第三者臨床試験現場で働く適格な治療士がわれわれの臨床試験でわれわれの研究用COMP 360裸蓋キノコ療法を管理しており,COMP 360あるいは任意の将来の候補治療薬が承認された後,この治療が継続されることが予想される。第三者サイトが十分な数のセラピストを募集し、保留することができない場合、または彼らのセラピストを効果的に管理することができなければ、私たちの業務、財務状況、および運営結果は実質的な損害を受けるだろう
•第三者の知的財産権は、私たちの研究療法の能力を開発または商業化することに悪影響を及ぼす可能性があるので、私たちは、私たちの研究療法を開発またはマーケティングするために、訴訟を提起したり、第三者からライセンスを取得したりすることを要求される可能性があります。このような訴訟またはライセンスは、費用が高いかもしれないし、商業的に合理的な条件では得られないかもしれない
•他の人たちは私たちの知的財産権と私たちの候補製品に所有権の権利を要求するかもしれません。これは私たちを訴訟に直面させ、私たちの将来性に重大な悪影響を及ぼすかもしれません
•公布と将来の立法は、COMP 360ヌードカバーキノコ治療または任意の将来の治療候補薬の発売承認および商業化の難しさとコストを増加させ、私たちの業務に実質的な悪影響を及ぼす可能性がある
•我々は第三者供給に依存してCOMP 360に含まれる裸蓋キノコおよび裸蓋キノコを製造し、将来任意の候補治療薬は第三者供給および製造に依存し続けることが予想され、承認されれば、これらの物質の商業供給のための第三者の生産に依存する。任意の第三者プロバイダがCOMP 360または将来の候補治療薬の生産義務を履行できなかった場合、または満足できる法規遵守を維持または達成できなかった場合、そのような物質の開発および任意の療法の商業化は、許可された場合、商業的に実行不可能、利益が低下するか、または私たちに対する法執行行動を引き起こす可能性がある
•多くの第三者が、我々が提供するCOMP 360を使用して、調査者によって開始された研究またはISSを行っている。第三者が我々の研究におけるCOMP 360ヌードカバーキノコ療法の臨床開発上の義務または任意の将来の候補療法を履行できない場合、規制部門のCOMP 360の承認を得る能力を延期または弱める可能性がある。COMP 360のIISSまたは任意の将来の候補治療レジメンは、COMP 360の安全性または有効性の懸念を引き起こす臨床試験データを生成する可能性があり、IISSで生成された任意のデータは、臨床試験を行っている人または適応の結果を予測することができないかもしれない
•不利なグローバル経済状況は、私たちの業務、財務状況、または経営結果に悪影響を及ぼす可能性がある。経済的不確実性と 悪化または悪化したグローバル経済状況および金融市場状況は、私たちの融資能力および財務業績を含む、私たちの業務に重大かつ不利な影響を及ぼす可能性がある
•伝染病や新冠肺炎の新変種の大流行、流行あるいは爆発は、私たちの臨床前研究、臨床試験、私たちが依存している第三者、私たちのサプライチェーン、私たちの資金調達能力、私たちが通常の業務を行う能力、そして私たちの財務業績を含む、私たちの業務に実質的な悪影響を及ぼすかもしれない
•私たちは競争に直面しています競争相手は私たちよりも早くあるいはより早く治療法の発見、開発、商業化に成功しているかもしれませんこれは私たちのビジネス機会を減らしたり排除したりするかもしれません
•私たちの業務は国際業務に関連する経済、政治、規制、その他のリスクの影響を受けている
•我々は、ネットワーク攻撃または他の原因による当社の情報技術システムの障害または深刻な停止によるトラフィック中断に直面する可能性があります。
第1部
プロジェクト1.ビジネス
概要
著者らは精神健康看護会社であり、患者が精神健康領域の根拠に基づく革新を獲得する機会を加速することに力を入れている。われわれの動機は,既存の治療法の助けが得られていない精神健康問題患者を支援するためのより良い方法を見つけることであり,率先して新たな裸蓋キノコ療法を開発しており,われわれの研究ではCOMP 360ヌードゲラクチンを心理的支援とともに使用している。COMP 360は私たちの特許裸蓋キノコ配合物であり、その中に私たちの薬用級多形結晶裸蓋キノコを含み、安定性と純度に対して最適化された。
私たちのCOMP 360ヌードカバーキノコ療法は-COMP 360ヌードカバーキノコ素を専門的に訓練されたセラピストが提供する心理的支持と組み合わせることで、深刻な精神健康問題の治療に新しい方法を提供することができると信じています難治性うつ病、またはTRD、重篤な抑うつ障害のサブセット、またはMDD、神経性拒食症および創傷後ストレス障害、またはPTSD.
我々の最初のポイントは,現在の治療例に十分なサービスを受けていない患者を含むTRDである。我々が開発した裸蓋キノコ製剤ではない学術研究を用いた早期シグナルは,裸蓋キノコ療法はTRD患者の予後を改善する潜在力がある可能性があり,単回大量服用後,抑うつ症状と効果は急速に減少し,6カ月間持続したことが示唆された。2018年,COMP 360治療に対するFDAのTRD突破療法指定を得た。2019年、私たちは89名の健康ボランティアにCOMP 360を応用し、心理支援を提供する第一段階の臨床試験を完成した。この実験では,COMP 360は全体的に耐性が良好であることが観察され,2 b期研究の継続的な進展を支持した。また,1:1の支援の下で,6名もの健康参加者にCOMP 360裸蓋キノコを同時に投与する可能性を証明した
はい2021年11月,われわれの2 b期臨床試験の陽性結果を発表し,COMP 360併用心理支持治療TRDの効果を評価した。2022年11月3日ニューイングランド医学雑誌世界をリードする同業者評議医学雑誌は、著者らの2 b期試験の積極的な結果を発表した。これは今までに完成した最大規模、ランダム、対照、双盲裸蓋キノコ素治療の臨床試験である。2 b期研究の目的は、1用量COMP 360裸蓋キノコ(25 mgまたは10 mg)と1 mg COMP 360裸蓋キノコ素によるTRD患者の治療効果および安全性を評価することである。233名の参加者が参加した試験のTOPLINEの結果によると、心理的支持の下で、COMP 360ヌードマスク治療を1回受けた患者は迅速かつ持続的な反応があり、3週目に29.1%の参加者の病状が緩和した(P)
COMP 360ヌードキノコ治療のTRDを評価するための第3段階計画を始めました第三段階計画は2つの重要な試験からなり、各試験には長期的な後続部分がある。キープログラミングは以下のとおりである
·キー試験1(COMP 005)(n=255):単剤(25 Mg)単一療法はプラセボと対照した。この試験は同社の2 b期試験(n=233)中の治療反応を複製することを目的とした。私たちは2024年夏に収益データを発表する予定だ。
·キー試験2(COMP 006)(n=568):反復用量単一療法を固定し、3用量群:25 mg、10 mg、および1 mgを使用した。この試験は,2回目の用量が治療応答者を増加させ,および/またはわれわれの2 b期試験で観察された反応を改善できるかどうかを調べ,COMP 360 10 mgの重複投与が意義のある治療反応の可能性を探ることを目的としている。私たちは2025年中に収益データを発表する予定だ。
·2つのキーテストの主な終点は、6週目のMADRS総得点とベースラインの変化である。
TRDのほかに,神経性拒食症や創傷後ストレス障害の第二段階試験が行われている。我々はまた,研究機関の支援を提供し,深刻に満たされていない需要分野でCOMP 360裸蓋キノコを用いて研究者による研究やISSを行っている。これらはシグナルを発生させる研究であり,これらの研究は新たな潜在的な兆候に信号を提供する可能性があると信じており,これらの兆候をさらに探索し,我々の開発プロセスに組み込むことができるかもしれない。例えばカリフォルニア大学サンディエゴ医学院はCOMP 360ヌードゲラニンの神経性拒食症におけるIISを完成し、2022年5月の生物精神医学学会年会でこの研究の積極的なデータを提出した。このIISで発生したデータに基づき,神経性拒食症の第二段階臨床試験を継続することにした。IISは,自閉症,身体変形障害,自殺願望,重篤なTRDを含む他の適応に関する他の研究が行われている
現在のモデルは数百万人にとって無効であることから、精神衛生保健分野の革新的な需要は巨大である。私たちのビジョンは精神的に健康な世界である--この世界では、精神健康は精神疾患がないだけでなく、勢いよく発展する能力がある。メンタルヘルスをめぐる恥を減らし、“誰もが物語を持っている”ことを認め、既存のシステムや既存の治療法の助けを得ていないすべての人のためのケアシステムを作成したい。
私たちの戦略
著者らの使命は患者の心理健康領域の根拠に基づく革新を加速することである。この目標を達成するための戦略の重要な要素は
•TRDを治療するためのCOMP 360ヌードカバーキノコ治療研究の第三段階登録計画を推進したはい2021年,われわれは233名のTRD患者に無作為対照2 b期臨床試験を完了し,北米とヨーロッパの22地点で臨床試験を行い,TRD患者19名に2期探索試験を完了した。私たちは発表しました2021年11月と12月のこれらの試験の背線結果は陽性であった。2 b期の臨床試験の結果は“ニューイングランド医学雑誌”2022年11月に。私たちは私たちの第3段階登録計画は,2024年夏に我々のCOMP 005研究と2025年中の我々のCOMP 006研究がバックラインデータを提供する予定である.
•われわれが検討しているCOMP 360裸蓋キノコ療法を新たな適応に拡張したわれわれが検討しているCOMP 360裸蓋キノコ療法は,精神健康面で高度に満足されていない他の分野で有益な効果をもたらす可能性が信じられている。われわれは2期試験を行い,COMP 360裸蓋キノコによる神経性拒食症や創傷後ストレス障害の治療を評価している。また,われわれは臨床前および臨床データを生成し,機序の理解を深め,他の適応におけるわれわれの裸蓋キノコ療法の潜在的利点を探索している。我々自身がこれらの研究を行っているいくつかは,IISSやわれわれの発見センターを含めて学術機関との協力により行われており,新化合物の臨床前研究を行っている。これらの研究の結果,どのような適応,化合物,治療法が求められるかが示唆される。
•他の化合物や療法を探索し,満たされていない需要分野を解決する私たちは最初にフィラデルフィアの科学大学に本部を置き、アメリカに広がる専門家チームネットワークを含み、私たちは5-HT 2 A受容体に対する最適化迷幻剤と関連化合物の開発に専念し、この受容体が幻覚剤の潜在的な治療効果を媒介すると考えられている。また、様々な幻覚や原因物質特許出願を含む知的財産権の組み合わせを買収し、発明家、スイスのバーゼルMiHKAL GmbHの創始者で最高経営責任者のMatthias Grill博士と共同で独自の研究プロジェクトを展開し、新たな候補製品を開発している前薬物開発研究はいくつかの潜在的な候補者の手がかり我々はさらなる研究に基づく開発を継続する予定であることを確認した。
•新しい精神衛生保健モデルを作成することによって、著者らの研究におけるCOMP 360裸蓋キノコ療法のカバー範囲と価値を最大限に拡大する。著者らは研究中のCOMP 360裸蓋キノコ療法の全世界開発権と商業化権利を保留し、監督機関の許可を得た後、支払人と協力して精算を実現し、医療システムと協力して、患者が患者にもっと広く接触できるように商業普及計画を制定している。私たちは未来に重要な市場に研究施設と革新実験室を設立し続ける可能性があり、私たちは卓越した中心と呼ばれている。これにより,エビデンスを収集して我々の治療パターンを最適化し,セラピストを訓練·認証し,患者の体験や結果を改善するためのデジタルテクニカルソリューションのプロトタイプを構築する予定である。2021年1月、私たちはシェパード·プラット高度診断·治療研究所とメリーランド州ボルチモアに最初の卓越したセンターを設立した。2022年3月、私たちはロンドン国王学院とロンドン南部国王学院、モデズリーNHS基金信託基金(SLAM)と戦略的協力を達成し、精神健康研究と革新センターを設立することを発表した。私たちは、卓越したセンターが私たちに堅固な基礎を提供して、その上で潜在的な新しいビジネスモデルを発展させ、開発することができると信じています。承認されれば、私たちの研究COMP 360ヌードカバーキノコ療法のルートを拡大することを求めます。
•デジタル技術を用いて,我々の研究におけるCOMP 360ヌードカバーキノコ療法の獲得と影響を改善した。我々は,デジタル技術を用いてわれわれの治療パターンをより拡張性を持たせ,患者の体験や結果を改善する方法を模索している。私たちは、私たちの臨床試験中に導入された技術に基づいて、患者が彼らのCOMP 360ヌードカバー治療体験の準備、および治療師のパートナー、私たちの対面と臨床を補充するためのネットワークベースの“共有知識”相互作用プラットフォームを含む、私たちのmyPathfinderアプリケーションを含む予定です
精神科医研修。我々はまた,Chanterelle,我々の人工知能(強化知能と人工知能と呼ぶ)と1つの分析解決策を開発しており,それにより,治療結果,患者体験,セラピスト表現の予測と駆動因子に新たな知見を与えることを目指している。私たちはこれが私たちが個人化、予防的、そして予測的な看護モデルを提供できるかもしれないと信じている
私たちの市場のチャンスは
われわれは一連の精神健康疾患の治療に用いられるCOMP 360ヌードカバーキノコ治療法を開発しており,最初のポイントはTRDである。新しい療法に対する大量の需要はまだ満たされておらず、TRD患者の応答率と反応持続性を向上させる。開発に成功し承認されれば,我々が検討しているCOMP 360裸蓋キノコ療法は,神経性拒食症や創傷後ストレス障害を含むTRDや他の精神健康や神経疾患を治療する潜在的な選択となると信じている
MDDとTRDの罹患率
世界的に3億2千万人以上がMDDを患っている。米国では,MDDによる経済的負担は年間2000億ドルを超えると推定されており,その中には身体と精神疾患の共病が含まれている。TRDは全世界の約1億人の患者に影響を与える疾患であり、これらの患者は2回或いは2回以上の現有のうつ病治療後に助けられず、その経済と社会コストは非TRD MDDよりも高い。TRD患者は、非TRD MDD患者と比較して、日常的な任務を実行することができず、障害または福祉福祉を得る可能性があり、より頻繁に疾患を合併する可能性がある。TRD患者の直接医療費は非TRD MDD患者より2~3倍高いと推定され,入院率の増加と平均入院期間の延長が原因である。TRD患者は非TRD MDD患者に比べて全因死亡率が高かった。
うつ病を有する患者は各種の方法で治療を行うことができ、すべての方法はある患者亜群に明らかな欠陥がある。うつ病を治療する薬物療法の多くは同じ作用機序を用いており,脳神経伝達物質モノアミンレベルの調節に対して,かなりの部分の患者で限られた治療効果を示し,高い再発率をきたす可能性がある。米国では、TRD:エスケタミン、およびオザピン(非定型抗精神病薬)とフルオキセチン(選択的セロトニン再取り込み阻害剤)の治療のための2つの薬物療法のみが特に承認されている。エスケタミンは2019年にFDAの承認を受けた。臨床試験では混合治療効果と限られた耐性、および分離と認知障害を含む潜在的な副作用が観察された。オザピンとフルオキセチンの併用も混合効果を示し,通常めまい,傾眠,体重増加などの副作用をきたす。薬物治療以外に、様々な形式の身体干与を使用し、これらの治療はよく侵襲性と/或いは激務であるにもかかわらず、その長期的な利益を支持するデータは限られている。心理治療はもう一つのよく見られる治療方法であるが、それは大量の時間投入を必要とし、しかも獲得性と管理の面で大きな差がある。うつ病の治療法や治療法は多いにもかかわらず、TRDを有する患者は依然として十分なサービスを受けることができず、深刻な健康、社会と経済的負担を延長した。TRDを有する患者には,彼らの抑うつを迅速かつ持続的に緩和するためのパラダイム転換の治療法が必要であると考えられる。
MDDは持続的な悲しみと高度な負の感情を特徴とする疾患である。単相状態と考えられ,MDDと双相抑うつとの違いを示唆しており,後者は通常抑うつと軽躁病や躁病との間で変動する情緒状態に関与している。MDDは1種の慢性、再発性、再発性と深刻な精神健康状況であり、高い死亡率、発病率と生活の質の低下と関係がある。世界保健機関(WHO)は2015年までに、全世界で3.2億人を超える人がMDDを患っており、現在MDDは全世界の障害による損失の寿命年数の7.5%を占めており、これは障害調整生命年(DALY)によって定義されており、DALYは死亡或いは非致命的な疾病或いは損傷によって損失した健康生命年数の和であると推定されている。
現在の治療の局限性のため、MDD患者の3分の1近くは2種類或いは2種類以上の現有のうつ病治療を受けた後に十分な助けを得られない。この場合をTRDと呼ぶ.2010年の最新データによると、世界のTRD人口は約1億人と推定されている
表はアメリカ国家精神衛生研究所が2006年に行ったStar*D試験のデータに基づいて、全世界の新発MDD、持続性MDDとTRD患者の推定人数、及び利用可能な主要な治療方案を示した。
| | | | | | | | | | | |
| 治療経路段階 | 新発うつ病
大うつ病(MDD) | 持続性うつ病
大うつ病(MDD) | 難治性うつ病(TRD) |
| 治療コース | 1行目 | 2行目 | 3行目+ |
| 患者(世界) | 3.2億 | 2億ドル | 1億円
(全体の約33%) |
| 利用可能な治療法 | •抗うつ薬 •CBTのような心理的介入* | •抗うつ薬 •抗うつ薬併用薬 •心理的介入 | •抗うつ薬 •強化治療(抗うつ薬、情緒安定剤、抗痙攣薬、非典型抗精神病薬。エスタミンケトン) •ケタミン •身体療法(rTMS*、tDCS*、ECT*、DBS*) •高強度心理介入 |
| 再発率 | 60-70% | 50-75% | 80-90% |
_____________
*CBT=認知行動療法;rTMS=反復経頭蓋磁気刺激;tDCS=経頭蓋直流刺激;ECT=電気痙攣治療;DBS=脳深部刺激。表を改編するラシュ,A.J.,Trivedi,M.H.,Wisniewski,S.R.,Nierenberg,A.A.,Stewart,J.W.,Warden,D.,...&Fava,M.(2006)。1つまたは複数の治療ステップを必要とするうつ病外来患者の急性および長期結果:STAR*D報告。“米国精神医学誌”163(11)、1905-1917。
経済的·社会的負担
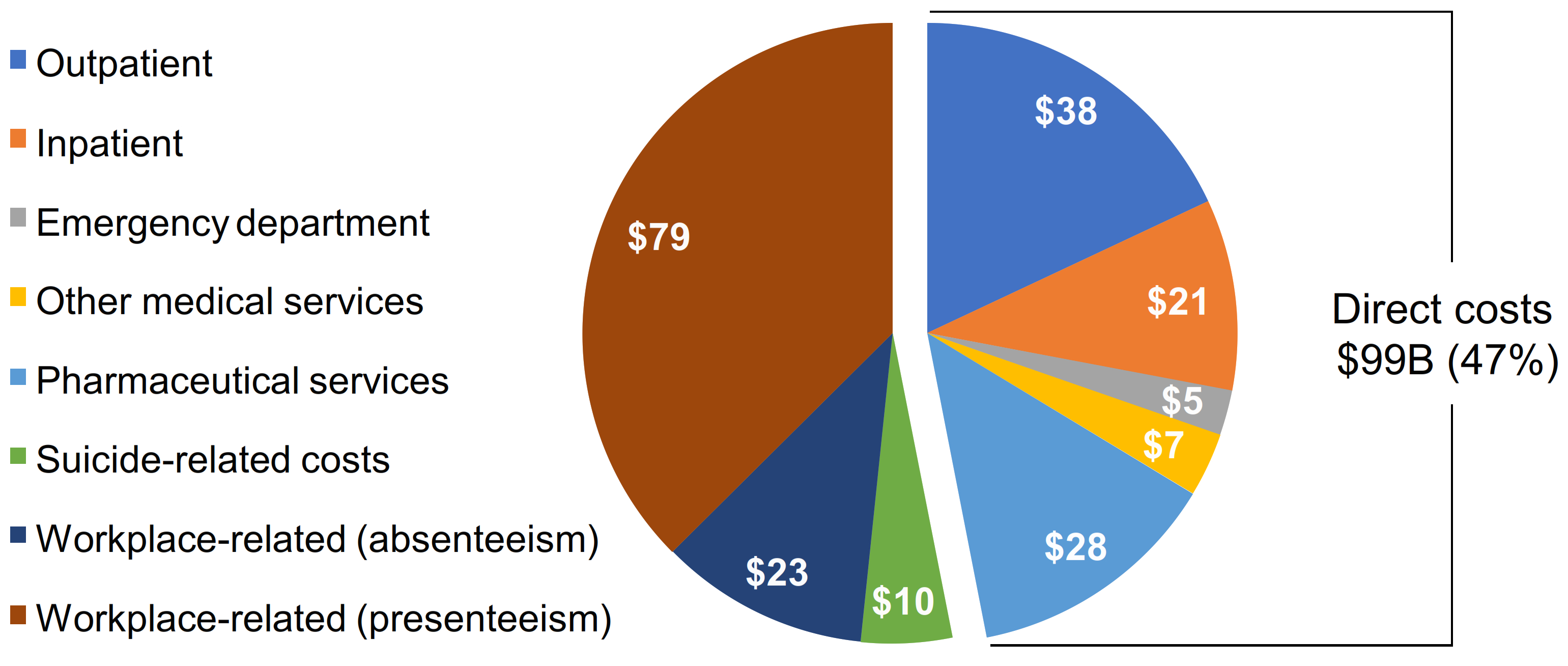
2010年現在,MDDの米国での経済的負担は年間2000億ドルを超えており,身体と精神疾患の共病が含まれていると推定されている。この数字の約47%は直接コストに起因することができ、外来、入院、緊急状況、医療と薬品コストを含み、残りは間接コストに起因し、生産性損失、欠勤と自殺を含む。2005年から2010年までの間に、MDDの経済負担は373億ドル増加し、21.5%増加した。この増加の大部分は外来や入院医療などの直接的なコストによるものである
サービス業は、2005年の775億ドルから2010年の989億ドルに増加し、27.5%増加した。この数字は,MDDの経済的負担が大きいことを示しており,時間の経過とともに増加し続ける可能性があると考えられる。
MDD患者の経済的負担
(U.S., 2010) in $B
総額=2110億ドル
TRD患者の仕事効率はよく低く、失業率は比較的に高い。 彼らはまた非TRD MDD患者よりも障害や福祉を受ける可能性がある。TRDを有する従業員の方が,メンタルヘルス問題のない従業員よりも職場での欠勤率が高い。また、TRD患者は非TRD MDD患者と比較して、高血圧、貧血と糖尿病などの共病の方がよく見られる
TRD患者の直接医療費は非TRD MDD患者より2~3倍高いと推定されている。米国の商業クレームと連邦医療保険/医療補助データからの分析では、TRD患者当たりの年間平均医療コストは17,000ドル~25,000ドルであることが指摘されている。対照的に、非TRD MDD患者の年間費用は10,000ドル未満である。TRD患者の方が処方費用が高く,受診回数が多く,入院率が高い。TRD患者の平均入院回数も非TRD MDD患者と比較して2倍であり,入院期間は平均約36%延長した
世界では毎年約80万人が自殺で死んでいる。成人1人当たりの自殺死は20件以上の他の未遂事件の可能性が推定されている。TRD患者は非TRD MDD患者に比べて全因死亡率が高かった。2018年に行われた研究によると、TRD患者の生涯に少なくとも1回自殺しようとする割合は30%に達する可能性がある。
うつ病の既存の治療法
うつ病は生物、社会、心理、環境、遺伝とストレスに関する決定要素があるため、その中の多くは共同で発生し、治療選択は広く、しかもよく連合している。現在の薬物治療と非薬物治療、例えば抗うつ薬物と心理治療は、MDD患者の一部に対して公認され、有効である。しかし,多くの患者が再発する。臨床医師は質の高い証拠が不足し、よく反復試験の方法に依存し、即ち患者がこれらの再発或いは困難な副作用を経験した時に過程を是正する。専門家たちはより多くのモードの治療に転換し、異なるタイプの治療を同時に行うことを提案し始めた(即ち薬物治療、心理/行為治療と設備干与の組み合わせ)
TRDを有する患者は様々な方法で治療することができ、各方法は重大な欠陥に関連している。そのため、依然として持続的な反応を提供するために、迅速かつ有効で耐性のある治療方法が必要である。この疾患は大きく異質性であるにもかかわらず,多くのうつ病の薬物治療は同じ作用機序を用いて,脳の神経伝達物質モノアミンレベルの調節を目指している。低反応と高再発率は、これらの治療は大量の患者に無効であることを証明した。長期的な利益を支持するデータが限られているにもかかわらず、様々な形態の身体介入も使用されている。エストロンはTRD療法であり,その重要な臨床試験で混合効果を示し,補助抗うつ薬や長期中止薬を用いても再発率が速い
反応する。現在利用可能な選択はTRDを有する患者のニーズを十分に満たすことができないため,新たな治療法が必要であると考えられる。
以下の表には,うつ病の既存治療法の代表的な範囲と大まかなコスト,およびそれらの交付方法がある
| | | | | | | | | | | | | | | | | |
| 治療法 | 路線.路線 | 頻度と持続時間 | 戦略.戦略 ¹ | 精算する² | 患者1人当たりの年間コストは³ |
| 抗うつ薬:SSRI/SNRI* | 口述 | 1/日、慢性 | モノラル/
補助治療 | 広くて広い | $500 - 900 |
| 非定型抗精神病薬 | 口述 | 1/日-慢性病 | 補助治療 | 広くて広い | $3,000 - 9,000 |
| CBT | 対面やオンライン | 10~20コース、3~4ヶ月 | 単一療法·補助療法 | 広くて広い | 平均1000ドル |
| エスタミンケトン | 鼻腔内 | 医療専門家の監督の下で毎年最大56回の会議があります | 補助治療 | 限られている | $33,000 - 49,000 |
| ケタミン** | 静脈注射 | 最大9回の注射 | 補助治療 | 違います。 | $2,500 - 5,000 |
| RTMS | 麻酔のいらない脳磁気刺激 | 5回/週、4~5週間 | 単一療法·補助療法 | 限られている | $6,000 - 12,000 |
| 電気ショック療法 | 麻酔下の脳電気刺激 | 週3回の会議、4週間以上 | 単一療法·補助療法 | 限られている | $5,000 - 15,000 |
| VNS | 脳に送られる電気パルスは | 持続時間は患者によって異なる−まず刺激器を移植し,昼から夜まで5分間隔で開始した低用量を投与しなければならない− | 単一療法·補助療法 | 限られている | 手術のために40,000~45,000ドル(術後調整器具の費用は含まれていません) |
| 星展銀行 | 埋め込まれた電極を介して脳に電気パルスを発する | 3-6時間実行;追跡アクセス | 単一療法·補助療法 | 限られている | 手術施行費は200,000~250,000ドル(12~24ヶ月ごとの電池交換費用は含まず、ハードウェア交換と手術費用は約95,000ドル) |
_____________
鍵:オレンジ:うつ病の常用薬物療法,青:うつ病のよく見られる心理療法,灰色:うつ病の新しい薬物療法,緑:うつ病の身体療法
*SSRI=選択的セロトニン再取り込み阻害剤;SNRI=セロトニン再取り込み阻害剤;** ケタミンはラベルの外に開いていて、うつ病の治療には許可されていません
1.1年間の治療に基づいて、米国は150 mg/日、米国はフルオキセチンまたはイギリスのシタロプラム、2.政府の精算または個人保険カバー、3.1年以内の1つの治療コースを仮定し、直接治療費用のみ(総医療費を含まない)。
薬物療法
市場には5種類の抗うつ薬が選択できる。これらは選択的セロトニン再取り込み阻害剤(SSRI)とセロトニンノルアドレナリン再取り込み阻害剤(SNRI),非定型抗うつ薬,モノアミンオキシダーゼ阻害剤(MAOI)および三環抗うつ薬(TCA)である。これらの薬剤はうつ病の第一線や二次治療によく用いられており,この点以降も使用可能である。研究により、約50%の患者は最初の抗うつ治療で助けられなかった。その後の治療では70%に達しています
現在承認されている抗うつ薬は大きな局限性があり、効果の遅延、治療コンプライアンスの低さと各種の副作用を含む。最もよく使われる抗うつ薬の効果開始時間は通常2~3週間である。コンプライアンスレベルは相対的に低く,一次および精神科看護では,約50%の人が処方された抗うつ薬を主張しなかった。
第一線の抗うつ薬物が反応或いは部分反応がない後、臨床意思決定を有効に指導する証拠は限られている。推奨される治療方法は、現在の抗うつ薬の用量を最適化すること、または同じまたは異なる種類の抗うつ薬に変更することを含む。異なる薬理分類の抗うつ薬或いは代替薬物の併用による部分反応或いは無反応を解決することを提案し、主に非典型的な抗精神病薬物であるが、情緒安定剤、抗けいれん薬、甲状腺ホルモンと覚せい剤及びN-メチル-D-アスパラギン酸或いはNMDA拮抗薬も含む。
抗精神病薬、例えばオザピン、キチオピンとアリピプラゾールは、通常抗うつ薬の顕著な治療効果が乏しい時に補助治療として使用される。TRDのためのオザピンおよびフルオキセチン(SSRI)の承認組み合わせがある。しかし、抗うつ薬と抗精神病薬の併用は、体重増加、他の代謝合併症、鎮静、錐体外系副作用(運動障害)およびQTC延長などの深刻な副作用を有する可能性があり、これは、心臓の心室が2回の拍動の間に通常よりも長い時間を充電する必要があることを意味する。
心理療法(認知行動療法やCBTを含む)
心理療法は談話療法の一形式であり,軽度うつ病の第一線の治療として推奨されることが多く,MDD患者の補助治療となることが多い。2つのよく使われるうつ病治療の心理療法はCBTと人間療法、あるいはIPTと呼ばれる。CBTは否定的な思考と行動パターンを変えることに集中している。IPTも負の思想や行動に注目しているが、人間関係や社会機能に適用されることに限定されている。より深刻な病例とその後の治療において、心理治療の増加効果は依然として疑わしい。心理治療方法は多くの人にとって有効であるかもしれないが、患者が大量の時間を投入する必要があり、しかも獲得性と送達の面で異なる要素の影響を受ける。
エスタミンケトン/ケタミン
ケタミンはNMDA受容体拮抗薬の一種であり、数十年来ずっと鎮静、麻酔と慢性疼痛に応用されている。ケタミンのS-エステレオマーエスケタミンはスプレーの形態で鼻腔投与され、急性自殺願望または行動を伴う成人MDDの治療のためのTRD(2019年)および抑うつ症状(2020)の治療がFDAによって許可されている。エスケタミンの使用に関連した治療効果の結果は半分であった。ケタミンとエスケタミンは複数回投与する必要があり,高乱用の可能性と関係がある。エスケタミン治療は通常,医療監督下の制御された環境で頻繁に使用される必要がある。この頻度は給付者の管理費用を高くし,患者に負担を与え,臨床採用と患者の接触が制限される。
身体療法
重症TRDを有し、いくつかの治療コースの抗うつ薬を試みた患者は、通常、電気痙攣治療(ECT)、反復経頭蓋磁気刺激(RTMS)、迷走神経刺激(VNS)、脳深部刺激(DBS)などの資源集約型身体療法の治療を受ける。これらの療法は通常入院環境で行われる。ECTとVNSなどの身体と設備に関連する干与措置は深刻な副作用と介入性問題と関係があり、例えばECTの全身麻酔と記憶喪失、及びVNS移植の手術干与と感染リスクと関係がある。RTMSの局限性は無意識にてんかん発作、疼痛、顔面痙攣と使用不快感を含む。同様に,外科手術の侵襲性により,星状細胞腫は疼痛やてんかん発作,感染のリスクが高い可能性がある。これらの治療は、一般に、他の治療の助けを得ていない患者のために保持され、コストの高い治療選択として記述されており、これらの治療のサブセットの精算は限られている。
MDDは各種の治療方法と治療方法があるにもかかわらず、TRDを有する患者は依然として十分なサービスを得られず、深刻な健康、社会と経済的負担を延長した。TRDを有する患者には,彼らの抑うつを迅速かつ持続的に緩和するためのパラダイム転換の治療法が必要であると考えられる
ヌードカバーキノコ治療研究の早期シグナル(COMP 360とは異なる裸蓋キノコ配合を使用)によると、これらの研究は、単回大量服用後、一部の患者の抑うつ症状と効果は迅速に減少し、持続時間は6ケ月に達し、ヌードカバーキノコ療法は現在TRDと他の精神健康と神経疾患に対する治療モードを変化させる可能性があると信じている。
神経性拒食症
神経性拒食症は重篤な精神健康状態であり,カロリー摂取を厳しく制限し,体重や体型に集中することが特徴である。神経性拒食症を有する人は、通常、彼らのカロリー摂取量を制限し、彼らが食べる食べ物のタイプは、激しい運動、嘔吐、下剤のような便通行為に従事する可能性がある。その死亡率はすべての精神疾患の中で最も高い。このような高い死亡率の原因の一部は,身体合併症(骨粗鬆症などの筋肉や骨の問題,脳損傷によるてんかん発作や記憶問題,および心不全を含む心臓問題)であり,一部の原因は自殺率の増加であり,神経性拒食症死亡の約20%が自殺によるものと考えられている。2019年現在,約390万人が神経性拒食症を有しており,女性の終身罹患率は約4%である。神経性拒食症の治療薬は現在承認されていないが,心理治療の再発率は52%と高い。
外傷後ストレス障害
創傷後ストレス障害は1種の深刻な心理健康問題であり、生活の質を影響し、認知と心理社会機能の低下、関係破裂、仕事を維持できない、薬物の乱用、高い医療保健費用、抑うつと自殺リスクを増加させる可能性がある。心的外傷後ストレス障害は,自然災害,重篤な事故,戦争や強姦などの創傷事件を経験あるいは目の当たりにした人に発生する可能性がある。外傷後ストレス障害を経験した人は,悪夢やフラッシュバックにより彼らの創傷経験,睡眠困難,疎遠あるいは疎遠を感じる可能性がある。創傷後ストレス障害を有する人は事件発生直後に症状が出現し、他の人の症状は数年後に出現する可能性がある。約3.11億人が生涯のある時点で心的外傷後ストレス障害を経験すると推定されている。現在承認されている創傷後ストレス障害薬物介入治療を受けている患者のうち、20%-30%の患者のみが完全な緩和に達する。
裸蓋キノコ治療
裸蓋キノコの使用歴史
幻覚剤は1種類の精神活性薬物であり、主に神経伝達物質受容体のアゴニスト作用を通じて、心理、視覚と聴覚の変化、及び意識状態の変化を招く。1970年代初めに迷幻薬が付表I薬に分類されるまで,幻覚薬の臨床研究は非常に一般的であり,40,000人以上の精神健康問題を有する患者が臨床研究や症例報告に参加していた。ますます多くの証拠により、多くの幻覚薬は脳に対して精神薬理作用がある可能性があり、神経細胞の数量、密度と連結を増加させることを含む。この証拠は,一連の精神健康疾患を治療するための幻覚薬の再評価に興味を持たせた。過去2年間、多くの主要な学術機関であるロンドン帝国工科大学、ジョンホプキンス大学、シナイ山健康システムは専門の幻覚研究センターを設立した
裸蓋キノコ素は、他の色アミン(例えば、ジメチルクロアミンまたはDMT)、エルゴリン(例えば、エルゴネートまたはLSD)およびフェニルエチルアミン(例えば、メスカリン)と共にセロトニン作動性幻覚剤と考えられる。それはいくつかの種類のキノコ中の活性成分であり、最初はホフマン博士が裸蓋キノコから分離し、20世紀50年代末に合成した。付表I薬物に分類されているが,FDAとDEAは20世紀90年代から臨床研究で裸蓋キノコを用いた一連の精神疾患の治療を許可されている。ヌードゲラニンは潜在的な中枢神経系疾患の治療方法として60年以上研究されてきた。
行動メカニズム
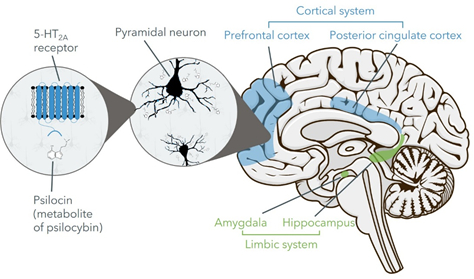
ますます多くの証拠は裸蓋キノコ素がうつ病とその他の精神健康状況に有益な影響を与える可能性があることを表明している。裸蓋キノコのメリットはその作用機序に大きく由来していると考えられる。次の図に示すように、ヌードカバーキノコは、脳中の情緒と認知に重要な領域の1組の異なる受容体を活性化することによって、一連の下流効果を産生し、脳機能に重要で持続的な影響を与える可能性がある。この方式により、中枢神経系中の裸蓋キノコの分子、細胞と全身作用の証拠は裸蓋キノコ素の精神健康疾患の治療における潜在力を支持した。
| | | | | | | | | | | | | | | | | | | | |
セロトニンの興奮作用2A受容体.中の結果下落はG蛋白シグナル経路で下りた。 | | 2. 変更後のドーパミンの細胞外放出は 鉛s積極的な気持ちを高める. | | 3.デフォルト·モード·ネットワークまたはDMNを引き下げる、そして大脳皮質活動の脱同期化や,脳全体の機能接続の新しいモデルの出現。 | | 4.持続的な細胞変化による神経可塑性と“治療の“機会の窓”。 |
ヌードカバーキノコの分子効果:セロトニン受容体の部分アゴニスト
分子レベルでは、裸蓋キノコは、いくつかのセロトニン(セロトニン)2 Aまたはセロトニン受容体の部分アゴニストであり、セロトニン受容体を含むセロトニン受容体とも呼ばれるいくつかのセロトニン(セロトニン)2 Aまたはセロトニン受容体の部分アゴニストである活性代謝物裸蓋キノコに迅速に代謝される2A, 2Cそして、そして 1A受容器です。これはヌードマウス毒素が結合してこれらの受容体を活性化し,これらの受容体すべてが中枢神経系の異なる領域のニューロンに発現することを意味する。特に、ヌードカバーキノコの多くの顕著な急性効果、例えば情緒および認知の変化は、セロトニンによって媒介されると考えられている2Aセロトニンを遮断する事実が支持されている受容体刺激は2A受容体は裸蓋キノコ素の人体に対する幻覚作用を防止できる。セロトニンの作用機序は2A受容体刺激は、シナプス前ニューロンのセロトニン再取り込みを抑制することによって達成されるが、SSRI抗うつ作用の一部である可能性もある。対照的に,裸菌はこの受容体を直接活性化することで抗うつ作用を開始すると考えられている。セロトニンの関連性2A抑うつ症状を調節する受容体も、これらの受容体が脳の複数の領域に大量に発現しており、これらの領域が認知や情緒処理を調節する上で重要な役割を果たしているという事実によって支持される可能性がある。例えばセロトニンは2A受容体は主に皮質錐体神経細胞に発現し、皮質錐体神経細胞は人類の大脳皮質で発見された最も豊富な神経細胞タイプであるため、実行機能と関係があるかもしれない。さらにセロトニンは2A受容体は脳の他の重要な領域で発現し、例えば海馬体と伏隔核、それらはそれぞれ記憶と奨励処理などの重要な生物機能と関係がある。
細胞効果:下流信号の低下を活性化
セロトニンの活性化2A受容体のアゴニストリガンド、例えばヌードマウスはいくつかの下流シグナルの下落を調節して神経細胞の構造と機能を変化させることができ、これは中枢神経系の主要なシグナル成分である。セロトニン.セロトニン2A受容体はGタンパク質共役受容体であり、これは主に一連のGタンパク質と呼ばれるタンパク質を介してシグナルを伝達することを意味する。具体的には下流の主なシグナルはセロトニンです2A受容体はGαを介して起こるq/11タンパク質は,細胞内カルシウム放出を増加させる。逆に、これはニューロンの成長と機能を促進するかもしれない。しかし非典型的なセロトニンは2Aいくつかの細胞または組織タイプ特有の受容体シグナルも存在する可能性があり、幻覚アゴニストのいくつかの下流効果がGαを介して起こることを示す証拠があるからであるI/O通常、ニューロン内のような神経伝達物質放出に関連するシグナル経路を下方制御するタンパク質。このような異なる範囲の細胞シグナルはヌードコリシンによって調節される可能性があり、下落は薬物局部回路レベル効果の基礎である可能性がある。
局所回路レベル効果:神経伝達物質放出と神経可塑性
セロトニン受容体シグナル伝達低下の結果は、(1)脳内ニューロン活性化の変化;(2)神経可塑性の変化;(3)神経伝達物質放出の変化を含む。ニューロンの活性化,あるいは脱分極は,陽イオンがこれらの細胞に流入することに対応して,最終的にニューロン間のシグナル伝達や交流を推進する
神経可塑性とは神経系がその構造、機能と連結を再構築する能力である。これは新しいニューロンの生成,ニューロン形態と連結性の変化,受容体と神経伝達物質レベルの神経生化学変化に関与する可能性がある。特に、早期増殖受容体−1またはEGR−1や早期増殖受容体−2またはEGR−2などの早期遺伝子またはIEGの発現は、ヌードマウス毒素によって誘導される。IEGは外界刺激に反応して活性化する遺伝子であり,脱分極に関与している。IEGsが産生した転写因子は遺伝子制御のより広範な変化を招く可能性があり、更にシナプスの構造と連結を変化させることによって、より長期的な神経可塑性変化を実現する可能性がある。実際,EGR−1やEGR−2は幻覚化合物によって特異的に誘導されているようであり,これらの遺伝子がこれらの薬物の急性および持続作用に関与している可能性が示唆された。
神経伝達物質放出の変化はpsiLocinのもう一つの局所回路レベルの結果であり、その精神活性と情緒効果と関係があるかもしれない。具体的には、げっ歯類研究からの証拠により、ヌードカバーキノコは前頭葉皮質中のセロトニンとドーパミンの細胞外放出のような脳領域を変化させる可能性がある.ある脳領域の細胞外神経伝達物質放出の変化によって、ヌードカバーキノコは積極的な情緒効果を駆動する可能性があり、例えば、実行機能においてすでに作用が確立されている。
システム効果:脳の活動と機能のつながりの変化
全身レベルでは、ヌードカバーキノコは、幻覚体験中と後に、異なる大脳ネットワーク内と異なる大脳ネットワークとの間のニューロン活性化の同期性を変化させることが証明されている。最近の研究では、ヌードカバーキノコ治療後に機能変化を示すネットワークがデフォルトモードネットワーク、すなわちDMNであり、これは、自己参照精神活動および以前の経験を想起する際に活性化が増加し、注意が要求されるタスクにおいて活性化が減少することを示す脳領域ネットワークである。急性体験では,ヌードゲラリンはDMN内領域の同期性を一時的に低下させたようであるが,他の脳領域とネットワークとの接続性は大きく増強している
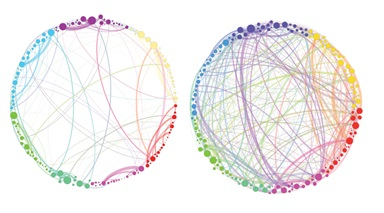
下の図は,健常ボランティアがプラセボ(左)または裸蓋キノコ(右)を服用した場合の大脳ネットワーク接続の急性変化の可視化画像である。線は大脳ネットワーク(ノードとして表示される)間または内部の接続を表し,これらの線の幅は各接続の重みを表す.各ノードの大きさは、その重み付けされた接続の総和に対応する。色は、異なるコミュニティにおけるネットワークではなく、互いに接続されたネットワークまたは領域のコミュニティを表す。
| | | | | | | | | | | |
簡略化するVの等級化AかわいいですねCひもを結ぶB雨NネットワークがありますC連結性 |
| プラセボ | 裸蓋キノコ | |
この研究は健康ボランティアからのfMRI(機能磁気共鳴画像)データを分析し、プラセボ静脈注射と裸蓋キノコ後の安静状態での脳機能接続を比較した。PETRICらが原作で、2014年。
これらの急性効果発生翌日には,ヌードゲラミンを服用した個体がDMN内同期性の増強や,DMN領域と他の脳領域との変化を示す可能性がある。これらの大脳ネットワークの変化は、DMNが結合した後に新しい接続パターンが出現し、感情処理の変化のようなより長期的な変化をもたらす可能性があり、最終的に行動に影響を与える可能性があることを示している可能性がある。
裸蓋キノコ素の学術研究
裸ゲニンの抑うつと焦慮条件下での治療潜在力はすでに過去10年間のいくつかの学術賛助の研究で証明された。これらの研究では,ヌードゲラリンと心理支持を組み合わせて使用した場合,単回大量後に迅速に抑うつ症状を軽減することができ,抗うつと不安緩和効果は服用当日に発生し,多くの参加者に対して6カ月のフォローアップ期間を持続させることができる。これらの研究は一連の広範に使用され、検証された尺度を用いて、抑うつと焦慮に関連する症状を評価する。これらの尺度の中のいくつかは自己報告であり、もういくつかは臨床医師によって評定された。
これらの研究により、裸蓋キノコ素は全体的に耐性が良好で、毒性が低く、深刻な副作用或いはSAE報告がないことを表明した。裸蓋キノコ素の低毒性特性は早期非臨床研究により実証され、これらの研究は極めて高いレベルの裸蓋キノコを静脈注射し、200 mg/kgを超えてこそ、げっ歯動物に毒性効果を産生できることを表明した.2004年の研究では、平均体重70キロの健康成人の中で、裸蓋キノコ素の致死量は6000 mgであり、治療量の範囲を大幅に超えたと推定された
ヌードゲニンは米国では付表I薬に分類され,イギリスではA類薬物に分類され,その乱用潜在力が1960年代に報告されたためである。しかし、裸蓋キノコの天然源が娯楽的に使用されていることを示す証拠があるにもかかわらず、最近の米国制御物質法案を使用した8つの要素の構造を全面的に検討して、医療用裸蓋キノコの乱用の潜在力を評価する。それは、医学背景の下で、裸蓋キノコは高い濫用潜在力がなく、しかも動物と人類のデータに基づいて、明確な証拠がなくて、身体依存の潜在力があることを表明した。
これらのデータの総和は,裸蓋キノコがうつ病や不安障害患者を治療する際に,専門的な訓練を受けたセラピストの心理的支持下で臨床活性を示す可能性を示唆している。ヌードゲラミンによる精神健康疾患の治療を支援すると考えられる学術助成研究の鍵となる発見を表にまとめた。これらの研究ではCOMP 360は1つも用いられていない.
| | | | | | | | | | | | | | | | | |
| カリフォルニア大学ロサンゼルス校 グローブらは (2011) (n=12)(a) | ニューヨーク大学 ロスらは (2016) (n=29)(a) | ジョン·ホプキンス·グリフィスらは (2016) (n=51)(a) | ロンドン帝国工科大学 カーハート·ハリスら (2016, 2018) (n=20)(a) | ジョンズ·ホプキンス デイビスらは (2020) (n=24)(a) |
| 順序を失う | 進行癌に関連する不安は | 癌に関連する不安や抑うつは | 生命を脅かす癌患者の不安や抑うつは | TRD | MDD |
| 設計する | 二重盲検、プラセボ対照 | 無作為、二重盲検、プラセボ対照 | 無作為·二重盲 | 開放ラベル | ランダム化 |
| 投与量 | 14 mg/70 kg | 21 mg/70 kg | 低い(1または3 mg/70 kg)高さ(22または30 mg/70 kg) | 10 mg、その後25 mg | 20 mg/70 kg(初回) 30 mg/70 kg(秒)(b) |
| 結果評価基準 | BDI、STAI、POMS | HADS、BDI、STAI | GRID-HAM-D、HAM-A | QDS−SR−16 | GRID-HAM-D |
| 安全調査結果 | 未分類SAE
裸蓋キノコまで
行政管理 | 未分類SAE
裸蓋キノコまで
行政管理 | 未分類SAE
裸蓋キノコまで
行政管理 | 未分類SAE
裸蓋キノコまで
行政管理;
ほんのわずかで短いだけです
不良事件 | ヌードゲラミン投与によるSAEはありません |
効能.効能
発見 | •BDI:1カ月と6カ月でベースラインより30%改善し,軽度から軽度抑うつまで有意に減少した •POMS:傾向は2週目に悪感情を減少させ、6ヶ月でベースラインに回復しました •統計:特性不安は各時点で6ヶ月間低下し続けています | •HADS、BDI、STAI対策は有意に減少した(軽度/中等度が正常/最低限に低下) •約60%~80%の参加者が抑うつや不安の面で臨床的に有意な反応を続けている | •5週間と6ケ月の時、それぞれ92%と79%の高用量参加者が抑うつおよび焦慮測定に対する臨床的有意な反応を示し続けた | •QDS−SR−16スコアは治療後の各時点で有意に改善した •5週間の最大有効率は65%(20%の緩和を含む) •ヌードゲラリン治療後5週間以内に通常の抗うつ薬治療を求める患者はいなかった | •71%の参加者は、1週間および4週間の抑うつスコアにおいて臨床的に有意な反応を示した。58%と54%の患者がそれぞれ1週間および4週間で臨床寛解を得た |
_____________
(a)N“の数字は、少なくとも1回の投与コースが完了した患者数を表す。いくつかの研究では、すべての患者のすべての投与治療コースおよび/または後続措置が完了したわけではない。患者が研究を完成していない原因は患者が癌進展による病状が加重し、癌による死亡或いは抗うつ薬物治療を回復することを含む
(b)一部の患者は2回目の注射時に再び20 mg/70 kgの用量を受けた。本文で使用されるように、“臨床的顕著な反応”は基線に対して抑うつ或いは焦慮スコアが>50%低下すると定義される。Davisらの研究では,“臨床緩解”はGRID−HAMDスコアとして定義されている
略称:BDI,ベーカー抑うつ尺度;GRID-HAM-D,メッシュハミルトン抑うつ尺度;HADS,病院焦慮と抑うつ尺度;HAM-A,ハミルトン焦慮評価表;HAM-D,ハミルトン抑うつ評価表;STAI,状態-特質不安尺度;POMS,情緒状態プロファイルアンケート;QDS-SR-16,抑うつ症状迅速調査表
カリフォルニア大学ロサンゼルス校,グローブら,2011年−生存ジレンマ:癌患者の実行可能性と安全性
この2011年の研究では,進行癌(急性ストレス障害,広汎性不安障害,癌による不安障害または不安を伴う適応障害の診断と定義される)に関連する不安障害患者12名が数週間ぶりに2回の実験を受けた。1つの治療コースにおいて、各患者は14 mg/70 kgの裸蓋キノコを服用し、別の治療コースでは、各患者はプラセボ対照(250 mgニコチン酸)を受け、彼らの投与順序はランダムであった。それぞれ治療前1日、治療後1日、治療後2週間にBDI、POMS、STAI評価表の評価を行った。最後の会議の後、毎月1回の措置が評価され、評価期間は6ヶ月に及ぶ。1回目の治療前日と比較して2週間でBDIスコアが低下する傾向が認められた。二回目の治療後一ケ月、BDI採点は30%近く低下した。この変化は持続的であり、6ヶ月で顕著になった。POMSは,裸蓋キノコ治療前日と比較して,初回治療後2週間の不良情緒基調が減少傾向にあることを示した。STAI状態焦慮採点は明らかな変化がなかったが、治療後1ケ月と3ケ月にSTAI特質焦慮採点は明らかに低下した。ヌードゲラミンの応用によるSAEは一例もなかった。
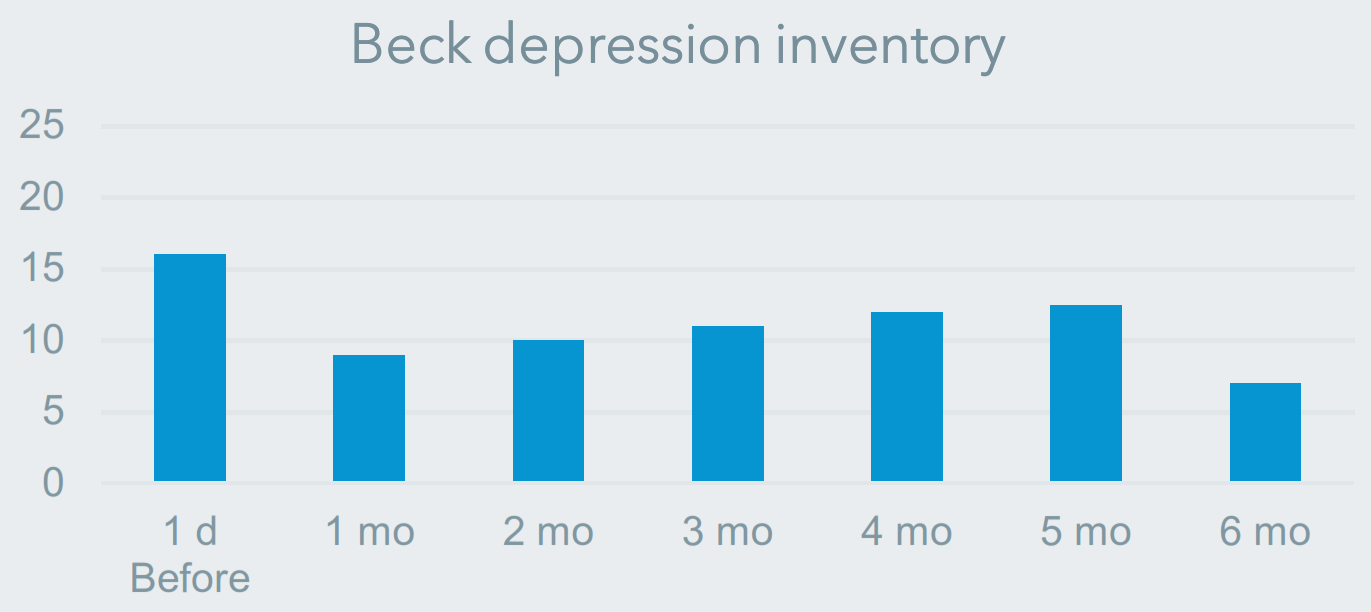
ベースラインと比較して,治療後6カ月のBDIスコアは有意に低下した
グラフは,2回目の投与後のベースラインと6カ月間のベック抑うつアンケート(BDI)得点に代表される抑うつ重症度の変化を示している。ベースラインと比較して6カ月の時点でBDIスコアが低下した。効果の大きさは報告されていない。P値=0.03であり,t検定を行うことにより6カ月の得点と1回目の投与前日の得点を比較して計算した。Grobら2011年を原作とした。
ニューヨーク大学ロスら2016年-生存困難
この2016年の研究は、生命を脅かす癌および臨床的有意な不安または抑うつ(急性ストレス障害、広汎性不安障害、癌によって引き起こされる不安障害、または不安および/または抑うつを伴う適応障害の予備診断として定義される)を有する29人の患者を募集した。患者は2回投与を受け,1回は21 mg/70 kgの裸蓋キノコ素,もう1回はプラセボ(250 mgニコチン酸)であった。投与時間間隔は7週間であり,投与順序はランダムであった。ベースライン測定は最初の会議の2~4週間前に収集された。ベースラインと比較して、1回目にヌードゲラニンを服用した患者は、2回目の服用後26週間以内に焦慮と抑うつの測定指標は統計学的に有意に低下した。プラセボ第1群は交差治療前に有意な変化は認められなかったが,これらの患者は裸蓋キノコ治療を受けた後,多くの不安や抑うつ指標(6分の5)も統計的に有意な持続的な減少を経験した。最終治療後の26週に、両群の患者はBDI緩解率と反応率及びHADSを含む各種指標において抗うつ或いは焦慮緩和或いは焦慮減少の有効率は60-80%であり、次の図に示す。ヌードゲラミンの応用によるSAEは一例もなかった。
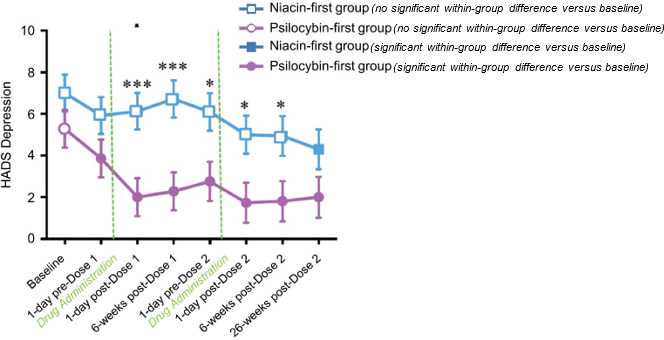
治療後26週間でHADS抑うつスコアは有意に低下した
グラフは,ニコチン酸優先(青色)と裸蓋キノコ優先(紫)群の2回目の治療26週間後のベースラインと26週の間のHADS抑うつスコアの平均変化を示している。1回目の投与後,ヌードゲラリン第1群はプラセボ群と比較して抑うつ症状が有意に減少した。ベースラインと比較して、ニコチン酸第一群は裸蓋キノコ治療を受けた26週間後にも抑うつ症状が有意に減少した。*第ローズたちは2016.
ジョン·ホプキンス大学グリフィスら2016年-生存困難
この2016年の研究では,生命を脅かす癌患者51名と,不安および/または情緒症状を含む精神疾患診断·統計マニュアル第4版(DSM−IV)診断を募集した。患者はランダムに低用量(1または3 mg/70 kg)または高用量(22または30 mg/70 kg)のヌードコリシン治療を受けた。5週間後の第2回投与会議では、まず低用量治療を受けた患者は高用量を投与され、高用量の第1グループの患者は低用量ヌードゲラリンが投与された。高用量第1群では、裸蓋キノコ治療による抑うつおよび不安の測定は、第1治療後5週間以内に有意に減少した。この5週間の時点で、高用量第1群の92%の患者は有意な臨床反応を示し(ベースラインと比較して格網-HAMD抑うつスコアは50%低下した)、低用量第1群のこの割合は32%であった。これらの顕著な変化は両群の6ケ月のフォローアップ中に持続的に存在し、高用量第1群の79%と低用量第1群の77%は引き続き臨床反応を示した。3分の2以上の患者は裸蓋キノコ治療を彼らの一生の中で最も意義のある5回の経験の一つとして描写し、子供の出生或いは両親の死亡と肩を並べ、彼らの裸蓋キノコ治療コースが終了した6ケ月後である。ヌードゲラミンの応用によるSAEは一例もなかった。
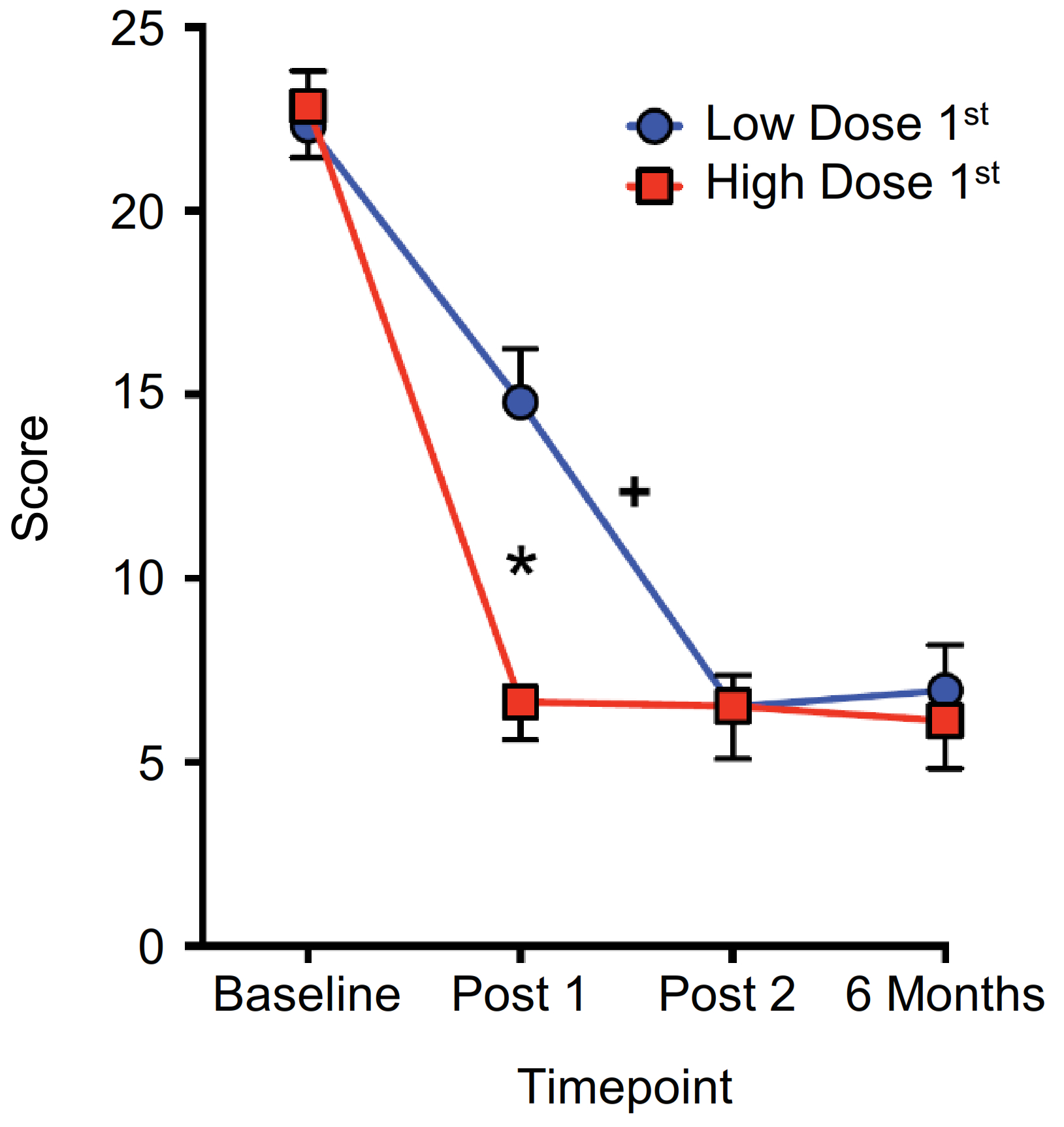
治療6ケ月後の抑うつと焦慮(GRID-HAMD)の顕著な低下
GRAPHは初回治療後6ケ月とベースラインの間のGRID-HAMD採点の変化を示し、まず裸蓋キノコ低用量群或いは先に裸蓋キノコ高用量群を受けた。これらの変化はこの群における裸蓋キノコの抗うつ作用を証明し、そして高用量の裸蓋キノコのもっと良い治療効果を支持した。*第グリフィithsらは2016.
ロンドン帝国工科大学、Carhart-Harrisら、2016,2018-TRD
この2016年に行われた研究では,中大うつ病を有するTRD患者20名が,2回の単独投与中にヌードゲラミン10 mgとヌードゲラミン25 mgをそれぞれ服用し,2回の投与時間は1週間離れていた。すべての患者は初回治療で低用量を受けた。フォローアップ期間全体を終えた19名の患者では,ベースラインと比較して6カ月に及ぶ間に抑うつ症状が統計的に有意に減少した。治療後5週間で最大効果の大きさ(QIDSSR−16)が認められ,このとき9名の患者が応答基準を達成した(ベースラインと比較してBDI分が50%低下した)。大量のヌードゲラリン治療を受けた5週間以内に、伝統的な抗うつ薬物治療を求める患者はいなかった。わずかかつ一時的な有害事象のみが観察され、裸蓋キノコの使用によるSAEはなかった。
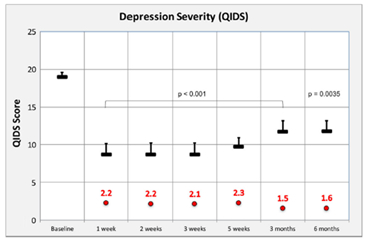
治療後6カ月以内に抑うつ症状は著明に減少した
グラフは,2回目の治療後のベースラインと6カ月の間のQDSスコアに代表される抑うつ重症度の変化を示している。これらの変化は,ヌードゲラリンによるTRD治療後,抑うつ症状が有意に減少したことを示唆している。治療前後のスコアの効果の大きさを比較するコーエンのd赤で表された値。改編したカーハート·ハリスら 2018.
ジョンホプキンス大学デイビスら2020-MDD
この研究は合計24名のMDD患者のデータを分析し、彼らはランダムに2群に分けられた。その中の1群はベースライン測定後すぐに治療(“直ちに治療”)を受け、リスト対照群はベースライン測定後8週間に治療を受けた(“遅延治療”)を待った。各患者は1回目の投与で20 mg/70キロの裸蓋キノコを服用し、2回目の投与で20または30 mg/70キロの裸蓋キノコを注射した。著者は,2つの治療群の治療後1週間と4週間にGRID−HAMDで測定した抑うつ症状の有意差(当時の“遅延治療”群はまだ彼らの最初の投与会議を待っていた)を報告し,これは“即時治療”群のスコア低下によるものであった。また、治療後4週間、71%と54%の研究参加者は臨床で顕著な緩和(GRID-HAMD抑うつスコアはベースラインと比較して>50%低下)と緩和(GRID-HAMDスコア)の標準に達した
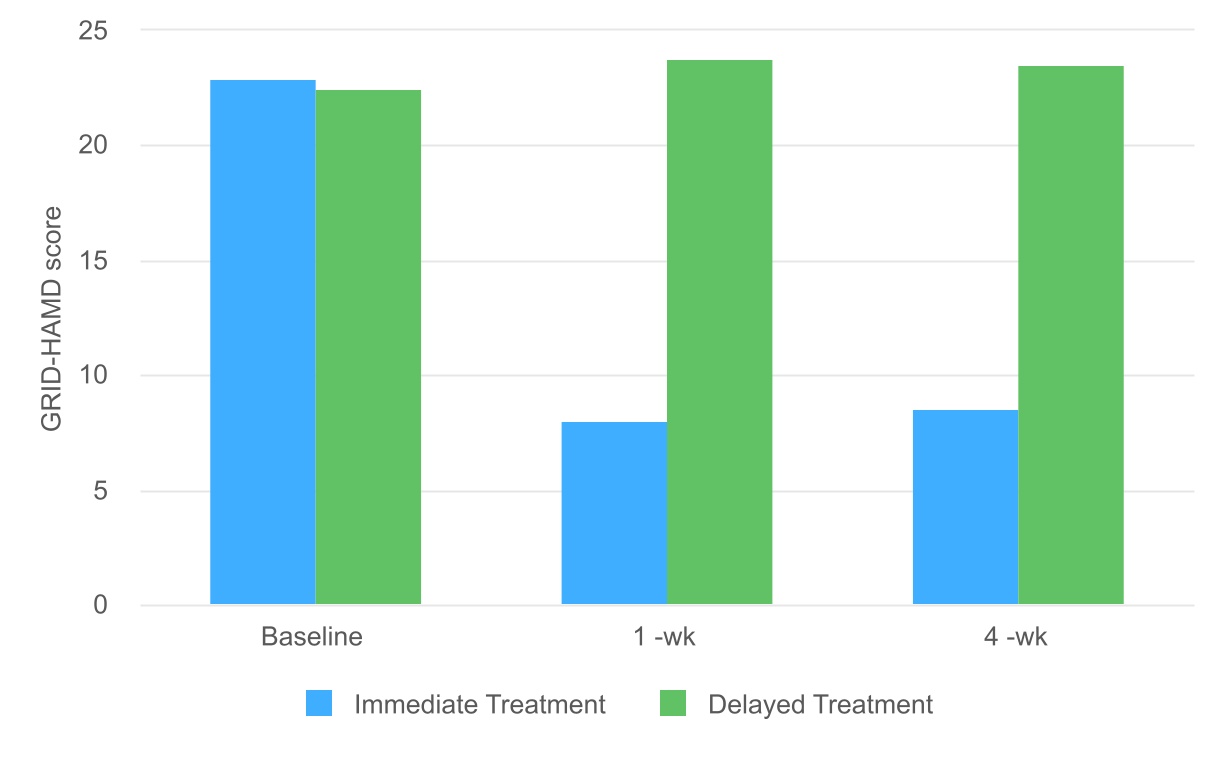
遅延治療群と比較して、直ちに治療群は治療後4週間以内に抑うつ症状が有意に減少した
グラフは“即時治療”グループのベースラインと治療後1週間から4週間のGRID-HAMD採点が代表する抑うつの重症度を示した。効果サイズ(Cohen‘s d):1週間=2.5、4週間=2.6。Davisらの2020年のデータに基づいて作成されたグラフ。
私たちのヌードゲラクチン研究療法はCOMP 360です
臨床総括
COMP 360は私たちの特許裸蓋キノコ配合物であり、その中に私たちの薬用級多形結晶裸蓋キノコを含み、安定性と純度に対して最適化された。我々の研究的COMP 360ヌードカバーキノコ療法は、特定の専門的かつ教育的資格を有する専門的な訓練を有するセラピストの心理的支援の下で、我々のCOMP 360を管理することを含む。われわれのCOMP 360ヌードゲラクチンによるTRD,神経性拒食症,創傷後ストレス障害の治療の安全性と有効性を検討している
我々が2019年に完成した89名の健康参加者に対する第1段階臨床試験では,COMP 360全体の耐性が良好であり,深刻な有害事象もなく,認知や情緒処置に臨床的に関連する短期的あるいは長期的な負の影響も認められなかった。この探索的研究の分析によると,試験期間中,広く受け入れられている臨床と学術テストに基づいて,ケンブリッジ神経心理テスト自動化電池や情緒処理(服用後12週から測定)に基づく一連の有効な測定は,認知(服用後4週間から測定)への負の影響はなかった。この実験は,1:1の支援の下で,6名もの健康参加者にCOMP 360裸蓋キノコを同時に投与する可能性を証明した。
I2021年、私たちは北米とヨーロッパ10カ国の22地点のTRD患者233名の中で、COMP 360ヌードカバーキノコ素治療の大規模無作為、対照、2 b期臨床試験を完成した。これはこれまでに完成した最大規模の裸ゲキノコ試験である。今回の用量発見試験はCOMP 360によるTRD治療の安全性と有効性を研究し、COMP 360の最適な投与量を確定し、そして3種類の用量(1 mg、10 mg、25 mg)を探索することを目的とした。2021年11月、私たちはこの試験のTOPLINE陽性結果を発表し、心理的支持下で単量COMP 360裸蓋キノコ治療を受けた患者が迅速かつ持続的な反応を示すことを示した。試験は最高用量の主要な終点に達し、25 mgのCOMP 360用量は統計学的有意差を示した(p
2021年12月,COMP 360裸蓋キノコ治療とSSRI抗うつ薬を併用した探索的研究結果を発表した。TRD患者19例がSSRI治療および併用治療を同時に受けた単一腕開放マーカー研究
COMP 360ヌードシスチン1用量25 mgで治療した患者の治療結果はわれわれの2 b期試験の患者と類似しており,2 b期試験ではCOMP 360ヌードゲラニン治療を受ける前に進行中の抗うつ薬の中止となった。この研究の結果は、広く考えられているセロトニンは抗うつ薬と裸蓋キノコの併用は裸蓋キノコの治療効果を妨害するという観点に挑戦し、そしてCOMP 360裸蓋キノコ素治療はSSRI抗うつ薬の補助治療である可能性があり、単一治療である可能性があるという強いシグナルを提供した。これは、彼らにとって抗うつ薬の使用を中止することが困難なステップであるので、いくつかのTRD患者に役立つかもしれない。
COMP 360ヌードカバーキノコ素治療案
我々のヌードゲラクチン療法には,専門的に訓練されたセラピストによる心理的支援を提供するCOMP 360が含まれている。心理支持は患者の安全と最適な治療結果を促進することを目的としている。我々の心理支援モデルは,我々のすべての試験地点で一致したサービスを提供するために手動で標準化されている.私たちのモデルは、準備、COMP 360管理会議、統合の3つの異なる段階に分けられます
私たちの裸蓋キノコ療法は数週間です
•準備の仕事:準備会議の目標は,患者とセラピストの間に治療連盟を構築し,自己誘導の問合せや経験処理のスキルを展示·練習することであり,ヌードゲラクチン投与会議における幻覚体験を抱きしめる鍵と考えられる。私たちは患者のためにオンライン準備プラットフォームを作り、そこで彼らは体験から何を期待し、どのように準備するかをより多く知ることができる。
•裸でキノコを投与します裸蓋キノコの投与過程は約6~8時間持続し,セラピストと補助療法士は全過程でその場にいた。治療期間中、セラピストの目標は心理安全を確立し、焦慮を最小限にし、すべての新しい体験に対して開放的であることを奨励することである。会議は環境、快適、そして静かな部屋で行われた。患者は眼帯を着用し,内部の注意力を集中させ,ベッドに横になり,高品質な音響システムやイヤホンで計画された音楽プレイリストを聴くことを支援した。ヌードゲニンの急性効果消退後,患者の安全性評価を行い退院した。
•管理後統合:統合会議の目標は、裸蓋キノコ会議によって促進された一連の感情と身体体験を患者が処理するのを助け、認知と行為の変化を招く可能性のある知見を産生することである。ヌードゲラニン療法は患者にエージェント感を与え,自分の症状から離れていることを感じさせ,彼らの生活を変えることができると信じている。
COMP 360ヌードカバーによるTRD臨床開発計画を治療するセラピストは有効で制限されない専門免許を持っていなければ、臨床心理学者、精神病学者、ソーシャルワーカー或いは精神健康顧問に従事することができる。治療士はまた、その所在地域で心理治療に従事するために必要な訓練と資格認証基準を達成しなければならない。精神健康看護師又は任意の他の精神健康専門家としての活躍を有する、制限されていない専門免許を有する者は、我々の臨床試験においてセラピストとして勤務する資格がある可能性があり、上記の専門者と同等の臨床経験及び心理治療訓練の基準を満たすことが条件である。
我々の心理支持方法は現在の裸蓋キノコの潜在力に対する理解に基づいており、それは新しい見解と観点を生成することができ、それによって思考中の硬直化を減少させることができる。このような思考パターンの変化は気分が悪くなったり不安を引き起こしたりする可能性がある。安全な理由でなければ、セラピストは患者の経験に介入しないだろう。この方法はある形式の心理治療とは異なり、後者はもっと指導性と介入性を持つことができる。著者らのセラピスト訓練計画は裸蓋キノコ素治療中の心理支持のために正式かつ拡張可能な方法を制定した。われわれが臨床試験によるCOMP 360裸蓋キノコ療法の推進に伴い、それは引き続き発展するが、このような訓練計画の手作業方法は心理支持の違いを減少させ、このような支持の枠組みを制定し、評価する重要な第一歩である。この計画の詳細は2021年2月に同業者評議誌に発表された精神医学の最前線です
臨床前と臨床経験
臨床前研究
著者らは以前、遺伝毒性と心臓毒性を評価する研究のテストを含む一連の体外と体内毒理学研究を行った。これらの研究の結果,TRDでわれわれの2 b期臨床試験を開始することができた。必要な一連の体外と体内安全性と毒理学研究はまだ計画通りに行われており、著者らの第三段階計画を有効に開始できるようにした
ステップ1:健康ボランティア試験
2019年,COMP 360の第1段階臨床試験を完了し,健康参加者の心理的支援を行った。この試験では健康参加者89名を募集し,そのうち41名が女性,48名が男性,平均年齢は36歳であった。この二重盲検、プラセボ対照試験は当時最大の裸蓋キノコ無作為対照試験であり、初めて裸蓋キノコ素を同時に投与した試験でもあり、臨床研究環境においてセラピストの1:1支持を得た。この実験はロンドンキングアカデミー精神医学心理学神経科学研究所で行われました 同業者評議を経て、2022年1月に“精神薬理学雑誌”に発表された
試行設計
就職する前に、出席者は2時間の準備グループ会議に参加した。参加者は、1:1:1の割合で、プラセボ、10 mgまたは25 mg用量のCOMP 360の3群にランダムに分けられた。この施設では,COMP 360を経口投与し,6名までの参加者に1:1の心理的支援を同時に提供している。参加者は服薬後12週間の追跡調査を受け、一連の認知機能と情緒処理の有効な測定方法を用いて安全性評価を完成した
肝心な学生募集基準
参加者は18歳から65歳までの男性または女性である。統合失調症、精神病、双極性感情障害、妄想障害、パラノイド人格障害、分裂感情障害、辺縁人格障害、深刻な抑うつ障害、恐怖障害、広汎性不安障害、強迫症、摂食障害または身体変形障害を有する参加者は除外された。これらの場合の一級親族や既往歴のある患者も除外された。また、参加者が現在または過去の薬物乱用または依存の基準に適合し、登録後1年以内に精神薬を服用したり、インフォームドコンセント書に署名してから1年以内にヌードカバー素に接触した場合には、資格があるとは考えられない。
臨床表現
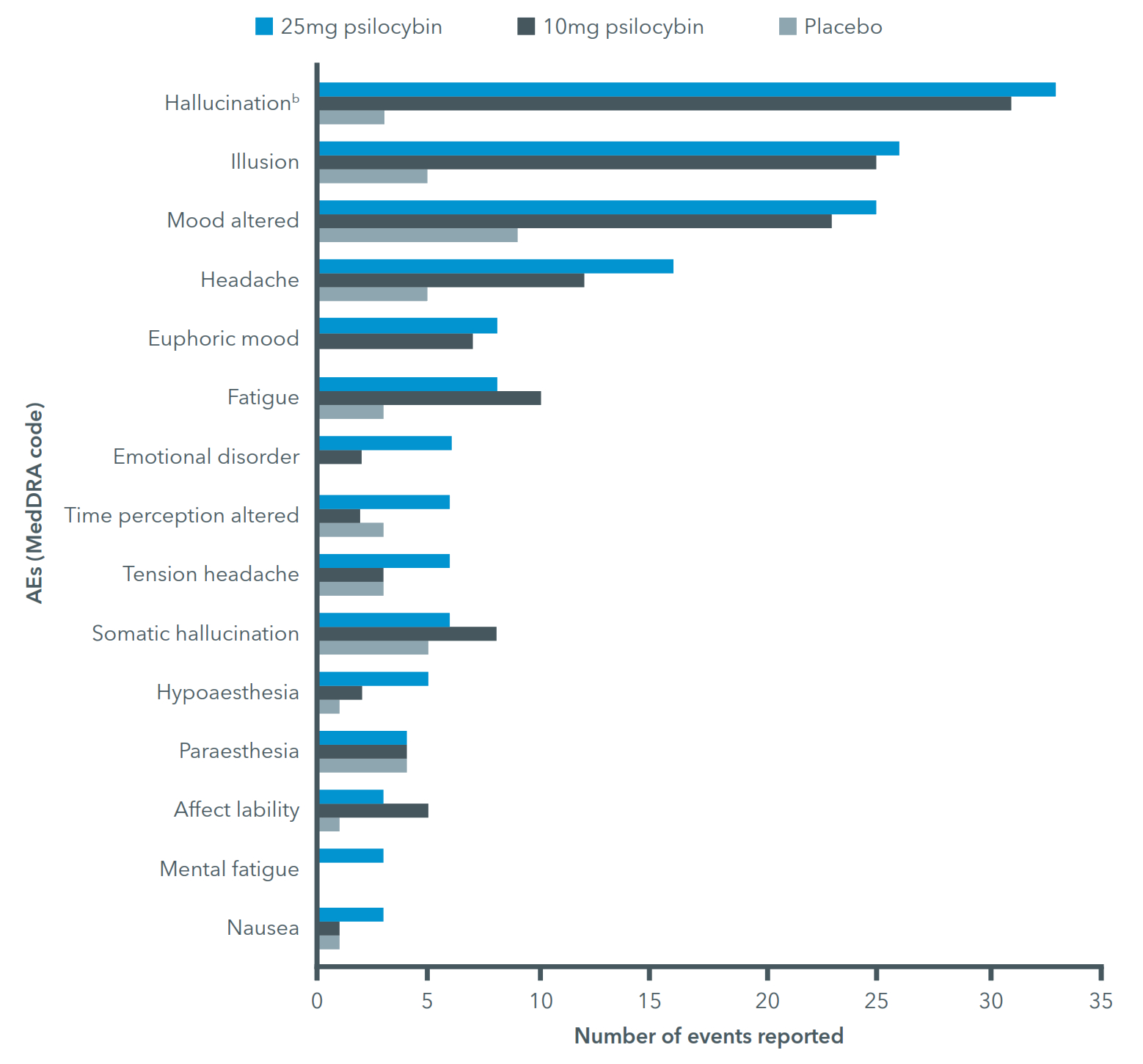
SAEの報告もなく,有害事象やAEsによる中止もなかった。12週間の試験期間中に、511例の急性脳血管障害を報告した。以下の表は最もよく見られる副作用をまとめ、治療群による副作用状況、及びCOMP 360 25 mgヌードシイタケ腕に基づく最もよく見られる副作用をグループごとにランキングした
| | | | | | | | | | | |
| プラセボ(n=29) | 10mg COMP360 (n=30) | 25mg COMP360 (n=30) |
| 報告された緊急治療救急総数 | 91 | 203 | 217 |
| 研究治療に関与していると考えられる,あるいは研究治療に関連する可能性のある緊急治療不良事象の総数 | 77 | 188 | 208 |
治療群がわれわれの健康ボランティア試験で報告した治療緊急有害事象(AEs)の数。
最もよく報告されている急性脳血管イベント(MedDRAコード)a私たちの最初の段階の健康ボランティア実験では
_____________
a発症率は25 mg COMP 360群でランキングされています
b聴覚味覚嗅覚触覚視覚幻覚が含まれています
有害事象を管理する医学辞書
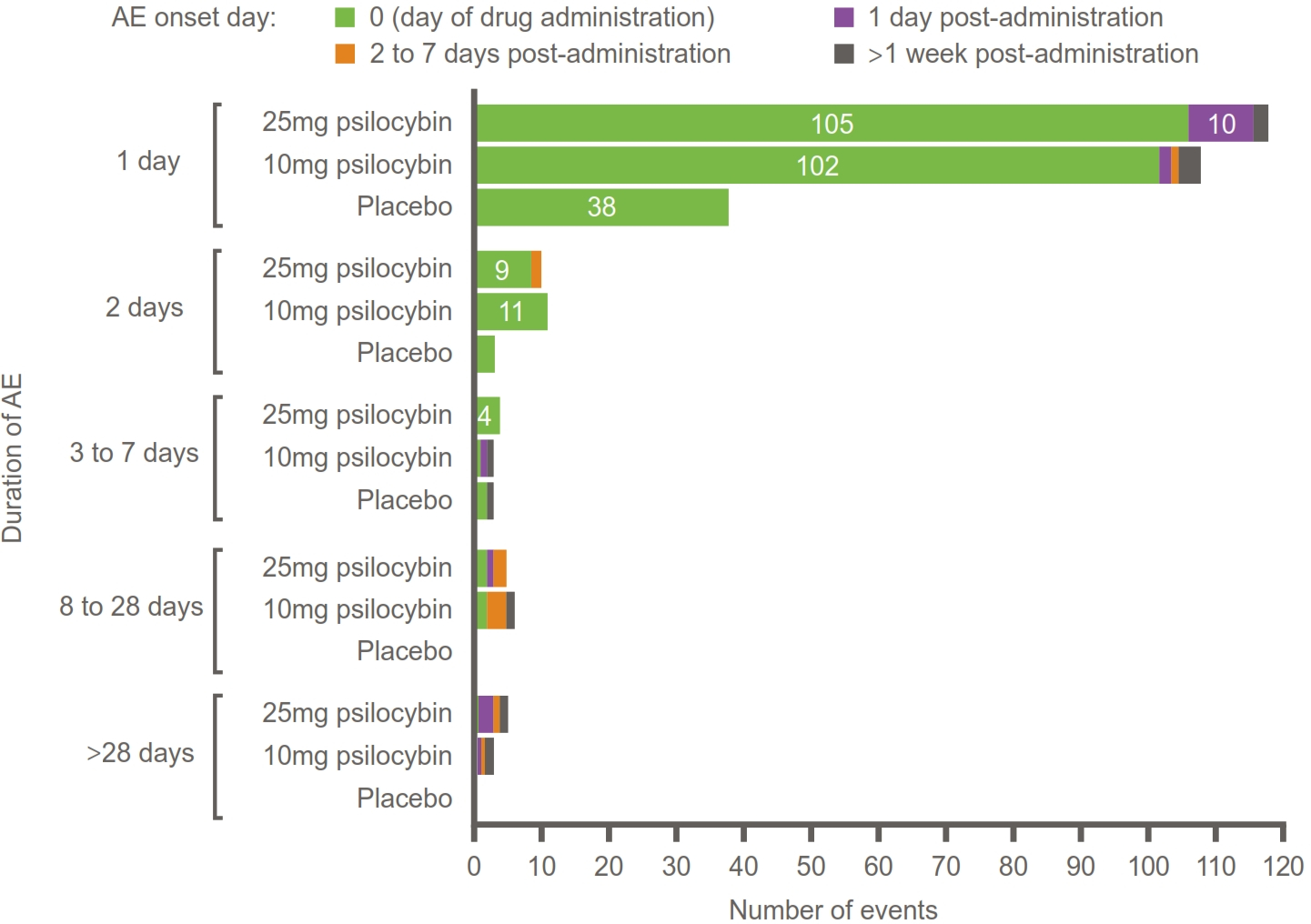
COMP 360は予想される幻覚体験を誘導し,服薬当日に解決するのが一般的である。これまでの第三者研究では,これらは治療効果との関連が認められてきた。すべての副作用のうち、68%の患者が投与当日に開始と緩解を報告している。12週間の試験では、すべての治療群の副作用持続時間の中央値は1日であった。
上図:最もよく見られる副作用:われわれの健康ボランティア試験において,治療腕別の発症と持続時間。
報告によると、57例の情緒変化があり、その中の2例のみが情緒の負の変化と関係がある。その中の1群はプラセボ群(“負の感情”、服用当日に緩和を開始)に出現し、もう1群はCOMP 360 10 mg裸蓋キノコ群に出現した(“気分は気まぐれ或いは敏感であり、翌日、8日後に緩和を開始した)
| | | | | | | | | | | |
| 25mg COMP360 (n=30) | 10mg COMP360 (n=30) | プラセボ(n=29) |
| “感情の変化”のAEは | 15 (50.0) | 13 (43.3) | 6 (20.7) |
| 内省 | 7 (23.3) | 5 (16.7) | 1 (3.4) |
| 反射する | 3 (10.0) | 2 (6.7) | 2 (6.9) |
| 共感心を増す | 2 (6.7) | 3 (10.0) | 0 |
| 合一的な感じ | 1 (3.3) | 4 (13.3) | 0 |
| 反省/反省 | 1 (3.3) | 1 (3.3) | 1 (3.4) |
| 笑い声がする | 1 (3.3) | 1 (3.3) | 0 |
| 新しい視点 | 1 (3.3) | 1 (3.3) | 0 |
| 他人のことを考えることの大切さを認識する | 1 (3.3) | 0 | 0 |
| 考え方がはっきりしている | 1 (3.3) | 0 | 0 |
| 沈思状態 | 1 (3.3) | 0 | 1 (3.4) |
| 思いやりを増やす | 1 (3.3) | 0 | 0 |
| 創造性を高める | 1 (3.3) | 0 | 0 |
| コネクティビティを高めた | 1 (3.3) | 0 | 0 |
| より楽観的な社交的な態度 | 1 (3.3) | 0 | 0 |
| 反省と新しい視点 | 1 (3.3) | 0 | 0 |
| 一体感と連通感 | 1 (3.3) | 0 | 0 |
| そんなに独断的にするな | 0 | 1 (3.3) | 0 |
| もっと感情的/敏感に感じる | 0 | 1 (3.3) | 0 |
| 休んだような気がする | 0 | 1 (3.3) | 0 |
| 知恵を増した | 0 | 1 (3.3) | 0 |
| 関係と社会への反省と新しい視点 | 0 | 1 (3.3) | 0 |
| 合一的な感じ | 0 | 1 (3.3) | 0 |
| 平静 | 0 | 0 | 1 (3.4) |
| アドレナリンが放出される感覚 | 0 | 0 | 1 (3.4) |
| マイナスの感情 | 0 | 0 | 1 (3.4) |
| 変わった音楽鑑賞 | 0 | 0 | 1 (3.4) |
_____________
上表:著者らの健康ボランティア試験において、COMP 360 25 mg群が報告した“情緒変化”AEsは発生率順に順位付けした。
情緒変化“のAEsは、参加者/研究者によって最初に報告された非MedDRA AEsの記述を保持しながら、このMedDRA第一選択用語に分類される。
参加者は一連の認知機能と情緒処理の評価を完了した。その中にケンブリッジ神経心理テスト自動化電池からの一連の検証された認知測定を含み、その中に空間工作記憶、迅速視覚情報処理とペアリングパートナー学習などの任務を含む。両群間で認知結果はやや異なるが,負の傾向は認められなかった
情緒処理に対する評価は社会認知任務、例えば絵共情テスト、眼読心テスト、社会責任尺度、社会価値方向とトロント共情アンケートを含む。情緒処理結果は一致した負の傾向がなく、COMP 360投与量はこれらの指標に短期或いは長期的な影響があることを示した。
分析によると,認知や情緒加工における負の傾向は認められなかった
結論.結論
この実験により、COMP 360は健康ボランティアにおける全体的な耐性が良好であることが示唆された。SAEなしでは、認知および情緒機能を評価する分析は、COMP 360が認知または情緒処理に臨床的に関連する短期的または長期的な負の影響を有さないことを示している。この試験は,1:1セラピストの支援の下,同一施設で最大6人がCOMP 360を同時に服用することが可能であることを示しており,将来の臨床試験や商業拡大を加速させることができると信じている
COMP 360裸蓋キノコ素治療TRDの2 b期試験
2021年、著者らは有効用量のCOMP 360(10 mgまたは25 mg)と1 mgのCOMP 360の心理的支持下でTRD患者に対する安全性と有効性を評価するために、2 b期の国際多点、ランダム、対照、二重盲検、用量発見臨床試験を完成し、北米とヨーロッパの10カ国と地域の22個の試験点に関連した。2022年11月ニューイングランド医学雑誌世界をリードする同業者評議医学雑誌は著者らのCOMP 360ヌードカバーキノコ素治療TRDの2 b期試験の積極的な結果を発表した。
試行設計
セロトニン作動薬を服用している患者は、ベースライン(1日目)の受診前に少なくとも2週間前に服薬を中止すべきである。投与前に,COMP 360ヌードゲラクチン会議の状況を理解し,準備するために,指定されたセラピストと少なくとも1回,最大3回の準備会議を行った。COMP 360裸蓋キノコ治療期間中、患者はCOMP 360を1剤服用するだけである。会議中に安全で支持的な環境を提供することを目的としている。患者は2回投与を受けてセラピストとの統合会議を行い,幻覚体験を検討した。患者には12週間のフォローアップを行い,投与後翌日に再訪問し,前3週は週1回,残りの9週間は3週間に1回訪問した。
主要、副次的、探索的端末
この実験の主な終点はMADRS総得点のベースラインから3週目への変化である.MADRSは独立した母国語評価者によって評価され,広く受け入れられている情緒障害評価である.この変数もベースラインから2日目,1,6,9,12週までの変化が分析されており,この2 b期臨床試験の目的はMADRを統計的に有意に低下させることである。
実験の副次的端末は、:
•3週目に反応した参加者の割合(総得点がベースラインより50%低下したと定義)
•3週目に緩和を有する参加者の割合(MADRS総得点10と定義);
•12週目に持続反応を有する参加者の割合。持続反応は、3週目および3週目までのいずれかの受診において反応基準を満たす患者の割合と、12週目以降のすべての後続診察においても反応基準を満たす患者の割合と定義される
•イベント発生の時間的措置:任意の理由で抗うつ薬治療の再開、自殺、抑うつによる入院、およびCOMP 360ヌードゲラリン治療に対する以前の反応の再発を含む。
副作用、バイタルサイン、臨床実験室評価、心電図結果と自殺願望/行為(すべての受診時にコロンビア自殺重症度評価表或いはC-SSRS採点)を用いてTRD患者におけるCOMP 360の安全性と耐性を評価した
この試験はまた、生活の質(EQ-5 D-3 L)、機能障害(ヒーン障害量表、SDS)、心理社会機能(仕事と社会適応尺度、WSAS)、認知(デジタル記号代替テスト、DSST)、焦慮(広汎性不安症、GAD-7)と自己報告の抑うつ重症度(QDS-SR-16)を含むが、探索的終点を評価した
学生募集基準
233名の成人TRD患者を募集して実験に参加した。TRD患者を“精神疾患診断と統計マニュアル”に適合する患者と定義し,5これは…。単発または反復発作に対するDSM-5
精神病的特徴のないMDDは、現在のうつ病発作の2つ、3つまたは4つの薬物治療の十分な用量および持続時間に反応しない
臨床表現
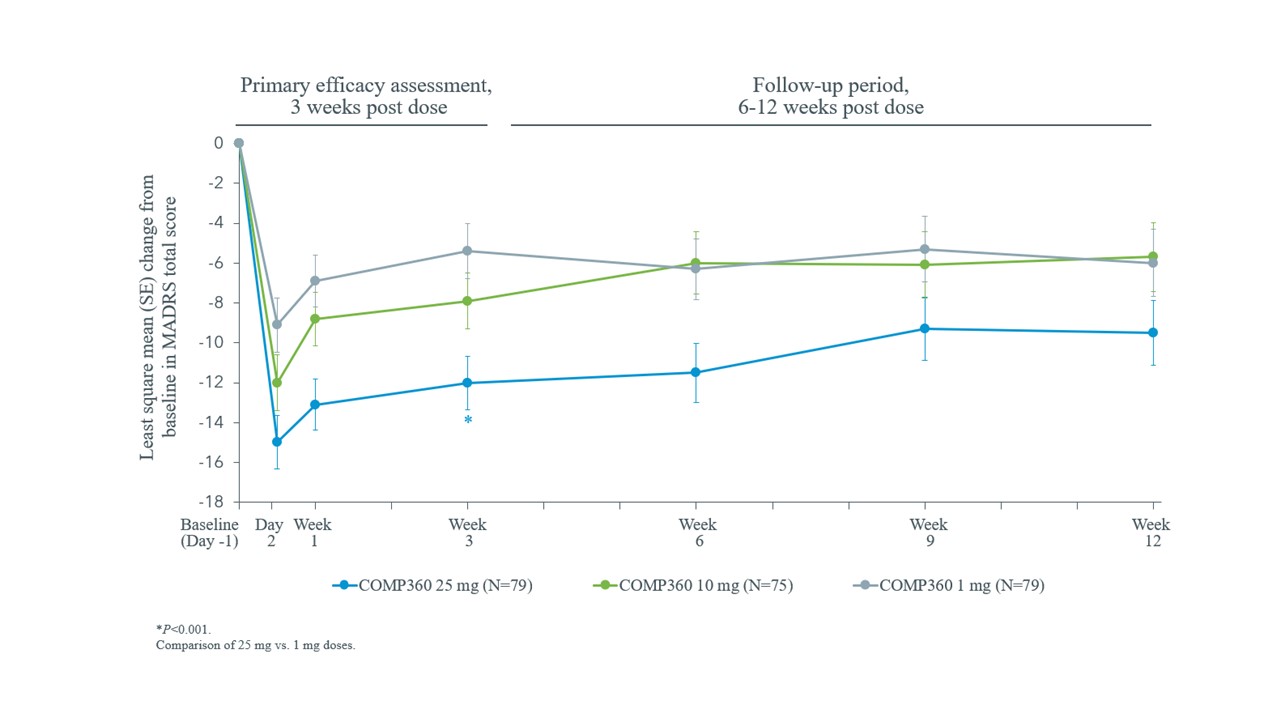
治療3週間、25 mg群と1 mg群のMADRS抑うつ尺度採点は統計学的有意差があった(P
MADRS総得点のベースラインに対する変化
MADRS=モンゴメリー·オズバーグ抑うつ尺度
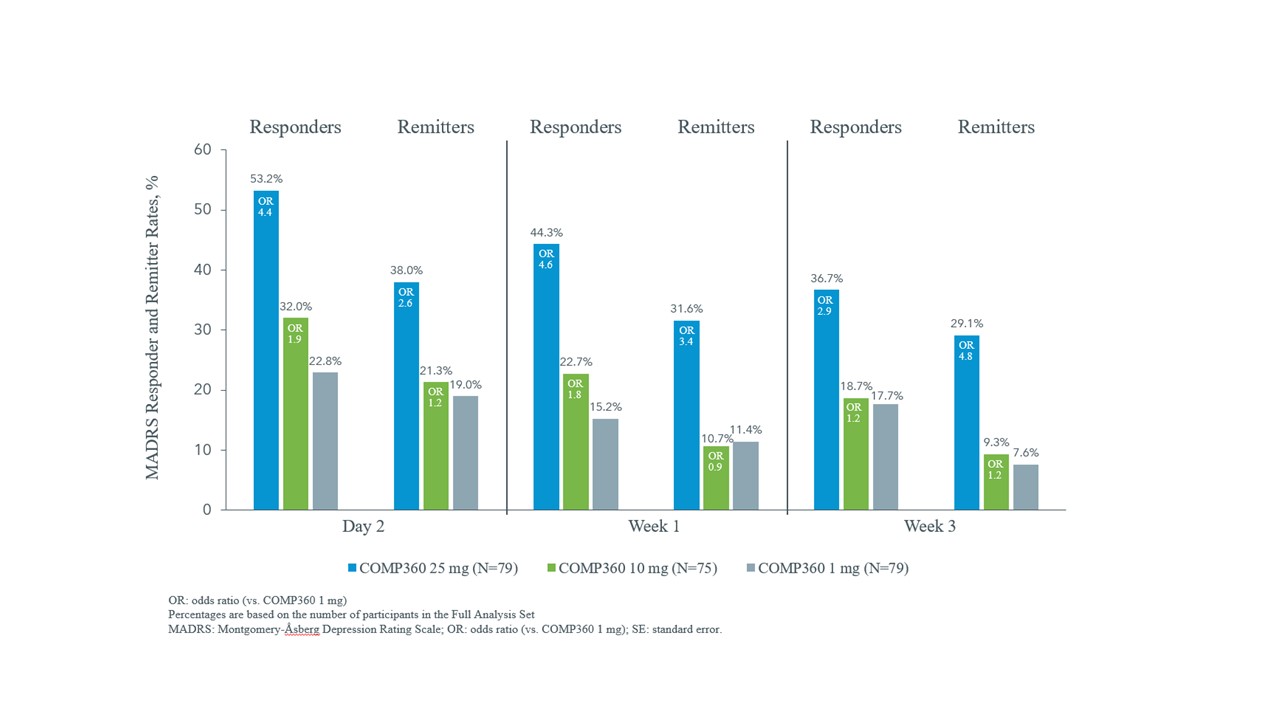
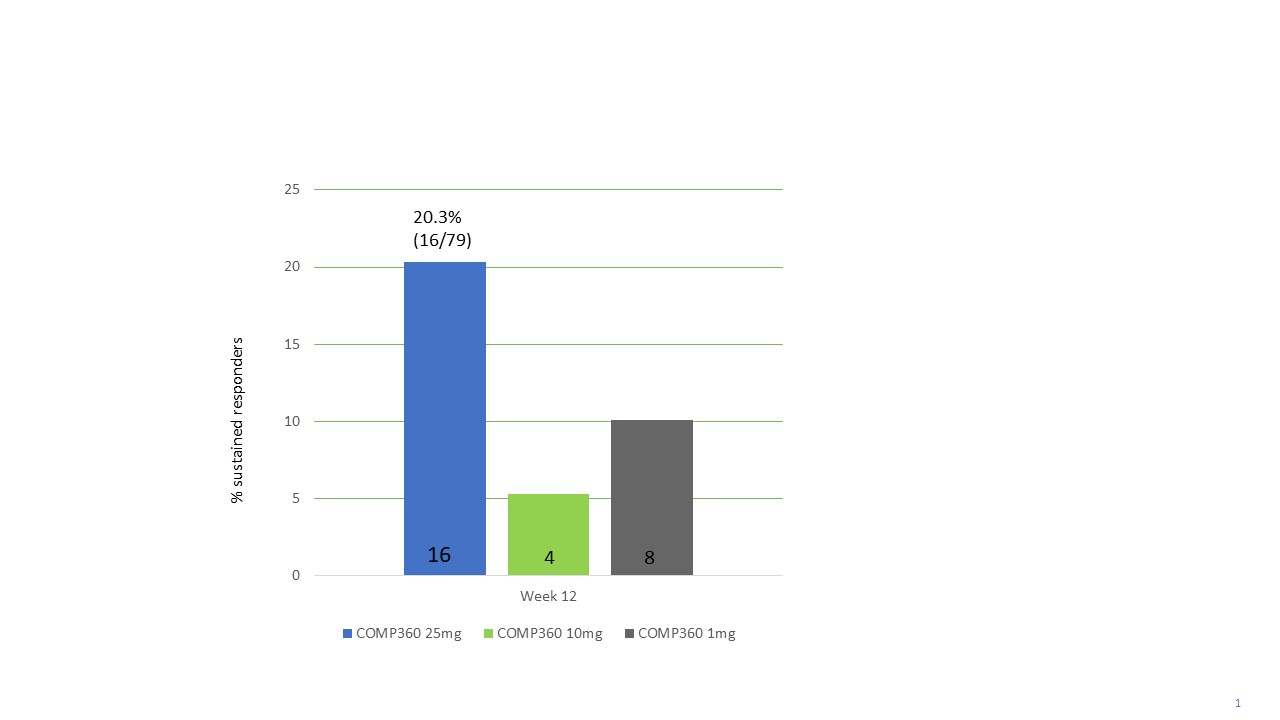
3週目には25 mg群の36.7%(29名)が有効(MADRS総得点はベースラインより50%低下)したが,1 mg群の有効率は17.7%(14名)であった。また,3週目では25 mg群で29.1%(23名)が緩解期(MADRS総得点10と定義)であったのに対し,1 mg群では7.6%(6名)であった。12週目には25 mg群で20.3%(16名)が持続的に有効であり(3週目と12週目にMADRS反応基準に達し,6週目と9週目に少なくとも1回受診したと定義されている),1 mg群では10.1%(8名)であった
MADRS応答率と緩解率
MADRS=モンゴメリー·オズバーグ抑うつ尺度
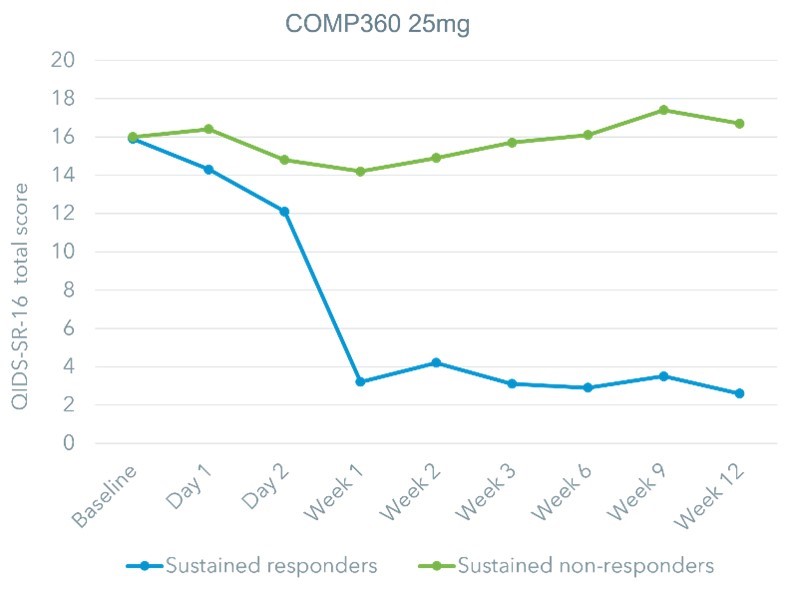
MADRS持続応答率
MADRS=モンゴメリー·オズバーグ不況評価表。継続応答人数(BAR単位)
MADRS反応基準に適合した患者は,3週目および3週目までのいずれの受診も,12週目およびそれまでのすべての後続受診,および新たなうつ病治療は開始されなかった。
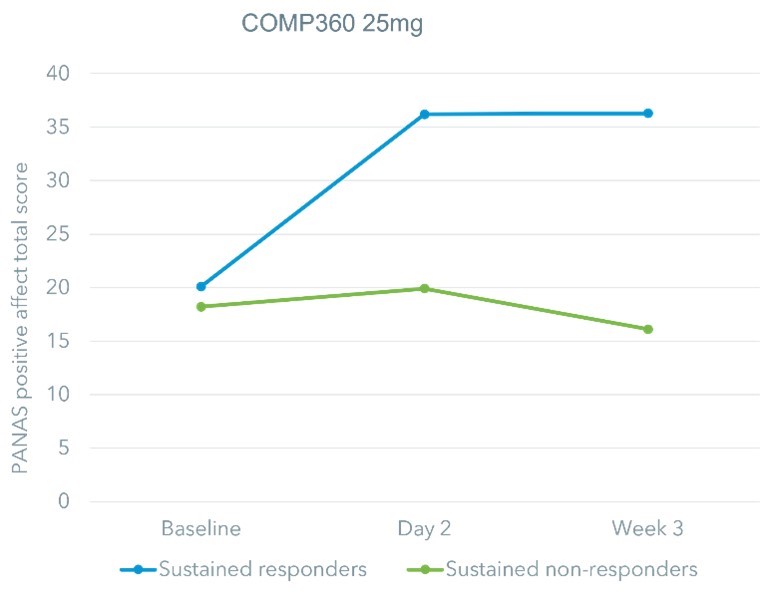
MADRSで臨床医師が評価したうつ病の重症度を観察する以外に、この試験はTRD患者に重要であると考えられている他の-回復に不可欠な面でもある-積極的と負の情緒、焦慮、自己評価のうつ病の重症度、生活の質、機能と認知を含む。これらの探索的措置は,COMP 360裸蓋キノコ治療25 mg投与群の患者が,1ミリグラム群と比較して利点があると報告していることを示している。積極と消極情緒を測定する積極と消極情緒尺度では、25 mg群患者はCOMP 360治療を受けた翌日とアンケート最終治療の3週目の時、積極情緒(例えば興味、興奮、強い)の増加は比較的に多く、消極情緒(苦悩、不安、恐怖を含む)の減少は比較的に大きかった。焦慮(広汎性焦慮障害-7項目尺度)、自己評価抑うつ(QDS-SR-16)と機能(ヒーン残疾病尺度と仕事と社会適応尺度)を測定した。25 mg群は1 mg群と比較して3週目にも大きな改善を示した。25 mg群中16名の持続応答者の事後分析により,生活の質,自己報告の抑うつの重症度と機能の変化は臨床的意義があり,これらの患者の平均得点は“正常”レベルに回復し,試験終了後12週間まで維持された。また,2日目と3週目には,持続応答者がベースラインよりも臨床的に意義のある積極的な影響の増加が認められた。
COMP 360は全体的に耐性が良好であり,90%以上の緊急治療不良事象(TEAE)の重症度は軽度あるいは中等度であり,77%以上のTEAEは服薬当日あるいは翌日に解決された。179人の患者は少なくとも1回のTEAEを報告した;治療群の中で最もよく見られるTEAE(全体>10%
発病率)は頭痛、吐き気、疲労と不眠である。12例の患者は緊急深刻な不良事件(TESAE)の治療を報告した。これらのTESAEには自殺行為,故意自己障害,自殺願望が含まれており,これらはTRD患者群でしばしば観察されている
患者の3分の2は以前に死亡を望む考えを持っていたが、これは患者のスクリーニング中に完了した自殺意思表によって評価された;これは、これらの有害事象のうちの1つを報告するすべての患者を含み、これは、試験中にこれらの事件を経験した患者が、試験前に自殺を考えたことがあることを患者スクリーニングで示していることを意味する。また,セキュリティデータの詳細な症例分析では,これらの自殺願望,自殺行為と故意自己傷害とCOMP 360服用TEAEとの因果関係は確立されていない。これらの事件はすべての治療群で発生し、発病時間と持続時間は異なる;大多数は裸蓋キノコ治療後1週間以上発生する。
•投与後、3群のMADRS第10項における点数に差はなく、MADRSは盲目的遠隔評価者によって自殺傾向を評価した;その後のすべての時点で、治療群の平均点数はベースラインより低かった
•自殺願望,自殺行為と故意に自己障害したTEAEは17例であり,その中に25 mg群7例,10 mg群6例,1 mg群4例であった
•これらの事件のうち14例は緊急重篤な有害事象(TESAE)の治療と報告されており,これらの事件は9名の患者のうち4名が25 mg群,4名が10 mg群,1名が1 mg群であった
•これらのTESAEの大多数(14イベント中10イベント)は、COMP 360ヌードゲラミン治療後少なくとも1週間後に発生します
•すべての自殺行為はヌードゲラニン治療コースの少なくとも1カ月後に発生し、これらの事件を報告したすべての患者は、事件発生前または事件発生時の最後の評価では反応しなかった
全体的に言えば、209名の患者はこの研究を完成した;25 mg群は5名の患者が退出し、10 mg群は9名の患者が退出し、1 mg群は10名の患者が退出した。
SSRI抗うつ薬補助治療としてのCOMP 360ヌードゲラリンの2期研究
われわれが完成した2 b期試験に加え,SSRIs補助投与時のTRD患者における安全性と有効性の第二段階試験をCOMP 360に完了した。この研究の結果は、より多くの詳細を含め、同業者評議の定期刊行物にも発表される。
この開放ラベルの研究はアイルランドとアメリカの臨床サイトからの19人の患者を含む。主要な終点は現有のSSRI抗うつ薬物方案に基づいて、COMP 360ヌードカバーキノコ25 mg治療を受けた患者の3週間時のベースラインMADRS総得点の変化である。
臨床表現
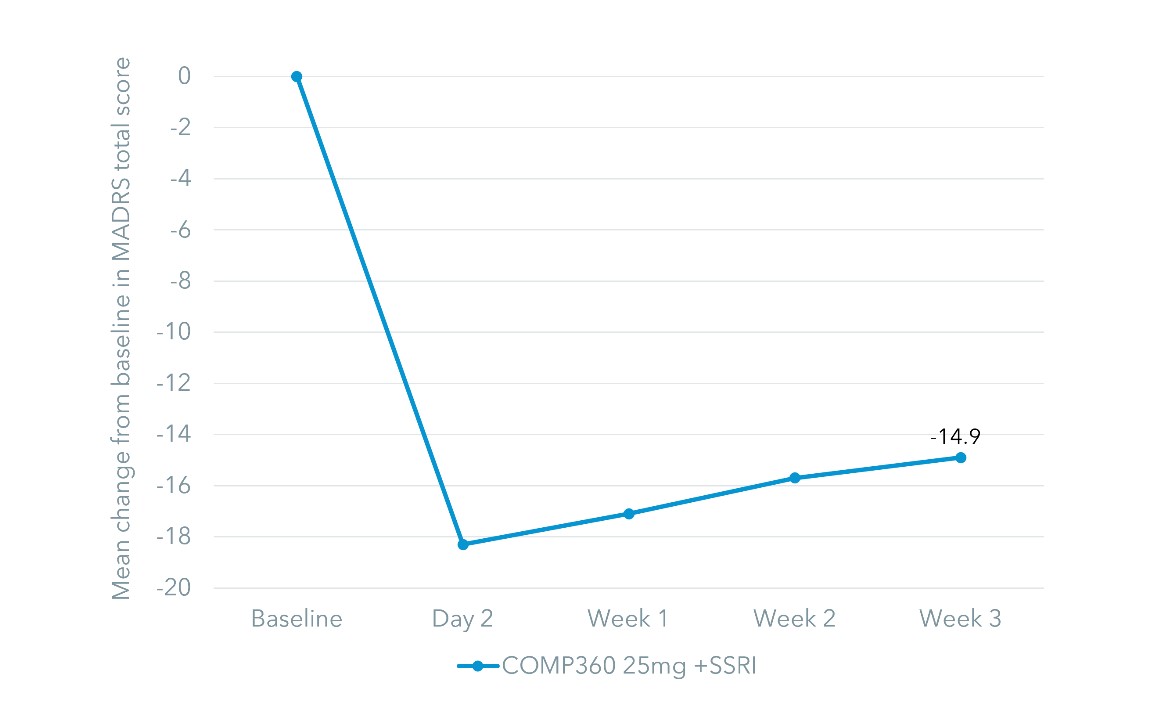
検討に入った患者のベースラインMADRSスコアは31.7であり,中等度から重度抑うつを代表した。3週目では19名中8名(42.1%)が応答者であり,全8名が送金者であった。3週目のMADRS総得点は治療前より平均14.9点低下した。COMP 360治療後2日目から3週目まで迅速に反応し、2 b期の結果と一致した
MADRS総得点のベースラインに対する変化
25 mg用量のCOMP 360ヌードカバーキノコ治療もまた、不安、臨床医および自己評価の抑うつ症状の改善、および積極的および消極的な影響を含む多くの他の指標の全体的な改善シグナルを示す。
患者の既存のSSRI治療と同時に25 mgのCOMP 360裸蓋キノコ治療を投与した時、それは通常耐性が良好であった。重篤なTEAE(生命の危険、障害の原因、入院、または一般的に重大な医学的意義を有する)に分類されず、自殺願望や行為または故意の自己障害に関連するTEAEもない。
長期第二段階研究
2022年には,我々の2 b期実験に参加した66人の参加者の長期追跡研究を完了した。 66名の被験者のうち,25 mg群22名,10 mg群19名,1 mg群17名,25 mg+SSRI群8名であった。この2 b期フォローアップ研究の主要な終点は新抑うつ事件の中央値時間である。予め指定された初歩的な分析は、長期フォローアップ研究に参加している人だけではなく、2 b期試験中のすべての参加者のこのようなイベントの中位時間を分析することである。COMP 360 25 mg群の新抑うつ事件の中位期間は92日であったが、10 mg群と1 mg群はそれぞれ86日と62日であった。
もう1つの主要終点のみを支持する事後分析には,我々2 b期研究における長期フォローアップ研究(COMP 004)に参加した参加者のみが含まれており,COMP 360 25ミリグラム群でこのような事件が発生した中間時間(189日)は,10ミリグラム群(43日)および1ミリグラム群(21日)(われわれ2 b期研究から入った患者)よりも長かった
27%または40.9%の参加者は、12週目に持続的または開始的な有害事象を有し、さらに、25 mgおよび10 mgを服用した群の参加者は、1 mg群と比較して新たなうつ病治療を開始する割合が低かった。 25 mg群では2回の自殺不良があり,10 mg群では2回,1 mg群では1回であった。 ♪the the the
長期追跡研究の結果は著者らの第三段階登録計画の設計に根拠を提供し、第二回COMP 360の服用がより良い耐性、反応と緩和結果を実現できるかどうかを調査することを含む
第3段階登録計画
COMP 360ヌードキノコ治療のTRDを評価するための第3段階計画を始めました第三段階計画は2つの重要な試験からなり、各試験には長期的な後続部分がある。キープログラミングは以下のとおりである
·キー試験1(COMP 005)(n=255):単剤(25 Mg)単一療法はプラセボと対照した。この試験は我々の2 b期試験(n=233)に見られる治療反応を複製することを目的とした。私たちは主にアメリカの地点でCOMP 005研究を行う予定です。2024年夏に主要データを発表する予定です。
·キー試験2(COMP 006)(n=568):反復用量単一療法を固定し、3用量群:25 mg、10 mg、および1 mgを使用した。この試験は,2回目の用量が治療応答者を増加させ,および/またはわれわれの2 b期試験で観察された反応を改善できるかどうかを調べ,COMP 360 10 mgの重複投与が意義のある治療反応の可能性を探ることを目的としている。私たちは2025年中に収益データを発表する予定だ。
·2つのキーテストの主な終点は、6週目のMADRS総得点とベースラインの変化である。
これらの実験のそれぞれには重要な部分と長期的な後続部分があるだろう。2つの試験の長期フォローアップ部分は類似している。長期後続行動部分は、26週間の延長を含むであろうが、その間、患者は元の割り当てられた治療アーム上に残り、再治療基準に適合する患者は、割り当てられた用量に応じてさらなる治療を受けることを選択することができるであろう。その後26週間の開放ラベル部分となり、その間、再治療基準に適合するすべての患者は、COMP 360ヌードゲニン25 mgの用量を受けることを選択することができるであろう。この設計は、COMP 360管理の永続性をより良く特徴付けることができると信じている
これらの研究の設計は,我々が実施している案修正案を反映しており,COMP 005サンプル量の再推定を反映し,長期追跡を2つの重要な研究に組み込むためである。我々のCOMP 005サンプルサイズの再推定は,チューリッヒ大学によるMDD中のCOMP 360のプラセボ対照研究の最新データ,および我々の2 b期データのさらなる分析に基づいており,特に1 mg群の中で最も少ない幻覚経験を有する参加者に注目した。2023年1月、COMP 005のスキーム修正案をFDAに提出し、フィードバックを要求し、FDAは2023年3月20日までにフィードバックを提供する予定であることを示した。私たちは私たちが受け取ったどんな意見も考慮するつもりだ。我々は最近、長期フォローアップをこの研究に組み入れ、すでにFDAによって審査されたCOMP 005方案修正案に反映された同じ設計原則に従うためにCOMP 006の方案修正案を提出した。
より多くの臨床試験
TRDに加えて,COMP 360裸蓋キノコ療法による神経性拒食症や創傷後ストレス障害の治療を評価している。著者らは二重盲検無作為対照第二段階臨床試験を行い、COMP 360裸蓋キノコ素が心理支持下で神経性拒食症患者を治療する安全性と有効性を調査している。60人の患者を募集するマルチセンター研究ですW神経性拒食症の第二段階試験の参加者募集とスクリーニングに挑戦したため,いくつかの遅延を経験した。これらの課題に対応するために,この高度に脆弱な患者群の実験負担を軽減するために,われわれの試験案を修正している。したがって、私たちは最初に予想したように、2023年にこの実験のデータを得ることはできない著者らはまた第二期臨床試験を行い、COMP 360ヌードカバーキノコによる創傷後ストレス障害の治療の安全性と耐性を評価している。これはマルチセンター、固定用量の開放ラベル研究で、20人の参加者を募集する。侵襲後ストレス障害研究のデータは2023年末に公表されると予想される。
機会を広げる
裸蓋キノコの活性代謝産物である裸蓋キノコは、セロトニン受容体を含むいくつかのセロトニン受容体の部分アゴニストである2A 受容体ですセロトニン.セロトニン2A受容体は脳の複数の領域に大量に発現し、これらの領域は認知と情緒処理において重要な役割を果たし、そして一連の認知と精神健康状況に影響する可能性がある。したがって、私たちは裸蓋キノコが横断的な診断作用を有する可能性があると信じ、著者らが開発した裸蓋キノコ治療TRDの核心計画ではなく、様々な拡張機会を探索するつもりである。例えば、COMP 360ヌードキノコによるPTSD患者の安全性および耐性を評価するための別の研究が行われている。私たちはまた、私たちの発見センターを通じて、アメリカペンシルベニア州フィラデルフィアの科学大学、アメリカカリフォルニア州サンディエゴのカリフォルニア大学サンディエゴ医学院、アメリカウィスコンシン州ミルウォーキーのウィスコンシン医学院と協力して、裸蓋キノコ素以外の化合物の潜在的な利益を研究した。“薬物発見センター”を見てください
機械学研究
著者らは学術研究者とCROと協力し、ヌードカバーキノコ治療の機序特徴を研究している。私たちはまた、この仕事の内容を研究するために、主にイギリス国内の博士課程ネットワーク(以下の大学:オックスフォード大学、ブリストル大学、レイディング大学、サウサンプトン大学)を構築した。私たちの機械学研究はCOMP 360を利用しており、現在は以下のテーマに集中しています
•裸蓋キノコ,我々の高純度多結晶型結晶製剤裸蓋キノコの活性部分及び他の幻覚剤が組換え細胞に基づく解析(オックスフォード大学トレバー·シャープ教授と協力),ヒト誘導多能性幹細胞由来ニューロン(マサチューセッツ州総病院−ハーバード医学院のStephen Haggarty教授と協力)及びローカル組織の機序を検討した。ここの目的はどのシステムが発見研究に最も適しているかを理解し、そして更に異なる薬物がどのように受容体を介したシグナル伝達に影響するかを理解することである
•ブリストル大学(特にマット·ジョーンズ教授)やCRO(例えばNeurotarとUlysses神経科学社)との協力により、神経細胞興奮活動の変化がどのように安静状態ネットワーク活動の全脳変化を媒介するかを決定するために、幻覚薬投与の総合電気生理反応を研究している
•ブリストル大学、ハーバード大学と南デンマーク大学の臨床前学術と協力し、著者らの高純度多結晶型裸蓋キノコ結晶製剤が多くの異なる行為に与える影響を研究し、感情偏見、報酬学習と強制行為を含み、これらは心理健康状況でよく観察される情報処理変化と関連する知見を提供する可能性がある
•レイディング大学とサウサンプトン大学との協力はまた、炎症調節過程がCOMP 360の作用機序において発揮する可能性のある潜在的な作用を理解することに重点を置いている
•フランスのボルドー大学との学術協力の一部として、遺伝子発現(MRNA)とエピジェネティック制御(miRNAとDNAメチル化)の短期と長期変化を調べることにより、著者らの高純度多型結晶配合裸蓋キノコの持続効果を研究した
•健康なボランティアはロンドン帝国工科大学で勉強し、COMP 360を用いてヌードゲラニン治療の急性と長期心理と脳影響を研究した
これらの研究は,我々の作用機序の理解をさらに深め,TRDやPTSD以外にどのような適応を探索するかを決定するであろう
その他の適応:臨床前研究
学術機関との連携により,臨床前と臨床データを生成し,TRD以外の適応におけるわれわれのヌードゲラクチン療法の利点を探索している
我々はブリストル大学やボルドー大学を含めてCROや学術機関と協力し,臨床前研究を行っている
他の適応:研究者が始めた研究やISS
臨床研究において、著者らはIIS臨床試験プロトコルに基づいて有力な学術機関と研究者と協力した。これらの機関はロンドン帝国工科大学、ロンドン国王学院、メリーランド腫瘍血液科、コロンビア大学医学センターニューヨーク州精神医学研究所、シェパード·プラット、カリフォルニア大学サンディエゴ校医学院、コペンハーゲン大学、チューリッヒ大学を含む。これらのIISシグナル生成および機序研究が以前に探索または現在探索されている適応は、神経性拒食症、自閉症、II型双極性感情障害、身体変形障害、慢性群集性頭痛、癌抑うつ、MDD、深刻なTRDおよび自殺願望を含む。
我々はIIS研究者にCOMP 360裸蓋キノコ素を提供し、すべての研究結果の公開を奨励した。COMP 360ヌードゲラニンを用いたIISが精神衛生保健を改善する可能性のある結果が生じた場合,事前に契約権がないにもかかわらず,臨床開発計画による研究の推進が求められる可能性がある。私たちのIIS研究者にCOMP 360ヌードカバーキノコを提供する以外に、私たちは過去に提供し、規制提出の支援を継続することが可能である。IISとの協力により,最終的にはできるだけ早く,可能な限り安全に患者により多くの革新をもたらしたいと考えている
2022年5月、COMP 360ヌードカバーキノコを使用して、COMP 360ヌードガイキノコがどのように自閉症成人の特定の脳経路に影響を与えるかを探索するIISを支援することを発表した。この二重盲検、無作為、プラセボ対照研究は自閉症と非自閉症成人の5-ヒドロキシルアミン脳ネットワーク機能に差があるかどうかを調べる。研究者は一連の画像技術と行動タスクを使用して、COMP 360裸蓋キノコ素がどのようにセロトニン系を調節するかを検査する。この探索的研究は、ロンドン国王学院の博士課程で、私たちに雇われた研究科学者によって行われた。 この研究はロンドン国王学院の精神医学,心理学,神経科学研究所(IoPPN)で行われ,King‘s IoPPNとSouth LondonおよびMaaudsley NHS Foundation Trustが共催した。40人の自閉症患者と30人の非自閉症患者を含む70人の成人参加者を募集する。
ISSからのデータ
2020年、イギリスロンドン帝国工科大学はCOMP 360のIISを完成し、“裸蓋キノコ素による深刻な抑うつ障害の治療:比較機序”(Psilodep-RCT,ClinicalTrials.gov標識:NCT 03429075)と題する。この無作為,二重盲検,探索的臨床試験では,COMP 360の奏効率と作用機序をSSRIのエスピランと6週間比較した。少なくとも中等度のMDDを有する成人参加者59名を、COMP 360を3週間毎に服用し、他の群は、1日6週間(10 mg 3週間連続、20 mg連続3週間)、および2剤1 mgのCOMP 360を3週間ごとに服用する2群にランダムに分けた。両試験群とも参加者は心理的支援を受け,実験の一部とした。16項目からなる抑うつ症状迅速リストである自己報告(QDS−SR−16)の主な治療効果の終点は,COMP 360群を使用する傾向があり,これは1週目から明らかであった。6週目には,QDS−SR−16の調整応答率(QDS−SR−16総得点でベースラインより50%低下したと定義)はCOMP 360群で70.2%,セチプララン群で48.0%,調整後緩解率(QDS−SR−16合計点5)であった。6週間はそれぞれ57.1%と29.1%だった。それぞれ分析を行った。MADRS-より広く使用され、受け入れられた臨床医師の評価基準に対して、Compassはそれを臨床試験の主要な終点として使用し、最小二乗平均治療差異は-7.2であることを発見した。仕事や社交機能、不安、回避、快感の欠如、幸福感を測定する他の副次的な終点にも類似したパターンが発見された。この仕事はすでに発表されている“ニューイングランド医学雑誌”(Carhart-Harrisら)2021年)。
2021年、米国メリーランド州ロクビルアキリノ癌センターのメリーランド州腫瘍血液科はCOMP 360のIISを完成させ、“深刻な抑うつ障害を有する癌患者におけるヌードホルモンの安全性と有効性”(ClinicalTrials.gov標識:NCT 04593563)と題する。癌と診断されMDDを有する30名の患者に関するオープンな研究では,25 mg用量のCOMP 360結合心理支持を受けた。患者開始時のMADRS平均得点は25.9であり,中等度抑うつを表し,COMP 360ヌードゲラリン治療後,平均得点は19.1点低下した。24名の患者の中で、持続的な反応が認められた(MADRS総得点はベースラインより50%低下し、3週目を含み、8週目にも満たされた);15名の患者は抑うつ症状の緩和(MADRSスコア)を認めた
2022年,シェパード·プラット健康システムはCOMP 360のIISを完成させた タイトルは“重症難治性うつ病(P−TRD)を有する参加者におけるCOMP 360の安全性と有効性の開放ラベル研究”である。 この研究者は2022年第2四半期の生物精神医学学会年次総会でこの研究のデータを公表した。この重症難治性うつ病患者12名に関連したオープン研究では,25 mg用量のCOMP 360と心理的支持を受けた。 この研究に参加する前に、すべての参加者は少なくとも5つの抗うつ薬治療を試みたが、成功しなかった。COMP 360裸蓋キノコ服用12週間後,58.3%(n=7)の参加者はMADRS反応基準を保持し,4分の1の参加者は緩和(n=3)を維持していることが分かった。全研究でMADRSによる自殺スコアは増加せず,治療に関連する重篤な有害事象も報告されていない。
2022年、カリフォルニア大学サンディエゴ医学院はCOMP 360のIISを完成させ、“神経性拒食症における裸ゲニンの評価:安全性と有効性”と題する。(ClinicalTrials.gov識別:NCT 04661514)。 この研究者は2022年第2四半期の生物精神医学学会年次総会でこの研究のデータを公表した。 神経性拒食症患者10名に関連したオープン研究では,25 mg用量のCOMP 360配合心理支持を受けた。この研究の主な目的は不良事件、バイタルサイン、心電図と臨床実験室テストに基づいて、単回25 mgのヌードゲラクチンの神経性拒食症参加者に対する安全性と耐性を評価することである。 食事障害検査(EDE)のグローバルスコアにより,40%(n=4)の患者は3カ月のフォローアップで臨床的に有意な減少を経験した。参加者は1カ月のフォローアップで名目的に統計的にEDEの形状懸念(治療前との平均変化=1.3 p=0.028)を有意に減少させた
3カ月のフォローアップでは,食事面の懸念は名目的に統計学的に有意に減少した(治療前との平均変化=1.1 p=0.047)。3カ月のフォローアップでは,EDEの体重懸念の変化は名目上の統計学的有意に近いが,統計学的有意差はなかった(治療前との平均変化=1.2)。COMP 360ヌードゲラニンの治療耐性は良好であり,治療に関連する重篤な有害事象は報告されていない
2022年、シェパード·プラット衛生システムは、“2型双極性感情障害(BP-II)うつ病を有する参加者における裸蓋キノコの安全性と有効性”と題するCOMP 360のIISを完了した。(ClinicalTrials.gov識別:NCT 0443384512)。 この研究者は,2022年12月に開催された米国神経精神薬理学会(ACNP)年次総会でこの研究のデータを公表した。 この14名の2型双極性感情障害患者に関する開放的研究では、患者は25 mg用量のCOMP 360を受け、心理的支持を与えた。 研究により、COMP 360裸蓋キノコ治療12週間後、86%の参加者(14人中12人)がMADRS尺度の反応と緩和標準に達した。研究経過を通して,MADRSによる自殺スコアは増加せず,躁病症状もなく,意外な有害事象や服薬困難もなかった。治療に関連した深刻な有害事象の報告はない。
2022年、チューリッヒ大学はCOMP 360のIIS研究を完成し、“第二段階、無作為、二重盲検、プラセボ対照、平行グループ分け、単中心裸蓋素の重度うつ病に対する治療効果の研究”と題した。(ClinicalTrials.gov識別:NCT 03715127)。研究者はこの研究のデータを“柳葉刀”(フォン·ロツら、“柳葉刀”2023年;56:101809)。この二重盲検無作為臨床試験において、52名の深刻な抑うつ障害を有する患者はランダムに2群に分けられ、1群は単一、中用量(0.215 mg/kg体重)のCOMP 360ヌードカバーキノコ素治療を受け、もう1群はプラセボ治療を受け、同時に心理支持を与えた。MADRSとBeck抑うつアンケート(BDI)採点を評価して抑うつの重症度を評価し、そして主要な終点をベースラインからCOMP 360服用後の2週間までの変化と定義した。2週間の終点では,MADRSの応答率は58%(COMP 360裸ゲラクチン:15/26対プラセボ:4/26;P=0.0034),BDI 54%(COMP 360裸ゲラクチン:14/26比プラセボ:3/26;P=0.0025)であった。2週間の終点で54%のMADRS患者は緩解率(COMP 360裸蓋キノコ:14/26対プラセボ:3/26;P=0.0023)を報告し,BDI評価の緩解率は46%(COMP 360裸蓋キノコ:12/26比プラセボ:3/26;P=0.013)であった。副作用は他の研究と一致し、頭痛、眩暈、吐き気と下痢を含む。約1カ月の試験期間中には自殺行為は発生せず,治療に関連した重篤な有害事象も報告されていない。
薬物発見センター
2020年8月5日,ペンシルベニア州フィラデルフィア科学大学(2022年にセントジョセフ大学に合併)との協賛研究協定に基づき,薬物発見センターを設立し,セロトニンに対する最適化迷幻剤や関連化合物の開発に専念した2A受容体は幻覚剤の潜在的な治療効果を媒介していると考えられている。協定によると、USciencesは、私たちに代わって研究サービスを提供し、再許可の権利、任意およびすべての目的のためのすべての共通所有の知的財産権、およびサービスの実行中に使用される任意の以前に存在する知的財産権の非独占的、全額支払いのグローバルライセンスを含む独占的で著作権付きのグローバルライセンスを付与します。協定によると、私たちは約50万ドルの研究サービス料を一度に支払い、USciencesがいくつかのマイルストーンを完了した後に分割して支払い、各ライセンス製品は最高90万ドルに達する。協定に基づいて私たちに許可された知的財産権に含まれる特許の有効な主張と、ライセンス製品の年間純売上高のより低い桁の特許使用料のパーセンテージを含む本協定によって我々に付与された知的財産権に含まれる特許の有効な権利要件は、カバーされるしかし、一定の削減が必要だ。また,第2段階実験の前に達成された合意については,USciencesは低い2桁の分割可収入率を得る権利があり,第2段階実験開始後に達成された合意に対しては,USciencesは中央値の分割可収入率を得る権利がある.事前に終了しない限り、協定は満了時に終了する共通知的財産権に含まれる任意の特許の最後の有効な権利要件を取り消すか. 一方に重大な違約が発生し、一定時間内にこのような違約を是正できなかった場合、私たちとUSciencesは合意を終了することができる。また,研究サービスに関する重大なセキュリティや規制問題が発生すれば,我々とUSCiencesは研究サービスを終了することができる.六十日前にUSciencesに書面で通知した後、任意に研究サービスを終了することもできます。 研究サービスがその運営に実質的な負の妨害を与える場合や,不可抗力イベントが継続して発生した場合,USciencesは研究サービスを終了することができる.協賛された研究協定によると、現在許可されている特許または特許出願はない。
2021年2月、カリフォルニア大学サンディエゴ校医学院(米国カリフォルニア州サンディエゴ)とウィスコンシン医学院(米ウィスコンシン州ミルウォーキー)との実験室協力により、発見センターを拡大した。これらのチームから来た科学者たちは、私たちとUSciencesのチームと違う場所で、仮想ネットワークで協力するだろう。
2021年9月、私たちは様々な幻覚や原因物質をカバーする特許出願を含む知的財産権の組み合わせを120万ドルで買収した。このIPは発明家のMatthias Grill博士と共同開発され、Matthias Grill博士はスイスのバーゼルMiHKAL GmbHの創始者で最高経営責任者であり、彼は私たちと協力して独占的な研究を行う
新製品候補製品を開発するプロジェクト。知的財産権の組み合わせがカバーする物質は、様々な幻覚および病原性化合物を含み、その中のいくつかはプロドラッグ、または体内で代謝されて活性薬物を産生する非薬理活性化合物である。新規物質は既知の化合物を含む新規誘導体であり、特性を最適化するとともに、治療効果や安全性に対する自信を増加させる。
前薬物開発研究はいくつかの潜在的な候補者の手がかり我々はさらなる研究に基づく開発を継続する予定であることを確認した。
投資する
デルix治療会社は
2020年3月6日,Delix Treateutics,Inc.8%(完全希釈に基づく),Delix Treeutics,Inc.は中枢神経系適応のための新しい小分子を研究する薬物発見·開発会社である戦略投資を行った。Delix治療会社は,幻覚作用を生じることなく,既存の幻覚剤を修正することで神経可塑性を促進することができる非幻覚性可塑剤を開発している。これらの化合物は一連の神経精神疾患を引き起こす可能性がある。
セラピスト養成
我々が構築したセラピスト訓練計画は,最初に心理学,精神医学,幻覚療法研究分野の専門家によって設計された。私たちは私たちのセラピスト訓練計画の質と拡張性を向上させるために機会を評価し続けている。これまで、私たちは200人以上のセラピストを訓練し、その中の約65人は独立して会議の司会を許可され、その中の約40人が私たちの積極的な臨床試験に参加した。臨床試験サイトは常にセラピストを推薦し、これらのサイトに雇われている。私たちのセラピスト訓練計画の詳細は2021年2月に同業者評議誌に発表されました精神医学の最前線です
私たちの中心的な訓練コースは
•第1レベル-理論訓練:私たちの相互作用療法士訓練プラットフォームを介して、セラピストマニュアル、全体の準備過程で必要な能力を説明するビデオ、裸蓋キノコ素管理、研究参加者との統合会議、および自己評価の知識検査を含む約5時間の自己進行オンライン学習を行う
•第二レベル--臨床実用技能訓練:約30時間の生中継、遠隔授業(Zoomによる)相互学習は、セラピスト養成士が指導した
•第三レベル-臨床訓練:この段階で、セラピスト実習生は、私たちの以前の裸蓋キノコ素治療研究(私たちの相互作用療法士訓練プラットフォーム上で)の一部の会議を審査し、独立して会議を指導する資格のあるセラピストと共にCOMP 360裸蓋キノコ治療研究に参加する参加者を支持する。第3レベルの授業を終えた後、セラピストは独立して授業を指導することができる
•第四レベル-持続的専門発展:セラピストは私たちの臨床研究に参加している間に団体指導と支持を受けている。指導者は、(参加者が同意した場合に)その指導者によって司会された授業のビデオ/音声記録を取得することができ、したがって、心理支援モードへの忠誠を保証するために十分なフィードバックを提供することができる。
私たちのセラピスト訓練プログラムは現在私たちが行っている研究に参加する専門家に利用可能です。規模の拡大に伴い、私たちは私たちの訓練をより多くの合格した精神衛生保健専門家に拡張するかもしれない。
デジタル技術を使って
デジタル技術は患者が心理治療サービスを獲得し、彼らの心理健康状況を管理する方法を変えると信じている。ソフトウェアアプリケーションは,従来の対面療法士による活動を強化することが予想される。遠隔コンサルテーションは,恥や交通機関の不足など,治療を得るための障害を除去するのに役立つと考えられる。さらに、デジタルツールは、患者自身が抑うつ発作を管理することを支持し、心理治療および薬物治療を補充および強化するために使用されるので、より大きな自己ケアを達成するであろう。
第三者と協力することで、私たちは現在、様々な方法でデジタル技術を使用しています
•TRD実験の参加者にオンライン準備プラットフォームを提供し、彼らを教育し、ヌードキノコの体験の準備を支援した
•私たちの全面的な対面訓練計画を補完するネットワークに基づく“共有知識”相互作用療法士訓練プラットフォーム
•我々の2 b期臨床試験では,モバイルデバイスを用いてデータを遠隔収集することを含む測定データを収集し,患者は研究地点へのすべての外来訪問を必要としない
•人とスマートフォンの相互作用を測定することでデジタル表現型情報を収集し
•人工知能と自然言語処理能力を利用して潜在的な地表徴候変化の機序を利用し、そして治療師の著者らの心理支持治療方案に対する忠誠度を評価した。私たちはデジタル技術、工学、人工知能の専門家からなる内部デジタルチームを構築しており、これを強化知能と人工知能と呼ぶ。我々は、他のデジタル会社と引き続き協力し、独自のデジタル技術ソリューションを研究、開発し、最終的に商業化し、これらの解決策は、我々が研究しているCOMP 360裸蓋キノコ療法を補完し、強化することが可能である。私たちはこれが私たちが個人化、予防的、そして予測的な看護モデルを提供できるかもしれないと信じている。
製造と供給
私たちは所有したり経営したりしないし、現在は製造施設を設立する計画もない。著者らは契約薬品製造組織或いはCDMOによってCOMP 360を含む活性薬物成分或いはAPIを合成し、API賦形剤を混合とカプセル化した。すべての製造過程は現行の良好な製造規範(CGMP)に適合している。私たちは引き続き第三者に依存して、私たちが使用する可能性のあるすべての臨床用品、薬品、薬品を生産する予定だ。私たちはもっと多くの契約製造業者を使用して、私たちの薬品を充填、ラベル、包装、保存、流通します。私たちは現在1つのサプライヤーに私たちの原料薬を提供することに依存しているが、他の適切な経験と専門知識を持つメーカーを見つけ、原料薬と充填剤サービスの予備サプライヤーとしている。私たちは、私たちの1つ以上の供給者を交換する必要がある任意の実質的な中断を避けるために、十分な原料薬供給を維持すると信じている。
商業化する
私たちのCOMP 360ヌードカバーキノコ療法が承認されれば、私たちは私たち自身の販売とマーケティング能力を利用して、アメリカと主要なヨーロッパ市場の公共および個人医療提供者と診療所ネットワークを狙う予定です。アジアや南米を含む選定された地域では、相補的な商業能力を有する第三者と商業的に協力する可能性がある。
承認されると、COMP 360が臨床現場で安全かつ有効に使用でき、心理的支援を提供できるように、一連のサービスを提供する予定である。これらのサービスには,セラピスト訓練,患者および医療提供者への情報および教育,設備調達と設置,認証および品質保証に関する指導などの治療センターの実施支援が予定されている。
卓越中心
我々が新たな精神衛生保健モデルを創造する雄心と一致するために,研究施設や革新実験室として卓越したセンターを設立する予定である。2021年1月、私たちはシェパード·プラット高度診断·治療研究所とアメリカメリーランド州ボルチモアに最初の卓越したセンターを設立した。2022年3月、著者らはロンドンと南ロンドン国王学院及びモデズリーNHS基金会信託基金(Maudsley NHS Foundation Trust、SLAMと略称する)と戦略協力を達成し、精神健康研究と革新センターを創立することを発表し、全体目標は仕事モード幻覚治療診療所、治療士訓練計画の開発、臨床試験とデータ分析などを行うことを通じて、幻覚療法の研究を推進することを通じて、患者が精神衛生保健根拠に基づく革新の機会を獲得することを加速することである
私たちの潜在的な未来卓越センターは“未来の診療所”のモデルとして設計され、それらの証拠を収集することで、患者体験を改善し、治療師を支援するために、私たちの治療モデルとデジタルテクニカルソリューションのプロトタイプを形作るつもりです。英才センターで開発された方法は私たちのパートナー診療所と共有される。
卓越センターは私たちが現有の行為健康提供者、コミュニティ精神健康チーム、個人診療所ネットワーク、一部の入院計画と外来診察計画を強化することができる革新的な看護モードの新しい青写真をテストと確立することを可能にする
いくつかの目的のために英才センターを設立しようとしています
•臨床試験を行い、概念検証研究を含み、著者らの治療モードを完備する
•臨床試験場として後期試験に参加し
•私たちの臨床試験を支援するセラピストを訓練し認証することができます
•安全および他のデータ、ならびに(許可可能な)知的財産権を生成して収集すること;
•患者の体験を改善するためのデジタルテクニカルソリューションの開発とテスト
•我々が考えている精神衛生保健の将来を示すことにより,科学的かつ臨床資源としての地域存在を強化し,患者,提供者,支払者,公共政策立案者を含む利害関係を促進する
•我々の方法を改善し、著者らの研究COMP 360ヌードカバーキノコ療法の安全とコスト効果を提供する。
競争
私たちの業界の特徴は多くの新興と革新的な技術があり、競争が激しく、自主製品の権利を非常に重視していることだ。他のTRD療法と比較して,我々が研究しているCOMP 360裸蓋キノコ療法は治療パラダイムの根本的な転換を代表していると信じているが,主要な製薬,専門製薬とバイオテクノロジー会社,学術機関,政府機関,医学研究組織を含む多くの異なる源からの潜在競争に直面している。我々が研究しているCOMP 360裸蓋キノコ療法を含め,我々が開発·商業化に成功した任意の候補製品は,将来発売される可能性のある看護基準や新たな薬理学的·身体療法と競合する。
現在、米国ではTRDの治療のための2種類の薬剤のみが許可されている:NMDA受容体拮抗薬Janssenによって販売されているSpravato(エスケタミン);および汎用のオザピンおよび塩酸フルオキセチンカプセル。定義によれば,TRDは2回以上のMDD治療後に助けられなかった患者を含むため,MDDに用いられる抗うつ薬はしばしば処方され,第2の薬剤と併用またはTRD患者の治療が増加する。いくつかの生物製薬会社は臨床開発中の療法を持っている。Sage治療会社やAxome治療会社などがTRDの治療法を開発していることが知られている
TRDにもECTやrTMSなど様々な身体療法が用いられている。CBTなどの心理治療方法は、MDDとTRD患者に用いられる
我々はまた,ウソナ研究所を含む501(C)(3)非営利医学研究組織からの競争に直面している。これらの非営利団体は、ヌードカバーキノコベースの製品を原価または無料で提供することを望んでいるかもしれませんが、これはCOMP 360の潜在的な市場を破壊しています。さらに、いくつかの営利生物技術会社または機関は、TRDを含む精神健康疾患を治療するために、裸蓋キノコの開発を専門に研究している。
他の組織や機関が,裸蓋キノコの精神健康や神経認知への使用を評価していることが知られている。また,他の幻覚化合物を探索しており,精神健康や神経認知疾患の治療に用いられている。
私たちがそれと競争するかもしれない多くの製薬、生物製薬とバイオテクノロジー会社はすでに彼らの治療法のために市場を設立して、私たちより多くの財力、技術、人力、その他の資源を持って、より優れた製品或いは治療法を開発、製造、マーケティングすることができるかもしれない。また、これらの潜在的競争相手の多くは、新しい治療物質の非臨床研究と人体臨床試験を行い、人類治療製品の監督許可を得る上で、私たちより多くの経験を持っている。したがって、私たちの競争相手は、代替または良質な製品に対するFDA、EMAまたはMHRAの承認に成功するかもしれない。また、多くの競争相手はより高い知名度とより広い協力関係を持っている。規模が小さく初期段階にある会社も重要な競争相手になる可能性があり、特に大手老舗会社との協力で手配されている。ますます多くの会社が新しい幻覚化合物を発見するために力を入れている。
特許その他の知的財産権及び独自の権利
特許や他の知的財産権(“IP”)の権利を独立して獲得し、維持し、守ることも、私たちのパートナーとの協力も、会社の革新療法の保護と商業化に重要である。私たちは引き続きアメリカ、EU、イギリス、および他の選択された司法管轄区域で私たちの革新のために特許、商標、商業秘密保護を求めます。これは、TRD、MDD、PTSDおよび拒食症を含む、我々の新規高純度多結晶型ヌードカバーキノコおよび関連する製造プロセス、医薬成分、製剤および精神および神経適応を治療する方法のための特許保護を求めることを含む。これはまた会社の様々な商標のための商標保護を求めることを含む。
特定の管轄区域が規制承認された後、既存の規制排他性(規制データ保護と市場排他性を含む)を主張することで、私たちの革新を有意義に保護することも求めます。例えば、米国FDAの承認を得た後、私たちは新しい化学物質(NCE)の5年間の規制排他性を得る権利があるかもしれないが、欧州医薬品局(EMA)の承認を得た後、私たちは10年間の規制の排他性を得る権利があるかもしれない。
もし私たちが第三者の挑戦(例えば、訴訟、認可後の審査、当事者間の審査、反対)を受けた場合、私たちはまた、必要に応じて私たちの特許および他の知的財産権および独自の権利を守るつもりだ
特許と特許出願
COMP 360に関連する特許の組み合わせは、以下の特許および公表された特許出願を含む
| | | | | | | | | | | | | | |
| 領土.領土 | 特許番号·出願番号 | 題材.題材 | 期日まで | 対応する前米国特許及び特許出願又はPCT国家段階出願 |
| アメリカです。 | 10,519,175 | 難治性うつ病の治療法 | ca.2038* | オーストラリア、ブラジル、カナダ、中国、コロンビア、ユーラシア特許機関、欧州特許庁、インドネシア、イスラエル、インド、日本、韓国、メキシコ、マレーシア、ニュージーランド、フィリピン、サウジアラビア、シンガポール、タイ、南アフリカで出願されている。 |
| アメリカです。 | 10,947,257 | 結晶型裸蓋キノコ経口剤形;重度抑うつ障害(MDD)の治療方法 | ca.2038* |
| アメリカです。 | 10,954,259 | 結晶型裸蓋キノコ;医薬製剤;MDDの治療法 | ca.2038* |
| アメリカです。 | 11,180,517 | 難治性うつ病の治療法 | ca.2038* |
| アメリカです。 | 11,505,564 | 製造方法 | ca.2038* |
| 国標 | 2571696 | 製造方法 | ca. 2037* |
| 国標 | 2572023 | 結晶型裸蓋キノコ;医薬製剤; 医療用途(難治性うつ病の治療を含む); 製造方法 | ca. 2038* |
| 国標 | 2576059 | 薬物製剤 | ca. 2038* |
| 国標 | 2588505 | 製造方法 | ca. 2038* |
| 国標 | 2588506 | 結晶型裸蓋キノコ;医薬製剤;
製造方法
| ca. 2038* |
| 徳 | 202018006384 | 結晶型裸蓋キノコ 薬物製剤 | ca. 2038* |
| % | WO/2020/212951
| 不安障害や他の病気を治療する方法は
| ca. 2040* | 米国、オーストラリア、カナダ、中国、欧州特許庁、日本、韓国の出願 |
| アメリカです。 | 17/540,962 | 外傷後ストレス障害の治療法 | ca. 2040* | |
| % | WO2020/212948
| 神経認知障害や他の疾患を治療する方法
| ca. 2040* | 米国、オーストラリア、カナダ、中国、欧州特許庁、日本、韓国の出願 |
| % | WO2020/212952
| うつ病や他の病気を治療する方法
| ca. 2040* | 米国、オーストラリア、カナダ、中国、欧州特許庁、日本、韓国、台湾地区の出願 |
| % | WO2022/207746 | 薬物製剤 | ca. 2042* | 台湾とアルゼンチンで提出された申請。国家段階申請は提出されるだろう。 |
*通常、米国特許およびほとんどの外国特許は、最初の有効出願日から20年後に満了します。米国では、販売前に規制部門の承認を必要とする特許期間(PTE)の延長を請求することにより、特許期間を20年以上に延長することができる。PTEは、規制審査によって実際に“失われた”特許期限を特許所有者の手に戻す。米国以外でも類似した特許期間延長を得ることができる。また、米国では、米国特許商標局による起訴遅延により、20年間の特許期間を延長する可能性もある。
2019年12月31日に付与された米国特許第10,519,175号は、Compass高純度結晶裸蓋キノコ素(COMP 360を含む)を用いた経口投与量製剤を用いて難治性うつ病を治療する方法に関する。これまで出願保留中に3つの第三者意見が提出されており,いずれも審査員が考慮し,特許出願の障害ではないことが発見された。 この特許付与後審査の請願書は2020年2月21日に提出され,2020年8月20日に却下された。
2021年12月15日、Freedom to Operate,Inc.は、米国第10,947,257号特許のライセンス後審査を要求する請願書を提出した。特許所有者の返事は2022年3月29日に提出された。2022年6月22日、米国特許商標局は支出後審査の機関を拒否した。 自由運営会社は2022年7月22日に再審請求を提出し、2022年8月16日に前例意見グループの請求を提出した。 USPTO取締役会は2023年2月10日に前例意見グループ(POP)審査の要請を拒否した。 USPTO取締役会はまだ再審請求について最終決定を下していない。
2021年12月22日、自由運営会社は、米国第10,954,259号特許のライセンス後審査を要求する請願書を提出した。特許権者の返事は2022年4月11日に提出された。2022年6月22日、米国特許商標局は支出後審査の機関を拒否した。 自由運営会社は2022年7月22日に再審請求を提出し、2022年8月16日に前例意見グループの請求を提出した。 USPTO取締役会は2023年2月10日に前例意見グループ(POP)審査の要請を拒否した。 USPTO取締役会はまだ再審請求について最終決定を下していない
GB 2571696番号GB 2571696であり、2020年5月に請求項が付与された英国特許は、裸蓋キノコの大規模生産、前記方法によって製造された裸蓋キノコ、および前記方法によって製造された裸蓋キノコを含む製剤に関する。 授与意向は2019年12月に出され、第三者意見は2020年1月下旬に提出され、最初の計画が授与される直前だった。この特許の付与は2020年5月27日に“特許雑誌”で発表された。この特許の有効期限は2037年10月8日です。 2020年6月11日、Kohn&Associates PLLCは、ライセンス発表後の特許主張の有効性に対する意見を要求する要求をイギリス知的財産局に提出した。 2021年4月27日、同機関は意見請求拒否の決定を発表し、いずれの場合もこのような意見を発表するのに適していないことが分かった。 規定された28日間の期間内に、誰もこの決定に上訴しなかった。
英国特許,番号GB 2572023は,2020年6月に付与される。この特許は、我々の結晶化裸蓋キノコ(COMP 360で使用される形態を含む)、結晶化裸蓋キノコの医薬製剤、結晶化裸蓋キノコの医療用途(難治性うつ病の治療のための使用を含む)、および結晶化裸蓋キノコの製造方法の請求項を含む。付与意向は2019年12月に出され、第三者意見は2020年1月下旬に提出される。付与通知は2020年6月23日に郵送され、2020年7月22日に“特許雑誌”で発表された。この特許の期限は2038年6月28日である。 2020年8月27日、Freedom to Operate,Inc.は、ライセンス後の特許請求の有効性に対する意見の発行を要求する要求をイギリス知的財産局に提出した。 2021年7月28日、機関は、承認された請求項1、3および10~20が創造的ではないと認定する拘束力のない意見を発表した。 私たちは、2021年11月5日に、修正された説明書が2021年12月1日に“特許雑誌”で反対意見を求める通知を出した特許請求に対する修正案を提出した。 2021年12月17日、機関は、この特許に対して撤回手続きを提起しない決定を発表した。
2022年11月22日、ポルタ·ソフィアは国際特許出願WO 2022/207746について第三者の意見を提出した。
商標
当社は、その商標の5、9、10、35、41、42、44またはそれらの様々な組み合わせの保護を求めている。 我々の商標組合せには,米国,EU,イギリスのコンパス,コンパス経路,C設計,MYPATHFINDER,chanterelleマークの出願が含まれており,詳細は次の表を参照されたい
同社はアメリカ、EU、イギリスでコンパス、コンパスパス、Cデザインマークの登録を持ち、イギリスではMYPATHFINDERマークの登録を持っている。MYPATHFINDER商標は米国とEUの申請が待っている;米国でのchanterelle商標の申請は待っている。同社はまた、他の国や地域に商標登録および処理すべき出願を有している
| | | | | | | | | | | | | | | | | |
標識 | 領土.領土 | クラス | 商標出願·登録 違います。 | 提出/登録日 | 状態.状態 |
羅針盤 | アメリカです。 | 5, 9, 10, 35, 41, 44 | 6648807 | 2022年2月22日 | 登録されている |
EU.EU | 5, 9, 10, 35, 41, 44 | 1568499 | May 25, 2021 | 登録されている |
イギリス.イギリス | 5, 9, 10, 35, 41, 44 | 3476175 | 2020年8月10日 | 登録されている |
羅針盤経路 | アメリカです。 | 5, 9, 10, 35, 41, 44 | 6648818 | 2022年2月22日 | 登録されている |
EU.EU | 5, 9, 10, 35, 41, 44 | 1570415 | June 1, 2021 | 登録されている |
イギリス.イギリス | 5, 9, 10, 35, 41, 44 | 3476163 | 2020年8月14日 | 登録されている |
C設計
 | アメリカです。 | 5, 35, 41, 42, 44 | 6836992 | 2022年9月6日 | 登録されている |
アメリカです。 | 9, 10 | 90801777 | June 29, 2021 | 未定である |
EU.EU | 5, 41, 44 | 1644148 | June 30, 2022 | 登録されている |
イギリス.イギリス | 5, 41, 44 | 1644148 | May 5, 2022 | 登録されている |
MYPATHFINDER | アメリカです。 | 9, 42 | 97174167 | 2021年12月15日 | 未定である |
EU.EU | 9, 42 | 1685580 | June 7, 2022 | 未定である |
イギリス.イギリス | 9, 42 | 1685580 | 2022年12月15日 | 登録されている |
チャニテーレ | アメリカです。 | 9, 42 | 97626719 | 2022年10月11日 | 未定である |
政府の監督管理
FDAと連邦、州と地方の各級及び外国のその他の監督管理機関は、その他の以外に、薬品の研究、開発、テスト、製造、品質管理、輸出入、安全、有効性、ラベル、包装、貯蔵、流通、記録保存、承認、広告、販売促進、マーケティング、承認後の監視と承認後の報告などの方面に対して広範な監督管理を行った。私たちのサプライヤー、契約研究組織、契約メーカーとは、私たちの候補製品を承認したい国家規制機関の様々な臨床前、臨床、製造、商業承認要件を満たすことを要求されます。薬品規制の承認を得て、その後適切な連邦、州、地方と外国の法規と条例を遵守する過程を確保するには大量の時間と財政資源が必要である。
米国では,FDAは改正された連邦食品,薬物,化粧品法案(FDCA),その実施条例,その他の法律に基づいて薬品を規制している。もし私たちが適用されるFDAまたは他の製品開発、臨床試験、承認に関する要件、または製品製造、加工、運搬、貯蔵、品質管理、安全、マーケティング、広告、販売促進、包装、ラベル、輸出、輸入、流通、または販売に関連する任意の他の法律要件を遵守できない場合、私たちは行政または司法制裁または他の法的結果を受ける可能性がある。これらの制裁または結果は、FDAが承認待ちの申請を拒否すること、進行中の研究のための臨床封印、承認された申請の一時停止または撤回、警告または無見出しの手紙の発行、製品の撤回またはリコール、製品の差し押さえ、再標識または再包装、製造または流通の完全または部分的な一時停止、禁止、罰金、民事処罰または刑事起訴を含むことができる。
FDAが我々の候補製品が治療適応薬として承認され、米国で発売される前に必要なプログラムには、一般に以下のような態様が含まれる
•良好な実験室実践或いはGLP要求による研究を含む、適用法規に従って広範な臨床前研究を完成する
•現在の良好な製造規範或いはcGMP条件下で、スポンサーが人体臨床試験に使用しようとしている薬物物質と薬物製品の製造、及び必要な分析と安定性テストを完成した
•臨床試験開始前に発効しなければならない研究用新薬出願またはINDをFDAに提出する
•各臨床試験が開始される前に、機関審査委員会またはIRBまたは各臨床試験場所の独立した倫理委員会によって承認される
•適用されたIND法規、良好な臨床実践或いはGCP要求及び他の臨床試験に関連する法規に基づいて十分かつ良好に制御された臨床試験に基づいて、各提案適応に対する研究製品の安全性と有効性を確定する
•FDAに新薬申請またはNDAを提出する
•FDAがNDAの使用料を審査するために支払う
•FDAは機密協定を受け取ってから60日以内に再審申請を受けることを決定した
•CGMP要件に適合する状況を評価して、施設、方法、および薬物の特性、強度、品質、および純度を維持するのに十分な制御を保証するために、医薬品を製造する1つまたは複数の製造施設の1つまたは複数の承認前検査を満足的に完了させる
•NDAをサポートするデータを生成する臨床試験場所に対するFDAの監査を満足できる可能性がある
•薬物が米国で任意の商業マーケティングまたは販売を行う前に、FDAによるNDAの審査および承認は、任意のFDA顧問委員会の意見を考慮することを含む。
薬物の前臨床研究と臨床試験
人体でいかなる薬物をテストする前に、候補製品は厳格な臨床前テストを経なければならない。臨床前研究は薬物化学、製剤、安定性の実験室評価、および体外培養安全性を評価し、場合によっては治療使用の理由を確立するための動物研究を提供する。臨床前研究の実施はGLPの安全/毒理学研究に対する要求を含む連邦と州の監督を受けている。臨床前研究の結果は,生産情報や分析データとともに,INDの一部としてFDAに提出されなければならない。INDはFDAがヒトに研究製品の使用を許可する要求であり,臨床試験開始前に発効しなければならない。IND提出後,いくつかの長期臨床前試験が継続される可能性がある。INDはFDAが受け取った30日後に自動的に発効し、FDAが30日以内に臨床試験の進行に対して懸念或いは問題を提起しない限り、人類の研究対象が不合理な健康リスクに直面することを懸念し、すべて或いは一部の臨床一時停止を強制的に実施することを含む。FDAは一時停止の理由をスポンサーに通知しなければならず,臨床試験が開始される前に決定された欠陥を解決しなければならない。INDの提出は、FDAが臨床試験の開始を許可しないか、または臨床試験をINDに最初に指定された条項に従って開始することを許可しない可能性がある。試験が開始されると,臨床休止を実施し,FDA解明の不足が是正されるまで試験を一時停止することも可能である。
臨床開発段階は、GCP要求に応じて、合格した研究者の監督の下で、すべての研究対象が任意の臨床試験に参加することにインフォームドコンセントを提供することを含む、試験スポンサーによって雇用されていないか、または試験スポンサーによって制御されていない医師である健康ボランティアまたは患者に候補製品を提供することを含む。臨床試験は,臨床試験の目標,管理手順,被験者の選択と排除基準,安全性と有効性をモニタリングするためのパラメータと基準を詳細に説明するプログラムに基づいて行われた。INDの一部として、すべての議定書とその後の議定書のいかなる修正もFDAに提出されなければならない。また,各臨床試験は,臨床試験を行う各機関の内部審査委員会によって審査·承認されなければならず,臨床試験に参加する個人が直面するリスクが最小限に減少し,期待される利益と比較して合理的であることを保証しなければならない。IRBはまた、各臨床試験対象またはその法律代表に提供されなければならないインフォームドコンセントを承認し、完成まで臨床試験を監視しなければならない。FDA、IRBまたはスポンサーは、対象が許容できない健康リスクに曝露されていることを発見することを含む、様々な理由で臨床試験を随時一時停止または中止することができる。実施中の臨床試験や完成した臨床試験を公的登録機関に報告することに関する要求もある。臨床試験に関する情報は,第一段階調査以外の臨床試験結果を含め,www.Clinicaltrials.gov上で発表するために特定の時間枠で提出しなければならず,米国国立衛生研究院がメンテナンスしている臨床試験データベースである。
米国国外で臨床試験を行うスポンサーはFDAの認可を得ることができるが,INDによる臨床試験を希望している。外国の臨床試験がINDで行われていなければ,研究がGCP要求に基づいて行われていれば,FDAはNDAを支持する研究結果を受け入れ,必要であればFDAは現場検査でデータを検証することができる。
治療適応を評価してNDAの発売承認を支持する臨床試験は通常3つの連続段階に分けて行われ、重なる可能性がある。
•第一段階-第1段階臨床試験は、研究製品を健康なヒトボランティアまたは標的疾患または疾患を有する患者に初歩的に導入することを含む。これらの研究は通常、人体内での製品の安全性、用量耐性、吸収、新陳代謝と分布、排泄、用量増加に関連する副作用をテストし、可能な場合に有効性の早期証拠を得ることを目的としている。
•第二段階-第二段階臨床試験は、一般に、この薬物の潜在的治療効果を評価し、最適な用量および投与計画を決定し、可能な不良副作用および安全リスクを決定するために、特定の疾患または状態の限られた患者集団に製品を使用することに関する。
•第3段階-第三段階の臨床試験は通常拡大した患者群に対する研究製品の使用に関連し、更に投与量を評価し、臨床治療効果の統計的顕著な証拠を提供し、そして更に安全性をテストし、通常は複数の地理的に分散した臨床試験地点で行われる。これらの臨床試験は研究製品の全体的なリスク/利益比率を確定し、製品の承認と医師ラベルに十分な基礎を提供することを目的としている。
承認後試験は,4期臨床試験や上場後研究と呼ばれることがあり,最初の上場承認後に行われる可能性がある。これらの試験は、通常、臨床環境において製品を使用するための追加の安全データを生成するために、予期される治療適応下で患者の治療から追加の経験を得るために使用される。場合によっては,FDAはNDA承認の条件として4期臨床試験を強制的に要求する可能性がある。
その他の情報に加えて,臨床試験結果を詳細に説明する進捗報告は少なくとも毎年FDAに提出されなければならない。INDセキュリティ書面報告書は、試験スポンサーにおいて、深刻かつ予期しない疑わしい有害事象、他の研究または動物を報告する資格があると判断しなければならない体外培養テストにより、人類ボランティアに対して重大なリスクがあり、及び方案或いは研究者マニュアルに記載されたテストと比べ、深刻な不良反応の発生率は臨床で任意の重要な増加があることを表明した。スポンサーはまた、FDAに任意の意外、致命的、あるいは生命に危害を及ぼす疑いのある副作用をできるだけ早く通知しなければならないが、いずれの場合も、スポンサーが初めて情報を受け取った後の7つの日数に遅れてはならない。
臨床試験と同時に、会社は通常追加の動物研究を完成し、候補製品の化学的および物理的特性に関する追加情報を開発し、cGMPの要求に基づいて最終的に商業的に薬物製品を量産するプロセスを決定しなければならない。製造過程は一貫して高品質の候補製品ロットを生産できる必要があり、メーカーは最終薬物製品の特性、強度、品質と純度をテストする方法などを開発しなければならない。また,適切な包装を選択·テストし,候補製品が賞味期限内に受け入れられない変質が生じないことを証明するために安定性研究を行わなければならない。
アメリカの薬品の発売審査
必要な臨床試験,臨床前研究や臨床試験の結果,製品の化学,製造,制御,提案されたラベルなどに関する詳細な情報を想定し,NDAパッケージの一部としてFDAに提出し,その製品を1つまたは複数の適応に使用することの承認を求めた。NDAは1つまたは複数の適応を指定する新薬発売に対する承認要求であり,要求される適応におけるその薬物の安全性と有効性の証拠を含まなければならない。マーケティング申請は臨床前研究と臨床試験の否定と曖昧な結果、そして積極的な発見を含まなければならない。データは、製品使用の安全性および有効性を試験するために、または研究者によって開始された研究を含む多くの代替源からの臨床試験からのものである可能性がある。上場承認を支持するためには、提出されたデータは研究製品の安全性と有効性を確定し、FDAを満足させるために、品質と数量で十分でなければならない。薬物がアメリカで発売される前に、FDAはNDAを承認しなければならない。
FDAは、提出されたすべてのNDA出願を受け入れる前にそれを検討し、NDA出願を受け入れるのではなく、より多くの情報の提供を要求する可能性がある。FDAはNDAを受信してから60日以内にNDA届出を受け入れる決定をしなければならず,このような決定にはFDAが届出を拒否することが含まれる可能性がある。提出された書類が届出を受けると、FDAは始まります
不拡散条約に対する深い実質的な検討。FDAは、薬物が求められた適応に対して安全かつ有効であるかどうか、およびその製造、加工、包装、または保有施設が、製品の持続的な安全、品質および純度を確保するための基準に適合しているかどうかを決定するために、セキュリティプロトコルを検討する。FDAが“処方薬ユーザ費用法案”(PDUFA)に基づいて達成した目標と政策によると,FDAは提出日から10カ月以内に新分子実体NDAの予備審査を完了して出願人に応答することと,新分子実体NDA提出日から6カ月以内に優先審査を行うことを目標としている。FDAは、そのPDUFA規格または優先NDAの目標日を常に満たすわけではなく、審査プロセスは、FDAがより多くの情報を提供または明確にすることを要求することによって延長されることが多い。
さらに、修正されたPDUFAによれば、各セキュリティプロトコルには、かなりの使用料が添付されなければならない。FDAは毎年PDUFAユーザ料金を調整する。場合によっては、小企業が初めて出願した出願料を免除することを含む、費用を免除または減免することができる。また,孤児薬として指定された製品については,NDAに対して使用料を評価せず,非孤児適応も含まれていない限りである。
FDAはまた、薬物の利点がそのリスクよりも大きいことを確実にするために、REMSを提出する必要があると考えられる場合、リスク評価および緩和戦略、またはREMSの提出を要求する可能性がある。REMSは、投与ガイドライン、医師コミュニケーション計画、評価計画、および/または制限された分配方法、患者登録、または他のリスク最小化ツールのような安全な使用を保証する要素のようなリスク評価および緩和戦略を使用することを含むことができる。
FDAは新薬の申請を諮問委員会に提出するかもしれない。諮問委員会は,臨床医や他の科学専門家を含む独立した専門家からなるグループであり,審査,評価を担当し,申請を承認すべきかどうか,どのような条件で提案すべきかについて提案している。FDAは諮問委員会の提案に制限されていないが、それは決定を下す時にこれらの提案を慎重に考慮するだろう。
秘密協定を承認する前に、FDAは通常、製品を生産する1つまたは複数の施設を検査する。FDAは、製造プロセスおよび施設がcGMP要件に適合していることを決定し、要求された仕様の下で製品が一貫して生産されることを保証するのに十分でない限り、申請を承認しないであろう。さらに、NDAを承認する前に、FDAは、GCPおよび他の要件に適合することを保証し、FDAに提出された臨床データの完全性を保証するために、1つまたは複数の臨床試験場所を検査することができる。
NDAとすべての関連情報を評価した後,諮問委員会のアドバイス(あれば)や製造施設や臨床試験地点に関する検査報告を含めて,FDAは承認状を発行する可能性があり,場合によっては完全な返信が発行される可能性がある。完全な返信状は、一般に、NDAの最終承認を保証するために満たされなければならない特定の条件の宣言を含み、FDAが出願を再検討するために追加の臨床または臨床前試験が必要とされる可能性がある。この補足情報を提出しても、FDAは最終的にその申請が承認された規制基準を満たしていないと決定する可能性がある。もしこのような条件がFDAの満足を得たら、FDAは通常承認書を発行するだろう。この薬物の商業マーケティングを許可し、特定の適応の具体的な処方情報を提供する。
FDAが製品を承認したとしても、解決すべき特定のリスクに応じて、承認された製品の使用適応を制限する可能性があり、製品ラベルに禁忌症、警告または予防措置を含むことが要求され、承認後に薬物の安全性をさらに評価するための第4段階の臨床試験を含む承認後の研究が要求され、商業化後に製品を監視するための試験および監視計画が要求されるか、または流通および使用制限またはREMS下の他のリスク管理メカニズムを含む他の条件が適用されることは、製品の潜在的な市場および利益に大きな影響を与える可能性がある。FDAは発売後の研究或いはモニタリング計画の結果に基づいて、製品の更なるマーケティングを阻止或いは制限することができる。承認後、新たな適応の追加、製造変更、および追加のラベル宣言など、承認された製品のいくつかのタイプの変更は、さらなるテスト要件およびFDAの審査および承認を受けるであろう。
薬品開発と審査計画を加速する
FDAは新薬開発と審査を促進と加速するためのいくつかの計画を維持し、深刻或いは生命に危害を及ぼす疾病或いは条件の治療において満たされていない医療需要を満たす。これらの計画は、迅速チャネル指定、突破的治療指定、優先審査、および承認の加速を含み、これらの計画の目的は、FDA標準審査スケジュールよりも一般的に許容されるよりも早く患者の手に到達するように重要な新薬の開発または審査を加速することである。
1つの薬剤が、深刻または生命に危険な疾患または状態を治療することを意図し、そのような疾患または状態を解決するための満たされていない医療需要の潜在力を示す場合、迅速なチャネル指定を得る資格がある。迅速チャネルはスポンサーに指定され、臨床前と臨床開発中にFDAと相互作用することで、より多くの機会を提供します
マーケティング申請が提出されると、スクロール審査が可能になります。スクロール審査は、スポンサーが完全な申請を提出する前に、機関がマーケティング申請の内容の一部を審査することができることを意味する。さらに、1つの薬剤が、深刻なまたは生命に危険な疾患または状態を治療することを意図しており、初歩的な臨床証拠が、1つまたは複数の臨床的に重要な終点において、例えば、臨床開発早期に観察された重大な治療効果のような既存の療法よりも有意な改善を示す可能性がある場合、画期的な治療指定を受ける資格がある可能性があることを示す。画期的な治療指定は,効率的な薬物開発計画の密な指導を提供するほか,迅速チャネル指定のすべての機能を提供し,適切な場合に高度管理者や経験豊富な審査者を学際的な審査に参加させることを含むFDAの開発加速に対する組織承諾を提供している。
迅速なチャネルまたは突破療法の称号を有する製品を含むFDA承認を提出する製品は、優先的な審査指定および承認の加速を含むFDAの審査および承認プロセスを加速させるための追加の計画を得る資格がある可能性もある。NDAまたはBLAが提出されると、マーケティング申請の対象となる薬剤が、重篤な疾患または状態の治療、診断または予防において顕著な安全性または有効性を提供する可能性がある場合、製品は、優先審査指定を受ける資格がある。優先審査によると、FDAがマーケティング申請に対して行動する目標日は6ヶ月であり、標準審査は10ヶ月である。製品が代替終点に対して合理的に臨床利益の影響を予測する可能性があることが証明されるか、または中間臨床終点への影響が不可逆的な発病率または死亡率の影響よりも早く測定されることができる場合、加速承認を得る資格があり、病状の重症度、希少性または流行率、および代替治療の利用可能性または不足を考慮すると、不可逆的な発病率または死亡率または他の臨床的利益への影響を予測する可能性が高い。
加速承認は、一般に、製品の臨床的利益を検証および説明するために、追加的な承認後の研究を行うことにスポンサーが同意することに依存する。2022年食品·薬物総合改革法案(FDORA)によると、FDAは、承認前または承認を加速させた製品の承認日後の特定の期間でこのような試験を適宜行うことを許可されている。スポンサーはこのような研究の最新状態を180日ごとにFDAに送信することも求められており,募集目標の達成を含め,FDAはこれらの情報を迅速に公開しなければならない。FDORAによれば、FDAは、例えば、スポンサーがそのような研究をタイムリーに行い、必要な更新をFDAに送信することができなかった場合、または検証的試験が製品の予期される臨床的利益を検証できなかった場合、迅速な承認の下で承認された薬物または適応の承認を撤回することができる。さらに、FDAは、承認を加速させる条件として、上場承認後120日以内に伝播または発行しようとするすべての広告および販売促進材料を、承認前の審査中に機関に提出しなければならないことを一般的に要求する。120日の期限が過ぎた後、すべての広告および宣伝材料は、少なくとも最初の伝播または出版の予定時間の30日前に提出されなければならない。
1つの製品が1つまたは複数のこれらの計画の条件に適合していても、FDAは、製品がもはや資格条件を満たしていないと後で決定することができ、またはFDAが審査または承認する期間が短縮されない可能性がある。さらに、迅速チャネル指定、突破的治療指定、優先審査、および加速承認は、開発または審査プロセスを加速させる可能性があるにもかかわらず、承認の科学的または医学的基準を変更することなく、または承認を支援するために必要な証拠の質を変更することはない。
アメリカの薬品承認後の要求
FDAによって生産または流通を許可された医薬品は、記録保存、定期報告、製品サンプルおよび流通、製品不良反応の報告、販売促進および広告要件の遵守に関連する要件を含み、未承認用途または患者集団普及製品(“ラベル外使用”と呼ばれる)への制限、および業界支援の科学的および教育活動の制限を含むFDAによって持続的に規制される。医師はラベル外の用途のために合法的な製品を処方する可能性があるが、メーカーはこのような用途を販売したり普及させたりしてはならない。FDAや他の機関はラベル外用途の普及を禁止する法律や法規を積極的に実行しており、ラベル外用途を不当に普及させていないことが発見された会社は、連邦や州当局の調査を含む重大な責任に直面している可能性がある。処方薬宣伝材料は初回使用または最初の発表時にFDAに提出されなければならない。さらに、薬物が適応、ラベルまたは製造プロセスまたは施設の変化を含む任意の修正がある場合、出願人は、新しいNDAまたはNDAサプリメントの承認を得るために提出および提出を要求される可能性があり、これは、追加のデータまたは臨床前研究および臨床試験を開発する必要があるかもしれない。
FDAはNDAを承認するための条件として、いくつかの承認後の要求を加えるかもしれない。例えば、FDAは、製品の商業化後の安全性および有効性をさらに評価および監視するために、第4段階の臨床試験およびモニタリングを含む上場後試験を要求する可能性がある。さらに、承認された医薬品の製造および流通に関与する医薬品製造業者および他のエンティティ、ならびに製品、成分および成分を提供するエンティティは、
FDAおよびいくつかの州機関にその機関を登録し、いくつかのプログラムおよびファイル要件を実施するcGMPを含む、いくつかのプログラムおよびファイル要件を実施することを含む、FDAおよび特定の州機関の定期的な抜き打ち検査を受ける必要がある。法律や法規の要求を守らない場合、メーカーは警告状、生産停止、製品差し押さえ、禁止、民事処罰、または刑事起訴などの法律または法規の制裁を受ける可能性がある。また、持続的で年に1回の処方薬製品計画使用料もある。
その後、製品には、予期されない深刻度または頻度の不良事象、または生産プロセス、または規制要件を遵守できなかったことを含む、以前に未知の問題が存在し、新しいセキュリティ情報を追加するために承認されたラベルの改訂を招く可能性があり、新しい安全リスクを評価するために発売後の研究または臨床試験を要求するか、またはREMSに従って流通または他の制限を実施することが可能であることが分かった。他の他の潜在的な結果には
•製品の販売や製造を制限し、市場から製品を完全に撤回したり、製品をリコールしたりする
•セキュリティ警報、親愛なるヘルスケア提供者への手紙、プレスリリース、または製品に関する警告または他のセキュリティ情報を含む他の通信;
•承認後の臨床試験には罰金、警告状、一時停止を科す
•FDAは、承認された出願の承認を拒否するか、または承認された出願を補充するか、または製品の承認を一時停止または撤回する
•製品の差し押さえ、差し押さえ、あるいは製品の輸出入を許可しないことを拒否した
•民事又は刑事処罰の禁止又は適用;及び
•法令、会社の誠実な合意に同意し、連邦医療計画への参加を禁止したり、連邦医療計画から除外したり、宣伝材料、ラベル、訂正情報を強制的に修正したりする。
規制対象物質
1970年の連邦制御物質法、あるいはCSA、及びその実施条例は、制御物質規制の“閉鎖システム”を構築した。CSAはDEAの監督下で登録、安全、記録保存と報告、貯蔵、製造、流通、輸入、その他の要求を規定している。DEAは制御物質の監督管理を担当する連邦機関であり、生産、輸入、輸出、流通、制御物質の研究或いは配布を要求する個人或いは実体は規制要求を遵守し、制御物質の不法商業ルートへの移転を防止する。
薬品監督管理局は,制御物質を−付表I,II,III,IVまたはV−の5つの付表の1つに分類し,付表ごとに資格が異なる。定義によると,付表一物質が濫用される可能性が高く,現在米国では受け入れられていない医療用途は,医療監督下で使用しても受け入れられる安全性に欠ける。他の方法で発売が許可されている現在許容されている医療用途を有する医薬品は、付表2、三、四または五物質とすることができ、その中で、別表2の物質は最大の乱用および身体または心理依存の可能性を有し、表5に添付する物質の相対的な乱用および依存の可能性は最も低い。COMP 360が米国で承認された場合、それはDEAが発売されるまで時間を再配置する必要があるだろう。
規制された物質を製造、流通、輸入または輸出する施設は毎年DEAに登録されなければならない。DEA登録は特定の地点,活動,制御物質リストに対して行われる
制御物質登録を発行する前に,DEAはすべての製造施設を検査し,安全,記録保存,報告,処理を審査する。具体的な安全要求は,商業活動のタイプや処理される制御物質のスケジュールや数によって異なる。最も厳しい要求は別表一と表二物質を添付する製造業者に適用される。必要な安全対策には,通常,従業員の背景調査を行い,承認された金庫,金庫,ケージに貯蔵すること,警報システムや監視カメラを用いた制御物質の実物制御がある。一旦登録されると、製造施設は、すべての制御物質の製造、受信、分配を記録する記録を保持しなければならない。メーカーは定期的にDEAに付表1と付表2制御物質,付表三麻酔物質とその他の指定物質の分配状況に関する報告を提出しなければならない。登録者は必ず
また、いかなる制御物質の盗難や重大な損失も報告されなければならず、制御された物質の廃棄または処分の許可を得なければならない。商業目的のための輸入別表1と付表2規制物質は,一般に国内仕入先から得られていない物質や国内仕入先との間で十分な競争がない物質に限られている。輸入業者或いは輸出業者の登録以外に、輸入業者と輸出業者は毎回輸入或いは輸出表一と表二物質或いは表三、表四と表五麻酔薬はすべて許可証を取得しなければならず、表三、表四と表五非麻酔品の輸出入申告書を提出しなければならない。場合によっては,必要であれば,米国が国際薬物規制条約に規定されている義務を遵守することを確保するために,表3の非麻酔物質は輸出入許可要求の制約を受けることができる。
米国で製造された薬物について、DEAはDEAによる合法的な医療、科学、研究、工業需要を満たすのに必要な数量の推定に基づいて、毎年付表IとIIの中でアメリカで製造或いは生産可能な物質の総量割当量を確立している。このような割当量は活性医薬成分の生産と剤形の生産にも同じく適用される。DEAは毎年何回か総生産割当量を調整することができ、そして1年の中で時々個別製造或いは調達割当量を調整することができ、DEAは個別会社に対してこのような調整を行うかどうかについてかなりの自由裁量権を持っている。
各州はまた、許可、記録保存、安全、分配、分配要求を含む単独の制御物質法律と法規を制定した。州当局は、薬局委員会を含めて、各州で制御物質の使用を管理している。適用される要求を遵守できず、特に規制物質の損失や移転を受けることは、法執行行動を招く可能性があり、我々の業務、運営、財務状況に実質的な悪影響を及ぼす可能性がある。DEAは民事処罰を求め、必要な登録の更新を拒否したり、手続きを開始してこれらの登録を撤回することができる。場合によっては、違反は刑事起訴につながる可能性がある。
アメリカの“海外腐敗防止法”
私たちが受けているアメリカの反海外腐敗法は、会社や個人が業務を取得または保留したり、公的な身分で仕事をしている人に影響を与えることを禁止しています。いかなる外国の政府職員、政府職員、政党または政治候補者に支払いを提案し、任意の価値のあるものを支払うことを提案して、業務を獲得または保留しようとしているか、または他の方法で公的身分で働く人に影響を与えることは、不法である
EUの薬品審査の法規と手続き
アメリカ国外で任意の製品をマーケティングするために、会社はまた他の国と司法管轄区域の品質、安全性と有効性及び製品に対する臨床試験、マーケティング許可、商業販売と流通などの方面の多くの異なる監督管理要求を守らなければならない。FDAによる製品の承認を得るか否かにかかわらず、出願人は、これらの国または司法管轄区で当該製品の臨床試験またはマーケティングを開始するために、外国の監督管理機関のような必要な承認を得る必要がある。具体的には、EUの医薬製品の承認手続きは、通常、米国で1つの医薬製品を承認することは、完全に、または米国の承認と同じ時間範囲内であっても、同じ製品がEUで承認されることを保証するものではないにもかかわらず、米国と同じ路線に従う。それは各提案適応に対する薬物の安全性と有効性を確定するために、薬物開発、非臨床研究及び十分かつ良好な制御の臨床試験を満足的に完成させる必要がある。また、関連当局に臨床試験許可を提出し、その後、マーケティング許可申請、またはMAAを提出し、その後、製品をEUまたはその任意の加盟国でマーケティングおよび販売することができるように要求されている。もし私たちが適用された要求を遵守できなかったら、私たちは規制の承認、製品のリコール、製品の差し押さえ、運営制限、刑事起訴を撤回されるかもしれない。
臨床試験許可
EUでは,臨床試験の認可申請者は,臨床試験を行うEU加盟国の国家主管当局の承認を事前に得なければならない。また,関連する独立倫理委員会が賛成の意見を発表した後のみ,申請者は特定の研究地点で臨床試験を開始することができる。2014年4月,EUは2022年1月31日に従来の臨床試験指令2001/20/ECに代わる新たな臨床試験条例(EU)第536/2014号を採択し,EUの臨床試験承認制度を徹底的に改革した。具体的には、これはすべてのEU加盟国の新しい立法に直接適用され(これは、EUの臨床試験の承認を簡略化し、簡素化することを目的として、各EU加盟国で国家立法を制定する必要がないことを意味する)。例えば,新たな臨床試験条例は,単一入口点による申請手続きの簡略化(試験を行う加盟国の各国の主管当局や倫理委員会にそれぞれ提出するのではなく)を規定し,臨床試験申請評価の最終期限を厳格に規定している。臨床試験条例はまたEU加盟国が臨床試験情報システムを通じて共同評価と許可申請をより効率的にする。新たな臨床試験条例の一過性条項は,2025年1月31日までに行われているすべての臨床試験を新たなEU臨床試験条例に移行しなければならないと規定している
マーケティング許可
欧州経済地域(EU加盟国にノルウェー、アイスランド、リヒテンシュタインからなる)または欧州経済区で医薬製品のマーケティング許可を得るためには、申請者はMAAを提出しなければならないか、EMAによって管理されている中央手続きに基づいているか、EU加盟国主管当局が管理する手続きのうちの1つ(分散プログラム、国家プログラム、または相互承認手続き)に基づいていなければならない。マーケティング許可はヨーロッパ経済地域に設立された申請者にのみ付与されることができる
集中手続きは、欧州経済地域全体で有効であり、HIV、エイズ、癌、神経変性疾患、糖尿病、自己免疫および他の免疫機能障害、およびウイルス性疾患の治療のための新しい活性物質を含む製品を含む欧州委員会によって単一マーケティング許可を付与することを規定している。集中プログラムを強制的に使用しない製品については、(EC)第726/2004号条例によれば、出願人は、製品が強制リストに記載されている疾患以外の疾患を治療するための新しい活性物質を含むか、または出願人が製品が重大な治療、科学的または技術革新を構成していることを証明することができるか、またはそれを集中的に許可することが公衆の健康に有利であることを証明することができる集中プログラムを使用することができる。われわれが検討しているCOMP 360裸蓋キノコ療法は,難治性うつ病治療のための新たな活性物質として集中プログラムで提出する権利がある。
中央プログラムの下で,ヒト用薬品委員会,あるいはCHMPは,EMAがヒト薬物を担当する委員会であり,薬物が必要な品質,安全性と有効性要求に適合しているかどうか,積極的なリスク/利益があるかどうかの評価を担当している。中央手続きによれば、重大な影響評価を評価する最長期限は、有効な重大な影響評価を受けた日から210日であり、CHMPからの質問に答えるために、出願人が補足情報または書面または口頭解釈を提供する必要はない。タイミングを停止することは、MAAを評価する時間フレームを210日を超えるように大幅に延長する可能性がある。CHMPが肯定的な意見を与えた場合、それは、マーケティング許可を付与する最終決定を下すために、支援ファイルと共にEU委員会に意見を提供する。EU委員会はCHMP意見発表日から67日以内にMAAに関する最終決定を採択する。特殊な場合、公衆衛生の観点、特に治療革新の観点から見ると、1種の医薬製品が重大な意義を持っている場合、CHMPは加速評価を承認することができる。CHMPがそのような要求を受け入れる場合、210日間の評価期限は150日(クロック停止を含まない)に減少するが、CHMPが申請が加速評価にもはや適していないと判断した場合、中央プログラムの標準時限に回復する可能性がある。
イギリス(イギリスと北アイルランドを含む)がEUを離れたので、イギリスはもはや集中マーケティング許可のカバーを受けていない(北アイルランド議定書によれば、集中マーケティング許可は北アイルランドで引き続き認められている)。現在の集中マーケティング許可を有するすべての医薬製品は、2021年1月1日にイギリスのマーケティング許可に自動的に変換される。2023年12月31日までに、MHRAは、新しいイギリスのマーケティング許可をより迅速に付与するために、欧州委員会が集中手続きで新しいマーケティング許可を承認する決定に依存する可能性があります。しかし、まだ個別的な申請が必要になるだろう。2023年1月24日 MHRAは、EMAや何らかの他の規制機関がマーケティング許可を承認することを考慮した新たな国際認可枠組みを2024年1月1日から構築すると発表した。
分散マーケティング許可プログラム 出願人が、1つ以上のEU加盟国において、どのEU加盟国でも承認されておらず、集中手続の強制範囲に属さない医薬製品を同時に承認することを可能にする
相互認識手続きの基礎は、EU加盟国の主管当局が別のEU加盟国の主管当局による1種類の薬品の販売許可を受け入れることだ。国家マーケティング許可の所有者は、EU加盟国の主管当局に申請を提出することができ、その主管部門に、他のEU加盟国の主管当局が提供するマーケティング許可を認めるように要求することができる
良質な案
2016年3月、EMAは、革新を刺激し、発展を最適化し、優先薬物またはPrimeの評価を加速させるために、EMAとの早期対話とEMAの規制支援を強化する計画を開始した。環境管理協会が提供する科学的提案計画と加速評価プログラムに基づくことを目的としている。この計画は自発的で、資格基準を満たさなければPrimeの資格を得ることができない
Prime計画は開発中の薬物を開放し,申請者は集中プログラムで初歩的なMAAを申請しようとしている。条件に適合する製品は、満たされていない医療需要が存在する条件(EUには満足できる診断、予防または治療方法がない、または、ある場合、新薬は重大な治療利点をもたらす)でなければならず、それらは、新しい治療方法を導入することによって、または既存の方法を改善することによって、満たされていない医療需要を満たす潜在力を示さなければならない。申請者は通常開発の探索性臨床試験段階にあり、そして患者の中で初歩的な臨床証拠を獲得し、この薬物の将来性の明るい活性及び満足されていない医療需要を大きく解決する潜在力を証明する。特殊な場合、関連モデルにおいて納得できる非臨床データが有望な活動の早期証拠を提供し、第1の人体研究が必要な薬物治療効果および耐性に十分な曝露があることを示す場合、学術部門または中小企業(中小企業)の申請者は、開発の早い段階で資格申請を提出することができる。
Primeプログラムのために薬を選ぶとEMA:
•CHMPまたは高度治療委員会(CAT)から調査委員を任命し、MAAを提出する前に持続的な支援を提供し、医学的知識を蓄積する
•申請者全体の発展計画と規制戦略に対する指導意見を発表した
•調査委員や環境管理協会関連委員会やワーキンググループの専門家とともに開始会議を組織した
•専任EMA連絡先を提供し、
•重要な発展マイルストーンで科学的な提案を提供し、必要な時にもっと多くの利害関係者を参加させ、例えば衛生技術評価機構と患者である。
Prime計画に選ばれた薬品も,EMAの上場許可申請時の加速評価プログラムから利益を得ることが予想される。研究開発過程において、もし1種の薬物が資格標準に符合しなくなったら、Prime計画下の援助を取り消すことができる。
孤児薬名
孤児医薬品法によれば、FDAは、まれな疾患または疾患を治療するための薬剤を孤児として指定することができ、このような疾患または疾患は、通常、米国では20万人未満に影響するか、または米国では20万人以上に影響を与え、そのような疾患または疾患を治療する薬剤を米国で開発および生産するコストは、製品の販売から回収されるであろう。秘密保持協定を提出する前に、指定孤児薬を申請しなければならない。FDAが孤児薬物指定を承認した後、FDAは、薬物の識別情報およびその潜在的な孤児用途を開示する。指定孤児薬は、規制審査と承認過程でいかなる利点も伝達されず、規制審査と承認過程の持続時間を短縮することもない
孤児薬物指定は、一方が臨床試験費用、税収優遇、ユーザー費用の減免のために贈与資金を提供する機会があれば、財政的インセンティブを得る権利がある。孤児として指定された薬物がその後、このような指定された疾患または状況を有するFDAの最初の承認を得た場合、この薬剤は、孤児薬物排他性を得る権利があり、これは、FDAが7年以内に同じ薬物を同じ適応で販売することができず、限定された場合、例えば孤児に対して排他性を有する薬物に対する臨床的利点を示さない限り、同じ適応で同一の薬物を販売することを意味する。しかし,競争相手は孤児薬に対して排他的な適応を持つ異なる薬物の承認を得るか,同一薬物に対して排他的であるが孤児薬に対して排他的な異なる適応の承認を得る可能性がある。競合他社がFDAで定義された同じ薬剤の承認を得た場合、または我々の治療候補薬が競合相手の薬剤に含まれていると決定された場合、同じ適応または疾患のために使用される場合、孤立薬物排他性も7年以内に候補治療薬の承認を阻止する可能性がある。孤児薬に指定された薬物が市販承認された場合,その適応範囲は指定されたものよりも広く,孤児薬物排他性を得る資格がない可能性がある。連合の孤児薬の地位は似たような利点を持っているが、同じではない
条例(EC)第141/2000号及び条例(EC)第847/2000号には、(1)生命又は慢性衰弱に危害を及ぼす疾患の診断、予防又は治療を目的としている製品のスポンサーが証明できる場合、欧州委員会により孤児医薬品として指定することができる。(2)または(I)申請時に、EUにおけるこのような疾患の影響が万分の5を超えないか、または(Ii)孤児のアイデンティティによるメリットがなければ、EUでの販売は、その開発に必要な投資が合理的であることを証明するために十分な見返りをもたらす可能性が低い場合、および(3)このような疾患を満足できる診断、予防または治療する方法がない
EUでの販売を許可するか、または、このような方法が存在する場合、製品は、この条件に適用される製品よりも顕著な利点を有するであろう
孤児として指定されたEUは、費用減免、規制援助、集中マーケティング許可を申請する能力を含む多くのメリットを提供している。上場許可を申請する前に、孤児指定申請を提出しなければならない。孤児指定は、規制審査および承認過程においていかなる利点も伝達されず、規制審査および承認過程の継続時間を短縮することもない。孤児薬品の販売許可を与えることは10年間の市場排他期につながるだろう。この市場排他期間内には,欧州医薬品管理局,欧州委員会,加盟国ともに申請を受けることができず,“類似薬品”の同じ治療適応の販売許可を承認することもできない。類似医薬製品“の定義は、承認された孤児医薬製品に含まれる1つ以上の類似活性物質を含む医薬製品であり、同じ治療適応のためのものである。しかしながら、製品が孤児指定の基準に適合していないことが5年目の終了時に決定された場合、例えば、製品の利益が十分に高く、市場排他性が合理的であることを証明するのに不十分である場合、適応の治療を許可する市場専門期間は6年に短縮されることができる。10年間の市場独占期間の欠陥も限られており、この期限に応じて、欧州委員会は同じ治療適応を有する類似医薬製品の販売を許可することができる。これらは:(I)第2の出願人は,彼らの製品が許可された孤児薬と類似しているにもかかわらず,第2の製品の方が安全であることを証明することができる, より効果的または臨床的治療効果がより良い;(Ii)孤児製品を許可する上場授権者は、2回目の孤児薬品の申請に同意するか、または(Iii)孤児製品を許可するマーケティング授権者は、十分な孤児薬品を供給することができない。
小児科発展
EUでは、新しい医薬製品を開発する会社はEMAの小児科委員会(PDCO)と小児科調査計画またはPIPについて合意しなければならず、EMAが特定の製品に対する免除、カテゴリ免除、またはPIPに含まれる1つまたは複数の措置を承認しない限り、このPIPに基づいて小児科臨床試験を行わなければならない。会社が認可された薬物のために新たな適応,薬物形式あるいは投与経路を増加させようとした場合にも,この要求は適用される。PIPは、マーケティング許可を求めている製品の小児科適応をサポートするためのデータを生成する時間およびアドバイスを規定する。製品のMAAは、PIPによる小児科臨床試験の結果を含まなければならず、適用免除が認められない限り、またはPDCOが成人における製品の有効性および安全性を証明するのに十分なデータが証明されるまで、PIPの実施を延期することが許可されている場合には、小児科臨床試験を遅く完了しなければならない。さらに、小児科臨床試験データが不要または不適切に提供される場合、PDCOは、子供に無効または安全でない可能性があるので、これらのデータを提供する義務を免除することができ、この製品は、治療のために使用される疾患または状態が成人集団でのみ発生することが予想される、または小児科患者の既存の治療に対して有意な治療利益がない場合である。PIPによる小児科臨床試験結果に基づいて発売許可を得た製品は,補充保護証明書やSPCによる6カ月間の保護延期(当該製品のSPC申請を提出するとともに延期申請を行うことを前提としている, あるいはSPCが満期になる2年前のいずれかであっても,試験結果が陰性であっても。孤児薬品の場合、孤児市場の独占権は2年間延長することができる。この小児科奨励は特定の条件の制約を受け,PIPに適合したデータを開発·提出する際に自動的に獲得されない。
データと市場排他性
EUでは、改正された(EC)第726/2004号条例と改正された2001/83/EC指令に基づいて、完全な独立データパケットによって承認された革新医薬製品は、8年間のデータ独占権と追加2年間の市場独占経営権を得る資格がある。データ排他性防止後発薬と生物類似申請者は発売許可を申請する時に製品ファイルに含まれる革新者の臨床前と臨床試験データを参考し、参考製品が初めてEUで許可を獲得した日から8年以内である。追加の2年間の市場専門期間内に、模倣薬または生物類似製品の上場許可申請を提出することができ、革新者のデータを参考にすることができるが、市場専門期間が満了するまで、いかなる模倣薬や生物類似薬品も発売できない。この10年の最初の8年間に、マーケティング許可所有者が1つまたは複数の新しい治療適応の許可を得た場合、10年全体の期間は最大11年に延長され、許可前の科学的評価期間中に、これらの適応は既存の治療法と比較して有意な臨床的利益をもたらすことができると考えられる。 1つの製品がEMAによって革新的な医薬製品とみなされることは保証されず、しかも製品はデータ独占性を得る資格がない可能性がある。1つの製品が革新的な医薬製品であると考えられても、革新者が所定のデータ独占期間を取得し、別の会社がMAAベースのマーケティング許可を取得した場合、同社は完全かつ独立した薬物試験、臨床前試験、および臨床試験データパケットを有し、同社はその製品の別のバージョンを販売することができる。
授権期間と継続期間
原則として、マーケティング許可の有効期間は5年であり、5年後にEMAまたはライセンスEU加盟国の主管当局によるリスク収益残高の再評価に基づいて更新することができる。一旦更新されると、上場許可の有効期限は無期限であり、欧州委員会または主管当局が薬物警戒に関する正当な理由に基づいて、追加の5年間の継続を決定しない限り。許可が失効してから3年以内に欧州経済地域市場に製品を投入しなかった場合(集中手続きの場合)、または許可されたEU加盟国の市場(国家手続きに対する)のいかなる許可も無効(いわゆる日没条項)である。
規制された薬物分類
イギリスでは,裸蓋キノコと裸蓋キノコは改正後の1971年の“薬物乱用法”によりA類薬物とされ,改正後2001年の“薬物乱用条例”により別表1薬物とされている。1971年の“薬物乱用法”によると、A類薬物は最も潜在的な有害性があると考えられ、最高レベルの制御を持っている。同様に,2001年の薬物乱用条例別表1には,合法的あるいは医療用途がないと考えられ,イギリス政府内務省が発行した許可証の下でのみ輸入,輸出,生産,供給などが適用される最も厳しい規制が適用されていることが表1に示されている。MHRAがイギリスでの発売を許可した場合、ヌードゲキノコは依然として表1の薬物に添付され、イギリス政府内務省が時間を再手配しない限り、表1の薬物となる。 2001年の薬物乱用条例によって裸蓋キノコが再配置されない限り、イギリスのマーケティング許可後および再手配時間の前にCOMP 360の法定免除によって免除されない限り、イギリスでは、どの処方医もCOMP 360を発行するために内務省免許を必要とし、同様に、COMP 360を処方した患者はCOMP 360を所有するために内務省免許を必要とする。 内務省がこのような許可証を発行する保証はなく、再手配が成功する保証もない。
EU加盟国の立場は調和していない:加盟国は関連する国連条約(“1961年麻酔薬単一条約”と“1971年精神薬物条約”)を自国の立法に実行しており、これによりEUの国によって規制物質の規制方法が異なる。したがって、国家レベルで物質が規制されているかどうかを決定し、適用される法的要求を遵守することが重要だ。もし私たちがEUの主要加盟国でマーケティング許可を得ることに成功すれば、裸蓋キノコの発売時間を再手配して処方する必要があるかもしれない。
営業許可後の規制要件
承認を得た後、上場許可の保有者は医薬製品の製造、マーケティング、普及と販売に適用される一連の要求を守らなければならない
これらの措置には,EUの厳格な薬物警戒や安全報告規則の遵守が含まれており,これらの規則により,認可後の研究や追加的なモニタリング義務を実施することができる。上場許可所持者は薬物警戒システムを構築·維持し,資格のある個人を指定して薬物警戒を担当し,このシステムの監督を担当しなければならない。主な義務は深刻な副作用が疑われる報告を加速させ、安全更新報告書を定期的に提出することを含む。
さらに、すべての新しいMAAは、製品に関連するリスクを防止または最大限に低減するための措置を記録するために、企業が実施するリスク管理システムを記述したリスク管理計画またはRMPを含まなければならない。規制部門はまた、上場許可の条件として特定の義務を規定することができる。このようなリスク最小化措置または認可後の義務は、追加の安全監視、PSURsのより頻繁な提出、または追加の臨床試験または認可後の安全性研究を含む可能性がある。RMPおよびPSURsは通常,アクセスを要求する第三者に利用可能であるが,限られた編集を行う必要がある.
また、ライセンス製品の製造は、2001/83/EC番号指令、2003/94/EC指令、(EC)第726/2004法規、および欧州委員会良好な製造規範ガイドラインを含む、適用されるEUの法律、法規、およびガイドラインを厳格に遵守しなければならない。これらの要件は、製品の製造、加工、およびパッケージで使用される方法、施設、および制御措置を規定して製品の安全およびアイデンティティを確保するEU cGMP規格を遵守することを含む
最後に、業界賛助の継続医学教育と製品処方者に対する広告を含むライセンス製品のマーケティングと普及は、EUで改訂された2001/83/EC指令の厳格な規制を受けている。2012年の“人間医薬品条例”によると、EUもイギリスも、処方薬のみの広告を一般公衆に発表することは許可されていない。医薬製品の広告や販売促進に対する一般的な要求はありますが
改正されたEU指令2001/83/ECに基づいて設立されたものであり、詳細はEU加盟国ごとの法規によって管轄されており、各国は異なる可能性がある。
上記のEU規則は,EU加盟国およびノルウェー,リヒテンシュタイン,アイスランドからなるヨーロッパ経済区に一般的に適用されている。
イギリスの離脱とイギリスの規制枠組み
イギリスは2020年1月31日にEU(通称離脱)を正式に離脱し、EUはイギリスと貿易·協力協定を締結し、TCAと略称し、2021年1月1日から暫定的に適用され、2021年5月1日から正式に適用される。TCAには薬品に関する具体的な条項が含まれており,その中にはGMP相互承認,医薬製品の製造施設の検査,発表されたGMP文書が含まれているが,イギリスとEUの薬品法規の大規模な相互承認は予想されていない。現在、イギリスは“2012年人類薬品条例”(改正された)(北アイルランド議定書に基づき、EU規制枠組みは引き続き北アイルランドに適用されている)を採択し、医薬製品のマーケティング、普及、販売に関するEUの立法を実施している。そのため,新たなEU臨床試験規制を除いて,イギリスの規制制度はEUの規制制度とほぼ一致しているが,イギリスの規制制度はEUから独立しており,“薬物規制法”もイギリスとEUの薬剤業立法について相互に認める規定がないため,これらの制度は後日より大きく異なる可能性がある
保証範囲·定価·精算
私たちが規制部門の承認を得た任意の候補製品のカバー範囲と精算状態には、重大な不確実性がある。米国および他の国/地域の市場では、任意の裸蓋キノコ療法の販売は、規制部門の商業販売許可を得た場合、政府医療計画(例えば、Medicare、Medicaid)、管理型医療保健提供者、個人健康保険会社、健康維持組織、その他の組織のような第三者支払者の私たちの製品に対する保証および精算状況にある程度依存するであろう。この第三者決済者たちは彼らがどのような薬を支払うかを決定し、清算水準を確立するだろう。政府や他の第三者支払者が提供する保険範囲や精算範囲は,多くの患者が新たな療法などの治療を負担できるようにするために重要である。米国では,新薬精算に関する主な決定は通常医療保険と医療補助サービスセンター(CMS)によって行われ,CMSは米国衛生·公衆サービス部(HHS)の一部である。CMSは私たちの製品がどの程度連邦医療保険の下でカバーと精算されるかを決定し、個人支払者はしばしばCMSに大きく従う。支払人が精算を決定する際に考慮する要素は、製品があるかどうかに基づいている
•健康計画の下で保障された福祉
•安全で効果的で医学的に必要なものです
•特定の患者に適しています
•費用対効果があります
•実験的でも調査的でもない。
私たちが私たちの候補製品を商業化することに成功するかどうかは、単一薬物としても併用療法としても、第三者支払者が私たちの製品と関連治療に提供するカバー範囲と十分な補償にある程度依存する。また、支払者が製品に保険を提供することを決定することは、十分な返済率を承認することを意味するものではない。保険を提供しても、承認された精算金額は、製品開発投資の適切なリターンを実現するのに十分な価格レベルを確立または維持するのに十分ではない可能性があります
米国では、第三者支払者は製品の保証と精算に対して統一的な政策を持っていない。そのため、私たちの製品の保証範囲と精算範囲は支払人によって違います。支払者が製品に保険を提供するかどうかを決定するプロセスは、支払者が製品のために支払う支払率を設定するプロセスと分離することができる。支払者は、医療製品又はサービスに保険を提供することを決定し、他の支払者もその医療製品又はサービスに保険を提供するか、又は適切な販売率で保険を提供することを保証することができない。第三者支払者は、承認されたリストまたは処方表上の特定の製品に保証範囲を制限することもでき、FDAによって承認された特定の適応のすべての製品を含まない可能性がある
第三者支払人は、私たちの製品を使用する医療製品や治療のために単独で精算しないか、単独で精算しないことを決定し、承認されると、医師の私たちの製品への使用を減らし、私たちの販売に実質的な悪影響を与える可能性があります
経営業績と財務状況。第三者支払者が我々の候補製品を保証したり,我々の候補製品を用いた療法を受けたりすると,それによる精算支払率が十分に高くない可能性があり,あるいは患者が受け入れられない高い共有率を発見する必要がある可能性がある。私たちは、現在または将来の候補製品またはそのような候補製品を使用する任意の手続きが米国の保証範囲および精算範囲で利用可能であるかどうかを保証することができず、入手可能な任意の精算が十分でない可能性があるか、または将来的に減少またはキャンセルする可能性がある。また、私たちまたは私たちの協力者が私たちの候補製品のための治療法を開発した場合、私たちまたは私たちの協力者は、これらの療法の単独の保証と精算を要求され、承認されると、私たちの候補製品のために求められている保証と精算を除いて。
また、第三者決済者は、価格、医療製品やサービスの医療必要性および費用便益、およびそれらの安全性および有効性を検討することに挑戦することが増えている。承認販売される可能性のある候補製品の任意の保険·精算を確保するためには、製品の医療必要性および費用効果を証明し、FDAまたは同様の規制承認を得るのに必要なコストを証明するために高価な薬物経済学的研究を行う必要があるかもしれない。さらに、購入者、個人健康計画、または政府医療計画に割引を提供する必要があるかもしれない。それにもかかわらず、私たちの候補製品は医学的に必要で費用効果的だと思われないかもしれない。第三者支払い者が、1つの製品が他の利用可能な療法と比較して費用対効果があると考えない場合、彼らは、承認後にその製品をその計画下の福祉としてカバーしないかもしれない、または、支払いレベルが、会社がその製品を利益を得るために販売することを許可するのに十分ではない可能性がある。製品が承認されると、第三者支払者が製品を保証しない決定は医師の使用率を減少させ、販売、私たちの運営、財務状況に実質的な悪影響を及ぼす可能性がある。私たちは、私たちの任意の候補製品を潜在的に販売する時、第三者支払人からの定価圧力に遭遇すると予想しています。
最後に、いくつかの外国の国では、薬品の提案価格は必ず承認されなければならず、合法的に発売されることができる。各国の薬品定価に対する要求は大きく異なる。例えば、連合では、様々な国の価格設定と補償プログラムの差が大きい。いくつかのEU加盟国は補償価格を合意した後にのみ製品を販売することができると規定している。いくつかのEU加盟国は、精算または定価承認を得るために、特定の候補製品の費用対効果を現在利用可能な療法(いわゆる健康技術評価)と比較することを追加的な研究を達成することを要求するかもしれない。例えば、EU加盟国は、その国の健康保険制度が精算を提供する製品範囲を制限し、人が使用する医療製品の価格を制御することを選択することができる。EU加盟国は、ある製品の具体的な価格を承認するか、またはその製品を市場に投入する会社の収益力に対して直接または間接的な制御制度をとることができる。連合加盟国間の接近法には食い違いが発生している。例えば,フランスでは,有効な市場参入は病院との合意によって支援され,製品は社会保障基金が精算する可能性がある。薬品価格は保健品経済委員会(CEPS)と協議した。薬品に対して価格制御や精算制限を実行することを保証できない国は、私たちの任意の候補製品に対して有利な精算と定価手配を許可する。他のEU加盟国は会社が自分の製品価格を固定することを許可したが、処方量を監視と制御し、医師に指導を発表して処方を制限した。最近は, EUの多くの国はすでに薬品に必要な割引レベルを高め、各国が医療支出を管理しようとするにつれて、これらの努力は継続する可能性があり、特にEUの多くの国が深刻な財政危機と債務危機を経験した場合である。全体的には,医療コスト,特に処方薬の下り圧力が大きくなっている。そのため、新製品の参入にはますます高い壁が設けられている。政治、経済、規制面の事態は定価交渉をさらに複雑化させる可能性があり、補償を受けた後、定価交渉が継続される可能性がある。EU加盟国が使用する参考価格と平行貿易(低価格と高価なEU加盟国間の裁定)はさらに価格を下げることができる。いずれの医療製品の精算を受けるかはコスト,用途,通常の数量制限を伴う可能性があり,これらの制限も国によって異なる可能性がある。しかも、成果に基づく精算規則が適用される可能性がある。薬品に対して価格制御や精算制限を実施することが保証されていない国は、これらの国で承認されれば、私たちのいかなる製品に対しても有利な精算と定価手配を許可する。歴史的に見ると、EUで発売された製品はアメリカの価格構造に従わず、通常価格ははるかに低くなることが多い。
上記のいずれかの規定にもかかわらず,“制御物質法”の付表によると,裸蓋キノコや裸蓋キノコは現在受け入れられていないと考えられており,裸蓋キノコや裸蓋キノコを用いた療法は現在米国では精算が禁止されている。
他の医療法とコンプライアンス要件
医療提供者、医師、第三者支払者は、私たちが市場で承認された任意の製品の推薦と処方において主な役割を果たすだろう。私たちの業務運営と現在または未来と
第三者支払者、医療提供者、医師は、私たちを広く適用される連邦と州詐欺と乱用法律、その他の医療法律と法規に直面させるかもしれない。これらの法律は私たちの商業的または財務的配置と関係に影響を与えるかもしれません。私たちはこれらの手配と関係を通じて、私たちが承認された裸蓋キノコ療法を研究、マーケティング、販売、流通します。また、私たちは連邦政府と私たちが業務を展開している州の健康情報プライバシー法規によって制限されるかもしれない。アメリカでは私たちの運営能力に影響を与える可能性のある法律には
•連邦反リベート法規は、他の事項に加えて、個人および実体が直接または間接的に、現金または実物で直接または間接的に現金または実物で直接または間接的に、公開または隠蔽的に請求、受領、提供、提供または見返りとして任意の報酬(任意のリベート、賄賂またはリベートを含む)を支払うことを禁止し、誘導または見返りとして、個人を紹介するか、または購入、レンタル、注文、手配、または任意の商品、施設、物品またはサービスを推薦して、連邦医療保険および医療補助などの連邦医療保健計画に従って全部または部分的な支払いを行うことを禁止する。報酬という単語は価値のあるものを含むと広く解釈されている。また、裁判所は、報酬の“一つの目的”が転転誘導であれば、連邦の“反リベート法規”に違反していることを発見した。連邦反リベート法規は、製造業者と処方者、購入者、および処方マネージャーとの間の配置に適用されると解釈される。個人や実体は連邦反リベート法規を実際に知る必要はなく、この法規に違反する具体的な意図を持つ必要もなく違反を実施することができる。違反行為には巨額の行政、民事、刑事罰金が科され、違反ごとに報酬の3倍までの罰、監禁、政府医療計画から除外される。また、政府は、連邦虚偽請求法案(FCA)または連邦民事罰金法規に基づいて、連邦反リベート法規違反による物品またはサービスのクレームが虚偽または詐欺的クレームを構成することを含むと断言することができる。いくつかの法定例外と規制避風港保護のいくつかの一般的な活動は起訴されない;しかし例外と避風港の範囲は狭く、保護を提供するために厳格に守らなければならない
•FCAのような連邦民事および刑事虚偽申告法は、個人または実体が虚偽、架空または詐欺的な連邦医療保険、医療補助または他の第三者支払者の支払いまたは承認クレームの提出または提出を意図的に、または使用することを禁止し、虚偽陳述または記録材料を使用して連邦政府に財産を支払うまたは詐欺的なクレームまたは義務を作成、または誘導することを禁止するか、または連邦政府に金銭を支払う義務を故意に隠蔽または故意に回避または不当に回避または減少させる。FCAによると、メーカーが政府支払人に直接クレームを提出していなくても、虚偽や詐欺的なクレームを“原因”とされていれば、責任を問われる可能性がある。“海外腐敗防止法”はまた、個人が“密告者”として、連邦政府を代表して訴訟を起こし、“反海外腐敗法”に違反し、いかなる金銭回収にも関与していることを告発している。1つのエンティティがFCA違反と判定された場合、政府は各虚偽クレームに対して民事罰金と罰を科すことができ、3倍の損害賠償を加え、そのエンティティを連邦医療保険、医療補助、他の連邦医療計画から除外することができる
•他の事項に加えて、提供または譲渡報酬に対して民事罰金を科す連邦民事罰金法であって、連邦医療保険または医療補助受益者に無料または公平な市場価値よりも低い価格で物品またはサービスを譲渡すること(限られた例外)を含むが、これらの物品またはサービスが、連邦または州医療計画によって精算可能な特定の提供者、従事者またはサプライヤーの選択に影響を与える可能性があることを知っているか、または知るべきである連邦民事罰金法
•1996年の連邦“健康保険携帯および責任法案”、またはHIPAAは、任意の医療福祉計画を詐欺するために、または任意の医療福祉計画を詐欺するために、または虚偽または詐欺的な言い訳、陳述または約束によって、支払者(すなわち、公共または個人)にかかわらず、任意の医療福祉計画が所有または保管または制御する任意の金銭または財産を取得し、故意に偽造、隠蔽、または隠蔽または隠蔽するか、または任意の提供、または任意の金銭または財産を取得することを規定する追加の連邦刑事責任を規定する。医療事項に関連する医療福祉、プロジェクト、サービスを支払うことができます。連邦反リベート法規と同様に、個人または実体は、この法規または法規違反の具体的な意図を実際に理解する必要がなく、違反を実施することができる
•HIPAAは、2009年の衛生情報技術促進経済と臨床衛生法案或いはHITECH及びそのそれぞれの実施条例の改正を経て、その他以外に、以下の方面に対していくつかの要求を提出した
特定の保険医療保健提供者、健康計画および医療情報交換センターおよびそのそれぞれの業務パートナーおよび保証下請け業者は、個人が健康情報を識別することができるプライバシー、安全および伝送に関する。他の事項に加えて、HITECHは、HIPAAのプライバシーおよびセキュリティ基準をビジネスパートナーに直接適用し、オーバーレイエンティティの作成、受信、保守、送信、または保護された健康情報を取得する独立した請負者またはエージェントを表す。HITECHはまた、実体、商業パートナー、および可能な他の人に適用される民事と刑事罰を増加させ、連邦裁判所に民事訴訟を提起し、連邦HIPAA法を実行するために損害賠償または禁止令を要求し、連邦民事訴訟に関連する弁護士費と費用を求めることができる州総検察長に新たな権力を与える
•“保健·教育調整法”改正された“患者保護と平価医療療法”によって創設された連邦“医師支払陽法”によると、総称して“平価医療法案”と呼ばれ、Medicare、Medicaidまたは児童健康保険計画に基づいて支払いを受けることができる適用薬品、設備、生物製品と医療用品メーカーは毎年CMSに医師(医師、歯科医師、検眼師、足科医師と脊医、ある他の免許を有する医療従事者を含む)と教育病院および上述の医師とその直系親族が持つ所有権と投資権益に関する支払いまたはその他の価値移転に関する情報をCMSに報告する
•連邦政府価格報告法は、複雑な価格指標を政府プロジェクトに正確かつタイムリーに計算し、報告することを要求している
•市場活動を広く規制し、消費者の活動を損なう可能性がある連邦消費者保護法および不正競争法
•上記の各医療保健法律法規と同様の州および外国等価物、例えば、反リベートおよび虚偽請求法のように、任意の第三者支払人(商業保険会社または患者を含む)の返済のプロジェクトまたはサービスに適用することができる;製造業者の州および地方マーケティングおよび/または透明性法律に適用され、その範囲は連邦要件よりも広い可能性がある;州法律は、2003年4月の“製薬メーカー総合計画ガイドライン”および/または“アメリカの製薬研究およびメーカーと医療保健専門家との相互作用基準”のような製薬会社に製薬業自発的コンプライアンスガイドラインおよび連邦政府が発行する他の関連コンプライアンスガイドラインを遵守することを要求する。州法律は、医薬品価格に関する情報を報告することを要求する;州法律は、医薬品製造業者に、医師および他の医療保健提供者への支払いまたは他の方法での価値移転に関する情報、またはマーケティング支出および定価情報を報告することを要求する;州および地方法律は、医薬品販売代表の免許および/または登録を要求する;および健康情報のプライバシーおよび安全を管理する州および外国の法律は、米国(例えば、GDPRを採用するEU)よりも厳しい可能性があり、多くの法律は重大な点で互いに異なり、HIPAAの先制者がなく、コンプライアンス作業を複雑化させることが多い
医薬製品の流通は広範な記録保存、許可、貯蔵と安全要求を含む追加の規定と条例を遵守し、許可されていない医薬製品の販売を防止しなければならない。
これらの法律のすべての範囲や執行は不確実であり,現在の医療改革環境の急速な変化の影響を受けている。連邦と州法執行機関は引き続き医療会社と医療保健提供者間の相互作用の審査を強化し、これは医療保健業界のいくつかの重大な調査、起訴、有罪判決と和解を招いた。政府当局は、私たちの業務やり方が現在または未来に適合していないと結論するかもしれないが、詐欺および乱用または他の医療保健法律および法規の適用に関する現行または未来の法規、法規または判例法に関連している。私たちの卓越したセンターやセラピストのような医師や他の医療提供者や実体との私たちの業務が含まれていれば、このような法律または私たちに適用される任意の他の政府法規に違反していることが発見された場合、私たちは行政、民事と刑事罰、損害、罰金、返還、契約損害、名声損害、利益減少と将来の収益、私たちの業務の縮小または再編、連邦医療保険や医療補助などの連邦·州医療保健計画から除外され、監禁、監禁、これらの法律を遵守しない疑惑および私たちの業務の縮小または再編を解決するために、当社の誠実な合意または同様の和解の制約を受けていれば、いずれも私たちの業務運営能力および私たちの財務業績に悪影響を及ぼす可能性がある追加の監督および報告義務。もし私たちが協力することを望むなら医者や他の医療提供者や実体が
企業は、我々の卓越したセンターやセラピストを含め、適用された法律を遵守していないことが発見され、彼らは類似した行動、罰、制裁を受ける可能性がある。
私たちの現在と将来の第三者との業務配置や、私たちの業務が全体的に適用される医療法律や法規に適合していることを確保し、政府当局が可能な調査に対応することは、時間と資源がかかり、会社の業務への関心を分散させる可能性があります
医療改革
米国や一部の外国司法管轄地域では、医療システムに関する複数の立法·規制改革および提案された改革が継続して存在する可能性があり、医療の獲得性を拡大し、医療の質を向上させ、医療のコストをコントロールまたは低減することを目的としている。例えば、2010年には、医療補助計画に売却された薬品のリベートが追加されたACAが公布され、医療補助薬品返却計画に基づいて大多数のメーカーが不足している医療補助計画のリベートを含み、リベート計画を医療補助管理組織に登録された個人に拡大し、ある連邦医療保険Dの一部の受益者に割引を強制的に実施し、製造業者は50%(2018年の両党予算法により、2019年1月から70%に増加)を提供しなければならず、製造業者として連邦医療保険D部分下の外来薬カバー範囲内で条件を満たす受益者にブランド薬品交渉価格を適用する販売時点割引を提供しなければならない。あるブランドの処方薬の薬品メーカーを新たな差し引くことのできない年間費用と税収に直面させる;医療詐欺と乱用法律(FCAと反リベート法規を含む)、政府が権力を調査し、違反行為に対する処罰を強化する;医療補助計画の資格基準を拡大し、それによってメーカーの医療補助リベート責任を潜在的に増加させる;340 B薬品定価計画によって割引を受ける資格がある実体を拡大する;この法律の定義に基づいて、報告と医師の財務手配の新しい要求を作成し、病院に教育を提供する, 一般的に医師支払い陽光法案と呼ばれる;新しい要求を作成し、毎年メーカーと許可記録販売業者が医師に提供する薬物サンプルの身分と数量を報告する;新しい患者を中心とした結果研究所を作成し、優先順位を監督、確定し、臨床有効性比較研究を行い、そしてこのような研究に資金を提供する;そしてCMSに連邦医療保険と医療補助革新センターを設立し、革新的な支払いとサービス交付モードをテストし、連邦医療保険と医療補助支出を下げる。
ACAが公布されて以来、アメリカはまた他の立法改正を提案し、採択した。例えば、2011年の“予算制御法案”(Budget Control Act)など、国会の支出削減のための措置が制定された。これには,各年度にプロバイダに支払われる連邦医療保険総額が最高2%減少することが含まれている。その後の立法は2%の支払い減免を2030年に延長する
“米国納税者救済法”は,病院,画像センター,癌治療センターを含むいくつかの提供者への医療保険支払いを減少させ,政府を提供者への多額の支払いを取り戻す訴訟時効を3年から5年に延長した
また、2018年5月30日には、“裁判権法案”が法律に署名された。他の事項以外に、この法律はある患者に連邦フレームワークを提供し、彼らがいくつかの完成したI期臨床試験を獲得し、そして調査を行ってFDAの許可を得た研究用新薬製品を得ることを許可した。場合によっては、条件を満たす患者は、臨床試験に参加することなく、FDA拡大参入計画に従ってFDA許可を得ることなく治療を求めることができる。“試用権法案”によると、薬品メーカーはその薬品を条件に合った患者に提供する義務がない。
2022年の“インフレ率低減法案”(IRA)のいくつかの条項は私たちの業務に異なる程度の影響を与える可能性があり、その中には2025年から連邦医療保険D部分の受益者の自己負担上限を2,000ドルに下げる条項が含まれている;連邦医療保険D部分の下である薬物に対して新しいメーカーの財務責任を規定する;アメリカ政府はある高コストの薬物と生物製品の連邦医療保険B部分とD部分の価格上限について交渉することを許可し、模造薬や生物類似競争が存在しない;会社はある価格がインフレより速い薬品の連邦医療保険にリベートを支払うことを要求し、薬局福祉マネージャーが費用を受け取ることができるリベート規則を延期する。また,IRAによると,孤児薬は連邦医療保険薬品価格交渉計画の影響を受けないが,まれな疾患の名称があることを前提としており,唯一承認された適応はこの疾患や条件に対するものである。 1つの製品が複数のまれな疾患の指定または複数の承認された適応を得た場合、孤児薬免除を受ける資格がない可能性がある。Ireland共和軍が私たちの業務と医療産業全体に及ぼす影響はまだ明確ではない。
また、支払い方法は医療立法と規制措置の影響を受ける可能性がある。例えば、CMSは、バンドル支払いモードのような新しい支払いおよび配信モードを開発することができる。最近では
政府はメーカーがその市場製品の価格設定の方式をより厳格に審査した。このような審査はアメリカ議会が最近数回の調査を行い、連邦と州立法を提出し、公布し、薬品定価の透明性を高め、定価とメーカー患者計画との関係を審査し、連邦医療保険下の薬品のコストを下げ、政府の薬品に対する計画精算方法を改革することを目的とした。いくつかの措置および他の提案された措置は発効するために追加の立法によって許可される必要があるかもしれないが、バイデン政府はこれらの措置を撤回または他の方法で変更する可能性があるが、バイデン政府と国会は薬品コストを制御するための新しい立法措置を求め続けると表明している。
州レベルでは、立法機関は、価格または患者の精算制限、割引、特定の製品参入およびマーケティングコスト開示の制限、および透明性措置を含む薬品の価格設定を制御するための法規を立法し、実施してきており、場合によっては、他の国からの輸入および大量購入を奨励することを目的としている
私たちは将来、より多くの外国、連邦、州医療改革措置を取ることが予想され、そのいずれも連邦と州政府が医療製品とサービスのために支払う金額を制限する可能性があり、これは限られたカバー範囲と精算、そして私たちの製品に対する需要の減少、承認されると、あるいは追加の価格設定圧力を招く可能性がある。政府はまた新冠肺炎の流行に対応するためにもっと多くの行動をとる可能性がある
人的資本管理
心理健康看護会社として、著者らは患者が心理健康領域の根拠に基づく革新を獲得する機会を加速することに取り組んでいる。私たちのグループは私たちの成功の鍵であり、私たちは、尊敬業、多様化、支持され、激励された労働力チームの構築に投資することが重要であり、彼らは私たちが精神的に健康な世界のビジョンを達成するのを助けることができると信じている。2022年12月31日まで、私たちは181人の従業員を持っている。134人の従業員が研究開発活動に従事し、47人の従業員が一般行政機能に従事している。2021年12月31日現在、114人の従業員を抱えており、2022年12月31日現在、私たちの従業員は59%増加しています。2022年12月31日まで、私たちの31%の従業員はアメリカに位置し、残りの69%はイギリスに位置している。
私たちは従業員たちと集団交渉合意に到達しなかったし、何の中断も経験しなかった。私たちは私たちが従業員と仲がいいと信じている
2021年には、以下に述べるように、最初の首席人事官を招いて、私たちの人的資本努力を指導しました。従業員を引き付け、維持し、発展させるための私たちの主な措置は、
心の健康と幸福
メンタルヘルスケア会社として、精神疾患の恥を減らし、従業員の福祉を促進する職場を建設するリーダーになることを渇望しています。私たちは羅針盤のすべての従業員のための心理的および身体的健康支援を含む健康支援に対して全面的な観点を取っている。
様々な福祉資源を提供しています
•認証コンサルタントが運営するグローバル従業員支援計画は、毎期にチームメンバーとその家族に10回以上の治療コースを提供している
•私たちの福祉コミュニティのリーダーと一対一の機密福祉のサイン、入社、離職
•コミュニティコミュニティは、従業員に同僚と任意の話題を議論するフォーラムを提供し、開放的なコミュニケーションと支援を提供する
•集団健康指導シリーズは、個人が健康目標に向かって進むのを助ける
•グループ会議には私たちの幸せなコミュニティが推進する幸せな部分が含まれています
•瞑想アプリを使って週に1回集団瞑想を行います
•会社が支払う従業員医療保険
•毎週合格した従業員が主導するヨガコース;
•チームメンバーが休憩時間に連絡を切断しやすいように、夏休みや年末休暇期間中は全社的に休業する。
2022年私たちは仕事で心を一つにして署名しました憲章. 心を一つにして働く職場の心理的健康と福祉のゴールドスタンダードの制定と実施に取り組むグローバル組織連合である。
参加、文化、価値観
私たちは私たちの使命に駆られた人たちを引き付け、維持し、心理的健康の挑戦に直面している人たちを助け、彼らに権力を与えるためのより良い方法を探すために努力している。私たちは皆思いやりがあり、大胆で、包容的で、厳格な価値観に同意する
2022年、私たちはベストプラクティス協会とその最も人気のある職場運営機関によって、内部調査、外部公衆格付け、会社関係者へのインタビューに基づいて、会社が従業員のために愛している職場を評価し、認証し、イギリスで31位にランクインした従業員に最も愛される職場として認証された。このランキングは、従業員を尊重、関心、鑑賞することをビジネスモデルの中心に置く会社を表彰している。
私たちは次のように肯定的な作業文化を作り続けている
•年次参加度調査を行い,調査結果は我々の上級指導者チームが行動計画を策定した。私たちの2022年の調査によると、私たちの純推進者の得点は依然として39%と非常に高く、2021年の純推進者の得点は45%であり、Qualtrics XM Instituteのデータによると、得点は10%~30%が良く、30%以上の得点が優れている。私たちは、私たちの作業環境を継続的に監視し、仕事の良い分野を褒め、改善すべき分野を決定するために、少なくとも年に1回の参加度と文化調査を行っている
•私たちの社会、福祉、環境、学習と発展、多様性、公平性、包括的なグループへの従業員の参加を支援します。これらのグループには、様々な計画を提唱するための一次から上級者までの従業員が含まれている
•毎年すべての従業員のために会社の価値観シンポジウムを開催し、私たちの価値観を討論し、それを実践している
•私たちの最高経営責任者とより広いチームに連絡し、彼らから最新情報を得るために、毎月全社規模のチーム会議が開催されている
•金曜日の5日間、ランダム5分間の“ウォーターサーバー”、様々なイベントによって開催される“昼食および学習”、遠隔および対面の社交活動、およびCEOとの“勤務時間”など、私たちのハイブリッドワークモードでは、より多くの連絡を維持する機会を提供する
•私たちの文化や参加度をより良く改善するために何ができるかを知るために退職インタビューを行いました
多様性公平性包括性
私たちは団結して、私たちの職場で安全、多元、包容、包容の文化を構築することを決意し、青少年指導計画や従業員慈善寄付計画に参加するなど、私たちのコミュニティの類似の努力に積極的に参加してきた
私たちの参加と文化調査はまた公平、多様性、包容性に対する人々の見方を調査した。今年、私たちは多様性、公平、包括性(DEI)従業員リーダーの委員会と協力し、雇用主平等かつ包容ネットワーク(ENI)と協力し続け、私たちはこのネットワークのメンバーであり、私たちの外部顧問を務めています。経社部委員会の重点分野は
•個人人口統計情報を自発的に提供する従業員を中心にデータ収集活動を継続し、労働力の多様性を測定し、多様性を改善する目標を立てることができるようにした
•訓練を通じてDei問題に対する認識を向上させる。私たちは従業員のために訓練と対話会議を開催し、どのように包容的に考え、行動するかを学ぶ。私たちはまた、認識と能力を向上させるために職場での嫌がらせ訓練を定期的に開催している。私たちのリーダーチームについては、どのように包括的なリーダーシップについての専門家会議と会話を行いました
•私たちのコミュニティを通じて、従業員に特別な空間を提供して、Deiをめぐって彼らの経験、懸念、提案を共有させます
•グループ討論やイベントで自慢の月を祝います
•様々な候補者を募集するために私たちの流れを修正します
◦私たちは私たちの候補者バンクを多様化することを支援するために、経験豊富なパートナーと連絡している。LGBTQ+、少数民族、神経分化求職者向けの求人ブロックも使用しています
◦私たちは私たちのウェブサイトが視力障害者に提供するアクセス可能性を改善した。また、面接中に障害のある便宜施設が必要な場合は、応募者を招待します
◦私たちはイギリスの障害自信計画の署名者であり、その計画は障害者の雇用を支援することを目的としている。障害自信は変革の運動を創造しており、雇用主が異なる方法で障害問題を考えることを奨励し、彼らの障害者の採用、維持、発展の方式を改善するために行動している。これには見える障害と見えない障害が含まれている。
2022年12月31日現在、私たちの取締役会の33%が女性代表で、私たちのより広い幹部管理チームの39%が女性です。全体的に言えば、2022年12月31日まで、会社中の女性の総割合は64%であり、生物技術革新組織の2022年報告の49%の平均割合よりはるかに高い
従業員の発展と訓練
私たちは時間が経つにつれて、私たちの従業員の個人的な成長は会社の発展を推進すると信じています。私たちの人材は私たちの創業仕事において独特の経験を持っているからです
私たちは従業員たちの持続的な発展に努力し、彼らの成長を支持する。優れたスタッフを発見し、育成し、維持するために、いくつかの計画があります
•従業員に職業発展と進歩の指導と明確な道、1年に2回の昇進周期を提供する仕事構造
•業績と発展目標の過程は、従業員が年間を通じてフィードバックを受け、年末に個人業績と奨励を評価することと関係がある
•従業員の個人発展および職業目標を支援するための専門的な内部リソースを提供し、指導および他の開発ツールの支援の下で開発目標を埋め込む
•人材審査は、年に2回、人材を評価と校正し、奨励と発展を目的としている
•外部資源によって提供される専門的な交渉およびコミュニケーションスキル訓練コース
•毎年一人の従業員に学習と発展手当を提供し、個人の発展/仕事に関する訓練に使用する
•成長日、対面の四半期半日会議、私たちの早期の職業人材を集め、ネットワーク、学習、社交を構築し、
•人力資源マネージャーにどのように維持、参加と激励に関する特別な学習シリーズを提供する
報酬と福祉
私たちは世界的な従業員たちに競争力のある報酬と全面的な福祉を提供する。私たちの給与プランには、基本給、年間ボーナス、年間株式奨励、会社が支払う医療計画、健康診断、寛大な有給休暇、旅行保険、生命/障害、収入保護保険、および会社のマッチング支払いを伴う退職貯蓄計画が含まれています。私たちも従業員の株式購入計画を持っています。この計画によると、条件を満たす従業員は6ヶ月ごとに給料減額で各発売期間の開始または終了時の市場価格よりも低い価格で私たちの株を購入する機会があります。低い者を基準とします
私たちの給与と福祉は、従業員に総報酬を提供し、私たちの同業者や他の私たちと人材を競争する会社が提供する報酬と競争力があることを目的としています。私たちは毎年私たちの製品を評価して、私たちのプロジェクトの競争力を確保し、必要に応じて調整します。
働き方
私たちの価値観を肝に銘じて、私たちは包容と思いやりのために、私たちはすべての人に彼らに最適な方法で働く能力を与えなければならないということを認識している。我々の働き方ガイドラインは,硬直したモデルを強制的に実行するのではなく,互いの期待を中心に中心的な原則を策定している。私たちはお互いの私たちの使命への奉仕を信じて、私たちはお互いが私たちの労働時間を最大限に利用できると信じている。私たちは私たちの勤務時間や職場ではなく、私たちの業績でこれを証明することを願う。私たちは大胆に違う方法で仕事をして、もしこれが最も効果的な方法なら、新しい働き方をテストし、私たちが進む過程でそれらを調整する。従業員が彼らに合った方法で働くことを可能にすることで、従業員は柔軟に自分の面倒を見ることができる。彼らはオフィスで働くか家で働くかを選ぶことができ、昼に散歩やジョギングに出かけることができ、彼らは柔軟に予約に参加することができる。私たちの働き方政策のほかに、従業員に在宅勤務予算を提供し、在宅勤務をより快適にし、人間工学の体験に合ったものを購入してもらいます。私たちは依然として同僚との対面連絡の重要性を認識しており、私たちのアメリカでの発展に伴い、今年私たちはニューヨーク市に最初の独立した事務所を開設した
企業情報
Compass Path plcは当初2020年6月にイングランドおよびウェールズ法律によりプライベート株式会社に登録され,名称はCompass Rx Limitedであり,Compass Pathfinder Holdings Limitedのホールディングスとなっている。Compass Rx Limitedは2020年8月に上場株式会社に再登録され,Compass Path plcと改称される.Compass探路者持株有限公司は当初、イングランドとウェールズの法律に基づいて2017年6月に登録設立された。私たちの登録事務所はイギリス柴郡Altrinchamアシュリー路1号3階にあります。郵便番号:WA 14 2 DT、私たちの電話番号は+1(646)905-3974です
私たちのサイトの住所はwww.Compasspathways.comです。当社のウェブサイト上の情報や当社のウェブサイトを介してアクセス可能な情報を本年度報告に組み込むことはできませんし、当社のウェブサイト上のいかなる情報や当社のサイトを介してアクセス可能な情報も本年度報告の一部としてはなりません。これらの資料を電子的に米国証券取引委員会に提出または提供した後、当社のForm 10-K年次報告、Form 10-Q四半期報告、Form 8-K現在の報告、および1934年の証券取引法第13(A)または15(D)節に基づいて提出または提供されたこれらの報告を、合理的で実行可能な範囲内でできるだけ早く無料で提供する。
第1 A項。リスク要因
閣下は、“経営陣の財務状況及び経営成果の検討及び分析”及び当社の総合財務諸表及び関連付記を含む、以下のリスク要因及び本年度報告に記載されたその他の資料を慎重に考慮すべきである。次のいずれのリスクも、当社の業務、財務状況、または経営結果に実質的な悪影響を及ぼす可能性があります。しかし、以下に説明する選択された危険は私たちが直面している唯一の危険ではない。私たちが現在知らないことや現在重要ではないと考えている他のリスクや不確実性もまた、私たちの業務、財務状況、または経営結果に重大で不利な影響を与える可能性があります。当社の業務に関する重大なリスク要約は、上記4ページの“前向き陳述に関する特別説明”に含まれている。
私たちの財務状況と追加資本需要に関連するリスク
私たちは臨床段階の精神健康看護会社で、設立以来すでに重大な損失が発生している。私たちは予測可能な未来に損失が出て、永遠に達成されたり利益を維持したりしないかもしれないと予想している
私たちは臨床段階の精神ヘルスケア会社で、これまで何の収入も生まれていません。設立以来、私たちは重大な運営損失が発生した。2022年12月31日と2021年12月31日までの年度の純損失総額はそれぞれ9150万ドルと7170万ドルです。2022年12月31日までの累計赤字は2兆611億ドル。我々の歴史的損失は,主に研究や開発活動に関するコストと,我々の運営に関する一般的かつ行政コストによるものである。未来、著者らは引き続き研究開発、臨床前テスト、臨床試験、法規遵守性、市場参入、商業化と業務発展活動を行い、予想される一般と行政費用を加えて、少なくとも今後数年で更なる重大な損失を招く。私たちの予想損失、その他の要素は、引き続き私たちの運営資金と株主権益の減少を招く可能性がある。私たちは、他の事項を除いて、私たちの費用が大幅に増加すると予想している
•私たちの第3段階計画を実施するTRDとTRDで行われたCOMP 360ヌードガイキノコ治療では神経性拒食症や心的外傷後ストレス障害など,われわれが検討しているCOMP 360裸蓋キノコ療法の他の適応への臨床発展を継続する;
•私たちの第3段階計画および臨床試験において私たちの研究COMP 360裸蓋キノコ療法を提供するために、治療士の訓練を継続する
•King‘s IoPPNおよびSouth LondonおよびMaudsley NHS Foundation Trustによって共同支援されたIISを含むIISSに投資し続けることで、COMP 360ヌードカバーキノコ療法を使用して、ヌードカバーキノコ療法が自閉症成人の特定の脳経路にどのように影響するかを探索する
•販売、マーケティング、流通インフラを確立し、製造能力を拡大し、COMP 360を含む規制の承認を得る可能性のある任意の候補治療薬を商業化する
•公立医療機関と個人診療所のネットワークを構築し、拡大し、私たちの研究性COMP 360ヌードカバーキノコ療法と心理支援を結合した
•デジタル技術を使って提案された治療製品を強化することを含めて北米やヨーロッパでのビジネス化戦略を推進しています
•われわれが検討しているCOMP 360裸蓋キノコ療法の他の適応を検討し,任意の将来の治療候補薬を発見·開発した
•治療法が開発される前薬物候補薬や幻覚化合物の開発に投資し続けています
•私たちの探索センターや卓越したセンターに投資し続けています
•臨床試験に成功した未来の候補治療薬のために監督管理の承認を求める
•より厳しい規制審査を経験しています
•米国薬品監督管理局(DEA)のスケジュールに関する必要な決定を求め、COMP 360を含む任意の未来に規制承認を得る可能性のある制御物質を含む治療候補薬を商業化できるようにした
•買収、協力、許可取引を通じて外部業務の発展機会を探索し、私たちの製品の組み合わせに未来の治療候補と技術を増加させる
•いわゆる特許または他の知的財産権侵害クレームの弁護に関連する訴訟費用を含む、私たちの知的財産権の取得、維持、拡大、および保護の組み合わせ
•私たちの治療開発および潜在的な将来の商業化努力を支援する人員を含む、臨床、科学、操作、財務および管理情報システムおよび人員を増加させる;
•例えば、新冠肺炎変種の復興または出現による遅延および他の影響を含む研究失敗、実験結果不明確、安全問題、または他の規制課題を含む、上記のいずれかに関連する任意の遅延または遭遇する任意の問題に遭遇する
•将来的にはアメリカヨーロッパ他の潜在的な地域での私たちの業務を拡大します
•イギリスに登録されている米国上場企業として発生する追加法律、会計、その他の費用。
これまで、私たちは私募株式と転換可能な手形を通じて私たちの業務に資金を提供し、2020年の初公募株(IPO)以来、公募株を通じて私たちの業務に資金を提供してきた。利益を実現し維持するためには,大量の収入を生み出す療法を継続し,最終的に商業化する必要がある。これは、TRDのCOMP 360第三段階臨床計画およびCOMP 360または任意の未来候補療法の他の臨床試験を完成させ、私たちの研究COMP 360ヌードマスクキノコ療法を提供するのに十分な数の合格療法士を訓練し、デジタル技術と解決策を使用して私たちの治療サービスを強化することを含む、一連の挑戦的な活動で成功することを要求する
サプライヤーと協力して追加の“卓越センター”を設立および/または開発し、ここでセラピストを訓練し、任意の未来の候補療法を発見し、開発し、COMP 360ヌードカバーキノコ療法および臨床試験に成功した任意の未来の候補療法の承認を得て、マーケティング能力を確立することができる。COMP 360ヌードゲラニン療法または私たちが開発する可能性のある任意の将来の候補療法が商業化販売されても、COMP 360または任意の他の承認された将来の候補療法を商業化することに関連する巨額のコストが生じることが予想される。私たちはこのような活動で決して成功しないかもしれないし、たとえ私たちが成功しても、利益を達成するのに十分な収入が生まれないかもしれない
治療開発に関連する多くのリスクや不確実性のため、費用を増加させる時間や金額、あるいはいつ、または利益を達成できるかどうかを正確に予測することはできない。FDA、EMA、MHRA、または他の同様の外国当局が、現在予想されている研究以外の研究を要求している場合、または私たちの臨床試験または私たちの研究COMP 360ヌードカバーキノコ療法または任意の将来の候補療法の開発に遅延が生じた場合、私たちの費用は現在の予想を超える可能性があり、収入はさらに遅れる可能性がある
たとえ私たちまたは任意の未来のパートナーが確かに売上を生み出しても、私たちは四半期や年度の収益性を実現、維持、または向上させることはできないかもしれない。もし私たちが持続的に利益を得ることができなければ、私たちのアメリカ預託証明書の市場価格を下げ、資金を調達し、業務を拡大し、私たちの治療製品を多様化し、あるいは運営を継続する能力を弱める可能性がある。もし私たちが引き続き損失を被ったら、投資家の投資は何の見返りも得られず、すべての投資を失うかもしれない
私たちは、私たちの研究COMP 360ヌードカバーキノコ療法または任意の将来の候補療法の開発と商業化を達成するために多くの追加資金を必要とするだろう。必要な時に必要な資金を得ることができない場合、いくつかの製品発見、治療開発、研究操作、または商業化努力を延期、制限、または終了させることを強要される可能性がある あるいは私たちが自分で開発してマーケティングした製品または治療候補薬を開発およびマーケティングする権利を与えることができる。
私たちは今後、私たちの運営を十分に支援し、COMP 360ヌードカバーキノコ療法または任意の将来の候補療法の開発を推進するために、多くの追加資金が必要であると予想しています。2022年12月31日までに、私たちの現金と現金等価物は1兆432億ドルで、少なくとも今後12ヶ月の運営費用と資本支出需要に資金を提供できるようになると予想されています。私たちは間違っていることが証明される可能性があるという仮定に基づいてこの推定をして、私たちは現在予想されているよりも早く私たちの資本資源を使用することができる。さらに、持続的に変化する環境、その中のいくつかは、インフレや金利の激化や変動など、私たちがコントロールできない可能性があり、私たちの資本消費速度が私たちの現在の予想よりも大きく速くなる可能性があり、私たちは計画よりも早く追加資金を求める必要があるかもしれない。私たちの将来の短期的かつ長期的な支出需要は、多くの要素に依存するだろう
•著者らは現在、TRDのCOMP 360ヌードカバーキノコ治療計画の第三段階臨床計画の進展、時間と完成状況に対して、神経性拒食症と創傷後ストレス障害に関する第二段階研究、および未来の適応または任意の未来の候補治療方案を決定するために、われわれの臨床前活動と臨床試験を行っている
•FDA、EMA、MHRA、および同様の外国規制機関の規制承認の結果、時間、およびコストを求め、取得し、これらの機関は、私たちが現在予想しているよりも多くの臨床前研究または臨床試験を行うことを要求するか、または以前に合意された研究に対する彼らの要求を変更することを要求するかもしれない
•DEA、各州、外国当局が下したスケジュールに関する任意の決定の結果と時間
•私たちは開発された将来の潜在的治療候補薬の数を決定し、私たちの研究開発努力によって内部で行われても、買収、許可、または他の協力協定による外部開発であっても、
•私たちの組織を、研究COMP 360ヌードカバーキノコ療法および任意の将来の候補療法の研究、開発、潜在的商業化に必要な規模に発展させるために必要なコスト、人員コストの増加を含む
•主要市場の公共および民間医療提供者および診療所ネットワークのコストを狙うための販売およびマーケティング能力を開発する
•私たちの第三段階計画と他の臨床試験では、COMP 360ヌードカバーキノコ療法のコストを管理するために治療師を訓練し、認証します
•私たちの卓越したセンターと精神健康研究センターを設立するコストは、臨床試験を行い、概念検証研究を含めて、私たちの治療モードを完備することを含む
•データを生成して収集し、私たちの知的財産権の組み合わせを推進し、そして科学と臨床資源としての私たちの地域の存在を強化する
•患者の体験および治療過程のコストを改善するためのデジタル技術解決策の開発、テスト、および展開
•特許出願の提出、特許の維持および実施、または第三者による侵害または無効クレームの抗弁に係る費用;
•COMP 360または任意の将来の候補治療薬の規制承認を得ることに関連する時間およびコスト、ならびにCOMP 360または任意の将来の候補治療薬に関する変化する規制要件または将来の候補治療薬に関する不利な結果に遭遇する可能性がある任意の遅延;
•我々の研究COMP 360ヌードカバーキノコ療法または任意の将来の候補療法の潜在的商業化に関連する販売およびマーケティング活動(承認された場合)、および効果的な販売およびマーケティング組織を作成することに関連するコスト;
•私たちは、COMP 360ヌードカバーキノコ療法および任意の将来の候補療法(承認された場合)の将来の販売から直接または特許使用料、マイルストーン、または他の形態で得られる収入金額;および
•上場企業の運営コストとして。
私たちが十分な収入を生み出して私たちの現金需要を満たすことができる前に、私たちは公開または私募株式発行、債務融資、戦略協力、連合、許可手配、または貨幣化取引を通じて、将来の現金需要に資金を提供する予定だ
私たちが必要な時に受け入れ可能な条件で追加資金を調達できるかどうかは、財政、経済、市場状況、その他の要素に依存し、私たちはこれらの要素をあるいは限度的にコントロールできないかもしれない。例えば、継続的な挑戦的な資本市場環境、多くの証券の価格下落、および潜在的衰退要因への懸念は、証券の売却や債務発行によって追加資金を調達する能力に影響を与える可能性があり、これは、私たちの流動性を損なう可能性があり、いくつかの製品の発見、治療開発、研究運営または商業化計画の延期、制限、または終了を迫るか、または、私たちが開発およびマーケティングをより望んでいた製品または候補治療薬を開発およびマーケティングする権利を与えることになるかもしれない。必要に応じて商業的に許容可能な条項で十分な資金を得ることができない場合、私たちは、私たちの研究計画の全部または一部を延期、減少または終了させることを余儀なくされるかもしれません、または私たちの研究COMP 360ヌードカバーキノコ療法または任意の将来の候補療法の開発または商業化、または将来のビジネス機会を利用できないかもしれません。市場変動、ウクライナとロシアとの間の持続的な戦争による地政学的緊張、インフレと金利の激化や変動、および米国と世界経済への関連影響や他の経済や他の要因は、必要なときに資本を得る能力に悪影響を与えたり、資金調達コストを増加させたりする可能性もある
私たちは未来の資金調達が十分な金額を持っているか、商業的に合理的な条項を持っているか、あるいは根本的にできないという保証はない。現在の資本市場状況は、インフレの影響を含めて借入金利が向上しており、前の時期に比べて我々の資本コストが大幅に上昇することが予想される。さらに、任意の融資条項は、私たちの米国預託証明書保有者の保有量または権利に悪影響を及ぼす可能性があり、私たちが発行した追加証券(株式または債務を問わず)、またはそのような発行の可能性は、私たちの米国預託証明書の市場価格を低下させる可能性がある。債務の発生は固定支払義務の増加を招く可能性があり、私たちは追加債務を発生させる能力の制限、私たちが知的財産権を得ることができるかもしれない能力の制限、私たちの業務を展開する能力に悪影響を及ぼす可能性のある他の運営制限など、いくつかの限定的な条約に同意する必要があるかもしれない。私たちはまた、適切でない場合に、協力者または他の人との手配によってより早く資金を求めることを要求される可能性があり、COMP 360または任意の将来の治療候補薬の権利を放棄すること、または他の方法で私たちに不利な条項に同意することが要求される可能性があり、いずれも、私たちの業務、経営業績、および見通しに重大な悪影響を及ぼす可能性がある。さらに、任意の追加的な拠出努力は、私たちの経営陣の日常活動への注意を移す可能性があり、これは、私たちの研究COMP 360ヌードカバーホルモン療法または任意の将来の候補療法の能力を開発し、商業化することに悪影響を及ぼす可能性がある
しかも、より厳格な規制検討は私たちの資金調達能力に否定的な影響を及ぼすかもしれない。私たちの業務活動は複数の管轄区域で法律法規を制定することに依存している。これは確定不可能な程度だ
提案される可能性のある任意の新しい法律、法規または計画の影響、または任意の提案が法律になるかどうか。我々の研究におけるCOMP 360ヌードカバーキノコ療法または任意の将来の候補療法をめぐる規制不確実性は、追加資本を調達する能力を含むが、これらに限定されないが、私たちの業務および運営に悪影響を及ぼす可能性がある。
私たちは臨床分期会社としての歴史が限られていて、これは私たちの業務のこれまでの成功度と私たちの未来の生存能力を評価することを困難にするかもしれません。
私たちは2016年に設立され、これまでに私たちのCOMP 360ヌードカバーキノコ治療研究の開発、私たちの知的財産権の組み合わせの構築、業務計画、資金調達、これらの業務のための行政支援に大部分の資源を投入してきました。著者らは最近COMP 360ヌードカバーキノコ治療TRDの第三段階臨床計画を開始したが、著者らはこのような後期臨床試験を行う能力があり、監督部門の許可を得て、商業規模の製品を製造し、製品の商業化に成功するために必要な販売とマーケティング活動を展開し、あるいは販売国で精算を得ることができることを証明していない。
私たちの業務目標を達成する時、私たちは予見できない費用、困難、複雑な状況、遅延、および他の既知または未知の要素に遭遇する可能性がある。もし私たちのCOMP 360ヌードカバーキノコ療法または任意の未来の候補製品が規制部門の承認を得たら、臨床開発に専念する会社から商業活動を支援できる会社に移行する必要があります。そのような移行で、私たちは成功しないかもしれない。
様々な要因により、私たちの財務状況と経営業績は四半期ごとと毎年大幅に変動し続け、その多くの要素はコントロールできないと予想しています。したがって、今後の経営業績の指標として、いかなる四半期や年度の業績にも依存してはいけません。
追加資本の調達は、私たちの普通株式または米国預託証明書の保有者に希釈をもたらし、私たちの業務を制限するか、またはCOMP 360または任意の将来の候補治療薬の権利を放棄することを要求するかもしれない。
私たちは株式発行、債務融資、戦略協力と連合、許可手配、または貨幣化取引の組み合わせによって追加資本を求めることができるかもしれない。もし私たちが株式、転換可能な債務証券、または他の株式ベースの派生証券を売却することによって追加資本を調達する場合、あなたの所有権権益は希釈され、条項は清算または株主としての他の権利に悪影響を及ぼす特典を含む可能性がある。私たちが発生したどんな債務も固定支払義務の増加を招き、例えば、追加債務の発生、可能な知的財産権の取得、配当金の発表、資本支出、および私たちの業務を展開する能力に悪影響を及ぼす可能性のある他の能力の制限など、限定的な契約に関連する可能性がある。さらに、我々は、株式や債務、またはそのような発行の可能性にかかわらず、米国預託証明書の市場価格の下落を招く可能性がある追加証券を発行し、既存の株主は、我々の融資計画またはそのような融資の条項に同意しない可能性がある。もし私たちが戦略的協力と連合、許可手配、または第三者との金銭化取引によってより多くの資金を調達する場合、私たちは、私たちの研究COMP 360ヌードマスク療法または任意の未来の候補療法に対する貴重な権利を放棄しなければならないかもしれないし、または他の方法で私たちに不利な条項に同意しなければならないかもしれません。いずれも、私たちの業務、運営結果、および見通しに実質的な悪影響を及ぼす可能性があります。私たちは受け入れ可能な条項で十分な追加融資を受けることができないかもしれないし、根本的にできないかもしれない。もし私たちが必要な時に追加の資金を集めることができなければ、私たちは延期、制限を要求されるかもしれない, 私たちの製品開発または将来の商業化努力を減少または終了するか、またはCOMP 360ヌードカバーキノコ療法または任意の未来を用いて私たちの研究を開発およびマーケティングする権利を付与し、マーケティングの候補療法をより望んでいます。さらに、任意の追加的な拠出努力は、私たちの経営陣の日常活動への注意を移す可能性があり、これは、私たちの研究COMP 360ヌードカバーホルモン療法または任意の将来の候補療法の能力を開発し、商業化することに悪影響を及ぼす可能性がある。
また、米国の株主を含む米国預託証明書の一部の株主及び所有者は、優先引受権が取り消されていない場合や制限されている場合であっても、登録された又は普通株の発行が関連規制の枠組み下での売却資格に適合しない限り、その等の権利を行使する権利がない可能性がある。したがって、投資家が優先株や私たちが将来行う可能性のある他の発行に参加することが許可されなければ、彼らの持ち株は希釈されるリスクを受ける可能性がある。
我々が研究しているCOMP 360ヌードカバーキノコ療法と任意の将来候補療法の開発,臨床試験と商業化に関するリスク
われわれの研究におけるCOMP 360裸蓋キノコ療法の成功開発に依存している。COMP 360が臨床試験に成功したり、規制部門の承認を得たりすることは保証されず、その商業化の前に必要である
我々は現在,商業販売が許可されていない治療法は,決して適切な治療法を開発できないかもしれない。今後数年間のわれわれの努力と支出の大部分は,われわれの研究COMP 360裸蓋キノコ療法に用いられることが予想され,これは現在臨床開発における唯一の候補療法である。したがって,我々の業務は現在,規制部門によるCOMP 360の成功承認と,我々が検討しているCOMP 360裸蓋キノコ療法の商業化に依存している。規制部門の承認を得ても、COMP 360が規制部門の承認を受けるかどうか、あるいは私たちの療法が商業化に成功するかどうかは決定できません。もし私たちがCOMP 360ヌードカバーキノコ療法の開発を中止することを要求された場合、あるいはCOMP 360が規制部門の承認を得なかったり、重大な市場承認を得られなかった場合、もしあれば、利益を達成する能力は何年も延期されるだろう。
裸蓋キノコ素の研究、テスト、製造、安全性、有効性、ラベル、承認、販売、マーケティングと流通は現在と将来すべてFDA、DEA、EMA、MHRAと類似の外国の監督管理機関の全面的な監督管理を受けている。アメリカ、ヨーロッパ、あるいは他の管轄区域で規制の承認を得られなければ、私たちはこれらの管轄区域で商業化し、私たちの研究をCOMP 360裸蓋キノコ療法で商業化することはできないだろう。
FDA、EMA、MHRA、および外国の規制機関のCOMP 360の承認を得ることに成功したとしても、どの承認も使用に関連する重大な制限、および特定の年齢層の制限、警告、予防、または禁忌症を含む可能性がある。また、規制機関のCOMP 360の承認を得ても、我々の研究におけるCOMP 360裸蓋キノコ療法を適切に管理し、適切な製造を確保し、合格したセラピストを訓練し、安全に接触させ、商業的に実行可能な価格設定構造を構築し、政府医療計画を含む第三者支払者から保険および十分な補償を得ることを含む商業インフラや協力者との関係を開発し、商業化を実現する必要がある。もし私たちまたは未来のパートナーが私たちの研究COMP 360ヌードカバーキノコ療法を商業化することに成功しなければ、私たちは私たちの業務を継続するのに十分な収入を得ることができないかもしれない。
われわれの研究におけるCOMP 360ヌードゲラクチン療法の成功と将来の候補療法は以下のような要因に依存する
•TRDの第3段階計画を含めて臨床試験に成功しました 神経性拒食症や心的外傷後ストレス障害の第二段階計画,および臨床前研究;
•必要な臨床前研究と臨床試験を完成させるために十分な財政と他の資源があります
•私たちが計画した臨床試験や将来の臨床試験を行うために規制部門の承認または許可を得る
•患者の登録と臨床試験に成功しました
•我々の臨床試験からの積極的なデータは、COMP 360の許容可能なリスク−利益の概要およびターゲット集団における任意の未来の候補治療レジメンをサポートする
•関連する規制機関から規制とマーケティング承認を受けて維持する
•COMP 360または任意の将来の候補治療薬が承認された場合、単独または第三者製造業者との臨床試験および商業製造に臨床供給を提供する製造能力を確立し、拡大する
•私たちの第三段階計画と他の臨床試験で私たちの研究COMP 360裸蓋キノコ療法を管理するための治療師を募集、訓練、認証します
•私たちの研究COMP 360ヌードカバーキノコ療法と任意の未来の候補療法をさらに開発するために協力した
•COMP 360および任意の将来の候補治療薬の特許および商業秘密保護および/または規制排他性を獲得し、維持し、擁護し、擁護する;
•私たちの研究におけるCOMP 360ヌードカバーキノコ療法の商業販売を開始することに成功し、承認されれば、任意の未来の候補療法;
•患者、医学界、および第三者支払人が承認された場合、COMP 360および任意の将来の候補治療の利益および使用を受ける
•COMP 360および任意の将来の候補治療薬の持続的に許容可能な安全性を維持する;
•コスト面で他社との他療法の適応を開発·商業化することを含めて効率的に競争し,COMP 360裸蓋キノコ療法の目標を検討している
•第三者支払者から医療保険と適切な補償を受けて維持すること
•私たちの名声を維持し
•制御された物質、データプライバシー、ビジネス前活動に適用される法律を含む法律法規を遵守する。
もし私たちがこれらの要素の1つまたは複数の点でタイムリーまたは完全に成功できなければ、私たちは私たちの研究COMP 360ヌードカバーキノコ療法または私たちが開発した任意の未来の候補療法を商業化することに大きな遅延や成功に遭遇する可能性があり、これは私たちの業務に実質的な損害を与えるだろう。COMP 360と未来の候補治療薬の発売承認を得なければ、私たちは私たちの運営を続けることができないかもしれない。
COMP 360裸蓋キノコ療法は現在、アメリカ、イギリス、ヨーロッパの他の地域の制御物質法律法規の制約を受けており、私たちが将来開発する可能性のあるいかなる候補療法も製品発売地域の制御物質法律法規の制約を受けており、これらの法律法規を遵守しない場合、あるいはこれらの法律法規を遵守するコストは、臨床開発中でも承認後であっても、私たちの財務状況に悪影響を及ぼす可能性がある。さらに、COMP 360ヌードマスク療法の審査中に、承認される前に、FDAおよび/または他の規制機関は、COMP 360が乱用または誤用の可能性があるかどうかに関するデータを含む追加のデータを必要とする可能性がある。これは承認と潜在的な再配置過程を延期するかもしれない。
米国では,裸蓋キノコとその活性代謝物である裸蓋キノコは,1970年の“全面薬物乱用予防·制御法”(“制御物質法”やCSAとも呼ばれる)に基づき,DEAが“制御物質”や規制物質,具体的には別表の物質とされている。DEAは化合物を付表I,II,III,IVまたはV類として管理している。定義によると,付表一物質は高い濫用の可能性があり,現在米国では“公認された医療用途”はなく,医療監督下での使用は公認の安全性に乏しく,米国で処方,販売,販売してはならない。米国で使用が許可されている薬剤は別表II,III,IVまたはVとすることができ,その中で付表II物質は最も乱用または依存する可能性のある物質と考えられ,付表V物質はこのような物質の中で相対的に乱用リスクが最も低い物質と考えられている。別表1と付表2の薬物は委員会の審議段階修正案の最も厳格な規制を受けなければならず、製造と調達割当量、保安規定と輸入基準を含む。また,別表二薬の投与もさらに制限されている。例えば、新しい処方がない場合、それらは再充填されない可能性があり、ブラックボックス警告がある可能性がある。また,米国の多くの州の法律は裸蓋キノコと裸蓋キノコを付表I規制物質に分類している。裸蓋キノコを含む任意の製品の米国での商業マーケティングについては、裸蓋キノコおよび裸蓋キノコは、DEAによってスケジュールII、III、IVまたはVを再配置しなければならないか、または製品自体は別表II、III、IVまたはVに配置されなければならない。米国での商業マーケティングはまた、スケジュールに関連する立法または行政行動を必要とする。
DEAのスケジュール決定は、1つの物質または1つの物質に対するFDAの特定の処方の承認に依存する。したがって,裸蓋キノコと裸蓋キノコは別表1の制御物質であるが,FDAの承認により米国で医療用途のための裸蓋キノコまたは裸蓋素を含む製品は別表II−Vに登録されるべきであり,FDAの承認が“許容可能な医療用途”の要求に適合しているためである。COMP 360がFDAの承認を得た場合、DEAはスケジュール決定を行い、米国の患者に開くために、別表I以外のスケジュールに置く予定である。このスケジュールの決定は、適切なスケジュールに関するFDAの承認とFDAの提案に依存するだろう。審査中、承認の前に、FDAは、物質が乱用または誤用の可能性があるかどうかに関するデータを含む、非臨床的または臨床的研究からの追加のデータを必要とすることを決定することができる。これは承認と潜在的な再配置過程の遅延を招く可能性がある。この遅延は、FDAによって要求される追加データ量に依存する。このスケジュール決定は,仮最終ルールの発行を含むDEAに通知やコメントルール作成を要求する.このような行動は大衆の意見や聴聞要請の影響を受けるだろうし、これはこれらの物質のスケジュールに影響を及ぼす可能性がある。DEAが有利なスケジューリング決定を行う保証はない.連邦レベルで付表2またはより低い制御物質(すなわち、付表3、4または5)に分類されると仮定しても、これらの物質は州法および条例に基づいて付表を決定する必要がある。
FDAの承認が得られ、COMP 360の完成剤形がDEAが別表II、IIIまたはIV制御物質として登録されている場合、その製造、輸入、輸出、国内流通、貯蔵、販売、および合法的な使用は、DEAによって厳格に規制され続けるであろう。また,計画過程はCSAで規定されている90日間の最終期限よりもはるかに長くなる可能性があり,われわれのCOMP 360ヌードカバーキノコ研究療法の米国での発売が延期されている。さらに、FDA、DEA、または任意の外国規制機関は、この物質がどの程度乱用の可能性があるかを決定するために、私たちが現在予想しているよりも多くの臨床または他のデータを生成することを要求することができ、これは、コストを増加させ、および/または、我々の研究COMP 360ヌードカバーキノコ療法および制御された物質を含む任意の将来の候補治療レジメンの発売を遅らせる可能性がある。また,制御物質を含む候補治療薬は,DEAの製造,貯蔵,流通,医師処方プログラムに関する規定を遵守する必要がある
•施設に対してDEA登録と検査を行う研究、製造、配布、輸入または輸出、または制御物質の配布を行う施設は、これらの活動を展開するために登録(許可されている)でなければならず、DEAに必要な安全、制御、記録保存、報告、および在庫メカニズムを有し、薬物損失および転移を防止する。調剤施設を除くすべての施設は年1回継続しなければならないが,調剤施設は3年ごとに更新されている。DEAはある規制対象物質を処理する登録機関を定期的に検査している。必要な登録の取得および維持は、COMP 360の輸入、製造、または流通の遅延をもたらす可能性があります。また、CSAを遵守できず、特に損失や移転を招く行為を遵守しないことは、規制行動を招く可能性があり、我々の業務、財務状況、運営結果に重大な悪影響を及ぼす可能性がある。DEAは民事処罰を求め、必要な登録の更新を拒否したり、制限、一時停止、またはこれらの登録の手続きを開始したりすることができる。場合によっては、違反は刑事訴訟を引き起こす可能性がある。
•国家規制物質法。米国の個別州でも制御物質法律法規が制定されている。州制御物質法律は常に連邦法律を反映しているが、各州は単独の司法管轄区であるため、それらは単独でCOMP 360を手配する可能性がある。一部の州は連邦行動によって自動的に薬物を手配し、他の州では規則や立法行動を制定することで薬物を手配する。州スケジュールは、連邦規制の承認を得た任意の製品の商業販売を延期する可能性があり、不利なスケジュールは、このような製品の商業的魅力に大きな悪影響を及ぼす可能性がある。私たちまたは私たちのパートナーはまた、臨床試験または商業販売のための制御された物質を取得、処理、配布するために、単独の州登録、許可または許可を取得しなければならず、適用された規制要件に適合しない場合、DEAまたは連邦法律によって規定された強制執行および制裁に加えて、各州で強制執行および制裁をもたらす可能性がある。
•臨床試験それは.我々の研究におけるCOMP 360裸蓋キノコ療法には裸蓋キノコが含まれているため,承認を得る前に米国でCOMP 360の臨床試験を行うためには,我々の各研究サイトはDEAに研究案を提出し,DEA研究者登録を取得·維持し,これらのサイトがCOMP 360を処理·分配し,我々の輸入業者から製品を得ることができるようにしなければならない。DEAが1つ以上の研究場所への研究者登録の許可を延期または拒否すれば、臨床試験は著しく遅れる可能性があり、私たちは臨床試験場所を失う可能性がある。臨床試験の輸入業者はまた別表一輸入業者の登録と毎回の輸入許可証を取得しなければならない。我々は現在、米国でCOMP 360またはその活性成分(すなわち裸蓋キノコ)の製造または再包装/再ラベルを行っていない。COMP 360は、その完全な完成品、包装、およびラベルの剤形で輸入される。
•輸入します。COMP 360が承認され、付表II、IIIまたはIV物質に分類された場合、輸入業者は、輸入業者が登録され、輸入毎に輸入許可証申請を提出すれば、その輸入を商業目的に使用することができる。DEAは国際麻酔品管理局に年間評価/推定を提供し、DEAが輸入を許可した制御物質の数量を指導する。輸入業者が特定の数量を含む必要な輸入許可を得ることができなかったことは、COMP 360の供給に影響を与え、私たちの業務、運営結果、財務状況に重大な悪影響を及ぼす可能性がある。また、別表二輸入業者の登録申請は連邦登録簿に公表されなければならず、第三者意見の提出には待機期間がある。不利な意見はいつも輸入業者登録の承認を遅延させる可能性がある。COMP 360が承認され、付表II制御物質に分類される場合、連邦法は、商業目的での輸入を禁止する可能性がある。COMP 360が別表II物質として登録されている場合、DEAが国内供給不足を決定しない限り、DEAがDEAで定義された物質に対して十分な競争がない限り、ビジネス目的のための薬剤の輸入は許可されないだろう。また,裸蓋キノコと裸蓋キノコを含む規制物質を付表し,商業目的のためにDEA局に輸入を登録したことはなく,科学と研究需要のためである。したがって,COMP 360も輸入もできなければ,COMP 360は完全に輸入せざるを得ない
米国製造では、この活動の個別DEA登録を取得し、維持することが要求されるメーカーを確保する必要がある。
•アメリカの製造業はそれは.別表II分類または自発的なため、米国で製造または再包装/再標識を行った場合、私たちの契約メーカーはDEAの年間製造および調達割当要求の制約を受けるだろう。さらに、COMP 360のスケジュールにかかわらず、最終剤形中の有効成分は現在、付表I制御物質であり、この物質は別表Iに記載されている可能性があるので、割当量によって制限されるであろう。私たちまたは私たちの契約メーカーに割り当てられたCOMP 360有効成分の年間割当量は、臨床試験を完了したり、商業的需要を満たすのに十分ではない可能性がある。したがって、DEAは、制御物質の調達および/または生産割当量に対する私たちまたは私たちの契約製造業者のいかなる遅延または拒否も、私たちの臨床試験または製品発表を延期または停止する可能性があり、これは、私たちの業務、財務状況、および運営結果に重大な悪影響を及ぼす可能性がある。
•アメリカでの流通それは.COMP 360が付表II、IIIまたはIV計画通りである場合、COMP 360および任意の将来の候補治療薬を流通させるために、適切なDEA登録および許可を有する卸売業者を決定する必要がある。これらの流通業者は別表II,IIIまたはIVの流通登録を得る必要がある。COMP 360の能力をより広く配信する上でのこのような制限は、商業アプリケーションを制限する可能性があり、私たちの将来性に悪影響を及ぼす可能性がある。このような登録の取得、遅延、または失われたことは、私たちのコストを増加させる可能性がある。COMP 360が別表II薬である場合、私たちのサプライチェーンの参加者は、警報および監視システムによってより高い安全性を維持し、記録保存および在庫要件を遵守することが要求される可能性があります。これはいくつかの薬局がこの製品を販売することを阻止するかもしれない。また,COMP 360は高い悪用の潜在力を持つことが確認できるため,我々の試験地点で管理する必要があり,ビジネスアプリケーションを制限する可能性がある.また,処方薬の乱用を減らすための州や連邦法執行行動,規制要求,立法は,医師に州処方薬モニタリング計画に相談することを要求すると,医師が別表II製品の処方をあまりしたくなくなり,薬局が配布する可能性がある。
•裸蓋キノコと裸蓋キノコはイギリスでは“規制された薬物”に属し、イギリスの2001年の“薬物乱用条例”の付表1に登録され、1971年の“薬物乱用法案”によってA類制御物質に分類された。2001年“薬物乱用条例”付表1に記載された物質は治療メリットがほとんどないか、ほとんどないと考えられ、最も厳しい規制を受けている。したがって、これらの物質はイギリス政府内務省が発行した許可証の下でしか輸入、輸出、生産、供給できない。裸蓋キノコと裸蓋キノコは2001年の薬物乱用条例によって再配置されないか、あるいはイギリスの1971年の薬物乱用法案によって再分類されないかもしれない。
米国では、裸蓋キノコと裸蓋キノコは再分類される可能性があり、これは私たちの業務に追加の規制負担をもたらし、私たちの業務結果に負の影響を与える可能性がある。
FDAによって承認された製剤に加えて、裸蓋キノコおよび/または裸蓋キノコが“修正案”の下で付表IIまたはより低い規制物質(すなわち、表III、IVまたはV)に再配置されれば、裸蓋キノコおよび裸蓋キノコ研究を行う能力が改善される可能性が高い。しかし、裸蓋キノコと裸蓋キノコを再配置することは、主にFDAとDEAである多くの連邦機関の法執行政策を実質的に変える可能性がある。FDAは“連邦食品、薬物と化粧品法”(FDCA)の執行権に基づいて、食品、薬品、サプリメント、化粧品などの製品の監督管理を通じて公共の健康と安全を確保する責任がある。FDAの役割は、州間貿易で販売されている薬品の成分を規制することと、マーケティングとラベルを含む。現在連邦法により,裸蓋キノコや裸蓋キノコの生産·販売は違法であり,連邦政府が認めている医療用途がないため,FDAは従来,裸蓋菌や裸蓋菌に関する法執行をDEAに延期してきた。もし裸蓋キノコと裸蓋キノコが連邦制御の合法物質に再配置されれば、FDAはより積極的な監督作用を発揮するかもしれない。DEAはこのような物質の製造、分配、そして分配を引き続き積極的に規制するだろう。多機関の実行後の再配置の可能性は、私たちの業務を脅かしたり、私たちの業務に実質的な悪影響を与える可能性があります。
COMP 360には制御物質が含まれており、これらの物質を使用することは公衆の議論を引き起こす可能性がある。裸蓋キノコ素または現在または将来の裸蓋キノコを使用した研究療法に対する公衆の否定的な宣伝または見方は、これらの療法の成功に負の影響を与える可能性がある。
制御された物質を含む治療法は大衆の論争を引き起こすかもしれない。政治的および社会的圧力および否定的な宣伝は、COMP 360および任意の将来の治療候補薬の承認遅延を招き、費用を増加させる可能性がある
発展するかもしれません。このような療法の反対者たちはマーケティングを制限してどんな規制承認も撤回することを求めることができる。また,これらの反対者は否定的な宣伝を起こそうとし,医学界を説得してこれらの療法を拒否しようとするかもしれない。例えば、私たちは私たちの臨床開発計画に対するメディアの批判に直面するかもしれない。ヌードカバーキノコの濫用による負の宣伝は著者らの研究中のCOMP 360ヌードカバーキノコ療法による商業成功或いは市場浸透に不利な影響を与える可能性がある。ファンタジー抗議は歴史的に起こったことがあり、未来にも起こりうるし、メディアの報道を引き起こしている。政治的圧力および否定的な宣伝は、私たちが研究しているCOMP 360ヌードカバーキノコ療法または任意の将来の候補療法の遅延および費用の増加をもたらし、その導入およびマーケティングを制限または制限する可能性がある。
COMP 360または任意の将来の候補療法が商業的販売を許可されれば、私たちの治療法の安全性と質に対する消費者の見方に強く依存するだろう。もし第三者治療サイト、セラピスト、患者がこのような新しい治療法を試みたくなければ、私たちは限られた採用に直面する可能性がある。ヌードゲラニンを含む幻覚物質に対するメディアの負の報道が存在しており,これはわれわれの治療法に対する公衆の見方に影響を与える可能性がある。また,ヌードゲラニンは強い心理体験を引き起こし,患者のこの治療コースの選択を阻止する可能性がある。もし私たちが否定的な宣伝を受けた場合、あるいは私たちの任意の治療法や他の会社が販売している任意の類似療法が証明されたり、患者に有害だと断言されたりすれば、私たちは悪影響を受けるかもしれない。私たちは消費者の認知に依存するため、疾患に関連する負の宣伝または患者が私たちの療法を使用または誤用したり、他社が流通している任意の類似療法によって生じる他の悪影響は、私たちの業務、将来性、財務状況、および運営結果に重大な悪影響を及ぼす可能性がある。
私たちの研究はうつ病と精神健康疾患の研究に重点を置いており、将来の不良事件も政府のより厳格な監督管理、より厳格なラベル要求、及び私たちの療法テスト或いは承認の潜在的な規制遅延を招く可能性がある。任意の増加した審査は、COMP 360または任意の将来の候補治療薬に対する規制部門の承認を得るコストを延期または増加させる可能性がある。
臨床薬物開発は長く高価な過程であり、不確定なスケジュールと不確定な結果を持っている。もしCOMP 360または任意の未来の候補治療薬の臨床試験が延長または延期された場合、私たちまたは私たちの現在または未来の協力者は必要な規制承認を得ることができないかもしれないので、私たちの研究におけるCOMP 360ヌードカバーキノコ療法または任意の未来の候補治療薬を商業化することは、私たちの業務に悪影響を及ぼすであろう
臨床試験費用は高価であり,完成まで数年かかる可能性があり,その結果自体も確定していない。臨床試験過程中にいつでも失敗が発生する可能性があり、著者らの未来の臨床試験結果は成功しないかもしれない
われわれのCOMP 360ヌードカバーキノコ治療TRDの第三段階臨床計画の完成、著者らが行っている神経性拒食症および創傷後ストレス障害の第二段階臨床試験の完了、および他の臨床試験の開始または完成に遅延が生じる可能性がある。例えば、神経性拒食症第2段階研究の参加者の募集やスクリーニングが困難であるため、神経性拒食症第2段階臨床試験ではいくつかの遅延に遭遇している。これらの課題に対応するために、この高度に脆弱な患者群の試験負担を軽減するための試験案を修正している。したがって、私たちは最初に予想したように、2023年にこの実験のデータを得ることはできない。私たちの臨床試験の間、私たちはまた、いくつかの場合、私たちの研究COMP 360ヌードカバーキノコ療法または任意の未来の候補治療薬が発売承認または商業化される能力を遅延または阻止することを経験した多くの予見不可能な事件に遭遇する可能性がある
•検査機関が様々な原因で一時的または永久的な臨床一時的一時的または永久的な臨床一時停止を実施することを含む、試験の開始または修正の規制承認を得ることができなかったか、または調査性新薬申請またはINDを審査すること、または改訂、臨床試験申請または改訂、または同等の申請または改訂を含むことを含む、原因は、試験が臨床試験参加者に対して不合理なリスクを構成することが発見されたこと、または著者らの臨床試験操作または研究場所の検査結果が陰性であること、または私たちが過去に経験した疑わしい、意外な深刻な副作用またはSUSAR、または深刻な副作用またはSAEが発生することである。私たちの臨床試験や研究者が始めた研究やIISSの間にCOMP 360を使用しています
•遅延または予期される契約研究組織またはCROと臨床試験地点と受け入れ可能な条項と合意することができず、その条項は広範な交渉を行うことができ、異なるCROと試験地点の間に有意差が存在する可能性がある
•各場所で機関審査委員会またはIRBまたは道徳委員会の承認を得ることが遅延または失敗した
•試験に参加するのに十分な数の適切な患者を遅延または募集できなかったか、または募集できなかった
•患者に試験を完成させなかったか、あるいは治療後のフォローアップを行った
•臨床サイトが試験案から外れているか、または試験から離脱した者
•試験中に失明またはプラセボまたは非シペソ効果を維持することが困難である可能性があるので、研究において適切な対照アームを設計することを含む、十分かつ良好な制御を行う臨床試験に関連する挑戦
•新しい臨床試験場所を増やし
•我々の第三段階計画と他の臨床試験では、準備、裸蓋キノコ素注射と治療経験の統合を含むCOMP 360裸蓋キノコ素治療のための訓練されたセラピストと適切な第三者臨床試験場所を提供した
•私たちが開発した任意の治療に関連する準備、統合、または長期フォローアップで構成される可能性のある任意のサポートデジタルサービスの十分性
•臨床試験のために十分な数の基礎治療物質をタイムリーに契約して生産しなかった
•第三者訴訟は、私たちの研究におけるCOMP 360ヌードカバーキノコ療法または任意の未来の臨床試験における候補療法が私たちの権利を侵害し、私たちの進展を妨害する禁止を得たと主張している
•もし私たちまたは私たちの協力者が参加者が受け入れられない健康リスクに直面していることを発見した場合、私たちまたは私たちの協力者(場合によっては)試験の一時停止または終了の安全または耐性の問題を引き起こす可能性がある
•規制要件、政策、指針の変化
•患者と患者の臨床試験における保持率は予想より低かった
•私たちの第三者研究請負業者は、法規の要求を適時に遵守できなかったか、または私たちに対する契約義務を履行できなかったか、または全く遵守しなかった
•臨床試験中の適切な投与量レベルの決定に遅延が出現した
•著者らの臨床試験は公衆衛生危機(例えば新冠肺炎大流行)によって遅延し、その原因は患者の臨床試験への参加意欲或いは可用性の低下、及び十分な潜在的治療物質の供給を得る上で挑戦に直面していることを含む
•基礎治療物質の品質または安定性が許容基準よりも低い;および
•地政学的行動による業務中断は、戦争やテロ、地震、台風、洪水や火災などの自然災害、大流行病、あるいは我々の情報技術システムがネットワーク攻撃やその他の原因による故障や重大な停止を含む。
臨床試験が我々、臨床試験を行う機関審査委員会または倫理委員会、データ審査委員会またはDRC、またはそのような試験のデータ安全監視委員会またはFDA、EMA、MHRAまたは他の規制機関によって一時停止または終了された場合、または臨床試験を行う調査員やサイトのDEA登録が撤回された場合、遅延に遭遇する可能性がある。このような主管部門は、法規の要求または私たちの臨床規程に従って臨床試験、FDA、EMA、MHRAまたは他の法規機関の臨床試験操作または試験場所の検査を行うことができず、過去または将来、私たちの試験またはCOMP 360を使用する任意のIISSまたは他の研究に出現する可能性のある任意のSUSARまたはSAE、ならびにCOMP 360または任意の未来の治療候補薬が属するカテゴリに関連するSUSARまたはSAEを含む、一連の要因によって臨床試験を一時停止または終了する可能性がある。政府法規や行政行為の変化或いは臨床試験を継続するのに十分な資金が不足している。例えば,2018年6月18日,FDAは我々が最初に提出したIND文書を審査した後,COMP 360を臨床棚上げ状態にし,ヌードゲラニン会議の構造,研究者,退院基準に関する追加情報が必要であることを理由とした。INDに応答情報を提出し,FDAは2018年8月8日に臨床放置を中止した。もし私たちが任意のCOMP 360臨床試験を完成または終了するか、または任意の未来の候補療法に遅延がある場合、私たちの研究におけるCOMP 360ヌードカバーキノコ療法のビジネスの将来性
そうでなければ、未来の候補療法はすべて損なわれ、私たちがこのような候補療法から収入を得る能力は延期されるだろう。さらに、臨床試験の完成のいかなる遅延も私たちのコストを増加させ、COMP 360または任意の未来の候補治療薬の開発と承認過程を緩和し、私たちの販売と収入を創出する能力を危険にさらす可能性がある。さらに、COMP 360または任意の将来の候補療法を変更する場合、これらの修正された候補療法をより早いバージョンに接続するために追加の研究を行う必要があるかもしれません。これは、私たちの臨床開発計画または私たちの研究COMP 360ヌードマスクキノコ療法または任意の未来の候補療法の発売承認を遅らせる可能性があります。重大な臨床試験遅延はまた、私たちの競争相手が治療法を市場に出し、あるいは私たちの研究用COMP 360ヌードカバーキノコ療法または任意の未来の候補療法を商業化する期限を独占的に持っていることを短縮し、私たちの研究用COMP 360ヌードカバーキノコ療法または任意の未来の候補療法を商業化する能力を弱化させ、私たちの業務と手術結果を損なう可能性がある
このようなどんな状況でも、私たちの業務、財政状況、そして見通しに大きな被害を及ぼす可能性がある。さらに、臨床試験の開始または完了遅延をもたらす多くの要因も、最終的にCOMP 360または任意の将来の候補療法の規制承認を拒否させるか、または我々の研究COMP 360ヌードカバーキノコ療法または任意の将来の候補療法の開発を早期に停止させる可能性がある
我々の臨床試験は、COMP 360または私たちが決定し、追求する可能性のある任意の未来の候補製品の安全性および有効性の実質的な証拠を証明できない可能性があり、これは、規制承認および商業化の範囲を阻止、延期、または制限するであろう。
我々の研究用COMP 360ヌードカバーキノコ療法または将来の候補治療薬の商業販売が規制される前に、適用される候補治療薬は各目標適応において安全かつ有効であることを、長い、複雑かつ高価な臨床前研究および臨床試験によって証明しなければならない。候補治療薬は、その予期される患者集団および予期される用途において、十分なリスクおよび収益状況を示さなければならない
臨床試験費用は高価であり,完成まで数年かかる可能性があり,その結果自体も確定していない。失敗は臨床開発過程中のいつでも発生する可能性があり,第三段階のキー試験期間を含めて,また我々が研究しているCOMP 360ヌードカバーキノコ療法がわれわれの臨床開発の唯一の製品であるため,失敗のリスクが高く,適切な製品の開発には決して成功しないかもしれない。臨床試験を開始した候補製品の多くは規制機関の商業化承認を得たことがない。著者らの管理後期臨床試験における経験は限られている;著者らがTRDで行ったCOMP 360の第三段階の肝心な試験は私たちの最初の重要な試験であり、私たちは私たちの第三段階の肝心な試験を成功に実行できないかもしれない。
TRDのCOMP 360の第3段階キー試験、私たちが行っている第2段階試験、または任意の他の未来の臨床試験が成功するかどうかは確認できません。われわれが行った臨床試験は,規制部門の承認を得てわれわれの研究をCOMP 360裸蓋キノコ療法で市場に出すために必要な有効性と安全性を証明できない可能性がある。ある場合、多くの要素のため、同じ候補治療方案の異なる臨床試験間の安全性或いは有効性結果は有意差が存在する可能性があり、方案中に規定された試験プログラムの変化、患者群の大きさとタイプの差異、臨床試験方案の変化と遵守及び臨床試験参加者の退学率を含む。もし私たちが行っているあるいは未来の臨床試験結果がCOMP 360の治療効果を決定できなければ、もし私たちが統計的かつ臨床的意義のある臨床終点に達していなければ、あるいはCOMP 360に関連する安全問題が存在すれば、上場承認を延期するかもしれないし、あるいは永遠に発売承認を得ないかもしれない。我々の目標適応のいずれの臨床試験で観察される任意の安全問題も、規制部門がこれらの適応および他の適応におけるCOMP 360の使用の将来性を許可することを制限する可能性があり、これは、私たちの業務、財務状況、および運営結果に大きな悪影響を及ぼす可能性がある
たとえ著者らの臨床試験が成功に完成しても、臨床前と臨床データはよく異なる解釈と分析の影響を受け、著者らはFDA、EMA或いは類似の外国の監督機関が著者らのように結果を解釈することを保証することができず、或いは著者らの臨床試験が適切な設計或いは支持を経て、COMP 360の安全性と有効性を証明することに同意する。したがって,COMP 360を承認に提出する前に,より多くの実験を行う必要があるかもしれない.FDA、EMA、または同様の外国の規制機関がマーケティング申請の支援に満足していない場合、COMP 360の承認は著しく延期される可能性があり、または潜在的なCOMP 360承認をサポートするために追加の実験を行うために多くのリソースが必要となる可能性がある。さらに、一方の法域が許容可能な支持承認の結果は、別の規制機関によって、別の法域の規制承認を支持するのに十分ではないと考えられる可能性がある。治療物質開発における固有のリスクにより,COMP 360や任意の将来の候補治療薬は開発に成功し,承認されない可能性が高い。多くの他の会社は彼らの候補療法は臨床前研究と臨床試験で満足できると考えているが、監督管理機関のその治療法に対するマーケティング許可を得られなかった。COMP 360や将来の候補治療薬の規制承認を得なければ、私たちは手術を続けることができないかもしれない。COMP 360や将来の治療薬の規制が承認されても
候補薬物の場合、このような承認された条項は、特定の候補治療薬の範囲および用途を制限する可能性があり、これは、その商業的潜在力を制限する可能性もある。
著者らが時々発表或いは公表した臨床試験の一時、主要と初歩データは更に多くの患者データの獲得に従って変化する可能性があり、そして監査と検証プログラムの影響を受け、これは最終データの重大な変化を招く可能性がある。このようなデータは規制の提出や承認を支持するのに十分ではないかもしれない。
われわれは過去に臨床試験の中期,頂線あるいは予備データを発表したことがあり,将来的にも時々発表される可能性がある。一定数または百分率の被験者を登録した後,試験が完了する前にデータの中期分析を行うことにする可能性がある。同様に、私たちは、最終的な試験結果が完了する前に、主要および重要な副次的端末の主要または予備結果を報告するかもしれない。より多くの患者データ或いは分析の出現に伴い、著者らの臨床試験の中期、主要と初歩的なデータは変化する可能性があり、必ずしも最終結果を予測できるとは限らない。更なる中期、トップクラスと初歩的なデータは患者登録の継続、より多くの患者データの獲得及び著者らが最終臨床試験報告を発表することに伴い、1つ或いは複数の臨床結果は実質的に変化する可能性があるというリスクに直面する可能性がある。一時的なデータ、主要なデータ、そして初歩的なデータは依然として監査と確認手続きを受ける必要があり、これは最終データが私たちが以前に公表した予備データと大きく異なる可能性がある。したがって、最終データが利用可能になる前に、中間データ、営業データ、および予備データは慎重に見られなければならない。中間データと比較して、最終データの重大な不利な変化は、私たちの業務の見通しを深刻に損なうか、私たちの株価を下落させる可能性があります
さらに、他の人は、規制機関を含み、私たちの仮定、推定、計算、結論または分析を受け入れないか、またはデータの重要性を異なる方法で解釈またはトレードオフする可能性があり、これは、特定の計画の価値、特定の候補治療薬、およびわが社の全体的な承認または商業化に影響を与える可能性があり、規制当局は、さらなるデータの提供を要求するかもしれない。さらに、あなたまたは他の人は、私たちが決定した重大な情報または他の適切な情報が私たちの開示に含まれていることに同意しない可能性があり、私たちが開示しないことを決定した任意の情報は、最終的に特定の候補治療計画に関する未来の決定、結論、観点、活動、または他の側面に対して大きな意味を有するとみなされる可能性がある。我々が報告した主なデータが実際の結果と異なる場合、または規制機関を含む他の人が、結論に同意しない場合、COMP 360または任意の将来の候補製品の承認を得て商業化する能力は、私たちの業務、経営結果、見通し、または財務状況が損なわれる可能性がある。
FDA、EMA、MHRAと類似外国機関の規制承認過程は長く、時間がかかり、しかも本質的に予測不可能であり、もし私たちが最終的にCOMP 360と任意の未来の候補治療薬の監督管理許可を得ることができなければ、私たちの業務は深刻な損害を受けるだろう
我々は以前FDAに新薬申請やNDAを提出したこともなく,EMAやMHRAに上場許可申請やMAAを提出したこともない。商業販売COMP 360または任意の将来の候補治療薬の規制承認を得る前に、COMP 360および任意の未来の候補治療薬は、各目標適応において安全かつ有効であることを、長く、複雑で高価な臨床前試験および臨床試験によって証明しなければならない。臨床試験費用は高価であり,完成まで数年かかる可能性があり,その結果自体も確定していない。臨床試験では随時失敗が発生する可能性があり,COMP 360は開発の後期段階であるが,失敗のリスクは依然として高く,適切な製品の開発には決して成功しない可能性がある
FDA、EMA、MHRA、および同様の外国当局の承認を得るのに要する時間は予測できないが、通常は臨床試験開始後数年が必要であり、規制機関のかなりの裁量権を含む多くの要素に依存する。また、承認政策、法規、あるいは承認を得るために必要な臨床データのタイプと数量は候補治療薬の臨床開発過程で変化する可能性があり、司法管轄区域によって異なる可能性がある。私たちはCOMP 360に対する規制部門の承認を受けていない。われわれは最近TRDでCOMP 360の第3段階臨床計画を開始した。FDAは著者らの第三段階計画の設計に同意しない可能性があり、この計画の設計はある方案の修正を反映し、ある程度著者らのCOMP 005サンプル量の再推定を反映し、そして長期フォローアップを2つの重要な研究に組み入れた。FDAは現在このような議定書修正案を検討しており、論評や提案があるかもしれない。FDAは、COMP 005試験の規模または2つの重要な計画の長期後続部分の設計をさらに変更することを要求する可能性があり、これは、私たちの第3段階の臨床計画を延期するか、またはCOMP 360新薬申請の審査過程に影響を与える可能性がある。COMP 360または私たちが将来開発を求める可能性のある任意の将来の治療候補薬は、規制部門の承認を得られないかもしれない
COMP 360または任意の将来の候補治療薬は、FDA、EMA、MHRAまたは同様の外国規制機関の規制承認を得ることができない可能性があり、または以下の理由を含む様々な理由で商業市場から除外される可能性がある
•FDA、EMA、MHRA、または同様の外国の規制機関は、私たちの臨床試験の規模、設計、または実施を変更することを同意、疑問、または要求しないかもしれない
•FDA、EMA、MHRAまたは同様の外国の規制機関は、COMP 360または任意の未来の候補治療薬が安全で有効ではなく、中程度のみ有効であるか、または不良または意外な副作用、毒性または他の特徴を有することを決定する可能性があり、上場承認を得ることができない、または商業使用を阻止または制限することができる
•臨床試験結果はFDA、EMA、MHRA或いは類似の外国監督管理機関が許可した統計的意義レベルに符合しない可能性がある
•私たちが研究しているCOMP 360ヌードカバーキノコ療法または任意の将来の候補療法の臨床的および他の利点がその安全リスクを超えていることを証明できないかもしれません
•FDA、EMA、MHRAまたは同様の外国の監督管理機関は、臨床前研究または臨床試験データの解釈に同意しないかもしれない
•我々が研究しているCOMP 360ヌードカバーキノコ療法または任意の将来の候補療法の臨床試験から収集されたデータは、NDAまたは他の提出の提出をサポートするのに十分ではないか、または米国または他の場所の規制承認を得るのに十分ではないかもしれない
•FDA、EMA、MHRA、または同様の外国の規制機関は、臨床および商業供給契約を締結した第三者メーカーの製造プロセスまたは施設に欠陥があるか、または承認されていないことを発見する可能性がある
•FDA、EMA、MHRAなどの外国の監督管理機関の承認政策や法規は大きく変化する可能性があり、私たちの臨床データは承認を得るのに十分ではない
•第三者臨床試験地点および治療士の使用を含む、我々の新しい治療および送達方法の潜在的リスク。
この長い承認過程、および将来の臨床試験結果の予測不可能性は、規制部門の承認を得ることができず、COMP 360または任意の未来の候補治療薬を販売することができず、これは私たちの業務、手術結果、および将来性を深刻に損なう可能性がある。FDA、EMA、MHRA、および他の同様の外国当局は、承認中に大きな自由裁量権を有し、任意のCOMP 360または任意の将来の候補治療薬の規制承認をいつまたは得るかどうかを決定する。COMP 360または任意の将来の候補治療薬の臨床試験から収集されたデータが有望であると信じていても、これらのデータは、FDA、EMA、MHRA、または任意の他の規制機関の承認をサポートするのに十分ではない可能性がある。COMP 360または任意の将来の候補治療薬が、任意の適用可能な簡素化された規制承認手順に従って承認されなかった場合、これは、候補治療薬がより短い時間で承認されることを阻止するか、または費用増加を全く引き起こさず、それによって、私たちの業務に実質的な損害を与えることになる。
さらに、私たちが承認されても、規制当局または価格決定当局は、COMP 360または任意の未来の治療薬候補の適応が私たちが要求しているよりも少ないか、あるいは私たちの治療法のために徴収しようとしている価格を承認しないかもしれないし、承認は高価な発売後の臨床試験の表現に依存するかもしれないし、あるいは候補治療薬を承認する可能性のあるラベルは、候補治療薬の商業化に必要または所望のラベル声明を含まないかもしれない。例えば、エスケタミンは重度抑うつ障害またはMDDに対する薬物であり、FDAの適用法規によると、リスク評価および緩和戦略(REMS)計画によってしか得られず、抗うつ薬によって要求されるように、ブラックボックス警告を有し、子供および若い成人患者の自殺アイデアおよび行動のリスク増加を警告する。上記のいずれの場合も、我々が研究しているCOMP 360ヌードカバーキノコ療法または任意の将来の候補療法の商業的将来性に負の影響を与える可能性がある
COMP 360または任意の将来の候補治療薬が規制によって承認されても、持続的な義務および持続的な規制審査の制約を受けることになり、多くの追加費用をもたらす可能性がある。また,このような候補療法のいずれかが承認されれば,ラベルや他の制限や市場撤退の制限を受ける可能性があり,法規制の要求を遵守できなかった場合,あるいは我々の研究におけるCOMP 360裸蓋キノコ療法や任意の将来の候補療法が予期せぬ問題に遭遇した場合,罰を受ける可能性がある
FDA、EMA、MHRA、または同様の外国の規制機関がCOMP 360または任意の将来の候補治療薬を承認する場合、製造プロセス、ラベル、包装、流通、有害事象報告、貯蔵、
この治療法と潜在的治療物質の広告、宣伝、記録保存は広範かつ持続的な法規制要求の制約を受ける。これらの要件は、承認後に行われた任意の臨床試験のための安全および他の発売後の情報および報告、登録を提出すること、および現在の良好な生産実践(CGMP)および良好な臨床実践(GCP)を継続的に遵守すること、および適用される製品追跡および追跡要件を含み、これらはすべて巨額の費用をもたらす可能性があり、このような治療法を商業化する能力を制限する。また、会社はその薬品の“ラベル外”用途を普及させてはならない。ラベル外使用とは,米国FDAが承認したラベルに記述されていない適応に1つの製品を用いることである.または他の司法管轄区域では、規制機関の承認を適用する用途とは異なる。一方,医師は非ラベル用途のための製品を開発する可能性がある。FDAおよび他の規制機関は、医師が独立した医療判断において行う薬物治療選択を規範化していないが、彼らは、マーケティング許可が発行されていない製品のラベル外用途に関連する会社またはその販売者からの販売促進情報を制限している。その後、任意の承認された候補治療レジメンには、予想外の深刻度または頻度の有害事象、または私たちの第三者製造業者または製造プロセスを含む、以前に未知の問題が存在することが発見され、または規制要件を遵守できなかったことは、他のことを除いて、以下のようになる可能性がある
•COMP 360または任意の将来の候補治療薬のラベル、流通、マーケティングまたは製造の制限は、製品を市場から撤回するか、または製品リコール;
•タイトルや警告状はなく、臨床試験を一時停止するか
•FDA、EMA、MHRA、または他の外国規制機関は、私たちが提出した係属中の出願または承認された出願の補充を承認することを拒否するか、または許可証の承認を一時停止または停止する
•発売後の研究や臨床試験が求められている
•第三者支払者の保証の制限
•罰金、利益または収入の返還、
•上場承認の一時停止または撤回
•製品を差し押さえたり、差し押さえたり、製品の輸出入を許可することを拒否したり;
•民事または刑事処罰を禁令または適用する。
さらに、COMP 360または任意の将来の候補治療薬のために得られる任意の規制された承認も、この療法が市販される可能性のある承認指示用途の制限または承認条件によって制限される可能性があり、または第4段階の臨床試験を含む可能性の高い市販後試験要件を含み、そのような候補治療薬の安全性および有効性のモニタリングを監視する可能性がある。例えば、承認された場合、COMP 360は、適用されるFDA法規のREMS計画によって制約されると考えられる。サプライヤーにとって、REMS計画は高価で時間がかかり、高い行政負担に関連しており、これは著者らの研究COMP 360裸蓋キノコ療法の商業化能力を延期または制限する可能性がある。
法律、法規または規制政策の適用が変化した場合、または私たちの研究におけるCOMP 360ヌードカバーキノコ療法または私たちの潜在的治療物質の製造に問題が発見された場合、または私たちまたは私たちの流通業者、ライセンシー、または共同営業者のうちの1つが規制要件を遵守できなかった場合、規制機関は様々な行動をとることができる。これらの措置には,我々に罰金を科し,治療薬やその製造に制限を加え,市場から治療薬のリコールや下積みを要求することが含まれている。規制当局はまた、私たちのマーケティング許可を一時停止または撤回し、より多くの臨床試験を行うこと、私たちの治療ラベルを変更すること、またはより多くのマーケティング許可申請を提出することを要求することができる。このような事件が発生した場合、私たちがこのような治療法を販売する能力が損なわれる可能性があり、私たちは法規の要求を遵守することによって多くの追加費用が発生する可能性があり、これは私たちの業務、財務状況、および運営結果に大きな悪影響を及ぼす可能性がある。
COMP 360と私たちが将来開発する可能性のある任意の候補治療薬は深刻な不良、不良、あるいは受け入れられない副作用がある可能性があり、発売承認を延期または阻止する可能性がある。COMP 360または任意の将来の候補薬剤の開発中に、または承認された後に、そのような副作用が発見された場合、そのような候補薬剤の開発を放棄する必要がある可能性があり、任意の承認されたラベルのビジネスイメージが制限される可能性があり、または他の重大な負の結果の影響を受ける可能性がある。
COMP 360または任意の将来の候補治療薬によって引き起こされる可能性のある副作用は、私たちまたは規制機関の臨床試験の中断、延期または停止、または臨床保留を引き起こす可能性があり、より厳しいラベルをもたらす可能性があり、治療の利点がそのリスクよりも大きいことを保証するためにREMS計画を実施するか、またはFDA、EMA、MHRA、または他の同様の外国機関の規制承認を延期または拒否することを要求する。我々または規制機関は、IISSまたは他のスポンサーによる研究において、臨床試験環境外で裸ゲニンを使用した自発的報告または文献中の安全性報告から、COMP 360またはCOMP 360に類似した化合物または任意の将来の候補治療薬に関連する副作用を知ることも可能であり、これらの副作用に基づいて同様の行動をとることができる。
将来の臨床研究結果は、COMP 360または任意の未来の候補治療薬が不良または許容できない副作用、さらには死亡をもたらす可能性があることを示しているかもしれない。例えば,TRDの2 b期臨床試験の結果では,いくつかの治療緊急有害事象が報告されている。死亡や重篤な副作用が起こらないことは保証されず,臨床環境においても同様である。深刻な副作用が発生した場合、私たちの試験は一時停止または終了される可能性があり、FDA、EMA、MHRA、または同様の外国の規制機関は、COMP 360または任意のまたはすべての標的適応を承認する任意の未来の候補治療薬のさらなる開発または拒否を停止または拒否するように命令することができる。薬物に関連する副作用は、患者の募集または患者の試験完了能力に影響を与える可能性があり、あるいは潜在的な製品責任クレームを招く可能性がある。また,裸蓋キノコに対する人によって反応に大きな差があるため,ある患者はこのような治療に対して負の体験を与える可能性があり,これは私たちに責任を負わせる可能性があり,公開されていれば名声を損なうこともある。このようなどんな状況でも、私たちの業務、財政状況、そして見通しに大きな被害を及ぼす可能性がある
臨床試験は潜在的な患者集団の代表的なサンプルで行われ、これらのサンプルは顕著な変異性を有する可能性がある。COMP 360あるいは任意の将来の候補治療薬に対する監督部門の承認を得ても、臨床試験期間中に限られた数の患者にのみテストを行った。臨床試験の設計は、限られた数の対象および限られた治療への曝露の持続時間に基づいて、潜在的な統計学的意義に基づいて、任意のこのような候補治療を達成できるかどうかの目標安全性および有効性プロファイルを決定するためのものである。任意の統計的サンプリングの結果と同様に、COMP 360または任意の将来の候補治療薬のすべての副作用が発見される可能性を保証することはできず、より多くの患者がそのような治療候補薬により長時間接触した場合にのみ、より完全な安全性プロファイルを決定することが可能である可能性がある。また,より規模の大きい臨床試験であってもまれな重篤な副作用を決定できない可能性があり,あるいはそのような研究の持続時間は,これらのイベントが発生する可能性のある時間を決定するのに不十分である可能性がある。もし私たちのマーケティング申請が承認されれば、より多くの患者が私たちの療法を使用し始め、私たちの療法に関連する新しいリスクと副作用が発見されるかもしれない。他の製品や療法は規制部門の承認を得ているが,承認された後に安全性の問題が発見された。このような安全性への懸念はラベルの変更や市場からの治療法の撤回を招いた, われわれが検討しているCOMP 360裸蓋キノコ療法と任意の将来の候補療法は類似したリスクに直面する可能性がある。私たちは、私たちの研究におけるCOMP 360ヌードカバーキノコ療法および任意の未来の市場での候補療法を撤回またはリコールしなければならないかもしれない。もし私たちの試験COMP 360ヌードカバーキノコ療法または任意の未来の候補療法が規制部門の承認を得たら、私たちの市場での名声が損なわれたり、集団訴訟を含めて訴訟を受けたりすれば、私たちの将来の潜在的な売上も大幅に減少する可能性がある。これらの結果のいずれも、私たちが承認した候補療法(あれば)の任意の販売を減少または阻止するか、またはCOMP 360裸蓋キノコ療法および任意の将来の候補療法の商業化およびマーケティングのコストおよび費用を大幅に増加させる可能性がある。
さらに、もし私たちの研究におけるCOMP 360ヌードカバーキノコ療法または任意の未来の候補療法が市販されて承認された場合、私たちまたは他の人はその後、このような候補療法による不良または許容できない副作用を発見し、以下を含むいくつかの潜在的な重大な負の結果を引き起こす可能性がある
•規制当局はこのような療法の承認を撤回し、承認された候補療法(あれば)を市場から撤退させることを要求するかもしれない
•規制当局は、医師および薬局にラベル宣言、具体的な警告、禁忌症、または現場警報を追加することを要求するかもしれない
•規制当局は、そのような副作用のリスクを概説して、患者に配布するために、または候補治療の利点がそのリスクよりも大きいことを確実にするためにREMS計画を実施するための薬物ガイドラインを必要とするかもしれない
•私たちは投与方法を変更し、追加の臨床試験を行うか、候補治療薬のラベルを変更することを要求されるかもしれない
•治療候補薬をどのように宣伝するかで制限されるかもしれません
•この治療法の売り上げは大幅に減少する可能性があります
•私たちは訴訟や製品責任クレームの影響を受ける可能性があります
•私たちの名声は損なわれるかもしれない。
これらのイベントのいずれも、影響を受ける候補治療レジメンに対する市場の受容度を達成または維持することを阻止するか、または商業化コストおよび費用を大幅に増加させる可能性があり、これは、逆に、COMP 360ヌードカバーキノコ療法または任意の将来の候補治療レジメンの販売からの私たちの研究の大量の収入を遅延または阻止する可能性がある
FDA、EMAまたはMHRAのCOMP 360の承認、または米国、ヨーロッパ、またはイギリスで決定され、追求される可能性のある任意の未来の治療薬の候補を獲得しても、これらの管轄区域以外で任意のこのような候補薬剤を商業化する承認を得ることは決して得られず、すべての市場潜在力を達成する能力を制限するであろう。
米国以外の市場で任意の製品を販売するためには、安全と有効性に関する他の国の多くの規制要件を確立し、遵守しなければならない。一国で行われる臨床試験は、他の国の規制部門に受け入れられない可能性があり、一国の規制承認は、他のどの国でも規制承認を受けることを意味するものではない。承認の流れは国/地域によって異なり、1つの管轄区域で行われる臨床試験は、他の管轄区域の規制機関によって受け入れられない可能性があるので、追加の製品試験および検証、および米国とは異なる追加または異なる行政審査期間が関連する可能性がある。米国以外の多くの管轄区では、候補治療薬は精算承認を受けなければならず、この司法管轄区で販売が許可される。場合によっては、私たちが私たちの製品のために受け取る価格もまた承認されなければならない。
外国の監督管理機関の承認を求めることは困難とコストを招く可能性があり、追加の臨床前研究或いは臨床試験が必要であり、これは高価で時間がかかる可能性がある。異なる国の規制要求は大きく異なる可能性があり、私たちの研究COMP 360裸蓋キノコ療法と任意の未来の候補療法がこれらの国で発売されることを延期または阻止する可能性がある。外国の規制承認プロセスには、FDA、EMA、またはMHRA承認の取得に関連するすべてのリスクが含まれる可能性があります。私たちはいかなる司法管轄区域(国際市場を含む)で販売を許可された候補薬剤もなく、私たちは国際市場でCOMP 360または任意の未来の候補薬の規制承認を得た経験もない。もし私たちが国際市場の規制要求を遵守できなかったり、必要な承認を得られなかったり、あるいは国際市場の規制承認が延期された場合、私たちの目標市場は削減され、私たちの研究COMP 360ヌードカバーキノコ療法および任意の将来の候補療法のすべての市場潜在力を達成する能力は損なわれるだろう。
われわれが検討しているCOMP 360裸蓋キノコ療法や任意の将来候補療法の臨床前研究や早期臨床試験の結果は後期臨床試験の結果を予測できない可能性がある。我々が行っている臨床試験の初歩的な成功は,これらの試験完了後や後期試験で得られた結果を示していない可能性がある
臨床前研究と初歩的な臨床試験で進展を得たが、臨床試験後期段階の候補治療薬物は期待される安全性と有効性特徴を示すことができない可能性がある。また、我々のいかなる臨床試験が最終的にCOMP 360あるいは任意の未来の候補治療薬の更なる臨床開発に成功するか、あるいは支持することは保証されない。臨床試験を行う薬物は第三段階の肝心な試験を含む非常に高い失敗率がある。製薬業界のいくつかの会社は臨床開発において重大な挫折を経験し、早期の研究においても奮い立つ結果を得た
また,われわれの過去,計画中,進行中のいくつかの臨床試験は“開放ラベル”試験設計を採用している。オープンタグ“臨床試験”とは、患者および研究者の両方が、患者が研究製品候補を受け入れているかどうかを知っているかどうか、または既存の承認薬またはプラセボを意味する。最も典型的には,オープンラベル臨床試験は候補の研究製品のみをテストし,異なる用量レベルで試験を行う可能性がある。開放ラベル臨床試験は様々な制限を受けており,これらの制限は任意の治療効果を誇張する可能性があり,開放ラベル臨床試験中の患者が治療を受ける際に知られているからである。オープンラベル臨床試験は“患者偏見”の影響を受ける可能性があり,すなわち患者が症状が改善したと考えているのは,実験的治療を受けていることを意識しているだけである。また,オープンラベル臨床試験は,“調査者偏見”の影響を受ける可能性があり,すなわち臨床試験の生理結果を評価·審査する人は,どの患者が治療を受けているかを知り,その知識を知っている場合に治療群の情報をより有利に解釈することが可能である。オープンラベル試験の結果は、我々の任意の候補製品の将来の臨床試験結果を予測できない可能性があり、制御された環境においてプラセボまたは能動対照を用いて研究を行う場合、われわれは開放ラベル臨床試験を含む。
中枢神経系に対する薬物の研究開発は特に困難であり、これは人々がなぜこのような薬物がいくつかの患者に対して積極的な作用があるのかを予測し理解することは困難であり、他の患者に対してはない。
中枢神経系(CNS)疾患に対する新薬の発見と開発は特に困難と時間があり,多くの他の薬物発見領域に比べてCNS疾患を治療する新薬失敗率が高いことが明らかである。我々の臨床開発におけるどのような挫折も,我々の業務や経営業績に実質的な悪影響を及ぼす可能性がある。さらに、我々の後期臨床試験は、試験中に失明またはプラセボまたは非シビタール効果を維持することが困難である可能性があるため、試験中に適切な比較アームを設計することを含む、十分かつ良好な制御を行う臨床試験に関連する挑戦をもたらす可能性がある。
人間の脳と中枢神経系の複雑さのため、COMP 360を含む1種の薬物を予測し理解することは困難である可能性があり、いくつかの患者に積極的な影響があるかもしれないが、他の患者に積極的な影響がないこと、及びなぜいくつかの人の薬物に対する反応が他の人と異なる可能性がある。たとえば,TRDを有する人群が多く,異種であり,個体は異なる程度のTRDを持つ可能性がある.これらの違いはさらに異なる反応を引き起こす可能性があり,われわれの研究におけるCOMP 360裸蓋キノコ療法の有効性に影響し,緩解期に入る患者のパーセンテージ(あれば)が変動する可能性がある。これらのすべての要素は、私たちの研究におけるCOMP 360ヌードカバーキノコ療法の以前の使用または全体的な治療効果を評価することを困難にするかもしれない。さらに、私たちは、いくつかの疾患や状況に対して、臨床開発においてより多くのまたはユニークな挑戦をもたらす可能性があると決定した。例えば,神経性拒食症に対する薬物開発は不明であり,神経性拒食症の第二段階研究の参加者の募集とスクリーニングに挑戦している。 私たちは私たちの経験から教訓を得て、この高度に脆弱な患者集団の実験負担を軽減するために、私たちの試験案を修正している。これらの修正は,我々の臨床開発を延期し,我々のコストを増加させ,規制機関やIRBsに受け入れられない可能性がある。さらに、このような増加した挑戦や独特な挑戦は、最終的には、これらの条件の下で規制の承認を求め、獲得する能力に影響を及ぼす可能性がある。
われわれはCOMP 360臨床試験に参加した患者の登録状況と任意の未来の候補治療方案に依存する。もし私たちが患者を私たちの臨床試験に参加させることができなければ、私たちの研究開発仕事及び業務、財務状況と運営結果は実質的な不利な影響を受ける可能性がある
患者を確定し、著者らの臨床試験に参加する資格を持たせることは著者らの成功のキーポイントである。患者の入選は多くの要素に依存しています
•試験の主な終点と患者の過程を決定するために必要な患者数を分析した
•既存の薬剤の使用を中止することを望む患者を含む、条件に適合する患者を決定し、募集すること
•臨床方案の設計及び試験の患者資格と排除基準
•これまで検討されてきた候補治療薬の安全性の概要
•制御物質の使用による既知のリスクおよび利点、恥または他の副作用を含む、患者が私たちの試験に参加する意思または獲得可能性;
•患者は任意の公衆衛生危機、例えば新冠肺炎の大流行と新しい新冠肺炎の変種の出現を含む著者らの試験に参加することができる
•私たちが適応を治療する方法が感じるリスクと利点は
•患者と臨床場所の距離
•私たちは適切な能力と経験を持つ臨床試験研究者を募集することができます
•競争的臨床試験の有用性
•臨床試験で調べられている適応が承認された新薬の供給状況
•他の既存療法に対する研究中の薬物の潜在的優位性に対する臨床医および患者の見方は、我々が調査している適応のための任意の新しい療法が承認される可能性がある;および
•私たちは患者のインフォームドコンセントを得て維持する能力を持っている。
一度登録しても、十分な数の患者を残して、私たちのどんな実験もできないかもしれません
さらに、COMP 360または任意の将来の候補療法の臨床試験において報告される可能性のある任意の負の結果は、候補療法の他の臨床試験の募集および維持を困難にするか、または不可能にする可能性がある。COMP 360または任意の未来の候補治療薬への参加を延期する臨床試験は、私たちのコストを増加させ、COMP 360の承認過程を緩和し、私たちの研究用COMP 360ヌードカバーキノコ療法を開始し、収入を創出する能力を遅延または危険にさらす可能性がある。神経性拒食症の第2期臨床試験では,神経性拒食症の第2段階研究の参加者の募集とスクリーニングに挑戦したため,いくつかの遅延に遭遇した。これらの課題に対応するために,この高度に脆弱な患者群の実験負担を軽減するために,われわれの試験案を修正している。これらの提案された案改正があっても,我々の神経性拒食症研究のための参加者募集の挑戦に遭遇する可能性がある。このような挑戦のせいで、私たちはもう私たちが最初に予想したように、2023年にこの実験のデータを得ることはできない。さらに、臨床試験の開始または完了遅延をもたらすいくつかの要因は、最終的には、COMP 360または任意の将来の候補治療薬の規制承認が拒否される可能性もある。
そのほか、臨床試験の適時登録は臨床試験地点に依存し、これらの地点は全世界の衛生問題の不利な影響を受ける可能性があり、その中に流行病を含む。例えば、私たちの臨床試験場所は、現在または未来に新冠肺炎の大流行の影響を受ける地域、あるいは未来に他の大流行の影響を受ける可能性のある地域に位置する可能性がある。例えば、過去には、参加者が限られていたため、患者、セラピスト、あるいは医師が私たちの実験、サプライチェーン中断、規制機関および他の類似機関の遅延に参加できなかったため、私たちの試験の登録人数は不利な影響を受けた。我々の実験の進行は,この影響を軽減しようと努力しているにもかかわらず,将来の公衆衛生危機の悪影響を受け続ける可能性がある。
私たちはこれまで候補療法を商業化したことがなく、必要な専門知識、人員、資源が不足して、私たちの療法を商業化したり、適切な協力者と協力したりすることに成功したかもしれない
現在、販売とマーケティングインフラを組み立てていますが、治療候補薬の販売やマーケティングにおける組織経験は限られています。任意の承認された療法を商業的に成功させるためには、販売およびマーケティング組織を開発または買収し、これらの機能を第三者にアウトソーシングするか、またはパートナー関係を確立しなければならない
もし私たちの研究COMP 360ヌードカバーキノコ療法が商業化販売を許可されれば、私たちは北米とEUの主要な市場で私たち自身の市場参入と商業化能力を確立することを計画している。選定された地域では,契約販売組織やCSOの支援に依存したり,関連する商業化能力を持つ会社と商業化手配を達成したりすることも考えられる.私たち自身の販売とマーケティング能力を確立し、第三者とこれらのサービスを提供する手配を達成することには、リスクがあります。私たちが販売とマーケティング能力を確立しても、治療物質の販売やマーケティングにおける組織経験が限られているので、私たちの療法を効果的に発売したり、効果的に私たちの療法をマーケティングすることができないかもしれません。また、1つの販売チームの採用と訓練は高価で時間がかかり、いかなる治療薬の発売を延期する可能性がある。もしこのような発表が延期されたり、何の理由でも発生しなかった場合、私たちはこれらの商業化費用を早期または不必要に発生させ、私たちの販売とマーケティング担当者を維持または再配置できなければ、私たちの投資は損失します。私たちの治療法の商業化を阻害するかもしれません
•COMP 360ヌードキノコ療法の需要を満たすのに十分な数のセラピストを訓練することはできません
•私たちのセラピストは私たちの訓練とCOMP 360裸蓋キノコ素治療研究ガイドラインに従って彼らの役割を果たすことができます
•私たちは効果的な市場参入とビジネスマンを募集し、訓練し、維持することができない
•事業者は十分な数の医師に触れることができないし、未来の治療法のメリットを出すことができず、彼らを教育する
•私たちの治療ニーズを満たすのに十分な数の治療センターを第三者の治療場所に見つけることはできません
•私たちのビジネススタッフは提供可能な補充療法が不足しており、より広い治療ラインを持つ会社と比較して競争的に不利になる可能性がある
•独立した市場アクセスおよび商業組織の構築に関連する予測不可能なコストおよび費用;
•市場参入と商業化の費用は私たちが予想していた費用より高い
もし私たちが第三者と合意し、任意の承認された療法に市場参入および商業サービスを提供すれば、これらの収入が私たちにもたらす収入や収益力は、私たちが自分たちが開発した任意の治療法を商業化する場合よりも低いかもしれない。このような協力配置は、任意の承認された療法の商業化を私たちの制御されないようにすることができ、私たちのパートナーが私たちの治療に投入するリソースの数または時間を制御できないかもしれないこと、または私たちの協力者がその義務を履行する意志または能力を含む多くのリスクに直面する可能性があり、私たちの手配の下での義務は、業務合併または私たちの協力者のビジネス戦略の重大な変化の悪影響を受ける可能性がある。私たちは第三者と私たちの療法を商業化することに成功できないかもしれないし、私たちに有利な条項ではできないかもしれません。受け入れ可能な第三者は、私たちの治療法を効果的に商業化するために必要な資源および注意を投入することができない可能性があり、第三者治療サイトに十分な数の治療センターを構築するか、または私たちの療法を管理するのに十分な数のセラピストを募集、訓練、および保持することができる。また,デジタル技術を用いて患者体験やわれわれの治療結果を改善する方法を模索している。商業化パートナーは我々のデジタル技術を普及させる原動力に欠けている可能性があり,このような第三者による第三者治療サイトで我々のデジタル技術を実施することは困難に直面する可能性がある
もし私たちがビジネス能力を構築することに成功できなければ、私たち自身も第三者と協力しても、私たちの療法を商業化することに成功できないかもしれません。これは逆に、私たちの業務、将来性、財務状況、および運営結果に実質的な悪影響を及ぼすでしょう
著者らの研究中のCOMP 360ヌードカバーキノコ療法或いは任意の未来の候補療法の将来の商業成功は医療保健専門家、患者、医療保健支払者、医療技術評価機構と医学界全体の著者らの潜在療法に対する市場参入と受け入れ程度に依存する
私たちは商業的に成功した治療法を決して持っていないかもしれない。今まで、私たちはまだ発売された治療法を許可していない。著者らが研究しているCOMP 360ヌードカバーキノコ療法は更なる臨床調査、監督審査、重大な市場参入とマーケティング努力及び大量の投資が必要であり、いかなる収入を産生することができる。また,承認されれば,われわれの療法は支払者,衛生技術評価機関,医療専門家,患者,医学界全体の十分な受容度を得ることができず,利益を得ることができない可能性がある。私たちが最終的に実現した受容度は、大衆の否定的な見方や歴史メディアが幻覚物質(裸蓋キノコ素を含む)の報道に影響を受ける可能性がある。この歴史のため、教育医学界、第三者支払人と健康技術評価機構は著者らの研究COMP 360ヌードカバーキノコ療法のメリットは大量の資源を必要とする可能性があり、しかも永遠に成功しないかもしれないことを理解し、これは私たちが相当な収入を産生することを阻止し、或いは利益を実現することを阻止する
医療専門家、患者、医療支払者、医療技術評価機関の将来の治療法に対する市場受容度は多くの要素に依存し、その中の多くの要素は私たちがコントロールできないが、以下の要素を含むが、これらに限定されない
•医療専門家、患者、医療支払者が各治療法を受けることは安全で、有効で、費用効果がある
•任意の候補治療レジメンに対する目標適応の看護基準を変更する
•実力のある販売、マーケティング、流通支援
•潜在的な製品責任クレーム
•代替療法と比較して、候補療法は相対的に便利で、使いやすい、使いやすい、他の感知可能な利点である
•有害事象や宣伝の流行率と深刻さ
•治療特徴の概要、患者情報チラシ、包装ラベル、または使用説明に列挙された制限、予防措置または警告;
•代替療法と比較して私たちの治療費は
•COMP 360は、制御物質と、その制御された物質状態に基づく既知のリスクとを考慮して、処方および調剤者が取らなければならないステップを含む
•十分な量と生産量で私たちの製品を生産することができます
•医療支払者の保険および補償の利用可能性および金額、および医療支払者が保証または適切な補償を受けることなく、患者が自腹を切る意思;
•対象患者群がこのような療法を試みる意思と,医療専門家が処方する意思
•裸蓋キノコを使用することに関連する娯楽または専門的な使用または乱用に関連する負の宣伝、または裸蓋キノコの使用によって生じる不良な結果または副作用に関連する負の宣伝、例えば、オレゴン州許可の裸蓋キノコサービスセンターの州許可の促進者の監視の下で裸蓋キノコを使用する不利な宣伝を含む、任意の潜在的な不利な宣伝;
•REMSを含む、私たちが研究しているCOMP 360ヌードカバーキノコ療法または任意の将来の候補療法の使用、販売、または流通の任意の制限;
•治療を病院や管理看護機関の処方に入れて精算することがどの程度承認されているか
•私たちの治療法は医者の治療ガイドラインに基づいても、精算ガイドラインによって一線、二線、三線あるいは最後の一線治療に指定されています。
もし私たちの研究COMP 360ヌードカバーキノコ療法または任意の未来の候補療法が市場参入および受け入れを得ることができなかった場合、これは、満足できる投資リターンを提供するための収入を創出する能力に重大な悪影響を及ぼす。いくつかの治療法が市場アクセスと受け入れを得ても、市場はまだ十分ではなく、私たちに相当な収入を与えるのに十分ではないことが証明されているかもしれない
我々の業務および商業化戦略は、COMP 360ヌードカバーキノコ治療を実施するために、当社の識別、同定、準備、認証、および第三者治療サイトをサポートする能力に依存する。もし私たちがこれができなければ、私たちの商業化の見通しは制限され、私たちの業務、財務状況、そして運営結果は損なわれるだろう。
もし私たちの研究におけるCOMP 360ヌードカバーキノコ療法または将来の療法を商業化することができれば、私たちの成功は、私たちの治療法の第三者治療サイトを識別、同定、準備、認証、支援し、管理する能力にかかっている。COMP 360ヌードカバーキノコ治療を提供するビジネスモデルはまた、COMP 360ヌードカバーキノコ投与会議の前、期間、および後に、第三者治療サイトのうちの1つで主催される第三者治療師に関するものである。我々は,合格した第三者治療サイトと密接な関係を築くことにより,我々の研究におけるCOMP 360ヌードカバーキノコ療法と任意の将来の候補療法を商業化する予定であり,これらのセラピストはこれらのサイト上で我々の研究におけるCOMP 360裸蓋キノコ療法を実施する。われわれのCOMP 360ヌードカバーキノコ療法はREMS計画に拘束されることが予想され,われわれの治療計画を厳格に遵守することに同意した第三者サイトやサプライヤーとのみ協力する予定であるため,我々の研究におけるCOMP 360ヌードカバーキノコ療法を実施するために利用可能なサイト数の制限に直面している可能性がある。どのような制限も、いくつかの潜在的な患者が私たちの研究におけるCOMP 360ヌードカバーキノコ療法を使用できないか、または使用できない可能性があり、承認されれば、これは私たちの潜在的な患者の全体的な規模を制限し、私たちの将来の手術結果を損なう可能性がある。われわれはこのような第三者治療サイトを研修·認証する卓越したセンターを開発し,われわれの治療案をさらに検討し改善していく予定であるが,これは大量のコスト,時間,資源に関連しており,われわれの努力は成功しない可能性が予想される。
ヌードゲラミン治療サービスを提供するために必要な適用基準(地域、国、州、または他の適用基準を含む)に基づいて、そのような第三者治療サイトが必要とする可能性のある認証を含む十分な第三者治療サイトネットワークを確立することができない場合、私たちの業務および成長能力に大きな悪影響を与え、私たちの運営および商業化努力に悪影響を及ぼすであろう。私たちはセラピストが第三者治療サイトに雇われ、そこでセラピストが私たちの治療を管理してほしい。様々な理由で、第三者治療サイトは、私たちの治療のためにより高い費用を支払うことを要求するか、または私たちの治療を販売することによって得られる彼らの収入を増加させることを要求する可能性があり、これは、支払人および私たちの患者が私たちの治療を得るコストをより高くする可能性がある。例えば、法制度は、より高いレベルの許可を有する可能性があり、これは、より高い料金率を要求する裸蓋キノコ治療サービスを提供する第三者治療サイトと契約することを可能にする。さらに、第三者治療サイトは規制や認証要件を満たすことが困難かもしれない。
我々の治療の新規性を考慮して、第三者治療サイトは、米国でREMS計画を遵守するか、またはヨーロッパでリスク管理計画またはRMPを遵守することを含む任意の承認された治療を提供するために、追加の財務的および行政的負担に直面する可能性がある。第三者治療サイトがREMS計画に従って証明書を取得する過程は非常に高価で時間がかかる可能性があり、これは第三者治療サイトが私たちの治療能力を提供することを延期し、私たちの商業化プロセスに重大な悪影響を与える可能性がある。さらに、第三者治療サイトは、十分な視聴覚装置、補助装置、および十分な治療室などの我々のCOMP 360ヌードカバーキノコ研究療法を提供するために、必要なインフラおよび装置を有することを確実にする必要がある。これは第三者治療サイトが私たちの治療案候補を提供することを阻止し、ネットワークを拡大し、収入を創出する能力を低下させるかもしれない。そうでなければ、私たちが第三者治療サイトの発展および満足な関係を維持する能力は、私たちの運営とは無関係な他の要素の負の影響を受ける可能性があり、場合によっては、ヌードカバーの治療使用に対する否定的な見方、Medicareおよび/またはMedicaidまたは商業支払者の清算レベルの変化、ならびに医療保健提供者が直面する他の圧力、ならびに病院、医師団体と提供者との間の統合活動など、私たちが直接または間接的に制御する要素でもない。精算レベルは、第三者治療サイトが私たちの研究COMP 360ヌードカバーキノコ療法を提供する費用を支払うのに十分ではないかもしれません。サードパーティ治療サイトとの新しい費用効果のある契約を維持または獲得できなかったことは、第三者治療サイトネットワーク、患者基盤、私たちの患者、および私たちのより高いコストを失うか、または発展させることができない可能性があります, ヘルスケアプロバイダーのネットワーク中断および/または規制または認証要件を満たすことが困難であり、いずれも、私たちの業務、財務状態、および運営結果に重大な悪影響を及ぼす可能性がある。
われわれは現在,第三者臨床試験現場で働く適格な治療士がわれわれの臨床試験でわれわれの研究用COMP 360裸蓋キノコ療法を管理しており,COMP 360あるいは任意の将来の候補治療薬が承認された後,この治療が継続されることが予想される。第三者サイトが十分な数のセラピストを募集し、維持することができない場合、または彼らのセラピストを効果的に管理することができなければ、私たちの業務、財務状況、および運営結果は実質的な損害を受けることになる。
著者らは現在、第三者臨床試験現場で働く合格した第三者療法士を通じて、著者らの臨床試験において著者らの研究COMP 360裸蓋キノコ療法を管理している。しかし、現在、私たちの研究COMP 360ヌードカバーキノコ治療のビジネス規模を行うのに十分な訓練されたセラピストはなく、私たちの計画の卓越したセンターを通じて成功しないかもしれないことを含め、セラピストの訓練と認証計画の努力を促進している。
現在はセラピストに研修を提供し、将来的にトレーニング(直接または第三者提供者を通じて間接的に提供)を提供することが予想されていますが、現在は患者に治療を提供するセラピストを雇っておらず、将来もそうするつもりはありません。このようなセラピストは通常第三者治療サイトに雇われています私たちの研究におけるCOMP 360ヌードカバーキノコ療法または任意の未来の候補療法が商業的に承認された場合、第三者治療サイトは、私たちの研究におけるCOMP 360ヌードキノコ療法または任意の未来の候補療法を管理するために、合格した治療師チームを募集し、保持するために、大量の財源を提供する必要があるかもしれない。第三者治療サイトが十分な数の治療士を募集、訓練、維持できなかった場合、または競合他社が同様の製品を開発し、セラピストを使用せずに有効であった場合、私たちの治療を提供し、管理する能力は大きく損なわれ、逆に私たちの治療の市場受入率を低下させたり、業務を増加させる能力を制限したりする可能性がある。このような状況が発生すれば、私たちの商業化の見通しは負の影響を受け、私たちの業務、財務状況、運営結果は損なわれるだろう。
私たちは現在トレーニングを提供し、セラピストにトレーニング(直接または第三者プロバイダを介して)を提供し続けることを望んでいるが、私たちは通常、合格および認証された第三者治療サイトに依存してセラピストを管理し、私たちの治療の管理を監視し、私たちの治療管理プロセスが私たちの既定の合意に適合することを保証する。しかし,適切な管理や監督がなければ,セラピストは我々の指導方針に従わないか,裸蓋キノコ投与中に患者を虐待するか,我々の訓練案から外れてしまう可能性がある。セラピストはまた,不正な裸蓋キノコ化合物を使用した患者に対して“地下”診療所で不正な治療を行う可能性がある。このような不法活動は患者を危険にさらし、潜在的な責任、訴訟、監督管理手続きと名声損害に直面させる。このような状況が発生すれば、私たちの商業化プロセスは深刻な挫折に直面する可能性があり、私たちの財務状況と運営結果は深刻な損害を受けるだろう。
我々のCOMP 360ヌードゲラニン療法または他の候補療法の商業化は、医師サービスを提供するために、付属専門実体(私たちはこれらの実体を持っていない)との関係に依存し、これらの関係が中断されれば、私たちの業務は悪影響を受けるであろう。
アメリカのある司法管轄区の州当局は、関連プロバイダと英才センターとの契約関係が、企業が医薬や他の健康職業に従事することを禁止する法律に違反していることを発見するかもしれない。これらの法律は、一般に、業界外の人々または実体が医学および何らかの他の健康職業に従事することを禁止し、許可されていない個人または実体が妨害または不適切な影響を防止することを目的としている
臨床医や他の衛生保健従事者の専門的な判断。会社の業務制限を受ける職業及び各司法管轄区は特定の行動或いは契約関係が専門判断に対する不当な影響を構成すると考える程度は司法管轄区によって異なり、州医薬委員会とその他の衛生職業と法執行機関などの変化と絶えず変化する解釈を受ける可能性がある。したがって、私たちは私たちが経営し続けている各管轄区域で私たちの法律の遵守状況を監視しなければなりません。その後の会社の実践法律の解釈が私たちの業務運営をさらに制限しない保証はありません。州企業勤務制限は,企業の業務違反行為に協力する健康専門家を処罰することも多く,臨床医や他の免許を有する専門家の我々の提供者ネットワークや卓越センターへの参加を阻害する可能性がある。臨床医を私たちのネットワークに参加させるいかなる困難も、私たちが治療を提供する能力を弱める可能性があり、私たちの業務に実質的な悪影響を与える可能性がある。
米国の少なくとも42州では、会社の実践制限は何らかの形で存在し、法規、法規、専門委員会あるいは司法長官指導でも、判例法であっても、この原則の適用と実行においては、司法管轄区域間に広範な差があるにもかかわらず、正確な計数を確立することは困難である。医療に対する企業勤務制限が一般的に存在するため,卓越センターが提供する提供者サービスや他のサービスとは様々な合意(例えばサービス協定)を介して雇用提供者ではなく契約を締結している。私たちはこのような関係が続くと予想しているが、私たちはそれらが続くことを保証できない。私たちは州企業の実践医学理論を守るための手配は、連邦と州監督機関の連邦と州詐欺と法律の濫用に関する追加審査を受けるかもしれない。また、私たちと提供者との関係の実質的な変化は、実体間の紛争、政府法規の変化によっても、これらの関連を失っても、私たちが治療を提供する能力を弱める可能性があり、私たちの業務、財務状況、運営結果に大きな悪影響を及ぼす可能性がある。
治療候補薬物の製造または処方を変更する方法は、追加のコストまたは遅延をもたらす可能性がある。
候補治療薬は臨床前研究から後期臨床試験まで開発され、承認と商業化される可能性があるため、開発計画の様々な面、例えば製造方法や調合は、過程と結果の最適化に努力するために、過程中に変更される可能性がある。これらのいずれの変化も、我々が研究しているCOMP 360ヌードカバーキノコ療法または任意の将来の候補療法の表現が異なり、計画中の臨床試験またはプロセスを変えて製造された材料を用いた他の将来の臨床試験の結果に影響を与える可能性がある。このような変化はまた、追加のテスト、FDA通知、またはFDA承認を必要とする可能性がある。これは臨床試験の完成を遅らせる可能性があり、移行臨床試験或いは1つ以上の臨床試験を繰り返し、臨床試験コストを増加させ、COMP 360或いは任意の未来の候補治療薬の承認を延期し、そして著者らの製品販売と収入を創造する能力を脅かす必要がある。
COMP 360または任意の将来の候補療法に対するFDAの画期的な治療指定は、より速い開発または規制審査または承認プロセスをもたらすことができない可能性があり、我々の研究におけるCOMP 360ヌードカバーキノコ療法または任意の将来の候補療法が市販される可能性を増加させることはない。
TRDを治療するためのCOMP 360の画期的な治療指定が得られ、将来の候補治療レジメンのために指定が求められる可能性がある。画期的な治療法は、1つまたは複数の他の薬剤と単独でまたは1つまたは複数の他の薬剤と組み合わせて重篤または生命を脅かす疾患または状態を治療することを意図した薬剤として定義され、初歩的な臨床証拠は、1つまたは複数の臨床的に重要な終点において、臨床開発早期に観察される実質的な治療効果のような既存の療法よりも有意な改善を示す可能性があることを示す。画期的な治療法として指定された薬物に対して,FDAと試験スポンサーとの相互作用やコミュニケーションは,臨床開発の最も有効な経路を決定するのに役立つとともに,無効対照案中の患者数を最小限にすることができる。FDAで画期的な治療法に指定されている薬物も加速承認を得る資格がある
画期的療法に指定されたのはFDAの裁量権である。したがって,将来の候補療法が画期的療法として指定された基準に適合していると考えても,FDAは同意せず,このような指定をしないことにする可能性がある。いずれの場合も、COMP 360および任意の将来の候補治療薬に対する画期的な治療指定を受けることは、非迅速FDA審査手順に従って承認を考慮する薬剤と比較して、より速い開発プロセス、審査または承認をもたらすことはなく、FDAの最終承認を保証することもできないかもしれない。また,COMP 360が画期的療法として指定されていても,FDAは後でそれまたは将来FDAによって画期的療法として指定された候補療法が資格条件を満たしていないことを決定する可能性がある
FDAが高速車線の称号を付与した場合、実際にはより速い開発や規制審査または承認過程をもたらさない可能性がある
私たちは私たちの任意の候補治療のための迅速な通路指定を求めるかもしれない。重症または生命に危険な疾患の治療に使用される薬剤が使用され、そのような疾患が満たされていない医療ニーズを解決する可能性を示す場合、薬物スポンサーは、迅速なチャネル指定を申請することができる。FDAは広範な裁量権を有しており,この称号が付与されているかどうかであるため,ある特定の治療薬候補がその称号を獲得する資格があると考えても,FDAがその称号を付与することを決定することは保証されない。将来の候補治療の迅速なチャネル指定を得ても,非加速FDA審査プログラムと比較して,より速い開発過程,審査,承認を経験しない可能性がある。また,FDAが我々の臨床開発計画のデータがFast Track指定を得た治療候補薬を支持しなくなったと考えた場合,その指定を取り消す可能性がある
私たちは、より多くの候補治療または研究計画を発見、開発、および/または商業化するために、将来的に協力することができる。このような協力は、商業的に実行可能な治療候補薬の開発や重大な将来の収入をもたらすことができないか、あるいは利益の関係に入ることができないかもしれない。
私たちは、将来の候補治療または研究計画を発見、開発および/または商業化するために、製薬会社または他の会社と協力するかもしれない。例えば、フィラデルフィア科学大学(2022年にセントジョセフ大学に合併)やUSciencesと賛助研究協定を締結し、カリフォルニア大学サンディエゴ校、カリフォルニア大学医学部(カリフォルニア州)、ウィスコンシン州医学院(ウィスコンシン州)の学術実験室、MiHKAL GmbH(スイス)最高経営責任者Matthias Grill博士との協力により、発見センターを設立した。もし私たちが合理的な条件で協力を維持したり、協力を維持することができなければ、将来の候補治療や研究計画を発見し開発する能力は延期されたり、より高価になる可能性がある。未来のどんな協力も私たちを以下のリスクを含む多くのリスクに直面させるかもしれない
•私たちのパートナーが将来の研究計画や候補治療プロジェクトに投入する資源の数と時間をコントロールすることはできません
•協力協定の場合、もし私たちが定義されたマイルストーン事件によって開発費用の完全または一部を援助することができれば、候補治療が規制の承認や商業的成功を得られなかった場合、私たちはこれらの投資のコストを決して回収しないかもしれない
•独立した検証を必要とすることなく、第三者から受信された研究計画および候補治療計画に関する情報およびデータに依存する可能性がある
•第三者がその研究計画および候補治療レジメンに関するデータを収集および合成するプロセスを制御することができない可能性があり、そのようなデータの品質および完全性に関する正式または適切な保証がない可能性がある
•私たちは第三者パートナーに借りがあるマイルストーン、特許使用料、または他の支払いを満たすのに十分な資金がないかもしれない
•私たちの協力協定には、私たちの業務運営および私たちが追求する可能性のある治療候補および/または適応を制限する競業禁止条項が含まれている可能性があります
•パートナーは、単独で、または他の人(私たちの1つまたは複数の競争相手を含む)と協力して、候補治療薬を開発または商業化することができる
•私たちのパートナーが私たちのパートナーに基づいてその義務を履行する意志または能力は、業務合併またはパートナー戦略の重大な変化の悪影響を受ける可能性があります
•私たちのパートナーは、私たちの将来の候補治療や研究プロジェクトの発見と開発の遅延やコスト増加に遭遇するかもしれません
•私たちは、特許権、主要候補治療薬の選択、契約解釈または第一選択開発プロセスの相違を含むパートナーとの相違がある可能性があり、これらの分岐は、候補治療薬の研究、開発または商業化の遅延または終了をもたらす可能性があり、候補治療薬に対して追加的な責任を負うこと、または訴訟または仲裁を引き起こす可能性があり、いずれも時間的で高価である可能性がある
•私たちのパートナーは知的財産権を適切に取得、維持、保護、または実行できないかもしれない;
•私たちのパートナーは第三者の知的財産権を侵害、流用、または他の方法で侵害する可能性があり、これは私たちを訴訟と潜在的な責任に直面させるかもしれない。
適切なパートナーを探すことで、私たちは激しい競争に直面するかもしれない。我々がパートナーシップについて最終的な合意を達成できるかどうかは,他に加えて,潜在協力者の資源や専門知識の評価,パートナーシップの条項や条件の提案,潜在協力者のいくつかの要因の評価に依存する.提案、交渉、協力、許可手配、合弁企業、戦略連合、またはパートナーシップの実施は長く複雑な過程である可能性がある。このような活動における私たちの機関知識や経験は限られており、私たちはこのような取引や手配の予想される利点を達成できないかもしれない。
上記のいずれのリスクも現実になれば、私たちが行っているいかなる協力も、商業的に実行可能な治療候補薬を開発したり、将来の収入を生み出すことができない可能性があり、これは私たちの業務に実質的な悪影響を及ぼす可能性がある。
私たちの業務戦略には発展の卓越した中心が含まれており、これは過去と未来に巨大なコスト、時間、資源に関連するだろう。もし私たちの努力が成功しなければ、私たちの業務、見通し、そして財政状況は不利な影響を受けるだろう。
私たちの業務戦略の重要な要素の一つは肝心な市場に研究機構と革新実験室を設立することであり、私たちは卓越中心と呼ばれている。2021年1月,メリーランド州ボルチモアのシェパード·プラット高度診断·治療研究所との協力を発表し,我々の最初の卓越したセンターを設立した。2022年3月、著者らはロンドンと南ロンドン国王学院及びモデズリーNHS基金会信託基金(Maudsley NHS Foundation Trust、SLAMと略称する)と戦略協力を達成し、精神健康研究と革新センターを創立することを発表し、全体目標は仕事モード幻覚治療診療所、治療士訓練計画の開発、臨床試験とデータ分析などを行うことを通じて、幻覚療法の研究を推進することを通じて、患者が精神衛生保健根拠に基づく革新の機会を獲得することを加速することである
著者らはこれらの卓越したセンターを利用して証拠を収集し、著者らの治療モードを最適化し、治療士を訓練と認証し、概念検証研究を含み、デジタル技術解決方案を開発とテストして患者の体験と結果を改善し、そして他の活動を展開して、私たちが安全かつ経済的かつ効率的にCOMP 360ヌードカバーキノコ治療を提供する方法を完備するつもりである。これらの卓越したセンターを設計、建設、配備するために努力したり、適切な第三者を探してこれらのセンターを開設したりすることは、設備の購入と開発や他の資源の潜在的な資本支出を含む多くの時間とコストに関連し、私たちの業務戦略を実行する他の重要な要素に集中しないように、私たちの管理チームの注意をそらすことができる。もし私たちが第三者と合意を締結したり、これらの卓越したセンターを合理的な条項で開発·運営できなかったり、全くなければ、私たちが将来の研究計画や候補療法を開発する能力は延期される可能性があり、私たちの療法のビジネス潜在力は変わる可能性があり、私たちの開発と商業化コストは増加するかもしれない。もし私たちがこれらの卓越したセンターを発展させる努力が成功しなければ、私たちの業務、将来の見通し、財務状況に実質的な悪影響を及ぼすだろう。
私たちは高価で破壊的な責任クレームに直面する可能性があります。私たちの研究COMP 360ヌードカバーキノコ療法をテストする時も、臨床または商業段階で任意の未来の候補療法をテストする場合も、私たちの製品責任保険は、このようなクレームのすべての損害をカバーしないかもしれません
私たちは潜在的な製品責任と専門賠償リスクに直面しており、これらのリスクは治療物質の研究、開発、製造、マーケティング、使用に固有のものである。現在、私たちはまだ商業販売のための治療法を承認されていません;しかし、私たちと私たちの会社の協力者は、臨床試験で現在と未来に私たちの研究で使用されているCOMP 360ヌードカバー療法または任意の未来の候補療法、および将来承認された治療法を販売する可能性があり、私たちを責任クレームに直面させる可能性があります。これらのクレームは、臨床試験において我々の研究COMP 360ヌードゲラニン療法を受けた患者によって提出される可能性があり、規制部門の承認を得た場合、処方に従ってこの療法を受けた患者、医療提供者、製薬会社、当社の協力者、またはCOMP 360ヌードゲラクチン療法を販売する他の第三者、または任意の将来の候補治療案である可能性がある。私たちのいかなるクレームに対しても、その是非曲直にかかわらず、弁護が困難でコストが高い可能性があり、COMP 360ヌードカバーキノコ療法または任意の未来の候補治療薬の市場またはCOMP 360ヌードシスチン療法または任意の未来の候補治療薬の商業化の将来性を研究するために重大な悪影響を及ぼす可能性がある。臨床試験過程は潜在的な副作用を識別と評価することを目的としているが、監督部門の許可後であっても、薬物は常に予測できない副作用を示す可能性がある。COMP 360または任意の将来の候補治療薬が臨床試験中または監督部門の承認後に副作用を引き起こす場合、私たちは重大な責任を負う可能性がある。医師および患者は、既知の潜在的副作用を決定し、どの患者がCOMP 360または任意の未来の候補治療を使用すべきでないかを説明する警告を遵守しない可能性がある。是非曲直や最終結果にかかわらず、責任クレームは, 他の事項以外にも、以下のことが含まれる
•公衆の否定的な見方のせいで私たちの治療への需要は減少しました
•私たちの名声を損なう
•臨床試験参加者は脱退したり、新しい試験参加者を募集することが困難である
•規制当局が調査を開始しました
•関連訴訟の弁護や和解の費用
•経営陣の時間と資源を移転する
•実験参加者や患者に多額の報酬を与え
•リコール、撤回またはラベル付け、マーケティング、または販売促進制限;
•販売収入の損失を治療し
•承認されれば,われわれの研究におけるCOMP 360裸蓋キノコ療法や任意の将来の候補療法は商業化できない。
私たちの負債は私たちの保険範囲を超える可能性がある。もし我々の研究COMP 360ヌードカバーキノコ療法や任意の将来の候補療法が市場に承認されれば,我々の保険カバー範囲を拡大し,商業療法の販売を含める予定である。しかし、私たちは合理的なコストで保険範囲を維持できないかもしれないし、起こりうるいかなる責任にも対応するのに十分な保険範囲を得ることができないかもしれない。もし成功した製品責任クレームまたは私たちの未保険負債または保険負債を超える一連のクレームがあれば、私たちの資産はこのようなクレームを支払うのに十分ではないかもしれません。私たちの業務、財務状況、および運営結果は重大な悪影響を受ける可能性があります
上記のいずれの事件による責任クレームも、当社の業務、財務状況、運営結果に重大な悪影響を及ぼす可能性があります
コンプライアンスに関するリスク
裸蓋キノコおよび裸蓋キノコは、米国CSAによって付表I規制物質として指定されているが、他の国の類似した規制物質法、およびこれらの法律および法規を遵守するための私たちの任意の重大な違反、または法律および法規の変更は、私たちの開発活動または業務の連続性中断を招く可能性がある
裸蓋キノコと裸蓋キノコはCSAにより付表I制御物質に分類され,イギリスの2001年の薬物乱用条例により表1薬物に分類され,多くの国で外国政府と類似して分類されている。COMP 360または将来的に裸蓋キノコまたは裸蓋キノコを含む任意の候補治療薬が、それらの商業マーケティングを可能にするために規制機関の承認および配置を得ると仮定しても、これらの治療候補薬剤中の成分は依然として別表I、または国または外国同等の薬剤である可能性がある。任意の連邦、州、または外国の法律および法規に違反することは、連邦政府または一般市民が提起した民事訴訟によって生じる巨額の罰金、処罰、行政制裁、有罪または和解、または利益返還、業務活動の停止、資産剥離または監禁を含むが、これらに限定されない刑事告発および処罰をもたらす可能性がある。これは私たちの名声と業務を展開する能力、私たちの財務状況、経営業績、収益力、あるいは流動性、あるいは私たちの上場アメリカ預託証明書の市場価格を含む、私たちに重大な悪影響を及ぼすかもしれない。さらに、必要な時間および資源は、関係当局が要求する任意の情報の性質および程度にある程度依存する可能性があり、このような時間または資源は、大量である可能性があるので、任意のそのような事項を調査したり、弁護したり、私たちの最終的な解決に要する時間または資源を推定することは困難である。このような活動に協力したり,そそのかしたり,このような活動に加担したりしようとしたりすることも不法である.投資家がこのような活動に参加または参加することは、そのすべての投資、罰金、および/または監禁を含むが、これらに限定されない連邦民事および/または刑事起訴をもたらす可能性がある。
他の連邦、州、省、地方の法律は、私たちが経営しているか、現在計画経営している司法管轄区での業務と、私たちがそれに輸出するか、あるいは現在私たちの製品を輸出することを計画している司法管轄区、健康と安全、私たちの運営行為、そして私たちの製品の生産、貯蔵、販売、流通に関する法律を含む。このような法律を遵守することは、私たちが複雑な連邦、州、省、および/または地方法律を同時に遵守することを要求する。このような法律はしばしば変化し、解釈して適用することが難しいかもしれない。私たちがこのような法律を遵守することを確実にするために、私たちは多くの財政と管理資源を投入しなければならない。これらの法律の代価や彼らが私たちに与える可能性を予測することはできません
未来の行動。このような法律を守らないことは私たちの業務に否定的な影響を与え、私たちの名声を損なうかもしれない。これらの法律の変化は、私たちの競争地位と私たちが経営する市場にマイナスの影響を与える可能性があり、私たちが経営する司法管轄区の各政府が私たちの業務に悪影響を与えない立法や法規を通過しないことを保証することはできません
さらに、私たちまたは第三者の活動が米国州や地方の法律または私たちが活動している他の国や地域の法律に適合していても、潜在的な法執行手続きは、主要幹部の注意をそらしながら、私たちまたは第三者に重大な制限を加えることにつながる可能性がある。このような訴訟は、このような訴訟の結果が私たちに有利であっても、私たちの業務、収入、運営結果および財務状況、および私たちの名声と将来性に実質的な悪影響を及ぼす可能性がある。極端な場合、このような訴訟は、最終的には、私たちの主要幹部に刑事訴訟を起こし、会社の資産を没収し、業務運営を継続できなくなる可能性があります。州と現地の裸蓋キノコと裸蓋キノコに関する法律を厳格に遵守することは、アメリカ連邦法律、EU法律、またはイギリス法律によって負う可能性のある責任を免除することはできず、私たちに提起される可能性のあるいかなる訴訟を弁護することもできない。私たちに提起されたどんな訴訟も私たちの運営と財政的業績に悪影響を及ぼすかもしれない。
裸蓋キノコと裸蓋キノコは現在アメリカで表I規制物質として指定されているが、アメリカのある都市或いは州の法律により、裸蓋キノコ或いは裸蓋キノコの地位は変化する可能性がある。例えば,デンバー市は2019年の投票で裸蓋キノコ保有を合法化することを決定し,オレゴン州では2020年11月に第109号措置を採択し,合法医療に魔力キノコを含む“裸蓋キノコ製品”を使用するための道を敷き,免許のある促進者の監督の下,免許のある施設で精神健康疾患を治療している。オレゴン州裸蓋キノコ素サービスセンターが開業し,免許を持つ促進員が2023年1月から21歳以上の成人にヌードゲラリンサービスを提供している。2022年11月、コロラド州の有権者は、州政府許可の促進者の監督の下、州規制の中心で裸蓋キノコと裸蓋キノコを使用することを可能にする投票措置を採択した。一部の都市では、ワシントンD.C.(2020年11月)、マサチューセッツ州サマービル(2021年1月)、マサチューセッツ州ケンブリッジ市(2021年2月)、マサチューセッツ州ノース·アンプトン(2021年4月)、ワシントン州シアトル(2022年2月)、カリフォルニア州サンフランシスコ(2022年9月)など、裸ゲキノコの法執行行動を合法化または最小化する措置も採択されている。規制監督や最低限の規制なしに裸蓋キノコを合法化することは、診療所の設置に適切な治療インフラや十分な臨床研究がない可能性があり、これは患者をリスクに直面させ、業界全体に名声と規制リスクをもたらす可能性があり、私たちは監督許可を得ることを更に難しくする。また、裸蓋キノコの合法化は、規制部門の承認を得たら、参入のハードルを下げ、競争を増加させる可能性があるため、私たちの商業販売にも影響を及ぼす可能性がある。
私たちは反腐敗法、そして輸出規制法、税関法、規制法、その他私たちの業務を管理する法律を守らなければならない。これらの法律を遵守しなければ、民事または刑事罰、他の救済措置および法的費用を受ける可能性があり、COMP 360の生産および我々の研究用COMP 360ヌードカバーキノコ療法または将来の米国以外の任意の候補療法の開発および販売が禁止されるか、または費用の高いコンプライアンス計画の開発と実施が要求される可能性があり、これは私たちの業務、運営結果、および財務状況に悪影響を及ぼす可能性がある。
我々の業務は、イギリスの“2010年収賄法”、米国の“海外腐敗防止法”または“海外腐敗防止法”、および私たちが業務を展開し、将来業務を展開する可能性のある国/地域に適用される他の反腐敗法律を含む反腐敗法律によって拘束されている。収賄法、海外腐敗防止法、およびその他の法律は、一般に、業務を獲得または保留し、またはいくつかの他の商業的利益を得るために、私たち、私たちの職員、および中間者が政府官僚または他の人に贈賄、贈賄され、または他の他の禁止された金を他人に支払うことを禁止している。
反収賄法、“海外腐敗防止法”および他の法律は、一般に、関連する機能または活動を不正に履行させるために、政府関係者または他の人々に財政または他の利益を提供、提供または提供するために、私たち、私たちの従業員および仲介機関が直接的または間接的に許可、承諾、提供または提供することを禁止している(またはそのような行為のために彼らを奨励する)。
反収賄法によると、私たちはまた、私たちと関連のある人が賄賂犯罪を犯すことを阻止できなかったために責任を負う可能性がある。私たちは、私たちを代表する人や私たちのビジネスパートナーと共に、“収賄法”や“海外腐敗防止法”に違反する可能性のある多くの司法管轄区で業務を展開しており、私たちは第三者との協力や関係に参加しており、これらの第三者の腐敗や不法活動は、このような活動を明確に許可していなくても、“収賄法”、“海外腐敗防止法”または現地反腐敗法に基づいて責任を負う可能性がある。また、将来の規制要求の性質、範囲、影響を予測することはできず、私たちの国際業務はこれらの要求によって制約される可能性があり、現行の法律が管理または解釈される可能性がある方式を予測することもできない
“反海外腐敗法”を遵守することは特に高価で困難であり、特に腐敗は公認問題である国である。また、海外腐敗防止法は製薬業に特別な挑戦をもたらしており、多くの国では病院が政府によって運営されているため、医師や他の病院従業員は外国人官僚とされている。臨床試験やその他の仕事に関連して病院に支払われた何らかの金は、政府関係者に支払われた不正金と考えられ、“海外腐敗防止法”の法執行行動につながった。
私たちは将来的に“収賄法”や“海外腐敗防止法”に違反する可能性のある高リスク司法管轄区域で業務を展開する可能性があり、私たちは第三者との協力や関係に参加する可能性があり、これらの第三者の行為は私たちに“反収賄法”、“海外腐敗防止法”あるいは現地反腐敗法に規定された責任を負わせる可能性がある。また、将来の規制要求の性質、範囲、影響を予測することはできず、私たちの国際業務はこれらの要求によって制約される可能性があり、現行の法律が管理または解釈される可能性がある方式を予測することもできない。私たちの業務を拡大すれば、私たちは各管轄区域で事業を展開することを計画している多くの法律や法規を遵守するために追加の資源を投入する必要があるだろう。
私たちはまた、私たちの国際業務を管理する他の法律と法規、イギリスとアメリカ政府およびEU当局が管理する法規を含み、適用される輸出規制法規、国と人員に対する経済制裁、税関要求と通貨両替法規を含み、総称して貿易制御法と呼ばれる。さらに、様々な法律、法規、および行政命令は、米国国外での使用および伝播を制限するか、または国家セキュリティ目的のために秘密にされた情報、および特定の製品およびこれらの製品に関連する技術データを特定の非米国国民と共有することも制限される。もし私たちが米国以外の地域に業務を拡張すれば、これらの法律を遵守するためにより多くの資源を投入する必要があり、これらの法律は、COMP 360の製造を阻止し、私たちの研究用COMP 360ヌードカバーキノコ療法や任意の未来のアメリカ以外の候補治療薬の開発と販売を阻止する可能性があり、これは私たちの成長潜在力を制限し、私たちの開発コストを増加させるかもしれない。
私たちが貿易統制法を含む“反収賄法”、“海外腐敗防止法”または他の法律要件を含むすべての適用された反腐敗法律を遵守することを完全かつ効果的に保証することはできない。私たちが“反収賄法”、“海外腐敗防止法”および他の腐敗防止法または貿易統制法を遵守しなければ、私たちは刑事および民事処罰、返還および他の制裁および救済措置、および法的費用を受ける可能性があり、これは私たちの業務、財務状況、運営結果、流動性に悪影響を及ぼす可能性がある。米国証券取引委員会は、発行者が海外腐敗防止法の会計規定に違反したため、発行者の米国取引所での証券取引を一時停止または禁止する可能性もある。イギリス、米国、または他の当局は、“反収賄法”、“反海外腐敗法”、他の腐敗防止法または貿易統制法に違反する可能性のあるいかなる調査も、私たちの名声、私たちの業務、運営結果、財務状況に悪影響を及ぼす可能性がある。
私たちはアメリカ連邦と州の没収法律の制約を受けるかもしれません。これは私たちの業務運営にマイナスの影響を与えるかもしれません
いかなる米国連邦の法律および法規に違反しても、連邦政府または一般市民が提起した民事訴訟によって生じる巨額の罰金、処罰、行政制裁、有罪または和解、または刑事告発は、資産の差し押さえ、利益の返還、業務活動の停止、または資産剥離を含むが、これらに限定されない。裸蓋キノコと裸蓋キノコ業務に従事する実体として、政府が犯罪活動の収益を没収することを可能にする連邦と州没収法(刑事と民事)の制約を受ける可能性がある。民事廃棄法は、連邦政府または任意の州(または地方警察部隊)に別の選択を提供することができ、これらの州または地方警察は、裸蓋キノコ素および裸蓋素に関連する企業との住民の取引を阻止することを望んでいるが、刑事責任は合理的な疑いを排除することは困難であると考えられる。また,犯罪所得と考えられる財産の没収を個人に求めることができ,その人が有罪判決を受けていなくても,民事没収事項の証明基準は刑事事件の証明基準よりも低い。適用される法律によると、連邦政府であっても州政府であっても、合理的な疑いを排除する責任を決定しなければならないのではなく、連邦政府または州が適用される場合、論争の金銭的または財産が犯罪の収益であるか、明確で納得できる証拠であるか、または証拠の利点であることを証明する必要があるかもしれない。
裸蓋キノコと裸蓋キノコは依然として不法な司法管轄区に位置する投資家は共謀、協力と教唆及びマネーロンダリング法規によって起訴されるリスクに直面し、没収法規によって投資或いは収益をさらに損失するリスクに直面する可能性がある。多くの司法管轄区域は依然として完全に行動し、裸蓋キノコ素と裸蓋キノコ業務の収益が彼らの州に入ることを阻止する能力がある。私たちの投資家と潜在的投資家は私たちに投資するかどうかを考慮する時、これらの潜在的な関連法律を認識すべきだ。
私たちは特定の税務リスクと待遇の影響を受けて、これらのリスクと待遇は私たちの運営結果に否定的な影響を与えるかもしれない
1986年に改正された国税法第280 E条は、企業が制御対象物質の販売に関連するいくつかの費用を差し引くことを禁止している(CSA別表1および付表2の意味で)。米国国税局(IRS)は、米国の州法適用が許可されている各種企業に対して税務監査を行う際、第280 E条を引用した。米国国税局は、ある費用の控除を許可する明確化を発表したが、これらのプロジェクトの範囲は非常に狭く解釈されており、運営コストの大部分と一般行政コストを差し引くことは許されていない。現在いくつかの未解決の事件が異なる行政や連邦裁判所でこれらの制限に挑戦しているが、これらの裁判所が裸蓋キノコ素や裸蓋素業務に有利な第280 E条の解釈を発表することは保証されない。
私たちは純営業損失と税収控除といくつかの内在的損失を使用して、将来の納税を減らしたり、有利なイギリス税法から利益を得ることができないかもしれません。
イギリスの登録会社と税務住民実体として、私たちは調整後の取引利益のためにイギリス会社税を支払う必要があります。私たちの業務性質のため、私たちは設立以来赤字が発生したため、イギリスの会社税は何も納めていません。2022年12月31日と2021年12月31日まで、英国での累計繰越取引損失はそれぞれ1兆769億ドルと1.44億ドルだった。任意の関連する使用基準及び制限(繰越損失から減少可能な利益パーセンテージを制限する基準及び繰越損失の使用を制限する基準及び繰越損失の使用を制限する基準及び過半普通株の所有権変更及び取引性質、行為又は規模が重大に変化した場合を含む)、これらの基準及び制限は将来の営業利益に適用されることが予想される。2017年4月1日以降に発生したイギリスの利益に関する損失繰越の使用制限は、グループごとに年間500万GBを超えてはならず、イギリスの課税利益の50%の増加を加えている。さらに、私たちの貿易行為が大きく変化すれば、損失繰越が制限されたり解消されたりする可能性がある。
広範な研究開発活動を展開している会社として、私たちはイギリスの研究開発税減免計画から利益を得ることを求めています。この計画は中小企業の研究開発税減免計画であり、もし私たちのプロジェクトが贈与援助や第三者が私たちに委託してくれた仕事に関連している場合、研究開発支出免除計画やRDEC計画の恩恵を受けることも求めています。中小企業計画によると、私たちは、このような合格研究開発支出の33.35%までの現金リベート(2023年4月1日以降に発生するこのような合格研究開発支出の現金リベートは最高23%に低減できると予想される)、または潜在的な未来利益の相殺に使用するために、私たちの合格研究開発活動による取引損失を返金することができるかもしれない(関連制限されている)。私たちの大多数の研究、臨床試験管理と製造開発活動はこれらの税金還付申請に含まれる資格があります。従業員数、売上高、総資産の規模基準によると、もし私たちが中小企業になる資格がなければ、私たちは将来、支払うべき研究開発税控除を申請し続けることができないかもしれない
中小企業案は、多倍賃金税に対するクレーム上限(広義には、最高支払控除は20,000 GBと会社総PAYEとNIC負債の3倍に相当する)を盛り込んでいるが、適用上限を阻止する例外がある。この例外は、会社に知的財産権の創造、措置の創造、管理、および関連側に関連する合格研究開発支出がクレーム総額の15%を超えないことを要求する。もしこのような例外が適用されなければ、これは私たちが要求する対応信用金額を制限するかもしれない。
また、最近公布または提案されたイギリスの研究開発税収減免立法の変化は2023年4月に施行される予定であり、これらの変化はそれぞれ中小企業計画下での研究開発現金還付を減少させ、RDEC計画下の信用限度額を高め、下請け研究開発活動の支出申請の減免を制限する可能性があり、このような活動に従事する労働者はイギリスPAYE税を納めなければならないこと、あるいは、イギリス以外で仕事を行う場合、これは以下の地理、環境、または社会条件によるものでなければならない。そして(Ii)イギリスで複製するのは完全に不合理だ。 このような変化と提案された制限は、私たちが未来に主張できる研究開発減免の数に影響を及ぼすかもしれない。 また、イギリス政府は現在、中小企業計画とRDEC計画の代わりに単一計画を使用する可能性について協議しており、この計画の運営はRDEC計画と類似しており、その中で現在の下請け研究開発事業の処理方式を変更し、支出や減免に異なるハードルや上限を導入する可能性がある。 採択されれば、新計画は2024年4月から発生する支出に影響を与えることが予想され、私たちが申請する資格のある研究開発減免数に実質的な影響を与える可能性がある
私たちは将来、特許製品収入(および他の資格に適合した収入)のいくつかの利益を追加的な税金減免を与えることで、10%の実際の税率で課税することを可能にするイギリスの“特許箱”制度の恩恵を受けるかもしれない。私たちは2つのイギリス特許を持っていて、私たちの研究COMP 360ヌードカバーキノコ療法をカバーしているので、将来の前払い、マイルストーン費用、製品収入、印税はこの減額を受ける資格があります。当に与る
私たちの研究開発支出の減免を強化するために、私たちは私たちの長期会社に適用される税率が法定税率を下回ると予想します。しかし、イギリスの研究開発税収控除制度や“特許箱”制度に予期せぬ不利な変化が生じた場合、あるいは何らかの理由で、このような優遇された税収立法を得ることができない場合、あるいは純運営損失と税収控除繰り越し、いくつかの内在的損失を利用して将来の納税を減少させることができない場合、私たちの業務、運営結果、財務状況は悪影響を受ける可能性がある。これは私たちの現在の投資需要と追加投資が必要な時間枠に影響を及ぼすかもしれない。
最近公布された立法および将来の立法は、研究中のCOMP 360ヌードカバーキノコ療法または任意の将来の候補療法の発売承認および商業化の難しさとコストを増加させ、私たちの業務に大きな悪影響を及ぼす可能性があります
米国、EU、その他の外国司法管轄地域では、医療システムの立法と規制面のいくつかの変化が、私たちの将来の運営結果に影響を与える可能性がある。特に,米国連邦や州レベルでは,医療コストの低減と医療の質の向上を図る取り組みが継続されている。例えば、2010年に“医療·教育調整法案”により改正された“患者保護·平価医療法案”、あるいは総称してACAと呼ばれ、政府や民間保険会社が医療に資金を提供する方法を大きく変え、米国のバイオ製薬業界に大きな影響を与えた
ACAの変化や挑戦,および将来とりうる他の医療改革措置は,連邦医療保険や他の医療資金のさらなる減少,より厳しいカバー基準,新たな支払い方法,および将来承認された任意の製品の価格低下への圧力をもたらす可能性が予想される。最近公布された将来の立法に関連するリスクに関するより多くの情報については、タイトルを参照してください“ビジネス-医療改革.”
2022年8月16日、バイデン総裁は米国の製薬業に重大な影響を与える可能性のある実質的な薬品定価改革を含む“2022年インフレ低減法案”(IRA)に署名した。これは、CMSがいくつかの高価な単一源Medicare薬物の最高公平価格を交渉することを可能にすることと、受益者の自己処方薬コストを低減するためにMedicare Part Dを再設計することとを含み、これは、計画および製造業者がより高い費用を支払うことをもたらす可能性がある。アイルランド共和軍はまた、メーカーが医療保険で覆われた単一由来薬物と生物製品の価格をインフレ調整後を超える比率に引き上げることを罰するために、薬品インフレ税還付要求を確立した。Ireland共和軍が私たちの業務と医療産業全体に及ぼす影響はまだ明確ではない。
新しい法律および追加の医療改革措置は、連邦医療保険および他の医療資金のさらなる減少をもたらす可能性があり、これは、私たちの研究COMP 360ヌードカバーホルモン療法および任意の将来の候補療法の顧客ニーズおよび負担能力に悪影響を与え、それに応じて私たちの財務運営の結果に影響を与える可能性がある
当社の業務運営および調査者、医療専門家、コンサルタント、第三者支払者および顧客との現在および将来の関係は、米国連邦および州医療詐欺および乱用法律、虚偽クレーム法律、医療情報プライバシーおよび安全法律、他の医療法律および法規、および他の外国のプライバシーおよび安全法律の制約を直接または間接的に受ける可能性があります。もし私たちがこのような法律を遵守できないか、または完全に遵守できなければ、私たちは巨額の処罰に直面するかもしれない
私たちは現在市場に何の治療方法もないにもかかわらず、私たちは現在と未来の業務は直接或いは間接的に私たちと調査人員、医療保健専門家、顧客と第三者支払人との関係を通じて、各種のアメリカ連邦と州医療保健法律と法規を遵守するかもしれないが、アメリカ連邦反バックル法規或いは連邦反リベート法規を含むが、これらに限定されない。私たちが市場で承認された任意の治療法の推薦と処方では,医療提供者,医師,他者が主な役割を果たしている。これらの法律は、私たちの研究活動と提案された販売、マーケティング、教育計画に影響を与え、私たちの業務および財務計画、ならびに第三者支払者、私たちの臨床研究計画に参加する医療専門家、私たちの承認された治療法を推薦、購入、または提供する他の人、ならびに私たちがマーケティング、販売、流通を通じてマーケティングの承認を得た療法を販売する他の当事者との関係を拘束します。また,米国連邦政府と我々が業務を行っている州や外国の規制機関(欧州データ保護機関を含む)の患者データプライバシーやセキュリティ法規の制約を受ける可能性がある.最後に、私たちが業務を展開している司法管轄区域では、現在も将来の業務も、医療に関する追加の法律と規制要求、外国の規制機関の強制執行を受けています。これらの法律法規に関連するリスクに関するより多くの情報は、タイトルを参照してください“業務-他の医療法とコンプライアンス要件
医薬製品の流通は許可証、広範な記録保存、保存と安全要求を含む追加の規定と条例を遵守し、許可されていない医薬製品の販売を防止しなければならない。
また,われわれの卓越したセンターで臨床研究を行えば,臨床試験サイトの運営に関与するリスクに直面する可能性がある。このようなリスクは不適切な行為と患者の負傷を研究することを含むことができるが、これらに限定されない。しかも、私たちは最終的に個別に識別できる多くの健康情報を持っているかもしれない。このような活動は様々な法的制約を受けており,たとえば上記の“HIPAA”である.
これらの法律の範囲も執行も不確定であり,現在の医療改革環境下では,特に適用の前例や法規が乏しい場合には,急速な変化が生じる可能性がある。連邦と州法執行機関は最近、医療保険会社と医療保健提供者の間の相互作用の審査を強化し、医療保健業界の一連の調査、起訴、有罪判決と和解を招いた。予防措置を講じても、政府当局は、現在または将来の詐欺および乱用または他の医療保健法律および法規の適用に関する現行または将来の法律、法規または判例法に適合していない可能性があると結論する可能性がある。もし私たちの運営がこれらの法律または任意の他の私たちに適用される可能性のある政府法規に違反していることが発見された場合、私たちは重大な民事、刑事と行政処罰、損害賠償、罰金、返還、監禁、医薬品を政府援助の医療計画(例えばMedicareおよびMedicaid)から除外し、追加の報告要件および監督に直面する可能性があり、もし私たちが会社の誠実な合意または同様の合意の制約を受けて、これらの法律違反に関する告発、名声損害、および私たちの業務の削減または再編を解決する。私たちがそれと業務を展開することが予想される任意の医師または他のヘルスケア提供者またはエンティティが、適用される法律に適合していないことが発見された場合、その個人またはエンティティは、政府によって援助された医療計画から除外されることを含む重大な刑事、民事または行政制裁を受ける可能性がある。今後発売される製品の販売を禁止または制限または撤回することは、不利な方法で業務に大きな影響を与える可能性がある。
私たちが第三者の業務配置と適用される医療法律や法規に適合するように努力することは、多くのコストに関連することを確実にします。これらの法律に違反して私たちにとった行動は、たとえ私たちが弁護に成功しても、巨額の法的費用を招き、私たちの経営陣の業務運営への注意をそらす可能性があります。持続的に変化するコンプライアンス環境、および異なるコンプライアンスまたは報告要件を有する複数の司法管轄区域の必要性に適合するために、穏健かつ拡張可能なシステムを確立し、維持することは、医療会社が1つまたは複数の要件と衝突する可能性を増加させる
健康とデータ保護の法律法規を守らないことは、民事或いは刑事処罰、個人訴訟と負の宣伝を含む米国連邦と州政府の法執行行動を招く可能性があり、私たちの経営業績と業務に負の影響を与える可能性がある。
私たちと任意の潜在的な協力者は、プライバシーおよびデータセキュリティに関する法律および法規のような、米国連邦および州データ保護法律および法規によって制約される可能性がある。アメリカでは、州データ漏洩通知法、州健康情報プライバシー法及び連邦と州消費者保護法を含む多くの連邦と州法律法規は、健康に関連する個人情報とその他の個人情報の収集、使用、開示と保護を管理する。また,HIPAA(HITECH改訂)のプライバシーやセキュリティ要求に制約されている臨床試験データを取得する研究機関を含む第三者から健康情報を取得する可能性がある。電子取引に従事する医療提供者のビジネスパートナーとしての私たちの行為についても、患者が識別可能な健康情報の使用および開示を制限し、患者が識別可能な健康情報のプライバシーおよびセキュリティに関する基準を強制的に採用するHITECHによって改正されたHIPAAのプライバシーおよびセキュリティ条項の制約を受ける可能性があり、そのような情報について特定のセキュリティ違反をヘルスケア提供者クライアントに報告することを要求する。しかも、多くの州でも似たような法律が公布されており、私たちのような実体にもっと厳しい要求を加えるかもしれない。事実や状況によると、HIPAAの許可されていない方法でHIPAAによってカバーされているエンティティによって維持されている個別に識別可能な健康情報を取得、使用、または開示する場合、私たちは重大な民事、刑事、および行政処罰を受ける可能性がある。
また、2018年6月、カリフォルニア州は2020年1月1日に施行され、2020年7月1日にカリフォルニア州総検察長によって強制執行される2018年カリフォルニア州消費者プライバシー法案を公布した。CCPAは消費者に新しいデータプライバシー権(この用語は広く定義されている)を提供し、会社に新しい運営要件を提供し、これは私たちのコンプライアンスコストと潜在的な責任を増加させる可能性がある。CCPAは、カバーする会社が、そのデータ収集、使用、および共有アプローチに関するいくつかの開示を消費者に提供し、影響を受けたカリフォルニア住民に、特定の個人情報販売または移転から撤退することを選択する方法を提供することを要求する。特に,CCPAはカリフォルニア州住民により大きな権利を与え,彼らの個人情報にアクセスし削除し,特定の個人情報を共有しないことを選択することができる
彼らの個人情報をどのように使用するかに関する詳細な情報を受信する。CCPAは,違反行為に対する民事処罰と,データ漏洩訴訟の増加を招くデータ漏洩行為に対する個人訴権を規定している。現在HIPAAと臨床試験法規に制約されている保護された健康情報は例外的な状況があるが、CCPAは著者らのいくつかの業務活動に影響を与える可能性がある。CCPAの実行と実施には依然として不確実性が存在し,我々の業務が個人データや保護された健康情報に関する変化する規制環境の影響を受けやすいことを示している
さらに、カリフォルニア州の新しい投票イニシアティブであるカリフォルニアプライバシー権法案、またはCPRAが、2020年11月に採択された。CPRAは、2023年1月1日から、立法がカバーする企業に追加的な義務を課し、特定の敏感な個人情報における消費者の権利を拡大することを含むCCPAを大幅に改正する。CPRAはまた、CCPAおよびCPRAを実施し実行する権限を付与される新しい国家機関を作成した。CCPAおよびCPRAの影響は重大である可能性があり、私たちのデータ収集または処理のやり方や政策を修正し、規制法および/または訴訟における私たちの潜在的なリスクを遵守し、増加させるために、大量のコストと支出を生成する必要があるかもしれない。
CCPAは、米国のより厳しい州プライバシー立法傾向の開始を示す可能性があり、これは私たちの潜在的な責任を増加させ、私たちの業務に悪影響を及ぼす可能性がある。いくつかの他の州の法律は類似したプライバシー義務を規定しており、より多くの州がCCPAのような立法を制定し、消費者に新たなプライバシー権を提供し、このような消費者の特定の個人情報を処理する実体のプライバシーとセキュリティ義務を増加させる可能性があると予想される。CCPAは一連の新しい連邦と州レベルのプライバシー立法の提案を促進した。このような提案された立法が通過されると、追加の複雑性、要求変化、制限、および潜在的な法的リスクが増加する可能性があり、コンプライアンス計画、影響戦略、および以前の有用なデータの利用可能性に追加のリソースを投入する必要があり、コンプライアンスコストの増加および/またはビジネス実践および政策の変化をもたらす可能性がある。
連邦レベルでは、包括的な連邦データプライバシー法案である“米国データプライバシーと保護法”が提案されており、可決されれば、プライバシーとデータセキュリティコンプライアンスの構造をさらに変えることになる。この提案された立法が採択されれば、私たちのいくつかのプライバシー義務を簡略化するのに役立ちますが、全米から収集された個人データに適用される新たな厳格なプライバシーおよびデータセキュリティ義務も導入されます。また、米国証券取引委員会が提出したネットワークセキュリティ規則は2023年に発効する可能性があり、その中でデータセキュリティ事件の監視と報告の強化が求められる可能性がある。
アメリカと外国のプライバシーとデータ保護法律法規を遵守することは、私たちがデータを収集、使用、開示する能力を制限し、または場合によってはいくつかの司法管轄区域で運営する能力に影響を与える契約の中でより重い義務を負うことを要求するかもしれません。これらの法律法規を遵守しないことは、政府の法執行行動(民事、刑事および行政処罰を含む可能性がある)、個人訴訟および/または負の宣伝をもたらす可能性があり、私たちの経営業績および業務に負の影響を与える可能性がある。さらに、私たちまたは私たちの潜在的な協力者が個人情報を取得する臨床試験被験者、従業員および他の個人、およびこの情報を共有する提供者は、情報を収集、使用、および開示する能力を制限する可能性がある。私たちがプライバシー権を侵害していると主張し、データ保護法を遵守できなかったり、私たちの契約義務に違反したりして、私たちが責任を負わなくても、弁護の費用が高く、時間がかかり、否定的な宣伝を招き、私たちの業務を損なう可能性があります。
ヨーロッパのデータ収集は厳しいプライバシーやセキュリティ法規に制約されており,これらの法規は個人情報の使用,処理,国境を越えた移行を管理している.
我々が欧州医薬品局加盟国で行っている臨床試験活動はGDPRによって規制されている。個人データ(臨床試験で処理された健康データを含む)の収集、使用、記憶、開示、転送、または他の処理(I)EU内の個人、および/または(Ii)任意のEU加盟国によって設立された機関の活動において行われる個人データの収集、使用、記憶、開示、移転または他の処理は、GDPRおよび関連加盟国の有効な他の国データ保護立法によって制限される
“個人資料保護法”は範囲が広く、個人データを処理する会社に多くの追加要求を加え、健康や他の敏感なデータの処理に特殊な要求を加えることを含み、場合によっては個人データに関連する個人の同意を得なければならないことを要求し、個人にデータ処理活動に関する情報をより多く開示することを要求し、個人データの安全と機密性を保護するための保障措置の実施を要求し、個人データの保持期間を制限し、健康データと仮名(すなわち鍵コード)データに関する要求を増加させ、場合によっては強制的なデータ漏洩通知要求を作成する。また、第三者加工業者を使用する際に(契約要件を含む)何らかの措置をとることを要求する。GDPRはまた,米国を含む欧州経済圏以外の国への個人データの移転に厳しいルールを実施し,データ保護当局が2000万ユーロや世界の年収の4%に達する可能性のある罰金を含むGDPR違反行為に巨額の処罰を与えることを許可している。GDPRは個人に様々な権利を提供しています
アクセス、削除、携帯、訂正、制限、および反対の権利を含む彼らの個人データを尊重する。GDPRはまた、データ主体と消費者協会に個人訴訟権利を与え、監督当局に苦情を提出し、司法救済を求め、GDPR違反による損害について賠償を受けることができる
GDPRは、欧州経済圏加盟国は、遺伝子、生体認証、または健康データ処理に関する独自のさらなる法律および法規を制定することができ、これは、加盟国間の差を招き、個人データの使用および共有能力を制限するか、または私たちのコストを増加させ、私たちの業務および財務状況を損なう可能性がある
また、個人データを欧州経済圏から米国などの第三国に移す上で、進化し、厳しいルールに制約されています。2020年、EU裁判所はEU-米国プライバシー盾の無効を宣言し、これは米国会社がGDPRの国境を越えたデータ伝送に基づいてヨーロッパからの個人情報の輸入を制限する主要なメカニズムの一つであり、欧州委員会の標準契約条項がプライバシー盾の主要な代替案の一つであり、欧州から米国または大多数の他の国への個人情報の送信に合法的に使用できるかどうかという疑問を引き起こした。同様に、スイス連邦データ保護および情報専門家は、スイス-米国プライバシーシールドは、スイスから米国にデータを送信するのに不十分であり、イギリス情報専門家事務室も、プライバシーシールドフレームワークは、イギリスから米国に送信するのに十分ではないと述べている。さらに、2021年6月4日、欧州委員会は、欧州経済地域のコントローラまたはプロセッサ(またはGDPRによって拘束されている)からヨーロッパ経済地域以外のコントローラまたはプロセッサにデータを送信するための新しい形式の標準契約条項を発表した。私たちは多くの努力と費用が必要かもしれない新しい形の標準契約条項に移行することを要求されるだろう。新しい標準契約条項は、譲渡影響評価の重い要求と新標準契約条項が輸出業者に課す重大な義務を考慮して、ヨーロッパに本部を置く会社は、新しい条項を利用して個人情報を第三国に移転することを合法化したくないかもしれないので、私たちの業務に影響を与える可能性もある。ヨーロッパのデータ保護機関の調査を受けたら, 私たちは罰金と他の処罰に直面するかもしれない。欧州データ保護当局のこのような調査または告発は、私たちの既存の業務および新しい顧客または製薬パートナーを引き付け、維持する能力にマイナスの影響を与える可能性がある。私たちはまた、いくつかのデータ保護機関がGDPRを含む現行の法律を解釈する際に彼らに課せられた現在(特に将来)のデータ保護義務に起因する潜在的リスクに遭遇し、それによって、私たちの製品の使用を躊躇、不快、または拒否することも可能である。これらの顧客や医薬パートナーも,任意の他のコンプライアンス方法はコストが高すぎ,負担が重すぎ,法的に不確実すぎたり反感を抱いたりする可能性があるため,我々と商売をしないことにした。上記のいずれも、我々の業務、見通し、財務状況、および経営結果に実質的な損害を与える可能性がある。
GDPRは,GDPRに拘束された個人データの処理における我々の責任と責任を増加させる可能性がある.我々は、GDPRを遵守し、適用されるEU加盟国で立法を実施しているが、制御者や共同制御者として行われる様々な処理活動のための適切な合法的な基盤の確立を求め、我々および我々の供給者および協力者のセキュリティ手順を検討し、関連する供給者および協力者とデータ処理協定を締結することを含むが、コンプライアンスを達成し、維持するための努力が完全に成功していることを確認することはできない
また、イギリスの投票はEU離脱を支持し、通常はイギリスの離脱と呼ばれ、イギリスで発生している事態の発展は、イギリスのデータ保護規制に不確実性をもたらしている。2020年12月31日以降、GDPRのデータ保護義務は、いわゆる“イギリスGDPR”(すなわちGDPR)に基づいて個人データを実質的に不変の形で行う連合王国に関する処理(すなわちGDPR)に適用され続けており、各種データ保護、プライバシー、電子通信(改正案等を含む)を改正した2018年EU(離脱)法案第3条により連合王国法律の一部となり続けている。(“2019年EU離脱条例”)。しかし,将来を展望すると,データ保護法の適用,解釈,施行における連合王国と欧州経済区の相違はますます大きくなるであろう。英国GDPRと2018年の英国データ保護法は、EUのデータ保護制度から独立した英国のデータ保護制度を規定しているが、現在もEUのデータ保護制度と一致している。イギリスのGDPR違反は、金額が高い者を基準に、1750万GBまたは世界収入4%の罰金を招く可能性があります。英国はEU GDPR下の第3の国とされているが、欧州委員会は現在、英国がEU GDPRで十分な保護を提供していることを認める決定を発表しているため、EU由来の個人データの英国への移行は依然として制限されていない。EU GDPRと同様に,イギリスGDPRは個人データをイギリス以外の国に移しており,これらの国はイギリスが十分な保護を提供しているとはみなされていない。それは新しい形式の標準契約条項の制約を受けないが、標準契約条項と同じように、独自の譲渡メカニズムである国際データ譲渡協定を発表した, 輸出業者に譲渡影響評価を要求する。イギリス政府は、イギリスからヨーロッパ経済圏への個人データ転送が依然として自由に流動していることを確認した。
我々の研究におけるCOMP 360ヌードカバーキノコ療法または任意の将来の候補療法の商業化の成功は、政府当局と健康保険会社が十分なものを確立することに部分的に依存するであろう
清算水準と定価政策。もし私たちの研究におけるCOMP 360ヌードカバーキノコ療法または任意の将来の候補療法が十分な保険および精算を獲得または維持できなかった場合、承認されれば、これらの療法をマーケティングする能力を制限し、私たちの収益能力を低下させる可能性がある
政府医療計画(例えば、MedicareおよびMedicaid)、個人健康保険会社および他の第三者支払者が提供する保険および精算の利用可能性および十分性は、大多数の患者が私たちの研究COMP 360ヌードキノコ療法または任意の将来の候補療法(承認されれば)を負担することができるために重要である。付表1として,CSA下の物質としては,裸蓋キノコや裸蓋キノコは受け入れられていないと考えられ,裸蓋キノコや裸蓋キノコを用いた療法は米国では精算から除外されている。私たちの製品は、表II以下の制御物質(すなわち、附表III、IVまたはV)として登録され、その後発売されなければならない。私たちは政府当局、個人健康保険会社、その他の組織の治療に対する許容可能なカバーと精算レベルを実現することができ、私たちの商業化に成功する能力に影響を与え、より多くのパートナーを私たちの研究COMP 360ヌードカバーキノコ療法または任意の未来の候補療法の開発に投資する。ヌードゲラニンによるTRD治療の長期治療効果に関する臨床データは限られている。いくつかの患者は再発を避けるために彼らの一生の間に繰り返し治療する必要があるかもしれない。これは治療費用を増加させ、私たちが精算を得るのをもっと難しくするかもしれない。第三者支払者により特定療法の保険を受けても,それによる精算支払率が十分高くない可能性があり,あるいは患者の自己払い費用が必要となる可能性があり,患者は受け入れられないほど高いと考える可能性がある。アメリカ、ヨーロッパ、その他の地域の保険と精算が私たちが開発する可能性のあるどんな治療法にも適用されることを保証することはできません, 得られる可能性のあるすべての精算は未来に減少またはキャンセルされるかもしれない。保険加入範囲と関連リスクの補償に関するより多くの情報は、タイトルを参照してください“業務-カバー範囲、定価、精算
我々の研究におけるCOMP 360裸蓋キノコ療法または将来の候補療法の承認を求めて,米国と選定された外国司法管轄区で販売する予定である。もし私たちが1つ以上の外国の管轄区域でCOMP 360または私たちの将来の候補治療薬の承認を得たら、私たちはこれらの管轄区域の規制によって制限されるだろう
いくつかの海外の国、特にヨーロッパのある国では、薬品の価格設定は政府のコントロールと他の市場によって規制されており、これは私たちが研究しているCOMP 360ヌードカバーキノコ療法あるいは私たちの未来の候補療法の価格設定と使用に圧力を与えるかもしれない。これらの国では,候補治療薬の発売承認を得た後,政府当局との定価交渉にかなりの時間を要する可能性がある。また,我々の研究におけるCOMP 360裸蓋キノコ療法や将来の候補療法の市場受容度や販売は,われわれの研究におけるCOMP 360裸蓋キノコ療法や将来の候補療法が十分な保証範囲と第三者支払者の精算を有するかどうかに大きく依存し,既存および将来の医療改革措置の影響を受ける可能性がある。
第三者支払者は治療物質やサービスの料金に対してますます大きな挑戦を提出しており、多くの第三者支払者は同等の後発薬あるいはより安い治療法がある場合、特定の薬物への保険と精算を拒否する可能性がある。第三者支払者は,我々が検討しているCOMP 360ヌードカバーキノコ療法や任意の将来の候補療法が代替可能であると考え,患者への精算が安価な治療法のみを提案する可能性がある。私たちの研究におけるCOMP 360ヌードカバーキノコ療法または任意の将来の候補療法がより良い治療効果またはより良い投与利便性を示しても、既存の薬剤の価格は、私たちが受け取ることができる金額を制限するかもしれない。これらの支払者は,特定の薬物製品の精算状態を拒否または撤回したり,新たなあるいは既存の発売療法の価格を低すぎるレベルに設定したりする可能性があり,製品開発投資から適切なリターンを実現することができない。精算が得られない場合や限られたレベルでしか精算が得られない場合には,我々の研究COMP 360裸蓋キノコ療法や将来の候補療法を商業化することに成功しない可能性があり,開発可能な候補療法から満足できる経済的見返りを得ることができない可能性がある
新たに承認された療法の保険カバーや精算に関する不確実性が大きい。米国では,連邦医療保険や医療補助計画のような第三者支払者,個人や政府支払者を含め,新薬のカバー範囲を決定する上で重要な役割を果たしている。連邦医療保険や医療補助計画は,個人支払者や他の政府支払者がどのように薬品保険や精算政策を策定するかのモデルとして利用されるようになってきている。一部の第三者支払者は、新しいまたは革新的な設備または薬物療法の保証範囲を事前に承認し、その後、このような治療法を使用する医療提供者に精算する必要があるかもしれない。第三者決済者が我々の研究COMP 360裸蓋キノコ療法や任意の将来の候補療法のカバー範囲や精算についてどのような決定を下すかを予測することは困難である
清算状態を獲得して維持するのは時間もかかるし、費用もかかる。米国では,第三者支払者の間に薬物治療のカバーや精算に関する統一政策はない。そのため、薬物治療のカバー範囲と精算範囲は支払人によって異なる。したがって、カバー範囲決定プロセスは一般的に時間がかかり、高価なプロセスであり、これは私たちのために使用することを要求するだろう
各支払者に単独で治療を提供するが、保証範囲および適切な補償が一貫して適用されるか、または最初に得られることは保証されない。また、精算に関する規則や条例は常に変化しており、場合によっては短時間で通知されており、これらの規則や条例が変わる可能性があると考えられる
アメリカでは、特殊薬品の価格設定に関する立法と法執行の関心が増加している。具体的には,米国議会は最近いくつかの調査を行い,薬品定価の透明性の向上,連邦医療保険下の処方薬のコスト低減,定価とメーカー患者計画との関係の審査,政府計画の薬品精算方法の改革を目的とした連邦と州立法を提案した。最近公布された“2022年インフレ率低減法案”には、米国の製薬業に重大な影響を与える可能性のある重大な薬品定価改革などが含まれている。これは、CMSがいくつかの高価な単一源Medicare薬物の最高公平価格を交渉することを可能にすることと、受益者の自己処方薬コストを低減するためにMedicare Part Dを再設計することとを含み、これは、計画および製造業者がより高い費用を支払うことをもたらす可能性がある
州レベルでは、地方政府は、価格または患者の精算制限、割引、特定の製品への参入の制限、マーケティングコスト開示および透明性措置を含む薬品の価格設定を制御するための法規を立法および実施することを非常に積極的に実施してきており、場合によっては、他の国からの輸入および大量購入を奨励することを目的としている。法律で規定されている第三者支払者の支払金額の価格制御またはその他の制限は、私たちの業務、運営結果、財務状況、見通しを損なう可能性があります。また,地域医療当局や個別病院では,どの薬品やサプライヤーが処方薬や他の医療計画に含まれるかを決定するために入札プログラムが使用されるようになってきている。これは私たちの治療に対する最終的な需要を減少させ、あるいは私たちの治療価格に圧力を与える可能性があり、これは私たちの業務、運営結果、財務状況、および将来性に負の影響を与えるかもしれない
アメリカ以外では、国際運営は一般的に広範な政府価格制御と他の市場によって規制されており、ヨーロッパと他の国のコスト制御措置はますます重視されており、私たちの研究COMP 360ヌードカバーキノコ療法または任意の未来の候補療法の価格設定と使用に圧力をかけ続けていると信じている。多くの国では、国家衛生システムの一部として、医療治療の価格は異なる価格制御メカニズムの制約を受けている。他の国は会社が自分の医療価格を固定することを許可しているが、会社の利益を監視し、コントロールしている。海外の追加価格規制または定価規制の他の変化は、COMP 360ヌードカバーキノコ療法または任意の将来の候補療法の料金を制限する可能性があります。したがって,米国以外の市場では,米国に比べてわれわれの療法の精算が減少する可能性があり,商業的に合理的な収入や利益を生み出すには不十分である可能性がある
EUで医療サービスを提供することは、医療サービスの確立と運営、薬品の定価と精算を含め、ほぼ完全に国家の法律と政策の問題であり、EU全体の法律や政策ではない。この点で,各国政府と衛生サービス提供者は,医療および治療の定価や精算を提供する上で異なる優先事項や方法がある。しかし、全体的に、多くのEU加盟国の保健予算制限は関連保健サービス提供者が薬品の定価と精算を制限した。加えて、EUや国は、開発やマーケティング療法を希望する人への規制負担が増えており、これは、我々が研究しているCOMP 360ヌードカバーキノコ療法または任意の将来の候補療法の発売承認を阻止または延期し、承認後の活動を制限または規制し、市販承認された治療法を商業化する能力に影響を与える可能性がある
EU医薬品マーケティング法規は私たちがEU加盟国で私たちの治療法を販売して受け入れる能力に実質的な影響を及ぼすかもしれない。アメリカ連邦反バックル法令で禁止されているように、医師に福祉や利点を提供し、処方、推薦、裏書き、購入、供給、注文または薬物療法を誘導または奨励するために、EUの多くの国でも禁止されている。不当行為を誘導または奨励するために利益または利益を提供することは、一般にEU加盟国の国家反賄賂法によって管轄され、イギリスでは“2010年反賄賂法”の管轄を受けている。このような法律に違反することは巨額の罰金と監禁につながるかもしれない。EU指令2001/83/ECは人用薬品に関するEUの指令であり、それは更に、処方或いは薬品を供給する資格のある人に薬品を販売する場合、これらの人にいかなるプレゼント、金銭利益或いは実物利益を提供、提供或いは承諾してはならず、これらのプレゼント、金銭利益或いは実物利益が高くなく、しかも医薬或いは薬局の実践と関係がない限り、規定している。この条項は2012年の人間薬物規制に移されたので、EUから離脱したにもかかわらず、イギリスに適用された。
いくつかのEU加盟国では、医師と他の医療専門家に支払われたお金は公開されなければならない。また,医師との合意は通常,医師に事前に通知して医師の承認を得なければならない
雇用主、その主管専門組織、および/または個別のEU加盟国の規制当局。これらの要求は、個別のEU加盟国に適用される国家法律、業界規則、または専門行動規則に規定されているため、EU加盟国間の具体的な要求は大きく異なる可能性がある。このような要求を守らないことは、名声のリスク、公開非難、行政処罰、罰金、または監禁につながる可能性がある。
また、大多数の外国国では、多くのEU加盟国を含め、薬品の提案価格は合法的に発売されるために承認されなければならない。各国の薬品定価と精算に対する要求は大きく異なる。例えば、EUの個別加盟国は、その国の健康保険制度が補償を提供する医療製品の範囲を制限し、人が使用する医療製品の価格を制御する能力がある。EUの各加盟国が使用する参考価格と平行分配、あるいは低価格と高価な会員国の間の裁定は、価格をさらに下げることができる。加盟国は医薬製品の具体的な価格を承認することができ、医薬製品を市場に投入する会社の収益力に対して直接或いは間接的に制御制度をとることもできる。いくつかの国では、臨床研究または他の研究を行う必要があるかもしれないが、私たちの研究性COMP 360ヌードカバーキノコ療法または将来の候補療法を他の既存療法の費用対効果と比較して、精算または価格決定の承認を得たり維持したりする。生物製薬製品に対して価格制御や精算制限を実施することを保証できない国は、私たちのいかなる治療法に対しても有利な精算と定価手配を許可する。歴史的に見ると、EUで発売された療法は米国の価格構造に沿っておらず、通常価格ははるかに低いことが多い。第三者支払者や主管当局が割引を公表することは、公布国や他の国の価格や補償レベルにさらなる圧力を与える可能性がある。もし価格が満足できないレベルに設定されている場合、あるいは私たちの治療が精算できない場合、あるいは範囲や金額に制限されています, 私たちの販売収入と私たちが研究しているCOMP 360ヌードカバーキノコ療法または将来これらの国または地域における私たちの任意の候補療法の潜在的な収益性は否定的な影響を受けるだろう。
さらに、EU、米国、および他の地域の政府および第三者支払者は、医療コストを制限または低減するためにますます努力しており、これらの組織が新しい承認療法のカバー範囲および精算レベルを制限する可能性があるため、彼らは、我々の研究COMP 360ヌードカバーマイシン療法または任意の将来の候補療法に十分な資金を提供することができないか、または十分な費用を支払うことができないかもしれない。国際市場では,精算や医療保険支払い制度は国によって異なり,多くの国で特定療法に価格上限が設定されている。管理的医療の傾向、健康維持組織の日々の影響力、および追加的な立法変化により、我々の研究COMP 360ヌードカバーホルモン療法または任意の将来の候補療法の販売は価格設定圧力に直面することが予想される。全体的に,医療コストの下振れ圧力は非常に大きくなり,特に処方薬,外科手術,その他の治療が行われている。そのため,新たな治療法の進入にはますます高い壁が設けられている
私たちは契約を実行する困難に直面するかもしれない。
私たちの業務的性質と、私たちのいくつかの契約は、ヌードカバーキノコと裸蓋キノコを含む幻覚剤に関連しており、アメリカ連邦法律といくつかの他の司法管轄区によると、これらの薬物の使用は不法であるため、私たちはアメリカ連邦と州裁判所で契約を実行する際に困難に直面する可能性がある。私たちのいかなる契約も実行できないことは、私たちの業務、経営業績、財務状況、または見通しに実質的な悪影響を及ぼす可能性があります。
私たちと請負業者との契約を管理するために、私たちはこれらの請負業者がアメリカの州と連邦レベル、その他の地域の適切なレベルで適切な許可を得ることを確実にします。これらの請負業者がこれらのライセンスの条項の外で運営されていれば、COMP 360ヌードカバーキノコ療法の開発速度、および任意の将来の治療候補薬の研究を含む、私たちの業務に悪影響を及ぼすかもしれません。
知的財産権に関するリスク
私たちは特許と他の知的財産権に依存して、私たちの研究におけるCOMP 360ヌードカバーキノコ療法を保護し、その実行、弁護、そして維持は挑戦的でコストがかかる可能性があります。これらの権利を十分に実行または保護できなければ、私たちの競争能力を損なう可能性があり、私たちの業務を損なう可能性がある
我々のビジネス成功は、COMP 360の特許および他の形態の知的財産権の取得および維持、任意の将来の候補療法および関連療法、デジタル療法、潜在的治療物質を製造するための方法、およびこれらの物質および療法を用いて患者を治療する方法、またはそのような権利の許可に依存する。十分な特許および他の知的財産権を獲得、維持、保護、実行または延長できなければ、私たちの研究用COMP 360ヌードカバーキノコ素の開発と販売に実質的な悪影響を及ぼす可能性がある
治療や未来の治療候補です私たちはまた私たちの独自と知的財産権の地位を発展させて維持するために商業秘密とノウハウに依存している。私たちのビジネス秘密とノウハウを保護できなかったいかなる行為も、私たちの運営と将来性に悪影響を及ぼす可能性がある
私たちは、現在未解決の特許出願について特許が発行または付与されるかどうか、または発行されたまたは付与された特許が後に無効であるか、または強制的に実行されないことが発見されるかどうかを決定することはできない。私たちのような会社の特許地位は一般的に不確実であり、複雑な法律と事実考慮に関連しているからだ。欧州特許庁,米国特許商標局,外国特許庁が特許を付与する際に採用する基準は,常に統一的または予測可能であるわけではない。例えば、医薬品特許において許容される特許標的または特許請求の範囲については、世界的に統一された政策はない。したがって,我々の未解決特許出願は特許を発行しない可能性があり,たとえ彼らが確かに特許を発行しても,これらの特許の発行形態は,他の人の競争療法の開発や商業化を効果的に阻止することはできない.したがって、私たちは私たちの特許療法が未来にどの程度保護されるのか分からない
特許訴訟プロセスは高価で複雑で時間がかかり、私たちと私たちの現在または未来の第三者パートナー、ライセンシー、ライセンシー、またはパートナーは、必要または望ましいすべての特許出願を合理的なコストまたはタイムリーに準備、提出、起訴することができないかもしれない。我々または我々のライセンシー,ライセンシーまたはパートナーも,研究,開発または商業化活動中になされた発明の特許可能な側面を識別できない可能性があり,そうでなければ遅すぎて特許保護ができない。さらに、私たちは、私たちの研究開発成果にアクセスできる機密または特許可能な当事者と、当社の従業員、会社協力者、外部科学協力者、契約製造業者、コンサルタント、コンサルタント、および他の第三者のような秘密および秘密協定を締結しているにもかかわらず、これらの当事者のいずれも、合意に違反し、特許出願を提出する前にそのような成果を開示し、特許保護を求める能力を危険にさらしている可能性がある。さらに、科学文献で発見された発表は、実際の発見よりも遅れがちであり、米国および他の管轄区域の特許出願は、通常、出願後18ヶ月以内に発行されるか、または場合によっては承認後に発行される場合がある。したがって、私たちは、私たちが私たちの特許または係属中の特許出願で保護を要求した最初の発明であるか、または私たちがそのような発明のために特許保護を申請した最初の人であることを確認することができない。同様に、許可された特許又は保留特許出願のいずれについても、指名された出願人が、当該等の特許又は保留特許出願において主張された発明を最初に下した者であるか、又は指名された出願人が、当該等の発明のために最初に特許保護を申請した者であることを決定することはできない。
また,我々と我々の現在または将来のライセンシー,ライセンシーまたはパートナーの特許権の発行,範囲,有効性,実行可能性,商業的価値は非常に不確定である。私たちと私たちの許可者たちの未解決および未来の特許出願は、私たちの療法の全部または一部を保護するために、または他社が競争技術および療法を商業化することを効果的に阻止するために、特許の発行を招くことができないかもしれない
さらに、場合によっては、私たちは、第三者に権限を与え、第三者に許可し、私たちのライセンシー、ライセンシー、またはパートナーに依存する技術を含む、特許出願の準備、提出および起訴を制御する権利がない場合がある。現在または将来の許可者、許可者、またはパートナーが、そのような特許および他の知的財産権を確立、維持または保護できない場合、そのような権利は減少またはキャンセルされる可能性がある。私たちのライセンシー、ライセンシー、またはパートナーがいかなる特許権の起訴、保守または実行においても私たちの意見に完全に協力しないか、または同意しない場合、そのような特許権は損害を受ける可能性があります。
特許審査プロセスは、私たちまたは私たちのライセンシー、ライセンシーまたはパートナーが、私たちまたは私たちのライセンシー、ライセンシーまたはパートナーの係属中および将来の特許出願の特許請求範囲を縮小することを要求することができ、これは、入手可能な特許保護範囲を制限することができる。私たちの特許と特許出願に関連する可能性のあるすべての既存技術が見つかったことを保証することはできません。そのような従来技術が存在する場合、それは、特許を無効にするか、または係属中の特許出願から特許を発行することを阻止することができる
特許の発行は,その発明性,範囲,有効性または実行可能性に関する決定的な要素ではなく,我々の特許は米国や海外の裁判所または特許庁で挑戦される可能性がある。特許が確実に発行されても、これらの特許がCOMP 360および任意の将来の治療候補特許をカバーしていても、第三者は、法廷または特許庁において反対、干渉、再審査、許可後審査、当事者間審査、無効または派生手続き、または同様の手続きを開始することができ、そのような特許の有効性、実行可能性または範囲を疑問視することができ、これは、特許権利要件の縮小または無効をもたらす可能性がある 私たちは私たちがこの挑戦や未来のどんな特許挑戦でも成功的に自分自身を弁護するということを保証できない。例えば、2021年12月、第3方向米国特許商標局特許裁判·控訴委員会またはUSPTO委員会は、我々の2つの特許(米国特許10,947,257および米国特許10,954,259)のライセンス後審査を要求する2つの請願書を提出した。USPTO取締役会は2022年6月22日、この2つのケースで決定を発表し、各挑戦で提起された論点の是非を支出して審査することを拒否した。開ける
2022年7月22日、第三者挑戦者はUSPTO取締役会にUSPTO取締役会の決定を再審理する要請を提出したASそして2022年8月16日に各挑戦で前例意見グループを要請した。USPTO取締役会はまだこのような要請について最終決定を下していない
私たちおよび私たちのライセンシー、ライセンシー、またはパートナーの特許出願は、特許が他の出願から発行されるまで、かつ、発行された特許要件が技術の範囲をカバーしない限り、これらの出願で要求される技術を実施する第三者に対して強制的に実行することはできない。さらに、特許および他の知的財産権も、私たちの競争相手を含む第三者が、私たちの保護された技術と私たちの研究を中心にCOMP 360裸ゲラニン療法を用いて設計されていれば、私たちの競争相手を含む第三者が、私たちの特許または他の知的財産権を侵害、流用、または侵害することなく、私たちの技術、COMP 360、および任意の未来の候補療法を保護しないだろう。しかも、私たちのいくつかの特許と特許出願は未来に第三者と共同で所有するかもしれない。もし私たちがこのような特許または特許出願における第三者共同所有者の権利の独占的許可を得ることができない場合、これらの共通所有者は、私たちの競争相手を含む他の第三者に権利を許可することができ、私たちの競争相手は、競争相手の治療法および技術を販売することができる。さらに、私たちは、第三者に対してそのような特許を強制的に実行するために、私たちの特許のどのような共通所有者の協力も必要とするかもしれませんが、そのような協力は私たちに提供されないかもしれません。上記のいずれも、我々の競争地位、業務、財務状況、経営結果、および見通しに重大な悪影響を及ぼす可能性がある
特許出願は提出後しばらくは秘密であり、いくつかの特許出願は発行前に秘密であったため、私たちまたは私たちの現在または未来の許可者、ライセンシーまたは協力者が治療候補薬に関連する特許出願を最初に提出する会社であるかどうかを決定することはできない。さらに、第三者の特許出願の有効提出日が2013年3月16日前である場合、そのような第三者は、誰が私たちの出願の特許請求項によってカバーされた任意の主題を最初に発明したかを決定するために、干渉プログラムを開始することができる。第三者の特許出願の有効出願日が2013年3月16日以降である場合、そのような第三者は、私たちの発明が彼らの発明に由来しているかどうかを決定するために派生プログラムを開始することができる。私たちが効果的で強制的に実行可能な特許を持っている場合であっても、他の当事者が彼らが私たちの出願日前にその発明を商業に使用していることを証明することができれば、または他方が強制許可から利益を得ることができれば、他の人が私たちの発明を実践することを排除することはできない。しかも、私たちは私たちの知的財産権を独占的に持っていることで第三者の挑戦を受けるかもしれない。もし第三者が私たちの任意の知的財産権の独占所有権に挑戦することに成功した場合、私たちはそのような知的財産権を使用する権利を失う可能性があり、この第三者はこのような知的財産権を私たちの競争相手を含む他の第三者に許可する可能性があり、私たちの競争相手はそれと競争する治療法および技術を販売するかもしれない。上記のいずれも、我々の競争地位、業務、財務状況、経営結果、および見通しに重大な悪影響を及ぼす可能性がある
私たちの1つまたは複数の研究療法をカバーする発行された特許は、法廷で疑問視されれば、無効または実行不可能と認定される可能性がある
私たちの競争的地位を保護するためには、私たちが私たちに所有または権限を与えてくれた任意の特許または他の知的財産権を強制的に実行または保護するために、時々訴訟に訴える必要があるかもしれないし、第三者特許または他の知的財産権の範囲または有効性を決定または疑問視する必要があるかもしれない。知的財産権の実行は困難で予測不可能で高価であり、私たちまたは私たちのライセンシーまたはパートナーの多くの相手は、これらの訴訟において、私たちまたは私たちのライセンシーまたはパートナーよりも多くの資源を投入して、このような法的行動を起訴することができるかもしれない。したがって、私たちまたは私たちのライセンシーまたはパートナーが努力したにもかかわらず、私たちまたは私たちのライセンシーまたはパートナーは、第三者の侵害、流用、または他の方法で私たちが所有または制御している知的財産権を侵害することを防ぐことができないかもしれない。特に法律では、イギリス、EU、およびアメリカのようにこれらの権利を十分に保護する国はないかもしれない。私たちは私たちの権利を実行できないかもしれないが、この場合、私たちの競争相手と他の第三者は、私たちに支払うことなく、私たちの治療法の使用を許可されるかもしれない
さらに、私たちの特許に関連する訴訟は、私たちの1つ以上の特許が縮小され、無効(逐一請求に基づいて、全部または部分的に無効)と認定されるか、または実行不可能と認定されるリスクがある。このような不利な裁判所判決は、第三者が私たちの治療法を商業化し、私たちに支払うことなく、私たちと直接競争することを可能にするかもしれない
もし私たちが第三者に対して法的訴訟を提起して、私たちの研究療法をカバーする特許を強制的に執行するならば、被告は私たちの特許が無効または強制執行できないと反論することができる。米国やヨーロッパの特許訴訟では,被告が無効または実行不可能と主張する反訴が一般的である。有効性疑問に対するクレームは、新規性の欠如、明らかな、または使用不可能性のような、いくつかの法定要件のいずれかを満たすことができなかったことに基づく可能性がある。実行不可能な主張は、特許起訴に関連する者が、起訴中に米国特許商標局に関連情報を隠蔽したり、誤って陳述したりした疑惑であってもよい。第三者は、訴訟の範囲外であっても、米国や海外の行政機関に我々の特許主張の有効性を疑問視する可能性がある。この仕組みには再審査、贈与後審査、各方面間審査手続き、介入手続き、派生手続きは外国司法管轄区と同等の手続き(すなわち反対手続き)である。このようなものは
訴訟は、COMP 360または任意の未来の候補治療薬をカバーしないように、私たちの特許が撤回、キャンセル、または修正される可能性がある。2022年7月22日、第三者挑戦者はUSPTO取締役会に、USPTO取締役会が米国特許10,947,257および米国特許10,954,259のライセンス後審査を拒否する決定の再審理請求を提出し、2022年8月16日にも、第三者挑戦者が各特許に対して前例意見グループの請求を行った。USPTO取締役会はまだこのような要請について最終決定を下していない。 特許訴訟または他の訴訟では、無効および実行不可能と法的に断言された後の結果は予測不可能である。例えば、有効性の問題については、私たちは無効な以前の技術がないとは確信できないが、私たちと特許審査員は起訴中にこれを知らない。被告または第三者が無効または強制不可能な法的主張に勝利した場合、COMP 360または1つまたは複数の将来の治療薬候補の少なくとも一部またはすべての特許保護を失うであろう。このような特許保護の喪失は、我々の業務財務状況、運営結果、および見通しに実質的な悪影響を及ぼす可能性がある。また、結果にかかわらず、訴訟は巨額のコストと管理資源の移転を招く可能性があり、これは私たちの業務や財務業績を損なう可能性がある
私たちの特許保護の獲得と維持は、政府特許機関によって提出された様々なプログラム、書類提出、費用支払い、および他の要求を遵守することに依存し、これらの要求に適合しなければ、私たちの特許保護は減少またはキャンセルされる可能性がある
発行された特許の定期維持費および年会費は、特許有効期間内にいくつかの段階で欧州特許庁、米国特許商標局、および外国特許機関に支払われる。欧州特許庁、米国特許商標局、各種外国政府特許機関も、特許出願過程において、いくつかのプログラム、文書、費用支払い、その他の同様の規定を遵守することを要求している。場合によっては、私たちは、私たちのパートナーに依存して、米国や同様の外国特許機関にこれらの費用を支払い、私たちの知的財産権に関するこのような要求を遵守するために必要な行動をとる。多くの場合、適用規則に従って滞納金を支払うか、または他の方法で不注意を是正することによって失効を是正することができるが、場合によっては、規定を遵守しないことは、特許または特許出願が放棄または失効され、関連法ドメインの特許権の一部または全部の喪失をもたらす可能性がある。特許または特許出願が放棄または失効される可能性のある規定を遵守しないイベントは、規定された期限内に公式行動に応答することができなかったこと、費用を支払わなかったこと、および適切に合法化されず、正式な文書を提出することを含む。もし私たちまたは私たちの許可者または協力パートナーが私たちの研究療法をカバーする特許および特許出願を維持できなかった場合、私たちの競争相手を含む第三者が類似または同じ療法または技術で市場に参入することができる可能性があり、これは私たちの業務、財務状況、運営結果、および将来性に大きな悪影響を及ぼすだろう
もし私たちがハッジ-ワックスマン修正案と似たような外国立法の保護を受けなければ、特許期間を私たちのすべての研究療法に延長すれば、私たちの業務は実質的な損害を受ける可能性がある
アメリカでは、すべての維持費を時間通りに支払うと、特許の自然失効時間は、通常、その最初の非臨時出願日から20年である。様々な延期があるかもしれないが、特許の有効期限とその提供される保護は限られている。我々の研究療法,その製造あるいは使用の特許が取得されても,特許有効期限が満了すると,競争療法からの競争に直面する可能性がある。新たな研究療法の開発,テスト,規制審査に要する時間を考慮すると,これらの候補や随伴療法の特許保護は,これらの候補や随伴療法の商業化前または直後に満了する可能性がある。したがって、私たちが持っている特許と許可された特許の組み合わせは、他の人が私たちと似ているか同じ治療法を商業化することを排除するのに十分な権利を提供してくれないかもしれない
FDAがCOMP 360および任意の将来の候補治療薬の発売を承認した時間、期限、および条件によると、私たちの1つ以上の米国特許は、1984年の“薬品価格競争および特許期限回復法”または“ハッジ-ワックスマン法案”およびEU同様の立法に従って限られた特許期間延長を受ける資格がある可能性がある。ハッジ·ワックスマン法は、製品開発、FDA規制審査中の有効特許期間の損失、および制御物質法案の発表に基づいて製品を制御する最終決定の補償として、承認された製品をカバーする特許を最大5年間延長することを可能にする。特許期間の延長は,製品が承認された日から14年間の余剰特許期間を超えてはならず,1つの特許しか延長できず,承認された薬物,その使用方法又はその製造方法に関する請求項を延長することしかできない。しかし,適用の最終期限内に出願を提出できなかったこと,関連特許の満了前に出願を提出できなかったことや適用の要求を満たしていなかったことなどにより延期が得られなかった可能性がある.しかも、延期の長さは私たちが要求したものより短いかもしれない。もし私たちが特許期間の延長を得ることができない場合、あるいはこのような延長の期限が私たちが要求しているよりも短い場合、私たちはその製品に対して特許権を行使することができる期限は延長されず、私たちの競争相手を含む第三者は私たちが予想していたよりも早く上場競争療法の承認を得ることができるかもしれない。したがって,適応療法からの収入は大幅に減少する可能性があり,我々の業務,財務状況,運営結果,見通しは実質的な被害を受ける可能性がある
知的財産権は必ずしも私たちの競争優位に対するすべての潜在的な脅威を解決できるとは限らない
私たちの知的財産権が提供する将来の保護の程度は不確定であり、知的財産権には限界があるため、私たちの業務を十分に保護できないか、あるいは競争優位性を維持することができるかもしれない。以下の例は例示的である
•他の人は、化合物を製造することができるか、または我々の研究におけるCOMP 360ヌードカバーキノコ療法と同じまたは同様のデジタル資産、任意の将来の候補治療レジメンおよびデジタル資産を開発することができるが、私たちが所有または制御する特許主張には含まれていない
•第三者の特許は私たちの業務に悪影響を及ぼすかもしれない
•私たちまたは私たちのライセンス者または任意の現在または未来のパートナーは、私たちが所有または制御している発表された特許または係属中の特許出願によってカバーされる発明を実施することを第1の構想または低減する人ではないかもしれない
•私たちまたは私たちのライセンス者または任意の現在または未来のパートナーは、私たちのいくつかの発明をカバーする特許出願を最初に提出した会社ではないかもしれない
•他の人は、私たちの知的財産権を侵害、流用、または他の方法で侵害することなく、類似または代替技術を開発したり、私たちの任意の技術を複製したりすることができる
•私たちが現在および未来に処理している特許出願は発行された特許を生成しない可能性がある
•私たちが所有または独占的に許可された発行された特許は、いかなる競争優位性も提供してくれないかもしれないし、第三者の法的挑戦によって無効または実行不可能と認定される可能性がある
•私たちの競争相手は特許権のない国で研究や開発活動を行い、これらの活動から学んだ情報を利用して競争力のある療法を開発し、私たちの主要な商業市場で販売するかもしれない
•私たちの療法または技術を使用して製造またはテストを行ってくれる第三者は、適切な許可を得ずに知らずに他人の知的財産権を使用する可能性がある
•他の特許を申請できる技術を開発することはできません
•いくつかの商業秘密またはノウハウを保護するために特許を出願しないことを選択することができ、その後、第三者は、そのような知的財産権をカバーする特許を提出するか、または同様の独自技術を他の方法で開発することができる。
これらの事件のいずれかが発生した場合、私たちの業務、財務状況、運営結果、および見通しに実質的な悪影響を及ぼす可能性がある
私たちは、私たちの従業員や私たちが彼らの知的財産権を流用したと主張したり、私たち自身の知的財産権の所有権を要求したりする第三者のクレームを受けるかもしれない
私たちの多くのコンサルタント、コンサルタント、従業員は、私たちの上級管理職を含めて、私たちの競争相手と潜在的な競争相手を含む他のバイオテクノロジーや製薬会社に雇われていた。その中には、従来の仕事に関する独占権、秘密、スポーツ禁止協定に署名した人もいる。私たちは、私たちのコンサルタント、コンサルタント、および従業員が、私たちのために働いているときに、その前の雇用主の固有情報またはノウハウを使用しないことを意図しているが、私たちまたはこれらの個人は、商業秘密または他の固有情報を含む任意のそのような個人の元雇用主の機密情報または知的財産権の使用または開示を告発される可能性がある。このような疑いに対抗するために訴訟を提起する必要があるかもしれない
もし私たちがこのようなクレームを起訴または弁護しなければ、金銭損害賠償の支払いに加えて、私たちは貴重な知的財産権や人員を失ったり、損害を受けたりする可能性がある。このような知的財産権は第三者に付与することができ、私たちの療法を商業化するためには第三者から許可を得る必要があるかもしれない。そのような許可は商業的に合理的な条項や根本的に存在しないかもしれない。このようなクレームの起訴や抗弁に成功しても、訴訟は巨額の費用を招き、私たちの経営陣の日常活動への注意を分散させる可能性がある
また、私たちの政策は、知的財産権の概念や開発に参加する可能性のある私たちの従業員と請負業者が合意に署名し、このような知的財産権を私たちに譲渡することを要求しているにもかかわらず、実際に私たちが自分の知的財産権と見なしているすべての当事者とこのような合意を実行することができないかもしれない。知的財産権の譲渡は自動的に実行されない可能性があり、あるいは譲渡協定が違反される可能性があり、私たちは第三者にクレームをつけさせられたり、私たちが私たちの知的財産権の所有権だと思うことを決定するために、私たちが提起する可能性のあるクレームを弁護したりすることができます。このようなクレームは、私たちの業務、財務状況、運営結果、および見通しに実質的な悪影響を及ぼす可能性があります
第三者の知的財産権は、私たちの研究療法を競争したり、商業化する能力に悪影響を及ぼす可能性がありますので、私たちは、私たちの研究療法を開発またはマーケティングするために、訴訟を提起したり、第三者からライセンスを取得したりすることを要求される可能性があります。そのような訴訟や許可証は費用が高いかもしれないし、商業的に合理的な条項では得られないかもしれない
私たちのビジネス成功は、私たちと私たちの将来の協力者が、第三者の知的財産権および独自の権利を侵害、流用、または他の方法で侵害することなく、私たちの独自の技術を開発、使用することができる、私たちと私たちの将来の協力者の開発、製造、マーケティング、および販売の能力に依存する。私たちはその中で運営される各市場が頻繁で広範な特許と他の知的財産権訴訟に直面していることを計画している。過去に、私たちは未来にCOMP 360または任意の未来の候補治療薬の知的財産権に対する抵抗性訴訟や訴訟の当事者になるか、またはこれらの訴訟の脅威になる可能性があるということに支配されてきた。もしこのような訴訟や訴訟の結果が私たちに不利なら、私たちの効果的な競争能力に影響を及ぼすかもしれない。
さらに、第三者に発行された特許または他の第三者知的財産権が、私たちの療法またはその要素、私たちの開発計画に関連する、COMP 360または任意の未来の候補療法の目標、または私たちの研究におけるCOMP 360ヌードカバーキノコ療法または任意の未来の候補療法の他の属性をカバーする場合、私たちの競争的地位は影響を受ける可能性がある。この場合、関連する第三者知的財産権を無効にするか、無効にするか、または知的財産権所有者と許可合意を達成できない限り、このような候補薬剤を開発または商業化することができない可能性があり、これらの合意は、商業的に合理的な条項または根本的に得られない可能性がある。このような研究療法や候補療法が承認された時点で特許が満了しておらず,特許所有者が侵害訴訟を起こしている場合,我々の研究療法や潜在的治療物質の製造や使用は関連特許の有効な主張を侵害していないと弁明せざるを得ないかもしれない。あるいは、もし私たちが法廷で発行されたすべてのアメリカ特許の有効性に挑戦するならば、私たちはすべてのアメリカ特許に添付された法的有効性推定を克服する必要があるだろう。これは、勝訴のために、特許請求の無効性について明確で納得できる証拠を提出する必要があることを意味する。これは他の管轄区域にも同じく適用される。第三者知的財産権主張に法的根拠がないと考えても,裁判所が侵害,有効性,実行可能性などの問題で我々に有利である保証はない, あるいは優先順位を考える。もし第三者が私たちにその特許を主張することに成功した場合、その第三者の特許が有効かつ強制的に実行可能であることが発見され、私たちの研究療法によって侵害される場合、私たちがこのような特許の許可を得ない限り、その許可は商業的に合理的な条項または全く存在しない可能性があり、そうでなければ、私たちの研究療法の継続または商業化を阻止されるかもしれない。同様に、我々が研究しているCOMP 360ヌードカバーキノコ療法の標的も、特許出願または標的のいくつかの態様またはその用途を有する特許を提出している他社研究のテーマである。このような特許が私たちに不利ではないという保証はなく、私たちがこのような第三者に許可を求める必要がないという保証もない。私たちは許容可能な条項でそのようなライセンスを得ることができないかもしれないし、全く得られないかもしれないが、どのような訴訟も高価で時間がかかるだろう。
私たちは失敗する可能性があり、未来にも失敗する可能性があり、私たちに不利になる可能性のある関連特許や出願を識別できない。例えば、2000年11月29日以降に提出されたいくつかの米国出願は、特許として発行されない限り、または特許として発行されない限り、出願に開示された発明がないことが前提であり、米国国外で提出された対応する出願の主題ともならないまで秘密にすることができる。一般に、米国および他の地方の特許出願は、優先権を要求する最初の出願の約18ヶ月後に発行され、この最も早い出願日は、一般に優先権日と呼ばれる。したがって、私たちの治療法に関する特許出願は、私たちが知らずに他の人によって提出されたかもしれない。また、私たちは競争の激しい分野で運営されており、私たちの限られた資源を考慮して、私たちの活発な分野のすべての特許出願を監視することは合理的ではない。さらに、公表された係属中の特許出願は、いくつかの制限された場合に、我々の療法または私たちの療法の使用をカバーするために、後で修正することができる
第三者知的財産権所有者は、我々の競争相手を含めて、既存または未来の知的財産権に基づいて、その是非曲直にかかわらず、積極的に権利侵害、流用または侵害クレームを提出する可能性がある。私たちはこのような侵害請求を成功的に解決したり、他の方法で解決できないかもしれない。もし私たちが
私たちが受け入れられる条項で将来のクレームを終わらせることに成功すれば、私たちは高価で予測不可能で時間のかかる訴訟を要求され、阻止されたり、私たちの治療法をマーケティングする上で重大な遅延に遭遇する可能性があります
もし私たちがこのようなクレームで弁護に失敗した場合、損害賠償の支払いを余儀なくされる以外に、私たちまたは私たちの許可された人は、私たちが権利侵害と認定された任意の研究療法を商業化することを一時的または永久的に禁止される可能性がある。可能であれば、私たちは、第三者の知的財産権をもはや侵害しないように、私たちの研究COMP 360ヌードカバーキノコ療法または任意の将来の候補療法を再設計することを余儀なくされるかもしれません。または、商業的に合理的な条項で提供されないか、または全く存在しない可能性がある許可を求めることができます。たとえ私たちまたは私たちの許可者や協力パートナーが許可を得ても、それは非排他的である可能性があり、それによって、私たちの競争相手が私たちまたは私たちの許可者または協力パートナーに許可された同じ技術にアクセスできるようにすることができ、これは、大量の許可および印税を支払う必要があるかもしれない。さらに、私たちが特許や他の知的財産権を故意に侵害していることが発見された場合、私たちは3倍の損害賠償と弁護士費を含む重大な金銭損害に責任があると判断される可能性がある。第三者の機密情報や商業秘密を盗用したと主張することは、当社の業務、財務状況、運営結果、見通しに類似した重大な悪影響を及ぼす可能性があります。これらのすべての事件は、私たちが最終的に勝っても、私たちが大量の財務と管理資源を移転する必要があるかもしれません。そうでなければ、私たちは私たちの業務に投入することができます
さらに、私たちまたは私たちの許可者またはパートナーの特許および特許出願によって提供される保護の広さまたは強度が脅かされている場合、会社が私たちと協力し、現在または将来の研究療法を許可、開発、または商業化することを阻止するかもしれない。さらに、知的財産権訴訟は大量の開示を必要とするため、このような訴訟の間、私たちのいくつかの機密情報は開示によって漏洩される可能性がある
知的財産権訴訟は、私たちに大量の資源を費やし、私たちの人員の正常な責任を分散させ、私たちの名声と私たちの業務運営を損なう可能性があります
解決策が私たちに有利であっても、知的財産権クレームに関連する訴訟や他の法的手続きは、巨額の費用を発生させ、私たちの技術や管理者の正常な責任を分散させる可能性があります。さらに、公聴会、動議、または他の一時的な手続きまたは事態の発展の結果が公表される可能性があり、証券アナリストまたは投資家がこれらの結果がマイナスであると考える場合、私たちの米国預託証明書の価格に大きな悪影響を及ぼす可能性がある。このような訴訟や訴訟は、私たちの運営損失を大幅に増加させ、開発や商業化活動に利用できる資源を減少させる可能性があります。私たちはそのような訴訟や法的手続きを適切に行うのに十分な財政的または他の資源がないかもしれない。私たちのいくつかの競争相手は、彼らの財政資源がはるかに大きいので、私たちよりもこのような訴訟や訴訟の費用を効果的に負担するかもしれない。さらに、知的財産権訴訟は大量の開示を必要とするため、このような訴訟の間、私たちのいくつかの機密情報は開示によって漏洩される可能性がある。特許訴訟または他の訴訟の開始と継続によって生じる不確実性は、市場での競争能力に重大な悪影響を及ぼす可能性がある
COMP 360または任意の将来の候補治療薬の必要な権利を買収およびライセンス内で取得または維持することに成功することはできないかもしれない
将来的に、私たちの手続きは第三者が持っている独占権を使用する必要があるかもしれませんが、私たちの業務の成長は、私たちがこれらの独占権を取得、許可、維持、または使用する能力にある程度依存するかもしれません。さらに、私たちが第三者と共同で所有している任意の特許については、このような特許におけるこれらの共同所有者の利益を許可する必要があるかもしれません。第三者からは入手できないかもしれませんが、COMP 360または任意の将来の候補治療レジメンに必要な任意の成分、使用方法、プロセス、または他の第三者知的財産権が考えられるかもしれません。第三者知的財産権の許可·買収は競争分野であり、一部のより成熟した企業は、魅力的または必要と考えられる第三者知的財産権許可または買収戦略をとる可能性がある。これらの老舗会社は私たちより競争優位を持っているかもしれません。それらの規模、現金資源及びより強い臨床開発と商業化能力のためです。しかも、私たちを競争相手と思っている会社は私たちに権利を譲渡したり許可したりしたくないかもしれない。研究療法やプロジェクトの開発に必要な第三者知的財産権の許可を得ることに成功しなければならない場合,この研究療法やプロジェクトの開発を放棄せざるを得ない可能性があり,我々の業務,財務状況,運営結果,将来性に大きな悪影響を及ぼす可能性がある
例えば,米国や外国の学術機関と協力し,これらの機関との書面合意に基づいて,われわれの臨床前研究や開発を加速する場合がある。通常これらの機関は私たちに選択肢を提供してくれます
協力によって生成された機関の技術的な任意の権利について交渉する。このようなオプションにかかわらず、私たちは指定された時間範囲内で、または私たちが許容できる条項の下でライセンスを交渉することができないかもしれない。もし私たちがそれができなければ、機関は知的財産権を他の側に提供する可能性があり、適用された研究治療や計画を継続する能力を阻止するかもしれない
もし私たちが第三者または第三者から知的財産権を許可する合意の下での義務を履行できなかった場合、または私たちとライセンシー、ライセンシーまたは協力者との業務関係が妨害された場合、私たちは私たちの業務に重要な知的財産権を失う可能性があります
私たちは第三者協定の当事者になっているか、あるいはこれらの合意に基づいて、私たちの業務に対して潜在的に重要な知的財産権を付与または付与されており、将来的に追加の許可または協力協定を締結する必要がある可能性が予想されます。我々の既存の第三者協定は,将来の許可協定は,治療開発や何らかのマイルストーンの実現に基づく印税や費用の支払いなどに関する様々な義務を規定していると予想される。また,我々のいくつかの協力協定により,このようなプロトコルで許可された療法と競合する療法の開発や商業化が禁止されている。もし私たちがこれらの合意の下で私たちの義務を履行できなかった場合、私たちの許可者またはパートナーは、そのような合意に含まれる任意の許可を含む合意を終了する権利があるかもしれない
任意の許可または協力プロトコルを終了するか、またはそのような許可プロトコルを十分に保護できないか、または協力することは、研究中のCOMP 360ヌードカバーキノコ療法またはプロトコルまたは許可知的財産権をカバーする任意の将来の候補療法を商業化することを阻止する可能性がある。例えば、私たちは、私たちが治療法を開発する際に使用するいくつかの知的財産権および独自材料の権利を付与する許可プロトコルに依存することができる。本プロトコルが終了すれば、私たちは商業的に合理的な条項、または類似の知的財産権および独自材料を他の源からタイムリーに許可することができず、私たちが研究しているCOMP 360ヌードカバーキノコ療法または任意の未来の候補療法の追加的な過渡的研究を要求される可能性があり、これは、私たちが研究しているCOMP 360ヌードカバー療法または任意の将来の候補療法の開発および商業化を延期するか、または他の方法でそれに重大な悪影響を及ぼす可能性がある
私たちの既存のいくつかのライセンスプロトコルは、知的財産権に関わる原始的な許可者ではない第三者からの従属ライセンスである。これらのプロトコルによれば、私たちは、知的財産権を適用する権利を取得する主なライセンスプロトコルの下での義務を私たちの許可者に履行しなければならず、私たちは、その権利のオリジナルライセンス者とは何の関係もないかもしれない。ライセンス者がこれらの上流ライセンスプロトコルの下での義務を履行できなかった場合、元の第三者ライセンス者は、元のライセンスを終了する権利がある可能性があり、これは、分割ライセンスを終了する可能性がある。このような状況が発生すれば、私たちは知的財産権を適用する権利をもはや持たなくなり、再許可の場合、関連する権利の所有者から私たち自身の直接許可を得ることができなければ、合理的なコストや合理的な条項でこれを行うことができなくなる可能性があり、これは、私たちの研究COMP 360ヌードカバー素療法または将来関連知的財産権に組み込まれる任意の候補療法の能力の開発と商業化に悪影響を及ぼす可能性がある
ライセンスや協力協定によると、知的財産権に関する紛争が発生する可能性がある
•プロトコルに従って付与された権利範囲および解釈に関連する他の問題;
•私たちの技術とプロセスは、合意に拘束されていないライセンス者またはパートナーの知的財産権をどの程度侵害しているか
•特許および他の権利は、任意の現在または未来の協力関係に従って再許可される;
•私たちは合意に基づいて勤勉な義務と、どのような活動がこれらの勤勉な義務を満たしているのか
•私たちのライセンス者および私たちおよびパートナーが知的財産権を共同で創造または使用することによって生成された発明およびノウハウの発明および所有権;
•特許技術発明の優先権。
また,我々の第三者プロトコルは複雑であり,このようなプロトコルのいくつかは様々な解釈の影響を受ける可能性がある.可能性のある契約解釈の相違は私たちの間に縮小されるかもしれません
または、関連協定の下での私たちの財務または他の義務を増加させることは、いずれも、私たちの業務、財務状況、運営結果、および見通しに重大な悪影響を及ぼす可能性があります。また、私たちが許可している知的財産権をめぐる紛争が、商業的に許容可能な条項で現在の許可手配の能力を維持していることを阻害したり、損害を与えたりすれば、影響を受ける候補治療薬の開発に成功し、商業化することができない可能性があり、これは、私たちの業務、財務状況、運営結果、および見通しに実質的な悪影響を及ぼす可能性がある
従業員や他の人と締結された秘密保持協定は、ビジネス秘密の漏洩を防ぐのに十分ではない可能性があり、他の固有情報を保護することもできない可能性がある
私たちは、独自のビジネス秘密、秘密のノウハウ、および非特許のノウハウが、私たちのビジネスに非常に重要であると考えています。私たちは、特に特許保護が価値が限られていると考えられる場合に、商業秘密または機密技術によって私たちの技術を保護する。しかし、商業秘密と機密技術は機密として維持することは難しい
このような情報が第三者や競争相手から開示されたり盗まれたりしないようにするために、私たちの政策は、私たちの従業員、コンサルタント、請負業者、コンサルタントが私たちと秘密協定を締結することを要求することです。しかし、私たちは私たちが私たちの商業秘密または機密技術に接触した可能性があるか、または接触したすべての当事者とこのような合意に到達したという保証はない。さらに、現従業員または元従業員、コンサルタント、請負業者、およびコンサルタントは、意図的に、または意図的に、私たちの競争相手および他の第三者に私たちの商業秘密および機密技術を漏らしたり、そのような合意に違反したりする可能性があり、私たちは、そのような違反について十分な救済措置を得ることができない可能性がある。第三者が商業秘密または機密技術を不正に入手して使用するという主張を実行することは困難であり、高価で、時間的であり、予測不可能である。秘密保持プロトコルの実行可能性は管轄地域によって異なる.さらに、競合他社または他の第三者が、当社の任意の商業秘密または機密ノウハウを合法的に取得または独立して開発した場合、競争相手または他の第三者が技術または情報を使用して私たちと競合することを阻止する権利はありません。これは、私たちの競争地位を損なう可能性があります。また,我々のビジネス秘密を守るための手順が不十分であると考えられれば,第三者による商業秘密の流用に対抗する十分な追跡権がない可能性がある.もし私たちの任意の商業秘密が競争相手または他の第三者に漏洩された場合、または競争相手または他の第三者によって独立して開発された場合、私たちの競争地位は実質的かつ不利な損害を受けるだろう
商業秘密または秘密を取得または維持できなかったノウハウ貿易保護は、私たちの競争的地位に悪影響を及ぼす可能性がある。また、我々の競争相手は、実質的に同等の独自情報を独立して開発することができ、さらにはこれらの情報について特許保護を申請することができる。もしこのような特許保護に成功すれば、私たちの競争相手は私たちの商業秘密や機密技術の使用を制限するかもしれない
もし私たちの商標と商号が十分に保護されていなければ、私たちは興味のある市場で知名度を作ることができないかもしれません。私たちの業務は悪影響を受けるかもしれません
私たちの登録または未登録商標または商号は、疑問、侵害、回避、または汎用商標として発表されるか、または他の商標を侵害していると認定される可能性がある。私たちはこれらの商標や商品名に対する私たちの権利を保護できないかもしれません。私たちは関心のある市場で潜在的なパートナーや顧客の知名度を確立するために必要です。もし私たちが私たちの商標と商号に基づいて名称を確立することができなければ、私たちは効果的に競争できない可能性があり、私たちの業務は不利な影響を受けるかもしれない。他のエンティティが異なる司法管轄区域で私たちの商標と類似した商標を使用したり、私たちの商標に対して優先的な権利を持っている場合、私たちが世界各地で現在の商標を使用することを妨害する可能性があります
私たちは世界各地で私たちの知的財産権を保護することができないかもしれないし、ある司法管轄区域で困難に直面する可能性があり、これはこれらの管轄区の知的財産権の価値を弱めるかもしれない
世界のすべての国と司法管轄区域で候補治療薬の特許を申請、起訴、擁護することは非常に高価になるだろうし、私たちはイギリスとアメリカ以外のいくつかの国の知的財産権にイギリスとアメリカの知的財産権が広くないかもしれません。権利はイギリスとアメリカで得られたと仮定しています。そのため、第三者がイギリスとアメリカ以外のすべての国で私たちの発明を実践したり、イギリスとアメリカや他の司法管轄地域で私たちの発明を使用して製造した治療法を販売したり、私たちの発明を使用して製造された治療物質を輸入したりすることは阻止できないかもしれません。しかも、私たちは付与される前に国と地域の特許出願を放棄することに決定するかもしれない。最後に、各国/地域特許の付与手続は独立した手続であり、これは、いくつかの法域において、出願が関連特許庁によって拒絶され、他の法域によって承認される可能性がある場合を招く可能性がある。同様に,国によっては,同じ候補療法や技術の特許保護範囲が異なる可能性がある
競争相手は、私たちが特許保護を受けていない司法管轄区域で、私たちと私たちの許可者またはパートナーの技術を使用して彼ら自身の治療法を開発することができ、また、他の侵害療法を私たちと私たちの許可者またはパートナーが特許保護を持っている地域に輸出することができるかもしれないが、法執行力はイギリスやアメリカに及ばない。これらの療法は、COMP 360または任意の将来の候補療法と競合する可能性があり、私たちと私たちの許可者またはパートナーの特許または他の知的財産権は、それらの競争を効果的にまたは阻止するのに十分ではないかもしれない
いくつかの司法管轄区の法律は知的財産権の保護程度はイギリスとアメリカの法律に及ばず、企業はこれらの司法管轄区の保護とこのような権利を保護する時に重大な困難に直面している。私たちまたは私たちの許可者が知的財産権の保護に困難に直面したり、他の理由でこれらの管轄地域の業務に重要な知的財産権を効果的に保護できない場合、これらの権利の価値は低下する可能性があり、私たちはこれらの管轄区域の他の人からの追加的な競争に直面する可能性がある
一部の国には強制許可法があり,これらの法律により特許権者は第三者に許可を強制的に付与される可能性がある。さらに、いくつかの国は、政府機関または政府請負業者に対する特許の実行可能性を制限している。これらの国では,特許権者の救済措置は限られている可能性があり,このような特許の価値を大幅に低下させる可能性がある。もし私たちまたは私たちの任意の許可者または協力パートナーが第三者に当社の業務に関連する任意の特許のライセンスを付与することを余儀なくされた場合、私たちの競争的地位が損なわれる可能性があり、私たちの業務および運営結果は悪影響を受ける可能性があります
私たちまたは私たちのライセンシーまたはパートナーが成功したかどうかにかかわらず、外国司法管轄区域で私たちと私たちのライセンシーまたはパートナーの特許権を強制的に実行することは、巨額のコストをもたらす可能性があり、私たちと私たちのライセンシーまたはパートナーの努力と注意を私たちの業務の他の側面から移し、私たちと私たちのライセンシーまたはパートナーの特許が無効または偏狭に解釈されるリスクに直面する可能性がある。さらに、このような訴訟は、私たちおよび私たちのライセンシーまたはパートナーの特許出願を発行できないリスクに直面させ、第三者が私たちまたは私たちのライセンシーまたはパートナーにクレームを提起する可能性がある。私たちまたは私たちのライセンシーまたはパートナーは、私たちまたは私たちのライセンシーまたはパートナーが起こしたいかなる訴訟でも勝訴しない可能性があり、判決された損害賠償または他の救済措置(ある場合)は商業的意味がない可能性がある。上記のいずれも、我々の業務、財務状況、経営結果及び見通しに実質的な悪影響を及ぼす可能性がある
私たちの第三者への依存に関するリスク
我々は第三者供給に依存してCOMP 360に含まれる裸蓋キノコおよび裸蓋キノコを製造し、将来任意の候補治療薬は第三者供給および製造に依存し続けることが予想され、承認されれば、これらの物質の商業供給のための第三者の生産に依存する。任意の第三者供給者がCOMP 360または将来の候補治療薬を生産する義務を履行できなかった場合、または満足できる法規遵守を維持または達成できなかった場合、そのような物質の開発および任意の療法の商業化は、(承認された場合)商業的に実行不可能であり、利益が低下するように停止、延期されるか、または私たちのための法執行行動につながる可能性がある
現在のところ、COMP 360または任意の将来の候補治療薬を製造するために必要なインフラまたは能力を得る計画もなく、そのような候補治療薬に組み込まれた裸蓋キノコおよび裸蓋キノコを含む計画もない。われわれは,我々の臨床試験で用いられている研究療法で使用されている裸蓋キノコや裸蓋キノコをCMOに依存して開発,製造していく予定であり,われわれの研究療法が承認されれば,このようなCMOに依存して任意の商業供給を開発,製造,生産していく。現在,我々はイギリスで複数の異なるCMOとCOMP 360に含まれるすべてのコンポーネントの開発,製造,生産に関する活動を行っている.CMOのような第三者サプライヤーに依存することは、COMP 360または任意の未来の候補治療薬を生産するよりも大きなリスクを直面させる。我々は、我々と契約したCMOの製造プロセスを制御せず、COMP 360または関連法規(例えば、FDAの良好な実験室実践、またはGLP、cGMPまたは米国以外の同様の法規要件)に従ってCOMP 360または任意の未来の候補治療薬を生産することに依存し、これらの法規は、品質管理、品質保証および記録および文書の維持を含むが、これらに限定されない。現在COMP 360生産過程に従事しているいくつかのサプライヤーは、私たちの現在の原料薬サプライヤーを含み、過去にFDAと/或いはEMAの検査を受けておらず、彼らがすべての適用法規に符合することを保証することもできない。私たちまたは第三者メーカーが適用された法規を遵守できなかったことは、罰金、禁止、民事処罰、遅延を含む私たちへの制裁を招く可能性があります, 許可の一時停止、免許取り消し、COMP 360の差し押さえまたはリコール、または任意の将来の候補治療薬、操作制限、および刑事起訴のいずれも、COMP 360または任意の将来の候補治療薬の供給に重大な悪影響を与え、私たちの業務および運営結果を損なう可能性がある。
もし私たちが意外な供給損失に遭遇した場合、または任意のサプライヤーがCOMP 360または任意の未来の候補治療薬に対する私たちの需要を満たすことができない場合、私たちの研究または計画における臨床研究または商業化は遅延する可能性がある。また,拡張活動中に品質の問題が生じる可能性がある.私たちは品質が受け入れられ、数量が適切で、コストが許容できる代替供給者を見つけることができないかもしれない。例えば、新冠肺炎の疫病は世界的に供給緊張をもたらした。また、私たちのサプライヤーは常に厳格な製造要件と厳しいテスト要件の制約を受けており、これは生産を制限または延期する可能性がある。必要であれば、メーカーやサプライヤーを交換するために必要な長い過渡期は、私たちの臨床研究や私たちの療法の商業化を大幅に遅らせる可能性があり、承認されれば、私たちの業務、将来性、財務状況、運営結果に大きな悪影響を及ぼすだろう
FDA、DEA、EMA、MHRAおよび他の類似外国機関の製造法規を遵守するために、私たちと私たちの第三者サプライヤーは、治療法が適用された規範と他の法規要件に適合することを保証するために、設計と開発、テスト、生産、記録保存と品質管理に多くの時間、お金と労力をかけなければならない。これらの要件を遵守しないことは、治療の没収および生産停止を含む、私たちに対する法執行行動をもたらす可能性があり、これらは、私たちの業務、将来性、財務状況、および運営結果に重大な悪影響を及ぼす可能性があります。私たちおよびこれらの第三者サプライヤーのいずれかも、FDA、DEA、EMA、MHRA、または他の同様の外国当局の監査を受ける可能性があります。もし私たちの任意の第三者サプライヤーがcGMPまたは他の適用可能な製造法規を遵守できない場合、私たちの開発と商業化治療の能力は深刻な妨害を受ける可能性がある。私たちは、火災、自然危険、破壊など、CMOのいかなる中断も、私たちの製造能力を深刻に中断する可能性があるため、限られた数のCMO固有のリスクに直面している。私たちは現在利用可能な災害復旧施設を持っていない。中断された場合、私たちは代替製造源を確立しなければならないだろう。これは私たちの多くの資金を必要とし、私たちは商業的に受け入れられる条項でこれらの資金を得ることができないかもしれないし、これらの資金を得ることができないかもしれないし、私たちは代替施設を建設したり探したりし、必要な規制承認を求めているので、数ヶ月の製造遅延を経験するかもしれない。もしこのような状況が発生したら、私たちは製造需要をタイムリーに満たすことができず、完全に満足できないだろう。また、どの新しい施設を運営することは、私たちの既存施設を運営するよりもコストが高いかもしれません, 業務中断保険は、私たちが発生する可能性のある損失を補償するのに十分ではないかもしれませんが、この場合、任意の中断の追加コストを負担しなければなりません。この場合,代替供給源の確立に伴い,われわれの臨床試験供給は著しく遅延する可能性がある。場合によっては、私たちの製品または候補製品を製造するために必要な技術スキルは、元のCMO固有または独自のものである可能性があり、困難に遭遇する可能性があり、またはそのようなスキルを予備または代替サプライヤーに譲渡することを禁止する契約制限が存在する可能性があり、またはそのようなスキルを根本的に譲渡できない可能性があります。また,我々が何らかの理由でCMOの交換を要求された場合,新たなCMOが品質基準とすべての適用法規に適合する施設やプログラムを保持していることを確認するように要求される.我々はまた、例えば比較可能な研究を製造することによって、任意の新しい製造プロセスが、以前にFDAまたは他の規制機関に提出された仕様に基づいて、私たちの候補製品を生産することを検証する必要がある。新しいCMO検証に関連する遅延は、私たちがタイムリーにまたは予算内で候補製品を開発したり、製品を商業化する能力に悪影響を及ぼす可能性があります。また,CMOはこのCMOが独立して持つ我々の候補製品の製造に関する技術を持つことができる.これは、私たちのこれらのCMOへの依存を増加させるか、または別のCMOが私たちの候補製品を生産するために、これらのCMOからライセンスを取得することを要求するだろう。また、製造業者の変化は、製造プロセスやプロセスの変化に関連することが多い, これは私たちが臨床試験で使用した以前の臨床供給と任意の新しいメーカーの臨床供給との間の架け橋研究を要求するかもしれない。臨床用品の比較可能性の証明には成功しない可能性があり,追加の臨床試験が必要かもしれない。
このような理由で、製造施設の重大な破壊事件は、私たちの財務安定を脅かすことを含む、私たちの業務に実質的な悪影響を及ぼす可能性がある
著者らは依存し、そして引き続き第三者に依存し、独立した臨床研究者、学術協力者とCROを含めて、著者らの臨床前研究と臨床試験を行う予定である。これらの第三者が彼らの契約義務を成功的に履行できない場合、または予想される最終期限までに完了することができない場合、私たちのCOMP 360ヌードカバーキノコ療法または任意の将来の候補療法に対する規制機関の承認を得ることができないか、または商業化することができず、私たちの業務は深刻な損害を受ける可能性がある
著者らはずっと独立した臨床研究者、学術協力者と第三者CROを含む第三者に依存し、引き続き第三者に依存することを計画し、著者らの臨床前研究と臨床試験を行い、そして著者らが行っている臨床前と臨床プロジェクトのためにデータを監視と管理する。私たちはこれらの方に依存して、私たちの臨床前研究と臨床試験を実行し、そして彼らの活動のいくつかの方面だけを制御する。しかし、私たちは私たちのすべての研究と実験が適用された議定書、法律と法規の要求、そして科学的基準に従って行われることを確実にする責任があり、私たちはこれらの第三者への依存が私たちの規制責任を免除しないだろう。私たちは第三者請負業者と
CROはGCP要求を遵守しなければならず,これらの要求はFDA,EMA,MHRAと類似した外国の規制機関がわれわれの臨床開発におけるすべての治療法に対して実行する法規とガイドラインである。規制当局は,試験スポンサー,主要調査者,試験地点を定期的に検査することでこれらのGCPを実行している。もし私たち、私たちの研究者、学術協力者、または私たちの任意のCROが適用されるGCPに従わなかった場合、私たちの臨床試験で生成された臨床データは信頼できないと考えられるかもしれません。FDA、EMA、MHRA、または同様の外国の規制機関は、私たちの上場申請を承認する前に追加の臨床試験を行うことを要求するかもしれません。特定の規制機関が検査を行った後、この監督機関は私たちのいかなる臨床試験がGCP規定に適合しているかどうかを確認することを保証することはできません。また,われわれの臨床試験はcGMP法規により生産された製品を用いて行わなければならない。私たちはこれらの規定を遵守できなかったか、あるいは私たちの第三者請負者とCROがこれらの規定を遵守できなかった場合、私たちは臨床試験を繰り返す必要があるかもしれません。これは規制の承認過程を延期し、民事と刑事罰に達する最高の法執行行動に直面させる可能性もあります
さらに、これらの研究者、学術協力者、およびCROは私たちの従業員ではなく、契約を除いて、私たちのCOMP 360ヌードカバーキノコ治療または任意の将来の候補治療および臨床試験に投入されるリソースの数を制御することはできません。もし独立した研究者、学術協力者、またはCROが私たちの研究COMP 360ヌードカバーキノコ療法または任意の未来の候補療法を開発するのに十分な資源を投入できなかった場合、または彼らの表現が目標に達していない場合、私たちの研究COMP 360裸蓋キノコ療法または私たちが開発した任意の未来の候補療法の承認および商業化の将来性を延期または影響する可能性がある。また、第三者サービス提供者を使用して、これらの側に独自の情報を開示することを要求することは、これらの情報が流用されるリスクを増加させる可能性がある。さらに、研究者、学術協力者、およびCROは、人員配置が困難であり、優先順位が変化したり、財務的ジレンマに陥ったり、または他のエンティティとの関係を確立したりする場合があり、その中のいくつかのエンティティは、私たちの競争相手である可能性があり、いずれも私たちの業務に実質的な悪影響を及ぼす
もし治癒されていない重大な違約が発生したら、私たちのCROは私たちとの合意を終わらせる権利がある。また、私たちの臨床試験に参加した被験者の安全が合意を終了する必要があることを合理的に証明できれば、債権者の利益のために一般的に譲渡するか、または清算されれば、私たちのCROのいくつかは私たちとの合意を終了することができる
我々の業務目標を実現するために必要な専門知識を専門的にあるいは持っている第三者サービスプロバイダの数は限られている.もし私たちがこれらの第三者CRO或いは臨床研究者とのいかなる関係も終了すれば、私たちは商業的に合理的な条項或いは他のCRO、学術協力者或いは研究者と手配を達成できないかもしれない。CRO、学術協力者、または臨床研究者が彼らの契約義務または義務を成功裏に履行できなかった場合、または予想された締め切り前に完了できなかった場合、または交換が必要である場合、または彼らが得た臨床データの品質または正確性が、私たちの臨床規程、規制要件または他の理由を遵守できなかった場合、私たちの臨床試験は延長、遅延または終了される可能性があり、私たちの研究用COMP 360裸蓋キノコ療法または任意の未来の候補療法に対する監督機関の承認または成功はそれを商業化することができないかもしれない。したがって、われわれの手術結果と我々の研究におけるCOMP 360ヌードカバーキノコ療法または任意の将来の候補療法のビジネスの将来性は損なわれ、私たちのコストは増加する可能性があり、私たちの創造能力は延期されるかもしれない
追加のCRO(または調査者)を交換または増加させることは、追加のコストに関連し、管理時間および重点を必要とする。また,新たなCROが作業を開始すると,自然過渡期に遅延が生じ,予想される開発スケジュールを満たす能力に実質的な影響を与える可能性がある。CROとの関係を慎重に管理しているにもかかわらず、将来的に同様の挑戦や遅延に遭遇しないこと、またはこれらの遅延や挑戦が私たちの業務や財務状況および見通しに実質的な悪影響を与えないことを保証することはできません
多くの第三者が私たちが提供したCOMP 360を使ってISSを行っている。一般に,我々はこれらのISSを支援せず,すべてのIISの調査結果の公開を奨励している.第三者が我々の研究におけるCOMP 360ヌードカバーキノコ療法の臨床開発上の義務または任意の将来の候補療法を履行できない場合、規制部門のCOMP 360の承認を得る能力を延期または弱める可能性がある。COMP 360のIISSまたは任意の将来の候補治療薬は、COMP 360の安全性または有効性の懸念を引き起こす臨床試験データを生成する可能性があり、IISSによって生成される任意のデータは、臨床試験を行っている人または適応の結果を予測することができないかもしれない。
多くの学術と個人非学術機関がCOMP 360に関連する臨床試験を行って賛助している。第三者によって開始されたIISSの設計または実施を制御することはなく、FDAまたは同様の外国の規制機関は、任意の1つまたは複数の原因(研究設計または実施の要素、セキュリティ問題、または他の研究結果を含む)に基づいて、これらのIISSが将来の臨床試験に十分な支援を提供できないと判断することができる。第三者調査者は動力不足のIISSを設計し、臨床端末を使用する可能性があります
我々自身が設計した臨床試験と比較して,広く受け入れられておらず,問題やより困難な項目,あるいは他の方法で臨床試験結果の負のリスクを増加させている。さらに、これらのIISS使用集団または適応は、より軽いまたは重い患者集団を含む、我々が後援する臨床試験またはIISSで使用されるものとは異なる可能性がある。私たちはまた、学術または私立非学術機関が情報を開示することを制御することができず、これらの当事者は、私たちの承認または同意を得ずに敏感な情報や研究結果を開示するかもしれない。
これらのIISSは第三者によって支援されているので、私たちは、私たち自身の規制届出を含む、アクセスおよび結果データの使用および参照能力を含むISSに関するいくつかの情報権を得る。しかし,ISSからのデータの時間や報告を制御することはできず,必ずしもISSからのデータを持ったり制御したりするとは限らない.IISSからの結果を確認または複製できなければ,あるいは陰性結果が得られれば,COMP 360や任意の将来の候補療法の臨床開発の推進をさらに延期または阻止する可能性がある。IISSによるいかなるデータも,われわれが臨床試験を計画している群や適応の結果を予測できない可能性がある。しかしながら、負のデータと考えられるいかなるものも、COMP 360ヌードカバーキノコ治療研究を進める臨床開発または任意の将来の候補治療の能力を損なう可能性があり、このような負の知覚されたデータがIISの設計および/または実施問題を反映しているかどうか、またはそれが実際に私たちの治療法の特徴を反映しているかどうかを調べることができないかもしれない。しかも、私たちは私たちの調査者たちと機関に依存して私たちにタイムリーな情報を提供してくれる。我々は,過去と将来にISSから報告可能な有害事象やSUSAR通知を受信することで遅延に遭遇する可能性がある.例えば,我々は2020年9月に通知を受け,チューリッヒ大学IISにおけるSUSARが数週間前に発生したが,現場調査員がこのような事件を直ちに報告する義務があったにもかかわらず。このような遅延や契約要求を提供できなかったいかなる情報も、私たちに否定的な影響を与えたり、適用される規制機関への要求の報告を遅延させたりする可能性があります。さらに進む, もし研究者や機関が我々のCOMP 360ヌードカバーキノコ治療または任意の将来の候補療法の臨床開発に対する彼らの義務に違反している場合、またはISSが私たちによって支援され、行われている場合に得られる可能性のある第一手の知識と比較して、データが十分でないことが証明された場合、私たち自身が将来の臨床試験を設計し、行う能力は不利な影響を受ける可能性がある。
さらに、FDAまたは同様の外国の規制機関は、これらのIISSによって生成された臨床前、製造または臨床データの参照権利の十分性、またはこれらのIISSの臨床前、製造または臨床データの解釈に同意しない可能性がある。もしそうであれば、FDAまたは他の同様の外国の規制機関は、追加の臨床前、生産、または臨床データを取得して提出することを要求し、その後、私たちの計画試験を開始することができ、および/またはこれらの追加データを受け入れない可能性があり、私たちの計画試験を開始するのに十分であるかもしれない。
私たちの業務運営、管理成長、従業員事務に関するリスク
大流行、流行病あるいは伝染病の爆発、例えば新冠肺炎の大流行は、私たちの臨床前研究、臨床試験、私たちが依存する第三者、私たちのサプライチェーン、私たちの資金調達能力、私たちの通常業務を行う能力、私たちの財務業績を含む、私たちの業務に実質的な悪影響を与えるかもしれない
私たちは新冠肺炎の大流行など公衆衛生危機に関連するリスクに直面している。新冠肺炎の大流行及び各国政府が新冠肺炎の大流行に対応するために実施した政策と法規--その大部分はすでに廃止された--直接と間接的に全世界の商業と商業に重大な影響を与えた。例えば、連合王国と米国の制限は一般的に廃止されたにもかかわらず、労働者不足やサプライチェーン制限のような他の間接的な影響は、依然として経済の様々な部分に影響を与えている。他の世界的な健康問題はまた、私たちまたは私たちと接触している第三者のいる国の社会、経済、労働力の不安定を招く可能性がある。
新冠肺炎の大流行は著者らの臨床前研究或いは臨床試験運営、著者らのサプライチェーンと製造及び著者らのオフィス業務運営の未来の影響程度は未来の発展に依存し、これらの発展は依然として非常に高い不確定性を持っており、例えば大流行の持続時間、他或いはより伝染性のある変種の出現、或いはコロナウイルス行動の制御と治療の有効性を自信に満ちて予測することができない。例えば,新冠肺炎の大流行開始時には,臨床試験における新患者の募集を中止した。将来、私たちはまた、サプライチェーンと運営の重大かつ実質的な中断、ならびにCOMP 360と任意の未来の候補治療薬の製造と供給に関する遅延を経験する可能性がある。将来の発展は本質的に予測が困難であり、患者をTRD或いは未来の臨床試験の3期試験に参加することを募集する時に困難に遭遇しないこと、あるいはコストを増加させることがないことを保証することはできず、予想された時間範囲内で研究の完全な登録を実現できることを保証することができず、あるいは供給中断が臨床前研究或いは臨床試験を開始と完成する能力に悪影響を与えないことを保証することはできない。
新冠肺炎の大流行も影響し、未来に著者らが臨床試験を行うことに依存する第三者CROの従業員に影響を与える可能性がある。新冠肺炎ウイルスの新しい変種が絶えず出現し、全世界に伝播するにつれて、私たちはもっと多くの中断を経験するかもしれません。これは私たちの業務と臨床試験に深刻な影響を与える可能性があります
医療資源の著者らの臨床試験からの移行、肝心な臨床試験活動の中断、監督管理機関の許可獲得における遅延、新冠肺炎の大流行への対応の一部として現地法規を変更する(これは臨床試験を行う方式を変更する必要があるかもしれない)、サプライチェーン中断と公開株式市場の持続的な変動、世界経済の中断などである。
新冠肺炎の大流行は、将来的に臨床試験活動のコストの高い遅延を招く可能性があり、これは、私たちの研究におけるCOMP 360裸蓋キノコ療法および任意の将来の候補療法が規制部門の承認を得て商業化する能力に悪影響を及ぼす可能性があり、承認されれば、私たちの運営費用を増加させ、私たちの財務業績に実質的な悪影響を与えるかもしれない。その他の要素以外に、新冠肺炎の疫病は過去にも公開株式市場の大幅な変動を招き、アメリカと世界経済に妨害を与えたことがある。変動的な増加と経済的混乱は、私たちがより有利な条件で資金を調達することを難しくするかもしれないし、根本的にそうではないだろう。新冠肺炎の疫病が私たちの業務と財務業績に悪影響を及ぼす程度については、本“リスク要素”の節で述べた多くの他のリスク、例えば、私たちの臨床試験の時間と完成、そして私たちが未来の融資を獲得する能力に関連するリスクを増加させる可能性がある。
私たちの将来の成長と効果的な競争の能力は、私たちの上級管理職の変動を管理する能力に依存し、私たちは重要な人員とより多くの合格者を募集する能力、そして私たちのパートナーが雇用するキーパーソンを維持します
私たちの成功は私たちの重要な管理、科学と技術者の持続的な貢献に依存しており、彼らの多くは私たちに助けを提供し、私たちの治療法と関連技術の面で豊富な経験を持っている。このような重要な管理者たちは私たちの取締役会のメンバーと特定の幹部たちを含む。私たちは現在どんな重要人物保険も持っていません。
2022年7月には、CEOと取締役会長職の分離を発表し、Kabir·ナートを新たなCEOに任命し、共同創業者のジョージ·ゴールドスミスを取締役会執行議長に任命しました。ゴールドスミスは2022年8月1日までCEOを務めています。ゴールドスミスは、2023年1月1日からさん取締役会非執行議長に移行。私たちが私たちの新しいリーダーシップに適応することと、私たちの新しいCEO(彼はこれまで上場企業のCEOの経験がなかった)が彼の役割と私たちの会社に完全に溶け込むにつれて、私たちは過渡期を持っています。指導部の交代は一般的に難しく、不確実性をもたらすだろう。もし私たちが今回の指導層の交代や未来の上級管理層のいかなる変動も管理することができなければ、私たちの企業文化にマイナスの影響を与える可能性があり、私たちと従業員、投資家、サプライヤー、CRO、主要な調査者、重要なオピニオンリーダー、監督機関と他の重要な利益関係者との関係に負の影響を与え、あるいは他の方法で私たちの業務運営を混乱させることは、私たちの業務と将来性に実質的な悪影響を及ぼす可能性がある。また、2021年末と2022年初めには、新たな首席財務官や総法律顧問の招聘、総裁·首席運営官の辞任など、他の上級経営陣の変動も行っている。また、これらの変化は、幹部チームの他のメンバー、重要なマネージャー、高級科学者への依存を増加させた。他の重要な幹部、マネージャー、高級科学者を失うことは私たちの研究開発活動を延期するかもしれない。また、私たちが競争の激しい製薬業で競争できるかどうかは、私たちが高い素質の管理職を誘致し、維持できるかどうかにかかっている, 科学技術者や医療従事者です私たちと適格な人材を競争している多くの他社や学術機関は、より多くの財務や他の資源、異なるリスク状況、および私たちよりも長い業界の歴史を持っています。したがって、経済的に受け入れられる条件で、私たちはこのような重要な人たちを引き付けたり維持することができないかもしれない。また,条件を満たす潜在的な従業員の中には,裸蓋キノコの治療法に否定的な見方をしたり,制御物質を用いた治療法に他の反対意見があったりするため,我々のために働かないことを選択する可能性がある。また、私たちがより多くのスキルを必要とする分野に拡張すれば、私たちの業務を発展させるために新しいマネージャーと合格した科学者を募集する必要があります。私たちはこれらのキーパーソンを引き付けることができず、目標を達成し、私たちの業務戦略を実施することを阻害する可能性があり、これは私たちの業務や将来性に実質的な悪影響を及ぼす可能性がある。
私たちは、特に販売とマーケティングの分野で、私たちの従業員数と業務範囲が大幅に増加することを予想しています。私たちが予想している将来の成長を管理するためには、私たちの管理、運営、財務システムを継続して実施し、改善し、私たちの施設を拡大し、より多くの合格者を募集し、訓練し続けなければならない。私たちの財力が限られているため、私たちは私たちの業務の拡張を効果的に管理できないかもしれないし、より多くの合格者を募集して訓練することもできないかもしれない。私たちの業務の拡張は巨大なコストを招き、私たちの管理と業務発展資源を移転する可能性があります。私たちの成長を支援するために成長を管理したり資金を調達できない場合は、私たちの業務計画の実行を延期したり、私たちの運営を妨害したりする可能性があります
また、ある重要な学術と科学者は私たちのパートナーの研究開発活動において重要な役割を果たしている。私たちの研究プロジェクトの開発に取り組んでいる重要な学術や科学者、私たちの研究COMP 360ヌードカバーキノコ療法、そして任意の未来の候補療法が私たちの協力から離れていれば
パートナー、私たちの研究計画の開発、私たちが研究しているCOMP 360ヌードカバーキノコ療法、および任意の将来の候補療法は延期されたり、他の方法で悪影響を受ける可能性があります。
IISSの従業員、独立請負業者、主要な調査者、機関と研究者、CRO、コンサルタント、サプライヤー、第三者治療サイト、セラピストとパートナー、および第三者は規制基準と要求およびインサイダー取引を遵守しないことを含む不当な行為または他の不適切な活動に従事する可能性があり、これは私たちの業務に重大な悪影響を与える可能性がある。
私たちは、IISSの従業員、独立請負業者、主要な調査者、機関と研究者、CRO、コンサルタント、サプライヤー、第三者治療サイト、セラピスト、およびパートナーが詐欺行為または他の不正活動に従事する可能性があるリスクに直面しています。これらの当事者の不正行為は、(I)FDA、EMA、MHRA、およびこれらの機関への真の、完全かつ正確な情報の報告を要求する法律を含む、故意、無謀、および不注意な行為、または不正な活動を含む可能性があり、(I)製造基準、(Iii)連邦および州データプライバシー、セキュリティ、詐欺および乱用、ならびに米国および海外の他の医療保健法律法規、または(Iv)真実、完全かつ正確な財務情報およびデータを報告することを要求する法律を含む。具体的には、医療業界の販売、マーケティング、および商業配置は、詐欺、不正行為、リベート、自己取引、および他の乱用行為を防止するための広範な法律法規によって制限されている。これらの法律法規は、広範な価格設定、割引、マーケティングおよび販売促進、販売手数料、顧客インセンティブ計画、および他のビジネス計画を制限または禁止する可能性があります。これらの法的制約を受けた活動はまた、臨床試験中に得られた情報の不適切な使用または虚偽陳述、または私たちの臨床前研究または臨床試験において虚偽データを作成することに関連する可能性があり、これは規制制裁を招き、私たちの名声に深刻な損害を与える可能性がある。
私たちの商業化モデルはまた、実際または告発されたセラピストの不適切な行為によって、私たちの第三者治療サイトと私たちの医療事故と専門責任クレームを提出するリスクをもたらす。我々と協力している第三者治療サイトが保険を受けている医療事故や専門責任クレームの金額は,我々の業務に伴うリスクに応じて適切であると考えられるが,成功した医療事故や専門責任クレームは,我々の保険カバー範囲や第三者治療サイトの保険カバー範囲を超えた巨額の損害賠償を招く可能性がある。また、職業責任保険は価格が高く、将来保険料は大幅に増加する可能性があり、特に私たちがサービスを拡大するにつれて。したがって、私たちのサプライヤーや私たちは将来許容可能な費用や完全に十分な専門責任保険を受けることができないかもしれない。私たちが提起した保険の全額にカバーされていないクレームは、高い抗弁コストを発生させ、私たちの巨額の損害賠償を招き、私たちの経営陣と私たちの第三者治療サイトの私たちの業務に対する注意を移動させる可能性があり、これは私たちの業務、財務状況、運営結果に実質的な悪影響を与える可能性がある。さらに、このようなクレームは、私たちの業務や名声に実質的な悪影響を及ぼす可能性がある。
従業員および他の第三者(私たちのセラピストを含む)の不適切な行為を常に識別し、阻止することができるわけではなく、そのような活動を発見し、防止するための予防措置は、未知または未管理のリスクまたは損失を効果的に制御することができないか、またはそのような法律または法規を遵守できないことによる政府の調査または他の行動または訴訟から私たちを保護することができない可能性がある。また、私たちは、起きていなくても、このような詐欺や他の不正行為を告発する可能性があるというリスクに直面している。もし私たちにこのような訴訟を提起し、私たちが私たちの権利を弁護または維持することに成功しなかった場合、これらの行動は、重大な民事、刑事および行政処罰、損害賠償、罰金、引き渡し、Medicare、Medicaidおよび他の米国連邦医療保健計画の外、監禁、追加の報告要件および監督に参加することから除外される可能性があります(もし私たちが会社の誠実な合意または同様の合意の制約を受けて、これらの法律に違反した疑い、他の制裁、契約損害、名声損害、利益減少、および将来の収益の減少および私たちの業務の削減を解決するために、私たちの業務および運営結果に重大な影響を与えるかもしれません)。いずれも私たちの業務運営能力と運営結果に悪影響を及ぼす可能性があります
私たちは激しい競争に直面しており、私たちの競争相手は私たちよりも早く、または成功的に治療法を発見、開発、または商業化することができ、これは私たちのビジネス機会を減少または除去するかもしれない。
製薬と幻覚薬業界の競争は激しく、迅速かつ重大な技術変革の影響を受けている。私たちの競争相手は多国籍製薬会社、大学、そして他の研究機関を含む。我々はまた,ウソナ研究所を含む501(C)(3)非営利医学研究組織からの競争に直面している。これらの非営利団体は、ヌードカバーキノコベースの製品を原価または無料で提供することを望んでいるかもしれませんが、これはCOMP 360の潜在的な市場を破壊しています。さらに、いくつかの営利生物技術会社または機関は、TRDを含む精神健康疾患を治療するために、裸蓋キノコの開発を専門に研究している。また、ますます多くの会社が
彼らは新しい幻覚化合物を発見するための努力をしている。幻覚製品の開発や精神健康疾患(うつ病など)の治療を求める会社数も増える可能性がある。もし私たちの競争相手が私たちの前に幻覚補助療法の秘密協定を獲得し、より広範な適応の承認を得て、それによってより広範な患者集団を獲得した場合、私たちはこのような潜在的幻覚補助療法からのより激しい競争に直面し、私たちの研究におけるCOMP 360ヌードカバーキノコ療法または任意の未来の候補療法の受け入れに市場を獲得する上でより大きな困難に直面するかもしれない。これらのリスクはすべて増加し,裸蓋キノコは自然に産生される物質であるため,特許保護を受けず,COMP 360の適切な代替品と考えられる可能性がある。
主要製薬,バイオ製薬,バイオテクノロジー社からの競争にも直面しており,これらの会社はMDDやTRDの治療のための非裸ゲラクチンや幻覚療法をすでに開発しており,将来的には我々の研究によるCOMP 360裸ゲラクチン療法による治療の他の適応を求める可能性のある競争にも直面するであろう。現在、多くの会社がうつ病治療のための製品または療法をマーケティングして販売しているか、またはSSRIsおよびセロトニンがノルアドレナリン再取り込み阻害剤を除去することができる抗うつ薬、またはSNRI、抗精神病薬、認知行動療法、またはCBT、エスタミンケトンおよびケタミン、反復経頭蓋磁気刺激、またはrTMS、電気ショック療法、ECT、迷走神経刺激、またはVNS、脳深部刺激、またはDBSなどの抗うつ薬を含むうつ病治療のための製品または療法が開発されている。多くの製薬、生物製薬、バイオテクノロジーの競争相手はすでに彼らの治療法のために市場を構築し、私たちよりも多くの財政、技術、人力、その他の資源を持っており、優れた製品や療法を開発、製造、販売することができるかもしれない。また、新しい治療物質の臨床前研究と人体臨床試験を行い、人類治療製品の監督管理許可を得る上で、多くの競争相手は私たちより多くの経験を持っている。したがって、私たちの競争相手は、代替または良質な製品に対するFDA、EMAまたはMHRAの承認に成功するかもしれない。また、多くの競争相手はより高い知名度とより広い協力関係を持っている。規模が小さく初期段階にある会社も重要な競争相手になる可能性があり、特に大手老舗会社との協力で手配されている
著者らが経営する領域の特徴は疾病生物学に対する理解が絶えず増加と変化し、絶えず変化する技術と強力な知的財産権が障壁に入り、多くの会社は新しい治療法と技術プラットフォームの創立、開発と商業化に参与した。私たちの競争相手は私たちの治療法よりも効果的で、便利で、応用が広く、コストが低い療法を開発するかもしれません。あるいはより良い安全性を持っているかもしれません。これらの競争相手は、彼らの療法を製造し、マーケティングする上で、私たちよりも成功しているかもしれません。さらに、私たちの競争相手が現在、または将来、我々が研究しているCOMP 360ヌードカバーキノコ療法または任意の将来の候補療法と同様またはより経済的に魅力的な技術および療法を開発しないことは保証されない。私たちと競争する代替療法または技術プラットフォームは、私たちの療法または技術プラットフォームよりも速いまたはより大きな市場受容度を得ることができ、競争相手の医学的進歩または迅速な技術発展は、私たちの研究COMP 360ヌードカバーキノコ療法または任意の未来の候補療法または技術プラットフォームをもたらす可能性があり、私たちの研究開発および商業化費用を回収することができる前に競争力がなく、あるいは時代遅れになる可能性がある。これらの会社と効率的に競争できなければ,我々の研究におけるCOMP 360裸蓋キノコ療法や任意の将来の候補療法を商業化することもできず,市場で競争的な地位を得ることもできないかもしれない。これは私たちの収益能力に重大で不利な影響を及ぼすだろう。著者らの競争相手はまた合格した科学、管理と商業人員を募集と維持し、臨床試験場所を確立し、臨床試験のために患者を登録する方面で著者らと競争している, 私たちの計画と補完的または必要な技術を得ることができます
新しい治療法の市場進出に伴い、激しい競争と日々の競争に直面することが予想される
買収と投資は経営困難、希釈、その他の有害な結果を招く可能性があり、私たちの業務、財務状況と経営結果に不利な影響を与える可能性がある。また、適切な事業を見つけて成功させることができなければ、私たちの経営業績や見通しが損なわれる可能性があります。
私たちは将来、従業員、補充会社、治療方法、製品、解決策、技術、または収入を増加させるために、より多くの買収や投資を行うかもしれない。このような取引は私たちの業務、財務状況、そして運営結果に大きな影響を及ぼすかもしれない。私たちはまた一連の潜在的な戦略取引について評価と討論を続ける予定だ。適切な買収または投資候補を決定することは困難であり、時間がかかり、高価である可能性があり、もしあれば、有利な条件で買収や投資を達成することができないかもしれない。買収された会社、業務、技術を統合し、私たちの将来の投資を管理する過程は、予見できない運営困難と支出をもたらす可能性がある。私たちが直面しているリスクの分野は
•買収された会社のキー社員を失ったことや、新入社員を私たちの文化に溶け込ませることに関する他の挑戦は、統合が成功しなければ、名声を損なうことになる
•管理時間と重点を経営業務から買収、統合、投資管理への挑戦に移す
•早期薬物発見と開発に従事する会社のいかなる投資に対しても高い不確実性があるが、概念は限られており、これは重大な投資損失を招く可能性があることを証明した
•デジタルヘルス市場の適切な投資機会を探す上での挑戦と、私たちがこの市場で経験が不足しているため、管理時間と資源を私たちの業務に移しています
•買収された任意の会社で制御、手続き、政策を実施または救済する
•買収された会社の合併業務、技術、技術プラットフォームおよび製品を統合して管理することは困難であり、予期される経済、業務および他の利益をタイムリーに実現することは困難であり、これは大量の費用および遅延または他の業務、技術または財務問題を招く可能性がある
•買収された会社の会計、人的資源、その他の管理システムを統合し、製品、工事、販売、マーケティング機能を調整する
•契約義務には、私たちに知的財産権を許可したり放棄したり、私たちの責任リスクを増加させることが必要な条項が含まれています
•得られた技術をさらに開発したり、私たちが予想していたビジネス戦略を実現することに成功しなかった
•知らない付属会社や買収された企業のパートナーに依存しています
•以前の経験が限られていたり経験のない市場に入ったり、競争相手がより強力な市場地位を持っている市場に入る不確実性
•投資や買収に関連した意外なコスト
•買収された会社の製品やサービスは商業的に成功できなかった
•買収した技術を既存のプラットフォームに移し、このような技術の安全基準を私たちの他の解決策と一致させることは困難である
•買収された企業に対する責任には、私たちに開示されていない、または私たちの推定を超えた責任が含まれているが、有効なデータ保護およびプライバシー制御を維持できず、適用された法規を遵守できなかったことによる責任に限定されない
•私たちの内部基準、制御プログラム、政策を維持することはできない
•買収に関連した予想された財務結果をタイムリーに達成できなかったか、または全く生じなかった
•反独占や他の政府法規を守ることは困難である
•買収された会社の財務諸表の統合と監査で直面している課題は、歴史的に米国公認会計基準に従って財務諸表を作成していない
•潜在会計費用とは、商業権のような買収に関連する無形資産を指す
•商標、顧客関係、または知的財産権は、後に減値として決定され、減額される
•買収取引の影響を正確に予測できなかった。
さらに、私たちは、知的財産権の創造、所有権および権利、オープンソースコードの存在、および法律および契約要件の遵守に関する陳述および保証を含む、買収された会社または戦略的パートナーの売り手が提供する陳述および保証に深刻に依存する可能性がある。これらの陳述および保証のいずれかが不正確または違反された場合、このような不正確または違反は、契約時間制限および責任制限の一部であり、これらの訴訟および責任評価は、そのような売り手に十分な追跡を行うことができない可能性がある。
将来の買収と投資はまた、大量の現金支出、株式証券の希釈発行、債務の発生、私たちの業務の制限、あるいは負債、償却費用、営業権の解約を招く可能性があり、これらはいずれも私たちの財務状況を損なう可能性がある。さらに、私たちが発表した任意の買収または投資は、パートナー、従業員、サプライヤー、患者、株主、または投資家の負の影響を受ける可能性がある。
また、私たちの業界内での事業、技術、資産の買収競争はさらに激しくなる可能性があります。私たちが達成したい買収や投資を決定することができても、商業的に合理的な条項で買収や投資を達成できない場合があり、あるいは目標が別の会社に買収される可能性がある。私たちは最終的に未完成の買収や投資について交渉するかもしれない。このような交渉は管理時間の移転と大量の自己負担費用をもたらす可能性がある。買収や投資の評価や実行に成功できなければ、これらの買収や投資のメリットを実現できない可能性があり、私たちの経営業績が損なわれる可能性があります。もし私たちがこのようなリスクのいずれにもうまく対応できなければ、私たちの業務、財務状況、そして運営結果は損害を受ける可能性がある。
もし私たちの名声とブランド認知度を維持して高めることができなければ、私たちの業務、財務状況と経営結果は損害を受けるだろう。
私たちの名声とブランド認知度を維持し、向上させることは、既存および未来の第三者治療サイト、セラピスト、患者、および協力者との関係を維持するために重要であり、診療所が治療を提供する第三者治療サイトになる能力を誘致するためにも重要であると信じている。私たちのブランドを普及させる必要があり、引き続き大量の投資が必要になる可能性があり、私たちの市場競争がますます激しくなるにつれて、これらのマーケティングや他の措置はますます難しくなり、高価になる可能性があると予想しています。ブランド普及とマーケティング活動は成功しないか、収入増加をもたらす可能性があり、私たちの未来に生じるいかなる収入についても、これらの活動によって生じる将来の収入増加の程度は、増加した収入は私たちが発生した費用を相殺できない可能性があり、私たちの業務、財務状況、運営結果は損害を受ける可能性がある。さらに、私たちまたは私たちの経営陣の名声を低下させる要素は、私たちの第三者治療サイト、セラピスト、および患者ネットワークの期待を達成できなかったことを含めて、私たちの名声とブランドを損なう可能性があり、新しい第三者治療サイト、セラピスト、および患者を引き付けることをより難しくしている。もし私たちが私たちの名声とブランド認知度を維持、保護、あるいは高めることに成功しなければ、私たちの業務は増加できないかもしれません。私たちは第三者治療サイト、セラピスト、患者との関係を失うかもしれません。これは私たちの業務、財務状況、そして運営結果を損なうことになります。
私たちの現在と潜在的な未来のデジタル技術は成功しないかもしれませんが、これは私たちの業務、財務状況、運営結果に悪影響を及ぼすかもしれません。
我々は現在,デジタル技術を用いてデータを収集し,患者やセラピストを教育し,デジタル表現型情報を収集し,人工知能を利用している。私たちの研究をデジタル技術に拡張して、私たちの現在または未来の研究療法を補完し、強化し、科学技術会社や他の第三者と協力して、新しい技術を獲得したり開発したりする可能性があります。私たちがこれらの技術を開発または獲得する努力は、大量の時間、コスト、および他の資源に関連し、私たちの戦略を実行する他の重要な要素に集中しないように、私たちの管理チームの注意を分散させる可能性がある。もし私たちがこれらのデジタル技術を開発または取得する努力が成功しなければ、私たちの業務、将来の見通し、財務状況に実質的な悪影響を及ぼす可能性がある。
私たちの現在または未来のデジタルテクニカルソリューションは、私たちの業務、患者、医療専門家、セラピスト、第三者治療サイトおよび協力者に関連する敏感な情報を漏洩するか、または私たちが重要な情報にアクセスすることを阻止し、私たちに責任を負わせる可能性があり、これは私たちの業務と私たちの名声に悪影響を及ぼすかもしれない。
私たちの現在および将来のデジタル技術解決策は、保護された健康情報(PHI)および他のタイプの個人データまたは個人識別情報(PII)を含む敏感なデータの収集、記憶、使用、または開示に関することができる。例えば,われわれの臨床試験の一部として,デジタル技術ソリューションを用いて治療過程を記録·分析することが可能である。私たちはまた、敏感な情報を処理して格納し、他の第三者を使用して、当社および当社の第三者パートナーの知的財産権および他の独自のビジネス情報を含む敏感な情報を処理して格納することも可能です。
我々はまた、これらの重要な情報を安全に処理、送信、および格納するために、インターネットおよび外部クラウドプロバイダを含む情報技術ネットワークおよびシステムに高度に依存する可能性がある。物理的または電子的侵入、コンピュータウイルス、ハッカー攻撃および同様の破壊、ならびに従業員または請負業者のミス、不注意または汚職を含むセキュリティイベントまたはこのインフラストラクチャの破壊は、システムの中断、閉鎖、または機密情報の不許可開示または修正をもたらし、患者の健康情報が不正にアクセス、取得または変更され、または公開利用可能になる可能性がある。また,我々が使用しているいくつかのシステムは機械学習システムに依存しており,これらのシステムは複雑であり,検出しにくい誤りや不足がある可能性がある.これらの機械学習システムは
無意識に私たちのシステムの効率を低下させたり、不正確、私たちの業務目標に符合しない、私たちの政策に符合しない、あるいは私たちの指導原則と使命と一致しない意外あるいは意外な出力を招く可能性がある。私たちのシステムやデータで発見されたどんなミスや抜け穴も、私たちの名声が損なわれたり、損害賠償責任を負う可能性があります。これらは、私たちの成長の見通しと私たちの業務に悪影響を及ぼす可能性があります。
我々は,第三者サービスプロバイダを用いて患者情報や他の機密および敏感な情報を収集,記憶,転送し,静的および転送中のデータを暗号化し,適切なシステムログおよびアクセス制御を行うため,重大なネットワークセキュリティリスクを持つ機能を第三者に依存して管理する.我々は、これらのリスクに対応するためのいくつかの行政および技術保障措置を講じており、例えば、患者の情報処理を処理または下請けするアウトソーシング請負者のための合意締結を要求し、契約義務に基づいて、これらの請負者および任意の下請け業者に、PHI、他のPII、および他の敏感な情報を保護するための合理的な努力を要求する。我々のシステム、下請けのシステムまたはPHI、他のPII、または当社または下請けが処理または維持する他の敏感なデータを保護するための措置は、そのような情報の収集、格納、および送信に関連するリスクから私たちを十分に保護できない可能性がある。私たちは、不正なアクセスまたは開示から機密および他の敏感な情報を保護するための措置を取っているが、私たちの情報技術およびインフラは、第三者の操作、従業員の不注意またはエラー、汚職または他の中断による故障または侵入のために、ハッカーまたはウイルスの攻撃を受けやすい可能性がある。
セキュリティホールやプライバシー侵害は、患者情報の開示または不正使用または修正、またはPHIまたは他のPIIを含む患者情報(PHIまたは他のPIIを含む)または私たちの下請け業者に影響を与えることを阻止し、または他の方法で処理された他の敏感な情報の機密性、安全性または完全性をもたらし、私たちの名声を損なう可能性があり、違反通知法の遵守を強要し、修復、罰金、処罰、個人の通知、およびシステムまたは技術の修復または交換を目的とし、将来発生することを防止するための措置において重大なコスト、潜在的な保険料を増加させ、データベースの内容の正確性を検証し、コスト増加または収入を損失させることを要求する。もし私たちがこのようなセキュリティホールやプライバシー侵害を防ぐことができない場合、あるいは満足できる救済措置を実施できない場合、あるいはそれができないと思われる場合、私たちの運営は中断される可能性があり、私たちはデジタル技術解決策とツールを提供できない可能性があり、私たちの臨床試験を行う能力は、患者が臨床試験に参加することと、私たちの臨床試験のためにセラピストを募集することを含む負の影響を受ける可能性があり、私たちは名声損失、患者、医師、臨床試験場所と投資家の信頼への悪影響、財務損失、政府調査または他の行動、規制または契約処罰、および他のクレームと責任を受ける可能性がある。さらに、セキュリティホールおよび情報への他の不適切なアクセス、取得、または処理は、そのようなイベントを決定すること、またはそのようなイベントを提供する任意の通知に関するいかなる遅延も、より大きな被害をもたらす可能性がある。
我々のシステムまたは任意の第三者情報技術パートナーの任意のそのような侵入または中断は、私たちのネットワークまたはデータセキュリティプロセスに危険を及ぼす可能性があり、敏感な情報は、アクセスできないか、または許可されていない当事者によってアクセスされる可能性があり、公開され、開示され、紛失され、または盗まれる可能性がある。このような任意の情報アクセス中断、不適切または許可されていないアクセス、開示、または他の情報損失は、法的クレームまたは訴訟、患者情報または他の個人情報のプライバシーを保護する法律および法規(例えば、HIPAA、GDPR、CCPA)によって負担される責任、および規制処罰をもたらす可能性がある。
許可されていないアクセス、紛失、または伝播は、COMP 360ヌードカバーキノコ療法または任意の将来の候補療法の臨床試験を行い、COMP 360ヌードカバーキノコ療法または任意の将来の候補療法の認可を受け、それを商業化し、研究および開発活動を行い、会社の財務情報を収集、処理し、準備し、現在および将来の候補療法に関する情報を提供する能力を含む、私たちの運営を混乱させる可能性もある。このような情報漏洩は、当社のビジネス秘密や他の独自情報の漏洩、またはその情報を維持する第三者の情報漏洩をもたらす可能性もあり、これは私たちの業務および競争地位に悪影響を及ぼす可能性があります。特定のセキュリティやプライバシー損害やクレーム費用に保険を提供していますが、すべての責任を補償するのに十分な保険に加入したり維持したりすることはできませんし、いずれの場合も、保険範囲はセキュリティ事件による名声被害を解決しません。
私たちの現在の業務本部は1つの場所に設置されており、私たちまたは私たちが依存している第三者は、自然災害や内乱発生の悪影響を受ける可能性があり、私たちの業務連続性と災害復旧計画は、地震、病気の発生、または他の自然災害など、深刻な災害の影響から私たちを十分に保護できないかもしれません。
私たちの現在の業務運営本部はイギリスロンドンの事務所にあり、ニューヨークとアメリカサンフランシスコに事務所を設置しています。洪水、火災、爆発、地震、極端な天気、医療疫病、電力不足、通信故障などの突発事件あるいはその他の自然、人為事故、事故が発生した
私たちの施設や私たちの第三者契約メーカーの製造施設を十分に利用できないという内乱事件を含めて、私たちの業務運営能力に実質的な悪影響を及ぼす可能性があり、特に日常生活において、私たちの財務や運営状況に大きなマイナス影響を与える可能性があります。これらの施設を使用できないことは、コスト増加、我々の研究COMP 360ヌードカバーキノコ療法の開発遅延、または任意の将来の候補療法、または私たちの業務運営中断を招く可能性があります。このような自然災害は、私たちの運営をさらに混乱させ、私たちの業務、財務状況、運営結果、見通しに実質的で不利な影響を及ぼす可能性がある。自然災害、停電、または他の事件が発生した場合、本社の全部または大部分を使用することができなくなり、私たちの研究施設や私たちの第三者契約メーカーの製造施設のような重要なインフラを破損したり、他の方法で運営を中断したりすることは難しいかもしれません。場合によっては、かなり長い間私たちの業務を継続することはできません。新冠肺炎の大流行に関連するリスクについては、“を参照されたい大流行、流行病あるいは伝染病の爆発、例えば新冠肺炎の大流行は、私たちの臨床前研究、臨床試験、私たちが依存する第三者、私たちのサプライチェーン、私たちの資金調達能力、私たちの通常業務を行う能力、そして私たちの財務業績を含む、私たちの業務に実質的な悪影響を及ぼすかもしれません.”
深刻な災害や同様の事件が発生した場合、我々の既存の災害復旧および業務連続計画は十分ではないことが証明される可能性がある。私たちの災害復旧と業務連続計画の限られた性質のため、私たちは大量の費用を発生する可能性があり、これは私たちの業務に実質的な悪影響を及ぼす可能性があります。私たちのリスク管理政策の一部として、私たちは私たちの業務に適していると思うレベルに保険範囲を維持します。しかし、これらの施設で事故や事故が発生すると、私たちはどんな損害や損失を補うのに十分な保険金額を確保することができません。もし私たちの工場や私たちの第三者契約メーカーの製造施設が事故や事件あるいは他のいかなる理由でも作動できなければ、短い時間であっても、私たちのいかなる研究開発プロジェクトも損害を受ける可能性があります。
ソーシャルメディアプラットフォームの使用はますます多くなり、新たなリスクと挑戦をもたらしている。
ソーシャルメディアは、私たちの臨床開発計画や、私たちが研究しているCOMP 360ヌードカバーキノコ療法または任意の将来の候補療法を交流するために使用されるようになってきており、COMP 360または将来の候補療法(あれば)が承認された後、私たちの研究COMP 360ヌードゲラクチン療法の商業化努力で適切なソーシャルメディアを使用することができるかもしれない。バイオ製薬業界のソーシャルメディア実践は引き続き発展しており、このような使用に関する法規や監督指導も発展しているが、常に明確ではない。この変化は、不確実性と、私たちの業務に適用される法規を遵守しないリスクをもたらし、私たちに対する規制行動と、いくつかの禁止された活動に関連する可能性のある訴訟を引き起こす可能性がある。例えば、患者は、進行中の臨床試験における彼らの経験をレビューするために、ソーシャルメディアチャネルを使用して、いわゆる有害事象を報告することができる。このような開示が発生した場合、以下のリスクがある:試験登録が悪影響を受ける可能性がある;私たちは適用される有害事象報告義務を監視し、遵守することができない;ソーシャルメディアによって生じる政治的および市場的圧力に直面して、私たちは私たちの業務または公衆の合法的な利益を守ることができないかもしれない。これは、私たちの研究COMP 360ヌードカバーキノコ療法または任意の未来の候補療法に対する発言が制限される可能性があるからである。いずれのSNSにおいても、敏感な情報または否定的または不正確な投稿またはコメントを不適切に開示するリスクがある。もしこのような事件が発生したり、私たちが適用された法規を遵守できなかった場合、私たちは責任を負い、規制行動に直面したり、私たちの業務に他の損害を与える可能性があります。
アメリカの預託証券の所有権に関連するリスクは
私たちのアメリカ預託証明書の市場価格はずっと変動し続けている可能性があります。あなたは投資の全部または一部を失うかもしれません
私たちのアメリカ預託証明書の市場価格はずっと高度に変動し続ける可能性があり、本節で議論したリスク要素と私たちがコントロールできない他の要素によって大幅に変動する可能性があります
•私たち、戦略的パートナー、または競争相手のテストおよび臨床試験の陽性または陰性結果
•第3段階の臨床計画を完成させる時間は
•我々の研究COMP 360ヌードカバーキノコ療法または任意の将来の治療候補薬の開発または商業化に関連する戦略的協力関係を遅延させる;
•私たちに有利と思われない条項で戦略関係に入る
•競争相手の技術革新やビジネス治療の導入
•政府の規制や医療支払い制度の変化
•特許と訴訟を含む専有権の発展について;
•私たちが研究している任意のCOMP 360ヌードカバーキノコ療法または任意の将来の候補療法の商業的価値または安全性に関心を持っている
•裸蓋キノコ療法は治療法として否定的に宣伝または認知されている
•資金調達や他の会社の取引
•証券や業界アナリストの研究報告書やコメントを発表する;
•私たちのアメリカ預託証券のナスダックでの取引量は
•私たち、私たちの上級管理職のメンバーと取締役、または私たちの株主が私たちのアメリカの預託証明書を売却したり、将来このような売却が起こる可能性が期待されています
•製薬業界や経済全体の一般的な市場状況
•最近の米国、イギリス、欧州のインフレ率の大幅な上昇、マクロ経済状況およびロシアとウクライナ間の衝突や類似事件などの要因による米国やイギリスの全体的な市場変動、および一般的な経済、政治、地政学的および市場状況
•他の事件と要素、その多くは私たちがコントロールできない。
近年,株式市場,特に製薬やバイオテクノロジー会社の株は,価格や出来高の変動を経験することがあり,これらの変動は影響を受けた会社の経営業績に関係なくあるいは比例しないことが多い。さらに、製薬やバイオテクノロジー株式市場またはより広範な株式市場が投資家信頼の喪失を経験し続ける場合、私たちの米国預託証券の取引価格は、私たちの業務、財務状況、または運営結果とは無関係に低下する可能性がある。我々の米国預託株式が初公開株で米国預託株式あたり17.00ドルで販売されて以来、米国預託株式価格は大幅に変動しており、2020年9月18日、つまりナスダック世界市場に上場した初日から、2022年12月31日まで、期間中のディスクは6.54ドル、ディスク高は61.69ドルとなっている。もし私たちのアメリカ預託証明書の市場価格があなたがそれらを購入した時の価格を超えていなければ、私たちの投資では何の見返りも達成できず、あなたの投資の一部または全部を失う可能性があります
我々の役員、取締役、いくつかの重要株主は、私たちの相当数の普通株式(米国預託証明書に代表される普通株を含む)を持っているので、株主投票の結果を含めて、私たちに支配権を行使することができるかもしれません。私たちのいくつかの役員と上級管理者はその中の一人の株主の権益を持っています。これらの株主は私たちまたはあなたの権益とは違うかもしれません
我々の2022年12月31日までの発行済み普通株によると、私たちの役員、取締役、5%以上の株主とその関連会社の実益は、約47%の普通株とアメリカ預託証明書を持っています。当社の株主総会に出席する人数に応じて、当該等株主は単独又は集団投票にかかわらず、当該等の株主総会が決定した結果を決定又は顕著に影響することができる。50%以上の株主を制御し、当社の株主総会で投票する株主或いは株主団体は、取締役会のメンバーの委任、いくつかの当社の資本構造に関連する決定、いくつかの重大な会社の取引の承認及び当社の定款の改訂を含む簡単な多数の可決を必要とする株主決議案を制御することができる。他の結果を除いて、このような所有権集中は、私たちの株主が株主としての最良の利益に合致すると考える能動的な買収提案を阻止または阻止する可能性がある。その中のいくつかの個人または実体は私たちの他の株主とは違う利益を持っているかもしれない。例えば、これらの株主の多くは、私たちの最初の公募時に米国預託証明書を売却する価格よりもはるかに低い価格で普通株を購入しているため、彼らは普通株を持っている時間が長く、他の投資家よりも私たちの会社を買収者に売却することに興味を持っているかもしれないし、他の株主の利益から離れる戦略をとることを望んでいるかもしれない。
私たちは現在予測可能な未来に普通配当金を支払うつもりがないので、資本付加価値(あれば)があなたの唯一の収益源になり、あなたの投資は永遠に見返りを得られないかもしれません
イギリスの現行法律によると、会社の累計実現利益は、その累積達成損失(非合併ベース)を超えて、配当金を発表し、支払うことができる。したがって、配当金を発表して支払う前に、私たちは分配可能な利益を持っていなければならない。私たちは過去に私たちの普通株に配当金を支払ったことがない。私たちは収益を維持して、私たちの業務のために、予測可能な未来に現金配当金を支払わないつもりです。したがって、予測可能な未来に、私たちのアメリカ預託証明書の資本増加(あれば)があなたの唯一の収益源になり、もしあなたが購入した時の価格であなたのアメリカ預託証明書を売ることができない場合、あなたの投資は損失を受けることになります。私たちの取締役会のいかなる配当提案も、私たちの財務状況(繰越赤字を含む)、経営業績、法律要求、その他の要素を含む多くの要素に依存するだろう。予測可能な未来に、私たちは配当金や他の分配を支払うことはあまりできない。もし私たちのアメリカ預託証明書価格が私たちが配当金を支払う前に下落すれば、あなたの投資は損失を受けますが、この損失は未来の潜在的な現金配当金によって部分的にまたは完全に相殺されません。
証券又は業界アナリストが我々の業務に関する研究報告を発表し続けない場合、又は不正確又は不利な研究報告を発表しなければ、我々の米国預託証明書の価格及び取引量が低下する可能性がある
私たちのアメリカ預託証券の取引市場は、証券や業界アナリストが発表した私たちまたは私たちの業務に関する研究と報告にある程度依存しています。私たちはこのようなアナリストを統制できない。私たちの1人以上のアナリストを追跡して私たちのアメリカ預託証明書の格付けを引き下げたり、私たちの業務に関する不正確または不利な研究報告を発表したりすれば、私たちのアメリカ預託証明書の価格は低下する可能性がある。これらのアナリストのうちの1人以上が私たちの会社の報道を停止したり、私たちに関する報告書を定期的に発表できなかったりすれば、私たちのアメリカ預託証明書に対する需要が減少する可能性があり、これは私たちのアメリカ預託証明書の価格や取引量を低下させる可能性がある
私たちのアメリカ預託証明書の所有者は、私たちの普通株式所有者と同じ投票権を持っていないであろうし、投票材料を受け取っていないかもしれないし、イギリスの会社法(2006年イギリス会社法または2006年会社法を含む)によって、彼らの投票権をタイムリーに行使するために、私たち株主に提供される他の文書を必要としているかもしれない。
預金協定に記載されている以外に、米国預託証明書所持者は、米国預託証明書に代表される普通株に付属する投票権を行使することができない。預金管理協定は、吾等の普通株式保有者の任意の会議の通知を受けた後、信託銀行は、投票権行使について指令を出す権利がある米国預託株式保有者を特定するために記録日を指定することを規定している。我々の要求に応じて,委託者は,(I)我々が発行した会議通知又は同意又は依頼を求めること,及び(Ii)所持者が指示を出す方法に関する声明を記録日に所持者に配布しなければならない。米国預託株式保有者が直ちに投票材料を受け取ることは保証されず、米国預託証明書に関連する普通株への投票を信託機関に指示できることを保証することはできない。
そうでなければ、米国預託株式保有者は、保有する米国預託証券に関する普通株を撤回しない限り、投票権を行使できないだろう。しかし、米国預託株式の保有者はこの会議を長く前に知らない可能性があるため、これらの普通株を撤回することはない。また,保管人とその代理人は,採決指示や採決指示を実行できなかった方式に対して無責任である.その結果、米国預託株式保有者は投票権を行使できない可能性があり、米国預託証明書関連普通株が彼らの要求に応じて投票していない場合、あるいは彼らの株が投票できない場合、彼らは何もできないかもしれない
アメリカの民事責任に対するクレームは私たちに強制的に施行できないかもしれない。
私たちの多くの上級管理職メンバーと一部の取締役会メンバーは非アメリカ住民であり、私たちのすべてまたは大部分の資産とこれらの人々の資産はアメリカ以外に位置している。したがって、米国連邦証券法の民事責任条項によると、米国にいるこのような個人や私たちに訴訟手続きを送達したり、米国裁判所で得られた彼らまたは私たちに対する判決を実行することができない可能性がある。
米国とイギリスには現在、民商事判決(仲裁裁決を除く)の承認と執行を規定する条約はない。したがって、米国裁判所が下した最終支払い判決は、米国証券法に完全に基づいているか否かにかかわらず、自動的にイギリスで認められたり強制的に執行されたりすることはない。また、イングランドとウェールズ裁判所は、イギリスで米国または米国のいずれの州の証券法に基づいて私たちまたは私たちの役員や上級管理職に提起されたオリジナル訴訟を受理するかどうかには、不確実性も存在する。米国裁判所で得られたいかなる最終的かつ決定的な金銭判決も,何らかの要求を満たす場合には,イングランドやウェールズ裁判所によって訴訟自体の原因とされ,一般法下の債務とみなされるため,これらの問題を再審する必要はない。米国証券法民事責任条項に基づく判決が,これらの要求に適合しているかどうかは,このような法律に基づいて金銭損害賠償が処罰となるかどうかを含む,このような裁決を下す裁判所の問題である。もしイングランドとウェールズ裁判所がアメリカの判決が支払うべき金額について判決を下したら、イギリスの判決は強制的に執行することができます
この目的のために一般的に利用可能な方法によって。このような方法は一般的にイングランドとウェールズ裁判所が実行方法を適宜規定することを可能にする。
したがって、アメリカの投資家は、アメリカ連邦証券法による判決を含む、私たちまたは私たちのいくつかの取締役に対して、アメリカ裁判所で得られたいかなる民商事判決も執行できないかもしれない。
ドルとポンドの間の為替レートの変動は私たちのアメリカ預託証明書を持つリスクを増加させるかもしれません
私どものアメリカ預託証明書はナスダック世界の精選市場でドルで取引されています。ドルとポンドの為替レートの変動は、私たちのアメリカ預託証明書の価値と私たちの普通株の価値との間に一時的な差をもたらす可能性があり、この違いを利用した投資家の大量取引を求めることになる可能性があります
また,ドルとポンドレートの変動により,米国預託証券保有者が英国で預託機関から抽出した任意の普通株を売却して得た収益のドル同値や,米国預託証明書に代表される我々の普通株がユーロで支払う任意の現金配当金のドル同値も低下する可能性がある
米国預託証明書保持者は、その米国預託証明書の譲渡と関連普通株の撤回に制限される可能性がある
アメリカ預託証明書は預かり人の帳簿に譲渡することができます。しかし,保管人は,職務遂行に関与していると考えられる場合には,その帳簿を随時あるいは随時閉鎖することができる。私たちの帳簿またはホスト銀行の帳簿が閉鎖されたとき、ホスト銀行は、一般に、米国預託証明書の交付、譲渡または登録を拒否することができ、または、私たちまたはホスト銀行が、法律、政府または政府機関の任意の要求、ホストプロトコルの任意の規定、または任意の他の理由から適切であると考えられるいつでも、米国預託株式保有者がその米国預託証明書を無効にし、関連する普通株を撤回する権利があると考えられる場合、信託銀行は、米国預託証明書の交付、譲渡、または登録を拒否することができる。あなたのアメリカ預託証明書の解約と関連する普通株の撤回は一時的な遅延が生じる可能性があります。信託機関が譲渡帳簿を閉鎖したので、あるいは私たちは譲渡帳簿を閉鎖しました。普通株式譲渡は株主総会での投票を許可するために阻止されましたか、または私たちは私たちの普通株のために配当金を支払っています。また、米国預託株式保有者は、手数料、税金、および同様の費用を借りた金、および米国預託証明書または普通株または他の預金証券に適用される任意の法律または政府法規を遵守するために引き出しを禁止する必要がある場合には、米国預託証明書を無効にし、関連する普通株を抽出することができない可能性がある
米国預託株式保有者は、預金協定に基づくクレームについて陪審裁判を行う権利がない可能性があり、このような訴訟において原告に不利な結果を招く可能性がある。
私たちの普通株式を管理するアメリカ預託証明書を管理する預金協定の規定は、法律で許可された最大範囲内で、アメリカ預託証明書の所有者と実益所有者は、私たちのアメリカ預託証明書または預金協定によって、私たちまたは受託管理人に対して提出された任意のクレームの陪審裁判の権利を撤回することができない。
法律が適用されてこの陪審裁判免除条項が許可されていない場合、訴訟は陪審裁判の保証金合意の条項によって行うことができる。もし私たち又は保管人が放棄に基づく陪審裁判要求に反対する場合、裁判所は適用された州及び連邦法律に基づいて、事件の事実及び状況に基づいて、放棄が強制的に執行できるか否かを決定する。私たちの知る限り、契約紛争前の陪審員による連邦証券法に基づくクレームの裁判免除の実行可能性は、米国最高裁判所の最終裁決を得ていない。しかし、契約紛争前の陪審裁判免除条項は、一般に、預金協定を管轄するニューヨーク州法律に基づいて、預金協定の下で生じる事項に対して非排他的管轄権を有するニューヨーク市の連邦または州裁判所によって実行されることができると考えられる。契約中の論争前の陪審裁判免除条項を執行するか否かを決定する際、裁判所は通常、一方の当事者が知っているかどうか、賢明かつ自発的に陪審裁判を受ける権利を放棄したかどうかを考慮する。私たちは預金協定と私たちのアメリカ預託証明書がこのような状況だと思う。保証金契約を締結する前に、陪審員免除条項に関する法律顧問に相談することをお勧めします。
もしあなたまたはアメリカ預託証明書の任意の他の所有者または実益所有者が預金契約または私たちのアメリカ預託証明書の下で発生した事項について、連邦証券法に基づいて提出されたクレームを含む場合、私たちまたは信託銀行にクレームを提出し、あなたまたはその他の所有者または実益すべての人は、このようなクレームについて陪審裁判を行う権利がないかもしれません。これは、私たちおよび/または信託銀行に対する訴訟を制限し、阻止することができます。預金協定に基づいて私たちおよび/または保管人に訴訟を提起した場合、適用される裁判裁判所の裁判官または裁判官によってしか審理されない場合、これは異なる民事手続きによって行われ、陪審裁判とは異なる結果をもたらす可能性がある
任意のこのような訴訟において原告に不利になる可能性のある結果は、他に加えて、クレームの性質、そのようなクレームを審理する裁判官または裁判官、および聴聞場所に依存する。
預金協定又は米国預託証明書のいかなる条件、規定又は規定は、米国預託証明書のいかなる所有者又は実益所有者を構成しないか、又は我々又は信託機関は、米国連邦証券法及びその公布された規則及び条例の遵守を放棄する。
我々の組織規約又は細則は、イングランド及びウェールズ裁判所は、すべての株主苦情を解決するための独占的なフォーラムであるが、証券法又は取引法に基づいて訴訟原因の苦情を提出する独占フォーラムを除くが、ニューヨーク南区米国地域裁判所は、証券法又は取引所法案に基づいて訴訟因を提起する株主苦情を解決する独占フォーラムである。
私たちの条項は、私たちが一般的な決議によって代替裁判所を選択することに同意しない限り、イングランドとウェールズ裁判所は、法律によって許容される最大範囲内で、以下の場合の独占裁判所となるべきである:(A)私たちが提起した任意の派生訴訟または法的手続きを代表する;(B)私たちの任意の取締役、上級管理者または他の従業員が私たちの受託責任違約を主張する訴訟または手続き、(C)“2006年会社法”または私たちの定款(時々改正可能)の任意の規定に基づいてクレームを提起する任意の訴訟または法的手続き;または(D)請求または他の方法で我々の事務またはイングランドおよびウェールズフォーラム条項に関連する任意の訴訟または手続きを主張する。イングランドとウェールズフォーラム条項は、証券法や取引法によって生じるいかなる訴訟根拠にも適用されない。私たちの条項はさらに、私たちが一般決議によって代替裁判所を選択することに同意しない限り、米国ニューヨーク南区地域裁判所は、証券法または取引法または米国連邦フォーラム条項に基づいて訴訟原因を提起する任意のクレームを解決するための独占的なフォーラムである。さらに、私たちの条項は、私たちの株式権益を購入または他の方法で獲得した個人または実体は、イングランドとウェールズフォーラム条項とアメリカ連邦フォーラム条項を通知し、同意したとみなされていると規定されている;しかし、私たちの株主は、アメリカ連邦証券法とその下の規則と法規の遵守を放棄するとみなされないことを前提としている。
私たちの文章のイングランドとウェールズフォーラム条項とアメリカ連邦フォーラム条項は私たちの株主にこのようなクレームの追加訴訟費用をもたらすかもしれません。さらに、私たちの条項のフォーラム選択条項は、私たちの株主が司法フォーラムで、私たちまたは私たちの役員、役員、または従業員との紛争のクレームに有利だと思う能力を提出することを制限するかもしれません。これは、訴訟が成功しても、私たちの株主に利益をもたらすかもしれません。また、デラウェア州最高裁判所は2020年3月に、デラウェア州法律によると、証券法に基づいて請求を要求する連邦裁判所選択条項は表面的に有効であると判断したが、他の裁判所は、イングランドとウェールズ裁判所、米国内の他の裁判所を含め、私たちの米国連邦フォーラム条項を実行するかどうかにはまだ不確実性がある。米国連邦フォーラムの条項が訴訟で適用されないか、実行できないことが発見されれば、他の管轄区域でこのような訴訟を解決するために追加コストが生じる可能性があり、これは私たちの運営結果や財務状況に悪影響を及ぼす可能性がある。米国連邦フォーラムの条項はまた、この条項が実行できないか無効であると主張する私たちの株主に追加の訴訟費用を適用するかもしれない。イングランドおよびウェールズ裁判所、および米国ニューヨーク南区地域裁判所も、訴訟を起こした株主がいる可能性があるか、または訴訟を提起する裁判所を選択することを考慮することを含む、他の裁判所とは異なる判決または結果を行う可能性があり、このような判決は、私たちの株主に多かれ少なかれ有利である可能性がある。
もし私たちが受動的な外国投資会社に分類されれば、アメリカの保有者に不利なアメリカ連邦所得税の結果をもたらすだろう
規則によれば、いずれの課税年度においても、(I)総収入の75%以上が受動的収入からなるか、または(Ii)資産の平均四半期価値の50%以上が受動的収入を生成するか、または受動的収入を生成するために保有する資産からなり、受動的外国投資会社またはPFICとなる。これらのテストの場合、受動的収入には、配当金、利息、投資財産の売却または交換の収益、ならびにいくつかのレンタル料および特許使用料が含まれる。また、上記の計算については、他の会社の少なくとも25%の株式を直接または間接的に所有する非米国会社は、その割合で共有された同社の資産および収入を直接保有し、受け入れているとみなされる。任意の課税年度内に、我々の米国所有者(以下“米国所有者の重要な米国連邦所得税考慮事項”で定義されるように)が我々の普通株式または米国預託証明書を保有している場合、私たちがPFICの資格を継続しているか否かにかかわらず、米国所有者は、資本利益または実際または配当とみなされる任意の優先税率、繰延される特定の税金項目の利息費用、および追加の報告要件を含む不利な税務結果に直面する可能性がある。我々の現在と期待されている収入と資産構成および我々の資産価値から,2022年12月31日までの納税年度には,米国連邦所得税目的のPFICであると考えられる。しかし、本課税年度や将来のいかなる課税年度にもPFICの地位に関する保証を提供することはできません
何年もです。私たちが個人投資委員会の決定であるかどうかについては、毎年多くの事実に基づいて決定されており、採用されている原則や方法は場合によっては不明であり、異なる解釈がある可能性がある。収入テストの下で、私たちのPFICとしての地位は私たちの収入構成に依存し、これは私たちが未来に行う取引と私たちの会社の構造に依存するだろう。私たちの収入と資産の構成はまた私たちがどの発行で調達した現金支出の影響を受けている。すべてのアメリカの所有者は自分の税務顧問に相談すべきで、もし私たちが今あるいは将来PFICになれば、アメリカに不利な税収結果をもたらすかもしれません。
もし私たちが支配された外国の会社なら、あるアメリカの保有者に不利なアメリカ連邦所得税の結果をもたらすかもしれません
非米国会社の各“10%株主”(以下に定義する)は、米国連邦所得税において“制御された外国会社”またはCFCに分類され、通常、CFCの“F分部収入”、“世界無形低税収入”、および米国財産への収益投資を含む10%の株主割合シェアを米国連邦税収に含めることが要求されており、CFCがその株主に何の分配も行われていなくても。さらに、非米国会社が少なくとも1つの米国子会社を有している場合、現行法によれば、非米国会社の現在の任意の非米国子会社および将来新たに設立または買収された任意の非米国子会社は、非米国会社がフッ素塩化炭素とみなされているか否かにかかわらず、フッ素塩化炭素とみなされる。F分割収入は、一般に、配当金、利息、レンタル料、特許使用料、証券売却の収益、および関連する当事者とのいくつかの取引の収入を含む。さらに、フルオロカーボンの株式を売却または交換することによって収益の10%を達成する株主は、このような収益の一部を資本収益ではなく配当収入に分類することを要求される可能性がある。米国連邦所得税については、一般に、10%の株主が当該会社が投票する権利を有する全てのカテゴリ株の総投票権または同社株の総価値の50%以上を直接または間接的に所有していれば、その会社はCFC株に分類される。“10%株主”とは、その会社が投票権を有すると考えられるすべてのカテゴリーの株式価値または総投票権の10%以上を有する米国人(“規則”の定義に基づく)を意味する
米国証券取引委員会に提出された利益所有権報告書の審査によると、2022納税年度にフッ化炭素に分類されているとは考えられない。しかしながら、クロロフッ化炭素の地位の決定は複雑であり、帰属規則を含み、これらの規則の適用は完全に決定されていない。フッ化炭素に関連する10%株主の個人は、通常、特定の減税または外国税収控除を受けることができないが、米国会社の10%株主は、このような減税または外国税収控除を受けることができる。フッ化炭素報告義務を守らなければ,米国の株主は巨額の罰金を受ける可能性がある。私たちは規則に基づくフルオロ塩化炭素規則の適用の申告と納税義務を履行するために、任意の10%の株主に必要可能な情報を提供することを保証することはできません
すべてのアメリカの所有者はフルオロカーボン10%株主の潜在的な不利なアメリカの税収結果について自分の税務顧問に相談すべきだ
イギリスに登録されている米国上場企業として、コストを増加させ続けており、当社の取締役会は、新たなコンプライアンス措置やコーポレートガバナンス実践を実施するために多くの時間を投入することを求められています
イギリスに登録され、アメリカに上場している上場企業として、私たちは民間会社としては起きていない多くの法律、会計、その他の費用を負担し続けています。また、サバンズ-オクスリ法案、ドッド-フランクウォール街改革と消費者保護法案、ナスダックの上場要求、その他の適用される証券規則と法規は様々な適用を加えている 外国報告上場企業に対する要求は、有効な開示、財務制御と会社管理やり方の確立と維持を含む。私たちの取締役会、管理職、そして他の人たちはこのようなコンプライアンス計画に多くの時間を投入しなければならない。さらにこれらのルールは 規制は増加し、私たちの法律と財務コンプライアンスコストを増加させ、いくつかの活動をより時間的で高価にするだろう。例えば、これらの規制は、取締役および上級管理職責任保険をより難しく、より高価にすることができ、逆に、合格した取締役会メンバーを引き付け、維持することを困難にする可能性がある。
しかし,これらの規則や条例は異なる解釈を受けることが多く,特殊性に欠ける場合が多いため,規制機関や理事機関が新たな指導意見を提供するにつれて,これらの規則や条例の実践への適用は時間とともに変化する可能性がある。これは遵守事項に関する持続的な不確実性と、開示と統治慣行を絶えず修正するために必要なより高いコストをもたらす可能性がある
サバンズ·オキシリー法第404条または第404条の規定によると、私たちは毎年Form 10-K年次報告書に経営陣によって提出された財務報告書の内部統制の有効性に関する報告書を提出しなければならない。しかし、私たちは財務報告書の内部統制に関する証明報告書を発行することを要求しないつもりだ
独立公認会計士事務所の2022年12月31日までの年度は、2022年6月30日の公開流通株によると、小さな報告会社になる資格があるため、2022年12月31日までの非加速申告とみなされる。第404条の遵守を達成し、維持するために、私たちはコストが高く、挑戦的である財務報告書に対する私たちの内部統制を記録して評価した。この点では、引き続き内部資源を投入し、外部コンサルタントを招聘し、財務報告内部統制の十分性を継続的に評価·記録するための詳細な作業計画を採択し、制御プログラムを適宜改善し、テスト検証制御が文書記録の役割を果たしていることを検証し、財務報告内部統制の継続報告及び改善手順を実施した。私たちは努力したにもかかわらず、どの年にもリスクがあり、すなわち私たちは規定された時間枠内で結論を出すことができない、すなわち私たちは財務報告の内部統制に有効であり、第404条の要求に適合する。これは、私たちの財務諸表の信頼性に自信を失ったため、金融市場に不利な反応をもたらす可能性がある。また、将来的に我々の独立公認会計士事務所が発行する財務報告内部統制証明報告が必要となる可能性があり、また、我々の独立公認会計士事務所が我々の財務報告の内部統制の有効性について意見を述べることができない場合、投資家は私たちの財務報告の正確性と完全性に自信を失う可能性があり、私たちの米国預託証券の市場価格は負の影響を受ける可能性があり、私たちは米国証券取引委員会または他の規制機関の調査または株主訴訟の対象となる可能性がある, これは市場価格や私たちのアメリカ預託証明書に悪影響を与え、追加料金を発生させる可能性がある。
私たちは“小さな報告会社”であり、より小さい報告会社に適用される開示要求が低下し、私たちの証券の投資家に対する吸引力を低下させる可能性がある。
私たちは2022年6月30日までに非関連会社が保有する株式時価が5億6千万ドル未満であるため、2022年6月30日現在の“小さな報告会社”になる資格があり、最近終了した会計年度では、年収は1.00億ドル未満である。私たちは、(I)私たちの非関連会社が保有する投票権と非投票権株式が、私たちの第2四半期の最終営業日に2.5億ドルを下回る限り、または(Ii)私たちの最近終了した会計年度の年収が1.00億ドル未満であり、私たちの非関連側が保有する投票権および非投票権株式が、私たちの第2四半期の最終営業日に7.00億ドルを下回る限り、小さな報告会社として続ける。小さな報告会社として、私たちの定期報告書や依頼書で役員報酬に関する開示義務を減らすことを含む、新興成長型企業と同じ開示要件免除を多く利用することができる。私たちは投資家が私たちがこのような免除に依存する可能性があるので、私たちの証券がそんなに魅力的ではないと思うかどうか予測できない。したがって、一部の投資家が私たちの証券の魅力が低下していることを発見すれば、私たちのアメリカ預託証明書の取引市場はそれほど活発ではなくなり、私たちのアメリカ預託証明書の価格はもっと変動する可能性がある。
あなたはあなたの利益を保護する上で困難に直面するかもしれません。あなたがアメリカ連邦裁判所を通じてあなたの権利を保護する能力は限られているかもしれません。私たちはイングランドとウェールズの法律登録によって設立され、アメリカ以外で大部分の業務を展開していますので、私たちの多くの高級管理職メンバーと私たちのいくつかの取締役会メンバーはアメリカ以外のところに住んでいます。
私たちは登録が成立し、イングランドとウェールズに登録事務所を設置し、現在イングランドとウェールズの法律に基づいて存在している。また、私たちの有形資産の大部分はアメリカ以外にあり、私たちの多くの高級管理職メンバーと一部の役員はアメリカ以外に住んでいます。したがって、米国証券法の民事責任条項によると、米国内で特定の役員または私たちに訴訟手続きを送達したり、米国裁判所で得られたこのような役員または私たちに対する判決を執行することができない可能性がある。したがって、投資家は、米国内でそのような人々に法的手続き文書を送達することができないか、または米国連邦証券法民事責任条項に基づく判決を含む、米国裁判所で得られた彼らまたは私たちに不利な判決を実行することができないかもしれない。
米国とイギリスには現在、民商事判決(仲裁裁決を除く)の承認と執行を規定する条約はない。したがって、米国裁判所が下した最終支払い判決は、米国証券法に完全に基づいているか否かにかかわらず、自動的にイギリスで認められたり強制的に執行されたりすることはない。また、イングランドとウェールズ裁判所がイングランドとウェールズがアメリカやアメリカの任意の州の証券法に基づいて私たちまたは私たちの役員や上級管理職に提起した元の訴訟を受理するかどうかには、不確実性がある。米国裁判所で得られたいかなる最終的かつ決定的な金銭判決も,何らかの要求を満たす場合には,イングランドやウェールズ裁判所によって訴訟自体の原因とされ,一般法下の債務とみなされるため,これらの問題を再審する必要はない。
米国証券法民事責任条項に基づく判決については,これらの要求に適合するかどうかは,このような法律に基づいて金銭損害賠償が処罰となるかどうかを含め,このような決定を下した裁判所に依存する。イングランドとウェールズ裁判所が米国の判決が支払うべき金額について判決を下した場合、イギリスの判決は通常この目的に利用可能な方法で実行されるだろう。このような方法は一般的にイングランドとウェールズ裁判所が実行方法を適宜規定することを可能にする。
したがって、アメリカの投資家は、アメリカ連邦証券法による判決を含む、私たちまたは私たちのいくつかの取締役に対して、アメリカ裁判所で得られたいかなる民商事判決も執行できないかもしれない。
イギリスに登録されている上場有限会社として、ある資本構造決定は株主の承認を得る必要があり、これは私たちが資本構造を管理する柔軟性を制限するかもしれない。
イギリスの法律では、取締役会は株主の事前許可を得た場合にのみ株式(または任意の証券の引受または任意の証券を株式に変換する権利を付与する)を発行することができ、この許可はそれがカバーする株式の額面総額を説明し、有効期間は最長5年であり、各許可は株主総会で採択された会社定款の細則または関連する一般決議に規定されている。当社の株主が2020年9月11日に可決した通常決議案には、2020年9月11日から5年以内に追加株式を発行する権限が含まれており、この認可は満期時(すなわち少なくとも5年ごと)に継続する必要がありますが、追加の5年間(または任意のより短い期間)については、より頻繁に継続を求める可能性があります。
イギリスの法律はまた、新株が現金形式で発行された場合、株主は優先的に権を購入できると規定している。しかし、組織規約の細則または株主総会では、この決議が少なくとも75%の投票で可決されれば、優先購入権を取り消すことができる特別決議が採択されることが可能である。このような優先購入権の不適用期間は、最長で会社定款が採択された日から最長5年であるが、これが適用されない株式の分配に関する認可期間を超えない、又は株主特別決議を超えない日(株主特別決議の方式では適用されない)。いずれの場合も、このようなキャンセル申請は、満期時に我々の株主によって更新される必要がある(すなわち、少なくとも5年に1回)。当社株主が2020年9月11日に可決した特別決議案には、当社株主が5年以内に優先購入権を適用しない権限が含まれており、満了時(すなわち少なくとも5年ごと)に継続して有効になる必要がありますが、追加の5年(またはより短い期間)には、優先購入権の適用が適用されないことがより頻繁に求められる可能性があります。
イギリスの法律では、上場企業が株主の事前承認なしに自分の株を買い戻すことも一般的に禁止されています。一般的な決議とは、簡単な多数投票で採択された決議、その他の手続きのことです。このような承認の期間は最長5年に達することができる。
私たちの中央管理·制御場所がまだイギリス以外(または海峡諸島またはマーン島)にある場合、イギリスの都市買収と合併規則または買収規則に基づく条項における株主保護は適用されない
“買収規則”の管轄基準については、私たちの現在の中央管理·制御場所はイギリス(あるいは海峡諸島やマーン島)にはないと考えられる。したがって、吾らは吾らが現在買収規則に制約されていないと信じているため、吾らの株主は現在、買収規則が提供するいくつかの買収要約保障を有しており、強制買収要約に関する規則を含む権利がない。
これが変化した場合、または買収規則に対する買収合併委員会または買収委員会の解釈や適用が変化した場合(買収委員会評価買収規則がイギリス以外に上場しているイギリス企業の株式の方式の変更を含む)、買収規則は将来的に我々に適用される可能性がある
“買収規則”は、“買収規則”に拘束された会社の買収を管理して行う枠組みを提供する。以下は、買収規則の中でいくつかの最も重要なルールの簡単な概要である
•任意の者(一定期間内の一連の取引を透過するか否かにかかわらず)が株式権益(当該者が保有している株式及びそれと一致して行動する者が保有又は取得した株式の権益とともに)を取得し、当該株式が買収規則により制限された会社の30%以上の投票権を有する場合、当該者は、一般に、当該会社の任意の種類の株式又は投票権を有する他の種別の譲渡可能な証券の所有者に強制的な申出をして、当該会社における権益の残高を取得しなければならない。
•誰もが彼または彼女と一致して行動する者が、買収規則により制限された会社の株式のうち、30%以上50%以下の投票権の権益を有し、その人または彼または彼女と一致して行動する任意の人が追加の株式権益を獲得し、その株式権益が彼または彼女の利害関係のある投票権付き株式のパーセンテージを増加させる場合、その人は、
一般的には、同社の投票権を持つ任意の種類の株式、株式または他のカテゴリ譲渡可能な証券のすべての所有者に強制的な要約を提出して、同社における権益バランスを取得することが要求される。
•上記2項で述べた場合にトリガされる強制要約は、現金(または現金代替案を伴う)でなければならず、要約を要求された人またはそれと一致して行動する任意の人が過去12ヶ月以内に会社の株式を買収するために支払う最高価格を下回らなければならない。
•任意の要約(すなわち非強制要約の任意の要約)については、要人(すなわち入札者)及びその任意の一致行動者が要件期間内及び前12ヶ月にあるカテゴリの株式の10%以上に相当する株式権益を現金で買収する場合には、要約は、現金又は当該カテゴリのすべての株主が要人及び任意の一致行動者がその期間中にそのカテゴリの株式権益について支払う最高価格でなければならない。また、要衝者が要件期間内に任意の株式権益を現金で買収する場合には、その種別の株式のいずれの権益に対しても支払われない最高価格で現金代替案を提供しなければならない。
•1つの会社に要約を提出した後、要人またはそれと一致して行動する誰もが被要約会社(すなわちターゲット会社)の株式権益を要約価値よりも高い価格で獲得した場合、要約は、このように取得した株式権益のために支払われる最高価格を下回らないようにしなければならない。
•被要約会社は適任な独立コンサルタントを任命しなければならず,その要約財務条項に関する意見はすべての株主に通知しなければならないことと,被要約会社取締役会の意見を任命しなければならない.
•場合によっては独立株主の承認を得て、要人の財務顧問が公平で合理的な手配に関するものであると考えない限り、選定された株主に対して特別または有利な取引を行うことは許可されない。
•すべての株主に同じ情報を提供しなければならない。
•要人又は被要人又はその代表の要約が発表した各文書について説明しなければならず,要人又は被要人の取締役(場合によっては)はその中に掲載されている情報に対して責任を負う。
•利益予測、数量化財務利益報告書および資産推定値は、規定された基準に従って行われなければならず、専門顧問が報告しなければならない。
•文書内またはメディアに発表された誤解、不正確、または確認されていない声明は、直ちに公開されて訂正されなければならない。
•被要約会社が要約過程で要約を挫折させる可能性がある行動は、株主がこれらの計画を承認しない限り、通常禁止されている。落胆させる行動は、例えば、サービス契約下での取締役の通知期間を延長すること、または目標集団の売却に同意することの重要な部分を含むであろう
•要約期間中に関連証券の取引を開示し、要約当事者及び任意(直接或いは間接)が1%以上の任意の種類の関連証券権益を持つ者を含む場合、迅速に持倉を開示し、関連証券取引を行う必要があり、すべて厳格な規定がある。
•契約者と要人会社の従業員および要人会社の年金計画の受託者に告知しなければなりません。また、要約会社の従業員代表と年金計画受託者は、要約会社取締役会に通知したり、サイト上で要約の雇用への影響に関する単独意見を発表したりする権利がある
私たちの株主の権利はアメリカの会社の株主に通常提供される権利とは異なるかもしれない。
私たちはイングランドとウェールズの法律登録に基づいて設立された。普通株式保有者の権利および米国預託証明書保持者のいくつかの権利は、2006年の会社法の規定、および私たちの定款を含むイングランドとウェールズ法律の管轄を受けている。このような権利はいくつかの側面で典型的なアメリカ会社の株主権利とは違う。第424条(B)条に基づいて米国証券取引委員会に提出された目論見書を参照してください。日付が2020年9月17日の目論見書の“株式説明と会社規約−会社法上の差異”という見出しの下の情報は、
私たちに適用される“2006年会社法”条項と、例えば株主権利および保護に関するデラウェア州一般会社法との間の主な差異を説明するために、参照によって本明細書に組み込まれる。
主な違いは以下の点である
•イギリスの法律と我々の条項によると、会議に出席する各株主は1票のみであり、投票投票を要求しない限り、この場合、各株主は株式を保有するごとに1票を有する。アメリカの法律によると、すべての株主は通常すべての会議で1株1票の権利を持っている。
•イギリスの法律によると、株式数は投票中にのみ持株者が投票できる数を決定することができる。しかし、あなたはアメリカの預金証明書の投票権もまた私たちの口座開設銀行との預金協定条項によって制限されているということを知らなければならない
•イギリスの法律によると、いくつかの例外および適用されない場合を除いて、各株主は、一般に、任意の普通株を比例的に引受する優先購入権を有するか、または証券を現金と交換するために証券を普通株に変換する権利を有する。米国の法律によると、株主は通常、会社登録証明書またはその他の面で特別に付与されない限り、優先購入権を持っていない。
•イギリスの法律および我々の定款の細則によると、いくつかの事項は、定款の細則の改正を含む、関連決議案(または75%の普通株式を代表する株主に投票する株主(自らまたは代表を委任)に投票する)の75%の株主によって承認されなければならない。これは私たちが取締役会が適切だと思う会社の取引を終わらせることをもっと難しくするかもしれない。米国の法律によると、会社の登録証明書を修正したり、他の重大な取引を承認するには、通常、大株主の承認を得るだけでよい。
•イギリスでは、買収の仕組みは買収要約である可能性があり、手配案である可能性もある。イギリスの法律によると、買収要約による買収を求める入札者は、私たちが発行したすべての普通株/アメリカ預託証明書に対して買収要約を提出する必要があります。約90%以上の普通株式/米国預託証明書の受け入れを受けていない場合、イギリスの法律によると、入札者は私たちの100%の支配権を得るために“押出”を完了することができない。したがって、我々の発行済み普通株式の90%(米国預託証明書に代表される普通株を含む)を受け入れることは、デラウェア州法律に基づいて会社を買収要約する際のより一般的な50%ではなく、我々の任意の買収要約を買収する条件である可能性がある。対照的に、手配計画の成功は、入札者が株主総会で投票し、75%の普通株式(米国預託証明書が代表する普通株を含む)の多数の株主承認を必要とする吾などの100%の支配権を獲得することになる。
•イギリスの法律及び当社の定款細則によると、株主及び当社の株式に利害関係があると信じている他の者は、当社の要求に応じて自社の株式の権益に関する資料を開示する必要がある可能性があり、必要な資料を提供できないことは、株式譲渡の禁止、配当の差し止め、投票権の喪失を含む株式付随権利の喪失や制限を招く可能性がある。アメリカの法律によると、一般的に似たような条項は存在しない。
•株主総会の定足数要求は、1人以上の合資格者が会議に出席し、少なくとも33%(33%)の発行済み株式(在庫株として保有する株式を含まない)を共同で保有(または株主の被委員会代表または会社代表として)を共有し、処理する業務に出席して投票する権利がある。米国の法律によると、投票資格のある株式の多くは通常、定足数を構成するために(自らまたは代表を依頼して)株主総会に出席しなければならない。定足数に必要な最低株式数は、会社登録証明書や定款の規定によって減少することができるが、通常は会議で投票する権利のある株式の3分の1を下回らない。
財務報告書の統制に関する私たちのリスク
もし私たちが効果的な財務報告内部統制制度を維持できなければ、私たちは私たちの財務結果を正確に報告したり、不正を防止することができないかもしれない。したがって、株主は私たちの財務や他の公開報告に自信を失う可能性があり、これは私たちの業務と私たちのアメリカ預託証明書の取引価格を損なうことになる
財務報告に対する効果的な内部統制は、信頼できる財務報告を提供するために必要であり、適切な開示制御や手順とともに詐欺を防止することを目的としている。必要な新しい制御措置や改善された制御措置を実施できなかったり、実行中に遭遇した困難は、私たちの報告義務を履行できない可能性があります。
さらに、第404条に基づく試験と、その後に我々の独立公認会計士事務所による試験が必要であり、財務報告の内部統制上の欠陥を明らかにすることができ、これらの欠陥は、重大な弱点と考えられているか、または私たちの財務諸表を前向きまたは追跡的に変更する必要があるか、またはさらなる関心または改善が必要な他の分野を決定する必要があるかもしれない。悪い内部統制はまた、投資家が私たちが報告した財務情報に自信を失う可能性があり、これは私たちのアメリカ預託証明書の取引価格に負の影響を与える可能性がある。
私たちは前に財務報告書の内部統制の重要な弱点を発見した。私たちは財務報告書の内部統制に対する私たちの未来の重要な弱点を発見するかもしれない。これらの重大な弱点を補うことができない場合、あるいは有効な内部統制を確立し、維持できなければ、タイムリーかつ正確な財務諸表を作成することができない可能性があり、財務報告書の内部統制に無効であり、投資家の信頼と米国預託株式価格に悪影響を及ぼす可能性があると結論するかもしれない。
2019年の財務諸表作成期間中、経営陣は、財務報告の内部統制における3つの大きな弱点を発見しました。重大な欠陥は、我々の年度または中期財務諸表の重大なミス報告が合理的な可能性があるように、財務報告の内部統制の欠陥または欠陥の組み合わせとして定義され、タイムリーに防止または発見および是正されないようにする。2020年12月31日までに発見された重大な弱点が修復されたことを確認しましたが、他の重大な弱点や欠陥は発見されないことを保証することはできません。これらの弱点や欠陥は、私たちの将来の運営結果に悪影響を及ぼす可能性があります。
より広く言えば、“サバンズ-オキシリー法案”を含む上場企業からの要求を満たすことができなければ、私たちは今後の時期に私たちの財務業績を正確に報告したり、法律や証券取引所の規制要件の時間範囲でそれらを報告することができないかもしれません。適用された場合に“サバンズ-オキシリー法案”を遵守できなければ、米国証券取引委員会や他の規制機関の制裁や調査を受ける可能性もある。必要な新しいまたは改善された制御を維持または実施できなかった場合、またはこれらの制御を実施する際に私たちが遭遇したいかなる困難も、追加の重大な弱点または重大な欠陥を招き、私たちが私たちの報告義務を履行できなかったこと、または私たちの財務諸表に重大な誤報を招く可能性がある。また、信頼できる財務報告を提供したり、詐欺を防止することができなければ、私たちの業務や運営結果が損なわれる可能性があり、投資家は私たちが報告した財務情報に自信を失う可能性があります。私たちはまたナスダック、アメリカ証券取引委員会、または他の規制機関の調査の対象になる可能性がある。参照してください“私たちのアメリカ預託証明書の所有権に関連するリスク-私たちはすでにアメリカに上場するイギリス上場企業としての運営によってコストを増加させ続け、私たちの取締役会は新しいコンプライアンスイニシアティブとコーポレートガバナンス実践のために多くの時間を投入することを要求されます.”
私たちは財務報告の内部統制が誤った陳述を防止したり発見したりすることができない可能性があり、その固有の限界は、可能な人為的な誤り、制御を回避したり、凌駕したり、詐欺を含むからである。有効な内部統制であっても、財務諸表の作成と公平な列報に合理的な保証を提供することしかできない。信頼できる財務報告を提供したり、詐欺を防止することができなければ、私たちの業務や運営結果が損なわれる可能性があり、投資家は私たちが報告した財務情報に自信を失う可能性があり、私たちの株の取引価格は下落する可能性があります。
一般リスク因子
為替レートの変動は私たちの経営結果と財務状況に大きな影響を及ぼすかもしれない。
私たちの業務の国際範囲のため、私たちの資産、収益、支出とキャッシュフローはいくつかの通貨為替レート変動の影響を受け、特にドル、ポンド、ユーロです。私たちの報告通貨はドルで、私たちの機能通貨はポンド(アメリカ子会社の機能通貨を除いてドル)で、私たちの運営費用の大部分はポンドで支払います。私たちはまた定期的にドル、ポンド、ユーロでサービス、消耗品と材料を購入する。将来的にもっと多くの潜在的収入は海外、特にアメリカから来るかもしれない。私たちのビジネスとアメリカの預託証明書の価格は影響を受けています 将来的にはポンドとこれらの他の通貨との為替変動の影響を受ける可能性があり、これは私たちの運営業績やキャッシュフローにも大きな影響を与える可能性がある。現在、私たちは為替レートのヘッジスケジュールを持っていません。外国為替リスクについての説明は、当社年度財務諸表付記2を参照されたい
さらに、1つ以上のEU加盟国またはEUはユーロを放棄する可能性があり、私たちの将来の業務に実質的な影響を及ぼすかもしれない。EUは財政難のあるEU加盟国に資金を提供する措置をとっており、一部の欧州諸国も経済の安定化と債務負担の軽減措置をとっているが、ユーロは将来的にユーロ用途の国に通貨として放棄される可能性がある。これは、1つ以上のEU加盟国が個別通貨を再導入したり、より極端な場合にEU解体を招いたりする可能性がある。EUが解体される可能性があり、1つ以上のEU加盟国がEUを脱退したり、通貨としてユーロを放棄したりすることが私たちの業務に与える影響は確実に予測できず、どのような事件も私たちの業務、財務状況、および運営結果に実質的な悪影響を及ぼす可能性がある
不利な世界経済の状況は過去と 将来的には私たちの業務、財務状況、または運営結果に悪影響を及ぼすかもしれない。
私たちの経営業績は過去と未来に世界経済と世界金融市場の全体的な状況の悪影響を受ける可能性があります。米国とイギリスを含む主要国経済は時々景気後退や衰退、サプライチェーン制限、インフレと金利の激化と変動、信用緊縮、流動資金不足、企業収益力の低下、信用、株式と外国為替市場の変動、破産と全体の経済不確定性の影響を受ける。例えば、私たちはロシアとウクライナで活動していませんが、持続的な衝突とこの紛争に関連するいかなる地政学的緊張のさらなるエスカレートは、米国や他の国が制裁を実施し、供給中断、為替変動、金融市場の変動を激化させる可能性があります。また、米国の債務上限と予算赤字への懸念は、信用格付けのさらなる引き下げ、経済減速、あるいは米国経済の衰退の可能性を増加させた。米議会議員は連邦債務上限を引き上げる立法を何度も採択しているが、格付け機関は米国の長期主権信用格付けを引き下げたり引き下げたりすると脅している。今回、または米国政府の主権信用格付けまたはそれが考慮される信用をさらに引き下げた影響は、米国や世界の金融市場や経済状況に悪影響を及ぼす可能性がある。これらの中断のいずれも、私たちの業務、運営結果、および財務状況に悪影響を及ぼす可能性がある
世界経済と金融市場の悪化は私たちの業務に様々なリスクをもたらすかもしれない。また、私たちの業務の国際範囲のため、私たちの財務状況は、私たちの機能通貨がポンドであるため、いくつかの通貨為替レート変動の影響を受け続けていますが、ドルで財務業績を報告します。例えば、インフレ率、特にアメリカでは、最近は長年見たことのないレベルに上昇しています。インフレの激化は、通貨のさらなる変動、運営コストの増加(労働コストを含む)、流動性の減少、および信用を獲得したり、他の方法で債務や株式資本を調達する能力が制限される可能性がある。また、米連邦準備委員会は金利を引き上げ、インフレへの懸念に応えるために再び金利を引き上げる可能性がある。 金利上昇、特に政府支出の減少や金融市場の変動に加えて、経済の不確実性をさらに増加させ、これらのリスクを悪化させる可能性がある。また、金利上昇や一般的な景気後退や衰退は、必要に応じて許容可能な条件で追加資本を調達する能力を低下させる可能性がある。経済が疲弊したり下落したり、供給中断や国際貿易紛争が私たちの第三者サプライヤーに圧力を与える可能性もあり、供給中断を招く可能性がある。上記のいずれも私たちの業務を損なう可能性があり、現在および将来の経済環境および金融市場状況が私たちの業務に悪影響を及ぼす可能性のあるすべての方法を予見することはできません。
私たちが事業を展開している国では、税制の変化や不確実性が私たちの財務状況や経営結果に大きな悪影響を与え、株主の純利益を減少させる可能性があります。
私たちは世界で事業を展開し、複数の管轄区域で所得税申告書を提出した。我々の総合的に有効な所得税率は、税法、法規、条約の変化、またはその解釈、実施または考慮されている税収政策の措置および改革(例えば、経済協力開発機構(OECD)、税ベース侵食および利益移転(BEPS)、欧州委員会の国家援助調査および他の措置に関する措置)、司法管轄区域の税務機関のやり方、税務監査または審査によって生じる問題の解決、および任意の関連する利息または処罰を含むいくつかの要因によって大きな悪影響を受ける可能性がある。このような変動は、限定される訳ではないが、営業収入、投資収入、受信された配当金、または(特定の源泉徴収の場合)支払いに対する配当課税を含むことができる。
将来どのような税制改革が提案され、実施されるか、またはこれらの変化が私たちの業務にどのような影響を与えるかは予測できないが、これらの変化は、それらが私たちが経営する司法管轄区の税収立法、法規、政策、または実践に組み込まれていれば、私たちがこれまで支出し、貸借対照表で支払ったか、または計算すべき推定税負担を増加させ、他の方法で私たちの財務状況、将来の運営結果、特定の時期のキャッシュフローに影響を与えるかもしれない
私たちが事業を展開している国では、将来の全体的または有効な税率は、株主の税引後リターンを低下させ、税収コンプライアンスの複雑さ、負担、コストを増加させます。
税務機関は、ある税金の立場に対する私たちの立場と結論に同意しないかもしれないし、予測できない方法で既存の規則を適用する可能性があり、意外なコスト、税収、または予想される収益を達成できない可能性がある。
税務機関は私たちが取った税金の立場に同意しないかもしれないが、これは税金負担の増加を招くかもしれない。例えば、イギリスの税務税関総署、アメリカ国税局、あるいは他の税務機関は、私たちの会社間の手配と譲渡定価政策に基づいて、私たちの知的財産権開発に関連する金額を含む、税収管轄権による収入分配と私たちの関連会社間で支払う金額を疑問視する可能性があります。同様に、税務機関は、私たちが課税連絡を確立していないと考えている司法管轄区域で納税していると断言することができ、国際税務条約によると、このような関連は一般に“常設機関”と呼ばれ、成功すれば、この断言は1つ以上の司法管轄区域での私たちの期待納税義務を増加させる可能性がある。もし私たちが追加的な税金を持っていると評価されれば、これは私たちの運営結果および/または財務状況に実質的な悪影響を及ぼすかもしれない
税務機関は、私たちが重大な所得税債務、利息、罰金を支払う立場を取ることができ、例えば、比較的新しい、広範な審査や解釈されていない相互矛盾した法律法規に技術的に違反している場合、このような評価に異議を唱える可能性があると予想される。有名会社は特に不明確な要求の急進的な応用の影響を受けやすいかもしれない。多くの会社は税務検査員と彼らの税金リストを交渉しなければならない。彼らは法律が規定されているように見えるより高い税金を要求するかもしれない。この評価に異議を唱えるのに時間がかかり、コストがかかる可能性があり、もし私たちが評価に異議を唱えて成功しなければ、その影響は私たちの予想される実際の税率を増加させたり、他の負債を招いたりする可能性がある。
FDA、米国証券取引委員会、その他の政府機関の資金不足は、彼らが重要な指導部や他の人員を採用し、維持する能力を阻害し、新しい療法の適時な開発や商業化を阻止するか、あるいはこれらの機関が私たちの業務運営に依存する可能性のある正常な業務機能を履行することを阻止する可能性があり、これは私たちの業務にマイナス影響を与える可能性がある。
FDAが新しい治療法を審査と承認する能力は各種の要素の影響を受ける可能性があり、政府予算と資金レベル、肝心な人員の雇用と維持及びユーザー費用の支払いを受ける能力、及び法定、監督と政策の変化を含む。したがって、その機関の平均検討時間は近年変動している。また、政府が米国証券取引委員会や我々の業務に依存する可能性のある他の政府機関に提供する資金は、研究開発活動に資金を提供する機関を含め、政治プロセスの影響を受けており、政治プロセス自体が不安定で予測不可能である。
FDAや他の機関の中断も、新薬が必要な政府機関によって審査および/または承認されるのに要する時間を遅らせる可能性があり、これは私たちの業務に悪影響を及ぼすだろう。例えば、ここ数年間、米国政府は何度か閉鎖されており、食品·医薬品局や米国証券取引委員会などのいくつかの規制機関は、肝心な従業員を休暇にし、キー活動を停止させなければならない。また,新冠肺炎の大流行や各国政府が大流行に対応するために実施した政策や法規は,食品や薬物管理局の検査を延期することを含めて食品や薬物管理局の運営に大きな影響を与えている。2020年3月に国内外の施設に対する検査は基本的に保留されて以来、FDAは常規のモニタリング、生物研究モニタリングと審査前検査を含む大流行前の検査活動の回復に努力している。FDAが承認を得るために検査を行う必要があると判断し、旅行制限のために審査期間内に検査を完了することができない場合、FDAは、遠隔相互作用評価が不十分であると考えており、機関は、場合によっては、検査が完了するまで、申請に完全な返信または行動を延期することを意図していることを示している。新冠肺炎突発公共衛生事件の期間中、アメリカ食品薬品監督管理局はその申請に対する規定検査を完成できなかったため、多くの会社は完全な回復状を受け取ることを発表した。アメリカ以外の監督管理機関は類似の制限或いは他の政策措置を取って新冠肺炎疫病に対応する可能性があり、監督活動の中で遅延に遭遇する可能性がある。
政府が長期的に停止している場合、または世界的な健康問題がFDAまたは他の規制機関の定期的な検査、審査、または他の規制活動を阻害し続けている場合、FDAが私たちが提出した規制文書を適時に審査し、処理する能力に深刻な影響を与える可能性があり、これは私たちの業務に実質的な悪影響を及ぼす可能性がある。将来的に政府の閉店は、適切に資本化し、私たちの業務を継続するために、私たちが公開市場に進出し、必要な資本を得る能力に影響を与えるかもしれない。
私たちは環境、健康、安全法律法規の制約を受けているため、私たちは環境コンプライアンスや救済活動に関連する責任と巨額の費用を負担する可能性があり、これは私たちの業務や財務状況に悪影響を及ぼす可能性がある
私たちの業務は、私たちの研究、開発、テストと製造活動を含めて、多くの外国、連邦、州と現地の環境、健康と安全法律法規の制約を受けています。その他の事項以外に、これらの法律と条例は危険物質の制御使用、製造、処理、放出と処置、及び危険材料の登録、例えば化学溶媒、人体細胞、発ガン化合物、変異原化合物、生殖、実験室プログラム及び血液伝播病原体に接触する毒性作用を有する化合物を管理する
私たちはこのような現在または未来の環境、健康、そして安全法律法規を遵守することで巨額のコストを発生させるかもしれない。しかも、もし私たちがこのような法律法規を守らなければ、私たちは罰金や他の制裁を受けるかもしれない
我々と類似した活動をしている他社と同様に,危険材料の放出や接触に関する責任を含む現在や歴史活動に固有の環境責任リスクに直面しているため,このような放出や接触により重大な責任を招く可能性がある。環境、健康、そして安全の法律法規はもっと厳しくなっている。私たちは現在または未来の任意の環境コンプライアンスや救済活動に多くの費用を発生させる可能性があり、この場合、私たちの生産·開発作業は中断または遅延する可能性があり、私たちの財務状況や運営結果は大きな悪影響を受ける可能性があります。このような危険材料に関わる事故が発生すれば,被害者側はそれによる被害に責任を負うことを求めることができる。
特許法や特許判例の変化は,特許の全体的な価値を低下させたり,特許取得を阻止したりして,研究療法を保護する能力を弱める可能性がある
私たちの業界内の他の会社と同様に、私たちの成功は私たちの知的財産権、特に特許に大きく依存している。製薬産業で特許を取得して施行することは複雑な技術と法的問題に関するものだ。したがって,治療学的特許の取得と実施は高価で時間がかかり,本質的には不確実である。米国又は他の管轄区域における特許法又は特許法解釈の変化は、特許出願をめぐる起訴及び発行された特許の実行又は弁護の不確実性及びコストを増加させる可能性がある。例えば、米国が2012年と2013年に公布した“米国発明法”(America Invents Act、略称AIA)は、米国特許制度の大きな変化を招いた
AIAが制定される前に,他の特許可能な要求を満たし,最初に発明が要求された発明の者が特許を取得する権利があると仮定するが,米国以外の国では,最初に特許出願を提出した者が特許を取得する権利がある。2013年3月16日以降、米国は、同一発明を主張する異なる当事者が2つ以上の特許出願を提出した場合、第三者が最初に発明したか否かにかかわらず、どちらが特許を付与されるべきかを決定する先行出願制度に移行した。その日または後に、私たちの前に米国特許商標局に特許出願を提出した第三者は、第三者の前にこの発明をしたとしても、我々の発明をカバーする特許を付与することができる。AIAは私たちに発明から特許出願までの時間を知ることを要求するが、状況は私たちの発明に関する特許出願を迅速に提出することを阻止するかもしれない
AIAが導入した他のいくつかの変化は、特許権者が特許侵害訴訟を提起することができる範囲を制限し、米国特許商標局で任意の未解決の特許出願または発表された特許に挑戦する機会を第三者に提供することを含む。この機会には、第三者が特許訴訟中に米国特許商標局に以前の技術を提出することを可能にすることと、ライセンス後審査を含む米国特許商標局が管理するライセンス後手続きとが含まれる各方面間審査と派生手続き。これは2013年3月16日までに発表された特許であっても、私たちのすべてのアメリカ特許に適用される。USPTO訴訟における証拠基準は,米国連邦裁判所が特許主張の無効を宣言するために必要な証拠基準を下回っているため,第三者はUSPTO訴訟においてUSPTOが我々の特許主張を無効と判断させるのに十分な証拠を提供する可能性があり,同じ証拠がまず地域裁判所訴訟で提出されても主張を無効にするには不十分である.したがって,第三者は米国特許商標局の手続きを用いて我々の特許主張の無効を宣言しようとする可能性があり,第三者が地域裁判所訴訟で最初に被告として疑問を提起すれば,我々の特許主張は無効ではない.AIAおよびその実施は、我々の特許出願をめぐる起訴および私たちが発行した特許の実行または保護の不確実性およびコストを増加させる可能性がある
また、米国最高裁判所は近年、いくつかの特許事件に対して裁決を下しているが、場合によっては特許保護範囲を縮小するか、場合によっては特許権者の権利を弱体化させている。我々の将来の特許取得能力に関する不確実性の増加に加えて,このようなイベントの結合は,いったん特許を取得する価値に関する不確実性をもたらしている.米国議会、連邦裁判所、および米国特許商標局の決定によると、特許を管理する法律および法規は予測不可能な方法で変化する可能性があり、それにより、私たちが新しい特許を獲得したり、私たちの既存の特許と私たちが将来獲得する可能性のある特許を強制的に執行する能力を弱める
私たちの業務は国際業務に関連する経済、政治、規制、その他のリスクの影響を受けている
私たちの業務は国際業務の展開に関連するリスクの影響を受けています。したがって、私たちの未来の結果は、以下のような要素を含む様々な要素の影響を受けるかもしれない
•経済の疲弊、インフレと金利の激化と変動、政治不安定、及び新冠肺炎の大流行の影響を含み、いかなる変種の出現や 未来の緩和努力と現在または未来の経済的影響
•薬品の審査に対する異なる規制要求;
•異なる法ドメインは、そのようなドメインで動作する自由を保障、維持、または獲得することに異なる問題をもたらす可能性がある
•知的財産権の保護を減らすことができます
•複数の法域の異なる、複雑で変化する法律、条例、裁判所システム、および様々な外国の法律、条約、条例を遵守することが困難である
•規制と税関、関税、貿易障壁の変化
•ユーロ、ドル、ポンド、通貨規制などの通貨為替レートの変化
•特定の国や地域の政治経済環境の変化
•貿易保護措置、輸出入許可要求、または政府が取った他の制限行動
•一部の国際市場では異なる補償制度と価格規制が実施されている
•税法や税法の変更による否定的な結果
•外国に住んだり旅行したりする従業員は税収、雇用、移民、労働法を遵守する
•労働騒乱がアメリカ、イギリス、EUよりも一般的な国では、労働力の不確実性
•異なる労使関係を含む人員配置と国際業務の管理に関する困難
•海外の原材料の供給や製造能力に影響を与える事件による生産不足;
•地政学的行動による業務中断は、戦争、テロ、流行病や地震、台風、洪水、火災などの自然災害を含む。
コンピュータシステムの障害、ネットワーク攻撃、または私たちのネットワークセキュリティ、または私たちの協力者、プロバイダ、および他のパートナーのネットワークセキュリティに欠陥がある場合、私たちの業務および運営は影響を受けるでしょう。
私たちの技術インフラへの依存を考慮して、私たちは内部安全措置と政策を評価し続けている。私たちの一部が第三者によって管理されている内部コンピュータシステムと、私たちが依存している現在および将来の第三者のコンピュータシステムは、コンピュータウイルス、不正アクセス、自然災害、テロ、戦争、流行病、および電気通信および電気故障の破壊を受けやすい可能性があります。私たち自身または第三者サービス供給者の運営中断を招くシステム障害、事故、またはセキュリティホールは、私たちの治療開発計画の実質的な中断を招く可能性があります。また,我々の情報技術や他の内部インフラシステムは,会社のファイアウォール,サーバ,レンタル回線,インターネット接続を含めて,系統的な障害のリスクに直面しており,我々の運営を乱す可能性がある.盗難または推定された証拠を使用して、第三者が従業員または顧客データにアクセスすること、コンピュータマルウェア、ウイルス、迷惑メール、ネットワーク釣り攻撃、恐喝ソフトウェア、盗難カードコード、および他の意図的な攻撃、および許可されていないアクセス権限を得ようと試みることを含む可能性があるネットワークイベントの複雑性および頻度が増加している。我々は定期的に浸透テストを行い,継続的なセキュリティ監視を実行しているが,我々のネットワークセキュリティや我々のサイトを浸透および破壊しようとするコンピュータプログラマが使用する技術はしばしば変化し,ターゲットに対して攻撃を開始する前に認識できない可能性があるため,これらの技術を予見できず,我々のネットワークやシステムを保護するコストが増加する可能性がある.
さらに、クライアント、プロバイダ、または他のプロバイダは、セキュリティ制御を不適切に使用することによって、顧客データへの不正アクセスを取得することも可能である。このリスクを修復するために時間と資源を投入し続けているが,今後このような攻撃が発生することは実質的な影響を与える可能性がある。
我々の知る限り,これまでこのような重大なシステム故障やセキュリティホールを経験したことはないが,このような事件が発生して我々の運営が中断されると,我々の開発計画や業務運営の実質的な中断を招く可能性がある.例えば、完成した或いは未来の臨床試験の臨床試験データの紛失は著者らの監督管理の承認作業を遅延させ、著者らのデータの回復或いは複製のコストを著しく増加させる可能性がある。同様に、我々は、第三者に依存してCOMP 360または任意の将来の候補治療薬を生産し、臨床試験を行い、彼らのコンピュータシステムに関連する同様のイベントも、私たちの業務に大きな悪影響を及ぼす可能性がある。任意の中断またはセキュリティホールが私たちのデータまたはアプリケーションを紛失または破損させ、または機密または独自の情報を適切に開示しない場合、私たちは責任を招く可能性があり、私たちの競争的地位が損なわれる可能性があり、私たちの研究におけるCOMP 360ヌードキノコ療法または任意の将来の候補療法のさらなる開発および商業化は阻害または延期される可能性がある。さらに、より多くの人員および保護技術の導入、従業員の訓練、および第三者の専門家およびコンサルタントを招聘する費用を含む、これらの中断またはセキュリティホールによる被害を修復するための追加費用が生じる可能性があります。私たちはネットワーク責任保険を維持しているにもかかわらず、私たちの保険範囲が実際に発生した責任を補うのに十分かどうかを確認することができないか、あるいは経済的に合理的な条項で保険を受け続けるか、あるいは根本的にはできない。
項目1 B。未解決従業員意見
適用されません。
項目2.財産
施設
ブロードウィック通り33番地にあるFora-Sohoのオフィススペースを借りました イギリスロンドンW 1 F 0 DQ、これは当社の本社です。レンタル契約は2023年に満期になります
2022年、私たちはWeWorkと会員契約を締結し、ニューヨーク州マディソン通り130号でオフィススペースを購入した。メンバー契約の初期期限は2023年8月に満了します。会員契約は3ヶ月前にキャンセルを通知することができます。
私たちの施設は私たちの現在の需要を満たすのに十分であり、必要に応じて適切な追加または代替空間を提供して、私たちの予想される需要を満たすだろうと信じている
項目3.法的手続き
私たちは現在、いかなる訴訟やクレームの当事者でもありません。もし判決が私たちに不利であれば、私たちの業務、経営業績、財務状況、あるいはキャッシュフローに重大な悪影響を及ぼすと思います。時々、私たちは訴訟の当事者であるか、または正常な業務過程でクレームの影響を受ける可能性がある。結果にかかわらず,弁護や和解コスト,管理資源分流などにより,訴訟は我々に悪影響を与える可能性がある。
プロジェクト4.鉱山安全開示
適用されません。
第II部
項目5.登録者普通株の市場
市場情報と普通株式とアメリカ預託証明書所持者
私たちのアメリカ預託株式(ADS)は1株当たりコンパス経路会社の普通株を表し、1株当たり額面0.008 GB。アメリカ預託株式はノースカロライナ州シティバンクが口座開設銀行として発行したアメリカ預託証明書を証明することができる。2020年9月18日から、私たちのアメリカ預託証明書はすでにナスダック全世界精選市場で取引され、取引コードはCMPSである。2023年2月22日まで、私たちの普通株は約10人の登録所有者、1株当たり額面0.008 GB、及び私たちのアメリカ預託証明書登録所有者は4名です。2023年2月22日、米預託株式のナスダック世界ベスト市場での終値は8.6ドルだった
配当をする
私たちはどんな現金配当金も発表したり支払ったりしたことがなく、私たちは予測可能な未来にもいかなる現金配当金も発表したり支払わないと予想している。私たちはすべての利用可能な資金と未来のどんな収益も残し、私たちの業務の発展と拡張に資金を提供するつもりだ
イギリスの法律によると、私たちが十分な分配準備金(非合併ベース)を持っている場合にのみ、配当金を支払うことができます。分配準備金は、私たちが以前に分配または資本化されていなかった累積達成利益から私たちが累積した達成損失を引いたものであり、これらの損失が以前に資本減少や再編で解約されなかった限りです。
私たちの株式報酬計画情報は
表格10-K第5項に要求された当社の株式報酬計画に関する資料は、本年度報告第III部第12項に引用的に組み込まれている。
未登録株式証券販売
2022年、私たちは登録されていない証券を何も売っていない。
発行人が株式証券を購入する
次の表は、2022年12月31日までの3ヶ月間の株式証券の払戻状況をまとめています
| | | | | | | | | | | | | | |
| 期間 | 購入株式総数(A) | 1株平均支払価格(A) | 公開発表の計画の一部として購入した株式総数 | これらの計画によるとまだ購入していない株の約ドルの価値があります |
| | | | |
| 2022年10月1日から10月31日まで | 0 | 0 | 0 | 0 |
| 2022年11月1日から11月30日まで | 0 | 0 | 0 | 0 |
| 2022年12月1日から12月31日まで | 8,986.00 | | $9.20 | 0 | 0 |
| 2022年12月31日までの3ヶ月間 | 8,986.00 | | $9.20 | 0 | 0 |
(A)は、当社の持分インセンティブ計画下の持分奨励帰属に関連する源泉徴収義務を履行するために当社に提出した普通株を表す。
高級証券違約
適用されない
第六項です[保留されている]
プロジェクト7.経営陣の財務状況と経営成果の検討と分析
私たちの財務状況と経営結果に関する以下の議論と分析、および連結財務諸表と本年度報告書に含まれるこれらの報告書に関する付記を読むべきです。歴史財務情報以外に、以下の討論は展望性陳述を含み、著者らがリスクと不確定要素に関連する計画、推定、信念と期待を反映している。私たちの実際の結果と事件の時間は、このような前向きな陳述で議論されているのとは大きく違うかもしれない。これらの差異を引き起こすかまたは促進する可能性のある重要な要素は、本年度報告における表格10−Kに関する以下および他の部分について議論される要素、特に第1の部分1 A項で議論される要素を含む。“リスク要因”と“前向き陳述に関する特別説明”というタイトルの章
“私たち”“私たちの”“私たち”“会社”とはコンパスパス会社のことです
経営実績
概要
著者らは精神健康看護会社であり、患者が精神健康領域の根拠に基づく革新を獲得する機会を加速することに力を入れている。我々の動機は,精神的健康挑戦を受けた人たちを支援し,許可するためのより良い方法を見つける必要があることであり,これらの人々は既存の治療法の助けを得ず,COMP 360ヌードガイキノコ療法を率先して開発しており,COMP 360ヌードガイキノコ療法を心理的支援とともに使用しており,COMP 360ヌードキノコ療法と呼ばれている
我々の最初のポイントは,現在の治療例に十分なサービスを受けていない患者を含むTRDである。我々が開発した裸蓋キノコ製剤ではない学術研究を用いた早期シグナルは,裸蓋キノコ療法はTRD患者の予後を改善する潜在力がある可能性があり,単回大量服用後,抑うつ症状と効果は急速に減少し,6カ月間持続したことが示唆された。2018年,COMP 360治療に対するFDAのTRD突破療法指定を得た。2019年、私たちは89名の健康ボランティアにCOMP 360を応用し、心理支援を提供する第一段階の臨床試験を完成した。この実験では,COMP 360は全体的に耐性が良好であることが観察され,2 b期研究の継続的な進展を支持した。また,1:1の支援の下で,6名もの健康参加者にCOMP 360裸蓋キノコを同時に投与する可能性を証明した
はい2021年11月,われわれの2 b期臨床試験の陽性結果を発表し,COMP 360併用心理支持治療TRDの効果を評価した。2022年11月3日ニューイングランド医学雑誌世界をリードする同業者評議医学雑誌は、著者らの2 b期試験の積極的な結果を発表した。これは今までに完成した最大規模、ランダム、対照、双盲裸蓋キノコ素治療の臨床試験である。2 b期研究の目的は、1用量COMP 360裸蓋キノコ(25 mgまたは10 mg)と1 mg COMP 360裸蓋キノコ素によるTRD患者の治療効果および安全性を評価することである。233名の参加者が参加した試験のTOPLINEの結果によると、心理的支持の下で、COMP 360ヌードマスク治療を1回受けた患者は迅速かつ持続的な反応があり、3週目に29.1%の参加者の病状が緩和した(P)
COMP 360ヌードキノコ治療のTRDを評価するための第3段階計画を始めました第三段階計画は2つの重要な試験からなり、各試験には長期的な後続部分がある。キープログラミングは以下のとおりである
·キー試験1(COMP 005)(n=255):単剤(25 Mg)単一療法はプラセボと対照した。この試験は同社の2 b期試験(n=233)中の治療反応を複製することを目的とした。私たちは2024年夏に収益データを発表する予定だ。
·キー試験2(COMP 006)(n=568):反復用量単一療法を固定し、3用量群:25 mg、10 mg、および1 mgを使用した。この試験は,2回目の用量が治療応答者を増加させ,および/またはわれわれの2 b期試験で観察された反応を改善できるかどうかを調べ,COMP 360 10 mgの重複投与が意義のある治療反応の可能性を探ることを目的としている。私たちは2025年中に収益データを発表する予定だ。
·2つのキーテストの主な終点は、6週目のMADRS総得点とベースラインの変化である。
TRDのほかに,神経性拒食症や創傷後ストレス障害の第二段階試験が行われている
私たちが設立して以来、私たちはほとんどの資源を臨床前研究と臨床試験、組織と私たちの会社、業務計画を配備し、資金を調達し、私たちの知的財産権の組み合わせを構築することに投入した。私たちは販売を許可された治療候補薬もなく、何の収入も得られなかった。これまで、私たちの運営資金は主に転換可能な優先株、転換可能な融資手形の売却、私たちの初公募株(IPO)および私たちがそれぞれ2020年9月と2021年5月に完成した米国預託株式(ADS)の後続発行または後続発行に由来しており、これらの収益はそれぞれ私たちの普通株を代表しています。2022年12月31日現在、転換可能な優先株と転換可能な融資手形の販売から1.164億ドルの現金純収益を獲得し、初公開株と米国預託証券の発行により1兆328億ドルを獲得した 1.548億ドル、私たちの後続製品からのアメリカ預託証明書販売です。2021年10月、Cowen and Company,LLCと販売契約を締結しました。この協定によると、1.5億ドルまでの米国預託証明書を時々市場価格で発行·販売することができ、これを私たちのATM施設と呼ぶことができます。2022年12月31日現在、私たちはATM機のメカニズムでアメリカの預託証明書を販売し、40万ドルの現金純収益を獲得した。
設立以来、私たちは深刻な運営損失が発生した。2022年12月31日と2021年12月31日までの年度の純損失総額はそれぞれ9150万ドルと7170万ドルです。2022年12月31日までの累計赤字は2兆611億ドル。我々の歴史的損失は,主に研究や開発活動に関するコストと,我々の運営に関する一般的かつ行政コストによるものである。未来、著者らは引き続き研究開発、臨床前テスト、臨床試験、法規遵守性、市場参入、商業化と業務発展活動を行い、予想される一般と行政費用を加えて、少なくとも今後数年で更なる重大な損失を招く。我々の運営損失は,主にTRDに対するCOMP 360ヌードカバーキノコ療法の研究開発に起因しており,これらの損失は今後も増加することが予想され,人員配置が増加しているため,TRDが我々の研究用COMP 360ヌードカバーキノコ治療候補に第3段階計画を実施し,神経性拒食症や創傷後ストレス障害に対してより多くの適応に拡大し,異なる治療候補に対して追加の臨床前·臨床計画の開発を開始し,デジタル技術と解決策を用いて治療提供を強化している可能性がある。また、初公募が完了して以来、重大な法律、会計、投資家関係、その他の費用を含む上場企業の運営に関する巨額のコストが発生し続けると予想されている。私たちは私たちの持続的な運営を支援し、私たちの成長戦略を実施するために多くの追加資金を必要とするだろう。治療候補薬の販売から大量の収入を生み出すことができます, 私たちは株式発行、債務融資、政府または他の第三者融資、マーケティングと流通手配、その他の協力、戦略連盟、許可手配を通じて、私たちの運営に資金を提供する予定です。
私たちがより多くの資金を調達する能力は、米国と世界各地のマクロ経済状況、信用と金融市場の中断と変動の悪影響、例えば金利とインフレ率や為替変動の激化や変動による状況、私たちの地域や国の潜在的な景気後退、ウクライナとロシアとの間の持続的な戦争、および新冠肺炎の大流行や他の公衆衛生危機による状況の変化を受ける可能性もある。私たちは必要な時に資金を集めることができず、これは私たちの財務状況や業務戦略を実行する能力に悪影響を及ぼす可能性がある。しかし、私たちの現在の業務計画が達成される保証はなく、私たちが受け入れられる条件で追加的な資金を提供するか、または全く保証されないという保証もない。
2022年12月31日現在、私たちは1億432億ドルの現金と現金等価物を持っている。私たちは、私たちの既存の現金と現金等価物が、少なくとも今後12ヶ月の運営費用と資本支出需要を支払うのに十分になると信じている。私たちは間違っていることが証明される可能性があるという仮定に基づいてこの推定をして、私たちは予想よりも早く利用可能な資本資源を枯渇させるかもしれない。以下の“流動資金と資本資源--資金要件”を参照。
マクロ経済状況
我々は、インフレと金利の激化や変動および米国と世界経済への関連影響、為替変動、ウクライナとロシアの間で行われている戦争、および新冠肺炎疫病による絶えずの変化の状況を含む現在のマクロ経済と地政学的事件に引き続き注目し、それらが私たちの業務にいかなる潜在的な影響を与える可能性があるかどうかを決定する。
私たちの運営結果の構成要素は
収入.収入
これまで、私たちは何の収入も生まれておらず、予測可能な未来に治療候補薬の販売から何の収入も生まれることを望んでいない。COMP 360ヌードゲラクチン療法の開発努力が成功し、規制部門のCOMP 360の承認を得られれば、将来収入が生じる可能性がある。
運営費
研究と開発
研究と開発費は主に
·CROおよびCMO、臨床試験、臨床前研究および他の科学開発サービスを行う調査地点およびコンサルタントとの合意に基づいて発生する費用、および生産拡大費用、臨床前研究および臨床試験および実験室および試験地点用品および設備調達および製造材料の費用を含む開発コスト
·研究·開発機能に従事する従業員の給料、関連福祉、旅費を含む人員費用
·研究·開発機能に従事する従業員に配当金を付与して生成された非現金株式報酬支出;
·その他の費用は、外部コンサルタントの費用、それらの費用および関連する出張費用、直接減価償却費用などの施設関連費用、分配された施設賃貸料および維持費用、およびその他の業務費用を含む。
私たちは発生した費用に応じて研究と開発費用を支払う。我々は,サービスプロバイダが提供してくれた情報に基づいて特定のタスク達成の進捗を評価し,外部開発コストを確認した.これらの活動の支払いは、発生したコストモデルとは異なる可能性がある個別合意に基づく条項であり、私たちの連結財務諸表に前払い費用または計算すべき研究および開発費用として反映される。
研究開発活動は私たちのビジネスモデルの核心だ。臨床開発後期の候補製品や治療薬の開発コストは通常,臨床開発の早期段階よりも高く,これは主に後期臨床試験の規模と持続時間の増加および関連製品製造費用によるものである。したがって,我々は今後数年間,我々の研究開発費が増加することが予想される:(I)TRDに対するCOMP 360裸蓋キノコ療法の臨床開発を求める,(Ii)神経性拒食症や外傷後ストレス障害を含む他の神経精神疾患適応のためのCOMP 360裸蓋素療法の研究に資金を提供する,(Iii)我々の治療法を補完·増強するためのデジタル技術の開発を求め,他の神経·関連適応症開発の新薬候補の獲得を求める,(Iv)第三者製造プロセスとサプライチェーンの効率とスケーラビリティを向上させる;(V)私たちの第三者または内部プロセスの開発、分析と関連能力を確立し、人員コストを増加させ、私たちの潜在的または未来の治療薬候補に関連する規制申告の準備をする。
我々が検討しているCOMP 360ヌードゲラニン療法の開発成功と商業化は非常に不確実である。これは開発と商業化に関連する多くのリスクと不確定要素が含まれているからです
•TRDの第三段階臨床試験を含む臨床試験と前臨床研究の登録に成功し、完成した
•私たちは必要な臨床前研究と臨床試験を達成するのに十分な財政と他の資源を持っていて、私たちは有利な条件であるいは根本的に資金を集めない能力があります
•私たちが計画した臨床試験や将来の臨床試験を行うために規制部門の承認または許可を得る
•私たちの臨床試験から積極的なデータを得て、これらのデータは、COMP 360ヌードカバーキノコ治療の許容可能なリスク-利益の概要およびターゲット集団中の任意の未来の候補治療レジメンをサポートする
•関連する規制機関から規制とマーケティング承認を受けて維持する
•第三者メーカーを通じて、任意の治療候補薬が承認されれば、私たちの臨床試験および商業製造に臨床供給を提供する製造能力を確立し、拡大する
•協力してCOMP 360ヌードカバーキノコ療法と将来の候補療法をさらに発展させます
•COMP 360および任意の将来の候補治療薬の特許および商業秘密保護または規制排他性を取得し、維持する;
•私たちの研究におけるCOMP 360ヌードカバーキノコ療法の商業販売を開始することに成功し、承認されれば、任意の未来の候補療法;
•患者、医学界、および第三者支払人が承認された場合、現在および将来の治療案の候補となる利点および用途を受け入れる;
•承認後,われわれが検討しているCOMP 360裸蓋キノコ療法と将来の候補療法は持続可能な安全性を維持している。
われわれの臨床前および臨床開発における研究的COMP 360ヌードカバーキノコ療法の開発に関するこれらの変数のいずれの結果の変化も,われわれの研究的COMP 360ヌードカバーキノコ療法の開発に関するコストとタイミングの大きな変化を意味する可能性がある。例えば、FDA、欧州医薬品局(European Medicines Agency)またはEMA、薬品および保健製品監督機関(Medicines And Healthcare Products Regulatory Agency)または他の規制機関が私たちの計画した臨床試験の開始を延期したり、現在予想されている臨床試験または他の試験を行うことを要求したり、あるいは任意の計画における臨床試験の登録に重大な遅延がある場合、私たちはこの候補療法の臨床開発を完成するために多くの追加の財務資源と時間を投入する必要があるかもしれない。
一般と行政
一般的で行政的な費用は主に
•いくつかの行政、財務および行政機能者の賃金および関連福祉、出張費およびその他の費用を含む人事費用
•株式奨励による非現金株式報酬支出は、特定の行政、財務、行政機能を担当する従業員のためのものである
•コンサルティング、会計および監査サービスを含む法律および専門費用;
•施設及びその他の費用は、減価償却コスト、施設賃貸料及びメンテナンスのための費用、役員及び役人保険、その他の運営コストを含む。
我々の持続的な研究活動と我々の研究COMP 360裸蓋キノコ療法の開発を支援するために,我々の一般的かつ行政的費用は引き続き大きいと予想される。
また、上場企業として、巨額の会計、監査、法律、規制、コンプライアンスコスト、および上場企業に関連する投資家や広報費用が引き続き発生すると予想しています。また,規制機関が候補治療薬を承認する可能性があると考える場合,ビジネス運営に備えているため,特に候補治療薬の販売やマーケティングに関連する費用,賃金やその他の費用が増加することが予想される。
その他の収入,純額
その他の収入
その他の収入は現金残高による利息と長期外国為替契約に関する確認損益に関連する。
為替損益
為替収益(損失)には外貨取引による為替影響が含まれており,主にポンド機能通貨実体の銀行口座中のドルに関係している.
研究開発税収控除の恩恵を受ける
研究開発税収控除収益には、イギリスで得られた研究開発税収控除が含まれており、この控除は他の収入(費用)、純額に記入されている。幅広い研究·開発活動を展開する会社として、中小企業計画からの利益を求めている。条件に合った支出は主に 研究者の雇用コスト,消耗品,関連する,許容される下請けコストの割合,および研究プロジェクトの一部として生じる何らかの内部間接費用は,収入を得られない。
英国税務·税関総署(HMRC)が制定した基準によると、2022年12月31日と2021年12月31日までの年度内に、我々の管路研究·開発、臨床試験管理、第三者製造開発活動に関する一部の支出は中小企業制度の資格に適合している。今後の会計期間中も、これらの支出要素は中小企業制度の資格に適合し続けることが予想される。
イギリスの研究開発税収控除は全額私たちに返還することができ、現在または未来の課税収入に依存しない。そこで,イギリスが開発した税収控除の全収益を1つの収益として記録し,この収益は我々の所得税前純損失に含まれているため,所得税支出には反映されていない。将来的にイギリスの企業所得税債務を相殺するためにイギリスの研究開発税控除が必要であれば、この部分は福祉として所得税支出に記録され、課税収入に依存しない返却可能な部分は他の収入(費用)純額に記録され続ける。
所得税費用
私たちはアメリカとイギリスで会社税を払わなければなりません。私たちの業務性質のため、私たちは設立以来赤字が生じたため、イギリスの会社税を納めていません。私たちの所得税支出はアメリカでは所得税だけを代表する。
未納のイギリスの赤字は無期限に繰り越す可能性があり、将来の課税利益によって相殺される可能性があるが、多くの利用基準と制限を守らなければならない。毎年相殺できる金額は500万GBとイギリスの課税利益の50%に制限されている。課税項目控除を計上した後、2022年と2021年12月31日まで、私たちのイギリスでの累計繰越取引損失はそれぞれ1兆769億ドルと1.44億ドルで、全額推定準備金によって相殺された。
2022年12月31日と2021年12月31日までの年間で,米国での運営会社の所得税義務に関連して40万ドルと20万ドルの税収配分を記録し,税収目的のための利益を生み出している
経営成果
2022年12月31日までおよび2021年12月31日までの年度比較
次の表は、2022年12月31日と2021年12月31日までの年間運営結果(単位:千)をまとめたものです
| | | | | | | | | | | | | | | | | | | | |
| 十二月三十一日までの年度 | | | |
| 2022 | | 2021 | | 変わる | |
| 運営費用: | | | | | | |
| 研究開発 | $ | 65,053 | | | $ | 44,027 | | | $ | 21,026 | | |
| 一般と行政 | 45,350 | | | 39,194 | | | 6,156 | | |
| 総運営費 | 110,403 | | | 83,221 | | | 27,182 | | |
| 運営損失 | (110,403) | | | (83,221) | | | (27,182) | | |
| 他の収入、純額: | | | | | | |
| その他の収入 | 4,061 | | | 40 | | | 4,021 | | |
| 外国為替収益 | 821 | | | 1,990 | | | (1,169) | | |
| 研究開発税収控除の恩恵を受ける | 14,424 | | | 9,648 | | | 4,776 | | |
| その他の収入合計,純額 | 19,306 | | | 11,678 | | | 7,628 | | |
| 所得税前損失 | (91,097) | | | (71,543) | | | (19,554) | | |
| 所得税費用 | (408) | | | (199) | | | (209) | | |
| 純損失 | $ | (91,505) | | | $ | (71,742) | | | $ | (19,763) | | |
研究と開発
次の表は、2022年12月31日と2021年12月31日までの年間で発生した研究開発費(単位:千)をまとめたものです | | | | | | | | | | | | | | | | | | | | |
| 十二月三十一日までの年度 | | | |
| 2022 | | 2021 | | 変わる | |
| 開発費 | $ | 34,342 | | | $ | 27,618 | | | $ | 6,724 | | |
| 人員費 | 16,662 | | | 10,538 | | | 6,124 | | |
| 非現金株式給与費用 | 7,358 | | | 4,569 | | | 2,789 | | |
| その他の費用 | 6,691 | | | 1,302 | | | 5,389 | | |
| 研究開発費総額 | $ | 65,053 | | | $ | 44,027 | | | $ | 21,026 | | |
2022年12月31日までの1年間で、研究開発費は2100万ドル増加し、2021年12月31日現在の4400万ドルから6510万ドルに増加した。研究開発費が増加した要因は
•外部開発費用は670万ドル増加し、主に臨床前研究費用460万ドル、薬物開発と製造費用260万ドル、デジタル活動費用50万ドル、セラピスト訓練費用30万ドルに関連しているが、第二段階研究を完成させるために減少した臨床試験費用130万ドルは増加した費用を相殺した
•人件費が610万ドル増加したのは主に私たちの研究と開発部門が人員を増やして、私たちの数字、臨床前、臨床チームの拡大を支持するからです
•従業員数が前年比増加したため、非現金株の報酬支出は280万ドル増加し、2022年8月に私たちの新任最高経営責任者にインセンティブが与えられ、2022年2月には全社のオプション奨励が授与された。2021年には同じような会社全体の支出がありませんでした
•その他の費用は540万ドル増加し、主に研究開発外部相談費用360万ドル、商業前支出110万ドル増加し、臨床試験保険、ITと出張コストは70万ドル増加した。
研究開発コストは近い将来大幅に増加することが予想され、これは引き続き推進していきます2023年TRD COMP 360ヌードカバーキノコ治療3期計画.
一般と行政
次の表は、2022年12月31日と2021年12月31日までの年度の一般と行政費用(千単位)をまとめています | | | | | | | | | | | | | | | | | |
| 十二月三十一日までの年度 | | |
| 2022 | | 2021 | | 変わる |
| 人員費 | $ | 17,160 | | | $ | 13,999 | | | $ | 3,161 | |
| 非現金株式給与費用 | 5,765 | | | 4,070 | | | 1,695 | |
| 弁護士費と弁護士費 | 11,404 | | | 8,654 | | | 2,750 | |
| 施設やその他の費用 | 11,021 | | | 12,471 | | | (1,450) | |
| 一般と行政費用総額 | $ | 45,350 | | | $ | 39,194 | | | $ | 6,156 | |
2022年12月31日までの1年間で、一般·行政費は620万ドル増加し、2021年12月31日現在の3920万ドルから4540万ドルに増加した。一般費用と行政費用が増加した要因は以下のとおりである
•人件費が320万ドル増加したのは、上場企業としての運営を含め、一般、行政、ビジネス部門の人員編成が増加したためである
•従業員数が前年比増加したことにより、非現金株の報酬支出が170万ドル増加し、2022年8月に私たちの新任最高経営責任者にインセンティブが与えられ、2022年2月に全社のオプション奨励が授与された。2021年には同じような会社全体の支出はありません
•法律や専門費用は280万元増加し、主に外部相談、公共関係、特許出願や法律相談に関する費用、上場企業の運営に関する持続的なコスト、およびわが業務の増加に伴う他社活動に用いられている
•施設やその他の費用は150万ドル減少しましたp主な原因は保険料は110万ドル、英才センター費用は60万ドル、通信費は20万ドルです。支援と他の寄付金は40万ドル増加し、この増加を相殺した
研究開発成長計画の継続的な一般的かつ行政的支援に加え、上場企業として、継続的な要求により、巨額の一般·行政費用が発生し続けることが予想される。
その他の収入,純額
その他の収入
2022年12月31日までの1年間、その他の収入は410万ドルで、2021年12月31日までの1年間、他の収入は10万ドル未満だった。その他の収入の増加は、主に現金預金金利の上昇による利息収入の増加と、2022年第3四半期に締結して決済した長期外国為替契約で確認された280万ドルの収益である。
為替損益
2022年12月31日までの1年間、外国為替収益は120万ドル減少し、収益は80万ドルだったが、2021年12月31日までの年間収益は200万ドルで、主に初公募株収益とその後の発行収益の転換による現金残高による収益に関係しており、これらの収益はドルで保持されており、外貨収益を発生させる法人実体の機能通貨(ポンド)とは異なる現在、私たちのドル残高はポンド機能通貨法人で持っていて、必要に応じてポンドに変換します。主な現金の流出はポンドですから。私たちの運営モデルと業務の発展に伴い、私たちは引き続き私たちの法人実体構造を監視して評価し、私たちの将来の現金流出はポンドで報告し続けるかドルで報告するか、為替レートが私たちの運営結果に与える持続的な影響を監視して評価します。
研究開発税収控除の恩恵を受ける
2022年と2021年12月31日までの年間で,英国からの研究開発税控除を他の収入(支出)における福祉として確認し,それぞれ純額は1,440万ドル,960万ドルであった。研究開発活動の増加により、2022年の研究開発税収控除の収益は2021年より480万ドル増加した。
所得税費用
この年度の所得税支出は40万ドルである2022年12月31日まで20万ドルを使って2021年12月31日までの年度それは.所得税支出は、米国における当社の運営会社の所得税義務に関係しており、同社は税収目的で利益を生み出している。
経営成果
2021年12月31日までと2020年12月31日までの年度比較
次の表は、2021年12月31日と2020年12月31日までの年間運営結果(単位:千)をまとめたものです
| | | | | | | | | | | | | | | | | |
| 十二月三十一日までの年度 | | |
| 2021 | | 2020 | | 変わる |
| 運営費用: | | | | | |
| 研究開発 | $ | 44,027 | | | $ | 23,366 | | | $ | 20,661 | |
| 一般と行政 | 39,194 | | | 28,027 | | | 11,167 | |
| 総運営費 | 83,221 | | | 51,393 | | | 31,828 | |
| 運営損失 | (83,221) | | | (51,393) | | | (31,828) | |
| その他の収入(費用)、純額: | | | | | |
| その他の収入 | 40 | | | 319 | | | (279) | |
| 為替損益 | 1,990 | | | (11,702) | | | 13,692 | |
| 転換可能手形の公正価値変動 | — | | | (1,771) | | | 1,771 | |
| 研究開発税収控除の恩恵を受ける | 9,648 | | | 4,245 | | | 5,403 | |
| その他の収入を合計して純額 | 11,678 | | | (8,909) | | | 20,587 | |
| 所得税前損失 | (71,543) | | | (60,302) | | | (11,241) | |
| 所得税費用 | (199) | | | (32) | | | (167) | |
| 純損失 | $ | (71,742) | | | $ | (60,334) | | | $ | (11,408) | |
研究と開発
2021年12月31日と2020年12月31日までの年間で発生した研究開発費(単位:千)をまとめた表 | | | | | | | | | | | | | | | | | |
| 十二月三十一日までの年度 | | |
| 2021 | | 2020 | | 変わる |
| 開発費 | $ | 27,618 | | | $ | 11,553 | | | $ | 16,065 | |
| 人員費 | 10,538 | | | 4,563 | | | 5,975 | |
| 非現金株式給与費用 | 4,569 | | | 6,336 | | | (1,767) | |
| その他の費用 | 1,302 | | | 914 | | | 388 | |
| 研究開発費総額 | $ | 44,027 | | | $ | 23,366 | | | $ | 20,661 | |
2021年12月31日までの1年間で、研究開発費は2070万ドル増加し、2020年12月31日までの2340万ドルから4400万ドルに増加した。研究開発費が増加した要因は
•外部開発費用が1,610万ドル増加したのは、主に臨床試験費用が1,510万ドル増加し、私たちの研究性COMP 360ヌードカバー素治療開発のために追加適応を評価する臨床前研究費用が40万ドル増加し、法規遵守費用が30万ドル増加し、薬物開発と製造コストが30万ドル増加したためである
•人員費が600万ドル増加したのは私たちの研究開発部門が私たちのデジタル活動の拡張と臨床活動の増加を支援するために人員を増加させたからです
•非現金株式の給与が180万ドル減少したのは、主に2020年5月に1人の従業員に多額のオプションが付与され、2020年8月17日に完全に帰属したため、2020年12月31日までの年間で株式ベースの報酬支出950万ドルが確認され、そのうち240万ドルが研究開発費に割り当てられており、これは間接的に研究開発活動を支援する時間から推定されている。また、株式購入条項に基づいて初回公開募集が完了した後にいくつかの他の購入株権の付与を加速し、2020年に350万ドルの株式ベースの報酬支出を確認し、その中の140万ドルは2020年12月31日までの年度末までの研究開発活動を支援するための時間に従って研究開発費を分配する。2021年12月31日までの年間では、類似支出は確認されていない。この前年比減少幅は、2021年12月31日までの年間に他の従業員に付与されたオプションによる非現金株報酬の200万ドル増加によって相殺された
•その他の費用は40万ドル増加し、主な理由は外部相談費用が増加したからだ。
一般と行政
次の表は、2021年12月31日と2020年12月31日までの一般と行政費用(千単位)をまとめています | | | | | | | | | | | | | | | | | |
| 十二月三十一日までの年度 | | |
| 2021 | | 2020 | | 変わる |
| 人員費 | $ | 13,999 | | | $ | 6,084 | | | $ | 7,915 | |
| 非現金株式給与費用 | 4,070 | | | 11,647 | | | (7,577) | |
| 弁護士費と弁護士費 | 8,654 | | | 6,827 | | | 1,827 | |
| 施設やその他の費用 | 12,471 | | | 3,469 | | | 9,002 | |
| 一般と行政費用総額 | $ | 39,194 | | | $ | 28,027 | | | $ | 11,167 | |
2021年12月31日までの1年間に、一般·行政費は1,120万ドル増加し、2020年12月31日現在の2,800万ドルから3,920万ドルに増加した。一般費用と行政費用が増加した要因は以下のとおりである
•人件費が790万ドル増加したのは、上場企業としての経営と、元法律顧問や首席法律幹事の退職に関する解散費など、一般的、行政、ビジネス機能の人員配置が増加したためである
•非現金株式の給与が760万ドル減少したのは、主に2020年5月に従業員に大型オプションが付与されたためであり、2020年8月17日に完全に帰属し、2020年12月31日までの年間株式ベースの報酬支出950万ドルが確認され、そのうち710万ドルが一般および行政費用に割り当てられており、一般および行政活動を間接的に支援する時間から推定されている。また、株式購入条項に基づいて初回公募後にいくつかの他の株式購入権の帰属を加速し、2020年に350万ドルの株式ベースの給与支出を確認し、その中の210万ドルは一般及び行政活動を支持するのにかかる時間によって一般及び行政支出に分配される。2021年12月31日までの1年間、同様の加速費用は確認されていない。2021年12月31日までの1年間で、他の従業員にオプションを付与したため、非現金株式の給与が160万ドル増加し、前年比低下の影響を相殺した
•法律および専門費用は180万ドル増加し、主に外部コンサルティング、特許出願、法律相談に関連する費用、および外国の民間発行者から新興成長型企業の地位およびSarbanes Oxley 404(B)要求に関連する追加監査費用への移行、および他の企業活動を含む上場企業の運営に関連する費用、および他の会社活動に関連して、先行準備上場企業の運営に関連する法律コストおよび他の間接費用と比較して、他の企業活動に関連する
•施設やその他の費用は900万ドル増加し、主に役員と役人の保険費用の360万ドルの増加、特許出願費用100万ドル、英才センター費用80万ドル、企業伝播戦略と実施費用70万ドル、ITと事務用品、サービスとソフトウェア100万ドル、レンタル料80万ドル、購読と会員費40万ドル、その他の費用70万ドルと関係があり、これらはすべて会社の2021年の増加と一致している。
その他の収入を合計して純額
研究開発税収控除の恩恵を受ける
2021年12月31日と2020年12月31日までの年間で,英国からの研究開発税控除を他の収入(支出)における福祉と確認し,それぞれ純額は960万ドルと420万ドルであった。研究開発活動の増加により、2021年の課税額は2020年に比べて増加している。2020年の税金控除は2021年に全額受領される。
転換可能手形の公正価値変動
交換可能手形の公正価値変動は2019年12月31日までに年度に発行された交換可能手形に関連し、この手形は2020年4月にBシリーズ交換可能優先株に変換される。2021年12月31日までの年間では,このような変化は認められなかった。
為替損益
2021年12月31日までの年度は、為替収益(赤字)が1370万ドル増加し、2020年12月31日までの年度損失1170万ドルから200万ドルに増加し、主に初公募株収益による現金残高転換による収益とドルで維持される後続発行収益に関係しており、外貨収益を発生させる法人実体の機能通貨(ポンド)とは異なる。現在、私たちのドル残高はポンド機能通貨法人実体に保管されており、必要に応じてポンドに変換されています。主な現金の流出はポンドですから。私たちの運営モデルと業務の成熟に伴い、私たちは私たちの法的実体構造と、私たちの将来の現金流出がポンドやドルで報告され続けるかどうかを監視し、評価し続けるつもりだ。
その他の収入
2021年12月31日と2020年12月31日までの年間収入は、それぞれ10万ドルと30万ドル未満。その他の収入減少の主な原因は現金預金金利の低下による利息収入の減少である。
所得税費用
2021年12月31日までの1年間の所得税支出は20万ドルで、2020年12月31日までの1年間、所得税支出は10万ドル未満だった。所得税支出は、米国における当社の運営会社の所得税義務に関係しており、同社は税収目的で利益を生み出している。
流動性と資本資源
私たちは臨床段階の精神ヘルスケア会社で、これまで何の収入も生まれていません。設立以来、私たちは重大な運営損失が発生した。候補治療薬はまだ商業化されておらず,将来的にはどの治療候補薬の販売からも収入は生じないと予想される。これまで、私たちの運営資金は主に私たちの初公募株と後続発行で転換可能な優先株、転換可能なローン手形、アメリカ預託証明書を売却した収益から来ています。2022年12月31日現在、転換可能な優先株と転換可能な融資手形の売却による現金純収益は1.164億ドル、IPOによる米国預託証券の売却による純収益は1.328億ドル、後続発行の純収益は1.548億ドルである。2022年12月31日現在、ATM施設下の米国預託証券を売却することで40万ドルの現金純収益を得た2022年12月31日現在、私たちの既存の1兆432億ドルの現金残高は、少なくとも今後12ヶ月の運営費用と資本支出需要を支払うのに十分だと信じている。
キャッシュフロー
次の表は、私たちの各時期のキャッシュフロー(千単位)をまとめています | | | | | | | | | | | | | | | | | |
| 十二月三十一日までの年度 |
| 2022 | | 2021 | | 2020 |
| 経営活動のための現金純額 | $ | (105,451) | | | $ | (67,745) | | | $ | (41,380) | |
| 投資活動のための現金純額 | (596) | | | (334) | | | (628) | |
| 融資活動が提供する現金純額 | 1,040 | | | 156,646 | | | 194,155 | |
| 現金、現金等価物および限定現金に及ぼす為替レート変動の影響 | (24,959) | | | (5,576) | | | 13,225 | |
| 現金、現金等価物および制限現金純額(減少)/増加 | $ | (129,966) | | | $ | 82,991 | | | $ | 165,372 | |
経営活動に使われている現金純額
2022年12月31日までの年間で、経営活動で使用されている現金純額は1.055億ドルで、主な原因は9140万ドルの純損失であり、110万ドルの外貨再計量非現金収益、1310万ドルの非現金株式による給与支出、30万ドルの減価償却と償却、210万ドルの非現金レンタル費用によって相殺されている。純損失はまた3070万ドルを調整し、これは運営資本構成要素の変化と関係があり、主に研究開発税収相殺と前払い研究開発支出に関する前払い支出とその他の流動資産の2880万ドルの増加、繰延と前払い税収資産の170万ドルの増加、実施コストの増加に関連する他の資産の30万ドルの増加、支出とその他の負債の30万ドルの減少、経営リース負債の200万ドルの減少を含むが、主に本四半期に受け取った研究と開発領収書に関する売掛金の250万ドルの増加が純損失の影響を相殺した。
2021年12月31日までの年間で、経営活動で使用されている現金純額は6770万ドルであり、主な原因は私たちの純損失7170万ドルであり、非現金株式による給与支出860万ドル、減価償却と償却20万ドルおよび非現金賃貸支出180万ドルで相殺されている。純損失も480万ドルの調整が行われ、これは主に研究開発税収控除と前払い研究開発費用に関する前払い費用とその他の流動資産の900万ドルの増加を含む運営資本構成要素の変化と関係があり、主に私たちの新しいロンドンオフィス賃貸の保証金に関する他の資産の20万ドルの増加、および繰延と前払い税金資産の90万ドルの増加を含むが、売掛金と主に臨床試験コストおよび法律と専門費用の増加に関連する課税費用の増加は530万ドルの増加を相殺した。この成長には、ASC 842の採用に関連する190万ドルの非現金運営リース負債も含まれている。
2020年12月31日までの年間で、経営活動で使用されている現金純額は4,140万ドルであり、主な原因は、私たちの純損失6030万ドルが、非現金株式による給与支出1800万ドル、減価償却、償却10万ドル、および転換手形公正価値変化180万ドルの損失によって相殺されているからである。純損失はまた、研究開発税控除と前払い保険に関連する前払い費用と他の流動資産の450万ドルの増加、繰延税金資産の20万ドルの増加、臨床前と臨床試験で発生した研究と開発費用の増加に関する売掛金と売掛金の390万ドルの増加によって相殺され、上場準備のために発生した専門と法律費用の増加による一般と行政支出の増加を含む運営資本の構成要素の変化に関連する90万ドルによって調整されている。
投資活動のための現金純額
2022年と2021年12月31日までの年間で、投資活動のための現金純額はそれぞれ60万ドルと30万ドルであり、主に物件や設備を購入したためであり、主に実験室とオフィス設備が含まれているからである。
2020年12月31日までの年間、投資活動のための現金純額は60万ドルで、Delix治療会社の8%(完全希釈ベース)の株式を買収する50万ドルの投資と、不動産や設備を購入する10万ドルを含む。Delix治療会社は中枢神経系の適応を研究する新しい小分子の薬物発見·開発会社である。
融資活動が提供する現金純額
2022年12月31日までの年間で、融資活動が提供する現金純額は100万ドルで、主にオプション行使の収益40万ドル、ATMによる普通株発行の収益40万ドル、従業員の株式購入計画に基づいて株を発行する収益20万ドルに及ぶ。
2021年12月31日までの年間で、融資活動が提供する現金純額は1兆566億ドルで、主に1億548億ドルの後続発行とオプション180万ドルの純収益に関係している。
2020年12月31日までの年間で、融資活動が提供する現金純額は1.942億ドルで、主にBシリーズ転換可能優先株の売却·発行による現金純額6,130万ドルと、初公募時の米国預託証券の売却·発行による現金純額1.328億ドルに関係している。
現金、現金等価物および限定現金に及ぼす為替レート変動の影響
2022年12月31日までの年間では、為替変動が現金、現金等価物、制限的現金に与える影響により為替損失が2,500万ドルになったが、前年同期に560万ドルの損失があり、2020年に1,320万ドルの利益が得られたのは、主に期間間の為替レートの変動により、ポンド機能通貨で保有している実体が保有する現金残高に為替損失が生じ、報告通貨ドルに換算されたためである。
資金需要
われわれが行っている活動に関する費用は引き続き大幅に増加することが予想され,特にTRDのCOMP 360第三段階臨床計画の推進およびCOMP 360の臨床前活動,製造,第二段階臨床試験を継続した場合である。また、上場企業として、重大な法律、会計、投資家関係、その他の費用を含む運営に関連した巨額のコストを引き続き発生させることを予想している。私たちの支出も増えますなぜなら私たちは
•TRDでの第3段階計画に関するコストを含めて,ヨーロッパや北米各地の積極的な臨床試験地点でCOMP 360ヌードカバーキノコ療法の臨床開発を継続している
•第二段階の研究を行い、COMP 360裸蓋キノコによる神経性拒食症と創傷後ストレス障害患者の安全性と耐性を評価した
•公立医療機関や個人診療所とネットワークを構築し、承認されれば、これらの機関と個人診療所は私たちの研究COMP 360ヌードカバーキノコ療法を管理します
•私たちの臨床試験で私たちの研究COMP 360ヌードゲラクチン療法を提供するために、合格した治療師、精神病学者、および他の医療専門家の訓練を継続した
•販売、マーケティング、流通インフラ、および大規模製造能力を確立し、COMP 360を含む任意の候補治療、治療会議、またはデジタル支援を商業化する
•デジタル技術と解決策を使って私たちの治療サービスを強化することを含め、ヨーロッパと北米でのビジネス化戦略を推進します
•他の臨床前段階候補治療計画と発見段階計画の研究開発計画を続けてください
•治療候補薬の発見および/または開発
•臨床試験に成功した候補治療薬のために監督管理の承認を求める
•規制承認を受ける可能性のある制御物質を含む候補治療薬を商業化することができるように、必要なスケジュールに関する決定を求めた
•買収、協力、許可取引を通じて外部業務の発展機会を探索し、私たちのルートを強化し、そして私たちの製品の組み合わせにもっと多くの候補治療薬物を増加させる
•いわゆる特許または他の知的財産権侵害クレームの弁護に関連する訴訟費用を含む、私たちの知的財産権の取得、維持、拡大、および保護の組み合わせ
•私たちの治療開発および潜在的な将来の商業化努力を支援する人員を含む、臨床、科学、操作、財務および管理情報システムおよび人員を増加させる;
•アメリカ、ヨーロッパ、その他の潜在的な地域での私たちの業務を拡大します
•米国に上場する上場企業としての運営に関する追加法律、会計、その他の費用;
•シェパード·プラットとのパートナーシップを通じて,新興ファンタジー療法の研究加速に努めている。
今持っている現金を信じています1兆432億ドル2022年12月31日までに、少なくとも今後12ヶ月の運営費と資本支出需要を支払うのに十分である。私たちは間違っていることが証明される可能性があるという仮定に基づいてこの推定をして、私たちは期待よりも早く利用可能な資本資源を利用することができる。我々の開発計画や規制審査過程の進展に伴い,製品製造,商業化前の活動,商業化に関連した巨額の商業化費用が発生することが予想される。
候補治療薬やプロジェクトの研究,開発,商業化に関連する多くのリスクと不確実性のため,我々の運営資金需要の正確な金額を見積もることはできない。私たちの将来の資金需要は多くの要素に依存し、それによって大幅に増加するかもしれない
•神経性拒食症および創傷後ストレス障害を含むTRD以外の適応またはTRD以外の任意の未来候補治療方法;COMP 360によるTRD治療の第3段階臨床計画の進展、時間および完了状況、ならびにTRD以外の適応またはTRD以外の任意の未来候補治療方法;
•FDA、EMA、MHRA、および同様の外国規制機関の規制承認の結果、時間、およびコストを求め、取得し、これらの機関は、私たちが現在予想しているよりも多くの非臨床研究または臨床試験を行うことを要求するか、または以前に合意された研究に対する彼らの要求を変更することを要求するかもしれない
•アメリカ麻薬取締局、各州、外国当局のようなスケジュールに関する決定の結果と時間
•私たちは開発された潜在的な新しい治療候補薬の数を決定し、私たちの研究開発努力によって内部で行われても、買収、許可、または他の協力協定によって外部で行われている
•英才センターを研究施設と革新実験室として設立と維持するコストは、著者らが新しい精神衛生保健モデルを創立する雄心と一致している
•私たちの研究開発部門ではデジタル活動の拡張にかかるコストを支援するために多くの人を雇っています
•私たちの組織を私たちの研究性COMP 360ヌードカバーキノコ療法と将来の候補療法の研究、開発、潜在的商業化に必要な規模に発展させるコストに発展させた
•特許出願の提出、特許の維持および実施、または第三者からの侵害クレームの抗弁に係る費用;
•COMP 360または将来の候補治療薬の規制承認を得ることに関連する時間およびコスト、ならびに持続的に変化する規制要件またはCOMP 360または任意の将来の候補治療薬に関する不利な結果によって遭遇する可能性のある遅延;
•我々の研究COMP 360ヌードカバーキノコ療法または任意の将来の候補療法の潜在的商業化に関連する販売およびマーケティング活動(承認された場合)、および効果的な販売およびマーケティング組織を作成することに関連するコスト;
•私たちは、COMP 360ヌードカバーキノコ療法および将来の候補療法(承認された場合)の将来の販売から直接または特許使用料の形で得られる収入金額;および
•上場企業の運営コストとして。
利益を達成するのに十分な製品収入を生成することができる前に、株式発行、債務融資、政府または他の第三者資金、マーケティングおよび流通手配、その他の協力、戦略連合、許可手配によって、私たちの現金需要を満たすことが予想される。他の資金調達は全く得られないかもしれないし、受け入れ可能な条項で提供できないかもしれない。ある程度、私たちは株式を売却することで追加資本を調達し、現在の所有権権益は希釈されるだろう。もし私たちが政府または第三者資金、協力協定、戦略連合、許可手配、またはマーケティングおよび流通手配を通じて追加資金を調達する場合、私たちは将来の収入源、研究計画または候補治療案を放棄しなければならないか、または私たちに不利になる可能性のある条項で許可証を付与しなければならないかもしれない。債務融資が可能であれば、追加債務を招く、資本支出を行う、または配当を宣言するなど、私たちが具体的な行動をとる能力を制限または制限する契約を含む高金利または合意に関連する可能性がある。もし私たちが必要な時に追加資金を集めることができない場合、私たちは私たちの製品開発や将来の商業化努力を延期、制限、減少または終了することを要求されるかもしれません。あるいは私たちが自分で開発し、マーケティングしたい製品または候補治療薬を開発し、マーケティングする権利を与えることができます。
重要な会計政策と重大な判断と見積もり
私たちの総合財務諸表はアメリカ公認会計基準に基づいて作成されました。我々の連結財務諸表および関連開示を作成する際には、総合財務諸表における資産、負債、コストおよび費用に影響を及ぼす報告金額、または資産および負債の開示に影響を及ぼす推定および判断を行う必要がある。我々は,歴史的経験,既知の傾向や事件,および当時の状況で合理的と考えられる様々な他の要因に基づいて推定し,これらの要因の結果は資産や負債の帳簿価値の判断の基礎を構成しているが,これらの資産や負債の帳簿価値は他の源から容易に見られるものではない.私たちは持続的な基礎の上で私たちの推定と仮定を評価する。異なる仮定や条件の下で、私たちの実際の結果はこれらの推定とは異なる可能性がある。
我々の主な会計政策は、我々の総合財務諸表付記2により詳細に記載されているが、以下の会計政策は、我々の総合財務諸表の作成に使用される判断と推定に最も重要であると考えられる。
前払いと課税の研究と開発費用
連結財務諸表作成過程の一部として,前払いと計上すべき研究·開発費用を見積もる必要がある。このプロセスは、未締結契約および調達注文を審査し、私たちの担当者とコミュニケーションして、私たちに代わって実行されるサービスを決定し、インボイスを受け取っていない場合、または他の方法で実際のコストを通知している場合に、実行されたサービスレベルおよびサービスによって生じる関連コストを推定することを含む。私たちは、私たちが当時知っている事実と状況に基づいて、連結財務諸表において、各貸借対照表の日付までの前払いと計上費用を推定します。我々は定期的にサービスプロバイダとこれらの推定の正確性を確認し,必要に応じて調整する.今まで、そのような調整は実質的ではなかった。前払いおよび計算すべき研究開発費用の推定部分は、CRO、CMOおよび他の第三者サービスプロバイダから受信されたタイムリーかつ正確な報告に依存する。推定された前払いおよび計算された研究および開発費用の例は、以下のように支払われる
•臨床前開発活動に参加したサプライヤー
•臨床前研究と臨床試験に関するCROと研究場所;
•臨床前研究と臨床試験材料の薬物物質と薬物製品の配合に関するCMOS。
我々は,臨床前研究や管理を行っている複数の研究機関とCROのオファーや契約に基づいて,受信したサービスや費用の見積もりに基づいて,前臨床研究や臨床試験に関する費用を計算している
私たちに代わって研究と臨床試験を行います。これらの合意の財務条項は交渉が必要であり、契約によって異なり、支払いの不均衡を招く可能性がある。場合によっては、私たちのサプライヤーに支払われるお金は、提供されたサービスレベルを超え、事前支払い費用につながる可能性があります。
その中のいくつかの契約下の支払いは患者の成功登録と臨床試験マイルストーンの完成などの要素に依存する。サービス料を計算する際に、サービスを提供する時間帯と各時間の努力度を見積もります。サービスの実行時間や努力の程度が推定値と異なる場合には,それに応じて計算すべき費用や前払い費用の金額を調整する.実際に発生した金額と実質的に異なることはないと予想されるが、提供されたサービスの実際の状態および時間に対する提供サービスの状態および時間の理解が異なる可能性があり、報告された金額が任意の特定の時期に高すぎたり、過小になったりする可能性がある。これまで,我々が計算した研究や開発費の先行推定には何の大きな調整もなかった.
研究開発奨励金と売掛金
私たちはイギリスで会社税を払わなければならない。私たちの業務の性質のため、私たちは設立以来赤字が発生しました。研究開発または研究開発税収控除からの収益は、私たちの総合運営と全面赤字報告書の中で他の収入(費用)の純額の構成要素として確認され、私たちがイギリスで回収可能な研究開発税収控除の合計を代表する。
各報告期間では、どのイギリスの研究開発税免除計画に参加する資格があると予想されているかを評価し、どのような申請を提出する予定であり、最終的にこの金額を達成することが合理的に保証されています。
イギリスの研究開発税収控除は全額私たちに返還することができ、現在または未来の課税収入に依存しない。そこで,イギリスが開発した税収控除の全収益を収益として記録し,我々の所得税前純損失に含まれているため,我々の所得税支出には反映されていない。将来的にイギリスの企業所得税債務を相殺するためにイギリスの研究開発税控除が必要であれば、この部分は福祉として所得税支出に記録され、課税収入に依存しない返却可能な部分は他の収入(費用)純額に記録され続ける。
ある会社として、私たちは広範な研究開発活動を展開しているため、イギリスの中小企業計画下の研究開発税収免除制度の恩恵を受けている。私たちは、これらの活動や支出の性質が中小企業制度下の信用条件に適合しているかどうか、およびクレームが最終的にイギリス政府が制定した精算許可基準に基づいて実現されるかどうかを決定するために、我々の研究開発活動と支出を評価した。中小企業制度の下で、資格に適合した研究開発活動による取引損失の一部を返金し、当該などの資格に適合した研究開発支出の33.35%までの現金リベートを得ることができる。私たちは中小企業制度の条件を満たしている。条件に適合した支出には,主に研究開発活動を直接または間接的に支援する研究者の雇用コスト,消耗品,アウトソーシング契約研究組織コスト(下請けコストとみなされる)と,我々の研究プロジェクトの一部として生じる公共事業コストがある。ある下請けの合格した研究開発支出は21.67%に達する現金リベートを得る資格がある。研究開発、臨床試験、製造活動に関連する大部分のコストは、私たちの税金控除現金払い戻し申請に含まれる資格があります。総雇用コストには,個人が研究開発活動にかかる時間配分に関する判断と見積りが含まれている。これらの推定は,異なるチームメンバにかかる時間,非研究開発関連イベントの考慮,および一般的な日常活動のようなリアルタイムデータに基づいている.これらの見積りは,条件を満たす研究開発活動にかかる総時間の最も正確な表示に基づいている.消耗品の分類, アウトソーシング契約研究組織費と公共事業費は、このような費用の直接的な性質に対する管理職の判断に基づいて決定される。発生するコストは会社が研究開発活動に従事することと直接関連している。
2022年、2021年、2020年12月31日までの会計年度には、それぞれ研究開発税控除から1440万ドル、960万ドル、420万ドルの純収益を得た。
払い戻しはポンドで計算されますので、売掛金は報告日ごとにドルに再計量されます。2022年と2021年12月31日までに、英国政府から得た税収インセンティブはそれぞれ1400万ドルと960万ドルだった。2021年に710万ポンドでクレームされたクレジットは2022年に全額受け取り、金額は850万ドル。
株式ベースの報酬
私たちは授与日の公正価値に基づいて、従業員、非従業員、取締役に付与された非現金株式奨励を測定します。没収は発生状況に応じて計算されます。私たちはサービスベースの帰属条件を持った非現金株式ベースの奨励を発行します。サービス条件に応じて付与された持分報酬については、非現金株式補償費用が必要なサービス期間内に直線ベースで確認される。
普通株式公正価値の決定
私たちの普通株の公正価値は私たちの普通株の市場見積もりに基づいて決定された。
当社が初めて公募する前に、当社の普通株は公開市場を持っていないため、当社の普通株の推定公正価値は当社取締役会が毎回の授与日に決定し、管理層の意見を考慮し、当社の普通株の最新の第三者推定値と、当社取締役会が関連していると考え、最近の推定日から授出日までの間に変化する可能性のある追加的な客観及び主観的要素の評価を考慮した。これらの第三者推定値は、発行された個人持株会社株式証券の推定値を補償するための米国公認会計士協会会計と推定ガイドラインで概説された指導に基づいて行われる。初公募終了後に私たちの普通株のための公開取引市場を構築した後、私たちの取締役会は私たちが付与した株式奨励の会計について私たちの普通株の公平な市場価値を推定する必要がなくなりました。
株式購入公正価値の決定
我々は、付与日の公正価値に基づいて、従業員及び取締役会メンバーに取締役としてのサービスの購入権を測定し、必要なサービス期間内の当該等購入持分の相応の補償費用を確認し、このサービス期間は、通常、相応の持分購入の帰属期間である。我々はサービス帰属条件に基づく株式オプションのみを発行し,直線法を用いてこれらの報酬の費用を記録した.
私たちは、私たちの普通株の最初の公募前の公正価値、または公正価値の推定、および私たちの普通株式変動性、私たちの株式オプションの期待期限、私たちの株式オプションの期待期間に近い期間の無リスク金利、および私たちの期待配当収益率に対する仮定を使用して、ブラック-スコアーズオプション価格モデルを使用して、付与された各株式オプションの公正価値を推定した。
私たちは以下に述べるように、ブラック·スコアーズオプション定価モデルの重要な仮定を決定した。これらの入力のいずれも主観的であり,通常決定するには重大な判断が必要である.
•私たちの普通株の公正な価値。私たちが初めて公募する前に、私たちの普通株は公開取引されていなかったので、上記の“普通株公正価値の決定”で述べたように、私たちの普通株の公正価値を推定した。
•予想される波動性。我々の普通株には長い取引履歴がないため、予想変動率はわが業界内のいくつかの上場企業の平均履歴株式変動率から算出されており、これらの会社は株式ベースの報酬の期待期間に相当する期間内に私たちの業務に相当すると考えられる。私たちは、私たち自身が取引した株価変動に関する十分な履歴データを持つまで、そうし続ける予定だ。
ブラック·スコアモデルで使用されている任意の仮定が大きく変化すれば、将来の報酬に基づく株式ベースの報酬は、以前に付与された報酬と大きく異なる可能性がある。
比較的小さな報告会社の状態
非関連会社が2022年6月30日に保有する株式の時価によると、我々は1934年に証券取引法(改正後)または取引法で定義された“比較的小さい報告会社”であり、2022年12月31日に“大型加速申告会社”の地位を脱退した。私たちはいくつかの規模の小さい報告会社を利用して開示することができるかもしれない。これらの措置には、役員報酬に関する開示義務の削減と、報酬慣行やプログラムを説明する報酬検討および分析を提供する要求を免除することが含まれているが、これらに限定されない。年収1億ドル以下の小さな報告会社として、独立公認会計士事務所が発行する財務報告内部統制の認証報告を提供する必要もありません。(I)投票権と無投票権がある限り,これらの比例した開示と免除を利用することができる
私たちの第2四半期の最終営業日には、非関連会社が保有する株式が2.5億ドル未満、または(Ii)最近終了した会計年度には、我々の年収が1.00億ドル未満であり、私たちの第2四半期の最終営業日には、非関連会社が保有する投票権および無投票権の株式が7.00億ドル未満である。
第七A項。市場リスクの定量的·定性的開示について
私たちは正常な業務過程で市場リスクに直面しており、主に金利変動と外貨為替レート変動に限られている。私たちは連邦保険の様々な通貨の限度額を超え、予想される流動性要件に応じて異なる時期に1つ以上の金融機関に保管されている大量の現金および現金等価物を持っている。
金利リスク
2022年12月31日現在、私たちは現金と現金等価物1兆432億ドルを持っている。私たちの金利感受性に対するリスクの開放はアメリカとイギリスの基礎銀行の金利変化の影響を受けています。私たちの黒字現金は時々利息貯蓄と通貨市場口座に投資する。私たちは取引や投機を目的として投資をしていない。私たちのポートフォリオの性質は保守的で、短期満期投資の元本に基づいているため、金利がすぐに1ポイント変化することが私たちのポートフォリオの公平な市場価値に大きな影響を与えるとは思わないので、私たちの経営業績やキャッシュフローは市場金利の変化の大きな影響を受けないと予想されます。
外貨両替リスク
我々は現在,Compass Path plcの統合財務諸表をポンドで作成しているが,財務報告の目的で,我々の統合財務諸表はドル(報告通貨)で表されている.機能通貨以外の通貨建ての貨幣資産と負債を貸借対照表日の現行為替レートで機能通貨に換算する。外貨建ての非貨幣性資産と負債を取引当日の為替レートで換算して機能通貨とする。外貨取引による為替損益は総合全面損失表における純額の他の収入(費用)に計上される。実体の財務諸表はその本位貨幣から報告通貨に換算し、資産と負債は資産負債表の日の為替レートで換算し、費用は関連期間の平均為替レートで換算し、株主権益(損失)は歴史的為替レートで換算する。換算調整は確定純損失に計上しないが、他の全面赤字に対する外貨調整として計上され、他の全面赤字は株主権益(損失)の一構成要素である。2022年12月31日までの年間では、80万ドルの外貨換算未実現収益が他の全面赤字に計上されているが、2021年12月31日までの年度の未実現収益は200万ドルである。
私たちは現在、私たちの通貨の開放を減らすために合成通貨のヘッジ活動に従事していませんが、私たちはドル、ポンド、ユーロの預金利差を維持して、時間の経過とともにこれらの通貨に対する予想支出を大体反映して、為替レート変動の影響に対する天然ヘッジを提供しますが、重大な外貨変動の影響を受けないように十分に保護される保証はありません。
項目8.財務諸表と補足データ
我々の総合財務諸表は本年度報告書の末尾に添付されており,ページからF-1,参照されて本明細書に組み込まれる
項目9.会計·財務開示面の変化と会計士との相違
ない
第9条。制御とプログラム
情報開示制御とプログラムの評価
我々の経営陣は、我々の最高経営責任者および最高財務責任者(それぞれ私たちの最高経営責任者およびCEO)の参加の下で、2022年12月31日までの我々の開示制御および手順(取引法規則13 a-15(E)および15 d-15(E)で定義されるような)の有効性を評価した。このような評価に基づいて、私たちの最高経営責任者とCEOは、私たちの開示制御と手続きは
吾等が取引所法案に基づいて提出又は提出された報告書において開示を要求する情報が、米国証券取引委員会規則及び表に指定された期間内に記録、処理、集計及び報告され、最高経営者及び最高財務官を含む、又は状況に応じて同様の機能を果たす者を含めて蓄積され、伝達され、必要な開示に関する決定をタイムリーに行うことができるようにする
経営陣財務報告内部統制年次報告書
我々の経営陣は、取引所法案第13 a-15(F)条の規定に基づいて、財務報告書の十分な内部統制を確立·維持する責任がある。我々の財務報告に対する内部統制は、公認会計原則に基づいて財務報告の信頼性と外部目的の財務諸表の作成に合理的な保証を提供することを目的とした過程である。その固有の限界のため、財務報告書の内部統制は誤った陳述を防止したり発見できない可能性がある。将来的にどのような有効性評価を行うかの予測には,条件の変化により制御が不十分になる可能性がある,あるいは政策やプログラムを遵守する程度が悪化する可能性があるというリスクがある
最高経営責任者や最高財務責任者を含む経営陣の監督と参加の下、トレデビル委員会後援組織委員会(2013年枠組み)で制定された基準(COSO基準)に基づいて、財務報告の内部統制の有効性を評価した。この枠組みでの我々の評価によると、我々の経営陣は、2022年12月31日から財務報告書の内部統制に有効であると結論した
このForm 10-K年度報告書には独立公認会計士事務所の認証報告書が含まれていません。私たちは加速申告者や大型加速申告者ではないからです
財務報告の内部統制の変化
2022年12月31日までの四半期内に、財務報告の内部統制に大きな影響を与えたり、合理的に財務報告の内部統制に大きな影響を与える可能性のある変化はありません。
制御措置の有効性の固有の制限
その固有の限界のため、財務報告書の内部統制は誤った陳述を防止したり発見できない可能性がある。将来的にどのような有効性評価を行うかの予測には,条件の変化により制御が不十分になる可能性がある,あるいは政策やプログラムを遵守する程度が悪化する可能性があるというリスクがある.
プロジェクト9 B。その他の情報
適用されません。
プロジェクト9 Cです。検査妨害に関する外国司法管区の開示
適用されません。
第三部
プロジェクト10.役員、役員、および企業管理
私たちの取締役会は、CEO、最高財務官、その他の幹部、および上級管理者を含む、私たちのすべての従業員、高級管理者、および取締役に適用されるビジネス行動および道徳基準を採択しました。私たちのビジネス行動と道徳基準は、私たちのサイトir.Compasspathwayの投資家関係の部分に全文掲載されています。私たちのウェブサイトは引用を通じてこの申請文書に組み込まれていない。私たちは、適用される法律またはナスダック証券市場上場基準に基づいて、私たちのウェブサイト上または取引所法案に基づいて提出された文書に、私たちの商業行為および道徳基準の任意の改正を開示するか、または私たちの主要幹部、主要財務官、主要会計官または財務総監または同様の機能を実行する者に付与された要件の免除を開示する。
本プロジェクトが提供を要求する残りの情報は、取締役、役員、監査委員会の情報を含み、2022年12月31日までの財政年度の120日以内に提出され、引用により本明細書に組み込まれる米国証券取引委員会に提出される2023年株主年次総会依頼書に記載される。
プロジェクト11.役員報酬
本プロジェクトに要求される情報は、2022年12月31日までの財政年度の120日以内に提出され、引用により本明細書に組み込まれる米国証券取引委員会に提出される2023年株主年次総会依頼書に記載される。
プロジェクト12.特定の実益所有者の保証所有権及び管理職及び株主に関する事項
本プロジェクトに要求される情報は、2022年12月31日までの財政年度の120日以内に提出され、引用により本明細書に組み込まれる米国証券取引委員会に提出される2023年株主年次総会依頼書に記載される。
第13項:特定の関係及び関係者取引、並びに取締役独立性
本プロジェクトに要求される情報は、2022年12月31日までの財政年度の120日以内に提出され、引用により本明細書に組み込まれる米国証券取引委員会に提出される2023年株主年次総会依頼書に記載される。
プロジェクト14.主な課金とサービス
本プロジェクトに要求される情報は、2022年12月31日までの財政年度の120日以内に提出され、引用により本明細書に組み込まれる米国証券取引委員会に提出される2023年株主年次総会依頼書に記載される。
第4部
プロジェクト15.証拠品および財務諸表の添付表
(A)ファイルリスト
1.財務諸表
以下の財務諸表は、本年度報告F−1ページから単独の節で提出され、以下のようになる
| | | | | |
| ページ |
独立公認会計士事務所レポート(PCAOB ID 876) | F-2 |
| 合併貸借対照表 | F-3 |
| 合併経営報告書と全面赤字 | F-4 |
| 転換可能優先株と株主権益連結報告書(損失) | F-5 |
| 統合現金フロー表 | F-6 |
| 連結財務諸表付記 | F-8 |
2.財務諸表明細書
必要ではない、適用されない、または他の方法で必要な情報が含まれているので、他のすべての計画は省略される。
3.陳列品
本年度報告添付ファイルインデックスに記載されているファイルは、参照により本年度報告に組み込まれているか、または本年度報告と共に保存されており、いずれの場合もその中に示されている(S−K規則に従って601番目の番号)。
索引.索引
| | | | | | | | | | | | | | | | | | | | |
展示品 番号をつける | | 説明する | 引用で法団として成立する |
| | | 別表/表 | 書類番号 | 展示品 | 書類の日付 |
| 3.2 | | 羅経航路協会の定款. | 表F-1/A | 333-248484 | 3.2 | 9/14/2020 |
| 4.1 | | 預金協定 | 表F-6/A | 333-248514 | 99.(A) | 9/17/2020 |
| 4.2 | | 米国預託証明書表(添付ファイル4.1に掲載)。 | | | | |
| 4.3* | | 証券説明書 | | | | |
| 10.1# | | Compass Rx Limitedと列挙された株主との間の投資と株主合意は、日付が2020年4月17日であり、2020年8月7日に改訂され、再記述される。 | 表F-1 | 333-248484 | 10.1 | 8/28/2020 |
| 10.2# | | Fora Space Limitedが当社と締結した賃貸契約は,2021年7月9日である | 表格6-K | 001-39522 | 10.1 | 8/11/2021 |
| 10.3# | | ジョージ·ゴールドスミスとの雇用協定です | 表格20-F | 001-39522 | 10.2 | 3/9/2021 |
| 10.4# | | Ekaterina Malievskaiaとの雇用協定。 | 表格20-F | 001-39522 | 10.7 | 3/9/2021 |
| 10.5 | | 2020年の従業員株式オプションとインセンティブ計画は、非員工サブ計画とアメリカサブ計画を含み、改訂された。 | 表F-1/A | 333-248484 | 10.2 | 9/14/2020 |
| 10.6 | | 2020年従業員株購入計画 | 表F-1/A | 333-248484 | 10.3 | 9/14/2020 |
| 10.7# | | Office GroupとCompass Path Limitedの間で2019年10月31日に締結されたライセンス契約。 | 表F-1/A | 333-248484 | 10.4 | 9/14/2020 |
| | | | | | | | | | | | | | | | | | | | |
| 10.8# | | BioInnovation Labs LLCとCompass Path,Inc.の間のサービス協定は、日付は2019年5月30日であり、2020年4月22日のサービス協定第1号修正案を経て改正され、2020年6月26日のサービス協定で補充される。 | 表F-1/A | 333-248484 | 10.5 | 9/14/2020 |
| 10.9 | | 羅針盤航路有限公司とその各役員及び高級職員との間の弁済証文形式。 | 表F-1/A | 333-248484 | 10.6 | 9/14/2020 |
| 10.10# | | マイケル·フォルヴィと雇用契約を結ぶ | 表格6-K | 001-39522 | 10.1 | 12/7/2021 |
| 10.11# | | 2020年株式オプションとインセンティブ計画下の会社員非限定株式オプション協定の形式。 | 表格8-K | 001-39522 | 10.2 | 02/04/2022 |
| 10.12#* | | Compass Path plc 2020株式購入とインセンティブ計画によると、会社員の制限的な株式単位奨励協定 | | | | |
| 10.13# | | マシュー·オーシャンズとの雇用協定 | 10-K | 001-39522 | 10.20 | 02/24/2022 |
| 10.14 | | 2022年1月31日にBioInnovation Labs LLCおよびCompass Path Inc.によって署名されたサービス契約 | 10-K | 001-39522 | 10.21 | 02/24/2024 |
| 10.15 | | Movassate Family TrustとCompass Path Inc.が2021年8月3日に締結したサービス契約 | 10-K | 001-39522 | 10.22 | 02/24/2022 |
| 10.16 | | Compass路探者有限公司、ロンドンと南ロンドン国王学院及びモスリーNHS基金会信託基金間の主な研究協力協定は、2022年3月22日である | 10-Q | 001-39522 | 10.1 | 05/10/2022 |
| 10.17# | | コンパスパス会社とKabir·ナートの間で2022年8月1日に締結された雇用協定。 | 8-K | 001-39522 | 10.1 | 07/19/2022 |
| 10.18 | | Compass Path plcとGeorge Goldsmithの間で2020年9月14日に署名された雇用協定改正案。 | 8-K | 001-39522 | 10.2 | 07/19/2022 |
| 10.19* | | 2022年8月22日にCompass Path Inc.および130 Madison Avenue Tenant LLCによって締結されたWeWork会員契約 | | | | |
| 10.20# | | 奨励形態は非制限株式オプション協定である。 | 10-Q | 001-39522 | 10.3 | 8/04/2022 |
| 21.1 | | コンパスパス会社の子会社です。 | 表F-1 | 333-248484 | 21.1 | 8/28/2020 |
| 23.1* | | 独立公認会計士事務所普華永道会計士事務所同意 | | | | |
| 31.1* | | 首席執行幹事2002年“サバンズ-オキシリー法”第302条規則13(A)-14(A)/15 d-14(A)による認証 | | | | |
| 31.2* | | 2002年“サバンズ·オキシリー法”第302条規則13(A)−14(A)/15 d−14(A)に基づく首席財務局長の証明 | | | | |
| 32.1** | | 最高経営責任者及び最高財務責任者が2002年“サバンズ·オキシリー法案”第906条に基づいて可決した“米国法典”第18編第1350条の証明 | | | | |
| 101.INS* | | XBRLインスタンスドキュメント | | | | |
| 101.SCH* | | インラインXBRL分類拡張アーキテクチャ文書. | | | | |
| 101.CAL* | | インラインXBRL分類拡張はリンクベース文書を計算する. | | | | |
| 101.DEF* | | XBRLソート拡張を連結してLinkbase文書を定義する. | | | | |
| 101.LAB* | | XBRL分類拡張ラベルLinkbase文書を連結する. | | | | |
| | | | | | | | | | | | | | | | | | | | |
| 101.PRE* | | XBRL分類拡張プレゼンテーションLinkbaseドキュメントを内部接続する. | | | | |
| 104 | | カバーインタラクションデータファイル(フォーマットは、添付ファイル101に含まれる適用分類拡張情報を含むイントラネットXBRLである)。
| | | | |
_________________
#は、管理契約または任意の補償計画、契約、またはスケジュールを表します。
*同封のアーカイブ
**本契約添付ファイル32.1および32.2に提供された証明は、本年度報告の10-K表とみなされ、登録者が参照によって明示的に組み込まれない限り、改正された1934年証券取引法第18条の目的について提出されたとはみなされない。登録者が引用によって明確に組み込まれていない限り、このような証明は、参照によって1933年証券法(改訂本)または1934年証券法(改訂本)の下に組み込まれたいかなる文書ともみなされない。
項目16.表格10-Kの概要
適用されません。
財務諸表索引
羅針盤航路会社合併財務諸表
| | | | | |
| 年度連結財務諸表索引 | |
| |
| ページ |
独立公認会計士事務所レポート(PCAOB ID)876) | F-1 |
合併貸借対照表 | F-3 |
合併経営報告書と全面赤字 | F-4 |
転換可能優先株と株主権益連結報告書(損失) | F-5 |
統合現金フロー表 | F-6 |
連結財務諸表付記 | F-8 |
独立公認会計士事務所報告
Compass Path Plc取締役会と株主へ
財務諸表のいくつかの見方
本監査人は添付Compass Path plc及びその付属会社(“貴社”)の二零二年十二月三十一日及び二零二一年十二月三十一日の総合貸借対照表、及び二零二二年十二月三十一日までの三年度の各年度の関連総合運営及び全面損益表、株主権益(損失)表及び現金流動表を審査し、関連付記(総称して“総合財務諸表”と呼ぶ)を含む。総合財務諸表は,すべての重要な面で,会社の2022年12月31日と2021年12月31日までの財務状況,および2022年12月31日までの3年度の経営結果とキャッシュフローを公平に反映しており,米国公認の会計原則に適合していると考えられる
会計原則の変化
総合財務諸表付記2で述べたように、当社は2021年にリースに対する会計処理方式を変更した。
意見の基礎
これらの連結財務諸表は会社の経営陣が責任を負う。私たちの責任は私たちの監査に基づいて会社の総合財務諸表に意見を発表することです。私たちは米国上場企業会計監督委員会(PCAOB)に登録されている公共会計士事務所であり、米国連邦証券法および米国証券取引委員会とPCAOBの適用規則と法規に基づいて、会社と独立しなければならない
私たちはPCAOBの基準に従ってこれらの連結財務諸表を監査した。これらの基準は、連結財務諸表に重大な誤報がないかどうかに関する合理的な保証を得るために、エラーによるものであっても不正であっても、監査を計画し、実行することを要求する。当社はその財務報告の内部統制を監査することを求められておらず、私たちも招聘されて監査を行っていません。私たちの監査の一部として、財務報告の内部統制を理解することが求められていますが、社内財務報告の内部統制の有効性に対する意見を表明するためではありません。したがって、私たちはそのような意見を表現しない。
我々の監査には、連結財務諸表の重大な誤報リスクを評価するプログラム、エラーによるものであっても詐欺であっても、これらのリスクに対応するプログラムを実行することが含まれる。これらの手続きは、連結財務諸表中の金額および開示に関する証拠をテストに基づいて検討することを含む。我々の監査には、経営陣が使用する会計原則の評価と重大な見積もり、合併財務諸表の全体列報の評価も含まれています。私たちは私たちの監査が私たちの観点に合理的な基礎を提供すると信じている。
重要な監査事項
以下に述べる重要な監査事項は、監査委員会に監査委員会に伝達または要求を伝達することを指し、(I)総合財務諸表に対して重大な意義を有する勘定または開示に関連し、(Ii)私たちが特に挑戦的、主観的または複雑な判断を有する当期総合財務諸表監査によって生じる事項に関するものである。重要監査事項の伝達は、総合財務諸表に対する私たちの全体的な意見をいかなる方法でも変えることはなく、以下の重要な監査事項を伝達することによって、重要な監査事項又はそれに関連する勘定又は開示について個別の意見を提供することもない。
研究開発税収控除の恩恵を受ける
総合財務諸表付記2及び付記5で述べたように、当社は研究開発活動を行い、中小企業計画下のイギリス研究開発(“R&D”)税務控除制度に恵まれている。同社は2022年12月31日までの1年間に、1440万ドルの研究開発税控除収益を確認した。経営陣が開示したように、彼らは会社が取得する資格があると予想される税控除計画を評価し、研究開発税収控除から得られるメリットを確認し、この費用の一部は経営陣がこの計画に基づいて条件を満たすことが予想され、その金額が最終的に実現されることを合理的に保証する。経営陣は、これらの活動と支出の性質が適合しているかどうかを決定するために、その研究開発活動と支出を評価した
税収免除計画下の免除、およびクレームが最終的にイギリス政府が制定した許可された精算可能な費用基準に基づいて実現されるかどうか。管理層は条件に合った研究開発支出を推定するために判断し、単一のチームメンバーが研究開発活動にかかる時間と非研究開発活動にかかる時間の分配を含む
研究開発税収控除に関する手続の実行が重要な監査事項であることを決定した主な考慮要因は、(I)研究開発活動のための時間配分を推定することを含む経営陣が税収控除計画資格に適合する費用の性質と金額を決定する際に採用された重大な判断であり、(Ii)監査人のプログラムの実行と研究開発税収控除利益に関する監査証拠の評価における高度な判断、主観性、努力である
この問題を処理することは、統合財務諸表に対する私たちの全体的な意見を形成するための実行手順および評価監査証拠に関するものである。これらのプログラムには、(I)企業が展開する活動に対する管理層の性質と、中小企業が利用可能な研究開発税収免除計画の資格の評価、(Ii)管理層が条件に適合した研究開発コストを推定する過程、(Iii)経営層の適格費用配分の合理性を評価すること、税収控除計画で概説された関連基準に基づいて達成される金額を決定すること、(Iv)税金控除計算を支援するデータの完全性と正確性をテストすること、を含む。(5)前年のクレームに関する現金受信の証拠を取得し、利益が最終的に実現される評価を支援する
| | |
/s/普華永道会計士事務所 |
| レイデン、イギリス |
| 2023年2月28日 |
|
| 2018年以来、当社の監査役を務めてきました。 |
コンパス経路PLC
合併貸借対照表
(単位は千で、1株当たりおよび1株当たりの金額は含まれていない)
(別の説明がない限り、ドルで表す)
| | | | | | | | | | | |
| 十二月三十一日 |
| 2022 | | 2021 |
| 資産 | | | |
| 流動資産: | | | |
| 現金と現金等価物 | $ | 143,206 | | | $ | 273,243 | |
| 制限現金 | 175 | | | 104 | |
| 所得税を前払いする | 575 | | | 332 | |
| 前払い費用と他の流動資産 | 47,695 | | | 21,621 | |
| 流動資産総額 | 191,651 | | | 295,300 | |
| 非流動資産: | | | |
| 投資する | 469 | | | 525 | |
| 財産と設備、純額 | 617 | | | 398 | |
| 経営的リース使用権資産 | 2,006 | | | 3,696 | |
| 繰延税金資産 | 2,224 | | | 766 | |
| その他の資産 | 327 | | | 213 | |
| 総資産 | $ | 197,294 | | | $ | 300,898 | |
| 負債と株主権益 | | | |
| 流動負債: | | | |
| 売掛金 | $ | 4,761 | | | $ | 2,564 | |
| 費用とその他の負債を計算すべきである | 9,325 | | | 10,308 | |
| レンタル負債を経営しています--流動負債 | 1,510 | | | 2,235 | |
| 流動負債総額 | 15,596 | | | 15,107 | |
| 非流動負債 | | | |
| レンタル負債を経営しています--非流動負債 | 418 | | | 1,379 | |
| 総負債 | 16,014 | | | 16,486 | |
| | | |
| 引受金及び又は有事項(付記15) | | | |
| 株主権益: | | | |
普通株式、GB0.008額面価値42,631,794そして42,019,874それぞれ2022年12月31日及び2021年12月31日に認可され、発行された株式及び発行済み株式 | 440 | | | 435 | |
繰延株、GB21,921.504額面価値1つは2022年12月31日と2021年12月31日に発行された株式 | 28 | | | 28 | |
| 追加実収資本 | 458,825 | | | 444,750 | |
| 累計その他総合(赤字)/収入 | (16,867) | | | 8,840 | |
| 赤字を累計する | (261,146) | | | (169,641) | |
| 株主権益総額 | 181,280 | | | 284,412 | |
| 総負債と株主権益 | $ | 197,294 | | | $ | 300,898 | |
| | | |
付記はこれらの連結財務諸表の構成要素である。
コンパス経路PLC
合併経営報告書と全面赤字
(単位は千で、1株当たりおよび1株当たりの金額は含まれていない)
(別の説明がない限り、ドルで表す)
| | | | | | | | | | | | | | | | | |
| 十二月三十一日までの年度 |
| 2022 | | 2021 | | 2020 |
| 運営費用: | | | | | |
| 研究開発 | $ | 65,053 | | | $ | 44,027 | | | $ | 23,366 | |
| 一般と行政 | 45,350 | | | 39,194 | | | 28,027 | |
| 総運営費 | 110,403 | | | 83,221 | | | 51,393 | |
| 運営損失: | (110,403) | | | (83,221) | | | (51,393) | |
| その他の収入(費用)、純額: | | | | | |
| その他の収入、純額 | 4,061 | | | 40 | | | 319 | |
| 為替損益 | 821 | | | 1,990 | | | (11,702) | |
| 転換可能手形の公正価値変動 | — | | | — | | | (1,041) | |
| 変換可能なチケットの公正価値変動−関連先への対応− | — | | | — | | | (730) | |
| 研究開発税収控除の恩恵を受ける | 14,424 | | | 9,648 | | | 4,245 | |
| その他の収入を合計して純額 | 19,306 | | | 11,678 | | | (8,909) | |
| 所得税前損失 | (91,097) | | | (71,543) | | | (60,302) | |
| 所得税費用 | (408) | | | (199) | | | (32) | |
| 純損失 | (91,505) | | | (71,742) | | | (60,334) | |
| その他の全面的な損失: | | | | | |
| 外国為替換算調整 | (25,707) | | | (5,745) | | | 14,683 | |
| 総合損失 | (117,212) | | | (77,487) | | | (45,651) | |
| 普通株株主は1株当たり純損失を占めるべきである−基本損失と希薄損失 | $ | (2.16) | | | $ | (1.79) | | | $ | (3.55) | |
| 加重平均発行済み普通株式-基本と希釈後の普通株式 | 42,436,292 | | 39,997,587 | | 16,991,664 |
付記はこれらの連結財務諸表の構成要素である。
コンパス経路PLC
合併株主権益報告書(損失)
(単位は千で、1株当たりおよび1株当たりの金額は含まれていない)
(別の説明がない限り、ドルで表す)
| | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | |
| | オープンカー | | オープンカー | | Bオープンカー | | 普通株GB0.008 | | 繰延株 | | 追加実収資本 | | 累計その他総合(赤字)/収入 | | 赤字を累計する | | 株主権益合計 |
| | 優先株 | | 優先株 | | 優先株 | | 額面.額面 | | £21,921.504額面.額面 | | | | |
| | 株式.株 | | 金額 | | 株式.株 | | 金額 | | 株式.株 | | 金額 | | 株式.株 | | 金額 | | 株式.株 | | 金額 | | 金額 | | 金額 | | 金額 | | 金額 |
| 2019年12月31日の残高 | | 2,650,980 | | | $ | 3,761 | | | 7,131,525 | | | $ | 35,147 | | | — | | | $ | — | | | 10,752,429 | | | $ | 111 | | | — | | | $ | — | | | $ | 7,162 | | | $ | (98) | | | $ | (37,565) | | | $ | (30,390) | |
| B類転換優先株を発行し,発行コストを差し引く | | — | | | — | | | — | | | — | | | 4,913,404 | | | 61,316 | | | — | | | — | | | — | | | — | | | — | | | — | | | — | | | — | |
| 手形をB類転換可能優先株に変換する | | — | | | — | | | — | | | — | | | 1,723,263 | | | 21,614 | | | — | | | — | | | — | | | — | | | — | | | — | | | — | | | — | |
| 購入権を行使する | | — | | | — | | | — | | | — | | | — | | | — | | | 197,702 | | | 2 | | | — | | | — | | | (2) | | | — | | | — | | | — | |
| 購入株権を行使したが株式は発行されなかった | | — | | | — | | | — | | | — | | | — | | | — | | | — | | | — | | | — | | | — | | | 16 | | | — | | | — | | | 16 | |
| 普通株の没収 | | — | | | — | | | — | | | — | | | — | | | — | | | (63,972) | | | (1) | | | — | | | — | | | 1 | | | — | | | — | | | — | |
| 優先株を普通株に転換することを含む会社再編の影響 | | (2,650,980) | | | (3,761) | | | (7,131,525) | | | (35,147) | | | (6,636,667) | | | (82,930) | | | 16,419,172 | | | 167 | | | 1 | | | 28 | | | 121,643 | | | — | | | — | | | 121,838 | |
| 普通株発行は発行コストを差し引く | | — | | | — | | | — | | | — | | | — | | | — | | | 8,625,000 | | | 88 | | | — | | | — | | | 132,677 | | | — | | | — | | | 132,765 | |
| 株式ベースの給与費用 | | — | | | — | | | — | | | — | | | — | | | — | | | — | | | — | | | — | | | — | | | 17,983 | | | — | | | — | | | 17,983 | |
| 外貨換算で収益が実現していない | | — | | | — | | | — | | | — | | | — | | | — | | | — | | | — | | | — | | | — | | | — | | | 14,683 | | | — | | | 14,683 | |
| 純損失 | | — | | | — | | | — | | | — | | | — | | | — | | | — | | | — | | | — | | | — | | | — | | | — | | | (60,334) | | | (60,334) | |
| 2020年12月31日残高 | | — | | | $ | — | | | — | | | $ | — | | | — | | | $ | — | | | 35,930,331 | | | $ | 367 | | | 1 | | | $ | 28 | | | $ | 279,480 | | | $ | 14,585 | | | $ | (97,899) | | | $ | 196,561 | |
| 購入権を行使する | | — | | | — | | | — | | | — | | | — | | | — | | | 1,244,709 | | | 14 | | | — | | | — | | | 1,891 | | | — | | | — | | | 1,905 | |
| 前年度行使のオプションで発行された株式 | | — | | | — | | | — | | | — | | | — | | | — | | | 232,227 | | | 3 | | | — | | | — | | | (3) | | | — | | | — | | | — | |
| 普通株発行は発行コストを差し引く | | — | | | — | | | — | | | — | | | — | | | — | | | 4,600,000 | | | 51 | | | — | | | — | | | 154,743 | | | — | | | — | | | 154,794 | |
| 既得限定株式単位を解決するために普通株を発行する | | — | | | — | | | — | | | — | | | — | | | — | | | 12,607 | | | — | | | — | | | — | | | — | | | — | | | — | | | — | |
| 株式ベースの給与費用 | | — | | | — | | | — | | | — | | | — | | | — | | | — | | | — | | | — | | | — | | | 8,639 | | | — | | | — | | | 8,639 | |
| 外貨換算で収益が実現していない | | — | | | — | | | — | | | — | | | — | | | — | | | — | | | — | | | — | | | — | | | — | | | (5,745) | | | — | | | (5,745) | |
| 純損失 | | — | | — | | — | | | — | | | — | | | — | | | — | | | — | | | — | | | — | | | — | | | — | | | — | | | (71,742) | | | (71,742) | |
| 2021年12月31日の残高 | | — | | | $ | — | | | — | | | $ | — | | | — | | | $ | — | | | 42,019,874 | | | $ | 435 | | | 1 | | | $ | 28 | | | $ | 444,750 | | | $ | 8,840 | | | $ | (169,641) | | | $ | 284,412 | |
| ATM機が普通株を発行し,発行コストを差し引く | | — | | | — | | | — | | | — | | | — | | | | | 44,416 | | | 1 | | | — | | | — | | | 439 | | | — | | | — | | | 440 | |
| 購入権を行使する | | — | | | — | | | — | | | — | | | — | | | | | 462,722 | | | 4 | | | — | | | — | | | 397 | | | — | | | — | | | 401 | |
| 既得限定株式単位を解決するために普通株を発行する | | — | | | — | | | — | | | — | | | — | | | | | 82,622 | | | — | | | — | | | — | | | — | | | — | | | — | | | — | |
| 2020年従業員株購入計画に基づいて普通株を発行する | | — | | | — | | | — | | | — | | | — | | | | | 22,160 | | | — | | | — | | | — | | | 199 | | | — | | | — | | | 199 | |
| 税金の前納を申請した株 | | | | | | | | | | | | | | — | | | — | | | — | | | — | | | (83) | | | — | | | — | | | (83) | |
| 株式ベースの給与費用 | | | | | | | | | | | | | | — | | | — | | | — | | | — | | | 13,123 | | | — | | | — | | | 13,123 | |
| 外貨換算で収益が実現していない | | | | | | | | | | | | | | — | | | — | | | — | | | — | | | — | | | (25,707) | | | — | | | (25,707) | |
| 純損失 | | — | | | — | | | — | | | — | | | — | | | | | — | | | — | | | — | | | — | | | — | | | — | | | (91,505) | | | (91,505) | |
| 2022年12月31日の残高 | | — | | | $ | — | | | — | | | $ | — | | | — | | | | | 42,631,794 | | | $ | 440 | | | 1 | | | $ | 28 | | | $ | 458,825 | | | $ | (16,867) | | | $ | (261,146) | | | $ | 181,280 | |
付記はこれらの連結財務諸表の構成要素である。
コンパス経路PLC
統合現金フロー表
(単位:千)
(別の説明がない限り、ドルで表す)
| | | | | | | | | | | | | | | | | |
| 十二月三十一日までの年度 |
| 2022 | | 2021 | | 2020 |
| 経営活動のキャッシュフロー: | | | | | |
| 純損失 | $ | (91,505) | | | $ | (71,742) | | | $ | (60,334) | |
| 純損失と経営活動で使用した現金純額の調整 | | | | | |
| 減価償却および償却 | 330 | | | 175 | | | 112 | |
| 転換可能手形は価値変動を公正に許容する | — | | | — | | | 1,771 | |
| 外貨再計量の非現金損失 | 1,141 | | | 22 | | | — | |
| 非現金株の報酬 | 13,123 | | | 8,639 | | | 17,983 | |
| 非現金レンタル費用 | 2,126 | | | 1,797 | | | — | |
| 経営性資産と負債の変動 | | | | | |
| 前払い費用と他の流動資産 | (28,760) | | | (8,984) | | | (4,490) | |
| 繰延と前払い税金資産 | (1,701) | | | (877) | | | (221) | |
| その他の資産 | (307) | | | (160) | | | (57) | |
| リース負債を経営する | (2,081) | | | (1,880) | | | — | |
| 売掛金 | 2,497 | | | (163) | | | 1,303 | |
| 費用とその他の負債を計算すべきである | (314) | | | 5,428 | | | 2,553 | |
| 経営活動のための現金純額 | (105,451) | | | (67,745) | | | (41,380) | |
| 投資活動によるキャッシュフロー: | | | | | |
| 財産と設備を購入する | (596) | | | (334) | | | (131) | |
| 購入投資 | — | | | — | | | (497) | |
| 投資活動のための現金純額 | (596) | | | (334) | | | (628) | |
| 資金調達活動のキャッシュフロー: | | | | | |
| 普通株を発行して得られる収益は,発行コストを差し引く | 440 | | | 154,794 | | | — | |
| 従業員の株購入計画に基づいて株を発行して得た金 | 199 | | | — | | | — | |
| 持分を行使して得た金 | 401 | | | 1,852 | | | 16 | |
| 初公開における米国預託証明書の発行は,発行コストを差し引く | — | | | — | | | 132,823 | |
| 優先株発行で得られた金は発行コストを差し引く | — | | | — | | | 61,316 | |
| 融資活動が提供する現金純額 | 1,040 | | | 156,646 | | | 194,155 | |
| 現金、現金等価物および限定現金に及ぼす為替レート変動の影響 | (24,959) | | | (5,576) | | | 13,225 | |
| 現金、現金等価物および制限現金純額(減少)/増加 | (129,966) | | | 82,991 | | | 165,372 | |
| 期初現金、現金等価物、および限定現金 | 273,347 | | | 190,356 | | | 24,984 | |
| 期末現金、現金等価物、および制限現金 | $ | 143,381 | | | $ | 273,347 | | | $ | 190,356 | |
| | | | | |
| キャッシュフロー情報の追加開示: | | | | | |
| 新しい経営リース負債と引き換えに使用権資産 | $ | 783 | | | $ | 5,562 | | | $ | — | |
| 課税負債その他の負債で確認された株式奨励未納税 | $ | 85 | | | $ | — | | | $ | — | |
| オプションを行使した収益は他の流動資産に受信されて記録されている | $ | — | | | $ | 53 | | | $ | — | |
| 費用に含まれる繰延発行コストを計算する | $ | — | | | $ | 856 | | | $ | — | |
| 変換可能手形を転換可能優先株に変換する | $ | — | | | $ | — | | | $ | 21,614 | |
以下の表は、上記の各期間の現金、現金等価物、および制限された現金残高の入金状況を示す | | | | | | | | | | | | | | | | | |
| 十二月三十一日までの年度 |
| 2022 | | 2021 | | 2020 |
| 現金と現金等価物 | $ | 143,206 | | | $ | 273,243 | | | $ | 190,327 | |
| 短期制限現金 | 175 | | | 104 | | | 29 | |
| 現金総額、現金等価物、および限定現金 | $ | 143,381 | | | $ | 273,347 | | | $ | 190,356 | |
付記はこれらの連結財務諸表の構成要素である。
コンパス経路PLC
連結財務諸表付記
1. 業務的性質
Compass Path plcあるいは同社は精神健康看護会社であり、患者が精神健康領域の証拠に基づく革新を獲得する機会を加速することに取り組んでいる。同社は,ヨーロッパや北米での難治性うつ病患者による晩期臨床試験により,COMP 360裸蓋キノコの研究療法を開発している。
同社は生物技術業界の臨床段階会社によく見られるリスクと不確定要素の影響を受け、競争相手の新技術革新に対する開発、肝心な人員への依存、独自の知的財産権と技術の保護、政府法規の遵守及び追加資本を獲得して運営に資金を提供する能力を含む。現在開発されている候補治療薬は商業化する前に臨床前と臨床テスト及び監督許可を含む大量の追加的な研究と開発努力が必要である。このような努力は大量の資本、十分な人員とインフラ、そして広範なコンプライアンス報告能力を必要とする。同社の治療開発努力が成功しても,同社がいつ(あれば)販売から収入を実現するかは定かではない。
同社の運営資金は,主に転換可能な優先株の売却,転換可能な手形の発行収益と,最近当社の2020年9月の初公開株(IPO)に関する米国預託株(ADS)の売却とそれによるものである154.82021年5月、ミリオンが続投発売された。2021年10月8日に、当社はCowen and Company、LLCまたはCowenと販売契約を締結し、この合意により、当社は最高$まで発行および販売することができます150.0何百万件ものアメリカの預託証明書は1つは普通株は、コーエンを通じて販売代理とする。会社の米国預託証明書(ADS)が販売されていれば、市場価格で販売されます。2022年12月14日、市場での見積もりによると、売りました44,416アメリカ預託証明書:$10.53アメリカごとに株式を預けています
同社は設立以来、純損失#ドルを含む経常赤字が発生している91.5百万ドルとドル71.72022年12月31日までと2021年12月31日までの年度はそれぞれ100万ドル。また、2022年12月31日現在、会社の累計損失は1ドルとなっている261.1百万ドルです。同社は予見可能な未来に引き続き営業赤字が生じると予想している。会社は、2022年12月31日現在の手元の現金と現金等価物は143.2100万ドルは今後12ヶ月の運営費用と資本支出需要を支払うのに十分です。私たちの進展を含めて第三段階臨床計画,われわれの第二段階では神経性拒食症と創傷後ストレス障害および上場企業運営に関するコストを検討した。添付された財務諸表は、持続経営をもとに作成され、正常業務過程における資産現金化と負債返済を考慮する。私たちは大量の追加資金が必要になります我々の第三段階臨床プロジェクトの開発と商業化,神経性拒食症と創傷後ストレス障害の第二段階研究である。同社は必要なときに資金を調達できず、その財務状況やその業務戦略を実施する能力にマイナス影響を与える可能性がある。現在の運営計画を実現する保証もなく、会社が受け入れ可能な条項で追加資金を得る保証もないし、全く保証されていない。
同社の将来の生存能力は、追加資本を調達してその運営に資金を提供する能力に依存する。同社は、株式発行、債務融資、協力、および他の戦略取引(マーケティング、流通、または許可手配を含む)によって追加資本を調達することができる。会社が受け入れられる条項でタイムリーにまたは追加的な資金を提供しないという保証はない。もし会社が必要な時に受け入れ可能な条件で十分な資金を得ることができなかった場合、会社の業務、経営結果、財務状況に重大な悪影響を及ぼす可能性がある。
新冠肺炎の大流行及び各国政府が新冠肺炎の大流行に対応するために実施した政策と法規--その大部分はすでに廃止された--直接と間接的に全世界の商業と商業に重大な影響を与えた。例えば、連合王国と米国の制限は一般的に廃止されたにもかかわらず、労働者不足やサプライチェーン制限のような他の間接的な影響は、依然として経済の様々な部分に影響を与えている。新冠肺炎の大流行は私たちの臨床前研究或いは臨床試験運営、私たちのサプライチェーンと製造、そして私たちのオフィスでの業務運営或いはそれが当社と業務を展開する任意の第三者(例えばCRO或いはCMO)の将来の影響の程度は未来の発展に依存し、これらの発展は依然として非常に高い不確実性を有し、大流行の持続時間、他の伝染性の変種の出現、或いはコロナウイルスの行動の制御と治療の有効性を自信に満ちて予測することができない。
2. 重要会計政策の概要
陳述の基礎
添付されている総合財務諸表はアメリカ公認会計原則あるいはアメリカ公認会計原則に従って作成された。
合併原則
添付されている総合財務諸表には、当社及びその完全子会社の勘定が含まれている。すべての会社間の残高と取引は合併時に中止されました。
予算の使用
米国公認会計原則に基づいて連結財務諸表を作成する際には、経営層は、連結財務諸表の日付の資産及び負債額、又は有資産及び負債の開示、及び報告期間内の収入及び支出の報告金額に影響を与える推定及び仮定を行わなければならない。これらの総合財務諸表に反映される重大な推定および仮定には、研究開発費の事前支払いおよび課税費用、株式ベースの報酬、および研究開発税控除が含まれるが、これらに限定されない。状況、事実、経験の変化に応じて、見積数を定期的に審査する。推定された変化は、それらが知られている期間に記録される。実際の結果はこのような推定とは大きく異なるかもしれない。
現金と現金等価物
当社は買収時満期日が三ヶ月以下のすべての高流動性投資を現金等価物と見なしています。その会社には現在、重大な現金同等物は何もない。
制限現金
2022年12月31日と2021年12月31日までの制限された現金は、従業員クレジットカードの担保預金を代表している。
投資する
この投資は簡単に決定できる公正な価値がなく、しかも当社が被投資会社の経営及び財務政策に重大な影響或いは制御を加えることができない場合、この投資はコストから減値を引いた推定公正価値の変動によって原始コストに調整される。
公正価値計量
当社のある資産と負債はアメリカ公認会計の原則で公正価値で勘定されています。公正価値は、計量日市場参加者間の秩序ある取引において、資産または負債が元金または最も有利な市場で負債を移転するために徴収または支払いされる交換価格として定義される。公正価値を計量するための推定技術は,観察可能な投入を最大限に利用し,観察不可能な投入を最大限に減少させなければならない。公正価値別帳簿の金融資産および負債は、公正価値レベルの以下の3つのレベルのうちの1つで分類され、開示されなければならず、最初の2つのレベルの投入は可視的であると考えられ、最後のレベルの投入は観察できないと考えられる
•第1レベル-活発な市場における同じ資産または負債の見積もり。
•第2レベル-観察可能な投入(第1レベルオファーを除く)、例えば、同様の資産または負債アクティブ市場のオファー、同じまたは同様の資産または負債非アクティブ市場のオファー、または観察可能な市場データによって確認され得る他の投入。
•第三レベル-価格設定モデル、現金フロー方法、および類似技術を含む市場活動支援の観察できない投入が少ないか、またはないかは、資産または負債の公正な価値を決定するために重要な意味を持つ
このようなツールの短期的な性質により、当社の総合貸借対照表に反映される現金および現金等価物、制限的現金、支払すべき帳簿および売掛金の帳簿金額は公正価値に近い。
当社が初公募前に発行した交換可能手形は、公正価値体系の第3級に分類され、その公正価値は推定モデルと重大な観察不可能な投入を用いて推定されるからである。これらの変換可能な手形は
情景に基づく割引キャッシュフロー解析を用いて推定を行った.2つの要因を考慮し,1枚あたりの変換可能チケットの推定値を得るために確率重み付けを行った.最初のシーンは、会社がGBを超える資金を調達した場合、規定の割引で発行価格に転換する価値の影響を考慮しました25.01回の株式融資1周年前の発行日には、条件を満たす融資、そうでなければ条件を満たしていない融資、第2の場合は転換可能な手形が満期まで保有されていると仮定する。交換可能手形の発行日に、隠れ収益率によって計算すると、交換可能手形の確率加重価値は元金投資額に等しい。先に発行された変換可能チケットの暗黙的収益率は繰り越され,その後の推定日の主な割引率として用いられる.当社は,i)適切な割引率で評価された日およびii)重み付けされて交換可能手形の価値指標を得るための転換予定日の将来価値から交換可能手形の公正価値を推定する。
価値オプションを公正に承諾する
会計基準アセンブリ825、金融商品、またはASC 825の許可に基づいて、会社は、公正価値オプションを選択して、その変換可能なチケットを会計処理する。ASC 825によると、会社は公正価値に従ってこれらの転換可能な手形を記録し、公正価値変動を他の収入(費用)の構成要素とし、総合経営報告書の中で純額と全面赤字とした。公正価値オプションが採用されているため、繰延ではなく、変換可能チケットに関連する直接コストおよび費用は、発生時に費用に計上される。当社の結論は、転換可能なチケットに関連する非または利益のある変換オプションがないため、公正価値オプションを変換可能チケットに適用することが適切である。
信用リスクが集中する
会社を信用リスクに直面させる金融商品には主に現金と現金等価物が含まれる。同社は現金と現金等価物を既存の金融機関に置いている。当社には、外国為替契約、オプション契約、その他の海外ヘッジ手配など、重大な表外リスクや集中信用リスクはありません。
財産と設備
財産と設備はコストごとに入金され、それぞれの資産の推定耐用年数内に直線法で減価償却され、具体的には以下のようになる | | | | | |
| 使用寿命を見込む |
| 実験室装置 | 5年.年 |
| 事務設備 | 3-5年.年 |
| 家具と固定装置 | 3年.年 |
| 賃借権改善 | 耐用年数または残存賃貸期間が短い |
廃棄又は販売時には、資産を処分するコスト及び関連減価償却は勘定から差し引かれ、それによって生じるいかなる収益又は損失も総合経営報告書及び全面赤字に計上される。修理費と維持費は発生時に料金を記入します。
長期資産減価準備
事件や環境変化が資産の帳簿価値を回収できない可能性があることを示した場合、当社は資産の潜在的減値を評価する。回収能力は,資産の帳簿価値と資産予想による予想将来の未割引純現金フローを比較することで測定した。当該等の資産が減値とみなされる場合、確認すべき減値は、資産の帳簿価値がその公正価値を超える金額で計量される。当社は2022年12月31日および2021年12月31日までに、減価損失やその関連資産に関するトリガーイベントの発生は確認されていません。
市場情報を細分化する
経営部門は企業の構成要素として定義され、その独立した離散情報は、首席経営決定者が資源をどのように分配するかを決定し、業績を評価する際に評価することができる。当社と当社の経営意思決定者、当社の最高経営責任者は、当社の運営と業務管理を単一の経営部門と見なしている二つ地理的地域:イギリスやイギリスとアメリカ。同社の固定資産は主にイギリスにある。同社は患者の心理健康領域の根拠に基づく革新を加速することに集中している。
研究開発コスト
研究·開発コストは発生時に費用を計上する。研究開発費には,研究開発活動を行うことによるコスト,報酬,株式ベースの報酬および福祉,招聘されて臨床開発活動を行う外部サプライヤーの出張および外部コスト,臨床試験および臨床試験材料の製造コストが含まれる。
契約コスト,前払金,課税項目を検討する
会社は研究機関や他社と様々な研究開発に関する契約を締結している。これらのプロトコルは通常キャンセル可能であり、関連支払いは発生時に研究および開発費用として記録される。同社は、推定された進行中の研究コストの前金および課税費用を記録し、毎月その第三者サービスプロバイダからコストおよび借金の最新推定を受信する。事前支払いおよび課税項目の十分性を評価する際に、同社は、イベントの段階または完了状況、第三者サービスプロバイダから受信された請求書および契約コスト推定値を含む研究または臨床試験の進展を分析する。任意の報告期間終了時の前払いおよび計上費用残高を決定する際に推定する。実際の結果は会社の見積もりとは違うかもしれません。同社の歴史的前金と未払い見積もりは実際のコストと実質的な差はありません。
株式ベースの報酬
当社は公正価値に応じて従業員と非従業員に付与されたすべての株式報酬を株式報酬支出として会計処理します。同社は、株式ベースの報酬計画に基づいて、株式オプションおよび制限株式単位を含む可能性がある株式奨励金を付与する。従業員および非従業員報酬の計算日は付与日であり、株式に基づく報酬コストは直線原則で必須サービス期間(すなわち帰属期間)の支出として確認される。株式に基づく補償費用は,関連サービスを提供する機能によって添付の総合経営報告書と全面損失に分類される。当社は一部の奨励金が付与された株式ベースの報酬支出を確認した。没収は発生時に記録された。
2021年10月1日、会社は株式インセンティブ計画と従業員の株購入計画を打ち出し、従業員はこの計画を通じて割引価格で株を購入することができる。同社は付与日にBlack-Scholesオプション定価モデルを用いてSIPとESPPによって発行される株式オプションと株式の公正価値を推定した。これらの計画により発行された株の公正価値は購入期間内に直線的に確認·償却され,購入期間は通常6カ月である。
これまで、当社が付与した購入権には何の履行条件も付加されていません。各株式オプション付与の公正価値は、付与された日にBlack-Scholesオプション定価モデルを用いて推定される。これらの総合財務諸表がカバーされている間に当社が行った引受権付与に関する仮定を理解するために、付記11を参照してください。オプション定価モデルで使用される仮定は、以下のことを含む
予想変動率それは.当社の普通株は会社の特定の歴史と隠れた変動率情報に十分な不足があります。そこで、上場同業者の履歴変動率に基づいて予想される株式変動率を推定し、自身の取引株価変動性に関する十分な履歴データを有するまで継続する予定である。
期限を見込む。当社の株式オプションの期待期限は、“通常”オプション資格に適合した奨励に適した“簡略化”方法で決定されている。当社の株式株式の上場時間が限られているため、当社は予想年間を推定するための合理的な基準を提供するのに十分な歴史的行使データを提供していないため、“簡略化”方法は適切であることが決定された
無リスク金利それは.無リスク金利は、奨励付与時に発効した米国債収益率曲線を参考にして決定され、期間は奨励の予想期限にほぼ等しい。
配当を期待する。期待配当収益率はゼロ当社が普通株について現金配当金を派遣したことがなく、将来的には何の現金配当も発行されないことを期待している。
普通株は価値を公平にする。初公募前に当社の普通株が活発な市場に不足していたことから、当社と当社取締役会(当社はそのメンバーが広範な商業、金融、リスク投資経験を持っていると考えている)は、当社の普通株の公正価値を推定しなければならない
初公募前に株式奨励金が付与されるたびに時間がかかる。制限された普通株と購入株式権の付与日公正価値は、関連する普通株の授与日公正価値に基づいて計算される。当社は米国公認会計士協会会計及び評価ガイドライン、補償として発行されたプライベート持株権証券推定値又は“実務補助”における指針に基づいて普通株の公正価値を計算する。同社の普通株の推定値は,株式の前例取引をもとに市場方法を用いて作成され,オプション定価法(OPM)を用いて会社の総株式価値を推定している。当社が初めて公募した後、普通株の公正価値はナスダック全世界精選市場アメリカ預託証明書を参考にして、授与日前或いは当日の収市価を決定する。
OPMによる権益価値は、普通株の価値と投資価格を一致させ、その権益価値を会社の証券ごとに分配する。OPMは様々な種類の普通株を会社総株式価値のコールオプションと見なし、行使価格は会社証券の異なる所有者間の分配に基づいて変化する価値敷居に基づいている。この方法によれば、普通株は、株主に割り当て可能な資金が流動性イベントが発生したときに優先株を有する普通株の株式清算優先重みを超えた場合にのみ価値を有する。OPM計算のキーデータには、無リスク金利、予想される流動性時間、および変動性が含まれる。市場価値が不足しているため、総株式価値に対して合理的な割引を行い、非流通基礎に基づく総持分公正価値の推定を得た。
賃貸借証書
当社は2021年1月1日から改訂されたASU番号2016-02レンタル(テーマ842)を採用し、改善された遡及方法を採用し、発効日をその初申請日とし、従来の期間はASC 840、レンタルまたはASC 840の先の指導に従ってリストアップした。当社は、(1)満期または既存契約がリース契約であるか否かまたはテナントを含むか否かを再評価しないこと、(2)満期または既存賃貸契約を含む任意の賃貸分類、または(3)任意の既存賃貸契約の初期直接コストを資本化することを要求する3つの方便を採用することを選択した。この基準を採用することにより、経営リース使用権資産と当期経営リース負債#ドルが記録された1.0発効日には、会社の貸借対照表の現金総額は100万ドルだった。この基準の採用は会社の経営報告書と全面的な損失、キャッシュフロー表あるいは累積損失に実質的な影響を与えていない。それぞれ2022年、2022年および2021年12月31日までに入金された使用権資産および負債は、付記14を参照されたい。
手配開始時に、当社は手配に存在する独特の事実と状況に基づいて、その手配が賃貸契約であるかどうかを決定する。レンタル期間が1年を超えるリースは、貸借対照表上で使用権資産および流動および非流動賃貸負債であることが確認されている(場合によっては)。エンティティはレンタルと非レンタル構成要素を分離しないことを選択することができる。当社は賃貸と非レンタル構成要素を一緒にすべての関連資産の単一賃貸構成要素として計算することを選択し、すべての契約の価格をレンタル構成要素のみに分配した。当社のすべての賃貸契約は運営賃貸に分類されています。
賃貸負債及びそれに対応する使用権資産は、最初に予想される残りのレンタル期間の賃貸支払い現在値に基づいて入金される。受け取った報酬などの項目については、使用権資産を何らかの調整する必要がある可能性がある。賃貸契約に隠されている金利は容易に確定できない。したがって、当社はその逓増借款金利を利用して賃貸支払いを割引しており、このことは、類似経済環境下で、当社が担保に基づいて同じ通貨、類似期限で賃貸支払いの固定金利を借り入れていることを反映している。当社は格付け機関に基づく信用格付けを行っていないため、それぞれのリース測定日の会社と市場ベースの要因に基づいて借入可能な推定担保金利を決定するために貸主からオファーを得る。当社は貸借対照表でオリジナル期限が1年以下であることを確認しない賃貸を選択しました。当社は通常、リーススケジュールを評価する際にのみ取消不可能なレンタル期間を計上しており、レンタル契約を延長する選択権が存在しない限り、合理的に決定された使用権を有している。当社は、直線賃貸料支出または受け取った任意の奨励について使用権資産を調整し、レンタル開始または移行日に発効する同じ逓増借款金利を使用して、純現在値で賃貸負債を再計量します。
経営リースコストはリース期間内に直線法で確認され,総合経営報告書と全面赤字では研究開発費と一般および行政費用に分類される。経営リースキャッシュフローは、統合キャッシュフロー表で経営活動で使用される現金純額に分類される。
外貨換算
同社はそのビットコインポンドでその連結財務諸表を維持している。機能通貨以外の通貨建ての貨幣資産と負債を貸借対照表日の現行為替レートで機能通貨に換算する。外貨建ての非貨幣性資産と負債を取引当日の為替レートで換算して機能通貨とする。外貨取引による為替損益は他の収入(費用)、総合経営報告書純額、全面赤字に計上されている。同社が記録した外国為替収益は約#ドル0.8百万ドルとドル2.02022年12月31日までと2021年12月31日までの年度はそれぞれ100万ドル。これらの収益はドルから来ています。これらのドルは私たちのイギリス子会社の金融機関に保管されています。この子会社の機能通貨はポンドです。
財務報告については、当社の総合財務諸表はいずれもドル(報告通貨)で列報されている。実体の財務諸表はその本位貨幣から報告通貨に換算し、資産と負債は資産負債表の日の為替レートで換算し、費用とその他の収入(費用)は列報期間の平均為替レートで換算し、株主権益は歴史的為替レートで換算する。換算調整は確定純損失には含まれないが、他の全面収益(株主権益の一構成要素)に対する外貨調整として計上される。
所得税
2019年12月、FASBは、会計基準の更新、またはASU、2019-12、“所得税--所得税の簡略化会計(主題740)”、またはASU 740を発表し、所得税の会計を簡略化した。新しい指針は、株式投資の繰延税項、実行期間内の税収分配の増加方法、および中期所得税の計算など、ASC 740における一般原則のいくつかの例外を削除する。この基準はまた、既存の指針を明確化と改訂することによって、アメリカ公認会計原則下の所得税の会計処理を簡略化し、営業権繰延税金の確認、合併グループメンバーへの税収分配、及び発行日を含む過渡期間内の年間有効税率計算に税法或いは税率公布の変化の影響を反映することを要求した。本ガイドラインは,2020年12月15日以降の年次期間とその後の移行期間に適用されるが,早期採用が許可されている。当社は2021年1月1日からこのASUを採用しており、連結財務諸表に実質的な影響はありません。
当社は、連結財務諸表またはその納税申告書で確認された事件の将来の税務結果を予想する繰延税金資産と負債の確認を要求する貸借対照法を用いて所得税を計算する。繰延税項資産及び負債は、財務諸表と資産及び負債の税ベースとの差額に基づいて、予想差額を用いて返送される年度の現行税率を決定する。繰延税金資産と負債の変動を所得税に計上する準備。当社は将来的に繰延税金資産を回収する可能性を評価しているが、既存の証拠の量によると、管理層は繰延税金資産のすべてまたは一部が現金化できない可能性が高いと考え、所得税支出を計上することで推定値を設定している。予想未来の課税オーバー額及び慎重かつ実行可能な税務計画策略を考慮して、繰延税金資産を回収する潜在力を評価する。
会社は、2段階法を用いて確認すべき税収割引額を決定することにより、連結財務諸表に所得税の不確実性を計上する。まず、税務機関が外部審査後にこのような状況を維持する可能性を決定するために、税収状況を評価しなければならない。税務状況がより持続可能であると考えられる場合、税務状況は、連結財務諸表で確認された利益金額として評価されるであろう。利用可能な利益金額は,最終和解時に実現される可能性が50%を超える最大額である。所得税の準備には、それによって生じる税収準備金または未確認の税収割引の影響が適切であると考えられ、関連する純利息および罰金が含まれる。2022年12月31日、2022年12月31日、2021年12月31日まで、当社はいかなる重大な不確定税務頭寸も発見していません。
同社は、添付されている総合経営報告書と全面赤字の中で、所得税支出項目で確認されていない税収割引に関する利息と罰金を確認した。2022年12月31日と2021年12月31日まで違います。利息または罰金を計算して総合貸借対照表の関連税務負債項目に計上しなければならない。
研究開発税収控除の恩恵を受ける
広範な研究·開発活動を展開している会社として、当社はイギリス中小企業計画下の研究開発税収免除制度の恩恵を受けている。中小企業制度の下で,会社は資格に応じた研究·開発活動による取引損失の一部を返納することができる
最高で現金のリベートがもらえます33.35条件に合った研究と開発支出の割合。同社は中小企業制度の条件を満たしている。条件に適合した支出には,主に研究者の雇用コスト,消耗品,アウトソーシング契約研究組織コスト,研究プロジェクトの一部として発生する公共事業コストがある。一部の下請けの資格に合った研究開発支出は最高に達する資格があります21.67%です。研究開発、臨床試験、製造活動に関連する大部分のコストはこれらの税収控除現金還付申請に含まれる資格がある。
その会社はイギリスで会社税を払わなければなりません。業務の性質上、当社は設立以来赤字が発生しています。研究開発または研究開発税収控除の収益は、総合経営と全面赤字報告書の中で他の収入(費用)の純額の構成要素として確認され、イギリスで回収可能な研究開発税収控除の総和を代表する。
イギリスの研究開発税収控除は全額会社に返却することができ、現在或いは未来の課税所得額に依存しない。そのため、当社はイギリスの研究開発税収控除からの全利益を所得税前純損失に計上しているため、所得税支出には反映されていない。将来的にイギリスの企業所得税債務を相殺するためにイギリスの研究開発税控除が必要であれば、この部分は福祉として所得税支出に記録され、課税所得額に依存しない返却可能な部分は他の収入(費用)純額に記録され続ける
同社は今後、中小企業の資格を満たしていない可能性があるため、中小企業制度下での研究·開発税免除を申請し続けることができないかもしれない。さらに、EU諸国の援助上限は、特定プロジェクトの申請可能な援助総額をユーロ以内に制限する7.5これは会社が将来税金控除を申請する能力に影響を及ぼすかもしれない。また,イギリスの“2021年金融法”は中小企業計画下でGBを超えるクレジット債権に上限を設定している20,0002021年4月から、広義には会社の総給与の3倍、またはPAYE、国家保険支払いやNICを参照しているが、この上限は適用されない例外がある。この例外は,企業に知的財産権の創造,措置の創造や管理,関連側に関する合格した研究や開発支出が求められているが,それを超えない15クレーム総額の%です。もしこのような例外が適用されなければ、これは私たちが要求する対応信用金額を制限するかもしれない。“2022-23年金融法”では、中小企業研究開発制度の税率が引き下げられ、2023年4月1日から有効信用が33.4ペンス/GBから18.6ペンス/GBに引き下げられる。
未納のイギリスの赤字は将来の課税利益を相殺するために無期限に繰り越す可能性があるが、多くの使用基準と制限を守らなければならない。毎年相殺できる金額はGB単位で5.0百万ドルと増額50イギリスの課税利益の%です。
総合損失
総合損失には,純損失および株主に関する取引や経済事件以外の取引や経済事件による株主権益の他の変化がある。2022年12月31日と2021年12月31日までに、他の総合損失を累計する唯一の構成要素は外貨換算調整である。
1株当たり純損失
同社は設立以来損失を報告しており、普通株株主の純損失を当期発行済み普通株の加重平均数量で割ることで、潜在的な希薄証券を考慮することなく、1株当たりの普通株基本純損失を計算している。当社は、希薄化を引き起こす可能性のあるすべての普通株を考慮した後、未帰属制限株式と既発行オプションを含む1株当たりの希薄化純損失を計算する。会社は設立以来純損失を報告してきたため、これらの潜在普通株はずっと赤字であり、1株当たりの基本損失と希釈後の1株当たりの損失はすべての届出期間で同じである。
派生商品
当社は、私どものキャッシュフローや収益が外貨レート変動により悪影響を受けるリスクを低減するために外貨契約を締結しています。当社は投機目的で外貨契約を締結していません。当社は、公正価値に応じて、ヘッジ会計資格を満たしていない派生ツールを貸借対照表上の資産または負債として確認します。当社はデリバティブツールの公正価値変動(損益)を添付の総合経営報告書に記入し、全面赤字を他の収入(費用)、純額としている。
最近発表された会計公告
同社は最近発表された会計声明を審査し、私たちの財務状況や経営結果に影響を与えないと判断した。
3. 公正価値計量
2022年12月31日と2021年12月31日まで、公正な価値で恒常的に計量された金融商品はない。経営陣は、当社の総合金融商品の帳簿は、現金及び現金等価物、制限的現金、支払すべき帳簿及び売掛金を含み、当該等のツールの短期的な性質により公正価値に近いと信じている。
当社は公正価値オプションを選択して2019年に発行された交換可能手形を会計処理します(付記8参照)。交換可能株式手形の公正価値は市場では観察できない重大な投入によって確定され、これは公正価値体系中の第三級計量である。
同社は#ドルの損失を記録した1.82020年12月31日までの年度の総合経営報告書及び全面赤字のうち、転換可能な手形の公正価値変動に百万元を支出した。
次の表は、会社の変換可能な手形の総公正価値の前転を提供し、公正価値は第3レベルの投入を使用して決定される(千単位)
| | | | | |
| 転換可能な手形 |
| 2019年12月31日現在の残高 | $ | 21,089 | |
| 価値変動を公平に承諾する | 1,771 | |
| 転換可能手形の決済 | (21,614) | |
| 為替差益 | (1,246) | |
| 2020年12月31日現在、2021年、2022年までの残高 | $ | — | |
4. 投資する
2020年3月6日、会社は戦略投資を行った0.5100万ドルで買収しました8完全に希釈したうえでDelix治療会社の株式を%保有しており,Delix治療会社は薬物発見·開発会社であり,中枢神経系あるいは中枢神経系適応のための新しい小分子を研究している。同社のDelix Treateutics,Inc.への投資は被投資先に大きな影響を与えない。この投資は簡単に決定できる公正な価値がないため、コストから減値を引いて計量し、減値は同一発行者が同じ或いは類似した投資の秩序ある取引に見られる価格変動によって調整される。重大な悪影響を及ぼす可能性のある事件や環境変化が発生した場合、この投資は公正な価値に基づいて非日常的に計量される。減価損失は総合経営報告書で確認されており、全面損失は帳簿価値が投資公正価値を超える金額に等しい。2022年12月31日までに違います。減価損失が確認されました。
5. 前払い費用と他の流動資産
前払い料金および他の流動資産には、以下のものが含まれている(千計)
| | | | | | | | | | | |
| 十二月三十一日 |
| 2022 | | 2021 |
| イギリスの研究開発税控除 | $ | 13,972 | | | $ | 9,587 | |
| 保険料を前払いする | 2,818 | | | 3,359 | |
| 前払い研究開発 | 28,211 | | | 4,562 | |
| 付加価値税は税金の払い戻しができる | 1,652 | | | 1,629 | |
| 繰延発売コスト | — | | | 840 | |
| 保証金 | 97 | | | 274 | |
| その他流動資産 | 945 | | | 1,370 | |
| $ | 47,695 | | | $ | 21,621 | |
6. 財産と設備、純額
財産と設備、純価値は以下の通り(千で計算)
| | | | | | | | | | | |
| 十二月三十一日 |
| 2022 | | 2021 |
| 実験室装置 | $ | 332 | | | $ | 370 | |
| 事務設備 | 637 | | | 315 | |
| 家具と固定装置 | 87 | | | 65 | |
| 賃借権改善 | 91 | | | 6 | |
| 1,147 | | | 756 | |
| 減算:減価償却累計 | (530) | | | (358) | |
| $ | 617 | | | $ | 398 | |
減価償却と償却費用は#ドルです0.3百万、$0.2百万ドルとドル0.12022年12月31日まで、2021年、2020年12月31日までの年度はそれぞれ100万ドル。
7. 費用とその他の負債を計算すべきである
計算すべき費用およびその他の負債には、以下の項目が含まれる(千で計算)
| | | | | | | | | | | |
| 十二月三十一日 |
| 2022 | | 2021 |
| 研究と開発費用を計算すべきである | $ | 1,684 | | | $ | 3,043 | |
| 専門費用を計算する | 1,284 | | | 1,386 | |
| 報酬と福祉費を計算しなければならない | 5,534 | | | 5,018 | |
| 賃金税を納める | 167 | | | 593 | |
| その他負債 | 656 | | | 268 | |
| $ | 9,325 | | | $ | 10,308 | |
8. 転換可能な手形
2020年4月17日,適格融資を構成するB系列転換可能優先株融資において,転換可能手形の未償還元金は$である18.4百万(GB)15.0百万)が自動的に1,723,263Bシリーズは優先株に転換可能で、2020年12月31日現在未返済残高はない。
当社は2019年の交換可能手形を計上するために公正価値オプションを選択します。当社は公正価値によって2019年の交換可能手形を記録し、その後、報告日ごとに公正価値によって再計量した。公正価値変動は、他の収入(費用)、連結経営報告書の純額と全面赤字の構成要素として確認された。会社は総合経営報告書で損失と総合損失を確認した#ドル1.8百万元は2020年12月31日までの年間交換可能手形の公正価値変動として。2022年12月31日または2021年12月31日までの年度内に、未償還の転換手形はない。
9. 転換可能優先株
2020年4月17日、同社は追加のBラウンド融資を完了した80.0Bシリーズ転換可能優先株を発行することで2019年の転換可能手形を含む百万ドルを融資する(付記8参照)。同社は$を受け取りました61.6発行された現金の収益は百万ドルです4,913,404Bシリーズの転換可能な優先株と発生する発行コストは$0.3百万株は、転換可能な優先株の減収に計上される。2019年に変換可能なチケットをへ1,723,263Bシリーズは優先株に転換できる。Bシリーズ転換可能優先株の発行価格は1ドルである1.42一株ずつです。
2019年12月31日現在、転換可能優先株とAシリーズ転換可能優先株には、以下が含まれている(株式金額を除く
| | | | | | | | | | | | | | | | | | | | | | | |
| 株 | | 清算優先権 | | 帳簿価値 |
| 授権 | | 卓越した | | |
| 転換可能優先株 | 2,650,980 | | | 2,650,980 | | | $ | 3,865 | | | $ | 3,761 | |
| Aシリーズ転換優先株 | 7,131,525 | | | 7,131,525 | | | 35,414 | | | 35,147 | |
| 9,782,505 | | | 9,782,505 | | | $ | 39,279 | | | $ | 38,908 | |
初公募完了時に、2019年12月31日に発行された転換可能優先株およびAシリーズ転換可能優先株は、2020年12月31日までに年度内に発行されたB系列転換可能優先株とともに、転換可能優先株に変換される16,419,172普通株です。会社の転換可能な優先株、Aシリーズの転換可能な優先株とBシリーズの転換可能な優先株の所有者は一定の投票権、配当と償還権、及び清算優先権と転換特権を持つ。転換可能優先株、Aシリーズ転換可能優先株、Bシリーズ転換可能優先株に関するすべての権利、優先権、特権は会社が初めて公募した時に終了し、同時に発行されたすべての転換可能優先株、Aシリーズ転換可能優先株、Bシリーズ転換可能優先株を普通株に変換する。
10. 普通株
2020年9月22日,当社はその普通株を代表する米国預託証券の初公募株を完成し,発行·販売した8,625,000アメリカの預託証明書、公開発行価格は$17.00アメリカに株式を預けて、純収益は約$です132.8引受料と発行コストを差し引いて100万ドルです。株式募集終了時に、転換可能優先株及びA系列転換可能優先株及びB系列転換可能優先株を16,419,172普通株です。
2021年5月4日、会社が販売4,000,000普通株を増発するより。2021年5月19日、引受業者は追加購入を行使した600,000普通株です。今回の募金による純収益は約#ドルであった154.8引受料と発行コストを差し引いて100万ドルです。
普通株ごとに所有者に権利を持たせる1つは会社の株主投票に提出されたすべての事項を採決する。一般株主は取締役会が発表する可能性のある配当金を得る権利がある。2022年12月31日まで違います。現金配当金は当社が発表または支払いしました。
2021年10月8日に、当社はCowen and Company、LLCまたはCowenと販売契約を締結し、この合意により、当社は最高$まで発行および販売することができます150.0何百万件ものアメリカの預託証明書は1つは普通株は、コーエンを通じて販売代理とする。会社の米国預託証明書(ADS)が販売されていれば、市場価格で販売されます。2022年12月14日、市場での見積もりによると、売りました44,416アメリカ預託証明書:$10.53アメリカごとに株式を預けています。
12月末現在の年度内2021年31日、当社は共同発行します1,476,936普通株式決済従業員及び非従業員が行使する株式オプション232,227普通株は2020年に行使されるオプションに関連し、その後2021年に株式を発行する。当社は2022年12月31日までに発行します462,722普通株式は、従業員及び非従業員が行使した株式オプションを決済するために使用される
2021年12月31日までの年間で70,482帰属制限株式単位、12,607株式は帰属して発行され,和解を達成した57,875株式は帰属しているが、2021年12月31日現在発行されていない
2022年12月31日までの年間で42,635帰属制限株式単位、24,747株式は帰属して発行され,和解を達成した17,888株式は帰属しているが、2022年12月31日現在発行されていない。2022年の間に82,622株式を決済として発行し、その中で57,8752021年に帰属し24,7472022年に授与される。
当社は2022年12月31日及び2021年12月31日までに発行します22,160そして0従業員は株式計画下の株式を購入する。
11. 株式ベースの報酬
2017持分インセンティブ計画
当社の歴史株主及び引受契約に基づき、当社は制限性株式、制限性株式単位及びオプションの発行を許可し、その従業員、非従業員及び取締役会メンバーへの激励とする。当該等奨励が株式オプション形式である範囲内で、当該等オプションは、2017年株式奨励計画又は2017年計画の条項に基づいて付与される。2019年7月、会社取締役会は“2017年度計画”を採択した。2017年計画では、そのイギリス人従業員に企業管理インセンティブまたはEMIオプションを付与し、そのアメリカ人従業員と会社非従業員にオプションを付与することが規定されています。2017年計画は取締役会が管理しています。
2017年計画により付与されたオプションは、通常付与されます三つあるいは…4年制サービス期間:33.3%和25%は、それぞれ、発効日1周年時に帰属する賠償金および残りの年度の月別帰属残高である。2017年計画により付与されたオプションは通常満期となります10授与の日から数年。2017年計画に基づいて付与された制限株式単位は、通常、超過付与される4年制サービス期間:25発効日1周年に付与された賠償金の割合は、その後四半期ごとに計算される
2020年6月30日に付与されたオプション25%は(I)以前に発生したものに帰属します1年授与日の記念日、又は(イ)会社の普通株式が任意の証券取引所に上場する日、その後直線的に帰属する3年余剰上の75%の割り当ては、すべての帰属まで。
2020年6月30日に付与される制限株式単位は遵守しなければならない25%は(I)の以前のものに帰属します1年又は(イ)当社の普通株式が任意の証券取引所に上場して六ヶ月後の初日であって、株式の市価が20少なくとも看板価格より%高いです5人いくつかの取引日が連続する
2022年12月31日現在、当社は共同発行を許可しています1,603,402普通株式はIPO前に2017年計画に基づいて付与された発行済みオプション。
2020年従業員株購入計画
当社の2020年従業員株式購入計画(ESPPと略称する)は2020年9月に取締役会で採択され、2020年9月に株主の承認を得て、当社の初公募に関するF-1表登録声明が発効した後に発効する。ESPPは最初に発行を保留して許可したのが合計で最大です340,053株主従業員に普通株を支給する。ESPPは,2022年1月1日から,保留と発行可能な株式数が自動的に増加し,2022年1月1日から,その後2020計画を終了することにより,毎年1月1日に(I)の少ない部分を自動的に増加させることを規定している1前年12月31日発行普通株式数の割合、(Ii)510,080普通株式又は(三)計画管理人が決定した数の少ない普通株式。株式分割、株式配当、または我々資本の他の変化の場合、ESPPによって保持されている株式数が変化する可能性がある。
2021年10月1日、会社は従業員増発計画と従業員増発計画を打ち出し、従業員はこの2つの計画を通じて割引価格で株を購入することができる。.の末尾に6か月株式は、自動的に貯蓄期間株の寄り付き価格と終値のうち低いものからaを引いた価格で購入される15割引率。
2020年株式オプション計画
2020年9月に、当社取締役会は、当社の株主から2020年の株式購入およびインセンティブ計画、または2020年計画を可決し、当社の初公募に関するF-1表登録説明書が発効した後に発効する予定である。2020年には、給与とリーダーシップ開発委員会が、会社の役員、従業員、役員、その他のキーパーソン(コンサルタントを含む)への株式および現金報酬を可能にする計画です。
2020計画に基づいて付与されたオプションは通常満期となる10授与された日から数年は4年間サービス期間、25発効日の1周年に帰属するオプションの割合と、残りの年度の月別帰属残高。
その会社は最初に保留した2,074,325その普通株式は2020年計画下の奨励発行に使用される。2020計画では、2022年1月1日から、この計画に基づいて保留と発行可能な株式数が自動的に増加し、最大増加することが規定されています4即時発行の普通株式数の割合
12月31日までに、または私たちの報酬とリーダーシップ開発委員会によって決定された少ない数の株。この数字は私たちの資本が分割、合併、株式配当、または他の変化が発生した場合に調整されるかもしれない。2020年計画により発行可能な普通株式総数は3,755,1192022年12月31日までの株式、そのうち667,802株式はまだ未来の付与に使用されることができる。
2020年計画によると2022年に従業員に付与されるオプションは一般的に満期になります10授与の日から数年。2022年の贈与には、(I)を含む3つの潜在的な帰属条項がある25毎年%を超える4年サービス期限:(Ii)4年サービス期間:25発効日1周年時に帰属する割合,残りの年度の残高は月ごとに帰属する;及び(Iii)毎月帰属する4年サービス期限。
当社は、2022年、2022年、2021年および2020年12月31日までの期間内に購入を付与します2,120,783, 1,043,702そして3,405,490普通株式はそれぞれ従業員と非従業員に支給される。
2022年誘因オプション賞
2022年8月1日、会社は私たちの新しい最高経営責任者に非限定的な株式オプションを授与して、最大購入可能です600,000奨励としての普通株。非限定株式オプションは101年の期限とベスト、その4分の1は2023年8月1日に満期になり、残りの4分の3は以下の時間で月平均分割払いになります36何ヶ月になりますか。無限買株権のその他の条項は、当社の2020年計画及び当社の無制限持分購入契約標準フォーマットに基づいて付与された無限制購入持分の条項と同じである
普通株
当社の2022年、2021年および2020年12月31日までの年度未帰属普通株式変動の概要は以下の通りです | | | | | | | | | | | |
| 株式数 | | 加重平均付与日公正価値 |
| 2020年12月31日までの未許可および未返済 | 13,757 | | | $ | 2.36 | |
| 授与する | — | | | $ | — | |
| 既得 | (13,757) | | | $ | 2.36 | |
| 没収される | — | | | $ | — | |
| 2022年12月31日と2021年12月31日までの未帰属·未返済 | — | | | $ | — | |
既存株式の総公正価値はゼロ$より少ない0.1百万ドルとドル1.32022年12月31日まで、2021年、2020年12月31日までの年度はそれぞれ100万ドル
限定株単位
当社の2022年、2022年、2021年および2020年12月31日までの未帰属制限株式単位変動の概要は以下の通りです
| | | | | | | | | | | | | | |
| 株式数 | | 加重平均付与日公正価値 | |
| 2020年12月31日までの未許可および未返済 | 217,482 | | | $ | 10.19 | | |
| 授与する | — | | | — | | |
| 既得 | (70,482) | | | 10.19 | | |
| 没収される | (31,860) | | | 10.19 | | |
| 2021年12月31日現在の未帰属と未返済 | 115,140 | | | $ | 10.19 | | |
| 授与する | 202,830 | | | 13.52 | | |
| 既得 | (42,635) | | | 9.77 | | |
| 没収される | (4,200) | | | 14.44 | | |
2022年12月31日現在の未帰属と未返済 | 271,135 | | | $ | 12.23 | | |
2022年2021年2020年12月31日までに2.6百万、$1.2百万ドルとドル2.0未帰属制限株単位に関する未確認補償コストは,#年加重平均期間で確認される予定である2.95数年の間2.5年和3.2それぞれ数年です。限定株の発行権価格は額面が国標より低い0.01一株ずつです。
株式オプション
次の表は、2022年、2021年、2020年12月31日までの会社の年間株式オプション活動をまとめています
| | | | | | | | | | | | | | | | | | | | | | | | | | |
| 株式数 | | 加重平均行権値 | | 加重平均残契約期間(年) | | 内在的価値を集める | |
| 2020年12月31日現在の未返済債務 | 4,430,340 | | | $ | 5.61 | | | 9.22 | | $ | 186,426 | | |
| 授与する | 1,043,702 | | | $ | 36.11 | | | | | | |
| 鍛えられた | (1,244,709) | | | $ | 1.55 | | | | | | |
| キャンセルまたは没収 | (313,830) | | | $ | 22.45 | | | | | | |
2021年12月31日現在の未返済債務 | 3,915,503 | | | $ | 13.53 | | | 8.64 | | $ | 51,162 | | |
| 授与する | 2,120,783 | | | $ | 13.49 | | | | | | |
| 鍛えられた | (462,722) | | | $ | 0.75 | | | | | | |
| キャンセルまたは没収 | (480,832) | | | $ | 11.09 | | | | | | |
2022年12月31日現在の未返済債務 | 5,092,732 | | | $ | 13.55 | | | 8.38 | | $ | 13,013 | | |
2022年12月31日から行使可能 | 2,342,389 | | | $ | 9.14 | | | 7.67 | | $ | 11,765 | | |
2022年12月31日現在帰属していません | 2,750,343 | | | $ | 17.31 | | | 8.99 | | $ | 1,247 | | |
2022年、2021年および2020年12月31日までの年間で、オプションを行使した内的価値の合計は5.5百万、$47.4百万ドルとドル12.8それぞれ100万ドルです
購入持分の内在価値の合計は、自社普通株公正価値よりも低い価格を行使する購入株式権の発行権価格と当社普通株公正価値との差額である。
購入株権を授与した加重平均授出日公正価値は#ドルである10そして$21.35そして$9.83それぞれ2022年、2021年および2020年12月31日までの年間1株当たり利益を上げている。
2022年2021年2020年12月31日までに30.4百万、$27.4百万ドルとドル18.1未帰属株式オプションに関する未確認補償コストは,加重平均期間中に確認される予定である2.8数年の間3.1年和3.5それぞれ数年です。
株式オプション推定値
ブラック·スコアーズオプション定価モデルにおける2022年、2022年、2021年、2020年12月31日までの年間に従業員と取締役に付与される株式オプションの公正価値を決定するための加重平均は、以下のように仮定される
| | | | | | | | | | | | | | | | | |
| 十二月三十一日までの年度 |
| 2022 | | 2021 | | 2020 |
| 期待オプション寿命(年) | 5.95年.年 | | 5.73年.年 | | 5.95年.年 |
| 予想変動率 | 80.76 | % | | 67.36 | % | | 66.10 | % |
| 無リスク金利 | 2.26 | % | | 0.95 | % | | 0.43 | % |
| 期待配当収益率 | — | % | | — | % | | — | % |
| 関連普通株の公正価値 | $ | 14.06 | | | $ | 35.21 | | | $ | 12.58 | |
株式ベースの給与費用
株式ベースの給与支出を研究開発費および一般·管理費と記すと、具体的には以下のようになる(単位:千)
| | | | | | | | | | | | | | | | | |
| 十二月三十一日までの年度 |
| 2022 | | 2021 | | 2020 |
| 研究開発 | 7,358 | | 4,569 | | 6,336 |
| 一般と行政 | 5,765 | | 4,070 | | 11,647 |
| 株式ベースの報酬総額 | $ | 13,123 | | | $ | 8,639 | | | $ | 17,983 | |
12. 所得税
所得税控除前の収入(赤字)には、以下のものが含まれています(千計)
| | | | | | | | | | | | | | | | | |
| 十二月三十一日までの年度 |
| 2022 | | 2021 | | 2020 |
| イギリス.イギリス | (92,841) | | | (72,397) | | | (60,522) | |
| 外国.外国 | 1,744 | | | 854 | | | 220 | |
| 所得税準備前の損失を差し引く | (91,097) | | | (71,543) | | | (60,302) | |
2022年12月31日まで、2021年、2020年12月31日までの年度の所得税は、英国の法定所得税率で計算される当年終了年度の所得税準備金には(千計)
| | | | | | | | | | | | | | | | | |
| 十二月三十一日までの年度 |
| 2022 | | 2021 | | 2020 |
| 現行の所得税支給 | | | | | |
| イギリス.イギリス | $ | — | | | $ | — | | | $ | — | |
| 外国.外国 | 1,865 | | | 744 | | | 253 | |
| 総当期費用: | $ | 1,865 | | | $ | 744 | | | $ | 253 | |
| | | | | |
| 繰延所得税割引: | | | | | |
| イギリス.イギリス | — | | | — | | | — | |
| 外国.外国 | (1,457) | | | (545) | | | (221) | |
| 繰延所得税の割引総額: | $ | (1,457) | | | $ | (545) | | | $ | (221) | |
| | | | | |
| 所得税引当総額 | $ | 408 | | | $ | 199 | | | $ | 32 | |
英国の法定所得税税率で計算される所得税費用と連結財務諸表に反映される所得税の入金は以下の通り(千で計算)
| | | | | | | | | | | | | | | | | |
| 十二月三十一日までの年度 |
| 2022 | | 2021 | | 2020 |
| 英国の法定税率で徴収される所得税 | $ | (17,309) | | | $ | (13,592) | | | $ | (11,458) | |
| 恒久的差異 | 14 | | | 69 | | | 340 | |
| イギリスの研究開発税控除 | 5,423 | | | 3,747 | | | 1,664 | |
| 評価免除額を変更する | 15,038 | | | 29,180 | | | 8,683 | |
| 州所得税 | 10 | | | 1 | | | (5) | |
| 繰延税金資産調整 | 8 | | | 80 | | | 919 | |
| 規定に戻る | 1,580 | | | (854) | | | — | |
| 持分補償 | (782) | | | (8,302) | | | — | |
| イギリスの税率の変化 | (3,609) | | | (10,147) | | | — | |
| 他にも | 35 | | | 17 | | | (111) | |
| $ | 408 | | | $ | 199 | | | $ | 32 | |
2022年、2022年、2021年、2020年12月31日までの繰延税金資産と負債の重要な構成要素には、以下の内容が含まれる(千計)
| | | | | | | | | | | | | | | | | | | | |
| 十二月三十一日までの年度 | |
| 2022 | | 2021 | | 2020 | |
| 純営業損失が繰り越す | $ | 44,227 | | | $ | 35,947 | | | $ | 10,075 | | |
| 準備金と課税項目 | 695 | | | 169 | | | 62 | | |
| 株式ベースの報酬 | 9,332 | | | 6,232 | | | 3,128 | | |
| 慈善寄付金 | 33 | | | — | | | — | | |
| 繰延税金資産総額 | 54,287 | | | 42,348 | | | 13,265 | | |
| 推定免税額 | $ | (51,909) | | | $ | (41,483) | | | $ | (13,000) | | |
| | | | | | |
| 減価償却 | (154) | | | (99) | | | (44) | | |
| 繰延税金負債総額 | (154) | | | (99) | | | (44) | | |
| 繰延税項目純資産 | $ | 2,224 | | | $ | 766 | | | $ | 221 | | |
同社の英国での純営業損失は、2022年12月31日、2021年12月31日、2020年12月31日現在、約$に転換している176.9百万、$144.0百万ドルとドル53.0それぞれ100万ドルで、無期限に繰り越すことができる。
2022年、2021年、2020年12月31日までの年間における繰延税項資産評価準備の変化は、主に純営業損失の増加に関係しており、具体的には以下の通り(千計)
| | | | | | | | | | | | | | | | | |
| 十二月三十一日までの年度 |
| 2022 | | 2021 | | 2020 |
| 年初の評価免税額 | $ | 41,483 | | | $ | 13,000 | | | $ | 3,665 | |
| 所得税計上の増加 | 15,038 | | | 29,180 | | | 8,683 | |
| CTAまでの増加を記録する | — | | | — | | | 652 | |
| CTAまでの減少を記録する | (4,612) | | | (697) | | | — | |
| 年末評価免税額 | $ | 51,909 | | | $ | 41,483 | | | $ | 13,000 | |
既存の一時的差額と純営業損失繰越の税額利益の将来実現は,最終的には繰越期間内に十分な課税所得額が存在するかどうかに依存する。会社は、2022年12月31日、2021年12月31日、2020年12月31日まで、推定手当が必要かどうかを決定する評価を行った。同社は現在と2008年の業務結果を含む既存のすべての積極的かつ消極的な証拠を審議した
数年前です。当社は将来の課税所得額を合理的に数量化することはできないと考え、すべての繰延税金資産が現金化できない可能性があると考えている。そのため、同社は2022年、2021年、2020年12月31日まで、英国の繰延税純資産に対して全額評価準備金を維持している。確認された繰延税金資産は完全にアメリカの実体と関連がある。
当社は権威的な指針を用いて、税務状況の不確実性について会計処理及び開示を行い、この指針は当社が税務状況の技術的価値に基づいて、審査(任意の訴訟手続に関する控訴を含む)を行った後、当社の税務状況がより持続可能であるかどうかを決定する。より課税点に達する可能性のある税務ヘッドについては、財務諸表で確認された税額から、最終的に関連税務機関と和解した場合に50%以上の最大利益を達成する可能性がある。2022年12月31日、2021年、2020年までに、実質的な不確定税収はない。
当社は課税所得額にある場合に所得税支出における不確定税額に関する利息と罰金を確認します。2022年、2021年、2020年12月31日まで、会社は違います。不確定な税務状況に関する計算利息または罰金および違います。金額は会社の経営報告書と全面赤字で確認されました
当社とその子会社はイギリスとアメリカで所得税申告書を提出します。当社が繰り越しの税務属性を持っていれば、その属性を生成した納税年度は連邦、州または外国の税務機関の審査後に調整することができ、このような税務属性が将来的に利用されれば。
2021年第2四半期、イギリスは“2021年金融法”(略称“金融法”)を公布した。同法は企業所得税税率を19%から25%に引き上げ、2023年4月1日から発効し、条件を満たす新工場や機械資産の初年度資本免税額を引き上げ、2021年4月1日から発効する。当社の既存の繰延税金残高への影響はすでに記録されており、当社のイギリス繰延税項目に対する純資産保持の推定値によって相殺される。
13. 1株当たり純損失
普通株主は1株当たりの基本純損失と償却純損失を以下のように計算する(1株と1株当たりの金額を含まず、単位は千)
| | | | | | | | | | | | | | | | | |
| 十二月三十一日までの年度 |
| 2022 | | 2021 | | 2020 |
| 分子.分子 | | | | | |
| 純損失 | $ | (91,505) | | | $ | (71,742) | | | $ | (60,334) | |
| 普通株主は純損失を占めるべきである−基本損失と希釈損失− | $ | (91,505) | | | $ | (71,742) | | | $ | (60,334) | |
| | | | | |
| 分母.分母 | | | | | |
| 加重-1株当たり純損失で使用される普通株平均-基本と削減 | 42,436,292 | | | 39,997,587 | | | 16,991,664 | |
| 1株当たり純損失--基本損失と赤字 | $ | (2.16) | | | $ | (1.79) | | | $ | (3.55) | |
当社の潜在的希薄化証券は、普通株に帰属していない、無帰属制限株単位、および授権されており、1株当たり純損失を減少させるため、1株当たり純損失の計算から除外されている。したがって、普通株株主が基本純損失と希釈後の1株当たり純損失を占めるべき加重平均既発行普通株数は同じである2022年、2022年、2021年、2020年12月31日までの年度普通株株主が純損失を占めるべきであると計算する際、会社は以下の潜在普通株を含まない。これらの株式を計上すると逆償却効果が生じるからである
| | | | | | | | | | | | | | | | | | | | |
| 十二月三十一日までの年度 |
| 2022 | | 2021 | | 2020 | |
| 未帰属限定株式単位 | 271,135 | | | 115,140 | | | 217,482 | | |
| 普通株に属していない | — | | | — | | | 13,757 | | |
| 未発行株の既得制限株式単位 | 17,888 | | | 57,875 | | | — | | |
| 株式オプション | 5,092,732 | | | 3,915,503 | | | 4,430,340 | | |
| 5,381,755 | | 4,088,518 | | 4,661,579 | |
14. 使用権資産
アメリカのニューヨーク
2022年8月、当社は契約を締結しました12か月WeWorkとオフィススペースをレンタルできる会員契約を締結する。会員資格は以下のようにキャンセルできます90数日前にお知らせします。当社はレンタル期間を12ヶ月以上に延長することを合理的に決定できないため、このメンバー資格は短期賃貸契約に計上されているため、当社の総合貸借対照表では確認されません
SOHOロンドンイギリス
2021年7月に当社が締結しました2年制Fora Space Limitedとの経営リースは2021年9月1日に開始された.キャンセルできない条項は24数ヶ月、そして賃貸契約を延長する選択はありません。毎月の日常的な宿泊料はGBです136,200会社は返金可能な保証金GBを支払いました136,200プロトコル実行時に.また,例年ごとに始まると,毎月の居住費は数年前のインフレにリンクした自動増加の影響を受ける。
デンマーク山、イギリスロンドン
2022年3月、当社はロンドン南部とモデズリーNHS基金信託基金と協定を締結し、イギリスロンドンデンマークサンモッドスリー病院ウィンザー路5号の土地と建物をレンタルした。借約は2022年6月21日に開始され、契約期間は5年それは.家賃はGBです180,000毎年のように違います。手付金に対応する。
次の表は、2022年12月31日と2021年12月31日までの年度の連結運営報告書に含まれるコストと使用権リース資産に関する全面的な損失(単位:千)をまとめています
| | | | | | | | | | | |
| 十二月三十一日までの年度 |
| 2022 | | 2021 |
| レンタル料 | | | |
| リースコストを経営する | $ | 2,263 | | $ | 1,844 |
| 可変リースコスト | — | | — |
| 短期賃貸コスト | 256 | | 86 |
| $ | 2,519 | | $ | 1,930 |
| その他の情報: | | | |
| 賃貸負債に含まれる金額を計量するために支払う現金: | | | |
| 経営的リース使用の経営的キャッシュフロー | $ | 2,219 | | $ | 1,971 |
| 新しい経営リース負債と引き換えに使用権資産 | 783 | | 4,513 |
| 加重平均残存賃貸年限(年) | 1.58 | | 1.64 |
| 加重平均割引率 | 5.70% | | 4.99% |
次の表は、2022年12月31日までの経営賃貸期限に応じた将来の最低賃貸支払い(千単位)をまとめています
| | | | | | | | |
| 2023年12月31日 | 1,537 | | |
| 2024年12月31日 | 218 | | |
| 2025年12月31日 | 218 | | |
| 2026年12月31日 | 54 | | |
| 将来の最低賃貸支払い総額 | $ | 2,027 | | |
| 差し引く:推定利息 | (99) | | |
| 合計する | $ | 1,928 | | |
15. 引受金とその他の事項
法律訴訟
時々、当社は訴訟の当事者であったり、正常な業務過程でクレームの制約を受けたりする可能性がある。同社は2022年12月31日、2021年12月31日または2020年12月31日まで、いかなる重大な訴訟にも参加しておらず、いかなる負債のための重大な緊急準備金も確立していない。
賠償する
通常の業務過程において、会社は、各種陳述及び保証を含む契約及び協定を締結し、一般賠償を規定する。同社のこれらの合意の下でのリスクは未知であり、将来同社にクレームをつける可能性があるためである。これまで、同社は何のクレームも支払っておらず、その賠償義務に関するいかなる訴訟も弁護されていない。しかし、このような賠償義務のため、会社は未来に費用を記録するかもしれない。
当社の定款によると、当社はある事件や事件についてその上級職員及び役員に対して賠償責任を負う責任がありますが、何らかの制限を受けなければなりませんが、当該等の高級職員及び取締役は当社の要求に応じて当該等の身分でサービスを提供しています。これまでクレームはありませんでしたが、同社には役員や高級社員保険があり、将来可能なクレームのために支払われた任意の金額の一部を回収することができる可能性があります。
16. 従業員福祉計画
イギリスでは、同社はその従業員を代表して個人固定年金計画に資金を供給している。その会社は$を支払った0.2百万、$0.2百万ドル以下0.12022年12月31日現在、2021年12月31日現在、2020年12月31日までの年間寄付金はそれぞれ100万ドル。
米国では,会社は国税法第401(K)条に基づいて固定払込貯蓄計画を確立した。この計画は、最低年齢とサービス要件に適合するほとんどのアメリカ人従業員をカバーし、参加者が税引前に年間給与の一部の支払いを延期することを可能にしている。その会社は$を支払った0.2百万、$0.1百万ドル以下0.12022年,2021年,2020年12月31日までの年度にそれぞれ100万ドルの寄付金を納めた。
サイン
1934年“証券法”第13又は15(D)節の要求に基づいて、登録者は、本10-K表年次報告が正式に許可された以下の署名者がその署名を代表するように正式に促した。
| | | | | | | | | | | |
| | 羅針盤経路会社 |
| | | |
| 日付: | 2023年2月28日 | 差出人: | /s/Kabir·ナート |
| | | Kabir·ナート |
| | | 最高経営責任者 |
| | | (首席行政主任) |
1934年証券法の要求に基づき、本10-K表年次報告は、以下の者代表登録者によって指定された身分及び日付で署名された。
| | | | | | | | | | | | | | |
| サイン | | タイトル | | 日取り |
| | | | |
| /s/Kabir·ナート | | 最高経営責任者
(首席行政主任) | | 2023年2月28日 |
| Kabir·ナート | | |
| | | | |
| /s/マイケル·フォルヴィ | | 首席財務官
(首席財務官と首席会計官) | | 2023年2月28日 |
| マイケル·フォルヴィ | | |
| | | | |
| ジョージ·ゴールドスミス | | 取締役会議長 | | 2023年2月28日 |
| ジョージ·ゴールドスミス | | |
| | | | |
| /s/Ekaterina Malievskaia | | 首席革新官兼取締役 | | 2023年2月28日 |
| Ekaterina Malievskaia | | |
| | | | |
| /s/Davidヨークノートン | | 役員をリードする | | 2023年2月28日 |
| デヴィッド·ヨーク·ノートン | | |
| | | | |
| /s/Annalisa Jenkins | | 役員.取締役 | | 2023年2月28日 |
| アナリザ·ジェンキンスMBBS | | |
| | | | |
| /s/トーマス·レングレン | | 役員.取締役 | | 2023年2月28日 |
| トーマス·レングレン | | |
| | | | |
| /s/ロバート·マグワイア | | 役員.取締役 | | 2023年2月28日 |
| ロバート·マグワイア | | |
| | | | |
| /s/リンダ·マゴドリック | | 役員.取締役 | | 2023年2月28日 |
| リンダ·マゴドリック | | |
| | | | |
| /s/ウェイン·ライリー | | 役員.取締役 | | 2023年2月28日 |
| ウェイン·ライリー医学博士公衆衛生修士商工管理修士です | | |
| | | | |