amgn-202212310000318154誤り2022会計年度Http://Fasb.org/us-GAAP/2022#OtherAssetsNonCurrentHttp://Fasb.org/us-GAAP/2022#OtherAssetsNonCurrentHttp://Fasb.org/us-GAAP/2022#AcruedLiabilitiesCurrentHttp://Fasb.org/us-GAAP/2022#AcruedLiabilitiesCurrentHttp://Fasb.org/us-GAAP/2022#その他の負債は現在ではありませんHttp://Fasb.org/us-GAAP/2022#その他の負債は現在ではありません00003181542022-01-012022-12-310000318154交換:XNGSアメリカ-アメリカ公認会計基準:普通株式メンバー2022-01-012022-12-310000318154取引所:XNYSAMGN:A 2.00プレミアムNotesDue 2026メンバー2022-01-012022-12-3100003181542022-06-30ISO 4217:ドル00003181542023-02-06Xbrli:共有0000318154アメリカ-公認会計基準:製品メンバー2022-01-012022-12-310000318154アメリカ-公認会計基準:製品メンバー2021-01-012021-12-310000318154アメリカ-公認会計基準:製品メンバー2020-01-012020-12-310000318154アメリカ-GAAP:ProductAndServiceOtherMember2022-01-012022-12-310000318154アメリカ-GAAP:ProductAndServiceOtherMember2021-01-012021-12-310000318154アメリカ-GAAP:ProductAndServiceOtherMember2020-01-012020-12-3100003181542021-01-012021-12-3100003181542020-01-012020-12-31ISO 4217:ドルXbrli:共有00003181542022-12-3100003181542021-12-310000318154アメリカ-アメリカ公認会計基準:普通株式メンバー2019-12-310000318154米国-米国公認会計基準:公共株には付加資産資本メンバーが含まれている2019-12-310000318154アメリカ-公認会計基準:前払いメンバーを保留2019-12-310000318154アメリカ公認会計原則:他の総合収入メンバーを累計2019-12-3100003181542019-12-310000318154SRT:累計調整有効期限調整メンバアメリカ-公認会計基準:前払いメンバーを保留2019-12-310000318154アメリカ公認会計原則:他の総合収入メンバーを累計SRT:累計調整有効期限調整メンバ2019-12-310000318154SRT:累計調整有効期限調整メンバ2019-12-310000318154アメリカ-公認会計基準:前払いメンバーを保留2020-01-012020-12-310000318154アメリカ公認会計原則:他の総合収入メンバーを累計2020-01-012020-12-310000318154アメリカ-アメリカ公認会計基準:普通株式メンバー2020-01-012020-12-310000318154米国-米国公認会計基準:公共株には付加資産資本メンバーが含まれている2020-01-012020-12-310000318154アメリカ-アメリカ公認会計基準:普通株式メンバー2020-12-310000318154米国-米国公認会計基準:公共株には付加資産資本メンバーが含まれている2020-12-310000318154アメリカ-公認会計基準:前払いメンバーを保留2020-12-310000318154アメリカ公認会計原則:他の総合収入メンバーを累計2020-12-3100003181542020-12-310000318154アメリカ-公認会計基準:前払いメンバーを保留2021-01-012021-12-310000318154アメリカ公認会計原則:他の総合収入メンバーを累計2021-01-012021-12-310000318154アメリカ-アメリカ公認会計基準:普通株式メンバー2021-01-012021-12-310000318154米国-米国公認会計基準:公共株には付加資産資本メンバーが含まれている2021-01-012021-12-310000318154アメリカ-アメリカ公認会計基準:普通株式メンバー2021-12-310000318154米国-米国公認会計基準:公共株には付加資産資本メンバーが含まれている2021-12-310000318154アメリカ-公認会計基準:前払いメンバーを保留2021-12-310000318154アメリカ公認会計原則:他の総合収入メンバーを累計2021-12-310000318154アメリカ-公認会計基準:前払いメンバーを保留2022-01-012022-12-310000318154アメリカ公認会計原則:他の総合収入メンバーを累計2022-01-012022-12-310000318154アメリカ-アメリカ公認会計基準:普通株式メンバー2022-01-012022-12-310000318154米国-米国公認会計基準:公共株には付加資産資本メンバーが含まれている2022-01-012022-12-310000318154アメリカ-アメリカ公認会計基準:普通株式メンバー2022-12-310000318154米国-米国公認会計基準:公共株には付加資産資本メンバーが含まれている2022-12-310000318154アメリカ-公認会計基準:前払いメンバーを保留2022-12-310000318154アメリカ公認会計原則:他の総合収入メンバーを累計2022-12-31AMGN:細分化市場Xbrli:純0000318154SRT:最小メンバ数2022-01-012022-12-310000318154SRT:最大メンバ数2022-01-012022-12-310000318154AMGN:Horizon治療メンバー2022-12-120000318154AMGN:Horizon治療メンバー2022-12-012022-12-31AMGN:製品AMGN:計画0000318154AMGN:Horizon治療メンバー2022-12-312022-12-310000318154AMGN:Horizon治療メンバー2022-12-22AMGN:Traunche0000318154AMGN:Horizon治療メンバーAMGN:ブリッジ証明書プロトコルメンバ2022-12-310000318154AMGN:Horizon治療メンバー2022-12-222022-12-220000318154AMGN:ChemoCentryxIncMember2022-10-200000318154AMGN:ChemoCentryxIncMember2022-10-202022-10-200000318154AMGN:ChemoCentryxIncMember2022-10-012022-12-310000318154AMGN:ChemoCentryxIncMember米国-GAAP:技術的権利の発達したメンバー2022-10-200000318154AMGN:ChemoCentryxIncMember米国-GAAP:技術的権利の発達したメンバー2022-10-202022-10-200000318154AMGN:Teneobioメンバー2022-01-012022-12-310000318154AMGN:Teneobioメンバー2022-12-312022-12-310000318154AMGN:Teneobioメンバー2022-12-310000318154米国-GAAP:InProcessResearchAndDevelopmentMembersAMGN:Teneobioメンバー2022-12-310000318154AMGN:RD技術権利メンバーAMGN:Teneobioメンバー2022-12-310000318154US-GAAP:ライセンスプロトコルのメンバーAMGN:Teneobioメンバー2022-12-310000318154米国-GAAP:InProcessResearchAndDevelopmentMembersAMGN:AMG 340メンバーAMGN:Teneobioメンバー2022-12-310000318154米国-GAAP:InProcessResearchAndDevelopmentMembersAMGN:Teneobioメンバー2022-01-012022-12-310000318154AMGN:RD技術権利メンバーAMGN:Teneobioメンバー2022-12-312022-12-310000318154US-GAAP:ライセンスプロトコルのメンバーAMGN:Teneobioメンバー2022-12-312022-12-310000318154AMGN:FivePrimeTreateuticsIncMembers2021-04-162021-04-160000318154AMGN:FivePrimeTreateuticsIncMembers2021-04-1600003181542022-11-022022-11-0200003181542022-11-020000318154AMGN:その他一般料金メンバー2022-01-012022-12-310000318154AMGN:強化メンバー国:アメリカ2022-01-012022-12-310000318154AMGN:強化メンバーアメリカ-GAAP:非アメリカのメンバー2022-01-012022-12-310000318154AMGN:強化メンバー2022-01-012022-12-310000318154AMGN:強化メンバー国:アメリカ2021-01-012021-12-310000318154AMGN:強化メンバーアメリカ-GAAP:非アメリカのメンバー2021-01-012021-12-310000318154AMGN:強化メンバー2021-01-012021-12-310000318154AMGN:強化メンバー国:アメリカ2020-01-012020-12-310000318154AMGN:強化メンバーアメリカ-GAAP:非アメリカのメンバー2020-01-012020-12-310000318154AMGN:強化メンバー2020-01-012020-12-310000318154AMGN:プロ会員国:アメリカ2022-01-012022-12-310000318154AMGN:プロ会員アメリカ-GAAP:非アメリカのメンバー2022-01-012022-12-310000318154AMGN:プロ会員2022-01-012022-12-310000318154AMGN:プロ会員国:アメリカ2021-01-012021-12-310000318154AMGN:プロ会員アメリカ-GAAP:非アメリカのメンバー2021-01-012021-12-310000318154AMGN:プロ会員2021-01-012021-12-310000318154AMGN:プロ会員国:アメリカ2020-01-012020-12-310000318154AMGN:プロ会員アメリカ-GAAP:非アメリカのメンバー2020-01-012020-12-310000318154AMGN:プロ会員2020-01-012020-12-310000318154AMGN:OtezlaMember国:アメリカ2022-01-012022-12-310000318154AMGN:OtezlaMemberアメリカ-GAAP:非アメリカのメンバー2022-01-012022-12-310000318154AMGN:OtezlaMember2022-01-012022-12-310000318154AMGN:OtezlaMember国:アメリカ2021-01-012021-12-310000318154AMGN:OtezlaMemberアメリカ-GAAP:非アメリカのメンバー2021-01-012021-12-310000318154AMGN:OtezlaMember2021-01-012021-12-310000318154AMGN:OtezlaMember国:アメリカ2020-01-012020-12-310000318154AMGN:OtezlaMemberアメリカ-GAAP:非アメリカのメンバー2020-01-012020-12-310000318154AMGN:OtezlaMember2020-01-012020-12-310000318154AMGN:XgevaMember国:アメリカ2022-01-012022-12-310000318154AMGN:XgevaMemberアメリカ-GAAP:非アメリカのメンバー2022-01-012022-12-310000318154AMGN:XgevaMember2022-01-012022-12-310000318154AMGN:XgevaMember国:アメリカ2021-01-012021-12-310000318154AMGN:XgevaMemberアメリカ-GAAP:非アメリカのメンバー2021-01-012021-12-310000318154AMGN:XgevaMember2021-01-012021-12-310000318154AMGN:XgevaMember国:アメリカ2020-01-012020-12-310000318154AMGN:XgevaMemberアメリカ-GAAP:非アメリカのメンバー2020-01-012020-12-310000318154AMGN:XgevaMember2020-01-012020-12-310000318154AMGN:AranespMember国:アメリカ2022-01-012022-12-310000318154AMGN:AranespMemberアメリカ-GAAP:非アメリカのメンバー2022-01-012022-12-310000318154AMGN:AranespMember2022-01-012022-12-310000318154AMGN:AranespMember国:アメリカ2021-01-012021-12-310000318154AMGN:AranespMemberアメリカ-GAAP:非アメリカのメンバー2021-01-012021-12-310000318154AMGN:AranespMember2021-01-012021-12-310000318154AMGN:AranespMember国:アメリカ2020-01-012020-12-310000318154AMGN:AranespMemberアメリカ-GAAP:非アメリカのメンバー2020-01-012020-12-310000318154AMGN:AranespMember2020-01-012020-12-310000318154国:アメリカAMGN:NplateMember2022-01-012022-12-310000318154AMGN:NplateMemberアメリカ-GAAP:非アメリカのメンバー2022-10-012022-12-310000318154AMGN:NplateMember2022-01-012022-12-310000318154国:アメリカAMGN:NplateMember2021-01-012021-12-310000318154AMGN:NplateMemberアメリカ-GAAP:非アメリカのメンバー2021-01-012021-12-310000318154AMGN:NplateMember2021-01-012021-12-310000318154国:アメリカAMGN:NplateMember2020-01-012020-12-310000318154AMGN:NplateMemberアメリカ-GAAP:非アメリカのメンバー2020-01-012020-12-310000318154AMGN:NplateMember2020-01-012020-12-310000318154AMGN:RepathavolocumabMember国:アメリカ2022-01-012022-12-310000318154AMGN:RepathavolocumabMemberアメリカ-GAAP:非アメリカのメンバー2022-01-012022-12-310000318154AMGN:RepathavolocumabMember2022-01-012022-12-310000318154AMGN:RepathavolocumabMember国:アメリカ2021-01-012021-12-310000318154AMGN:RepathavolocumabMemberアメリカ-GAAP:非アメリカのメンバー2021-01-012021-12-310000318154AMGN:RepathavolocumabMember2021-01-012021-12-310000318154AMGN:RepathavolocumabMember国:アメリカ2020-01-012020-12-310000318154AMGN:RepathavolocumabMemberアメリカ-GAAP:非アメリカのメンバー2020-01-012020-12-310000318154AMGN:RepathavolocumabMember2020-01-012020-12-310000318154AMGN:Kyprolisメンバー国:アメリカ2022-01-012022-12-310000318154AMGN:Kyprolisメンバーアメリカ-GAAP:非アメリカのメンバー2022-01-012022-12-310000318154AMGN:Kyprolisメンバー2022-01-012022-12-310000318154AMGN:Kyprolisメンバー国:アメリカ2021-01-012021-12-310000318154AMGN:Kyprolisメンバーアメリカ-GAAP:非アメリカのメンバー2021-01-012021-12-310000318154AMGN:Kyprolisメンバー2021-01-012021-12-310000318154AMGN:Kyprolisメンバー国:アメリカ2020-01-012020-12-310000318154AMGN:Kyprolisメンバーアメリカ-GAAP:非アメリカのメンバー2020-01-012020-12-310000318154AMGN:Kyprolisメンバー2020-01-012020-12-310000318154AMGN:Neulastaメンバー国:アメリカ2022-01-012022-12-310000318154AMGN:Neulastaメンバーアメリカ-GAAP:非アメリカのメンバー2022-01-012022-12-310000318154AMGN:Neulastaメンバー2022-01-012022-12-310000318154AMGN:Neulastaメンバー国:アメリカ2021-01-012021-12-310000318154AMGN:Neulastaメンバーアメリカ-GAAP:非アメリカのメンバー2021-01-012021-12-310000318154AMGN:Neulastaメンバー2021-01-012021-12-310000318154AMGN:Neulastaメンバー国:アメリカ2020-01-012020-12-310000318154AMGN:Neulastaメンバーアメリカ-GAAP:非アメリカのメンバー2020-01-012020-12-310000318154AMGN:Neulastaメンバー2020-01-012020-12-310000318154国:アメリカAMGN:ナイト会員2022-01-012022-12-310000318154AMGN:ナイト会員アメリカ-GAAP:非アメリカのメンバー2022-01-012022-12-310000318154AMGN:ナイト会員2022-01-012022-12-310000318154国:アメリカAMGN:ナイト会員2021-01-012021-12-310000318154AMGN:ナイト会員アメリカ-GAAP:非アメリカのメンバー2021-01-012021-12-310000318154AMGN:ナイト会員2021-01-012021-12-310000318154国:アメリカAMGN:ナイト会員2020-01-012020-12-310000318154AMGN:ナイト会員アメリカ-GAAP:非アメリカのメンバー2020-01-012020-12-310000318154AMGN:ナイト会員2020-01-012020-12-310000318154国:アメリカAMGN:その他の製品メンバ2022-01-012022-12-310000318154AMGN:その他の製品メンバアメリカ-GAAP:非アメリカのメンバー2022-01-012022-12-310000318154AMGN:その他の製品メンバ2022-01-012022-12-310000318154国:アメリカAMGN:その他の製品メンバ2021-01-012021-12-310000318154AMGN:その他の製品メンバアメリカ-GAAP:非アメリカのメンバー2021-01-012021-12-310000318154AMGN:その他の製品メンバ2021-01-012021-12-310000318154国:アメリカAMGN:その他の製品メンバ2020-01-012020-12-310000318154AMGN:その他の製品メンバアメリカ-GAAP:非アメリカのメンバー2020-01-012020-12-310000318154AMGN:その他の製品メンバ2020-01-012020-12-310000318154国:アメリカアメリカ-公認会計基準:製品メンバー2022-01-012022-12-310000318154アメリカ-公認会計基準:製品メンバーアメリカ-GAAP:非アメリカのメンバー2022-01-012022-12-310000318154国:アメリカアメリカ-公認会計基準:製品メンバー2021-01-012021-12-310000318154アメリカ-公認会計基準:製品メンバーアメリカ-GAAP:非アメリカのメンバー2021-01-012021-12-310000318154国:アメリカアメリカ-公認会計基準:製品メンバー2020-01-012020-12-310000318154アメリカ-公認会計基準:製品メンバーアメリカ-GAAP:非アメリカのメンバー2020-01-012020-12-310000318154国:アメリカアメリカ-GAAP:ProductAndServiceOtherMember2022-01-012022-12-310000318154アメリカ-GAAP:ProductAndServiceOtherMemberアメリカ-GAAP:非アメリカのメンバー2022-01-012022-12-310000318154国:アメリカアメリカ-GAAP:ProductAndServiceOtherMember2021-01-012021-12-310000318154アメリカ-GAAP:ProductAndServiceOtherMemberアメリカ-GAAP:非アメリカのメンバー2021-01-012021-12-310000318154国:アメリカアメリカ-GAAP:ProductAndServiceOtherMember2020-01-012020-12-310000318154アメリカ-GAAP:ProductAndServiceOtherMemberアメリカ-GAAP:非アメリカのメンバー2020-01-012020-12-310000318154国:アメリカ2022-01-012022-12-310000318154アメリカ-GAAP:非アメリカのメンバー2022-01-012022-12-310000318154国:アメリカ2021-01-012021-12-310000318154アメリカ-GAAP:非アメリカのメンバー2021-01-012021-12-310000318154国:アメリカ2020-01-012020-12-310000318154アメリカ-GAAP:非アメリカのメンバー2020-01-012020-12-31AMGN:お客様0000318154アメリカ-公認会計基準:製品メンバーAMGN:クライアント2人のメンバ2022-01-012022-12-310000318154アメリカ-公認会計基準:製品メンバーAMGN:クライアント2人のメンバ2021-01-012021-12-310000318154アメリカ-公認会計基準:製品メンバーAMGN:クライアント2人のメンバ2020-01-012020-12-310000318154AMGN:CustomerOneメンバーアメリカ-公認会計基準:製品メンバー2022-01-012022-12-310000318154AMGN:CustomerOneメンバーアメリカ-公認会計基準:製品メンバー2021-01-012021-12-310000318154AMGN:CustomerOneメンバーアメリカ-公認会計基準:製品メンバー2020-01-012020-12-310000318154アメリカ-公認会計基準:製品メンバーAMGN:お客様3者メンバー2022-01-012022-12-310000318154アメリカ-公認会計基準:製品メンバーAMGN:お客様3者メンバー2021-01-012021-12-310000318154アメリカ-公認会計基準:製品メンバーAMGN:お客様3者メンバー2020-01-012020-12-310000318154米国-GAAP:制限株式単位RSUメンバー2022-01-012022-12-310000318154AMGN:性能単位メンバ2022-01-012022-12-310000318154米国-GAAP:制限株式単位RSUメンバー2021-01-012021-12-310000318154米国-GAAP:制限株式単位RSUメンバー2020-01-012020-12-310000318154AMGN:性能単位メンバ2021-01-012021-12-310000318154AMGN:性能単位メンバ2020-01-012020-12-310000318154米国-公認会計基準:従業員株式オプションメンバー2022-01-012022-12-310000318154米国-公認会計基準:従業員株式オプションメンバー2021-01-012021-12-310000318154米国-公認会計基準:従業員株式オプションメンバー2020-01-012020-12-310000318154米国-GAAP:制限株式単位RSUメンバー2021-12-310000318154米国-GAAP:制限株式単位RSUメンバー2022-12-310000318154米国-公認会計基準:従業員株式オプションメンバー2021-12-310000318154米国-公認会計基準:従業員株式オプションメンバー2022-12-310000318154AMGN:性能単位メンバ2022-12-310000318154AMGN:性能単位メンバ2021-12-310000318154米国-GAAP:国内/地域メンバー2022-01-012022-12-310000318154米国-GAAP:国内/地域メンバー2021-01-012021-12-310000318154米国-GAAP:国内/地域メンバー2020-01-012020-12-310000318154アメリカ-公認会計基準:外国人メンバー2022-01-012022-12-310000318154アメリカ-公認会計基準:外国人メンバー2021-01-012021-12-310000318154アメリカ-公認会計基準:外国人メンバー2020-01-012020-12-310000318154米国-GAAP:国内/地域メンバー2022-12-310000318154AMGN:2023年から2043年までの税金支出米国-GAAP:国内/地域メンバー2022-12-310000318154アメリカ-公認会計基準:州と地方法律法規のメンバー2022-12-310000318154アメリカ-公認会計基準:外国人メンバー2022-12-310000318154アメリカ-公認会計基準:外国人メンバーAMGN:2022と2031の間の運用損失が予想を上回る2022-12-310000318154米国-GAAP:国内/地域メンバー2021-05-31AMGN:ノード数0000318154米国-GAAP:国内/地域メンバー2022-04-280000318154米国-GAAP:国内/地域メンバー2022-12-19AMGN:ケース0000318154AMGN:北京遺伝子メンバー2020-01-020000318154AMGN:北京遺伝子メンバー2020-01-022020-01-020000318154AMGN:北京遺伝子メンバー米国-公認会計基準:研究·開発費メンバー2022-01-012022-12-310000318154AMGN:北京遺伝子メンバー米国-公認会計基準:研究·開発費メンバー2021-01-012021-12-310000318154AMGN:北京遺伝子メンバー米国-公認会計基準:研究·開発費メンバー2020-01-012020-12-310000318154AMGN:北京遺伝子メンバーAMGN:北京遺伝子メンバー2022-01-012022-12-310000318154AMGN:北京遺伝子メンバーAMGN:北京遺伝子メンバー2021-01-012021-12-310000318154アメリカ-公認会計基準:販売一般と管理費用メンバーAMGN:北京遺伝子メンバー2022-01-012022-12-310000318154アメリカ-公認会計基準:販売一般と管理費用メンバーAMGN:北京遺伝子メンバー2021-01-012021-12-310000318154AMGN:北京遺伝子メンバーアメリカ-公認会計基準:貿易売掛金メンバー2022-12-310000318154AMGN:北京遺伝子メンバーアメリカ-公認会計基準:貿易売掛金メンバー2021-12-310000318154AMGN:北京遺伝子メンバー米国-公認会計基準:その他の現在の資産メンバー2022-12-310000318154AMGN:北京遺伝子メンバー米国-公認会計基準:その他の現在の資産メンバー2021-12-310000318154AMGN:アスリコンメンバー米国-公認会計基準:研究·開発費メンバー2022-01-012022-12-310000318154AMGN:アスリコンメンバー米国-公認会計基準:研究·開発費メンバー2021-01-012021-12-310000318154AMGN:アスリコンメンバー米国-公認会計基準:研究·開発費メンバー2020-01-012020-12-310000318154アメリカ-公認会計基準:販売一般と管理費用メンバーAMGN:アスリコンメンバー2022-01-012022-12-310000318154アメリカ-公認会計基準:販売一般と管理費用メンバーAMGN:アスリコンメンバー2021-01-012021-12-310000318154アメリカ-公認会計基準:販売一般と管理費用メンバーAMGN:アスリコンメンバー2020-01-012020-12-310000318154米国-GAAP:販売コストメンバーAMGN:アスリコンメンバー2022-01-012022-12-310000318154米国-GAAP:販売コストメンバーAMGN:UCBMember2022-01-012022-12-310000318154米国-GAAP:販売コストメンバーAMGN:UCBMember2021-01-012021-12-310000318154米国-GAAP:販売コストメンバーAMGN:UCBMember2020-01-012020-12-310000318154AMGN:ノワ製薬のメンバー米国-公認会計基準:研究·開発費メンバー2022-01-012022-12-310000318154AMGN:ノワ製薬のメンバーアメリカ-公認会計基準:販売一般と管理費用メンバー2021-01-012021-12-310000318154AMGN:ノワ製薬のメンバーアメリカ-公認会計基準:販売一般と管理費用メンバー2020-01-012020-12-310000318154米国-GAAP:販売コストメンバーAMGN:ノワ製薬のメンバー2021-01-012021-12-310000318154米国-GAAP:販売コストメンバーAMGN:ノワ製薬のメンバー2020-01-012020-12-310000318154AMGN:Kyowa麒麟有限公司のメンバー2021-07-012021-09-300000318154AMGN:Kyowa麒麟有限公司のメンバー2022-12-310000318154アメリカ-公認会計基準:アメリカ証券メンバー2022-12-310000318154US-GAAP:アメリカReasuryBillSecuritiesMembers2022-12-310000318154アメリカ公認会計基準:MoneyMarketFundsMembers2022-12-310000318154AMGN:OtherShortTermInterestBearingSecuritiesMember2022-12-310000318154アメリカ-公認会計基準:アメリカ証券メンバー2021-12-310000318154US-GAAP:アメリカReasuryBillSecuritiesMembers2021-12-310000318154アメリカ公認会計基準:MoneyMarketFundsMembers2021-12-310000318154AMGN:OtherShortTermInterestBearingSecuritiesMember2021-12-310000318154AMGN:AvailableForSalesInvestmentsメンバー2022-12-310000318154AMGN:AvailableForSalesInvestmentsメンバー2021-12-310000318154米国-GAAP:他の非現在の資産メンバ2022-12-310000318154米国-GAAP:他の非現在の資産メンバ2021-12-310000318154AMGN:北京遺伝子メンバー2020-01-020000318154SRT:最小メンバ数AMGN:北京遺伝子メンバー2022-01-012022-12-310000318154SRT:最大メンバ数AMGN:北京遺伝子メンバー2022-01-012022-12-310000318154AMGN:北京遺伝子メンバー2022-01-012022-12-310000318154AMGN:北京遺伝子メンバー2021-01-012021-12-310000318154AMGN:北京遺伝子メンバー2020-01-012020-12-310000318154AMGN:北京遺伝子メンバー2022-12-310000318154AMGN:北京遺伝子メンバー2021-12-310000318154AMGN:北京遺伝子メンバー2022-12-310000318154AMGN:北京遺伝子メンバー2021-12-310000318154AMGN:Neumora治療会社のメンバー2021-09-300000318154AMGN:Neumora治療会社のメンバー2021-09-300000318154AMGN:Neumora治療会社のメンバー2021-09-302021-09-300000318154AMGN:Neumora治療会社のメンバー2022-01-012022-12-310000318154AMGN:Neumora治療会社のメンバー2022-12-310000318154AMGN:Neumora治療会社のメンバー2021-12-310000318154AMGN:Neumora治療会社のメンバー2022-12-310000318154AMGN:Neumora治療会社のメンバー2021-12-310000318154AMGN:Neumora治療会社のメンバー2022-01-012022-12-310000318154AMGN:Neumora治療会社のメンバー2021-01-012021-12-310000318154US-GAAP:FairValueMeasuredAtNetAssetValuePerShareMemberSRT:パートナー興味メンバ2022-12-310000318154US-GAAP:FairValueMeasuredAtNetAssetValuePerShareMemberSRT:パートナー興味メンバ2021-12-310000318154US-GAAP:FairValueMeasuredAtNetAssetValuePerShareMemberSRT:パートナー興味メンバ2022-01-012022-12-310000318154US-GAAP:FairValueMeasuredAtNetAssetValuePerShareMemberSRT:パートナー興味メンバ2021-01-012021-12-310000318154US-GAAP:FairValueMeasuredAtNetAssetValuePerShareMemberSRT:パートナー興味メンバ2020-01-012020-12-310000318154SRT:最小メンバ数US-GAAP:改善メンバーの構築と構築2022-01-012022-12-310000318154SRT:最大メンバ数US-GAAP:改善メンバーの構築と構築2022-01-012022-12-310000318154SRT:最小メンバ数AMGN:製造設備メンバ2022-01-012022-12-310000318154SRT:最大メンバ数AMGN:製造設備メンバ2022-01-012022-12-310000318154SRT:最小メンバ数AMGN:ラボ装置のメンバー2022-01-012022-12-310000318154AMGN:ラボ装置のメンバーSRT:最大メンバ数2022-01-012022-12-310000318154AMGN:固定デバイスメンバ2022-01-012022-12-310000318154SRT:最小メンバ数米国-GAAP:ソフトウェアとソフトウェア開発コストメンバー2022-01-012022-12-310000318154SRT:最大メンバ数米国-GAAP:ソフトウェアとソフトウェア開発コストメンバー2022-01-012022-12-310000318154SRT:最小メンバ数US-GAAP:PropertyPlantAndEquipmentOtherTypesMember2022-01-012022-12-310000318154US-GAAP:PropertyPlantAndEquipmentOtherTypesMemberSRT:最大メンバ数2022-01-012022-12-310000318154国:アメリカ2022-12-310000318154国:アメリカ2021-12-310000318154国:メディア2022-12-310000318154国:メディア2021-12-310000318154AMGN:RestOfWorldMembers2022-12-310000318154AMGN:RestOfWorldMembers2021-12-310000318154米国-GAAP:技術的権利の発達したメンバー2022-12-310000318154米国-GAAP:技術的権利の発達したメンバー2021-12-310000318154US-GAAP:ライセンスプロトコルのメンバー2022-12-310000318154US-GAAP:ライセンスプロトコルのメンバー2021-12-310000318154米国-公認会計基準:市場関連無形資産メンバー2022-12-310000318154米国-公認会計基準:市場関連無形資産メンバー2021-12-310000318154AMGN:研究開発技術権利獲得メンバー2022-12-310000318154AMGN:研究開発技術権利獲得メンバー2021-12-310000318154米国-GAAP:InProcessResearchAndDevelopmentMembers2022-12-310000318154米国-GAAP:InProcessResearchAndDevelopmentMembers2021-12-310000318154AMGN:レンタル放棄メンバー2022-12-310000318154アメリカ-GAAP:NoteesPayableto BanksMembersAMGN:ZeroPointFortyOnePercent SwissFrancBondsDue 2000とTwentyThreeMembers2022-12-31ISO 4217:スイスフラン0000318154アメリカ-GAAP:NoteesPayableto BanksMembersAMGN:ZeroPointFortyOnePercent SwissFrancBondsDue 2000とTwentyThreeMembers2021-12-310000318154AMGN:2つの点2つの5つのパーセントノードDuewoZeroTwoThreeMembersアメリカ-GAAP:NoteesPayableto BanksMembers2022-12-310000318154AMGN:2つの点2つの5つのパーセントノードDuewoZeroTwoThreeMembersアメリカ-GAAP:NoteesPayableto BanksMembers2021-12-310000318154AMGN:ThreePointSixTwoFivePercentNotesDue 2024メンバーアメリカ-GAAP:NoteesPayableto BanksMembers2022-12-310000318154AMGN:ThreePointSixTwoFivePercentNotesDue 2024メンバーアメリカ-GAAP:NoteesPayableto BanksMembers2021-12-310000318154AMGN:A 190 NotesDue 20251902025注意メンバーアメリカ-GAAP:NoteesPayableto BanksMembers2022-12-310000318154AMGN:A 190 NotesDue 20251902025注意メンバーアメリカ-GAAP:NoteesPayableto BanksMembers2021-12-310000318154AMGN:ThreePointOneTwoFivePercent NotesDuewoZeroTwoFiveMemberアメリカ-GAAP:NoteesPayableto BanksMembers2022-12-310000318154AMGN:ThreePointOneTwoFivePercent NotesDuewoZeroTwoFiveMemberアメリカ-GAAP:NoteesPayableto BanksMembers2021-12-310000318154AMGN:TwoPercentEuroNotesDuewo千とTwentySixMemberアメリカ-GAAP:NoteesPayableto BanksMembers2022-12-31ISO 4217:ユーロ0000318154AMGN:TwoPercentEuroNotesDuewo千とTwentySixMemberアメリカ-GAAP:NoteesPayableto BanksMembers2021-12-310000318154AMGN:TwoPointSixZeroNotesDuewoZeroTwoSixMemberアメリカ-GAAP:NoteesPayableto BanksMembers2022-12-310000318154AMGN:TwoPointSixZeroNotesDuewoZeroTwoSixMemberアメリカ-GAAP:NoteesPayableto BanksMembers2021-12-310000318154AMGN:FivePointFiveZeroPercent PoundSterlingNotesDue 2026メンバーアメリカ-GAAP:NoteesPayableto BanksMembers2022-12-31ISO 4217:ポンド0000318154AMGN:FivePointFiveZeroPercent PoundSterlingNotesDue 2026メンバーアメリカ-GAAP:NoteesPayableto BanksMembers2021-12-310000318154AMGN:TwoPointTwoZeroPercent NotesDuewoZeroTwoSevenメンバーアメリカ-GAAP:NoteesPayableto BanksMembers2022-12-310000318154AMGN:TwoPointTwoZeroPercent NotesDuewoZeroTwoSevenメンバーアメリカ-GAAP:NoteesPayableto BanksMembers2021-12-310000318154アメリカ-GAAP:NoteesPayableto BanksMembersAMGN:ThreePointTwoZeroNotesDue 2027メンバー2022-12-310000318154アメリカ-GAAP:NoteesPayableto BanksMembersAMGN:ThreePointTwoZeroNotesDue 2027メンバー2021-12-310000318154AMGN:A 165 NotesDue 20281652028メンバーアメリカ-GAAP:NoteesPayableto BanksMembers2022-12-310000318154AMGN:A 165 NotesDue 20281652028メンバーアメリカ-GAAP:NoteesPayableto BanksMembers2021-12-310000318154AMGN:A 300 NotesDue 20293002029注意メンバーアメリカ-GAAP:NoteesPayableto BanksMembers2022-12-310000318154AMGN:A 405 NotesDue 20294052029メンバー注意アメリカ-GAAP:NoteesPayableto BanksMembers2022-12-310000318154AMGN:4%PoundSterlingNotesDue 2029メンバーアメリカ-GAAP:NoteesPayableto BanksMembers2022-12-310000318154AMGN:4%PoundSterlingNotesDue 2029メンバーアメリカ-GAAP:NoteesPayableto BanksMembers2021-12-310000318154AMGN:TwoPointFourFivePercent NotesDue 2030メンバーアメリカ-GAAP:NoteesPayableto BanksMembers2022-12-310000318154AMGN:TwoPointFourFivePercent NotesDue 2030メンバーアメリカ-GAAP:NoteesPayableto BanksMembers2021-12-310000318154AMGN:TwoPointThreeZeroPercent NotesDue 2031メンバーアメリカ-GAAP:NoteesPayableto BanksMembers2022-12-310000318154AMGN:TwoPointThreeZeroPercent NotesDue 2031メンバーアメリカ-GAAP:NoteesPayableto BanksMembers2021-12-310000318154AMGN:2点0パーセント2032注意メンバーアメリカ-GAAP:NoteesPayableto BanksMembers2022-12-310000318154AMGN:2点0パーセント2032注意メンバーアメリカ-GAAP:NoteesPayableto BanksMembers2021-12-310000318154AMGN:A 335 NotesDue 20323352032メンバーに注意アメリカ-GAAP:NoteesPayableto BanksMembers2022-12-310000318154AMGN:A 420 NotesDue 20334202033メンバーに注意アメリカ-GAAP:NoteesPayableto BanksMembers2022-12-310000318154AMGN:6点3個7個5パーセントノードDue 2037メンバーアメリカ-GAAP:NoteesPayableto BanksMembers2022-12-310000318154AMGN:6点3個7個5パーセントノードDue 2037メンバーアメリカ-GAAP:NoteesPayableto BanksMembers2021-12-310000318154AMGN:SixPointNineZeroPercent NotesDue 2038メンバーアメリカ-GAAP:NoteesPayableto BanksMembers2022-12-310000318154AMGN:SixPointNineZeroPercent NotesDue 2038メンバーアメリカ-GAAP:NoteesPayableto BanksMembers2021-12-310000318154AMGN:SixPointFourZeroPercent NotesDue 2039メンバーアメリカ-GAAP:NoteesPayableto BanksMembers2022-12-310000318154AMGN:SixPointFourZeroPercent NotesDue 2039メンバーアメリカ-GAAP:NoteesPayableto BanksMembers2021-12-310000318154AMGN:ThreePointOneFivePercentNoteesDue 2040メンバーアメリカ-GAAP:NoteesPayableto BanksMembers2022-12-310000318154AMGN:ThreePointOneFivePercentNoteesDue 2040メンバーアメリカ-GAAP:NoteesPayableto BanksMembers2021-12-310000318154AMGN:5分7分5分ノード2040メンバーアメリカ-GAAP:NoteesPayableto BanksMembers2022-12-310000318154AMGN:5分7分5分ノード2040メンバーアメリカ-GAAP:NoteesPayableto BanksMembers2021-12-310000318154AMGN:TwoPointEightZeroPercent 2041ノードメンバアメリカ-GAAP:NoteesPayableto BanksMembers2022-12-310000318154AMGN:TwoPointEightZeroPercent 2041ノードメンバアメリカ-GAAP:NoteesPayableto BanksMembers2021-12-310000318154アメリカ-GAAP:NoteesPayableto BanksMembersAMGN:FourPointNine 5%ノード:2041メンバー2022-12-310000318154アメリカ-GAAP:NoteesPayableto BanksMembersAMGN:FourPointNine 5%ノード:2041メンバー2021-12-310000318154AMGN:FivePointOneFivePercentNoteesDue 2041メンバーアメリカ-GAAP:NoteesPayableto BanksMembers2022-12-310000318154AMGN:FivePointOneFivePercentNoteesDue 2041メンバーアメリカ-GAAP:NoteesPayableto BanksMembers2021-12-310000318154AMGN:FivePointSixFivePercentNoteesDue 2042メンバーアメリカ-GAAP:NoteesPayableto BanksMembers2022-12-310000318154AMGN:FivePointSixFivePercentNoteesDue 2042メンバーアメリカ-GAAP:NoteesPayableto BanksMembers2021-12-310000318154AMGN:FivePointThreeSeven FivePercent NotesDue 2043 Membersアメリカ-GAAP:NoteesPayableto BanksMembers2022-12-310000318154AMGN:FivePointThreeSeven FivePercent NotesDue 2043 Membersアメリカ-GAAP:NoteesPayableto BanksMembers2021-12-310000318154アメリカ-GAAP:NoteesPayableto BanksMembersAMGN:FourPointFourZeroPercent NoteesDuewoZeroFourFiveMember2022-12-310000318154アメリカ-GAAP:NoteesPayableto BanksMembersAMGN:FourPointFourZeroPercent NoteesDuewoZeroFourFiveMember2021-12-310000318154AMGN:FourPointFiveSixThrePercent NotesDuewoZeroFourEight Memberアメリカ-GAAP:NoteesPayableto BanksMembers2022-12-310000318154AMGN:FourPointFiveSixThrePercent NotesDuewoZeroFourEight Memberアメリカ-GAAP:NoteesPayableto BanksMembers2021-12-310000318154AMGN:3分3分7分5分ノードDue 2050メンバーアメリカ-GAAP:NoteesPayableto BanksMembers2022-12-310000318154AMGN:3分3分7分5分ノードDue 2050メンバーアメリカ-GAAP:NoteesPayableto BanksMembers2021-12-310000318154AMGN:FourPointSixSixThreePercentNotesDuewoZeroFiveOneMembersアメリカ-GAAP:NoteesPayableto BanksMembers2022-12-310000318154AMGN:FourPointSixSixThreePercentNotesDuewoZeroFiveOneMembersアメリカ-GAAP:NoteesPayableto BanksMembers2021-12-310000318154AMGN:A 300 NotesDue 20523002052メンバーに注意アメリカ-GAAP:NoteesPayableto BanksMembers2022-12-310000318154AMGN:A 300 NotesDue 20523002052メンバーに注意アメリカ-GAAP:NoteesPayableto BanksMembers2021-12-310000318154AMGN:A 420 NotesDue 20524202052メンバーに注意アメリカ-GAAP:NoteesPayableto BanksMembers2022-12-310000318154AMGN:A 4875 NotesDue 205348752053メンバーに注意アメリカ-GAAP:NoteesPayableto BanksMembers2022-12-310000318154AMGN:2点7%ノード2つのゼロビット5人の3人のメンバを繰り返すアメリカ-GAAP:NoteesPayableto BanksMembers2022-12-310000318154AMGN:2点7%ノード2つのゼロビット5人の3人のメンバを繰り返すアメリカ-GAAP:NoteesPayableto BanksMembers2021-12-310000318154AMGN:A 440 NotesDue 20624402062メンバーに注意アメリカ-GAAP:NoteesPayableto BanksMembers2022-12-310000318154AMGN:A 440 NotesDue 20624402062メンバーに注意アメリカ-GAAP:NoteesPayableto BanksMembers2021-12-310000318154AMGN:OtherNotesDue 2097メンバーアメリカ-GAAP:NoteesPayableto BanksMembers2022-12-310000318154AMGN:OtherNotesDue 2097メンバーアメリカ-GAAP:NoteesPayableto BanksMembers2021-12-310000318154AMGN:SixPointNineZeroPercent NotesDue 2038メンバーアメリカ-GAAP:NoteesPayableto BanksMembers2022-01-012022-12-310000318154AMGN:2点7%ノード2つのゼロビット5人の3人のメンバを繰り返すアメリカ-GAAP:NoteesPayableto BanksMembers2022-01-012022-12-310000318154アメリカ-GAAP:NoteesPayableto BanksMembersAMGN:FourPointNine 5%ノード:2041メンバー2022-01-012022-12-310000318154アメリカ-GAAP:NoteesPayableto BanksMembersAMGN:FourPointFourZeroPercent NoteesDuewoZeroFourFiveMember2022-01-012022-12-310000318154AMGN:2つの点2つの5つのパーセントノードDuewoZeroTwoThreeMembersアメリカ-GAAP:NoteesPayableto BanksMembers2022-01-012022-12-310000318154AMGN:TwoPointFourFivePercent NotesDue 2030メンバーアメリカ-GAAP:NoteesPayableto BanksMembers2022-01-012022-12-310000318154AMGN:6点3個7個5パーセントノードDue 2037メンバーアメリカ-GAAP:NoteesPayableto BanksMembers2022-01-012022-12-310000318154AMGN:ThreePointOneTwoFivePercent NotesDuewoZeroTwoFiveMemberアメリカ-GAAP:NoteesPayableto BanksMembers2022-01-012022-12-310000318154AMGN:FivePointFiveZeroPercent PoundSterlingNotesDue 2026メンバーアメリカ-GAAP:NoteesPayableto BanksMembers2022-01-012022-12-310000318154AMGN:TwoPointTwoZeroPercent NotesDuewoZeroTwoSevenメンバーアメリカ-GAAP:NoteesPayableto BanksMembers2022-01-012022-12-310000318154AMGN:FivePointSixFivePercentNoteesDue 2042メンバーアメリカ-GAAP:NoteesPayableto BanksMembers2022-01-012022-12-310000318154AMGN:A 405 NotesDue 20294052029メンバー注意アメリカ-GAAP:NoteesPayableto BanksMembers2022-01-012022-12-310000318154AMGN:A 440 NotesDue 20624402062メンバーに注意アメリカ-GAAP:NoteesPayableto BanksMembers2022-01-012022-12-310000318154AMGN:4%PoundSterlingNotesDue 2029メンバーアメリカ-GAAP:NoteesPayableto BanksMembers2022-01-012022-12-310000318154AMGN:TwoPointThreeZeroPercent NotesDue 2031メンバーアメリカ-GAAP:NoteesPayableto BanksMembers2022-01-012022-12-310000318154AMGN:FourPointSixSixThreePercentNotesDuewoZeroFiveOneMembersアメリカ-GAAP:NoteesPayableto BanksMembers2022-01-012022-12-310000318154AMGN:ThreePointOneFivePercentNoteesDue 2040メンバーアメリカ-GAAP:NoteesPayableto BanksMembers2022-01-012022-12-310000318154AMGN:A 4875 NotesDue 205348752053メンバーに注意アメリカ-GAAP:NoteesPayableto BanksMembers2022-01-012022-12-310000318154AMGN:TwoPointSixZeroNotesDuewoZeroTwoSixMemberアメリカ-GAAP:NoteesPayableto BanksMembers2022-01-012022-12-310000318154AMGN:A 300 NotesDue 20293002029注意メンバーアメリカ-GAAP:NoteesPayableto BanksMembers2022-01-012022-12-310000318154AMGN:5分7分5分ノード2040メンバーアメリカ-GAAP:NoteesPayableto BanksMembers2022-01-012022-12-310000318154AMGN:TwoPercentEuroNotesDuewo千とTwentySixMemberアメリカ-GAAP:NoteesPayableto BanksMembers2022-01-012022-12-310000318154AMGN:SixPointFourZeroPercent NotesDue 2039メンバーアメリカ-GAAP:NoteesPayableto BanksMembers2022-01-012022-12-310000318154アメリカ-GAAP:NoteesPayableto BanksMembersAMGN:ThreePointTwoZeroNotesDue 2027メンバー2022-01-012022-12-310000318154AMGN:FivePointThreeSeven FivePercent NotesDue 2043 Membersアメリカ-GAAP:NoteesPayableto BanksMembers2022-01-012022-12-310000318154AMGN:A 300 NotesDue 20523002052メンバーに注意アメリカ-GAAP:NoteesPayableto BanksMembers2022-01-012022-12-310000318154AMGN:FourPointFiveSixThrePercent NotesDuewoZeroFourEight Memberアメリカ-GAAP:NoteesPayableto BanksMembers2022-01-012022-12-310000318154AMGN:A 190 NotesDue 20251902025注意メンバーアメリカ-GAAP:NoteesPayableto BanksMembers2022-01-012022-12-310000318154AMGN:3分3分7分5分ノードDue 2050メンバーアメリカ-GAAP:NoteesPayableto BanksMembers2022-01-012022-12-310000318154AMGN:A 335 NotesDue 20323352032メンバーに注意アメリカ-GAAP:NoteesPayableto BanksMembers2022-01-012022-12-310000318154AMGN:A 200 NotesDue 20322002032 NotesMemberアメリカ-GAAP:NoteesPayableto BanksMembers2022-01-012022-12-310000318154アメリカ-GAAP:NoteesPayableto BanksMembersAMGN:A 280 NoteesDue 2041メンバー2022-01-012022-12-310000318154AMGN:A 165 NotesDue 20281652028メンバーアメリカ-GAAP:NoteesPayableto BanksMembers2022-01-012022-12-310000318154アメリカ-GAAP:NoteesPayableto BanksMembersAMGN:ZeroPointFortyOnePercent SwissFrancBondsDue 2000とTwentyThreeMembers2022-01-012022-12-310000318154AMGN:A 420 NotesDue 20334202033メンバーに注意アメリカ-GAAP:NoteesPayableto BanksMembers2022-01-012022-12-310000318154AMGN:ThreePointSixTwoFivePercentNotesDue 2024メンバーアメリカ-GAAP:NoteesPayableto BanksMembers2022-01-012022-12-310000318154AMGN:FivePointOneFivePercentNoteesDue 2041メンバーアメリカ-GAAP:NoteesPayableto BanksMembers2022-01-012022-12-310000318154AMGN:A 420 NotesDue 20524202052メンバーに注意アメリカ-GAAP:NoteesPayableto BanksMembers2022-01-012022-12-310000318154AMGN:ZeroPointFortyOnePercent SwissFrancBondsDue 2000とTwentyThreeMembers2022-12-310000318154SRT:最小メンバ数米国-公認会計基準:債務証券化支払可能メンバー2022-01-012022-12-310000318154米国-公認会計基準:債務証券化支払可能メンバーSRT:最大メンバ数2022-01-012022-12-310000318154アメリカ-GAAP:NoteesPayableto BanksMembers2022-12-310000318154アメリカ-GAAP:NoteesPayableto BanksMembers2021-12-310000318154AMGN:A 200 NotesDue 20322002032 NotesMemberアメリカ-GAAP:NoteesPayableto BanksMembers2021-12-310000318154アメリカ-GAAP:NoteesPayableto BanksMembersAMGN:A 280 NoteesDue 2041メンバー2021-12-310000318154アメリカ-GAAP:NoteesPayableto BanksMembers2020-12-310000318154AMGN:A 190 NotesDue 20251902025注意メンバーアメリカ-GAAP:NoteesPayableto BanksMembers2020-12-310000318154AMGN:TwoPointTwoZeroPercent NotesDuewoZeroTwoSevenメンバーアメリカ-GAAP:NoteesPayableto BanksMembers2020-12-310000318154AMGN:TwoPointFourFivePercent NotesDue 2030メンバーアメリカ-GAAP:NoteesPayableto BanksMembers2020-12-310000318154AMGN:TwoPointThreeZeroPercent NotesDue 2031メンバーアメリカ-GAAP:NoteesPayableto BanksMembers2020-12-310000318154AMGN:ThreePointOneFivePercentNoteesDue 2040メンバーアメリカ-GAAP:NoteesPayableto BanksMembers2020-12-310000318154AMGN:3分3分7分5分ノードDue 2050メンバーアメリカ-GAAP:NoteesPayableto BanksMembers2020-12-3100003181542022-10-012022-12-310000318154アメリカ-GAAP:NoteesPayableto BanksMembers2022-01-012022-12-310000318154アメリカ-GAAP:NoteesPayableto BanksMembers2021-01-012021-12-310000318154AMGN:OnePointTwoFivePercentNoteesDuewoZeroTwoTwoTwoMemberアメリカ-GAAP:NoteesPayableto BanksMembers2021-01-012021-12-310000318154AMGN:OnePointTwoFivePercentNoteesDuewoZeroTwoTwoTwoMemberアメリカ-GAAP:NoteesPayableto BanksMembers2021-12-310000318154AMGN:TwoPointSevenゼロノードパーセント2022メンバーアメリカ-GAAP:NoteesPayableto BanksMembers2021-01-012021-12-310000318154AMGN:TwoPointSevenゼロノードパーセント2022メンバーアメリカ-GAAP:NoteesPayableto BanksMembers2021-12-310000318154AMGN:TwoPointSixFivePercentNoteesDuewoZeroTwoTwoTwoMemberアメリカ-GAAP:NoteesPayableto BanksMembers2021-01-012021-12-310000318154AMGN:TwoPointSixFivePercentNoteesDuewoZeroTwoTwoTwoMemberアメリカ-GAAP:NoteesPayableto BanksMembers2021-12-310000318154AMGN:ThreePointSixTwoFivePercentNotesDue 2022メンバーアメリカ-GAAP:NoteesPayableto BanksMembers2021-01-012021-12-310000318154AMGN:ThreePointSixTwoFivePercentNotesDue 2022メンバーアメリカ-GAAP:NoteesPayableto BanksMembers2021-12-310000318154アメリカ-GAAP:NoteesPayableto BanksMembers2020-01-012020-12-310000318154AMGN:FourPointFiveZeroPercent NotesDue 20 Memberアメリカ-GAAP:NoteesPayableto BanksMembers2020-01-012020-12-310000318154AMGN:FourPointFiveZeroPercent NotesDue 20 Memberアメリカ-GAAP:NoteesPayableto BanksMembers2020-12-310000318154AMGN:TwoPointOneTwoFivePercentNotesDuewoZeroTwoZeroMemberアメリカ-GAAP:NoteesPayableto BanksMembers2020-01-012020-12-310000318154AMGN:TwoPointOneTwoFivePercentNotesDuewoZeroTwoZeroMemberアメリカ-GAAP:NoteesPayableto BanksMembers2020-12-310000318154AMGN:FloatingRateNotesDue 2020メンバーアメリカ-GAAP:NoteesPayableto BanksMembers2020-01-012020-12-310000318154アメリカ-GAAP:NoteesPayableto BanksMembersAMGN:TwoPointTwoZeroNotesDue 2020メンバー2020-01-012020-12-310000318154アメリカ-GAAP:NoteesPayableto BanksMembersAMGN:TwoPointTwoZeroNotesDue 2020メンバー2020-12-310000318154AMGN:3点4,5ノードパーセンテージ20 Membersアメリカ-GAAP:NoteesPayableto BanksMembers2020-01-012020-12-310000318154AMGN:3点4,5ノードパーセンテージ20 Membersアメリカ-GAAP:NoteesPayableto BanksMembers2020-12-310000318154AMGN:FourPointOneZeroPercent NoteesDue 2021メンバーアメリカ-GAAP:NoteesPayableto BanksMembers2020-01-012020-12-310000318154AMGN:FourPointOneZeroPercent NoteesDue 2021メンバーアメリカ-GAAP:NoteesPayableto BanksMembers2020-12-310000318154AMGN:OnePoint 8 ightFivePercentNoteesDuewoZeroTwoOneMembersアメリカ-GAAP:NoteesPayableto BanksMembers2020-01-012020-12-310000318154AMGN:OnePoint 8 ightFivePercentNoteesDuewoZeroTwoOneMembersアメリカ-GAAP:NoteesPayableto BanksMembers2020-12-310000318154AMGN:3点8個7個5%ノードDue 2021メンバーアメリカ-GAAP:NoteesPayableto BanksMembers2020-01-012020-12-310000318154AMGN:3点8個7個5%ノードDue 2021メンバーアメリカ-GAAP:NoteesPayableto BanksMembers2020-12-310000318154US-GAAP:DesignatedAsHedgingInstrumentMemberUS-GAAP:InterestRateSwapMember2021-12-310000318154US-GAAP:DesignatedAsHedgingInstrumentMemberUS-GAAP:InterestRateSwapMember2020-12-310000318154US-GAAP:DesignatedAsHedgingInstrumentMemberUS-GAAP:InterestRateSwapMemberAMGN:InterestRateSwapOneMember2020-12-310000318154AMGN:ThreePointSixTwoFivePercentNotesDue 2024メンバーアメリカ-GAAP:NoteesPayableto BanksMembers2020-12-310000318154AMGN:TwoPointSixZeroNotesDuewoZeroTwoSixMemberアメリカ-GAAP:NoteesPayableto BanksMembers2020-12-310000318154AMGN:FourPointSixSixThreePercentNotesDuewoZeroFiveOneMembersアメリカ-GAAP:NoteesPayableto BanksMembers2020-12-310000318154AMGN:ThreePointSixTwoFivePercentNotesDue 2022メンバーアメリカ-GAAP:NoteesPayableto BanksMembers2020-12-310000318154AMGN:ThreePointOneTwoFivePercent NotesDuewoZeroTwoFiveMemberアメリカ-GAAP:NoteesPayableto BanksMembers2020-12-310000318154US-GAAP:DesignatedAsHedgingInstrumentMemberUS-GAAP:InterestRateSwapMember2020-01-012020-12-310000318154AMGN:InterestRateSwapTwoMemberUS-GAAP:DesignatedAsHedgingInstrumentMemberUS-GAAP:InterestRateSwapMember2020-12-310000318154AMGN:ThreePointSixTwoFivePercentNotesDue 2024メンバー米国-GAAP:NoteesPayableOtherPayableメンバー2022-12-310000318154AMGN:ThreePointSixTwoFivePercentNotesDue 2024メンバー米国-GAAP:NoteesPayableOtherPayableメンバー2021-12-310000318154AMGN:ThreePointSixTwoFivePercentNotesDue 2024メンバーUS-GAAP:ロンドン銀行間同業借り換え金利LIBORメンバー米国-GAAP:NoteesPayableOtherPayableメンバー2021-12-310000318154AMGN:ThreePointSixTwoFivePercentNotesDue 2024メンバーUS-GAAP:ロンドン銀行間同業借り換え金利LIBORメンバー米国-GAAP:NoteesPayableOtherPayableメンバー2022-12-310000318154AMGN:ThreePointOneTwoFivePercent NotesDuewoZeroTwoFiveMember米国-GAAP:NoteesPayableOtherPayableメンバー2022-12-310000318154AMGN:ThreePointOneTwoFivePercent NotesDuewoZeroTwoFiveMember米国-GAAP:NoteesPayableOtherPayableメンバー2021-12-310000318154US-GAAP:ロンドン銀行間同業借り換え金利LIBORメンバーAMGN:ThreePointOneTwoFivePercent NotesDuewoZeroTwoFiveMember米国-GAAP:NoteesPayableOtherPayableメンバー2022-12-310000318154US-GAAP:ロンドン銀行間同業借り換え金利LIBORメンバーAMGN:ThreePointOneTwoFivePercent NotesDuewoZeroTwoFiveMember米国-GAAP:NoteesPayableOtherPayableメンバー2021-12-310000318154米国-GAAP:NoteesPayableOtherPayableメンバーAMGN:TwoPointSixZeroNotesDuewoZeroTwoSixMember2022-12-310000318154米国-GAAP:NoteesPayableOtherPayableメンバーAMGN:TwoPointSixZeroNotesDuewoZeroTwoSixMember2021-12-310000318154US-GAAP:ロンドン銀行間同業借り換え金利LIBORメンバー米国-GAAP:NoteesPayableOtherPayableメンバーAMGN:TwoPointSixZeroNotesDuewoZeroTwoSixMember2021-12-310000318154US-GAAP:ロンドン銀行間同業借り換え金利LIBORメンバー米国-GAAP:NoteesPayableOtherPayableメンバーAMGN:TwoPointSixZeroNotesDuewoZeroTwoSixMember2022-12-310000318154米国-GAAP:NoteesPayableOtherPayableメンバーAMGN:TwoPointFourFivePercent NotesDue 2030メンバー2022-12-310000318154米国-GAAP:NoteesPayableOtherPayableメンバーAMGN:TwoPointFourFivePercent NotesDue 2030メンバー2021-12-310000318154US-GAAP:ロンドン銀行間同業借り換え金利LIBORメンバー米国-GAAP:NoteesPayableOtherPayableメンバーAMGN:TwoPointFourFivePercent NotesDue 2030メンバー2022-12-310000318154US-GAAP:ロンドン銀行間同業借り換え金利LIBORメンバー米国-GAAP:NoteesPayableOtherPayableメンバーAMGN:TwoPointFourFivePercent NotesDue 2030メンバー2021-12-310000318154米国-GAAP:NoteesPayableOtherPayableメンバーAMGN:TwoPointThreeZeroPercent NotesDue 2031メンバー2022-12-310000318154米国-GAAP:NoteesPayableOtherPayableメンバーAMGN:TwoPointThreeZeroPercent NotesDue 2031メンバー2021-12-310000318154US-GAAP:ロンドン銀行間同業借り換え金利LIBORメンバー米国-GAAP:NoteesPayableOtherPayableメンバーAMGN:TwoPointThreeZeroPercent NotesDue 2031メンバー2022-12-310000318154US-GAAP:ロンドン銀行間同業借り換え金利LIBORメンバー米国-GAAP:NoteesPayableOtherPayableメンバーAMGN:TwoPointThreeZeroPercent NotesDue 2031メンバー2021-12-310000318154AMGN:FourPointSixSixThreePercentNotesDuewoZeroFiveOneMembers米国-GAAP:NoteesPayableOtherPayableメンバー2022-12-310000318154AMGN:FourPointSixSixThreePercentNotesDuewoZeroFiveOneMembers米国-GAAP:NoteesPayableOtherPayableメンバー2021-12-310000318154AMGN:FourPointSixSixThreePercentNotesDuewoZeroFiveOneMembersUS-GAAP:ロンドン銀行間同業借り換え金利LIBORメンバー米国-GAAP:NoteesPayableOtherPayableメンバー2022-12-310000318154AMGN:FourPointSixSixThreePercentNotesDuewoZeroFiveOneMembersUS-GAAP:ロンドン銀行間同業借り換え金利LIBORメンバー米国-GAAP:NoteesPayableOtherPayableメンバー2021-12-310000318154米国-GAAP:NoteesPayableOtherPayableメンバー2022-12-310000318154米国-GAAP:NoteesPayableOtherPayableメンバー2021-12-310000318154AMGN:2点7%ノード2つのゼロビット5人の3人のメンバを繰り返すアメリカ-GAAP:NoteesPayableto BanksMembers2020-12-310000318154AMGN:6点3個7個5パーセントノードDue 2037メンバーアメリカ-GAAP:NoteesPayableto BanksMembers2020-01-012020-12-310000318154AMGN:SixPointNineZeroPercent NotesDue 2038メンバーアメリカ-GAAP:NoteesPayableto BanksMembers2020-01-012020-12-310000318154AMGN:SixPointFourZeroPercent NotesDue 2039メンバーアメリカ-GAAP:NoteesPayableto BanksMembers2020-12-310000318154AMGN:SixPointFourZeroPercent NotesDue 2039メンバーアメリカ-GAAP:NoteesPayableto BanksMembers2020-01-012020-12-310000318154AMGN:5分7分5分ノード2040メンバーアメリカ-GAAP:NoteesPayableto BanksMembers2020-01-012020-12-310000318154AMGN:FivePointOneFivePercentNoteesDue 2041メンバーアメリカ-GAAP:NoteesPayableto BanksMembers2020-01-012020-12-310000318154AMGN:FivePointSixFivePercentNoteesDue 2042メンバーアメリカ-GAAP:NoteesPayableto BanksMembers2020-01-012020-12-310000318154AMGN:FivePointThreeSeven FivePercent NotesDue 2043 Membersアメリカ-GAAP:NoteesPayableto BanksMembers2020-01-012020-12-310000318154米国-GAAP:NoteesPayableOtherPayableメンバーAMGN:ZeroPointFortyOnePercent SwissFrancBondsDue 2000とTwentyThreeMembers2022-12-310000318154AMGN:TwoPercentEuroNotesDuewo千とTwentySixMember米国-GAAP:NoteesPayableOtherPayableメンバー2022-12-310000318154AMGN:クロス通貨スワップ契約メンバーアメリカ公認会計基準:キャッシュフローヘッジメンバーAMGN:OnePointTwentyFivePercentEuroNotesDueTwoToudTwoMember2021-12-310000318154AMGN:OnePointTwentyFivePercentEuroNotesDueTwoToudTwoMemberアメリカ-GAAP:NoteesPayableto BanksMembers2021-12-310000318154US-GAAP:LineOfCreditMember2022-12-310000318154US-GAAP:LineOfCreditMember2022-01-012022-12-31AMGN:更新_オプション0000318154US-GAAP:LineOfCreditMemberAMGN:SecuredOvernightFinancingRateMembers2022-12-012022-12-310000318154US-GAAP:LineOfCreditMemberアメリカ-公認会計基準:連邦基金調達メンバー2022-12-012022-12-310000318154US-GAAP:LineOfCreditMember2021-12-310000318154AMGN:Horizon治療メンバー2022-12-310000318154AMGN:ブリッジ証明書プロトコルメンバ2022-12-3100003181542022-01-012022-03-3100003181542021-01-012021-03-3100003181542020-01-012020-03-3100003181542022-04-012022-06-3000003181542021-04-012021-06-3000003181542020-04-012020-06-3000003181542022-07-012022-09-3000003181542021-07-012021-09-3000003181542020-07-012020-09-3000003181542021-10-012021-12-3100003181542020-10-012020-12-310000318154AMGN:株式買い戻しプロトコルを加速するメンバー2022-01-012022-03-310000318154AMGN:株式買い戻しプロトコルを加速するメンバーアメリカ-公認会計基準:前払いメンバーを保留2022-01-012022-03-310000318154AMGN:株式買い戻しプロトコルを加速するメンバー米国-米国公認会計基準:公共株には付加資産資本メンバーが含まれている2022-01-012022-03-310000318154AMGN:株式買い戻しプロトコルを加速するメンバー2022-10-012022-12-310000318154AMGN:株式買い戻しプロトコルを加速するメンバーアメリカ-公認会計基準:前払いメンバーを保留2022-10-012022-12-310000318154AMGN:株式買い戻しプロトコルを加速するメンバー2022-01-012022-12-3100003181542022-10-3100003181542021-12-012021-12-3100003181542022-03-012022-03-3100003181542022-08-012022-08-3100003181542022-10-012022-10-3100003181542021-10-012021-10-3100003181542020-12-312020-12-3100003181542021-03-012021-03-3100003181542021-07-012021-07-3100003181542019-12-012019-12-3100003181542020-03-012020-03-3100003181542020-07-012020-07-3100003181542020-10-012020-10-310000318154SRT:シーン予測メンバ2023-03-012023-03-3100003181542022-12-012022-12-310000318154米国-GAAP:累積換算調整メンバー2019-12-310000318154アメリカ-GAAP:累積GainLossNetCashFlowHedgeParentMember2019-12-310000318154米国-GAAP:累計純未現金投資GainLossMembers2019-12-310000318154AMGN:他の調整属性表を親レベルに累積する2019-12-310000318154米国-GAAP:累積換算調整メンバー2020-01-012020-12-310000318154アメリカ-GAAP:累積GainLossNetCashFlowHedgeParentMember2020-01-012020-12-310000318154米国-GAAP:累計純未現金投資GainLossMembers2020-01-012020-12-310000318154AMGN:他の調整属性表を親レベルに累積する2020-01-012020-12-310000318154米国-GAAP:累積換算調整メンバー2020-12-310000318154アメリカ-GAAP:累積GainLossNetCashFlowHedgeParentMember2020-12-310000318154米国-GAAP:累計純未現金投資GainLossMembers2020-12-310000318154AMGN:他の調整属性表を親レベルに累積する2020-12-310000318154米国-GAAP:累積換算調整メンバー2021-01-012021-12-310000318154アメリカ-GAAP:累積GainLossNetCashFlowHedgeParentMember2021-01-012021-12-310000318154米国-GAAP:累計純未現金投資GainLossMembers2021-01-012021-12-310000318154AMGN:他の調整属性表を親レベルに累積する2021-01-012021-12-310000318154米国-GAAP:累積換算調整メンバー2021-12-310000318154アメリカ-GAAP:累積GainLossNetCashFlowHedgeParentMember2021-12-310000318154米国-GAAP:累計純未現金投資GainLossMembers2021-12-310000318154AMGN:他の調整属性表を親レベルに累積する2021-12-310000318154米国-GAAP:累積換算調整メンバー2022-01-012022-12-310000318154アメリカ-GAAP:累積GainLossNetCashFlowHedgeParentMember2022-01-012022-12-310000318154米国-GAAP:累計純未現金投資GainLossMembers2022-01-012022-12-310000318154AMGN:他の調整属性表を親レベルに累積する2022-01-012022-12-310000318154米国-GAAP:累積換算調整メンバー2022-12-310000318154アメリカ-GAAP:累積GainLossNetCashFlowHedgeParentMember2022-12-310000318154米国-GAAP:累計純未現金投資GainLossMembers2022-12-310000318154AMGN:他の調整属性表を親レベルに累積する2022-12-310000318154アメリカ-GAAP:累積GainLossNetCashFlowHedgeParentMember米国-米国公認会計原則:他の総合収入を累積メンバーに再分類するアメリカ-公認会計基準:製品メンバー米国-米国公認会計基準:外国為替契約メンバー2022-01-012022-12-310000318154アメリカ-GAAP:累積GainLossNetCashFlowHedgeParentMember米国-米国公認会計原則:他の総合収入を累積メンバーに再分類するアメリカ-公認会計基準:製品メンバー米国-米国公認会計基準:外国為替契約メンバー2021-01-012021-12-310000318154アメリカ-GAAP:累積GainLossNetCashFlowHedgeParentMember米国-米国公認会計原則:他の総合収入を累積メンバーに再分類するアメリカ-公認会計基準:製品メンバー米国-米国公認会計基準:外国為替契約メンバー2020-01-012020-12-310000318154アメリカ-GAAP:累積GainLossNetCashFlowHedgeParentMember米国-米国公認会計原則:他の総合収入を累積メンバーに再分類するAMGN:クロス通貨スワップ契約メンバー2022-01-012022-12-310000318154アメリカ-GAAP:累積GainLossNetCashFlowHedgeParentMember米国-米国公認会計原則:他の総合収入を累積メンバーに再分類するAMGN:クロス通貨スワップ契約メンバー2021-01-012021-12-310000318154アメリカ-GAAP:累積GainLossNetCashFlowHedgeParentMember米国-米国公認会計原則:他の総合収入を累積メンバーに再分類するAMGN:クロス通貨スワップ契約メンバー2020-01-012020-12-310000318154アメリカ-GAAP:累積GainLossNetCashFlowHedgeParentMember米国-米国公認会計原則:他の総合収入を累積メンバーに再分類する2022-01-012022-12-310000318154アメリカ-GAAP:累積GainLossNetCashFlowHedgeParentMember米国-米国公認会計原則:他の総合収入を累積メンバーに再分類する2021-01-012021-12-310000318154アメリカ-GAAP:累積GainLossNetCashFlowHedgeParentMember米国-米国公認会計原則:他の総合収入を累積メンバーに再分類する2020-01-012020-12-310000318154米国-米国公認会計原則:他の総合収入を累積メンバーに再分類する米国-GAAP:累計純未現金投資GainLossMembers2022-01-012022-12-310000318154米国-米国公認会計原則:他の総合収入を累積メンバーに再分類する米国-GAAP:累計純未現金投資GainLossMembers2021-01-012021-12-310000318154米国-米国公認会計原則:他の総合収入を累積メンバーに再分類する米国-GAAP:累計純未現金投資GainLossMembers2020-01-012020-12-310000318154アメリカ-公認会計基準:公正価値入力レベル1メンバーアメリカ-公認会計基準:アメリカ証券メンバー2022-12-310000318154アメリカ-公認会計基準:公正価値入力レベル2メンバーアメリカ-公認会計基準:アメリカ証券メンバー2022-12-310000318154アメリカ-公認会計基準:アメリカ証券メンバーアメリカ-公認会計基準:公正価値投入レベル3メンバー2022-12-310000318154アメリカ-公認会計基準:公正価値入力レベル1メンバーUS-GAAP:アメリカReasuryBillSecuritiesMembers2022-12-310000318154アメリカ-公認会計基準:公正価値入力レベル2メンバーUS-GAAP:アメリカReasuryBillSecuritiesMembers2022-12-310000318154アメリカ-公認会計基準:公正価値投入レベル3メンバーUS-GAAP:アメリカReasuryBillSecuritiesMembers2022-12-310000318154アメリカ-公認会計基準:公正価値入力レベル1メンバーアメリカ公認会計基準:MoneyMarketFundsMembers2022-12-310000318154アメリカ-公認会計基準:公正価値入力レベル2メンバーアメリカ公認会計基準:MoneyMarketFundsMembers2022-12-310000318154アメリカ-公認会計基準:公正価値投入レベル3メンバーアメリカ公認会計基準:MoneyMarketFundsMembers2022-12-310000318154アメリカ-公認会計基準:公正価値入力レベル1メンバーAMGN:OtherShortTermInterestBearingSecuritiesMember2022-12-310000318154アメリカ-公認会計基準:公正価値入力レベル2メンバーAMGN:OtherShortTermInterestBearingSecuritiesMember2022-12-310000318154アメリカ-公認会計基準:公正価値投入レベル3メンバーAMGN:OtherShortTermInterestBearingSecuritiesMember2022-12-310000318154アメリカ-公認会計基準:公正価値入力レベル1メンバー2022-12-310000318154アメリカ-公認会計基準:公正価値入力レベル2メンバー2022-12-310000318154アメリカ-公認会計基準:公正価値投入レベル3メンバー2022-12-310000318154アメリカ-公認会計基準:公正価値入力レベル1メンバー米国-米国公認会計基準:外国為替契約メンバー2022-12-310000318154アメリカ-公認会計基準:公正価値入力レベル2メンバー米国-米国公認会計基準:外国為替契約メンバー2022-12-310000318154アメリカ-公認会計基準:公正価値投入レベル3メンバー米国-米国公認会計基準:外国為替契約メンバー2022-12-310000318154米国-米国公認会計基準:外国為替契約メンバー2022-12-310000318154アメリカ-公認会計基準:公正価値入力レベル1メンバーAMGN:クロス通貨スワップ契約メンバー2022-12-310000318154アメリカ-公認会計基準:公正価値入力レベル2メンバーAMGN:クロス通貨スワップ契約メンバー2022-12-310000318154AMGN:クロス通貨スワップ契約メンバーアメリカ-公認会計基準:公正価値投入レベル3メンバー2022-12-310000318154AMGN:クロス通貨スワップ契約メンバー2022-12-310000318154アメリカ-公認会計基準:公正価値入力レベル1メンバーUS-GAAP:InterestRateSwapMember2022-12-310000318154アメリカ-公認会計基準:公正価値入力レベル2メンバーUS-GAAP:InterestRateSwapMember2022-12-310000318154アメリカ-公認会計基準:公正価値投入レベル3メンバーUS-GAAP:InterestRateSwapMember2022-12-310000318154US-GAAP:InterestRateSwapMember2022-12-310000318154AMGN:ForwardInterestRateContractメンバーアメリカ-公認会計基準:公正価値入力レベル1メンバー2022-12-310000318154AMGN:ForwardInterestRateContractメンバーアメリカ-公認会計基準:公正価値入力レベル2メンバー2022-12-310000318154AMGN:ForwardInterestRateContractメンバーアメリカ-公認会計基準:公正価値投入レベル3メンバー2022-12-310000318154AMGN:ForwardInterestRateContractメンバー2022-12-310000318154アメリカ-公認会計基準:公正価値入力レベル1メンバーアメリカ-公認会計基準:アメリカ証券メンバー2021-12-310000318154アメリカ-公認会計基準:公正価値入力レベル2メンバーアメリカ-公認会計基準:アメリカ証券メンバー2021-12-310000318154アメリカ-公認会計基準:アメリカ証券メンバーアメリカ-公認会計基準:公正価値投入レベル3メンバー2021-12-310000318154アメリカ-公認会計基準:公正価値入力レベル1メンバーUS-GAAP:アメリカReasuryBillSecuritiesMembers2021-12-310000318154アメリカ-公認会計基準:公正価値入力レベル2メンバーUS-GAAP:アメリカReasuryBillSecuritiesMembers2021-12-310000318154アメリカ-公認会計基準:公正価値投入レベル3メンバーUS-GAAP:アメリカReasuryBillSecuritiesMembers2021-12-310000318154アメリカ-公認会計基準:公正価値入力レベル1メンバーアメリカ公認会計基準:MoneyMarketFundsMembers2021-12-310000318154アメリカ-公認会計基準:公正価値入力レベル2メンバーアメリカ公認会計基準:MoneyMarketFundsMembers2021-12-310000318154アメリカ-公認会計基準:公正価値投入レベル3メンバーアメリカ公認会計基準:MoneyMarketFundsMembers2021-12-310000318154アメリカ-公認会計基準:公正価値入力レベル1メンバーAMGN:OtherShortTermInterestBearingSecuritiesMember2021-12-310000318154アメリカ-公認会計基準:公正価値入力レベル2メンバーAMGN:OtherShortTermInterestBearingSecuritiesMember2021-12-310000318154アメリカ-公認会計基準:公正価値投入レベル3メンバーAMGN:OtherShortTermInterestBearingSecuritiesMember2021-12-310000318154アメリカ-公認会計基準:公正価値入力レベル1メンバー2021-12-310000318154アメリカ-公認会計基準:公正価値入力レベル2メンバー2021-12-310000318154アメリカ-公認会計基準:公正価値投入レベル3メンバー2021-12-310000318154アメリカ-公認会計基準:公正価値入力レベル1メンバー米国-米国公認会計基準:外国為替契約メンバー2021-12-310000318154アメリカ-公認会計基準:公正価値入力レベル2メンバー米国-米国公認会計基準:外国為替契約メンバー2021-12-310000318154アメリカ-公認会計基準:公正価値投入レベル3メンバー米国-米国公認会計基準:外国為替契約メンバー2021-12-310000318154米国-米国公認会計基準:外国為替契約メンバー2021-12-310000318154アメリカ-公認会計基準:公正価値入力レベル1メンバーAMGN:クロス通貨スワップ契約メンバー2021-12-310000318154アメリカ-公認会計基準:公正価値入力レベル2メンバーAMGN:クロス通貨スワップ契約メンバー2021-12-310000318154AMGN:クロス通貨スワップ契約メンバーアメリカ-公認会計基準:公正価値投入レベル3メンバー2021-12-310000318154AMGN:クロス通貨スワップ契約メンバー2021-12-310000318154アメリカ-公認会計基準:公正価値入力レベル1メンバーUS-GAAP:InterestRateSwapMember2021-12-310000318154アメリカ-公認会計基準:公正価値入力レベル2メンバーUS-GAAP:InterestRateSwapMember2021-12-310000318154アメリカ-公認会計基準:公正価値投入レベル3メンバーUS-GAAP:InterestRateSwapMember2021-12-310000318154US-GAAP:InterestRateSwapMember2021-12-310000318154AMGN:ForwardInterestRateContractメンバーアメリカ-公認会計基準:公正価値入力レベル1メンバー2021-12-310000318154AMGN:ForwardInterestRateContractメンバーアメリカ-公認会計基準:公正価値入力レベル2メンバー2021-12-310000318154AMGN:ForwardInterestRateContractメンバーアメリカ-公認会計基準:公正価値投入レベル3メンバー2021-12-310000318154AMGN:ForwardInterestRateContractメンバー2021-12-310000318154AMGN:TeneobioIncMember2022-12-310000318154米国-公認会計基準:長期契約メンバーUS-GAAP:DesignatedAsHedgingInstrumentMember2022-12-310000318154米国-公認会計基準:長期契約メンバーUS-GAAP:DesignatedAsHedgingInstrumentMember2021-12-310000318154米国-公認会計基準:長期契約メンバーUS-GAAP:DesignatedAsHedgingInstrumentMember2020-12-310000318154AMGN:クロス通貨スワップ契約メンバーアメリカ公認会計基準:キャッシュフローヘッジメンバーAMGN:ZeroPointFortyOnePercent SwissFrancBondsDue 2000とTwentyThreeMembers2022-12-310000318154通貨:スイスフランAMGN:クロス通貨スワップ契約メンバーアメリカ公認会計基準:キャッシュフローヘッジメンバーAMGN:ZeroPointFortyOnePercent SwissFrancBondsDue 2000とTwentyThreeMembers2022-12-310000318154AMGN:クロス通貨スワップ契約メンバーアメリカ公認会計基準:キャッシュフローヘッジメンバー通貨:ドルAMGN:ZeroPointFortyOnePercent SwissFrancBondsDue 2000とTwentyThreeMembers2022-12-310000318154AMGN:TwoPercentEuroNotesDuewo千とTwentySixMemberAMGN:クロス通貨スワップ契約メンバーアメリカ公認会計基準:キャッシュフローヘッジメンバー2022-12-310000318154AMGN:TwoPercentEuroNotesDuewo千とTwentySixMemberAMGN:クロス通貨スワップ契約メンバーアメリカ公認会計基準:キャッシュフローヘッジメンバー通貨:ユーロ2022-12-310000318154AMGN:TwoPercentEuroNotesDuewo千とTwentySixMemberAMGN:クロス通貨スワップ契約メンバーアメリカ公認会計基準:キャッシュフローヘッジメンバー通貨:ドル2022-12-310000318154AMGN:FivePointFiveZeroPercent PoundSterlingNotesDue 2026メンバーAMGN:クロス通貨スワップ契約メンバーアメリカ公認会計基準:キャッシュフローヘッジメンバー2022-12-310000318154AMGN:FivePointFiveZeroPercent PoundSterlingNotesDue 2026メンバーAMGN:クロス通貨スワップ契約メンバーアメリカ公認会計基準:キャッシュフローヘッジメンバー通貨:ポンド2022-12-310000318154AMGN:FivePointFiveZeroPercent PoundSterlingNotesDue 2026メンバーAMGN:クロス通貨スワップ契約メンバーアメリカ公認会計基準:キャッシュフローヘッジメンバー通貨:ドル2022-12-310000318154AMGN:クロス通貨スワップ契約メンバーAMGN:4%PoundSterlingNotesDue 2029メンバーアメリカ公認会計基準:キャッシュフローヘッジメンバー2022-12-310000318154AMGN:クロス通貨スワップ契約メンバーAMGN:4%PoundSterlingNotesDue 2029メンバーアメリカ公認会計基準:キャッシュフローヘッジメンバー通貨:ポンド2022-12-310000318154AMGN:クロス通貨スワップ契約メンバーAMGN:4%PoundSterlingNotesDue 2029メンバーアメリカ公認会計基準:キャッシュフローヘッジメンバー通貨:ドル2022-12-310000318154AMGN:ForwardInterestRateContractメンバーUS-GAAP:DesignatedAsHedgingInstrumentMember2022-12-310000318154アメリカ公認会計基準:キャッシュフローヘッジメンバー米国-米国公認会計基準:外国為替契約メンバー2022-01-012022-12-310000318154アメリカ公認会計基準:キャッシュフローヘッジメンバー米国-米国公認会計基準:外国為替契約メンバー2021-01-012021-12-310000318154アメリカ公認会計基準:キャッシュフローヘッジメンバー米国-米国公認会計基準:外国為替契約メンバー2020-01-012020-12-310000318154AMGN:クロス通貨スワップ契約メンバーアメリカ公認会計基準:キャッシュフローヘッジメンバー2022-01-012022-12-310000318154AMGN:クロス通貨スワップ契約メンバーアメリカ公認会計基準:キャッシュフローヘッジメンバー2021-01-012021-12-310000318154AMGN:クロス通貨スワップ契約メンバーアメリカ公認会計基準:キャッシュフローヘッジメンバー2020-01-012020-12-310000318154AMGN:ForwardInterestRateContractメンバーアメリカ公認会計基準:キャッシュフローヘッジメンバー2022-01-012022-12-310000318154AMGN:ForwardInterestRateContractメンバーアメリカ公認会計基準:キャッシュフローヘッジメンバー2021-01-012021-12-310000318154AMGN:ForwardInterestRateContractメンバーアメリカ公認会計基準:キャッシュフローヘッジメンバー2020-01-012020-12-310000318154アメリカ公認会計基準:キャッシュフローヘッジメンバー2022-01-012022-12-310000318154アメリカ公認会計基準:キャッシュフローヘッジメンバー2021-01-012021-12-310000318154アメリカ公認会計基準:キャッシュフローヘッジメンバー2020-01-012020-12-310000318154US-GAAP:DesignatedAsHedgingInstrumentMemberUS-GAAP:InterestRateSwapMember2022-12-310000318154AMGN:長期債務満期現在のメンバー2022-12-310000318154AMGN:長期債務満期現在のメンバー2021-12-310000318154米国-公認会計基準:長期債務メンバー2022-12-310000318154米国-公認会計基準:長期債務メンバー2021-12-310000318154US-GAAP:InterestRateSwapMember2022-01-012022-12-310000318154US-GAAP:InterestRateSwapMember2021-01-012021-12-310000318154US-GAAP:InterestRateSwapMember2020-01-012020-12-310000318154AMGN:外国為替通貨とクロスマネースワップメンバ2022-12-310000318154米国-公認会計基準:非指定メンバー米国-公認会計基準:長期契約メンバー2022-12-310000318154米国-公認会計基準:非指定メンバー米国-公認会計基準:長期契約メンバー2021-12-310000318154米国-公認会計基準:非指定メンバー米国-公認会計基準:長期契約メンバー2020-12-310000318154US-GAAP:DesignatedAsHedgingInstrumentMemberAMGN:その他現在の非現在資産メンバ米国-米国公認会計基準:外国為替契約メンバー2022-12-310000318154US-GAAP:DesignatedAsHedgingInstrumentMemberAMGN:現在の負債を計上していないその他の負債メンバー米国-米国公認会計基準:外国為替契約メンバー2022-12-310000318154AMGN:クロス通貨スワップ契約メンバーUS-GAAP:DesignatedAsHedgingInstrumentMemberAMGN:その他現在の非現在資産メンバ2022-12-310000318154AMGN:クロス通貨スワップ契約メンバーUS-GAAP:DesignatedAsHedgingInstrumentMemberAMGN:現在の負債を計上していないその他の負債メンバー2022-12-310000318154US-GAAP:DesignatedAsHedgingInstrumentMemberUS-GAAP:InterestRateSwapMemberAMGN:その他現在の非現在資産メンバ2022-12-310000318154US-GAAP:DesignatedAsHedgingInstrumentMemberUS-GAAP:InterestRateSwapMemberAMGN:現在の負債を計上していないその他の負債メンバー2022-12-310000318154AMGN:ForwardInterestRateContractメンバーUS-GAAP:DesignatedAsHedgingInstrumentMemberAMGN:その他現在の非現在資産メンバ2022-12-310000318154AMGN:ForwardInterestRateContractメンバーUS-GAAP:DesignatedAsHedgingInstrumentMemberAMGN:現在の負債を計上していないその他の負債メンバー2022-12-310000318154US-GAAP:DesignatedAsHedgingInstrumentMember2022-12-310000318154US-GAAP:DesignatedAsHedgingInstrumentMemberAMGN:その他現在の非現在資産メンバ米国-米国公認会計基準:外国為替契約メンバー2021-12-310000318154US-GAAP:DesignatedAsHedgingInstrumentMemberAMGN:現在の負債を計上していないその他の負債メンバー米国-米国公認会計基準:外国為替契約メンバー2021-12-310000318154AMGN:クロス通貨スワップ契約メンバーUS-GAAP:DesignatedAsHedgingInstrumentMemberAMGN:その他現在の非現在資産メンバ2021-12-310000318154AMGN:クロス通貨スワップ契約メンバーUS-GAAP:DesignatedAsHedgingInstrumentMemberAMGN:現在の負債を計上していないその他の負債メンバー2021-12-310000318154US-GAAP:DesignatedAsHedgingInstrumentMemberUS-GAAP:InterestRateSwapMemberAMGN:その他現在の非現在資産メンバ2021-12-310000318154US-GAAP:DesignatedAsHedgingInstrumentMemberUS-GAAP:InterestRateSwapMemberAMGN:現在の負債を計上していないその他の負債メンバー2021-12-310000318154AMGN:ForwardInterestRateContractメンバーUS-GAAP:DesignatedAsHedgingInstrumentMemberAMGN:その他現在の非現在資産メンバ2021-12-310000318154AMGN:ForwardInterestRateContractメンバーUS-GAAP:DesignatedAsHedgingInstrumentMemberAMGN:現在の負債を計上していないその他の負債メンバー2021-12-310000318154US-GAAP:DesignatedAsHedgingInstrumentMember2021-12-310000318154AMGN:サンドフIncMember2018-06-012018-06-30AMGN:訴訟0000318154AMGN:サンドフIncMemberアメリカ-公認会計基準:係争中のメンバー2021-09-282021-09-28AMGN:特許0000318154AMGN:サンドフIncMemberアメリカ-公認会計基準:係争中のメンバー2021-10-122021-10-120000318154AMGN:SanofiRegeneronPatentLitigationMemberアメリカ-公認会計基準:係争中のメンバー2014-10-012014-10-310000318154AMGN:SanofiRegeneronPatentLitigationMemberアメリカ-公認会計基準:係争中のメンバー2016-02-012016-02-280000318154AMGN:SanofiRegeneronPatentLitigationMemberアメリカ-公認会計基準:係争中のメンバー2018-03-012018-03-310000318154AMGN:JanssenBiotechIncVsAmgenIncMemberアメリカ-公認会計基準:係争中のメンバー2022-11-292022-11-290000318154AMGN:SensiparAntitrustClassActionsMemberアメリカ-公認会計基準:係争中のメンバー2019-02-012019-04-30AMGN:原告数AMGN:宣言数0000318154AMGN:SensiparAntitrustClassActionsMemberアメリカ-公認会計基準:係争中のメンバー2018-06-012018-06-300000318154AMGN:SensiparAntitrustClassActionsMemberアメリカ-公認会計基準:係争中のメンバー2022-03-11AMGN:州0000318154アメリカ-公認会計基準:係争中のメンバーAMGN:Regeneron PharmPharmticalsIncAntitrustActionMembers2022-05-27AMGN:パラメータ0000318154AMGN:ChemoCentryxIncSecuritiesMattersMember2021-05-052021-06-08AMGN:分割払い アメリカです
アメリカ証券取引委員会
ワシントンD.C.,20549
表10-K
(マーク1)
| | | | | |
| ☒ | 1934年証券取引法第13条又は15条に基づいて提出された年次報告 |
本財政年度末まで十二月三十一日, 2022
あるいは…。
| | | | | |
| ☐ | 1934年証券取引法第13条又は15条に基づいて提出された移行報告 |
手数料書類番号001-37702
安進。
(登録者の正確な氏名はその定款に記載)
| | | | | | | | |
| デラウェア州 | | 95-3540776 |
(明またはその他の司法管轄権
会社や組織) | | (税務署の雇用主
識別番号) |
| 中心通りに1本入っている | | 91320-1799 |
| 千本のオークの木 | |
| カリフォルニア州 | |
| (主にオフィスアドレスを実行) | | (郵便番号) |
(805) 447-1000
(登録者の電話番号、市外局番を含む)
同法第12条(B)に基づいて登録された証券:
| | | | | | | | |
| クラスごとのタイトル | 取引コード | 登録された各取引所の名称 |
| 普通株、額面0.0001ドル | AMGN | ナスダック株式市場有限責任会社 |
| 優先債券は2026年に満期、金利は2.00% | AMGN 26 | ナスダック株式市場有限責任会社 |
同法第12条(G)に基づいて登録された証券:ありません
登録者が証券法規則405で定義されている経験豊富な発行者である場合は、再選択マークで示してくださいはい、そうです ý No ¨
登録者がこの法第13節または第15節(D)節に基づいて報告を提出する必要がないかどうかを再選択マークで示す。 はい、そうです¨ 違います。 ý
再選択マークは、登録者が(1)過去12ヶ月以内(または登録者がそのような報告の提出を要求されたより短い期間)に、1934年の証券取引法第13節または第15(D)節に提出されたすべての報告書を提出したかどうか、および(2)過去90日以内にそのような提出要件に適合しているかどうかを示す。 はい、そうです ý No ¨
再選択マークは、登録者が過去12ヶ月以内(または登録者がそのような文書の提出を要求されたより短い時間以内)に、S−T規則405条(本章232.405節)に従って提出を要求した各相互作用データファイルを電子的に提出したか否かを示す。 はい、そうです ý No ¨
登録者が大型加速申告会社,加速申告会社,非加速申告会社,小さな報告会社,あるいは新興成長型会社であることを再選択マークで示す。取引法第12 b-2条の規則における“大型加速申告会社”、“加速申告会社”、“小申告会社”、“新興成長型会社”の定義を参照されたい。
| | | | | | | | | | | | | | |
| 大型加速ファイルサーバ | ファイルマネージャを加速する | 非加速ファイルサーバ | 規模の小さい報告会社 | 新興成長型会社 |
| ☒ | ☐ | ☐ | ☐ | ☐ |
新興成長型企業であれば、登録者が延長された移行期間を使用しないことを選択したか否かを再選択マークで示し、取引所法第13(A)節に提供された任意の新たまたは改正された財務会計基準を遵守する¨
登録者が報告書を提出したかどうかを再選択マークで示し、その経営陣が“サバンズ-オクスリ法案”(“米国連邦法典”第15編、第7262(B)節)第404(B)条に基づいてその財務報告の内部統制の有効性を評価したことを証明する。この評価は、その監査報告書を作成または発行する公認会計士事務所によって行われる☒
登録者が空殻会社であるか否かをチェックマークで示す(同法第12 b-2条で定義される) はい、そうです☐ No ý
登録者の非関連会社が保有する議決権と無議決権株の総時価は約#ドルである129,940,091,621 as of June 30, 2022.(A)
(A)役員や役員が保有する818,128株の普通株と、2022年6月30日現在の保有株が発行済み株式の10%を超えるいかなる株主も含まれていない。いかなる人が保有する株式を排除することは、その人が登録者の管理者または政策の指示を直接または間接的に指導または誘導する権利があることを示すものとして解釈されてはならず、またはその人は登録者によって制御されるか、または登録者と共同で制御されるべきである。
533,976,238
(2023年2月6日現在発行済み普通株式数)
引用で編入された書類
登録者は,2023年5月19日に開催される2023年株主総会の委託書に関する具体的な部分を引用して本年度報告の第3部に組み込む。
索引.索引
| | | | | | | | |
| | ページ番号. |
| 定義された用語と製品 | II |
第1部 | | 1 |
| 第1項。 | 商売人 | 1 |
| 重大な発展 | 1 |
| マーケティング、流通、精選された市場製品 | 3 |
| 精算する | 9 |
| 製造·流通·原材料 | 11 |
| 政府の監督管理 | 13 |
| 研究開発と選定された候補製品 | 16 |
| 業務関係 | 22 |
| 人的資本資源 | 23 |
| 私たちの執行官に関する情報は | 26 |
| 地理地域金融情報 | 27 |
| 投資家情報 | 27 |
| 第1 A項。 | リスク要因 | 27 |
| 項目1 B。 | 未解決従業員意見 | 51 |
| 第二項です。 | 特性 | 52 |
| 第三項です。 | 法律手続き | 52 |
| 第四項です。 | 炭鉱安全情報開示 | 52 |
第II部 | | 53 |
| 五番目です。 | 登録者普通株市場、関連株主事項、発行者による株式証券の購入 | 53 |
| 第六項です。 | 保留されている | 54 |
| 第七項。 | 経営陣の財務状況と経営成果の検討と分析 | 55 |
| 第七A項。 | 市場リスクの定量的·定性的開示について | 75 |
| 第八項です。 | 財務諸表と補足データ | 77 |
| 第九項です。 | 会計·財務開示面の変化と会計士との相違 | 77 |
| 第9条。 | 制御とプログラム | 78 |
| プロジェクト9 B。 | その他の情報 | 80 |
第三部 | | 80 |
| 第10項。 | 役員、行政、会社の管理 | 80 |
| 第十一項。 | 役員報酬 | 80 |
| 第十二項。 | ある実益所有者の担保所有権及び経営陣及び株主に関する事項 | 81 |
| 十三項。 | 特定の関係と関連取引と取締役の独立性 | 82 |
| 14項です。 | チーフ会計士費用とサービス | 82 |
第4部 | | 83 |
| 第十五項。 | 展示品と財務諸表の付表 | 83 |
| 第十六項。 | 表格10-Kの概要 | 89 |
サイン | | 90 |
定義された用語と製品
定義的用語
この10−K表では,以下に示すように,金融,法規,疾患に関連する用語や他社の名称を含むがこれらに限定されないいくつかの用語を用いた。
| | | | | | | | | |
| 用語.用語 | 説明する | | | | |
| | | | | |
| 2017年税法 | 2017年減税·雇用法案 | | | | |
| AbbVie | エーバービー社です。 | | | | |
| 改訂された2009年計画 | 2009年の株式インセンティブ計画の改訂と再策定 | | | | |
| 安達 | 簡明新薬申請 | | | | |
| AOCI | その他の総合収益を累計する | | | | |
| ASCVD | アテローム性動脈硬化性心血管疾患 | | | | |
| ASR | 株式買い戻しを加速する | | | | |
| アスリーカン | アスリーカン | | | | |
| 百済神州 | 百済神州株式会社です。 | | | | |
| ベガモ | 実験室Quimico農場有限会社 | | | | |
一口かむ® | 二重特異性T細胞活性化子 | | | | |
| BPCIA | 2009年バイオ製品価格競争と革新法 | | | | |
| CCPA | “2018年カリフォルニア消費者プライバシー法” | | | | |
| セルキング | Celgene社 | | | | |
| CGRP | カルシトニン遺伝子関連ペプチド | | | | |
| ChemoCentryx | ChemoCentryx,Inc. | | | | |
| 化学療法 | 抗がん剤 | | | | |
| CHMP | 人用薬品委員会 | | | | |
| 細胞質 | 医療保険と医療補助サービスセンター | | | | |
| COSO | トレデビル委員会は組織委員会を後援しています | | | | |
| 新冠肺炎 | 2019年コロナウイルス病 | | | | |
| 心電 | 心血管疾患 | | | | |
| DDL 3 | デルタ様リガンド3 | | | | |
| アメリカ司法省 | アメリカ司法省 | | | | |
| ヨーロッパ共同体 | 欧州委員会 | | | | |
| Eczac | EIS Eczac,Sanayi ve Ticaret A. | | | | |
| EMA | ヨーロッパ医薬品局は | | | | |
| 仕事がしやすい | 1株当たりの収益 | | | | |
| ESG | 環境、社会、ガバナンス | | | | |
| EU.EU | EU.EU | | | | |
| FASB | 財務会計基準委員会 | | | | |
| “反海外腐敗法” | アメリカの“海外腐敗防止法” | | | | |
| 林業局 | アメリカ食品医薬品局は | | | | |
| FDCA | 連邦食品医薬品化粧品法案 | | | | |
| 恵誉 | 恵誉格付け会社 | | | | |
| 5つの素数 | Five Prime治療会社 | | | | |
| 連邦貿易委員会 | 連邦貿易委員会 | | | | |
| 会計原則を公認する | アメリカは会計原則を公認している | | | | |
| GDPR | 一般資料保障規程 | | | | |
| GEJ | 胃食道接合部 | | | | |
| 根森塔 | Gensenta a la゚sanayi ve Ticaret A.゚ | | | | |
| HHS | アメリカ衛生·公衆サービス部 | | | | |
| 水平線 | Horizon治療会社 | | | | |
| | | | | | | | | |
| 用語.用語 | 説明する | | | | |
| 伊 | インターロイキン2 | | | | |
| 工業 | 研究中の新薬の応用 | | | | |
| 知的財産権研究開発 | 現在行われている研究と開発 | | | | |
| アイルランド共和軍 | “インフレ低減法案” | | | | |
| アメリカ国税局 | アメリカ国税局 | | | | |
| ジェイソン | ヤンソン生物科学技術会社は | | | | |
| K-A | 麒麟安進株式会社 | | | | |
| KKC | 京華麒麟株式会社 | | | | |
| KRAS | コルシュラット肉腫ウイルス癌遺伝子 | | | | |
| 低密度リポ蛋白質コレステロール | 低密度リポ蛋白質コレステロール | | | | |
| ロンドン銀行の同業借り換え金利 | ロンドン銀行間同業借り換え金利 | | | | |
| リリー | 礼来会社 | | | | |
| LP(A) | リポ蛋白質(A) | | | | |
| MD&A | 経営陣の議論と分析 | | | | |
| ムーディ | ムーディーズ投資家サービス会社 | | | | |
| MRD | 微小残留病 | | | | |
| ニューモラ | Neumora治療会社 | | | | |
| いいえ | 純営業損失 | | | | |
| ノバ会社 | ノワ製薬は | | | | |
| 非小細胞肺癌 | 非小細胞肺癌 | | | | |
| OECD | 経済協力開発機構 | | | | |
| OIG | 監察長室 | | | | |
| オライ | オープンラベル拡張 | | | | |
| あるいは… | 客観応答率 | | | | |
| PBM | 薬局福祉マネージャー | | | | |
| PCSK 9 | 枯草菌/信頼性原蛋白変換酵素9型 | | | | |
| PDE 4 | ホスホジエステラーゼ4 | | | | |
| PFS | 進展がなく生存する | | | | |
| PNH | 発作性睡眠性ヘモグロビン尿 | | | | |
| 利益を計画に分ける | アンはアイルランドに入って従業員の利益共有計画 | | | | |
| 研究開発 | 研究と開発 | | | | |
| ランク | 核因子kappaB受容体活性化剤リガンド | | | | |
| RAR | 収入代理報告書 | | | | |
| REMS | リスク評価と緩和戦略 | | | | |
| ROU | 使用権 | | | | |
| はい | 世界の他の地域 | | | | |
| RSU | 制限株式単位 | | | | |
| スタンダード(S&P) | スタンダード&プアーズ金融サービス有限責任会社 | | | | |
| アメリカ証券取引委員会 | アメリカ証券取引委員会 | | | | |
| SG&A | 販売、一般、行政 | | | | |
| 小干渉RNA | 小干渉RNA | | | | |
| 軟性 | 担保付き隔夜融資金利 | | | | |
| ティニオビオ | Teneobio,Inc. | | | | |
| アメリカ財務省は | アメリカ財務省は | | | | |
| USPTO | アメリカ特許商標局は | | | | |
| UTB | 未確認税収割引 | | | | |
| | | | | |
| | | | | |
| | | | | |
| | | | | |
| | | | | |
| | | | | |
| | | | | |
| | | | | |
| | | | | |
| | | | | |
| | | | | |
製品
以下に私たちの製品のブランド名、私たちの輸送設備、そして私たちのいくつかの候補製品とそれに関連する汎用名を提供します。
| | | | | |
| 用語.用語 | 説明する |
| Acapatamab | Acapatamab(旧AMG 160) |
| エモヴィグ | エモヴィグ®(エロナブ·オオエ) |
| AMGEVITA | AMGEVITA™ (アダモズマブ) |
| AMJEVITA | AMJEVITA™(adalimumab-atto) |
| Aranesp | Aranesp®(Darbepoetin Alfa) |
| 自動タッチ | 自動タッチ® |
| AVSOLA | AVSOLA®(インフリキシマブ-axxq) |
| BLINCETO | BLINCETO®(Blinatumab) |
| |
| コランノ | コランノ®(エヴラジン) |
| エフバルキンアルファ | Eavaleukin Alfa(前身はAMG 592) |
| Emirodatamab | Emirodatamab(前身はAMG 427) |
| Enbrel | Enbrel®(イナシップ) |
| Enbrel Mini | Enbrel Mini® |
| Epogen | Epogen®(Epoetin Alfa) |
| 事件.事件 | 事件.事件®(romozumab-aqqg) |
| できません | できません®(Talimogene Laherparepvec) |
| カンジンティ | カンジンティ®(トラツズマブ-ANS) |
| ケプロリス | ケプロリス®(Carfilzomib) |
| LUMAKRAS/LUMYKRA | ルマカラス®/LUMYKRAS™(Sotorasib) |
| MVASI | MVASI®(ベバシズマブ-awwb) |
| ニューラス塔 | ニューラス塔®(Pegfilgratim) |
| Neupogen | Neupogen®(文書検索時間) |
| ナンバープレート | ナンバープレート®(ロミプシム) |
| オルパシーランド | Olpasiran(前身はAMG 890) |
| OnPro | OnPro® |
| Ordesekimab | Ordesekimab(前AMG 714) |
| ウルトラツラ | ウルトラツラ®(アプミスト) |
| パサビフ | パサビフ®(Etelcalcetie) |
| プロリア | プロリア®(Denosumab) |
| 再修術 | 再修術®(Evocumab) |
| レベニー | レベニー®(メロワ-arrx) |
| Rocatinlimab | Rocatinlimab(前AMG 451) |
| Rozibafuspアルファ | Rozibafusp Alfa(前身はAMG 570) |
| センシパル/ミンパラ | センシパル®/ミムパラ™(Cinacalcet) |
| SureClick | SureClick® |
| Tarlaamab | Tarlaamab(前身はAMG 757) |
| TAVNEOS | TAVNEOS®(アボカド) |
| TEZSPIRE | TEZSPIRE® (tezepelumab-Ekko) |
| Vectibix | Vectibix®(Panitumab) |
| シグワ | シグワ®(Denosumab) |
本報告に上記リストに含まれていない製品は、それぞれの所有者の商標である。彼らはアバスティンだ®,Cosentyx®DARZALEX®,EYLEA®フルフェラ®ヘキセチン®、HUMIRA®Pomalyst®/imnovid®PRALUENT®Procrit®Promacta®/Revolade™レクシェード®Revlimid®、RINVOQ®Rituxan®/MabThera®スカイrizi®ソロris®ステララ®タルツ®Teribone™,トレムフィア®,UDENYCA®、VELCADE®Xeljanzと®.
第1部
安進(その子会社、略称“安進”、“当社”、“私たち”、“私たち”或いは“私たち”)は生物技術会社であり、発見、開発、製造と革新的な人類療法を提供することによって、深刻な疾病を有する患者に生物学的潜在力を放出することに取り組んでいる。この方法はまず先進的な人類遺伝学などのツールを用いて疾病の複雑性を解明し、人類生物学の基本原理を理解する。
安進は高度に満足されていない医療需要分野に集中し,その専門知識を利用して解決策を求め,健康結果を改善し,人々の生活を著しく改善するために努力している。バイオテクノロジーの先駆者として,安進は世界有数の独立バイオテクノロジー会社の一つに成長し,世界各地の数百万人の患者に接触し,分離潜在力のある薬物パイプラインを開発している。
安進は1980年にカリフォルニア州に登録設立され、1987年にデラウェア州の会社となった。私たちの業務は世界約100カ国·地域に及んでいる。安進はただ一つの業務部門を経営している:人間療法。
重大な発展
以下は,2021年12月31日までの10-K表年次報告を提出して以来,我々の業務に影響を与える重大な事態の概要である
買収する
Horizon Treateutics Plcを買収しようとしている
•2022年12月12日、安進はHorizonの全株式を1株116.50ドルの現金で買収する取引合意に達し、取引株式価値は約278億ドルであることを発表した。提案されたHorizon買収については,2022年12月に過渡的信用協定と定期融資信用協定を締結し,元金総額は285億ドルであった。Horizonはアイルランドダブリンに本部を置くグローバルバイオテクノロジー会社であり、薬物の発見、開発と商業化に集中し、稀、自己免疫と深刻な炎症性疾患の影響を受ける人々の重要な需要を満たす。Horizonは12種類の市販薬と20以上の開発プロジェクトのパイプラインを持っている。この取引の完了は、いくつかの規制機関(FTC審査を含む)と他の慣用的な完了条件の満足に依存する。
◦2023年1月30日、当社とHorizonは、それぞれ、当社がHorizon買収を提案する補足情報および文書材料の審査に関する連邦貿易委員会の要請を受けた(第2次請求)。第二の請求の効果は、会社とHorizonが第二の請求を実質的に遵守した後30日まで、会社およびHorizonが自発的に延長するか、または連邦貿易委員会によって早期に終了しない限り、1976年の“ハート-スコット-ロディノ反トラスト改善法案”(改正)に規定された待機期間を延長することである。
ChemoCentryx,Inc.
•2022年10月20日、ChemoCentryxの買収を1株52.00ドルの現金で完了し、買収した現金を差し引いた総金額は約38億ドルだった。
製品·配管
心臓代謝
再修術
•2022年、我々はRepatha FOURIER-OLE研究の結果を公表し、これは2つの開放ラベル拡張(OLE)研究(6,635名の患者)から3期FOURIER心血管(CV)までの結果試験である。フーリエ-OLEは臨床で明らかなアテローム性動脈硬化性心血管疾患(ASCVD)成人患者に対するRepathaの長期安全性と耐性を評価することを目的としている。これらの研究において,探索的分析により,心血管死亡,心筋梗塞(MI)と脳卒中の複合終点定義により,早期からRepathaは比較的に低い心血管結果のリスクを招き,重篤な有害事象の発生率は時間の経過とともに増加しないことが示唆された。
オルパシーランド
•2022年11月、我々はリポ蛋白質(A)或いはLp(A)レベルが150 nmol/Lを超え、ASCVDの病歴を有する成人患者のオパシランを評価する第2段階SEA(A)用量研究の陽性治療結果を公表した。Olpasiranは1種の小干渉RNA(SiRNA)であり、体内のアポリポタンパク質(A)の産生を低下させることを目的とし、アポリポタンパク質(A)はリポ蛋白(A)の重要な成分であり、心血管イベントのリスク増加と関係がある。二重盲検プラセボ対照治療中、オパシランは、ベースラインLp(A)の中央値が約260 nmol/Lである225ミリグラムLp(A)を12週ごとに皮下注射した。12週ごとに75 mg以上の用量を受けた患者は、36週でLp(A)がプラセボより95%以上低下した。全体的に言えば、オパシラン群とプラセボ群の不良事件発生率は類似している。
炎症が起こる
TEZSPIRE
•2022年9月、欧州委員会は、12歳以上の重篤な喘息を有する患者のための追加療法として、EUにおいてTEZSPIREを承認し、これらの患者は、大量の吸入コルチコステロイドおよび維持治療のための別の薬剤を使用して十分に制御できない。この承認は2022年7月にEMA CHMPによって提案された提案に従った。
アブダビ654
•2022年4月、著者らは治療中の重度斑塊型乾癬成人患者におけるABP 654とStelara(Ustekinumab)の治療効果と安全性を評価した第3段階研究の初歩的な結果を発表した。この研究は主要な治療効果の終点を達成し,ABP 654とStelaraは臨床的に有意差がないことを示唆している。
腫瘍学/血液学
LUMAKRAS/LUMYKRA
•2022年4月、著者らはLUMAKRAS/LUMYKRAS治療を受けたKRAS G 12 C突然変異末期非小細胞肺癌(NSCLC)患者におけるCodeBreaK 100 1/2期試験の長期治療効果と安全性データを発表した。大量の前治療を受けた174名の患者のうち(172名の患者はベースライン測定可能な病変があり)、LUMAKRAS/LUMYKRAS中央で確認された客観的有効率(OOR)は40.7%、疾患コントロール率は83.7%、中位反応持続時間(DOR)は12.3ケ月であった。その結果,中位無進展生存期間(PFS)は6.3カ月,総生存期間は12.5カ月であり,その中の32.5%の患者は2年後も生存していることが示された。長期フォローアップ中、LUMAKRAS/LUMYKRASの新しい安全信号は発見されなかった。
•2022年9月、著者らは全世界第三段階CodeBureaK 200試験の結果を発表し、その結果、静脈化学療法ドセタキセルと比較して、LUMAKRAS/LUMYKRASを毎日1回経口投与することにより、KRAS G 12 C変異NSCLC患者のPFS(主要な終点)とOOR(1つの肝心な副次終点)が著しく向上したことを示した。ドセタキセルと比べ、LUMAKRAS/LUMYKRASは大量の前治療を受けた患者のPFSを明らかに改善した。LUMAKRAS/LUMYKRAS群の1年以内にPFSが出現した患者の割合は25%であったが、ドセタキセル群は10%であった。LUMAKRAS/LUMYKRAS群のORRはドセタキセルより明らかに高く、その効率はLUMAKRAS/LUMYKRAS群の2倍(それぞれ28%と13%)であった。
アブダビ959
•2022年8月、著者らはDahlia研究の正の結果を発表し、これはランダム、二重盲検、積極対照、2つの時期の交差第三段階研究であり、成人陣発性睡眠性ヘモグロビン尿(PNH)患者におけるSoliris(Eculizumab)生物に類似した候補薬物ABP 959とSolirisの治療効果と安全性を評価した。この研究はその主要な終点に達しており,ABP 959とSolirisの間に臨床的意義の差はないことが示唆された。ABP 959の安全性と免疫原性はSolirisに相当する。
新しい製造施設
•2022年3月にノースカロライナ州に工場を設立しました製造ネットワーク能力を向上させます
マーケティング、流通、精選された市場製品
私たちの販売とマーケティング力が最も集中しているところはアメリカとヨーロッパです。近年、我々は製品の商業化とマーケティングを他の地理的地域に拡張しており、日本、中国、アジアの他の地域、ラテンアメリカ、中東を含む。このような拡張が発生し、自社の付属会社を設立することにより、既存の第三者業務又は製品権利を買収することにより、又は第三者と連携することにより、引き続き発生することが予想される。私たちの重要な連合については、業務関係を参照してください。私たちが自分の販売とマーケティング力を使っても、第三者のサービスを使用しても、これらの市場は違います。このような使用は、一般に、新しい市場に入る性質、機会の大きさ、および運営能力を含むいくつかの要因に依存する。私たちは私たちの協力者と共に、医師や彼らの診療所、透析センター、病院、薬局を含む医療提供者に私たちの製品を販売します。
アメリカでは、私たちのほとんどの販売は薬品卸売流通業者に販売されています。これは私たちの製品をヘルスケア提供者に分配する主な方法です。私たちはまた、印刷、テレビ、オンラインメディアを含む、消費者向けの直接チャネルを通じていくつかの製品をマーケティングします。さらなる議論については、政府法規-米国の法規-製品マーケティングおよび販売促進の法規を参照されたい。米国以外では,主に医療提供者および/または薬品卸売流通業者に販売されており,具体的には個々の国/地域の流通実践に依存している。アジア太平洋地域では、アステラス製薬会社、百済神州、KKC、武田薬業有限会社、第一三共株式会社を含む他社と協力して当社の製品を販売しています。
2022年、2021年、2020年には、マケソン社、アメリカベルゲン社、紅衣主教保健会社の3つの大手卸売業者に対する製品売上高はそれぞれ総収入の10%以上を占めている。2022年、2021年、2020年、これらの卸売業者の総収入はそれぞれ世界の総収入の82%、82%、83%を占めている。私たちは大きな顧客の財務状況を監視し、信用限度額を設定し、場合によっては信用状を要求したり、信用保険を獲得したりすることで、私たちの信用リスクの開放を制限します。
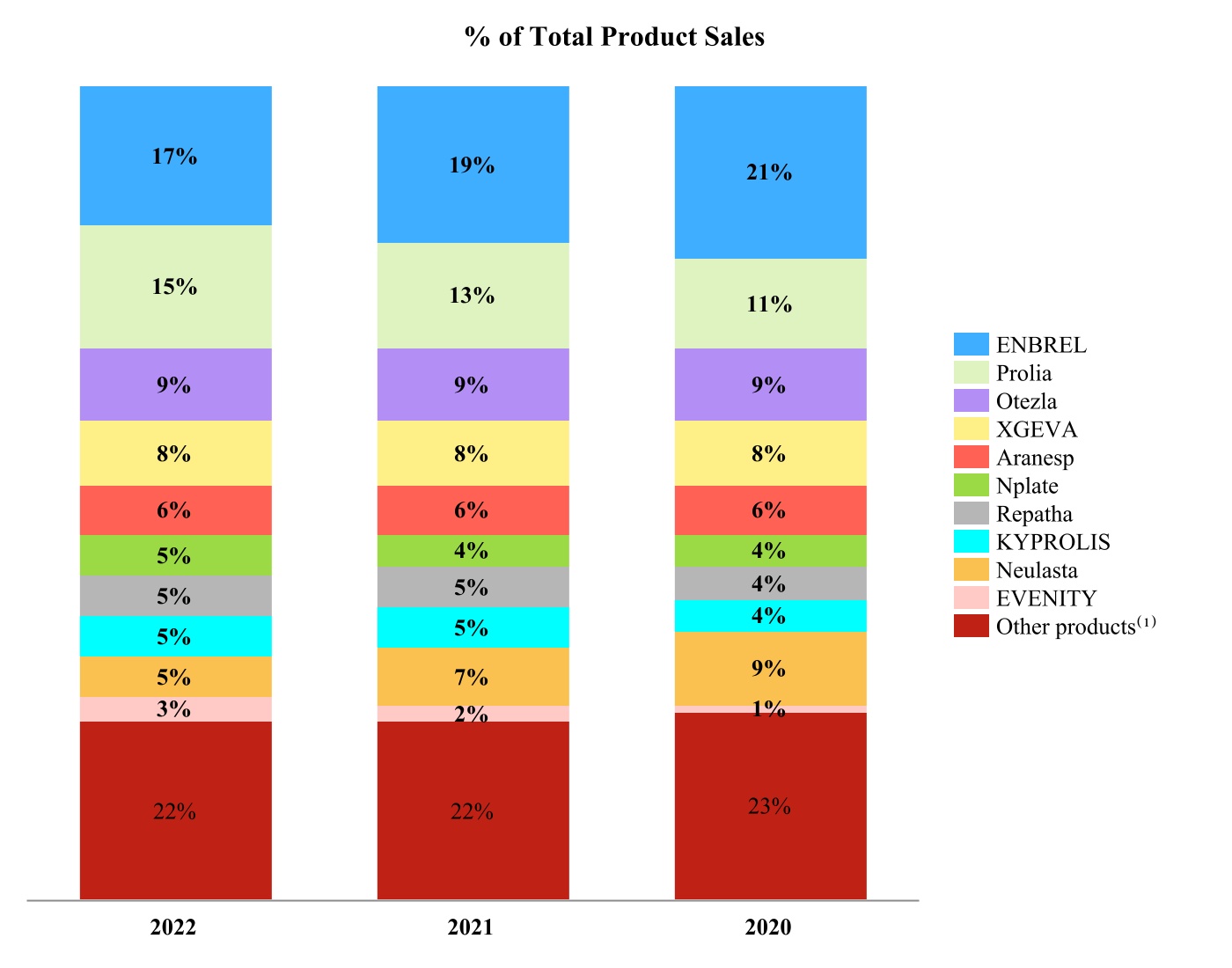
私たちの製品は世界各地に販売されています。アメリカは私たちの最大の市場です。次の表は主な製品で私たちの製品の売上を示し、下の表(百万ドル単位)は地理的位置別に2022、2021、2020年の製品の売上を示します。
| | | | | | | | | | | | | | | | | | | | | | | | | | |
| 2022 | | 2021 | | 2020 |
| 地域別製品売上高: | | | | | | | | |
| アメリカです。 | $ | 17,743 | | 72 | % | | $ | 17,286 | | 71 | % | | $ | 17,985 | | 74 | % |
| はい | 7,058 | | 28 | % | | 7,011 | | 29 | % | | 6,255 | | 26 | % |
| 合計する | $ | 24,801 | | 100 | % | | $ | 24,297 | | 100 | % | | $ | 24,240 | | 100 | % |
____________
(1) 私たちの非主要製品の製品販売と、私たちのGensentaとBergamo子会社を含めて。
Enbrel
私たちはアメリカとカナダで腫瘍壊死因子遮断薬ENBRELを販売している。Enbrel社は1998年に発売され,主に中等度から重度の活動期関節リウマチを有する成人患者,系統的治療や光線療法が必要な慢性中重度斑塊型乾癬患者および活動期乾癬患者の治療に用いられている。
プロリア
私たちは世界の多くの国と地域でプロリアを販売している。プロリアにはXGEVAと同様の活性成分が含まれているが,異なる適応,患者数,用量,投与頻度への使用が許可されている。Proliaは2010年にアメリカとヨーロッパで発売された。アメリカでは、それは主に閉経後骨粗鬆症女性の適応の治療に用いられ、これらの女性は高骨折リスクがあり、骨粗鬆症性骨折病歴或いは骨折の多種の危険因子と定義されている;或いは失敗或いは他の利用可能な骨粗鬆症治療方案に耐えられない患者に使用されている。ヨーロッパでは,プロリアは主に骨折リスクが増加する閉経後女性の骨粗鬆症の治療に用いられている。
ウルトラツラ
私たちはホスホジエステラーゼ4(PDE 4)を阻害する小分子であるOtezlaを世界の多くの国で販売している。OtezlaはCelgeneを買収した後、2019年11月に百時美施貴宝社から買収した。Otezlaは経口療法であり,様々な重症度の斑塊型乾癬(米国と日本)や中から重度の斑塊型乾癬(ヨーロッパを含む他のグローバル市場),活動期乾癬関節炎成人,Beh≡et‘s病に関連する口腔潰瘍の成人の治療に許可されている。
シグワ
私たちは世界の多くの国と地域でXGEVAを販売している。XGevaは2010年に発売され、主に固形腫瘍と多発性骨髄腫骨転移患者の骨関連事件(病理性骨折、骨放射、脊髄圧迫或いは骨手術)の予防に応用されている。
Aranesp
私たちは主にアメリカとヨーロッパでAranespを販売しています。Aranespは2001年に発売され、透析患者と非透析患者の中で慢性腎臓疾患(CKD)による正常数より低い赤血球(貧血)の治療に用いられている。Aranespは,ある非髄系悪性腫瘍患者に伴う骨髄抑制化学療法による貧血の治療や,Aranesp開始後に少なくとも2カ月間化学療法を行う場合にも用いられている。
ナンバープレート
私たちは世界の多くの国でニプランドを販売している。Nplateは2008年に発売され、コルチコステロイド、免疫グロブリンまたは脾臓切除術に対する反応が不足している慢性免疫性血小板減少症(ITP)患者の血小板減少症の治療に用いられている。
再修術
私たちは世界の多くの国でPCSK 9阻害剤Repathaを販売している。Repathaは2015年に発売され、心血管疾患を有する成人心筋梗塞、脳卒中と冠状動脈血行再建のリスクを低下させることを目的とした。Repathaはまた,ヘテロ性家族性高コレステロール血症(HeFH)を含む原発性高脂血症を有する成人の低密度リポ蛋白質コレステロール(LDL−C)を低下させることが証明されている。
ケプロリス
私たちは主にアメリカとヨーロッパでKyprolisを販売している。ケプロリス DARZALEXは2012年に発売され、(I)デキサメタゾン、(Ii)レナデキサメタゾンと(Iii)DARZALEX+デキサメタゾンと併用して再発或いは難治性多発性骨髄腫患者を治療し、これらの患者は以前1~3種類の治療方案を受けたことがある。1つ以上の以前の治療を受けた再発または難治性多発性骨髄腫患者のための単一薬剤としても承認されている。
ニューラス塔
私たちは主にフィガチウム分子に基づくペグ化タンパク質であるNeulastaをアメリカとヨーロッパで販売している。Neulastaは2002年に発売され、主に適応に用いられ、あるタイプの癌(非髄細胞癌)患者が白血球数が低いことによる感染機会を減少させることを助けるために使用され、これらの患者が受けた抗癌薬(化学療法)は発熱と赤血球数の低下を招く可能性がある。2015年,Neulasta Onproキットが米国で発売された。Neulasta Onproキットは医師にNeulasta管理を開始する機会を提供しました 化学療法と同じ日に,推奨用量のニューレスタ薬を化学療法後翌日に自宅で送達し,患者が医師に戻るまでの道のりを省略した。
事件.事件
私たちは私たちのパートナーと共に、世界の多くの国と地域でEVENITYをマーケティングしています。EVENITYは2019年に米国と日本で発売された。米国では閉経後骨粗鬆症のハイリスク骨折女性の治療に用いられている。日本では,EVENITYは主に閉経後骨折リスクの高い女性や男性の骨粗鬆症の治療に用いられている。
その他の発売製品
MVASI、Vectibix、BLINCyTO、Epogen、AMGEVITA、Aimovig、Parsabiv、KANJINTI、LUMAKRAS/LUMYKRAS、TEZSPIRE、NEUPOGEN、SENIPAR/MIMPAR、TAVNEOSなど、世界の様々な市場で多くの他の製品を販売しています。
特許
以下の表に,我々が未完成の指定製品の重大な特許を地域,一般テーマ,最新満期日に示した。いくつかのヨーロッパ特許は補完保護証明書の主体であり、これらの証明書は、表に記載された日付の後に、いくつかのヨーロッパ諸国の製品に追加の保護を提供する。次の特許表の脚注を見てください。
同じまたはそれ以上の満期日を有する1つまたは複数の特許は、単独では列挙されない同じ一般的な主題に属する可能性がある。
| | | | | | | | | | | | | | | | | | | | |
| 製品 | | 領土.領土 | | 一般題材 | | 満期になる |
Enbrel® (イナシップ) | | アメリカです。 | | 含水配合物を用いた処理方法 | | 6/8/2023 |
| アメリカです。 | | 製剤及び製剤の製造方法 | | 10/19/2037 |
| アメリカです。 | | 融合タンパク質及び医薬組成物 | | 11/22/2028 |
| アメリカです。 | | 融合タンパク質をコードするDNA及びその製造方法 | | 4/24/2029 |
プロリア®/XGEVA®(Denosumab) | | アメリカです。 | | RANKL抗体をコードする核酸及びRANKL抗体の製造方法 | | 11/30/2023 |
| アメリカです。 | | 配列を含むRANKL抗体 | | 2/19/2025 |
| ヨーロッパ.ヨーロッパ | | 配列を含むRANKL抗体(1) | | 6/25/2022 |
ウルトラツラ® (アプミスト) | | アメリカです。 | | 組成物及び化合物 | | 2/16/2028 |
| アメリカです。 | | 結晶形 | | 12/9/2023 |
| アメリカです。 | | 治療法(2) | | 5/29/2034 |
| ヨーロッパ.ヨーロッパ | | 組成物、化合物及び処理方法(1) | | 3/20/2023 |
Aranesp®(Darbepoetin Alfa) | | アメリカです。 | | エリスロポエチン蛋白のグリコシル化類似体 | | 5/15/2024 |
ナンバープレート® (ロミプシム) | | アメリカです。 | | 融合タンパク質をコードするポリヌクレオチド | | 7/25/2023 |
| アメリカです。 | | 製剤 | | 2/12/2028 |
| ヨーロッパ.ヨーロッパ | | 凝固促進化合物(1) | | 10/22/2019 |
| ヨーロッパ.ヨーロッパ | | 製剤 | | 4/20/2027 |
再修術® (Evocumab) | | アメリカです。 | | 抗体.抗体(3) | | 10/25/2029 |
| アメリカです。 | | 治療法 | | 10/8/2030 |
| ヨーロッパ.ヨーロッパ | | 作文を書く(1) | | 8/22/2028 |
| ヨーロッパ.ヨーロッパ | | 治療法 | | 5/10/2032 |
| ヨーロッパ.ヨーロッパ | | 製剤 | | 5/3/2033 |
ケプロリス®(Carfilzomib) | | アメリカです。 | | 組成物及び化合物 | | 12/7/2027 |
| アメリカです。 | | 治療法 | | 4/14/2025 |
| アメリカです。 | | 作り方 | | 5/8/2033 |
| ヨーロッパ.ヨーロッパ | | 組成物、化合物及び処理方法(1) | | 12/7/2025 |
| | | | | | | | | | | | | | | | | | | | |
| 製品 | | 領土.領土 | | 一般題材 | | 満期になる |
事件.事件® (romozumab-aqqg) | | アメリカです。 | | 抗体.抗体 | | 4/25/2026 |
| アメリカです。 | | 治療法 | | 4/9/2033 |
| アメリカです。 | | レシピ及びレシピの使用方法 | | 5/11/2031 |
| ヨーロッパ.ヨーロッパ | | 抗体.抗体(1) | | 4/28/2026 |
| ヨーロッパ.ヨーロッパ | | 治療法 | | 4/18/2032 |
| ヨーロッパ.ヨーロッパ | | レシピ及びレシピの使用方法 | | 5/11/2031 |
BLINCETO®(Blinatumab) | | アメリカです。 | | 医薬組成物及び二機能性ポリペプチド | | 4/6/2030 |
| アメリカです。 | | 管理方法 | | 9/28/2027 |
| ヨーロッパ.ヨーロッパ | | 二機能性ポリペプチド(1) | | 11/26/2024 |
| ヨーロッパ.ヨーロッパ | | 管理方法 | | 11/6/2029 |
エモヴィグ®(エロナブ·オオエ) | | アメリカです。 | | カルシトニン遺伝子関連ペプチド受容体抗体 | | 5/17/2032 |
| アメリカです。 | | 治療法 | | 4/22/2036 |
| アメリカです。 | | 組成物及び医薬製剤 | | 4/1/2039 |
| ヨーロッパ.ヨーロッパ | | カルシトニン遺伝子関連ペプチド受容体抗体(1) | | 12/18/2029 |
| ヨーロッパ.ヨーロッパ | | 治療法 | | 8/10/2035 |
パサビフ® (Etelcalcetie)
| | アメリカです。 | | 化合物及び医薬組成物 | | 2/7/2031 |
| アメリカです。 | | 製剤 | | 6/27/2034 |
| アメリカです。 | | 作り方 | | 8/9/2035 |
| ヨーロッパ.ヨーロッパ | | 化合物及び医薬組成物(1) | | 7/29/2030 |
| ヨーロッパ.ヨーロッパ | | 製剤 | | 6/27/2034 |
| LUMAKRAS/LUMYKRAS(Sotorasib) | | アメリカです。 | | 化合物及び医薬組成物 | | 5/21/2038 |
| アメリカです。 | | 結晶形態、医薬組成物及び治療方法 | | 5/20/2040 |
| アメリカです。 | | 治療法 | | 8/11/2040 |
| ヨーロッパ.ヨーロッパ | | 化合物、医薬組成物及び治療方法 | | 5/21/2038 |
| | | | | | |
| | | | | |
| | | | | |
TEZSPIRE® (tezepelumab-Ekko) | | アメリカです。 | | ポリペプチド.ポリペプチド(3) | | 2/3/2029 |
| アメリカです。 | | 治療法 | | 8/23/2038 |
| ヨーロッパ.ヨーロッパ | | ポリペプチド.ポリペプチド | | 9/9/2028 |
TAVNEOS®(アボカド) | | アメリカです。 | | 化合物及び医薬組成物(3) | | 2/3/2031 |
(1)この主題を有する欧州特許もまた、欧州の1つまたは複数の国で補足保護を受ける権利がある可能性があり、どのような延期の長さも国によって異なるであろう。例えば、少なくとも以下の国では、指定された製品に特許補足保護証明書が発行されている
•Denosumab-フランス、ドイツ、イタリア、スペイン、連合王国、2025年満期
•Apremilast-フランス、ドイツ、イタリア、スペイン、イギリスは2028年に満了します
•Carfilzomib-フランス、ドイツ、イタリア、スペイン、連合王国は2030年に満了します
•Volocumab-フランス、スペイン、連合王国、2030年満期
•RomiplosTim--フランス、ドイツ、イタリア、スペイン、連合王国、2024年満期
•Romosozumab-フランス、イタリア、スペイン、連合王国、2031年の期限
•Blinatumab-フランス、ドイツ、イタリア、スペイン、2029年満期
•--フランス、イタリア、スペイン、連合王国、2033年の期限
•Etelcalcetie-フランス、ドイツ、イタリア、スペイン、連合王国、2031年満期
(2)米国特許番号10092541はニュージャージー州地域裁判所によって無効と判断された。私たちは裁判所の判決に同意せず、私たちはこの判決を控訴している。連結財務諸表第四部--付記19、あるいは事項と引受金があり、安進はサントス社らの事件を訴えた。
(3)このテーマを持つ特許は米国で特許期間を延長することができる。
競争
私たちは競争の激しい環境で運営している。私たちの多くの市場製品は疾病分野に使用されており、これらの分野では、私たちの競争相手は現在、研究開発活動を通じて他の製品や治療法を獲得しているか、または研究開発活動によって他の製品や治療法を獲得している。また、いくつかの競争相手がマーケティングしている製品は、私たちが最近発売したマーケティング製品や現在開発中の製品と同じ遺伝的経路を持っている。この競争は私たちの製品の定価と市場シェアに影響を及ぼすかもしれない。私たちは引き続き薬品ライフサイクルの中で革新を行うことによって薬品価値を増加させる方法を求めている。その中には、著者らの製品が対象とする疾病領域を拡大し、新しい方法を見つけて、私たちの薬品送達をより容易で、コストを低くすることを含む。そのような活動は重要な差別化された機会を提供することができる。例えば、医師に推奨用量のNeulastaの使用を開始する機会を提供するNeulasta Onproキットを販売します 化学療法と同じ日に化学療法翌日に自宅で投与し,医師に戻るまでの道のりを省略した。私たちは私たちの競争地位を強化するために革新に引き続き努力する予定だ。このような地位は安全性、有効性、信頼性、可用性、患者の利便性、輸送設備、価格、精算、市場に入る機会とタイミング及び特許地位と満期などの要素に基づく可能性がある。
私たちの主要製品のいくつかの既存の特許が満期になり、私たちは生物模倣薬と模倣薬からの競争を含む新しい競争と日々の激しい競争に直面している。生物学的類似とは、市場によって承認された生物製品の別のバージョンを求めるか、または取得したことを意味し、その基礎は、元の参照製品と“高度に類似している”ことを証明することである。私たちは生物類似競争が私たちのオリジナル製品の販売に悪影響を及ぼすことを経験した。会社はEpogen,NEUPOGEN,Neulastaの生物類似バージョンを発売し,ENBRELの生物模倣薬を承認した。私たちの1つのオリジナル製品が複数の生物類似バージョンを発売すると、競争は迅速に激化し、参考と生物類似製品の純価格の下げ幅がもっと大きくなり、製品の販売にもっと大きな影響を与える。また政府の規制-アメリカの規制-生物模倣薬の承認を見た。競争相手の生物模倣薬は価格に競争が存在するが、著者らは多くの患者、サプライヤーと支払人が引き続き著者らの製品の名声、供給信頼性と安全性を高度に重視すると信じている。より多くの生物類似競争相手が市場に参入するにつれて、私たちは引き続き私たちの世界的な経験を利用して、ブランド競争と生物類似競争の中で頭角を現していく。
私たちはアメリカやアメリカ以外の市場でも自分の生物類似製品を持っていて、私たちの競争相手のブランドや生物似バージョンの製品と競争しています。安進は2019年にアヴァスティン生物に類似したMVASIと,ヘキセチン生物に類似したKANJINTIを発売し,2018年には米国以外の市場でHUMIRA生物に類似したAMGEVITAを発売した。我々はまたFDAによるAMJEVITAの許可を得て、AMJEVITAは生物に似たHUMIRAであり、2023年1月にアメリカ市場を発売した。2020年にはRemicadeに似たバイオ製品であるAVSOLAを発売しました 2021年にRituxanに類似した生物製剤であるRIABNIを発売した。将来、各市場で、私たちのブランドと生物類似製品はより多くの生物類似競争に直面することを予想しています。
私たちの製品の大部分は生物製品ですが、一部は小分子製品もあります。FDAの承認手続きは後発薬メーカーが革新者製品の安全性と有効性データに依存することを許可しているため、自分の高価で時間のかかる臨床試験を行うことなく、模倣薬メーカーは通常私たちの小分子製品の競争バージョンを開発と販売することができる。例えば、Cinacalcetに対する特許の独占特許権を失った後、私たちは短い時間でかなりの市場シェアとそれに応じた収入を失った。Cinacalcetは私たちの小分子模倣剤Sensiar中の活性成分である。連結財務諸表の第四部--付記19“または事項と引受金”を参照。
新製品の発売、競争相手の新プロセスまたは技術の開発、または既存製品に関する新情報の出現は、(I)我々が販売する製品に対する競争を激化させる可能性があり、さらには、特許保護された製品に対しても同様であり、および/または(Ii)販売製品から得られる価格を低下させる可能性がある。また,新たな治療案や看護基準を開発することは,我々の製品の使用を減少させるか,あるいは我々が行っている候補製品の臨床試験の実用性や応用を制限する可能性がある。(本文書で用いられるように、用語臨床試験前向き臨床試験、観察性研究、登録、その他の研究が含まれる可能性がある)。第1 A項を参照。リスク要因-私たちの製品は激しい競争に直面して、私たちの候補製品も激しい競争に直面するかもしれません第1 A項ですリスク要因-我々は現在,生物模倣薬と後発薬からの競争に直面しており,将来的には生物模倣薬と模倣薬からの日々の激しい競争に直面することが予想される.
次の表は私たちの主な競争相手を反映しているが、詳細ではない。
| | | | | | | | | | | | | | | | | | | | |
| 製品 | | 領土.領土 | | ライバルがマーケティングした製品 | | 競争相手 |
| Enbrel | | アメリカとカナダ | | フミラ | | AbbVie |
| アメリカです。 | | シェルヤンツ | | ファイザー。 |
| アメリカとカナダ | | RINVOQ | | AbbVie |
| プロリア | | アメリカ、ヨーロッパ、アジア太平洋地域 | | アレンドロネート、レロキシフェン、およびゾレホスホイミ製薬 | | 多種多様である |
| ウルトラツラ | | アメリカとヨーロッパは | | フミラ† | | AbbVie |
| アメリカとヨーロッパは | | コゼンティックス | | ノバ会社 |
| アメリカとヨーロッパは | | タルツ | | リリー |
| アメリカとヨーロッパは | | トレムフィア | | ジェイソン(1) |
| アメリカとヨーロッパは | | 天の子 | | AbbVie |
| アメリカとヨーロッパは | | アモンシロチョウ模造製薬 | | 多種多様である |
シグワ | | アメリカとヨーロッパは | | ゾレドロン酸塩模倣製薬 | | 多種多様である |
| Aranesp | | アメリカです。 | | 製品(2) | | ジェイソン(1) |
| アメリカとヨーロッパは | | エポチンアルファ生体模倣薬 | | 多種多様である |
ナンバープレート | | アメリカとヨーロッパは | | Promacta/Revolade | | ノバ会社 |
再修術 | | アメリカ、ヨーロッパ、アジア太平洋地域 | | プルート | | Regeneron製薬会社
セノフィ |
| ケプロリス | | アメリカです。 | | VELCADE | | ミレニアム製薬会社(4) |
| アメリカとヨーロッパは | | Revlimid(3) | | 多種多様である |
| アメリカとヨーロッパは | | Pomalyst/Innovid | | セルキング(5) |
| アメリカとヨーロッパは | | Darzalex | | ジェイソン(1) |
ニューラス塔(6) | | アメリカとヨーロッパは | | UDENYCA | | Coherus BioSciences,Inc. |
| アメリカとヨーロッパは | | フルフェラ | | Mylan機関会社です。 |
| アメリカとヨーロッパは | | 非グリタゾン生物模倣薬 | | 多種多様である |
| 事件.事件 | | アメリカです。 | | アレンドロネート、レロキシフェン、およびゾレホスホイミ製薬 | | 多種多様である |
| 日本です | | Teribone | | 朝日嘉誠薬業 |
†承認された生物模倣薬はヨーロッパとカナダで使用可能だ。
(1)ジョンソンの子会社です。
(2)Procritは支持性癌看護と透析前設置においてAranespと競合している。
(3)Revlimidには汎型も含まれる.
(4)武田薬品工業株式会社の子会社です。
(5)百時美施貴宝社の子会社です。
(6)アメリカとヨーロッパで規制審査を受けている他の生物模倣薬。
精算する
私どもの製品の販売は第三者支払者の保証範囲と精算範囲に依存しています。世界各地の多くの市場では、政府医療システム、私営医療保険会社、その他の組織を含むこれらの支払者は依然として医療コストの低減に集中している;医療コストの上昇、経済圧力及び新冠肺炎疫病によるより広範な挑戦により、彼らの努力は強化されている。薬品は依然として費用を抑えるために厳格に検討されている。そのため,支払者は生物製薬製品の使用をより厳しくし,これらの製品の価格を精査するとともに,これらの製品が患者やより広範な医療システムにもたらすメリットを支援するために,より高いレベルの臨床証拠が求められている。 私たちの製品が生物模倣薬からの競争を含めて競争されると、これらの圧力は悪化するだろう。
米国では、医療提供者および他の実体(例えば、薬局およびPBM)は、個人支払者および政府医療計画(例えば、MedicareおよびMedicaid)によって提供される保証サービスおよび製品によって精算される。我々は医療保健提供者,個人支払者,政府支払者,PBMに協議リベートを提供した。さらに、(I)いくつかの政府計画(MedicareおよびMedicaidを含む)で精算された製品にリベートまたは割引を提供し、(Ii)連邦340 B医薬品定価計画に従って条件に適合する医療提供者に割引を提供しなければならない
個人と一部の政府支払者は処方を使用して薬品の取得と使用を管理する。患者が特定の薬剤を得ることができることを確実にするためには、薬剤の収録および処方における有利な位置が不可欠である。使用可能な場合でも,経済的理由で処方を断念する患者もいる。支払者は、医薬品使用率および/または支出を低減し、および/またはより大きな割合のコストを患者に転嫁するために、コスト低減および抑制措置を継続して実施する。これらの措置は、より限られた福祉計画設計、より高い患者自己負担または共同保険義務、患者に対する商業製造業者自己支払い援助計画の使用の制限(自己アキュムレータによる調整または最大化計画を含む)、患者が薬物を取得する前により厳しい使用管理基準、患者自己負担コストレベルを増加させるより高いレベルの処方配置、および処方排除を含むが、これは、患者および提供者が代替治療または100%の薬物コストの支払いを求めることを効果的に奨励する。PBMや保険会社はこのような措置の使用を強化し続け,安入製品の使用と販売を制限している。また、過去数年間に、多くのPBMと保険会社が統合され、PBMと保険会社の数が減少し、それらはアメリカの大部分の保証人寿を監督している。したがって、PBMおよび保険会社は、より大きな市場力および交渉チップを有し、より厳しい使用基準を強制的に要求することができ、および/または彼らの処方から薬物を排除し、競争相手の薬物または代替治療を支持することができる。ENBREL、Otezla、Repatha、Aimovigのような競争の激しい治療市場で, PBMはまた、製造業者に増分リベートを提供することを要求することによって、それらがその処方地位を獲得および/または維持するように交渉チップを適用することができる。
米国の民間と政府支払者がとった市場行動を除いて、米国の二大政党の政策立案者は薬品コストを低減する政策を支持している。第1 A項を参照。リスク要因-私たちの販売は政府と商業第三者支払人の保証と精算に依存していますが、定価と精算圧力はすでに私たちの収益力に影響を与え続ける可能性がありますそれは.2022年8月、“インフレ低減法”(IRA)が公布され、その中には、(1)2026年から、医療保険でBとD部分によって支払われたいくつかの薬品に対して強制的な定価を実施することが含まれており、この規定によると、メーカーは政府が制定した価格を受け入れなければならず、そうでなければ、すべてのアメリカ販売に対する処罰に直面する(2026年の10種類の薬品から、2027年と2028年に15種類増加し、2029年およびその後数年に20種類増加し、2031年までに、約100種類の薬品がこの設定された価格の影響を受ける可能性がある)。(2)2024年から、連邦医療保険D部分は、受益者の自腹コストを制限し、2025年1月1日から連邦再保険を減少させる(このようなコスト移転とD部分計画やメーカーへの増加を招き、メーカーにある薬物の割引を要求することを含む)、および(3)2022年10月1日から、価格がインフレを超えた場合、メーカーは現在、連邦医療保険D部分で精算された薬物にリベートを支払い、2023年1月1日から価格上昇がインフレを超えた場合、現在連邦医療保険B部分によって精算されている薬品はリベートされる。アイルランド共和軍が採択されたにもかかわらず、環境は依然として活力に満ちており、政府と議会は薬品価格改革を考慮し続けている。
他の可能な政策は、他の国からの薬品の輸入を許可すること、薬品価格の透明性を向上させること、および第三者価値評価を使用して薬品価格を決定することを含む幅広い分野をカバーする。2021年11月15日に法律となるインフラ投資·雇用法案の要求に署名し、2023年から使い捨て容器に包装されたいくつかのB部分で覆われた医薬品のメーカーは、廃棄された金額を政府に返還しなければならない
米国以外の多くの国では,政府が援助している医療システムは薬品や生物製品の主要な支払者である。ますます多くの予算制限および/または薬品の価値を理解しにくいに伴い、多くの国の政府と支払人は様々な措置を取って価格下圧力をかけている。これらの措置は、強制価格制御、価格基準、治療基準定価の増加、強制要件の増加、模倣薬代替および生物学的類似使用の奨励、および政府の強制値下げを含むことができる。この方面で、多くの国は衛生技術評価組織があり、それらはコスト効果などの正式な経済指標を使用して新しい治療法の価格、カバー範囲と精算状況を確定する;これらの組織は老舗市場と新興市場に拡張している。多くの国では、私たちの製品ラベルで指定された人よりも狭い人々にカバー範囲を制限したり、使用量を制限するための数量上限を実施したりしています。各国は医薬品や生物製品の支出の削減を求める積極的な行動を続けていくと予想される。同様に、財政的制限はまた、各国が新しい治療法および革新的な治療法をどの程度承認したいか、および/または新しい技術の獲得をどの程度許可するかに影響を与える可能性がある。EUは現在、その薬品立法の審査と可能な改正を行っており、現在は2023年上半期に終了し、2025年または2026年に実施される予定だ。この審査は新製品の知的財産権保護を減らす提案を提出し、現在予測困難な方法で精算と監督管理構造を変更する可能性が高い。
上で議論された動きと発展は、私たちの製品の価格設定と潜在的な用途、業界に圧力を与えた。支払者,バイオ製薬メーカー,政策立案者,ヘルスケア提供者と独立組織との異なる利益から,関係者が上記の議論の問題で合意できるかどうかは不明であり,どのような一致の結果も予測は困難である。私たちは依然として責任を持って私たちの製品に価格を設定し、満たされていない医療需要に突破的な治療を提供することに集中している。安進は医療コミュニティ全体と協力して持続的な革新を確保し,患者の必要な薬物獲得を促進することに取り組んでいる。私たちは次のようにします
•毎年数十億ドルを研究開発に投入しています
•私たちの薬品に価格を設定して価値を反映しています
•より負担の高い治療選択を高品質で信頼性の高い生体模倣薬の形で開発する
•支払い者と協力して健康結果のリスクと責任を負います
•患者の支援や教育プログラムを提供し
•経済的に必要な患者が私たちの薬を手に入れるのを助け
•政策立案者,患者,その他の利害関係者と連携して持続可能な医療システムを構築し,負担できる医療サービスを得ることができ,患者とその医療専門家が主要な意思決定者である。
第1 A項を参照。リスク要因-私たちの販売は政府と商業第三者支払人の保証と精算に依存していますが、定価と精算圧力はすでに私たちの収益力に影響を与え続ける可能性があります第1 A項ですリスク要因-様々な組織が発表したガイドラインと提案は私たちの製品の使用を減らすことができます。
製造·流通·原材料
製造業
私たちは私たちが生物製品製造の先駆者であり、私たちの製造能力は競争優位性を代表すると信じている。私たちが生産した製品には生物製品もあれば、小分子薬もあります。我々の製品の多くは生細胞で生産された生物製剤であり,自然に発生する分子変異により,それら自体が複雑である。高度に専門化された知識と広範な技術と製品特性が必要であり、実験室規模の技術を再使用可能な商業製造技術に転換することができる。また、著者らの生物製剤製造における専門知識は世界の生物模倣薬市場における著者らのリード的な地位に良好な基礎を築いた。製造施設に関するより多くの情報は、第2項.属性を参照されたい。
私たちは、私たちの製造ネットワークを最適化することによって、および/または、私たちの製品の十分な供給を確保しながらリスクを低減することによって、私たちの製造メリットを拡大することを目指して、私たちの製造施設を革新してきた。例えば,シンガポールやロードアイランド州シーグリニッジで運営許可を得た次世代生物製造工場では,多様な革新技術を1つの工場に統合している。次世代生物製造工場はより小さい製造足跡を必要とし、水とエネルギーの消費を減少させ、より低い炭素排出レベルを含む、より大きな環境効果を提供する。このような工場では,設備は携帯的であり,より小さく,異なる薬物を同時に生産するためにより大きな柔軟性と速度を提供している。これにより、安進はより高い柔軟性で絶えず変化する薬品需要に反応することができる。シンガポール工場はFDAやEMAを含む複数の機関の承認を得ており,商業生産用の小分子薬を生産することができる工場を有している。
我々の内部製造ネットワークは,バッチ製造,配合,充填,表面処理,圧片,設備組み立ての商業生産能力を有している。これらの活動は,米国とその領土内のプエルトリコ,ロードアイランド,カリフォルニア州の施設,国際的なアイルランド,オランダ,シンガポールの施設で行われている。また、私たちは第三者代行製造業者を使用して、私たちの商業製造ネットワークの能力を補完する。
私たちの臨床試験を支持するために、私たちは主に私たちのカリフォルニア工場で候補製品を生産します。私たちはまた第三者契約製造業者を使用して、私たちの臨床製造ネットワーク全体の能力を補充する。
第1 A項を参照。リスク要因は、私たちの製造業務や私たちの製品のグローバル供給に悪影響を及ぼす可能性のある要因を検討します
分布
プエルトリコ、ケンタッキー州、カリフォルニア州とオランダに配送センターを設置し、全世界で私たちの大部分の商業と臨床製品を流通しています。私たちはまた第三者ディーラーを使用して、私たちの製品の世界での流通を補充します。
他にも
上記の製造と流通活動を除いて、私たちの各製造場所は品質管理、技術開発、工程、調達、生産スケジュール、倉庫などの重要な製造支援機能を含む。その中のいくつかの製造と流通活動はFDAと国際規制機関によって高度に規制されている。政府法規-アメリカ法規-製造標準規制を参照してください。
製造業計画
以上のように、私たちは複数の進行中のプロジェクトを通じて生産能力を拡大し、新たな革新を推進してきた。
私たちはロードアイランド州西グリニッジ園区に位置する次世代生物製造工場はアメリカ初のこのような工場であり、すでにFDAとEMAの許可を得た。この工場は私たちがこれらの市場で規制部門の承認を得たので、アメリカと世界市場のために特定の製品を生産する能力を拡大した。
2021年11月、私たちはオハイオ州ニューオルバニにある最新の生物製造工場が着工した。この最終製品の組み立てと包装工場はアメリカの安入薬品の日々増加する需要を支持し、最先端の技術を使用する。
2022年3月、私たちはノースカロライナ州ホリスプリングスの新しい多製品薬物製造工場で着工した。新工場は、従来のステンレス鋼の量産と次世代使い捨て技術を同時にサポートし、1つの工場で多様な製品を柔軟に生産することを可能にする。
安進は環境持続可能性を我々の新施設の前期設計,開発,実行に取り入れ続けている。ノースカロライナ州とオハイオ州で建設中の新施設には,この2地点の現場太陽光再生可能エネルギー発電を含む多くの環境進歩の例が含まれている。ノースカロライナ州工場の炭素,廃棄物,水足跡は従来の薬物製造工場の炭素,廃棄物,水足跡よりも大きく低いと予想され,オハイオ州工場の単位生産足跡も既存の類似施設よりも低くなると予想される。
第1 A項を参照。リスク要因-製造困難、中断、遅延は私たちの製品の供給を制限し、私たちの製品の販売を制限するかもしれません。
原材料と医療機器
我々の製品の商業および/または臨床製造に必要ないくつかの原材料、医療機器(セット診断を含む)、および構成要素は、独立した第三者仕入先によって提供され、これらの供給者の独自の製品であり、いくつかの供給者は、そのような材料を得るための唯一の源である可能性がある。私たちは現在、在庫管理、関係管理、および実行可能な代替源を評価することで、このようなサプライヤーに関連するリスクを管理しようとしている。私たちはまた特定の供給者たちの財務状況と彼らが私たちの要求を満たす能力を監視する。第1 A項を参照。リスク要因-私たちの特定の原材料、医療機器、そして部品は第三者供給者たちに依存している。
私たちは、私たちの製品を製造するための中間材料を含む原材料の出所の検証を支援するために様々なプログラムを実行し、これらのプログラムは、原産地の検証を含み、当社と第三者契約製造業者が実行する製造過程に組み込まれています。
供給をよりよく確保するために、安進は、複数のソースまたはキー原材料のバックアップ在庫を含む様々な方法を組み合わせたリスク緩和戦略を策定した。新冠肺炎の流行に対応し、私たちの持続的な業務の連続的な努力の一部として、私たちは引き続き私たちの在庫レベルを密接に監視し、原材料供給中断の影響を緩和するための追加措置を取った。第1 A項を参照。リスク要因は、私たちの製造業務や私たちの製品のグローバル供給に悪影響を及ぼす可能性のある要因を検討します。
政府の監督管理
アメリカや他の国の政府当局の規制は、私たちの製品の生産とマーケティング、そして私たちが行っている研究開発活動の重要な要素の一つです。臨床で治療用製品を試験、製造、販売するためには、強制的な手続き及び各種規制機関が構築した安全と有効性基準を満たさなければならない。このような基準を遵守することは複雑であり、このような基準のいずれも遵守しないことは重大な影響をもたらす可能性がある。第1 A項を参照。リスク要因は、世界的な規制影響を含む、我々の商業製品開発やマーケティングに悪影響を及ぼす可能性のある要因を検討する。
アメリカの規制
アメリカでは、“公衆衛生サービス法”、FDCA及びその公布された条例及びその他の連邦と州法規は、他の事項のほかに、著者らの製品の生産、研究、開発、テスト、製造、品質管理、ラベル、貯蔵、記録保存、承認、広告、販売促進と流通、及び医療保健専門家と教育病院にある支払いとその他の価値移転を報告することを管理する。
臨床開発と製品審査。私たちの業界の薬物開発は複雑で挑戦的でリスクがあり、失敗率が高い。製品開発サイクルは通常長い--発見から発売まで約10年から15年。潜在的な新薬は、適切な用量レベルおよび許容可能なリスク-利益条件下でヒトの安全性および有効性のために使用されることを決定するために、数年の臨床前および臨床試験を経なければならない。著者らは引き続き著者らの人類遺伝学方面の専門知識及び技術、臨床試験と実世界証拠の革新を応用することによって周期を短縮することに取り組んでいる。
実験室分析と動物臨床前試験後,INDをFDAに提出してヒト試験を開始した。通常、FDAが指定した三段階人体臨床試験計画を担当しています。
•第一段階では、少数の人体被験者における製品候補製品の安全性と適切な用量範囲を調査するための小型臨床試験を行った。
•第2段階では、研究中の疾患または状態を有する患者群における副作用プロファイルおよび第1段階を超えるが比較的少ない患者群における我々の製品候補製品の治療効果を調査するための臨床試験を行った。
•第3段階では、我々の候補製品が通常使用されている治療法と比較して、研究中の疾患または状態を有する多くの患者における短期的および長期的安全性および有効性を調査するための臨床試験を行う。
FDAはINDによる各試験の進展を監視し、そして当時蓄積されたデータとFDAによる試験に参加した患者のリスク効果評価に基づいて、適宜再評価、変更、一時停止或いはテストを終了することができる。臨床前及び臨床試験の結果は、生物製品の生物製品ライセンス申請又は小分子製品の新薬申請の形態でFDAに提出される。FDAが私たちのマーケティング申請を承認するまで、私たちは新製品のマーケティングや普及を許可されません。
生体模倣薬の承認. 平価医療法案“は、FDAが単独で簡略化された経路で生物模倣薬を承認することを許可する。この経路は、生物類似体の発起人が、生物類似体がそれと高度に類似しており、安全性、純度および効力の面で臨床的意義の差がないことが証明された発起者製品の非臨床試験および臨床試験データに部分的に基づいて、規制許可を求め、獲得することを可能にする。“類似性”を証明する相関性は,多くの場合,生物模倣薬は,リスク効果が以前に決定されていたため,発起者が通常要求される臨床試験全般を行わずに市場に出すことができることである。将来の革新へのインセンティブを維持するために、この法律は発起人の製品のための排他期を設立し、これは通常、生物模倣薬がFDAの承認を得ることを禁止し、一部の理由はFDAが最初に発起人製品を承認してから12年以内に、生物模倣薬がFDAに提出された申請において発起人のデータに依存または参考するためである。この法律は生物製品に付与された特許の期限を変えなかった。生物模倣薬を実施して承認経路を簡略化する一部として、FDAはいくつかの指導文書を発表し、その中のいくつかはまだ草稿形式にある。第1 A項を参照。リスク要因-我々は現在,生物模倣薬と後発薬からの競争に直面しており,将来的には生物模倣薬と模倣薬からの日々の激しい競争に直面することが予想される.
製品マーケティングと販売促進活動を規範化するそれは.FDAは薬品のマーケティングと販売促進を規制している。承認された製品適応に対する製品販売促進は,FDCAの法定基準とFDAが実施した法規とガイドラインに適合しなければならない。FDAのマーケティングおよび販売促進活動の審査には、消費者向けの広告、ヘルスケア提供者が指導する広告および販売促進、医療専門家とのコミュニケーション、販売促進番組、および電子メディアに関連する販売促進活動が含まれるが、これらに限定されない。FDAはまた、販売促進を背景に製品の安全性または有効性について述べる業界スポンサーの科学的および教育活動を検討する可能性がある。FDAは、承認されていない製品用途またはFDA広告およびラベル法律に違反する他の企業を推進するための法執行行動をとることができる。法執行行動には、製品差し押さえ、禁止、民事または刑事処罰または監督管理書簡が含まれる可能性があり、これは、医療保健専門家に是正広告または他の是正コミュニケーションを発行する必要があるかもしれない。FDAの規定を守らないことは、米国議会や他の立法者が会社活動を否定的に宣伝したり、審査を強化したりする可能性もある。また,以下に述べるように,米国の医療詐欺や法律の乱用により,このような失敗は追加的な責任を招く可能性がある。
製造基準に関する規定それは.FDAは製品の発売を許可する前に、製品の製造とテストに使用する設備、施設、実験室、技術に対して監督と検査を行う。FDAの承認を得た後、製造設備、場所、またはプロセスを大きく変更した場合、追加の規制審査が必要になる可能性があります。FDAがその施設検査計画で実行している現行の良好な製造規範法規と製品特定法規も遵守しなければならない。FDAは初歩的な承認を得た後、定期的に私たちの設備、施設、実験室と流れを再検査します。
組合せ製品に対する監督管理それは.FDAは、組合せ製品を、2つ以上の規制された成分からなる製品(例えば、生物学的および/または薬物および装置)として定義する。生物製品/薬物と器械はそれぞれ自分の監督管理要求があり、組合せ製品は追加の要求があるかもしれない。私たちの多くの上場製品はこの定義に適合し、この枠組みの下で規制されており、私たちのいくつかの候補パイプライン製品もこの枠組みの下で評価を受け、規制部門の承認を得ることが予想される。
アメリカ以外の規制
EU諸国およびイギリス、スイス、カナダ、オーストラリア、日本では、監督管理要求と承認手続きは原則的に米国と似ている。
EUでは、現在、任意のEU加盟国の許可されていない製品の上場承認を求める2つの可能な方法がある:分散手順と集中手続き。はい分散プログラム同じ上場許可申請は同時に国家規制機関に提出される。規制審査は、安全性、品質、有効性の評価に基づいて申請者が承認を求める他の加盟国(関連加盟国)によって審査·承認される1つの加盟国(参照加盟国)が先頭に立っている(公共健康に対する製品の深刻なリスクに対する懸念は存在しないと仮定する)。分散された手続きはすべての関連国で一連の単一国家承認をもたらす。はい集中手順これはすべてのバイオテクノロジー製品に必要であり、ある会社はEMAに単一のマーケティング許可申請を提出し、EMAはヨーロッパ各地の科学資源を用いてアーカイブを評価する。もし薬品が品質、安全性と有効性の要求に符合することが証明されたら、EMAのCHMPは積極的な意見を取り、それをECに伝え、最終的に発売を承認するかどうかを決定する。欧州委員会が全体的にCHMPの意見に従っていても、それは必ずしもそうする必要はない。その後の商業化は国ごとの精算承認によって実現される。
連合では、生物模倣薬は集中手続きの専門的な経路で承認された。米国経路と同様に、原始参照製品のデータ独占期間が満了すると、申請者は、生物類似製品に対する監督部門の許可を求め、得られ、一部は原始製品のために提出されたデータに依存し、生物類似製品が品質、安全性、有効性の面でヨーロッパ経済区が許可した原始参照製品と“高度に類似している”ことを証明するデータに依存する。第1 A項を参照。リスク要因-我々は現在,生物模倣薬と後発薬からの競争に直面しており,将来的には生物模倣薬と模倣薬からの日々の激しい競争に直面することが予想される.
ラテンアメリカや中東の国のような他の国には、EUと同様の審査手続きやデータ要件もあり、場合によっては米国やEU規制機関の事前マーケティング承認に依存することができる。これらの国の規制手続きには、製造/試験施設検査、薬品輸入時のテスト、その他の国内要求が含まれている可能性がある。
アジア太平洋地域では、全世界の臨床試験以外に、中国、日本、韓国と台湾などのいくつかの国はまた局部の臨床試験データを薬物登録過程の一部として必要とする可能性があり、これは全体の薬物開発と登録のスケジュールを増加させる可能性がある。ほとんどのアジア市場で、登録スケジュールはアメリカやEUの上場承認にかかっている。中国、インドネシア、タイなどアジアの一部の市場では、規制スケジュールの予測がより難しいかもしれない。規制手続きには、製造/試験施設検査、薬品輸入時のテスト、その他の国内要求も含まれる可能性がある。オーストラリアや日本などはより成熟した制度を持ち、より競争力のある時間枠で申請を提出することを許可している。生物模倣薬については、その中のいくつかの国に生物模倣薬を登録する経路(例えばオーストラリア、インド、シンガポール、韓国と台湾)があり、市場にはすでに生物類似製品(例えばオーストラリアと韓国)がある。
いくつかの国、例えば日本とEUでは、医療機器は規制制度の制約を受ける可能性があり、メーカーは彼らの医療機器が特定の機器カテゴリに対する法律の基本的な要求に適合していることを証明しなければならない。例えば,EUでは,限られた例外を除いて,市場に投入された医療機器は,法的要求に適合していることを示すためにヨーロッパ基準に適合したマークを持たなければならない。
承認後の段階
承認を得た後、我々の製品を使用した後に報告された有害事象および製品苦情を、通常の発売後のモニタリングと研究(適用される場合)によって監視し続けます。現地法規の要求に基づき,このような事件を適切な規制機関に報告し,個別事例とまとめ報告を報告する。我々は(良好な薬物警戒実践に基づいて)能動的にモニタリングし,我々の製品の使用に関連する可能性のある有害事象の信号検出,評価,コミュニケーションを実施することを確保した。私たちはまた、私たちの薬物送達設備に設備苦情、不良事件、故障が存在するかどうかを評価することを含む、私たちの品質システムを通じて製品苦情を能動的に監視します。規制当局はまた、私たちが発売した製品に対してさらなる臨床試験を行い、承認の条件として、あるいは安全性と有効性に関するより多くの情報を提供することを要求するかもしれない。FDAを含む衛生規制機関は、新たなセキュリティ情報に基づいて、または特定のカテゴリの製品が変化するラベルの一部として、製品ライフサイクルの任意の時点で製品のラベル変更を強制する権利がある。
FDAを含む衛生規制機関も、承認前と後に企業に製品のリスク管理計画を実施して、薬物のメリットがリスクよりも大きくなることを確保する権利がある。それぞれのリスク管理計画は唯一無二であり、必要な具体的な要素によって異なる。米国では,このようなリスク管理計画はREMSと呼ばれており,現在Prolia,Nplateに対するREMSがある BLINCETOと。
その他の法規
また,リベート法や虚偽申告法など,医療詐欺や乱用に関する様々な法律の制約を受けている。反リベート法は、州または連邦計画によって精算された特定の薬物の購入または発行を含む企業の転転を引換えまたは誘導するために、任意の報酬を請求、提供、受信または支払いすることが不法であると規定されている。虚偽クレーム−法律は、インフォームドコンセントおよび自発的な状況下で第三者支払者(MedicareおよびMedicaidを含む)に提出するか、または任意の虚偽または詐欺的な精算薬またはサービスクレーム、クレームに従って提供されていない物品またはサービスのクレーム、または医療上不要な物品またはサービスのクレームを提出することを禁止する。詐欺や法律違反行為は、罰金および民事罰金、連邦医療保険および医療補助を含む連邦医療計画(連邦医療保険および医療補助を含む)から除外される可能性がある刑事および/または民事制裁を受ける可能性がある。基礎製品に関連するいくつかの法律または法規(例えば、不正販売促進活動または不正支払いに関する違反)に違反して虚偽請求を提出した場合、虚偽請求法下の責任が生じる可能性もある。
2019年4月25日、私たちは、患者の経済援助を支援する独立した慈善団体が薬品を獲得することに関するいくつかの疑惑を解決するために、米司法省とHHSのOIGと和解合意に達した。また、5年以内に企業コンプライアンス計画を維持し、明確な企業誠実義務を負うことを求める企業誠実協定を締結しました。法律規定の広汎性と、私たちのいくつかのやり方に対する法規や裁判所の裁決形態の指導が不足しているため、私たちのやり方は将来的に反リベートまたは同様の法律のさらなる挑戦を受ける可能性がある
“海外腐敗防止法”は、米国の会社およびその代表が海外業務を獲得または保留するために、任意の外国政府官僚、政府職員、政党または政治候補者に金を提供、承諾、許可、または支払うことを禁止する。FCPAの範囲には,多くの国のある医療専門家とのインタラクションが含まれているといえる。他の国々も同様の反腐敗法律および/または法規を公布した。もし私たちの従業員、代理店、請負業者、サプライヤー、許可された人、パートナー、または協力者が“海外腐敗防止法”およびその他の反腐敗法律および/または法規を遵守できなかった場合、重大な民事または刑事罰を招く可能性がある。
私たちはプライバシーとデータ保護の面で世界の様々な法律法規によって制限されている。これらの法律法規は、個人データの収集、記憶、処理、使用、開示、送信、およびセキュリティに関する。プライバシーとデータ保護に関する立法と規制環境は絶えず変化と発展しており、これらの問題は世界各国でますます注目されているからである。例えば、2018年5月25日に発効するEU GDPR、2020年1月1日に施行されるCCPA、CCPAを改正し2023年1月1日に施行される2020年カリフォルニアプライバシー権法案、2021年11月1日に施行される中国個人情報保護法。私たちが業務を展開している他の管轄区域でも同様の法律および/または法規が制定または提案されている。 例えば、バージニア州、コロラド州、ユタ州、コネチカット州はその後、同様の消費者プライバシー法が成立し、これらの法律は2023年1月1日にバージニア州で施行され、2023年遅くにコロラド州、ユタ州、コネチカット州で施行される。このような法律を守らないことは深刻な処罰につながるかもしれない。
私たちの業務はアイルランド共和軍の規定を含む様々な他のアメリカと外国の法律、規則、規制によって拘束され続けている。上の精算部分を参照してください。
研究開発と選定された候補製品
私たちは重篤な疾患を治療する新しいヒト療法の開発に集中している。私たちはヒト遺伝学、新生物学、タンパク質工学の利点を利用しています我々は我々の生物学的専門知識を利用して,薬物標的と疾患のための最適なモデルを選択することを求めた。我々は先端科学と技術を用いて微妙な生物機序を研究し,疾患患者の生活を改善できる治療法を探している。
したがって,我々の発見研究計画は目標を生じる可能性があり,巨大分子,小分子,他の組み合わせモデルや新しいモデルの形でヒト療法を提供することが発展している。私たちは私たちのポートフォリオを再構築し、可能な状況でますます私たちの努力を人類遺伝学に集中させて、成功の可能性を高めている。
2021年初め以来、新冠肺炎の疫病をコントロールする努力はずっと行われている。しかし、大流行の持続的な発展の軌跡については、これらの活動の効力には依然として不確実性が存在する。ワクチン接種が直面している挑戦、新しい変種とウイルス伝播の他の原因は各国政府が異なる地区の制限と/或いは閉鎖要求を変える必要があるかもしれない。したがって,各国政府が現在の現地状況に反応するにつれて,少なくとも大流行期間中に疫病は持続的に変動することが予想される。われわれの臨床試験活動では,新変種の変化を含めて新冠肺炎感染率を継続的にモニタリングしており,われわれの臨床試験の将来の研究登録への影響を軽減するために努力しており,すべての関連国の影響を評価している。私たちは依然として私たちの活発な臨床サイトを支持して患者に看護を提供し、研究薬物の供給を提供することに集中している。
2022年、2021年、2020年12月31日までの年間、私たちの研究開発費はそれぞれ44億ドル、48億ドル、42億ドルです。
私たちは千樫市とカリフォルニア州サンフランシスコ、アイスランドとイギリスに大型研究開発センターを設置し、世界に小さい研究センターと開発施設を設置している。第2項.属性を参照.
我々の臨床試験活動は我々の内部従業員と第三者契約臨床試験サービスプロバイダが行った。われわれの臨床試験登録に利用可能な患者数と多様性を増加させるために,すでに臨床サイトを開設し,引き続き臨床サイトを開設し,複数の地理的位置で患者を募集する。臨床開発に対する政府の規制の検討については,政府規制−米国の規制−臨床開発と製品承認を参照されたい。また項目1 Aを参照。リスク要因-任意の候補製品や既存製品を新たな適応に適用し,商業化·販売する前に,人体で臨床試験を行わなければならない。
私たちのいくつかの競争相手は、私たちの既存製品や既存製品のための候補製品や新適応を開発している分野の研究開発に積極的に参加しています。例えば、私たちは他の臨床試験と条件を満たした患者を競争し、これはいくつかの臨床試験基準に適合する利用可能な患者の数を制限する可能性がある。私たちの候補製品の競争市場は市場に入るタイミングに大きく依存しています。早期参入は製品の受容度を獲得する上で重要な優勢があり、それによって製品の最終的な成功と利益に役立つ。したがって、場合によっては、私たちが製品を開発し、臨床テストを完了し、監督部門の許可を得て、商業ロット製品を市場に供給する相対速度は、私たちの競争地位に重要になると予想される。
内部研究開発仕事を通じて発生した候補製品とマーケティング製品以外に、著者らは会社を買収し、ある製品と研究開発技術権利を獲得し、許可し、そして第三者と研究開発手配を構築し、私たちの研究開発能力、製品パイプラインとマーケティング製品基礎を強化と多様化することによって、業界における私たちの戦略地位を強化し、多様化する。これらの研究開発手配や許可や買収活動を行う際には,他の製薬やバイオテクノロジー会社からの競争に直面しており,これらの会社も研究開発を行う実体から許可を得たり,技術,候補製品や市場製品を獲得したりすることを求めている。
次の表は,2023年1月31日現在,別の説明がない限り,我々のいくつかの候補製品が治療重点領域の開発段階で選択されていることを示している。もっと候補製品情報を知りたいのですが、私たちのサイトwww.amgen.comにアクセスしてください。(サイトアドレスはハイパーリンクとして利用する予定はなく,我々のサイトに含まれる情報も本出願の一部とする予定はない.本節の情報には,我々が行うことが可能な他の非登録臨床試験は含まれておらず,規制機関に新製品適応を承認するための提出は含まれていない。
実世界の結果を評価したり、製品使用に関する追加のセキュリティ情報を収集したりすることを含む、様々な理由で非登録臨床試験を行う可能性がある。
| | | | | | | | |
| 分子.分子 | | 調査性適応症 |
| 第3段階計画 | | |
| AMJEVITA | | 互換性 |
| Bemarituzumab | | GEJ腺癌 |
| BLINCETO | | PH陰性のB細胞前駆体急性リンパ球性白血病 |
| 事件.事件 | | 男性骨粗鬆症 |
| ケプロリス | | 再発性多発性骨髄腫の治療を毎週投与する |
| LUMAKRAS/LUMYKRA | | 末期結腸直腸癌 |
| ナンバープレート | | 化学療法による血小板減少症 |
| オルパシーランド | | 心血管病 |
| ウルトラツラ | | 生殖器乾癬 |
| 再修術 | | 心血管病 |
| Rocatinlimab | | アトピー性皮膚炎 |
| TEZSPIRE | | 慢性鼻−副鼻腔炎合併鼻ポリープ;好酸炎;重篤な喘息 |
| アブダビ654 | | Stelaraの研究生物と似ています |
| ABP 938 | | EYLEAに類似した研究生物(AfLibercept) |
| アブダビ959 | | Solirisと似た研究生物 |
| 第二段階計画 | | |
| エフバルキンアルファ | | 全身性エリテマトーデス |
| LUMAKRAS/LUMYKRA | | 非小細胞肺癌単一療法;他の固形腫瘍合併KRASG 12 C突然変異を起こす |
| Ordesekimab | | 乳糜潟 |
| Rozibafuspアルファ | | 全身性エリテマトーデス |
| Tarlaamab | | 小細胞肺癌 |
| TEZSPIRE | | 慢性閉塞性肺疾患 |
| AMG 133 | | 太っている |
| 第一段階計画 | | |
| Acapatamab | | 前立腺がん |
| Bemarituzumab | | 非小細胞肺癌や他の腫瘍は |
| Emirodatamab | | 急性骨髄性白血病 |
| Latikafusp | | 固形腫瘍 |
| Tarlaamab | | 神経内分泌前立腺癌 |
| AMG 104 | | 喘息.喘息 |
| AMG 119 | | 小細胞肺癌 |
| AMG 176 | | 悪性血液病 |
| AMG 193 | | 固形腫瘍 |
| AMG 199 | | 固形腫瘍 |
| AMG 340 | | 前立腺がん |
| AMG 404 | | 固形腫瘍 |
| AMG 509 | | 前立腺がん |
AMG 609 | | 非アルコール性脂肪性肝炎 |
| AMG 650 | | 固形腫瘍 |
| AMG 651 | | 結腸直腸癌 |
| AMG 786 | | 太っている |
| AMG 794 | | 固形腫瘍 |
| AMG 994 | | 固形腫瘍 |
| | |
| | | | | |
| 第3段階 | 臨床試験では,通常の治療法と比較して,研究中の疾患や状況を有する多くの患者におけるわれわれの候補製品の短期的および長期的安全性と有効性を調査した。 |
| 第二段階 | 臨床試験では,第1段階よりも多くの患者群における副作用プロファイルや候補製品の有効性が調査されたが,研究中の疾患や状況を有する患者は比較的少なかった。 |
| ステップ1 | 臨床試験は少数の人体被験者の中で候補製品の安全性と適切な投与量範囲を調査した。 |
第3段階製品候補計画変更
2022年2月8日まで、私たちは13の第3段階プロジェクトを持っている。2023年1月31日までに、私たちは18の第3段階プロジェクトがあり、5つのプロジェクトが第3段階研究を開始したからです。次の表にこれらの変更を示します。
| | | | | | | | | | | | | | |
| 分子.分子 | | 調査性適応症 | | 計画変更 |
| LUMAKRAS/LUMYKRA | | 末期結腸直腸癌 | | 第3段階研究を開始する |
| オルパシーランド | | 心血管病 | | 第3段階研究を開始する |
| ウルトラツラ | | 掌底部膿疱症 | | 第3段階研究を開始する |
| Rocatinlimab | | アトピー性皮膚炎 | | 第3段階研究を開始する |
| TEZSPIRE | | 好酸性食道炎 | | 第3段階研究を開始する |
第3段階製品候補特許情報
次の表は,これまで我々が第3段階で開発した候補製品に発行されてきた物質構成特許を紹介し,これらの特許は米国やEUでは何も承認されていない。米国またはEUで1つまたは複数の適応が承認されているが、現在より多くの適応が行われている第3段階臨床試験の製品の特許は先に記載されている。マーケティング、流通、選択された市場製品-特許を参照してください。
| | | | | | | | | | | | | | | | | | | | |
| 分子.分子 | | 領土.領土 | | 一般題材 | | 満期予定時刻* |
Bemarituzumab | | アメリカです。 | | ポリペプチド.ポリペプチド | | 2029 |
| ヨーロッパ.ヨーロッパ | | ポリペプチド.ポリペプチド | | 2029 |
| オルパシーランド | | アメリカです。 | | 化合物 | | 2036 |
| ヨーロッパ.ヨーロッパ | | 化合物 | | 2036 |
| Rocatinlimab | | アメリカです。 | | ポリペプチド.ポリペプチド | | 2027 |
| ヨーロッパ.ヨーロッパ | | ポリペプチド.ポリペプチド | | 2026 |
*特許満了推定は、競合他社の疑問、無効、または回避される可能性がある発行された特許に基づいています。推定数は、これらの日を延長するために、将来取得可能な任意の期限調整、延期、または補足保護証明書を含まない。該当する特許出願は他の司法管轄区域で決定されている。より多くの特許を出願または発行することができ、候補製品またはその使用に追加的な排他性を提供することができる。
第3段階と第2段階の計画説明
以下に人体臨床試験に入った選定候補製品に関するより多くの情報を提供する。
AMJEVITA
AMJEVITAはHUMIRAと類似した生物製剤であり、HUMIRAは腫瘍壊死因子αと細胞表面腫瘍壊死因子受容体/腫瘍壊死因子-αの結合を抑制できるモノクロナル抗体である。
Bemarituzumab
Bemarituzumabは線維芽細胞増殖因子受容体2 b(FGFR 2 B)を抑制するモノクロナル抗体である。進行胃食道接合部(GEJ)腺癌の治療に研究されている。
BLINCETO
BLINCETOは抗CD 19 x抗CD 3抗体である®分子です。40歳以上でPh陰性のB細胞前駆体急性リンパ球性白血病(ALL)を有する新診断成人が検討されている。
エフバルキンアルファ
Eavaleukinαはインターロイキン2突起変異体Fc融合蛋白の一種である。全身性エリテマトーデスや潰瘍性大腸炎の治療に研究されている。
事件.事件
EVENITYは硬化素作用を抑制するモノクロナル抗体である。それは男性の骨粗鬆症を治療する方法として評価されている。UCBと協力してEVENITYを開発している。
ケプロリス
Kyprolisは小分子プロテアソーム阻害剤である。レナドアミンとデキサメタゾンの併用による再発性多発性骨髄腫の毎週投与量を検討している。
LUMAKRAS/LUMYKRA
LUMAKRAS/LUMYKRASはKRASですG 12 C小分子阻害剤。非小細胞肺癌、結腸直腸癌、その他の固形腫瘍癌を含む様々な固形腫瘍の治療に研究されている。
2022年2月、著者らはLUMAKRAS/LUMYKRAS治療を受けたKRAS G 12 C変異末期膵臓癌患者におけるCodeBreaK 100 1/2期試験の治療効果と安全性データを発表した。
2022年4月、著者らはLUMAKRAS/LUMYKRAS治療を受けたKRAS G 12 C突然変異末期非小細胞肺癌患者におけるCodeBreaK 100 1/2期試験の長期治療効果と安全性データを発表した。
2022年8月、著者らは毎日1回LUMAKRAS/LUMYKRASを内服する全世界第三段階CodeBreaK 200試験がPFSの主要な終点に達したことを評価し、統計学的意義と標準治療化学療法とドセタキセル静脈注射より優れた優勢を示した。初のKRASの無作為臨床試験G 12 C阻害剤は345名の以前に少なくとも白金類二重化学療法とチェックポイント阻害剤治療を受けたKRAS G 12 C変異非小細胞肺癌患者におけるLUMAKRAS/LUMYKRASの有効性と安全性を評価した。
2022年9月、著者らは全世界の第三段階CodeBureaK 200試験の詳細な結果を発表し、この試験は静脈化学療法ドセタキセルと比べ、LUMAKRAS/LUMYKRASを毎日1回経口投与することによるKRAS G 12 C突然変異のNSCLC患者のPFS(主要な終点)とOOR(1つの肝心な副次終点)が明らかに向上したことを示した。著者らはまたその1 b期CodeBureaK 101研究の最新データを発表し、この研究はKRAS G 12 C突然変異結腸直腸癌患者に対する最も全面的な全世界臨床開発計画の一つである。これらのデータは、LUMAKRAS/LUMYKRASと安進会社の抗表皮成長因子受容体(抗EGFR)モノクロナル抗Vectibixを併用し、鼓舞的な有効性と安全性を示した。
ナンバープレート
ネプランはトロンボポエチン受容体アゴニスト(TPO-RA)の一種である。化学療法による血小板減少症(CIT)の治療に研究されている。
オルパシーランド
OlpasiranはLp(A)を低下させるsiRNAである。現在,ASCVDの治療を3期検討している。
2022年11月、Lp(A)レベルが150 nmol/Lを超え、ASCVDの病歴を有する成人患者のオパシランを評価する第2段階SEA(A)用量研究の陽性治療終了データを発表した。この研究は確定診断されたASCVD患者に対するオパシランのLp(A)の安全性、耐性と最適な投与量を評価することを目的としている。
Ordesekimab
OrdesekimabはIL-15作用を抑制できるモノクロナル抗体である。乳糜潟の治療に研究されており,Provention Bio,Inc.と協力して開発されている。
ウルトラツラ
OtezlaはPDE 4を抑制する小分子である。治療中の重度生殖器乾癬患者の3期研究中である。掌底膿疱症を治療する2期研究でも研究されている。
2022年9月,Otezla経口投与の2つの重要な3期臨床研究の結果を発表し,中から重度斑塊型乾癬を有する小児患者と中から重度生殖器乾癬を有する成人患者に対する効果を示した。
再修術
再修術 PCSK 9を抑制するヒトモノクロナル抗体である。現在、ASCVDを治療する1つの方法として、心臓発作或いは脳卒中病歴のない高密度リポ蛋白質コレステロールハイリスク患者に適用することが研究されている。
2022年には、Repatha OLE研究の結果を第3段階FOURIER CV結果試験に提出した。これらの研究は臨床で明らかなASCVD成人患者に対するRepathaの長期安全性と耐性を評価することを目的としている
Rocatinlimab
RocatinlimabはOX-40を抑制するモノクロナル抗体である。重度アトピー性皮膚炎の治療に研究されている。KKCと協力してRocatinlimabを開発している。
Rozibafuspアルファ
Rozibafusp alfaは新しい抗体-ポリペプチド結合体であり、B細胞活性化因子(BAFF)と共刺激リガンド(ICOSL)の活性を同時に遮断することができる。全身性エリテマトーデスの治療法として検討されている。
Tarlaamab
Tarlaatamabは半減期延長(HLE)の抗DLL 3 x抗CD 3抗体である®分子です。それは小細胞肺癌の治療に研究されている。
TEZSPIRE
TEZSPIREはヒトモノクロナル抗体であり、胸腺マトリックスリンポエチンの作用を抑制できる。重症喘息と慢性副鼻腔炎合併鼻ポリープの治療の3期研究として評価されている。慢性閉塞性肺疾患や慢性自発性蕁麻疹の治療の第二段階研究としても行われている。TEZSPIREはアスリーカンと協力して開発している。
2022年2月,キーナビゲーション段階3と経路段階2 b試験を併用した分析結果を発表した結果,TEZSPIREは重篤な喘息患者のバイオマーカー亜群の経年化喘息増悪率(AAER)の低下を示した。
好酸性食道炎患者におけるTEZSPIREの3期研究が開始されている。
AMG 133
AMG 133は胃抑制ポリペプチド受容体(GIPR)拮抗薬とグルカゴン様ペプチド1(GLP-1)受容体アゴニストの一種である。肥満の治療の研究に使われています
アブダビ654
ABP 654はStelara生物と類似した候補であり、IL−12とIL−23を抑制するモノクロナル抗体である。それはStelaraとの生物学的類似性を決定するために第3段階の研究を行っている。参考製品の主な疾患は乾癬,乾癬関節炎,クローン病である。
2022年4月、著者らは治療中の重度斑塊型乾癬成人患者におけるABP 654とStelaraの有効性と安全性を評価する第3段階研究の初歩的な結果を発表した。この研究は主要な治療効果の終点を達成し,ABP 654とStelaraは臨床的に有意差がないことを示唆している。
ABP 938
ABP 938は1種の血管内皮増殖因子受容体(VEGFR)Fc融合蛋白であり、EYLEAと生物類似性を有する。EYLEAとの生物学的類似性を決定するために第3段階の研究を行っている。参考製品の基本は湿性年齢関連性黄斑変性(AMD),網膜静脈閉塞後の黄斑浮腫,糖尿病黄斑浮腫と糖尿病網膜症である。
アブダビ959
ABP 959はSoliris生物に類似した候補抗体であり、補体蛋白C 5に特異的に結合できるモノクロナル抗体である。それはSolirisとの生物学的類似性を決定するために第3段階の研究を行っている。参考製品の基本条件はPNHと非典型溶血性尿毒症症候群(AHUS)である。
2022年8月、著者らはDahlia研究の正の結果を発表し、これはランダム、二重盲検、積極的対照、二期交差の第三段階研究であり、成人PNH患者におけるSoliris生物に類似した候補薬物ABP 959とSolirisの治療効果と安全性を評価した。
業務関係
私たちは時々、合弁企業と協力手配を含む、製品および/または候補製品の研究開発、製造および/または商業化について業務関係を構築する。また、私たちは製品と研究開発技術の権利を獲得し、第三者と研究開発協力を構築し、私たちの研究開発能力、製品パイプラインと市場製品基礎を強化し、多様化することによって、業界における私たちの戦略的地位を強化する。これらの手配は、通常、払い戻し不可能な前払い許可料、開発および商業業績マイルストーン支払い、コスト分担、印税および/または利益共有を規定する。これらの協力協定の下での活動は,技術やビジネスの成功を保証することなく行われ,すべての活動は唯一無二である.
私たちの非特許機密と固有情報の商業秘密保護は私たちに重要だ。私たちのビジネス秘密を保護するために、私たちは通常、取引相手が私たちと業務関係を始める時に秘密保持協定に署名することを要求します。しかし、他の人たちは同じまたは類似した情報を独立して開発したり、私たちの情報を不正に取得したりするかもしれない。
百済神州株式会社です。
2020年1月には、中国腫瘍科業務の拡大の一環として、百済神州の株式を約28億ドルの現金で買収した。百済神州への株式投資についての詳細は、連結財務諸表第4部-付記9投資を参照されたい。協力の下、百済神州は2020年に中国でXGEVAの販売を開始し、2021年にBLINCYTOの販売を開始し、2022年に中国でKyprolisを販売し、最初の特定製品の商業化期間中に安進二等分損益を販売し、その後、製品権利は安進に回復する可能性があり、安進は特定の期限内に百済神州に同製品が中国で販売されている特許権使用料を支払う。安進は百済神州に協力製品を製造し、提供した。
また,百済神州と共同で我々腫瘍学ポートフォリオの一部を開発し,後者は12.5億ドルまでの現金と開発サービスを提供することで世界の研究開発コストを分担した。監督部門の許可を得た後、百済神州は特定の期間内に中国の商業化権利を負担し、安進と百済神州は利益を折半し、これらの製品権利のいくつかの権利が安進の手に戻るまで。製品権利返還後、安進は百済神州に特定期間内に中国で販売される特許権使用料を支払う。中国以外の製品販売については、安進は百済神州に特許使用料も支払う。
アスリーカン
私たちはアスリカンと協力してTEZSPIREを開発し、商業化している。私たちの協力の下で、アスリコンが安進に1桁の中央値特許権使用料を支払った後、両社は世界コストと利益と損失を折半した。アスリコンは全世界の発展をリードし、安進とアスリコンは共同でTEZSPIREを北米で商業化した。北米では安進が元金としてTEZSPIREの米国での製品販売を確認し,アスリコンが元金としてTEZSPIREのカナダでの製品販売を確認した。アスリカンは北米以外でのTEZSPIREの商業化のトップである。安進はTEZSPIREを世界で製造し供給している。
連合信用銀行
我々はUCBと協力してEVENITYを開発し,商業化している。私たちの協力の下で、連合銀行はヨーロッパの大部分の国と中国(香港を含まない)でのEVENITYの商業化をリードする権利がある。安進は責任者として、EVENITYの商業化をリードし、米国を含む他のすべての地域での製品の販売を認めている。協力に関するグローバル開発コストと商業化損益が二分されている。安進は世界的にEVENITYを製造し、供給している。
我々の重要な連携手配の財務情報については、連結財務諸表の第4部である付記8“連携”を参照されたい。
人的資本資源
概要
安進の人力資本資源管理方法は著者らが患者にサービスする使命から始まった。科学とバイオテクノロジーの約束を健康回復や生命を救う能力のある療法に変えることで患者に奉仕するように努力している。私たちのビジネス方式は私たちの安進価値観を指導しています
| | | | | | | | | | | |
安根値 |
科学を基礎とする | 熾烈な競争に勝つ | 患者、従業員、株主のために価値を創造する | 道徳的な人になる |
相互信頼、相互尊重 | 品質を確保する | チームワーク | 協力、コミュニケーション、責任 |
私たちの従業員も、世界中で業務を展開しているすべての人(すべての従業員、管理職、コンサルタント、契約社員、およびアルバイトを含む)を代表して彼らへの期待を理解することを目的とした会社の行動基準に従っています。
私たちの産業は複雑な規制と精算環境に存在する。私たちの業界の独特な需要と、革新薬物の発見、開発、製造と商業化に専念する企業を経営する挑戦は、高度に参加し、責任を果たす従業員チームが必要である。
安進は2022年12月31日現在、50以上の国·地域に約25,200人の従業員を有しており、既存の業界情報に比べて世界的な離職率が相対的に低い。私たちはまた必要に応じて独立請負業者、アルバイト、アルバイトで私たちの労働力を補充します。アメリカ以外で、私たちの何人かの従業員たちは労働組合や労働組合によって代表されている。我々のスタッフ関係が良好であることは,幅広いテーマ(柔軟な作業環境,多様性,包摂性,帰属感,コンプライアンス文化の維持を含む)に関連したスタッフ敬業度調査の定期的な評価の支持を得ていると考えられる。私たちは職員たちと取締役会とこのような調査の結果について議論する。新冠肺炎に関する制限の緩和とサイトのアクセスが容易になるにつれて、私たちの従業員は仮想仕事の柔軟性を維持したいと思って、私たちは多くの従業員が彼らのマネージャーと一緒に彼らの手元の仕事に最適な位置を確定することができ、仮想仕事をサポートし、現場仕事もサポートできるように柔軟な作業空間計画を実施した。
報酬、福祉、発展
著者らは従業員の報酬と福祉に対するやり方は生物技術と製薬業界のリード会社が提供する計画と競争する現金、株式と福祉計画を提供し、そして人材を誘致、激励と維持し、重点的に業績を奨励し、責任を促進し、会社の価値観を遵守し、そして会社の株主の利益と一致することを目的としている。
私たちの基本給プログラムは、各ポストを履行するために必要なスキル、知識、能力、および仕事にもたらす経験を考慮したスタッフの役割貢献価値に応じて補償することを目的としています。私たちはまた、当社の従業員を奨励し、会社の範囲内の目標を達成するための年次インセンティブ計画を提供しており、これらの目標は、当社の戦略的優先順位の様々な側面を推進し、当社全体の戦略を支援し推進することを目的としています。私たちのほとんどの従業員も、私たちの長期インセンティブ計画に基づいて配当金を得る資格があります。この計画は、私たちの従業員の利益を私たちの株主の利益と一致させることを目的としています。高級従業員にとって、株式奨励価値の大部分は会社の業績に基づいている。
すべてのスタッフはまた定期的な業績測定プログラムに参加し、このプログラムを通じて、従業員は業績と発展フィードバックを受け、報酬は業績と関連している。安進の価値観と指導行為は私たちの従業員業績評価の構成部分であり、これらの評価は給与決定の重要な情報ツールと基礎である。
我々従業員の発展を支援するために,リーダーシップ開発計画,授業や仮想講師指導に基づく授業,カスタマイズ進捗の学習オプション,指導,ネットワーク,指導機会など様々な計画を提供している.
私たちの福祉計画も一般的に広く、健康と全体的な福祉を促進し、退職貯蓄として強調されている。すべてのアメリカの正式なスタッフは同じ核心健康、福祉、退職貯蓄計画に参加する資格がある。他の米国人従業員福祉には、医療計画、歯科計画、養子縁組援助、有給育児休暇計画、児童保育、従業員援助計画、従業員株式購入計画、柔軟な支出口座、生活、長期介護、ビジネス旅行意外保険、短期および長期障害福祉、健康福祉、および仕事-生活資源および転職が含まれる。類似した計画や福祉は世界的に得られ、同じ健康と福祉の意図を持ち、法定要求と一致している。
私たちの給与と管理開発委員会は私たちの報酬計画、政策、そして計画を監督する責任がある。
安全と健康そして進化し続ける新冠肺炎の大流行への対応
私たちの従業員のために安全で健康な職場を作ることは安入の重要な優先順位だ。我々の目標は,セキュリティリーダー,リスク管理実践,セキュリティを我々のワークフローに統合することで,世界的なセキュリティ記録を持つことである.私たちの安全文化を育成するために、私たちは全面的な安全計画を実施し、予想される安全行為を強化し、安全事件の根本的な原因を理解し、減少させ、変異性を管理·制御した。我々は先行指標を用いて我々の安全計画の有効性を評価し,必要に応じて針路修正を行う.また、著者らは四半期ごとに運営、全世界の商業運営と研究開発の機能安全業績に対して正式な実行管理層審査を行い、重点的に早期信号を識別し、行動を取って持続的な改善を推進することである
2022年、新冠肺炎疫病の絶えずの変化に対応するため、安入地点にもっと大きな柔軟性と効率を高めると同時に従業員の安全を維持するために、著者らは分散した新冠肺炎意思決定モードに転換し始め、現地チームが現地法規と現地疫学標準のリスク評価に基づいて、それぞれの場所或いは地区の新冠肺炎安全ガイドライン(例えばマスクとその他の個人防護用品の使用、入居制限、温度測定と測定)を調整することを許可した。私たちは未来の必要性に適応するためにこの方法を学習して調整し続けるつもりだ。
私たちの企業責任とコンプライアンス委員会は私たちの安全計画と計画を全面的に監督し、私たちの取締役会は全体として私たちの新冠肺炎疫病に対する具体的な対応を監督する。
多様性、包括性、帰属感
私たちは、多様性と包括的な文化が革新を促進し、これは私たちが患者にサービスする能力を支持すると信じている。また、私たちのサービスの患者の多様性を反映した従業員チームを持つことで、世界的な業務が強化されると信じています。このような信念を持って、私たちは私たちの多様性、包容性、そして帰属感文化を強化し、発展させ続けている。私たちの多元化、包括性と帰属感理事会は私たちの行政指導者が指導し、私たちの多元化と包括的な職場を促進する戦略を監督する。我々は,様々な多様性,包括性,帰属感訓練や学習計画を提供し,強化されたツールや資源を導入し続け,組織全体が多様性,包摂性,帰属感を創造する上でスタッフの役割を指導している。また,臨床試験設計,調達,立地を含めて多様性,包括性,帰属性を我々の業務運営に取り入れていきたい。
安進の各従業員資源グループは上級管理指導部によって賛助されている。私たちの従業員資源グループは、メンバーのリーダーシップ、発展、帰属感を促進するとともに、業務計画を指導し、異なる視点と経験を提供することで、私たちの業務に影響を与えるように努力しています。2022年、安進は原住民、価値観、環境資源、あるいは川を認め、原住民の伝統、価値観、文化を共有し、継続するという最新の全世界従業員資源グループを設立した。
| | | | | |
グローバル従業員リソースグループ |
| 安進アジア協会(AAA) | 黒人従業員ネットワークに入って(アベン) |
| リーダーシップと教育改善能力(ABLE)により、見える障害者や見えない障害者に資源を提供する組織であり、安進サービスを含む患者も経験している |
| 安進職業初期プロ(AECP) | 安進国際ネットワーク(AIN) |
| アンインラテン従業員ネットワーク(ALEN) | LGBTQおよび盟友ネットワーク(PROID)に安進 |
| 安進南アジアネットワーク(ASAN) | 安進退役軍人従業員ネットワーク(AVEN) |
| 先住民、価値観、環境資源(川)を認める |
| 権力を与えられて非凡な女性(WE 2) | STEM増収中の女性(WISE) |
私たちの年間インセンティブ計画の下で2021年のESG目標の採用に成功した上で、2022年に強化されたESG目標を通じて、組織においてリーダー所有権と多様性、包摂性、帰属感に対する責任をより深く推進し、多様性、包括性、帰属感行動計画の策定、記録および実行を担当する指導者数を拡大することを含む、重要なESGイニシアティブの進展を推進している。
2022年12月31日現在、女性は世界の労働力の52%以上を占め、少数族は私たちのアメリカとプエルトリコの労働力の約52%を占めている。代表性が不足している分野では,我々の代表性と獲得可能性を一致させることを目標とした計画を立てた.私たちは外展の仕事に力を入れて、より多くの女性と少数民族を誘致、維持と抜擢して私たちの仕事チームに参加します。例えば、私たちは、全国黒人MBA協会や工学女性協会、歴史上の黒人学院や大学のような多様な候補者源となることができる組織との関係を強化するために、多様な候補者募集庫を強化してきた。2021年、安進とハワード大学は人材バンクを拡大し、研究開発チームを多様化させる奨学金計画を設立した
また、私たちはOneTenの創設メンバーの一人で、OneTenは世界最大で最も有名な会社の連合で、今後10年以内に100万人のアメリカの黒人(特に4年間の大学学歴のない人)を高給、家族を養う仕事に従事することを目標としています。安進は、OneTen組織の連合の拡大を支援するために、本社がある大ロサンゼルス地域でリーダーシップを発揮しており、これらの組織は、私たちと同様に、異なる人材に機会を提供したいと思っており、OneTenコミットメントを支援するための内部見習い計画を策定しています。私たちがこの分野でとっている他の行動は、医療業界の女性企業家協会(Healthcare Business Women‘s Association)(医療業界の女性発展とビジネスネットワークに集中したグローバル組織)への投資と参加と、女性や不足を代表する人材に対するカリフォルニア大学ロサンゼルス校アンダーソン管理学院(UCLA Anderson School Of Management)のリーダーシップ向上計画を含む。
私たちの2021年総合EEO-1報告は私たちのサイトwww.amgen.comで見ることができます(サイトアドレスはハイパーリンクとして使うつもりはなく、私たちのサイトに含まれている情報も本ファイルの一部とするつもりはありません)。
2022年、私たちの給与·管理開発委員会は、多様性、包括性、帰属感に関する政策、案、イニシアティブを含む、私たちの労働·雇用政策、プログラム、イニシアティブを監督します。
私たちの執行官に関する情報は
当社の2023年2月9日までの幹部リストは以下の通りです
ホワイトドウェイさんは現在60歳で、2011年から当社の取締役を務め、2013年から取締役会の議長を務めている。ホワイトドウェイさんは2010年から当社の社長を務め、2012年から当社の最高経営責任者を務めている。2010年から2012年にかけて、ホワイトドウェイ·さんは当社の総裁兼最高経営責任者を務めた。ホワイトドウェイさんは2006年に入社し、運営戦略副総裁を務め、2007年から2010年まで執行副総裁兼首席財務官を務めた。当社に入社する前に,Bradwayさんはロンドンのモルガン·スタンレー法律事務所の取締役社長であり,2001年からヨーロッパにおける銀行部や企業融資活動を担当しています。ブラッドウェルは2016年以来、ボーイング社の役員社員である。ボーイング社は航空宇宙会社で、商用飛行機、国防、宇宙、安全システムを生産している。2014年以来、南カリフォルニア大学の取締役会のメンバーを務めてきた。ブラッドウェイは2011年から2017年まで、運送会社ノーフォーク南方社の役員社員だった。
さん·ムルド·ゴードンは、56歳で、2018年にグローバルビジネス運営実行副社長になりました。Gordonさんは、当社に入社する前に、2016-2018年の間に、製薬会社百時美施貴宝(BMS)の首席ビジネス官を務めました。ゴードンは2015年から2016年までBMSグローバル市場部の主管を務めていた。これまで、ゴードン·さんはBMSで25年以上にわたって様々な指導者を務めてきました。
ジョナサン·P·グレアムさんは62歳で、2019年に常務副秘書長、法律顧問総総裁に就任しました。グレアムは2015年に同社に入社した。2015年から2019年にかけて、グラハム·さんは上級副総裁兼法律顧問兼事務総長を務めています。アンインに加入する前に、グラハム·さんは、2006年から2015年まで、デンナハ社の上級副社長兼総法律顧問を務めていました。2004年から2006年まで、グレアム·さんはゼネラル·エレクトリック社において訴訟·法律政策部の副主任を務めている。ゼネラル·エレクトリックに参入する前にグレアムはWilliams&Connolly LLPのパートナーであった。
ピーター·H·グリフィスさんは現在64歳で、2020年には執行副総裁兼最高財務責任者に就任します。グリフィスさんは、財務執行副社長を務める2019年に当社に参加しました。アンインに加入する前に、グリフィスさんは、私募株式会社シャーウッド·キャニオンの有限責任会社の社長です。1997年から2019年までの間、グリフィスさんは会計·プロフェッショナル·サービス会社のパートナーであり、様々な上級指導者の職を務め、最後にはグローバル副社長であり、企業開発を担当するポストです。安永に入社する前に、グリフィスさんは取締役社長とウェドブッシュ証券会社投資銀行部の責任者であった。
55歳のナンシー·A·グリギルは2020年に上級副総裁兼首席コンプライアンス官になった。グリジルさんは2015年に同社に入社した。2016年から2020年まで、グリジルさんはコンプライアンス総裁副主任を務めた。入社前、2011年から2015年まで、グリジルさんはエル建会社でコンプライアンス、企業、国際副総裁を務めていた。Allerganに加入する前に、GrygielさんはMylan製薬会社でいくつかの管理職を務めた。
現在50歳のラチナ·コスラは2021年に高級副総裁となり、業務発展を担当している。コスラさんは2013年に入社し、企業開発役員を務めた。2018年から2021年まで、コスラさんは副総裁を務め、業務発展を担当し、2016年から2018年にかけて、役員幹部を務め、業務発展を担当している。当社に入社する前、コスラさんはラザド株式会社(ラザド)の役員主管で、ヘルスケアM&Aを担当していました。Lazardに加入する前、コスラはスイスの信用グループ、セノフィアンバンテ、アンバンテ資本、モルガン大通、ソロモン兄弟会社で様々な職務を担当していた。
デレク·ミラーさんは、現在50歳で、2022年に人的資源省の上級副社長になります。Mr.Millerは2003年に入社し,会社の各主要業務機能を支援する人的資源指導職を務めた。Mr.Millerは2020年から2022年まで全世界総奨励部副総裁を務め、2018年から2020年までは人的資源部副総裁を務める。2015年から2018年まで、Mr.Millerは取締役人事幹部を務めた。Mr.Millerは2015年までに人的資源組織でシニアマネージャーを務め,その後取締役,人的資源部に昇進し,戦略取締役に昇進した。
David·M·リス博士は、現在60歳で、2018年に研究開発部門常務副総裁となった。リース博士は2005年に入社し、開発、医学科学、発見研究で指導職を務めた。リス博士は2017年から2018年まで翻訳科学と腫瘍学主任の高級副総裁を務め、2015年から2017年まで翻訳科学主任の高級副総裁を務めた。安進に加入する前に、リス博士は2001年から2003年まで乳癌国際研究グループの臨床研究の取締役主任を務め、2003年から2005年まで非営利性学術臨床研究組織である国際翻訳腫瘍学研究会社の共同創業者兼首席医療官を務めた。リース博士は以前カリフォルニア大学ロサンゼルス校とカリフォルニア大学サンフランシスコ校で教えていました。
エステワン·サントスは現在55歳で、2016年に運営執行副総裁となった。サントスさんは2007年に入社し、製造技術省役員を務めている。サントスは2013年から2016年まで製造業の上級副社長だった。サントスさんは、2008年から2013年にかけて、エンジニアリング、製造、オンサイト運営、医薬品生産に関わる複数の副社長を務めました。サントスさんは当社に入社する前に、プエルトリコでジョンソン(ジョンソン)コーディスの現場社長を務めていました。ジョンソンに加入する前に、サントスは汎用電気の工業や輸送業務でいくつかの管理職を務めていた。
地理地域金融情報
我々が経営している地理的地域の財務情報については、連結財務諸表の第4部である付記3(収入)と付記11(財産、工場、設備)を参照。
投資家情報
私たちの財務やその他の情報については、私たちのサイトwww.amgen.comにアクセスしてください。これらの資料を電子的に米国証券取引委員会(米国証券取引委員会)に提出または提供した後、合理的で実行可能な範囲内で、当社の年間報告書(Form 10-K)、四半期報告(Form 10-Q)、現在の報告(Form 8-K)、および取引法第13(A)または15(D)節に基づいて提出または提供される報告をできるだけ早く無料で提供します。しかも、私たちは以前にアメリカ証券取引委員会に登録声明と他の文書を提出した。私たちが提出したどんな書類もアメリカ証券取引委員会のウェブサイトwww.sec.govで無料で閲覧できます。(これらのサイトアドレスはハイパーリンクとして利用するつもりはなく,我々のサイトや米国証券取引委員会サイトに含まれる情報も本届出文書の一部とする予定はない
この報告書と私たちがアメリカ証券取引委員会に提出した他の文書は、私たち、私たちの未来の業績、私たちの業務、私たちの信念、および私たちの経営陣の仮定に対する現在の予想、推定、予測、および予測に基づく前向きな声明を含む。これらの陳述は未来の業績の保証ではなく、いくつかの予測困難なリスク、不確定要素、仮説に関連している。あなたは私たちの業務が直面している危険と不確実性を慎重に考慮しなければならない。以下に説明する危険は私たちが直面している唯一の危険ではない。私たちの業務は、雇用関係、全体的な経済状況、地政学的事件、国際業務など、多くの他社のリスクに影響を与える影響を受けています。さらに、私たちは現在知られていないか、または現在重要ではないと考えている追加リスクは、将来的に私たちの業務、運営、流動性、および株価に大きな悪影響を及ぼす可能性がある
要約.要約
新冠肺炎の大流行中に含まれる経済状況とグローバル業務の経営に関連するリスク
•新冠肺炎の大流行及び公衆と政府が疾病伝播を抑制するための努力は、すでに著者らの臨床試験、運営、製造、サプライチェーン、流通システム、製品開発、製品販売、業務と運営結果に不利な影響を与え、実質的な悪影響を与える可能性があると予想されている。
•私たちの情報技術システムの崩壊、ネットワーク攻撃、または情報セキュリティホールは、私たちの情報技術システム、ネットワーク制御システム、および/または私たちのデータのセキュリティ、完全性および可用性を危険にさらし、私たちの業務運営を中断し、および/または私たちの名声に影響を与える可能性があります。
•私たちの販売と運営は新興市場を含めて国際業務リスクの影響を受けている。
政府法規と第三者政策に関連するリスク
•私たちの販売は政府と商業第三者支払者の保証と精算に依存しており、定価と精算圧力はすでに私たちの収益力に影響を与え続けている可能性があります。
•様々な組織が発表したガイドラインと提案は私たちの製品の使用を減らすことができます。
•新しい税法を採用して説明したり、追加の税務負担を負担したりすることは、私たちの収益性に影響を及ぼすかもしれない。
•私たちの業務は訴訟と政府調査の影響を受けるかもしれない。
競争に関連するリスク
•私たちの製品は激しい競争に直面しており、私たちの候補製品も激しい競争に直面しているかもしれません。
•私たちの知的財産権の地位は挑戦、無効、または回避されるかもしれないし、私たちは現在と未来の知的財産権訴訟で勝つことができないかもしれない
•我々は現在,生物模倣薬と後発薬からの競争に直面しており,将来的には生物模倣薬と模倣薬からの日々の激しい競争に直面することが予想される。
•販売が私たちのある卸売業者、流通業者、個人支払者に集中している合併は私たちの業務にマイナス影響を与える可能性があります。
研究開発に関わるリスク
•私たちは研究開発に多くの資金を投入しているにもかかわらず、私たちは商業製品を開発できないかもしれない。
•任意の候補製品や既存製品を新たな適応に適用し,商業化·販売する前に,人体で臨床試験を行わなければならない。
•私たちの現在の製品と開発中の製品は規制部門の承認なしでは販売できません。
•私たちのいくつかの製品は薬物送達またはセット診断装置と一緒に使用され、これらの設備自体に監督、製造、その他のリスクが存在する。
•私たちのいくつかの薬品パイプラインや商業製品販売は第三者との協力に依存しており、これは私たちの製品の開発と販売に悪影響を及ぼす可能性があります。
•他の会社、製品または技術と協力したり、他社、製品または技術を買収したりする努力、および会社が買収した製品や技術を運営または支援する努力を統合することは、成功しない可能性があり、予期しないコスト、遅延、失敗を招き、取引のメリットを実現できない可能性がある。
運営に関するリスク
•私たちの大部分の商業製造活動はアメリカプエルトリコにある工場で行われ、私たちの臨床製造活動の大部分はカリフォルニア州千樫市にある工場で行われています。これらの施設の深刻な中断や生産故障は私たちの製品を供給したり、臨床試験を継続する能力を深刻に弱めるかもしれません。
•私たちの特定の原材料、医療機器、そして部品は第三者供給者たちに依存している。
•製造困難、中断、遅延は私たちの製品の供給を制限し、私たちの製品の販売を制限するかもしれません。
•私たちの業務と運営は、私たちの環境、社会、そしてガバナンス目標を達成できなかったり、失敗したと思われたりすることによってマイナスの影響を受ける可能性があります。
•世界的な気候変動や関連自然災害の影響は、私たちの業務や運営に悪影響を及ぼす可能性がある。
一般リスク因子
•世界的な経済状況は私たちに否定的な影響を与える可能性があり、私たちの業務に影響を及ぼすいくつかのリスクを拡大する可能性がある。
•私たちの株価は変動が大きい。
•私たちは私たちに有利な条項で資本と信用市場に入ることができないかもしれないし、全く入らないかもしれない。
新冠肺炎の大流行中に含まれる経済状況とグローバル業務の経営に関連するリスク
新冠肺炎の大流行及び公衆と政府が疾病伝播を抑制するための努力は、すでに著者らの臨床試験、運営、製造、サプライチェーン、流通システム、製品開発、製品販売、業務と運営結果に不利な影響を与え、実質的な悪影響を与える可能性があると予想されている。
2019年末に発見された新型コロナウイルスSARS-CoV-2はこのような新冠肺炎と呼ばれる疾病を招き、それは持続的な全世界の大流行であり、公共と政府が疾病の伝播を抑制或いは緩和する努力を招き、広範な現地避難令、社会距離干与、隔離、旅行制限と各種形式の運営閉鎖を含む。新冠肺炎の大流行とそれに伴う対応は、我々の業務(私たちの研究開発、臨床試験、運営、製造、サプライチェーン、流通システム、製品開発と販売活動を含む)、業務活動と
私たちのサプライヤー、顧客、第三者支払人、そして私たちの患者。参照してください現在の製品と開発中の製品は監督部門の許可を得て販売してはいけません; また見られる私たちは人体で臨床試験を行ってから、私たちの任意の候補製品あるいは新しい適応のための既存製品を商業化して販売することができますそれは.疫病とこれらの措置とその影響により、私たちはすでに私たちのある製品に対する予測できない需要低下を経験し続けることが予想され、新冠肺炎の急増はある地域の繰り返し閉鎖と/あるいは中断を招いて需要低下を悪化させた。
連邦、州と地方及び国際政府は新冠肺炎伝播を減少させるための政策と計画もまた診断、選択、専門とその他の手続きと予約のキャンセル或いは遅延を招き、不必要な患者が医療環境に暴露され、潜在的な新冠肺炎感染を回避し、そして限られた資源と人員を新冠肺炎の治療に集中する。例えば、米国国家公共放送局とハーバード大学が2021年に行った世論調査では、病院が新冠肺炎でいっぱいになるにつれて、米国の家庭の5分の1が深刻な病気の看護を延期せざるを得ないことが分かった。これらの措置と挑戦は異なる程度で継続し、患者が私たちのいくつかの薬物を獲得し、管理することを著しく減少させるかもしれない。例えば,Proliaは医療提供者に医師室や他の新冠肺炎の影響を受けるヘルスケア設置で管理することが求められている。Proliaの米国タグは,医療提供者からの投与を必要としない口腔治療を含むProliaの医療専門家の使用停止を指示し,患者を代替抗吸収薬に移行させる。また,新冠肺炎の存在により,腫瘍患者は医師に相談した後,免疫抑制の程度の低い療法や病院環境下で服用する必要のない療法を選択する可能性があり,いくつかの製品の販売に悪影響を及ぼす可能性がある。また,大流行期間中には,新患者が診断および/または治療を開始される可能性は低く,継続することが予想され,これらの影響は,大流行期間中の低い治療率に加え,すでにわれわれの業務のビジネス業績に累積的な負の影響を与えることが予想される。大流行期間中の確定診断例の減少は治療を開始した新患者数を抑制した, 私たちはこれが私たちの業務に引き続き影響を及ぼすと予想している。新冠肺炎感染率の消長に伴い,周期的に蓄積している患者が様々な医療条件に関連した医師の予約を求める可能性が予想されるため,我々のある製品を用いた治療を求める患者は,低いプロバイダ能力で対応せざるを得ない可能性があり,このような低いプロバイダ能力が販売に持続的な悪影響を及ぼす可能性がある。また,新冠肺炎の大流行の影響は,医療専門家や患者の医療専門家の管理や医療機関訪問を必要としない治療に対する選好を長期的に変化させる可能性がある。
大流行の継続に伴い、状況が悪化した場合、あるいは大流行の持続時間が著しく延長されれば、私たちの発展、業務と商業活動、顧客調達、私たちの売掛金入金により多くの悪影響を及ぼすことが予想される。状況が改善され始めるにつれて、これらの悪影響が私たちの将来の運営と商業活動、顧客購入と私たちのコレクションにどの程度影響するかは、現在のところ確定していない。2022年、新冠肺炎感染は複数の司法管轄区で息を吹き返し、アメリカ、ヨーロッパ、アジア太平洋地域を含むいくつかの司法管轄区はより厳格な制限と閉鎖を回復した。大流行は引き続き起伏が定まらず、大流行期間中、異なる司法管轄区の感染レベルは他の司法管轄区より高いと予想される。SARS−CoV−2ウイルスの新たな変種はすでに出現しており,Delta型やオミック変異型とその亜変異型を含め,多くの地域に存在することが証明されており,他の変種よりも容易かつ迅速に伝播しているようである。また、いくつかの研究により、現在許可されているワクチンから産生された抗体はこれらの変種に有効である可能性があるが、現在利用可能なワクチンが未来のウイルス変種に対する効力を維持するかどうかはまだ確定していない。また,ある患者がワクチンを接種することができても,持続的なワクチン接種をためらうことで接種不足になる可能性があり,新冠肺炎の大流行の持続時間を延長し,我々のサービスを妨害し続ける患者が受ける医療サービスを妨害し続ける可能性がある。管轄区域は国境閉鎖を実施、継続、または回復することができます, 長期隔離を実施または再実施し、旅行や商業活動をさらに制限する。これらの措置は、私たちの運営と顧客を支持する能力、および私たちの従業員が職場で私たちの候補製品と製品を発見、研究、開発、生産する能力に著しく影響し、サプライチェーンにおける私たちの製品の移動を妨害し、さらに患者が私たちの臨床試験に参加し、医療サービスを求め、私たちのいくつかの製品を管理することを阻止または阻止するかもしれない。新型肺炎の流行に対応するため、遠隔作業手配の可用性が増加し、私たちの従業員と応募者を競争できる会社池を拡大した。さらに、世界での新冠肺炎の爆発と蔓延、および必要な医療製品のより広範な供給を増加させるために、私たちまたは私たちのサプライヤーが選択するかもしれない、あるいは政府は私たちの正常な運営、顧客関係、財務業績に悪影響を与えるように私たちまたは私たちのサプライヤーに不利な方法で生産能力を構成することを要求するかもしれない(例えば、アメリカ国防生産法に基づく)。米国では、2021年1月21日、バイデン総裁は、連邦機関に“国防生産法案”を含むすべての利用可能な法的権力を利用して、現在と未来の大流行対応と生物脅威準備を改善するよう指示する行政命令を発表した。新冠肺炎の治療と予防の資源の迅速な再分配(新冠肺炎ワクチンまたは関連療法の生産、例えば礼来社のための新冠肺炎抗体療法の生産に同意することを含む)および/または大流行はグローバルサプライチェーンの中断および不足をもたらし、開発、製造に使用される材料または部品の競争の激化または減少を招く可能性もある, 私たちの製品を扱ったり管理したりします。例えば、2021年第2四半期に、私たちの活動を支援するために必要ないくつかの実験室キット用品は業界全体で不足しています
臨床試験が発展し、私たちは積極的に監視して管理している。我々のスタッフに新冠肺炎抗原迅速検査キットを提供することを含む、いくつかの新冠肺炎に関連する物資の獲得にも挑戦しており、これはオミック変異急増期間中の高い需要と限られた供給によるものである。また、私たちのいくつかの製品に対する予測不可能な需要増加は、私たちがこのような需要を満たす能力を超える可能性があり、これは私たちの財務業績と顧客関係に悪影響を及ぼす可能性がある。
新冠肺炎疫病及びそれによって引き起こされる動揺したグローバル経済状況は、本節“リスク要素”の部分的に記述された他のリスクを誘発または拡大する可能性があり、これらのリスクは、私たちの業務、運営および財務状況と業績に実質的な悪影響を及ぼす可能性がある。例えば、自然災害または他の潜在的破壊事件が新冠肺炎疫病と同時に発生した場合、このような災害または事件は私たちの在庫レベルを枯渇させる可能性があり、私たちは製造または製品供給能力の中断を経験する可能性がある。
この流行病の急速な発展と流動性は新冠肺炎が私たちに最終的に影響するいかなる予測も排除した。当局が講じている新冠肺炎の伝播を抑制するための措置(ワクチンの配布および/またはワクチンの提供と強化ワクチンを含む)の持続時間、およびこれらの措置の有効度(あれば)は依然として非常に不確定である。新冠肺炎が私たちの業務(私たちの製品開発、製品販売、経営業績とそれによって発生したキャッシュフローを含む)と財務状況に悪影響を与える程度と程度は疫病の深刻性と持続時間、疫病がアメリカと全世界経済に与える影響、及び連邦、州、地方と国際政府が疫病に対応する時間、範囲と有効性に依存する。疫病の緩和がさらにその場避難令および閉鎖令および/または個人および/または団体行動の制限を必要とする場合、新冠肺炎の大流行のいかなる悪影響も増加し持続する可能性があり、私たちの業務および財務状況は実質的な悪影響を受ける可能性がある。
私たちの情報技術システムの崩壊、ネットワーク攻撃、または情報セキュリティホールは、私たちの情報技術システム、ネットワーク制御システム、および/または私たちのデータのセキュリティ、完全性および可用性を危険にさらし、私たちの業務運営を中断し、および/または私たちの名声に影響を与える可能性があります。
我々の業務目標を達成するために、我々は、ソフトウェア、モバイルアプリケーション、クラウドサービス、およびネットワーク制御システムを含む複雑な情報技術システムに依存し、いくつかは、サードパーティによって管理され、ホストされ、提供され、またはサービスされる。私たちのシステムおよびデータの機密性、完全性、および可用性を脅かす内部または外部イベントは、私たちのビジネス運営を深刻に中断し、重大なコストおよび/または私たちの名声に悪影響を及ぼす可能性があります。
私たちの情報技術システムは私たちの業務に高度に統合されて、私たちの研究開発仕事、私たちの臨床と商業製造プロセス、そして私たちの製品販売と流通プロセスを含みます。また,我々の多くの従業員が我々のハイブリッド勤務環境で遠隔作業を行うにつれて,我々と第三者情報技術システムへの依存が大幅に増加し,増加し続けることが予想される.我々のシステムの複雑さと相互接続性は,障害や他のサービス中断の影響を受けやすいようにしている.私たちが使用するシステムやソフトウェアをアップグレードしたり変更したりすると、新しいネットワークセキュリティホールやリスクが導入される可能性があります。2022年には、私たちが購入してインストールしたソフトウェアで発見された欠陥の結果であり、いくつかのシステムに緊急パッチを適用することを要求する情報システムを導入したセキュリティホールがいくつか発見されました。私たちはこのような抜け穴によるいかなる重大な悪影響も経験していないが、私たちが未来の抜け穴を直ちに識別して解決するという保証はない。我々のシステムはまた,周辺パトロールやスキャン,ネットワーク釣り,他のネットワーク攻撃をよく受ける.ネットワーク脅威構造の変化に伴い、これらの攻撃の頻度、複雑性、強度は増加しており、検出が難しくなってきている。このような攻撃は、ソフトウェアサプライチェーン、電子メール、悪意のあるウェブサイト、および/または社会工学を利用することができる様々な手段によって配備されることができる恐喝ソフトウェアまたはサービスの提供を拒否する他のソフトウェアを含む有害および致命的なマルウェアの使用を含むことができる。このような攻撃は成功しなかったにもかかわらず、私たちのネットワークに対するサービス拒否攻撃を経験しました, 様々な種類の潜在攻撃技術を防ぐための我々の努力が将来成功する保証はない.政府エンティティ(EMAのような私たちの製品を承認および/または規制するエンティティを含む)および他の多国籍企業(私たちの一部の同業者を含む)が遭遇する攻撃は、重要な業務システムを使用したり、重要なデータにアクセスしたり、保護することができず、私たちの製品の開発、監督部門の承認、製造、販売、および/または流通を含む、私たちの業務運営能力に実質的な悪影響を及ぼす可能性がある。例えば、2017年、ある製薬会社は猛毒マルウェアに関するサイバー攻撃を経験し、その研究開発と販売業務、一部の薬品とワクチンの生産を含むその運営を深刻に混乱させた。今回のサイバー攻撃により、同社のある市場でのある製品の注文と販売はマイナスの影響を受けた。2020年末には,ネットワークセキュリティ事件に遭遇し,攻撃者がその製品の合法的なソフトウェア更新に悪意のあるコードを挿入し,これらの更新を無数の個人や政府クライアントが実装し,攻撃者がこのようなシステムのバックドアにアクセスできるようにした先行する情報技術インフラ監視·管理ソフトウェアプロバイダSolarWinds Corporationが開示されている.2022年には、数百社の顧客がセキュリティホールの攻撃を受けやすいことを、会社がユーザの認証を管理するソフトウェア提供者Okta,Inc.が開示した
攻撃者はオクタの内部ネットワークに入る。この違反事件は私たちの業務に大きな影響はありませんが、将来的に似たような違反が私たちの業務や運営結果に大きな悪影響を与えない保証はありません。
私たちのシステムはまた、知的財産権、商業秘密、財務情報、規制情報、戦略計画、販売傾向および予測、訴訟材料および/または私たち、私たちに属する従業員、私たちの患者、顧客、および/または他の当事者の個人情報を含む大量の敏感なデータを含み、使用する。場合によっては、第三者サービスプロバイダを利用して、そのようなデータを処理、格納、管理、または送信することができ、これは、私たちのリスクを増加させる可能性がある。従業員、サービスプロバイダ(情報技術特定サービスプロバイダを含む)、ビジネスパートナー、国家政府(外国情報機関と関連しているか、または外国情報機関によって支持されている組織を含む)、組織犯罪組織、“ハッカー活動家”または他の人の攻撃またはミスは、意図的または意図的でないデータプライバシーまたはセキュリティホール(ネットワーク攻撃を含む)をもたらし、私たちの敏感なデータが許可されていない人、私たちの競争相手、または公衆のリスクにさらされる可能性がある。我々の第三者サービスプロバイダが経験するシステム脆弱性および/またはネットワークセキュリティホールは、我々の情報セキュリティリスクに影響を与えるかなりの部分を構成する。例えば、2021年上半期に、あるプロバイダがデータ漏洩に遭遇し、許可されていない第三者がサービスを提供する間に、商業文書および個人の識別可能ないくつかの患者情報(社会保障または他の金融または医療保険情報を含まない)を含む供給者によって提供されるいくつかの情報へのアクセス権限を取得する。要求に応じて,適用される州総検事長とその個人身分情報が影響を受けた個人仕入先のデータ漏洩事件を直ちに通知した。2022年第3四半期, 別のサービスプロバイダは、同様のネットワークセキュリティホールを経験し、攻撃者は、サービスプロバイダのシステムからいくつかのデータ(重要でないセキュリティデータを含む)を盗み取る。これらのベンダーのデータ漏洩は、当社の業務に大きな悪影響を与えていませんが、将来的に類似したネットワークセキュリティイベントが当社の業務や運営結果に大きな悪影響を与えない保証はありません。また,我々はこのようなイベントに影響を与え,その深刻さを軽減する能力に影響を与えることをタイムリーに認識している.例えば、2020年と2022年には、私たちの2つのサプライヤーがネットワーク攻撃を経験し、各サプライヤーは最初に私たちのデータに関連していないと報告してくれた。しかし,さらに調査した後,攻撃者が限られた重要でない安入情報を取得したことをそれぞれ後で通知してくれた.この2つの侵入事件はいずれも私たちの業務に大きな悪影響を与えていないにもかかわらず、将来的には再びサイバーセキュリティ事件の報告を受けることができなくなり、このような事件は私たちの業務に実質的な悪影響を与える可能性がある。
ネットワーク攻撃者は,共有またはオープンソースコードからのビジネスソフトウェアにおける脆弱性を利用するようになってきている.私たちはこのような脆弱性がある可能性のある第三者ビジネスソフトウェアに依存していますが、オープンソースコードの使用は通常開示されていないため、システムが直面しているこのようなリスクを完全に評価する能力は限られています。例えば、2021年12月、様々な商業ソフトウェアおよびサービスのためのリモートコード実行脆弱性が、広く使用されているソフトウェアライブラリに発見された。この脆弱性は私たちに重大な悪影響を与えていませんが、私たちが使用しているソフトウェアやサービスの将来の類似した脆弱性が、私たちの業務や運営結果に実質的な悪影響を与えないという保証はありません
国内とグローバル政府規制機関、私たちの業務パートナー、私たちと業務往来のあるサプライヤー、私たちまたは私たちのパートナーに業務サービスを提供する会社、および私たちが買収または買収する可能性のある会社は、そのシステムのセキュリティホールやサービス中断が私たちのセキュリティに悪影響を与える可能性があり、重要なシステム、製品、原材料、コンポーネント、サービスまたは情報にアクセスできない、あるいは私たちの機密データや敏感な個人情報を暴露する可能性があります。例えば,2019年には,我々が製品を開発·製造するためのテスト·分析サービスを実行する2社のサプライヤーがネットワーク攻撃に遭遇し,2020年4月と9月には,それぞれ情報技術サービスと臨床データサービスを提供してくれたサプライヤーがそれぞれ恐喝ソフトウェア攻撃に遭遇した。我々のシステムは破壊されていないが,これらのイベントのたびにシステムとベンダのシステムの接続を切断することを要求している.これらの供給者の能力を回復した後に、製品利用可能性に著しく影響を与えることなく、我々のシステムを再接続することができるが、これらまたは他の供給者のより長時間のサービス中断に影響を与え、特にこれらの供給者がサービスを取得する唯一の源である場合には、我々の業務または運営結果に実質的な悪影響を及ぼす可能性がある。また、私たちはアメリカで主に3つの薬品問屋を通じて私たちの製品を流通していますが、卸売業者の流通運営を損なうセキュリティホールは、医療提供者や患者に製品を提供する能力を深刻に弱める可能性があります。
我々はシステム障害,攻撃,情報セキュリティ脆弱性を経験しているが,このような障害,攻撃,脆弱性が我々の業務や運営結果に実質的な悪影響を与えるとは考えていない.私たちは引き続き私たちの重要なデータおよび/または敏感なデータとシステムの監視、保護、および回復能力に投資し続ける。しかしながら、私たちの努力は、システムまたはデータを検出、阻止、または完全に回復し、私たちのシステムに障害、サービス中断、攻撃、および/または破壊を発生させ、それによって、私たちの業務および運営に悪影響を与え、および/または、キー、専有、個人、機密または他の敏感なデータの損失または暴露をもたらすことは保証されず、これは、私たちに重大な財務、法律、商業または名声の損害、または私たちの株価に負の影響をもたらす可能性がある。私たちはネットワーク責任保険を維持していますが、私たちの保険は、サービス中断、私たちのシステムが破壊された、または私たちの重要なデータまたは敏感なデータ損失によって引き起こされる可能性のあるすべての損失をカバーするのに十分ではありません。
私たちは、個人データの収集、保存、処理、使用、開示、送信、およびセキュリティに関する法律および法規を含む、プライバシーおよびデータ保護に関する様々な法律および法規によって世界的にも制約されています。プライバシーとデータ保護に関する立法と規制環境は絶えず進化し、発展しており、全世界で高い関心のテーマとなっている。例えば、我々は2018年5月に発効したEU GDPRと2020年1月に発効したCCPAの制約を受けており、この2つの規定は違反行為を実質的に処罰している。CCPAは2020年末に改正され、敏感な個人データを使用する選択加入要求を制定するためのカリフォルニアプライバシー権法案を作成し、新たな専門法執行機関であるカリフォルニアプライバシー保護局を設立した。バージニア州、コロラド州、ユタ州、コネチカット州ではその後、同様の消費者プライバシー法が成立し、これらの法律は2023年1月1日にバージニア州で施行され、2023年遅い時期にコロラド州、ユタ州、コネチカット州で施行される。私たちが事業を展開している他の管轄区域は、同様の立法および/または法規を採択または継続して提出している。たとえば,中国案では,個人や非個人データに関するデータ処理活動を規範化する個人情報保護法やデータセキュリティ法が発効しており,既存のネットワークセキュリティ法に基づいている.これらの現行及び将来の法律を遵守しないことは、重大な処罰及び名声の損害を招く可能性があり、我々の業務及び運営結果に実質的な悪影響を及ぼす可能性がある。
私たちの販売と運営は新興市場を含む国際業務リスクの影響を受けています.
世界中の新興市場で拡大し続けるにつれて許可取引を通じても、独立しても、あるいは協力によって(百済神州との連携など)新しい市場で私たちの製品を開発·導入しても、私たちの業務は多くのリスクに直面しています。新興市場での私たちの販売拡大の努力と戦略が必ず成功する保証はありません。私たちの国際業務は、中国と新興市場国の業務を含み、特に地政学的関係問題、特定の国の行動に対する国際制裁および/または主権債務問題を含む世界的および現地の政治、法律、規制および金融不安定期の影響を受けやすいかもしれない。また,2022年に2023年初めまで続いており,アジア太平洋地域でも新冠肺炎感染の急増を経験している。この地区のある国は最初に厳格な抑制措置を開始することによって疫病の急増に対応したが、2022年末に、同国は突然これらの措置を撤回し、重大な新冠肺炎疫病を招き、病院の能力不足などの問題を引き起こし、現地の突発的な衛生事件を招く可能性がある。米国と他国政府との関係が悪化すれば、これらの市場での私たちの業務や投資も悪影響を受ける可能性がある。また、新興市場で協力したり買収したりしていた会社が以前使用していた操作や手配を含む第三者エージェントや不慣れな運営や手配への依存を増加させることが求められる可能性がある。参照してください私たちは人体で臨床試験を行ってから、私たちの任意の候補製品あるいは新しい適応のための既存製品を商業化して販売することができますそれは.私たちの中国と世界各地の新興市場での拡張努力は予測可能、ナビゲーションと生物製薬革新を支持する環境、私たちの製品の持続的な参入と予測可能な定価制御の構築に依存している。例えば、中国は引き続き中国人類の遺伝資源の収集、利用と伝達に対する監督管理を強化し、中国の生物技術研究開発活動に対する監督管理を拡大した。2020年から2022年までの間に,中国のヒト遺伝資源管理局に中国での臨床試験を申請する申請に遅延が生じた。我々の国際業務および業務はまた、より少ない知的財産権または他の適用される法律、多様なデータプライバシーおよび保護要件、変化する税法および関税、貿易制限、または外国の競争から自国の工業を保護するための他の障壁、影響の深い反賄賂および反腐敗法律法規、および/または変化する法律および規制環境の制約を受ける可能性がある
ウクライナの持続的な武力衝突に対応するために、アメリカ政府、多くの州政府、EU、私たちが業務を展開している他の国は広範な経済制裁を実施し、ロシア、ウクライナのある地域およびある実体と個人との商業と商業往来を制限している。この紛争はまた、ネットワークセキュリティ、グローバル経済状態、臨床試験、およびサプライチェーンに関連するリスクを含む本明細書に記載された他のリスクを誘発または増幅する可能性があり、これらのリスクは、私たちの業務、運営、および財務状態および業績に悪影響を及ぼす可能性がある。
私たちの国際拡張に伴い、私たちは外貨対ドルレートの変動の影響を受けている。そして当を受ける私たちは外貨ヘッジスケジュールを通じて外貨為替レートの変動に対するリスクを減らすための計画を立てましたが、私たちのヘッジ努力はこれらの変動が私たちの収入と収益に与える影響を完全に相殺することはできません。全体的に、私たちの国際業務運営の法律と運営挑戦、および政府が合格者をコントロール、誘致、維持し、そして私たちの製品に対する必要な規制または定価の承認を獲得および/または維持する挑戦は、私たちの国際製品販売、業務、運営結果に重大な悪影響を及ぼす可能性がある。
政府法規と第三者政策に関連するリスク
私たちの販売は政府と商業第三者支払者の保証と精算に依存しており、定価と精算圧力はすでに私たちの収益力に影響を与え続けている可能性があります。
私たちの製品の販売は第三者支払者(政府医療計画や個人保険計画を含む)の保険範囲と精算範囲に依存します。各国政府と個人支払者は,薬物使用の管理と費用抑制の取り組みを継続している。また、疫病、経済低迷、インフレによる医療予算への圧力は続いており、私たちがサービスする市場で増加する可能性がある。支払者はコストにますます注目しており,これらのコストは我々の製品の販売率をより低くし続けたり,支払者が精算する人口範囲を狭くしたりすることが予想される.医薬品や他の医療コスト価格の継続的な厳しい審査に加え,支払者の動向に加えて,製品価値に応じて製品価格を設定または調整する能力が制限されており,これは我々の能力を制限し続ける可能性があり,我々の業務に大きな悪影響を及ぼす可能性がある。米国では、特に過去数年間に、いくつかの立法および規制提案が提出され、/または法律に署名して、薬品価格を低下させようとしている。その中にはアイルランド共和軍が公布した立法が含まれており、この立法はアメリカ政府が連邦医療保険中のいくつかの薬品に価格を設定し、連邦医療保険D部分の福祉を再設計し、より大きな割合のコストをメーカーに転嫁し、アメリカ政府が薬品価格の上昇速度がインフレより速い場合に処罰を実施することを許可する。薬品価格に集中した他の提案はまだ議論中であり、薬品定価と競争に重点を置いた他の行政命令は何らかの形で通過し、実行される可能性がある。州レベルの政府行動や投票計画もまた決定と実験の非常に活発な分野だ, 参考価格制限国営医療補助計画下での薬品精算やカナダからの薬品輸入許可を求める提案も含まれている。そのような州政策は最終的に連邦レベルで採択されるかもしれない。
最終的にどのような政策、法規、行政、あるいは立法変化があるかを予測することはできませんし、公布と実施が私たちの業務に与える影響を効果的に見積もることもできません。しかし、支払人の行動が私たちの製品の保証範囲や精算範囲をさらに減少または修正し、より多くのリベートを支払うことを要求したり、他のコストを私たちに転嫁したり、製品の価格設定や他の方法で使用を減らすことに関する私たちの決定に制限または影響を与える場合、これらの行動は私たちの業務および運営結果に実質的な悪影響を及ぼす可能性がある。
-変化する米国連邦保険および清算政策およびやり方は、当社の製品の取得、定価、販売に影響を与え続ける可能性があります
私たちのアメリカ業務の大部分は連邦政府医療計画と連邦や州政府によって規制されている商業保険計画の精算に依存しています。第1部を参照して、項目1.業務--精算。私たちの業務はずっとアメリカ連邦補償政策の変化の立法行動の影響を受け続けるだろう。例えば、“アイルランド共和法”は2022年8月に公布され、その中には、(1)2026年から、医療保険でBとDによって部分的に支払われたいくつかの薬品に対して強制価格が施行され、メーカーは政府が制定した価格を受け入れなければならず、そうでなければ、すべての米国販売に対する処罰に直面する(2026年の10種類の薬品から、2027年と2028年に15種類増加し、2029年以降は20種類増加し、2031年までには約100種類の薬品がこの設定された価格の影響を受ける可能性がある)。(2)2024年から、連邦医療保険D部分は、受益者の自腹コストを制限し、2025年1月1日から連邦再保険を減少させる(このようなコスト移転をもたらし、ある薬物の割引を要求することを含むD部分計画とメーカーに増加する)、および(3)2022年10月1日から、価格上昇がインフレを超えた場合、メーカーは連邦医療保険D部分で精算された薬品にリベートし、2023年1月1日から、価格上昇幅がインフレを超えた場合、連邦医療保険B部分によって精算された薬品をリベートする。アイルランド共和軍の薬品定価制御と医療保険の再設計は、私たちの販売(特に連邦医療保険の精算により依存している製品)、私たちの業務、そして私たちの運営結果に実質的な悪影響を及ぼすかもしれない。しかし、この立法が私たちの業務に与える影響の程度は多くの実施決定に依存するため、アイルランド共和軍の私たちの販売に対する影響の程度、さらには, 私たちの業務はまだ不透明です。また,アイルランド共和軍通過後も環境は活力に満ちており,2022年10月,政府は米国人の処方薬コストの低減に関する行政命令を発表し,HHSに90日以内に薬物コストを低減し,連邦医療保険や医療補助受益者の革新薬物療法の獲得を促進する革新センターモデルに関する報告書を発表するよう呼びかけた。この行政命令は2021年の行政命令に従っているFDAに処方薬輸入計画の策定を呼びかけることや、連邦貿易委員会が反競争活動のより厳しい審査を行うことを含む医療業界競争のスケジュールを増やすことを目的としている。この命令に対する応答は、衛生·公衆サービス部が報告を発表し、競争を促進する薬品の価格設定を求める提案を提出し、米国特許商標局が措置を講じて、FDAとの協調を強化し、模倣薬と生物類似薬の競争の障害を解決することを含む。CMS政策の変化と新しい看護、交付と支払いモードをテストするためのモデルプロジェクトも私たちの製品を含む薬品の保証と精算方式に著しく影響することができる。2021年9月、HHSは将来可能な強制モードを含む薬品定価問題を解決する計画を発表し、処方薬と生物製品の支払いを全体看護コストを含むいくつかの要素と関連させた。
私たちはまた報告価格データと関連するリスクに直面しています。これは私たちの製品の精算と割引に影響を与えます。米国政府の価格報告法規は複雑であり,バイオ製薬メーカーに以前に提出された何らかのデータの更新を要求する可能性がある。もし私たちが提出した価格設定データが正しくなければ、私たちは巨額の罰金と罰金や他の政府の法執行行動を受ける可能性があり、これは私たちの業務と運営結果に実質的な悪影響を及ぼすかもしれない。さらに、以前に報告された価格データを繰り返すため、私たちは追加の返却点を支払い、追加の割引を提供する必要があるかもしれない
-州によって変化する精算および価格設定行動は、私たちの製品の販売に負の影響を与え、製品の獲得に悪影響を与え続ける可能性があります
州レベルでは、政府行動や投票計画はまた、私たちの製品の保証と精算方法に影響を与え、および/または私たちの価格決定に追加的な圧力をもたらすだろう。現有と提案された国家定価法は薬品定価の複雑性を増加させ、すでに業界の定価決定に影響を与えている可能性がある。一部の州はすでに医薬品輸入計画または他の価格設定行動をとっており、他の多くの州は、バイオ製薬メーカーに独自の価格設定情報を州政府に報告することや、ある価格上昇の提案を事前に通知することを要求することを含む行動を検討している。例えば、カリフォルニアの法律は、バイオ製薬メーカーが、少なくとも所定の処方薬の値上げがいくつかのハードルを超える60日前に医療保険会社および政府医療計画に通知することを要求する。オレゴン州とワシントン州にも似たような法律がある。医療補助の他の提案に対しては,一定の定価が一定のハードルを超えるメーカーを懲罰したり,バイオ製薬製品の支出を制限したりすることを求めている。各州でも州計画でカバーされている患者に薬品を支払う方法の変更が求められている。ニューヨーク州はすでに医療補助薬品支出上限を確立し、マサチューセッツ州は新たな審査と補充税金還付交渉手続きを実施した。6つの州(コロラド州、メイン州、ニューハンプシャー州、メリーランド州、オレゴン州とワシントン州)はすでに法律を公布し、処方薬負担可能性委員会(PDAB)を設立し、薬品価格を研究し、負担能力の挑戦を構成する薬品を確定し、3つの州(コロラド州、メリーランド州とワシントン州)で、州PDABは州監督計画中のいくつかの薬品に支払い上限を設定する権利がある。他の州は似たような政策と法律を施行することを考慮するかもしれない。また、コロラド州、フロリダ州、メイン州、ニューハンプシャー州、ニューメキシコ州、バーモント州はすでに法律を公布し、他のいくつかの州も法案を提出した, カナダからの薬品輸入を実施する。FDAはコロラド州,フロリダ州,メイン州,ニューメキシコ州の代表と面会しており,これらの州で提案されている輸入計画を検討しており,FDAはこれらの計画を承認しようと努力しているかもしれない。他の州は同様の方法をとることができ、異なる政策変化を求めて、コスト削減に努力し続けることもできる。最終的には、米国連邦政府の行動と同様に、既存または未来の州政府行動または投票イニシアティブも、我々の製品販売、業務、および運営結果に実質的な悪影響を及ぼす可能性がある。
-アメリカの商業支払者の行動は、私たちの製品の取得と販売に影響を与え続ける可能性があります
医療保険会社,PBM,統合医療交付システム(医療保険会社とPBMを合併した垂直統合組織)や共同購入組織を含む支払者がコスト低減方法を求めるようになってきている。頻度の増加に伴い,支払者は福祉計画の変化を採用しており,より大きな割合の薬品コストを患者に移している。これらの措置には、より限られた福祉計画設計、より高い賠償免除計画、より高い患者自己負担または共同保険義務、および製造業者商業自己負担援助計画の使用に対する患者のより大きな制限が含まれる。しかも、支払者に対する政府の規制はこのような傾向に影響を及ぼすかもしれない。例えば、CMSは、商業支払者が共同支払いアキュムレータ調整計画をより広く採用することをもたらす2021年1月1日以降から開始される計画年度の政策を決定する。PBMを含む支払者は、我々の製品を彼らの処方または彼らが管理する製品に配置することに関連する価格割引またはリベートを求め続け、患者に製品を保証する前に支払者の事前許可を得ること、および/または私たちの製品が承認されたいくつかの適応を排除することを選択することを要求する、我々の製品の取得または使用に制限を加えている。例えば、一部の支払人は、Repatha処方を発行した患者が彼らの使用基準に適合することを医師に証明または記録することを要求し、これらの要件は制限され、患者がRepatha治療を受けることを制限し続ける可能性がある。取得障害を低減するために、我々は、支払者(Medicare Part D処方薬計画を管理するPBMを含む)により大きな割引およびリベートを提供することによって、Repathaの正味価格を低減する, 高い割合の連邦医療保険患者が彼らの自己支払い費用を支払うのではなくRepatha処方を放棄するために、著者らは新しい国家薬品コードを導入し、Repathaをより低い価格で獲得させた。しかし,患者の自己負担費用の負担能力は限られており,患者の使用を制限し続ける可能性がある。さらに、これらの正味価格および価格の低下にもかかわらず、一部の支払者は制限されており、患者の接触を制限し続ける可能性があり、Repathaの処方カバー範囲を変更するなど、さらなる割引またはリベートを求めるか、または他の行動をとることができ、これは私たちのRepathaの販売を減少させる可能性がある。これらの要因はすでに制限されており,患者の負担能力や使用を制限し続け,Repathaの販売に負の影響を与える可能性がある。
そのほか、健康保険業界の重大な統合はいくつかの大型保険会社とPBMの出現を招き、これは生物製薬メーカーとの定価と使用交渉に更に大きな圧力をもたらし、割引とリベート要求を著しく増加させ、そして患者の接触と使用を制限した。例えば,米国では,2023年初めまでに上位5位の総合健康計画とPBMが約92%の薬局処方をコントロールしている。この高さの
保険会社、PBM、および他の支払者との間の統合は、統合された医療送達システムおよび/または専門または通販薬局および薬局小売業者との統合を含み、これらのエンティティの私たちと他のバイオ製薬メーカーとの交渉チップを増加させ、これらの支払者が私たちの業務からより大きな価格割引、リベート、およびサービス料を達成することをもたらす。CVS、Express Script、United Health Group(上位5位の総合健康計画、PBM)にはバックポイント管理組織があり、これらの組織はより深い割引を交渉するチップをさらに増加させている。最終的に、これらの商業支払者が適用する追加割引、リベート、費用、カバー範囲の変更、計画変更、制限、または排除は、私たちの製品販売、業務、および運営結果に大きな悪影響を及ぼす可能性があります。国会あるいは政府が提出した政策改革は、米国市場におけるPBMの役割を細分化し、私たちの業務及び私たちとこれらの実体との相互作用方式に下流影響或いは結果を与える可能性がある。例えば、2022年6月7日、連邦貿易委員会はPBMの商業やり方に対して調査を展開し、調査結果はメーカーとPBMの相互作用に影響を与え、ある薬品の獲得方式を変化させる可能性がある。私たちのを見てください販売が私たちのある卸売業者、流通業者、個人支払者に集中している合併は私たちの業務にマイナス影響を与える可能性があります。
我々の業務は,連邦医療保険のクレームを処理する民間医療実体が実施する政策の影響も受けており,連邦医療保険行政請負者を含む。例えば,2022年第2四半期には,いくつかのMedicare行政請負者がTEZSPIREのFDA承認のラベルに違反し,TEZSPIREを彼らの“自己管理薬物”排除リストに追加する通知を発表した。連邦医療保険行政請負業者はその後、TEZSPIREをその除外リストから削除したが、これらの排除を再導入および/または実施すれば、深刻な喘息を有する連邦医療保険受益者は連邦医療保険B部分下のTEZSPIRE保険を獲得できず、連邦医療保険優勢項の下にもある可能性がある。
-米国以外の政府および商業支払者の行動は、私たちの製品の取得および販売に影響を与え続けるだろう
アメリカ以外にも、私たちは各国が薬品支出を減らすための行動を続けると予想している。第1部を参照して、項目1.業務--精算。新冠肺炎の疫病が政府予算を逼迫させることと、ある地域の経済状況が引き続き悪化することに伴い、ヨーロッパを含む高インフレとロシア-ウクライナ衝突に関連するエネルギー危機はこの地域の経済に挑戦しており、薬品支出の減少を要求する圧力はさらに増大する可能性がある。国際参考定価は米国以外の多くの国で広く使用されており、他国の製品価格の外部基準に基づいてコストを抑えている。国際参考定価政策は迅速かつ頻繁に変化することができ、疾病負担、適応、市場構造或いは各国或いは地区負担能力の違いを反映しない可能性がある。その他の支出制御方法は、使用収入の回収、リベート、値上げ率の上限を含むが、複数の外国司法管轄区でも使用されている。さらに、国家衛生技術評価が1種の薬物が既存の治療法の外で十分な臨床利益を示すことができないと判断した場合、或いはいくつかの費用効果閾値を達成することができない場合、各国はその製品の精算人口を清算或いは制限することを拒否することができる。例えば、EMAは2020年までに決定されたアテローム性動脈硬化性疾患患者の治療にRepathaを承認したにもかかわらず, フランスでは、国家衛生技術評価を経た後、Repathaの精算は比較的に狭い患者群(例えば純合子家族性高コレステロール血症(HoFH)患者)に限られている。多くの国は、国または地域入札によって、互いに競争する可能性のある製品間の補償を決定し、これは、1つの製品がその国または地域の大部分または全部の売上を得ることをもたらすことが多い。私たちの製品のために保証と精算を得ることができず、その現有の保証と精算状況が悪化し、あるいは支払人が医師と他の提供者に支払う即時性或いは確定性の低下は、医療保健提供者がその患者のために私たちの製品を出す能力或いは意志にマイナス影響を与え、更に負の影響を与える可能性があり、そうでなければ、私たちの製品の使用或いは私たちがこれらの製品のために実現した価格にマイナス影響を与える可能性がある。これらの変化は、将来的に私たちの製品販売、業務、経営結果に実質的な悪影響を及ぼす可能性がある。
様々な組織が発表したガイドラインと提案は私たちの製品の使用を減らすことができます。
政府機関は私たちと私たちの製品に直接適用される法規とガイドラインを公布する。各種疾病に関連する専門協会、実践管理団体、保険会社、医師団体、個人健康と科学財団と組織も医療保健提供者、管理者と支払人及び患者コミュニティにガイドラインと提案を発表した。政府機関や他の団体や組織の提案は,関連療法の使用,投与量,投与経路,使用などの事項に関与する可能性がある。そのほか、ますます多くの組織は生物製薬製品の価値と定価の評価を提供しており、甚だしきに至ってはそのガイドラインは従来から臨床問題に重点を置いてきた組織も各種の治療に対する費用効果分析をその治療ガイドラインと提案に組み入れるようになった。価値評価は、個人組織から来ている可能性があり、これらの組織は彼らの調査結果を発表し、政府と個人支払者の製品の返済について提案する。一部の会社と支払人は、個人組織の評価に部分的に基づく定価と支払い決定を発表した。そのほか、多くの国の政府衛生技術評価組織は新しい、新興と現有の薬物と治療の臨床効果、コスト効果とサービス効果に基づいて、その管轄範囲内の支払人に精算提案を提出した。このような健康技術評価組織は
将来的には、適用される規制機関が承認した範囲よりも精算範囲が狭いか、または完全に精算しないことを提案することが可能であり、将来的には私たちのいくつかの製品の精算を提案することができる。参照してください私たちの販売は政府と商業第三者支払者の保証と精算に依存しており、定価と精算圧力はすでに私たちの収益力に影響を与え続けている可能性がありますこのような提案またはガイドラインは私たちの名声に影響を与える可能性があり、私たちの製品の使用、用量、または精算を減少させるいかなる提案またはガイドラインも、私たちの製品販売、業務、および運営結果に重大な悪影響を及ぼす可能性があります。また、投資界や株主は、これらの提案やガイドラインが私たちの製品の使用量や用量を減少させると考えており、これは私たちの普通株の市場価格に悪影響を及ぼす可能性がある。
新しい税法を採用して説明したり、追加の税務負担を負担したりすることは、私たちの収益性に影響を及ぼすかもしれない。
アメリカと私たちが業務を展開している他の管轄区域では、私たちは所得税と他の税金を払わなければならない。したがって、私たちの所得税の支出は私たちが経営している地域別の適用税率を組み合わせたものだ。私たちの所得税の準備を決定する時、重要な判断が必要だ。
私たちの1つ以上の法人実体はアメリカ連邦司法管轄区、アメリカ各州司法管轄区、いくつかの外国司法管轄区で所得税申告書を提出します。私たちの所得税申告書はこのような司法管轄区の税務機関によって定期的に検討されている。税務法律、法規、関連事実の異なる解釈により、税務当局(米国国税局を含む)は監査面でより積極的になり、特にこれらの問題に注目しているため、控除の時間と金額、税収控除の使用、および異なる税務管轄区域間の収入と費用分配問題に関連して、税務当局と重大な紛争が発生している可能性がある。2017年、私たちは米国国税局から2010-2012年のRARと修正されたRARを受け取り、主にアメリカのあるエンティティとアメリカ領土プエルトリコ間の利益分配に関連する重大な調整を提案した。我々は提案された調整と計算に同意せず、米国国税局行政控訴事務所と解決策を求めたが、解決策を達成することはできなかった。2021年7月、私たちは、2021年5月と7月に受信した2つの重複した2010-2012年度法定欠税通知(通知)に異議を提出し、2010-2012年度の米国課税所得額を増加させることを目的とした請願書を米国税務裁判所に提出した
2020年には、米国国税局から2013-2015年のRARと修正されたRARを受け取り、2010-2012年の提案された利益分配と同様に、米国のあるエンティティと米国領土プエルトリコとの間の利益分配に主に関連する重大な調整を提案した。我々は提案された調整と計算に同意せず、米国国税局控訴事務所と解決策を求めたが、解決策を達成することはできなかった。2022年7月、私たちは、2013-2015年度の米国課税所得額の増加を求め、処罰を主張する2022年4月に受信した2013-2015年度通知に異議を提起する請願書を米国税務裁判所に提出した。
私たちは2010-2012年と2013-2015年の通知で国税局が提起した立場に根拠がないと信じている。私たちは司法手続きを通じて2010-2012年と2013-2015年の通知に異議を唱えている。これらの事件は2022年12月19日に合併された
私たちは現在、2010年から2015年までの間と同様の問題に関連して、国税局2016-2018年の審査を受けている。しかも、私たちはいくつかの州と外国税務管轄区域の検討を受けている。
このような複雑な税務問題は今後12ヶ月以内に最終的に解決される可能性が低い。過去の経験、税法の解釈、税法の私たちの事実への適用、および税務機関が行動する可能性のある判断によると、私たちは依然として私たちの所得税負債の課税項目が適切であると考えているが、しかし、所得税の準備の複雑さとこれらの問題の不確定な解決策により、任意の税務事項の最終結果は、支払う金額が課税金額をはるかに超え、私たちの運営結果に大きな悪影響を及ぼす可能性がある
第二部を参照して、プロジェクト7.経営層の財務状況と経営成果の討論と分析--経営成果、所得税と連結財務諸表の第四部分--所得税を付記する。
私たちの所得税の支出と将来の経営業績は、私たちの経営構造の変化、異なる税率の国の収入と費用の組み合わせの変化、繰延税金資産と負債推定値の変化、適用される税収法律、法規、あるいは行政解釈の変化によって不利な影響を受けるかもしれない。2017年の税法は複雑で、多くの法規や指導意見が発表されており、異なる解釈があるかもしれません。私たちは2017年の税法を適用する時、監査の挑戦に直面するかもしれない。また、2017年税法には、2025年末に発効予定の外国収入や輸出収入の税率引き上げなど、これから発表される条項がいくつかあり、実際の税率引き上げにつながる可能性があります
政府と国会は現行税法の改正を検討し続けており、これは米国で納めた税金を大幅に増加させる可能性がある。また、OECDは、各国が最低企業税率と市場国の税権拡大で一致させることで合意した。EU諸国を含むいくつかの国は
世界で最も低い税金協定の立法が施行される。しかし、米国などの他の国では、OECD協定の実行状況には大きな不確実性が存在している。OECDのすべての加盟国または個別国が一方的にこの合意を公布した場合、この合意は増税または二重課税を招く可能性があり、それにより、私たちのアメリカまたは外国の納税義務に影響を与える可能性がある。米国、米国領土プエルトリコまたは他の管轄区域の現行税法の変化は、上記の変化と潜在的な変化を含み、私たちが業務を展開している地方の増税を招く可能性があり、私たちの業務結果に実質的な悪影響を及ぼす可能性がある。
私たちの業務は訴訟と政府調査の影響を受けるかもしれない。
私たちは私たちの特定の子会社たちと法的訴訟に巻き込まれた。連結財務諸表の第四部--付記19“または事項と引受金”を参照。民事·刑事訴訟は本質的に予測不可能であり、その結果、代償の高い裁決、罰金、罰金、連邦医療計画から除外され、および/または私たちの業務運営方式に影響を与える禁止救済をもたらす可能性がある。訴訟クレームの弁護は高価で、時間がかかり、注意を分散させる可能性があり、私たちは判決を招いたり、金銭損害クレームの和解を招いたり、私たちの業務運営方式を変更したりする可能性があり、これは私たちの製品販売、業務、運営結果に実質的な悪影響を与える可能性がある。しかも、製品責任はバイオテクノロジーと医薬製品テストとマーケティングにおける大きなリスクだ。私たちは人体臨床試験中と監督管理の承認後に販売された製品は巨大な製品責任の開放に直面しているかもしれません。製品責任クレームは、その是非にかかわらず、コストが高く、経営陣の注意を分散させ、私たちの名声と私たちの製品の需要に悪影響を及ぼす可能性がある。私たちと私たちのいくつかの子会社は以前私たちのいくつかの製品の製品責任訴訟で被告とされていました。
私たちはまた正常な業務過程で発生した政府調査に参加した。近年,米国でも世界各地でも,我々の業界で経営している会社に対する政府調査や訴訟が増加傾向にある。参照してください私たちの販売は政府と商業第三者支払者の保証と精算に依存しており、定価と精算圧力はすでに私たちの収益力に影響を与え続けている可能性があります。私たちのアメリカ以外の業務活動は、イギリスの“反賄賂法”を含む“海外腐敗防止法”および私たちの国の反賄賂または反腐敗法律、法規または規則のような制約を受けている。私たちは私たちのすべての従業員、代理店、請負業者、サプライヤー、許可された人、パートナー、または協力者がすべての適用された法律と法規を遵守することを確実にすることはできません。2019年4月25日、私たちは、患者に財政援助を提供する独立した慈善団体が薬品を獲得することに関連したいくつかの疑惑を解決するために、米司法省とHHSのOIGと和解合意に達した。したがって、私たちはOIGと企業誠実協定を達成し、企業コンプライアンス計画を維持し、5年以内に明確な企業誠実義務を負担することを要求した。企業の誠実な合意の下でのすべての義務を完全に履行することが予想されるが,そうしなければ巨額の処罰を招き,政府医療計画から除外される可能性がある。私たちはまた政府が新しい蘇生理論を引用して私たちに新しい調査をしたり行動したりすることを見ることができるかもしれない。例えば、検察官は、商業共同支払い援助計画を含む患者支援計画をより厳格に検討しており、このような計画に関するさらなる法執行行動および調査は、商業患者に自己援助を提供する能力を制限する可能性がある。スポンサー、講演番組、および他のスケジュールについてもより厳しい審査が行われており、医療専門家は、これらのスケジュールの中で何らかの活動に参加するための報酬、旅行、または他の価値を得ることができ、さらなる法執行行動は、このような手配に参加する能力を制限する可能性がある。これらの結果のいずれも、我々の業務および運営結果に実質的な悪影響を及ぼす可能性がある。
競争に関連するリスク
私たちの製品は激しい競争に直面しており、私たちの候補製品も激しい競争に直面しているかもしれません。
私たちは競争の激しい環境で運営している。プロジェクト1.ビジネス--マーケティング、流通、および選択された市場製品--競争を参照。我々の製品や候補品は,既存薬,現在開発中の新薬,現在他の適応用が承認されている薬剤(後に我々の製品と同じ適応が承認される可能性がある),ラベル外使用のための他の適応が承認された薬剤と競合することが予想される。大手製薬会社や製薬製品の後発薬メーカーはすでにバイオテクノロジー分野への拡張が予想されており,一部の製薬会社と後発薬メーカーは生体模倣薬を追求するためのパートナー関係を構築している。ますます多くの会社がバイオ製薬を追求するにつれて、私たちのいくつかの生物類似製品はすでに1つ以上の競争相手またはこれから来る競争相手市場に進出しており、私たちのいくつかの候補製品も市場に入るかもしれない。さらに、私たちのいくつかの競争相手は、技術およびプロセスの開発、または特定の治療分野でのより多くの経験において、私たちよりも技術的、競争的、または他の利点を持っているかもしれないが、製薬とバイオテクノロジー会社との間の統合は、これらの利点を強化することができる。これらの優位性は私たちが彼らとの競争に成功して、新製品を発見、開発、販売することを難しくし、私たちの既存の製品を市場に出す可能性のある新製品あるいは新製品マークと競争することを困難にするかもしれない。したがって、私たちの製品は常に競争しており、競争を続ける可能性があり、私たちの候補製品は、より高い割引または割引、より低い価格、同等またはより良い治療効果、より良い安全性、より管理しやすい、より早い発売、または他の競争を提供する製品または候補製品と競争する可能性がある
機能します。もし私たちが効果的に競争できなければ、これは私たちの売上を減少させる可能性があり、これは私たちの業務と運営結果に実質的な悪影響を及ぼすかもしれない。
私たちの知的財産権の地位は挑戦、無効、または回避されるかもしれないし、私たちは現在と未来の知的財産権訴訟で勝つことができないかもしれない。
私たちの成功は、特許権や他の知的財産権を獲得して守る能力にある程度依存しており、これらの権利と知的財産権は、私たちの製品や候補製品の商業化に非常に重要です。製薬と生物技術会社の特許地位は非常に不確定である可能性があり、よく複雑な法律、科学と事実問題に関連する。コスト圧力に押されて、私たちの業界の特許保護を制限または弱める努力が増加している。例えば、新冠肺炎疫病はアメリカと国際上の薬品調達に関する強制許可、介入権利或いは他の政府介入に対する興味を増加させ、世界貿易機関はすでに知的財産権免除手続き中の貿易関連の方面を通じて新冠肺炎ワクチンの知的財産権保護を免除することに同意した。参照してください新冠肺炎の大流行及び公衆と政府が疾病伝播を抑制するための努力は、すでに著者らの臨床試験、運営、製造、サプライチェーン、流通システム、製品開発、製品販売、業務と運営結果に不利な影響を与え、実質的な悪影響を与える可能性があると予想されている第三者は、私たちの製品、候補製品、および技術に関連する特許および特許出願に挑戦し、無効にし、または回避し続ける可能性がある。特許への挑戦は、潜在的な競争相手から来る可能性があり、潜在的な侵害製品をマーケティングする他の当事者からのものである可能性もある。さらに、私たちの特許地位は、競合製品または技術が私たちの特許を侵害しない可能性があるので、類似した製品や技術を有する競争相手から私たちを保護できないかもしれない。私たちのいくつかの候補製品については、第三者が特許または未解決の特許出願を持っており、彼らは印税を支払う必要があると主張したり、いくつかの地域でこれらの候補製品を商業化することを阻止したりするかもしれない。特許紛争は頻繁で費用が高く、製品の商業化のコストを阻害、延期、または増加させる可能性がある。私たちは過去、現在、そして未来に特許訴訟に巻き込まれている。これらの問題は、将来的には、私たちのいくつかの製品の生物模倣品であると主張するメーカーに対する特許侵害訴訟と、BPCIAのいくつかの条項を遵守できなかったことを含む可能性がある。例えば、侵害、有効性、実行可能性、強制命令または経済的救済方法または特許保護権に関する裁判所、機関、または法廷による裁決は、通常、上訴または行政審査を受ける。再審時、再審法廷はこのような初歩的な裁定を少ない、あるいは根本的に遵守することができ、さらなる手続きを通じて確認、覆し、または再議対象になることができる。特許紛争や訴訟は落胆しておらず,将来落胆しないかもしれない, 潜在的な違反者は、紛争や訴訟が最終的に解決される前に、告発された侵害製品を市場に投入する。特許係争または訴訟の開始から解決までの時間は、紛争または訴訟が解決される裁判所、機関、または仲裁庭の利用可能性およびスケジュールに依存する。その間、私たちは競争の影響を受けてきました。たとえ私たちが勝訴しても、競争相手製品の侵害によって受けた損失、損害、損害を完全に回復することができないかもしれません。さらに、ある段階または完全に現在または未来の訴訟で敗訴または和解が達成された場合、私たちは、侵害された製品または技術のために第三者許可を締結することが要求されるか、または論争のある技術または製品の使用を停止することが要求される競争および/または重大な責任の影響を受ける可能性がある。しかも、私たちはこのような許可書が私たちが受け入れられる条項で提供されるか、または根本的にできないということを保証できない。
また、“ハッジ·ワクスマン法”によると、“ハッジ·ワックスマン法”に規定されている5年間のデータ独占期間が満了する前と、当該製品に列挙された特許が満了する前に、FDAによりFDCAによって承認された我々の製品は、将来的にも後発薬との競争相手との特許訴訟の対象となる可能性がある。同様に、私たちの革新的な生物製品は、私たちの特許が満期になるまで、将来的にも特許訴訟の対象となる可能性があり、私たちの製品の生物類似または交換可能なバージョンの承認を求める競争相手は、BPCIAが規定する12年排他期の前にある。さらに、将来的に特許訴訟に直面する可能性があり、これらの訴訟は、私たちが開発しようとしている生物類似候補製品が、適用可能な基準製品を製造、マーケティングまたは販売している会社、またはそのような製品を開発または開発している他の生物類似バージョンの会社を含む他の会社の特許を侵害していることに関連する。あるいは、他のエンティティが持っている特許は、これらの会社が持っているすべての同じラベルとの適応を追求しないように、将来的に決定するのに役立つかもしれない。私たちはすでに他社が持っている特許に挑戦しようとしていると予想されていますが、私たちの努力は成功しないかもしれません。特許訴訟の例及び関連情報については、連結財務諸表の第4部である付記19“又は事項及び承諾”を参照されたい。
私たちの製品のいくつかの既存の特許は期限が切れているか、期限が近づいています。項目1.ビジネス--マーケティング、流通、および選択された発売製品である特許を参照。我々の特許が満了するにつれて、競争相手は、生物模倣薬を含む類似の製品または技術を合法的に生産および販売することができ、これは、我々の製品販売、業務、および運営結果に重大な悪影響を及ぼす可能性がある。さらに、競争相手は、私たちの特許を無効にし、設計、または他の方法で私たちの特許を迂回し、競争相手の製品を販売し続けることができるかもしれない。
我々は現在,生物模倣薬と後発薬からの競争に直面しており,将来的には生物模倣薬と模倣薬からの日々の激しい競争に直面することが予想される。
我々は現在,米国とヨーロッパを含む大多数の地域で生物模倣薬と後発薬からの競争に直面しており,今年および今後ますます激しくなる生物類似薬および/または後発薬の競争に直面することが予想される。適用特許権の満期または成功挑戦または適用特定期間の満了は、このような競争を加速させ、我々の特許の有効性および/または範囲に関するより多くの訴訟に直面することが予想される。私たちの製品も低コストの生体模倣薬や模倣薬からのより大きな競争を経験し、私たちの製品と競争しているブランド製品が自分の特許保護を失った時、これらの模倣薬や模倣薬は市場に参入する。ある程度、政府がより緩和された規制承認基準を採用すれば、競争相手がより広範あるいはより速い生体模倣薬と模倣薬の発売許可を得ることができれば、私たちの製品の競争が激化する速度が加速する可能性がある。
EUでは、生物模倣薬は汎用および製品カテゴリ固有のガイドラインに従ってマーケティング許可評価を行っている。さらに、生物学的類似薬物の使用を刺激し、および/または潜在的な医療節約を増加させるために、いくつかのEU諸国およびカナダのいくつかの省は、医師が割当量を発行するか、または自動薬局が対応する参考製品の代わりに生物模倣薬を使用するような生物類似吸収措置を採用することを検討している。いくつかのEU諸国は1つ以上の生物的に似た競争者が市場に参入する時に自動的に値下げする。2022年9月、欧州医薬品管理局とEU医薬品主管機関(HMA)は、EUで承認された生物類似薬物がその参考製品と同じ参考製品の他の生物模倣薬と“交換”できることを規定する共同声明を発表した。EMA−HMAのこの声明は、生物模倣薬の処方とヨーロッパとのより大きな競争にさらに寄与する可能性がある。生物類似競争の競争影響の程度はEU諸国間と製品間で異なるが,EUでは生体模倣薬の全体使用および革新製品の製品販売が生物類似競争の影響を受ける比率が増加している。
米国では、BPCIAはFDAが単独で簡略化された経路で生体模倣薬を許可することを許可している。項目1.企業-政府規制--アメリカの監督管理--生物模倣薬の承認を参照。米国では,FDAはNeulasta,Epogen,ENBRELの生物類似バージョンを含む多くの生物模倣薬を承認しており,ますます多くの会社が我々の製品の生物類似バージョンを開発していると発表している。例えば、6つの生物類似バージョンのNeulastaは現在米国で承認されており、私たちは将来的に他の生物類似バージョンのNeulastaが発売されるか、承認される可能性があると予想される。より多くの競争相手の発売に伴い、私たちNeulasta販売への影響も加速した。プロジェクト1.ビジネス--マーケティング、流通、および選択された市場製品--競争を参照。生体模倣薬製造業者は、将来的に、より低い価格、より大きな割引またはバックルを提供すること、または長期価格またはより広い他の製品の組み合わせを提供する契約を提供することによって、私たちの製品と競争しようと試みるかもしれない。私たちの製品の生物類似バージョンを開発することを求めている会社は私たちの特許に挑戦しており、私たちの材料特許が満期になる前に私たちの特許に挑戦し続けるかもしれません。生物模倣薬及び後発薬特許訴訟の例及び関連情報については、連結財務諸表の第4部である付記19“又は事項及び承諾”を参照されたい。参照してください私たちの知的財産権の地位は挑戦、無効、または回避されるかもしれないし、私たちは現在と未来の知的財産権訴訟で勝つことができないかもしれない。
米国の生物類似経路は、いくつかの基準に適合する生物類似製品が、その基準製品と交換可能なオプションとして許可されていることを含む。生物模倣薬を開発または販売しているいくつかの会社は、FDAから交換可能な地位を得ることを求める可能性があり、これは、薬剤師が州法で規定されていないほとんどの州の処方者が事前に承認した場合に、これらの生物模倣薬を我々の参考製品の代わりにすることを可能にする可能性がある。FDAは2021年に最初の交換可能な生物模倣薬を承認し、その後、他の3つの生物模倣薬の交換名を承認した。2019年、FDAは生物類似と交換可能なインスリン製品が一般的に比較免疫原性研究を行うべきではないことを規定する指導意見草案を発表した。これは、他の製品固有のガイドラインを制定するためにドアを開き、いくつかの研究への期待を解消し、これは私たちの革新製品の生物類似競争の激化に役立つかもしれない。例えば、FDAは、2022年8月に、交換決定をサポートするために切り替える研究を行う必要がなく、生物学的に類似したモノクロナル抗体を交換可能に指定する。また、2022年9月、FDAは、比較臨床試験は引き続き多くの生物類似開発計画の要求であるが、この機構は一連の統計、分析と薬理学的方法を通じて将来の比較臨床試験に対する需要を減少させることに集中している。
さらに、生物類似経路法における12年排他期の批評者は、データ排他期を短縮することを求め続け、および/または、どの新製品がデータ排他性を獲得するかに関する法律条項を狭く解釈することをFDAに奨励する可能性がある。2019年,政府は米国−メキシコ−カナダ協定から生物製品の少なくとも10年間のデータ排他性の要求を撤廃することに同意した。また,FDAは,許可生物の後続変更が参考製品の最初の12年排他期の残り時間によって保護されるかどうかを考えている(模倣薬文脈では,この概念は“傘形排他性”と呼ばれる)。FDAが保護傘の排他性を生物参照製品や排他性期限を他の変更に適用しないと決定した場合,
これは私たちが生物的に似たような競争にもっと早く直面するようにするかもしれない。生物学的類似性または互換性を証明する基準の低減、訴訟が提起される可能性のある特許および/または特許の和解を制限し、生体模倣薬の優遇補償政策を実施し、新しい法律によって、FDAのオレンジおよび紫の書籍におけるより多くの開示を要求することを含む、模倣薬および生物類似薬の承認および商業化を容易にする政策によって競争を促進する立法および規制努力もある。例えば、FDAは2021年にUSPTOに書簡を送り、2つの機関間の協調を強化する方法を紹介し、既存技術の識別を助ける訓練を提供し、市場排他性を拡大するやり方、薬品特許審査員が追加資源を必要とするかどうか、特許裁判と控訴委員会が授与された後、薬品特許への影響に挑戦してUSPTOの意見を求める。米国特許商標局は2022年7月にFDAに応答として手紙を送り、それが正式なメカニズムを構築し、模倣薬と生物類似製品の進入時間に影響を与える可能性のある特許問題でFDAと協力する予定であることを宣言した。2023年1月、USPTOとFDAは、USPTOとFDAの協力努力について共同ヒアリングを行った。
私たちの製品の特許保護および/または適用される独占経営権が満期または喪失すると、私たちは短い時間で製品の収入の大部分を失う可能性がある。プロジェクト1.ビジネス--マーケティング、流通、および選択された市場製品--競争を参照。また、もし私たちの製品がFDAの書面要求による小児科研究の対象であり、私たちはこれらの研究を十分に完成できなければ、私たちは小児科独占権を得ることができず、この製品(と小分子製品の既存特許)の未期限規制独占経営権をさらに6ヶ月延長することができないかもしれない
私たちの製品に対する生物模倣薬と後発薬の正確な影響を予測することはできないが、生物模倣薬と後発薬の競争のため、私たちは現在アメリカ、ヨーロッパ、他のところでより大きな競争に直面することが予想され、逆に、私たちの製品価格と販売も下振れ圧力に直面している。このような競争は、私たちの製品販売、業務、そして運営結果に実質的な悪影響を及ぼす可能性が高まっている。州法はまた私たちの業務に影響を及ぼすかもしれない。例えば、カリフォルニア州は、立法によって2020年1月1日に施行された最初の、模倣薬または生体模倣薬製造業者によって提起された特許侵害クレームに反対する“遅延支払い”和解、すなわち和解と引き換えに価値のあるものを提供する。この法律によると、このような和解協定は反競争と推定される。この法律は長引く訴訟とより少ない和解をもたらすかもしれない。他の州は、コネチカット州、ニューヨーク州、イリノイ州、ミネソタ州を含み、類似した法律が可決されるか、あるいは連邦レベルで類似の法律が可決される可能性がある。
販売が私たちのある卸売業者、流通業者、個人支払者に集中している合併は私たちの業務にマイナス影響を与える可能性があります。
私たちの一部の流通業者、顧客、支払人は大きな購入レバーを持っています。これは彼らが私たちの製品の数を購入したからです。あるいは彼らが保険を提供してくれた患者の生命の数です。私たちのアメリカでの製品の大部分は3つの薬品卸売業者に販売されています:McKesson社、amerisourceBergen社、Cardinal Health,Inc.です。これらの流通業者は逆に彼らの顧客に私たちの製品を販売しています。これらの顧客は医者や彼らの診療所、透析センター、病院、薬局を含みます。同様に、上述したように、健康保険業は重大な統合が現れ、少数の医療保険管理人を含めて現在アメリカの保険総生命保険のかなりの割合を監督している。参照してください私たちの販売は政府と商業第三者支払者の保証と精算に依存しており、定価と精算圧力はすでに私たちの収益力に影響を与え続けている可能性があります米国最大のPBM 3社は現在主要な医療保険提供者の一部である。これらの実体がますます集中している購買力と交渉力は、彼らが私たちの製品の価格割引、他のサービスの費用、またはリベートを得ることができ、それによって私たちの交渉価格の地位、販売および/または利益率にマイナスの影響を与えるため、私たちの価格設定に圧力をかけ続ける可能性がある。さらに、調達量の理由により、これらのエンティティは、競争相手の製品を支援するために当社の製品を購入またはカバーしないことを決定し、私たちの製品販売、業務、および運営結果に大きな悪影響を及ぼす可能性がある。さらに、私たちの重要な卸売流通業者が財務や他の困難に遭遇した場合、その流通業者が私たちのすべてのお金を支払うことができないか、または支払いたくない場合、これは私たちの業務や運営結果にマイナスの影響を与える可能性がある。さらに、私たちの重要な卸売業者が倒産したり、他の方法で現在の形で私たちとビジネス関係を構築し続けることができない場合、私たちの業務を深刻に混乱させ、適切な代替案がタイムリーに見つからない限り、または損失した販売が別の販売業者に吸収されない限り、私たちの製品販売、私たちの業務、および運営結果に悪影響を及ぼす可能性がある。
研究開発に関わるリスク
私たちは研究開発に多くの資金を投入しているにもかかわらず、私たちは商業製品を開発できないかもしれない。
安進は研究開発に大量の資金を投入し、生物技術業界が成功した製品開発は非常に高い不確定性を持っており、研究開発プロジェクトが承認された商業実行可能性のある製品を産生することは少ない。生物学的に類似した候補製品、または既存製品の新しい適応(総称して候補製品と呼ばれる)を含む候補製品は、開発の初期段階では有望であるように見えるが、様々な理由で市場に進出できなかった
•候補製品は許容可能な臨床試験結果を示さず、それが主要な終点に達し、および/または陽性を示す前または早期臨床試験結果に達しても、原因は薬物看護標準の変化または衛生当局の期待を含む可能性がある
•候補製品は、特定の状況または疾患の治療において有効ではないか、または現在利用可能なまたは潜在的競争力を有する治療法よりも有効ではない
•既存または潜在的な競争療法によれば、候補製品のコスト効果は高くない
•候補製品は動物や人間に有害な副作用がある
•FDAやEMAのような必要な規制機関は、製品の予期される用途を承認していない
•規制部門が承認したにもかかわらず、候補製品の精算は限られている
•候補品は私たちの生産と商業化には割に合わない
•他の当事者は、特許権のような私たちの候補製品に関連する独占権を持っていたか、またはそれを合理的な条項で販売することを許可しなかったか、または全く許可されていなかった
•私たちと私たちのいくつかの許可者、パートナー、契約組織、または独立した調査者は、臨床開発または臨床製造活動を効率的に行うことができなかった
•候補製品の規制承認または補償を得るための方法は不確定または定義が不明確である
•候補生物類似製品は、適用される参照製品と必要な生物学的類似性を証明することができなかったか、または規制当局によって他の方法で適用された承認基準に適合していないと決定された
•候補製品の使用に必要なセット診断設備は必要な監督管理機関の許可を得ていない。
著者らはすでにかなりの時間、精力と資源を使って、人類遺伝学方面の専門知識を発展させ、そして遺伝情報バンクを訪問する機会を獲得し、遺伝学は有効に新薬を探すのを助けることができ、そして著者らの研究開発の決定と投資を指導するのを助けることができると信じている。我々は,遺伝子や他の納得できるヒト証拠によって検証された薬物標的に開発戦略の重点を置いている。しかし、遺伝子検証標的に基づく候補製品は依然として薬物開発過程の不確定性の影響を受け、上述した要素を含む多種の原因で発売できない可能性がある。
任意の候補製品や既存製品を新たな適応に適用し,商業化·販売する前に,人体で臨床試験を行わなければならない。
製品が販売できる前に、私たちの候補製品が人類の使用に安全かつ有効であることを証明するために、臨床試験を行わなければならない。これらの臨床試験の結果は,FDAやEMAなどの規制機関の承認を得るための基礎として用いられている。参照してください現在の製品と開発中の製品は監督部門の許可を得て販売してはいけませんそれは.製品ラベル宣言を支援するために,適切な数の試験地点と患者を用いた臨床試験が求められている。臨床試験に要する時間の長さ、試験地点数と患者数はそれぞれ異なり、著者らはいくつかの臨床試験を完成するのに数年かかる可能性があり、そして大量の費用を招くかもしれない。また,われわれの臨床試験に参加するのに十分な数の臨床試験場所および/または患者を見つけることは困難である可能性があり,特に競争相手が類似した患者群で臨床試験を行う場合。参照してください新冠肺炎の大流行及び公衆と政府が疾病伝播を抑制するための努力は、すでに著者らの臨床試験、運営、サプライチェーン、流通システム、製品開発、製品販売、業務と運営結果に不利な影響を与え、実質的な悪影響を与える可能性があると予想されている患者はいつでも臨床試験を脱退することができ、ある国のプライバシー法及び/或いはその他の制限は臨床試験研究者がこのような患者に対して更なるフォローアップを行う能力を制限する可能性があり、これは研究結果の解釈に不利な影響を与える可能性がある。遅延と複雑化
計画中の臨床試験は開発コストの増加、監督管理承認と候補製品の発売に関する遅延、及び現有製品ラベルの改訂を招く可能性がある。
また,われわれの臨床試験に登録可能な患者数を増加させるために,われわれはすでに臨床試験経験の限られた複数の場所に臨床サイトを開設し,インド,中国,韓国,フィリピン,シンガポール,一部の中米と南アメリカ国を含め,第三者契約臨床試験プロバイダを完全に利用するか,現地スタッフと組み合わせて使用するかを募集している。著者らの経験が限られているところで臨床試験を行うには大量の時間と資源が必要であり、個別国家の独特な監督管理環境を理解する。中国における臨床試験のリスクの他の例については,参照されたい私たちの販売と運営は新興市場を含む国際業務リスクの影響を受けていますそれは.また、私たちの候補製品の臨床供給が適時に生産、流通、そして多くの異なる臨床試験場所に提供されることを確保しなければならない。また、自然災害や人為的災害を含む地域的妨害、衛生緊急事態(例えば、私たちが現在経験している新冠肺炎事件)や地政学的衝突(例えば、ウクライナの持続的な武力衝突)は、臨床試験のスケジュールを深刻に乱しており、将来的には臨床試験の時間、実行、および結果を混乱させる可能性がある。私たちの臨床試験の設計、実行、様々な規制面を十分に管理できない場合、あるいは私たちの臨床供給の生産または流通を管理できない場合、あるいはこのようなサイトが自然/人為的災害、衛生緊急事態、または地政学的衝突によって中断され、対応する規制承認が延期される可能性があり、あるいは候補製品の承認を得ることができない可能性があり、あるいはいくつかの治療分野または全分野で既存製品をマーケティングする能力を失う可能性がある。例えば,われわれの臨床試験は新冠肺炎の大流行の悪影響を受けている。参照してください新冠肺炎の大流行及び公衆と政府が疾病伝播を抑制するための努力は、すでに著者らの臨床試験、運営、サプライチェーン、流通システム、製品開発、製品販売、業務と運営結果に不利な影響を与え、実質的な悪影響を与える可能性があると予想されている私たちが製品戦略を実行するのに必要な時間枠内で私たちの製品や候補製品をマーケティングして販売したり、承認を得ることができなければ、私たちの業務や運営結果は実質的な悪影響を受ける可能性があります。
著者らは独立した第三者臨床研究者に依存し、適用された研究方案、法律と法規に基づいて患者を募集し、著者らを代表して臨床試験を行った。また、私たちは独立した第三者サプライヤーに依存して、私たちの臨床試験操作のいくつかの側面を実行する。場合によっては、他の製薬や医療機器会社と共同開発計画を達成し、別の会社が私たちが共同開発した製品のためのいくつかの臨床試験を行うことを可能にしたり、私たちの臨床試験において患者をスクリーニングまたは監視するための診断試験を開発することができる。参照してください私たちのいくつかの薬品パイプラインや商業製品販売は第三者との協力に依存しており、これは私たちの製品の開発と販売に悪影響を及ぼす可能性があります私たちはまた、すでにまたは臨床試験を行っている会社、または臨床試験を行っている製品または候補製品の権利を買収することも可能である。これらの試験は私たちと同じ基準で行われていないかもしれないが、買収が完了すると、過去と未来にこれらの試験を行うことに関する任意の潜在的なリスクと責任を含むこれらの試験を行う責任を負う。規制当局が、私たちのライセンシーまたは共同開発パートナーを含む、または私たち、私たちの共同開発パートナー、または私たちが製品または候補製品の権利を取得または取得した会社によって選択された独立した調査者またはサプライヤーを含むと認定された場合、これらの当局は、臨床試験に適用される法規を遵守していない場合、これらの当局は、臨床試験データの一部または全部を拒否または拒否するか、または製品または適応の上場承認を取得または維持する可能性のある他の方法でマイナス影響を与える行動をとる可能性がある。そのほか、著者らの臨床試験のために診断テストの遅延或いは失敗はこのような試験の適時な登録に影響する可能性があり、そして遅延或いは上場許可を得られないことを招く可能性がある。もし私たちが私たちの製品や候補製品をマーケティングして販売することができなければ、私たちの業務と運営結果は実質的な悪影響を受けるかもしれません。
また,われわれのいくつかの臨床試験は他の製薬会社が生産·販売している薬剤を使用している。これらの薬剤は,我々の1つの製品や候補製品と連携して臨床試験を行うことができ,製品や候補製品の相対的有効性と安全性を比較する対面研究でも使用可能である。これらのサプライヤーまたは製薬会社のいずれかに予測不可能な問題が発生した場合、その作業製品の品質に負の影響を与えたり、供給不足をもたらしたり、他の薬剤の供給を他の方法で十分に得ることができない場合、適用される臨床試験を完了し、および/または臨床結果を評価する能力も悪影響を受ける可能性がある。したがって、このような品質または供給問題は、私たちが直ちに世界的に申請し、監督管理の承認を得たり、維持したりする能力に悪影響を及ぼす可能性がある。
臨床試験は通常現在の医療基準に基づいて設計されなければならない。しかし、いくつかの疾患では、例えば癌、看護基準が急速に変化している。場合によっては,我々が期待している研究完了時に存在する看護基準に基づいて臨床試験を設計する可能性がある。ある臨床試験を完成するのに要する時間はこのような臨床試験の設計は医療保健標準を基礎とする可能性があり、これらの標準はこのような試験が完成した時に現在の標準になっていないか、あるいはまだ現在の標準になっていないため、このような試験の効用と応用を制限している。また、監督管理機関の承認要求の加速に対する見方は時間の経過とともに変わる可能性があり、ある腫瘍学製品の承認加速を支持するのに十分な試験設計は十分ではないと考えられるかもしれない
後の候補者にとっては。有利な臨床試験結果が得られない可能性があるため、規制部門の新製品候補または既存製品の新適応の承認および/または現在の製品ラベルを維持することができない可能性がある。私たちの製品および候補製品の臨床試験の参加者はまた、不良な医療事象または副作用を受ける可能性があり、その中で、臨床試験計画を延期または終了する可能性があり、および/または承認を得るために追加的またはそれ以上の時間を必要とする可能性がある。
1つの製品が発売された後であっても、安全上の考慮のために、我々の製品リスク管理計画の一部として、追加的またはより広範な臨床試験が必要となるか、または新たな適応が承認される可能性がある。FDAが要求する臨床試験を含む他の臨床試験を開始することは、大量の追加費用をもたらす可能性があり、結果として、さらなるラベル制限または承認された適応に対する規制の承認を失う可能性があり、いずれも、私たちの製品販売、業務、および運営結果に実質的な悪影響を及ぼす可能性がある。また、このような試験のどんな負の結果も、承認の程度、私たちの製品の使用、精算と販売、私たちの業務と運営結果に大きな影響を与える可能性があります
私たちの現在の製品と開発中の製品は規制部門の承認なしでは販売できません。
私たちの業務はアメリカの多くの州と連邦政府機関(FDAを含む)および外国規制機関(EMAを含む)によって広く規制されている。私たちは、アメリカおよび私たちまたは私たちのパートナーと付属会社が製品を販売する他の地域と国/地域で、私たちの製品を製造、マーケティング、販売する前に規制機関の承認を得ることを要求しています。我々の製品が承認されると、FDAおよび他の米国および元米国規制機関は、追加のテストおよび報告、検査の実行、製品ラベルの変更、または私たちの製品の強制撤回を要求する権利がある。適用された規制要件を遵守しないことは、私たちに行政および/または司法制裁または罰金、そして名声および他の損害を受ける可能性がある。制裁には、FDAまたは前米国規制機関が未解決の申請の承認を拒否し、承認の遅延または撤回、臨床試験の遅延または一時停止、警告状、製品のリコールまたは差し押さえ、私たちの業務、禁止、罰金、民事処罰、および/または刑事起訴の完全または部分的な一時停止を含むことができる。
規制承認を得て維持することはずっとそうであり、ますます難しくなり、時間がかかり、高価になるだろう。立法機関または規制機関は、新しい法律または法規を随時制定し、既存の法律または法規を変更したり、法律または法規の解釈を変更したりすることができ、これは、私たちの製品または候補製品の承認を獲得または維持する能力に影響を与える可能性がある。市場の現有の法律法規と監督管理予想の変化の速度と程度が加速し、新興市場の監督管理期待は絶えず変化している。 医薬品および候補薬物製品に関連する製造業者の通信を管理する法律または法規の変化、およびこれらの変化が、私たちの製品販売、業務、および運営結果に大きな悪影響を及ぼすかどうかなど、私たちの業務に影響を与える法律または規制政策のさらなる変化が発生するかどうか、およびいつ発生するかを予測することはできません。しかも、私たちは規制機関が私たちの製品を評価して承認するために必要な資源を持っていることに依存する。米国では、2018年12月下旬から2019年1月下旬にかけて、連邦政府の一部停止により、多くの連邦機関とその従業員の作業が一時停止されている。その後の長時間の閉鎖は、我々が行っている臨床計画、私たちの製品および候補製品の製造、および私たちの製品承認を含むFDAの活動の減少または遅延をもたらす可能性がある。
規制機関はすでに未来に私たちが臨床試験のために選択した終点が承認されるのに十分かどうかに疑問を提起するかもしれない。著者らの多くの製品と候補製品はすでに臨床試験において代替終点を用いて評価され、これらの終点は最終臨床利益に関連することが知られている効果を測定した。例えば、治療腫瘍学的候補製品は、微小残留病(MRD)を減少または除去する能力に基づいて評価するか、または治療中および治療後の患者の生存期間を延長することによって、PFSによって測定することができる。候補製品がMRD陰性反応をもたらすか、またはPFSにおける統計的有意な改善をもたらすことは、必ずしも候補製品が全体生存率または患者生存時間において統計的に有意な改善を示すことを意味するとは限らない。心血管疾患治療環境において、低密度リポ蛋白レベルを低下させる能力に基づいて心臓病候補治療方案を評価することができ、上昇した低密度リポ蛋白レベルはすでに心血管イベント(例えば死亡、心臓発作と脳卒中)の代替終点になっているからである。他の臨床的利益測定が乏しい場合、PFSや低密度リポ蛋白-Cのような代替終点を使用することは、これらの結果が統計学的意義を有していても、広く使用または承認するのに十分ではないかもしれない。規制当局はまた、承認または適応を得るための条件として、検証的研究の登録または結果研究または結果研究を完了する意義のある部分のような新たな要求を追加することができる。例えば,Repathaは多くの患者の低密度リポ蛋白−Cレベルを低下させることを証明しているにもかかわらず, 著者らがRepathaが心血管イベントを予防する能力を評価した大型第三段階の結果研究がそのいくつかの主要な複合終点と肝心な二次複合終点に達した後、FDAはRepathaがある心血管イベントのリスクを低減するためにRepathaをより広く承認することを許可した。他の既存の治療レジメンに対する優位性を示すことができない限り、候補製品の有効性および安全性を証明することは、規制部門の承認を得るのに不十分である可能性もある。追加的な要求の適用や、私たちはこれらの要求を直ちに満たすことができないか、またはこれらの要求を完全に満たすことができず、将来的に私たちの臨床開発と監督管理申告を延期し、規制部門の新製品候補製品または既存製品に対する新しい適応の承認を得ることを延期または阻止するか、または既存の製品ラベルを維持することを阻止する可能性がある。
私たちの製品のいくつかは米国と元米国規制機関の加速承認または条件付き承認を得ており、完全に承認された条件は規制機関の要求を満たすことである。例えば、2021年5月には、FDAがLUMAKRAS加速承認を承認し、KRAS G 12 C変異の治療のための局所末期または転移性非小細胞肺癌成人患者を発表し、FDA承認試験に従って、これらの患者は以前に少なくとも1回のシステム治療を受けたことがある。この適応の持続的な承認は検証性試験中の臨床利益に対する検証と記述に依存し、FDAは著者らが発売後の試験を完成することを要求し、比較的に低い用量が著者らの発売前の試験で示した結果と類似した臨床効果があるかどうかを調べる。それ以来,我々はこのような発売後の試験データを受け取り,要求に応じてFDAに提出する予定である。規制当局は、最初に加速または条件付きで承認された製品の監視と、そのような製品の発起人が加速または条件付き承認の条件を満たしているかどうかをより重視している。もし私たちが規制機関の要求、すなわち製品の加速または条件付き承認の条件を満たすことができない場合、および/または規制機関が私たちの製品のデータやリスク利益プロファイルを再評価した場合、条件付き承認が完全な承認を招くか、撤回または更新されない可能性がある。あるいは、私たちは製品のラベル適応を変更し、製品を市場から撤回することを要求されるかもしれない。
監督管理部門はまた発売後の小児科研究要求を強制的に実施することができる。これらの要件を満たしていないことは、罰金や製品マーケティング許可の無効を含む規制または法執行行動を引き起こす可能性がある。
臨床試験(研究者が後援する研究を含む)で我々の製品や候補製品を評価する場合、あるいは臨床現場で我々が発売した製品を使用する場合、安全問題や信号が発生する可能性がある。私たちは、私たちに報告された不良事件を継続的に収集し、評価し、これらの不良事件と私たちの製品に関する安全信号を規制機関に伝達することを要求された。規制機関は定期的に私たちの有害事象報告を含めて私たちの薬物警戒プロセスを検査する。米国では,REMSによって承認された製品(項目1.企業−政府規制−承認後段階参照)については,REMSの目標が達成されていることを証明するために定期的な評価報告書をFDAに提出する必要がある。REMSおよび他のリスク管理計画は、1つの薬剤の利点がリスクよりも大きいことを保証し、それらに含まれる要素が異なることを保証することを目的としている。FDAが任意のREMSのために提出した定期的な評価報告書の結果に満足していない場合、FDAはまた、修正または制限ラベルを実施するなど、私たちのREMSを修正するか、または他の規制行動をとることができる。私たちの製品との併用が許可された薬物送達設備も監督監督と安全と故障審査を受けている。参照してください私たちのいくつかの製品は薬物送達またはセット診断装置と一緒に使用され、これらの設備自体に監督、製造、その他のリスクが存在するもし規制当局が私たちまたは他の当事者(私たちの臨床試験調査者、私たちの患者支援計画を操作する者、または私たちの製品の許可証取得者を含む)が適用された報告、他の薬物警戒、または他の安全または品質評価要件を遵守していないと判断した場合、私たちは罰金、マーケティング許可の撤回、および他の処罰を含む追加の検査、警告状、または他の法執行行動を受けるかもしれない。私たちの候補製品と発売製品はまた私たちと似たような製品や製品カテゴリ全体に関連する安全問題や信号の影響を受ける可能性があります。また,我々や他の人が行った臨床試験には,早期臨床試験のサブアナリシスやメタアナリシス(メタアナリシスは,様々な統計的手法を用いて以前の独立したが関連する研究結果を組み合わせることに関連する)が含まれているため,製品承認ラベルに基づくデータや研究の十分性が懸念される可能性がある。このような実際的または知覚されたセキュリティ問題または懸念は、:
•私たちの製品の修正や制限ラベル、または制限ラベルの可能性は、将来的に候補製品を商業化しないことを決定する可能性があります
•製品の普及および販売に関連するリスク管理または最小化活動または他の規制機関のコンプライアンス行動の要件;
•私たちが承認した製品の発売後の約束、強制発売後の要求または薬物警戒計画
•私たちが承認した製品のリコール
•私たちの製品の製造過程で使用されるプロセスを必要に変更することは、私たちの製造コストを増加させ、このような製造を支援するために使用できる契約メーカーの可用性に影響を与える可能性があります
•私たちの製品の市場承認を完全にまたは特定の治療分野または患者タイプで撤回すること
•FDAまたは他の規制機関によって承認された時間の延長または遅延;および/または
•規制機関によって承認されていない治療または候補製品。
例えば,EVENITYの1つである3期臨床試験で積極的に判定されたCV重篤な有害事象不平衡が観察された後,もう1つのより大きな3期研究では観察されず,FDAは2019年4月にEVENITYの使用を許可した
閉経後骨折リスクの高い女性の骨粗鬆症、及び発売後の要求を治療する。この要求には5年間の観察可能性研究が含まれており、その後比較安全性研究や試験が行われる可能性がある。
私たちの革新製品に加えて、現在他の製薬会社が製造、マーケティング、販売しているいくつかの製品の生物類似バージョンの開発と商業化に努めています。いくつかの市場では、生物模倣薬の立法や規制方法がまだ承認されていない。アメリカでは、“BPCIA”はそのような道を規定している。FDAと他の規制機関内部および規制機関とスポンサーとの間では,特定製品の生物学的類似性や互換性を証明するために必要な証拠について議論が続いている。参照してください我々は現在,生物模倣薬と後発薬からの競争に直面しており,将来的には生物模倣薬と模倣薬からの日々の激しい競争に直面することが予想される。このような経路の開発または実施の遅延または不確実性、または規制基準の低下を含む既存の規制経路の変化は、私たちの生物類似製品が規制機関の承認を得る遅延または困難をもたらす可能性があり、予期しない開発コストに直面したり、生物模倣薬分野での私たちの投資価値を他の方法で低下させたりする可能性がある。さらに、私たちは、いかなる潜在的な立法や政策措置が生物類似の経路にどの程度影響を与えるか、あるいは私たちの生物模倣薬の開発や私たちが発売している生物模倣薬に実質的な悪影響を及ぼすかを予測することができない。また、私たちの生物類似製品を直ちに市場に投入し、“率先して発売”または他の優勢な地位を確保できなければ、私たちの未来の生物類似製品の販売、業務、運営結果は実質的で不利な影響を受ける可能性がある。
私たちのいくつかの製品は薬物送達またはセット診断装置と一緒に使用され、これらの設備自体に監督、製造、その他のリスクが存在する。
私たちの多くの製品および候補製品は、注射器または他の送達システムのような薬物送達装置と組み合わせて使用することができる。例えば,NeulastaはNeulasta Onproキットの一部として提供されており,我々のAutoTouchは自動シリンジをENBREL Mini単剤予備充填カートリッジとともに再使用することができる。さらに、LUMAKRAS/LUMYKRASおよびbemarituzumabを含む、我々の多くの腫瘍候補製品および製品を含むいくつかの製品または候補製品は、患者が私たちの薬剤を使用する資格があるかどうかを決定するか、またはその安全で有効な使用を保証するためのデバイスのようなセットまたは他の診断デバイスを使用する必要があるかもしれない。アメリカを含むいくつかの地区では、監督機関はセット診断設備と治療製品が同時に許可を得ることを要求する可能性がある;他の地区では、監督機関はセット診断設備の単独研究を要求する可能性がある。そのようなデバイスの開発または承認が遅延し、そのようなデバイスも規制承認または許可を取得または維持していない場合、またはそのようなデバイスが商用化を継続できない場合、私たちの候補製品またはそのようなデバイスと共に使用される製品の拡張適応は、承認されないか、または規制承認を得る際に大幅に延期される可能性がある。単一上場薬物申請の下で製品や設備が承認を求める場合、審査過程の複雑さが増加し、規制部門の承認を受けることが延期される可能性がある。さらに、いくつかのデバイスは、単一ソースの非関連第三者会社によって提供される可能性がある。私たちは、場合によってはこれらの第三者会社の持続的な協力と努力に依存して、場合によってはデバイスを供給および/またはマーケティングする, 関連する規制機関が承認または承認した研究が行われる。私たちはまたその第三者会社たちが適用される規制や他の要求を満たし続けることに依存している。装置の開発、修正または供給に成功しなかったか、安進または第三者研究の遅延または失敗、または当社または第三者会社が設備の規制許可または許可を得ることができなかったか、または開発コストの増加を招く可能性があり、規制承認を遅延または維持することができなかったか、および/または候補製品の発売または既存製品のための新しい適応を増加させる関連遅延。私たちはまた、私たちのデバイスに関連するユーザ苦情、有害事象および故障、ならびに私たちの製品と共に使用されるデバイスの実際または感知されたセキュリティ問題または懸念を収集して評価することを要求され、規制行動および私たちの製品への悪影響をもたらす可能性がある。参照してください現在の製品と開発中の製品は監督部門の許可を得て販売してはいけませんそれは.また、規制機関は、私たちの設備の潜在的な問題を識別して評価するために、定期的な監視と検査を行う。例えば、2017年、FDAはその有害事象報告システムで、私たちのNeulasta Onproキットを評価していると報告した。その後、私たちは装置で受け取った製品の苦情を解決するために設備とラベル改善を実施した。私たちは不満事項と有害事象を持続的に監視し、必要に応じて追加的な改善措置を実施する。私たちの製品と一緒に使用する設備の規制承認を失うことは、私たちの製品が市場から上下する可能性もあるかもしれません。さらに、これらの設備の開発、供給、取得、または維持に成功しなければ、関連承認製品の販売に悪影響を及ぼす可能性がある。
私たちのいくつかの薬品パイプラインや商業製品販売は第三者との協力に依存しており、これは私たちの製品の開発と販売に悪影響を及ぼす可能性があります。
私たちは製薬やバイオテクノロジー会社、サプライヤー、サービスプロバイダを含む他の会社との連合に依存し、私たちの製薬パイプライン内の製品の一部を開発し、私たちのいくつかの商業製品を商業化し、販売しています。例えば、私たちは第三者と協力し、これらの協力に基づいて、開発権利、義務およびコストおよび/または商業権利と義務を共有する。項目1.業務-業務関係を参照。
もしこれらの当事者が私たちの契約、法規または他の義務を履行できなかった場合、または私たちとこれらの第三者との関係のいかなる中断も、私たちの薬品パイプラインおよびトラフィックに実質的な悪影響を及ぼす可能性がある。さらに、研究開発および/または商業化および販売における私たちの協力関係は、通常、長年継続されており、知的財産権および関連する権利および義務の所有権または起訴を含む、私たちと私たちのパートナーとの相対的な権利、義務および収入に関する紛争を引き起こす可能性がある。これは知的財産権や保護を失い、潜在的な薬品の開発と販売を延期し、私たちの商業化製品の販売と交付に影響を与え、長く高価な訴訟、行政訴訟、または仲裁を招く可能性がある
他の会社、製品または技術と協力したり、他社、製品または技術を買収したりする努力、および会社が買収した製品や技術を運営または支援する努力を統合することは、成功しない可能性があり、予期しないコスト、遅延、失敗を招き、取引のメリットを実現できない可能性がある。
我々は内部研究開発と外部取引における重大な投資を通じて革新を求め、協力、パートナーシップ、連盟、許可証、合弁企業、合併と買収(総称して買収活動と呼ぶ)を含む。買収活動は規制部門の承認や私たちの統制範囲内ではない他の要求を得る必要があるかもしれない。このような規制や他の承認を得ることは保証されず、私たちの買収活動に関連するすべての成約条件が満たされたり放棄される保証もなく、計画中の買収活動を達成できない可能性がある。また、規制機関の反独占審査および米国と外国の管轄区域の監督管理審査プロセスの変化は、承認が期待よりも長い時間を要し、得ることができない、あるいは重い条件を含む可能性があり、これは買収がもたらす予想利益を危険にさらし、延期したり、減少させたりする可能性があり、私たちの業務戦略の実行を阻害する可能性がある。
買収活動は複雑で、時間と費用がかかり、買収された会社と業務のわが社との統合に関連する意外なコスト、遅延或いはその他の運営或いは財務問題を招く可能性があり、これは私たちの管理層の他の業務問題と機会に対する注意を分散させ、このような取引を予想時間の枠組み内で制限するか、あるいは期待された利益を十分に達成できないかもしれない。私たちは買収活動を支払うために大量の現金を支払い、債務を発生させたり、株式証券を発行したりする可能性があり、これは私たちの流動性に悪影響を与えたり、株主がそれぞれ希釈されたりする可能性がある。さらに、新規従業員を統合または維持したり、私たちが買収した業務、製品または資産の運営(関連技術、商業運営、コンプライアンス計画、製造、流通、および一般業務運営およびプログラム、ならびにESG活動を含む)を統合することは、取引収益を達成し、業務を発展させる能力に影響を与え、資産減価または再構成費用を発生させる可能性がある。これらおよび他の挑戦は、私たちがOtezla、Five Prime、Teneobio、ChemoCentryx、Horizonおよび/または私たちが百済神州およびKKCとの協力または他の買収活動と関連している可能性があり、これは私たちの業務、運営業績、および株価に大きな悪影響を及ぼすかもしれない。
運営に関するリスク
私たちの大部分の商業製造活動はアメリカプエルトリコにある工場で行われ、私たちの臨床製造活動の大部分はカリフォルニア州千樫市にある工場で行われています。これらの施設の深刻な中断や生産故障は私たちの製品を供給したり、臨床試験を継続する能力を深刻に弱めるかもしれません。
私たちの商業販売と臨床試験のための製品と候補製品の世界的な供給は、私たちの製造施設の不連続かつ効率的な運営、特にアメリカ領プエルトリコとカリフォルニア州千樫市に位置する製造施設に大きく依存している。参照してください製造困難、中断、遅延は私たちの製品の供給を制限し、私たちの製品の販売を制限するかもしれません。
私たちは現在カリフォルニア州千樫市の工場で大部分の臨床製造を行い、私たちの候補製品を支持しています。私たちがアラカシ製造工場を運営する能力に重大な中断が発生し、私たちが臨床試験に候補製品を供給する能力に実質的な悪影響を与え、私たちの候補製品の開発遅延を招く可能性がある。
また、私たちの現在の商業製造活動の大部分は、私たちがアメリカ領プエルトリコにある工場で行われています。近年、プエルトリコはハリケーン·マリア(2017)、地震(2020)、ハリケーン·フィオナ(2022)など、多くの自然災害の影響を受けている。このような自然災害はすでにプエルトリコの公共財産と個人財産、電力網と通信ネットワークに影響を与え続ける可能性がある。我々の商業製造施設の重要な製造地域はこれらの自然災害の深刻な影響を受けていないが,ハリケーンマリアの後,島での電力サービスの回復は緩やかな過程であり,我々の施設はしばらく予備ディーゼル発電機に依存している。プエルトリコで2020年初めに地震が発生した後、予備発電機の数週間の操作も行った。2021年プエルトリコ電力局の基本負荷発電ユニット
10年以上の間十分な維持が不足し、全島の選択的停電を招いた。2022年9月、ハリケーン·フィオナが島の公共インフラをさらに破壊し、再び広範囲の停電と給水問題を招いた。これらの事件は私たちの業務に直接的な実質的な影響はありませんが、島での第三者サプライヤーの中断を招いています。電力網のさらなる不安定化には,発電機の使用増加,あるいは発電機のみの使用が要求される可能性がある。さらに、将来の嵐、地震、または他の自然または人為的な災害または事件(政治的動揺や労働力不足を含む)は、私たちの製造業運営により大きな影響を与える可能性がある。新型肺炎の流行はまた島の活動を中断させた。2020年3月、プエルトリコ総督は、企業や政府施設を封鎖し、企業経営を制限し、住民に夜間外出禁止を実施し、新冠肺炎に対応するよう行政命令を出した。また、2021年夏には、海運埠頭運営会社と国際埠頭労働者協会(ILA)に代表される従業員との間で労使紛争が発生し、ストライキが発生し、サンフアン港務区の貨物輸送が数日遅れた。ハリケーン·マリアとフィオナは、2020年の地震、新冠肺炎の大流行とイラストもすでに挑戦に直面していた台湾経済にさらに大きな圧力を与えた。2016年からプエルトリコ政府は約720億ドルの債務を滞納している。これに応じて、米議会はプエルトリコ監督、管理、経済安定法案を可決し、プエルトリコのための金融監督委員会を設置した。債券保有者と他の債権者と長年交渉した後, この金融監督委員会は米国プエルトリコ地域裁判所と合意し、2022年3月に発効した。これまで、私たちが製品を製造して供給する能力は、自然災害、信頼できない電力サービス、ストライキ、大流行病封鎖、または島経済挑戦の大きな影響を受けていなかったにもかかわらず、これらまたはこれらの挑戦の組み合わせや他の問題は、プエルトリコの製造施設を運営したり、用品や製品をその場所に輸送したり、その場所から輸送する能力に大きな妨害を与え、プエルトリコで事業を展開するコストをより高くまたは困難にする可能性があり、私たちの製品を供給する能力に実質的かつ悪影響を与える可能性があり、私たちの製品販売に影響を与える可能性がある。参照してください製造困難、中断あるいは遅延は私たちの製品の供給を制限し、私たちの製品の販売を制限するかもしれません.
私たちの特定の原材料、医療機器、そして部品は第三者供給者たちに依存している。
私たちは独立した第三者サプライヤーに依存して、私たちの商業と臨床製品を製造するために必要ないくつかの原材料、医療機器と部品を提供します。その中のいくつかの原材料、医療機器、および構成要素は、独立した第三者供給者の独自製品であり、規制機関に提出された薬品申請において明確に参照されているので、規制機関が供給者を承認しない限り、1つまたは複数の特定の唯一の供給源から取得しなければならない。例えばSureClickの単一のソースに依存しています Repatha、ENBREL、Aimovig、AMGEVITA、およびAranesp薬物送達のための自動注射器。さらに、我々の製品の商業および臨床製造に必要ないくつかの原材料は、哺乳動物組織、ウシ血清およびヒト血清アルブミンを含む他の国および/または生物由来の生物由来である。
これらの原材料や医療機器や部品を手に入れることができない理由は
•規制機関や他の側面の規制要件や行動;
•サプライヤーの不利な財務または他の戦略発展または影響は、破産を含む
•原材料、医療機器、部品の意外な需要や不足
•品質および製品の故障、製品汚染および/またはリコールをもたらす品質基準を遵守できませんでした
•材料不足、汚染、リコール、および/またはいくつかの生体由来物質または他の原材料の使用制限;
•以前に未知または検出されなかった欠陥が、原材料、医療機器または部品で発見された
•供給者システムへのネットワーク攻撃;
•ハリケーン、地震、火山、火災などの自然災害や他の災害
•労使紛争または不足は、突発的な衛生事件(例えば、私たちが現在経験している新冠肺炎などの新型ウイルスまたは流行病)または自然災害の影響を含む
•地政学的衝突。
例えば、数年前、私たちはプエルトリコ工場のいくつかの製品の調合、充填、表面処理に必要ないくつかの部品が不足し、私たちは使い捨てシステムと包装に関する不足を経験し、私たちの製造計画を中断させた。さらなる品質の問題は
いくつかの部品の意外な追加需要は不足を招き、将来的には必要な原材料または部品の不足を招く可能性がある(Epogenガラス瓶で経験したように)。私たちは未来に類似或いは他の不足に遭遇し、出荷遅延、供給制限、臨床試験遅延、契約紛争、および/あるいは私たちの製品の欠品を招く可能性があります。これらまたは他の同様のイベントは、製品の需要を満たすこと、または臨床試験を行う能力に悪影響を及ぼす可能性があり、これは、私たちの製品販売、業務、および運営結果に重大な悪影響を及ぼす可能性がある。
製造困難、中断、遅延は私たちの製品の供給を制限し、私たちの製品の販売を制限するかもしれません。
生物と小分子人体治療製品を生産することは困難であり、複雑と監督管理が厳しい。私たちの多くの商業製品と候補製品は国内で生産されている。さらに、私たちは現在、第三者契約製造業者を使用して、私たちの多くの製品を生産または協力しており、私たちは現在、いくつかの後期候補製品および薬物送達装置の生産を生産または協力するために契約メーカーを使用しています。項目1.業務−製造、流通、原材料−製造を参照。私たちの製品(および私たちの臨床試験を支援する候補製品)を十分かつタイムリーに製造し、供給する能力は、私たちの施設と私たちの第三者契約メーカーの施設の絶え間ないかつ効率的な運行に依存しており、これは以下の要素の影響を受ける可能性がある
•施設を作る能力
•微生物やウイルスや製造過程の外来粒子で汚染されています
•ハリケーン、地震、火山、火災などの自然災害や他の災害
•労使紛争や不足は、突発的な衛生事件(例えば、新型ウイルスまたは流行病、例えば、私たちが現在経験している新冠肺炎)や自然災害の影響を含む
•法規の要求を守る
•未来の需要の予測を変えることです
•生産運転の時間と実際の回数、生産成功率と生産量
•製造仕様を更新する
•私たちのサプライヤーと契約メーカーとの契約紛争;
•製品品質検査の時間と結果
•電力障害および/または他のユーティリティ障害;
•供給者システムへのネットワーク攻撃;
•デバイス(我々の情報技術システムおよびネットワーク制御システム、または私たちの契約製造業者または第三者サービスプロバイダのシステムを含む)の障害、障害、性能不良、またはインストールまたは動作が不適切である;
•FDAまたは外国規制機関は、その後の米国連邦または他の政府の延長による停止を含む必要な審査、検査、および承認の能力遅延を私たちに提供する
•地政学的衝突
上記または他の任意の問題が私たちの1つまたは複数の工場または第三者契約製造業者の生産に影響を及ぼす場合、または私たちの製品の需要または臨床試験に必要な候補製品数を正確に予測していない場合、影響を受けていない工場で生産を開始または増加させて需要を満たすことができない可能性がある。もし私たちの製品或いは候補製品の効率的な製造と供給が中断すれば、私たちは出荷遅延、臨床試験遅延、供給制限、欠品、不良事件傾向、契約紛争及び/或いは製品リコールの状況に遭遇する可能性があります。私たちは時々特定のロットの製品にリコールを開始する。例えば、2014年7月、EU流通のAranespロットが配布後の品質管理サンプルで粒子を検出した後、私たちは自発的なリコールを開始した;2018年4月、いくつかの製品ボトルの金属密封で潜在的なカール欠陥が発見された後、私たちは予防的なリコールを開始し、スイスで配布された2ロットのVectibixをリコールした。もし私たちがいつでも患者に絶え間ない製品供給を提供できなければ、私たちは患者を失う可能性があり、医者は私たちの製品ではなく競争療法を選択するかもしれません。これは私たちの製品販売、業務、運営結果に実質的な悪影響を与えるかもしれません。
私たちの製造過程、私たちの第三者契約メーカーの製造過程、そして私たちのいくつかの第三者サービスプロバイダの製造過程は、規制承認手続きを経て、FDAと他の監督管理機関の持続的な審査を受けなければならない。別の製造工場の建設、検証、許可には5年以上かかる可能性があるが、新たな契約メーカーまたはサービスプロバイダの資格認証および許可には3年以上かかる可能性がある。もし私たちが新しい法規の要求、既存の要求の新しい解釈、または他の理由で私たちの製造プロセスを変更することを要求された場合、これは私たちの製造コストを増加させ、出荷遅延、私たちの臨床試験の遅延、供給制限、欠品、不良事件の傾向、または契約交渉または紛争を招く可能性がある。もし私たちの既存の契約製造業者がこのような変化をタイムリーに実施することができないか、または全く望まない場合、このような製造挑戦も発生する可能性がある。
また、規制機関は、私たちの製造施設とプロセス、ならびに私たちの第三者契約製造業者とサービスプロバイダの施設とプロセスを定期的に監視し、検査しています。規制当局が、私たちまたは私たちの第三者契約製造業者または私たちのいくつかの第三者サービスプロバイダが規定に違反していると判断した場合、彼らは、私たちまたは影響を受けた第三者契約製造業者または第三者サービスプロバイダが遵守または無期限に遵守されるまで、是正措置および/または警告状を強制的に発行し、さらには、私たちの以前の承認を制限、一時停止または撤回し、私たちの製品の生産または臨床試験またはマーケティング製品の販売を禁止する可能性がある。別項参照私たちの現在の製品と開発中の製品は規制部門の承認なしでは販売できませんこのような問題は、規制機関が議論している製品、設備、またはプロセスと直接関係がなくても、規制機関が審査した候補製品の承認を延期する可能性がある。我々の第三者契約製造業者およびいくつかの第三者サービスプロバイダは、FDAおよび外国規制機関によって制約されているため、適格な第三者契約製造業者および第三者サービスプロバイダの代わりにタイムリーに入手できないか、または全く得られない可能性がある。私たちまたは私たちの第三者契約製造業者または第三者サービスプロバイダが生産を停止または中断した場合、または当社の第三者契約製造業者および第三者サービスプロバイダが材料、製品またはサービスを提供できなかった場合、出荷遅延、臨床試験遅延、供給制限、契約紛争、欠品および/または製品リコールに遭遇する可能性があります。また、私たちはアメリカケンタッキー州ルイビルの主な配送センターとオランダのレーダーのヨーロッパと世界の他の大部分の地域の主要な配送センターを通じて大量の商業製品を流通しています。私たちはまたヨーロッパと世界の他の大部分の地域で販売されている製品の大部分のラベルと包装を担当しています。私たちが製品を適時に供給する能力は私たちの配送と物流センター、私たちの第三者物流サプライヤー、そして私たちのレーダーのラベルと包装施設の絶え間ないと効率的な運営に依存します。また、私たちは航空便と海運を含む商業輸送に依存しており、私たちの製品を私たちの顧客に流通させており、これは進行中の新冠肺炎疫病の負の影響を受けており、自然災害や地政学的安全の脅威の負の影響を受ける可能性がある。
米国のより多くの薬品製造を奨励することを求める立法や行政提案もあり、米国の供給信頼性の向上を目指している。例えば,2020年8月6日,前回政府は基本薬,医療対策,キー投入の国内生産を促進するための行政命令を発表し,“基本薬品の確保,医療対策,米国生産へのキー投入に関する行政命令”と題した。また、ある立法は、米国退役軍人事務部が米国国外で生産された活性医薬成分を含むいくつかの薬剤の購入を禁止することを提案する。私たちの商業製造活動の大部分はアメリカで行われていますが、アメリカ領プエルトリコで行われていますが、私たちの臨床製造活動の大部分はカリフォルニア州千樫市にある工場で行われていますが、このような立法の採択は外国政府の報復立法や規制行動をもたらす可能性があり、これは私たちの製品販売、業務、運営結果に悪影響を及ぼす可能性があります。
私たちの業務と運営は、私たちの環境、社会、そしてガバナンス目標を達成できなかったり、失敗したと思われたりすることによってマイナスの影響を受ける可能性があります。
私たちは環境に責任を持って社会的に包容的に私たちの業務を運営するために努力し続けている。我々の投資家および従業員を含む利害関係者は、ますます注目され、私たちのESG実践に注目し続けることが予想される。私たちのESG実践がこれらの利害関係者の期待および基準を満たすことができない場合、私たちの名声、サービス、および最終的には私たちの株価に実質的な悪影響を及ぼす可能性がある。
我々のESG報告は、我々のウェブサイト上で提供され、調査、インタビュー、およびいくつかの企業責任フレームワークに基づいて、我々のESG目標および我々の外部および内部利害関係者にとって最も重要と考えられるESG問題における我々の進展を説明する。我々のESG目標を達成するためには、長期的な投資および広範で調整された活動が必要であり、我々は、我々のESG実践を監視、報告、および実施するために追加のコストを生成するか、または追加のリソースを割り当てる必要があるかもしれない。さらに、このような優先順位が変化し続けているので、利害関係者のESG優先順位を正確に評価することができない可能性がある。数年前に設定された目標の大部分を達成したが、現在および未来のESG目標を達成できるかどうかは依然として不確定であり、変化する規制要件およびESG実践に影響を与える社会的期待、多様な従業員の能力の採用、発展、保持、私たちのESG目標を達成できる供給者およびパートナーの可用性、わが業務の有機的な成長と潜在力の影響を含む多くのリスクの影響を受けている
他のサービスの買収は、我々のESGパフォーマンス、および炭素クレジットのような我々の目標をサポートする技術またはリソースの利用可能性およびコストに依存する。例えば、ウクライナの武力衝突が商品市場やサプライチェーンに与える影響は、電気自動車部品の供給を制限し、いくつかの環境持続可能な目標を達成する能力を損なう可能性がある。当社のESG計画の優先順位を満たしていないか、または満たされていないと考えられる場合は、当社の名声、サービス、および株価に大きな悪影響を及ぼす可能性があります。
世界的な気候変動や関連自然災害の影響は、私たちの業務や運営に悪影響を及ぼす可能性がある。
私たちの多くの業務と施設は、私たちの製造、研究開発、流通活動に重要な業務と施設を含み、干ばつ、火災、極端な温度、ハリケーン、熱帯嵐、および/または洪水を含む自然災害の影響を受けやすい地域に位置しています。例えば、2017年のハリケーンマリアはアメリカ領プエルトリコに悲劇的な破壊をもたらし、2022年のフィオナハリケーンは破壊を激化させ、私たちの商業製造活動の大部分はプエルトリコで行われた。私たちのサイトはよく保護されていて、被害が小さいにもかかわらず、私たちが未来の自然災害の前でも似たような結果になる保証はありません。世界的な気候変動は天気に関連する自然災害の深刻さと頻度を拡大し、拡大し続けることが予想される。このような自然災害は、将来的には私たちの運営に損害および/または中断をもたらす可能性があり、これは、私たちの製品販売、業務、および運営結果に大きな悪影響を及ぼす可能性があります。私たちのサプライヤー、サプライヤー、ビジネスパートナーも同様のリスクに直面しており、彼らの運営のいかなる中断も私たちのサプライチェーンと製造チェーンに悪影響を及ぼす可能性があります。また、私たちの多くの重要な施設はプエルトリコ、シンガポール、アイルランドを含む島に位置しており、これらの島は基本的な港施設に依存しており、これらの施設は気候変動や他の自然災害の影響を受けやすいかもしれない。詳細な業務連続計画を策定し、定期的に自然災害リスクを評価しているにもかかわらず、いかなる自然災害も当社の重要な運営や業務活動を長期的に中断させる可能性があり、このような自然災害の影響を修復し、運営を全面的に再開するために巨額のコストが必要となる可能性があり、製品販売、業務、運営結果に大きな悪影響を与える可能性がある。参照してください私たちの大部分の商業製造活動はアメリカのプエルトリコにある工場で行われています。私たちの臨床製造活動の大部分はカリフォルニア州の千樫市にある工場で行われています。これらの施設の深刻な中断や生産故障は私たちの製品を供給したり、臨床試験を継続する能力を深刻に弱めるかもしれませんそして製造困難、中断、遅延は私たちの製品の供給を制限し、私たちの製品の販売を制限するかもしれません。
一般リスク因子
世界的な経済状況は私たちに否定的な影響を与える可能性があり、私たちの業務に影響を及ぼすいくつかのリスクを拡大する可能性がある。
私たちの業務と業績はずっと影響を受けており、世界経済状況の影響を受け続ける可能性がある。新冠肺炎大流行病による経済衰退は世界的な衰退を引き起こし、さらにある地域で出現した高インフレ率とエネルギー供給問題に加え、地域と(あるいは)世界のマクロ経済挑戦を招き、その影響は長期的である可能性がある。特に,エネルギーコストの急激な上昇は欧州の生産性や経済状況にさらに悪影響を及ぼす可能性がある。また,財政的圧力は,政府や他の第三者支払者が医療や他の環境においてコスト制御措置をより積極的に求めることになる可能性がある。参照してください私たちの販売は政府と商業第三者支払者の保証と精算に依存しており、定価と精算圧力はすでに私たちの収益力に影響を与え続けている可能性があります世界経済状況のため、一部の第三者支払者はその返済義務を延期または履行できない可能性がある。失業または他の経済的困難(インフレを含む)は、自己負担または控除可能義務の増加、既存の自己支払いまたは控除可能義務に対するより高いコスト感受性、医療保険カバー範囲の喪失、または他の理由によって、患者が医療保健を支払う能力に影響を与える可能性もある。このような状況は、私たちの製品に対する需要の減少を招き続ける可能性があり、これは私たちの製品販売、業務、運営結果に実質的な悪影響を及ぼす可能性があると信じています。現在の総需要増加に関連するインフレ環境、サプライチェーン制限、ウクライナ武力衝突の影響(衝突に対応するための制裁の影響、それによる商品市場やサプライチェーンへの影響を含む)も私たちの業務費用を増加させ、引き続き私たちの業務費用に影響を与える可能性がある。我々の運営コストは,エネルギー,材料,労働力,流通コスト,その他の運営や施設コストを含め,市場状況の影響を受け,インフレ圧力の悪影響を受けている。経済状況は、私たちの流通業者、顧客、サプライヤーが在庫や原材料を購入するために必要な流動性を獲得し、私たちと合意した義務を履行する能力に悪影響を及ぼす可能性もあり、私たちの運営を混乱させる可能性があります。私たちは流通業者、顧客、サプライヤーの財務状況とその流動性を監視して私たちの業務リスクを低下させますが、私たちのいくつかの流通業者、顧客、サプライヤーは債務を返済しないかもしれません。これは私たちの製品販売、業務、運営結果に重大な悪影響を及ぼす可能性があります。世界の経済状況の著しい悪化は本明細書に記載された他のリスクを引き起こすか、または実質的に増幅する.
私たちは大量のポートフォリオを持っていて、私たちの総合貸借対照表に現金等価物と有価証券の形で開示されています。新冠肺炎の世界的な広がりはまた、世界の資本市場の混乱と変動を招いた。私たちは株式投資を含めて、市場変動の影響を受けるかもしれない、持続的な資産を持っています
繰り返し発生する一連の市場混乱は、減値を招く。私たちの投資価値はまた、金利変動、インフレ、信用格付けの引き下げ、資本市場の流動性不足、その他、私たちの投資価値の一時的な低下を招く可能性のある要因の悪影響を受ける可能性がある。これらの事件のいずれも、ポートフォリオの減価費用を記録したり、投資販売の損失を達成したりする可能性がある。
私たちの株価は変動が大きい。
バイオテクノロジーと製薬産業の同業者と同じように、私たちの株価も不安定だ。様々な理由で、私たちの収入と経営業績は異なる時期に変動する可能性があります。製品開発の遅延、私たちの期待あるいは戦略の変化、甚だしきに至っては比較的小さい収入不足などの事件は、一定期間の財務業績が私たちの予想や予測を下回る可能性がある。したがって、私たちの収入と経営業績、そして私たちの株価は大きな変動の影響を受ける可能性があります。政府または個人支払者がとる可能性のある制限行動の公告または議論(ソーシャルメディアチャネルを介したことを含む)は、最終的に実施または採用される場合、私たちの業務または業界に負の影響を与え、そのような制限行動が実際に発生しているかどうかにかかわらず、私たちの株価変動を引き起こす可能性がある。同様に、我々の製品又は類似製品の実際又は感知された安全問題又は意外な臨床試験結果は、我々の株価に直接的な影響を与える可能性があり、我々の経営業績が実質的な影響を受けるか否かにかかわらず、我々の株価に顕著な影響を与える可能性がある。
私たちは私たちに有利な条項で資本と信用市場に入ることができないかもしれないし、全く入らないかもしれない。
資本と信用市場は極端な変動と混乱を経験する可能性があり、これは借り手や投資家に不確実性と流動性の問題をもたらす可能性がある。例えば、2020年初め、商業手形市場に深刻な混乱が生じ、いくつかの借り手が正常金利や満期日に資金を得ることができず、銀行から抽出された企業信用限度額が大幅に増加した。同様に、債券市場は金利と信用利差の面で極端な変動を経験しており、数日で新たに発行された社債はない。私たちは時々資本市場を利用して、私たちの既存の資金と運営によって生成された現金を補充して、私たちの運営資本の需要を満たすことを望みます。資本支出と債務超過要求、私たちの配当金の支払いと株の買い戻し計画、およびHorizonの買収や許可活動など、私たちの戦略的に計画されている他の業務措置を実施します。不利な資本や信用市場の状況が生じた場合、同様の有利な条件で資本市場融資を得ることができない場合や、資本市場融資をまったく得ることができない可能性があり、私たちの業務や運営結果や事業買収を完了する能力に大きな悪影響を及ぼす可能性がある。国が認可した信用格付け機関が発表した信用格付けの変化は、資本市場融資を受ける能力やこのような融資のコストに悪影響を与え、わが証券の市場価格に悪影響を及ぼす可能性がある。
ない。
2022年12月31日まで、私たちは約150カ所の不動産を所有またはレンタルしました。次の表に重要物件の位置と主な機能をまとめた
| | | | | | | | | | | | | | | | | | | | |
| アメリカの場所: | 製造業 | 行政性 | 研究開発 | 販売とマーケティング | 貨物倉庫 | 配送センター |
| カリフォルニア州千樫市* | P | P | P | P | P | P |
| カリフォルニア州サンフランシスコ | | | P | | | |
| ケンタッキー州ルイビル | | | | | P | P |
| マサチューセッツ州ケンブリッジ | | | P | | | |
| プエルトリコジュコス | P | P | | | P | P |
| ミズーリ州シグリニッジ | P | P | | | P | |
| フロリダ州タンパ市 | | P | | | | |
| アメリカの他の都市 | | P | | P | | |
* 会社本部
| | | | | | | | | | | | | | | | | | | | |
| 行位置: | 製造業 | 行政性 | 研究開発 | 販売とマーケティング | 貨物倉庫 | 配送センター |
| ブラジル | P | P | | P | P | P |
| カナダ | | P | P | P | | |
| 中国 | | P | | P | | |
| デンマーク | | P | P | P | | |
| ドイツ | | P | P | P | | |
| アイスランド | | P | P | | | |
| アイルランド | P | P | | P | P | P |
| 日本です | | P | | P | | |
| オランダ | P | P | | P | P | P |
| シンガポール.シンガポール | P | P | | P | P | |
| スイス | | P | | P | | |
| イギリス.イギリス | | P | P | P | | |
| 他の国 | | P | P | P | P | |
上記の資料には,(I)放棄された未開発土地および賃貸物件,および(Ii)我々が所有しているが我々の業務には使用されていないいくつかの建物は含まれていない。私たちが持っている財産には何の物質的負担もない。
私たちの施設は彼らの予想される用途に適しており、私たちの第三者契約製造協定と組み合わせて、私たちの予想される需要を満たすのに十分な生産能力を提供すると信じています。第1 A項を参照。リスク要因は、私たちの製造業務や私たちの製品のグローバル供給に悪影響を及ぼす可能性のある要因を検討します。
項目1.業務--製造、流通、原材料を参照。
私たちが参加したいくつかの法律手続きは、連結財務諸表の第4部である付記19“または事項および引受”で議論され、ここに参考に入れられる。
適用されません。
第II部
| | | | | |
| 五番目です。 | 登録者普通株市場、関連株主事項、発行者による株式証券の購入 |
普通株
私たちの普通株はナスダック世界の精選市場で取引され、コードはAMGNです。2023年2月6日現在、私たちの普通株は約4838人の登録保有者がいます。
性能グラフ
次の図は2017年12月31日の安進普通株、アメリカ運通生物技術指数、アメリカ運通製薬指数と標準プール500指数に対する各100ドルの投資価値を示している。すべての価値は配当税前価値の再投資を仮定し、毎年12月31日まで計算される。業績グラフに示されている会社普通株の歴史的株価表現は、必ずしも未来の株価表現を示しているとは限らない。
| | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | |
| 12/31/2017 | | 12/31/2018 | | 12/31/2019 | | 12/31/2020 | | 12/31/2021 | | 12/31/2022 |
| 安進(Amgen) | $100.00 | | $115.08 | | $146.87 | | $143.93 | | $145.19 | | $174.94 |
| アメリカンエキスプレスバイオテクノロジー(Amex Biotech) | $100.00 | | $100.26 | | $120.75 | | $137.14 | | $132.31 | | $127.01 |
| アメリカン·エキスプレス(Amex Pharmtics) | $100.00 | | $107.45 | | $127.20 | | $138.31 | | $170.64 | | $183.88 |
| 標準プール500指数(S&P 500) | $100.00 | | $95.63 | | $125.73 | | $148.86 | | $191.54 | | $156.74 |
上記業績グラフ中の材料は募集材料ではなく、米国証券取引委員会に届出されたものとはみなされず、引用によって当社が証券法や取引法に基づいて提出したいかなる届出文書にも組み込まれておらず、当該書類が本届出書類の日、前または後に作成されていても、当該書類中の任意の一般登録言語にかかわらず、含まれている。
株買い戻し計画
2022年12月31日までの3ヶ月と年度内に、未完成の株式買い戻し計画があり、この計画によると、買い戻し活動は以下の通りである
| | | | | | | | | | | | | | | | | | | | | | | | | | |
| | 合計する
量
株
購入した | | 平均値 支払いの価格 1株当たり(1) | | 総数
の株
購入方式は
部分
公
宣言
もくろみ | | 最大額 価値可能性 しかしまだ購入されます はい もくろみ(2) |
| 十月一日-十月三十一日 | | — | | | | | — | | | $ | 6,979,263,848 | |
| 十一月一日-十一月三十日 | | — | | | | | — | | | $ | 6,979,263,848 | |
| 十二月一日-十二月三十一日 | | — | | | | | — | | | $ | 6,979,263,848 | |
| | — | | | | | — | | | |
一月一日-十二月三十一日(3) | | 26,147,900 | | | $ | 241.32 | | | 26,147,900 | | | |
(1)1株当たりの平均支払い価格には関連費用が含まれています。
(2)2022年10月、私たちの取締役会は株式買い戻し計画に基づいて24億ドルのライセンス金額を追加しました。
(3)第三者金融機関と締結した売掛金協定の影響を含め、同協定に基づき、1株当たり約242.09ドルの価格で計24,784,400株の普通株を交付した。
配当をする
2022年と2021年12月31日までの数年間、私たちは四半期配当金を支払った。今後どの配当金の金額と時間は取締役会の承認を待たなければならないにもかかわらず、四半期配当金の支払いを継続する予定だ。本プロジェクトによって要求される他の情報は、連結財務諸表において第4の部分-付記16“株主権益”を参照して組み込まれる。
既存持分補償計画に基づいて発行された証券
既存持分補償計画に従って発行された証券に関する情報は、第3部第12項-既存持分補償計画に従って発行された証券を参照することによって発行される。
以下のMD&Aは,読者が安進の業務を理解するのを支援することを目的としている.MD&Aは我々の総合財務諸表と付記の補足であり,それと併せて読むべきである.我々がMD&Aで検討した操作結果はGAAPと一致する.安進はただ一つの業務部門を経営している:人間療法。したがって、私たちは総合的な基礎の上で私たちの運営結果について議論するつもりだ。
前向きに陳述する
この報告書と私たちがアメリカ証券取引委員会に提出した他の文書は、私たち、私たちの未来の業績、私たちの業務、私たちの信念、および私たちの経営陣の仮定に対する現在の予想、推定、予測、および予測に基づく前向きな声明を含む。さらに、私たちまたは私たちを代表する他の人は、プレスリリース、書面声明、または通常の業務中に会議、ネットワーク放送、電話、および電話会議を介して投資家およびアナリストとのコミュニケーションおよび討論で前向きな声明を発表することができるかもしれません。“期待”、“予想”、“展望”、“可能”、“目標”、“プロジェクト”、“計画”、“計画”、“信じる”、“求める”、“推定する”、“すべき”、“可能”、“仮説”および“継続”などの語彙、およびそのような語彙および類似表現の変形は、このような前向き表現を識別することを意図している。これらの陳述は未来の業績の保証ではなく、それらはいくつかの予測困難なリスク、不確定要素、仮説に関連している。第1部1 A項では、私たちがそれぞれ業務成果に影響を与える可能性のあるリスク、不確実性、仮説について説明します。リスク要因です我々の前向きな陳述は,経営陣が前向きな陳述を行う際に把握した情報に基づいている経営陣の信念と仮定に基づいている。私たちはあなたに実際の結果と結果が私たちの前向きな陳述で表現されたこと、暗示的、または予測された内容と大きく異なる可能性があるということを想起させる。本文は特に製品販売、監督管理活動、臨床試験結果、精算、費用、1株当たり収益、流動性と資本資源、傾向、計画配当、株買い戻し、協力と流行病の影響に関する展望性表現に言及した。連邦証券法と米国証券取引委員会の規則要件を除いて, 私たちは、新しい情報、未来のイベント、仮説の変化、または他の理由による、本報告書の配布後に任意の前向きな陳述を公開更新する意図または義務はありません。
概要
安進は生物技術会社であり、深刻な疾病を有する患者のために生物学的潜在力を放出することに力を入れている。1980年以来,バイオテクノロジーの先駆者として,安進は世界をリードする独立バイオテクノロジー会社の一つに成長し,世界各地の数百万人の患者に接触し,分離潜在力のある薬物パイプラインを開発している。
主な製品はENBREL、PROLIA、OTEZLA、XGEVA、ARANESP、NPLATE、Repatha、Kyprolis、Neulasta、EVENITYです。MVASI、Vectibix、BLINCyTO、Epogen、AMGEVITA、Aimovig、Parsabiv、KANJINTI、LUMAKRAS/LUMYKRAS、TEZSPIRE、NEUPOGEN、SENSIPAR/MIMPAR、TAVNEOSなど、多くの他の製品も販売しています。当社の製品についての詳細は、第1部、項目1.ビジネス-マーケティング、流通、および厳選されたマーケティング製品を参照してください。
私たちの戦略は産業における私たちの競争的地位を強化するための総合的な活動を含む。著者らは6つの商業領域で業務を展開した:炎症、腫瘍学/血液学、骨健康、心血管疾患、腎臓病と神経科学。著者らは主に三つの治療領域で発見研究を行った:炎症、腫瘍学/血液学と一般医学。2022年、私たちは革新的なパイプを推進し、国際業務を発展させ、戦略的取引を完成し、私たちのマーケティング製品の組み合わせを拡大し、Horizonを買収する意図を発表し、新冠肺炎流行の3年目に引き続き世界的に私たちの薬品を提供した。私たちはこれらの目標を達成し、戦略と規律を維持した資本分配方法を維持し、私たちのESG努力を進めた。
2022年、私たちは引き続き私たちの計画を推進し、末期結腸直腸癌のためのLUMAKRAS/LUMYKRAS、CV疾患のためのオパシラン、およびアトピー性皮膚炎のためのロカチリムを含む一連の計画の第3段階臨床試験を開始した。EUと日本でTEZSPIREのキー規制承認を得ることを含め、私たちの国際業務を発展させていきます。我々の2022年の外部業務開発活動には,ChemoCentryxの買収,最近発売されたTAVNEOSを炎症製品の組合せに追加することが含まれている。私たちはまた新しい市場で私たちの生物類似計画を推進し続けている。私たちの生物模倣薬は2023年1月にアメリカで発売されたAMJEVITAを含む2023年全体で新しい市場で発売される予定だ。
2022年の間、全世界の大流行から次第に回復し、生物模倣薬と後発薬からの日々の激しい競争に直面しているが、製品の総売上高は2%増加し、主にあるブランドの販売量の増加によるものであるが、ある製品の純販売価格の低下と不利な外貨為替レートの変化はこの増加を部分的に相殺した。米国の製品売上高が3%増加したのは、主に販売量の増加、一部は純販売価格の低下によって相殺されたが、連続的に増加したのは1%であり、主に販売量の増加により、一部は外国為替レートの不利な変化と純販売価格の低下によって相殺された。総運営費が9%低下したのは,Five Primeの取得した知的財産権の研究開発抹消および2021年にKKCに支払われた許可に関する前金が原因であったが,一部は2022年の非戦略的資産剥離の損失によって相殺された。
経営活動からのキャッシュフローは合計97億ドルであり、これは我々の業務への投資を支援するとともに、現金配当金と株式買い戻しを支払うことで株主に資金を返還する。2022年には、四半期現金配当金を1株当たり1.94ドルに10%増加させた。2022年12月、2023年第1四半期の普通株の1株当たり現金配当金は2.13ドルで、同期は10%増加し、2023年3月に支払うと発表した。私たちは2022年に2610万株の普通株を買い戻し、総コストは63億ドルだった。2022年には69億ドルの債券発行純収益を受け取り、3億ドルの債務を解消した。2022年12月,Horizonの提案買収については,過渡的信用協定と定期融資信用協定を締結し,合計285億ドルの借入金を規定した。
安進の人力資本資源管理方法と投資は人材を誘致、激励、発展と維持し、革新薬物の発見、開発と商業化に専念する経営企業の挑戦に対応することを目的としている。私たちの報酬、福祉、発展計画は、業績を奨励し、責任を促進し、会社の価値観を遵守し、会社の株主の利益と一致することを目的としています。また、多様性と包括的な文化が革新を促進し、患者に奉仕する能力を支持すると信じている。私たちは多様性、包容性、帰属感への関心を改善するために活動を展開し、目標を設定している。これらの努力や他の努力のさらなる資料については,第1部,項目1.業務である人的資本資源を参照されたい。
私たちには環境に責任を負う長期的な抱負があり、私たちは常に目標を設定し、自分に挑戦し、さらなる改善を実現しています。私たちは2013-2020年期間の目標を達成し、同期収入は増加し、生産能力は増加し、約100カ国に拡大した。より良い環境持続可能性を実現し続けるために,2021年1月までに炭素中和の実現,用水使用量の40%削減,廃棄物処理の75%削減を含む新たな長期環境目標を発表した。(1)(2) また、2022年には、特定の基準に適合した合格項目に資金を提供し、環境への影響を減らすための最初のグリーン債券を発行した。
私たちの長期的な成功は、革新的な製品を発見、開発、商業化し続ける能力と、他社が現在開発している治療法を買収または協力する能力に大きく依存している。私たちは収入増加を実現し、製品の独占経営権を失ったり、競争製品を発売したことによる収入損失を補うために新製品を開発しなければならない。私たちのいくつかの製品は生物模倣薬と模倣薬を含むますます大きな競争圧力に直面している。その他の情報には、各種製品特許の満了に関する情報が含まれており、第1部分、項目1.企業--マーケティング、流通および精選上場製品である特許、および第1部分、プロジェクト1.企業--マーケティング、流通および精選マーケティング製品--競争を参照する。我々は研究開発活動に大量の資源を投入したが,バイオテクノロジー業界の製品開発の成否には大きな不確実性がある。私たちはまた、製品発売前後の安全性と有効性のますます厳しい監督管理審査に直面している。
上昇し続ける医療コスト、不確定なマクロ経済状況(より高いインフレと上昇する金利を含む)、および地政学的衝突は引き続き私たちの業務に挑戦となっている。公共および民間の医療保健提供者の関心により、この業界は純価格の低下を含むコスト制御措置と重大な価格設定圧力の影響を受け続けている。また,アイルランド共和軍の規定を含む医療支出削減のための立法は,我々の業務に影響を与え続ける可能性がある。最後に、卸売とエンドユーザーの購入モードは私たちの製品販売に影響を与えます。これらの購入パターンは四半期製品売上高の変動を招く可能性があるが,通年製品表現を前年と比較した場合,これまでは通常は明らかではなかった。第1部分、プロジェクト1.ビジネス--マーケティング、流通、および選択された上場製品、ならびに第1部分、プロジェクト1 Aを参照。リスク要素は、私たちの未来の製品販売に影響を与える可能性のある要素をさらに議論するために。
新冠肺炎が大流行する
2020年の大流行が勃発して以来、私たちは大流行が私たちの全世界業務に与える影響を密接に監視してきた。従業員が直面するリスクを最小限に抑えるための適切な措置を継続し、その中の相当部分の従業員が仮想的な仕事を続けている。これまで、私たちの遠隔作業スケジュールは重要な業務運営を維持する能力に大きな影響を与えておらず、薬品供給の中断や不足にも遭遇していない。
大流行期間中、患者が医師室を受診する頻度の変動が既存の患者に治療を提供し、新しい患者の診断を減少させたため、私たちのいくつかの製品に対する需要は変化した。2021年には受診率と診断率が徐々に回復し,大流行前のレベルに近づいた。2022年、大流行は引き続き医療部門と私たちの業務に影響を与え、私たちの市場で異なる程度の影響を与えている。2022年には,アジア太平洋地域が1年の大部分で封鎖の影響を受けているほか,受診者数や需要パターンがより安定しており,ウイルス急増に直面している地域でも同様であることが分かった。新冠肺炎の発売以来の変化、変種の急増を含むため、著者らは未来のウイルス急増が著者らの業務に与える影響を予測できず、そして引き続き新冠肺炎が著者らの業務と更に広範な医療保健業界に与える影響を密接に注目する。
2021年初め以来、新冠肺炎の疫病をコントロールする努力はずっと行われている。しかし、大流行の持続的な発展の軌跡については、これらの活動の効力には依然として不確実性が存在する。ワクチン接種が直面している挑戦、新しい変種とウイルス伝播の他の原因は各国政府が異なる地区の制限と/或いは閉鎖要求を変える必要があるかもしれない。したがって,各国政府が現在の現地状況に反応するにつれて,少なくとも大流行期間中に疫病は持続的に変動することが予想される
われわれの臨床試験活動では,新変種の変化を含めて新冠肺炎感染率を継続的にモニタリングしており,われわれの臨床試験の将来の研究登録への影響を軽減するために努力しており,すべての関連国の影響を評価している。私たちは依然として私たちの活発な臨床サイトを支持して患者に看護を提供し、研究薬物の供給を提供することに集中している。新冠肺炎の大流行が我々の結果にもたらす可能性のあるリスクに関する検討は、第1部、項目1 Aを参照されたい。本表の格子10−Kのリスク要因。
(1) 代表的な既定基準に対する削減は,確認された削減項目のみを考慮し,会社の収縮や拡張に関する変化は考慮しない.
(2)炭素中和目標とは範囲1と範囲2である。
財務情報を精選する
以下は、私たちの運営結果の概要です(百万単位で、百分率および1株当たりのデータは含まれていません)
| | | | | | | | | | | | | | | | | |
| 2022年12月31日までの年度 | | 変わる | | 2021年12月31日までの年度 |
| 製品販売: | | | | | |
| アメリカです。 | $ | 17,743 | | | 3 | % | | $ | 17,286 | |
| はい | 7,058 | | | 1 | % | | 7,011 | |
| 製品総売上高 | 24,801 | | | 2 | % | | 24,297 | |
| その他の収入 | 1,522 | | | (10) | % | | 1,682 | |
| 総収入 | $ | 26,323 | | | 1 | % | | $ | 25,979 | |
| 運営費 | $ | 16,757 | | | (9) | % | | $ | 18,340 | |
| 営業収入 | $ | 9,566 | | | 25 | % | | $ | 7,639 | |
| 純収入 | $ | 6,552 | | | 11 | % | | $ | 5,893 | |
| 1株当たりの収益を薄める | $ | 12.11 | | | 18 | % | | $ | 10.28 | |
| 希釈後株 | 541 | | | (6) | % | | 573 | |
製品販売の変化に関する以下の議論では、販売量の増加や低下に言及した内容は、医療保健提供者(例えば、医師や彼らの診療所)、透析センター、病院、薬局が私たちの製品を購入する変化を指す。また、在庫の増加または減少に関するいずれの引き上げ方法も、卸顧客およびエンドユーザ(例えば薬局)が保有する在庫の変化を意味する。
2022年の製品総売上高の増加は、主にあるブランドの販売量の増加に推進され、Repatha、Prolia、EVENITY、Nplate、LUMAKRAS/LUMYKRAS、Kyprolis、OtezlaとTEZSPIREであるが、一部はNeulasta、RepathaとMVASIを含むいくつかの製品の純販売価格の低下及び為替レートの不利な変化によって相殺される。2023年には、競争激化に押されて、純販売価格はポートフォリオレベルで低下し続けると予想される。また,歴史的には,1年中第1四半期は1年間で製品売上が最も低い四半期であり,一部の原因は計画変化,保険再確認および米国患者が免責額で働いた場合の自己負担費用の増加,特に薬局福祉計画で得られた製品である。
マクロ経済状況が不確定なため、外貨為替レートをめぐる変動が続くことが予想される。為替レートの不利な変化の影響は私たちの国際運営費用の相応の減少分によって相殺されるだろう。私たちのヘッジ活動は外貨変化に完全に対応するためではありませんが、私たちのヘッジ活動も私たちの純外貨開放を突破しようとしています。主にユーロ建ての製品販売について、私たちの純収入への影響をある程度相殺しようとしています。
以上のように,新冠肺炎の流行により需要が減少し,我々の製品販売が影響を受けている。全体的に言えば、大流行の最初の数ヶ月で、大流行の動態は私たちの製品販売に最も影響を与え、需要は2020年末からいくつかの回復を示した。2021年末と2022年初めには、ウイルス変種(オミックを含む)による感染率の上昇によりヘルスケア部門の能力が減弱し、当社自身の営業日が減少し、業務に影響を与えています。2022年第2四半期までに、これらの変種の多くの市場での影響が弱まっていることを見て、より多くの実地向け活動を行うことができますそれは.サプライヤーや患者の活動も増加し、私たちの製品に対する需要が大流行前のレベルに向上した。しかし,大流行期間中の確定診断例の累積減少は,治療を開始する新患者数を抑制し,われわれの業務に影響を与え続けている。 大流行の予測不可能性から,医師と患者のインタラクションが間欠的に中断する可能性があるため,四半期から四半期への変化を経験する可能性がある。また,ヘルスケア生態系の他の変化は,変異性を製品販売傾向に導入する可能性がある。例えば、アメリカの雇用の変化は保険人口の変化を招いた。医療補助登録者数や未加入個人数の増加,アイルランド共和軍の規定は,製品販売に悪影響を及ぼす可能性がある。全体的に言えば、新冠肺炎の疫病発生期間中、著者らの販売のタイミングと規模は依然として不確定性が存在する。第1部1 A項のリスク要因を参照。この表の10-K
2022年に他の収入が低下した原因は、新冠肺炎抗体材料と許可関連収入の低下である。
2022年の運営費減少は,Five Prime買収の一部として買収されたbemarituzumab計画に関する知的財産権の研究開発抹消と,2021年の許可に関する前払金がKKCに支払われたが,一部の損失が相殺されたためである
2022年の非戦略的資産剥離について。連結財務諸表の第4部--付記2(購入および資産剥離)と付記8--の協力を参照。
経営成果
製品販売
世界の製品売上高は以下の通り(単位:百万ドル):
| | | | | | | | | | | | | | | | | | | | | | | | | | | | | |
| 2022年12月31日までの年度 | | 変わる | | 2021年12月31日までの年度 | | 変わる | | 2020年12月31日までの年度 |
| Enbrel | $ | 4,117 | | | (8) | % | | $ | 4,465 | | | (11) | % | | $ | 4,996 | |
| プロリア | 3,628 | | | 12 | % | | 3,248 | | | 18 | % | | 2,763 | |
| ウルトラツラ | 2,288 | | | 2 | % | | 2,249 | | | 2 | % | | 2,195 | |
| シグワ | 2,014 | | | — | % | | 2,018 | | | 6 | % | | 1,899 | |
| Aranesp | 1,421 | | | (4) | % | | 1,480 | | | (6) | % | | 1,568 | |
| ナンバープレート | 1,307 | | | 27 | % | | 1,027 | | | 21 | % | | 850 | |
| 再修術 | 1,296 | | | 16 | % | | 1,117 | | | 26 | % | | 887 | |
| ケプロリス | 1,247 | | | 13 | % | | 1,108 | | | 4 | % | | 1,065 | |
| ニューラス塔 | 1,126 | | | (35) | % | | 1,734 | | | (24) | % | | 2,293 | |
| 事件.事件 | 787 | | | 48 | % | | 530 | | | 51 | % | | 350 | |
その他の製品(1) | 5,570 | | | 5 | % | | 5,321 | | | (1) | % | | 5,374 | |
| 製品総売上高 | $ | 24,801 | | | 2 | % | | $ | 24,297 | | | — | % | | $ | 24,240 | |
| アメリカを総計する | $ | 17,743 | | | 3 | % | | $ | 17,286 | | | (4) | % | | $ | 17,985 | |
| 本店 | 7,058 | | | 1 | % | | 7,011 | | | 12 | % | | 6,255 | |
| 製品総売上高 | $ | 24,801 | | | 2 | % | | $ | 24,297 | | | — | % | | $ | 24,240 | |
____________
(1) 私たちの非主要製品の製品販売と、私たちのGensentaとBergamo子会社を含めて。
私たちの製品の将来の販売は、概要、第1の部分、プロジェクト1.ビジネス-マーケティング、流通および選択された市場製品-競争、第1の部分、プロジェクト1 Aで議論される要因にある程度依存するであろう。リスク要因、および以下の各製品部分で議論される任意の他の要因。また、わが製品の主な競争相手のリストについては、第1部、項目1.ビジネス−マーケティング、流通、および精選された市場製品−競争を参照されたい。
Enbrel
地理地域別ENBREL総売上高は以下の通り(単位:百万ドル):
| | | | | | | | | | | | | | | | | | | | | | | | | | | | | |
| 2022年12月31日までの年度 | | 変わる | | 2021年12月31日までの年度 | | 変わる | | 2020年12月31日までの年度 |
| Enbrel-アメリカ | $ | 4,044 | | | (7) | % | | $ | 4,352 | | | (10) | % | | $ | 4,855 | |
| Enbrel-カナダ | 73 | | | (35) | % | | 113 | | | (20) | % | | 141 | |
| 総環境品質 | $ | 4,117 | | | (8) | % | | $ | 4,465 | | | (11) | % | | $ | 4,996 | |
2022年のENBREL売上高低下の要因は、推定販売控除の不利な変化、販売量の低下、純販売価格の低下である。2023年、ENBRELは、福祉計画の変化、保険回復、および米国患者が免責額によって増加した自己負担費用の影響で、第1四半期の売上がその後のいくつかの四半期を下回る歴史的モデルに従うと予想される。また、2023年の純販売価格はさらに低下すると予想されています。
2021年のENBREL売上高の低下は、低い純販売価格、販売量、不利な在庫変化によって推進されている。
プロリア
地理的地域別Prolia総売上高は以下の通り(単位:百万ドル):
| | | | | | | | | | | | | | | | | | | | | | | | | | | | | |
| 2022年12月31日までの年度 | | 変わる | | 2021年12月31日までの年度 | | 変わる | | 2020年12月31日までの年度 |
| プロリア-アメリカ | $ | 2,465 | | | 15 | % | | $ | 2,150 | | | 17 | % | | $ | 1,830 | |
| Prolia-ROW | 1,163 | | | 6 | % | | 1,098 | | | 18 | % | | 933 | |
| 総合意 | $ | 3,628 | | | 12 | % | | $ | 3,248 | | | 18 | % | | $ | 2,763 | |
世界的な合意の増加 2022年の売上高は販売台数の増加とより高い純販売価格によって推進されているが、一部は外貨為替レートの不利な変化によって相殺されている。
2021年のProlia世界売上高の増加は主に販売台数の増加によって推進されている。
ウルトラツラ
地理的地域別Otezla総売上高は以下の通り(単位:百万ドル):
| | | | | | | | | | | | | | | | | | | | | | | | | | | | | |
| 2022年12月31日までの年度 | | 変わる | | 2021年12月31日までの年度 | | 変わる | | 2020年12月31日までの年度 |
Otezla-アメリカ | $ | 1,886 | | | 5 | % | | $ | 1,804 | | | 1 | % | | $ | 1,790 | |
Otezla-ROW | 402 | | | (10) | % | | 445 | | | 10 | % | | 405 | |
| Total Otezla | $ | 2,288 | | | 2 | % | | $ | 2,249 | | | 2 | % | | $ | 2,195 | |
世界のOtezlaの数の増加は 2022年の販売は主に販売台数の増加によって推進され、一部は低い純販売価格によって相殺されている。ROW Otezlaの2022年の売上高は外貨為替レートの悪影響を受けている。2023年、Otezlaは、福祉計画の変化、保険回復、および米国患者が免責額によって増加した自己負担費用の影響で、第1四半期の売上がその後のいくつかの四半期を下回る歴史的モデルに従うと予想される。
世界のOtezlaの数の増加は 2021年の売上高は販売台数の増加によって推進されているが、一部は低い純販売価格と不利な在庫変化によって相殺されている。
現在行われているOtezlaに関する訴訟に関する検討は、連結財務諸表第4部である付記19“または事項と引受金”を参照されたい。
シグワ
地理地域別XGEVA総売上高は以下の通り(単位:百万ドル):
| | | | | | | | | | | | | | | | | | | | | | | | | | | | | |
| 2022年12月31日までの年度 | | 変わる | | 2021年12月31日までの年度 | | 変わる | | 2020年12月31日までの年度 |
| Xgeva-アメリカ | $ | 1,480 | | | 3 | % | | $ | 1,434 | | | 2 | % | | $ | 1,405 | |
| Xgeva-ROW | 534 | | | (9) | % | | 584 | | | 18 | % | | 494 | |
| 総XGEVA | $ | 2,014 | | | — | % | | $ | 2,018 | | | 6 | % | | $ | 1,899 | |
2022年の世界XGEVA売上高は相対的に横ばいであり、より高い純販売価格が競争激化と不利な外貨為替レート変化による販売量低下によって相殺されたためである。
2021年のXGEVAの世界売上高の増加は主に販売台数の増加によって推進されているが、純販売価格の低下分はこの増加を相殺している。
Aranesp
地理的地域別Aranesp総売上高は以下の通り(単位:百万ドル):
| | | | | | | | | | | | | | | | | | | | | | | | | | | | | |
| 2022年12月31日までの年度 | | 変わる | | 2021年12月31日までの年度 | | 変わる | | 2020年12月31日までの年度 |
| Aranesp-アメリカ | $ | 521 | | | (3) | % | | $ | 537 | | | (15) | % | | $ | 629 | |
| Aranesp-ROW | 900 | | | (5) | % | | 943 | | | — | % | | 939 | |
| 合計Aranesp | $ | 1,421 | | | (4) | % | | $ | 1,480 | | | (6) | % | | $ | 1,568 | |
2022年のAranesp世界売上高の低下は、純販売価格の低下と外貨為替レートの不利な変化によって推進されているが、販売減額と販売台数増加の有利な変化部分はこの低下を相殺していると予想される。
2021年にAranespの世界売上高が低下した要因は純販売価格の低下である。
Aranespは長時間作用型赤血球生成刺激剤(ESA)と 生物学的に似たバージョンからのEpogenは、未来の純販売価格と販売量に影響を及ぼすだろう。
ナンバープレート
地理的地域別Nplate総売上高は以下の通り(単位:百万ドル):
| | | | | | | | | | | | | | | | | | | | | | | | | | | | | |
| 2022年12月31日までの年度 | | 変わる | | 2021年12月31日までの年度 | | 変わる | | 2020年12月31日までの年度 |
| Nplate-アメリカ | $ | 848 | | | 50 | % | | $ | 566 | | | 17 | % | | $ | 485 | |
| ナンバープレート-列 | 459 | | | — | % | | 461 | | | 26 | % | | 365 | |
| 総網板 | $ | 1,307 | | | 27 | % | | $ | 1,027 | | | 21 | % | | $ | 850 | |
2022年の世界のネットディスク販売台数の増加は販売台数の増加によって推進されている。2022年のNplateの売上高には、第4四半期の米国政府からの2.07億ドルの注文が含まれている。
2021年の世界のネットボード販売台数の増加は主に販売台数の増加によって推進されている。
再修術
地理地域別のRepatha総売上高は以下の通り(単位:百万ドル):
| | | | | | | | | | | | | | | | | | | | | | | | | | | | | |
| 2022年12月31日までの年度 | | 変わる | | 2021年12月31日までの年度 | | 変わる | | 2020年12月31日までの年度 |
再修術 — U.S. | $ | 608 | | | 9 | % | | $ | 557 | | | 21 | % | | $ | 459 | |
再修術 -わかった | 688 | | | 23 | % | | 560 | | | 31 | % | | 428 | |
| 完全に修復する | $ | 1,296 | | | 16 | % | | $ | 1,117 | | | 26 | % | | $ | 887 | |
世界的な修復率の増加 2022年の売上高は販売台数の増加によって推進されているが、一部は低い純販売価格と不利な外貨為替レートの変化によって相殺されている。販売量は連邦医療保険D部分と商業患者参入の契約変化を支持と改善し、2022年1月1日までにRepathaを中国の国家精算薬品リストに組み入れ、この2項目はいずれも2022年の純販売価格の低下を招いた。
世界的な修復率の増加 2021年の売上高は販売台数の増加によって推進されているが、一部は低い純販売価格によって相殺されている
現在行われているRepathaに関する訴訟の検討については、連結財務諸表第4部である付記19“または事項と引受”が参照される。
ケプロリス
Kyprolisの地理的地域別総売上高は以下の通り(単位:百万ドル):
| | | | | | | | | | | | | | | | | | | | | | | | | | | | | |
| 2022年12月31日までの年度 | | 変わる | | 2021年12月31日までの年度 | | 変わる | | 2020年12月31日までの年度 |
| Kyprolis-アメリカ | $ | 850 | | | 15 | % | | $ | 736 | | | 4 | % | | $ | 710 | |
| Kyprolis-row | 397 | | | 7 | % | | 372 | | | 5 | % | | 355 | |
| Kyprolisの総数 | $ | 1,247 | | | 13 | % | | $ | 1,108 | | | 4 | % | | $ | 1,065 | |
2022年と2021年のKyprolis世界売上高の増加は主に販売台数の増加によって推進されている。
FDA報告書は、いくつかの会社が提出した後発薬carfilzomibのANDAを一時的または最終的に承認したと報告している。後発薬carfilzomib製品を承認するANDAの日付は、“ハッチ·ワックスマン法案”および模倣薬carfilzomib製品の開発を求めるいくつかの会社との間の任意の適用と和解協定によって制限される。
ニューラス塔
Neulastaの地理的地域別総売上高は以下の通り(単位:百万ドル):
| | | | | | | | | | | | | | | | | | | | | | | | | | | | | |
| 2022年12月31日までの年度 | | 変わる | | 2021年12月31日までの年度 | | 変わる | | 2020年12月31日までの年度 |
| ニューラスタ--アメリカ | $ | 959 | | | (37) | % | | $ | 1,514 | | | (24) | % | | $ | 2,001 | |
| ニューラスタ街 | 167 | | | (24) | % | | 220 | | | (25) | % | | 292 | |
| 全ニューラス塔 | $ | 1,126 | | | (35) | % | | $ | 1,734 | | | (24) | % | | $ | 2,293 | |
2022年と2021年のNeulastaグローバル売上高の低下は、純販売価格と販売台数の低下に拍車をかけている
生物類似バージョンのNeulastaによる競争が激化し、純価格侵食の加速や販売量の低下を含むブランド販売に大きな悪影響を与え続ける。我々はまた、我々Onpro注射器と競合する体内注射器を使用する生体模倣薬を含む他の生物類似バージョンが、将来的に承認されると予想している。
事件.事件
地理地域別のEVENITY総売上高は以下の通り(単位:百万ドル):
| | | | | | | | | | | | | | | | | | | | | | | | | | | | | |
| 2022年12月31日までの年度 | | 変わる | | 2021年12月31日までの年度 | | 変わる | | 2020年12月31日までの年度 |
| 活動-アメリカ | $ | 533 | | | 61 | % | | $ | 331 | | | 73 | % | | $ | 191 | |
| 事件-はい | 254 | | | 28 | % | | 199 | | | 25 | % | | 159 | |
| 総事件数 | $ | 787 | | | 48 | % | | $ | 530 | | | 51 | % | | $ | 350 | |
2022年と2021年の世界EVENITY売上高の増加は、私たちの市場全体の販売台数の増加によって推進されている
その他の製品
地理的地域別の他の製品売上高は以下の通り(単位:百万ドル):
| | | | | | | | | | | | | | | | | | | | | | | | | | | | | |
| 2022年12月31日までの年度 | | 変わる | | 2021年12月31日までの年度 | | 変わる | | 2020年12月31日までの年度 |
| MVASI-アメリカ | $ | 602 | | | (27) | % | | $ | 826 | | | 26 | % | | $ | 656 | |
| MVASI-ROW | 299 | | | (12) | % | | 340 | | | * | | 142 | |
Vectibix — U.S. | 396 | | | 14 | % | | 347 | | | 1 | % | | 342 | |
Vectibix -わかった | 497 | | | (6) | % | | 526 | | | 12 | % | | 469 | |
| BLINCETO-アメリカ | 336 | | | 21 | % | | 278 | | | 20 | % | | 231 | |
BLINCETO -わかった | 247 | | | 27 | % | | 194 | | | 31 | % | | 148 | |
| Epogen-アメリカ | 506 | | | (3) | % | | 521 | | | (13) | % | | 598 | |
AMGEVITA -わかった | 460 | | | 5 | % | | 439 | | | 33 | % | | 331 | |
| Aimovig-アメリカ | 398 | | | 27 | % | | 313 | | | (17) | % | | 378 | |
| Aimovig-ROW | 16 | | | * | | 4 | | | NM | | — | |
| パサビフ-アメリカ | 253 | | | 69 | % | | 150 | | | (75) | % | | 605 | |
| Parsabiv-ROW | 129 | | | (1) | % | | 130 | | | 17 | % | | 111 | |
| KANJINTI-アメリカ | 257 | | | (46) | % | | 479 | | | 1 | % | | 475 | |
| カンジンティ-ROW | 59 | | | (37) | % | | 93 | | | 1 | % | | 92 | |
ルマカラス — U.S. | 222 | | | * | | 82 | | | NM | | — | |
ルミクラス -わかった | 63 | | | * | | 8 | | | NM | | — | |
| TEZSPIRE-アメリカ | 170 | | | NM | | — | | | NM | | — | |
| Neupogen-アメリカ | 87 | | | (14) | % | | 101 | | | (30) | % | | 144 | |
| Neupogen-ROW | 57 | | | (15) | % | | 67 | | | (17) | % | | 81 | |
| Sensiar-アメリカ | 10 | | | 67 | % | | 6 | | | (93) | % | | 92 | |
| センシパル/ミンパロ | 54 | | | (31) | % | | 78 | | | (60) | % | | 196 | |
TAVNEOS-アメリカ(1) | 16 | | | NM | | — | | | NM | | — | |
TAVNEOS-ROW(1) | 5 | | | NM | | — | | | NM | | — | |
他にも — U.S.(2) | 296 | | | 47 | % | | 202 | | | 85 | % | | 109 | |
他の行(2) | 135 | | | (1) | % | | 137 | | | (21) | % | | 174 | |
| その他製品販売総額 | $ | 5,570 | | | 5 | % | | $ | 5,321 | | | (1) | % | | $ | 5,374 | |
| アメリカ-その他の製品総数 | $ | 3,549 | | | 7 | % | | $ | 3,305 | | | (9) | % | | $ | 3,630 | |
| 合計行-その他の製品 | 2,021 | | | — | % | | 2,016 | | | 16 | % | | 1,744 | |
| その他製品販売総額 | $ | 5,570 | | | 5 | % | | $ | 5,321 | | | (1) | % | | $ | 5,374 | |
NM=意味がない
*100%を超える変化
____________
(1) TAVNEOSは2022年10月20日にChemoCentryxの買収により獲得した
(2) Corlanor、AVSOLA、IMLIGIC、RIABNI、および当社のGensentaとBergamo子会社の販売が含まれています
運営費
運営費は以下の通り(単位:百万ドル):
| | | | | | | | | | | | | | | | | | | | | | | | | | | | | |
| 2022年12月31日までの年度 | | 変わる | | 2021年12月31日までの年度 | | 変わる | | 2020年12月31日までの年度 |
| 販売コスト | $ | 6,406 | | | (1) | % | | $ | 6,454 | | | 5 | % | | $ | 6,159 | |
| 製品の売り上げのパーセントを占める | 25.8 | % | | | | 26.6 | % | | | | 25.4 | % |
| 総収入のパーセントを占める | 24.3 | % | | | | 24.8 | % | | | | 24.2 | % |
| 研究開発 | $ | 4,434 | | | (8) | % | | $ | 4,819 | | | 15 | % | | $ | 4,207 | |
| 製品の売り上げのパーセントを占める | 17.9 | % | | | | 19.8 | % | | | | 17.4 | % |
| 総収入のパーセントを占める | 16.8 | % | | | | 18.5 | % | | | | 16.5 | % |
| 現在行われている研究と開発を買収する | $ | — | | | NM | | $ | 1,505 | | | NM | | $ | — | |
| 製品の売り上げのパーセントを占める | — | % | | | | 6.2 | % | | | | — | % |
| 総収入のパーセントを占める | — | % | | | | 5.8 | % | | | | — | % |
| 販売、一般、行政 | $ | 5,414 | | | 1 | % | | $ | 5,368 | | | (6) | % | | $ | 5,730 | |
| 製品の売り上げのパーセントを占める | 21.8 | % | | | | 22.1 | % | | | | 23.6 | % |
| 総収入のパーセントを占める | 20.6 | % | | | | 20.7 | % | | | | 22.5 | % |
| 他にも | $ | 503 | | | * | | $ | 194 | | | 3 | % | | $ | 189 | |
| 総運営費 | $ | 16,757 | | | (9) | % | | $ | 18,340 | | | 13 | % | | $ | 16,285 | |
NM=意味がない
*100%を超える変化
販売コスト
新冠肺炎抗体出荷量と製造コストの低下により,販売コストは2022年の総収入の24.3%に低下したが,我々の製品組合せの変化部分はこの影響を相殺した。
販売コストは2021年の総収入の24.8%を占めているが、これは我々の製品構造の変化とより高い利益シェアと特許権使用料によるものであるが、一部は買収関連資産の低い償却費用と低い製造コストによって相殺されている。
研究開発
同社はそのすべての研究開発活動と関連支出を3種類に分けた:(I)研究と早期パイプライン、(Ii)後期臨床計画と(Iii)上場製品。これらのカテゴリは以下のとおりである
| | | | | | | | |
| カテゴリー | | 説明する |
| 研究と早期準備 | | 第一段階の臨床試験の完成を通じて早期研究の活動による研究開発費用を大幅に支持し、薬物発見、毒理学、薬物動態学と薬物新陳代謝及び技術開発を含む |
| 後期臨床案 | | 第二段階および第三段階の臨床計画において発生する、またはそれに関連する研究開発費は、新製品または既存製品の新しい適応をもたらすことを目的としており、主に米国またはEUに登録されている |
| 発売製品 | | 主に米国やEUで販売されている市場製品を支援するための研究開発費。臨床試験を含み、製品の安全性に関する情報(その中のいくつかは規制当局が要求している可能性がある)と、規制の承認を得た後の製品の特徴と、米国またはEUの承認を得た後、新しい市場で規制の承認を受けるコストを収集することを目的としている |
カテゴリー別の研究開発費は以下の通り(単位:百万)
| | | | | | | | | | | | | | | | | |
| 十二月三十一日までの年度 |
| 2022 | | 2021 | | 2020 |
| 研究と早期準備 | $ | 1,611 | | | $ | 1,670 | | | $ | 1,405 | |
| 後期臨床案 | 1,627 | | | 1,726 | | | 1,365 | |
| 発売製品 | 1,196 | | | 1,423 | | | 1,437 | |
| 研究開発費総額 | $ | 4,434 | | | $ | 4,819 | | | $ | 4,207 | |
2022年の研究開発費の低下は、2021年に後期臨床計画と研究および早期パイプライン·マーケティング製品支援に含まれる業務開発活動が増加したが、後期臨床計画支援と研究および早期パイプライン支出の増加部分がこの影響を相殺したためである。
2021年の研究開発費の増加は、後期臨床計画に含まれる許可関連KKC前払い、および研究および早期パイプライン(他の事業開発活動を含む)支出の増加によるものである。
現在行われている研究と開発を買収する
2021年に買収された知的財産権研究開発費は、2021年のFive Prime買収の一部であるbemarituzumab計画と関係がある。連結財務諸表の第四部--付記2“購入と資産剥離”を参照。
販売、一般、行政
2022年のSG&A費用の増加は主に買収に関する費用の増加によるものである。
2021年のSG&A費用の減少は、主にマーケティング製品の支出の減少と一般と管理費用の減少によるものである。
他にも
2022年の他の運営費には主に非戦略的資産剥離の損失が含まれる。連結財務諸表の第四部--付記2“購入と資産剥離”を参照。
2021年の他の業務費用には、主にコスト削減措置や法律判決に関する費用が含まれています。
2020年の他の運営費用は主に法的和解費用を含む。
営業外費用/所得税と所得税
営業外費用/所得税と所得税は以下の通り(単位:百万ドル):
| | | | | | | | | | | | | | | | | |
| 十二月三十一日までの年度 |
| 2022 | | 2021 | | 2020 |
| 利子支出,純額 | $ | (1,406) | | | $ | (1,197) | | | $ | (1,262) | |
| その他の収入,純額 | $ | (814) | | | $ | 259 | | | $ | 256 | |
| 所得税支給 | $ | 794 | | | $ | 808 | | | $ | 869 | |
| 実際の税率 | 10.8 | % | | 12.1 | % | | 10.7 | % |
利子支出,純額
2022年の純利息支出の増加は主に未返済債務総額の増加と債務LIBORの増加によるものであり、我々は金利スワップを使用することで実際にこれらの債務に変動金利を支払った。
2021年の利息支出純額の減少は、主に2020年の債務早期返済に関する純コストの上昇と、2021年の債務のLIBORの低下により、金利スワップを使用することでこれらの債務に効果的に可変金利を支払っているが、一部は全体の未返済債務増加によって相殺されている。
その他の収入,純額
2021年と比較して,2022年のその他(費用)収入純額の変化は,主に百済神州投資に関する確認損失の増加と,有限組合企業,上場株式証券,その他の戦略投資への投資確認損失によるものである。
2021年のその他(支出)収入純額の変化は,主に我々の百済神州投資に関する損失が2020年比で減少したためであるが,2021年の利上げ投資の収入減少と2020年に確認された他の非日常的収益部分によって相殺されている。
所得税
2021年と比較して、2022年の有効税率が低下したのは、主に前年にFive Primeを買収したことによる相殺不可能な知的財産権研究開発費であるが、2022年の非戦略的資産剥離による相殺不可能損失と前年に比べた純不利項目は部分的に相殺されている。
2020年と比較して、2021年の有効税率が増加したのは、主にFive Primeの買収による相殺できない知的財産権研究開発費であり、一部は利益組合と前年の税収負債の調整によって相殺された。
政府と国会は現行税法の改正を検討し続けており、米国政府に納める税金を大幅に増加させる可能性がある。また、経済協力開発機構は最近、最低企業税率と市場国の税権拡大について各国を調整する合意に達した。OECDのすべての加盟国または個別の国が一方的にこの合意を公布した場合、この合意は増税を招き、私たちのアメリカと外国の納税義務に影響を与える可能性がある
米国財務省は2021年12月に最終的な外国税控除規定を発表し、2023年からプエルトリコに対する米国の消費税の信用を廃止し、米国での納税負担を増加させる。これに応じて、2022年6月30日、米国領土プエルトリコは工業発展収入の代替固定税率を規定する第52-2022年法案を公布し、米財務省は連邦法律によると、この税率は免除されることを明らかにした。この新しい法律の一部として、条件を満たした企業はプエルトリコ消費税の代わりに増分所得税と源泉徴収税を徴収されるだろう。代替固定税率を享受する資格があるため、現在プエルトリコ政府との税収補助は2022年12月に改正されている。2023年1月1日から、私たちはこの代替固定税率を受ける資格があり、私たちの税金は増加するだろう
2017年、私たちは米国国税局から2010-2012年のRARと修正されたRARを受け取り、主にアメリカのあるエンティティとアメリカ領土プエルトリコ間の利益分配に関連する重大な調整を提案した。我々は提案された調整と計算に同意せず、米国国税局控訴事務所と解決策を求めたが、解決策を達成することはできなかった。2021年7月、私たちは、2021年5月と7月に受信した2つの重複した2010-2012年度法定欠税通知(通知)に異議を求める請願書を米国税務裁判所に提出し、私たちの2010-2012年度の米国課税所得額を約36億ドル増加させ、利息を追加することを目的とした。2010年~2012年の間に徴収される可能性のある任意の追加税収は、最大約9億ドルの以前の私たちの海外収入に計上されていた送金税を減らすだろう
2020年には、米国国税局から2013-2015年のRARと修正されたRARを受け取り、2010-2012年の提案された利益分配と同様に、米国のあるエンティティと米国領土プエルトリコとの間の利益分配に主に関連する重大な調整を提案した。我々は提案された調整と計算に同意せず、米国国税局控訴事務所と解決策を求めたが、解決策を達成することはできなかった。2022年7月、私たちは米国税務裁判所に請願書を提出し、私たちが以前に報告した2022年4月に受け取った2013-2015年度通知に異議を唱え、2013-2015年度の米国課税所得額を約51億ドル増加させ、利息を追加することを求めた。しかも、通知は罰金が約20億ドルだと主張した。2013-2015年度に徴収される可能性のある任意の追加税収は、約22億ドルに達する以前の私たちの海外収入に計上されていた送金税を減少させるかもしれない
私たちは2010-2012年と2013-2015年の通知で国税局が提起した立場に根拠がないと信じている。私たちは司法手続きを通じて2010-2012年と2013-2015年の通知に異議を唱えている。この2つの事件は2022年12月19日に米国税務裁判所で合併された。
私たちは現在、2010年から2015年までの問題と類似している国税局2016-2018年の審査を受けている。しかも、私たちはいくつかの州と外国税務管轄区域の検討を受けている。
このような複雑な問題の最終的な解決は今後12ヶ月以内に達成される可能性はあまりない。私たちはまだ、過去の経験、税法の解釈、税法の私たちの事実への適用、および税務機関が取る可能性のある行動の判断に基づいて、私たちの所得税負債に対する課税は適切であると考えている。しかし、所得税の準備の複雑さと
これらの事項の解決が不確定であるため、任意の税務事項の最終結果は、支払金額が計算金額を大幅に超える可能性があり、我々の総合財務諸表に重大な悪影響を及ぼす可能性がある。
第1部、第1 A項を参照。リスク要因-新しい税法を説明したり、追加の税務責任を負うことは、私たちの収益性に影響を及ぼす可能性があります第2部は、項目7.経営層の議論と分析または財務状況と経営成果--キー会計政策と推定数、所得税、および第4部--所得税を付記し、合併財務諸表に入れ、さらなる議論に供する。
財務状況、流動性、資本源
厳選された財務データは以下の通り(単位:百万)
| | | | | | | | | | | |
| 十二月三十一日 |
| 2022 | | 2021 |
| 現金、現金等価物、有価証券 | $ | 9,305 | | | $ | 8,037 | |
| 総資産 | $ | 65,121 | | | $ | 61,165 | |
| 長期債務の当期部分 | $ | 1,591 | | | $ | 87 | |
| 長期債務 | $ | 37,354 | | | $ | 33,222 | |
| 株主権益 | $ | 3,661 | | | $ | 6,700 | |
現金、現金等価物、有価証券
2022年12月31日現在、私たちの現金、現金等価物、有価証券残高は93億ドルです。私たちのポートフォリオの主な目標は、元本の安全性、慎重な流動性レベル、許容可能なリスクレベルを維持することだ。私たちの投資政策は、利息証券投資をいくつかのタイプの債務と通貨市場ツールに限定し、これらのツールは主に投資レベルの信用格付けを持つ機関によって発行され、資産の種類と発行者によって期限と集中度を制限する。
資本配置
資本構造の最適化の目標と一致して、私たちは私たちが蓄積した現金残高を戦略的に配置し、内部および外部の革新的な投資、戦略的取引(治療分野での私たちの製品の組み合わせを拡大する取引を含む)、債務の返済、配当金の支払い、株式買い戻しを含む多くの代替案を考慮する。
私たちは引き続き私たちの業務に投資し、現金配当金と株の買い戻しを支払うことで株主に資本を返還することで、私たちの業務の将来のキャッシュフローへの自信と資本コストの最適化に対する私たちの願いを反映したいと思います。将来の配当金と株式買い戻しの時間と金額は多くの要素によって変化し、未来の戦略取引の資本要求、受け入れ可能な条件下での融資可用性、債務超過要求、私たちの信用格付け、適用税法または会社法の変化、私たちの業務モデルの変化、および私たちの取締役会は定期的に現金配当金および/または株式買い戻しが株主の最適な利益に符合し、適用法律と会社協定に符合することを決定する。また、株式買い戻しの時間や金額も、私たちの全体的な現金レベル、株価、販売禁止期間の影響を受ける可能性があり、その間、私たちは株の買い戻しを制限されています。株式買い戻し方式には、大口購入、要約買収、株式買い戻し、市場取引の加速が含まれることができる。
取締役会は、2022年、2021年、2020年にそれぞれ支払う普通株1株当たり1.94ドル、1.76ドル、1.60ドルの四半期現金配当金を、2022年と2021年ともに前年より10%増加させたと発表した。2022年12月、取締役会は2023年第1四半期の普通株1株当たり2.13ドルの現金配当金を発表し、この期間は10%増加し、2023年3月に支払うことになった。
私たちはまた株式買い戻し計画を通じて株主に資金を返還する。2022年には、ASR協定による60億ドルの買い戻し、64億ドルの株式買い戻しを現金で決済した63億ドルの普通株を買い戻した。2021年には50億ドルの普通株を買い戻し、現金決済を行った。2020年には35億ドルの普通株を買い戻し、現金決済を行った。2022年10月、取締役会は私たちの株式買い戻し計画に基づいてライセンス金額を24億ドル増加させた。2022年12月31日現在、株式買い戻し計画によると、まだ70億ドルが利用可能だ。
株式買い戻しと四半期配当金の支払いにより、2022年12月31日と2021年までに赤字を累積した。私たちが予想している持続的な収益性と強い財務状況を考慮すると、私たちの累積赤字は、私たちの将来の運営、株の買い戻し、配当金の支払い、または債務返済能力に影響を与えないと予想される。
私たちは、既存の資金、運営によって生成された現金、既存の融資源、および融資ルートは、運営資本、資本支出、債務超過要求に対する私たちの需要を満たすのに十分であると信じており、配当金の支払いおよび株の買い戻し計画、および買収および許可活動を含む戦略的に実施される他の業務計画を計画している。私たちの流動資金需要は、経営活動が提供する現金、有価証券の売却、商業手形および/または銀団信用による借金の手配、その他の国内外の債務市場と株式市場への参入を含む様々な供給源によって満たすことができると予想される。第1部、第1 A項を参照。リスク要因-世界の経済状況は私たちにマイナスの影響を与える可能性があり、私たちの業務に影響を与えるいくつかのリスクを拡大する可能性があります.
融資手配
私たちの流動資金需要を満たすのを助けるために、私たちは様々な資金調達計画を達成した。2022年12月31日と2021年12月31日まで、我々の長期借入金の非流動部分はそれぞれ374億ドルと332億ドルだった。私たちの長期借入金の帳簿価値は、金利スワップを差し引いた公正価値調整および未償却割引、割増価格、発売コストを差し引いた純価値です。2022年12月31日現在、標普、ムーディーズとHPはそれぞれ私たちの未償還優先手形BBB+、BBa 1とBBB+に信用格付けを与え、これらの手形は投資レベルとされている。このような格付けの不利な変化は未来の資金調達に悪影響を及ぼすかもしれない。
2022年、2021年、2020年には、元金総額がそれぞれ70億ドル、50億ドル、90億ドルの債券を発行した。2022年の間、私たちは3億ドルのコストで債務の一部を買い戻した。2021年と2020年には、それぞれ42億ドルと65億ドルの債務を返済し、償還した。また,2020年には金利が低く,満期日の遅い9億ドルの新発行手形で7億ドルのいくつかの未償還手形を交換した。
固定金利と変動金利債務の理想的な組合せを実現するために、金利交換契約を締結し、我々が発行したいくつかの債務の固定金利利札をそれぞれの手形の有効期限内のLIBORに基づく変動利札に効率的に変換する。これらの金利スワップ契約は条件を満たし、公正価値ヘッジとして指定されている。2022年12月31日と2021年12月31日まで、名目総金額67億ドルの金利交換契約を持っています。
ある外貨建ての長期手形に関する外貨為替リスクをヘッジするために、クロス通貨スワップ契約を締結し、それぞれの手形の利息支払いと元金返済をユーロ、ポンド、スイスフランからドルに効果的に変換した。これらのクロスマネースワップ契約は条件を満たし,キャッシュフローヘッジとして指定されている.2022年12月31日と2021年12月31日までに、総名目金額34億ドルのクロス通貨スワップ契約を持っています。
2022年12月31日現在、25億ドルまでの無担保商業手形を発行して、私たちの運営資金需要を満たすことができる商業手形計画があります。2022年、2021年、そして2020年の間、私たちは何の商業手形も発行しなかった。2022年と2021年12月31日現在、未返済の商業手形はない。
2019年、私たちは一般企業用途にも使用可能であり、私たちの商業手形計画の流動性支援としても使用できる25億ドルの銀団無担保循環信用協定を修正し、再説明しました。銀行の同意の場合、循環信用協定での承諾額は最大で7億5千万ドル増加する可能性がある。協定締約国である1銀行あたりの初期承諾期間は5年である。銀行の同意により、この期限は最大2回、1年間延長することができる。私たちの現在の信用格付けによると、この協定の年間承諾料は、この融資未使用部分の0.1%だ。本循環信用協定は2022年12月に更なる改訂を行い、SOFRがロンドン銀行の同業解体を参考金利とし、その中の段階的淘汰或いは現有の指定参考金利が使用できない場合に後継金利を決定する規定に符合する。一般的に、私たちの現在の信用格付けによると、(I)SOFRプラス1.125%または(II)(A)銀団代理銀行基本商業ローン金利、(B)隔夜連邦基金金利プラス0.50%または(C)1ヶ月SOFRプラス1.1%のうち最高者に、この手配に基づいて借り入れた任意の金額の利息を受け取る。この融資では、2022年12月31日と2021年12月31日までに未返済の金額はない。
2022年12月,Horizonの提案買収については,過渡的信用協定と定期融資信用協定を締結し,合計285億ドルの借入金を規定した。2022年12月31日まで、この二つの合意は借金をしていない。連結財務諸表の第四部--付記2“購入と資産剥離”を参照。
2023年までに、ドルLIBOR金利は段階的に廃止され、代わりになると予想される。別の基準金利委員会は、米国連邦準備委員会(Federal Reserve Board)とニューヨーク連邦準備銀行(Federal Reserve Bank Of New York)によって招集された民間市場参加者のグループであり、ドルLIBORからより強い参考金利への移行に成功したことを確保することを目的としている。同委員会は、ドルLIBOR代替案としてSOFRを提案している。したがって、私たちはSOFRが市場参加者によって広く採用されると予想する。私たちはこの変化が私たちの連結財務諸表に実質的な影響を与えないと予想する。第1部、第1 A項を参照。リスク要因-私たちの販売と運営は新興市場を含めて国際業務リスクの影響を受けている。
2020年2月、私たちは米国証券取引委員会に棚上げ登録声明を提出し、金額不明の債務証券;普通株、優先株、債務証券、普通株、優先株または預託株式の権利証、普通株または優先株購入権、証券購入契約、証券購入単位、および預託株式を発行することを許可した。この保留登録声明によると、発行可能なすべての証券は時々発売することができ、発行条項は発行時に確定するこの棚登録声明は2023年2月に満了し、私たちの取締役会はそれの代わりに新しい棚登録声明を承認しました。
私たちの特定の資金調達計画には非金融契約が含まれている。さらに、私たちの循環信用プロトコル、過渡的信用プロトコル、および定期ローン信用プロトコルは、指定された最低利息カバー率、すなわち(I)総合純収入、利息支出、所得税支出、減価償却費用、償却費用、非常または非日常的費用、および他の非現金項目(総合EBITDA)~(Ii)の総合利息支出の合計を維持することを要求する金融契約を含み、各項目はそれぞれのプロトコルで定義され説明されている。2022年12月31日まで、私たちはこのような計画の下で適用されるすべての条約を遵守した。
これらの融資手配は、総合財務諸表第IV部分付記15(融資手配)と付記18(デリバティブ)においてより十分に論じられている。
キャッシュフロー
我々がまとめたキャッシュフロー活動は以下のとおりである(百万単位)
| | | | | | | | | | | | | | | | | |
| 十二月三十一日までの年度 |
| 2022 | | 2021 | | 2020 |
| 経営活動が提供する現金純額 | $ | 9,721 | | | $ | 9,261 | | | $ | 10,497 | |
| 投資活動が提供する現金純額 | $ | (6,044) | | | $ | 733 | | | $ | (5,401) | |
| 融資活動のための現金純額 | $ | (4,037) | | | $ | (8,271) | | | $ | (4,867) | |
運営中です
経営活動が提供する現金は、私たちの主な経常的な資金源であり続けることが予想される。2022年の経営活動が提供する現金の増加は、主に販売奨励と割引、サプライヤー調達、税務機関への負債と会社パートナーからの収入の支払いスケジュールによるものであるが、今年度の製造活動増加分によって相殺される。経営活動が提供する現金が2021年に減少したのは、主に2020年に発生した金利交換貨幣化および販売奨励と割引の支払い時間によるものである。
投資する
2022年の投資活動で使用された現金は、主にChemoCentryxを38億ドルで買収したことと、有価証券関連の14億ドルの現金が純流出したためだ。2021年の投資活動で提供される現金は主に有価証券関連の現金純流入43億ドルであるが、TeneobioとFive Prime買収に用いられた現金25億ドル分で相殺されている。2020年の投資活動のための現金は、主に私たちが購入した権益法投資(主に百済神州)の32億ドルと、有価証券に関する現金の純流出15億ドルから来ている。2022年、2021年、2020年の資本支出はそれぞれ9.36億ドル、8.8億ドル、6.08億ドル。私たちは現在、2023年の資本プロジェクトへの支出は約9.25億ドルと推定している。支出増加の大部分は製品と候補製品を供給できるように製造能力を拡大するために使用される。
融資する
2022年の融資活動のための現金は、主に64億ドルの普通株の買い戻しと支払いのための42億ドルの配当金だが、一部は69億ドルの債務発行収益によって相殺されている。2021年の融資活動のための現金は主に我々の普通株50億ドルの買い戻しと40億ドルの配当金の支払いであるが、一部は発行債務の収益によって相殺され、返済純額は8億ドルである。2020年に融資活動に用いられた現金は主に38億ドルの配当金と35億ドルの普通株買い戻しが支払われたが、一部は債務発行収益で相殺され、純額は25億ドルだった。
連結財務諸表の第4部--付記9(投資)、付記15(融資手配)、および付記16(株主権益)を参照。
資本要求
以下に説明する様々な契約義務に基づいて、私たちは第三者への支払いを要求する大量の現金を持っています。
私たちの様々な融資スケジュールによると、私たちは、私たちのいくつかの長期債務義務に関連する金利スワップとクロス通貨スワップ契約下の金額を含む利息と元金の返済を義務化しています。予定債務満期日及び我々の長期債務責任に関するデリバティブ契約に基づいて支払う資料については、総合財務諸表第IV-付記15“融資手配”及び付記18“派生ツール”を参照されたい。
私たちは、放棄された賃貸契約とまだ開始されていない賃貸契約に対する賃貸承諾を含む経営賃貸契約の費用を支払う義務があります。これらの債務に関する資料は、連結財務諸表第4部である付記13“リース”を参照されたい。
2017年税法によると、私たちは8年分に分けて主に私たちの海外業務の以前の無期限投資収益に関する送金税を支払うことを選択しました。予定送還税余剰分割払いの資料については、連結財務諸表第4部--付記19、“事項と引受金--米国送還税”がある。
35億ドルの購入義務があり、主に(I)新製品および既存製品に対する研究開発約束(臨床試験に関する約束を含む)、(Ii)資本支出、および(Iii)通常の業務中に商品およびサービスを調達する公開調達注文に関連する。これらの債務の大部分は1年以内に支払うことが予想され、その中のいくつかの金額の支払いは将来発生するいくつかの事件に応じて減少する可能性がある。
上記の購入義務に加えて、契約に基づいて、当社が第三者と合意した各種開発、規制、ビジネスマイルストーンを実現する際に、TeneobioやK-Aの買収による価格の合計を含む合計重大な追加金額を支払う義務があります。これらの支払いは未来に発生する様々なイベントに依存し、基本的にこれらのすべてのイベントは高度な不確実性を有し、それによって生じる現金需要はすべて私たちの業務予算プログラムによって管理される。約3億ドルまたは価格の公正価値を除いて、これらの債務は私たちの総合貸借対照表に記録されていない。2022年12月31日現在、我々が第三者と合意した将来支払う可能性のある最高額は56億ドル。
私たちは違法建築の負債を記録しました。それらの性質のため、将来の現金支払いの時間とこれらの負債を除去する他の事件に対して高い不確実性を持っています。連結財務諸表の第四部--付記6、所得税を参照。
重要な会計政策と試算
公認会計原則に基づいて私たちの総合財務諸表を作成する際には、経営陣は、財務諸表と財務諸表の付記に報告された金額に影響を与える推定と仮定を行う必要がある。その中のいくつかの判断は主観的で複雑である可能性があるため,異なる仮定や条件では,実際の結果は推定値と大きく異なる可能性がある.私たちの重要な会計政策は第四部分である付記1、重要会計政策の概要に含まれている。以下の内容は、最も困難、最も主観的、または最も複雑な判断を行う必要があるため、我々の連結財務諸表に重要であると考えられ、通常は本質的に不確実な事項を見積もる必要があるためである。
製品売上高と販売控除額
製品販売収入は、製品制御権が顧客に譲渡される際に確認され、通常、交付時には、私たちが獲得する権利があることが予想される対価格を反映した金額に基づいて、推定リベート、卸返金、割引、その他の控除(総称して販売控除と呼ぶ)と販売時に決定された返金後の課税項目を差し引く。
私たちは四半期ごとに販売減額計算項目の十分性を分析します。傾向または重大なイベントが調整が適切であることを示す場合には、販売減額の課税金額を調整する。応募項目も実際の結果を反映するように調整した。総合貸借対照表の計上すべき負債に記録されている販売控除額は以下のとおりである(百万計)
| | | | | | | | | | | | | | | | | | | | | | | |
| 戻ってきて | | 記憶容量に応じて料金を計算する | | その他減額項目 | | 合計する |
| 2019年12月31日現在の残高 | $ | 3,165 | | | $ | 559 | | | $ | 156 | | | $ | 3,880 | |
| 製品販売に受け取った金額 | 9,167 | | | 8,223 | | | 1,818 | | | 19,208 | |
| 支払い | (8,353) | | | (8,191) | | | (1,735) | | | (18,279) | |
| 2020年12月31日の残高 | 3,979 | | | 591 | | | 239 | | | 4,809 | |
| 製品販売に受け取った金額 | 10,195 | | | 9,619 | | | 2,065 | | | 21,879 | |
| 支払い | (10,027) | | | (9,413) | | | (2,074) | | | (21,514) | |
| 2021年12月31日現在の残高 | 4,147 | | | 797 | | | 230 | | | 5,174 | |
| 製品販売に受け取った金額 | 12,500 | | | 10,630 | | | 2,288 | | | 25,418 | |
| 支払い | (11,768) | | | (10,578) | | | (2,260) | | | (24,606) | |
| 2022年12月31日現在の残高 | $ | 4,879 | | | $ | 849 | | | $ | 258 | | | $ | 5,986 | |
2022年、2021年、2020年12月31日までの年間で、販売減額総額はそれぞれGDP売上高の51%、47%、44%を占めている。2021年12月31日と比較して、2022年12月31日現在の総販売減額残高が増加したのは、主に米国の返金と商業折り返し割引率の上昇の影響と、総売上高の増加によるものであるが、一部は支払い時間によって相殺されている。額には見積数の変化による前年度売上高に関する非実質的純額調整が含まれている
アメリカでは、私たちの製品を医療提供者に分配する主な手段として、卸売業者を使用しています。例えば、医師や彼らの診療所、透析センター、病院、薬局です。ヨーロッパで販売されている製品は主に病院および/または卸売業者に流通しており、これは各販売国における製品の流通実践に依存している。卸売業者や他の第三者のデータを用いて卸売業者の製品在庫レベルを監視することで、卸売業者の在庫はエンドユーザのニーズを満たすために適切なレベル(通常は2~3週間)に維持されていると信じている。そのため、卸売業者の在庫レベルの歴史的変動は販売減額や返品方法に顕著な影響を与えないと予想される。
販売減額の課税費用は、主に関連販売で稼いだ金額や精算すべき金額の見積もりに基づいている。これらの推定は、現在の契約および法的要件、特定の既知の市場イベントおよび傾向、内部および外部履歴データ、および予測された顧客購入パターンを考慮する。販売控除額は基本的に製品に特定されるため,任意の所与の年に対して販売製品の組合せの影響を受ける.
リベートには、主に米国の支払者および提供者に支払われる金額が含まれ、州医療補助計画に支払われる金額を含み、契約手配または法定要求に基づいて、これらの手配または要求は製品、支払者、個人支払者計画によって異なる。私たちが製品を販売する時、私たちは販売した製品、契約条項、推定された患者数、歴史経験と卸売業者の在庫レベルから私たちが支払うリベート金額を推定します。私たちは記録関連販売中にこれらのリベートを蓄積します。そして、より多くの情報が利用できるように、リベート金額を調整して、反映させます
実際に経験をクレームする。このようなリベートは複雑であると予想され,一部の原因は販売日と実際の債務清算との間に時間遅延があるためである.現在の事実や状況を考慮して,リベートに用いる方法は合理的で適切であるが,実際の結果は異なる可能性があると考えられる
卸売業者の返金は、私たちが卸売業者から受け取った価格よりも低い固定価格でアメリカのヘルスケアプロバイダーに製品を販売する私たちの契約契約に関連しています。医療提供者が卸売業者を通じてこれらの値下げで私たちの製品を購入すると、卸売業者は彼らの買収価格と安進とヘルスケア提供者との契約価格との差額に基づいて料金を徴収してくれる。記憶容量に応じた課金を使用するための準備は、私たちの卸売業者の顧客の医療提供者に対する予想される売上に基づいています。卸売業者が返金すべき費用は返却点のように見積もることが困難ではなく、それらは実際の結果に非常に近い。払い戻し金額は医療保険提供者が購入した日に確定したので、私たちは通常数週間以内にこれらの減額の責任を清算します。
製品を返品する
返品は履歴返品データを生産ロットに基づく関連販売と比較することで推定される。履歴収益率は、各製品のために決定され、適切なときに、各製品に固有の市場の既知または予想変化に応じて調整される。過去3年間の毎年、総売上高に占める販売返品準備金の割合は1%未満だった。歴史的には、前年の販売差し戻し準備金の見積もり変化は重要ではない。
所得税
私たちは税引前収入と私たちが経営している各管轄区の適用税率に基づいて所得税を計算します。
税務機関が税務状況の技術的利点に基づいて審査を行った後、さらにその税務状況を維持する可能性がある場合にのみ、不確定税務状況からの税務利益を確認する。連結財務諸表で確認されたある特定の税務状況の税収割引は、最も実現可能な税収割引に基づいている。違例違約金の額は、現行税法の重大な改正、税務機関の新規定或いは解釈、税務審査期間中に取得した新しい資料或いは審査結果など、事実と状況の変化に応じて適切に調整される。私たちは不確定税務状況の推定が適切で十分で、私たちの納税申告書を審査した後に生じる可能性のあるいかなる評価にも使用できると信じています。私たちは適切な時に所得税支出における違約金に関する計算利息と罰金を確認します。
いくつかの項目は、財務諸表に反映される時間とは異なり、資産および負債の課税ベースとその報告された金額との間に一時的な差をもたらす。この一時的な違いは繰延税金資産と負債を生む。繰延税金資産とは、通常、来年度の納税申告書で減額または控除として使用できる項目を指しますが、連結財務諸表に税金割引を記録しました。将来の課税所得額が減額や控除の使用をサポートする可能性が低いと予想される場合、私たちは私たちの繰延税金資産に対して推定免税額を確立します。繰延税金負債とは、(I)総合財務諸表で確認された繰延支払いされた税務支出、(Ii)納税申告書から差し引かれているが総合財務諸表で確認されていない支出、または(Iii)多くの企業合併で買収された無形資産の帳簿ベースと課税基礎との間の差額負債であり、これらの資産に関連する将来の支出は通常課税できないためである
私たちは垂直に統合された企業で、アメリカと違う外国の司法管轄区域で業務をしています。私たちが業務を展開している管轄区では、この管轄区の税法と原則、その管轄区で行われている機能、リスク、活動に基づいて所得税を納めています。したがって、私たちの税引き前収入は、各場所で行われる業務と負担のリスクと、それぞれの税務管区の税法と原則に基づいて、国内または海外の出所に起因する。例えば、私たちはプエルトリコで大量の業務を展開しています。プエルトリコはアメリカの領土であり、アメリカの税金の目的で、製造、流通、その他の関連機能に関連して、世界での私たちの製品需要を満たすために外国の管轄区域とみなされています。2050年までに、プエルトリコでの私たちの業務収入は税金優遇贈与によって制限されるだろう。
2017年、私たちは米国国税局から2010-2012年のRARと修正されたRARを受け取り、主にアメリカのあるエンティティとアメリカ領土プエルトリコ間の利益分配に関連する重大な調整を提案した。我々は提案された調整と計算に同意せず、米国国税局控訴事務所と解決策を求めたが、解決策を達成することはできなかった。2021年7月、私たちは、2021年5月と7月に受信した2つの重複した2010-2012年度法定欠税通知(通知)に異議を求める請願書を米国税務裁判所に提出し、私たちの2010-2012年度の米国課税所得額を約36億ドル増加させ、利息を追加することを目的とした。2010年~2012年の間に徴収される可能性のある任意の追加税収は、最大約9億ドルの以前の私たちの海外収入に計上されていた送金税を減らすだろう。
2020年には、米国国税局から2013-2015年のRARと修正されたRARを受け取り、2010-2012年の提案された利益分配と同様に、米国のあるエンティティと米国領土プエルトリコとの間の利益分配に主に関連する重大な調整を提案した。我々は提案された調整と計算に同意せず、米国国税局控訴事務所と解決策を求めたが、解決策を達成することはできなかった。2022年7月、私たちは米国税務裁判所に請願書を提出し、私たちが2022年4月に受け取った2013-2015年度通知に異議を唱え、2013-2015年度の米国課税所得額を約51億ドル増加させ、利息を追加することを求めた。しかも、通知は罰金が約20億ドルだと主張した。2013-2015年度に徴収される可能性のある任意の追加税収は、約22億ドルに達する以前の私たちの海外収入に計上されていた送金税を減少させるかもしれない。
私たちは2010-2012年と2013-2015年の通知で国税局が提起した立場に根拠がないと信じている。私たちは司法手続きを通じて2010-2012年と2013-2015年の通知に異議を唱えている。この2つの事件は2022年12月19日に米国税務裁判所で合併された。
私たちは現在、2010年から2015年までの問題と類似している国税局2016-2018年の審査を受けている。また、私たちは複数の州と外国税務管轄区の試験に合格した。
これらの複雑な問題の最終的な解決はLiではない次の12ヶ月以内に。過去の経験、税法の解釈、税法の私たちの事実への適用、および税務機関の潜在的な行動の判断によると、私たちの所得税負債の計算項目は適切であると信じている。しかし、所得税の準備の複雑さとこれらの事項の不確定な解決策により、任意の税務事項の最終結果は、支払う金額が課税金額を大幅に超え、私たちの総合財務諸表に重大な悪影響を及ぼす可能性があると信じている。第1部、第1 A項を参照。リスク要因-新しい税法を説明したり、追加の税務責任を負うことは、私たちの収益性に影響を及ぼす可能性があります第二部は、項目7.経営層の財務状況及び経営成果の検討及び分析--経営成果、所得税、及び連結財務諸表第四部--更なる検討のために所得税を付記する。
私たちの業務はアメリカ、プエルトリコアメリカ領土、アメリカ各州司法管轄区域と私たちが業務を展開している他の国の税収法律、法規、行政やり方に制約されています。このような規則の大きな変化は私たちの運営結果に実質的な悪影響を及ぼすかもしれない。第1部、第1 A項を参照。リスク要因-新しい税法を採用して説明したり、追加の税務責任を負うことは私たちの収益力に影響を与える可能性があります.
事件があったり
正常な業務過程において、著者らは各種の法律手続き、政府調査とその他の事項、例えば知的財産権紛争、契約紛争と集団訴訟に関連し、性質が複雑で、結果は予測が困難である。私たちは、連結財務諸表の第4部である付記19“または事項および引受”で、私たちの法的手続きおよびその他の重大または重要になる可能性があると考えている事項を説明します。負債が発生している可能性が高く、関連損失の金額を合理的に見積もることができると結論すれば、損失の計上項目を記録したり、損失したりする必要がある。私たちは、法律手続きの発展や他の以前に蓄積された負債額の増加または減少を招く可能性のある事項を四半期ごとに評価します。
これらのプロジェクトの最終結果を正確に予測または決定することは不可能であるが、現在未解決の1つまたは複数のプロジェクトに対する不利な決定は、私たちの総合的な運営結果、財務状態、またはキャッシュフローに重大な悪影響を及ぼす可能性がある。
買収に関連する資産と負債の評価
私たちは事業合併や資産買収に関連する無形資産を買収し、引き続き買収していく。これらの無形資産は主に現在市場で販売されている人類治療製品と候補知的財産権研究開発製品に関連する技術を含む。割引キャッシュフローモデルは、一般に、買収で得られた純資産に支払いの対価格を割り当てるために、これらの無形資産の公正価値を決定するために使用される。連結財務諸表の第四部--付記2“購入と資産剥離”を参照。これらのモデルは、これらに限定されるものを含むが、重要な推定および仮定を使用する必要がある
•買収日の完了段階を考慮しながら、進行中のプロジェクトの完了時間および予想コストを決定する
•候補製品がFDAおよび他の規制機関の上場承認を獲得する可能性と時間を予測する
•完成した製品および進行中のプロジェクトによって生成される製品販売の時間および将来の純現金流量を推定する;および
•適切な割引率を作成してキャッシュフローの現在値を計算する
業務合併日を決定する際には、業務合併に関連する任意のまたは対価格債務の公正な価値を決定するために、重大な推定および仮定を行う必要がある。さらに、私たちは関連または問題が解決され、収益にその公正な価値の変化を記録するまで、その後の各報告期間にこれらの債務を再評価しなければならない。買収日に買収中に発生したり負担したりする或いは対価格債務の公正価値は総合推定技術を用いて決定される。これらの推定に必要な重大な推定や仮定には,規制マイルストーンを実現する時間や可能性,様々な場合の製品販売予測,必要な支払現在値を計算するための割引率があるがこれらに限定されない。これらの推定数および仮定は、各報告期間においてこれらまたは対価格債務を再推定するために更新される必要がある。したがって、基本的な事実および状況のその後の変化は、これらの推定および仮定の変化をもたらす可能性があり、これは、これらの債務の推定将来の公正価値に大きな影響を与える可能性がある。
吾らは,関連推定日の事実や状況に基づいて,購入した無形資産や業務合併や資産買収に関連して生じたあるいは代償債務の公正価値を記録するために,合理的な推定や仮定に基づいていると信じている。
長期資産減価準備
事件或いは環境変化がある資産の帳簿額面が回収できない可能性があることを示した時、著者らは物件、工場及び設備及び有限年期無形資産の帳簿額面を審査して減価を計算する。このような場合、長期資産が生じる未割引の将来のキャッシュフローの推定は、減値が存在するか否かを決定するために帳簿価値と比較される。1つの資産が減値として決定された場合、損失は、資産の公正価値とその帳簿価値との差に基づいて計量される。
無期限無形資産は買収時にまだ技術実行可能性に達していない或いは監督管理機関の許可を得ていない業務組合せで買収した知的財産権研究開発プロジェクトから構成され、事件或いは状況の変化が帳簿額面が回収できない可能性があることを表明するたびに、及び技術実行可能性或いは監督管理機関の許可を確定した後、毎年減値状況を審査する。私たちは資産の公正価値とその帳簿価値を比較することで減値を決定する。資産の帳簿価値がその公正価値を超えると、差額に減値費用が計上され、その帳簿価値はそれに応じて減少する。
減価分析について言えば、知的財産権研究開発製品候補製品の将来のキャッシュフローを推定するには、プロジェクト完成のコスト金額と時間及び完成した製品から収入を得る金額、時間と可能性について重大な推定と仮定を行う必要があり、上述したプロジェクト買収日の公正価値の確定方式に類似している。知的財産権研究開発プロジェクトは往々にして重大なリスクと不確定性が存在し、私たちは監督管理部門の許可を得て、これらの製品を市場に出すことができるからである。このような承認には臨床試験が必要であり,候補製品が安全かつ有効であることを証明する必要がある。そのため、買収した知的財産権研究開発プロジェクトの最終実現価値は買収の日の公正価値と異なる可能性があり、未来の期間中に知的財産権研究開発減価費用が発生する可能性があり、これは私たちの運営業績に重大な不利な影響を与える可能性がある。
長期資産減価を評価するための将来のキャッシュフローの推定は,評価関連日を考慮した事実や状況を考慮した合理的な仮定に基づいていると信じている。
権益法投資減価
事件や環境変化が一つの投資の帳簿価値が回収できない可能性があることを示すたびに、私たちの権益法投資の帳簿価値を審査します。もし私たちが減値が非一時的だと思うなら、私たちは私たちの権益法投資に減価損失を記録するだろう。私たちは様々な要素に基づいて減価を非一時的と見なし、公正価値が帳簿価値より低い時間長と程度、証券価格の変動性、発行者の財務状況、投資利益の潜在力を損なう可能性のある技術変化、および公正価値回収を実現するために投資を保留する意図と能力を含む
吾らは,権益法投資減値を評価する際に用いられる判断は,関連日の事実や状況を評価するための合理的な仮定に基づいていると信じている。
最近発表された会計基準
2022年12月31日現在採用されていない最近発表された会計公告の検討については、連結財務諸表第4部である重要会計政策概要付記1を参照。
私たちが直面している市場リスクは、金利、外貨為替レート、株価ツール価格の変化、そして私たちが業務を展開している国の全体的な経済状況の変化かもしれません。何らかのリスクを低減するために,我々のリスク管理計画の一部として,様々な種類の外貨と金利デリバティブヘッジ取引を行った。私たちは投機取引目的に派生商品を使用しないつもりだ。
次の議論では、金利が2022年12月31日と2021年12月31日の金利より100ベーシスポイント変化すると仮定します。以下の説明のほか、2022年12月31日と2021年12月31日の外貨対ドルレートの他の通貨に対する為替レートに基づいて、外貨対ドルレートが20%変化すると仮定する。
金利に敏感な金融商品
2022年12月31日と2021年12月31日までに、我々の売却可能なポートフォリオのほぼすべてが米国債と通貨市場共同基金で構成されている。2022年12月31日と2021年12月31日まで、私たちが売却できる投資の公正価値はそれぞれ43億ドルと73億ドルです。存続期間は感度指標であり、金利変化100ベーシスポイントによる証券価値の変化を推定するために用いることができる。長期モデルを用いて、2022年12月31日と2021年12月31日に100ベーシスポイント利上げすると仮定すると、これらの証券の公正価値が大幅に低下することはない。また、2022年12月31日と2021年12月31日の金利が100ベーシスポイント低下したと仮定すると、その後の年間収入に実質的な影響を与えない。
2022年12月31日まで、私たちの未返済債務の帳簿価値は389億ドル、公正価値は350億ドルです。2021年12月31日現在、私たちの未返済債務の帳簿価値は333億ドル、公正価値は379億ドルです。私たちの未済債務は固定金利の債務で構成されている。金利の変化は固定金利債務の利息支出に影響を与えない。しかし、金利の変化は固定金利債務の公正な価値に影響を及ぼすだろう。2022年と2021年12月31日の金利が金利に対して100ベーシスポイント低下したと仮定すると、この3日の未返済債務公正価値総額はそれぞれ35億ドルと45億ドル増加する。債務の分析は、想定される金利変化が以下に議論する関連金利スワップ契約およびクロス通貨スワップ契約に及ぼす影響を考慮していない。
固定金利と変動金利債務の理想的な組み合わせを実現するために、条件を満たし、特定の固定金利債務の公正価値ヘッジとして指定された金利交換契約を締結しました。これらの金利交換契約は、固定金利額面金利をLIBORによる変動金利額面金利に効率的に変換する。2022年12月31日と2021年12月31日まで、名目総金額67億ドルの金利スワップ契約は決済されていない。2022年と2021年12月31日の金利が金利に対して100ベーシスポイント上昇すると、公正価値が約210ドル減少すると仮定する これらの日に、私たちの金利スワップ契約はそれぞれ3.3億ドルと3.3億ドルだ。金利交換契約の分析は、仮定された金利変動が、これらの金利感知型ツールが相殺することを目的とした関連債務公正価値に与える影響を考慮していない
発行が予想される長期固定金利債務については、私たちがこれらの契約を締結してから関連債務を発行するまでの間、適用される米国債の金利変化によるキャッシュフローの変化をヘッジするための長期金利契約をたまに締結します。2022年12月31日まで、未平倉長期金利契約があり、名義総金額は7億ドルである;2021年12月31日まで、未平倉長期金利契約はない。2022年12月31日に金利が金利に対して100ベーシスポイント低下すると、公正価値が約60ドル減少すると仮定する この日、私たちの長期金利契約の金利は100万ドルです。
2022年12月31日と2021年12月31日まで、私たちは未返済のクロス通貨スワップ契約を持っていて、名目総金額は34億ドルで、私たちの外貨建て債務と関連利息で支払います。これらの契約は実際にこの債務の利息支払いと元金返済をユーロ、ポンド、スイスフランからドルに変換し、会計上キャッシュフローヘッジとして指定されている。2022年12月31日現在と2021年12月31日現在の金利の逆変動100ベーシスポイントを想定すると、我々のクロス通貨スワップ契約の公正価値はそれぞれ約9000万ドルと1.7億ドル減少する。
外国為替に敏感な金融商品
私たちの国際業務は外国通貨(主にユーロ)に対するドルの価値変動の影響を受けている。為替レート変動による国際製品売上高の増減部分は私たちの国際運営費用の相応の増減によって相殺されます。外貨為替レートの変動により私たちの外貨資産の増減部分は私たちの外貨負債の相応の増減によって相殺されます。外貨為替レート変動が私たちの経営業績に与える純影響をさらに減らすために、外貨長期とクロス通貨スワップ契約を締結しました。
2022年12月31日まで、私たちはユーロ、ポンド、スイスフラン建ての未返済債務があり、元金の帳簿価値と公正価値はそれぞれ30億ドルと29億ドルです。2021年12月31日まで、私たちはユーロ、ポンド、スイスフラン建ての未返済債務があり、元金の帳簿価値と公正価値はそれぞれ32億ドルと36億ドルです。2022年12月31日現在、外貨為替レートがドルレートに対して20%の不利な変動が生じたと仮定すると、この債務の公正価値はこの日に約5.8億ドル増加し、次の年に約6億ドル減少する。2021年12月31日現在、外貨為替レートがドルレートに対して20%の不利な変動が生じたと仮定すると、この債務の公正価値はこの日に7.1億ドル増加し、次の年に6.4億ドル減少する。外貨為替レートのこれらの仮定変化が収入に与える影響は、このような変化が関連するクロス通貨交換契約に与える影響によって大きく相殺され、これらの契約は関連する外貨建て債務のために制定されている。
私たちはクロス通貨スワップ契約を持っています。これらの契約はユーロ、ポンド、スイスフラン建ての債務のキャッシュフローヘッジに指定されています。2022年12月31日と2021年12月31日まで、名目総金額は34億ドルです。ドルレートに対して外貨為替レートがこれらの日付に対して20%の不利な変動があると仮定すると、これらの日におけるこれらの契約の公正価値はそれぞれ約5.4億ドルと7億ドル減少する。外貨為替レートのこの仮定不利な変動がその後数年のこれらの契約からの収入に与える影響は、関連するヘッジ債務帳簿金額の対応する仮定変化によって完全に相殺される。
私たちは外貨長期契約を締結し、会計目的のためにある予想外貨取引のキャッシュフローヘッジとして指定します。2022年12月31日現在、これらの契約の公正価値は2.88億ドルの資産と7600万ドルの負債である。これらの契約の公正価値は、2021年12月31日現在、1.83億ドルの資産と3900万ドルの負債である。2022年12月31日現在、私たちは主にユーロベースの未平倉外貨長期契約を持っており、名目金額は60億ドルです。2021年12月31日現在、私たちは主にユーロベースの未平倉外貨長期契約を持っており、名目金額は57億ドルです。2022年12月31日までに平倉していない外貨長期契約については,2022年12月31日現在の外貨レートがドルレートに対して20%の不利な変動があると仮定すると,これらの契約はこの日と来年度の公正価値が約11億ドル減少し,収入が約5.9億ドル減少する。2021年12月31日現在の未平倉契約については、2021年12月31日現在の外貨為替レートがドルレートに対して20%の不利な変動があると仮定すると、これらの契約の当日と来年度の公正価値が約11億ドル減少し、収入が3.9億ドル減少する。この分析は、外貨為替レートの仮定変化が、これらの外貨に敏感なツールが相殺しようとしている予想取引に与える影響を考慮していない。
2022年12月31日と2021年12月31日まで、1ヶ月以下で満期となる短期未平倉外貨長期契約があり、名目金額はそれぞれ5億ドルと7億ドルであり、いくつかの外貨建て資産や負債の変動が生じているが、会計上ヘッジとして指定されていない。2022年12月31日と2021年12月31日まで、これらの契約は実質的な純収益や損失を実現していない。これらの2022年12月31日までと2021年12月31日までに平倉されていない外貨長期契約については、これらの日付の外貨レートがドルレートに対して5%の不利な変動があると仮定し、これらの契約の公正価値またはその後数年の関連収入に実質的な影響を与えないと仮定する。この分析は、外貨為替レートの仮定変化が、これらの外貨に敏感なツールが相殺しようとしている資産や負債に与える影響を考慮していない。
市場価格に敏感な金融商品
2022年12月31日と2021年12月31日現在、我々のポートフォリオに含まれる株式証券は価格リスクに直面しており、これらの証券の買収は主に業務と戦略目標を促進するためである。これらの投資には公共と個人が保有する小時価株、早期バイオテクノロジー会社に投資する有限組合企業が含まれています
百済神州への投資もあります2022年と2021年12月31日まで、私たちの株式ポートフォリオの総価値は20%低下し、それぞれ約11億ドルと14億ドルの公正価値損失を招くことになる。
取引相手信用リスク
我々の金融商品は,デリバティブを含み,取引相手の信用リスクの影響を受けており,全体的な公正価値計測の一部であると考えられる.我々の金融リスク管理政策はデリバティブ取引を制限し、信用格付けが最低A-あるいはスタンダード、ムーディーズ或いはHPと同等の格付けを獲得した機関としか取引できないことを要求し、任意の単一の取引相手との取引金額に対してリスク開放制限を設定する。さらに、我々の投資政策は、投資レベルの信用格付けを有する機関によって発行され、資産種別および発行者によって期限および集中度を制限するいくつかのタイプの債務および通貨市場ツールに投資を制限する。
本プロジェクトに要求される資料は、本年度報告において、表格10−Kに記載されている財務諸表および付表の形態で本報告に組み込まれる。
| | | | | |
| 第九項です。 | 会計·財務開示面の変化と会計士との相違 |
ない。
我々は、証券取引法第13 a-15(E)条に定義されている“開示制御及び手順”を維持し、米国証券取引委員会規則及び表に規定されている時間内に安進取引法報告書に開示すべき情報を記録、処理、まとめ、報告し、そのような情報を蓄積し、その最高経営者及び最高財務官を含む安進管理層に伝達し、必要な開示について決定することを目的としている。開示制御及びプログラムを設計·評価する際に、安進の管理層は、任意の制御及びプログラムは、設計及び操作がどんなに良好であっても、予想される制御目標を達成するために合理的な保証を提供することしかできず、合理的な保証レベルに達した場合、安進の管理層は、その判断を用いて、可能な制御とプログラムのコスト−収益関係を評価しなければならないことを認識している。我々は、安進最高経営責任者と最高財務官を含む経営陣の監督と参加の下で、安進情報開示制御とプログラムの設計と動作の有効性を評価した。上記の評価によると、最高経営責任者と財務責任者は、2022年12月31日に我々の開示制御および手続きが発効すると結論した。
経営陣は、2022年12月31日現在、2022年12月31日までの財政四半期内に、財務報告の内部統制に大きな影響を与えていないか、または合理的に財務報告の内部統制に大きな影響を与える可能性があると認定している。
財務報告の内部統制に関する経営陣の報告
会社経営陣は、1934年の証券取引法下の規則13 a-15(F)で定義されている財務報告の十分な内部統制の確立と維持を担当している。会社の財務報告に対する内部統制は財務報告の信頼性とアメリカ公認会計原則に基づいて外部財務諸表を作成するために合理的な保証を提供することを目的としている。しかし,すべての内部制御システムには,どんなに良く設計されていても,固有の限界がある.したがって、有効と判断された制度であっても、財務諸表の作成や報告に合理的な保証を提供することしかできない。
経営陣は、2022年12月31日までの社内財務報告の内部統制の有効性を評価した。この評価を行う際には,管理層はCOSOが“内部制御である統合フレームワーク”(2013年フレームワーク)で提案した基準を用いた.我々の評価によると、経営陣は、COSO基準に基づき、2022年12月31日現在、会社が財務報告に対して有効な内部統制を維持していると考えている。
当社の財務報告内部統制の有効性は、独立公認会計士事務所安永会計士事務所が監査しており、その認証報告は以下のとおりであり、この報告は、当社の2022年12月31日までの財務報告内部統制の有効性について保留のない意見を示している。
独立公認会計士事務所報告
安進の株主と取締役会へ
財務報告の内部統制については
我々は、テレデビル委員会後援組織委員会が発表した“内部統制-総合枠組み(2013年枠組み)”(COSO基準)で確立された基準に基づき、安進社の2022年12月31日までの財務報告内部統制を監査した。安進(当社)はCOSO基準に基づき,2022年12月31日から各重大な面で財務報告に対して有効な内部統制を実施していると考えられる。
我々もすでにアメリカ上場会社会計監督委員会(PCAOB)の基準に従って、当社の2022年12月31日、2022年12月31日及び2021年12月31日までの総合貸借対照表、2022年12月31日までの3年間の各年度の関連総合収益表、全面収益表、株主権益及びキャッシュフロー表、及び指数15(A)の2項目に記載された関連付記及び財務諸表付表を監査し、2023年2月9日の報告について保留なし意見を発表した。
意見の基礎
当社経営陣は、効果的な財務報告内部統制を維持し、添付されている“経営陣財務報告内部統制報告”に掲載されている財務報告内部統制の有効性を評価する責任がある。私たちの責任は私たちの監査に基づいて、会社の財務報告書の内部統制に意見を述べることです。私たちはPCAOBに登録されている公共会計士事務所で、アメリカ連邦証券法およびアメリカ証券取引委員会とPCAOBの適用規則と法規に基づいて、私たちは会社と独立しなければなりません。
私たちはPCAOBの基準に従って監査を行っている。これらの基準は、財務報告の有効な内部統制がすべての重要な面で維持されているかどうかを決定するために、合理的な保証を得るために監査を計画し、実行することを要求する。
我々の監査には,財務報告の内部統制を理解すること,重大な弱点があるリスクを評価すること,評価されたリスクテストに基づいて内部統制の設計·運用有効性を評価すること,および状況下で必要と考えられる他のプロセスを実行することが含まれる。私たちは私たちの監査が私たちの観点に合理的な基礎を提供すると信じている。
財務報告の内部統制の定義と限界
会社の財務報告に対する内部統制は、公認された会計原則に基づいて、財務報告の信頼性と外部目的の財務諸表の作成に合理的な保証を提供することを目的としたプログラムである。会社の財務報告に対する内部統制には、(1)合理的で詳細かつ正確かつ公平に会社の資産を反映した取引および処分に関する記録の保存、(2)公認された会計原則に従って財務諸表を作成するために必要な取引が記録されている合理的な保証を提供し、会社の収入および支出は会社の経営陣と取締役の許可のみに基づいて行われる。(三)財務諸表に重大な影響を及ぼす可能性のある不正買収、使用、または処分会社の資産を防止またはタイムリーに発見する合理的な保証を提供する。
その固有の限界のため、財務報告書の内部統制は誤った陳述を防止したり発見できない可能性がある。また,将来的にどのような有効性評価を行うかの予測は,条件の変化により制御不足のリスクが生じる可能性があり,あるいは政策やプログラムの遵守度が悪化する可能性がある.
/s/ 安永法律事務所
カリフォルニア州ロサンゼルス
2023年2月9日
適用されません。
第三部
当社取締役に関する資料は、当社が2022年12月31日から120日間、米国証券取引委員会に提出した2023年株主周年大会依頼書(依頼書)の第1項-取締役選挙の節で引用します。株主が取締役会の有名人を推薦するプログラムに関する情報は引用的に付録A-安進に格納される.我々の委託書では,取締役会が役員資格や評価等の事項に関するガイドラインである株主から2024年年次総会への提言を行っている。当社の審査委員会、審査委員会のメンバー及び審査委員会の財務専門家に関する資料は、委託書の“会社管理-審査委員会”の節に参考方式で組み入れられている。我々の実行幹事に関する情報は,第1部,項目1.業務--我々が幹事を実行する情報についての議論に掲載されている.
道徳的規則
私たちは、最高経営責任者と上級財務官のために、私たちの最高経営責任者、最高財務官、最高会計官または財務総監、および同様の機能を実行する他の人に適した道徳的基準を制定した。本道徳基準を無料で確認するためには、私たちのサイトwww.amgen.comにアクセスしてください。(サイトアドレスはハイパーリンクとして利用する予定はなく,我々のサイトに含まれる情報も本出願の一部とする予定はない.我々は,我々のサイト上で上記の情報を配布することで,Form 8-K第5.05項における本道徳規則の改正または免除に関する開示要件を満たす予定である.
役員と役員の報酬に関する情報は、私たちの依頼書の給与議論と分析、役員報酬表、役員報酬と会社管理と給与比率部分を参考にした。給与委員会の件に関する資料は、当社の委託書に“会社管理-報酬及び管理発展委員会”および“会社管理-報酬委員会報告”の2節から引用されている。
| | | | | |
| 第十二項。 | ある実益所有者の担保所有権及び経営陣及び株主に関する事項 |
既存持分補償計画に基づいて発行された証券
次の表は、2022年12月31日現在、私たちの有効な配当補償計画に従って付与された任意の形態の奨励(オプションの行使、RSU奨励、または業績単位の獲得、関連配当等価物の付与を含む)によって発行される可能性のある普通株式のいくつかの情報を示している。
| | | | | | | | | | | | | | | | | | | | |
| | (a) | | (b) | | (c) |
| 計画種別 | | まだ行使されていないオプションと権利を行使する際に発行しなければならない証券数 | | 未償還オプションと権利の加重平均行権価格 | | 株式補償計画に基づいて将来発行可能な証券の数(含まれていない)
(A)欄) |
| 安進証券所有者が承認した持分補償計画: | | | | | | |
2009年の株式インセンティブ計画の改訂と再策定(1) | | 10,235,620 | | | $ | 207.29 | | | 15,255,297 | |
1991年の株式インセンティブ計画を改訂し再確認します(2) | | 2,191 | | | | | |
| 従業員の株購入計画を改訂·再策定する | | | | | | 4,180,287 | |
| 承認された図の総数 | | 10,237,811 | | | 207.29 | | | 19,435,584 | |
| 株式補償計画は安進証券所有者の許可を得ていない: | | | | | | |
アンはアイルランドに入って従業員の利益共有計画(3) | | | | | | 222,310 | |
| 未承認の計画の総数 | | — | | | — | | | 222,310 | |
| すべての計画合計 | | 10,237,811 | | | $ | 207.29 | | | 19,657,894 | |
(1)改訂後の2009年計画は、この計画の下で発行可能な株式数を決定するために代替可能な株式計算式を採用した。この公式により、各オプション或いは株式付加価値権は1株に計上され、1株当たりRSU、業績単位或いは配当等価物は1.9株に計上される。(A)欄の数字は、代替株式計算式を採用することなく、未償還報酬に基づいて発行可能な実株式数を表す。(C)欄下の数字は、本計画により発行可能な株式数を示し、発行可能株式毎に1株とする。二零一二年四月に発行された授与から、RSU及び履行単位は配当金等価物を計算し、この等の配当等価物は、関連RSUの帰属又は関連履行単位がすでに獲得した及び関連株式が発行された授与者の場合にのみ株式で支払われる。本計画により付与された業績単位は、それぞれ3年間の業績期間終了時に指定された業績目標を達成したものであり、授与された業績単位数は目標業績を代表し、著者らの業績によって獲得できる最大単位数は2020、2021、2022年に授与された業績単位の200%である
2022年12月31日現在、(A)欄下の未償還奨励数は、(I)5,322,407株が加重平均行権価格207.29ドルの未行使購入株を行使することにより発行可能な株式、(Ii)3,173,806株が発行されたRSUに帰属することができる株式(307,825株関連配当等価物を含む)、および(Iii)1,739,407株は、2020年、2021年および2022年の未償還実績単位制限を受けなければならない株式(84,603株関連配当等価物を含む)を含む。(B)の欄に示す重み付き平均行重みは,未平倉オプションのみである.(C)欄下の利用可能株式数は、2022年12月31日現在も将来発行可能な株式数を表し、代替株式式を採用し、2020、2021年、2022年に付与された業績単位および関連配当等価物から目標株式を発行すると仮定する。(A)及び(C)項の数字には、当該等の未完了業績単位の業績目標が目標以上に達したときに発行可能な追加株式は含まれていない。これらの目標の下での最大業績は、2020年、2021年、2022年に付与された業績単位が目標株式の200%を獲得する可能性がある。
(2)未来の支出について、この計画は終了した。本計画に関連する(A)欄数字は、繰延RSUの決済時に発行可能な株式(519株関連配当金等価物を含む)2,191株を含む。
(3)利益共有計画は2011年7月28日に取締役会の承認を得た。利益共有計画は、利益共有計画に記載されているように、利益共有計画に参加する会社のアイルランドに位置する子会社の合格従業員が、その合格ボーナスおよび賃金の一部を、第三者受託者が公開市場で市場価格で会社の普通株を購入するために使用することを可能にする。
役員、行政員、およびある実益所有者の保証所有権
いくつかの実益所有者および経営層の担保所有権に関する情報は、我々の委託書に、取締役および役員担保所有権および特定の実益所有者という担保所有権の章を引用している。
ある関係や関連取引と取締役独立性に関する情報は,我々の依頼書に“ある関係と関連取引とコーポレートガバナンス−取締役独立性”と題する章から引用されている。
当社の独立公認会計士が提供する専門サービス費用に関する資料は、当社の委託書に引用で“監査事項-独立公認会計士”と題する節に組み込まれています。
第4部
(a)1.財務諸表索引
本報告書には、以下の連結財務諸表が含まれています
| | | | | |
| | ページ
番号をつける |
独立公認会計士事務所レポート(PCAOB ID:42) | F-1 |
| |
2022年12月31日までの3年度における各年度の連結損益表 | F-4 |
| |
2022年12月31日までの3年度の総合総合収益表 | F-5 |
| |
2022年と2021年12月31日までの連結貸借対照表 | F-6 |
| |
2022年12月31日までの3年度の株主権益合併報告書 | F-7 |
| |
2022年12月31日までの3年度の連結現金フロー表 | F-8 |
| |
| 連結財務諸表付記 | F-9 |
(a)2.財務諸表明細表索引
以下の付表は、本年度報告の10-K表の一部として提出される
| | | | | |
| | ページ
番号をつける |
| 別表2.評価及び合資格勘定 | F-55 |
他のすべての付表は、適用されない、必要ではない、または必要な情報が連結財務諸表または付記に含まれるため、省略される。
(a)3.陳列品
| | | | | | | | |
| 証拠品番号: | | 説明する |
| 2.1 | | 資産購入契約は、2019年8月25日に安進会社とCelgene社が署名した。(8-Kフォームの証拠品として2019年8月26日に提出され、参照によって本明細書に組み込まれます。) |
| | |
| 2.1.1 | | 安進会社とCelgene社の間で2019年10月17日に署名された資産購入協定の改正案第1号。(8-Kフォームの証拠品として2019年10月17日に提出され、参照によって本明細書に組み込まれます。) |
| | |
| 2.1.2 | | 安進会社とCelgene社の間で2019年10月17日に署名された資産購入協定の修正案第2号。(2020年2月12日に2019年12月31日現在の10-K表の証拠品として提出され、参照により本明細書に組み込まれる。) |
| | |
| 2.2 | | 2019年11月21日、Amgen Inc.と指名された当事者との間で署名された書簡協定Re:AmgenによるOtezla買収に関連するいくつかの製品在庫の処理(2020年2月12日に2019年12月31日現在の10-K表の証拠品として提出され、参照により本明細書に組み込まれる。) |
| | |
| 2.3 | | 保証を取り消すことはできません。日付は2019年8月25日で、安進会社と百時美施貴宝社の間で提供されます。(8-Kフォームの証拠品として2019年8月26日に提出され、参照によって本明細書に組み込まれます。) |
| | |
| 2.4 | | 協議と合併計画は,期日は2021年7月27日であり,安進,テネオビオ社,Tuxedo合併子会社と富通コンサルタント有限責任会社が署名した。(一部の展示品は省略されている。(I)は実質的ではないので、(Ii)は、会社が個人または機密とみなす情報タイプである)(展示品として2021年11月3日現在2021年9月30日までの10-Q表に提出され、参照により本明細書に組み込まれる。) |
| | |
| | | | | | | | |
| 証拠品番号: | | 説明する |
| 2.5 | | ChemoCentryx,Inc.,Amgen Inc.と自動車連結子会社との間の合併協定と計画は,2022年8月3日である。(2022年8月4日に8-K表の証拠品として提出され、参照によって本明細書に組み込まれる。) |
| | |
| 2.6 | | 安進,Pillartree LimitedとHorizon Treeutics plcが署名した取引合意は,2022年12月11日である.(2022年12月12日に8-K表の証拠品として提出され、参照によって本明細書に組み込まれる。) |
| | |
| 2.7 | | ルール2.7公告付録3,日付は2022年12月12日(条件付録).(2022年12月12日に8-K表の証拠品として提出され、参照によって本明細書に組み込まれる。) |
| | |
| 3.1 | | 安進が再述した会社登録証明書。(2013年3月6日再確認。)(2013年3月31日現在の第10-Q表の証拠として2013年5月3日に提出され、引用によって本明細書に組み込まれる。) |
| | |
| 3.2 | | “安進定款”を改正·再制定する。(改訂され、2016年2月15日に再決定されました。)(2016年2月17日に8-K表の証拠品として提出され、参照によって本明細書に組み込まれる。) |
| | |
| 4.1 | | 普通株の株式形式は、額面は.0001ドルです。(1997年3月31日現在のForm 10-Qが1997年5月14日に提出された証拠として、参照によって本明細書に組み込まれる。) |
| | |
| 4.2 | | 義歯の形式は,期日は1992年1月1日であった。(1991年12月19日に提出され、S-3登録声明を形成する証拠として提出され、参照によって本明細書に組み込まれる。) |
| | |
| 4.3 | | 2008年2月15日の辞任、任命、そして合意を受け入れる。(2007年12月31日現在の10-K表の証拠品として2008年2月28日に提出され、参照によって本明細書に組み込まれる) |
| | |
| 4.4 | | 初回補充義歯は1997年2月26日であった。(1997年3月14日に8-K表の証拠品として提出され、参照によって本明細書に組み込まれる。) |
| | |
| 4.5 | | 2097年4月1日に満期となった8-1/8%債券。(1997年4月8日に8-K表の証拠品として提出され、参照によって本明細書に組み込まれる。) |
| | |
| 4.6 | | 安進高級職員証明書は、1997年4月8日に、“8 1/8%債券、2097年4月1日に満期”という一連の証券を設立した(1997年4月8日に8-K表の証拠品として提出され、参照によって本明細書に組み込まれる。) |
| | |
| 4.7 | | 契約,日付は2003年8月4日である.(2003年8月4日に証拠品として提出され、S-3登録声明を形成し、参照によって本明細書に組み込まれる。) |
| | |
| 4.8 | | 会社商業手形-安進は発行人として,預託信託会社の代理人として会社を譲り,シティ銀行は支払いエージェント間の主手形とする.(1998年5月13日から1998年3月31日までのForm 10-Qの証拠として提出され、参照によって本明細書に組み込まれる。) |
| | |
| 4.9 | | 安進高級職員証明書は、日付は2007年5月30日で、当社の2037年満期の6.375%優先債券のフォーマットを含む(2007年5月30日に8-K表の証拠品として提出され、参照によって本明細書に組み込まれる) |
| | |
| 4.10 | | 安進高級社員証明書は、2008年5月23日に、当社が2038年に満期になった6.90%の高級債券のフォーマットを含む。(8-Kフォームの証拠品として2008年5月23日に提出され、参照によって本明細書に組み込まれる) |
| | |
| 4.11 | | 安進高級社員証明書、日付は2009年1月16日、当社が2039年に満期になった6.40%の高級債券の表を含む(証拠品として2009年1月16日にForm 8-Kに提出され、参照によって本明細書に組み込まれる。) |
| | |
| 4.12 | | 安進高級社員証明書は、期限は2010年3月12日で、当社が2040年に満期となる5.75分の高級債券のフォーマットを含む。(証拠物として2010年3月12日にForm 8-Kに提出され、参照によって本明細書に組み込まれる。) |
| | |
| 4.13 | | 安進高級社員証明書は、2010年9月16日で、当社が2041年に満期になった4.95%高級債券のフォーマットを含む(2010年9月17日に8-K表の証拠品として提出され、参照によって本明細書に組み込まれる。) |
| | |
| 4.14 | | 安進高級社員証明書は、2011年6月30日に、当社が2042年に満期になった5.65%の高級債券のフォーマットを含む。(2011年6月30日に8-K表の証拠品として提出され、参照によって本明細書に組み込まれる。) |
| | |
| 4.15 | | 安進高級社員証明書は、2011年11月10日に、当社が2041年に満期となった5.15分の高級債券のフォーマットを含む。(2011年11月10日に8-K表の証拠品として提出され、参照によって本明細書に組み込まれる。) |
| | |
| | | | | | | | |
| 証拠品番号: | | 説明する |
| 4.16 | | 安進高級社員証明書は、2011年12月5日で、当社が2026年に満期となった5.50%の高級債券のフォーマットを含む。(2011年12月5日に8-K表の証拠品として提出され、参照によって本明細書に組み込まれる。) |
| | |
| 4.17 | | 安進高級社員証明書は、2012年5月15日で、当社が2043年に満期になった5.375%高級債券のフォーマットを含む。(2012年5月15日に8-K表の証拠品として提出され、参照によって本明細書に組み込まれる。) |
| | |
| 4.18 | | 安進高級社員証明書は、2012年9月13日に、当社が2029年に満期となった4.000%の高級債券のフォーマットを含む。(2012年9月13日に8-K表の証拠品として提出され、参照により本明細書に組み込まれる。) |
| | |
| 4.19 | | 契約は,日付は2014年5月22日で,Amgen Inc.とニューヨークメロン銀行信託会社が受託者としている。(8-K表の証拠品として2014年5月22日に提出され、参照によって本明細書に組み込まれる。) |
| | |
| 4.20 | | 安進高級社員証明書は、2014年5月22日に、当社の2024年満期の3.625%高級債券のフォーマットを含む。(8-K表の証拠品として2014年5月22日に提出され、参照によって本明細書に組み込まれる。) |
| | |
| 4.21 | | 安進高級社員証明書は、2015年5月1日に、当社が2025年に満期となる3.125分の高級債券と、2045年に満期となる4.400分の高級債券のフォーマットを含む。(2015年5月1日にForm 8-Kに証拠品として提出され、参照によって本明細書に組み込まれる。) |
| | |
| 4.22 | | 安進高級社員証明書は、2016年2月25日に、当社が2026年に満期となった2.000%優先債券の形式を含む。(2016年2月26日にForm 8-Kに証拠品として提出され、参照によって本明細書に組み込まれる。) |
| | |
| 4.23 | | 2023年に満期になった会社の0.410%債券の永久グローバル証明書形式。(2016年3月8日にForm 8-Kに証拠品として提出され、参照によって本明細書に組み込まれる。) |
| | |
| 4.24 | | 当社は2023年満期の0.410%債券の債券条項を発行します。(2016年3月8日にForm 8-Kに証拠品として提出され、参照によって本明細書に組み込まれる。) |
| | |
| 4.25 | | 安進高級社員証明書は、2016年6月14日付で、当社の2048年満期の4.563分の高級債券と2051年に満期の4.663分の高級債券のフォーマットを含む。(2016年6月14日に8-K表の証拠品として提出され、参照によって本明細書に組み込まれる。) |
| | |
| 4.26 | | 安進高級社員証明書は、2016年8月19日に、当社の2023年満期の2.250分の高級債券と2026年に満期の2.600分の高級債券のフォーマットを含む。(8-K表の証拠品として2016年8月19日に提出され、参照によって本明細書に組み込まれる。) |
| | |
| 4.27 | | 安進高級社員証明書は、2017年11月2日に、当社が2027年に満期となった3.200%優先債券の形式を含む。(8-K表の証拠品として2017年11月2日に提出され、参照によって本明細書に組み込まれる。) |
| | |
| 4.28 | | 安進高級社員証明書は、期限は2020年2月21日で、当社の2025年満期の1.900%優先債券、2027年満期の2.200%優先債券、2030年満期の2.450%優先債券、2040年満期の3.150%優先債券、2050年満期の3.375%優先債券を含む。(2020年2月21日に8-K表の証拠品として提出され、参照によって本明細書に組み込まれる。) |
| | |
| 4.29 | | 安進高級職員証明書は、期日は2020年5月6日で、当社の2031年満期の2.300%優先債券の形式を含む。(2020年5月6日に8-K表の証拠品として提出され、参照によって本明細書に組み込まれる。) |
| | |
| 4.30 | | 安進高級職員証明書は、期日は2020年8月17日で、当社の2053年満期の2.770%優先債券のフォーマットを含む。(2020年8月18日に8-K表の証拠品として提出され、参照によって本明細書に組み込まれる。) |
| | |
| 4.31 | | 安進高級社員証明書は、2021年8月9日に、当社の2028年満期の1.650%高級債券、2032年満期の2.000%高級債券、2041年満期の2.800%高級債券、2052年満期の3.000%の高級債券を含む。(8-Kフォームの証拠品として2021年8月9日に提出され、参照によって本明細書に組み込まれる。) |
| | |
| 4.32 | | 安進高級社員証明書は、2022年2月22日に、当社の2029年満期の3.000%高級債券、2032年満期の3.350%高級債券、2052年満期の4.200%高級債券、2062年満期の4.400%の高級債券を含む。(2022年2月22日に8-K表の証拠品として提出され、参照によって本明細書に組み込まれる。) |
| | |
| 4.33 | | 安進高級社員証明書は、期日は2022年8月18日で、当社の2029年満期の4.050分の高級債券、2033年に満期の4.200分の高級債券、2053年に満期の4.875分の高級債券のフォーマットを含む。(2022年8月18日に8-K表の証拠品として提出され、参照によって本明細書に組み込まれる。) |
| | | | | | | | |
| 証拠品番号: | | 説明する |
| | |
| 4.34* | | 安進1934年証券取引法第12条に基づいて登録された証券の概要 |
| | |
| 10.1+ | | 安進。2009年の株式インセンティブ計画を改訂し、再編成する。(添付表14 Aの最終委託書付録Cとして2013年4月8日に提出され、参照により本明細書に組み込まれる。) |
| | |
| 10.2+ | | “安進修正案”は2009年の株式激励計画を改訂し、2015年3月4日から施行された。(2015年4月27日は、2015年3月31日現在の第10-Q表の証拠として提出され、引用により本明細書に組み込まれる。) |
| | |
| 10.3+ | | “安進修正案”改正で再確認された2009年株式激励計画は、2016年3月2日から施行されるそれは.(2016年3月31日現在の第10-Q表の証拠として2016年5月2日に提出され、引用により本明細書に組み込まれる。) |
| | |
| 10.4+* | | 安進株式オプション協定の付与形式。2009年の株式インセンティブ計画を改訂し、再編成する。(2022年12月12日に改訂·再確認されました。) |
| | |
| 10.5+* | | 安進限定株契約フォーマット。2009年の株式激励計画を再改訂する。(2022年12月12日に改訂·再確認されました。) |
| | |
| 10.6+ | | 安進。2009年度公演奨励計画。(2017年12月12日改訂。)(2018年2月13日に2017年12月31日現在の10-K表の証拠品として提出され、参照により本明細書に組み込まれます。) |
| | |
| 10.7+* | | 2009年度業績奨励計画業績単位合意書フォーマットに安進した。(2022年12月12日に改訂され、再開される。) |
| | |
| 10.8+ | | 安進。2009年取締役持分激励計画。(2020年10月21日に改訂され、再改訂される。)(2020年12月31日現在の年間10-K表の証拠品として2021年2月9日に提出され、参照により本明細書に組み込まれる。) |
| | |
| 10.9+ | | 安進2009年取締役持分インセンティブ計画制限株式単位合意フォーマット。(2019年12月11日に改訂します。) (2020年2月12日に2019年12月31日現在の10-K表の証拠品として提出され、参照により本明細書に組み込まれる。) |
| | |
| 10.10+ | | 安進2009年取締役持分インセンティブ計画現金決済制限株式単位合意フォーマット。(2019年12月11日に改訂します。)(2020年2月12日に2019年12月31日現在の10-K表の証拠品として提出され、参照により本明細書に組み込まれる。) |
| | |
| 10.11+ | | 安進。退職計画を補充する。(2013年10月16日に施行されたことが改訂され、再決定されました。)(2014年2月24日に2013年12月31日現在の10-K表の証拠品として提出され、参照によって本明細書に組み込まれる。) |
| | |
| 10.11.1+ | | “安進補充退職計画第1改正案”は、2016年10月14日から施行された。(2016年9月30日現在の第10-Q表の証拠として2016年10月28日に提出され、引用によって本明細書に組み込まれる。) |
| | |
| 10.11.2+ | | “安進補充退職計画第2改正案”は、2019年10月23日から施行される。 (2020年2月12日に2019年12月31日現在の10-K表の証拠品として提出され、参照により本明細書に組み込まれる。) |
| | |
| 10.11.3+ | | “安進補充退職計画第3改正案”は、2021年10月20日から施行される。(2021年12月31日現在の10-K表の証拠品として2022年2月16日に提出され、参照によって本明細書に組み込まれる。) |
| | |
| 10.11.4+* | | “安進補充退職計画第4改正案”は、2022年10月20日から施行される。 |
| | |
| 10.12+ | | 安進制御権変更分流計画を改訂し,再策定した。(改正·再改訂され、2010年12月9日に施行され、その後改正され、2011年3月2日に施行された。)(2011年5月10日、2011年3月31日現在の第10-Q表の証拠として提出され、引用により本明細書に組み込まれる。) |
| | |
| 10.13+ | | 安進です。幹部は計画を激励します。(改正および改訂され、2022年1月1日から施行)(2022年3月31日現在の第10-Q表の証拠として2022年4月28日に提出され、参照によって本明細書に組み込まれる。) |
| | |
| | | | | | | | |
| 証拠品番号: | | 説明する |
| 10.14+ | | 不合格繰延補償計画を安進する。(2013年10月16日に施行されたことが改訂され、再決定されました。)(2014年2月24日に2013年12月31日現在の10-K表の証拠品として提出され、参照によって本明細書に組み込まれる。) |
| | |
| 10.14.1+ | | 安進非限定延期補償計画第1改正案が、2016年10月14日に発効した。(2016年9月30日現在の第10-Q表の証拠として2016年10月28日に提出され、引用によって本明細書に組み込まれる。) |
| | |
| 10.14.2+ | | 安進非限定延期補償計画第2改正案は、2020年1月1日に発効する。(2020年2月12日に2019年12月31日現在の10-K表の証拠品として提出され、参照により本明細書に組み込まれる。) |
| | |
| | |
| 10.14.3+ | | 安進非限定延期補償計画第3改正案は、2022年1月1日に発効する。(2021年12月31日現在の10-K表の証拠品として2022年2月16日に提出され、参照によって本明細書に組み込まれる。) |
| | |
| 10.15+ | | 飛行機分時協定は,期日は2021年12月3日であり,安進会社とロバート·A·ブラッドビルが署名した。(2021年12月31日現在の10-K表の証拠品として2022年2月16日に提出され、参照によって本明細書に組み込まれる。) |
| | |
| 10.16 | | 2回目の改正と再署名された信用協定は、日付は2019年12月12日、安進で、その中で銀行はシティバンクを行政エージェント、モルガン大通銀行はシンジケートエージェントを指定した。(8-Kフォームの証拠品として2019年12月12日に提出され、参照によって本明細書に組み込まれます。) |
| | |
| 10.16.1* | | 第2次改正と再署名された信用協定の第1号改正案は,期日は2022年12月29日であり,安進社とノースカロライナ州シティバンクが行政代理と開証行としている。 |
| | |
| 10.17 | | 橋信用協定は、期日は2022年12月12日で、シティバンク(行政代理)、アメリカ銀行(シンジケート代理)、シティバンクとアメリカ銀行(先頭手配行と帳簿管理人)及びその他の銀行が締結した。(2022年12月12日に8-K表の証拠品として提出され、参照によって本明細書に組み込まれる。) |
| | |
| 10.18 | | 定期融資信用協定は、期日は2022年12月22日であり、シティバンクが行政代理として、アメリカ銀行がシンジケート代理として、シティバンク、アメリカ銀行、ゴールドマン·サックスアメリカ銀行とみずほ銀行が先頭手配行と帳簿管理人として、ゴールドマン·サックス銀行とみずほ銀行有限公司が文書代理及びその他の銀行として署名した。(2022年12月22日に8-K表の証拠品として提出され、参照によって本明細書に組み込まれる。) |
| | |
| 10.19 | | 2002年5月10日に安進社がCelltech R&D Limitedと締結した協力·許可協定(秘密処理要求により一部の展示品が省略されている)と、2003年6月9日に発効した安進社とCelltech R&D Limitedとの連携·許可協定の第1号改正案(秘密処理要求により一部の展示品は省略されている)。(2012年12月31日現在の10-K/A表の証拠品として2013年7月31日に提出され、参照により本明細書に組み込まれる。) |
| | |
| 10.19.1 | | 2016年11月14日に施行された安進会社とCelltech R&D Limitedとの連携と許可協定の第2号改正案(秘密処理の請求により、一部の展示品は省略されている)。(2016年12月31日現在の10-K表の証拠品として2017年2月14日に提出され、参照により本明細書に組み込まれる。) |
| | |
| 10.20 | | Angen Inc.とUCB Celltechとの間の手紙プロトコルは、2019年6月25日である(それら(I)は実質的ではないので、展覧会の部分は省略されているので、(Ii)開示されていれば競争にダメージを与える)。(2019年6月30日現在の第10-Q表の証拠として2019年7月31日に提出され、引用によって本明細書に組み込まれます。) |
| | |
| 10.21 | | 提携協定は、2019年10月31日、安進社と百済神州スイス有限公司との間の協力協定、百済神州株式会社の完全子会社となる。(一部の展示品は省略されているが、それらは実質的でもなく、(Ii)開示されていれば競争に有害であるからである)。 (2020年2月12日に2019年12月31日現在の10-K表の証拠品として提出され、参照により本明細書に組み込まれる。) |
| | |
| 10.21.1 | | “協力協定第一修正案”は、2022年4月20日に安進会社、百済神州スイス有限公司、百済神州有限公司が署名した。(一部の展示品は省略されている。(I)は実質的ではないので、(Ii)は会社が個人または機密とみなす情報タイプである。)(2022年8月5日まで2022年6月30日までのForm 10-Qの証拠として提出され、参照によって本明細書に組み込まれる。) |
| | |
| | | | | | | | |
| 証拠品番号: | | 説明する |
| 10.22 | | 保険日は2019年10月31日で、百済神州有限公司と安進が共同で発行します。(2020年2月12日に2019年12月31日現在の10-K表の証拠品として提出され、参照により本明細書に組み込まれる。) |
| | |
| 10.23 | | 安進株式会社と百済神州株式会社との間で2019年10月31日に締結された株式購入契約。(一部の展示品は省略されているが、それらは実質的でもなく、(Ii)開示されていれば競争に有害であるからである)。(2020年1月8日に別表13 Dの証拠品として提出され、参照によって本明細書に組み込まれる。) |
| | |
| 10.23.1 | | 百済神州有限公司と安進が2019年12月6日に署名した株式購入協定第1号改正案。(2020年1月8日に別表13 Dの証拠品として提出され、参照によって本明細書に組み込まれる。) |
| | |
| 10.23.2 | | 百済神州株式会社と安進は2020年9月24日に株式購入協定第2号改正案を再述した(2020年9月30日現在の第10-Q表の証拠として2020年10月29日に提出され、参照によって本明細書に組み込まれる。) |
| | |
| 10.24 | | 2012年3月30日Amgen Inc.とアスリコン製薬有限公司の完全子会社アスリコン協力リスク投資会社との協力合意(一部の展示品は省略されている。(I)は実質的ではないので、(Ii)は会社が個人または機密とみなす情報タイプである。)(2022年8月5日まで2022年6月30日までのForm 10-Qの証拠として提出され、参照によって本明細書に組み込まれる。) |
| | |
| 10.24.1 | | 安進,アスリコン協力リスク投資会社とアスリコン製薬有限責任会社との間で2014年10月1日に調印された協力協定の改正案第1号(一部の展示品は省略されている。(I)は実質的ではないので、(Ii)は会社が個人または機密とみなす情報タイプである。)(2022年8月5日まで2022年6月30日までのForm 10-Qの証拠として提出され、参照によって本明細書に組み込まれる。) |
| | |
| 10.24.2 | | 2012年5月2日と27日および2016年10月2日、2018年1月31日および2020年5月15日に調印されたAmgen Inc.とAstraZeneca Collaboration Ventures,LLC間の連携協定修正案2~6(一部の展示品は省略されている。それらは実質的でもなく、(Ii)公開開示されていれば競争に有害であるからである。)(2020年6月30日現在の第10-Q表の証拠として2020年7月29日に提出され、引用により本明細書に組み込まれる。) |
| | |
| 10.24.3 | | Amgen Inc.とAstraZeneca Collaboration Ventures,LLCの間で2020年12月17日に署名された協力協定の第7号改正案(一部の展示品は省略されている。それらは実質的でもなく、(Ii)公開開示されていれば競争に有害であるからである。)(2020年12月31日現在の年間10-K表の証拠品として2021年2月9日に提出され、参照により本明細書に組み込まれる。) |
| | |
| 10.24.4 | | 安進社とアスリコン協力リスク投資会社との間で2021年11月19日に調印された協力協定の改正案第8号(一部の展示品は省略されている。(I)は実質的ではないので、(Ii)は会社が個人または機密とみなす情報タイプである。)(2021年12月31日現在の10-K表の証拠品として2022年2月16日に提出され、参照によって本明細書に組み込まれる。) |
| | |
| 10.25 | | 許可と協力協定は、期日は2021年6月1日であり、Amgen Inc.とKyowa麒麟Co.,Ltd.によって署名された(一部の展示品は省略されているが、それらは実質的でもなく、(Ii)開示されていれば競争に有害であるからである)。(2021年6月30日現在の第10-Q表の証拠として2021年8月4日に提出され、参照によって本明細書に組み込まれる。) |
| | |
| 21* | | 当社の付属会社です。 |
| | |
| 23 | | 独立公認会計士事務所が同意します。本10-K年度報告書91ページに掲載することに同意した。 |
| | |
| 24 | | 授権書。許可書は本年度報告書の表格10-K 92ページに掲載されている。 |
| | |
| 31* | | ルール13 a-14(A)証明書. |
| | |
| 32** | | 1350節認証。 |
| | |
| 101.INS | | 連結されたXBRLインスタンス文書−インスタンス文書は、そのXBRLタグがイントラネットXBRL文書に埋め込まれているので、相互作用データファイルには現れない。 |
| | |
| 101.SCH* | | インラインXBRL分類拡張アーキテクチャ文書. |
| | |
| | | | | | | | |
| 証拠品番号: | | 説明する |
| 101.CAL* | | インラインXBRL分類拡張はリンクベース文書を計算する. |
| | |
| 101.DEF* | | XBRLソート拡張を連結してLinkbase文書を定義する. |
| | |
| 101.LAB* | | XBRL分類拡張ラベルLinkbase文書を連結する. |
| | |
| 101.PRE* | | XBRL分類拡張プレゼンテーションLinkbaseドキュメントを内部接続する. |
| | |
| 104 | | 表紙対話データファイル(添付ファイル101に含まれるイントラネットXBRLのフォーマット)。 |
____________________________
(*=通信アーカイブ付き)
(*=付箋提供、改正された1934年証券取引法第18条施行のための“提出”ではありません)
(+=契約または補償計画またはスケジュールを管理する)
適用されません。
サイン
1934年の証券取引法の要求によると、登録者は本年度報告を正式に許可した署名者が代表して署名することを正式に促した。
| | | | | | | | | | | | | | |
| | 安進。 |
| | (登録者) |
| | | | |
| 日付: | 2023年2月9日 | 差出人: | | /s/ピーター·H·グリフィス |
| | | | ピーター·H·グリフィス |
| | | | 常務副総裁兼首席財務官 |
| | | | (首席財務官) |
添付ファイル23
独立公認会計士事務所の同意
私たちは、以下の登録声明で登録が成立することを引用することに同意します
•安進の登録声明(表S-3第333-236351号)
•安進の登録に関する声明(表S-8第333-159377号)。2009年の株式インセンティブ計画の改訂と再改訂、
•安進の登録声明(S-8表第33-39183号)について
•安進退職·貯蓄計画に関する登録声明(表S-8第33-39104号、表S-8第333-144581及び333-216719号改訂)
•安進製造株式会社の退職·貯蓄計画(前身は安進製造会社の退職·貯蓄計画)に関する登録声明(S-8表33-47605、333-144580、333-216715)、
•安進非制限繰延賠償計画に関する登録声明(表S-8第333-81284、第333-177868、第333-216723及び第333-260723号)、及び
•アイルランド従業員安入利益共有計画に関する登録表(表S-8第333-176240及び第333-260724号);
我々の2023年2月9日の報告では,安進会社の連結財務諸表と,安進会社の2022年12月31日までの年次報告(Form 10−K)における安進会社財務報告の内部統制の有効性に触れている。
/S/安永法律事務所
カリフォルニア州ロサンゼルス
2023年2月9日
添付ファイル24
授権依頼書
私はすべての男性と女性を知っています。以下に署名したすべての人は、ロバート·A·ブラッドビル、ピーター·H·グリフィス、ジョナサン·P·グレアム、またはそれらのいずれかを構成し、任命する権利があり、彼らのいずれも、任意のおよびすべての身分で彼または彼女を代替または再置換し、本報告書の任意の修正に署名し、それを証拠品および他の関連文書と共にアメリカ証券取引委員会に提出し、上述したすべての事実上の弁護士、または彼または彼女の1人以上の代替弁護士を承認し、確認する権利がある。この規定によって作られたり手配されたりすることができる。
1934年の証券取引法の要求によると、本報告は、次の日に登録者として次の日に署名された
| | | | | | | | | | | | | | |
| サイン | | タイトル | | 日取り |
| | | | |
| ロバート·A·ブラッドウェイ | | 取締役会長、最高経営責任者
社長、役員
(首席行政主任) | | 2/9/2023 |
| ロバート·A·ブラッドウェイ | | | |
| | | | |
| /S/ピーターH.Griffith | | 常務副秘書長総裁と
首席財務官
(首席財務官) | | 2/9/2023 |
| ピーター·H·グリフィス | | | |
| | | | |
| /S/リンダH.Louie | | 総裁副財務長
首席会計官
(首席会計主任) | | 2/9/2023 |
| リンダ·H·ルイ | | | |
| | | | |
| /S/万達·M·オースティン | | 役員.取締役 | | 2/9/2023 |
| 万達·M·オースティン | | | | |
| | | | |
| /S/Michael V.Drake | | 役員.取締役 | | 2/9/2023 |
| マイケル·V·ドレック | | | | |
| | | | |
| /S/Brian J.Druker | | 役員.取締役 | | 2/9/2023 |
| ブライアン·J·ドラッカー | | | | |
| | | | |
| ロバート·A·エクター | | 役員.取締役 | | 2/9/2023 |
| ロバート·エクター | | | | |
| | | | |
| /S/グレッグ·C·ガラン | | 役員.取締役 | | 2/9/2023 |
| グレッグ·C·ガラン | | | | |
| | | | |
| チャールズ·M·ホリーJr. | | 役員.取締役 | | 2/9/2023 |
| チャールズ·M·ホーリー | | | | |
| | | | |
| /S/S.オマール·イシュラック | | 役員.取締役 | | 2/9/2023 |
| S·オマール·イシュラック | | | | |
| | | | |
| /S/テイラー·ジャック | | 役員.取締役 | | 2/9/2023 |
| テイラー·ジャックス | | | | |
| | | | |
| /S/Ellen J.Kullman | | 役員.取締役 | | 2/9/2023 |
| アラン·J·コールマン | | | | |
| | | | |
| /エイミー·E·マイルズ | | 役員.取締役 | | 2/9/2023 |
| エイミー·E·マイルズ | | | | |
| | | | |
| /S/ロナルド·D·砂糖 | | 役員.取締役 | | 2/9/2023 |
| ロナルド·D·スガー | | | | |
| | | | |
| サンダース·ウィリアムズ | | 役員.取締役 | | 2/9/2023 |
| サンダース·ウィリアムズ | | | | |
独立公認会計士事務所報告
安進の株主と取締役会へ。
財務諸表のいくつかの見方
添付されている安進(当社)の2022年12月31日現在、2022年12月31日および2021年12月31日までの連結貸借対照表、2022年12月31日までの各年度に関する総合収益表、全面収益表、株主権益表とキャッシュフロー表、および指数15(A)の2項目に記載されている関連付記と財務諸表(総称して“連結財務諸表”と呼ぶ)を監査した。総合財務諸表は、すべての重要な面で、2022年12月31日、2022年12月31日、2021年12月31日までの会社の財務状況、および2022年12月31日までの3年度の経営結果とキャッシュフローを公平に反映しており、米国公認会計原則に適合していると考えられる。
また、米国上場企業会計監督委員会(PCAOB)の基準に基づき、テレデビル委員会協賛組織委員会が発表した“内部統制-総合枠組み(2013枠組み)”で確立された基準に基づいて、2022年12月31日までの財務報告内部統制を監査し、2023年2月9日に発表された報告書について保留意見を発表した。
意見の基礎
これらの財務諸表は会社の経営陣が責任を負う。私たちの責任は私たちの監査に基づいて会社の財務諸表に意見を発表することです。私たちはPCAOBに登録されている公共会計士事務所で、アメリカ連邦証券法およびアメリカ証券取引委員会とPCAOBの適用規則と法規に基づいて、私たちは会社と独立しなければなりません
私たちはPCAOBの基準に従って監査を行っている。これらの基準は、財務諸表に重大な誤報がないかどうかに関する合理的な保証を得るために、エラーによるものであっても不正であっても、監査を計画し、実行することを要求する。我々の監査には、財務諸表の重大な誤報リスクを評価するプログラム、エラーによるものであれ詐欺であっても、これらのリスクに対応するプログラムを実行することが含まれています。これらの手続きは、財務諸表中の金額および開示に関連する証拠をテストに基づいて検討することを含む。我々の監査には、経営陣が使用する会計原則の評価と重大な見積もり、財務諸表の全体列報を評価することも含まれています。私たちは私たちの監査が私たちの観点に合理的な基礎を提供すると信じている。
重要な監査事項
以下に述べる重要な監査事項とは、監査委員会に伝達または要求が監査委員会に伝達された当期財務諸表監査によって生じる事項である:(1)財務諸表に対して重大な意義を有する勘定または開示に関するものであり、(2)特に挑戦的で主観的または複雑な判断に関するものである。重要な監査事項の伝達は、総合財務諸表に対する私たちの全体的な意見をいかなる方法でも変えることはなく、以下の重要な監査事項を伝達することによって、重要な監査事項またはそれに関連する勘定または開示について個別の意見を提供することもない。
| | | | | | | | |
| | 販売減額 |
関係事項の記述 | | 同社が記録した売上は2022年12月31日現在、60億ドルに減額された。財務諸表に付記されている1“製品販売および販売減額”に記載されているように、製品販売収入は、販売時に決定された推定リベート、卸売業者返金、割引、および他の減額(総称して販売減額)を計算した後に確認されるべき純額である。 監査製品売上高から差し引かれた販売控除額の見積もりは複雑であり、重大な判断が必要であり、また関連する金額は財務諸表全体にとって重要である。製品販売収入は,製品制御権が顧客に譲渡された場合に確認され,通常は納入時に確認され,会社が獲得する権利があると予想される対価格を反映した金額,すなわち推定販売控除対象金額を差し引いた金額に基づく.推定された販売控除額は、現在の契約および法律要件、市場イベントおよび傾向、内部および外部履歴データ、および予測された顧客購入モデルに基づく。 |
| | |
私たちが監査でどのようにこの問題を解決したのか | | 我々は,販売控除フローの内部制御について理解し,内部制御の操作有効性を設計·テストした.これには、実際の売上高、契約条項、歴史的経験、卸売在庫レベル、需要データ、および推定された患者数を含む、管理層審査が推定販売減額に使用される重要な仮定および入力のテスト制御が含まれる。著者らはまた、管理層の需要活動予測の正確性の制御、及び最終販売減額推定に含まれる重要な構成部分の完全性と正確性をテストした 経営陣の推定販売控除額をテストするために、経営陣のそれぞれの見積もりの計算を取得し、以下の手順などを実行した。我々は、推定された計算すべき残高の独立した予想を確立することによって、管理層が記録した計算すべき残高を履歴支払い傾向に隠された残高と比較することを含む管理層の販売割引課税残高の決定に関する推定プロセスをテストし、実際の履歴データを用いて回顧分析を実行して予測金額を評価し、後続のイベントを評価して、初期計算項目を調整する必要がある新しい情報が存在するかどうかを決定し、実際の販売および割引残高の傾向を評価し、現金領収書と製品販売を比較し、契約サンプルの条項と条件を確認し、年間発行と支払いの信用サンプルをテストし、基本契約条項と合意した。 |
| | |
| | | | | | | | |
| | 未確認税収割引 |
| 関係事項の記述 | | 総合財務諸表付記1及び付記6で述べたように、当社は異なる司法管轄区で経営しており、その中で複雑な税務法律及び法規の異なる解釈に不確定性を与えるため、重大な判断を用いて、当社と異なる司法管轄区(“移転定価”)の間に利益を分配することに関する未確認税務利益(“移転定価”)を決定する必要があり、特に当社に大量の資産と業務を持つアメリカ連邦税務司法管轄区を決定する必要がある。この点で,当社は,(1)税務状況の技術的優位性が持続可能であるかどうか,および(2)有資格確認の税収割引額を測定するために重大な判断を用いている。同社は2022年12月31日現在、譲渡定価に関する税収割引を含む38億ドルの未確認税収割引総額を蓄積している。会社が確認していない税収利益の技術的利点と評価を監査することは挑戦的であり、複雑で高度に判断される可能性があり、税収法律と法規の解釈およびこれらの解釈の会社の事実と状況への応用に基づいている。 |
| | |
| 私たちが監査でどのようにこの問題を解決したのか | | 我々は、内部制御の設計を理解、評価し、内部制御の動作有効性をテストし、当社がその税務状況を評価する技術的利点の流れと、管理層がそれなどの税務状況を測定する未確認税務利益の流れ、特に譲渡定価の面で評価した。これには、管理職の審査投入、計算、仮説、および方法の制御をテストすることが含まれ、これらの投入、計算、仮説、および方法は、確認資格に適合する税金割引金額を測定するために選択される 私たちは税務と譲渡定価の専門家を招いて技術的優位性の評価に協力し、会社のいくつかの確認されていない税収優遇を測定する。特定の税務状況の性質および関連税務機関との発展に応じて、当社とそのような税務機関との通信の取得と審査と、当社の評価·記録を支援する立場を支援するための第三者の提案を評価することが含まれています。吾らは、譲渡定価に関する所得税法律及び法規に関する我々の知識及び経験を利用して、当社の税務利益が確認されていない会計処理を評価している。私たちは、会社の記録の頭寸への潜在的な影響を評価するために、規制環境を適用した発展を評価した。私たちは現在の税務論争、訴訟、税務訴訟の傾向に対する管理職の考慮を評価した。私たちは、企業が確認する税金優遇金額を決定する際に使用する仮説とデータを分析し、適用される利息と罰金を含め、これらの基本計算の正確性をテストした。私たちもこのような事項について当社が付記6に記載されている所得税の開示を評価しました。 |
| | |
| | /s/ 安永法律事務所 |
1980年以来、当社の監査役を務めてきました。
カリフォルニア州ロサンゼルス
2023年2月9日
安進。
合併損益表
2022年、2021年、2020年12月31日までの年度
(単位:百万、1株当たりのデータを除く)
| | | | | | | | | | | | | | | | | |
| 2022 | | 2021 | | 2020 |
| 収入: | | | | | |
| 製品販売 | $ | 24,801 | | | $ | 24,297 | | | $ | 24,240 | |
| その他の収入 | 1,522 | | | 1,682 | | | 1,184 | |
| 総収入 | 26,323 | | | 25,979 | | | 25,424 | |
| | | | | |
| 運営費用: | | | | | |
| 販売コスト | 6,406 | | | 6,454 | | | 6,159 | |
| 研究開発 | 4,434 | | | 4,819 | | | 4,207 | |
| 現在行われている研究と開発を買収する | — | | | 1,505 | | | — | |
| 販売、一般、行政 | 5,414 | | | 5,368 | | | 5,730 | |
| 他にも | 503 | | | 194 | | | 189 | |
| 総運営費 | 16,757 | | | 18,340 | | | 16,285 | |
| | | | | |
| 営業収入 | 9,566 | | | 7,639 | | | 9,139 | |
| | | | | |
| その他の収入(支出): | | | | | |
| 利子支出,純額 | (1,406) | | | (1,197) | | | (1,262) | |
| その他の収入,純額 | (814) | | | 259 | | | 256 | |
| | | | | |
| 所得税前収入 | 7,346 | | | 6,701 | | | 8,133 | |
| | | | | |
| 所得税支給 | 794 | | | 808 | | | 869 | |
| | | | | |
| 純収入 | $ | 6,552 | | | $ | 5,893 | | | $ | 7,264 | |
| | | | | |
| 1株当たりの収益: | | | | | |
| 基本的な情報 | $ | 12.18 | | | $ | 10.34 | | | $ | 12.40 | |
| 薄めにする | $ | 12.11 | | | $ | 10.28 | | | $ | 12.31 | |
| | | | | |
| 1株当たりの収益を計算する際に使用する株: | | | | | |
| 基本的な情報 | 538 | | 570 | | 586 |
| 薄めにする | 541 | | 573 | | 590 |
添付の説明を参照してください。
安進。
総合総合収益表
2022年、2021年、2020年12月31日までの年度
(単位:百万)
| | | | | | | | | | | | | | | | | |
| 2022 | | 2021 | | 2020 |
| 純収入 | $ | 6,552 | | | $ | 5,893 | | | $ | 7,264 | |
| 再分類調整と税引き後の他の全面収益(損失): | | | | | |
| 外貨換算収益 | 496 | | | (135) | | | 9 | |
| 現金流動保証収益(赤字) | 67 | | | 324 | | | (438) | |
| 証券売却可能な損失 | — | | | (1) | | | (21) | |
| 他にも | 2 | | | 1 | | | (7) | |
| その他総合収益(損失)、税引き後純額 | 565 | | | 189 | | | (457) | |
| 総合収益 | $ | 7,117 | | | $ | 6,082 | | | $ | 6,807 | |
添付の説明を参照してください。
安進。
合併貸借対照表
2022年12月31日と2021年12月31日
(単位:百万、1株当たりのデータを除く)
| | | | | | | | | | | |
| 2022 | | 2021 |
| 資産 |
| 流動資産: | | | |
| 現金と現金等価物 | $ | 7,629 | | | $ | 7,989 | |
| 有価証券 | 1,676 | | | 48 | |
| 売掛金純額 | 5,563 | | | 4,895 | |
| 棚卸しをする | 4,930 | | | 4,086 | |
| その他流動資産 | 2,388 | | | 2,367 | |
| 流動資産総額 | 22,186 | | | 19,385 | |
| | | |
| 財産·工場·設備·純価値 | 5,427 | | | 5,184 | |
| 無形資産、純額 | 16,080 | | | 15,182 | |
| 商誉 | 15,529 | | | 14,890 | |
| 他の非流動資産 | 5,899 | | | 6,524 | |
| 総資産 | $ | 65,121 | | | $ | 61,165 | |
| | | |
| 負債と株主権益 |
| 流動負債: | | | |
| 売掛金 | $ | 1,572 | | | $ | 1,366 | |
| 負債を計算すべきである | 12,524 | | | 10,731 | |
| 長期債務の当期部分 | 1,591 | | | 87 | |
| 流動負債総額 | 15,687 | | | 12,184 | |
| | | |
| 長期債務 | 37,354 | | | 33,222 | |
| | | |
| 長期納税義務 | 5,757 | | | 6,594 | |
| 他の非流動負債 | 2,662 | | | 2,465 | |
| | | |
| あるいは事項と支払いがあります | | | |
| | | |
| 株主権益: | | | |
普通株式と追加実収資本0.0001一株当たりの額面2,750.0授権株534.02022年と558.32021年の株 | 32,514 | | | 32,096 | |
| 赤字を累計する | (28,622) | | | (24,600) | |
| その他の総合損失を累計する | (231) | | | (796) | |
| 株主権益総額 | 3,661 | | | 6,700 | |
| 総負債と株主権益 | $ | 65,121 | | | $ | 61,165 | |
添付の説明を参照してください。
安進。
合併株主権益報告書
2022年、2021年、2020年12月31日までの年度
(単位:百万、1株当たりのデータを除く)
| | | | | | | | | | | | | | | | | | | | | | | | | | | | | |
| 番号をつける
の株
普通のもの
在庫品 | | ごく普通である
株と
その他の内容
実収資本 | | 積算
赤字.赤字 | | 積算
他にも
全面的に
収入を損ねる | | 合計する |
| 2019年12月31日現在の残高 | 591.4 | | | $ | 31,531 | | | $ | (21,330) | | | $ | (528) | | | $ | 9,673 | |
税引後会計原則変動の累積影響 | — | | | — | | | (2) | | | — | | | (2) | |
| 純収入 | — | | | — | | | 7,264 | | | — | | | 7,264 | |
| その他総合損失、税引き後純額 | — | | | — | | | — | | | (457) | | | (457) | |
普通株発表の配当金6.561株当たり) | — | | | — | | | (3,843) | | | — | | | (3,843) | |
会社持分奨励計画に関する普通株式発行 | 2.1 | | | 91 | | | — | | | — | | | 91 | |
| 株に基づく報酬費用 | — | | | 349 | | | — | | | — | | | 349 | |
従業員の株式報酬支出に関する税収の影響 | — | | | (169) | | | — | | | — | | | (169) | |
| 普通株買い戻し | (15.2) | | | — | | | (3,497) | | | — | | | (3,497) | |
| 2020年12月31日の残高 | 578.3 | | | 31,802 | | | (21,408) | | | (985) | | | 9,409 | |
| | | | | | | | | |
| 純収入 | — | | | — | | | 5,893 | | | — | | | 5,893 | |
| その他の総合収益、税引き後純額 | — | | | — | | | — | | | 189 | | | 189 | |
普通株発表の配当金7.221株当たり) | — | | | — | | | (4,098) | | | — | | | (4,098) | |
会社持分奨励計画に関する普通株式発行 | 1.7 | | | 82 | | | — | | | — | | | 82 | |
| 株に基づく報酬費用 | — | | | 361 | | | — | | | — | | | 361 | |
従業員の株式報酬支出に関する税収の影響 | — | | | (149) | | | — | | | — | | | (149) | |
| 普通株買い戻し | (21.7) | | | — | | | (4,987) | | | — | | | (4,987) | |
| 2021年12月31日現在の残高 | 558.3 | | | 32,096 | | | (24,600) | | | (796) | | | 6,700 | |
| | | | | | | | | |
| 純収入 | — | | | — | | | 6,552 | | | — | | | 6,552 | |
| その他の総合収益、税引き後純額 | — | | | — | | | — | | | 565 | | | 565 | |
普通株発表の配当金7.951株当たり) | — | | | — | | | (4,264) | | | — | | | (4,264) | |
会社持分奨励計画に関する普通株式発行 | 1.8 | | | 138 | | | — | | | — | | | 138 | |
| 株に基づく報酬費用 | — | | | 419 | | | — | | | — | | | 419 | |
従業員の株式報酬支出に関する税収の影響 | — | | | (139) | | | — | | | — | | | (139) | |
| 普通株買い戻し | (26.1) | | | — | | | (6,310) | | | — | | | (6,310) | |
| | | | | | | | | |
| 2022年12月31日現在の残高 | 534.0 | | | $ | 32,514 | | | $ | (28,622) | | | $ | (231) | | | $ | 3,661 | |
添付の説明を参照してください。
安進。
統合現金フロー表
2022年、2021年、2020年12月31日までの年度
(単位:百万)
| | | | | | | | | | | | | | | | | |
| 2022 | | 2021 | | 2020 |
| 経営活動のキャッシュフロー: | | | | | |
| 純収入 | $ | 6,552 | | | $ | 5,893 | | | $ | 7,264 | |
| 減価償却、償却その他 | 3,417 | | | 3,398 | | | 3,601 | |
| 株に基づく報酬費用 | 401 | | | 341 | | | 330 | |
| 所得税を繰延する | (1,198) | | | (453) | | | (287) | |
| 現在行われている研究と開発を買収する | — | | | 1,505 | | | — | |
| 権益法投資の調整 | 891 | | | 33 | | | 65 | |
| 資産剥離損失 | 567 | | | — | | | — | |
| その他のプロジェクト、純額 | (176) | | | (262) | | | (260) | |
| 経営性資産と負債の変動、買収を差し引く: | | | | | |
| 売掛金純額 | (746) | | | (429) | | | (427) | |
| 棚卸しをする | (742) | | | (165) | | | (215) | |
| その他の資産 | 258 | | | (237) | | | 129 | |
| 売掛金 | 154 | | | (69) | | | 45 | |
| 課税所得税純額 | (647) | | | (854) | | | (249) | |
| 長期納税義務 | 229 | | | 204 | | | (482) | |
| その他負債 | 761 | | | 356 | | | 983 | |
| 経営活動が提供する現金純額 | 9,721 | | | 9,261 | | | 10,497 | |
| 投資活動によるキャッシュフロー: | | | | | |
| 有価証券を購入する | (2,587) | | | (8,900) | | | (8,477) | |
| 有価証券を売却して得られる収益 | 98 | | | 4,403 | | | 2,597 | |
| 有価証券満期日収益 | 1,120 | | | 8,831 | | | 4,381 | |
| 家屋·工場·設備を購入する | (936) | | | (880) | | | (608) | |
| 買収のために支払った現金を差し引く | (3,839) | | | (2,529) | | | — | |
| 購買権益法投資 | (18) | | | (157) | | | (3,219) | |
| 業務剥離収益は、剥離現金を差し引いた純額です | 130 | | | — | | | — | |
| 他にも | (12) | | | (35) | | | (75) | |
| 投資活動が提供する現金純額 | (6,044) | | | 733 | | | (5,401) | |
| 資金調達活動のキャッシュフロー: | | | | | |
| 債券発行の純収益 | 6,919 | | | 4,945 | | | 8,914 | |
| 債務の弁済 | (297) | | | — | | | — | |
| 債務を返済する | — | | | (4,150) | | | (6,450) | |
| 普通株買い戻し | (6,360) | | | (4,975) | | | (3,486) | |
| 支払済み配当金 | (4,196) | | | (4,013) | | | (3,755) | |
| | | | | |
| 他にも | (103) | | | (78) | | | (90) | |
| 融資活動のための現金純額 | (4,037) | | | (8,271) | | | (4,867) | |
| 現金および現金等価物の増加 | (360) | | | 1,723 | | | 229 | |
| 年初現金および現金等価物 | 7,989 | | | 6,266 | | | 6,037 | |
| 年末現金および現金等価物 | $ | 7,629 | | | $ | 7,989 | | | $ | 6,266 | |
添付の説明を参照してください。
安進。
連結財務諸表付記
2022年12月31日
1. 重要会計政策の概要
業務.業務
安進(その子会社、略称“安進”、“当社”、“私たち”、“私たち”あるいは“私たち”)は発見、開発、製造と革新的な人類療法を提供するグローバルバイオテクノロジーの先駆者である。私たちの業務は1つはビジネスプレート:人間治療学
合併原則
連結財務諸表には安進及びその持株子会社の勘定が含まれている。私たちが可変利益実体の主要な受益者であるかどうかを決定する時、私たちは実体の活動を指導する権利があるかどうかを考慮し、その実体の経済表現に最も重大な影響を与え、またその実体の損失を負担する義務があり、あるいはその実体からその実体に対して重大な意義を持つ可能性のある利益を得る権利がある。私たちは私たちがその主な受益者である任意の可変利益実体の中に重大な権利がない。すべての重要な会社間取引と残高は合併で流された。
予算の使用
公認会計基準に従って連結財務諸表を作成することは、合併財務諸表と付記中の報告書の金額に影響を与えるために、経営陣に推定と仮定を要求する。実際の結果はこれらの推定とは異なる可能性がある。
収入.収入
製品売上高と販売控除額
製品販売収入は、製品制御権が顧客に譲渡される際に確認され、通常、交付時には、私たちが獲得する権利があることが予想される対価格を反映した金額に基づいて、推定リベート、卸返金、割引、その他の控除(総称して販売控除と呼ぶ)と販売時に決定された返金後の課税項目を差し引く。
私たちは四半期ごとに販売減額計算項目の十分性を分析します。傾向または重大なイベントが調整が適切であることを示す場合には、販売減額の課税金額を調整する。応募項目も実際の結果を反映するように調整した。販売減額の課税費用は、主に関連販売で稼いだ金額や精算すべき金額の見積もりに基づいている。これらの推定は、現在の契約および法的要件、特定の既知の市場イベントおよび傾向、内部および外部履歴データ、および予測された顧客購入パターンを考慮する。販売控除額は基本的に製品に特定されるため,任意の所与の時期に販売製品の組合せの影響を受ける.売上高控除には見積数の変化による前期売上高に関する非実質的純額調整が含まれています。
返品は履歴返品データを生産ロットに基づく関連販売と比較することで推定される。履歴収益率は、各製品のために決定され、適切なときに、各製品に固有の市場の既知または予想変化に応じて調整される。歴史的に見ると、販売返品準備金の総額は1総売上高の%を占めています。歴史的には、前期販売差し戻し準備金見積もりの変化は重要ではない。
私たちの支払い条件はお客様のタイプと場所、提供される製品やサービスによって異なります。支払い条件は管轄区域とお客様によって異なりますが、通常支払いを要求する期限は30至れり尽くせり120船積み日から又は義務履行日からの日数。いくつかの製品またはサービスおよびいくつかの顧客タイプについては、お客様に製品を渡す前に、またはサービスを提供する前に支払いを要求することができます。
顧客から受け取って政府当局に送金する会社の製品販売に関する間接税は、主にヨーロッパであり、収入には含まれていない。
実際の便宜策として、販売手数料は、償却期間が本来1年以下であるため、発生時に差し引かれる。これらのコストは統合損益表のSG&A費用に記録される.
その他の収入
他の収入には主に特許使用料収入と会社パートナー収入が含まれる。被許可者の印税は,ライセンス製品の第三者販売に基づいており,関連第三者製品販売が発生したときに記録される。特許使用料収入は歴史と予測された販売傾向に基づいて推定される。企業パートナーの収入は主にライセンス料と儲けのマイルストーンと私たちの協力から生じるビジネス利益シェアからなります。以下に議論する多重履行義務手配を参照する.
多重義務履行の手配を持つ
私たちは時々製品と候補製品の研究開発、製造、および/または商業化について合意した。このような構成は、知的財産権/許可、研究開発サービス、製造サービス、および/または商業化サービスを含む様々な権利、サービスおよび/または商品を提供することを必要とする場合がある。これらの手配の基本条項は、通常、払戻できない前払い許可料、開発および商業業績マイルストーン支払い、特許権使用料および/または利益共有の形態で安進に考慮を提供する。
1つ以上の履行義務に関連する手配では、各要求の履行義務は、固有の履行義務として資格があるかどうかを決定するために評価され、その根拠は、(I)顧客が単独で、または他のいつでも利用可能なリソースと共に貨物またはサービスから利益を得ることができ、(Ii)貨物またはサービスを契約内の他の約束とは別に識別することができるということである。この手配された対価格は、その後、それぞれの相対的に独立した販売価格に応じて、個々の異なる履行義務に割り当てられる。個々の成果の推定販売価格は,納入可能成果の定期独立販売に対する我々の最適な推定を反映しているか,あるいは独立販売価格がない場合には,調整された市場評価方法を用いる.
関連貨物またはサービスの制御権が移転した場合、項目ごとに異なる履行義務に割り当てられた対価格が収入として確認される。確認された累積収入が大きく逆転しない可能性が高い場合には,リスク実質的業績マイルストーンに関する対価格が収入として確認される。我々は、知的財産権許可による取り決めにおいて、販売及び使用に基づく特許権使用料例外を利用して、基礎販売発生時に特許権使用料又は利益共有による収入を確認する。
研究開発コスト
研究開発コストは発生時にコストを計上し、主に賃金、福祉及びその他の従業員に関連するコスト;施設と管理費用;臨床試験及び関連する臨床製造コスト;契約サービス及びその他の外部コスト;情報システムコスト;及び研究開発のために使用した購入した技術を償却して後日の他の用途に供する。研究開発費には、第三者研究開発計画に関する費用とコスト回収も含まれており、第三者に支払われる技術実行可能性や将来代替用途のない技術に関する前払い費用やマイルストーンが含まれている。債務が発生したり、コストを回収する権利がある場合は、研究開発費の純支払いまたは返済を確認します。付記8を参照し、協力する。
販売、一般、行政費用
SG&Aコストは、主に販売およびマーケティング、財務、法律および他の行政関係者に関連する賃金、福祉および他の従業員に関連するコスト、施設および管理費用、外部マーケティング、広告および法律費用、米国医療改革がブランド処方薬メーカーおよび輸入業者に徴収する連邦消費税、およびその他の一般的および行政コストを含む。広告費用は発生時に費用を計上し、実際は#ドルである841百万、$843百万ドルとドル9622022年12月31日、2021年、2020年12月31日までの年間で、それぞれ100万ドル。SG&A費用には、いくつかの協力手配下のマーケティングと普及作業に関連するコストとコスト回収も含まれている。債務が発生した場合やコストを回収する権利がある場合は、SG&A費用の純支払いまたは精算を確認します。付記8を参照し、協力する。
賃貸借証書
契約の開始時、私たちは一つの手配がレンタルであるか、あるいはレンタルを含むかどうかを確認します。すべてのレンタルについて、経営性あるいは融資性に分類することを確定しました。経営リースは、バランスシートの他の非流動資産、負債、その他の非流動負債を総合的に計上しています。
ROU資産は私たちがレンタル期間内に対象資産を使用する権利を表し、リース負債は私たちが賃貸に応じてレンタル金を支払う義務を代表します。リース確認は開始日に発生し、リース負債金額はレンタル期間内に支払われたリース支払いの現在値に基づいている。私たちのレンタル条項には、私たちがその選択権を行使することを合理的に決定する時に、レンタル契約を延長または終了する選択権が含まれているかもしれません。私たちのほとんどの賃貸契約は暗黙的な金利を決定するために情報を提供しないので、私たちは増加借款金利を使用して賃貸支払いの現在値を決定します。ROU資産には、開始日前に支払われた任意のレンタル支払いから受信されたレンタル報酬を減算することも含まれる。経営リース費用はレンタル期間内に直線法で確認します。
私たちはレンタルと非レンタル構成要素の両方とレンタル契約を持っています。この2つの構成要素は通常1つのレンタル構成要素として計算されます。また、ある車両と設備レンタルについては、ポートフォリオ方法を適用してレンタル期間と割引率を決定します。
株に基づく報酬
株式ベースの報酬計画があり、この計画によると、RSU、業績単位、株式オプションを含む様々な株式ベースの奨励を与えることができる。RSUと株式オプション報酬の公正価値は,階層的に帰属するサービス条件のみの影響を受け,一般にサービス期間内に補償費用として直線的に確認され,推定された没収が差し引かれる.業績単位報酬の公正価値は報酬支出として確認され、一般的に直線をもとに、授与日から業績期間が終了する。付記4を参照して、株の報酬に基づく。
所得税
私たちは税引前収入と私たちが経営している各管轄区の適用税率に基づいて所得税を計算します。私たちの所得税と所得税の資産と負債の準備を決定する際には、会計原則の評価と複雑な税法の適用における不確実性を含む重大な判断が必要だ。繰延所得税は、資産と負債基盤との間の一時的な差異による予期される税務結果、および財務報告目的のために繰り越された損失と税額控除、および所得税目的で確認された金額について記録される。私たちは私たちの繰延税金資産をより実現可能な将来の税金優遇金額に減らすための推定準備金を記録した。
税務機関が税務状況の技術的利点に基づいて審査を行った後、さらにその税務状況を維持する可能性がある場合にのみ、不確定税務状況からの税務利益を確認する。連結財務諸表で確認されたある特定の税務状況の税収割引は、最も実現可能な税収割引に基づいている。違例違約金の額は、現行税法の重大な改正、税務機関の新規定或いは解釈、税務審査期間中に取得した新しい資料或いは審査結果など、事実と状況の変化に応じて適切に調整される。私たちは適切な時に所得税支出における違約金に関する計算利息と罰金を確認します。付記6、所得税を参照。
買収する
私たちはまず、買収した一連の資産が企業を構成するかどうか、企業合併として入金すべきかどうかを決定する。買収した資産が企業を構成していなければ、当該取引を資産買収として会計処理する。企業合併は会計買収法を用いて計算される。買収方法によると、買収された資産(知的財産権研究開発プロジェクトを含む)と負担した負債は、買収日にそれぞれの公正価値で総合財務諸表に入金される。譲渡の価格の公正価値が取得した純資産の公正価値の部分を超えて営業権に計上される。業務合併に関連して発生した又は対価格債務(買収前に完了した買収により被買収者が負担した負債を含む)は、買収日にその公正価値で入金され、その後の各報告期間において、関連事項が解決されるまで、その公正価値に従って再計量される。これにより生じた公正価値変動は収益に計上される.対照的に、資産買収はコスト累積と分配モデルを用いて計算される。このようなモデルでは、買収のコストは買収された資産と負担する負債に割り当てられる。将来的に他の用途のない知的財産権研究開発プロジェクトは買収時に研究開発費を計上し、資産買収に関連して発生する或いは価格義務が発生する可能性があり、合理的に推定できる場合に計上する。付記2、買収及び資産剥離、及び付記17、公正価値計量を参照。
現金等価物
現金等価物とは,流動性が高く,現金に変換しやすく,購入日から3カ月以内に満期になる投資のみを指すと考えられる。
利上げ証券
我々の配当証券ポートフォリオは売却可能であると考えられるため,これらの投資は公正価値で記録されており,収益や損失はAOCIに記録されていない.総合貸借対照表では、満期日が1年を超える投資が短期有価証券に分類される可能性があるが、これは、高い流動性を有し、当社が現在の業務に利用可能な投資を表しているからである。付記9、投資、付記17、公正価値計量を参照。
棚卸しをする
在庫はコストまたは現金化可能な純価値の中で低いものに記載します。コストは、材料、人工および間接費用に関する金額を含み、先進的な先出し方法に近い方法で決定される。現金化可能な純価値とは、正常な業務過程で推定された販売価格から合理的に予測された完成、処分と輸送コストを差し引くことである。付注10、在庫を参照。
派生商品
私たちは総合貸借対照表で公正な価値ですべての派生ツールが資産または負債であることを確認した。派生ツールの公正価値変動の会計処理は、派生ツールが正式に適用会計基準下のヘッジ関係の一部として指定され、条件を満たしているかどうかに依存し、更にヘッジ関係のタイプに依存する。ヘッジされたデリバティブが正式に指定された場合,開始時とその後の四半期にヘッジされたバリュー項目の公正価値やキャッシュフローの変化を相殺する上で非常に有効であるかどうかを評価する.私たちが指定されていない、およびヘッジ資格を満たしていない派生商品は、現在の収益によって公正な価値に調整されている。付記17、公正価値計量、および付記18、派生ツールを参照。
財産·工場·設備·純価値
物件、工場及び設備は歴史コスト、減価償却、償却及び減価償却費用の純額に基づいて入金される。事件や環境変化がある資産の帳簿価値が回収できない可能性があることを示すたびに、私たちは私たちの財産、工場と設備資産の減値を審査します。減価償却は資産の耐用年数内に直線的に記録されている。レンタル改善は、使用年数またはレンタル期間が短い短い時間で直線的に償却すると推定される。付記11、財産、工場及び設備を参照。
営業権とその他の無形資産
有限年限無形資産は、コスト、累積償却額、減価費用(例えば適用)で入金される。有限年限無形資産の償却は、資産の推定利用可能年数に応じて直線的に、または経済的利益に応じた消費パターン(確実に決定された場合)で記録される。イベントや環境変化が資産の帳簿価値を回収できない可能性があることを示す場合、限られた年限の無形資産の減値を検討します。付記12、商業権、その他無形資産を参照。
企業合併で買収した未完成の知的財産権研究開発プロジェクトの公正価値は資本化され、関連研究開発活動が完成或いは放棄されるまで無期限無形資産に計上される。プロジェクトが成功した後、資本化金額はその予想耐用年数内に償却される。もし一つのプロジェクトが放棄されたら、残りのすべての資本化金額はすぐに無効になるだろう。重大なリスクと不確実性は、最終製品を販売する前に監督部門の承認を得る必要があるため、知的財産権研究開発プロジェクトと関連することが多い。このような承認には臨床試験が必要であり,候補製品が安全かつ有効であることを証明する必要がある。そのため、買収した知的財産権研究開発プロジェクトの最終実現価値は買収の日における公正価値とは異なる可能性があり、知的財産権研究開発減価費用は未来の期間に発生する可能性がある。
資本化知的財産権研究開発プロジェクトは毎年及び事件或いは環境変化が帳簿額面が回収できない可能性があることを示す時に減値テストを行う。私たちは現在の法律と規制環境、競争構造を含む潜在的減値の様々な要素を考慮した。不利な臨床試験結果、上場承認を獲得した重大な遅延、製品を市場に出すことができない及び競争相手製品の発売或いは向上は関連無形資産の一部或いはすべての減値を招く可能性がある。
私たちは毎年営業権の減価テストを行い、事件や状況が変化するたびに帳簿が回収できない可能性があることを示します。今まで、営業権の減価は記録されていない。付記12、商業権、その他無形資産を参照。
事件があったり
正常な業務過程において、私たちは各種の法律手続き、政府調査、その他の性質が複雑で、結果が予測しにくい事項に関連している。その中のいくつかの手続きは付記19“または事項と引受金”で議論されている。負債が発生している可能性が高く、関連損失の金額を合理的に見積もることができると結論すれば、損失の計上項目を記録したり、損失したりする必要がある。私たちは、法律手続きの発展や他の以前に蓄積された負債額の増加または減少を招く可能性のある事項を四半期ごとに評価します。
外貨換算
機能通貨はドルの国際子会社の純資産ではなく現在の為替レートでドルに換算されています。これらの子会社の純資産が変動率換算によるドル影響はAOCIで確認されている。これらの子会社の収益は平均為替レートを使うことでドルに換算される。
株式投資
有価証券と非有価証券
公正価値が随時確定可能な上場株式証券への投資は同じ証券の見積市場価格で入金し、公正価値変動を総合収益表に記入するその他(費用)収入純額。いつでも公正価値を決定できる権益証券のない投資は、コストから減値(あればある)を引いて入金し、同じ或いは類似した証券秩序取引に見られる価格変動に基づいて調整する。このような調整は,合併損益表に記入されている他の(費用)収入純額に記入される.
権益法投資
公正価値オプションを選択していない被投資者に重大な影響を与えることができるようにしたが、コントロールできない株式投資は、権益会計方法に従って計算することができる。被投資者に大きな影響を与える能力があるかどうかをまとめる際には、持ち株比率、投票権、他の株主権利、取締役会代表、他の協力やビジネス関係があるかどうかなどを考慮します。権益会計法は,買収証券の公正価値と比例配分された対象資産の帳簿価値との差額(基差)を各項目に割り当て,その使用年数内にその差額を償却することを求めている。我々は被投資者の収益又は損失におけるシェアと償却の基差があれば、総合損益表におけるその他(費用)収入純額に第1四半期の借金を記入する。もし私たちが減値が非一時的だと思うなら、私たちは私たちの権益法投資に減価損失を記録するだろう。我々は、公正価値が帳簿価値よりも低い時間長、証券価格の変動性、および公正価値回収を実現するために投資を保留する意図と能力を含む、様々な要素に基づいて減価を非一時的と見なしている。
公正価値オプションを選択した権益法投資については,公正価値の変化は総合収益表におけるその他(費用)収入純額に記録されている。
また、私たちは有限組合企業にも投資し、主に初期段階のバイオテクノロジー会社に投資しています。実際の方便として,このような有限パートナーシップ投資の計測方法は,我々が有限パートナーシップが持つ基礎投資に占める資産純値の割合シェアを用いて,このような変動を総合損益表に計上した他の(費用)収入純額である。
最近の会計声明
FASBは2020年3月、LIBORと他の銀行間同業借り換え金利から代替参考金利への移行による財務報告負担を緩和するための新たな会計基準を発表し、一般に参考金利改革と呼ばれている。新しい基準は、契約修正およびヘッジ会計に関する現行GAAPの指導に一時的、オプション的な便宜的および例外を提供する。具体的には、代替参照レートへの変更は、従来の会計処理の契約再計量や再評価を必要としないイベントとみなされる。さらに、すべてのタイプのヘッジ関係について、エンティティは、指定されたヘッジ関係をキャンセルすることなく、参照金利を変更することを許可される。FASBは2021年1月に新たな会計基準を発表し、従来の2020年3月基準の範囲を取引割引を含むデリバティブツールに拡大した。これらの基準の規定はまだ我々の連結財務諸表に実質的な影響を与えておらず、それに実質的な影響を与えることもないと予想される。
FASBは2021年11月、企業合併において顧客と締結した収入契約における契約資産と契約負債の確認と計量をめぐる新たな会計基準を発表した。新基準は、企業合併において被買収者から得られた契約資産及び契約負債は、当初、公正な価値で確認するのではなく、収入確認原則を適用すべきであることを明らかにする。この基準は2023年1月1日から中期と年度内に発効し、早期採用が許可されている。この基準の影響は未来の取引の事実と状況に依存するだろう。
2. 買収と資産剥離
Horizon Treateutics Plcを買収しようとしている
2022年12月12日、安進はHorizonの全株式を#ドルで買収する取引合意に達したと発表した116.501株当たりの現金、取引権益価値は約$27.8十億ドルです。Horizonはアイルランドダブリンに本部を置くグローバルバイオテクノロジー会社であり、薬物の発見、開発と商業化に集中し、稀、自己免疫と深刻な炎症性疾患の影響を受ける人々の重要な需要を満たす。地平線がある12発売された薬品やパイプラインでは20発展計画。この取引の完了は、いくつかの規制機関(FTC審査を含む)と他の慣用的な完了条件の満足に依存する。
提案されたHorizonの買収について、安進は1つのことを達成した364-複数の銀行グループと1日間のブリッジクレジット契約を締結し、合計金額は$28.52022年12月12日、10億ドル。2022年12月22日、私たちは元金総額ドルの定期融資信用協定を締結した4.010億ドルこれは二つ等額の定期ローンは、1つの期限は18ヶ月、もう1つの期限は3年である。したがって、過渡的な信用協定は定期融資信用協定の金額を#ドルに減少させた24.5十億ドルです。2022年12月31日までに違います。すでに橋越し信用協定あるいは定期融資信用協定によって金額を抽出した。これらの信用協定に関連して、安進は約$を発生させた97融資コスト百万ドルは、主に我々の総合貸借対照表中の他の流動資産に資本化され、合意条項の下の総合収益表で利息支出純額として償却される。しかも、私たちは現金残高#ドルを維持することに同意する2.96過渡性信用協定と定期融資信用協定下の任意の借金と一緒に、買収融資のための資金源に使用することができる。
2023年1月30日、当社とHorizonは、それぞれ、当社がHorizon買収を提案する補足情報および文書材料の審査に関する連邦貿易委員会の要請を受けた(第2次請求)。第二の請求の効果は、会社とHorizonが第二の請求を実質的に遵守した後30日まで、会社およびHorizonが自発的に延長するか、または連邦貿易委員会によって早期に終了しない限り、1976年の“ハート-スコット-ロディノ反トラスト改善法案”(改正)に規定された待機期間を延長することである。
ChemoCentryx,Inc.
2022年10月20日、私たちはChemoCentryxの全流通株を買収しました。これは市販のバイオテクノロジー会社で、経口療法による自己免疫疾患、炎症性疾患、癌の治療に専念し、価格は1ドルです52.001株当たりの現金は,総対価$に相当する3.9十億ドルです。この業務合併とみなされる買収は、TAVNEOS、経口選択的補体5 a受容体阻害剤であり、2021年10月に米国FDAによって成人重症活動性抗好中球細胞質自己抗体関連脈管炎(ANCA関連脈管炎)の補助療法として承認された。TAVNEOSは我々が米国で商業化し,米国以外の市場ではTAVNEOSはパートナーから商業化され,安進は製品の将来の販売状況に応じて印税とマイルストーンを得る権利がある。買収後、ChemoCentryxは安進の完全子会社となり、買収日からその業務が我々の総合財務諸表に含まれている。
2022年12月31日までの3ヶ月間に、会社は約$を発生させた106株式ベースの支払いを含むChemoCentryxの買収に直接関連する百万ドルのコストは、合併後のサービス、解散費、および他の取引コストに起因することができる非既得持分奨励金を決済することを含む。これらのコストは主に総合損益表におけるSG&A費用に計上される.
次の表は、総対価格と分配の買収日、買収資産の公正価値と負担する負債(単位:百万)をまとめた
| | | | | | | | |
| | 金額 |
| 現金と現金等価物 | | $ | 86 | |
| 有価証券 | | 235 | |
| 棚卸しをする | | 41 | |
| 有限寿命無形資産−開発−製品−技術権 | | 3,497 | |
| 商誉 | | 667 | |
| その他の負債、純額 | | (85) | |
| 繰延税金負債,純額 | | (516) | |
| 買収した総資産,純額 | | $ | 3,925 | |
これは1ドルです3.9億ドルの総対価格は(I)オーストラリアドルを含む3.7ChemoCentryxの発行済み普通株主に10億ドルの現金と(Ii)Aドルを支払う181ChemoCentryx持分奨励計画によると、ChemoCentryx持分奨励所有者に100万現金を支払い、2022年10月20日の買収日までに提供されるサービスを奨励する。
獲得した開発製品の技術権はTAVNEOSと関係があり、この薬はアメリカとEUで承認され、ANCA関連性脈管炎に応用されている。公正価値を#ドルと推定する3.5多期超過収益法により計算し、将来の現金流量を現在値に割引することを期待し、割引率は市場参加者を代表して無形資産価値の推定率を評価する。開発した製品の技術権は直線的に償却されており,加重平均期間は約11年は直線方法を用いた。
購入した在庫の見積もり公正価値は#ドルです41比較販売法で決定された販売収入は1000万ユーロであり,在庫の実際または予想販売価格を基準金額とし,販売努力と買い手努力利益の調整を行う.在庫公正価値調整は在庫回転時に償却します。私たちは約13何ヶ月になりますか。
繰延納税純負債#ドル516百万ドルで確認されているのは、買収された識別可能な資産と負債を担う帳簿基礎と課税基盤に関する一時的な違いであり、主に買収された無形資産によって推進されている。
買収日対価格は、買収資産と負担した負債に割り当てられた公正価値の差額#ドルを超える667100万ドルは営業権として記録されており、納税時に控除することはできない。営業権価値は主にTAVNEOS資産からの予想協同効果に起因する。
私たちは今回買収した会計計算は初歩的で、私たちの分析を完成した後に決定して、買収日、負担するいくつかの資産の公正価値と税務関連プロジェクトを確定します。私たちは買収日から最大1年間の測定期間中に追加の情報を得たからです。
Teneobio,Inc.
2021年10月19日,Teneobioの全流通株を買収し,Teneobioは個人持株の臨床段階バイオテクノロジー社であり,ヒト重鎖ドメインからなる単鎖抗体であるヒト重鎖抗体という新しい生物製剤を開発している。この取引は、Teneobio社独自の二重特異性と多重特異性抗体技術を含むビジネス合併とみなされ、これらの技術は安進会社の既存の抗体能力と二重特異性T細胞加入者BITを補充する®このプラットフォームは核心治療領域の疾病の治療の速度と効率を治療するために、新しい分子の発見と開発を著しく加速する。買収後、Teneobioは安進の完全子会社となり、その業務は買収日から我々の総合財務諸表に計上される。
2022年12月31日終了年度の計量期間調整は、購入価格配分と総対価格の変化を含め、純増加#ドル22100万人が営業権に転じる。計量期調整は主に買収日の後に発生した事件によるものではなく、買収日の後に発生した事件によるものではなく、買収日に存在する事実と状況に基づいてある買収資産に関する推定投入に起因する。これらの調整は、安進の2022年12月31日までの年度内の運営業績に大きな影響を与えることはなく、買収日にこれらの調整を行えば、前四半期の業績に大きな影響を与えることもない次の表は、計算法期間調整(百万単位)を含む最終総対価格と分配の買収日買収資産と負担する負債の公正価値をまとめた
| | | | | | | | |
| | 金額 |
| 現金買い入れ価格 | | $ | 993 | |
| 値段が合うかもしれない | | 299 | |
| 総掛け値 | | $ | 1,292 | |
| | |
| 現金と現金等価物 | | $ | 100 | |
| 知的財産権研究開発 | | 991 | |
| 有限寿命無形資産−研究開発技術権 | | 115 | |
| 有限寿命無形資産--許可権 | | 41 | |
| 商誉 | | 273 | |
| その他の資産、純額 | | 16 | |
| 繰延税金負債 | | (244) | |
| 買収した総資産,純額 | | $ | 1,292 | |
この取引の対価格は:(一)前払い現金#ドルを含む993運営資本調整が含まれている100万ドル、および(2)将来Teneobio前持分所有者に支払われるか、またはマイルストーン支払いがあり、金額は最高$に達する1.6主要資産(AMG 340,前身はTNB−585)の各種開発と規制マイルストーンおよび他の候補薬物の各種開発マイルストーンの実現に基づき,10億ドルの現金を提供した。価格債務の推定公正価値の合計は#ドルです299買収日には、確率による期待リターン方法を決定する。この方法における仮定は、マイルストーンを達成する可能性と予想される支払日とを含み、私たちの税引前債務コストに基づいてその金額を現在の値に割引する。2022年12月31日現在のこれらの債務の見積公正価値に関する情報は、付記17、公正価値計量を参照されたい。
買収した知的財産権研究開発資産の推定公正価値は合計#ドルである991100万ドルのうち784100万はAMG 340と関係があり、即ち転移性去勢耐性前立腺癌(MCRPC)を治療する第一段階の臨床試験において、残りは四つ独立した臨床前腫瘍学プロジェクト。ドルの研究開発技術権115100万ドルはTeneobio社独自の二重特異性と多重特異性抗体技術と関連があり、この金額は償却されている10年、直線法を使う。Teneobioはまた、その技術およびいくつかの決定された目標を、#ドルの契約合意を表す様々な第三者に許可する41百万ドルです。これらの無形資産の推定公正価値は,割引率を用いて将来のキャッシュフローを現在値に割引する多期超過収益法を用いて決定され,割引率は市場参加者が無形資産を推定するための推定比率を代表する。予測キャッシュフローは、将来の収入および支出の推定、開発完了に要する時間および資源、およびFDAおよび他の規制機関の上場承認を得る可能性を含む、それぞれの無形資産に起因できるいくつかの仮定に基づいている。
繰延税金負債#ドル244主に買収された無形資産によって駆動される,買収された識別可能資産と負債を担う帳簿基準と計税基準に関する一時的な差は百万ドルであることが確認された。
買収日対価格は、買収資産と負担した負債に割り当てられた公正価値の差額#ドルを超える273100万ドルは営業権として記録されており、納税時に控除することはできない。商標価値はAMG 340と買収技術の予想される相乗効果を代表する。
Five Prime治療会社を買収しました
2021年4月16日、安進はFive Primeの買収を完了し、総現金の対価格はドルとなった1.610億ドル、現金を買収した純額を差し引く。購入価格は手元の現金で払います。この取引は資産買収に計上されており、ほとんどの買収資産の価値がbemarituzumabの知的財産に集中しているため、bemarituzumabは胃癌治療の第3段階の一流計画である。Primeの5つの業務は、買収日後に開始された連結財務諸表に含まれています。
私たちはFive Primeを買収した価格をbemarituzumab IPR&D計画に割り当て、金額は$1.5合併損益計算書で買収された知的財産の研究開発費に直ちに支出する10億ドル;繰延税金資産#ドル177100万ドルです他の純負債$47百万ドルです。買収された知的財産権研究開発費は税金を支払うことができない。
Gensenta la≡sanayi ve Ticaret A.゚を剥離する。
2022年11月2日、トルコ子会社Gensentaの株式をEczac≡baに売却し、純現金収益は約$となった130百万ドルです。この取引は企業を売却すると記載されており、非持続的な経営に分類される基準を満たしていない。取引完了後,Gensentaに関する純資産は$となる862022年12月31日までの年度中に資産剥離損失$を確認しました567総合損益表に他の業務費の百万ドルを記入したのは,主に#ドルの変更によるものである615AOCIは外貨換算で百万ドルの赤字を計上して収益に転化する。付記16、株主権益を参照。
3. 収入.収入
私たちの業務は1つはビジネスプレート:人間治療学したがって,我々の運営結果は合併に基づいて報告されており,部門報告に用いられ,内部管理報告と一致している。顧客所在地による製品と地理地域別の収入は以下のとおりである。ROWの収入の大部分はヨーロッパで販売されている製品と関係がある
収入状況は以下の通り(単位:百万):
| | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | |
| | 2022年12月31日までの年度 | | 2021年12月31日までの年度 | | 2020年12月31日までの年度 |
| | アメリカです。 | | はい | | 合計する | | アメリカです。 | | はい | | 合計する | | アメリカです。 | | はい | | 合計する |
| Enbrel | | $ | 4,044 | | | $ | 73 | | | $ | 4,117 | | | $ | 4,352 | | | $ | 113 | | | $ | 4,465 | | | $ | 4,855 | | | $ | 141 | | | $ | 4,996 | |
| プロリア | | 2,465 | | | 1,163 | | | 3,628 | | | 2,150 | | | 1,098 | | | 3,248 | | | 1,830 | | | 933 | | | 2,763 | |
| ウルトラツラ | | 1,886 | | | 402 | | | 2,288 | | | 1,804 | | | 445 | | | 2,249 | | | 1,790 | | | 405 | | | 2,195 | |
| シグワ | | 1,480 | | | 534 | | | 2,014 | | | 1,434 | | | 584 | | | 2,018 | | | 1,405 | | | 494 | | | 1,899 | |
| Aranesp | | 521 | | | 900 | | | 1,421 | | | 537 | | | 943 | | | 1,480 | | | 629 | | | 939 | | | 1,568 | |
| ナンバープレート | | 848 | | | 459 | | | 1,307 | | | 566 | | | 461 | | | 1,027 | | | 485 | | | 365 | | | 850 | |
再修術 | | 608 | | | 688 | | | 1,296 | | | 557 | | | 560 | | | 1,117 | | | 459 | | | 428 | | | 887 | |
| ケプロリス | | 850 | | | 397 | | | 1,247 | | | 736 | | | 372 | | | 1,108 | | | 710 | | | 355 | | | 1,065 | |
| ニューラス塔 | | 959 | | | 167 | | | 1,126 | | | 1,514 | | | 220 | | | 1,734 | | | 2,001 | | | 292 | | | 2,293 | |
| 事件.事件 | | 533 | | | 254 | | | 787 | | | 331 | | | 199 | | | 530 | | | 191 | | | 159 | | | 350 | |
その他の製品(1) | | 3,549 | | | 2,021 | | | 5,570 | | | 3,305 | | | 2,016 | | | 5,321 | | | 3,630 | | | 1,744 | | | 5,374 | |
製品総売上高(2) | | 17,743 | | | 7,058 | | | 24,801 | | | 17,286 | | | 7,011 | | | 24,297 | | | 17,985 | | | 6,255 | | | 24,240 | |
| その他の収入 | | 852 | | | 670 | | | 1,522 | | | 908 | | | 774 | | | 1,682 | | | 511 | | | 673 | | | 1,184 | |
| 総収入 | | $ | 18,595 | | | $ | 7,728 | | | $ | 26,323 | | | $ | 18,194 | | | $ | 7,785 | | | $ | 25,979 | | | $ | 18,496 | | | $ | 6,928 | | | $ | 25,424 | |
____________
(1) 私たちの非主要製品の製品販売と、私たちのGensentaとBergamo子会社を含めて。
(2) 製品販売に含まれるヘッジ損益は,2022年,2021年,2020年12月31日までの数年間重要ではない。
アメリカでは、私たちは主に薬品卸売流通業者に販売しています。これらの流通業者は私たちが製品を医療サービス業者に分配する主要な手段です。米国以外では,主に医療提供者および/または薬品卸売流通業者に販売されており,具体的には個々の国/地域の流通実践に依存している。私たちは大きな顧客の財務状況を監視し、信用限度額を設定し、場合によっては信用状を要求したり、信用保険を獲得したりすることで、私たちの信用リスクの開放を制限します。
私たちの製品販売は三つ2022年、2021年、2020年12月31日までの毎年、個人収入が総収入の10%以上を占める顧客。2022年12月31日までの年間で、これらのお客様の合計は82総収入に占める割合を次の表に示すこれらの顧客に関するいくつかの情報は以下のとおりである(単位:百万ドル):
| | | | | | | | | | | | | | | | | |
| 十二月三十一日までの年度 |
| 2022 | | 2021 | | 2020 |
| McKesson社: | | | | | |
| 総生産販売総額 | $ | 17,305 | | | $ | 15,187 | | | $ | 13,779 | |
| 毛収入総額のパーセント | 35 | % | | 33 | % | | 32 | % |
| アメリカのベルゲン社は | | | | | |
| 総生産販売総額 | $ | 15,443 | | | $ | 14,783 | | | $ | 14,743 | |
| 毛収入総額のパーセント | 31 | % | | 32 | % | | 34 | % |
| 枢機卿健康会社: | | | | | |
| 総生産販売総額 | $ | 8,319 | | | $ | 7,681 | | | $ | 7,332 | |
| 毛収入総額のパーセント | 16 | % | | 17 | % | | 17 | % |
2022年12月31日と2021年12月31日までに三つ各顧客は貿易売掛金総額の10%を超えています75%和73合併に基づいて、それぞれ貿易売掛金の純額のパーセンテージを占める。2022年と2021年12月31日までに26%和27売掛金の純額の割合はそれぞれ米国以外の顧客から来ており、その大部分はヨーロッパから来ている。2022年12月31日と2021年12月31日まで、私たちの不良債権準備総額はそれほど大きくありません。
4. 株に基づく報酬
私たちが改訂した2009年計画は、RSU、株式オプション、業績単位を含む、安進の従業員と私たちの取締役会の非従業員に私たちの普通株の株式を発行することを許可し、付与された株式ベースの奨励に基づいて、RSU、株式オプション、業績単位を含む。改正された2009年計画によると、利用可能な株式プールは減少した1つは付与された1株当たりオプションの株式は、1.9付与された他の種類の奨励金の株式は、全額奨励を含む。一般に、改訂された2009年計画に従って奨励金が付与された任意の株式が満期になったり、未発行株式の場合に没収、終了、またはログアウトされた場合、その奨励された株式は、除去された基準と同じベースで許可プールに再加入される。また、改正された2009年計画によると、全額奨励に関する最低法定納税義務を支払うために源泉徴収された株式は、認可プールに再加入する1.9株式です。2022年12月31日現在、改正後の2009年計画では、将来の贈与及び/又は発行額は最高約15百万株の私たちの普通株です。我々の従業員補償計画によると、株式ベースの報酬は、その目的のために予約された新規発行株で行われる。
次の表は、私たちの合併損益表で確認された株式ベースの報酬費用の構成要素(百万単位)を反映しています
| | | | | | | | | | | | | | | | | |
| 十二月三十一日までの年度 |
| 2022 | | 2021 | | 2020 |
| RSU | $ | 227 | | | $ | 183 | | | $ | 178 | |
| 業績単位 | 132 | | | 121 | | | 118 | |
| 株式オプション | 42 | | | 37 | | | 34 | |
| 株式に基づく報酬総支出、税引前 | 401 | | | 341 | | | 330 | |
| 株式の報酬支出に基づく税収割引 | (86) | | | (74) | | | (72) | |
| 株式の報酬支出総額に基づいて税額を差し引く | $ | 315 | | | $ | 267 | | | $ | 258 | |
制限株式単位及び株式オプション
条件を満たした従業員は一般に毎年RSUを獲得し,ある幹部レベルの従業員に対しては株式オプションも獲得し,奨励の規模やタイプは通常従業員の賃金レベルと業績レベルによって決定される。一部の管理職および専門職は通常、就職開始時にRSU補助金を受ける。私たちの取締役会の非従業員会員たちも毎年RSUの補助金を受けている。
我々のRSUおよび株式オプション付与は、死亡、障害、制御権変更による終了、および特定のサービスおよび/または年齢要件を満たす従業員の退職を含む、計画および関連付与プロトコル定義の特定の場合に、帰属を加速または継続することを提供するRSUおよび株式オプションは、通常、付与日の第2、第3および第4の記念日に等額付与される。RSUは配当等価物を計算すべきであり、通常、基礎RSUが帰属して受信者に発行された場合にのみ、株式で支払われる。
制限株式単位
与えられた日、RSUの公正な価値は、RSUがその帰属中に配当等価物を計算すべきであるので、付与日の私たちの普通株式の終値に等しい。2022年,2021年および2020年12月31日までの年間で,単位買い戻し単位あたりの加重平均承認日公正価値は$である234.47, $233.10そして$235.63それぞれ,である
次の表に我々のRSUに関する情報をまとめる
| | | | | | | | | | | |
| 2022年12月31日までの年度 |
| 職場.職場
(単位:百万) | | 加重平均
授与日
公正価値 |
2021年12月31日現在の未帰属残高 | 3.0 | | | $ | 217.95 | |
| 授与する | 1.0 | | | $ | 234.47 | |
| 既得 | (0.9) | | | $ | 201.47 | |
| 没収される | (0.3) | | | $ | 226.15 | |
2022年12月31日現在の未帰属残高 | 2.8 | | | $ | 228.71 | |
2022年12月31日,2021年,2020年12月31日までの年間で,帰属するRSUの総授権日公正価値は$である192百万、$166百万ドルとドル161それぞれ100万ドルです
株式オプション
株式オプションの発行価格は、我々普通株の付与日の終値に設定されており、付与された関連株式数はその時点で固定されている。賞が満期になる10授与の日から数年。我々はBlack-Scholesオプション推定モデルを用いて株式オプション付与日の公正価値を推定した
オプション推定モデルで用いられる重み付き平均仮定とそれによる株式オプション付与の重み付き平均付与日公正価値は以下のとおりである
| | | | | | | | | | | | | | | | | |
| 十二月三十一日までの年度 |
| 2022 | | 2021 | | 2020 |
| 普通株は授与日の終値です | $ | 230.92 | | $ | 237.17 | | | $ | 236.36 | |
| 期待変動率(隠れ変動率と履歴変動率の平均値) | 24.5 | % | | 25.6 | % | | 28.1 | % |
| 予想寿命(年) | 5.7 | | 5.7 | | 5.8 |
| 無リスク金利 | 2.8 | % | | 1.0 | % | | 0.4 | % |
| 期待配当収益率 | 3.3 | % | | 2.9 | % | | 3.0 | % |
| 付与された株式オプションの公正価値 | $ | 42.43 | | $ | 40.43 | | | $ | 42.34 | |
次の表は、私たちの株式オプションに関する情報をまとめています
| | | | | | | | | | | | | | | | | | | | | | | |
| 2022年12月31日までの年度 |
| オプション
(単位:百万) | | 重み付けの-
平均値
行権価格 | | 重み付けの-
平均値
残り
契約書
寿命(年単位) | | 骨材
固有の
価値がある
(単位:百万) |
| 2021年12月31日現在の未行使残高 | 5.1 | | | $ | 197.27 | | | | | |
| 授与する | 1.1 | | | $ | 230.92 | | | | | |
| 鍛えられた | (0.7) | | | $ | 167.44 | | | | | |
| 期限切れ·没収 | (0.2) | | | $ | 226.35 | | | | | |
2022年12月31日現在の未行使残高 | 5.3 | | | $ | 207.29 | | | 7.0 | | $ | 295 | |
すでに帰属していますか、あるいは2022年12月31日に帰属する予定です | 5.2 | | | $ | 206.47 | | | 7.0 | | $ | 290 | |
2022年12月31日から行使可能 | 2.2 | | | $ | 177.48 | | | 5.3 | | $ | 187 | |
2022年,2021年および2020年12月31日までに年度内に行使されるオプション総内的価値は67百万、$56百万ドルとドル98それぞれ100万ドルです2022年12月31日現在、2021年と2020年12月31日までの年度のオプション減税による実質税務利益は14百万、$12百万ドルとドル21それぞれ100万ドルです
2022年12月31日までにドル362百万ドルの未確認補償費用は、RSUおよび未帰属株式オプションに関連しており、#年加重平均期間中に確認される予定である1.7何年もです。
業績単位
ある管理レベルの従業員はまた、業績単位の年間贈与を獲得し、これは、受給者が普通株を獲得する権利があり、これは、業績期間中に特定の予め定められた目標を達成することに依存し、これは通常、3年それは.2022年,2022年,2021年,2020年12月31日までの年度内に付与された単位の業績目標を株式奨励とし,(I)比較可能な会社グループに対する安進の株主リターンに基づいて,これらのリターンが市場状況とみなされるため,付与日単位の公正価値に反映され,(Ii)業績条件とされる安進の独立財務業績測定に反映される。奨励のための費用は,付与日単位の公正価値に関連業績条件に応じて稼ぐことが予想される単位数を乗じ,推定を差し引いた没収であることを確認した。これらの業績目標の結果に基づいて、受賞者は最終的に付与された単位数よりも多いまたは少ない単位を獲得することが可能となる。私たちの普通株は1つは-稼いだ各業績単位に1対1の基礎を提供します。一般に、パフォーマンス単位報酬は、パフォーマンス期間終了時に付与される。業績奨励計画は、特定のサービスおよび/または年齢要件を満たす従業員の死亡、障害、制御権の変更、および退職時を含む、計画に定義されている場合に許可を加速または継続することを規定している。業績単位は配当等価物を計算すべきであるが、配当等価物は通常関連業績単位の帰属時及びある程度株式で支払い、獲得した業績単位の数量に影響を与える市場と業績条件を含む受給者に発行される。
我々は支払シミュレーションモデルを用いて業績単位の付与日公正価値を推定した支出シミュレーションモデルで用いた重み付き平均仮定とそれによるパフォーマンス単位の重み付き平均付与日の公正価値は以下のとおりである
| | | | | | | | | | | | | | | | | |
| 十二月三十一日までの年度 |
| 2022 | | 2021 | | 2020 |
| 普通株は授与日の終値です | $ | 230.92 | | | $ | 239.64 | | | $ | 236.36 | |
| 波動率 | 28.1 | % | | 29.3 | % | | 27.5 | % |
| 無リスク金利 | 0.3 | % | | 0.3 | % | | 0.2 | % |
| すでに部門の公正価値を承認した | $ | 247.48 | | | $ | 254.68 | | | $ | 249.07 | |
支出シミュレーションモデルは,我々の普通株と比較会社グループの普通株の株価リターンと比較会社グループの株価変動との相関を仮定し,株主の業績期間中のリターンと業績単位契約条項に基づく支払割合への影響をシミュレーションする.
2022年12月31日と2021年12月31日までに1.6100万個の業績単位がまだ決済されておらず,単位あたりの加重平均付与日公正価値は#ドルである250.27そして$229.39それぞれ単位ごとである.2022年12月31日までの年間で0.6百万個の業績単位,単位あたりの加重平均付与日の公正価値を$とする247.48承認されました0.1百万個の業績単位,単位あたりの加重平均付与日の公正価値を$とする250.94全部没収されました。
2022年,2021年,2020年12月31日までの年度内に支払われる業績単位の公正価値総額は#ドルである150百万、$149百万ドルとドル230業績単位数に応じて私たち普通株の業績期間最終日の終値を乗じて、それぞれ百万ドルです。
2022年12月31日までにドル132未確認の補償費用のうち100万は非既得業績単位に関係しており,#年加重平均期間内に確認される予定である1年.
5. 固定払込計画
当社はすでに出資計画を確定し、当社及び参株付属会社のある従業員は所得税の目的で補償の支払いを遅延させることができる。会社の他の貢献のほかに、参加者には彼らの貢献に応じてマッチングの貢献を得る資格がある。固定払込計画費用は$243百万、$279百万ドルとドル2312022年12月31日まで、2021年、2020年12月31日までの年度はそれぞれ100万ドル。
6. 所得税
所得税前収入には以下(単位:百万)が含まれる
| | | | | | | | | | | | | | | | | |
| 十二月三十一日までの年度 |
| 2022 | | 2021 | | 2020 |
| 国内では | $ | 3,026 | | | $ | 1,850 | | | $ | 4,087 | |
| 外国.外国 | 4,320 | | | 4,851 | | | 4,046 | |
| 所得税前総収入 | $ | 7,346 | | | $ | 6,701 | | | $ | 8,133 | |
所得税の支出には、以下の内容が含まれている
| | | | | | | | | | | | | | | | | |
| 十二月三十一日までの年度 |
| 2022 | | 2021 | | 2020 |
| 現在準備している: | | | | | |
| 連邦制 | $ | 1,721 | | | $ | 865 | | | $ | 921 | |
| 状態.状態 | 44 | | | 18 | | | 34 | |
| 外国.外国 | 304 | | | 359 | | | 277 | |
| 総当期に準備する | 2,069 | | | 1,242 | | | 1,232 | |
| 繰延収益: | | | | | |
| 連邦制 | (1,185) | | | (308) | | | (321) | |
| 状態.状態 | (27) | | | (9) | | | 9 | |
| 外国.外国 | (63) | | | (117) | | | (51) | |
| 繰延収益総額 | (1,275) | | | (434) | | | (363) | |
| 所得税引当総額 | $ | 794 | | | $ | 808 | | | $ | 869 | |
繰延所得税は、財務報告目的のための資産および負債の帳簿価値と、所得税目的のための金額、税収控除およびNOL繰越の税収影響との間の一時的な差の税収影響を反映する。2022年12月31日まで、私たちは米国が私たちの外国子会社の収益に対する最低税額について繰延税金項目を設立し、今後数年で臨時プロジェクトを打ち消すことを選択した私たちの繰延税金資産と負債の重要な構成要素は以下の通りです(百万単位)
| | | | | | | | | | | |
| 十二月三十一日 |
| 2022 | | 2021 |
| 繰延所得税資産: | | | |
| NOLと貸記繰り越し | $ | 1,344 | | | $ | 1,065 | |
| 費用を計算する | 584 | | | 600 | |
| 資本化研究と開発費 | 515 | | | — | |
| 投資する | 270 | | | — | |
| 課税資本化費用 | 211 | | | 244 | |
| 外国子会社の収益 | 192 | | | — | |
| 株に基づく報酬 | 104 | | | 96 | |
| 他にも | 317 | | | 326 | |
| 繰延所得税の資産総額 | 3,537 | | | 2,331 | |
| 推定免税額 | (718) | | | (663) | |
| 所得税純資産を繰延する | 2,819 | | | 1,668 | |
| | | |
| 繰延所得税負債: | | | |
| 買収した無形資産 | (1,238) | | | (824) | |
| 債務 | (272) | | | (275) | |
| 固定資産 | (112) | | | (129) | |
| 他にも | (254) | | | (221) | |
| 繰延所得税負債総額 | (1,876) | | | (1,449) | |
| 繰延所得税の総額,純額 | $ | 943 | | | $ | 219 | |
将来控除可能な金額を実現するために必要な将来の課税収入の推定を含むプラスおよび負の証拠の評価によると、繰延税金資産の金額をより顕在化する可能性のある金額に減らすための推定免税額を提供します。
推定手当は2022年に増加し、主に会社がある国の研究開発控除が満期になると予想して使用していないためだ。
2022年12月31日までに170百万ドルの連邦税控除は未来の連邦所得税を減少させ、#ドルの推定手当を提供することができます6その中には数百万人の連邦税金が繰越免除されている。連邦税収控除は2023年から2042年の間に満期になる。1元持っています896100万ドルの州税控除は、将来の州所得税を減らすために使用でき、#ドルの推定手当を提供します813その中には数百万の州税金が繰越免除されている。1元持っています51私たちの海外司法管轄区に関係する百万の税収控除は、私たちが提供した未来の外国所得税を相殺することができます違います。推定免税額
2022年12月31日までに1.310億ドルの連邦NOL繰越は、将来の連邦所得税を低減し、提供されています違います。その連邦NOL繰越に対する推定手当。さらに、$1.0その中で10億ドルの連邦NOL繰り越しは満期になっていない;残りは2023年から2037年の間に満期になり始めた。1元持っています536百万の州NOL繰越は将来の州所得税を削減し、$を提供することができます415この州の何百万人もの人々が転換した。1元持っています1.910億ドルの外国NOL繰越は、将来の外国所得税の低減に使用でき、#ドルの推定手当を提供します186何百万人もの外国人がNOLを持っている。外国のNOLと違います。推定免税額を提供します。$640100万は期限が切れていない;残りは2023年から2051年の間に期限が切れる。
建設工事総額の入金状況は以下のとおりである(百万単位)
| | | | | | | | | | | | | | | | | |
| 十二月三十一日までの年度 |
| 2022 | | 2021 | | 2020 |
| 期初残高 | $ | 3,546 | | | $ | 3,352 | | | $ | 3,287 | |
| 本年度に関連する納税状況に基づいて計算される増加額 | 151 | | | 171 | | | 165 | |
| 数年前に関連した納税状況に基づいて計算した増加額 | 90 | | | 35 | | | 3 | |
| 先日の減税状況 | (14) | | | (4) | | | (35) | |
| 訴訟の時効成立時の減額 | (3) | | | — | | | — | |
| 集まって落ち合う | — | | | (8) | | | (68) | |
| 期末残高 | $ | 3,770 | | | $ | 3,546 | | | $ | 3,352 | |
2022年12月31日までの違約金のほとんどが、確認されれば、実際の税率に影響を与える。2020年12月31日までの1年間、米国国税局といくつかの問題を効果的に解決した。そこで私たちはUTBを再測定しました
違約金に関連した利息と罰金は私たちの所得税条項に含まれている。2022年、2021年、2020年12月31日までの年間で確認しました189百万、$98百万ドルとドル116総合収益表の所得税の計上により、利息と罰金はそれぞれ100万ドルとなる。2022年12月31日までの1年間、利息支出が増加した主な原因は2022年の金利上昇である。2022年と2021年12月31日現在、違反建築に関する課税利息と罰金は#ドルである1.110億ドル881それぞれ100万ドルです
所得税前収入に適用される連邦法定税率と私たちの有効税率との間の入金は以下の通りです
| | | | | | | | | | | | | | | | | |
| 十二月三十一日までの年度 |
| 2022 | | 2021 | | 2020 |
| 連邦法定税率 | 21.0 | % | | 21.0 | % | | 21.0 | % |
| 海外収益 | (5.6) | % | | (7.8) | % | | (4.7) | % |
| 外国由来の無形収入 | (1.3) | % | | (1.0) | % | | (0.7) | % |
| はい、プエルトリコの消費税です | (2.8) | % | | (3.4) | % | | (2.9) | % |
| | | | | |
| 不確定税収頭寸の利子 | 1.9 | % | | 1.1 | % | | 1.1 | % |
| 信用は主に連邦研究開発です | (2.0) | % | | (2.1) | % | | (1.4) | % |
| 知的財産権の研究開発を買収する | — | % | | 4.9 | % | | — | % |
| 監査決算 | — | % | | — | % | | (1.0) | % |
| その他、純額 | (0.4) | % | | (0.6) | % | | (0.7) | % |
| 実際の税率 | 10.8 | % | | 12.1 | % | | 10.7 | % |
2022年12月31日,2021年,2020年12月31日までの年度の有効税率は連邦法定税率と異なり,主に収入と支出の司法組み合わせの影響によるものである。私たちの有効税率による収益のほとんどは、プエルトリコでの同社の業務から来ています。プエルトリコはアメリカの領土であり、アメリカの税務目的でプエルトリコは外国司法管轄区とされています。2050年まで、プエルトリコでの私たちの業務は税金優遇支出によって制限されるだろう。また、同社がシンガポールで展開している事業は2034年までに税収割引を受ける。私たちの海外収入もアメリカ税率10.5%の減税を払わなければなりません。
米国の属地プエルトリコは、プエルトリコのメーカーが社内から購入した商品やサービスの総価格に4%の消費税を課し、2022年12月31日から発効する。2022年には、消費税を製造コスト、このコストを在庫に計上し、関連製品の販売時に販売コストを計上する。アメリカ所得税については、消費税による外国税控除は、通常、消費税が発生したときに私たちの所得税の支出で確認されています
2022年12月31日、2021年及び2020年12月31日までの年間に納められる所得税は2.4億ドルだ1.910億ドル1.4それぞれ10億ドルです
私たちの1つ以上の法人実体はアメリカ連邦司法管轄区、アメリカ各州司法管轄区、いくつかの外国司法管轄区で所得税申告書を提出します。私たちの所得税申告書はこのような司法管轄区の税務機関によって定期的に検討されている。税収法律、条例と関連事実の異なる解釈のため、異なる税務管轄区の間にはすでに重大な紛争が発生している可能性があり、控除の時間と額、税収控除の使用及び収入と費用の分配などの問題に関連している。米国国税局を含む税務当局は特にこのような問題に注目するようになっている
2017年、私たちは米国国税局から2010-2012年のRARと修正されたRARを受け取り、主にアメリカのあるエンティティとアメリカ領土プエルトリコ間の利益分配に関連する重大な調整を提案した。我々は提案された調整と計算に同意せず、米国国税局控訴事務所と解決策を求めたが、解決策を達成することはできなかった。2021年7月アメリカ税務裁判所に嘆願書を提出しました二つ私たちが2010年5月と7月に受け取った2010-2012年の法定欠税通知(通知)のコピーは、2010年から2012年までの米国の課税所得額を増加させ、追加の連邦税を約$とすることを目的としています3.6十億ドルと利息がつきます。2010年から2012年までに徴収される可能性のあるいかなる追加税金も最大約#ドル減少するだろう900以前私たちの海外収入は数百万ドルの送金税を計上しました。
2020年には、米国国税局から2013-2015年のRARと修正されたRARを受け取り、2010-2012年の提案された利益分配と同様に、米国のあるエンティティと米国領土プエルトリコとの間の利益分配に主に関連する重大な調整を提案した。我々は提案された調整と計算に同意せず、米国国税局控訴事務所と解決策を求めたが、解決策を達成することはできなかった。2022年7月、私たちは米国税務裁判所に請願書を提出し、私たちが以前に報告した2022年4月に受け取った2013-2015年度の通知に異議を唱え、2013-2015年度のアメリカの課税所得額を増加させ、約ドルの追加連邦税を招くことを求めています5.1十億ドルと利息がつきます。しかも、その通知は罰金が約#ドルだと主張した2.0十億ドルです。2013-2015年度に徴収される可能性のある任意の追加税金は最大約#ドル減少するだろう2.2以前私たちの海外収入は10億ドルの送金税を計上しました。
私たちは2010-2012年と2013-2015年の通知で国税局が提起した立場に根拠がないと信じている。私たちは司法手続きを通じて2010-2012年と2013-2015年の通知に異議を唱えている。♪the the the二つ事件は2022年12月19日に米国税務裁判所で合併された。
私たちは現在、2010年から2015年までの問題と類似している国税局2016-2018年の審査を受けている。しかも、私たちはいくつかの州と外国税務管轄区域の検討を受けている。
このような複雑な問題の最終的な解決は今後12ヶ月以内に達成される可能性はあまりない。過去の経験、税法の解釈、税法の私たちの事実への応用、および税務機関の潜在的な行動の判断によると、私たちは依然として私たちの所得税負債の計算項目が適切であると信じている;しかし、所得税の準備の複雑さとこれらの問題の不確定な解決策のため、任意の税務事項の最終結果は、支払う金額が計算された金額を大幅に超え、私たちの総合財務諸表に重大な悪影響を及ぼす可能性がある。
2009年12月31日までに終了した年間で、私たちは米国連邦所得税審査を受け入れない。
7. 1株当たりの収益
基本的な1株当たり収益の計算は私たちが発行した普通株の加重平均に基づいている。1株当たりの収益を希釈する計算は、私たちの発行済み普通株と希釈性潜在普通株の加重平均に基づいており、主に私たちの株式オプション、制限株、業績単位奨励計画によって発行可能な株式(総称して希釈性証券と呼ぶ)を含み、これは在庫株方法によって決定される。
基本1株当たり収益と希釈後の1株当たり収益の計算は以下のとおりである(単位:百万、1株当たりデータを含まない)
| | | | | | | | | | | | | | | | | |
| 十二月三十一日までの年度 |
| 2022 | | 2021 | | 2020 |
| 収入(分子): | | | | | |
| 基本的に1株当たり収益と希釈後の1株当たり純収益 | $ | 6,552 | | | $ | 5,893 | | | $ | 7,264 | |
| | | | | |
| 株式(分母): | | | | | |
| 基本1株当たりの収益の加重平均株式 | 538 | | | 570 | | | 586 | |
| 希釈証券の影響 | 3 | | | 3 | | | 4 | |
| 希釈後の1株当たり収益の加重平均株式 | 541 | | | 573 | | | 590 | |
| | | | | |
| 基本1株当たりの収益 | $ | 12.18 | | | $ | 10.34 | | | $ | 12.40 | |
| 1株当たりの収益を薄める | $ | 12.11 | | | $ | 10.28 | | | $ | 12.31 | |
2022年12月31日までの3年間で、1株当たりの収益を希釈する計算に含まれていない逆償却従業員の株式奨励数は顕著ではない。
8. 協力する
協力計画は共同経営活動に関連した契約計画だ。このような配置は、(1)活動の積極的な参加者であり、(2)大きなリスクおよび報酬に直面しており、活動の商業的成功に依存する2人以上の当事者に関するものである。
私たちは時々、製品および/または候補製品の研究開発、製造、および/または商業化について協力計画を達成する。これらの協力は、通常、払戻不可能な前払い許可料、開発および商業業績マイルストーン支払い、コスト分担、印税および/または利益共有を提供する。私たちの協力計画は技術や商業の成功を保証することなく行われ、各手配は唯一無二である。このような手配により確認された収入のさらなる検討については、付記1、主要会計政策概要を参照されたい。これらの手配により発生したコストの運営費用は,総合損益表におけるそれぞれの費用項目で報告され,我々パートナーが支払うべきいかなる金や対応の精算も差し引かれ,このような精算は当事者が支払い義務がある場合に確認する。私たちの重要な手配は以下のとおりです。
百済神州株式会社です。
2020年1月に百済神州の株式を約1ドルで買収しました2.8中国腫瘍科での事業拡大の一環として10億ドルの現金。百済神州への株式投資に関するより多くの情報は、付記9、投資を参照されたい。協力の下、百済神州は2020年に中国でXGEVAの販売を開始し、2021年にBLINCYTOの販売を開始し、2022年に中国でKyprolisを販売し、最初の特定製品の商業化期間中に安進二等分損益を販売し、その後、製品権利は安進に回復する可能性があり、安進は特定の期限内に百済神州に同製品が中国で販売されている特許権使用料を支払う。安進は百済神州に協力製品を製造し、提供した。
また,百済神州と共同で我々腫瘍学ポートフォリオの一部を開発し,後者はドルまでの現金と開発サービスを提供することで世界の研究開発コストを分担している1.25十億ドルです。監督部門の許可を得た後、百済神州は特定の期間内に中国の商業化権利を負担し、安進と百済神州は利益を折半し、これらの製品権利のいくつかの権利が安進の手に戻るまで。製品権利返還後、安進は百済神州に特定期間内に中国で販売される特許権使用料を支払う。中国以外の製品販売については、安進は百済神州に特許使用料も支払う。
2022年,2021年,2020年12月31日までの年間で,百済神州から回収された腫瘍学候補製品の純コストは199百万、$220百万ドルとドル225総合損益表には,それぞれ研究開発費相殺と記す。2022年12月31日と2021年12月31日までの年間で安進する
百済神州は協力して$を獲得した64百万ドルとドル72それぞれ100万ドルであり,総合損益表の製品販売に記録されている。2022年12月31日と2021年12月31日までの年間で、最初の特定製品商業化期間に関する損益分担費用は53百万ドルとドル64総合損益表には,それぞれ1,000,000,000,000,000,000,000,000,000,000,000,000,000,000,000,000,000,000,000,000,000,000,000,000,000元が記入されている。安進は2020年12月31日までに百済神州の製品販売や損益償却に重大な事項とはならない。百済神州の借りた製品の売上高は#ドルだった6百万ドルとドル212022年、2022年、2021年12月31日現在、連結貸借対照表における売掛金純額がそれぞれ計上されている。百済神州の回収コストと損益シェアの支払純額は#ドル47百万ドルとドル612022年、2022年、2021年12月31日現在、それぞれ総合貸借対照表の他の流動資産に計上されている。
アスリーカン
私たちはアスリカンと協力してTEZSPIREを開発し、商業化している。私たちの協力の下で、アスリコンが安進に1桁の中央値特許権使用料を支払った後、両社は世界コストと利益と損失を折半した。アスリコンは全世界の発展をリードし、安進とアスリコンは共同でTEZSPIREを北米で商業化した。北米では安進が元金としてTEZSPIREの米国での製品販売を確認し,アスリコンが元金としてTEZSPIREのカナダでの製品販売を確認した。アスリカンは北米以外でのTEZSPIREの商業化のトップである。安進はTEZSPIREを世界で製造し供給している。
2022年、2021年、2020年12月31日までの年間で、アスリコンの世界開発への純コストは74百万、$49百万ドルとドル52総合損益表では,研究開発費はそれぞれ研究開発費に計上されている。2022年、2021年、2020年12月31日までの世界商業化のためのアスリコンの純コストは60百万、$39百万ドルとドル16総合損益表には,それぞれ1,000,000,000,000,000,000,000,000,000,000,000,000,000,000,000,000,000,000,000,000,000,000,000,000,000元が記入されている。2022年12月31日までの年間における世界損益シェア支出は119総合損益表では、販売コストは主に販売コストに計上されている。TEZSPIREは2022年1月に米国で発売された。
連合信用銀行
我々はUCBと協力してEVENITYを開発し,商業化している。私たちの協力の下で、連合銀行はヨーロッパの大部分の国と中国(香港を含まない)でのEVENITYの商業化をリードする権利がある。安進は責任者として、EVENITYの商業化をリードし、米国を含む他のすべての地域での製品の販売を認めている。協力に関するグローバル開発コストと商業化損益が二分されている。安進は世界的にEVENITYを製造し、供給している。
2022年、2021年、2020年12月31日までの年間における世界損益分担費用は255百万、$186百万ドルとドル115総合損益表では、販売コストは主に販売コストに計上されている。2022年、2021年、2020年12月31日までの年度内に、連合銀行から合同銀行への純コストを回収して対応することは実質的ではない。
ノワ製薬は
私たちはノワール社と協力してAimovigを共同開発して商業化している。2022年1月31日、私たちは協力条項を修正した。2022年1月1日から、ノバ社は安進会社と協力せず、エモビヒの商業化コストを分担したりマイルストーン費用を支払ったりし、安進社も米国でエモヴィヒを販売する使用料をノバ社に支払うことはなくなった。ノヴァ社は引き続きAimovigの米国と日本以外の世界共同開発権と独占商業権を保有している。安進とノワールは世界開発費を分担し、ノファはこの製品の米国と日本以外の純売上高に2桁の印税を支払った。アン進はエモビグを世界的に製造して供給している。
2022年12月31日までの1年間に、ノファ社から回収された片頭痛製品の純コストは53百万ドル、総合損益表の研究開発費に入金されています。2021年12月31日と2020年12月31日までの年間で,ノファ社から回収された片頭痛製品の純コストは160百万ドルとドル192総合損益表では、主に総合損益表のSG&A支出が入金されている。2021年12月31日と2020年12月31日までの年間で、ノバ社がAimovigに支払う特許使用料は116百万ドルとドル139販売コストはそれぞれ総合損益表の販売コストに記入する。2022年12月31日、2021年、2020年12月31日までの年間で、ノワールがAimovigに支払うべき特許権使用料は重要ではない。
京華麒麟株式会社
2021年7月30日、我々はKKCとの協力および許可協定を終了し、世界的に(日本を除く)OX 40全人モノマブに対する抗OX 40全ヒトモノクロナル抗体であるロカトリアムモノクロナル抗体を共同開発し、商業化した。Rocatinlimabはアトピー性皮膚炎の治療に応用され、他の自己免疫性疾患を治療する潜在力がある。
合意条項によると、私たちは日本以外のグローバルロカルチリムの開発、製造、商業化をリードしている。KKCは安進社と米国でロカチリム·モノクロナル·抗体を共同で普及させ、欧州とアジアを含めて米国以外の様々な市場でロカチリム·モノクロナル·抗体を共同で普及させる権利がある。
前払いしました4002021年第3四半期に確認されたKKC研究開発費は100万ドル。安進とKKCは世界開発コスト(日本を除く)と米国の商業化コストを平均的に分担している。米国や日本以外では、KKCによるいかなる商業化費用も安進によって精算される。$までのマイルストーンの支払いを要求されるかもしれません850百万ドルは、特定の規制事件と商業的限界の達成にかかっている。日本以外の世界で販売されている2桁の印税もKKCに支払います。2022年12月31日および2021年12月31日までに,KKCからKKCへの純コストの回収および対応は大きなものではない。
他にも
以上で議論した連携以外にも様々な連携があり,これらの連携は現在のところ我々の業務にとって重要ではない.これらの協定の条項によると、私たちは追加金額の支払いを要求されるかもしれないし、様々な開発やビジネスマイルストーンを実現する際に追加金額を得ることができるかもしれません。これらの開発と商業マイルストーンの合計は巨大かもしれません。もし関連する候補製品が後期臨床試験に入ったら、私たちはまた巨額の研究開発コストを発生或いは清算している可能性がある。また、これらの協力に関連する任意の製品が販売を許可されれば、大量の印税の支払いを要求されるかもしれませんし、将来の販売で大量の印税を受ける可能性があります。しかしながら、これらの額の支払いは、様々な未来のイベントの発生に依存し、これらのイベントは高い不確実性を有する。
9. 投資する
売却可能な投資
証券タイプ別に販売可能な有利子証券の償却コスト、未実現収益総額、未実現損失総額と公正価値は以下のとおりである(単位:百万)
| | | | | | | | | | | | | | | | | | | | | | | | | | |
| 2022年12月31日までの証券タイプ | | 償却する
コスト | | 毛収入
実現していない
利得 | | 毛収入
実現していない
損 | | 公平である
価値がある |
| アメリカ国庫券 | | $ | — | | | $ | — | | | $ | — | | | $ | — | |
| アメリカ国庫券 | | 1,676 | | | — | | | — | | | 1,676 | |
| | | | | | | | |
| | | | | | | | |
| | | | | | | | |
| | | | | | | | |
| | | | | | | | |
| | | | | | | | |
| 貨幣市場共同基金 | | 2,659 | | | — | | | — | | | 2,659 | |
| 他の短期利上げ証券 | | — | | | — | | | — | | | — | |
| 売却可能投資総額 | | $ | 4,335 | | | $ | — | | | $ | — | | | $ | 4,335 | |
| | | | | | | | | | | | | | | | | | | | | | | | | | |
| 2021年12月31日現在の証券タイプ | | 償却する
コスト | | 毛収入
実現していない
利得 | | 毛収入
実現していない
損 | | 公平である
価値がある |
| アメリカ国庫券 | | $ | 47 | | | $ | — | | | $ | — | | | $ | 47 | |
| アメリカ国庫券 | | 1,400 | | | — | | | — | | | 1,400 | |
| | | | | | | | |
| | | | | | | | |
| | | | | | | | |
| | | | | | | | |
| | | | | | | | |
| | | | | | | | |
| 貨幣市場共同基金 | | 5,856 | | | — | | | — | | | 5,856 | |
| 他の短期利上げ証券 | | 1 | | | — | | | — | | | 1 | |
| | | | | | | | |
| | | | | | | | |
| 売却可能投資総額 | | $ | 7,304 | | | $ | — | | | $ | — | | | $ | 7,304 | |
総合貸借対照表における場所別の売却可能な投資の公正価値は以下のとおりである(百万単位)
| | | | | | | | | | | | | | |
| | 十二月三十一日 |
| 連結貸借対照表位置 | | 2022 | | 2021 |
| 現金と現金等価物 | | $ | 2,659 | | | $ | 7,256 | |
| 有価証券 | | 1,676 | | | 48 | |
| | | | |
| 売却可能投資総額 | | $ | 4,335 | | | $ | 7,304 | |
上の表の現金と現金等価物には銀行口座現金#ドルは含まれていません4,970百万ドルとドル733それぞれ2022年12月31日と2021年12月31日まで。
2022年12月31日と2021年12月31日までのすべての利上げ証券が1年以下の期間で満期となる。
2022年、2021年、2020年12月31日までの年間で、利上げ証券の実現損益は重要ではない。計上証券の実現済み収益と損失は合併損益表に他(費用)収入純額を記入する。証券を売るコストは特定の識別方法に基づいている。
私たちのポートフォリオの主な目標は、元本の安全性、慎重な流動性レベル、許容可能なリスクレベルを維持することだ。我々の投資政策は、投資レベルの信用格付けを有する機関が発行するいくつかのタイプの債務や通貨市場ツールに証券投資を制限し、資産種別および発行者に応じて期限と集中度を制限する。
株式証券
私たちは公正な価値が確定しやすい株式証券投資(上場取引証券)を持っている共$480百万ドルとドル611連結貸借対照表には、2022年12月31日現在、2021年12月31日現在、それぞれ他の非流動資産が含まれている。2022年、2021年、2020年12月31日までの年度、上場取引証券の未実現純収益と純損失は#ドルの赤字となった165百万ドルの収益は$です161百万ドルとドル174それぞれ100万ドルです2022年12月31日,2021年,2020年12月31日までの年度では,上場証券の実現損益は重要ではない
私たちが持っている投資金額は$です233百万ドルとドル262他の非流動資産負債表に含まれる、2022年、2022年、2021年12月31日に公正価値が確定されていない権益証券統合貸借対照表のETS。12月31日までの年度20222020年には収益を引き上げ資産を処分して収益を実現します
これらの証券は重要ではない。2021年12月31日までの1年間、引き上げによる収益は152100万ドルでこれらの証券を処理する収益は$です41百万ドルです。2022年12月31日までに、当該等証券の帳簿価値を下方調整し$とする67百万ドルです。2021年12月31日と2020年12月31日までの数年間、引き下げ幅は大きくなかった。調整は観察可能な価格取引に基づいて行われる。
権益法投資
百済神州株式会社です。
2020年1月2日に20.5百済神州の%所有権を$で購入する2.8億ドルですその中で2.6当社の百済神州への株式投資は総合貸借対照表の他の非流動資産に計上されています。自分から2022年12月31日私たちは百済神州に重大な影響を与える能力があるため、私たちの株式投資は権益会計方法の下で計算します。百済神州に大きな影響を与えることができる要因については、付記1、重大会計政策の概要を参照されたい。買収した持分証券の公正価値は関連純資産の帳簿価値におけるわれわれの割合を上回っている百済神州セットは、価格は約1ドルです2.4十億ドルです♪the the the資本会計方法は、基本差が生じる項目の金額を決定して分配し、これらの項目の使用年数内にこれらの項目を償却することを要求する。この償却は、私たちが共有している百済神州の経営成果とともに、私たちの総合損益表の他の収入純額に計上されています。2020年第2四半期から、4分の1の借金が確認された。基礎差は有限年限無形資産、無期限年限無形資産、権益法営業権と関連繰延税金に分配される。限られた年限の無形資産は一定期間償却し,時間範囲は8至れり尽くせり15何年もです。
12月31日までの年間で2022, 2021 and 2020投資の帳簿価値から私たちが分担すべき百済神州の純損失$を差し引く394百万、$265百万ドルとドル229100万ドルで#ドルを償却しました190百万、$172百万ドルとドル109それぞれ100万ドルです二零二一年十二月三十一日及び二零二年十二月三十一日までに、私たちは帳簿価値を増加させます50百万ドルとドル569十二月三十一日までの年中、吾らは百済神州の追加株式を購入していなかった2022それは.また、12月31日までの年間では2022, 2021 and 2020帳簿価値が1ドル増加しました11百万、$265百万ドルとドル34それぞれ百済神州の他の株式取引の影響を受けている。
2022年12月31日と2021年12月31日まで、私たちの百済神州に対する所有権は約18.2%和18.4%です。2022年12月31日と2021年12月31日まで、百済神州への投資の帳簿価値は$2.210億ドル2.8それぞれ10億ドルです2022年12月31日と2021年12月31日まで、百済神州投資に対する公正価値は4.210億ドル5.1それぞれ10億ドルです2022年12月31日まで、百済神州での株式投資の帳簿価値は完全に回収できると信じています。この投資について百済神州との協力協定についての情報は、付記8、協力を参照されたい。
2023年1月30日から、百済神州取締役会メンバーに取締役を任命する権利を放棄した。私たちは百済神州に重大な影響を与えることができなくなったので、私たちは公正価値に基づいて私たちの株式投資を計上し、公正価値の変化は2023年第1四半期から収益を計上します。
Neumora治療会社
2021年9月30日には25.9個人持株会社Neumoraの%所有権、価格は$257百万ドルは、#ドルと引き換えに、総合貸借対照表の他の非流動資産に含まれています100百万の現金支払いと$157百万ドルの非現金対価格は、主に未来のサービスと関連がある。私たちの株式投資はNeumoraに重大な影響を与える能力を提供してくれたが、私たちは公正な価値オプションを選択して私たちの株式投資を計算した。公正価値選択により,投資の公正価値変動は報告期間ごとの収益で確認された。公正価値オプションは標的取引の経済性を最も反映していると考えられる。2022年12月31日までの1年間に追加収入を得ました10Neumoraの次の融資に参加することで100万の現金投資を得る。2022年12月31日と2021年12月31日まで、Neumoraにおける私たちの所有権は約24.9%和25.9%私たちの投資の公正価値は$です335百万ドルとドル220それぞれ100万ドルです12月31日までの年間で2022 and 2021, 私たちは純収益が#ドルであることを確認した105百万ドル純損失$37総合損益表における他の(費用)収入純額の公正価値変動にそれぞれ用いた。公正価値を決定する情報については,付記17,公正価値計量を参照されたい。
有限共同企業
私たちは限られた共同投資を持っていて、金額は$です249百万ドルとドル573連結貸借対照表には、2022年12月31日現在、2021年12月31日現在、それぞれ他の非流動資産が含まれている。これらの投資は主に初期段階にある生物技術会社の投資基金であり、権益会計方法を用いて入金し、実際の便宜策として、有限組合企業の持つ基礎投資の中で著者らが占める資産純資産値の割合シェアを用いて計量を行う。これらの投資は通常、対象資産の清算時に分配によって償還されることしかできない。2022年12月31日まで、今後数年間、これらの投資のための資金支援のない追加的な約束は187百万ドルです。2022年,2021年,2020年12月31日までに,我々の有限共同投資で確認した純損益は純損失$である284百万ドルの純収益は$です143百万ドルとドル241それぞれ100万ドルです
10. 棚卸しをする
在庫には以下の内容(百万単位)が含まれる
| | | | | | | | | | | |
| 十二月三十一日 |
| 2022 | | 2021 |
| 原料.原料 | $ | 828 | | | $ | 647 | |
| Oracle Work in Process | 3,098 | | | 2,367 | |
| 完成品 | 1,004 | | | 1,072 | |
| 総在庫 | $ | 4,930 | | | $ | 4,086 | |
11. 財産·工場·設備
不動産、工場、設備は以下の部分から構成されている(百万ドル)
| | | | | | | | | | | | | | | | | |
| | | 十二月三十一日 |
| 使用寿命(年単位) | | 2022 | | 2021 |
| 土地 | — | | $ | 292 | | | $ | 279 | |
| 建物と改善策 | 10-40 | | 4,201 | | | 4,028 | |
| 製造設備 | 8-12 | | 3,105 | | | 3,080 | |
| 実験室装置 | 8-12 | | 1,277 | | | 1,193 | |
| 固定設備 | 12 | | 2,478 | | | 2,402 | |
| 大文字ソフト | 3-5 | | 1,215 | | | 1,151 | |
| 他にも | 5-10 | | 929 | | | 862 | |
| 建設中の工事 | — | | 1,213 | | | 987 | |
| 財産·工場·設備の損失額 | | | 14,710 | | | 13,982 | |
| 減価償却累計と償却を差し引く | | | (9,283) | | | (8,798) | |
| 財産·工場·設備·純価値 | | | $ | 5,427 | | | $ | 5,184 | |
2022年,2021年,2020年12月31日までの年度内に,物件,建屋,設備に関する減価償却と償却費用$を確認した661百万、$644百万ドルとドル640それぞれ100万ドルです
地理情報
不動産、建屋、設備のある地理情報について、純額(長期資産)は以下のようになる(百万計)
| | | | | | | | | | | |
| | 十二月三十一日 |
| | 2022 | | 2021 |
| アメリカです。 | $ | 3,154 | | | $ | 2,801 | |
| プエルトリコ | 1,247 | | | 1,311 | |
| はい | 1,026 | | | 1,072 | |
| 財産·工場と設備を合計して純額 | $ | 5,427 | | | $ | 5,184 | |
12. 営業権とその他の無形資産
商誉
商誉帳簿金額の変動状況は以下の通り(単位:百万):
| | | | | | | | | | | |
| 十二月三十一日 |
| 2022 | | 2021 |
| 期初残高 | $ | 14,890 | | | $ | 14,689 | |
買収と資産剥離による営業権変動,純額(1) | 651 | | | 251 | |
| 貨幣換算調整 | (12) | | | (50) | |
| 期末残高 | $ | 15,529 | | | $ | 14,890 | |
____________
(1) 2022年、事業権の変化には、ChemoCentryxの買収による商標権の取得、Teneobioの買収時の資産純価、非戦略的Gensenta資産剥離の買収日の変化が含まれる。付記2、買収及び資産剥離を参照。
その他無形資産
他の無形資産には、以下のものが含まれる(単位:百万):
| | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | |
| 十二月三十一日 |
| | 2022 | | 2021 |
| | 毛収入
携帯する
金額 | | 積算
償却する | | その他無形資産
資産、純額 | | 毛収入
携帯する
金額 | | 積算
償却する | | その他無形資産
資産、純額 |
| 有限寿命無形資産: | | | | | | | | | | | |
| 開発済み製品-技術的権利 | $ | 29,028 | | | $ | (15,045) | | | $ | 13,983 | | | $ | 25,561 | | | $ | (12,769) | | | $ | 12,792 | |
| 許可権 | 3,864 | | | (3,123) | | | 741 | | | 3,807 | | | (2,973) | | | 834 | |
| マーケティングに関する権利 | 1,326 | | | (1,167) | | | 159 | | | 1,354 | | | (1,112) | | | 242 | |
| 研究開発技術権 | 1,378 | | | (1,190) | | | 188 | | | 1,377 | | | (1,133) | | | 244 | |
| 有限寿命無形資産総額 | 35,596 | | | (20,525) | | | 15,071 | | | 32,099 | | | (17,987) | | | 14,112 | |
| 無期限-生きている無形資産: | | | | | | | | | | | |
| 知的財産権研究開発 | 1,009 | | | — | | | 1,009 | | | 1,070 | | | — | | | 1,070 | |
| その他無形資産総額 | $ | 36,605 | | | $ | (20,525) | | | $ | 16,080 | | | $ | 33,169 | | | $ | (17,987) | | | $ | 15,182 | |
開発された製品技術権には,買収により得られた販売製品に関する権利が含まれている。ライセンス権は、主に、将来のマイルストーン、特許権使用料および利益共有支払いを得るために買収で取得された契約権、規制部門が製品の商業化に関連する第三者への支払いを承認するマイルストーン資本化支払い、および上場製品の特許権使用料義務に関連する前払いを含む。マーケティングに関連する権利は、主に販売および流通販売製品に関する権利を含む。研究開発技術権利は研究開発に使用される、将来代替用途のある技術と関係がある。製品技術を開発する権利には、ChemoCentryxを買収することで得られた資産が含まれる。知的財産権、研究開発技術権、許可権には、Teneobioの買収によって得られた資産が含まれている。付記2、買収及び資産剥離を参照。
知的財産権研究開発は、買収時に残りの技術リスクおよび/または必要な規制承認を受けていないために完成していない事業組合の形態で買収された研究開発プロジェクトを含む。すべての知的財産権研究開発プロジェクトには、候補製品の開発と商業化の適時と成功に関連する重大なリスクと不確定性が存在し、著者らは臨床試験データに基づいて安全性と有効性を確認する能力、必要な監督管理許可を得る能力、および予算コスト内でこれらの任務を成功させる能力を含む。規制部門の承認を得ずにヒト治療薬の販売は許可されておらず,この承認は臨床試験を完了し,候補製品が安全かつ有効であることを証明する必要がある。また、第三者支払者(政府医療計画や個人保険計画および競合製品の発売を含む)のカバー範囲や精算範囲は、製品が発生することができる収入に影響を与える。そのため、買収した知的財産権研究開発プロジェクトの最終実現価値(あれば)は、その推定の公正価値とは異なる可能性がある。著者らは毎年知的財産権研究開発プロジェクトの減値を審査し、発生した事件或いは状況の変化が帳簿価値が回収できない可能性があることを表明し、技術の実行可能性或いは監督管理の承認を確定した後に行う。
2022年,2021年,2020年12月31日までの年間で,有限寿命無形資産に関する償却を確認した2.6億ドルだ2.610億ドル2.8それぞれ10億ドルです無形資産の償却は主に総合損益表の販売コストに計上される。2023年12月31日、2024年12月31日、2025年12月31日、2026年12月31日、2027年12月31日、2025年12月31日、2025年12月31日、2026年12月31日、2027年12月31日、2025年12月31日、2025年12月31日、2025年12月31日、2025年12月31日、2025年12月31日、2025年12月31日、2025年12月31日、2027年12月31日、2025年12月31日、2025年12月31日、2025年12月31日、2025年12月31日、2025年12月31日、2026年12月31日、2027年12月31日の年度まで、有限寿命無形資産の総額を推定する2.8億ドルだ2.7億ドルだ2.5億ドルだ2.110億ドル2.1それぞれ10億ドルです
13. 賃貸借証書
私たちは主に研究開発、行政、商業活動に関連する施設と設備をレンタルします。リース期間が12ヶ月以下のリースは発生した費用に応じて総合貸借対照表に計上し、総合貸借対照表には計上しない。
ほとんどのレンタル契約には1つ以上の更新オプションが含まれており、更新条項はレンタル期間を延長することができます7年になるそれは.私たちはレンタル期間選択権を行使するかどうかを自ら決定する権利がある。しかも、私たちのいくつかのレンタル協定はインフレに応じて定期的にレンタル料を調整することを含む。私たちの賃貸契約には余剰価値保証もなければ、重大な制限や契約も含まれていない。私たちは特定の不動産を第三者に転貸する。私たちの転貸組合には、以前の研究開発と行政空間から得られた運営レンタルが含まれています。
次の表は私たちのレンタルに関する情報をまとめていますが、これらのレンタルは運営に分類されており、私たちの総合貸借対照表(百万単位)に含まれています
| | | | | | | | | | | | | | |
| | 十二月三十一日 |
| 連結貸借対照表位置 | | 2022 | | 2021 |
| 資産: | | | | |
| 他の非流動資産 | | $ | 579 | | | $ | 566 | |
| 負債: | | | | |
| 負債を計算すべきである | | $ | 156 | | | $ | 145 | |
| 他の非流動負債 | | 539 | | | 525 | |
| リース総負債 | | $ | 695 | | | $ | 670 | |
レンタル費用純額は以下のように構成されている(百万計)
| | | | | | | | | | | | | | | | | | | | |
| | 十二月三十一日までの年度 |
| レンタル料 | | 2022 | | 2021 | | 2020 |
運営中です(1) | | $ | 218 | | | $ | 237 | | | $ | 223 | |
| | | | | | |
| | | | | | |
| | | | | | |
| | | | | | |
| | | | | | |
| | | | | | |
| 転貸収入 | | (32) | | | (38) | | | (34) | |
| 賃貸純コスト合計 | | $ | 186 | | | $ | 199 | | | $ | 189 | |
____________
(1) 短期賃貸と可変賃貸コストを含め、2022年、2022年、2021年、2020年12月31日までの年間では重要ではない。
2022年12月31日までの賃貸負債満期日は以下の通り(単位:百万)
| | | | | | | | | | | | |
| 期日まで | | 金額 | | | | |
| 2023 | | $ | 172 | | | | | |
| 2024 | | 109 | | | | | |
| 2025 | | 80 | | | | | |
| 2026 | | 70 | | | | | |
| 2027 | | 64 | | | | | |
| その後… | | 286 | | | | | |
賃貸支払総額(1) | | 781 | | | | | |
| 計上された利息を差し引く | | (86) | | | | | |
| 賃貸負債現在価値 | | $ | 695 | | | | | |
____________
(1) 賃貸契約放棄を含む将来の賃貸料負担額#ドル90百万ドルです。将来の総賃貸料収入は$と予想されています76廃棄施設の転貸キャンセル不可と関連した100万ドル。
加重平均残存賃貸期間と加重平均割引率は以下のとおりである
| | | | | | | | | | | | | | |
| | | | 十二月三十一日 |
| | | | 2022 | | 2021 |
| 加重平均残存賃貸年限(年) | | | | 8.2 | | 8.3 |
| 加重平均割引率 | | | | 2.7 | % | | 2.5 | % |
私たちのレンタルに関する現金と非現金情報は以下の通りです(百万単位)
| | | | | | | | | | | | | | | | | | | | |
| | | | 十二月三十一日までの年度 |
| | | | 2022 | | 2021 | | 2020 |
| 賃貸負債に含まれる金額を計量するために支払う現金: | | | | | | | | |
| レンタル経営キャッシュフロー | | | | $ | 171 | | | $ | 190 | | | $ | 177 | |
| | | | | | | | |
| | | | | | | | |
| 賃貸義務と引き換えの純収益資産: | | | | | | | | |
| 賃貸借契約を経営する | | | | $ | 191 | | | $ | 340 | | | $ | 101 | |
| | | | | | | | |
2022年12月31日現在、レンタルを開始していない未割引の将来の賃貸支払い総額は重要ではない。
14. その他流動資産と負債
他の流動資産には以下の内容が含まれる(百万単位)
| | | | | | | | | | | |
| 十二月三十一日 |
| 2022 | | 2021 |
| 前払い費用 | $ | 1,204 | | | $ | 1,223 | |
| 企業パートナー売掛金 | 700 | | | 780 | |
| 税金を受け取るべきだ | 129 | | | 164 | |
| 他にも | 355 | | | 200 | |
| その他流動資産総額 | $ | 2,388 | | | $ | 2,367 | |
計算すべき負債は以下の部分からなる(単位:百万)
| | | | | | | | | | | |
| 十二月三十一日 |
| 2022 | | 2021 |
| 販売減額 | $ | 5,986 | | | $ | 5,174 | |
| 所得税に対処する | 1,195 | | | 701 | |
| 配当金に応じる | 1,137 | | | 1,083 | |
| 従業員補償と福祉 | 1,099 | | | 1,081 | |
| 販売返品準備金 | 548 | | | 542 | |
| 他にも | 2,559 | | | 2,150 | |
| 負債総額を計算すべきである | $ | 12,524 | | | $ | 10,731 | |
15. 融資手配
私たちの借金には以下のものが含まれています
| | | | | | | | | | | |
| 十二月三十一日 |
| 2022 | | 2021 |
0.41%スイスフラン7002023年満期のミリオン債券(0.41%2023年スイスフラン債券) | $ | 757 | | | $ | 767 | |
2.25% notes due 2023 (2.25% 2023 Notes) | 750 | | | 750 | |
3.625% notes due 2024 (3.625% 2024 Notes) | 1,400 | | | 1,400 | |
1.90% notes due 2025 (1.90% 2025 Notes) | 500 | | | 500 | |
3.125% notes due 2025 (3.125% 2025 Notes) | 1,000 | | | 1,000 | |
2.00% €7502026年満期の百万ユーロ債券(2.00%2026年ユーロ債券) | 803 | | | 853 | |
2.60% notes due 2026 (2.60% 2026 Notes) | 1,250 | | | 1,250 | |
5.50% £4752026年満期の百万ポンド債券(5.50%2026年ポンド債券) | 574 | | | 643 | |
2.20% notes due 2027 (2.20% 2027 Notes) | 1,724 | | | 1,750 | |
3.20% notes due 2027 (3.20% 2027 Notes) | 1,000 | | | 1,000 | |
1.65% notes due in 2028 (1.65% 2028 Notes) | 1,234 | | | 1,250 | |
3.00% notes due 2029 (3.00% 2029 Notes) | 750 | | | — | |
4.05% notes due 2029 (4.05% 2029 Notes) | 1,250 | | | — | |
4.00% £7002029年満期の百万ポンド債券(4.00%2029年ポンド債券) | 846 | | | 947 | |
2.45% notes due 2030 (2.45% 2030 Notes) | 1,250 | | | 1,250 | |
2.30% notes due 2031 (2.30% 2031 Notes) | 1,250 | | | 1,250 | |
2.00% notes due 2032 (2.00% 2032 Notes) | 1,051 | | | 1,250 | |
3.35% notes due 2032 (3.35% 2032 Notes) | 1,000 | | | — | |
4.20% notes due 2033 (4.20% 2033 Notes) | 750 | | | — | |
6.375% notes due 2037 (6.375% 2037 Notes) | 478 | | | 478 | |
6.90% notes due 2038 (6.90% 2038 Notes) | 254 | | | 254 | |
6.40% notes due 2039 (6.40% 2039 Notes) | 333 | | | 333 | |
3.15% notes due 2040 (3.15% 2040 Notes) | 2,000 | | | 2,000 | |
5.75% notes due 2040 (5.75% 2040 Notes) | 373 | | | 373 | |
2.80% notes due 2041 (2.80% 2041 Notes) | 1,110 | | | 1,150 | |
4.95% notes due 2041 (4.95% 2041 Notes) | 600 | | | 600 | |
5.15% notes due 2041 (5.15% 2041 Notes) | 729 | | | 729 | |
5.65% notes due 2042 (5.65% 2042 Notes) | 415 | | | 415 | |
5.375% notes due 2043 (5.375% 2043 Notes) | 185 | | | 185 | |
4.40% notes due 2045 (4.40% 2045 Notes) | 2,250 | | | 2,250 | |
4.563% notes due 2048 (4.563% 2048 Notes) | 1,415 | | | 1,415 | |
3.375% notes due 2050 (3.375% 2050 Notes) | 2,250 | | | 2,250 | |
4.663% notes due 2051 (4.663% 2051 Notes) | 3,541 | | | 3,541 | |
3.00% notes due 2052 (3.00% 2052 Notes) | 1,254 | | | 1,350 | |
4.20% notes due 2052 (4.20% 2052 Notes) | 1,000 | | | — | |
4.875% notes due 2053 (4.875% 2053 Notes) | 1,000 | | | — | |
2.77% notes due 2053 (2.77% 2053 Notes) | 940 | | | 940 | |
4.40% notes due 2062 (4.40% 2062 Notes) | 1,250 | | | — | |
| 2097年に満期となったその他の手形 | 100 | | | 100 | |
| 未償却債券割引、割増、発行コスト、純額 | (1,246) | | | (1,213) | |
| 公正価値調整 | (437) | | | 284 | |
| 他にも | 12 | | | 15 | |
| 債務総帳簿価値 | 38,945 | | | 33,309 | |
| 比較的小さな電流部分 | (1,591) | | | (87) | |
| 長期債務総額 | $ | 37,354 | | | $ | 33,222 | |
私たちのどの借金の実際の金利と額面金利の間に大きな差はありませんが4.563%2048メモ、4.663%2051チケットおよび2.77%2053年債、実質金利は6.3%, 5.6%和5.2%です。
私たちのすべての未償還手形の条項によると、2097年に満期になった他の手形を除いて、制御権変更トリガ事件が発生した場合、私たちは以下の価格に相当する価格でこれらの債務証券の全部または一部を購入する必要があるかもしれません101手形元金の%には計上利息と未払い利息が加算されます。しかも私たちの未返済手形は0.412023年のスイスフラン債券および2097年に満了した他の手形-私たちの選択に応じて随時償還することができます-償還手形の元金に、課税および未払い利息および全体金額を加えることができます。これは、手形条項によって定義されます。一部の償還可能な手形は、手形の満期日直前の指定された期間に償還された場合、全数金を支払う必要がない。これらの期間の範囲は1か月至れり尽くせり6か月成熟する前に。
債務発行
2022年、2021年、2020年12月31日までの年間で、以下の製品を通じて債務証券を発行しました
•2022年にはドルを発行しました7.010億ドルの債務があります750百万ドルの3.00% 2029 Notes, $1.2510億ドル4.05% 2029 Notes, $1.010億ドル3.35% 2032 Notes, $750百万ドルの4.20% 2033 Notes, $1.010億ドル4.20% 2052 Notes, $1.010億ドル4.875%2053ドルのチケットと額面1.2510億ドル4.40%2062メモ。♪the the the3.00%2029発行されたチケットは、環境への影響を低減するために、指定された基準に適合する合資格プロジェクトを支援します。
•2021年にはドルを発行しました5.010億ドルの債務があります1.2510億ドル1.65% 2028 Notes, $1.2510億ドル2.00% 2032 Notes, $1.1510億ドル2.80%2041ドルのチケットおよび$1.3510億ドル3.00% 2052 Notes.
•2020年にはドルを発行しました9.010億ドルの債務があります500百万ドルの1.90% 2025 Notes, $1.7510億ドル2.20% 2027 Notes, $1.2510億ドル2.45% 2030 Notes, $1.2510億ドル2.30% 2031 Notes, $2.010億ドル3.15%2040ドルのチケットと額面2.2510億ドル3.375% 2050 Notes.
債務が返済される
2022年には一部を買い戻しました2.20%2027メモ、1.65%2028メモ、2.00%2032メモ、2.80%2041チケットおよび3.00%2052債券、総原価$297百万ドルこれが1ドルの確認につながりました78総合損益表のその他(費用)収入に純額の債務弁済収益を記入する。
債務償還·償還
2022年、2021年、2020年12月31日までの年間で、債務返済/償還を行いました。具体的には以下の通りです
•In 2022, 違います。債務は既に償還された.
•2021年にはドルを償還しました4.2ユーロを含む数十億ドルの債務1.25元金総額(億ドル)1.4関連するクロスボーダー通貨交換決済時)1.25%2022年ユーロ債券、ドル500元金総額2.70%2022年手形、$1.5億ドルの元金総額2.65%2022年債および$750元金総額3.625%2022メモ。この紙幣の償還については$を支払いました24総合損益表の利息支出純額で100万ドルを確認し、関連する課税利息と未払い利息を加えた。
•2020年にはドルを返済·償還しました6.5満期返済を含む10億ドルの債務300元金総額4.50%2020年手形、$750元金総額2.125%2020年手形、$3002020年に満期になる百万ドルの利上げ債券とドル700元金総額2.20%2020年チケット。ドルの償還に関係しています900元金総額3.45%2020年手形、$1.0億元の元金総額4.10%2021年手形、$750まとめ元金残高1.85%2021年債券およびドル1.75億元の元金総額3.875%2021手形、合計$を支払いました96総合損益表の利息支出純額で100万ドルを確認し、関連する課税利息と未払い利息を加えた。
金利が入れ替わる
固定金利と変動金利債務の理想的な組合せを実現するために、我々が発行したいくつかの債務の固定金利利札を、それぞれの手形の有効期限内にLIBORに基づく変動利札に効率的に変換する金利交換契約を締結した。これらの金利交換契約は条件を満たし、公正価値ヘッジとして指定されている。
二零二一年十二月三十一日までに、私たちは金利スワップ契約を締結し、名義総金額は$です1.010億ドルに対して2.45%2030ドル債券および総額面$500百万ドルと2.30%2031個を付記します。償還と引き換えに3.625%2022上述したように、関連金利スワップ契約の名目合計金額は$です750100万人が中止されました
先に述べた2020年12月31日までの年度内にいくつかの手形を償還することについて、関連金利スワップ契約の総名目価値は#ドルである3.6510億人が中止されましたまた、金利は過去下位にあるため、2020年12月31日までの年間で、名目総金額がドルである金利スワップを終了しました5.210億ドルがヘッジされた3.625%2024ノート、2.60%2026ノート、4.663%2051注釈および部分3.625%2022手形および3.125%2025件のチケットによって#ドルが受信されました576百万の現金と取引相手の信用リスクを下げる。これらの契約が終了した後、私たちは直ちに新しい金利スワップ協定を締結しました。当時の金利は5.2元金は10億元の手形である.付記18、派生道具を参照。
2022年12月31日と2021年12月31日までに、金利交換契約を締結した手形の実金利とこれらの契約に関する名目金額は以下の通りです(百万ドル単位)
| | | | | | | | | | | |
| 備考 | | 名目金額 | 実利率 |
3.625%2024備考 | | $ | 1,400 | | Libor+3.2% |
3.125%2025ノート | | 1,000 | | Libor+1.8% |
2.60%2026ノート | | 1,250 | | Libor+1.8% |
2.45%2030ノート | | 1,000 | | Libor+1.0% |
2.30%2031備考 | | 500 | | Libor+0.8% |
4.663%2051備考 | | 1,500 | | Libor+4.1% |
| 名目総金額 | | $ | 6,650 | | |
債務交換
2020年には、ドルと引き換えに2037年から2043年までの未償還優先手形(総称して旧手形と総称する)を交換する非公開発行を完了した940新発行債券元金百万元2.77%2053チケット(交換要約)。
一連の古い債券ごとに以下の元本が有効に入札され、その後交換要約により抹消された(単位:百万)
| | | | | |
| 為替元金 |
6.375%2037付記 | $ | 74 | |
6.90%2038備考 | $ | 37 | |
6.40%2039備考 | $ | 133 | |
5.75%2040備考 | $ | 39 | |
5.15%2041備考 | $ | 245 | |
5.65%2042備考 | $ | 72 | |
5.375%2043備考 | $ | 76 | |
♪the the the2.77%2053は、交換された旧債券と比較して、債券は低い固定額面金利で利下げされるが、より後の満期日に高い元金を償還する必要がある。旧手形と旧手形との間の条項には他に大きな変更はない2.77%2053備考。交換要約については、$85古い手形所持者に100万ユーロ(現金対価)を支払った。
交換要約は債務修正に計上されるため、古い手形、現金対価格、ドルに関する繰延融資コストと割引264以下の項目に関する百万割引2.77%2053手形は、これらの新規発行手形の期限内に増加し、総合損益表に支払利息純額として記載されています。
クロス通貨交換
ある外貨建ての長期手形に関する外貨為替リスクをヘッジするために、クロス通貨スワップ契約を締結した。これらの契約の条項は効果的に私たちの利息支払いと元金を返済します0.412023年のスイスフラン債券2.00%2026ユーロ債券、5.50%2026ポンド紙幣と4.00%二零二九ポンドをユーロ、ポンド、スイスフランからドルに両替します。これらのクロス通貨交換契約はキャッシュフローヘッジとして指定されている。これらの契約条項に関する情報は、付記18、派生ツールを参照されたい。
償還と引き換えに1.25%2022ユーロ手形は、上で議論された、総名目金額がユーロであるクロス通貨スワップ契約に関連しています1.2510億人が中止されました
棚登録表と他の施設
2022年12月31日までに、最大$の発行を許可する商業手形計画があります2.5私たちの運営資金需要を満たすために、10億ドルの無担保商業手形。2022年と2021年12月31日までに違います。私たちの商業手形計画の下で返済されなかった金額。
2019年、私たちはドルを修正して再申告しました2.5一般企業用途または我々の商業手形計画としての流動性支援のために使用することができる10億銀団、無担保、循環信用協定。循環信用協定での承諾額は最大#ドル増加することができる750銀行の同意で100万ドルです合意側である各銀行の初期承諾期限は5年それは.この期限は最大で延長できます二つその他の内容1年制銀行が同意した場合。本協定の年間承諾料は0.1私たちの現在の信用評価によると、融資で使用されていない部分の割合。本循環信用協定は2022年12月に更なる改訂を行い、SOFRがロンドン銀行の同業解体を参考金利とし、その中の段階的淘汰或いは現有の指定参考金利が使用できない場合に後継金利を決定する規定に符合する。一般的に、私たちの現在の信用評価によると、私たちがこのローンの下で借りたどんな金額も利息(I)Sofr plusを受け取るだろう1.125%または(II)(A)銀団代理銀行基本商業ローン金利、(B)隔夜連邦基金金利プラスの最高者0.50% or (C) 1ヶ月のSofr追加する1.1%です。2022年と2021年12月31日までに違います。このローンの下で返済されていない金額があります。
2020年2月、私たちは米国証券取引委員会に棚上げ登録声明を提出し、金額不明の債務証券;普通株、優先株、債務証券、普通株、優先株または預託株式の権利証、普通株または優先株購入権、証券購入契約、証券購入単位、および預託株式を発行することを許可した。この保留登録声明によると、発行可能なすべての証券は時々発売することができ、発行条項は発行時に確定する。この棚登録声明は2023年2月に満了し、私たちの取締役会はそれの代わりに新しい棚登録声明を承認しました。
2022年12月、Horizonの買収が提案されたことについて、私たちは過渡的な信用協定と定期融資信用協定を締結し、借金総額を#ドルとした28.5十億ドルです。2022年12月31日までに違います。どんな合意にも基づいて、多くの資金が借りられた。付記2、買収及び資産剥離を参照。
私たちの特定の資金調達計画には非金融契約が含まれている。さらに、私たちの循環信用プロトコル、過渡的信用プロトコル、および定期融資プロトコルは、指定された最低利息カバー率、すなわち(I)総合純収入、利息支出、所得税支出、減価償却費用、償却費用、非常または非日常的費用、および他の非現金項目(総合EBITDA)~(Ii)の総合利息支出の合計を維持することを要求する財務契約を含み、各項目はそれぞれのプロトコルで定義され説明されている。2022年12月31日まで、私たちはこのような計画の下で適用されるすべての条約を遵守した。
債務契約満期日
2022年12月31日以降に満期となるすべての借入金の合計契約満期日は以下の通り(単位:百万)
| | | | | | | | |
| 期日まで | | 金額 |
| 2023 | | $ | 1,509 | |
| 2024 | | 1,400 | |
| 2025 | | 1,500 | |
| 2026 | | 2,627 | |
| 2027 | | 2,724 | |
| その後… | | 30,868 | |
| 合計する | | $ | 40,628 | |
利子コスト
利子コストは発生時に費用に計上され、当該利息が建設工事に関係していない限り、この場合、利息は資本化される。2022年12月31日現在、2021年と2020年12月31日までの年度資本化の利息コストは重要ではない。2022年、2021年、2020年12月31日までの毎年、支払う利息は、金利と通貨スワップ契約の継続的な影響を含めて#ドルです1.2十億ドルです。
16. 株主権益
株買い戻し計画
私たちの株式買い戻し計画の下で、取引日別に計算する活動は以下の通りです(百万単位)
| | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | |
| 十二月三十一日までの年度 |
| 2022 | | 2021 | | 2020 |
| 株 | | ドル | | 株 | | ドル | | 株 | | ドル |
| 第1四半期 | 24.6 | | | $ | 5,410 | | | 3.7 | | | $ | 865 | | | 4.3 | | | $ | 933 | |
| 第2四半期 | — | | | — | | | 6.5 | | | 1,592 | | | 2.6 | | | 591 | |
| 第3四半期 | 1.5 | | | 900 | | | 4.6 | | | 1,069 | | | 3.0 | | | 752 | |
| 第4四半期 | — | | | — | | | 6.9 | | | 1,461 | | | 5.3 | | | 1,221 | |
| 株買い戻し総額 | 26.1 | | | $ | 6,310 | | | 21.7 | | $ | 4,987 | | | 15.2 | | $ | 3,497 | |
2022年第1四半期、当社は第三者金融機関(トレーダー)とASR協定を締結し、これにより当社は総額#ドルを支払いました6.0ディーラーに10億ドルを支払い最初に退職しました23.3取引業者からの百万株会社普通株。このような支払いは#ドルを含む株主資本の減少として記録されている5.1累計赤字が10億ドル増加し,受け取った初期株の価値を反映している0.9追加実収資本が10億円減少したことは、取引業者がまだ納入しなければならない株の価値を反映している。2022年第3四半期にはまた増加しました1.5ASR協定により,取引業者から会社普通株の100万株を受け取り,最終和解となったため,ドル0.9第1期に記録された追加実収資本は10億元減少し、累積赤字に再分類された。全体的に、私たちは買い戻しました26.12022年12月31日までの年度内に、普通株式百万株を保有し、主に含まれている24.8ASR協定に基づいて受け取った百万株。
2022年10月、私たちの取締役会は私たちの株式買い戻し計画に基づいて追加的に$を増加させました2.4十億ドルです。2022年12月31日までにドル7.0私たちの株買い戻し計画によると、まだ10億ドルが利用可能だ
配当をする
私たちの取締役会は四半期配当金を1株当たり#ドルと発表した1.94, $1.76そして$1.60それぞれ、2022年、2021年、2020年の4四半期ごとに支払われる。
歴史的に見ると、我々は毎年12月に配当を発表し、配当金は次年度の第1四半期に支払い、3月、7月、10月に支払い、それぞれ同前期の第2四半期、第3四半期、第4四半期に支払う。また、取締役会は2022年12月12日に四半期現金配当金を#ドルと発表した2.13普通株1株は、2023年2月15日終値時点で登録されている全株主に2023年3月に支給される。
その他の総合損失を累計する
AOCIの構成は以下のとおりである(百万単位)
| | | | | | | | | | | | | | | | | | | | | | | | | | | | | |
| 外国.外国
貨幣
訳す | | キャッシュフロー
期日保証 | | 販売可能である
証券 | | 他にも | | AOCI |
| 2019年12月31日現在の残高 | $ | (718) | | | $ | 175 | | | $ | 22 | | | $ | (7) | | | $ | (528) | |
| 外貨換算調整 | 9 | | | — | | | — | | | — | | | 9 | |
| 未達成収益 | — | | | (61) | | | 6 | | | — | | | (55) | |
| 収入の再分類調整 | — | | | (501) | | | (33) | | | — | | | (534) | |
| その他の損失 | — | | | — | | | — | | | (7) | | | (7) | |
| 所得税 | — | | | 124 | | | 6 | | | — | | | 130 | |
| 2020年12月31日の残高 | (709) | | | (263) | | | 1 | | | (14) | | | (985) | |
| | | | | | | | | |
| 外貨換算調整 | (135) | | | — | | | — | | | — | | | (135) | |
| 未達成収益 | — | | | 159 | | | (1) | | | — | | | 158 | |
| 収入の再分類調整 | — | | | 253 | | | — | | | — | | | 253 | |
| その他の収益 | — | | | — | | | — | | | 1 | | | 1 | |
| 所得税 | — | | | (88) | | | — | | | — | | | (88) | |
| 2021年12月31日現在の残高 | (844) | | | 61 | | | — | | | (13) | | | (796) | |
| | | | | | | | | |
| 外貨換算調整 | 496 | | | — | | | — | | | — | | | 496 | |
| 未実現収益 | — | | | 84 | | | — | | | — | | | 84 | |
| 収入の再分類調整 | — | | | 2 | | | — | | | — | | | 2 | |
| その他の収益 | — | | | — | | | — | | | 2 | | | 2 | |
| 所得税 | — | | | (19) | | | — | | | — | | | (19) | |
| 2022年12月31日現在の残高 | $ | (348) | | | $ | 128 | | | $ | — | | | $ | (11) | | | $ | (231) | |
上表については,損益を実現していない所得税支出や利益およびキャッシュフローヘッジ収入に関する再分類を#ドルに調整した19100万ドルの支出と0百万2022年の支出は1ドルです33100万ドルの支出と552021年の支出は100万ドルです14百万ドルの収益と1102020年にはそれぞれ100万人が利益を得る。損益を達成していない所得税支出または利益、および売却可能な証券収入に関する再分類を#ドルに調整する1100万ドルの支出と72020年にはそれぞれ100万人が利益を得る。
AOCIから収入への再分類は以下のとおりである(百万単位)
| | | | | | | | | | | | | | | | | | | | | | | | | | |
| | 十二月三十一日までの年度 | | |
| AOCIの構成要素は | | 2022 | | 2021 | | 2020 | | 合併収入地点報告書 |
| キャッシュフローのヘッジ: | | | | | | | | |
| 外貨契約損益 | | $ | 231 | | | $ | (8) | | | $ | 178 | | | 製品販売 |
| クロスマネースワップ契約収益 | | (233) | | | (245) | | | 323 | | | その他の収入,純額 |
| | | | | | | | |
| | (2) | | | (253) | | | 501 | | | 所得税前収入 |
| | — | | | 55 | | | (110) | | | 所得税支給 |
| | $ | (2) | | | $ | (198) | | | $ | 391 | | | 純収入 |
| 販売可能な証券: | | | | | | | | |
| 純収益を実現した | | $ | — | | | $ | — | | | $ | 33 | | | その他の収入,純額 |
| | — | | | — | | | (7) | | | 所得税支給 |
| | $ | — | | | $ | — | | | $ | 26 | | | 純収入 |
他にも
普通株式以外に、私たちの法定資本はまた5百万株優先株、$0.0001額面価値。2022年と2021年12月31日までに違います。優先株は発行されたか発行された。
17. 公正価値計量
私たちの金融資産と負債の公正な価値を推定するために、観察可能な投入が利用可能なときに観察可能な投入を使用することによって、観察可能な投入を最大化し、観察できない投入を最大限に削減することを要求する階層構造において推定方法を使用する。観察できる投入は,市場参加者が当社以外のソースから得られた市場データに基づいて資産や負債を定価する際に使用する投入である。観察できない投入は、市場参加者が資産や負債の価格設定のために使用されるという会社の仮定を反映し、その時点で入手可能な最適な情報に基づいて制定される。公正価値レベルは投入源によって3つの階層に分けられ、以下のようになる
| | | | | | | | |
| レベル1 | — | 企業が取得する能力のある同じ資産または負債の活発な市場での未調整見積もりに基づいて評価する |
| レベル2 | — | すべての重要な投入は直接あるいは間接的に観察できる推定値であるレベル1投入は除外した |
| レベル3 | — | 観察不可能かつ全体的な公正価値計測に重大な意義のある投入に基づく推定値 |
観察可能な投入の可獲得性は金融資産と負債によって異なる。ある程度、推定値は市場で観察または観察できないモデルや投入に基づいており、公正価値の決定にはより多くの判断が必要である。場合によっては、公正価値を計量するための投入は、公正価値レベルの異なるレベルに属する可能性がある。この場合、財務諸表開示の目的で、公正価値計量に基づく公正価値レベルにおけるレベルは、全体の公正価値計量に重要な最低投入レベルに基づく。
公正価値によって恒常的に計量される会社の各主要金融資産と負債の公正価値は以下のとおりである(百万単位)
| | | | | | | | | | | | | | | | | | | | | | | | | | |
2022年12月31日までの公正価値計測、使用: | | 見積もりはありますか
活発な市場
同じ資産
(レベル1) | | 大切な他の人
観察できるのは
入力
(レベル2) | | 意味が重大である
見えない
入力
(レベル3) | | 合計する |
| 資産: | | | | | | | | |
| 販売可能な証券: | | | | | | | | |
| アメリカ国庫券 | | $ | — | | | $ | — | | | $ | — | | | $ | — | |
| アメリカ国庫券 | | 1,676 | | | — | | | — | | | 1,676 | |
| | | | | | | | |
| | | | | | | | |
| | | | | | | | |
| | | | | | | | |
| | | | | | | | |
| | | | | | | | |
| 貨幣市場共同基金 | | 2,659 | | | — | | | — | | | 2,659 | |
| 他の短期利上げ証券 | | — | | | — | | | — | | | — | |
| その他の投資 | | — | | | 130 | | | — | | | 130 | |
| 株式証券 | | 480 | | | — | | | 335 | | | 815 | |
| 派生商品: | | | | | | | | |
| 外貨長期契約 | | — | | | 287 | | | — | | | 287 | |
| クロス通貨交換契約 | | — | | | 54 | | | — | | | 54 | |
| 金利交換契約 | | — | | | — | | | — | | | — | |
| 総資産 | | $ | 4,815 | | | $ | 471 | | | $ | 335 | | | $ | 5,621 | |
| 負債: | | | | | | | | |
| 派生商品: | | | | | | | | |
| 外貨長期契約 | | $ | — | | | $ | 76 | | | $ | — | | | $ | 76 | |
| クロス通貨交換契約 | | — | | | 541 | | | — | | | 541 | |
| 金利交換契約 | | — | | | 776 | | | — | | | 776 | |
| 長期金利契約 | | — | | | 5 | | | — | | | 5 | |
対価格債務があります | | — | | | — | | | 270 | | | 270 | |
| 総負債 | | $ | — | | | $ | 1,398 | | | $ | 270 | | | $ | 1,668 | |
| | | | | | | | | | | | | | | | | | | | | | | | | | |
2021年12月31日までの公正価値計測、使用: | | 見積もりはありますか
活発な市場
同じ資産
(レベル1) | | 大切な他の人
観察できるのは
入力
(レベル2) | | 意味が重大である
見えない
入力
(レベル3) | | 合計する |
| 資産: | | | | | | | | |
| 販売可能な証券: | | | | | | | | |
| アメリカ国庫券 | | $ | 47 | | | $ | — | | | $ | — | | | $ | 47 | |
| アメリカ国庫券 | | 1,400 | | | — | | | — | | | 1,400 | |
| | | | | | | | |
| | | | | | | | |
| | | | | | | | |
| | | | | | | | |
| | | | | | | | |
| | | | | | | | |
| 貨幣市場共同基金 | | 5,856 | | | — | | | — | | | 5,856 | |
| 他の短期利上げ証券 | | — | | | 1 | | | — | | | 1 | |
| その他の投資 | | — | | | — | | | — | | | — | |
| 株式証券 | | 611 | | | — | | | 220 | | | 831 | |
| 派生商品: | | | | | | | | |
| 外貨長期契約 | | — | | | 183 | | | — | | | 183 | |
| クロス通貨交換契約 | | — | | | 66 | | | — | | | 66 | |
| 金利交換契約 | | — | | | 16 | | | — | | | 16 | |
| 総資産 | | $ | 7,914 | | | $ | 266 | | | $ | 220 | | | $ | 8,400 | |
| 負債: | | | | | | | | |
| 派生商品: | | | | | | | | |
| 外貨長期契約 | | $ | — | | | $ | 39 | | | $ | — | | | $ | 39 | |
| クロス通貨交換契約 | | — | | | 339 | | | — | | | 339 | |
| 金利交換契約 | | — | | | 156 | | | — | | | 156 | |
| 長期金利契約 | | — | | | — | | | — | | | — | |
| 対価格債務があります | | — | | | — | | | 342 | | | 342 | |
| 総負債 | | $ | — | | | $ | 534 | | | $ | 342 | | | $ | 876 | |
利上げ証券と持分証券
我々の米国債、通貨市場共同基金、公開取引証券の株式投資の公正価値は、活発な市場のオファーに基づいており、推定調整は行われていない。その他の投資には、償却コスト値に応じた利息預金が含まれており、その最近の満期日を考慮すると、償却コストは公正な価値に近い。公正価値オプションを選択した権益証券の公正価値は、最初に取引価格で推定され、その後、観察可能な価格取引(例えば、あり)、市場表現及び取引権益証券を活発に取引する類似会社の公開市場情報に基づいて推定される。付記9、投資-Neumora治療会社
派生商品
私たちの外貨長期契約、クロス通貨スワップ契約、金利スワップ契約の取引相手の最低信用格付けはA-または標準プール、ムーディーズまたはホイホマレの同等の格付けを獲得します。これらの契約の公正価値を推定する際には、収入に基づく業界標準推定モデルを採用し、そのすべての重要な投入を直接または間接的に観察できる第三者推定サービスから得られる推定値を考慮する。適用されれば、これらの入力には外貨為替レート、ロンドン銀行の同業借り換え金利、スワップ金利、債務者信用違約スワップ金利とクロスマネーベースのスワップ利差が含まれる。適用の場合,ある入力は通常参照の間隔で行われる.付記18、派生道具を参照。
対価格債務があります
私たちの業務買収により、以下に述べるように対価格義務が生じたか、またはあります。または有価負債が確率調整された割引現金流量を用いてその公正価値で入金されている場合には、関連または事項が解決されるまで、報告期間毎にその負債を再推定する。これらの債務の公正価値計測は、商業合併で得られた許可権と候補製品に関する重大な観察不可能な入力に基づいており、四半期ごとに我々の研究開発および商業販売組織の経営陣が審査を行う。これらの投入には、適用されるように、推定の可能性と、特定の開発、規制および商業マイルストーンを実現する時期、および推定された年間売上高が含まれる。このような投入の重大な変化は債務の公正な価値を適切に増加または減少させるだろう。または対価債務のある公正価値変動は、合併損益表の他の業務費用で確認される。
または対価格債務のある帳簿金額の変動状況は以下の通りである(百万で計算)
| | | | | | | | | | | | | | | | | | | | |
| | 十二月三十一日までの年度 |
| | 2022 | | 2021 | | 2020 |
| 期初残高 | | $ | 342 | | | $ | 33 | | | $ | 61 | |
| 足し算 | | — | | | 309 | | | — | |
| 支払い | | (7) | | | (7) | | | (6) | |
| 評価純変動 | | (65) | | | 7 | | | (22) | |
| 期末残高 | | $ | 270 | | | $ | 342 | | | $ | 33 | |
2021年にTeneobioを買収したため、私たちはその前の株主に最高$を支払う義務があります1.610億ドルで、様々な研究開発計画の面で単独の開発と規制マイルストーンを実現した。付記2、買収及び資産剥離を参照。
2018年にK-Aを買収したため、Brodalabの販売に応じて麒麟ホールディングスに1桁の特許権使用料を支払う義務がある。
2011年にBioVex Group Inc.を買収したため、何らかの販売限界に達した場合には、イリッジに関する単独販売マイルストーンを実現する際に前株主に支払う義務がある。二零年十二月三十一日までの年間で、私たちはこれらのマイルストーンを達成する可能性がないと考え、債務を売却した。
他の金融商品の公正価値の概要
現金等価物
このような金融商品の短期的な性質により、現金等価物の公正価値はその帳簿価値に近い。
借金をする
私たちは二次投入を使用して借金の公正な価値を推定した。2022年12月31日と2021年12月31日まで、私たちの借金の総公正価値は#ドルです35.010億ドル37.9それぞれ10億ドルで帳簿価値は38.910億ドル33.3それぞれ10億ドルです
百済神州に投資する
百済神州への投資の公正価値を1級投入を用いて試算した。2022年12月31日と2021年12月31日までの公正価値は4.210億ドル5.110億ドル帳簿価値は$2.210億ドル2.8それぞれ10億ドルです
2022年12月31日及び2021年12月31日までの年度まで、公正価値計量レベルの間に資産或いは負債移転がなく、公正価値ではなく恒常的に計量された資産と負債の公正価値に対して重大な再計量を行うこともない。
18. 派生ツール
当社はその業務運営に関する外貨為替レートと金利リスクに直面しています。このようなリスクに関連するリスクを低減するために、私たちは、外貨長期、外貨オプション、クロス通貨スワップ、長期金利、および金利スワップ契約を含むいくつかの派生ツールを使用または使用している。私たちはいくつかのデリバティブをキャッシュフローと公正価値ヘッジに指定しました;私たちはヘッジに指定されていないデリバティブもあります。私たちは投機取引目的に派生商品を使用しないつもりだ。
キャッシュフローヘッジ
主にユーロ建ての国際製品販売に関連する外貨為替レートの変化により、私たちはいくつかの予想外貨キャッシュフローの価値変化の影響を受けるかもしれません。私どもの国際製品販売の現金流入に関する外貨レート変動リスク部分は私たちの国際運営費用に応じた現金流出によって相殺されます。このリスクをさらに減らすために、私たちは私たちが予想している国際製品の売上の一部をヘッジするために、外貨長期契約を締結しました3年任意の所与の時点において、最近予想される製品販売のヘッジパーセンテージは、連続するいくつかの期間よりも高い。
2022年12月31日、2021年12月31日、2020年12月31日まで、私たちは外貨未返済長期契約を持っており、名目総金額は#ドルです6.0億ドルだ5.710億ドル5.1それぞれ10億ドルです私たちはこれらの主にユーロに基づく外貨長期契約をキャッシュフローヘッジとして指定した。そこで,これらの契約の未実現損益を総合貸借対照表中のAOCIで報告し,ヘッジ取引影響収益の同時期に総合収益表における製品販売に再分類した.
ある外貨建ての長期債務に関する外貨為替リスクをヘッジするために、クロス通貨スワップ契約を締結した。このような契約の条項によると、私たちは契約開始時にユーロ、ポンド、スイスフランを支払い、ドルを受け取りました。これらの名義金額に基づいて、私たちはドルを支払うことによって、ユーロ、ポンド、スイスフランを獲得し、契約の有効期間内に固定金利で利息を交換して支払います。また、契約満期日に同じ名目金額で取引相手にドルを支払い、取引相手からユーロ、ポンド、スイスフランを得る。これらの契約の条項は、関連するヘッジ債務に対応し、債務の利息支払いおよび元金返済をユーロ、ポンド、スイスフランからドルに効率的に変換する。私たちはこのような交差通貨スワップ契約をキャッシュフローヘッジとして指定した。そこで,これらの契約の未実現収益と損失は合併貸借対照表のAOCIで報告され,ヘッジ債務が収益に影響する同時期の連結損益表では他(費用)収入純額に再分類される.
2022年12月31日現在、クロスマネースワップの名目金額と金利は以下の通りです(名目金額は百万単位)
| | | | | | | | | | | | | | | | | | | | | | | | | | |
| | 外貨?外貨 | | ドル |
| 期限付き手形 | | 名目金額 | | 金利.金利 | | 名目金額 | | 金利.金利 |
| | | | | | | | |
| 0.41%2023年スイスフラン債券 | | CHF | 700 | | | 0.4 | % | | $ | 704 | | | 3.4 | % |
| 2.00%2026年ユーロ債券 | | € | 750 | | | 2.0 | % | | $ | 833 | | | 3.9 | % |
| 5.50%2026ポンド紙幣 | | £ | 475 | | | 5.5 | % | | $ | 747 | | | 6.0 | % |
| 4.00%2029ポンド紙幣 | | £ | 700 | | | 4.0 | % | | $ | 1,111 | | | 4.6 | % |
発行が予想される長期固定金利債務については、これらの契約を締結してから関連債務を発行するまでの間、適用される米国債の金利変化によるキャッシュフローの変化をヘッジするための長期金利契約を締結することが多い。長期金利契約の収益と損失はキャッシュフローヘッジに指定され,総合貸借対照表ではAOCIと確認され,関連債務発行期間の総合収益表では利子支出純額として償却される。2022年12月、私たちは長期金利契約を締結し、名義総金額は#ドルです700百万ドルです。その後12カ月以内に長期金利契約について確認されると予想される金額は重大ではない。
AOCIで確認されたキャッシュフローヘッジに指定されたデリバティブの未実現収益と損失は以下のとおりである(百万単位)
| | | | | | | | | | | | | | | | | | | | | | | | | | |
| | | | 十二月三十一日までの年度 |
| キャッシュフロー対沖関係におけるデリバティブ | | | | 2022 | | 2021 | | 2020 |
| 外貨長期契約 | | | | $ | 308 | | | $ | 373 | | | $ | (251) | |
| クロス通貨交換契約 | | | | (219) | | | (214) | | | 190 | |
| 長期金利契約 | | | | (5) | | | — | | | — | |
| 未達成収益の合計 | | | | $ | 84 | | | $ | 159 | | | $ | (61) | |
公正価値ヘッジ
固定金利と変動金利債務の理想的な組み合わせを実現するために、公正価値ヘッジ条件に適合し、公正価値ヘッジに指定された金利交換契約を締結した。これらの金利交換契約は、固定金利チケットをLIBORによる変動金利チケットに効果的に変換し、関連ヘッジ契約の条項を超える。2022年12月31日と2021年12月31日まで、名目総金額1ドルの金利スワップ契約を持っています6.7私たちの長期債務発行のいくつかの部分をヘッジした10億ドル。金利スワップに関する資料は、付記15、融資手配を参照してください。
公正価値ヘッジ資格に適合し、公正価値ヘッジに指定された金利スワップ契約について、著者らは総合収益表の利息支出純額の中で、期間内に公正価値変動による派生ツールが収益或いは損失を実現していないことを確認し、ヘッジプロジェクトがヘッジリスクによる公平価値変動による相殺未実現損失或いは収益を実現しなかった。金利交換契約に関する裁定関係が終了した場合、契約終了時に実現される収益または損失は、債務帳簿価値の調整として記録され、以前にヘッジされた債務の残存寿命内に利息支出純額として償却される。
これらの負債の満期負債及びその公正価値ヘッジに関する累積ベース調整は、総合貸借対照表に以下のように入金される(百万計)
| | | | | | | | | | | | | | | | | | | | | | | | | | |
| | 帳簿金額 ヘッジ負債(1) | | ヘッジ負債帳簿金額に関する公正価値ヘッジ調整累計金額(2) |
| | 十二月三十一日 | | 十二月三十一日 |
| 連結貸借対照表位置 | | 2022 | | 2021 | | 2022 | | 2021 |
| 長期債務の当期部分 | | $ | 82 | | | $ | 85 | | | $ | 82 | | | $ | 85 | |
| 長期債務 | | $ | 6,017 | | | $ | 6,729 | | | $ | (519) | | | $ | 199 | |
____________
(1)長期債務の当期部分は#ドルを含む82百万ドルとドル85それぞれ2022年、2022年、2021年12月31日にヘッジ関係を終了した帳簿価値は百万ドルである。長期債務は#ドルを含む357百万ドルとドル440それぞれ2022年、2022年、2021年12月31日にヘッジ関係を終了した帳簿価値は百万ドルである。
(2)長期債務の当期部分は#ドルを含む82百万ドルとドル852022年12月31日と2021年12月31日までに,終了したヘッジ関係をそれぞれ100万回のヘッジ調整を行った。長期債務は#ドルを含む257百万ドルとドル3402022年12月31日と2021年12月31日までに,終了したヘッジ関係をそれぞれ100万回のヘッジ調整を行った。
再取引の影響
下表は、中止のヘッジ関係(百万単位)を含む収入と支出内訳に記録されている金額および公正価値とキャッシュフローのヘッジの影響をまとめた
| | | | | | | | | | | | | | | | | | | | |
| | 2022年12月31日までの年度 |
| | 製品販売 | | その他の収入,純額 | | 利子支出,純額 |
| 総合損益表列報の収入と行項目に記録された総金額 | | $ | 24,801 | | | $ | (814) | | | $ | (1,406) | |
| キャッシュフローと公正価値ヘッジの影響: | | | | | | |
| キャッシュフローヘッジリッジ関係の収益(損失)AOCIから再分類: | | | | | | |
| 外貨長期契約 | | $ | 231 | | | $ | — | | | $ | — | |
| クロス通貨交換契約 | | $ | — | | | $ | (233) | | | $ | — | |
| 公正価値ヘッジ関係の収益(損失)−金利交換協定: | | | | | | |
期日保証項目(1) | | $ | — | | | $ | — | | | $ | 716 | |
| ヘッジツールとして指定された派生ツール | | $ | — | | | $ | — | | | $ | (636) | |
| | | | | | | | | | | | | | | | | | | | |
| | 2021年12月31日までの年度 |
| | 製品販売 | | その他の収入,純額 | | 利子支出,純額 |
| 総合損益表列報の収入と行項目に記録された総金額 | | $ | 24,297 | | | $ | 259 | | | $ | (1,197) | |
| キャッシュフローと公正価値ヘッジの影響: | | | | | | |
| キャッシュフロー対沖関係損失はAOCIに再分類される: | | | | | | |
| 外貨長期契約 | | $ | (8) | | | $ | — | | | $ | — | |
| クロス通貨交換契約 | | $ | — | | | $ | (245) | | | $ | — | |
| 公正価値ヘッジ関係の収益(損失)−金利交換協定: | | | | | | |
期日保証項目(1) | | $ | — | | | $ | — | | | $ | 281 | |
| ヘッジツールとして指定された派生ツール | | $ | — | | | $ | — | | | $ | (192) | |
| | | | | | | | | | | | | | | | | | | | |
| | 2020年12月31日までの年度 |
| | 製品販売 | | その他の収入,純額 | | 利子支出,純額 |
| 総合損益表列報の収入と行項目に記録された総金額 | | $ | 24,240 | | | $ | 256 | | | $ | (1,262) | |
| キャッシュフローと公正価値ヘッジの影響: | | | | | | |
| キャッシュフローヘッジリッジ関係の報酬はAOCIに再分類される: | | | | | | |
| 外貨長期契約 | | $ | 178 | | | $ | — | | | $ | — | |
| クロス通貨交換契約 | | $ | — | | | $ | 323 | | | $ | — | |
| | | | | | |
| 公正価値ヘッジ関係の収益(損失)−金利交換協定: | | | | | | |
期日保証項目(1) | | $ | — | | | $ | — | | | $ | 315 | |
| ヘッジツールとして指定された派生ツール | | $ | — | | | $ | — | | | $ | (204) | |
__________
(1)満期プロジェクトの収益は、関連指定スリーブ期間ツールの損失を完全に相殺することができないが、これは、対沖関係のセット期間債務帳簿額面に含まれる公正価値セット期間調整累積金額の償却を終了することと、対応するセット期間項目が返済されたときにセット期間を終了する収益の確認によるものである。
私たちのキャッシュフローヘッジ契約のどの部分もヘッジ有効性の評価から除外されていません。2022年12月31日までに159今後12ヶ月間、私たちの外貨とクロス通貨スワップ契約の純収益はAOCIから収益に移行する
ヘッジデリバティブに指定されていない
外貨建ての資産や負債の中で外貨変動の影響を受けることを減らすために、ヘッジ取引に指定されていない外貨長期契約を締結しました。これらの開放口はたいてい月ごとにヘッジされている.2022年12月31日、2021年、2020年まで、これらの外貨長期契約の名目総金額は#ドルです517百万、$680百万ドルとドル1.0それぞれ10億ドルです2022年,2021年,2020年12月31日までの年間で,ヘッジツールに指定されていないデリバティブの収益のうち確認された収益や損失は重要ではない。
派生ツールの公正価値
総合貸借対照表における派生ツールの公正価値は以下のとおりである(百万単位)
| | | | | | | | | | | | | | | | | | | | | | | | | | |
| | | 派生資産 | | 派生負債 |
| 2022年12月31日 | | 連結貸借対照表位置 | | 公正価値 | | 連結貸借対照表位置 | | 公正価値 |
| ヘッジツールとして指定された派生ツール: | | | | | | | | |
| 外貨長期契約 | | その他流動資産/その他非流動資産 | | $ | 287 | | | 負債/その他非流動負債 | | $ | 76 | |
| クロス通貨交換契約 | | その他流動資産/その他非流動資産 | | 54 | | | 負債/その他非流動負債 | | 541 | |
金利交換契約 | | その他流動資産/その他非流動資産 | | — | | | 負債/その他非流動負債 | | 776 | |
| 長期金利契約 | | その他流動資産/その他非流動資産 | | — | | | 負債/その他非流動負債 | | 5 | |
ヘッジツールに指定されたデリバティブ総額 | | | | 341 | | | | | 1,398 | |
| | | | | | | | |
| | | | | | | | |
| | | | | | | | |
| 総派生商品 | | | | $ | 341 | | | | | $ | 1,398 | |
| | | | | | | | |
| | | 派生資産 | | 派生負債 |
| 2021年12月31日 | | 連結貸借対照表位置 | | 公正価値 | | 連結貸借対照表位置 | | 公正価値 |
| ヘッジツールとして指定された派生ツール: | | | | | | | | |
| 外貨長期契約 | | その他流動資産/その他非流動資産 | | $ | 183 | | | 負債/その他非流動負債 | | $ | 39 | |
| クロス通貨交換契約 | | その他流動資産/その他非流動資産 | | 66 | | | 負債/その他非流動負債 | | 339 | |
金利交換契約 | | その他流動資産/その他非流動資産 | | 16 | | | 負債/その他非流動負債 | | 156 | |
| 長期金利契約 | | その他流動資産/その他非流動資産 | | — | | | 負債/その他非流動負債 | | — | |
ヘッジツールに指定されたデリバティブ総額 | | | | 265 | | | | | 534 | |
| | | | | | | | |
| | | | | | | | |
| | | | | | | | |
| 総派生商品 | | | | $ | 265 | | | | | $ | 534 | |
より多くの情報については、付記17、公正価値計量を参照されたい。
私たちが2022年12月31日までに負債状態にあるデリバティブ契約には、(I)私たちがコントロール権変更を経験し、(Ii)私たちまたは存続エンティティの信用が悪化する場合、通常、コントロール権変更後の信用格付けが投資レベルよりも低いか、信用状況が大幅に低下すると定義されるいくつかの信用リスクに関連する条項が含まれています。これらの事件が発生した場合、当事者には、事前終了条項に従って契約を終了する義務があるのではなく、権利があるだろう。この場合,相手側はこれらの契約の即時決済を要求することができ,金額は当時の契約の公正価値に近い.さらに、私たちの派生契約は、いかなるタイプの総純額決済スケジュールの制約を受けず、契約の下で対応または取引相手からのお金は、違約または終了事件が発生した場合にのみ、同じ取引相手からの他の金額を相殺することができる。
クロス通貨スワップ名義金額を決済する以外に、総合キャッシュフロー表では派生契約のキャッシュフローの影響はすでに経営活動が提供する現金純額に含まれており、クロス通貨スワップの名目金額は融資活動で使用される現金純額に含まれている。
19. あるいは事項と支払いがあります
事件があったり
正常な業務過程において、私たちは各種の法律手続き、政府調査、その他の性質が複雑で、結果が予測しにくい事項に関連している。第1部、第1 A項を参照。リスク要因-私たちの業務は訴訟と政府調査の影響を受けるかもしれない私たちはこの脚注で私たちの法的手続きと他の重要な事項、あるいは私たちが重要になる可能性があると思う事項を説明した。
負債が発生している可能性が高く、関連損失の金額を合理的に見積もることができると結論すれば、損失の計上項目を記録したり、損失したりする必要がある。私たちは、法律手続きの発展や他の以前に蓄積された負債額の増加または減少を招く可能性のある事項を四半期ごとに評価します。
私たちの法律手続きは、私たちの業務の様々な側面と様々なクレームに関連しており、その中のいくつかは斬新な事実告発および/または独特の法的理論を提出している。この文書に記載されているすべてのことの中で、私たちは責任を招く可能性があり、私たちの相手はまだ数量化されていない損害賠償金額または実質的な金額を賠償することを要求します。また、私たちが直面しているいくつかの未解決の問題はまだ法的手続きの非常に早い段階にあり、私たちが直面しているこのような複雑な手続きでは、法律手続きは数年続くことが多い。したがって,重要な事実情報や法的問題を発見および/または発展させることで,一連の可能な損失(あれば),あるいはそのような金額が実質的ではないことを見積もることができ,本文書に記載されている我々が責任を招く可能性のある事項は十分に進展していない.これらの事項の最終結果を正確に予測または決定することは不可能であるが、現在懸案されている1つまたは複数のそのような事項に対する不利な決定は、我々の総合的な運営結果、財務状態、またはキャッシュフローに重大な悪影響を及ぼす可能性がある。
以下は、私たちの法的手続きとその他の事項に関する最新の発展状況です
安達特許訴訟
Otezla Anda特許訴訟
安進、サントス社、などを訴えます。
Celgeneは2018年6月から19米国ニュージャージー州地域裁判所(ニュージャージー州地域裁判所)は、Alkem実験室株式会社(Alkem)、Amneal PharmPharmticals LLC(Amneal)、Annora Pharma Private Ltd.,Hetero USA Inc.(総称してHetero)、Aurobindo Pharma Ltd.,Aurobindo Pharma USA Inc.(総称してAurobindo)、Cipla Limited(Cipla Ltd)、DRL、Emcute製薬株式会社およびHeritage PharmPharmticals Inc.(総称してEmcuse)、Glenmark(Macodenmark)、Macleenmark(Macods、Maclemark)をそれぞれ起訴した。MSN実験室プライベート株式会社(MSN);Pharmascience Inc.(Pharmascience);Prinston Pharmtics Inc.(Prinston);Sandoz Inc.(Sandoz);Shilpa Medicare Ltd.(Shilpa);Teva PharmPharmticals USA,Inc.とActavis LLC(総称してActavis);Torrent PharmPharmticals Ltd.(Torrent);米国特許番号6,962,940号(‘940号特許)、7,208,516号(’516号特許)、7,427,638号(‘638号特許)、7,659,302号(’302号特許)、7,893,101号(‘101号特許)、8,455,536号(’536号特許)、8,802,717号(‘717号特許)、9,018,243号(’243号特許)、および9,872,854号(‘854号特許)。いずれの訴訟も被告一人一人が提出したANDA申請に基づいており,FDAにOtezlaの後発薬の販売許可を求めている。ニュージャージー州地方裁判所はこれらを統合しました19証拠提示と事件管理を目的とした訴訟は単一事件に統合されたCelgene Corp.はSandoz Inc.らを訴えた。各訴訟はニュージャージー地方裁判所の命令を求め,それぞれの被告のANDAに対するFDAのいかなる承認も適用特許の満期よりも早く発効しないようにした。
2018年8月、CelgeneはAlkem、Amneal、Aurobindo、Cipla Ltd、DRL、Glenmark、Pharmascience、Sandoz、Actavis、Unicem、Zydusに対して修正された訴えを行い、また米国特許番号9,724,330(‘330特許)を主張し、この特許はOtezlaのオレンジブックに記載されている。Celgeneは2018年10月15日から11月27日までの間に,Alkem,Amneal,Hetero,Aurobindo,Cipla Ltd,DRL,Emcuve,Glenmark,Macleods,Mankind,MSN,Pharmascience,Prinston,Sandoz,Actavis,Torrent,Unicem,Zydusに対して修正された訴えを行い,Otezlaのオレンジブックに記載されている米国特許番号10,092,541(‘541号)を主張している。Celgeneは、2019年3月1日から4月4日までの間、Hetero、MSN、およびEmcureに対して、上述した1つまたは複数の特許侵害に対する修正を申し立てた。2019年10月1日、Celgeneは、人間侵害‘940、’302、‘536、’243、および‘330特許について修正された起訴状を提出した。2019年10月8日、Celgeneは、Otezlaのオレンジブックに記載されていない米国特許番号8,093,283(‘283特許)および8,629,173号を侵害したとして、ニュージャージー州地域裁判所でZydusを単独で提訴した。2019年12月19日、ニュージャージー州地方裁判所は、証拠提示と事件管理目的のこの訴訟を既存の合併事件に統合したCelgene Corp.Sandoz Inc.らそれは.各被告は、その主張に対する特許の侵害および/または有効性に異議を唱えた上記の訴えおよび修正された訴えに対する回答を提出した。彼らの回答に加えて、Alkem、Hetero、Cipla Ltd、DRL、Emcuve、Glenmark、Macleods、Man、Pharmascience、Sandoz、Shilpa、Actavis、Torrent、Unicem、Zydusのそれぞれは、特許の一部または全部が侵害および/または無効でないと主張する宣言的判決反訴を提出した。2019年8月、CelgeneとGlenmarkの共同要求に基づいて、ニュージャージー州地域裁判所は、秘密協定に従って許可されない限り、‘940、’638、‘302、’101、‘536、’243、‘330、および’541号の特許期間内に製造、製造、使用、販売、販売、輸入、またはGlenmarkのapremilast製品の製造、製造、使用、販売、提供を禁止する同意判決および禁止令を発表した
安進がOtezlaを買収した訴訟特許と新薬出願後,2020年2月14日,ニュージャージー州地域裁判所は,安進がCelgeneの代わりに合併訴訟およびすべての関連訴訟の原告とし,Celgeneの合併訴訟およびすべての関連訴訟における原告の身分を終了し,合併訴訟およびすべての関連訴訟における案件説明を修正し,安進が唯一の原告であることを反映するように命令を出した。
2020年3月25日、安進と連合昌の共同要求に基づいて、ニュージャージー州地方裁判所は、秘密和解協定に従って許可されない限り、‘940、’638、‘302、’101、‘536、’243、‘330、および’541号の特許期間内に販売、販売、販売または輸入の主要製品の製造、使用、販売、提供または輸入を禁止する同意判決および禁止令を下した。2020年4月3日、安進とHeteroの共同要求に基づいて、ニュージャージー州地域裁判所は、秘密和解協定に従って許可されない限り、‘940、’516、‘638、’302、‘101、’536、‘717、’243、‘330、’854および‘541特許の間にHeteroのapremilast製品の製造、使用、販売、提供、または輸入を禁止する同意判決および禁止令を発表した。2020年5月28日、安進とエムクールの共同要求に基づいて、ニュージャージー州地域裁判所は、秘密和解協定に従って許可されない限り、“638、‘101、”854、および“541特許の有効期間内にエムクールの主要製品の製造、使用、販売、提供、または輸入を禁止する同意判決および禁止令を発表した。2020年7月7日、ニュージャージー州地域裁判所は、安進とサントスとの間の“717、516および”854特許に関するすべての主張、反訴、および肯定抗弁を損なうことなく、安進が訴訟でサントスに対して主張した“940、302、”536、“243、”330、“638、”101、および“541の特許を残すことを規定した。2020年8月6日、安進とマンゴールドの共同請求に基づいて、ニュージャージー州地域裁判所は、特許期間中にマンゴールドの主要製品の製造、使用、販売または輸入を禁止する同意判決および禁止令を下した, 秘密と和解協定によって許可されない限り。2020年8月14日、AmgenとMacleodsの共同要請に基づいて、ニュージャージー州地域裁判所は、秘密和解協定に従って許可されない限り、‘638および’541特許期間内のMacleodsのapremilast製品の製造、使用、販売、提供、または輸入を禁止する同意判決および禁止令を下した。2020年10月7日、AmgenとAmnealの共同請求に基づいて、ニュージャージー州地域裁判所は、秘密和解協定に従って許可されない限り、‘101、’940、‘638、’302、‘536、’243、‘330、および’541号の特許期間内のAmnealのapremilast製品の製造、使用、販売、提供または輸入を禁止する同意判決および禁止令を発表した。2020年12月30日、AmgenとShilpaの共同請求に基づいて、ニュージャージー州地域裁判所は、秘密和解協定に従って許可されない限り、‘638、’101および‘854特許期間内のShilpaのapremilast製品の製造、使用、販売、提供、または輸入を禁止する同意判決および禁止令を発表した。2021年1月26日、安進とアトビスの共同要求に基づいて、ニュージャージー州地方裁判所は、秘密和解協定に従って許可されない限り、‘940、’516、‘638、’302、‘536、’717、‘330、’854、および‘541号の特許の有効期間内に製造、使用、販売、販売または輸入ビスのapremilast製品を製造、使用、販売、提供することを禁止する同意判決および禁止を下した。2021年3月24日、安進とプリンストンの共同請求に基づいて、ニュージャージー州地域裁判所は、“638および‘541特許期間内のプリンストンのapremilast製品の製造、使用、販売、提供または輸入を禁止する同意判決および禁止令を下した, 秘密と和解協定によって許可されない限り。2021年4月6日、安進とAurobindoの共同要求に基づいて、ニュージャージー州地域裁判所は、秘密和解協定に従って許可されない限り、‘940、’516、‘638、’302、‘101、’536、‘717、’243、‘330、’854および‘541特許の有効期間内にAurobindoのapreamast製品の製造、使用、販売、提供、または輸入を禁止する同意判決および禁止令を下した。
2021年5月5日、AmgenとCiplaの共同請求に基づいて、ニュージャージー州地域裁判所は、秘密和解協定に従って許可されない限り、‘940、’638、‘302、’536、‘330、および’541号の特許期間内にCiplaの主要製品の製造、使用、販売、提供、または輸入を禁止する同意判決および禁止令を下した。2021年5月14日、安進とTorrentの共同要求に基づいて、ニュージャージー州地域裁判所は、秘密和解協定に従って許可されない限り、‘101、’638、‘854、および’541特許期間内のTorrentの主要製品の製造、使用、販売、提供、または輸入を禁止する同意判決および禁止令を発表した。2021年5月19日、安進とAlkemの共同要求に基づいて、ニュージャージー州地域裁判所は、秘密和解協定に従って許可されない限り、‘940、’638、‘302、’536、‘330、および’541特許中のAlkemのapremilast製品の製造、使用、販売、提供、または輸入を禁止する同意判決および禁止令を発表した。2021年5月25日、安進とMSNの共同要求に基づいて、ニュージャージー州地域裁判所は、秘密和解協定に従って許可されない限り、‘940、’638、‘302、’536、‘330、および’541特許中のMSNの主要製品の製造、使用、販売、提供、または輸入を禁止する同意判決および禁止令を下した。2021年6月11日、AmgenとPharmascienceの共同要求に基づいて、ニュージャージー州地域裁判所は、秘密和解協定に従って許可されない限り、‘243、’940、‘638、’302、‘101、’536、‘330、および’541号の特許の有効期間内に製造、使用、販売、販売、または輸入されたPharmascienceのapremilast製品の製造、使用、販売、提供、または輸入を禁止する同意判決および禁止を下した。六月十七日, 2021年、安進とDRLの共同要求に基づいて、ニュージャージー州地域裁判所は、秘密和解協定に従って許可されない限り、“638、‘101、’536、および‘541特許期間内のDRLの主要製品の製造、使用、販売、提供、または輸入を禁止する同意判決および禁止令を下した。
SandozとZydusに対する合併特許侵害訴訟は2021年6月14日から25日までニュージャージー州地区裁判所で審理され、2021年7月28日に結審陳詞が行われた
2021年9月28日、その2021年9月20日の意見および命令に基づいて、ニュージャージー州地域裁判所は、“638特許の請求項3および6、‘536特許の請求項6および”283特許の請求項2および27について、安進に有利であり、安進に不利であるという最終判決を下し、“101特許の請求項1および15および”541特許の請求項2、19および21について、安進および安進反対を有利にする。最終判決命令Zydusに対するFDAのANDAの任意の最終承認の発効日は三つ侵害された特許(‘638、’536、および‘283特許)、および安進が獲得する権利がある可能性のある任意の規制排他性。最終判決はまた、ZYDUSが任期中に米国でZYDUSの模造薬apremilast製品を製造、使用、提供、販売または販売することを禁止する禁止令、または米国への輸入を禁止する禁止令を含む三つ特許を侵害しました。2021年10月27日、Zydusは‘638特許について連邦巡回裁判所に控訴通知を提出した。2021年10月28日、安進は連邦巡回裁判所に控訴した。
2021年10月12日、ニュージャージー州地域裁判所はまた、“638特許の請求項3および6、‘536特許の請求項6および”101特許の請求項1および15について、安進に有利であり、安進に不利であるという最終判決を下し、“541特許の請求項2、19および21に関する最終判決は、安進および安進反対を有利にする。最終判決命令は、Sandozに対するFDAのANDAの任意の最終承認の発効日は必ず三つ侵害された特許(‘638、’536、および‘101特許)、および安進が獲得する権利がある可能性のある任意の規制排他性。最終判決はまた、Sandozが任期中に米国でSandozの模造薬apremilast製品を製造、使用、提供、販売または販売することを禁止する禁止令、または米国への輸入を禁止する禁止令を含む三つ特許を侵害しました。2021年11月9日、Sandozは‘638および’101特許について連邦巡回裁判所に控訴通知を提出した。2021年11月10日、安進は連邦巡回裁判所に控訴した。
2023年2月8日、安進、サントス、ジダースの控訴について口頭弁論が行われた。
安進はApotex Inc.
2022年6月14日、安進はApotex Inc.(Apotex)が“638特許、854特許、および‘541特許を侵害したと告発するニュージャージー州地域裁判所に提訴した。この訴訟は,Apotexが提出したANDA申請に基づいて,FDAがOtezlaの後発薬の販売を許可することを求め,ニュージャージー州地域裁判所の命令を求め,FDAがApotexを承認したANDAが適用特許の満期よりも早くないようにした。
Apotexは2022年10月14日に答弁を提出し,訴訟における特許の侵害および/または有効性に異議を唱えた。回答とともに,Apotexは訴訟中の特許が侵害されていないことおよび/または無効であると主張する宣言的判決反訴を提出した
2023年1月20日、AmgenとApotexの共同要請に基づいて、ニュージャージー州地域裁判所は、秘密和解協定に従って許可されない限り、‘638、’854および‘541特許の有効期間内にApotexのapomilast製品を製造、使用、販売、提供、または輸入することを禁止する同意判決および禁止を下した。
Repatha特許訴訟
安進ら。V.Sanofiら
2014年10月、安進は一連の訴訟を起こし、これらの訴訟は2014年12月に米国デラウェア州地方裁判所(デラウェア州地方裁判所)によってセノフィ、セノフィ-アンバンテ米国有限責任会社、アンバンテ子有限責任会社に対する単一事件に合併され、これまでの業務はアンバンテ製薬会社(総称してセノフィと呼ばれる)とRegeneron製薬会社(Regeneron)であった7人私たちの特許では:米国特許番号8,563,698;8,829,165(‘165特許);8,859,741(’741特許);8,871,913;8,871,914;8,883,983;および8,889,834。これらの特許は、PCSK 9のモノクロナル抗体を記載し、その権利を保護することを要求する。苦情を通じて、安進はセノフィとRegeneronのalirocumabの侵害の製造、使用、販売を防止するための禁止令を求めた。alirocumabはPCSK 9に対する単一抗体である。2016年1月、デラウェア州地方裁判所は安進の動議を承認し、起訴状を修正し、その付属会社安進製造有限会社と安進アメリカ会社を原告として追加し、セノフィとRegeneronが安進特許を故意に侵害した疑いを追加した。
2016年2月、デラウェア州地域裁判所は、alirocumabおよびその薬剤を含む薬剤を裁定し、PRALUENTは、“165特許の請求項2、7、9、15、19および29および”741特許の請求項7を含む安進の特定の特許を侵害したと判断する規定の命令を発表した。2016年3月、デラウェア州地方裁判所は安進に有利な判決を下した5日間陪審員の裁判と陪審員の一致した判決は、これらの特許主張が有効であることを示している。2017年1月、デラウェア州地域裁判所はセノフィとRegeneronが再審と判決を求める審後動議を却下し、米国における権利侵害の製造、使用、販売、要約販売または輸入alirocumabの輸入を禁止する安進の永久禁止動議を承認した。セノフィとRegeneronは判決と永久禁止について連邦巡回裁判所に控訴した。2017年2月、セノフィとRegeneronが動議を提出した後、連邦巡回裁判所は控訴保留中に永久禁止令の執行を一時停止した。2017年10月、連邦巡回裁判所はデラウェア州地区裁判所の判決の一部を覆し、再審を返送した二つ“165特許請求項2、7、9、15、19および29ならびに”741特許請求項7および第3の特許有効性抗弁に関する“165特許請求項2、7、9、15、19および29”の侵害に関するデラウェア州地域裁判所の判決を確認する(請求された発明は、特許分野の一般技術者にとって明らかではない)。
2018年3月、連邦巡回裁判所は事件をデラウェア州地区裁判所に返送して再審理する命令を出した二つ私たちの特許有効性に対するセノフィおよびRegeneronの挑戦(要求された発明の書面記述および支持が不足している)、および永久禁止をさらに考慮する。2018年7月、安進は米国最高裁判所に移審書を提出し、安進特許の有効性を確認する判決は書面説明法への誤適用にある程度基づいているという連邦巡回裁判所の結論の再審を求めた。2019年1月7日、米国最高裁判所は安進の移審申請を却下した。再拘留に関して、デラウェア州地域裁判所は、私たちの特許の有効性に対するセノフィとRegeneronの疑問に基づいて、書面による記述と主張された発明への支持が不足しているため、新しい裁判を手配した。デラウェア州地区裁判所はまた、セノフィとRegeneronの安進に対する故意侵害疑惑に対する抗弁に対して判決を下した。
2019年2月25日、デラウェア州地域裁判所陪審員は再び一致して、“165特許請求項19および29および”741特許請求項7の有効性を支持した。陪審員はまた、‘165特許の請求項7および15がイネーブル要件に適合しているが、書面記述要件を満たしていない場合は無効であることを発見した。2019年3月18日、セノフィとRegeneronは裁判後動議を提出し、陪審員の彼らに対する裁決または再審を覆すことを求め、安進は永久禁止動議を提出した。2019年8月28日、デラウェア州地区裁判所は裁判後の動議に対して裁決を下し、セノフィとRegeneronの再審の請求及び陪審員の裁決を覆す請求を却下した、すなわち“165号特許と”741号特許は保護を要求した発明に書面記述支援を提供した。デラウェア州地域裁判所はまた、“165特許中の請求項19および29および”741特許における請求項7がイネーブル要求を満たしていないため無効であり、陪審員の裁決を覆したと法的事項として裁定した
2019年10月23日、安進は連邦巡回裁判所に上訴通知を提出し、その後の聴取に基づいて、2021年2月11日、連邦巡回裁判所は裁定を下し、デラウェア州地区裁判所の裁決を確認した。安進はEN BANCの再審理の請願書を提出したが,2021年6月21日に却下された。2021年11月18日、安進は、特許請求の範囲19および29および741号の特許請求の範囲7の無効の再審査を要求する移送命令状を米国最高裁判所に提出した
2022年11月4日、米国最高裁判所は、下級裁判所が“165年特許請求項19および29および”741特許請求項7のライセンス開示の欠如を宣言して適切な基準を適用することについて、移審を要求する再審を安進に承認した。安進は2022年12月27日に開廷ブリーフィングを提出した。2023年2月3日、セノフィとRegeneronは応答としてブリーフィングを提出した。 米国最高裁の口頭弁論は2023年3月27日に行われる予定だ。
国際地域の特許紛争
私たちは他の管轄地域や地域で巻き込まれ、将来的には私たちのPCSK 9特許に関するより多くの紛争に巻き込まれることが予想されます。これには私たちに対する訴訟と、私たちがドイツ、スペイン、そして日本で提起した訴訟が含まれている
2016年2月,欧州特許庁(EPO)は安進に欧州特許番号2,215,124(EP 2,215,124)を付与した。この特許はPCSK 9に対するモノクロナル抗体および治療法の保護を要求しており,セノフィは欧州特許庁でこの特許に反対し,無効化を求めている。2016年11月、セノフィ-アンバンテドイツ有限公司、セノフィ-アンバンテグループ、セノフィ-ウィンスロープ工業社は共同で安進特許反対出願を提出し、礼来社、Regeneron、Strawman Ltd.もそれぞれ安進特許反対出願を提出した。2018年11月,欧州特許庁は安進2,215,124番EPの有効性を確認し,技術控訴委員会(TBA)に上訴した。2020年10月29日、TBAは、Repathaのクレームを保護することを含むいくつかのクレームの有効性を維持したが、PRALUENTをカバーするより広範なクレームは無効であると判断した。TBAの決定により,ヨーロッパPRALUENTに関する国家訴訟が解決されている。ドイツでは、セノフィ·アンバンテドイツ有限公司とRegeneronがPRALUENTに対する禁止を一時的に執行したことによる損害賠償を求める訴訟を起こしている。この禁止はTBAが2020年10月29日に裁決された後に解除された。
2022年3月23日,安進はPRALUENTが安進の欧州特許番号2,641,917(‘917特許)を侵害したことを告発した。セノフィが2021年2月5日に提出した欧州特許庁の‘917特許に対する反対意見が審理中であり,欧州特許庁反対部の公聴会は2023年2月21日に開催される予定である。
2022年7月21日、セノフィバイオテクノロジー社は、Repathaが欧州特許番号2,756,004(EP‘004特許)を侵害したと告発し、侵害損害賠償および禁止救済を求める安進株式会社と安進(ヨーロッパ)有限会社をデュッセルドルフ地区裁判所に起訴した。EP‘004特許は現在、安進および匿名の第3方向欧州特許庁によって提起された反対訴訟中である。2022年6月8日と9日,欧州特許庁反対部は公聴会を行い,2022年8月16日,野党は論争のあるEP‘004特許請求の有効性を支持する書面決定を発表し,縮小修正を行った。TBAの訴訟手続きは2022年8月17日に開始された。2022年11月22日,安進はTBAに控訴理由を提出し,2022年12月30日にRegeneronはTBAに控訴理由を提出した。2023年1月23日、TBA招待安進は、2023年5月23日までにRegeneron控訴理由に対する任意の応答を提出する。
2020年4月24日、日本の最高裁判所はセノフィK.K.の控訴を拒否し、最終的に日本高裁はPRALUENTが日本での有効な特許権を侵害したと裁定した。安進は2020年6月24日、Regeneronが2020年2月12日に起こした無効裁判に対する書面回答を日本特許庁に提出し、これまでPRALUENTに侵害され、セノフィK.K.に挑戦していた安進の日本特許を有効に無効にすることを求めた。2021年4月15日、日本特許庁はRegeneronの無効裁判を却下し、2021年8月にRegeneronは日本高裁に控訴した。2023年1月26日,日本高裁は安進の特許主張が無効であると判断し,十分な支持が不足していることを理由とした。この決定は日本の最高裁に上訴することができる。セノフィK.K.に対する損害賠償訴訟は東京地裁で行われており,セノフィK.K.はそこで安進の日本での特許に新たな有効性に挑戦している
ABP 654(Ustekinumab)特許訴訟
楊森生物科学技術会社は安進事件に訴えた
2022年11月29日、ヤンソンは安進が侵害したことを告発するため、デラウェア州地方裁判所に提訴した二つ安進がFDAによるABP 654の許可申請を提出することにより,安進の生物類似バージョンのJanssenのStelara(Ustekinumab)が,その侵害に対する宣言的判決を求めた二つ特許です。
反独占集団訴訟
センシパル反独占集団訴訟
2019年2月から4月まで四つ原告は安進会社とTeva米国製薬会社(Teva)に関連する様々なエンティティに対して可能な集団訴訟を提起し、安進会社と後発薬Cinacalcet製品メーカーとの間の和解に反競争行為が存在することを告発した二ついくつかの訴訟はデラウェア州地方裁判所で提起されましたUFCW地方1500福祉基金は安進らの事件を訴えた。(2019年2月21日)(現地時間1500)セサル·カスティリョ社は安進らの事件を訴えた。(2019年2月26日)(カスティー略)。3つ目の訴訟はニュージャージー州地方裁判所で提起されましたトラック運転手地方237福祉基金など。安進ら。(2019年3月14日)(現地時間237)、4件目の訴訟は、米国ペンシルベニア州東区地方裁判所(ペンシルベニア州東部地域裁判所)で提起されたKph Healthcare Services,Inc.a/k/a Kinney製薬会社が安進らを訴えた事件(2019年4月10日)(キロ/時間)。すべての訴訟はSensiarの仮定のような直接または間接購入者を代表して提起され、原告はAmgenが模造薬Cinacalcet製品メーカーの市場進出を不当に延期した疑いでSensiarに過大な価格を支払ったと告発した
これらの訴訟は主に安進、ワトソン実験室会社(Watson)とTevaの間で双方の特許侵害訴訟に関する和解に集中している。その他の事項を除いて、各訴訟は3倍の損害賠償、公平救済、弁護士費、費用を要求している。2019年4月10日,KPH訴訟中の原告が動議を提出し,要求した四つペンシルベニア州東部地域裁判所では,訴訟が合併して多地域訴訟(MDL)に指定され,現地1500訴訟における原告が動議を提出し,求めている四つ訴訟、そしてCipla Ltd.は安進事件に訴えた。デラウェア州地域裁判所ではMDLを統合して指定する
2019年7月31日、MDLグループはデラウェア州地域裁判所で命令を発表した四つ集団訴訟。2019年9月13日、原告は修正後の訴状を提起し、2019年10月15日、安進は動議を提出し、直接購入者原告の合併集団訴訟と間接購入者最終支払人原告の訴状を却下した。2019年12月6日,原告は安進の却下動議に応じ,2020年1月10日,安進は答弁状を提出した。2020年2月6日、集団訴訟における動議は米デラウェア州地域治安裁判官(地方裁判官)に引き渡されて推薦された。MDLグループは2020年2月6日に条件付き移譲令を証明し,米国フロリダ州南区地域裁判所に提訴した追加集団訴訟を移管した商務部は安進らの代償要求を訴えた。, デラウェア州地方裁判所に提出します
2020年7月22日、治安裁判官はデラウェア州地区裁判所に提案し、安進に対するクレームを却下したが、原告がその訴えを修正することを許可した。2020年8月5日,原告は治安裁判官の報告と提案に異議を唱えた。2020年8月19日、安進は原告の異議に答弁した。2020年11月30日、地裁は治安裁判官の一部の提案を採択し、一部否定し、原告が逆支払いクレームを十分に告発したことを理由に安進の却下動議を却下したが、他の連邦反独占クレームに関する安進の却下動議を承認した。2020年12月23日,Teva,Watson,Actavisは中間控訴と控訴猶予の動議を提出し,安進は合併動議(1292動議)を提出した。2021年1月5日、デラウェア州地区裁判所に通知する共同状況報告が提出され、被告は1292動議と原告が提出した棚上げ証拠を撤回するかどうかを考慮しており、修正された訴えを却下する動議のさらなる裁決を待っている。2021年1月19日、デラウェア州地域裁判所は2021年1月6日の命令に基づいて共同状況報告を提出し、改正された訴えの裁決後に1292動議を延期することを規定した。
2021年2月16日,Sensiarの直接または間接購入者の推定種別を代表する反独占集団訴訟の原告が改正訴えを行った。2021年3月4日、トラック運転手西部地域と地方177医療保険基金を増加させるために、第2次改正訴えの提起に関する規定及び命令が提出された。2021年3月17日、被告MSP Recovery Claims Series LLCは自発的解雇通知を提出した。2021年3月30日、安進を含む残りの被告は、第二次改正された起訴状の却下を要求する動議を提出した。
2021年4月27日、原告は被告(安進を含む)が提出した却下動議に異議を唱え、被告は2021年5月25日に答弁した。2021年7月13日、デラウェア州地方裁判所で被告の却下動議に関する公聴会が行われた。
2022年3月11日、デラウェア州地域裁判所は、被告(安進を含む)が被告を却下する動議を承認したが、逆支払いに関するクレームと由来10個原告のいる州。2022年5月11日、双方は中間控訴を求めることを許可する動議を提出した。原告は安進の動議に反対するのではなく、すべての問題はこの時点で控訴すべきだと弁明した。安進は2022年6月10日に原告動議に対する反対意見を提出し,2022年6月24日に答弁状を提出した。
Regeneron製薬会社の反独占行動
2022年5月27日、Regeneron製薬会社(Regeneron)はデラウェア州地区裁判所に訴訟を提起し、安進が連邦と州の反独占と不正競争行為に違反し、権利侵害が未来の商業関係を妨害することを告発した。Regeneronは、安進が主要な保険会社、第三者支払人とPBMとRepatha、ENBREL、Otezlaの販売契約を締結するやり方はその製品PRALUENTの販売を損害し、それに集中していると主張している二つ主な論点:安進はRepathaの販売をENBREL、Otezla、および可能な他の製品と不適切に束ね、Repathaの独占的または事実上の独占処方の位置づけを求める。安進の最初の反応性抗弁は2022年8月1日に提出された却下動議である。
2022年8月11日,安進はこの事件を棚上げにし,安進とRegeneronの間で行われている特許訴訟の是非曲直に対する最終裁決を待つ行動をとった安進ら。V.Sanofiら2023年1月6日、デラウェア州地方裁判所は棚上げ動議と却下動議に関する口頭弁論を聴取した。
アメリカ税務訴訟です。
安進および付属会社は税務署局長を訴えた
米国国税局税務紛争と会社の米国税務裁判所における請願書の検討については、付記6、所得税を参照されたい。
ChemoCentryx,Inc.証券が重要である
2021年5月5日と6月8日にChemoCentryxとその最高経営責任者が指定された二つ米国カリフォルニア州北区地方裁判所(カリフォルニア州北区裁判所)に提起された推定株主集団訴訟。これらの事件は合併されてホモックはChemoCentryx,Inc.を訴えた原告は証券取引法第10(B)と20(A)条に違反し、TAVNEOS新薬申請と基礎3期臨床試験の声明に関連し、損害賠償金、利息、弁護士費の賠償を求めた。2022年3月28日,原告は改訂された合併訴えを提出し,2022年5月19日,ChemoCentryx動議はこれらの訴えを却下した。
2022年1月25日、カリフォルニア州北部地域裁判所が提起した仮定した株主派生訴訟では、ChemoCentryxの取締役会と一部の幹部が被告とされたナポリはシャルル事件を訴えた2022年3月11日カリフォルニア州北区裁判所は判決が出るまで訴訟を棚上げしましたホモックはChemoCentryx,Inc.を訴えた行動する。2022年12月5日原告はナポリ自発的な却下通知を提出し、2022年12月22日、裁判所はこの事件の却下を命じた。
アメリカに送金することを約束しました
2017年の税法によると8人年間分割払いは主に私たちの海外業務先の無期限投資収益に関する振り戻し税です次の表は、2022年12月31日現在の残りの帰国予定税金(単位:百万)をまとめています
| | | | | |
| 金額 |
| 2023 | $ | 1,100 | |
| 2024 | 1,467 | |
| 2025 | 1,834 | |
| アメリカの残りの送還税約束総額 | $ | 4,401 | |
別表II
安進。
評価および合資格勘定
2022年、2021年、2020年12月31日までの年度
(単位:百万)
| | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | |
| 不良債権準備 | | てんびん
最初の時に
周期の | | 足し算
料金は…
コストと
費用.費用 | | 他にも
内容を追加する | | 控除額 | | てんびん
最後尾に
周期の |
2022年12月31日までの年度 | | $ | 26 | | | $ | — | | | $ | — | | | $ | (4) | | | $ | 22 | |
2021年12月31日までの年度 | | $ | 32 | | | $ | — | | | $ | — | | | $ | (6) | | | $ | 26 | |
2020年12月31日までの年度 | | $ | 26 | | | $ | 8 | | | $ | — | | | $ | (2) | | | $ | 32 | |