
ルール424(B)(3)に従って提出する
登録番号:333-268701
目論見書
7207,208株 株
普通株 株

アリディス製薬会社
本募集説明書は、本募集説明書で決定されたAridis PharmPharmticals,Inc.(“Aridis”,“当社”,“br}”We“,”Our“または”Us“)のある販売株主が最大7,207,208株の普通株(”転売 株“)普通株を転売し、1株当たり額面価値0.0001ドルであり、売却株主が期日2022年10月5日の証券購入契約(”購入プロトコル“)によって得られた未承認株式証を行使することにより発行することができる。すべての転売株は私募取引方式で当社から購入しており、売却した株主のみ転売しています。
転売株式は、売却株主によって引受業者または取引業者に売却されてもよく、または引受業者または取引業者を介して、買い手に直接販売されてもよく、または時々指定された代理店を介して販売されてもよい。販売方法に関するその他の情報は、本募集説明書の“流通計画”と題する章を参照してください。
売却株主が転売株式を売却可能な価格は、br社普通株の現行市場価格または私的協議の取引によって決定される。売却株主から転売株 を売却することから何の収益も得ないが,任意の株式承認証の現金行使から収益を得ることを前提としている.
私たちの普通株はナスダック資本市場に上場し、株式コードは“ARDS”です。2022年12月6日、ナスダック資本市場における私たちの普通株の最新終値は0.91ドルだった。
2012年のJumpStart Our Business Startups ActやJOBS Actが使用しているように、私たち は“新興成長型会社”であるため、いくつかの低下した上場企業の報告要求を遵守することを選択しました。
私たちの普通株に投資することは高い危険と関連がある。参照してください“リスク要因“7ページ目から本募集説明書を参照して、私たちの普通株に投資する際に考慮すべき情報を検討してください。
米国証券取引委員会およびどの州証券委員会もこれらの証券を承認または承認しておらず、本入札説明書が真実または完全であるかどうかも決定されていない。どんな反対の陳述も刑事犯罪だ。
本募集説明書の日付は2022年12月14日です
カタログ表
| ページ | |
| 募集説明書の概要 | 1 |
| リスク要因 | 7 |
| 前向き陳述に関する注意事項 | 8 |
| 収益の使用 | 9 |
| 配当政策 | 10 |
| 売却株主 | 11 |
| 配送計画 | 12 |
| 法律事務 | 13 |
| 専門家 | 13 |
| そこでもっと多くの情報を見つけることができます | 13 |
| いくつかの資料を引用して組み込む | 13 |
あなたはこの目論見書に含まれている情報だけに依存しなければなりません。私たちは、誰もいかなる情報を提供したり、いかなる陳述をすることも許可していませんが、本入札説明書または吾などまたは私たちを代表して作成された任意の無料書面入札説明書または私たちが推薦するbr}に含まれる情報または陳述は除外します。他の人があなたに提供するかもしれない他の情報については、私たちは何の責任も負いませんし、その信頼性を保証することもできません。本入札明細書に含まれる情報は、本募集説明書の交付時間または私たちの普通株式の任意の販売時間にかかわらず、本入札説明書の日付のみが正確である。
あなたはこの目論見書に含まれている情報だけに依存しなければなりません。ディーラー、販売者、または他の人員は、本募集説明書に含まれていない情報 を提供する権利がない。本募集説明書は、売却要約でもなく、いかなる要約や売却も許可されていない司法管轄区でこれらの証券の購入を求める要約でもない。本募集説明書中の情報は、本募集説明書の日付までのみ正確であり、本募集説明書の交付時間またはこれらの証券のいずれの販売状況にもかかわらず正確である。
募集説明書 概要
以下の情報は株式募集説明書の要約であり、私たちの普通株に投資する前に考慮すべきすべての情報 は含まれていません。本募集説明書の他の部分に記載されている“リスク要因”、“br}”管理層の財務状況および経営結果の議論および分析“および私たちの合併財務諸表および連結財務諸表に関連する付記を含む、株式募集説明書全体をよく読まなければなりません。文脈に別の要求がない限り、言及された“Aridis”、“Company”、“We”、“Us”または“Our” は、Aridis製薬会社、デラウェア州の会社およびその子会社を意味する。
概要
我々は末期生物製薬会社であり,完全ヒトモノクロナル抗体を用いて生命にかかわる感染を治療する標的免疫療法の発見と開発に専念している。モノクロナル抗体は伝染病市場上の1種の新しい治療方法を代表し、現在の治療方法と関連する肝心な問題を克服することを目的とし、薬剤耐性、反応持続時間が短く、耐性、人体微生物群に対する負の影響及び治療代替方案の間に区別が乏しい。我々の特許製品brは生命を脅かす細菌とウイルス感染に関連する特定の病原体に対する完全ヒトmAbからなり、brは主に病院獲得性肺炎、呼吸器関連肺炎、嚢胞性繊維化と新冠肺炎である。著者らの臨床段階候補製品はすでに良好な臨床前データと臨床データを示した。我々の主要候補製品AR-301はグラム陽性細菌から産生されたアルファ毒素を対象としています黄色ブドウ球菌あるいは、あるいは黄色ブドウ球菌HAPやVAPに関連するよく見られる病原体。現在の臨床開発活動は主にAR-301、AR-320とAR-501に集中している。
我々の製品ラインの候補の多くは,MabIgXと呼ばれる差別化抗体発見プラットフォームを用いることで得られているTM λPEXとTMそれは.このプラットフォームは、B細胞バンクを完全にスクリーニングし、特定の病原体感染を克服することに成功したか、または特定の病原体ワクチンを接種した個人からヒト抗体を産生するB細胞を単離することを目的としている。これらの患者のB細胞は高度な保護と有効なモノクロナル抗体を産生する理想的な源であり、これらのモノクロナル抗体は他の患者に安全に応用できると信じている。λPEXTMMabIgXの能力を補充し、更に拡張し、迅速 で患者の体内から大量の抗体産生B細胞をスクリーニングし、そしてこれまでにない速度 で高mAbを産生して哺乳動物細胞系を産生する。したがって,従来法と比較して抗体発現や製造時間を有意に減少させることができる。
我々の最初の臨床適応はAR-301であり、HAPとVAPの標準看護またはSOC抗生物質の治療を補助するために使用される。AR-320は、集中治療室(ICU)におけるHAPやVAPに関連する死亡率と発症率の予防的治療として開発されている。SOC抗生物質を用いた積極的な治療にもかかわらず、AR-320の死亡率と発症率は依然として高い。現在、HAPとVAPの治療に用いられるSOC抗生物質は通常いくつかの広域抗生物質の組み合わせを含み、これらの抗生物質は治療開始時に経験的に処方されている。処方された特定の経験的抗生物質方案は医者の間で非常に差があり、多くの原因により、抗生物質方案と病原体はよく一致しない及び/或いは抗生物質耐性菌株に感染し、通常はあまり大きな臨床利益を産生しない。最近、感染病原体を数時間以内に識別することができる迅速診断テストが導入されている。brなどの日々一般的なテストは、医師がより適切な抗生物質レジメンを処方し、最終的に感染中にAR-301およびAR-320のような抗感染薬 をより早く治療することを可能にする。この根拠に基づく治療方法は経験的な広域抗生物質と関連する問題、例えば不適切な抗生物質の選択と抗生物質の耐性を高めることを目的としている。SOC抗生物質の間に差異性が乏しいのと比較して、mAbsは作用機序、薬物動態学と薬効学の面でSOC抗生物質と大きく異なるため、併用に非常に適している。補助治療として、AR-301 はSOC抗生物質の有効性を高め、抗生物質耐性をカバーする可能性がある黄色ブドウ球菌抗生物質と直接競争するのではなく菌株。われわれの候補製品の補助療法としての利点を強調するために,優位終点に基づく臨床試験を設計した。
2021年7月、私たちはアスリコンの完全子会社MedImmune Limitedと許可協定を達成し、Suvratoxumabの世界商業権を獲得することを発表し、Suvratoxumabは半減期が延長したヒトIgG 1モノクロナル抗体であり、また、Suvratoxumabは半減期が延長したヒトIgG 1モノクロナル抗体であることを発表した黄色ブドウ球菌それは.Suvratoxumabは完全にヒトに対するIgG 1モノクロナル抗体である黄色ブドウ球菌アルファ毒素です。この製品は ,製品コードは‘AR−320’である。AR−301と同様に、AR−320の作用パターンは抗生物質耐性とは無関係である黄色ブドウ球菌MRSAやMSSAによる感染に積極的な役割を果たしている。SuvratoxumabおよびAR−301は相補的なbr製品である。Suvratoxumabのポイントは予防的治療です黄色ブドウ球菌肺炎はAridisのAR−301第3段階mAb計画の補完であり,治療に開発中である黄色ブドウ球菌肺炎です。AR-320は黄色ブドウ球菌定植患者の第一線の治療、初めて発売され、一流の予防的治療になると信じている。同様の一線,最初の発売と一流の戦略は,モノクロナル抗体AR−301を用いた急性治療にも適しており,この分野のグローバルリーダーとなると信じている。
| 1 |
AR-320 は開発中であり、黄色ブドウ球菌のハイリスク患者に対して予防的治療を行うために使用されており、現在の看護標準は抗生物質 と呼吸器関連肺炎(VAP)束などの感染制御措置を含むが、黄色ブドウ球菌は依然として顕著な発病率と死亡率を有する。現在、ハイリスク患者を予防或いは早期予防的に管理する治療方法はまだない黄色ブドウ球菌肺炎です。Suvratoxumabは以下の疾患の発生率を減少させることで、この満たされていない医療需要を満たす可能性がある黄色ブドウ球菌ICUで人工呼吸器を使用している患者のような肺炎感染のハイリスク患者黄色ブドウ球菌呼吸器の中にあります
HAPとVAPは病院環境において深刻な挑戦となっており,SOC抗生物質が感染患者の治療に不足しているためである。米国で毎年報告されている肺炎症例は約300万例である。このうち約628,000例はグラム陰性細菌とMRSAによるHAPとVAP (DRG,2016)であった。これらの患者は通常非常に高い死亡リスクがあり、それに加えて他の生命に危害を及ぼす合併症と抗生物質耐性の増加がある。疫学研究では死亡確率は黄色ブドウ球菌29%から55%まで様々ですそのほか、肺炎感染は患者のICU滞在時間を延長し、機械換気を使用することができ、患者、病院システムと支払人に重大な経済負担を与える。例えば,米国では,呼吸器肺炎患者のICU看護費用は1日約10,000ドルであり,ICU滞在時間は通常非呼吸器患者の2倍(感染コントロールと病院疫学)である。2010年、第31巻、第509-515ページ)。肺炎患者1人あたりの平均看護費用は約41,250ドルであり,HAP/VAP患者の費用は86%増加し,約76,730ドルに達した。私たちの3つの候補シーツ抗は250億ドルの潜在的な市場を有し、米国の約325,000人のHAPおよびVAP患者の需要を満たす可能性があると推定される。
著者らの独自製品ラインは主に深刻な肺感染に集中し、6種類の全額候補製品から構成され、以下のように強調表示される。
図 1
私たちのbr製品ルート
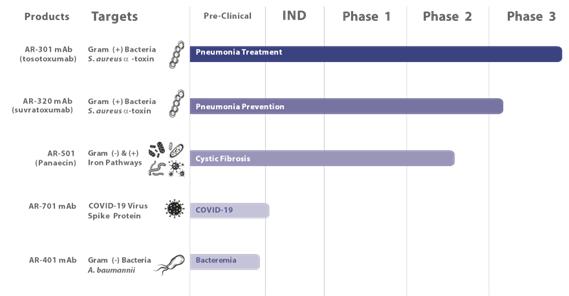
| ● | AR-301 はグラム陽性細菌に対する全ヒト免疫グロブリン1またはIgG 1モノクロナル抗体である黄色ブドウ球菌アルファ毒素です。我々はAR−301を開発しており,最初は補助免疫療法としてSOC抗生物質を組み合わせて以下の原因による急性肺炎を治療していた黄色ブドウ球菌 感染します。我々は2015年6月にAR-301の調査新薬申請、またはINDを提出した。著者らは48名のHAPとVAP患者の中でランダム、二重盲検、プラセボ対照の2 a期試験を完成した。試験は耐性の主要な終点に達した。AR-301は一般的に耐性が良好であり、候補製品に関連する深刻な有害事象またはSAEがなく、その薬物動態学的特性はヒトIgG 1と一致する。また,この試験は,VAP患者の呼吸器使用時間,微生物除去率,微生物根絶時間,AR−301にSOC抗生物質を加えた総ICUと在院日数など,患者福祉に関する様々な終点の恩恵傾向を示した。われわれは,2022年12月に行われているVAP患者の第3段階キー試験の主要データ を報告する予定である。AR-301はFDAによって迅速チャネル称号、br}EU孤児薬物称号を授与され、米国で孤児薬物称号を申請した。 |
| 2 |
| ● | AR-320 は完全にヒトに対するIgG 1モノクロナル抗体である黄色ブドウ球菌アルファ毒素です。AR−320はMRSAやMSSAによる感染に積極的な役割を果たしている。Suvratoxumabのポイントは予防的治療です黄色ブドウ球菌肺炎はAridis AR−301第3段階mAb計画の補完であり,治療に開発中である黄色ブドウ球菌肺炎です。アスリカン(n=196名の患者)による多国籍、無作為、二重盲検、プラセボ対照の2期研究により、人工呼吸のICU患者は黄色ブドウ球菌Suvratoxumab治療を受けた全体意思治療(ITT)研究群では,肺炎のリスクは相対的に32%低下し,あらかじめ指定された65歳以下群で47%低下し,計画の第3段階研究における目標群であった。目標群の相対リスク低下は統計学的意義を達成し、ICUと病院に必要な看護時間の大幅な短縮にも関係している。最近、第3段階の肝心な試験を開始し、人工呼吸を受けるICU患者を積極的に募集した黄色ブドウ球菌. | |
| ● | AR-501 (Panaecin)は私たちが開発している広域小分子抗感染薬であり、私たちは目標mAb候補製品を開発している。この候補製品は現在1/2 a期の臨床研究にあり、嚢胞性繊維化基金会によって援助されている。AR-501は、嚢胞性線維症患者の肺感染を治療するための吸入可能エアロゾルとして使用される。臨床前研究によるとbrに感染したマウスは緑膿菌救助は、1回の吸入曝露された霧化AR−501によって行うことができる。IND申請を提出し,その後2018年12月に1/2 a段階試験を開始した。健常成人臨床研究の第1段階が完了し,2020年に結果が報告された。2021年上半期に嚢胞性線維症患者の2 a期臨床研究が開始される予定である。AR-501はFDAから迅速チャネルと合格した感染症製品(QIDP)認証が授与されている。第2 a段階試験の登録は最近終了しており,2023年第1四半期に最も良い結果が予想される。 | |
| ● | AR-701 は新冠肺炎回復期患者から発見されたSARS-CoV-2ウイルス上の複数の蛋白エピトープに対する全ヒトモノクロナル抗体のカクテルである。その処方は筋肉注射やネブライザーを用いて吸入される。AR-701カクテルの2つのモノクロナル抗体は、すべての本格的なSARS-CoV-2ベータ、ガンマ、デルタ、エシロン、オミック変異株を中和した体外培養単独あるいは併用した場合、オミック感染マウスのウイルスを完全に根絶し、マウスを疾患病理影響から保護することができる。 | |
| ● | AR-401 は我々のmAb発見計画であり、治療を目的としているバウマンアシネトバクター血流、肺、および皮膚感染において流行しているグラム陰性細菌。著者らは我々のMabIgX技術を用いて新しい標的 を識別し、細菌外膜蛋白に結合する全ヒトmAb候補をいくつか選択した。我々はより多くの臨床前研究のために開発候補案を選択する予定である。 |
これまで、私たちは公共投資と個人投資を通じて1億53億ドル以上を調達した。また、衛生公衆サービス部(DHHS)、国家衛生研究院(NIH)と生物医学高度研究開発機構(BARDA)からの約3,200万ドル、国防部、PATH/ゲイツ財団、嚢胞性繊維化財団と他の戦略研究と開発協力からの約1,200万ドルを含む約5,300万ドルの非希釈報酬と贈与を得て、私たち自身の財務資源を増加させた。私たちは、私たちが大量の財務投資と贈与資金を誘致することができ、これは新しい抗感染製品に対する公認の需要と私たちの候補製品の組み合わせの実力を顕著にすると信じている。
著者らは高級管理チームを結成し、豊富な製品開発経験を持ち、複雑な薬物開発と監督経路を制御することに成功した記録がある。我々の管理チームは,Abgenix,Inc.,Aviron,Genentech,Inc.,グラクソ史克,羅氏,医療免疫(アスリーカン),ノワールなどの検証されたバイオ製薬会社で175年を超える共同薬物開発経験を有し,年間売上高数十億ドルの製品の開発と発売に貢献している。
| 3 |
私たちの業務に関するリスク
私たちbrは後期バイオ製薬会社で、私たちの業務と業務戦略を実行する能力は多くのリスクの影響を受けています。あなたが私たちの普通株を購入することを決定する前に、あなたはこれらのリスクを意識すべきです。特に、“リスク要因”というタイトルの章で詳細に議論されているリスクを考慮すべきですが、これらに限定されません
| ● | 私たち は予測可能な未来に、純損失は引き続き増加し、私たちは永遠に実現したり、利益を維持したりしないかもしれないと予想している。 | |
| ● | 今回の発売後の利用可能な現金資源は、今後12ヶ月後の運営資金需要を満たすのに十分ではないかもしれません。 | |
| ● | もし私たちが臨床試験を成功させられなかったり、監督部門の許可を得られなかったり、私たちの候補製品を商業化することに成功しなかったら、私たちの業務は損害を受け、私たちの証券価値は低下するだろう。 | |
| ● | われわれ,br}やわれわれの協力者は,臨床試験の完成に遅れている可能性があり,全く達成できない可能性がある。 | |
| ● | 我々のbr候補製品は新しい技術に基づいており,これは我々が解決できない可能性のある開発問題を引き起こす可能性があり,承認を延期したり阻止したりする規制問題,あるいは候補製品の開発を阻害する人員問題を引き起こす可能性がある. | |
| ● | 規制機関は臨床試験で安全性と有効性の終点に達していても、私たちの候補製品を承認しないかもしれない。 | |
| ● | 私たちは広範な研究開発努力と迅速な技術進歩を特徴とする業界で競争している。私たちの競争相手の新しい発見や商業開発は私たちの潜在的な製品を時代遅れにしたり競争力を失ったりするかもしれません。 | |
| ● | 私たちの競争相手は、私たちの候補製品よりも安く、より効果的で、より安全で、またはより早く発売された製品 を開発し、販売するかもしれません。これは、私たちが商業化する可能性のある任意の製品のビジネス成功を弱めるか、または除去することができます。 | |
| ● | 製品の販売とマーケティングを許可するほか、バイオ製薬業界はアメリカで厳しい監督と監督を受けている。 | |
| ● | 私たちは財務報告書の内部統制のいくつかの重大な欠陥を発見した。 | |
| ● | もし私たちが私たちの固有の権利を保護したり、権利侵害のクレームを弁護することができない場合、私たちは や利益運営を効果的に競争することができないかもしれない。 |
新興成長型会社としての影響
前期収入が10.7億ドルを下回る会社として、2012年に公布された“私たちの企業創業法案”や“雇用法案”で定義されている新興成長型企業の資格に適合している。新興成長型企業としては,低減された報告要求を利用する予定であるが,これらの要求はもともと上場企業に適用されている。これらの規定は含まれているが、これらに限定されない
| ● | 本募集説明書では、規定されている任意の監査されていない中期財務諸表に加えて、2年間の監査済み財務諸表の提出のみが許可されており、それに応じて“経営層の財務状況および経営結果の検討および分析” 開示が減少している | |
| ● | 2002年に改正されたサバンズ-オキシリー法第404節の監査役認証要件の遵守が要求されていない | |
| ● | 私たちの定期報告書、依頼書、登録書における役員報酬に関する開示義務を減少させた | |
| ● | 役員報酬および株主承認前に承認されなかった金パラシュート支払いについての拘束力のない諮問投票の要求を免除し、 | |
| ● | 民間会社の締め切りに応じて新しい会計基準を採用することができます。 |
| 4 |
私たちは5年以上の間にこれらの準備を利用して、私たちが新興成長型会社の資格を持たなくなるようにすることができます。しかし、いくつかの事件がこの5年末までに発生すれば、私たちが大型加速申告会社になること、私たちの年間総収入が10.7億ドルを超えること、あるいは任意の3年間で10億ドルを超える転換不可能な債券を発行した場合、私たちはこの5年末までに新興成長型会社ではなくなります。
我々 は、本募集説明書 が属する登録説明書のいくつかの減少した開示義務を利用することを選択し、将来の届出文書において他の減少した報告要件を利用することを選択することが可能である。したがって、私たちが株主に提供する情報は、あなたが株式を持っている他の公共報告会社から得た情報とは異なる可能性があります。
また、雇用法案は、新興成長型会社が延長された過渡期を利用して新たなまたは改正された会計基準を遵守することができると規定している。この規定は、これらの基準が民間企業 に適用されるまで、上場企業と民間企業に対して異なる移行日を有する新規または改訂された会計基準の採用を延期することを可能にする。私たちはこの延長された過渡期を使用することを選択した。今回の選挙のため、私たちがこれらの基準を遵守したスケジュールは、今回の選挙を利用する資格がない他の上場企業や今回の選挙を行う資格のない上場企業よりも遅れることが多い。したがって、我々の財務諸表は、上場企業のこれらの基準の発効日を満たす会社の財務諸表と比較できない可能性があります。
我々 は現在“小さな報告会社”の資格を満たしているが,この用語は1934年の証券取引法 でのルール12 b−2で定義されているからである。新興成長型企業になる資格がなくなった後、“小規模報告会社”の資格を引き続き満たしていれば、新興成長型企業として得られるいくつかの免除は、(1)サバンズ オックススリー法案404(B)節の監査役認証要件を遵守する必要がないこと、(2)役員報酬を比例的に開示すること、および(3)3年ではなく、2年間の監査済み財務諸表の提供のみを要求することを含む、新興成長型会社になる資格がなくなる可能性がある。
企業情報
我々brは2003年4月24日にカリフォルニア州で“Aridis,LLC”という名称で設立された有限責任会社である。2004年8月30日、私たちは“アリディス製薬有限責任会社”と改称した。2014年5月21日、私たちはデラウェア州の“Aridis PharmPharmticals,Inc.”という会社に変わりました。私たちの財政年度は12月31日に終わるだろう。私たちの主な実行事務室はカリフォルニア州ロスガトス大学通り983 B棟にあり、郵便番号:95032。私たちの電話番号は(408)385-1742です。私たちのサイトの住所はWww.aridispharma.com. 本募集説明書には、本募集説明書に含まれる情報や、本サイトを介してアクセス可能な情報は含まれていません。本募集説明書には、非アクティブテキストとしてのみ、当社のサイトアドレスが含まれています。
我々 は,本入札明細書で使用されている複数の商標の専有権を有しており,これらの商標は我々の業務にとって非常に重要である.便宜上、本募集説明書に記載されている商標及び商品名は含まれていません®商標記号であるが、そのような参照は、そのそれぞれの所有者が、適用法に従ってその権利を最大限に主張するいかなる指示もしないと解釈されるべきではない。本明細書に記載されている他のすべての商標、商号、サービスマークは、そのそれぞれの所有者の財産である。
| 5 |
製品
| 売却株主が提供する普通株 | 7,207,208株普通株式は、発行された株式承認証を行使する際に発行することができる | |
| 見積もり 価格 | 株式を売却する株主は、公開または私的取引により、その株式の全部または一部を現行の市場価格または私的に合意された価格で売却することができる。 | |
| 今回の発行後すぐに普通株式 を発行します | 28,012,008 shares | |
| 収益を使用する | 私たち は株を売る株主から普通株を売却して何の収益も得ません。しかし、すべての株式承認証が現金で行使されれば、私たちは約8,000,000ドルの毛収入を得るだろう。本募集説明書の“収益の使用”と題する章を参照してください。 | |
| リスク要因 | あなたは7ページ目からの“リスク要因”の部分を読んで、 が私たちの普通株に投資することを決定する前によく考慮すべき要素を知るべきです。 | |
| 配当政策 | 私たちは私たちの普通株に配当金を支払ったことがなく、予測可能な未来にも何の配当も支払わないだろう。 | |
| ナスダック資本市場記号 | “ARDS” |
今回の発行後に発行される普通株式数 は、2022年11月30日までに発行された普通株の20,804,800株 に基づいており、含まれていない
| ● | 2,117,847株私たちの普通株は、オプションを行使する時に発行することができ、2022年11月30日までの発行済み普通株を購入することができ、加重平均行権価格は1株当たり7.35ドルである | |
| ● | 14,846,404株の私たちの普通株式は、引受権証を行使する際に発行することができ、2022年11月30日までの発行済み普通株を購入することができ、加重平均行権価格は1株当たり1.19ドルである | |
| ● | 私たちが予約した765,711株普通株は、私たちの株式激励計画の下での将来の付与または奨励に使用される |
| 6 |
リスク要因
私たちの証券に投資することは高度な危険と関連がある。あなたが私たちの証券を購入することを決定する前に、本募集説明書と私たちが引用して本募集説明書に含まれるすべての情報をよく考慮して評価しなければなりません。あなたは特に2021年12月31日までのForm 10-K年次報告書の“リスク要因”のタイトルに記載されているリスクと不確実性を慎重に考慮して評価しなければならない。以下および年間報告書に記載されている任意のリスクおよび不確実性は、当社の業務、経営業績および財務状況に重大な悪影響を及ぼす可能性があり、これらのリスクおよび不確定要素は、本募集説明書が提供する任意の証券の価値に重大な悪影響を及ぼす可能性がある。したがって、あなたは投資の全部または一部を失うかもしれない。
| 7 |
前向き陳述に関する警告的説明
この目論見書にはリスクと不確実性に関する前向きな陳述が含まれている。あなたはこのような前向きなbr陳述に過度に依存してはいけない。多くの理由から、私たちの実際の結果は、 私たちの“目論見説明書要約”、“収益の使用”、“リスク要因”の部分に記載されている理由を含む前向き陳述の予想と大きく異なる可能性がある。 は、場合によっては、“予想”、“信じ”、“継続”、“可能”、“依存”、“推定”、“予想”、“意図”、“可能”、“進行中”などの用語で識別することができる。すべての前向き表現がこれらの語を含むわけではないが、“ ”“計画”、“潜在”、“予測”、“プロジェクト”、“すべき”、“会する”、“できる”、またはこれらの用語の否定または他の類似表現である。
私たちの運営と業務の見通しは常にリスクと不確実性の影響を受けています
| ● | 規制当局が申請を提出した時間 | |
| ● | 私たちは、私たちの既存の候補製品と私たちが開発する可能性のある他の候補製品に対する規制部門の承認と、私たちが得る可能性のある任意の承認下のラベルを取得して維持することができます | |
| ● | 臨床試験の承認は規制機関によって延期されたり差し止めされる可能性がある | |
| ● | 臨床前と臨床研究は成功せず、早期の結果を確認することもなく、期待に達することもなく、監督管理要求を達成することもなく、商業成功の性能閾値を達成することもない | |
| ● | 臨床試験の時間とコスト、その他の費用の時間とコストに関するリスク | |
| ● | 第三者からの資金獲得に関するリスク ; | |
| ● | 管理と従業員の操作とリスクの実行 | |
| ● | キーパーソン流失 ; | |
| ● | 競争する | |
| ● | 製品市場受容度に関するリスク ; | |
| ● | 知的財産権リスク ; | |
| ● | Br市場規模、私たちの製品のメリット、製品定価、製品発表時間を仮定します | |
| ● | 将来の財務結果の不確実性に関するリスク ; | |
| ● | この製品に関するリスク ; | |
| ● | 協力者やパートナーを引き付ける能力と | |
| ● | 我々は第三者組織に依存するリスク である. |
本募集説明書におけるbr前向き陳述は、目論見書の発表日までの我々の観点を代表する。私たちは後続の事件と事態の発展が私たちの観点を変化させると予想している。しかし、私たちは将来のある時点でこれらの前向き宣言を更新することを選択するかもしれませんが、法的要求が適用されない限り、私たちは現在そうするつもりはありません。したがって、あなたはこのような展望的な陳述に依存して、本募集説明書の日付の後の任意の日付として私たちの観点に依存してはいけません。
| 8 |
収益を使用する
私たちは今回の発行で私たちの普通株のいかなる株式も売却しませんし、売却株主が私たちの普通株を売却した株式から何の収益も得ません。株を売却する株主は、当社がここで発売した普通株を売却するすべての収益を得ることになる。
我々 は,任意の権利行使時に行使価格を受け取るが,現金で行使する.もしすべての株式証明書が現金で行使されれば、私たちは約8,000,000ドルの毛収入を得るだろう。しかし、株式承認証所有者は持分証を行使する義務がなく、著者らは持分証保有者がいつ全部或いは部分的に株式承認証を行使することを選択するかどうかを予測できない。したがって、このような行使の任意の収益は、一般会社用途および運営資本に使用されるだろう。
| 9 |
配当政策
私たちは私たちの普通株についていかなる現金配当金を支払うか発表したことがありません。私たちは予測可能な未来に私たちの普通株に対していかなる現金配当金も支払わないと予想しています。私たちはすべての利用可能な資金と任意の未来の収益を維持して、私たちの業務の発展と拡張に資金を提供するつもりです。 将来配当金を派遣するかどうかは私たちの取締役会が適宜決定し、多くの要素に依存して、私たちの運営結果、財務状況、将来の見通し、契約制限、法律適用制限 及び私たちの取締役会が関連していると思う他の要素を含む。
| 10 |
売却株主
2022年10月5日、吾らはある認可投資家と証券購入協定を締結し、この合意に基づいて、吾らは合計1,800,000株の普通株、1株当たり額面0.0001ドル及び予融資権証を売却し、登録直接発売方式で購入価格1,11ドルで合計5,407,208株の普通株を購入した。株式と事前資金の引受権証を売却するとともに、登録されていない引受権証を投資家に売却し、私募で最大7,207,208株の普通株を購入し、本募集説明書によると、これらの普通株はすべて転売が登録されている。
証券br法案の登録条項によると、売却株主が転売株式を獲得する取引は影響を受けない。
以上述べた転売株式は、転売株式の公開発行を許可するために登録されており、売却株主は、本募集説明書に基づいて転売株式を随時提供することができる。株式を売却する株主は、証券法の登録要求に制限されないか、またはこれらの株式に関する別の有効な登録声明に基づいて、取引中にその株式の全部または一部を売却、譲渡またはその他の方法で処分することができる。
以下の表には、本募集明細書における売却株主および転売株式に関するいくつかの情報が示されている。表足注で述べたことや、我々の株式や他の証券の買収によるものを除き、売却株主は過去3年間で吾などと大きな関係はない。
利益を得たbrの所有権は米国証券取引委員会の規則によって決定される。次の表の売却株主の私たちが発行した普通株に対する所有率は、2022年11月30日現在の20,804,800株の発行済み普通株に基づいている。
| 売却株主名 | 株式の数 ごく普通である 在庫品 有益な 持っている その前に 製品(1) | パーセント 共通の 在庫品 有益な 持っている その前に 奉納する | の株 提供 | の株 在庫品 有益な 持っている この後 製品(2) | パーセント 共 個 在庫品 実益は を持つ この後 製品(2) | |||||||||||||||
| 停戦資本主基金有限会社(3) | 2,080,000 | 9.9 | 7,207,208 | 2,080,000 | 9.9 | |||||||||||||||
(1) 適用された米国証券取引委員会規則によれば、誰もが、その人が60日以内に任意のオプションまたは株式承認証を行使することによって、または転換可能な証券を変換することによって得られる権利を有するとみなされる。また、適用される米国証券取引委員会規則によれば、 個人は、それが直接または間接的に所有する証券の“実益所有者”、または証券に対する投票権または直接投票権、または(B)投資権を含む株式(A)投票権、または(B)投資権を含み、いずれの場合も、その人の証券における経済的利益にかかわらず、br}を処分または直接処分する権限を含む。我々の知る限り,コミュニティ財産法が適用される場合,表に記載されている各人は,表の足注で別途説明されない限り,その売却株主実益が持つ普通株に対して唯一の投票権と投資権を持つ.
(2) は,売却株主が今回の発売完了後に保有する株式数を表し,その根拠は,(A)今回の発売完了まで,売却株主が本募集説明書に登録売却されたすべての転売株式を買収または売却しないこと,および(B)我々普通株の他の株式は売却されないという仮定である.しかしながら、各売却株の株主は、本願明細書に従って提供された全て、一部または全部の転売株式を売却することができ、規則144に基づくことを含む、証券法の下の別の登録声明に従って、彼らが所有する可能性のある我々の普通株の他の株式を売却するか、または証券法登録条項の免除に従って、規則144に基づく株式の一部または全部を売却することができる。
(3) は、(I)1,800,000株の普通株式および(Ii)280,000株が事前資本承認株式証を行使する際に発行可能な普通株を含み、 は、売却株主が保有するいくつかの実益所有権の制限によって制限される。これらの株式は、ケイマン諸島免除会社(“総基金”)を獲得した停戦資本総基金有限会社が直接保有しており、(I)停戦資本有限責任会社(“停戦資本”)は、総基金の投資マネージャーとして、および(Ii)Steven Boydは、停戦資本の管理メンバーとしての間接実益と見なすことができる。停戦資本とSteven Boydは実益株式の所有を拒否したが、彼らそれぞれの金銭的利益の範囲内では除外した。停戦資本主基金有限会社の住所はC/o停戦資本有限責任会社で、住所:ニューヨークマディソン大通り510号、7階、NY 10022。報告された株式所有権には、本プロトコルに従って登録された引受権を行使する際に発行可能な7,207,208株の普通株式(Br)は含まれておらず、この等株式権証は現在行使できないためである。
| 11 |
流通計画
証券の売却株主およびその任意の質権者、譲受人および利益相続人は、本合意でカバーされている任意または全部の証券を、ナスダック資本市場または任意の他の証券取引所、市場または取引機関でいつでも販売することができる。これらの販売は固定または協議された価格かもしれない。株式を売却する株主は、証券を売却する際に、以下のいずれか1つまたは複数の方法を使用することができる
| ● | 一般ブローカー取引と自営業業者がバイヤーを誘致する取引 | |
| ● | 取引業者は、代理として証券を販売しようと試みるが、第brブロックの一部を依頼者として頭寸および転売して取引を促進することができる | |
| ● | 仲買業者は元金として購入し、仲買自営業者が転売した | |
| ● | 取引所を適用する規則による取引所割当; | |
| ● | 個人的に協議した取引 | |
| ● | 本募集説明書に属する登録説明書の発効日後に達成される空売り決済; | |
| ● | ブローカーによる取引では,販売株主と合意し,証券ごとの約定価格で一定数のこのような証券を販売する | |
| ● | オプション取引所を通過しても他の方法でも、オプションまたは決済オプションまたは他のヘッジ取引によって取引される | |
| ● | このような販売方法の組み合わせ;または | |
| ● | 法律で許可されている他のどんな方法も適用される。 |
株式を売却する株主は、規則144または改正された1933年証券法(“証券法”) に従って得られた任意の他の免除により、本募集説明書に従って証券を売却するのではなく、任意の他の免除登録売却証券を取得することができる。
販売株主が招聘した自営業者は他の経営者を手配して販売に参加することができる。ブローカーは、売り手株主(または、任意のブローカーが証券買い手の代理人として機能する場合、買い手)から手数料または割引 を受け取ることができ、金額は交渉される必要があるが、本募集明細書の付録に記載されていることを除いて、代理取引がFINRA規則2121に規定された慣行ブローカー手数料を超えない場合、および主要取引の場合、FINRAルール2121に従って値上げまたはbr}が値下げされる。
証券又はその権益を売却する過程において、株式を売却する株主は、仲買業者又は他の金融機関とヘッジ取引を行うことができ、ブローカー又は他の金融機関は、その保有株式をヘッジする過程で空売り証券を行うことができる。株式を売却する株主は、空売りしてこれらの証券を平倉に渡したり、証券をブローカーに貸し出したり、自営業者に譲渡したりすることができ、ブローカーはこれらの証券を売却することができる。株式を売却する株主は、ブローカーまたは他の金融機関とオプションまたは他の取引を締結することもでき、または本募集明細書によって提供される証券をブローカーまたは他の金融機関に渡すことを要求する1つまたは複数の派生証券を締結することができ、ブローカーまたは他の金融機関は、本募集説明書に従って証券を転売することができる(これらの取引を反映するために補充または改訂される)。
株式を販売する株主および証券の販売に関与する任意のブローカーまたは代理人は、証券法が指すそのような販売に関連する“引受業者”と見なすことができる。この場合、そのようなブローカーまたは代理人が受信した任意の手数料およびその購入した証券を転売する任意の利益は、証券法に規定された引受手数料または割引とみなされる可能性がある。株式を売却した各株主は、任意の者と直接または間接的な書面または口頭協定または了解br}分譲証券を持っていないことを当社に通知した。
Br社は証券登録による何らかの費用と支出を支払う必要がある。会社のbrは、証券法に基づく責任を含む、売却株主のいくつかの損失、クレーム、損害、責任の賠償に同意した。
我々は、株を売却する株主 が株式承認証または株式承認証の行使後に発行可能な普通株を所有しなくなるまで、ビジネス上の合理的な努力を尽くして本登録声明を常に有効にすることに同意する。
“取引法”が適用される規則と条例によると、証券の販売販売に従事している人は同時に を販売開始前の適用制限期間内に、規則Mで定義されているように、普通株に関する市活動に従事してはならない。また、株式を売却する株主は、株式を売却する株主又は他の人が普通株を購入及び売却する時間を制限することができる規則Mを含む取引法及びその下の規則及び条例の適用条項に制限される。株式を売却する株主に本募集説明書のコピー を提供し、売却時または前に、本募集説明書のコピーを各バイヤーに渡す必要があることを通知した(証券法第172条の規定を遵守することを含む)。
| 12 |
法務
我々が今回の発行で提供した普通株式発行の有効性は,ニューヨークLLPニューヨークのSeppard,Mullin,Richter& Hamptonによって伝達される.
専門家
Ardis PharmPharmticals,Inc.(“会社”)2021年12月31日までおよび2020年12月31日までの年度連結財務諸表は,会社が2021年12月31日までの年次報告Form 10−Kに掲載され,独立公認会計士事務所Mayer Hoffman McCann P.C.がその報告に監査を行っている(この報告には説明的な 段落が含まれており,会社が経営を継続できるかどうかを説明している),また、上記の報告を行う際には、会計および監査専門家事務所の権威に依存して引用によって本明細書に組み込まれる。
ここで詳細な情報を見つけることができます
本募集説明書は、我々が証券法に基づいて米国証券取引委員会に提出したS-1表登録説明書の一部であり、 は登録説明書及びその添付ファイルのすべての情報を含まない。本入札明細書および本入札明細書によって提供される普通株式に関するより多くの情報は、登録説明書およびファイルの一部としてアーカイブされた証拠物を参照しなければならない。 本入札説明書に含まれる任意の契約または言及された任意の他の文書の内容に関する記述は必ずしも完全ではなく、 は、それぞれの場合、登録説明書の証拠物としてアーカイブされた契約または他の文書のコピーを参照してください。これらの陳述の各々 は,すべての点で本参考文献によって制限されている.
我々 は“取引法”の報告要求を遵守し,年度,四半期と現在の報告,依頼書,その他のbr情報を米国証券取引委員会に提出する。あなたはインターネットを通じて私たちのアメリカ証券取引委員会の届出書類を読むことができます。登録声明、アメリカ証券取引委員会のサイト を含むHttp://www.sec.govそれは.ウェブサイトを維持していますHttp://www.aridispharma.comこれらの材料を電子的にアーカイブしたり、米国証券取引委員会に提供したりした後、合理的で実行可能な範囲でできるだけ早く無料で取得することができます。本入札説明書には、本入札明細書に含まれる、または本サイトを介してアクセス可能な情報 は含まれていない。
いくつかの情報を引用統合することにより
アメリカ証券取引委員会は、私たちが引用合併を通じて彼らに提出した情報を許可する。引用統合により、他の文書を参照して、 の重要な情報を開示することができます。引用によって組み込まれた情報は、本入札説明書の重要な構成要素であり、後で米国証券取引委員会に提出された情報は、この情報の代わりに自動的に更新され、代替される。我々は、証券法に基づいて、本募集説明書に基づいて発行された証券に関するS-1表登録声明を米国証券取引委員会に提出した。米国証券取引委員会が許可した場合、本募集説明書は、登録説明書に含まれるいくつかの情報を見落としている。私たちおよび本募集説明書に従って発行された証券のより多くの情報については、証拠物を含む登録声明を参照してください。登録説明書に提出するか、または参照して登録説明書中のいくつかの文書に組み込む条項に関する本入札明細書の宣言は、必ずしも完全ではなく、各宣言は、すべての態様で参照によって制限される。本明細書の全部または任意の部分のコピーは、本明細書に記載された文書または証拠品を参照することによって、所定のレートの支払い後に、上述した“どこでより多くの情報を見つけることができるか”に列挙された米国証券取引委員会事務所で取得することができる。私たちが参照することによって、私たちがアメリカ証券取引委員会に提出した次の書類と、その後、取引法第13(A)、13(C)、14または15(D)条に従って提出されたすべての文書を入れましたが、このような条項に従って提出された任意の未来の報告または文書の任意の部分は除外されていません
1. 社の2021年12月31日までのForm 10-K年報は、2022年4月13日に米国証券取引委員会に提出された
2.br社が2022年4月19日に米国証券取引委員会に提出した付表14 Aに関する最終委託書;
3.br社が2022年5月16日に米国証券取引委員会に提出した2022年3月31日までの3カ月間の10-Q表四半期報告
| 13 |
4.br社は2022年8月16日に2022年6月30日までの3ヶ月間の10-Q表季報を米国証券取引委員会に提出した
5. 社は2022年11月21日に2022年9月30日までの3ヶ月間の10-Q表季報を米国証券取引委員会に提出した
6.付表14 Aに関する会社の最終委託書が2022年4月19日に米国証券取引委員会に提出された
7.br社が2022年1月19日、2022年4月15日、2022年6月6日、2022年6月27日、2022年8月15日、2022年10月5日に提出した現在の8-Kレポート
8.募集説明書に含まれる会社普通株の説明は、当該説明を更新するために提出された任意の改訂または報告を含む改訂(第333-226232号文書)のS-1表における登録説明の一部を構成する。
私たちはまた、その後、第13(A)、13(C)条に従って米国証券取引委員会に提出されたすべての文書(Form 8-K第2.02項または第7.01項によって提供された現在の報告およびこの表に保存されているこのような項目に関連する証拠)を引用により統合した。本募集説明書が作成した証券の発売を終了する前に、取引所法第14又は15(D)条の規定 (本募集説明書が属する初期登録書の日付の後、登録書が発効する前に提出された書類を含む)。これらのファイルは、Form 10-K年間レポート、Form 10-Q四半期レポート、およびForm 8-K現在のレポート、および依頼書のような定期的なレポートを含む。
本募集説明書または参照によって本明細書に組み込まれ、または本明細書に組み込まれた文書に含まれる任意の 陳述は、修正または置換とみなされるであろう。ただし、本募集説明書またはその後に提出された任意の引用によって本明細書に組み込まれた文書 に含まれるとみなされる陳述は、その陳述を修正または置換している
電話(408)385-1742に電話することによって、または以下のアドレスに手紙を書くことで、これらのファイルのコピーを要求することができます
アリディス製薬会社
大学通り983号B棟
カリフォルニア州ロスガトス95032 送信者:秘書
| 14 |