
アメリカです
アメリカ証券取引委員会
ワシントンD.C.,20549
表格8-K
現在 報告
第十三条又は十五条によれば
“1934年証券取引法”
報告日(最初の報告事件日):2022年12月6日
YUMANITY治療会社は
(登録者の正確な氏名はその定款に記載)
| デラウェア州 | 001-37695 | 20-8436652 | ||
| (国やその他の管轄区域 法団に成立する) |
(手数料) ファイル番号) |
(税務署の雇用主 識別番号) |
| お客様街40号、4410号室 マサチューセッツ州ボストン |
02135 | |||
| (主にオフィスアドレスを実行) | (郵便番号) | |||
登録者の電話番号は市外局番を含んでいます617-409-5300
適用されない
(前の名前または前の住所は、前回の報告から変更された場合)
Form 8-K届出の目的が登録者が次のいずれかの規定(一般説明A.2参照)の届出義務を同時に満たすことである場合は,次の該当する枠をチェックしてください。以下に示す):
| 証券法第425条に基づく書面通知(“連邦判例編”第17巻、230.425ページ) |
| ☐ | “取引法”規則14 a−12による材料募集(17 CFR 240.14 a−12) |
| ☐ | 取引法第14 d-2(B)条(“連邦判例アセンブリ”第17編240.14 d-2(B)条)に基づいて開市前通信を行う |
| ☐ | 取引法第13 E-4(C)条(17 CFR 240.13 E-4(C))に基づいて開業前通信を行う |
同法第12条(B)に基づいて登録された証券:
| クラスごとのタイトル |
取引 記号 |
各取引所名 それに登録されている | ||
| 普通株は一株当たり0.001ドルの価値があります | YMTX | ナスダック資本市場 |
登録者が1933年“証券法”第405条(本章230.405節)又は1934年“証券取引法”第12 b-2条(本章第240.12 b-2節)で定義された新興成長型会社であるか否かをフックで示す
新興成長型会社☐
新興の成長型企業であれば、登録者が延長された移行期間を使用しないことを選択したかどうかを再選択マークで示して、取引所 法案第13(A)節に従って提供された任意の新しいまたは改正された財務会計基準を遵守してください
| 7.01項。 | “FD開示条例” |
先に開示したように、2022年6月5日、デラウェア州のYumanity治療会社(Yumanity)はJanssen製薬会社(Janssen PharmPharmtica NV)と資産購入協定(資産購入協定)を締結した。資産購入協定に署名するとともに、2022年6月5日、Yumanityはワシントン社Kineta,Inc.およびYacht Merge Sub,Inc.と協定および合併計画 を締結し、Kineta Inc.はワシントン会社であり、Yumanityの完全子会社でもある
Kinetaは2022年11月29日、Kineta最高経営責任者Shawn Iadonato博士が、仮想投資家活動であるJMP証券血液学と腫瘍学サミット(The Summit)に出席することを発表し、2022年12月6日から7日まで開催される。2022年12月6日,Iadonato博士はKVA 12123(従来KVA 12.1と呼ばれていた),KinetaのVista遮断免疫療法の企業更新と概説を紹介した。以下,首脳会議で作成したスライドプレゼンテーションを添付ファイル99.1として添付する
本項目7.01の情報は、本明細書に添付された添付ファイル99.1を含めて提供され、改正された1934年の証券取引法(“証券取引法”)第18節に基づいて提出されたとみなされてはならないし、この部分の責任を他の方法で担っているものとみなされてはならないし、このような文書にこのような文書に明記されていない限り、改正された“証券法”(“証券法”)または“取引法”に基づいて提出された任意の文書を参照して組み入れられたものとみなされてはならない
重要な情報とどこで見つかりますか
このbr通信は、YumanityとKinetaとの間およびYumanityとJanssenとの間の提案取引に関する募集材料と見なすことができる。提案された取引について、Yumanityは2022年8月29日に米国証券取引委員会(米国証券取引委員会)にS-4表登録声明(初期登録声明)を提出し、2022年10月3日に米国証券取引委員会の初期登録声明修正案1、2022年10月24日に米国証券取引委員会の初期登録声明修正案2、2022年11月4日に米国証券取引委員会の初期登録声明修正案3(初期登録声明、登録声明とともに)を提出した後、その中には初歩的な委託書と目論見書が含まれている。登録声明は2022年11月10日に米国証券取引委員会 によって発効が発表された。Yumanityはその後、2022年11月10日に登録された株主に郵送された最終的な依頼書/目論見書(依頼書)を2022年11月10日に提出した。Yumanityは2022年12月5日、米国証券取引委員会に申請を提出し、登録 声明(募集説明書補編)に記載されている依頼書と募集説明書の補充として、2022年11月4日の終値時に登録されている株主に郵送した。YumanityおよびKinetaの投資家および証券所有者は、Yumanity、Kineta、および提案された取引に関する重要な情報を含むので、これらの材料が利用可能なときにこれらの材料を読むことを提案する。本通信は、登録声明、依頼書、目論見書の補編又はその他の書類の代わりにすることはできません
Yumanityは、提案中の取引について米国証券取引委員会に申請を提出するか、証券保有者に送信する可能性がある。投資家および証券所有者は、米国証券取引委員会に提出された文書を取得すると、ユーマンニのウェブサイトwww.yumanity.comまたは米国証券取引委員会のウェブサイトwww.sec.gov上で無料コピーを取得するか、またはユーマニーの投資家関係部に電話(212)213−0006 extで要求することができる。331
本通信は、売却要項を構成したり、売却要項を求めたり、任意の証券を購入する要約を求めたりするものではなく、いかなる司法管区の証券が法律に規定されている登録又は資格の前に、いかなる司法管区でこのような要約を売却し、勧誘又は売却することが違法である証券を販売してもならない。証券法第10節の要求に適合する目論見書を通過しない限り、証券を発行してはならない
活動の参加者を募集する
Yumanity、Kinetaおよびそのそれぞれの役員および幹部は、提案取引についてYumanity株主に依頼書を募集する活動に参加すると見なすことができる。Yumanity幹部と取締役に関する情報は,Yumanityが2022年4月25日に米国証券取引委員会に提出した2022年株主総会の付表14 Aに関する最終依頼書 に掲載されている。これらの個人の利益に関する他の情報は、委託書に記載されており、米国証券取引委員会に提出された任意の他の関連文書で明らかにされる。これらの個人は、Yumanity株主のための依頼書募集活動に参加しているとみなされる可能性がある。上述したように、これらの文書のコピーを無料で得ることができます
前向きな陳述に関する警告的声明
この現在の8-K表報告書および添付文書によって提供される添付ファイルは、1995年の民間証券訴訟改革法の安全港条項に基づいて行われた陳述を含む前向きな陳述を含む。これらの陳述は、前向き陳述を識別することを目的とした目標、予測、信じ、可能、意図、推定、期待、予測、目標、意図、意図、可能、可能、潜在、探索、意志、類似の語およびフレーズによって識別されることができる。これらの展望的陳述は、取引がいつ完了するか、提案された取引の構造、時間、および完了に関する陳述、合併後の会社が提案された後にナスダックに上場することに関する提案、合併後の会社の所有権構造の予想、合併後の会社の予想幹部および取締役、合併後のユマンおよびKinetaおよび合併後の会社のそれぞれの提案合併終了時の予想現金状況を含むが、これらの展望的陳述は、ユマニニとKineta間の提案合併およびヤンソンへの資産売却に関する提案を含むが、これらに限定されない。合併後の会社の将来業務;合併後の会社の性質、戦略と重点;合併後の会社の任意の候補製品の開発と商業潜在力及び潜在利益;合併後の会社の幹部と取締役会構造;合併後の会社本部の所在地;期待される臨床前と臨床薬物開発活動と関連スケジュール, データおよび他の臨床および臨床前結果の予想される時間を含む;Kinetaはそのパイプラインを推進するのに十分な資源を持っている;および他の非歴史的事実の陳述。これらのリスクおよび不確実性のため、実際の結果およびイベントの時間は、このような前向き陳述において予想されるものと大きく異なる可能性があり、これらのリスクおよび不確実性は、(1)取引の完了条件が満たされていないリスクを含むが、これらに限定されない。(Ii)提案取引完了時期に関する不確実性、ならびにYumanity、Kineta、Janssen、および証券購入協定の当事者(期日は2022年6月5日、2022年10月24日および2022年12月5日に改正された)のそれぞれが、提案合併、資産売却、または証券購入協定によって予想される取引を完了する能力(適用状況に応じて決定される)。(Iii)Yumanityがその運営費用を管理する能力に関連するリスクと、完成しようとする取引に関連する費用と、(Iv)取引所の完了を完了するために必要な任意の政府または半政府エンティティの承認を得ることができないか遅延することに関連するリスク、(V)交換比率の調整により、Yumanity株主とKineta株主が合併後の会社のより多くまたは少ない株式を所有する可能性があるリスク、(Vi)交換比率に対するYumanity普通株の市場価格に関連するリスク、(Vii)意外なコスト, 1つまたは2つの提案取引所によって生成される費用または支出;(Viii)提案取引の発表または完了によってビジネス関係に生じる潜在的な不良反応または変化;(Ix)#でYumanity株主に割り当てられた配当金の金額
資産売却との関連(あれば)は現在の予想を下回る可能性がある;(X)合併後の会社は、これらの候補製品およびその臨床前計画を推進し続けるために十分な追加資本を得ることができないリスク、(Xi)候補製品のための成功した臨床結果の不確実性、およびそれによって引き起こされる可能性のある意外なコスト、(Xii)候補製品および開発および予想されている臨床前計画から任意の価値を達成できなかったリスク、これらのリスクは、候補製品を市場に押し上げることに成功した内在的なリスクおよび困難に基づいて開発された。およびbr(13)は、将来の財務および経営業績を含む、提案された取引を達成できない可能性のある予想収益に関連するリスクである。これらのリスクおよび不確実性のため、実際の結果およびイベントの時間は、これらの前向き陳述において予想されるものと大きく異なる可能性がある。これらおよび他のリスクおよび不確実性は、Yumanityが米国証券取引委員会に提出された最新年度または四半期報告書のリスク要因と題する章と、Yumanityが米国証券取引委員会に提出される予定の提案取引に関連する他の文書に記載された要因とを含む、米国証券取引委員会に提出された定期文書により包括的に記述されている。これらの前向きな陳述に過度に依存してはいけません。これらの前向きな陳述は、本プレスリリースの日または展望的な陳述で指摘された日にのみ行われてはなりません。法律に別の要求があることに加えて、Yumanityは、これに対する予期される任意の変化またはイベントの任意の変化を反映するために、本明細書に含まれる任意の前向きな陳述を更新または修正する義務を負わないか、または修正することを明確に示している, このような 宣言に基づいている条件や場合は任意である.
| 9.01項目。 | 財務諸表と証拠品です |
(D)展示品
| 99.1 | プレゼンテーションスライドは,2022年12月6日である. | |
| 104 | 表紙インタラクションデータファイル(イントラネットXBRL文書に埋め込まれている). | |
サイン
1934年の“証券取引法”の要求によると、登録者は本報告が正式に許可された署名名人がその署名を代表することを正式に促した
| ユーマニー治療会社は | ||||||
| 日付:2022年12月6日 | 差出人: | /s/リチャード·ピーターズ | ||||
| リチャード·ピーターズ | ||||||
| 社長と最高経営責任者 | ||||||

展示品99.1 2022年12月6日JMP証券血液学と腫瘍学サミット癌免疫耐性を解決する次世代免疫療法の開発

免責声明およびその他の情報本プレゼンテーションは、1995年の“プライベート証券訴訟改革法”の安全港条項に基づいて行われた陳述を含む前向き陳述を含む。これらの表現は、“目標”、“予想”、“信じ”、“可能”、“意図”、“推定”、“予想”、“予測”、“目標”、“意図”、“可能”、“潜在”、“求める”、“意志”などの語彙およびフレーズ、ならびにこれらの語彙およびフレーズの変形または同様の表現によって識別することができる。これらの前向き陳述は、Yumanity治療会社(“Yumanity”)とKineta社(“Kineta”)との間で提案された合併、および取引がいつ完了するかどうかを含むヤンソン製薬会社(“ヤンソン”)への資産売却に関する提案を含むが、提案された取引の構造、タイミング、完了に関する陳述、合併後の会社の提案合併終了後のナスダック上場に関する陳述、合併終了後の合併会社の所有権構造に関する予想;合併後の会社の期待幹部と取締役;合併後の会社と合併後の会社のそれぞれの期待現金状況;合併後の会社の将来業務;合併後の会社の性質、戦略と重点;合併後の会社の任意の候補製品の開発と商業潜在力及び潜在的利益;合併後の会社の幹部と取締役会構造;合併後の会社の会社本部所在地;期待される臨床前と臨床薬物開発活動と関連スケジュール, データおよび他の臨床および臨床前結果の予想される時間を含む;Kinetaはそのパイプラインを推進するのに十分な資源を持っている;および他の非歴史的事実の陳述。実際の結果およびbr}は、これらのリスクおよび不確実性のため、イベントの時間は、このような前向き陳述において予想されるものと大きく異なる可能性があり、これらのリスクおよび不確実性は、(I)提案された取引が条件を満たしていないリスクを含むが、これらに限定されない。(Ii)提案取引の完了時期に関する不確実性、ならびにYumanity、Kineta、Janssenおよび証券購入協定の当事者(期日は2022年6月5日、2022年10月24日および2022年12月5日に改正された)のそれぞれが、提案の合併、資産売却、または証券購入協定によって予想される取引を完了する能力(適用状況に応じて決定される)。(Iii)Yumanityがその運用費を管理する能力に関連するリスク、および完了しようとする取引に関連する支出、(Iv)提案取引所の完了に必要な任意の政府または半政府エンティティの承認を得ることができないかまたは遅延することに関連するリスク、(V)交換比率の調整により、Yumanity株主およびKineta株主が現在予想されている合併後の会社の株式を所有またはそれ以下である可能性があるリスク;(Vi)Yumanity普通株の為替レートに対するYumanityの市場価格に関連するリスク;(Vii)意外なコストコスト, 1つまたは2つの提案取引によって生じる費用または支出;(Viii)提案取引の発表または完了による潜在的な副作用またはビジネス関係の変化;(Ix)Yumanity株主に割り当てられた資産売却に関連する配当金額は、現在予想されているリスクを下回る可能性があり、(X)合併後の会社 とは、これらの候補製品およびその臨床前計画に関連するリスクを継続的に推進するために十分な追加資本を得ることができない、(Xi)候補製品が成功した臨床結果の不確実性およびそれによって引き起こされる可能性のある意外なコスト; (Xii)候補製品が市場への進出に成功したことに関連する固有のリスクおよび困難のため、候補製品および開発および開発されている臨床前計画から任意の価値を達成できなかったことに関連するリスク、および(Xiii)将来の財務および運営結果を含む、提案された取引を達成できない可能性のある予想収益に関連するリスク。これらのリスクおよび不確実性のため、実際の結果およびイベントの時間は、これらの前向き陳述において予想されるものと大きく異なる可能性がある。これらおよび他のリスクおよび不確実性は、Yumanityが米国証券取引委員会に提出した最新年度または四半期報告書の“リスク要因”と題する節に記載された要因、およびYumanityが米国証券取引委員会に提出した提案取引に関する他の文書を含む、米国証券取引委員会(“米国証券取引委員会”)に提出された定期文書により包括的に記述されている。あなたはこのような展望的な陳述に過度に依存してはいけない, これらの声明は、本プレスリリースが発行された日または展望的陳述で指摘された日にのみ行われる。法的に別の要求がない限り、Kinetaは、これに対する予期される任意の変化、またはそのような陳述に基づくイベント、条件、または状況の任意の変化を反映するために、本明細書に含まれる任意の前向きな陳述を更新または修正する義務を明確に負わない。2

免責宣言および他の情報、ならびに情報本プレゼンテーションをどこで検索するかは、YumanityとKinetaおよびYumanityとJanssenとの間の提案取引に関する募集材料とみなされる可能性がある。提案された取引に関連して、Yumanity は2022年8月29日に米国証券取引委員会にS-4表登録声明(“初期登録声明”)を提出し、2022年10月3日に米国証券取引委員会の初期登録声明の第1号修正案、2022年10月24日に米国証券取引委員会の初期登録声明を提出する第2号改正案、2022年11月4日に提出された米国証券取引委員会の初期登録声明の第3号改正案(初期登録声明、すなわち“登録 声明)を改正した後、その中には初歩的な委託書と目論見書が含まれている。“登録声明”は2022年11月10日に米国証券取引委員会によって発効が発表された。Yumanityはその後、2022年11月10日に登録された株主に郵送された最終的な依頼書/目論見書(“依頼書”)を2022年11月10日に提出した。Yumanityは2022年12月5日に米国証券取引委員会に申請を提出し、登録説明書に記載されている依頼書と募集説明書(“目論見補編”)の補充として、2022年11月4日の終値時に登録株主に郵送した。YumanityおよびKinetaの投資家および証券所有者は、Yumanity、Kineta、および提案取引に関する重要な情報を含むので、これらの材料が利用可能なときにこれらの材料を読むことを提案する。本プレゼンテーションは登録声明·依頼書の代わりにはなりません, 株式募集説明書Yumanityは、米国証券取引委員会に提出された、または提案取引に関連する任意の他の文書または証券所有者に送信された文書を送信することができる。投資家および証券所有者は、米国証券取引委員会に提出された文書を取得すると、ユーマンニのウェブサイトwww.yumanity.comまたは米国証券取引委員会のウェブサイトwww.sec.gov上で無料コピーを取得するか、またはユーマニーの投資家関係部に電話(212)213−0006 extで要求することができる。331.本陳述は、売却要約、要約売却又は任意の証券購入の要約を構成すべきではなく、いかなる司法管轄区でもこのような要約、勧誘又は売却を行ってはならず、任意のこのような司法管区の証券法に基づいて登録又は取得資格を取得する前に不正とみなされる任意の証券売却を行ってはならない。株式募集説明書が改正された“1933年証券法”第10節の要求に適合しない限り、証券を発行してはならない。株式募集書の参加者Yumanity、Kinetaおよびそれらのそれぞれの役員および幹部は、Yumanity株主に依頼書を求める提案取引に関連する参加者と見なすことができる。Yumanity幹部と取締役に関する情報は,Yumanityが2022年4月25日に米国証券取引委員会に提出した2022年株主総会に関する付表14 Aの最終依頼書に掲載されている。このような個人の利益に関する他の情報は、依頼書に記載され、米国証券取引委員会に提出された任意の他の関連文書に記載される。これらの個人は、Yumanity株主の依頼書募集に参加しているとみなされる可能性がある。上述したように、これらの文書の無料コピーを取得することができます。3

Kinetaは癌免疫耐性に対する次世代免疫療法 免疫耐性KVA 12123を開発している:潜在的に分化したVista遮断免疫療法は、2022年第4四半期にCD 27とCD 24腫瘍に対する免疫単一抗体計画固形腫瘍領域の巨大な市場機会 KAのナスダック上場予定2022年第4四半期に発売予定とYumanity治療会社計画の逆合併終了後、Yumanity治療会社は既存の投資家が約束したYumanity+PIPE融資から3750万ドルの財務状況現金滑走路は逆合併終了後18~24ヶ月以内にbr運営資金提供予定*今後18ヶ月以内に価値の顕著なYumanityを提供する予定である。KinetaとYumanityの逆合併が完了した後,Genentechに付与された腫瘍学的薬物開発計画とFair Treateuticsを付与する嚢胞性線維化薬物開発計画4は合併後の組織に温存される。

免疫抵抗は現在の癌治療の主要な挑戦であるbr}次世代癌治療の需要:チェックポイント遮断の生存率の向上と免疫反応抑制物(CPI)無応答者の機序(70%-80%)*T細胞が抗癌免疫機能抵抗を失って癌腫瘍細胞を攻撃して免疫システムを攻撃し、天然と獲得性免疫反応を統合した*公開情報5に基づく

Kinetaパイプラインは天然免疫と獲得性免疫を統合し、癌耐性の機序を解決するために、天然免疫は癌の早期適応免疫の適切な適応免疫の検出に参与する必要な駆動要素癌耐性の重要な原因適応性免疫の大多数の競争相手の薬物開発はT細胞適応免疫のみに集中している6

Kinetaの免疫腫瘍学パイプライン癌免疫耐性の機序を解決するための薬物前計画は臨床第一段階第二段階第三段階予想のマイルストーン免疫抑制を発見した:αVista mAb 4 Q 2022:IND承認と起動第一段階適応:末期固形腫瘍2023年第二四半期:Pembrolizumab連合行列KVA 12123非小細胞肺癌、結腸直腸癌を起動した。OC 4 Q 2023:第1段階データ読み出し枯渇T細胞:αCD 27 mAb 1 H 2024:IND申請適応:末期固形腫瘍1 H 2024年:第1段階臨床研究開始Kinetaはまた、TMEにおける腫瘍免疫原性の悪い問題を解決するために、抗CD 24アンタゴニストモノクロナル抗体免疫治療計画を開始し、リードする候補7を決定するために努力している

KVA 12123潜在分化Vista遮断免疫療法8 8
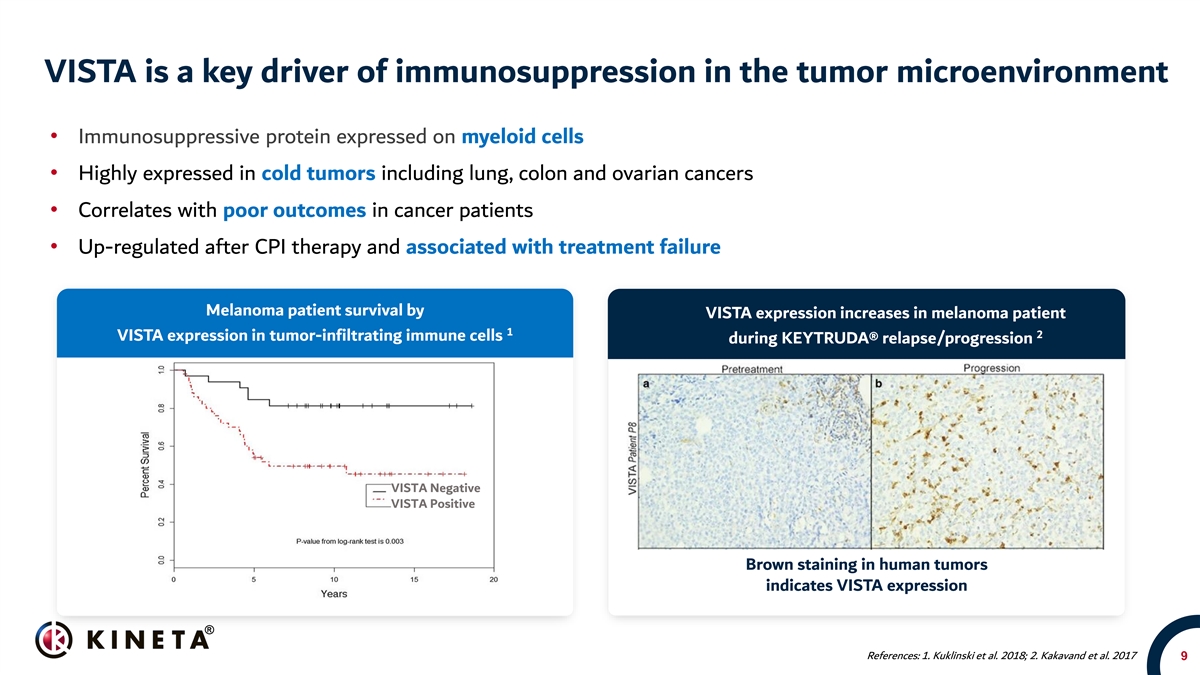
VISTAは、腫瘍微小環境における免疫抑制の重要な駆動因子であるbr}·免疫抑制タンパク質の髄系細胞への発現·肺癌、結腸癌、卵巣癌を含む冷腫瘍で高発現·癌患者の不良予後に関連する·CPI治療後に上昇し、治療失敗に関連する。VISTA発現は黒色腫患者において1 2増加し、腫瘍浸潤性免疫細胞におけるVISTA発現KEYTRUDA再発/進展VISTA陰性VISTA陽性のヒト腫瘍における茶色発現は、VISTA発現:1.Kuklinskiらを示している。2018年;2.カヴァンダーら。2017年9

KVA 12123:潜在的分化のVista遮断免疫療法pH 単剤腫瘍製品開発段階同型結合モデル効率CRSサイトカイン放出強力か工学IgG 1 Kineta Start段階生理pH単剤腫瘍成長CRS関連サイトカインモノクロナル抗体と2022年第4四半期KVA 12123結合と酸性pH中のTME抑制結合し、そして臨床前モデル中の臨床前モデルで見られた独特なエピトープPD-1の放出或いは神経毒性Curis*腫瘍壊死因子α,インターフェロンγ,第1段階IgG 1生理性中等CI-8993 IL 2と結合し、IL-1βPierre Fabreフェーズ1 WO 180ハチドリステージ1 Ig G 4生理中等度IL-6 HMBD 002 Pharmabine臨床前IgG 1酸性および生理中等度インターフェロンγPMC 309 Sensei臨床前IgG 1酸性弱腫瘍壊死因子αSNS-101他の発見段階計画:Apexigen,Five Prime Treeutics/BMS,xCella Biosciences空細胞は公開データがないことを示した*Curtは2022年11月9日に“資源を集中してemavusertibを集中して加速する”、“br}社の主要資産と”その他の計画の剥奪“(CI-8993)Kinetaデータ分析ファイル10ファイル分析ファイル10

Vistaを遮断することでTME免疫抑制機構を逆転させる腫瘍免疫耐性抑制MDSC促進T細胞機能Eff増強NK細胞活性化増強単球活性化11

KVA 12123によるVISTAの遮断は先天免疫と獲得性免疫細胞を同時に活性化し、ヒト白血球抗原依存性を増加させ、MDSC媒介増加単球T細胞の活性化分化を増加させ、T細胞を活性化して1000 HLADR 3000 100000 2000 500 1000 50000 250 0 0 KVA 12123 KVA 12123 NK 依存作用機序を抑制し、NK細胞活性化(CD 56+)+NK-NKゲート制御NK細胞のCD 137発現を促進する。24時間3000 1000 2000 750 500 1000 250 0 0 KVA 12123ファイル上のKinetaデータ12 IgG 1 3μg/ml KVA 12123 0.03μg/ml KVA 12123 0.3μg/ml KVA 12123 30μg/ml BG 1 3μg/ml KVA 12123 0.03μg/ml KVA 12123 0.3μg/ml KVA 12123 3μg/ml I PBMC単独IgG 1 KVA 12123 PBG+MonoのIgG 1 3μg/ml KVA 12123 0.03μg/ml KVA 12123 3μg/ml KVA 120.03μg/ml KVA 120.3μg/ml KVA 12123 3μg/mlKVA 12123 0.03μg/ml KVA 12123 0.3μg/ml KVA 12123 3μg/ml HLA−DR MFI増殖細胞絶対計数CD 137 MFIインターフェロン(pg/mL)

KVA 12123は臨床前モデル、連合治療、連合治療、単一治療、結腸癌モデル、膀胱癌モデルMB 49、膀胱癌モデルMB 49、T細胞リンパ腫モデルEG 7、hVISTA Kiマウス、平均腫瘍体積1500、平均腫瘍体積、ヒトIgG 1 3000、IgG対照、KVA 12.1 2000、対照MS、IgG 2 a、KVA 12.2 a、抗MPD 1、KVA-12.2 a、12.2 a KVA 12.1/anti-mpd 1組合せKVA 12.2 a/anti-mpd-1 1000 1500 2000 1000 500 0 0 5 10 15 20 25 0 2 4 6 8 12 14 16 20 22 24 26 0 2 4 6 8 10 12 14 16 18 20 22 24 26 0 10 20 20 30 40日移植後の腫瘍成長抑制抗Vista:75%抗Vista:35-4%anti-Vista:{br40%抗Vista:66%抗PD 1:42-60%抗PD 1:67%コンボ:68%コンボ:85%*併用治療研究最適用量の各製剤KVA 12.2 a:マウスはKVA 12123のKinetaデータファイル13 3 Avgに同等であった。腫瘍体積(Mm)3平均。腫瘍体積(Mm)3腫瘍体積(Mm)3平均。腫瘍体積(Mm)

NHP毒理学研究において、KVA 12123耐性が良好であることが観察された CRSサイトカインは治療に関連する死亡率レベル(IL 6或いは腫瘍壊死因子α)の結果を変化させず、良好な臨床バイタルサイン耐性或いは体重減少KinetaはNHPで何度も、単回と反復用量の毒理学研究を完成し、KVA 12123の投与量は100 mg/kg Kinetaデータに達し、ファイル14にあった
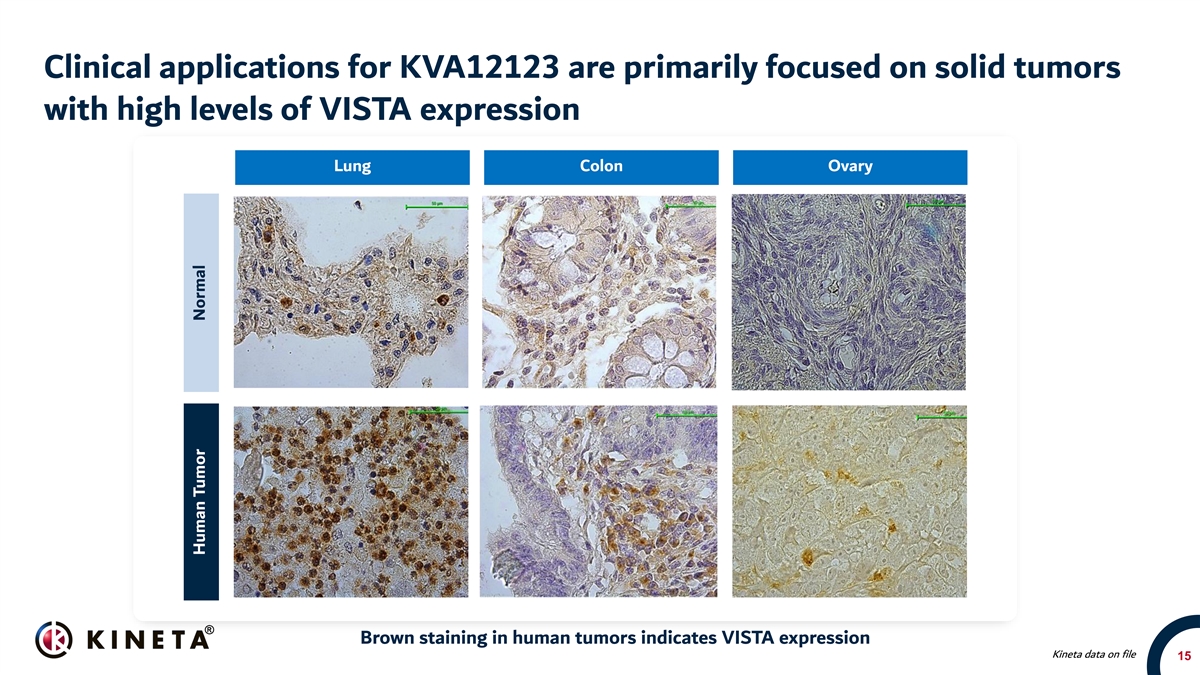
KVA 12123の臨床応用は主にVista高レベル発現固形腫瘍(Br)ヒト腫瘍中の肺、結腸、卵巣20 x 20 x茶色染色に集中しており、Vista発現Kinetaデータファイル15ヒト腫瘍は正常であることを示した

1期用量逓増研究単一療法とペブロモリズマブ併用による末期固形腫瘍患者群の治療:末期固形腫瘍患者の主要な目標:KVA 12123の安全性と耐性、推奨される2期用量(RP 2 D)或いは最大耐性用量(MTD)の二次目標:iRECIST(OOR)末期固形腫瘍患者の薬物動態学、免疫原性、腫瘍反応探索性目標:バイオマーカーと受容体占有率B部分KVA 12123単剤投与量増加計画用量レベルKVA 12123用量逓増計画用量レベル連合静脈注射;Q 2 W=2週間ごと(KVA 12123)=IV;Q 2 W=2週ごと(KV 12 123);Q 6 W=6週間ごと(Pbro)3 10 30 100 300 1000 30 100 300 1000 mg 3-6被験者3-6被験者1列当たり1-6被験者KVA 12123研究は1/2期臨床試験であった。A部分とB部分は上述したとおりである.C部分とD部分は第2段階拡張キューであり,A部分およびB部分で定義される腫瘍タイプの患者16を募集する

1大型商業市場NSCLC 980 K初期患者年間新機会$318億KVA 12123 2 270万結腸直腸癌年度新患者110万年度新患者$103億市場機会3卵巣癌66万年度新患者$59億市場源:1.NSCLC GlobalData:2028年の全世界薬物予測と市場分析2.CRC GlobalData:2028年の全世界薬物予測と市場分析17.OC GlobalData:2028年の全世界薬物予測と市場分析

戦略的パートナーシップは、慢性神経筋疾患神経病理性疼痛疾患-ALS(Kineta)(Yumanity)パートナーの3.59億ドルに達するマイルストーン5.3億ドルのマイルストーンキー取引条項にKCP 506の持続的な協力を提供し、2100万ドルの開発資金版税純売上を獲得し、設立以来研究協力高桁とライセンス契約低青少年印税研究協力、オプションとライセンス契約YumanityのALS薬物開発計画はメルク社と協力し、KinetaとYumanityの逆合併が完了した後,Genentechに付与された腫瘍学的薬物開発計画とFair Treateuticsを付与する嚢胞性線維化薬物開発計画は合併後組織に温存される

今後18ヶ月間の予期される重要な触媒2022 2023 1 H 2024 4 Q:KVA 12123 1 Q:KVA 27 mAb 1 H:KVA 12123とメルク社の臨床協力開始INDイネーブル研究第1段階合併の安全データ(KEYTRUDA薬品供給プロトコル)読み出し2 Q:KVA 121231 H:αCD 27 mAb 4 Q:KVAA 12123共同キューIND提出IND承認2 Q:マーカーパートナー社(ALS)1 H:αCD 27 mAb 4 Q:KVAA 12123潜在的研究開始段階1末期固形腫瘍臨床研究4 Q: KVHαCD 12 HαCD 24 mQKCP 506)INDサポート研究開始潜在フェーズ1 SAD/MAD/Pilot 4 Q:Genentechパートナーシップ(KCP 506)HEMPマイルストーンGenentechオプション 19

経験豊富な指導チームCraig Philps Shawn Iadonato、博士総裁 最高経営責任者Keith Baker Thierry Guillaudeux、博士首席財務官首席科学官Jacques Bouchy Pauline Kenny、投資家関係総法律顧問兼業務発展20

Kinetaは、癌免疫耐性KVA 12123を解決するための次世代免疫療法を開発している:潜在的に分化するVista遮断免疫療法は、2022年第4四半期にCD 27とCD 24腫瘍に対する免疫モノクロナル抗体(MAb)計画が2022年第4四半期にナスダックに上場する予定である固形腫瘍KAは、2022年第4四半期に発売計画とYumanity治療会社計画の逆合併が完了した後、Yumanity+PIPEは3750万ドルの既存投資家が約束した3,750万ドルの財務状況Cash Runway が逆合併パートナーシップ終了後18~24ヶ月以内に運営資金を提供する予定であることを予定している3,750万ドルの財務状況Cash Runway が逆合併パートナーシップ終了後18~24ヶ月以内に運営資金を提供する予定である。Genentechに付与された腫瘍学的薬物開発計画とFair Treeuticsを付与する嚢胞性線維化薬物開発計画21は,KinetaとYumanityの逆合併が完了した後に合併後の組織に温存される。

癌患者のための次世代免疫療法 www.kinetabio.com i ir@kinete.us 22 22