アメリカです
アメリカ証券取引委員会
ワシントンD.C.,郵便番号:20549
表
(マーク1)
1934年証券取引法第13条又は15(D)条に規定する四半期報告 |
本四半期末まで
あるいは…。
1934年証券取引法第13条又は15条に基づいて提出された移行報告 |
そこからの過渡期について
依頼書類番号:
(登録者の正確な氏名はその定款に記載)
(明またはその他の司法管轄権 会社や組織) |
(税務署の雇用主 |
(主にオフィスアドレスを実行) |
(郵便番号) |
登録者の電話番号、市外局番を含む:(
同法第12条(B)に基づいて登録された証券:
クラスごとのタイトル |
|
取引 記号 |
|
登録された各取引所の名称 |
|
|
それは.. |
||
|
|
それは.. |
再選択マークは、登録者が(1)過去12ヶ月以内(または登録者がそのような報告の提出を要求されたより短い期間)に、1934年の証券取引法第13条または15(D)節に提出されたすべての報告書を提出したかどうか、および(2)過去90日以内にそのような提出要件に適合しているかどうかを示す
再選択マークは、登録者が過去12ヶ月以内(または登録者がそのような文書の提出を要求されたより短い時間以内)に、S−T規則405条(本章232.405節)に従って提出を要求した各相互作用データファイルを電子的に提出したか否かを示す
登録者が大型加速申告会社,加速申告会社,非加速申告会社,小さな報告会社,あるいは新興成長型会社であることを再選択マークで示す。取引法第12 b-2条の規則における“大型加速申告会社”、“加速申告会社”、“小申告会社”、“新興成長型会社”の定義を参照されたい。
大型加速ファイルサーバ |
|
☐ |
|
ファイルマネージャを加速する |
|
☐ |
|
|
|
|
|||
|
☒ |
|
規模の小さい報告会社 |
|
||
|
|
|
|
|
|
|
新興成長型会社 |
|
|
|
|
|
|
新興成長型企業であれば、登録者が延長された移行期間を使用しないことを選択したか否かを再選択マークで示し、取引所法第13(A)節に提供された任意の新たまたは改正された財務会計基準を遵守する
登録者が空殻会社であるか否かをチェックマークで示す(取引法第12 b-2条で定義されている)。はい、違います
2022年11月10日までに
カタログ表
|
|
ページ |
第1部: |
財務情報 |
|
第1項。 |
財務諸表 |
1 |
|
監査されていない簡明な総合貸借対照表2022年9月30日と2021年12月31日まで |
1 |
|
監査されていない簡明な合併経営報告書2022年と2021年9月30日までの3ヶ月と9ヶ月の全面赤字 |
2 |
|
監査されていない株主権益簡明合併報告書 2022年9月30日までの3ヶ月と9ヶ月 |
3 |
|
2021年9月30日までの3ヶ月と9ヶ月監査されていない償還可能な転換可能な優先株と株主権益簡明合併報告書 |
4 |
|
2022年9月30日と2021年9月30日までの9ヶ月間監査されていないキャッシュフロー表簡明連結レポート |
5 |
|
監査されていない簡明な連結財務諸表付記 |
6 |
第二項です。 |
経営陣の財務状況と経営成果の検討と分析 |
18 |
第三項です。 |
市場リスクの定量的·定性的開示について |
27 |
第四項です。 |
制御とプログラム |
27 |
|
|
|
第二部です。 |
その他の情報 |
|
第1項。 |
法律訴訟 |
29 |
第1 A項。 |
リスク要因 |
29 |
第二項です。 |
未登録株式証券販売と収益の使用 |
44 |
第三項です。 |
高級証券違約 |
44 |
第四項です。 |
炭鉱安全情報開示 |
44 |
五番目です。 |
その他の情報 |
44 |
第六項です。 |
陳列品 |
45 |
サイン |
46 |
|
i
前向き陳述に関する警告説明
この報告書に含まれているいくつかの陳述は連邦証券法の意味での展望的な陳述に属する。展望的陳述は、予想、信念、予測、未来計画および戦略、予期されたイベントまたは傾向、および非歴史的事実に関連する同様の表現に関する。これらの展望性表現は蘇羅岑の未来の財務と経営業績に関する表現、蘇羅岑の未来経営の計画、戦略と目標に関する表現、及び未来の業績に関する表現を含む。場合によっては、これらの前向きな陳述は、“展望”、“信じ”、“予想”、“潜在”、“継続”、“可能”、“将”、“すべき”、“可能”、“求める”、“約”、“予測”、“計画”、“計画”、“推定”、“予想”またはこれらの語または他の類似語またはフレーズの負のバージョンなどの用語を使用することによって識別することができる。
これらの陳述は,本報告日までに我々が把握した情報に基づいており,これらの情報はこのような陳述の合理的な基礎を構成していると考えられるが,このような情報は限られているか不完全である可能性があり,これらの陳述は,我々が入手可能なすべての関連情報を詳細に調査または検討していることを示していると解釈されてはならない.これらの陳述は本質的に不確実であり、投資家にこのような陳述に過度に依存しないように注意する。法的要件が適用されない限り、私たちは新しい情報、未来のイベント、または他の状況に基づいて私たちの前向きな陳述を更新または修正する義務がありません(そのような義務を明確に拒否します)
記載されたトランザクションおよびイベントが上述したように発生することは保証されない(または全く発生しない)。本報告に含まれる展望的陳述は、多くの既知および未知のリスク、不確実性、仮説および環境変化の影響を受けることができ、これらのリスク、不確実性、仮説および環境変化は、私たちの実際の結果が任意の前向き陳述で表現された結果とは大きく異なる可能性がある。これらおよび他の我々の将来の結果、業績、または取引をもたらす可能性がある任意の前向き陳述で表現されている大きく異なる要因のさらなる議論については、本報告書のタイトルを参照してください“リスク要因” and “第1 A項。リスク要因2021年12月31日までの10-K表年次報告は、2022年3月28日に米国証券取引委員会に提出された。
II
第1部-財務情報
プロジェクト1それは.財務諸表
SURROZEN社
簡明総合貸借対照表
(千単位で、1株当たりを除く)
|
|
九月三十日 |
|
|
十二月三十一日 |
|
||
|
|
(未監査) |
|
|
|
|
||
資産 |
|
|
|
|
|
|
||
流動資産: |
|
|
|
|
|
|
||
現金と現金等価物 |
|
$ |
|
|
$ |
|
||
短期有価証券 |
|
|
|
|
|
|
||
前払い費用と他の流動資産 |
|
|
|
|
|
|
||
流動資産総額 |
|
|
|
|
|
|
||
|
|
|
|
|
|
|
||
財産と設備、純額 |
|
|
|
|
|
|
||
経営的リース使用権資産 |
|
|
|
|
|
|
||
長期有価証券 |
|
|
|
|
|
|
||
制限現金 |
|
|
|
|
|
|
||
その他の資産 |
|
|
|
|
|
|
||
総資産 |
|
$ |
|
|
$ |
|
||
|
|
|
|
|
|
|
||
負債と株主権益 |
|
|
|
|
|
|
||
流動負債: |
|
|
|
|
|
|
||
売掛金 |
|
$ |
|
|
$ |
|
||
負債その他の負債を計上しなければならない |
|
|
|
|
|
|
||
賃貸負債、流動部分 |
|
|
|
|
|
|
||
流動負債総額 |
|
|
|
|
|
|
||
|
|
|
|
|
|
|
||
賃貸負債、非流動部分 |
|
|
|
|
|
|
||
株式証負債 |
|
|
|
|
|
|
||
総負債 |
|
|
|
|
|
|
||
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
||
株主権益: |
|
|
|
|
|
|
||
優先株、$ |
|
|
|
|
|
|
||
普通株、$ |
|
|
|
|
|
|
||
追加実収資本 |
|
|
|
|
|
|
||
その他の総合損失を累計する |
|
|
( |
) |
|
|
( |
) |
赤字を累計する |
|
|
( |
) |
|
|
( |
) |
株主権益総額 |
|
|
|
|
|
|
||
総負債と株主権益 |
|
$ |
|
|
$ |
|
||
付記はこのような監査されていない簡明な総合財務諸表の構成要素だ。
1
SURROZEN社
経営報告書と全面赤字を簡明に合併する
(未監査)
(千単位で、1株当たりを除く)
|
|
9月30日までの3ヶ月間 |
|
|
9月30日までの9ヶ月間 |
|
|
||||||||||
|
|
2022 |
|
|
2021 |
|
|
2022 |
|
|
2021 |
|
|
||||
運営費用: |
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
研究開発 |
|
$ |
|
|
$ |
|
|
$ |
|
|
$ |
|
|
||||
一般と行政 |
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
総運営費 |
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
運営損失 |
|
|
( |
) |
|
|
( |
) |
|
|
( |
) |
|
|
( |
) |
|
利子収入 |
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
その他の収入,純額 |
|
|
|
|
|
( |
) |
|
|
|
|
|
( |
) |
|
||
純損失 |
|
|
( |
) |
|
|
( |
) |
|
|
( |
) |
|
|
( |
) |
|
取引可能証券の未実現収益(赤字),税引き後純額 |
|
|
|
|
|
( |
) |
|
|
( |
) |
|
|
( |
) |
|
|
総合損失 |
|
$ |
( |
) |
|
$ |
( |
) |
|
$ |
( |
) |
|
$ |
( |
) |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
1株当たりの純損失は普通株に帰する |
|
$ |
( |
) |
|
$ |
( |
) |
|
$ |
( |
) |
|
$ |
( |
) |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
算入の加重平均シェアを計算する |
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
付記はこのような監査されていない簡明な総合財務諸表の構成要素だ。
2
SURROZEN社
株主権益簡明合併報告書
(未監査)
(単位:千)
|
|
|
|
|
|
|
|
その他の内容 |
|
|
積算 |
|
|
|
|
|
合計する |
|
||||||
|
|
普通株 |
|
|
支払い済み |
|
|
全面的に |
|
|
積算 |
|
|
株主の |
|
|||||||||
|
|
株 |
|
|
金額 |
|
|
資本 |
|
|
損 |
|
|
赤字.赤字 |
|
|
株権 |
|
||||||
2021年12月31日の残高 |
|
|
|
|
$ |
|
|
$ |
|
|
$ |
( |
) |
|
$ |
( |
) |
|
$ |
|
||||
株式項下の普通株の発行 |
|
|
|
|
|
— |
|
|
|
|
|
|
— |
|
|
|
— |
|
|
|
|
|||
事前に行使した株式オプションを買い戻す |
|
|
( |
) |
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
— |
|
早期に行使された株式オプションの帰属 |
|
|
— |
|
|
|
— |
|
|
|
|
|
|
— |
|
|
|
— |
|
|
|
|
||
株に基づく報酬費用 |
|
|
— |
|
|
|
— |
|
|
|
|
|
|
— |
|
|
|
— |
|
|
|
|
||
その他総合損失 |
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
( |
) |
|
|
— |
|
|
|
( |
) |
純損失 |
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
( |
) |
|
|
( |
) |
2022年3月31日の残高 |
|
|
|
|
|
|
|
|
|
|
|
( |
) |
|
|
( |
) |
|
|
|
||||
事前に行使した株式オプションを買い戻す |
|
|
( |
) |
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
— |
|
早期に行使された株式オプションの帰属 |
|
|
— |
|
|
|
— |
|
|
|
|
|
|
— |
|
|
|
— |
|
|
|
|
||
株に基づく報酬費用 |
|
|
— |
|
|
|
— |
|
|
|
|
|
|
— |
|
|
|
— |
|
|
|
|
||
その他総合損失 |
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
( |
) |
|
|
— |
|
|
|
( |
) |
純損失 |
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
( |
) |
|
|
( |
) |
2022年6月30日の残高 |
|
|
|
|
|
|
|
|
|
|
|
( |
) |
|
|
( |
) |
|
|
|
||||
事前に行使した株式オプションを買い戻す |
|
|
( |
) |
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
— |
|
早期に行使された株式オプションの帰属 |
|
|
— |
|
|
|
— |
|
|
|
|
|
|
— |
|
|
|
— |
|
|
|
|
||
株に基づく報酬費用 |
|
|
— |
|
|
|
— |
|
|
|
|
|
|
— |
|
|
|
— |
|
|
|
|
||
その他総合収益 |
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
|
|
|
— |
|
|
|
|
||
純損失 |
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
( |
) |
|
|
( |
) |
2022年9月30日の残高 |
|
|
|
|
$ |
|
|
$ |
|
|
$ |
( |
) |
|
$ |
( |
) |
|
$ |
|
||||
付記はこのような監査されていない簡明な総合財務諸表の構成要素だ。
3
SURROZEN社
転換可能優先株と株主権益簡明連結報告書を償還可能
(未監査)
(単位:千)
|
|
償還可能なオープンカー |
|
|
|
|
|
|
|
|
その他の内容 |
|
|
積算 |
|
|
|
|
|
合計する |
|
|||||||||||
|
|
優先株 |
|
|
普通株 |
|
|
支払い済み |
|
|
全面的に |
|
|
積算 |
|
|
株主の |
|
||||||||||||||
|
|
株 |
|
|
金額 |
|
|
株 |
|
|
金額 |
|
|
資本 |
|
|
損 |
|
|
赤字.赤字 |
|
|
株権 |
|
||||||||
2020年12月31日現在の残高は、前述のとおり |
|
|
|
|
$ |
|
|
|
|
|
$ |
|
|
$ |
|
|
$ |
|
|
$ |
( |
) |
|
$ |
( |
) |
||||||
資本再編の遡及応用 |
|
|
( |
) |
|
|
( |
) |
|
|
|
|
|
|
|
|
|
|
|
— |
|
|
|
— |
|
|
|
|
||||
2020年12月31日の残高は |
|
|
— |
|
|
|
— |
|
|
|
|
|
|
|
|
|
|
|
|
— |
|
|
|
( |
) |
|
|
|
||||
株式オプションの行権 |
|
|
— |
|
|
|
— |
|
|
|
|
|
|
— |
|
|
|
|
|
|
— |
|
|
|
— |
|
|
|
|
|||
付与制限株 |
|
|
— |
|
|
|
— |
|
|
|
|
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
事前に行使した賠償責任に再分類する |
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
( |
) |
|
|
— |
|
|
|
— |
|
|
|
( |
) |
早期に行使された株式オプションの帰属 |
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
|
|
|
— |
|
|
|
— |
|
|
|
|
||
株に基づく報酬費用 |
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
|
|
|
— |
|
|
|
— |
|
|
|
|
||
純損失 |
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
( |
) |
|
|
( |
) |
2021年3月31日の残高は |
|
|
— |
|
|
|
— |
|
|
|
|
|
|
|
|
|
|
|
|
— |
|
|
|
( |
) |
|
|
|
||||
株式オプションの行権 |
|
|
— |
|
|
|
— |
|
|
|
|
|
|
— |
|
|
|
|
|
|
— |
|
|
|
— |
|
|
|
|
|||
付与制限株 |
|
|
— |
|
|
|
— |
|
|
|
|
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
没収制限株 |
|
|
— |
|
|
|
— |
|
|
|
( |
) |
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
— |
|
事前に行使した賠償責任に再分類する |
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
( |
) |
|
|
— |
|
|
|
— |
|
|
|
( |
) |
早期に行使された株式オプションの帰属 |
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
|
|
|
— |
|
|
|
— |
|
|
|
|
||
事前に行使した株式オプションを買い戻す |
|
|
— |
|
|
|
— |
|
|
|
( |
) |
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
— |
|
株に基づく報酬費用 |
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
|
|
|
— |
|
|
|
— |
|
|
|
|
||
純損失 |
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
( |
) |
|
|
( |
) |
2021年6月30日の残高は |
|
|
— |
|
|
|
— |
|
|
|
|
|
|
|
|
|
|
|
|
— |
|
|
|
( |
) |
|
|
|
||||
企業合併後の普通株の発行 |
|
|
— |
|
|
|
— |
|
|
|
|
|
|
|
|
|
|
|
|
— |
|
|
|
— |
|
|
|
|
||||
株式オプションの行権 |
|
|
— |
|
|
|
— |
|
|
|
|
|
|
— |
|
|
|
|
|
|
— |
|
|
|
— |
|
|
|
|
|||
早期に行使した株に対する負債に再分類する |
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
( |
) |
|
|
— |
|
|
|
— |
|
|
|
( |
) |
早期に行使された株式オプションの帰属 |
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
|
|
|
— |
|
|
|
— |
|
|
|
|
||
株に基づく報酬費用 |
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
|
|
|
— |
|
|
|
— |
|
|
|
|
||
その他総合損失 |
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
( |
) |
|
|
— |
|
|
|
( |
) |
純損失 |
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
— |
|
|
|
( |
) |
|
|
( |
) |
2021年9月30日の残高 |
|
|
— |
|
|
$ |
— |
|
|
|
|
|
$ |
|
|
$ |
|
|
$ |
( |
) |
|
$ |
( |
) |
|
$ |
|
||||
付記はこのような監査されていない簡明な総合財務諸表の構成要素だ。
4
SURROZEN社
キャッシュフロー表簡明連結報告書
(未監査)
(単位:千)
|
9月30日までの9ヶ月間 |
|
|||||
|
2022 |
|
|
2021 |
|
||
経営活動: |
|
|
|
|
|
||
純損失 |
$ |
( |
) |
|
$ |
( |
) |
純損失と経営活動で使用される現金純額の調整: |
|
|
|
|
|
||
減価償却 |
|
|
|
|
|
||
株に基づく報酬 |
|
|
|
|
|
||
非現金でレンタル料金を扱っております |
|
|
|
|
|
||
有価証券の割増償却純額 |
|
|
|
|
|
||
株式証負債の公正価値変動を認める |
|
( |
) |
|
|
( |
) |
リンカーン公園に発行された承諾株に関するその他の費用 |
|
|
|
|
|
||
企業合併に関する権利証配分の取引コスト |
|
|
|
|
|
||
経営性資産と負債変動状況: |
|
|
|
|
|
||
前払い費用と他の流動資産 |
|
( |
) |
|
|
( |
) |
その他の資産 |
|
( |
) |
|
|
( |
) |
売掛金 |
|
( |
) |
|
|
|
|
負債その他の負債を計上しなければならない |
|
( |
) |
|
|
|
|
リース負債を経営する |
|
( |
) |
|
|
( |
) |
経営活動のための現金純額 |
|
( |
) |
|
|
( |
) |
|
|
|
|
|
|
||
投資活動: |
|
|
|
|
|
||
財産と設備を購入する |
|
( |
) |
|
|
( |
) |
有価証券を購入する |
|
( |
) |
|
|
( |
) |
有価証券の販売 |
|
|
|
|
|
||
有価証券満期日収益 |
|
|
|
|
|
||
投資活動提供の現金純額 |
|
|
|
|
( |
) |
|
|
|
|
|
|
|
||
融資活動: |
|
|
|
|
|
||
企業合併とPIPE発行普通株の収益 |
|
|
|
|
|
||
株式オプションを行使して得られる収益 |
|
|
|
|
|
||
事前に行使した株式オプションを買い戻す |
|
( |
) |
|
|
( |
) |
融資活動が提供する現金純額 |
|
( |
) |
|
|
|
|
|
|
|
|
|
|
||
現金、現金等価物、および制限的現金純増加 |
|
( |
) |
|
|
|
|
期初現金、現金等価物、および限定現金 |
|
|
|
|
|
||
期末現金、現金等価物、および制限現金 |
$ |
|
|
$ |
|
||
|
|
|
|
|
|
||
非現金投資と融資活動を追加開示します |
|
|
|
|
|
||
償還可能な転換可能優先株を普通株に変換する |
$ |
|
|
$ |
|
||
企業合併における株式証責任の引き受けについて |
$ |
|
|
$ |
|
||
企業合併における取引コスト計上すべき負債 |
$ |
|
|
$ |
|
||
売掛金に掲げる財産と設備の購入 |
$ |
|
|
$ |
|
||
株式オプション先行権の帰属 |
$ |
|
|
$ |
|
||
早期に行使された株式オプションを負債に再分類する |
$ |
|
|
$ |
|
||
賃貸延期により増加した使用権資産と賃貸負債 |
$ |
|
|
$ |
|
||
次の表は、会社が監査されていない簡明総合貸借対照表中の現金、現金等価物、および制限現金の入金状況を示している
|
九月三十日 |
|
|||||
|
2022 |
|
|
2021 |
|
||
現金と現金等価物 |
$ |
|
|
$ |
|
||
制限現金 |
|
|
|
|
|
||
現金、現金等価物、および限定現金 |
$ |
|
|
$ |
|
||
付記はこのような監査されていない簡明な総合財務諸表の構成要素だ。
5
SURROZEN社
監査を経ず簡明に連結財務諸表を付記する
注1.組織と業務
組織する
Surrozen,Inc.あるいは当社は,前身はCononance-HFW Acquisition Corp.,あるいはCononanceであり,臨床段階のバイオテクノロジー会社であり,Wnt経路を選択的に調節するために候補薬物の発見と開発に取り組んでおり,これはヒト疾患を治療する広範な器官と組織中の重要な組織修復メディエーターである。同社はカリフォルニア州サンフランシスコ南部にあるデラウェア州の会社です。
企業合併と民間投資の公共実体融資への応用
Cononanceは空白小切手会社で、2020年8月21日にケイマン諸島免除会社として登録された。その設立の目的は、1つまたは複数の企業との合併、株式交換、資産買収、株式購入、再編または同様の業務合併である。
2021年8月11日、Cononanceは、Cononance、Cononanceの子会社Persistance Merge Sub Inc.と2015年8月12日に設立されたデラウェア州会社Surrozen,Inc.またはLegacy Surrozen間の業務合併、すなわち業務合併を完了した。業務合併終了後,Cononanceはデラウェア州の会社となりSurrozen,Inc.,Legacy SurrozenはSurrozen Operating,Inc.,Legacy Surrozenは引き続き会社の完全子会社となった。注3を見て、“資本再編“もっと詳しい情報を知ります。
2022年5月、蘇羅岑オランダ有限公司は、蘇羅岑運営会社の完全子会社としてオランダロッテルダムに登録設立された。
流動性
当社は設立以来純損失を出しています。同社は従来、主に私募償還可能な転換可能優先株方式でこれらの業務に資金を提供してきた。2022年9月30日現在、会社は現金、現金等価物、有価証券を持っている
2022年10月会社はバーリングインゲルハイム国際有限公司(BI)と協力·許可協定(CLA)を締結し、この協定によると、会社は払い戻しできない前金$を得る資格がある
経営陣は、既存の現金、現金等価物、有価証券に、現金収益総額#ドルを加えているとしている
付記2.主要会計政策の概要
陳述の基礎
会社が監査を受けていない簡明な総合財務諸表と付記は、アメリカ公認会計原則とアメリカ証券取引委員会(アメリカ証券取引委員会)の規定に基づいて作成された。これらの規則が許可される場合、GAAPは、一般に要求されるいくつかの脚注または他の財務情報が簡略または省略されているので、2021年12月31日までの簡明な総合貸借対照表は、会社がその日に監査された総合財務諸表に由来するが、GAAPが総合財務諸表を完了するために必要なすべての情報は含まれていない。これらの審査されていない簡明な総合財務諸表は、会社年度総合財務諸表の作成基準と同じであり、経営陣は、これらの報告書は、公正な列報会社の総合財務諸表に必要なすべての調整を反映していると考えている(通常の経常的調整を含む)
6
財務諸表。2022年9月30日までの3ヶ月と9ヶ月の経営結果は、2022年12月31日までの1年または任意の他の中期または今後1年の予想結果を示すとは限らない。
監査されていない簡明総合財務諸表は、当社及びその付属会社の勘定を含む。すべての会社間取引と残高は無効になりました。
付記1で検討した業務合併は逆資本再編とみなされ、Legacy Surrozenは会計買収側、Cononanceは被買収会社である。そのため、審査簡明総合財務諸表に提出されていないすべての歴史財務資料はLegacy Surrozenがその歴史コストで計算した勘定を代表して、まるでLegacy Surrozenが当社の前身であるようである。業務合併終了後の未審査簡明総合財務諸表は合併後の実体の経営結果を反映している。すべての発行および発行された普通株、償還可能な転換可能な優先株及びLegacy Surrozenの株式奨励、及び業務合併が2021年8月11日終了前の審査簡明総合財務諸表に記載されていない1株当たりの金額は、すべて遡及して説明し、業務合併で確立された両替比率を反映する。注3を見て、“資本再編“もっと詳しい情報を知ります。
添付されている簡明総合財務諸表及び関連財務資料は、2021年12月31日までの年度の審査された総合財務諸表及びその関連付記と併せて読まなければならない会社が2022年3月28日に米国証券取引委員会に提出したForm 10-K年度報告書に含まれる。
予算の使用
公認会計基準に基づいて未監査の簡明連結財務諸表を作成する本グループは管理層に判断、推定及び仮定を要求し、簡明な総合財務諸表を審査していない期日までの報告された資産及び負債額及び或いは有資産及び負債の開示、及び報告期間内に提出された支出金額に影響する。添付されている監査されていない簡明総合財務諸表で作成された重大な推定および仮定は、研究および開発活動のいくつかの計算すべき費用、業務合併前の普通株の公正価値、株式ベースの報酬支出および所得税を含むが、これらに限定されない。管理職は過去の経験と当時の状況で部下が合理的であると信じている他の市場特定および関連仮定に基づいて推定しているが、これらの仮説の結果は資産や負債の帳簿価値を判断する基礎を構成しており、そのような資産や負債の帳簿価値は他の出所から容易に見られるわけではない。実際の結果はこのような推定とは大きく異なるかもしれない。
信用リスクが集中する
金融商品には現金、現金等価物、有価証券が含まれており、会社を高度に集中した信用リスクに直面させる可能性がある。同社の現金は金融機関が保有しており、経営陣は金融機関の信用が良いと考えている。金融機関に保管されているこのような預金は、連邦保険の限度額を超える場合があるが、金融機関が違約した場合、それが直面する信用リスクは、監査されていない簡明総合貸借対照表に記録されている金額に限られる。当社はこれらの金融機関の相対信用状況を評価し、信用リスクを制限する。その会社の政策は現金を信用の質の高い機関通貨市場基金と有価証券に投資し、信用開放の数を制限することだ。同社は現在、通貨市場基金、米国政府債券、商業手形、会社債務証券を含む様々な証券の現金等価物と有価証券ポートフォリオを持っている。同社の現金等価物や有価証券には実現した損失は何も出ていない。
有価証券
同社はその余分な現金を米国政府債券、商業手形、会社債務証券に投資している。すべての有価証券は売却可能な証券に分類され、類似した証券の見積市場価格或いは定価モードに基づいて、見積もり公正価値によって勘定される。当社が証券を購入または保有する主な目的は近い将来に売るためではありません。同社の政策は資本、流動性、リターンの保存に重点を置いている。会社は時々いくつかの証券を売るかもしれないが、通常は短期価格の違いから利益を稼ぐことを目標としていない。
短期有価証券の貸借対照表日の満期日は1年以下である。貸借対照表の日付まで、長期有価証券の満期日は1年を超えている。これらの有価証券は推定公正価値に基づいて入金され、実現されていない保有損益は累積した他の株主権益総合損失を計上し、実現するまでである。有価証券取引の損益は特定の識別方法で報告する。利子収入は審査されていない簡明総合経営報告書で確認し、稼いだときに全面赤字を確認した。
7
株式証負債
当社の公開株式証、私募株式承認証及びパイプ株式証はいずれも負債としている(付記9参照)。各報告期間が終了した時、期間内の公正価値のいかなる変動も他の収入、審査簡明総合経営報告書内の純額及び全面損失から確認された。当社は引き続き公正価値の変動について株式証負債を調整し、a)株式証の行使または満期またはb)株式証の償還時(早い者を基準とする)まで調整し、その際、当該等株式証は追加実収資本に再分類される。
1株当たり純損失
1株あたりの基本純損失の計算方法は,普通株が純損失を当期発行普通株の加重平均株式数で割るべきであり,潜在的な希釈証券は考慮しない。当社は上記期間中に赤字状態にあるため、1株当たりの基本純損失は希釈後の1株当たり純損失と同じであり、潜在的な希薄化証券の影響は逆薄であるためである
|
|
九月三十日 |
|
|||||
|
|
2022 |
|
|
2021 |
|
||
|
|
|
|
|
|
|
||
未償還オプション |
|
|
|
|
|
|
||
無帰属制限株 |
|
|
|
|
|
|
||
買い戻し可能な未帰属普通株 |
|
|
|
|
|
|
||
普通株購入引受権証 |
|
|
|
|
|
|
||
合計する |
|
|
|
|
|
|
||
注3.資本再編
2021年8月11日、和声は業務合併を完了した(注1参照)。事業合併が完了した後,一部の投資家は直ちに購入を引き受けた
そのため、会計目的のために逆資本再編は遺産蘇ローソンが調和純資産のために株を発行し、資本再編に伴うものとみなされている。調和のとれた純資産を歴史的コストで列記し,その中に
8
業務合併協定によると、業務合併が完了した場合、(I)Legacy Surrozen 1株当たり交換可能株式優先株(普通株基準に変換されたもの)およびLegacy Surrozen 1株当たり(帰属または非帰属にかかわらず)に変換することができる
付記4.公正価値計量
以下の表は、会社が公平な価値で恒常的に計測している金融資産と負債(千計)をまとめている
|
|
2022年9月30日 |
|
|||||||||||||
|
|
レベル1 |
|
|
レベル2 |
|
|
レベル3 |
|
|
合計する |
|
||||
資産: |
|
|
|
|
|
|
|
|
|
|
|
|
||||
貨幣市場基金(1) |
|
$ |
|
|
$ |
|
|
$ |
|
|
$ |
|
||||
商業手形 |
|
|
|
|
|
|
|
|
|
|
|
|
||||
社債 |
|
|
|
|
|
|
|
|
|
|
|
|
||||
政府債券 |
|
|
|
|
|
|
|
|
|
|
|
|
||||
公正な価値で計量された金融資産総額 |
|
$ |
|
|
$ |
|
|
$ |
|
|
$ |
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
負債.負債(2): |
|
|
|
|
|
|
|
|
|
|
|
|
||||
株式証を公開する |
|
$ |
|
|
$ |
|
|
$ |
|
|
$ |
|
||||
私募株式証明書 |
|
|
|
|
|
|
|
|
|
|
|
|
||||
喉頭管捜査令状 |
|
|
|
|
|
|
|
|
|
|
|
|
||||
公正な価値で計量された金融負債総額 |
|
$ |
|
|
$ |
|
|
$ |
|
|
$ |
|
||||
|
|
2021年12月31日 |
|
|||||||||||||
|
|
レベル1 |
|
|
レベル2 |
|
|
レベル3 |
|
|
合計する |
|
||||
資産: |
|
|
|
|
|
|
|
|
|
|
|
|
||||
貨幣市場基金(1) |
|
$ |
|
|
$ |
|
|
$ |
|
|
$ |
|
||||
商業手形 |
|
|
|
|
|
|
|
|
|
|
|
|
||||
社債 |
|
|
|
|
|
|
|
|
|
|
|
|
||||
政府債券 |
|
|
|
|
|
|
|
|
|
|
|
|
||||
外国債券 |
|
|
|
|
|
|
|
|
|
|
|
|
||||
公正な価値で計量された金融資産総額 |
|
$ |
|
|
$ |
|
|
$ |
|
|
$ |
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
負債.負債(2): |
|
|
|
|
|
|
|
|
|
|
|
|
||||
株式証を公開する |
|
$ |
|
|
$ |
|
|
$ |
|
|
$ |
|
||||
私募株式証明書 |
|
|
|
|
|
|
|
|
|
|
|
|
||||
喉頭管捜査令状 |
|
|
|
|
|
|
|
|
|
|
|
|
||||
公正な価値で計量された金融負債総額 |
|
$ |
|
|
$ |
|
|
$ |
|
|
$ |
|
||||
いくつありますか
社債、商業手形、外国債券および政府債券は、アクティブ市場の同種のツールの市場オファー、非アクティブ市場の同じまたは同様のツールのオファー、およびすべての重大な投入が、資産の全期間の観察可能な市場データによって実証されることができるモデルベースの推定技術に基づいて、第2のレベルに分類されることができる。
9
活発な市場で観察可能な市場オファーを使用するため、公共株式証は1段階に分類される。同じまたは同様の負債の観察可能な市場データを使用するため、私募株式証および管理権証はレベル2に分類される。各私募株式承認証及びPIPE株式承認証の公平価値は公開株式証の公平価値と一致することが確定された。私募持分証及びPIPE株式承認証も完全償還機能によって制限されているため、当社は株価が$#を介する時に類似条項に従ってこの2種類の株式承認証を償還することができる
次の表は、証券タイプ別に会社の有価証券を提供しています(千で計算)
|
|
2022年9月30日 |
|
|||||||||||||
|
|
原価を償却する |
|
|
未実現収益総額 |
|
|
未実現損失総額 |
|
|
公正価値 |
|
||||
商業手形 |
|
$ |
|
|
$ |
|
|
$ |
|
|
$ |
|
||||
社債 |
|
|
|
|
|
|
|
|
( |
) |
|
|
|
|||
政府債券 |
|
|
|
|
|
|
|
|
( |
) |
|
|
|
|||
短期有価証券総額 |
|
$ |
|
|
$ |
|
|
$ |
( |
) |
|
$ |
|
|||
|
|
2021年12月31日 |
|
|||||||||||||
|
|
原価を償却する |
|
|
未実現収益総額 |
|
|
未実現損失総額 |
|
|
公正価値 |
|
||||
商業手形 |
|
$ |
|
|
$ |
|
|
$ |
|
|
$ |
|
||||
社債 |
|
|
|
|
|
|
|
|
( |
) |
|
|
|
|||
外国債券 |
|
|
|
|
|
|
|
|
( |
) |
|
|
|
|||
短期有価証券総額 |
|
$ |
|
|
$ |
|
|
$ |
( |
) |
|
$ |
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
政府債券 |
|
$ |
|
|
$ |
|
|
$ |
( |
) |
|
$ |
|
|||
社債 |
|
|
|
|
|
|
|
|
( |
) |
|
|
|
|||
長期有価証券総額 |
|
$ |
|
|
$ |
|
|
$ |
( |
) |
|
$ |
|
|||
次の表は単一証券が未実現損失を続けている時間の長さを示している2022年9月30日(千ドル):
|
|
|
|
|
|
|
12ヶ月以下です |
|
||||||
|
|
|
|
投資数量 |
|
|
公正価値 |
|
|
未実現損失 |
|
|||
社債 |
|
|
|
|
|
|
$ |
|
|
$ |
|
|||
政府債券 |
|
|
|
|
|
|
|
|
|
|
|
|||
合計する |
|
|
|
|
|
|
$ |
|
|
$ |
|
|||
すべての短期取引可能証券の満期日は、2022年9月30日と2021年12月31日まで1年以下である。2022年9月30日及び2021年9月30日までの3ヶ月及び9ヶ月以内に、短期及び長期有価証券は重大な収益又は損失を達成していないそれは.当社は非一時的減価損失の売却可能投資を定期的に審査しています。赤字を達成していないすべての投資は12ヶ月未満の赤字状態にある。当社は、未実現損失は主に現在の市場金利の変化によるものであり、信用品質ではないと確定した。当社は赤字を実現していない状態の有価証券を売却するつもりはなく、自社に償却コストベース回収前に有価証券の売却を要求することも不可能であり、償却コストベースが満期になっている可能性がある。その結果、その会社は一時的な減価損失以外のいかなる損失も確認する2022年9月30日.
10
付記5.貸借対照表の構成要素
前払い費用と他の流動資産
前払い料金および他の流動資産には、以下のものが含まれている(千計)
|
|
九月三十日 |
|
|
十二月三十一日 |
|
||
前払い保険 |
|
$ |
|
|
$ |
|
||
研究開発費を前払いする |
|
|
|
|
|
|
||
賃料を前払いする |
|
|
|
|
|
|
||
利子その他売掛金 |
|
|
|
|
|
|
||
他にも |
|
|
|
|
|
|
||
前払い費用と他の流動資産 |
|
$ |
|
|
$ |
|
||
負債その他の負債を計上しなければならない
負債およびその他の負債には、以下の項目が含まれる(千で計算する)
|
|
九月三十日 |
|
|
十二月三十一日 |
|
||
給料と関連費用を計算しなければならない |
|
$ |
|
|
$ |
|
||
研究と開発費用を計算すべきである |
|
|
|
|
|
|
||
弁護士費と監査費用を計算する |
|
|
|
|
|
|
||
株式オプションの責任を繰り上げて行使する |
|
|
|
|
|
|
||
他にも |
|
|
|
|
|
|
||
負債その他の負債を計上しなければならない |
|
$ |
|
|
$ |
|
||
注6.ライセンス契約
スタンフォード大学許可協定
2016年3月に、当社はスタンフォード大学とライセンス契約を締結し、または2016年7月、2016年10月および2021年1月に改訂された“スタンフォード協定”は、特定の特許、権利または許可された特許および技術に基づいて、当社は、ヒトおよび獣医疾患を治療、診断および予防するために、特定の特許、権利または許可された特許および技術を使用または統合するために、スタンフォード大学と世界的に独占的に再許可可能な許可の許可を取得し、使用、使用、輸入、カプセル販売または販売する。同社はスタンフォード大学に合計$を支払うことに同意しました
2018年6月、当社はスタンフォード大学と別のライセンス契約、または2018年スタンフォード大学協定を締結し、その代理R-Respondinタンパク質に関連する特定の特許権またはライセンス特許に基づいて、当社は、ヒトおよび獣医疾患または独占分野の製品の治療、診断および予防または独占分野の製品を主張するために、スタンフォード大学から世界的に独占的な再許可許可を取得し、使用、輸入、要約販売および販売許可特許を主張する。さらに、スタンフォード大学は、ライセンス製品を製造および使用して独占分野の研究および開発を促進するために、ライセンス特許に基づいて同社に世界的に非独占的に再許可可能なライセンスを付与し、同社が他の使用分野のライセンス製品を製造、使用および輸入するが他の使用分野のライセンス製品を提供または販売しないグローバル非独占ライセンスを付与する。同社はスタンフォード大学に合計$を支払うことに同意しました
11
2022年9月30日までの3ヶ月と9ヶ月その会社はDe Minimisと$を招いた
カリフォルニア大学サンフランシスコ校の許可とオプション協定
当社は2016年9月および10月に、それぞれカリフォルニア大学の取締役と2つの独立した許可およびオプション協定、またはUCSF協定を締結し、これにより、当社はカリフォルニア大学サンフランシスコ校の独占許可を得て、内部研究および抗体発現用途に使用し、UCSFと交渉して、UCSFの適用ライブラリーにおける独占許可を取得し、当社がこのライブラリーを使用することにより識別または産生された抗体を含む製品、または特許製品を製造、使用、販売、発売および輸入する権利がある。
2020年1月、同社は、特定のヒト天然バクテリオファージ展示ライブラリーを製造および使用するために非排他的許可を提供するために、カリフォルニア大学サンフランシスコ校の合意を修正し、再確認し、内部研究および抗体発見目的のためにラクダVHH単一ドメイン抗体ライブラリを提供および使用し、UCSFと交渉して非独占的商業許可を得ることを選択し、適用ライブラリーにおけるUCSFの権利に基づいて、会社がライブラリーを使用することによって決定または産生された抗体を含む製品を製造、使用、販売、提供、および輸入することができるかもしれない。
2022年3月、同社はUCSFプロトコル下の選択権を行使し、バクテリオファージがラクダVHH単一ドメイン抗体ライブラリを示す許可製品を製造および使用するための非独占商業許可契約を締結した。商業許可協定によると、会社はUCSFに象徴的な許可発行費を支払い、象徴的な年間許可維持費を支払うことに同意し、規制マイルストーンに達したときに各許可製品の5~6桁の支払い、名目上の最低年間特許権使用料、および会社と会社の再許可者が製品の純売上高の1桁未満の割合で稼いだ特許権使用料を支払うことに同意する。
2022年9月30日までの3ヶ月と9ヶ月その会社はDe Minimisと$を招いた
分散Bio購読プロトコル
2016年9月、当社はCharles River実験室国際会社(前身はDistributed Bio,Inc.)と抗体ライブラリ購読協定を締結し、2019年1月に協定を改訂し、この合意に基づき、当社はDistributed Bioの抗体バンクから会社独自の目標に対する無限数の抗体を識別する非独占許可を取得し、会社が決定した抗体を含む製品を生産、使用、販売、要約、輸入、開発することができるかもしれない。同社は最初の3年後にDistributed Bioに6桁以下の年会費を支払うことに同意した。また、同社は分散生物会社に合計#ドルを支払うことに同意した
2022年9月30日までの3ヶ月と9ヶ月その会社は$を生み出しました
付記7.支払いの引受やその他の事項
賃貸契約
2016年8月、当社は約を含むオフィスと実験室空間レンタル契約を締結しました
12
当社は2020年1月に賃貸契約を締結し、レンタル期間は
2022年と2021年9月30日まで3ヶ月と9ヶ月の経営レンタル料金はい$です
経営賃貸契約の下で将来最低賃貸料支払い合計2022年9月30日の状況は以下の通り(単位:千):
2022年12月31日までの残り3ヶ月 |
|
$ |
|
|
2023年12月31日までの年度 |
|
|
|
|
2024年12月31日までの年度 |
|
|
|
|
2025年12月31日までの年度 |
|
|
|
|
賃貸支払総額 |
|
|
|
|
差し引く:推定利息 |
|
|
( |
) |
リース負債を経営する |
|
$ |
|
付記8.株主権益
株式購入協定
2022年2月に、当社はリンカーン公園と持分購入契約を締結し、この協定によると、リンカーン公園は最も多く購入する責任がある
株式購入契約に調印した後,当社は発行する
株式購入契約の想定では、会社の普通株の終値が$を超える限り
会社はリンカーン公園に通常の購入限度額以下ではありませんが、超えないように指示することもできます
2022年9月30日まで会社が所有しています
13
注9.普通株式承認証
業務合併については,Legacy Surrozenは会計買収側として,Cononanceを担う株主が保有する引受権証,あるいは公共株式承認証,およびCononanceの保証人が保有する引受権証,あるいは私募株式権証とみなされる。また、PIPE融資では、一部の投資家が購入と購入を認めている一つの集合
タイプ |
|
分類する |
|
期日まで |
|
1部当たりの株式証の行使価格 |
|
|
手令の数 |
|
|
公正価値 |
|
|||
株式証を公開する |
|
|
|
$ |
|
|
|
|
|
$ |
|
|||||
私募株式証明書 |
|
|
|
|
|
|
|
|
|
|
|
|||||
喉頭管捜査令状 |
|
|
|
|
|
|
|
|
|
|
|
|||||
合計する |
|
|
|
|
|
|
|
|
|
|
|
$ |
|
|||
株式証を公開する
各完全な公共株式証明書は所有者に#ドルの価格で会社の普通株を購入する権利を持たせる
会社は未発行の引受権証を償還することができ、価格は$です
いずれの場合も、当社は現金純額決済による株式公開承認証の公開を要求されません。公共権証所持者は、その公共権証を行使して普通株式を取得するまで、普通株式株主の権利又は特権及びいかなる投票権も有していない。
私募株式証明書
私募持分証は公開持分証と同じ条項と規定を有しており、異なる点は、それらが協和した保証人またはその任意の許可譲渡者が保有している限り、私募持分証:(I)現金または無現金基礎で行使することができ、(Ii)譲渡、譲渡または販売することができない点である
喉頭管捜査令状
全管理権証は所有者に会社の普通株を購入する権利を持たせ、価格は#ドルである
14
分類する
株式証明書合意のある条項はこの等株式証の決済金額を変更する可能性があるため、株式承認証、私募株式証及びパイプ株式承認証を公開することは当社の普通株とリンクしているとはみなされていない。したがって、それらは、負債に分類され、公正価値で記録され、その後、他の収入(費用)で確認されたそれぞれの公正価値の変化、監査されていない簡明な総合経営報告書における純額、および各報告日における全面的な損失に分類される。権証推定値に関する検討は,付記4を参照されたい。
注10.株ベースの報酬計画
同社は2021年株式インセンティブ計画、または2021年計画を維持しており、従業員、取締役、コンサルタントに株式奨励を付与することを規定している。2021年計画に従って付与されるオプションは、奨励株式オプション、またはISO、または非限定株式オプション、またはNSOであってもよい2021年計画によると付与されたオプションは
同社は2021年8月に2021年従業員の株式購入計画、略称ESPPを採択したESPPは条件を満たす従業員が賃金減額で割引価格で会社の普通株を購入することを許可し、最高で
ESPP項における株式ベースの報酬支出は,発行期間開始時にBlack-Scholesオプション定価モデルを用いて測定し,発行期間内に直線ベースで確認した.
株式オプション
以下に株式オプション活動の概要を示す
|
|
未償還オプション |
|
|||||||||||||
|
|
|
|
|
|
|
|
重みをつける |
|
|
|
|
||||
|
|
|
|
|
重みをつける |
|
|
平均値 |
|
|
骨材 |
|
||||
|
|
量 |
|
|
平均値 |
|
|
残り |
|
|
固有の |
|
||||
|
|
オプション |
|
|
トレーニングをする |
|
|
契約期限 |
|
|
価値がある |
|
||||
|
|
(単位:千) |
|
|
値段 |
|
|
(単位:年) |
|
|
(単位:千) |
|
||||
未返済-2021年12月31日 |
|
|
|
|
$ |
|
|
|
|
|
|
|
||||
授与する |
|
|
|
|
|
|
|
|
|
|
|
|
||||
没収される |
|
|
( |
) |
|
|
|
|
|
|
|
|
|
|||
期限が切れる |
|
|
( |
) |
|
|
|
|
|
|
|
|
|
|||
未返済-2022年9月30日 |
|
|
|
|
|
|
|
|
|
|
$ |
|
||||
行使可能-2022年9月30日 |
|
|
|
|
|
|
|
|
|
|
|
|
||||
発行済みと行使可能オプションの総内在価値は、オプションの行使価格と会社普通株の2022年9月30日の公正価値との差額である。
2022年9月30日までの9ヶ月間当社は加重平均授与日公正価値を$とするオプションを付与している
15
オプションの公正価値は付与日にブラック·スコアーズオプション定価モデルを用いて推定され、その加重平均は以下のように仮定される
|
|
9月30日までの3ヶ月間 |
|
|
9月30日までの9ヶ月間 |
|
||||||||||
|
|
2022 |
|
|
2021 |
|
|
2022 |
|
|
2021 |
|
||||
予想期限(年単位) |
|
|
|
|
|
|
|
|
|
|
|
|
||||
予想変動率 |
|
|
% |
|
|
% |
|
|
% |
|
|
% |
||||
無リスク金利 |
|
|
% |
|
|
% |
|
|
% |
|
|
% |
||||
配当率 |
|
|
|
|
|
|
|
|
|
|
|
|
||||
制限株式賞
以下の表は、会社の制限的な株式奨励活動をまとめたものである
|
|
|
|
|
重みをつける |
|
||
|
|
量 |
|
|
平均値 |
|
||
|
|
株 |
|
|
授与日 |
|
||
|
|
(単位:千) |
|
|
公正価値 |
|
||
RSA、2021年12月31日は帰属していません |
|
|
|
|
$ |
|
||
既得 |
|
|
( |
) |
|
|
|
|
RSA、2022年9月30日まで帰属していません |
|
|
|
|
|
|
||
2022年9月30日までの9ヶ月以内に帰属する制限株式奨励の公正価値はい$です
株に基づく報酬
監査されていない簡明な合併経営報告書に記録されている株式報酬支出総額および株式オプション、制限株式報酬、ESPPに関する全面的な損失は以下の通り(千で計算)
|
|
9月30日までの3ヶ月間 |
|
|
9月30日までの9ヶ月間 |
|
||||||||||
|
|
2022 |
|
|
2021 |
|
|
2022 |
|
|
2021 |
|
||||
研究開発 |
|
$ |
|
|
$ |
|
|
$ |
|
|
$ |
|
||||
一般と行政 |
|
|
|
|
|
|
|
|
|
|
|
|
||||
株式に基づく報酬総支出 |
|
$ |
|
|
$ |
|
|
$ |
|
|
$ |
|
||||
2022年9月30日まで約一ドルです
注11.後続事件
オプション取引所
2022年10月、会社報酬委員会は、既存従業員が保有するいくつかの未償還株式オプションを1対1に基づいて、当日当時の市場価格の取引価格を交換して株式オプションとして交換する株式オプション取引所を許可し、承認した。この交換の結果として
16
協力と許可協定
2022年10月、同社はBIとCLAに署名し、SZN−413を含む会社SWAP?技術設計のFZD 4二重特異性抗体を研究、開発、商業化した。BIと同社は1年間でSZN−413に重点を置いた共同研究を行い,BIは最大6カ月延長する権利がある。共同研究が完了した後、BIは独占的で、印税を負担する、全世界範囲で再許可可能な許可証を持ち、すべての更なる研究、臨床前と臨床開発、製造、監督許可と許可製品の商業化を担当し、費用はBIが負担する。
CLAの条項によると、会社は払い戻しできない前払い$を受け取るだろう
17
項目2.経営陣の財務状況と経営結果の検討と分析
以下の議論と分析は、本Form 10-Q四半期報告または本報告の他の部分に含まれる監査されていない簡明総合財務諸表および関連付記および2022年3月28日に提出されたForm 10-K年度報告書に含まれる2021年12月31日までの総合財務諸表および関連付記とともに読まなければならない。別の説明がない限り、用語“Surrozen”、“私たち”、“私たち”または“私たち”とは、Cononance-HFW Acquisition Corp.およびSurrozen,Inc.(前身はCononance-HFW Acquisition Corp.)との業務合併前のSurrozen Operating,Inc.またはLegacy Surrozen,Inc.,および業務合併発効後の合併子会社を意味する。
前向きに陳述する
以下の我々の財務状況及び経営結果の検討には、1933年証券法第27 A条(改正)及び“1934年証券取引法”(改正)第21 E条の意味を満たす前向きな陳述が含まれている。前向きな陳述は、私たちの経営陣の信念と仮定と、私たちの経営陣が現在把握している情報に基づいている。これらの規定について言えば、歴史的事実陳述以外のすべての陳述は、未来の事件または私たちの未来の財務業績と財務指針に関する陳述を含む“前向き陳述”である。場合によっては、前向き陳述は、“可能”、“予想”、“予想”、“計画”、“予想”、“プロジェクト”、“信じ”、“推定”、“予測”、“潜在”、“意図”または“継続”などの用語によって識別することができ、これらの用語または他の同様の用語の否定、ならびに将来の運営または財務業績に関する任意の議論に関連する他の言葉または同様の意味の用語を識別することができる。これらの声明はただ予測に過ぎない。
本文書に含まれるすべての前向き記述は,本プレスリリースの日に得られた情報に基づいており,このような前向き記述を更新する義務はない.私たちのここでの任意またはすべての展望的な陳述は間違っていることが証明されるかもしれない。実際の事件や結果は大きく違うかもしれない。私たちの展望的な陳述は、私たちがし得る不正確な仮定または既知または未知のリスク、不確実性、および他の要素の影響を受けるかもしれない。これらの陳述を評価する際には、本報告第2部1 A項“リスク要因”で概説されたリスクや、米国証券取引委員会に時々提出された他の文書に含まれるリスクを含む様々な要因を具体的に考慮すべきである。私たちは投資家たちに、私たちの業務と財務業績が重大なリスクと不確定要素の影響を受けることを想起させる。
概要
我々はWnt経路を選択的に調節するための生物候補薬を発見·開発しており,組織修復の重要な媒体であり,広範な臓器や組織においてヒト疾患の治療に用いられている。著者らの創始者と科学顧問はWnt遺伝子とWnt経路の重要な制御因子を発見し、彼らの先駆的な仕事に基づいて、著者らは突破的な発見を得て、これらの発見は以前のWnt生物学的潜在力を利用する上での制限を克服すると信じている。これらの突破により,Wntシグナルを調節する組織標的療法を迅速かつ柔軟に設計することができる。著者らの発見により、著者らはWntシグナル選択性活性化の先駆を開拓し、Wnt経路シミュレーションを設計と設計し、組織特異性Wnt候補遺伝子を提案した。
著者らの主要な候補製品は多重特異性、抗体による療法であり、それらは自然に産生されるWnt或いはR-Respondinタンパク質の作用を模倣し、この2種類のタンパク質はそれぞれWnt経路の活性化と増強に参与する。Wntシグナルは体全体の組織維持と再生に不可欠であることから、著者らは腸管、肝臓、網膜、角膜、肺、腎臓、蝸牛、皮膚、膵臓と中枢神経系を悩ませる疾患を含む様々な深刻な疾患を対象とする可能性がある。これらの領域のすべての領域において,我々の方法は疾患の治療様式を変化させ,患者の結果に大きく影響する可能性があると信じている。
われわれの戦略は,Wnt調節反応に対する疾患状態を認識することにより,Wntシグナルのすべての潜在力を開発し,組織特異的療法を設計し,需要を満たしていない標的適応の中で候補薬物の臨床開発を進めることである。私たちの独特な方法とプラットフォーム技術は二つの有力な候補製品の発見と進歩を招いた。
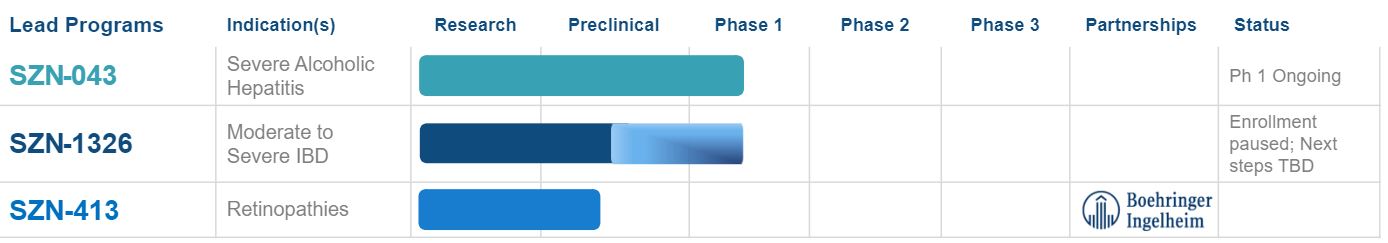
われわれは2022年第2四半期にSZN−1326の第1段階臨床試験を開始し,SZN−1326はわれわれが開発した中重度炎症性腸疾患(IBD)の候補薬であり,潰瘍性大腸炎(UC)をわれわれの第1の推奨適応とした。SZN−1326はFZD 5に対する二重特異性抗体であり,SurrozenのSWAP技術を用いて設計された最初の開発候補抗体であり,腸管上皮中のWntシグナル経路を目指している。急性および慢性大腸炎の前臨床動物モデルでは,SZN−1326は病変腸管中のWntシグナルを瞬時に活性化し,腸管上皮細胞再生を刺激し,炎症を減少させ,疾患活動性を低下させることが証明されており,ラットや非ヒト霊長類動物(NHP)13週の毒理学的評価では治療に関連する副作用は認められなかった。
2022年11月、我々は、治療に関連する有害事象が観察された後、我々の第1段階臨床試験におけるSZN-1326の単一漸増用量またはSAD部分の登録を自発的に一時停止することを発表した。一部の被験者は無症状の肝トランスアミナーゼの上昇が出現し、3級ALTとAST上昇の被験者を含む。総ビリルビンはそれに応じて増加せず,凝固マーカーやアルブミンなどの肝機能指標も何の変化もなかった。他に臨床的意義のある実験室異常は認められず,すべての被験者のトランスアミナーゼ上昇は自発的に消失した。
18
研究期間中に重篤な副作用は認められなかった。著者らは研究調査者と更に既存の臨床データを分析し、追加の臨床前実験を行い、トランスアミナーゼ上昇の潜在機序を確定し、開発計画の次のステップを確定するつもりである。
我々は2022年第2四半期にSZN−043の第1段階臨床試験を開始し,SZN−043はわれわれが開発した重症アルコール性肝炎またはAHの候補薬である。SZN-043はASR 1の肝細胞特異的R-応答素に対して二重特異性融合タンパク質をシミュレートし、蘇羅岑の甘い技術を用いて開発された最初の候補タンパク質であり、細胞標的方式でWntシグナルを増強することによってタンパク質R-応答素の再生特性をシミュレートすることを目的としている。多くの肝障害と肝線維化の臨床前動物モデルにおいて、SZN−043は肝臓中のWntシグナルを選択的に活性化し、一時的な肝細胞増殖を刺激し、肝機能を改善し、線維化を軽減することが証明されており、マウスとNHPの4週間のGLP毒理学評価では治療に関連する副作用は認められなかった。Surrozenは重篤な肝疾患のためのSZN−043を開発しており,最初は重篤なアルコール性肝炎に集中していた。
2022年11月,健康ボランティアで行われたSZN−043試験のSAD部分の最新状況を提供した。SZN−043を服用した数名の被験者は,1級と2級治療に関連する無症状肝トランスアミナーゼの上昇を認めた。これらの被験者では,総ビリルビンやGGTはそれに応じて増加せず,凝固マーカーやアルブミンなどの肝機能マーカーにも変化はなかった。他に臨床的意義のある実験室異常は認められず,これらの被験者のトランスアミナーゼ上昇は自発的に消失した。これまで行われてきた研究では深刻な有害事象は観察されていない。私たちはこの計画の全体的な臨床開発スケジュールを再評価するつもりだ。
2022年第1四半期、我々は網膜血管関連疾患を治療する開発候補薬としてFZD 4標的二重特異性抗体SZN-413を指名した。FZD 4を介したWntシグナルは網膜血管の完全性と機能において重要な役割を果たしている。臨床前網膜病変モデルで産生したデータにより、SZN-413はWntシグナルを刺激し、そして正常な網膜血管再生を誘導でき、同時に病理性血管成長を抑制できることを表明した。私たちは最近、ブリンガー-インゲルハイム国際有限会社(BI)とSZN-413を含むFzd 4二重特異性抗体を研究、開発、商業化するCLA、同社のSWAP技術を用いて設計されたFzd 4二重特異性抗体を締結した。
以下のグラフは、私たちが所有している候補製品の概要です

私たちの科学的能力と方法を利用することで、私たちは20種類以上の潜在的な組織タイプを決定して探索した。肺,涙腺,角膜,膵,皮膚などの臓器組織損傷を引き起こす疾患における組織修復推進の潜在力を評価している。
次のグラフは私たちが所有している研究プロジェクトの概要です
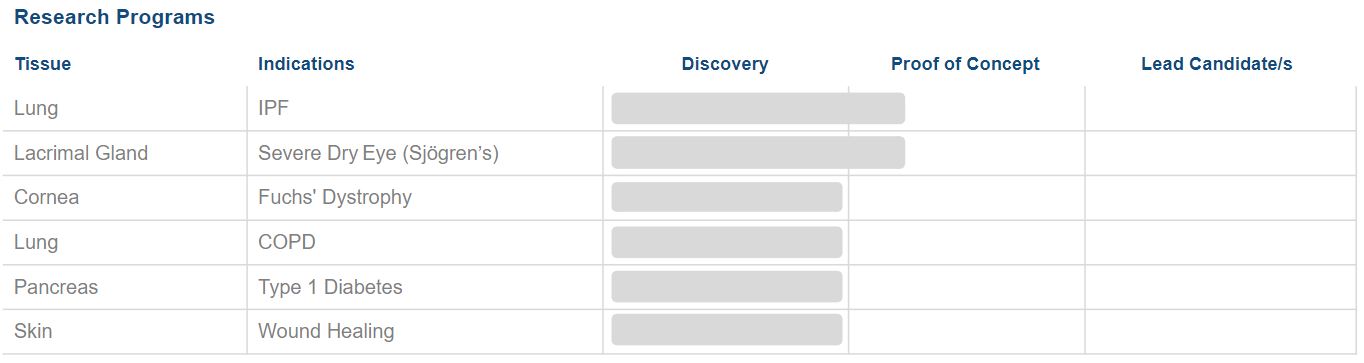
2015年の設立以来、私たちはほとんどの努力と財務資源を会社の組織と人員の配置、業務計画、資金の調達、私たちのWNT治療プラットフォームの開発と最適化、潜在的な候補製品の決定、研究開発活動の展開、戦略取引の展開、私たちの確立と強化に投入した
19
知的財産権を組み合わせて、これらの業務に一般的で行政的な支援を提供する。設立以来、私たちは純損失を受けた。2022年9月30日と2021年9月30日までの3ヶ月間、1340万ドルと1400万ドルの純損失が発生した。2022年9月30日と2021年9月30日までの9ヶ月間、3520万ドルと3970万ドルの純損失が発生した。2022年9月30日までの累計赤字は1兆779億ドル、現金、現金等価物、有価証券は7840万ドル。
私たちは予測可能な未来に損失が続くと予想し、私たちのパイプラインを拡大し、臨床開発と監督提出を通じて私たちの候補製品を推進することに伴い、より多くの費用が発生すると予想される。具体的には,短期的には,われわれの第一段階臨床試験,われわれの製造プロセスの開発と検証,その他の研究·開発活動に関する多くの費用が生じることが予想される。
オウ紛争と新冠肺炎の流行の影響
ロシアは2022年2月にウクライナに侵入し、現在もウクライナに対する武力衝突に積極的に参加している。全世界の新冠肺炎の疫病は引き続き変化し、私たちは引き続き事態の発展を密接に注視する。現在まで、私たちの財務状況と運営はロシアとウクライナの間の衝突や新冠肺炎の疫病の大きな影響を受けていない。私たちの業務、運営と臨床開発スケジュールと計画への影響の程度はまだ不確定であり、これは米国と外国政府がロシアに対する制裁と新冠肺炎の伝播を緩和するための行動及び私たちの臨床前開発活動、監督機関、臨床研究組織或いはCRO、第三者メーカーと他の私たちと業務往来のある第三者の影響、及びもし私たちが監督部門の許可を得たら人体投与の開始、試験登録と試験場所を含むいくつかの事態の発展に依存する。私たちは引き続き迅速に変化する情勢を積極的に監視し、連邦、州、あるいは地方当局が要求する可能性のある行動を含む、私たちの運営を変える行動を取るかもしれないし、私たちの従業員や他の私たちとの業務往来のある第三者の利益に最も適合すると思う行動を取るかもしれない。
インフレの影響
インフレ率は上昇しており、近い将来も上昇し続けると予想される。インフレは一般的に労働コスト、研究、そして臨床試験コストを増加させることで私たちに影響を及ぼす。我々はインフレが我々の財務状況や本報告で述べた期間の経営結果に実質的な影響を与えるとは考えていないが、予測可能な将来にコストを増加させ、我々の業務や財務状況に悪影響を及ぼす可能性がある。また、インフレは、全体的な経済状況においてより大きな不確実性を経験し、我々の普通株式市場価格のさらなる変動をもたらす可能性があり、これらは金利上昇とウクライナの持続的な軍事衝突の影響を受けている。これらの状況が悪化したり改善されなければ、私たちの資金調達能力と私たち株主の株式売却能力は悪影響を受けるだろう。
知的財産権と許可手配
2022年9月30日現在、私たちの特許組み合わせは、米国および他の国で国家段階に入った15個のファミリー、2つの係属中の特許協力条約またはPCT出願ファミリーを含む20個以上の係属中の特許出願ファミリーを含み、それらはまた、いくつかの非PCT国(例えば、台湾)で出願され、5つの係属中の米国仮出願ファミリーを含む。例えば、これらの特許出願は、SWAPおよびSCOTS?プラットフォーム、我々の2つの主要製品候補分子SZN−043およびSZN−1326の親構造、最近許可されたSZN−413、ならびに肝臓、腸管、網膜、角膜、涙腺および腎臓疾患を治療する方法を対象としている。
また、本報告財務諸表付記6に記載されているように、第三者と特許及び研究ツール許可手配を達成した。ライセンス協定は特定の規制と開発段階に達した後に記念碑的なお金を支払うことを要求する。しかも、私たちは特定の許可された製品の販売に印税を支払うことを要求されるだろう。2022年9月30日まで、私たちの許可協定によると、象徴的な費用とマイルストーンの支払いが発生しました。さらなる規制と発展のマイルストーンやライセンス製品の販売を実現した後、これらの許可に基づいて多くの費用と印税が発生する可能性があります。
本報告財務諸表付記11に記載されているように、我々は、SZN−413を含むFZD 4二重特異性抗体を研究、開発および商業化するために、2022年10月にBIとCLAに署名した。我々とBIは1年以内にSZN−413に重点を置いた共同研究を行い,BIは最大6カ月延長する権利がある。共同研究が完了した後、BIは私たちが適用する特許と技術の下で独占的で、印税があり、世界的に再許可可能な許可証を持って、すべての用途のための抗体およびその誘導体を開発、製造、商業化し、BIはすべてのさらなる研究、臨床前と臨床開発、製造、規制承認と許可製品の商業化を担当し、費用はBIが負担する。
20
経営成果の構成部分
収入.収入
2022年9月30日まで、2022年10月にCLAが実行されるまで、私たちは何の収入も生じなかった。CLAによれば、本報告財務諸表脚注11に記載されているように、1,250万ドルの払戻不能前金を得る資格があります。私たちが規制部門の承認や承認を得ない限り、私たちは私たちの製品を販売することから何の収入も得られないと予想される。
運営費
運営費を,(I)研究および発展費および(Ii)一般および行政支出の2つに分類した。
研究と開発費
設立以来、私たちは私たちの研究開発活動に大量の資源を集中させてきた。私たちの研究開発費には、私たちの研究活動や開発計画に関する外部と内部費用が含まれています。
外部費用には、
内部費用には、
私たちの追跡は私たちの臨床開発候補者の外部費用に直接起因することができる。私たちは具体的なプロジェクトに基づいて私たちの臨床開発候補者に内部費用を分配する。我々の内部資源,従業員,インフラは通常複数の計画に配置されているため,早期研究や発見計画の内部費用は割り当てられない.したがって、早期研究·発見計画に生じるコストに関する財務情報を、計画に基づいて具体的に提供することはできない。
予測可能な未来には,候補製品の決定と開発に伴い,我々の研究開発費は大幅に増加すると予想され,特に臨床試験の継続を求め,SZN−1326とSZN−043の規制承認と商業化を求める場合である。
私たちの候補製品が開発に成功するかどうかは大きな不確実性を持っている。現在、SZN−1326、SZN−043、およびSZN−413の残りの開発または任意の将来の候補製品を完成させるのに必要な性質、時間、またはコストを合理的に推定することはできない。これは、候補製品開発に関連する多くのリスクおよび不確実性が原因であり、その多くのリスクおよび不確実性は、以下の点に関連するリスクおよび不確実性を含む、私たちの制御範囲内にないからである
21
これらの変数の任意の結果の任意の変化は、私たちの候補薬物開発に関連するコストと時間の大きな変化を意味するかもしれない。
一般と行政費用
一般および行政費用は、主に人事関連費用を含み、行政、財務、人的資源、業務および会社発展、法律、情報技術および他の行政機能者の賃金、ボーナス、福祉、株式ベースの給与費用を含む。一般および行政費用には、弁護士費、会計、監査、相談、税務と投資家関係サービスの専門費用、保険料と研究開発費に計上されていない施設コスト、および米国証券取引委員会やナスダック規則の遵守に関連するコストも含まれる。私たちは、予測可能な未来に、私たちの一般的かつ行政的費用が大幅に増加し、拡大していく従業員数と運営を支援することを予想している。
利子収入
利息収入には主に現金等価物と有価証券による利息が含まれる。
その他の収入,純額
その他の収入(支出)、純額には、株式証明負債公平値変動の収益と、持分購入協定に従ってリンカーン公園資本基金またはリンカーン公園に発行された承諾株式に関する支出が含まれる。
経営成果
2022年9月30日までおよび2021年9月30日までの3カ月間の比較
表に示した各期間の業務成果(千ドル単位)をまとめた
|
|
9月30日までの3ヶ月間 |
|
|
$ |
|
|
% |
|
|||||||
|
|
2022 |
|
|
2021 |
|
|
変わる |
|
|
変わる |
|
||||
運営費用: |
|
|
|
|
|
|
|
|
|
|
|
|
||||
研究開発 |
|
$ |
8,624 |
|
|
$ |
10,418 |
|
|
$ |
(1,794 |
) |
|
|
-17 |
% |
一般と行政 |
|
|
4,981 |
|
|
|
3,287 |
|
|
|
1,694 |
|
|
|
52 |
% |
総運営費 |
|
|
13,605 |
|
|
|
13,705 |
|
|
|
(100 |
) |
|
|
-1 |
% |
運営損失 |
|
|
(13,605 |
) |
|
|
(13,705 |
) |
|
|
100 |
|
|
|
-1 |
% |
利子収入 |
|
|
198 |
|
|
|
14 |
|
|
|
184 |
|
|
* |
|
|
その他の収入,純額 |
|
|
50 |
|
|
|
(328 |
) |
|
|
378 |
|
|
|
-115 |
% |
純損失 |
|
$ |
(13,357 |
) |
|
$ |
(14,019 |
) |
|
$ |
662 |
|
|
|
-5 |
% |
22
*百分率は意味がない
研究と開発費
表に示した期間の研究と開発費用(千ドル単位)をまとめた
|
|
9月30日までの3ヶ月間 |
|
|
$ |
|
|
% |
|
|||||||
|
|
2022 |
|
|
2021 |
|
|
変わる |
|
|
変わる |
|
||||
SZN-1326 |
|
$ |
2,808 |
|
|
$ |
4,505 |
|
|
$ |
(1,697 |
) |
|
|
-38 |
% |
SZN-043 |
|
|
3,545 |
|
|
|
2,023 |
|
|
|
1,522 |
|
|
|
75 |
% |
発見と臨床前 |
|
|
2,271 |
|
|
|
3,890 |
|
|
|
(1,619 |
) |
|
|
-42 |
% |
総研究と |
|
$ |
8,624 |
|
|
$ |
10,418 |
|
|
$ |
(1,794 |
) |
|
|
-17 |
% |
2021年9月30日までの3カ月と比較して,2022年9月30日までの3カ月のSZN−1326計画費用は170万ドル減少し,減少幅は38%であり,これは主に麻薬物質の製造が完了したためである。2021年9月30日までの3カ月と比較して、2022年9月30日までの3ヶ月間、SZN-043計画支出は150万ドル、すなわち75%増加した。これは、主に分配された人員コストと株式ベースの報酬支出が60万ドル増加したことと、米国国家衛生研究院が2020年9月に付与した政府支出が90万ドル減少したためである。2021年9月30日までの3カ月と比較して,2022年9月30日までの3カ月で,臨床前段階計画との費用の160万ドル,または42%の減少が認められたのは,われわれを支援する臨床計画に資源を移したためである。
一般と行政費用
2021年9月30日までの3カ月と比較して、2022年9月30日までの3ヶ月間の一般·行政費が170万ドル、または52%増加したのは、主に従業員数の増加、専門費用の30万ドルの増加と、主に業務増加と会社保険の10万ドルの増加、人員関連費用の100万ドルの増加によるものである。
利子収入
2021年9月30日までの3ヶ月間と比較して、2022年9月30日までの3ヶ月間の利息収入が20万ドル増加したのは、主に通貨市場基金や有価証券への投資金利が上昇したためである。
その他の収入,純額
2022年9月30日までの3カ月間の他の収入(支出)純額は、2021年9月30日までの3カ月より40万ドル増加し、115%に増加したが、これは主に2021年9月30日までの3カ月間に発生した2021年8月に完了した業務合併に関する権証債務に関する取引コストによるものである。2022年9月30日までの3ヶ月間、このようなコストは発生しなかった。
経営成果
2022年9月30日までおよび2021年9月30日までの9カ月間の比較
表に示した各期間の業務成果(千ドル単位)をまとめた
|
|
9月30日までの9ヶ月間 |
|
|
$ |
|
|
% |
|
|||||||
|
|
2022 |
|
|
2021 |
|
|
変わる |
|
|
変わる |
|
||||
運営費用: |
|
|
|
|
|
|
|
|
|
|
|
|
||||
研究開発 |
|
$ |
27,576 |
|
|
$ |
29,284 |
|
|
$ |
(1,708 |
) |
|
|
-6 |
% |
一般と行政 |
|
|
14,594 |
|
|
|
10,112 |
|
|
|
4,482 |
|
|
|
44 |
% |
総運営費 |
|
|
42,170 |
|
|
|
39,396 |
|
|
|
2,774 |
|
|
|
7 |
% |
運営損失 |
|
|
(42,170 |
) |
|
|
(39,396 |
) |
|
|
(2,774 |
) |
|
|
7 |
% |
利子収入 |
|
|
307 |
|
|
|
30 |
|
|
|
277 |
|
|
|
923 |
% |
その他の収入,純額 |
|
|
6,634 |
|
|
|
(328 |
) |
|
|
6,962 |
|
|
* |
|
|
純損失 |
|
$ |
(35,229 |
) |
|
$ |
(39,694 |
) |
|
$ |
4,465 |
|
|
|
-11 |
% |
*百分率は意味がない
23
研究と開発費
表に示した期間の研究と開発費用(千ドル単位)をまとめた
|
|
9月30日までの9ヶ月間 |
|
|
$ |
|
|
% |
|
|||||||
|
|
2022 |
|
|
2021 |
|
|
変わる |
|
|
変わる |
|
||||
SZN-1326 |
|
$ |
7,914 |
|
|
$ |
11,613 |
|
|
$ |
(3,699 |
) |
|
|
-32 |
% |
SZN-043 |
|
|
9,410 |
|
|
|
7,382 |
|
|
|
2,028 |
|
|
|
27 |
% |
発見と臨床前 |
|
|
10,252 |
|
|
|
10,289 |
|
|
|
(37 |
) |
|
|
0 |
% |
総研究と |
|
$ |
27,576 |
|
|
$ |
29,284 |
|
|
$ |
(1,708 |
) |
|
|
-6 |
% |
2021年9月30日までの9カ月と比較して,2022年9月30日までの9カ月間のSZN−1326計画費用は370万ドル減少し,減少幅は32%であり,これは主に麻薬物質の製造が完了したためである。2021年9月30日までの9カ月と比較して、2022年9月30日までの9カ月間のSZN-043計画支出は200万ドル増加し、27%に増加したが、これは主にこの計画に割り当てられた人員コストと株式報酬支出が高いためである。2022年9月30日までの9カ月間の臨床前·発見·その他の研究開発コストは,2021年9月30日までの9カ月に近い。
一般と行政費用
2021年9月30日までの9カ月と比較して、2022年9月30日までの9ヶ月間の一般·行政費が450万ドル、または44%増加したのは、主に従業員数と従業員に付与されたオプションの増加により、会社保険が120万ドル増加し、主に運営の増加、求人コストが20万ドル増加し、人員関連費用が310万ドル増加したためである。Cononance−HFW買収会社との業務統合を開始することが決定するまで,潜在的な初公募株に関する専門やコンサルティングサービス費用は40万ドル減少した。
利子収入
2021年9月30日までの9カ月と比較して、2022年9月30日までの9カ月間の利息収入が20万ドル増加し、923%に増加したのは、主に通貨市場基金や有価証券への投資の増加と、通貨市場基金や有価証券への投資の金利上昇によるものである。
その他の収入,純額
2022年9月30日までの9カ月間は、2021年9月30日までの9カ月と比較して、他の収入(支出)の純額が700万ドル増加し、主な原因は株式証負債の公正価値変化収益が690万ドル増加し、2021年8月に完了した業務合併関連発行の引受権証負債に関する支出が40万ドル減少したが、2022年2月に株式購入合意によるリンカーン公園への約束株式関連支出が30万ドル増加したためである。
流動性と資本資源
設立以来、私たちは大量の純運営損失と運営からのマイナスキャッシュフローが発生した。歴史的に見ると、私たちの運営資金は主に私たちの償還可能な転換可能な優先株の売却から来ている。2022年9月30日現在、私たちは7840万ドルの現金、現金等価物、有価証券を持っており、累計赤字は1兆779億ドル。
私たちは2022年2月にリンカーン公園と購入契約と登録権協定を締結し、この協定によると、リンカーン公園は2022年4月27日から36ヶ月以内に、自ら適宜最大5000万ドルの普通株を購入する義務がある。今まで、私たちは購入合意に従ってどんな普通株も売っていなかった。
私たちは2022年10月にCLAに署名しました。CLAによると、払い戻しできない1,250万ドルの前金を受け取ります。このうち1050万ドルの前金は2022年第4四半期に受信される予定で、残りの200万ドルは2023年6ヶ月前に受信される予定だ。また、成功に基づくマイルストーン支払いを受ける資格があり、最高5.87億ドルに達し、ライセンス製品の純売上高の中央値から1桁から2桁低い印税を受ける資格がある。
私たちの現在の運営計画によると、私たちの既存の現金、現金等価物、有価証券に、CLAに関連する1250万ドルの総現金収益を加えて、スタンフォード大学とカリフォルニア大学の取締役会に支払われた130万ドルの費用を差し引くと、私たちの運営に少なくとも本報告の発表日から今後12ヶ月の資金を提供するのに十分であると信じている。しかし、将来予想される運営結果を達成できない場合、私たちは予想よりも早く私たちの資本資源を使用することができ、これは、将来の計画支出を減少させ、および/または追加の資本を調達して運営に資金を提供し続ける必要がある可能性がある。
24
将来の資金需要
これまでBIとのパートナーシップからのみ収入を得てきたが,これらのパートナーシップは2022年10月に署名されたCLAに関係している。私たちは、規制部門の承認を得て、私たちの候補製品の一つを商業化しなければ、私たちの製品を販売することから何の収入も得たくありません。これがいつ、または起こるかどうかはわかりません。私たちは引き続き私たちの候補製品を開発し、予測可能な未来に運営に資金を提供するために多くの追加資金を必要とするだろう。2015年の設立以来、私たちはほとんどの努力と財務資源を投入して、私たちの会社の人員、業務計画、資金を組織し、調達し、私たちのWNT治療プラットフォームを開発と最適化し、潜在的な候補製品を決定し、研究開発活動を展開し、戦略取引に従事し、私たちの知的財産権の組み合わせを構築し、強化し、これらの業務に一般的かつ行政的な支持を提供している。私たちが引き続き臨床開発と規制承認を通じて私たちの候補製品を推進することに伴い、私たちが行っている活動に関連する費用は引き続き増加すると予想される。また、上場企業として、運営に関連した追加コストを発生させていきます。
私たちは、私たちの現金、現金等価物、および有価証券が短期的に私たちの運営に必要な資本を提供すると予想している。長期的には、政府支出、他社との潜在的な協力、または他の戦略的取引を含む追加資本を公開または私募株式発行、債務融資、または他の資本源で調達する必要があると予想される。なぜなら、私たちが独立して収入を生み出すことができる前に、リンカーン公園に普通株を売却し、CLAから得られる収入がすべての必要な融資を提供するのに十分ではないと予想されるからである。私たちは私たちがこのような出所から十分な資金を得る必要がある時、私たちが完全にまたは魅力的な条件で十分な資金を得ることを保証することはできない。必要に応じてこれらや他のソースから追加資金を得ることができなければ、リストラや延期、運営の削減、またはいくつかの研究開発計画の停止によって支出を大幅に削減する必要があるかもしれない。
私たちの運営資本需要の予測は、正しくないことが証明される可能性があるという仮定に基づいており、私たちは予想よりも早くすべての利用可能な資本資源を使用するかもしれない。医薬製品の研究、開発と商業化に関連する多くのリスクと不確定性のため、私たちの運営資本需要の正確な金額を見積もることができない。私たちの未来の資金需要は多くの要素に依存するだろうが、これらに限定されない
また、将来的に株式証券の売却によるいかなる融資も、リンカーン公園への普通株の売却を含めて、私たちの株主が希釈されることになる。もし私たちが債務融資を通じて追加資本を調達すれば、私たちは私たちが保有権または追加債務を発生させること、配当金の支払い、私たちの普通株の買い戻し、いくつかの投資、および特定の合併、合併、または資産売却取引に従事する能力の制限を含む、私たちが運営する契約を制限することができるかもしれない。私たちが調達した任意の債務融資または追加株式には、私たちまたは私たちの株主に不利な条項が含まれているかもしれない。もし私たちが必要な時に追加資金を集めることができなければ、私たちは私たちの開発計画と臨床試験の一部または全部を延期、減少または終了することを要求されるかもしれない。私たちはまた、私たちの現在または未来の任意の製品候補製品または発見計画の権利を他の人に販売することを要求されるかもしれないが、これらの製品または発見計画はいくつかの地域に位置しているか、または私たちが開発と商業化を望んでいる兆候である。
25
キャッシュフローの概要
次の表に、以下の期間の現金、現金等価物、および限定的な現金の主な供給源および用途(千計)を示す
|
|
9月30日までの9ヶ月間 |
|
|||||
|
|
2022 |
|
|
2021 |
|
||
|
|
|
|
|
|
|
||
経営活動のための現金純額 |
|
$ |
(43,940 |
) |
|
$ |
(37,270 |
) |
投資活動提供の現金純額 |
|
|
36,396 |
|
|
|
(61,087 |
) |
融資活動が提供する現金純額 |
|
|
(16 |
) |
|
|
124,471 |
|
現金、現金等価物、および制限的現金純増加 |
|
$ |
(7,560 |
) |
|
$ |
26,114 |
|
経営活動用の現金
2022年9月30日までの9カ月間で,運営活動で使用された現金は4390万ドルであり,これは主に運営に資金を使用したことによる純損失3520万ドル,我々の純運営資産と負債の純変化780万ドル,非現金費用100万ドルであった。営業資産と負債の純変化は,主に前払い費用,売掛金,売掛金のための現金によるものである。2021年9月30日までの9カ月間、経営活動で使用された現金は3730万ドルであったが、これは主に運営に資金を使用し、純損失3970万ドル、純運営資産と負債が200万ドル変化したが、440万ドルの非現金費用によって部分的に相殺されたためである。営業資産と負債の純変化は主に前払い費用、売掛金、売掛金の純増加によるものである。
投資活動によって提供される現金
2022年9月30日までの9ヶ月間、投資活動が提供した現金は3640万ドルで、主に5790万ドルの有価証券の満期収益と関係があるが、実験室やコンピュータ設備の購入に使用された60万ドルの現金と有価証券を購入するための2090万ドルの現金で相殺された。2021年9月30日までの9ヶ月間、投資活動で使用された現金は6110万ドルで、主に有価証券を購入するための7430万ドルの現金と実験室設備を購入するための90万ドルの現金を含み、1420万ドルの販売収益と有価証券の満期日を部分的に相殺した。
融資活動のための現金
2022年9月30日までの9ヶ月間、融資活動で使用された現金16,000ドルは、早期に行使されたオプションの買い戻しに関係している。2021年9月30日までの9カ月間、融資活動が提供した現金は1兆245億ドルで、主に2021年8月に完了した業務合併の1億241億ドルの純収益とオプションを行使した40万ドルの収益を含む。
契約義務と約束
2022年9月30日まで、私たちの契約義務は経営陣の財務状況と経営成果の検討と分析2021年12月31日までのForm 10−K年次報告書に含まれている。
重要な会計政策、重大な判断と見積もりの使用
著者らが監査していない簡明総合財務諸表はアメリカ公認会計原則或いはGAAPによって作成された。このような審査されていない簡明総合財務諸表を作成する際に、著者らは審査簡明総合財務諸表の日付を審査されていない既報資産及び負債額、或いは有資産及び負債の開示、及び報告期間内に提出された支出に影響するため、推定と仮定を行う必要がある。我々の見積もりは,我々の歴史的経験と,当時の状況では合理的な様々な他の要因に基づいており,これらの要因の結果は資産や負債の帳簿価値を判断する基礎を構成しているが,これらの資産や負債の帳簿価値は他の源からは明らかではないように見える。実際の結果はこれらの推定とは大きく異なる可能性がある。
2022年9月30日までの9ヶ月間、私たちの重要な会計政策や以下の項目を推定する方法に大きな変化はありません経営陣の財務状況と経営成果の検討と分析2021年12月31日までの年次報告Form 10−Kである。
新興成長型会社の地位
私たちは2012年のJumpStart Our Business Startups ActやJOBS Actで定義されているように、新興成長型会社、あるいはEGCと呼ばれています。JOBS法案は、EGCの地位を有する会社が、延長された過渡期間を利用して新しい会計基準または改正会計基準を遵守することを許可し、これらの会計基準の採用を民間会社に適用されるまで延期する。私たちは選びました
26
この延長された移行期間を利用して、会社(I)がEGCまたは(Ii)が“雇用法案”に規定されている延長移行期間から脱退することを明確かつ撤回できなくなるまで、新しいまたは改正された会計基準を遵守することができるようにする。そのため、上場会社の発効日まで、私たちが監査していない簡明な総合財務諸表は、新しい会計基準に符合したり、会計基準を改訂したりする会社と比較できない可能性がある。
また,JOBS法案が提供する他の免除と減少の報告要求に依存する予定である。JOBS法案に規定されているいくつかの条件に適合する場合、EGCとして、このような免除に依存しようとする場合、他の事項を除いて、(I)サバンズ-オキシリー法第404条(B)条に基づいて、私たちの財務報告内部制御システムに関する監査員証明報告書を提供すること、(Ii)ドッド·フランクウォールストリート改革および消費者保護法によって要求される可能性のある非新興成長型上場企業のすべての報酬開示を提供すること、(Iii)上場企業会計監督委員会が採用する可能性のある要件を遵守すること。(Iv)行政職員の報酬と業績との関連性、および行政総裁の報酬と従業員の報酬の中央値との比較など、行政職員の報酬に関連するいくつかの項目を開示する。
雇用法案によると、(I)2025年財政年度の最終日までEGCとなり、(B)我々の年間総収入が少なくとも12.35億ドルの年度、または(C)大規模加速申告機関の年度とみなされるか、または(Ii)前3年以内に10億ドルを超える転換不可能債務証券を発行した日である。
プロジェクト3.数量と品質市場リスクに関する義務的な開示。
改正された1934年証券取引法規則12 b-2または取引法の定義によると、我々は比較的小さな報告会社であり、本項の他の要求に関する情報を提供する必要はない。
プロジェクト4それは.制御とプログラムです
情報開示制御とプログラムの管理職の評価
我々の経営陣は、取引法ルール13 a-15(F)によって定義された財務報告の十分な内部統制の確立と維持を担当している。我々の経営陣は、我々の最高経営責任者及び最高財務官の監督の下で、本報告で述べた期間終了までの開示制御及び手順(取引所法案第13 a−15(E)及び15 d−15(E)規則で定義されるような)の設計及び運営の有効性を評価した。取引法第13 a-15条の開示制御及びプログラムの評価によると、我々のCEO及び最高財務官は、本報告で述べた期間が終了するまで、以下に述べる重大な弱点により、我々の開示制御及び手続は合理的な保証レベルでは有効ではないと結論している。
物質的弱点
先に述べたように、2020年12月31日までの年次財務諸表を監査する際に、我々と独立公認会計士事務所は、財務報告の内部統制に大きな弱点があることを発見しました。2022年9月30日現在、このような実質的な疲弊が続いている。重大な欠陥は財務報告内部統制の欠陥または欠陥の組み合わせであり、私たちの年度または中期財務諸表の重大なミス報告は合理的な可能性があり、適時に防止または発見できないようにする。私たちが発見した重大な弱点は、公認会計基準とアメリカ証券取引委員会規則を適用する上で必要な知識と経験を持つ十分な会計と財務報告者の不足と関係がある。
重大な弱点に対応するために、財務報告に対する私たちの内部統制を救済し、改善するために、多くの努力と資源を投入し、引き続き投入することを計画している。我々は、財務報告の内部統制を改善し、財務報告の深刻な脆弱化を招く制御欠陥を是正し、会計担当者の招聘を含め、公認会計基準と米国証券取引委員会関連業界報告経験を有する専門顧問からコンサルティングサービスを取得し、研究材料や文書を取得し、複雑な会計アプリケーションについて相談を提供する第三者専門家とのコミュニケーションを増加させ、継続的な訓練と教育により、既存の会計·財務者の能力を向上させ、米国汎用会計基準と米国証券取引委員会規則及び規定下の会計·報告要求を理解するための措置を実施している。効果的な内部統制を設計·実施するプロセスは継続的な努力であり、私たちの業務および経済·規制環境の変化を予測し、対応し、上場企業としての私たちの報告義務を満たすのに十分な内部制御システムを維持するために大量の資源を費やす必要がある。
財務報告の内部統制の変化
私たちの最近の財政四半期内で、私たちは財務報告の内部統制に何の変化も生じておらず(取引法第13 a-15(F)および15 d-15(F)規則で定義されているように)、これは私たちの財務報告の内部統制に大きな影響を与えたり、合理的にそれに大きな影響を与える可能性がある。
制御とプログラムの有効性の制限
私たちは私たちの開示統制と手続きがすべてのミスとすべての詐欺を防ぐことを期待していない。制御とプログラムを開示することは、どんなにアイデアや操作が完全であっても、絶対的な保証ではなく、合理的な保証しか提供できない
27
開示された統制と手続きに適合する。さらに、開示制御およびプログラムの設計は、リソース制限が存在し、そのコストに対する利点を考慮しなければならないという事実を反映しなければならない。すべての開示制御およびプログラムの固有の制限のため、開示制御およびプログラムの評価は、私たちが私たちのすべての制御欠陥および詐欺事例(あれば)を発見したことを絶対的に保証することはできない。開示制御およびプログラムの設計もまた、将来のイベント可能性のいくつかの仮定に部分的に基づいており、どの設計もすべての潜在的な将来の条件でその目標を成功的に達成することを保証することはできない。
28
第2部-その他の資料
項目1.法的訴訟
時々、私たちは法的手続きの影響を受けるかもしれない。私たちは現在、個別または全体が私たちの業務、財務状況、または経営結果に重大な悪影響を及ぼすと考えている訴訟には参加していません。結果にかかわらず、弁護や和解コスト、管理資源の移転などの要因により、訴訟は私たちに悪影響を及ぼす可能性がある。
イットM 1 A型です。リスク要因です
以下の議論を除いて、当社が先に2021年12月31日までの10-K年報に開示したリスク要因と、2022年3月28日に米国証券取引委員会に提出された“第1 A項”に開示されたリスク要因とは実質的な変化はない。参照によって以下の修正または更新されていない範囲内で本明細書に組み込まれる。私たちの証券に投資することは高度な危険と関連がある。あなたが私たちの証券に投資決定を下す前に、上記の“前向きな陳述に関する警告説明”で議論されたリスクと不確実性に加えて、以下および2022年3月28日に米国証券取引委員会に提出された2021年12月31日までの10-K表年次報告書“プロジェクト1 A”に記載されているリスクおよび不確実性を慎重に考慮しなければならない。リスク要因です我々の証券への投資を決定する前に、これらのリスクは、本報告書に含まれる他のすべての情報と共に、我々の連結財務諸表および関連注釈を含むことを考慮しなければならない。もし私たちのリスク要素に記述された任意の事件や発展が発生した場合、私たちの業務、将来性、経営業績、財務状況は重大な影響を受ける可能性があり、私たちの証券の取引価格は低下する可能性があり、あなたはすべてまたは一部の投資を損失する可能性があります。以下と私たちの年間報告書に記載されているリスクと不確定要素は、私たちが直面している唯一のリスクと不確実性ではない。私たちは今知らないか、あるいは私たちが現在どうでもいいと思っている他のリスクと不確実性が重大になり、私たちの業務に悪影響を及ぼす可能性がある。
以下のリスク要因は年次報告に含まれるリスク要因の補完である。
リスク要因の概要
以下は,我々の普通株投資に投機的あるいはリスクを持たせる重要な要素の要約である.この結論は私たちが直面しているすべての危険を解決していない。私たちの業務は重大なリスクに関連しており、私たちの業務、財務状況、運営結果、見通し、株価に実質的な悪影響を及ぼす可能性があります。以下では、これらのリスクについてより包括的に説明する
29
私たちの業務に関わるリスク
私たちは臨床段階のバイオ製薬会社で、赤字の歴史があります。私たちは予測可能な未来に引き続き大きな損失を受け、永遠に利益を達成したり維持したりすることができないかもしれません。これは私たちの普通株の時価低下を招く可能性があります。
私たちは臨床段階のバイオ製薬会社で、赤字の歴史があります。設立以来、著者らはほとんどの資源を研究開発、臨床前研究、臨床試験、著者らの管理チームの構築と著者らの知的財産権の組み合わせに投入し、そして重大な運営損失を発生した。我々のほとんどの損失は,その研究開発計画に関する費用と我々の運営に関する一般的かつ行政コストによるものである。これまで、私たちは製品販売から何の収入も得ておらず、どの候補製品のためにも規制部門の承認を求めたり、獲得したりしていない。また、予測可能な未来には、製品販売から何の収入も得られないことが予想され、研究開発、臨床前研究、臨床試験のコスト、および私たちの現在と潜在的な未来候補製品の規制承認手続きにより、引き続き重大な運営損失を受けることが予想される。
我々の主要候補製品SZN−1326,SZN−043,SZN−413の臨床開発の進展に伴い,純損失は大幅に増加すると予想される。しかし、私たちの未来の損失額は不確実だ。私たちが利益を達成または維持する能力は、もしあれば、候補製品の開発成功、SZN-1326の臨床試験の回復、SZN-043の臨床試験の継続、バーリングインゲルハイム国際会社との協力によるSZN-413の開発成功とテストに依存する
30
GMBH、又はBIは、規制部門の承認を得てマーケティング及び商業化候補製品を取得し、商業的に合理的な条件で任意の承認された製品を製造し、潜在的な将来連合を構築し、任意の承認された製品の販売及びマーケティング組織又は適切な第三者代替品を確立し、十分な資金を調達して業務活動に資金を提供する。もし私たちまたは私たちの現在および潜在的な未来のパートナーが私たちの1つまたは複数の候補製品を商業化できない場合、または承認された候補製品の販売収入が不足している場合、私たちは利益を達成したり維持することができなくなり、これは私たちの業務、財務状況、運営結果、および見通しに実質的な悪影響を及ぼすかもしれない。
治療に関連する有害事象が観察されたため、健康ボランティアにおけるSZN−1326の第1段階の臨床試験は自発的に一時停止され、我々の開発計画が遅延し、追加資金が必要となり、いつまたはSZN−1326の臨床試験および開発が回復および完了できるかどうかは分からない。
治療に関連する有害事象が観察された後、SZN−1326の臨床試験は自発的に一時停止された。一部の被験者は無症状トランスアミナーゼの上昇が出現し、3級ALTとAST上昇の被験者を含む。すべての被験者のトランスアミナーゼ上昇は自発的に緩和し、研究過程中に深刻な副作用は観察されなかった。私たちは、これらの観察された問題を理解し、解決するために、既存の臨床データをさらに分析し、より多くの臨床前試験を行うつもりであるが、この追加の仕事は、私たちの開発計画の遅延を招き、SZN-1326に対する私たちの開発努力と臨床試験を回復し、完成させるための追加の資金を必要とする。これらの発見の原因を見つけ、直ちに解決策を策定することができない場合、または全くできない場合、SZN-1326の開発はさらに延期または臨床開発に失敗し、私たちの財務状況および運営結果に悪影響を及ぼす可能性がある。
SZN−043は健常ボランティアにおける第1段階臨床試験が行われているが,治療に関連する有害事象が観察されており,これらの発見が継続または悪化すれば,SZN−043の開発計画を延期し,SZN−043の臨床試験および開発を完了するための追加の資金が必要となる可能性がある。
SZN−043の臨床試験が行われているが,SZN−043を服用した数名の被験者では,1級と2級治療に関連する無症状トランスアミナーゼの上昇が認められた。これらの被験者のトランスアミナーゼ上昇は自発的に軽快し,研究期間中に重篤な副作用は認められなかった。我々は,既存の臨床データをさらに分析し,必要に応じて臨床研究を修正し,これらの観察された問題を理解·安全に解決する予定である。これらの観察結果が持続的または悪化した場合、より多くの臨床前試験を実行するために試験を一時停止する必要があり、我々の開発計画を遅延させ、SZN−043に対する我々の開発努力および臨床試験を回復および完成させるための追加の資金が必要となるかもしれない。SZN−043の試験を安全に継続し、これらの観察結果を解決できない場合、SZN−043の開発は大幅に延期または放棄され、私たちの財務状況および運営結果に悪影響を及ぼす可能性がある。
私たちは製品が発売されていないし、規制部門の承認を受けた製品もない。私たちの候補製品のうち2つだけが人体臨床試験を開始したばかりであり、私たちが利益を達成し、維持する能力は、規制部門の候補製品の承認を得て、単独でもパートナーとも商業化に成功することに依存する。
監督管理機関が私たちの候補製品の商業流通を許可する前に、私たち或いは協力者は広範な臨床前研究を行い、それから臨床試験を行い、私たちの候補製品の人体における安全性、純度と効力或いは有効性を証明しなければならない。米国食品医薬品局、FDAまたは他の規制機関が臨床試験を許可することは保証されない。そのほか、著者らは著者らの臨床前研究が適時に完成或いは結果を確定することができず、FDA或いは他の監督機関が著者らが提出した臨床計画、著者らの臨床方案を受け入れるかどうか、或いは著者らの臨床前研究結果が最終的に著者らの臨床前計画或いは人体試験の更なる発展を支持するかどうかを予測することができない。したがって、私たちは、私たちが提案した臨床計画の研究新薬やINDまたは同様の申請を予想されるタイムラインで提出できることを保証することができず、INDまたは同様の申請を提出することがFDAまたは他の規制機関が私たちの任意の候補製品の臨床試験を開始することを可能にすることを保証することはできない。
SZN−043は臨床開発中であり,SZN−1326の臨床試験は上記のように休止している。新たな方法,目標,行動メカニズムに基づく候補製品の開発過程において,我々は固有の失敗リスクに直面している.健康ボランティアにおけるSZN−1326の第1段階臨床試験を回復し、健康ボランティアおよび肝機能障害患者においてSZN−043の第1段階臨床試験を継続するように努力しているにもかかわらず、これらの候補製品のいずれかの臨床開発を継続できる保証はなく、またはこれらの候補製品をさらに推進する際に、いずれの候補製品も臨床的利益を示すであろう。したがって、あなたは私たちが直面しているコスト、不確実性、遅延と困難、そして私たちのような臨床段階のバイオ製薬会社がよく直面する問題を考慮しなければならない。
私たちは、SZN-1326、SZN-043、または任意の潜在的な将来の候補製品を回復または継続するために財務リソースを得ることができないかもしれない、または任意の協力を行う。規制部門の承認を遅延させたり、候補製品を商業化したりする問題に遭遇した場合、このような状況は悪化する可能性があります
31
さらに、私たちはどんな潜在的な未来のパートナーともマーケティングや商業化の任意の候補製品の承認を得ることができないかもしれない。私たちまたは将来の潜在的協力者が規制の承認を得ても、承認された対象、疾患適応、または患者集団は、予想または期待されるように広くない可能性があり、または重大な使用または配布制限または安全警告を含むラベルが必要とされる可能性がある。私たちまたは潜在的な未来のパートナーは、規制部門の承認を維持するために、上場後のテスト要求を遵守する必要があるかもしれない。
SZN-1326、SZN-043、SZN-413、および将来人体で試験される任意の候補製品は、承認または商業的に実行可能であるために必要な安全性、純度および効力または効果を証明できない可能性がある。
最終的には、SZN−1326、SZN−043、およびSZN−413は、治療の有効性および安全性に寄与すると考えられるいくつかの特性を有していないことが発見されるかもしれない。例えば、SZN−043とSZN−1326は、様々な肝障害動物モデルにおいて肝機能を改善することを含む動物研究において鼓舞的な結果を示しているにもかかわらず、ヒトに異なる特性を示す可能性があり、上述した無症状トランスアミナーゼ上昇の観察から示されたように、予見できない、無効または有害な方法でヒト生物系と相互作用する可能性がある。したがって、私たちは私たちの現在または未来の任意の候補製品に基づいて適切な製品を開発することに決して成功しないかもしれない。SZN-1326、SZN-043、SZN-413、または私たちの将来の任意の潜在的候補製品が無効、安全でないこと、または商業的に不可能であることが証明された場合、私たちの生産ライン全体にあまり価値がないかもしれません(もしあれば)、これは、抗体ベースの発見および開発の重点および方法を変更し、私たちの業務、財務状況、運営結果、および見通しに重大で不利な影響を与える必要があるかもしれません。
私たちは私たちのWNT治療プラットフォームを使用して拡張して候補製品パイプラインを構築する努力は成功しないかもしれない。
我々の戦略の重要な要素の1つは、様々な重篤な疾患を有する患者の損傷組織の修復および/または再生を促進することができるWNT候補製品の組み合わせを発見および開発するために、我々のWNT治療プラットフォームを使用および拡張することである。これまで、我々の研究および開発作業は、SZN−1326、SZN−043、SZN−413および他の潜在的な候補製品を発見し、開発してきたが、現在の候補製品は安全または有効な治療薬ではない可能性があり、成功した候補製品を開発できない可能性がある。私たちのプラットフォームは発展しており、候補製品のパイプラインを構築するにはまだ達していないかもしれない。私たちが候補製品チャネルの確立に成功したとしても、私たちが決定した潜在的候補製品は、受け入れられない毒性または他の特徴を有することが証明されたので、FDAまたは他の規制機関の上場承認または市場承認を得る製品ではないことを示すことを含む、臨床開発に適していないか、または許容可能な臨床データを生成する可能性がある。2022年11月に発表されたSZN-1326およびSZN-043臨床試験で観察された無症状トランスアミナーゼの上昇は、これらの観察結果を成功的に解決できなければ、WNTプラットフォームを確立し、拡張する能力を弱める可能性もある。もし私たちが候補製品の開発に成功して商業化しなければ、私たちは未来に製品収入を生み出すことができないだろう。
32
SZN-1326、SZN-043、SZN-413、または任意の潜在的な将来の候補製品が臨床試験を開始するか、または発売承認を得た後に副作用が生じる場合、私たちのマーケティングおよび候補製品から収入を得る能力は影響を受ける可能性がある。
SZN-1326、SZN-043、SZN-413、または任意の潜在的な将来の候補製品によって引き起こされる不良副作用は、私たちまたは規制機関の臨床試験の中断、延期、または停止をもたらす可能性があり、より厳しいラベルまたはFDAまたは他の規制機関の規制承認の延期または拒否をもたらす可能性がある。SZN−1326とSZN−043の臨床試験を開始したが,SZN−1326臨床試験を自発的に休止させ,SZN−043臨床試験を調整する知見を得た。私たちの候補製品をテストしたり使用したりすることも副作用が生じるかもしれない。われわれの臨床試験結果は,これらの副作用の重症度と普遍性を明らかにする可能性があり,受け入れられない。この場合、私たちの実験は(SZN-1326に対して私たちがしたように)または終了することができ、FDAまたは他の規制機関は、任意またはすべての目標適応の候補製品のさらなる開発を停止するか、または承認を拒否するように命令するかもしれない。このような副作用はまた、患者が試験を完了する能力を募集したり、組み入れたり、あるいは潜在的な製品責任クレームを招く可能性がある。例えば,Wntシグナルの下流の影響により,Wnt経路に対する治療薬が腫瘍の形成や増殖を引き起こす可能性が指摘されている。今まで、著者らは臨床前毒理学研究と臨床試験においてSZN-1326或いはSZN-043のどのような腫瘍形成も観察されなかったが、現在或いは未来の候補製品が腫瘍形成を引き起こさないことを保証することはできない。これらのイベントまたはSZN-1326およびSZN-043に関連する調査結果を解決できなかった場合、いずれも、私たちのビジネスおよび財務状況に重大な悪影響を与え、私たちの収益能力を弱める可能性があります。
また,臨床試験には本質的に潜在患者群のサンプルを用いた。患者数および曝露時間が限られている場合、より多くの患者が候補製品に接触しているか、または患者がより長い時間接触している場合にのみ、候補製品のまれかつ深刻な副作用が発見される可能性がある。
もし私たちが現在または潜在的な未来の候補製品のいずれかが規制部門の承認を得て、私たちまたは他の人がこれらの製品の1つによる副作用を発見すれば、以下のいずれかの不良事件が発生する可能性があり、これは私たちの重大な収入損失を招き、私たちの運営と業務結果に重大で不利な影響を与える可能性がある
私たちは候補製品と私たちのWNT治療プラットフォームの開発を進めるために大量の追加資金が必要になるが、様々な市場条件と要素のため、必要な時や私たちに有利な条項の下で、十分な資金がない可能性があり、候補製品の開発と商業化を延期、制限、または廃止する。
バイオ製薬候補製品の開発は資本集約型である。SZN-1326、SZN-043、SZN-413、または将来の潜在的候補製品が臨床前研究および臨床試験によって進展した場合、私たちは私たちの開発、監督、製造、マーケティング、および販売能力を拡大するために多くの追加資金を必要とするだろう。著者らはすでに大量の資金を使用して、著者らのWNT治療プラットフォームSZN-1326、SZN-043と他の候補製品を開発し、私たちのプラットフォームを引き続き開発し、SZN-1326の臨床試験を回復し、SZN-043の臨床試験を継続し、臨床前研究と臨床試験を含む更なる研究開発を行う。
これまで、私たちは主に株式証券を売却することで私たちの運営に資金を提供してきた。私たちの候補製品を販売することで十分な収入を得ることができる前に、公開または私募株式発行、債務融資、または他の資本源(政府調達、他社との潜在的な協力、または他の戦略取引を含む)によって、私たちの運営に資金を提供する予定です。2022年2月、私たちはリンカーン公園資本基金有限責任会社またはリンカーン公園と購入契約と登録権協定を締結しました。協定によると、私たちは権利がありますが、リンカーン公園に株を売却する義務はありません。リンカーン公園は36ヶ月以内に時々最大5,000万ドルの普通株を購入する義務がありますが、いくつかの条件と制限を守らなければなりません。リンカーン公園からすべての資金を得ることができないかもしれません。購入協定に含まれている制限、制限、要求、違約事件、その他の条項はリンカーンにつながるかもしれません
33
パーカーは私たちの普通株を買います。もし私たちの株価が下落すれば、私たちはリンカーン公園に株式を売却できないかもしれないし、十分な金額で必要な融資を受けることができないかもしれない。
私たちはもっと多くの資金を集めることができないかもしれないし、優遇条件でこのような合意や手配を達成できない、あるいは全くできないかもしれない。我々がより多くの資金を調達する能力は、世界の経済状況の潜在的な悪化の悪影響を受ける可能性があり、新冠肺炎の大流行とロシアとウクライナとの衝突は、米国と世界各地の信用と金融市場の中断と変動を招く可能性がある。これらの事件の我々の業務全体への影響は,米国や外国政府による新冠肺炎の伝播速度の鈍化やロシアへの制裁行動の重大な影響を受ける可能性がある。これらの事件や行動は、流動性や信用供給の深刻な減少、消費者自信の低下、経済成長の鈍化、失業率の上昇、経済安定性の不確定を招く可能性がある。株式市場と信用市場が悪化すれば、任意の必要な債務や株式融資をより困難にし、コストをより高く、希釈度をより高くする可能性がある。
もし私たちが受け入れられる方法や条項で十分な追加資本を調達できなければ、私たちは私たちの製品ラインや他の研究開発計画の開発を大幅に延期、削減、または停止しなければならないかもしれない。私たちはまた、他の場合が望ましいのではなく、私たちの製品ラインおよび任意の未来の候補製品のためのパートナーを探すことを要求されるかもしれませんし、他の方法よりも不利な条項でパートナーを探したり、不利な条項で放棄したりすることができるかもしれませんが、私たちの製品ラインおよび任意の未来の製品候補の権利は、そうでなければ、私たちは自分の開発または商業化を求めます。
私たちの将来の資本需要と私たちは既存の資源が私たちの運営を支援する期限が私たちが予想しているのとは大きく違うかもしれないと予想しています。例えば,(I)SZN−1326の臨床試験をいつ回復できるか,できれば,(Ii)SZN−1326の臨床試験を軌道に戻すためにどの程度の資源を投入すればよいかは不明である。私たちの毎月の支出レベルは新しいものと行っている研究開発や他社の活動によって違います。候補製品の成功した研究や開発に関連する時間や活動の長さは非常に不確定であるため、開発および任意の承認されたマーケティングおよび商業化活動のためにどれだけの実際の資金が必要かを見積もることはできない。私たちの運営費の時間と金額は主に見られるだろう
必要な時に十分な資本を集めることができなければ、私たちの業務、財務状況、運営結果が損なわれ、私たちの運営計画を大幅に修正する必要があります。私たちはまた資産を清算しなければならないかもしれません。私たちが清算または解散で得た任意の資産の価値は、私たちの財務諸表に反映された価値よりもはるかに低いかもしれません。
私たちは、より利益的またはより成功する可能性の高い候補製品を利用することなく、特定の候補製品を追求するために限られた資源を使うかもしれない。
私たちの財務と管理資源が限られているため、SZN-1326、SZN-043、SZN-413の臨床開発を含む具体的な研究開発プロジェクトに私たちの努力を集中させるつもりだ。したがって、私たちは、後により大きなビジネス潜在力を有することが証明された潜在的な未来製品候補を含む、他の機会の追求を放棄または延期するかもしれない。私たちの資源配分決定は私たちが実行可能な商業製品候補品や利益のある市場機会を利用できないかもしれない。現在および将来の研究開発計画および特定の適応の候補製品への支出は、いかなる商業的に実行可能な候補製品も生じない可能性がある。私たちがSZN-1326の臨床試験を回復しなければ、私たちはSZN-1326を開発する資本リターンを見ることができず、私たちの財務状況や他の機会を求める能力に悪影響を及ぼすだろう。もし私たちが特定の候補製品の商業潜在力や目標市場を正確に評価しなければ、私たちは放棄するかもしれない
34
私たちが候補製品の独占的な開発と商業化の権利を保持している場合、私たちは協力、許可、または他の印税手配によって、その候補製品の独占的な開発と商業化の権利を得ることができる。
著者らが時々発表或いは公表した臨床試験の中期、主要と初歩データはより多くの患者データの出現或いはより多くの分析に伴い変化する可能性があり、しかもこれらのデータは監査と検証プログラムの制約を受け、最終データの重大な変化を招く可能性がある。
私たちは時々私たちの臨床前研究と臨床試験の中期、初歩或いは主要なデータを公開するかもしれない。これらのデータは当時利用可能なデータの初歩的な分析に基づいており、結果及び関連する発見と結論は特定の試験に関連するデータをより全面的に審査した後に変化する可能性がある。私たちはまた、そのデータ分析の一部として、すべてのデータを全面的かつ詳細に評価する機会がないか、または受け取る機会がないかもしれないという仮説、推定、計算、および結論を下した。したがって、追加のデータが受信され、十分に評価されると、私たちの報告の中期、予備、またはバックライン結果は、同じ試験の将来の結果とは異なる可能性があり、または異なる結論または考慮要因が、これらの結果を合格させる可能性がある。例えば,2022年11月にSZN−1326やSZN−043臨床研究に関する所見が報告されており,これらの所見は将来の発現と実質的に異なる可能性がある。バックラインデータはまだ監査と確認手続きを受ける必要があり、これは最終データが私たちが以前に発表した予備データと大きく異なる可能性がある。したがって、最終データが利用可能になる前に、バックラインデータは慎重に表示されなければならない。時々、私たちはまた私たちの臨床研究の中期、初歩的、または背線データを開示することができる。著者らが完成する可能性のある臨床試験の中期、ベースライン或いは初歩的なデータは、患者登録の継続とより多くの患者データの獲得に伴い、1つ以上の臨床結果が実質的に変化する可能性のあるリスクに直面する可能性がある。予備、バックライン、または中間データと最終データとの間の不利な差は、私たちのビジネスの将来性を深刻に損なう可能性があります。
さらに、規制機関を含む他の人は、私たちの仮定、推定、計算、結論または分析を受け入れないか、またはデータの重要性を異なる方法で解釈またはトレードオフする可能性があり、これは、特定の計画の価値、特定の候補製品または製品の承認または商業化、および私たちの全体的な価値に影響を与える可能性がある。さらに、私たちが開示された特定の研究または臨床試験に関する情報を選択することは、一般に、広範な情報に基づいており、あなたまたは他の人は、私たちが決定した我々の開示に含まれる重要な情報または他の適切な情報に同意しない可能性があり、私たちが開示しないことを決定したいかなる情報も、最終的には、特定の製品、候補製品、または私たちの業務に関する将来の決定、結論、観点、活動、または他の側面に対して大きな意味を有すると考えられるかもしれない。もし私たちが報告したバックラインデータが実際の結果と異なる場合、あるいは規制機関を含めて他の人が結論を出すことに同意しない場合、私たちが承認を得て私たちの候補製品を商業化する能力が損なわれる可能性があり、これは私たちの業務、経営業績、見通し、または財務状況を損なう可能性がある
私たちは受け入れ可能な条項で戦略的取引を行うことができないかもしれませんが、これは私たちが現在と潜在的な未来の候補製品を開発し、商業化する能力に悪影響を与え、私たちの現金状況に影響を与え、私たちの費用を増加させ、私たちの経営陣に大きな妨害をもたらすかもしれません。
私たちは時々、協力、買収会社、資産購入、合弁企業、および製品候補または技術の対外または内部許可のような戦略取引を考慮する。例えば,2022年10月初め頃にBIと戦略的パートナーシップを構築し,網膜疾患治療のためのSZN−413を開発した。戦略的に魅力があれば、バイオテクノロジーやバイオ製薬会社や病院との連携を含めた協力を求めていくと評価していきます。パートナーの競争は非常に激しく、交渉過程は時間がかかって複雑だ。もし私たちが戦略取引に入ることができなければ、私たちは私たちの潜在的な未来の製品候補製品または私たちのWNT治療プラットフォームをさらに開発するために必要な流動性または専門知識を得ることができないかもしれない。このような協力または他の戦略的取引は、非日常的または他の費用を生成し、その短期的および長期的な支出を増加させ、重大な統合または挑戦をもたらし、または私たちの管理または業務を混乱させることを要求するかもしれない。
我々は、より多くの技術や資産を得ることも可能であり、第三者と戦略同盟を構成したり、合弁企業を作成したりして、既存の業務を補完または拡大すると考えていますが、このような資産を買収するメリットは実現できないかもしれません。代わりに、私たちが加入したどんな新しい協力条項も私たちまたは私たちの候補製品に最適ではないかもしれない。これらの取引は、多くの業務と財務リスクをもたらすだろう
35
したがって、私たちが上述した性質の任意の取引を行うか、または成功することは保証されないが、任意の現在または未来のパートナー関係および取引は、前述のまたは他のリスクの影響を受ける可能性があり、私たちの業務は、そのような取引の大きな損害を受ける可能性がある。逆に、私たちに有利な協力や他の戦略取引に参加できなければ、候補製品の開発や潜在的な商業化を延期し、市場に進出する任意の候補製品の競争力に悪影響を及ぼす可能性がある。
さらに、現在または将来の任意のパートナーが協力協定を終了した場合、私たちは、臨床前研究または臨床試験の支援、マーケティングおよび流通コストの負担、知的財産権の維持、実行および保護、または場合によっては候補製品を完全に放棄することを含む、現在および将来の候補製品を独立して開発することを余儀なくされる可能性があり、いずれも、私たちの業務計画を変化させ、その業務、財務状況、運営結果、および見通しに実質的な損害を与える可能性がある。
私たちと私たちの協力者は、これらの協力者が発表した時間範囲で予想される発見と開発マイルストーン、および他の予想された重要なイベントを達成できないかもしれません。これは私たちの業務に悪影響を与え、私たちの株価を下落させる可能性があります。
私たちは時々いくつかのマイルストーンと重要な事件の予想時間について公開声明を発表し、例えば、私たちの内部薬物発見計画における臨床前とINDを有効にする研究の開始と完成、そして私たちの計画の臨床試験の開始と完成を予定している。多くの要因の影響により、これらの活動の実際の時間は、例えば、私たちまたは任意の未来の協力者の薬物発見および開発計画の遅延または失敗、私たちおよび任意の未来の協力者が投入する時間、努力および資源の数、および薬物開発に固有の多くの不確実性など、大きく異なる可能性がある。したがって、私たちまたは任意の現在または未来の協力者の計画が、私たちまたは彼らが発表または予想される時間範囲内で推進または完了することを保証することはできない。もし私たちまたは任意の協力者がこれらのマイルストーンのうちの1つまたは複数または他の重要なイベントを計画的に達成できなかった場合、私たちとBIプロトコルのマイルストーンを含めて、私たちの業務は実質的な悪影響を受ける可能性があり、普通株価格は下落する可能性がある。
臨床試験は高価で、時間がかかり、設計と実施が困難である。
人体臨床試験は費用が高く、設計と実施が困難であり、一部の原因はそれらが厳格な監督管理要求を受けているからである。私たちの現在と潜在的な未来の候補製品は新しい技術と発見方法に基づいているため、広範な研究と開発が必要であり、相当な製造と加工コストが必要であると予想される。また,Wnt経路に対する候補薬剤数が限られているため,FDAや他の規制機関は,臨床試験を開始または回復する前に追加的なテストを行うことを要求する可能性があり,その標的疾患適応の影響を受ける患者を第1段階試験に組み込むことを許可するかどうか迷っている可能性がある。現在と計画の第1段階試験で目標疾患適応の影響を受ける患者を募集できなければ,潜在的な人体概念検証データの獲得を延期または延期し続ける可能性があり,開発スケジュールを延長する可能性がある。さらに、患者の治療および我々の候補製品の治療に起因する可能性のある潜在的な副作用のコストが高い可能性がある。そのため、私たちの臨床試験コストは非常に高い可能性があり、私たちの業務、財務状況、運営結果と将来性に実質的な悪影響を与える可能性がある。
われわれが臨床試験で患者を募集する際に困難に遭遇すると,われわれの臨床開発活動は延期されたり,他の悪影響を受けたりする可能性がある。
FDAや他の規制機関の要求に基づいて、これらの試験に参加するのに十分な数の合格患者を見つけることができなければ、現在または潜在的な将来の候補製品の臨床試験を開始、回復、または継続できない可能性がある。特に,健康ボランティアにおけるSZN−1326の第1段階臨床試験の回復に努め,健常ボランティアや肝機能障害患者ではSZN−043の第1段階臨床試験を継続している。これらの人々の中で患者試験登録を保持することの難しさを予測することはできない。様々な理由から,臨床試験では患者登録の困難に遭遇する可能性がある。患者の登録は多くの要素に依存している
36
さらに、私たちの将来の臨床試験は、私たちの試験に参加することを選択する可能性のある患者の中には、競争相手による試験に参加することを選択する可能性があるので、私たちの候補製品と同じ治療分野の製品を他の臨床試験と争奪するであろう。合格臨床研究者の数は限られているため、著者らはいくつかの競争相手が使用している同じ臨床試験地点で著者らのいくつかの臨床試験を行い、これらの臨床試験地点で臨床試験を行う患者数を減少させることが予想される。さらに,われわれのいくつかの臨床試験は末期疾患を有する患者で行われるため,これらの患者は候補製品とは無関係な疾患進展や有害事象を経験する可能性があるため,これらの患者は試験中に評価できない可能性があるため,追加的な登録が必要となる可能性がある。患者登録の遅延はコスト増加を招く可能性があり,あるいは計画中の臨床試験の時間や結果に影響を与える可能性があり,これらの試験の完了を阻止し,候補製品開発を進める能力に悪影響を及ぼす可能性がある。
もし私たちがSZN-1326の臨床試験を回復できない場合、あるいは候補製品の臨床試験が延長され、延期され、停止された場合、私たちは規制部門の承認を求めたり、直ちに私たちの候補製品を商業化することができないか、あるいは全く実現できないかもしれません。これは、追加的なコストを発生させ、どんな製品収入を受け取るかを延期する必要があります。
著者らはすでに著者らが行っている或いは未来の臨床前研究或いは臨床試験の遅延を更に経験する可能性があり、著者らは臨床前研究或いは臨床試験が時間通りに開始し、適時に回復するかどうか、再設計、時間通りに十分な数量の患者を募集する或いは時間通りに完成する必要があるかどうかを知らない。SZN-1326臨床試験の回復および著者らの臨床試験の開始または完成は、多くの要素によって大幅に延期または阻止される可能性がある:
37
規制要求、政策、ガイドラインも変化する可能性があり、私たちは適切な監督管理機関と共にこれらの変化を反映するために、私たちの臨床開発計画を大幅に修正する必要があるかもしれない。これらの変化は,CROとの再交渉条項やIRBsに臨床試験案を再提出して再検査する必要がある可能性があり,臨床試験のコスト,時間,あるいは成功達成に影響する可能性がある。私たちの臨床試験は彼ら、FDA、他の監督機関、関連する臨床試験を監督するIRB、私たちがこのサイトに関連する任意の臨床試験サイト、あるいはいつでも一時停止または終了することができる。
私たちの候補製品の臨床試験の開始または完了の任意の失敗または重大な遅延、臨床試験から積極的な結果を得ることができなかった、私たちの候補製品に関連する任意の安全問題、または私たちの候補製品に対して現在予想されている追加の臨床試験または他のテストを行う任意の要求は、私たちが規制承認を得る能力に悪影響を与え、私たちのビジネスの将来性と製品収入を創出する能力は弱化されるだろう。
もし私たちの現在および潜在的な将来の候補製品(SZN-1326、SZN-043、およびSZN-413を含む)の市場機会が私たちが考えているより小さい場合、私たちの将来の製品収入は不利な影響を受ける可能性があり、私たちの業務は影響を受けるかもしれない。
SZN-1326、SZN-043およびSZN-413がそれぞれ治療可能ないくつかのタイプのうち、重度IBD、重度AHおよび網膜血管関連疾患までの患者数についての理解は、推定に基づいている。これらの推定は不正確であることが証明される可能性があり,新しい研究はこれらの疾患の推定発症率や流行率を減少させる可能性がある。米国または他の地域の患者数は予想を下回る可能性があり、現在または潜在的な将来の候補製品の治療を受け入れられないかもしれない、または患者はますます識別および接触が困難になる可能性があり、これらすべては私たちの業務の将来性および財務状況に悪影響を及ぼすであろう。特に、私たちの候補治療可能集団の推定が間違っている場合、または患者のサブ集団がSZN−1326、SZN−043、またはSZN−413から利益を得ていない場合、我々の候補治療可能集団はさらに減少する可能性がある。
さらに、いくつかの要因は、私たちの現在または潜在的な将来の製品候補製品を受け入れる実際の患者数を潜在的な潜在的市場よりも少なくする可能性がある。これらの問題は多くの未発達市場の新しい治療法の不足の広範な獲得性と限られた精算を含む。
私たちの国際業務は、アメリカ以外での業務展開に関連するビジネス、政治、運営、金融リスクに直面するかもしれません。
私たちの業務は国際業務の展開に関連するリスクの影響を受けています。私たちのいくつかのサプライヤーはアメリカ以外に位置しており、私たちはすでに行って、将来的により多くの臨床試験を行う予定で、アメリカ以外のSZN-1326とSZN-043の第一段階試験を含む。また、私たちまたは任意の現在または未来のパートナーが任意の製品の開発に成功すれば、EUや米国以外の他の司法管轄区でこれらの製品を販売する予定です。承認されれば,我々または任意の将来の協力者は販売代表を招聘し,米国以外の場所で医師や患者協会の外連活動を行うことができる。国際的な業務展開は多くのリスクに関連しているが、これらに限定されない
38
これらの要素のいずれも、私たちの現在の国際業務とサプライチェーン、および将来の任意の国際拡張および業務を損なう可能性があり、それによって私たちの業務、財務状況、経営の見通し、結果を損なう可能性がある。
私たちの業務には重大な製品責任リスクがあり、私たちが十分な保険範囲を得ることができないことは、私たちの業務、財務状況、運営結果、見通しに実質的な悪影響を及ぼす可能性があります。
SZN-1326、SZN-043、SZN-413、および他の潜在的な未来の候補製品に対して臨床前研究および臨床試験を行う時、私たちはこれらの候補製品の開発、テスト、製造、およびマーケティング過程に固有の重大な製品責任リスクに直面している。製品責任クレームは開発計画の完了を延期または阻止する可能性がある。もし私たちがマーケティング製品の面で成功した場合、このようなクレームは、FDAが私たちの製品、製造プロセス、および施設またはマーケティング計画の安全性と有効性を調査し、製品をリコールするか、またはより深刻な法執行行動を取り、承認の適応を制限し、承認を一時停止または撤回する可能性がある。是非曲直や最終結果にかかわらず、責任クレームは、私たちの製品に対する需要の減少、私たちの名声が損なわれたこと、関連訴訟の弁護コスト、管理職の時間と私たちの資源が移転されたこと、実験参加者や患者への巨額のお金の奨励、そして私たちの株価の下落を招く可能性がある。私たちが持っているか得ることができるどんな保険も潜在的な責任に十分な保険を提供できないかもしれない。しかも、臨床試験と製品責任保険はますます高くなっている。したがって、私たちまたは任意の現在または未来のパートナーは、製品責任クレームによる損失から私たちを保護するために、合理的なコストで十分な保険を得ることができないかもしれません。これらの損失は、私たちの業務、財務状況、運営結果、および見通しに実質的な悪影響を及ぼす可能性があります。
もし私たちがいかなる許可、協力、または他の知的財産権関連協定の下での義務を履行できなかった場合、私たちは損害賠償金の支払いを要求され、現在または未来の技術または製品候補に必要な知的財産権を開発、商業化、保護することができないか、または再許可を付与するいくつかの権利を失う可能性がある。
私たちはスタンフォード大学と1つ以上の候補製品に関連する特許をカバーする独占許可協定に署名しました。私たちはCLAのメンバーで、SZN-413に関連する商業知能を持っていて、私たちの研究開発活動を推進するために他の人から追加の許可を得る必要があるかもしれません。あるいは私たちの現在と未来の候補製品の商業化を可能にして、私たちは確定して追求するかもしれません。スタンフォード大学とBIと締結されたライセンス契約、および私たちが将来締結する任意のライセンス契約は、様々な開発、商業化、資金、マイルストーン、特許使用料、勤勉、再許可、保険、特許起訴、強制執行、または他の義務を私たちに強要することができます。スタンフォードとのライセンス契約の詳細については、2021年12月31日現在のForm 10-Kのタイトルを参照してください“スタンフォード·ライセンス契約はBIとのライセンス契約のより詳細な説明については、2022年10月6日に米国証券取引委員会に提出された現在の8−K表報告および本報告書の添付ファイル10.1を参照されたい。もし私たちがこれらの義務に違反したり、許可された知的財産権を無許可で使用したりすれば、私たちは損害賠償金の支払いを要求される可能性があり、許可者は許可を終了する権利があるかもしれない。ライセンス終了は、ライセンス技術によってカバーされた製品を開発、製造、販売することができない場合があり、または競合他社がライセンス技術を得ることができるようにする可能性があります。さらに、私たちは第三者から許可された特許と特許出願の準備、提出、起訴、維持、実行、および弁護を制御する権利がないかもしれない。場合によっては、我々が許可した特許権は、その特許訴訟および維持費用を許可者に精算する必要がある。私たちのライセンシーおよび未来のライセンシーが、私たちが許可する可能性のある特許を起訴、維持、強制実行、保護できなかった場合、または特許または特許出願を許可する権利を失った場合、私たちのライセンス権利は減少またはキャンセルされる可能性がある。この場合、このような許可権利の対象となる任意の製品または候補製品の権利を開発して商業化することは、実質的な悪影響を受ける可能性がある。
さらに、私たちの現在または未来の許可者は、私たちに許可されていない知的財産権を所有または制御する可能性があり、したがって、その是非にかかわらず、私たちは侵害、流用、または他の方法でライセンシーの知的財産権を侵害するクレームを受ける可能性がある。また,侵害や流用行為が発見されれば,将来の製品の販売にどの程度の印税義務を支払うことが求められるかは定かではないが,これらの金額は大きい可能性がある。将来の印税義務の金額は、私たちが開発や商業化に成功した製品で使用する技術や知的財産権にかかっています(あれば)。したがって、私たちが製品を開発して商業化することに成功しても、私たちは利益を達成したり維持することができないかもしれない。
さらに、ライセンス契約によると、知的財産権に関する紛争が生じる可能性があります
39
また,我々が現在第三者から知的財産権や技術許可を得ているプロトコルは複雑であり,このようなプロトコルのいくつかは様々な解釈の影響を受ける可能性がある.可能性のある契約解釈の相違の解決は、関連する知的財産権または技術に対する私たちの権利と考えられる範囲を縮小するか、または関連協定の下での私たちの財務または他の義務を増加させる可能性があり、いずれも、私たちの業務、財務状況、運営結果、および見通しに実質的な悪影響を及ぼす可能性があります。また、我々が許可している知的財産権をめぐる紛争が、商業的に許容可能な条項で現在の許可スケジュールを維持する能力を阻害したり、弱体化したりすれば、影響を受けた候補製品の開発に成功し、商業化することができない可能性があり、これは、私たちの業務、財務状況、運営結果、および見通しに大きな悪影響を及ぼす可能性がある。
政府の規制に関連するリスク
臨床開発には長く高価な過程が含まれており、結果は不確定であり、早期研究と試験の結果は未来の試験結果を予測できない可能性がある。
我々の候補製品SZN−1326とSZN−043はすでに臨床開発を開始しており,失敗のリスクが高い。私たちの候補薬や任意の潜在的な未来の製品候補薬がいつ、あるいは人間に有効であることが証明されるか、または規制部門の承認を得るかどうかを予測することはできない。監督管理部門の許可を得て任意の候補製品を販売する前に、著者らは臨床前研究を完成し、それから広範な臨床試験を行い、この候補製品の人体上の安全性、純度と有効性を証明しなければならない。臨床試験は費用が高く,完成までに数年かかる可能性があり,その結果自体も不明であり,特に最近のSZN−1326やSZN−043の臨床試験に関する観察を考慮すると。開発中のいつでも故障が発生する可能性がある。現在あるいは潜在的な未来候補製品の臨床前研究と臨床試験の結果は後期臨床試験の結果を予測できないかもしれない。臨床前研究と初歩的な臨床試験で進展を得たが、臨床試験後期段階の候補製品は期待した安全性と有効性特徴を示すことができないかもしれない。製薬業のいくつかの会社は高級臨床試験で重大な挫折を経験し、早期の試験で良好な結果を得たにもかかわらず、有効性或いは安全性に乏しいためである。我々は2022年第3四半期にSZN-1326とSZN-043の初の人体試験を開始した。我々は(上記のように)経験しており,臨床研究の開始または完成の遅れをさらに経験する可能性がある。計画の臨床試験が予定通りに完成するかどうか、あるいは計画された臨床試験が時間通りに始まるかどうか、再設計する必要があるかどうかはわかりません(SZN-1326とSZN-043にしなければならないように)、時間通りに患者を募集したり、予定通りに完成したりするかどうか, もし本当にあれば。我々の開発計画は,以下に関連する遅延を含む様々な原因で遅延する可能性がある
40
処方医が現在または潜在的な未来候補製品への患者の参加を募集する臨床試験に関する未解決の倫理的問題に遭遇した場合、安全性と有効性の概況が確立された既存の治療案を作成するのではなく、遅延に遭遇する可能性がある。さらに、臨床試験は、法規の要求または私たちの臨床規程に基づいて臨床試験を行うことができなかったこと、FDAまたは他の監督機関による臨床試験操作または試験場所の検査が実施されなかったこと、臨床休止、予見できない安全問題または副作用、薬物または治療生物の利益を証明できなかったことを含む、我々、著者らの協力者、そのような試験を行う機関のIRBs、そのような試験のデータ安全監視委員会またはFDAまたは他の規制機関によって一時停止または終了する可能性がある。政府法規や行政行為の変化或いは臨床試験を継続するのに十分な資金が不足している。現在または潜在的な将来の候補製品の任意の臨床試験が遅延または終了した場合、候補製品の商業的将来性が損なわれ、候補製品から製品収入を得る能力は延期されるであろう。また、臨床試験を完成するいかなる遅延も私たちのコストを増加させ、私たちの製品開発と審査過程を緩和し、そして私たちの製品販売と収入を創造する能力を危険にさらす。これらのいずれも、私たちの業務、財務状況、経営結果、および見通しに重大な悪影響を及ぼす可能性があります。さらに、原因や原因は, 臨床試験の開始または完了遅延は、最終的に、私たちの現在または潜在的な未来の候補製品が規制部門の承認を得ることを拒否される可能性がある。
私たちは米国または外国の規制機関の承認を得ることができないかもしれないので、SZN-1326、SZN-043、SZN-413、または将来の潜在的な候補製品を商業化することはできない。
SZN-1326、SZN-043、SZN-431、および任意の潜在的な未来候補製品は、治療用生物製剤の研究、試験、開発、製造、安全、効果、承認、記録、報告、ラベル、貯蔵、包装、広告および販売促進、定価、マーケティングおよび流通に関する広範な政府法規に準拠しなければならない。新薬或いは治療性生物製剤が発売される前に、アメリカと多くの外国司法管轄区で厳格な臨床前テストと臨床試験及び広範な監督管理許可手続きを成功に完成する必要がある。これらと他の規制要件を満たすことは高価で、時間がかかり、不確定であり、予期しない遅延が生じる可能性がある。私たちが開発する可能性のある候補製品は、私たちまたは未来の潜在的なパートナーがこれらの製品の販売を開始するために、規制部門の承認を得ないだろう。
著者らは、FDAと他の規制機関の承認を含む規制承認を得るために必要な臨床試験の実施と管理に必要な臨床試験の経験が限られている。FDAおよび他の承認を得るのに要する時間は予測不可能であるが、一般に、候補製品のタイプ、複雑性、および新規性に依存する臨床試験の開始後数年後に必要である。FDAとその外国の同業者が私たちを監督する時に使用する基準は判断する必要があり、しかも変化する可能性があり、これはこれらの標準がどのように適用されるかを確定的に予測することを困難にする。著者らは臨床前と臨床活動データに対するいかなる分析も監督管理機関の確認と解釈を得る必要があり、これは監督部門の承認を延期、制限或いは阻止する可能性がある。我々はまた、将来の立法または行政行動、または製品開発、臨床試験、およびFDA規制審査中の米国および他の司法管轄区域の規制政策の変化など、新しい政府法規による予期しない遅延またはコスト増加に遭遇する可能性がある。立法変化が公布されるかどうか、あるいはFDAや外国の法規、指導や解釈が変わるかどうか、あるいはこれらの変化の影響(あれば)が何であるかは予測できない。
必要な承認を得る上でのどんな遅延や失敗も、私たちが承認を求めている特定の候補製品から収入を創出する能力に重大で不利な影響を与える可能性があります。さらに、私たちと私たちの未来の潜在的なパートナーは、いかなる候補製品を市場に出して商業化するかの承認を決して得られないかもしれない。私たちまたは将来の潜在的協力者が規制の承認を得ても、承認された対象、疾患適応、または患者集団は、その期待または期待のように広くない可能性があり、または重大な使用または配布制限または安全警告を含むラベルが必要とされる可能性がある。私たちまたは潜在的な未来のパートナーは、規制部門の承認を維持するために、上場後のテスト要求を遵守する必要があるかもしれない。もし私たちの候補製品が無効で安全でないこと、または商業的に不可能であることが証明された場合、私たちは候補製品を再設計しなければならないかもしれません。私たちのパイプライン全体にはあまり価値がないかもしれません。これは、私たちの業務、財務状況、運営結果、および見通しに実質的な悪影響を及ぼす薬物発見および治療開発の重点および方法を変更する必要があるかもしれません。
私たちはまた多くの外国の規制要求の制約を受け、その中には臨床試験の進行、製造とマーケティング許可、定価と第三者精算を含む。外国監督審査手続きは国/地域によって異なり、上述したFDA承認に関連するすべてのリスクと、外国司法管轄区の現地法規を満たすことによるリスクが含まれる可能性がある。さらに、承認を得るのに要する時間は、FDA承認を得るのに要する時間とは異なる可能性がある。
私たちはアメリカ以外のところで私たちの候補製品のためにいくつかの臨床試験を行うかもしれない。しかしながら、FDAおよび他の外国の同業者は、このような試験からのデータを受け入れない可能性があり、この場合、その開発計画が延期され、その業務に実質的な損害を与える可能性がある。
我々はすでに米国以外で我々の候補製品の臨床試験を行い,さらに臨床試験を行う可能性がある。例えば、オーストラリアとニュージーランドでSZN-1326とSZN-043の第1段階試験を行った。FDAは臨床からのデータを受け入れるかもしれませんが
41
米国国外で行われた実験では、これらのデータを受け入れるかどうかはFDAが適用したいくつかの条件に依存する。外国の臨床試験のデータを米国の上場承認の基礎として利用しようとする場合、FDAは、(I)これらのデータが米国の人口および米国の医療実践に適用されない限り、(I)これらのデータが米国の人口および米国の医療実践に適用されない限り、(Ii)研究は公認能力のある臨床研究者によって行われること、および(Iii)データは有効であると考えられ、FDAが現場検査を行う必要があると判断した場合、FDAは現場検査や他の適切な方法でデータを検証することができる。そのほか、十分な患者群と統計能力を含むFDAの臨床試験要求を満たさなければならない。米国以外の地点でのみ行われINDに拘束されていない研究では,FDAは臨床試験をGCPに基づいて行うことが求められており,FDAが現場検査が必要であると考えていれば,現場検査で臨床試験のデータを検証できる必要がある。INDに拘束されていないこのような研究については、FDAは通常、研究の臨床レジメンについて事前評価を提供しないので、FDAは非米国の臨床試験の研究設計またはレジメンが不十分であることを決定する可能性があり、追加の臨床試験を行う必要があるかもしれない。FDAが米国国外で行った臨床試験のデータを受ける保証はない。FDAが候補製品の臨床試験データを受け入れなければ,追加の臨床試験が必要となる可能性が高い, これは高価で時間がかかるだろうし、私たちの候補製品開発を遅延したり永久に停止したりするだろう。
多くの外国の規制機関もまた似たような承認要求を持っている。また、このような外国裁判は、裁判を行う外国司法管轄区域に適用される現地法によって管轄される。FDAや同様の外国規制機関が米国や適用司法管轄区域以外で行われた試験データを受け入れることは保証されない。FDAや同様の外国の規制機関がこれらのデータを受け入れない場合、追加の試験が必要になり、これは高価で時間がかかり、私たちの業務計画のいくつかの側面を遅延させることになり、これは、私たちの候補製品が適用される司法管轄区域で商業的な承認や許可を得ることができない、あるいは候補製品の開発を永久的に停止させる可能性がある。
アメリカ国外で臨床試験を行うことも、以下の方面と関連するリスクを含むより多くのリスクに直面させる
私たちが現在または潜在的な未来の候補製品が規制部門の承認を得ても、私たちは持続的な規制義務と持続的な規制審査の制約を受けることになり、これは多くの追加費用を招く可能性がある。また、私たちの現在または潜在的な未来の候補製品は、承認されれば、ラベルや他の制限や市場撤退を受ける可能性があり、規制要求を遵守していない場合や、私たちの製品が予期せぬ問題に遭遇した場合、処罰を受ける可能性があります。
私たちまたは私たちの現在または潜在的な未来のパートナーは、SZN-1326、SZN-043、SZN-413、または任意の潜在的な未来の候補製品のために得られる任意の規制された承認を受けるかもしれないし、上場の承認された使用のために使用される可能性のある製品の制限または承認条件によって制限される可能性があり、または“第4段階”の臨床試験、および候補製品の安全性および有効性を監視する監視を含む可能性の高い発売後試験要件を含む。さらに、FDAまたは任意の他の規制機関がSZN-1326、SZN-043、SZN-413、または私たちの将来の任意の候補製品を承認した場合、このような製品の製造プロセス、ラベル、包装、流通、有害事象報告、貯蔵、輸出入、広告、販売促進および記録は、広範かつ持続的な規制要件の制約を受けるであろう。これらの要求には,安全性や他の上場後の情報や報告,登録の提出,cGMPやわれわれが承認後に行った任意の臨床試験の良好な臨床実践を継続することが含まれている。その後、候補製品には、予期されない深刻度または頻度の有害事象、または我々の第三者製造業者または製造プロセス、または規制要件を遵守できなかったことを含む以前に未知の問題が存在することが発見され、以下のことが含まれる可能性がある
42
また、FDAは市場に投入された製品のマーケティング、ラベル、広告、販売促進を厳格に規制している。製品は承認された適応と承認されたラベルの規定でしか販売促進できません。医師は彼らの独立した専門医学判断でラベル外使用のための製品を出すことができるが、FDAは医師が薬物治療を選択する行為を規範化していないため、FDAはラベル外でその製品を使用する問題におけるメーカーのコミュニケーションを制限している。会社はFDAが承認した製品ラベルと一致する真の情報と非誤解的な情報しか共有できない。FDAと他の当局はラベル外用途の普及を禁止する法律と法規を積極的に実行し、ラベル外用途を不当に普及させていないことが発見された会社は重大な責任に直面する可能性があり、その他を除いて、不良宣伝、警告状、広告の是正、および可能な民事と刑事罰を含む。連邦政府は、ラベル外使用の不当な普及の疑いがある会社に巨額の民事と刑事罰金を科し、会社がラベル外販売促進に従事することを禁止している。FDAおよび他の規制機関はまた、企業に同意法令または永久禁止を締結し、これらの法令または永久禁止に基づいて、特定の販売促進行為を変更または制限することを要求する。
上記のいずれの状況の発生も、我々の業務や経営結果に重大な悪影響を及ぼす可能性がある。FDAや他の規制機関の政策は変わる可能性があり、私たちの候補製品に対する規制承認を阻止、制限、または延期するための追加の政府法規が公布されるかもしれない。米国や海外の将来の立法や行政行動によって生じる可能性のある政府規制の可能性、性質、程度を予測することはできない。私たちが既存の要求の変化に緩やかに適応できない場合や、新しい要求や政策を採用することができない場合、または規制適合性を維持できない場合、私たちが得る可能性のあるマーケティング承認を失う可能性があり、収益性を実現または維持できない可能性があり、これは私たちの業務に悪影響を及ぼすだろう。
私たちの株式所有権に関するリスク
私たちの株価は変動する可能性があり、私たちの普通株を購入した人は大きな損失を受けるかもしれない。
私たちの株価は変動するかもしれません。このような変動により、投資家は初回公募株(IPO)よりも高い価格で普通株を売ることができない可能性がある。私たちの普通株の市場価格はこの部分で述べられた他のリスクを報告することを含む多くの要素の影響を受けるかもしれないリスク要因“および以下の事項:
43
また,株式市場,特に製薬,生物製薬,バイオテクノロジー株式市場は極端な変動を経験しており,この変動は発行者の経営業績とは無関係であることが多い。これらの広範な市場と業界要素は、私たちの経営業績にかかわらず、私たちの普通株の市場価格を深刻に損なうかもしれない。
私たちの経営陣は現金の分配に柔軟性があり、あなたは私たちがそれらをどのように使用するかに同意しないかもしれないので、現金は投資に成功できないかもしれません。
我々は現在,First in人体実験を回復·継続することにより,SZN-1326およびSZN-043の開発に資金を提供し,我々が行っている他の研究や発見計画に資金を提供し,運営資金や他の一般会社の目的のために,我々の現金(主に先の株式発行によって得られる)を使用する予定である.私たちはまた、一部の現金を使用して、相補的な業務、技術、製品、または資産に許可、買収または投資することができます。しかし、私たちとBIのCLAを除いて、私たちは現在そうする約束や義務を持っていない。したがって、私たちの経営陣は私たちの現金を柔軟に分配することができるだろう。したがって、あなたは私たちの経営陣の現金分配に対する判断に依存して、あなたの投資決定の一部として、現金が適切に割り当てられているかどうかを評価する機会がないだろう。現金の投資方法は私たちの会社に有利な見返りや何の見返りも与えない可能性がある。
プロジェクト2それは.未登録株式証券の販売及び収益の使用。
我々の証券の未登録販売は、2022年9月30日までの9ヶ月間、Form 8−Kの現在の報告書に開示されている。
第3項それは.高級証券は約束を破った。
ない。
プロジェクト4それは.炭鉱の安全情報開示。
適用されません。
第5項それは.他の情報。
ない。
44
プロジェクト6それは.展示品です。
展示品 番号をつける |
|
説明する |
|
|
|
2.1 |
|
商業合併協定は、日付は2021年4月15日であり、CHFW、Persistance Merge Sub Inc.およびSurrozen,Inc.(2021年4月15日に米国証券取引委員会に提出された現在の8-K表報告(ファイル番号001-39635)の添付ファイル2.1を参照して編入される)。 |
3.1 |
|
Surrozen,Inc.の会社登録証明書(2021年8月17日に米国証券取引委員会に提出された8−Kフォーム現在報告(文書番号001−39635)の添付ファイル3.1を参照して編入される)。 |
3.2 |
|
Surrozen,Inc.の規約(2021年8月17日に米国証券取引委員会に提出された8−Kフォーム現在報告(文書番号001−39635)の添付ファイル3.2を参照して編入)。 |
4.1 |
|
授権書サンプル(2020年10月13日に米国証券取引委員会に提出されたS-1/A表登録声明(文書番号333-249394)添付ファイル4.3を参照して編入)。 |
4.2 |
|
Cononance-HFW Acquisition Corp.とContinental Stock Transfer&Trust Companyとの間の権証合意は,2020年11月18日である(2020年11月25日に米国証券取引委員会に提出された現在の8-K表報告の添付ファイル4.1(文書番号001-39635)を参照して統合される)。 |
4.3 |
|
単位証明書サンプル(2020年10月13日に米国証券取引委員会に提出されたS-1/A表登録声明(文書番号333-249394)添付ファイル4.1を参照して編入)。 |
4.4 |
|
普通株式証明書サンプル(2020年10月13日に米国証券取引委員会に提出されたS-1表登録説明書添付ファイル4.2(文書番号333-249394)合併参照)。 |
4.5 |
|
ハーモニー社の企業現地化証明書-HFW買収会社(2021年8月17日に米国証券取引委員会に提出された現在の8-K表報告(ファイル番号001-39635)の添付ファイル4.5を参照して編入)。 |
4.6* |
|
Cononance−HFW Acquisition Corp.とContinental Stock Transfer&Trust Companyとの引受権証プロトコルは,2021年8月11日である。 |
4.7* |
|
証券説明書 |
10.1* |
|
協力と許可協定は、期日は2022年9月30日で、バーリンガー-インゲルハイム国際有限公司と蘇羅岑運営会社が署名した。 |
31.1* |
|
2002年のサバンズ·オキシリー法第302節で可決された1934年の証券取引法第13 a−14(A)及び15 d−14(A)条に基づいて発行された首席執行幹事証明書。 |
31.2* |
|
2002年サバンズ−オキシリー法第302節で可決された1934年証券取引法第13 a−14(A)及び15 d−14(A)条に基づいて首席財務幹事が認証された。 |
32.1* |
|
2002年にサバンズ·オクスリ法案第906条で可決された“米国法典”第18編1350条に規定されている最高経営責任者証明書。 |
32.2* |
|
2002年の“サバンズ-オックススリー法案”906節で採択された“米国法典”第18編1350条による首席財務官の認証。 |
101.INS |
|
連結されたXBRLインスタンス文書−インスタンス文書は、XBRLタグがイントラネットXBRL文書に埋め込まれているので、相互作用データファイルには表示されない。 |
101.衛生署署長 |
|
イントラネットXBRL分類拡張アーキテクチャ文書 |
101.CAL |
|
インラインXBRL分類拡張計算リンクライブラリ文書 |
101.DEF |
|
インラインXBRL分類拡張Linkbase文書を定義する |
101.LAB |
|
XBRL分類拡張ラベルLinkbase文書を連結する |
101.価格 |
|
インラインXBRL分類拡張プレゼンテーションLinkbaseドキュメント |
104 |
|
表紙インタラクションデータファイル(イントラネットXBRL文書に埋め込む) |
|
|
|
*アーカイブをお送りします。
+管理契約または補償計画またはスケジュールを示します。
S-K規則601(B)(2)項により,本プロトコルの付表と証拠物は省略されている.任意の漏れたスケジュールおよび/または展示品のコピーは、要求に応じて米国証券取引委員会に提供される。
当社はS-K規則第601(B)(10)項に基づいて本展示品の条項または条項を編集した。会社は編集されていない展示品のコピーをアメリカ証券取引委員会に提供することに同意しなければならない。
45
サイン性質.性質
1934年の証券取引法の要求によると、登録者はすでに正式に本報告を正式に許可した署名者がそれを代表して署名することを促した。
|
|
SURROZEN社 |
|
|
|
|
|
日付:2022年11月14日 |
|
差出人: |
/s/クレイグ·パーカー |
|
|
|
クレイグ·パーカー |
|
|
|
社長と取締役CEO (首席行政主任)
|
|
|
|
|
日付:2022年11月14日 |
|
差出人: |
チャールズ·ウィリアムズ |
|
|
|
チャールズ·ウィリアムズ |
|
|
|
首席財務官 (首席財務官と首席会計官)
|
46