添付ファイル99.1
Adverum BioTechnologies報告書2022年第3四半期の財務業績
-私たちの第2段階ルナ試験でIxO-VEC(Ixoberogene Soroparvovec、以前はADVM-022と呼ばれていた)を使用した第1の被験者は、2023年に予備データがあると予想される
-2025年に入るキャッシュ滑走路湿性加齢黄斑変性(湿性AMD)を優先したIXO−VEC臨床開発
カリフォルニア州レイドウッドシティ(2022年11月10日)−遺伝子療法を高度に流行する眼科疾患ケアの新基準として確立するための臨床段階会社Adverum BioTechnologies,Inc.(ナスダック:ADVM)が本日,2022年9月30日までの第3四半期財務業績を発表した。
Adverumバイオテクノロジー社の最高経営責任者、医学博士ローラン·フィッシャー、社長は“第3四半期はAdverumに非常に重要である。私たちは第2段階のルナIXO-VEC試験で私たちの最初の被験者に調剤し、2 E 11用量および新しいより低い6 E 10用量を評価し、湿性AMDを治療するための増強予防ステロイド療法を評価するからである。私たちは2023年全体でルナの中期データを共有することを期待している。著者らは著者らの遺伝子治療候補薬物IXO-VECの進展を推進することに信じられない興奮を感じ、この薬物は湿性老年性黄斑変性患者の治療モードを変化させ、そして抗血管内皮増殖因子の頻繁な注射の負担を減少させる可能性があると信じている。今年の夏初め、欧州薬品管理局は優先薬品名を持つIXO-VECを承認し、IXO-VECの変革の潜在力を認識した“と述べた
Fischer博士は続けて、“著者らは最近開催された網膜学会年会で著者らの視光試験の2年間の研究終了時の安全性と有効性データを公表し、IXO-VEC単回静脈注射は全体的に耐性が良好で、視力を維持或いは改善でき、そして湿性AMD患者の網膜内と網膜下液量を改善できることを表明した。我々が鼓舞したのは,IXO−VECの一次硝子体内注射が3年以内に安定かつ持続的なAFLibercept蛋白レベルをもたらし,液体制御を改善することができ,良好な視力結果と関係があり,毎年平均81%−98%の抗血管内皮増殖因子注射を減少させることにより治療負担を減少させることであることを示唆している。ルナの2 E 11および6 E 10用量をさらに評価したところ、これらのデータは、IXO−VECが出現している利益−リスクプロファイルを強化した。数年来afLiberceptを表現し続けるIXO-VECは生活の質が向上した患者、看護人員、網膜専門家、支払者と医療保健システムに巨大な価値をもたらすことができると信じている“と述べた
最近のハイライト
·2022年7月、Adverumは米国食品医薬品局とIXO-VECの湿性AMDにおける第2段階試験を推進するための調査性新薬改正案を完成させた。
·2022年9月、Adverumは、その第2段階ルナ試験において、IXO-VECを評価する2 x 10 ̄11 Vg/眼(2 E 11)および6 x 10^10 Vg/眼(6 E 10)の用量レベルを第1の被験者に使用し、予防的ステロイドレジメンを強化した
·Adverumは3つの重要な科学会議でIXO-VEC光学試験のデータを紹介した:
オスミウムは米国網膜専門家協会の口頭報告で毎年注射されている抗血管内皮増殖因子薬物が81%-98%減少したことを詳細に紹介し,IXO−VECを単回硝子体内投与してから3年間の持続治療のAFLibercept蛋白レベルを証明した。2 E 11用量では、IXO-VECの全体的な耐性は良好であり、同時にデータは、光学試験において、被験者の平均最適矯正視力と中央子野厚さは維持或いは改善したことを示した。
著者はアメリカ眼科学会2022年年会での口頭報告の中で網膜内液と網膜下液の解剖学的改善を詳しく紹介した。2 E 11用量群では、単回IVT用量IXO−VEC後、ベースラインから48週まで、平均IRFおよびSRF体積はそれぞれ93%および55%減少した
網膜学会2022年年会での口頭報告はすべての視神経列の2年間の研究終了データを詳しく紹介し、新しいデータ記録を含み、6 x 10 ̄11 VG/眼と2 E 11用量群のそれぞれ80%と53%の参加者は2年以内に補充注射を行わなかった
2022年9月30日までの3カ月間の財務実績
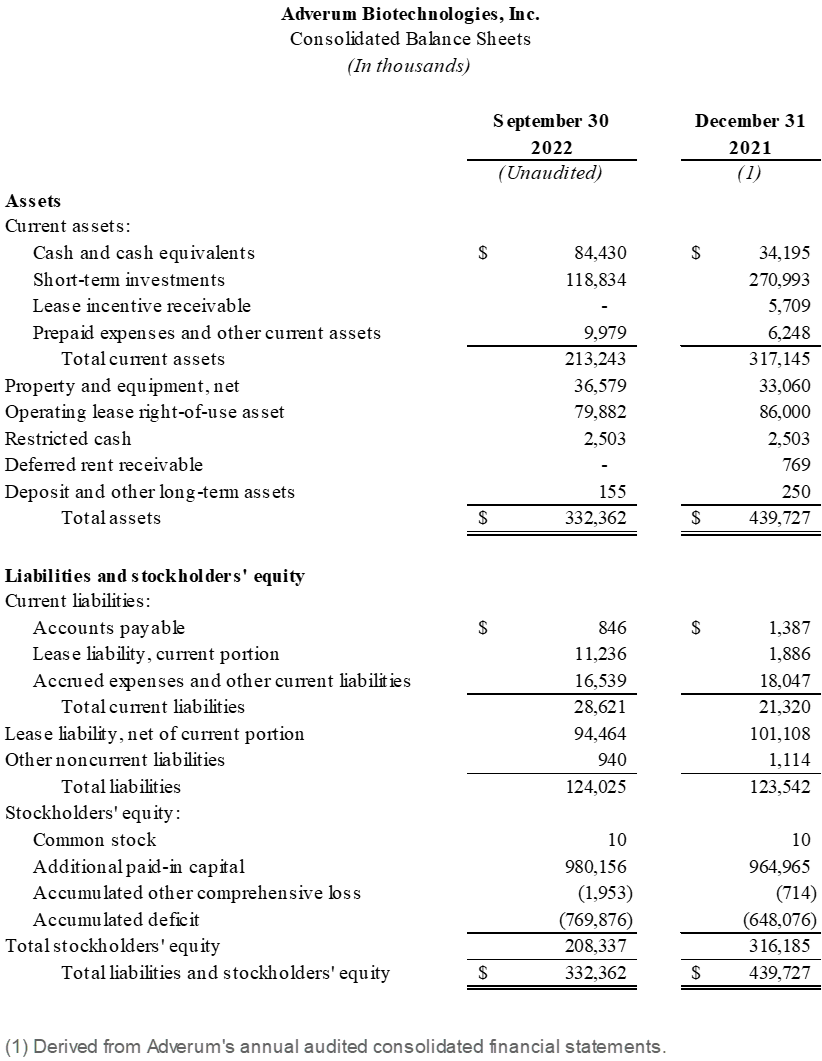
·現金、現金等価物、短期投資は2022年9月30日現在で2.033億ドルであるが、2021年12月31日現在、現金、現金等価物、短期投資は3.052億ドルである。Adverumは、2022年9月30日の現金状況が2025年までの運営に資金を提供すると予想している
·2022年9月30日までの3カ月間の研究開発支出は2380万ドルだったが、2021年同期は2410万ドルだった。研究開発費減少の主な原因は,施設関連費用の減少,再編後の従業員数の減少およびコンサルタントコストの低下であり,一部は再編コストと臨床試験に関する費用増加によって相殺されている。2022年第3四半期、研究開発費に含まれる株式報酬支出は140万ドルだった。
·2022年9月30日までの3カ月間、一般·行政費は1720万ドルだったが、2021年同期は1450万ドルだった。一般と行政費用増加の主な原因は転貸収入と再編費用の償却であり,一部は再編後の人員関連費用と施設関連費用の減少で相殺されている。2022年第3四半期、一般および行政費に含まれる株式ベースの報酬支出は310万ドル。
·2022年9月30日までの3ヶ月間の純損失は4010万ドル、1株当たり基本と希釈後の収益は0.40ドル、2021年同期は3840万ドル、または基本と希釈後の1株当たり収益は0.39ドル。
湿性加齢性黄斑変性について
湿性AMDは,新生血管性AMDあるいはNAMDとも呼ばれ,AMDの高級形式であり,約10%のAMD患者が影響を受ける。湿性AMDは65歳以上の患者の失明の主な原因であり,全世界で約2000万人がこの疾患を患っている。人口高齢化に伴い、湿性AMD新病例の発病率は全世界範囲内で著しく増加すると予想される。2040年までにAMDは世界2.88億人に影響すると予想され,そのうち湿性AMDはこれらの症例の約10%を占めている
ADVM−022の湿性AMDにおける光学試験について
ADVM−022,Ixo−berogene soroparvovec(IXO−VEC)は,Adverumが開発している治療湿性AMDの臨床期遺伝子治療製品候補薬である。IXO-VECは独自ベクターシェルAAV.7 m 8を用いて,独自発現カセットの制御下でafLiberceptコード配列を携帯する.網膜(網膜下経路)下で遺伝子治療を実施できる他の手術が必要な眼科遺伝子療法と異なり、IXO-VECはオフィスで使い捨てIVT注射としての優勢があり、長期治療効果を提供し、頻繁に抗血管内皮増殖因子を注射する負担を軽減し、患者のコンプライアンスを最適化し、そして湿性AMD患者の視力結果を改善することを目的としている。
OPTION試験は多中心、開放ラベル、用量範囲、安全性と有効性のIXO-VEC試験として設計され、対象は血管内皮増殖因子治療に反応する湿性AMD患者である。OPTEMの患者はいずれも治療経験があり,従来は抗血管内皮増殖因子を頻繁に注射して湿性AMDを管理し,機能性視力を維持する必要があった。
ルナの湿性黄斑変性治療に関する臨床試験
Ixoberogene soroparvovec(IXO−VEC)はAdverumが開発している湿性AMD治療のための臨床期遺伝子治療製品候補薬である。IXO-VECは、改造された独自ベクターカプシドAAV.7 m 8を利用して、独自発現カセットの制御下でafLiberceptコード配列を搬送する。網膜(網膜下経路)下で遺伝子治療を実施できる他の手術が必要な眼科遺伝子療法と異なり、IXO-VECはオフィスで使い捨てIVT注射としての優勢があり、長期治療効果を提供し、頻繁に抗血管内皮増殖因子(VEGF)を注射する負担を軽減し、患者のコンプライアンスを最適化し、そして湿性AMD患者の視力結果を改善することを目的としている
ルナ試験は多中心、二重盲検、ランダム、平行グループ分けの第二段階研究であり、2 x 10 ̄11 Vg/眼(2 E 11)用量と新しいより低い6 x 10 ̄10 Vg/眼(6 E 10)用量を含む2種類の用量のIXO-VECを評価し、湿性AMDに用いる。この試験は,72名までの参加者を米国とヨーロッパの40地点でランダムにグループ化し,2種類の用量と4種類の予防性ステロイドレジメンを用いた。主要な終点はベースラインから一年までの最適矯正視力(BCVA)の平均変化及び不良事件の発生率と深刻性を含む。
Adverumバイオテクノロジー会社について
Adverumバイオテクノロジー社(ナスダックコード:ADVM)は臨床段階の会社であり,遺伝子療法を高度に流行している眼科疾患の新しい看護基準として確立することを目指し,これらの疾患のために機能的治療法を開発し,視力回復と失明予防を希望している。Adverumは,その独自の硝子体内(IVT)プラットフォームの研究能力を利用して,これらの疾患を治療する頻繁な眼部注射の需要を解消するための医師室への提供を目的とした耐久性のある単回投与療法を開発している。Adverumはその新たな遺伝子治療候補薬であるIxoberogene soroparvovec(IXO−VEC,従来はADVM−022)を評価しており,新生血管や湿性年齢関連黄斑変性患者の使い捨てIVT注射として評価されている。現在これらの衰弱した眼疾患の治療モードによる挑戦を克服することによって、Adverumは看護標準を変え、視力を保護し、そして全世界範囲内で深い社会影響を与えることを渇望している。もっと情報を知りたいのですが、www.Adverum.comをご覧ください。
前向きに陳述する
本プレスリリースに含まれる将来発生する可能性のある事件または結果に関する陳述は、“1995年個人証券訴訟改革法”が指す“前向き陳述”に属する。これらの陳述には、IXO−VECの潜在的利点、ルナ試験の予備データの評価に関する時間スケジュール、および2025年の運営に資金を提供する現金滑走路が含まれるが、これらに限定されない。様々なリスクと不確実性のため、実際の結果は展望性声明で予想される結果と実質的に異なる可能性があり、これらのリスクと不確実性は、Adverumの新しい技術が臨床試験の開始と完了時間を予測しにくくすること、規制の不確実性;募集の不確実性;早期臨床試験の結果が常に未来の臨床試験と結果を予測するわけではない;およびIXO-vecの使用に関連する将来の合併症または副作用の可能性を含むが、これらに限定されない。Adverumが直面する他のリスク·不確定要因は、Adverumが米国証券取引委員会(米国証券取引委員会)に提出した文書と報告書に“リスク要因”というタイトルで述べられており、Adverumが2022年8月11日に米国証券取引委員会に提出した2022年6月30日現在のForm 10−Q四半期報告を含む。本プレスリリースに含まれるすべての前向き陳述は発表の日にのみ発表される。Adverumは,宣言発表日以降に発生したイベントや存在する状況を反映するために,これらの宣言を更新する義務はない.
企業や投資家コンサルティング
アナンド·レディ
総裁副、企業戦略、対外事務と交渉担当者
Adverumバイオテクノロジー社は
T: 650-649-1358
電子メール:areddi@adverticum.com
メディア
メーガン·タロン
企業伝播部アシスタント取締役
Adverumバイオテクノロジー社は
T: 650-649-1006
電子メール:mtalon@adverticum.com