カタログ表
アメリカです
アメリカ証券取引委員会
ワシントンD.C.,20549
表格10-Q
1934年“証券取引法”第13又は15(D)節に基づいて発表された四半期報告
現在の四半期:2022年9月30日
1934年“証券取引法”第13又は15(D)節に提出された移行報告書
_から_への過渡期
依頼公文番号:001-41282
日光生物製薬会社
(登録者の正確な氏名はその定款に記載)
| (法団の他の管轄区域として設立された国) | (国税局雇用主身分証明書番号) |
6500カナダのショッキングな金属加工
4階
カナダケベック州Pointte-Claire H 9 R 0 A 5
(主にオフィスアドレスを実行)
(514) 426-6161
(発行人の電話番号)
同法第12条(B)に基づいて登録された証券:
| クラスごとのタイトル | 取引記号 | 登録された各取引所の名称 |
|
普通株 普通株引受権証 |
SBFM SBFMW |
ナスダック株式市場有限責任会社 ナスダック株式市場有限責任会社 |
登録者(1) が過去12ヶ月以内(または登録者がこのような報告の提出を要求された短い期間内)に1934年の証券取引法第13条または15(D)節に提出されたすべての報告を再選択マークで示し、(2)過去90日以内にこのような届出要求に適合するか否か:YES☐
再選択マークは、登録者が過去12ヶ月以内(または登録者がそのような文書の提出を要求されたより短い時間以内)に、S−T規則405条(本章232.405節)に従って提出を要求した各相互作用データファイルを電子的に提出したか否かを示す。はい No☐
登録者が大型加速申告会社,加速申告会社,非加速申告会社,小さな報告会社,あるいは新興成長型会社であることを再選択マークで示す。取引法12 b-2条の規則における“大型加速申告会社”、“加速申告会社”、“小申告会社”、“br}”新興成長型会社“の定義を参照してください。(一つを選んで)
| 大型加速ファイルサーバ☐ | ファイルマネージャを加速する☐ | |
| 規模の小さい報告会社 | ||
| 新興成長型会社 |
新興成長型会社である場合、登録者が延長された過渡期間を使用しないことを選択したかどうかを再選択マーク で示して、取引法第13(A)節に従って提供された任意の新しいまたは改正された財務会計基準 を遵守してください。ガンギエイ
登録者が空殻会社であるかどうかをチェックマークで表す(取引法第12 b-2条で定義されるように)。゚ は☒違います
2022年11月7日現在、登録者の普通株式数は22,585,632株であり、額面は0.001ドルである。
カタログ
| ページ番号 | ||
| 第1部財務情報 | ||
| 第1項。 | 財務諸表 | 2 |
| 2022年9月30日(未監査)及び2021年12月31日までの簡明総合貸借対照表 | 2 | |
| 2022年9月30日と2021年9月30日までの3ヶ月と9ヶ月の簡明総合業務報告書(未監査) | 3 | |
| 2022年9月30日と2021年9月30日までの9ヶ月簡明現金フロー表(監査なし) | 4 | |
| 簡明株主権益総合報告書(監査なし) | 5 | |
| 監査されていない簡明な連結財務諸表付記 | 6 | |
| 第二項です。 | 経営陣の財務状況と経営成果の検討と分析 | 12 |
| 第三項です。 | 市場リスクの定量的·定性的開示について | 18 |
| 第四項です。 | 制御とプログラム | 18 |
| 第2部:その他の情報 | ||
| 第1項。 | 法律訴訟 | 19 |
| 第1 A項。 | リスク要因 | 19 |
| 第二項です。 | 未登録株式証券販売と収益の使用 | 19 |
| 第三項です。 | 高級証券違約 | 19 |
| 第四項です。 | 炭鉱安全情報開示 | 19 |
| 五番目です。 | その他の情報 | 19 |
| 第六項です。 | 陳列品 | 19 |
| サイン | 20 | |
| 2 |
第1部財務情報
項目1.財務諸表
陽光生物医薬有限公司
簡明総合貸借対照表
| 九月三十日 | 十二月三十一日 | |||||||
| 2022 | 2021 | |||||||
| 監査を受けていない | ||||||||
| 資産 | ||||||||
| 流動資産: | ||||||||
| 現金と現金等価物 | $ | $ | ||||||
| 売掛金 | ||||||||
| 在庫品 | ||||||||
| 前払い費用 | ||||||||
| 預金.預金 | ||||||||
| 流動資産総額 | ||||||||
| 装置、ネットワーク | ||||||||
| 総資産 | $ | $ | ||||||
| 負債と株主権益 | ||||||||
| 流動負債: | ||||||||
| 売掛金と売掛金 | $ | $ | ||||||
| 支払利息 | ||||||||
| 流動負債総額 | ||||||||
| 支払手形の長期部分 | ||||||||
| 総負債 | ||||||||
| 株主権益 | ||||||||
| 優先株、Bシリーズ$1株当たりの額面; ライセンス株式; と それぞれ2022年9月30日と2021年12月31日に発行された株 | ||||||||
| 普通株、$1株当たりの額面; ライセンス株式; と それぞれ2022年9月30日と2021年12月31日に発行された株 | ||||||||
| 額面超過支払資本 | ||||||||
| 総合(損失)を累計する | ( | ) | ( | ) | ||||
| (赤字を)累計する | ( | ) | ( | ) | ||||
| 株主権益総額 | ||||||||
| 総負債と株主権益 | $ | $ | ||||||
添付の説明を参照してください。
| 3 |
陽光生物医薬有限公司
経営報告書と全面赤字を簡明合併(未監査)
| 3ヶ月まで | 9ヶ月まで | |||||||||||||||
| 九月三十日 | 九月三十日 | 九月三十日 | 九月三十日 | |||||||||||||
| 2022 | 2021 | 2022 | 2021 | |||||||||||||
| . | . | |||||||||||||||
| 収入.収入 | $ | $ | $ | $ | ||||||||||||
| 販売コスト | ||||||||||||||||
| 毛利 | ||||||||||||||||
| 一般的かつ行政的費用: | ||||||||||||||||
| 会計計算 | ||||||||||||||||
| 広告とマーケティング | ||||||||||||||||
| 相談する | ||||||||||||||||
| 法律.法律 | ||||||||||||||||
| オフィス | ||||||||||||||||
| 将校と役員の報酬 | ||||||||||||||||
| 特許料 | ||||||||||||||||
| 研究開発 | ||||||||||||||||
| 減価償却 | ||||||||||||||||
| 総務と行政費用の合計 | ||||||||||||||||
| 運営(赤字) | ( | ) | ( | ) | ( | ) | ( | ) | ||||||||
| その他の収入(支出): | ||||||||||||||||
| 外国為替収益 | ||||||||||||||||
| 利子収入 | ||||||||||||||||
| 利子支出 | ( | ) | ( | ) | ( | ) | ( | ) | ||||||||
| 債務減免 | ||||||||||||||||
| 債務転換損失 | ( | ) | ( | ) | ||||||||||||
| その他収入合計 | ( | ) | ( | ) | ||||||||||||
| 所得税前純損失 | ( | ) | ( | ) | ( | ) | ( | ) | ||||||||
| 所得税支給 | ||||||||||||||||
| 純額(赤字) | $ | ( | ) | $ | ( | ) | $ | ( | ) | $ | ( | ) | ||||
| 外貨換算(損失) | ( | ) | ( | ) | ( | ) | ( | ) | ||||||||
| 全面的(赤字) | $ | ( | ) | $ | ( | ) | $ | ( | ) | $ | ( | ) | ||||
| 普通株1株当たり基本(損失) | $ | ( | ) | $ | ( | ) | $ | ( | ) | $ | ( | ) | ||||
| 加重平均普通株式流通株(基本) | ||||||||||||||||
添付の説明を参照してください。
| 4 |
陽光生物医薬有限公司
簡明合併現金フロー表(監査なし)
| 9ヶ月まで | ||||||||
| 九月三十日 | 九月三十日 | |||||||
| 2022 | 2021 | |||||||
| 経営活動のキャッシュフロー: | ||||||||
| 純額(赤字) | $ | ( | ) | $ | ( | ) | ||
| 純損失と経営活動で使用される現金純額の調整: | ||||||||
| 減価償却および償却 | ||||||||
| 為替損 | ( | ) | ||||||
| サービスに発行された株 | ||||||||
| 利子支払いのために発行された株 | ||||||||
| 債務転換損失 | ||||||||
| 債務減免 | ( | ) | ( | ) | ||||
| 売掛金が減る | ||||||||
| 在庫を増やす | ( | ) | ( | ) | ||||
| 前払い費用が減る | ( | ) | ||||||
| 売掛金と売掛金を増やす(減らす) | ( | ) | ||||||
| 利子の増加に対処する | ( | ) | ||||||
| 純キャッシュフローを運営する | ( | ) | ( | ) | ||||
| 資金調達活動のキャッシュフロー: | ||||||||
| 公募収益,純額 | ||||||||
| 優先株を買う | ( | ) | ||||||
| 支払手形の支払い | ( | ) | ( | ) | ||||
| 融資活動が提供するキャッシュフロー純額 | ||||||||
| 期初現金及び現金等価物 | ||||||||
| 現金と現金等価物の純増加 | ||||||||
| 為替レート変動が現金に与える影響 | ( | ) | ||||||
| 外貨換算調整 | ( | ) | ||||||
| 期末現金および現金等価物 | $ | $ | ||||||
| キャッシュフロー情報の追加開示: | ||||||||
| 利子を含めて手形に転換して発行する株 | $ | $ | ||||||
| 利子を支払う現金 | $ | $ | ||||||
| 所得税の現金を納める | $ | $ | ||||||
添付の説明を参照してください。
| 5 |
陽光生物医薬有限公司
簡明株主権益総合報告書(監査なし)
| 公用数 | 超過支払資本 | 第一選択数量 | ||||||||||||||||||||||||||||||
| 株 | ごく普通である | のパーです | 株 | 優先して優先する | 全面的に | 積算 | ||||||||||||||||||||||||||
| が発表されました | 在庫品 | 価値がある | が発表されました | 在庫品 | 収入.収入 | 赤字.赤字 | 合計する | |||||||||||||||||||||||||
| 3か月の間 | ||||||||||||||||||||||||||||||||
| 2022年6月30日の残高 | $ | $ | $ | $ | ( | ) | $ | ( | ) | $ | ||||||||||||||||||||||
| 純額(赤字) | – | – | ( | ) | ( | ) | ( | ) | ||||||||||||||||||||||||
| 2022年9月30日の残高 | $ | $ | $ | ( | ) | $ | ( | ) | ||||||||||||||||||||||||
| 9か月の間 | ||||||||||||||||||||||||||||||||
| 残高2021年12月31日 | $ | $ | $ | $ | ( | ) | $ | ( | ) | $ | ||||||||||||||||||||||
| 普通株式と事前資本権証brは引受の公開と非公開発行で発行され,発行コストを差し引く | – | |||||||||||||||||||||||||||||||
| 株式証の行使 | – | |||||||||||||||||||||||||||||||
| 関連先から購入した優先株 | – | ( | ) | ( | ) | ( | ) | |||||||||||||||||||||||||
| 純額(赤字) | – | – | ( | ) | ( | ) | ( | ) | ||||||||||||||||||||||||
| 2022年9月30日の残高 | $ | $ | $ | $ | ( | ) | $ | ( | ) | $ | ||||||||||||||||||||||
| 3か月の間 | ||||||||||||||||||||||||||||||||
| 残高2021年6月30日 | $ | $ | $ | $ | ( | ) | $ | ( | ) | $ | ( | ) | ||||||||||||||||||||
| 支払手形と支払利息を減らすために発行された普通株 | – | |||||||||||||||||||||||||||||||
| 純額(赤字) | – | – | ( | ) | ( | ) | ( | ) | ||||||||||||||||||||||||
| 2021年9月30日の残高 | $ | $ | $ | $ | ( | ) | $ | ( | ) | $ | ( | ) | ||||||||||||||||||||
| 9か月の間 | ||||||||||||||||||||||||||||||||
| 残高2020年12月31日 | $ | $ | $ | $ | ( | ) | $ | ( | ) | $ | ( | ) | ||||||||||||||||||||
| 支払手形と利息支払いを減らすために発行された普通株 | – | |||||||||||||||||||||||||||||||
| サービスのために発行する普通株 | – | |||||||||||||||||||||||||||||||
| 純額(赤字) | – | – | ( | ) | ( | ) | ( | ) | ||||||||||||||||||||||||
| 2021年9月30日の残高(監査なし) | $ | $ | $ | $ | ( | ) | $ | ( | ) | $ | ( | ) | ||||||||||||||||||||
添付の説明を参照してください。
| 6 |
陽光生物医薬有限公司
監査されていない簡明財務諸表に合併財務諸表を付記する
2022年と2021年9月30日までの3ヶ月と9ヶ月の移行期間
注1 --業務の性質
陽光生物科技有限公司(以下“当社”と略す)は2006年8月31日にコロラド州でMountain West Business Solutions,Inc.の名称登録で設立された。2009年10月まで、同社は商業コンサルティング会社であった。
2009年10月15日から、当社は逆買収に分類された取引で陽光生物医薬会社を買収した。陽光生物医薬会社は新しい抗癌薬の独占的な許可を持っており、この薬の実験室名はAdva-27 A(“許可協定”)である。逆買収取引が完了した後,同社は陽光バイオ医薬会社と改名し,製薬会社として許可されたAdva−27 A抗癌剤の開発に専念し始めた。
当社は2015年12月、関連先のAdvanome CorporationにAdva−27 A抗癌化合物のすべての発行済み特許(米国特許番号8,236,935および10,272,065)および出願中の特許(PCT/FR 2007/000697およびPCT/CA 2014/000029 )を買収し、ライセンス契約を終了した。2016年、このような特許の残存価値は損なわれた。しかし、同社はこれらの特許がカバーするAdva−27 A抗癌薬の開発を続けている。
同社は2018年12月に、ヒトでは産生できない9(9)種類の必須アミノ酸からなる非処方薬カプセルである科学に基づく栄養サプリメント製品Essential 9™を発売した。Essential 9™はすでに をカナダ衛生部によってNPN 889663に従って発売された。
同社は2020年5月22日,米国でコロナウイルス感染を治療する新しい療法の臨時特許出願を提出した。同社の特許出願は,主なコロナウイルスプロテアーゼMPROを抑制するための小分子に関連する組成物のテーマをカバーしており,MPROはウイルス複製に重要な酵素である。この特許出願の優先日は2020年5月22日である。2021年4月30日、同社は、新たな研究成果を含み、コロナウイルス系パパイヤプロテアーゼ、br}PLProを含むまでカバー範囲を拡大するPCT出願を提出した。新たに提出されたPCT出願では、2020年5月22日の優先日が維持されている。同社の先行抗コロナウイルス化合物はこれらの特許から由来しており,その実験室名はSBFM−PL 4である。
2021年1月26日、当社はカナダ知的所有権局から許可通知を受け、Adva-27 Aをカバーする新しい特許出願を承認した。新たに発表された特許には新たなテーマが含まれており、カナダにおけるAdva−27 Aの独自保護は2033年に延長されている。
2021年3月9日、同社はAdva-27 A新特許出願に関する欧州特許庁の手当通知を受けた。新たに発表された特許は、新たなテーマを含み、欧州におけるAdva−27 Aの独自保護を2033年に延長する。米国の同等特許 は2019年に発行された(米国特許番号10,272,065)。
当社は2022年2月15日、引受業者であるイージス資本会社と引受契約を締結し、1,882,353単位の引受公開発売方式で発行及び販売し、1単位当たり1株普通株及び2つの株式承認証(“取引可能株式権証”)を含み、単位当たり4.25ドルの公開発行価格で普通株を購入し、総収益は8,000,000ドル(“公開発売”)である。2022年2月17日、公開発売が終了し、会社は純収益6,833,071ドルを受け取った。 公開発売により、会社は合計1,882,353株の普通株と4,102,200株の取引可能株式権証を発行·売却した(一部の行使により引受業者に付与された超過配給選択権を行使するため、承認持分証1部当たり0.01ドルで購入した337,494件の取引承認株式証を含む)。これらの取引に関連して,会社の普通株と取引可能株式証の株はナスダックで取引を開始し,普通株の取引コードは“SBFM”,取引可能株式証の取引コードは“SBFMW”である.
| 7 |
2022年2月18日,会社はアリゾナ大学と研究協定(“SRA”)を締結し,アリゾナ大学が持つ3種類のPLPro阻害剤の体内安全性,薬物動態,用量選択特性を重点的に決定し,SARS−CoV−2に感染したマウスで治療効果テスト(“研究プロジェクト”)を行うことを目的とした。アリゾナ大学は,br}SRAにより,アリゾナ大学員が研究プロジェクトの下で開発したすべての知的財産権 について商業使用料許可の優先選択権を交渉することを同社に付与した。また,当社はアリゾナ大学 とオプション契約を締結し,この合意により,当社は最初のオプションを獲得し,研究プロジェクトの基礎技術 について特許権使用料の商業許可を徴収することを交渉した。同社はこの技術の発展を推進するため、2022年9月13日にアリゾナ大学に選択権行使の通知を提出した。
2022年2月22日、当社は会社の最高経営責任者から99万株のBシリーズ優先株を償還し、償還価格は1株0.10ドルの償還価格に相当する。
2022年3月14日、当社は指向性増発を完了し、(I)2,301,353を販売した普通株式は,引受権証(“投資家株式承認証”)の株式とともに,最大で購入可能である普通株;及び(Ii)1,302,251株事前資本権証(“予資権証”)は、各予備資本権証は1株の普通株として行使することができ、投資家
引受権証と一緒に、最大1,302,251株の普通株を購入することができる。1株当たり普通株は付属投資家株式承認証と一緒に販売し、合併発行価格は2.22ドルであり、1部の予融資権証と付属投資家株式承認証は一緒に販売し、合併発行価格は2.219ドルである。同社は約800万ドルの毛収入と#ドルを受け取った
2022年4月28日、会社は別の方向性増発を完了し、純収益16,752,915ドルを獲得した. は次方向性増発であり,当社は(I)を発行する普通株は引受権証(“4月株式承認証”)とともに、最大4,945,640株を購入することができる普通株株前資資本権証(“予資資権証”)は、1部当たりの資本資本権証は1株普通株で行使することができ、4月の引受権証と一緒に、最大4,780,050株の普通株を購入することができる。1株当たり普通株と付属の2部の4月株式証明書を一緒に販売し、合併発行価格は4.01ドルである;1部の予資権証と付属の2部の4月権証は一緒に販売し、合併発行価格は4.01ドルである;1部の予融資権証と付属の2部の4月権証は一緒に販売し、合併発行価格は4.009ドルである。事前出資株式証は即時に行使することができ、名義使用価格は0.001ドルであり、すべての事前出資株式証がすべて行使されるまで随時行使することができる。4月の権利証の発行価格は3.76ドルです1株(権利証に記載された調整を受ける必要がある)は、 発行時に行使することができ、発行日から5年で満了する。
2022年10月20日、会社はカナダの模倣薬会社Nora Pharma Inc.(“Nora Pharma”)を買収した。Nora Pharma本社は大モントリオール地域に位置し,36人の従業員を有し,カナダ衛生部が認証した15,000平方フィートの施設で運営されている。Nora Pharmaは現在、非特許処方薬、非処方薬、および生物模倣薬を含む50種類以上の薬品を提供している。Nora Pharmaの売上高は2022年6月30日までの会計年度で1070万ドル(ドル)となった。
付記2 --根拠を述べる
当社の2022年、2022年及び2021年9月30日までの9ヶ月間の未審査財務諸表 は、米国公認の中期財務資料会計原則 及び表格10-Q及びS-X届出の要求に基づいて作成されています。したがって、それらはアメリカ合衆国で一般的に受け入れられている完全な財務諸表会計原則によって要求されるすべての情報および脚注を含まない。しかし、これらの情報は、経営陣が財務状況や業務結果を公平に報告するために必要なすべての調整(通常の経常的調整のみを含む)を反映している。表示された中期結果は必ずしも財政年度全体で得られる結果を代表するとは限らない。2021年12月31日現在の貸借対照表情報は、会社が2022年3月21日に米国証券取引委員会(“米国証券取引委員会”)に提出した 表格10−K年度報告書に含まれる2021年12月31日現在及び2012年12月31日現在の年次財務諸表に含まれる監査された財務諸表に由来する。このような財務諸表はその報告書と一緒に読まなければならない。
注3 −コロナウイルス(新冠肺炎)大流行の影響
2020年3月、世界保健機関はコロナウイルス及びその関連疾患の新冠肺炎を全世界大流行と発表した。コロナウイルスが突然発生する周辺の状況はずっと急速に変化し続けている。米国と世界各地の政府当局はウイルスの伝播を緩和するための緊急措置を実施している。疫病と関連緩和措置はすでに発表されており、世界経済や当社の業務活動に重大な悪影響を与え続ける。会社は疫病発生の不利な条件の持続時間或いは程度及び会社の業務或いは資金調達能力への影響を予測できない。この事件により、会社の財務諸表に報告されている金額は何も調整されていません。
| 8 |
注4-逆株分割
2019年2月1日から、当社は普通株20対1の逆分割(“初の逆株式分割”)を完了した。
2020年4月6日から、当社は20対1の普通株式逆分割(“2回目の逆株式分割”)を完了した。
同社は2022年2月9日から普通株1対200の逆分割(“第3回逆株式分割”)を完了した。
特に説明されない限り、会社の財務諸表は、列報のすべての期間および一般株式に対するbr}のすべての参照において、第1、第2および第3の逆分割を遡及的に反映する。
付記5 -支払手形
2022年9月30日と2021年12月31日までの会社の支払手形残高はそれぞれ0ドルと1,900,000ドルである。2022年9月30日と2021年12月31日までの支払手形の累計利息はそれぞれ0ドルと48,287ドル。
当社が2021年12月31日に満期にした支払手形には、以下の内容が含まれています
2021年4月20日、会社は500,000ドルの支払手形を受け取りました利息計上
当社は2021年7月6日に、2023年7月6日に満期となる額面900,000ドル、利息5%の支払手形と引き換えに金を受け取りました。この手形は発行180日後に普通株に転換でき、価格は1株当たり0.30ドルに相当する。当社は2022年2月17日に927,863ドルを現金で支払い、本手形の全元金残高および受取利息27,863ドルを返済した。
当社は2021年8月18日に、額面500,000ドルの支払手形と引き換えに、利息5%を受け取り、2023年8月18日に満期となった。この手形は発行180日後に普通株に転換でき、価格は1株当たり0.30ドルに相当する。当社は2022年2月17日に、本手形の全元金残高と、現金支払い512,534ドルで計算すべき12,534ドルを返済しました。
付記6 -株主権益
2022年2月17日、公開発売が終了し、会社は純収益6,833,071ドルを獲得したお供えからもらいました。公開発売によると、当社は合計1,882,353株の普通株および4,102,200件の取引可能株式証(部分的に引受業者に付与された超過配給選択権を行使することによる337,494件の取引可能株式証を含む)を発行·販売する。
2022年2月22日、会社は会社の最高経営責任者から99万株のBシリーズ優先株を償還し、償還価格は1株0.10ドルの償還価格に相当する。
2022年3月14日、会社は方向性増発を完了し、純収益6,781,199ドルを獲得した。次個人配給と関連して、当社は最大2,301,353株の普通株を購入するために、(I)2,301,353株の普通株を発行する;及び(Ii)1,302,251株の資本金権証(“資本権証”) を発行し、1部の資本資本権証ごとに1株の普通株を行使することができ、投資家株式承認証と一緒に最大1,302,251株の普通株を購入することができる。1株当たり普通株は付属投資家株式承認証と一緒に販売し、合併発行価格は2.22億ドル であり、1部の予融資権証は付属投資家株式承認証と一緒に販売し、合併発行価格は2.219ドルである。あらかじめ出資したbr権証は直ちに行使可能であり,名義行使価格は0.001ドルであり,あらかじめ出資したすべてのbr承認持分証がすべて行使されるまで随時行使可能である。投資家株式証の行使価格は1株2.22ドル(権利証の説明に従って調整しなければならない)であり、発行時に行使することができ、発行日から5年で満了する。
| 9 |
2022年4月28日、同社は別の方向性増発を完了し、純収益16,752,915ドルを獲得した。次個人配給と関連して、当社は(I)2,472,820株普通株と引受権証(“4月株式承認証”)を発行して最大4,945,640株普通株を購入し、及び(Ii)2,390,025部の資本資本権証(“予資権証”) を発行し、予資資権証1部当たり1株普通株を行使することができ、4月承認株式証とともに最大4,780,050株普通株 を購入することができる。1株当たり普通株と付属の2つの4月株式証を一緒に販売し、合併発行価格は4.01 br}であり、各事前資金権証と付属の2つの4月株式証は一緒に販売し、合併発行価格は4.009ドルである。あらかじめ出資したbr権証は直ちに行使可能であり,名義行使価格は0.001ドルであり,あらかじめ出資したすべてのbr承認持分証がすべて行使されるまで随時行使可能である。4月の権利証の行使価格は1株3.76ドル(権利証に記載された調整を受ける必要がある)であり、発行時に行使することができ、発行日から5年で満了する。
同社は2022年9月30日まで配当金を派遣しないと発表した。
付記7-引受権証
ASC 480−10またはASC 815−40によれば、会社は、発行された権利証を負債または権益として入金する。ASC 480−10によれば、株式承認証が強制的に償還され、現金、他の資産、または可変数の株式で決済される必要がある場合、株式承認証 は負債とみなされる。株式証明書がASC 480-10下の負債分類に適合しない場合、当社はASC 815-40の要求を考慮して、株式承認証を負債に分類すべきか権益に分類すべきかを決定する。ASC 815−40によれば、トリガイベントが発生する確率にかかわらず、現金決済が必要となる可能性がある契約は負債である。負債分類株式証は発行日及び各報告期間が終了した時に公正価値に従って計量した。権利証は発行日 以降のいずれの公正価値変動も総合経営報告書に損益として入金される。株式証明書がASC 815-40による負債分類を行う必要がない場合、権利証を株式に分類すべきであるという結論を得るために、当社は株式証明書がその普通株にリンクしているかどうかを評価し、権利証がASC 815-40または他の適用可能なGAAP規格に基づいて株式に分類されるかどうかを評価する。株式分類権証 は発行日に公正価値で入金され、発行後に確認された公正価値は変動しない。
2022年9月30日までの9ヶ月間に、同社は3回の融資事件を完了し、以下の株式証明書を発行した
| タイプ | 番号をつける | 行権価格 | 期日まで |
| あらかじめ出資して株式証明書を発行する | $ |
||
| 流通権証 | $ |
||
| 投資家株式証明書 | $ |
||
| 4月の引受権証 | $ |
| * |
2022年9月30日までの9ヶ月間、すべての事前出資の引受権証と合計3,138,507取引可能株式証を行使し,総収益を$とする
2022年9月30日現在、会社が発行していない引受権証は、以下の通り
| タイプ | 番号をつける | 行権価格 | 期日まで |
| あらかじめ出資して株式証明書を発行する | ありません | $ |
|
| 流通権証 | $ |
||
| 投資家株式証明書 | $ |
||
| 4月の引受権証 | $ |
| 10 |
1株当たり基本純損失 の計算方法は,純損失を期間中に発行された普通株の加重平均株式数で割ったものであり, は普通株等価物を考慮しない。
1株当たり純損失を希釈する計算方法は,純損失を 期間に発行された普通株の加重平均株式数で除算し,普通株等価物を考慮することである。
2022年2月、同社は4,102,200を発行した取引可能株式証
は会社の公開により発売される。2022年3月と4月、会社は投資家
権証と9,725,6904月
2回の私募株式証明書に基づき。2022年9月30日までに取引可能株式証、2,802,703件投資家引受権証、および--4月に逮捕状が行使され963,693人が残った取引可能なbr権証、
202年3月と4月に、当社は予融資権証を発行及び販売し、1株0.001ドルの名義で合計3,692,276株の普通株を購入した(付記3参照)。二零二年九月三十日までの九ヶ月以内に、この等承認持分証はすべてbrを行使したため、薄い効力は残っていない。
注9[br]-経営陣と役員報酬
同社はその管理者に現金報酬を合計595,000ドル支払ったそして
$
当社が取締役に支払う現金報酬は、2022年と2021年9月30日までの3ヶ月と9ヶ月の間、それぞれ100,000ドルと200,000ドルです。
注10 --後続活動
2022年10月20日、同社はカナダの後発薬会社Nora Pharma Inc.の全流通株を買収した。総買収価格は30,000,000カナダドル(約21,900,000ドル),支払い方法は20,000,000カナダドル(約14,600,000ドル)の現金,3,700,000株の会社普通株を発行し,5,000,000カナダドル(約3,650,000ドル),および5,000,000カナダドル(約3,650,000ドル), は将来的に目標売上高に応じて収益額を支払う可能性がある.または収益を得ることによって、売り手のMalek Chamounさん は、 Nora Pharma 2022年6月30日の総売上高を1,000,000カナダドル(約3,000,000ドル)ずつ増加させるために、250,000カナダドル(約20)の250,000カナダドルを支払うことができました。
| 11 |
項目2.経営陣の財務状況と経営成果の検討と分析。
以下の議論は、私たちの連結財務諸表とその付記と一緒に読まなければならない。本討論は“1933年証券法”(改訂本)第27 A節又は“証券法”と“1934年証券取引法”(改正本)第21 E節に示された前向き陳述を含む。本報告に含まれる太陽光生物製薬会社に関する表現は歴史的表現ではなく、特に“可能”、“会”、“すべき”、“可能”、“予想”、“推定”、“信じる”または“計画”または同様の用語を使用する表現は、現在の期待と仮定に基づく前向き表現であり、様々なリスクと不確実性が存在し、実際の結果がこのような前向き表現の内容と大きく異なる可能性がある。本報告と2021年12月31日までの年次報告書10−K表では,このような大きな違いを引き起こす可能性があることが知られている重要な要因 を決定した。私たちは新しい情報、未来の事件、または他の理由でも、法律が適用されなければ、他の要求がなければ、いかなる前向きな陳述を修正したり更新したりする義務はない。しかし、私たちが将来アメリカ証券取引委員会に提出された報告書で関連テーマについて何でも開示することを参考にすることをお勧めします.
概要
著者らは特許薬物の研究と開発に専念している製薬会社であり、著者らの抗癌化合物Adva-27 A、著者らの抗癌K 1.1 mRNA分子 と抗コロナウイルス先導化合物SBFM-PL 4を含む。
また,我々はカナダの完全子会社である陽光生物科技カナダ株式会社(“サンシャインカナダ”)を通じて科学に基づく栄養補助剤を開発し,現在1種の栄養補助剤製品,Essential 9 Tmを販売している。
2022年10月20日、カナダのジェネリック医薬品会社Nora Pharma Inc.(“Nora Pharma”)の買収を完了した。Nora Pharmaは大モントリオール地域に本部を置き,36名の従業員 を有し,カナダ衛生部が認証した15,000平方フィートの施設で運営されている。Nora Pharmaは現在、後発薬、非処方薬、生物模倣薬を含む50種類以上の薬品を提供している。Nora Pharmaの2022年6月30日までの会計年度売上高は1070万ドル、同期純収入は30万ドル(ドル)だった。
独自の薬物開発業務
SBFM−PL 4抗コロナウイルス治療
以下に我々のコロナウイルス治療プロジェクトのこれまでの発展の概要を示す
| · | 2020年5月22日、我々は米国に特許出願を提出し、コロナウイルス感染を治療する新しい方法を出願した。我々の特許出願は,コロナウイルス主プロテアーゼ(MPRO)およびパパイヤ様プロテアーゼ(PLPro)の小分子の阻害に関連する組成物の主題をカバーしている。この2つの酵素はウイルス複製に不可欠である。特定のウイルス蛋白の成熟に参与する以外に、PLProはヒト免疫系を抑制し、ウイルスの毒性を更に強くすることを担当する。特許出願に含まれている小分子は、私たちの最高経営責任者スティーブ·N·スリラティ博士によって設計されました。この特許出願の優先日は2020年5月22日である。 | |
| · | 2020年8月、著者らは4種類の異なる潜在的なPLPro阻害剤の合成を完成した。これらの化合物は、2020年5月22日に我々が出願した特許出願に記載されている技術に基づいている。 | |
| · | 2020年9月、著者らは4種類の化合物のスクリーニングを完成し、その後1種の主要な抗コロナウイルス候補薬物(SBFM-PL 4)を確定した。先導化合物の同定スクリーニングはジョージア大学薬学院で行われた。 | |
| · | 著者らのSBFM-PL 4薬物開発計画の次のステップは、より多くの体外研究を行い、その後、ヒト臨床試験に入る前にコロナウイルスに感染したマウスの細胞培養分析と評価を行うことを含む。 | |
| · | 2022年2月,他のPLPro阻害剤の検索を拡大し,アリゾナ大学と研究合意を達成し,アリゾナ大学が持つ3種類のPLPro阻害剤の体内安全性,薬物動態,用量選択特性を決定し,SARS−CoV−2に感染したマウスで治療効果試験を行うことに重点を置いた(“研究プロジェクト”)。協定によると、アリゾナ大学は同社にアリゾナ大学員が同研究プロジェクトに基づいて開発したすべての知的財産権交渉商業、印税許可の優先選択権を付与した。また、当社はアリゾナ大学とオプション契約を締結しており、この合意により、当社は最初のオプションを取得し、研究プロジェクトの基礎技術交渉について特許権使用料の商業許可を徴収していますこの技術の発展を進めるために,2022年9月13日にアリゾナ大学にオプション行使通知を提出した。 |
| 12 |
ADVA−27 A抗癌化合物
腫瘍学の分野では,われわれの特許薬物開発活動は,侵襲性癌 の治療に用いられるAdva−27 Aという小分子の開発に専念してきた。トポイソメラーゼII阻害剤Adva-27 Aは、膵臓癌細胞、乳癌細胞、小細胞肺癌細胞および子宮肉腫細胞を含む多剤耐性癌細胞を有効に破壊することが証明されている(2012年10月に発表された“抗癌研究”第32巻、第4423-4432ページ)。サンシャインバイオ製薬会社は、米国特許番号8,236,935および10,272,065を含むAdva−27 Aに関連するすべての発行された特許の直接所有者である。

図1
ADVA−27 Aは鬼臼毒素の宝石ジフルオロカーボン誘導体である(図1参照)。鬼臼毒素のもう一つの誘導体はエトポシドと呼ばれ、現在市場で各種の癌の治療に応用されており、白血病、リンパ腫、精巣癌、肺癌、脳癌、前立腺癌、膀胱癌、結腸癌、卵巣癌、肝癌とその他のいくつかの癌を含む。エトポシドは最も広く応用されている抗癌薬物の一つである。ADVA-27 Aとエトポシドの類似点は、いずれも癌細胞中の同じ標的、すなわちDNA解離酵素トポイソメラーゼIIを攻撃することである。しかし、エトポシドとは異なり、AdVA-27 Aは多剤耐性癌細胞を透過して破壊することができる。また,Adva−27 Aはエトロポシドと比較して独特かつより理想的な生物学的および薬理学的特性を有することが証明されている。多剤耐性乳腺癌細胞とエトポシドを参照物とした並列研究では,Adva−27 Aは有意に強い細胞傷害活性 を示した(図2参照)。
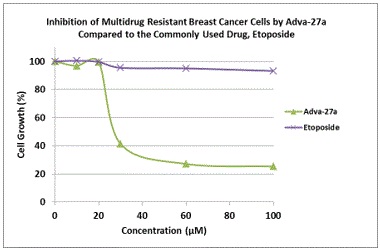
図2
| 13 |
私たちのAdva-27 A開発計画の次のステップは、
| · | INDイネーブル研究とI期臨床試験のための2 kg GMP製造 | |
| · | INDの研究を支援する | |
| · | 監督管理届出(高速チャネル状態の予定) | |
| · | I期臨床試験(膵癌適応) |
ADVA−27 Aの最初の適応は膵癌であり,現在のところ利用可能な治療選択はほとんどない。私たちはカナダモントリオールのマギル大学ユダヤ総合病院で臨床試験を行う予定です。カナダの臨床試験のすべての面ですべてのレベルでFDA基準が採用される。
米国癌協会のデータによると,米国では毎年150万近くの新たに確定診断された癌症例がある。多剤耐性癌には特に有効であるが,Adva−27 Aはすべてのタイプの癌,特にトポイソメラーゼIIが増幅された癌を潜在的に治療できると信じている。第1段階臨床試験を成功させた後,大手製薬会社から1つ以上の購入が可能であるかもしれないというオファーを受ける可能性があると信じている。しかし、私たちの第一段階の試験が成功する保証はありません。あるいは成功すれば、どの製薬会社も私たちに受け入れ可能な見積もりを出してくれます。もし私たちがこのような取引を完了しなければ、私たちは規制部門の許可を得て、自分で新薬を製造し、販売するために、大量のbr資金が必要になるだろう。
K 1.1抗癌遺伝子
2021年6月、私たちは新しい研究プロジェクトを開始し、いくつかのメッセンジャーリボ核酸分子が抗癌薬として使用できるかどうかの決定に着手した。これまでに収集されたデータは、選択されたmRNA分子のセットが、多剤耐性乳癌細胞(MCF−7/MDR)、卵巣腺癌細胞(OVCAR−3)、膵臓癌細胞(Suit−2)を含む癌細胞をインビトロで破壊することができることを示している。他の未形質転換(正常)ヒト細胞(HMEC細胞)を用いた研究では,これらのmRNA分子は細胞毒性作用がほとんどないことが示唆されている。これらの新しいメッセンジャーリボ核酸分子は実験室名K 1.1を有し、メッセンジャーリボ核酸ワクチン技術を使用した患者体内に容易に適応できる。2022年4月、我々は主題mRNA分子をカバーする臨時特許出願を米国に提出した。我々は現在,我々のK 1.1 mRNA分子を脂質ナノ粒子(K 1.1::LNP)にすることを目的として,いくつかの潜在的なパートナーと交渉している。K 1.1::LNP製剤を用いて,約12カ月以内にマウス異種移植研究を開始する予定である。
栄養補助剤業務
私たちはカナダの完全子会社サンシャインカナダで科学に基づく栄養補助剤の開発とマーケティングに集中しています。2018年12月、私たちは最初の栄養補助食品製品の開発を完了し、Essential 9™と命名しました。2018年12月14日、カナダ保健省はNPN 889663を発表し、Essential 9™ 製品の製造と販売を許可しました。我々のEssential 9™栄養補助食品は当初タブレットとして発売されていたが,現在では純粋なベジタリアンカプセルに再フォーマットされている。私たちの精華9TMカプセルは人体では産生できない9種類の必須アミノ酸のバランス配合を含む。必須アミノ酸はタンパク質合成に必要な20種類のアミノ酸のうち9種類である。タンパク質 は人体のすべての機能である筋肉と免疫系からホルモンと神経伝達物質まで参与する。ビタミンのように、人体は必要なアミノ酸を合成できず、食事で得なければならない。9種類の必須アミノ酸の1つ以上のbrの不足はスポーツ選手の筋肉品質の低下、疲労、体重増加と筋肉組織能力の低下を招く。我々のEssential 9™は,すべての9種類の必須アミノ酸を自由形態およびカナダ保健省が推奨した割合で提供した。Essential 9™は現在、Amazon.comおよびAmazon.caで提供されています。以下の図3に我々が再フォーマットした60カプセルEssential 9™製品を示す。
| 14 |
図3
2019年11月、カナダ保健省から承認されたもう一つの栄養補助剤、新しいカルシウム-ビタミンD錠剤を取得した。カナダ衛生部はNPN 80093432を発表し、新しいカルシウム-ビタミンDサプリメントの生産と販売を許可した。ブランド名はEssentialカルシウム-ビタミンD™である。br}ビタミンDはステロイド分子のセットであり、腸管のカルシウム、マグネシウムとリン酸塩に対する吸収を増加させることを担当している。brはまた免疫系の正常な機能を含み、骨の健康な成長を促進し、炎症を減少させるなど、多種の他の生物学的機能に関与している。この群の中で最も重要な化合物はエルゴカルビル(ビタミンD 2)とコレカルシフェロール(ビタミンD 3)である。日光生物薬業の基本的なカルシウム-ビタミンD™錠剤はこの2種類の化合物とカルシウム を含み、最適な健康効果を実現する。私たちは2023年にこの製品を発売する可能性を考えている。
経営成果
2022年9月30日と2021年9月30日までの3ヶ月間の経営実績比較
2022年9月30日までの3ヶ月間の収入は132,808ドルですが、2021年9月30日までの3ヶ月の収入は50,376ドルです。 成長はマーケティングを強化したためです。このようなすべての収入は私たちの科学に基づく栄養補助食品業務から来ている。2022年9月30日までの3カ月間、これらの収入を発生させる直接コストは65,783ドル(49.5%)だったが、2021年9月30日までの3カ月間の直接コストは19,506ドル(38.7%)だった。2022年の販売コストの増加は製造コストの増加による である。2022年9月30日までの3ヶ月間、私たちの毛利益は67,025ドルに増加したが、2021年同期の毛利益は30,870ドルであった。
2022年9月30日までの3カ月間の一般·行政費は1,785,005ドルだったが、2021年9月30日までの3カ月間は527,129ドルと1,257,876ドル増加した。全体的に言えば、2022年9月30日までの3ヶ月間の運営損失は1,717,980ドルだったのに対し、2021年同期の運営損失は496,259ドルであった。
また、2022年9月30日までの3ヶ月間、私たちの利息収入は260,938ドル、利息支出は2ドル、債務減免は0ドルですが、2021年9月30日までの3ヶ月間、私たちの利息収入は0ドル、利息支出は46,849ドル、債務減免は7,688ドルです。これは主に私たちの融資が転換可能な債券から株式に移行するためだ。2022年9月30日までの3ヶ月間、債務転換に関する損失は発生しなかったのに対し、2021年9月30日までの3ヶ月で、債務転換は3,504,000ドルの損失が生じた。これはまた私たちの融資が転換可能な債券から株式に移行するためだ。
そのため、2022年9月30日までの3ヶ月間の純損益は1,457,019ドルでしたが、2021年9月30日までの3ヶ月間の純損失は4,039,383ドルでした。
| 15 |
2022年9月30日と2021年9月30日までの9ヶ月間の経営実績比較
2022年9月30日までの9カ月間で405,760ドルの収入を創出したが,2021年9月30日までの9カ月の収入は143,308ドルであった。成長 はマーケティングを強化したことによるものだ。これらすべての収入は、私たちの科学に基づく栄養サプリメント業務から来ています。 2022年9月30日までの9ヶ月間、これらの収入を発生させる直接コストは200,311ドル(49.4%)ですが、2021年9月30日までの9ヶ月の直接コストは56,541ドル(39.5%) です。2022年の販売コストの増加は製造コストの増加によるものである。2022年9月30日までの9ヶ月間、私たちの毛利益は205,449ドルに増加したが、2021年同期の毛利益は86,767ドルであった。
2022年9月30日までの9カ月間の一般·行政費は3,842,589ドルであったが,2021年9月30日までの9カ月間は2,247,270ドルと1,595,319ドル増加した。全体的に言えば、2022年9月30日までの9ヶ月間、私たちの運営損失は3,637,140ドルだったのに対し、2021年同期の運営損失は2,160,503ドルだった。
また、2022年9月30日までの9ヶ月間、私たちの利息収入は406,984ドル、利息支出は12,866ドル、債務減免は10,852ドルですが、2021年9月30日までの9ヶ月間、私たちの利息収入は0ドル、利息支出は292,188ドル、債務減免は58,940ドルです。これは主に私たちの融資が転換可能債務から持分に転換されたためです。2022年9月30日までの9カ月間、債務転換に関する損失 は発生しなかったが、2021年9月30日までの9カ月間、債務転換には10,709,843ドルの損失 が生じた。これはまた私たちの融資が転換可能な債券から株式に移行するためだ。
そのため、2022年9月30日までの9カ月間の純損失は3,232,125ドルだったが、2021年9月30日までの9カ月間の純損失は13,103,563ドルだった。
流動性と資本資源
2022年9月30日まで、私たちの現金と現金等価物は40,555,931ドルです。
2022年9月30日までの9カ月間の経営活動で使用された純現金は3,001,746ドルであったが,2021年9月30日までの9カ月間は1,517,015ドルであった。この増加は,マーケティングや研究開発活動の増加と,ナスダック上場企業となることに関する専門費用の増加によるものである
2022年9月30日までの9カ月間、融資活動が提供したキャッシュフローは41,561,363ドルだったが、2021年9月30日までの9カ月間は2,928,339ドルだった。この増加は,2022年2月,3月,4月に完了した三次融資事件および株式証承認演習の結果によるものである。
2022年9月30日と2021年9月30日までの9ヶ月間、投資活動で使用されたキャッシュフローは0ドルだった。
我々は我々の運営から十分なbr収入を得ておらず,ここで提案した業務計画を全面的に実施している.2022年2月17日、私たちは普通株と引受権証を公開発行することで約680万ドルの純収益を得た。2022年3月14日,私たちは私募方式で普通株と引受権証を売却し,約680万ドルの純収益を得た。2022年4月28日、私たちは私募方式で普通株と引受権証を販売し、約1,680万ドルの純収益を得た。私たちの既存の現金は、一般的かつ行政費用、拡大された研究開発活動、br、栄養補助剤業務を含む、私たちの運営に資金を提供するのに十分であると信じています。私たちの推定が正確になるという保証はない。私たちは約束されたbr資金源を持っていません。私たちは将来、さらなる研究開発活動と可能な臨床試験、およびNora Pharmaの買収によって私たちの模倣薬業務を拡大することを含むより多くの資金を集める必要があると予想されます。追加資金は私たちが受け入れた条項で提供できないかもしれない、あるいは全く提供できないかもしれません。
| 16 |
重要な会計政策と試算
肝心な会計見積もり
私たちの財務状況と経営結果の検討と分析は私たちの財務諸表に基づいており、これらの報告書はアメリカで公認されている会計原則に従って作成されています。これらの財務諸表を作成するには、資産、負債、収入および支出金額、または資産および負債の関連開示に影響を与える推定および判断を行う必要があります。継続的なうえで,我々の見積りは歴史的経験や様々な他の仮定に基づいて評価されており, は当時の場合には合理的であると考えられ,これらの仮定の結果は,他のソースからは見えにくい資産や負債の帳簿価値 を判断する基礎となっている.異なる仮定または条件では、実際の結果は、これらの推定値とは異なる可能性がある。
重要会計政策の詳細リストについては、2021年12月31日現在の会計年度10-K表の年次報告書を参照し、2022年3月21日に米国証券取引委員会に提出された当社の財務諸表およびその付記を含む
最近採用された会計基準
FASBは2020年2月にASU 2020-02を発表しました金融商品-信用損失(特別テーマ326)とリース(特別テーマ842)-“米国証券取引委員会職員会計公報”第119号による“米国証券取引委員会”段落の改訂、及び“米国証券取引委員会”章の会計基準更新第2016−02号に関する発効日の更新(特別テーマ842)これは規模の小さい報告会社に対して元の公告の施行日を修正した。ASU 2016-13 とその修正案は、2022年12月15日以降の会計年度の中期と年度中に会社に発効するとしている。 社は、この改正案を採用することで会社が金融商品を分析する方式を変更するとしているが、運営業績に大きな影響を与えることはないと予想している。会社はこの技術を採用してその連結財務諸表に及ぼす影響を決定している。
2020年8月にFASBはASU 2020-06を発表しました債務--転換可能な債務およびその他のオプション(主題470-20)および派生ツールおよびヘッジ--エンティティ自己資本契約(主題815-40)(“アリゾナ州立大学2020-06”)。ASU 2020-06は、変換可能なツールおよびエンティティの自己資本の契約を含む、負債および権益の特徴を有するいくつかの金融商品の会計処理を簡略化する。ASU 2020-06修正案は、2023年12月15日以降の会計年度およびこれらの年度内の移行期間内に有効である。早期採用は許可されているが、これらの事業年度内の移行期間を含む2020年12月15日以降の事業年度より早くしてはならない。同社は、監査されていない総合財務諸表に対するこの指導の影響を評価している。
表外手配
ない。
| 17 |
第3項市場リスクの定量的·定性的開示について
我々は小さな報告会社 であり、本プロジェクトでの情報を提供する必要はありません。
項目4.制御とプログラム
情報開示制御とプログラムの評価
我々の経営陣は、CEOおよび最高財務官の参加の下で、本報告で述べた期間終了までの開示制御およびプログラムの有効性 (取引所法案下のルール13 a-15(E)および15 d-15(E)で定義されている)を評価した。
これらの制御は、取引法に基づいて提出または提出された報告書において開示を要求する情報が、米国証券取引委員会の規則および表に指定された期間内に記録、処理、集約および報告されることを保証し、必要なbr}開示をタイムリーに決定するために、我々のCEOおよび最高財務官を含む、そのようなbr情報が蓄積されて我々の管理層に伝達されることを保証することを目的としている。
この評価によると、私たちの経営陣は、CEOやCEOを含め、2022年9月30日までに、私たちの開示統制や手続きが合理的な保証レベルで有効であると結論した。
財務報告の内部統制の変化
2022年9月30日までの四半期内に、財務報告の内部統制には何の変化もなく、これらの変化は、我々の財務報告の内部統制に大きな影響を与えているか、または大きな影響を与えている可能性が高い。
| 18 |
第2部:その他の情報
項目1.法的訴訟
私たちはいかなる実質的な法的手続きの当事者でもなく、私たちの財産 もいかなる重大な法的手続きの標的でもない。
第1 A項。リスク要因です
我々は小さな報告会社 であり、本プロジェクトでの情報を提供する必要はありません。
第二項株式証券の未登録販売及び募集資金の使用。
ない。
第3項高級証券違約
ない。
第4項鉱山安全情報開示
適用されません。
第5項その他資料
ない。
プロジェクト6.展示品。
| 証拠品番号: | 説明する | |
| 31.1 | 2002年のサバンズ·オキシリー法第302条による最高経営責任者の認証* | |
| 31.2 | “2022年サバンズ-オキシリー法”第302条に基づく認証首席財務官* | |
| 32.1 | 2002年のサバンズ·オクスリ法第906条に基づく認証* | |
| 101 | 本四半期報告10-Q表の第1項の財務諸表および付記設定のための連結XBRLファイル。* | |
| 104 | 表格10-Q上の本四半期報告表紙のイントラネットXBRLは、添付ファイル101に内蔵されたXBRLドキュメントセットに含まれています。* |
| * | 本局に提出します。 |
| 19 |
サイン
1934年の証券取引法の要求によると、登録者は2022年11月7日に以下の署名者代表登録者が本報告書に署名することを正式に許可した。
| 日光生物製薬会社 | |||
| 差出人: | スティーブ·N·スリラーティ博士 | ||
| スティーブ·N·スリラティ博士 | |||
| 最高経営責任者(CEO) | |||
| 差出人: | /s/Camille Sebaaly | ||
|
カミーユ·セバリ 首席財務官(首席財務·会計官) |
|||
| 20 |