mrna-20220630偽2022Q2000168285212 月 31 日http://fasb.org/us-gaap/2022#OtherLiabilitiesCurrenthttp://fasb.org/us-gaap/2022#OtherLiabilitiesCurrenthttp://fasb.org/us-gaap/2022#OtherLiabilitiesCurrenthttp://fasb.org/us-gaap/2022#OtherLiabilitiesCurrent00016828522022-01-012022-06-3000016828522022-07-29エクセルリ:シェア00016828522022-06-30ISO 4217: 米ドル00016828522021-12-31ISO 4217: 米ドルエクセルリ:シェア0001682852NAさん:製品販売メンバー2022-04-012022-06-300001682852NAさん:製品販売メンバー2021-04-012021-06-300001682852NAさん:製品販売メンバー2022-01-012022-06-300001682852NAさん:製品販売メンバー2021-01-012021-06-300001682852米国会計基準:補助金メンバー2022-04-012022-06-300001682852米国会計基準:補助金メンバー2021-04-012021-06-300001682852米国会計基準:補助金メンバー2022-01-012022-06-300001682852米国会計基準:補助金メンバー2021-01-012021-06-300001682852MrNA: コラボレーションアレンジメントメンバー2022-04-012022-06-300001682852MrNA: コラボレーションアレンジメントメンバー2021-04-012021-06-300001682852MrNA: コラボレーションアレンジメントメンバー2022-01-012022-06-300001682852MrNA: コラボレーションアレンジメントメンバー2021-01-012021-06-3000016828522022-04-012022-06-3000016828522021-04-012021-06-3000016828522021-01-012021-06-300001682852米国会計基準:普通株式会員2022-03-310001682852米国会計基準:追加払込資本構成員2022-03-310001682852米国会計基準:その他の包括利益の累計メンバー2022-03-310001682852米国会計基準:利益剰余金メンバー2022-03-3100016828522022-03-310001682852米国会計基準:普通株式会員2022-04-012022-06-300001682852米国会計基準:追加払込資本構成員2022-04-012022-06-300001682852米国会計基準:その他の包括利益の累計メンバー2022-04-012022-06-300001682852米国会計基準:利益剰余金メンバー2022-04-012022-06-300001682852米国会計基準:普通株式会員2022-06-300001682852米国会計基準:追加払込資本構成員2022-06-300001682852米国会計基準:その他の包括利益の累計メンバー2022-06-300001682852米国会計基準:利益剰余金メンバー2022-06-300001682852米国会計基準:普通株式会員2021-03-310001682852米国会計基準:追加払込資本構成員2021-03-310001682852米国会計基準:その他の包括利益の累計メンバー2021-03-310001682852米国会計基準:利益剰余金メンバー2021-03-3100016828522021-03-310001682852米国会計基準:普通株式会員2021-04-012021-06-300001682852米国会計基準:追加払込資本構成員2021-04-012021-06-300001682852米国会計基準:その他の包括利益の累計メンバー2021-04-012021-06-300001682852米国会計基準:利益剰余金メンバー2021-04-012021-06-300001682852米国会計基準:普通株式会員2021-06-300001682852米国会計基準:追加払込資本構成員2021-06-300001682852米国会計基準:その他の包括利益の累計メンバー2021-06-300001682852米国会計基準:利益剰余金メンバー2021-06-3000016828522021-06-300001682852米国会計基準:普通株式会員2021-12-310001682852米国会計基準:追加払込資本構成員2021-12-310001682852米国会計基準:その他の包括利益の累計メンバー2021-12-310001682852米国会計基準:利益剰余金メンバー2021-12-310001682852米国会計基準:普通株式会員2022-01-012022-06-300001682852米国会計基準:追加払込資本構成員2022-01-012022-06-300001682852米国会計基準:その他の包括利益の累計メンバー2022-01-012022-06-300001682852米国会計基準:利益剰余金メンバー2022-01-012022-06-300001682852米国会計基準:普通株式会員2020-12-310001682852米国会計基準:追加払込資本構成員2020-12-310001682852米国会計基準:その他の包括利益の累計メンバー2020-12-310001682852米国会計基準:利益剰余金メンバー2020-12-3100016828522020-12-310001682852米国会計基準:普通株式会員2021-01-012021-06-300001682852米国会計基準:追加払込資本構成員2021-01-012021-06-300001682852米国会計基準:その他の包括利益の累計メンバー2021-01-012021-06-300001682852米国会計基準:利益剰余金メンバー2021-01-012021-06-300001682852米国会計基準:累積純未実現投資利益損失メンバー2021-12-310001682852米国会計基準:指定または適格キャッシュフロー・エッジ会員からの累積純利益損失2021-12-310001682852米国会計基準:累積純未実現投資利益損失メンバー2022-01-012022-03-310001682852米国会計基準:指定または適格キャッシュフロー・エッジ会員からの累積純利益損失2022-01-012022-03-3100016828522022-01-012022-03-310001682852米国会計基準:累積純未実現投資利益損失メンバー2022-03-310001682852米国会計基準:指定または適格キャッシュフロー・エッジ会員からの累積純利益損失2022-03-310001682852米国会計基準:累積純未実現投資利益損失メンバー2022-04-012022-06-300001682852米国会計基準:指定または適格キャッシュフロー・エッジ会員からの累積純利益損失2022-04-012022-06-300001682852米国会計基準:累積純未実現投資利益損失メンバー2022-06-300001682852米国会計基準:指定または適格キャッシュフロー・エッジ会員からの累積純利益損失2022-06-300001682852NAさん:製品販売メンバー国:米国2022-04-012022-06-300001682852NAさん:製品販売メンバー国:米国2021-04-012021-06-300001682852NAさん:製品販売メンバー国:米国2022-01-012022-06-300001682852NAさん:製品販売メンバー国:米国2021-01-012021-06-300001682852SRT: ヨーロッパメンバーNAさん:製品販売メンバー2022-04-012022-06-300001682852SRT: ヨーロッパメンバーNAさん:製品販売メンバー2021-04-012021-06-300001682852SRT: ヨーロッパメンバーNAさん:製品販売メンバー2022-01-012022-06-300001682852SRT: ヨーロッパメンバーNAさん:製品販売メンバー2021-01-012021-06-300001682852ナ氏:世界のその他のメンバーNAさん:製品販売メンバー2022-04-012022-06-300001682852ナ氏:世界のその他のメンバーNAさん:製品販売メンバー2021-04-012021-06-300001682852ナ氏:世界のその他のメンバーNAさん:製品販売メンバー2022-01-012022-06-300001682852ナ氏:世界のその他のメンバーNAさん:製品販売メンバー2021-01-012021-06-300001682852NAさん:製品販売メンバー2022-06-300001682852NAさん:製品販売メンバー2021-12-310001682852NAさん:国防高等研究計画局メンバー2020-09-012020-09-300001682852MrNA: 契約オプションメンバーNAさん:国防高等研究計画局メンバー2022-06-300001682852NAさん:バイオメディカル先端研究開発局委員2020-04-012020-04-30MRNA: 参加者0001682852NAさん:バイオメディカル先端研究開発局委員2022-03-012022-03-310001682852NAさん:バイオメディカル先端研究開発局委員2020-04-012022-06-300001682852NAさん:バイオメディカル先端研究開発局委員2022-06-300001682852NAさん:バイオメディカル先端研究開発局委員2016-09-012016-09-300001682852NAさん:バイオメディカル先端研究開発局委員2021-01-012021-12-310001682852NAさん:バイオメディカル先端研究開発局委員2016-09-30MrNa: オプションの数0001682852NAさん:バイオメディカル先端研究開発局委員MrNA: 契約オプションメンバー2022-06-300001682852ナ氏:ビル・アンド・メリンダ・ゲイツ財団会員Mr Na: 最初のプロジェクトメンバー2022-06-300001682852NAさん:バイオメディカル先端研究開発局委員米国会計基準:補助金メンバー2022-04-012022-06-300001682852NAさん:バイオメディカル先端研究開発局委員米国会計基準:補助金メンバー2021-04-012021-06-300001682852NAさん:バイオメディカル先端研究開発局委員米国会計基準:補助金メンバー2022-01-012022-06-300001682852NAさん:バイオメディカル先端研究開発局委員米国会計基準:補助金メンバー2021-01-012021-06-300001682852NA氏:その他の助成金収益メンバー米国会計基準:補助金メンバー2022-04-012022-06-300001682852NA氏:その他の助成金収益メンバー米国会計基準:補助金メンバー2021-04-012021-06-300001682852NA氏:その他の助成金収益メンバー米国会計基準:補助金メンバー2022-01-012022-06-300001682852NA氏:その他の助成金収益メンバー米国会計基準:補助金メンバー2021-01-012021-06-300001682852MRNA:アフィリエイトメンバーとの取り決めを含むコラボレーションの取り決めMr Na: アストラゼネカマー2022-04-012022-06-300001682852MRNA:アフィリエイトメンバーとの取り決めを含むコラボレーションの取り決めMr Na: アストラゼネカマー2021-04-012021-06-300001682852MRNA:アフィリエイトメンバーとの取り決めを含むコラボレーションの取り決めMr Na: アストラゼネカマー2022-01-012022-06-300001682852MRNA:アフィリエイトメンバーとの取り決めを含むコラボレーションの取り決めMr Na: アストラゼネカマー2021-01-012021-06-300001682852MRNA:アフィリエイトメンバーとの取り決めを含むコラボレーションの取り決めNA氏:メルクメンバー2022-04-012022-06-300001682852MRNA:アフィリエイトメンバーとの取り決めを含むコラボレーションの取り決めNA氏:メルクメンバー2021-04-012021-06-300001682852MRNA:アフィリエイトメンバーとの取り決めを含むコラボレーションの取り決めNA氏:メルクメンバー2022-01-012022-06-300001682852MRNA:アフィリエイトメンバーとの取り決めを含むコラボレーションの取り決めNA氏:メルクメンバー2021-01-012021-06-300001682852NAさん:頂点メンバーMRNA:アフィリエイトメンバーとの取り決めを含むコラボレーションの取り決め2022-04-012022-06-300001682852NAさん:頂点メンバーMRNA:アフィリエイトメンバーとの取り決めを含むコラボレーションの取り決め2021-04-012021-06-300001682852NAさん:頂点メンバーMRNA:アフィリエイトメンバーとの取り決めを含むコラボレーションの取り決め2022-01-012022-06-300001682852NAさん:頂点メンバーMRNA:アフィリエイトメンバーとの取り決めを含むコラボレーションの取り決め2021-01-012021-06-300001682852NA氏:その他の協力パーティーメンバーMRNA:アフィリエイトメンバーとの取り決めを含むコラボレーションの取り決め2022-04-012022-06-300001682852NA氏:その他の協力パーティーメンバーMRNA:アフィリエイトメンバーとの取り決めを含むコラボレーションの取り決め2021-04-012021-06-300001682852NA氏:その他の協力パーティーメンバーMRNA:アフィリエイトメンバーとの取り決めを含むコラボレーションの取り決め2022-01-012022-06-300001682852NA氏:その他の協力パーティーメンバーMRNA:アフィリエイトメンバーとの取り決めを含むコラボレーションの取り決め2021-01-012021-06-300001682852MRNA:アフィリエイトメンバーとの取り決めを含むコラボレーションの取り決め2022-04-012022-06-300001682852MRNA:アフィリエイトメンバーとの取り決めを含むコラボレーションの取り決め2021-04-012021-06-300001682852MRNA:アフィリエイトメンバーとの取り決めを含むコラボレーションの取り決め2022-01-012022-06-300001682852MRNA:アフィリエイトメンバーとの取り決めを含むコラボレーションの取り決め2021-01-012021-06-300001682852MRNA:アフィリエイトメンバーとの取り決めを含むコラボレーションの取り決め2021-12-310001682852MRNA:アフィリエイトメンバーとの取り決めを含むコラボレーションの取り決め2022-06-300001682852米国会計基準:現金および現金同等物メンバー米国会計基準:フェアバリューインプットレベル1メンバー2022-06-300001682852米国会計基準:現金および現金同等物メンバー米国会計基準:現金および現金同等物メンバー米国会計基準:フェアバリューインプットレベル1メンバー2022-06-300001682852米国会計基準:現金および現金同等物メンバーMrNA: 現在の有価証券のメンバー米国会計基準:フェアバリューインプットレベル1メンバー2022-06-300001682852米国会計基準:現金および現金同等物メンバーNA氏:非流動有価証券会員米国会計基準:フェアバリューインプットレベル1メンバー2022-06-300001682852米国会計基準:預金証書メンバー米国会計基準:公正価値インプットレベル2メンバー2022-06-300001682852米国会計基準:預金証書メンバー米国会計基準:現金および現金同等物メンバー米国会計基準:公正価値インプットレベル2メンバー2022-06-300001682852MrNA: 現在の有価証券のメンバー米国会計基準:預金証書メンバー米国会計基準:公正価値インプットレベル2メンバー2022-06-300001682852NA氏:非流動有価証券会員米国会計基準:預金証書メンバー米国会計基準:公正価値インプットレベル2メンバー2022-06-300001682852米国会計基準:米国財務省証券会員米国会計基準:公正価値インプットレベル2メンバー2022-06-300001682852米国会計基準:米国財務省証券会員米国会計基準:現金および現金同等物メンバー米国会計基準:公正価値インプットレベル2メンバー2022-06-300001682852米国会計基準:米国財務省証券会員MrNA: 現在の有価証券のメンバー米国会計基準:公正価値インプットレベル2メンバー2022-06-300001682852NA氏:非流動有価証券会員米国会計基準:米国財務省証券会員米国会計基準:公正価値インプットレベル2メンバー2022-06-300001682852米国会計基準:米国政府機関債務証券メンバー米国会計基準:公正価値インプットレベル2メンバー2022-06-300001682852米国会計基準:現金および現金同等物メンバー米国会計基準:公正価値インプットレベル2メンバー米国会計基準:米国政府機関債務証券メンバー2022-06-300001682852MrNA: 現在の有価証券のメンバー米国会計基準:公正価値インプットレベル2メンバー米国会計基準:米国政府機関債務証券メンバー2022-06-300001682852NA氏:非流動有価証券会員米国会計基準:公正価値インプットレベル2メンバー米国会計基準:米国政府機関債務証券メンバー2022-06-300001682852米国会計基準:企業債務証券メンバー米国会計基準:公正価値インプットレベル2メンバー2022-06-300001682852米国会計基準:企業債務証券メンバー米国会計基準:現金および現金同等物メンバー米国会計基準:公正価値インプットレベル2メンバー2022-06-300001682852MrNA: 現在の有価証券のメンバー米国会計基準:企業債務証券メンバー米国会計基準:公正価値インプットレベル2メンバー2022-06-300001682852NA氏:非流動有価証券会員米国会計基準:企業債務証券メンバー米国会計基準:公正価値インプットレベル2メンバー2022-06-300001682852米国会計基準:米国政府債務証券メンバー米国会計基準:公正価値インプットレベル2メンバー2022-06-300001682852米国会計基準:米国政府債務証券メンバー米国会計基準:現金および現金同等物メンバー米国会計基準:公正価値インプットレベル2メンバー2022-06-300001682852MrNA: 現在の有価証券のメンバー米国会計基準:米国政府債務証券メンバー米国会計基準:公正価値インプットレベル2メンバー2022-06-300001682852NA氏:非流動有価証券会員米国会計基準:米国政府債務証券メンバー米国会計基準:公正価値インプットレベル2メンバー2022-06-300001682852米国会計基準:公正価値インプットレベル2メンバー2022-06-300001682852米国会計基準:現金および現金同等物メンバー米国会計基準:公正価値インプットレベル2メンバー2022-06-300001682852MrNA: 現在の有価証券のメンバー米国会計基準:公正価値インプットレベル2メンバー2022-06-300001682852NA氏:非流動有価証券会員米国会計基準:公正価値インプットレベル2メンバー2022-06-300001682852米国会計基準:現金および現金同等物メンバー米国会計基準:フェアバリューインプットレベル1メンバー2021-12-310001682852米国会計基準:現金および現金同等物メンバー米国会計基準:現金および現金同等物メンバー米国会計基準:フェアバリューインプットレベル1メンバー2021-12-310001682852米国会計基準:現金および現金同等物メンバーMrNA: 現在の有価証券のメンバー米国会計基準:フェアバリューインプットレベル1メンバー2021-12-310001682852米国会計基準:現金および現金同等物メンバーNA氏:非流動有価証券会員米国会計基準:フェアバリューインプットレベル1メンバー2021-12-310001682852米国会計基準:預金証書メンバー米国会計基準:公正価値インプットレベル2メンバー2021-12-310001682852米国会計基準:預金証書メンバー米国会計基準:現金および現金同等物メンバー米国会計基準:公正価値インプットレベル2メンバー2021-12-310001682852MrNA: 現在の有価証券のメンバー米国会計基準:預金証書メンバー米国会計基準:公正価値インプットレベル2メンバー2021-12-310001682852NA氏:非流動有価証券会員米国会計基準:預金証書メンバー米国会計基準:公正価値インプットレベル2メンバー2021-12-310001682852米国会計基準:米国財務省証券会員米国会計基準:公正価値インプットレベル2メンバー2021-12-310001682852米国会計基準:米国財務省証券会員米国会計基準:現金および現金同等物メンバー米国会計基準:公正価値インプットレベル2メンバー2021-12-310001682852米国会計基準:米国財務省証券会員MrNA: 現在の有価証券のメンバー米国会計基準:公正価値インプットレベル2メンバー2021-12-310001682852NA氏:非流動有価証券会員米国会計基準:米国財務省証券会員米国会計基準:公正価値インプットレベル2メンバー2021-12-310001682852米国会計基準:米国政府機関債務証券メンバー米国会計基準:公正価値インプットレベル2メンバー2021-12-310001682852米国会計基準:現金および現金同等物メンバー米国会計基準:公正価値インプットレベル2メンバー米国会計基準:米国政府機関債務証券メンバー2021-12-310001682852MrNA: 現在の有価証券のメンバー米国会計基準:公正価値インプットレベル2メンバー米国会計基準:米国政府機関債務証券メンバー2021-12-310001682852NA氏:非流動有価証券会員米国会計基準:公正価値インプットレベル2メンバー米国会計基準:米国政府機関債務証券メンバー2021-12-310001682852米国会計基準:企業債務証券メンバー米国会計基準:公正価値インプットレベル2メンバー2021-12-310001682852米国会計基準:企業債務証券メンバー米国会計基準:現金および現金同等物メンバー米国会計基準:公正価値インプットレベル2メンバー2021-12-310001682852MrNA: 現在の有価証券のメンバー米国会計基準:企業債務証券メンバー米国会計基準:公正価値インプットレベル2メンバー2021-12-310001682852NA氏:非流動有価証券会員米国会計基準:企業債務証券メンバー米国会計基準:公正価値インプットレベル2メンバー2021-12-310001682852米国会計基準:米国政府債務証券メンバー米国会計基準:公正価値インプットレベル2メンバー2021-12-310001682852米国会計基準:米国政府債務証券メンバー米国会計基準:現金および現金同等物メンバー米国会計基準:公正価値インプットレベル2メンバー2021-12-310001682852MrNA: 現在の有価証券のメンバー米国会計基準:米国政府債務証券メンバー米国会計基準:公正価値インプットレベル2メンバー2021-12-310001682852NA氏:非流動有価証券会員米国会計基準:米国政府債務証券メンバー米国会計基準:公正価値インプットレベル2メンバー2021-12-310001682852米国会計基準:公正価値インプットレベル2メンバー2021-12-310001682852米国会計基準:現金および現金同等物メンバー米国会計基準:公正価値インプットレベル2メンバー2021-12-310001682852MrNA: 現在の有価証券のメンバー米国会計基準:公正価値インプットレベル2メンバー2021-12-310001682852NA氏:非流動有価証券会員米国会計基準:公正価値インプットレベル2メンバー2021-12-310001682852米国会計基準:米国財務省証券会員2022-06-300001682852US-GAAP: 米国財務省証券会員2022-06-300001682852米国会計基準:企業債務証券メンバー2022-06-300001682852米国会計基準:米国政府債務証券メンバー2022-06-300001682852米国会計基準:米国財務省証券会員2021-12-310001682852US-GAAP: 米国財務省証券会員2021-12-310001682852米国会計基準:企業債務証券メンバー2021-12-310001682852米国会計基準:米国政府債務証券メンバー2021-12-31MRNA: セキュリティ0001682852US-GAAP: マネー・マーケット・ファンド・メンバー米国会計基準:公正価値測定経常委員2022-06-300001682852US-GAAP: マネー・マーケット・ファンド・メンバー米国会計基準:公正価値測定経常委員米国会計基準:フェアバリューインプットレベル1メンバー2022-06-300001682852US-GAAP: マネー・マーケット・ファンド・メンバー米国会計基準:公正価値測定経常委員米国会計基準:公正価値インプットレベル2メンバー2022-06-300001682852米国会計基準:預金証書メンバー米国会計基準:公正価値測定経常委員2022-06-300001682852米国会計基準:預金証書メンバー米国会計基準:公正価値測定経常委員米国会計基準:フェアバリューインプットレベル1メンバー2022-06-300001682852米国会計基準:預金証書メンバー米国会計基準:公正価値測定経常委員米国会計基準:公正価値インプットレベル2メンバー2022-06-300001682852米国会計基準:米国財務省証券会員米国会計基準:公正価値測定経常委員2022-06-300001682852米国会計基準:米国財務省証券会員米国会計基準:公正価値測定経常委員米国会計基準:フェアバリューインプットレベル1メンバー2022-06-300001682852米国会計基準:米国財務省証券会員米国会計基準:公正価値測定経常委員米国会計基準:公正価値インプットレベル2メンバー2022-06-300001682852米国会計基準:公正価値測定経常委員米国会計基準:米国政府機関債務証券メンバー2022-06-300001682852米国会計基準:公正価値測定経常委員米国会計基準:米国政府機関債務証券メンバー米国会計基準:フェアバリューインプットレベル1メンバー2022-06-300001682852米国会計基準:公正価値測定経常委員米国会計基準:公正価値インプットレベル2メンバー米国会計基準:米国政府機関債務証券メンバー2022-06-300001682852米国会計基準:企業債務証券メンバー米国会計基準:公正価値測定経常委員2022-06-300001682852米国会計基準:企業債務証券メンバー米国会計基準:公正価値測定経常委員米国会計基準:フェアバリューインプットレベル1メンバー2022-06-300001682852米国会計基準:企業債務証券メンバー米国会計基準:公正価値測定経常委員米国会計基準:公正価値インプットレベル2メンバー2022-06-300001682852米国会計基準:米国政府債務証券メンバー米国会計基準:公正価値測定経常委員2022-06-300001682852米国会計基準:米国政府債務証券メンバー米国会計基準:公正価値測定経常委員米国会計基準:フェアバリューインプットレベル1メンバー2022-06-300001682852米国会計基準:米国政府債務証券メンバー米国会計基準:公正価値測定経常委員米国会計基準:公正価値インプットレベル2メンバー2022-06-300001682852米国会計基準:公正価値測定経常委員2022-06-300001682852米国会計基準:公正価値測定経常委員米国会計基準:フェアバリューインプットレベル1メンバー2022-06-300001682852米国会計基準:公正価値測定経常委員米国会計基準:公正価値インプットレベル2メンバー2022-06-300001682852US-GAAP: マネー・マーケット・ファンド・メンバー米国会計基準:公正価値測定経常委員2021-12-310001682852US-GAAP: マネー・マーケット・ファンド・メンバー米国会計基準:公正価値測定経常委員米国会計基準:フェアバリューインプットレベル1メンバー2021-12-310001682852US-GAAP: マネー・マーケット・ファンド・メンバー米国会計基準:公正価値測定経常委員米国会計基準:公正価値インプットレベル2メンバー2021-12-310001682852米国会計基準:預金証書メンバー米国会計基準:公正価値測定経常委員2021-12-310001682852米国会計基準:預金証書メンバー米国会計基準:公正価値測定経常委員米国会計基準:フェアバリューインプットレベル1メンバー2021-12-310001682852米国会計基準:預金証書メンバー米国会計基準:公正価値測定経常委員米国会計基準:公正価値インプットレベル2メンバー2021-12-310001682852米国会計基準:米国財務省証券会員米国会計基準:公正価値測定経常委員2021-12-310001682852米国会計基準:米国財務省証券会員米国会計基準:公正価値測定経常委員米国会計基準:フェアバリューインプットレベル1メンバー2021-12-310001682852米国会計基準:米国財務省証券会員米国会計基準:公正価値測定経常委員米国会計基準:公正価値インプットレベル2メンバー2021-12-310001682852米国会計基準:公正価値測定経常委員米国会計基準:米国政府機関債務証券メンバー2021-12-310001682852米国会計基準:公正価値測定経常委員米国会計基準:米国政府機関債務証券メンバー米国会計基準:フェアバリューインプットレベル1メンバー2021-12-310001682852米国会計基準:公正価値測定経常委員米国会計基準:公正価値インプットレベル2メンバー米国会計基準:米国政府機関債務証券メンバー2021-12-310001682852米国会計基準:企業債務証券メンバー米国会計基準:公正価値測定経常委員2021-12-310001682852米国会計基準:企業債務証券メンバー米国会計基準:公正価値測定経常委員米国会計基準:フェアバリューインプットレベル1メンバー2021-12-310001682852米国会計基準:企業債務証券メンバー米国会計基準:公正価値測定経常委員米国会計基準:公正価値インプットレベル2メンバー2021-12-310001682852米国会計基準:米国政府債務証券メンバー米国会計基準:公正価値測定経常委員2021-12-310001682852米国会計基準:米国政府債務証券メンバー米国会計基準:公正価値測定経常委員米国会計基準:フェアバリューインプットレベル1メンバー2021-12-310001682852米国会計基準:米国政府債務証券メンバー米国会計基準:公正価値測定経常委員米国会計基準:公正価値インプットレベル2メンバー2021-12-310001682852米国会計基準:公正価値測定経常委員2021-12-310001682852米国会計基準:公正価値測定経常委員米国会計基準:フェアバリューインプットレベル1メンバー2021-12-310001682852米国会計基準:公正価値測定経常委員米国会計基準:公正価値インプットレベル2メンバー2021-12-310001682852米国会計基準:キャッシュフロー・ヘッジングメンバー米国会計基準:ヘッジング・インストゥルメント・メンバーに指定米国会計基準:外国為替契約メンバー2022-06-300001682852米国会計基準:非指定メンバー米国会計基準:外国為替契約メンバー2022-06-300001682852米国会計基準:キャッシュフロー・ヘッジングメンバー米国会計基準:ヘッジング・インストゥルメント・メンバーに指定米国会計基準:外国為替契約メンバー2021-12-310001682852米国会計基準:非指定メンバー米国会計基準:外国為替契約メンバー2021-12-310001682852米国会計基準:セールスメンバー米国会計基準:外国為替契約メンバー2022-04-012022-06-300001682852米国会計基準:セールスメンバー米国会計基準:外国為替契約メンバー2021-04-012021-06-300001682852米国会計基準:セールスメンバー米国会計基準:外国為替契約メンバー2022-01-012022-06-300001682852米国会計基準:セールスメンバー米国会計基準:外国為替契約メンバー2021-01-012021-06-300001682852米国会計基準:その他の営業外収益費用構成メンバー米国会計基準:外国為替契約メンバー2022-04-012022-06-300001682852米国会計基準:その他の営業外収益費用構成メンバー米国会計基準:外国為替契約メンバー2021-04-012021-06-300001682852米国会計基準:その他の営業外収益費用構成メンバー米国会計基準:外国為替契約メンバー2022-01-012022-06-300001682852米国会計基準:その他の営業外収益費用構成メンバー米国会計基準:外国為替契約メンバー2021-01-012021-06-300001682852米国会計基準:機器メンバー2022-06-300001682852米国会計基準:機器メンバー2021-12-310001682852米国会計基準:リースホールド改善メンバー2022-06-300001682852米国会計基準:リースホールド改善メンバー2021-12-310001682852US-GAAP: 不動産プラントおよび設備その他のタイプメンバー2022-06-300001682852US-GAAP: 不動産プラントおよび設備その他のタイプメンバー2021-12-310001682852米国会計基準:コンピュータ機器メンバー2022-06-300001682852米国会計基準:コンピュータ機器メンバー2021-12-310001682852US-GAAP: ソフトウェア開発メンバー2022-06-300001682852US-GAAP: ソフトウェア開発メンバー2021-12-310001682852NAさん:資産会員の財務権2022-06-300001682852NAさん:資産会員の財務権2021-12-310001682852米国会計基準:建設中メンバー2022-06-300001682852米国会計基準:建設中メンバー2021-12-310001682852米国会計基準:補助金メンバー2021-12-310001682852米国会計基準:補助金メンバー2022-06-300001682852MrNA: コラボレーションアレンジメントメンバー2021-12-310001682852MrNA: コラボレーションアレンジメントメンバー2022-06-30MRNA: キャンパス0001682852NA氏:マサチューセッツ州ケンブリッジのメンバー2022-06-30UTR: 平方フィート0001682852ナ氏:MTCサウス、MTCノース、MTCイーストのメンバーMr Na: マサチューセッツ州ノーウッドのメンバー2022-06-30Naさん:建物の数0001682852ナさん:MTCサウスメンバーMr Na: マサチューセッツ州ノーウッドのメンバー2022-06-300001682852Mr Na: マサチューセッツ州ノーウッドのメンバーナ氏:MTCノースメンバー2022-06-300001682852ナ氏:東山会員Mr Na: マサチューセッツ州ノーウッドのメンバー2022-06-300001682852ナ氏:MTCサウス、MTCノース、MTCイーストのメンバー2022-06-30NAさん:延長期間の数0001682852NAさん:組み込みリースメンバー2022-06-300001682852NAさん:組み込みリースメンバー2021-12-310001682852NA氏:供給・製造契約メンバー2022-06-300001682852NAさん:臨床サービスメンバー2022-06-300001682852MRNA: 臨床手術およびサポートコミットメントメンバー2022-06-300001682852NAさん:現代科学センター会員2022-06-300001682852NAさん:現代科学センター会員2022-01-012022-06-300001682852米国会計基準:従業員ストックオプションメンバー2022-04-012022-06-300001682852米国会計基準:従業員ストックオプションメンバー2021-04-012021-06-300001682852米国会計基準:従業員ストックオプションメンバー2022-01-012022-06-300001682852米国会計基準:従業員ストックオプションメンバー2021-01-012021-06-300001682852MRNA: 制限付株式と制限付株式ユニット RSU メンバー2022-04-012022-06-300001682852MRNA: 制限付株式と制限付株式ユニット RSU メンバー2021-04-012021-06-300001682852MRNA: 制限付株式と制限付株式ユニット RSU メンバー2022-01-012022-06-300001682852MRNA: 制限付株式と制限付株式ユニット RSU メンバー2021-01-012021-06-300001682852米国会計基準:従業員株式会員2022-04-012022-06-300001682852米国会計基準:従業員株式会員2021-04-012021-06-300001682852米国会計基準:従業員株式会員2022-01-012022-06-300001682852米国会計基準:従業員株式会員2021-01-012021-06-300001682852米国会計基準:売上原価メンバー2022-04-012022-06-300001682852米国会計基準:売上原価メンバー2021-04-012021-06-300001682852米国会計基準:売上原価メンバー2022-01-012022-06-300001682852米国会計基準:売上原価メンバー2021-01-012021-06-300001682852米国会計基準:研究開発費メンバー2022-04-012022-06-300001682852米国会計基準:研究開発費メンバー2021-04-012021-06-300001682852米国会計基準:研究開発費メンバー2022-01-012022-06-300001682852米国会計基準:研究開発費メンバー2021-01-012021-06-300001682852米国会計基準:一般管理費メンバー2022-04-012022-06-300001682852米国会計基準:一般管理費メンバー2021-04-012021-06-300001682852米国会計基準:一般管理費メンバー2022-01-012022-06-300001682852米国会計基準:一般管理費メンバー2021-01-012021-06-300001682852NA氏:2021年の買戻しプログラムのメンバーです2021-08-020001682852NA氏:2022年の買戻しプログラムのメンバーです2022-02-220001682852NA氏:2022年の買戻しプログラムのメンバーです2022-01-012022-06-300001682852NA氏:2021年の買戻しプログラムのメンバーです2022-01-012022-06-300001682852NA氏:2022年の買戻しプログラムのメンバーです2022-06-30エクセルリ:ピュア0001682852米国会計基準:後任イベントメンバー2022-07-282022-07-28MRNA: 用量0001682852米国会計基準:後任イベントメンバー2022-08-012022-08-010001682852Na氏:2022年の2回目の買戻しプログラムメンバー米国会計基準:後任イベントメンバー2022-08-01 米国
証券取引委員会
ワシントンD.C. 20549
(マークワン)
☒ 1934年の証券取引法のセクション13または15 (d) に基づく四半期報告書
四半期終了時 2022年6月30日
または
☐1934年の証券取引法第13条または第15 (d) 条に基づく移行報告書
_ から _ への移行期間
コミッションファイル番号: 001-38753
株式会社モデルナ
(憲章に明記されている登録者の正確な名前)
| | | | | | | | | | | |
| デラウェア州 | | 81-3467528 |
| (法人または組織の州またはその他の管轄区域) | | (IRS 雇用者識別番号) |
| | | |
| 200 テクノロジースクエア | | |
| ケンブリッジ、 | マサチューセッツ | | 02139 |
| (主要執行機関の住所) | | (郵便番号) |
(617) 714-6500
(登録者の電話番号、市外局番を含む)
同法第12条 (b) に従って登録された証券:
| | | | | | | | |
| 各クラスのタイトル | 取引シンボル | 登録された各取引所の名前 |
| 普通株式、額面価格1株あたり0.0001ドル | MRNA | ナスダック・ストック・マーケットLLC |
登録者が (1) 1934年の証券取引法第13条または第15条 (d) 条により提出が義務付けられているすべての報告書を過去12か月間(または登録者がそのような報告を提出する必要があったほど短い期間)に提出したかどうか、および(2)過去90日間にそのような申告要件の対象であったかどうかをチェックマークで示してください。 はい☒ いいえ ☐
登録者が、過去 12 か月間(または登録者がそのようなファイルの提出を求められたほど短い期間)に、規則 S-T の規則 405(本章の § 232.405)に従って提出する必要のあるすべてのインタラクティブデータファイルを電子的に提出したかどうかをチェックマークで示してください。 はい☒ いいえ ☐
登録者が大規模な加速申告者、加速申告者、非加速申告者、小規模報告会社、または新興成長企業のいずれであるかをチェックマークで示してください。取引法規則12b-2の「大規模加速申告者」、「優先申告者」、「小規模報告会社」、「新興成長企業」の定義を参照してください。
| | | | | | | | | | | | | | | | | | | | | | | | | | |
| 大型加速フィルター | ☒ | | アクセラレーテッド・ファイラー o | | 非加速ファイラー o | | 小規模な報告会社 | ☐ |
| | | | | | | 新興成長企業 | ☐ |
新興成長企業の場合は、登録者が取引法第13条 (a) に従って規定された新規または改訂された財務会計基準を遵守するために延長された移行期間を使用しないことを選択したかどうかをチェックマークで示してください。☐
登録者がシェル会社(同法の規則12b-2で定義されている)であるかどうかをチェックマークで示してください。 はい ☐いいえ ☒
2022年7月29日の時点で、 391,199,544登録者の普通株式、額面1株あたり0.0001ドル、発行済の普通株式。
将来の見通しに関する記述に関する特記事項
このForm 10-Q(Form 10-Q)の四半期報告書には、明示的または黙示的な将来の見通しに関する記述が含まれています。このフォーム10-Qに含まれる歴史的事実以外のすべての記述は、当社の経営陣の信念と仮定、および経営陣が現在入手可能な情報に基づいています。このフォーム10-Qの将来の見通しに関する記述には、以下に関する記述が含まれますが、これらに限定されません。
•COVID-19ワクチンに関する当社の活動、およびSARS-CoV-2ウイルスの変異株に対応して開発する可能性のあるブースターを含む次世代のCOVID-19ワクチンに関する計画と期待、進行中の臨床開発、製造と供給、価格設定、商品化、承認された場合、規制事項(ワクチンの投与量、追加薬の承認または承認を含む)、COVID-19ワクチンの需要、第三者および政府の取り決めと潜在的な取り決めと潜在的な取り決めなど。
•第三者のサプライヤー、流通業者、製造業者と契約する当社の能力と、特に許可があれば、変異型追加ワクチン候補を含む当社のCOVID-19ワクチンのタイムリーな製造と納品に関して、それらの能力が適切に行えます。
•当社の能力と、当社の商用製品を大規模に製造する契約を結んでいる第三者の能力、ならびに原薬、配送手段、開発候補、および前臨床および臨床使用のための治験薬の製造を成功させる能力。
•社内外のCOVID-19ワクチンを含む当社製品の製造拡大に関連する費用、および当社のCOVID-19ワクチンの製造に関連する第三者の製造業者またはサプライヤーとの関係または契約の終了または終了に関連する費用。
•当社の商用製品、治験薬、技術を対象とする知的財産権について、当社が確立および維持できる保護範囲。
•当社の研究開発プログラム、現在および将来の前臨床研究と臨床試験の開始、時期、進捗、結果、費用。これには、研究または試験および関連する準備作業の開始と完了、試験の結果が発表される期間、および研究開発プログラムに関する記述が含まれます。
•COVID-19パンデミックまたは将来の大規模な健康有害事象の直接的または間接的な影響に関連するリスク。たとえば、発生の範囲と期間、それに対応して実施される政府の措置と制限措置、開発候補と治験薬によって対処できる可能性のある疾患の診断、開始、治療継続、または臨床試験、潜在的な臨床試験、規制審査、またはサプライチェーンの混乱への患者登録における重大な遅れ、および当社の事業へのその他の潜在的な影響はパンデミックの影響を緩和するために当社が講じた措置の有効性または適時性、およびCOVID-19パンデミックまたは将来の大規模な健康障害によって引き起こされる混乱に対処するための事業継続計画を実行する能力。
•COVID-19パンデミックの影響により開発が遅れる可能性のある開発候補薬や治験薬について、特に連邦政府がそのような資源の転用を要求する場合、私たちのリソースをCOVID-19ワクチンの取り組みに大幅に転用することが含まれます。
•研究の優先順位を特定し、リスク軽減戦略を適用して、開発候補と治験薬を効率的に発見・開発する能力。これには、あるプログラムから学んだことを他のプログラムに、あるモダリティから別のモダリティに応用することも含まれます。
•治験薬に関する規制当局の承認を取得し、維持する当社の能力
•承認されれば、当社の製品を商品化する能力。
•当社の医薬品の価格設定と払い戻し(承認された場合)
•私たちのビジネスモデルと、私たちの事業、治験薬、技術に関する戦略計画の実施。
•将来の経費、収益、資本要件、および追加資金の必要性の見積もり
•戦略的協力契約の潜在的なメリット、戦略的協力や取り決めを締結する能力、開発、規制、商業化の専門知識を持つ協力者を引き付ける能力。
•当社の治験薬の商業化に関連する第三者との将来の契約(承認された場合)
•当社の治験薬市場の規模と成長の可能性、およびそれらの市場へのサービス能力。
•当社の財務実績
•当社の治験薬が市場で受け入れられている割合と程度。
•米国および海外における法的および規制上の進展。
•納期や製造コストの面で有利な製品や治験薬を製造する当社の能力。
•利用可能な、または利用可能になる可能性のある競合治療法の成功。
•主要な科学または管理職の人材を引き付けて維持する当社の能力、および
•競合他社や業界に関する進展。
将来の見通しに関する記述には、「する」、「可能性がある」、「すべき」、「期待する」、「意図」、「計画」、「目的」、「予想する」、「信じる」、「見積もる」、「潜在的」、「継続する」などの言葉が含まれることがよくありますが、すべての将来の見通しに関する記述にこれらの言葉が含まれているわけではありません。これらの将来の見通しに関する記述に反映されている期待は妥当だと考えていますが、これらの記述は将来の出来事、または当社の業務上または財務上の業績に関するものであり、リスク、不確実性、その他の要因を伴い、当社の実際の結果が、これらの将来の見通しに関する記述によって表明または暗示される将来の結果と大きく異なる可能性があります。したがって、これらの将来の見通しに関する記述に過度に依存すべきではありません。実際の結果が現在の予想と大きく異なる原因となる可能性のある要因には、とりわけ、「リスク要因」というタイトルのセクションやこのフォーム10-Qの他のセクションに記載されているものが含まれます。これらのリスクや不確実性の1つ以上が発生した場合、または当社の基礎となる仮定が正しくないことが判明した場合、実際の結果は将来の見通しに関する記述で明示または暗示されているものと大きく異なる可能性があります。
このフォーム10-Qの将来の見通しに関する記述は、このフォーム10-Qが発行された時点での当社の見解を表しています。当社は、適用される証券法で義務付けられている場合を除き、将来の見通しに関する記述を更新する義務を負わないものとします。したがって、これらの将来の見通しに関する記述を、このフォーム10-Qの日付以降の日付における当社の見解を表すものとして当てにしないでください。ただし、その後の証券取引委員会に提出する報告書で、関連する主題についてさらに開示された場合は、参照してください。
商標
このフォーム10-Qには、当社の商標およびその他の団体が所有する商標への言及が含まれています。あくまで便宜上、言及されている商標や商号は ®または™ の記号。ただし、そのような言及は、それぞれの所有者が適用法の下で最大限の範囲でそれに対する権利を主張しないことを示すことを意図したものではありません。私たちは、他社の商号や商標を参照して、他の企業との関係、他社による当社への推薦や後援を暗示することを意図していません。
会社の参考文献に関する注記
文脈上別段の定めがない限り、このForm 10-Qの「Moderna」、「当社」、「当社」という用語は、Moderna, Inc. とその連結子会社を指します。
追加情報
当社のウェブサイト(www.modernatx.com)には、投資家向け情報セクション(www.investors.modernatx.com)、企業ブログwww.modernatx.com/moderna-blog、およびソーシャルメディアチャンネル(Facebook、www.facebook.com/modernatx、Twitter、www.twitter.com/modernatx、Linkedin.com/company/modernatx)には、財務情報などを含む当社に関する大量の情報が含まれています。投資家向けの情報。情報は頻繁に更新され、新しい情報が共有されるため、投資家にはこれらのウェブサイトやソーシャルメディアチャネルにアクセスすることをお勧めします。当社のウェブサイト、企業ブログ、ソーシャルメディアチャネルに含まれる情報は、このフォーム10-Qに組み込まれたり、このフォーム10-Qの一部になったりしてはなりません。
目次
| | | | | | | | |
第一部。 | | ページ |
| アイテム 1. | 財務諸表 (未監査) | 5 |
| 2022年6月30日および2021年12月31日現在の要約連結貸借対照表 | 5 |
| 2022年6月30日および2021年6月30日までの3か月および6か月の要約連結損益計算書 | 6 |
| 2022年6月30日および2021年6月30日までの3か月および6か月間の要約連結包括利益計算書 | 7 |
| 2022年6月30日および2021年6月30日までの3か月および6か月間の要約連結株主資本計算書 | 9 |
| 2022年6月30日および2021年6月30日までの6か月間の要約連結キャッシュフロー計算書 | 10 |
| 要約連結財務諸表の注記 | 11 |
| アイテム 2. | 経営陣による財政状態と経営成績に関する議論と分析 | 29 |
| アイテム 3. | 市場リスクに関する定量的・質的開示 | 43 |
| アイテム 4. | 統制と手続き | 43 |
第二部 | | |
アイテム 1. | 法的手続き | 44 |
アイテム 1A. | リスク要因 | 44 |
アイテム 2. | 持分証券の未登録売却および収益の使用 | 45 |
| アイテム 6. | 展示品 | 45 |
署名 | | 47 |
アイテム 1.財務諸表
モデルナ株式会社
要約連結貸借対照表
(1株あたりのデータを除く、未監査、百万単位)
| | | | | | | | | | | |
| 6月30日 | | 12月31日 |
| 2022 | | 2021 |
資産 | | | |
流動資産: | | | |
現金および現金同等物 | $ | 2,873 | | | $ | 6,848 | |
投資 | 5,024 | | | 3,879 | |
売掛金 | 2,691 | | | 3,175 | |
| インベントリ | 1,921 | | | 1,441 | |
前払費用およびその他の流動資産 | 1,054 | | | 728 | |
流動資産合計 | 13,563 | | | 16,071 | |
投資、非流動投資 | 10,162 | | | 6,843 | |
資産および設備、純額 | 1,324 | | | 1,241 | |
| 使用権資産、オペレーティングリース | 122 | | | 142 | |
制限付現金、非流動現金 | 12 | | | 12 | |
| 繰延税金資産 | 785 | | | 326 | |
その他の非流動資産 | 75 | | | 34 | |
総資産 | $ | 26,043 | | | $ | 24,669 | |
負債と株主資本 | | | |
流動負債: | | | |
買掛金 | $ | 181 | | | $ | 302 | |
未払負債 | 1,780 | | | 1,472 | |
繰延収益 | 4,093 | | | 6,253 | |
| 支払うべき所得税 | 349 | | | 876 | |
その他の流動負債 | 409 | | | 225 | |
流動負債合計 | 6,812 | | | 9,128 | |
繰延収益、非流動収益 | 405 | | | 615 | |
| オペレーティングリース負債、非流動負債 | 87 | | | 106 | |
| ファイナンスリース負債、非流動性 | 641 | | | 599 | |
その他の非流動負債 | 113 | | | 76 | |
| 負債総額 | 8,058 | | | 10,524 | |
コミットメントと不測の事態 (ノート 12) | | | |
| 株主資本: | | | |
優先株式、額面価格 $0.0001; 1622022年6月30日および2021年12月31日に発行された株式が承認されました。 いいえ2022年6月30日および2021年12月31日に発行または発行された株式 | — | | | — | |
普通株式、額面価格 $0.0001; 1,6002022年6月30日および2021年12月31日に発行された株式が承認されました。 392そして 403それぞれ2022年6月30日および2021年12月31日の時点で発行された株式および発行済株式 | — | | | — | |
追加払込資本 | 2,413 | | | 4,211 | |
| その他の包括損失の累計 | (240) | | | (24) | |
| 利益剰余金 | 15,812 | | | 9,958 | |
株主資本の総額 | 17,985 | | | 14,145 | |
負債総額と株主資本 | $ | 26,043 | | | $ | 24,669 | |
添付の注記は、これらの未監査の要約連結財務諸表の不可欠な部分です。
モデルナ株式会社
要約連結損益計算書
(1株あたりのデータを除く、未監査、百万単位)
| | | | | | | | | | | | | | | | | | | | | | | | | | |
| | 6月30日に終了した3か月間 | | 6月30日に終了した6か月間 |
| | 2022 | | 2021 | | 2022 | | 2021 |
| 収益: | | | | | | | | |
| 製品販売 | | $ | 4,531 | | | $ | 4,197 | | | $ | 10,456 | | | $ | 5,930 | |
| 助成金収入 | | 183 | | | 139 | | | 309 | | | 333 | |
| コラボレーション収益 | | 35 | | | 18 | | | 50 | | | 28 | |
| 総収入 | | 4,749 | | | 4,354 | | | 10,815 | | | 6,291 | |
| 営業経費: | | | | | | | | |
| 売上原価 | | 1,381 | | | 750 | | | 2,398 | | | 943 | |
| 研究開発 | | 710 | | | 421 | | | 1,264 | | | 822 | |
| 販売、一般および管理 | | 211 | | | 121 | | | 479 | | | 198 | |
| 営業費用の合計 | | 2,302 | | | 1,292 | | | 4,141 | | | 1,963 | |
| 事業からの収入 | | 2,447 | | | 3,062 | | | 6,674 | | | 4,328 | |
| 利息収入 | | 40 | | | 3 | | | 55 | | | 7 | |
| その他の費用、純額 | | (13) | | | (2) | | | (26) | | | (12) | |
| 税引前利益 | | 2,474 | | | 3,063 | | | 6,703 | | | 4,323 | |
| 所得税引当金 | | 277 | | | 283 | | | 849 | | | 322 | |
| 当期純利益 | | $ | 2,197 | | | $ | 2,780 | | | $ | 5,854 | | | $ | 4,001 | |
| | | | | | | | |
| 一株当たり利益: | | | | | | | | |
| ベーシック | | $ | 5.55 | | | $ | 6.93 | | | $ | 14.66 | | | $ | 9.98 | |
| 希釈 | | $ | 5.24 | | | $ | 6.46 | | | $ | 13.85 | | | $ | 9.30 | |
| | | | | | | | |
| 1株当たり利益の計算に使用される加重平均普通株式: | | | | | | | | |
| ベーシック | | 396 | | | 402 | | | 399 | | | 401 | |
| 希釈 | | 419 | | | 431 | | | 423 | | | 430 | |
添付の注記は、これらの未監査の要約連結財務諸表の不可欠な部分です。
モデルナ株式会社
要約連結包括利益計算書
(未監査、百万単位)
| | | | | | | | | | | | | | | | | | | | | | | | | | | |
| | 6月30日に終了した3か月間 | | 6月30日に終了した6か月間 | |
| | 2022 | | 2021 | | 2022 | | 2021 | |
| 当期純利益 | | $ | 2,197 | | | $ | 2,780 | | | $ | 5,854 | | | $ | 4,001 | | |
| その他の包括利益(損失)利益(税引後): | | | | | | | | | |
| 販売可能な証券: | | | | | | | | | |
| 売却可能な債務証券の含み損失 | | (80) | | | (5) | | | (258) | | | (7) | | |
| 控除:純利益に再分類された売却可能有価証券の純実現損失(利益) | | 8 | | | (1) | | | 15 | | | (1) | | |
| 売却可能な負債による純減少 | | (72) | | | (6) | | | (243) | | | (8) | | |
| キャッシュフローヘッジ: | | | | | | | | | |
| デリバティブ商品の未実現利益 | | 46 | | | 21 | | | 71 | | | 21 | | |
| 控除:デリバティブ商品の純実現額(利益)が純利益に再分類されました | | (30) | | | — | | | (44) | | | — | | |
| ヘッジ商品として指定されたデリバティブによる純増額 | | 16 | | | 21 | | | 27 | | | 21 | | |
| その他の包括利益(損失)総額 | | (56) | | | 15 | | | (216) | | | 13 | | |
| 包括利益 | | $ | 2,141 | | | $ | 2,795 | | | $ | 5,638 | | | $ | 4,014 | | |
添付の注記は、これらの未監査の要約連結財務諸表の不可欠な部分です。
モデルナ株式会社
要約連結株主資本計算書
2022年6月30日および2021年6月30日までの3か月と6か月間
(未監査、百万単位)
| | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | |
| 普通株式 | | 追加払込資本 | | その他の包括損失の累計 | | 利益剰余金 | | 株主資本の総額 |
| 株式 | | 金額 | | | | |
| 2022年3月31日現在の残高 | 400 | | | $ | — | | | $ | 3,644 | | | $ | (184) | | | $ | 13,615 | | | $ | 17,075 | |
| | | | | | | | | | | |
| 普通株式購入オプションの行使 | 1 | | | — | | | 8 | | | — | | | — | | | 8 | |
| | | | | | | | | | | |
| 従業員株式購入プランに基づく普通株式の購入 | — | | | — | | | 9 | | | — | | | — | | | 9 | |
| 株式報酬制度 | — | | | — | | | 50 | | | — | | | — | | | 50 | |
| その他の包括損失(税引後) | — | | | — | | | — | | | (56) | | | — | | | (56) | |
| 普通株式の買戻し | (9) | | | — | | | (1,298) | | | — | | | — | | | (1,298) | |
| 当期純利益 | — | | | — | | | — | | | — | | | 2,197 | | | 2,197 | |
| 2022年6月30日時点の残高 | 392 | | | $ | — | | | $ | 2,413 | | | $ | (240) | | | $ | 15,812 | | | $ | 17,985 | |
| | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | |
| 普通株式 | | 追加払込資本 | | その他の包括利益の累計 | | 利益剰余金
(累積赤字) | | 株主資本の総額 |
| 株式 | | 金額 | | | | |
| 2021年3月31日時点の残高 | 401 | | | $ | — | | | $ | 4,860 | | | $ | 1 | | | $ | (1,023) | | | $ | 3,838 | |
| | | | | | | | | | | |
| | | | | | | | | | | |
| 普通株式購入オプションの行使 | 2 | | | — | | | 31 | | | — | | | — | | | 31 | |
| 従業員株式購入プランに基づく普通株式の購入 | — | | | — | | | 5 | | | — | | | — | | | 5 | |
| 株式報酬制度 | — | | | — | | | 35 | | | — | | | — | | | 35 | |
| その他の包括利益(税引後) | — | | | — | | | — | | | 15 | | | — | | | 15 | |
| 当期純利益 | — | | | — | | | — | | | — | | | 2,780 | | | 2,780 | |
| 2021年6月30日時点の残高 | 403 | | | $ | — | | | $ | 4,931 | | | $ | 16 | | | $ | 1,757 | | | $ | 6,704 | |
| | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | |
| 普通株式 | | 追加払込資本 | | その他の包括損失の累計 | | 利益剰余金 | | 株主資本の総額 |
| 株式 | | 金額 | | | | |
| 2021年12月31日時点の残高 | 403 | | | $ | — | | | $ | 4,211 | | | $ | (24) | | | $ | 9,958 | | | $ | 14,145 | |
| | | | | | | | | | | |
| 普通株式購入オプションの行使 | 2 | | | — | | | 20 | | | — | | | — | | | 20 | |
| | | | | | | | | | | |
| 従業員株式購入プランに基づく普通株式の購入 | — | | | — | | | 9 | | | — | | | — | | | 9 | |
| 株式報酬制度 | — | | | — | | | 94 | | | — | | | — | | | 94 | |
| その他の包括損失(税引後) | — | | | — | | | — | | | (216) | | | — | | | (216) | |
| 普通株式の買戻し | (13) | | | — | | | (1,921) | | | — | | | — | | | (1,921) | |
| 当期純利益 | — | | | — | | | — | | | — | | | 5,854 | | | 5,854 | |
| 2022年6月30日時点の残高 | 392 | | | $ | — | | | $ | 2,413 | | | $ | (240) | | | $ | 15,812 | | | $ | 17,985 | |
| | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | |
| 普通株式 | | 追加払込資本 | | その他の包括利益の累計 | | 利益剰余金
(累積赤字) | | 株主資本の総額 |
| 株式 | | 金額 | | | | |
| 2020年12月31日時点の残高 | 399 | | | $ | — | | | $ | 4,802 | | | $ | 3 | | | $ | (2,244) | | | $ | 2,561 | |
| | | | | | | | | | | |
| | | | | | | | | | | |
| 普通株式購入オプションの行使 | 4 | | | — | | | 59 | | | — | | | — | | | 59 | |
| 従業員株式購入プランに基づく普通株式の購入 | — | | | — | | | 5 | | | — | | | — | | | 5 | |
| 株式報酬制度 | — | | | — | | | 65 | | | — | | | — | | | 65 | |
| その他の包括利益(税引後) | — | | | — | | | — | | | 13 | | | — | | | 13 | |
| 当期純利益 | — | | | — | | | — | | | — | | | 4,001 | | | 4,001 | |
| 2021年6月30日時点の残高 | 403 | | | $ | — | | | $ | 4,931 | | | $ | 16 | | | $ | 1,757 | | | $ | 6,704 | |
添付の注記は、これらの未監査の要約連結財務諸表の不可欠な部分です。
モデルナ株式会社
要約連結キャッシュフロー計算書
(未監査、百万単位)
| | | | | | | | | | | |
| 6月30日に終了した6か月間 |
| 2022 | | 2021 |
営業活動 | | | |
| 当期純利益 | $ | 5,854 | | | $ | 4,001 | |
| 純利益を営業活動によって提供される純現金と調整するための調整: | | | |
株式報酬制度 | 94 | | | 65 | |
減価償却と償却 | 155 | | | 84 | |
投資の償却/増加 | 29 | | | 13 | |
| | | |
| 繰延所得税 | (376) | | | (72) | |
| その他の現金以外の商品 | 15 | | | — | |
資産と負債の変動: | | | |
売掛金 | 484 | | | (629) | |
前払費用およびその他の資産 | (324) | | | (110) | |
| インベントリ | (480) | | | (596) | |
使用権資産、オペレーティングリース | 20 | | | (14) | |
買掛金 | (56) | | | 44 | |
未払負債 | 305 | | | 367 | |
繰延収益 | (2,370) | | | 3,433 | |
| 支払うべき所得税 | (527) | | | 377 | |
オペレーティングリース負債 | (19) | | | 8 | |
その他の負債 | 263 | | | 63 | |
| 営業活動による純現金 | 3,067 | | | 7,034 | |
投資活動 | | | |
有価証券の購入 | (8,734) | | | (6,559) | |
有価証券の満期による収入 | 1,409 | | | 860 | |
有価証券の売却による収入 | 2,506 | | | 1,706 | |
資産および設備の購入 | (219) | | | (65) | |
| 転換社債への投資 | (35) | | | — | |
投資活動に使用された純現金 | (5,073) | | | (4,058) | |
資金調達活動 | | | |
| | | |
| エクイティプランによる普通株式の発行による収入 | 29 | | | 64 | |
| | | |
| 普通株式の買戻し | (1,921) | | | — | |
| ファイナンスリース負債の変化 | (77) | | | (62) | |
| 財務活動によって提供された純現金(使用量) | (1,969) | | | 2 | |
| 現金、現金同等物および制限付現金の純増加(減少) | (3,975) | | | 2,978 | |
現金、現金同等物および制限付現金、期初 | 6,860 | | | 2,636 | |
現金、現金同等物および制限付現金、期末 | $ | 2,885 | | | $ | 5,614 | |
非現金投資および資金調達活動 | | | |
買掛金および未払負債に含まれる資産および設備の購入 | $ | 49 | | | $ | 45 | |
| ファイナンスリースの変更と再評価により取得した使用権資産 | $ | — | | | $ | 363 | |
| リース負債の融資と引き換えに取得した使用権資産 | $ | 94 | | | $ | 126 | |
添付の注記は、これらの未監査の要約連結財務諸表の不可欠な部分です。
モデルナ株式会社
要約連結財務諸表の注記
(未監査)
1. 事業の説明
Moderna, Inc.(その連結子会社と合わせて、Moderna、当社、または当社のいずれか)は、メッセンジャーRNA(mRNA)治療薬とワクチンの先駆者であり、患者の生活を改善する新世代の革新的な医薬品を開発するバイオテクノロジー企業です。私たちのプラットフォームは、基礎および応用mRNA科学、デリバリー技術、製造における継続的な進歩に基づいて構築されており、新しい開発候補の強固なパイプラインを並行して追求する能力を備えています。私たちは、感染症、免疫腫瘍学、希少疾患、自己免疫疾患、心血管疾患の治療薬とワクチンを独立して、また戦略的協力者と共同で開発しています。
2020年12月18日、Spikevaxというブランド名で販売されているモデルナのCOVID-19ワクチン(mRNA-1273とも呼ばれる)の緊急使用について、米国食品医薬品局(FDA)から緊急使用許可(EUA)を受け取りました。®)18歳以上の個人を対象に、100 µgの初回シリーズを2回投与。2022年1月、米国で18歳以上の個人を対象にCOVID-19を予防するための100µgのプライマリシリーズを2回投与するスパイクバックスの商業的承認を受けました。スパイクバックスは、80か国以上で18歳以上の個人を対象に承認または認可されています。さらに、当社のCOVID-19ワクチンは、12〜17歳の青少年には100 µgの一次シリーズを2回投与、6歳から11歳の小児には50 µgの一次シリーズとして2回投与する承認を40か国以上のグローバル規制当局から受けています。さらに、米国、カナダ、オーストラリア、およびその他の管轄区域では、生後6か月から5歳までの幼児を対象に、25µgのCOVID-19ワクチンの2回接種の初回シリーズが承認されています。
FDA、欧州医薬品庁(EMA)、スイスメディック、その他世界中の保健機関は、18歳以上の成人を対象に、当社のCOVID-19ワクチンを50 µgの用量で追加接種することを承認しました。FDAやその他の保健機関も、50歳以上の成人とある種の免疫不全のある18歳以上の成人を対象に、50 µgの用量レベルで2回目の追加投与を許可しています。
2. 提示基準と最新の会計基準の要約
プレゼンテーションの基礎と統合の原則
これらの注記に添付されている添付の未監査の要約連結財務諸表は、米国の一般会計原則(GAAP)および中間財務報告に関する証券取引委員会(SEC)の適用規則および規制に従って作成されており、すべての重要な点において、2021年12月31日に終了した年度のForm 10-Kの年次報告書(2021 Form 10-K)に適用されているものと一致しています。これらの注記における該当するガイダンスへの言及は、財務会計基準審議会(FASB)の会計基準体系化(ASC)および会計基準更新(ASU)に記載されている、米国で一般に認められている正式な会計原則を参照することを意図しています。このレポートは、当社の2021年のForm 10-Kの監査済み連結財務諸表と併せて読む必要があります。
要約連結財務諸表には、モデルナ社とその子会社が含まれています。すべての会社間取引と残高は、連結により廃止されました。2022年6月30日までの3か月および6か月間の要約連結財務諸表の作成に使用された重要な会計方針は、当社の2021年のフォーム10-Kに記載されているものと一致しています。2022年6月30日までの3か月および6か月の経営成績は、必ずしも会計年度または将来の営業期間で予想される経営成績を示すものではありません。
見積もりの使用
要約連結財務諸表とそれに付随する注記に報告された金額に影響する見積もりと判断を行いました。私たちの見積もりは、過去の経験と、その状況下では妥当と思われるさまざまな関連仮定に基づいています。その結果に基づいて、財務諸表の日付における資産と負債の帳簿価額と、他の情報源からは容易にはわからない報告期間中に報告された収益と費用の金額を判断します。これらの財務諸表の作成に依拠する重要な見積もりには、収益認識、所得税、繰延税金資産の評価引当金、リース、金融商品の公正価値、デリバティブ金融商品、在庫、企業購買契約負債、資産および設備の耐用年数、研究開発費、および株式ベースの報酬に関連する重要な会計方針または見積もりが含まれますが、これらに限定されません。私たちが経験する実際の結果は、私たちの見積もりとは大きく異なる場合があります。
包括利益
包括利益には、当期の純利益とその他の包括利益/損失が含まれます。その他の包括損失は、ヘッジ手段として指定された当社の投資およびデリバティブの未実現損益です。表示されているすべての期間の包括利益の合計は、要約連結包括利益計算書に開示されています。
2022年6月30日までの3か月および6か月間のその他の包括損失の累積の構成要素は次のとおりです(百万単位)。
| | | | | | | | | | | | | | | | | |
| 売却可能債務証券の含み損失 | | ヘッジ商品として指定されたデリバティブの純未実現利益 | | 合計 |
| その他の包括損失の累計、2021年12月31日時点の残高 | $ | (40) | | | $ | 16 | | | $ | (24) | |
| その他の包括損失 | (171) | | | 11 | | | (160) | |
| その他の包括損失の累計、2022年3月31日時点の残高 | (211) | | | 27 | | | (184) | |
| その他の包括損失 | (72) | | | 16 | | | (56) | |
| その他の包括損失の累計、2022年6月30日時点の残高 | $ | (283) | | | $ | 43 | | | $ | (240) | |
| | | | | |
| | | | | |
| | | | | |
制限付き現金
制限付現金残高は、要約連結キャッシュフロー計算書の現金、現金同等物、および営業、投資、財務活動の制限付現金調整に含めています。
次の表は、要約連結貸借対照表にある現金、現金同等物、および制限付現金の調整を示しています。これらの合計は、要約連結キャッシュフロー計算書に示されている金額と同じ金額 (百万単位) になります。
| | | | | | | | | | | | | | |
| | 6月30日 |
| | 2022 | | 2021 |
| 現金および現金同等物 | | $ | 2,873 | | | $ | 5,603 | |
| | | | |
| 制限付現金、非現金 | | 12 | | | 11 | |
要約連結に表示されている現金、現金同等物、制限付現金の総額
キャッシュフロー計算書 | | $ | 2,885 | | | $ | 5,614 | |
最近発行された会計基準はまだ採用されていません
時々、FASBまたはその他の標準設定機関によって新しい会計申告書が発行され、指定された発効日をもって当社が採択します。特に説明しない限り、最近発行されたまだ有効ではない基準の影響は、当社の要約連結財務諸表や開示に重大な影響を与えることはないと考えています。
3. 製品販売
製品の販売は主に、米国政府、その他の国際政府、およびGAVI(COVAXファシリティに代わって)とのCOVID-19ワクチン供給契約に関連しています。
顧客の地理的位置別の製品売上は次のとおりです(百万単位)。
| | | | | | | | | | | | | | | | | | | | | | | | | | |
| | 6月30日に終了した3か月間 | | 6月30日に終了した6か月間 |
| | 2022 | | 2021 | | 2022 | | 2021 |
| 米国 | | $ | 1,450 | | | $ | 2,093 | | | $ | 2,395 | | | $ | 3,451 | |
| ヨーロッパ | | 1,390 | | | 1,056 | | | 3,466 | | | 1,340 | |
その他の地域 (1) | | 1,691 | | | 1,048 | | | 4,595 | | | 1,139 | |
| 合計 | | $ | 4,531 | | | $ | 4,197 | | | $ | 10,456 | | | $ | 5,930 | |
_______
(1) Gaviとの契約に基づいて認められた製品販売を含みます。これにより、世界中、特に低中所得国向けに、当社のCOVID-19ワクチンの配分と配布が容易になります。
2022年6月30日現在、当社のCOVID-19ワクチン(Spikevaxというブランド名で販売されている)は、使用が許可されている唯一の市販製品です。
2022年6月30日および2021年12月31日の時点で、当社の繰延収益はドルでした4.310億ドルと6.7それぞれ10億ドル、顧客の預金に関連しています。私たちは$を期待しています4.02022年6月30日現在の顧客預金に関連する当社の繰延収益のうち10億ドルは、1年以内に実現する予定です。製品の製造、納品、および市販承認の受領のタイミングによって、製品の売上が認められる期間が決まります。
4. 助成金収入
2020年9月、私たちは国防高等研究計画局(DARPA)と最大$の賞金に関する契約を締結しました。56治療薬やワクチンを迅速に製造できる既存の製造技術を活用したモバイル製造プロトタイプの開発に何百万ドルもの資金を提供します。2022年6月30日現在、コミットされた資金は、稼いだ収益を差し引いた額です。7百万。追加の $30DARPAが追加の契約オプションを行使すれば、何百万もの資金が利用可能になります。
2020年4月、私たちは米国保健社会福祉省(HHS)内の準備・対応担当次官補室の一部門である生物医学先端研究開発局(BARDA)と、最大$の賞金を出す契約を締結しました。483COVID-19に対するワクチン候補であるmRNA-1273の開発を加速するために何百万ドルも寄付します。この契約は2020年と2021年の両方で修正され、mRNA-1273のさまざまな後期段階の臨床開発活動を支援するための追加のコミットメントが規定されました。 30,000参加者:第3相試験、小児臨床試験、ファーマコビジランス研究。2022年3月、私たちはBARDA契約をさらに修正し、潜在的な償還額を$増やしました308100万ドル。これは、青年期および小児科の研究および第3相ピボタル研究の臨床開発に関連する費用に関連しています。2020年、2021年、2022年の改正を含め、BARDAから授与される最大裁定額はおよそ $1.710億。すべての契約オプションが行使されました。2022年6月30日現在、収益を差し引いた残りの利用可能な資金はs $203百万.
2016年9月、BARDAから最大$の賞を授与されました126百万、その後ドルに調整されました1172021年には100万ドルを、当社のジカワクチンプログラムへの資金提供に充てます。 三の 四契約オプションが行使されました。2022年6月30日現在、収益を差し引いた残りの利用可能な資金は、ドルでした42百万、追加のドルで8最終的な契約オプションが行使されれば、100万ユーロが利用可能になります。助成金の実施期間は2022年9月30日に満了し、満了時に残っている資金は没収されます。
2016年1月、私たちはビル・アンド・メリンダ・ゲイツ財団(ゲイツ財団)とグローバルヘルスプロジェクトの枠組み契約を締結しました。これは、ヒト免疫不全ウイルス(HIV)を含むさまざまな感染症のmRNAベースの開発プロジェクトを進めるためです。2022年6月30日現在、稼いだ収益を差し引いた利用可能な資金は、ドルでした7100万、最大1ドルの追加で80追加の後続プロジェクトが承認されれば、100万件が利用可能になります。
次の表は、提示された期間の助成金収入 (百万単位) をまとめたものです。
| | | | | | | | | | | | | | | | | | | | | | | |
| 6月30日に終了した3か月間 | | 6月30日に終了した6か月間 |
| 2022 | | 2021 | | 2022 | | 2021 |
| バルダ | $ | 179 | | | $ | 134 | | | $ | 301 | | | $ | 326 | |
| その他の助成金収入 | 4 | | | 5 | | | 8 | | | 7 | |
| 助成金の総収入は | $ | 183 | | | $ | 139 | | | $ | 309 | | | $ | 333 | |
5. コラボレーション契約
私たちは、治療分野にわたる潜在的なmRNA医薬品の発見と進歩を加速するために、戦略的協力者と協力契約を締結しました。2022年6月30日と2021年12月31日の時点で、アストラゼネカ社(アストラゼネカ)、メルク社(メルク)、バーテックス・ファーマシューティカルズ・インコーポレイテッド、バーテックス・ファーマシューティカルズ(ヨーロッパ)リミテッド(合わせてバーテックス)などとコラボレーション契約を結んでいます。これらの協力契約の詳細については、「第三者による戦略的提携」という見出しの下にある2021年のフォーム10-Kと、当社の連結財務諸表の注記5を参照してください。
次の表は、提示された期間における戦略的協力者からの連結収益の合計 (百万単位) をまとめたものです。
| | | | | | | | | | | | | | | | | | | | | | | |
| 6月30日に終了した3か月間 | | 6月30日に終了した6か月間 |
| 戦略的コラボレーター別のコラボレーション収益: | 2022 | | 2021 | | 2022 | | 2021 |
| アストラゼネカ | $ | 4 | | | $ | 4 | | | $ | 4 | | | $ | 4 | |
| メルク | 5 | | | 4 | | | 15 | | | 4 | |
| 頂点 | 25 | | | 9 | | | 29 | | | 18 | |
| その他 | 1 | | | 1 | | | 2 | | | 2 | |
| コラボレーション総収益 | $ | 35 | | | $ | 18 | | | $ | 50 | | | $ | 28 | |
次の表は、2022年6月30日までの6か月間の戦略的協力契約に関連する売掛金と契約負債の残高の変化(百万単位)を示しています。
| | | | | | | | | | | | | | | | | | | | | | | | | | |
| | 2021年12月31日 | | 追加 | | 控除 | | 2022年6月30日 |
| 契約資産: | | | | | | | | |
| 売掛金 | | $ | 9 | | | $ | 13 | | | $ | (11) | | | $ | 11 | |
| 契約負債: | | | | | | | | |
| 繰延収益 | | $ | 204 | | | $ | 6 | | | $ | (43) | | | $ | 167 | |
2022年6月30日現在、当社のコラボレーション契約に基づく履行義務に充当された取引価格のうち、履行不履行または一部履行されなかったものの合計金額はドルでした236百万。
上記のコラボレーション契約に加えて、現時点では、当社のビジネスにとって個人的には重要ではないと考えられる他の協力契約やライセンス契約もあります。これらの契約に従い、前払い、および開発、規制、および商業上のさまざまなマイルストーンの達成時に支払いを行う必要がある場合があり、これは合計するとかなりの額になる可能性があります。将来のマイルストーンの支払いがあれば、該当する事象が発生しそうになったときに、当社の連結財務諸表に反映されます。さらに、これらの取り決めに関連する製品が商品化された場合、将来の売上に対して多額のロイヤルティを支払う必要があるかもしれません。
6. 金融商品
現金および現金同等物および投資
次の表は、2022年6月30日と2021年12月31日時点の当社の現金と売却可能有価証券を重要な投資カテゴリー別にまとめたものです(百万単位)。
| | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | |
| | 2022年6月30日 |
| | 償却済み
費用 | | 未実現
利益 | | 未実現
損失 | | 推定公正価値 | | 現金と
現金
同等物 | | 現在の
市場性のある
証券 | | 非-
現在の
市場性のある
証券 |
| 現金および現金同等物 | | $ | 2,873 | | | $ | — | | | $ | — | | | $ | 2,873 | | | $ | 2,873 | | | $ | — | | | $ | — | |
| 売りに出されています: | | | | | | | | | | | | | | |
| 預金証書 | | 348 | | | — | | | — | | | 348 | | | — | | | 348 | | | — | |
| 米国財務省短期証券 | | 259 | | | — | | | (2) | | | 257 | | | — | | | 257 | | | — | |
| 米国財務省証券 | | 8,231 | | | — | | | (189) | | | 8,042 | | | — | | | 3,054 | | | 4,988 | |
| 企業債務証券 | | 6,597 | | | — | | | (181) | | | 6,416 | | | — | | | 1,352 | | | 5,064 | |
| 政府債務証券 | | 129 | | | — | | | (6) | | | 123 | | | — | | | 13 | | | 110 | |
| 合計 | | $ | 18,437 | | | $ | — | | | $ | (378) | | | $ | 18,059 | | | $ | 2,873 | | | $ | 5,024 | | | $ | 10,162 | |
| | | | | | | | | | | | | | |
| | 2021年12月31日 |
| | 償却済み
費用 | | 未実現
利益 | | 未実現
損失 | | 推定公正価値 | | 現金と
現金
同等物 | | 現在の
市場性のある
証券 | | 非-
現在の
市場性のある
証券 |
| 現金および現金同等物 | | $ | 6,848 | | | $ | — | | | $ | — | | | $ | 6,848 | | | $ | 6,848 | | | $ | — | | | $ | — | |
| 売りに出されています: | | | | | | | | | | | | | | |
| 預金証書 | | 80 | | | — | | | — | | | 80 | | | — | | | 80 | | | — | |
| 米国財務省短期証券 | | 479 | | | — | | | — | | | 479 | | | — | | | 479 | | | — | |
| 米国財務省証券 | | 6,595 | | | — | | | (31) | | | 6,564 | | | — | | | 1,984 | | | 4,580 | |
| 企業債務証券 | | 3,508 | | | — | | | (20) | | | 3,488 | | | — | | | 1,323 | | | 2,165 | |
| 政府債務証券 | | 112 | | | — | | | (1) | | | 111 | | | — | | | 13 | | | 98 | |
| 合計 | | $ | 17,622 | | | $ | — | | | $ | (52) | | | $ | 17,570 | | | $ | 6,848 | | | $ | 3,879 | | | $ | 6,843 | |
2022年6月30日と2021年12月31日の契約満期別の売却可能有価証券の償却費用と推定公正価値は次のとおりです(百万単位)。
| | | | | | | | | | | | | | |
| | 2022年6月30日 |
| | 償却済み
費用 | | 推定
公正価値 |
| 期限が1年以内 | | $ | 5,079 | | | $ | 5,024 | |
| 1年後から5年後に期限切れ | | 10,485 | | | 10,162 | |
| 合計 | | $ | 15,564 | | | $ | 15,186 | |
| | | | | | | | | | | | | | |
| | 2021年12月31日 |
| | 償却済み
費用 | | 推定
公正価値 |
| 期限が1年以内 | | $ | 3,882 | | | $ | 3,879 | |
| 1年後から5年後に期限切れ | | 6,892 | | | 6,843 | |
| 合計 | | $ | 10,774 | | | $ | 10,722 | |
当社の投資方針に従い、信用力の高い発行体による投資適格証券に投資し、通常、信用エクスポージャーの額は発行者1社に限定しています。各報告期間の終わりに、有価証券の減損評価を行います。障害は多くの要因を考慮して評価され、その相対的な重要性は状況によって異なります。
考慮される要因には、償却原価基準を下回る公正価値の下落が信用関連要因によるものか非信用関連要因によるものか、発行体の財政状態と短期的な見通し、予想される公正価値の回復に備えて投資を保有する当社の意図と能力などがあります。信用に関連しない減損は、適用される税金を差し引いたその他の包括的損失に計上されます。信用関連の減損は、貸借対照表上の引当金として計上され、それに応じて収益が調整されます。やりました いいえ2022年6月30日および2021年6月30日までの3か月および6か月間の販売可能有価証券に関連する減損費用は計上されません。やりました いいえ2022年6月30日および2021年12月31日の時点で、販売可能な有価証券に対するクレジット関連の引当金を記録します。
次の表は、2022年6月30日と2021年12月31日の時点で有価証券が未実現損失ポジションにあった期間別に、未実現損失ポジションにある当社の売却可能有価証券の未実現損失総額と推定公正価値(百万単位)をまとめたものです。
| | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | |
| | 12 か月未満 | | 12 か月以上 | | 合計 |
| | 未実現損失総額 | | 推定公正価値 | | 未実現損失総額 | | 推定公正価値 | | 未実現損失総額 | | 推定公正価値 |
2022年6月30日現在: | | | | | | | | | | | | |
| | | | | | | | | | | | |
| 米国財務省短期証券 | | $ | (2) | | | $ | 256 | | | $ | — | | | $ | — | | | $ | (2) | | | $ | 256 | |
| 米国財務省証券 | | (185) | | | 7,873 | | | (4) | | | 132 | | | (189) | | | 8,005 | |
| 企業債務証券 | | (164) | | | 5,388 | | | (17) | | | 385 | | | (181) | | | 5,773 | |
| 政府債務証券 | | (6) | | | 123 | | | — | | | — | | | (6) | | | 123 | |
| 合計 | | $ | (357) | | | $ | 13,640 | | | $ | (21) | | | $ | 517 | | | $ | (378) | | | $ | 14,157 | |
| | | | | | | | | | | | |
2021年12月31日現在: | | | | | | | | | | | | |
| | | | | | | | | | | | |
| 米国財務省短期証券 | | $ | — | | | $ | 329 | | | $ | — | | | $ | — | | | $ | — | | | $ | 329 | |
| 米国財務省証券 | | (31) | | | 6,332 | | | — | | | — | | | (31) | | | 6,332 | |
| 企業債務証券 | | (20) | | | 2,573 | | | — | | | 1 | | | (20) | | | 2,574 | |
| 政府債務証券 | | (1) | | | 112 | | | — | | | — | | | (1) | | | 112 | |
| 合計 | | $ | (52) | | | $ | 9,346 | | | $ | — | | | $ | 1 | | | $ | (52) | | | $ | 9,347 | |
2022年6月30日と2021年12月31日に開催しました 634そして 384当社の全投資ポートフォリオのうち、未実現損失が続いていた売出し可能な証券。私たちはこれらの投資を売却するつもりはありません。また、帳簿価額が回復する前に売却しなければならないと結論付ける可能性も高いとは考えていません。また、満期時に当社に支払うべき元本と利息の両方を回収できると考えています。
経常的に公正価値で測定される資産および負債
資産と負債の評価に使用される観察可能なインプットと観察不可能なインプットに基づいて資産と負債を分類するには、次の公正価値階層を使用します。
•レベル1:同一の無制限資産または負債について、測定日時点で入手可能な、活発な市場における調整前の相場価格
•レベル2: 活発な市場における類似の資産と負債の相場価格、活発でない市場の相場価格、または資産または負債のほぼ全期間にわたって、直接的または間接的に観察可能なインプット。または
•レベル3: 公正価値の測定にとって重要であり、かつ観察不能な(つまり、市場活動がほとんど、またはまったくサポートされていない)インプットを必要とする価格または評価手法。
次の表は、2022年6月30日および2021年12月31日現在の当社の金融資産と負債を公正価値で経常的に測定したもの(百万単位)をまとめたものです。
| | | | | | | | | | | | | | | | | | | | |
| | 2022年6月30日時点の公正価値 | | を使用した公正価値の測定 |
| | | レベル 1 | | レベル 2 |
| 資産: | | | | | | |
| マネー・マーケット・ファンド | | $ | 1,242 | | | $ | 1,242 | | | $ | — | |
| 預金証書 | | 348 | | | — | | | 348 | |
| 米国財務省短期証券 | | 257 | | | — | | | 257 | |
| 米国財務省証券 | | 8,042 | | | — | | | 8,042 | |
| 企業債務証券 | | 6,416 | | | — | | | 6,416 | |
| 政府債務証券 | | 123 | | | — | | | 123 | |
デリバティブ商品 (ノート 7) | | 58 | | | — | | | 58 | |
| 合計 | | $ | 16,486 | | | $ | 1,242 | | | $ | 15,244 | |
| 負債: | | | | | | |
デリバティブ商品 (ノート 7) | | $ | 2 | | | $ | — | | | $ | 2 | |
| | | | | | | | | | | | | | | | | | | | |
| | 2021年12月31日時点の公正価値 | | を使用した公正価値の測定 |
| | | レベル 1 | | レベル 2 |
| 資産: | | | | | | |
| マネー・マーケット・ファンド | | $ | 2,329 | | | $ | 2,329 | | | $ | — | |
| 預金証書 | | 80 | | | — | | | 80 | |
| 米国財務省短期証券 | | 479 | | | — | | | 479 | |
| 米国財務省証券 | | 6,564 | | | — | | | 6,564 | |
| 企業債務証券 | | 3,488 | | | — | | | 3,488 | |
| 政府債務証券 | | 111 | | | — | | | 111 | |
デリバティブ商品 (ノート 7) | | 21 | | | — | | | 21 | |
| 合計 | | $ | 13,072 | | | $ | 2,329 | | | $ | 10,743 | |
| 負債: | | | | | | |
デリバティブ商品 (ノート 7) | | $ | 7 | | | $ | — | | | $ | 7 | |
2022年6月30日および2021年12月31日現在、当社には定期的な公正価値で測定された非金融資産または負債はなく、レベル3の金融資産または金融負債もありませんでした。
また、2022年6月30日の時点で、私たちにはドルがありました30容易に決定できる公正価値のない株式投資。これらは当社の要約連結貸借対照表の他の非流動資産に記録され、上記の公正価値測定表からは除外されています。やりました じゃない2021年12月31日現在、株式投資を行っています。
7. デリバティブ金融商品
私たちはさまざまな外貨で取引を行っており、海外での売上と経費は外貨建てです。そのため、私たちは事業運営と経済状況の両方から生じる一定のリスクにさらされています。当社のリスク管理戦略には、デリバティブ金融商品を使用してヘッジすることが含まれます。(1)外貨建ての予測商品売上、(2)外貨建ての金銭的資産または負債の外貨為替レートの変動。私たちは、投機的または取引目的でデリバティブ金融契約を締結しません。取引相手は大規模でグローバルで資本の豊富な金融機関であるため、外貨ヘッジでわずかな金額以上の信用リスクにさらされているとは考えていません。要約連結キャッシュフロー計算書では、デリバティブ取引によるキャッシュフローを営業活動によるキャッシュフローとして分類しています。
キャッシュフローヘッジ
私たちは、ユーロ建ての外貨建て商品の売上の変動から生じる為替リスクを、先渡契約や超過しない外貨オプションを使用する外貨キャッシュフローヘッジプログラムを通じて軽減しています 15期間は数ヶ月です。私たちは、為替レートの変動によって収益とキャッシュフローが悪影響を受けるリスクを軽減するために、これらのキャッシュフローエクスポージャーをヘッジしています。ヘッジ会計の扱いを受けるには、すべてのヘッジ関係がヘッジ開始時に正式に文書化され、ヘッジはヘッジ取引における将来のキャッシュフローの変化を相殺する上で非常に効果的でなければなりません。当社のヘッジ活動に関連するデリバティブ資産または負債は、それぞれ他の流動資産またはその他の流動負債に公正価値で記録されます。 要約連結貸借対照表。これらのヘッジの公正価値の変動による損益は、最初は株主資本のその他の包括利益(損失)(AOCI)の累計の一部として記録され、 その後、ヘッジ取引が収益に影響する期間の製品販売に再分類されました。定義されたヘッジ期間内に基礎となる予測取引が行われなかった場合、または発生しない可能性が高まった場合、関連するキャッシュフローヘッジの損益をAOCIからその他の費用(純額)に再分類します 当社の要約連結損益計算書では。私たちは、ヘッジの開始時にヘッジの有効性を将来的に評価し、遡及的にも将来的にも継続的に評価します。ヘッジ会計を選択しない場合、または契約がヘッジ会計処理の対象とならない場合は、期間ごとの公正価値の変化が記録されます その他の費用の一部として、当社の要約連結損益計算書を差し引いた金額. 2022年6月30日現在、当社の純繰延利益はドルです55AOCIに含まれる外貨先渡契約で、今後12か月以内に商品売上に計上される予定の100万ドルです。
貸借対照表ヘッジ
私たちは、ヘッジ会計処理の対象とならない外貨建ての金銭的資産および負債、主にユーロ、日本円、スイスフランでの売掛金、買掛金、リース負債に関連する変動をヘッジするために外貨先渡契約を締結します。したがって、これらの先渡契約はデリバティブとして会計処理され、契約の公正価値は他の流動資産またはその他の流動負債として当社の要約連結貸借対照表に報告され、公正価値の変動による損益は、その他の費用の一部として、当社の要約連結損益計算書に控除されます。これらの外貨先渡契約の損益は、通常、基礎となる外貨建て資産および負債の損益を相殺し、これらも当社の要約連結損益計算書にその他の費用(純額)に記録されます。
当社の外貨デリバティブの想定総額と公正価値の合計は次のとおりです(単位:百万単位)。
| | | | | | | | | | | | | | | | | | | | |
| | 2022年6月30日 |
| | 想定金額 | | 公正価値 |
| | | アセット (1) | | 責任 (2) |
| キャッシュフローヘッジ商品として指定されているデリバティブ: | | | | | | |
| 外貨先渡契約 | | $ | 1,153 | | | $ | 37 | | | $ | — | |
| | | | | | |
| ヘッジ商品として指定されていないデリバティブ: | | | | | | |
| 外貨先渡契約 | | 957 | | | 21 | | | 2 | |
| デリバティブの合計 | | $ | 2,110 | | | $ | 58 | | | $ | 2 | |
| | | | | | | | | | | | | | | | | | | | |
| | 2021年12月31日 |
| | 想定金額 | | 公正価値 |
| | | アセット (1) | | 責任 (2) |
| キャッシュフローヘッジ商品として指定されているデリバティブ: | | | | | | |
| 外貨先渡契約 | | $ | 565 | | | $ | 20 | | | $ | — | |
| | | | | | |
| ヘッジ商品として指定されていないデリバティブ: | | | | | | |
| 外貨先渡契約 | | $ | 1,370 | | | $ | 1 | | | $ | 7 | |
| デリバティブ総額 | | $ | 1,935 | | | $ | 21 | | | $ | 7 | |
_________
(1) 前払費用およびその他の流動資産に含まれる要約連結貸借対照表に示されているとおり。
(2) その他の流動負債を含む要約連結貸借対照表に示されているとおり。
2022年6月30日および2021年に終了した3か月および6か月間の包括利益の要約連結計算書に計上された当社の外貨デリバティブの税引後利益は次のとおりです(百万単位)。
| | | | | | | | | | | | | | | | | | | | | | | | | | |
| | 6月30日に終了した3か月間 | | 6月30日に終了した6か月間 |
| | 2022 | | 2021 | | 2022 | | 2021 |
| キャッシュフローヘッジ関係におけるデリバティブ: | | | | | | | | |
| 外貨先渡契約 | | $ | 46 | | | $ | 21 | | | $ | 71 | | | $ | 21 | |
2022年6月30日および2021年6月30日までの3か月および6か月間の要約連結損益計算書における当社の外貨デリバティブの影響は次のとおりです(百万単位)。
| | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | |
| | | | 6月30日に終了した3か月間 | | 6月30日に終了した6か月間 |
| | 損益計算書分類表 | | 2022 | | 2021 | | 2022 | | 2021 |
| キャッシュフローヘッジ関係におけるデリバティブ: | | | | | | | | | | |
| 外貨先渡契約 | | | | | | | | | | |
| 純利益はAOCIから収入に再分類されました | | 製品販売 | | $ | 30 | | | $ | — | | | $ | 44 | | | $ | — | |
| | | | | | | | | | |
| ヘッジ商品として指定されていないデリバティブ: | | | | | | | | | | |
| 外貨先渡契約 | | | | | | | | | | |
| 純実現利益と未実現利益 (損失) | | その他の費用、純額 | | $ | 41 | | | $ | (54) | | | $ | 69 | | | $ | (19) | |
2021年6月30日までの3か月と6か月の間に、重要ではない利益がAOCIから製品売上に再分類されました。2021年6月30日までの3か月と6か月間、キャッシュフローヘッジ活動はありませんでした。
8. インベントリ
2022年6月30日および2021年12月31日現在の在庫は以下のとおりです(百万単位)。
| | | | | | | | | | | | | | | | |
| | 6月30日 | | 12月31日 | | |
| | 2022 | | 2021 | | |
| 原材料 | | $ | 1,400 | | | $ | 870 | | | |
| 作業中です | | 379 | | | 338 | | | |
| 完成品 | | 142 | | | 233 | | | |
| 在庫合計 | | $ | 1,921 | | | $ | 1,441 | | | |
在庫は、原価または正味実現可能価値のいずれか低い方で記録されます。四半期ごとに在庫の構成を評価して、過剰品、時代遅れの商品、動きの遅い商品、または販売できない商品を特定します。また、第三者ベンダーとの供給契約に基づく、四半期ごとに超過した、取消不能な購買契約負債があるかどうかも評価しています。在庫と企業購買契約負債の正味実現可能価値を決定するには、将来の製品需要の見積もり、現在および将来の市況、製品の陳腐化の可能性、確定購買契約に基づく原材料の有効期限と利用、契約上の最低額など、多くの要因を考慮した判断が必要です。
過剰、陳腐化、廃棄、またはその他の理由による在庫減価償却や、確定購入契約による損失は、売上原価の一部として当社の要約連結損益計算書に記録されます.2022年6月30日までの3か月と6か月間、在庫償却額はドルでした499百万と $689それぞれ百万。在庫の減価償却は 重要ではありません2021年6月30日までの3か月と6か月の間。2022年6月30日までの3か月と6か月間、企業購買契約による損失はドルでした184百万と $342それぞれ百万。2022年6月30日現在、当社の要約連結貸借対照表にある企業の将来の購入契約における損失に対する未払負債はドルでした342百万。あった いいえこのような2021年の費用、または2021年12月31日の未払負債。
発売前のインベントリ
規制当局の承認に先立つ製品発売の準備のための原材料と在庫生産に関連する費用は、将来の商品化が見込まれ、将来の経済的利益の実現が見込めるときに資産計上され、最終的な規制当局の承認に関連する重大な不確実性が大幅に減少したと考えています。資本化される発売前の在庫については、その時点で入手可能な情報に基づいてさまざまな要素を検討します。たとえば、医薬品開発および規制当局の承認プロセスにおける製品候補の現状、関連する臨床試験の結果、規制当局への申請前に関連規制機関との会合の結果、製品の安全性や有効性などの承認プロセスの潜在的な障害、歴史的経験、商品化の実行可能性、市場動向などです。
2022年6月30日の時点で、オミクロン含有ブースター候補(mRNA-1273.214)に関する発売前の在庫を資本化しました。155要約連結貸借対照表には百万ドルあります。
9. 資産および設備、純額
2022年6月30日および2021年12月31日現在の資産および設備の純額は以下のとおりです(百万単位)。
| | | | | | | | | | | | | | |
| | 6月30日 | | 12月31日 |
| | 2022 | | 2021 |
| 製造および実験装置 | | $ | 201 | | | $ | 175 | |
借地権の改善 | | 365 | | | 313 | |
| 家具、備品、その他 | | 17 | | | 11 | |
コンピュータ機器とソフトウェア | | 17 | | | 16 | |
社内開発ソフトウェア | | 8 | | | 9 | |
使用権資産、資金調達(ノート 11) | | 898 | | | 857 | |
建設中 | | 284 | | | 212 | |
| 合計 | | 1,790 | | | 1,593 | |
控除:減価償却累計額 | | (466) | | | (352) | |
資産および設備、純額 | | $ | 1,324 | | | $ | 1,241 | |
| | | | |
2022年6月30日までの3か月と6か月の減価償却費は、ドルでした76百万と $155それぞれ百万。2021年6月30日までの3か月と6か月の減価償却費は、ドルでした69百万と $84それぞれ百万。
10. その他の貸借対照表の構成要素
前払費用およびその他の流動資産
2022年6月30日および2021年12月31日時点の前払費用およびその他の流動資産は、以下で構成されています(百万単位)。
| | | | | | | | | | | | | | |
| | 6月30日 | | 12月31日 |
| | 2022 | | 2021 |
| 材料や物資の頭金 | | $ | 474 | | | $ | 287 | |
| 製造業者への頭金 | | 183 | | | 118 | |
| プリペイドサービス | | 110 | | | 126 | |
| 付加価値税の売掛金 | | 45 | | | 70 | |
| テナント改善手当売掛金 | | 51 | | | 51 | |
| 売掛金 | | 57 | | | 27 | |
| デリバティブ資産 | | 58 | | | 21 | |
| | | | |
| その他の流動資産 | | 76 | | | 28 | |
前払費用およびその他の流動資産 | | $ | 1,054 | | | $ | 728 | |
未払負債
2022年6月30日および2021年12月31日現在の未払負債は以下のとおりです(百万単位)。
| | | | | | | | | | | | | | |
| | 6月30日 | | 12月31日 |
| | 2022 | | 2021 |
| 臨床試験 | | $ | 324 | | | $ | 283 | |
| 原材料 | | 317 | | | 260 | |
| ロイヤリティ | | 158 | | | 241 | |
| 開発事業 | | 65 | | | 137 | |
| 製造業 | | 244 | | | 227 | |
| その他の外部の商品やサービス | | 100 | | | 79 | |
将来の企業購入契約による損失(1) | | 342 | | | — | |
| 報酬関連 | | 128 | | | 126 | |
| その他 | | 102 | | | 119 | |
| | | | |
| | | | |
未払負債 | | $ | 1,780 | | | $ | 1,472 | |
______
(1) 将来の原材料購入の確固たる取消不可の約束から生じると予想される損失に関連しています(ノート 8).
その他の流動負債
2022年6月30日および2021年12月31日現在のその他の流動負債は次のとおりです(百万単位)。
| | | | | | | | | | | | | | |
| | 6月30日 | | 12月31日 |
| | 2022 | | 2021 |
リース負債-資金調達(ノート 11) | | $ | 121 | | | $ | 165 | |
リース負債-営業中(ノート 11) | | 38 | | | 46 | |
| | | | |
| その他 | | 250 | | | 14 | |
| その他の流動負債 | | $ | 409 | | | $ | 225 | |
繰延収益
次の表は、の繰延収益の活動をまとめたものです 6 か月が終了2022年6月30日 (百万単位):
| | | | | | | | | | | | | | | | | | | | | | | | | | |
| | 2021年12月31日 | | 追加 | | 控除 | | 2022年6月30日 |
| 製品販売 | | $ | 6,658 | | | $ | 1,834 | | | $ | (4,166) | | | $ | 4,326 | |
| 助成金収入 | | 6 | | | — | | | (1) | | | 5 | |
| コラボレーション収益 | | 204 | | | 6 | | | (43) | | | 167 | |
| 繰延収益の合計 | | $ | 6,868 | | | $ | 1,840 | | | $ | (4,210) | | | $ | 4,498 | |
11. リース
私たちは、2042年までのさまざまな時期に期限が切れる施設や設備について、キャンセル不可の長期リース契約を締結しています。これらの契約の中には、無料のレンタル期間や家賃の支払い条項がエスカレートするものがあります。このような契約に基づくリース費用は、リースの全期間にわたって定額で計上されます。私たちは 二マサチューセッツ州のキャンパス、ケンブリッジキャンパス、ノーウッドにある工業技術センターであるモデルナテクノロジーセンター(MTC)。また、事業運営のために他のオフィスや研究室のスペースをグローバルにリースしています。
オペレーティングリース
ケンブリッジキャンパス
私たちは、マサチューセッツ州ケンブリッジのテクノロジースクエアにある複数棟のキャンパスを占めています。オフィスと研究室のスペースが混在しているのは、およそ 261,000平方フィート。ケンブリッジのキャンパスリースの有効期限は2024年から2029年です。
さらに、次の発見の章をサポートするための専用スペースを作るために、ケンブリッジの新しいモデルナサイエンスセンター(MSC)に投資しています(参照 ノート 12)。MSCへの投資に関連して、2021年9月にリース契約を修正し、リースの一部または全部の早期終了が可能になりました。オプションを行使する意向の通知は、2023年8月までに行う必要があります。このオプションを行使することはまだ選択していません。
ファイナンスリース
モデルナテクノロジーセンター
私たちのMTCは 三主な建物:MTCサウス、MTCノース、MTCイースト。MTCサウスとMTCノースはそれぞれ、およそ 200,000平方フィートで、オフィス、研究所、照明製造スペースを提供し、製造能力の向上を直接サポートします。MTCイーストはおよそ 240,000商業活動および臨床活動用の平方フィートです。MTCキャンパスは2042年までリースされており、期間を延長することもできます 三の延長期間 五年.
組み込みリース
私たちは、ASC 842の範囲内の組み込みリースを含む複数の受託製造サービス契約を第三者と締結しています。これらのリースの有効期限は2022年から2023年までです。2022年6月30日および2021年12月31日の時点で、当社のリース負債はドルでした129百万と $166埋め込みリースに関連するのはそれぞれ100万です。2022年6月30日と2021年12月31日の時点で、当社の使用権資産は米ドルでした101百万と $173埋め込みリースに関連するのはそれぞれ100万です。
2022年6月30日および2021年12月31日現在の運営および資金調達のリース使用権資産とリース負債は以下の通りです(百万単位)。
| | | | | | | | | | | | | | |
| | 6月30日 | | 12月31日 |
| | 2022 | | 2021 |
| 資産: | | | | |
使用権資産、営業、純額 (1) (2) | | $ | 122 | | | $ | 142 | |
使用権資産、資金調達、純額 (3) (4) | | 619 | | | 665 | |
| 合計 | | $ | 741 | | | $ | 807 | |
| | | | |
| 負債: | | | | |
| 現在: | | | | |
オペレーティングリース負債 (5) | | $ | 38 | | | $ | 46 | |
ファイナンスリース負債 (5) | | 121 | | | 165 | |
| 現在のリース負債総額 | | 159 | | | 211 | |
| 非電流: | | | | |
| オペレーティングリース負債、非流動負債 | | 87 | | | 106 | |
| ファイナンスリース負債、非流動性 | | 641 | | | 599 | |
| 非流動リース負債の合計 | | $ | 728 | | | $ | 705 | |
| 合計 | | $ | 887 | | | $ | 916 | |
_______
(1) これらの資産は、土地、オフィス、実験室を含む不動産関連資産です。
(2) 累積償却額を差し引いたものです。
(3) これらの資産は、MTCリースに関連する不動産資産と、受託製造サービス契約に関連する資産です。
(4) 要約連結貸借対照表の資産および設備に含まれており、減価償却累計額を差し引いたものです。
(5) 要約連結貸借対照表のその他の流動負債に含まれています。
2022年6月30日現在の解約不可のリース契約に基づく将来の最低リース支払い額は以下の通りです(百万単位)。
| | | | | | | | | | | | | | | |
会計年度 | オペレーティングリース | | ファイナンスリース (1) |
| 2022 | (今年の残りの期間) | $ | 23 | | | $ | 121 | | |
| 2023 | | 39 | | | 38 | | |
| 2024 | | 15 | | | 21 | | |
| 2025 | | 16 | | | 22 | | |
| 2026 | | 16 | | | 22 | | |
| その後 | 51 | | | 1,111 | | |
最低リース料総額 | 160 | | | 1,335 | | |
| 利息または帰属(帰属)を表す金額が少ない | (35) | | | (573) | | |
リース負債の現在価値 | $ | 125 | | | $ | 762 | | |
______
(1) 主にMTCリースに関連する特定のオプションリース期間の延長を含み、合計で$になります662将来のリース料の割引なしの100万円。
12. コミットメントと不測の事態
法的手続き
私たちは、私たちのビジネスでは普通の流れと考えられている性質のさまざまな請求や法的手続きに関与しています。このような手続の結果は、そのメリットにかかわらず、本質的に不確実です。したがって、損失の可能性や推定損害額を評価することは難しく、かなりの判断が必要です。現在、重大な損失が発生する可能性がある、または現時点で損失が合理的に推定できる法的手続きの当事者ではありません。
補償義務
デラウェア州の法律で認められているとおり、役員、取締役、従業員に特定の事象が発生した場合、その役員、取締役、従業員に補償を行います。補償期間は、役員または取締役の生涯です。
研究室やオフィススペースのリースには、特定の行為、違反、違反、または当社のリースに基づく不履行に起因する請求、訴訟、手続き、または費用による傷害、損失、事故、または損害に対する責任について家主に補償することを義務付ける標準的な補償契約があります。
私たちは、通常の業務過程で取引相手、通常はビジネスパートナー、請負業者、臨床施設、顧客との契約に基づいて補償条項を締結します。これらの規定に基づき、私たちは通常、私たちの活動の結果として被補償者が被った、または被った損失について、被補償者に補償し、免責します。これらの補償条項は、通常、基礎となる契約の終了後も存続します。これらの補償条項に基づいて当社が行う必要がある可能性のある将来の支払いの最大額は無制限です。
2022年6月30日までの3か月と2021年12月31日に終了した年度を通じて、これらの補償義務に関連する重大な損失は発生しておらず、未解決の重大な請求もありませんでした。これらの補償義務に関連する重大な請求はないと予想しているため、これらの義務の公正価値はごくわずかであり、関連する準備金は設定されていないと結論付けました。
購入契約と購入注文
私たちは、原材料や製造サービスについてはベンダーや委託製造機関、前臨床研究、臨床試験、その他の商品やサービスについてはベンダーと通常の業務の中で契約を締結します。2022年6月30日現在、私たちはへ $3.4原材料や製造契約に関連する何十億ものキャンセル不可の購入契約。支払いは2025年までに予定されています。2022年6月30日現在、$342原材料に関連する購入契約のうち100万件は、将来の企業購入契約の損失に対する未払負債として記録されました。2022年6月30日の時点で、私たちにはドルがありました179百万オンスC以外の場合2026年までの支払いが予定されている臨床サービスやその他の商品やサービスに関するキャンセル可能な購入契約。これらの金額は、解約料を含む当社の最低契約上の義務を表しています。
購入契約に加えて、臨床業務やサポートや受託製造に関連するサービスなど、さまざまな商品やサービスについて第三者と契約を結んでいますが、便宜上契約を解除したり、ベンダーに対する将来の義務を回避したりすることはできません。一部の契約では、解約料または清算費用を条件として、解約権を規定しています。このような契約に基づき、私たちは契約上、ベンダーに特定の支払いを行う義務があります。これは主に、キャンセル前に発生した回収不能な費用をベンダーに払い戻すためです。2022年6月30日の時点で、$の未処理注文がキャンセル可能でした2.5このような契約に基づく当社の重要な臨床業務とサポート、および受託製造については、合計で10億ドルです。これらの金額は、2022年6月30日に支払いを契約上約束した品目の見積もりにすぎません。ただし、これらの契約はキャンセルしないと仮定しています。そのような契約に基づいて当社が将来ベンダーに支払う実際の金額は、注文金額と異なる場合があります。
特許技術のライセンス
2017年6月26日、私たちはCellscript, LLCとその関連会社であるmRNA RiboTherapeutics, Inc. と、特定の特許権をサブライセンスするためのサブライセンス契約を締結しました。各契約に従い、特定の製品の開発、規制、および商業上の特定のマイルストーンの達成を条件として、特定のライセンス料、年間維持費、将来の純売上高に対する最低ロイヤルティ、およびマイルストーンの支払いを製品ごとに支払う必要があります。治療薬および予防薬のライセンス製品の年間純売上高に基づく商業マイルストーンの支払いとロイヤルティは、対応する販売が行われた期間における関連製品の売上の追加費用として計上されます。2022年6月30日までの3か月と6か月間、私たちはドルを認識しました157百万と $364製品販売に関連するロイヤルティ費用は、それぞれ100万ドルです。これは、要約連結損益計算書の売上原価に記録されています。2021年6月30日までの3か月と6か月間、私たちはドルを認識しました148百万と $232製品販売に関連するロイヤルティ費用は、それぞれ100万ドルです。これは、要約連結損益計算書の売上原価に記録されています。
さらに、私たちは第三者とライセンス契約を結んでおり、それらの契約では、将来の開発、規制、商業上のマイルストーンの支払い、および契約に関連する特定の製品に対する売上ベースのロイヤルティを義務付けています。2022年6月30日の時点で、これらのマイルストーンが達成される可能性は低いと考えられていました。
モデルナ・サイエンス・センター
2021年9月、マサチューセッツ州ケンブリッジのMSCへの投資を発表しました。MSCは、主要なエグゼクティブオフィスを含め、科学分野と非科学分野を統合することが期待されています。また、mRNA医薬品のパイプラインをさらに発展させていく中で、私たちの成長を支えるものとなるでしょう。投資に関連して、私たちはおおよそのリース契約を締結しました 462,000平方フィートで、およそ 二年間建築プロジェクト。建築プロジェクト後のリース期間は 15何年も、リースを最大まで延長する当社の権利を条件とします 二追加 7 年間規約。このリース契約に基づき、私たちは約$を約束します1.1最初のリース期間における10億件のキャンセル不可の家賃支払い。2023年に入居手続きを開始する予定です。
13. 株式ベースの報酬と自社株買いプログラム
株式ベースの報酬
次の表は、2022年6月30日および2021年6月30日までの3か月および6か月間の株式ベースの報酬費用の構成要素と分類を以下に示します(百万単位)。
| | | | | | | | | | | | | | | | | | | | | | | | | | |
| | 6月30日に終了した3か月間 | | 6月30日に終了した6か月間 |
| | 2022 | | 2021 | | 2022 | | 2021 |
[オプション] | | $ | 27 | | | $ | 24 | | | $ | 52 | | | $ | 46 | |
| 制限付普通株式 (RSU) とパフォーマンス株式ユニット (PSU) | | 22 | | | 10 | | | 39 | | | 17 | |
| 従業員株式購入制度 (ESPP) | | 1 | | | 1 | | | 3 | | | 2 | |
合計 | | $ | 50 | | | $ | 35 | | | $ | 94 | | | $ | 65 | |
| | | | | | | | |
| 売上原価 | | $ | 13 | | | $ | 8 | | | $ | 21 | | | $ | 12 | |
| 研究開発 | | 19 | | | 15 | | | 39 | | | 29 | |
| 販売、一般および管理 | | 18 | | | 12 | | | 34 | | | 24 | |
合計 | | $ | 50 | | | $ | 35 | | | $ | 94 | | | $ | 65 | |
2022年6月30日の時点で、ドルがありました575付与されたオプション、RSU、PSUに関する未確定株式ベースの報酬に関連する未認識報酬費用の総額は100万です。その費用は、加重平均期間にわたって計上されると予想されます 3.2年は2022年6月30日時点のものです。
株式買戻しプログラム
2021年8月2日、当社の取締役会は、当社普通株式の自社株買戻しプログラム(2021年買戻しプログラム)を承認しました。2021年の買戻しプログラムにより、最大$までの買戻しを許可されました1.0有効期限が2023年8月2日までの10億株の発行済み普通株式。2022年1月末までに、全額を買い戻しました1.02021年の買戻しプログラムに基づいて承認された10億株の普通株式。
2022年2月22日、当社の取締役会は、有効期限のない当社普通株式の新しい自社株買戻しプログラム(2022年買戻しプログラム)を承認しました。2022年の買戻しプログラムに従い、最大$まで買い戻すことがあります3.010億株の発行済み普通株式。買い戻される株式のタイミングと実際の数は、価格、一般的なビジネスおよび市場の状況、その他の投資機会など、さまざまな要因によって決まります。株式は、改正された1934年の証券取引法に基づく規則10b5-1に基づく資格取得を目的とした取引プランを使用して、公開市場での購入を通じて買い戻すことができます。
2022年6月30日までの6か月間に、買い戻しました 132021年と2022年の買戻しプログラムに基づく当社の普通株式100万株(総額)1.910億。手数料や手数料を含みます。2022年6月30日の時点で、合計金額は1.2残りの10億ドルは、2022年の買戻しプログラムに基づく当社の普通株式の買戻しに充てられます。
14. 所得税
次の表は、提示された期間の所得税費用をまとめたものです(百万単位、パーセンテージを除く)。
| | | | | | | | | | | | | | | | | | | | | | | | | | |
| | 6月30日に終了した3か月間 | | 6月30日に終了した6か月間 |
| | 2022 | | 2021 | | 2022 | | 2021 |
| 税引前利益 | | $ | 2,474 | | | $ | 3,063 | | | $ | 6,703 | | | $ | 4,323 | |
| 所得税引当金 | | $ | 277 | | | $ | 283 | | | $ | 849 | | | $ | 322 | |
| 実効税率 | | 11.2 | % | | 9.2 | % | | 12.7 | % | | 7.5 | % |
2022年6月30日までの3か月と6か月の実効税率は、主に外国由来の無形所得控除(FDII)の利点と、株式ベースの報酬に関連する超過税制上の優遇措置の個別項目という利点により、米国の法定税率よりも低くなりました。2022年6月30日までの3か月および6か月間の実効税率の引き上げは、主に当社の繰延税金資産の大部分に対する評価引当金の解除に関連して2021年に記録された税制上の優遇措置と、株式ベースの報酬による超過利益の減少によるもので、2022年のFDII給付の増加によって一部相殺されました。
私たちは、米国連邦所得税申告書と所得税申告書をさまざまな州、地方、外国の管轄区域に提出しています。現在、米国やその他の主要な課税管轄区域での所得税審査による課税評価の対象ではありません。
2022年1月1日より、研究開発費は米国の税務上の目的で資産計上および償却する必要があります。修正または廃止されない限り、また現在の仮定に基づくと、資本化が義務付けられると、現金課税負債が増えるだけでなく、FDII控除額も増え、実効税率が下がります。
15. 一株当たり利益
1株当たりの基本利益 (EPS) の計算は、発行済普通株式の加重平均数に基づいています。希薄化後EPSの計算は、自己株式法を用いて決定された、期間中の当社発行普通株式および潜在希薄化対象普通株式の加重平均数に基づいています。
2022年6月30日および2021年6月30日までの3か月および6か月間の基本および希薄化後EPSは、次のように計算されました(1株あたりのデータを除き、百万単位)。
| | | | | | | | | | | | | | | | | | | | | | | | | | |
| | 6月30日に終了した3か月間 | | 6月30日に終了した6か月間 |
| | 2022 | | 2021 | | 2022 | | 2021 |
| 分子: | | | | | | | | |
| 当期純利益 | | $ | 2,197 | | | $ | 2,780 | | | $ | 5,854 | | | $ | 4,001 | |
| 分母: | | | | | | | | |
| 基本加重平均発行済普通株式 | | 396 | | | 402 | | | 399 | | | 401 | |
| 希薄化証券の影響 | | 23 | | | 29 | | | 24 | | | 29 | |
| 希薄化後の加重平均発行済普通株式 | | 419 | | | 431 | | | 423 | | | 430 | |
| | | | | | | | |
| ベーシックEPS | | $ | 5.55 | | | $ | 6.93 | | | $ | 14.66 | | | $ | 9.98 | |
| 希釈後のEPS | | $ | 5.24 | | | $ | 6.46 | | | $ | 13.85 | | | $ | 9.30 | |
| | | | | | | | |
| 上記のEPS計算から除外された希薄化防止潜在普通株式 | | 4 | | | 1 | | | 3 | | | 1 | |
16. 後続イベント
2022年7月28日、私たちは米国政府と最初の供給契約を締結しました 66当社のCOVID-19二価ブースターワクチン候補(mRNA-1273.222)を100万回接種し、米国政府が最大で追加購入するオプションもあります 234100万回分投与。2022年8月1日、米国政府は購入オプションを行使しました 4私たちのCOVID-19二価ブースターワクチン候補を小児に100万回接種した結果、合計は 70100万回分を購入、オプションで追加購入も可能 230100万回分投与。
2022年8月1日、当社の取締役会は、有効期限のない当社普通株式の新たな自社株買戻しプログラム(2022年の第2次買戻しプログラム)を承認しました。2022年の2回目の買戻しプログラムに従い、最大で1ドルまで買い戻すことが可能です3.010億株の発行済み普通株式。買い戻される株式のタイミングと実際の数は、価格、一般的なビジネスおよび市場の状況、その他の投資機会など、さまざまな要因によって決まります。株式は、1934年の証券取引法(取引法)に基づく規則10b5-1に基づく資格取得を目的とした取引プランを使用して、公開市場での購入を通じて買い戻すことができます。
アイテム 2.経営陣による財政状態と経営成績の議論と分析
このフォーム10-Qに含まれる未監査の財務情報および関連メモ、および2022年2月25日に証券取引委員会(SEC)に提出された2021年12月31日に終了した年度のフォーム10-Kの年次報告書(2021年フォーム10-K)にある連結財務諸表と関連注記およびその他の財務情報とともに、当社の財政状態と経営成績に関する以下の説明と分析をお読みください。当社の事業計画や戦略に関する情報を含め、この議論や分析に含まれている、またはこのフォーム10-Qの他の場所に記載されている情報の一部には、リスクと不確実性を伴う将来の見通しに関する記述が含まれています。パートII、項目1A(このフォーム10-Qのリスク要因)に記載されている要因を含む多くの要因により、当社の実際の結果は、以下の説明と分析に含まれる将来の見通しに関する記述に記載された、または暗示される結果と大きく異なる可能性があります。
[概要]
私たちは、メッセンジャーRNA(mRNA)治療薬とワクチンの先駆者であり、患者の生活を改善する新世代の革新的な医薬品を開発しているバイオテクノロジー企業です。私たちのプラットフォームは、基礎および応用mRNA科学、デリバリー技術、製造における継続的な進歩に基づいて構築されており、新しい開発候補の強固なパイプラインを並行して追求する能力を備えています。私たちは、感染症、免疫腫瘍学、希少疾患、自己免疫疾患、心血管疾患の治療薬とワクチンを独立して、また戦略的協力者と共同で開発しています。私たちのプラットフォームでは、さまざまな用途のmRNA医薬品の開発を可能にする技術を開発しています。製品の特徴を共有した潜在的なmRNA医薬品の新しいグループを可能にすると私たちが信じる技術を特定するとき、そのグループを「モダリティ」と呼びます。 これまでに7つのモダリティを作成しました。
•予防ワクチン;
•全身分泌薬および細胞表面治療薬;
•がんワクチン;
•腫瘍内免疫腫瘍学;
•局所的な再生治療薬;
•全身の細胞内治療薬、および
•吸入肺治療薬。
2020年12月18日、モデルナのCOVID-19ワクチン(mRNA-1273とも呼ばれ、Spikevaxというブランド名で販売されています)を18歳以上の個人に2回投与する100 µgのプライマリシリーズとして緊急使用することについて、米国食品医薬品局(FDA)から緊急使用許可(EUA)を取得しました。2022年1月、米国で18歳以上の個人を対象にCOVID-19を予防するための100µgのプライマリシリーズを2回投与するスパイクバックスの商業的承認を受けました。スパイクバックスは、80か国以上で18歳以上の個人を対象に承認または認可されています。さらに、当社のCOVID-19ワクチンは、12〜17歳の青少年には100 µgの一次シリーズを2回投与、6歳から11歳の小児では50 µgの一次投与シリーズとして40か国以上の世界規制当局から承認を受けています。さらに、米国、カナダ、オーストラリア、およびその他の管轄区域では、6か月から5歳までの幼児を対象に、25µgのCOVID-19ワクチンの2回接種の初回シリーズが承認されています。
FDA、欧州医薬品庁(EMA)、スイスメディック、その他世界中の保健機関は、18歳以上の成人を対象に、当社のCOVID-19ワクチンを50 µgの用量レベルで追加投与することを承認しました。2022年3月、FDAと他の保健機関は、50歳以上の成人と特定の種類の免疫不全のある18歳以上の成人を対象に、50 µgの用量レベルで2回目の追加投与を承認しました。
ビジネスのハイライトと最近の動向
モデルナのCOVID-19ワクチンの臨床研究
•オミクロン固有のブースター候補 (mRNA-1273.529/.214/.222):当社のオミクロン含有ワクチン候補は、18歳以上の成人を対象とした単回追加投与としてのmRNA-1273.529とmRNA-1273.214の免疫原性、安全性、反応原性を評価するために研究されています。mRNA-1273.529は、懸念されるオミクロン株に特異的なワクチン候補です(BA.1)。 mRNA-1273.214は、当社のオミクロン特異的(BA.1)候補(mRNA-1273.529)とmRNA-1273を組み合わせた二価の候補です。また、BA.4/5オミクロン株とmRNA-1273をベースにした二価ワクチン候補(mRNA-1273.222)を開発中です。mRNA-1273.214は、米国で進行中の登録第2/3相試験と英国での第3相試験で評価されています。間もなく、米国で第2/3相試験でmRNA-1273.222の投与を開始する予定です。
•2022年6月の臨床データによると、50 µgのmRNA-1273.214の追加投与量は、元のmRNA-1273ワクチンと比較して、投与後1か月後にオミクロン株に対する優れた中和抗体反応(幾何平均比)を含む事前に指定されたすべてのエンドポイントを満たしました。mRNA-1273.214の追加投与量は一般的に耐容性が高く、50 µgの用量レベルでmRNA-1273の追加投与と同等の副作用がありました。さらに、以前にワクチンを接種して追加接種した参加者に投与してから1か月後に、50 µgのmRNA-1273.214の追加投与により、以前の感染に関係なく、すべての参加者でオミクロンサブバリアントBA.4とBA.5に対する強力な中和抗体反応が誘発されました。今後数週間以内に、ブースターワクチンの組成をmRNA-1273.214に更新するよう求める規制当局への提出を完了するよう取り組んでいます。
•オミクロン株のさまざまな市場ニーズに基づいて、2022年秋に向けてmRNA-1273.214とmRNA-1273.222の両方を進めています。2022年7月28日、私たちは米国政府と最初に6,600万回分のmRNA-1273.222用量の供給契約を締結しました。米国政府は最大2億3,400万回分の追加購入も可能です。また、秋のブースターシーズンに向けたmRNA-1273.214の供給について、他の政府と供給契約を結んでいます。
•ベータ特異的二価ブースター (mRNA-1273.211):mRNA-1273.211は、当社のベータ特異的候補(mRNA-1273.351)とmRNA-1273を組み合わせた二価ワクチン候補です。懸念されるベータ変異株に見つかったいくつかの突然変異は、オミクロンを含む最近懸念された亜種でも持続しています。投与の1か月後に、懸念されるベータ、デルタ、オミクロン株に対して、mRNA-1273の50 µgの追加投与量と比較して、mRNA-1273の50 µgの追加投与よりも優れていることが示されました。懸念されるベータ株とオミクロン株についても、投与後6か月間優勢が続きました。50 µgのmRNA-1273.211のブースター用量は一般的に忍容性が高く、50 µgの用量レベルでmRNA-1273の追加投与と同等の反応原性プロファイルを示しました。
•青少年と子供のためのモデルナのCOVID-19ワクチン: 12〜17歳の青少年を対象に、当社のCOVID-19ワクチンの初回シリーズ(100 µgを2回投与)は40か国以上で承認されています。
6〜11歳の小児を対象に、当社のCOVID-19ワクチンの初回シリーズ(50 µgを2回投与)は、米国、EU、オーストラリア、カナダを含む40か国以上で承認されています。
生後6か月から5歳の小児を対象に、当社のCOVID-19ワクチンの初回シリーズ(25 µgを2回投与)は、米国、カナダ、オーストラリア、およびその他の法域で承認されています。
•新型コロナウイルスに対する次世代ワクチン候補(mRNA-1283):mRNA-1283はCOVID-19に対する次世代のワクチン候補であり、医療提供者による配布と投与を容易にする潜在的な冷蔵庫で安定性のあるmRNAワクチンとして開発されています。mRNA-1283の第1相試験では、mRNA-1283を低用量レベル(10 µg、30 µg)で一次シリーズとして投与した場合、100 µgのmRNA-1273の一次シリーズに匹敵する強力な抗SARS-CoV-2中和抗体反応を誘発することが暫定結果から示されています。低用量(10 µg、30 µg)で投与されたmRNA-1283プライマリシリーズの局所的および全身的に求められる副作用の頻度は、全体的にmRNA-1273と同等でした。mRNA-1283、mRNA-1283.211(SARS-CoV-2/ベータ二価)、およびmRNA-1283.529(オミクロン一価)の追加投与量を評価する第2相試験への登録が完了しました。
•2022年第2四半期には、新型コロナワクチンの売上による製品売上高は45億ドルでしたが、2021年第2四半期は42億ドルでした。
その他のビジネスアップデート
2022年6月、私たちは英国政府と原則として英国にmRNAイノベーションアンドテクノロジーセンターを設立する契約を締結しました。この最先端のmRNAワクチン製造施設により、パンデミックへの迅速な対応能力と当社の呼吸器ウイルスワクチン候補を入手できるようになることを期待しています。また、研究開発活動への投資を通じて、英国でのプレゼンスを拡大する予定です。英国の協定は、ケニア共和国政府、オーストラリア連邦政府、カナダ政府と締結した、これらの国に最先端のmRNAワクチン製造施設を設立するという以前の合意に続くものです。
その他の開発候補者のための主な最新情報
•季節性インフルエンザ (インフルエンザ) (mRNA-1010、mRNA-1011、mRNA-1012、mRNA-1020、mRNA-1030):インフルエンザワクチン開発戦略の一環として、5種類のインフルエンザワクチンを開発しています。mRNA-1010は、当社独自のLNPのA H1N1、H3N2、B型インフルエンザB系統をコードする4つの異なるmRNA配列からなる単一の治験用ワクチンです。mRNA-1011とmRNA-1012は、WHOが推奨する4つの菌株で、ヘマグルチニン(HA)抗原(H3N2、H1N1など)の追加を目指しています。mRNA-1020とmRNA-1030は、ノイラミニダーゼ(NA)の追加を目的とした治験中のワクチンです抗原。
2022年3月、mRNA-1010の第2相試験の中間分析では、安全性に関する重大な懸念は確認されませんでした。免疫原性データは、インフルエンザA株(成人の病気の大部分を占める)の標準用量ワクチンよりも優れている可能性と一致しています。中間データは、B型インフルエンザ株のワクチンが標準用量よりも劣っていない可能性と一致しています(主に小児科で懸念されます)。2022年6月、最初の参加者はmRNA-1010に関する第3相安全性および免疫原性試験に投薬されました。南半球の国では約6,000人の成人が入学する予定です。さらに、必要に応じて、2022年秋に第3相有効性試験を実施する準備をしています。
4月に、mRNA-1020とmRNA-1030の第1/2相試験が最初の参加者に投与されたことを発表しました。現在、試験は完全登録されています。第1/2相ランダム化、観察者盲検、用量決定試験では、米国の18歳以上の健康な成人を対象としたmRNA-1020またはmRNA-1030の単回投与の安全性、反応原性、免疫原性を評価します。mRNA-1020とmRNA-1030の候補にはそれぞれ8つのmRNAが含まれており、ヘマグルチニンとノイラミニダーゼの両方を異なる用量で標的としていますと比率。
•呼吸器合胞体ウイルス (RSV) ワクチン (mRNA-1345):mRNA-1345は、融合後の状態と比較して優れた中和抗体反応を誘発する融合前のF糖タンパク質をコードするRSVに対するワクチンです。若年成人、高齢者、出産可能年齢の女性、日系高齢者、小児におけるmRNA-1345の耐容性、反応原性、免疫原性を評価するためのmRNA-1345の第1相研究が進行中です。現在進行中のRSV血清陽性の小児コホートを除いて、すべてのコホートが満員登録されています。高齢者コホートからのフェーズ1の中間データによると、50 µg、100 µg、または200 µgのmRNA-1345ワクチンを1回接種すると、RSV-Aに対する中和抗体価が約14倍、RSV-Bに対する中和抗体価が約10倍に上昇しました。約34,000人の参加者を対象としたmRNA-1345の重要なグローバル第2/3相試験の第3相試験の第3相部分が現在登録中です。さらに、50歳以上の成人を対象に、mRNA-1345を単独で、または季節性インフルエンザワクチンと同時投与した場合のmRNA-1345の安全性、忍容性、免疫原性を評価する第3相試験が完全登録されています。FDAは、60歳以上の成人を対象としたmRNA-1345のファストトラック指定を付与しました。
•COVIDとインフルエンザの複合ワクチン(mRNA-1073):mRNA-1073は、COVIDスパイクタンパク質とインフルエンザHA糖タンパク質をコードする混合ワクチンです。mRNA-1073とmRNA-1010とmRNA-1273を同時投与、およびmRNA-1010とmRNA-1273のみを比較する第1/2相試験が、18〜75歳の約1,050人の参加者を対象に進行中であり、試験は完全登録されています。
•HIVワクチン (mRNA-1644およびmRNA-1574):私たちは現在、生殖細胞を標的とするアプローチと免疫に焦点を当てたアプローチに基づく2つのHIV予防ワクチン戦略を進めています。私たちのmRNA-1644プログラムは、mRNAによって送達されるHIV免疫原のプライミングとブーストを連続的に投与することで、特定のクラスのB細胞応答を誘発し、それらの早期成熟を広域中和抗体(BnAb)の開発へと導くことができるという仮説を検証するために設計されています。BNAbの誘導はHIVワクチン接種の目標であると広く考えられており、これがそのプロセスの第一歩です。IAVI G002でテストされている免疫原は、IAVIとスクリップスリサーチの科学チームによって開発され、モデルナのmRNA技術を介して提供される予定です。IAVIが後援し、ゲイツ財団が支援する第1相試験が進行中です。さらに、mRNA-1574のHIV三量体mRNAワクチンの試験も進めています。主な仮説は、可溶性で膜結合型のHIVエンベロープ三量体mRNAワクチンは、HIVに感染していない人でも安全で耐容性が高く、自家中和抗体を誘発するというものです。第1相試験は現在進行中で、国立衛生研究所(NIH)内の国立アレルギー感染症研究所(NIAID)のエイズ部門(DAIDS)が後援し、資金提供しています。
•ニパワクチン (mRNA-1215):ニパウイルス(NiV)に対するワクチン候補であるmRNA-1215の第1相試験の最初の参加者は、2022年7月に投与されました。この試験はNIAIDが後援し、資金提供しています。mRNA-1215はNIHのワクチン研究センターと共同開発されたもので、第1相臨床試験はパンデミックへの備えに焦点を当てています。
•プロピオン酸血症 (PA) (mRNA-3927):プロピオン酸血症(PA)の治療薬であるmRNA-3927の第1/2相臨床試験が進行中で、第2コホートは定員に達しました。他の患者さんを追加のコホートに登録しています。第1/2相試験は、PA患者におけるmRNA-3927の安全性と忍容性を評価することを目的としています。PAは、ミトコンドリア酵素プロピオニルCoAカルボキシラーゼ(PCC)の欠陥によるまれな、生命を脅かす遺伝性代謝障害です。主に小児集団に影響を及ぼします。PAには、承認された酵素補充療法を含め、承認された治療法はありません。PAプログラムでは、FDAから希少小児疾患指定と希少疾病用医薬品指定を受け、欧州委員会から希少疾病用医薬品指定を受けています。FDAはmRNA-3927にもファストトラック指定を与えました。これは、私たちの細胞内治療モダリティでクリニックに入る最初の開発候補です。
•メチルマロン酸血症 (MMA) (mRNA-3705):メチルマロン酸血症(MMA)の治療薬であるmRNA-3705の第1/2相臨床試験が進行中で、最初のコホートは定員に達しました。この研究は現在、英国、カナダ、米国で開始されています。Modernaは、患者を他のコホートに登録しています。第1/2相試験は、MMA患者のmRNA-3705の安全性と忍容性を評価することを目的としています。MMAは、主にミトコンドリアの酵素メチルマロニル-コエンザイムAムターゼ(MUT)の欠損が原因で、生命を脅かすまれな遺伝性代謝障害です。主に小児集団に影響を及ぼします。タンパク質は複雑でミトコンドリアに局在しているため、酵素補充療法など、基礎疾患に対処する承認された治療法はありません。
•グリコーゲン蓄積症タイプ1a (GSD1a) (mRNA-3745): 2022年6月、当社のGSD1a治療薬候補であるmRNA-3745の第1相試験の最初の参加者に投与が行われました。GSD1aを患っている人は、グルコース-6-ホスファターゼが不足しているため、病的な血糖値のバランスが崩れます。 mRNA-3745は、ヒトG6Pase酵素をコードするIV投与mRNAで、GSD1a患者の細胞内酵素活性の不足または欠陥を回復させるように設計されています。FDAはmRNA-3745希少疾病用医薬品の指定を付与しました。
•IL-12 (MEDI1191): アストラゼネカは、MEDI1191を単独で、またはチェックポイント阻害薬であるデュルバルマブと組み合わせて腫瘍内注射する初期の臨床開発と進行中のオープンラベル多施設共同第1相臨床試験を主導しています。2022年4月、アストラゼネカは米国がん研究協会(AACR)の会議で最新のフェーズ1データを発表しました。腫瘍内投与のMEDI1191とデュルバルマブの併用は安全で、その併用により臨床的有益性に関する予備的な証拠が示されました。患者の 29% が部分奏効または12週間以上の病勢安定を示し、全体奏効が最も良好でした.
•個別化がんワクチン (mRNA-4157): 当社の個別化がんワクチン(PCV)は、現在、第1相および第2相試験で評価中です。高リスク切除された黒色腫の補助療法として、1mg用量のmRNA-4157をメルクのペムブロリズマブ(KEYTRUDA®)と併用して、ペムブロリズマブ単独と比較して調査したランダム化プラセボ対照第2相試験は、完全に登録されました(n=150)。第2相試験の主要評価項目は、12か月時点での無再発生存率です。複数のコホートのフェーズ1が進行中です。モデルナはmRNA-4157の世界的な商業権をメルクと共有しています。
私たちのパイプライン
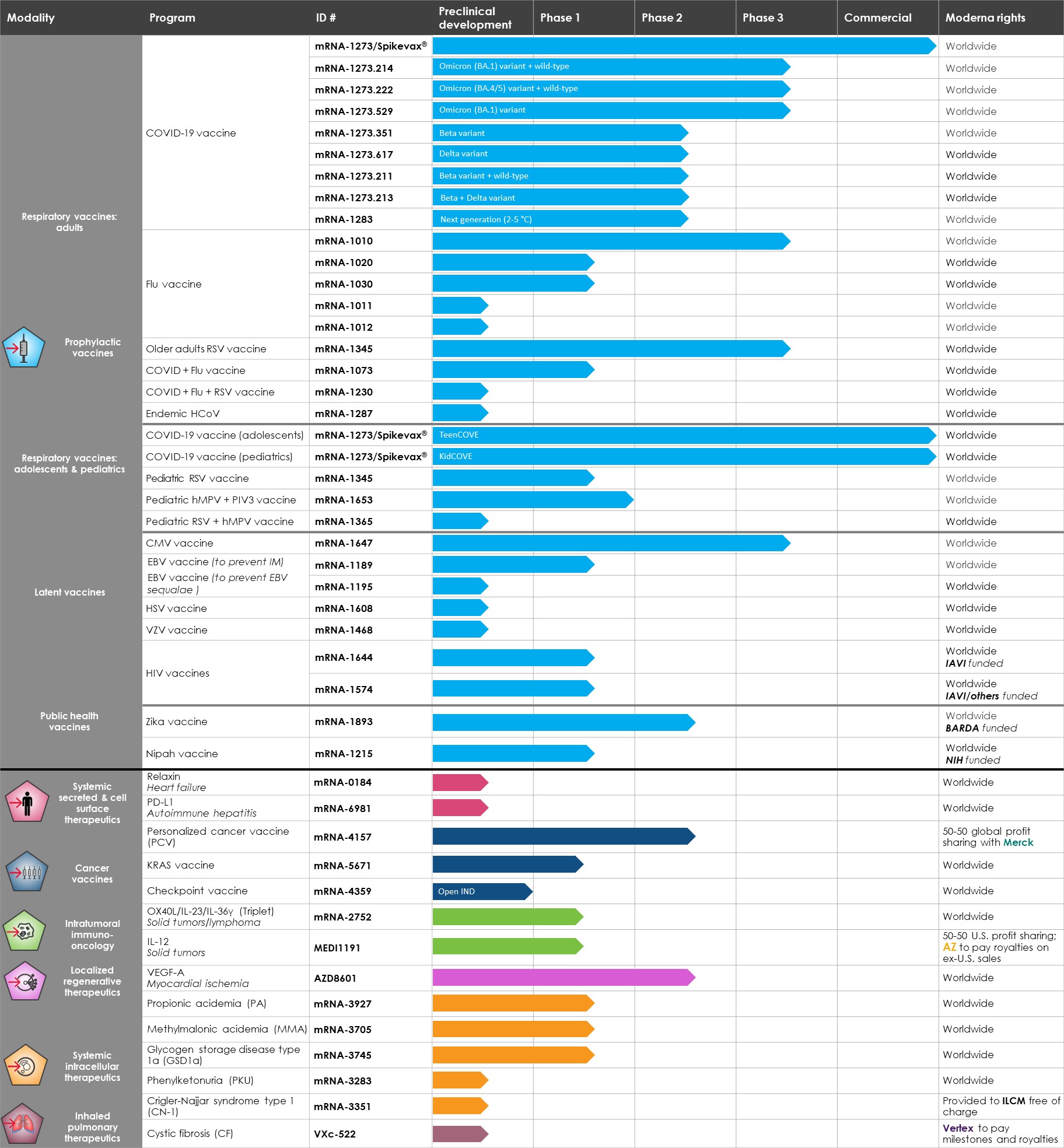
次のグラフは、呼吸器ワクチン、潜伏ワクチン、公衆衛生ワクチン、治療法別にグループ化された46の開発プログラムの現在のパイプラインを示しています。
略称:AZ、アストラゼネカ、BARDA、生物医学先端研究開発局、CMV、サイトメガロウイルス、DARPA、国防高等研究計画局、EBV、エプスタインバーウイルス、HIV、ヒトメタニューモウイルス、ILCM、人生を変える医薬品研究所、IL-12、インターロイキン12、IL-23、インターロイキン 23; IL-36γ、インターロイキン-36ガンマ、NIH、国立衛生研究所、OX40L、野生型OX40リガンド、RSV、呼吸器合胞体ウイルス、VEGF-A、血管内皮増殖因子A
私たちは7つのモダリティを開発しました。まとめると次のようになります。
•予防ワクチン: 当社の予防ワクチンのモダリティには現在32の開発プログラムが含まれており、そのうち23件が臨床試験に入っています。小児科では、RSVワクチン(mRNA-1345)、インフルエンザワクチン(mRNA-1020とmRNA-1030)、COVIDとインフルエンザの混合ワクチン(mRNA-1073)、HMPV/PIV3ワクチン(mRNA-1653)、EBVワクチン(mRNA-1189)、HIVワクチン(mRNA-1644とmRNA-15など)の第1相試験が進行中です。そしてニパワクチン(mRNA-1215)。ジカワクチン(mRNA-1893)の第2相試験が進行中です。インフルエンザワクチン(mRNA-1010)、高齢者を対象としたRSVワクチン(mRNA-1345)、CMVワクチン(mRNA-1647)の第3相試験が進行中です。当社のCOVID-19ワクチン(mRNA-1273)は、上記で詳細に説明されています。予防ワクチンのモダリティに含まれる8つの前臨床プログラムは、COVID-19、インフルエンザとRSVの複合ワクチン(mRNA-1230)、小児用RSVとHMPVの複合ワクチン(mRNA-1365)、汎HCoVワクチン(mRNA-1278)、季節性インフルエンザワクチン(mRNA-1011とmRNA-1012)、長期の後遺症を防ぐためのEBVワクチンです。(mRNA-1195)、VZVワクチン (mRNA-1468)、およびHSVワクチン (mRNA-1608)。公衆衛生プログラムの一環として提供されている他の3つのワクチン、H10N8ワクチン(mRNA-1440)、H7N9インフルエンザワクチン(mRNA-1851)、チクングニアワクチン(mRNA-1388)のフェーズ1の測定値が陽性でしたが、政府やその他の資金提供なしに開発が進められていません。
•全身分泌薬および細胞表面治療薬: 現在、全身分泌薬と細胞表面治療薬の開発候補が2つあります。私たちの秘密プログラムには、心臓疾患用のリラキシン(mRNA-0184)と自己免疫性肝炎用のPD-L1(mRNA-6981)があり、現在前臨床開発中です。初期の臨床データが得られた後、また進化する競争環境に対応して、IL-2プログラム(mRNA-6231)を中止します。以前、このモダリティにおけるチクングニア抗体プログラム(mRNA-1944)の陽性データを発表しましたが、外部からの資金提供なしにチクングンヤ抗体プログラムを進めることは考えておらず、現時点ではさらなる開発は進めていません。
•がんワクチン:私たちは現在、がんワクチンのモダリティの中で3つのプログラムを開発しています。私たちの個別化がんワクチンプログラム(mRNA-4157)は、メルクと共同で開発されており、多剤併用第I相試験とランダム化第2相試験が進行中で、完全登録されています。このモダリティの2つ目のプログラムは、KRASワクチン(mRNA-5671)です。私たちはメルクのKRASワクチンのすべての権利を保有しており、プログラムの次のステップを検討しています。3つ目のプログラムは、チェックポイントワクチン(mRNA-4359)です。 これはFDAから安全審査を受けています。
•腫瘍内免疫腫瘍学: このモダリティには2つのプログラムがあります。私たちの最初のプログラムであるOx40L/IL-23/IL-36γ(トリプレット)(mRNA-2752)は、トリプレット(mRNA-2752)を単独で、またはデュルバルマブ(抗PD-L1)と組み合わせて腫瘍内注射するオープンラベルの多施設共同研究として設計された第1相試験中です。2つ目のプログラムであるIL-12(MEDI1191)は、アストラゼネカと共同で開発中です。アストラゼネカは現在、MEDI1191を単独で、またはチェックポイント阻害薬であるデュルバルマブと組み合わせて腫瘍内注射するオープンラベル多施設共同第1相臨床試験を登録しています。
•局所的な再生治療薬:アストラゼネカと共同で開発した当社のローカライズされたVEGF-AプログラムであるAZD8601は、糖尿病患者における安全性、忍容性、タンパク質産生、および活性を説明する第1a/b相試験を完了しました。この研究は、安全性と忍容性を説明するという主な目的と、AZD8601投与後のタンパク質産生と血流の変化を実証するという副次的な目的を達成しました。これらのデータは、ワクチンの設定以外での当社のmRNA技術のメカニズムの臨床的証拠を提供すると信じています。 2021年、第2相試験は、3 mgの用量に対するAZD8601の安全性と忍容性という主要評価項目を達成しました。11人の患者を対象とした研究では、7人がAZD8601 VEGF-A mRNAで治療され、4人がプラセボ注射を受けました。プラセボと比較して、心不全有効性領域のエンドポイントでは、左心室駆出率(LVEF)の増加や患者報告の転帰などの数値的傾向が観察されました。さらに、AZD8601で治療された7人の患者全員が、6か月のフォローアップ時にNT-proBNP(心不全患者で上昇するホルモンレベルを測定するバイオマーカー)のレベルが心不全限界を下回っていました。これは、プレースで治療された患者4人のうちの1人と比較していいえ。ポートフォリオレビューの結果、アストラゼネカはAZD8601の権利を当社に返還しました。プログラムの次のステップを検討しています。
•全身の細胞内治療薬: 現在、全身性細胞内治療薬の開発候補が5つあります。私たちの細胞内プログラムは、プロピオン酸血症(PA)(mRNA-3927)、メチルマロン酸血症(MMA)(mRNA-3705)、グリコーゲン貯蔵障害1a型(GSD1a)(mRNA-3745)、フェニルケトン尿症(PKU)(mRNA-3283)、およびクリグラー・ナジャー症候群1型(CN-1) (mRNA-3351)。PA (mRNA-3927)、MMA (mRNA-3705)、GSD1a (mRNA-3745) の第1相臨床試験が進行中です。PKU (mRNA-3283) とCN-1 (mRNA-3351) は現在前臨床開発中です。私たちは、生活を変える医薬品研究所(ILCM)と、mRNA-3351を前払い金なしで、下流への支払いなしにILCMにライセンスする契約を締結しました。ILCMはmRNA-3351の臨床開発を担当します。
•吸入肺治療薬:現在、吸入肺治療薬の開発候補が1つあります。私たちのプログラムは、バーテックス・ファーマシューティカルズと共同で、嚢胞性線維症(CF(VxC-522)に対処しています。VXC-522は、CFTRタンパク質をまったく産生しない10%の患者を治療するために、肺の細胞が機能性嚢胞性線維症の膜貫通コンダクタンス調節因子(CFTR)タンパク質を産生できるようにすることで、CFの根本的な原因を治療するために設計されたmRNA治療薬です。INDを可能にする研究が進行中で、バーテックスは2022年にこのプログラムのINDを提出する予定です。モデルナは、VXC-522の世界的な商業権をVertexにライセンスしています。
金融業務の概要
収益
次の表は、表示されている期間の収益をまとめたものです (百万単位)。
| | | | | | | | | | | | | | | | | | | | | | | | | | |
| | 6月30日に終了した3か月間 | | 6月30日に終了した6か月間 |
| | 2022 | | 2021 | | 2022 | | 2021 |
収益: | | | | | | | | |
| 製品販売 | | $ | 4,531 | | | $ | 4,197 | | | $ | 10,456 | | | $ | 5,930 | |
| 助成金収入 | | 183 | | | 139 | | | 309 | | | 333 | |
| コラボレーション収益 | | 35 | | | 18 | | | 50 | | | 28 | |
総収入 | | $ | 4,749 | | | $ | 4,354 | | | $ | 10,815 | | | $ | 6,291 | |
2022年6月30日までの3か月間で、当社のCOVID-19ワクチンの製品売上高は45億ドルに達しました。そのうち15億ドルは米国で、31億ドルはヨーロッパやその他の国々で生み出されました。2021年6月30日までの3か月間で、当社のCOVID-19ワクチンの製品売上高は42億ドルに達しました。そのうち21億ドルは米国で、21億ドルはヨーロッパやその他の国々で生み出されました。
2022年6月30日までの6か月間で、当社のCOVID-19ワクチンの製品売上高は105億ドルに達しました。そのうち24億ドルは米国で、81億ドルはヨーロッパやその他の国々で生み出されました。2021年6月30日までの6か月間で、当社のCOVID-19ワクチンの製品売上高は59億ドルに達しました。そのうち34億ドルは米国で、25億ドルはヨーロッパやその他の国々で生み出されました。
2022年6月30日現在、2023年までのCOVID-19ワクチンの納入について、供給契約に基づいて受領または請求可能な顧客預金に関連する43億ドルの繰延収益がありました。現在締結されている2022年のCOVID-19ワクチンの供給契約に基づくと、当社のCOVID-19ワクチン製品の売上は、上半期と比較して2022年の後半も概ね横ばいになると予想しています。また、当社のCOVID-19二価ブースター候補の潜在的な販売承認のタイミングにより、2022年の第4四半期の製品売上高は2022年の第3四半期よりも大きくなると予想しています。
製品販売以外では、当社の収益は主にBARDA、DARPA、ゲイツ財団などの政府支援機関や民間組織、および潜在的なmRNA医薬品の発見、開発、商品化のためのアストラゼネカ、メルク、バーテックスとの戦略的提携から得られています。
助成金収入は、提示期間における以下のようになっていました(単位:百万単位)。
| | | | | | | | | | | | | | | | | | | | | | | |
| 6月30日に終了した3か月間 | | 6月30日に終了した6か月間 |
| 2022 | | 2021 | | 2022 | | 2021 |
| 助成金収入: | | | | | | | |
バルダ (1) | $ | 179 | | | $ | 134 | | | $ | 301 | | | $ | 326 | |
| その他 | 4 | | | 5 | | | 8 | | | 7 | |
| 助成金の総収入は | $ | 183 | | | $ | 139 | | | $ | 309 | | | $ | 333 | |
_______
(1) 2022年6月30日までの3か月間、BARDAの助成金収入のうち1億7,500万ドルが当社のmRNA-1273プログラムに関連し、400万ドルがジカワクチンプログラムに関連していました。2022年6月30日までの6か月間、BARDA助成金の収入のうち2億9,500万ドルは当社のmRNA-1273プログラムに関連し、600万ドルはジカワクチンプログラムに関連していました。
当社の戦略的提携によるコラボレーション収益は、提示された期間における以下のようになっていました(百万単位)。
| | | | | | | | | | | | | | | | | | | | | | | |
| 6月30日に終了した3か月間 | | 6月30日に終了した6か月間 |
| 2022 | | 2021 | | 2022 | | 2021 |
コラボレーション収入: | | | | | | | |
アストラゼネカ | $ | 4 | | | $ | 4 | | | $ | 4 | | | $ | 4 | |
メルク | 5 | | | 4 | | | 15 | | | 4 | |
頂点 | 25 | | | 9 | | | 29 | | | 18 | |
| その他 | 1 | | | 1 | | | 2 | | | 2 | |
コラボレーション総収益 | $ | 35 | | | $ | 18 | | | $ | 50 | | | $ | 28 | |
BARDAとの契約から引き続き資金を受け取ることを期待しています。2022年6月30日現在、当社のmRNA-1273ワクチンの開発のためにBARDAとの契約に基づいて得た収益を差し引いた残りの資金は2億300万ドルでした。既存または将来の潜在的な製品が収益を生み出す範囲で、将来の製品需要、当社のmRNA医薬品の開発、その他の要因における多くの不確実性により、当社の収益は変動する可能性があります。
研究開発費用
私たちは、従業員やインフラ資源をプラットフォームの発展やプログラムの発見と開発に使用しています。進行中のプログラムの数が多く、複数のプロジェクトにまたがってリソースを使用できるため、研究開発プログラムで発生する間接的または共同運営費は、通常、プログラムやモダリティごとに記録または管理されません。次の表は、当社の研究開発費を反映しています。これには、2022年6月30日および2021年6月30日までの3か月および6か月の間に、モダリティ別にまとめられた直接的なプログラム固有の費用と、その他の研究開発費に要約された間接的または共有された運営費(百万単位)が含まれます。
| | | | | | | | | | | | | | | | | | | | | | | | | | |
| | 6月30日に終了した3か月間 | | 6月30日に終了した6か月間 |
| | 2022 | | 2021 | | 2022 | | 2021 |
| モダリティ別のプログラム費用: | | | | | | | | |
| 予防ワクチン | | $ | 336 | | | $ | 241 | | | $ | 526 | | | $ | 489 | |
| 全身分泌薬と細胞表面治療薬 | | 2 | | | 1 | | | 3 | | | 2 | |
| がんワクチン | | 2 | | | 7 | | | 5 | | | 24 | |
| 腫瘍内免疫腫瘍学 | | 6 | | | 7 | | | 12 | | | 13 | |
| | | | | | | | |
| 全身の細胞内治療薬 | | 9 | | | 6 | | | 13 | | | 11 | |
吸入肺治療薬 (1) | | 3 | | | — | | | 5 | | | — | |
モダリティ別のプログラム固有の費用の総額 (2) | | $ | 358 | | | $ | 262 | | | $ | 564 | | | $ | 539 | |
| その他の研究開発費: | | | | | | | | |
| ディスカバリープログラム | | 41 | | | 15 | | | 71 | | | 28 | |
| プラットフォームリサーチ | | 31 | | | 27 | | | 65 | | | 52 | |
| 技術開発と未配分製造費 | | 195 | | | 53 | | | 329 | | | 86 | |
| 発見および開発費の共有 | | 66 | | | 49 | | | 196 | | | 88 | |
| 株式報酬制度 | | 19 | | | 15 | | | 39 | | | 29 | |
| 研究開発費の合計 | | $ | 710 | | | $ | 421 | | | $ | 1,264 | | | $ | 822 | |
__________
(1)吸入肺治療薬モダリティは2021年の第4四半期に追加されました。
(2)2022年6月30日と2021年6月30日の時点で、それぞれ合計43人と30人の開発候補者が含まれています。プログラム固有の費用には、外部費用と、発売前のインベントリ、mRNAの供給と消耗品の割り当てられた製造コストが含まれ、プログラムが社内で開発に進められた期間の開始時に反映されるか、開発が中止された場合は中止されます。
A「モダリティ」共通の製品機能と、それに関連するmRNA技術、デリバリー技術、製造プロセスの組み合わせを備えたプログラムのグループを指します。上の表にまとめられているモダリティ別のプログラム固有の費用には、主に外部コンサルタント、中央研究所、研究施設、委託製造機関に支払う手数料、発売前の在庫、mRNA供給、消耗品の配分製造コストなど、外部費用で構成される外部費用が含まれます。発売前のインベントリ、前臨床研究および臨床試験のためのmRNA供給の取得と製造にかかる費用は、発生した場合は未配分の製造費に計上され、プログラム固有の製造が完了した後にプログラム固有の製造コストに配分されます。特定のプログラムに製造コストを配分するタイミングは、プログラムの開発と制作スケジュールによって異なります。私たちは通常、株式ベースの報酬、一般的なプラットフォーム研究、技術開発に関連する費用、その他の共有費用を含む人事関連の費用をプログラムごとに配分しません。そのため、これらの費用は、モダリティ別のプログラム別経費の概要から除外されました。
創薬プログラムの費用は、前臨床発見段階における当社のプログラムの研究活動に関連する費用で、主にCROとラボサービスの外部費用、および前臨床mRNAの供給と消耗品の配分製造費で構成されています。
プラットフォームの研究費は、主にmRNA科学、デリバリーサイエンス、製造プロセス設計の技術的進歩を開発するための費用です。これらの費用には、人件費、コンピューター機器、設備、前臨床mRNAの供給と消耗品、およびプラットフォーム研究を支援するためのその他の管理費が含まれます。技術開発と未配分製造費は、主にプログラム以外の製造プロセス開発と製造コストに関連しています。
共同開発費とは、人件費やその他の費用などの研究開発費で、開発プログラム、発見プログラム、プラットフォーム研究、技術開発および未配分製造費、株式ベースの報酬、その他の費用には含まれません。
これまで、当社の総営業費の最大の構成要素は、製品候補の前臨床および臨床開発、プラットフォームの開発、mRNA技術、製造技術などの研究開発活動への投資でした。
私たちは引き続きmRNA-1273の適応拡大を追求し、変異型特異的COVID-19ワクチン候補と次世代COVID-19ワクチン候補の開発を続けているため、引き続き多額の追加費用が発生すると予想されます。mRNA-1273の開発を加速するというBARDAの合意に関連して、公約された資金提供の範囲内の助成金の収入と費用は2022年も継続すると予想されます。BARDAの資金は、BARDAから払い戻しを受けることを条件として、BARDA契約の対象となる費用を相殺することが期待されます。2022年6月30日現在、収益を差し引いた残りの利用可能な資金は2億300万ドルでした。
既知または未知のリスクや不確実性に対する期待や結果の変化は、予想される研究開発費に重大な影響を与える可能性があります。継続的な研究開発は、私たちの事業の継続的な活動の中心です。CMVワクチン、RSVワクチン、インフルエンザワクチン、COVID-19ワクチンなど、臨床開発の後期段階にある治験薬は、主に後期段階の臨床試験の規模と期間が長くなるため、一般的に臨床開発の初期段階にあるものよりも開発コストが高くなります。治験薬が開発段階を経て追加のプログラムを特定して開発するにつれて、研究開発コストは当面の間増加し続けると予想しています。私たちの治験薬の商業化の成功には、将来の試験デザインやさまざまな規制要件など、さまざまな要因が関係していますが、その多くは、治験薬の開発の初期段階のため、現時点では正確に決定できません。さらに、私たちの制御が及ばない将来の商業的要因や規制要因は、私たちの臨床開発プログラムや計画に影響を与えます。
重要な会計方針と重要な判断と見積もり
2022年6月30日までの3か月間、当社の要約連結財務諸表の作成における重要な会計方針と見積もりに、2021年のForm 10-Kで開示されているものと比べて重要な変更はありませんでした。
操作の結果
次の表は、提示された各期間の要約連結損益計算書(百万単位)をまとめたものです。
| | | | | | | | | | | | | | | | | | | | | | | |
| 6月30日に終了した3か月間 | | 2022年と2021年を比較して変化させましょう |
| 2022 | | 2021 | | $ | | % |
収益: | | | | | | | |
| 製品収益 | $ | 4,531 | | | $ | 4,197 | | | $ | 334 | | | 8% |
| 助成金収入 | 183 | | | 139 | | | 44 | | | 32% |
| コラボレーション収益 | 35 | | | 18 | | | 17 | | | 94% |
総収入 | 4,749 | | | 4,354 | | | 395 | | | 9% |
営業経費: | | | | | | | |
| 売上原価 | 1,381 | | | 750 | | | 631 | | | 84% |
| 研究開発 | 710 | | | 421 | | | 289 | | | 69% |
| 販売、一般および管理 | 211 | | | 121 | | | 90 | | | 74% |
営業費用の合計 | 2,302 | | | 1,292 | | | 1,010 | | | 78% |
| 事業からの収入 | 2,447 | | | 3,062 | | | (615) | | | (20)% |
利息収入 | 40 | | | 3 | | | 37 | | | 1,233% |
| その他の費用、純額 | (13) | | | (2) | | | (11) | | | 550% |
| 税引前利益 | 2,474 | | | 3,063 | | | (589) | | | (19)% |
| 所得税引当金 | 277 | | | 283 | | | (6) | | | (2)% |
| 当期純利益 | $ | 2,197 | | | $ | 2,780 | | | $ | (583) | | | (21)% |
| | | | | | | | | | | | | | | | | | | | | | | |
| 6月30日に終了した6か月間 | | 2022年と2021年を比較して変化させましょう |
| 2022 | | 2021 | | $ | | % |
収益: | | | | | | | |
| 製品収益 | $ | 10,456 | | | $ | 5,930 | | | $ | 4,526 | | | 76% |
| 助成金収入 | 309 | | | 333 | | | (24) | | | (7)% |
| コラボレーション収益 | 50 | | | 28 | | | 22 | | | 79% |
総収入 | 10,815 | | | 6,291 | | | 4,524 | | | 72% |
営業経費: | | | | | | | |
| 売上原価 | 2,398 | | | 943 | | | 1,455 | | | 154% |
| 研究開発 | 1,264 | | | 822 | | | 442 | | | 54% |
| 販売、一般および管理 | 479 | | | 198 | | | 281 | | | 142% |
営業費用の合計 | 4,141 | | | 1,963 | | | 2,178 | | | 111% |
| 事業からの収入 | 6,674 | | | 4,328 | | | 2,346 | | | 54% |
利息収入 | 55 | | | 7 | | | 48 | | | 686% |
| その他の費用、純額 | (26) | | | (12) | | | (14) | | | 117% |
| 税引前利益 | 6,703 | | | 4,323 | | | 2,380 | | | 55% |
| 所得税引当金 | 849 | | | 322 | | | 527 | | | 164% |
| 当期純利益 | $ | 5,854 | | | $ | 4,001 | | | $ | 1,853 | | | 46% |
収益
2022年6月30日までの3か月間の総収益は、2021年の同時期と比較して3億9,500万ドル、つまり 9% 増加しました。これは主に、当社のCOVID-19ワクチンの販売による製品売上の増加によるものです。2022年6月30日までの3か月間の製品収益は、2021年の同時期と比較して3億3,400万ドル、つまり 8% 増加しました。これは主に、良好な顧客構成による平均販売価格の上昇によるものです。2022年6月30日までの3か月間の助成金収入は、2021年の同時期と比較して4,400万ドル(32%)増加しました。これは主に、当社のmRNA-1273ワクチン開発に関連するBARDAからの収益の増加によるものです。
2022年6月30日までの6か月間の総収益は、2021年の同時期と比較して45億ドル、つまり 72% 増加しました。これは主に、当社のCOVID-19ワクチンの販売による製品売上の増加によるものです。2022年6月30日までの6か月間の製品収益は、主に製造能力の増強により、2021年の同時期と比較して45億ドル、つまり 76% 増加しました。2022年6月30日までの6か月間の助成金収入は、2021年の同時期と比較して2,400万ドル、つまり 7% 減少しました。これは主に、mRNA-1273ワクチン開発に関連するBARDAからの収益の減少によるものです。
営業経費
売上原価
2022年6月30日までの3か月間の売上原価は、第三者からのロイヤルティ1億5,700万ドルを含めて14億ドルでした。2022年6月30日までの3か月間の売上原価は、2021年の同時期と比較して6億3,100万ドル、つまり 84% 増加しました。2022年6月30日までの3か月間の製品売上に対する売上原価の割合は 30% でした。これに対し、2021年同期は 18% でした。これらの増加は主に、当社のCOVID-19ワクチンに関連する過剰在庫や古くなった在庫の減価償却、原材料の確約による損失、製品需要の変化による未使用の製造能力によるものです。
2022年6月30日までの6か月間の売上原価は、第三者からのロイヤルティ3億6,400万ドルを含めて24億ドルでした。2022年6月30日までの6か月間の売上原価は、2021年の同時期と比較して15億ドル、つまり 154% 増加しました。これは主に、販売量の増加、在庫の減少、原材料の確定購入契約による損失によるものです。2022年6月30日までの6か月間の製品売上に対する売上原価の割合は 23% でした。これに対し、2021年同期は 16% でした。この増加は主に、当社のCOVID-19ワクチンに関連する過剰在庫や陳腐な在庫、原材料の確定購入契約による損失による減価償却によるもので、程度は低いものの、製造能力の未利用と、2021年の第1四半期にプラスの影響を与えた発売前の在庫特典の欠如によるものです。2021年6月30日までの6か月間に販売された在庫を原価で評価すると、その期間の売上原価は製品売上の11億ドル、つまり19%になります。
COVID-19ワクチンのパンデミックから季節的な市場環境に移行するにつれて、製造コストが増加すると予想しています。 この変化により、2022年通年の売上原価は、2021年に経験した割合よりも製品売上高に占める割合が高くなると予想しています。
研究開発費用
2022年6月30日までの3か月間の研究開発費は、2021年の同時期と比較して2億8,900万ドル、つまり 69% 増加しました。この増加は主に、臨床試験費用が1億6200万ドル、人事関連費用が5,700万ドル、コンサルティングと外部サービスが3,900万ドル増加したことによるものです。
2022年6月30日までの6か月間の研究開発費は、2021年の同時期と比較して4億4,200万ドル、つまり 54% 増加しました。この増加は主に、臨床試験費用が2億ドル、人件費が9,600万ドル、コンサルティングと外部サービスが6,200万ドル、技術と施設関連の費用が3,200万ドル、臨床試験材料の製造コストが2,700万ドル増加したことによるものです。2022年の3か月と6か月の期間のこれらの増加は、主に臨床開発の増加、特にCOVID-19ワクチンとRSVプログラム、および人員数の増加によるものです。
mRNA-1273の適応拡大を継続的に進め、パイプラインの開発を続け、製品候補を後期段階の開発、特にRSV、インフルエンザ、CMVワクチンのプログラムに進めるため、2022年には研究開発費が増加すると予想しています。さらに、変異特異的なCOVID-19候補と次世代のCOVID-19ワクチン候補の開発に関連して、多額の費用が発生することも予想されます。
販売費、一般管理費
2022年6月30日までの3か月間の販売費、一般管理費は、2021年の同時期と比較して9,000万ドル、つまり 74% 増加しました。この増加は主に、ディストリビューター手数料とマーケティング費が3,100万ドル増加し、人件費が2,700万ドル増加したことによるものです。2022年の3か月間のこれらの増加は、主に当社のCOVID-19ワクチンの商品化関連の活動と人員数の増加によるものです。
2022年6月30日までの6か月間の販売費、一般管理費は、2021年の同時期と比較して2億8,100万ドル、つまり 142% 増加しました。この増加は主に、ディストリビューター手数料の6,600万ドルの増加、人事関連費用の5,800万ドルの増加、モデルナ慈善財団(財団)への寄付が5,000万ドル、コンサルティングと外部サービスの増加が3,700万ドル、マーケティング費が2,700万ドル増加したことによるものです。2022年の6か月間のこれらの増加は、主に当社のCOVID-19ワクチンの商品化関連の活動、人員の増加、および財団の立ち上げによるものです。
COVID-19ワクチンの商業化を支援するためのグローバルな商業、規制、販売、マーケティングのインフラを構築し続け、プログラムの数と事業運営を拡大し続けるため、2022年には販売費、一般管理費が増加すると予想しています。
利息収入
2022年6月30日までの3か月間の利息収入は、2021年の同時期と比較して3,700万ドル増加しました。2022年6月30日までの6か月間の利息収入は、2021年の同時期と比較して4,800万ドル増加しました。2022年の3か月と6か月間の有価証券への投資による利息収入の増加は、主に投資残高の増加と全体的な金利環境の上昇によるものです。
その他の費用、純額
次の表は、提示された各期間の純額 (百万単位) のその他の費用をまとめたものです。
| | | | | | | | | | | | | | | | | | | | | | | |
| 6月30日に終了した3か月間 | | 2022年と2021年を比較して変化させましょう |
| 2022 | | 2021 | | $ | | % |
| 投資による(損失)利益 | $ | (8) | | | $ | 2 | | | $ | (10) | | | (500)% |
| 支払利息 | (5) | | | (5) | | | — | | | —% |
| その他の収益、純額 | — | | | 1 | | | (1) | | | (100)% |
| その他の費用合計、純額 | $ | (13) | | | $ | (2) | | | $ | (11) | | | 550% |
| | | | | | | | | | | | | | | | | | | | | | | |
| 6月30日に終了した6か月間 | | 2022年と2021年を比較して変化させましょう |
| 2022 | | 2021 | | $ | | % |
| 投資による(損失)利益 | $ | (14) | | | $ | 2 | | | $ | (16) | | | (800)% |
| 支払利息 | (11) | | | (8) | | | (3) | | | 38% |
| その他の費用、純額 | (1) | | | (6) | | | 5 | | | (83)% |
| その他の費用合計、純額 | $ | (26) | | | $ | (12) | | | $ | (14) | | | 117% |
2022年6月30日までの3か月間のその他の費用の合計は、2021年の同時期と比較して1,100万ドル増加しました。2022年6月30日までの6か月間のその他の費用の合計、純額は、2021年の同時期と比較して1,400万ドル増加しました。2022年の3か月と6か月の期間のその他の費用の純増加は、主に売却可能な債券の実現損失によるものです。当社の支払利息は、主にファイナンスリースに関連しています。参照してください ノート 11当社の要約連結財務諸表へ
所得税
2022年6月30日までの3か月間の所得税引当金は、2021年の同時期と比較して600万ドル減少しました。これは主に税引前利益の減少によるものですが、実効税率の引き上げにより一部相殺されました。2022年6月30日までの6か月間の所得税引当金は、主に税引前利益の増加と実効税率の引き上げにより、2021年の同時期と比較して5億2,700万ドル増加しました。2022年6月30日までの3か月および6か月間の実効税率の上昇は、主に当社の繰延税金資産の大部分に対する評価引当金の解除に関連して2021年に記録された税制上の優遇措置と、株式ベースの報酬による超過利益の減少によるもので、2022年の外国由来の無形資産所得給付の増加によって一部相殺されました。当社の実効税率は、主に2021年に繰延税金資産の大部分に対する評価引当金が解除されることにより、2021年と比較して2022年通年の実効税率が上昇すると予想しています。
流動性と資本資源
次の表は、提示された各期間の現金、現金同等物、投資、および運転資金をまとめたものです(百万単位)。
| | | | | | | | | | | | | | |
| | 6月30日 | | 12月31日 |
| | 2022 | | 2021 |
| 金融資産: | | | | |
| 現金および現金同等物 | | $ | 2,873 | | | $ | 6,848 | |
| 投資 | | 5,024 | | | 3,879 | |
| 投資、非流動投資 | | 10,162 | | | 6,843 | |
| 合計 | | $ | 18,059 | | | $ | 17,570 | |
| | | | |
| 運転資本: | | | | |
| 流動資産 | | $ | 13,563 | | | $ | 16,071 | |
| 流動負債 | | 6,812 | | | 9,128 | |
| 合計 | | $ | 6,751 | | | $ | 6,943 | |
当社の現金、現金同等物および投資は、主に流動性と資本保全を目的として、当社の投資方針に従って投資されます。主に政府債と社債で構成される投資は、公正価値で記載されています。2022年6月30日現在の現金、現金同等物、投資は、2021年12月31日と比較して4億8,900万ドル、つまり 3% 増加しました。2022年6月30日までの6か月間で、営業から生み出された現金は31億ドルでしたが、19億ドルの普通株式の買戻し、2億1,900万ドルの不動産および設備の購入、および3億2,600万ドルの売却可能な負債の含み損失によって一部相殺されました。
2022年6月30日現在、流動資産から流動負債を差し引いた運転資本は、2021年12月31日と比較して1億9,200万ドル、つまり 3% 減少しました。これは主に、受領した顧客預金を超える繰延収益から計上される収益が22億ドル減少したことと、支払われる所得税が5億2,700万ドル減少したことによるものです。これは、主に長期有価証券の購入、当社の普通株式の買戻し、および所得税の支払いにより、現金、現金同等物および短期投資が28億ドル減少したことで相殺されました。
2022年6月30日現在、貸借対照表外の取り決めはありませんでした。
キャッシュフロー
次の表は、提示された各期間の主な資金源と使用方法をまとめたものです (百万単位)。
| | | | | | | | | | | |
| 6月30日に終了した6か月間 |
| 2022 | | 2021 |
| 提供した純現金(使用量): | | | |
営業活動 | $ | 3,067 | | | $ | 7,034 | |
投資活動 | (5,073) | | | (4,058) | |
資金調達活動 | (1,969) | | | 2 | |
| 現金、現金同等物および制限付現金の純増加(減少) | $ | (3,975) | | | $ | 2,978 | |
営業活動
当社の事業からのキャッシュフローは、主に、当社のCOVID-19ワクチン供給契約に関連する顧客の預金や売掛金、および特定の政府支援機関や民間組織、戦略的提携から集められた現金から得ています。営業活動によるキャッシュフローは、事業を支援するための営業費用と運転資金に現金を使用することに大きく影響されます。
2020年の第3四半期から、COVID-19ワクチンの供給について、米国政府、その他の国際政府、Gaviと供給契約を締結し、前払い金を受け取りました。2022年6月30日現在、受領または請求可能な顧客預金に関連する繰延収益は43億ドルです。さらに、私たちのmRNA-1273プログラムに関連して、BARDAとの契約から引き続き資金提供を受ける予定です。2022年6月30日現在、BARDAからの残りの資金は、収益を差し引いて2億300万ドルでした。
2022年6月30日までの6か月間の営業活動によって提供された純現金は31億ドルで、59億ドルの純利益と8,300万ドルの非現金調整で構成され、27億ドルの資産と負債の純変動によって一部相殺されました。非現金項目には、主に3億7,600万ドルの繰延所得税、1億5,500万ドルの減価償却、および9,400万ドルの株式報酬が含まれていました。資産と負債の純変動は、主に繰延収益の24億ドルの減少、支払われる所得税の5億2,700万ドルの減少、4億8,000万ドルの在庫の増加、および前払費用およびその他の資産の増加によるもので、売掛金の4億8,400万ドルの減少、未払負債の3億500万ドルの増加によって一部相殺されましたその他の負債は2億6,300万ドルの増加。
営業活動によって提供された純現金は、2022年6月30日までの6か月間で2021年の同時期と比較して40億ドル、つまり 56% 減少しました。これは主に、受領した顧客預金を超える繰延収益と所得税の支払いの増加による収益によるものですが、製品売上の増加と売掛金の回収量の増加により一部相殺されました。
投資活動
私たちの主な投資活動は、借地権の改善、製造、研究所、コンピューター機器、ソフトウェアのための投資と資本支出の購入、売却、満期です。
2022年6月30日までの6か月間の投資活動に使用された純現金は51億ドルで、これには主に87億ドルの有価証券の購入と2億1,900万ドルの資産および設備の購入が含まれていますが、25億ドルの有価証券の売却による収益と14億ドルの有価証券の満期による収益によって一部相殺されました。
投資活動に使用された純現金は、2022年6月30日までの6か月間で2021年の同時期と比較して10億ドル、つまり 25% 増加しました。これは主に、有価証券の購入、売却、満期に関連する時期の違いと、当社の投資ポートフォリオ構成の変化によるものです。
資金調達活動
2022年6月30日までの6か月間の財務活動に使用された純現金は20億ドルでした。これは主に19億ドルの普通株式の買戻しによるものです。
財務活動に使用された純現金は、主に普通株式の買戻しにより、2022年6月30日までの6か月間で2021年の同時期と比較して20億ドル増加しました。
運営と資金の要件
2022年6月30日現在の当社の主な資金源は、現金および現金同等物、投資、および事業から生み出されると予想される現金でした。2020年12月に最初の商用製品が承認された後、2021年に終了した年度の純利益は122億ドルになりました。創業から2020年末まで、多額の研究開発費により、事業から多額の損失を被りました。2022年6月30日現在、私たちは158億ドルの収益を留保しています。
研究開発活動の実施、組織の運営、資本支出のニーズへの対応、自社株買いプログラムの資金調達に必要な予想営業費用など、将来的に多額の資本要件があります(参照 ノート 13当社の要約連結財務諸表へ)。特に開発候補の研究開発や治験薬の臨床活動を続ける中で、継続的な活動に関連して経費が増えると予想しています。また、国際的な供給パートナーや製造パートナーとの取り決めを含め、製造コストに関連する費用も増加すると予想しています。SARS-CoV-2の変異株に対する新世代のブースターやワクチンの開発、COVID-19ワクチンの商品化を支援するためのグローバルな商業、規制、販売、マーケティングのインフラの構築など、COVID-19ワクチンに関する当社の継続的な取り組みには、2022年に多額の現金流出が必要になりますが、そのほとんどは、パートナーや協力者からの払い戻しやその他の支払いができない可能性があります。さらに、当社にはかなりの施設、リース、購入義務があります(参照 ノート 11そして ノート 12当社の要約連結財務諸表へ)。私たちは、特定の研究開発活動への資金提供、および将来のマイルストーンや当社によるロイヤルティの支払いを含む、特定のコラボレーションおよびライセンス契約を第三者と締結しました。
2022年6月30日現在の現金、現金同等物、投資は、事業から生み出されると予想される現金と合わせて、このフォーム10-Qに含まれるこれらの財務諸表の発行から少なくとも今後12か月間、予定されている事業、資本支出、および自社株買いの資金を調達するのに十分であると考えています。私たちは、新薬の開発と商品化に関連するすべてのリスクにさらされており、予期せぬ費用、困難、合併症、遅延、その他の未知の要因に遭遇する可能性があり、それが当社の事業に悪影響を及ぼす可能性があります。当社の財源が事業を支えるのに十分な期間を予測しているのは、将来の見通しに関する記述であり、リスクと不確実性を伴います。実際の結果は、さまざまな要因の結果として異なる可能性があります。この見積もりは、間違っていることが判明する可能性のある仮定に基づいており、現在の予想よりも早く利用可能な資本資源を活用することができました。
契約上の義務
2022年6月30日現在、社内で開示されている以外 ノート 11そして ノート 12当社の要約連結財務諸表では、当社の2021年のForm 10-Kに含まれている「経営陣による財政状態と経営成績の議論と分析」に記載されている内容から、当社の契約上の義務およびコミットメントに重大な変更はありません。
アイテム 3.市場リスクに関する定量的・質的開示
当社の市場リスクとその管理方法は、2021年のフォーム10-KのパートII、項目7A「市場リスクに関する量的および質的開示」にまとめられています。2022年6月30日までの3か月と6か月間、当社の市場リスクやそのようなリスクの管理に重大な変更はありませんでした。
アイテム 4.統制と手続き
開示管理と手続き
当社の経営陣は、最高経営責任者と最高財務責任者の参加を得て、2022年6月30日現在の開示管理と手続きの有効性を評価しました。取引法上の規則13a-15 (e) および15d-15 (e) で定義されている「開示管理および手続き」とは、取引法に基づいて提出または提出する報告書において企業が開示する必要のある情報が、SECの規則および書式で指定された期間内に記録、処理、要約、報告されることを保証するように設計された会社の管理およびその他の手続きを意味します。開示の管理と手続きには、取引法に基づいて会社が提出または提出する報告書において開示が義務付けられている情報を蓄積し、必要な開示について適時に決定できるようにするための管理と手続きが含まれますが、これらに限定されません。経営陣は、どんなにうまく設計され運用されていても、その目的の達成を合理的に保証することしかできないことを認識しています。経営陣は、可能な統制や手続きの費用対効果の関係を評価する際に、必然的にその判断を適用します。2022年6月30日現在の開示管理と手続きの評価に基づいて、当社の最高経営責任者および最高財務責任者は、その日付の時点で、当社の開示管理と手続きは妥当な保証レベルで有効であると結論付けました。
財務報告に関する内部統制の変更
2022年6月30日までの3か月間、財務報告に関する内部統制(取引法に基づく規則13a-15(f)および15d-15(f)で定義されているとおり)に変更はありませんでした。これらの変更は、財務報告の内部統制に重大な影響を及ぼした、または重大な影響を与える可能性がかなり高いです。
統制の有効性に関する固有の制限
最高経営責任者、最高財務責任者を含む当社の経営陣は、当社の開示管理と手続き、および財務報告に関する内部統制は、目的の達成を合理的に保証するように設計されており、妥当な保証レベルで有効であると考えています。しかし、当社の経営陣は、当社の開示管理と手続き、または財務報告に関する内部統制によってすべての誤りや詐欺が防止されるとは考えていません。制御システムは、どれほどよく考えられ運用されていても、制御システムの目的が達成されているという絶対的な保証ではなく、合理的にしか提供できません。さらに、制御システムの設計は、資源の制約があるという事実を反映していなければならず、統制のメリットはコストと比較して考慮されなければなりません。すべての統制システムには固有の制限があるため、統制を評価しても、すべての統制上の問題や詐欺の事例が検出されたことを絶対的に保証することはできません。これらの固有の制限には、意思決定の判断に誤りがある場合や、単純な間違いや間違いが原因で故障が発生する可能性があるという現実が含まれます。さらに、統制は、一部の個人の行為、2人以上の共謀、または管理者が統制を無効化することによって回避される可能性があります。また、統制システムの設計は、将来起こる可能性に関する特定の仮定に一部基づいており、将来起こり得るすべての条件のもとで、その設計が定められた目標を正常に達成できるという保証はありません。時間が経つにつれて、状況の変化により統制が不十分になったり、方針や手続きの遵守度が低下したりする可能性があります。費用対効果の高い管理システムには固有の制限があるため、エラーや詐欺による虚偽表示が発生し、発見されないことがあります。
パート 2
アイテム 1.法的手続き
私たちは、以下に説明する知的財産訴訟を含む、当社の事業では通常の流れと考えられる性質のさまざまな請求や法的手続きに関与しています。これらの主張によって提起される問題のほとんどは非常に複雑で、かなりの不確実性が伴います。これらおよび当社が直面するその他の法的手続きに関連するリスクの説明については、「当社の知的財産に関連するリスク」と「当社の市販品、開発候補、治験薬、および将来のパイプラインの製造に関連するリスク」という見出しの下の説明を含め、2021年のフォーム10-KのパートIの項目1A「リスク要因」を参照してください。
このような手続の結果は、そのメリットにかかわらず、本質的に不確実です。したがって、損失の可能性や推定損害額を評価することは難しく、かなりの判断が必要です。以下に、(i)重大な損失が発生する可能性はあるが起こりそうにない、および(ii)現時点で合理的に見積もることができない法的事項について説明します。
Arbutusが所有する特許に関連する訴訟
2022年2月28日、アービュタス・バイオファーマ・コーポレーション(Arbutus)とGenevant Sciences GmbH(Genevant)は、Modernaが米国内でのCOVID-19ワクチンの製造、使用、販売の申し出、販売(および米国への輸入)を行っているとして、米国デラウェア州地方裁判所にModernaに対して訴状を提起しました。、脂質ナノ粒子に関する米国特許番号8,058,069、8,492,359、8,822,668、9,364,435、9,504,651、および11,141,378号を故意に侵害しています。アクションは アービュータス・バイオファーマ社ら対モデルナ社ら、ケース番号 1:22-CV-00252-Mn (D. Del.)。ArbutusとGenevantは、モデルナのCOVID-19ワクチンのマーケティングや販売を阻止したり、中止したりしようとはしていません。訴状は、主張されている特許の侵害、金銭的損害賠償(および利息)、訴訟の費用と費用、弁護士費用の判決を求めています。
アルニラムが所有する特許に関連する訴訟
2022年3月17日と2022年7月12日、Alnylam Pharmaceuticals, Inc.(Alnylam)は、ModernaによるCOVID-19ワクチンの製造、使用、販売の申し出、販売(および米国への輸入)が米国特許第11号を侵害しているとして、米国デラウェア州地方裁判所にModernaに対して訴状を提起しました。カチオン性脂質に関する2022年2月15日に発行された246,933と、2022年7月12日に発行された脂質ナノ粒子に関する米国特許第11,382,979号。アクションは アルニラム・ファーマシューティカルズ社対モデルナ社ら、ケース番号 1:22-CV-00335-CFC (D. Del.) および アルニラム・ファーマシューティカルズ社対モデルナ社ら、ケース番号 1:22-CV-00925-CFC (D. Del.)。アルニラムは、モデルナのCOVID-19ワクチンのマーケティングや販売を阻止したり、中止したりしようとはしていません。訴状は、主張されている特許の侵害、金銭的損害賠償(および利息)、訴訟の費用と費用、弁護士費用の判決を求めています。
アイテム 1A.リスク要因
私たちの事業に関連するリスクと不確実性に関する情報は、パートIの項目1Aに記載されています。2021年のフォーム10-Kの「リスク要因」。2022年3月31日に終了した四半期のForm 10-Qの四半期報告書に記載され、2022年5月4日にSECに提出されたもの以外に、2021年のフォーム10-Kで以前に開示されたリスク要因から重大な変化はありません。
アイテム 2.持分証券の未登録売却および収益の使用
発行者による株式の購入
次の表は、2022年6月30日までの3か月間に当社が買い戻した普通株式に関する情報を示しています。
| | | | | | | | | | | | | | | | | | | | | | | | | | |
| ピリオド | | 購入した株式の総数 | | 一株当たりの平均支払価格 (1) | | 公に発表されたプログラムの一環として購入された株式の総数 | | プログラムの下でまだ購入されている可能性のある株式のおおよそのドル価値
(百万単位) |
| | | | | | | | |
| | | | | | | | |
| | | | | | | | |
| 2022年4月1日-4月30日 | | 2,491,413 | | | $ | 155.34 | | | 5,702,838 | | | $ | 2,133 | |
| 2022年5月1日-5月31日 | | 3,459,344 | | | $ | 137.64 | | | 9,162,182 | | | $ | 1,657 | |
| 2022年6月1日-6月30日 | | 3,221,557 | | | $ | 135.03 | | | 12,383,739 | | | $ | 1,222 | |
| 合計 | | 9,172,314 | | | | | | | |
_______
(1) 1株あたりの平均支払価格には、関連費用が含まれています。
を参照してください ノート 13当社の株式買戻しプログラムに関する情報は、要約連結財務諸表へ。
アイテム 6.展示品
下記の展示品は、このForm 10-Qの一部として提出または参照により組み込まれたものです。
| | | | | | | | |
| 展示品番号 | | 展示物索引 |
| | |
| 10.1*# | | 2022年4月28日発効の非従業員取締役報酬方針の改正および改訂版。 |
| 10.2# | | ModernaTX, Inc. とDavid Melineとの間の2022年5月27日付けの役員退職および戦略的コンサルティング契約を更新しました(2022年6月1日に提出されたフォーム8-K/Aの当社の最新報告書の別紙10.1を参照して組み込まれています)。 |
| 10.3# | | 2022年5月13日付けのModerna TX, Inc.とホルヘ・ゴメスの間の役員分離契約およびリリース (2022年5月13日に提出された当社の最新報告書の別紙10.1を参照して組み込まれています)。 |
| 10.4*† | | 契約番号の修正第13号HHSO100201600029C、ModernaTX, Inc.と生物医学先端研究開発局との間で、2022年3月23日付けで結ばれています。 |
| 10.5† | | アワード契約番号の修正第P00022号およびP00023号2020年8月9日付けのModerna US Inc. と米国国防総省の陸軍契約司令部によるW911QY20C0100(2022年3月31日に終了した四半期期間の当社の四半期報告書のフォーム10-Qの別紙10.5を参照して組み込まれています)。 |
| 10.6*† | | 修正条項番号P00024をアワード契約番号にしました。2020年8月9日付けのW911QY20C0100、Moderna US Inc. と米国国防総省の陸軍契約司令部による、または米国国防総省の陸軍契約司令部との間で締結されました。 |
| | |
| | |
| | |
| 31.1* | | 2002年のサーベンス・オクスリー法第302条に従って採択された、1934年の証券取引法の規則13a-14 (a) および規則15d-14 (a) に基づく最高執行役員の認定 |
| 31.2* | | 2002年のサーベンス・オクスリー法第302条に従って採択された、1934年の証券取引法の規則13a-14 (a) および規則15d-14 (a) に基づく最高財務責任者の認定 |
| 32.1+ | | 2002年のサーベンス・オクスリー法第906条に従って採択された、米国法第18条第1350条に基づく認証 |
| 101.インチ* | | XBRL インスタンス文書-インスタンス文書のXBRLタグはインラインXBRL文書に埋め込まれているため、インタラクティブデータファイルには表示されません |
| 101.SCH* | | XBRL タクソノミー拡張スキーマドキュメント |
| 101.CAL* | | XBRL タクソノミー拡張計算ドキュメント |
| 101.DEF* | | XBRL タクソノミー拡張定義リンクベースドキュメント |
| 101.LAB* | | XBRL タクソノミー拡張ラベルリンクベースドキュメント |
| 101.PRE* | | XBRL タクソノミー拡張プレゼンテーションリンク文書 |
| 104* | | カバーページインタラクティブデータファイル(Inline XBRL形式で、該当する分類拡張情報は別紙101に記載されています) |
| | | | | |
| † | 証券取引委員会の規則により、この展示の一部(アスタリスクで示されている)は省略されています。 |
| # | 管理契約、または補償計画、契約、または取り決めを示します。 |
+
| 本書の別紙32.1に記載されている証明書は、このForm 10-Qに添付されているものとみなされ、改正された1934年の証券取引法第18条の目的上「提出」されたとはみなされません。このような証明書は、登録者が特に参照により組み込んだ場合を除き、改正された1933年の証券法または改正された1934年の証券取引法に基づく申告書に参照により組み込まれたとはみなされません。 |
| |
署名
1934年の証券取引法第13条または第15条 (d) の要件に従い、登録者は、正式に権限を与えられた署名者に、この報告書に代理で署名させたものです。
| | | | | | | | | | | |
| | | モデルナ株式会社 |
| | | |
| 日付: | | 作成者: | /s/ ステファン・バンセル |
| 2022年8月3日 | | | |
| | | ステファン・バンセル |
| | | 最高経営責任者兼取締役 |
| | | ((最高執行役員) |
| | | |
| 日付: | | 作成者: | /s/ デビッド・W・メライン |
| 2022年8月3日 | | | |
| | | デビッド・W・メライン |
| | | 最高財務責任者 |
| | | (最高財務責任者) |
| | | |