| 2023 年年度报告 |
| 02Calliditas Therapeutics | 2023 年年度报告关于 Calliditas 03 2023 简介 04 首席执行官声明 06 我们的产品线 08 关键事件 09 股票 10 TARPEYO:全面批准 12 商业概览 14 患者访谈 16 IGA 肾病 18 我们的商业合作伙伴关系 20 访谈 Everest Medicines 首席执行官罗杰斯先生 21 扩大 TARPEYO 的 IP 22 iGaN 市场机会 23 管道:氮氧化物抑制剂平台 24 管道:Setanaxib 26 访谈来自内部 28 可持续发展 30 董事会 32 集团 合并收益表 40 的合并报表综合收益 41 合并财务状况表 42 合并权益变动表 43 合并现金流量表 44 合并财务报表附注 45 母公司 母公司收益表 70 母公司综合收益表 70 母公司资产负债表 71 母公司股东权益变动表 73 母公司现金流量表 74 财务报表附注 75 审计师报告 80 公司治理报告 88 董事会 94管理团队 96 科学指导委员会 100 财经日历 101 词汇表 102 内容 Calliditas Therapeutics AB(publ)的年度报告,556659-9766,由 的董事报告、集团和母公司的财务 报表以及附注和审计报告组成(第 32-87 页)。 Calliditas Therapeutics | 2023 年年度报告 02 |
| 03Calliditas Therapeutics | 2023年年度报告Calliditas Therapeutics利用科学专业知识和特定疾病的见解来帮助改善患者的生活。我们是一家处于商业阶段的生物制药公司,致力于研究、开发 和商业化新疗法,旨在解决与罕见疾病治疗 相关的重大未满足需求。我们致力于扩大治疗选择,为罕见病患者建立 新的护理标准,我们针对未满足的医疗需求的创新医疗产品线反映了这一点。 我们的主要产品提供了一种治疗方案,该方案已被证明可以改善IgA肾病(IGaN)(也称为伯杰氏病)的疾病。伯杰氏病是一种进行性自身免疫性肾脏疾病 ,对许多患者来说会导致终末期肾脏疾病(ESRD),需要透析或 器官移植。该药物产品以Nefecon® 的名义开发,于2021年获得美国食品药品管理局的加速批准,并于2023年12月获得全面批准,如今 以TARPEYO® 品牌在美国上市。TARPEYO现在是第一种也是唯一一种完全获得 批准的iGaN疗法,是根据肾功能的衡量标准获得批准的。Nevecon 还获得了欧盟委员会以 品牌名称 Kinpeygo® 在欧洲经济区(EEA)和英国的有条件上市许可。欧盟委员会目前正在审查Kinpeygo 的全面上市许可。 Nefecon 还获得了中国和新加坡的有条件批准,并在 Ma-Cau 获得批准,并正在接受香港和韩国的监管机构的审查。Calliditas还与 建立了合作伙伴关系,在日本开发和商业化Nefecon。 IgA 肾病是全球最常见的原发性肾小球肾炎,因此,Nevecon 的市场潜力巨大,我们早期的商业成功和超额许可 交易的潜在付款超过3亿美元,包括预付款、 预定义的里程碑以及持续的特许权使用费义务即证明了这一点。 我们的后期产品线基于同类首创的氮氧化物抑制剂平台。我们的主要化合物 setanaxib 可抑制参与炎症和纤维化途径的酶,是 同类药物中第一种进入临床阶段的药物。Setanaxib目前正在进行针对以炎症和纤维化为特征的罕见 疾病的临床试验,包括PBC和Alport综合征, 也是一项由研究人员主导的正在IPF进行的试验。此外,基于令人鼓舞的临床前发现, 我们正在对头颈癌进行概念验证试验,以进一步支持该类别药物的 作用模式。 虽然我们的总部位于瑞典斯德哥尔摩,但我们在美国 州保持着重要的影响力,在纽约和新泽西设有办事处。我们还在法国和瑞士设有办事处, 是我们的探索团队的所在地。Calliditas Therapeutics普通股于2018年在斯德哥尔摩纳斯达克 (CALTX)上市,随后代表我们普通股票的美国存托股票于2020年在美国纳斯达克全球精选市场(CALT)上市。 Calliditas — 开创性的 罕见疾病新疗法 03Calliditas Therapeutics | 2023 年年度报告 |
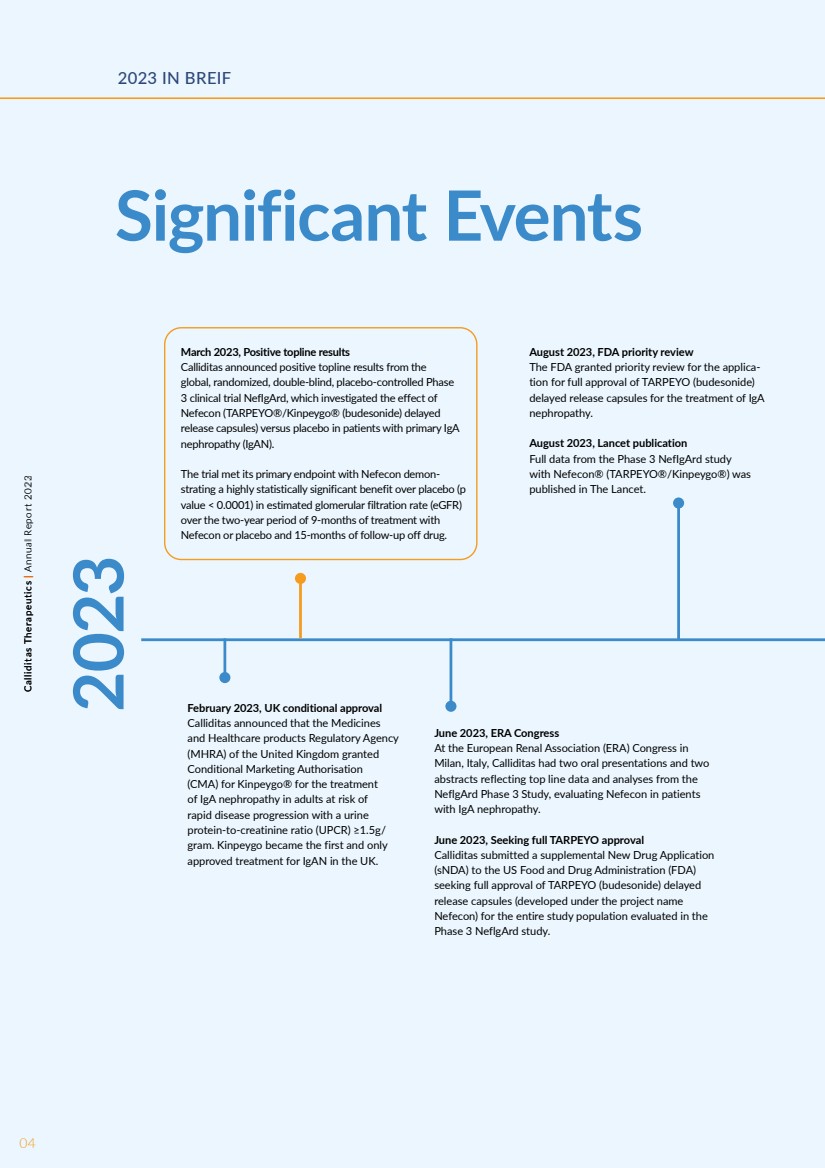
| 2023年8月,美国食品药品管理局优先审查 美国食品药品管理局批准了全面批准用于治疗IgA 肾病的TARPEYO(布地奈德) 延迟释放胶囊的申请的优先审查。 2023 年 8 月,《柳叶刀》出版物 与 Nevecon®(TARPEYO® /Kinpeygo®)联合开展的 NeviGard 三期研究 的完整数据发表在《柳叶刀》上。 04Calliditas Therapeutics | 2023 年年度报告 In BREIF 重大事件 2023 年 2 月,英国有条件批准 Calliditas 宣布,英国药品 和保健产品监管局 (MHRA) 授予 Kinpeygo® 有条件上市许可 (CMA),用于治疗成人 IgA 肾病 尿液 蛋白质与肌酐比率 (UPCR) ≥1.5g/ 克时, 出现疾病快速进展的风险。Kinpeygo成为英国第一种也是唯一一种 获批准的iGaN疗法。 2023 年 3 月,Calliditas 宣布了 全球随机、双盲、安慰剂对照的 3 期临床试验 nefiGard 的积极结果,该试验调查了 Nevecon(TARPEYO® /Kinpeygo®(布地奈德)延迟 释放胶囊)与安慰剂对原发性IgA患者的影响 br} 肾病 (iGaN)。 该试验达到了其主要终点,Nevecon 证明其优于安慰剂(p 值)具有很高的统计学意义 |
| 2023年9月,寻求Kinpeygo 的全面批准 STADA和Calliditas宣布向Kinpeygo提交在欧盟的全面上市许可 申请 。 2023 年 11 月,Calliditas的合作伙伴珠穆朗玛峰药业在中国获得有条件的批准 宣布,中国 国家药品监督管理局(NMPA)批准 Nevecon 用于治疗有疾病进展风险的成人 的原发性IgA肾病。 2023 年 11 月,Alport 研究启动 Calliditas 宣布启动 2 期临床研究,以 评估 Alport 综合征中的 setanaxib。 2023年11月,ASN肾脏周刊 取得了科学进展,当时Calliditas的研究人员 对NepiGard的3期研究 进行了更多分析,强调了TARPEYO具有统计学意义和临床意义的治疗益处。在与主要意见领袖、 肾脏科医生和患者组织的会晤中,共提交了七份摘要, ,其中包括经科学审查的 Negan 生物标志物数据 出版物。 2023 年 12 月,美国专利批准 Calliditas 获得了 TARPEYO® 美国专利申请的批准(许可通知)。2024年第一季度, 专利发布并列在 橙皮书中,该专利为美国 提供至2043年的专利保护。 2023 年 12 月,TARPEYO® 获得全面批准美国食品药品管理局完全批准 TARPEYO®,用于减少有疾病进展风险的成年 iGaN 患者的肾脏流失。 05Calliditas Therapeutics | 集团2023年年度报告财务摘要 (以千瑞典克朗计,每股金额或另有说明除外)2023 年 2021 2020 2019 年净销售额(千瑞典克朗)1,206,888 802,879 229,347 874 184,829 所得税前亏损(千瑞典克朗)(457,017) (409,373) (513,373) (513,373) (513,373) (513,373) (513,373) (513,373) (513,373) (513,373) (513,373) (513,373) 436,151) (32,501) 总资产(千瑞典克朗)1,859,245 1,952,973 1,459,910 1,463,908 845,200 平均员工人数 181 86 56 23 14 2024 |
| 06Calliditas Therapeutics | 2023年年度报告首席执行官声明 充满成功的一年 2023 年 3 月,我们宣布,全球 NeviGard 3 期试验成功达到了其 主要终点,即估计的肾小球滤过率 (eGFR),其统计意义为 p |
| 07Calliditas Therapeutics | 2023 年年度报告 Renée Aguiar-Lucander,首席执行官 9月,我们参加了在日本东京举行的 IiGann 半年度会议,会上我们展示了 5 张海报,其中包括显示 GD-Iga1 显著减少的确认性生物标志物分析,以及支持疾病修改 机制的循环免疫 复合物 (Iga-IC) 药物。我们还进行了两次口头陈述, 包括一次研究种族差异,另一次显示 使用Nefecon治疗使无微血尿的 患者数量从34%增加到60%,而安慰剂的患者数量从32%增加到39%,这具有统计学意义 (p=0.0001)。 11月,美国肾脏病学会在费城举行了 年度肾脏周会议,这为 我们提供了许多与全国各地的 肾脏科医生会面和互动的机会。在会议上,我们 展示了几张海报,包括对NeviGard 3期试验的 2年eGFR斜率进行建模,该斜率预测了现实人群的长期临床益处,在支持TARPEYO的 疾病改变影响的本已大量科学证据的基础上增加了 。我们还有 有机会会见了 100 多位肾脏科医生,他们 提供了有关 iGaN 治疗模式以及 TARPEYO 在实践中的使用方式的宝贵见解。听到所有关于患者 预后的正面故事,以及这种药物对以前面临不确定未来的年轻人和 最终接受透析的风险所带来的改变, 非常有成就感。同样显而易见的是,来自南加州Kaiser Perma-Nente队列的雷达注册数据和类似的纵向数据 的发布对肾脏病学界开始考虑这些患者群体的方式产生了深远影响。 数据反映出进展速度快于预期,并且观察到的患者中观察到的进展风险明显更高 以前被视为 “稳定” 或 “受控”。这些数据 与最近公布的临床试验数据相结合,这些数据显示 经过优化的RAS 阻滞剂的患者的表皮生长因子显著下降,显然反映了患有这种疾病的 患者的前景比以前想象的更为严峻。因此,除 控制蛋白尿外,肾脏科医生真正开始关注病理生理学和潜在疾病的治疗。 11月还见证了Nevecon在 中国的有条件批准,考虑到中国庞大的患者群体,这是一个重大事件。我们还宣布了一项涵盖TARPEYO的新专利的许可通知 ,该专利显著增强了 产品的保护。我们认为,这两项活动 对全球 Nevecon 系列的长期价值创造具有重大影响,我们期待今年晚些时候在中国推出 商业版。 2023 年 12 月 20 日,我们获得了 美国食品药品管理局 (FDA) 的全面批准,TARPEYO 是我们针对原发性 IgA 肾病的靶向治疗药物。在 多年努力为患有这种罕见疾病的 患者提供经批准的药物之后,这是一项了不起的成就。现在,我们的标签反映了 肾脏流失的减少,使我们能够应对面临疾病进展风险的全体成人 IgAn 人群,这对患者和医生来说都是一个值得欢迎的扩大范围。 我们报告的2023年总收入为12亿瑞典克朗,其中 来自TARPEYO的净产品收入为 11亿瑞典克朗(1.02亿美元),与 相比增长了190%。我们认为,这种非常强劲的增长反映了 未得到满足的潜在医疗需求以及TARPEYO令人信服的临床 数据,推动其成为iGaN新护理标准的基石 。独特 处方肾脏科医生的增长也有所加速,仅在 第四季度就达到301人,比2023年第三季度增长了50%以上。处方 全年也持续增长,第四季度达到555个, 比第三季度增长了50%以上。在这一显著的 收入增长的推动下,第四季度现金流为正,今年最后9个月,运营现金净使用量 为2.03亿瑞典克朗。因此,我们的现金状况仍然强劲 ,资产负债表上有9.74亿瑞典克朗,假设TARPEYO的收入持续增长,我们认为 足以使我们实现盈利。 关于我们的产品线,我们在7月份报告了setanaxib头颈癌试验的支持性生物标志物 数据,在报告无进展存活率的7名患者中, 有6名属于治疗组。转录组学分析 支持调节肝纤维化途径和 IPF 纤维化途径,这支持了我们正在进行的针对这些罕见疾病的试验 。在第四季度,我们启动了针对Alport综合征的2期概念验证试验。Alport综合征是一种肾脏孤儿病 ,存在大量未得到满足的医疗需求,今天没有获批 。我们期待在整个 2024年期间读出正在进行的四项使用setanaxib的2期试验中的三项 。 2023年对卡利迪塔斯来说是多事且非常积极的一年。 始于 2008 年 iGaN 的 2a 期 POC 试验,这段旅程现已在美国获得全面批准, 在 商业化的第一个全年创造了超过1亿美元的收入。 获得了其他地区的批准,有了欧洲和美国经验丰富且强大的组织 ,我们正在努力实现 我们的目标,即创建一家成功、可持续和盈利的 罕见病公司。Calliditas拥有一支强大、才华横溢和 目标明确的团队,他们实现了这一成功。 我要感谢这个团队中的每一个人 在这个令人惊叹的执行年中,你 付出的所有辛勤工作、敏捷性、聪明才智和毅力。我还 要感谢所有支持我们的患者、护理人员、KOL和投资者,尤其是那些多年来参与了 NetiGard研究的患者,这使得 有可能向患有这种罕见疾病的患者 提供经批准的药物。没有你,我们不可能做任何这些 。 谢谢! *KOL:关键意见领袖 |
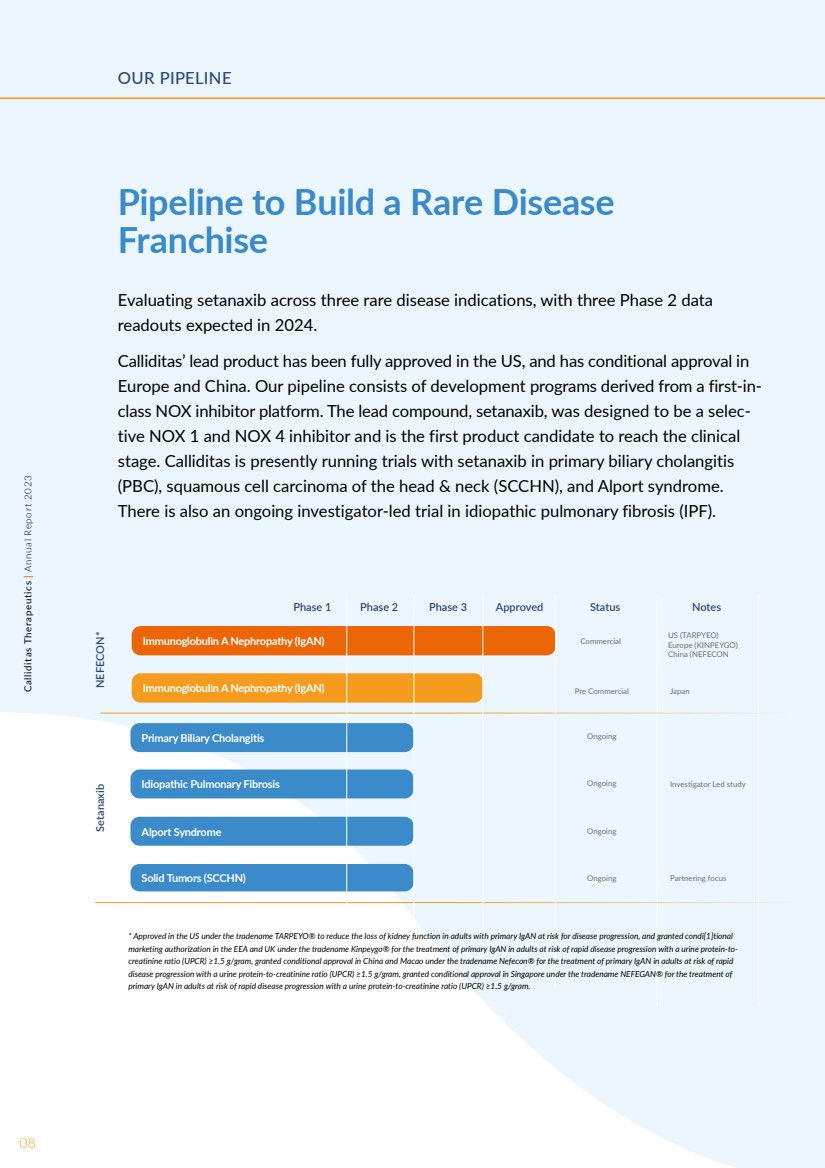
| 08Calliditas Therapeutics | 2023年年度报告标题 建立罕见病 特许经营权的管道 评估三种罕见病适应症的setanaxib,预计将在2024年公布三份第二阶段数据 。 Calliditas的主要产品已在美国获得全面批准,并在 欧洲和中国获得了有条件的批准。我们的产品线包括源自同类首创的氮氧化物抑制剂平台的开发项目。主要化合物setanaxib被设计为选择性氮氧化物1和氮氧化物4抑制剂,是第一个进入临床 阶段的候选产品。Calliditas目前正在试用setanaxib治疗原发性胆源性胆管炎 (PBC)、头颈部鳞状细胞癌(SCCHN)和Alport综合征。 还有一项由研究者主导的特发性肺纤维化(IPF)试验正在进行中。 我们的产品线 Calliditas Therapeutics | 2023 年年度报告 NEFECON* Setanaxib 第 1 阶段 2 期 3 期批准状态说明 免疫球蛋白 A 肾病 (iGaN) 商业美国 (TARPYEO) 欧洲 (KINPEYGO) 中国 (NEFECON 日本 研究者主导的研究 合作重点 br} Immunoglobulin A 肾病 (IGaN) 预商用 正在进行中 特发性肺纤维化正在进行中 Alport 综合征正在进行中 实体瘤 (SCCHN) 正在进行中 原发性胆源性胆管炎 * 在美国获得批准,商品名为 TARPEYO®,以减少肾脏流失患有原发性IgAn、有疾病进展风险的成年人体内的功能,并获得相应的条件[1]欧洲经济区和英国的国家 商品名为Kinpeygo® 的上市许可,用于治疗有快速疾病进展风险且尿蛋白与肌酐比 (UPCR) ≥1.5 g/g的成人的原发性IgAn,在中国和澳门获得有条件批准,商品名为Nevecon®,用于使用尿蛋白对有快速进展风险的成年人治疗原发性IgAn 肌酐比率 (UPCR) ≥1.5 g/g,在新加坡获得有条件批准,商品名为 NEFEGAN®,用于治疗成人的 原发性 IgAN尿蛋白与肌酐比例(UPCR)≥1.5 g/g时,有快速疾病进展的风险。 |
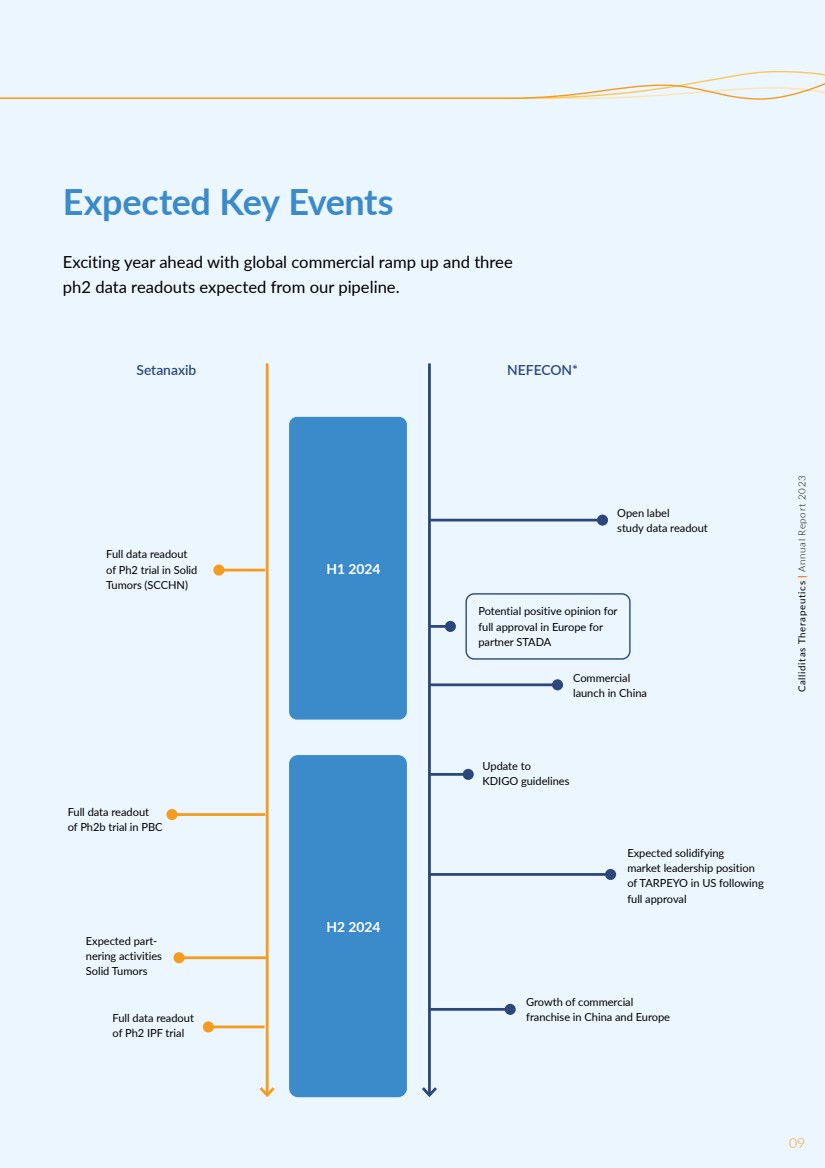
| 09Calliditas Therapeutics | 2023年年度报告预期关键事件 未来是激动人心的一年,全球商业增长以及我们的管道预计将发布三份 ph2 数据。 09Calliditas Therapeutics | 2023年年度报告 实体瘤 (SCCHN) Ph2 试验的完整数据读取 PBC ph2 IPF 试验的完整数据读取 Ph2 IPF 试验的完整数据读取 开放标签 研究数据读出 预期巩固 市场领导地位 br} 在 获得全面批准后 在美国的 br} 更新 KDIGO 指南 中国和欧洲的商业 特许经营权的增长 预期的合作活动 实体瘤 商业 在欧洲获得全面批准可能获得积极评价适用于 合作伙伴 STADA 2024 年上半年 2024 年下半年 Setanaxib NEFECON* |
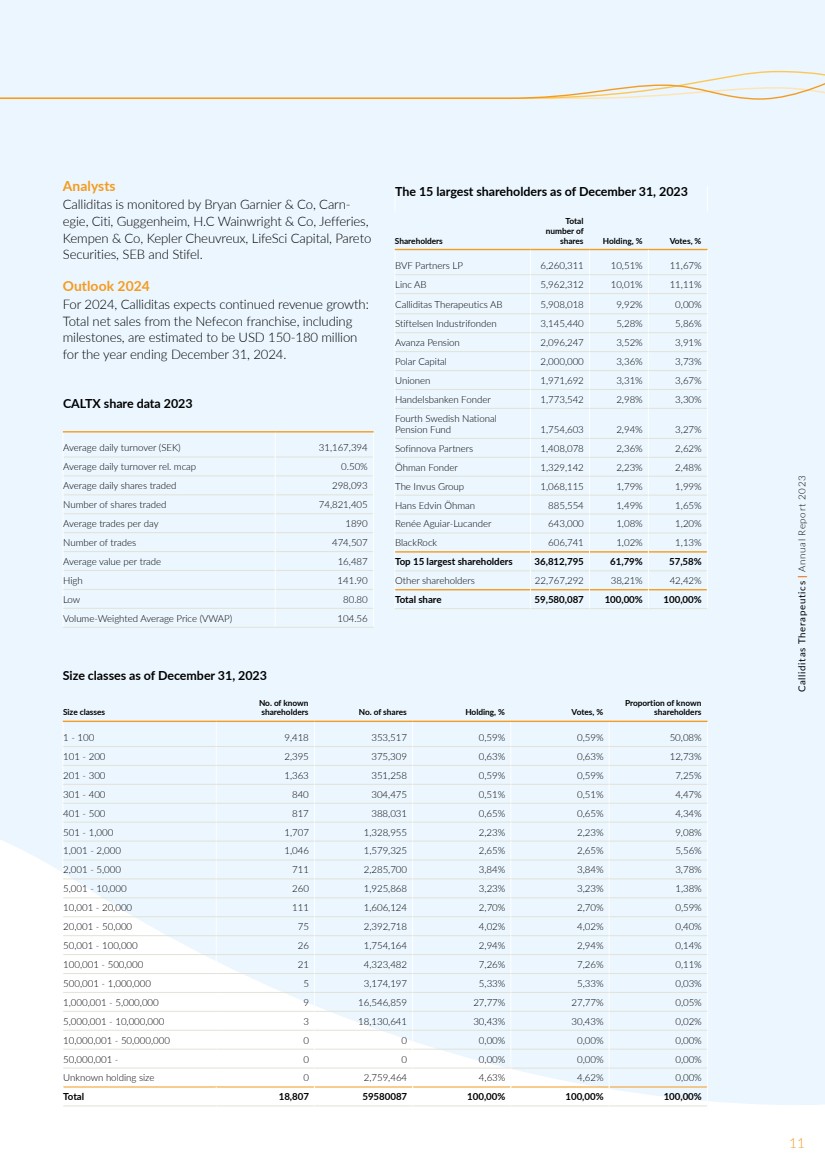
| 股票 来源:Monitor by Modular Finance AB 股票表现 纳斯达克斯德哥尔摩 Calliditas于2018年6月29日 在纳斯达克斯德哥尔摩中型股上市。截至2023年12月31日, 的收盘利率为127.10瑞典克朗。 当年的最高收盘价为141.90瑞典克朗,最低收盘价为81.85瑞典克朗。 美国纳斯达克 Calliditas于2020年6月5日在美国 的纳斯达克全球精选市场上市。在美国上市的ADS对应于两股普通股。2023年12月31日, 的收盘价为25.74美元,全年最高收盘价 为28.99美元,最低收盘价为15.68美元。 成交量 纳斯达克斯德哥尔摩 2023年共交易7,490万股股票, 总价值为78.23亿瑞典克朗。平均而言, 每天交易298,093股股票。 美国纳斯达克 在2023年1月至12月期间,共交易了290万只美国存托凭证。平均每天交易11,626只美国存托凭证。 股东 截至 2023 年 12 月 31 日,Calliditas 拥有 18,784 名股东。20名最大股东控制了每个类别的 所有权,% 交易平台,% 瑞典机构所有者 27,08% 外国机构所有者 23,45% 瑞典私人 25,94% 其他 18,90% 未知所有者类型 4,62% ITG Posit 0,32% Nasdaq 56,40% Instinet Blockmatch Europe 0,09% Cboe 37,82% Aquis 证券交易所 1,04% Sigma x 0,29% Liquidnet 欧盟有限股票 MTF 0,01% 伦敦证券交易所 4,03% 瑞典 69,90% 美国 14,73% 英国 4,60% 法国 3,51% 挪威 0,94% 挪威 0,94% 未知国家 4,63% 年底其他1,69% 65.96%的资本。最大的三个 股东是BVF Partners、Linc AB和Stiftelsen Industrifonden。外国股东占资本的30.44%。 股本 截至 2023 年 12 月 31 日,Calliditas 的股本为 238.3 万瑞典克朗。 股数量为59,580,087股,相当于每股商数 为0.04瑞典克朗。根据 公司章程,股本不得低于 10 万瑞典克朗,不超过 4万瑞典克朗。股票数量不得少于 25,000,000 股且不得大于 1亿股。 可供交易的股票比例(自由流动) 在年底约为66,25%。 投资者关系工作 2023 年的投资者关系工作侧重于 继续在北欧地区、欧洲和美国的首都 市场建立Calliditas。 管理层参加了许多 特定行业的会议,这些会议在这一年中既有面对面的也有虚拟的。Calliditas还就 的销售和买方进行了大量的面对面和虚拟会议,以教育市场 并确保市场上对 公司有广泛的了解。 10Calliditas Therapeutics | 2023 年年度报告 THE SHARE |
| 截至 2023 年 12 月 31 日的 15 大股东股东 总持有的 股票数量,% BVF Partners LP 6,260,311 10,51% 11,67% Linc AB 5,962,312 10,01% 11,11% Calliditas Therapeutics AB 5,908,018 92% 0,00% Stiftelsen Industrisen 基金 3,145,440 5,28% 5,86% Avanza Pension 2,096,247 3,52% 3,91% Polar Capital 2,000,36% 3,73% Unionen 1,971,692 3,31% 3,67% Handelsbanken Fonder 1,773,542 2,98% 3,30% 第四瑞典国民 养老基金 1,754,6% 603 2,94% 3,27% Sofinnova Partners 1,408,078 2,36% 2,62% Öhman Fonder 1,329,142 2,23% 2,48% Invus 集团 1,068,115 1,79% 1,99% 汉斯·埃德文·奥曼 885,554 1,49% 1,65% 蕾妮·阿吉亚尔-卢坎德 643,000 1,08% 1,20% 贝莱德 606,741 1,02% 1,13% 前 15 名最大股东 36,812,795 6795 67,795 9% 57,58% 其他股东 22,767,292 38,21% 42% 总股份 59,580,087 100,00% 100,00% CALTX 股票数据 2023 年平均每日成交量(瑞典克朗)31,167,394 平均每日成交量 0.50% 每日平均交易量 298,093 股交易量 74,82401,394 5 每天平均交易次数 1890 交易数量 474,507每笔交易的平均价值 16,487 高点 141.90 低点 80.80 成交量加权平均价格 (VWAP) 104.56 截至 2023 年 12 月 31 日的规模类别 已知股东数量持股数量、% 选票、% 已知 股东比例 1-100 9,418 353,517 0,59% 0,59% 50,08% 101-200 2,395 375,309 0,63% 0,63% 12,73% 201-300 1,363 351,258 0,59% 0,59% 7,25% 301-400 840 304,475 0,51% 4,47% 401-500 817 388,031 0,65% 4,34% 501-1,000 1,707 1,328,955 2,23% 2,23% 9,08% 1,001-2,000 1,046 1,579,325 2,65% 2,65% 2,65% 2,65% 5,56% 2,001-5,000 711 2,285,700 3,84% 3,84% 5,001-10,000 260 1,925,868 3,23% 3,23% 1,38% 10,001-20,000 111 1,606,124 2,70% 2,70% 20,001-50,000 75 2,392,718 4,02% 4,02% 0,40% 50,001-20,70% 0,70% 20,001-50,000 75 2,392,718 4,02% 0,40% 50,001-100,000 26 1,754,164 2,94% 2,94% 0,14% 100,001-500,000 21 4,323,482 7,26% 7,26% 0,11% 500,001-1,000,000 5 3,174,197 5,33% 5,33% 1,000,001-5,000,000 9 16,546,859 27,77% 0,77% 0,05% 5,000,001-10,000,000 3 18,130,641 30,43% 30,43% 0,02% 10,000,001-50,000,000 0 0 0,00% 0,00% 0,00% 0,00% 0,00% 50,000,001-0 0 0,00% 0,00% 未知持股规模 0 2,759,464 4,63% 4,62% 0,00% 合计 18,807 59587% 100,00% 100,00% 100,00% 100,00% 分析师 Calliditas 由布莱恩·卡尼尔公司、花旗、古根海姆、H.C Wainwright & Co、Jefferies、 Kempen & Co. 监控 Kepler Cheuvreux、LifeSCI Capital、Pareto 证券、SEB和Stifel。 2024年展望2024年,Calliditas预计收入将持续增长: 截至2024年12月31日的财年,Nevecon特许经营权的总净销售额,包括 里程碑在内,估计为1.5亿至1.8亿美元 。 11Calliditas Therapeutics | 2023 年年度报告 |
| Calliditas的主要产品于2023年12月获得美国食品药品监督管理局(FDA)的全面 批准,成为第一个也是唯一一款完全获得美国食品药品管理局批准的自身免疫性肾脏 疾病IgA肾病(IGaN)的 治疗药物。 本产品以 的名义 Nevecon® 开发,在美国获得批准,品牌名称为 TARPEYO®。TARPEYO 最初于 2021 年 12 月获得 FDA 的加速批准 ,成为 iGaN 中首款获批准的产品。Nevecon在中国和欧洲也获得了有条件的 批准,分别以Nefecon和Kinpeygo® 的品牌获得批准 。Calliditas及其合作伙伴STADA已在欧洲申请 全面批准Kinpeygo,并预计 将在2024年上半年根据人用医疗产品委员会的意见做出决定。 NeviGard 试验 Calliditas向美国食品药品管理局和欧洲药品管理局(EMA)提交的全面批准的监管申请是 基于NetfiGard 3期研究的积极数据。该试验在三月份公布了阳性的主要数据 TARPEYO:有史以来第一个 获得完全批准的IGaN - 2023年疗法,证明经过9个月的治疗和 15个月的药物随访, Nevecon的表皮生长因子比安慰剂具有很高的统计学意义,从而达到了其主要终点。 我们很高兴能够在《柳叶刀》的一篇同行评审文章中发布我们的三期数据试验。 全文可在此处查阅,发布于 ,此前 9 月份的 IgA 肾病国际研讨会 (IiGann) 以及 最大的肾脏病学家年会美国肾脏病学会 (ASN) 于 11 月初举行的 肾脏周。 在这些会议期间,我们从与医生的无数 互动中得到了积极的反馈,这让我们深受鼓舞。 Nevecon 对 整个研究人群的强大肾脏保护作用被评论为 令人印象深刻,与所有其他 候选药物区别开来,即使 在停药 15 个月后仍能保持这种作用。在 FDA 于 2023 年 12 月获得全面批准后,我们更新的标签反映了这些 结果,我们很高兴我们的销售队伍 能够在我们强大的 eGFR 数据基础上与肾脏科医生接触。 NeviGard 试验设计 NeviGard 试验是一项关键的全球性 3 期试验 12Calliditas Therapeutics | 2023 年年度报告数据发布 |
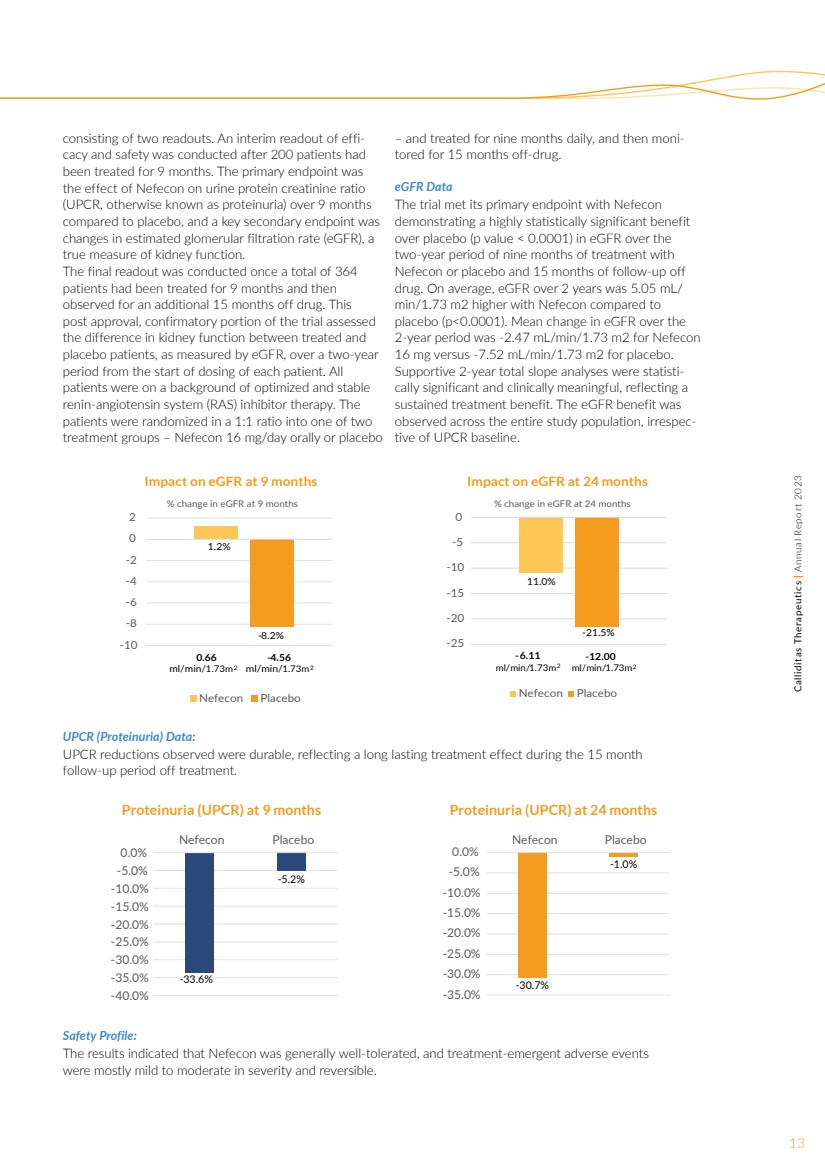
| -10 -8 -6 -4 -2 0 2% 表皮生长因子在 9 个月时变化 对 9 个月时表皮生长因子的影响 Nevecon Placebo 0.66 ml/min/1.73m2 1.2% -8.2% -8.2% -8.2% -8.2% -4.56 ml/min/1.73m2 -33.6% -5.2% -35.0% -35.0% -35.0% -35.0% -35.0% -35.0% -30.0% -25.0% -20.0% -15.0% -5.0% -5.0% nevecon 安慰剂 9个月时蛋白尿 (UPCR) -25 -20 -15 -5 0% 24 个月时表皮生长因子变化 24 个月时表皮生长因子的影响 } Nevecon 安慰剂 -6.11 ml/min/1.73m2 -12.00 ml/min/1.73m2 11.0% -21.5% -30.7% -1.0% -35.0% -35.0% -5.0% -5.0% -5.0% -5.0% -5.0% -5.0% -5.0% -5.0% -5.0% -5.0% -5.0% -5.0% -5.br} 0。0% Nevecon 安慰剂 24 个月时蛋白尿 (UPCR) 包括两次读数。在 200 名患者 接受了 9 个月的治疗后,对疗效和安全性进行了临时读取。主要终点是 与安慰剂相比,Nevecon 在 9 个月内对尿蛋白肌酐比率 (UPCR,也称为蛋白尿)的影响 ,关键次要终点是 估计肾小球滤过率(eGFR)的变化,这是 肾功能的真实衡量标准。 最终读数是在总共364名患者接受了9个月的治疗,然后 观察又停药15个月后进行的。该试验的这个 批准后的确认性部分评估了 接受治疗的患者和 安慰剂患者在每位患者开始给药后的两年 期内的肾功能差异(以 eGFR 衡量)。所有 患者均在经过优化和稳定的 肾素-血管紧张素系统 (RAS) 抑制剂治疗的背景下。 患者以 1:1 的比例随机分为两个 治疗组之一,即每天口服Nevecon 16 mg或安慰剂 ,每天治疗九个月,然后停药15个月。 表皮生长因子数据 该试验达到了其主要终点,Nevecon 显示出与安慰剂(p 值)相比具有高度统计学意义的益处 |
| 在美国,TARPEYO的患者注册人数和新开处方者均实现了显著的同比增长, 有1,753名患者注册了TARPEYO治疗 ,997名新开处方者,这表明对该产品的强劲需求。 我们为 iGaN患者提供TARPEYO的工作的一个重要方面是我们的患者支持服务TARPEYO Touchpoints,该服务旨在让患者及时获得TARPEYO ,并为iGaN患者提供个性化的 体验。TARPEYO Touch-points 团队由报销专家 组成,他们与 组护士和药剂师一起指导保险流程,他们都致力于指导患者和医生完成 访问 TARPEYO 的过程。 2023 年,我们在患者教育 和围绕 iGaN 疾病和 TARPEYO 方面的参与度加大了力度, 突显了我们的战略优先事项。我们将继续 与知名的 倡导组织合作并支持其举措,包括 IgA 肾脏学 基金会、NephCure、国家肾脏基金会、 美国肾脏患者协会和美国 肾脏基金。 值得注意的是,在7月, Calliditas连续第二年成为IgA Nephropathy 基金会SPARK 2023患者会议的主要赞助商。我们 的长期支持凸显了我们 的承诺,即扩大基金会的使命,即教育、 赋权和参与 iGaN 患者和护理人员社区。此外,今年标志着我们的患者大使计划的推出。通过 这项计划,我们努力增强患者能力,并丰富 他们对治疗选择的理解。 2023 年,Calliditas 达到了一个关键的里程碑,美国食品药品管理局于 12 月 20 日批准了 TARPEYO 。该批准确立了TARPEYO作为第一种也是唯一获得批准的 治疗方法,用于减少原发性免疫球蛋白 A 肾病(IGaN)成人肾功能丧失,无论蛋白尿水平如何, 都有可能成为IGaN治疗的基石。 TARPEYO 的商业之旅 14Calliditas Therapeutics | 2023 年年度报告商业概览 2023 年注册新患者, 2023 年新增处方者 69% LTD 处方者:1,637 55% 2023 年 TARPEYO 年净收入 1753 997 1.014亿美元 |
| 我们的医疗和商业团队通过在包括国际 肾脏病学会(ISN)、国家肾脏基金会(NKF)、欧洲肾脏协会(ERA)和 美国肾脏病学会(ASN)在内的著名的 肾脏病学会议上展出和发表演讲,产生了重大影响。这些平台为Calliditas提供了宝贵的机会 引入新数据和促进有意义的科学 讨论。 此外,我们的数据展示广受好评,其在领先科学期刊上的接受和发表就证明了这一点。这些成就 凸显了我们对推进IgA肾病(iGaN)治疗格局和巩固TARPEYO作为IgA潜在疾病改变疗法的作用的承诺。 除了 TARPEYO上提供的综合数据外,英国罕见肾脏疾病国家登记处Radar的发现,以及美国最大的 健康计划之一凯泽永在ASN上提供的 数据,都揭示了IgA肾病的疾病进展 。这些研究突出表明,几乎所有 IgAn 患者无论蛋白尿水平如何,在 一生中都有肾衰竭的风险。 这凸显了对像 TARPEYO 这样的有效治疗的需求。作为唯一获批的免疫调节 疗法,TARPEYO 的独特设计旨在解决致病性 Gd-Iga1 的 产生,从而产生显著的 表皮生长因子益处。TARPEYO作为基石 疗法与标准支持治疗相结合,对于 解决驱动IgAn的潜在自身免疫机制 至关重要。 15Calliditas Therapeutics | 2023 年年度报告激动人心的前进之旅 SCIENTIC 亮点 KDIGO 指南 3 期试验的完整结果预计将于 2024 年更新 NefiGard 3 期试验的完整结果发表在 IiGann 的 7 演讲中,其中包含来自 NefLGard 3 期试验和生物标志物数据 7 摘要的分析 ASN。 发表在 KI 靶向释放布地奈德 靶向释放布地奈德 靶向释放布地奈德 的二期试验 的同行评审文章修改了免疫球蛋白 中的关键致病性 生物标志物 A 肾病:来自 NEPHROPATION 的见解 FIGAN 试验 有能力通过最近增加的 现场组织促进全面批准 标签 开放标签延期 (OLE) 来自接受第二次 9 个月治疗 患者的数据 预计将于 2024 年上半年读出 |
| 你最初是什么时候被诊断出患有 iGaN 的? 当你收到这份诊断书时,你的感觉如何? 我对自己的 iGaN 诊断感到震惊。我来自英国, 但现在我和我的丈夫以及我们的寄养狗 一起住在阿拉巴马州。当我计划移居美国时, 我必须完成签证健康评估。通过 这些例行体检,发现 我尿液中的蛋白质水平升高, 最终导致了我的诊断。回想起来,我以前曾几次 在尿液中发现有血液, 但我从来没有真正想过,因为我 总是感觉很健康。 在我诊断时,我非常沮丧。我在 2011 年被诊断出患有 iGaN。那是几年前的事了,所以 当时可用的研究和治疗方案远远落后于现在的水平。当我 只有 25 岁的时候想到要在余生中服药真是太可怕了。我爸爸一直为自己的 肾脏健康状况而苦苦挣扎,所以我明白了 这样的旅程会带来什么。 与 iGaN 共处对你有何影响? 由于疫情和我的旅行日程安排,我失去了 与 TARPEYO 患者 Cathrin 的谈话 有一段时间无法获得我的治疗。我立刻开始 又看到尿液中有血了。看到像 这样的东西太可怕了,我甚至无法开始解释。但是, 更可怕的是 iGaN 可能对我的生活产生的影响。 努力保持肾脏健康,使我的疾病 不会发展到需要透析或 移植的地步,对我来说非常重要。我是一名天文摄影师,这意味着我很幸运能通过我的画作 和探索之旅帮助他人分享宇宙的 之美。我也喜欢音乐;我曾经经常在世界各地做过 DJ。我过着快速而充实的生活,有大量的 旅行和自发性,因此 管理好我的 iGaN 对我来说非常重要。 你的治疗经历了什么? 我曾与一位推荐服用 ACE 抑制剂的肾脏科医生合作。我当时的肾功能仅低于正常水平 。但是,尽管我努力用一些药物治疗 我的 iGaN,并改变了我的 饮食,但我没有看到我想要的效果。我丈夫和 我一直在谈论如何组建家庭,所以我 知道仅仅看着并等待我的 病情进展是不够的,是时候控制 过程了。 16Calliditas Therapeutics | 2023 年年度报告患者访谈 |
| “在被告知没有治疗iGaN的药物 多年后,听说有一种针对潜在疾病来源 的治疗方法感觉就像我又走上了 前进的道路。” 你和肾脏科医生的关系 是什么样的? 在我居住的地方,这种疾病的专家并不多, 所以我优先考虑找一个可以帮助我的人。 我的医生实际上是我的绘画客户之一, 我们谈话是偶然的。他提到 他是一名肾脏科医生,我们从那里开始了。我在州外旅行 去找他,我们建立了良好的关系。 他说,我治疗的目标是将我的 表皮生长因子保持在正常范围内,以此作为帮助保持 肾脏正常运作的指标。 当你的医生告诉 你将 TARPEYO 作为一种治疗选择时,你的感觉如何? 诊断后,我与一位肾脏科医生合作,他 建议服用 ACE 抑制剂。当时我的肾功能略低于正常水平。 当我的肾脏科医生向我介绍TARPEYO时,他 提到这些研究看起来很有希望,特别是治疗结束后的长期数据。我 几乎在网上阅读了我能读的所有内容,包括 查看所有的研究。在线解释 TARPEYO 工作原理的视频甚至教会了我很多关于 状况的知识。 多年来一直被告知没有针对 iGaN 的药物,听说有一种针对 潜在疾病来源的治疗感觉就像我又走上了前进的道路 。 因为 TARPEYO 是一个 9 个月的疗程,我觉得 正在尽我所能,等我 9 个月的治疗周期结束后,我的 医生对这个计划感到满意,我的 医生对这个计划感到满意。 TARPEYO 是如何为你工作的? 我和我的医生对我们到目前为止看到的 结果感到满意!我的肾功能相对没有变化 ,尿液中的蛋白质和血液明显下降 。起初,我遇到了一些轻微的 副作用,但是我的肾脏科医生和我一起寻找了 解决方案。我很感激我的医生一直与我 合作,确保我为 的经历做好充分的准备。 他警告我,我可能不会立即看到结果 。但幸运的是,经过三个月 的治疗,我第一次预约时确实在实验室看到了阳性结果 。他还告诉我,即使在我完成了 九个月的治疗之后,TARPEYO 仍可能继续影响我的结果。 在服用 TARPEYO 的同时,我也一直在关注自己的生命值,我很高兴地说我感觉 真的很好。 你对 TARPEYO Touchpoints 计划的体验如何? 在我开了 TARPEYO 处方后,我和 TARPEYO Touchpoints 团队合作了。他们引导我完成了 这个过程。最初,我的保险实际上拒绝了我的 索赔,但在后续行动之后,他们接受了申诉 的信。我在 TARPEYO 的治疗已完全保障 ,而且我的自付额为 0 美元。 几周之内,TARPEYO 就直接邮寄到我家 ,每个月都会直接发货给我。 现在 你已经能够使用 TARPEYO 作为 治疗选项后,你对自己的疾病有何感想? 再过几个月,我就会用 TARPEYO 完成治疗。我感觉真的很好,我很兴奋 组建我的家庭。现在我可以自信地说,我的 iGaN 掌握在我手中。 17Calliditas Therapeutics | 2023 年年度报告 |
| IgAn 疾病背景 iGaN 是一种严重的 肾脏进行性自身免疫性疾病。最近发表的注册分析1显示 ,大多数IgAn患者无论诊断时的年龄如何,都会在10-15年内发展为肾衰竭 , 的肾衰竭中位时间约为 10年。即使是以前被视为 “良性” 的 蛋白尿水平相对较低的患者, 也被证明在 长期内存在显著的肾衰竭风险,这突显了对该疾病进行缓解疾病的 治疗的必要性。 iGaN是一种孤儿病,据我们估计,在美国影响多达13万至15万人,在欧洲影响多达 20万人。在亚洲,包括 大中华区,已观察到iGaN的流行率明显更高,它历来是ESRD的主要病因,据估计,iGaN 影响约5,000,000人。 IgAn 病理生理学 尽管 IgAn 在肾脏中表现出来,但证据 表明它是一种始于肠道远端 部分,特别是回肠的疾病。Peyer's 贴片集中在回肠的肠道相关淋巴组织中,已被确定 是粘膜型 IgA1 抗体的主要来源。 IgA1 抗体在免疫系统中起着关键作用, 保护人体免受 食物衍生因子、细菌和病毒等异物的侵害。 IgA 肾病患者的粘膜型 IgA 水平升高,研究表明 IgA 患者肾小球中 沉积的 IgA 类型与肠道中产生的粘膜型 IgA 相同。 血液循环中的大部分 IgA 是 单体,高度半乳糖基化,源自 驻留在骨髓中的浆细胞。相比之下, Peyer's 贴片产生的粘膜型 IgA 抗体主要是二聚体或聚合物 ,并且缺乏半乳糖。在 IgAn 患者中,遗传易感性与环境、 细菌和饮食因素的结合可导致 这些缺乏半乳糖的 IgA 疾病概述 铰链区域 Iga1 骨髓 IgA1 的铰链区域是 高度糖化 粘膜表面 } IgA1 的铰链区域 糖基化不良或半乳糖缺乏 J 链 galnaC GAL galNaC GAL SA SA SA GalnAC GAL GalnAC GAL GalnaC GAL GalnaC GAL GalnaC GAL GalnaC GAL GalnaC GAL GalnaC GAL GalnaC} IgA 肾病(IGaN)——也称为伯杰氏病——是西方世界最常见的 肾小球肾炎,这是一种慢性肾脏炎症性疾病。 1 CJASN 18:727—738, 2023 18Calliditas Therapeutics | 2023 年年度报告 IGA NEPHROPATHY |
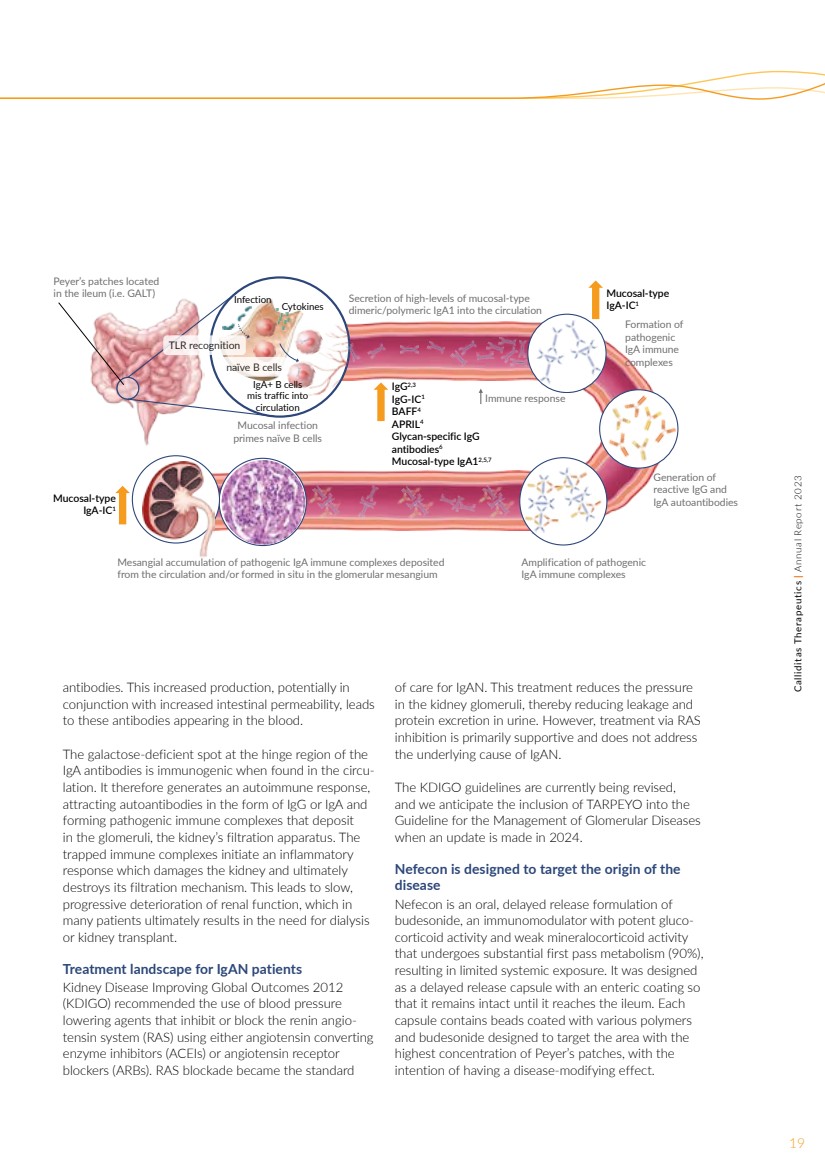
| 抗体。这种产量的增加,可能与 肠道通透性的增加相结合,导致 这些抗体出现在血液中。 IgA 抗体铰链区域的半乳糖缺陷点在循环中发现时具有免疫原性。因此,它会产生自身免疫反应, 吸引 IgG 或 IgA 形式的自身抗体, 形成致病性免疫复合物,沉积 在肾脏的过滤装置肾小球中。 捕获的免疫复合物会引发炎症 反应,损害肾脏并最终 破坏其过滤机制。这会导致 缓慢进行性肾功能恶化, 许多患者最终需要进行透析 或肾脏移植。 iGaN 患者的治疗概况 《2012年改善肾脏疾病全球疗效》(KDIGO)建议使用使用血管紧张素转换 酶抑剂 (ACEI) 或血管紧张素受体 阻滞剂 (ARB) 抑制或阻断肾素血管紧张素系统 (RAS) 的降压剂 。RAS 封锁成为 iGaN 的护理标准 。这种治疗可降低肾小球中的压力 ,从而减少尿液中的渗漏和 蛋白排泄。但是,通过 RAS 抑制剂进行治疗主要是支持性的,不能解决 IgAn 的根本原因。 KDIGO指南目前正在修订中, ,我们预计在2024年更新时将TARPEYO纳入 肾小球疾病管理指南 。 Nevecon 旨在靶向 疾病的起源 Nevecon 是 布地奈德的口服延迟释放配方,布地奈德是一种免疫调节剂,具有强效的糖皮质激素活性和较弱的盐皮质激素活性 ,经过大量的首次代谢(90%), 导致全身暴露有限。它被设计成一种带有肠溶涂层的延迟释放胶囊,因此 在到达回肠之前保持完好无损。每个 胶囊都含有涂有各种聚合物 和布地奈德的珠子,旨在靶向 Peyer's 贴剂浓度最高的区域, 的目的是起到改善疾病的作用。 19Calliditas Therapeutics | 2023 年年度报告 Peyer 的斑块位于回肠(即 GALT)中的 粘膜感染 primes 天真 B 细胞 IgG2,3 IgG-IC1 BAFF4 APRIL4 聚糖特异性 IgA 抗体6 粘膜型 IgA12,5,7 致病性 IgA 免疫系膜积累从循环中沉积 和/或在肾小球系膜中原位形成 致病性 IgA 免疫复合物的扩增 反应性 IgG 和 IgA 自身抗体的产生 致病性 IgA 免疫 复合物的形成 iga-ic1 免疫反应 感染细胞因子 Iga+ B 细胞 误导流入 循环 将高水平的粘膜型 二聚体/聚合物 IgA1 分泌到循环中 粘膜型 Iga-IC1 TLR 识别 naíve B 细胞 |
| 我们的商业合作伙伴关系 20Calliditas Therapeutics | 2023 年欧洲年度报告 Nevecon® 于 2022 年 7 月获欧盟委员会授予有条件的 上市许可 (CMA),随后于 2023 年 2 月获得英国 药品和保健产品 监管局 (MHRA) 以 Kinpeygo® 的品牌授予 的有条件上市许可 (CMA) br} 用于治疗有快速疾病进展风险的成年人 的 IgAn ,尿蛋白与肌酐比例 (UPCR) >1.5 g/g, 成为首个获批的 IgAn 治疗药物欧盟。 Kinpeygo在欧洲经济区(EEA)、 英国和瑞士销售,如果在该司法管辖区获得批准,则由 STADA Arzneimittel 股份公司独家销售, Calliditas于2021年7月与该公司签订了许可 协议,在 欧洲注册 并将Kinpeygo商业化。STADA 于 2022 年 9 月在德国推出了 Kinpeygo , 随后还会有其他欧洲国家 。 继从NetiGard完整试验中读出阳性数据 以及 向 食品药品管理局提交snDA之后,Calliditas正在与STADA合作 ,寻求欧洲 委员会和MHRA在 完整研究人群中对Kinpeygo的全面批准 。预计CHMP将在2024年上半年发表意见 。 大中华区 2019年,Calliditas与Everest Medicines(HKEX 1952.HK)签订了 许可协议,让EV-Erest在大中华区 和新加坡为iGaN开发和商业化 Nevecon。2022年3月, 该协议扩展到 包括韩国。 珠穆朗玛峰于 2023 年 4 月首次在中国海南博鳌试验区推出 Nevecon,作为 肾病的首发疗法。该 计划允许在 NMPA 监管批准 之前,在其他 地区批准的海外创新药物和医疗器械 在海南 省的 现实临床环境中销售和使用。数百名 名患者报名参加了这项提前 准入计划,使其成为 在中国启动的最成功的 EAP 项目之一。 2023 年 10 月,珠穆朗玛峰获得了 澳门特别行政区 地区制药 管理局的 批准,在存在疾病进展风险的 iGaN 患者中使用 Nevecon,成为珠穆朗玛峰地区第一个获得 Nevecon 批准的地区 。2023年11月24日,珠穆朗玛峰宣布, 中国国家药品监督管理局(NMPA)有条件地批准Nevecon® 用于治疗有疾病进展风险的成人 的原发免疫球蛋白A肾病(IGaN)。 中国是全球 中原发性肾小球疾病患病率最高的国家,估计有五百万 IgAn 患者。在美国肾脏病学会 (ASN) 2023 年 肾脏周 上发表的 中国亚群分析 的结果提供了证据,表明在肾功能、蛋白尿和微观方面,Nevecon 对中国队列的 治疗效果大于 的全球数据集 血尿。在 中国队列中, 24 个月时表皮生长因子与基线相比的平均绝对变化显示,使用 Nevecon 的这项 衡量肾功能的损失减少了大约 66%,而 全球数据集中表皮生长因子的损失减少了 50% 。 日本 2022年底,Calliditas 与 Viatris Inc.(纳斯达克股票代码: VTRS)的子公司 Viatris Pharmicals Japan 建立了合作伙伴关系, 将 Nevecon 在日本商业化 。Viatris 是一家全球医疗保健 公司,总部设在美国, 业务遍及超过 165 个国家 和地区,还经营大约 40 个制造 工厂。 |
| 对于中国IGaN患者来说,NFECON的有条件批准是一个重要的里程碑。 获得此次批准的过程是怎样的? 该批准是监管事务、临床开发等不同部门 以及我们的合作伙伴 Calliditas之间的良好合作,旨在为中国患者提供IgAn的首次入院治疗 选项。据估计,中国有500万IgAn患者。 由于我们团队的共同努力,Nevecon® 是中国第一种获得突破性疗法称号的非肿瘤学 药物, 也获得了优先审评地位,这有助于促进 NDA的批准。由于有了 Nevecon,CDE 已开始接受 替代终点作为加快肾脏病学领域药物批准的基础,这将有利于未来该领域新药的研发 。 珠穆朗玛峰团队 从海南的抢先体验患者项目中收到了什么样的反馈? 抢先体验计划的成功超出了我们的预期。 没有任何销售代表,尽管 飞往海南博鳌会带来不便,但仍有大约700名患者 报名参加该计划。这种强劲的需求凸显了中国庞大的iGaN患者群体 的紧迫性 和大量未得到满足的医疗需求。 对 Nevecon 的批准有何反应? 中国医生和患者对Nevecon 的批准感到非常兴奋,因为他们终于有了经批准的具有IGaN适应症 的药物来治疗这种疾病。不幸的是,肾素-血管紧张素系统 (RAS) 抑制剂等 IgAN 的当前治疗方案是非靶向的, 无法从根本上改变疾病进展。此外,中国 IgAn 患者在传统治疗下有更快疾病进展的风险,而3期临床研究表明,在24个月时,中国亚组的肾功能恶化减少了约66%,而全球IgAn人群的肾功能下降幅度为50% 。在中国 接受Nevecon® 治疗的患者在24个月时与安慰剂 相比,UPCR的降低幅度也增加了43%,而 全球人群的UPCR下降幅度增加了30%。根据亚组 的分析,Nefecon® 组中没有微血尿的中国患者比例从基线 的26.9%增加到观察随访期间的57.7%。这些数据支持中国对Nefecon® 的更迫切需求。 你 从中国的肾脏科医生那里收到了什么样的反馈? 中国的肾脏科医生对Nevecon的批准感到非常兴奋。 作为靶向疾病起源的B细胞免疫调节剂和 采访 珠峰药业首席执行官罗杰斯先生 减少Gd IgA1抗体的产生,中国的肾脏病学家 都同意,Nevecon在2022年和2023年的临床数据和海外销售显示出为 IgA1患者带来了显著的益处。该疗法将为中国的iGaN 治疗开启新的篇章。此外,由于其靶向性质和 高首次代谢,Nefecon® 可以避免全身性糖皮质激素的不利影响 ,同时对免疫系统的抑制有限。 珠穆朗玛峰团队是如何为 在中国市场推出Nefecon做准备的? 自海南博鳌EAP项目于2023年4月启动以来,我们 一直在对患者和医生进行有关iGaN的教育。 大约有700名患者报名参加EAP,我们已经 将Nevecon® 确立为中国IgAn患者 的首选治疗药物。通过慈善基金会资助的 iGaN 计划中注册了大约 20,000 名患者,据我们了解 患者需求巨大。珠穆朗玛峰已经有一个集成的中央商业平台,为Nevecon在中国的推出 做好了准备。我们已经开始组建一线销售 团队,并正在加快供应链的准备工作,以尽快在中国市场推出 Nevecon®。 您 最初计划为发布会部署多少销售人员? 我们将逐步组建销售团队,争取2024年在中国推出Nefecon® ,到年底,将有多达120名销售代表,涵盖核心医院。我们已经建立了一个集中式商业平台,包括医疗 事务、营销和市场准入,这对 的发布也至关重要。 成功商业推出 Nefecon 的关键组成部分是什么? Everest Medicines 致力于采用业内最佳的商业化实践,以快速高效地使大多数患者受益 。我们已经建立了一个高效而有针对性的 商业基础设施,其中包括渠道和商业运营、营销、 市场准入、医疗事务和销售以及物流 和质量控制方面经验丰富且能力强的 团队,以确保我们的产品成功商业发布的所有视角都得到充分覆盖 。我们还将通过战略合作伙伴关系 加快商业化,并通过患者准入计划、 商业保险覆盖范围和全国报销 药品清单以及全国报销药品清单来增加患者的可及性。 Calliditas Therapeutics | 2023 年年度报告 21 |
| 2023年12月,美国专利 和商标局(USPTO)发布了 允许Calliditas的专利 申请的通知。 美国专利商标局随后于 2024 年 1 月 24 日发布了名为 “新药物成分” 的第 11896719 号专利 ,有效期自 2024 年 2 月 13 日。 这成为Calliditas在美国获得的第二项TARPEYO 专利,并在2043年之前提供产品保护 。 该专利涵盖了一种治疗IgA肾病的方法,其组合物包括以 “NEFECON®” 的名义开发的 (布地奈德)延迟释放胶囊。该专利已在《橙皮书》中列出 。 扩大TARPEYO的 知识产权 Calliditas打算在包括欧洲和中国在内的全球其他地区 提交相应的专利申请。 继TARPEYO于2023年12月获得全面批准后, 美国食品药品管理局还批准了TARPEYO的七年孤儿药 独家经营期,该期限将于 2030年12月到期。 在2023年12月获得全面批准后,TARPEYO® (布地奈德)被指示 “减少有疾病进展风险的原发性免疫球蛋白A 肾病(IGaN)患有原发性免疫球蛋白 A 肾病(IGaN)的成年人肾脏功能丧失”。孤儿药独家期反映了 新适应症,该适应症涵盖所有存在疾病进展风险的 原发性IgAn的成年患者,其依据是 已证实的肾脏流失减少反映了 原发性IgAn对成年 患者的肾功能有临床益处。 22Calliditas Therapeutics | 2023 年年度报告数据发布 |
| IgA 肾病 -一个重要的市场机会 TARPEYO 和 Kinpeygo 分别是 美国食品药品管理局和欧盟委员会批准的首批用于iGaN的药物,也是唯一专为 设计的靶向 iGaN 起源和改善疾病的治疗药物。TARPEYO 是 唯一获得美国食品药品管理局批准的 iGaN 疗法,也是唯一获批的基于保护肾功能的 疗法。 • 需要遗传易感 ,但还不够;大多数患者在 20 多岁和 30 多岁时被诊断出来 • 超过 50% 的患者有 在 10-20 年内患上 ESRD 的风险, 导致肾移植 • 治疗目标是保持 — 肾脏功能 • 最近公布的纵向数据表明 疾病正在进展比以前想象的更快,前景更糟 iGaN 患者: • 尽管 IgAn 是一种罕见的疾病,但它是最常见的原发性肾小球肾炎形式。 在美国的患病率估计在13万到 15万名患者之间,欧洲约为20万名患者, 中国的患病率高达500万人。 • 在美国,我们估计 大约有 12,000 名肾脏科医生,其中多达 三分之二用于治疗 IgAn 患者。大多数 患者由大约 4,000 到 5,000 名专家看病。大约40%的患者在学术环境中接受 治疗,其余 则在社区环境中接受治疗。1 • 根据KDIGO指南的定义,估计有疾病进展风险的IgAn患者群体 在美国约有45,000至60,000名患者 。2 • 如今,这些患者中的大多数主要接受支持性治疗,例如仿制药 ACE和/或ARB 控制血压,辅以其他广泛适用的有氧运动和 肾脏保护药物。 • 随着经批准的 特别指向和批准用于 iGaN 的药物的可用性和熟悉度增加,以及医生考虑采取更积极的 干预措施来保持肾脏功能,我们 估计全球 IgAn 市场将增长到 50亿至80亿美元。 1Veeva OpenData 2023 年,包括所有以肾脏病学为主要专业的活跃医疗机构 2Spherix RealWorld Dynamix 23Calliditas Therapeutics | 2023 年年度报告 |
| 24Calliditas Therapeutics | 2023年年度报告 PIPELINE 氮氧化物酶抑制剂 氮氧化物酶抑制剂是新治疗类别中一系列有前途的新型 实验药物,自2019年世卫组织批准 “naxib” 作为新药干以来,一直受到世卫组织的认可。烟酰胺腺嘌呤二核苷酸磷酸盐 (NADPH) 氧化酶,也称为 NOX 酶,是唯一已知的 专门用于产生活性氧 (ROS) 作为其主要功能的酶。它们是跨膜酶,可将来自 中 NADPH 的电子转移到细胞质穿过细胞膜,导致 形成 ROS。 在适当的浓度下,活性氧在细胞信号传导过程中具有必不可少的 功能,但有人牵涉到氧化还原动态平衡的破坏 Calliditas的产品线包括基于同类首创的氮氧化物 抑制剂平台的开发计划。Calliditas目前正在对头颈部鳞状细胞癌(SCCHN)以及原发性胆源性胆管炎(PBC)和Alport 综合征中的先导化合物 setanaxib进行临床试验,后者于2023年7月公布了 中期数据。还有一项由研究人员主导的试验,调查了特发性 肺纤维化(IPF)中的setanaxib。 先导化合物Setanaxib,第一种达到 临床阶段的氮氧化物抑制剂,预计将在12个月内实现里程碑 管道:氮氧化物抑制剂平台 用于多种疾病途径。当细胞受损时, 过多的氮氧化物活性会被触发,氧化还原顺势反应变得不平衡,从而导致 促纤维化途径的激活。肿瘤微环境中与癌症相关的成纤维细胞 还表达 NOX 酶,这可能导致肿瘤的免疫学活性低下,并且对 免疫肿瘤药物(例如检查点inhi-bitors)的作用具有相对抵抗力。Setanaxib是第一种通过氮氧化物平台进入临床的 候选药物,其设计目的是 专门减少与纤维化 和炎症途径有关的活性氧。 PBC H&N CANCER 转化试验 的二期研究 其他 适应症 CAF 阳性的 SCCHN 癌症的概念验证研究 50 名患者使用setanaxib + pembrolizumab 或安慰剂 + pembrolizumab 支持性临时读取 预计在 2024 年第二季度完成第 2 阶段最终数据正在进行的 2b 期初级 胆汁性胆管炎 (PBC) 试验 协议将修订 允许在 2024 年第三季度读出数据 2b 部分 数据预计在 2024 年第三季度读出 FDA Fast Track 称号 Setanaxib 在 2 期试验中评估在 IPF(研究者主导的 试验)中。 预计将在2023年11月启动的2024年第四季度Alport 综合征的2期试验中获得数据 |
| 氮氧化物酶生成 ROS 是 生化级联的重要组成部分,这些级联调节正常细胞生长、免疫 反应、细胞信号传导和自噬 细胞生长 免疫反应 细胞信号传导正常 ROS NOX4 02 — 02 H202 NOX1 细胞受损时会诱发过度的 NOX1/4 表达, 导致氧化还原失衡动态平衡以及最终 纤维发生 细胞损伤 炎症 纤维化 NOX4 02 02 — 02 H202 NOX1 失衡 细胞损伤 NOX(NADPH 氧化酶)酶催化氧气的转化进入活性氧物种 (ROS) 25Calliditas Therapeutics | 2023 年年度报告 1.Watson S、Padala SA、Hashmi MF 等阿尔波特综合症。 [2023 年 8 月 14 日更新]。在:StatPearls [因特网]。金银岛(佛罗里达州):StatPearls 出版社;2023 年 1 月 可从以下网址获得:https://www.ncbi.nlm.nih.gov/books/NBK470419/ Alport 综合症 Alport 综合征是一种遗传性疾病,源自编码 4 型胶原蛋白的基因中的 突变。 4 型胶原蛋白 α链主要位于 肾脏、眼睛和耳蜗,因此该病以肾脏疾病、听力丧失、 和眼睛异常为特征。最终,患者出现 蛋白尿、高血压、 肾功能进行性丧失(GFR 逐渐下降)和末期 肾脏疾病(ESRD)。 据估计,美国 约有67,000人患有这种疾病,它是慢性肾脏病(CKD)的重要原因,导致青少年和年轻人出现 ESRD,在欧盟和美国接受肾脏替代 疗法的儿童中, 占1.5%至3.0%。 基于支持性的体内临床前研究,Calliditas 启动了一项针对Alport综合征的随机、安慰剂对照的临床试验 ,包括约20名患者,评估了整体安全性以及对蛋白尿的影响。 该研究于2023年11月启动,在 读取的数据基础上,Calliditas将决定Alport的全面的 监管计划。 Calliditas 于 2023 年 9 月被美国食品药品管理局授予 使用 setanaxib 治疗 Alport 综合征的孤儿药称号,并于 2023 年 11 月获欧洲药品管理局 授予孤儿药称号。 原发性胆源性胆管炎 PBC 是一种进行性慢性肝脏自身免疫性疾病 ,它导致 胆道上皮细胞免疫损伤循环,导致胆汁淤积和 纤维化。它是一种孤儿病,根据其已知的 患病率,我们估计美国大约有14万名患者,每年 发病率为每10万例0.3至5.8例。 Calliditas 于 2021 年 8 月在 PBC 中获得了 FDA 的 setanaxib 快速通道设计证书。 熊去氧胆酸,一种仿制药也被称为 ursodiol 或 UDCA,以及被称为 Ocaliva 的奥贝胆酸,是唯一获得 美国食品药品管理局和欧盟委员会批准的 PBC 治疗方法。但是, 尽管有这些治疗选择,但PBC患者仍有未得到满足的 医疗需求,尤其是当涉及到重要的生活质量结果时。 在PBC中使用setanaxib对 111名患者进行的一项试验的2期数据表明,对于估计肝纤维化阶段为F3或更高的患者,setanaxib对纤维化和ALP降低(碱性磷酸酶,PBC中广为公认的独立性 预后预测因子)具有更明显的作用。 肝硬度升高的患者出现疾病 进展的风险更大。 Calliditas正在对 肝硬度升高的PBC患者进行一项随机、安慰剂对照的双盲2b期试验。我们预计将在2024年第三季度读出 数据。 |
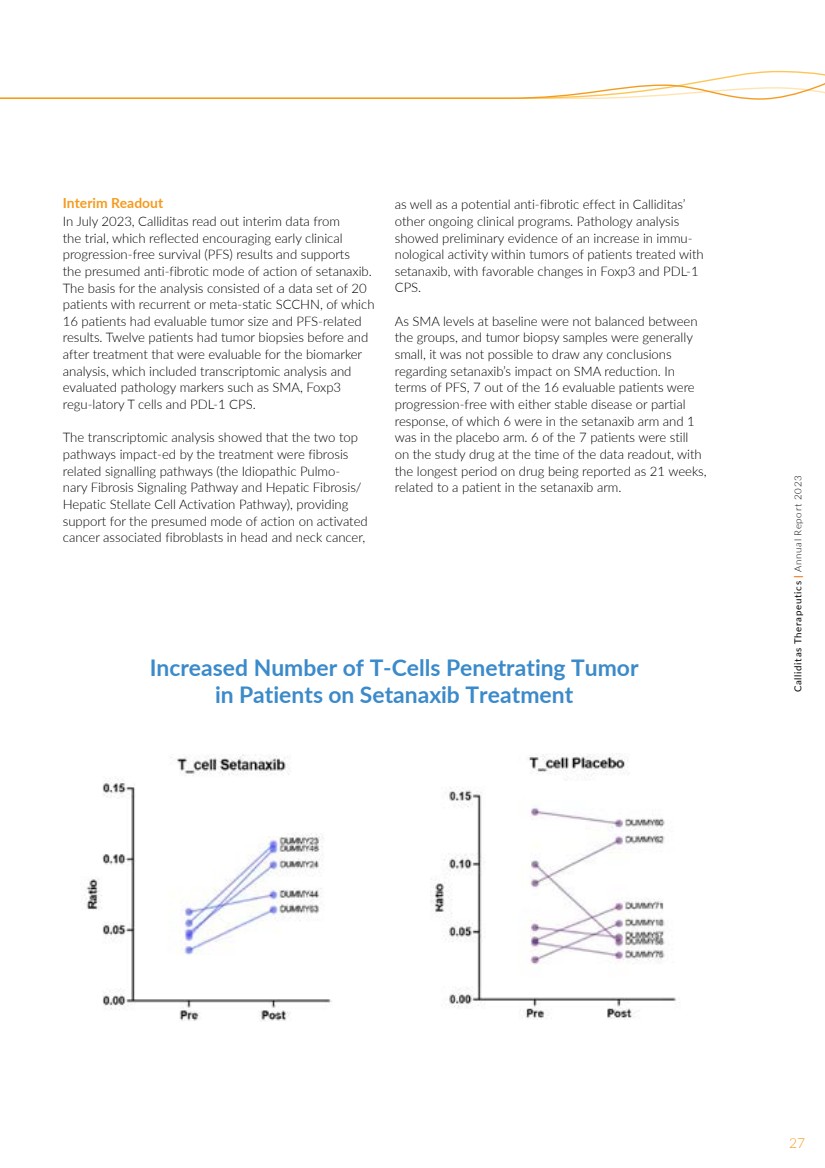
| 回归 NOX1/4 抑制 CAF 激活 TGF-β,Shh CD8 T 细胞成纤维细胞肌成纤维细胞肿瘤细胞 肿瘤微环境 26Calliditas Therapeutics | 2023 年年度报告 PIPELINE 患者对免疫疗法的反应可能会受到肿瘤微环境的影响,尤其是 的肿瘤数量浸润淋巴细胞 (TIL) 和 癌症相关成纤维细胞 (CAF)。CAF与头颈部鳞状细胞癌瘤(SCCHN)预后的关系 已经建立,其中氮氧化物在CAF中过度表达。这种 过度表达会驱动 肿瘤内的肌纤维细胞激活,并保护它们免受 CD8+ TIL 的侵害。Calliditas正在评估头颈部 癌症临床研究中的setanaxib,其基础是有希望的体内临床前数据 ,这些数据表明setanaxib可以显著增强 免疫肿瘤学疗法的作用。 Setanaxib 治疗头颈部癌症 我们正在进行一项双盲、随机、 安慰剂对照、概念验证的第二期研究, 该研究正在研究setanaxib 800mg 每日两次与pembrolizumab 200mg 联合给药,每三周给药一次,对至少 50 名复发或 患者的作用转移性 SCCHN 和 中度或高水平的癌症相关纤维细胞的肿瘤。 肿瘤活检在随机分组之前进行, 在治疗大约 9 周后再次进行。按照肿瘤学试验的标准惯例 , 治疗将持续到不可接受的毒性或 疾病进展为止。Calliditas于2023年7月宣读了 该研究的中期数据,并预计将在2024年第二季度读出最终的 试验数据。 |
| 2 接受Setanaxib治疗的患者中穿透肿瘤 的T细胞数量增加 27Calliditas Therapeutics | 2023年年度报告中期报告 2023年7月,Calliditas宣读了 该试验的中期数据,这反映了令人鼓舞的早期临床 无进展生存(PFS)结果,并支持 setanaxib假定的抗纤维化作用模式。 分析的基础包括20名复发性或转移性SCCHN患者的数据集,其中 16名患者的肿瘤大小和PFS相关的 结果可评估。十二名患者在治疗前和治疗后进行了肿瘤活检,生物标志物 分析可对这些活检进行评估,其中包括转录组学分析和 评估了诸如 SMA、Foxp3 调节 T 细胞和 PDL-1 CPS 等病理标志物。 转录组学分析显示,该治疗影响最大的两个 途径是与纤维化 相关的信号通路(特发性肺动脉纤维化信号通路和肝纤维化/ 肝星状细胞激活途径),为头颈癌中活化 癌症相关成纤维细胞的假定作用模式提供支持, 以及Calliditas的 其他正在进行的临床项目中可能产生的抗纤维化作用。病理学分析 显示出初步证据,表明 setanaxib 治疗的患者肿瘤内的免疫学活性增加,Foxp3 和 PDL-1 CPS 的变化良好。 由于 两组之间基线的 SMA 水平不平衡,而且肿瘤活检样本通常 很小,因此无法就setanaxib对SMA减少的影响得出任何结论 。在 方面,在 16 名可评估患者中,有 7 名 没有进展,病情稳定或部分 反应,其中 6 名在塞塔那西布组,1 名在安慰剂组。在读取数据时,7 名患者中有 6 名仍在服用研究药物, 报告的最长服药期为 21 周, } 与 setanaxib 手臂中的一名患者有关。 |
| 去年,卡利迪塔斯向美国食品药品管理局申请了对 TARPEYO 的全面批准。那个过程 是什么样的?你怎么能在三月份的数据读出和几个月后的6月的 申报之间如此快速地实现周转? 我们的提交团队积极进取, 倾向于前进,在团队的共同努力下, 向美国食品和药物管理局申请 TARPEYO® 的全面批准已成功完成 。我们设法压缩了 时间表,方法是在临床研究结果出来时提前加载提交文件 的写作, 最终确定了相互依存的文件,并在个人文件可用时将其添加到电子提交档案 中。 在高级别文件的 故事情节中纳入并实施了基于数据的 商业角度考虑的因素,因此 提交的周转速度很快,同时 我们可以确保针对竞争性标签的谈判对档案进行优化 。 优先审核申请包含在 的全面批准申请中,并获得了 FDA 的批准, 此请求与提前提交的申请相结合,使 的批准日期定为 2023 年 12 月。 我们的监管团队还一直在支持 STADA向EMA和英国MHRA 提交申请——该程序进展如何? 自2023年6月以来,我们的监管团队 一直支持STADA向EMA和 MHRA提交全面批准,并履行有条件批准的 “特定义务”。在STADA提交之前,我们与STADA就特定的 申报策略达成了一致,一些提交文件 是由Calliditas 团队准备并提供给STADA的。EMA/CHMP 审查和英国 MHRA 审查 正在进行中。 Calliditas 监管事务副总裁 Frank Bringstrup 28Calliditas Therapeutics | 2023 年年度报告 | 内部访谈 |
| “我的主要重点是通过 第一周期批准和有竞争力的标签快速进入市场。这对患者至关重要,对卡利迪塔斯的成功也至关重要。” 监管团队如何支持其合作伙伴 珠峰药业成功向 中国国家药监局申请? 中国新药管理局申请文件是Calliditas和 珠穆朗玛峰监管团队密切合作编写的 ,2022年10月,珠穆朗玛峰向CDE/NMPA 提交了 保密协议,申请人为卡利迪塔斯。2022年11月, NDA被CDE/NMPA接受审查, 2022年12月,国家药监局批准了对用于治疗有快速疾病进展风险的成人的原发性免疫球蛋白 A 肾病 (IGaN) 的 Nevecon 进行优先审查。 从中国保密协议审查程序一开始, Calliditas-Everest内部就制定了预定义的 “问答” 流程 ,以确保我们可以就监管机构提出的任何问题 共同制定最佳回应策略,以有效管理 应对准备工作。这一监管性的 “问答阶段” 已成功管理,2023年11月,国家药监局批准Nevecon® 用于治疗有疾病进展风险的成年人的 原发性IgAn。 你自2019年以来一直担任 Calliditas的监管事务副总裁,并监督了 一个非常激动人心的时刻,包括TARPEYO和Kinpeygo最初获得的 批准,以及现在 对TARPEYO的全面批准。作为这个职位的领导者,你 的主要重点是什么? 我的主要重点是通过第一周期批准和有竞争力的标签快速进入市场 。 缩短治疗IGaN等 严重疾病的药物的上市时间对患者至关重要, 对于该产品和Calliditas的成功也至关重要。执行我们的战略 是我们成功的关键部分。 成功将 首款获批准的面向 IgAn 患者的产品推向市场真是令人兴奋。 29Calliditas Therapeutics | 2023 年年度报告 |
| 30Calliditas Therapeutics | 2023年年度报告可持续发展 让我们的可持续发展工作经得起未来考验 从业务和可持续发展的角度来看,Calliditas所做的最重要的事情是开发和提供改善 罕见肾脏和肝脏疾病患者生活质量的药物。我们的核心业务有助于改善 人们的生活,这一事实本身就具有巨大的价值。但是我们不能满足于此。积极的可持续发展 工作意味着从各个角度考虑:影响、风险和机遇——无论是对于 环境、我们整个本地和全球价值链中的员工,还是对公司的 Calliditas 来说。 更加关注可持续发展 在这一年中,我们加强了可持续发展工作 ,并有目的地采取长期方针 来设定重点领域和目标,以增进对我们足迹的了解,包括我们 对我们产生何种影响和影响以及这反过来如何影响我们。这种深入的 知识使我们能够专注于可以产生 最大积极影响的地方。 我们工作的推动力之一是即将出台的 欧盟可持续发展报告要求—— 《企业可持续发展报告指令》(CSRD) 和 《欧洲可持续发展报告标准》(ESRS)。 这些强制性要求将对 我们处理和报告最重要的 可持续发展问题提出要求。 管理层的参与 变得越来越重要 当管理团队和董事会积极参与时,公司的变更管理会产生最大的 影响。这就是为什么我们的管理层和 董事会在这一年接受了有关 CSRD 和 ESRS 要求 的培训的原因。此外,一些管理 团队在年内积极参与了我们的 可持续发展方针的进一步发展。 双重重要性评估 为了推动Calliditas的可持续发展工作向前发展,于2023年进行了双重 重要性评估。双重 重要性包括考虑对 人和环境的影响,以及对 公司财务业绩的影响。 |
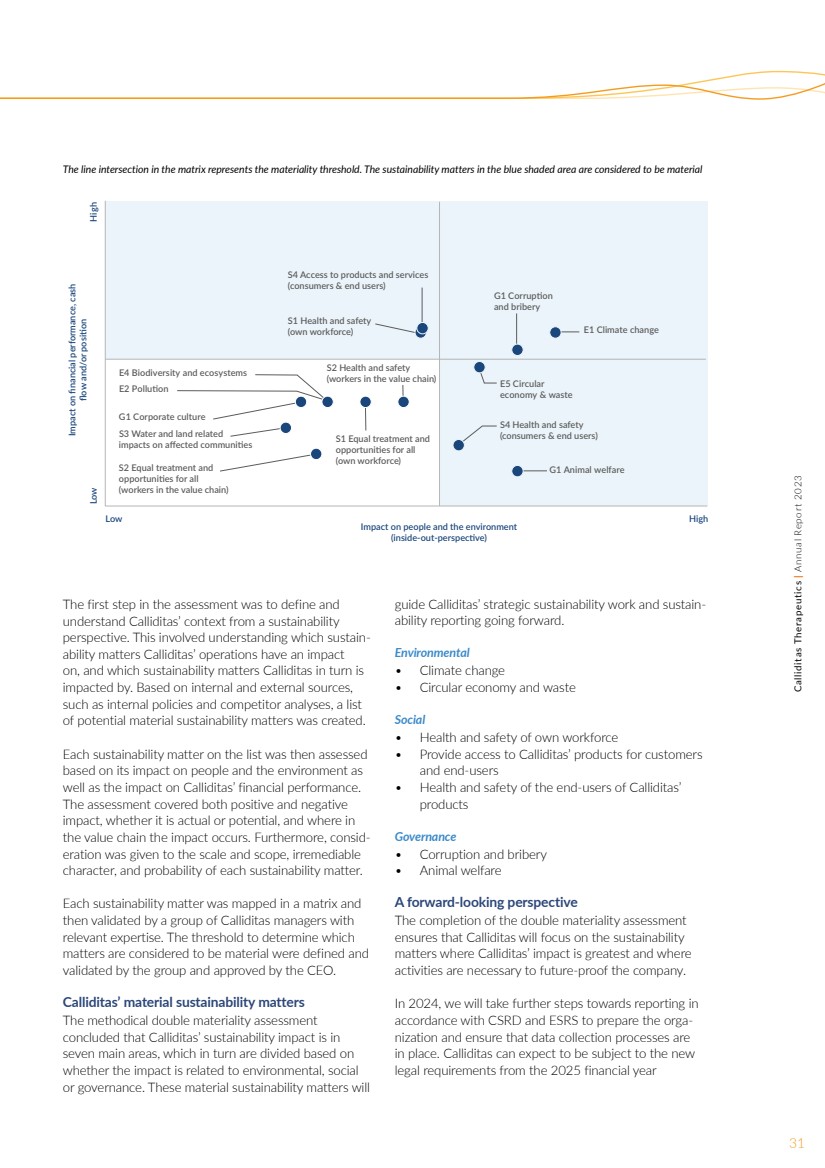
| 31Calliditas Therapeutics | 2023年年度报告矩阵中的线交点代表重要性阈值。蓝色阴影区域的可持续发展问题被认为是实质性的 评估的第一步是从可持续性 的角度定义和 了解Calliditas的背景。这涉及了解哪些可持续发展问题Calliditas的运营会影响 ,以及Calliditas反过来又受哪些可持续发展问题的影响 。根据内部和外部来源, (例如内部政策和竞争对手分析),创建了一份潜在的材料可持续性问题清单 。 然后,根据清单上的每个可持续发展事项对人和环境的影响以及对Calliditas财务业绩的影响对其进行了评估 。 评估涵盖了正面和负面 影响,无论是实际影响还是潜在影响,以及影响发生在 价值链中的哪个位置。此外,还考虑了每个可持续发展问题的规模和范围、不可补救的 特征以及概率。 每个可持续发展问题都绘制在一个矩阵中, 然后由一组具有 相关专业知识的Calliditas经理进行验证。确定哪些 事项被视为重大事项的阈值由该小组定义和 验证,并得到首席执行官的批准。 Calliditas的物质可持续性很重要 有条不紊的双重实质性评估 得出结论,Calliditas的可持续发展影响分为 七个主要领域,这七个领域反过来又根据影响是与环境、社会 还是治理有关 来划分。这些物质可持续性问题将 指导Calliditas未来的战略可持续发展工作和可持续发展报告。 环境 • 气候变化 • 循环经济和废物 社会 • 自身员工的健康和安全 • 为客户 和最终用户提供获得 Calliditas 产品的机会 • Calliditas 产品最终用户的健康和安全 治理 • 腐败和贿赂 • 动物福利 前瞻性视角 双重实质性评估的完成 确保了Calliditas将重点放在可持续性问题上 ,其中Calliditas的影响力最大, 活动是必要的让公司经得起未来考验。 2024 年,我们将采取进一步措施,按照 CSRD 和 ESRS 在 中进行报告,为组织做好准备,并确保 数据收集流程到位。预计Calliditas将受到2025财年新的 法律要求的约束 E1 气候变化 E2 污染 E4 生物多样性和生态系统 E5 通告 G1 企业文化 G1 Corrupon 和贿赂 G1 动物福利 对财务业绩、现金 流量和/或的影响 posion 对人和环境的影响 (由内而外的视角) 低 Lo Lo 高 高 S4 获得产品和服务 (消费者和最终用户) S1 健康与安全 (自有员工) S3 水和土地相关的 对受影响社区的影响 S2 所有人 (价值链中的员工)享有平等待遇和 机会 S1 为所有人 (自己的员工)提供平等待遇和 机会 S2 健康与安全 (价值链中的员工) S4 健康与安全 (消费者和最终用户) |
| 董事会报告 多年摘要,集团 多年摘要,母公司 运营 Calliditas Therapeutics 是一家商业阶段的生物制药 公司,总部位于瑞典斯德哥尔摩,专注于 发现、开发和商业化孤儿适应症的新型 疗法,最初的重点是医疗 需求未得到满足的 肾脏和肝脏疾病。 我们的主要产品提供了一种治疗方案, 已被证明可以改善IgA 肾病(IGaN)(也称为伯杰氏病 )的疾病。伯杰氏病是一种进行性自身免疫性肾脏疾病, 对许多患者来说会导致终末期肾脏疾病 (ESRD),需要透析或器官移植。这款 药物产品以Nevecon® 的名义开发, 于2021年获得美国食品药品管理局的加速批准,并于2023年12月获得全面批准,如今 以TARPEYO® 品牌在美国上市。 TARPEYO 现在是第一种也是唯一一种完全获美国食品药品管理局批准的 基于肾脏 功能衡量标准的 iGaN 疗法。Nevecon还获得了欧盟委员会 以Kinpeygo® 品牌在欧洲 经济区(EEA)和英国的有条件的 上市许可。Kinpeygo 目前正在接受欧盟委员会的全面上市许可的审查。 Nevecon 也已在中国 获得有条件批准,在澳门获得批准,并正在接受新加坡、香港和韩国监管机构的审查。 Calliditas还建立了合作伙伴关系,共同开发 并在日本实现Nefecon的商业化。 IgA 肾病是全球最常见的原发性 肾小球肾炎,因此 的市场潜力巨大,我们早期 的商业成功以及潜在付款超过3亿美元、包括预先付款和预先设定的里程碑、 以及持续的特许权使用费义务的超额许可协议就证明了这一点。 我们的后期产品线基于同类首创的氮氧化物抑制剂平台。我们的主要化合物setanaxib, 可抑制参与炎症和纤维化 途径的酶,并且是该类别中第一个进入临床阶段的候选药物。Setanaxib目前正在进行针对以炎症和纤维化为特征的 罕见疾病的临床试验,包括IPF和PBC, ,Calliditas还启动了一项使用setanaxib 治疗Alport综合征的试验。此外,基于令人鼓舞的 临床前发现,我们正在对头颈癌进行概念验证试验,以进一步支持 该类别药物的作用模式。 2023 2022 2021 2020 2019 年净销售额(千瑞典克朗)1,206,888 802,879 229,347 874 184,829 所得税前亏损(千瑞典克朗)(457,017) (409,417) (513,373) (436,151) (32,501) 总资产(千瑞典克朗)1,859,245 1,952,973 1,952,973 459,910 1,463,908 845,200 平均员工人数 181 86 56 23 14 2020 2020 2019 年净销售额(千瑞典克朗)805,551 548,977 229,347 874 184,829 所得税前亏损(千瑞典克朗)(273,518) (208,548) (354,405) (407,363) (36,186) 总计资产(千瑞典克朗)2,255,130 2,173,639 1,528,439 1,318,525838,249平均员工人数58 45 29 15 13 32Calliditas Therapeutics | 2023年年度报告Calliditas Therapeutics AB(publ)的董事会和首席执行官特此提交2023财年的年度报告和合并 财务报表,注册办事处位于瑞典斯德哥尔摩 ,公司注册号为556659-9766。除非另有说明,所有金额均以百万瑞典克朗表示。 |
| 33Calliditas Therapeutics | 2023年年度报告虽然我们的总部位于瑞典斯德哥尔摩,但我们 在美国保持着重要的影响力, 在纽约和新泽西设有办事处。我们还在法国和瑞士设有 办事处,我们的发现 团队就设在那里。Calliditas Therapeutics普通股 于2018年在纳斯达克斯德哥尔摩上市(CALTX) ,随后代表我们普通股的美国存托股份 于2020年(CALT)在美国纳斯达克全球精选市场上市。 该集团由母公司Calliditas Therapeutics AB、美国子公司Calliditas NA Enterprises Inc、Calliditas Therapeutics 美国公司、 法国子公司Calliditas Therapeutics France SAS、 瑞士子公司Calliditas Therapeutics Suisse S.A. 瑞典子公司Nevecon AB没有持续的 业务组成。 年度重大事件 第一季度 2023 年 2 月,Calliditas 宣布,英国 药品和保健产品监管局 (MHRA) 授予了 Kinpeygo® 有条件的 上市许可 (CMA),用于 治疗有快速发病风险的成年人的免疫球蛋白 A (IgA) 肾病 尿蛋白与肌酐比率 (UPCR) ≥1.5g/g时进展。 Kinpeygo 成为英国第一种也是唯一获得批准的 iGaN 治疗药物。 2023 年 3 月,Calliditas 宣布了全球随机、双盲、 安慰剂对照的 3 期临床试验 nefiGard 的阳性 结果,该试验调查了 Nevecon(TARPEYO®/ Kinpeygo®(布地奈德)延迟释放胶囊) 与安慰剂对原发性 IgA 肾病患者的影响疗法 (iGaN)。 该试验达到了其主要终点,与安慰剂(p 值)相比,Nefecon 具有极高的统计学意义 |
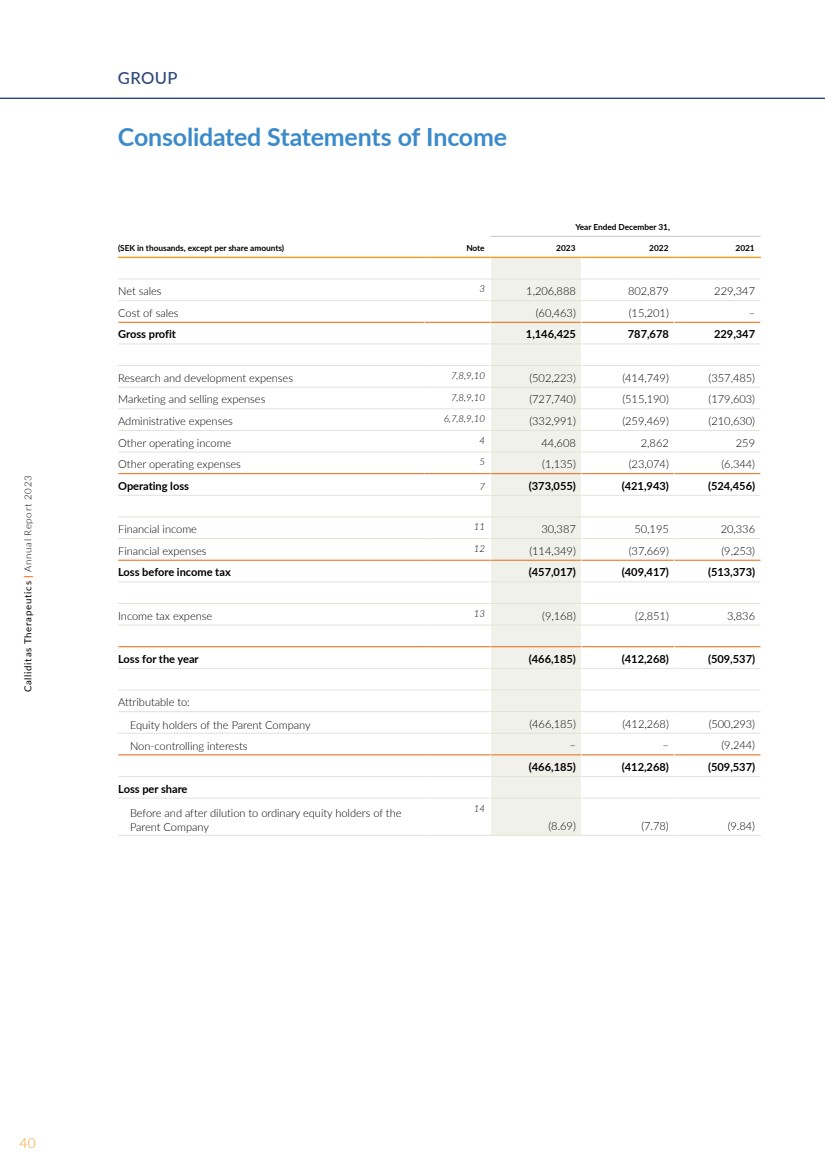
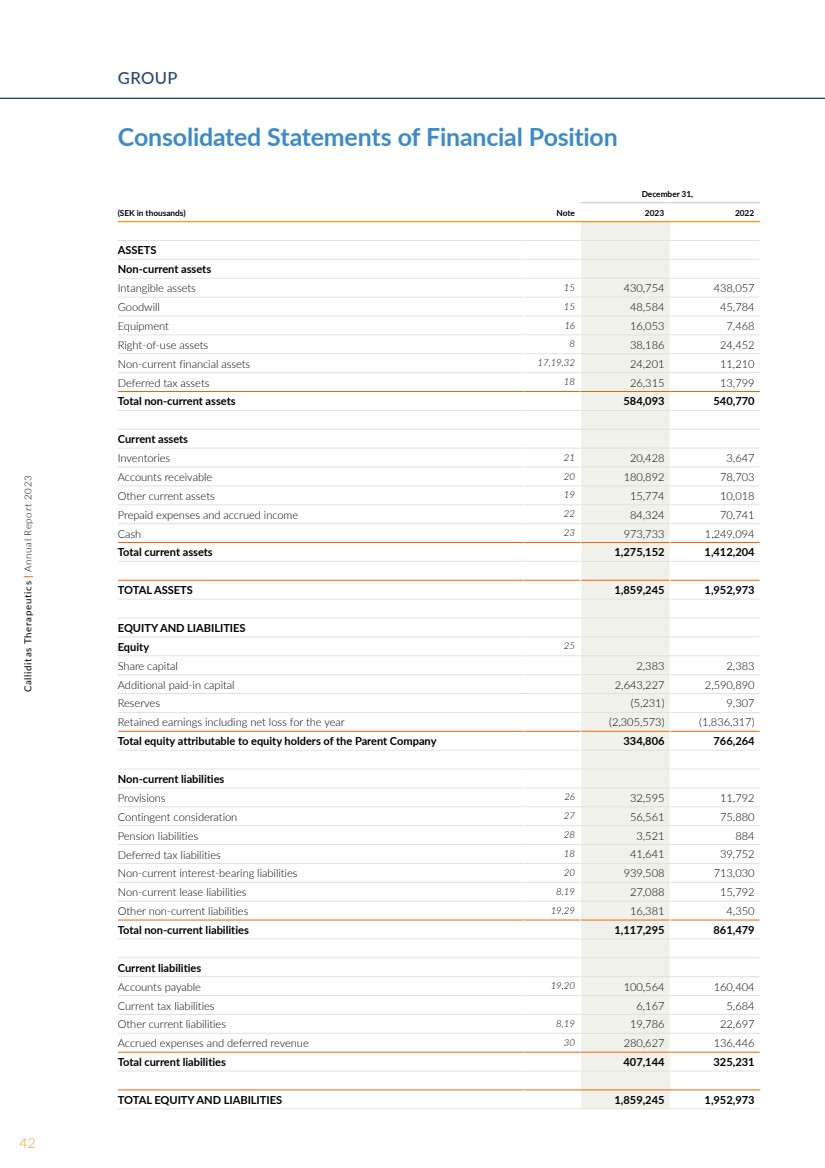
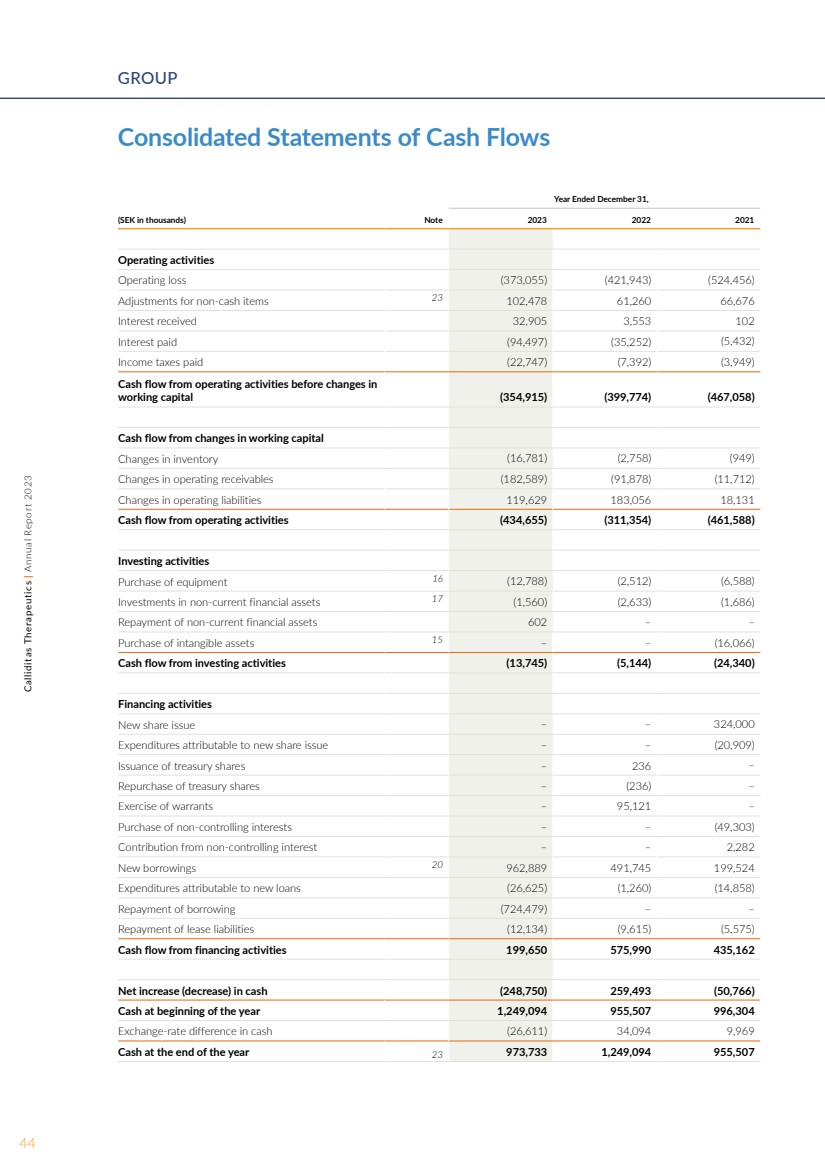
| 销售额和收益 截至2023年12月31日和2022年12月31日,集团的收入分别为12.069亿瑞典克朗 和8.029亿瑞典克朗, 主要来自TARPEYO在美国的净销售额以及我们在欧洲、中国 和日本合作伙伴关系的里程碑。截至2023年12月31日和2022年12月31日的 年度,TARPEYO的总净销售额分别为10.758亿瑞典克朗和3.722亿瑞典克朗。截至2023年12月31日和2022年12月31日止年度,我们的合作伙伴关系 的里程碑和特许权使用费分别为1.195亿瑞典克朗和4.274亿瑞典克朗 。 销售成本 截至2023年12月31日和2022年12月31日止年度的销售成本分别为6,050万瑞典克朗和1,520万瑞典克朗。 研发费用 截至2023年12月31日和2022年12月31日止年度 的研发费用分别为5.022亿瑞典克朗和4.147亿瑞典克朗。 增加了8,750万瑞典克朗,这主要是由于setanaxib平台的临床活动,包括 正在进行的setanaxib试验,与去年相比。 营销和销售费用 截至2023年12月31日和2022年12月31日止年度的营销和销售费用分别为7.277亿瑞典克朗和5.152亿瑞典克朗。 增加2.125亿瑞典克朗主要与 TARPEYO在美国 的销售和营销成本有关。 管理费用 截至2023年12月31日和2022年12月31日的年度管理费用分别为3.33亿瑞典克朗和2.595亿瑞典克朗。与去年相比,7,350万瑞典克朗的增长主要与组织规模扩大以及监管 要求的提高所导致的总体成本增加有关。 截至2023年12月31日和2022年12月31日的年度其他营业收入/支出,净额 其他营业收入/(支出),净额分别为 4,350万瑞典克朗和(2,020万瑞典克朗)。 这种改善主要归因于与营业应收账款和负债相关的汇率变动。 财务收入/支出 截至2023年12月31日和2022年12月31日止年度的财务收入分别为3,040万瑞典克朗和5,020万瑞典克朗,主要与未实现的货币收益有关。截至2023年12月31日和2022年12月31日的 年度财务支出分别为1.143亿瑞典克朗和3,770万瑞典克朗, 增长主要包括利息支出和与借款有关的 费用,主要来自翻译效应 。 税 截至2023年12月31日和2022年12月31日止年度的所得税/(支出)总额分别为(920万瑞典克朗)和(290万瑞典克朗)。 的增长主要是由美国子公司确认的应纳税 利润来解释的。集团结转的税收损失 未被确认为递延 税收资产,除非此类税收亏损 可用于抵消临时差额。 收益 截至2023年12月31日和2022年12月31日的财年, 集团的净亏损分别为4.662亿瑞典克朗和4.123亿瑞典克朗,摊薄前后的相应每股亏损分别为8.69瑞典克朗和7.78瑞典克朗。 截至2023年12月31日和2022年12月31日, 流动性和财务状况 现金分别为9.737亿瑞典克朗和12.491亿瑞典克朗, 。截至2023年12月31日和2022年12月31日,与母公司 股东相关的股东权益分别为3.348亿瑞典克朗和7.663亿瑞典克朗。 现金流 截至2023年12月31日和2022年12月31日的年度中,用于经营活动的现金流分别为4.347亿瑞典克朗和3.114亿瑞典克朗。 减少的主要原因是 当前应收账款的变化。截至2023年12月31日和2022年12月31日止年度, 用于投资活动的现金流分别为1,370万瑞典克朗和510万瑞典克朗。 的增长主要是由于购置了 设备。 截至2023年12月31日和2022年12月31日的年度中, 来自融资活动的现金流分别为1.997亿瑞典克朗和5.76亿瑞典克朗。 34Calliditas Therapeutics | 2023 年年度报告董事会报告 |
| 下降的主要原因是 净借款与去年同期相比减少。 截至2023年12月31日和2022年12月31日止年度,现金净增加/(减少)分别为(2.488亿瑞典克朗)和2.595亿瑞典克朗。 人员 截至 2023 年 12 月 31 日和 2022 年 12 月 31 日,集团的员工人数分别为 195 名和 102 名员工。截至2023年12月31日和2022年12月31日,包括顾问在内的全职同等学历 (全职员工)的总人数分别为217和178人。在截至2023年12月31日和2022年12月31日的 年度中, 的平均员工人数分别为181和86人,其中 58%为女性,42%为男性。 环境 Calliditas积极努力减少其 对环境的不利影响,并发展成为一家可持续发展的 公司。Calliditas的产品对 环境的影响有限。相反,在产品和服务购买、 能源消耗和旅行等领域,环境影响是 。Calliditas的目标是 为可持续发展做出贡献,因此 正在努力在经济可行的范围内积极改善环境绩效。 长期激励计划 该集团目前有三个未完成的期权计划 ,即2021年ESOP、2022年ESOP和2023年ESOP 2023。这些选项将免费授予参与者 。自授予之日起,这些期权的三年归属期 ,前提是 参与者仍受雇于/仍向Calliditas提供 服务,但通常例外。行使期权后,可以在一年内行使。每个 既得期权使持有人有权以预定价格收购公司的一股 股份。每股 股的价格应相当于授予日 前十个交易日公司股票在 斯德哥尔摩纳斯达克交易的加权平均 价格的 115%。2021年ESOP的期权最早可以在2024年第二季度 期间行使。2022年ESOP的期权最早可以在2025年第三季度行使 。 2023年ESOP的期权最早可以在2026年第三季度的 行使。截至年底, 共分配了6,098,730份期权。 Calliditas还为Calliditas的 董事会成员制定了三项长期激励计划,即LTIP 2021、LTIP 2022和 LTIP 2023。该计划的参与者将免费获得 基于绩效的股票奖励。 2021年LTIP中的股票奖励视业绩为基础的收益而定,该收益基于 Callidita自2021年年度股东大会之日起至2024年7月1日的股价走势。2022年LTIP中的股票奖励 以业绩为基础的收益 视Callidita从2022年年度股东大会之日起 至 2025年7月1日的股价变化而定。2023年LTIP中的股票奖励受 基于业绩的收益的限制,该收益基于Callidita自2023年年度 股东大会之日起至2026年7月1日的股价走势。总的来说, 共有相当于 100,975股在年底完全归属时的未偿股票奖励。有关 有关认股权证计划的更多信息,请参阅 附注 10 基于股份的付款。 股本和股东 年底的股本为 240万瑞典克朗,分为59,580,087股, 的商值为0.04瑞典克朗。所有股份均为普通 股,对公司利润 享有同等权利,每股在年度股东大会 上有一票表决权,不包括Calliditas持有的股份。自2018年6月29日起,Calliditas的股票已获准在斯德哥尔摩纳斯达克证券交易中型股板块交易 ,自2020年6月5日起, 美国存托凭证获准在美国纳斯达克环球精选上市。 截至2023年底,Calliditas拥有19,000(18,585)名 股东,十大股东拥有 47.4(48.3)%的所有已发行股份,其中不包括Calliditas持有的 股票。截至2023年12月31日, BVF Partners LP、Linc AB和Stiftelsen Industrifonden 是该公司的单一最大股东, 共有6,260,311股、5,962,312股和3,145,440股,分别相当于选票和资本的10.5%、10.0% 和5.3%。 有关股票的更多信息,请参阅 第 10-11 页。 董事会的工作 Calliditas董事会由包括主席在内的六名董事会 成员组成,主席当选 任期至2024年股东周年大会。董事会 遵循书面程序,该程序每年 修订一次,并在董事会每年的第一次例行董事会会议上确定 。除其他外, 议事规则规定了董事会的职能 以及 35Calliditas Therapeutics 之间的职能和工作分工 | 2023 年年度报告 |
| 董事会成员和首席执行官。 在董事会会议方面, 董事会还制定了对首席执行官的指示, 包括财务报告。董事会按照年度时间表举行会议。除了这些董事会 会议外,还可能召开 其他董事会会议,以解决可能未提交定期的 董事会会议的问题。2023 年,董事会举行了 13 次会议。在 中,除了董事会会议外, 董事会主席和首席执行官就 公司的管理层进行了持续的对话。 有关 董事会工作的更多信息,请参阅第 88-93 页的公司治理报告 。 现行高管薪酬指导方针 集团的执行管理层属于 本准则的规定范围。执行管理是指 执行管理层的首席执行官和其他成员,以及董事会成员。 指导方针具有前瞻性,即 在2020年年度股东大会通过指导方针 之后,它们适用于 商定的薪酬,以及已经商定的薪酬修正案。这些准则 不适用于股东大会决定或批准 的任何薪酬。 该指南促进了Calliditas的业务战略、 的长期利益和可持续性 Calliditas的业务战略是推动其主要候选人Nefecon完成第三阶段临床开发, 朝着监管部门批准以及随后的商业化和许可方向发展。在加快 的批准之后,Calliditas通过与名为Kinpeygo的欧洲STADA 合作,开始在美国单独将用于IgA 肾病的Nevecon商业化, 品牌为TARPEYO,并在中国和日本等其他地区签署了合作伙伴关系。 Calliditas还将有选择地探索 Nevecon和setanaxib以及 正在研发的其他候选药物的产品线延长,这些药物具有强有力的科学和临床依据以及具有吸引力的商业 机会的其他疾病,例如某些肾脏和肝脏疾病。 Calliditas也可以选择性地考虑利用 集团的能力,为开发和商业化寻找与 Nevecon 具有强烈战略和商业契合度的其他产品 候选产品。 Calliditas的业务战略和保障 其长期利益,包括其可持续性, 假定Calliditas能够招聘和留住 合格人员。为此, Calliditas必须提供有竞争力的薪酬。这些 指导方针使Calliditas能够为高管 管理层提供有竞争力的总薪酬。 薪酬类型等。 Calliditas应按照 市场惯例提供薪酬,从而可以招聘和留住合格的高管。 集团内部的薪酬应基于绩效、 竞争力和公平原则。 执行管理层的薪酬可能包括固定薪酬、可变薪酬、 份额和股价相关激励计划、 养老金和其他福利。如果当地条件证明薪酬原则的 变动是合理的,则可能会发生这种差异。 固定薪酬应反映个人的 责任和经验水平。固定薪酬应每年审查一次。 这些 指南所涵盖的可变现金薪酬应旨在促进Calliditas的业务 战略和长期利益,包括其可持续性,例如与 业务战略明确挂钩或促进高管的长期 发展。 可变现金薪酬奖励标准的满足程度应在一年内衡量 。以现金支付的可变薪酬 不得超过年度固定现金 工资的60%。可变薪酬应与 预先确定和可衡量的标准相关联, 的设计目的是促进集团的长期价值 创造。应在衡量期 结束时评估/确定在多大程度上满足了可变现金薪酬的标准。薪酬委员会负责 评估,因为评估涉及首席执行官和其他高管的可变薪酬。对于财务 目标,评估应基于集团公布的最新 财务信息。 养老金应以保费为基础。可变现金薪酬不符合领取养老金福利的资格。对于 首席执行官和其他高管,在适用保费型养老金的 情况下, 的保费最高可达年度 固定现金工资的30%。尽管如此, 董事会有权提供其他解决方案, 就成本而言,该方案与上述方案相同。 36Calliditas Therapeutics | 2023 年年度报告董事会报告 |
| 高管可以按惯例获得其他福利, 例如公司汽车、职业健康服务等。 此类其他福利金额可能不超过固定年现金工资的15%。 已在Calliditas中实施了针对员工、 顾问和董事会成员的长期股票相关激励计划。此类计划已由 股东大会解决,因此不在 本指南中。有关这些 激励计划的更多信息,包括 结果所依赖的标准,请参阅 https://www.calliditas。 se/en/治理/薪酬/。 在Calliditas和首席执行官之间, 的通知期限为公司发出通知后的12个月。经首席执行官通知 ,通知期限为 6 个月。对于 其他执行管理层成员,请注意 期限为 3 至 12 个月。在通知 期内,应支付正常的现金工资。此外,可以为非竞争承诺支付 报酬。此类薪酬应补偿 收入的损失,并且只能在先前 雇用的高管无权获得遣散费的情况下支付。 薪酬应不超过终止雇用时固定现金工资的60%,应在 竞业禁止承诺适用期间支付,但不得超过终止雇佣关系后的12个月。 如果董事会成员为 Calliditas 工作,除了董事会工作外,还可能需要为此类工作支付咨询 费用和其他报酬。对于受瑞典以外其他规则 管辖的就业,可以在 尽可能 考虑这些指导方针的总体目的的前提下,对养老金福利和其他福利进行适当调整,使之符合强制性规则 或当地既定惯例。 员工的工资和就业条件 在起草董事会关于这些薪酬指导方针的提案 时, 通过在 薪酬委员会和董事会中纳入有关 员工总收入、薪酬组成部分以及随时间推移的增长和增长率的信息, 考虑到了Calliditas员工的工资和就业条件 br} 评估此处规定的指导方针和限制是否合理时的决策依据。 确定、审查和 实施指导方针的决策过程 董事会已成立薪酬 委员会。该委员会的任务包括准备 董事会关于提出高管薪酬指导方针 的决定。董事会 应至少每四年 编制一份新指导方针提案,并将其提交给股东大会。 在股东大会通过新的指导方针 之前,该指导方针将一直有效。薪酬 委员会还应监督和评估执行管理层可变薪酬计划 、高管 薪酬指导方针的适用情况以及集团目前的薪酬 结构和薪酬水平。薪酬委员会的 成员独立于Calliditas及其执行管理层。 首席执行官和执行管理层的其他成员 不参与董事会对薪酬相关事项的处理 和有关此类事项的决议。 偏离准则 如果在 的具体案例中有特殊的减损理由,且 为了维护Calliditas的长期 利益,包括其可持续性,或为了确保 集团的财务可行性, 需要减损,则董事会可以暂时决定 全部或部分减损准则。如上所述,薪酬委员会的任务包括编写 董事会关于薪酬相关事项的决议。此 包括任何偏离指导方针的决议。 风险管理 Calliditas的董事会和管理层持续工作 ,以识别和评估公司运营的风险,并采取措施降低 这些风险的影响。针对每个 重大风险制定风险管理策略。这项工作涉及商业化、监管策略以及 临床试验的设计和实施等 领域专业知识的支持。 风险和不确定性 Calliditas的运营受到影响集团收益和财务状况的许多因素 的影响, 在某些方面, 无法由Calliditas部分或全部控制 。在评估Calliditas的未来发展时,除了利润增长机会外,还必须考虑这些风险。下面列出了集团 未来发展方面最重要的 重大风险和不确定性,不按 的优先顺序排列。 37Calliditas Therapeutics | 2023 年年度报告 |
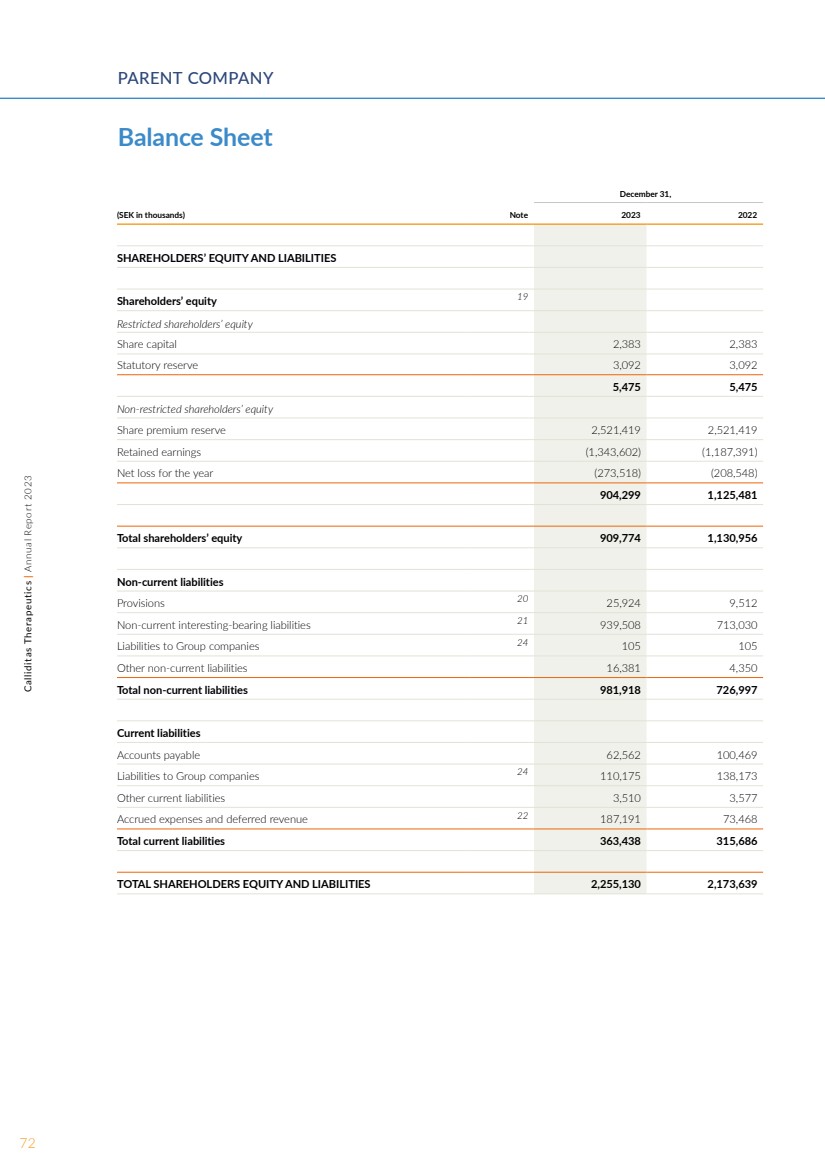
| 运营风险 Callidita的主要活动是药品的研发 和商业化,这是一个 领域,在很大程度上既是风险又是资本密集型的。Calliditas有一款处于 商业阶段的产品,即Tarpeyo/Kinpeygo/Nefecon,该产品 已获准在美国、中国 和欧洲上市。存在以下风险: 无法按计划进行商业化,接受治疗 医生的接受程度将低于计划,或者药物 不会产生足够的效果或显示出不良的副作用,这可能会对销售产生负面影响。Calliditas 有两种候选产品正在临床开发中, Nevecon 和 setanaxib,分别用于治疗 IgA 肾病和原发性胆源性胆管炎以及头部 和颈部癌,而且 这些项目有可能永远无法进入市场注册或获得 的全面批准,因为这些药物可能不具有 足够的效果或显示出不想要的副作用。即使 在药物上市之后,如果出现严重的副作用,也可撤回市场注册。 Calliditas对其候选产品 进行临床研究。临床研究既耗时又昂贵 ,涉及诸如难以寻找 诊所、难以招募合适患者、每位患者的 成本超出预算以及参与研究的诊所 的研究表现存在缺陷等风险。Nevecon 和 setanaxib 都是孤儿药候选药物,分别为 IgA 肾病和原发性胆源性胆管炎。因此,适合临床试验 的患者数量低于常见疾病的患者人数,对于Calliditas来说,招募患者实施治疗原发性胆源性胆管炎的2b期研究和治疗头颈部癌和Alport 综合征的2期研究 可能是一项挑战。 如果竞争药物占据市场份额或竞争性 研究项目取得更好的效果并更快地进入 市场,则产品组合 的未来价值可能会低于预期。Calliditas 提交的专利申请可能永远不会获得批准,批准的 专利可能会被取消,这可能会导致 Calliditas 失去专利保护。该业务还受到批准和价格 变更等政府决定的影响。关于 认为孤儿药定价过高的政治辩论仍在继续,尤其是在美国 。新规定有可能对未来的孤儿药价格产生 负面影响。 在 产品的制造方面也存在风险,选定的制造商可能在 交付足够的质量和/或数量 时遇到 问题,或者失去必要的制造许可证。 Callidita战略的一部分是研究 开发其他适应症产品的可能性。但是, Calliditas尚未完成任何其他适应症的临床 试验。进行临床试验 总是与研究的实施、结果和监管机构的批准相关的风险相关,因此,目前尚不确定Callidita开发用于治疗其他适应症的产品 的雄心是否会实现。 乌克兰战争和欧盟对俄罗斯和白俄罗斯实施的制裁 的风险预计将是有限的,不会直接影响该集团,因为 与欧盟限制性措施所列的国家或实体没有直接联系或风险。将来对任何强制性制裁或局势的发展进行监测和解决 。 流动性风险 Calliditas通过持续监控现金流来管理流动性风险,从而降低流动性风险和 确保其偿付能力。Calliditas有盈利能力,但是 它目前无法支付其成本,因此Calliditas 可能依赖外部融资,并且存在 在需要时无法向Calliditas 提供外部融资的风险。 金融风险 Calliditas管理金融风险的财务政策由 董事会设计,以风险法定和限制 的形式代表了指导方针和规则框架,适用于金融活动。除了上述流动性 风险外,集团还主要受到 外汇风险的影响,因为Nevecon和setanaxib的开发成本 主要以美元 和欧元支付。此外,集团持有美元应收账款以及美元和欧元现金,以支付与TARPEYO在美国商业化和临床开发计划有关的 未来美元和欧元预期成本。集团目前对外部贷款没有 可变利率,因此 没有利息成本增加的重大风险。 母公司 Calliditas Therapeutics AB专注于集团的管理、研发、拥有 和管理子公司以及为商业 子公司和商业合作伙伴提供支持。 母公司的净销售额为8.056亿瑞典克朗, 38Calliditas Therapeutics | 2023年年度报告董事会报告 |
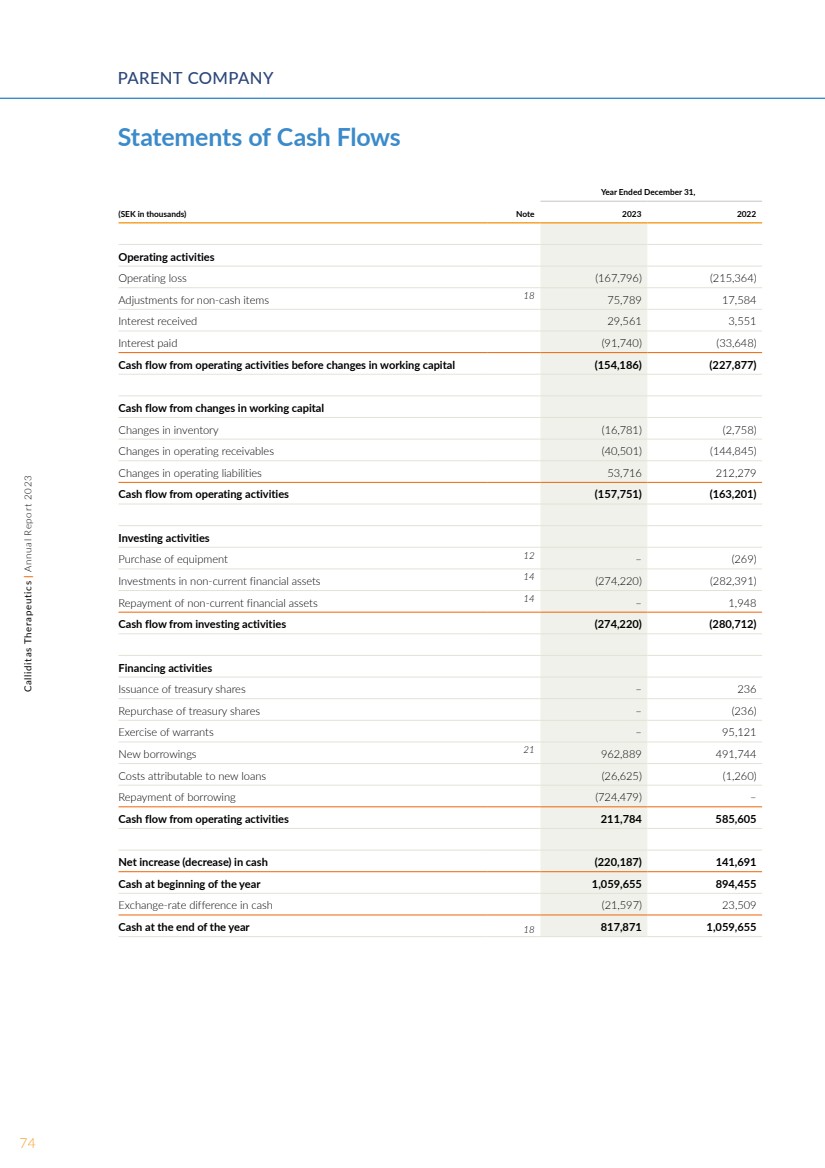
| 截至2023年12月31日的年度, 2023年和2022年12月31日的年度分别为5.49亿瑞典克朗。与去年相比,增长主要是TARPEYO的 销售额。 截至2023年12月31日和2022年12月31日止年度, 的营业亏损分别为1.678亿瑞典克朗和 2.154亿瑞典克朗。 营业亏损的改善主要源于 收入与去年相比的增长。截至2023年12月31日和2022年12月31日,非流动 金融资产分别为11.252亿瑞典克朗和 8.875亿瑞典克朗。2.377亿瑞典克朗的增长主要来自公司间交易。 截至2023年12月31日和 2022年,母公司的现金分别为8.179亿瑞典克朗 和10.597亿瑞典克朗。 Outlook Callidita的药物Nevecon在美国以 的名称TARPEYO商业化,具有巨大的市场潜力,2023年12月20日,美国食品药品管理局的历史性批准达到了一个里程碑式的裁决 。当时,该药物 成为第一种也是唯一一种获得完全批准的用于减少患有 原发性IgAn的成年人肾功能丧失的治疗药物。美国食品药品管理局的批准适用于患有 原发性IgAn的成年人,无论蛋白尿水平如何,都有疾病进展的风险,并为IgAn的 治疗设定了新的标准。2022年,Kinpeygo获得了欧洲合作区(EEA) 的有条件批准,2023 年,Nevecon 在中国获得了有条件的批准 。因此,这些批准标志着Calliditas向一家处于 商业阶段的生物制药公司过渡。 Callidita与关键利益相关者 一起在肾脏病学科学领域 的强大影响力 反映了继续开展科学交流活动 的战略工作。随着美国商业 业务和临床研发研究的继续, 运营是资本密集型的,在Nefecon/ Tarpeyo/KinpeyGO带来超过 成本的收入之前,可能需要外部融资。截至2023年12月31日,该集团的 现金状况为9.737亿瑞典克朗,并视Tarpeyo在美国的持续成功商业化而定,目前认为 在实现运营正现金流之前 已经足够了。 公司 收益的拟议拨款 拟议收益拨款 以下收益(TSEK)由 年度股东大会支配, 股票溢价储备 2,521,419 留存收益(1,343,602) 年度净亏损(273,518) 904,299 董事会提议 904,299 万瑞典克朗已结转。 股息政策 未来的任何股息及其规模将根据长期增长、收益趋势 和Calliditas的资本要求来确定。 董事会认为,Calliditas应优先考虑发展计划的进展,在 未来的收入大大超过 的运营成本之前,财务资源应主要用于 为Calliditas的发展计划提供资金。 鉴于公司的财务状况和负 收益,董事会不打算在公司产生 长期可持续利润和正现金流之前 提议任何股息。 就拟议的分红而言, 股息应在业务风险方面保持平衡。 董事会提议,鉴于股息 政策,2023财年 不支付任何股息。 有关集团和母公司 收益和财务状况的更多信息,请参阅以下 收入和财务状况表、 股东权益和现金流变动以及随附的 补充披露。 39Calliditas Therapeutics | 2023 年年度报告 |
| 合并收益表 截至12月31日的年度, (千瑞典克朗,每股金额除外)附注 2023 2021 年净销售额 3 1,206,888 802,879 229,347 销售成本 (60,463) (15,201) — 毛利 1,146,425 787,678 229,347 研发费用 7,8,9,10 (502,223) (4,223) (4,223) 14,749) (357,485) 营销和销售费用 7,8,9,10 (727,740) (515,190) (179,603) 管理费用 6,7,8,9,10 (332,991) (259,469) (210,630) 其他营业收入 4 44,608 2,862 259 其他运营费用 5 (1,135) (2335) (2335) (233) ,074) (6,344) 正在运行亏损 7 (373,055) (421,943) (524,456) 财务收入 11 30,387 50,195 20,336 财务费用 12 (114,349) (37,669) (9,253) 所得税前亏损 (457,017) (409,417) (513,373) 所得税支出 13 (9,168)) (2,851) 3,836 本年度亏损 (466,185) (412,268) (509,537) 归属于: 母公司 (466,185) (412,268) (500,293) 非控股权益 — — (9,244) (466,185) (412,268) (412,268) (500,293) (466,185) (412,268) (500,293) (466,185) (412,268) (500,293) (466,185) (412,268) (500,293) 509,537) 每股亏损 母公司普通股持有人摊薄前后的每股亏损 14 (8.69) (7.78) (9.84) 40Calliditas Therapeutics | 2023 年年度报告集团 |
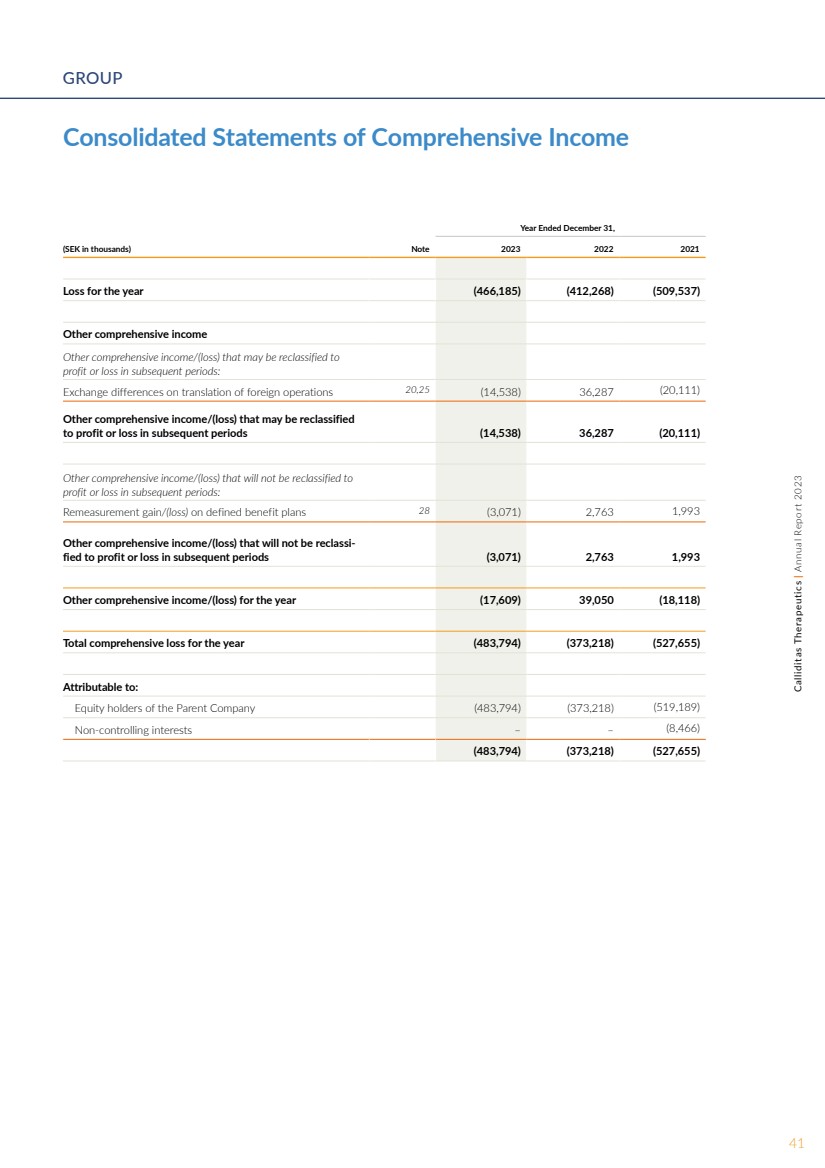
| 合并综合收益表 截至12月31日的年度综合收益表, (千瑞典克朗)附注 2023 2021 年年度亏损 (466,185) (412,268) (509,537) 其他综合收益 后续时期可能重新归类为 损益的其他综合收益/(亏损): 对外业务折算的汇兑差额 20,25 (14,538) 36,287 (20,111) 后续时期可能重新归类为损益的其他综合收益/(亏损)(14,538)36,287(20,111) 其他综合收益/(亏损)在后续时期不得重新归类为 损益: 固定福利计划的调整收益/(亏损)28 (3,071) 2,763 1,993 其他综合收益/(亏损)在后续时期不会重新归类为损益(3,071)2,763 1,993 该年度(17,609)39,09 的其他综合收益/(亏损)39,09 50 (18,118) 年度综合亏损总额 (483,794) (373,218) (527,655) 归属于: 母公司 (483,794) (373,218) (519,189) 非控股权益 — — (8,466) (483,794) (373,218) (527,218) (527,655) 41Calliditas Therapeutics | 2023 年年度报告集团 |
| 合并财务状况表 12 月 31 日, (千瑞典克朗)附注 2023 年资产 非流动资产 无形资产 15 430,754 438,057 商誉 15 48,584 45,784 设备 16 16,053 7,468 使用权资产 8 38,186 24,452 非流动金融资产 17,19,32 24,201 11,210 递延所得税资产 18 26,210 ,315 13,799 非流动资产总额 584,093 540,770 流动资产 存货 21 20,428 3,647 应收账款 20 180,892 78,703 其他流动资产 19 15,774 10,018 预付费用和应计收入 22 84,324 70,741 现金 23973,733 1,249,094 流动资产总额 1,275,152 1,412,204 总资产 1,859,245 1,952,973 权益和负债 权益 25 股本 2,383 额外实收资本 2,643,227 2,590,890 储备金 (5,231) 9,307 包括年度净亏损在内的留存收益 (2,305,573) (1,836,317)) 归属于母公司股东的权益总额 334,806 766,264 非流动负债 条款 26 32,595 11,792 或有对价 27 56,561 75,880 养老金负债 28 3,521 884 递延所得税负债 18 41,641 39,752 非流动负债计息负债 20 939,508 713,030 非流动租赁负债 8,19 27,088 15,792 其他非流动负债 19,29 16,381 4,350 非流动负债总额 1,117,295 861,479 流动负债 应付账款 19,20 100,564 160,404 流动税负债 6,167 5,684 其他流动负债 8,19 19,786 22,697 支出和递延收入 30 280,627 136,446 流动负债总额 407,144 325,231 总权益和负债 1,859,245 1,952,973 42Calliditas Therapeutics | 2023 年年度报告 GROUP |
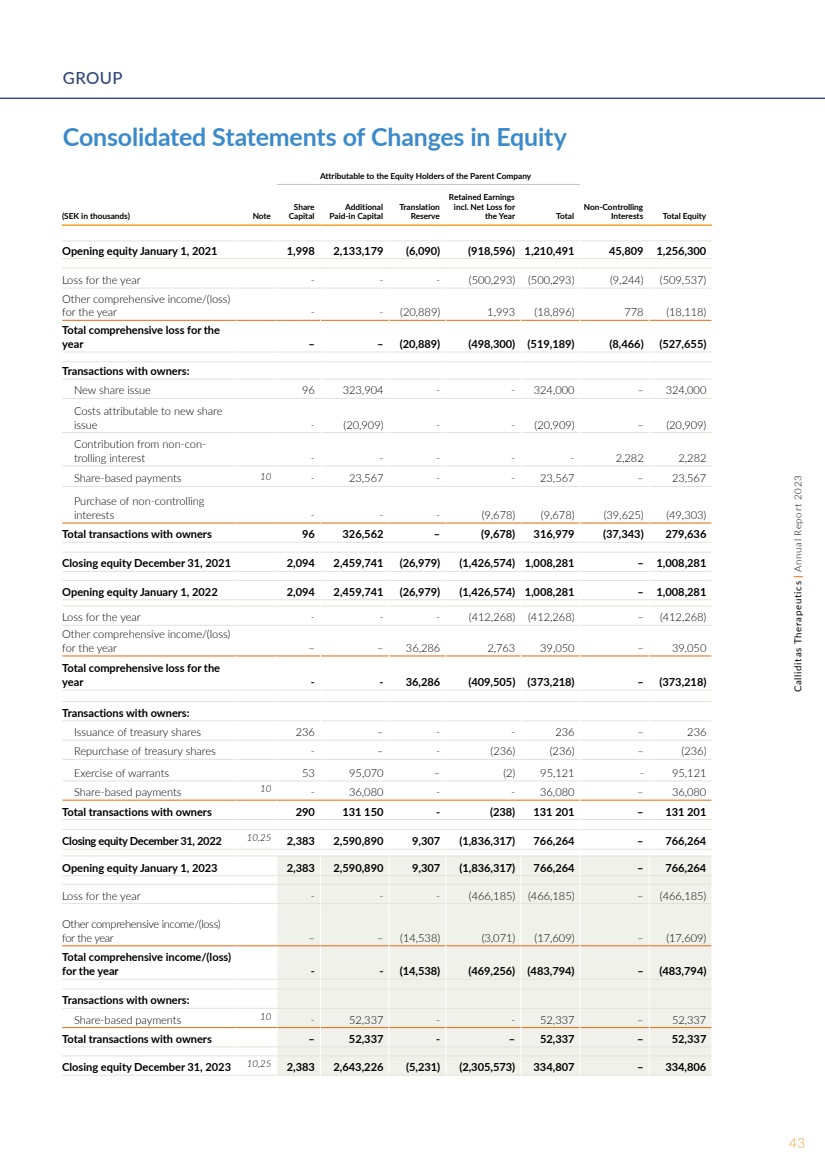
| 归属于母公司权益持有人的权益变动合并报表 (千瑞典克朗)附注 股份 资本 额外 实收资本 折算 储备 留存收益 年度净亏损 非控股 权益总股权 开盘权益 2021 年 1 月 1 日 998 2,133,179 (6,090) (918,596) 1,210,491 45,809 1,256,300 年度亏损--(500,293) (500,293) (9,244) (509,537) 年度其他综合收益/ (亏损) -(20,889) 1,993 (18,896) 796 78 (18,118) 年度综合亏损总额 — — (20,889) (498,300) (519,189) (8,466) (527,655) 与所有者的交易: 新股发行 96 323,904--324,000 — 324,000 归因于新股 发行的成本-(20,909)-(20,909) — (20,909) — (20,909) — (20,909) — (20,909) — (20,909) — (20,909) — (20,909) — (20,909) — (20,909) — (20,909) — (20,909) — (20,909) ,909) 非控股权益出资----2,282 2,282 2,282 股权支付 10-23,567--23,567 — 23,567 购买非控股权 权益--(9,678) (9,678) (39,625) (49,303) 与所有者的交易总数 96 326,562 — (9,662) 678) 316,979 (37,343) 279,636 2021 年 12 月 31 日收盘股权 2,094 2,459,741 (26,979) (1,426,574) 1,008,281 — 1,008,281 2022年1月1日 2,094 2,459,741 (26,979) (1,426,574) 1,008,281 — 1,008,281 — 1,008,281 年度亏损--(412,268) (412,268) — (412,268) — (412,268) — (412,268) — (412,268) — (412,268) — (412,268) — (412,268) — (412,268) — (412,268) — (412,26268) 本年度其他综合收益/(亏损) — — 36,286 2,763 39,050 — 39,050 年度的综合亏损总额--36,286 (409,505) (373,218) — (373,218) 与所有者的交易: 发行库存股 236 —--236 回购国库股票-—-(236) (236) — (236) 行使认股权证 53 95,070 — (2) 95,121-95,121 股基础付款 10-36,080--36,080 — 36,080 与所有者的交易总数 290 131 150-(238) 131 201 — 131 201 2022年12月31日收盘股权 10,25 2,383 2,590,890 9,307 (1,836,317) 766,264 — 766,264 2023年1月1日 2,383 2,590,317 (1,836,317) 766,264 — 766,264 期初净值 2,383 2,590,317) 766,264 — 766,264 年度亏损--(466,185) (466,185) — (466,185) 本年度其他综合收益/ (亏损) — (14,538) (3,071) (17,609) 年--(14,538) (469,256) (483,794) — (483,794) 与所有者的交易: 基于股份的支付 10-52,337--52,337 — 52,337 与所有者的交易总数 — 52,337-— 52,337 — 52,337 2023 年 12 月 31 日收盘股权 10,25 2,383 2,383 2,643,226 (5,231) (2,305,573) 334,807 — 334,806 43Calliditas Therapeutics | 2023 年年度报告集团公司 |
| 合并现金流量表 截至12月31日的年度, (千瑞典克朗)附注 2023 2021 年经营活动 营业亏损 (373,055) (421,943) (524,456) 非现金项目的调整 23 102,478 61,260 66,676 收到的利息 32,905 3,553 102 已付利息 (94,497) (35,252) (5,432) 已缴所得税 (22,747) (7,392) (3,949) 营运资金变动前的经营活动现金流 (354,915) (399,774) (467,058) 来自营运资金变动的现金流 库存变动 (16,781) (2,758) (949) 变动在营业应收账款 (182,589) (91,878) (11,712) 运营负债变动 119,629 183,056 18,131 经营活动产生的现金流 (434,655) (311,354) (461,588) (461,588) (461,588) 投资活动 购买设备 16 (12,788) (2,512) (6,588) 非流动金融投资资产 17 (1,560) (2,633) (1,686) 偿还非流动金融资产 602 — — 购买无形资产 15 — — (16,066) 投资活动现金流 (13,745) (5,144) (24,340) 融资活动 新股发行 — — 324,000 支出归因于新股发行 — — (20,909) 发行库存股 — 236 — 回购库存股 — (236) — 行使认股权证 — 95,121 — 购买非控股权益 — — (49,303) 非控股权益出资 — — 2,282 新借款 20 962,889 491,745 199,524 转为新贷款 (26,625) (1,260) (14,858) 偿还借款 (724,479) — — 偿还租赁负债 (12,134) (9,615) (5,575) 来自融资活动的现金流 199,650 575,990 435,162 净增加(减少)现金 (248,750) 259,493 (50,766) 年初现金 1,249,094 955,507 996,304 现金汇率差 (26,611) 34,094 9,969 年末现金 23 973,733 1,249,094 955,507 44Calliditas Therapeutics | 2023 年年度报告集团 |
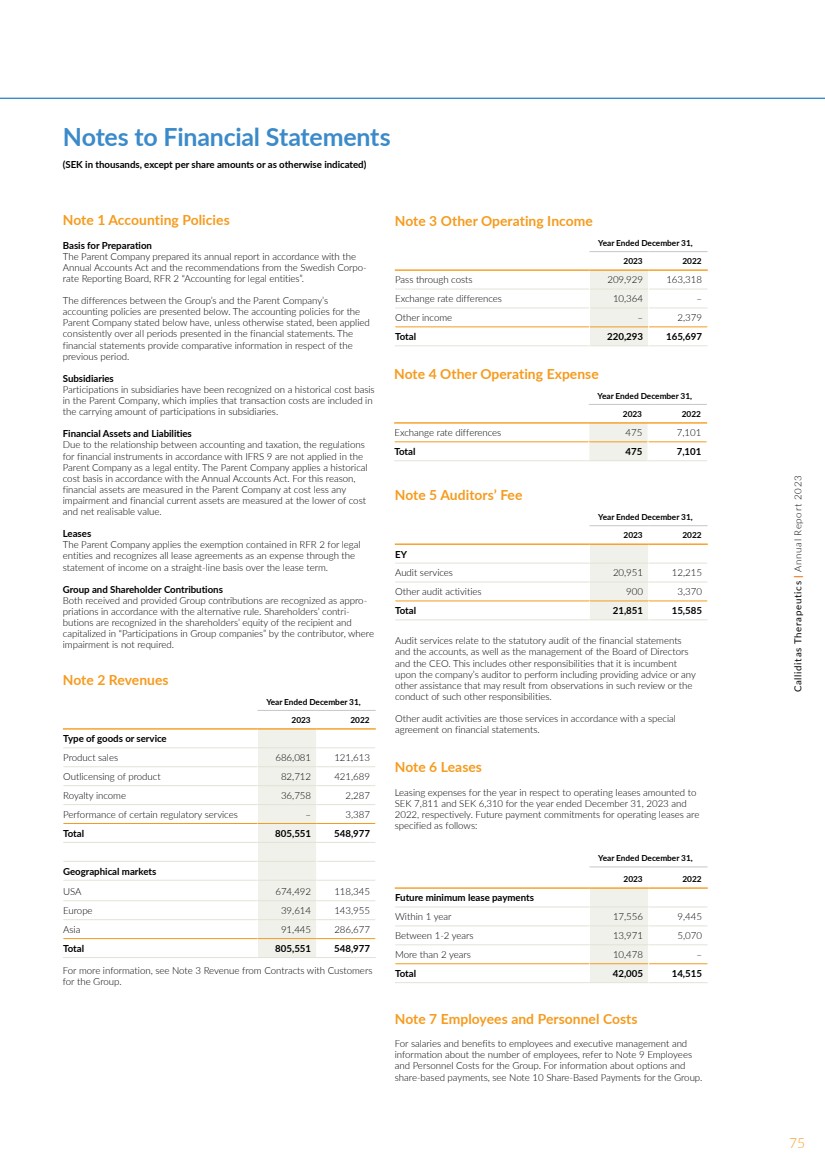
| 业务描述 Calliditas Therapeutics AB(publ)(“Calliditas” 或 “母公司”), ,公司注册号为556659-9766,及其子公司 (统称 “集团”)在药品领域进行开发和商业活动 。 这些合并财务报表涵盖分别注册于瑞典斯德哥尔摩 的集团及其截至2023年12月31日、2022年和2021年12月31日 的年度的子公司。除了国际财务报告准则要求的时期外,集团还选择提交合并收益表 表、综合收益表、合并现金流量表 和合并权益变动表,并附加 个比较期。 Calliditas是一家商业阶段的生物制药公司,专注于识别、 开发和商业化孤儿适应症的新疗法, 最初的重点是具有重大未得到满足的医疗需求的肾脏和肝脏疾病。公司总部的注册地址是 Kungsbron 1,D5,瑞典斯德哥尔摩。 Calliditas根据瑞典 法律于2004年2月20日作为一家上市有限责任公司成立,名为Pharmalink AB ,并于2004年4月15日在瑞典公司注册局注册。截至2023年12月31日,Calliditas是位于瑞典、法国和美国的四家子公司的母公司 。 瑞典子公司是Nefecon AB,该公司不开展任何经营 活动。美国的子公司是Calliditas Therapeutics US Inc和Calliditas NA Enterprises Inc,它们分别在美国进行商业化活动。法国子公司是位于法国的 Calliditas Therapeutics France SAS,该公司正在开展 临床前活动。 董事会(“董事会”)于2024年4月24日批准并授权发布 这些合并财务报表, 将在2024年6月17日的年度股东大会上提交给通过。 附注 1 重要会计政策 编制依据 这些合并财务报表是根据 国际会计准则委员会(IASB)发布的、由欧盟 (欧盟)通过的《国际财务报告准则》(R)编制的。此外,合并财务报表符合瑞典公司报告委员会RFR 1, 集团补充会计条例的 建议。 重大会计政策 如果基础交易是重要的 且会计政策中的信息对理解 交易具有重要意义,例如,如果集团已做出政策选择或会计 政策是公司特定的,则集团提供重要会计政策的披露, 会计政策是重要的。当集团适用适用的国际财务报告准则中所述的会计政策 时,集团不提供 所适用会计政策的任何披露。除了本附注中描述的重要 会计政策外,集团还决定 在与 政策相关的相应附注中介绍重要会计政策。 主要财务报表 该集团选择除了国际财务报告准则 要求的最低期限外,还提交合并损益表、 综合收益表、合并现金流量表和合并日期的权益变动表,再提交一个比较期。 集团已决定根据支出函数提交合并收益表 。 估值基础和当前与非流动分类 本集团根据当前/非流动分类在财务状况表中列报资产和负债。如果 预计将在报告期后的十二个月内变现,则该资产即为流动资产。 所有其他资产均归类为非流动资产。如果 应在报告期后的十二个月内结算,则该负债即为当前负债。 集团将所有其他负债归类为非流动负债。 本位币和申报货币 母公司的本位币是瑞典克朗(SEK), 也是集团的列报货币。这意味着财务报表以瑞典克朗(SEK)列报,除非另有说明,否则所有金额 均四舍五入到最接近的千位(000瑞典克朗)。 与营业应收账款和负债相关的外币 交易产生的外汇收益和亏损在营业利润净额 中确认为其他营业收入或其他运营支出, ,而金融应收账款和负债的外汇损益作为金融项目净额确认。 销售成本 销售成本包括库存销售成本、人工成本、制造 管理费用和预期废品储备金以及运费 和运费。销售成本还包括与许可协议相关的特许权使用费成本。 研究与开发 研发费用主要包括 集团开发活动所产生的成本,包括 集团候选产品的开发。本集团将研发费用按发生时支出。该集团使用Calliditas的服务提供商提供的信息,根据对完成特定任务进展情况的评估 来确认外部开发成本 。 这些活动的付款基于个别协议的条款, 可能不同于所产生的成本模式,并作为预付费用或应计费用反映在 合并财务报表中。 研发税收抵免在瑞典和 法国得到承认。在瑞典,税收抵免是根据社会保障费用确认的,在 法国,对经认证的供应商进行税收抵免。在合并损益表中,这些研究 和开发税收抵免被视为对研究和 开发费用的抵消。 营销和销售费用 营销和销售费用包括集团人员的工资和其他相关成本 以及市场准入、商业化和 业务发展。 管理费用 管理费用包括集团、财务、公司和管理职能中 人员的工资和其他相关费用。 管理费用还包括法律、专利、 会计、审计、税务和咨询服务的专业费用、相关的差旅费用 和设施相关费用,其中包括分配的租金 和设施维护费用以及其他运营成本。与收购有关的 成本包含在合并收入报表中的管理费用中,并在提供服务时记作支出。 新的和经修订的标准和解释 在截至2023年12月31日的年度中生效的国际会计准则理事会和IFRIC解释 的更新标准和解释 对集团没有产生任何实质性影响。该集团尚未提前通过任何 已经发布但 尚未生效的 标准、解释或修正案。 未来准则和新解释 国际会计准则理事会 发布的其他未来或变更的标准或解释预计不会对集团的财务 报表产生任何重大影响。 现金流量 合并现金流量表按照 间接法编制。 注2 重要会计判断、 估计和假设 根据国际财务报告准则编制集团在 中的合并财务报表要求管理层做出影响收入、支出、 资产和负债的记录金额以及随之披露的判断、估计 和假设。 这些假设和估计的不确定性可能导致需要对未来时期受影响 的资产或负债账面金额进行 实质性调整的结果。 合并财务报表附注 (千瑞典克朗,每股金额或另有说明除外) 45Calliditas Therapeutics | 2023 年年度报告集团 |
| 对判断、估计和假设进行持续评估。 判断、估计和假设的变化在 周期内得到承认。如果变更仅影响该时段,则变更发生了 ;如果变更同时影响当前时段和未来 时段,则在未来时段。 重要的会计判断、估计和假设在 与判断、估计和假设相关的相应附注中详细披露。重要的会计判断、估计 和假设涉及: • 收入确认——附注3, • 亏损结转——附注13、 • 无形资产——附注15和 • 预期信贷损失——附注20。 每项重要会计判断、 估计值和假设的摘要说明如下。有关 重要会计判断、估计和假设的更多详情,请参阅上述 附注。 收入确认 产品许可超过许可 的收入在 知识产权控制权转移的时刻予以确认,而 提供某些监管服务的收入则随着时间的推移在 服务的执行过程中进行报告。分配给胜出许可的绩效义务的收入基于剩余方法,监管服务绩效义务的收入分配 基于提供服务的预期成本,另外还根据可比公司增加了利润 利润率。因此,在这些履约义务之间确定和分配交易价格 会对集团的收入确认产生重大影响,因为履约义务之间的收入 确认模式不同。 收入合同还包含以 监管和商业里程碑形式的可变薪酬。起初 将可变薪酬视为受限,因为 相关的里程碑是否会实现存在很大的不确定性。只有在导致 特许权使用费的销售发生后,才能确认归因于基于销售的 里程碑或特许权使用费的报酬。因此,确定可变薪酬的 确认标准是否得到满足,会对收入确认产生重大影响,需要 管理层做出重大判断。 总计转净额 美国有各种与产品销售 相关的销售扣除和返利,作为 收入确认流程的一部分,从总销售额中扣除。由于销售时的实际销售扣除额 未知,因此在确定返利的初始扣除额 时会进行估算,然后在获得实际数据后进行调整。 无形资产 尚未可供使用的商誉和无形资产 商誉和尚未可供使用的无形资产在每个报告日根据其可收回金额进行减值评估, 包括潜在商业化时机、市场规模、市场份额、进入市场的概率和 折扣率等关键假设。 无形资产的资本化 本集团将开发 药品的支出资本化,以期根据 IAS 38(无形资产)预计符合 的标准。该评估基于管理层做出的重大判断,包括完成无形资产以供使用 或出售的技术可行性,以及用于证明该资产将产生 可能的未来经济收益的假设(例如,预计的现金流预测, 折扣率)。支出资本化通常在开发的后期 阶段进行,例如在获得全面批准之后,具体取决于 何时认为符合标准。其原因是, 在此之前,尚不确定这笔支出是否会产生未来的 经济利益,而且资产竣工的融资尚无保障。 应收账款预期信用损失的损失备抵金 管理层为与其到期日相对应的 应收账款的预期信用损失提供损失备抵金。该估算基于个人或集体的任何 增加的信用风险,考虑原因 附注 3 运营分部和 与客户签订的合同的收入 实质性会计政策-运营部门 运营分部是集团的一部分,从事可产生收入和产生成本的业务 活动,以及可获得独立财务信息的 。 细分市场的确定基于向首席运营决策者 制定者(“CODM”)提交的内部报告。集团的CODM是首席执行官 (“首席执行官”)。集团不将其业务划分为不同的部门 ,CODM将集团的整个业务作为 一个分部来运营和管理,这与集团的内部组织 和报告系统一致。该集团的收入归属于瑞典的母公司 和美国子公司Calliditas Therapeutics US Inc。非流动资产位于瑞典、美国、法国和 瑞士。 材料会计政策-与客户签订合同的收入 该集团的业务是识别、开发和商业化孤儿适应症的新疗法。营业收入 主要包括产品销售、向我们在欧洲、中国和日本的合作伙伴 授予Nefecon的许可以及特许权使用费收入。收入按以下方式确认 : 产品销售 产品销售收入按所售商品 的交易价格确认,不包括销售税、折扣和退货。在交付时,当 将货物的控制权移交给客户时,收入将全额确认 ,因为这代表了交易中的单一履约义务。客户被定义为向最终用户分发 商品的专业药房。由于交易价格取决于支付给患者保险公司或政府付款人的 返利,因此 交易价格在交付时未知。这是根据统计数据、实际发生金额和/或历史趋势计算的 模型计算得出的集团中 应计退税额计算得出的 。这些预期回报和返利负债基于 对相关销售所收到或将要索赔的金额的估计。 此外,专家组估计 过期药品的预期回报负担。 产品许可超过许可 归因于对Nevecon的许可的收入包括与STADA的欧洲协议 、将珠穆朗玛峰药业扩展到韩国 以及与Viatris签订的日本协议。超出许可 的收入是在某个时间点确认的,这种情况发生在将 无形资产的控制权移交给交易对手时,也就是 与各方签订协议时。这些与 客户签订的合同包括固定薪酬、监管和商业里程碑形式的可变对价 以及基于销售的 可支持的信息,包括前瞻性信息。 预期信用风险备抵额是根据到期日 结构应收账款和特定客户知识得出的估算。通常, 发票应在 30-45 天内付款。 Loss carryForwards 截至2022年12月31日,集团结转的税收亏损尚未在财务状况表中确认为 递延所得税资产,除非未来存在临时的 差额可以用来抵消。递延所得税资产将 确认未使用的税收损失,前提是有可能有 应纳税利润可用来抵消亏损。 该集团已确定与 历史上交易导致的法国结转的税收损失有关 的纳税状况不确定。结转的相关税收损失在合并财务状况表中未被确认为递延所得税资产 。 估算不确定性的关键来源 报告日有关未来和其他关键估计不确定性来源的关键假设存在导致 在下一个财政年度内对资产和负债账面金额进行 重大调整的重大风险。该集团的假设和估计 基于编制合并日期财务报表 时可用的参数。但是,关于未来 发展的现有情况和假设可能会因市场变化或出现的超出集团控制范围的情况而发生变化。这样的变化 在发生时会反映在假设中。 46Calliditas Therapeutics | 2023 年年度报告集团——合并财务报表附注 (千瑞典克朗,每股金额或另有说明除外) |
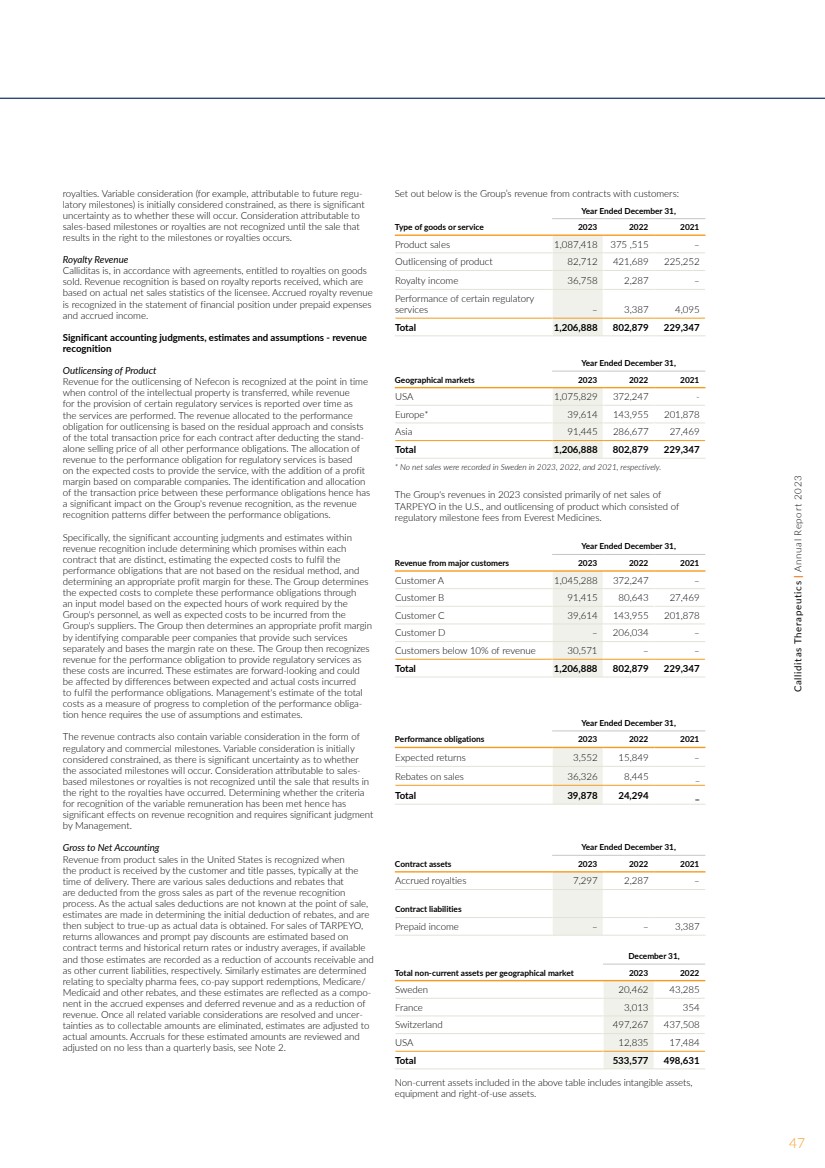
| 特许权使用费。变量考量(例如,可归因于未来的监管里程碑)最初被认为是有限的,因为 这些因素是否会发生存在很大的不确定性。在 导致里程碑权或特许权使用费的销售发生之前,不确认归因于 基于销售的里程碑或特许权使用费的对价。 特许权使用费收入 根据协议,Calliditas有权获得所售商品的特许权使用费。收入确认基于收到的特许权使用费报告, 基于被许可方的实际净销售统计数据。应计特许权使用费收入 在财务状况表中的预付费用 和应计收入项下确认。 重要的会计判断、估计和假设-收入 确认 超出产品许可的收入 在知识产权控制权转移时 确认,而提供某些监管服务的收入 则随着时间的推移在 服务的提供时予以列报。分配给超出许可的履行 义务的收入基于剩余方法,由 扣除所有其他履约义务的独立销售价格后的每份合约的总交易价格组成。 收入分配给监管服务履行义务的依据是 提供服务的预期成本,并根据可比公司增加利润 利润率。因此,这些履约义务之间交易价格的确定和分配 对集团的收入确认产生了重大影响,因为履约义务之间的收入 确认模式不同。 具体而言, 收入确认中的重要会计判断和估计包括确定每份 合同中哪些承诺是不同的,估计履行不基于剩余法的 履约义务的预期成本,以及 为这些承诺确定适当的利润率。集团根据 集团人员所需的预期工作时间以及 集团供应商产生的预期成本,通过 输入模型确定 完成这些履约义务的预期成本。然后,集团通过确定分别提供此类服务的可比同行公司 来确定适当的利润率 ,并以此为基础确定利润率。然后,集团将提供监管服务的履约义务的 收入予以确认,因为这些费用是产生的。这些估计是前瞻性的, 可能受到 为履行履约义务而产生的预期成本和实际成本之间差异的影响。因此,管理层对 总成本的估计,以此来衡量业绩义务的完成进展情况,需要使用假设和估计值。 收入合同还以 监管和商业里程碑的形式包含可变对价。最初 将变量考虑视为受限,因为 相关里程碑是否会出现存在很大的不确定性。在导致 特许权使用费的销售发生之前,归因于销售里程碑或特许权使用费的对价不予确认。因此,确定可变薪酬的确认标准 是否已满足 会对收入确认产生重大影响,需要管理层做出重大判断 。 会计总额转净额 在美国的产品销售收入将在买家收到 商品并获得所有权证书时予以确认,通常在 交付时。作为收入确认 流程的一部分, 会从总销售额中扣除各种销售扣除和返利。由于销售点的实际销售扣除额尚不清楚, 是在确定折扣的初始扣除额时进行估算的, 然后在获得实际数据后进行校准。对于 TARPEYO 的销售, 退货补贴和即时薪酬折扣是根据 合同条款和历史回报率或行业平均值(如果有)估算的 ,这些估计值分别记录为应收账款和 作为其他流动负债的减少。同样,估算值是确定的 与特种药品费用、自付补助兑换、Medicare/ 医疗补助和其他回扣有关,这些估计值作为应计费用和递延收入的组成部分以及 收入的减少反映出来。一旦解决了所有相关的可变因素并消除了有关可收款金额的不确定性,估算值将调整为 实际金额。对这些估计金额的应计金额进行审查, 不少于每季度进行一次调整,见附注 2。 以下是集团与客户签订合同的收入: 截至12月31日的年度, 2023 年 2021 年商品或服务类型:产品销售额 1,087,418 375 ,515 — 超出产品许可 82,712 421,689 2252 特许权使用费收入 36,758 2,287 — 某些监管 服务的业绩 — 3,387 4,07 总计 1,206,888 802,879 229,347 截至12月31日的年度, 地理市场 2023 2021 美国 1,075,829 372,247- 欧洲* 39,614 143,955 201,878 亚洲 91,445 286,677 27,469 总计 1,206,888 802,879 229,347 * 瑞典未记录净销售额分别在 2023 年、2022 年和 2021 年。 该集团2023年的收入主要包括 TARPEYO在美国的净销售额,以及由珠穆朗玛峰药业的 监管里程碑费用组成的产品的许可额。 截至 12 月 31 日的年度, 来自主要客户的收入 2023 年 2021 年客户 A 1,045,288 372,247 — 客户 B 91,415 80,463 27,469 客户 C 39,614 143,955 201,878 客户 D — 206,034 — 总计 1,206,888 802,879 229,389 229,389 截至12月31日的财年, 2023 年 2021 年业绩义务预期收益 3,552 15,849 — 销售回扣 36,326 8,445 _ 总计 39,878 24,294 _ 截至12月31日的年度, 合同资产 2023 2021 应计特许权使用费 7,297 2,287 — 合同负债 预付收入— — 3,387 12月31日, 2023 年每个地理市场的非流动资产总额瑞典 20,462 43,285 法国 3,013 354 瑞士 497,267 437,508 美国 12,835 17,484 总计 533,577 498,631 上表中包含的非流动资产包括无形资产、 设备和使用权资产。 47Calliditas Therapeutics | 2023 年年度报告 |
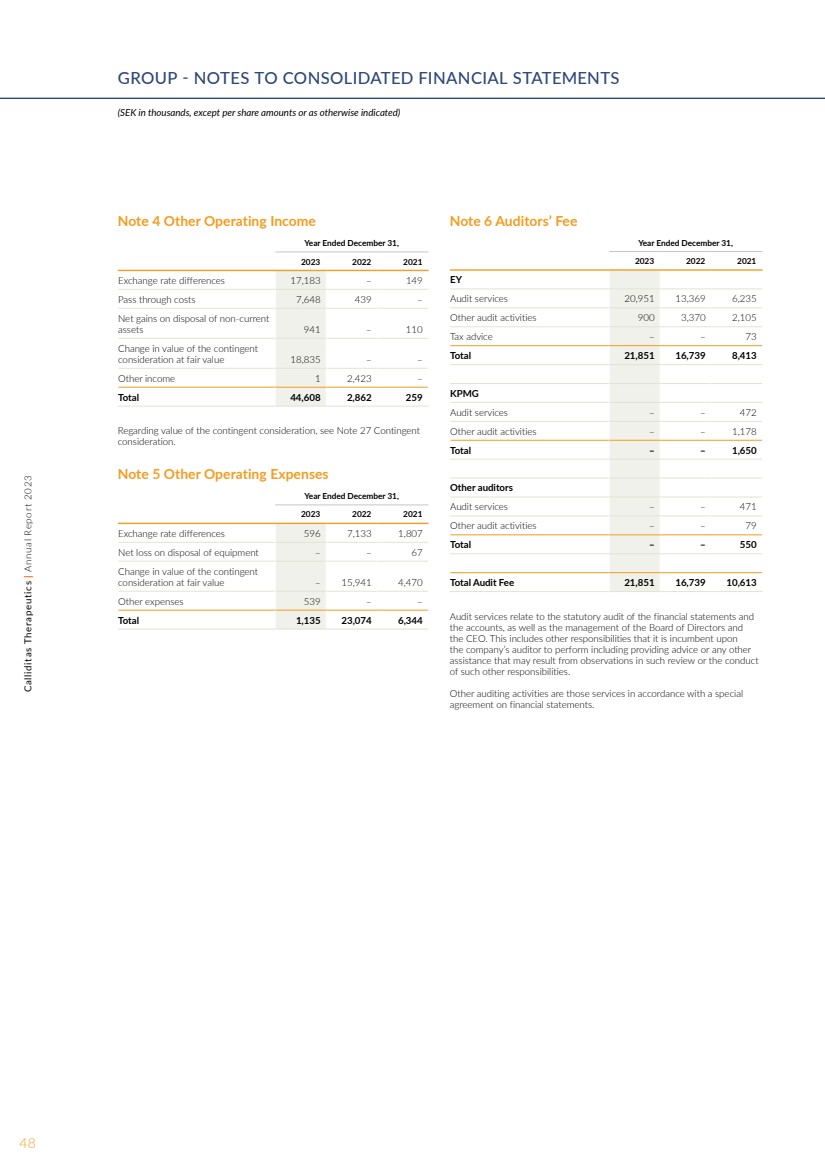
| 附注 5 其他运营费用 截至 2023 年 12 月 31 日的年度 2021 年汇率差额 596 7,133 1,807 设备处置净亏损 — — 67 按公允价值计算的或有的 对价的价值变动 — 15,941 4,470 其他费用 539 — — 总计 1,135 23,074 6,344 附注 4 其他营业收入 截至2023年12月31日的年度 2022 2021 年汇率差异 17,183 — 149 过关成本 7,648 439 — 处置非流动 资产的净收益 941 — 110 按公允价值计算的或有的 对价的价值变动 18,835 —— 其他收入 1 2,423 — 合计 44,608 2,862 259 关于或有对价的价值,见附注 27 或有对价 对价。 附注 6 审计师费 截至 2021 年 12 月 31 日的年度安永 审计服务 20,951 13,369 6,235 其他审计活动 900 3,370 2,105 税务建议 — — 73 共计 21,851 16,739 8,413 毕马威 审计服务 — — 472 其他审计活动 — — 1,178 总计 — — 1,650 名其他审计师 审计服务 — — 471 其他审计活动 — — 79 总计 — — 550 审计费用总额 21,851 16,739 10,613 审计服务与财务报表和 账目的法定审计以及董事会和 首席执行官的管理有关。这包括 公司审计师有义务履行的其他职责,包括提供建议或任何其他 协助,这些建议或任何其他 协助,这些援助可能源于此类审查中的观察或此类其他职责的履行 。 其他审计活动是根据财务报表特别 协议提供的服务。 48Calliditas Therapeutics | 2023 年年度报告集团——合并财务报表附注 (千瑞典克朗,每股金额或另有说明除外) |
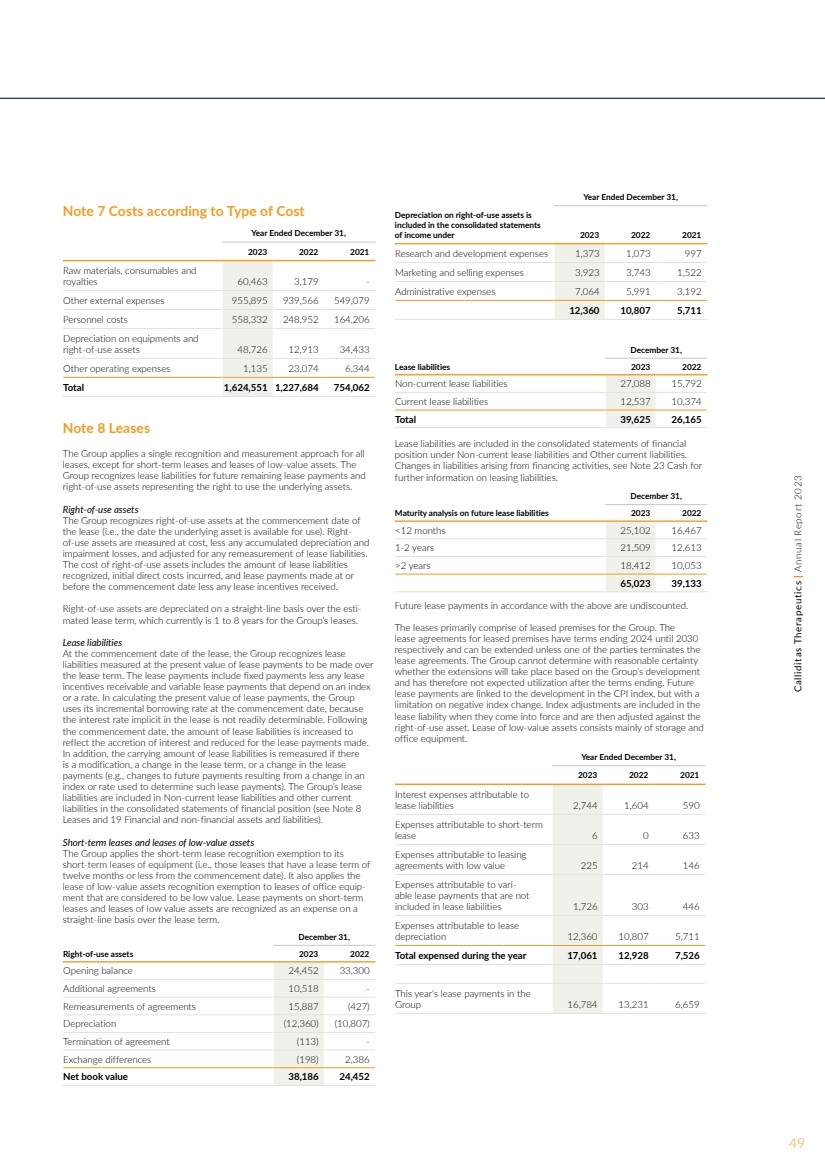
| 注8 租赁 集团对所有 租赁采用单一确认和衡量方法,短期租赁和低价值资产租赁除外。 集团确认未来剩余租赁付款的租赁负债以及 代表基础资产使用权的使用权资产。 使用权资产 集团在 租赁开始之日(即标的资产可供使用的日期)承认使用权资产。使用权资产按成本计量,减去任何累计折旧和 减值损失,并根据租赁负债的任何调整进行调整。 使用权资产的成本包括确认的租赁负债金额 、产生的初始直接成本以及在开始日期或 之前支付的租赁款项减去获得的任何租赁激励。 使用权资产在估计的租赁期限内按直线折旧,目前集团的租赁期为1至8年。 租赁负债 在租赁开始之日,集团确认按租赁付款的现值计量的租赁 负债将在租赁期限内支付。租赁付款包括固定付款减去任何应收租赁 激励措施和取决于指数 或利率的可变租赁付款。在计算租赁付款的现值时,集团 使用其在开始日期的递增借款利率,因为 租赁中隐含的利率不容易确定。在 生效日期之后,租赁负债金额增加到 ,以反映利息的增加,并减少所支付的租赁款项。 此外,如果 发生修改、租赁期限变更或租赁 付款发生变化(例如,由于用于确定此类租赁付款的 指数或利率的变化而导致未来付款的变化),则将重新衡量租赁负债的账面金额。集团的租赁 负债包含在合并财务状况表中的非流动租赁负债和其他流动 负债中(见附注8租赁和19金融和非金融资产和负债)。 短期租赁和低价值资产租赁 集团对其 短期设备租赁(即自开始之日起租赁期为 十二个月或更短的租赁)适用短期租赁确认豁免。它还将 租赁低价值资产确认豁免适用于被视为低价值的办公设备租赁。短期 租赁的租赁付款和低价值资产的租赁在租赁期内按 直线法确认为支出。 12 月 31 日, 使用权资产 2023 年 2022 年期初余额 24,452 33,300 额外协议 10,518- 协议重估 15,887 (427) 折旧 (12,360) (10,807) 协议终止 (113)- 汇兑差额 (198) 2,386 账面净值 38,186 24,452 附注 7 成本根据成本类型 截至2023 年 12 月 31 日的年度原材料、消耗品和 特许权使用费 60,463 3,179- 其他外部费用 955,895 939,566 549,079 人员成本 558,332 248,952 164,206 设备折旧和 使用权使用资产 48,726 12,913 34,433 其他运营费用 1,135 23,074 6,344 总计 1,624,551 1,227,684 754,062 截至12月31日的年度, 使用权资产折旧已包含在 2023 年 2022 2021 年收入合并报表 中研究与开发费用 1,373 1,073 997 营销和销售费用 3,923 3,743 1,743 522 管理费用 7,064 5,991 3,192 12,360 10,807 5,711 12 月 31 日, 2023 年租赁负债 27,088 15,792 流动租赁负债 12,537 10,374 合计 39,625 26,165 租赁负债包含在合并财务 状况报表中,列在非流动租赁负债和其他流动负债项下。 融资活动产生的负债变动, 有关租赁负债的更多信息,请参阅附注23 Cash。 12月31日, 2023 年 2 年未来租赁负债的到期日分析 18,412 10,053 65,023 39,133 根据上述条款支付的未来租赁款项未贴现。 租约主要包括集团的租赁场所。租赁场所的 租赁协议的期限分别在2024年到2030年结束,除非其中一方终止 租赁协议,否则可以延长。集团无法合理确定延期 是否将根据集团的发展 进行,因此预计在条款到期后不会得到利用。未来的 租赁付款与消费者价格指数的发展有关,但是 对负指数变动有限制。指数调整在生效时包含在 租赁负债中,然后根据 使用权资产进行调整。低价值资产的租赁主要包括存储和 办公设备。 截至12月31日的年度, 2023 2021 归属于 租赁负债的利息支出 2,744 1,604 590 归属于短期 租赁的支出 6 0 633 归属于低价值租赁 协议的支出 225 214 146 不包括在租赁负债中的可变租赁付款的支出 1,726 303 446 归属于租赁 的费用 12,360 10,800 7 5,711 年内总支出 17,061 12,928 7,526 今年 集团的租赁付款 16,784 13,231 6,659 49Calliditas Therapeutics | 年度2023 年报告 |
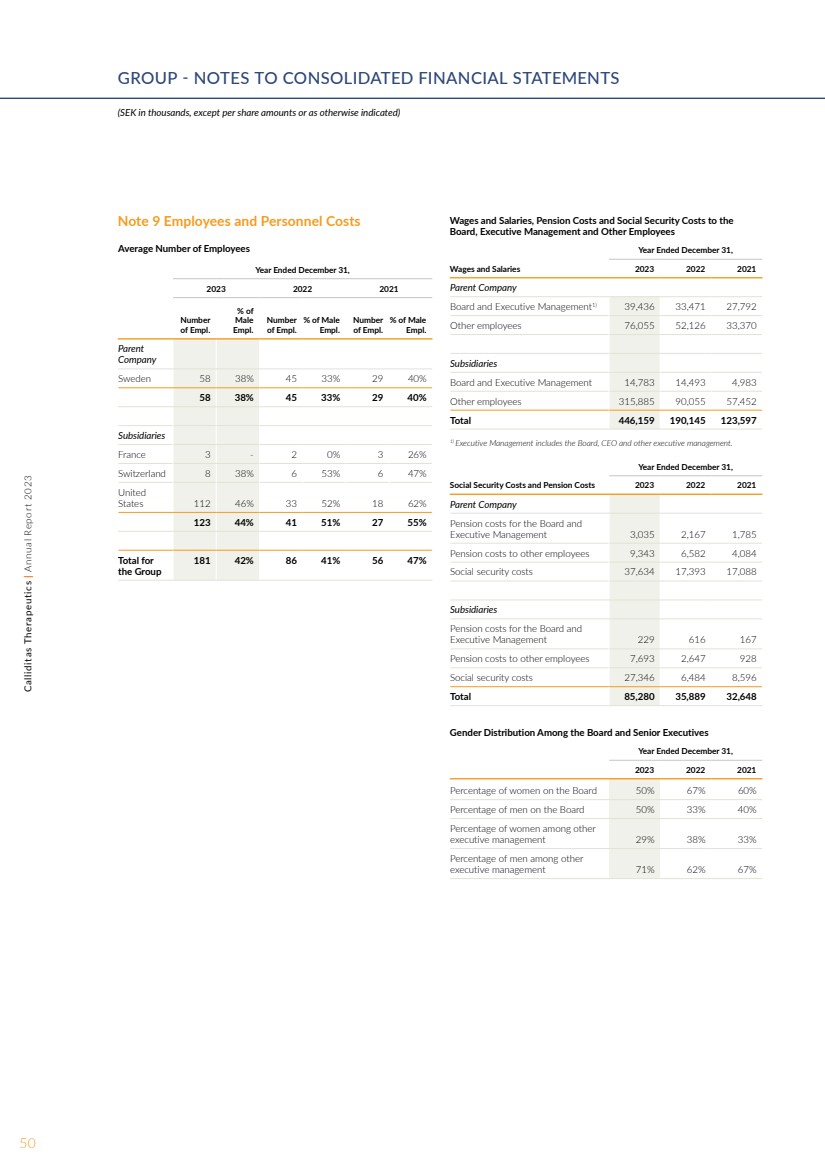
| 董事会、执行管理层和其他员工的工资和薪金、养老金成本和社会保障成本 截至12月31日的年度 2023 年工资与薪金母公司 董事会和执行管理层1) 39,436 33,471 27,792 其他员工 76,055 52,126 33,370 子公司 董事会和执行管理层 14,783 14,493 4,983 其他员工 76,055 52,126 33,370 子公司 董事会和执行管理层 14,783 14,493 4,983 其他员工 315,885 90,055 57,452 总计 446,159 190,145 123,597 1) 执行管理层包括董事会、首席执行官和其他执行管理层。 截至12月31日的年度, 2023 年社会保障成本和养老金成本 2022 2021 年母公司 董事会和 执行管理层的养老金成本 3,035 2,167 1,785 其他员工的养老金成本 9,343 6,582 4,084 社会保障成本 37,634 17,393 17,088 子公司 董事会和 执行管理层的养老金成本 229 616 167 养老金成本给其他员工 7,693 2,647 928 社会保障费用 27,346 6,484 8,596 总计 85,280 35,889 32,648 32,648 董事会和高级管理人员的性别分布 截至12月31日的年度, 2023 20232021 年董事会中女性所占百分比 50% 67% 60% 董事会中男性百分比 50% 33% 40% 在其他 执行管理层中的女性百分比 29% 38% 33% 在其他 执行管理层中所占百分比 71% 62% 67% 注9 员工和人事成本 平均员工人数 2023 2021 年 12 月 31 日止年度 } of Empl。 % 的 男性 Empl。 Empl 的数字 。 % 的男性 Empl。 Empl 的数字 。 % 的男性 Empl。 母公司 瑞典 58 38% 45 33% 29 40% 58 38% 45 33% 29 40% 子公司 法国 3-2 0% 3 26% 瑞士 8 38% 6 53% 6 47% 美国 112 46% 33 52% 18 62% 123 44% 41 51% 27 55% 总计} 该集团 181 42% 86 41% 56 47% 50Calliditas Therapeutics | 2023 年年度报告集团-合并财务报表附注 (千瑞典克朗,每股金额或另有说明除外) |
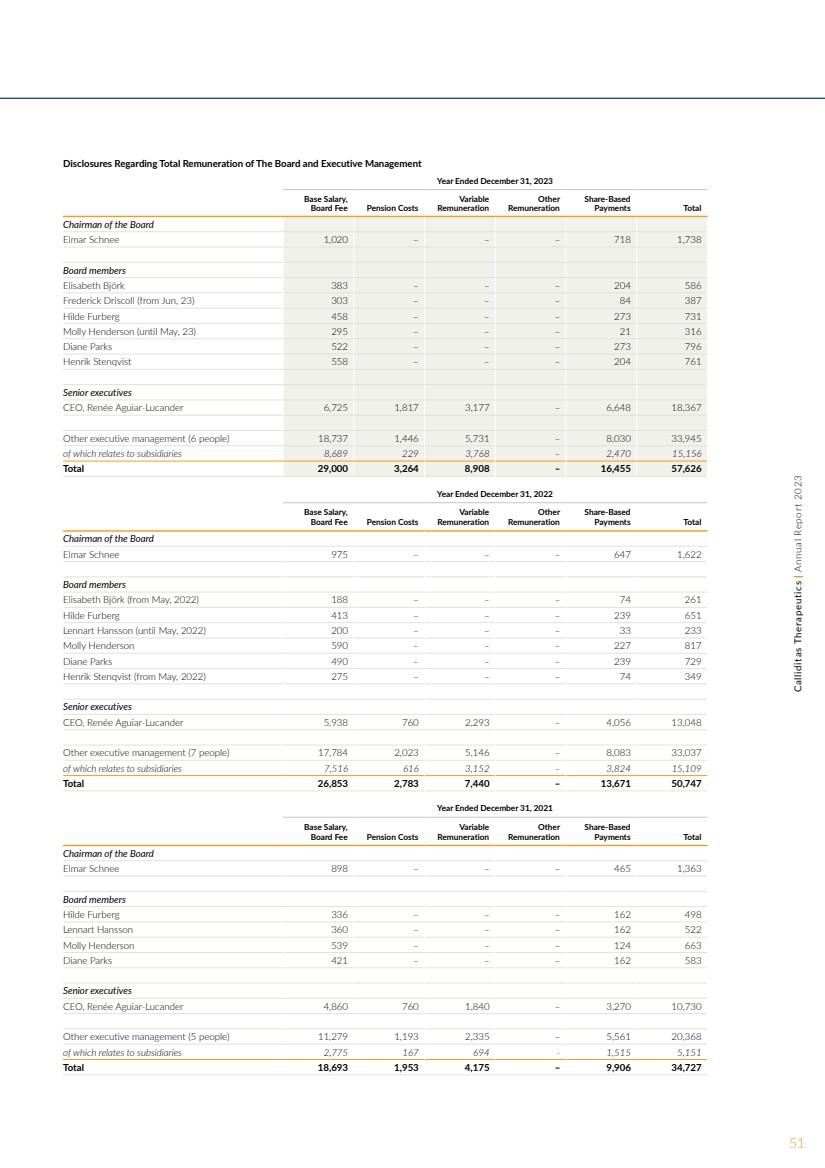
| 关于董事会和执行管理层薪酬总额的披露 截至2023年12月31日的年度基本工资, 董事会费用养老金成本 其他薪酬 基于股份的付款总计 董事会主席 Elmar Schnee 1,020 — — — 718 1,738 名董事会成员 伊丽莎白·比约克 383 — — 204 586 弗雷德里克·德里斯科尔(从6月23日起)303 — — — 84 387 Hilde Furberg 458 — — — 273 731 莫莉·亨德森(直到5月23日)295 — — — 21 316 黛安·帕克斯 522 — — — 273 796 Henrik Stenqvist 558 — — 204 761 名高级管理人员 首席执行官,蕾妮Aguiar-Lucander 6,725 1,817 3,177 — 6,648 18,367 其他执行管理人员(6 人)18,737 1,446 5,731 — 8,030 33,945 其中与子公司有关 8,689 229 3,768 — 2,470 15,156 总计 29,000 3,264 8,908 — 16,455 57,626 截至2022年12月31日的年度基本工资, 董事会费用养老金成本 可变 薪酬 其他 薪酬 基于股份的 付款总额 董事会主席 Elmar Schnee 975 — — — 647 1,622 名董事会成员 伊丽莎白·比约克(自2022年5月起)188 — — — 74 261 Hilde Furberg 413 — — 239 651 伦纳特·汉斯儿子(直到五月,2022) 200 — — — 33 233 莫莉·亨德森 590 — — — 227 817 黛安·帕克斯 490 — — — 239 729 亨里克·斯滕克维斯特(自2022年5月起)275 — — — 74 349 名高级管理人员 首席执行官,蕾妮·阿吉亚尔-卢坎德 5,938 760 2,293 — 4,056 13,048 其他执行管理人员(7 人)17,784 023 5,146 — 8,083 33,037 其中与子公司 7,516 616 3,152 — 3,824 15,109 总计 26,853 2,783 7,440 — 13,671 50,747 截至2021年12月31日的年度基本工资、 董事会费用养老金成本 可变 薪酬 其他 薪酬 基于股份的薪酬 付款总计 委员会主席董事会 Elmar Schnee 898 — — — 465 1,363 名董事会成员 Hilde Furberg 336 — — — 162 498 伦纳特·汉森 360 — — — 162 522 莫莉·亨德森 539 — — — — 124 663 黛安·帕克斯 421 — — — — 162 583 名高级管理人员 首席执行官,蕾妮·阿吉亚尔-卢坎德 4,860 760 1,840 — 3,270 10,730 其他执行管理人员(5 人)11,279 1,193 2,335 — 5,561 20,368 其中 20,368 与子公司有关 2,775 167 694-1,515 5151 合计 18,693 1,953 4,175 — 9,906 34,727 51Calliditas Therapeutics | 2023 年年度报告 |
| 注 10 基于股份的付款 期权计划 Calliditas在Calliditas为员工和关键顾问 实施期权计划。这些期权免费授予给 计划的参与者。期权的三年归属期从 授予之日算起,前提是,除惯例外,参与者 仍是Calliditas的雇员或继续为其提供服务。一旦 期权归属,即可在一年内行使。 每种既得期权使持有人有权以 预定价格收购Calliditas的一股股份。每股价格将等于授予日前十个交易日公司股票在 斯德哥尔摩纳斯达克交易所交易的加权平均价格的 的115%。 期权在每次发行时均根据 Black-Scholes估值模型进行估值。 归因于 员工的股票相关工具的社会保障费用,作为购买服务的报酬,应在 提供服务的期限内支出。然后,应使用 发行期权时使用的相同估值模型来衡量成本。必须在每个报告期 根据对行使这些工具时可能支付的社会保障费用的计算结果对已确认的准备金进行重新估值 。 一段时间内确认的薪酬成本取决于 与激励计划参与者签订合同 之日的最初估值、授予其期权所需的 服务月数(应计 在此期间计算)、计划条款预计归属 的期权数量并持续重新评估 计划下参与者的税收优惠的价值(用于 确定社会保障条款)安全费用)。那些 影响一段时间内成本的估计值以及相应的净值增加 主要是指期权估值的投入。所有期权都被归类为股权结算,因为既得期权以股权结算。行使期权 时,公司发行新股。 执行管理层的薪酬 首席执行官和其他执行管理层的薪酬包括 基本工资、养老金福利和可变薪酬。其他高管 管理层包括七(五)个人,他们与 首席执行官一起构成执行管理层。其他执行管理层包括: 首席财务官、首席医疗官、监管 事务副总裁、北美总裁、集团总法律顾问和 人力资源主管。 养老金 所有养老金承诺都是高管 管理层的固定缴款计划。集团为固定缴款计划支付的款项在相关期间的合并 业务报表中确认为支出。 首席执行官的退休年龄为65岁,养老金保费为基本工资的20%。其他瑞典执行管理层的养老金 承诺在基本工资的15%至20%之间。所有其他高管 管理层的退休年龄为65岁。只有在法律 或其他法规要求的情况下,才会有固定福利养老金计划。在这种情况下,固定福利水平应限于 为强制性水平。没有其他养老金义务。 可变薪酬 可变薪酬是指基于基本工资的固定 百分比的可变奖金。结果以一年 年的归属期为基础,取决于预先确定的 个人目标和业务目标的实现情况。根据执行管理层 薪酬指导方针,首席执行官 和其他执行管理层的最高业绩为60%。 遣散费 如果 首席执行官终止雇用,则适用六个月的通知期。如果集团终止雇佣 ,则适用十二个月的通知期。首席执行官无权单独领取遣散费,但 有资格在通知期内领取工资。 集团与执行管理层之间适用 为期三到十二个月的相互通知期,并支付工资。不向董事会 成员支付遣散费。 高管薪酬指南 在 2023 年年度股东大会上,最近通过的高管薪酬指南 获得批准。集团内部的薪酬 应基于绩效、竞争力和公平的原则。 有关董事会工作的更多信息,请参阅第 88-93 页的 公司治理报告。 执行管理层是指首席执行官和执行管理层的其他成员,以及董事会成员。该指导方针适用于在斯德哥尔摩纳斯达克上市后签订的 雇佣协议, 以及上市后现有协议的变更。 执行管理层的薪酬可能包括固定薪酬、可变薪酬、与股票和股价相关的激励 计划、养老金和其他福利。如果当地条件证明薪酬原则的变化是合理的,则可能会发生这种差异。固定薪酬应反映个人的责任和经验水平。 固定薪酬应每年进行审查。可以向执行管理层 提供以现金支付的可变薪酬。此类薪酬 不得超过年度固定薪酬的60%。可变 薪酬应与预先确定的可衡量标准挂钩, 的设计旨在促进集团的长期价值创造。 CEO 的薪酬和其他雇佣条款由 薪酬委员会编制并由董事会决定。 执行管理层其他成员的薪酬和其他雇用条件由 CEO 根据董事会和薪酬委员会决定的原则决定。 如果 董事会在特定情况下认为 有充分的理由偏离准则,则董事会有权偏离指导方针。关于首席执行官和 执行管理层其他成员当前薪酬水平和 其他雇用条件的决定已由董事会决定。 之前没有未到期的付款。 52Calliditas Therapeutics | 2023 年年度报告集团——合并财务报表附注 (千瑞典克朗,每股金额或另有说明除外) |
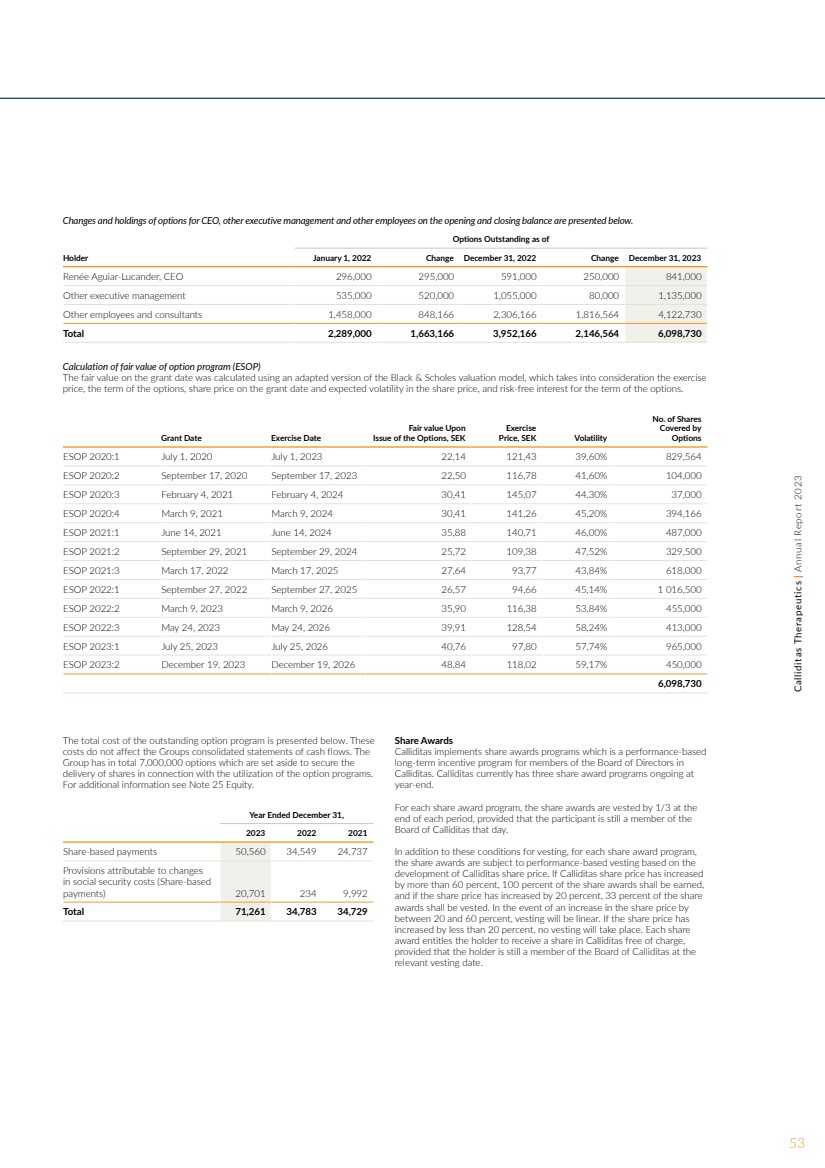
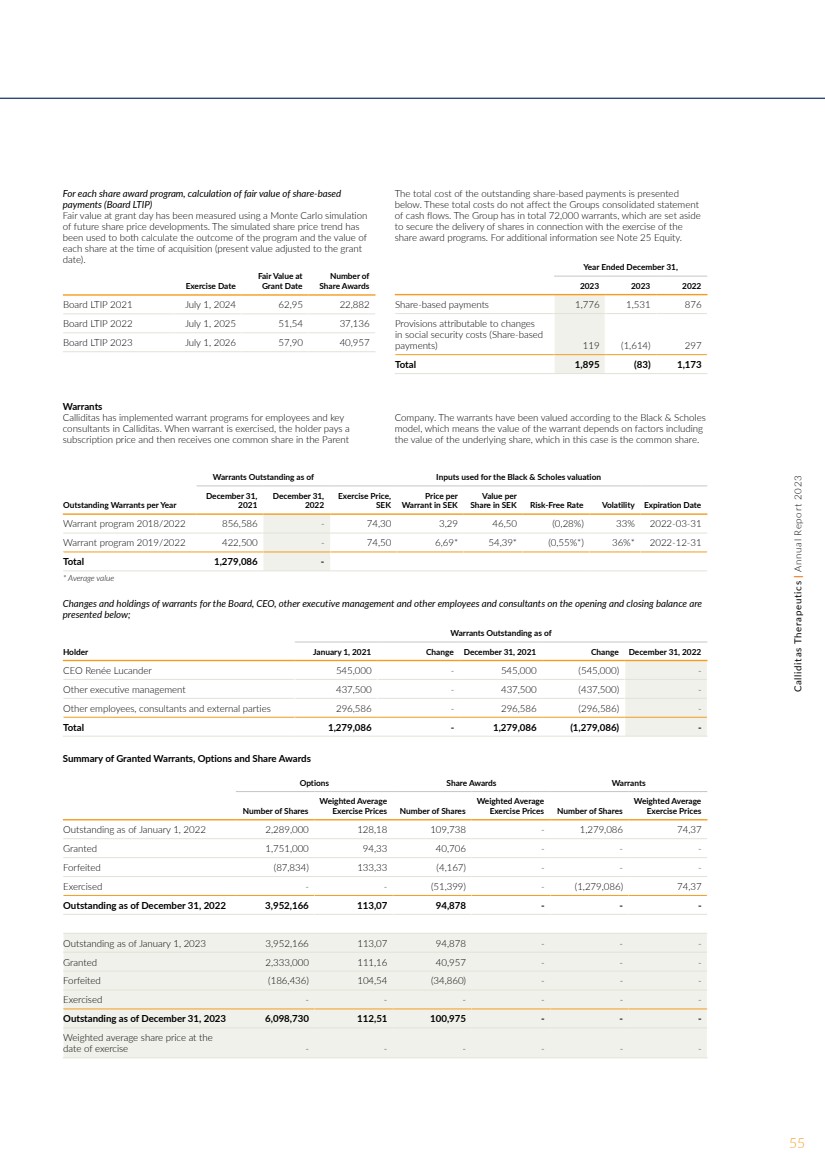
| 首席执行官、其他执行管理层和其他雇员在期初和期末余额中的期权变动和持有情况如下所示。 截至 持有人的未偿期权2022年1月1日变更2023年12月31日变更首席执行官蕾妮·阿吉亚尔-卢坎德 296,000 295,000 591,000 250,000 841,000 其他高管 535,000 1,055,000 80,000 80,000 1,135,000 1,135,000 其他员工和顾问 1,458,000 848,166 2,8166 1,816,564 4,122,730 共计 2,289,730 3,166 3,952,166 2,146,564 6,098,730 期权计划公允价值的计算(ESOP) 授予日的公允价值是使用Black & Scholes估值模型的改编版本计算得出的,该模型考虑了考虑行使价 、期权期限、授予日的股票价格和股价的预期波动率,以及期权期限内的无风险利息。 授予日期 行使日期 公允价值发行期权时,瑞典克朗 行使 价格,瑞典克朗波动率 股票数量 ESOP 2020:1 2020 年 7 月 1 日 2023 年 7 月 1 日 22,14 121,43 39,60% 829,564 ESOP 2020:2 2023 9月 17 日 22,50 1165 78 41,60% 104,60% 104,000 ESOP 2020:3 2021 年 2 月 4 日 2024 年 2 月 4 日 30,41 145,07 44,30% 37,000 ESOP 2020:4 2021 年 3 月 9 日 30,41 141,26 45,20% 394,166 ESOP 2021:1 2024 6 6 6 月 14 日 35,88 140,71 46,00% 487,00% ESOP 2021:2 9月29日 2024 年 9 月 29 日 25,72109,38 47,52% 329,500 ESOP 2021:3 2025 年 3 月 17 日 27,64 93,77 43,84% 618,000 ESOP 2022:1 2025 年 9 月 27 日 26,57 94,66 45,14% 1 016,500 ESOP 2022:2 2023 3 年 3 月 9 日 35,90 116,38 53,84% 45,14% 1 016,500 ESOP 2022:2 2026 3月9日 35,90 116,38 53,84% 45,84% 45,000 ESOP 2022:3 53,84% 24, 2023 年 5 月 24 日 2026 39,91 128,54 58,24% 413,24% 413,000 ESOP 2023:1 2026 7,76 97,80 574% 965,74% 965,000 ESOP 2023:2 2026 年 12 月 19 日 48,84 118,02 59,17% 450,000 6,098,730 份股票奖励 Calliditas 实施基于绩效的股票奖励计划 长期激励 Calliditas 的董事会成员计划。Calliditas目前有三项股票奖励计划正在进行中,截至 年底。 对于每个股票奖励计划,股票奖励将在每个期末 的三分之一之前归还,前提是参与者当天仍是Calliditas的 董事会成员。 除了这些归属条件外,对于每个股票奖励计划, 股票奖励将根据Callidita股价的 走势进行基于业绩的归属。如果Calliditas的股价上涨了 超过60%,则应获得100%的股票奖励, ;如果股价上涨了20%,则应归属33%的股份 奖励。如果股价上涨 在20%至60%之间,则归属将是线性的。如果股价上涨幅度小于 20%,则不会进行归属。每股奖励 使持有人有权免费获得Calliditas的股份, 前提是持有人在 相关归属日期仍是Calliditas董事会成员。 未完成期权计划的总成本如下所示。这些 成本不影响集团合并现金流量表。 集团共有7,000,000份期权,这些期权是为了确保与期权计划的使用有关的 股票的交付。 有关更多信息,请参阅附注 25 股权。 截至 2023 年 12 月 31 日的年度 2021 年 2021 年基于股份的付款 50,560 34,549 24,737 可归因于社会保障成本 变化的准备金(基于股份的 付款)20,701 234 9,992 总计 71,261 34,783 34,729 53Calliditas Therapeutics | 2023 年年度报告 |
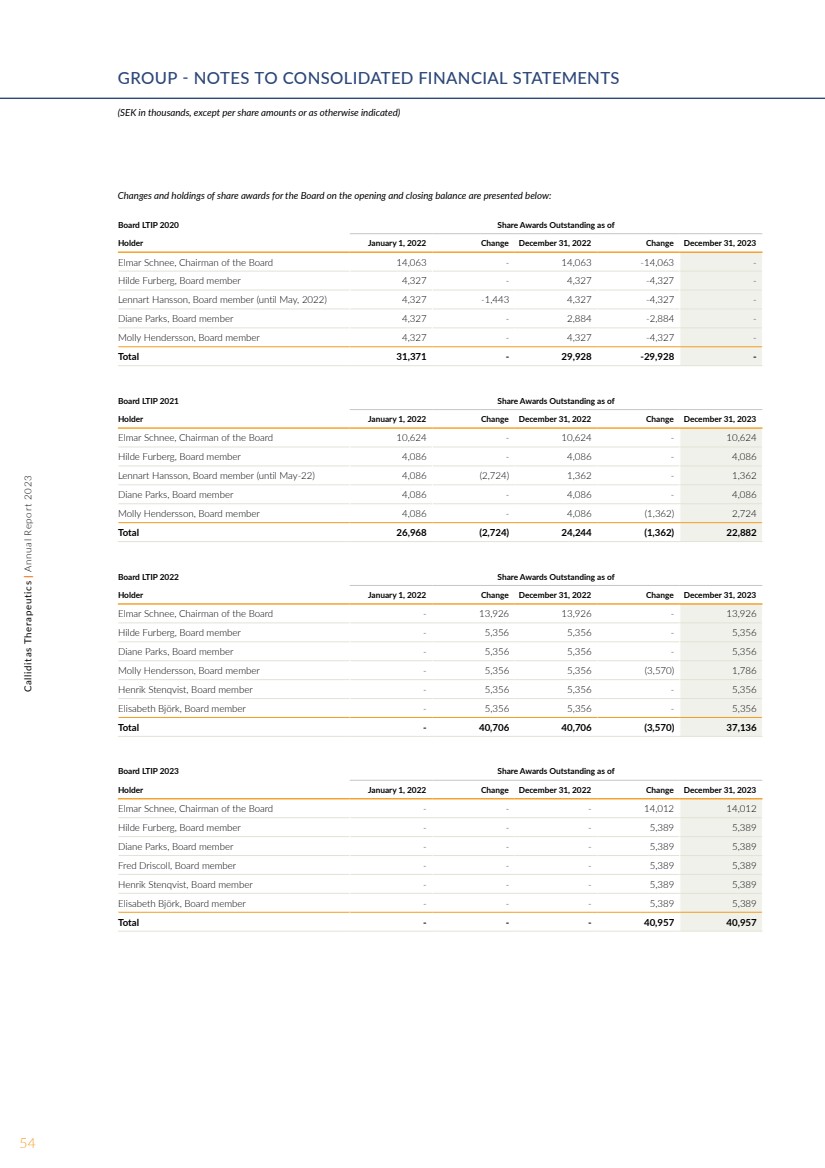
| 董事会股票奖励的期初和期末余额变动和持有情况如下: 董事会 LTIP 2020 年股票奖励截至 持有人 2022 年 1 月 1 日变动 2023 年 12 月 31 日变动 2023 年 12 月 31 日变动 14,063-14,063 -14,063- Hilde Furberg,董事会成员 4,327-4,327-4,327-4,327- 伦纳特·汉森,董事会成员(直到 2022 年 5 月)4,327 -1,443 4,327 -4,327- 黛安·帕克斯,董事会成员 4,327-2,884- 莫莉·亨德森,董事会成员 4,327-4,327- 总计 31,371-29,928 -29,928-29,928-29,928,董事会成员 4,327-4,327- - 董事会 LTIP 2021 年未偿还股票奖励截至 持有人 2022 年 1 月 1 日变更 2023 年 12 月 31 日变更 2023 年 12 月 31 日 Elmar Schnee,董事会主席 10,624-10,624 Hilde Furberg,董事会成员 4,086-4,086 Lennart Hansson,董事会成员(直到 5 月 22 日)4,086 (2,724) 1,362-1,362 Diane Parks,董事会成员 4,086-4,086 Molly Hendersson,董事会成员 4,086-4,086 (1,362) 2,724 总计 26,968 (2,724) 24,244 (1,362) 22,882 截至 持有人截至 持有人的 2022 年 LTIP 未偿还股票奖励变更2023 年 12 月 31 日 Elmar Schnee,董事会主席-13,926 13,926 希尔德·弗伯格,董事会成员-5,356 5,356 Diane Parks,董事会成员-5,356 5,356 Molly Hendersson,董事会成员-5,356 5,356 (3,570) 1,786 Henrik Stenqvist,董事会成员-5,356 5,356-5,356 伊丽莎白·比约克,董事会成员-5,356 5,356 总计-40,706 40,706 (3,570) 37,136 截至 持有人 2022 年 1 月 1 日未偿还的董事会 LTIP 2023 年股票奖励变更 2023 年 12 月 31 日变更 2023 年 12 月 31 日更改董事会主席 Elmar Schnee--14,012 14,012 Hilde 弗伯格,董事会成员---5,389 5,389 黛安·帕克斯,董事会成员---5,389 5,389 弗雷德·德里斯科尔,董事会成员---5,389 5,389 Henrik Stenqvist,董事会成员---5,389 5,389 总计--40,957 40,957 54Calliditas Therapeutics | 2023 年年度报告集团——合并财务报表附注 (以千瑞典克朗计,每股金额或另有说明除外) |
| 未付股份付款的总成本如下所示 。这些总成本不影响集团合并现金流报表 。集团共有72,000份认股权证,这些认股权证被预留 ,以确保与行使 股票奖励计划相关的股票交付。有关更多信息,请参阅附注25股权。 截至 2023 年 12 月 31 日的年度 2023 年 2022 年基于股份的支付 1,776 1,531 876 归因于社会保障成本 变动的准备金(基于股份的 付款)119 (1,614) 297 共计 1,895 (83) 1,173 对于每个股票奖励计划,基于股份的付款(董事会 LTIP) 公允价值的计算使用了授予日的公允价值对未来股价走势的蒙特卡罗模拟 。模拟股价趋势 既用于计算该计划的结果,也用于计算收购时每股 的价值(现值根据授予日期 进行调整)。 行使日期 授予日的公允价值 股票奖励数量 董事会 LTIP 2021 年 7 月 1 日 62,95 22,882 2025 年 7 月 1 日 51,54 37,136 董事会 LTIP 2023 2026 年 7 月 1 日 57,90 40,957 份认股权证 Calliditas 已针对员工和关键 顾问实施了认股权证计划 ditas。当认股权证行使时,持有人支付 的认购价格,然后获得母公司 公司的一股普通股。认股权证是根据Black & Scholes 模型估值的,这意味着认股权证的价值取决于包括 标的股的价值在内的因素,在本例中为普通股。 截至Black & Scholes估值投入的未偿还认股权证 每年未偿还的认股权证 2021 年 12 月 31 日, 2022年行使价, 每份 权证的价格 瑞典克朗每股的价值无风险利率波动到期日 权证计划 2018/2022 856,586-74,30 3,29 46,50 (0,28%) 33% 2022-03-31 认股权证计划 2019/2022 422,500-74,50 6,69* 54,39* (0,55% *) 36% * 2022-12-31 合计 1,279,086- * 董事会、首席执行官、其他执行管理层和其他人员认股权证变动和持有的平均价值期初和期末余额中的员工和顾问 如下所示; 持有人2021年1月1日的未偿认股权证变更2021年12月31日变更首席执行官蕾妮·卢坎德 545,000-545,000 (545,000)- 其他执行管理人员 437,500-437,500 (437,500)- 其他员工、顾问和外部各方 296,586-296,586 (296,586)- 合计 1,279,086-1,279,086 (1,279,086)- 授予的认股权证、期权和股票奖励摘要 期权股票奖励认股权证 股票数量 加权平均值 行使量价格 加权平均数 行使价格截至2022年1月1日的已发行股票数量 加权平均值 行使价 2,289,000 128,18 109,738-1,279,086 74,37 已授予 1,751,000 94,33 40,706-- 没收 (87,834) 133,33 (4,167)-- 已行使--(51,399)-(1,279,086) 74,37 截至2022年12月31日的未偿还款额 3,952,166 113,07 94,878-- 截至2023年1月1日的未偿还款额 3,952,166 113,07 113,07 94,878-- 已没收 (186,467) 36) 104,54 (34,860)--- 已行使------ 截至 2023 年 12 月 31 日的已发行股价 6,098,730 112,51 100,975-- 行使之日的加权平均股价----- 55Calliditas Therapeutics | 2023 年年度报告 |
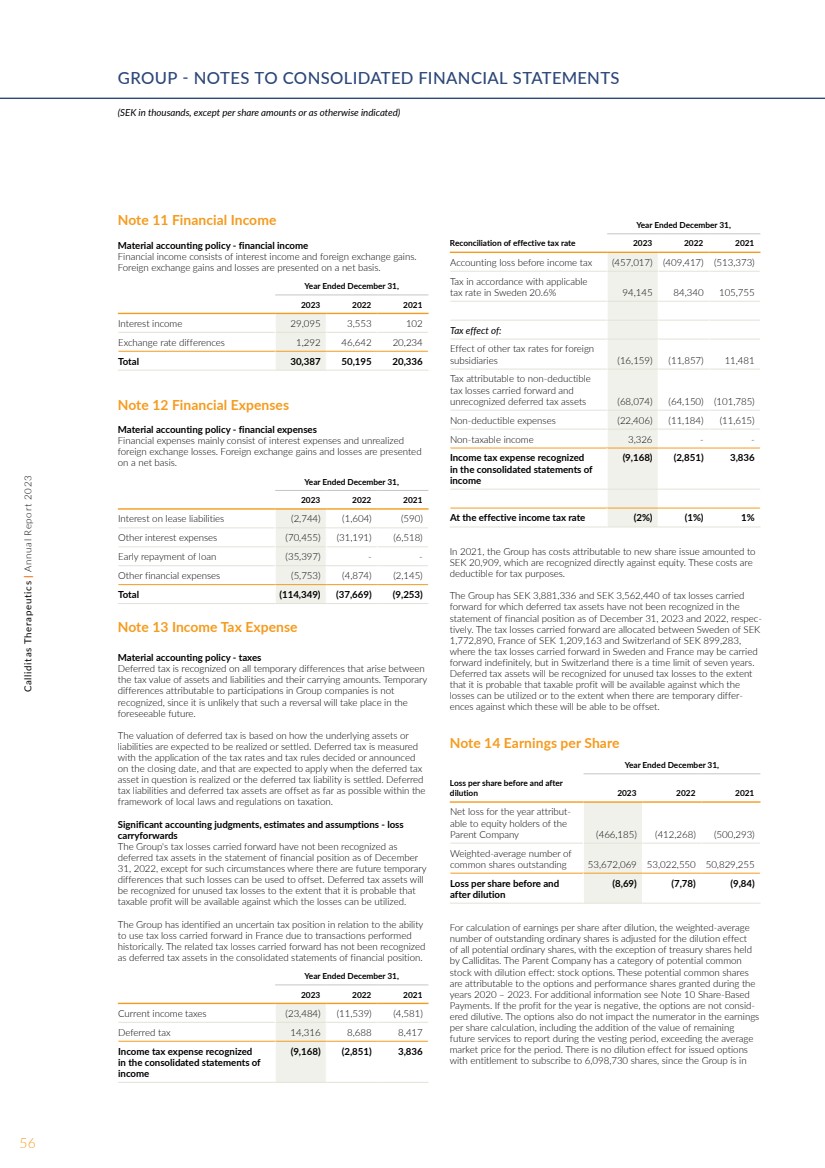
| 附注 14 截至12月31日的每股收益 年度, 稀释前后的每股亏损 2023 年 2021 年 2021 年度归属于母公司股权持有人的净亏损 (466,185) (412,268) (500,293) 已发行普通股的加权平均数 53,672,069 53,022,550 50,8299 ,255 稀释前和摊薄后每股亏损 (8,69) (7,78) (9,84) 为计算稀释后的每股收益,已发行普通股的加权平均数 根据所有潜在普通股的稀释效应 进行了调整股票,Calliditas持有 的库存股除外。母公司有一类具有稀释效应的潜在普通 股票:股票期权。这些潜在的普通股 归因于2020年至2023年 年度授予的期权和绩效股份。有关更多信息,请参阅附注 10 基于股份的 付款。如果该年度的利润为负数,则期权不被视为稀释期权。这些期权也不会影响计算每股收益 的分子,包括将归属期内要报告的剩余 未来服务的价值相加,超过该期间的平均 市场价格。由于集团采用 附注12财务费用 重大会计政策——财务费用 财务费用 重大会计政策——财务费用 财务费用 财务支出主要包括利息支出和未实现的 外汇损失,因此对有权认购6,098,730股股票的已发行期权 没有摊薄影响。外汇收益和亏损按净额列报 。 截至12月31日的年度, 2023 2021 年租赁负债利息 (2,744) (1,604) (590) 其他利息支出 (70,455) (31,191) (6,518) 提前偿还贷款 (35,397)-- 其他财务费用 (5,753) (4,874) (2,145) 总计 (114,349) (37,669) (9,253) 附注 11 财务收入 重大会计政策——财务收入 财务收入由利息收入和外汇收益组成。 外汇损益按净额列报。 截至12月31日的年度, 2023 2021 年利息收入 29,095 3,553 102 汇率差异 1,292 46,642 20,234 合计 30,387 50,195 20,336 附注 13 所得税支出 重大会计政策——税 资产和负债的税值与账面金额之间产生的所有临时差异均确认递延税。 不承认因参与集团公司而产生的临时 差异,因为这种逆转在 可预见的将来不太可能发生。 递延所得税的估值基于标的资产或 负债的预期变现或结算方式。递延税是根据截止日期决定或宣布的税率和税收规则来衡量的 ,预计将在相关递延税 资产变现或递延所得税负债结算时适用。递延的 纳税负债和递延所得税资产尽可能在当地税收法律法规框架内抵消。 重要的会计判断、估计和假设-亏损 结转 截至2022年12月31日,集团结转的税收损失尚未在财务状况表中确认为 递延所得税资产,除非未来存在临时的 差额可以用来抵消。递延所得税资产将 确认未使用的税收损失,前提是有可能有 应纳税利润可用来抵消亏损。 该集团已确定与 历史交易导致的法国结转的税收损失有关 的纳税状况不确定。结转的相关税收损失在合并财务状况表中未被确认为递延所得税资产 。 截至12月31日的年度, 2023 年 2021 年 2021 年 2021 年当前所得税 (23,484) (11,539) (4,581) 递延税 14,316 8,68 8,417 收入 合并报表中确认的所得税支出 (9,168) (2,851) 3,836 年截至12月31日的年度, 2023 年有效税率对账表 2021 年所得税前会计亏损 (457,017) (409,417) (513,373) 根据瑞典适用的 税率征税 20.6% 94,145 84,340 105,755 税收影响: 其他税率对外国 子公司 (16,159) (11,857) 11,481 税收的影响归因于结转的不可扣除的 税收损失和 未确认的递延所得税资产 (68,074) (64,150) (101,785) 不可扣除的费用 (22,406) (11,184) (11,615) 非应纳税收入 3,326-- 在 收入合并报表中确认的所得税支出 (9,168) (2,851) 3,836 按有效所得税税率 (2%) (1%) 1% 2021年,集团新股发行的成本为 20,909瑞典克朗,直接计入权益。出于税收目的,这些费用可以扣除 。 集团结转了3,881,336瑞典克朗和3,562,440瑞典克朗的税收亏损 ,截至2023年12月31日和2022年12月31日, 财务状况表中分别未确认递延所得税资产。结转的税收损失在瑞典 1,772,890瑞典克朗、法国1,209,163瑞典克朗和瑞士之间分配899,283瑞典克朗, 其中瑞典和法国结转的税收损失可以无限期结转 ,但在瑞士,时限为七年。 递延所得税资产将确认未使用的税收损失,前提是 很可能有可利用 亏损的应纳税利润,或者只要存在临时差异可以抵消这些损失。 56Calliditas Therapeutics | 2023 年年度报告集团——合并财务报表附注 (千瑞典克朗,每股金额或另有说明除外) |
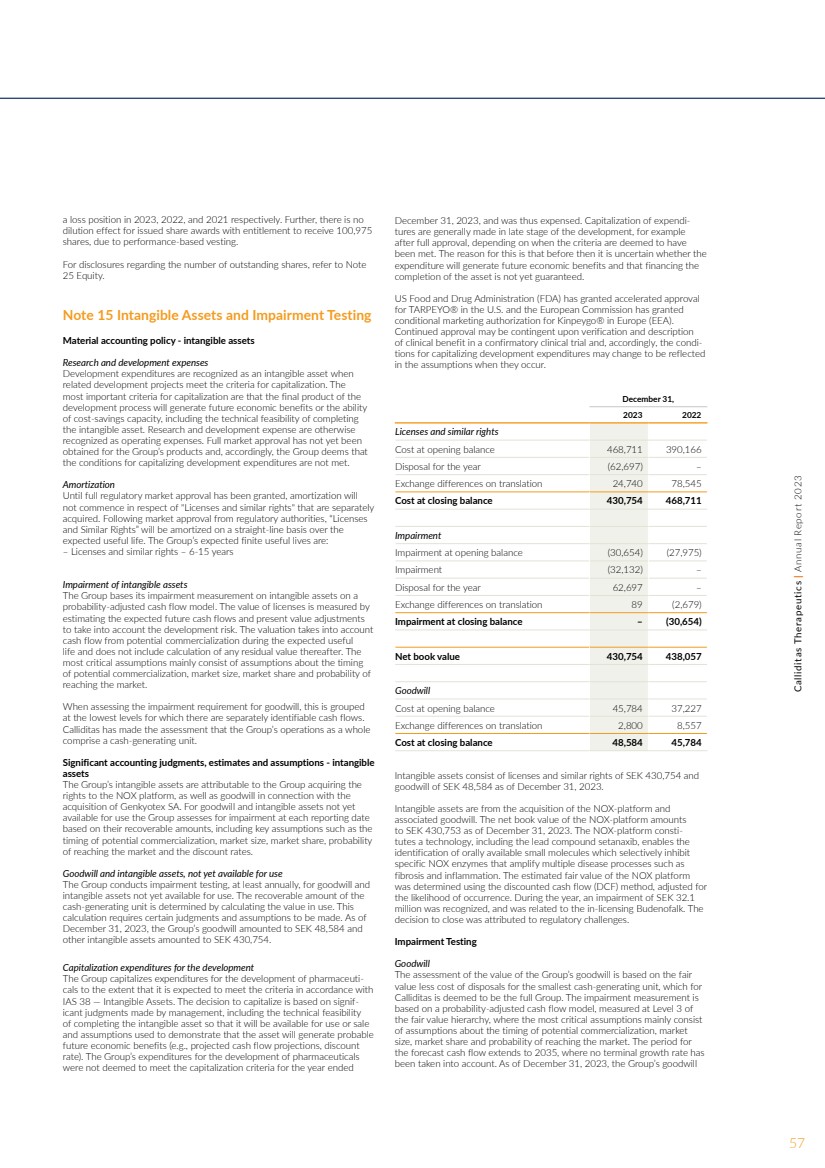
| 附注15 无形资产和减值测试 材料会计政策-无形资产 研发费用 当 相关开发项目符合资本化标准时,开发支出被确认为无形资产。 最重要的资本化标准是, 开发过程的最终产品将产生未来的经济效益或 成本节约能力,包括完成 无形资产的技术可行性。研发费用在其他方面被认定为 运营费用。集团的产品尚未获得 的全面市场批准,因此,集团认为 开发支出资本化的条件未得到满足。 摊销 在监管市场获得全面批准之前, 不会开始分开收购的 “许可证和类似权利” 的摊销。在监管机构的市场批准后,“许可证 和类似权利” 将在 的预期使用寿命内按直线摊销。集团的预期有限使用寿命为: — 许可证和类似权利 — 6-15 年 无形资产减值 该集团对无形资产的减值计量基于 概率调整后的现金流模型。许可证的价值是通过 估算预期的未来现金流和考虑到开发风险的现值调整 来衡量的。估值考虑了 预期使用寿命内潜在商业化产生的 现金流,不包括此后任何剩余价值的计算。 最关键的假设主要包括对潜在商业化的时间 、市场规模、市场份额和 进入市场的概率的假设。 在评估商誉减值要求时,将 归入有可单独识别现金流的最低水平。 Calliditas评估认为,该集团的整个业务 包括一个现金生成单位。 重要的会计判断、估计和假设——无形 资产 集团的无形资产归因于集团收购氮氧化物平台的 版权以及与 收购Genkyotex SA相关的商誉。对于尚未可供使用的商誉和无形资产 ,集团在每个报告日 根据其可收回金额进行减值评估,包括 潜在商业化的时间、市场规模、市场份额、进入市场的概率 和贴现率等关键假设。 尚未可供使用的商誉和无形资产 本集团至少每年对商誉和 尚未可供使用的无形资产进行减值测试。 现金产生单位的可收回金额是通过计算所用价值来确定的。这个 计算需要做出一定的判断和假设。截至 2023年12月31日,该集团的商誉为48,584瑞典克朗, 其他无形资产为430,754瑞典克朗。 开发的资本化支出 本集团将药品开发的支出资本化,以达到预期符合 IAS 38(无形资产)标准的水平。资本化的决定是基于管理层做出的重大判断,包括完成无形资产以供使用或出售的技术可行性 ,以及用于证明该资产将产生可能的未来经济收益的假设(例如,预计的现金流预测、折扣 率)。该集团的药品开发支出 被认为不符合截至 2023 年 12 月 31 日止年度的资本化标准,因此被记作支出。支出资本化通常在开发的后期阶段进行,例如 在获得全面批准后,具体取决于何时认为符合 标准。其原因是,在此之前,尚不确定 支出是否会产生未来的经济利益,并且尚无法保证为资产完工 提供资金。 美国食品药品监督管理局(FDA)已批准TARPEYO® 在美国的加速批准 ,欧盟委员会已授予Kinpeygo® 在欧洲(EEA)的有条件上市许可 。 持续批准可能取决于对确认性临床试验中临床益处的验证和描述 ,因此,开发支出的资本化条件可能会发生变化,在发生时反映在假设中 。 2023 年 12 月 31 日, 2023 年许可证和类似权利 期初余额中的成本 468,711 390,166 年度的处置(62,697)— 折算后的汇兑差额 24,740 78,545 期末余额成本 430,754 468,711 减值 期初余额 (30,654) (27,975) 减值 (32,132) — 年度处置 62,697 — 折算后的汇兑差额 89 (2,679) 期末余额减值 — (30,654) 账面净值 430,754 438,057 商誉 期初余额成本 45,784 37,227 折算后的交易所差额 2,800 8,557 按期末余额计算的成本48,584 45,784无形资产包括许可证和类似权利430,754瑞典克朗以及截至2023年12月31日的48,584瑞典克朗的 商誉。 无形资产来自对NOX平台的收购和 相关的商誉。截至2023年12月31日,氮氧化物平台的净账面价值为 至430,753瑞典克朗。氮氧化物平台构成一项技术,包括主导化合物setanaxib,使 能够鉴定口服可用的小分子,这些小分子有选择地抑制 特异性氮氧化物酶,这些酶会放大 纤维化和炎症等多种疾病过程。氮氧化物平台 的估计公允价值是使用贴现现金流 (DCF) 方法确定的,并根据 发生的可能性进行了调整。在这一年中,确认了3,210万瑞典克朗的减值,与许可中的Budenofalk有关。 的关闭决定归因于监管方面的挑战。 减值测试 商誉 对集团商誉价值的评估基于公平的 价值减去最小的现金产生单位的处置成本,对于 Calliditas 来说,该单位被视为整个集团。减值衡量标准是 基于概率调整后的现金流模型,在 公允价值层次结构的第 3 级进行测量,其中最关键的假设主要由关于潜在商业化时机、市场 规模、市场份额和进入市场概率的 假设组成。 预测现金流的时期延至2035年,在此期间没有考虑任何最终增长率 。截至2023年12月31日,该集团的商誉 分别在2023年、2022年和2021年处于亏损状态。此外,由于基于业绩的归属,已发行的有权获得100,975股股票的股票奖励没有 稀释效应。 有关已发行股票数量的披露,请参阅附注 25 股权。 57Calliditas Therapeutics | 2023 年年度报告 |
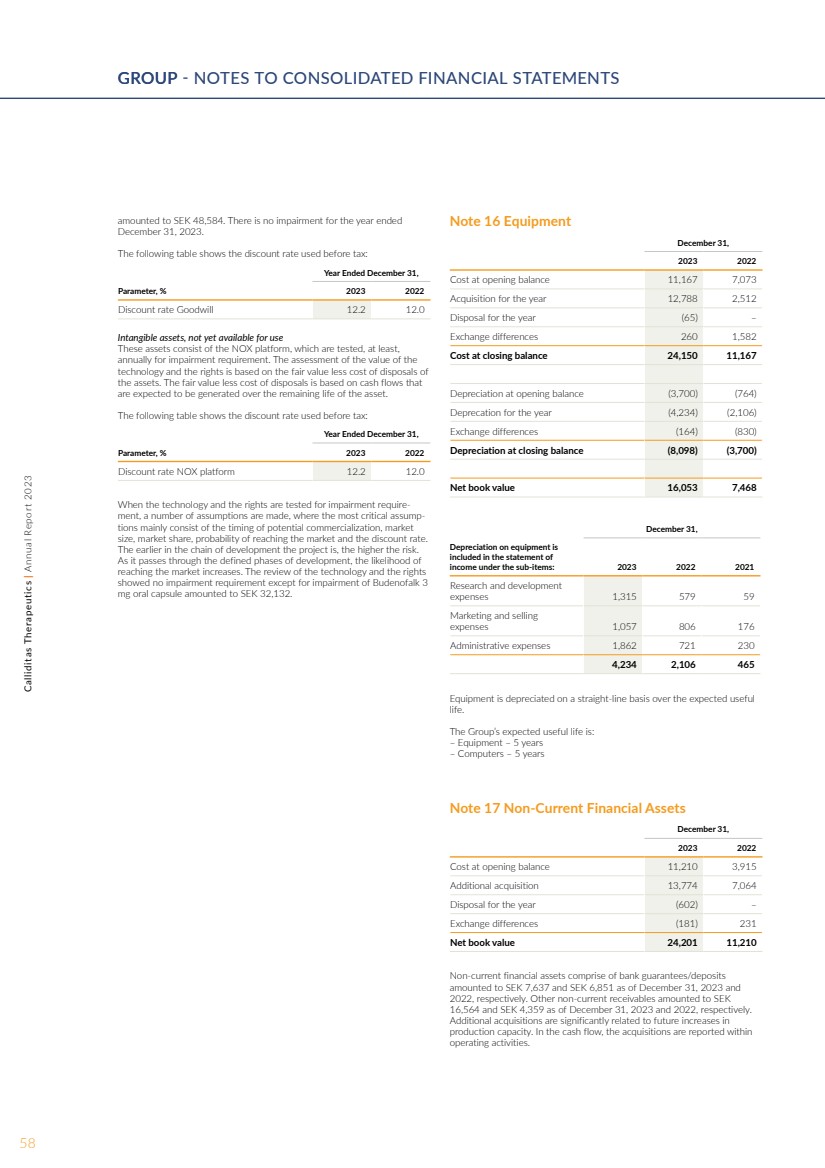
| 附注 16 设备 2023 年 12 月 31 日, 以期初余额计算的成本 11,167 7,073 年度的收购 12,788 2,512 年度的处置 (65) — 汇兑差额 260 1,582 期末余额 24,150 11,167 期初余额折旧 (3,700) (764) 该年度的折旧 (4,234) (2,106) 交易所差额 (164) (830) 期末余额折旧 (8,098) (3,700) 账面净值 16,053 7,468 12 月 31 日, 设备折旧包含在 收入报表下子项下:2023 年 2022 年 2021 研究和开发 费用 1,315 579 59 营销和销售 费用 1,057 806 176 管理费用 1,862 721 230 4,234 2,106 465 设备按直线折旧,超过预期的使用寿命 。 集团的预期使用寿命为: — 设备 — 5 年 — 计算机 — 5 年 附注 17 非流动金融资产 2023 年 12 月 31 日, 2023 年 12 月 31 日,按期初余额计算的成本 11,210 3,915 额外收购 13,774 7,064 年度处置额 (602) — 231 账面净值 24,201 11,210 非当前截至2023年12月31日和 2022年,由银行担保/存款 组成的金融资产分别为7,637瑞典克朗和6,851瑞典克朗。截至2023年12月31日和2022年12月31日,其他非流动应收账款分别为16,564瑞典克朗和4,359瑞典克朗。 额外收购与未来 产能的增加密切相关。在现金流中,收购在 经营活动中报告。 总额为 48,584 瑞典克朗。截至 2023 年 12 月 31 日 的年度没有减值。 下表显示了税前使用的折扣率: 截至12月31日的年度, 参数,2023 年折现率百分比商誉 12.2 12.0 尚未可供使用的无形资产 这些资产由氮氧化物平台组成,至少每年对该平台进行减值要求测试 。 技术和权利的价值评估以公允价值减去 资产处置成本为基础。公允价值减去处置成本的计算依据是 在资产剩余寿命内预计产生的现金流。 下表显示了税前使用的折扣率: 截至12月31日的年度, 参数,% 2023 年折扣率 NOX 平台 12.2 12.0 在对技术和权利进行减值要求测试时,会做出许多假设,其中最关键的假设主要包括潜在商业化的时机、市场 规模、市场份额、进入市场的概率和折扣率。 项目在开发链中越早,风险越高。 随着它经历定义的开发阶段, 进入市场的可能性增加。对该技术和权利 的审查显示,除减值外,没有减值要求,Budenofalk 3 mg口服胶囊总额为32,132瑞典克朗。 58Calliditas Therapeutics | 2023 年年度报告集团集团-合并财务报表附注 |
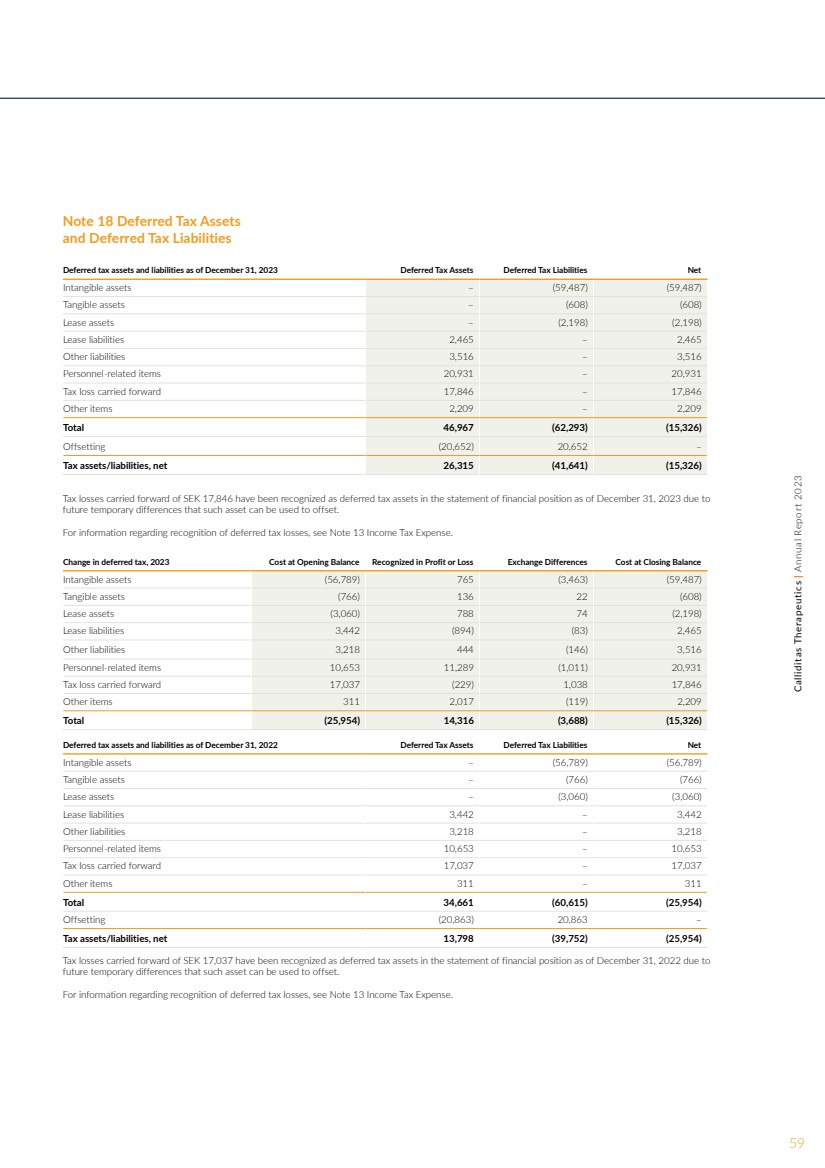
| 附注 18 截至2023年12月31日的递延所得税资产 和递延所得税负债 递延所得税资产和负债净额 无形资产 — (59,487) (59,487) 有形资产 — (608) (608) 租赁资产 — (2,198) (2,198) 租赁负债 2,465 — 2,465 其他负债 3,565 16 — 3,516 个人事相关项目 20,931 — 20,931 结转的税收亏损 17,846 — 17,846 其他项目 2,209 — 2,209 共计 46,967 (62,293) (15,326) 抵消 (20,652) 20,652 — 税收资产/负债,净额 26,315 (41,641) (15,326) 结转的17,846瑞典克朗的税收损失已在截至2023年12月31日的财务状况表中被确认为递延所得税资产,这是由于 该资产可用于抵消的未来临时差异。 有关确认递延所得税损失的信息,请参阅附注 13 所得税支出。 递延所得税变动,2023 年期初余额成本在期末余额中确认的损益汇兑差额成本 无形资产 (56,789) 765 (3,463) (59,487) 有形资产 (766) 136 22 (608) 租赁资产 (3,060) 788 (2,198) 租赁负债 3,442 (894) (83) 2,465 其他负债 3,218 444 (146) 3,516 人事相关项目 10,653 11,289 (1,011) 20,931 结转的税收亏损 17,037 (229) 1,038 17,846 其他项目 311 2,017 (119) 2,209 总计 (25,954) 14,316 (3,688) (15,326) 截至止的递延所得税资产和负债2022年12月31日递延所得税资产递延所得税负债净额 无形资产 — (56,789) (56,789) 有形资产 — (766) (766) 租赁资产 — (3,060) 租赁负债 3,442 — 3,442 其他负债 3,218 — 3,218 个人相关项目 10,653 — 10,653 结转的税收损失 17,653 037 — 17,037 其他项目 311 — 311 共计 34,661 (60,615) (25,954) 抵消 (20,863) 20,863 — 税收资产/负债,净额 13,798 (39,752) (25,954) 结转的17,037瑞典克朗的税收损失在报表中被确认为递延所得税资产截至2022年12月31日的财务状况是由于 此类资产可用于抵消的未来临时差异。 有关确认递延所得税损失的信息,请参阅附注 13 所得税支出。 59Calliditas Therapeutics | 2023 年年度报告 |
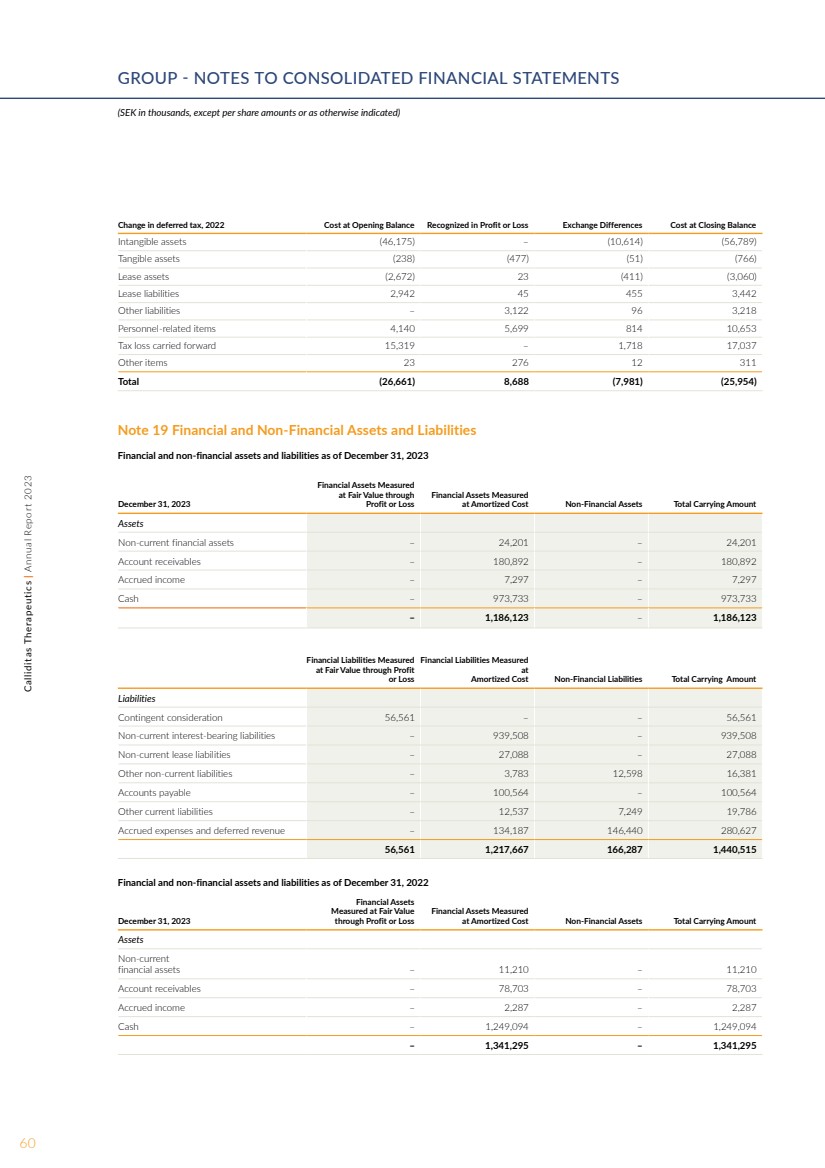
| 附注 19 金融和非金融资产及负债 截至 2023 年 12 月 31 日,金融和非金融资产及负债 按公允价值计量 的金融资产按摊销成本计量 非金融资产账面总额 资产 非流动金融资产 — 24,201 — 24,201 应收账款 — 180,892 — 180,892 应计收入 — 7,297 — 7,297 现金 — 973,733 — 973,733 — 1,186,123 — 1,186,123 金融负债按公允价值计量 计入利润 或亏损 以 计量的金融负债摊销成本非金融负债账面总额 负债 或有对价 56,561 — — 56,561 非流动计息负债 — 939,508 — 939,508 非流动租赁负债 — 27,088 — 27,088 其他非流动负债 — 3,783 12,598 16,381 应付账款 — 100,381 564 — 100,564 其他流动负债 — 12,537 7,249 19,786 应计费用和递延收入 — 134,187 146,440 280,627 56,561 1,217,667 166,287 1,440,515 金融和非金融资产及负债为2022 年 12 月 31 日 2023 年 12 月 31 日金融资产 以公允价值 计入损益的金融资产 按摊销成本计量的金融资产账面总额 资产 非流动 金融资产 — 11,210 — 11,210 应收账款 — 78,703 — 78,703 应计收入 — 2,287 — 2,287 现金 — 1,249,07 94 — 1,249,094 — 1,341,295 — 1,341,295 递延所得税变动,2022年期初余额成本在期末余额中确认的损益汇兑差额成本 无形资产 (46,175) — (10,614) (56,789) 有形资产 (238) (477) (51) (766) 租赁资产 (2,672) 23 (411) (3,060) 租赁负债 2,942 45 455 3,442 其他负债 — 3,122 96 96 3,218 人事相关项目 4,140 5,699 814 10,653 结转的税收损失 15,319 — 1,718 17,037 其他项目 23 276 12 311 Total (26,661) 8,688 (7,981) (25,954) 60Calliditas Therapeutics | 2023年年度报告集团——合并财务报表附注 (千瑞典克朗,每股金额或另有说明除外) |
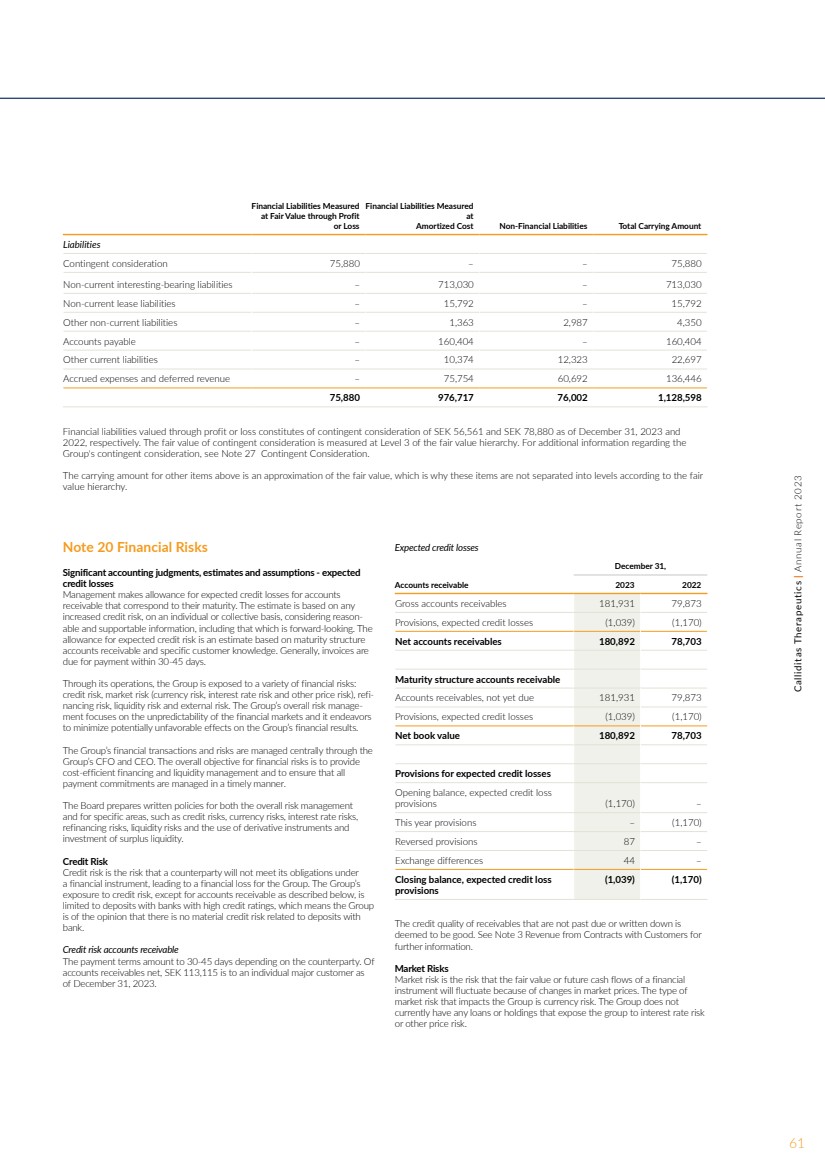
| 金融负债按公允价值计量 计入利润 或亏损 的金融负债以 摊销成本计量非金融负债账面总额 负债 或有对价 75,880 — — 75,880 非流动计息负债 — 713,030 — 713,030 非流动租赁负债 — 15,792 — 15,792 其他非流动负债 — 1,363 2,992 87 4,350 应付账款 — 160,404 — 160,404 其他流动负债 — 10,374 12,323 22,697 应计费用和递延收入 — 75,754 60,692 136,446 75,880 976,717 76,002 1,128,598 笔以损益计值的金融负债分别构成截至2023年12月31日和2022年12月31日的56,561瑞典克朗和78,880瑞典克朗的或有对价。或有对价的公允价值在公允价值层次结构的第三级进行衡量。有关 集团或有对价的更多信息,请参阅附注 27 或有对价。 上述其他项目的账面金额是公允价值的近似值,这就是为什么没有根据公平 价值层次结构将这些项目分成多个级别的原因。 附注 20 财务风险 重要的会计判断、估计和假设-预期 信用损失 管理层为与到期日相对应的 应收账款的预期信用损失留出了备抵金。该估算基于个人或集体的任何 增加的信用风险,同时考虑合理和可支持的信息,包括前瞻性信息。 预期信用风险备抵额是根据到期结构 应收账款和特定客户知识得出的估算。通常, 发票应在 30-45 天内付款。 通过其运营,集团面临各种金融风险: 信用风险、市场风险(货币风险、利率风险和其他价格风险)、再融资风险、流动性风险和外部风险。集团的整体风险管理侧重于金融市场的不可预测性,并努力 最大限度地减少对集团财务业绩的潜在不利影响。 集团的财务交易和风险由 集团的首席财务官兼首席执行官集中管理。金融风险的总体目标是提供 具有成本效益的融资和流动性管理,并确保及时管理所有 付款承诺。 董事会为整体风险管理 和特定领域(例如信用风险、货币风险、利率风险、 再融资风险、流动性风险、衍生工具的使用和 剩余流动性的投资)制定书面政策。 信用风险 信用风险是指交易对手无法履行其在 金融工具下的义务从而导致集团遭受财务损失的风险。除下述应收账款外,集团的 信用风险敞口仅限于信用评级较高的银行的存款,这意味着集团 认为不存在与 银行存款相关的重大信用风险。 信用风险应收账款 付款期限为30-45天,视交易对手而定。截至2023年12月31日 净应收账款中,113,115瑞典克朗是向个人主要客户支付的。 预期信贷损失 12月31日, 2023 年应收账款总额 181,931 79,873 准备金,预期信贷损失 (1,039) (1,170) 应收账款净额 180,892 78,703 到期应收账款 尚未到期的应收账款 181,931 79,873 准备金,预期信贷损失 (1,039) (1,170) 账面净值 892 78,703 预期信贷损失准备金 期初余额、预期信贷损失 准备金 (1,170) — 今年的准备金 — (1,170) 反向准备金 87 — 交易所差异 44 — 期末余额、预期信用损失 准备金 (1,039) (1,170) 未逾期或减记的应收账款的信贷质量被视为 良好。有关 的更多信息,请参阅附注 3 与客户签订合同的收入。 市场风险 市场风险是指金融 工具的公允价值或未来现金流因市场价格变动而波动的风险。影响集团的 市场风险类型是货币风险。该集团 目前没有任何贷款或持股使集团面临利率风险 或其他价格风险。 61Calliditas Therapeutics | 2023 年年度报告 |
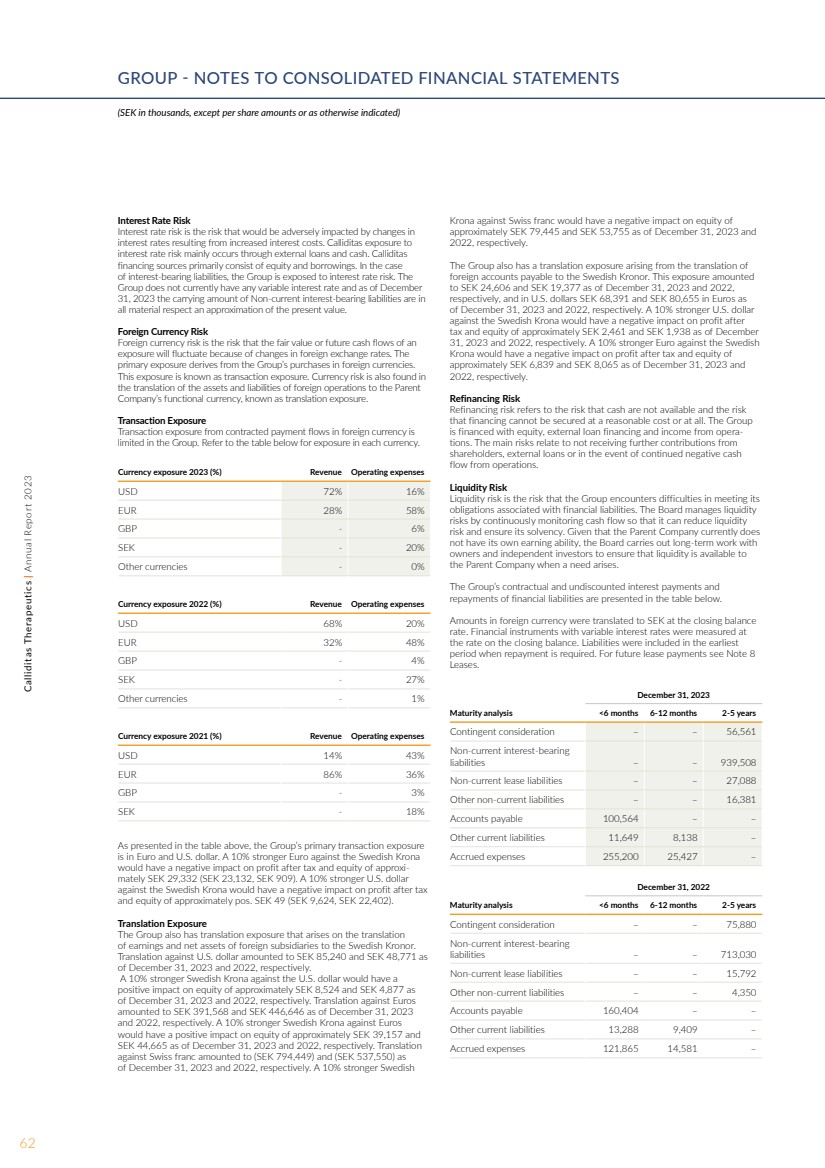
| 利率风险 利率风险是指利息成本增加导致的 利率变化可能受到不利影响的风险。Callidita 面临的 利率风险主要来自外部贷款和现金。Callidita 的融资来源主要包括股权和借款。就 计息负债而言,集团面临利率风险。 集团目前没有任何可变利率,截至2023年12月 31日,非流动计息负债的账面金额在 所有重要方面均为现值的近似值。 外币风险 外币风险是指 敞口的公允价值或未来现金流因外汇汇率变动而波动的风险。 的主要风险敞口来自集团的外币购买。 这种风险被称为交易风险。货币风险还存在于 将外国业务的资产和负债转换为母公司 公司的本位货币,即折算风险敞口。 交易敞口 本集团中来自合同外币支付流的交易风险受限 。请参阅下表,了解每种货币的风险敞口。 2023 年货币敞口 (%) 收入运营费用 美元 72% 16% 欧元 28% 58% 英镑-6% 瑞典克朗-20% 其他货币-0% 2022年货币敞口 (%) 收入运营费用 美元 68% 20% 欧元 32% 48% 英镑-4% 瑞典克朗-27% 其他货币-1% 其他货币-1% br} 2021 年货币敞口 (%) 收入运营支出 美元 14% 43% 欧元 86% 36% 英镑-3% 瑞典克朗-18% 如上表所示,集团的主要交易敞口 以欧元和美元计算。欧元兑瑞典克朗上涨10% 将对约29,332瑞典克朗(23,132瑞典克朗,909瑞典克朗)的税后利润和权益产生负面影响。美元兑瑞典克朗上涨10% 将对税后利润 和大约pos的股权产生负面影响。49 瑞典克朗(9,624 瑞典克朗,22,402 瑞典克朗)。 翻译风险 该集团还存在折算风险,该风险来自外国子公司的收益和净资产折算成瑞典克朗。截至2023年12月31日和2022年12月31日 , 兑美元的折算分别为85,240瑞典克朗和48,771瑞典克朗。 截至2023年12月31日和2022年12月31日 ,瑞典克朗兑美元汇率上涨10%将对股票产生约8,524瑞典克朗和4,877瑞典克朗的积极影响。截至2023年12月31日和2022年12月31日,对欧元 的折算分别为391,568瑞典克朗和446,646瑞典克朗。截至2023年12月31日和2022年12月31日,瑞典克朗兑欧元 上涨10%将对股票产生积极影响,分别达到约39,157瑞典克朗和 44,665瑞典克朗。截至2023年12月31日和2022年12月31日, 兑瑞士法郎的折算分别为(794,449瑞典克朗)和(537,550瑞典克朗)。截至2023年12月31日,瑞典 克朗兑瑞士法郎上涨10%将对 的股票产生负面影响,截至2023年12月31日和2022年12月31日分别约79,445瑞典克朗和53,755瑞典克朗。 该集团还面临因应付给瑞典克朗的 国外账款的折算而产生的翻译风险。截至2023年12月31日和2022年12月31日, 的风险敞口分别为24,606瑞典克朗和19,377瑞典克朗, ;截至2023年12月31日和2022年12月31日 ,该风险敞口分别为68,391瑞典克朗和80,655瑞典克朗。美元兑瑞典克朗上涨10%将对扣除 税后的利润产生负面影响,截至2023年12月31日和2022年12月 31日和2022年12月31日的股权分别为约2461瑞典克朗和1,938瑞典克朗。欧元兑瑞典 克朗上涨10%将对截至2023年12月31日和 2022年12月31日约6,839瑞典克朗和8,065瑞典克朗的 税后利润和股权产生负面影响。 再融资风险 再融资风险是指无法获得现金的风险以及无法以合理成本或根本无法担保融资的风险 。集团 的资金来自股权、外部贷款融资和运营收入。主要风险与无法从 股东那里获得更多捐款、外部贷款或运营现金流持续出现负数有关。 流动性风险 流动性风险是指集团在履行与金融负债相关的 义务时遇到困难的风险。董事会通过持续监控现金流来管理流动性 风险,从而降低流动性 风险并确保其偿付能力。鉴于母公司目前确实没有自己的盈利能力,董事会与 所有者和独立投资者开展长期合作,确保 母公司在需要时有流动性。 集团的合同利息和未贴现利息支付以及 金融负债的偿还额如下表所示。 外币金额按期末余额 汇率折算成瑞典克朗。具有浮动利率的金融工具以 期末余额的利率计量。负债包含在需要还款的最早 期内。有关未来的租赁付款,请参阅附注8 租赁。 2023 年 12 月 31 日成熟度分析 |
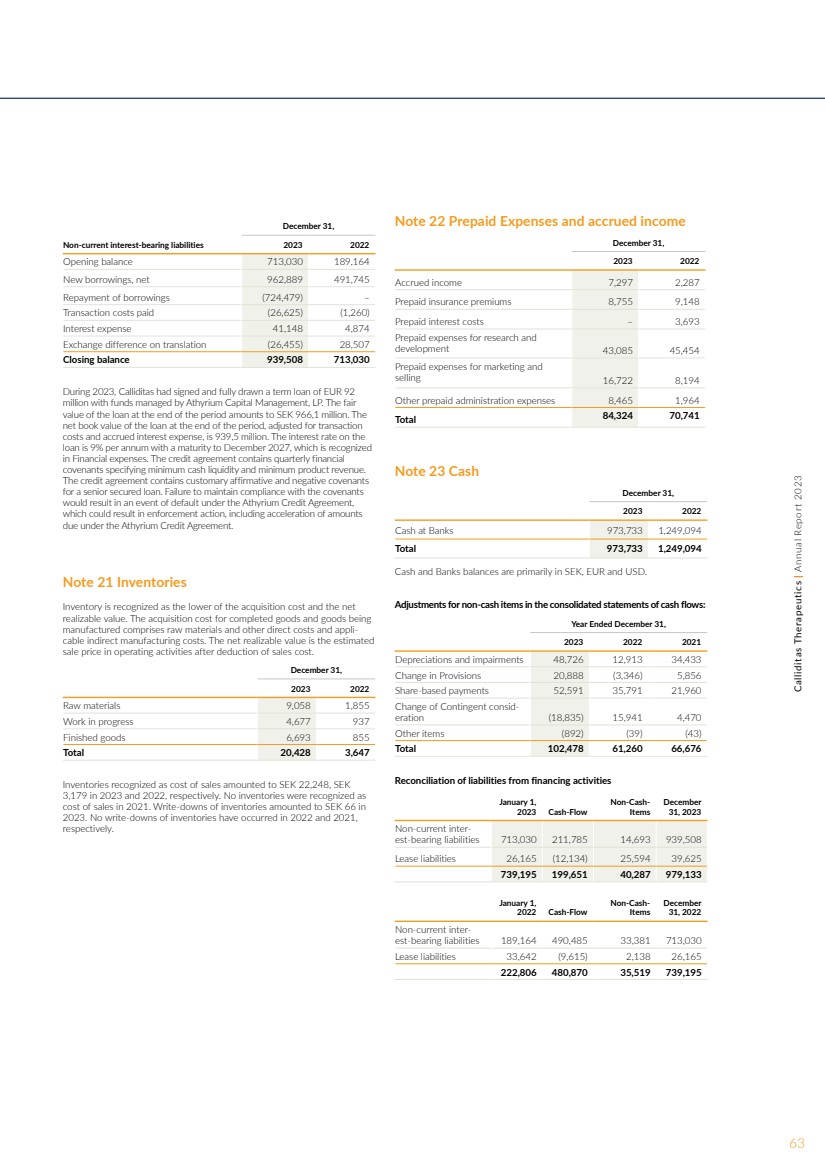
| 注 21 库存 库存被视为购置成本和 可变现净值中的较低值。成品及制造 货物的购置成本包括原材料和其他直接成本以及适用的电缆间接制造成本。净可变现价值是扣除销售成本后的经营活动中估计的 销售价格。 2023 年 12 月 31 日, 2023 年原材料 9,058 1,855 在建工程 4,677 937 制成品 6,693 855 总计 20,428 3,647 份确认为销售成本的库存在 2023 年和 2022 年分别为 22,248 瑞典克朗、 3,179 瑞典克朗。2021 年,没有任何库存被认定为 销售成本。 2023 年,库存减记额为 66 瑞典克朗。 分别在2022年和2021年没有发生库存减记。 附注 22 预付费用和应计收入 2023 年 12 月 31 日应计收入 7,297 2,287 预付保险费 8,755 9,148 预付利息成本 — 3,693 研究和 开发的预付费用 43,085 45,454 销售和 的预付费用 16,722 8,194 其他预付管理费用 8,465 1,964 总计 84,324 70,764 41 附注 23 现金 2023 年 12 月 31 日, 2022 年银行现金 973,733 1,249,094 总计 973,733 1,249,094 现金和银行余额主要以瑞典克朗、欧元和美元计算。 合并现金流量表中非现金项目的调整: 截至12月31日, 2023 2021 年折旧和减值 48,726 12,913 34,433 准备金变动 20,888 (3,346) 5,856 基于股份的付款 52,591 35,791 21,960 或有对价变动 (18,835) 15,941 4,470 其他项目 (892)) (39) (43) 共计 102,478 61,260 66,676 融资活动负债对账 1 月 1 日, 2023 年现金流 非现金项目 2023 年 12 月 31 非流动利息负债 713,030 211,785 14,693 939,508 租赁负债 26,165 (12,134) 25,594 39,625 739,195 199,651 40,287 979,133 1 月 1 日, 2022年1月1日 非现金项目 31 年 12 月 31 日 189,164 490,485 33,381 713,030 租赁负债 33,642 (9,615) 2,138 26,165 222,806 480,870 35,519 739,195 12 月 31 日, 2023 年期初余额 713,030 189,164 新借款,净额 962,889 491,745 偿还借款 (724,479) — 已支付的交易成本 (26,625) (1,260) 利息费用 41,148 4,874 交易所翻译差额(26,455)28,507 期末余额939,508 713,030 2023年期间,Calliditas用Athyrium Capital Management, LP管理的资金签署并全额提取了9200万欧元的定期贷款。期末,该贷款的公允价值为9.661亿瑞典克朗。经交易 成本和应计利息支出调整后,期末贷款的 净账面价值为9.395亿美元。 贷款的年利率为9%,到期日为2027年12月,在财务支出中确认 。信贷协议包含季度财务 契约,规定了最低现金流动性和最低产品收入。 信贷协议包含优先担保贷款的惯常肯定和否定承诺 。不遵守契约 将导致 Athyrium 信贷协议 下的违约事件,这可能会导致执法行动,包括加快根据 Athyrium 信贷协议应付的款项 。 63Calliditas Therapeutics | 2023 年年度报告 |
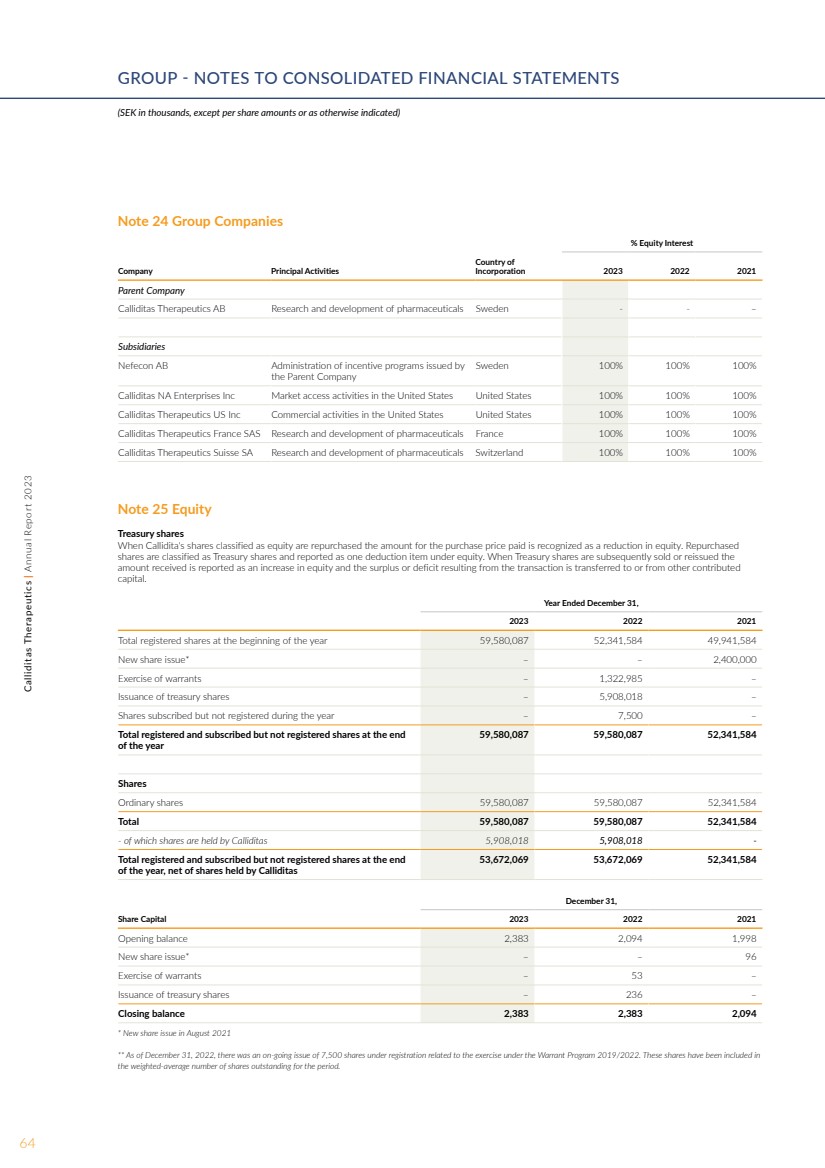
| 附注 24 集团公司 % 股权 公司主要活动 注册国 2023 年 2021 年母公司 Calliditas Therapeutics AB 药品研发瑞典--— 子公司 Nevecon AB 管理母公司 瑞典发布的激励计划 100% 100% 100% Calliditas NA Enterprises Inc在美国的市场准入活动各州 100% 100% 100% Calliditas Therapeutics US Inc 在美国的商业活动美国 100% 100% 100% 100% 100% Calliditas Therapeutics France SAS 药品研究与开发法国 100% 100% 100% Calliditas Therapeutics Suisse SA 瑞士制药研究与开发 100% 100% 100% 附注 25 股权 库存股 当回购Callidita被归类为股权的股票时,支付的收购价金额被视为权益减少。回购的 股票被归类为库存股,在权益项下列为一个扣除项目。随后出售或重新发行美国库存股时,收到的 金额将报告为权益的增加,交易产生的盈余或赤字将转移到其他出资 资本或从其他出资资本中转出。 截至12月31日的年度, 2023 2021 年年初的注册股份总数 59,580,087 52,341,584 49,941,584 股新股发行* — — 2,400,000 股权证行使 — 1,322,985 — 发行库存股 — 5,908,018 — 年初已认购但未注册的股份 — 7,500 — 截至年底 注册和认购但未注册的股票总数 59,580,087 59,580,087 52,341,584 股 普通股 59,580,087 59,580,087 52,580,087 52,341,584 股——其中股份由 Calliditas5,908,018 5,908,018- 年底注册和认购但未注册的总股份,扣除Calliditas 53,672,069 53,672,069 52,341,584 52,341,584 12 月 31 日, 股本 2023 2021 年期初余额 2,383 2,094 1,998 新股发行* — — 96 认股权证行使 ants — 53 — 库存股的发行 — 236 — 期末余额 2,383 2,383 2,094 * 2021 年 8 月新股发行 ** 截至2022年12月31日,正在发行与2019/2022年认股权证计划下的行使相关的注册7,500股股票。这些股票已包含在该期间已发行股票的加权平均数中。 64Calliditas Therapeutics | 2023 年年度报告集团——合并财务报表附注 (千瑞典克朗,每股金额或另有说明除外) |
| 股本 所有股份均已全额支付,没有股票可供出售。所有 股均为普通股,具有相同的资本权利, 持有一票。商值为每股0.04瑞典克朗。 库存股交易 截至2023年12月31日,Calliditas共有5,908,018股普通股由母公司作为库存股持有 。在2023年年度股东大会 上,授权Calliditas可以转让(出售)这些 普通股,目的是为收购业务提供资金, 筹集资金以资助项目开发、偿还贷款 或将Calliditas的产品商业化。截至2023年12月31日,尚未转让(出售)库存股 。截至2023年12月31日的已发行股票总数 如上表所示。 翻译储备 这些储备金全部与翻译储备有关。折算 储备金包括因折算外国业务财务报表 而产生的所有汇率差异。 12月31日, 2023 年 2021 年翻译储备金期初余额 9,307 (26,979) (6,090) 年度变动 (14,538) 36,286 (20,889) 期末余额 (5,231) 9,307 (26,979) 附注 26 条款 重要会计政策-准备金 准备金与其他负债有所不同是付款时间或结清准备金金额的不确定性。当某一事件导致现有法律或非正式债务时, 将在集团的财务状况表中报告准备金, ,并且很可能需要资金外流才能清偿债务,并且可以对金额进行可靠的估计。准备金 的金额是资产负债表日结清现有债务所需金额的最佳估计。如果 按时付款的影响很大,则准备金是通过对预期的未来现金流进行折扣来计算的。 截至2023年12月31日的准备金 股份支付的社会保障费用其他准备金,净额 期初余额 11,792 — 11,792 年度的准备金 21,109 — 21,109 汇兑差额 (306) — (306) 截至2022年12月31日的共计32,595 — 32,595笔准备金 基于股份的支付其他准备金,净额 br} 期初余额 13,084 1,446 14,530 年度准备金 1,027-1,027 年度索赔额 (204)-(204) 冲销未使用金额 (2,666) (1,573) (4,239) 汇兑差额551 127 678 共计 11,792 — 11,792 份基于股份的支付的社会保障成本 未来何时支付基于股份的支付的社会保障成本,以及最终将调整为多少金额尚不确定,因为这取决于使用绩效份额时的市场价值。 65Calliditas Therapeutics | 2023 年年度报告 |
| 附注28 养老金负债 养老金债务估值中的假设 养老金债务和养老金成本的估值基于精算假设。 固定福利养老金计划 固定福利养老金债务基于精算原则。 Calliditas为法国 和瑞士的子公司制定了针对退休、死亡和残疾的固定福利养老金计划。根据国际会计准则第19号, 债务的现值包括 瑞士养老金计划的特殊工资税。养老金支出在研究 项下确认,开发费用和管理费用在合并收入报表中确认。 12月31日, 2023年每个国家的净负债瑞士(3,394)(789) 法国(127)(94) 合计(3,521)(884) 附注27或有对价 重大会计政策——或有对价 本集团的或有对价被归类为以公允价值确认的金融负债 ,以公允价值计入损益。在集团的 合并财务状况表中,初始和后续时期均以 的公允价值进行计量,其中公允价值的变动 在集团的合并收益表中确认。与汇率影响 相关的公允价值变动的 组成部分在净财务项目中确认,公允价值的其他变动在 中确认营业损益。 2023 年 12 月 31 日, 2023 年期初余额 75,880 54,399 年度变动 (18,835) 15,942 汇兑差额 (484) 5,539 账面净值 56,561 75,880 或有对价 关于Genkyotex SA的业务合并,该集团 已承诺在未来支付与持续对价相关的潜在里程碑付款,前提是未来的监管部门批准或已获得有关 setanaxib 的营销 许可。该交易规定了 以下或有对价: 里程碑1:如果美国食品药品管理局授予Genkyotex在美国商业制造、营销和销售setanaxib的权利,则为3,000万欧元。 里程碑2:如果 欧盟委员会授予Genkyotex在欧盟进行商业制造、营销和销售setanaxib的权利,则为1,500万欧元。 里程碑3:如果美国食品药品管理局或欧洲 委员会授予Genkyotex在美国或欧盟商业制造、营销和销售用于治疗IPF或 1型糖尿病的 setanaxib的权利,则为1,000万欧元。 或有对价的公允价值在公平 价值层次结构的第 3 级进行衡量。或有对价在合并财务状况表中被确认为财务负债 ,每个报告期按公允价值 进行重新估值。任何重估收益和亏损均在合并损益表中确认 。偶然对价 是根据现值法计算的,如果以及何时出现各种里程碑 ,已经考虑了 的概率。计算基于 12.2% 的贴现率。影响或有对价估值的最重要因素是 公司对实现里程碑概率的估计,而 年度的变化主要来自对临床试验成功概率的假设。 该小组评估了截至2023年12月31日和2022年12月31日的加权平均结果概率分别为19.7%和20.8%。截至2023年12月31日 和2022年12月31日,临床试验的成功概率提高10% 将分别对约5,656瑞典克朗和7,588瑞典克朗的税后利润产生负面影响 。临床 试验的成功概率越高将增加负债的公允价值,而较低的概率将 降低公允价值。公允价值衡量中使用的不可观察的 输入之间没有相互关系。 66Calliditas Therapeutics | 2023 年年度报告集团——合并财务报表附注 (千瑞典克朗,每股金额或另有说明除外) |
| 固定福利养老金债务的变化 固定福利 计划债务 (瑞士) 计划债务 (法国) 计划资产的公允价值 (瑞士) 员工 福利 债务 2023 年 1 月 1 日 (6,027) (94) 5,238 (884) 服务成本 (1,599) (18) — (1,617) 利息支出 (117) (4) 119 (1) 员工缴款 — — 920 920 合并收益表中包含的营业亏损小计 (1,716) (21) 1,039 (698) 已付/收到的金额 2,441 — (2,441) — 回报率资产(不包括利息支出)— —(67)(67) 与人口假设变化相关的精算收益/(亏损)—(13)—(13) 与财务假设变化相关的精算收益/(亏损)(2,316)— —(2,316) 其他精算收益/(亏损)52 — — 52 计划修正案(433)—(433) 其他综合收益中包含的小计 (2,697) (13) (67) (2,777) 雇主缴款 — — 920 920 货币折算效应 (397) 2 313 (82) 2023 年 12 月 31 日 (8,395) (127) (127) 5,001 (3,521) 固定福利 计划债务 (瑞士) 固定福利 计划债务 (法国) 计划资产的公允价值 (瑞士) 员工 福利 债务 2022年1月1日 (7,942) (111) 4,871 (3,182) 服务成本 (1,530) (26) — (1,556) 利息支出 (27)) (1) 18 (10) 员工缴款 — — 887 887 合并收益表中营业亏损中包含小计 (1,558) (27) 906 (679) 已付/收到的金额 2,140 — (2,140) — 资产回报率(不包括利息支出)— — 34 34 与人口结构变化相关的精算收益/(亏损)假设 — 54 — 54 与财务假设变化相关的精算收益/(亏损)2,846 — — 2,846 其他精算收益/(亏损)(454) — — (454) 其他综合收益中包含的小计 2,392 54 34 2,480 雇主缴款 — — 887 887 货币折算影响 (1,059) (9) 679 (390) 2022年12月31日 (6,059) 27) (94) 5,238 (884) 67Calliditas Therapeutics | 2023 年年度报告 |
| 12月31日, 按计划资产分配(瑞士)2023 年现金 430 137 债券 515 3,048 笔抵押贷款 75 655 股 1,450 126 房地产 1,581 901 其他投资 950 372 共计 5,001 5,238 在上述计划资产中,截至2023年12月31日,分别为515瑞典克朗和3,048瑞典克朗的报价处于活跃市场。 对于法国的养老金债务,没有计划资产。 与固定福利养老金计划相关的风险 通过其离职后福利的固定福利养老金计划, 集团面临多种风险。最重要的风险是: 预期寿命假设:大多数养老金承诺意味着 计划所涵盖的员工将获得终身福利, 因此,较长的预期寿命假设将导致 养老金负债增加。这在瑞士的计划中尤其重要,在该计划中, 通货膨胀率的上升使人们对预期寿命 假设变化的敏感度更高。 通货膨胀风险:该计划的某些养老金承诺与 通货膨胀有关。较高的通货膨胀会导致更高的负债(尽管在大多数情况下, 已经为通货膨胀水平设定了上限,以保护该计划免受 通货膨胀异常上升的影响)。大多数计划资产要么不受(固定利率债券)影响,要么与(股票)通货膨胀的相关性很弱, 这意味着通货膨胀的增加也会增加赤字。 贴现率:降低公司债券利率将 增加该计划的负债,尽管这会被 持有债券价值的增加部分抵消。瑞士养老金计划 受《瑞士联邦职业退休法》、《幸存者 和残疾养老金计划(BVG)管辖。 法国养老金计划受劳动法和制药行业集体 谈判协议的保护。瑞士和法国 计划以最终工资为基础。 12 月 31 日, 2023 年瑞士养老金计划期末余额的精算假设 折扣率 1.45% 2.30% 死亡率表 LPP 2020 代 LPP 2020 代 工资重估率 2.00% 1.00% 退休金通货膨胀率 1.00% 0.50% 储蓄账户存款利率 1.50% 1.00% 周转率 1.50% 1.00% 周转率 10.00% 10.00% 退休后的剩余预期寿命 23.1 年 18.6 年 退休年龄 65 岁 65 岁 12 月 31 日, 2023 年敏感度分析 2023 年根据当前 假设的养老金承诺瑞士养老金计划 8,395 6,027 折扣率,-0.5% 9,426 6,615 折扣率,+0.5% 7,511 5,518 退休金通货膨胀率,-0.5% 7,940 5,797 退休金通货膨胀率,+0.5% 8,902 6,281 工资重估率,+0.5% 8,567 6,131 上面的金额显示了它的价值养老金义务 本应假设个人假设发生了变化。 灵敏度分析基于一个假设的变化,所有其他 假设保持不变。实际上,这种情况发生的可能性极小 ,并且假设的某些变化可能是相关的。在 计算固定福利债务对重大 精算假设的敏感度时,采用了与计算合并财务状况表中确认的养老金负债 相同的方法(在 报告期末应用预计单位抵免法的固定福利债务的现值)。 由于法国的固定福利养老金计划被视为集团的微不足道,因此没有提供进一步的信息。 预计2023年和2022年离职后福利计划的缴款分别为941瑞典克朗和813瑞典克朗。在 2023年和2022年,该债务的加权平均到期日估计分别为23.1年和18.6年。 附注 29 其他非流动负债 2023 年 12 月 31 日, 2022 年期初余额 4,350- 额外负债 12,031 4,350 账面净值 16,381 4,350 附注 30 应计费用和递延收入 2023 年 12 月 31 日, 2023 年假期工资负债 11,257 8,310 应计工资和董事会费用 52,502 28,186 社会保障成本 8,935 7,065 销售应计返利 36,326 15,849 特许权使用费应计费用 37,419 12,023 研究和 开发应计费用 107,302 34,637 营销和 销售的应计费用 10,773 21,543 应计费用管理费用 16,113 8,833 合计 280,627 136,446 68Calliditas Therapeutics | 2023 年年度报告集团——合并财务报表附注 (千瑞典克朗,每股金额或另有说明除外) |
| 注33个报告期之后的事件 2024年2月13日,Calliditas Therapeutics AB宣布,美国专利和 商标局(USPTO)于2024年1月24日颁发了名为 “新 药物成分” 的第11896719号专利,有效期自今天,即2024年2月13日 开始。这是Calliditas在美国 获得的第二项TARPEYO专利,其产品保护期至2043年。 该专利涵盖了一种使用复合型 - 治疗IgA肾病的方法,该组合物包括以 “NEFECON®” 的名义开发的TARPEYO®(布地奈德)延迟释放胶囊 。因此,已申请在 Orange 书中列出。Calliditas打算在包括欧洲和 中国在内的全球其他地区提交相应的专利 申请。这本书就是这样写的。Calliditas打算在全球其他地区(包括 欧洲和中国)提交相应的 专利申请。 2024年3月6日Calliditas Therapeutics AB宣布,美国食品药品管理局已批准TARPEYO® 的 孤儿药独家经营期为七年,该期限将于 2030 年 12 月 到期,具体取决于该公司获得 该药物新适应症的全面批准。在 2023 年 12 月获得全面批准后,TARPEYO®(布地奈德)表示 “可减少 有疾病进展风险的原发性免疫球蛋白 A 肾病 (IGaN) 成人肾脏功能丧失”。排他期反映了新的 适应症,涵盖所有有疾病进展风险的原发性IgAn的成年患者,其依据是经证实的肾脏流失减少反映了原发性IgAn对成年患者肾功能的临床益处。 附注 32 质押资产、或有负债 和其他债务 根据集团与阿基米德签订的 协议,集团必须向协和麒麟服务有限公司(“阿基米德”)支付固定特许权使用费,金额为许可所涵盖的 Nefecon/Tarpeyo净销售额的3% (i) 与阿基米德 开发的联合知识产权的 独家许可,以及 (ii) 对阿基米德某些专有技术的非排他性许可,因为 对开发和将 Nevecon 或其他 候选产品商业化。 根据与阿基米德签订的许可协议,集团拥有使用、开发和销售配方 的专有权利,而阿基米德仅在产品销售时拥有 的特许权使用费。然后,在涵盖 Nevecon 配方的专利的独家许可于 2029 年到期之前,集团将有义务根据 净销售额支付较低的个位数百分比的特许权使用费。 截至2023年12月31日和2022年12月31日,该集团的质押资产分别为943,364瑞典克朗和6,859瑞典克朗。该年度的认捐 分别指截至2022年12月31日和2022年12月31日的限制性银行账户和租赁存款7,637瑞典克朗和6,859瑞典克朗。为 贷款人受益的其他质押资产是指截至12月31日对集团公司和 金融资产的参与为935,727瑞典克朗。 计息负债的财务契约,见附注20。 附注 31 关联方交易 有关执行管理层薪酬的信息,请参阅 附注 9 员工和人事成本和附注 10 基于股份的 付款。 与关联方没有其他协议或交易, 除附注 9 员工和人员成本和 10 基于股份的付款中所述的协议或交易外。 69Calliditas Therapeutics | 2023 年年度报告 |
| 收益表 综合收益表 截至12月31日的年度, (千瑞典克朗,每股金额除外)附注 2023 年净销售额 2 805,551 548,977 销售成本 (60,399) (15,141) 毛利 745,151 533,836 研发费用 7 (456,970) (384,453) 市场营销和销售费用 7 (402,436) (310,372) 管理费用 5,6,7 (273,359) (212,971) 其他营业收入 3 220,293 165,697 其他运营费用 4 (475) (7,101) 营业亏损 (167,796) (215,364) 财务利润/(亏损)项目 收到的其他利息及类似项目 8 42,626 43,259 利息支出及类似项目 9 (148,348) (36,443) 所得税前亏损 (273,518) (208,548) 所得税支出 10-- 年度亏损 (273,518) (208,548) 截至12月31日的年度(千瑞典克朗)2023 年票据 2022 年度亏损 (273,518) (208,548) 其他综合收益/ (亏损)- 综合亏损总额 (273,518) (208,548) 70Calliditas Therapeutics | 2023 年年度报告母公司 |
| 资产负债表 12 月 31 日, (千瑞典克朗)附注 2023 年资产 非流动资产 无形资产 许可证和类似权利 11 — 32,132 有形资产 设备 12 342 567 342 567 非流动金融资产 集团公司的非流动金融资产 13 450,904 425,589 应收账款 14 653,815 453,815 537 其他非流动金融资产 15 20,467 8,329 1,125,186 887,456 非流动资产总额 1,125,528 920,154 流动资产 库存 16 20,428 3,647 应收账款 49,777 6,877 应收账款 49,777 6,877 应收账款公司 164,441 115,676 其他流动资产 9,481 6,537 预付费用 17 67,603 61,092 311,730 193,830 193,830 现金 18 817,871 1,059,655 流动资产总额 1,129,602 1,253,485 总资产 2,255,130 2,173,639 71Calliditas Therapeutics | 2023 年年度报告母公司 |
| 资产负债表 12月31日, (千瑞典克朗)附注 2023 年股东权益与负债 股东权益 19 限制性股东权益 股本 2,383 2,383 3,092 3,092 5,475 5,475 非限制性股东权益 股票溢价准备金 2,521,419 2,521,419 留存收益 (1,343,602) (1,187,602) (1,187,602) 1) 年度净亏损 (273,518) (208,548) 904,299 1,125,481 股东权益总额 909,774 1,130,956 非流动负债 准备金 20 25,924 9,512 非流动计息负债 21939,508 713,030 对集团公司的负债 24 105 105 其他非流动负债 16,381 4,350 非流动负债总额 981,918 726,997 流动负债 应付账款 62,562 100,469 对集团公司的负债 24 110,175 138,173 其他流动负债 3,577 应计费用和递延收入 22 187,191 73,468 流动负债总额 363,468 438 315,686 股东权益和负债总额 2,255,130 2,173,639 72Calliditas Therapeutics | 2023 年年度报告母公司 |
| 股东权益变动表 受限制股东权益非限制性股东权益 (千瑞典克朗,每股金额除外)股本法定储备金 储备金 留存 收益 年度净亏损 2022年1月1日期初净亏损 2,094 3,092 2,420,698 (863,175) (354,175) (354,175) (354,175) (354,175) (354,175) (354,175) (354,175) (354,175) (354,175) (354,175) (354,175) 405) 1,208,303 上一年亏损的转移 — — — (354,405) 354,405 — 年度亏损 — — — (208,548) (208,548) 其他综合收益/ (亏损) — — — — — — — 总综合收益/ (亏损) — — —(208,548) (208,548) 与所有者的交易: 发行库存股 236 — — — — — 236 回购库存股 — — — -236 — -236 认股权证的行使 53 — 100 721 -5 654 — 95 121 股权支付 — — — 36 080 与所有者的交易总额 290 — 100,721 30,190 — 131,201 2022年12月31日收盘股权 2,383 3,092 2,521,419 (1,187,391) (208,548) 1,130,956 2023 年 1 月 1 日期初净资产 2,383 3,092 2,521,419 (1,187,391) (208,548) 1,130,956 转移 — — (208,548) 208,548 — 年度亏损 — — — (278,548) 3,518) (273,518) 其他综合收益/(亏损)— — — — — 总综合收入/(亏损)— — —(273,518)(273,518) 与所有者的交易: 基于股份的付款 — — — 52,337 — 52,337 与所有者的交易总额— — — 52,337 — 52,337 12月31日收盘股权,2023 2,383 3,092 2,521,419 (1,343,602) (273,518) 909,774 73Calliditas Therapeutics | 2023 年年度报告母公司 |
| 现金流量表 截至12月31日的年度, (千瑞典克朗)附注 2023 年经营活动 营业亏损 (167,796) (215,364) 非现金项目的调整 18 75,789 17,584 收到的利息 29,561 3,551 已付利息 (91,740) (33,648) 工作变更前来自经营活动的现金流资本 (154,186) (227,877) 营运资金变动产生的现金流 库存变动 (16,781) (2,758) 营业应收账款变动 (40,501) (144,845) 运营负债变动 53,716 212,279 现金流来自经营活动 (157,751) (163,201) 投资活动 购买设备 12 — (269) 非流动金融资产投资 14 (274,220) (282,391) 偿还非流动金融资产 14 — 1,948 投资活动产生的现金流 (274,220) (280,712) 融资活动 发行236股库存股 — 回购库存股 — (236) 行使认股权证 — 95,121 新借款 21 962,889 491,744 归属于新贷款的成本 (26,625) (1,260) 偿还借款 (724,479) — 运营现金流活动 211,784 585,605 现金净增加(减少)(220,187)141,691 年初现金 1,059,655 894,455 现金汇率差额(21,597)23,509 年末现金 18 817,871 1,059,655 74Calliditas Therapeutics | 2023 年年度报告母公司 |
| 附注1 会计政策 编制依据 母公司根据 年度账目法和瑞典公司利率报告委员会的建议 RFR 2 “法人实体会计” 编制了年度报告。 集团和母公司 会计政策之间的差异如下所示。除非另有说明,否则下述 母公司的会计政策一直适用于财务报表中列报的所有期间。 财务报表提供了 上一期间的比较信息。 子公司 子公司的参与是按历史成本计算的 在母公司中确认的,这意味着交易成本包含在 子公司参与的账面金额中。 金融资产和负债 由于会计与税收之间的关系,根据国际财务报告准则第9号制定的金融工具法规 不适用于作为法人实体的 母公司。母公司根据《年度账目法》采用历史 成本基础。出于这个原因, 金融资产在母公司中按成本减去任何 减值进行计量,金融流动资产按成本 和可变现净值的较低值计量。 租赁 母公司对合法 实体适用 RFR 2 中包含的豁免,并通过 损益表将所有租赁协议视为租赁期内的直线支出。 集团和股东缴款 根据替代规则,收到和提供的团体缴款均被视为拨款。股东的出资在接受者的股东权益中确认, 由出资人在 “集团公司参股” 中资本化,其中 不需要减值。 财务报表附注 (以千瑞典克朗计,每股金额或另行说明除外) 附注 7 员工和人事成本 有关员工和执行管理层的工资和福利以及 有关员工人数的信息,请参阅附注 9 集团员工 和人事成本。有关期权和 股权付款的信息,请参阅附注 10 集团基于股份的付款。 附注 6 租赁 截至2023年12月31日的年度和 2022年的年度与经营租赁有关的租赁费用分别为7,811瑞典克朗和6,310瑞典克朗。经营租赁的未来付款承诺为 具体说明如下: 截至 2023 年 12 月 31 日的年度未来最低租赁付款 1 年内 17,556 9,445 1-2 年之间 13,971 5,070 两年以上 10,478 — 共计 42,005 14,515 附注 5 审计师费 2023 年 12 月 31 日止年度 EY } 审计服务 20,951 12,215 其他审计活动 900 3,370 共计 21,851 15,585 审计服务与财务报表 和账目的法定审计以及董事会 和首席执行官的管理有关。这包括公司审计师 有义务履行的其他职责,包括提供建议或因此类审查中的观察或 履行此类其他职责而可能产生的任何 其他协助。 其他审计活动是根据财务报表特别 协议提供的服务。 附注 4 其他运营费用 截至 2023 年 12 月 31 日的年度汇率差额 475 7,101 合计 475 7,101 附注 3 其他营业收入 2023 年 12 月 31 日止年度 209,929 163,318 汇率差 10,364 — 其他收入 — 2,379 总计 220,293 165,697 附注 2 收入 截至2023年12月31日的年度 2023 年商品或服务类型 产品销售额 686,081 121,613 产品许可超过许可 82,712 421,689 特许权使用费收入 36,758 2,287 某些监管服务的业绩 — 3,387 总计 805,551 548,977地理市场 美国 674,492 118,345 欧洲 39,614 143,955 亚洲 91,445 286,677 共计 805,551 548,977 欲了解更多信息,请参阅附注3 该集团与客户签订合同的收入 。 75Calliditas Therapeutics | 2023 年年度报告 |
| 附注 12 设备 2023 年 12 月 31 日, 2022 年期初余额成本 795 526 年度收购-269 期末余额成本 795 795 期初余额折旧 (228) (12) 年度折旧 (225) (216) 期末余额折旧 (453) (228) 账面净值 342 567 附注 11 无形资产 12 月 31 日 许可证和类似权利 2023 年期初余额成本 32,132 32,132 年度处置 (32,132) — 期末余额成本 — 32,132 减值 期初余额减值 — — 减值 (32,132) — 32,132 年度的处置 — 期末余额减值 — — 账面净值 — 32,132 有关母公司无形资产的更多信息, 请参阅附注15集团无形资产和减值测试。 附注 10 所得税支出 截至 2023 年 12 月 31 日的年度当期所得税 — — 损益表中确认的所得税支出 — — 有效税率对账 税前会计亏损 (273,518) (208,548) 按母公司 适用税率征税 20.6% 56,345 445 442 961 税收影响: 归因于不可扣税款损失的税款 结转和未确认的递延 税收资产 (36,030) (34,371) 不可扣除的费用 (20,315) (8,590) 中确认的所得税支出 损益表-- 按实际所得税税率计算-- 母公司结转了1,769,195瑞典克朗和1,594,293瑞典克朗的税收损失 ,截至2023年12月31日和2022年12月31日的财务状况表 中分别未确认递延所得税资产。结转的税收损失不受时间限制。 递延所得税资产将确认未使用的税收损失,但前提是 很可能有可用 亏损的应纳税利润。 附注 9 利息支出及类似项目 截至12月31日的年度, 2023 年利息支出 70,386 31,569 提前偿还贷款 35,397 — 其他财务费用 5,753 4,874 汇率差额 36,812 — 共计 148,348 36,443 附注 8 收到的其他利息和类似项目 截至 2023 年 12 月 31 日的年度利息来自集团公司的收入 17,263 9,296 其他利息收入 25,363 3,551 汇率差异 — 30,412 合计 42,626 43,259 76Calliditas Therapeutics | 2023 年年度报告母公司-财务附注声明 (以千瑞典克朗计,每股金额或另有说明除外) |
| 附注 16 库存 2023 年 12 月 31 日原材料 9,058 1,855 在建工程 4,677 937 制成品 6,693 855 总计 20,428 3,647 附注 17 预付费用和应计收入 2023 年 12 月 31 日, 2023 年应计收入 7,297 2,287 预付租金 3,862 1,876 预付保险费 8,048 8,827 预付利息费用 — 3,693 研究 和开发的预付费用 43,085 43,472 其他预付的管理费用 5,311 937 总计 67,603 61,092 附注 15 其他非流动金融资产 2023 年 12 月 31 日, 2023 年期初余额8,329 3,762 额外收购 12,215 4,349 交易所差额 (77) 218 账面净值 20,467 8,329 其他收购与 产能未来增长密切相关。在现金流中,收购在 经营活动中报告。 附注 14 来自集团公司的应收款 2023 年 12 月 31 日, 2022 年期初余额 453,537 142,724 额外应收账款 289,582 296,928 应收账款的偿还-(1,948) 重新归类为流动应收账款 (83,478) (5,526) 汇兑差额 (5,826) 21,360 账面净值 653,815 453,537 附注 13 参与者集团公司 2023 年 12 月 31 日 2023 年 12 月 31 日按期初余额计算的成本 429,328 410,177 年度收购-- 股东出资 25,315 19,151 期末余额的成本 454,643 429,328 期初余额减值 (3,739) (3,739) 期末余额减值 (3,739) (3,739) 账面净值450,904 425,589股东的出资相当于子公司确认的基于股份的薪酬 。 12 月 31 日, 公司/公司注册号/ 注册办事处 2023 年 Nefecon AB,556604-9069,斯德哥尔摩 2023 年 2022 股权份额 100% 100% 参与权数量 100% 100% 账面净值 100 100 Calliditas Therapeutics NA Enterprice Inc., 83-4094951,美国 100% 股权份额 投票权份额 100% 100% 参与权数量 1,000 1,000 账面净值 44,264 27,107 Calliditas Therapeutics US Inc.,86-3169403 美国 股权份额 100% 100% 投票份额权力 100% 100% 参与权数量 1,000 1,000 账面净值 10,507 3,313 Calliditas Therapeutics France SAS,439 489 022,法国 股权份额 100% 100% 参与权数量 14,074,165 14,074,165 账面净值 396,033 395,069 77Calliditas Therapeutics | 2023 年年度报告 |
| 附注 24 关联方交易 子公司 商品/ 服务的销售 购买 商品/ 服务其他 应收账款 期末余额 负债 截至年度 12 月 31 日, 2023 年 879,645 437,786 — 818,256 ,280 截至2022年12月31日 282,288 332,971 — 569,213 138,278 有关执行管理层薪酬的信息,请参阅 集团的附注9员工和人事成本。 附注 23 质押资产和或有负债 有关 母公司质押资产和任何或有负债的信息,可在集团附注32质押资产、 或有负债和其他债务中找到。截至2023年12月31日和2022年12月31日,母公司 的限制性银行账户和租赁存款分别为3,902瑞典克朗和 3,987瑞典克朗,截至2023年12月的 ,用于贷款人的其他 质押资产为1,342,414瑞典克朗。其他质押资产是指参与集团 公司和金融资产。 附注 22 应计费用和递延收入 2023 年 12 月 31 日 2022 年应计工资和董事会费用 13,201 10,094 假期工资负债 6,123 5,475 社会保障成本 8,688 675 特许权使用费应计支出 37,419 12,023 研发应计费用 106,964 33,642 营销和销售应计费用 — 418 管理费用 14,796 4,941 合计 187,191 73,468 附注 21 非流动计息负债 2023 年 12 月 31 日 2023 年 1 至 5 年内到期 非流动计息负债 非流动计息负债负债939,508 713,030共计939,508 713,030欲了解更多信息,请参阅附注20集团财务风险。 附注 20 条款 2023 年 12 月 31 日, 2023 年期初余额 9,512 9,075 年度的准备金 16,411 641 年度的索赔额 — (204) 共计 25,924 9,512 有关母公司准备金的更多信息,请参阅集团备注 26 条款。 附注 19 股东权益 截至2023年12月31日,股本由59,580,087股组成,其中 5,908,18股由Calliditas持有。截至 2023 年 12 月 31 日,股本为 59,580,087。截至2023年12月31日和2022年12月31日的商值分别为0.04瑞典克朗和0.04瑞典克朗 0.04瑞典克朗。除Calliditas持有的无权获得公司股息的库存 股外,所有股票都拥有相同的公司利润权利。 欲了解更多信息,请参阅集团的附注25股权。 股票溢价储备是指 发行的新股所产生的资本,其发行价格超过商值减去归因于新股发行的成本 。 拟议收益拨款 以下收益可供年度股东大会支配: 2023 年 12 月 31 日 2022 年股票溢价储备 2,521,419 2,521,419 留存收益 (1,343,602) (1,187,391) 年度净亏损 (273,518) (208,548) 904,299 1,125,481 至分配方式如下: 待结转 904,299 1,125,481 附注 18 现金 2023 年 12 月 31 日, 2023 年 12 月 31 日 817,871 1,059,655 共计 817,871 1,059,655 非现金项目调整: 2023 年 12 月 31 日折旧 32,356 217 变动在条款中 16,411 438 股权支付 27,022 16,929 共计 75,789 17,584 对账融资活动负债: 2023 年 1 月 1 日, 非现金项目 2023 年 12 月 31 日, 非流动 计息 负债 713,030 211,785 14,693 939,508 总计 739,508 13,030 211,785 14,693 939,508 1 月 1 日, 2022 年现金流 非现金项目 12 月 31 日, 2022 年非流动 计息 负债 189,164 490,485 713,030 78Calliditas Therapeus Tics | 2023 年年度报告 PARENT公司——财务报表附注 (千瑞典克朗,每股金额或另有说明除外) |
| 下列签署人声明,年度报告是根据瑞典普遍接受的 会计原则编制的,这些合并财务报表是根据欧盟(EU)通过的《国际财务报告准则》(R)会计准则编制的。年度报告和合并财务报表分别为集团和母公司的财务状况和收益 提供了公允而准确的印象。 母公司和集团董事会报告真实而公允地描述了母公司和集团的运营、状况和业绩,并描述了母公司和集团所含公司面临的重大风险 和不确定性。 斯德哥尔摩,2024 年 4 月 24 日 Elmar Schnee 董事会主席 Renee Aguiar-Lucander 首席执行官 伊丽莎白·比约克 董事会成员 Frederic Driscoll 董事会成员 Henrik Stenqvist 董事会成员 Henrik Stenqvist br} 董事会成员 我们的审计报告已于 2024 年 4 月 24 日提交 Ernst & Young AB Jakob Grunditz 授权会计师 79Calliditas Therapeutics | 2023 年年度报告 |
| 年度账目和合并账目报告 意见 我们已经审计了Calliditas Therapeutics AB(publ)2023年 的年度账目和合并账目。公司的年度账目和合并 账目包含在本文件第32-79页中。 我们认为,年度账目是 根据《年度账目法》编制的 ,并在所有重大方面公允地列报了母公司截至2023年12月31日的财务 状况以及截至当日年度 年度的财务业绩和现金流,根据《年度 账户法》。合并账目是根据《年度账目法》 编制的,并在所有重大方面公允列报了集团截至2023年12月31日的财务 状况以及 当时根据欧盟通过的国际金融 报告准则(IFRS)和 《年度账目法》结束的年度财务业绩和现金流。法定管理 报告与年度 账户和合并账户的其他部分一致。 因此,我们建议股东大会 通过母公司的损益表和 资产负债表以及 集团的损益表和财务状况表。 我们在本报告中对年度账目和 合并账目的意见与根据 《审计条例》(537/2014)第11条提交给 母公司审计委员会的补充报告的内容 一致。 意见依据 我们根据国际审计准则(ISA)和瑞典公认的 审计准则进行了审计。审计师职责部分进一步描述了我们在这些标准下的责任 。根据瑞典会计师职业道德 ,我们 独立于母公司和 的集团,并在其他方面根据这些要求履行了我们的道德 责任。 这包括,根据我们所知 和信念, 审计条例(537/2014)第5.1条中提及的 未向被审计公司或 其母公司或其在欧盟 境内的控股公司提供(如适用)中提及的违禁服务。 我们认为,我们获得的审计证据 足以为我们的 意见提供依据。 关键审计事项 审计的关键审计事项是那些根据我们的专业判断, 在我们对当期年度账目和合并 账目的审计中最为重要的事项 。 在我们对年度账目和整个合并账目进行审计和构成 意见的背景下解决了这些问题,但我们没有就这些事项提供 个别意见。对于下面的每个问题 ,我们对审计如何处理 事项的描述都是在这种背景下提供的。 我们已经履行了 审计师对我们报告财务 报表的审计责任部分中所述的职责,包括与这些事项有关的 。因此,我们的审计包括 程序的执行情况,该程序旨在回应我们对 财务报表重大错报风险的评估。我们的审计程序结果,包括为解决 以下事项而采取的程序,为我们对所附财务报表的审计 意见提供了依据。 审计师报告 致Calliditas Therapeutics AB股东大会,公司标识号为556659-9766 80Calliditas Therapeutics | 2023年年度报告审计师报告 |
| 收入确认的可变对价的估计 描述 如合并财务 报表附注3所述,截至2023年12月31日的财年, 集团的产品销售收入为1,087,418万瑞典克朗。正如附注 2 和 3 中更全面地描述的那样,商品销售收入是扣除向政府 付款人提供的实际和预计回扣以及其他扣除额后计算得出的。集团于 2023 年 12 月 31 日确定可变对价 要求管理层假设 由于出售控制权已转让 的产品而将由集团 支付的返佣金额。 我们确定收入确认的可变对价 的估计是一个关键的审计事项,因为 审计管理层对可变考虑因素的估计很复杂,因为该计算涉及到 管理层的重大判断,以确定应付给政府付款人的 返利。 我们的审计如何解决这一关键审计问题 为了测试可变对价的估计,我们的 审计程序包括执行 分析程序,通过将先前对付款人返佣的估计值与后续时期的实际 付款金额进行比较,评估管理层估计值的历史准确性 。在可能的情况下, 我们测试了管理层截至 2023 年 12 月 31 日的估计,并将之与随后收到的实际发票进行比较。我们还测试了集团在 确定预计付款人组合时使用的发放数据的完整性和 准确性,即 同意第三方数据。 我们聘请了具有政府定价 主题经验的专业人员来协助评估 管理层用于 衡量应付给政府付款人的回扣的方法和计算方法。 我们审查了年度 报告中提供的披露。 81Calliditas Therapeutics | 2023 年年度报告 |
| 无形资产减值评估 描述 截至2023年12月31日,集团的无形资产总额为430,754万瑞典克朗。正如 合并 财务报表附注2和附注15所解释的那样,集团每年或在有迹象表明资产可能减值时,对尚未可供使用 的无形资产进行减值评估。集团对无形资产的减值评估包括 将每项资产或 现金产生单位的可收回金额与其账面价值进行比较。 无形资产的可收回金额是根据概率调整后的现金流 模型估算的,该金额是通过估计 预期的未来现金流和现值 调整(包括进入 市场的概率)来确定的。管理层 使用的假设变更可能会对可收回的 金额产生重大影响。 我们确定无形资产的减值评估是关键的审计事项,因为审计 对无形资产的减值评估很复杂,这是因为 管理层做出了估算可收回金额的重大判断, 包括与潜在商业化时机、市场规模、 进入市场的概率和使用的折扣率相关的假设。 我们的审计如何解决这一关键审计问题 我们执行了与无形资产减损评估相关的审计程序,其中包括 评估管理层的方法, 测试管理层在假设中使用的输入 的完整性和准确性,包括 潜在商业化的时机、预期的 市场规模和产品到达 市场的概率。为此,我们将这些输入与 目标临床适应症以及 行业内其他开发项目的 第三方统计数据进行了比较。 在估值专家的协助下,我们 评估了贴现现金流方法 ,并通过与基础来源 信息进行比较,测试 计算的数学准确性,根据市场和同行公司的可观测数据 和 与管理层使用的数据进行比较来评估折扣现金流方法 并评估了在使用价值 中使用的折扣率。 我们审查了年度 报告中提供的披露。 82Calliditas Therapeutics | 2023 年年度报告审计师报告 |
| 除年度账户和 合并账户以外的其他信息 本文档还包含除 年度账户和合并账户以外的其他信息, 位于第 1-31 页和 88-103 页。董事会和 董事总经理对这些其他 信息负责。 我们对年度账目和合并 账户的意见不包括这些其他信息, 我们没有就这些其他信息发表任何形式的保证结论 。 在审计年度账目和 合并账户时,我们的责任是阅读上述 信息,并考虑 信息是否与年度 账户和合并账户存在重大不一致。在本程序 中,我们还考虑了我们在审核中获得的其他 知识,并评估这些信息是否存在重大误报。 如果我们根据就此 信息所做的工作得出结论,认为该其他信息存在重大误报,则我们需要报告 该事实。我们在这方面没有什么可报告的。 董事会和董事总经理的责任 董事会和董事总经理 负责编制年度账目 和合并账目,并根据《年度账目 法》以及欧盟通过的《国际财务报告准则》在合并账目方面提供公平的 列报。 董事会和董事总经理还负责进行内部控制,因为他们认为 是编制年度账目 和合并账目所必需的,这些账目不存在因欺诈或错误而出现的重大 误报。 在编制年度账目和合并 账目时,董事会和经理 董事负责评估 公司以及集团继续作为经营 企业的能力。他们酌情披露与持续经营有关的 事项,并使用 会计的持续经营基础。但是,如果董事会和 董事总经理打算清算公司、 停止运营或者除了 之外别无选择,则持续经营会计基础不适用。 审计委员会应在不影响 董事会总体责任和任务的前提下, 除其他事项外,监督公司的财务 报告流程。 审计师的责任 我们的目标是合理保证 整个年度账目和合并账户 是否存在重大误报, 是由于欺诈还是错误造成的,并发布一份包含我们意见的审计报告 。合理保证是 高水平的保证,但不能保证根据瑞典国际审计准则和普遍接受的审计准则进行的 审计总能发现 存在重大误报。错误陈述可能源于欺诈或错误,如果可以合理地预期错误陈述会影响用户在这些年度 账户和合并账户基础上做出的经济 决策,则将其视为实质性的 。 作为根据 ISA 进行审计的一部分,我们行使 专业判断力,并在整个审计过程中保持专业怀疑态度。我们还会: • 识别和评估年度账目和合并 账户因欺诈或错误而出现重大误报的风险,设计 并执行针对这些 风险的审计程序,并获取足够 且适当的审计证据,为我们的意见提供依据。 由于欺诈可能涉及串通、伪造、 故意遗漏、虚假陈述或 推翻内部控制,因此未发现欺诈导致的重大错误陈述的风险高于 由错误导致的重大误报。 • 了解与我们的审计相关的公司内部 控制,以便设计适合具体情况的 审计程序,但其目的不是对公司 内部控制的有效性表示 的意见。 83Calliditas Therapeutics | 2023 年年度报告 |
| • 评估所使用的会计政策 的适当性以及 董事会和董事总经理的会计估算和相关披露的合理性。 • 就 董事会和董事总经理在编制 年度账目和合并账目时使用 持续经营会计基础的适当性得出结论。我们 还根据获得的审计证据 得出结论,说明是否存在与可能使公司和 集团继续作为持续经营企业的能力产生重大怀疑的事件或条件相关的任何重大不确定性。如果我们 得出结论认为存在重大不确定性,则我们 必须在审计师报告中提请注意 年度账目和 合并账目中的相关披露,或者,如果此类披露不足,则修改我们对年度 账户和合并账目的看法。我们的结论基于截至我们的审计报告发布之日获得的 审计证据。但是,未来的 事件或情况可能会导致公司和 集团停止继续作为持续经营企业。 • 评估年度账目和合并 账户的总体列报方式、结构和 内容,包括披露内容,以及 年度账目和合并账目是否以 方式代表标的交易和事件,以实现公平列报。 • 获取有关实体 的财务信息或集团内部业务活动的充足和适当的审计证据 ,以表达 对合并账目的意见。我们 负责集团审计的指导、监督和绩效。我们仍然对自己的意见负全部责任。 除其他 事项外,我们必须向董事会通报审计的计划范围和时间。我们 还必须告知我们 审计期间的重大审计结果,包括我们发现的内部 控制中的任何重大缺陷。 我们还必须向董事会提供一份 声明,表明我们遵守了有关独立性的相关道德 要求,并与他们沟通 可能合理地认为会影响我们独立性的所有关系和其他事项,并在适用的情况下,为消除 威胁而采取的行动或适用的相关保障措施。 根据与 董事会沟通的事项,我们确定在年度账目 和合并账目审计中最重要的 事项,包括最重要的重大错报评估风险,因此 是关键审计事项。除非法律或法规 禁止披露这些 事项,否则我们会在审计师的报告中描述这些 事项。 84Calliditas Therapeutics | 2023 年年度报告审计师报告 |
| 关于其他法律和监管要求的报告 关于行政部门审计和公司损益拟议拨款的报告 意见 除了我们对年度账目和 合并账目的审计外,我们还审计了Calliditas Therapeutics AB(publ) 董事会和 董事总经理在2023年和2023年的 管理层 公司损益的拟议拨款。 我们建议股东大会 根据法定管理报告中的 提案拨出利润, 解除董事会成员和 董事总经理在 财政年度的责任。 意见依据 我们根据瑞典普遍接受的 审计准则进行了审计。审计师职责部分进一步描述了我们在这些标准下的责任 。根据瑞典会计师职业道德 ,我们 独立于母公司和 的集团,并在其他方面根据这些要求履行了我们的道德 责任。 我们认为,我们获得的审计证据 足以为我们的 意见提供依据。 董事会和管理董事的责任 董事会负责提案 拨出公司损益。在 的分红提案中,这包括评估 分红是否合理,考虑公司和集团 的业务类型、规模和风险对 母公司和集团的股权规模、合并要求、流动性和总体状况的要求。 董事会负责公司的 组织和公司 事务的管理。除其他外,这包括对公司和集团的财务 状况进行持续 评估,并确保公司的组织 的设计能够以令人放心的方式控制 资产的会计、管理以及公司其他方面 的财务事务。管理层 董事应根据董事会的指导方针和 的指示管理正在进行的管理 ,除其他事项外,应采取必要措施 ,以依法完成公司会计 ,并以令人放心的方式处理 资产的管理。 审计师的责任 我们关于行政部门审计的目标,以及我们对解除 责任的看法,是获取审计证据,以 合理的保证评估董事会成员或董事总经理在 任何重大方面是否有任何成员: • 已采取任何行动或犯有任何 疏忽的罪行向 公司追究责任,或 • 以任何其他方式违反了 公司法、《年度账目法》或 条款协会的。 我们对拟议的 公司损益拨款的审计,以及 因此我们对此的看法,是以 合理的保证评估提案 是否符合《公司法》。 合理保证是一种高水平的保证,但是 并不能保证在瑞典 按照公认的审计准则进行的审计总能发现 可能导致公司责任的行为或不作为,或者 拟议的公司损益拨款 不符合《公司法》。 作为根据瑞典普遍接受的 审计准则进行审计的一部分,我们行使 专业判断力,并在整个审计过程中保持专业偏见。对 管理和 85Calliditas Therapeutics 拟议拨款的审查 | 2023 年年度报告 |
| 审计师对ESEF报告的审查 Opinion 除了我们对年度账目和 合并账目的审计外,我们还审查了 董事会和董事总经理 已按照 {第 16 章第 4 (a) 节采用统一电子报告( Esef 报告)的格式编制了年度账目和合并账目 br} Calliditas Therapeutics AB 2023 财年的《瑞典证券市场法》(2007:528)。 我们的审查和意见仅与法定要求有关。 我们认为,Esef报告是以 的格式编写的,这种格式在所有重要方面都支持统一的 电子报告。 意见依据 我们根据 FAR 的建议进行了审查 revR 18 对ESEF 报告的审查。审计师责任 部分详细描述了我们在该建议下的责任。根据瑞典会计师的职业道德,我们独立于Calliditas Therapeutics AB,并在其他方面根据这些要求履行了我们的道德 责任。 我们认为,我们获得的证据足以为我们的观点提供依据。 董事会和董事总经理的责任 董事会和董事总经理 负责根据瑞典 证券市场法(2007:528)第 16 章第 4 (a) 款编写 中的 Esef 报告,并负责董事会和管理层 的内部 控制董事决定在编写 Esef 报告时必须避免重大误报,无论是因为 欺诈还是错误。 审计师的责任 我们的责任是根据所执行的程序,获得合理的保证 Esef报告在所有重要方面 是否以符合《瑞典证券市场法》(2007:528)第16章第4(a)节的要求的格式编写。 RevR 18 要求我们规划和执行程序 ,以合理保证 Esef 报告 以符合这些要求的格式编写。 合理保证是一种高水平的保证,但是 它并不能保证根据 RevR 18 和瑞典公认的审计 标准进行的 业务在存在时总能发现重大的 错误陈述。 错误陈述可能源于欺诈或错误,如果可以合理地预计 会影响用户在 Esef 报告基础上做出的经济决策,则这些错误陈述可以被视为实质性陈述。 公司的盈亏主要基于对账户的审计 。执行的其他审核程序 基于我们的专业判断,从 点开始是风险和重要性。这意味着我们 将审查的重点放在对运营至关重要以及 偏离和违规行为对公司状况特别重要的行动、领域和关系上。我们会审查和测试作出的 决定、对决定的支持、所采取的行动 以及与我们关于免责的 意见相关的其他情况。作为我们对董事会提议 拨款公司损益的意见的依据,我们研究了该提案是否符合 公司法。 86Calliditas Therapeutics | 2023 年年度报告审计师报告 |
| 斯德哥尔摩 2024 年 4 月 24 日 Ernst & Young AB Jakob Grunditz 授权会计师 审计公司对财务报表进行审计或审查或其他要求公司设计、实施 和运营质量管理体系,包括 有关遵守 专业人员的政策和程序,采用 ISQM 1 质量管理道德要求、专业标准 和适用的法律和监管要求。 审查涉及通过 各种程序获取证据,证明Esef报告的编制格式为 ,可以对年度账目和合并账目进行统一的电子 报告。所选择的 程序取决于审计师的判断,包括对报告中因欺诈或 错误而导致的重大 错误陈述风险的评估。在进行风险评估时,为了 设计适合 情况的审计程序,审计师会考虑与董事会和管理 董事编写 Esef 报告有关的 内部控制要素,但其目的不是就这些内部控制的有效性发表意见 。考试还包括评估 董事会和董事总经理做出的假设的适当性 和合理性。 程序主要包括验证Esef 报告是否以有效的XHTML格式编写,以及对Esef报告与经审计的年度 账目和合并账目进行对账。 此外,程序还包括评估是否根据Esef 法规的规定将Esef报告中的合并财务 业绩、财务状况、权益变动、现金 流量和披露表标有 为ixBRL。 安永会计师事务所,Hamngatan 26,111 47 斯德哥尔摩, 在 2023 年 5 月 30 日的股东大会上被任命为 Calliditas Therapeutics AB 的审计师,自 2004 年 4 月 15 日起担任该公司的审计师。 87Calliditas Therapeutics | 2023 年年度报告 |
| 公司治理报告 简介 Calliditas Therapeutics AB(publ),“Calliditas” 是一家 瑞典上市有限责任公司,注册办事处设在斯德哥尔摩。该公司的股票于2018年6月29日在斯德哥尔摩纳斯达克上市, 于2020年6月5日在美国纳斯达克环球精选上市, 的股票交易代码分别为CALTX和CALT。这份 报告涉及2023财政年度, 已由公司的审计师审查。 背景 公司治理是指股东通过 直接或间接控制 公司的系统。良好的公司治理是为Calliditas股东创造价值的努力中必不可少的一部分。Calliditas的公司治理基于 瑞典法律、纳斯达克斯德哥尔摩的发行人规则手册 以及内部规章制度。该公司 还适用瑞典公司治理守则 (“守则”)。该守则适用于所有股票在 瑞典 监管市场上市的瑞典公司。公司无需遵守《守则》的所有 规则,因为《守则》本身提供了偏离规则的机会,前提是 对任何 此类偏差以及选择的替代解决方案进行描述,并在公司 治理报告中解释原因(根据遵守或解释 原则)。但是,该公司在当年 期间没有偏离 守则中制定的任何规则。根据美国证券交易委员会 (SEC)制定的法规,该公司被归类为外国私人 发行人(FPI),因此遵循 国内市场的市场惯例,即瑞典公司治理。 重要规章制度示例 重要的内部规章制度 • 公司章程 • 董事会和 委员会的议事规则 • 首席执行官指令 • 政策文件 重要外部规章制度 • 瑞典和国际会计立法 • 纳斯达克斯德哥尔摩发行人规则手册 • 纳斯达克美国发行人规则手册 • 瑞典公司治理守则 • 萨班斯-奥克斯利法案 股东 Calliditas的股票是2018年6月获准在斯德哥尔摩纳斯达克 中型股上市,并于2020年6月5日获准在纳斯达克全球 Select上市。截至2023年底,Calliditas拥有 18,807(18,585)名股东,十大股东拥有所有已发行股份的47.0(48.3)%, 不包括Calliditas持有的股份。截至2023年12月31日,BVF Partners LP、Linc AB和Stiftelsen Indus-Trifonden是这家 公司的单一最大股东,分别占资本的10.5%、10.0%和5.3%。 股息政策 该公司迄今尚未支付任何股息。任何 未来的股息及其规模将根据Calliditas的长期增长、收益趋势和资本 要求确定 。董事会 认为,Calliditas应优先考虑发展计划的进展 和美国 TARPEYO的商业化,因此,财务资源 应主要用于为Calliditas的开发计划和商业化活动提供资金。鉴于 公司的财务状况和负收益, 董事会不打算在公司产生长期 可持续利润和正现金流之前提议 任何股息。就拟议的分红而言,股息 应与 在业务风险方面进行平衡。 年度股东大会 参与年度股东大会的权利 希望参加年度 股东必须在会议前六个工作日的 列入瑞典欧洲结算组织保存的股东名册, 并在召开 会议的通知规定的日期之前 将其参与情况通知公司通知中规定的日期通知公司。股东可以亲自或通过代理人出席股东会议,最多可以有两名助手陪同。通常, 股东可以通过几种不同的方式注册年度股东大会 ,如 会议通知中所示。股东可以投票选出股东拥有或代表的所有公司 股份。 股东周年大会通知应在《瑞典公司法》(2005:551)规定的时间内 在瑞典的 官方公报和公司的网站上发布。将在 Svenska Dagbladet 中宣布已发布通知。 88Calliditas Therapeutics | 2023 年年度报告 |
| 2024年年度股东大会 Calliditas的2024年股东大会将于2024年6月17日星期一下午14点在斯德哥尔摩Klarabergsvia-Dukten 90的Klara Konferens举行。 股东周年大会的会议纪要将在 www.calliditas.se 上公布。 参加年度股东大会 年度股东大会的通知中将提供有关参与年度股东大会 会议的信息。该通知将在年度股东大会 前四周不晚于 分发,并将在www.calliditas.se上公布。 希望在股东周年大会之前提出 事项的股东必须向 董事会提交书面申请。通常,董事会必须不迟于会议前七周 收到此类请求。 提名委员会 适用《守则》的公司应设立提名 委员会。根据该守则,股东周年大会应 任命提名委员会成员或 决定任命成员的程序。根据《守则》, 提名委员会应由至少三名成员组成,其中大多数 应独立于 Calliditas 和 集团管理层。此外,提名委员会中至少有一名成员 在 的表决权方面应独立于 的最大股东或在公司管理层的 方面进行合作的股东群体。 在 2017 年 9 月 14 日举行的 特别股东大会上,决定提名国委员会应由董事会主席 以及三大股东各有一名代表组成,其基础是 截至本财年第三季度末在 Calliditas 的所有权。 2024 年的提名委员会包括: • 帕特里克·索博基,由 Stiftelsen Industrifonden 任命 • 斯派克·洛伊,由 BVF 任命 • 卡尔·托比森,由 Linc AB 任命 • 董事会主席埃尔玛·施尼 如果三大股东中的任何一位放弃 任命一名代表的权利提名委员会,此类权利应转让给股东,而股东继而成为Calliditas的最大 股东,仅次于这三个股东。董事会应 召集提名委员会。代表最大股东的成员 应被任命为提名委员会主席,除非 提名委员会一致任命其他人 。如果最迟在股东周年大会前三个月 已任命提名委员会代表的股东不再是三大股东中的 ,则该股东任命的 代表应 辞职,当时属于三个 大股东的股东有权任命一名 名代表加入提名委员会。除非 有其他具体原因, 但是,如果 所有权的变更微不足道或发生在股东周年大会之前的三个月期间,则提名委员会的组成应保持不变。如果股东 成为三大股东之一,原因是 在股东周年大会前三个月 发生重大所有权变动,则在任何情况下,这个 股东都有权 参与提名委员会 的工作并参加其会议。如果成员在其 工作完成之前辞去提名委员会的 职务,则任命 该成员的股东应任命一名新成员,除非 该股东不再是三大 股东之一,在这种情况下, 轮的最大股东应任命替代成员。已任命提名 委员会代表的股东 有权解除该代表的职务并任命新的代表。 提名 委员会组成的变更应立即宣布。提名委员会任期 在 下一个提名委员会被任命时结束。 提名委员会应履行《守则》中规定的 职责。 提名委员会将成立, 将在2024年股东周年大会之前举行会议,其提案 将在股东周年大会的召集通知 和Calliditas的网站上公布。股东可以在股东周年大会之前,按照公司 网站www.calliditas.se上发布的内容向提名委员会提交 提案。 审计师 根据公司章程,Callid-itas必须任命注册会计师事务所作为 外部审计师。2023 年股东大会选出了注册的 89Calliditas Therapeutics | 2023 年年度报告 |
| 会计师事务所安永会计师事务所担任审计师,截至 2024年股东大会。负责审计师是雅各布·格伦-迪茨。审计师代表 年度股东大会审查母公司和 集团的账目和管理。对母公司 和集团账目以及董事会和首席执行官的 管理的外部审计是使用瑞典公认的 审计准则进行的。公司委托 审计师在 2023 年审查一份符合《守则》要求的中期报告 。有关 有关审计师薪酬的信息,请参阅 附注 6 审计师费。 董事会 董事会是公司继股东周年大会之后的第二高决策机构。 根据《瑞典公司法》, 董事会负责Callid-itas的组织和公司事务的管理, 这意味着董事会负责 除其他外,设定目标和战略, 确保评估设定 目标的程序和系统,持续评估财务状况 和利润以及评估运营情况管理。董事会还负责 确保 及时编制年度报告和中期报告。此外, 董事会任命首席执行官。 董事会成员通常由股东周年大会任命 ,任期至下一次 年度股东大会结束为止。根据Calliditas的公司章程,由股东周年大会选出 的董事会成员应不少于三名且不超过十名 成员, 董事会没有副成员。 根据《守则》,董事会主席 将由股东周年大会选出,并负有 特殊责任,负责领导董事会 的工作并确保 董事会的工作得到有效组织。 董事会适用书面议事规则,该议事规则每年修订并由 的首次董事会会议通过。除其他 规定外,议事规则规定了 董事会的做法、职能以及 董事会成员与 CEO 之间的工作分工。在 首次董事会会议上,董事会还 采纳了对 CEO 的指示,包括 的财务报告指令。 董事会根据每年 预先确定的时间表举行会议。除了这些会议外,还可以召开 额外的董事会会议来处理 问题,这些问题不能推迟到下一次普通董事会会议。除了董事会会议外, 董事会主席和 CEO 还不断讨论公司的管理问题。 目前,公司董事会由股东周年大会选出的六名普通成员组成。 董事会独立性 公司符合《守则》的要求,因为 股东大会选出的大多数董事会成员 独立于公司和管理层,而且 其中至少有两名与 大股东的关系是独立的。下表显示了本 报告发布之日成员的 独立性。 2023 年董事会成员的独立性、出席率和薪酬 与出席情况无关 姓名职位 董事会成员 自 起公司 和 管理层 主要股东 董事会 会议 会议 会议 总薪酬 , 千瑞典克朗 2019 年 Elmar Schnee 董事会主席 2019 年是的 13/13-5/5 1,738 Hilde Furberg 董事会成员 2014 是是 13/13 11/11-731 Diane Parks 董事会成员 2019 是是 13/13-5/5 796 莫莉·亨德森 (直到 2023 年 5 月) 2020 年董事会成员是是 5/5 5/6-316 Henrik Stenqvist 董事会成员 2022 是是 8/13 11/11-761 伊丽莎白·比约克董事会成员 2022 是是 13/13-5/5 586 弗雷德·德里斯科尔 (从 2023 年 5 月起) 董事会成员 2023 是是 8/8 5/5-387 90Calliditas Therapeutics | 2023 年年度报告公司治理报告 |
| 2023 年董事会的工作在 2023 年期间,董事会共举行了 13 次会议,其中 10 次是普通会议,3 次是 次特别会议。Calliditas的首席执行官参加 董事会会议,公司的首席财务官和担任会议秘书的 总法律顾问也参加董事会会议。 来自Calliditas的其他员工在会议上报告了 的特定问题。 董事会薪酬 董事会费用应向董事会主席支付 940,000 瑞典克朗,向未在集团工作的每位其他成员支付 365,000 瑞典克朗,向 审计委员会主席支付 200,000 瑞典克朗,向 未在集团工作的审计委员会其他成员支付 100,000 瑞典克朗,以及 50,000 瑞典克朗 薪酬委员会主席,向未在集团工作的薪酬 委员会其他成员发放25,000瑞典克朗 。 除了上述提议的普通董事会工作的薪酬外,还建议居住在美国的董事会成员 额外获得14万瑞典克朗的 ,居住在欧洲但北欧以外的董事会成员 应额外获得50,000瑞典克朗。有关董事会成员薪酬的更多 信息, 请参阅附注 9 员工和人事成本。 董事会委员会 审计委员会 Calliditas 的审计委员会由三名 成员组成:亨里克·斯滕克维斯特(主席)、弗雷德·德里斯科尔 和希尔德·弗伯格。审计委员会应在不影响董事会 职责和任务的前提下,监督公司的财务报告, 监控公司内部 控制、内部审计和风险管理的效率,向 通报年度报告和 合并账目的审计情况,审查和监督审计师的公正性和独立性,并密切关注 除了为公司提供审计服务外,审计师是否在提供其他 服务,以及 协助为股东周年大会关于选举审计师的 决定起草提案。 委员会在 2023 年举行了 11 次会议。 公司的审计师参加了其中五次会议, 会议的讨论包括审计师对 审计的规划、他们对 公司和公司财务报表的观察和审查以及 对财务报告的内部控制。 薪酬委员会 Calliditas的薪酬委员会由三名成员组成:埃尔玛·施尼(主席)、伊丽莎白 比约克和黛安·帕克斯。薪酬委员会 应为 首席执行官和执行管理层准备与薪酬原则、薪酬和其他雇佣条款有关的事项。 委员会在 2023 年举行了五次会议。在这些 会议上,委员会讨论了公司当前的 薪酬体系,包括 首席执行官和高级 高管薪酬提案以及激励 计划的方向和条款,该计划已于 2023 年 5 月 30 日由 年度股东大会批准实施。 首席执行官和高管 管理层的薪酬 2024年股东周年大会提出了以下关于首席执行官和执行管理层薪酬的原则 。Calliditas应根据市场惯例以 提供薪酬,以便招聘和留住合格的执行管理人员。Calliditas内部的薪酬应以 绩效、竞争力和 公平原则为基础。执行管理层将首席执行官 和执行管理层的其他成员称为 以及董事会成员。执行管理层的薪酬可能包括固定薪酬、 可变薪酬、股票和股价相关的 激励计划、养老金和其他福利。如果当地 条件证明薪酬原则的变化是合理的,则可能会发生这种差异。固定薪酬 应反映个人的责任和经验水平。应每年对固定薪酬进行审查 。执行管理层可能会获得 现金奖励。以现金支付的可变薪酬 不得超过年度固定薪酬的80%。 可变薪酬应与预先确定和可衡量的标准相关联,其设计目的是 促进公司的长期价值创造。 与股票和股价相关的激励计划, 如果决议通过,则应由股东周年大会决定。 在可能的情况下,养老金应以保费为基础。对于首席执行官和 其他执行管理层成员,在 适用保费型养老金的情况下,保费 最多可达固定 工资的30%。尽管如此,董事会有权提供其他解决方案,就成本而言,这些解决方案与 相同。 对董事会和首席执行官的评估 每年,董事会主席都会启动对 董事会工作的评估。评估旨在征求董事会成员对 董事会工作进展情况以及可以采取哪些措施来提高董事会效率的看法 的意见。 的目的还在于就董事会的问题类型征求意见 91Calliditas Therapeutics | 2023 年年度报告 |
| 认为应该为董事会提供更多空间和可能需要 更多专业知识的领域。 董事会通过对照既定目标监控运营绩效来持续评估 CEO 的工作,并每年进行 正式评估。 首席执行官和管理团队 首席执行官的角色隶属于 董事会,他或她的主要任务是处理 公司在 公司的日常管理和运营。董事会决策程序规则 和 CEO 的指示提出 哪些问题需要公司董事会 考虑和决定,哪些是 CEO 的责任。首席执行官还负责 在董事会会议之前为 决策准备报告和所需文件,并且是董事会会议材料的 报告人。 Calliditas的管理层由七人组成 ,除首席执行官外,还包括首席财务官、首席医疗官、监管事务副总裁、北美总裁、人力资源 主管和集团总法律顾问。有关 Calliditas 现任高级管理人员、 他们何时就职、出生日期、教育、经验、公司股权以及 当前和以前的任务的信息,请参阅第 96-99 页和公司的网站 www.calliditas.se。 内部控制和风险管理 董事会对内部 控制的责任受《瑞典公司法》、 瑞典年度报告法管辖,该法要求有关Calliditas每年与财务 报告相关的 内部控制和风险管理系统的主要特征的信息必须包含在公司利率治理报告中,以及该守则。除其他任务外, 董事会应确保Calliditas 有足够的内部控制和正式的例行程序, 确保财务报告 和内部控制的既定原则得到遵守,并确保有 有效的系统来监控和控制公司 的运营以及与公司 及其运营相关的风险。 内部控制的总体目的是确保 对公司的运营战略和目标 进行监控,并在合理的程度上保护所有者的投资。此外, 内部控制应确保外部财务报告在合理的确定性下是可靠的 ,并根据公认的 会计惯例编制,遵守适用的法律法规 ,并遵守对 上市公司的要求。内部控制 主要由以下五个组成部分组成。 控制环境 董事会全面负责 与财务报告相关的内部控制。 为了创建和维护有效的控制 环境,董事会通过了 多项有关财务 报告的政策和准则。这些文件主要包括 董事会议事规则、首席执行官指示、审计 委员会议事规则和财务报告指示。 董事会还通过了 签字权下放和财政政策。公司 还有一份财务手册,其中包含会计和 财务报告的原则、 指南和流程描述。此外,董事会 成立了审计委员会,其主要任务是 监控公司的财务状况,监测 公司内部控制的有效性, 内部审计和风险管理,向 通报年度报告和合并 财务报表的审计情况,并审查和监督 审计师的公正性和独立性。正在进行的 财务报告内部控制工作的责任已委托给纽约公司的首席执行官。首席执行官根据首席执行官的既定指示和财务 报告指示,定期向 董事会报告。董事会还收到公司审计师的报告 。 首席执行官负责对日常运营进行内部的、特定业务的 控制。 风险评估 风险评估包括确定在公司财务 报告的基本要求未得到满足时可能出现的 风险。Calliditas的 管理团队已在特定的风险登记册中识别和评估了公司运营中出现的风险,并评估了如何管理这些风险 。Calliditas的管理层应每年对战略、运营和 财务风险进行风险评估,并将评估结果提交审计 委员会和董事会。首席执行官 对演示负责。 首席财务官应每年对管理层的 风险评估进行审查。 控制活动 控制活动限制已识别的风险,并确保 准确可靠的财务报告。 董事会负责公司管理层的内部控制和 监控。完成了 92Calliditas Therapeutics | 2023 年年度报告公司治理报告 |
| 通过内部和外部控制活动,以及 通过审查和监督公司与风险管理有关的 指导方针。控制活动的有效性 每年进行评估,这些评估的 结果将报告给董事会 和审计委员会。在与主要分包商签订的协议 中,公司已确保 有权对每个分包商履行相关服务(包括质量方面)的情况进行审计。 监控 持续监控内部 控制措施的遵守情况和有效性。首席执行官确保 董事会持续收到关于公司活动发展的 报告,包括公司 业绩和财务状况的发展,以及 有关重要事件的信息,例如研究结果和 重要合同。首席执行官还在每次董事会例会上报告这些 事项。每年评估公司对相关政策和指导方针的遵守情况 。这些评估结果由公司首席财务官编制, 然后,每年向董事会和审计 委员会报告。 信息和沟通 公司拥有信息和沟通 渠道来提高财务 报告的准确性,并促进运营部门向董事会和高级 管理层进行报告和反馈 ,例如,向相关员工提供内部政策、准则 和有关财务报告 的说明等公司治理文件。 董事会还通过了管理公司信息披露的信息 政策。该公司还在 2021 年开始根据《萨班斯-奥克利法案》实施内部控制结构,以满足 对在美国上市的公司的要求。除了上述 内部控制外,还对研究 和开发方面的数据进行内部的 特定业务控制,以及质量控制,包括 对纽约公司的开发和制造业务进行系统监控和评估。 内部审计 董事会已经评估了是否需要设立 内部审计职能,并决定,考虑到运营范围 ,Calliditas没有理由设立这样的职能 ,并且董事会对内部 控制的监督被认为足以确保内部 控制的有效性。当发生可能导致 重新评估的变更时,董事会每年至少重新评估一次 要求。 审计师关于公司治理声明的报告 致Calliditas Therapeutics AB(Publ)股东大会,公司标识号556659-9766 斯德哥尔摩,2024 年 4 月 24 日安永会计师事务所 授权会计师 参与和责任 由董事会负责 公司治理声明 2023 年第 88-93 页,它是根据《年度账目法》在 中编制的。 审计范围 我们的审查是按照 的标准 RevR 16 进行的。审计师对公司治理声明的审查 。这意味着 我们对公司治理声明 的审查与根据国际审计准则 和瑞典公认的审计标准进行的审计 不同且范围要小得多。我们认为,考试 为我们的意见提供了足够的依据。 意见 公司治理声明已经编写。 根据第 6 章第 6 节、 第二段第 2-6 点、《年度账目法》 和第 7 章第 31 条第 2 款进行披露。 同一法律与年度账目和 合并账户一致,符合 《年度账目法》。 93Calliditas Therapeutics | 2023 年年度报告 |
| 董事会 Henrik Stenqvist 非执行董事 生于 1967 年。自 2022 年起成为董事会成员。 教育: 林雪平大学 工商管理与经济学理学硕士。 董事会委员会: 审计委员会主席。 经验: Henrik Stenqvist曾担任 多家上市生命科学公司的首席财务官, 目前,他是SOBI的首席财务官。之前的 职位包括Recipharm的首席财务官、Meda的首席财务官 、阿斯利康的区域财务总监、阿斯利 出口与贸易的财务总监以及 MedCap AB的董事会成员。 当前的其他任务: Midsona AB 和 Orion 公司的董事会成员(自 2024 年 3 月 20 日起)。 公司持股: Henrik Stenqvist 持有 Calliditas 的 10,000 股股票,在 LTIP 2022 中持有 5,356 股股票奖励,在 LTIP 2023 中持有 5,389 股奖励。 独立于公司 及其管理层以及 大股东。 Hilde Furberg 非执行董事 生于 1958 年。自 2014 年起成为董事会成员。 教育: 挪威 奥斯陆大学理学硕士。 董事会委员会: 审计委员会成员。 经验: 希尔德·弗伯格是一位独立顾问 和专业的董事会成员。自 在制药/生物技术领域从事销售、营销、战略 和管理工作的 35 年以来,她拥有 丰富的领导经验。她的 在各种治疗领域积累了经验 ,这些经验是在小型公司和大型跨国公司工作的。Hilde 曾在Genzyme 和百特等公司工作,她最近在赛诺菲健信担任高级副总裁和 总经理/欧洲罕见 疾病主管。除在 Genzyme/Sanofi Genzyme 工作外, Hilde 自 2005 年起还担任普诺碧、 Pronova、Clavis、Bergenbio 和 Algeta 的非执行董事兼董事会成员。 当前的其他任务: 她目前是 Investinor的工业顾问,也是PCI 生物技术、Herantis Pharma、Sedana Medical、 Bio-Me、Pluvia Biotech和Borkenholm AS的董事会成员。 公司持股: Hilde Furberg 持有 公司53,199股股份,2021年LTIP持有4,086股股票奖励,2022年LTIP持有5,356股股票奖励,2023年LTIP中持有5,389份股票奖励。 独立于公司 及其管理层以及 大股东。 Elmar Schnee 主席 生于 1959 年。自 2019 年起成为董事会成员。 教育: SIB 市场营销与管理硕士学位。 董事会委员会: 薪酬 委员会主席。 经验: Elmar Schnee曾担任 默沙东雪兰诺的首席执行官,并在默沙东集团收购 Serono 的 过程中发挥了重要作用。他 还曾担任默沙东 KGaA的普通合伙人和 执行委员会成员,此前曾在 UCB 和赛诺菲担任过多个 高级全球管理职位。 当前的其他任务: ProCom Rx SA、Moleac Pte Lts 和 Noorik Biopharmaceuticals AG 的董事会主席、EnteroBiotix 执行董事会主席以及 Kuste Biopharma、Mindmaze SA 和 Damian 制药股份公司董事会成员。 公司持股: Elmar Schnee 持有 公司33,236股股份,2021年LTIP 10,624股股票奖励,2022年LTIP 13,926份股票奖励,2023年LTIP 14,012份股票奖励。 独立于公司 及其管理层以及 大股东。 94Calliditas Therapeutics | 2023 年年度报告 |
| 黛安·帕克斯 非执行董事 生于 1952 年。自 2019 年起成为董事会成员。 教育: 堪萨斯州立大学 硕士学位和乔治亚州立大学 大学工商管理硕士学位。 董事会委员会: 薪酬委员会成员。 经验: 黛安·帕克斯是一位高级管理人员,拥有 在美国 的丰富销售和营销经验,她曾担任过诸如 Kite 制药公司美国商业主管、安进销售副总裁和Pharmacyclics全球营销主管 等职务。 当前的其他任务: Kura Oncology、Soligenix 和 Celularity 的董事会成员。 公司持股: 黛安·帕克斯持有 公司8,499股股份,2021年LTIP 4,086股股票奖励,2022年LTIP 5,356份股票奖励,2023年LTIP 5,389份股票奖励。 独立于公司 及其管理层以及 大股东。 Fred Driscoll 非执行董事 生于 1950 年。自 2023 年起成为董事会成员。 教育: 本特利大学会计学学士学位。 董事会委员会: 审计委员会成员。 经验: 德里斯科尔先生于2022年10月至2023年5月在Invivyd, Inc.担任临时首席财务官 。自2021年5月至 2021年11月,德里斯科尔先生在被帕西拉生物科学收购的Flexion Therapeutics 担任首席财务官, 此前他在2013年至2017年期间担任该职务,领导了2014年的首次公开募股 。在加入Flexion Thera-Peutics之前,他在2009年至2013年期间在上市的生物制药公司 Novavax, Inc. 担任首席财务官。从 2008年到2009年,德里斯科尔先生担任Genelabs Technologies, Inc. 的首席执行官。Genelabs Technologies, 公司是一家上市的生物制药 和诊断公司,后来被葛兰素史克收购 。他曾在 2007 年至 2008 年期间担任 Genelabs 的首席财务官 。从 2003 年到 2006 年, Driscoll 先生在生物制药公司 OxiGene, Inc. 担任首席执行官,并于 2000 年至 2003 年担任首席财务 官。德里斯科尔先生还曾在OxiGene担任 董事会主席和审计委员会 主席以及赛纳普斯的 审计委员会成员,赛纳普斯于2016年被出售给了Sunovion Pharmicals 。 当前的其他任务: 德里斯科尔先生目前担任 Cellectar BioSciences、Cue BioPharma 和 MEI Pharma 的董事会 成员。 在公司持有的股份: 2023 年 LTIP 中有 5,389 股股票奖励。 独立于公司 及其管理层以及与 主要股东的关系。 伊丽莎白·比约克 非执行董事 生于 1961 年。自 2022 年起成为董事会成员。 教育: 斯德哥尔摩卡罗林斯卡学院医学博士学位和 乌普萨拉大学 董事会委员会医学副教授: 薪酬委员会成员。 经验: 伊丽莎白·比约克是一名受过 培训的内分泌学家,也是瑞典乌普萨拉大学的 医学副教授。 伊丽莎白·比约克自2012年以来一直担任阿斯利康生物制药 研发高级副总裁兼心血管、肾脏和 代谢(CVRM)后期 开发(CVRM)负责人,领导该领域的全球 药物开发。在 阿斯利康的整个职业生涯中,她积累了丰富的药物 开发经验,涵盖临床 一至四期开发阶段、大型成果 项目、主要的全球申请和健康 权威机构相互作用(FDA、EMA、日本) 以及商业战略/实施。 其他当前任务: Rocket Pharmace-Cals、Pharvaris NV、Vicore Pharma AB、 查尔姆斯理工大学、Betula 咨询公司董事会成员。 公司持股: Elisabeth Björk 在 2021 年 LTIP 中持有 4,086 份股票奖励 ,在 LTIP 2022 中持有 5,356 份股票奖励,在 LTIP 2023 中持有 5,389 份股票奖励。 独立于公司 及其管理层以及 大股东。 95Calliditas Therapeutics | 2023 年年度报告 |
| 管理团队 弗雷德里克·约翰逊 首席财务官 生于 1977 年。 自 2017 年起担任首席财务官。 教育: 在延雪平国际商学院 学习商法。曾在乔治亚州立大学、南卡罗来纳大学 和隆德大学学习商业和美国法、经济学和 金融。 经验: 弗雷德里克·约翰逊在高管职位上拥有丰富的经验,主要是在电信和软件领域。此前,他曾在奥斯陆证券交易所 上市的Birdstep Technology/Techstep ASA担任首席财务官兼首席运营官,除其他外,他负责Teki Solutions的收购和反向上市。 之前的首席财务官职位还包括Phone Family、Teleligent 电信和Wayfinder Systems。 持有的公司: 弗雷德里克·约翰逊持有公司42,750股股份和 30.5万股期权。 蕾妮·阿吉亚尔-卢坎德 首席执行官 生于 1962 年。 自 2017 年起担任首席执行官。 教育: 斯德哥尔摩经济学院金融学学士学位。来自 欧洲工商管理学院的工商管理硕士。 经验: 在加入Calliditas之前,蕾妮·阿吉亚尔-卢坎德曾是欧米茄基金管理公司的合伙人 兼首席运营官。欧米茄基金管理是一家国际风险投资 资本公司,专注于生命科学 领域的投资。在此之前,她曾在伦敦风险投资 group 3i Group plc 担任合伙人,负责管理 上市资产,并担任全球医疗保健和 技术投资组合的联席主管。在此之前,蕾妮·阿吉亚尔-卢坎德曾在一家全球投资银行担任 欧洲集团负责人兼董事总经理,在企业 融资领域拥有超过12年的经验。在从事投资银行业务之前,她曾在一家专注于 金融服务软件销售的公司担任 欧洲销售和营销主管。 其他当前任务:— 公司持股: 蕾妮·阿吉亚尔-卢坎德持有该公司 的64.3万股股票和84.1万股期权。 96Calliditas Therapeutics | 2023 年年度报告 |
| 弗兰克·布林斯特鲁普 监管事务副总裁 生于 1959 年。 自 2019 年起担任监管事务副总裁。 教育: 哥本哈根大学的医学教育。他拥有 哥本哈根经济学院的 管理医疗产品创新(MMPI)文凭、华威大学的商业 管理文凭以及丹麦国家卫生委员会 公共卫生科学的研究生 专业课程。 经验: 弗兰克·布林斯特鲁普在制药行业拥有超过17年的监管事务和卫生局 互动方面的经验。在加入 Calliditas 之前,他曾在 Novo Nordisk A/S 担任各种 职位。他的职业生涯始于 最初是一名诊所医生,然后是弗雷德里克斯堡县医疗 顾问。 持有该公司的股份: 弗兰克·布林斯特鲁普持有公司8,000股股票和 13.5万股期权。 桑德拉·弗里西奥夫 人力资源主管 生于 1975 年。 自 2020 年起担任人力资源主管。 教育: 瑞典厄勒布鲁 大学人力资源管理学士学位。 经验: 桑德拉·弗里西奥夫在 不同行业拥有超过23年的人力资源经验。在加入 Calliditas 之前,桑德拉曾在 Ramberg Advokater 担任 人力资源主管兼首席运营官。之前的人力资源职位还包括卡罗林斯卡大学医院、UTC、CGI 和 Manpower Group。 持有的公司: 桑德拉·弗里西奥夫持有10.5万份期权。 97Calliditas Therapeutics | 2023 年年度报告 |
| Management team Richard Philipson Chief Medical Officer Born 1964. Chief Medical Officer since 2020. Education: BSc in Biomedical Sciences at London University and MB MS, Middlesex Hospital Medical School. Fellow of the Royal College of Physicians and Fellow of the Faculty of Pharmaceutical Medicine. Experience: Dr. Richard Philipson is a physician with 24 years of experience in the pharmaceutical industry from both large pharmaceutical companies and smaller biotechs. He has extensive experience in rare diseases, having brought several products from early devel-opment to the market. Prior to joining Calliditas, Richard worked as CMO with the UK-based biotech company Trizell where he led the Adstiladrin® phase 3 clinical program and Biologics License Application in non-muscle invasive bladder cancer, submitted to the FDA in September 2019. Before Trizell, he worked for Takeda as an Executive Medical Director and spent 16 years at GlaxoSmithKline, where he held a number of senior positions, including Disease Area Head and Acting Chief Medical Officer for the Rare Diseases Unit. Before joining the industry, Richard worked as a physician in several clinical positions with various patient populations, including patients with IgA nephropathy. Holdings in the Company: Richard Philipson holds 270,000 options. Maria Törnsén President North America Born 1978. President, North America since 2024. Education: MSc in International Business Administration from Lund Univer-sity, Sweden. Experience: Maria Törnsén has more than 20 years of experience in the pharmaceutical industry. Maria is currently a Board Director for Immunic Therapeutics and before joining Calliditas, she worked as Chief Commercial Officer at Passage Bio. Prior to Passage Bio, Maria held various commercial leadership roles at Sarepta, Sanofi and Shire. Maria began her career at Eli Lilly in sales and also worked at Merck KGaA in sales and marketing. Holdings in the Company: Maria Törnsén holds 125,000 options. 98Calliditas Therapeutics | Annual Report 2023 |
| Brian Gorman Group General Counsel Born 1976. Group General Counsel since 2023. Education: Bachelor’s Degree from Gettysburg College, J.D from Villanova University School of Law. Experience: Brian is an accomplished legal and business executive with more than 20 years of experience advising corporate boards and executive management teams of life science companies. He joins Calliditas after having served most recently as Executive Vice President, Corporate Development & General Counsel at Opiant Pharmaceuticals, which was acquired by Indivior PLC. Prior to Opiant, Brian held senior legal leadership roles at Endo Pharma-ceuticals, AstraZeneca and Wyeth Pharmaceuticals (now Pfizer). He began his career at the international law firm, Cleary Gottlieb Steen & Hamilton. Holdings in the Company: Brian Gorman holds 75,000 options. Lars Stubberud Head of Technical Operations Born 1964. Head of Technical Operations since 2023. Education: Master of Science (candidatus pharmaciae) and PhD in Pharma-ceutical Science from the University of Oslo, Norway. Experience: Lars Stubberud has more than 30 years experience in the pharmaceutical industry, within the broader CMC area, including Formulation Sciences, Product Development, Technology Transfer/Technical Stewardship as well as Regulatory Affairs-CMC and Quality Assurance. Prior to joining Calliditas Lars has held various positions, including leadership roles, at Nyomed AS, Norway, AstraZeneca Sweden, as well as Cubist Pharmaceuticals GmbH, Biogen International GmbH and Alexion Pharma GmbH in Switzerland. Holdings in the company: Lars Stubberud holds 100 000 options. 99Calliditas Therapeutics | Annual Report 2023 |
| Scientific Steering Committee Some of the most prominent IgA nephropathy specialists in the world serve as external advisors and members of the Company’s advisory board. Brad H. Rovin Professor, Director of the Division of Nephrology and Vice Chairman of Medicine for Research at the Ohio State University Wexner Medical Center, Columbus, Ohio, US Heather N. Reich Department Division Director of Nephrology, University of Toronto; Senior Scientist, Toronto General Hospital Research Institute; Nephrologist, University Health Network, Toronto, Ontario, Canada Hérnan Trimarchi Professor of Medicine, Universidad Católica Argentina; Head, Nephrology Service, Hospital Británico; Head, Kidney transplant unit, Hospital Británico, Buenos Aires, Argentina Hong Zhang Professor of Medicine and Doctoral supervisor, Nephrology Division, Peking University First Hospital, Peking University Institute of Nephrology, Beijing, China Jonathan Barratt Professor, Department of Infection, Immunity and Inflam-mation, University of Leicester; Honorary Consultant Nephrologist in the John Walls Renal Unit, Leicester General Hospital, Leicester, UK Jürgen Floege Professor, head of the Department of Renal and Hyper-tensive Diseases, Rheumatological and Immunological Diseases (Medicine II) at the Aachen University Hospital; Director of the Department of Nephrology and Clinical Immunology at the University of Aachen, Aachen, Germany Richard Lafayette Professor of Medicine (Nephrology), the Stanford University Medical Center; Director, the Stanford Glomerular Disease Center, Stanford, California, US Vladimir Tesar Professor, Head of the Department of Nephrology, 1st Faculty of Medicine, Charles University, Prague, Czech Republic 100Calliditas Therapeutics | Annual Report 2023 |
| Financial Calendar Interim Report for the period January 1–March 31, 2024 May 23, 2024 Annual General Meeting 2024 June 17, 2024 Interim Report for the period January 1–June 30, 2024 August 13, 2024 Interim Report for the period January 1–September 30, 2024 November 11, 2024 Year-End Report for the period January 1–December 31, 2024 February 20, 2025 101Calliditas Therapeutics | Annual Report 2023 |
| Glossary ACE inhibitors (ACEIs): Angiotensin Converting Enzyme inhibitors (ACEis) are a type of blood pressure medication that work by limiting the effects of the hormone angio-tensin II, which has a constricting effect on blood vessels and stim-ulates salt and water retention in the body and thus increases blood pressure. Angiotensin II is activated by a molecule called Angiotensin Converting Enzyme (ACE,) which is blocked by ACE inhibitors Adaptive Design: An adaptive design trial is one in which the design allows for modifications to the trial and/or statistical proce-dures of the trial after its initiation without undermining its validity and integrity ALP: Alkaline phosphatase (ALP) is an enzyme which is used as a marker in PBC. A rise in ALP levels indicates impaired bile flow in the liver Angiotensin Receptor Blockers (ARBs): ARBs work by blocking the AT1 receptors that the hormone angiotensin II acts on, thereby limiting its action and lowering blood pressure Autoimmune disease: Disease that is manifested because of the immune system's harmful attack with autoantibodies on the body's own tissue. All people have some degree of autoimmunity, but when it gets too high it becomes harmful Budesonide: a potent glucocor-ticoid with rapid elimination that fits very well with local treatment where you want to minimize systemic side effects CAF: A cancer-associated fibroblast (CAF) is a key cell type within the tumor microenvironment. CAFs promote tumor growth via a variety of mechanisms, including initiating the remodelling of the extracellular matrix or secreting cytokines Corticosteroids: a class of steroid hormones and synthetic analogues. Corticosteroids are used systemi-cally for the treatment of inflamma-tory and immunological diseases, including IgA nephropathy, autoim-mune hepatitis and primary biliary cholangitis Creatinine: a chemical substance made by muscles. Measured in the blood circulation and produced in a relatively even amount. Eliminated through the kidneys. Too high a concentration in the blood is a measure of impaired kidney func-tion. It is used to calculate eGFR. High creatinine corresponds to low eGFR Dimeric: Also known as ‘polymeric’, a dimeric molecule is composed of two identical simpler molecules (monomers) DKD: Diabetic kidney disease (DKD,) also called diabetic nephro-pathy, is kidney disease that is due to Type 1 or Type 2 diabetes Double blind: A double-blind study is one in which neither the participants nor the experimenters know who is receiving a particular treatment eGFR: estimated glomerular filtra-tion rate. A measure of the kidney's ability to filter and purify the blood. When a kidney disease worsens, eGFR decreases EMA: European Medicines Agency ESRD: end-stage renal disease Enteric: relating to or occurring in the small intestine. The enteric coating on Nefecon refers to the fact that it is designed to dissolve in the ileum, which is in the distal part of the small intestine FDA: US Food and Drug Adminis-tration Galactose: a type of sugar that is similar to glucose. Antibodies such as IgA have sugar chains attached to them. These sugar chains contain, among other things, galactose Glomerulus: An anatomical struc-ture of the kidney. Blood vessel bundles where the blood is filtered to urine Glomerulonephritis: an inflamma-tion of the glomeruli, the kidney's filtration function HbA1c: HbA1c is a term commonly used in relation to diabetes and is a measure of average blood sugar levels. The term refers to glycated haemoglobin, which develops when haemoglobin joins with glucose in the blood, becoming ‘glycated’ IgA: Immunoglobulin A (an anti-body.) Also referred to as IgA1 IgA Nephropathy (IgAN): a rare autoimmune kidney inflammatory disease, within the glomerulone-phritis class Ileum: the distal end of the small intestine, also called the bowel arm, is 2–4 meters long and connects to the colon 102Calliditas Therapeutics | Annual Report 2023 |
| Immunoglobulin: antibodies (proteins) used by the body's immune system to detect and identify foreign substances that can cause damage Incidence: number of new patients per year in a disease Immunosuppressive agents: a class of drugs that suppress, or reduce, the strength of the body's immune system Immunotherapy: Immunotherapy is the treatment of disease by acti-vating or suppressing the immune system Investigator-Led Study: Inves-tigator led studies are clinical studies initiated and managed by a non-pharmaceutical company researchers, like individual inves-tigators, institutions, collaborative study groups or cooperative groups IPF: Idiopathic pulmonary fibrosis (IPF) is a condition in which the lungs become scarred and breathing becomes increasingly difficult, the causes of which are unclear KDIGO: Kidney Disease: Improving Global Outcomes, a non-profit organization that develops global guidelines for treatment in kidney disease Monomeric: a monomeric molecule is one that is a single unit and can be bonded to other identical mole-cules to form a polymer NADPH Oxidase: NADPH oxidase (nicotinamide adenine dinucleotide phosphate oxidase,) also known as NOX enzymes, are membrane-bound enzyme complexes, which catalyse the production of reactive oxygen species Nephrologist: a physician special-ized in kidney disease Off-label prescription: prescription of an approved drug outside the approved indication On-label: prescription of an approved drug within the approved indication Open-label: An open-label trial is one in which information about which treatment is being admin-istered is not withheld from trial participants and researchers Orphan disease: a rare disease that falls within the criteria of orphan drug law Oxidative Stress: Oxidative stress is when there is an imbalance between the production and the accumulation of reactive oxygen species (ROS) in cells and tissues and the body’ ability to detoxify these reactive products PBC: Primary biliary cholangitis, a rare autoimmune fatty liver disease Peyer's patches: lymph tissue of the ileum, the distal part of the small intestine, part of the body's immune system Prevalence: number of people in a population having a disease Proteinuria: a condition charac-terized by the presence of greater than normal amounts of protein in the urine; a measure of leakage in the kidney's filtration function Proof of Concept Trial: Proof of Concept Principle studies are an early stage of clinical drug develop-ment when a compound has shown potential in animal models and early safety testing, and often is the step between a Phase 1 and a dose ranging Phase 2 study RAS: Renin-angiotensin system, which regulates blood pressure and fluid in the body; a RAS blocker lowers blood pressure; RAS blockade is when a patient is on drugs that block RAS, which can be ACEIs and/or ARBs Randomised: A randomised trial is one in which participants are randomly assigned to 2 or more groups Reactive Oxygen Species: Reactive oxygen species are highly reactive chemical molecules formed through the electron acceptability of O₂ Redox Homeostasis: Redox homeostasis is attained by the regulation of the formation and removal of reactive oxygen species (ROS) from the body system RRT: renal replacement therapy; a treatment for terminal kidney failure where the function of the diseased kidney is replaced by dial-ysis or kidney transplantation Transient Elastography: Transient elastography (FibroScan) is an ultra-sound exam that uses pulse-echo ultrasound acquisitions to measure liver stiffness in kilopascals (kPa,) which allows for a noninvasive assessment of liver stiffness UPCR: Urine protein creatinine ratio, a measure of leakage in the kidney's filtration function 103Calliditas Therapeutics | Annual Report 2023 |
| Calliditas Therapeutics AB Kungsbron 1, D5 SE-111 22 Stockholm Sweden Phone: +46 (0)8 411 3005 Email: info@calliditas.com Web: www.calliditas.com |