2022年8月12日,公司得知与本销售协议相关的S-3表格(文件编号333-231923)(“注册声明”)已于2022年6月21日到期。在得知到期之前,公司共出售了 132,473在注册声明到期后以及2022年8月12日之前,按市场价格出售其普通股,总收益约为美元2,721,187。2022年8月12日之后没有出售股票。这些股份的出售受某些股东可能的撤销权的约束。由于这些潜在的撤销权,公司进行了重新分类 207,807股票(包括 75,333出售的股票(该公司未获得任何收益),总收购价为美元4,494,496在2023年8月这些撤销权到期日之前,其普通股为股东权益以外的股票。在计算截至2023年3月31日的三个月中,每股基本亏损和摊薄亏损时,这些股票被视为已发行和流通。这些股票的撤销权已经失效,这些股票被重新归类为永久股权。没有人要求或要求行使这些权利。
2022年8月15日,由于注册声明的到期,销售协议相互终止。总共有 218,738股份,总收益约为 $7.6百万美元,已根据销售协议出售。
认股证
2023 年 12 月认股权证
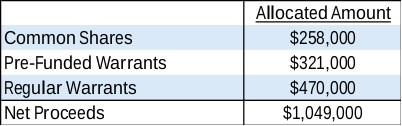
截至2024年3月31日,认股权证共购买了 419,925根据2023年12月融资交易中的证券购买协议发行的普通股仍在流通。总共有 396,156认股权证,包括 7,956同时私募发行的认股权证自发行之日起可立即行使,有效期为 七年发行之日后,行使价为美元3.19每份认股权证。再进一步 23,769在并行配售机构协议中发行的认股权证可自发行之日起立即行使,有效期为 五年发行之日后,行使价为美元4.14375每份认股权证。
有 不在截至2024年3月31日的三个月内行使这些认股权证。
2020年12月认股权证
截至2024年3月31日,认股权证 44,657根据2020年12月融资交易中的证券购买协议发行的普通股仍在流通。每份认股权证应从发行之日起的12个月周年纪念日开始行使,有效期为 五年发行之日后,行使价为美元61.95每份认股权证。如认股权证中所述,如果发生任何股票分红和拆分、反向股票拆分、资本重组、重组或类似交易,认股权证的行使价将进行调整。认股权证可以在 “无现金” 的基础上行使。
有 不在截至2024年3月31日或2023年3月31日的三个月内行使这些认股权证。
2020年4月认股权证
截至2024年3月31日, 146,000根据与2020年4月股权融资相关的证券购买协议发行的认股权证仍未兑现,每份认股权证的行使价为美元75.00. 普通认股权证可立即行使,并将在原发行日期五周年之际到期。如果发生影响公司普通股的股票分红、股票分割、重组或类似事件,则行使时可发行的普通股的行使价和数量将进行适当调整。普通认股权证与普通股分开发行,发行后有资格立即转让。普通的购买权证 一本次发行中每购买一股普通股,就会发行普通股。
普通认股权证可由每位持有人选择全部或部分行使,方法是向公司交付正式执行的行使通知,同时全额支付普通认股权证数量的款项