目录
ROC
美国
证券交易委员会
华盛顿特区 20549
表单
(Mark One)
根据1934年《证券交易法》第13条或第15(d)条提交的季度报告 |
在截至的季度期间
或者
根据1934年《证券交易法》第13条或第15(d)条提交的过渡报告 |
|
在过渡期内 |
|
到 |
|
|
委员会档案编号:
(注册人的确切姓名如其章程所示)
|
|
|
|
||
(州或其他司法管辖区 公司或组织) |
|
(美国国税局雇主 证件号) |
(主要行政办公室地址)(邮政编码)
(
(注册人的电话号码,包括区号)
根据该法第12(b)条注册的证券:
每个班级的标题 |
|
交易 符号 |
|
注册的每个交易所的名称 |
|
|
这个 |
用勾号指明注册人 (1) 是否在过去 12 个月内(或在要求注册人提交此类报告的较短时间内)提交了 1934 年《证券交易法》第 13 条或第 15 (d) 条要求提交的所有报告,以及 (2) 在过去的 90 天内是否受到此类申报要求的约束。
用复选标记表明注册人是否在过去 12 个月内(或者在要求注册人提交此类文件的较短时间内)以电子方式提交了根据第 S-T 法规(本章第 232.405 节)第 405 条要求提交的所有交互式数据文件。
用复选标记指明注册人是大型加速申报人、加速申报人、非加速申报人、小型申报公司还是新兴成长型公司。请参阅《交易法》第12b-2条中对大型加速申报人、加速申报人、小型申报公司和新兴成长型公司的定义。
大型加速过滤器 |
|
☐ |
|
加速过滤器 |
|
☐ |
|
☒ |
|
规模较小的申报公司 |
|
||
新兴成长型公司 |
|
|
|
|
|
如果是新兴成长型公司,请用复选标记表明注册人是否选择不使用延长的过渡期来遵守根据《交易法》第13(a)条规定的任何新的或修订后的财务会计准则。☐
用复选标记表明注册人是否为空壳公司(定义见《交易法》第12b-2条)。是 ☐ 不是
截至2024年5月6日,发行人普通股的已发行股票数量为面值0.00000002美元
目录
MEI 制药有限公司
的表内容
|
|
|
|
|
|
|
|
|
|
|
页面 |
|
|
|
|
|
||||
第一部分 |
|
财务信息 |
|
|
3 |
|
|
|
|
||||
第 1 项。 |
|
简明合并财务报表 |
|
|
3 |
|
|
|
|
|
|
|
|
|
|
简明合并资产负债表(未经审计) |
|
|
3 |
|
|
|
|
|
|
|
|
|
|
简明合并运营报表(未经审计) |
|
|
4 |
|
|
|
|
|
|
|
|
|
|
股东权益简明合并报表(未经审计) |
|
|
5 |
|
|
|
|
|
|
|
|
|
|
简明合并现金流量表(未经审计) |
|
|
6 |
|
|
|
|
|
|
|
|
|
|
简明合并财务报表附注(未经审计) |
|
|
7 |
|
|
|
|
|
|
|
|
第 2 项。 |
|
管理层对财务状况和经营业绩的讨论和分析 |
|
|
19 |
|
|
|
|
|
|
|
|
第 3 项。 |
|
关于市场风险的定量和定性披露 |
|
|
31 |
|
|
|
|
|
|
|
|
第 4 项。 |
|
控制和程序 |
|
|
32 |
|
|
|
|
||||
第二部分 |
|
其他信息 |
|
|
33 |
|
|
|
|
|
|
|
|
第 1 项。 |
|
法律诉讼 |
|
|
33 |
|
|
|
|
|
|
|
|
第 1A 项。 |
|
风险因素 |
|
|
33 |
|
|
|
|
|
|
|
|
第 2 项。 |
|
未注册的股权证券销售和所得款项的使用 |
|
|
33 |
|
|
|
|
|
|
|
|
第 3 项。 |
|
优先证券违约 |
|
|
33 |
|
|
|
|
|
|
|
|
第 4 项。 |
|
矿山安全披露 |
|
|
33 |
|
|
|
|
|
|
|
|
第 5 项。 |
|
其他信息 |
|
|
33 |
|
|
|
|
|
|
|
|
第 6 项。 |
|
展品 |
|
|
34 |
|
|
|
|||||
签名 |
|
|
35 |
|
||
2
目录
第一部分财务信息
第 1 项。简明合并财务报表
MEI 制药有限公司
简明的合并资产负债表
(以千计,面值数据除外)
|
|
3月31日 |
|
|
6月30日 |
|
||
|
|
2024 |
|
|
2023 |
|
||
|
|
(未经审计) |
|
|
|
|
||
资产 |
|
|
|
|
|
|
||
流动资产: |
|
|
|
|
|
|
||
现金和现金等价物 |
|
$ |
|
|
$ |
|
||
短期投资 |
|
|
|
|
|
|
||
未开单应收账款 |
|
|
|
|
|
|
||
预付费用和其他流动资产 |
|
|
|
|
|
|
||
流动资产总额 |
|
|
|
|
|
|
||
经营租赁使用权资产 |
|
|
|
|
|
|
||
财产和设备,净额 |
|
|
|
|
|
|
||
总资产 |
|
$ |
|
|
$ |
|
||
|
|
|
|
|
|
|
||
负债和股东权益 |
|
|
|
|
|
|
||
流动负债: |
|
|
|
|
|
|
||
应付账款 |
|
$ |
|
|
$ |
|
||
应计负债 |
|
|
|
|
|
|
||
递延收入 |
|
|
|
|
|
|
||
经营租赁责任 |
|
|
|
|
|
|
||
流动负债总额 |
|
|
|
|
|
|
||
长期递延收入 |
|
|
|
|
|
|
||
长期经营租赁负债 |
|
|
|
|
|
|
||
负债总额 |
|
|
|
|
|
|
||
|
|
|
|
|
|
|||
股东权益: |
|
|
|
|
|
|
||
优先股,$ |
|
|
|
|
|
|
||
普通股,$ |
|
|
|
|
|
|
||
额外的实收资本 |
|
|
|
|
|
|
||
累计赤字 |
|
|
( |
) |
|
|
( |
) |
股东权益总额 |
|
|
|
|
|
|
||
负债和股东权益总额 |
|
$ |
|
|
$ |
|
||
见附带的简明合并财务报表附注(未经审计)。
3
目录
MEI 制药有限公司
简明合并运营报表
(未经审计)
(以千计,每股金额除外)
|
|
在截至3月31日的三个月中, |
|
|
在截至3月31日的九个月中 |
|
||||||||||
|
|
2024 |
|
|
2023 |
|
|
2024 |
|
|
2023 |
|
||||
收入: |
|
|
|
|
|
|
|
|
|
|
|
|
||||
来自客户的收入 |
|
$ |
|
|
$ |
|
|
$ |
|
|
$ |
|
||||
来自合作协议的收入 |
|
|
|
|
|
|
|
|
|
|
|
|
||||
总收入 |
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
运营费用: |
|
|
|
|
|
|
|
|
|
|
|
|
||||
研究和开发 |
|
|
|
|
|
|
|
|
|
|
|
|
||||
一般和行政 |
|
|
|
|
|
|
|
|
|
|
|
|
||||
运营费用总额 |
|
|
|
|
|
|
|
|
|
|
|
|
||||
运营收入(亏损) |
|
|
( |
) |
|
|
( |
) |
|
|
|
|
|
( |
) |
|
其他收入(支出): |
|
|
|
|
|
|
|
|
|
|
|
|
||||
认股权证负债公允价值的变化 |
|
|
|
|
|
|
|
|
|
|
|
|
||||
利息和股息收入 |
|
|
|
|
|
|
|
|
|
|
|
|
||||
其他费用,净额 |
|
|
( |
) |
|
|
( |
) |
|
|
( |
) |
|
|
( |
) |
其他收入总额,净额 |
|
|
|
|
|
|
|
|
|
|
|
|
||||
净(亏损)收入 |
|
$ |
( |
) |
|
$ |
( |
) |
|
$ |
|
|
$ |
( |
) |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
每股净(亏损)收益——基本收益和摊薄后收益 |
|
$ |
( |
) |
|
$ |
( |
) |
|
$ |
|
|
$ |
( |
) |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
用于计算净额(亏损)的加权平均份额 |
|
|
|
|
|
|
|
|
|
|
|
|
||||
见附带的简明合并财务报表附注(未经审计)。
4
目录
MEI 制药有限公司
简明的股东权益合并报表
(未经审计)
(以千计)
|
|
常见 |
|
|
额外 |
|
|
累积的 |
|
|
总计 |
|
||||
截至 2023 年 6 月 30 日的余额 |
|
|
|
|
$ |
|
|
$ |
( |
) |
|
$ |
|
|||
净收入 |
|
|
— |
|
|
|
— |
|
|
|
|
|
|
|
||
基于股份的薪酬 |
|
|
— |
|
|
|
|
|
|
|
|
|
|
|||
截至 2023 年 9 月 30 日的余额 |
|
|
|
|
|
|
|
|
( |
) |
|
|
|
|||
净亏损 |
|
|
— |
|
|
|
— |
|
|
|
( |
) |
|
|
( |
) |
申报的现金分红 ($) |
|
|
— |
|
|
|
( |
) |
|
|
— |
|
|
|
( |
) |
基于股份的薪酬 |
|
|
— |
|
|
|
|
|
|
— |
|
|
|
|
||
截至2023年12月31日的余额 |
|
|
|
|
|
|
|
|
( |
) |
|
|
|
|||
净亏损 |
|
|
— |
|
|
|
— |
|
|
|
( |
) |
|
|
( |
) |
基于股份的薪酬 |
|
|
— |
|
|
|
|
|
|
— |
|
|
|
|
||
截至 2024 年 3 月 31 日的余额 |
|
|
|
|
$ |
|
|
$ |
( |
) |
|
$ |
|
|||
|
|
常见 |
|
|
额外 |
|
|
累积的 |
|
|
总计 |
|
||||
截至2022年6月30日的余额 |
|
|
|
|
$ |
|
|
$ |
( |
) |
|
$ |
|
|||
净亏损 |
|
|
— |
|
|
|
— |
|
|
|
( |
) |
|
|
( |
) |
为既得限制性股票单位发行普通股 |
|
|
|
|
|
( |
) |
|
|
— |
|
|
|
( |
) |
|
基于股份的薪酬 |
|
|
— |
|
|
|
|
|
|
— |
|
|
|
|
||
2022 年 9 月 30 日的余额 |
|
|
|
|
|
|
|
|
( |
) |
|
|
|
|||
净收入 |
|
|
— |
|
|
|
— |
|
|
|
|
|
|
|
||
基于股份的薪酬 |
|
|
— |
|
|
|
|
|
|
— |
|
|
|
|
||
截至2022年12月31日的余额 |
|
|
|
|
|
|
|
|
( |
) |
|
|
|
|||
净收入 |
|
|
— |
|
|
|
— |
|
|
|
( |
) |
|
|
( |
) |
发行认股权证 |
|
|
— |
|
|
|
|
|
|
|
|
|
|
|||
基于股份的薪酬 |
|
|
— |
|
|
|
|
|
|
— |
|
|
|
|
||
截至2023年3月31日的余额 |
|
|
|
|
$ |
|
|
$ |
( |
) |
|
$ |
|
|||
见附带的简明合并财务报表附注(未经审计)。
5
目录
MEI 制药有限公司
简明的合并现金流量表
(未经审计)
(以千计)
|
|
在截至3月31日的九个月中 |
|
|||||
|
|
2024 |
|
|
2023 |
|
||
来自经营活动的现金流: |
|
|
|
|
|
|
||
净收益(亏损) |
|
$ |
|
|
$ |
( |
) |
|
为将净收益(亏损)与经营活动中使用的净现金进行对账而进行的调整: |
|
|
|
|
|
|
||
认股权证负债公允价值的变化 |
|
|
|
|
|
( |
) |
|
基于股份的薪酬 |
|
|
|
|
|
|
||
发行认股权证 |
|
|
|
|
|
|
||
非现金租赁费用 |
|
|
|
|
|
|
||
折旧费用 |
|
|
|
|
|
|
||
运营资产和负债的变化: |
|
|
|
|
|
|
||
未开单应收账款 |
|
|
|
|
|
|
||
预付费用和其他流动资产 |
|
|
|
|
|
( |
) |
|
应付账款 |
|
|
( |
) |
|
|
( |
) |
应计负债 |
|
|
( |
) |
|
|
|
|
递延收入 |
|
|
( |
) |
|
|
( |
) |
经营租赁责任 |
|
|
( |
) |
|
|
( |
) |
用于经营活动的净现金 |
|
|
( |
) |
|
|
( |
) |
|
|
|
|
|
|
|
||
来自投资活动的现金流: |
|
|
|
|
|
|
||
购买短期投资 |
|
|
( |
) |
|
|
( |
) |
短期投资到期所得收益 |
|
|
|
|
|
|
||
出售财产和设备的收益 |
|
|
|
|
|
|
||
购买财产和设备 |
|
|
( |
) |
|
|
|
|
投资活动提供的净现金 |
|
|
|
|
|
|
||
|
|
|
|
|
|
|
||
来自融资活动的现金流: |
|
|
|
|
|
|
||
支付与限制性股票单位归属相关的预扣税 |
|
|
|
|
|
( |
) |
|
支付现金分红 |
|
|
( |
) |
|
|
|
|
用于融资活动的净现金 |
|
|
( |
) |
|
|
( |
) |
现金和现金等价物的净减少 |
|
|
( |
) |
|
|
( |
) |
期初的现金和现金等价物 |
|
|
|
|
|
|
||
期末的现金和现金等价物 |
|
$ |
|
|
$ |
|
||
|
|
|
|
|
|
|
||
补充现金流信息: |
|
|
|
|
|
|
||
为换取运营而获得的经营租赁使用权资产 |
|
$ |
|
|
$ |
|
||
应付账款中包含的融资成本 |
|
$ |
|
|
$ |
|
||
见附带的简明合并财务报表附注(未经审计)。
6
目录
MEI 制药有限公司
未经审计的简明合并财务报表附注
1。业务描述和陈述基础
业务描述
MEI Pharma, Inc.(纳斯达克股票代码:MEIP)是一家临床阶段的制药公司,致力于开发新的差异化癌症疗法。我们通过收购有前途的抗癌药物来建立我们的产品线,并酌情通过开发、战略合作伙伴关系、外包许可或商业化为项目创造价值。我们的肿瘤药物开发方法是评估我们的候选药物与标准护理疗法的组合,以克服已知的耐药机制,满足明确的医疗需求,从而改善患者的受益。我们的产品线包括口服细胞周期素依赖性激酶 9 (CDK9) 抑制剂 voruciclib 和 ME-344,一种线粒体氧化磷酸化静脉注射小分子抑制剂 (OXPHOS)。
合作协议
2023年10月31日,我们宣布与Anson Funds和Cable Car Capital签订合作协议(合作协议),该协议以及其他非财务相关项目,如概述部分所述 第 2 项。管理层对财务状况和经营业绩的讨论和分析, 提供给以股息的形式向股东返还资本,金额为美元
2024 年 4 月,该公司报告称,其董事会一致同意一项战略,将voruciclib的临床开发作为优先事项,同时允许为1期研究开发新的 ME-344 配方。此外,公司董事会一致决定不根据2023年10月31日的合作协议进行潜在的第二次资本回报,以节省资源和调整战略投资,从而延长公司的运营轨道。
作为合作协议的一部分,Anson和Cable Car撤回了合作协议不进行招标,并同意遵守惯常的停顿条款。此外, 截至合作协议签订之日,我们偿还了Anson和Cable Car与他们与我们合作的相关费用和开支,金额为 $
现金分红
流动性
我们累计亏损为 $
迄今为止,我们主要通过股权融资和许可协议获得了现金并为我们的运营提供资金。为了继续开发我们的候选药物,我们预计将在未来的某个时候进行一项或多项资本交易,无论是通过出售股权证券、债务融资、许可协议还是建立战略合作伙伴关系。无法保证我们将来能够继续筹集更多资金。
7
目录
列报基础和合并原则
简明合并财务报表是根据美国普遍接受的中期财务信息会计原则(美国公认会计原则)以及10-Q表的说明和第S-X条例第10条编制的。因此,随附的财务报表不包括美国公认会计原则要求的完整财务报表的所有信息和附注。管理层认为,所附的简明合并财务报表反映了公允列报所列期间的财务状况、经营业绩和现金流量所需的所有调整(包括正常的经常性调整)。
随附的未经审计的简明合并财务报表包括MEI Pharma, Inc.和我们的全资子公司Meadow Merger Sub, Inc.的账目。我们在合并中取消了所有重要的公司间账目和交易。
随附的截至2024年3月31日的季度未经审计的简明合并财务报表应与截至2023年6月30日的财政年度的经审计的财务报表及其附注一起阅读,包含在我们于2023年9月26日向美国证券交易委员会提交的10-K表年度报告(2023年年度报告)中。中期业绩不一定代表全年的业绩。该公司对截至简明合并财务报表发布之日的后续事件进行了评估。
2。重要会计政策摘要
与2023年年度报告中所载经审计的简明合并财务报表附注中所述的政策相比,我们的重要会计政策没有重大变化。
风险和不确定性
估算值的使用
分部报告
运营部门被确定为企业的组成部分,我们的首席运营决策者(CODM)首席执行官在做出有关资源分配和评估绩效的决策时,可以对这些部门进行单独的离散财务信息进行评估。CODM 将其运营视为并管理其业务
信用风险的集中度
可能使我们面临大量信用风险集中的金融工具主要包括现金、现金等价物和短期投资。我们的支票和货币市场账户中的存款存放在联邦保险的金融机构中,并受联邦保险限额或证券投资者保护公司设定的限额的约束。
短期投资
短期投资是有价证券,其原始到期日超过三个月,但自购买之日起不到一年。截至2024年3月31日和2023年6月30日,我们的短期投资包括 $
8
目录
分红
由于我们的净亏损历史,我们选择首先将额外实收资本(APIC)减少至
收入确认
来自客户的收入
根据ASC主题606, 与客户签订合同的收入(主题606),当承诺的商品或服务的控制权移交给我们的客户时,我们会确认收入,金额反映了我们为换取这些商品或服务而预计有权获得的对价。对于与客户签订的可执行合同,我们首先确定合同中不同的履约义务或会计单位。履约义务是合同中向客户转让特殊商品或服务的承诺。
根据商业安排(例如技术权利许可)收到的款项可能包括协议开始时不可退还的费用、协议中规定的特定成就的里程碑付款以及产品销售的特许权使用费。在包括里程碑付款的安排之初,我们使用判断来评估里程碑是否有可能实现,并使用最可能的方法估算交易价格中应包含的金额(如果有)。如果可能不会发生重大的收入逆转,则预计金额将包含在交易价格中。在获得批准之前,不在我们或被许可方控制范围内的里程碑付款,例如监管部门的批准,不包含在交易价格中。在每个报告期结束时,我们会重新评估实现发展里程碑和任何相关制约因素的可能性,并在必要时调整对总体交易价格的估计。
我们可能会签订包含多项履约义务的安排。此类安排可能包括我们交付成果的任意组合。如果合同包含多项承诺的交付成果,我们将进行判断,以确定承诺的交付物在合同背景下是否能够与众不同。如果不满足这些标准,则将承诺的交付项作为综合履约义务入账。对于具有多个不同绩效义务的安排,我们将与50-50的开发服务成本分摊额相关的可变对价直接分配给相关的绩效义务,然后根据其相对的独立销售价格在绩效义务之间分配剩余的对价。
独立销售价格是我们单独向客户出售承诺的商品或服务的价格。当无法直接观察时,我们通常会估算每项不同履约义务的独立销售价格。与我们履行特定履约义务的努力相关的可变对价完全分配给这些履约义务。交易价格的其他组成部分是根据相对的独立销售价格分配的,管理层对此做出了重要的判断。我们制定的假设需要做出判断,以确定与许可证相关的履约义务的独立销售价格,其中可能包括预测的收入、开发时间表、人员成本补偿率、贴现率以及技术、监管和商业成功的概率。我们通过预测履行履约义务的预期成本加上适当的利润率来估算研发绩效义务的独立销售价格。
如果许可证是单独的履约义务,则在许可证转让给被许可人且被许可人可以使用许可证并从中受益时,我们会从不可退还的预付费用中确认分配给许可证的收入。对于与其他不同或合并义务捆绑在一起的许可证,我们使用判断来评估履约义务的性质,以确定履约义务是否在一段时间内得到履行,如果在一段时间内得到履行,则采用适当的方法来衡量进展情况,以确认收入。如果绩效义务在一段时间内得到履行,我们会评估每个报告期的进展衡量标准,并在必要时调整业绩衡量标准和相关的收入确认。
选择衡量完成进展情况的方法需要作出判断,并以所提供的产品或服务的性质为基础。收入按成本发生的比例记录。我们通常使用成本对成本的进度衡量标准,因为它最能描述在我们产生成本时向客户转移控制权的情况。在衡量进展的成本对成本的衡量标准下,完成工作的进展程度是根据迄今发生的费用与履行义务完成时估计总成本的比率来衡量的(主题606下的输入法)。我们使用判断来估算完成研发绩效义务的预期总成本,其中包括分包商的成本、劳动力、材料、其他直接成本和间接成本的分配。我们会评估这些成本估算值和每个报告期的进展情况,并在必要时调整进展衡量标准和相关的收入确认。
9
目录
对于包括基于销售或基于使用量的特许权使用费的安排,我们在 (i) 相关销售发生时或 (ii) 部分或全部特许权使用费分配的履约义务得到履行或部分履行时,以较晚者为准。迄今为止,我们尚未确认来自许可协议的任何基于销售或基于使用量的特许权使用费收入。
关于我们 2020 年 4 月的协和麒麟有限公司 (KKC) 许可、开发和商业化协议(KKC 商业化协议)如中所述 注意事项 7.许可协议,该协议于 2023 年 7 月终止,我们提供了与 50-50 成本分摊安排相关的开发服务,该安排的收入将随着时间的推移予以确认。此外,我们不时应KKC的要求为他们提供服务,其费用已全额报销给我们。我们将此类直通服务的报销记录为收入
我们确认了本报告所述期间与KKC商业化协议相关的收入(以千计):
|
|
在截至3月31日的三个月中, |
|
|
在截至3月31日的九个月中 |
|
||||||||||
|
|
2024 |
|
|
2023 |
|
|
2024 |
|
|
2023 |
|
||||
收入确认时间: |
|
|
|
|
|
|
|
|
|
|
|
|
||||
一段时间内提供的服务 |
|
$ |
|
|
$ |
|
|
$ |
|
|
$ |
|
||||
在某个时间点传递服务 |
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
$ |
|
|
$ |
|
|
$ |
|
|
$ |
|
||||
合约余额
在我们的简明合并资产负债表中,应收账款包含在预付费用和其他流动资产中,合同负债包含在递延收入和长期递延收入中。我们在主题606下记账的合同负债与分配给开发服务绩效义务的初始预付金额有关。合同负债根据发生的成本相对于预期总成本在履约义务期内予以确认。
截至 2024 年 3 月 31 日、2023 年 6 月 30 日和 2022 年 6 月 30 日,我们有
|
|
2024年3月31日 |
|
|
2023年6月30日 |
|
|
2022年6月30日 |
|
|||
未开单应收账款 |
|
$ |
|
|
$ |
|
|
$ |
|
|||
合同负债包含在递延收入和递延收入中 |
|
$ |
|
|
$ |
|
|
$ |
|
|||
合同负债的期初和期末金额的对账情况如下(以千计),合同负债主要与KKC商业化协议下开发服务转让的合并履约义务有关,根据协议下的研究计划,合同负债是公司合同中的一项单独履约义务:
|
|
2024年3月31日 |
|
|
2023年6月30日 |
|
||
期初余额 |
|
$ |
|
|
$ |
|
||
确认为收入: |
|
|
|
|
|
|
||
在履行义务后确认的收入 |
|
|
( |
) |
|
|
( |
) |
因履约义务估计值变动而确认的收入 |
|
|
|
|
|
( |
) |
|
已确认的履约义务的收入将不再有效 |
|
|
|
|
|
( |
) |
|
期末余额 |
|
$ |
|
|
$ |
|
||
收入确认、开具发票和现金收款的时机会产生已开票的应收账款和未开票的应收账款(合同资产)和递延收入(合同负债)。我们根据商定的合同条款向客户开具发票,通常是定期开具或在合同里程碑完成后开具发票。开具发票可能会在收入确认之后发生,从而产生未开票的应收账款。我们可能会在确认收入之前收到客户的预付款,从而产生合同负债。与KKC商业化协议相关的简明合并资产负债表中报告的未开票应收账款和递延收入。
10
目录
来自合作者的收入
在合同开始时,我们会评估合作安排是否在ASC主题808的范围内, 合作安排 (主题808),以确定此类安排是否涉及既积极参与活动又面临重大风险和回报的各方开展的联合经营活动,这取决于此类活动的商业成功。该评估是根据协议中所有各方的责任进行的。对于主题808范围内包含多个记账单位的合作安排,我们首先确定该安排中的哪些记账单位属于主题808的范围,哪些要素属于主题606的范围。对于合作安排中根据主题808核算的记账单位,通过类比权威会计文献,确定并一致地应用适当的确认方法。对于根据主题606核算的合作安排要素,我们按上文所述确认收入。收到的不符合主题606收入确认标准要求的对价在随附的简明合并资产负债表中记录为递延收入,根据我们对何时确认此类金额的最佳估计,归类为当期或长期递延收入。
每股净收益(亏损)
每股基本和摊薄后的净收益(亏损)是使用该期间已发行普通股的加权平均数减去任何可能被回购或没收的股票计算得出的。曾经有
就截至2024年3月31日和2023年3月31日的三个月和九个月的摊薄后每股净收益(亏损)的计算而言,潜在的稀释后每股净收益(亏损)不包括在计算摊薄后的每股净收益(亏损),因为截至2024年3月31日和2023年3月31日,它们的加权平均行使价分别高于我们的加权平均股价;因此,三个月和九个月的每股基本净收益(亏损)相同 2024 年 3 月 31 日和 2023 年 3 月 31 日结束。
下表列出了在摊薄后每股净收益(亏损)(以千计)计算中排除的潜在稀释性股票:
|
|
在截至3月31日的三个月中, |
|
|
在截至3月31日的九个月中 |
|
||||||||||
|
|
2024 |
|
|
2023 |
|
|
2024 |
|
|
2023 |
|
||||
股票期权 |
|
|
|
|
|
|
|
|
|
|
|
|
||||
认股证 |
|
|
|
|
|
|
|
|
|
|
|
|
||||
反摊薄股票总额 |
|
|
|
|
|
|
|
|
|
|
|
|
||||
最近的会计公告
最近采用
2016年6月,财务会计准则委员会(FASB)发布了第2016-13号会计准则更新, 金融工具——信用损失(主题 326):金融工具信用损失的衡量(亚利桑那州立大学 2016-13),经修订。亚利桑那州立大学2016-13年度的修正案除其他外,要求按摊销成本计量的金融资产按预期收取的净额列报,而先前的美国公认会计原则将确认推迟到可能发生亏损之后。亚利桑那州立大学2016-13年度的修正案对2022年12月15日之后开始的财政年度有效,包括这些财政年度内的过渡期,允许提前通过。亚利桑那州立大学2016-13年度的通过并未对我们的财务报表和相关披露产生重大影响。
最近发行
财务会计准则委员会或其他准则制定机构不时发布新的会计公告,这些公告自规定的生效日期起通过。我们认为,除下文所述准则外,最近发布的准则以及任何已发布但尚未生效的准则的影响在采用后不会对我们的简明合并财务报表产生重大影响。
2023 年 11 月,财务会计准则委员会发布了 ASU 第 2023-07 号 细分市场报告(主题 280):对可报告的细分市场披露的改进,它要求公共实体每年和中期披露重要的分部支出和其他分部项目,并在过渡期内提供目前每年要求的有关应申报细分市场的损益和资产的所有披露。此外,它要求公共实体披露首席运营决策者的头衔和职位。该亚利桑那州立大学不会改变公共实体识别其运营部门、汇总运营部门或将量化阈值应用于
11
目录
确定其可报告的细分市场。新标准对2023年12月15日之后开始的财政年度以及2024年12月15日之后开始的财政年度内的过渡期有效,允许提前采用。公共实体应将本亚利桑那州立大学中的修正案追溯应用于财务报表中列报的所有先前时期。我们预计,该亚利桑那州立大学只会影响我们的披露,不会影响我们的经营业绩、现金流和财务状况。
2023 年 12 月,财务会计准则委员会发布了 ASU 第 2023-09 号 所得税(主题 740):所得税披露的改进,重点是税率对账和缴纳的所得税。亚利桑那州立大学第2023-09号要求公共企业实体(PBE)每年披露使用百分比和货币金额的表格汇率对账表,细分为特定类别,某些对账项目按性质和管辖范围进一步细分,只要这些项目超过规定的阈值。此外,如果金额至少占所得税缴纳总额的5%,则所有实体都必须披露已缴纳的所得税,扣除收到的退款后,按联邦、州/地方和外国以及司法管辖区分类。对于PBE,新标准自2024年12月15日之后的年度内生效,允许提前采用。实体可以通过提供截至2025年12月31日的经修订的披露并继续提供前一时期的亚利桑那州立大学前期披露信息,来预期地适用本亚利桑那州立大学的修正案,也可以通过提供所有报告期的修订后的披露来追溯适用修正案。我们预计,该亚利桑那州立大学只会影响我们的披露,不会影响我们的经营业绩、现金流和财务状况。
3。资产负债表详情
财产和设备,净额
财产和设备,净额包括以下各项(以千计):
|
|
2024年3月31日 |
|
|
2023年6月30日 |
|
||
家具和设备 |
|
$ |
|
|
$ |
|
||
租赁权改进 |
|
|
|
|
|
|
||
|
|
|
|
|
|
|
||
减去:累计折旧 |
|
|
( |
) |
|
|
( |
) |
财产和设备,净额 |
|
$ |
|
|
$ |
|
||
截至2024年3月31日和2023年3月31日的三个月,财产和设备的折旧费用为 $
应计负债
应计负债包括以下各项(以千计):
|
|
|
|
|
|
|
||
|
|
2024年3月31日 |
|
|
2023年6月30日 |
|
||
应计临床前和临床试验费用 |
|
$ |
|
|
$ |
|
||
应计薪酬和福利(1) |
|
|
|
|
|
|
||
应计法律和专业服务 |
|
|
|
|
|
|
||
向 KKC 提供的应计补偿 |
|
|
|
|
|
|
||
其他 |
|
|
|
|
|
|
||
应计负债总额 |
|
$ |
|
|
$ |
|
||
4。公允价值测量
由于这些工具的短期到期,现金等价物、短期投资和应付账款等金融工具的账面金额接近相关的公允价值。我们将多余的现金投资于易于兑换成现金的金融工具,例如货币市场基金和美国政府证券。根据公允价值层次结构的定义,现金等价物和短期投资被归类为第一级。截至 2024 年 3 月 31 日和 2023 年 6 月 30 日,我们有
12
目录
2018年5月,我们发行了与私募普通股相关的认股权证。根据认股权证的条款,如果收购我们,本可以要求我们以现金结算认股权证,因此,认股权证必须按公允价值计量,并在简明的合并资产负债表中列报为负债。我们在发行时使用Black-Scholes估值模型记录了认股权证的公允价值,并被要求在每个报告日对认股权证进行重估,并在我们的简明合并运营报表中记录公允价值的任何变化,直至2023年5月到期。认股权证的估值被视为公允价值层次结构的第三级,因为在估值中需要使用对公允价值衡量重要且不可观察的假设。用于确定认股权证负债估计公允价值的输入包括标的股票在估值日的估计公允价值、认股权证的估计期限、无风险利率、预期分红和标的股票的预期波动率。权证负债公允价值衡量中使用的不可观察的重要输入是波动率和认股权证的估计期限。通常,标的股票公允价值和预计期限的增加(减少)将导致与公允价值衡量的方向相似的影响。三级认股权证负债公允价值的变化反映在截至2023年3月31日的三个月和九个月的简明合并运营报表中。在截至2024年3月31日的三个月和九个月以及截至2023年6月30日的年度中,有
计算截至当日认股权证负债的公允价值 2023 年 6 月 30 日,使用了以下假设:
无风险利率 |
|
|
% |
|
预期寿命(年) |
|
|
|
|
预期波动率 |
|
|
% |
|
股息收益率 |
|
|
% |
|
加权平均拨款日期公允价值 |
|
$ |
|
下表汇总了我们的三级认股权证负债的估计公允价值的变化 截至 2023 年 3 月 31 日的九个月(以千计):
截至2022年6月30日的余额 |
|
$ |
|
|
负债分类认股权证的估计公允价值的变化 |
|
|
( |
) |
截至2023年3月31日的余额 |
|
$ |
|
5。一次性员工解雇补助金
关于我们共同决定停止在日本以外地区开发赞德利西布,我们于2022年12月宣布调整临床开发工作,精简了我们的组织,以继续对我们较早的两个临床阶段资产voruciclib和 ME-344 进行临床开发。因此,我们的董事会批准了分期裁员(裁员),其影响是
下表汇总了我们与应计负债中包含的一次性员工解雇补助金相关的活动(以千计):
|
|
一次性员工解雇补助金 |
|
|
截至 2023 年 6 月 30 日的余额 |
|
$ |
|
|
应计重组增加 |
|
|
|
|
现金支付 |
|
|
( |
) |
截至 2024 年 3 月 31 日的余额 |
|
$ |
|
|
13
目录
6。承诺和意外开支
我们已经与各种顾问和第三方签订了合同,以协助我们为领先的药物化合物进行临床前研发和临床试验工作。合同可以随时终止,但我们有义务向供应商偿还截至终止之日所产生的任何时间或费用。我们还与某些在职员工签订了雇佣协议,其中规定,如果他们在特定情况下终止雇用,则应支付遣散费,并加快股份奖励的归属。
诉讼
我们可能会不时参与正常业务过程中出现的各种诉讼、法律诉讼或索赔。管理层认为,截至2024年3月31日,没有针对我们的索赔或诉讼待处理,这些索赔或诉讼将对我们的业务、流动性、财务状况或经营业绩产生重大不利影响。但是,诉讼存在固有的不确定性,这些或其他问题可能会不时产生不利结果,这可能会损害我们的业务。
赔偿
根据我们修订和重述的公司注册证书和章程,我们对我们的高级管理人员和董事在担任此类职务期间的某些事件或事件负有赔偿义务,但须遵守一定的限制。迄今为止没有索赔,而且我们有一份董事和高级管理人员责任保险单,这可能使它能够收回为未来索赔支付的任何金额的一部分。
预售许可协议
如中所述 注释 8.其他许可协议,我们是与Presage Biosciences, Inc.(Presage)签订的许可协议的当事方,根据该协议,我们可能需要在实现某些开发、监管和商业里程碑后支付未来款项,并可能根据净销售额支付未来的特许权使用费。截至 2024 年 3 月 31 日,我们有
7。许可协议
协和麒麟有限公司许可、开发和商业化协议
2020年4月,我们签订了KKC商业化协议,根据该协议,我们根据我们控制的某些专利和专有技术向KKC授予了共同独家、可再许可、付费的许可,用于在美国开发和商业化赞德利西布和任何含有赞德利西布的药品(美国许可证),以及独家的(受某些保留的履行KKC商业化义务的保留权利的约束)协议),可再许可,付款,根据受控制的某些专利和专有技术进行许可我们将在美国以外的国家为所有人体适应症开发和商业化赞德利西布和任何含有赞德利西布的药品。KKC根据KKC控制的某些专利和专有技术授予我们共同独家、可再许可、许可证,用于在美国开发和商业化赞德利西布用于所有人体适应症,并根据某些专利和专有技术授予共同独家、可再许可、免版税、全额付费的许可由 KKC 控制,以履行我们在前美国境内的义务KKC 还向我们支付了首笔不可退还的款项 $
2022年11月,我们和KKC共同决定停止在美国开发赞德利西布,2023年5月,KKC决定停止在日本开发赞德利西布。考虑到停止在全球范围内开发zandelisib的决定,双方签订了终止协议
我们确定KKC商业化协议是根据主题808的合作安排,该协议包含多个记账单位,因为我们和KKC都是开发和商业化活动的积极参与者,面临的重大风险和回报取决于该安排活动的商业成功。我们确定美国许可证是主题808范围内的单独记账单位,不是主题606下的交付品,而在其领土内发放给KKC的许可证和相关开发服务属于主题606的范围。参见内部讨论 收入确认的子节 注意事项 2。重要会计政策摘要.
14
目录
我们评估了ASC 606下的终止协议,并确定该协议符合合同修改的要求,该修改改变了KKC商业化协议的范围,与清盘活动相关的剩余商品和服务有待转让。履行我们向KKC提供同情用途供应的履约义务的成本确定为 最低限度因此,在KKC商业化协议的背景下,这并不重要。截至2023年9月30日,与同情用途供应相关的活动已经完成。
8。其他许可协议
预售许可协议
2017年9月,我们作为被许可方与Presage签订了许可协议。根据许可协议条款,Presage授予我们开发、制造和商业化voruciclib(一种临床阶段、口服和选择性CDK抑制剂)及相关化合物的全球独家权利。作为交换,我们支付了 $
百济神州合作
2018年10月,我们与百济神州有限公司(百济神州)开展临床合作,评估赞德利西布与百济神州的zanubrutinib(名为Brukinsa®)(一种布鲁顿酪氨酸激酶抑制剂)联合用于治疗B细胞恶性肿瘤患者的安全性和有效性。根据临床合作协议的条款,我们修改了正在进行的1b期试验,将赞德利西布与扎努布替尼联合用于B细胞恶性肿瘤患者的评估纳入其中。研究费用由各方平均分担,我们同意提供赞德利西布,百济神州同意提供扎努布替尼。我们将百济神州报销的费用记录为研发费用的减少额。我们保留了赞德利西布的全部商业权利,百济神州保留了zanubrutinib的全部商业权利。随着日本以外的赞德利西布计划的终止,该临床合作于2023年9月28日终止。在截至2024年3月31日和2023年3月31日的三个月中,成本报销在简明的合并运营报表中记录为研发成本的减少大约是
9。租赁
2020年7月,我们签订了租赁协议(初始租赁协议),价格约为
15
目录
修订后的租赁协议还规定了额外的
租赁协议在所列期间的总运营租赁成本如下(以千计):
|
|
在截至3月31日的三个月中, |
|
|
在截至3月31日的九个月中 |
|
||||||||||
|
|
2024 |
|
|
2023 |
|
|
2024 |
|
|
2023 |
|
||||
运营租赁成本 |
|
$ |
|
|
$ |
|
|
$ |
|
|
$ |
|
||||
可变租赁成本 |
|
|
|
|
|
|
|
|
|
|
|
|
||||
总租赁成本包含在一般和管理费用中 |
|
$ |
|
|
$ |
|
|
$ |
|
|
$ |
|
||||
与我们的经营租赁相关的补充现金流信息如下(以千计):
|
|
在截至3月31日的三个月中, |
|
|
在截至3月31日的九个月中 |
|
||||||||||
|
|
2024 |
|
|
2023 |
|
|
2024 |
|
|
2023 |
|
||||
为计量中包含的金额支付的现金 |
|
|
|
|
|
|
|
|
|
|
|
|
||||
来自经营租赁的运营现金流 |
|
$ |
|
|
$ |
|
|
$ |
|
|
$ |
|
||||
以下是截至目前租赁协议下与经营租赁负债对账的未来最低租赁付款明细表 2024 年 3 月 31 日(以千计):
截至 2024 年 6 月 30 日的财政年度的剩余时间 |
|
$ |
|
|
截至6月30日的年份 |
|
|
|
|
2025 |
|
|
|
|
2026 |
|
|
|
|
2027 |
|
|
|
|
2028 |
|
|
|
|
此后 |
|
|
|
|
租赁付款总额 |
|
|
|
|
减去:现值折扣 |
|
|
( |
) |
经营租赁负债总额 |
|
$ |
|
|
|
|
|
|
|
资产负债表分类-经营租赁 |
|
|
|
|
经营租赁责任 |
|
$ |
|
|
长期经营租赁负债 |
|
|
|
|
经营租赁负债总额 |
|
$ |
|
|
|
|
|
|
|
其他资产负债表信息-经营租赁 |
|
|
|
|
加权平均剩余租赁期限(以年为单位) |
|
|
|
|
加权平均折扣率 |
|
|
% |
|
10。股东权益
股权交易
认股证
2023 年 5 月,未兑现的认股权证
16
目录
截至2024年3月31日,我们有未兑现的认股权证待购
资本存量描述
我们的总法定股本为
常见 股票
普通股持有人有权
市场发行协议
2024年2月20日,我们与JoneStrading Institution Services LLC签订了按需资本销售协议,根据该协议,我们能够发行和出售总发行价不超过美元的股票
首选 股票
我们的董事会有权发布最多
权利协议
开启
11。基于股份的薪酬
我们使用基于股份的薪酬计划为员工提供长期绩效激励。这些激励措施主要包括股票期权和限制性股票单位(RSU)。2008年12月,我们通过了经不时修订和重述的MEI Pharma, Inc.2008年股票综合股权补偿计划(综合计划),根据该计划
2021年5月,我们通过了2021年激励计划(激励计划),根据该计划
17
目录
所有股票奖励的基于股份的薪酬支出总额包括所列期间的以下各项(以千计):
|
|
在截至3月31日的三个月中, |
|
|
在截至3月31日的九个月中 |
|
||||||||||
|
|
2024 |
|
|
2023 |
|
|
2024 |
|
|
2023 |
|
||||
研究和开发 |
|
$ |
|
|
$ |
|
|
$ |
|
|
$ |
|
||||
一般和行政 |
|
|
|
|
|
|
|
|
|
|
|
|
||||
基于股份的薪酬总额 |
|
$ |
|
|
$ |
|
|
$ |
|
|
$ |
|
||||
股票期权
授予员工的股票期权背心
我们的股票期权活动和相关数据摘要如下:
|
|
的数量 |
|
|
加权平均值 |
|
|
加权平均值 |
|
|
聚合 |
|
||||
截至 2023 年 6 月 30 日的未付款 |
|
|
|
|
$ |
|
|
|
|
|
|
|
||||
已授予 |
|
|
|
|
$ |
|
|
|
|
|
|
|
||||
被没收 |
|
|
( |
) |
|
$ |
|
|
|
|
|
|
|
|||
截至 2024 年 3 月 31 日未缴清 |
|
|
|
|
$ |
|
|
|
|
|
$ |
|
||||
已归属,预计将于 2024 年 3 月 31 日归属 |
|
|
|
|
$ |
|
|
|
|
|
$ |
|
||||
截至2024年3月31日,未偿还期权的总内在价值是根据标的期权的行使价与我们的普通股收盘价之间的差额计算得出的 $
与非既得股票期权相关的未确认薪酬支出总计 $
Black-Scholes期权定价模型中用于确定期权授予公允价值的加权平均假设如下:
|
|
在截至3月31日的九个月中 |
|
|||||
|
|
2024 |
|
|
2023 |
|
||
无风险利率 |
|
|
% |
|
|
% |
||
预期寿命(年) |
|
|
|
|
|
|
||
波动率 |
|
|
% |
|
|
% |
||
股息收益率 |
|
|
% |
|
|
% |
||
加权平均拨款日期公允价值 |
|
$ |
|
|
$ |
|
||
18
目录
第 2 项。管理层对财务状况和经营业绩的讨论和分析
本10-Q表季度报告(季度报告)包括经修订的1933年《证券法》(《证券法》)第27A条和经修订的1934年《证券交易法》(《交易法》)第21E条所指的前瞻性陈述。除本季度报告中包含的历史事实陈述以外的所有陈述,包括有关未来财务状况、业务战略以及管理层未来运营计划和目标的陈述,均为前瞻性陈述。相信、可能、将、估计、继续、预期、打算、应该、计划、预期以及与我们相关的类似表述旨在识别前瞻性陈述。我们的这些前瞻性陈述主要基于当前对未来事件和财务趋势的预期和预测,我们认为这些事件和财务趋势可能会影响我们的财务状况、经营业绩、业务战略和财务需求。这些前瞻性陈述受许多风险、不确定性和假设的影响,包括但不限于我们在2023年9月26日向美国证券交易委员会提交的2023年10-K表年度报告(2023年年度报告)中描述的风险、不确定性和假设。以下是我们面临的主要风险的摘要:
摘要风险因素
我们的业务面临许多风险和不确定性,在投资我们的普通股之前,您应该考虑这些风险和不确定性。以下是我们面临的主要风险的摘要:
19
目录
20
目录
这些风险并非穷尽无遗。本报告的其他部分以及我们向美国证券交易委员会(SEC)提交的其他文件包括可能对我们的业务和财务业绩产生不利影响的其他因素。此外,我们在竞争激烈且瞬息万变的环境中运营。新的风险因素不时出现,我们无法预测所有风险因素,也无法评估所有因素对我们业务的影响,也无法评估任何因素或因素组合在多大程度上可能导致实际结果与任何前瞻性陈述中包含的结果存在重大差异。
您不应依赖前瞻性陈述作为对未来事件的预测。我们无法向您保证,前瞻性陈述中反映的事件和情况将会实现或发生。尽管我们认为前瞻性陈述中反映的预期是合理的,但我们无法保证未来的业绩、活动水平、业绩或成就。过去的表现可能不是未来业绩的指标。以下讨论完全受本季度报告其他地方的简明合并财务报表及其附注中列出的更详细信息的限制,以及我们向美国证券交易委员会提交的2023年年度报告中包含的经审计的财务报表及其附注中列出的更详细的信息,应与这些信息一起阅读。经营业绩不一定代表未来可能出现的业绩。
概述
MEI Pharma, Inc.(纳斯达克股票代码:MEIP)是一家临床阶段的制药公司,致力于开发新的差异化癌症疗法。我们通过收购有前途的抗癌药物来建立我们的产品线,并酌情通过临床开发、战略合作伙伴关系、外包许可或商业化为项目创造价值。我们的肿瘤药物开发方法是评估我们的候选药物与标准护理疗法的组合,以克服已知的耐药机制,满足明确的医疗需求,从而改善患者的受益。候选药物管道包括口服细胞周期蛋白依赖性激酶9(CDK9)抑制剂voruciclib和静脉注射线粒体氧化磷酸化(OXPHOS)小分子抑制剂 ME-344。我们的普通股在纳斯达克资本市场上市,股票代码为MEIP。
我们认为,我们的现金足以为至少12个月的运营提供资金。2023年10月31日,我们宣布与安信基金(安生)和缆车资本(缆车)签订合作协议(合作协议),其中包含以下关键条款:
21
目录
作为合作协议的一部分,Anson和Cable Car撤回了征求同意的请求,并同意遵守惯常的停顿条款。此外,我们偿还了截至合作协议签署之日Anson和Cable Car与我们合作的相关费用和开支,金额为110万美元。
2024 年 4 月,该公司报告称,其董事会一致同意一项战略,将voruciclib的临床开发作为优先事项,同时允许为1期研究开发新的 ME-344 配方。此外,公司董事会一致决定不根据2023年10月31日的合作协议进行潜在的第二次资本回报,以节省资源和调整战略投资,从而延长公司的运营轨道。
临床开发项目
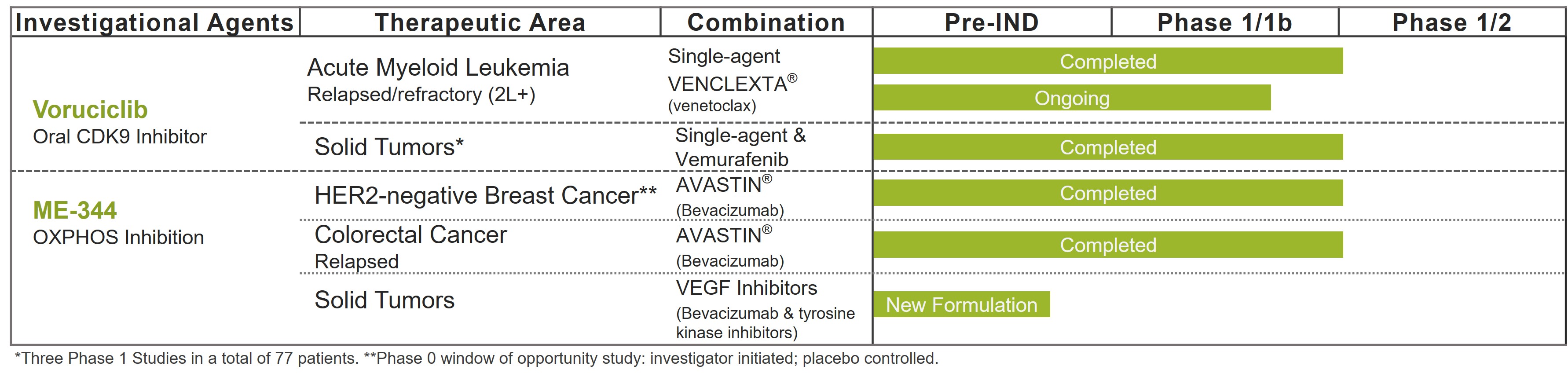
我们的临床阶段候选药物管线包括口服CDK9抑制剂voruciclib和静脉注射小分子抑制剂线粒体氧化磷酸化(OXHPHOS)ME-344。

Voruciclib:1期研究中的强效口服CDK9抑制剂
Voruciclib 是一种选择性口服的 CDK9 抑制剂。Voruciclib正在一项1期试验中进行研究,该试验目前正在评估急性髓系白血病(AML)患者与B细胞淋巴瘤2(BCL-2)抑制剂venetoclax(名为Venclexta®)联合使用的剂量和时间表。Voruciclib还在临床前研究中接受评估,以探索各种实体瘤癌的潜在活性,包括与靶向RAS信号通路的疗法(例如KRAS抑制剂)联合使用。
Voruciclib 科学概述:细胞周期信号
CDK9在细胞周期调节中具有重要功能,包括调节癌症的两个治疗靶标:
从历史上看,直接抑制MCL1和MYC一直很困难,但是CDK9是间接靶向这些致癌基因的一种有前途的方法。
22
目录
Voruciclib:抑制 MCL1
CDK9 是 MCL1 的已知转录调节剂。MCL1 的过度表达经常出现在许多肿瘤类型中,与肿瘤发生、预后不良和耐药性密切相关。在急性髓细胞白血病中,大约一半的患者的MCL1被上调 复发和难治性(R/R)疾病并且与这些患者的预后不佳有关。同样重要的是,高水平的MCL1表达与对venetoclax的耐药性有关。
在临床前研究中,voruciclib显示出对MCL1的剂量依赖性抑制;2017年12月,发表在《自然科学报告》杂志上的一项针对voruciclib的研究报告称,voruciclib与 BCL-2 抑制剂venetoclax的组合能够抑制两种细胞存活的主要调节剂,MCL-1 和 BCL-2,并在DLBCL细胞的侵袭性子集中产生协同抗肿瘤作用。
在2020年发表的一份经过同行评审的手稿中,有报道称,在急性髓细胞白血病临床前模型中,voruciclib对CDK9的抑制会协同增强 BCL-2 抑制剂venetoclax诱导的细胞死亡。数据表明,voruciclib与venetoclax协同作用,在急性髓细胞白血病细胞系和原发患者样本中诱导程序性细胞死亡或细胞凋亡。研究还表明,voruciclib下调了MCL1,这与voruciclib和venetoclax之间的协同作用有关,而且voruciclib下调了MYC,这也有助于与venetoclax的协同作用。
随后,与报告的临床前研究一致,正在进行的一项评估voruciclib作为单一药物以及与venetoclax联合治疗复发或难治性(R/R)急性髓细胞白血病患者的1期研究的数据也表明,Mcl-1蛋白的预期降低。
该研究表明,voruciclib有可能成为一种有吸引力的治疗药物,用于与venetoclax或其他 BCL-2 抑制剂联合治疗癌症,以解决与MCL1相关的潜在耐药性,并支持我们正在进行的急性髓细胞白血病中voruciclib的临床评估。
Voruciclib:抑制 MYC
许多癌症与 MYC 的过度表达有关,MYC 是一种调节细胞增殖和生长的转录因子。CDK9 是已知的 MYC 转录调节剂,也是 MYC 蛋白磷酸化的调节剂。美国癌症研究协会(AACR)2021年年会上在临床前模型中报告的数据表明,voruciclib:
提出的研究表明,视MYC的活性而定,voruciclib可能是治疗血液癌和实体瘤的有吸引力的治疗药物。
临床项目
在1期临床试验中,我们目前正在评估voruciclib与Venetoclax(一种 BCL-2 抑制剂 venetoclax)联合治疗复发/难治性急性髓细胞白血病患者的剂量和时间表。该试验首先评估了先前标准疗法失败后复发和难治性B细胞恶性肿瘤和急性髓细胞白血病患者的单一疗法voruciclib的剂量和时间表,以确定安全性、初步疗效和最大耐受剂量。该研究的主要目标是确定voruciclib单一疗法或voruciclib与venetoclax联合使用的安全性和生物有效剂量。该研究的次要目标包括评估voruciclib单一疗法或voruciclib与venetoclax联合使用的初步疗效、药代动力学、药效学和生物标志物。
正如我们在2023年12月的美国血液学会(ASH)年会上发布的海报中所报道的那样,该研究的voruciclib单一疗法剂量增加/扩大阶段共招收了40名患者并已完成。大多数患者(n=21)患有急性髓细胞白血病,其余患者(n=19)患有B细胞恶性肿瘤。在40名入组患者中,前16名患者每天连续给药50和100毫克,接下来的24名患者间歇性给药(28天周期内连续14天接受治疗),分别为100、150和200 mg。所有患者均接受了大量预先治疗,平均值为先前三种疗法(范围为1-9),有五名患者先前接受过造血干细胞移植。在28天周期(队列2)中连续14天给药的剂量高达200 mg的Voruciclib耐受性良好,没有报告剂量限制毒性(DLT)。最常见的不良事件(≥ 20% 的患者)是腹泻、恶心、贫血和疲劳。绝大多数不良事件为1-2级;值得注意的是,队列2中唯一的3-4级不良事件是腹泻(n=1)和贫血(n=5)。药代动力学是剂量成比例的,平均半衰期约为24小时,支持每天给药一次。
23
目录
在选择进一步开发的间歇给药计划中,没有观察到DLT,没有发现3级或更高的药物相关毒性,在达到最大耐受剂量之前,剂量递增停止在200 mg,因为血浆浓度达到了被认为足以抑制靶点的水平。在21名加入急性髓细胞白血病的患者中,一名100 mg的患者达到无形态白血病状态,9名患者病情稳定,两名患者病情持续了至少三个月。在入组的19名B细胞恶性肿瘤患者中,有4名患者病情稳定,肿瘤大小减小。评估髓系白血病细胞分化蛋白(Mcl-1)和Ser2(RNA Pol II p-s2)上RNA Pol II磷酸化的相关研究的初步结果表明,表达的降低与voruciclib对Mcl-1和RNA Pol II p-s2的预期靶药效学作用一致。
自报告该研究单一疗法阶段的数据以来,我们已进入下一阶段的研究,即评估7种voruciclib剂量水平,在28天周期内连续14天与标准剂量venetoclax联合治疗复发/难治性急性髓细胞白血病患者的标准剂量venetoclax。2024年4月,我们报告说,共有29名复发/难治性急性髓细胞白血病患者参加了评估voruciclib与venetoclax联合使用的研究的剂量递增阶段,中位年龄为67岁(范围在34-89岁之间)。这些患者通常接受了大量的预治疗;先前治疗的中位数为3例(范围为1-7),15例(52%)患者先前有≥3例。在早期的治疗方案中,几乎所有患者(28/29)都接受了venetoclax的治疗。此外,由于不良的细胞遗传学和分子突变,有21名(72%)患者被列为2017年ELN不良风险类别。
在与venetoclax联合使用剂量为100 mg或以上的voruciclib的20名患者中,有三名患者取得了缓解,其中包括两名获得完全缓解但血液学恢复不完整(CRi)的患者和一名达到形态学无白血病状态(MLFS)的患者,每例患者均在较早的治疗中接受了venetoclax。一名患者的反应持续了7个月,第二名患者的反应持续了5个月,第三名患者被转诊接受干细胞移植。此外,另有14名患者的病情稳定,在5名患者中持续了90天以上。
在与venetoclax联合使用剂量为100 mg或以上的voruciclib的20名患者中,对接受该组合治疗的患者可用样本的相关生物标志物分析研究的初步结果也表明,Mcl-1的预期降低,包括更高剂量下Mcl-1的降幅更大。这支持了我们的假设,即作为抑制剂或CDK9的voruciclib可以调节Mcl-1,因此可以解决与venetoclax相关的MCL1的上调。50%(10/20)的可评估患者在voruciclib/venetoclax给药后与给药前相比,给予voruciclib/venetoclax的骨髓爆炸次数有所降低,这也证明了抗白血病活性的其他证据。
Voruciclib在28天周期内连续14天给药,剂量高达300毫克,与标准剂量venetoclax联合使用,耐受性良好,未观察到剂量限制毒性。根据本附表与venetoclax一起给药的voruciclib的最大耐受剂量尚未确定。迄今为止,没有因药物相关不良事件而停药,也没有观察到重叠毒性的证据。最常见的(≥5%的患者)的3级不良事件是与急性髓细胞白血病相关的骨髓抑制。只有 1 名患者被观察到出现非血液学的 3 级药物相关不良事件(di腹泻)。
该研究仍在进行中,还在评估与venetoclax联合使用的一组12名患者的voruciclib,在28天周期内连续14天给药,每天300毫克。该研究将进一步评估服用超过21的voruciclib剂量不断增加的剂量28 天周期中的连续天数与venetoclax联合使用可增加剂量强度,并有可能优化患者的反应。预计将在2024年的剩余时间内公布正在进行的1期临床试验的临床数据,该试验评估了复发/难治性急性髓细胞白血病患者中的voruciclib加venetoclax。
此前,在多项1期研究中,Voruciclib还对70多名实体瘤患者进行了评估。所有临床数据以及临床前研究的数据表明,voruciclib能够在预计的每日剂量低至150 mg的情况下抑制其分子靶标。在一项临床研究中,评估了voruciclib与vemurafenib(以Zelboraf® 的名义销售)联合使用九名BRAF突变晚期/无法手术的恶性黑色素瘤患者。所有三名BRAF/MEK天真患者都取得了反应:两次部分反应和一次完全反应。在这项研究中,voruciclib的剂量为每天150毫克,外加vemurafenib 720 mg或960毫克,每天两次,周期为28天。最常见的不良事件是疲劳、便秘、腹泻、关节痛和头痛。3级疲劳的一个例子是剂量限制,没有报告与voruciclib相关的严重不良事件。其他临床研究评估了voruciclib在实体瘤患者中的剂量高达850 mg,这表明有更多证据表明了潜在的生物活性,而且不良事件概况与同类其他药物基本一致。
24
目录
ME-344:具有组合潜力的临床阶段线粒体抑制剂
ME-344 是一种抑制线粒体 OXPHOS 的新型候选药物,线粒体 OXPHOS 是参与线粒体中三磷酸腺苷 (ATP) 生成的基本代谢途径。ATP 提供能量来推动许多代谢细胞过程,包括分裂、增殖和生长。通过干扰 ATP 的产生,在非临床模型中,ME-344 已被证明可诱发癌细胞死亡,并且在临床研究中与抗肿瘤活性有关。 ME-344 在包括贝伐珠单抗(阿瓦斯汀®)在内的多项临床研究中也显示出临床活性。
目前, 我们正在通过开发一种新配方来推进 ME-344 的发展,目标是提高生物活性,改善患者的给药便利性并增加商业机会。在评估先前的 ME-344 配方与贝伐珠单抗(阿瓦斯汀®)联合使用的两项临床研究中,我们观察到令人鼓舞的数据后,我们认为新配方是挖掘该项目潜力的最佳方法。
ME-344 科学概述:癌症代谢
以 ATP 形式提供的能量可促进肿瘤新陈代谢,支持细胞分裂和生长。因此, 肿瘤细胞通常表现出较高的代谢率,以支持肿瘤细胞的存活和增殖。这种新陈代谢的增强需要以ATP的形式持续供应能量。 抗血管生成药物,例如血管内皮生长因子(VEGF)抑制剂贝伐珠单抗,有可能使血管系统正常化并减少ATP对糖酵解的依赖。由此产生的糖酵解减少可能引发对线粒体ATP产生能量的依赖增加,以支持肿瘤的持续增殖。在这种肿瘤可塑性情况下,ME-344 和贝伐珠单抗的组合可能会诱发代谢合成杀伤力,从而提供一种新的治疗策略。具体而言,利用贝伐珠单抗等抗血管原药物的能力来减少糖酵解,迫使肿瘤细胞通过受 ME-344 抑制的 OXPHOS 转向线粒体呼吸,可能会减少获得肿瘤细胞分裂和生长所需的 ATP 的机会。
我们在以下方面获得了有关这种方法的初步临床数据 一项已完成的由研究者发起的、多中心、随机、对照的机会窗口临床试验,评估 ME-344 与贝伐珠单抗联合使用,共招收了 42 名人类表皮生长因子受体 2 (HER2) 阴性乳腺癌患者。2024 年 4 月,一项针对以下患者的1b期研究报告了联合使用 ME-344 与贝伐珠单抗的进一步临床支持 标准疗法失败后复发的转移性结直肠癌(“mCRC”)。该研究显示了临床活性,包括对23名患者无进展存活率的影响。
较早的一项评估 ME-344 作为难治性实体瘤患者的单一药物的 1 期临床研究也显示出抗肿瘤活性,进一步证实了线粒体抑制作为一种有前途的治疗方式的潜力。
临床项目
ME-344 已作为单一药物进行了临床前和临床评估,并与贝伐珠单抗等抗血管生成药物联合使用。当作为单一药物进行评估时,ME-344 在 1b 期试验中显示出对难治性实体瘤具有活性的证据,在临床前研究中,使用 ME-344 治疗的肿瘤细胞会导致 ATP 快速流失和癌细胞死亡。除了单一药物活性外,ME-344 还显示出与抗血管生成疗法联合使用的巨大潜力。
临床前研究表明,抗血管生成药的一个结果是降低肿瘤糖酵解率,这是减缓肿瘤生长的一种机制。但是,当面对糖酵解减少和ATP产生减少时,肿瘤代谢能够转向线粒体代谢以产生能量,从而支持肿瘤的持续增殖。在这种情况下,在使用抗血管生成药物治疗的情况下出现肿瘤可塑性,同时使用 ME-344 靶向线粒体作为 ATP 的替代代谢来源,可能会开启重要的开发机会。
对这种组合使用 ME-344 的支持首次发表在 2016 年 6 月版的《细胞报告》上;与马德里西班牙国家癌症研究中心合作的临床前数据表明,ME-344 对癌细胞具有线粒体特异性作用,包括与抑制血管内皮生长因子活性的药物联合使用时的抗肿瘤活性显著增强。这些数据表明,由于抑制线粒体和糖酵解代谢,ME-344 与血管内皮生长因子抑制剂联合使用具有潜在的抗癌作用,为研究者发起的 ME-344 与贝伐珠单抗联合用于 HER2 阴性乳腺癌患者的试验提供了基础。
一项由研究者发起的多中心随机对照临床试验的结果发表在 2019 年 11 月号《临床癌症研究》上,该试验评估了 42 名早期 HER2 阴性乳腺癌女性中 ME-344 和贝伐珠单抗的组合,为联合使用 ME-344 与抗血管生成疗法提供了证据。
该试验的主要目的是证明 ME-344 的生物活性,衡量标准是与单独接受贝伐珠单抗的对照组相比,核蛋白 Ki67(其表达与肿瘤细胞增殖和生长密切相关)在第 0 天至第 28 天降低。次要目标包括确定 ME-344 生物活性是否与血管正常化相关。数据显示 ME-344 治疗组具有显著的生物活性:
25
目录
治疗的耐受性总体良好;报告了三起 3 级高血压不良事件,两起发生在 ME-344 组,一起发生在贝伐珠单抗组。
在评估乳腺癌患者的临床研究的基础上,一项 1b 期研究评估了标准疗法失败后复发转移性结直肠癌(“mCRC”)患者的 ME-344 联合贝伐珠单抗。该研究旨在评估多达两组患者的 ME-344 加贝伐珠单抗,每组大约 20 名患者。选择加入第二个队列的前提是队列 1 在四个月内达到预先确定的至少 20% 的非进展阈值。研究中的患者一直接受治疗,直到疾病进展或无法耐受。该研究的主要终点是16周的无进展生存期(“PFS”),次要终点包括总PFS、反应持续时间、总存活率和安全性。
ME-344 在第 1、8 和第 15 天每周给药一次,在每 28 天周期的第 1 天和第 15 天与贝伐珠单抗联合给药一次。第一组共招收了23名复发的mCRC患者。患者通常接受了大量的预治疗;先前治疗的中位数为4个(范围为1-8),18(78%)患者先前有≥3条临床治疗,所有患者之前都接受过贝伐珠单抗和标准化疗。正如2024年4月报告的那样,该组合的耐受性总体良好,未观察到重叠的毒性。两名患者(9%)因不良事件停止治疗:疲劳被认为与研究药物有关,败血症被认为无关。最常见(≥ 10% 的患者)药物相关不良事件(所有等级/等级≥3)是8(35%)/3(13%)名患者的疲劳和3(13%)名患者的腹痛(13%)/2(9%)。
另据报道,在第一组队列中,20名(25%)可评估患者中有5名在没有疾病进展证据的情况下完成了16周的治疗,超过了临床研究协议中规定的进入队列2的20%预定阈值。PFS中位数为1.9个月,4个月的PFS率为31.2%,中位总存活率为6.7个月,分析时有15名患者接受了检查。在20名可评估的患者中,有9名(45%)患有稳定的疾病。尽管队列1超过了预先确定的PFS门槛,但公司决定不启动第二个队列的注册。
早些时候针对难治性实体瘤患者进行的 ME-344 首次人体单药物 1 期临床试验的结果发表在 2015 年 4 月 1 日版的《癌症》上。结果表明,在接受 ME-344 治疗的 21 名可评估患者中,有 8 名(38%)的病情稳定或更好,其中包括五名无进展存活期的患者,其存活时间至少是进入试验前最后一次治疗的两倍。此外,其中一名患者,一名经过大量预先治疗的小细胞肺癌患者,已得到证实的部分缓解,并进行了两年的研究。当剂量等于或小于 10 mg/kg 时,ME-344 的耐受性通常良好,每周一次交付,持续时间较长。与治疗相关的不良事件包括恶心、头晕和疲劳。在15 mg/kg和20 mg/kg的剂量水平下均观察到剂量限制毒性,主要包括3级周围神经病变。
我们将继续通过开发一种新配方来研究 ME-344,以推进我们与贝伐珠单抗(阿瓦斯汀®)等血管内皮生长因子抑制剂联合使用诱导肿瘤合成杀伤力的新方法。该公司已经启动了新配方的研发活动,目标是提高生物活性,改善管理便利性并增加商业机会。
Zandelisib:PI3K抑制剂概述
赞德利西布是一种口服、每天一次的选择性PI3K△抑制剂,根据2020年4月签订的全球许可、开发和商业化协议,我们与KKC共同开发。
2022年3月,我们和KKC报告了与美国食品药品管理局第二阶段会议结束的结果,在该会议中,该机构不鼓励根据单臂TIDAL二期试验的数据提交申请。在这次会议上,美国食品药品管理局表示,单臂研究(例如TIDAL二期试验)生成的数据不足以充分评估评估惰性非霍奇金淋巴瘤的PI3K√抑制剂的风险/益处。当时,美国食品药品管理局强调,该公司将继续努力进行正在进行的评估复发或难治性滤泡性或边缘区淋巴瘤患者的随机3期COAST试验。随后,在美国食品药品管理局肿瘤药物咨询委员会2022年4月的会议上,该委员会投票决定,未来对用于血液系统恶性肿瘤的PI3K√抑制剂的批准应得到随机数据的支持。
2022年11月,我们和KKC在2022年3月第二阶段会议结束后的后续会议上与美国食品药品管理局会面。在这次会议上,美国食品和药物管理局为COASTAL三期试验的设计和统计分析提供了进一步的指导。在11月的会议之后,两家公司共同得出结论,一项临床试验符合美国食品药品管理局最近的指导方针,包括
26
目录
修改正在进行的COASTAL试验,可能无法在支持进一步投资或充分确定监管要求以获得批准以证明持续全球发展努力合理的时间内完成。因此,我们和KKC共同决定停止在全球范围内开发zandelisib用于治疗日本以外的惰性非霍奇金淋巴瘤。停止在日本以外的地区开发赞德利西布是基于美国食品药品管理局最新监管指导的商业决策,与迄今生成的赞德利西布临床数据无关。在共同决定终止日本境外开发后,我们和KKC开始关闭日本以外所有正在进行的zandelisib临床研究,包括COASTAL三期试验、TIDAL二期试验和CORAL二期试验。
随后,在2023年5月,KKC决定停止在日本开发赞德利西布。日本停用赞德利西布是KKC根据日本制药和医疗器械管理局的最新监管指导做出的商业决定,与迄今为止生成的zandelisib临床数据无关。
2023年7月14日,我们与KKC签订了终止协议(终止协议),终止双方之间的所有协议,并在全球范围内停止进一步的zandelisib临床开发。与同情用途供应相关的活动已在2024财年上半年完成。我们预计将在2024财年完成与KKC商业化协议相关的清盘活动。
KKC 许可、开发和商业化协议
2020年4月,我们签订了KKC商业化协议,根据该协议,我们根据我们控制的某些专利和专有技术向KKC授予了共同独家、可再许可、付费的许可,用于在美国开发和商业化赞德利西布和任何含有赞德利西布的药品(美国许可证),以及独家的(受某些保留的履行KKC商业化协议义务的保留权利的约束))、可再许可、付费、根据我们控制的某些专利和专有技术进行许可开发和商业化赞德利西布和任何含有赞德利西布的药品,用于美国以外的国家(前美国和前美国)的所有人体适应症许可证)。同样根据KKC商业化协议,我们在KKC控制的某些专利和专有技术下获得了共同独家、可再许可的许可,用于在美国开发和商业化zandelisib,用于所有人体适应症;根据KKC控制的某些专利和专有技术,我们获得了共同独家、可再许可、免版税、全额付费的许可,以履行我们在美国的义务,并获得了1亿美元的首期不可退还的付款。此外,在日本,KKC商业化协议包括潜在的监管和商业化里程碑付款,以及zandelisib在日本的净销售额的特许权使用费,这些特许权使用费从青少年时期开始分级。在2023年7月14日执行终止协议之前,KKC负责zandelisib在前美国的开发和商业化,除某些例外情况外,所有与之相关的费用全权负责。我们还向KKC提供了某些在前美国开发和商业化赞德利西布所需的药品供应,前提是KKC将在切实可行的情况下尽快承担出境美国的生产责任。
如上所述,2023年7月14日,我们与KKC签订了终止协议,共同终止了KKC商业化协议和双方之间的所有其他相关协议。根据条款国家协议:
截至2023年6月30日,我们有6,490万美元与KKC商业化协议相关的递延收入总额,其中6,450万美元分配给美国许可,30万美元用于开发服务绩效义务,这些义务是根据相关试验结束后这些开发活动的比例绩效进行确认的。正如进一步讨论的那样 注意事项 7。许可协议,在截至2023年9月30日的三个月中,与终止协议的执行有关,我们确认了与美国许可证相关的6,450万美元非现金长期递延收入,以及与完成基础比例绩效活动相关的剩余30万美元非现金递延收入。截至2023年9月30日,与KKC商业化协议相关的所有递延收入均已确认。
运营结果的组成部分
运营费用
27
目录
研究和开发
研发费用主要包括临床试验成本,包括向合同研究组织(CRO)支付的款项、临床前研究费用以及为非临床和临床研究生产候选药物的成本。其他研发费用主要包括工资和人员成本、基于股份的薪酬以及其他未分配给特定药物计划的成本。
我们将研发费用按实际支出支出。研发活动是我们商业模式的核心。购置研发所用技术但尚未获得监管部门批准且预计将来不会有其他用途的许可费和其他费用在发生时计为支出。
我们预计,在可预见的将来,随着我们对当前正在开发的候选产品进行临床试验,并继续发现和开发更多候选产品,研发费用将继续增加,占总支出的比例将更大。
一般和行政
一般和管理费用主要由人事成本组成,其中包括工资和其他相关费用,包括我们的行政、财务、业务发展、运营和管理职能人员的股份薪酬。一般和管理费用还包括与知识产权和公司事务有关的法律费用;会计、审计、税务和咨询服务的专业费用;保险费用;差旅费;设施相关费用,包括直接折旧费用和设施租金和维护费用以及其他不专门归因于研究活动的运营成本。
其他收入(支出)
其他收入(支出)主要与我们的短期投资所获得的投资收益有关。在2023财年,其他收入(支出)还包括与我们的认股权证负债相关的公允价值的变化。
运营结果
截至2024年3月31日和2023年3月31日的三个月的比较
下表汇总了我们经营业绩的某些组成部分(以千计):
|
|
在截至3月31日的三个月中, |
|
|
|
|
||||||||||
|
|
2024 |
|
|
2023 |
|
|
$ Change |
|
|
% 变化 |
|
||||
收入 |
|
$ |
— |
|
|
$ |
5,894 |
|
|
$ |
(5,894 |
) |
|
|
(100.0 |
)% |
研究和开发 |
|
|
5,220 |
|
|
|
15,104 |
|
|
|
(9,884 |
) |
|
|
(65.4 |
)% |
一般和行政 |
|
|
4,609 |
|
|
|
7,181 |
|
|
|
(2,572 |
) |
|
|
(35.8 |
)% |
其他收入,净额 |
|
|
702 |
|
|
|
953 |
|
|
|
(251 |
) |
|
|
(26.3 |
)% |
收入:截至2024年3月31日的三个月,我们没有确认任何收入,而截至2023年3月31日的三个月为590万美元。收入减少是由于 KKC商业化协议于2023年7月终止,在截至2023年9月30日的三个月中,所有剩余的递延收入均已确认。
研究和开发:以下是我们的研发费用摘要,以补充以下更详细的讨论(以千计)。
|
|
在截至3月31日的三个月中, |
|
|||||
|
|
2024 |
|
|
2023 |
|
||
赞德利西布 |
|
$ |
26 |
|
|
$ |
7,763 |
|
voruciclib |
|
|
1,382 |
|
|
|
698 |
|
ME-344 |
|
|
1,791 |
|
|
|
205 |
|
其他 |
|
|
2,021 |
|
|
|
6,438 |
|
研发费用总额 |
|
$ |
5,220 |
|
|
$ |
15,104 |
|
28
目录
与赞德利西布相关的成本减少了770万美元,这主要是由于该计划在2023财年终止。与voruciclib相关的费用增加了70万美元,这主要是由于1期研究的临床成本增加。与 ME-344 相关的成本增加了 160 万美元,这是由于与 1b 期研究相关的临床成本增加以及 ME-344 支持临床和非临床研究的制造成本增加。其他研发成本减少了440万美元,这主要是由于我们的裁员,包括一次性员工解雇补助金减少了110万美元,导致人员成本减少了420万美元。
一般和行政: 截至2024年3月31日的三个月,一般和管理费用减少了260万美元,至460万美元,而截至2023年3月31日的三个月为720万美元。减少的主要原因是我们裁员导致人事成本减少了100万美元,律师费减少了70万美元,外部专业服务减少了60万美元。
其他收入,净额:截至2024年3月31日的三个月,其他收入净额减少了30万美元,至70万美元,而截至2023年3月31日的三个月为100万美元,这主要是由于短期投资减少导致利息和股息收入减少。
截至2024年3月31日和2023年3月31日的九个月的比较
下表汇总了我们经营业绩的某些组成部分(以千计):
|
|
在截至3月31日的九个月中 |
|
|
|
|
||||||||||
|
|
2024 |
|
|
2023 |
|
|
$ Change |
|
|
% 变化 |
|
||||
收入 |
|
$ |
65,297 |
|
|
$ |
47,359 |
|
|
$ |
17,938 |
|
|
|
37.9 |
% |
研究和开发 |
|
|
12,617 |
|
|
|
49,880 |
|
|
|
(37,263 |
) |
|
|
(74.7 |
)% |
一般和行政 |
|
|
19,158 |
|
|
|
23,163 |
|
|
|
(4,005 |
) |
|
|
(17.3 |
)% |
其他收入,净额 |
|
|
2,662 |
|
|
|
3,875 |
|
|
|
(1,213 |
) |
|
|
(31.3 |
)% |
收入:截至2024年3月31日的九个月中,我们确认的收入为6,530万美元,而截至2023年3月31日的九个月的收入为4,740万美元。收入的增加主要是由于确认了与之相关的所有剩余递延收入 KKC商业化协议于2023年7月终止,但被截至2024年3月31日的九个月中与KKC商业化协议中的成本分摊相关的确认收入减少所抵消。
研究和开发:以下是我们的研发费用摘要,以补充以下更详细的讨论(以千计)。
|
|
在截至3月31日的九个月中 |
|
|||||
|
|
2024 |
|
|
2023 |
|
||
赞德利西布 |
|
$ |
417 |
|
|
$ |
27,634 |
|
voruciclib |
|
|
1,570 |
|
|
|
1,859 |
|
ME-344 |
|
|
4,396 |
|
|
|
1,053 |
|
其他 |
|
|
6,234 |
|
|
|
19,334 |
|
研发费用总额 |
|
$ |
12,617 |
|
|
$ |
49,880 |
|
与赞德利西布相关的成本减少了2720万美元,这主要是由于该计划在2023财年中止,2024财年与清盘活动相关的成本降低。与voruciclib相关的成本减少了30万美元,这主要是由于制造成本的降低。与 ME-344 相关的成本增加了 330 万美元,这是由于与 1b 期研究相关的临床成本增加,以及 ME-344 支持临床和非临床研究的制造成本。其他研发成本减少了1,310万美元,这主要是由于我们的裁员导致人员成本减少了1160万美元,包括一次性员工解雇补助金减少了170万美元,非现金股票薪酬减少了100万美元。
一般和行政: 截至2024年3月31日的九个月中,一般和管理费用减少了400万美元,至1,920万美元,而截至2023年3月31日的九个月为2320万美元。减少的主要原因是裁员使人事成本减少了330万美元,减少了70万美元,减少了外部专业服务,减少了60万美元
29
目录
公司管理费用减少了100万美元,非现金股票薪酬减少了40万美元,部分抵消了主要与合作协议相关的100万美元律师费的增加。
其他收入,净额:截至2024年3月31日的九个月中,其他净收入减少了约120万美元,至270万美元,而截至2023年3月31日的九个月为390万美元。在截至2023年3月31日的九个月中,我们确认了160万美元的非现金收益,这是由于标的认股权证将于2023年5月到期,我们的认股权证负债的公允价值发生了变化,在截至2024年3月31日的九个月中没有类似的收益。此外,截至2024年3月31日的九个月中,我们获得的利息和股息收入为270万美元,而截至2023年3月31日的九个月为230万美元。利息和股息收入的增加主要是由于截至2024年3月31日的九个月中收益率与截至2023年3月31日的九个月相比有所提高。
流动性和资本资源
自成立以来,我们已累计亏损3.698亿美元,预计在可预见的将来将出现营业亏损并产生负的运营现金流。截至2024年3月31日,我们有5,660万美元的现金和现金等价物以及短期投资。我们认为,自本季度报告发布以来,这些资源将足以为我们的运营提供至少12个月的资金。我们目前的业务运营侧重于继续进行候选药物的临床开发。我们的研发计划的变更或其他影响我们运营和运营支出的变化可能会影响现有现金资源的未来实际使用。我们无法确定与正在进行和未来的临床试验或监管批准程序相关的成本。与开发我们的候选产品相关的持续时间、成本和时间将取决于多种因素,包括与我们的临床试验结果相关的不确定性。
迄今为止,我们主要通过股权融资和许可协议获得了现金并为我们的运营提供资金。为了继续开发我们的候选药物,我们预计将在未来的某个时候进行一项或多项资本交易,无论是通过出售股权证券、债务融资、许可协议还是建立战略合作伙伴关系。无法保证我们将来能够继续筹集更多资金。
现金流
我们现金的来源和用途
截至2024年3月31日的九个月中,用于经营活动的净现金为3,250万美元,其中包括我们的3,620万美元净收入和330万美元的非现金项目,被主要由于确认了6,490万美元的非现金递延收入而产生的7190万美元运营资产和负债变动所抵消。截至2023年3月31日的九个月中,用于经营活动的净现金为4,120万美元,其中包括我们的2180万美元净亏损以及2,290万美元的运营资产和负债变动,部分被350万美元的非现金项目所抵消。
截至2024年3月31日的九个月中,投资活动提供的净现金为2960万美元,而截至2023年3月31日的九个月中,投资活动提供的现金为3,430万美元。增长主要是由于截至2024年3月31日的九个月中短期投资的购买和到期日与同期的时间差异。
在截至2024年3月31日的九个月中,由于支付了合作协议中商定的股息,用于融资活动的净现金为1170万美元。在截至2023年3月31日的九个月中,用于融资活动的净现金为40,000美元,这是在限制性股票单位(RSU)的归属时缴纳的预扣税,以换取RSU持有人交出的普通股。
资本资源需求
2022年1月,我们修改了设施租约,延长了20个月,直至2029年11月。修订后的租赁协议还规定了额外的租赁空间,我们于2022年7月1日控制了该空间。根据租赁条款,截至2024年3月31日,我们有义务支付总额为1,460万美元的剩余租赁款项,其中不包括租赁协议规定的公共区域维护和其他可变对价。截至2024年6月30日的财年剩余时间,预计租赁付款为60万美元,其中不包括租赁协议规定的公共区域维护和其他可变对价。
截至2024年3月31日,我们有以下潜在的收购义务,其发生的时间和/或可能性尚不清楚;但是,如果将来出现此类索赔,它们可能会对我们的财务状况、经营业绩和现金流产生重大影响。
30
目录
我们未来的资本要求将取决于许多因素,包括:
与宏观经济条件和其他地缘政治条件相关的估算注意事项
由于最近银行倒闭、宏观经济和地缘政治状况导致的银行存款和贷款承诺中断,全球经济和金融市场出现了不确定性和混乱。截至2024年3月31日,我们不知道有任何需要更新我们的估计值或判断或修订其资产或负债账面价值的具体事件或情况。尽管截至2024年3月31日的三个月和九个月中,我们的简明合并财务报表没有重大影响,但随着新事件的发生和获得的更多信息,这些估计可能会发生变化,这可能会对我们未来报告期的简明合并财务报表产生重大影响。
关键会计政策与管理估计
我们在中描述了我们的重要会计政策 注意事项 1.公司和重要会计政策摘要,我们2023年年度报告中包含的财务报表附注。我们在此讨论我们的关键会计估算第 7 项。管理层对财务状况和经营业绩的讨论和分析,在我们的 2023 年年度报告中。自2023年6月30日以来,我们的重要会计政策或关键会计估计没有变化。
最近的会计公告
参见 注意事项 2。重要会计政策摘要 在本季度报告的简明合并财务报表附注中。
第 3 项。关于市场风险的定量和定性披露
利率风险
我们的市场利率敞口主要与现金余额和短期投资的投资有关。我们有以美元持有的现金储备,并将资金存入金融机构,这些资金随时可用。我们的短期投资仅包括期限为三到十二个月的美国政府证券。
31
目录
我们将现金存款存入信贷质量高的金融机构,并通过保单限制任何一家公司或银行的信贷敞口金额。这些存款超过了联邦存款保险公司(FDIC)的保险限额。我们不利于本金损失,我们通过限制违约风险、市场风险和再投资风险来确保投资资金的安全和保全。我们力求通过向信贷质量高的金融机构存入资金、限制对任何一家公司或银行的信贷敞口、购买由美国政府证券组成的短期投资以及调整我们的投资组合以适当应对任何此类金融机构信用评级的大幅下降来降低来降低违约风险。
我们不认为利率变动的影响对我们的财务状况构成重大风险。
第 4 项。控制和程序
(a) 披露控制和程序
我们的管理层在首席执行官或首席执行官和首席财务官或首席财务官的参与下,评估了截至2024年3月31日我们的披露控制和程序(定义见交易法第13a-15(e)条和第15d-15(e)条)的有效性。根据此类评估,我们的首席执行官兼首席财务官得出结论,截至2024年3月31日,我们的披露控制和程序是有效的,可确保我们在根据《交易法》提交或提交的报告中要求披露的信息在美国证券交易委员会(SEC)的规则和表格规定的时间内记录、处理、汇总和报告,并积累并传达给我们的管理层,包括我们的首席执行官和首席财务官(视情况而定),以便及时就所需的披露做出决定。
财务报告内部控制的变化
在截至2024年3月31日的财政季度中,我们对财务报告的内部控制(定义见《交易法》第13a-15(f)条)没有发生任何变化,这些变化对我们的财务报告内部控制产生了重大影响,也没有合理地可能产生重大影响。
内部控制的固有局限性
我们的管理层,包括首席执行官和首席财务官,预计我们的披露控制和程序或财务报告的内部控制不会防止或发现所有错误和所有欺诈行为。控制系统,无论设计和操作多么精良,都只能为控制系统的目标得到满足提供合理的保证,而不是绝对的保证。由于所有控制系统的固有局限性,任何控制措施评估都无法绝对保证我们公司内部的所有控制问题和欺诈事件(如果有)都已被发现。这些固有的限制包括这样的现实,即决策中的判断可能是错误的,而崩溃可能是由于简单的错误或错误造成的。此外,可以通过某些人的个人行为、两人或更多人的串通或管理层无视控制来规避控制。任何控制系统的设计也部分基于对未来事件可能性的某些假设,因此无法保证任何设计在未来所有潜在条件下都能成功实现其既定目标。随着时间的推移,由于条件的变化,控制措施可能会变得不足,或者对政策或程序的遵守程度可能会恶化。由于具有成本效益的控制系统固有的局限性,由于错误或欺诈而导致的错误陈述可能会发生而无法被发现。
32
目录
第二部分其他信息
第 1 项。法律程序种子
没有。
第 1A 项。风险因素
与2023年年度报告中所包含的风险因素相比,我们的风险因素没有实质性变化。
第 2 项。未注册 S股权证券的出售和所得款项的使用
没有。
第 3 项。Seni 的默认设置或证券
没有。
第 4 项矿山安全ty 披露
不适用。
第 5 项。其他信息愤怒的
(a) 无。
(b) 无。
(c) 交易计划。在截至2024年3月31日的三个月中,公司没有董事或高级管理人员
33
目录
第 6 项。展品
展品索引
|
|
|
|
此处以引用方式纳入 |
||||||
展览 数字 |
|
描述 |
|
时间表/ 表单 |
|
文件编号 |
|
展览 |
|
申报日期 |
10.1* |
|
经修订和重述的 2008 年股票综合股权薪酬计划(2023 年 12 月) |
|
|
|
|
|
|
|
|
10.2 |
|
MEI Pharma, Inc. 与 Richard Ghalie 于 2024 年 1 月 16 日签订的 |
|
10-Q |
|
001-41827 |
|
10.4 |
|
2024年2月13日 |
31.1* |
|
根据根据2002年《萨班斯-奥克斯利法案》第302条通过的1934年《证券交易法》第13a-14(a)条和第15d-14(a)条对首席执行官进行认证。 |
|
|
|
|
|
|
|
|
31.2* |
|
根据根据2002年《萨班斯-奥克斯利法案》第302条通过的1934年《证券交易法》第13a-14 (a) 条和第15d-14 (a) 条对首席财务官进行认证。 |
|
|
|
|
|
|
|
|
32.1** |
|
《美国法典》(18 U.S.C 1350)第13a-14(b)条或第15d-14(b)条和第18编第63章第1350条要求对首席执行官和首席财务官进行认证。 |
|
|
|
|
|
|
|
|
101 英寸 |
|
行内 XBRL 实例文档 — 实例文档未出现在交互式数据文件中,因为 XBRL 标签嵌入在行内 XBRL 文档中。 |
|
|
|
|
|
|
|
|
104 |
|
封面交互式数据文件 — 封面交互式数据文件不出现在交互式数据文件中,因为其 XBRL 标签嵌入在 XBRL 文档中。 |
|
|
|
|
|
|
|
|
* |
|
随函提交 |
** |
|
随函提供 |
34
目录
签名
根据1934年《证券交易法》的要求,注册人已正式促使经正式授权的下列签署人代表其签署本报告。
|
MEI Pharma, Inc |
|
|
|
/s/ 贾斯汀 J. 档案 |
|
贾斯汀·J·文件 首席财务官兼秘书
|
|
|
|
日期:2024 年 5 月 9 日 |
35