
附录 99.1

摩根大通第 42 届年度医疗保健会议 1 © 2024 NOVAVAX。版权所有。纳斯达克:NVAX | 2024 年 1 月

本演示文稿包括前瞻性陈述。这些前瞻性陈述通常可以通过使用 “预测”、“期望”、“计划”、“可能”、“将”、“相信”、“估计”、“预测”、“目标”、“项目” 等词语以及其他具有类似含义的词语来识别。这些前瞻性陈述涉及各种问题,包括与Novavax的未来有关的信息、包括降低支出率、管理现金流和改变其规模和结构在内的短期优先事项、其全球重组和成本削减计划的金额和影响、其运营计划、目标和前景、2023年和2024年全年财务指导、其未来财务或业务业绩、状况或战略、CZ制造设施的潜在出售、公司的合作伙伴关系,包括和关于R 21/Matrix-M疟疾疫苗的推出、其更新的COVID-19疫苗、COVID-19流感组合(CIC)研究候选疫苗和流感疫苗候选物的持续开发、疫苗的交付和分发时间、未来和待处理的监管文件和行动的范围、时间和结果,包括预期的U.S。其更新后的COVID-19疫苗的生物制剂许可证申请(BLA)、将CIC候选疫苗推进到第三阶段及其可能商业上市的时机、预期的标签扩张和市场准入,以及2024年和未来的全球COVID-19流感和组合市场机会,都是前瞻性声明。Novavax警告说,这些前瞻性陈述存在许多风险和不确定性,可能导致实际结果与此类陈述所表达或暗示的结果存在重大差异。这些风险和不确定性包括但不限于Novavax成功制造、分销或销售其2023-2024年及未来疫苗接种季节的更新后的COVID-19疫苗的能力;单独或与合作伙伴一起满足各种安全性、有效性和产品特性要求的挑战,包括满足相关监管机构要求所必需的与工艺认证、化验验证和稳定性测试相关的挑战;开展临床试验的挑战或延迟;获得方面的挑战或延迟其候选产品的监管授权,包括未来的COVID-19变种菌株变化;COVID-19、流感和组合市场的规模;2023-2024年和2024-2025年疫苗接种季节的潜在发展;制造、分销或出口延迟或挑战;Novavax对印度血清研究所私人公司的完全依赖。Ltd. 和Serum Life Sciences Limited负责共同配方和灌装以及PCI Pharma服务,负责完成Novavax的COVID-19疫苗及其运营延迟或中断对客户订单交付的影响;难以获得稀缺的原材料和供应;资源限制,包括人力资本和制造能力,以及对Novavax单独或与合作伙伴同时在多个司法管辖区采取计划监管途径的能力的限制,导致监管申报错开来,和潜力监管行动;美国未来资金的损失美国政府;争议中可能出现不利结果,包括与全球疫苗免疫联盟的待决仲裁;实施全球重组和成本削减计划面临的挑战;其疫苗或候选疫苗在获得商业采用、市场准入和市场认可方面面临的挑战;满足与多个商业、政府和其他实体协议下的合同要求的挑战,包括要求交付剂量,这可能要求Novavax退还部分预付款和其他款项根据此类协议收到或导致未来付款减少;与COVID-19、季节性流感或其他疾病疫苗接种季节性相关的挑战;以及Novavax最新的10-K表年度报告和随后的10-Q表季度报告以及随后向美国证券交易委员会提交的文件中 “风险因素” 标题下确定的风险。Novavax提醒投资者不要过分依赖本演示文稿中包含的前瞻性陈述。鼓励投资者阅读Novavax向美国证券交易委员会提交的文件,这些文件可在www.sec. gov和我们的网站www.novavax.com上查阅,以讨论这些风险和其他风险和不确定性。本演示文稿中的前瞻性陈述仅代表截至本演讲之日,我们没有义务更新或修改任何陈述。我们的业务面临重大风险和不确定性,包括上述风险和不确定性。投资者、潜在投资者和其他人应仔细考虑这些风险和不确定性。关于前瞻性陈述的警示说明 2 © 2024 NOVAVAX。版权所有。

简介 SE C T I O N 3 © 2024 NOVAVAX。版权所有。

4 © 2024 NOVAVAX。版权所有。“这只是另一个数字”... 还是呢?3,000,000 1,300 630,000 来源:WHO.int、CDC.gov、ourWorldinData.org。41,000,000 710,000 52,000 710,000 52,000

5 © 2024 NOVAVAX。版权所有。在2021年至2030年之间,通过免疫接种可以预防5000万人死亡。在1980年至2018年期间,仅天花疫苗接种就挽救了1.5亿至2亿条生命来源:CDC.gov,OurWorldinData.org。

6 Novavax 来这里是为了有所作为。我们是一家生物技术公司,专注于开发拯救生命的疫苗以对抗传染病。© 2024 NOVAVAX。版权所有。作为一个行业,我们所做的事情很重要,我们已经并将继续对全球数百万人的健康产生积极影响。“除了创造生活外,一个人能做的最好的事情就是拯救生命。”亚伯拉罕·林肯 “知道哪怕是一条生命也会更轻松一些,因为你已经活过了。这本来是成功的。”Ralph Waldo Emerson 我们从不间断地寻求保护世界各地人们的健康。

C o m p a any 概述 SE C T I O N 7 © 2024 NOVAVAX。版权所有。

Novavax 企业亮点 8 © 2024 NOVAVAX。版权所有。有望通过成熟技术的商业化实现长期价值创造专有矩阵-M TM 佐剂可分化产品线快速将COVID-19-流感组合(CIC)疫苗推进到3期1期基于经过验证的蛋白质技术平台COVID-19疫苗有望在长期市场中获得份额完全整合的商业阶段生物技术公司1。须经监管部门对研究设计的最终同意。

全面整合的商业阶段生物技术公司,业务遍及全球 9 © 2024 NOVAVAX。版权所有。全球总部和公司办公室 • 研发和发现实验室 • 制造业务 • 商业 Novavax 总部 Novavax 总部马里兰州盖瑟斯堡 Novavax AB 瑞典乌普萨拉 Novavax CZ Bohumil 捷克共和国血清研究所 SK 生物科学武田欧盟商业运营瑞士苏黎世亚太商业运营新加坡 Novavax AB — Matrix-M 辅助剂 Novavax CZ — 抗原 Novavax Ma nuf ac 图灵北美欧盟(EU)亚太地区(APAC)Novavax C o mm e r c ia l 印度运营血清研究所(SII)SK 生物科学武田Str a t例如 ic Partners 北美商业运营马里兰州盖瑟斯堡
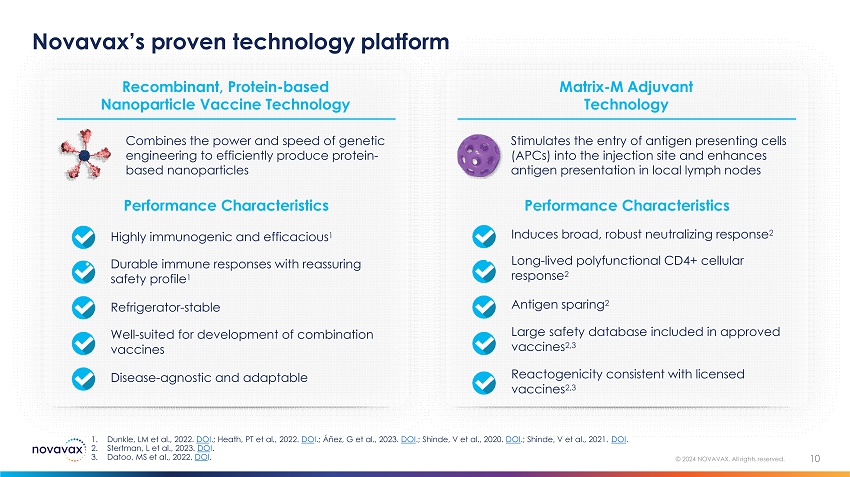
Novavax 久经考验的技术平台 10 © 2024 NOVAVAX。版权所有。• 抗原保存 2 • 批准的疫苗中包含大型安全数据库 2,3 • 反应原性与许可疫苗一致 2,3 Matrix-M辅助技术性能特征 • 诱导广泛而强大的中和反应 2 • 长寿的多功能 CD4+ 细胞反应 2 刺激抗原呈递细胞 (APC) 进入注射部位并增强局部淋巴结的抗原呈现 • 冰箱稳定 • 非常适合开发复合疫苗 • 疾病-不可知且适应性强重组、基于蛋白质的纳米颗粒疫苗技术性能特点 • 免疫原性高、效果好 1 • 持久的免疫反应和令人放心的安全性 1 结合基因工程的力量和速度,有效生产基于蛋白质的纳米颗粒 1.邓克尔,LM 等人,2022年。DO I.;Heath,PT 等人,2022年。DO I.;阿涅斯,G 等人,2023 年。DOI。;Shinde,V 等人,2020 年。DOI。;Shinde,V 等人,2021 年。DOI。2.Stertman,L 等人,2023 年。我这么做。3.Datoo,MS 等人,2022年。我做。

Novavax 的核心疫苗产品线未来发展的重大机遇 11 © 2024 NOVAVAX。版权所有。1.以 Novavax COVID-19 疫苗、Adjuvanted、Covovax TM 和 Nuvaxovid 的商品名在特定地区获得授权。2.在美国获得授权,商品名为Novavax COVID-19疫苗,佐剂(2023-2024年配方);正在进行授权后的3期菌株变更试验。3.在加纳、尼日利亚和布基纳法索获得授权;由印度血清研究所商业化;获得世卫组织资格预审。疾病产品临床前 1 期 2 期 3 期授权 Novavax 临床——冠状病毒阶段 NVX——CoV2373 1 矩阵——M 矩阵——M 单价 XBB.1.5 NVX——COV2601 2 COVID/流感联合疫苗 (CIC) 矩阵——M 季节性流感流感(老年人)矩阵——M 合作临床——疟疾阶段 R21/Matrix-M 佐剂 3 矩阵——M 型季节性流感(老年人)矩阵——M 合作临床——疟疾阶段 R21/Matrix-M 佐剂 3 矩阵——M

R21/Matrix——抗疟疾的M疫苗获准帮助解决迫切的全球公共卫生需求 12 © 2024 NOVAVAX。版权所有。高效疫苗展现了Novavax技术平台的前景 • 采用Novavax的矩阵-M佐剂 1 配制而成 • 2023 年 12 月通过世卫组织资格预审;2024 年上市 • 75% 的疗效 2;超出目前的护理标准 • 被世卫组织总干事视为 “重要工具” ——全球三级疟疾是人类历史上最致命的疾病之一 • 四年级造成63万人死亡,包括约1300名儿童/第4天五岁以下儿童约占疟疾死亡人数的78%5 •巨大的经济、社会和健康公平负担 1.由牛津大学开发,由印度血清研究所制造和商业化。2.Datoo,MS 等人,2023 年。我这么做。3.世卫组织于 2023 年 2 月 10 日发布的新闻稿。4.OurworldindaTa.org。5.Who.int。照片来源:牛津大学 “作为一名疟疾研究人员,我曾经梦想有一天我们会有一种安全有效的抗疟疫苗。现在我们有两个。” 世卫组织总干事特德罗斯·阿达诺姆·盖布雷耶苏斯博士说。“对RTS、S疫苗的需求远远超过供应,因此第二种疫苗是更快地保护更多儿童、使我们更接近无疟疾未来的愿景的重要额外工具。” 4

2023 年:一年回顾 SE C T I O N 13 © 2024 NOVAVAX。版权所有。

14 © 2024 NOVAVAX。版权所有。2023年是Novavax发生重大变化的一年,重点是建立稳健和可持续的业务 • 根据监管机构的要求交付了更新的疫苗 • 兑现了我们的APA承诺,积累了在美国市场的经验 • 概述了我们的流感/Covid联合疫苗计划的更快前进道路,预计将于2026年启动* 简化菌株选择和制造流程为推进CIC开发计划采取了关键措施 • 将流动负债减少了约10亿美元 2023 年 9 月 30 日包括解决疫情时代的制造业承诺 • 计划在2023年将销售和并购和研发费用减少25%以上,与2022财年的基准相比减少55%重组成本并大幅减少流动负债 • 设立了首席安全官、首席运营官和公司事务职位,任命了新的研发总裁,聘请了新的总经理和首席人力资源官等变动 • 2023年我们的员工人数减少约20%,并准备在2024年进一步缩小运营规模和经营范围重组后的管理团队重组缩小全球足迹规模 1.*视乎研究设计的最终监管部门同意和临床开发计划的成功完成而定。2.*如果获得批准,打算在2026年推出CIC疫苗。

展望未来:Novavax SE C T I O N 15 的重大未来机遇 © 2024 NOVAVAX。版权所有。

为 2024+ 年更强劲的美国商业表现奠定基础 1.IPSOS 联合发布的意识、试用和使用情况追踪器(2023 年 3 月至 2023 年 9 月),HCP 月度脉搏(从 2023 年 10 月开始)。2.IQVIA NPA 数据和索赔数据。16 © 2024 NOVAVAX。版权所有。2023-2024 年疫苗接种季节 2024-2025 年疫苗接种第 5 季-剂量瓶产品展示单剂量介绍 E UA FDA 授权状态 BLA 预计年龄 12 岁以上标签扩展寻求年龄 10 月 6 日产品上市时间目标截至 2023 年 6 月 46% 1 截至2024年1月 HCP-辅助宣传率达到 80% 1 并非所有零售连锁店都处于平等地位。零售渠道约占市场机会的90% 2 市场准入预计将扩大Novavax疫苗的覆盖范围和可获得性

0 20 40 60 80 1 0 0 1 0 1 2 0 1 4 0 1 6 0 流感 COVID-19 百万剂 2019-2022 年平均 1.3 亿-1.4 亿剂美国未来联合呼吸道疫苗的重大市场机遇 • 对流感和 COVID 联合疫苗的高需求和偏好-19 疫苗组合可能增加 COVID-19 疫苗接种率 • 流感是 2019 年至 2022 年美国流感季节平均接种剂量的重大机会:1.3 亿至 1.4 亿剂 1 o 每年的美国流感市场机会:40亿美元+ 2 3000万美元至3500万美元 3 17 1。NVAX使用CDC FluvaxView的两个数据源对季节平均水平进行内部估计:a) NIS——6个月——17岁的流感数据;b) 通过IQVIA LRx和Dx数据为18岁以上的成年人接种的每周累计流感疫苗接种估计值。2.杰富瑞,《全球疫苗深度研究》,《股票研究报告》,2023年5月30日。3.根据IQVIA Rx Rapid每周数据,NVAX内部预计的截至12月22日的零售疫苗接种总量。2023年9月至2024年3月的2023-2024季节。4.根据2023年4月和6月进行的NVAX内部消费者和HCP需求研究,基于潜在峰值剂量给药的说明性市场份额百分比。混合疫苗剂量等于接种两剂。© 2024 NOVAVAX。版权所有。说明性未来美国市场季节性剂量百分比 4 美国市场季节性剂量 C O VI D-19 Flu C o m bo o m bo 对复方呼吸道疫苗的偏好为 Novavax 4 创造了重要机会 2023-2024 年预计可能超过 50%

18 © 2024 NOVAVAX。版权所有。Novavax完全有能力提供差异化组合疫苗并利用成熟技术平台1抓住重大市场机会。蛋白质接受性研究(2022年1月)。2.IQVIA 需求研究(2023 年)。3.IPSOS 联合发布的认知度、试用和使用情况追踪报告(2023 年 3 月至 2023 年 9 月),HCP 月度脉搏(从 2023 年 10 月开始)。• 约 25-30% 的受访者 1 和医疗保健专业人员 2 更喜欢基于蛋白质的选项 Novavax 在美国的知名度增长 1 0 0% 0% 4 0% 0% 72% 44% 46% 3月-6月23日-1月23日-1月23日-24日% HCPs对基于蛋白质的选择有强烈的偏好 • 商业化的COVID-19疫苗具有显著的疗效和耐受性 • Matrix-M 诱导广泛的抗体反应且寿命长细胞反应 • 三期结果呈阳性的四价流感候选疫苗 o 有与市场竞争的潜力-领先的独立流感疫苗美国 HCP-辅助意识 3

CIC/流感 2 期研究摘要观察结果 19 © 2024 NOVAVAX。版权所有。S t 和-a lo ne 流感疫苗 CIC 疫苗将独立流感疫苗和 NVX-CoV 2373 组合在单一注射矩阵中-M a d j uv ant + 四价疫苗含有四个流感血凝素基因矩阵-M a d j uv ant + CIC 疫苗 • 初步安全性可与 Fluzone HD® 和 FLUAD® 相媲美 • 抗 S IgG 和中和反应达到了 Nuvaxovid 3 期研究中看到的水平 • HAI 1 几何平均比率符合许可标准独立四价流感疫苗 • 初步安全性令人放心,反应原性可与Fluzone HD和FLUAD相媲美 • 与FLUAD相比,所有四种菌株的HAI 1反应比Fluzone高31-56% • A菌株的HAI 1反应比Fluzone HD高44-89% FLUAD® 是英国Seqirus有限公司的注册商标;Fluzone High-Dose Quadrivalent® 是赛诺菲巴斯德公司的注册商标 1。三种菌株的基线调整后的野生型HAIs将纳入未来的疫苗。

20 © 2024 NOVAVAX。版权所有。Novavax 有望支持扩大我们的产品组合产品组合 Novavax Readiness Posture T 今天的 COVID-19 疫苗 R21/M a tr i x-M 疟疾疫苗 1 CIC 疫苗可能于 2026 年推出 2 COVID-19 疫苗 R21/M a tr i x-M 疟疾疫苗 1 2026 • 现金和 APA 支持我们在非 APA 市场(美国、欧洲,低)在全球范围内抓住机会的能力中等收入国家)• 大幅降低我们2024财年的支出o 目标是与2022财年相比,销售和收购+研发的总体减少55%以上 • 再增加2次COVID-19 个季节将进一步为 CIC 的启动做准备 • CIC 临床项目支持独立流感后期开发选项 1。牛津大学和SII开发的R21疫苗包括Novavax的Matrix-M佐剂作为关键成分。该疫苗由SII销售。2.如果获得批准,打算在2026年推出CIC疫苗。
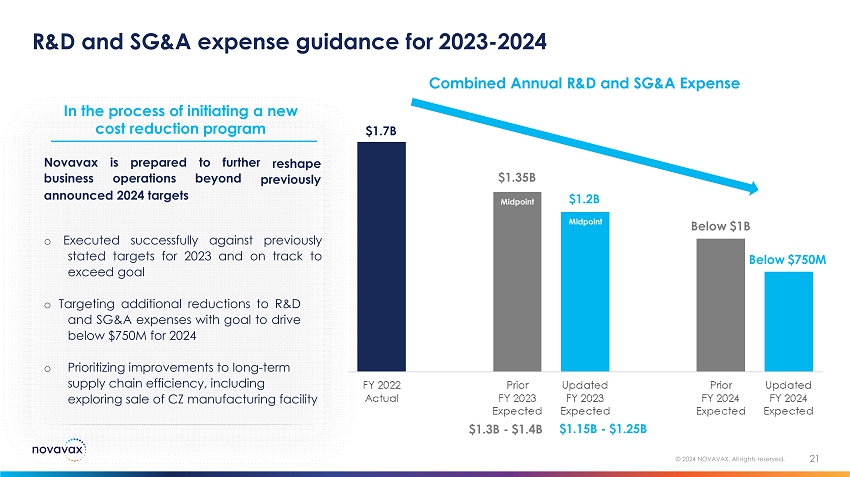
2023-2024年的研发和销售与收购费用指南 21 © 2024 NOVAVAX。版权所有。17亿美元 11.5亿美元至12.5亿美元的成本削减计划重塑了Novavax业务已准备好在先前宣布的2024年目标之外继续开展业务 o 已成功执行并有望超过目标 o 将进一步削减研发和销售与收购开支作为目标,目标是在2024年降至7.5亿美元以下 o 优先改善长期供应链效率,包括探索出售瑞士制造设施如下 10亿美元的年度研发和销售与收购合并支出正在启动中新增13亿美元-14亿美元低于7.5亿美元13.5亿美元中点12亿美元中点

22 © 2024 NOVAVAX。版权所有。摘要:2023年取得的进展和经验为2024年以上的发展奠定了坚实的基础 • CIC疫苗可能在2026年秋季推出第2季 • 市场庞大,差异化潜力为Novavax确定了重要的未来机遇 • 财务状况的重大改善使我们能够在2024年下半年独立将CIC疫苗推进到第三阶段 1做好准备,重点是CIC • 重组管理团队 • 显著减少开支 • 不断发展企业文化创建了一个更加精益和专注的组织 1.视乎研究设计的最终监管部门同意和临床开发计划的成功完成而定。2.如果获得批准,打算在2026年推出CIC疫苗。

23 © 2024 NOVAVAX。版权所有。我们从不间断地寻求保护世界各地人们的健康。

问答 24 © 2024 NOVAVAX。版权所有。