
蓝鸟生物摩根大通2024年1月在纳斯达克发表演讲:BLUE 附录 99.2

机密的前瞻性陈述 2 这些幻灯片和随附的口头陈述包含前瞻性陈述和信息。使用 “可能”、“可能”、“将”、“应该”、“期望”、“计划”、“预测”、“相信”、“估计”、“项目”、“打算”、“未来”、“潜在” 或 “继续” 等词语以及其他类似的表述旨在识别前瞻性陈述。例如,我们就我们对我们的计划和疗法的期望发表的所有声明,包括但不限于监管机构申报和批准的时间或可能性;我们的制造和商业化计划,包括但不限于患者对我们疗法的需求、我们建立商业基础设施以支持及时、公平获得我们的疗法的能力、我们成功与付款人和CMMI合作的能力、我们对激活QTC时机的期望,以及我们对时机的期望我们的 QTC 规模网络以及我们的疗法在QTC上市的时机;我们疗法的潜在市场;截至2023年12月31日的未经审计的初步现金状况;以及我们的现金流都具有前瞻性。所有前瞻性陈述均基于管理层的估计和假设,尽管我们认为这些估计和假设是合理的,但本质上是不确定的。所有前瞻性陈述都受到风险和不确定性的影响,这些风险和不确定性可能导致实际结果与我们的预期存在重大差异。这些陈述还受到许多重大风险和不确定性的影响,这些风险和不确定性在我们最新的10-Q表季度报告以及我们随后向美国证券交易委员会提交的文件中都有描述。任何前瞻性陈述仅代表其发表之日。除非法律要求,否则我们没有义务公开更新或修改任何前瞻性陈述,无论是由于新信息、未来事件还是其他原因。

CONFIDENTIAL 3 让患者及其家人有更多的蓝鸟时光

机密唯一一家拥有三种 FDA 批准产品的商业基因疗法公司 4

机密信息随着商业发布而势头增强;有机会为患者和股东创造巨大价值 5 13K — 1.5K 患者可能有资格获得 ZYNTEGLO™ 的β地中海贫血 40 名患者可能有资格获得 SKYSONA™ 脑肾上腺素白质营养不良症患者 F U TU RE G ROW TH CI CO M M ER CI AL O PP O RT U N IT Y 患者数量 2万名患者可能有资格获得 LYFEGNIA™ 镰状细胞病
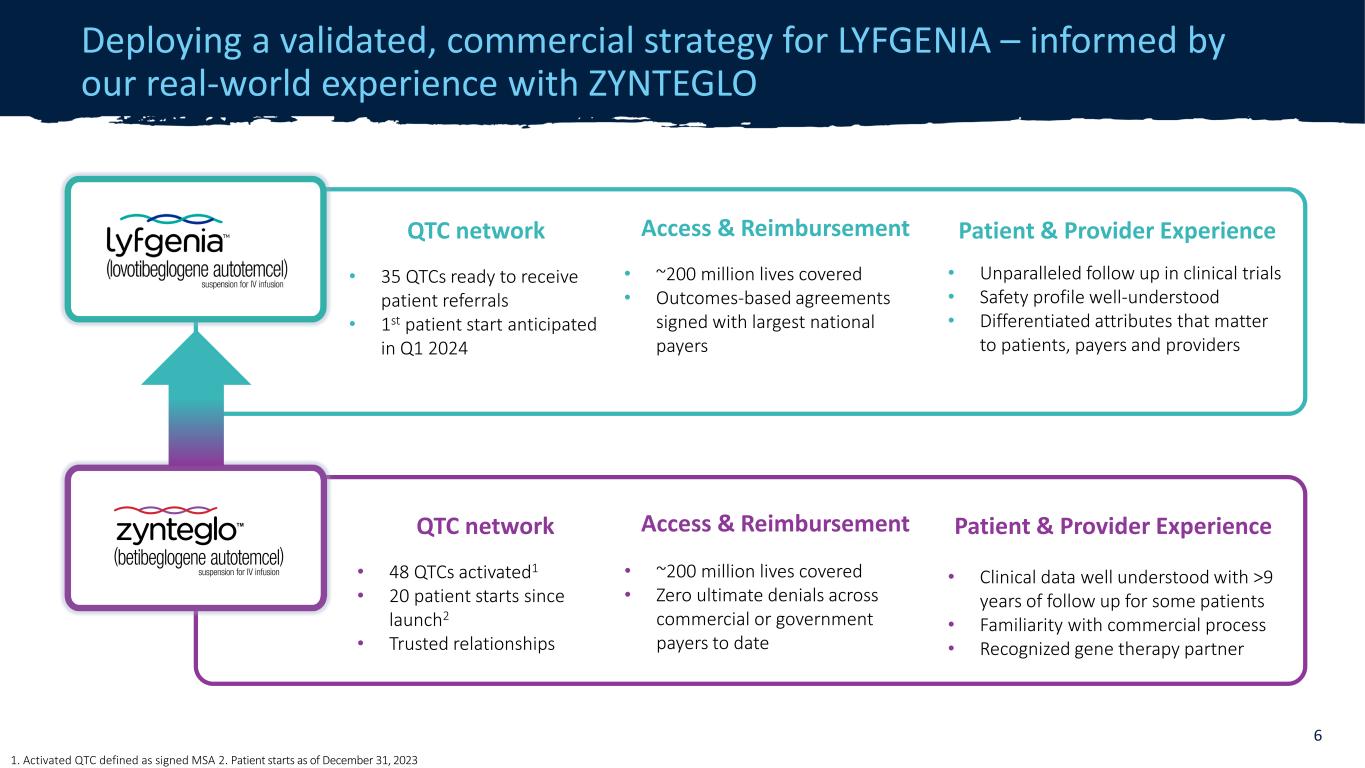
机密访问和报销 • 覆盖约2亿人的生命 • 与最大的全国支付方签署了基于结果的协议患者和提供者经验 • 临床试验中无与伦比的后续行动 • 安全概况广为人知 • 对患者、付款人和提供者至关重要的差异化属性 QTC 网络 • 35 个 QTC 准备接受患者转诊 • 第一位患者预计于 2024 年第一季度开始为 LYFGENIA 部署经过验证的商业策略——以我们在ZYNTEGLGENIA的实际经验为依据 O 6 QTC 网络 • 48 个 QTC 已激活1 • 20 名患者自启动以来开始2 • 可信关系访问和报销 • 覆盖约2亿条生命 • 迄今为止,商业或政府支付方的最终拒绝次数为零患者和提供者体验 • 临床数据广为人知,对某些患者进行了超过9年的随访 • 熟悉商业流程 • 公认的基因疗法合作伙伴 1.已激活 QTC,定义为已签名的 MSA 2。患者从 2023 年 12 月 31 日开始治疗

7 QTC 网络

机密 48 个合格治疗中心 (QTC) 已激活 ZYNTEGLO 并迅速加入 LYFGENIA 8 35 个 QTC 已准备好接收 SCD 患者转诊现已激活 ZYNTEGLO QTC* Shading 表示目标 SCD 市场计划于 2024 年 QTC 扩张 100% 的 ZYNTEGLO QTC 已启动 LYFGENIA 的激活程序预计 ZYNTEGLO 网络将完全激活在 2024 年第一季度末之前适用于 LYFGENIA *已激活 QTC 定义为已签署的 MSA

机密优化的 QTC 网络旨在覆盖患有 SCD 9 1 的个人。潜在的潜在目标人口为20,000;2. 70% 的数字得到了七年的内部和外部市场研究的支持;3.存档数据;4.科莫多声称数据对基因疗法的强劲需求有望满足患者的需求 95% 的 SCD 患者2 距离计划的 QTC3 在 200 英里以内 88% 的目标 SCD 患者正在医疗系统中积极接受治疗4 80%的提供者希望自己的机构同时提供LYFEGNIA及其竞争对手3 > 70% 的SCD患者1如果得到医生的推荐会考虑基因疗法2

准入和报销 10

ZYNTEGLO的机密价值得到认可,合同或保险单涵盖了约1,12亿人的生命 ~ 90% 公布的保险单对ZYNTEGLO持积极态度 ZYNTEGLO迄今为止,商业和政府支付方最终拒绝了β-地中海贫血患者获得准入

机密经过验证的准入和报销策略旨在实现及时、公平地获得LYFGENIA治疗镰状细胞病12签署了代表约2亿受保人寿的基于结果的协议与超过15家医疗补助机构进行了深入的讨论1 积极参与CMMI进行创新支付示范(预计2025年)鼓励付款人互动表现出强劲而持续的临床益处(持续超过5年)反映了减少或消除VOE的终身影响 •医疗保健利用率•未来收益•生活机会310万美元价格与价值挂钩有意义的风险分担与VOE相关的住院患者跟踪了3年商业付款人和医疗补助选项旨在提供可预测性和易操作性基于结果的协议产品 1.数据基于2012年每1,000名医疗补助受益人的SCD患病率。

13 治疗经验
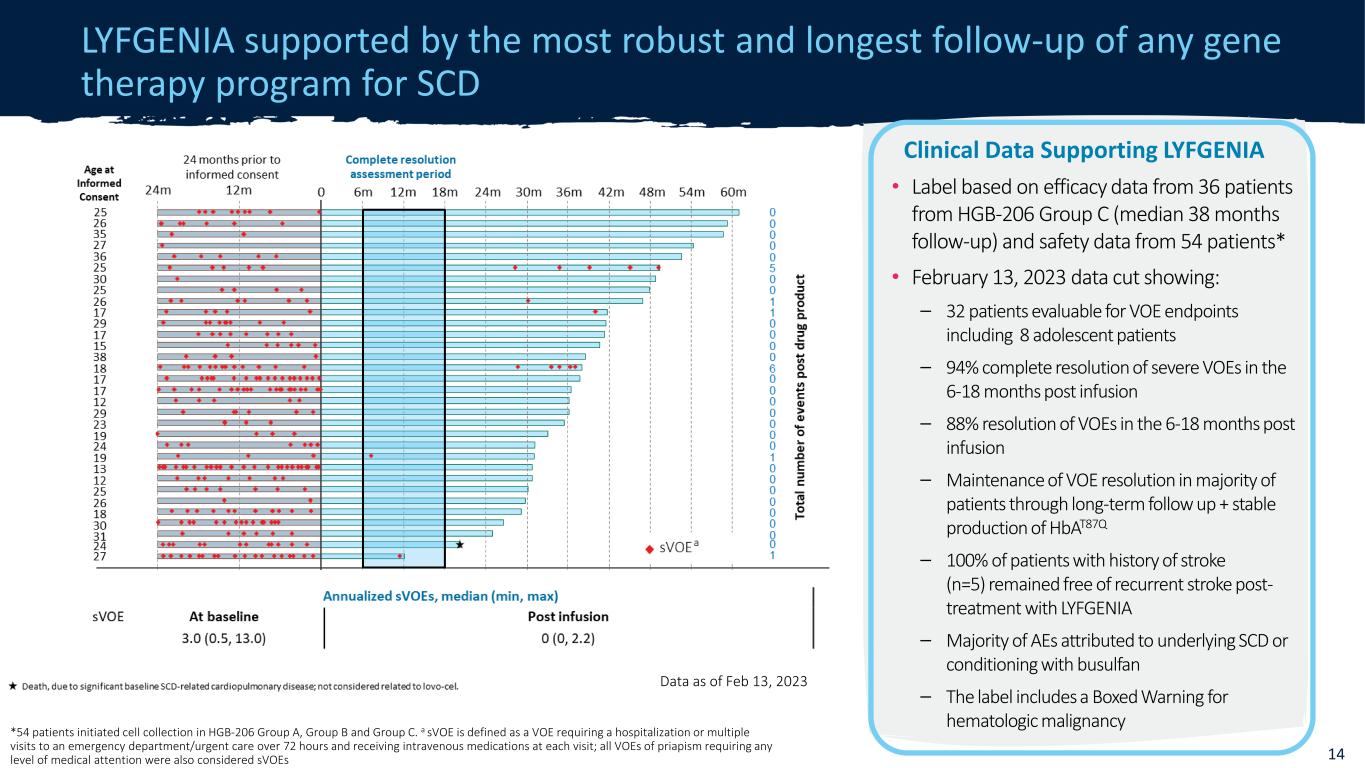
机密 LYFGENIA 得到所有基因治疗计划中最有力、最长的 SCD 数据的随访支持,截至 2023 年 2 月 13 日 14 *54 名患者启动了 HGB-206 A 组、B 组和 C 组的细胞采集。sVoE 被定义为需要住院或多次就诊超过 72 小时的急诊科/紧急护理并在每次就诊时接受静脉药物治疗的 VOE;所有阴茎异常勃起的 VOE 需要任何程度的医疗救助还被视为支持 LYFGENIA 的 SVoE 临床数据 • 基于来自 36 名患者的疗效数据来自 HGB-206 C 组(中位数 38 个月随访)和 54 名患者的安全性数据* • 2023 年 2 月 13 日截止的数据显示:— 32 名患者可对 VOE 终点进行评估,包括 8 名青少年患者 — 输液后 6-18 个月内重度 VOE 完全消退 94% — 输液后 6-18 个月内 VOE 分辨率达到 88% — 通过长期随访维持大多数患者的VOE分辨率+ Hbat87q的稳定产生 — 100% 有中风史的患者(n=5)在接受LYFGENIA治疗后仍然没有复发的中风——大多数归因于潜在的 SCD 或使用白消安调理的不良反应——标签上包含血液系统恶性肿瘤的方框警告
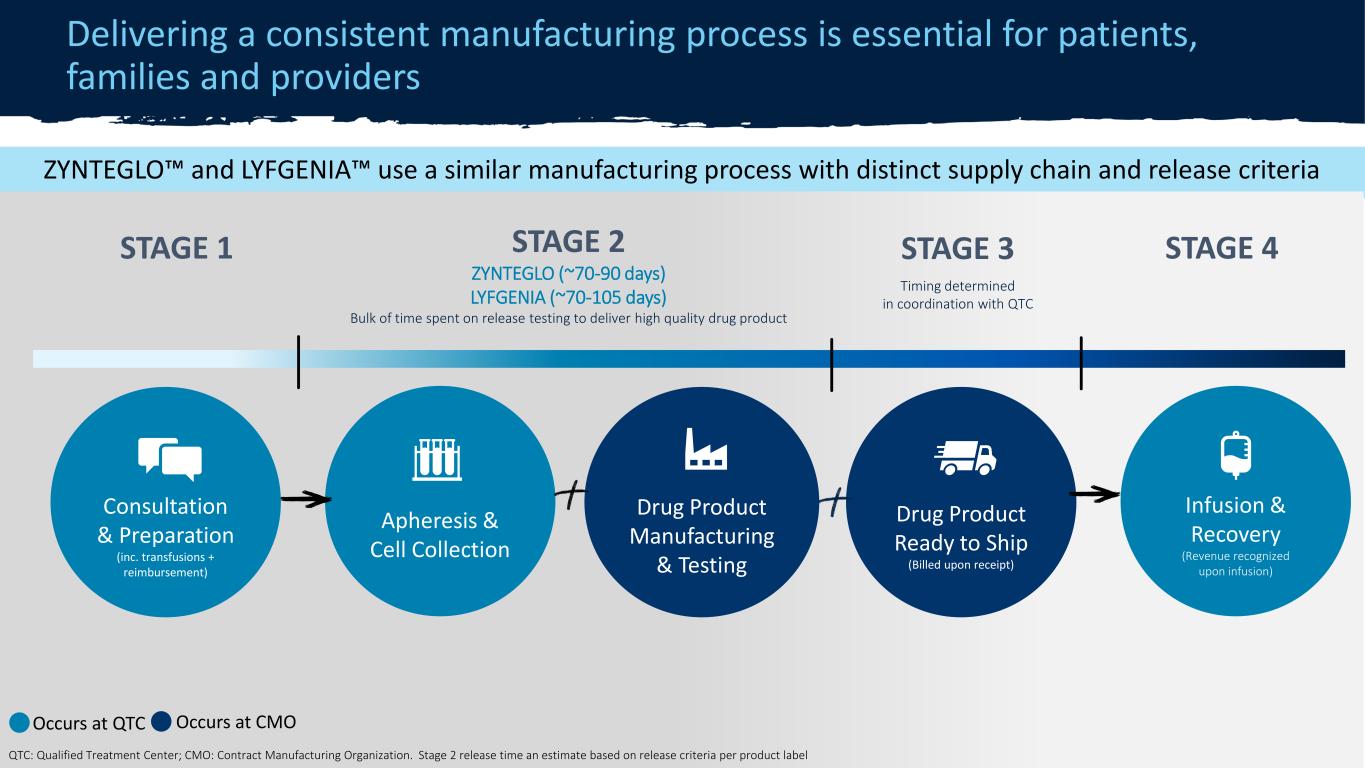
机密 ZYNTEGLO® 制造流程提供一致的制造流程对患者、家属和医疗服务提供者至关重要 15 阶段 2◇ 70-90 天大部分时间用于发布测试,以交付高质量药物产品血液分离和细胞收集药物产品制造和测试药物产品准备就绪(QTC 计费)输液和恢复(输液后确认收入)咨询和准备(包括超额输血 + 报销确认)第 1* 阶段 *发生在 QTC ◇ 发生在 CMO QTC:合格治疗中心;首席营销官:合同制造组织在临床试验中,大约20%的病例出现了回忆。在商业环境中,所有患者都有 [已完成]回忆后的治疗过程。ZYNTEGLO™ 和 LYFGENIA™ 使用相似的制造工艺,具有不同的供应链和发布标准第 2 阶段 ZYNTEGLO(约 70-90 天)LYFGENIA(约 70-105 天)用于交付高质量药物产品的发布测试的大部分时间(按收据计费)咨询和准备(包括输血 + 报销)第 1 阶段 4 发生在 QTC 发生在 CMO QT Lified 治疗 C inter;CMO:合约制造和组织。第 2 阶段发布时间根据每个产品标签的发布标准估算第 3 阶段与 QTC 协调确定时机

机密LYFGENIA的差异化属性对患者、付款人和提供者都很重要 16 以临床特征为基础——包括>5年的随访、深入的安全性分析和针对SCD并发症的数据,包括中风细胞采集在临床试验中,85% 的必填项

17 2 潜在的数十亿美元机会,美国约有22,000名患者可寻址;制定了商业战略和预计的患者和医生需求经验丰富的商业基因疗法团队完全有能力在血红蛋白病领域处于领先地位 18个月的商业化起步——相同的治疗医生,相同的QTC,相同的支付者 1 3 具有深厚基因疗法专业知识、制造经验和商业基础设施的知名基因疗法领导者

SKYSONA™ 18

CONFIDENTIALI SKYSONA™ 用于脑肾上腺白质营养不良症商用 • SKYSONA 可减缓 4-17 岁患有早期活动性脑肾上腺皮质营养不良症 (CALD) 的男孩的神经系统功能障碍进展 • 自启动以来有 6 名患者开始治疗*;激活了 4 个 QTC;政府和商业支付方最终拒绝的案例为零 • 所有临床试验均治疗了 67 名患者 • 加速批准基于对11名患者的事后分析;估计在24个月时出现严重功能障碍无存活的可能性为72% • 5名男孩接受了治疗临床试验开发了骨髓增生异常综合征;标签中包含血液系统恶性肿瘤的方框警告** 21患者开始治疗定义为细胞采集(血液分离);Activated QTC定义为具有MSA签名的合格治疗中心。*患者自2023年12月31日起开始接受**蓝鸟密切监测接受SKYSONA治疗的患者的潜在和确诊的血液系统恶性肿瘤病例,随着时间的推移,预计还会出现更多病例。蓝鸟定期与主治医生和监管机构沟通。

闭幕 20

机密知名基因疗法领导者有望为股东创造价值 21 确立的临床领导地位 • 10 多年的基因疗法研究 • 200 多名患者接受了治疗 • 8 项临床试验显示监管成功 • LVV 平台建立了良好的往绩记录 • 3 家获美国食品药品管理局批准的基因疗法商业基因疗法领导者 • 扩展了三次商业发布 • 协同移植和细胞疗法基础设施 • 可靠的报销当前财务状况未经审计的2.75亿美元现金、现金等价物、限制性现金和有价证券余额20231 年 12 月 31 日,预计在 2024 年 LYFGENIA、ZYNTEGLO 和 SKYSONA 共有 85-105 名患者开始发病 1.现金余额包含5300万美元的限制性现金;2.Cash Runway 使用现金余额/净消耗率(收入中的现金减去支付的支出现金)计算,包括现金、现金等价物和有价证券,不包括限制性现金;患者起始定义为细胞收款今天资产负债表上的零负债评估额外的非稀释性资金以实现2025年第一季度的短期盈利能力现金跑道

CONFIDENTIAL bluebird 作为一家独立的基因疗法公司占有独特的战略地位 22 • 基因疗法研究已有 10 年以上 • 200 名患者接受了治疗 • 8 项临床试验 • LVV 平台的良好记录 • 3 次商业化发布 • 移植和细胞疗法基础设施 • 久经考验的报销CL in ic al c om pa ni es Large cap pharm a 制造体验研发专业知识商业基础设施
