

2024 年 1 月公司介绍附录 99.1

前瞻性陈述本演示文稿包含1995年《私人证券诉讼改革法》所指的前瞻性陈述。“相信”、“可能”、“将”、“估计”、“继续”、“预测”、“打算”、“期望” 等词语以及类似的表述旨在识别前瞻性陈述。本演示文稿中所有与历史事实无关的陈述均应被视为前瞻性陈述,包括有关公司2025年第一季度的现金流、公司的候选产品线、ENLIGHTEN第三阶段计划的注册和成功、报告公司临床试验前线数据的时机、公司内部生产候选产品的能力、公司候选产品的安全性和有效性、临床试验数据的陈述在适用的临床研究报告、2期BEACON试验的结果以及候选产品的商业承诺完成之前,可能会发生变化。这些陈述既不是承诺也不是担保,但涉及已知和未知的风险、不确定性和其他重要因素,这些因素可能导致公司的实际业绩、业绩或成就与前瞻性陈述所表达或暗示的任何未来业绩、业绩或成就存在重大差异,包括但不限于以下内容:公司自成立以来蒙受了重大损失,并预计在可预见的将来将蒙受额外损失;公司对额外资金的需求,这可能不可用;公司的运营历史有限;公司没有批准的产品这一事实;公司的候选产品处于不同的开发阶段;公司从未扩大过用于临床或商业用途的内部制造设施的事实;或者公司可能无法成功识别候选产品并成功将其商业化;公司候选产品所需的临床试验成本高昂而且很耗时,而且其结果尚不确定;FDA可能无法得出该公司的候选产品符合第505(b)(2)条监管批准途径要求的结论;公司无法获得所需的监管批准;最近颁布和未来立法的影响;系统故障或安全漏洞的可能性;激烈竞争的影响;公司候选产品的成功商业化将部分取决于政府当局和健康保险公司制定承保范围、充足的报销水平和定价政策;未能获得市场认可;产品责任诉讼;公司必须扩大内部制造能力或依赖第三方为其研究项目、临床前研究和临床试验及商业供应制造材料;公司依赖第三方进行临床前研究和临床试验;公司无法成功建立和维持合作关系;公司的依赖某些对其生产至关重要的供应商;未能获得、维护或充分保护公司的知识产权;未能留住关键人员或招聘合格人员;难以管理公司的增长;自然灾害、恐怖主义和战争的影响;COVID-19 造成的全球疫情可能对公司的业务和运营,包括公司的临床试验产生不利影响;公司普通股价格可能波动和波动实质上;作为上市公司运营和任何证券集体诉讼所产生的巨额成本和所需的管理时间。公司于2023年11月7日向美国证券交易委员会提交的10-Q表季度报告及其向美国证券交易委员会提交的其他文件中,在 “风险因素” 标题下讨论的这些和其他重要因素可能导致实际业绩与本演示文稿中前瞻性陈述所示的业绩存在重大差异。任何此类前瞻性陈述均代表管理层截至本演讲之日的估计。尽管公司可能会选择在未来的某个时候更新此类前瞻性陈述,但它不承担任何更新此类前瞻性陈述的义务,即使随后发生的事件导致其观点发生变化。本演示还包括我们从行业、出版物和研究、第三方或我们进行的调查和研究中获得的统计和市场数据。行业出版物和第三方研究、调查和研究通常表明,他们的信息是从被认为可靠的来源获得的,尽管它们不能保证此类信息的准确性或完整性。本演示文稿中使用的所有市场数据都涉及许多假设和局限性,提醒您不要过分重视此类估计。尽管我们认为这些行业出版物和第三方研究、调查和研究是可靠的,但我们尚未独立验证此类数据。由于各种因素,我们经营的行业面临高度的不确定性、变化和风险,这可能导致结果与独立合作伙伴和我们的估计结果存在重大差异。Lyra 的候选产品 LYR-210 和 LYR-220 尚未获得 FDA 的批准。本演示文稿仅适用于投资者社区。此处没有任何内容旨在推广公司的候选产品。

1) 美国成年人健康统计汇总表:2018年全国健康访谈调查,表A-2b、A-2c;2) Baguley等人。Int Forum Allergy Rhinol,2014;4 (7): 525-3;生物可吸收鼻腔植入物旨在为疾病部位提供 6 个月的持续抗炎疗法。适应症:慢性鼻窦炎 (CRS) 约 12% 的美国人口1 ~ 50% 的患者药物治疗失败2 关键性三期试验正在进行专利保护至2036年的临床阶段生物技术公司为局部治疗开发创新的抗炎疗法慢性鼻窦炎公司概述

慢性鼻窦炎(CRS):“无法识别的流行病” 1 CRS 主要症状1 鼻塞和充血面部疼痛和压力鼻腔分泌物美国每年治疗2名CRS患者治疗2名医疗管理失败的CRS患者3~800万约400万名CRS患者目前正在接受ENT4 约140万 1) Tan BK等人Am J Respir Crit Care Med,2013 年;188 (11): 1275—7;2) Jang 等人。Otolaryngol Head Neck Surg,2018 年;3) Baguley 等人。Int Forum Allergy Rhinol,2014 年;4 (7): 525-32;4) OM1 Real World Data Cloud(OM1,Inc,美国马萨诸塞州波士顿),2015 — 2019 年 4 月。分析 9/2019
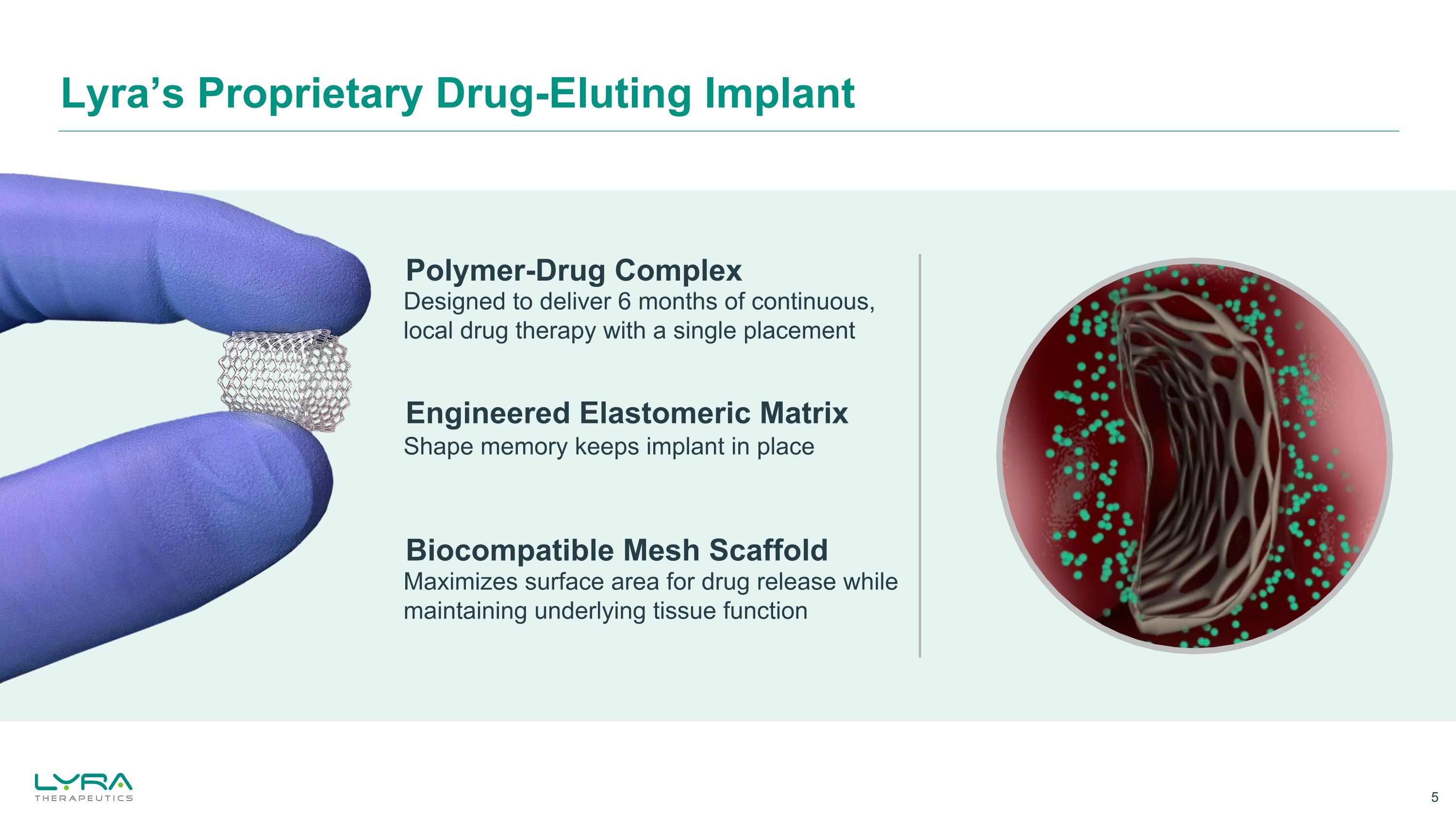
Lyra 的专有药物洗脱植体工程弹性体矩阵形状记忆可保持植入物原位聚合物药物复合物专为一次放置即可提供 6 个月的连续局部药物治疗生物相容性网状支架最大化药物释放的表面积,同时保持基础组织功能

Lyra 的 CRS 候选产品 “系列” 更大尺寸适用于因先前的 ethmoid 鼻窦手术而出现解剖结构扩大的患者(包括未接受手术的患者)更小的尺寸 LYR-210 和 LYR-220 旨在满足全方位的 CRS 患者,其中 ENT 根据患者解剖结构选择尺寸

LYR-210 和 LYR-220 旨在针对全方位的 CRS 患者,其中 ENT 根据患者解剖结构选择规模 Lyra Pipeline 候选患者 CRS 患者类型 2 期 LYR-210 长效糠酸莫米松 LYR-220 长效糠酸莫米松 ENLIGTEN 3 期计划解剖结构狭窄的慢性鼻窦炎患者(包括手术天真的患者)1 慢性鼻窦解剖学炎由于先前而肿大的患者鼻窦手术1 BEACON二期试验 1) “手术天真” 和 “鼻窦手术” 指的是埃氏窦手术。
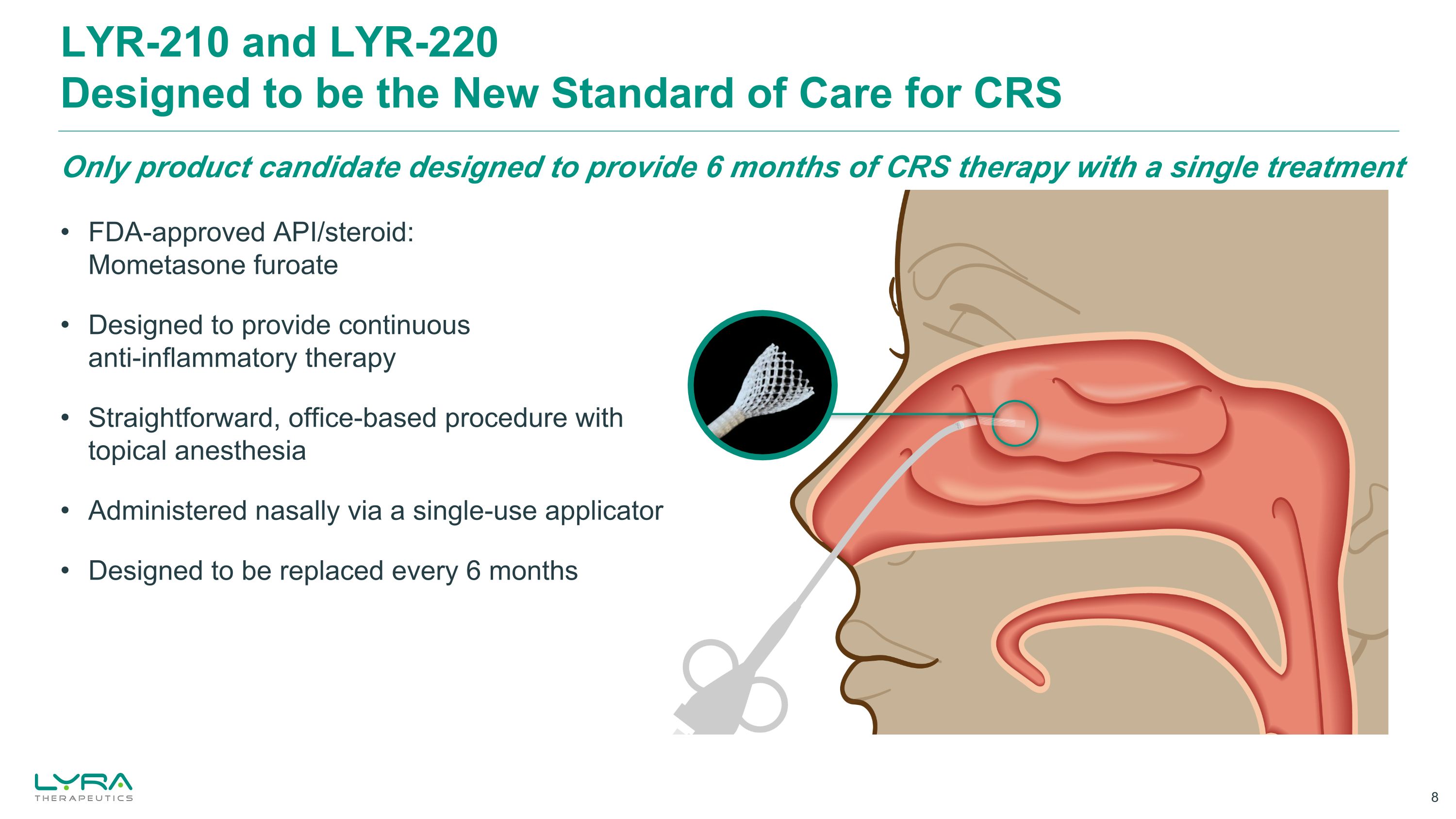
经美国食品药品管理局批准的 API/类固醇:糠酸莫米松旨在提供持续的抗炎治疗采用局部麻醉的直接办公室手术通过一次性涂抹器进行鼻腔给药设计每 6 个月更换一次 CRS 疗法的唯一候选产品 LYR-210 和 LYR-220 设计成为 CRS 的新护理标准
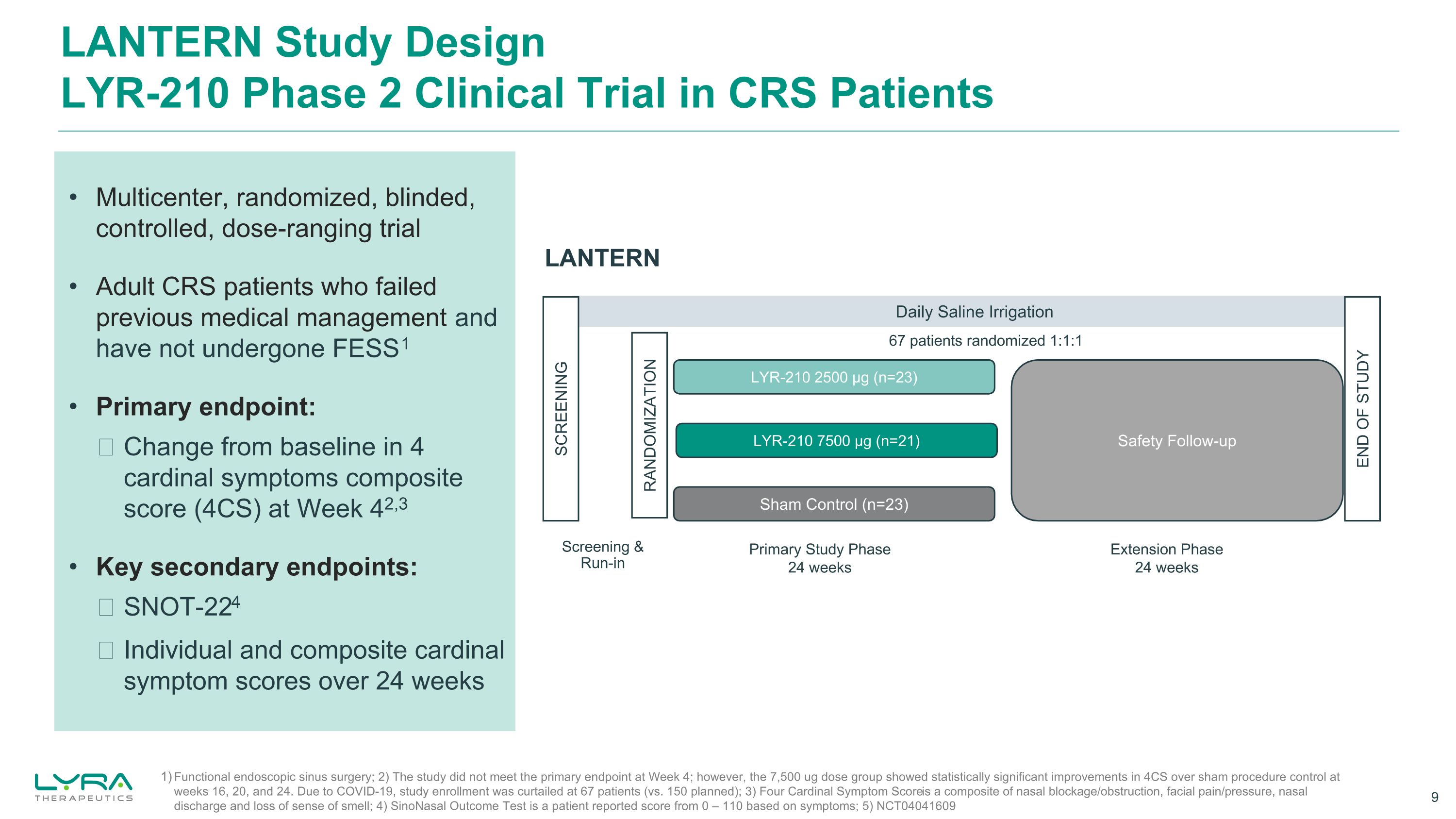
LANTERN Study designLYR-210 针对 CRS 患者的二期临床试验 LANTERN 每日盐水灌溉假设对照(n=23)LYR-210 2500 μg(n=23)随机筛查研究结束 LYR-210 7500 μg(n=21)初步研究阶段 24 周筛查和试用安全随访功能性内窥镜鼻窦手术;2)该研究在第 4 周未达到主要终点;但是,7,500 微克的剂量该组在第16、20和24周显示,与假手术控制相比,4CS有统计学上的显著改善。由于 COVID-19,研究入组人数减少到 67 名患者(计划为 150 名);3) 四项基本症状评分由鼻塞/梗阻、面部疼痛/压力、鼻腔分泌物和嗅觉丧失组成;4) SinonAsal 结局测试是患者报告的根据症状得分为 0 — 110 的患者;5) NCT04041609 67 名患者随机分配 1:1:1 多中心、随机、失明、对照、剂量范围试验先前未通过医疗管理且未接受 FESS1 治疗的成年CRS患者主要终点:4种主要症状与基线相比的变化第 42,3 周的综合评分 (4CS) 关键次要终点:SNOT-224 24 周内的个人和综合主要症状分数
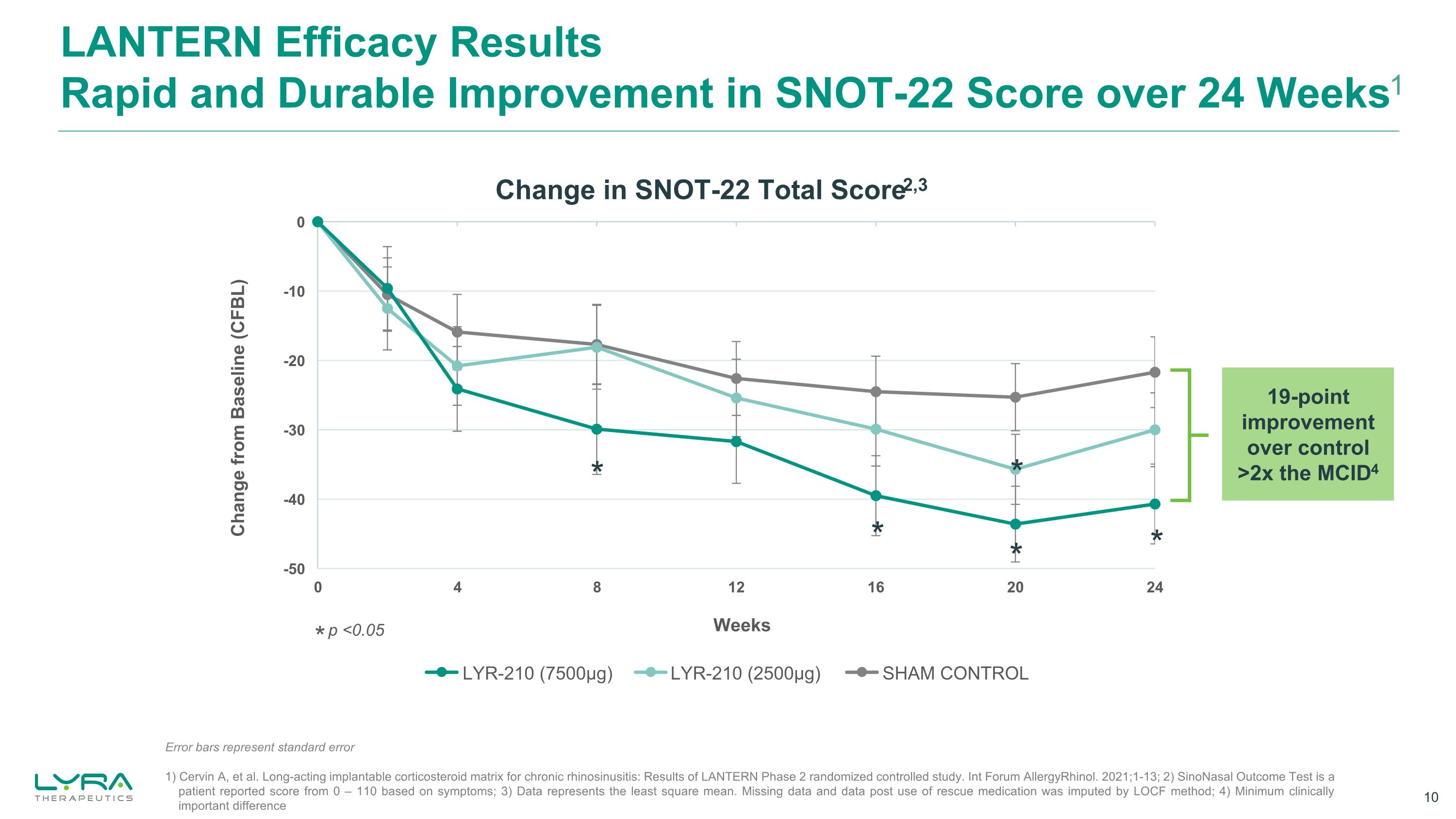
LANTERN 功效结果在 24 周内快速而持久地提高 SNOT-22 分数1) Cervin A 等人治疗慢性鼻窦炎的长效可植入皮质类固醇基质:LANTERN 2期随机对照研究的结果。Int Forum AllergyRhinol。2021;1-13;2) SinoNasal 结局测试是患者报告的根据症状得出的分数介于 0 — 110 之间;3) 数据代表最小二乘均值。使用救援药物后缺失的数据和数据是由 LOCF 方法归咎的;4) 最小的临床重要差异 * p 2 x MCID4 LYR-210 (2500μg) LYR-210 (7500μg) SHAM 控制误差条代表标准误差
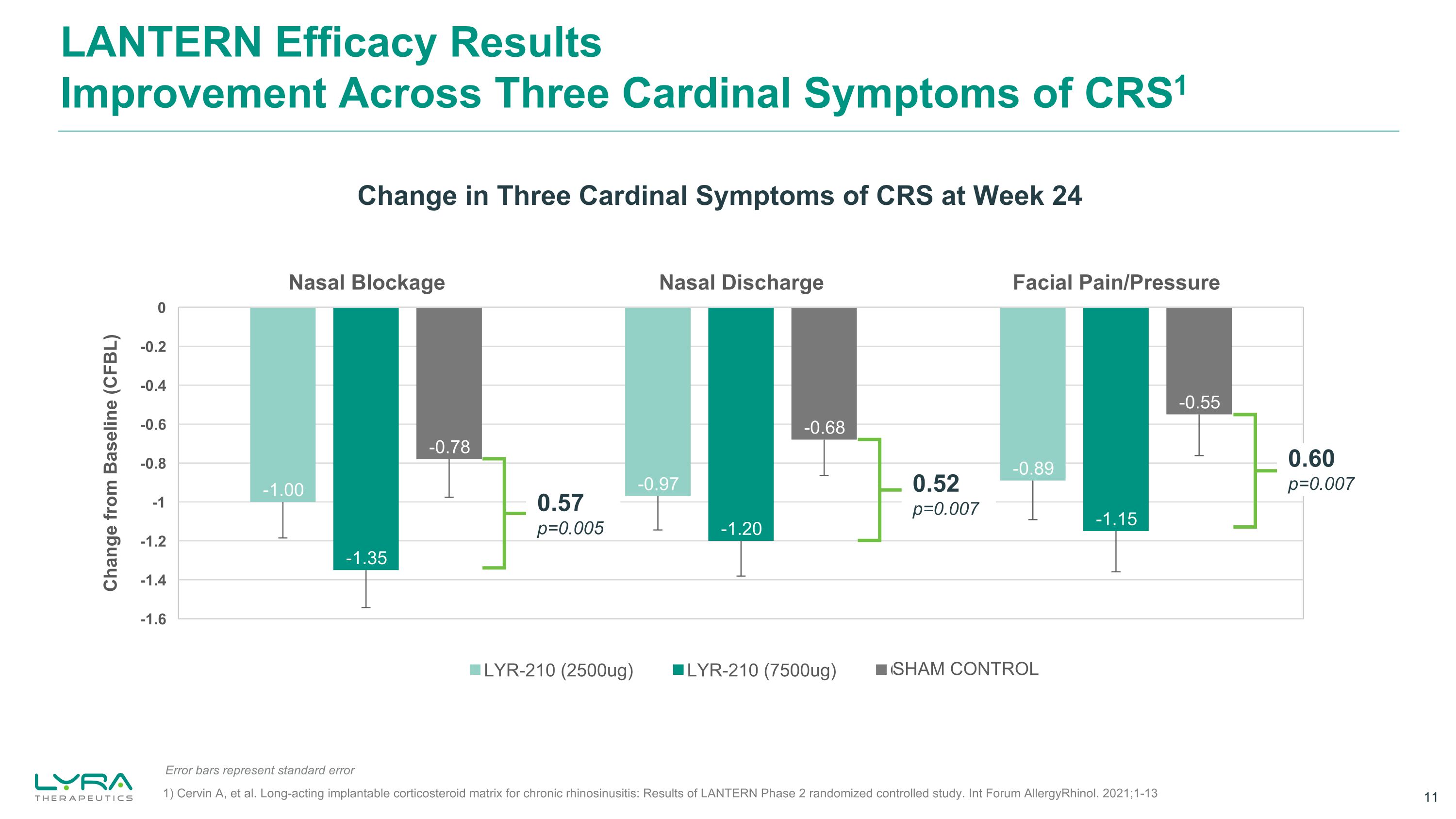
LANTERN 疗效结果改善CRS1的三个主要症状在第24周CRS的三个主要症状发生变化 0.57 p=0.005 0.52 p=0.007 0.60 p=0.007 0.60 p=0.007 SHAM 控制误差条代表标准误差 1) Cervin A 等治疗慢性鼻窦炎的长效可植入皮质类固醇基质:LANTERN 2期随机对照研究的结果。AllergyRhinol 国际论坛。2021;1-13
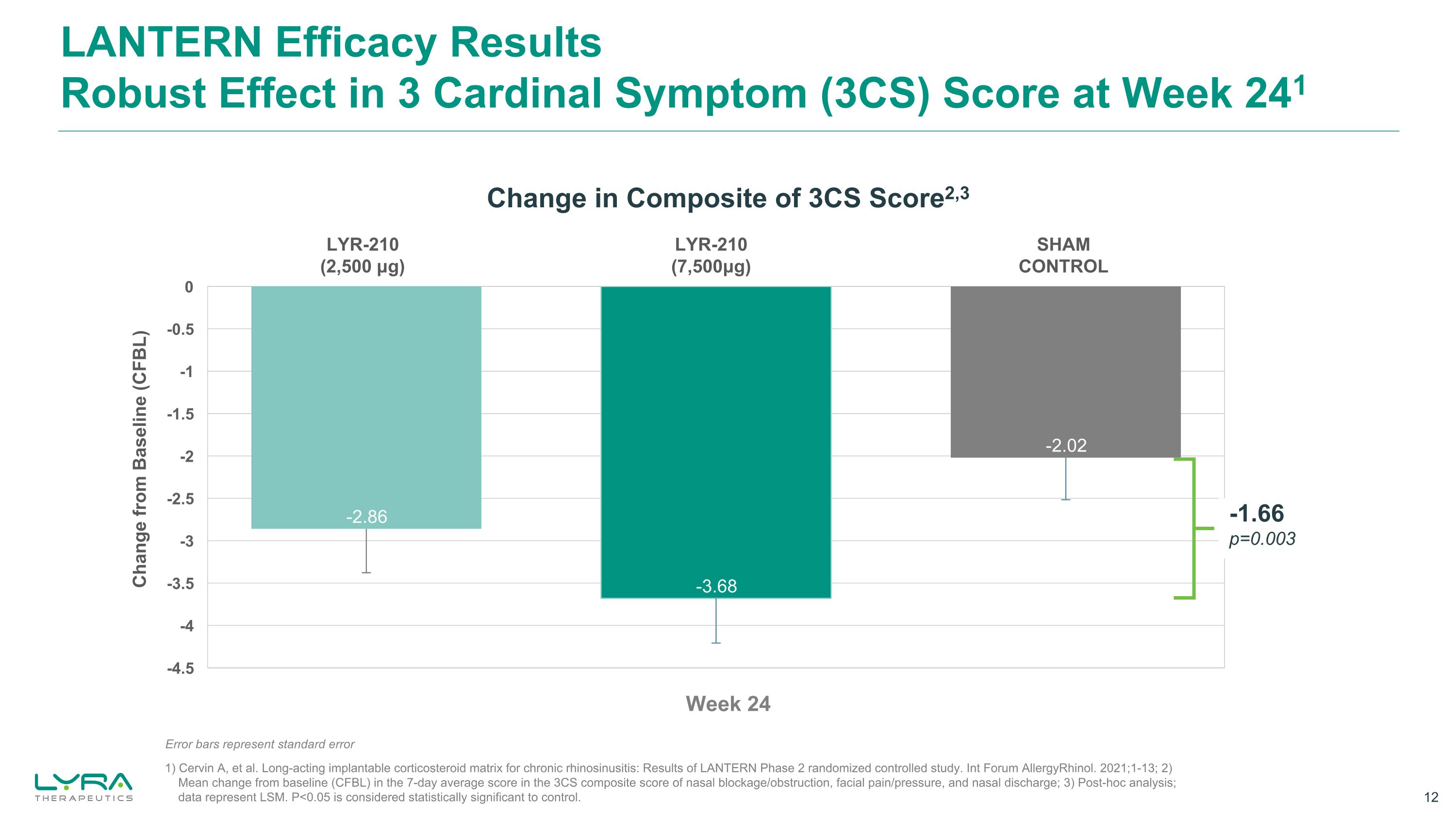
LANTERN 功效结果第 241 周的 3 种主要症状 (3CS) 评分效果强劲 1) Cervin A 等人治疗慢性鼻窦炎的长效可植入皮质类固醇基质:LANTERN 2期随机对照研究的结果。Int Forum AllergyRhinol。2021;1-13;2) 鼻塞/梗阻、面部疼痛/压力和鼻腔分泌物3CS综合评分中7天平均分数与基线(CFBL)的平均变化;3)事后分析;数据代表LSM。P
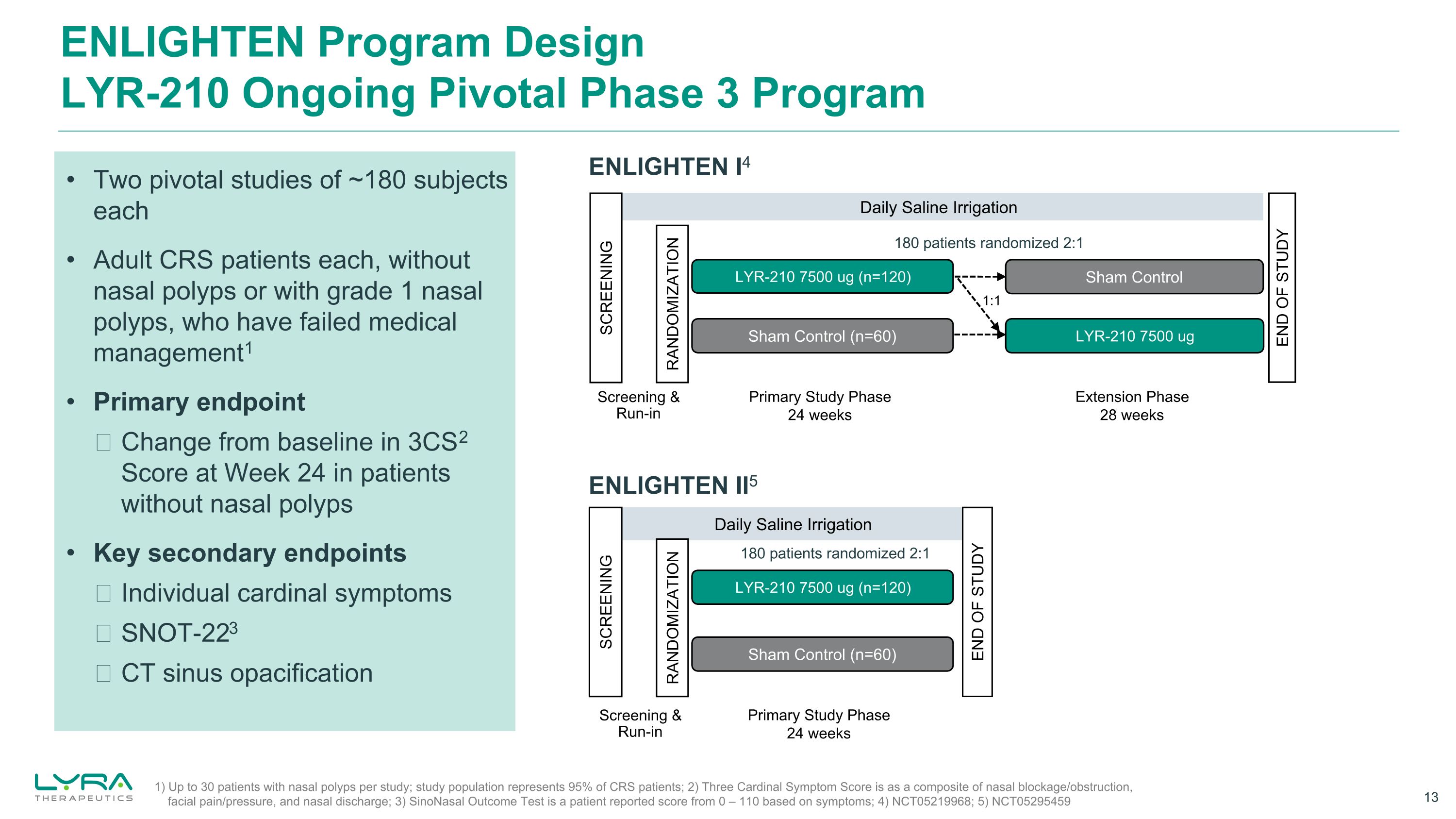
ENLIGTEN 计划 designLYR-210 正在进行中的关键三期项目 ENLIGHTEN I4 每日盐水灌溉假对照(n=60)LYR-210 7500 ug(n=120)LYR-210 7500 ug 筛查随机化初级研究 24 周延期阶段 28 周筛查和运行 1:1 研究结束 1) 每项研究最多30名鼻息肉患者;研究人群占CRS患者的95%;2)三种主要症状评分为由鼻塞/梗阻、面部疼痛/压力和鼻腔分泌物组合而成;3) SinoNasal 结果测试是患者报告的分数从 0 开始— 110 基于症状;4) NCT05219968;5) NCT05295459 ENLIGHTEN II5 每日盐水灌溉假设对照(n=60)LYR-210 7500 ug(n=120)筛查随机化初级研究阶段 24 周筛查和运行两项关键研究,每位受试者约180名受试者,每位成年CRS患者,没有鼻息肉或患有1级鼻息肉,他们没有药物管理失败1 主要终点与基线的变化没有鼻息肉的患者在第 24 周得分关键次要终点个人主要症状 SNOT-223 CT 鼻窦混浊 180 名患者随机 2:1 180 名患者随机分配 2:1
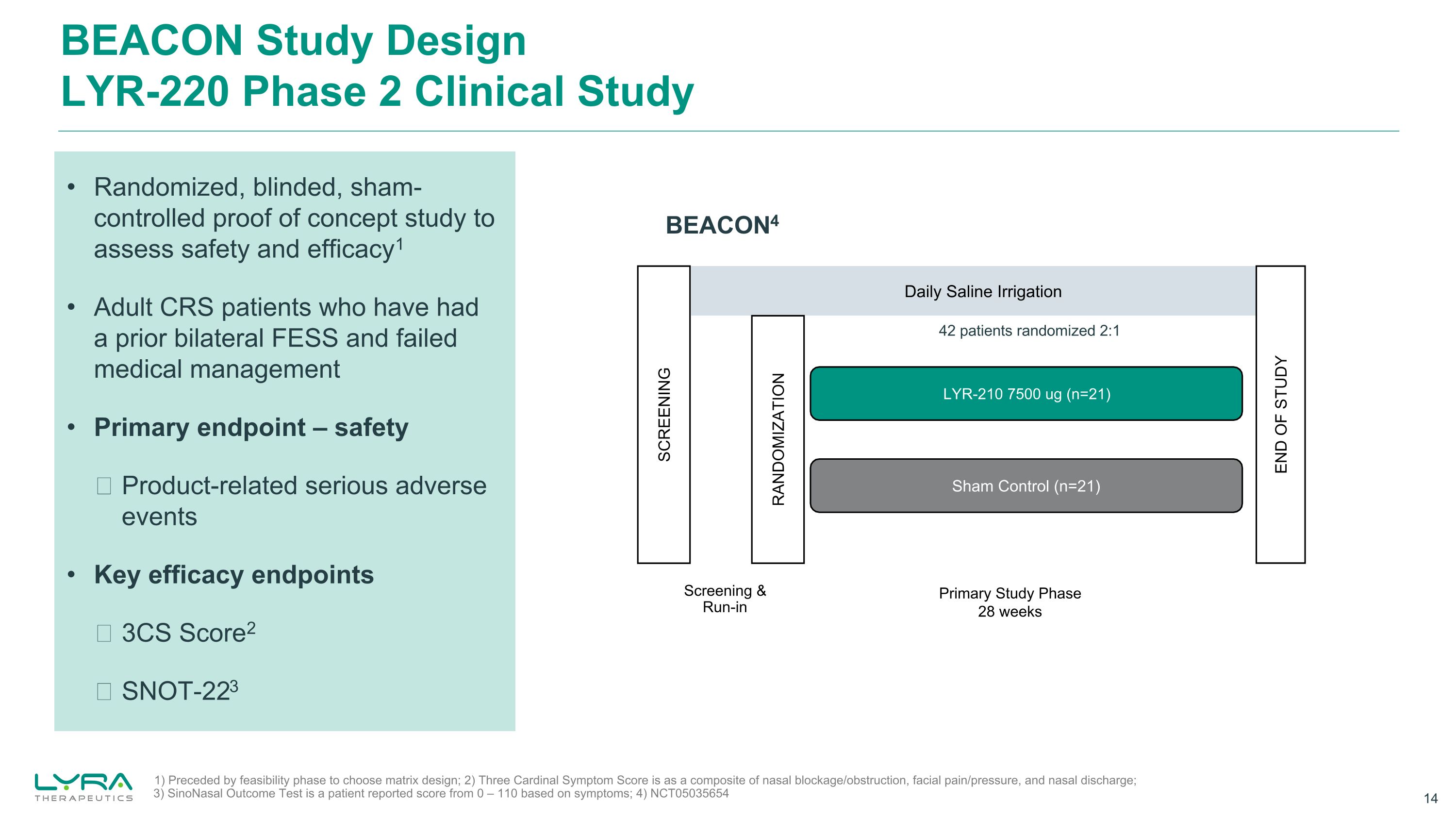
BEACON 研究 designLYR-220 2 期临床研究随机、盲目、虚假对照的概念验证研究,旨在评估安全性和有效性1 先前有双侧 FESS 且医疗管理失败的成人 CRS 患者主要终点——与安全产品相关的严重不良事件关键疗效终点 3CS 评分2 SNOT-223 1) 在选择基质设计的可行性阶段之前;2) 三种主要症状评分是鼻塞/梗阻的复合物,面部疼痛/压力和鼻腔分泌物;3) SinoNasal 结果测试是患者报告的分数根据症状从 0 — 110 不等;4) NCT05035654 BEACON4 每日盐水灌溉假设控制 (n=21) LYR-210 7500 ug (n=21) 随机筛查研究结束初级研究阶段 28 周筛查和试验 42 名患者随机分配 2:1
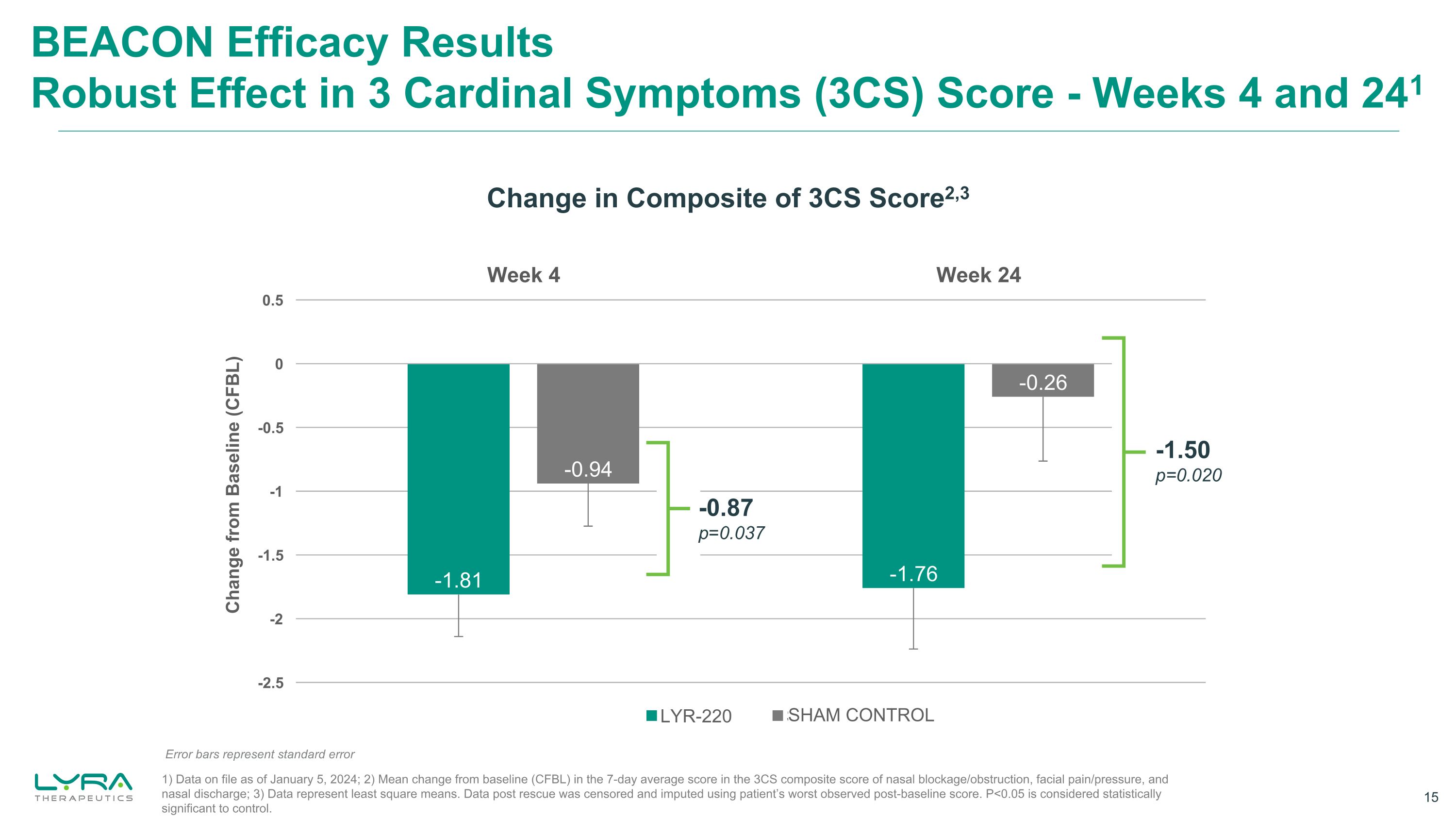
BEACON 疗效结果对 3 个主要症状 (3CS) 评分的强劲效果——第 4 周和 241 周 -0.87 p=0.037 -1.50 p=0.020 与基线 (CFBL) 的变化,3 SHAM 控制误差条代表标准误差 1) 截至 2024 年 1 月 5 日的存档数据;2) 鼻腔阻塞 3CS 综合评分中 7 天平均分与基线 (CFBL) 的平均变化年龄/梗阻、面部疼痛/压力和鼻腔分泌物;3) 数据代表最小二乘均值。使用患者观察到的最差的基线后分数对救援后的数据进行了审查和归因。P
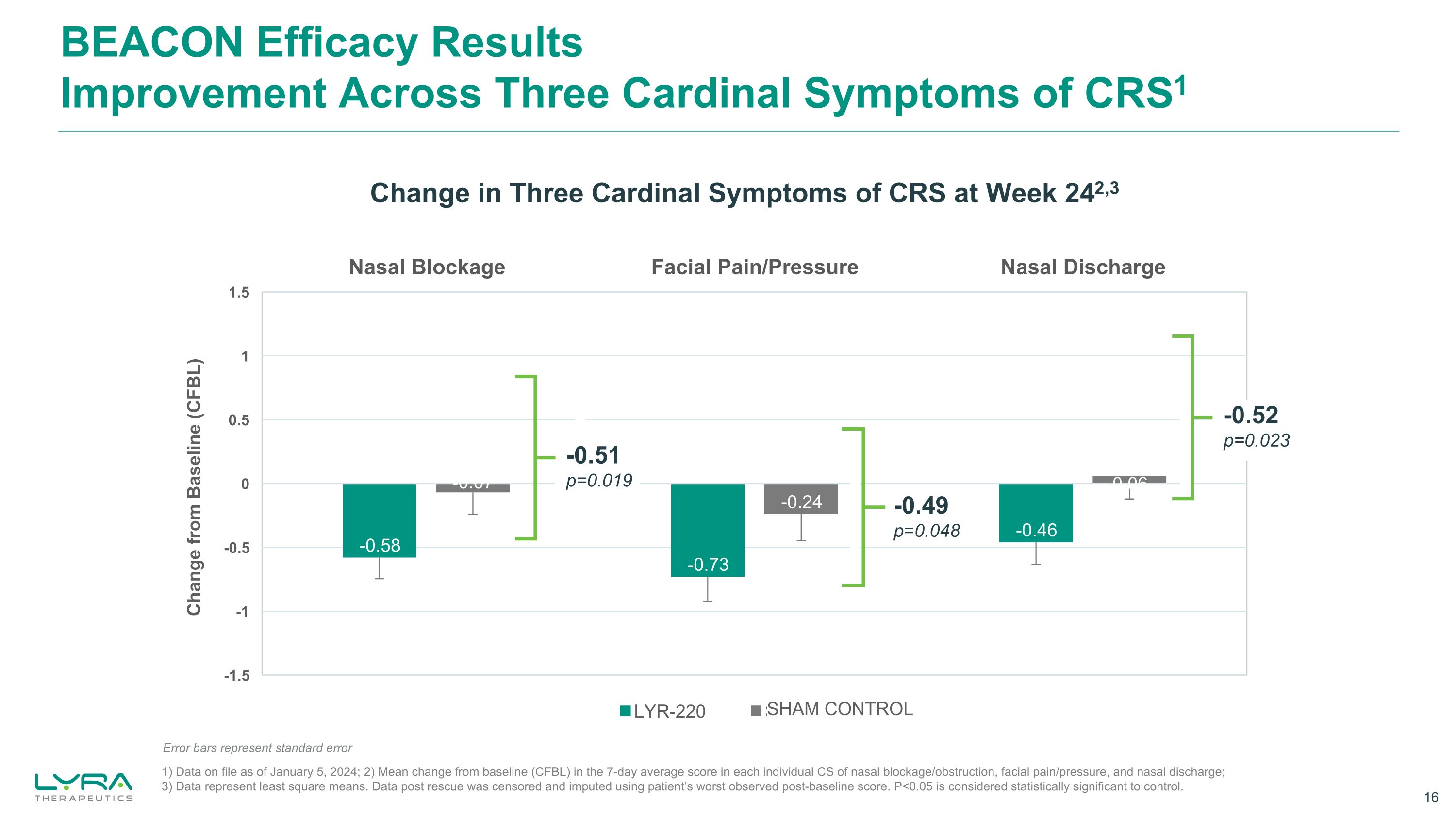
BEACON 疗效结果对 CRS1 的三个主要症状有所改善 -0.49 p=0.048 -0.52 p=0.023 -0.019 与基线 (CFBL) 相比的变化第 242,3 周 CRS 三种主要症状的变化 1) 截至 2024 年 1 月 5 日的存档数据;2) 鼻塞/梗阻、面部疼痛/每个 CS 的 7 天平均评分与基线 (CFBL) 的平均变化压力和鼻腔分泌物;3) 数据表示最小二乘均值。使用患者观察到的最差的基线后分数对救援后的数据进行了审查和归因。P
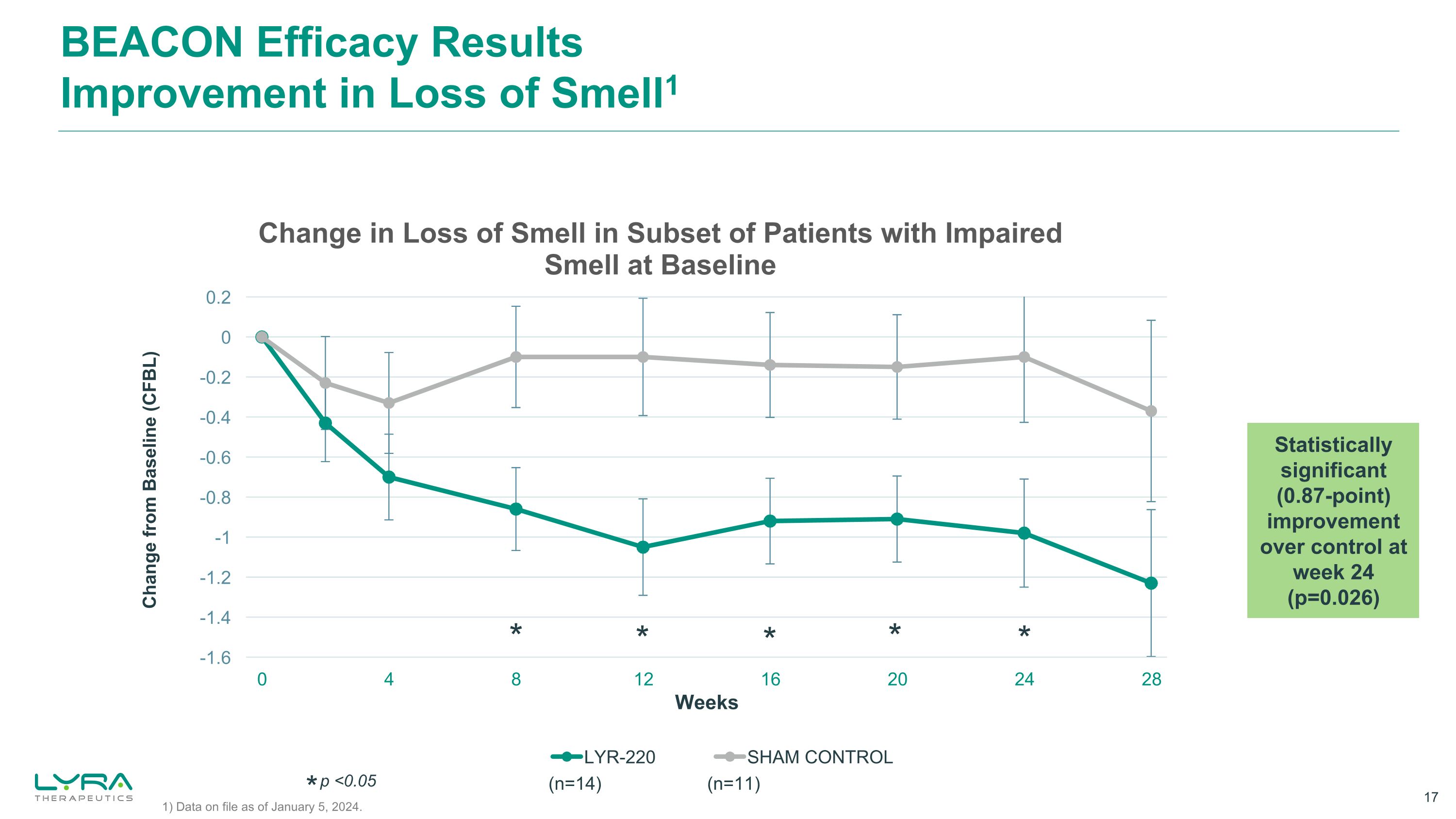
BEACON 功效结果气味损失改善1 与基线 (CFBL) 相比变化* * * * * * * 在第 24 周(p=0.026)具有统计学意义(0.87 个百分点)的改善(p=0.026)* p
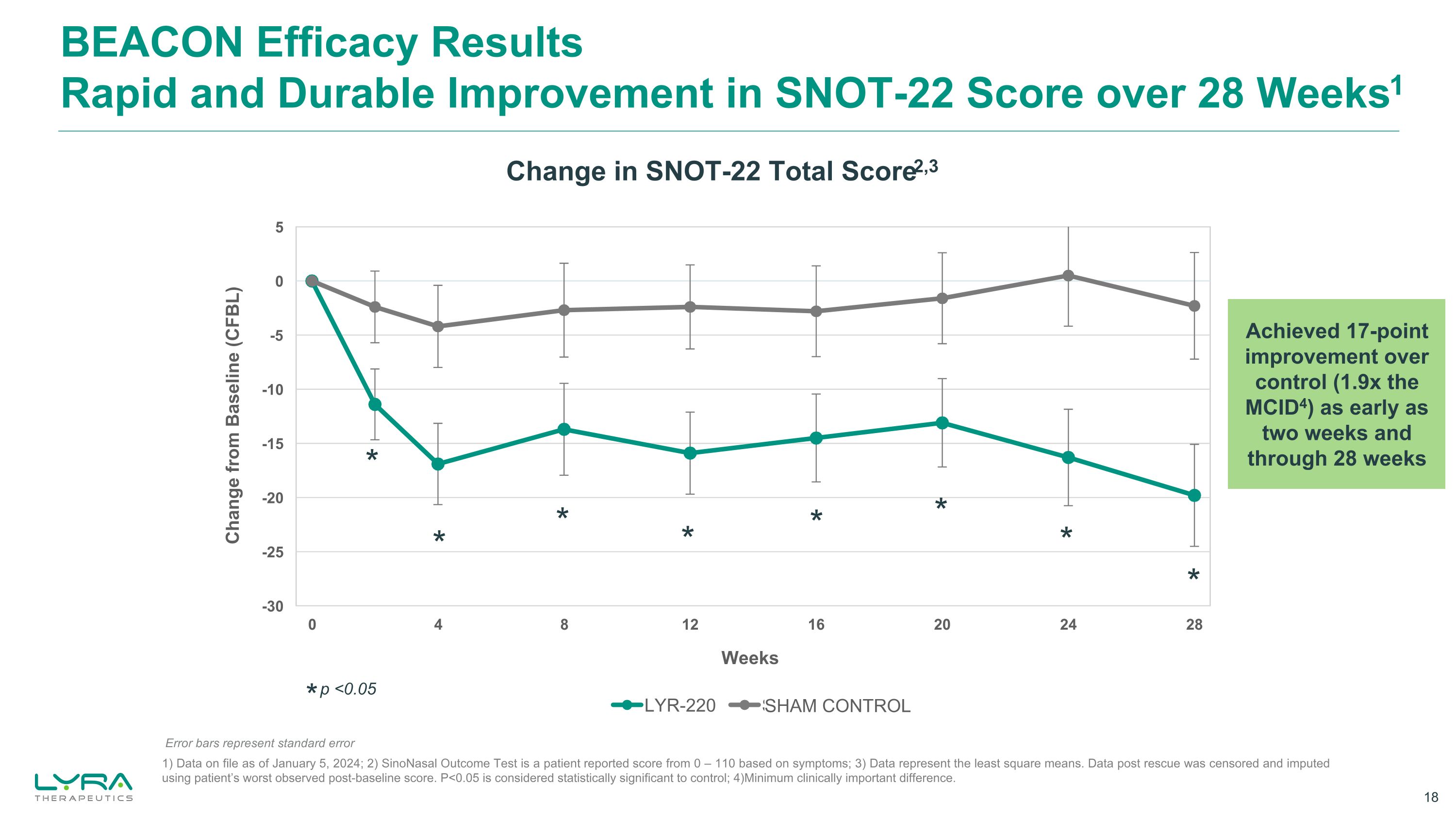
BEACON 功效结果在 28 周内快速而持久地改善 SNOT-22 分数1 * p

LYRA候选产品如果获得批准,预计将与目前的耳鼻喉科实践办公室的程序保持一致,即耳鼻喉科医生习惯于为不愿接受手术的患者提供治疗选择,从而使耳鼻喉科医生能够为更多的患者提供护理服务,预计将符合耳鼻喉科诊所的报销模式
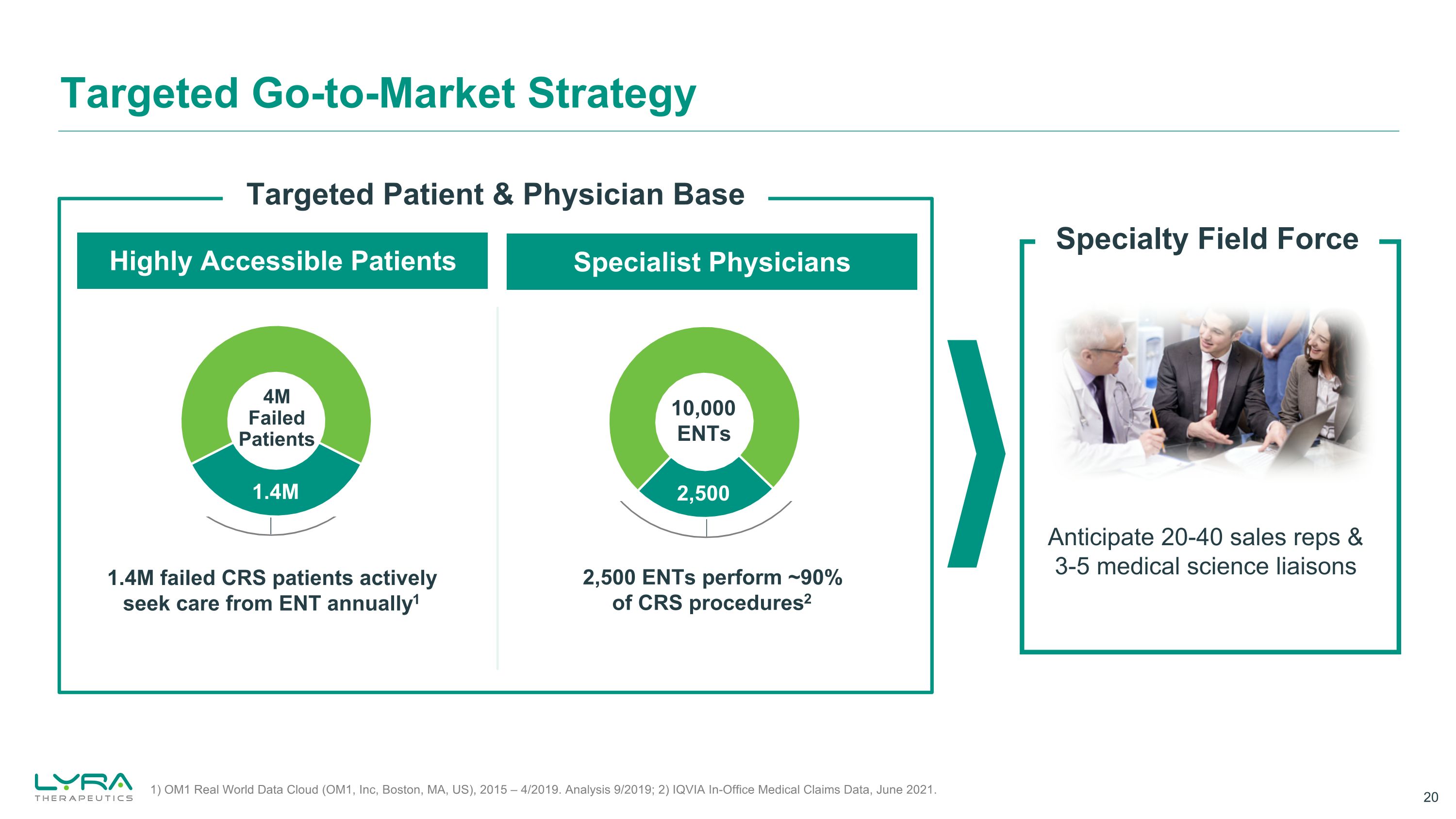
有针对性的市场进入战略预计将有20-40名销售代表和3-5名医学联络员专业野战部队目标患者和医师基地2,500例接受约90%的CRS手术2 2,500名专科医生140万失败的CRS患者每年积极寻求耳鼻喉科失败患者140万高度可访问的患者10,000 eNT 1) OM1真实世界数据云(OM1,Inc,美国马萨诸塞州波士顿),2015 — 2019 年 4 月。2019年9月分析;2) IQVIA办公室内医疗索赔数据,2021年6月。

预期里程碑 LYR-210:ENLIGHTEN 第 3 阶段计划 LYR-220:BEACON 第 2 阶段计划 2023 年中期:2024 年第 2 季度完成 ENLIGHTEN I 第 2 季度入学的关键数据:来自 ENLIGTEN I 2024 年下半年的扩展研究数据:2023 年初完成 ENLIGHTEN II 的招生:2024 年 9 月完成注册:2024 年第 2 阶段会议结束

财务概况截至2023年9月30日的现金、现金等价物和短期投资为1.026亿美元 2023年10月2日,公司根据自动柜员机销售协议共出售了3,017,568股普通股,加权平均价格为每股3.71美元,净收益为1,090万美元。截至2023年9月30日,这些净收益未包含在现金和现金等价物或短期投资中,截至2023年11月1日已发行的5,260万股普通股
