
执行副本1-资产购买协议本资产购买协议(“协议”)日期为2023年7月31日(“生效日期”),由InDior UK Limited(Co.)与C4x Discovery Limited(Co.)签订,Indior UK Limited(Co.)是一家在英格兰和威尔士注册成立的公司,公司编号7183451,注册办事处位于HU4 7DY Priory Park,Priory Park Henry Boot Way(Chapleo Building Henry Boot Way,Priory Park,HU4 7DY);C4x Discovery Limited(C4x Discovery Limited)是一家在英格兰和威尔士注册成立的公司,注册地址为曼彻斯特One,53 Portland Street,曼彻斯特,M1 3LD(“卖方”),每个“党”和共同的“党”。鉴于,卖方就许可化合物和许可产品的开发、制造、营销、销售和分销拥有许可技术的权利;而卖方和买方于2018年3月28日签订了许可协议(“许可协议”),据此卖方授予许可技术项下独家、可再许可、永久、可转让的许可,以开发、使用、制造、制造、进口、出口、获得监管批准并将许可化合物(S)和/或许可产品(S)商业化;鉴于卖方现在希望向买方出售,买方现在希望从卖方购买所购买的资产(如本协议所定义的);鉴于双方希望在完成交易时终止许可协议,所有条款均符合本协议现在规定的条件,因此,考虑到本协议所包含的相互契诺以及其他良好和有价值的对价,买方和卖方同意如下:第一条定义第1.1节定义。本协议中使用的下列术语应具有以下赋予它们的含义。第1.2节“关联方”对于一方来说,是指直接或间接控制、由该方控制或与该方处于共同控制之下的任何人;在本定义中,“控制”应指:(1)直接或间接拥有指导一个实体的管理或政策的权力,无论是通过拥有代表股权、证券或合伙利益的权益、合同或其他方式,或(2)直接或间接拥有一个实体的有表决权证券或股本或其他所有权权益的50%(50%)以上。第1.3节“适用法律(S)”是指适用于本协议项下特定活动和司法管辖区的所有联邦、州、国家和地方法律、法规、条例、规则、条例、规章、指南,包括适用的贿赂立法、GCP、国内生产总值、GMP、GLP以及对许可产品的开发、制造和/或商业化具有管辖权的相关政府机构的规则和条例。第1.4节“C4x技术诀窍”是指在生效日期由卖方控制的所有技术诀窍(包括数据),这些技术诀窍对于开发、制造或使用经许可的化合物是合理必要的或有用的DocuSign信封ID:556FC81F-BAFA-4B3A-BC64-1F8758E4C0D1本展品的4.22部分已经过编辑。某些确定的信息已被排除在本展览之外,因为它既不是实质性的,也是(Ii)如果公开披露可能会造成竞争损害的。编辑过的材料上标有[***].

Execution Copy-2-或开发、制造、商业化、使用、进口、提供销售或销售许可产品,明确不包括Conformetrix技术。第1.5节“C4x专利”是指在生效日期由C4x或其关联公司(S)控制的、要求许可化合物和/或许可产品的组成、开发、制造、商业化或使用的所有专利,这些专利具体列于表A中。第1.7节“索赔”是指买方就本协议的任何规定(包括违反任何保证)可能拥有或提出的任何诉讼权利或索赔(无论是在合同、侵权行为、虚假陈述或其他方面)。第1.8节“Conformetrix数据”是指动态分子在溶液中的三维结构,包括用于推导最终配体结构和构象特征的计算或基本原理,以及基于核磁共振和其他数据的计算,这些数据用于生成分子或配体在使用卖方专有的Conformetrix技术生成的3D空间中的动态行为。第1.9节“Conformetrix技术”是指卖方专有的分析软件、技术以及相关的科学和其他诀窍和信息、商业秘密、知识、技术、手段、方法、过程、实践、公式、指令、技能、技术、程序、经验、想法、技术援助、设计、图纸、组装程序、计算机程序、仪器、规格、数据、结果、实验室笔记和笔记本在生效日期和期间存在,用于确定动态分子在溶液中的三维结构,包括用于推导最终配体结构和构象特征的计算或原理,以及基于核磁共振(核磁共振)和用于生成分子或配体在三维空间中的动态行为的其他数据的计算,以及关于分子形状的一般学习,包括但不限于构象线和4Sight(为清楚起见,这包括从特许化合物中获得的一般形状学习)。第1.10节“产权负担”指任何性质的抵押、抵押、信托契约、留置权、担保权益、地役权、通行权、质押、评估、产权负担或限制。第1.11节“政府实体”是指适用司法管辖权的任何法院、行政机关或委员会或其他政府机关或工具,无论是国内的还是国外的。第1.12节的“债务”是指任何和所有债务、债务和义务,无论是应计的还是固定的、已知的还是未知的、绝对的或有的、到期的或未到期的、到期的或即将到期的、确定的或可确定的,包括任何税收和根据任何适用法律、合同或其他规定产生的债务、债务和义务。第1.13节“许可化合物”指(I)C4x_3256;(Ii)C4x专利权利要求所涵盖的任何其他化合物;(Iii)双方之间开发和商业化(I)和/或(Ii)具有与(I)和/或(Ii)所述分子相同作用机制的任何化合物变体的专有权利;(Iv)在双方之间,开发和商业化从(I)、(Ii)和/或(Iii)中描述的任何分子中具体衍生的任何分子的独家权利,并使用C4x技术,并被确定具有与上述(I)、(Ii)和/或(Iii)中所述分子相同的作用机制;和(V)在双方之间,开发和DocuSign信封ID:556FC81F-BAFA-4B3A-BC64-1F8758E4C0D1的独家权利

Execution Copy-3-将使用C4x专有技术或与任何许可产品的开发相关的任何分子商业化,并确定其具有与上文(I)、(Ii)和/或(Iii)中描述的分子相同的作用机制。第1.14节“许可产品”是指含有许可化合物的成品(在所有配方、剂量和给药系统中)。第1.15节“许可技术”是指C4x专有技术和C4x专利。第1.16节“重大不利影响”是指对许可产品或任何已购买资产产生重大不利影响的变化、情况或影响,但不包括买方不知道的、由以下因素引起或与之相关的任何变化、情况或影响:(A)通常影响(I)医疗保健或生物技术行业或(Ii)美国或世界经济或证券市场的条件变化;(B)任何适用法律的变化;(C)本次交易的公告;或(D)采取本协议要求或预期采取的任何行动。第1.17节“记录”指与卖方开发许可化合物、许可产品或购买的资产以及C4X专利记录有关的卖方的所有文件、文件和记录,但在许可协议中尚未提供此类内容。第1.18节“监管申请”是指在任何司法管辖区内开发、测试(包括进行临床试验)、制造、加工、分销、进口、营销、商店、标签、包装、促销、销售或要约销售许可产品及其所有补充、修订和修订的任何和所有申请,无论批准与否由卖方或卖方的任何关联公司拥有或控制。第1.19节“监管批准”是指与卖方或卖方的任何关联公司拥有或控制的许可院落或许可产品有关的任何政府实体的所有许可证、许可、豁免、同意、证书、登记、批准(包括但不限于NDA和ANDA的批准、定价和第三方补偿批准以及标签批准)。第1.20节“税收”是指所有国内和国外的税费和评估,包括与此相关的所有利息、罚款和附加费。第1.21节“纳税申报单”指与任何税项(包括估计税项)有关并须向税务机关提交或须提交予税务机关的任何报告、申报表、选举、通知、预算、声明、资料声明及其他表格及文件(包括所有附表、证物及其他附件)。第1.22节:“2006年企业转让(就业保障)规例”及任何先前的规例,包括“1981年企业转让(就业保障)规例”。DocuSign信封ID:556FC81F-BAFA-4B3A-BC64-1F8758E4C0D1

执行本-第四条--第二条购置资产的销售、购买和许可2.1节购买和销售。根据本协议的条款及条件,于成交日期(即2023年8月4日星期五),卖方应向买方出售、转让及交付,而买方应购买、收购及接受卖方对所购资产及其之下的所有权利、所有权及权益,并于成交时无任何产权负担地转让及转让予买方。在结束的同时,卖方和买方之间的许可协议将终止,任何一方不再承担任何义务,为清楚起见,许可协议第19.1.2至19.1.4条和第19.3条所述的终止后果不适用。第2.2节购买的资产。(A)“购买的资产”是指卖方或卖方的任何关联公司的所有下列财产、资产和权利:(I)许可技术;(Ii)监管申请和监管批准(如果适用);(Iii)监管文件(如果适用)(电子形式或硬拷贝);(Iv)记录;(V)C4x 3256临床前毒性研究的样本;以及(Vi)与前述相关的任何和所有商誉。(B)即使第2.2(A)节有任何相反规定,卖方除购买资产外的所有有形和无形资产,包括但不限于卖方的背景药物发现技术和方法及其任何不涉及任何许可化合物或许可产品的开发计划,均应排除在本协议所设想的购买和销售之外。第2.3节承担某些资产、负债和义务。根据许可协议,买方自2018年3月28日起独家负责特许化合物和特许产品的开发。自2018年3月28日以来,因买方为开发特许化合物和特许产品而进行的开发活动而产生的任何知识产权、正在进行的工程、权利、资产或责任(不包括因卖方的任何过错而产生的负债和/或卖方在成交前知悉的未披露的负债),应转让给买方,但不得转让给买方。成交后,买方应对成交后产生的与所购资产有关的任何负债(不包括成交前到期和应付的、因卖方的过错而产生的或卖方在成交前已知晓的负债)承担全部责任,包括但不限于提交、维护、起诉和以其他方式处理c4x专利的成本、因任何特许产品的制造或商业化而产生的任何负债,包括但不限于产品责任索赔或与侵犯第三方知识产权有关的索赔(统称为“承担的负债”):除承担的负债外,双方明确理解并同意:买方不承担卖方或其关联公司的任何责任(统称为“保留负债”),也不承担任何责任。DocuSign信封ID:556FC81F-BAFA-4B3A-BC64-1F8758E4C0D1

执行副本-5-第2.4节存档副本。卖方可保留卖方或卖方任何关联公司交付给买方的本合同项下文件的全部或任何部分的副本,但此类档案副本应遵守本合同规定的保密条款,直到此类档案副本退还或销毁给买方为止。第三条购进价格3.1节购进价格。购买资产的总收购价为1595万英镑(GB 15,950,000)加增值税(“收购价”)。这笔款项将在成交时到期并以电汇方式立即支付给卖方指定的一个或多个账户(统称为“收购价”)。第3.2节购进价格的分配。收购价格应根据任何适用的法律,自成交之日起在所购买的资产中进行分配。买卖双方同意(A)以符合任何适用法律和本协议条款的方式报告(并促使其各自的关联公司报告)本协议预期的交易,并且(B)不在任何纳税申报表、任何退税要求、任何诉讼或其他方面采取任何与本协议不一致的立场。根据第X条支付的所有款项应被视为对采购价格的调整。第3.3节购买价格应被视为减去就索赔或赔偿索赔向买方支付的任何款项,减额应尽可能分配给与违约或赔偿有关的所购资产,如果这不可行或不可能,则以买方决定的方式分配。第3.4节转让税。在支付给任何政府实体的范围内,与本协议拟进行的交易相关的所有转让、销售、增值税、印花税和类似税款应由买方承担。第四条本协议拟进行的交易的结束(“结束”)应于英国夏令时间2023年8月4日(星期五)(“结束日”)17时01分进行,买方收到所有完成的交付成果(不包括双方书面同意的C4X3256临床前毒性研究的样本)后,本协议的所有计算、调整和转移将于17时01分起生效。截止日期为英国夏令时。第五条卖方的陈述和担保卖方向买方陈述并保证本条款第五条所载的陈述是真实和正确的。DocuSign信封ID:556FC81F-BAFA-4B3A-BC64-1F8758E4C0D1

执行文案-6-第5.1节组织;信誉良好。卖方是根据其成立所在司法管辖区的法律正式成立、有效存在和信誉良好的公司。卖方有必要的权力和权限拥有所购买的资产,并按照目前进行的方式继续其与许可产品有关的业务。卖方在其注册成立的管辖区以外的任何司法管辖区具有作为外国公司经营业务的正式资格,并且在其所经营的业务的性质需要这种资格的每个司法管辖区具有良好的信誉,但如果不具备这种资格或不具备良好的信誉将不会单独或总体上造成重大不利影响的情况除外。第5.2节授权;执行和交付。卖方拥有订立本协议和完成本协议所设想的交易所需的法人权力和授权。卖方签署和交付本协议以及完成本协议的交易,已得到卖方采取一切必要的公司行动的适当和有效的授权。本协议已由卖方正式签署和交付,假设买方适当授权、签署和交付本协议,本协议将构成卖方的法律、有效和具有约束力的义务,可根据其条款对卖方强制执行,但须遵守适用的破产、破产、重组、暂停、欺诈性转让和其他不时生效的影响债权人权利的类似法律,并遵守衡平法的一般原则,无论是在衡平法诉讼中考虑还是在法律上考虑。第5.3节:无违规行为;反对。除附表5.3中披露的情况外,本协议的执行和交付并不违反本协议的执行和交付,并且完成本协议预期的交易并遵守本协议的条款不会:(A)违反适用于卖方或所购买资产的任何适用法律;(B)要求向任何人提供任何批准、授权、同意、许可、豁免、备案或登记,但已获得或作出的批准、授权、同意、许可、豁免、备案或登记除外,或如果未取得或作出此类批准、授权、同意、许可、许可、豁免、备案或登记,将不会单独或整体对卖方履行其在本合同项下的义务造成重大不利影响或实质性干扰;或(C)与本章程或卖方章程或类似组织文件的任何规定相冲突或违反。第5.4节购买资产的所有权。卖方对所购买的每项资产拥有良好的、可出售的和有效的所有权(视属何情况而定),没有任何产权负担。不存在与许可技术有关的现有许可或其他协议,也不存在影响买方在本协议中的权利或对买方施加任何义务的情况。第5.5节诉讼或潜在的第三方索赔。未就卖方开发、测试、制造、分销或销售许可化合物或许可产品或与其他许可技术相关的诉讼、听证、调查、指控、投诉、索赔、要求、通知、审查或询问提起或展开任何诉讼、诉讼、程序、听证、调查、指控、投诉、索赔、要求、通知、审查或询价,或据卖方所知,尚未进行或受到针对卖方的威胁。卖方未收到第三方的书面通知,声称C4x专利或许可技术的实践侵犯了该第三方的专利或其他所有权;卖方不知道C4x专利或许可技术的开发、制造、销售或商业化将侵犯任何第三方的任何知识产权;卖方未收到针对其提出的任何C4x专利的无效或不可强制执行的书面索赔(不包括任何搜索报告和与专利局的通信或通信),也未向卖方提出任何人的书面索赔或要求,以挑战卖方对任何许可技术的所有权或卖方使用或许可任何许可技术的权利;卖方在开发许可技术时没有挪用商业秘密或滥用任何第三方的机密信息;卖方并不实际知道第三方正在侵犯或挪用许可技术(为清楚起见,DocuSign信封ID:556FC81F-BAFA-4B3A-BC64-1F8758E0C0C0A-BC64-1F8758E0C0C0A

执行副本7-卖方未进行任何文献搜索或竞争对手分析);且卖方未向任何第三方(包括卖方的任何关联公司或投资者)授予对许可技术的任何权利、所有权或权益,或对许可技术的任何产权负担。第5.6节C4x专利。截至生效日期存在的所有C4x专利如表A所示。卖方、其附属公司和C4x专利的任何发明人已就在美国被起诉的C4x专利遵守了他们向美国专利商标局(USPTO)坦诚和披露的义务,也遵守了适用于C4x专利被起诉的任何相关外国专利局的任何类似规则;C4x专利的所有材料先前技术均已引用USPTO。除为当前交易向买方披露外,卖方已采取合理措施保护C4x专有技术的机密性,据卖方所知,C4x专有技术仍是卖方受保护的商业秘密。与C4x专利有关的所有申请、提交、注册、续期和应付费用均已在到期时提出/支付,截至生效日期没有尚未完成的申请。第5.7节许可技术。截至生效日期,没有任何许可、协议、授权和许可(无论是以何种形式以及无论是明示还是默示)授权或以其他方式允许第三方使用许可技术。第5.8节限制使用。据卖方所知,自2018年3月28日以来,卖方并未就竞争对手的活动、经营自由或一般情况作出任何查询,并在下述第5.18节的规限下,并无任何情况会以任何方式限制所购资产的使用。第5.9节遵守许可协议。卖方已在所有重要方面遵守许可协议的条款。第5.10节商业协议。没有与所购资产相关的协议或合同。第5.11节就业。卖方并无雇用或聘用任何人士(不论是临时或永久的,亦不论是根据服务合约或服务合约)购买的资产,因此就本协议而言,TUPE并不相关。第5.12节业务行为卖方始终按照适用法律处理与所购资产有关的业务,并一直遵守任何相关司法管辖区的所有适用法律和法规。第5.13节定罪:卖方及其任何董事或雇员(现任或前任)均未被定罪。第5.14节无力偿债。卖方并非破产或无力偿还1986年破产法或任何其他适用的破产法所指的债务,也没有在债务到期时停止偿还债务。第5.15节债权人诉讼。在任何适用的司法管辖区均未采取任何步骤或提出任何建议,以启动下列程序:DocuSign信封ID:556FC81F-BAFA-4B3A-BC64-1F8758E4C0D1

执行副本-8-a)卖方债权人采取任何行动强制执行其债务的能力被暂停、限制或阻止,包括(但不限于)根据《1986年破产法》第A1部分的暂停;B)卖方的部分或全部债权人通过协议或依据法院命令接受少于应付给他们的款项以清偿这些款项,或与卖方作出任何其他妥协或安排(包括但不限于1986年破产法第1部下的公司自愿安排、2006年《破产管理法》第26部下的安排计划或2006年《破产管理法》第26A部下的重组计划);c)委任某人代表其债权人管理卖方的事务、业务和资产;或d)指定对出卖人的任何资产进行抵押的持有人控制出卖人的业务和/或任何资产。关于卖方:a)没有指定管理人;b)没有向法院提交文件,也没有向法院提出指定管理人的申请;c)卖方、其董事或符合资格的浮动抵押持有人(定义见《1986年破产法》附表B1第14段)没有发出有意指定管理人的通知。D)没有提出将卖方清盘的请愿书或命令,没有通过或提议将卖方清盘的决议,也没有启动可能导致卖方清盘或其资产在债权人、股东或其他出资人之间分配或卖方解散的其他程序。E)没有对卖方的任何货物或资产启动、征收或强制执行扣押、执行或其他程序,也没有债权人或产权负担人控制或占有卖方的任何货物或资产。第5.17节其他司法管辖区。在英国以外的任何司法管辖区,没有发生任何事件,也没有就卖方提起任何诉讼,其效力等同于或类似于上文第5.13段至第5.16段(含)所指的任何事项。第5.18节除本第5节明确规定外,不对购买的资产作出任何明示或默示的担保,包括不对用途的适用性作出担保,或对任何许可产品将成功开发或商业化作出任何担保。第5.19节禁止经纪。卖方并未与任何人士订立任何协议、安排或谅解,以致有义务支付与本协议所拟进行的交易有关的任何寻找人费用、经纪佣金或类似款项。免责声明DocuSign信封ID:556FC81F-BAFA-4B3A-BC64-1F8758E4C0D1

执行文案-9-第5.20节-在法律允许的最大范围内,卖方不作出任何其他类型的担保,包括关于(I)许可技术的适销性或适用性、(Ii)不侵犯第三方知识产权、(Iii)任何许可产品成功开发和商业化的可能性、(Iv)C4x专利中的任何专利申请是否将被授予、或(V)任何C4x专利是否将被成功强制执行的明示或默示保证。第六条买方的陈述和担保买方向卖方陈述并保证,本第六条所载的陈述在本条款之日是真实和正确的。第6.1节组织;良好声誉。买方是一家根据其成立的管辖权法律正式成立、有效存在和信誉良好的公司。买方拥有一切必要的权力和权力,可以按照目前的情况继续经营业务。买方具有作为外国公司开展业务的正式资格,并且在其所进行的业务的性质需要这种资格的每个司法管辖区内都具有良好的信誉,但如果不具备这种资格或不具备良好的信誉不会阻止或实质性地推迟本协议所述交易的完成。第6.2节授权;执行和交付。买方有必要的权力和授权订立本协议并完成本协议所设想的交易。买方签署和交付本协议以及完成本协议所预期的交易均已得到适当和有效的授权。本协议已由买方正式签署和交付,假设卖方适当授权、签署和交付本协议,本协议构成买方的法律、有效和具有约束力的义务,可根据其条款对买方强制执行,但须遵守适用的破产、破产、重组、暂停、欺诈性转让和其他不时生效的影响债权人权利的类似法律以及衡平法的一般原则,无论是在衡平法诉讼中考虑还是在法律上考虑。第6.3节禁止违规;反对。本协议的执行和交付不会违反适用于买方的任何适用法律,也不会导致(I)违反或违约(Ii)终止或取消或加速履行买方所要求的履行义务,或(Iii)在买方作为当事一方或以其他方式约束买方的任何重大合同上设立或施加任何担保权益、留置权或任何其他产权负担,除非此类违反或冲突不会对买方履行本协议项下的义务造成实质性干扰;(B)要求向任何人提供任何批准、授权、同意、许可、豁免、备案或登记,但已取得或作出的批准、授权、同意、许可、豁免、备案或登记除外,或如果未取得或作出该等批准、授权、同意、许可、许可、豁免、备案或登记,将不会对买方履行本合同项下的义务造成实质性干扰;或(C)与《宪章》或买方章程或类似组织文件的任何规定相抵触或违反。第6.4节禁止经纪。买方未与任何人达成任何协议、安排或谅解,导致买方有义务支付与本协议所述交易相关的任何寻找人费用、经纪佣金或类似付款。DocuSign信封ID:556FC81F-BAFA-4B3A-BC64-1F8758E4C0D1

执行副本--第十条--第七条契约和协定第7.1节记录。买卖双方均应自成交之日起至少五(5)年内保存所有记录的副本,并在卖方或其关联方或买方或其关联方出于税务、诉讼、法律、监管或其他合规目的,在合理要求和合理通知的情况下,提供此类记录的检查和复制(符合买方的合理规则和法规以及任何适用法律S的规定)。第7.2节向专利局发出通知。交易结束后,买方和卖方应立即共同努力,向所有适用的专利机构提交与转让许可技术(包括C4X专利)有关的所有申请并发出所有通知。7.3节竞业禁止。除非获得买方书面许可,且除以下规定外,卖方或其附属公司不得自行或通过任何第三方开发或商业化针对食欲素-1受体拮抗剂的化合物、分子和/或产品,自生效之日起十(10)年内。如果卖方收购或被第三方收购,而第三方在收购时已在其产品组合或开发项目中拥有食欲素-1受体拮抗剂,卖方应提前向买方发出关于此类收购的书面通知,除非买方在两(2)个工作日内对交易程序提出合理异议,否则交易可以继续进行,不适用前一句中规定的限制。此外,各方承认并同意,本协议中的任何规定均不限制卖方在关闭后的业务执行中使用匿名的Conformetrix数据或从许可化合物获取的通用形状信息的能力,但本节7.3节前面的句子所规定的情况除外。如果买方仅为开发许可化合物或许可技术而需要与C4x专有技术有关的任何Conformetrix数据,且在任何情况下都不能用于发现目的,则买方可请求仅将此类Conformetrix数据用于开发目的的许可,卖方不得无理拒绝此类Conformetrix数据,但应理解此类Conformetrix数据是匿名的。第7.4节挑战。卖方永久且不可撤销地承诺不对买方或买方的任何关联公司主张任何许可技术,或在任何法院或美国专利局诉讼程序(如知识产权或PGR)中挑战许可技术的有效性。第7.5节免除责任。除本协议所述外,双方特此同意终止许可协议,双方均不承担任何义务或义务。第7.6节进一步保证。在交易结束时及之后,买卖双方应不时签立和交付或安排签立和交付其他转让和转让文书,并采取另一方可能合理要求的其他行动,以便将所购资产的合法和实益所有权完全授予买方。第八条[故意遗漏]第九条结算交货DocuSign信封ID:556FC81F-BAFA-4B3A-BC64-1F8758E4C0D1

执行副本-11--第9.1节卖方的交割结束。闭幕式将于2023年8月4日星期五英国夏令时17点01分举行。自成交之日起生效(或在成交后三(3)个月内生效),卖方应已签署并向买方交付下列各项,连同买方可能合理要求的任何附加物品,以实现本协议中预期的交易:(A)卖方拥有的C4x专利记录,以及一封致卖方专利代理人的信函,授权他们接受买方关于C4x专利的指令,其实质形式为附件D(“委托书”);(B)买方尚未拥有的任何记录;(C)储存在MIB和BioAscent的C4X3256和食欲素-1化合物的临床前毒性研究的样本(但所有相关的运输费用应由买方承担);(D)一份实质上与本协议附件附件E所示形式相同的卖据、转让和假设协议(“卖单”)和一份实质上与本协议附件附件B相同的专利转让协议(“专利转让协议”),以及买方为完成本协议所述交易而合理要求的、在截止日期由卖方正式签立的销售、转让、转让和转让文书;(E)经卖方秘书认证的卖方董事会决议副本一份,该决议授权卖方进行本协议的交易,以及卖方签署、交付和履行本协议及本协议中预期的其他文件;(F)本协议中预期的任何其他文件或协议。第9.2节买方的结算交货。自成交之日起生效,买方应已向卖方交付下列各项,连同卖方可能合理要求的任何附加物品,以实现本协议中预期的交易:(A)确认已全额支付购买价款;(B)由买方正式签署的卖单和专利转让;(C)本协议中预期的任何其他文件或协议。第十条卖方责任的赔偿与限制第10.1款卖方赔偿。除下列第10.2款规定外,卖方同意赔偿买方及其关联公司及其各自的高级管理人员、董事、雇员、继任者和受让人一段时间[***]自生效之日起,第三方因下列原因或与之相关的任何索赔或行动而遭受损失,并同意不对其造成损害:(I)卖方违反本协议中包含的任何陈述或保证;(Ii)卖方违反本协议中包含的任何契诺或协议,无论是要求在成交之时或之后履行;或(Iii)保留的责任。DocuSign信封ID:556FC81F-BAFA-4B3A-BC64-1F8758E4C0D1

执行文案-12-第10.2节第10.1节下的赔偿对于因违反第5.4节下的保证或卖方在任何C4x专利中错误的库存陈述而导致的第三方索赔或诉讼而产生的损失,应适用七(7)年的期限。第10.3节买方赔偿。买方同意赔偿卖方及其关联公司及其各自的高级管理人员、董事、雇员、继任者和受让人,并同意使他们免受因以下原因引起的任何损失:(I)买方违反其在本协议中的任何陈述或担保;(Ii)买方违反本协议中包含的任何契诺或协议;(Iii)任何已承担的债务;或(Iv)在成交日期后所购资产的所有权、运营或使用。第10.4节限制。卖方不应对索赔负责,除非卖方收到买方的书面索赔通知(合理详细说明引起索赔的事项、索赔的性质和索赔金额),该通知是在下列日期或之前按照第11.3条送达的:(I)在与5.4节下的违反保修有关的任何索赔结束后七(7)年;或(Ii)在所有其他索赔结束后三十六(36)个月。对卖方提出的任何索赔(以前未得到满足、和解或撤回)应被视为已被撤回,并在按照上一句话向卖方发出索赔通知之日起十二(12)个月内完全被禁止和不可执行(如果是基于或有负债的索赔,自或有负债成为实际负债之日起十二(12)个月期满时),除非有关索赔的法律程序已适当发出并已有效送达卖方(如适用)。对于买方在成交时实际知悉(在根据许可协议开发许可技术的过程中在许可协议日期之后获得的)任何事实、事项、事件或情况的任何索赔,卖方不承担任何责任,并且买方知道该事实、事项、事件或情况将使其有权提出索赔。对于因任何适用法律或任何当局的任何行政做法的通过或生效,或任何当局的任何行政做法在成交时并非实际或预期有效的任何此等情况下通过或生效,或在成交后发生任何变化而引起或增加的任何索赔,卖方概不负责。卖方的最高总负债在任何情况下都不得超过买入价。本协议中的任何规定均不解除买方或买方集团任何成员根据适用法律所承担的责任,即减轻因引起索赔的任何事项或情况而产生的任何损失或损害。卖方不对因引起索赔的任何事项或情况而造成的任何业务或利润损失(不论是否间接或后果性损失)、任何间接或后果性损失或任何惩罚性或加重损害赔偿承担任何责任。对于因违反本协议或以上第9.2节所列并在成交时签署和交付的任何索赔、责任、诉讼、成本、损害或开支,在成交日期后买卖双方的法律和衡平法上,本条款的规定应是唯一的和排他性的补救措施;前提是,本条款X中的任何规定不得以任何方式限制或排除双方获得特定履行或其他衡平法补救的机会。第10.5款双方应合理地相互合作,对本条规定的赔偿所涵盖的任何诉讼、索赔或责任进行调查和辩护。X.DocuSign信封ID:556FC81F-BAFA-4B3A-BC64-1F8758E4C0D1

执行文案-第13条xi总则第11.1款费用。除本协议另有规定外,与本协议及拟进行的交易有关的所有成本和支出(包括律师、财务顾问和会计师的费用和支出)将由产生此类成本和支出的一方支付。第11.2节条款的机密性。买方应对本协议的条款和存在以及本协议各方及其关联方的身份保密,现在或今后不会向任何第三方泄露任何此类信息,除非(A)经卖方;(B)事先书面同意,法律或法律程序可能另有要求,包括但不限于,在诉讼过程中以法律和财务顾问的身份就此类事项向买方提供建议的法律和财务顾问,只要此类条款和条件的披露受到与其他诉讼各方;的机密信息相同的限制,;(D)保密给其法律顾问,会计师、保险人及其顾问仅在履行其在本协议项下的义务;(E)为完善买方在许可技术中的权益而向任何政府机构(包括但不限于在任何专利局记录证据B的已签立转让);(F)将卖方转让给买方的资产告知买方的现有被许可人或潜在被许可人,但仅限于为此目的所需的最低程度的披露;或(G)强制执行买方的权利、所有权、(I)在上述(B)和(C)项中,(I)在法律允许的范围内,买方将使用所有可用的合法和合法手段,将向第三方披露的信息降至最低,包括但不限于,只要适当或可用的时候,寻求保密的处理请求或保护令,以及(Ii)买方应至少提前十(10)个日历天向另一方提供关于该披露的书面通知。卖方可自行决定向任何第三方披露本协议的条款和存在,以及本协议各方及其附属公司的身份。尽管有上述披露限制,接受方仍可披露任何法律、规则、法规、命令、决定、法令、传票或其他需要披露的法律程序所要求披露方的保密信息,包括但不限于美国证券交易委员会(“美国证券交易委员会”)或其他公开披露要求。如果买方根据本条款威胁或以其他方式发生任何违约或违约,双方承认并同意,仅靠损害赔偿不足以补偿任何此类违约或违约,且此类违约或违约将造成不可弥补的损害。因此,在买方发生任何此类违约或违约,或买方威胁此类违约或违约的情况下,卖方将有权获得临时或永久禁令救济、具体履行以及在特定情况下适当的其他衡平法救济,以限制或禁止此类违约或违约。这些补救办法不是对违反本节所载保密义务条款的唯一补救办法,而是对当事人在法律上或衡平法上可获得的所有其他补救办法的补充。第11.3条通知。本合同项下的所有通知、请求和其他通信应以英语书面形式,并应发送、交付或邮寄,地址如下:如果发送给买方,请发送至:公司秘书文件信封ID:556FC81F-BAFA-4B3A-BC64-1F8758E4C0D1

执行副本-14-Indior UK Limited The Chapleo Building Henry Boot Way,Priory Park Hull UK HU4 7DY副本请注意:Indior Inc.欧洲、中东和非洲地区副总法律顾问,Indior UK Limited另一份副本发送至:Indior Inc.10710 Midlothian Turnpike Suite 430 Richmond,VA 23235注意:首席法务官如果给卖方,请发送至:C4x Discovery Limited曼彻斯特One 53波特兰街曼彻斯特M1 3LD Attn:Emma Blaney(COO)每个此类通知、请求或其他通信应通过:(A)亲手递送;或(C)国际公认的快递服务。每一此类通知、请求或通信在第11.3节规定的地址(或按照接收方最近未撤销的指示)送达时应有效。第11.4节标题。本协议中包含的目录和标题仅供参考,不以任何方式影响本协议的含义或解释。第11.5节可分割性。如果本协议的任何条款或其他条款无效、非法或不能根据任何适用的法律或公共政策执行,本协议的所有其他条款和条款仍应保持完全有效,只要本协议预期的交易的经济或法律实质不受任何对任何一方不利的任何方式的影响。在确定任何条款或其他条款无效、非法或无法执行后,本协议各方应真诚协商修改本协议,以尽可能接近本协议双方的初衷,以使本协议所设想的交易按最初设想的最大可能完成。第11.6条对应条款。本协议可通过DocuSign或其他电子方式以及一份或多份副本签署,所有这些副本均应被视为同一份协议,并在本协议各方签署并交付给另一方时生效,但应理解,本协议各方无需签署相同的副本。DocuSign信封ID:556FC81F-BAFA-4B3A-BC64-1F8758E4C0D1

执行副本-15-第11.7节整个协议;证物和其他文件。本协议(连同本协议所附附件)构成整个协议,并取代双方先前就本协议标的达成的所有书面和口头协议和谅解。本协议中特别提及并依据本协议交付的展品和通知是本协议不可分割的一部分。第11.8节第三方受益人。除本协议特别规定外,本协议的目的完全是为了本协议的每一方及其各自的继承人或允许的受让人的利益,不打算授予本协议双方以外的任何人本协议项下的任何权利或补救措施。第11.9节适用法律。本协议应由英格兰和威尔士的法律解释、执行和管辖,而不影响其法律冲突的原则。第11.10条修订及豁免。除非以本协议各方的名义签署书面文件,否则不得对本协议进行修改。有权享受本协议任何条款或条件的一方可随时放弃本协议的任何条款或条件,但除非放弃该条款或条件的一方或其代表正式签署书面文书,否则该放弃无效。任何一方在任何一个或多个情况下放弃本协议的任何条款或条件,不得被视为或解释为在任何未来情况下放弃本协议的相同或任何其他条款或条件。11.11节公示。作为附件C所附的新闻稿可由双方在结案后发布。除上一句所述外,未经本协议其他各方事先书面同意,任何一方均不得就本协议或本协议任何条款和条件所拟进行的交易作出任何公告,或以其他方式公开披露与本协议或本协议任何条款和条件有关的任何信息,而同意不会被无理拒绝、附加条件或延迟。尽管有上述规定,任何一方均可就拟进行的交易作出任何公开披露,而该方的律师认为适用法律或任何证券交易所的规则可能会要求该一方或其联属公司进行证券交易;但条件是,作出披露的一方应在公开发布前合理地并在可行的范围内向未披露的一方提供拟披露的副本,而双方应就披露的形式和内容相互协调。第11.12节转让。未经另一方事先书面同意,任何一方均不得转让其在本协议项下的权利或义务;但只要任何此类继承人或受让人以书面形式同意受本协议约束,买方可在未经卖方事先书面同意的情况下,将其在本协议项下的权利和义务因合并、出售其全部或基本上所有资产或股票或任何类似交易而转让给转让方的关联公司或继承人;但条件是,在转让之前,转让方应向非转让方提供关于此类转让的书面通知。任何许可受让人应承担其转让人在本协议项下的所有义务(尽管在转让许可产品的情况下,此类义务仅限于本协议项下与许可产品有关的义务)。任何转让均不解除任何一方履行任何义务的责任。除前述规定外,本协议对本协议双方及其各自的继承人和允许受让人具有约束力,并符合其利益。[签名页面如下]DocuSign信封ID:556FC81F-BAFA-4B3A-BC64-1F8758E4C0D1

签署副本-16-自本协议之日起,双方已由各自正式授权的代表签署本协议,特此为证。个人英国有限公司:__姓名:Bhavna Hunjan职务:首席商务官DocuSign信封ID:556FC81F-BAFA-4B3A-BC64-1F8758E4C0D1/S/阿比盖尔·谢泼德/S/Bhavna Hunjan
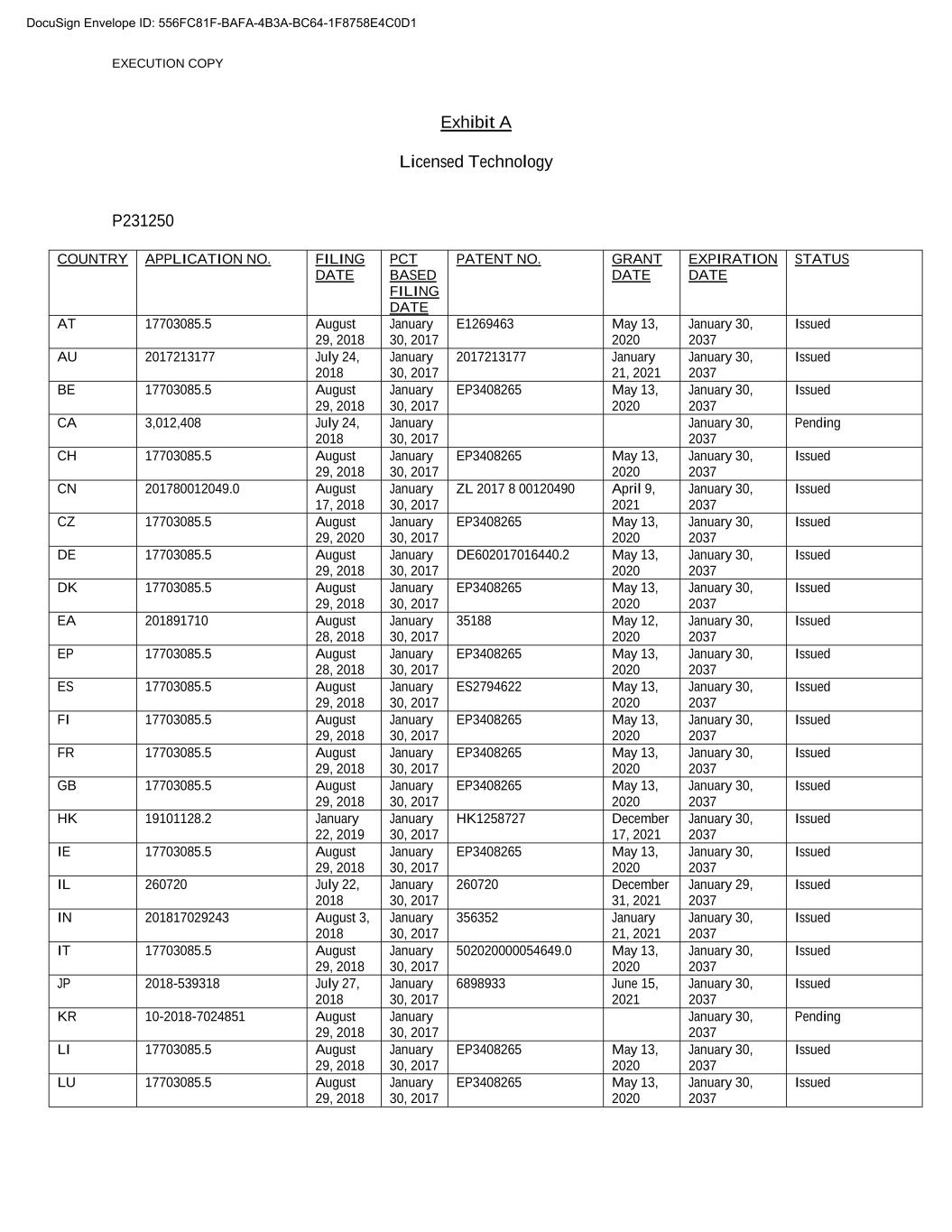
签约复印件A授权技术P231250国家申请号申请日基于PCT的申请日专利号授予日期到期日状态2018年08月29日2018年1月30日发布AU 2017213177 2018年07月24日2018年1月30日发布2017213177 2031年1月30日发布BE 17703085.5 2018年8月29日2018年1月30日发布EP3408265 2037年5月13日发布CA 3,012,408 2037发布CA 3,012,408 2037待批CH 17703085.5 2018年8月29日2018年1月30日2017EP3408265 2037年5月13日发布CN 201780012049.0 2018年1月30日2017年ZL 2017年8 00120490 2037年04月9日2021年1月30日发布CZ 17703085.5 2037年08月29日EP3408265 2037年1月30日发布DE 17703085.5 2018年08月29日2018年1月30日DE602017016440.2 2037年5月13日发布DK 17703085.5 2018年01月30日EP3408265 2037年01月30日发布EA 2018891710 2018年01月30日35188 05.12 2037年1月30日发布EP 1740703085.5 2018年01月30日2037年01月30日发布ES 17703085.5 2018年08月29日2018年1月30日发布ES 17703085.5 2037年08月29日2018年1月30日发布FI 17703085.5 2037年1月30日发布FR 17703085.5 2018年1月30日EP3408265 2037年5月13日发布GB 17703085.5 2018年1月30日EP3408265 2037年5月13日2037年发布香港19101128.2 2037年1月30日香港12587272037年发布IE 2018年8月29日2018年1月30日EP3408265 2037年5月13日2018年1月30日发布IL 260720 2018年1月30日260720 2018年12月31日2021年1月29日发布时间201817029243 2018年8月3日356352 2031年1月30日发布IT 17703085.5 2018年8月29日2018年1月30日发布JP 2018年-539318 2037年7月27日6898933 2037年6月15日6898933 2037年发布KR 10-2018年1月30日-7024851 8月29日2018年01月30日待发Li 17703085.5 2018年08月29日2037年01月30日发布Lu 2018年08月29日2018年01月30日发布Lu 2037年05月30日发布文件签名信封ID:556FC81F-BAFA-4B3A-BC64-1F8758E4C0D1
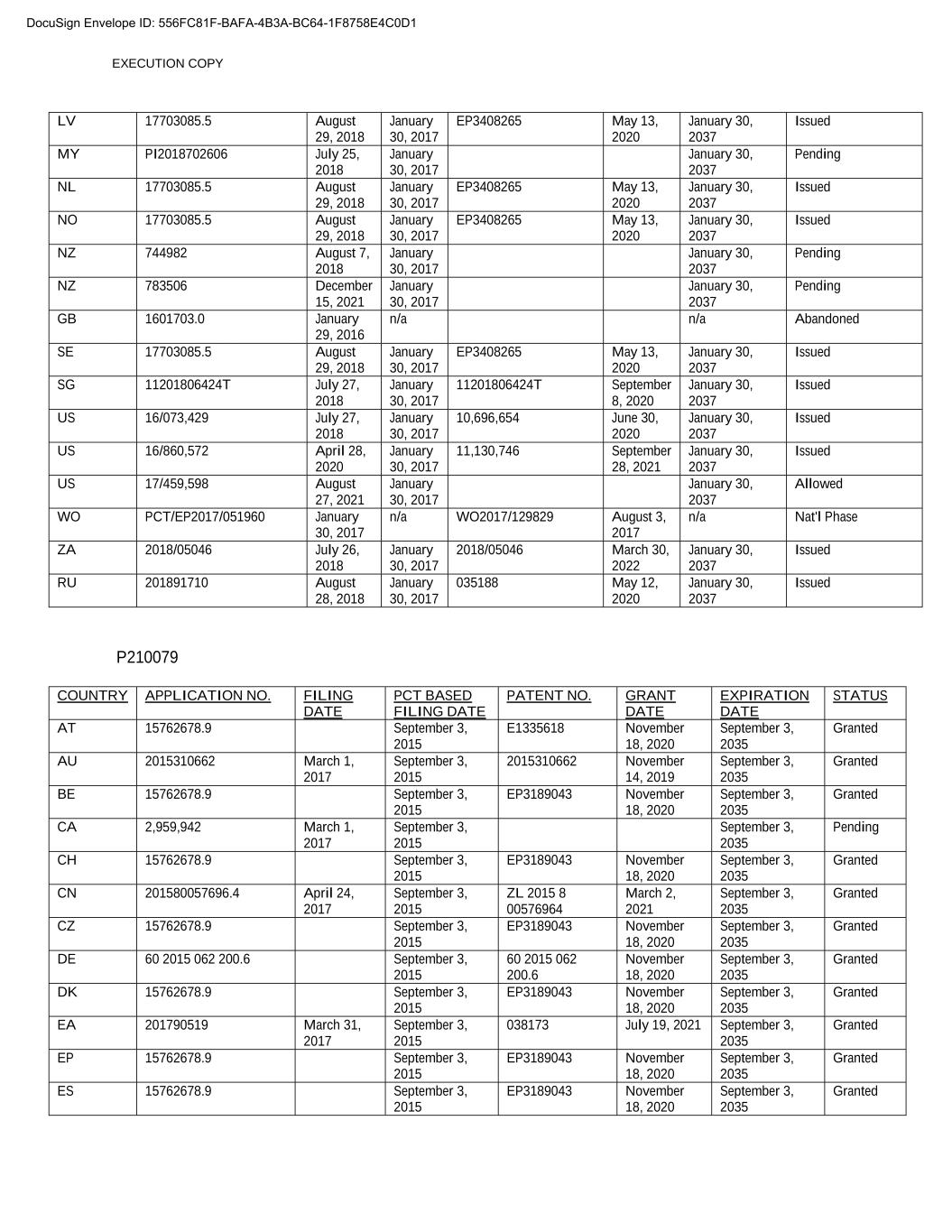
执行副本LV 17703085.5 2018年8月29日2018年1月30日EP3408265 2037年5月13日2020年1月30日发布我的PI2018702606 2037年7月25日2018年1月30日待批NL 17703085.5 2018年1月30日EP3408265 2037年5月13日2018年1月30日EP3408265 2037年5月13日发布编号17703085.5 2018.29 2018年1月30日EP3408265 2037年5月13日发布2037年8月7日2018年1月30日2017年1月30日待批新西兰783506 2017年1月30日2037年待批GB 1601703.0 2016.01.29不适用不适用废弃SE 17703085.5 2018.29 2018.29 2020年1月30日EP3408265 2037年5月13日发布SG 11201806424T 2018年1月30日11201806424T 2037年1月30日发布美国16/073,429 2037年1月30日10,696,654 2037年1月30日发布美国16/860,572 2020年1月30日2017.11,130,746 2021年9月30日发布美国17/459,5462037年允许使用WO PCT/EP2017/051960 2017n/a WO2017/129829 2017n/a NAT‘L阶段ZA 2018年/05046 2018年7月26日发布2018年1月30日/05046 2037年3月30日发布RU 201891710 2018年08月28日035188 2037年5月12日2037年1月30日发布P210079国家申请编号申请日基于PCT的申请日专利号授予日期到期日状态2015.9.03 2015.E1335618 2015.9.03授予AU 2015310662 2017.9.01 2015.9.03 2015310662 2019 9.3授予BE BE 2015.9.03 2015.EP3189043 2015.9.18 2015.9.03授予CA 2,959,942 2015.9.03待批准的CH 15762678.9 2015.9.03 EP3189043 2015.9.18 2015.9.03授予CN 201580057696.4 2017.9.3 8 00576964 3.032035年9月3日授予深圳15762678.9 2035年9月3日授予DE 60 2015 062 200.6 2035年9月3日授予DE 60 2015 062 200.6 2015.11月18日2020年9月3日授予EA 201790519 2035年3月31日授予EP 15762678.9 2021年9月3日授予EP 15762678.92015 EP3189043 2020年11月18日2035年9月3日授予DocuSign信封ID:556FC81F-BAFA-4B3A-BC64-1F8758E4C0D1
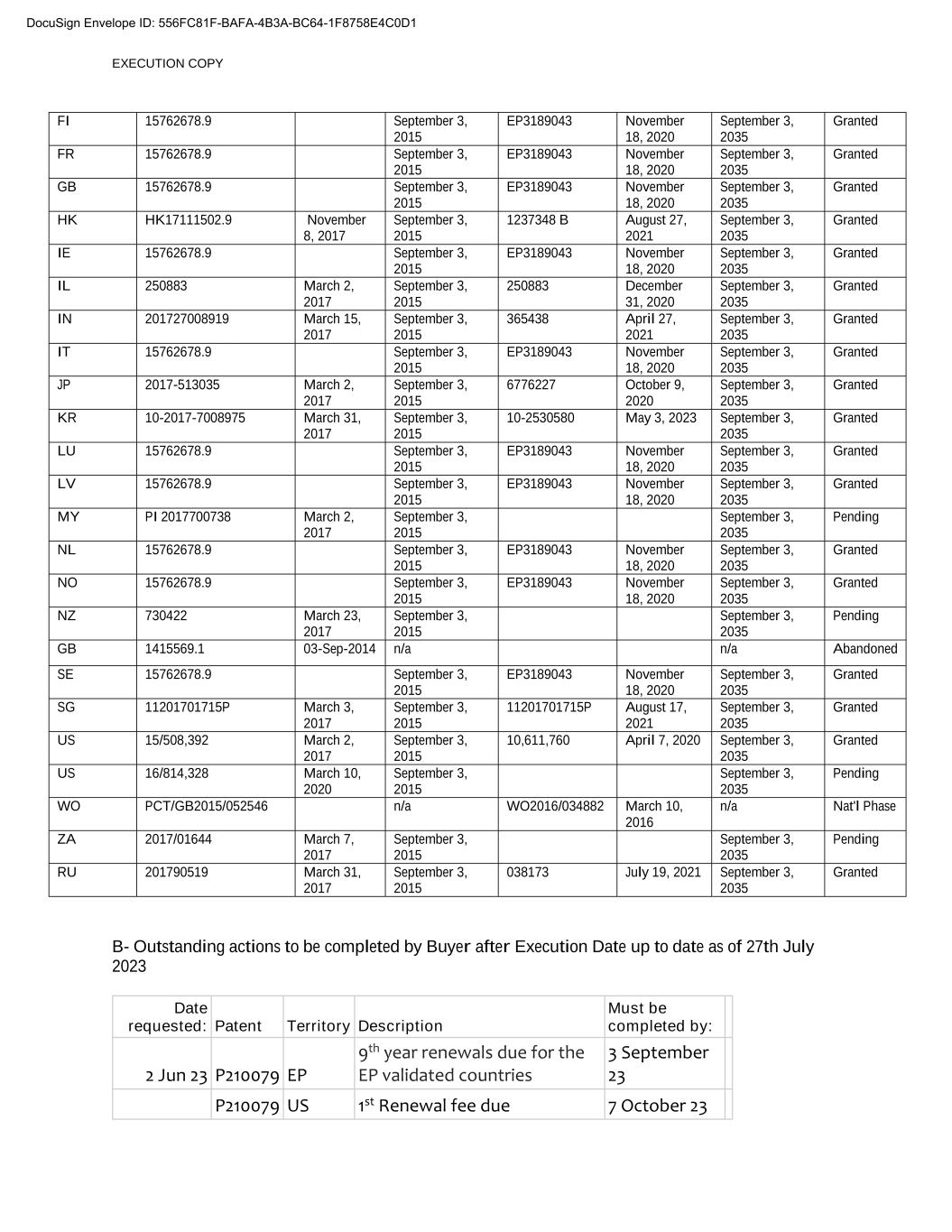
执行副本FI 15762678.9 2015.9.03授予FR 15762678.9 2015.9.03授予EP3189043 2015.9.03授予GB 15762678.9 2015.9.03 2015.EP3189043授予HK17111502.9 2015.9.03授予IE 2015.8.27 20219.03授予IE 15762678.9 2015.9.03授予IL 250883 2015.9.032015.03.15-513035 2015.9.03授予Lu 15762678.9 2015.9.03-513035 2015.9.03授予Lu 2035年9月3日-2035年9月3日授予Lu 2035年9月3日-2035年9月3日授予Lu 2035年9月3日-2031年9月3日授予IT 2015.09.03-2015.EP3189043 2035年11月18日授予JP 2017.03.02-2015.09.03授予LV 2035.032015.EP3189043 2035年11月18日授予我的PI 2017700738 2035年3月2日待批2015.9.03待批NL 15762678.9 2035.9.3批准否15762678.9 2015.9.3批准EP3189043 2030年9月3日批准不批准15762678.9 2039.03批准新西兰730422 2033.03待批GB 1415569.1 2015.9.03不适用于废弃SE 15762678.9 2035年9月3日批准2015.9.03 11201701715P 2035年8月17日2015.9.03 392 2017.09.3 2015.9.3 10,611,760 2035年4月7日2035年9月3日美国16/814,328 2020年9月3日未完成的WO PCT/GB2015/052546 n/a WO2016/034882 2016.NAT‘l阶段ZA 2017年3月7日2015.9.3未完成的RU 201790519 2015.9.31 2015.0381732035授予B-截至2023年7月27日的执行日期后由买方完成的未完成操作请求日期:专利区域描述必须在以下日期之前完成:2月23日P210079 EP有效国家/地区的9年续订3月23日P210079美国首次续期费10月7日到期DocuSign信封ID:556FC81F-BAFA-4B3A-BC64-1F8758E4C0D1
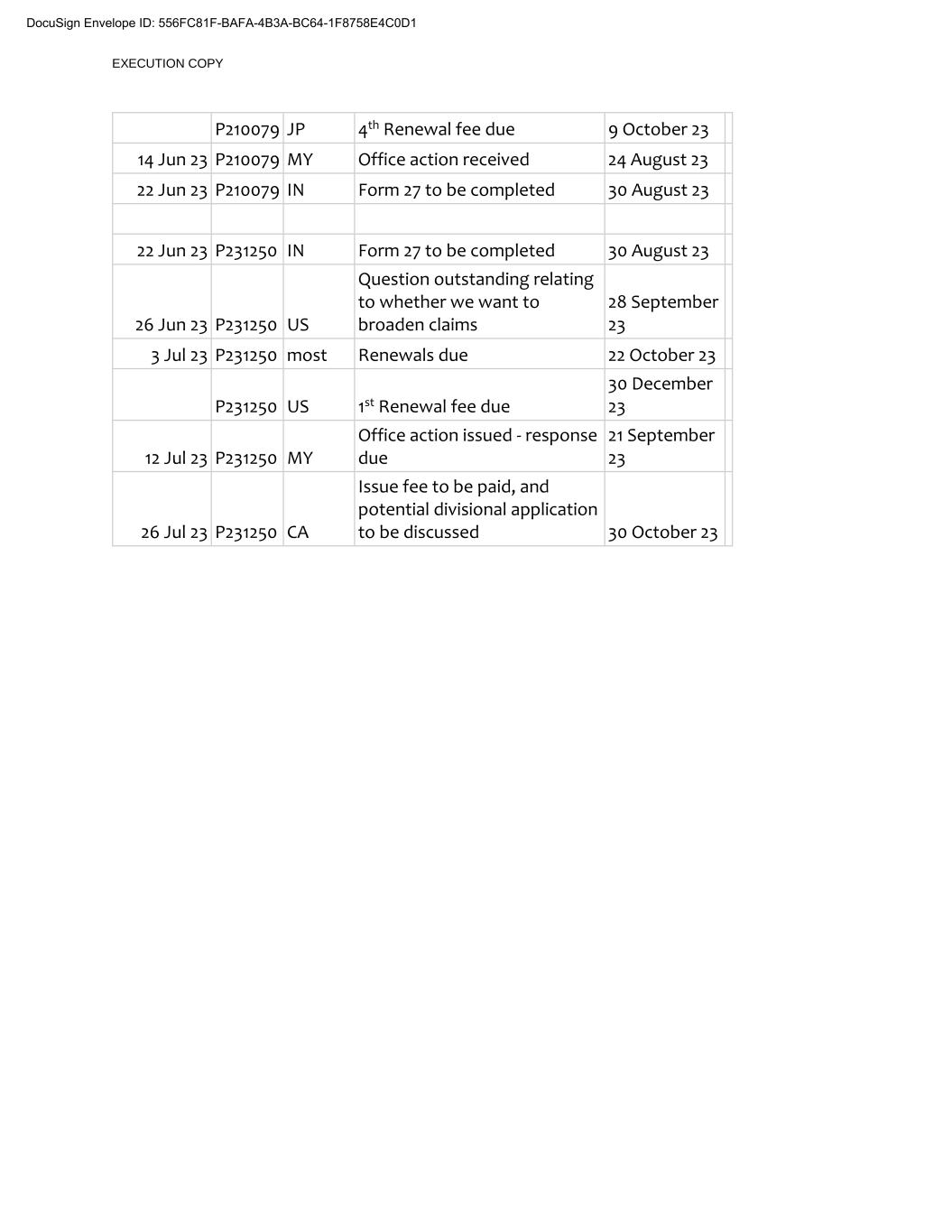
执行副本P210079 JP第4次续约费10月9日到期10月23日14月23日23日P210079我的办公室行动收到24 8月23 22月23日23 P210079表格27中的P210079待填写30 8月23日23月23日P231250表格27中待填写的30月23日26月23日23日P231250美国问题悬而未决有关我们是否希望扩大索赔范围的问题9月23日3月23日P231250大部分10月22日到期的续约费P231250美国第一次续约费12月23日12月23日P231250我的办公室行动已发出回复,9月23日26日23月23日P231250 CA问题费用将支付,和潜在的分区应用将于10月30日讨论DocuSign信封ID:556FC81F-BAFA-4B3A-BC64-1F8758E4C0D1

NY:1242891-3专利权转让附件B本专利权转让(“转让”)日期为2023年8月4日(“生效日期”),是根据生效日期为2023年7月31日的资产购买协议(以下简称“协议”)的条款和条件,由InDior UK Limited(Co.)和C4x Discovery Limited(Co.)之间进行的,Indior UK Limited(Co.)是一家在英格兰和威尔士注册成立的公司,公司编号为7183451,其注册地址为伯克郡斯劳夫市巴斯路103-105号,SL1 3UH(“受让人”)为买方,C4x Discovery Limited,一家在英格兰和威尔士注册成立的公司,公司编号为06324250,其注册地址为曼彻斯特M13LD波特兰街53号曼彻斯特一号(“转让人”)。“专利”是指本协议所附专利附件中确定的专利。因此,现在致所有IT相关人士:出于良好和有价值的对价,转让人同意并确实在此不可撤销地向上述受让人出售、转让、转让和转让,并且受让人在此接受转让人对专利和对专利的所有权利、所有权和利益,这些权利、所有权和权益将由上述受让人持有和享有,供其自己使用,并供其继承人、受让人、或其他法律代表,在期限结束时,所述专利可被授予与出让人持有和享有的专利完全和完全相同,(I I)在;和(Ii)诉讼原因和专利的执法权,包括就过去和将来的专利侵权行为寻求损害赔偿、禁令救济和其他补救措施的所有权利。尽管本协议有任何相反规定,转让人仍按照本协议的所有条款和规定执行和交付本转让。如果本转让的条款与本协议的条款有任何冲突,本协议的条款以本协议的条款为准。这项转让对双方及其各自的继承人和受让人具有约束力,并符合其利益。本转让应受英格兰和威尔士法律管辖,并按照英格兰和威尔士法律解释,但不影响其法律冲突规则。自本协议签订之日起,双方经各自正式授权的代表签署本协议,特此为证。受让人:_

2作者:_名称:标题:DocuSign信封ID:556FC81F-BAFA-4B3A-BC64-1F8758E4C0D1
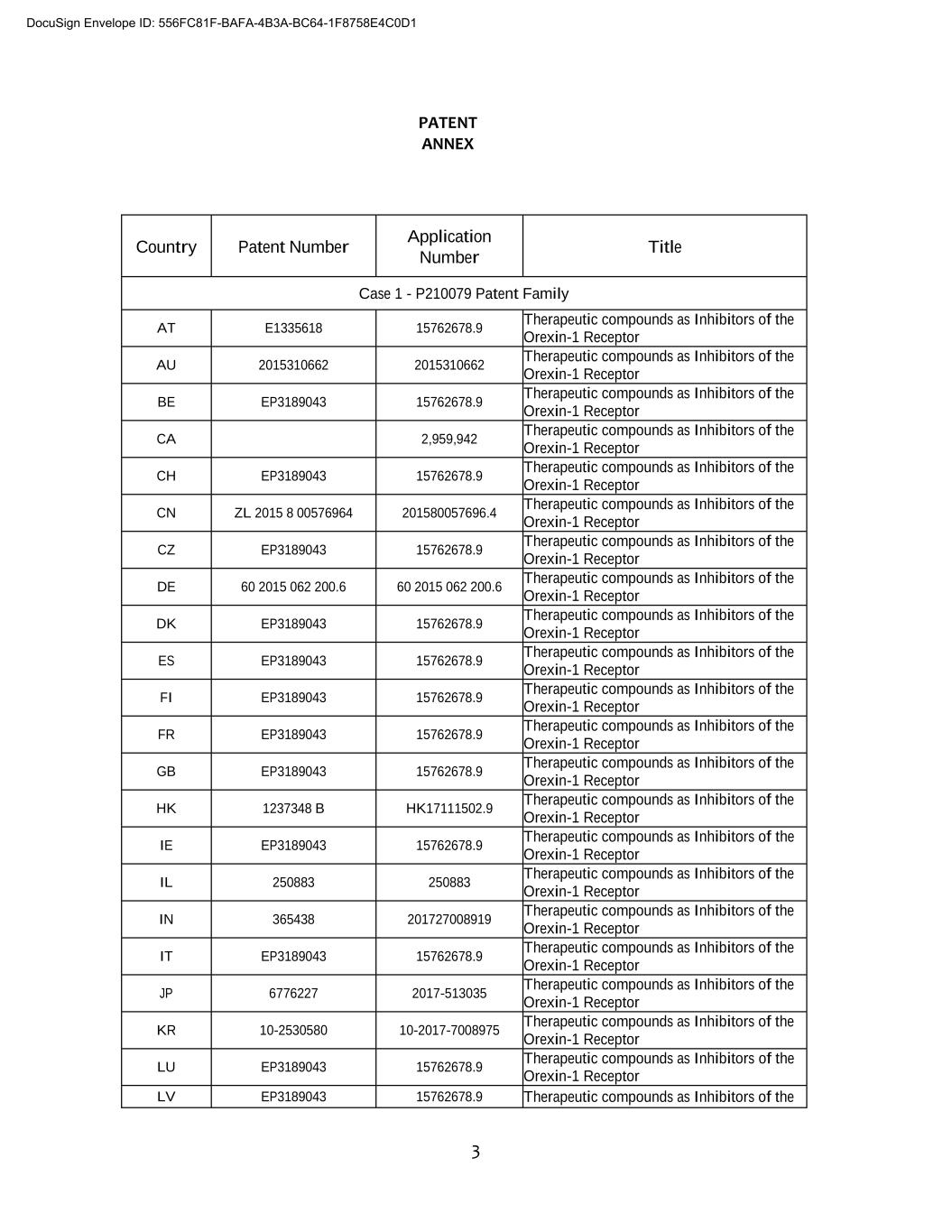
3专利附件国家专利申请号标题案例1-P210079专利家族E1335618 15762678.9作为食欲素-1受体的抑制剂的治疗性化合物AU 2015310662 2015310662作为食欲素-1受体的抑制剂的治疗性化合物BE EP3189043 15762678.9作为食欲素-1受体的抑制剂的治疗性化合物CA 2,959,942作为食欲素-1受体的抑制剂的治疗性化合物CHEP3189043 15762678.9作为食欲素-1受体的抑制剂8 00576964 201580057696.4作为食欲素-1受体的抑制剂的治疗性化合物CEP3189043 157678.9作为食欲素-1受体的抑制剂的治疗性化合物作为食欲素-1受体抑制剂的治疗性化合物DK EP3189043 15762678.9作为食欲素-1受体的抑制剂的治疗性化合物15762678.9作为食欲素-1受体的抑制剂的治疗性化合物EP3189043 15762678.9作为食欲素-1受体的抑制剂的治疗性化合物EP3189043 15762678.9作为食欲素-1受体的抑制剂的治疗性化合物GB EP3189043 15762678.9作为食欲素-1受体的抑制剂的治疗性化合物HK1237348BHK17111502.9作为食欲素-1受体的抑制剂的治疗性化合物EP3189043 15762678.9。食欲素-1受体抑制剂IL 250883 250883食欲素-1受体抑制剂治疗化合物365438 201727008919食欲素-1受体抑制剂治疗化合物EP3189043 15762678.9食欲素-1受体抑制剂治疗性化合物JP 6776227 2017-713035食欲素-1受体抑制剂治疗性化合物KR 10-2530580 10-2017-7008975治疗化合物作为食欲素-1受体抑制剂Lu EP3189043 15762678.9治疗化合物作为食欲素-1受体抑制剂LEP3189043 15762678.9治疗包膜化合物ID:556FC81F-BAFA-4B3A-BC64-1F87584E0C01
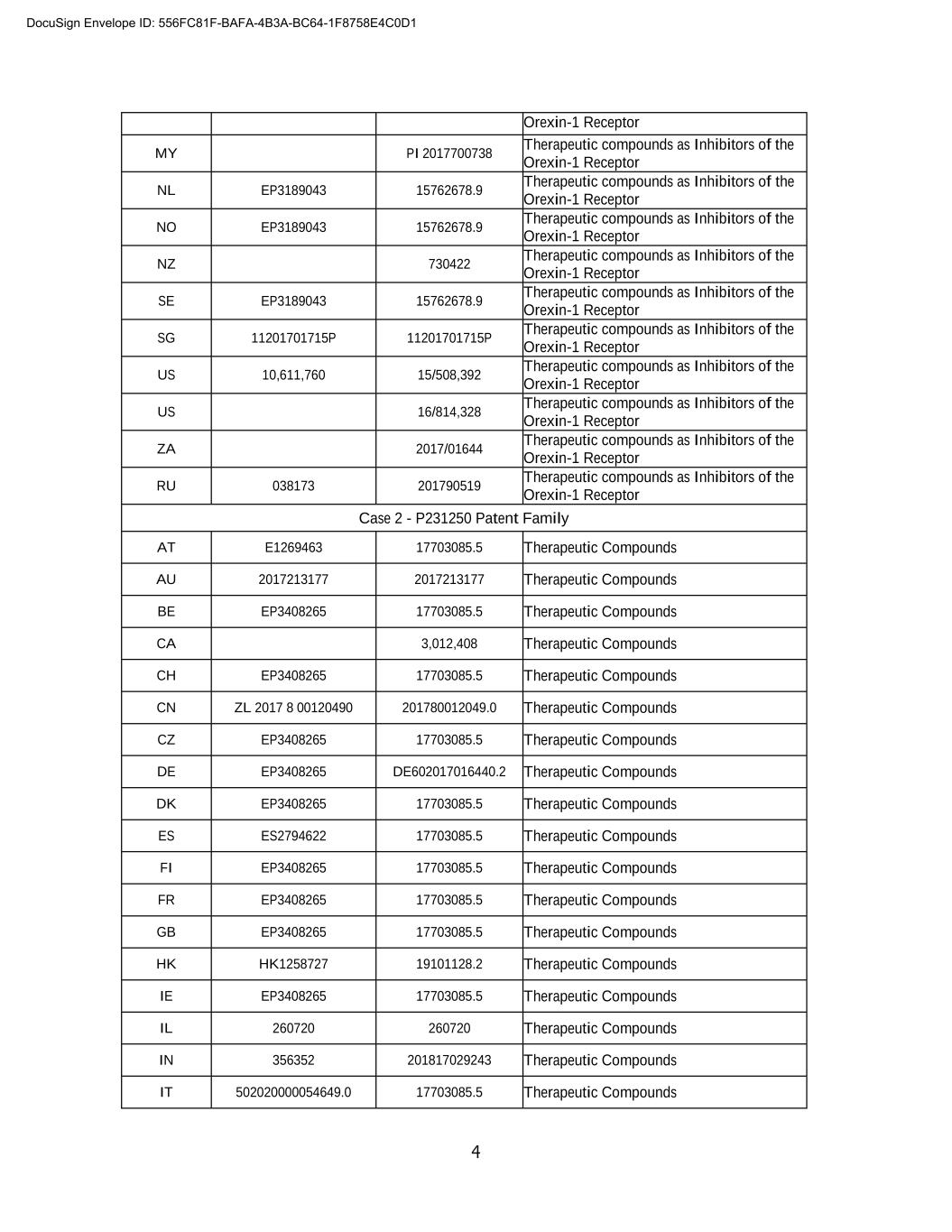
4食欲素-1受体My PI 2017700738作为食欲素-1受体的抑制剂NL EP3189043 15762678.9作为食欲素-1受体的抑制剂治疗化合物作为食欲素-1受体的抑制剂NZ730422治疗化合物作为食欲素-1受体的抑制剂SEEP3189043 15762678.9作为食欲素-1受体的抑制剂的治疗化合物SG11201701715P 11201701715P作为食欲素-1受体的抑制剂US 10,611,760 15/508,392作为食欲素-1受体的抑制剂US10,611,760 15/508,392治疗化合物作为食欲素-1受体的抑制剂01644治疗化合物作为增食欲素-1受体的抑制剂RU 038173 201790519治疗化合物作为增食欲素-1受体的抑制剂案例2-P231250专利家族AT E1269463 17703085.5治疗化合物AU 2017213177 2017213177治疗化合物BE EP3408265 17703085.5治疗化合物CA 3,012,408治疗化合物CHEP3408265 17703085.5治疗化合物CNZL2017 8 00120490 201780012049.0治疗化合物CZ EP3408265 DE607020116440.2治疗化合物DEPK 340840265 17703083085.5治疗化合物ESEP340317703085.5治疗化合物香港260720 260720 19101128.2治疗化合物IE EP3408265 17703085.5治疗化合物IL 126352 201817029243治疗化合物IT 502020000054649.0 17703085.5治疗化合物文件信封ID:556FC81F-4B3A-BC64-1F8758E4C0D1
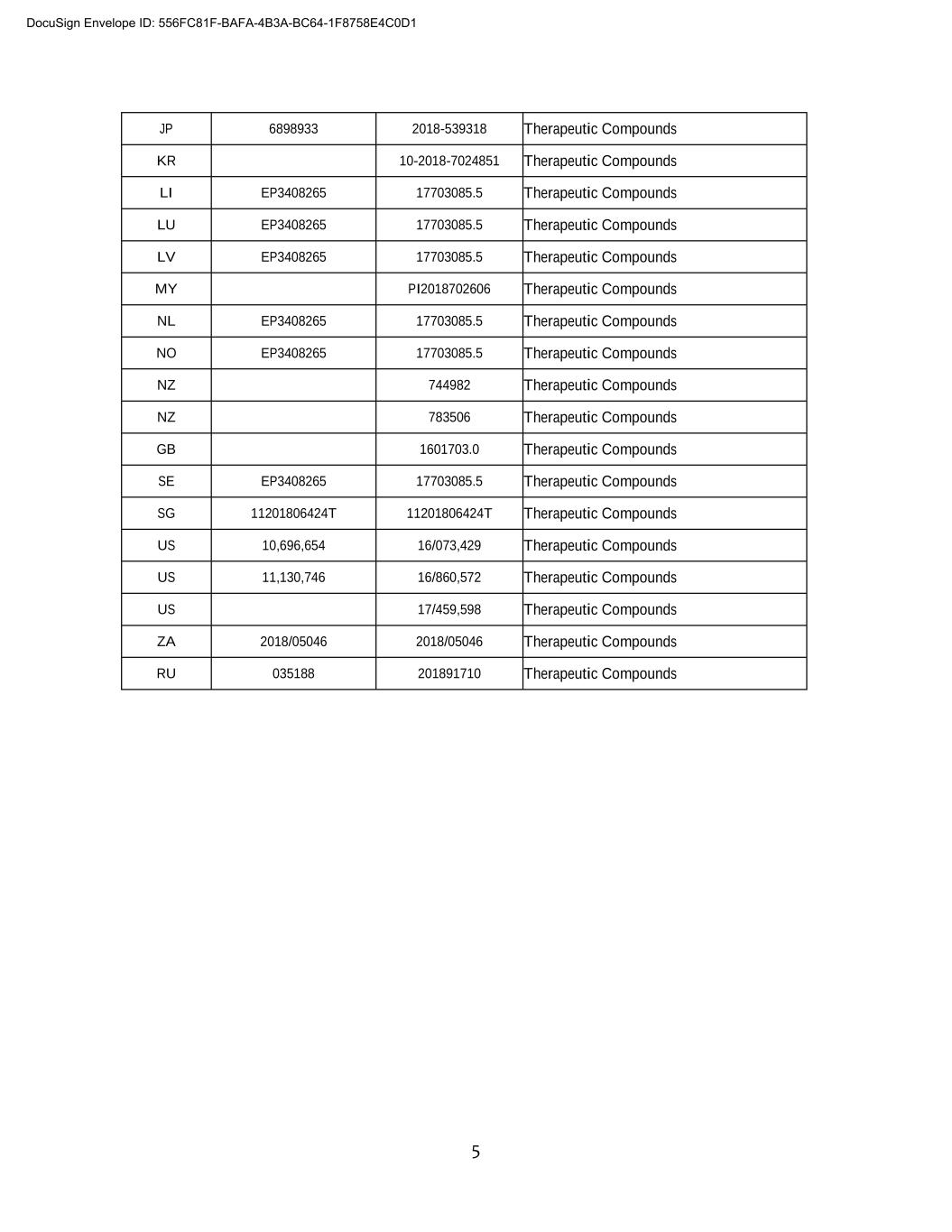
5 JP 6898933 2018年-539318治疗化合物KR 10-2018年-7024851治疗化合物Li EP3408265 17703085.5治疗化合物Lu EP3408265 17703085.5治疗化合物LV EP3408265 17703085.5治疗化合物My PI2018702606治疗化合物NL EP3408265 17703085.5治疗化合物NO EP3408265 17703085.5治疗化合物ZZ 744982治疗化合物2018年/05046治疗化合物GB 1601703.0治疗化合物SE EP3408265 17703085.5治疗化合物SG 11,696,654 16/073,429治疗化合物US 11,188,746,746,572治疗化合物US 17/459,598治疗化合物ZZ 783506治疗化合物GB 1601703.0治疗化合物SE EP3408265 17703085.5治疗化合物SG 11,696,654 16/073,429治疗化合物US 11,188,746,860,572治疗化合物US 17/459,598治疗化合物治疗性化合物DocuSign信封ID:556FC81F-BAFA-4B3A-BC64-1F8758E4C0D1

6附件C本公告包含内部信息C4x Discovery Holdings plc(“C4XD”、“C4x Discovery”或“公司”)以1595万英镑的价格将C4XD的食欲素-1受体拮抗剂计划战略性地出售给Indior公司包括所有权利并能够立即确认收入非稀释收益以加快免疫炎症投资组合的进展2023年8月1日-C4x Discovery Holdings plc(AIM:C4XD)是一家领先的药物发现公司,今天宣布签署一项资产购买协议,收购Indior PLC(LSE:INDV)(“Indior”)的资产购买协议,以获得C4XD的口服增食素-1受体拮抗剂的专有权。C4X_3256(INV-2000)适用于物质使用障碍,适用于GB 1595万。这一非稀释性战略撤资的完成是C4XD向免疫炎症治疗公司演变的一部分。正如C4XD公司2023年4月的中期业绩所示,该公司的投资组合将专注于免疫炎症性疾病的治疗,包括其领先的小分子α4β7整合素抑制剂计划,该计划旨在扩大炎症性肠病患者获得疾病修饰治疗的机会。该公司相信,通过进一步推进这些计划,它可以为股东带来更大的价值,并打算将α4β7计划推向临床,并将另外两个免疫炎症计划推向Lead优化。根据协议条款,先前于2018年3月29日宣布的许可协议将终止,InDior将承担与开发和使用C4X_3256(INV-2000)及相关化合物相关的所有权利1。2019年,InDior从美国国立卫生研究院(NIH)Hear(帮助长期结束成瘾)倡议获得了1,060万美元的赠款,用于开发C4X_3256(INV-2000),该倡议旨在改善阿片类药物滥用和成瘾的预防和治疗战略。此前,C4x Discovery有资格从InDior获得潜在的里程碑式付款,如果所有临床开发、监管和商业目标都能实现,随着时间的推移,总计可能达到2.84亿美元,以及C4x_3256净销售额的特许权使用费(INV-2000)。第一阶段多次递增剂量(MAD)研究目前正在进行中。DocuSign信封ID:556FC81F-BAFA-4B3A-BC64-1F8758E4C0D1

7 Indior PLC首席技术官克里斯蒂安·海德布雷德博士说:“收购INDV-2000的全部权利符合我们的目标,即建立一条专注于成瘾治疗的强大而平衡的渠道。重要的是,我们对这项资产非常了解,因为我们与C4x Discovery密切合作了五年多。我们认识到它令人兴奋的潜力,并将继续将其作为治疗阿片类药物使用障碍以及更广泛的物质使用障碍的一种新方法。“C4x Discovery的CBO Bhavna Hunjan补充说:“Indior在我们的oresin-1候选项目上取得了很好的进展,我们感到自豪的是,他们现在希望完全在内部进行这个项目。他们的决定突显了他们对该计划的信心,并进一步突显了我们的药物发现专业知识在生产有价值的、具有商业意义的小分子候选药物方面的力量。该协议还为我们提供了一个机会,让我们尽早明确该计划的价值,并巩固和加快我们的新战略。这笔非稀释资金,加上我们与赛诺菲和阿斯利康就C4XD免疫炎症资产达成的许可协议可能产生的临床前里程碑付款,将使我们能够进一步推动我们新专注的投资组合向临床和进入临床。随着我们的内部投资组合进展良好,并开始与我们的MALT-1计划合作,我们期待着作为一家免疫炎症治疗公司的强劲未来。“1.C4XD将不会从InDior获得任何进一步的里程碑或特许权使用费付款,用于C4X_3256(INV-2000)的开发或商业化-END-DocuSign信封ID:556FC81F-BAFA-4B3A-BC64-1F8758E4C0D1

+44(0)20 7862500鲁伯特·迪尔登(企业经纪)+44(0)20 7886 2500鲁伯特·迪尔登(企业经纪)C4x发现媒体-Consilium战略通联部玛丽-简·埃利奥特、克里斯·加德纳、马修·尼尔+44(0)203 7095700编辑请注意:关于C4x发现公司C4x发现公司(“C4XD”)是一家开创性的药物发现公司,将科学专业知识与尖端药物发现技术相结合,高效地提供世界领先的药物。通过我们增强的候选分子设计和患者分层能力,我们拥有一种非常有价值的差异化药物发现方法,在专注于免疫炎症的多个疾病领域产生小分子候选药物。我们的投资组合具有商业吸引力,从早期的目标机会到后期的药物发现计划,我们有三个商业合作计划,其中一个是临床开发的候选者。欲了解更多信息,请访问我们的网站www.c4xdiscovery.com或关注我们的Twitter@C4XDiscovery。DocuSign信封ID:556FC81F-BAFA-4B3A-BC64-1F8758E4C0D1

9本授权书由C4x Discovery Limited于2023年8月4日发出,C4x Discovery Limited是一家在英格兰和威尔士注册成立的公司,公司编号06324250,其注册办事处位于曼彻斯特一号,53 Portland Street,曼彻斯特,M1 3LD(C4x),此前其C4x专利转让给Indior UK Limited(Co.),Indior UK Limited(Co.),一家在英格兰和威尔士注册的公司,公司编号7183451,其注册地址为103105 Bath Road,Slough,Berkshire,SL1 3UH(Indior),以确认和任命HGF Limited一家在英格兰和威尔士注册成立的公司,公司编号08998652.其注册办事处为英国利兹利兹市1号City Walk,LS11 9DX,作为其受权人(代理人),按照以下规定的条款,出席、签署、存档、签立所有文件,并采取Indior为管理、维护和起诉C4x专利而要求和/或指示的行动。1.委任及授权C4X及Indior各自委任HGF Limited一间在英格兰及威尔斯成立为法团的公司,公司编号为08998652,其注册办事处为英国利兹1 City Walk,LS11 9DX,并以C4X或Indior的名义及代表委任为其受权人:a)考虑、存档、呈交、批准、签署、签立、交付及发出受权人凭其绝对酌情决定权认为合宜或为提交、检控、自2023年8月4日英国夏令时17时01分起,根据主要协议第9.1(A)条的条款,维持及管理C4x专利(定义见InDior UK Limited与C4x Discovery Limited于2023年7月31日订立的资产购买协议(“主要协议”))(专利维持及检控);以及b)采取律师根据其绝对酌情决定权认为与专利维持和起诉的实施有关的任何步骤或做任何事情。2.法人团体受权人可将本授权书授予受权人的一项或多於一项权力,转授予为该目的而委任的一名或多於一名高级人员。3.有效性C4X及Indior各自声明,真诚地与受权人交易的人可接受由该受权人签署的书面陈述,表明本授权书并未被撤销,作为该事实的确证。DocuSign信封ID:556FC81F-BAFA-4B3A-BC64-1F8758E4C0D1

10.管辖法律及司法管辖权本授权书及因本授权书、其标的物或其组成而引起或与其相关的任何争议或申索(包括非合约争议或申索),须受英格兰及威尔士法律管限及按照其解释。双方不可撤销地同意,英格兰和威尔士法院应拥有非排他性司法管辖权,以解决因本授权书或其标的或构成而引起或与之相关的任何争议或索赔(包括非合同争议或索赔)。本文件已作为契约签署,并已交付,并于其开头所述的日期生效。DocuSign信封ID:556FC81F-BAFA-4B3A-BC64-1F8758E4C0D1

11由C4x Discovery Limited在以下人面前签署为契据:………….授权签字人..................................................................[证人的签署][证人姓名][证人地址][证人的职业]在……………面前签署为Indior UK Limited的地契.获授权签署人.[证人的签署][证人姓名][证人地址][证人的职业]DocuSign信封ID:556FC81F-BAFA-4B3A-BC64-1F8758E4C0D1

本销售、转让及承担协议(本“协议”)于英国夏令时间2023年8月4日星期五(“生效日期”)17时01分由C4x Discovery Limited(于英格兰及威尔士注册成立,公司编号06324250,注册地址为曼彻斯特One,53 Portland Street,曼彻斯特,M1 3LD(“委托人”))与Indior UK Limited(于英格兰及威尔士注册成立,公司编号7183451)订立。其注册地址为巴斯路103-105,Slough,Berkshire,SL13UH(“受让人”)。W I T N E S E TH:鉴于,转让人及受让人均为日期为2023年7月31日的该等资产购买协议(“购买协议”)的订约方,据此,转让人已同意按购买协议所载条款及条件,向受让人出售转让资产(定义见购买协议)的所有权利、所有权及权益。因此,现在,出于良好和有价值的对价,在此确认已收到和充分,并根据《购买协议》的条款和条件,受让人和转让人同意如下:1.明确的条款。此处使用但未定义的大写术语应具有《购买协议》中赋予它们的含义。2.出售和转让资产。根据《购买协议》的条款和条件(自本协议生效之日起生效),转让人特此向受让人及其继承人和受让人出售、转让、交付、转让和转让,受让人在此接受并获得转让人对本协议附表A所述知识产权、知识产权的所有权利、所有权和权益。3.承担责任。根据自本协议生效之日起生效的《购买协议》的条款和条件,受让人特此承担、并应在到期时支付和履行本协议附表A所述知识产权所产生的所有责任和义务,在每种情况下,自生效日期起及之后。4.解释;继承人。本协议中包含的任何内容不得以任何方式取代、修改、替换、修改、更改、撤销、放弃、超出、扩大、扩大或以任何方式影响《采购协议》中规定的条款,也不得减少、扩大或扩大《购买协议》项下的任何补救措施。本协议仅用于将转让人在本协议中指定的转让资产出售、转让、转让和交付给受让人,以及受让人承担承担的负债,每种情况下均为DocuSign信封ID:556FC81F-BAFA-4B3A-BC64-1F8758E4C0D1

13购买协议所设想的,并应完全按照购买协议的条款和条件进行管理。根据《采购协议》的条款,本协议仅对转让人、受让人及其各自的继承人和受让人的利益具有约束力和效力。5.适用法律;修正案。本协议应由英格兰和威尔士的法律解释、执行和管辖,而不影响其法律冲突的原则。除非以本协议各方的名义签署书面文件,否则不得放弃或修改本协议。6.电子签名;对应方。所有各方(A)同意各自可以使用电子签名,并且(B)通过这样做同意遵守美国《电子签名法》(即《全球和国家商务电子签名法》(2000年6月30日颁布,编入《美国法典》第15编第7001节及其后)的规定)。本协议可以一份或多份副本或电子签名的形式签署,其效力应与实体副本的湿签名相同,每一份应被视为正本,所有此类副本或电子签名文件应被视为同一份协议,并在本协议各方签署并交付给另一方的一份或多份此类副本或电子签名文件后生效。以“.pdf”或其他电子影像方式交付本协议签字页的已签署副本应与交付手动签署的本协议副本一样有效。[页面的其余部分故意留空]DocuSign信封ID:556FC81F-BAFA-4B3A-BC64-1F8758E4C0D1

[销售、转让和承担协议清单的签字页]兹证明,以下签署人已由其正式授权的代表于上述第一年签署了本《销售、转让和承担协议》。
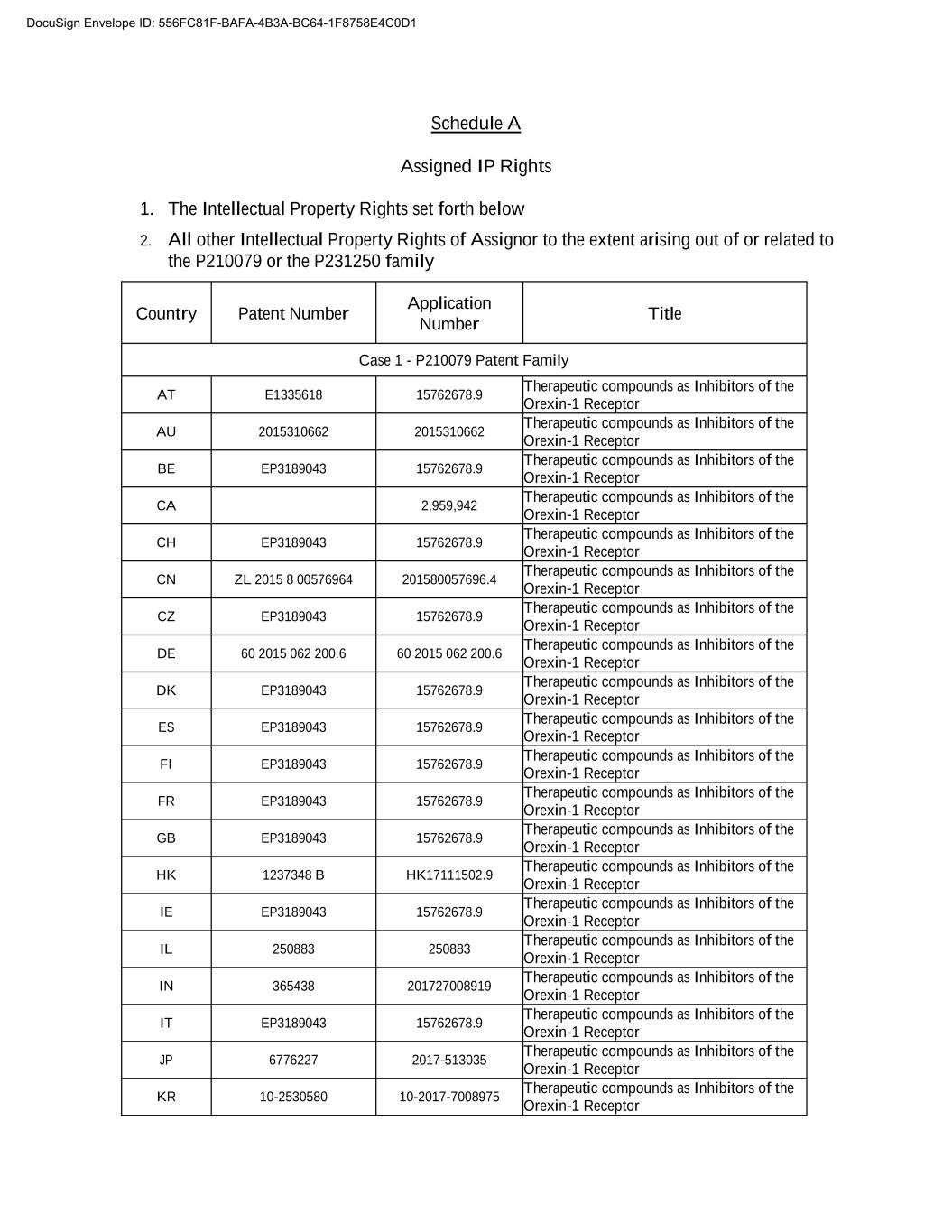
附表A分配的知识产权1.下文所列的知识产权2.转让人的所有其他知识产权,以P210079或P231250家族国家专利号申请号为限,或与之相关。案件1-E1335618专利家族中的P210079专利家族。作为食欲素-1受体的抑制剂的治疗性化合物AU 2015310662 15762678.9 2015310662作为食欲素-1受体的抑制剂的治疗性化合物BE EP3189043 15762678.9作为食欲素-1受体的抑制剂的治疗性化合物2,959,942作为食欲素-1受体的抑制剂的治疗性化合物CHEP3189043 15762678.9CNZL2015 8 00576964 201580057696.4食欲素-1受体抑制剂治疗化合物CZ EP3189043 15762678.9食欲素-1受体抑制剂治疗化合物DE 60 2015 062 200.6 60 2015 062 200.6食欲素-1受体抑制剂治疗化合物DK EP3189043 15762678.9食欲素-1受体抑制剂治疗化合物EP3189043 15762678.9食欲素-1受体抑制剂治疗化合物EP3189043 15762678.9治疗化合物作为食欲素-1受体EP3189043 15762678.9治疗化合物作为食欲素-1受体EP3189043 15762678.9治疗化合物。9抑制食欲素-1受体的治疗性化合物HK 1237348 B HK17111502.9抑制食欲素-1受体的治疗性化合物IE EP3189043 15762678.9治疗化合物作为食欲素-1受体的抑制剂IL 250883 250883治疗性化合物作为食欲素-1受体的抑制剂治疗性化合物ID:556FC81F-BFA-B3A-BC64-1F875E0D1E0C0C075治疗性化合物作为食欲素-1受体的抑制剂JP 6776227 2017-513035治疗性化合物作为食欲素-1受体的抑制物KR 10-2530580-2017-7008975治疗性化合物作为食欲素-1受体的抑制物包络ID:556FC81F-BFA-B3A-BC64-1F875E0D1C0C0C0
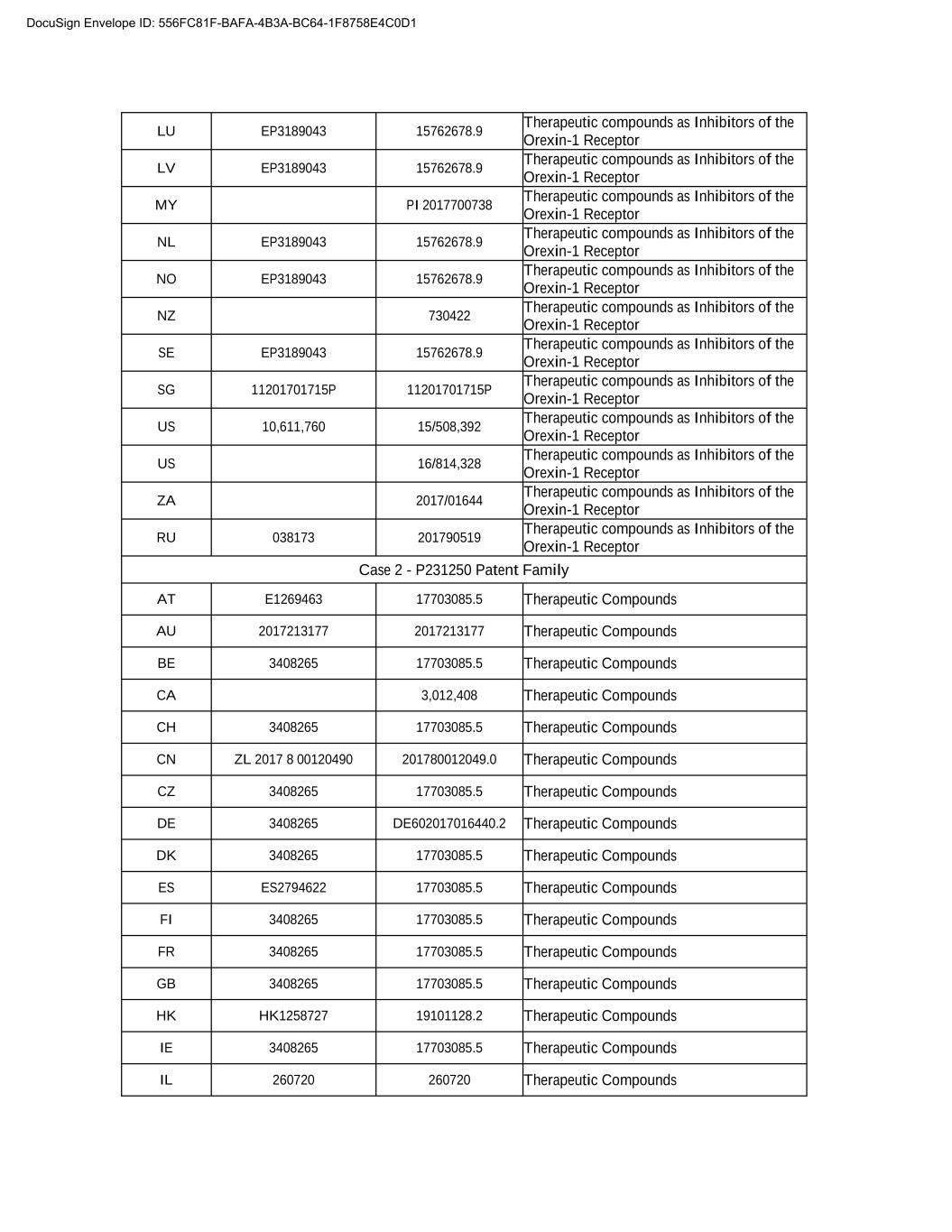
Lu EP3189043 15762678.9抑制食欲素-1受体LV EP3189043 15762678.9治疗化合物抑制食欲素-1受体My PI 2017700738治疗化合物作为食欲素-1受体抑制剂NL EP3189043 15762678.9治疗化合物作为食欲素-1受体抑制剂NZ 730422治疗化合物作为食欲素-1受体抑制物SE EP3189043 15762678.9治疗化合物作为食欲素-1受体抑制剂SE EP3189043 15762678.9治疗化合物作为食欲素-1受体抑制者化合物SG11701715P 2011715P作为食欲素-1受体的抑制剂US 16/814,328治疗化合物作为食欲素-1受体的抑制剂ZA 2017/01644治疗化合物作为食欲素-1受体的抑制剂RU 038173 201790519 201790519治疗化合物作为食欲素-1受体案例2的抑制剂治疗化合物AT E1269463 17703085.5治疗化合物AU2017213177 2017213177治疗化合物BE 3408265 17703085.5治疗化合物CA 3,012,408治疗化合物CH 3408265 17703085.5治疗化合物ZL2017 8 00120490 7800120465治疗化合物ZCZ 3403408265治疗化合物201607016440.2 DK 40340340865治疗化合物BE 3408265 17703085.5治疗化合物CA 3,012,408治疗化合物CH3408265 17703085.5治疗化合物ZL2017 8 00120490 780012049.0治疗化合物ZL2017 8 00120490 7800120465治疗化合物ZCZ 3408265治疗化合物201607016440.2 DK 340340340865治疗化合物BE 3408265 17703085.5治疗化合物CA 3,012,408治疗化合物CH3408265 17703085.5治疗化合物ZL2017 8 00120490 7800120465治疗化合物ZL2017 8 00120490 7800120465治疗化合物ZL2017 8 00120465 17708308305DE607016440.2治疗化合物DK 40340340340865治疗化合物BE 3408265 17703085.5治疗化合物CA 3,012,408治疗化合物CH3408265 17703085.5治疗化合物ZL2017 8 00120490 7800120465治疗化合物ZL2017 8 00120490 7800120465治疗化合物ZCZ 3403408265治疗化合物201607016440.2 DK 3403403405治疗化合物FI 3408265 17703085.5治疗化合物FR 3408265 17703085.5治疗化合物GB 3408265 17703085.5治疗化合物香港HK1258727 19101128.2治疗化合物IE 3408265 17703085.5治疗化合物IL 260720 260720治疗化合物文件签名ID:556FC81F-BAFA-4B3A-BC64-1F8758E4C0D1
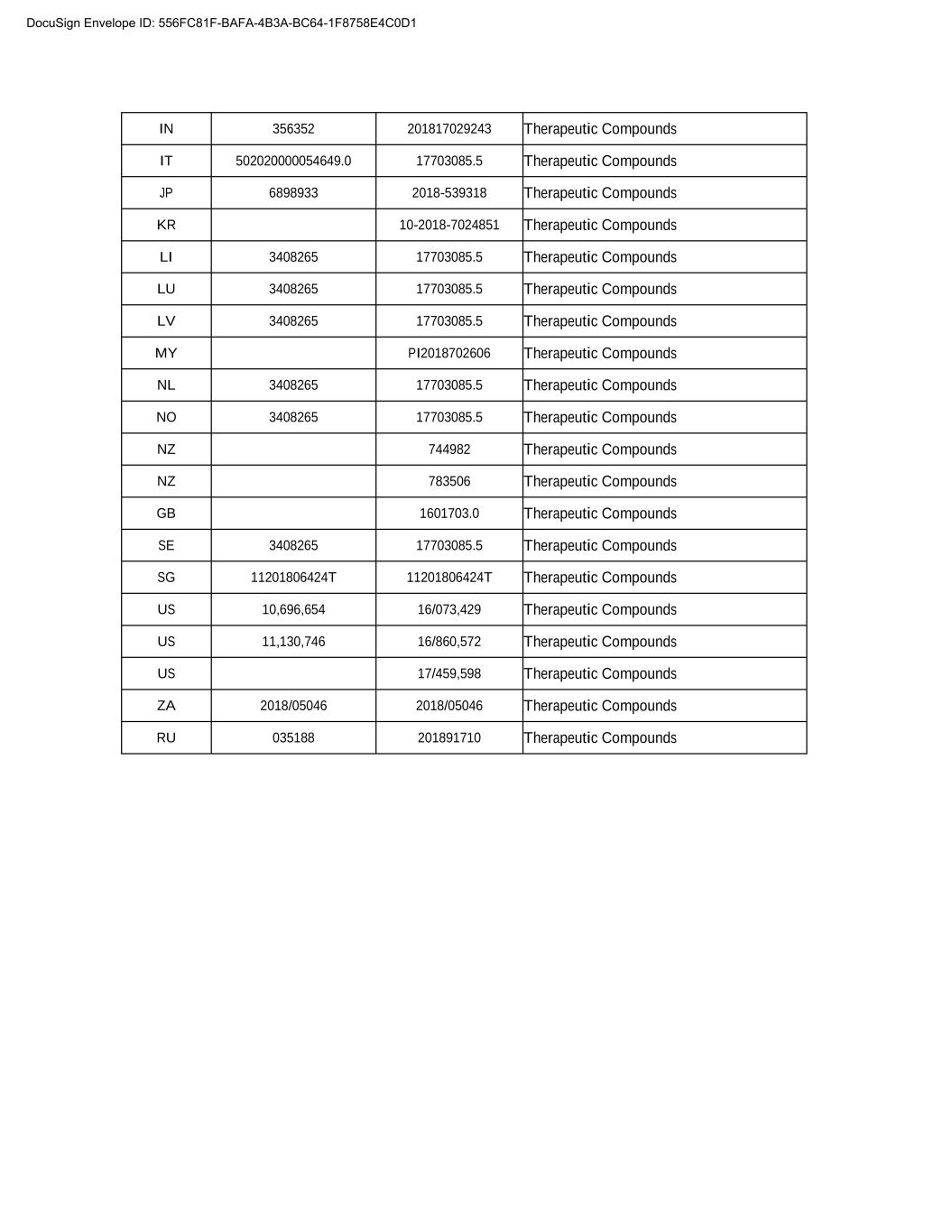
2018年201817029243治疗化合物IT 502020000054649.0 2018年治疗化合物JP 6898933 2018年-539318治疗化合物KR 10-2018年-7024851治疗化合物Li 3408265 17703085.5治疗化合物Lu 3408265 17703085.5治疗化合物LV 3408265 17703085.5治疗化合物My PI2018702606治疗化合物NL 3408265 17703085.5治疗化合物编号3408265 1770Z3085.5治疗化合物NZ 744982治疗化合物GB 1601703.0治疗化合物SE 340865 177085.5治疗化合物2018年11802464T 2011164654/073,446治疗化合物US 11,1308265 17703085.5治疗化合物2018年治疗化合物GB 1601703.0治疗化合物SE 340865 17703085.5治疗化合物US 69654/073,44605046治疗性化合物RU 035188 201891710治疗性化合物DocuSign信封ID:556FC81F-BAFA-4B3A-BC64-1F8758E4C0D1