
附录 99.1

ADC Therapeutics 业务概览 Cowen 会议,2024 年 3 月 5 日

2 前瞻性陈述本演示文稿及任何随附的口头陈述由ADC Therapeutics SA(“ADC Therapeutics”、“我们” 或 “我们”)编写,仅供参考,不用于任何其他目的。本演示文稿中包含的任何内容都不是,也不应被解释为主讲人或ADC Therapeutics或ADC Therapeutics的任何高管、董事、员工、代理人或顾问的建议、承诺或陈述。本演示文稿并不旨在包罗万象,也不包含您可能想要的所有信息。本陈述中提供的信息以及随附的任何口头陈述仅适用于截至本文发布之日。本演示文稿包含1995年《私人证券诉讼改革法》安全港条款所指的前瞻性陈述。在某些情况下,您可以使用 “可能”、“假设”、“将”、“应该”、“将”、“期望”、“打算”、“计划”、“预期”、“相信”、“估计”、“预测”、“潜在”、“看起来”、“寻找”、“未来”、“继续” 或 “出现” 或否定这些术语或否定词语来识别前瞻性陈述类似的表达方式,尽管并非所有前瞻性陈述都包含这些识别词。前瞻性陈述受某些风险和不确定性的影响,这些风险和不确定性可能导致实际结果与所描述的结果存在重大差异。可能导致这种差异的因素包括但不限于:Zynlonta2023年第四季度的实际收入,公司更新后的公司战略的成功;2025年第四季度初的预期现金流,新商业进入市场战略的有效性,来自新技术的竞争,Comp Any在美国增长ZYNLONTA® 收入的能力;瑞典Orphan Biovitrum AB(Sobi)®) 有能力在欧洲经济区成功实现ZYNLONTA® 商业化,市场接受度高,报销范围充足,以及未来的收入;国家药监局批准了Overland ADCT BioPharma在中国提交的ZYNLONTA® 的BLA及其未来收入;我们的战略合作伙伴,包括麻省理工学院田边制药公司,在外国司法管辖区获得监管部门批准ZYNLONTA® 的能力,以及此类合作伙伴关系未来收入和向我们付款的时间和金额;公司的时机和结果或其合作伙伴的研发项目或临床试验,包括LOTIS 5和7、ADCT 601和602以及IIT在佛罗里达州和马里兰州,以及对某些具有不同靶标、连接剂和有效载荷的实体瘤的早期研究;公司产品或候选产品的监管申报的时间和结果;FDA或外国监管机构的行动;预计的收入和支出;公司的债务,包括医疗保健特许权使用费管理以及蓝猫头鹰和橡树设施,以及此类债务对公司活动施加的限制,遵守能力各种年龄补助金的条款并偿还此类债务以及偿还此类债务所需的大量现金;以及公司为其研究、开发、临床和商业活动获得财务和其他资源的能力。有关这些因素和其他可能导致实际业绩与前瞻性陈述中的预期存在重大差异的因素的更多信息载于公司20-F表年度报告的 “风险因素” 部分以及公司向美国证券交易委员会提交的其他定期和当前报告以及文件中。这些陈述涉及已知和未知的风险、不确定性和其他因素,这些因素可能导致实际业绩、业绩、成就或前景与此类前瞻性陈述所表达或暗示的任何未来业绩、业绩、成就或前景存在重大差异。该公司提醒投资者不要过分依赖本文件中包含的前瞻性陈述。前瞻性陈述基于我们管理层的信念和假设以及管理层目前可获得的信息。无法保证将来会取得这样的结果。本演讲中所载的此类前瞻性陈述仅代表截至本次演讲之日。除非适用法律要求,否则公司明确披露任何义务或承诺更新本演示文稿中包含的这些前瞻性陈述,以反映我们期望的任何变化或此类声明所依据的事件、条件或情况的任何变化。对于任何此类前瞻性陈述的准确性,不作任何陈述或保证(明示或暗示)。本演示文稿中包含的某些信息涉及或基于第三方来源的研究、出版物、调查和其他数据以及我们自己的内部估计和研究。尽管我们认为截至本演示之日这些第三方来源是可靠的,但我们尚未独立核实,对于从第三方来源获得的任何信息的充分性、公平性、准确性或完整性,我们也没有做出任何陈述。此外,本演示文稿中包含的所有市场数据都涉及许多假设和局限性,无法保证此类假设的准确性或可靠性。最后,尽管我们认为自己的内部研究是可靠的,但此类研究尚未得到任何独立来源的证实。

3 ADC 治疗概览实体瘤在临床中推进靶向 AXL 的 ADCT-601 和多个在研的 ADC 血液学在 3L+ DLBCL 中最大化 ZYNLONTA®,并寻求扩展到早期的 DLBCL 和惰性淋巴瘤系列;将靶向 CD22 企业现金跑道的 ADCT-602 推进 2025 年第四季度,在 2024 年使用多种催化剂平台凭借强大的技术工具箱和专业终端开创性 ADC 领域-终端能力 ADC:抗体药物偶联物;DLBCL:弥漫性大 B 细胞淋巴瘤

4 个关键业务更新 DLT:剂量——限制毒性;MTD:最大耐受剂量。注意:财务状况未经审计。▪ 截至2023财年末现金流约为2.785亿美元 ▪ 现金流预计将延续至2025年第四季度;与2022年相比,2023年运营支出下降两位数 ▪ LOTIS-7(使用双特异性剂的ZYNLONTA):清除了前两个剂量队列,没有DLT且有抗肿瘤活性的早期迹象 ▪ LOTIS-5(ZYNLONTA含利妥昔单抗的ZYNLONTA)): 2023 年加速入组,完成了三分之二以上的入组 ▪ ADCT-601(靶向 AXL):R 已达到 MTD,目前处于剂量优化阶段;e 单一疗法和单一疗法均出现抗肿瘤活性的早期迹象肉瘤组合 ▪ ADCT-901(靶向 KAAG1):由于剂量增加的疗效迹象有限,停止向优先项目重新分配资金 ▪ 2023 年第四季度收入预计约为 1650 万美元,与 2023 年第三季度管道企业 ZYNLONTA(隆卡妥昔单抗泰西林——lpyl)相比增长了两位数的百分比注:截至 2024 年 3 月 4 日的更新

5 释放强大的 ADC 产品组合在血液学和实体瘤领域的价值 DLBCL:弥漫性大 B 细胞淋巴瘤;FL:滤泡性淋巴瘤;MZL:边缘区淋巴瘤;NSCLC:非小细胞肺癌;ALL:急性淋巴细胞白血病。短期-中期、中长期血液学产品组合实体瘤产品组合 ZYNLONTA ▪ 在 3L+ DLBCL 中最大化 ZYNLONTA ▪ 寻求将 ZYNLONTA 扩展到早期的 DLBCL 和其他惰性淋巴瘤(例如 FL、MZL)作为首选单剂和组合药物 ZYNLONTA + 利妥昔单抗(LOTIS-5)YNLONTA + 双特异性 (LOTIS-7) ADCT-602 (CD22) ▪ 逐步增加和扩大 r/r ALL ADCT-601 (AXL) 的 1 期剂量 ▪ 优化肉瘤、胰腺和 NSCLC 下一代 ADC 中的单一药物和/或组合扩张剂量 ▪推进研究型 ADC 产品组合 — 基于差异化 exatecan 的有效载荷和新型亲水性连接剂 − 靶向 Claudin-6、napi2b、PSMA ▪ 继续使用一系列有效载荷、连接剂和偶联技术对未公开靶标进行研究

6 按治疗系列划分的患者比例* DLBCL、FL 和 MZL 占成熟 B 细胞淋巴瘤的约 60% 1 * 1L (~ 70%) 1L (~ 65%) 1L (~ 61%) DLBCL FL MZL 关键:目前批准的当前开发领域推进 B-细胞淋巴瘤 ZYNLONTA 的开发 2L (~ 24%) 2L (~ 27%)) 3L+ (~ 11%) 3L+ (~ 12%) 2023 年美国市值 2、5 年患病率 3 31亿美元 2,~10.9 万名患者 26亿美元 2,~61 万名患者 14亿美元 2,约 38 万名患者 1.根据白血病和淋巴瘤协会的数据;2.Clarivate & Global Data 用于估算美国的市场价值;3.Cerner Enviza CancerMpact 数据库,2023 年。注意:按疗法线划分的分布基于发病率、药物治疗人群。▪ LOTIS-5和LOTIS-7有可能使ZYNLONTA进入2L+ DLBCL。LOTIS-5:20 患者安全运行——数据显示 ORR 为 80%,CR 为 50%,无新的安全信号;预计在 2024 年加快患者入组/完成——LOTIS-7:剂量——前两个给药水平的限制毒性期已获批准两组的 ZYNLONTA(90 µg/kg,120 µg/kg);目前在 150 µg/kg 当前发展区域招收患者 ▪ IIT 表明 ZYNLONTA 方案可以提供在 2L+ 高风险 FL(96% ORR,85% CR,N=27)中获益;印度理工学院研究 2L+ MZL 中的 ZYNLONTA ——这些人群中未得到满足的需求意义重大 − 评估监管路径和纲要策略 ▪ ZYNLONTA 与双特异性药物(LOTIS-7)的组合目前正在研究 r/r FL 和 r/r MZL

7 尽管市场高度发展,但Zynlonta在2L+中的组合仍然存在重大机遇 1.Epcoritamab或Glofitamab。资料来源:普特南协会初步研究。关键最近批准改用 1L 使用无标准护理学术界 1L(约 30 K 名患者)2L(约 11 万名患者)3L+(约 6 K 名患者)R-CHOP ~ 35% Polivy + R-CHP R-CHOP Polivy + R-CHP CAR-T 临床试验 Zynlonta CAR-T 临床试验 Zynlonta BSABs 1 Monjuvi + Len Polivy + BR Zynlonta Monjuvi + Len Polivy + BR R-Based Chemo ~ 30% ~ 70% R-Based Chemo Monjuvi + Len Pola-BR ~ 65% ~ 60% ~ 40% CAR-T 临床试验 Salvage +/-ASCT 说明性市场演变 ▪ 尽管最近取得了进步,但真正的 SoC 只存在于 1L 和学术环境中 CAR-T ▪除CAR-T外,市场正在向以现成药物为基石的组合发展 ▪ 随着波拉妥珠单抗进入1L,在2L+中使用基于pola的组合进行再治疗的可能性可能较小 ▪ 需要在社区中心的2L和3L+以及学术环境中的3L+中使用具有更好疗效和耐受性的新组合 ZYNLONTA OPPORTUNITY LOTIS-5 LOTIS-7 ZYNLONTA OPPORTINITY LOTIS-5 LOTIS-7 ZYNLONTA OPPORTINITY LOTIS-5 LOTIS-7 ZYNYNTA Lonta + Bispecifics 组合可以:▪ 在 2L+ 学术环境中与 bsaB 和其他组合相比,可提高疗效 ▪ 提高 CRS 率,扩大社区的可及性2L+ Zynlonta + R 的中心有潜力:▪ 以熟悉的安全配置提供具有竞争力的功效 ▪ 成为社区中心的 2L+ 环境中的 SoC,在学术环境中成为 3L+ 环境中的 SoC
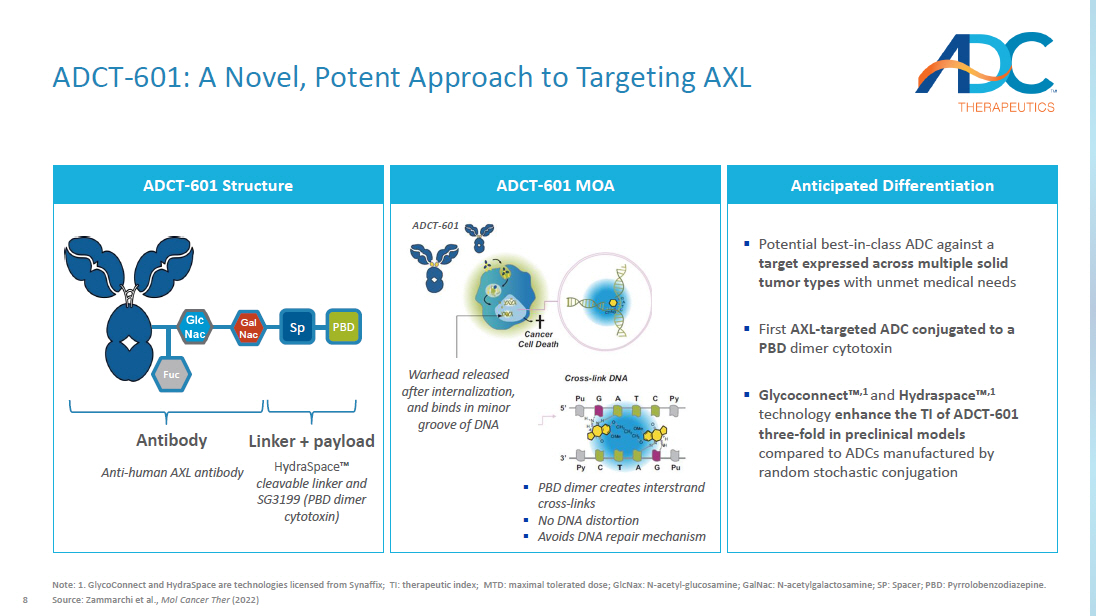
8 ADCT-601:一种靶向 AXL 的新型、有效的方法注:1.GlycoConnect 和 HydraSpace 是 Synaffix 授权的技术;TI:治疗指数;MTD:最大耐受剂量;glcNax:N-乙酰-葡萄糖胺;GalnaC:N-乙酰半乳糖胺;SP:间隔;PBD:吡咯苯二氮卓类。来源:Zammarchi 等人,《Mol Cancer Ther》(2022年)ADCT-601 结构预期分化 ▪ 针对在多种未满足医疗需求的实体瘤类型中表达的靶标的潜在同类最佳抗药剂 ▪ 第一个 AXL-靶向 ADC 偶联与 PBD 二聚体细胞毒素 ▪ Glyconnect 适用于由随机偶联法制造的 ADC PBD Sp Gal Nac Fuc Fuc HydraSpace Ω 可分解连接剂和 SG3199(PBD 二聚体细胞毒素)抗人类 AXL 抗体抗体链接器 + 有效载荷 ADCT-601 MOA 弹头在内化后释放,并在 DNA 的小凹槽中结合 ▪ PBD 二聚体产生链间交叉链接 ▪ 无 DNA 失真 ▪ 避免 DNA 修复机制 ADCT-601

9 ADCT-601 靶向 AXL:理由和区别说明:1 数据截至 2024 年 9 月 2 日。2 基于试验 601-102 中用于确定高表达/阳性患者的评分算法和截止值:STS = AXL+ 肿瘤 ce lls 2+/ 3+ 强度 ≥ 75%,PAAD = AXL+ 肿瘤细胞 2+/ 3+ 强度 ≥ 10%,NSCLC = 膜 AXL+ 肿瘤细胞 (任何强度)≥ 1%。3 膜表达通常与 2+/3+ 肿瘤细胞的表达相关。▪ 一项 1b 期研究正在进行中,包括一个单一疗法组招募肉瘤、胰腺癌和表达 NS 的 AXL 患者对于肉瘤和胰腺癌患者,CLC和与吉西他滨的复方组合 ▪ 达到13mg的推荐剂量;剂量优化正在进行中 o 在肉瘤中,在单一疗法中已出现抗肿瘤活性的早期迹象,在测试的剂量范围内具有可耐受的安全性 ▪ 在胰腺癌中,单一疗法组最近启动了筛查临床研究现状和后续步骤 ▪ AXL在多种肿瘤类型中表达-包括非小细胞肺癌、胰腺和肉瘤 ▪ AXL 的高表达与病情恶化相关这些癌症类型的总存活率高 AXL 表达的病例百分比任何 AXL 表达肉瘤 (STS) 病例的 2% ~ 30% ~ 90% 胰腺腺癌 ~ 35% 60 — 70% 非小细胞肺部 3 20 — 25% 50 — 60% 目标相关性 AXL 表达 1

10 具有一系列有效载荷、连接剂和偶联技术的成长型工具箱注:1 DAR:药物抗体比率 Antiby ▪ 在识别和推进具有高度未满足需求的引人注目的靶标方面拥有丰富的经验 ▪ 专注于掩盖结合、条件结合部分、双特异性和双偏热性连接剂 ▪ 专有连接剂,可通过可调的 DAR 1 提高血浆稳定性并控制有效载荷释放不可分割的连接器 Payload ▪ 将下一代多溴联苯伪造为新弹头;第一个带来 PBD ADC 的弹头从概念到市场 ▪ 推进下一代有效载荷以提高选择性、效力、治疗指数 — 喜树碱衍生物 — DNA 损伤剂 — 免疫调节剂 — 双有效载荷偶联技术 ▪ 可实现精确定位的技术 — 不同有效载荷的特定附着 — 正交偶联方法

11 Exatecan 有可能与 dxD 等商用阶段毒素进行差异化注意:1 pgP:P-糖蛋白;2 细胞系衍生异种移植 (CDX) 模型是一种肾平滑肌母细胞瘤模型,全臂静脉注射 qdx1 来源:Weng 等人,Cancer Discov (2023) EXATECAN V. DXD ▪ 效力更好 ▪ 没有 pGP 1 运输,增强细胞内存在感 ▪ 增加旁观者效应,导致更多细胞死亡,增强治疗效果与 dxD Exatecan DxD 载体同型(10 mg/kg)抗体——D Xd(15 mg/kg)抗体——exatecan(6.6 mg/ kg)抗体——exatecan(6.6 mg/ kg)kg) 抗体——依沙替康(10 mg/kg)▪ ADCT 开发了一种新型的亲水性连接剂,可实现依沙替康的有效偶联 ▪ 我们的基于依沙替康的 ADC 可在内化后实现无痕释放 ▪ 优异的体内疗效和出色的耐受性,在 CDX MODEL 2 EXATECAN ADVANTE 中没有任何迹象的 ILD EXATECAN ADC V. DXD ADC ADC。ADC 疗法平台的优势

12 目标描述磷酸转运蛋白粘附蛋白酶糖蛋白氨基酸转运蛋白肿瘤感兴趣的类型 NSCLC 卵巢癌子宫内膜癌前列腺癌 NSCLC 结直肠癌有效载荷 Exatecan Exatecan Exatecan Exatecan Exatecan Exatecan 体外验证数据体外功效 NHP 毒理学体外表征 NHP 毒理学正在进行的体外表征 NHP 毒理学体内功效 NHP 毒理学正在进行的体外表征 NHP 毒理学 ology 2 候选人选择 1 完成 2024 年 2024 年 2024 年 ADC 资产对照经验证的目标高未满足需求的适应症注意:1项支持IND的研究可以在选择候选人后的18个月内完成;2项使用嵌合候选药物Napi2b Claudin完成的NHP研究-6 PSMA未公开的靶标

13 ADCT投资组合的企业业务发展战略 HEMETALOGY ZYNLONTA,ADCT-602 SOLID TUMOL S ADCT-601,解锁价值的研究资产业务发展目标:美国EX-美国公司开发与公司-推广*特许权使用费和里程碑加速和扩大资产开发 3 非稀释性融资 2 最大化交易价值和价值拆分 1 直接伙伴关系 *可根据经济状况灵活选择其他结构。陆路合资企业

14 Cash Runway 将支持多种潜在的近期价值——推动因素 □ ZYNLONTA:□ 在 2024 年实现商业品牌盈利 □ LOTIS-5:2024 年完成注册 □ LOTIS-7:2024 年全年的剂量升级和扩张更新 □ 佛罗里达州和 MZL IIT:2024 年 ADCT-602 (CD22):2024 年 1 期研究的其他数据更新 ▪ 探索潜在的合作伙伴关系和许可协议 ▪ 到2025年第四季度的现金流将支持公司实现价值创造里程碑*血液学 □ ADCT-601(AXL):2024年肉瘤、胰腺和非小细胞肺癌的1期研究的更多数据更新 □ 临床前:推进在研的ADC实体瘤产品组合 * Cash runway 假设根据公司的合作协议收到预期的监管里程碑付款,并使用贷款协议要求维持的金额