

附录 99.1 用于广泛性焦虑症 (GAD) 的 MM120 第 2b 期完整 标题数据 ODT PK 桥接研究突破性疗法称号 2024 年 3 月
免责声明本演示文稿(“演示文稿”)由 Mind Medicine (MindMed) Inc.(“MindMed”、“公司”、“我们”、“我们的” 或 “我们”)编写,仅供参考。MindMed、其关联公司或其各自的员工、 董事、高级职员、承包商、顾问、成员、继任者、代表或代理均不对本演示文稿中包含的任何信息的准确性或完整性作出任何陈述或保证,也不对本演示文稿中包含的任何 陈述(明示或暗示)或任何遗漏承担任何责任。本演示文稿不构成MindMed证券的发行或收购要约的邀请,在任何情况下, 都不得将其解释为招股说明书、广告或证券公开发行。此处包含的任何商标均为其所有者的财产,仅用于参考目的。此类使用不应被解释为对 MindMed 产品或服务的认可 。除非另有说明,否则任何金额均以美元为单位。MindMed 的证券未经美国证券交易委员会(SEC)或任何州、省或其他 证券监管机构的批准或拒绝,美国证券交易委员会或任何州、省或其他证券监管机构也未透露本演示文稿的准确性或充分性。任何与此相反的陈述均属刑事犯罪。关于前瞻性陈述的警示说明 本演示文稿包含1995年美国私人 证券诉讼改革法案和其他适用的证券法安全港条款所指的 “前瞻性陈述”,我们的高级管理人员和代表可能会不时作出。前瞻性陈述通常可以用诸如 “计划”、“预期”、“预期”、 “预算”、“计划”、“估计”、“预测”、“打算”、“预期”、“将”、“项目” 或 “相信” 或变体(包括负面的 变体)等词语来识别,或某些行动、事件、结果或条件的陈述 “可能”、“可能”、“将”、“可能” 或 “将” 被采取、发生或实现, 对未来时期的类似提法。除历史事实陈述外,前瞻性陈述的示例包括与以下内容有关的陈述:任何药物或疗法的开发和商业化,或上述任一药物或疗法的 疗效,我们开发活动的成功和时机;我们计划进行的临床试验的成功和时机;我们实现本文规定的里程碑的能力;任何临床试验 成功或获得食品药品管理局或其他监管机构批准的可能性;我们的现金跑道通过关键临床为业务提供资金读数及2026年;获得专利的可能性或此类专利一旦获得批准的效力,以及MindMed预期进入的市场潜力 。前瞻性陈述既不是历史事实,也不是对未来表现的保证。相反,它们仅基于我们当前对我们 业务的未来、未来计划和战略、预测、预期事件和趋势、经济以及截至本演示文稿之日的其他未来状况的信念、预期和假设。尽管 MindMed 认为这些假设是合理的,但 本质上会受到难以预测的重大业务、社会、经济、政治、监管、竞争和其他风险和不确定性的影响,其中许多风险和不确定性不在 MindMed 的控制范围内,实际业绩和 财务状况可能与前瞻性陈述中显示的存在重大差异。因此,您不应依赖这些前瞻性陈述中的任何一项。可能导致实际业绩和财务状况 与前瞻性陈述中指出的有重大差异的重要因素包括:我们筹集资金以完成计划和资助其研究的能力;正在开发的 药物和治疗的医疗和商业可行性;MindMed的负现金流历史;MindMed的有限运营历史;未来出现亏损;遵守法律法规;相关困难研究和 开发;与临床试验或研究相关的风险;加强监管审查;早期产品开发;临床试验风险;监管批准程序;迷幻药行业的新颖性;以及 MindMed最近向美国证券交易委员会提交的10-K表年度报告以及我们未来向美国证券交易委员会和 证券监管机构提交的其他文件中的 “风险因素” 部分中讨论或提及的风险因素加拿大所有省份和地区,可在公司在 SEDAR 上的简介,网址为 www.sedar.com。MindMed在本演示文稿中做出的任何前瞻性陈述仅基于公司目前可用的信息 ,并且仅代表截至发表之日的信息。MindMed 没有义务公开更新可能不时发表的任何前瞻性陈述,无论是书面还是口头陈述,无论这些陈述是新信息、未来发展还是其他原因造成的。关于监管事项的警示说明美国联邦政府通过《管制物质法》对药物进行监管。MM120 是专有的、经过药物优化的 形式的 D-酒石酸麦角苷,而 MM402 或 R (-)-MDMA 是我们专有的 MDMA(3,4-亚甲二氧基甲基苯丙胺)的 R-对映异构体。根据《管制物质法》,Lysergide和MDMA是附表一物质。尽管公司 专注于使用迷幻或致幻化合物以及这些化合物的非致幻衍生物的项目,包括其 MM120、MM402 和其他候选产品,但该公司并未直接或间接参与 在其经营所在司法管辖区非法销售、生产或分销任何物质的活动。该公司是一家神经药物开发公司,不经营迷幻或致幻物质,除非是在批准的监管框架内进行的 实验室和临床试验环境中。公司的产品在获得适用的监管批准之前不会商业化,只有在成功开发出用于预期用途的安全性和有效性 的临床证据后,才会获得批准。市场和行业数据本演示文稿包括从第三方来源(包括行业出版物)获得的市场和行业数据。MindMed 认为行业数据 是准确的,估计和假设是合理的,但无法保证这些数据的准确性或完整性。第三方消息来源通常表示,其中包含的信息是从被认为可靠的 来源获得的,但无法保证所含信息的准确性或完整性。尽管数据被认为是可靠的,但MindMed尚未独立验证本演示文稿中提及 的第三方来源的任何数据,也没有确定这些来源所依据的基本经济假设。本演示文稿中对研究报告或文章和出版物的引用不应解释为描述了整个引用报告或文章的 的完整发现。MindMed 对此类信息的准确性不作任何陈述。投资者演示文稿 | 2024 年 3 月 2

今天的议程演讲主题罗布·巴罗介绍性讲话 MindMed 首席执行官 MindMed Rakesh Jain,医学博士,公共卫生硕士 KOL 对未满足需求的看法,德克萨斯理工大学广泛性焦虑症(GAD)和医学院精神病学和行为科学临床教授 — 二叠纪盆地阶段 2b 试验结果 Daniel R Karlin,医学博士,马萨诸塞州 Mind2b 期首席医学官的完整顶线结果摘要 GAD 的 MM120 试验 Francois Lilienthal,医学博士,工商管理硕士商业机会首席商务官,MindMed Rob Barrow 摘要 评论适用于 MM120 发展计划首席执行官、MindMed 闭幕词和问答(问答)所有演讲者投资者演示文稿 | 2024 年 3 月 3 日

介绍性发言罗伯特·巴罗首席执行官

我们的目标是成为大脑健康管道管理领域的全球领导者 针对大量未满足的医疗需求的药物开发项目具有多元化的临床专业知识渠道 通过关键研究 利用数十年的临床前和临床预期现金流 在2b期临床报告和2026年取得令人鼓舞的结果*旨在最大限度地提高市场排他性和保护的知识产权和研发策略*公司的现金和现金等价物为美元截至 12 月,9,970 万预计2023年31日和承诺信贷额度将为2026年的运营提供资金。投资者演示文稿 | 2024 年 3 月 5 日

经验丰富的领导层拥有良好的往绩记录在 1 大脑健康创新方面的丰富经验 1.包括投资者演示文稿 | 2024 年 3 月 6 日

MM120 有可能解决广泛性焦虑症 (GAD) 中大量未得到满足的 GAD 需求 1 • GAD 是成人中第二常见的精神障碍,但可能存在同类最佳治疗选择有限的新型 MOA 疗法 • 症状可能会使人衰弱,治疗 疗效不佳会导致完全缓解和不可忍受的副作用。1 大型市场 650 万对 1300 万左右没有反应百万患有 GAD 3 1 2 一线治疗的美国成年人接受治疗机会 77% 中度至重度 1 SSRI/SNRI:50%失败率常伴有不良副作用苯二氮卓类药物:成瘾、耐受风险;通常用于短期新疗法的重大需求 4 丁螺环酮:疗效差抗精神病药物:短期和长期风险; 耐受性差 1.精神和药物使用障碍患病率研究(MDPSU):2023年调查结果报告。2.凯斯勒 RC、Chiu WT、Demler O 等。全国合并症中12个月的DSM-IV疾病的患病率、严重程度和合并症 调查-复制。2005 年 Arch Gen Psychiatry;62 (6):617-627。投资者演示文稿 | 2024 年 3 月 7 日 3.安萨拉,耐药性广泛性焦虑症管理,Ment Health Clin 2020 年 11 月;10 (6) 326-334) 美国人口普查局, 公司计算。4.Garakani A等人,(2020)焦虑症的药物疗法:当前和新兴的治疗选择。正面。精神病学 11:595584. doi:10.3389/fpsyt.2020.595584

MindMed 研发管道产品候选适应症 临床前 1 期 2 期 3 期注册精神病学项目广泛性焦虑 MM120 1 障碍 (GAD) (Lysergide d-酒石酸盐) 其他精神病学 2 适应症 MM402 自闭症谱系 1 障碍 (ASD) (R (-)-MDMA) 早期研究和 合作 IITs 1 各种(UHB 合作)各种早期研究(Mindshift 合作)1.完整的试验详情和 clinicaltrials.gov 链接可在 mindmed.co/clinical-digital-trials/ 2 上获得。研究处于勘探和/或规划阶段。 投资者演示文稿 | 2024 年 3 月 8 日 LSD:lysergide;MDMA:3,4-亚甲二氧基甲基苯丙胺。IIT:研究者发起的试验(预计不会将结果用于我们的监管批准申请);UHB:巴塞尔大学医院

MM120 项目更新的主要亮点 1 GAD 2b 期试验中 12 周耐久性阳性 • 主要和次要终点具有统计学意义 • 与安慰剂相比改善了 7.7 个百分点(d=0.81;p=0.003)• 第 12 周突破性疗法称号的临床缓解率为 48% • 认可 SOC 实质性改善的初步证据 • FDA 组织承诺和高效开发支持 MM120 ODT 产品概况增强 • PK 桥接结果研究显示差异化 特征 • 吸收速度快,效果更好生物利用度和更高的治疗性 AUC 可扩展上市的商业模式和战略 • 广泛认识到 GAD 的负担和未满足的需求 • 对 MM120 作为潜在的 游戏规则改变者的热情市场保护战略和知识产权组合 • 以知识产权为导向的研发战略,最大限度地发挥市场保护潜力 • 通过近期和短期的关键拨款推进知识产权组合 1.来源:研究 MMED008 内部研究 文件和计算。投资者演示文稿 | 2024 年 3 月 9 2.来源:https://www.fda.gov/patients/fast-track-breakthrough-therapy-accelerated-approval-priority-review/breakthrough-therapy

在 单剂量 1,2 后,GAD 中 MM120 的结果已在目标产品概况中公布,所有终点均有显著改善 24 小时内快速降低 CGI-S 1.8 个百分点(p

观察到 12 周耐久性,效果大小是 1,3 种护理标准 的两倍以上 GAD 周结果中 2b 12 期比较效果大小的关键要点 • 最大观测效果大小为 0.81 2 MM120 100 µg 0.81 是 2,3 care 4 苯二氮卓类药物标准的两倍多 0.38 • 快速和 持久的临床反应 3 在没有心理治疗干预的情况下观察到的临床活性 4 SSRIs 0.36 • 临床活性 4 丁螺环酮 0.17 超出研究药物 0 0.2 0.4 0.6 0.8 1。来源:研究 MMED008 内部研究 文件和计算。2.HAM-A 分数基于 MMED008 研究中的 ANCOVA LS 平均值。效应大小基于使用组间的 LS 均值变化和组间第 12 周 HAM-A 分数的合并标准差进行事后计算。投资者 演示文稿 | 2024 年 3 月 11 日 3.基于 100 微克剂量组。4.资料来源:RB Hidalgo,J Psychopharmacol。2007 年 11 月;21 (8): 864-72。

美国食品和药物管理局已将 MM120 指定为 GAD 的突破性疗法 MM120 获得 突破性疗法 1 种疗法称号 • • FDA 组织承诺认可 GAD 是一种涉及高级管理人员的严重疾病 • 2b 期结果表明 • 对有效药物的强化 指导初步证据表明 MM120 与现有疗法相比可能有重大改进 • 加速批准和 3 优先审查 4 • NDA 1 的滚动审查。更多详情请访问美国食品药品管理局的网站:https://www.fda.gov/patients/fast-track-breakthrough-therapy-accelerated-approval-priority-review/breakthrough-therapy 2.基于临床重要终点 3.如果符合相关标准 投资者演示文稿 | 2024 年 3 月 12 4.意味着制药公司可以将其新药申请(NDA)的完整部分提交给FDA审查,而不是等到NDA的每个部分都完成后才能对整个申请进行审查 。保密协议的审查通常要等到制药公司向FDA提交整个申请后才开始。

PK 桥接研究表明,MM120 ODT 的产品特性得到增强 1 对比 PK Profile 2.5 MM120 胶囊的差异化性能 MM120 ODT MM120 ODT 2 2 起作用的速度加快 50% 1.5 3 17% 生物利用度提高 1 4 0.5 23%。AUC 0 5 0 2 4 6 8 10 12 14 16 18 20 22 24 减少胃肠道副作用时间(小时)1.公司对来自 MM120-101 研究的药代动力学数据的分析。PK 分析基于完成两次给药的 n=24 名受试者。2.基于达到大于 1 ng/mL 的目标浓度的时间。3.基于 曲线下总面积的几何平均比率的比较。投资者演示文稿 | 2024 年 3 月 13 日 4.基于平均AUC的比率。目标浓度定义为高于该水平会出现感知效应。>1ng/mL 5。基于 GAD 中 MM120 胶囊的 2b 期研究与 MM120 ODT 的 PK 桥接研究的 比较:曲线下方区域;胃肠道;ODT:口服溶解片;PK:药代动力学 MM120 浓度 (ng/mL)
在大量未满足的需求和成熟的扩张途径的推动下,MM120 迎来了引人注目的商业机遇。大量未满足的需求市场显著成熟的一流报销商业概况框架潜在的庞大而强劲的增长价值基础设施主张投资者演讲 | 2024 年 3 月 14

KOL 对 GAD 影响和未满足需求的看法 Rakesh Jain,医学博士,MPH 德克萨斯理工大学医学院二叠纪盆地精神病学和行为科学临床教授

对 GAD 影响和未满足需求的看法 • GAD 对患者生活的许多方面都有负面影响,这种影响随着严重程度而增加 • GAD 本质上是慢性的,会随着时间的推移而恶化,通常会出现其他精神疾病 1 • 焦虑作为大脑 健康障碍的主要驱动因素重新成为人们关注的焦点 • 当前药物对患者的治疗不足 1 • GAD 患者表示渴望新的治疗方案 2 • GAD 的创新有限几十年来-Cymbalta 最后一款获准用于 GAD 的药物(2007 年 2 月) • 目前的治疗方法通常不是有效或耐受,可能需要多个周期的切换和剂量调整 3 • LSD 数十年的精神疾病临床研究支持其独特的潜力 1. “儿童和青少年的焦虑:筛查”(2022年)。美国预防服务工作组;“成人焦虑症:筛查” 建议草案(2022年)。美国预防服务工作组 部队。2.基于 MindMed 在 2023 年进行的患者研究。投资者演示文稿 | 2024 年 3 月 16 日 3. https://investor.lilly.com/news-releases/news-release-details/fda-approves-cymbaltar-treatment-generalized-anxiety-disorder #. 4.Rucker 2016, Gasset 2014,Holze、Gasser 等人,2023 年 4 月 UHB 演讲。

广泛性焦虑症概述广泛性焦虑症 (GAD) 焦虑流行病学 •• 以持续10%的患病率为特征的流行性疾病在过去二十年中增长了两倍,并且对生活的各个方面过度担忧 • 女性比男性更常见(~ 2:1)• GAD 患者通常难以控制焦虑,导致严重的困扰发作通常发生在青春期或成年初期,日常功能受损 • 常见的合并精神疾病, 例如 • 通常表现为伴有躁动、疲劳、重度抑郁症和其他焦虑症难以集中注意力、易怒、肌肉紧张和睡眠障碍 nd • 18 至 65 岁成年人中最常见的 2 种精神障碍投资者演示文稿 | 2024 年 3 月 17 日

GAD 对患者生活的许多方面产生负面影响, 随严重程度而增加 按严重程度划分的平均健康公用事业指数 GAD 对患者的影响 40 (25) 日常生活中的残疾 Revicki 等人 (2008) 投资者演示文稿 | 2024 年 3 月 18 日

GAD 本质上是慢性的,会随着时间的推移而恶化,通常早于 其他 1 种精神疾病药物使用恐慌症 MDD 自发作以来的时间 1.焦虑与抑郁之间的关键关系——2020 年 5 月 1 日 https://doi.org/10.1176/appi.ajp.2020.20030305 投资者演示文稿 | 2024 年 3 月 19 严重程度和合并症

随着主流对焦虑的关注回归,患者 当前药物的治疗仍然不足 人群推荐等级 8 岁儿童和青少年 USPSTF 建议对 B 1 18 岁儿童和 8 至 18 岁的青少年进行焦虑筛查。USPSTF 建议对成人、64 岁或以下的成年人 B 2(包括孕妇和产后人士)进行焦虑筛查。USPSTF推荐的 “B” 级建议表明:“USPSTF推荐该服务。可以肯定的是, 净收益是中等的,或者可以肯定净收益是中等到可观的。”一般是前线,50% 的失败率,3. 性副作用可以持久 1.“儿童和青少年的焦虑:筛查” (2022)。美国预防服务工作组。2. “成人焦虑症:筛查” 建议草案(2022年)。美国预防服务工作队。1.“儿童和青少年的焦虑: 筛查”(2022年)。美国预防服务工作组投资者演示文稿 | 2024年3月20日 2. “成人焦虑症:筛查” 建议草案(2022年)。美国预防服务工作组 部队。3.安萨拉,心理健康诊所,2020年11月;10(6):326-334)。fda.gov/。美国人口普查局,公司计算。

GAD 患者表示渴望新的治疗方案 1 GAD 患者当前 SOC 报价的局限性 他们告诉我,这种药物需要 6 周才能起到缓效作用。我不想再有 6 周有这样的感觉如果我与药物不一致,或者用完一天,Non-Durable Activity 停药一天会让我感觉很糟糕。我的目标是缓解,我不想与服用 Limited Response 药丸起作用有关系。我不喜欢性副作用,感觉就像药物中的副作用 负担僵尸。1.基于 MindMed 在 2023 年进行的患者研究。投资者演示文稿 | 2024 年 3 月 21 日 GAD:广泛性焦虑症;SOC:护理标准

目前的治疗通常无效或不能耐受, 可能需要多个周期的转换和剂量调整初级保健随访、每日口服诊断 + 处方药转换和剂量患者治疗调整投资者演示文稿 | 2024 年 3 月 22 日来源:。公司市场 研究。

LSD 数十年的精神疾病临床研究支持其 独特的潜在投资者演讲 | 2024 年 3 月 23 日

MM120 LSD-D-酒石酸盐治疗广泛性焦虑症 (GAD) 2b 期试验 完整结果摘要 Daniel R Karlin,医学博士,马萨诸塞州首席医学官

GAD 2b 期研究的 12 周积极结果显示:单剂量 MM120 后效果强 耐久性 1 • 达到具有统计学意义的主要和所有次要终点 • MCP-Mod 分析结果支持 GAD 3,4 中 MM120 的剂量反应关系 • 12 周时观测到的 d=0.81 的 效应大小是护理标准的两倍多 o 单剂后耐久性至少 3 个月 MM120 已观察 • 在统计学和临床上均显著改善 HAM-A 分数在第 12 周的 21.9 分(p=0.0025)表示 3与四周的头号数据相比,进一步改善 o 临床活性快速持久,在 12 周观察期内,临床缓解率持续改善 5 至 48% 2 o 第 12 周所有分析的次要终点均有显著改善 • MM120 耐受性良好,无相关的严重不良事件 o 与药物类别和先前的研究一致,多为短暂的、轻度至中度的不良事件 6 o 无 药物相关严重不良事件 (SAE) 且没有与自杀相关的安全信号 • 长期支持单次给药 MM120 的耐久性,我们认为这进一步支持将 100 µg MM120 推进 GAD 1 的第 3 阶段开发。 来源:研究 MMED008 内部研究文件和计算。报告了 100 µg 剂量组与安慰剂的个体组结果。2.代表第12周顶线分析中所有分析的次要终点,包括HAM-A、CGI-S和MADRS。 3。基于 100 µg 剂量组;HAM-A 分数基于 ANCOVA LS 平均值。效应大小基于研究统计学家使用组间的 LS 均值变化和各组期末 HAM-A 分数的合并标准差进行的事后计算。4. 检查所有研究的基线组分配(20项研究使用HAM-A(汉密尔顿焦虑量表),1项研究使用PARS(小儿焦虑量表)进行主要结局测量。资料来源:RB Hidalgo,J Investor 演示文稿 | 2024 年 3 月 25 日 Psychopharmacol。2007 年 11 月;21 (8): 864-72. 5.缓解的定义是 HAM-A 分数为 ≤7. 6。根据报告的不良事件进行自杀性评估。

MM120 的 2b 期试验采用标准 GAD 设计和终点, 1 与 FDA 药物类别指南草案一致 • 标准 GAD 研究设计,其终点支持批准药物的注册 • 随机、双盲、安慰剂对照 12 周试验 o 单次给药 MM120 或安慰剂 o 不进行心理治疗干预 2 o 试验设计与随后发布的 FDA 2023 年焦虑药物治疗患者指南草案紧密一致进行随机分组 • 入组 198 名 GAD 患者 • 五臂患者采用 1:1:1:1:1 随机分配的剂量优化设计 • 主要终点:第 4 周汉密尔顿焦虑量表 (HAM-A) 的变化 o 由对治疗分配和就诊次数 1 视而不见的中心评估员进行评估。来源:研究 MMED008 内部研究文件和计算。投资者演示文稿 | 2024 年 3 月 26 日 2.FDA 2023 年指南草案:迷幻药物:临床研究注意事项。

1 2b 期试验示意图共有 198 名参与者(实际)研究 MMED008 | GAD 第 8 周 12 -5 至 -1 1 2 4 A 2b 期全剂量随访筛查中单剂量 MM120 的剂量优化研究 MM120 200 µg 关键进入标准 MM120 100 µg • 男性和女性 • 年龄 18-74 MM120 50 µg • GAD MM120 25 µg 的诊断 • HAM-A ≥ 20 安慰剂额外安慰剂端点 • MADRS• EQ-5D-5L • CGI-S/I• PSQI 随机化主要终点次要终点 • PGI-S/C• ASEX (HAM-A) (HAM-A) (HAM-A) • SDS 1. MM120来源:MMED008 研究内部研究文件。μg:微克;HAM-A:汉密尔顿焦虑评级量表;MADRS:蒙哥马利-阿斯伯格抑郁评级量表;CGI-S:临床全球印象- 严重程度;PGI-S:患者全球印象——投资者报告 | 2024 年 3 月 27 日严重程度;SDS:希恩残疾量表;EQ-5D-5L:EuroQol-5 维度;PSQI:匹兹堡睡眠质量指数;ASEX:亚利桑那州性行为指数体验规模

2b 期治疗模式:独立药物效应,第 1 种心理治疗干预措施 • 房间内给药监测 (DSM) 不提供心理治疗干预 2 • 交付方案与 2023 年 FDA 指南草案一致 • 治疗后治疗期间 2 期和第 3 阶段预治疗之间未计划更改药物递送 ✓ 全面的知情同意程序 ✓ 由 dSM 持续监测 ✓ 随访仅用于评估的患者 ✓ 资格评估 ✓ 音乐、眼睛 shades、reading,在 MMED008 中写作《旅程》✓当出院标准满足时得出结论 x 没有 “准备” x 没有 “辅助治疗” x 没有 “整合” 不是 x 预治疗活动中的患者旅程 包括 x 没有心理治疗,也没有治疗 x 没有持续的治疗参与,因为临床试验活动中研究药物部分之外的 MMED008 全面知情同意程序干预 1.来源:研究 MMED008 内部研究 文件。投资者演示文稿 | 2024 年 3 月 28 日 2.FDA 2023 年指南草案:迷幻药物:临床研究注意事项。
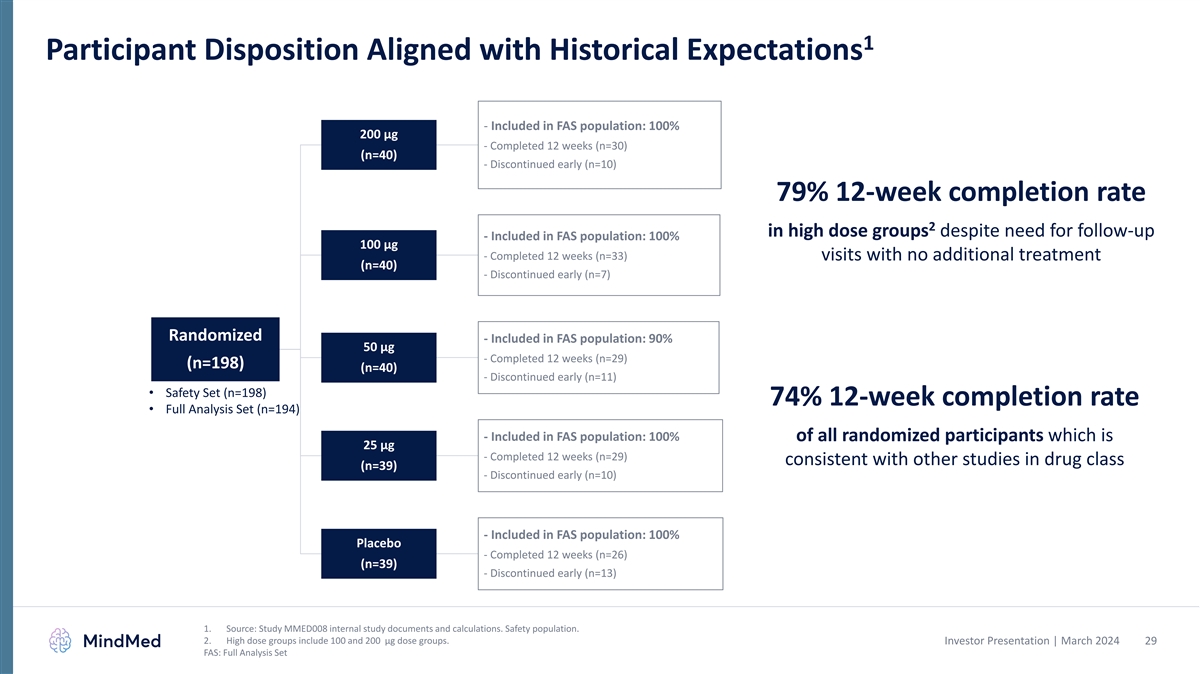
1 参与者的倾向符合历史预期- 包括在 FAS 人群中:100% 200 µg-已完成 12 周 (n=30) (n=40)-尽管需要随访,但仍提前停止 (n=10) 12 周完成率 79% 2-包括在 FAS 人群中:100% 100 µg-已完成 12 周 (n=33) 次就诊 (n=40)-提前停诊 (n=7)) 随机化-包含在 FAS 人群中:90% 50 µg-已完成 12 周 (n=29) (n=198) (n=40)-提前停产 (n=11) • 安全套装 (n=198) 74% 12 周 完成率 • 已满分析集(n = 194)-包含在 FAS 人群中:100% 的随机参与者,即 25 µg-完成了 12 周(n = 29),与其他药物类别的研究(n=39)一致-提前停止(n = 10)- 包含在 FAS 人群中:100% 安慰剂-完成 12 周(n = 26)(n = 39)-提前停止(n = 13)1。来源:研究 MMED008 内部研究文件和计算。安全人群。2.高剂量组包括 100 和 200 微克剂量 组。投资者演示文稿 | 2024 年 3 月 29 日 FAS:完整分析集

参与者人口统计学和基线特征 各组均衡 1 MM120 安慰剂人口统计 (n=194) 25 µg 50 µg 100 µg 200 µg (n=39) (n=36) (n=40) (n=40) (n=39) (n=39) (n=39) 平均年龄 38.0 45.3 42.7 38.7 性别、女性 (%) 51.3% 40.0% 70.0% 60.0% 6% 6.7% 种族(% 白人)84.6% 80.6% 90.0% 82.5% 76.9% 基线 HAM-A 分数 30.2 30.3 29.3 31.0 30.3 30.3 30.3 30.3 30.3 基线 CGI-S 分数 4.9 4.9 4.9 4.9 1。来源:研究 MMED008 内部研究文件和计算。完整的分析集合群体。投资者演示文稿 | 2024 年 3 月 30 日

HAM-A 评分在统计学和临床上均显著下降 为第 12 周 HAM-A 与基线 2 0 相比变化 • 第 4 周:-21.3 分 • 第 12 周:-21.9 分 -5 2 比安慰剂 -10 改善 • 第 4 周:-7.6 分,p=0.0004 • 第 12 周:-7.7 分,p=0.003 -15 -20 *** *** *** -25 ** ** **p
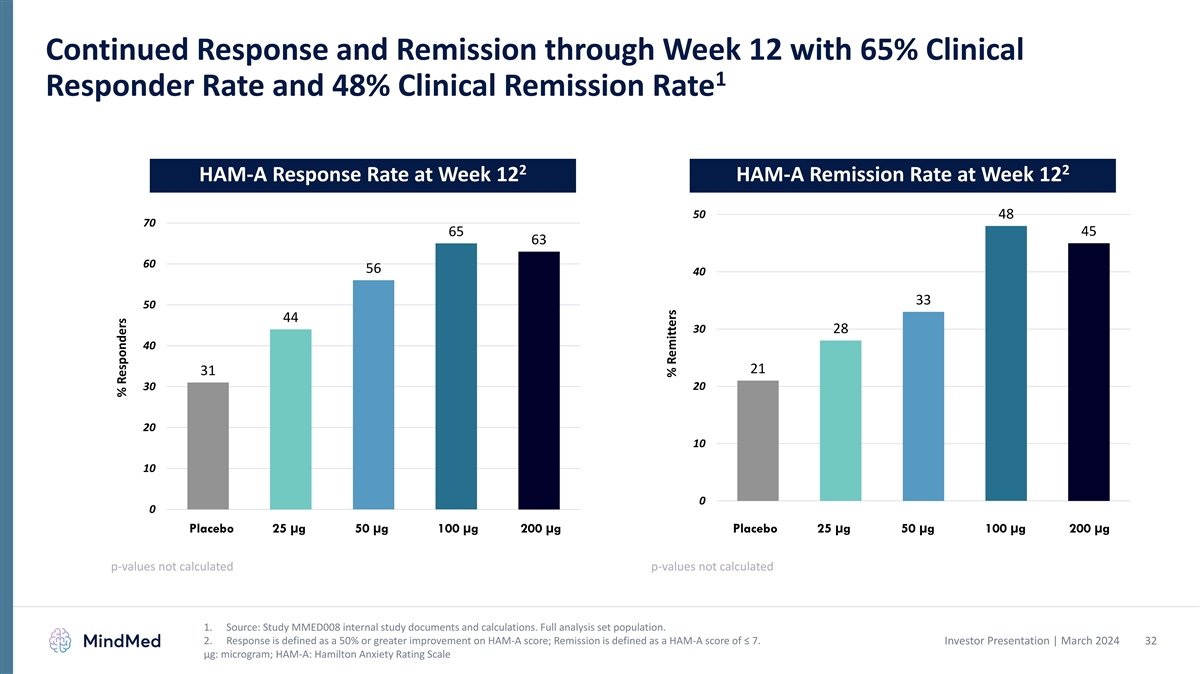
在第 12 周持续反应和缓解,临床 1 反应者率为 65%,临床缓解率为 48% 2 2 HAM-A 第 12 周的缓解率 HAM-A 缓解率 12 周 50 48 70 65 45 63 60 56 40 33 50 44 30 21 31 30 20 10 10 0 0 0 安慰剂 25 µg 50 µg 100 µg 200 µg 安慰剂 25 µg 50 µg 100 µg 200 µg p值不是计算出的 p 值未计算 1。来源:研究 MMED008 内部研究文件和计算。完整分析集合群体。2.反应定义为比 HAM-A 分数提高 50% 或以上;缓解定义为 HAM-A 分数小于 7。投资者演示文稿 | 2024 年 3 月 32 μg:微克;HAM-A:汉密尔顿焦虑评级量表受访者百分比汇款人

主要和关键二次分析 (MCP-Mod) 支持剂量反应 1 GAD 2 中 MM120 的关系 MCP-Mod 分析的关键要点 • 具有统计意义的剂量反应关系,多模型拟合的剂量反应关系具有统计学意义 • 支持 GAD 后续研究的剂量选择 100 µg • 预先指定的模型估计值和观察到的反应驱动 3 期研究剂量 1 的剂量选择。来源:研究 MMED008 内部研究文件和计算。完整分析集合群体。2.来源:诺华。“MCP-Mod 方法 — 剂量反应的统计方法。投资者演示文稿 | 2024年3月 33"模型意味着

全球临床印象快速持续改善 — 严重程度 1 (CGI-S) 从第 2 天开始一直持续到第 12 周 2 CGI-S 第 12 周 100 µg 组 CGI-S 分数有所改善 6 — 重病 • 到第 2 天和第 5 天统计学和临床均有显著改善 — 在第 12 周一直保持不变 4 — 中度疾病 • 到第 12 周 CGI-S 评分改善幅度超过 2 个单位 **** 3 — 轻度疾病 *** • 参与者平均只有 2 人 — 第 12 周处于临界病情的临界病情到轻度疾病 1 — 正常,基准第 2 天根本没有生病第 4 周第 12 周安慰剂 100 µg *p
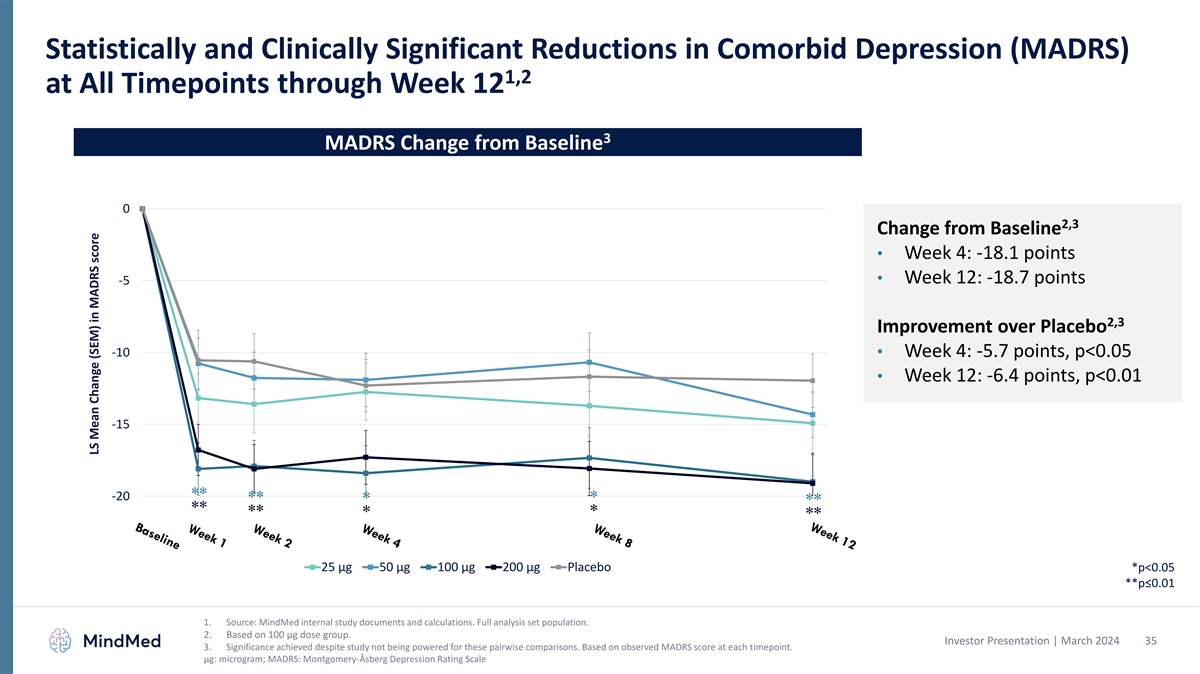
截至第12周的所有时间点,合并症 抑郁症(MADRS)1,2 的统计学和临床显著下降 3 MADRS 与基线的变化 0 2,3 与基线相比变化 • 第 4 周:-18.1 点 • 第 12 周:-18.7 点 -5 2,3 比安慰剂改善 -10 • 第 4 周:-5.7 点,p

MM120 耐受性良好,多为短暂性、轻度至中度 不良事件,符合药物类别预期 • 几乎所有 AE(99%)的严重程度均为轻度至中度良好的耐受性 • 极少(2.5%)TEAE 导致研究退出概况 2 • 没有与药物相关的严重不良事件 (SAE) 无关 • 只有 SAE 在 50 µg 剂量组中,被视为无关的研究药物 • 不良事件概况一致包括历史研究和药物类别 • 没有自杀或自残行为没有自杀 行为 • 每只手臂 ≤ 2 名参与者在研究期间报告了自杀意念3或自杀信号 •没有自杀或自杀相关风险增加的迹象 1.来源:研究 MMED008 内部研究文件和 计算。安全人群。2.在50 µg剂量组中观察到一种严重的不良事件(SAE):研究日第98天的惊恐发作,被认为与治疗无关。投资者演示文稿 | 2024 年 3 月 36 3.根据报告的不良事件进行自杀性评估 。

高剂量组中最常见 (≥ 10%) TEAE 表现出良好的1,2 耐受性 MM120 首选术语安慰剂 (n=39) 25 µg 50 µg 100 µg 200 µg (n=39) (n=40) (n=40) (n=40) (%) 有 AE DD AFT DD AFT DD AFT DD AFT DD AFT DD AFT Illusion 12 (31) 1 (2.6) 18 (45) 1 (%) 2.5) 24 (60) 1 (2.5) 30 (75) — 3 (7.7) — 恶心 3 (7.7) — 11 (28) — 16 (40) 1 (2.5) 24 (60) 2 (5.0) 1 (2.6) 2 (5.1) 头痛 4 (10) 2 (5.1) 9 (23) 2 (5.0) 10 (25) 1 (2.5) 8 (21) 1 (2.6) 幻觉,视觉 6 (15) 1 (2.6) 9 (23) — 9 (23) — 6 (15) — 1 (2.6) — 欣快情绪 2 (5.1) — 5 (13) — 11 (28) — 6 (15) — 1 (2.6) — 焦虑 1 (2.6) 3 (7.7) 3 (7.5) 3 (7.5) 4 (10) — 5 (13) 1 (2.5) — 2 (5.1) Mydriasis 1 (2.6) — 7 (18) — 8 (20) — 4 (10) — 1 (2.6) — Hyperhiasis 1 (2.6) — 7 (18) — 8 (20) — 4 (10) — 1 (2.6) — Hyperhiasis 1 (2.6) — 4 (10) — 9 (23) — 5 (13) — — — 麻醉 2 (5.1) — 2 (5.0) — 2 (5.0) — 8 (20) — 2 (5.1) 1 (2.6) 血压升高 3 (7.7) — 5 (13) — 4 (10) — 4 (10) — — — 头晕 3 (7.7) — 2 (5.0) — 2 (5.0) — 3 (7.5) — 5 (13) — 1 (2.6) — 震颤 — — 3 (7.5) — 2 (5.0) 1 (2.5) 8 (20) — — — 思维异常 1 (2.6) — 2 (5.0) — 4 (10) 1 (2.5) 5 (13) — — — 假幻觉— — 3 (7.5) — 3 (7.5) — 4 (10) — — — 感觉 异常 1 (2.6) — 2 (5.0) — — — 4 (10) 1 (2.6) 1 (2.6) COVID-19 — 1 (2.6) — 2 (5.0) — 1 (2.5) — 4 (10) — — 1.来源:研究 MMED008 内部研究文件和计算。 安全人群。2.高剂量组包括 100 和 200 微克剂量组。投资者演示文稿 | 2024年3月37日AFT:给药日后;DD:给药日;TEAE:治疗紧急不良事件。

MM120 LSD-D-酒石酸盐治疗广泛性焦虑症 (GAD) MM120 ODT PK 桥接研究 Daniel R Karlin,医学博士,马萨诸塞州首席医学官
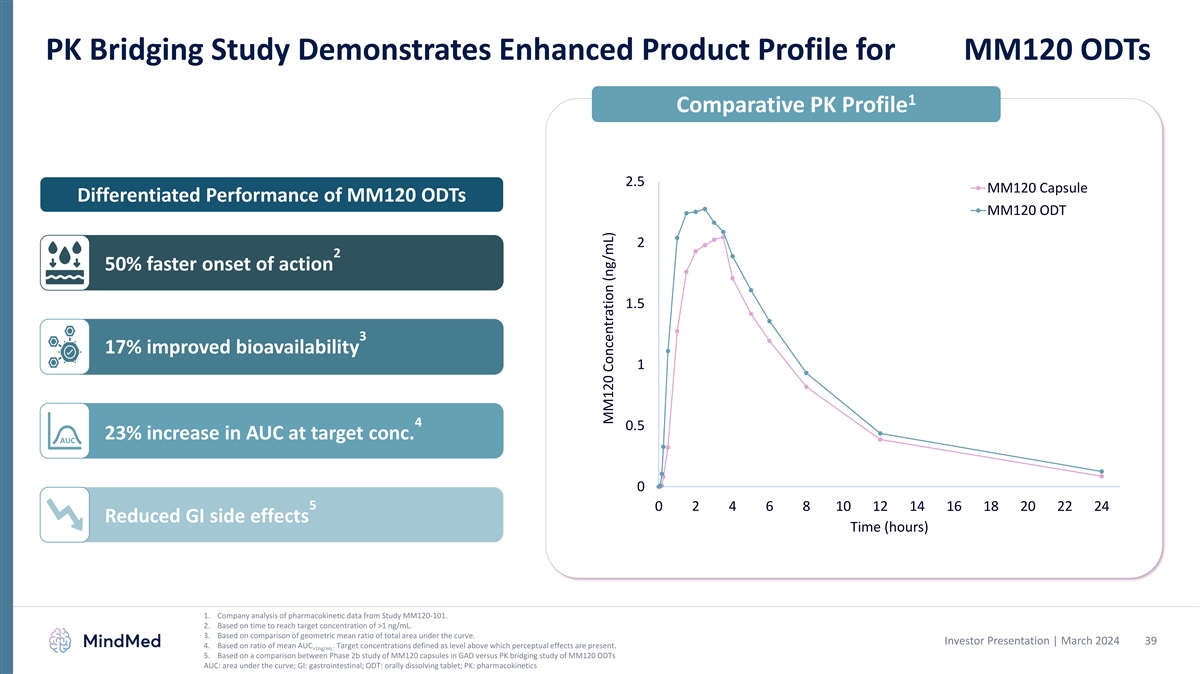
PK 桥接研究表明,MM120 ODTs 的产品特性得到增强 1 对比 PK Profile 2.5 MM120 胶囊的差异化性能 MM120 ODT MM120 ODT 2 2 起作用的速度加快 50% 1.5 3 17% 生物利用度提高 1 4 0.5 23%。AUC 0 5 0 2 4 6 8 10 12 14 16 18 20 22 24 减少胃肠道副作用时间(小时)1.公司对来自 MM120-101 研究的药代动力学数据的分析。2.基于达到大于 1 ng/mL 的目标浓度的时间。3.基于曲线下总面积的几何平均比率的比较。 投资者演示文稿 | 2024 年 3 月 39 4.基于平均AUC的比率。目标浓度定义为高于该水平会出现感知效应。>1ng/mL 5。基于 GAD 中 MM120 胶囊的 2b 期研究与 MM120 ODT 的 PK 桥接研究的比较 AUC:曲线下方区域;胃肠道;ODT:口服溶解片剂;PK:药代动力学 MM120 浓度 (ng/mL)

1 MM120 ODT PK 桥接研究示意性研究 MM120-101 | ODT-PK 共有 29 名参与者(实际)一项第一阶段开放标签研究,旨在比较两种制剂的药代动力学第 -21 天到 -1 1 2-13 14 15-29 的健康志愿者剂量 2 后续冲洗剂量 1 筛查 MM120 MM120 准入标准 Zydis ODT Zydis ODT • 男性和女性 (100 µg) (100 µg) • 年龄 18-55 岁 • 健康志愿者 • 无违禁药物 MM120 MM120 胶囊胶囊(100 µg)(100 µg)(100 µg)注册人数 1。MM120基于 MM120-101 研究投资者演示文稿的内部研究 文件 | 2024 年 3 月 40 日 ODT:口服溶解片剂

MM120 ODT 与胶囊的对比 PK 显示 1 MM120 ODTs 2.5 MM120 胶囊 MM120 ODT MM120 1 2 PK 参数 MM120 ODT 1.5 T (hr) 2.25 2.0 max C (ng/mL) 2.63 2.68 1 max AUC (ng*hr/mL) 15.7 18.7 0-Ÿ 0.5 AUC (ng*HR/mL) 9.7 12.0 >1ng/mL 0 2 4 6 8 10 12 14 16 18 20 22 24 时间 (小时)1.公司对来自 MM120-101 研究的药代动力学数据的分析。PK 分析基于完成两次给药的 n=24 名受试者。投资者演示文稿 | 2024 年 3 月 41 AUC:曲线下方区域;C:最大达到浓度; ODT:口服溶解片剂;PK:药代动力学;T:达到最大浓度的时间 MM120 最大浓度 (ng/mL)

MM120 ODT 表现出更快的吸收速度和更短的达到 目标浓度的时间 1.2 MM120 Capsule 1 MM120 ODT 的差异化 PK 分布图 MM120 ODT 1 2 起作用的速度快 50% 0.8 0.6 3 17% 生物利用度提高 0.4 4 0.2 23%,高于目标浓度 0.4 4 0.2 23%。AUC 0 0 10 20 30 时间(分钟)1. 公司对来自 MM120-101 研究的药代动力学数据的分析。PK 分析基于完成两次给药的 n=24 名受试者。2.基于达到大于 1 ng/mL 的目标浓度的时间。3.基于曲线下方 总面积的几何平均比率的比较。投资者演示文稿 | 2024 年 3 月 42 4.基于平均AUC的比率。目标浓度定义为高于该水平会产生感知效应。>1ng/mL AUC:曲线下方区域;ODT:口服溶解片剂; PK:药代动力学 MM120 浓度 (ng/mL)
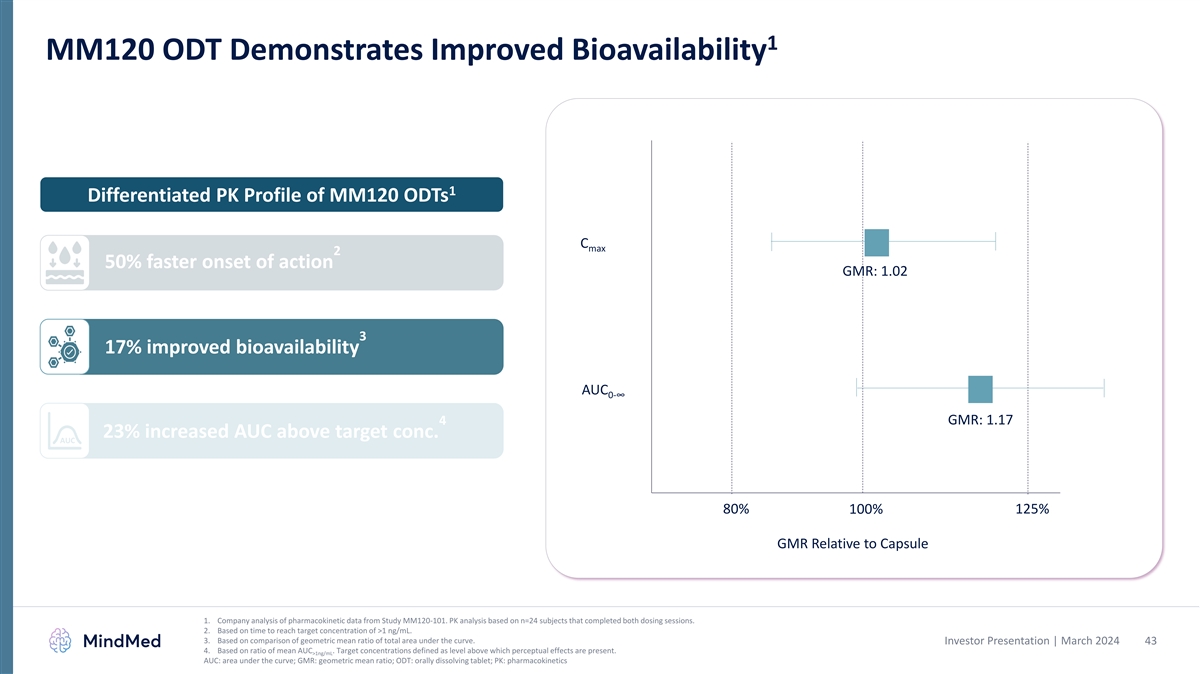
1 MM120 ODT 显示生物利用度得到提高 1 MM120 ODTs 的差异化 PK 概况起效速度最多快 2 50% GMR:1.02 3 生物利用度提高 17% AUC 0-Ÿ GMR:AUC 比目标浓度增加 1.17 4 23%。AUC 80% 100% 125% GMR 相对于胶囊 1。公司对来自 MM120-101 研究的药代动力学数据的分析 。PK 分析基于完成两次给药的 n=24 名受试者。2.基于达到大于 1 ng/mL 的目标浓度的时间。3.基于曲线下总面积的几何平均比率的比较。投资者 演示文稿 | 2024 年 3 月 43 4.基于平均AUC的比率。目标浓度定义为高于该水平会产生感知效应。>1ng/mL AUC:曲线下方区域;GMR:几何平均比率;ODT:口服溶解片剂;PK: 药代动力学
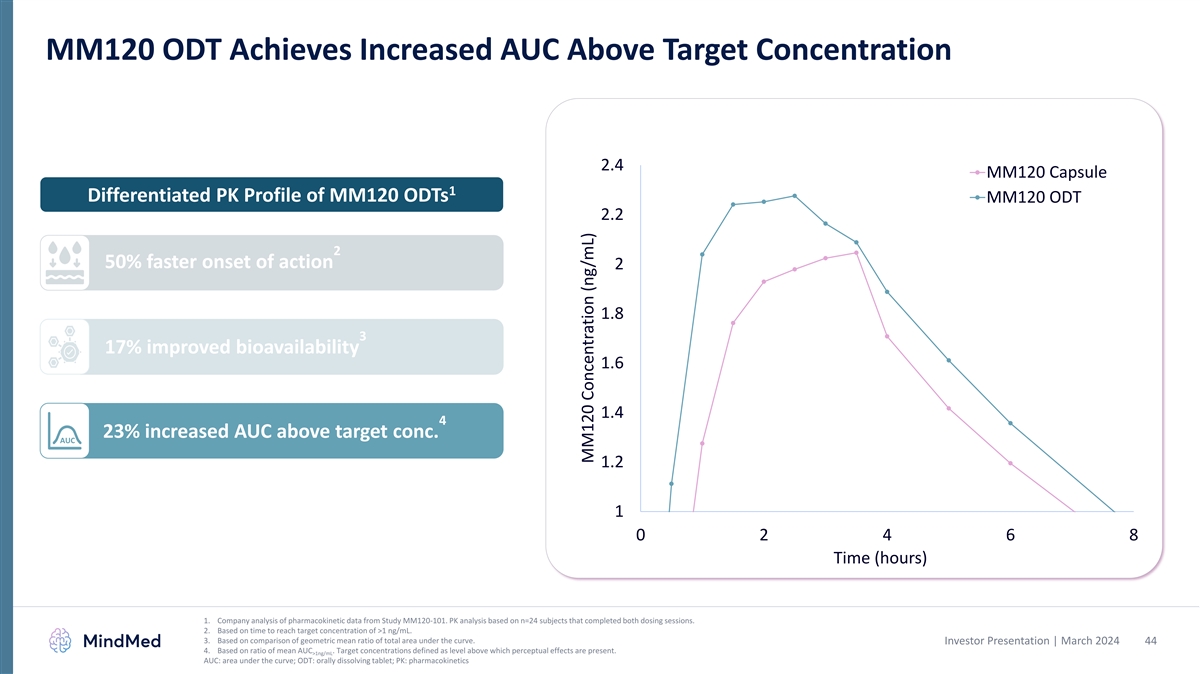
MM120 ODT 实现了高于目标浓度的 AUC 2.4 MM120 Capsule 1 差异化 MM120 ODT MM120 ODT 2.2 2 起作用的速度提高 50% 2 1.8 3 17% 生物利用度提高 1.6 1.4 4 23% AUC 高于目标浓度 1.6 1.4 4 23%。AUC 1.2 1 0 2 4 6 8 时间(小时)1.公司对来自 MM120-101 研究的药代动力学 数据的分析。PK 分析基于完成两次给药的 n=24 名受试者。2.基于达到大于 1 ng/mL 的目标浓度的时间。3.基于曲线下总面积的几何平均比率的比较。投资者 演示文稿 | 2024 年 3 月 44 4.基于平均AUC的比率。目标浓度定义为高于该水平会产生感知效应。>1ng/mL AUC:曲线下方区域;ODT:口服溶解片剂;PK:药代动力学 MM120 浓度 (ng/mL)

MM120 LSD-D-酒石酸盐商业机会弗朗索瓦·利林塔尔,医学博士, 工商管理硕士首席商务官

为 MM120 带来重大商业机会的关键因素已经到位 大量未满足的需求市场显著成熟的一流报销商业概况框架潜在的庞大而强劲的增长价值基础设施主张投资者演讲 | 2024 年 3 月 46

精神科医疗保健提供者预计迷幻药将从根本上改变焦虑和抑郁的 治疗方法% GAD 提供者同意所有提供商 2 Spravato 提供商 86% 84% 78% 74% 73% 62% 美国食品药品管理局批准的迷幻迷幻疗法的可用性将是有价值的我预计从根本上讲 焦虑和抑郁的迷幻疗法将是未来焦虑症的治疗选择,并改变焦虑症的治疗方式焦虑和改变我对待焦虑和抑郁的方式抑郁抑郁症 1.精神科医生和精神病学执业护士 2.来源:MindMed主要市场研究——Spravato® 提供商和GAD处方者的主要客户看法(2024年2月)。非 Spravato® 提供商总数(n=125),投资者演示文稿 | 2024 年 3 月 47 家 Spravato® 提供商(n=50)。3.Spravato 提供者:本人或其诊所或办公室的某个人推荐、推荐或处方 Spravato® 治疗,并监测或实施了 Spravato® 治疗。

MM120 的临床活动和 的总体概况给大多数精神科医生留下了深刻的印象 1,2% 的精神科医生对 MM120 留下了深刻的印象 87% 87% 86% * 73% 总体临床活动起始耐久性总体印象(HAM-A 降低)(第 2 天的 CGI-S)(第 12 周的 HAM-A)1。来源:MindMed 主要市场研究——Spravato® 提供商和GAD处方者的主要客户看法(2024年2月)。非 Spravato® 提供商总数(n=125)、Spravato® 提供商总数(n=50)。投资者演示文稿 | 2024 年 3 月 48 2. 精神科医生和精神科执业护士 CGI-S:临床全球印象——严重程度;HAM-A:汉密尔顿焦虑量表
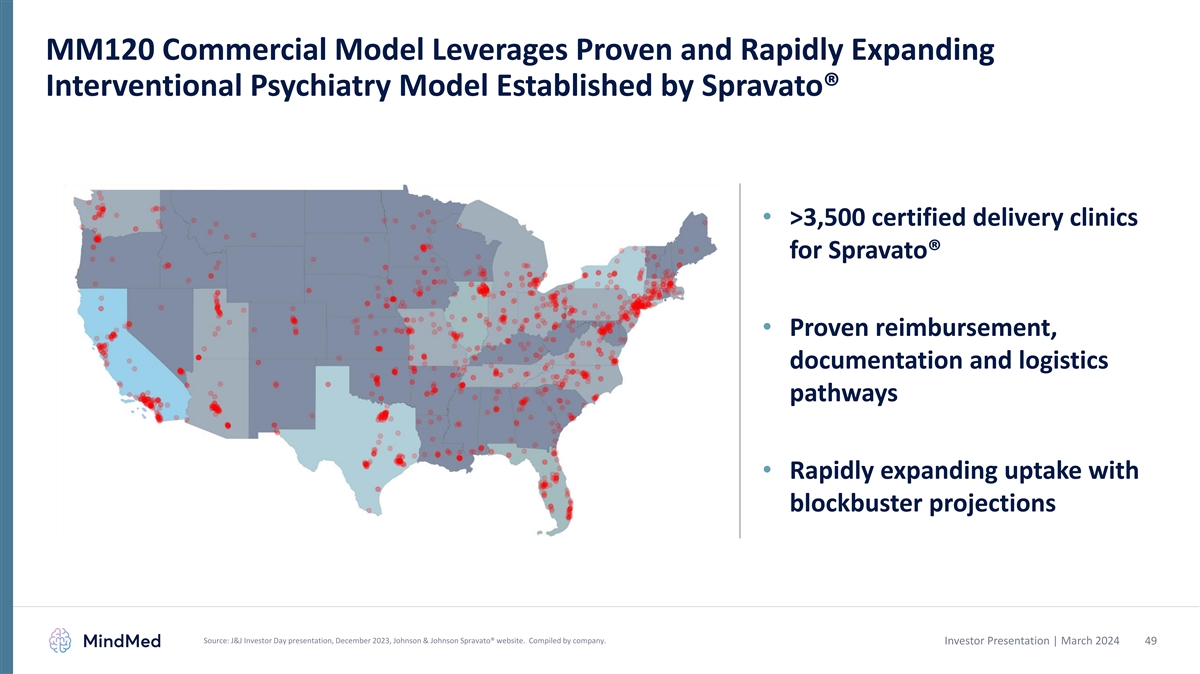
MM120 商业模式利用由 Spravato® 建立的成熟且快速扩展的 介入精神病学模型 • 超过 3,500 家经认证的 Spravato® 分娩诊所 • 行之有效的报销、文件和物流途径 • 通过轰动一时的 预测迅速扩大吸收率来源:强生投资者日演讲,2023 年 12 月,强生 Spravato® 网站。由公司编写。投资者演示文稿 | 2024 年 3 月 49

患者护理和报销的行之有效的途径已经存在 诊断 + 处方治疗药物患者精神科医生/由持牌分销商通过专业分销商 1 2 处方 HCP 药房报销付款人 1 进行监测。获准向患者开药的HCP。2.获得 执业许可的HCP,其中可能包括医生、临床心理学家、执业护士、护士、持牌临床社会工作者、持牌家庭和投资者演示| 2024年3月50名婚姻治疗师等。

为所有利益相关者制定了报销途径,包括 药品和疗程配送年度费用 Spravato® 利益相关者报销/编码活动本地或远程医疗福利 3 高达 1,200 美元的评估和处方 1 处方者 E&M 代码 (992XX) 或 G 代码 4 ~25,000 美元 — 通过药房福利药品生产的 62,000 美元制造商,不包括折扣和专业药房 J 或 S 代码 + 配药费返还给当地 HCP 的医疗福利 2 E&M Code 5 最高 17,000 美元会话交付监护治疗长期按小时报销 临床疗程人员服务 1.获准向患者开药的HCP。2.获得执业许可的HCP,可能包括医生、临床心理学家、执业护士、护士、持牌临床 社会工作者、持牌家庭和婚姻治疗师等。3.基于最多8次评估访问,假设每次访问费用为150美元。MM120 的 CPT 代码和补偿尚未确定。投资者演示文稿 | 2024 年 3 月 51 4. 制造商价格基于每次 2 或 3 个罐子乘以每年 34 到 56 次疗程。MM120 的 CPT 代码和补偿尚未确定。5.基于长达112小时的所需监测,报销费约为每小时150美元(来源:MindMed初步研究)。MM120 的 CPT 代码和补偿尚未确定。

与 Spravato® 相比,MM120 在 临床和疗程交付方面均具有显著优势 1 2 MM120 活动耐久性 1 周或更短 3 个月 + 接受治疗的时间长达 112 小时 ~ 8 至 32 小时/年治疗次数最多 56 次 1 至 4 次疗程/年最多 56 次提交 1-4 次提交保险和 REMS 负担 REMS 要求的 2b 期研究效果中良好的耐受性生理侧心率监测监控 1.基于 Spravato 处方信息和 Spravato REMS 下包含的信息 ,网址为 https://www.spravatorems.com。2.如果 MM120 获得 FDA 批准并上市。耐久性、耐受性和相关的治疗间隔假设基于投资者演示文稿中显示的统计学显著下降 ,2024 年 3 月 52 日 2b 期临床试验 MMED008 的第 12 周为哈姆-A。假设每次 MM120 给药会话平均监测 8 小时。
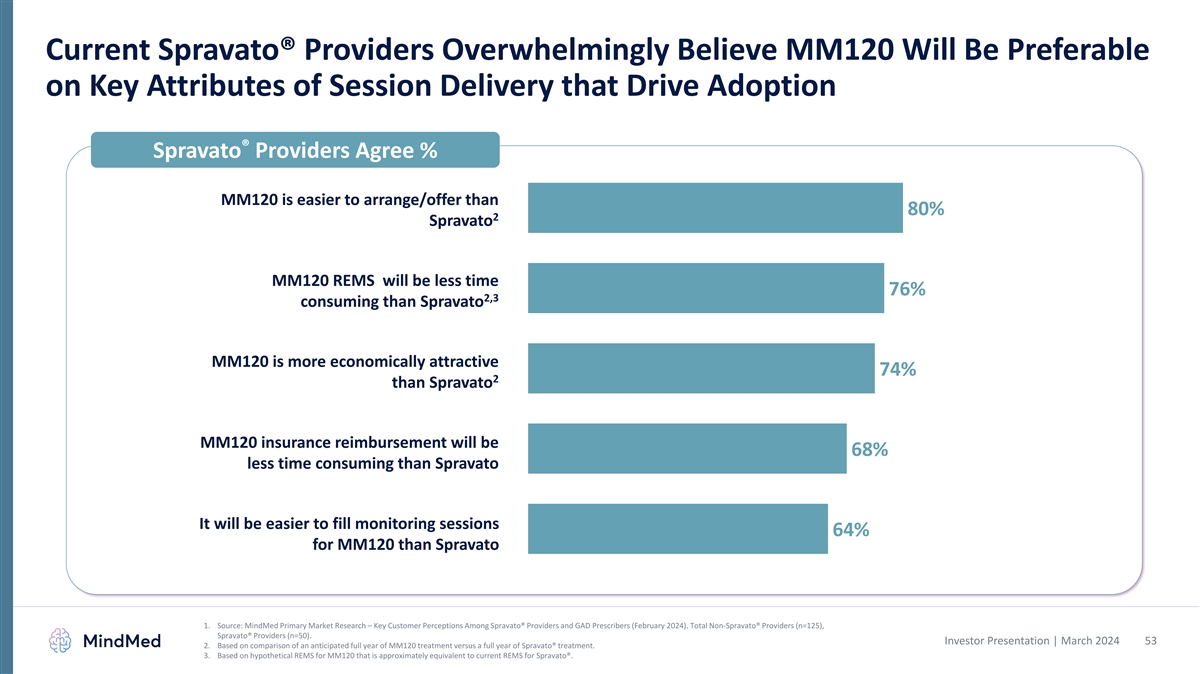
当前 Spravato® 提供商压倒性地认为,在推动采用的会话交付的关键属性上,MM120 将更受欢迎® Spravato 提供商同意 MM120 比 80% 更容易安排/提供 2 Spravato MM120 REMS 将比 Spravato 少 76% 2,3 耗时 76% MM120 更具经济效益 比 Spravato MM120 保险报销耗时少 68% 比 Spravato 1 更容易填充 MM120 的 64% 的监控会话。来源:MindMed 主要市场研究——Spravato® 提供商和 GAD 处方者的主要客户看法(2024 年 2 月)。非 Spravato® 提供商总数(n=125)、Spravato® 提供商总数(n=50)。投资者演示文稿 | 2024 年 3 月 53 2.基于预期全年的 MM120 治疗与全年 Spravato® 治疗的比较。3.基于假设的 MM120 REMS,该系统大致相当于当前 Spravato® 的 REMS。

® 当前 Spravato 提供商中的绝大多数 Spravato 提供者表示他们可能会转诊,1 开处方和给药 MM120 92% 84% 当前的 Spravato® 提供者可能会推荐当前 Spravato® 提供者可能为 2 2 名患者开出 MM120 处方并给药 MM120 1。来源:MindMed 初级市场研究 — Spravato® 提供商和 GAD 处方者的主要客户看法(2024 年 2 月)。非 Spravato® 提供商总数(n=125)、Spravato® 提供商总数(n=50)。投资者演示文稿 | 2024 年 3 月 54 2.如果 MM120 获得 FDA 批准 并上市。

付款人对 MM120 潜在价值的看法 反应的可预测性早期耐受性和依从性持续减少治疗过程中的焦虑可以支持低浪费和合并症降低资源的有效利用预算影响医疗利用率和成本负担 2 1 3 治疗过程早期反应的可预测性行为健康问题推动成本... 当你考虑行为健康的发展可以有效利用空间时,所有雇主都对此感兴趣。我说得还不够 。... 我们有观察覆盖范围、资源心理评估覆盖范围、E&M 守则... 先例包括 Spravato、睡眠 “研究... 如果获得 FDA 批准,需求未得到满足,就会得到保障... 1 — BCBS 区域付款人来源:公司与美国付款人进行了定性研究;MindMed 2023 分析师日。投资者演示文稿 | 2024 年 3 月 55

GAD 通过推动员工脱离参与度 和被诊断为严重的工作生产力损失对雇主产生重大影响 1 群组控制 2 GAD • MM120 的潜在影响不仅限于直接的健康益处,还会推动广义缺勤率 6.0% 21.0% 主张 • 雇主在Presenteism 中发挥重要作用 14.1% 47.5% 推动报销工作 16.4% 53.0% 生产力损失来源:NHWS 2022年年度调查 1.根据 GAD-7 衡量的没有 GAD 症状的普通人群投资者演示文稿 | 2024 年 3 月 56 2 由 GAD-7 测得的严重症状

推进重点战略,为 MM120 提供商业机会 教育利益相关者最大限度地提高准入以及关于 GAD 和 MM120 报销的信息 MM120 价值主张将 MM120 会话交付纳入当前基础设施投资者演示文稿 | 2024 年 3 月 57

MM120 发展计划摘要评论罗伯特·巴罗首席执行官 执行官

多项研究支持 MM120 1 的第 3 期开发 • 实现了 2 期开发的目标 o 为GAD中的剂量选择提供信息的特征剂量反应 o GAD 中具有统计学意义且具有临床意义的效果 o 在没有心理治疗干预的情况下对经过验证的终点 o 独立药物效果具有快速和持久的治疗益处 • 多项支持 MM120 o 2b 期随机、安慰剂对照试验活性的双盲、安慰剂对照研究在 GAD(研究 MMED008)o 一个前现代的 中,焦虑症中麦草吉的随机、安慰剂对照IIT o 超过二十多项关于麦角苷治疗焦虑症和其他神经质疾病的传统研究 • 2b 期数据支持剂量选择和进入第 3 阶段开发 1。来源:研究 MMED008 内部研究文件和计算。投资者演示文稿 | 2024 年 3 月 59

MM120 开发途径 1 • 两项三期关键临床试验 计划进行为期 12 周的随机、安慰剂对照的主要疗效研究设计 o 开放标签延期,以确定再治疗参数 o 预计将于 2024 年下半年启动 3 期开发 • 第 4 周汉密尔顿焦虑量表 (HAM-A) 的 2b 期和 3 期研究的关键设计要素预计将保持一致 预期主要终点 o 关键纳入/排除标准的变化有限 o 未计划更改剂量会话监控协议 1。第 3 阶段和 后续临床研究设计尚待监管讨论和审查,包括可能的第 2 阶段结束会议。投资者演示文稿 | 2024 年 3 月 60

MM120 和管道项目的下一步措施和预期里程碑 2024 年第一季度第二季度 2024 年第四季度 MM120 GAD MM120 GAD 第 2b 期/12 周科研会议上的完整数据介绍 MM120 GAD Zydis ODT PK 桥接数据 MM120 GAD MM120 GAD 第 3 阶段启动会议与 FDA MM120 评估 UHB 赞助)Topline 投资者演示文稿 | 2024 年 3 月 61 日 MM120

问答投资者演示文稿 | 2024 年 3 月

附录

1,3 65% HAM-A 回复率 (HAM-A) 在第 12 周达到 HAM-A 一段时间内的回复率 90 78 78 78 80 75 70 68 70 68 65 63 58 60 54 53 51 50 50 50 50 50 47 44 44 38 31 31 31 30 20 10 0 第 1 周第 4 周 12 p 值未计算安慰剂 25 µg 50 µg 100 µg 200 µg 1。 来源:研究 MMED008 内部研究文件和计算。完整分析集合群体。2.回应定义为HAM-A分数提高50%或以上。投资者演示文稿 | 2024 年 3 月 3.基于 100 µg 剂量组。μg: 微克;HAM-A:汉密尔顿焦虑评级量表。受访者百分比

1,3 48% 的缓解率 (HAM-A) 在第 12 周达到 HAM-A 一段时间内的缓解率 60 50 50 48 45 45 45 45 45 43 40 38 33 33 33 33 33 33 33 33 33 33 28 26 25 21 21 21 20 18 15 10 0 第 1 周第 4 周第 8 周 p 值未计算安慰剂 25 µg 50 µg 100 µg 200 µg 1。来源: Study MMED008 内部研究文件和计算。完整分析集合群体。2.缓解的定义是 HAM-A 分数为 ≤ 7。投资者演示文稿 | 2024 年 3 月 3.基于 100 µg 剂量组。μg:微克;HAM-A:汉密尔顿 焦虑评级量表。% 汇款者

临床全球印象有统计学上的显著改善 — 严重程度 (CGI-S) 1,2 分在第 2 天达到,并持续到第 12 周 CGI-S 分数 6 — 重病 5 — 严重疾病 4 — 中度疾病 * *** * *** * * *** 2 — 临界疾病 1 — 正常,不是基线第 2 周第 2 周第 4 周第 8 周 12 完全没病 *p
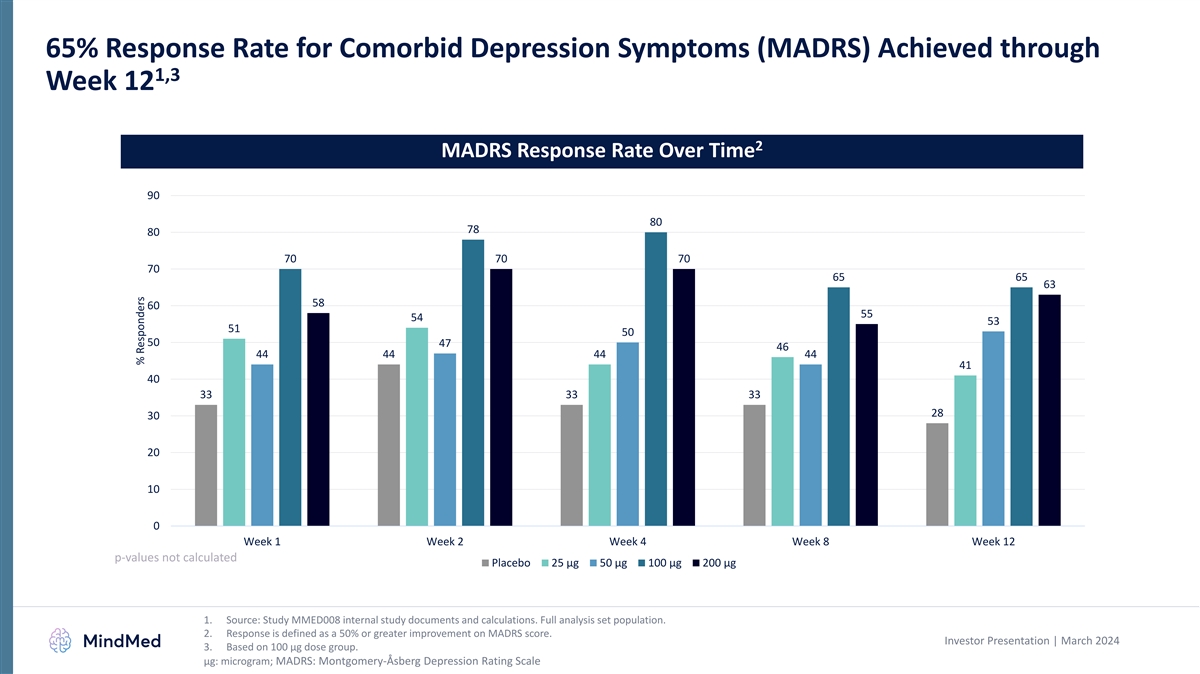
抑郁症合并症状(MADRS)的反应率为 65%,通过1,3 周 12 2 MADRS 在一段时间内的反应率达到 90 80 70 70 70 70 70 65 65 63 58 60 54 53 51 50 47 44 44 44 44 44 44 41 40 33 33 33 30 10 0 第 2 周 4 周 8 周 12 p 值未计算安慰剂 25 µg 100 µg 200 µg 1。来源:研究 MMED008 内部研究文件和计算。完整分析集合群体。2.回应定义为MADRS分数提高50%或以上。投资者演示文稿 | 2024 年 3 月 3.基于 100 µg 剂量组。μg:微克;MADRS:蒙哥马利-阿斯伯格抑郁评级量表受访者百分比
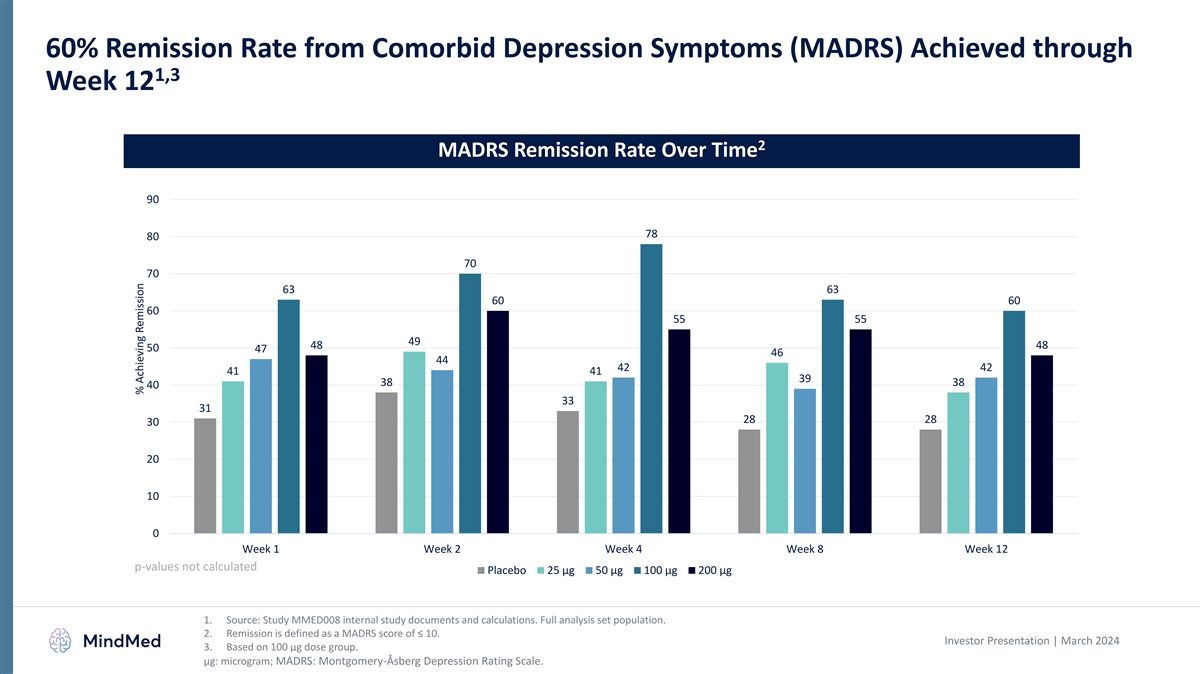
在 1,3 周 12 2 MADRS 一段时间内实现了 60% 的合并抑郁症状 (MADRS) 缓解率 90 78 80 70 70 63 63 60 60 55 55 49 48 50 47 46 44 42 41 41 39 38 38 40 33 31 28 30 10 0 第 2 周 4 周 8 周 12 p 值未计算安慰剂 25 µg 50 µg 100 µg 200 µg 1.来源:研究 MMED008 内部研究文件和计算。完整分析集合群体。2.缓解的定义是 MADRS 分数为 ≤ 10。投资者演示文稿 | 2024 年 3 月 3.基于 100 微克剂量组。 μg:微克;MADRS:蒙哥马利-阿斯伯格抑郁症评级量表。实现缓解的百分比
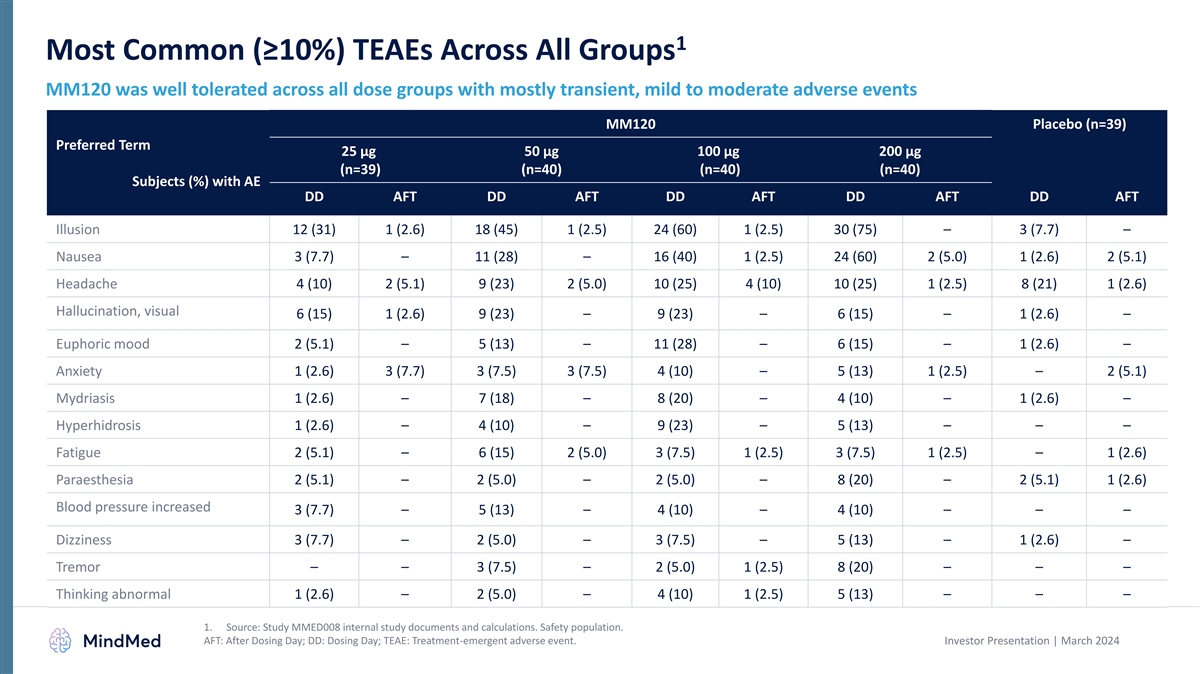
1 所有剂量组中最常见 (≥ 10%) 的 TEAE MM120 耐受性良好 ,主要是短暂的、轻度至中度的不良事件 MM120 安慰剂 (n=39) 首选期限 25 µg 50 µg 100 µg 100 µg 200 µg (n=40) (n=40) (n=40) (%) AFT DD AFT DD AFT DD AFT DD AFT DD AFT DD AFT DD AFT DD AFT DD AFT DD AFT DD AFT DD AFT DD AFT DD AFT DD AFT DD AFT DD AFT DD AFT DD AFT DD 幻觉 12 (31) 1 (2.6) 18 (45) 1 (2.5) 24 (60) 1 (2.5) 30 (75) — 3 (7.7) — 恶心 3 (7.7) — 11 (28) — 16 (40) 1 (2.5) 24 (60) 2 (5.0) 1 (2.6) 2 (5.1) 头痛 4 (10) 2 (5.1) 9 (23) 2 (5.0) 10 (25) 4 (5) 10) 10 (25) 1 (2.5) 8 (21) 1 (2.6) 幻觉,视觉 6 (15) 1(2.6) 9 (23) — 9 (23) — 6 (15) — 1 (2.6) — 欣快情绪 2 (5.1) — 5 (13) — 11 (28) — 6 (15) — 1 (2.6) — 焦虑 1 (2.6) 3 (7.7) 3 (7.5) 3 (7.5) 4 (10) — 5 (13) 1 (2.5) — 2 (5.1) Mydriasis 1 (2.6) — 2 (5.1) mydriasis 1 (2.6) — 2 (5.1) 2.6 (2.6) — 1 (2.6)) — 7 (18) — 8 (20) — 4 (10) — 1 (2.6) — 多汗症 1 (2.6) — 4 (10) — 9 (23) — 5 (13) — — — 疲劳 2 (5.1) — 6 (15) 2 (5.0) 3 (7.5) 1 (2.5) 3 (7.5) 1 (2.5) — 1 (2.6) — 2 (5.0) — 2 (5.0) — 8 (20) — 2 (5.1) 1 (2.6) 血压升高 3 (7.7) — 5 (13) — 4 (10) — 4 (10) — — — 头晕 3 (7.7) — 2 (5.0) — 3 (7.5) — 5 (13) — 1 (2.6) — 震颤 —— 3 (7.5) — 2 (5.0) 1 (2.5) 8 (20) — — — 思维异常 1 (2.6) — 2 (5.0) — 4 (10) 1 (2.5) 5 (13) — — 1.来源:研究 MMED008 内部研究文件和计算。安全人群。AFT:给药日后;DD:给药日;TEAE:治疗紧急不良事件。投资者演示文稿 | 2024 年 3 月

1 所有组中最常见(≥ 10%)TEAE(续)MM120 在所有剂量组中耐受性良好,主要是短暂的、轻度至中度的不良事件 MM120 安慰剂(n=39)首选术语 25 µg 50 µg 100 µg 100 µg 200 µg(n=39)(n=40)(n=40)(n=40)受试者(%)AE DD AFT DD AFT DD AFT DD AFT DD AFT DD AFT 平衡障碍 — — 4 (10) — 3 (7.5) — 2 (5.0) — 1 (2.6) — 假幻觉 — — 3 (7.5) — 4 (10) — — — 呕吐 — — 2 (5.0) — 2 (5.0) — 5 (13) — 5 (13) — 1 (2.5) — 1 (2.5) — — — 感觉异常 1 (2.6) — 2 (5.0) — — — — 4 (10) 1 (2.6) 1 (2.6) COVID-19 — 1 (2.6) — 2 (5.0) — 1 (2.5) — 4 (10) — — 1。来源:研究 MMED008 内部研究文件和计算。安全人群。AFT:给药日后;DD:给药日;TEAE:治疗紧急不良 事件。投资者演示文稿 | 2024 年 3 月