
投资者和分析师活动系列 — 第 8 卷转变肌强直性营养不良症全球第 3 期 HARBOR 试验和长期的 MARINA-OLE 数据 2024 年 3 月 4 日纳斯达克:RNA | aviditybio.com

2 前瞻性陈述我们提醒读者,本演示文稿包含涉及重大风险和不确定性的前瞻性陈述。本演示文稿中除历史事实陈述以外的所有陈述均为前瞻性陈述。前瞻性陈述包括但不限于以下方面的陈述:我们未来的经营业绩;我们的业务战略;我们正在进行的临床试验的预期时间、设计和进行;我们正在进行的临床项目数据的发布时间;临床试验数据和结果的特征以及从中得出的结论;研发计划;AOC 1001、AOC 1020和AOC 1044的计划和预计时间表;安全性和耐受性概况我们的候选产品;AOC 平台的潜力;我们的候选产品治疗罕见疾病的能力;成功的时机和可能性;潜在的产品;产品批准;未来运营的管理计划和目标;以及预期产品开发工作的未来结果。在某些情况下,读者可以通过诸如 “可能”、“将”、“应该”、“预期”、“计划”、“预期”、“可能”、“打算”、“目标”、“项目”、“考虑”、“相信”、“估计”、“潜在” 或 “继续” 等术语来识别前瞻性陈述,或者这些术语或其他类似表述的否定词。纳入前瞻性陈述不应被视为Avidity对我们任何计划将实现的陈述。由于我们的业务固有风险和不确定性,无法控制,实际结果可能与本演示文稿中列出的有所不同,包括但不限于:我们可能无法完全解决与AOC 1001相关的部分临床搁置问题,这可能会导致AOC 1001的临床开发延迟;与部分临床搁置相关的额外数据请求或其他可能导致大量额外费用和时间延迟;向FDA交付的相关数据部分临床封存可能不是令美国食品药品管理局满意;持续可用的与AOC 1001相关的其他参与者数据可能与截至最近截止日期的数据不一致,对现有数据的进一步分析和对新数据的分析可能会得出与截止日期不同的结论;我们的候选产品的意外不良副作用或疗效不足可能会延迟或限制其开发、监管批准和/或商业化,或可能导致额外的临床搁置,召回或产品责任声明;我们处于开发初期;我们在AOC平台上发现和开发候选产品的方法尚未得到证实,我们不知道我们是否能够开发出任何具有商业价值的产品;我们的临床前研究和候选产品的临床试验的成功;早期临床试验的结果不一定能预测未来的结果;临床试验的开始、注册和完成可能出现延迟;我们对第三方的依赖与临床前和临床前有关临床测试和产品制造;我们可能无法意识到与第三方合作的预期收益,我们现有的合作可能比预期更早终止,或者我们可能无法形成新的合作;美国和国外的监管发展,包括接受IND和类似的外国监管文件以及我们对未来临床试验的拟议设计;FDA的快速通道指定可能无法加快开发或监管审查或批准程序;我们的获得能力和维持对候选产品和专有技术的知识产权保护;我们可能比预期更快地耗尽资本资源,无法筹集额外的所需资金;以及我们在向美国证券交易委员会提交的文件中描述的其他风险,包括我们在2024年2月28日向美国证券交易委员会提交的截至2023年12月31日的10-K表格以及随后向美国证券交易委员会提交的文件中 “风险因素” 标题下的风险。提醒读者不要过分依赖这些前瞻性陈述,这些陈述仅代表截至本文发布之日。除非适用法律要求,否则我们不计划公开更新或修改此处包含的任何前瞻性陈述,无论是由于任何新信息、未来事件、情况变化还是其他原因。本警示声明是根据1995年《私人证券诉讼改革法》的安全港条款作出的,对所有前瞻性陈述进行了全面的限定。本演示文稿还包含独立方和我们提供的与市场规模和增长相关的估计和其他统计数据,以及有关我们行业的其他数据。这些数据涉及许多假设和局限性,提醒读者不要过分重视此类估计。此外,对我们未来表现的预测、假设和估计以及我们经营的市场的未来表现必然受到高度的不确定性和风险的影响。这些因素和其他因素可能导致结果与独立各方和我们在估计中表达的结果存在重大差异。本演示不应构成卖出要约或征求购买证券要约,在根据任何此类州或司法管辖区的证券法进行注册或获得资格认证之前,在任何州或司法管辖区出售证券是非法的,也不得出售任何证券。

3 我们的愿景通过革新 RNA 疗法的交付来深刻改善人们的生活 Luke Living with DM1

4 AOC 1044 在 DMD44 中约有 900 名患者在 2024 年交付:在 3 种罕见疾病的 3 个临床项目中读出 3 个数据 AOC 1044 在 DMD44 中约有 900 名患者 1020 个 FSHD 约16,000-38,00 名患者预计 2024 年第二季度约一半参与者的 1/2 期 FORTITUDE 初步数据在 DM1 中读取 >40,000 名患者 2024 年第一季度美国 MARINA-OLE 数据 2024 年第二季度全球三期 HARBOR 试验的启动轨迹预计 2024 年下半年 1/2 期 EXPLORE44 患者数据

每日的 5 个目标分享全球 3 期 HARBORTM 试验设计 • 研究设计监管协议 • 有望在 2024 年第二季度启动来自 MARINA-OLETM 的长期数据 • 包括 vHOT、手抓力、肌肉力量和日常生活活动在内的多种指标的持续和持久改善 • 良好的长期安全性和耐受性 END-DM1 自然史研究的首次数据表明,与自然史相比,疾病进展出现逆转 delpacibart etedesiran 缩写:-desiran(原名为 AOC 1001)

6 Avidity 管理团队 John W. Day,医学博士,斯坦福大学医学院神经病学和儿科教授兼神经肌肉医学部主任 G U E S P E A K E R Steve Hughes,医学博士首席医学官莎拉·博伊斯总裁兼首席执行官 W. Michael Flanagan 博士首席科学和技术官杰夫·格兰德投资者关系与企业传播转型副总裁肌强直性营养不良

7 议程/大纲彻底改变核糖核糖核酸的交付 Sarah Boyce,总裁兼首席执行官进入第三阶段:HARBORTM 试验 Steve Hughes,医学博士,首席营销官 • MARINA-OLETM 长期疗效和安全性数据 John W. Day,博士,斯坦福大学医学院神经病学和儿科教授兼神经肌肉医学部主任 • 为DM1患者提供服务 Steve Hughes,医学博士首席营销官闭幕词莎拉·博伊斯,总裁兼首席执行官问答环节 Avidity Management 和戴博士,斯坦福大学主持人:IR/CC 副总裁杰夫·格兰德

8 0 获批准的疗法 DM1:患者负担沉重且需求未得到满足 >40,000 美国有 DM1 的人 • 主要影响骨骼、心脏和平滑肌的神经肌肉疾病未被充分认识、进行性且往往是致命的 • 严重程度代代增加 • 对生活质量的重大影响 • del-Desiran 旨在解决 DM1 的根本原因 Loraine、Kristl & Zen 使用 DM1 生活
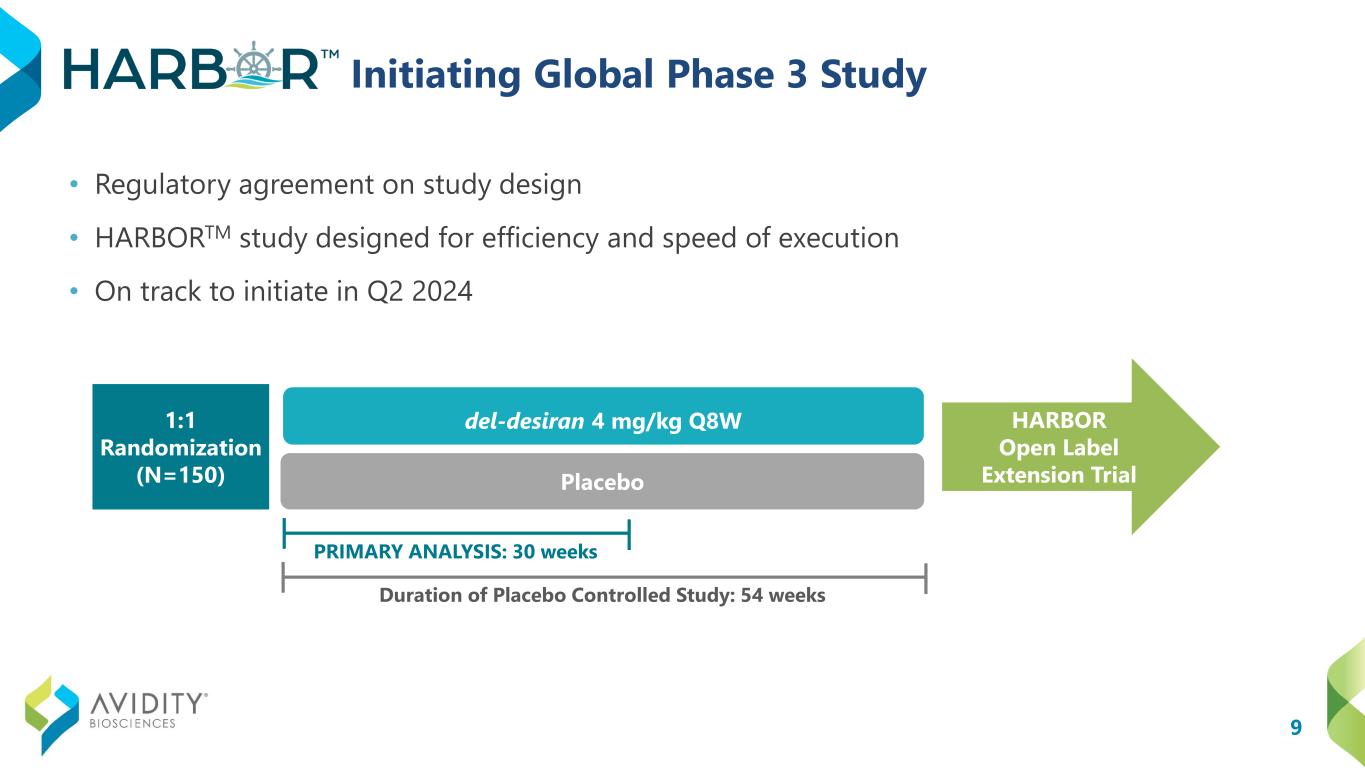
9 启动全球 3 期研究 • 研究设计监管协议 • HARBORTM 研究旨在提高执行效率和速度 • 有望在 2024 年第二季度启动 del-desiran 4 mg/kg Q8W 安慰剂安慰剂对照研究时间:54 周 HARBOR 开放标签延期试验 1:1 随机化(N=150)主要分析:30 周
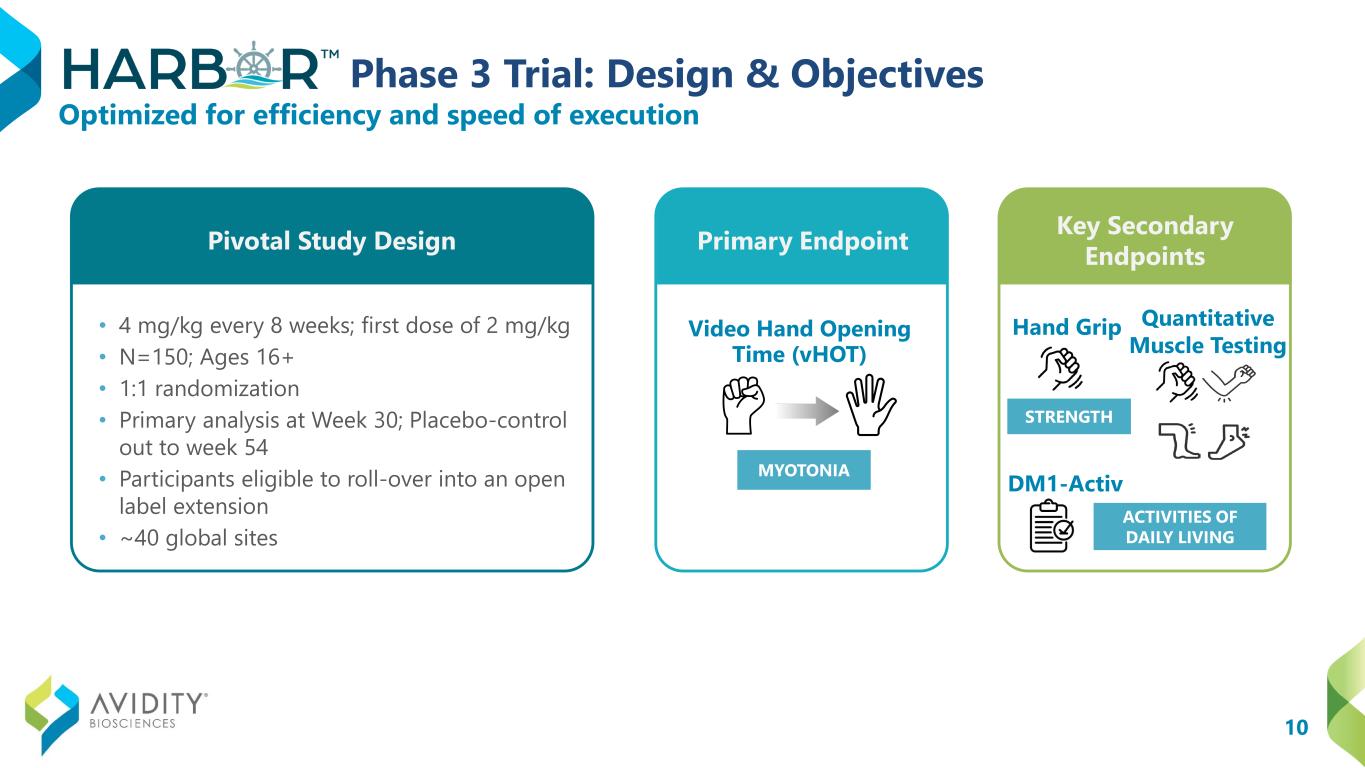
10 期 3 期试验:设计与目标 • 每 8 周 4 mg/kg;第一剂量 2 mg/kg • N = 150;年龄 16 岁以上 • 1:1 随机分配 • 第 30 周初步分析;安慰剂对照至第 54 周 • 参与者有资格延长开放标签期限 • 约 40 个全球站点视频手掌定量肌肉测试 dm1-Activ 针对执行效率和速度进行了优化日常生活活动关键研究设计主要终点关键次要终点

11 议程/大纲彻底改变核糖核糖核酸的交付 Sarah Boyce,总裁兼首席执行官进入第三阶段:HARBORTM 试验 Steve Hughes,医学博士,首席营销官 • MARINA-OLETM 长期疗效和安全性数据 John W. Day,博士,斯坦福大学医学院神经病学和儿科教授兼神经肌肉医学部主任 • 为DM1患者提供服务 Steve Hughes,医学博士首席营销官闭幕词莎拉·博伊斯,总裁兼首席执行官问答环节 Avidity Management 和戴博士,斯坦福大学主持人:IR/CC 副总裁杰夫·格兰德

John W. Day,医学博士,斯坦福大学医学院神经病学、儿科(遗传学)和病理学教授,神经肌肉医学部主任 John W. Day 是斯坦福大学神经病学、儿科(遗传学)和病理学教授兼神经肌肉医学系主任。戴博士在明尼苏达大学获得医学博士学位,在阿尔伯特·爱因斯坦医学院获得神经科学博士学位,在那里他研究了突触生理学和可塑性。在加州大学旧金山分校完成神经病学和神经肌肉训练后,他被明尼苏达大学招募到明尼苏达大学,作为神经病学、儿科和遗传学教授,他创立并领导了保罗和希拉·韦尔斯通肌肉萎缩症中心。2011年,他被斯坦福大学招募到斯坦福大学,成立了全面的神经肌肉医学部。戴博士研究了神经肌肉疾病的遗传原因和多系统影响,在设计和指导包括反义寡核苷酸和基因替代疗法在内的新疗法的临床试验方面拥有30多年的经验。12

识别 DM1 13 的频谱
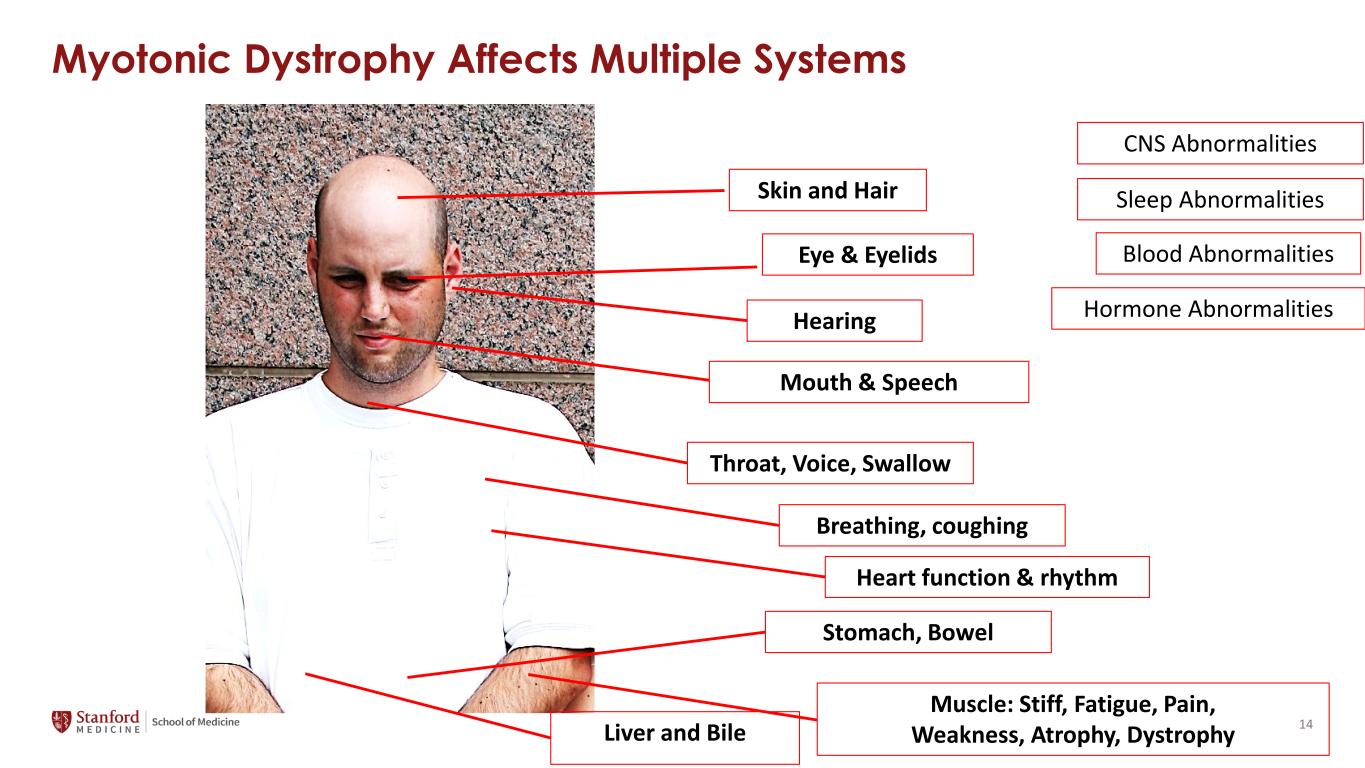
肌强性营养不良会影响多个系统眼睛和眼皮:听力、口腔和言语、皮肤和头发、喉咙、声音、吞咽呼吸、咳嗽、心脏功能和节奏胃、肠胃和肝脏和胆汁:僵硬、疲劳、疼痛、虚弱、萎缩、营养不良睡眠异常血液异常激素异常中枢神经系统异常 14
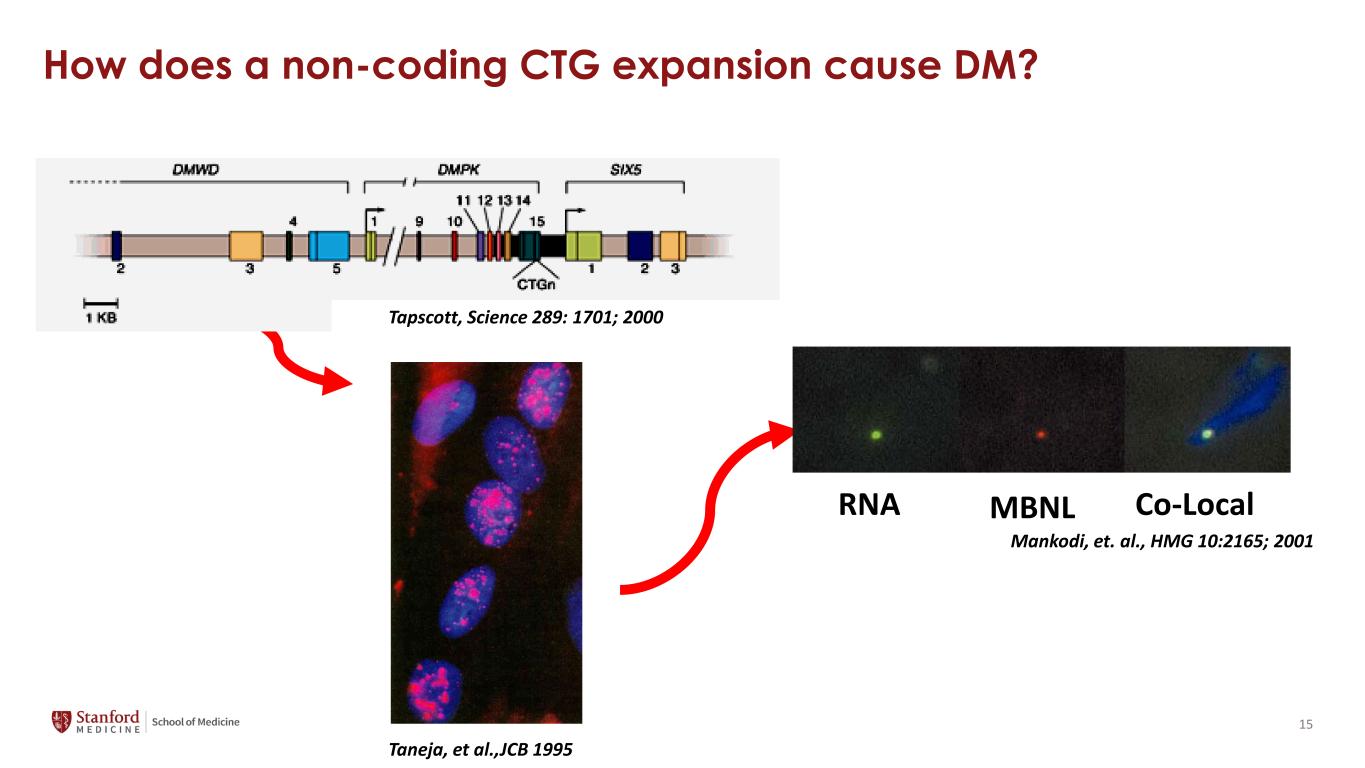
非编码 CTG 扩展如何导致 DM?Taneja 等人,JCB 1995 RNA MBNL Co-Local Mankodi 等人,HMG 10:2165;2001 Tapscott,Science 289:1701;2000 15
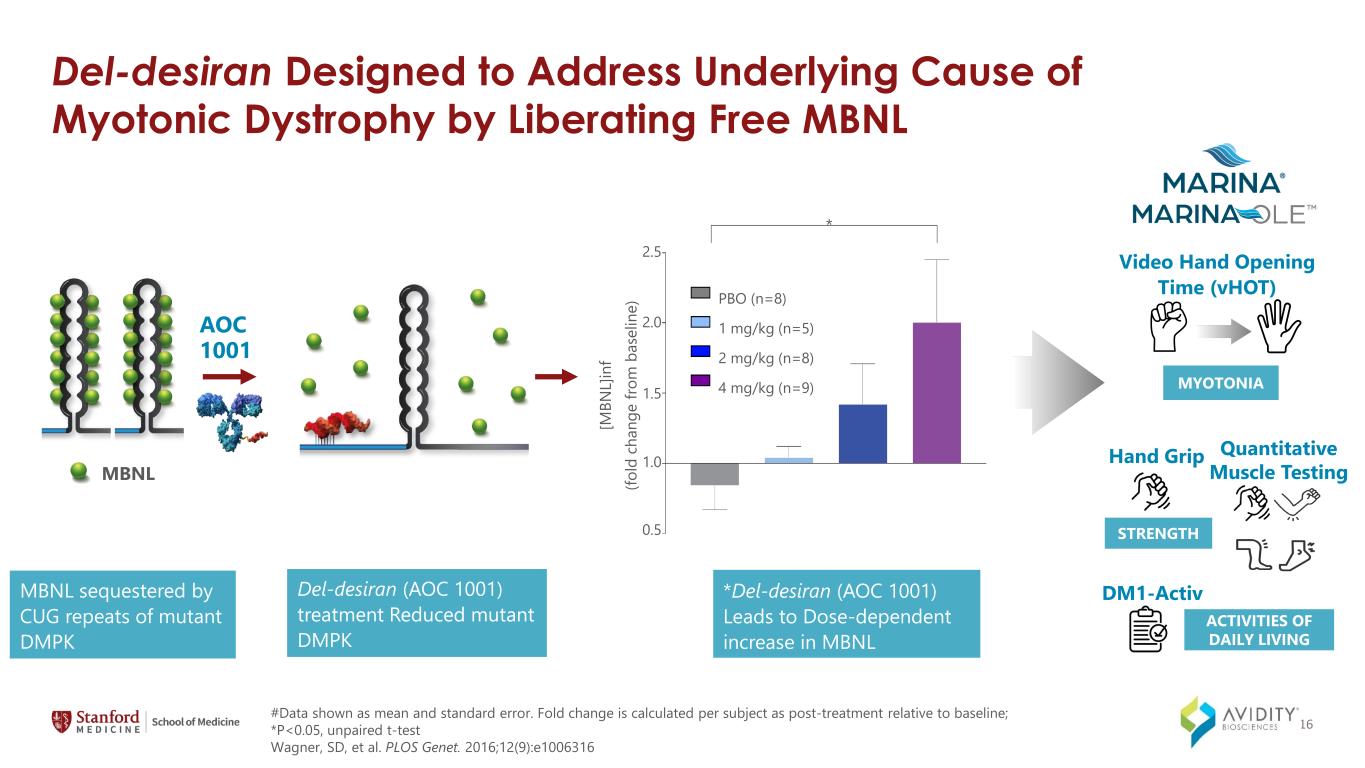
del-Desiran 旨在通过释放游离 MBNL del-Desiran (AOC 1001) 治疗来解决肌强直性营养不良症的根本原因 del-Desiran (AOC 1001) 治疗被突变体 DMPK AOC 1001 MBNL 的 CUG 重复序列隔离 DMPK MBNL [M BN L]在 f (fo ld c ha ng e from m b as el in e) 2.5 2.0 1.5 1.0 0.5 * PBO (n=8) 1 mg/kg (n=5) 2 mg/kg (n=8) 2 mg/kg (n=8) 4 mg/kg (n=9) #Data 显示为平均误差和标准误差。折叠变化是根据每个受试者的治疗后相对于基线计算的;*P

来自针对 DM1 17 患者的MARINA-OLE试验的长期安全性和有效性数据
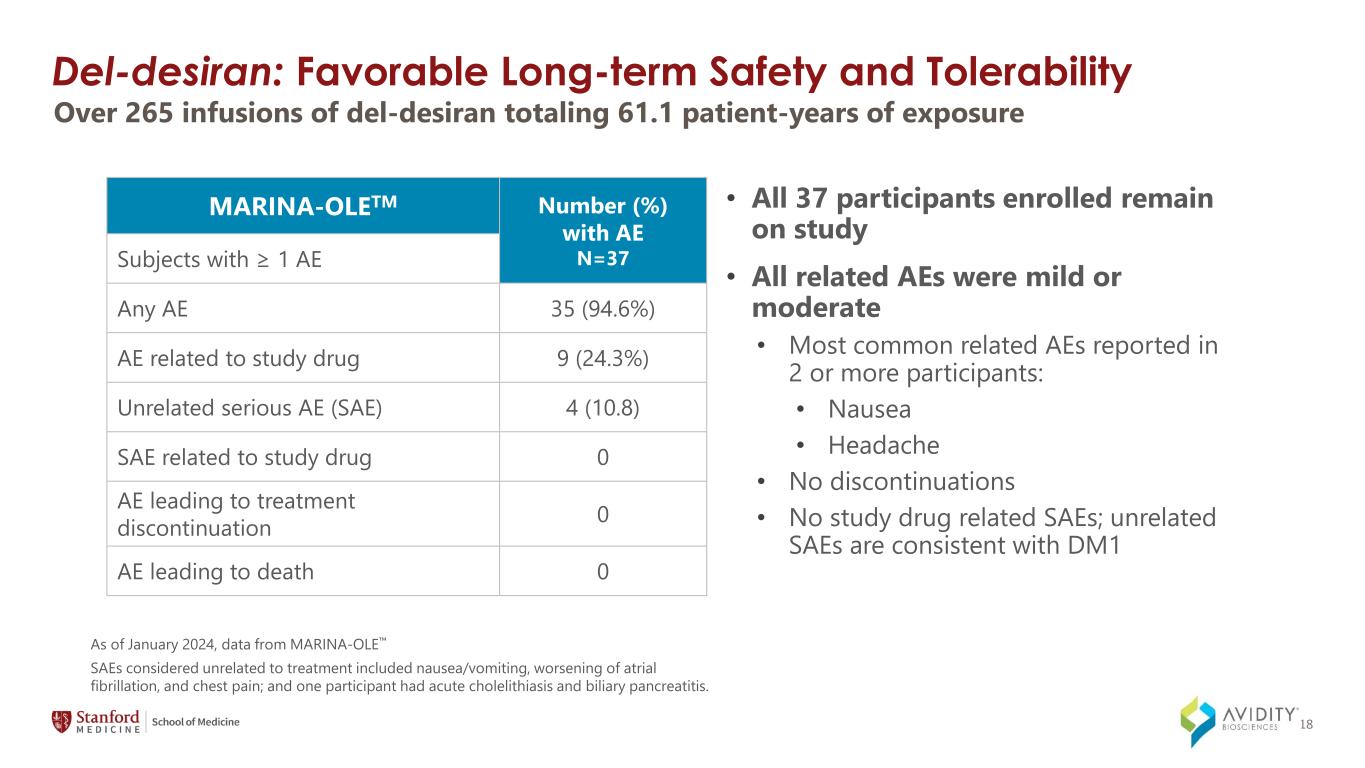
18 del-Desiran:良好的长期安全性和耐受性截至2024年1月,来自MARINA-OLE的数据 • 所有37名受试者仍在研究中 • 所有相关不良反应均为轻度或中度 • 在2名或更多参与者中报告的最常见的相关不良反应:• 恶心 • 头痛 • 未停药 • 无研究药物相关SAE;与治疗无关的DM1 SAE一致,包括恶心/呕吐、心房颤动恶化,以及胸痛;一名参与者患有急性胆石症和胆源性胰腺炎。超过 265 次 del-desiran 注射总计 61.1 个患者年数 MARINA-OLETM 数量 (%),AE N=37 AE ≥ 1 的受试者任何 AE 35 (94.6%) AE 与研究药物 9 (24.3%) 无关的重度 AE (SAE) 4 (10.8) SAE 导致中止治疗 0 AE 导致死亡

19 • 非介入性 NHS 旨在增进对 DM1 患者疾病进展的理解 • 侧重于临床结果评估,以支持 DM1 疗法的开发 • 700 名患者,2 年研究,约 20 个中心 • 由肌张力萎缩症临床研究网络 (DMCRN) 设计和运营 • 获得 FDA、MDA、MDF 支持;Avidity 是多个赞助组织之一 END-DM1 自然史研究:了解 DM1 疾病进展

20 个 END-DM1 数据依据设计 MARINA® 和 3 期 HARBOR 试验的相同终点测得出的临床试验地点与 MARINA® 和 HARBOR 基于护理标准的当代数据集重叠在 END-DM1 自然史研究中接受了至少一年的随访数百名患者今天首次公布了为期一年的数据
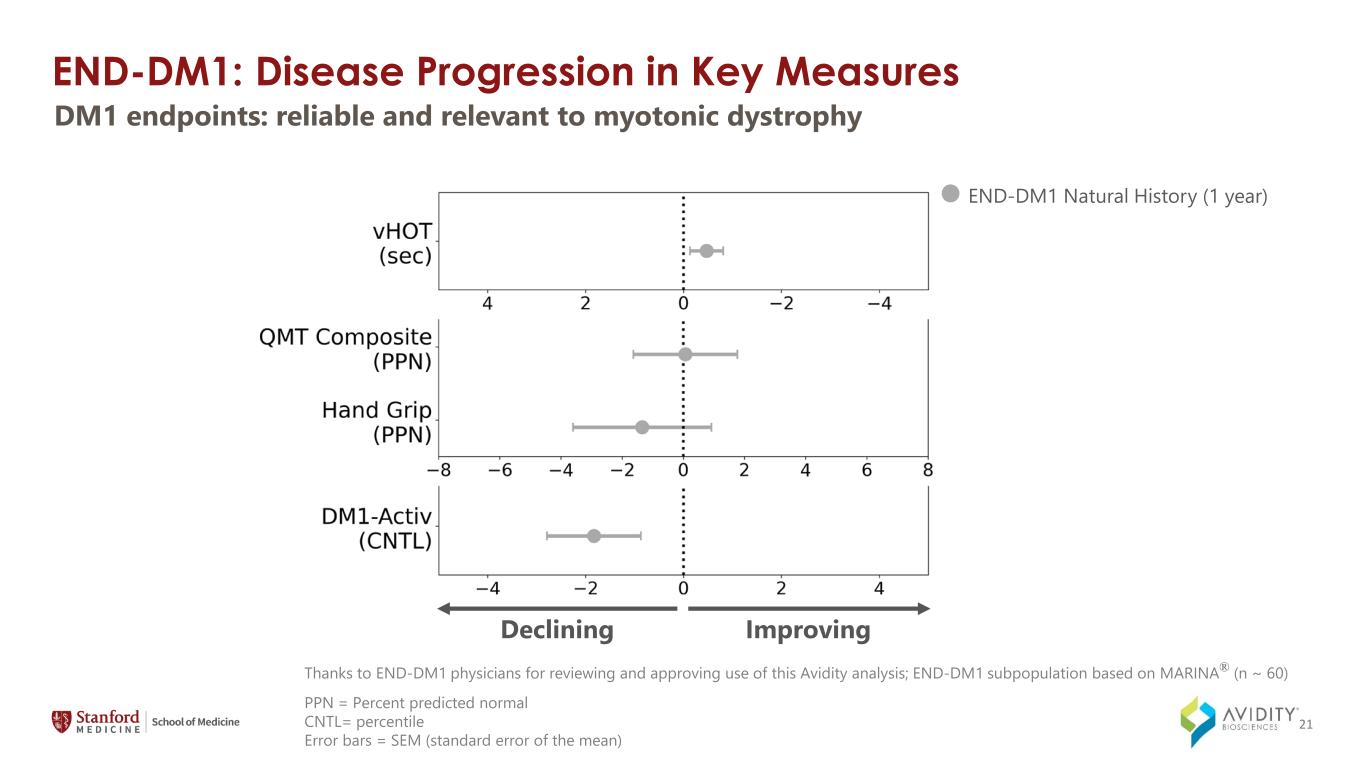
END-DM1:关键指标中的疾病进展 END-DM1 自然史(1 年)4 mg/kg Q12W(1 年)改善/下降的 DM1 终点:可靠且与肌强直性营养不良相关 PPN = 预测正常 CNTL= 百分位误差条 = SEM(平均值的标准误差)感谢 END-DM1 医生审查并批准使用此 Avidity 分析;END-DM1 亚群基于 MARINA® (n ~ 60) 21
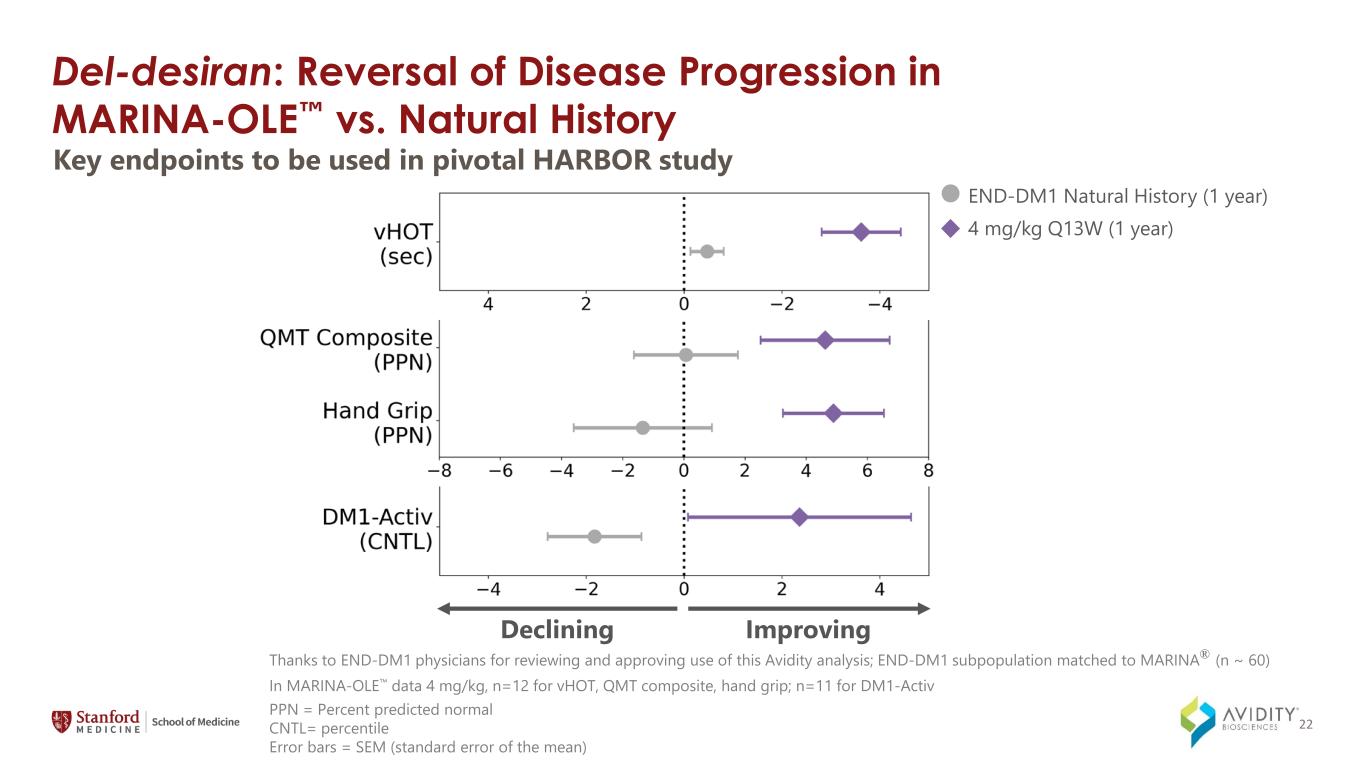
del-Desiran:MARINA-OLE 与自然史的疾病进展逆转关键终点将用于关键的 HARBOR 研究改善/下降的 PPN = 预测的正常 CNTL 百分比误差条 = SEM(平均值的标准误差)感谢 END-DM1 医生审查并批准使用这种 Avidity 分析;END-DM1 亚群与 MARINA®(n ~ 60)相匹配,在 MARINA-OLE 数据中 4 mg/kg,vHOT,QMT 的 n=12 复合材料,握把;对于 DM1-Activ END-DM1 自然历史(1 年)4 mg/kg Q13W(1 年),n=11
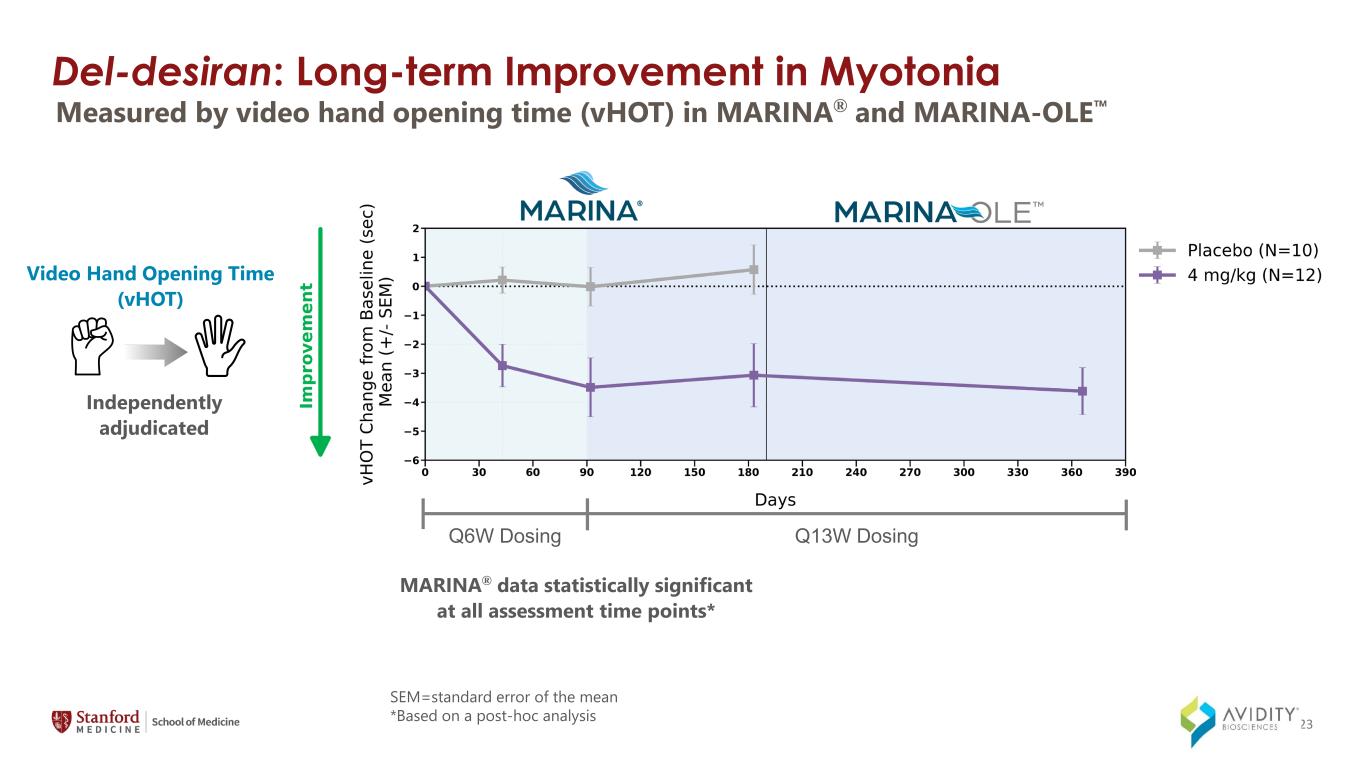
del-Desiran:肌张力长期改善以视频手开时间 (vHOT) 衡量的 MARINA® 和 MARINA-OLE MARINA® 数据在所有评估时间点均具有统计学意义* 视频开手时间 (vHOT) 独立裁定 Q6W 剂量 Q13W 剂量 SEM=平均值的标准误差 *基于事后分析 23
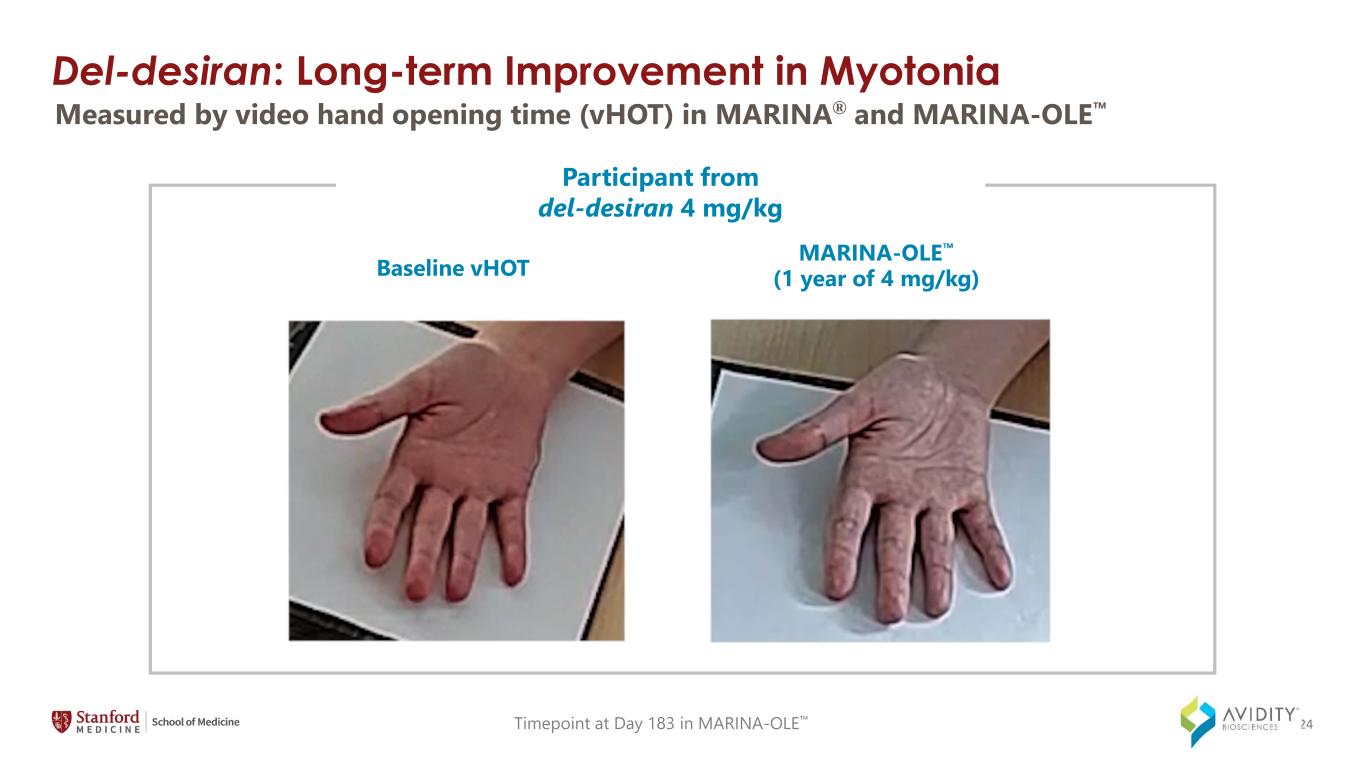
del-Desiran:肌张力基线 vHOT MARINA-OLE(1 年 4 mg/kg)的长期改善 `来自 del-Desiran 的参与者在 MARINA-OLE 第 183 天的 4 mg/kg 时间点以 MARINA® 和 MARINA-OLE 24 中的视频开手时间 (vHOT) 测量
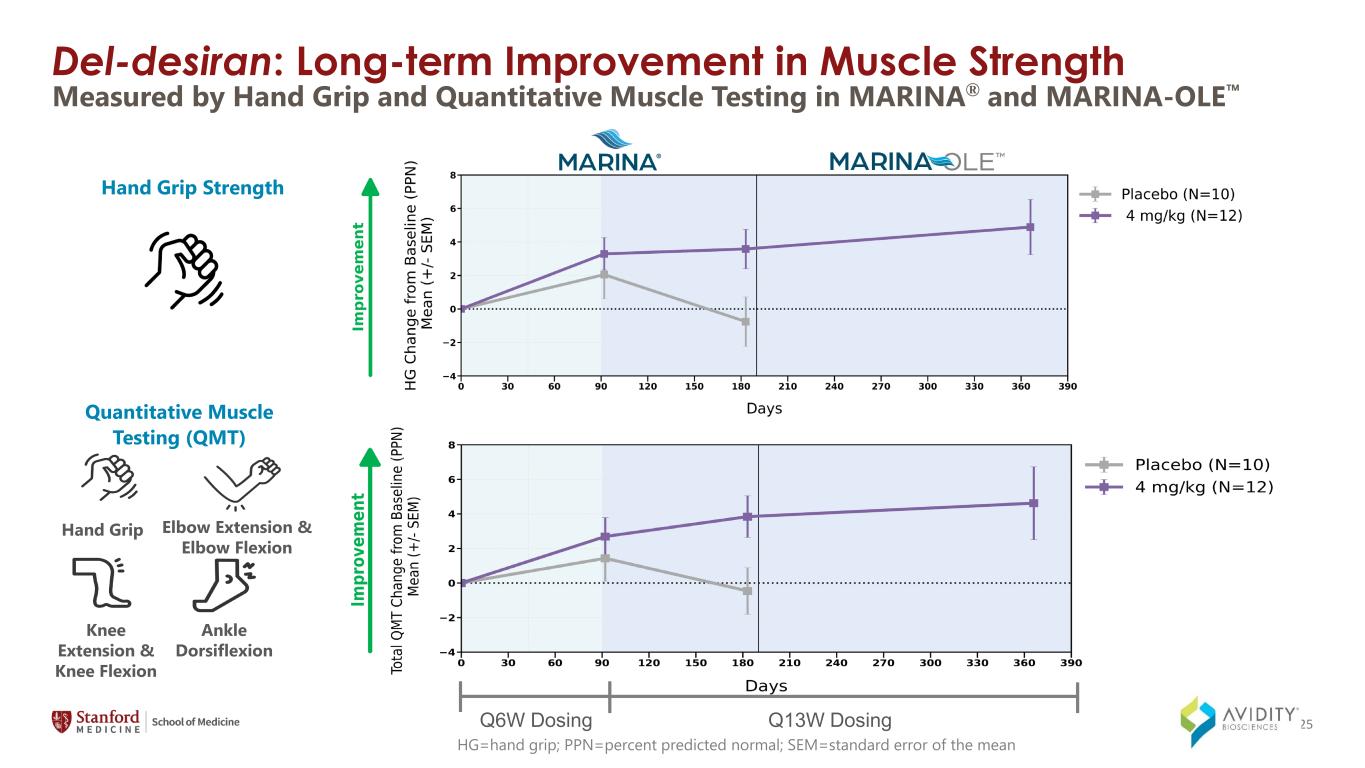
del-Desiran:肌肉力量的长期改善 hg=手部握力;PPN=预测正常百分比;sem=平均定量肌肉测试 (QMT) 手握肘部伸展和肘部屈曲膝盖伸展和膝盖屈曲脚踝背屈手握力 Q6W 剂量 Q13W 剂量通过MARINA® 和 MARINA-OLE 25 中的手握和定量肌肉测试测量
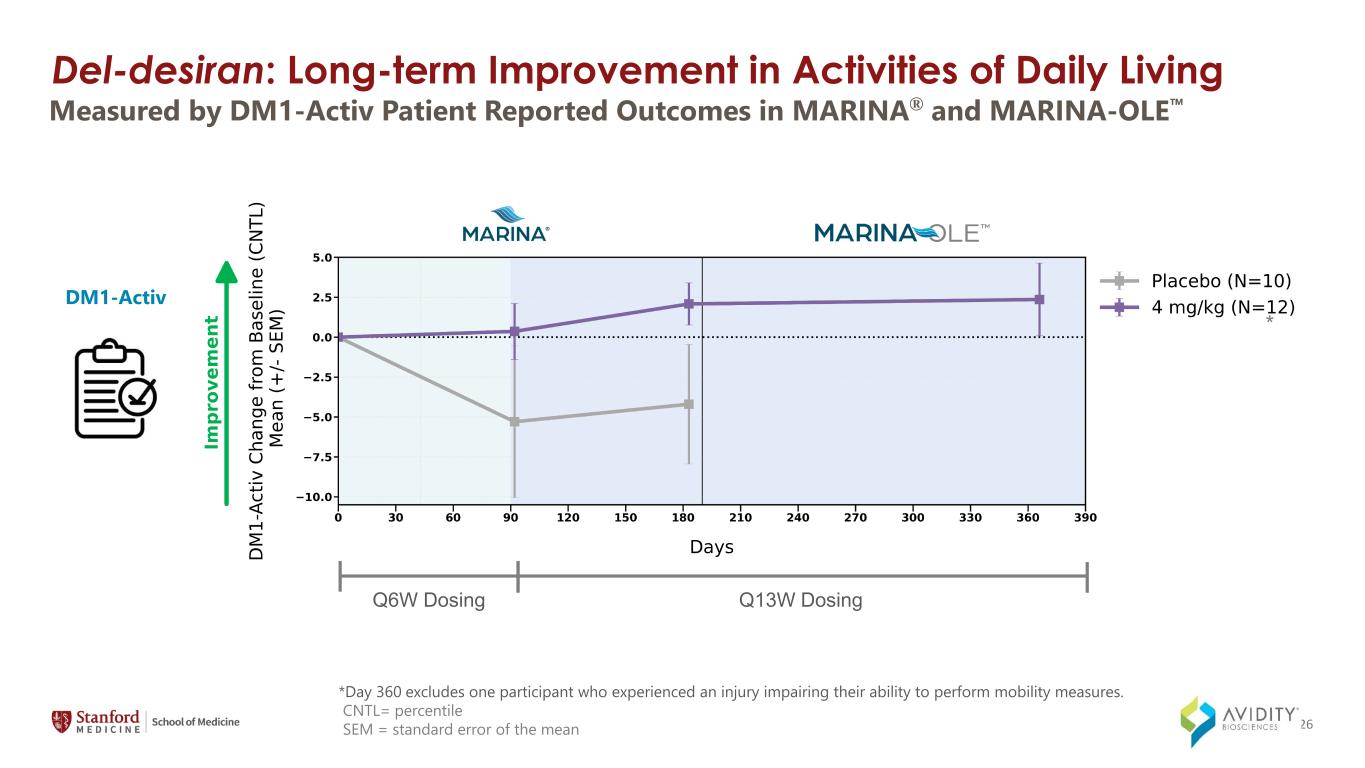
*第 360 天不包括一名因受伤而无法采取行动措施的参与者。CNTL= 百分位数 SEM = 由 DM1-Activ 患者报告的 MARINA® 和 MARINA-OLE DM1-Activ Q6W 剂量 Q13W 剂量 Q13W 剂量测得的平均值的标准误差 * 26 del-Desiran:日常生活活动的长期改善

27 del-Desiran 4 mg/kg • 表现出良好的长期安全性和耐受性 • 与 END-DM1 自然史数据相比,MARINA® 和 MARINA-OLE 的疾病进展出现逆转 • 对多个临床终点进行了持续而持久的改进 Global HARBOR 试验启动 2024 年第二季度 MARINA-OLE 数据摘要 del-desiran 有可能成为 DM1 患者的变革性疗法 END-DM1 自然史(1 年)4 mg/kg Q13W(1 年)

28 议程/概要彻底改变核糖核酸的交付 Sarah Boyce,总裁兼首席执行官进入第三阶段:HARBORTM 试验 Steve Hughes,医学博士,首席营销官 • MARINA-OLE 长期疗效和安全性数据 John W. Day,医学博士,斯坦福大学医学院神经病学和儿科教授兼神经肌肉医学部主任 • 为DM1患者提供服务 Steve Hughes,医学博士,首席营销官闭幕词莎拉·博伊斯,总裁兼首席执行官问答环节 Avidity Management 和戴博士,斯坦福大学主持人:IR/CC 副总裁杰夫·格兰德

29 患者体验:del-desiran 对他们生活的影响我在 6 月份开始服用这种药物,大概在我第一次输液两周后,我打开了一个气泡瓶,这是我永远做不到的。那是一个扭曲的流行酒瓶... 它马上就打开了。我的力量更好了,我的视野更好了,我的双手也在工作。我有更多的力量,我可以把它们伸出来。我可以打开东西,我可以打开门把手以及所有这些更难的东西。比如,我的上臂力量好多了。我能走得更好。我不需要一直戴护颈,一切都改善了很多。“”

30 位患者体验:del-desiran 对他们生活的影响在研究之前我无法站稳脚跟,自从我恢复锻炼以来,我实际上可以重新站起来了。所以希望能增强一些力量。肌张力障碍,如果我能挥出拳头,我就无法张开手... 我能够毫无问题地挤出拳头张开手。我说话的时候我的舌头会抽筋,而且自从第一次服药以来我就没有出现过任何这种情况的迹象。“”

31 患者体验:del-desiran 对他们生活的影响我注意到一个非常大的不同,那就是在我出现更多症状之前,我曾经是一个非常活跃的人。经过几轮输液,我实际上已经能够回到健身房开始锻炼身体,与教练一起工作。这都是因为我的机动性肯定提高了。我的活动范围也扩大了。我认为令人惊讶的是,当我被诊断出来时,我被告知没有治疗方法,没有治愈方法。这项研究给了我很多希望。我希望能够与社区中拥有 DM1 的其他人分享。“”

32 议程/大纲彻底改变核糖核酸的交付 Sarah Boyce,总裁兼首席执行官进入第三阶段:HARBORTM 试验 Steve Hughes,医学博士,首席营销官 • MARINA-OLE 长期疗效和安全性数据 John W. Day,医学博士,斯坦福大学医学院神经病学和儿科教授兼神经肌肉医学部主任 • 为DM1患者提供服务 Steve Hughes,医学博士,首席营销官闭幕词莎拉·博伊斯,总裁兼首席执行官问答环节 Avidity Management 和戴博士,斯坦福大学主持人:IR/CC 副总裁杰夫·格兰德

33 我们的愿景通过革新 RNA 疗法的交付来深刻改善人们的生活 Luke Living with DM1

投资者和分析师活动系列 — 第 8 卷转变肌强直性营养不良症全球第 3 期 HARBOR 试验和长期 MARINA-OLE 数据问答 2024 年 3 月 4 日纳斯达克:RNA | aviditybio.com

投资者和分析师活动系列 — 第 8 卷转变肌强直性营养不良症全球第 3 期 HARBOR 试验和长期的 MARINA-OLE 数据 2024 年 3 月 4 日纳斯达克:RNA | aviditybio.com