

附录 99.1 开发治疗癌症的精准药物 来自 KOMET-007 的初步数据 — 2024 年 1 月 30 日

欢迎和介绍特洛伊·威尔逊博士、法学博士 — Kura Oncology 总裁 兼首席执行官

前瞻性陈述本演示文稿包含前瞻性 陈述。此类声明包括但不限于有关我们的研究、临床前和临床开发活动、齐夫托美尼、替匹法尼和 KO-2806 的计划和预计时间表、监管 申报计划、我们对候选产品相对于竞争疗法相对优势的预期、我们对候选产品治疗和商业潜力的预期、我们对现金 跑道的期望以及我们对预期用途的预期的净收益的私募于 2024 年 1 月 26 日结束。“相信”、“可能”、“应该”、“将”、 “估计”、“承诺”、“计划”、“继续”、“预期”、“打算”、“预期”、“潜在” 等词语以及类似的表达(包括其否定性), 旨在识别前瞻性陈述。由于此类陈述受风险和不确定性的影响,因此实际结果可能与此类前瞻性陈述所表达或暗示的结果存在重大差异。导致前瞻性陈述 不确定性的风险包括:我们的临床前研究和临床试验可能不成功;美国食品药品监督管理局(FDA)可能不同意我们对 候选产品临床试验数据的解释;我们可能会决定,或者 FDA 可能要求我们进行额外的临床试验或修改正在进行的临床试验;我们可能会延迟开始、注册、完成或分析 我们的候选产品的临床测试,或可能会出现与我们的临床试验设计充分性或临床试验执行有关的重大问题,这可能会导致成本增加和延迟,或限制我们获得监管机构 批准的能力;临床试验的开始、注册和完成以及从中报告数据;COVID-19 疫情可能会干扰我们和我们所依赖的第三方的业务,包括延迟或以其他方式干扰 我们的临床试验和临床前研究、制造和供应链,或损害员工生产力;我们的候选产品可能无法获得监管部门的批准或成功商业化;我们的候选产品出现意想不到的不良副作用或 疗效不足可能会延迟或阻碍监管部门的批准或商业化;我们可能无法获得额外的融资;与私募相关的市场状况和成交条件满意度相关的风险;与我们的现金需求相关的风险;以及与我们的业务和总体财务相关的风险和不确定性。额外的风险和不确定性可能会不时出现,库拉的管理层不可能预测所有的风险因素和不确定性。本演示文稿中包含的所有前瞻性陈述仅代表其发表之日。 在我们向美国证券交易委员会提交的文件中更全面地描述了影响我们的其他风险和不确定性。我们没有义务更新此类声明以反映在声明发表之日后发生的事件或存在的情况。本演示文稿 还包含从第三方获得并由第三方编制的统计和临床数据。提醒收件人不要过分重视此类披露。在本演示之日之后,公司或任何其他人均未对此类数据的准确性或 完整性作出任何陈述,也没有承担任何更新此类数据的义务。3
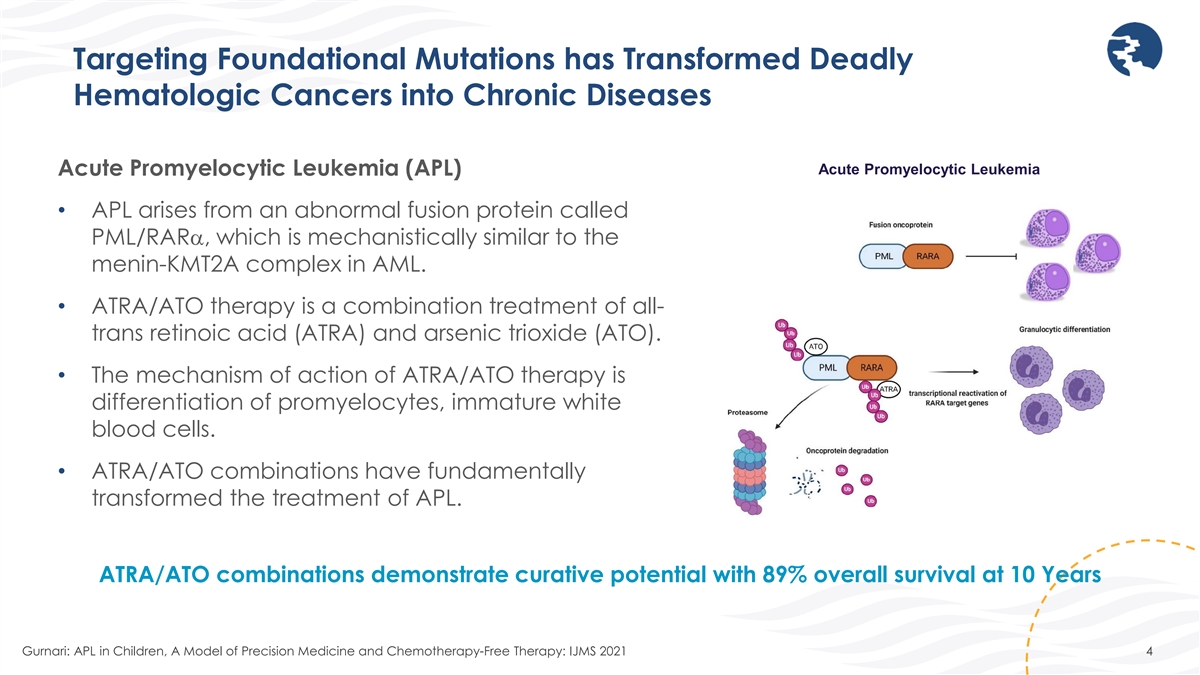
靶向基础突变已将致命的血液学 癌转化为慢性疾病急性早幼粒细胞白血病急性早幼粒细胞白血病 (APL) • APL 源自一种名为 PML/RARα 的异常融合蛋白,其机制与急性髓细胞白血病中的脑膜-KMT2A 复合物的机制相似。• ATRA/ATO 疗法是全反式视黄酸 (ATRA) 和三氧化二砷 (ATO) 的联合疗法。• ATRA/ATO 疗法的作用机制是分化早幼粒细胞,即未成熟的白细胞。• ATRA/ATO 组合从根本上改变了 APL 的治疗。ATRA/ATO 组合显示出治疗潜力,10 岁时总存活率为 89% Gurnari:儿童APL,精准医疗和无化疗疗模型:IJMS 2021 4
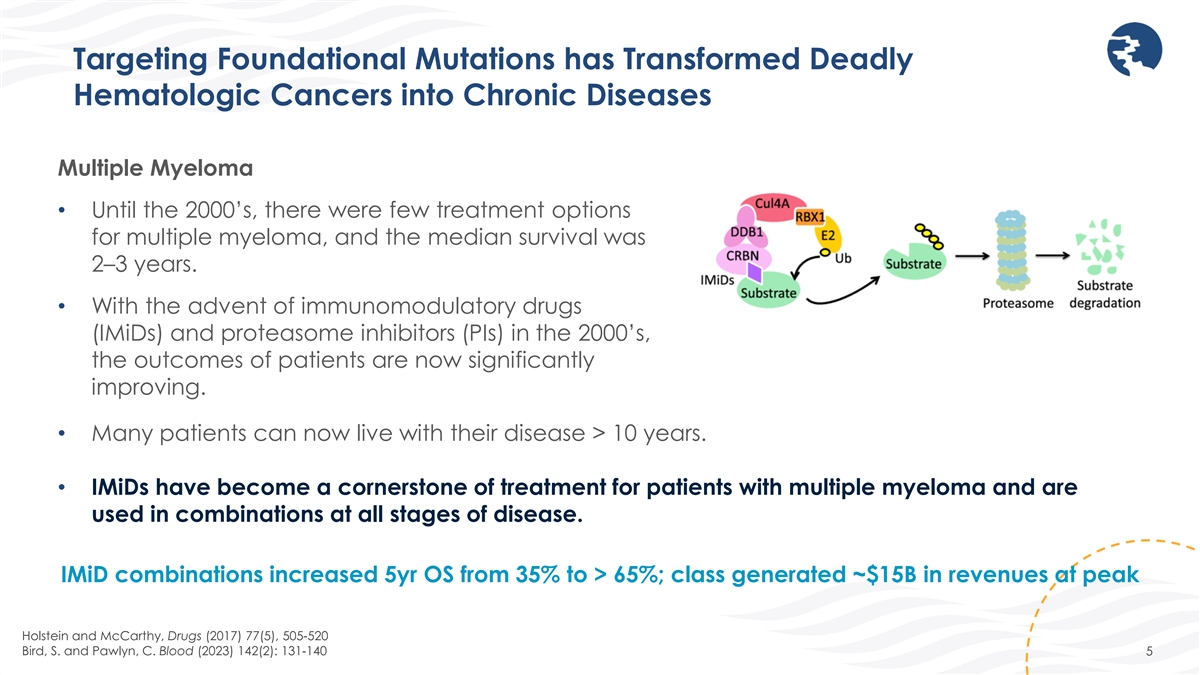
靶向基础突变已将致命的血液学 癌转变为慢性病多发性骨髓瘤 • 直到 2000 年代,多发性骨髓瘤的治疗选择很少,中位存活率为 2-3 年。• 随着 2000 年代免疫调节药物 (IMID) 和 蛋白酶体抑制剂 (PI) 的问世,患者的预后现已显著改善。• 许多患者可以现在患病已超过 10 年。• IMID 已成为 多发性骨髓瘤患者治疗的基石,可组合使用于疾病的各个阶段。iMid 组合将5年操作系统从35%提高到65%以上;该类别在荷斯坦和麦卡锡的峰值时创造了约150亿美元的收入,药物(2017)77(5)、505-520 Bird,S. 和 Pawlyn,C. Blood(2023)142(2):131-140 5

ZIFTOMENIB KOMET-007 研究人员的机会和简介 Stephen Dale,医学博士 — Kura Oncology 首席医学官

Ziftomenib 显示出成为反洗钱疗法基石的潜力 靶向高达 50% 的急性髓细胞白血病病例的核心突变 • 良好的耐受性状况,可与SOC联合使用持续给药 • 组合 似乎可以降低分化综合征的风险 • 未观察到或预测的药物相互作用 • 临床活性的初步证据令人鼓舞 • 快速入组证明了研究者的强烈热情 跨研究 • 前 20在不到四个月的时间内参加 KOMET-007 联合试验的患者 • KOMET-001 单一疗法注册试验预计将在 2024 年中期完成入组 7

KOMET-007 调查人员阿米尔·法西,医学博士 Amer Zeidan,MBBS • 白血病中心项目主任,• 麻省总医院癌症中心恶性肿瘤血液学科临时主任、耶鲁癌症中心血液学早期治疗研究主任 • 哈佛医学院 医学副教授 • 耶鲁大学医学(血液学)副教授 8

ZIFTOMENIB 作为单一疗法/组合机会 Amir Fathi,医学博士 — 麻省总医院

KOMET-001 齐托美尼在复发/难治性急性髓细胞白血病 1a 阶段 1b 阶段第 2 阶段 1b 剂量递增注册支持验证队列(正在进行中)已完成 600 mg QD 队列 1 的持续扩展:200 mg QD 50 mg 100 mg 1000 mg 600 mg QD QD QD 队列 2:600 mg QD npm1-m,Kmt2a-r、其他 npm1-m npm1-m npm1-m 或 Kmt2a-R 目标 • 安全性和耐受性继续注册阶段 • 主要终点:• 安全性和耐受性 • cr/CRH • 药代动力学 1b 验证 队列 • 药代动力学 •抗肿瘤的早期证据与美国食品药品管理局的项目一致 • 临床活性 • 次要终点:Optimus • CR/CRH 持续时间 • 安全性和耐受性 • 输血独立性 • 药代动力学 • CR/CRH MRD 阴性 • 不良事件 • 临床活性 CR,完全缓解;cRH,完全缓解,部分血液学恢复;FDA、美国食品药品监督管理局 管理局;MRD,可测量的残留物疾病;R/R,复发/难治性;RP2D,推荐的第 2 期剂量。10 ~
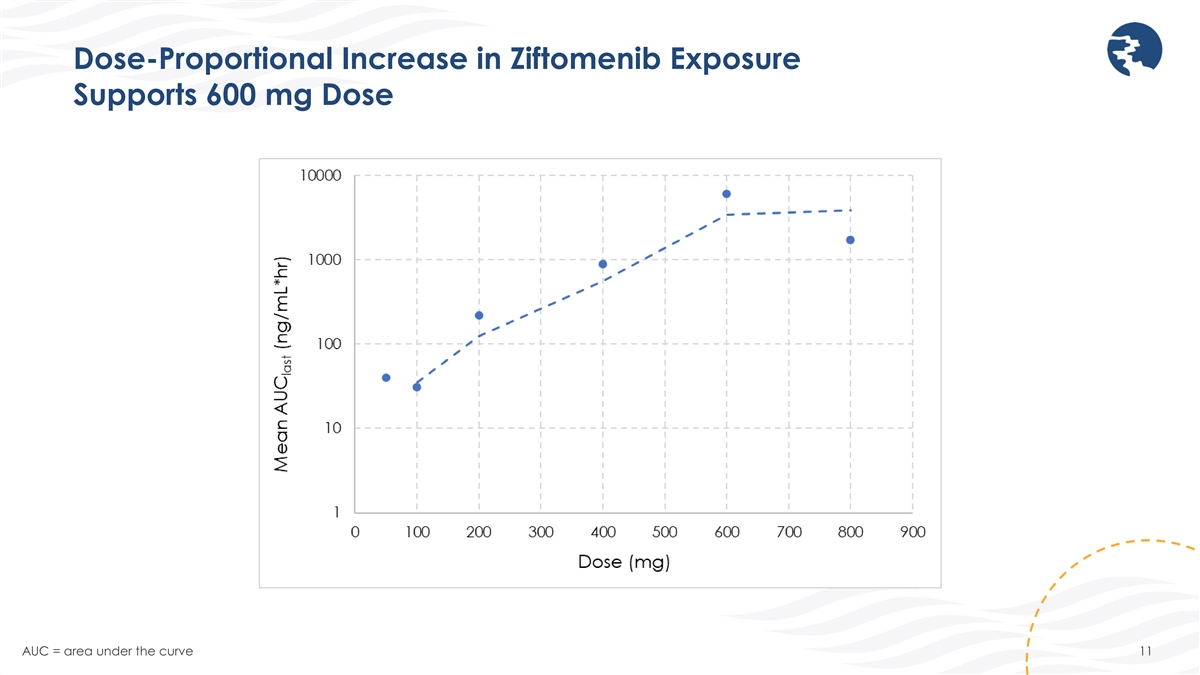
Ziftomenib 暴露量的剂量成比例增加支持 600 mg 剂量 AUC = 曲线下方的面积 11

Ziftomenib 在 1b 期表现出令人鼓舞的安全性 • 采用缓解策略的 npm1-m 单一疗法患者中分化综合征 (DS) 似乎可以控制 • 轻度至中度 DS 的发生率为 20% • Kmt2a-R 单一疗法患者的分化综合征 20% 在 200 mg 时为 38.5%,600mg 时为 37.5%;联合使用 有可能缓解 • DS 是靶向不良反应,代表临床活性的证据 • 无报告药物诱导的 qTc 延长 • 维持计数恢复表明没有药物诱发的骨髓抑制 Fathi 等人EHA 2023 #LB2713(截至 2023 年 4 月 12 日的初步数据)12

Ziftomenib 具有高度差异化的单一疗法总体反应最佳 在 npm1-m 期 600 mg 差异化 CR 率与 SOC 的比较 1a + 1b (n=20) 40% 的 NPM1 重度预治疗患者患者 CR 7 (35.0) 在 cRC 8 (40.0) npm1m 的先前疗程中实现了中位数 cr/crH 7 (35.0) 突变 CR% mdOR CR 35% 研究 Ziftomenib 1 MRD 阴性 4 (50.0) flt3m-3 33% 600mg QD IDH 1/2-50% ORR 9 (45.0) Gilteritinib flt3m 14.2% 14.8 mo 1 kmt2a-R 期 1a + 1b (n=18) Enasidenib IDH2 19% 8.2 mo 2 cr/CRH 2 (11.1) Ivosidenib IDH2 19% 8.2 cr/CRH 2 (11.1) Ivosidenib IDH2 H1 25% 10.1 mo 2 cRC 3 (16.7) *未经审查的 cRC DoR 中位数 HSCT MRD 阴性 3 (100.0) 来源:USPI 的 ORR 3 (16.7)(截至 2023 年 4 月 10 日的初步数据)Ø 活性高、反应持久、良好的形象表明 ziftomenib 有可能成为 在整个急性髓细胞白血病护理过程中的骨干疗法 1 对 6/8 cRC 患者进行了评估;在这6名患者中,有4名接受了评估接受检测的患者(67%)为 MRD 阴性 13 cRC 包括 CR、cRH、cRi、cRp;ORR 包括 CR、crH、cRi、cRi、cRp、MLFS
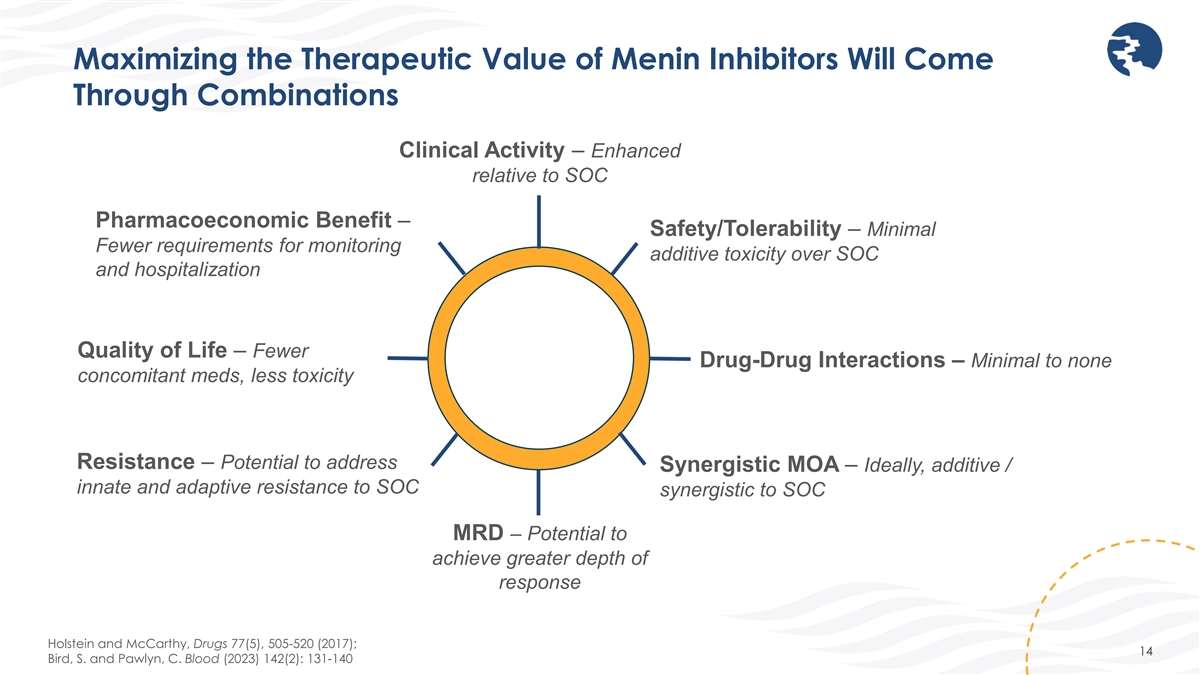
最大限度地提高梅宁抑制剂的治疗价值将通过 组合临床活性 — 相对于 SOC 药物经济效益而言得到增强 — 安全性/耐受性 — 最低监测添加剂毒性比 SOC 和住院生活质量的要求更低 — 更少 药物相互作用 — 几乎没有伴随药物,毒性耐药性更低 — 可能解决协同性 MOA — 理想情况下,对 SOC 协同作用的添加剂/先天和适应性耐药性到 SOC MRD — 有可能实现更大的响应深度 Holstein 和McCarthy,Drugs 77 (5),505-520 (2017);14 Bird、S. 和 Pawlyn,C. Blood (2023) 142 (2):131-140

来自 KOMET-007 试验的初步组合数据 Amer Zeidan,MBBS — 耶鲁癌症中心披露:Kura Oncology 提供的酬金或咨询费

KOMET-007:齐托莫尼布对新诊断或复发性急性髓细胞白血病患者的1期联合试验 ziftomenib/cytarabine/Daunorubicin(7+3)组合患者 • 齐夫托莫尼布的给药将从第 1 周期开始,之后持续给药 • 阿糖胞苷将在 C1 第 1-7 天给药; 再给药骨髓活检结果 • Daunorubicin 将在 C1 第 1-3 天给药;根据 C1 骨髓活检结果再给药一个周期 • 对有 不良风险的患者进行剂量递增* *年龄 >60 年和/或治疗相关急性髓细胞白血病和/或不良风险细胞遗传学根据 ELN 16 DL = 齐夫托美尼剂量水平;zifto = 齐夫托美尼;7+3 = 阿糖胞苷/柔红霉素;RP2D = 推荐的 2 期剂量;1L = 一线;IC = 强化 化疗
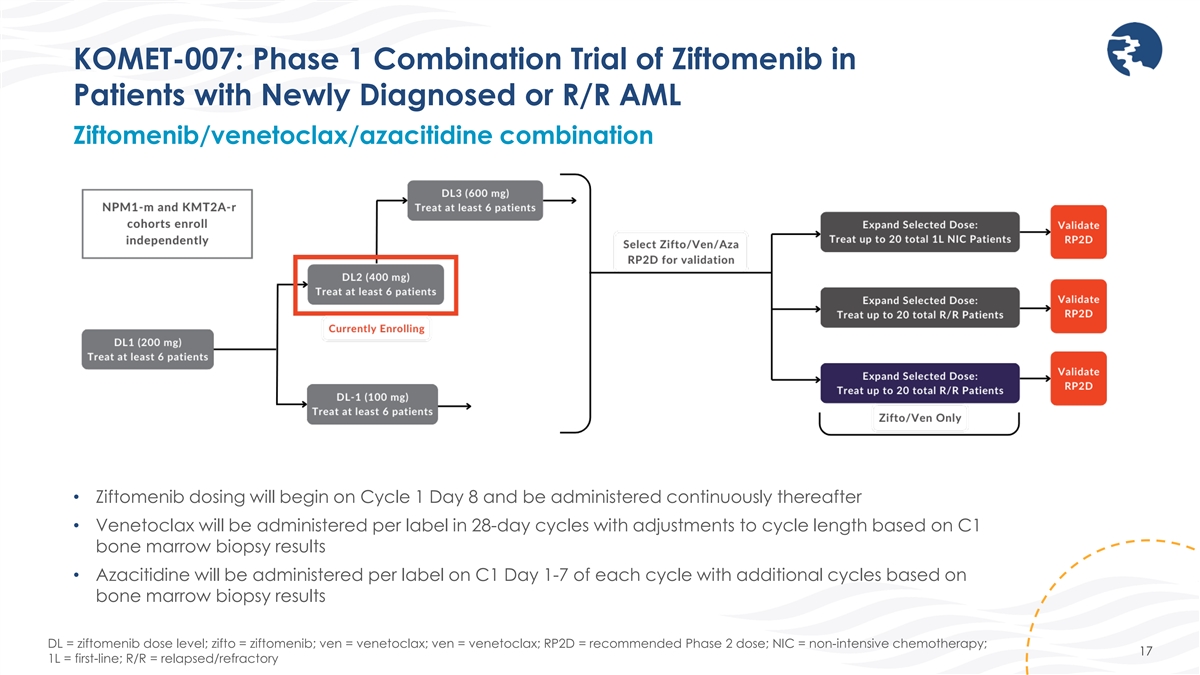
KOMET-007:齐托莫尼布对新确诊或复发性急性髓细胞白血病患者的1期联合试验 ziftomenib/Venetoclax/Azacitidine 组合患者 • 齐夫托莫尼布的给药将从第 1 周期开始,之后持续给药 • Venetoclax 将以 28 天为周期给药, 将根据 C1 骨髓活检结果调整周期长度 • 阿西替丁将在每个周期的 C1 第 1-7 天按标签给药,并根据骨髓活检结果延长周期 DL = 齐夫托美尼的剂量水平;zifto = ziftomenib;ven =venetoclax;ven = venetoclax;RP2D = 推荐的 2 期剂量;NIC = 非强化化疗;17 1L = 一线;R/R = 复发/难治性
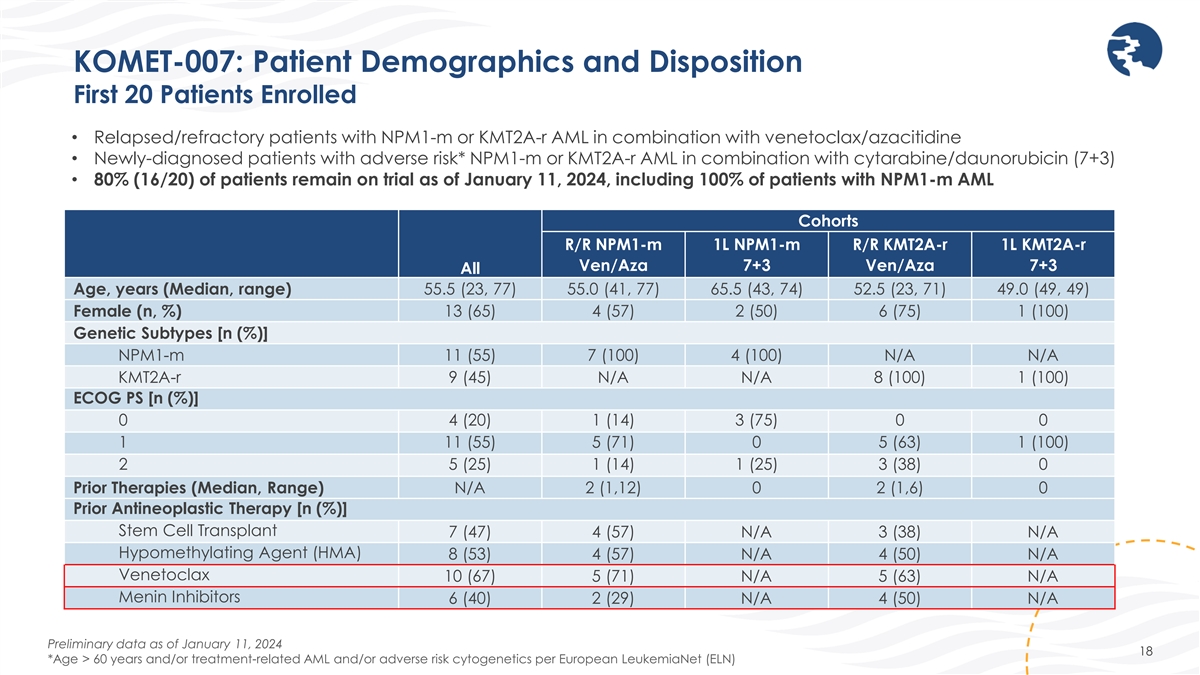
KOMET-007:患者人口统计和处置前 20 名患者 入组患者 • npm1-m 或 kmt2a-R 急性髓细胞白血病联合使用 venetoclax/azacitidine 的复发/难治性患者 • 新诊断的不良风险患者* npm1-m 或 Kmt2a-R 急性髓细胞白血球联合阿糖滨/柔比星 (7+3) • 80% (16/20)) 的患者截至 2024 年 1 月 11 日仍在试验中,包括 100% 的 npm1-m AML 同期患者 R/R npm1-m 1L npm1-m R/R kmt2a-R 1L kmt2a-R 1L kmt2a-R Ven/Aza 7+3 Ven/Aza 7+3 所有年龄、年龄(中位数,范围)55.5 (23, 77) 55.0 (41, 77) 65.5 (43, 74) 65.5 (43, 74) 52.5 (23, 71)) 49.0 (49, 49) 13 (65) 4 (57) 2 (50) 6 (75) 1 (100) 雌性 (n,%) 遗传亚型 [n (%)]npm1-m 11 (55) 7 (100) 4 (100) N/A N/A kmt2a-R 9 (45) N/A 8 (100) 1 (100) ECOG PS [n (%)]0 4 (20) 1 (14) 3 (75) 0 0 1 11 (55) 5 (71) 0 5 (63) 1 (100) 2 5 (25) 1 (14) 1 (25) 1 (25) 3 (38) 0 先前的疗法(中位数,范围)N/A 2 (1,12) 0 2 (1,6) 0 先前的抗肿瘤疗法 [n (%)]干细胞移植 7 (47) 4 (57) N/A 3 (38) N/A 低甲基化剂 (HMA) 8 (53) 4 (57) N/A 4 (50) N/A Venetoclax 10 (67) 5 (71) N/A 5 (63) N/A Menin 抑制剂 6 (40) 2 (29) N/A 4 (50) N/A 截至2024年1月11日的初步数据 18 *年龄 > 60 岁和/或治疗相关 AMS 根据欧洲白血病网 (ELN) 的 L 和/或不良风险细胞遗传学

KOMET-007:组合 组合具有良好的安全性和耐受性可降低分化综合征 (DS) 等级 ≥ 3 TEAE (≥ 10%) n (%) ≥ 3 级 Ziftomenib 相关不良反应(全部)n (%) ≥ 3 级患者齐夫托梅尼布相关不良反应的患者 18 (90) Ziftomenib 相关 AE 的患者 6 (30) 血小板计数减少 6 (30) 血小板计数减少 3 (15) 发热性中性粒细胞减少症 5 (25) 贫血 1 (5) 白细胞计数下降 4 (20) 发热性中性粒细胞减少症 1 (5) 肺炎 3 (15) 白细胞减少症 1 (5) 缺氧 2 (10) 中性粒细胞计数 1 (5) 中性粒细胞计数减少了 2 (10) 血小板减少症 1 (5) 败血症 2 (10) 血小板减少症 2 (10) • 未报告 DS 事件 • 迄今未观察到剂量限制毒性 (DLT),包括血液学计数恢复延迟 • 未观察到 qtC 延期 • TEAE 与基础疾病和骨干疗法一致 2024 年 1 月 11 日的初步数据 19 TEAES = Treatment-emerment-emergent 严重的不良事件
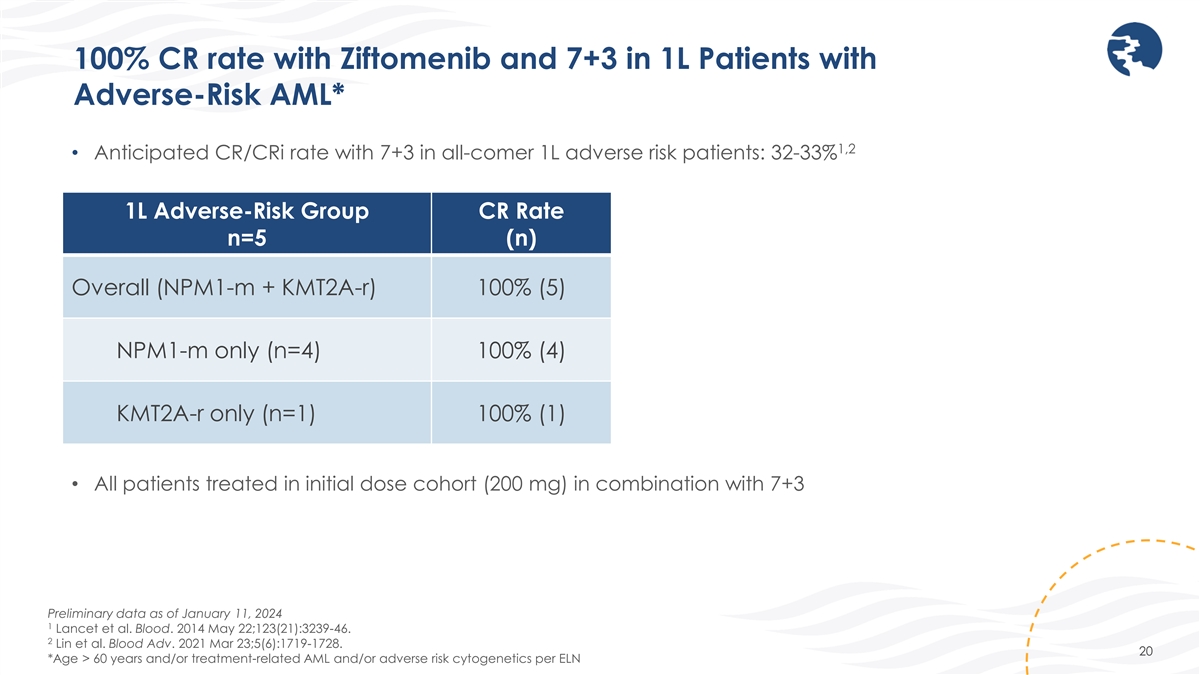
齐托莫尼布的CR率为100%,1L不良风险患者的CR率为7+3 AML* 1,2 • 全来者 1L 不良风险患者的预期 CR/CRI 率为 7+3:32-33% 1L 不良风险组 cr 率 n=5 (n) 总体 (npm1-m + kmt2a-r) 100% (5) 仅限 npm1-m (n=4) 100% (4) 仅限 Kmt2a-R (n=1) 100% (1) • 所有患者 在初始剂量队列(200 mg)中联合使用 7+3 截至2024年1月11日的初步数据 1 Lancet 等人Blood。2014 年 5 月 22 日;123 (21): 3239-46. 2 Lin 等人。Blood Adv. 2021 年 3 月 23 日;5 (6): 1719-1728. 20 *根据ELN,年龄 > 60 岁和/或 治疗相关急性髓细胞白血病和/或不良风险细胞遗传学

Ziftomenib + Ven/Aza 在脑膜抑制剂中具有明显活性 天真患者 1 • ven-naive 复发/难治性患者 cr/CRI 预计约为 35-45% 2 • Kmt2a-R 复发/难治性 AML 的预期反应率
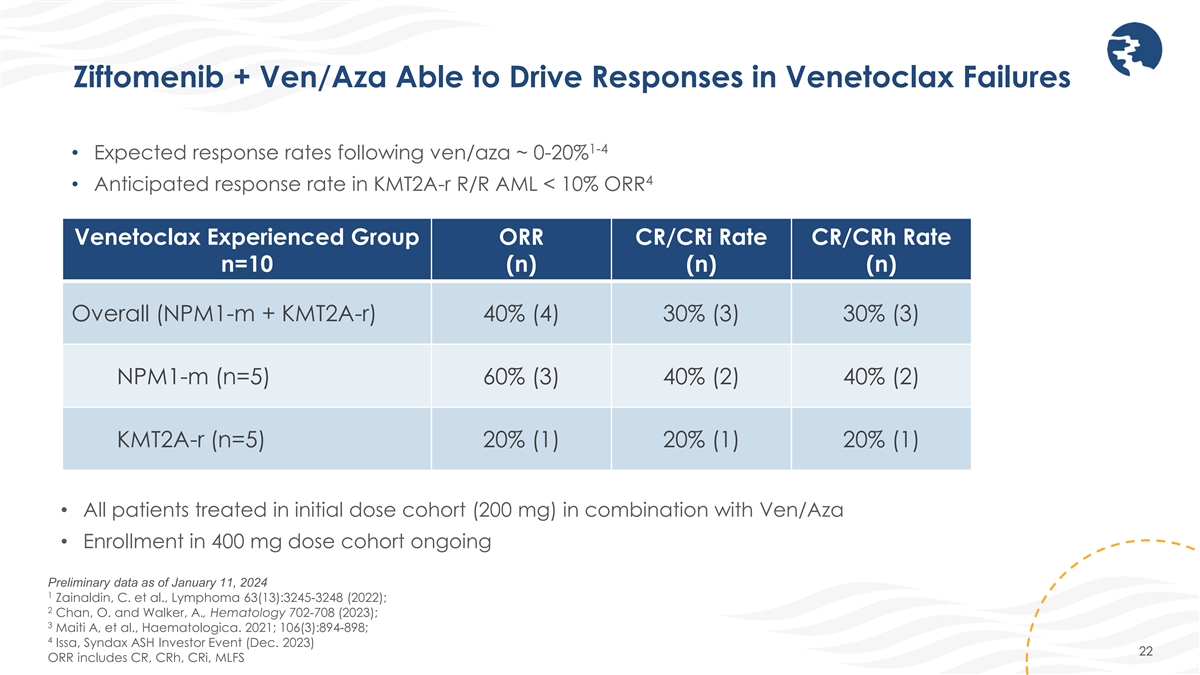
Ziftomenib + Ven/Aza 能够在 Venetoclax 失败 1-4 中推动响应 • ven/aza 之后的预期响应率 ~ 0-20% 4 • Kmt2a-R R/R AML 的预期响应率
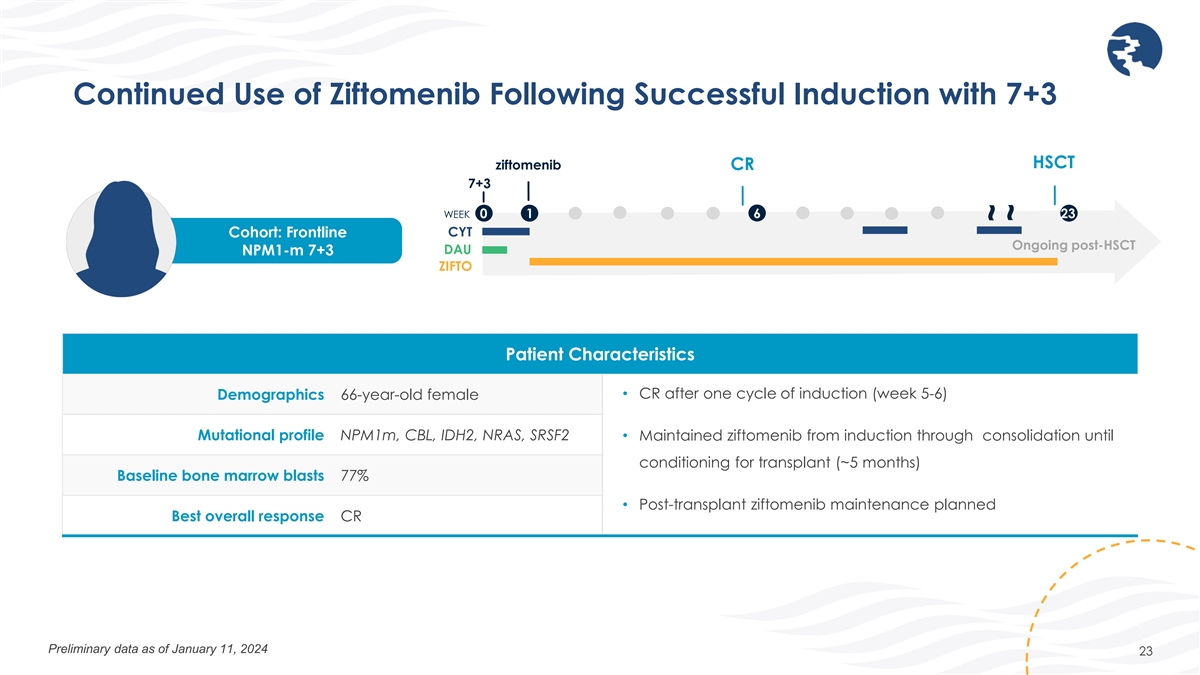
成功引导 7+3 HSCT ziftomenib CR 7+3 WEEK 0 1 6 23 CYT 队列后继续使用 Ziftomenib 后继续使用 Ziftomenib DAU npm1-m 7+3 ZIFTO 患者特征 • 一个诱导周期(第 5-6 周)后的 CR 人口统计 66 岁女性突变概况 npm1m、CBL、IDH2、NRAS、 SRSF2 • 从诱导到巩固直至移植条件维持齐夫托美尼(约 5 个月)基线骨髓爆发 77% • 计划移植后齐夫托美尼维持最佳总体反应 CR 截至1月11日的初步数据 2024 23 ~~
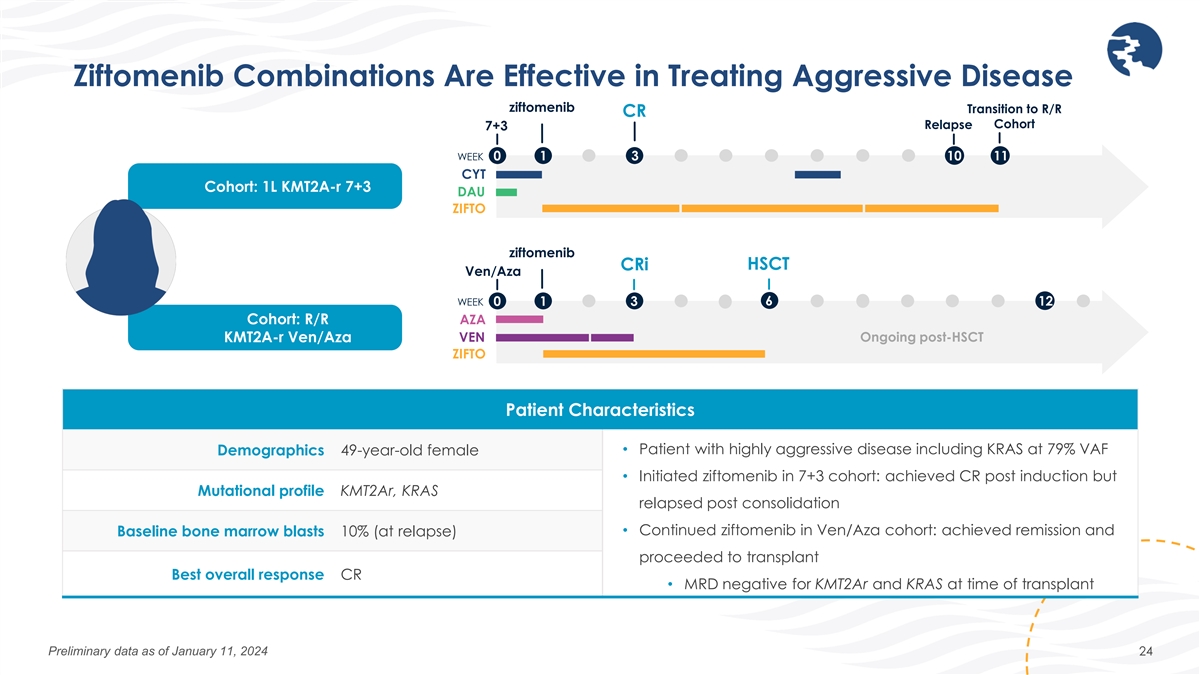
齐托莫尼布组合可有效治疗侵袭性疾病 ziftomenib 过渡到复发/R CR 复发队列 7+3 周 0 1 3 10 11 CYT 队列:1L kmt2a-R 7+3 DAU ZIFTO ziftomenib crI HSCT ven/Aza 6 周 0 1 3 12 队列:R/R AZA kmt2a-R Ven/Aza VEN/AZA 后仍在继续 sct ZIFTO 患者特征人口统计 49 岁女性 • 患有高侵袭性疾病的患者,包括 KRAS,VAF 为 79% • 在 7+3 队列中开始使用齐托美尼:诱导后获得 CR 但突变特征 kmt2ar,KRAS 在巩固后复发 • 续 ziftomenib 在 Ven/Aza 队列:已实现缓解,基线骨髓爆炸 10%(复发时)继续移植最佳总体反应 CR • 移植时 KMT2ar 和 KRAS 的 MRD 阴性截至2024年1月11日的初步数据 24
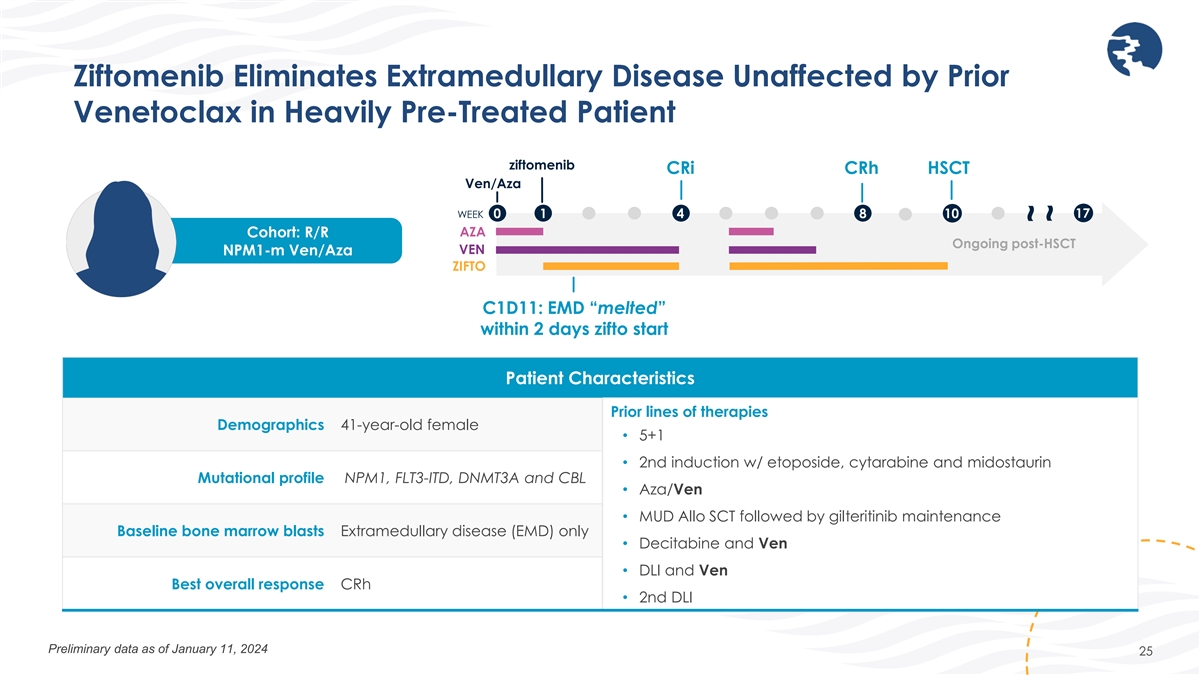
Ziftomenib 可消除未受先前 Veneclax 影响的重度预治疗患者中的髓外疾病 ziftomenib crI crH HSCT Ven/Aza 17 周 0 1 4 8 10 AZA 队列:R/R 后 HSCT 正在进行中 Venpm1-m Ven/Aza ZIFTO C1D11:EMD 在 2 天内 “融化” 了 zifto 开始患者特征 疗法的先前线路人口统计 41 岁女性 • 5+1 • 使用依托泊苷、阿糖胞苷和米多司他林进行第二次诱导 Mutational profice NPM1、FLT3-ITD、DNMT3A 和 CBL • Aza/Ven • MUD Allo SCT 其次是吉特替尼维持基线 骨髓细胞外爆炸仅限疾病(EMD)• 地西他滨和 Ven • DLI 和 Ven Best 总体反应 crH • 第 2 次 DLI 截至 2024 年 1 月 11 日的初步数据 25 ~ ~

临床开发计划 Mollie Leoni,医学博士 — 临床开发执行副总裁

Ziftomenib 临床开发路径开发方法计划中的研究 启动阶段 1 注册定向试验 NPM1 突变体急性髓系白血病 (AML) 单一疗法 non-npm1-m/kmt2a-R 急性髓细胞白血病(复发/难治性)KMT2A-重排所有与 NPM1 突变体 AML VENETOCLAX + 阿扎西替丁 KMT2A-重排的 AML (复发/难治性,前线)与 NPM1 突变体 AML 阿糖胞苷 + 柔红霉素 (7+3) KMT2A 重组急性髓细胞白血病(复发/难治性,前线)联合吉利替尼、NPM1 突变体 AML FLAG-IDA、LDAC KMT2A-重排急性髓细胞白血病 (复发/难治性)npm1-突变体急性髓细胞白血病研究员/公司-移植后维护赞助的研究 KMT2A 重新安排的 AML 儿科急性髓细胞白血病和所有联合疗法 FLA 研究者赞助的研究儿科全部与 BV-DAM 联合使用 27

市场机会和即将到来的里程碑特洛伊·威尔逊博士、法学博士 — Kura Oncology 总裁兼首席执行官

Ziftomenib 在反洗钱及其他领域提供了数十亿美元的机会 有可能改变整个护理过程的预后 • 初步批准占潜在患者复发的 30%/• KOMET-001 注册导向的研究获得 FDA 全面批准的难治剂 • 1L 反洗钱和维护前线的重大机遇/• 有可能推动超过 50% 的收入维持 • 安全性、耐受性和临床活动预计将是与 SOC 和 SOC 联合治疗的理想选择维护指示 • 除 AML 之外还有引人注目的 其他机会提供数十亿美元的其他潜在适应症 • 早期转化数据支持实体瘤和非肿瘤学适应症的潜力 29

齐托莫尼布在急性白血病中的即将到来的里程碑预计时间 成就里程碑与 FLT3 抑制剂吉利替尼联合使用 KOMET-008 试验的首批患者剂量,2024 年第一季度 LDAC 和 FLAG-IDA 启动移植后维持计划 2024 年第一季度将齐夫托莫尼的开发扩展到急性淋巴细胞 白血病 (ALL) 2024 年第一季度完成 KOMET-001 注册中期试验中 85 名患者的入组 2024 确定与 ven/aza 联合使用的推荐的 2 期剂量 2024 年中期在 1L 中与 ven/aza 联合使用启动剂量验证/扩展 AML 2024 年中期提供 2024 年下一次 KOMET-007 组合更新 • 5.7 亿美元的预计现金*为进入 2027 年提供了机会,使齐夫托梅尼布和其他管道 资产的价值最大化 * 包括截至2023年12月31日的4.24亿美元现金、现金等价物和短期投资,以及2024年1月26日结束的私募中扣除发行费用后的1.46亿美元估计收益 30

开发治疗癌症的精准药物来自 KOMET-007 的初步 数据 — 2024 年 1 月 30 日