| 公司介绍 LEAP THERAPEUTICS 2024 年 1 月 23 日 |
| 前瞻性陈述 2 本演示文稿包含涉及重大风险和不确定性的前瞻性陈述 。 本演示文稿中包含的所有陈述,除历史事实陈述外, ,包括有关我们 战略、未来运营、临床试验、合作和 合作伙伴关系、未来财务状况、未来收入、预计成本、管理前景、计划和目标的陈述, 均为美国 证券法所指的前瞻性陈述。“预期”、“相信”、“估计”、 “期望”、“打算”、“可能”、“计划”、“预测”、“项目”、“目标”、 “潜力”、“将”、“可能”、“应该”、“继续”、 等词语旨在识别前瞻性 陈述,尽管并非所有前瞻性陈述都包含 陈述 br} 这些识别词。 前瞻性陈述既不是历史事实,也不是对未来表现的保证。相反,它们仅基于我们当前对 业务的未来、未来计划和战略、 预测、预期事件和趋势、经济和 其他未来状况的信念、预期和假设。 由于前瞻性陈述与未来有关, 它们受固有的不确定性、风险 和难以预测的情况变化影响 ,其中许多是我们无法控制的。我们 可能无法实际实现我们在前瞻性陈述中披露的计划、意图或预期 ,并且您 不应过分依赖我们的前瞻性 陈述。实际结果或事件可能与我们在前瞻性陈述中披露的计划、意图和预期 存在重大差异。 在向美国证券交易所 委员会提交的报告中不时列出这些和其他风险因素 ,包括但不限于我们的10-K表年度 报告和10-Q表季度报告 。除非适用法律要求 ,否则我们认为没有义务更新 任何前瞻性陈述。 本演示不构成任何证券的卖出要约、 或购买要约的邀请。 |
| 为癌症患者开发生物标志物靶向抗体疗法 3 两个临床阶段 抗体项目 — DKN-01 靶向 CLDN18.2 两个 随机临床试验即将推出的多个 里程碑 生物标志物策略, 将重点放在胃肠癌 2025 年第二季度现金流失至 2025 年第二季度, 2023 年 12 月 31 日, 7,000 万美元 FL-301 |
| 管道 4 适应症:治疗:临床前 1 期 2 期 3 期合作伙伴: DKN-01 抗 DKK1 抗体 替雷利珠单抗 + 化疗 br} + 化疗 pembrolizumab FL-302 (NBL-016) 抗 CLDN18.2/CD137 双特异性抗体 FL-301 (NBL-015) 抗 CLDN18.2 抗体 胃 癌 胃 癌 结直肠癌 子宫内膜 癌 子宫内膜 癌 FL-501 抗 GDF15 抗体 胰腺癌 癌 |
| DKN-01 抗 DKK1 单克隆 抗体 |
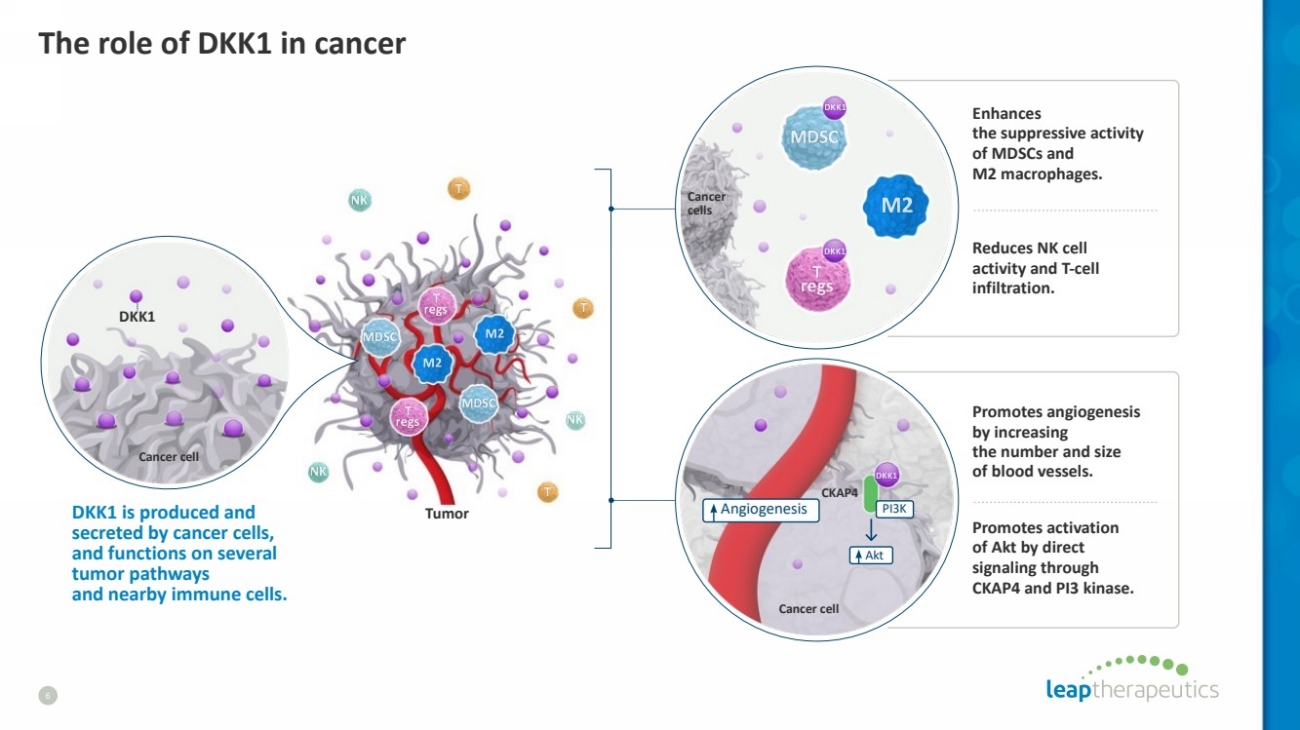
| DKK1 在癌症中的作用 6 肿瘤 CKAP4 血管新生 Akt PI3K 癌细胞 Cancer 细胞 DKK1 由癌细胞、 分泌和 在几个 肿瘤通路 和附近的免疫细胞上起作用。 增强 MDSC 和 M2 巨噬细胞的抑制活性 。 降低 NK 细胞 活性和 T 细胞 浸润。 通过增加 血管的数量和大小 来促进血管生成 。 通过 CKAP4 和 PI3 激酶直接 信号,促进 Akt 的激活 。 癌细胞 DKK1 |
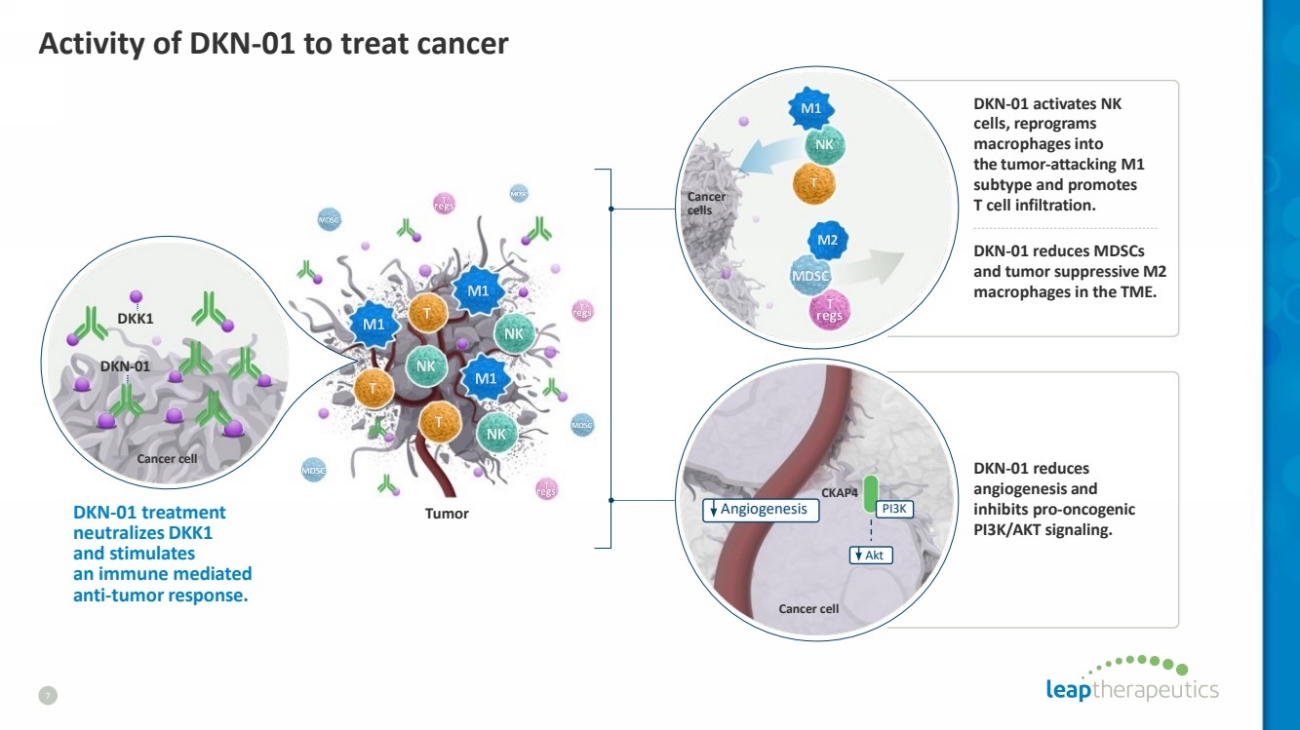
| DKN-01 治疗癌症的活性 7 CKAP4 血管新生 Akt PI3K 癌细胞 癌细胞 肿瘤 癌细胞 癌细胞 DKK1 DKN-01 治疗 可中和 DKK1 并刺激 免疫介导的 抗肿瘤反应。 DKN-01 DKN-01 激活 NK 细胞,将 巨噬细胞重新编程为攻击肿瘤的 M1 亚型 并促进 T 细胞浸润。 DKN-01 可减少 TME 中的 mdSC 和抑制肿瘤的 M2 巨噬细胞。 DKN-01 可减少 血管新生, 抑制促癌 PI3K/AKT 信号传导。 |
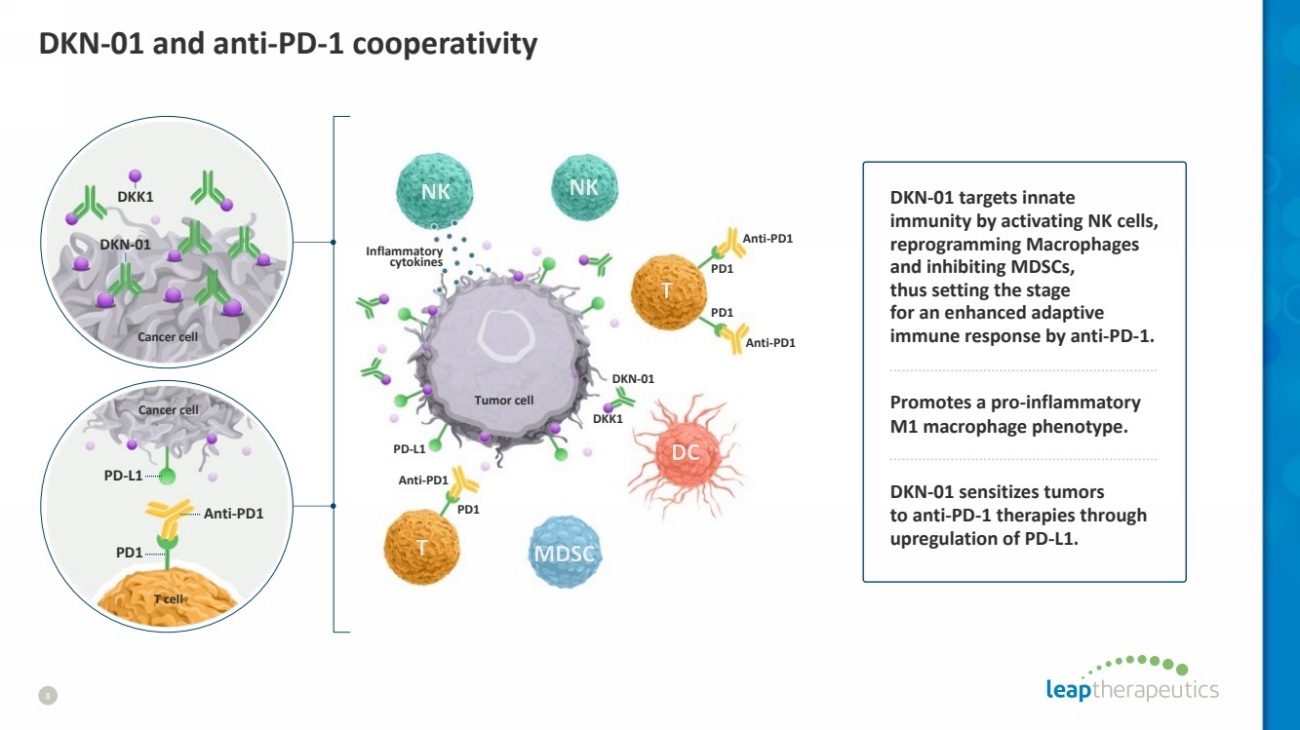
| DKN-01 和抗 PD-1 合作性 8 抗 PD1 抗 PD1 DKN-01 通过激活 NK 细胞、 重编程巨噬细胞 和抑制 mDSC 来靶向先天的 免疫力, 从而为抗 PD-1 增强适应性 免疫反应奠定了基础 。 促进促炎 M1 巨噬细胞表型。 DKN-01 通过 上调 PD-L1 使肿瘤 对抗 PD-1 疗法过敏。 PD1 抗 PD1 PD-L1 癌细胞 T 细胞 癌细胞 DKK1 DKN-01 炎症细胞因子 PD1 抗 PD1 PD-L1 肿瘤细胞 DKK1 DKN-01 |
| DKN-01 胃癌的发展 |
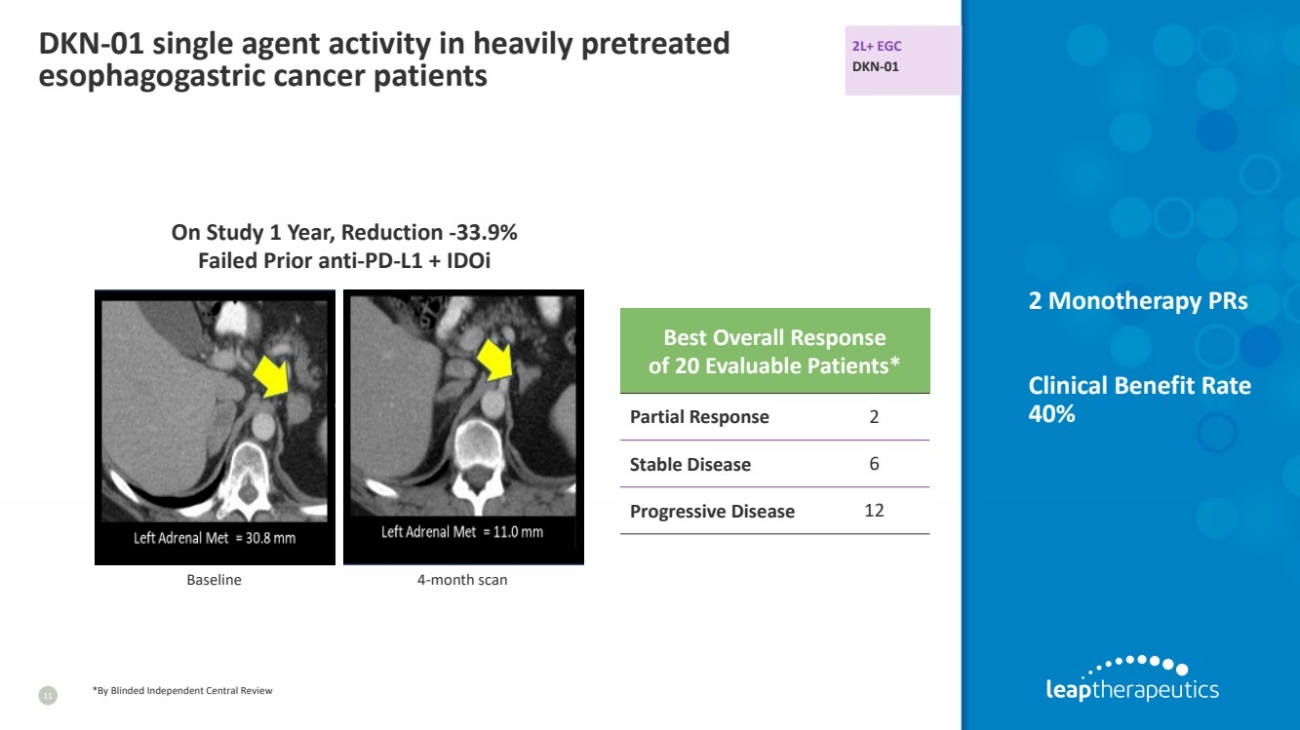
| DK1 水平高与胃癌存活率低有关 10 Strata 21 34 7 1 1 20 4 0 0 0 100 200 300 停药时间(天) 高水平的 DKK1 与较短的总存活率相关 在胃癌中 TCGA STAD 数据集 dk1-High 与对一线铂的反应不佳有关 + fluoropypypy基因/胃癌患者使用基于利米定的疗法 与 Tempus DK1 高患者 合作 高 dk1 患者 操作系统缩短 2.5 年 总体存活率 总体存活率 总体存活率 dk1-Low患者 天 0 1000 2000 3000 4000 100 存活概率 50 0 25 75 dkk1-High (n=175) dkk1-Low (n=175) p-val = 0.0164 (Mantel-Cox) 0.00 存活概率 0.00 0.75 0.25 p = 0.31 总生存率 } DKK1- 高 DKK1-low 有风险的数字 |
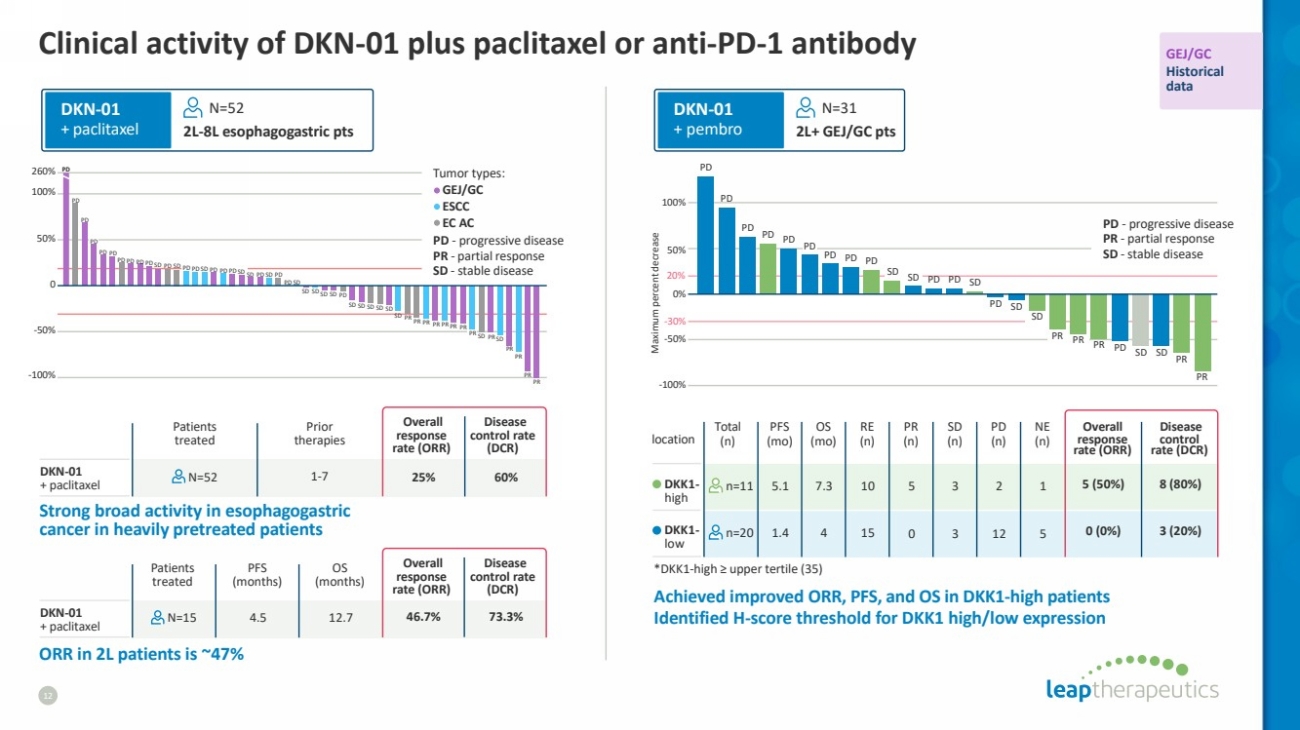
| 经过大量预先治疗的 食管胃癌患者的 DKN-01 单药活性 11 基线 4 个月扫描 研究 1 年,降低 -33.9% 先前抗PD-L1 + iDOI 20 名可评估患者的最佳总体反应 * 部分反应 2 稳定疾病 6 进展性疾病 12 *由盲人独立中心评论 2LD + EGC DKN-01 2 单一疗法 pR 临床获益率 40% |
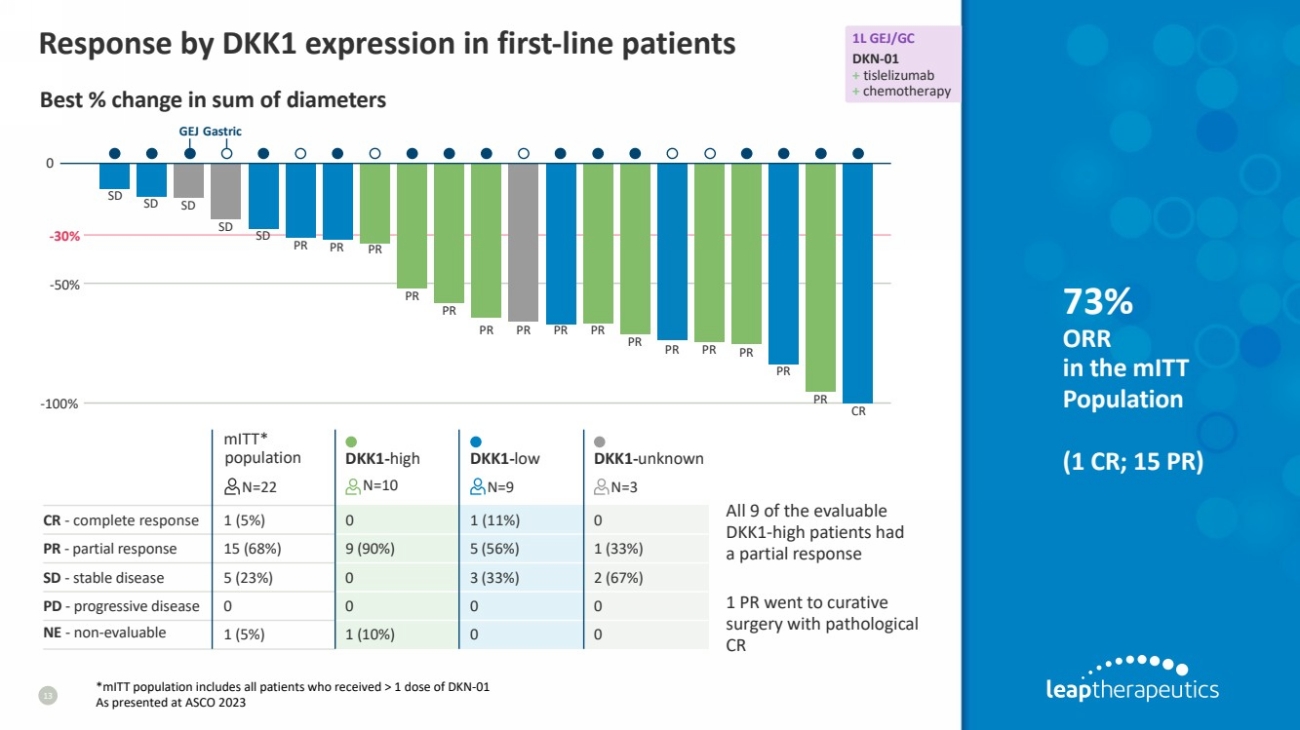
| *DK1-高 ≥ 上三分之一 (35) DKN-01 加紫杉醇或抗 PD-1 抗体的临床活性 12 PD PD PD PD PD PD PDPD PD PD PD PD SD SD SD SD SD SD PD PD SD SD SD SD PD PD SD SD SD SD PD PD PD SD SD SD SD PD PD PD SD SD SD PD PD PD PD SD SD SD SD PD PD PD PD SPD PD PD PD PD PD PD PR PR PR PR PR PR PR PR PR PD PD PD PD PD PD PD PD PD PD PD PD PD PD PD PD PD PD PD PD PD PD PD PD PD PD PD PD PD PD PD PD PD PD {br br} PR PR PR PR PR 50% -50% -100% 100% DKN-01 + 紫杉醇 N=52 DKN-01 + 紫杉醇 治疗的患者 之前的 治疗 N=52 60% 疾病 控制率 (DCR) 25% 总体 反应 率 (ORR) 2L-8L 食管胃病 GEJ/GC ESCC EC AC PD-进展性疾病 PR-部分反应 SD-稳定疾病 肿瘤类型: } 0 260% 2L 患者的 ORR 约为 47% 在经过大量预治疗的患者中,食道胃癌 具有很强的广泛活性 DKN-01 + 紫杉醇 治疗 PFS (月) (月) (月) (月) (月) N=15 12.7 73.3% OS (月) 疾病 (月) 控制率 (DCR) 46.7% 总体 响应 率 (ORR) 4.5 1-7 最大百分比减少 -100% 50% -50% -30% 100% 20% GEJ/GC 历史 数据 DKN-01 + pembro N=31 2L+ GEJ/GC pts 总地点 (n) RE (n) PR (n) PR (n) PR (n) } SD (n) PD (n) NE (n) 疾病 控制 率 (DCR) 总体反应 率 0% DKK1 高/低患者的 ORR、PFS 和 OS 得到改善 已确定 DKK1 高/低的 H 分阈值表情 n=11 n=20 10 5 3 2 1 0 3 12 5 8 (80%) 3 (20%) 5 (50%) 0 (0%) 0 (0%) 1-高 DKK1- 低 15 PD-进行性疾病 PR-部分响应 SD-稳定疾病 OS (mo) 7.3 4 PFS (mo) (mo) 5.1 1.4 |
| mitt* 人口 N=22 dkk1-高 N=10 dkk1-Low N=9 dkk1-未知 N=3 CR-完全反应 1 (5%) 0 1 (11%) 0 PR-部分反应 15 (68%) 9 (90%) 5 (56%) 1 (33%) SD-稳定疾病 5 (23%) 0 3 (33%) 2 (67%) PD-进行性疾病 0 0 0 0 NE-不可评估 1 (5%) 1 (10%) 0 0 0 MitT 人群中 DKK1 表达的反应 13 73% ORR (1 CR; 15 PR) {在 ASCO 2023 上,直径总和的最佳变化百分比 全部 9 个 DKN-01可评估 高 dk1 的患者 出现部分反应 1 PR 因病理 CR 1L GEJ/GC DKN-01 + 替雷利珠单抗 + 化疗 GEJ Gastric SD SD PR PR PR PR PR PR PR PR PR PR PR PR PR PR PR PR PR PR PR PR PR PR PR PR PR PR PR PR PR PR CR -50% -30% -30% 0 -100% |
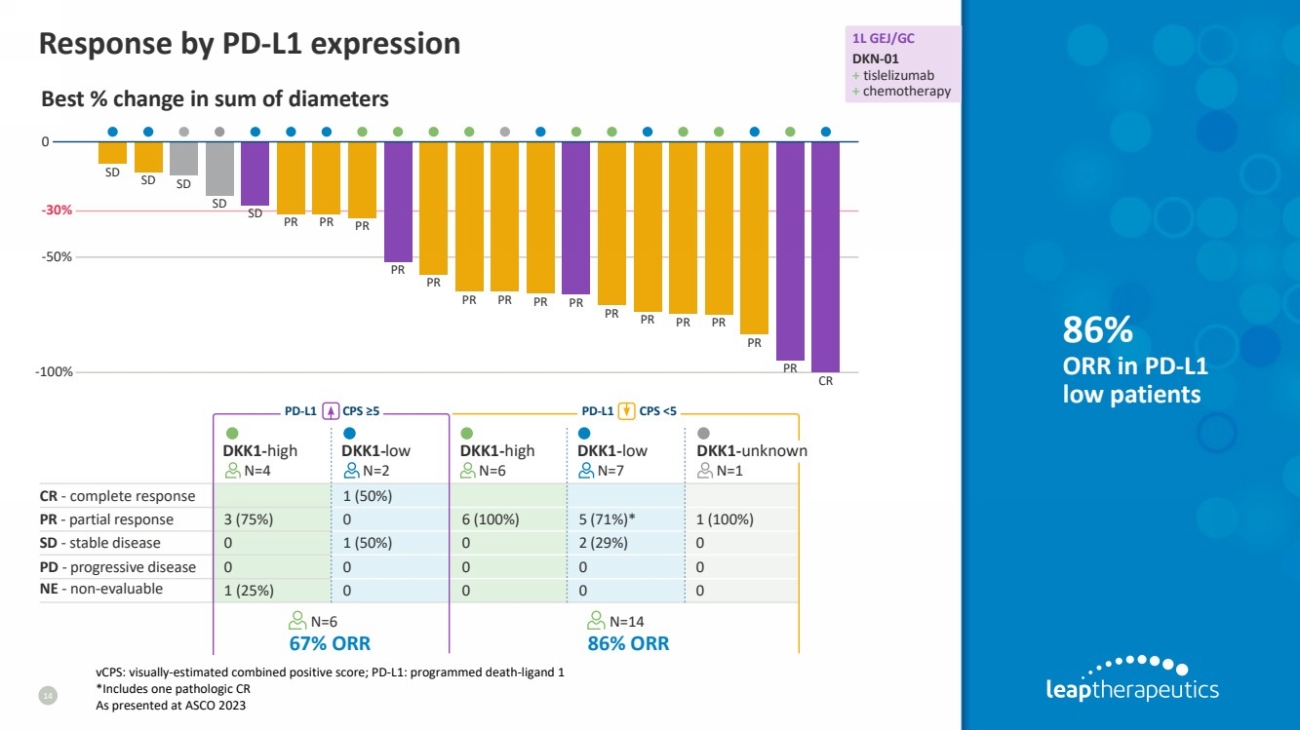
| PD-L1 表达 14 86% OR在 PD-L1 低位患者中的反应 直径总和的最佳变化百分比 vCPs:视觉估计的组合阳性评分;PD-L1:程序性死亡配体 1 *包括一种病理 CR 如在 ASCO 2023 1L GEJ/GC DKN-01 + 替利利单抗 + 化疗 -完成回应 1 (50%) PR-部分反应 3 (75%) 0 6 (100%) 5 (71%) * 1 (100%) SD-稳定疾病 0 1 (50%) 0 2 (29%) 0 PD-渐进性疾病 0 0 0 0 0 0 NE-不可评估 1 (25%) 0 0 0 DKK1-高 DKK1-低 DKK1-低 dk1-未知 N = 4N=2 N=6 N=7 N=1 N=6 N=14 PD-L1 CPS ≥5 67% 或 86% ORR PD-L1 CPS |
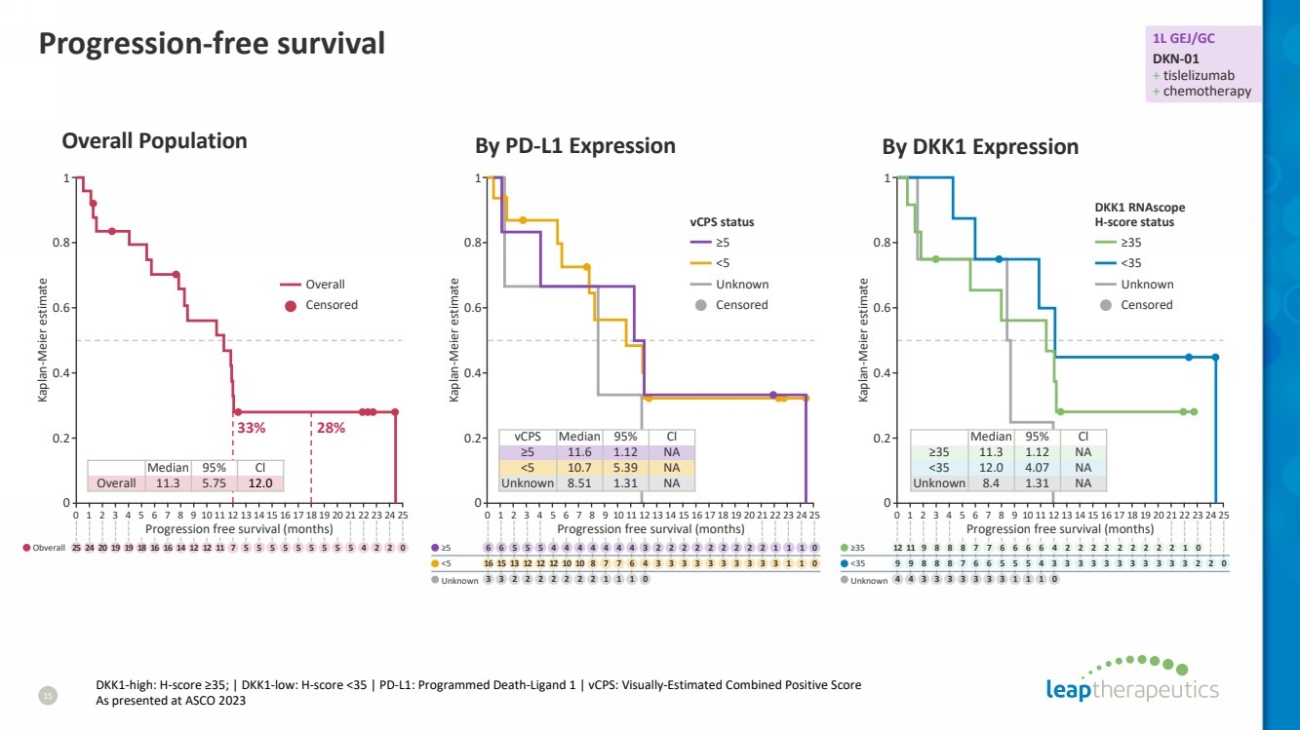
| 无进展存活率 15 总人群 dk1-高:H 分数 ≥35;| dkk1-低:H 分数 |
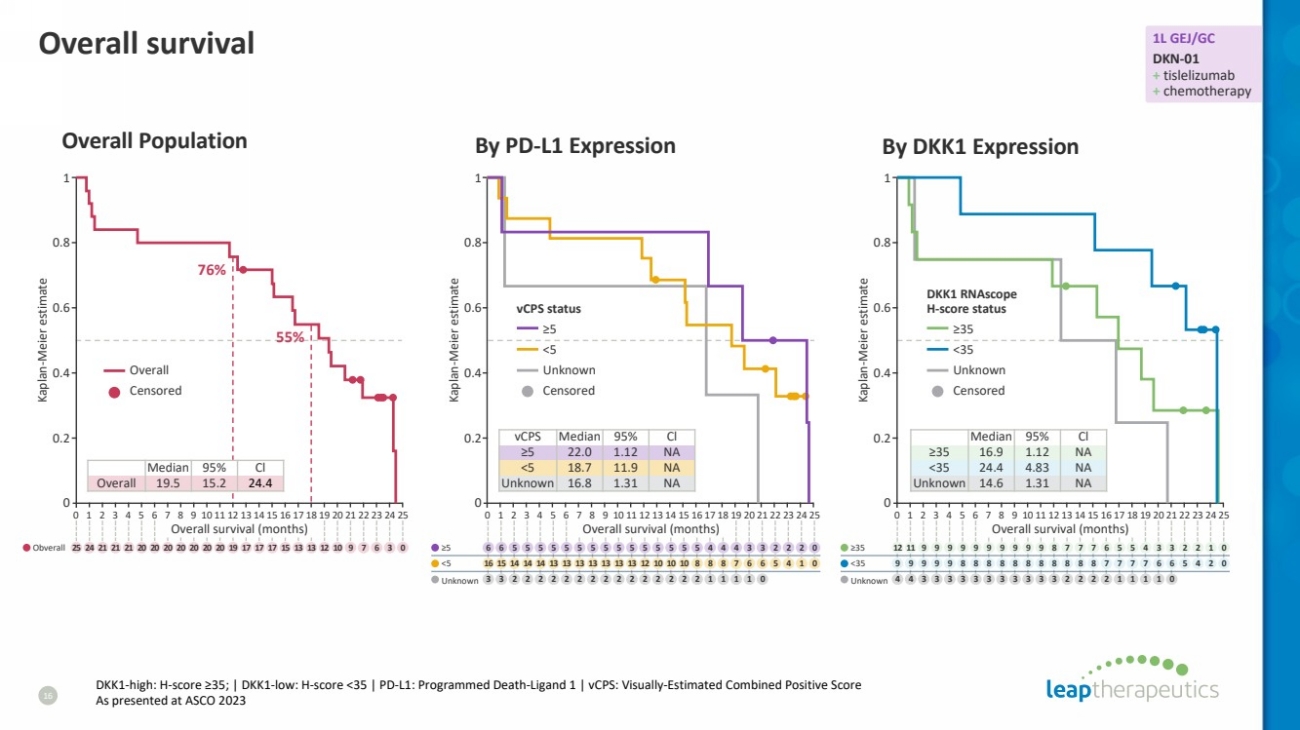
| 总存活率 16 dkk1-高:H 分数 ≥35;| dkk1-Low:H 分数 |
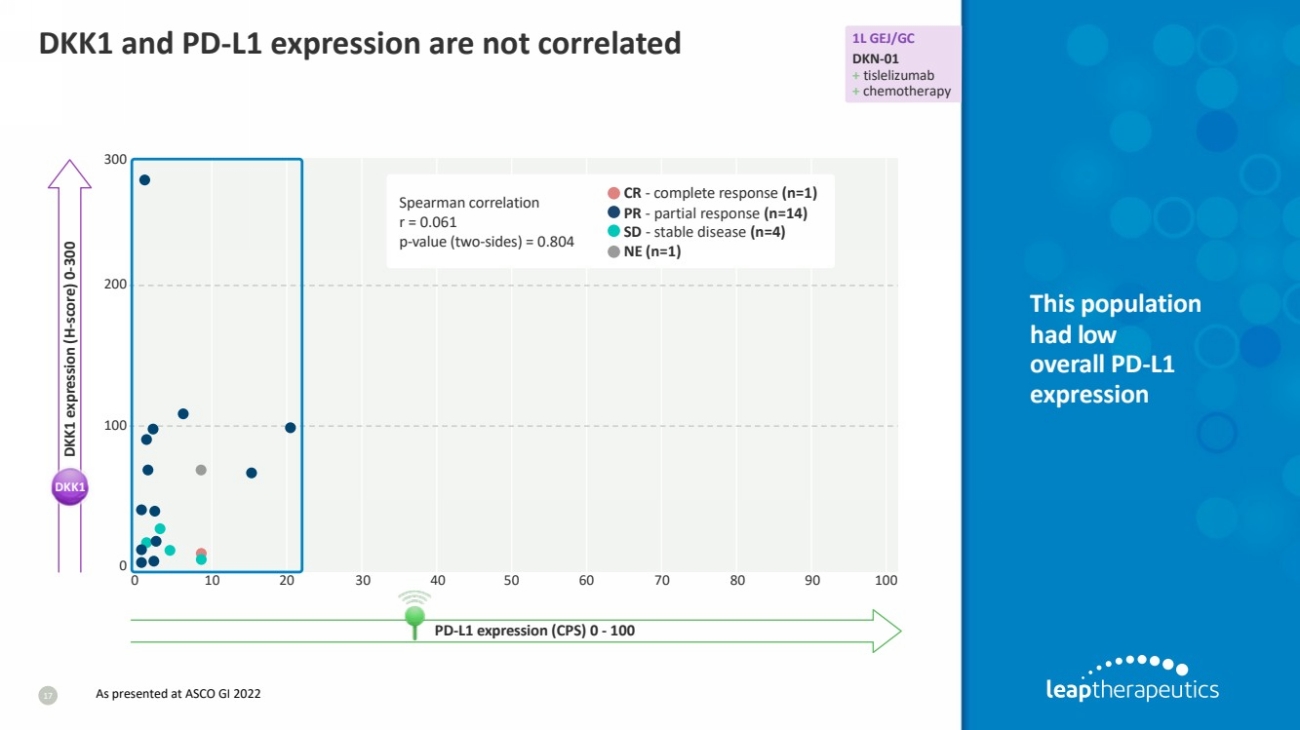
| DKK1 和 PD-L1 的表达不相关 17 该人群 的 PD-L1 总表达量低 1L GEJ/GC DKN-01 + 替雷利珠单抗 + 化疗 200 300 100 10 20 30 40 50 60 70 90 100 0 DKK1 表达 (H 分数) 0-300 PD-L1 表情 (CPS) 0-100 DKK1 0 Spearman 相关性 r = 0.061 p 值(双面)= 0.804 CR-完全反应 (n=1) PR-部分反应 (n=14) SD-稳定疾病 (n=4) NE (n=1) 如在 ASCO GI 2022 上所述 |
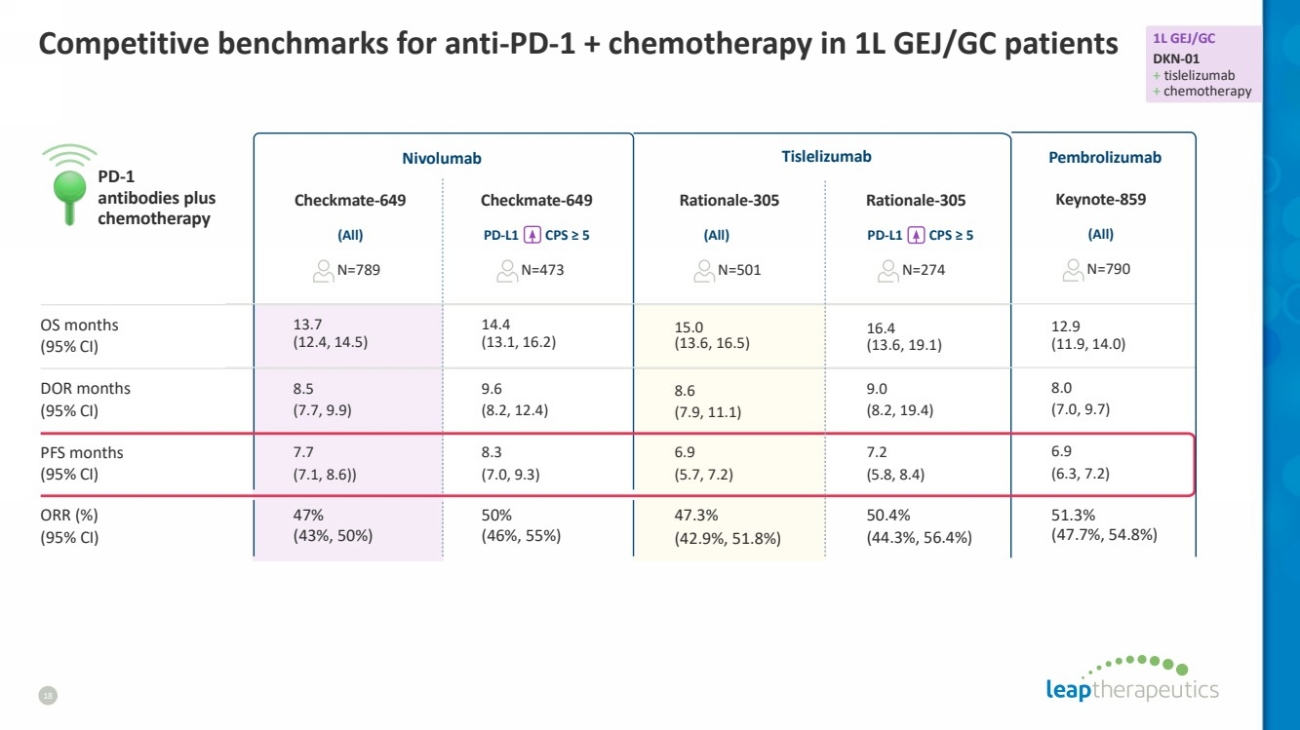
| 1L GEJ/GC 患者抗PD-1 + 化疗的竞争基准 18 Nivolumab Checkmate-649 ORR (%) (95% CI) 50.4% (44.3%,56.4%) 50% (46%,55%) 47% (43%,50%) 9.0 (8.2, 19.4) 9.6 (8.2, 12.4) 8.5 (7.7, 9.9) 8.3 (7.0, 9.3) 7.7 (7.1, 8.6)) 8.6 (7.9, 11.1) DOR 月 (95% CI) Checkmate-6649 Rationale-305 Tislelizumab PD-1 抗体加 化疗 N=789 N=473 N=501 N=274(全部)PD-L1 CPS ≥ 5 16.4(13.6、19.1) 14.4(13.1、16.2) 13.7(12.4、14.5) 15.0(13.6、16.5)) OS 月 (95% 置信区间) 7.2 (5.8, 8.4) 6.9 (5.7, 7.2) 47.3% (42.9%,51.8%) 1L GEJ/GC DKN-01 + 替雷利珠单抗 + 化疗 Rationale-305(全部)PD-L1 CPS ≥ 5 51.3% (47.7%,54.8%) 8.0 (7.0, 9.7) Keynote-859 Pembrolizumab N=790 12.9 (11.9, 14.0) 6.9 (6.3, 7.2) (全部) |
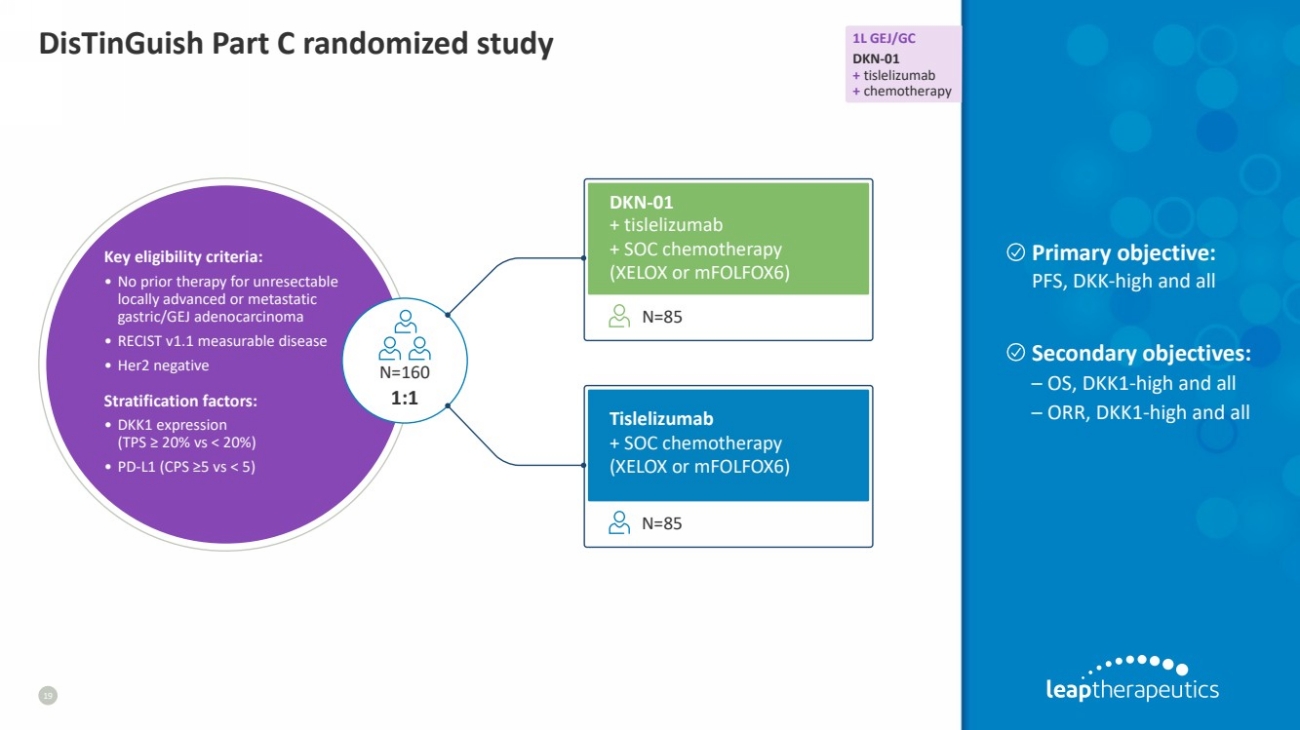
| 区分 C 部分随机研究 1L GEJ/GC DKN-01 + 替雷利珠单抗 + 化疗 19 DKN-01 + 替雷利珠单抗 + SOC 化疗 (XELOX 或 mfolFox6) + SOC 化疗 (XELOX 或 mfolFox6) 85 N=85 分层因子: • DKK1 表达式 (TPS ≥ 20% vs |
| DKN-01 结直肠癌的发展 |
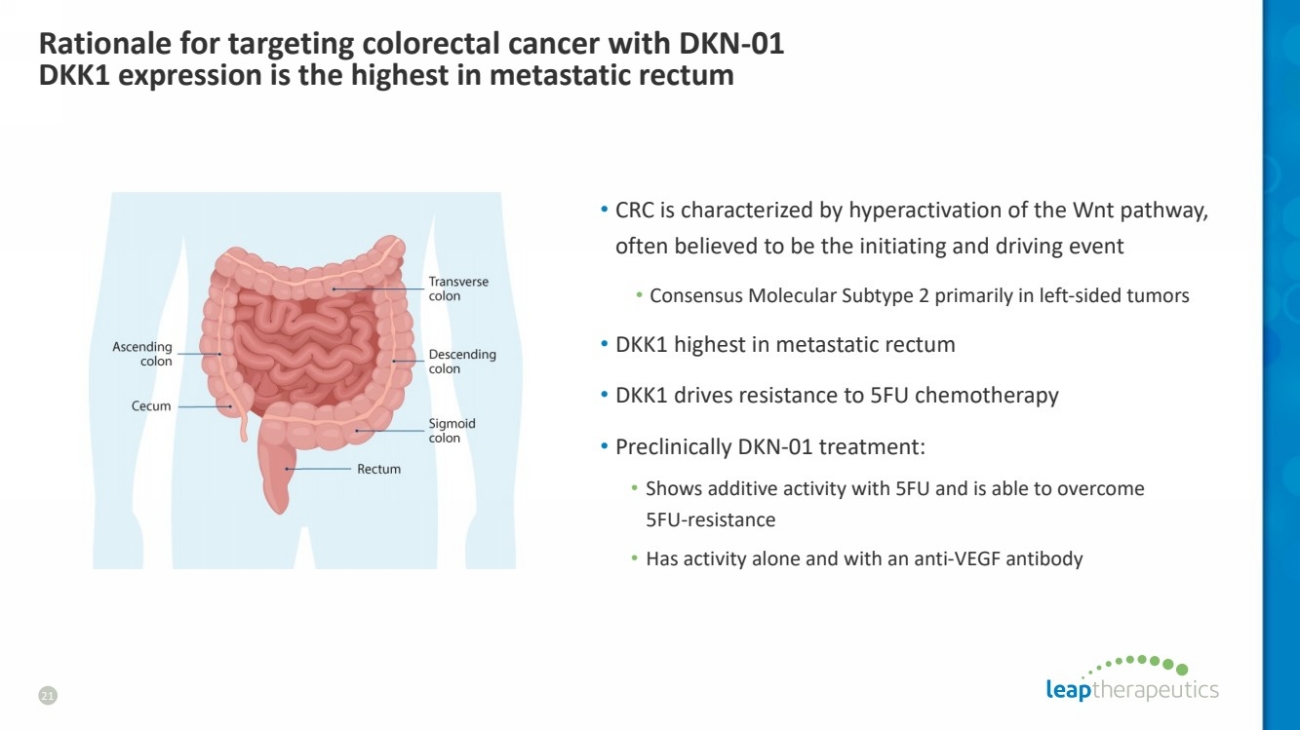
| 使用 DKN-01 靶向结直肠癌的理由 DKK1 表达在转移直肠中最高 21 • 结直肠癌的特征是 Wnt 通路的过度激活, 通常被认为是引发和驱动事件 • 共识分子亚型 2 主要出现在左侧肿瘤中 • DKK1 在转移性直肠中最高 • DKK1 驱动对 5FU 化疗的耐药性 • Preper 临床上 DKN-01 治疗: • 显示出 5FU 的添加活性,能够克服 5FU 耐药性 • 单独具有活性,使用抗血管内皮生长因子抗体 |
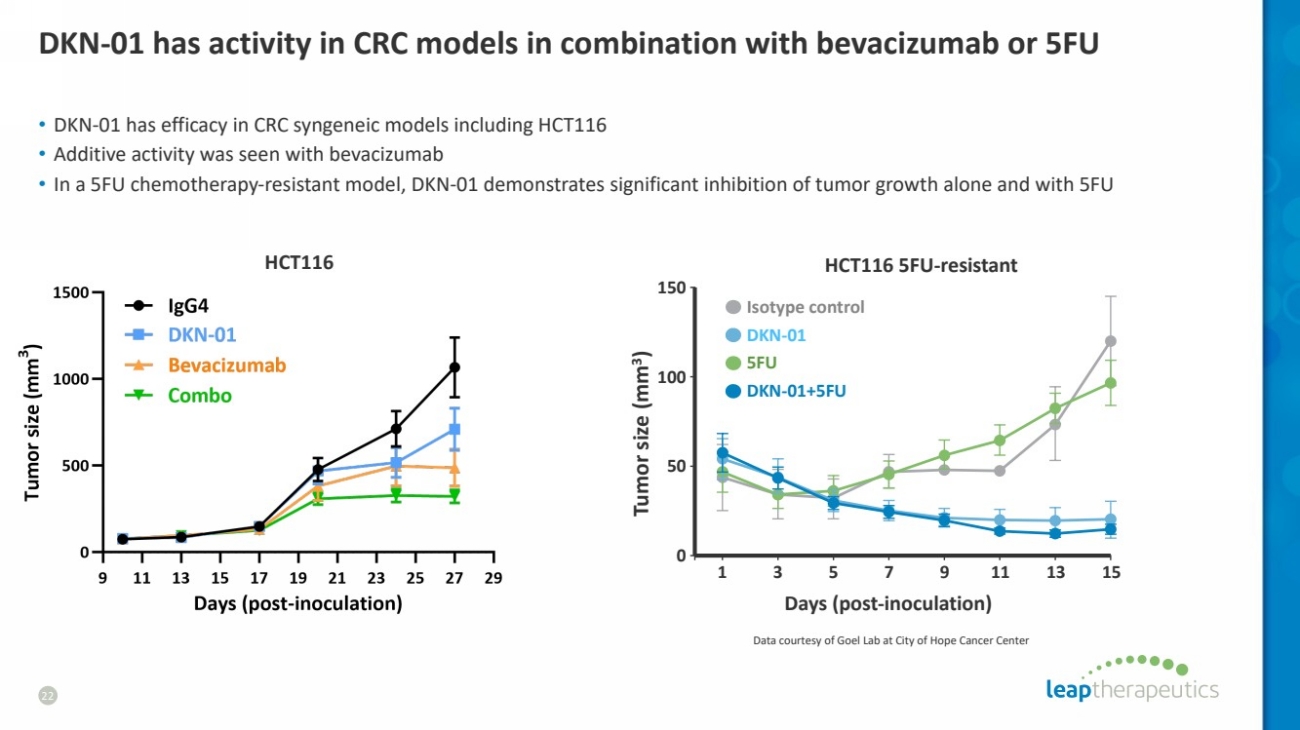
| DKN-01 与 bevacizumab 或 5FU HCT116 联合使用,在 CRC 模型中具有活性 • DKN-01 在包括 HCT116 在内的 CRC 同源模型中有效 • 在 5FU 化疗耐药模型中,DKN-01 单独使用 5FU 22 HCT116 5FU 耐药 150 100 50 0 肿瘤大小 (mm ) 3) 天数(接种后) 1 3 5 7 9 11 13 15 同型对照 DKN-01+5FU DKN-01 5FU 5FU 数据由希望之城癌症中心的戈尔实验室提供 |
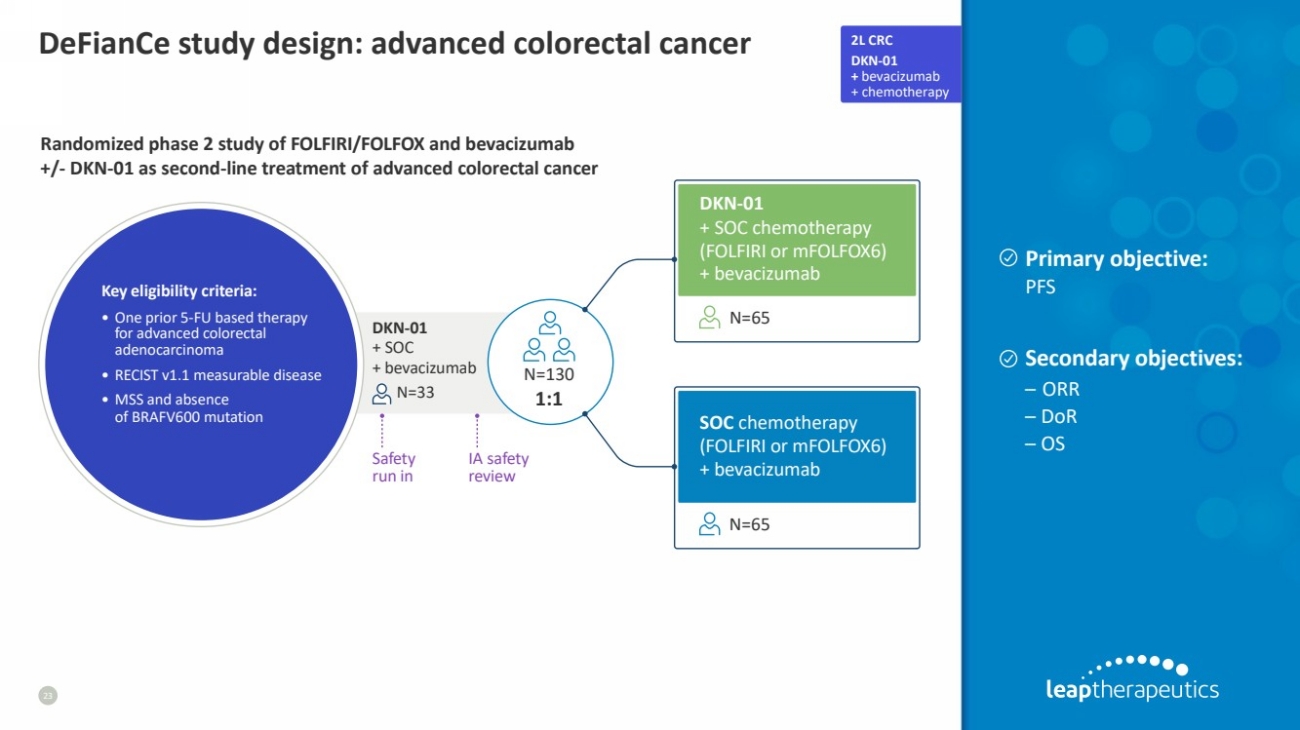
| DeFiance 研究设计:晚期结直肠癌 23 FOLFIRI/FOLFOX 和贝伐珠单抗 +/-DKN-01 作为晚期结直肠癌二线治疗的随机二期研究 2L CRC DKN-01 + 贝伐珠单抗 + 化疗 主要目标: PFS 次要目标: — ORR } — doR — OS DKN-01 + SOC 化疗 (FOLFIRI 或 mfolFox6) + 贝伐珠单抗 SOC 化疗 (FOLFIRI 或 mfolfox6) 直肠 腺癌 • RECIST v1.1 可衡量的疾病 • MSS 和没有 BRAFV600 突变 N=130 1:1 Safety 在 IA 安全 审核 + SOC + bevacizumab N=33 DKN-01 |
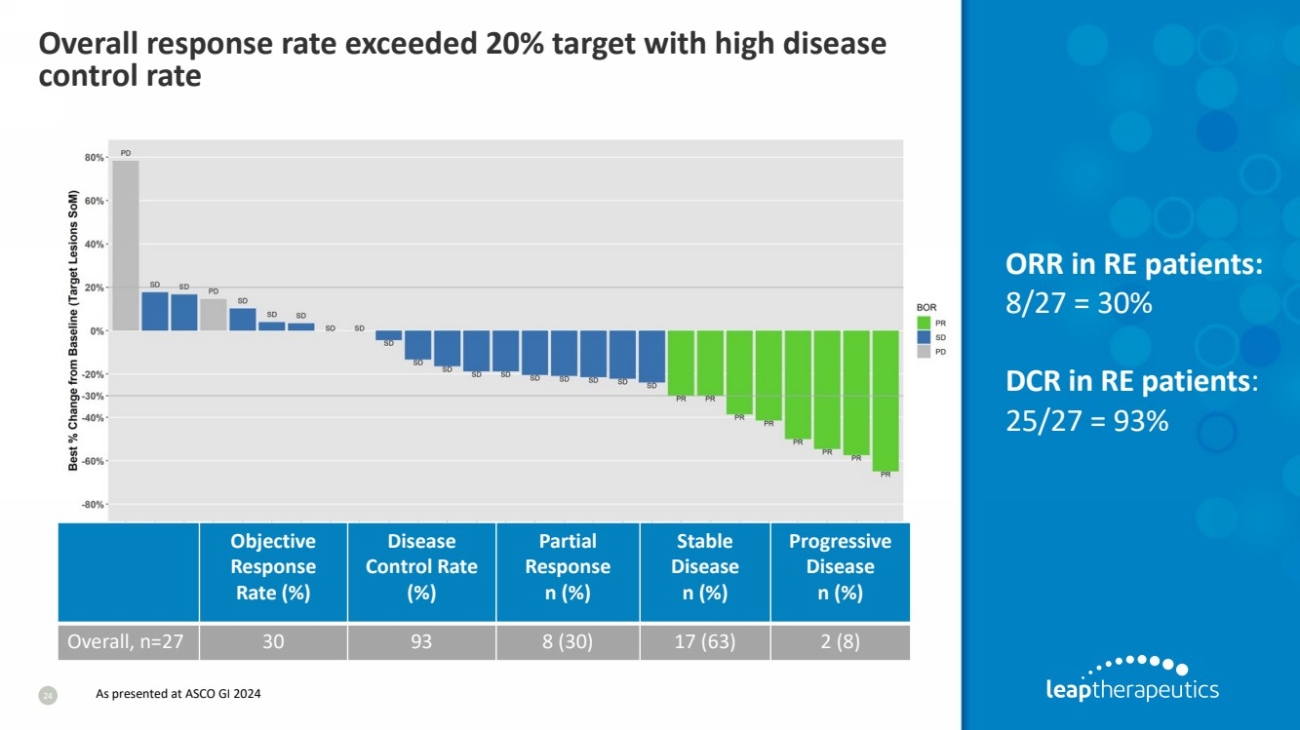
| RE 患者的总体缓解率超过 20%,疾病控制率高 24 ORR:RE 患者的 8/27 = 30% DCR: 25/27 = 93% 目标 目标 率 (%) 疾病 控制率 (%) 部分 反应 n (%) 稳定 疾病 n (%) 进行性 疾病 n (%) 总体而言,n=27 30 93 8 (30) 17 (63) 2 (8) 如在 ASCO GI 2024 上所述 |
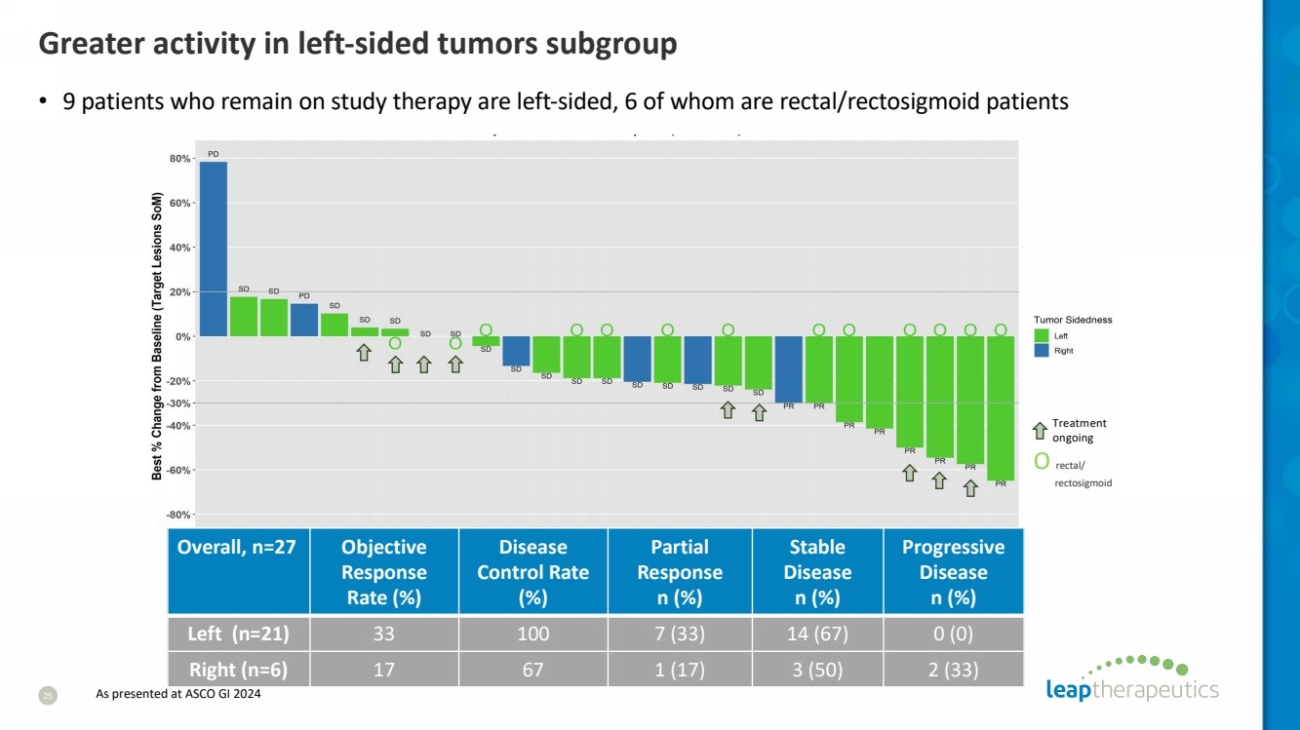
| 左侧肿瘤亚组 25 • 9 名仍在接受研究治疗的患者为左侧患者,其中 6 名为直肠/直肠乙状结肠炎患者 正在进行治疗 总体而言,n=27 目标 反应 率 (%) 疾病 控制率 (%) 部分 反应 n (%) 稳定 疾病 n (%) 进行性 n (%) 左 (n=21) 33 100 7 (33) 14 (67) 0 (0) 右 (n=6) 17 67 1 (17) 3 (50) 2 (33) O 直肠/ rectosigmoid As 在 ASCO GI 2024 上展出 |
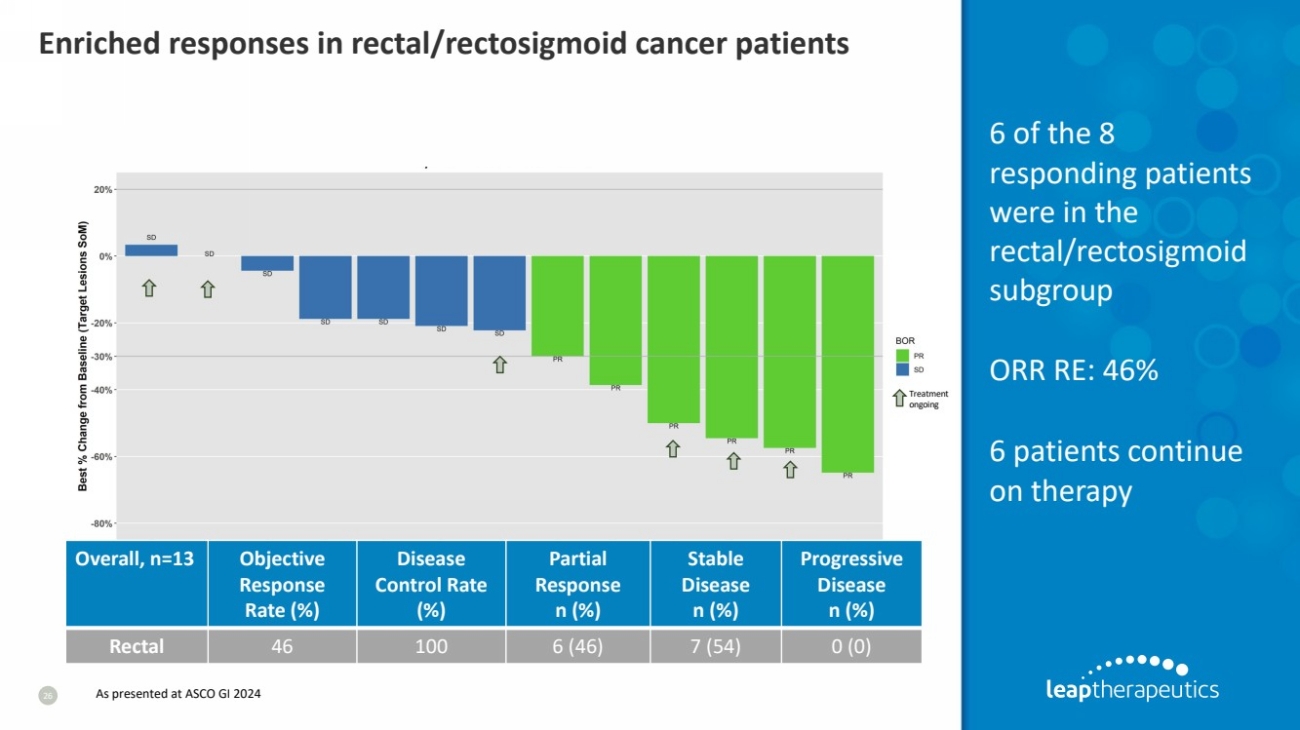
| 直肠/直肠乙状结肠癌患者的丰富反应 26 总体而言,n=13 目标 反应 率 (%) 疾病 控制率 (%) 部分 反应 n (%) 稳定 疾病 n (%) 疾病 n (%) 疾病 n (%) br} 直肠 46 100 6 (46) 7 (54) 0 (0) 8 名有反应的患者中有 6 名 属于 直肠/直肠乙状结肠亚组 ORR RE:46% 6 名患者继续 治疗 正在进行治疗 如在 ASCO GI 2024 上所述 |
| 27 临床受益期限 肿瘤侧面亚组 如在 ASCO GI 2024 上所述 |
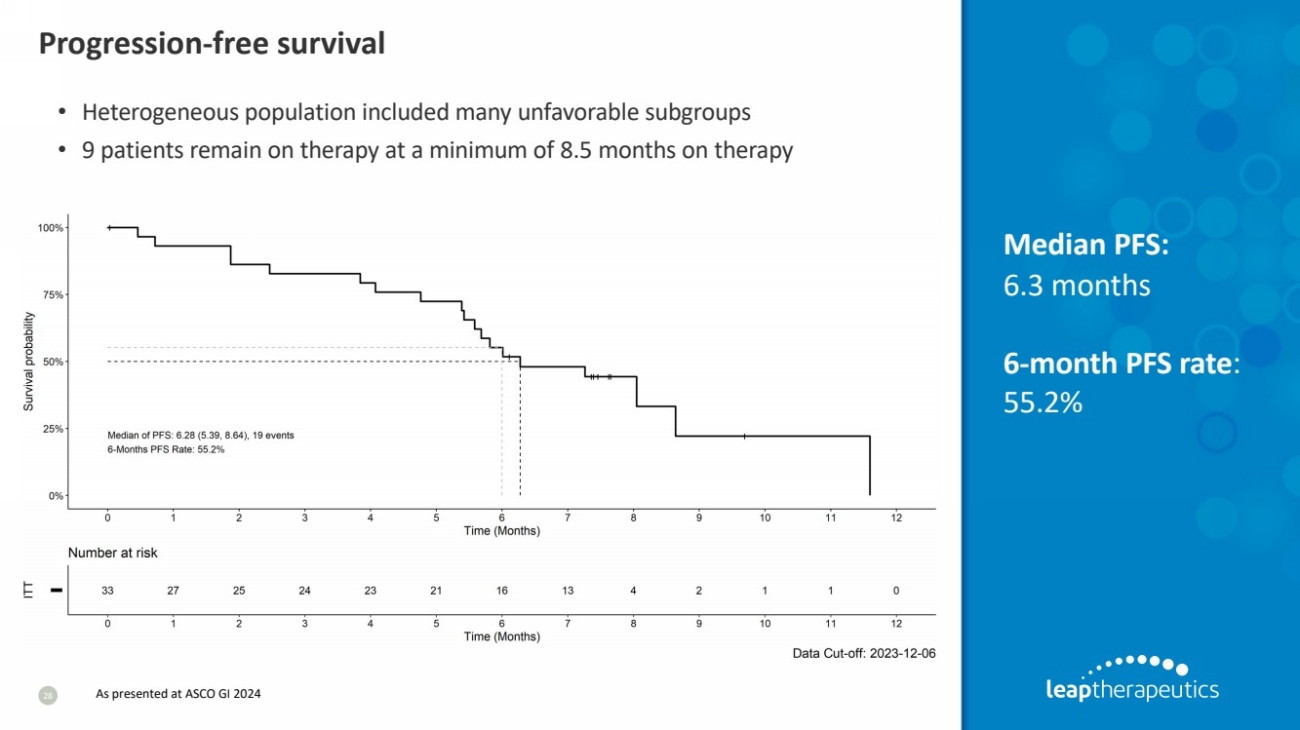
| 无进展存活率 28 PFS 中位数: 6.3 个月 6 个月 PFS 率: 55.2% • 异质人群包括许多不利的亚组 • 9 名患者仍在接受治疗至少 8.5 个月的治疗 如在 ASCO GI 2024 上所述 |
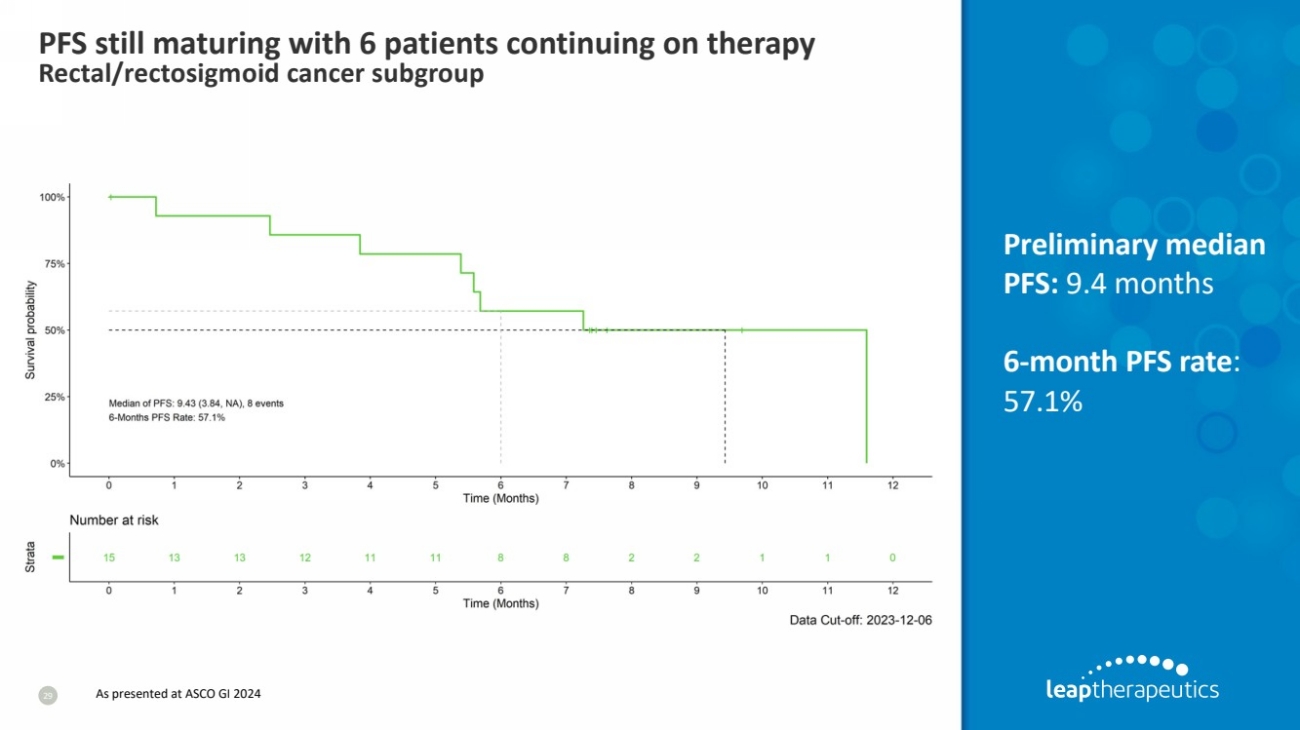
| PFS 仍在成熟,6 名患者继续接受治疗 直肠/直肠乙状结肠癌亚组 29 初步中位数 PFS:9.4 个月 6 个月 PFS 率: 57.1% 如在 ASCO GI 2024 上所述 |
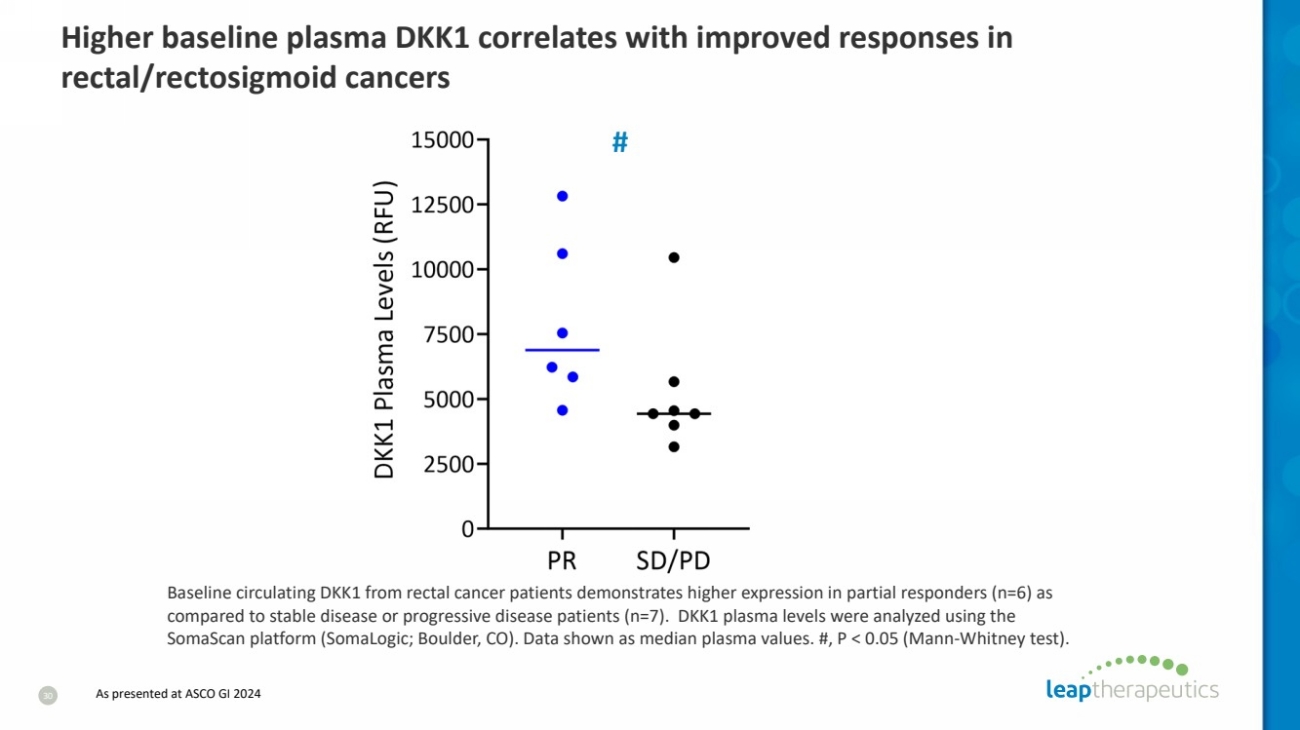
| 与稳定疾病或进行性疾病患者(n=7)相比,来自直肠癌患者的基线循环DKK1表现出较高的部分反应者(n=6)的表达 。使用 SomaScan 平台(SomaLogic;科罗拉多州博尔德)分析了 DKK1 血浆水平。数据显示为等离子体中值。#, P |
| DKN-01 子宫内膜癌的发展 |
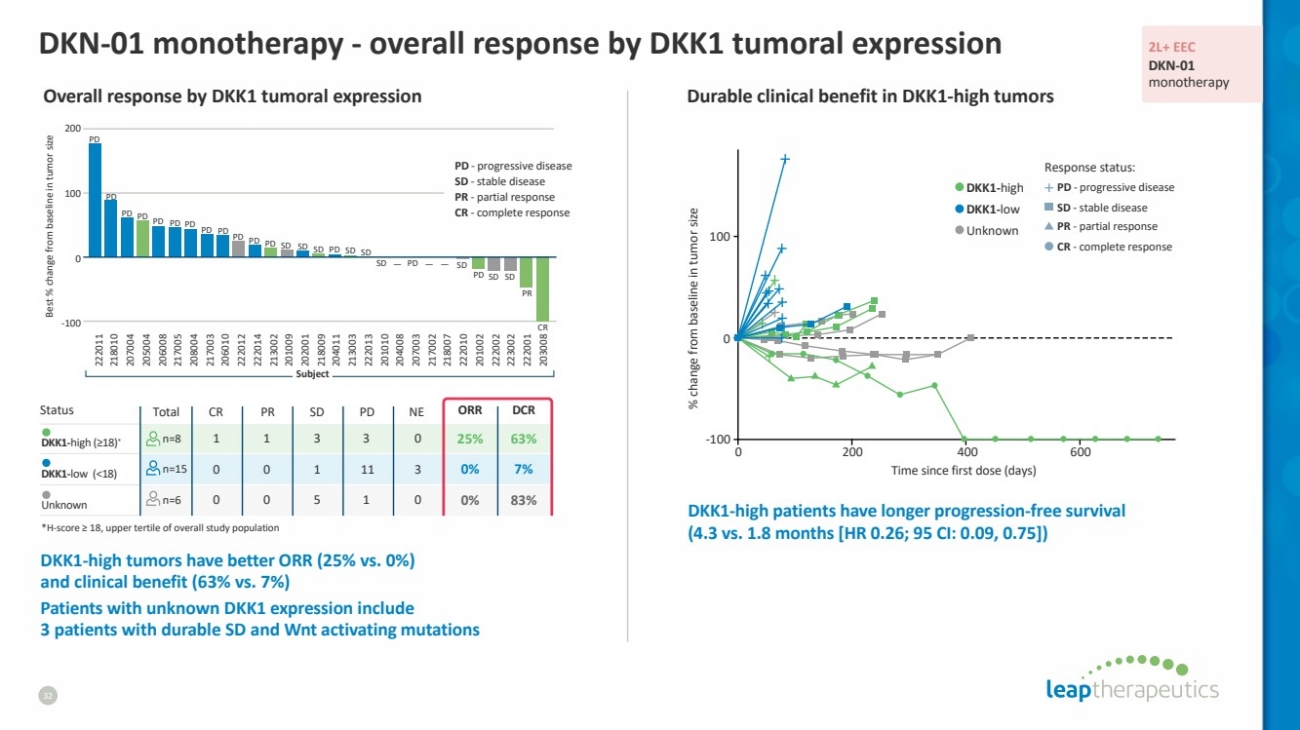
| 状态 Total CR PR SD PD NE ORR DCR dk1-High (≥18) * n=8 1 1 3 3 0 25% 63% 63% dkk1-Low ( |
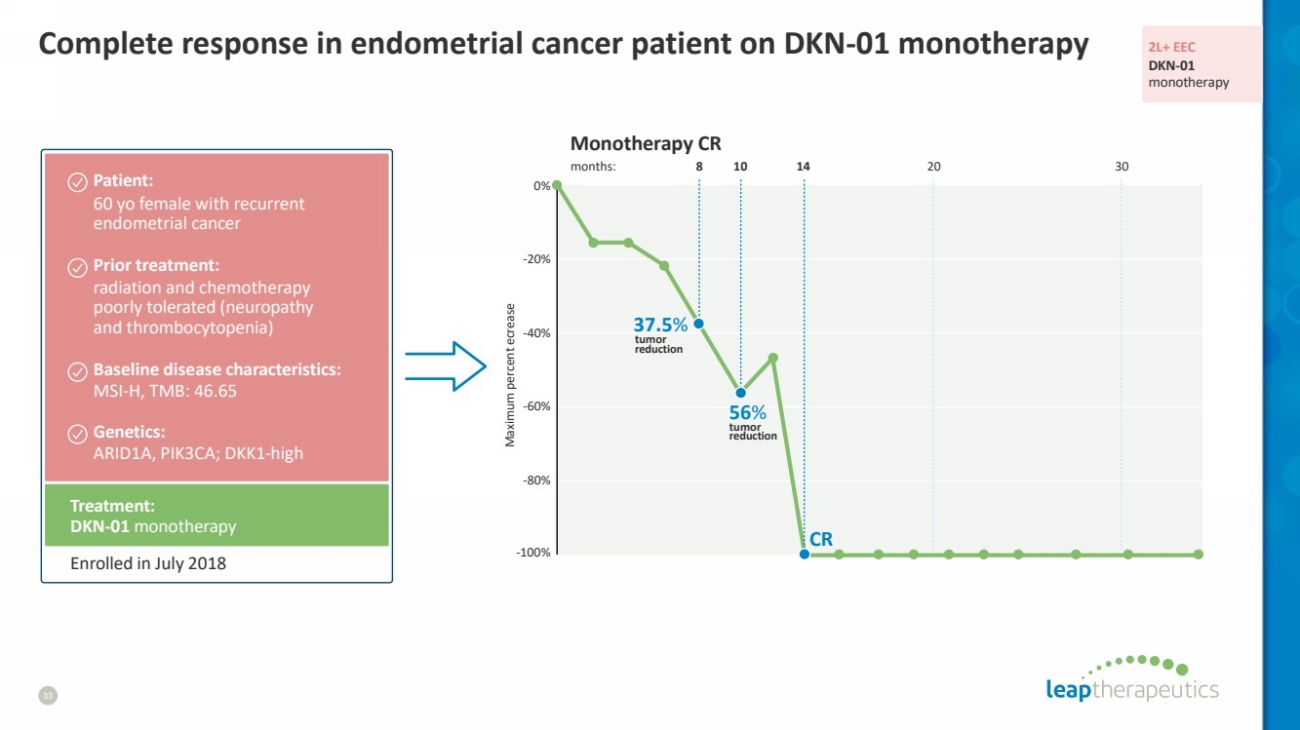
| DKN-01 单一疗法对子宫内膜癌患者的完全反应 33 最大下降百分比 -100% -60% -20% -80% -40% 0% 37.5% 56% 肿瘤 减少 治疗: DKN-01 单一疗法 患者: 60 至女性 子宫内膜癌 先前的治疗: 放射和化疗 耐受性差(神经病变 和血小板减少症) 基线疾病特征: MSI-H,TMB:46.65 遗传学: ARID1A、PIK3CA;DKK1 高 2018 年 7 月入学月份:30 单一疗法 CR 肿瘤 br 减少 810 14 20 2L+ EEC DKN-01 单一疗法 |
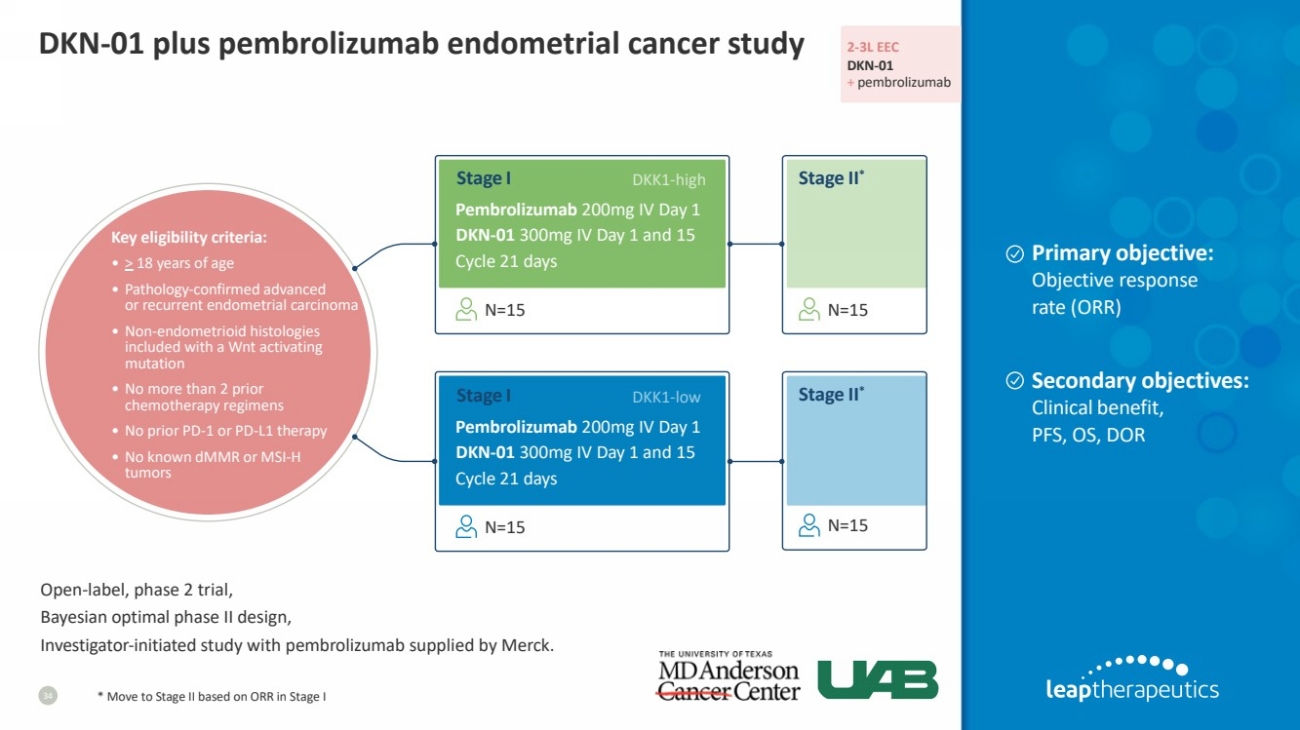
| DKN-01 加上 pembrolizumab 子宫内膜癌研究 34 * 基于 I 期的 ORR 进入第二阶段 2-3L EEC DKN-01 + pembrolizumab 关键资格标准: • > 18 岁 • 病理学证实的晚期 或复发性子宫内膜癌 • 非子宫内膜癌类组织学 包含在 Wnt 激活 突变中 • 之前不超过 2 个 化疗方案 • 之前没有 PD-1 或 PD-L1 疗法 • 没有已知的 dmMR 或 MSI-H 肿瘤 主要目标: 客观反应 率 (ORR) 次要目标: 临床好处, PFS、OS、DOR 开放标签、2 期试验、 贝叶斯最佳 II 期设计、 研究者发起的使用默沙东提供的派姆罗利珠单抗的研究。 Pembrolizumab 200mg 静脉注射第 1 天 DKN-01 300mg 静脉注射第 1 天和 15 天周期 21 天 Pembrolizumab 200mg 静脉注射第 1 天 DKN-01 300mg 静脉注射第 1 天和 15 个周期 21 天 高 低 N=15 N=15 N=15 I 阶段* 第二阶段* 第一阶段 |
| FL-301 (NBL-015) FL-302 (NBL-016) Anti-Claudin18.2 抗体 |
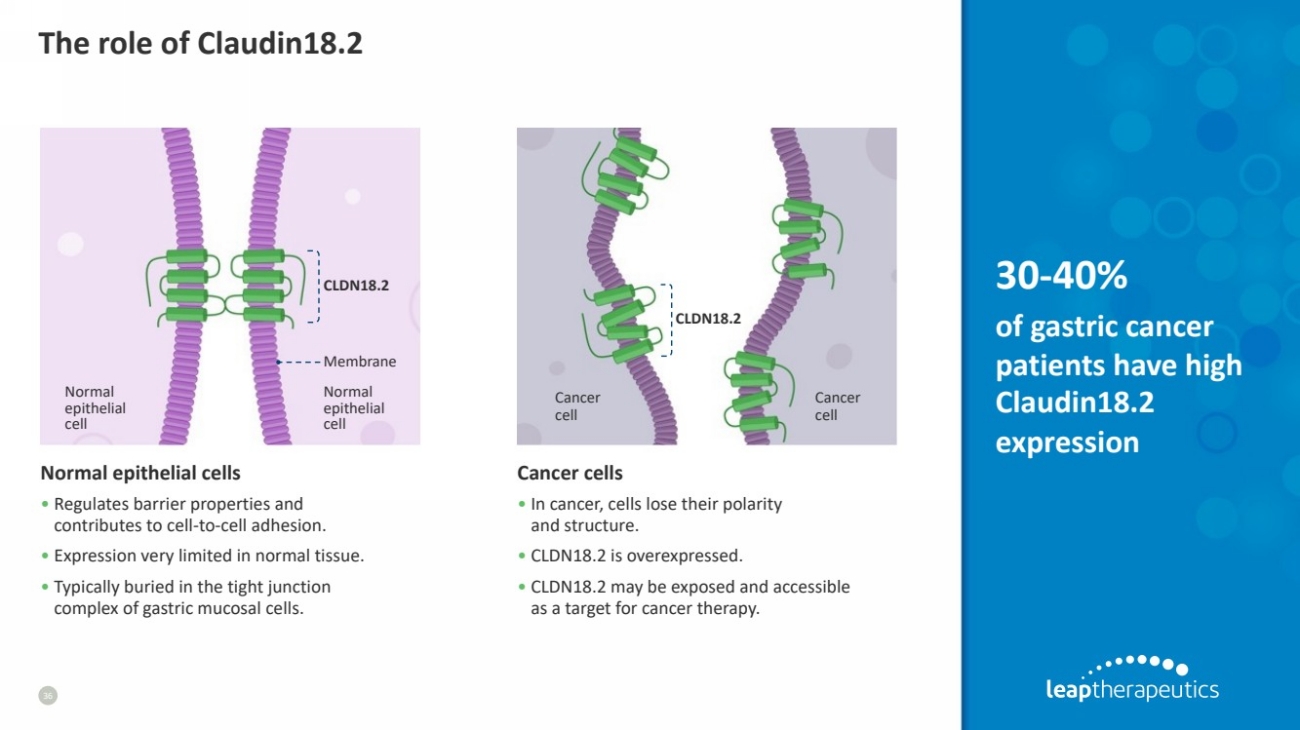
| Claudin18.2 36 正常上皮细胞 • 调节屏障特性, 有助于细胞间的粘附。 • 正常组织中的表达非常有限。 • 通常埋在胃粘膜细胞的紧密交界处 复合体中。 癌细胞 • 在癌症中,细胞会失去极性 和结构。 • CLDN18.2 过度表达。 • CLDN18.2 可能会暴露并获得 作为癌症治疗的靶标。 CLDN18.2 CLDN18.2 膜 正常 上皮 细胞 正常 上皮 细胞 癌症 细胞 癌症 细胞 30-40% 患者 Claudin18.2 的表达量很高 |
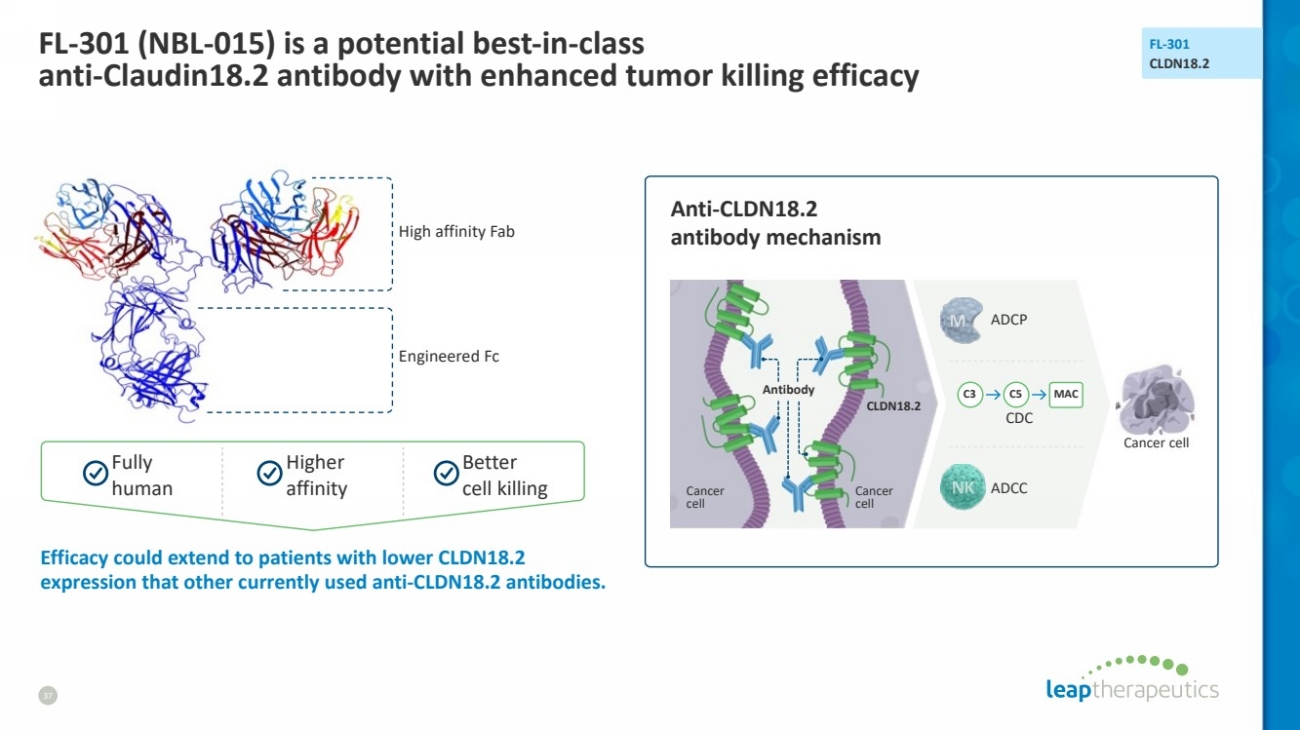
| FL-301 (NBL-015) is a potential best-in-class anti-Claudin18.2 antibody with enhanced tumor killing efficacy 37 FL-301 CLDN18.2 Efficacy could extend to patients with lower CLDN18.2 expression that other currently used anti-CLDN18.2 antibodies. Engineered Fc High affinity Fab Higher affinity Fully human Anti-CLDN18.2 antibody mechanism CLDN18.2 Antibody Cancer cell Cancer cell Better cell killing CDC ADCP C3 C5 MAC Cancer ADCC cell |
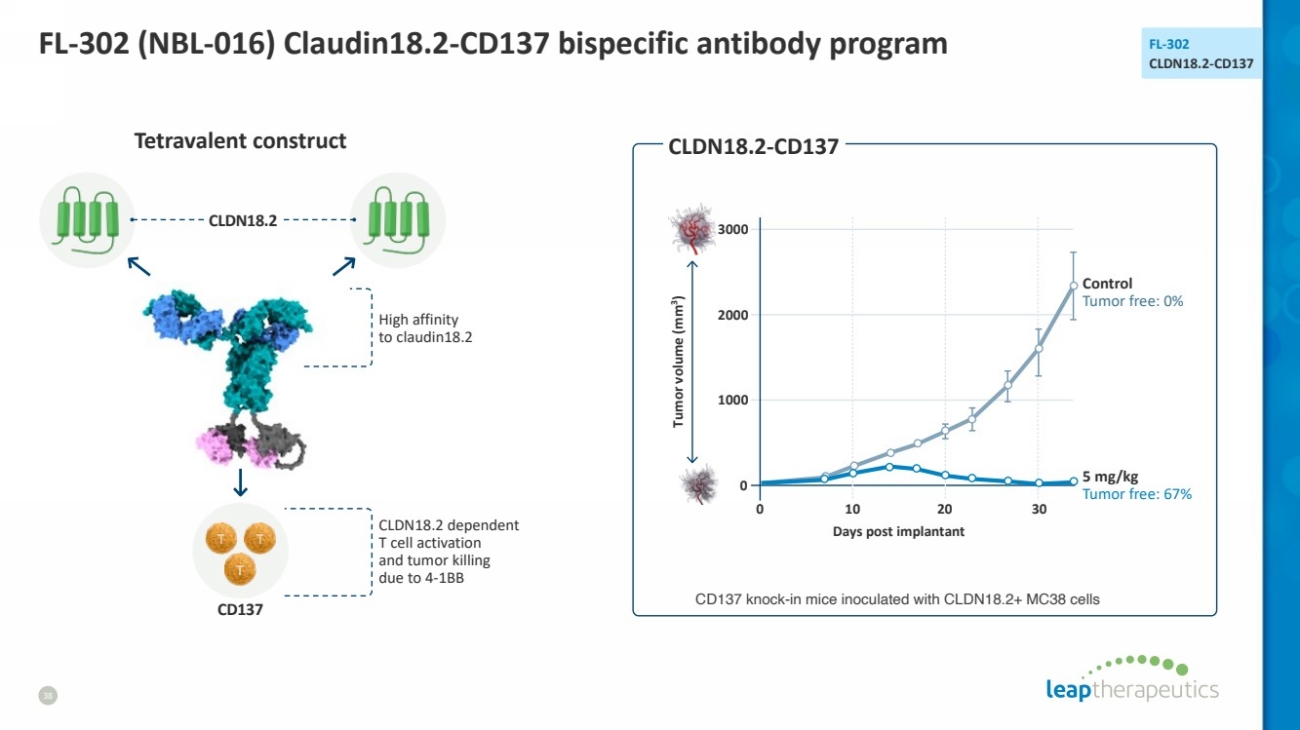
| FL-302 (NBL-016) Claudin18.2-CD137 bispecific antibody program 38 FL-302 CLDN18.2-CD137 0 30 3000 2000 1000 0 Tumor volume (mm3 ) Days post implantant Control Tumor free: 0% 5 mg/kg Tumor free: 67% Tetravalent construct СLDN18.2-CD137 High affinity to claudin18.2 СLDN18.2 CD137 CLDN18.2 dependent T cell activation and tumor killing due to 4-1BB 10 20 CD137 knock-in mice inoculated with CLDN18.2+ MC38 cells |
| FL-501 Anti-GDF15 monoclonal antibody |
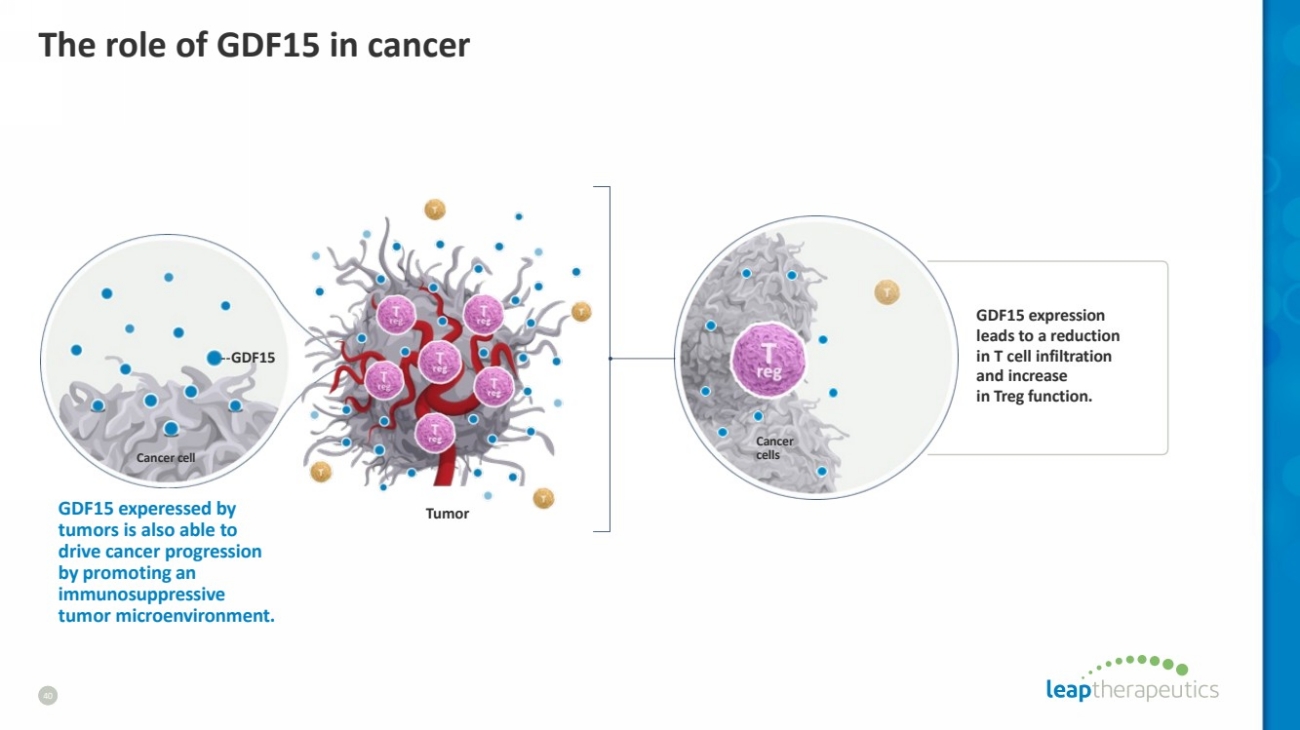
| The role of GDF15 in cancer 40 Cancer cells GDF15 expression leads to a reduction in T cell infiltration and increase in Treg function. Cancer cell GDF15 GDF15 experessed by tumors is also able to drive cancer progression by promoting an immunosuppressive tumor microenvironment. Tumor |
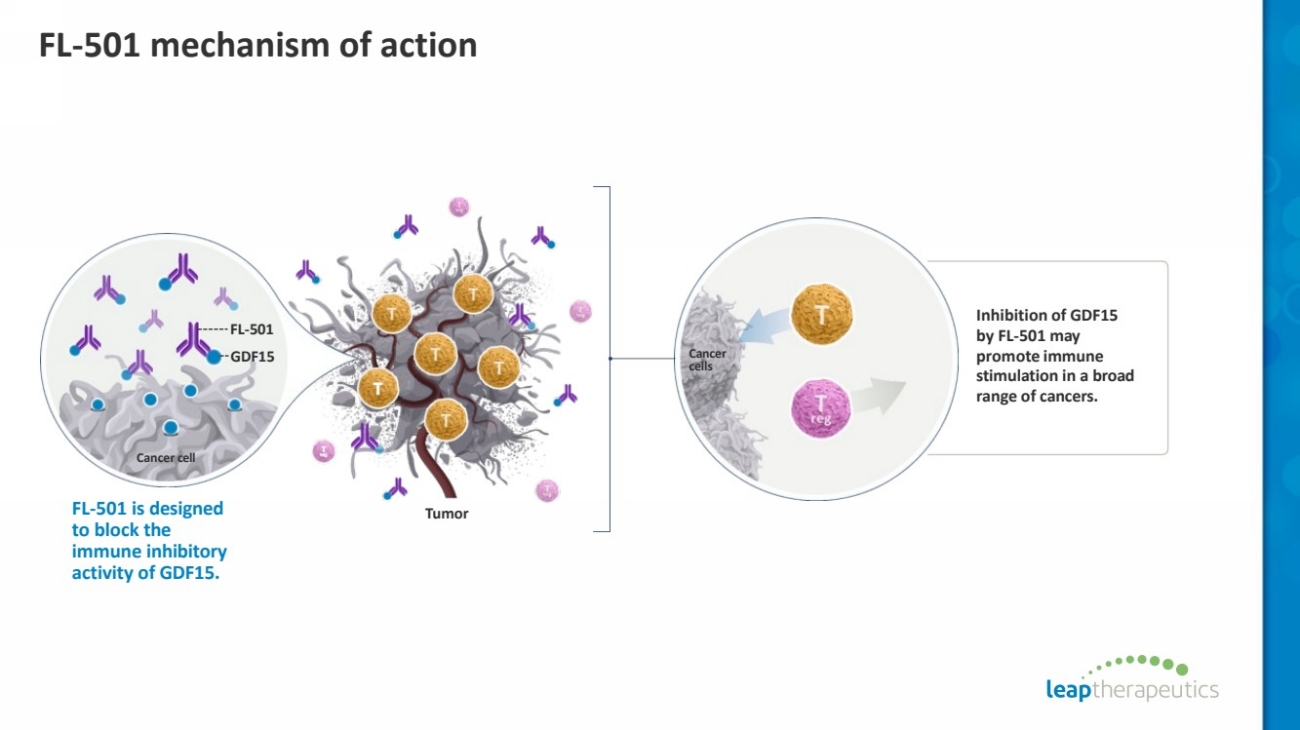
| FL-501 mechanism of action Cancer cells Inhibition of GDF15 by FL-501 may promote immune stimulation in a broad range of cancers. T T reg FL Tumor -501 is designed to block the immune inhibitory activity of GDF15. Cancer cell FL-501 GDF15 |
| CORPORATE |
| Management team 43 Christine Granfield Vice president, head of regulatory affairs and quality Cyndi Sirard, MD Chief medical officer Jason Baum, PhD Chief scientific officer Walter Newman, PhD Senior research fellow Douglas Onsi President & chief executive officer Mark O’Mahony Chief manufacturing officer Christopher Mirabelli, PhD Chairman of the board Gus Lawlor Chief operating officer |
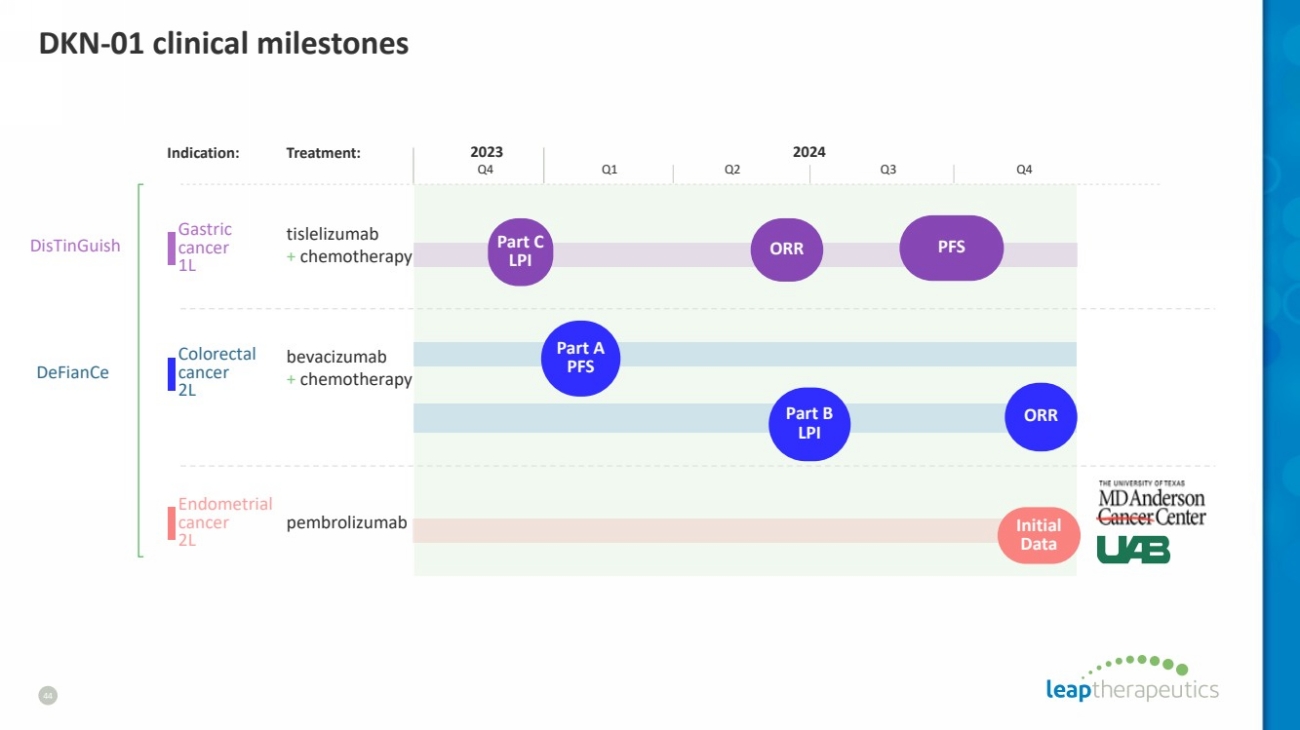
| DKN-01 clinical milestones 44 Indication: Treatment: tislelizumab + chemotherapy bevacizumab + chemotherapy pembrolizumab Gastric cancer 1L Colorectal cancer 2L Endometrial cancer 2L Q4 2023 2024 Q1 Q2 Q3 Q4 ORR PFS Initial Data Part A PFS Part B LPI ORR Part C LPI DisTinGuish DeFianCe |