自摩根大通 2023 年以来,ATTR-CM 的经验教训提供了前所未有的
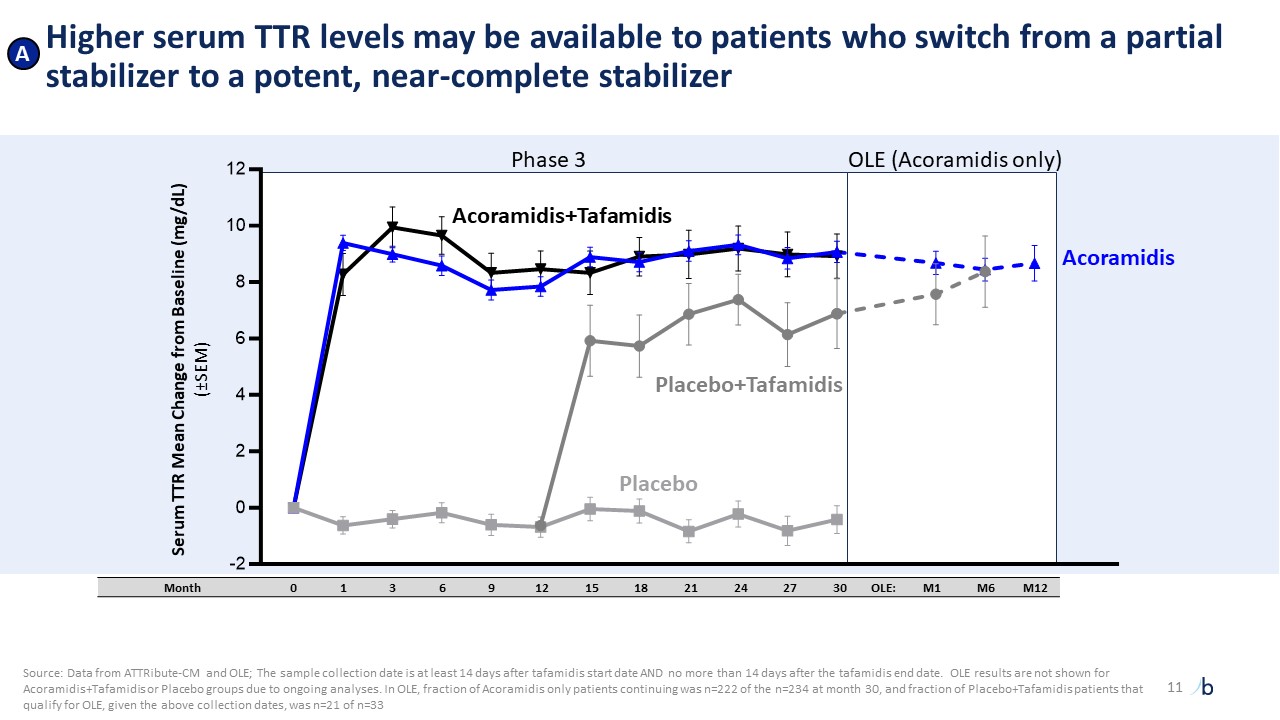
绝对存活率和住院率。作为一种高效的下一代稳定剂,acoramidis的绝对存活率和住院率接近与年龄相匹配的普通人群1,2,3 Acoramidis在ACM+CVH上显示出3个月的分离
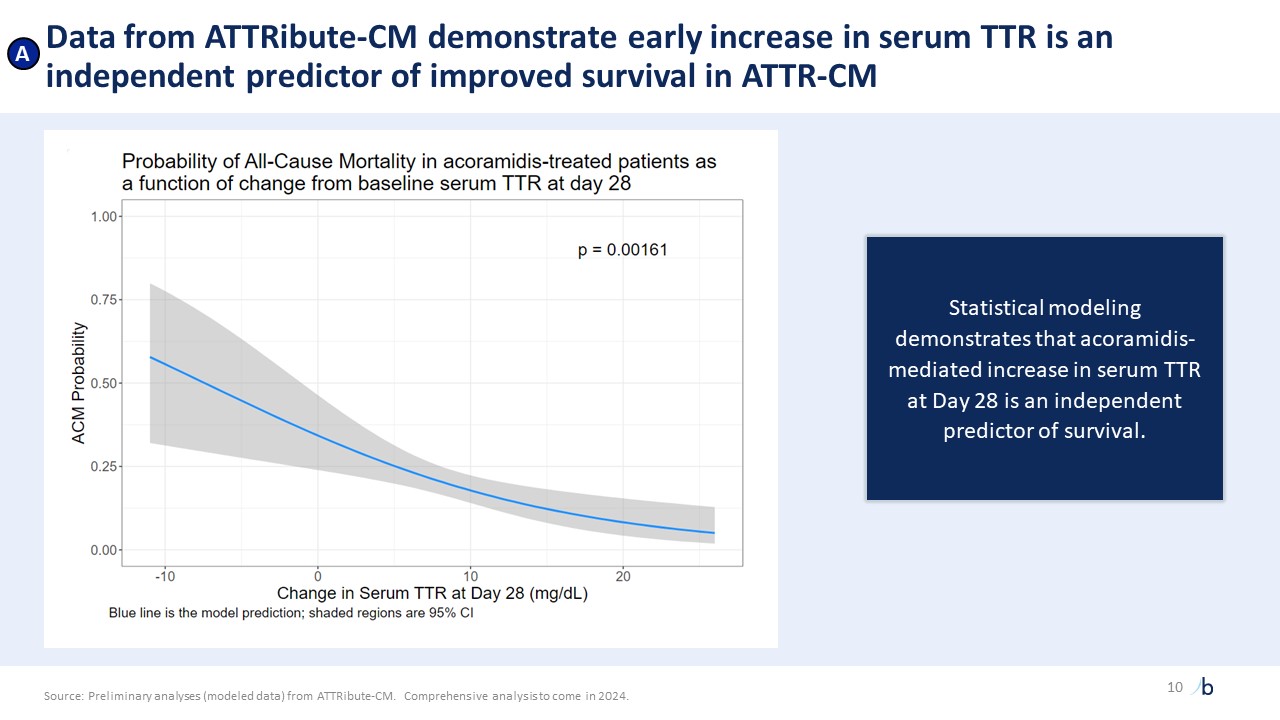
,这是迄今为止已知的最早分离4统计学上阿科拉米德达到的稳定水平与下游死亡率相关,达到前所未有的水平5 显著的临床改善,与新型
无关疗法 ATTR-CM 患者的临床环境已显著改善 ATTR-ACT6 的安慰剂组表现优于活跃的塔非米迪斯组 ATTR-CM 市场经久耐用且不断增长 ATTR-CM
市场在第7季度以约15%的速度增长。欧盟反对部听取了有关多态专利中塔法米迪斯索赔有效性的争论,并同意辉瑞的观点,维持了新颖性和创造性主张,
预计 Vyndaqel 将在欧盟八国在 2035 年 8 月之前保持市场排他性对识别现有治疗进展者的认识不断提高。尽管目前市场上有
疗法,但ATTR-CM仍有大量未得到满足的需求通过NT-proBNP识别 “无反应者”,即在现有治疗上取得进展的患者 1ssa.gov. 2美国卫生与公共服务部,2018年。3自然史反映了美国医疗保险非新生儿、
非孕产妇的住院情况。Attribute-CM 数据反映了与心血管相关的住院情况。4Attribute-CM 数据,复合 ACM/CVH 的 Kaplan-Meier。5来自 Attribute-CM 的初步分析(建模数据)。将在
2024 年进行全面分析。6Masri等人,HFSA 2023 “一项多中心研究 Tafamidis 在转甲状腺素淀粉样心肌病中的实际结果”。注意:直接的交叉研究比较可能表明存在误导性的相似之处或不同之处。7Corporate SEC 文件。
8欧洲专利局,异议处,档案 #EP3191461