
附录 99.2

将我们的使命变为现实摩根大通首席执行官凯特·哈维兰德医疗会议2024年1月8日艾德里安·克林顿患有系统性肥大细胞增多症的患者

前瞻性陈述本演示文稿包含经修订的1995年《私人证券诉讼改革法》所指的前瞻性陈述,包括但不限于关于公司未来业务增长的计划、战略、时间表和预期的声明,包括其2024年的增长战略;AYVAKIT在SM抓住重磅市场机会的潜力;BLU-808是否有药丸潜力;是否有该公司的产品候选人将讲述的未满足的医疗需求;2024年公司现金消耗的减少;有关公司当前或未来批准的药物和候选药物的计划和预期的声明;公司当前或未来批准的任何药物或候选药物在治疗患者方面的潜在益处;以及公司的财务业绩、战略、目标和预期里程碑、业务计划和重点。“目标”、“可能”、“将”、“可以”、“应该”、“计划”、“预测”、“打算”、“相信”、“估计”、“预测”、“项目”、“潜力”、“继续”、“目标” 等类似表述旨在识别前瞻性陈述,尽管并非所有前瞻性陈述都包含这些识别词。本演示文稿中的任何前瞻性陈述均基于管理层当前的预期和信念,受许多风险、不确定性和重要因素的影响,这些风险和不确定性可能导致实际事件或结果与本演示文稿中任何前瞻性陈述所表达或暗示的重大差异,包括但不限于公司继续扩大商业基础设施、成功推出、营销和销售当前或未来批准产品的能力和计划;公司的能够成功扩大AYVAKIT/AYVAKYT的批准适应症或将来在其他地区获得AYVAKIT/AYVAKYT的上市许可;推迟任何当前或计划中的临床试验或公司当前或未来的候选药物的开发;公司推进多项早期阶段工作;公司成功证明其候选药物的安全性和有效性并获得候选药物批准的能力及时提供依据(如果有的话);临床前和临床结果公司的候选药物,可能不支持单一疗法或与其他药物联合使用等候选药物的进一步开发,也可能影响数据或监管机构提交的预期时间;在临床试验场所启动临床试验和试验群组的时间以及患者入组率;监管机构的行动,可能影响临床试验的启动、时间和进展;公司获得、维持和执行专利和其他知识产权保护的能力适用于 AYVAKIT/AYVAKYT或其正在开发的任何候选药物;公司为AYVAKIT/AYVAKYT或其当前和未来的任何候选药物开发和商业化伴随诊断测试的能力;公司成功扩大其业务、研究平台和候选药物组合及其时机和成本的能力;以及公司当前和未来合作、融资安排、合作伙伴关系或许可安排的成功;以及风险和相关不确定性考虑到COVID-19大流行对世界的影响公司的业务、运营、战略、目标和预期里程碑,包括公司正在进行和计划中的研究和发现活动、进行正在进行和计划中的临床试验的能力、当前或未来候选药物的临床供应、当前或未来批准产品的商业供应,以及当前或未来批准产品的上市、营销和销售。公司向美国证券交易委员会(SEC)提交的文件中标题为 “风险因素” 的部分对这些风险和不确定性进行了更详细的描述,包括该公司最新的10-K表年度报告,并辅之以其最新的10-Q表季度报告以及该公司已经或将来可能向美国证券交易委员会提交的任何其他文件。本演示文稿中的前瞻性陈述仅在发布之日作出,除非法律要求,否则公司没有义务根据新信息、未来事件或其他原因更新本演示文稿中包含的任何前瞻性陈述。因此,提醒读者不要过分依赖这些前瞻性陈述。本演示文稿还包含独立各方和公司就市场规模和增长做出的估计、预测和其他统计数据,以及有关公司行业的其他数据。这些数据涉及许多假设和局限性,提醒您不要过分重视此类估计。此外,对公司未来业绩的预测、假设和估计以及公司经营所在市场的未来表现必然受到高度的不确定性和风险的影响。Blueprint Medicines、AYVAKIT、AYVAKYT 和相关徽标是蓝图药品公司的商标。2

Blueprint Medicines 的加速增长概况 3 在SM中树立领导地位加速增长孵化创新通过专有研究平台有机建立广泛的产品组合在美国和欧盟批准和推出AdvSM和ISM的AYVAKIT®(阿伐替尼)重磅机遇,专注于引人入胜的增长机会以及盈利之路 2011 — 2021 — 2023 — 2024 — FUTURE Avritapinib 获得批准,商品名为 AYVAKYT® 在欧洲。advSM,晚期系统性肥大细胞增多症;ISM,惰性系统性肥大细胞增多症;SM,系统性肥大细胞增多症一家完全整合、商业化的全球生物制药公司,增长速度加快

在 2024 年及以后实现业务增长 4 项成就 2024 年增长战略在 ISM 中启动 AYVAKIT 交付了四个第一阶段临床数据集为未来投资提供信息提名的 3 个发展中国家,包括口服野生型 KIT 抑制剂 BLU-808 运营费用持续下降随着AYVAKIT在SM的推出实现收入大幅增长专注于具有重要价值驱动力的引人注目的增长机会持久的资本状况可以独立于资本市场 DC,开发候选者

2024年的三个关键增长驱动力 5 过敏/免疫学肿瘤学/血液学投资可持续创新保持财务实力强劲稳定的全球上市在未来十年实现增长抓住重大机遇

AYVAKIT 拥有独特的多维价值主张 6 重磅市场机遇引人注目的临床概况多种增长机会积极的接受能力推动需求

AYVAKIT 在 SM 7 中抓住了重大的机会 $28.6 $30.1 $39.9 $39.9 54.2 2023年第一季度第二季度2023年第二季度AYVAKIT 净产品收入(百万美元)+36% 2023年5月22日:美国食品药品管理局批准ISM的人群明显增加,有可能接受长期治疗的高利润率特种药物具有可操作的治疗潜在驱动因素的疗法由于长期的知识产权保护、知识产权、知识产权,预计未来十年将持续增长

AYVAKIT 提供持久的症状控制和耐受性良好的每日一次药丸 8 广泛而持久的疗效改善涵盖广泛的皮肤、胃肠道、神经认知和其他症状安全配置支持在 PIONEER 1 中长达 4 年以上的慢性治疗治疗;长期安全数据将于 2024 年公布剂量范围多剂量满足各种 SM 患者的医疗需求 1.蓝图药品数据存档。截至2023年11月,PIONEER(n = 251)的平均治疗时间为25.1个月(运行年龄:0.2-52.9个月)。8

强劲的资金比率和执行广度推动了短期增长轨迹 9 1.蓝图药品数据存档。百分比基于SP/HUB频道中可见的2023年第三季度新增SM患者开诊情况,该频道反映了AYVAKIT的大部分交易量。不同提供商类型和渠道的广泛需求量受新开处方者与现有处方者的驱动量约60/ 40% 学术与社区账户推动的交易量 ~50/ 50% 商业和医疗执行推动知名度与推出之前相比 AYVAKIT 意识的增长 3.5X 患者可能会向医生询问 AYVAKIT ~ 65% SM 出版物 70+ 教育演讲者项目 230 多个区域 SM 会议 300+ 易于获取从处方到发货的转化率 ~ 95% 可填充大多数患者 95%

随着SM市场的增长,有很大的上行空间 10 • 扩大医疗保健提供商对AYVAKIT(符合条件的患者)的视角,使其与我们的广泛标签保持一致 • 通过更有效的诊断建立市场 •进入美国以外的新市场美国约9,500例确诊和不受控制的ISM 1 ~32,000例美国SM患病率2>同比增长约21,000例 1 1.蓝图药品数据存档,基于美国索赔数据中独特患者的可见性。2.Cohen 等人 2014 年。

抓住重磅机遇 2024年的三个关键增长动力 11 过敏/免疫学肿瘤学/血液学投资可持续创新保持财务实力重点投资推动长期增长

BLU-222 CDK2 正在进行的合作讨论 BLU-956(下一代)CDK2 靶向蛋白降解剂 CDK2 全球靶向蛋白降解剂未公开的 AYVAKIT®(阿伐替尼)1 试剂盒 D816V 全球不包括大中华区 4 埃莱尼斯替尼(下一代)试剂盒 D816V Global BLU-808 野生型试剂盒其他未公开的肥大细胞靶标/模式在两个重点和令人兴奋的科学领域建立规模 12 Inn Dolent SM 2 Advanced SM 3 Indolent SM 慢性荨麻疹 HR+/HER2-乳腺癌其他 CDK2 脆弱癌症 HR+/HER2-乳腺癌项目 TARGET DISCOVERY临床商业权利 HR+/HER2-乳腺癌肥大细胞疾病过敏/炎症重点:实体瘤肿瘤肿瘤学重点:1.美国还批准用于携带 PDGFRA 外显子 18 突变的不可切除或转移性 GIST 的成年人,包括 P DGF RA D842V 突变。欧洲(AYVAKYT®)获批准,用于携带 PDGFRA D842V 突变的不可切除或转移性 GIST 的成年人。2.在美国获准用于患有惰性 SM 的成年人。在欧洲(AYVAKYT)获批,用于对症治疗无法充分控制的惰性 SM 的成年人,其发生率为中等至严重症状。在美国获准用于晚期SM(包括侵袭性SM(ASM)、伴有相关血液学肿瘤(SM-AHN)的SM和肥大细胞白血病(MCL)的成年人。在欧洲(AYV AKYT®)获得批准,适用于至少经过一次全身治疗后患有 ASM、SM-AHN 或 MCL 的成年人。4.基石制药拥有在大中华区开发和商业化阿伐替尼的独家权利。更新于 2024 年 1 月 8 日。其他项目未公开全球

肥大细胞是一系列炎症性疾病生物学的核心驱动力 13 • KIT-介导的信号传导在肥大细胞的存活、增殖和激活中起着核心作用 • 当脱颗粒发生时,炎症分子的释放会产生广泛的生理影响 KIT 是一种经临床验证的肥大细胞靶向前列腺素 KIT 组胺细胞因子胰蛋白酶脱颗粒 MCAS、肥大细胞激活综合征;GI,胃肠道

Elenestinib,一种正在研究的下一代强效选择性 KIT D816V 抑制剂 14 — 22.2 — 28.5 — 31.8 — 33.6 — 40.0 — 35.0 — 30.0 — 25.0 — 20.0 — 15.0 — 10.0 — 5.0 0.0 0.0 安慰剂(n=10)埃莱内斯替尼 25 mg QD(n=10)Elenestinib 50 mg QD(n =10)Elenestinib 50 mg QD(n =10)Elenestinib 50 mg QD(n = 10)Elenestinib 100 mg QD(n=8)与基线相比的平均变化百分比依来替尼在ISM中的降低-SAF总症状评分为1。Tashi T. 等人在 ASH 2023 上展出。耐受性良好,没有因不良反应而中断治疗;经验证的ISM-SAF评估的大多数AE的1/2级改善疾病相关症状减少了肥大细胞负担的多种生物标志物在不同剂量下观察到稳健的临床活性和良好的耐受性 HARBOR 第 1 部分试验结果在 ASH 2023 1 上公布:

野生型 KIT 抑制剂 BLU-808 在药丸中处于首位、也是同类最佳的管道中,计划于 2024 年第二季度提交 15 款车辆 IND 属性理想候选药物 BLU-808 PKit /增殖 IC 50 50x/> 50x >300/>9600 激酶选择性;S (10)

通过口服疗法靶向试剂盒以满足大量未得到满足的医疗需求 16 荨麻疹或荨麻疹的典型表现,这是慢性荨麻疹的常见症状 1 由肥大细胞驱动的疾病生物学靶向验证 WTKit 抑制已为慢性荨麻疹方法建立了临床概念验证小分子 TKI;有机会通过口服疗法推动市场扩张由于瘙痒、荨麻疹、肿胀和相关焦虑导致的重大疾病负担和生活质量影响,睡眠不足美国和欧盟4国约有68万名患者对口服治疗的需求未得到满足核心生物学机会 TKI,酪氨酸激酶抑制剂;QoL,生活质量;EU4 包括法国、德国、意大利、西班牙 1。抗组胺耐药物,声称——在美国和欧盟4国已确定患有CU的患者

BLU-222 CDK2 正在进行的合作讨论 BLU-956(下一代)CDK2 靶向蛋白降解剂 CDK2 全球靶向蛋白降解剂未公开的 AYVAKIT®(阿伐替尼)1 试剂盒 D816V 全球不包括大中华区 4 埃莱尼斯替尼(下一代)试剂盒 D816V Global BLU-808 野生型试剂盒其他未公开的肥大细胞靶标/模式在两个重点和令人兴奋的科学领域建立规模 17 Dolent SM 2 Advanced SM 3 Indolent SM 慢性荨麻疹 HR+/HER2-乳腺癌其他 CDK2 脆弱癌症 HR+/HER2-乳腺癌项目 TARGET DISCOVERY临床商业权利 HR+/HER2-乳腺癌肥大细胞疾病过敏/炎症重点:实体瘤肿瘤肿瘤学重点:1.美国还批准用于携带 PDGFRA 外显子 18 突变的不可切除或转移性 GIST 的成年人,包括 P DGF RA D842V 突变。欧洲(AYVAKYT®)获批准,用于携带 PDGFRA D842V 突变的不可切除或转移性 GIST 的成年人。2.在美国获准用于患有惰性 SM 的成年人。在欧洲(AYVAKYT)获批,用于对症治疗无法充分控制的惰性 SM 的成年人,其发生率为中等至严重症状。在美国获准用于晚期SM(包括侵袭性SM(ASM)、伴有相关血液学肿瘤(SM-AHN)的SM和肥大细胞白血病(MCL)的成年人。在欧洲(AYV AKYT®)获得批准,适用于至少经过一次全身治疗后患有 ASM、SM-AHN 或 MCL 的成年人。4.基石制药拥有在大中华区开发和商业化阿伐替尼的独家权利。更新于 2024 年 1 月 8 日。其他项目未公开全球

借助BLU-222,我们解决了CDK2抑制的选择性挑战 18 CDK2是经过临床验证的细胞周期靶标大型市场仍有大量未得到满足的需求的全面计划将2023年用于HR+/HER2乳腺癌的CDK4/6抑制剂的全球销售价值提高和解决CDK4/6耐药性作为联合疗法的支柱高度选择性方法最大限度地减少靶向毒性,使联合合作伙伴成为首选的药物下一页-实现长期价值最大化的发电资产 CDK、细胞周期蛋白依赖激酶;HR+,激素受体阳性;HER2-,人类表皮生长因子受体 2 阴性;SOC,标准护理标准选择性 CDK2 抑制历来难以实现

BLU-222 有可能成为首款也是最佳的 CDK2 同类选择性抑制剂 19 BLU-222 1 PF-4091 2 临床前概况选择性评分/SI (10) 0.045 0.127 CDK2 效力/CDK2 酶 IC 50 (nM) 2.6 7.2 1 期单一疗法剂量递增数据患者 27 名患者 35 名患者剂量范围 50 mg — 800 mg BID(MTD 未确定)75 mg — 500 mg BID(MTD:300 mg BID)PK(平均有效半衰期)~12 小时 ~2-3 小时治疗紧急不良事件 (TEAE) 无 Gr5;1 Gr4(低钾血症;无关)1 Gr5(无关);1 Gr4(中性粒细胞减少)血液学 TEAE s ALL GR3 GR4 ALL GR3 GR4 • 贫血 29.6% 3.7% 45.7% 8.6% • 中性粒细胞减少症 3.7% 28.6% 14.3% 2.9% • 血小板减少症 3.7% 3.7% 20.0% 2.9% 1.Patel、M.R. 等人、ASCO 2023 和存档的蓝图数据。数据已于 2023 年 4 月 25 日发布。2.是的,T.A. 等人,ASCO 2023

抓住重大的机遇 f 2024 年的三大增长驱动力 20 过敏/免疫学肿瘤学/血液学投资可持续创新保持财务实力持久的资本状况有明确的盈利路径

21 美元 53 美元 111 美元 2020 年 2021 年 2022 2023 2024 2026 2026 2027+ AYVAKIT 正在抓住一个重大的机会 SM AYVAKIT 将在 2023 财年第四季度财报电话会议上提供 2023 财年财务状况和 2024 年 AYVAKIT 产品收入指导。估计超过15亿美元的全球小企业峰值收入21 AYVAKIT年度净产品收入(百万美元)数字以图形形式提供,不作为财务指导。
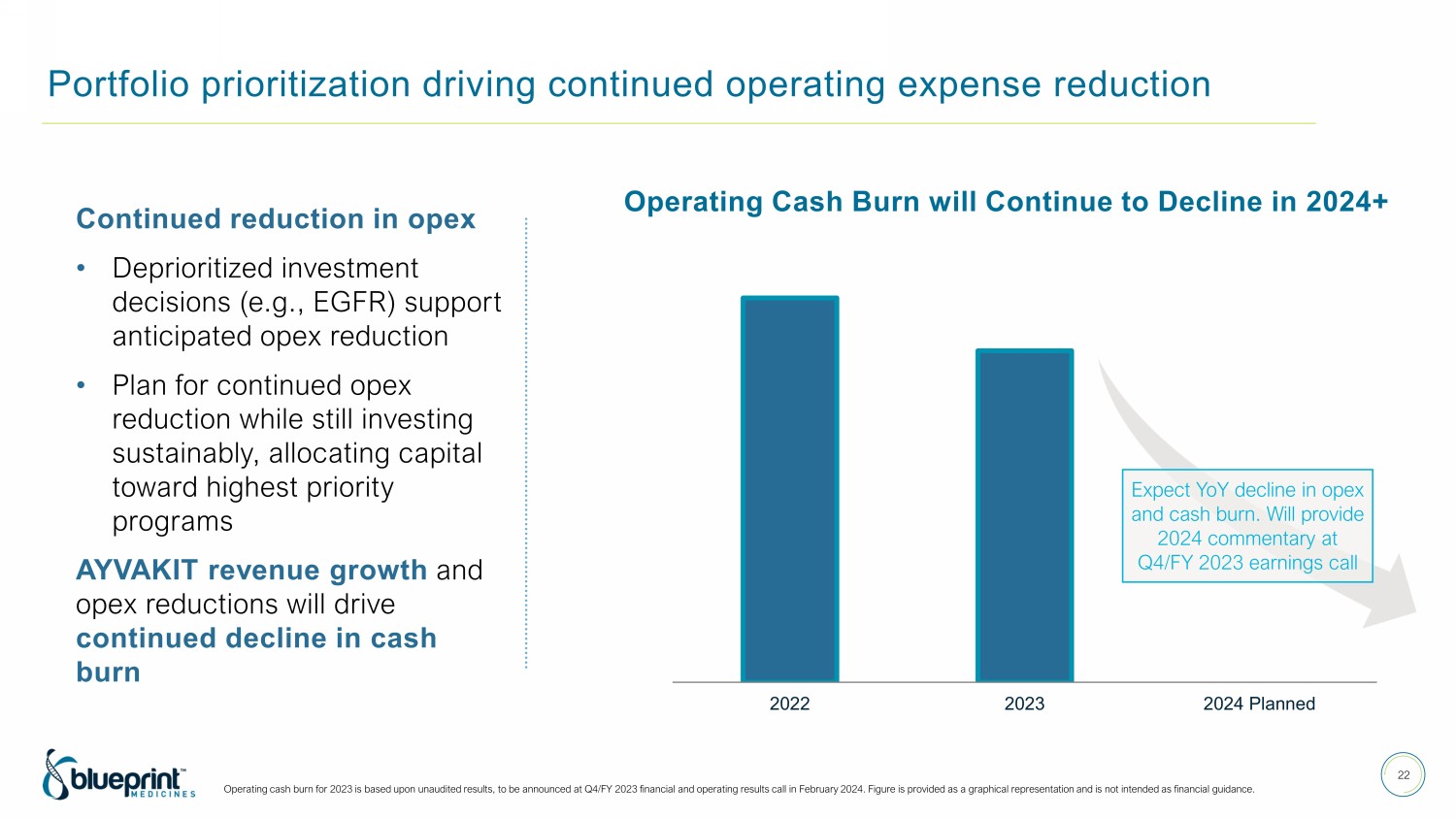
投资组合优先顺序推动运营支出持续减少 22 运营支出持续减少 • 非优先级投资决策(例如EGFR)支持预期的运营支出减少 • 计划在持续投资的同时继续减少运营支出,将资本分配给最优先项目 AYVAKIT 收入增长和运营支出的减少将推动现金消耗的持续下降 2024 年以上的运营现金消耗将继续下降 2023 年的运营现金消耗基于未经审计的业绩,将在上公布 2023 财年第四季度财务和运营结果全部在 2024 年 2 月。该数字以图形形式提供,不作为财务指导。2022-2023年计划预计运营支出和现金消耗同比下降。将在 2023 财年第四季度财报电话会议上提供 2024 年评论

2024 年的主要预期产品组合里程碑 23 个区域项目里程碑计时肥大细胞疾病 AYVAKIT 目前在 ISM 1H 2024 年 BLU-808 IND 提交的长期安全性和有效性数据 Elenestinib 启动注册——启用 2024 年下半年的 HARBOR 试验第 2 部分实体瘤 BLU-222 与 ribociclib 和 fulvestrant 联合用于 HR+/HER2 的数据-乳腺癌 2024 年上半年提供HR+/HER2-2024年下半年乳腺癌注册计划的最新情况除AYVAKIT收入增长外,Blueprint预计还会出现以下情况2024 年与数据相关的里程碑:

蓝图有望在2024年及以后加速我们的业务增长。AYVAKIT正在SM中抓住一个重大的机遇。SM 中的 AYVAKIT 是当今发布的最激动人心的罕见疾病之一。利用我们的专业知识,重点投资增长机会。在我们对核心生物学和业务战略的深刻理解的基础上,追求令人兴奋的科学领域,通过杠杆和规模推动增长。走上盈利之路。通过增加收入和有针对性的支出计划,我们保持了持久的资本状况,同时还投资于长期增长的机会。

BLU-222 CDK2 正在进行的合作讨论 BLU-956(下一代)CDK2 靶向蛋白降解剂 CDK2 全球靶向蛋白降解剂未公开的 AYVAKIT®(阿伐替尼)1 试剂盒 D816V 全球不包括大中华区 4 埃来斯替尼(下一代)试剂盒 D816V Global BLU-808 野生型试剂盒其他未公开的肥大细胞靶标/模式蓝图药品管线 25 Indolent SM 2 Advanced SM 3 Indolent SM 慢性荨麻疹 HR+/HER2-乳腺癌其他 CDK2 脆弱癌症 HR+/HER2-乳腺癌项目 TARGET DISCOVERY 临床商业权利 HR+/HER2-乳腺癌肥大细胞疾病过敏/炎症重点:实体瘤肿瘤学重点:1.美国还批准用于携带 PDGFRA 外显子 18 突变的不可切除或转移性 GIST 的成年人,包括 P DGF RA D842V 突变。欧洲(AYVAKYT®)获批准,用于携带 PDGFRA D842V 突变的不可切除或转移性 GIST 的成年人。2.在美国获准用于患有惰性 SM 的成年人。在欧洲(AYVAKYT)获批,用于对症治疗无法充分控制的惰性 SM 的成年人,其发生率为中等至严重症状。在美国获准用于晚期SM(包括侵袭性SM(ASM)、伴有相关血液学肿瘤(SM-AHN)的SM和肥大细胞白血病(MCL)的成年人。在欧洲(AYV AKYT®)获得批准,适用于至少经过一次全身治疗后患有 ASM、SM-AHN 或 MCL 的成年人。4.基石制药拥有在大中华区开发和商业化阿伐替尼的独家权利。更新于 2024 年 1 月 8 日。其他项目未披露的全球