根据规则 424(B)(4)提交
注册号码333-234408
1,333,360股美国存托股份

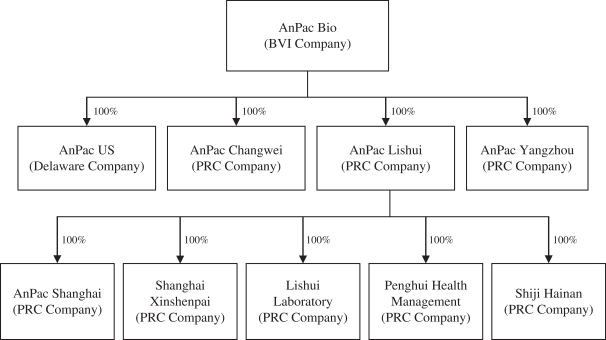
安派科股份有限公司。
相当于1,333,360股A类普通股
这是美国存托股份(ADS)的首次公开发行,相当于Anpac 生物医学科学有限公司的A类普通股。
我们提供1,333,360份美国存托凭证。每一张美国存托股份代表一股我们的A类普通股 ,每股票面价值0.01美元。
在此次发行之前,美国存托凭证或我们的股票还没有公开市场。这些美国存托凭证已获准在纳斯达克全球市场上市,交易代码为ANPC。
我们是一家新兴的成长型公司,因为该术语在2012年的JumpStart Our Business Startups Act中使用,因此,我们已选择遵守某些降低的上市公司报告要求。
我们已经并将保持双层股权结构。我们的已发行普通股包括A类普通股和B类普通股。除投票权和转换权外,A类普通股和B类普通股的持有人拥有相同的权利。每股A类普通股有权投一(1)票,每股B类普通股有权投十(10)票。每股B类普通股可由其持有人随时转换为一股A类普通股。A类 普通股在任何情况下都不能转换为B类普通股。当持有人将B类普通股转让给任何并非持有人联营公司的人士或实体时,该等B类普通股应自动及即时转换为相同数目的A类普通股。
本公司创办人兼主席常裕博士连同张江市古可有限公司及智骏四航集团有限公司就其部分普通股实益拥有本公司所有已发行B类普通股。假设承销商不行使其 超额配售选择权,并且不包括因行使未行使的期权或我们同意授予承销商代表的认股权证或嘉兴智骏投资管理有限公司向我们提供的可转换贷款而可发行的股份,则所有B类普通股约占本次发行完成后我们的全部流通股总数的25.6%,以及紧接本次发行完成后我们总流通股的77.4%。见主要股东。
一名个人投资者已认购并获配发145,881股美国存托凭证,或约10.9%的美国存托凭证,按首次公开发售价格及按与本次发售的其他美国存托凭证相同的条款计算。承销商从该投资者购买的任何美国存托凭证 获得的承销折扣和佣金,将与他们在本次发行中向公众出售的任何其他美国存托凭证获得的承销折扣和佣金相同。
投资美国存托凭证涉及高度风险。请参阅第14页开始的风险因素,了解在购买美国存托凭证前应考虑的因素。
美国证券交易委员会和任何州证券委员会都没有批准或不批准这些证券,也没有确定本招股说明书是否真实或完整。任何相反的陈述都是刑事犯罪。
每个美国存托股份售价12美元
| 价格至公众 | 承销折扣和佣金(1) | 净收益为我们 | ||||||||||
| 每个美国存托股份 |
美元 | 12.00 | 美元 | 0.84 | 美元 | 11.16 | ||||||
| 总计 |
美元 | 16,000,320 | 美元 | 1,120,022.40 | 美元 | 14,880,297.60 | ||||||
| (1) | 有关承保补偿的其他信息,请参阅承保。 |
承销商有30天的选择权,以首次公开发行价格减去承销折扣和佣金从我们购买总计200,004份额外的美国存托凭证。
承销商预计将于2020年2月3日在纽约交割美国存托凭证。
联合簿记管理经理
| Westpark Capital,Inc. | Univest Securities,LLC |
招股说明书日期:2020年1月28日